Данное изобретение относится к водным офтальмологическим композициям в виде раствора, содержащим (1S,2Е)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициютопентил]-1-(2-фенилэтил)-2-пропен-1-иловый эфир 6-(нитроокси)-гексановой кислоты в качестве активного ингредиента и макрогол 15 гидроксистеарат.
6-(Нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1 -иловый эфир имеет следующую формулу (I)

Это соединение показало свою эффективность в качестве средства, снижающего внутриглазное давление (IOP) (F. Impagnatiello, С.В. Toris, М. Batugo, G. Prasanna, V. Borghi, Е. Bastia, Е. Ongini, А.Н.Р. Krauss; Invest Ophthalmol Vis Sci. 2015; 56:6558-64).
В WO 2009/136281 (Nicox SA) раскрыто применение (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира 6-(нитроокси)-гексановой кислоты для лечения глаукомы и глазной гипертензии.
В Impagnatiello Francesco et al; British Journal of Pharmacology (2018), c. 1-11 раскрыты неклинические фармакологические исследования, показывающие более высокую IOP-понижающую эффективность NCX 470, чем у эквимолярных доз биматопроста. Оба соединения растворяли в носителе, содержащем 0,25% Tween 80, 0,02% BAK (бензалкония хлорид), 2% глицерина и 0,1% EDTA (этилендиаминтетрауксусная кислота).
Местная инсталляция является наиболее предпочтительным неинвазивным путем введения лекарственного средства для лечения повышенного внутриглазного давления. Большинство обычных лекарственных форм представленных на рынке IOP-снижающих лекарственных средств представляют собой глазные капли в форме водного раствора, однако при этом, при местном капельном введении, глазная биодоступность активного начала является очень низкой. Многочисленные анатомические и физиологические факторы, такие как быстрая прекорнеальная элиминация лекарственного средства из-за стекания раствора и системной абсорбции из конъюктивального мешка и эпителиальный барьер роговицы, ограничивают глазную абсорбцию применяемых местно лекарственных средств. Важной целью фармацевтических композиция является обеспечение возможности проникновения IOP-понижающего лекарственного средства в глаз после единственной или многократных местных капельных инсталляций. Известно, что время удерживания лекарственного средства на поверхности глаза является очень коротким после однократного капельного применения. В результате обычно используют несколько подходов к составлению композиций для обеспечения больших возможностей проникновения лекарственного средства внутрь глаза после нанесения на глазную поверхность и, в идеале, с режимом наименьшего дозирования, например один раз в сутки, чтобы способствовать соблюдению пациентом режима лечения.
Один из подходов заключается в увеличении вязкости офтальмологического раствора. В результате раствор будет иметь лучшую адгезию к поверхности глаза и соответственно увеличится время удерживания лекарственного средства на этой поверхности. В результате предполагается, что внутрь глаза проникает увеличенное количество лекарственного средства. Например, в WO 2012/001009 раскрыта система доставки, состоящая из гелеобразующей системы, основанной на комбинации двух гелеобразующих агентов, с получением невязкой полимерной системы доставки, которая обеспечивает необходимый уровень вязкости и способствует растворимости активного ингредиента, простагландина.
Другой подход заключается в использовании агента, усиливающего проникновение в глаз. Одним из наиболее известных усилителей проникновения является бензалкония хлорид (BAK). В случае офтальмологической композиции простагландина этот подход используется компанией Allergan в их продукте Lumigan®. В серийное производство был запущен продукт первого поколения, где доза простагландина Bimatoprost составляла 0,03%. В этом продукте, доза бензалкония хлорида составляла 0,005%. Эту дозу бензалкония хлорида в основном использовали для обеспечения антимикробной защиты раствора. Несколько лет позднее в серийное производство запустили Lumigan® второго поколения с той же эффективностью, что и у старого поколения продукта. Эта новая композиция имеет более низкую концентрацию биматопроста (0,01%), но 4-кратное увеличение количества бензалкония хлорида (0,02%) по сравнению с исходной композицией (0,005%).
Другая техническая проблема офтальмологических фармацевтических композиций заключается в стабилизации активного начала. Можно отметить, что для некоторых композиций глазных капель требуется холодное хранение для сохранения уровня их активного ингредиента, что влечет за собой такой недостаток как плохие потребительские свойства; например, для многодозовых флаконов содержание активного ингредиента может уменьшаться со временем, если препарат не хранится должным образом при низкой температуре. Глазные капли для лечения глаукомы или глазной гипертензии часто назначают пожилым людям, у которых могут быть трудности с обеспечением необходимых "холодных" условий для хранения лекарственных средств.
В US 8772337 (Thea Laboratories) раскрыты стабильные при комнатной температуре офтальмологические растворы, содержащие простагландин и Solutol HS15 (макрогол 15-гидроксистеарат), не содержащая противомикробного консерванта.
В US 8772337 раскрыто, что Solutol® HS15 способен солюбилизировать некоторые простагландины, такие как Латанопрост, и придает стабильность раствору при температуре окружающей среды в отсутствие четвертичного аммониевого агента, такого как бензалкония хлорид, используемого здесь в качестве обычного солюбилизатора для такого аналога простагландина. Более конкретно, он придает стабильность раствору аналога простагландина к упаковке, в частности к пластиковой упаковке типа LDPE (полиэтилен низкой плотности) со свойствам, соответствующими Европейской фармакопее (ЕР). Следовательно, Solutol® HS15 можно использовать как альтернативу полисорбату 80 в качестве солюбилизирующего агента.
В тестовых примерах в US 8772337 раскрыты офтальмологические "носители", содержащие Solutol® HS15 (0,5%), фосфатный буфер, сорбитол и EDTA.
В WO 2013/003827 (Allergan) раскрыты композиции, содержащие макрогол 15-гидроксистеарат и консервант.В этой патентной заявке раскрыто, что применение макрогол 15-гидроксистеарата (Solutol® HS15) в качестве поверхностно-активного вещества вместо полиэтоксилированных поверхностно-активных веществ (полисорбат 80/Tween® 80) имеет ряд преимуществ, таких как повышение растворимости API (активный фармацевтический ингредиент), улучшенная стабильность API, подверженных деградации посредством окислительных механизмов, улучшенная эффективность консервации бензалкония хлоридом, улучшенная переносимость при офтальмологическом применении.
В WO 2009/084021 (Sun Pharmaceutical) раскрыто, что добавление стабилизирующего количества полигликолевого эфира 12-гидроксистеариновой кислоты (Solutol® HS15) к офтальмологической композиции, содержащей один или более производных простагландина, снижает сорбцию производных простагландина на полиэтиленовых контейнерах и что добавление небольшого количества масла дополнительно снижает сорбцию производных простагландина на контейнеры из полиэтилена низкой плотности.
В US 8795634 (Critical Pharma.) раскрыто применение Solutol HS15 в качестве усилителя абсорбции для улучшения системной абсорбции местно применяемых терапевтических средств через слизистые оболочки полости носа, щечной полости и дыхательных путей. Однако механизмы адсорбции активного вещества, применяемого местно на слизистые оболочки, отличаются от пути, используемого терапевтическим агентом, применяемым местно для прохождения через глаз; действительно, терапевтический агент должен пересечь анатомические барьеры, которые присущи и уникальны для анатомии глаза (то есть эпителий роговицы, конъюнктиву и склеру), и обойти защитные механизмы глаза (то есть моргание, обновление слезной пленки и отток).
Макрогол 15 гидроксистеарат (Kolliphor® HS15 от BASF, ранее известный, как Solutol® HS15) представляет собой основной эксципиент композиции по настоящему изобретению; как сообщалось выше, существует несколько документов предшествующего уровня техники, которые раскрывают использование макрогол 15 гидроксистеарата в качестве эксципиента офтальмологической композиции.
Термин "макрогол 15 гидроксистеарат" относится к смеси главным образом моноэфиров и диэфиров 12-гидроксистеариновой кислоты и макроголов, полученных этоксилированием 12-гидроксистеариновой кислоты. Макрогол 15 гидроксистеарат также известен как сополимер полиэтиленгликоля и 12-гидроксистеариновой кислоты, полиэтиленгликоль-15-гидроксистеарат и полиэтиленгликоль 660 12-гидроксистеарат.В USP-NF (Фармакопея США - Национальный Формуляр) это соединение также указано как полиоксил 15 гидроксистеарат.
Как сообщалось выше, несколько документов предшествующего уровня техники раскрывают использование макрогол 15 гидроксистеарата в качестве эксципиента офтальмологических композиций, однако на сегодняшний день в Европе одобрены только одни глазные капли, включающие макрогол 15 гидроксистеарат и аналог простагландина. Это лекарственное средство зарегистрировано компанией Rafarm S.A под названием Provastor и содержит Travoprost в качестве аналога простагландина и BAK в качестве антимикробного консерванта.
6-(Нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-иловый эфир представляет собой вязкое масло, имеющее минимальную растворимость в воде 0,02 мг/мл, следовательно, водные фармацевтические композиции 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира должны содержать солюбилизирующие вещества, которые повышают растворимость этого соединения в воде и позволяют достичь терапевтически активных концентраций соединения.
В WO 2009/136281 раскрыта композиция, содержащая 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-l-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-иловый эфир в носителе, содержащем 0,5% полисорбата 80 (Tween® 80), 0,02% бензалкония хлорида, цитратный буфер, воду, и имеющая рН 5,5.
Полисорбат 80 широко используют в качестве эксципиента офтальмологических композиций. Например, в продукте Rescula®, поставляемом компанией Novartis, объединены унопростон со смесью бензалкония хлорида и полисорбата 80 в количестве 0,015% от массы раствора.
Настоящее изобретение относится к офтальмологической водной композиции в виде раствора, содержащая 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-иловый эфир и макрогол 15 гидроксистеарат, где макрогол 15 гидроксистеарат предпочтительно является единственным солюбилизирующим агентом.
Офтальмологические водные композиции по изобретению обеспечивают более высокую проницаемость в глаз активного вещества, 6-(нитроокси)-гексановой кислоты (1S,2Е)-3-[1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира, по сравнению с известной композицией, таким образом обеспечивая повышенную глазную абсорбцию терапевтически активного вещества.
В изобретении также предложены офтальмологические водные композиции в форме растворов, содержащих 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-иловый эфир, которые являются как химически, так и физически стабильными при хранении при комнатной температуре.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
В настоящем изобретении предлагается офтальмологическая водная композиция в виде раствора, содержащая 0,005%-0,18% масс./масс. 6-(нитроокси)-гексановой кислоты (1S,2Е)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира, от 0,5% масс./масс. до 1,5% масс./масс. макрогол 15 гидроксистеарата, где макрогол 15 гидроксистеарат предпочтительно представляет собой единственный солюбилизирующий агент.
Другим воплощением является офтальмологическая водная композиция в виде раствора, содержащая 0,005%-0,10% масс./масс. 6-(нитроокси)-гексановой кислоты (1S,2Е)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира, от 0,5% масс./масс. до 1,5% масс./масс. макрогол 15 гидроксистеарата, где макрогол 15 гидроксистеарат предпочтительно представляет собой единственный солюбилизирующий агент.
В предпочтительном воплощении настоящего изобретения предлагается офтальмологическая водная композиция в виде раствора, содержащая от 0,005% масс./масс. до 0,065% 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира, от 0,5% масс./масс. до 1,5% масс./масс. макрогол 15 гидроксистеарата и фармацевтически приемлемый водный носитель, где макрогол 15 гидроксистеарат предпочтительно представляет собой единственный солюбилизирующий агент.
В области офтальмологии и, в частности, в водных офтальмологических композициях солюбилизирующие агенты представляют собой соединения, которые улучшают растворение биологически активного компонента с относительно низкой растворимостью в воде.
Предпочтительно, количество 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира в офтальмологическом растворе составляет от 0,01% до 0,065% масс./масс., наиболее предпочтительно 0,021% масс./масс., 0,042% масс./масс. или 0.065% масс./масс.
Офтальмологический водный раствор может содержать бензалкония хлорид (BAK) в качестве антимикробного консерванта в количестве от 0,013% до 0,02% масс./масс. и эдетатную соль (EDTA), такую как динатриевая соль этилендиаминтетрауксусной кислоты, в количестве от 0,03% масс./масс. до 0,07% масс./масс. в качестве вспомогательного антимикробного консерванта; предпочтительное количество бензалкония хлорида (BAK) составляет от 0,013% до 0,02% масс./масс. и количество эдетатной соли (EDTA) составляет 0,05% масс./масс.; наиболее предпочтительное количество бензалкония хлорида (BAK) составляет 0,016% масс./масс., и количество эдетатной соли (EDTA) составляет 0,05% масс./масс.
Водная офтальмологическая композиция по изобретению дополнительно включает буфер, выбранный из: дигидрофосфата натрия, динатрия гидрофосфата гептагидрата, дигидрофосфата калия или дикалия гидрофосфата, борной кислоты и ее солей, ацетатов, таких как ацетат натрия, и предпочтительно их смесей. Предпочтительно, буфер водной офтальмологической композиции по изобретению представляет собой смесь гептагидрата двухосновного фосфата натрия и борной кислоты или смесь лимонной кислоты и гептагидрата двухосновного фосфата натрия. Предпочтительное значение рН для композиции составляет 6,0. Было обнаружено, что это значение рН является оптимальным для обеспечения как приемлемой стабильности композиции в условиях длительного хранения, так и подходящей глазной переносимости при доставке композиций на поверхность глаза.
рН водной офтальмологической композиции предпочтительно устанавливают в диапазоне от 5,5 до 6,5, более предпочтительно рН 6,0.
Водная офтальмологическая композиция по изобретению может включать рН-регулирующий агент, выбранный из соляной кислоты, лимонной кислоты, фосфорной кислоты, уксусной кислоты, винной кислоты, гидроксида натрия, гидроксида калия, карбоната натрия и бикарбоната натрия; предпочтительно, водная офтальмологическая композиция по изобретению содержит соляную кислоту и/или гидроксид натрия в таком количестве, чтобы установить рН в диапазоне от 5,5 до 6,5; более предпочтительно рН 6,0.
Офтальмологический водный раствор может содержать регуляторы тоничности, используемые для регулировки осмоляльности композиции и достижения необходимой изотоничности. Предпочтительные регуляторы тоничности представляют собой хлорид натрия, сорбитол, глицерин (или глицерол) и маннитол. Изотоничность устанавливают на уровне 300 мосмоль/кг, но более широкий диапазон от 260 до 340 мосмоль/кг обычно является приемлемым для составления офтальмологических растворов. Предпочтительно, осмоляльность раствора находится в диапазоне 280-320 мосмоль/кг.
Офтальмологический водный раствор по изобретению может содержать регулирующий вязкость агент, используемый для улучшения контакта между раствором и глазом и способствующий улучшенному растеканию продукта по поверхности глаза. Предпочтительные регулирующие вязкость агенты представляют собой полимерные производные целлюлозы, такие как карбоксиметилцеллюлоза или гидроксипропилметилцеллюлоза, гиалуроновую кислоту, поливиниловый спирт, полимеры карбоновых кислот, такие как карбомеры или поликарбофилы. Наиболее предпочтительно, регулирующий вязкость агент представляет собой гидроксипропилметилцеллюлозу в концентрации менее 0,5% масс./масс. Вязкость офтальмологического водного раствора устанавливают от 5 до 10 мПа⋅с для Ньютоновских растворов при использовании производных целлюлозы, но она может быть выше с высоковязким раствором с Неньютоновским/псевдопластическим реологическим поведением, обычно получаемым при использовании карбоксилсодержащих полимеров.
В другом воплощении изобретения предлагается офтальмологическая водная композиция в виде раствора, содержащая 0,005% масс./масс. - 0,10% 6-(нитроокси)-гексановой кислоты (1S,2Е)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира, 0,5%-1,5% масс./масс. макрогол 15 гидроксистеарата, 0,013% масс./масс. - 0,02% масс./масс. бензалкония хлорида, 0,03%-0,07% масс./масс. дигидрата динатриевой соли этилендиаминтетрауксусной кислоты, гептагидрат двухосновного фосфата натрия, борную кислоту и воду, где рН офтальмологического раствора равен 6 и где макрогол 15 гидроксистеарат представляет собой единственный солюбилизирующий агент.
В другом воплощении изобретения предлагается офтальмологическая водная композиция в виде раствора, содержащая 0,005%-0,065% 6-(нитроокси)-гексановой кислоты (1S,2Е)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира, 0,5%-1,5% масс./масс. макрогол 15 гидроксистеарата, 0,013%-0,02% масс./масс. бензалкония хлорида, 0,03%-0,07% масс./масс. дигидрата динатриевой соли этилендиаминтетрауксусной кислоты, гептагидрат двухосновного фосфата натрия, борную кислоту и воду, где рН офтальмологического раствора равен 6 и где макрогол 15 гидроксистеарат представляет собой единственный солюбилизирующий агент; предпочтительно количество 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира в офтальмологическом растворе составляет от 0,01% до 0,065% масс./масс., наиболее предпочтительно 0,042% масс./масс., 0,021% масс./масс. или 0,065% масс./масс. возможно офтальмологический раствор дополнительно содержит 1,2 М HCl /1 М NaOH для доведения рН до 6,0.
В другом воплощении изобретения предлагается офтальмологическая водная композиция в виде раствора, содержащая 0,005% 0,10% 6-(нитроокси)-гексановой кислоты (1S,2Е)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира, 1,0% масс./масс. макрогол 15 гидроксистеарата, 0,016% масс./масс. бензалкония хлорида, 0,05% масс./масс. дигидрата динатриевой соли этилендиаминтетрауксусной кислоты, гептагидрат двухосновного фосфата натрия, борную кислоту и воду, где рН офтальмологического раствора равен 6 и где макрогол 15 гидроксистеарата представляет собой единственный солюбилизирующий агент.
В другом воплощении изобретения предлагается офтальмологическая водная композиция в виде раствора, содержащая 0,005%-0,065% масс./масс. 6-(нитроокси)-гексановой кислоты (1S,2Е)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира, 1,0% масс./масс. макрогол 15 гидроксистеарата, 0,016% масс./масс., бензалкония хлорида, 0,05% масс./масс., дигидрата динатриевой соли этилендиаминтетрауксусной кислоты, гептагидрата двухосновного фосфата натрия, борную кислоту и воду, где рН офтальмологического раствора равен 6 и где макрогол 15 гидроксистеарат представляет собой единственный солюбилизирующий агент; предпочтительно количество 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира в офтальмологическом растворе составляет от 0,01% до 0,065% масс./масс., наиболее предпочтительно 0,042% масс./масс., 0,021% масс./масс. или 0,065% масс./масс.; возможно офтальмологический раствор дополнительно содержит 1,2 М HCl/1 М NaOH для доведения рН до 6,0.
В другом воплощении изобретения предлагается офтальмологическая водная композиция в виде раствора, состоящая из: от 0,005% до 0,10% 6-(нитроокси)-гексановой кислоты (1S,2Е)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира, от 1,0% до 1,5% масс./масс. макрогол 15 гидроксистеарата, 0,016% масс./масс. бензалкония хлорида, 0,05% масс./масс. дигидрата динатриевой соли этилендиаминтетрауксусной кислоты, 2,76% масс./масс. сорбитола, 1,33% масс./масс. гептагидрата двухосновного фосфата натрия (Na2HPO4⋅7H2O), 0,5% масс./масс. борной кислоты и воды, где рН офтальмологического раствора равен 6 и где макрогол 15 гидроксистеарат является единственным солюбилизирующим агентом.
В другом воплощении изобретения предлагается офтальмологическая водная композиция в виде раствора, состоящая из: от 0,005% до 0,065% 6-(нитроокси)-гексановой кислоты (1S,2Е)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира, 1,0% масс./масс. макрогол 15 гидроксистеарата, 0,016% масс./масс. бензалкония хлорида, 0,05% масс./масс. дигидрата динатриевой соли этилендиаминтетрауксусной кислоты, 2,76% масс./масс. сорбитола, 1,33% масс./масс. гептагидрата двухосновного фосфата натрия (Na2HPO4⋅7H2O), 0,5% масс./масс. борной кислоты и воды, где рН офтальмологического раствора равен 6 и где макрогол 15 гидроксистеарат представляет собой единственный солюбилизирующий агент; предпочтительно количество 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира в офтальмологическом растворе составляет от 0,01% до 0,065% масс./масс., наиболее предпочтительно 0,021% масс./масс., 0,042% масс./масс. или 0,065% масс./масс.; возможно офтальмологический раствор дополнительно содержит 1,2 М HCl/1 М NaOH для доведения рН до 6,0.
Конкретными примерами офтальмологической водной композиции по изобретению в виде раствора являются:
0,042% масс./масс.6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-l-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира, 1,0% масс./масс. макрогол 15 гидроксистеарата, 0,016% масс./масс. бензалкония хлорида, 0,05% масс./масс. дигидрата динатриевой соли этилендиаминтетрауксусной кислоты, 2,76% масс./масс. сорбитола, 1,33% масс./масс. гептагидрата двухосновного фосфата натрия, 0,5% масс./масс. борной кислоты и вода, и имеющая рН 6;
0,021% масс./масс. 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-l-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира, 1,0% масс./масс. макрогол 15 гидроксистеарата, 0,016% масс./масс. бензалкония хлорида, 0,05% масс./масс. дигидрата динатриевой соли этилендиаминтетрауксусной кислоты, 2,76% масс./масс. сорбитола, 1,33% масс./масс. гептагидрата двухосновного фосфата натрия, 0,5% масс./масс. борной кислоты и вода, и имеющая рН 6;
- 0,065% 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира, 1,0% масс./масс. макрогол 15 гидроксистеарата, 0,016% масс./масс. бензалкония хлорида, 0,05% масс./масс. дигидрата динатриевой соли этилендиаминтетрауксусной кислоты, 2,76% масс./масс. сорбитола, 1,33% масс./масс. гептагидрата двухосновного фосфата натрия, 0,5% масс./масс. борной кислоты и вода, и имеющая рН 6;
- 0,10% масс./масс. 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира, 1,5% масс./масс. макрогол 15 гидроксистеарата, 0,016% масс./масс. бензалкония хлорида, 0,05% масс./масс. дигидрата динатриевой соли этилендиаминтетрауксусной кислоты, 0,52% масс./масс. глицерола, 2,33% масс./масс. гептагидрата двухосновного фосфата натрия, 0,36% масс./масс. лимонной кислоты и воды, и имеющая рН 6.
В вышеуказанных офтальмологических водных композициях в качестве регуляторов рН можно использовать соляную кислоту или гидроксид натрия.
Вышеуказанные офтальмологические водные растворы могут быть упакованы в первичные контейнеры из полиэтилена низкой плотности (LDPE), обычно в многодозовые офтальмологические бутыли с колпачком и насадкой-капельницей, позволяющей получать калиброванные капли с контролируемым размером капель. Примером таких первичных контейнеров могут быть бутыли Rispharm® от Berry-Plastics, Boston Round® от Amcor, трехэлементные бутылки от Gerresheimer, Philips-Medisize, Bormioli или эквивалентные.
Офтальмологическая водная композиция в виде раствора может быть представлена в виде офтальмологических водных растворов, не содержащих антимикробного консерванта.
В одном воплощении изобретения предлагается офтальмологическая водная композиция в виде раствора, не содержащая антимикробного консерванта, содержащая от 0,005% до 0,10% 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира, от 0,5% до 1,5% масс./масс. макрогол 15 гидроксистеарата, гептагидрат двухосновного фосфата натрия, борную кислоту и воду, где рН офтальмологического раствора равен 6, дополнительно содержащая агент тоничности и возможно дополнительный рН-регулирующий агент, где макрогол 15 гидроксистеарат представляет собой единственный солюбилизирующий агент.
Конкретным примером офтальмологической водной композиции в виде раствора, не содержащей консерванта, является следующая композиция, состоящая из: 0,042% масс./масс.6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира, 1,0% масс./масс. макрогол 15 гидроксистеарата, 2,76% масс./масс. сорбитола, 1,33% масс./масс. гептагидрата двухосновного фосфата натрия, 0,5% масс./масс. борной кислоты и воды, и имеющая рН 6.
Другими конкретными примерами офтальмологической водной композиции в виде раствора, не содержащей консервантов, являются следующие композиции:
- 0,042% масс./масс. 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира, 1,0% масс./масс. макрогол 15 гидроксистеарата, 2,76% масс./масс. сорбитола, 1,33% масс./масс. гептагидрата двухосновного фосфата натрия, 0,5% масс./масс. борной кислоты и вода, и имеющая рН 6.
- 0,021% масс./масс. 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1 -илового эфира, 1,0% масс./масс. макрогол 15 гидроксистеарата, 2,76% масс./масс. сорбитола, 1,33% масс./масс. гептагидрата двухосновного фосфата натрия, 0,5% масс./масс. борной кислоты и вода, и имеющая рН 6.
- 0,065% масс./масс. 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира, 1,0% масс./масс. макрогол 15 гидроксистеарата, 2,76% масс./масс. сорбитола, 1,33% масс./масс. гептагидрата двухосновного фосфата натрия, 0,5% масс./масс. борной кислоты и вода, и имеющая рН 6.
- 0,10% масс./масс. 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира, 1,5% масс./масс. макрогол 15 гидроксистеарата, 0,52% масс./масс. глицерина, 2,33% масс./масс. гептагидрата двухосновного фосфата натрия, 0,36% масс./масс. лимонной кислоты и вода, и имеющая рН 6.
В вышеуказанных офтальмологических водных композициях в качестве регуляторов рН можно использовать соляную кислоту или гидроксид натрия.
Офтальмологические водные композиции по изобретению, не содержащие антимикробного консерванта, упаковывают в контейнеры, которые предупреждают микробное загрязнение композиций даже после многократных применений, или офтальмологические водные композиции, не содержащие антимикробных консервантов, упаковывают в однодозовые контейнеры, которые являются стерильными в неоткрытом виде.
Такая не содержащая консервантов композиция может быть упакована либо в первичной LDPE упаковке с однократной или единичной дозой, либо в многодозовой контейнерной системе, не содержащей консервантов.
Обычно не содержащие консервантов водные композиции по изобретению упаковывают в однодозовые контейнеры, предназначенные для одноразового использования пациентом. В другом воплощении, офтальмологические водные композиции, не содержащие антимикробных консервантов, упаковывают в многодозовые контейнеры, не содержащие консервантов, которые обеспечивают возможность сохранения композиции стерильной даже после многократных использований пациентом. Примерами многодозовых контейнеров, не содержащих консервантов, являются: OSD® от Aptar, Novelia® от Nemera, 3K® от Aeropump или эквивалентные устройства.
Макрогол 15 гидроксистеарат, используемый в изобретении, представляет собой имеющийся в продаже Kolliphor® HS15, ранее известный как Solutol® HS15, а также указанный в USP как полиоксил-15 гидроксистеарат; он состоит из полигликолевых моно- и диэфиров 12-гидроксистеариновой кислоты и из примерно 30% свободного полиэтиленгликоля.
Водные офтальмологические композиции в виде раствора по изобретению продемонстрировали эффективность в снижении внутриглазного давления, поэтому их можно использовать в лечении глазной гипертензии, глаукомы или в способе снижения внутриглазного давления.
Другой объект изобретения относится к офтальмологической водной композиции в виде раствора по изобретению для использования в лечении глазной гипертензии, глаукомы или в способе снижения внутриглазного давления.
Другой объект изобретения относится к вышеуказанным офтальмологическим водным композициям в виде раствора для использования в лечении глазной гипертензии, глаукомы или для снижения внутриглазного давления.
Другое воплощение изобретения относится к офтальмологической водной композиции в форме раствора, содержащей от 0,005% до 0,18% масс./масс.6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира, от 0,5% масс./масс. до 1,5% масс./масс. макрогол 15 гидроксистеарата, где макрогол 15 гидроксистеарат является единственным солюбилизирующий агентом, для применения в лечении глазной гипертензии, глаукомы или для снижения внутриглазного давления.
Другое воплощение изобретения относится к офтальмологической водной композиции в форме раствора, содержащей от 0,005% до 0,10% масс./масс. 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира, от 0,5% масс./масс. до 1,5% масс./масс. макрогол 15 гидроксистеарата, где макрогол 15 гидроксистеарат является единственным солюбилизирующий агентом, для применения в лечении глазной гипертензии, глаукомы или для снижения внутриглазного давления.
Другое воплощение изобретения относится к способу лечения глазной гипертензии или глаукомы или к способу снижения внутриклеточного давления, включающему введение пациенту, нуждающемуся в этом, терапевтически эффективного количества вышеуказанной офтальмологической водной композиции в виде раствора.
Другое воплощение изобретения относится к способу лечения глазной гипертензии или глаукомы или к способу снижения внутриглазного давления, включающему введение пациенту, нуждающемуся в этом, терапевтически эффективного количества офтальмологической водной композиции в виде раствора, содержащей от 0,005% до 0,065% 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2 г)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира, от 0,5% до 1,5% масс./масс. макрогол 15 гидроксистеарата и фармацевтически приемлемый водный носитель, где макрогол 15 гидроксистеарат представляет собой единственный солюбилизирующий агент.
Другое воплощение изобретения относится к способу лечения глазной гипертензии или глаукомы или к способу снижения внутриглазного давления, включающему введение пациенту, нуждающемуся в этом, терапевтически эффективного количества офтальмологической водной композиции в виде раствора, содержащей от 0,005% до 0,065% 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира, 1,0% масс./масс. макрогол 15 гидроксистеарата, 0,016% масс./масс. бензалкония хлорида, 0,05% масс./масс. дигидрата динатриевой соли этилендиаминтетрауксусной кислоты, гептагидрат двухосновного фосфата натрия, борную кислоту и воду, где рН офтальмологического раствора равен 6 и где макрогол 15 гидроксистеарата представляет собой единственный солюбилизирующий агент; предпочтительно, количество 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира в офтальмологическом растворе составляет от 0,01% до 0,065% масс./масс., наиболее предпочтительно 0,042% масс./масс., 0,021% масс./масс. или 0,065% масс./масс.; возможно офтальмологический раствор дополнительно содержит 1,2 М HCl /1 М NaOH для доведения рН до 6,0.
Другое воплощение изобретения относится к способу лечения глазной гипертензии или глаукомы или к способу снижения внутриглазного давления, включающему введение пациенту, нуждающемуся в этом, терапевтически эффективного количества офтальмологической водной композиции в виде раствора, состоящей из: от 0,005% до 0,065% 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-l-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира, 1,0% масс./масс. макрогол 15 гидроксистеарата, 0,016% масс./масс. бензалкония хлорида, 0,05% масс./масс. дигидрата динатриевой соли этилендиаминтетрауксусной кислоты, 2,76% масс./масс. сорбитола, 1,33% масс./масс. гептагидрата двухосновного фосфата натрия, 0,5% масс./масс. борной кислоты и воды, и имеющей рН 6; предпочтительно в офтальмологической водной композиции в виде раствора, используемой в вышеуказанном способе, количество 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-l-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира составляет от 0,01% до 0,065% масс./масс., наиболее предпочтительно 0,042% масс./масс., 0,021% масс./масс. или 0,065% масс./масс.; возможно вышеуказанная офтальмологическая водная композиция в виде раствора дополнительно включает 1,2 М HCl/1 М NaOH для доведения рН до 6,0.
Офтальмологические композиции по изобретению можно вводить в виде глазных капель для лечения хронических заболеваний, таких как глаукома или глазная гипертензия. Офтальмологический раствор, как правило, предназначен для введения раз в день в каждый глаз ежедневно.
Другое воплощение изобретения относится к способу изготовления офтальмологического водного раствора по изобретению, включающем следующие стадии:
Стадия 1) приготовление концентрированного раствора 6-(нитроокси)-гексановой кислоты (1S,2Е)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира (концентрированный раствор API), которое включает:
1а) нагревание смеси воды для инъекции и полиоксил 15 гидроксистеарата при температуре 32°С, пока полиоксил 15 гидроксистеарат не расплавится;
1б) добавление смеси расплавленный полиоксил 15 гидроксистеарат/вода к предварительно взвешенному 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-иловому эфиру (API).
1в) перемешивание полученной смеси до полного растворения 6-(нитроокси)-гексановой кислоты (1S,2Е)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен- 1-илового эфира с поддержанием смеси при температуре 32°С; количество воды для инъекции, используемое на стадии (1а), составляет примерно 1,5% от общей массы воды, используемой в препарате; количества полиоксил 15 гидроксистеарата и 6-(нитроокси)-гексановой кислоты (1S,2Е)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира представляют собой их общие массы, соответствующие их процентному содержанию в конечном растворе.
Стадия 2) Приготовление водного раствора остальных ингредиентов носителя путем добавления в производственный бак, содержащий воду для инъекции, эксципиентов в следующем определенном порядке: дигидрат динатрия эдетата, буфер, выбранный из борной кислоты и гептагидрата двухосновного фосфата натрия или лимонной кислоты и гептагидрата двухосновного фосфата натрия, сорбитол или глицерин, и бензалкония хлорид; где каждый эксципиент полностью растворяют перед добавлением следующего эксципиента и приготовление раствора осуществляют при температуре от 25°С до 30°С; количество каждого эксципиента представляет собой его общую массу, соответствующую его процентному содержанию в конечном офтальмологическом растворе; вода для инъекции, используемая на стадии (2), составляет от примерно 80% до 90% общей массы в конечном офтальмологическом растворе.
Вышеописанный порядок добавления эксципиентов должен соблюдаться для того, чтобы соответствовать требованиям рН и тоничности, рН 6,0 и 300 мосмоль/кг.
Стадия 3) Приготовление нерасфасованного офтальмологического раствора путем добавления концентрированного раствора API со Стадии 1 в производственный бак, содержащий водный раствор со Стадии 2, и воды для инъекции вплоть до целевой конечной массы.
рН нерасфасованного офтальмологического раствора возможно доводят до рН 6,0 с помощью 1 М гидроксида натрия или 1,2 М соляной кислоты.
Стадия 4) Стерилизация нерасфасованного офтальмологического раствора посредством фильтрования нерасфасованного офтальмологического раствора со Стадии 3 через полиэфирсульфоновые (PES) фильтры, имеющие размер пор примерно 0,2 мкм.
Стадия 5) Нерасфасованный офтальмологический раствор возможно упаковывают в первичные офтальмологические контейнеры из полиэтилена низкой плотности (LDPE).
Возможно, когда офтальмологический водный раствор дополнительно включает агент, регулирующий вязкость, на Стадии (2) вязкостный агент добавляют в производственный бак, содержащий воду для инъекции, в качестве первого компонента и, когда он полностью растворяется, добавляют другие эксципиенты.
Другое воплощение изобретения относится к способу получения офтальмологического водного раствора по изобретению, не содержащего антимикробного консерванта, включающему следующие стадии:
Стадия 1) приготовление концентрированного раствора 6-(нитроокси)-гексановой кислоты (1S,2Е)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира (концентрированный раствор API), включающее:
1а) нагревание смеси воды для инъекции и полиоксил 15 гидроксистеарата при 32°С, пока не расплавится полиоксил 15 гидроксистеарат;
1б) добавление смеси расплавленный полиоксил 15 гидроксистеарат/вода к предварительно взвешенному 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-иловому эфиру (API).
1в) смешивание полученной смеси до полного растворения 6-(нитроокси)-гексановой кислоты (1S,2Е)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира при поддержании смеси при температуре 32°С; количество воды для инъекции, используемое на Стадии (1а) составляет примерно 1,5% от общей массы воды, используемой в приготовлении; количества полиоксил 15 гидроксистеарата и 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира представляют собой их общие массы, соответствующие их процентному содержанию в конечном растворе.
Стадия 2) Приготовление водного раствора остальных ингредиентов носителя путем добавления в производственный бак, содержащий воду для инъекции, эксципиентов в следующем порядке: буфер и регулятор тоничности; при этом каждый эксципиент полностью растворяют перед добавлением следующего эксципиента и приготовление раствора выполняют при температуре от 25°С до 30°С; количество каждого эксципиента представляет собой общую массу, соответствующую его процентному содержанию в конечном офтальмологическом растворе; вода для инъекции, используемая на Стадии (2) составляет от примерно 80% до 90% общей массы в конечном офтальмологическом растворе.
Вышеописанный порядок добавления эксципиентов должен соблюдаться, чтобы соответствовать требованиям рН и тоничности, рН 6,0 и 300 мосмоль/кг.
Стадия 3) Приготовление нерасфасованного офтальмологического раствора путем добавления концентрированного раствора API со Стадии 1 в производственный бак, содержащий водный раствор со Стадии 2, и воды для инъекции до целевой конечной массы.
При необходимости рН нерасфасованного офтальмологического раствора доводят до рН 6,0 с помощью 1 М гидроксида натрия или 1,2 М соляной кислоты.
Стадия 4) Стерилизация нерасфасованного офтальмологического раствора посредством фильтрования нерасфасованного офтальмологического раствора со Стадии 3 через полиэфирсульфоновые (PES) фильтры, имеющие размер пор примерно 0,2 мкм.
Стадия 5) При необходимости нерасфасованный офтальмологический раствор заполняют в офтальмологические первичные контейнеры из полиэтилена низкой плотности (LDPE).
Когда офтальмологический водный раствор дополнительно включает агент, регулирующий вязкость, на Стадии (2) вязкостный агент добавляют в производственный бак, содержащий воду для инъекции, в качестве первого компонента и, как только он полностью растворяется, добавляют другие эксципиенты.
Пример 1
Приготовление офтальмологической композиции, содержащей 6-(нитроокси)-гексановой кислоты (1S,2Е)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-иловый эфир (NCX 470) 0,042% масс./масс. (партия 100 литров)
Ингредиенты офтальмологической композиции перечислены ниже:
Стадия 1) Приготовление концентрированного раствора API
1,5 л воды для инъекции при примерно 32°С добавляли к 1,000 г Полиоксил 15 гидроксистеарата, предварительно взвешенного в контейнере, который помещали в ванну с горячей водой вплоть до полного расплавления полиоксил 15 гидроксистеарата. Расплавленную смесь полиоксил 15-гидроксистеарат/вода, добавляли в 4 л порционную емкость, содержащую 42 г NCX-470.
4-литровую порционную емкость термостатировали при температуре 32°С на водяной бане, и раствор API перемешивали до полного растворения всех ингредиентов и поддерживали при непрерывном перемешивании до его добавления в раствор носителя остальных эксципиентов.
Стадия 2) Приготовление раствора носителя остальных эксципиентов
100 л воды для инъекции вливали в производственный бак, изготовленный из нержавеющей стали (марка 316L) и охлаждали до 25°С-30°С. Примерно 12 литров этой воды для инъекции извлекали из бака и хранили в другом контейнере для использования во время приготовления.
Следующие соединения были добавлены точно в следующем порядке в производственный бак, содержащий воду, при непрерывном перемешивании; каждое соединение полностью растворяли перед добавлением следующего соединения:
50 г динатрия эдетата дигидрата;
500 г борной кислоты;
1326 г гептагидрата двухосновного фосфата натрия (Na2HPO4⋅7H2O);
2760 г сорбитола;
32 г 50% раствора бензалкония хлорида;
сосуд, содержащий раствор бензалкония хлорид, промывали несколько раз достаточным количеством воды для инъекции, и промывки добавляли в производственный бак для завершения переноса.
Стадия 3) Приготовление нерасфасованного офтальмологического раствора
Концентрированный раствор API переносили в производственный бак; 4 л порционную емкость промывали водой для инъекции и промывки добавляли к основной массе для завершения переноса.
Воду для инъекции добавляли в производственный бак для получения конечной целевой массы 100 кг.
Стадия 4) Стерилизация нерасфасованного офтальмологического раствора
Офтальмологический раствор стерилизовали посредством дополнительного фильтрования через полиэфирсульфоновые (PES) фильтры (Supor®) 0,2 мкм.
Стадия 5) Розлив нерасфасованного офтальмологического раствора в офтальмологические LDPE бутыли
После стадии фильтрования офтальмологический раствор помещали в многодозовые контейнеры LDPE подходящего объема в зоне стерильности класса А в соответствии с обычной практикой асептического процесса.
Пример 2
Исследование стабильности
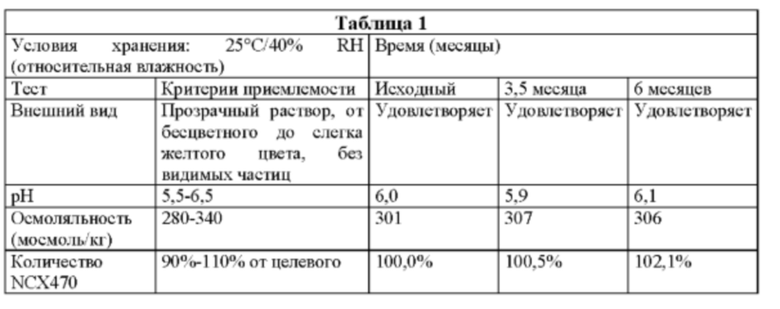
Офтальмологические композиции по изобретению, хранящиеся в многодозовых контейнерах из полиэтилена низкой плотности (LDPE), стерилизованных разными методами стерилизации, были проверены на стабильность. Стабильность офтальмологических композиций, содержащих 0,042% масс./масс. NCX 470, оценивали при 25°С в исходном состоянии, через 3,5 месяца и 6 месяцев, 9 месяцев (условия длительного хранения) и ускоренную стабильность при температуре 40°С, при относительной влажности не более 25% (RH), в исходном состоянии, через 3,5 месяца и 6 месяцев.
Состав офтальмологических композиций:
Результаты представлены в Таблицах 1-4
Результаты испытаний на стабильность при 25°С (Таблицы 1 и 3) и 40°С (Таблицы 2 и 4) показали хорошую стабильность офтальмологических растворов по изобретению; таким образом, ожидается, что офтальмологические растворы, помещенные в первичные LDPE контейнеры будут иметь срок годности продукта, составляющий по меньшей мере 24 месяца в условиях хранения при температуре окружающей среды.
Пример 2А:
Первичный контейнер: Прозрачный LDPE/Предварительно стерилизованный облучением (гамма лучи /25 кГр)
Конфигурация первичного контейнера: 2,5 мл помещают в 7,5 мл бутыль.

Пример 2В:
Первичный контейнер: LDPE/Предварительная стерилизация с помощью этиленоксида
Конфигурация первичного контейнера: 2,5 мл помещают в 7,5 мл бутыль
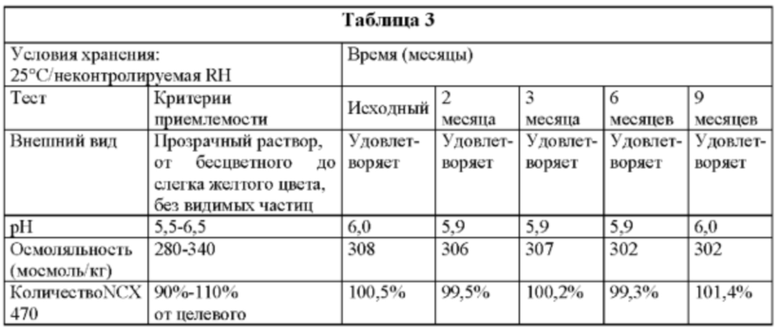

В заключение следует отметить, что офтальмологический раствор по настоящему изобретению можно упаковать в первичные LDPE контейнеры, независимо от характера предварительной стерилизации таких контейнеров. Многодозовые первичные контейнеры могут быть стерилизованы при помощи либо гамма-излучения, либо газообразного этиленоксида. Одноразовые или однодозовые контейнеры, производимые посредством BFS® (выдувание-заполнение-запаивание) технологии, обеспечивают получение нативных LDPE контейнеров, естественным образом стерильных, и такое получение LDPE материала также подходит для упаковки офтальмологического раствора по настоящему изобретению, не содержащего консерванта.
Пример 3
Тесты антимикробной эффективности Пример 3А
Тесты антимикробной эффективности выполняли для оценки способности офтальмологических растворов по настоящему изобретению удовлетворять критериям эффективности антимикробных консервантов.
Тестировали офтальмологические растворы, содержащие 0,05% (масс./масс.) динатрия эдетата (см. Таблица 5) и разные концентрации бензалкония хлорида (см. Таблицу 6). Офтальмологические композиции получали, применяя способ, раскрытый в Примере 1. Тесты выполняли в соответствии с процедурой проведения теста, описанной в Фармакопее США, монография <51>, "Тестирование антимикробной эффективности" (АЕТ). Успех этого USP теста эквивалентен соответствию критериям В Европейской фармакопеи.
Результаты, представленные в Таблице 6, показали, что офтальмологические композиции, содержащие бензалкония хлорид в диапазоне от 0,012% до 0,02% (масс./масс.), соответствовали критериям микробиологической эффективности и проходили Тестирование антимикробной эффективности (АЕТ).
NCX 470 = 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-иловый эфир


Пример 3В
Для оценки эффекта EDTA как вспомогательного антимикробного консерванта, оценивали соответствие критериям консервации для офтальмологической композиции, содержащей бензалкония хлорид (0,016% масс./масс.) и динатрия эдетат (0,05% масс./масс.) (Композиция А - Таблица 7), и офтальмологической композиции, содержащей бензалкония хлорид (0,016% масс./масс.), но не динатрия эдетат (Композиция В - Таблица 7).
Результаты показали, что присутствие динатрия эдетата требуется для соответствия критериям консервации, определенным в монографии <51> US Фармакопеи или критериям В Европейской Фармакопеи.

В WO 2013/003827 (Allergan) раскрыто, что полиоксил 15 гидроксистеарат повышает антимикробную эффективность консерванта, позволяя снизить дозу антимикробного консерванта бензалкония хлорида для соответствия USP <51> или критериям В ЕР. Исследования консерванта, проведенные с офтальмологическими растворами по изобретению, показали, что полиоксил 15 гидроксистеарат не улучшает антимикробную эффективность консерванта бензалкония хлорида и что, для обеспечения антимикробной эффективности консерванта, офтальмологические растворы должны содержать количество бензалкония хлорида, которое должно быть выше 0,12% масс./масс. в присутствии 0,5% масс./масс. EDTA. Наиболее подходящая целевая доза антимикробного консерванта была достигнута при использовании смеси 0,16% масс./масс. бензалкония хлорида и 0,05% масс./масс. EDTA.
Пример 4
Фармакокинетическая оценка однократной глазной инстилляции у голландских кроликов
Исследование 1
6-(Нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-иловый эфир является производным аналога простагландина двойного действия, которое сочетает в себе фармакологическую активность биматопроста с оксидом азота. Биматопрост в форме свободной кислоты, представляет собой один из активных метаболитов 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира; в данном исследовании уровень биматопроста в форме свободной кислоты использовали в качестве маркера для сравнения проникновения в глаз 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира после местной инсталляции водного офтальмологического раствора по изобретению по сравнению с имеющимися в продаже глазными каплями, содержащими биматопрост, и эталонной композицией, содержащей 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-иловый эфир.
Целью данного исследования была сравнительная оценка количеств биматопроста в форме свободной кислоты в образцах внутриглазной жидкости человека, взятых после инсталляции тестируемых водных офтальмологических растворов.
Два разных водных офтальмологических раствора, содержащие 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-l-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-иловый эфир (Композиции 1 и 2) и имеющиеся в продаже глазные капли, содержащие биматопрост, (Композиция 3) оценивали в глазном фармакокинетическом исследовании на кролике.
Два разных водных раствора, содержащие 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-иловый эфир, представляют собой офтальмологический раствор по изобретению (Композиция 1) и композицию, раскрытую в WO 2009/136281 (Композиция 2).
Тестируемые растворы
В таблице 8 представлены носители двух водных офтальмологических растворов, содержащих 0,042% масс./масс. 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира.
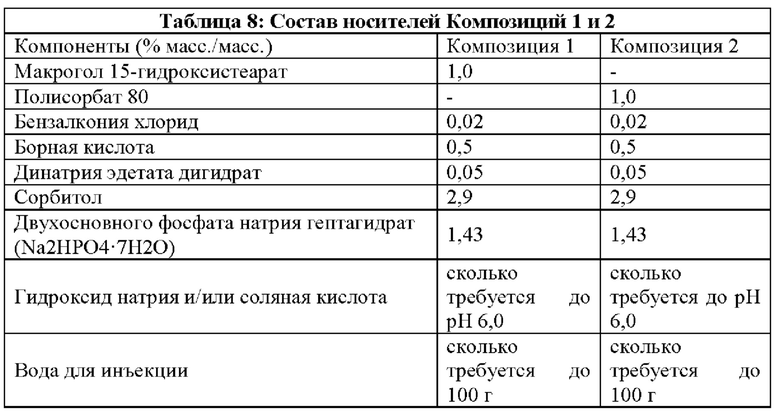
Композиция 3 (Имеющиеся в продаже глазные капли/Lumigan®. Allergan)
Активное начало: Биматопрост 0,03%;
Концентрация 0,042% масс./масс. 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира является эквимолярной по отношению к молям биматопроста имеющихся в продаже глазных капель (Композиция 3).
Вещество
Макрогол 15-гидроксистеарат представляет собой имеющийся в продаже Kolliphor® HS15 (BASF). Полисорбат 80 представляет собой имеющийся в продаже Polysorbate 80 Super Refined® (Croda).
Методика эксперимента
В исследование были включены группы из 10, ранее не подвергавшихся воздействию, самцов голландских кроликов, которым вводили либо композиции 1 и 2, либо композицию 3 посредством инсталляции в каждый глаз установленных целевых доз 12,6 мкг/глаз для композиций 1 и 2 и 9 мкг/глаз для раствора биматопроста. Дополнительную группу из 5 самцов использовали, чтобы обеспечить матрицу пустой пробы (внутриглазная жидкость) для биоаналитических целей.
В ходе исследования проводили измерения массы тела и клинические наблюдения, а в заранее определенные моменты времени животных умерщвляли для сбора внутриглазной жидкости в 1 ч, 2 ч, 4 ч и 8 ч.
Во время исследования не наблюдалось никаких клинических признаков, связанных с введением доз.
Результаты
Результаты, представленные в Таблице 9, показали, что водный офтальмологический раствор по изобретению (Композиция 1) демонстрирует более высокую концентрацию кислоты биматопроста (согласно значениям Cmax и AUC (площадь под кривой) по сравнению с той, которая достигается после введения эталонного препарата (Композиция 2) и имеющихся в продаже глазных капель (Композиция 3).
Cmax представляет собой максимальную концентрацию, которую свободная кислота биматопрост достигает во внутриглазной жидкости.
AUC (площадь под кривой) представляет общее количество свободной кислоты биматопроста во внутриглазной жидкости в течение времени, имеющегося для осуществления биологического эффекта.

Исследование 2
Целью данного исследования была оценка содержания свободной кислоты биматопроста во внутриглазной жидкости после местного дозирования в глаз трех разных водных офтальмологических растворов, содержащих 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-иловый эфир (0,042% масс./масс.) в трех разных носителях, представленных в Таблице 10.
Носитель 1 и 2 содержат полисорбат 80, который представляет собой солюбилизирующий агент композиции, раскрытой в документе предшествующего уровня техники WO 2009/136281; носитель 1 отличается от носителя 2 тем, что он содержит бензалкония хлорид, в то время как носитель 2 не содержит бензалкония хлорид.
Носитель 3 содержит смесь полисорбата 80 и макрогол 15-гидроксистеарата.
Протестированные растворы
В таблице 10 представлены данные о носителях водных офтальмологических растворов, содержащих 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-иловый эфир в количестве 0,042% масс./масс.
Была протестирована дополнительная эталонная композиция; эта композиция представляет собой имеющиеся в продаже глазные капли, содержащие 0,03% активного биматопроста.

Вещество
Макрогол 15-гидроксистеарат представляет собой имеющийся в продаже Kolliphor® HS15 (BASF). Полисорбат 80 представляет собой имеющийся в продаже Polysorbate 80 Super Refined® (Croda).
Методика эксперимента
В исследование были включены сорок животных. Они были разделены на четыре группы по 10 животных/группа и им были введены вышеописанные, протестированные водные офтальмологические растворы.
Всем животным, включенным в исследование, проводили глазную инсталляцию в оба глаза с помощью градуированной пипетки в объеме 30 мкл/глаз. Двух животных на композицию умерщвляли в 0 ч (перед дозированием), через 1 ч, 2 ч, 4 ч и 8 ч, и немедленно получали образцы внутриглазной жидкости из обоих глаз.
Результаты
Фармакокинетические данные, представленные в Таблице 11, показали, что концентрация кислоты биматопроста (согласно значениям Cmax и AUC) водных офтальмологических растворов, содержащих Носитель 1 или Носитель 2, является эквивалентной, в то время как водный офтальмологический раствор, содержащий Носитель 3, показал более высокую концентрацию (более высокую концентрацию свободной кислоты биматопроста во внутриглазной жидкости) биматопроста в форме свободной кислоты.
Самые низкие показатели концентрации для кислоты биматопроста были получены в группе эталонной композиции.
Кроме того, результаты показали, что бензалкония хлорид не оказывал никакого влияния на проникновение в глаз 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира гексаноата вплоть до концентрации 0,02% масс./масс.; действительно, фармакокинетические данные являются эквивалентными для двух водных офтальмологических растворов, содержащих носители 1 или 2.

В заключение, результаты вышеуказанных исследований показали, что макрогол 15-гидроксистеарат способен усиливать проникновение в глаз 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира. Усиленная абсорбция является неожиданным эффектом, поскольку она не зависит от известной солюбилизирующей активности макрогол 15-гидроксистеарата, так как во всех исследованных водных офтальмологических растворах терапевтическое активное соединение было солюбилизировано.
Действительно, растворимость 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира в водных растворах при рН 6,0, содержащих 0,5% (масс./масс.) макрогол 15-гидроксистеарата (Kolliphor® HS15) или 0,5% (масс./масс.) полисорбата 80 (Tween® 80), составляет 0,070% (масс./масс.) и 0,074% (масс./масс.) соответственно, и, таким образом, является по существу эквивалентной, следовательно, во всех исследованных носителях 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-иловый эфир был солюбилизирован.
Кроме того, результаты исследования 2 показали, что бензалкония хлорид не оказывал влияния на глазную биодоступность активного соединения; действительно, носитель 1, который содержит полисорбат 80 и бензалкония хлорид, и носитель 2, который содержит полисорбат 80, но не содержит бензалкония хлорид, показали эквивалентную концентрацию свободной кислоты биматопроста во внутриглазной жидкости.
Пример 5
Внутриглазное давление у собак породы бит ль с нормальным глазным давлением
В данном исследовании определяли эффективности снижения внутриглазного давления (ЮР) у собак породы бигль с нормальным глазным давлением с помощью офтальмологической водной композиции по настоящему изобретению.
Исследованные композиции
Композиция 1
Композиция 1 содержит:
0,042% масс./масс. 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира;
Макрогол 15-гидроксистеарат: 1,0% масс./масс.
Бензалкония хлорид: 0,016% масс./масс.
Борная кислота: 0,5% масс./масс.
Динатрия эдетат: 0,05% масс./масс.
Сорбитол: 2,76% масс./масс.
Двухосновного фосфата натрия гептагидрат (Na2HPO4⋅7H2O): 1,326% масс./масс.
Вода для инъекции сколько требуется до 100 г
Композиции имеют конечное значение рН 6,0 и осмоляльность примерно 300 мосмоль/кг
Методика эксперимента
Исследуемые водные композиции вводили посредством местного введения в конъюнктивальный мешок обоих глаз собак породы бигль два раза в сутки, примерно с 4-часовыми интервалами в течение 28 суток. Были включены две группы, каждая из которых содержала трех самцов и трех самок собак породы бигль:
Группа 1 (контрольные животные): носитель
Группа 2: Композиция 1
Каждое животное получало по 30 мкл/глаз указанных веществ на каждую обработку.
Первую дозу в день вводили между 7 и 9 часами утра, каждый день примерно в одно и то же время.
Объект тестирования вводили с помощью автоматической пипетки в конъюнктиву обоих глаз каждого животного после мягкого оттягивания нижнего века от глазного яблока. Затем веки осторожно удерживали вместе в течение примерно одной секунды для предотвращения потери объекта тестирования.
Внутриглазное давление измеряли при помощи электронного тонометра до введения и через 1-1,5 часа после суточной дозы во 2, 4, 8, 20 и 27-е сутки лечения.
В зрачки закапывали глазные капли оксибупрокаина гидрохлорида (Prescaina® 0,4%) или оксибупрокаина гидрохлорида, тетракаина гидрохлорида (Colircusi Doble® Anestesico) перед измерением внутриглазного давления.
Результаты
Результаты представлены в таблице 12 в виде изменения IOP по сравнению с исходным уровнем.
Водные композиции по изобретению были эффективными в снижении IOP у собак с нормальным глазным давлением. Кроме того, повторяющееся ежесуточное введение водных композиций по изобретению приводило к устойчивой активности IOP-снижающей активности в течение продолжительного периода.

Пример 6
Исследование стабильности
Стабильность офтальмологической композиции по изобретению, содержащей 0,065% масс./масс. NCX 470, хранящейся в 7,5 мл LDPE емкостях, стерилизованных с помощью гамма-лучей, оценивали при температуре 25°С, в исходном состоянии, через 3 месяца и через 6 месяцев и ускоренную стабильность оценивали при 40°С, при относительной влажности воздуха (RH) не более 25%, в исходном состоянии, через 3 месяца и через 6 месяцев.
Офтальмологическую композицию готовили способом, описанным в Примере 1.
Состав офтальмологической композиции:
- 0,065% масс./масс.6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира (NCX470);
- 1,0% масс./масс. макрогол 15 гидроксистеарата;
- 0,016% масс./масс. бензалкония хлорида;
- 0,05% масс./масс. динатриевой соли этилендиаминтетрауксусной кислоты дегидратированной;
- 2,76% масс./масс. сорбитола;
- 1,326% масс./масс. двухосновного фосфата натрия гептагидрата;
- 0,5% масс./масс. борной кислоты; и
- Вода для инъекции - сколько требуется до 100% масс./масс.;
Конфигурация первичного контейнера: 2,5 мл, помещенные в 7,5 мл бутыль.


Результаты исследования стабильности при 25°С (Таблица 13) и при 40°С (Таблица 14) показывают, что офтальмологические композиции по изобретению были стабильными, таким образом, ожидается, что офтальмологические растворы будут иметь срок годности по меньшей мере 24 месяца в условиях хранения при температуре окружающей среды, при хранении в LDPE контейнерах.
Пример 7
Получение офтальмологической композиции, не содержащая консервантов, содержащей 0,065% масс./масс. 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира (NCX470).
Ингредиенты офтальмологической композиции указаны ниже:
Стадия 1) Приготовление концентрированного раствора API
1,5 л воды для инъекции при примерно 32°С добавляли к 1000 г полиоксил 15 гидроксистеарата, предварительно взвешенного в контейнере, который помещали на горячую водяную баню до полного расплавления полиоксил 15 гидроксистеарата. Расплавленную смесь полиоксил 15-гидроксистеарат/вода добавляли в 4-хлитровую порционную емкость, содержащую 65 г NCX-470.
4-хлитровую порционную емкость термостатировали при температуре 32°С на водяной бане, и раствор API перемешивали до полного растворения всех ингредиентов и поддерживали при непрерывном перемешивании вплоть до его добавления к раствору остальных эксципиентов.
Стадия 2) Приготовление раствора остальных эксципиентов
100 л воды для инъекции заливали в производственный бак, изготовленный из нержавеющей стали (марки 316L) и охлаждали до 25°С-30°С. Примерно 12 литров этой воды для инъекции отбирали из бака и хранили в другом контейнере для использования во время приготовления.
Следующие соединения добавляли в соответствии со следующим порядком в производственный бак, содержащий воду, при непрерывном перемешивании; каждое соединение полностью растворяли перед добавлением следующего соединения:
500 г борной кислоты;
1300 г двухосновного фосфата натрия гептагидрата (Na2HPO4⋅7H2O);
2760 г сорбитола;
Сосуд, содержащий раствор, несколько раз промывали достаточным количеством воды для инъекции, и промывки добавляли в производственный бак для завершения переноса.
Стадия 3) Приготовление нерасфасованного офтальмологического раствора
Концентрированный раствор API переносили в производственный бак; 4-хлитровую порционную емкость промывали несколько раз водой для инъекции, и промывки добавляли к основной массе для завершения переноса.
Воду для инъекции добавляли в производственный бак для доведения конечной целевой массы до 100 кг.
рН можно более точно скорректировать путем использования гидроксида натрия и/или соляной кислоты.
Стадия 4) Стерилизация нерасфасованного офтальмологического раствора
Офтальмологический раствор стерилизовали посредством дополнительного фильтрования через полиэфирсульфоновые (PES) фильтры (Supor® от Pall) 0,2 мкм.
Стадия 5) Помещение нерасфасованного офтальмологического раствора в офтальмологические первичные LDPE контейнеры.
После стадии фильтрования офтальмологический раствор помещали в систему многодозовых первичных LDPE контейнеров, не содержащих консерванта (например в систему Aptar OSD®) подходящего объема в условиях зоны стерильности класса А в соответствии с обычной практикой асептического процесса. В качестве еще одного варианта системы первичных контейнеров, не содержащей консервантов, нерасфасованный стерильный раствор может быть заполнен в однодозовые первичные контейнеры, например однодозовые первичные контейнеры, изготовленные по технологии BFS (Blow-Fill-Seal®/Rommelag).
Пример 8
Исследование стабильности
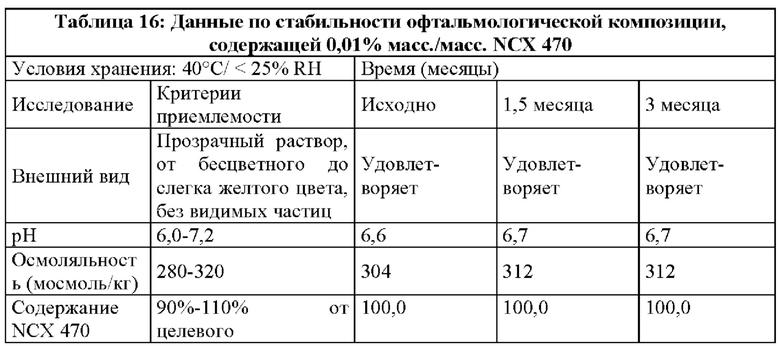
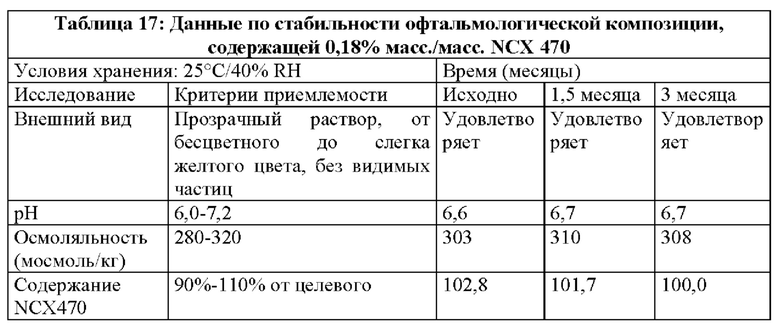
Стабильность не содержащая консерваторов офтальмологических композиций по изобретению, содержащих 0,01% масс./масс. NCX 470 и 0,18% NCX 470 и хранящихся в 5 мл стеклянных емкостях, оценивали при 25°С и при 40°С, в разные моменты времени.
Офтальмологические композиции получали способом, описанным в Примере 7. В этих композициях буферная система представляет собой смесь гептагидрата двухосновного фосфата натрия и моногидрата лимонной кислоты, и регулятор тоничности представляет собой глицерин.
Состав офтальмологической композиции, содержащей 0,01% масс./масс. NCX 470:
- 0,01% масс./масс. 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира (NCX470);
- 1,5% масс./масс. макрогол 15 гидроксистеарат (Kolliphor® HS15);
- 0,52% масс./масс. глицерина;
- 2,33% масс./масс. гептагидрата двухосновного фосфата натрия;
- 0,36% масс./масс. моногидрат лимонной кислоты; и
- вода для инъекции сколько требуется до 100% масс./масс.
Конфигурация первичного контейнера: 3 мл помещали в 5 мл стеклянную емкость.
Состав офтальмологический композиции, содержащей 0,18% масс./масс. NCX 470:
- 0,18% масс./масс. 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира (NCX470);
- 1,5% масс./масс. макрогол 15 гидроксистеарата (Kolliphor® HS15);
- 0,52% масс./масс. глицерина;
- 2,33% масс./масс. гептагидрата двухосновного фосфата натрия;
- 0,36% масс./масс. моногидрата лимонной кислоты; и
- вода для инъекции, сколько требуется до 100% масс./масс.
Конфигурация первичного контейнера: 3 мл помещали в 5 мл емкость.
Результаты стабильности двух офтальмологических композиций представлены в нижеприведенных таблицах 15-18; результаты показали, что офтальмологические композиции, не содержащие консерванта, были стабильными.


Пример 9 (вязкий раствор)
Приготовление офтальмологической композиции, содержащей 6-(нитроокси)-гексановой кислоты (1S,2Е)-3-[(1R,2R,3S,5R)-2-[(27)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-иловый эфир (NCX 470) 0,065% масс./масс., и агент, регулирующий вязкость.
Ингредиенты офтальмологической композиции представлены ниже:
Стадия 1) Приготовление концентрированного раствора API
1,5 л воды для инъекции при примерно 32°С добавляли к 1000 г полиоксил 15 гидроксистеарата, предварительно взвешенного в контейнере, который помещали в горячую водяную баню до полного расплавления полиоксил 15 гидроксистеарата. Расплавленную смесь полиоксил 15-гидроксистеарат/вода добавляли в 4-литровую порционную емкость, содержащую 65 г NCX-470. 4-литровую порционную емкость термостатировали при температуре 32°С на водяной бане и раствор API перемешивали до полного растворения всех ингредиентов и поддерживали при непрерывном перемешивании вплоть до его добавления к раствору носителя остальных эксципиентов.
Стадия 2) Приготовление раствора носителя остальных эксципиентов (пример вязких растворов)
100 л воды для инъекции помещали в производственный бак, изготовленный из нержавеющей стали (марка 316L) при температуре выше 85°С. Примерно 12 литров этой воды для инъекции извлекали из резервуара и помещали в другой контейнер для использования во время приготовления.
200 г НРМС (гидроксипропилметилцеллюлоза) (Metolose®/Shin-Etsu) медленно вводят в бак при перемешивании. Целлюлозу вводят медленно в течение 15 минут. После того как полимер будет полностью диспергирован в баке, продолжают перемешивание в течение еще 15 мин при температуре по меньшей мере 85°С. После этого периода выдержки охлаждают нерасфасованный раствор до температуры 25°С-30°С.
Затем при непрерывном перемешивании следующие соединения точно в следующем порядке добавляли в производственный бак, содержащий воду; при этом каждое соединение полностью растворялось перед добавлением следующего соединения:
50 г динатрия эдетат дигидрата;
500 г борной кислоты;
1326 г гептагидрата двухосновного фосфата натрия (Na2HPO4⋅7H2O);
2760 г сорбитола;
32 г раствора 50% бензалкония хлорида;
сосуд, содержащий раствор бензалкония хлорид, промывали несколько раз достаточным количеством воды для инъекции, и промывки добавляли в производственный бак для завершения переноса.
Стадия 3) Приготовление нерасфасованного офтальмологического раствора
Концентрированный раствор API переносили в производственный бак; 4-литровую порционную емкость промывали водой для инъекции, и промывки добавляли к основной массе для завершения переноса.
Воду для инъекции добавляли в производственный бак для получения конечной целевой массы 100 кг.
Стадия 4) Стерилизация нерасфасованного офтальмологического раствора
Офтальмологический раствор стерилизовали посредством дополнительного фильтрования через 0,2 мкм полиэфирсульфоновые (PES) фильтры (Supor® Pall);
Стадия 5) В некоторых случаях нерасфасованный офтальмологический раствор помещают в офтальмологические первичные контейнеры из полиэтилена низкой плотности (LDPE). Как правило, композицию можно упаковывать в многодозовую офтальмологическую бутыль с колпачком и насадкой-капельницей, позволяющей получать калиброванные капли с контролируемым размером капель. Примерами таких первичных контейнеров могут быть бутыли Rispharm® от Berry-Plastics, бутыли Boston Round® от Amcor, трехэлементные бутылки от Philips-Medisize, Bormioli или их эквиваленты.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМБИНАЦИИ АЛЬФА-2-ДЕЛЬТА-ЛИГАНДА С СЕЛЕКТИВНЫМ ИНГИБИТОРОМ ЦИКЛООКСИГЕНАЗЫ-2 | 2003 |
|
RU2286151C2 |
| ПРОИЗВОДНЫЕ ДИКЕТОГИДРАЗИНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ТАКИЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ АКТИВНОГО ИНГРЕДИЕНТА, И ИХ ПРИМЕНЕНИЕ | 2003 |
|
RU2368600C2 |
| ТЕРАПЕВТИЧЕСКИЕ ЗАМЕЩЕННЫЕ ЦИКЛОПЕНТАНЫ | 2009 |
|
RU2501789C2 |
| СОЕДИНЕНИЯ И КОМПОЗИЦИИ, ПРИМЕНЯЕМЫЕ ДЛЯ ЛЕЧЕНИЯ РАССТРОЙСТВ, СВЯЗАННЫХ С NTRK | 2016 |
|
RU2744974C2 |
| ГИПОГЛИКЕМИЧЕСКОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО, СОДЕРЖАЩЕЕ ПОЛИГИДРОКСИБУТИЛПИРАЗИНЫ, НОВЫЕ ПОЛИГИДРОКСИБУТИЛПИРАЗИНЫ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 1998 |
|
RU2186773C2 |
| СРЕДСТВА, ИНДУЦИРУЮЩИЕ АПОПТОЗ, ДЛЯ ЛЕЧЕНИЯ РАКА, ИММУННЫХ И АУТОИММУННЫХ ЗАБОЛЕВАНИЙ | 2011 |
|
RU2568611C2 |
| ИНДАНИЛЬНЫЕ СОЕДИНЕНИЯ | 2009 |
|
RU2474572C1 |
| КОМБИНИРОВАННОЕ ЛЕЧЕНИЕ АГОНИСТОМ ТОЛЛ-ПОДОБНОГО РЕЦЕПТОРА (TLR7) И ИНГИБИТОРОМ СБОРКИ КАПСИДА ВИРУСА ГЕПАТИТА В | 2016 |
|
RU2718917C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМБИНАЦИЯ НА ОСНОВЕ ИНГИБИТОРОВ PRMT5 | 2020 |
|
RU2830439C1 |
| Аналоги сплицеостатина | 2013 |
|
RU2618523C2 |
Группа изобретений относится к области медицины, а именно к офтальмологии и фармакологии, и предназначена для получения композиции в виде раствора для местного введения в глаз. Офтальмологическая водная композиция в виде раствора для местного введения в глаз содержит 6-(нитроокси)-гексановую кислоту (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира, макрогол 15 гидроксистеарата, по меньшей мере буфер, регулятор тоничности. Компоненты используются в заявленных количествах. При этом pH раствора находится в диапазоне от 5,5 до 6,5, осмоляльность находится в диапазоне от 280 до 320 мосмоль/кг. Макрогол 15 гидроксистеарат является единственным солюбилизирующим агентом. Также представлен способ изготовления указанной композиции. Использование группы изобретений обеспечивает повышенную глазную абсорбцию терапевтически активного вещества. 2 н. и 22 з.п. ф-лы, 18 табл., 9 пр.
1. Офтальмологическая водная композиция в виде раствора для местного введения в глаз, содержащая от 0,005% масс./масс. до 0,18% масс./масс. 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира, от 0,5% масс./масс. до 1,5% масс./масс. макрогол 15 гидроксистеарата, по меньшей мере буфер, регулятор тоничности, где pH находится в диапазоне от 5,5 до 6,5, осмоляльность находится в диапазоне от 280 до 320 мосмоль/кг, и где макрогол 15 гидроксистеарат является единственным солюбилизирующим агентом.
2. Офтальмологическая водная композиция по п. 1, содержащая от 0,005% масс./масс. до 0,10% масс./масс. 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира.
3. Офтальмологическая водная композиция по п. 2, содержащая от 0,005% масс./масс. до 0,065% масс./масс. 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира.
4. Офтальмологическая водная композиция по п. 1, где количество 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира составляет 0,021% масс./масс., 0,042% масс./масс., 0,065% масс./масс. или 0,10% масс./масс.
5. Офтальмологическая водная композиция по любому из пп. 1-4, которая дополнительно содержит от 0,013% масс./масс. до 0,02% масс./масс. бензалкония хлорида, от 0,03% масс./масс. до 0,07% масс./масс. эдетатной соли.
6. Офтальмологическая водная композиция по п. 5, где количество бензалкония хлорида составляет от 0,013% масс./масс. до 0,02% масс./масс. и количество эдетатной соли составляет 0,05% масс./масс.
7. Офтальмологическая водная композиция по п. 6, где количество бензалкония хлорида составляет 0,016% масс./масс. и количество эдетатной соли составляет 0,05% масс./масс.
8. Офтальмологическая водная композиция по любому из пп. 1-7, имеющая pH 6.
9. Офтальмологическая водная композиция по любому из пп. 1-8, где буфер представляет собой смесь гептагидрата двухосновного фосфата натрия и борной кислоты.
10. Офтальмологическая водная композиция по любому из пп. 1-9, дополнительно содержащая pH-регулирующий агент.
11. Офтальмологическая водная композиция по любому из пп. 1-10, где регулятор тоничности представляет собой сорбитол или глицерин.
12. Офтальмологическая водная композиция по п. 1 или 2, где количество макрогол 15 гидроксистеарата составляет 1,0% масс./масс., и она дополнительно содержит 0,016% масс./масс. бензалкония хлорида, 0,05% масс./масс. дигидрата динатриевой соли этилендиаминтетрауксусной кислоты, 2,76% масс./масс. сорбитола, 1,33% масс./масс. гептагидрата двухосновного фосфата натрия, 0,5% масс./масс. борной кислоты и воду, и где pH равен 6.
13. Офтальмологическая водная композиция по п. 12, где количество 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира составляет 0,021% масс./масс., 0,042% масс./масс., 0,065% масс./масс или 0,10% масс./масс.
14. Офтальмологическая водная композиция по любому из пп. 1, 2, где количество 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира составляет 0,1% и количество макрогол 15 гидроксистеарата составляет 1,5% масс./масс., и она дополнительно содержит 0,016% масс./масс. бензалкония хлорида, 0,05% масс./масс. дигидрата динатриевой соли этилендиаминтетрауксусной кислоты, 0,52% масс./масс. глицерина, 2,33% масс./масс. гептагидрата двухосновного фосфата натрия, 0,36% масс./масс. моногидрата лимонной кислоты и воду, и где pH равен 6.
15. Офтальмологическая водная композиция по любому из пп. 12-14, дополнительно содержащая pH-регулирующий агент, выбранный из соляной кислоты или гидроксида натрия.
16. Офтальмологическая водная композиция по любому из пп. 1-15, дополнительно содержащая агент, регулирующий вязкость.
17. Офтальмологическая водная композиция по п. 16, где агент, регулирующий вязкость, представляет собой гидроксипропилметилцеллюлозу в концентрации менее 0,5% масс./масс.
18. Офтальмологическая водная композиция по любому из пп. 1-4, представляющая собой офтальмологическую водную композицию, не содержащую антимикробный консервант.
19. Офтальмологическая водная композиция по любому из пп. 1-18 для применения в качестве лекарственного средства.
20. Офтальмологическая водная композиция по любому из пп. 1-18 для применения в лечении глазной гипертензии, глаукомы или для снижения внутриглазного давления.
21. Способ изготовления офтальмологической водной композиции по любому из пп. 1-18, включающий следующие стадии:
Стадия 1) приготовление концентрированного раствора 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира, включающее:
1а) нагревание смеси воды для инъекции и полиоксил 15 гидроксистеарата при 32°C, пока не расплавится полиоксил 15 гидроксистеарат;
1б) добавление расплавленной смеси полиоксил 15 гидроксистеарат/вода к предварительно взвешенному 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-иловому эфиру;
1в) перемешивание полученной смеси до полного растворения 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира при поддержании смеси при температуре 32°C; где количества полиоксил 15 гидроксистеарата и 6-(нитроокси)-гексановой кислоты (1S,2E)-3-[(1R,2R,3S,5R)-2-[(2Z)-7-(этиламино)-7-оксо-2-гептен-1-ил]-3,5-дигидроксициклопентил]-1-(2-фенилэтил)-2-пропен-1-илового эфира соответствует их количествам в конечной композиции, и количество воды для инъекции, используемое на Стадии (1а), составляет примерно 1,5% от общей массы воды, используемой в приготовлении;
Стадия 2) приготовление водного раствора остальных ингредиентов носителя продукта путем добавления в производственный бак, содержащий воду для инъекции, эксципиентов в следующем определенном порядке: дигидрат динатрия эдетат, буфер, выбранный из борной кислоты и гептагидрата двухосновного фосфата натрия или лимонной кислоты и гептагидрата двухосновного фосфата натрия, сорбитол или глицерин, и бензалкония хлорид, где каждый эксципиент полностью растворяют перед добавлением следующего эксципиента и приготовление раствора выполняют при температуре от 25°C до 30°C;
Стадия 3) приготовление нерасфасованного офтальмологического раствора путем добавления раствора со Стадии 1 в производственный бак, содержащий водный раствор со Стадии 2 и воду для инъекции вплоть до получения целевой конечной массы;
Стадия 4) стерилизация нерасфасованного офтальмологического раствора посредством фильтрования нерасфасованного офтальмологического раствора со Стадии 3 через полиэфирсульфоновые (PES) фильтры, имеющие размер пор примерно 0,2 мкм.
22. Способ по п. 21, где на стадии (3) pH нерасфасованного офтальмологического раствора доводят до pH 6,0 с помощью гидроксида натрия или соляной кислоты.
23. Способ по п. 21 или 22, где на стадии (2) регулирующий вязкость агент добавляют в производственный бак, содержащий воду для инъекции, в качестве первого компонента и, как только он полностью растворится, добавляют другие эксципиенты.
24. Способ по пп. 21-23, где стерилизованный нерасфасованный офтальмологический раствор со стадии (4) помещают в офтальмологические первичные контейнеры из полиэтилена низкой плотности (LDPE).
| US 8772337 B2, 08.07.2014 | |||
| WO 2009136281 A1, 12.11.2009 | |||
| WO 2013003827 A2, 03.01.2013 | |||
| US 8637054 B2, 28.01.2014 | |||
| KRAUSS AHP et al | |||
| УСТРОЙСТВО для БАЗИРОВАНИЯ КАРТЕРОВ ВЕДУЩИХ МОСТОВ АВТОМОБИЛЕЙ НА АВТОМАТИЧЕСКИХ ЛИНИЯХ | 0 |
|
SU303259A1 |
| Exp Eye Res., 2011, 93(3):250-5. | |||
Авторы
Даты
2022-10-04—Публикация
2019-07-10—Подача