Изобретение относится к производству керамических материалов медицинского назначения, а именно к способу получения порошка кристаллического гидроксиапатита кальция (ГАП) стехиометрического состава высокой текучести, пригодного для плазменного напыления на керамические и металлические имплантаты, применяемые в стоматологии, челюстно-лицевой хирургии и ортопедии, а также для 3d-печати керамических биорезорбируемых имплантатов.
Изобретение позволяет получить порошок гидроксиапатита с преимущественным размером частиц 90-40 мкм высокой текучести, который можно использовать при изготовлении медицинских имплантатов путем плазменного напыления [1.Патент РФ 24443 434 С1 опубл.27.02.2012; 2. Патент РФ 21146535 С1, опубл. 20.03.2000], а также 3d-печати керамических биорезорбируемых имплантатов [3.Ferrage L., Bertrand G., Lenormand P., D. Grossin, Ben-Nissan B. A review of the additive manu-facturing (3DP) of bioceramics: alumina, zirconia (PSZ) and hydroxyapatite. Aust Ceram Soc. 2017. vol. 53. P.11-20].
Гидроксиапатит кальция - Ca10(PO4)6(OH)2 является структурным аналогом минеральной составляющей костного вещества, имеет сходные физические и механические свойства, обладает уникальной биологической совместимостью и способностью активно стимулировать размножение клеток соединительной ткани и новообразование костной ткани, что определяет использование ГАП в качестве материала для медицинских целей: покрытий имплантатов, изготовления биосовместимой керамики, лекарственных, косметических и стоматологических средств.
Химический и фазовый состав покрытия, получаемого при плазменном напылении порошка ГАП, зависит не только от параметров напыления, но и от фракционного состава напыляемого материала. Авторы работы [4.Cheang P., Khor K.A. Thermal spraying of hydroxyapatite (HA) coatings: Effects of powder feedstock // J Mater Process Technol.1995.vol. 48, iss. 1-4. p. 429-436], путем проведения анализа структуры порошков ГАП различного фракционного состава после нахождения в плазменной струе установили, что частицы диаметром менее 30 мкм расплавлены полностью и имеют аморфную структуру, а частицы диаметром 55 мкм и более имеют наряду с расплавом кристаллическое ядро, соответствующее структуре ГАП. Известно, что аморфные фосфаты кальция имеют более высокую скорость растворения [Dorozhkin S.V. Bioceramics of calcium prthophosphates // Biomaterials. 2010. Vol. 31. P.1465-1485], что приведет быстрой деградации полученного биопокрытия. Следовательно, при получении биопокрытий на основе ГАП методом плазменного напыления необходимо использовать частицы размером более 50 мкм. Авторы работы [6.Tong W., Chen J. Effect of particle size on molten states of starting powder and degradation of the relevant plasma-sprayed hydroxyapatite coatings// Biomaterials.1996.vol. 17. iss. 15. P. 1507-1513] исследовали микроструктуру покрытий, полученных плазменным напылением порошков ГАП с различным распределением частиц по размерам (от 1 до 180 мкм) на титановые подложки и установили, что, не смотря на высокую кристалличность покрытий, образованных из крупных частиц гидроксиапатита размером более 125 мкм, замечена их быстрая деградация при погружении в деионизированную воду и, как результат, высокая пористость покрытий.
В работе [7. P. Navarrete-Segado, C. Frances, D. Grossin, M. Tourbin. Tailoring hydroxyapatite microspheres by spray drying for powder bed fusion feedstock. Preprint. engrXiv, 11 Oct. 2021. Web. DOI: 10.31224/osf.io/jctr2] сообщается, что для 3d-печати путем лазерной обработки порошкового слоя рекомендуется использовать частицы размером более 20 мкм. Верхняя граница размера определяется толщиной создаваемого при печати слоя. Кроме того, для данного способа печати важным параметром является текучесть порошка [8. D. Grossin, A. Montуn, P. Navarrete-Segado, E. Цzmen, G. Urruth, F. Maury, D. Maury, C. Frances, M. Tourbin, P. Lenormand, G. Bertrand. A review of additive manufacturing of ceramics by powder bed selective laser processing (sintering/melting): Calcium phosphate, silicon carbide, zirconia, alumina, and their composites // Open Ceramics. 2021. Vol.5. P. 100073]. Чем выше текучесть, тем ровнее насыпной слой, подготавливаемый для лазерной обработки.
Известен способ гидротермального получения порошка гидроксиапатита с регулируемым гранулометрическим составом [9. Патент РФ 2717064 C1, «Способ получения гидроксиапатита с регулируемым гранулометрическим составом», опубл. 17.03.2020]. Данный способ включает в себя приготовление смеси, содержащей нитрат кальция, гидрофосфат аммония и воду, выдерживание смеси в автоклаве при давлении 150-200 атм. и температуре 200-250°С в течение 1-1,5 ч и рН смеси 10-12. Промытый осадок сушат в разреженной атмосфере при давлении 10-5 мм рт.ст. и температуре не более -55°С. Затем суспензию из этилового спирта, воды и сухого осадка обрабатывают ультразвуком и проводят грануляцию с использованием распылительной сушки при температуре в рабочей камере 200-220°С и скорости подачи суспензии 13-15 мл/мин с последующим сбором сферических гранул с комплекса циклонных фильтров. Изобретение позволяет получить гранулы гидроксиапатита с размером от 5 до 25 мкм и пригодно для аддитивных технологий, но не позволяет получать гранулы гидроксиапатита размером 40-90 мкм, это технически сложно.
Известен способ получения гранулированных частиц гидроксиапатита осаждением из раствора [10. Патент РФ 2717275 C2 Способ получения гранулированных частиц гидроксиапатита, опубл.19.03.2020], состоящий в приготовлении прекурсоров в виде растворов, содержащих ионы кальция, ионы аммония и фосфат-ионы, осаждении гидроксиапатита из растворов прекурсоров при постоянном значении рН, отделении осадка, сушку и термообработку. В качестве прекурсоров готовят раствор нитрата кальция, раствор аммиака и раствор фосфорной кислоты или аммония фосфорнокислого. Формирование осадка гидроксиапатита осуществляют при постоянном соотношении Са2+/PO43-, находящемся в интервале 1,5-1,8, и постоянном значении рН, находящемся в интервале 7-9. Способ получения обеспечивает получение сферических частиц размером 20-60 мкм. Недостатками данного способа являются необходимость непрерывного контроля рН.
Наиболее близким к изобретению по технической сущности и достигаемому результату является способ получения порошка гидроксиапатита для плазменного напыления [11. UA 19491A опубл. 25.12.1997], включающий двухстадийный синтез гидроксиапатита методом химического осаждения из водных растворов нитрата кальция и гидрофосфата аммония, в котором сначала смешивают с нитратом кальция 3-7 об.% от всего объема раствора фосфата аммония, перемешивают и доливают остальной раствор гидрофосфата аммония, затем следуют старение, промывание, отделение и сушка образованного осадка до влагосодержания 1-2 мас.%, с последующим его измельчением, обкаткой и обжигом. В результате получают порошок гидроксиапатита с размером частиц 63-80 мкм; 80-100 мкм и текучестью 74-78 с/50 г. Данный способ получения длителен и многостадиен.
В основу предлагаемого изобретения поставлена задача получения порошка гидроксиапатита повышенной текучести с дисперсностью 90-40 мкм, пригодного для изготовления плазмонапыленного покрытия и в аддитивном производстве.
Поставленная задача решается благодаря тому, что в заявляемом техническом решении, включающем размол синтезированного гидроксиапатита в механической ступке до получения порошка с размером частиц не более 90 мкм, обжига в высокотемпературной печи при 1200°С в атмосфере воздуха, отсев мелкой фракции на сите с размером ячеек 40 мкм проводят сухим, мокрым и мокро-сухим способами. В результате получают порошок гидроксиапатита с преимущественным размером частиц 90-40 мкм, малым содержанием частиц размером менее 15 мкм и, как результат, с высокой текучестью (73-55 с/50 г), который можно использовать при изготовлении медицинских имплантатов путем плазменного напыления, а также 3d-печати керамических биорезорбируемых имплантатов путем лазерной обработки слоя порошка.
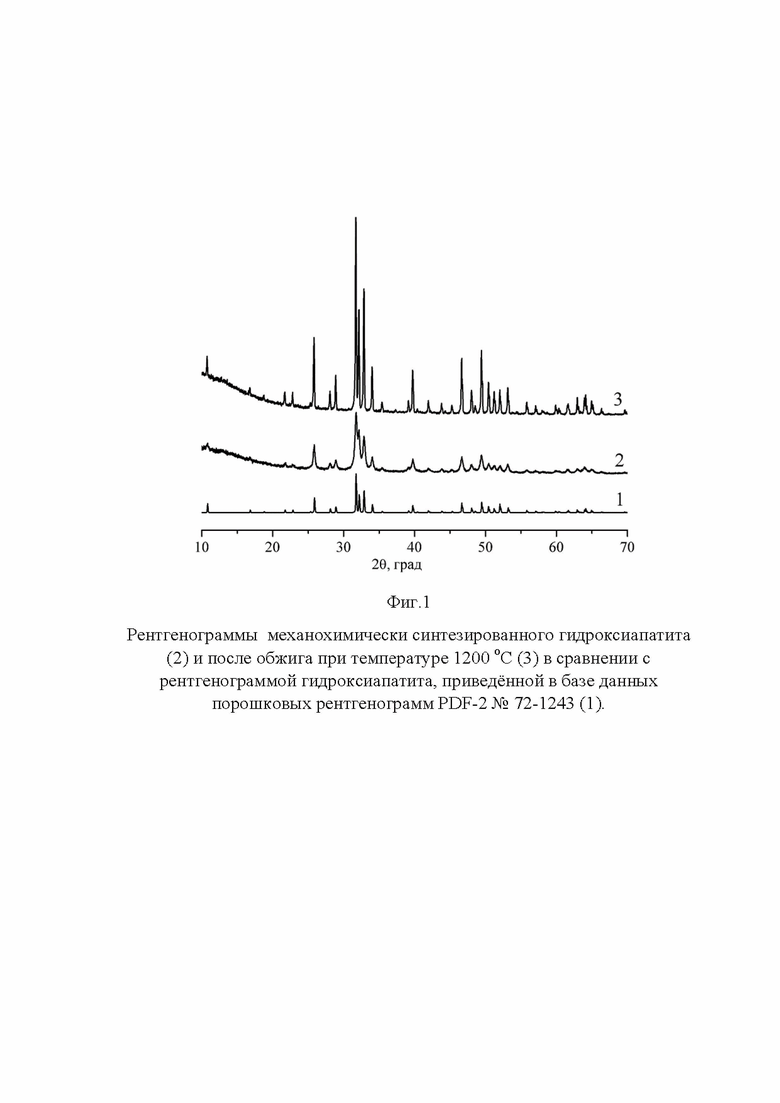
В качестве исходного сырья используется готовый гидроксиапатит, синтезированный механохимическим способом [12. Chaikina M.V., Bulina N.V., Vinokurova O.V., Prosanov I.Yu. Dudina D.V. Interaction of calcium phosphates with calcium oxide or calcium hydroxide during the “soft” mechanochemical synthesis of hydroxyapatite. Ceram. Int. 2019. Vol.45. P.16927-16933, способ 5]. Согласно данным рентгенофазового анализа синтезированный продукт представляет собой гидроксиапатит, рентгенограмма которого идентична приведенной в базе данных PDF-2 за номером 72-1243, без примеси исходных компонентов и других фаз (фиг. 1).
Производится размол синтезированного гидроксиапатита в механической ступке до получения порошка с размером частиц не более 90 мкм с последующим обжигом в высокотемпературной печи при 1200°С в атмосфере воздуха в течение 1 часа для достижения высокой степени кристалличности синтезированного ГАП. После естественного остывания продукта в печи проводится отсев мелкой фракции на сите с размером ячеек 40 мкм различными способами: сухим (пример 1), мокрым (пример 2), мокро-сухим (пример 3). В результате получены продукты повышенной текучести, значения которой приведены в таблице 1. Как видно из табл. 1, все порошки имеют текучесть ниже значения 74 с/50 г, которое приведено в патенте [11. UA 19491A опубл. 25.12.1997]. Наилучшее значение текучести получено для мокро-сухого способа отсева.
Из фиг. 2 видно, что при сухом способе отсева мелкой фракции образец содержит отдельно лежащие мелкие частицы, при мокром способе наблюдается наличие большого количества налипших мелких частиц, а при мокро-сухом их присутствие минимально. Данные гранулометрического состава (фиг. 3) так же указывают на то, что мокро-сухой способ наиболее эффективно удаляет фракцию менее 30 мкм.
Известно, что содержание фракции с размером частиц менее 15 мкм в порошке оказывает отрицательное влияние на его текучесть [13. Борисов Ю.С., Борисова А.Л., Туник А.Ю. и др. Структура и свойства порошков для получения биокерамических покрытий способом плазменного напыления// Автоматическая сварка. 2007. №4.С. 12-16]. Таким образом, в предлагаемом изобретении повышенная текучесть достигается не путем процедуры овализации, как в патенте [11. UA 19491A опубл. 25.12.1997], а за счет удаления мелкой фракции. Использование сухого способа отсева мелкой фракции (пример 1) позволяет получать порошок гидроксиапатита повышенной текучести без использования стадии овализации. Мокрый способ отсева мелкой фракции (пример 2) позволяет провести операцию отсева гораздо быстрее, чем это возможно сухим способом (меньше забиваются сита) и с меньшим остаточным содержанием. Добавление этапа сухого отсева после операции мокрого отсева при мокро-сухом способе (пример 3) позволяет освободить порошок от мелких частиц, оставшихся в результате слипания при стадии мокрого рассева. Содержание фракции частиц менее 15 мкм в полученных образцах приведено в табл. 1.
Заявляемое техническое решение позволяет получать порошок гидроксиапатита высокой текучести, которая достигается путем максимально возможного отсева мелкой фракции сухим (пример 1), мокрым (пример 2), мокро-сухим (пример 3) способами без дополнительной стадии овализации.
Текучесть определяли по ISO 4490:2018(E) посредством калиброванной воронки Холла (табл.1). Морфологию частиц (фиг.2) исследовали с помощью метода сканирующей электронной микроскопии. Определение гранулометрического состава (фиг.3) проводили с помощью метода лазерного светорассеяния.
Примеры конкретного выполнения способа.
Пример1.
Этот пример относится к сухому способу удаления мелкой фракции порошка ГАП. Образец гидроксиапатита после размола и высокотемпературного обжига помещается на сито с размером ячеек 40 мкм, проводится отсев мелкой фракции сухим способом по ГОСТ18318-94.
Пример 2.
Этот пример относится к мокрому способу удаления мелкой фракции порошка ГАП. Образец гидроксиапатита после размола и высокотемпературного обжига помещается на сито с размером ячеек 40 мкм, проводится отсев мелкой фракции мокрым способом до чистых промывных вод.
Пример 3.
Этот пример относится к комбинированному способу удаления мелкой фракции порошка ГАП. Образец гидроксиапатита после размола и высокотемпературного обжига помещается на сито с размером ячеек 40 мкм, проводится отсев мелкой фракции мокрым способом до чистых промывных вод, а затем, после сушки порошка на сите при температуре 105-110°С, проводится сухой доотсев мелких частиц до постоянного веса по ГОСТ 18318-94.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПОРОШКА БРУШИТА | 2009 |
|
RU2431599C2 |
| СПОСОБ ПОЛУЧЕНИЯ СУБМИКРОННОЙ БИФАЗНОЙ КЕРАМИКИ НА ОСНОВЕ ТРИКАЛЬЦИЙФОСФАТА И ГИДРОКСИАПАТИТА | 2013 |
|
RU2555685C2 |
| Способ получения мелкодисперсной суспензии гидроксилапатита | 2021 |
|
RU2780217C1 |
| СПОСОБ ПОЛУЧЕНИЯ КЕРАМИКИ НА ОСНОВЕ ГИДРОКСИАПАТИТА, СОДЕРЖАЩЕГО ОКСИД ЦИНКА | 2007 |
|
RU2372313C2 |
| Способ получения наноразмерного гидроксиапатита | 2020 |
|
RU2736048C1 |
| СПОСОБ ПОДГОТОВКИ ШИХТЫ ДЛЯ ПОЛУЧЕНИЯ КЕРАМИЧЕСКОГО БИОДЕГРАДИРУЕМОГО МАТЕРИАЛА | 2010 |
|
RU2456253C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРИСТОГО МАТЕРИАЛА НА ОСНОВЕ ФОСФАТА КАЛЬЦИЯ | 2008 |
|
RU2392007C2 |
| Остеопластический материал для замещения дефектов костной ткани | 2024 |
|
RU2824989C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОРАЗЛАГАЕМОГО КОМПОЗИТА НА ОСНОВЕ АЛИФАТИЧЕСКИХ СЛОЖНЫХ ПОЛИЭФИРОВ И ГИДРОКСИАПАТИТА | 2016 |
|
RU2664432C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОСТРУКТУРИРОВАННОГО КАЛЬЦИЙ-ФОСФАТНОГО ПОКРЫТИЯ ДЛЯ МЕДИЦИНСКИХ ИМПЛАНТАТОВ | 2013 |
|
RU2523410C1 |


Изобретение относится к производству керамических материалов медицинского назначения, а именно к способу получения порошка кристаллического гидроксиапатита кальция (ГАП) стехиометрического состава высокой текучести, пригодного для плазменного напыления на керамические и металлические имплантаты, применяемые в стоматологии, челюстно-лицевой хирургии и ортопедии, а также для 3D-печати керамических биорезорбируемых имплантатов. Предложен способ получения порошка гидроксиапатита повышенной текучести, включающий размол гидроксиапатита до получения порошка, обжиг в высокотемпературной печи в атмосфере воздуха с последующим отсевом, отличающийся тем, что для получения порошка гидроксиапатита высокой текучести размол механохимически синтезированного гидроксиапатита производится в механической ступке до получения порошка с размером частиц не более 90 мкм, обжиг производят при 1200°С, отсев мелкой фракции на сите с размером ячеек 40 мкм проводится сухим, мокрым или мокро-сухим способами. Технический результат – способ позволяет получить порошок гидроксиапатита повышенной текучести с дисперсностью 90-40 мкм, пригодный для изготовления плазмонапыленного покрытия и в аддитивном производстве. 2 ил., 1 табл., 3 пр.
Способ получения порошка гидроксиапатита повышенной текучести, включающий размол гидроксиапатита до получения порошка, обжиг в высокотемпературной печи в атмосфере воздуха с последующим отсевом, отличающийся тем, что для получения порошка гидроксиапатита высокой текучести размол механохимически синтезированного гидроксиапатита производится в механической ступке до получения порошка с размером частиц не более 90 мкм, обжиг производят при 1200°С, отсев мелкой фракции на сите с размером ячеек 40 мкм проводится сухим, мокрым или мокро-сухим способами.
| Станок для снятия обуви с колодки | 1929 |
|
SU19491A1 |
| Способ получения гидроксиапатита кальция | 1991 |
|
SU1834836A3 |
| Способ получения гидроксилапатита кальция | 1977 |
|
SU710928A1 |
| CN 101343056 B, 25.08.2010 | |||
| ПЛИТНЫЙ ОЧАГ С РУССКОЙ (ХЛЕБОПЕКАРНОЙ) ПЕЧЬЮ | 1923 |
|
SU1032A1 |
| CN 103588186 A, 19.02.2014 | |||
| FR 2849384 A1, 02.07.2004. | |||
Авторы
Даты
2022-10-11—Публикация
2021-12-27—Подача