Область изобретения
Настоящее изобретение относится к гетеродимерному биспецифическому антителу против TNFα/против IL-17A, по структуре напоминающему природное антитело, и способу его получения. В частности, в изобретении предложено высокостабильное гетеродимерное биспецифическое антитело против TNFα/против IL-17А, обладающее характеристиками природного IgG и не имеющее не соответствующих друг другу тяжелых и легких цепей, и способ его получения.
Предшествующий уровень техники
TNFα (фактор некроза опухоли а) представляет собой воспалительный цитокин, который индуцирует секрецию других воспалительных факторов путем связывания с его рецепторами TNFR1 и TNFR2. Антагонисты TNFα могут предупреждать такое связывание таким образом, чтобы уменьшать активности сигнального пути TNFα для ингибирования воспалительных реакций. Антагонисты TNFα, в настоящее время имеющиеся в продаже, в основном содержат растворимые рецепторы TNFα и моноклональные антитела против TNFα. Растворимый рецептор TNFα получают путем слияния внеклеточной области TNFR2 с константной областью IgG, такой как этанерцепт, представленный в продаже от Pfizer Pharmaceutical Ltd. в 1998. Моноклональное антитело против TNFα представляет собой генетически сконструированное антитело, которое специфически распознает TNFα и способно нейтрализовать TNFα, где в настоящее время в продаже имеются инфликсимаб и голимумаб от Johnson & Johnson Pharmaceuticals Ltd., цертолизумаб от UCB Pharma S.A., и адалимумаб от Abbott Laboratories Ltd. (Clinical Immunology, 2008, 126: 13-30). Клинические применения демонстрируют, что антагонисты TNFα могут эффективно облегчать воспаление при RA (ревматоидном артрите) и облегчать радиологическое прогрессирование суставов, и уровень улучшения индекса ACR20 для пациентов достигает вплоть до 50-70%. Тем не менее также было обнаружено, что 20-30% пациентов демонстрируют плохую реакцию на антагонисты TNFα или действия постепенно уменьшаются после проведения длительного лечения антагонистами TNFα (Biodrugs, 2009, 23 (2): 111-124).
В недавних исследованиях обнаружено, что клеточные уровни Th17 и уровни экспрессии цитокинов IL-17A повышаются у пациентов, страдающих от RA, которые демонстрируют плохую реакцию, или у которых эффекты лечения постепенно ухудшаются после лечения. Это явление также обнаружено на животных моделях, где клеточные уровни Th17 и уровни экспрессии цитокина IL-17A повышаются у животных, которые демонстрируют плохую реакцию на антагонисты TNFα. Во множестве источников сообщалось, что IL-17A может действовать синергически с TNFα, вызывая или усиливая воспалительные ответы, и что повышенные уровни Th17 и IL-17A в организме могут представлять собой важные механизмы для неудовлетворительного ответа на антагонисты TNFα (Trends Pharmacol Sci. 2015 Apr; 36 (4): 189-95. Ann Rheum Dis. 2012 Oct; 71 (10): 1741-8. PLoS ONE 2014, 9 (5): e95346.). Таким образом, резонно полагать, что одновременное ингибирование TNFα и IL-17A может приводить к более хорошему лечению пациентов, страдающих от RA, и пациентов, подверженных другим связанным с TNFα и IL-17A аутоиммунным заболеваниям, таким как псориаз, псориатрический артрит, и приводит к улучшению качества жизни.
В свете вышеизложенного, существует потребность в разработке нового терапевтического агента, способного одновременно блокировать сигнальные пути TNFα и IL-17А.
Краткое изложение сущности изобретения
В изобретении предложено новое и высокостабильное гетеродимерное бифункциональное антитело, которое обладает структурными характеристиками природного IgG, и не имеет не соответствующих друг другу тяжелых и легких цепей, и способно одновременно блокировать TNFα и IL-17A, и способ его получения. Это бифункциональное антитело обладает тенденцией избирательно связываться с опухолевыми клетками, которые одновременно и в высокой степени экспрессируют TNFα и IL-17A, таким образом, вызывая высокоэффективное и специфическое уничтожающее действие при более низких токсических и побочных эффектах.
Первый аспект настоящего изобретения относится к гетеродимерному биспецифическому антителу, содержащему первую цепь Fc, и вторую цепь Fc, и первую антигенсвязывающую функциональную область, способную специфически связываться с TNFα, и вторую антигенсвязывающую функциональную область, способную специфически связываться с IL-17A;
где как первая цепь Fc, так и вторая цепь Fc представляют собой фрагменты Fc иммуноглобулина G, содержащие аминокислотные замены, и вместе образуют гетеродимер, который может связываться с рецептором Fc;
где первая цепь Fc и вторая цепь Fc связаны с первой и второй антигенсвязывающими функциональными областями, соответственно, посредством ковалентной связи или линкера; и
где любая из первой цепи Fc и второй цепи Fc содержит аминокислотные замены в положениях 366 и 399, а другая цепь содержит аминокислотные замены в положениях 351, 407 и 409, где положения аминокислот пронумерованы в соответствии с системой нумерации Kabat EU.
Первая цепь Fc и вторая цепь Fc определены здесь исключительно для различения двух существующих цепей Fc, но не предполагается, что эти две цепи имеют различные уровни значимости или демонстрируют различный порядок. Кроме того, эти первая и вторая цепи Fc могут быть связаны с первой и второй антигенсвязывающими функциональными областями любыми произвольными путями, то есть первая цепь Fc может быть связана с первой или второй антигенсвязывающей функциональной областью, как может и вторая цепь Fc.
В некоторых воплощениях аминокислотные замены для первой цепи Fc и второй цепи Fc представляют собой следующие:
а) L351G, L351Y, L351V, L351P, L351D, L351E, L351K или L351W;
б) T366L, Т366Р, T366W или T366V;
в) D399C, D399N, D399I, D399G, D399R, D399T или D399A;
г) Y407L, Y407A, Y407P, Y407F, Y407T или Y407H; и
д) K409C, K409P, K409S, K409F, K409V, K409Q или K409R.
В некоторых воплощениях аминокислотные замены включают:
а) замены T366L и D399R в любой из первой цепи Fc и второй цепи Fc и замены L351E, Y407L и K409V в другой цепи;
б) замены T366L и D399C в любой из первой цепи Fc и второй цепи Fc и замены L351G, Y407L и K409C в другой цепи;
в) замены T366L и D399C в любой из первой цепи Fc и второй цепи Fc и замены L351Y, Y407A и K409P в другой цепи;
г) замены Т366Р и D399N в любой из первой цепи Fc и второй цепи Fc и замены L351V, Y407P и K409S в другой цепи;
д) замены T366W и D399G в любой из первой цепи Fc и второй цепи Fc и замены L351D, Y407P и K409S в другой цепи;
е) замены Т366Р и D399I в любой из первой цепи Fc и второй цепи Fc и замены L351P, Y407F и K409F в другой цепи;
ж) замены T366V и D399T в любой из первой цепи Fc и второй цепи Fc и замены L351K, Y407T и K409Q в другой цепи; и
з) замены T366L и D399A в любой из первой цепи Fc и второй цепи Fc и замены L351W, Y407H и K409R в другой цепи.
В некоторых воплощениях либо первая цепь Fc, либо вторая цепь Fc имеет аминокислотные замены T366L и D399R, а другая цепь имеет аминокислотные замены L351E, Y407L и K409V.
В некоторых воплощениях как первая антигенсвязывающая функциональная область, так и вторая антигенсвязывающая функциональная область выбраны из группы, состоящей из фрагмента Fab, фрагмента scFv, фрагмента вариабельного домена Fv и фрагмента вариабельной области тяжелой цепи VHH антитела из тяжелых цепей.
В некоторых воплощениях как первая антигенсвязывающая функциональная область, так и вторая антигенсвязывающая функциональная область представляют собой фрагменты Fab.
В некоторых воплощениях одна из первой антигенсвязывающей функциональной области и второй антигенсвязывающей функциональной области представляет собой фрагмент Fab, а другая представляет собой фрагмент scFv.
В некоторых воплощениях фрагменты Fab включают вариабельную область первой тяжелой цепи и вариабельную область второй тяжелой цепи, которые отличаются друг от друга, и вариабельную область первой легкой цепи и вариабельную область второй легкой цепи, которые отличаются друг от друга.
В некоторых воплощениях первая цепь Fc и первая антигенсвязывающая функциональная область, ковалентно связанная с ней, и вторая цепь Fc и вторая антигенсвязывающая функциональная область, ковалентно связанная с ней, образуют гомодимер в растворе в присутствии восстановителя и в отсутствие любых других полипептидов, отличающихся от первой цепи Fc и первой антигенсвязывающей функциональной области, ковалентно связанной с ней, и второй цепи Fc и второй антигенсвязывающей функциональной областью, ковалентно связанной с ней, в массовом отношении менее 50% относительно всех полипептидных цепей.
В некоторых воплощениях первая антигенсвязывающая функциональная область содержит аминокислотные последовательности SEQ ID NO: 2 и 6.
В некоторых воплощениях вторая антигенсвязывающая функциональная область содержит аминокислотные последовательности SEQ ID NO: 10 и 12.
В некоторых воплощениях первая антигенсвязывающая функциональная область дополнительно содержит аминокислотные последовательности SEQ ID NO: 4 и 8.
В некоторых воплощениях вторая антигенсвязывающая функциональная область дополнительно содержит аминокислотные последовательности SEQ ID NO: 4 и 14.
В некоторых воплощениях аминокислотные последовательности биспецифического антитела представляют собой соответствующие комбинации SEQ ID NO: 2, 4, 6, 8, 10, 12 и 14. Например, SEQ ID NO: 2, 4, 6 и 8 комбинированы друг с другом, SEQ ID NO: 10, 4, 12 и 14 комбинированы друг с другом, и затем обе комбинации рекомбинированы с образованием биспецифического антитела по настоящему изобретению.
Второй аспект настоящего изобретения относится к выделенному полинуклеотиду, кодирующему гетеродимерное биспецифическое антитело в соответствии с первым аспектом.
В некоторых воплощениях нуклеотидные последовательности, кодирующие аминокислотные последовательности первой антигенсвязывающей функциональной области, выбраны из группы, состоящей из: SEQ ID NO: 1 и 5.
В некоторых воплощениях нуклеотидные последовательности, кодирующие аминокислотные последовательности второй антигенсвязывающей функциональной области, выбраны из группы, состоящей из: SEQ ID NO: 9 и 11.
В некоторых воплощениях нуклеотидные последовательности, кодирующие аминокислотные последовательности первой антигенсвязывающей функциональной области, дополнительно выбраны из группы, состоящей из: SEQ ID NO: 3 и 7.
В некоторых воплощениях нуклеотидные последовательности, кодирующие аминокислотные последовательности второй антигенсвязывающей функциональной области, дополнительно выбраны из группы, состоящей из: SEQ ID NO: 3 и 13.
В некоторых воплощениях последовательности полипептидов представляют собой соответствующие комбинации SEQ ID NO: 1, 3, 5, 7, 9, 11 и 13. Например, SEQ ID NO: 1, 3, 5 и 7 комбинированы друг с другом и SEQ ID NO: 9, 3, 11 и 13 комбинированы друг с другом.
Третий аспект настоящего изобретения относится к рекомбинантному экспрессионному вектору, содержащему выделенный полинуклеотид в соответствии со вторым аспектом.
В некоторых воплощениях экспрессионный вектор представляет собой плазмидный вектор X0GC, модифицированный на основе pCDNA.
Четвертый аспект настоящего изобретения относится к клетке-хозяину, содержащей выделенный полинуклеотид в соответствии со вторым аспектом или рекомбинантный экспрессионный вектор в соответствии с третьим аспектом.
В некоторых воплощениях клетка-хозяин выбрана из группы, состоящей из эмбриональной клетки почки человека HEK293 или клетки HEK293T, клетки HEK293E и клетки HEK293F, имеющих происхождение от клетки HEK293; клетки яичника китайского хомячка СНО или клетки CHO-S, клетки CHO-dhfr, клетки CHO/DG 44 и клетки ExpiCHO, имеющих происхождение от клетки СНО; Escherichia coli или Escherichia coli BL21, BL21 (DE3), Rosetta, Origami, имеющих происхождение от Escherichia coli; дрожжей или Pichia pastoris, Saccharomyces cerevisiae, Kluyveromyces lactis и Hansenula polymorpha, имеющих происхождение от дрожжей; клетки насекомого или клетки High 5 и клетки SF 9, имеющих происхождение от клетки насекомого; растительной клетки; клетки молочной железы млекопитающего, соматической клетки млекопитающего.
Пятый аспект настоящего изобретения относится к композиции, содержащей гетеродимерное биспецифическое антитело в соответствии с первым аспектом, или выделенный полинуклеотид в соответствии со вторым аспектом, или рекомбинантный экспрессионный вектор в соответствии с третьим аспектом, или клетку-хозяина в соответствии с четвертым аспектом, и фармацевтически приемлемый носитель.
Шестой аспект настоящего изобретения относится к способу получения гетеродимерного биспецифического антитела в соответствии с первым аспектом, включающему стадии:
1) экспрессирования выделенного полинуклеотида в соответствии со вторым аспектом или рекомбинантного экспрессионного вектора в соответствии с третьим аспектом, соответственно, в клетке-хозяине;
2) восстановления каждого белка, соответственно экспрессированного в клетках-хозяевах; и
3) смешивания восстановленных белков и затем окисления смеси.
В некоторых воплощениях клетка-хозяин выбрана из группы, состоящей из эмбриональной клетки почки человека HEK293 или клетки HEK293T, клетки HEK293E и клетки HEK293F, имеющих происхождение от клетки FIEK293; клетки яичника китайского хомячка СНО или клетки CHO-S, клетки CHO-dhfr, клетки CHO/DG 44 и клетки ExpiCHO, имеющих происхождение от клетки СНО; Escherichia coli или Escherichia coli BL21, BL21 (DE3), Rosetta, Origami, имеющих происхождение от Escherichia coli; дрожжей или Pichia pastoris, Saccharomyces cerevisiae, Kluyveromyces lactis и Hansenula polymorpha, имеющих происхождение от дрожжей; клетки насекомого или клетки High 5 и клетки SF 9, имеющих происхождение от клетки насекомого; растительной клетки; клетки молочной железы млекопитающего, соматической клетки млекопитающего.
В некоторых воплощениях стадия восстановления включает 1) проведение реакции восстановления в присутствии восстановителя, выбранного из группы, состоящей из 2-меркаптоэтиламина, дитиотреитола, трис(2-карбоксиэтил)фосфина или его химических производных; 2) удаление восстановителя. Например, реакцию восстановления осуществляют в присутствии дитиотреитола в концентрации 0,1 мМ или выше при 4°С в течение по меньшей мере 3 часов. Определения восстановителя и условий реакции восстановления применимы в отношении других случаев, когда здесь используются восстановитель и реакция восстановления.
В некоторых воплощениях стадия окисления представляет собой окисление воздухом или реакцию окисления в присутствии окислителя, выбранного из группы, состоящей из L-дегидроаскорбиновой кислоты или ее химических производных. Например, реакцию окисления осуществляют в присутствии L-дегидроаскорбиновой кислоты в концентрации 0,5 мМ или выше при 4°С в течение по меньшей мере 5 часов.
В некоторых воплощениях способ дополнительно включает стадию выделения и очистки.
Седьмой аспект настоящего изобретения относится к применению гетеродимерного биспецифического антитела в соответствии с первым аспектом, и/или выделенного полинуклеотида в соответствии со вторым аспектом, и/или рекомбинантного экспрессионного вектора в соответствии с третьим аспектом, и/или клетки-хозяина в соответствии с четвертым аспектом, и/или композиции в соответствии с пятым аспектом в изготовлении лекарственного средства для предупреждения и/или лечения заболевания у субъекта.
Восьмой аспект настоящего изобретения относится к гетеродимерному биспецифическому антителу в соответствии с первым аспектом, и/или выделенному полинуклеотиду в соответствии со вторым аспектом, и/или рекомбинантному экспрессионному вектору в соответствии с третьим аспектом, и/или клетке-хозяину в соответствии с четвертым аспектом, и/или композиции в соответствии с пятым аспектом для применения в качестве лекарственного средства для предупреждения и/или лечения заболевания у субъекта.
Девятый аспект изобретения относится к способу предупреждения и/или лечения заболевания, включающему стадию введения субъекту, нуждающемуся в этом, гетеродимерного биспецифического антитела в соответствии с первым аспектом, и/или выделенного полинуклеотида в соответствии со вторым аспектом, и/или рекомбинантного экспрессионного вектора в соответствии с третьим аспектом, и/или клетки-хозяина в соответствии с четвертым аспектом, и/или композиции в соответствии с пятым аспектом.
В некоторых воплощениях субъект представляет собой млекопитающее, предпочтительно субъекта-человека.
В некоторых воплощениях заболевание выбрано из группы, состоящей из ревматоидного артрита, остеоартрита, псориатического артрита, анкилозирующего спондилита, подагрического артрита, ювенильного ревматоидного артрита, гнойного артрита, псориаза, сахарного диабета I типа, рассеянного склероза, аутоиммунного энцефаломиелита, болезни Крона, системого васкулита, дерматомиозита, смешанного заболевания соединительной ткани, системной красной волчанки, идиопатической тромбоцитопенической пурпуры, первичного синдрома Шегрена, гломерулонефрита, подагры, отторжения трансплантата органа, астмы или атеросклероза.
В настоящем изобретении разработано новое гетеродимерное биспецифическое антитело против TNFα/против IL-17A, по структуре напоминающее природное антитело, которое представляет собой высокостабильное гетеродимерное биспецифическое антитело против TNFα/против IL-17A, обладающее характеристиками природного IgG и не имеющее не соответствующих друг другу тяжелых и легких цепей. Биспецифическое антитело, полученное в изобретении, может одновременно блокировать сигнальный путь TNFα и сигнальный путь IL-17A и может оказывать более хорошие эффекты, чем одиночный терапевтический агент при применении для лечения сложных заболеваний. В то же время, по сравнению с комбинированным лечением множеством лекарственных средств, биспецифическое антитело, служащее в качестве одиночной молекулы для лечения, не только облегчает применение пациентами и медицинским персоналом, но также упрощает сложный процесс разработки новых лекарственных средств. Кроме того, в настоящем изобретении обнаружено, что по сравнению со случаем, когда отсутствует IL-17A, нейтрализующая TNFα активность части биспецифического антитела, направленной против TNFα, существенно увеличивается, когда присутствует IL-17A, что свидетельствует о том, что указанное биспецифическое антитело обладает более сильной активностью, нейтрализующей TNFα, в очаговом сайте, имеющем высокий уровень IL-17A, и демонстрирует более слабую активность, нейтрализующую TNFα, в системе кровообращения, имеющей низкий уровень IL-17А, таким образом, указывая на то, что биспецифическое антитело может эффективно лечить заболевания при сохранении меньших токсических и побочных эффектов.
Краткое описание графических материалов
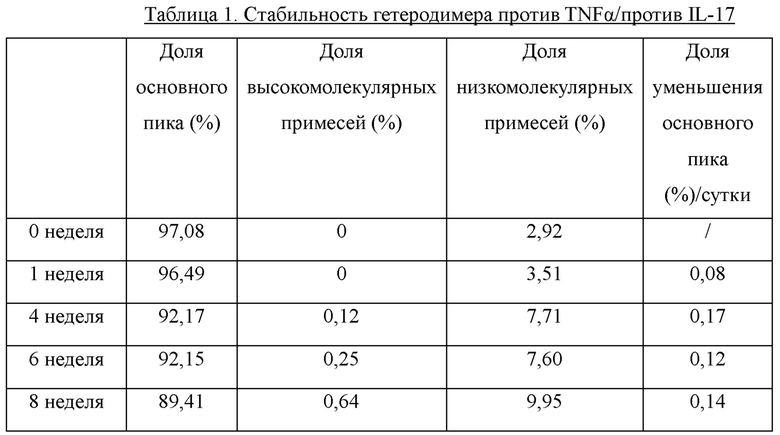
Фиг. 1 демонстрирует хроматограмму пиков элюции продукта экспрессии антитела против TNFα и продукта экспрессии антитела против IL-17A, где А представляет собой хроматограмму пика элюции продукта экспрессии антитела против TNFα и В представляет собой хроматограмму пика элюции продукта экспрессии антитела против IL-17А.
Фиг. 2 демонстрирует структуру молекулы гетеродимерного антитела против TNFα/против IL-17A.
Фиг. 3 демонстрирует структуру половины молекулы антитела, содержащей одну тяжелую цепь и одну легкую цепь.
Фиг. 4 демонстрирует результаты анализа посредством SEC (гель-проникающей хроматографии) половины молекулы антитела, содержащей одну тяжелую цепь и одну легкую цепь, где А представляет собой половину молекулы антитела против TNFα, имеющую чистоту 98%, и В представляет собой половину молекулы антитела против IL-17A, имеющую чистоту 90,2%.
Фиг. 5 демонстрирует результаты капиллярного электрофореза в невосстанавливающих условиях молекулы гетеродимерного антитела против TNFα/IL-17А, где пик 1 соответствует одиночной легкой цепи, пик 2 соответствует одной тяжелой цепи с одной легкой цепью, пик 3 соответствует двум тяжелым цепям, пик 4 соответствует двум тяжелым цепям с одной легкой цепью, пик 5 соответствует двум тяжелым цепям с двумя легкими цепями.
Фиг. 6 демонстрирует пик элюции молекулы гетеродимерного антитела против TNFα/против IL-17A.
Фиг. 7 демонстрирует результаты капиллярного электрофореза в невосстанавливающих условиях окончательно очищенной молекулы гетеродимерного антитела против-TNFα/против-IL-17А, где пик 1 соответствует одиночной легкой цепи, пик 2 соответствует двум тяжелым цепям, пик 3 соответствует двум тяжелым цепям с одной легкой цепью и пик 4 соответствует двум тяжелым цепями с двумя легкими цепями.
Фиг. 8 демонстрирует результаты анализа посредством SEC молекулы гетеродимерного антитела против TNFα/против IL-17A, имеющего чистоту 99,9%.
Фиг. 9 демонстрирует нейтрализующую антиген-мишень активность in vitro гетеродимерного антитела ВН1657 против TNFα/против IL-17A, где А демонстрирует нейтрализующую TNFα активность ВН1657, В демонстрирует нейтрализующую IL-17A активность ВН1657 и С демонстрирует нейтрализующую активность ВН1657 в присутствии как TNFα, так и IL-17.
Фиг. 10 демонстрирует, что на активность против TNFα гетеродимерного антитела ВН1657 против TNFα/против IL-17A влияет присутствие или отсутствие IL-17А, где А демонстрирует эффект IL-17A в отношении блокирования ВН1657 активности TNFα/TNFR2 и В демонстрирует эффект IL-17A в отношении нейтрализующей TNFα активности ВН1657.
Фиг. 11 демонстрирует нейтрализующую антиген-мишень активность in vivo гетеродимерного антитела ВН1657 против TNFα/против IL-17A. ##р менее 0,01 по сравнению с антителом против TNFα; **р менее 0,01 по сравнению с антителом против IL-17A.
Фиг. 12 демонстрирует эффективность гетеродимерного антитела ВН1654 против мышиного TNFα/против мышиного IL-17A в модели индуцированного коллагеном II типа артрита у мышей (mCIA). *р менее 0,5, **р менее 0,01, *** р менее 0,001 по сравнению с носителем; #р менее 0,05, #р менее 0,001 по сравнению со 140 нмоль/кг ВН1654.
Фиг. 13. демонстрирует эффективность гетеродимерного антитела ВН1654 против мышиного TNFα/против мышиного IL-17Ab модели индуцированного глюкозо-6-фосфатизомеразой артрита у мышей (mGPI). #р менее 0,5, #р менее 0,01, #р менее 0,001 по сравнению с носителем; *р менее 0,05, **р менее 0,01 по сравнению с 70 нмоль/кг ВН1654.
ФИГ. 14. демонстрирует эффективность гетеродимерного антитела ВН1654 против мышиного TNFα/против мышиного IL-17A в модели индуцированного зимозаном псориатрического артрита у мышей SKG (PsA). #р менее 0,5 по сравнению с носителем.
Подробное описание изобретения
Определения:
Ковалентная связь означает, что две цепи Fc или любая из цепей Fc и связанная с ней антигенсвязывающая функциональная область в гетеродимерном биспецифическом антителе связаны друг с другом посредством ковалентной связи с образованием единичной молекулы. Среди них цепи Fc содержат первую антигенсвязывающую функциональную область и вторую антигенсвязывающую функциональную область, связанные посредством одной или более чем одной ковалентной связи (например дисульфидной связи); первая и вторая цепи Fc связаны с антигенсвязывающей функциональной областью посредством ковалентной связи (например иминовой или амидной связи), соответственно;
Антигенсвязывающая функциональная область представляет собой область, которая может специфически взаимодействовать с молекулой-мишенью, такой как антиген, и действие которой является высоко селективным, и последовательность, которая распознает одну молекулу-мишень, как правило, не способна распознавать другие молекулярные последовательности. Типичная антигенсвязывающая функциональная область включает вариабельную область антитела, структурный вариант вариабельной области антитела, домен связывания с рецептором, домен связывания с лигандом или домен связывания с ферментом.
Одна или более чем одна связь между цепями относится к образованию гетеродимерного фрагмента посредством связей между первой цепью Fc и второй цепью Fc посредством одной или более чем одной дисульфидной связи. В настоящем изобретении одна или более чем одна дисульфидная связь может быть образована, когда первая цепь Fc и вторая цепь Fc или первая цепь Fc и вторая цепь Fc и антигенсвязывающие функциональные области, связанные с ними, синтезируются в одной клетке, или может быть образована посредством восстановления-окисления in vitro после того, как первая цепь Fc и вторая цепь Fc или первая цепь Fc и вторая цепь Fc и антигенсвязывающие функциональные области, связанные с ними, синтезируются в различных клетках, соответственно.
Первая цепь Fc и вторая цепь Fc относятся к связывающему фрагменту, образованному посредством ковалентной связи, где ковалентная связь содержит дисульфидную связь, каждая цепь содержит по меньшей мере одну часть константной области тяжелой цепи иммуноглобулина; и первая цепь Fc и вторая цепь Fc отличаются друг от друга по своим аминокислотным последовательностям и содержат по меньшей мере одну отличающуюся аминокислоту. В отношении как первой, так и второй цепей Fc по настоящему изобретению имеется мощная взаимная отталкивающая сила между идентичными цепями, и притягивающая сила существует между различными цепями. Соответственно, первая и вторая цепи Fc или первая и вторая цепи Fc и связанные с ними антигенсвязывающие функциональные области имеют тенденцию претерпевать образование гетеродимера при одновременной экспрессии в клетке. Когда первая и вторая цепи Fc или первая и вторая цепи Fc и связанный с ними антигенсвязывающий домен экспрессируются в двух клетках-хозяевах, соответственно, тогда первые цепи Fc или первая цепь Fc и связанный с ней антигенсвязывающий домен не имеют тенденции претерпевать образование гомодимера, и вторые цепи Fc или вторая цепь Fc и связанный с ней антигенсвязывающий домен не имеют тенденции претерпевать образование гомодимера. В настоящем изобретении, когда первая и вторая цепи Fc или первая и вторая цепи Fc и связанные с ними антигенсвязывающие функциональные области экспрессируются в двух клетках-хозяевах, соответственно, и присутствует восстановитель, тогда процентная доля гомодимеров составляет менее 50%, то есть процентная доля мономеров (одна цепь Fc или одна цепь Fc и одна связанная с ней антигенсвязывающая функциональная область) превышает 50%.
Иммуноглобулин имеет симметричную структуру, имеющую четыре полипептидные цепи, где две цепи идентичны тяжелым цепям, которые являются относительно длинными и имеют относительно высокую молекулярную массу, каждая из которых содержит 450-550 аминокислотных остатков и имеет относительную молекулярную массу 55000-70000 Да; а две другие цепи идентичны легким цепям (L-цепям), которые являются относительно короткими и имеют относительно низкую молекулярную массу, включая приблизительно 210 аминокислотных остатков и имея относительную молекулярную массу приблизительно 24000 Да. Последовательности длиной приблизительно 110 аминокислот около N-концов тяжелых и легких цепей иммуноглобулина являются высоковариабельными и называются вариабельными областями (V-областями), тогда как остальные аминокислотные последовательности около их С-концов являются относительно стабильными и называются константными областями (С-областями). Вариабельная область в тяжелой цепи занимает приблизительно 1/4 длины тяжелой цепи, и константная область занимает приблизительно 3/4 длины тяжелой цепи. Известные пять типов Ig представляют собой IgG (γ), IgA (α), IgD (δ), IgM (μ) и IgE (ε). Среди них первые три типа Ig имеют три константные области в Н-цепи (тяжелой цепи), а именно CH1, СН2 и СН3. Последние два типа Ig (IgM и IgE) имеют одну область VH и четыре константные области в Н-цепи, а именно СН1-СН4. Обе константные области представляют собой каркас молекулы иммуноглобулина, и одна из областей активирует иммунные ответы. Хотя примеры по изобретению относятся к IgG, специалисту в данной области техники понятно, что класс антител по изобретению при желании можно изменять известными способами. Например, класс антитела по изобретению, которое исходно представляет собой IgM, может быть изменен на антитело IgG по изобретению. Кроме того, методики изменения классов можно использовать для превращения одного подкласса IgG в другой, например из IgG1 в IgG2. Таким образом, эффекторные функции антител по изобретению могут быть изменены по изотипу, например на антитела IgG1, IgG2, IgG3, IgG4, IgD, IgA, IgE или IgM для различных терапевтических применений. В одном воплощении антитело по изобретению представляет собой антитело IgG1, такое как IgG1, к.
Часть константной области в соответствии с настоящим описанием включает по меньшей мере область взаимодействия первой цепи Fc и второй цепи Fc, и в случае IgG эта область располагается в нескольких аминокислотных положениях в домене СН3 и включает по меньшей мере GLN 347, TYR 349, THR 350, LEU 351, SER 354, ARG 355, ASP 356, GLU 357, LYS 360, SER 364, THR 366, LEU 368, LYS 370, ASN 390, LYS 392, THR 394, PRO 395, VAL 397, ASP 399, SER 400, PHE 405, TYR 407, LYS 409 и LYS 439.
Каждая из первой цепи Fc и второй цепи Fc, связанная с одной антигенсвязывающей функциональной областью посредством ковалентной связи или линкера, обозначает первую цепь Fc и вторую цепь Fc, каждая из которых связана с антигенсвязывающим фрагментом антитела, или одноцепочечное антитело, способное распознавать антиген, или другой вариабельный фрагмент антитела, способный распознавать антиген, или рецептор, способный распознавать лиганд, или лиганд, способный распознавать рецептор посредством ковалентной связи или линкера. Ковалентная связь представляет собой разновидность химической связи, в которой два или более чем два атома вместе используют свои внешние электроны для достижения в идеальных условиях состояния электронного насыщения, таким образом образуя относительно стабильную химическую структуру, называемую ковалентной связью, или взаимодействие между атомами образуется посредством общей пары электронов. Все атомы одного и того же элемента или атомы различных элементов могут быть связаны посредством ковалентной связи. Ковалентная связь между первой цепью Fc и второй цепью Fc в соответствии с изобретением включает, без ограничения, амидную связь, образованную путем дегидратации между аминогруппой аминокислоты одной молекулы и карбоксильной группы аминокислоты другой молекулы, или амидной связи или иминовой связи, образованной между альдегидной группой этиленгликоля или полиэтиленгликоля, или другого соединения, или его полимера и аминогруппой аминокислоты молекулы; где линкер представляет собой один участок аминокислотной последовательности или одно соединение, или один мультимер одного соединения, способный связывать две полипетидные цепи посредством ковалентной связи, где указанный один участок аминокислотной последовательности включает небольшой пептид, такой как GGGGSGGGGSGGGGS, и первую цепь Fc или вторую цепь Fc, и одноцепочечное антитело, способное распознавать антиген, или другой структурный вариант фрагмента антитела, способный распознавать антиген, путем амидной связи, но не ограничивается ими.
Первая цепь Fc и вторая цепь Fc имеют тенденцию претерпевать образование гетеродимера и не имеют тенденции образовывать гомодимер, что означает, что как для первой цепи Fc, так и второй цепи Fc, существует отталкивающая сила между идентичными полипептидными цепями, и сила притяжения существует между различными полипептидными цепями, и, таким образом, первая цепь Fc и вторая цепь Fc, или первая и вторая цепи Fc и связанные с ними антигенсвязывающие функциональные области имеют тенденцию претерпевать образование гетеродимера в случае совместной экспрессии в клетке. Когда первая цепь Fc и вторая цепь Fc, или первая и вторая цепи Fc и связанные с ними антигенсвязывающие функциональные области экспрессируются в двух клетках-хозяевах, соответственно, первые цепи Fc или первая цепь Fc и связанная с ней антигенсвязывающая функциональная область не имеют тенденции претерпевать образование гомодимера, и вторые цепи Fc или вторая цепь Fc и связанная ней антигенсвязывающая функциональная область также не имеют тенденции претерпевать образование гомодимера.
Система нумерации Kabat означает, что Kabat присваивает номер каждой аминокислоте в последовательности антитела с использованием способа, и такой способ присваивания остатку номеров стал стандартным способом в области техники. Протокол Kabat распространим на другие антитела, не представленные в данном исследовании, путем выравнивания целевого антитела с одной из консенсусных последовательностей в Kabat относительно консервативных аминокислот.
Домен Fc относится к фрагменту кристаллизуемого (Fc), соответствует доменам СН2 и СН3 в Ig и представляет собой сайт, по которому Ig взаимодействует с эффекторной молекулой или клеткой.
IgG представляет собой сокращение для иммуноглобулина G (IgG) и представляет собой основной тип антитела в сыворотке крови. Человеческий IgG имеет четыре подкласса, а именно IgG1, IgG2, IgG3 и IgG4, на основе антигенных различий по r-цепям в молекулах IgG.
Половина молекулы антитела относится к структуре, образованной одной тяжелой цепью и одной легкой цепью антитела, где тяжелая цепь и легкая цепь могут быть связаны посредством или не посредством ковалентной связи, и представляет собой моновалентную структуру антитела, распознающую антиген. Фрагмент Fab представляет собой последовательность, распознающую молекулу, и фрагмент связывания антигена (Fab), и соответствует двум плечам молекулы антитела, состоящим из полноразмерной легкой цепи и доменов VH и СН1 тяжелой цепи. scFv представляет собой последовательность, распознающую молекулы, и представляет собой структурный вариант фрагмента антитела, получаемый путем генно-инженерной модификации вариабельной области легкой цепи и вариабельной области тяжелой цепи антитела. Внеклеточная область мембранного рецептора представляет собой последовательность, распознающую молекулу, и мембранный рецептор, как правило, содержит внеклеточную область, располагающуюся вне клетки, которая распознает соответствующий антиген или лиганд и связывается с ним, трансмембранную область, которая заякоривает рецептор на поверхности клетки, и внутриклеточную область в клетке, которая обладает киназной активностью или передает сигнал. Лиганд рецептора клеточной мембраны относится к белку, небольшому пептиду или соединению, которое может распознаваться и связываться внеклеточной областью мембранного рецептора. Цитокины представляют собой низкомолекулярные растворимые белки, продуцируемые различными типами клеток, индуцированные иммуногенами, митогенами или другими стимуляторами, и обладают различными функциями, такими как регулирования врожденного иммунитета и адаптивного иммунитета, гемопоэз, рост клеток, плюрипотентные клетки APSC и восстановление поврежденной ткани и тому подобные. Цитокины могут быть классифицированы на интерлейкины, интерфероны, супер семейства фактора некроза опухоли, колониестимулирующие факторы, хемокины, факторы роста и тому подобное. Метка белковой экспрессии обозначает аминокислотную последовательность, добавленную по N-концу или С-концу белка-мишени, и может представлять собой небольшие пептиды или длинную аминокислотную последовательность. Добавление метки может быть благоприятно для правильного фолдинга белков, выделения и очистки белков и уменьшения внутриклеточного разрушения белков. Часто используемые метки могут включать, без ограничения, НА, SUMO, His, GST, GFP и Flag.
Отсутствует ограничение по антителам, которые подходят для гетеродимерного биспецифического антитела по настоящему изобретению. Предпочтительно, антитела, известные в области техники, полезные при лечении и/или предупреждении заболеваний, можно применять в настоящем изобретении.
Гетеродимерное биспецифическое антитело по изобретению может иметь одну или более чем одну замену, делецию, добавление и/или вставку. Например, некоторые аминокислоты могут заменять другие аминокислоты в структуре белка без существенной утраты способности связываться с другими полипептидами (например, антигенами) или клетками. Поскольку связывающая способность и свойства белка определяют биоактивности и функции белка, замены некоторых аминокислот в белковой последовательности могут не вызывать существенной утраты его биологической эффективности или активностей.
Во многих случаях вариант полипептида включает одну или более чем одну консервативную замену. "Консервативные замены" относятся к таким заменам, при которых аминокислоты в полипептиде заменяются другими аминокислотами, имеющими похожие свойства, таким образом, что специалист в области пептидной химии может предположить, что вторичная структура и гидрофильная природа полипептида не будут существенно изменены.
Аминокислотные замены, как правило, основаны на относительном сходстве заместителей по аминокислотным боковым цепям, таком как гидрофобность, гидрофильность, заряды, размер и тому подобное. Примеры альтернатив, принимающие во внимание различные вышеупомянутые характеристики, хорошо известны специалистам в данной области техники и включают аргинин и лизин; глутаминовую кислоту и аспарагиновую кислоту; серии и треонин; глутамин и аспарагин; и валин, лейцин и изолейцин.
Используемый здесь термин "идентичность" имеет значение, обычно известное в области техники, и специалисты в данной области техники также знакомы с правилами, критериями определения идентичности между различными последовательностями, и "идентичность" относится к процентной доле гомологии между остатками варианта полинуклеотидной или полипептидной последовательности и остатками невариантной последовательности после выравнивания последовательностей и включения пропусков (при необходимости для достижения максимальной процентной доли гомологии). В настоящем изобретении, когда удовлетворено определение идентичности, также требуется, чтобы полученный вариант последовательности обладал биологическими активностями, которыми обладает родительская последовательность. Способы и средства для скрининга вариантов последовательностей с использованием указанных выше активностей хорошо известны специалистам в данной области техники. Такие вариантные последовательности могут быть легко получены специалистом в данной области техники в свете настоящего описания. В конкретных воплощениях полинуклеотидные и полипептидные варианты имеют по меньшей мере приблизительно 70%, по меньшей мере приблизительно 75%, по меньшей мере приблизительно 80%, по меньшей мере приблизительно 90%, по меньшей мере приблизительно 95%, по меньшей мере приблизительно 98% или по меньшей мере приблизительно 99%, или по меньшей мере приблизительно 99,1%, 99,2%, 99,3%, 99,4%, 99,5%, 99,6%, 99,7%, 99,8% или 99,9% полинуклеотидной или полипептидной идентичности с описанным здесь полинуклеотидом или полипептидом. Вследствие вырожденности генетических кодонов существуют варианты этих последовательностей, кодирующие одну и ту же аминокислотную последовательность.
В еще одном воплощении настоящего изобретения предложена полинуклеотидная композиция, способная гибридизироваться с полинуклеотидными последовательностями, предложенными по настоящему изобретению, или их фрагментами, или комплементарными им последовательностями в условиях гибридизации от умеренных до строгих. Методики гибридизации хорошо известны в области молекулярной биологии. Для задач иллюстрации подходящие умеренно строгие условия гибридизации для тестирования гибридизации полинуклеотидов по настоящему изобретению с другими полинуклеотидами включают предварительное отмывание раствором 5×SSC (раствор цитрата и хлорида натрия), 0,5% SDS (додецилсульфат натрия), 1,0 мМ EDTA (этилендиаминтетрауксусная кислота) (рН 8,0); гибридизацию в 5×SSC при 50-60°С в течение ночи; и двукратное промывание 2×, 0,5× и 0,2×SSC, содержащим 0,1% SDS, в течение 20 минут при 65°С. Специалистам в данной области техники понятно, что строгостью условий гибридизации можно легко управлять, например, путем изменения содержания соли в растворе для гибридизации и/или температуры гибридизации. Например, в еще одном воплощении подходящие условия гибридизации высокой строгости включают условия, описанные выше, за исключением того, что увеличена температура гибридизации, например до 60-65°С или 65-70°С.
Клетка-хозяин по настоящему изобретению может представлять собой любую клетку, экспрессирующую чужеродный ген, и может включать, без ограничения, E.coli, дрожжи, клетку насекомого, растительную клетку, клетку млекопитающего.
Вектор по настоящему изобретению включает вектор, который может реплицироваться в любом типе клеток или организмов, включая, например, плазмиды, фаги, космиды и мини-хромосомы. В некоторых воплощениях этот вектор, содержащий полинуклеотид по настоящему изобретению, представляет собой вектор, подходящий для увеличения числа копий или репликации полинуклеотида, или вектор, подходящий для экспрессии полипептида по настоящему изобретению. Такие векторы известны в области техники и имеются в продаже.
"Вектор" включает шаттл-вектор и экспрессионный вектор. Как правило, плазмидная конструкция также включает точку начала репликации (например, точку начала репликации ColE 1) и селективный маркер (например, резистентность к ампициллину или тетрациклину), которые предназначены для репликации плазмиды и отбора в бактериях, соответственно. "Экспрессионный вектор" относится к вектору, включающему контрольные последовательности или регуляторные элементы, которые требуются для экспрессии антитела по настоящему изобретению, включая фрагменты антитела, в бактериальной или эукариотической клетке.
Вектор по настоящему изобретению может представлять собой любой вектор, используемый для экспрессии чужеродного гена, включая, без ограничения, плазмидный вектор, где плазмидный вектор включает по меньшей мере точку начала репликации, промотор, интересующий ген, сайт множественного клонирования, селективный маркерный ген, и, предпочтительно, вектор по настоящему изобретению включает, без ограничения, плазмидный вектор, полученный на основе pCDNA, такой как вектор X0GC.
Субъект по настоящему изобретению включает птиц, рептилий, млекопитающих и тому подобных. Предпочтительно, млекопитающее включает грызуна и примата. Предпочтительно, примат включает человека.
Объем заболеваний, охваченных в настоящем изобретении, включает, без ограничения, воспаления, аутоиммунные заболевания, предпочтительно, заболевание выбрано из группы, состоящей из ревматоидного артрита, остеоартрита, псориатического артрита, анкилозирующего спондилита, подагрического артрита, ювенильного ревматоидного артрита, гнойного артрита, псориаза, сахарного диабета I типа, рассеянного склероза, аутоиммунного энцефаломиелита, болезни Крона, системного васкулита, дерматомиозита, смешанного заболевания соединительной ткани, системной красной волчанки, идиопатической тромбоцитопенической пурпуры, первичного синдрома Шегрена, гломерулонефрита, подагры, отторжения трансплантата, астмы или атеросклероза, более предпочтительно, заболевание выбрано из группы, состоящей из ревматоидного артрита, остеоартрита, псориатического артрита, подагрического артрита, ювенильного ревматоидного артрита, гнойного артрита.
Фармацевтически приемлемый носитель означает фармацевтический носитель, обычно используемый в фармацевтической области, например разбавители, эксципиенты, вода и тому подобное, наполнители, такие как крахмал, сахароза, лактоза, микрокристаллическая целлюлоза и тому подобное; связывающие вещества, такие как производные целлюлозы, альгинаты, желатин и поливинилпирролидон; увлажнители, такие как глицерин; разрыхлители, такие как карбоксиметилкрахмал натрия, гидроксипропилцеллюлоза, кроскармеллоза, агар, карбонат кальция и гидрокарбонат натрия и тому подобное; усилители абсорбции, такие как четвертичные аммониевые соединения; поверхностно-активные вещества, такие как цетанол, лаурилсульфат натрия и тому подобное; адсорбирующие носители, такие как каолинит и бентонит; смазывающие вещества, такие как тальк, стеарат кальция и магния, аэросил, полиэтиленгликоль и тому подобное. В композицию также могут быть добавлены другие адъюванты, такие как ароматизаторы, подсластители и тому подобное.
Изобретение далее будет дополнительно проиллюстрировано со ссылкой на следующие не ограничивающие объем изобретения примеры. Специалистам в данной области техники понятно, что могут быть произведены различные модификации без отклонения от сущности и объема настоящего изобретения, и такие модификации также включены в объем настоящего изобретения.
Если не указано иное, то все следующие экспериментальные способы представляют собой обычные способы, и используемые экспериментальные материалы, если не указано иное, легкодоступны от коммерческих компаний. Все различные антитела, используемые в следующих примерах по настоящему изобретению, представляют собой стандартные антитела, имеющиеся в продаже.
Примеры
Пример 1. Конструирование вектора для молекулы гетеродимерного антитела против TNFα/против IL-17A
Конструировали экспрессионные векторы X0GC, включающие тяжелые и легкие цепи антитела против человеческого TNFα (Adalimumab), соответственно. Последовательности вариабельных областей антитела получены из https://www.drugbank.ca/drugs/DB00051. Нуклеотидная последовательность вариабельной области легкой цепи представлена в SEQ ID NO: 1, и ее аминокислотная последовательность представлена в SEQ ID NO: 2; нуклеотидная последовательность константной области легкой цепи представлена в SEQ ID NO: 3, и ее аминокислотная последовательность представлена в SEQ ID NO: 4; нуклеотидная последовательность вариабельной области тяжелой цепи представлена в SEQ ID NO: 5, и ее аминокислотная последовательность представлена в SEQ ID NO: 6; нуклеотидная последовательность константной области тяжелой цепи представлена в SEQ ID NO: 7, и ее аминокислотная последовательность представлена в SEQ ID NO: 8. Вариабельную область и константную область легкой цепи и вариабельную область и константную область тяжелой цепи амплифицировали посредством PCR (полимеразной цепной реакции). Во всех реакциях PCR в соответствии с настоящим описанием использовали сверхточную ДНК-полимеразу Phusion super-fidelity DNA polymerase (F-530L) от NEB Inc. Праймеры PCR конструировали обычным образом в соответствии с принципом комплементарности оснований и потребностью в сайтах разрезания ферментами рестрикции. Каждая реакционная система состоит из 8,9 мкл Н2О, 4 мкл 5× буфера для сверхточной ДНК-полимеразы Phusion super-fidelity DNA polymerase, 4 мкл 1 мМ dNTP (дезоксирибонуклеотидтрифосфаты), 1 мкл прямого праймера, 1 мкл обратного праймера, 0,1 мкл сверхвысокоточной ДНК-полимеразы Phusion super-fidelity DNA, 1 мкл матрицы. Продукты PCR вариабельной и константной областей подвергали электрофорезу в 1,5% агарозном геле, и соответствующие фрагменты выделяли с использованием набора для выделения ДНК DNA recovery kit (Promega, А9282, его же применяют далее). Выделенный фрагмент вариабельной области и фрагмент константной области использовали в качестве матриц, и прямой праймер вариабельной области и обратный праймер константной области использовали для осуществления следующего раунда PCR. Затем соответствующие фрагменты выделяли с получением полноразмерных фрагментов тяжелой цепи и легкой цепи. Вектор X0GC и полноразмерные фрагменты подвергали ферментативному разрушению при помощи EcoRI (NEB, cat#R3101L) и HindIII (NEB, cat#R3104L). Условия для ферментативного разрушения состоят из 2 мкл 10×буфера 3, 0,5 мкл каждого из EcoRI и HindIII, 3 мкл полноразмерных фрагментов, выделенных из геля, и 14,5 мкл Н2О. Систему разрушения оставляли при 37°С в течение 3 часов. Продукты разрушения лигировали с использованием Т4 ДНК-лигазы (NEB, cat#M0202V) (ее же применяют далее), и условия реакции состоят из 2 мкл 10×буфера для лигазы, 0,5 мкл лигазы, 3 мкл полноразмерных фрагментов, выделенных из геля, 3 мкл вектора X0GC, выделенного из геля, 11,5 мкл Н2О, лигирование осуществляли при комнатной температуре в течение 12 часов. Продукт лигирования трансформировали в компетентные клетки E.coli DH5α (Tiangen, СВ 104, их же применяют далее). Экспрессионные векторы X0GC, содержащие тяжелые и легкие цепи антитела, получали для экспрессии тяжелых и легких цепей антитела в эукариотических клетках, соответственно.
Конструировали экспрессионные векторы X0GC, содержащие тяжелые и легкие цепи антитела против человеческого IL-17A (BJHM), соответственно. Последовательности вариабельных областей антитела получены из заявки на патент WO 2018050028. Нуклеотидная последовательность вариабельной области легкой цепи представлена в SEQ ID NO: 9, и ее аминокислотная последовательность представлена в SEQ ID NO: 10; нуклеотидная последовательность константной области легкой цепи представлена в SEQ ID NO: 3, и ее аминокислотная последовательность представлена в SEQ ID NO: 4; нуклеотидная последовательность вариабельной области тяжелой цепи представлена в SEQ ID NO: 11, и ее аминокислотная последовательность представлена в SEQ ID NO: 12; нуклеотидная последовательность константной области тяжелой цепи представлена в SEQ ID NO:13, и ее аминокислотная последовательность представлена в SEQ ID NO: 14. Экспрессионные векторы X0GC, содержащие тяжелые и легкие цепи антитела, получали для экспрессии тяжелой и легкой цепей антитела в эукариотических клетках, соответственно.
Пример 2. Экспрессия молекулы гетеродимерного антитела против TNFα/против IL-17A
Экспрессионные векторы, содержащие тяжелые и легкие цепи антитела против человеческого или против мышиного TNFα, трансфицировали в клетки ExpiCHO (ExpiHO™ Cells, кат #А29127, invitrogen), соответственно, и экспрессионные векторы, содержащие тяжелые и легкие цепи антитела против человеческого или против мышиного IL-17A, также трансфицировали в клетки ExpiCHO, соответственно. За одни сутки до трансфекции клетки засевали с плотностью 3,5×106 клеток/мл. В день трансфекции клетки разбавляли свежей средой для экспрессии ExpiCHO (ExpiHO™ Expression Medium, кат #A29100-01, invitrogen) до конечной плотности 6×106 клеток/мл. Плазмиды отбирали в соответствии с трансфицируемым объемом до конечной концентрации 0,5 мкг/мл, и плазмиды разбавляли до 4% от трансфицируемого объема с использованием среды OptiPRO™ SFM (OptiPRO™ SFM, кат #12309-019, invitrogen), и гомогенно перемешивали путем переворачивания. Отбирали реактив для трансфекции ExpiFectamine™ transfection reagent (ExpiFectamine™CHO Transfection Kit, кат #A29129, invitrogen) в количестве 6,4 кратном относительно объема плазмиды и разбавляли до 4% от объема трансфекции с использованием среды OptiPRO™SFM, и гомогенно перемешивали путем переворачивания. К разбавленным плазмидам добавляли разбавленный реактив для трансфекции и смесь осторожно перемешивали, и оставляли при комнатной температуре в течение 1-5 минут, и медленно по каплям добавляли к клеткам. Затем клетки помещали в инкубатор для клеток (концентрация СО2: 8%) при 37°С в течение 20 часов на шейкере при 120 об/мин. К клеткам по каплям медленно добавляли 0,006 крат относительно объема трансфекции ExpiCHO™ Enhancer (ExpiFectamine™CHO Transfection Kit, кат #A29129, invitrogen) и 0,24 крат относительно объема трансфекции ExpiCHO™Feed (ExpiCHO™Feed, кат #А29101-02, invitrogen). Инкубирование осуществляли на шейкере при 120 об/мин при 32°С. Супернатанты клеточной культуры, трансфицированные в течение 10 суток, собирали путем центрифугирования.
Уровни экспрессии определяли при помощи анализа ELISA (твердофазный иммуноферментный анализ). Перед очисткой с использованием хроматографической колонки осадок удаляли путем фильтрования через мембрану для фильтрования 0,2 мкм. Эту процедуру осуществляли при 4°С.
Пример 3. Очистка продукта экспрессии молекулы гетеродимерного антитела против TNFα/против IL-17A
Очистку осуществляли при комнатной температуре с использованием системы очистки белка AKTA explorer type 100 (GE Healthcare) и колонки для аффинной хроматографии Mabselect SuRe (16 мм в.д., 27 мл, GE Healthcare). Колонку сначала уравновешивали подвижной фазой А (20 мМ буфер фосфата натрия, рН 7,4). После стабилизации базовой линии супернатанты клеток, обработанные выше, наносили при скорости потока 5 мл/мин. После нанесения уравновешивание осуществляли с использованием подвижной фазы А. Образцы представляли собой продукты экспрессии антител против TNFα и продукты экспрессии антител против IL-17A, описанные в Примере 2, соответственно. Затем подвижную фазу В1 (подвижная фаза А, содержащая 1М хлорид натрия) сначала использовали для элюирования 3 объемов колонки и затем раствор для уравновешивания А (20 мМ буфер фосфата натрия, рН 7,4) использовали для промывания одного объема колонки; наконец, подвижную фазу В2 (100 мМ глицин, 10 мМ хлорид натрия, рН 3,3) использовали для элюирования 5 объемов колонки для сбора пика элюции, то есть пика интересующего белка; скорость потока во время описанных выше стадий элюирования всегда составляла 5 мл/мин. Хроматограмма пика элюции антитела против TNFα представлена на Фиг. 1 А, и хроматограмма пика элюции антитела против IL-17A представлена на Фиг. 1 В. Указанные пики элюции (представленные серой областью) собирали, и рН корректировали до 7,0 путем добавления по каплям 1М раствора Tris.
Пример 4. Очистка молекулы гетеродимерного антитела против TNFα/против IL-17A
Структура молекулы гетеродимерного антитела против TNFα/против IL-17A проиллюстрирована на Фиг. 2.
Продукты экспрессии антитела против TNFα и против IL-17A, полученные в Примере 3 выше путем очистки на колонке Mabselect SuRe (16 мм в.д., 27 мл, GE Healthcare), подвергали восстановлению in vitro с получением гетеродимера. Во-первых, белковые растворы, очищенные и собранные выше, концентрировали путем ультрафильтрования в пробирку для концентрирования путем ультрафильтрования (номинально отсекаемая молекулярная масса 10 кДа) и раствор заменяли на забуференный фосфатом физиологический раствор (PBS) (рН=7,4). Полученные продукты экспрессии против TNFα и против IL-17A доводили до 1 мг/мл путем добавления PBS и добавляли 1/200 крат относительно конечного объема 1М DTT (дитиотреитол) таким образом, что конечная концентрация DTT составила 5 мМ, соответственно. Восстановление осуществляли при 4°С (3-8 часов), и дисульфидные связи открывались в процессе восстановления, а дисульфидные связи шарнирных областей небольшого количества гомодимерных молекул антитела, содержащихся в продуктах экспрессии антител против TNFα и против IL-17A, также открывались, таким образом, образуя половину молекулы антитела, содержащую одну тяжелую цепь и одну легкую цепь, структура которой проиллюстрирована на Фиг. 3. Восстановленные образцы анализировали посредством SEC-HPLC (гель-фильтрационная высокоэффективная жидкостная хроматография), содержащей восстановитель 1 мМ DTT в буфере подвижной фазы. Результаты представлены на Фиг. 4А и Фиг. 4В. Все массовые отношения гомодимерных молекул антител против TNFα и против IL-17A составляли менее 10%. В соответствии с этим, массовые отношения всех молекул половины антитела составляли более 90%.
Затем восстановленные молекулы антитела против TNFα и против IL-17A смешивали в эквимолярном отношении, и реакцию рестрикции осуществляли в течение 24 часов при 4°С. Во время рестрикции молекулы половины антитела против TNFα и против IL-17A образовывали гетеродимерное биспецифическое антитело, содержащее молекулы половины антител как против TNFα, так и против IL-17A, посредством нековалентного взаимодействия между СН2/СН3. Затем белковый раствор концентрировали путем ультрафильтрования в пробирку для концентрирования путем ультрафильтрования (номинальная отсекаемая молекулярная масса 10 кДа), и раствор заменяли на фосфатный раствор (PBS, рН=7,4) для прекращения восстановления. Этот раствор подвергали окислению на воздухе или при помощи окислителя для обеспечения возможности образования дисульфидных связей в гетеродимерном биспецифическом антителе. Реакции окисления были следующими: добавляли 100 мМ L-дегидроаскорбиновой кислоты в качестве окислителя, и конечная концентрация белка составляла 1 мг/мл, и конечная концентрация окислителя составляла 1 мМ, и окисление осуществляли при 4°С в течение 24 часов. Образец, полученный посредством указанной выше реакции окисления, подвергали анализу путем капиллярного электрофореза, и результаты представлены на Фиг. 5.
Гетеродимерные молекулы, полученные посредством указанных выше процессов восстановления/окисления молекул половины антитела против TNFα и против IL-17A, концентрировали путем ультрафильтрования в пробирку для концентрирования путем ультрафильтрования (номинальная отсекаемая молекулярная масса 10 кДа), и раствор заменяли на 10 мМ буфер фосфата натрия (рН 5,8). Очистку осуществляли при 4°С с использованием системы очистки белка AKTA explorer type 100 (GE Healthcare) и колонки для ионной хроматографии Source 15S (10 мм в.д., 2 мл, GE Healthcare). Во-первых, подвижную фазу А (10 мМ фосфат натрия, рН 7,0) использовали для уравновешивания хроматографической колонки. После стабилизации базовой линии обработанный выше белковый раствор наносили при скорости потока 1 мл/мин. После нанесения образца уравновешивание осуществляли с использованием подвижной фазы А. Затем 20 объемов колонки (0% В - 100% В, 80 мин, скорость потока: 0,5 мл/мин) промывали градиентом от А (10 мМ фосфат натрия, рН 5,8) до В (10 мМ фосфат натрия, рН 5,8). Основной пик элюции собирали (Фиг. 6) и собранный белковый раствор концентрировали путем ультрафильтрования в пробирку для концентрирования путем ультрафильтрования (номинальная отсекаемая молекулярная масса 10 кДа). Раствор заменяли на фосфатный раствор (PBS, рН=7,4), стерилизованный путем фильтрования и затем хранили при 4°С. Гетеродимерное антитело против человеческого TNFα/против человеческого IL-17A названо ВН1657. Очищенные продукты анализировали посредством капиллярного электрофореза, и результаты представлены на Фиг. 7. В качестве результата анализа чистоты посредством SEC-HPLC, чистота составляла 99,9%), как представлено на Фиг. 8.
Пример 5. Получение молекулы гетеродимерного антитела против мышиного TNFα/против мышиного IL-17A
В соответствии со способами, описанными в Примерах 1-4, экспрессионные векторы X0GC, содержащие тяжелые и легкие цепи антитела против мышиного TNFα (последовательности вариабельных областей тяжелых и легких цепей клонировали из клеток гибридомы V1q, секретирующих крысиное антитело против мышиного TNFα (Echtenacher et al., J. Immunol. 145: 3762-3766 (1990)), и экспрессионных векторов XOGC, содержащих тяжелые и легкие цепи антитела против мышиного IL-17A (последовательности вариабельных областей тяжелых и легких цепей получены из патента США No. 7846443, ID 10) одновременно конструировали в настоящем изобретении, соответственно. Для антитела против мышиного TNFα нуклеотидная последовательность константной области легкой цепи представлена в SEQ ID NO: 3, и ее аминокислотная последовательность представлена в SEQ ID NO: 4; нуклеотидная последовательность константной области тяжелой цепи представлена в SEQ ID NO: 7, и ее аминокислотная последовательность представлена в SEQ ID NO: 8. Для антитела против мышиного IL-17A нуклеотидная последовательность вариабельной области легкой цепи представлена в SEQ ID NO: 15, и ее аминокислотная последовательность представлена в SEQ ID NO: 16; нуклеотидная последовательность константной области легкой цепи представлена в SEQ ID NO: 3, и ее аминокислотная последовательность представлена в SEQ ID NO: 4; и нуклеотидная последовательность вариабельной области тяжелой цепи представлена в SEQ ID NO: 17, и ее аминокислотная последовательность представлена в SEQ ID NO: 18; нуклеотидная последовательность константной области тяжелой цепи представлена в SEQ ID NO: 13, и ее аминокислотная последовательность представлена в SEQ ID NO: 14. Затем получали экспрессионные векторы X0GC, содержащие тяжелые и легкие цепи этих антител, и использовали для экспрессии тяжелых и легких цепей антител в эукариотических клетках, соответственно. Затем путем экспрессии/очистки получали гетеродимерное антитело против мышиного TNFα/против мышиного IL-17A, обозначенное ВН1654, имеющее чистоту, близкую к чистоте ВН1657 (данные не представлены).
Пример 6. Стабильность молекулы гетеродимерного антитела против TNFα/против IL-17A
Хорошо закрытый образец 1 мг/мл гетеродимерного антитела против TNFα/против IL-17A (ВН1657), полученный в Примере 4, помещали в термостат при 40°С (инкубатор Boxun Biochemical BSP-400). 10 мкг образца отбирали в соответствующие моменты времени (базовый (0 неделя), 1 неделя, 4 неделя, 6 неделя, 8 неделя) для гель-фильтрационной высокоэффективной жидкостной хроматографии (SEC-HPLC). Условия для вышеприведенной SEC-HPLC были следующими: (1) колонка для гель-фильтрации: waters xbridge ВНЕ200 3,5 мкм, 7,8 мм×30 см; (2) подвижная фаза: 0,1М РВ рН 6,7+0,1 М Na2SO4, рН 6,7; (3) скорость потока: 0,6 мл/мин; (4) длина волны для ультрафиолетового выявления: 280 нм; (5) время регистрации: 40 мин. Используемый прибор представлял собой хроматограф Agilent 1200 Infinity, хроматограмму регистрировали с использованием Agilent ChemStation и рассчитывали отношение оставшихся мономеров. Как представлено в Таблице 1, доля основного пика демонстрировала небольшое изменение при экспериментальных условиях 40°С, таким образом, сделали заключение, что гетеродимерное антитело против TNFα/против IL-17A обладает более хорошей температурной стабильностью.
Пример 7. Активность связывания с мишенью гетеродимерного антитела против TNFα/против IL-17A
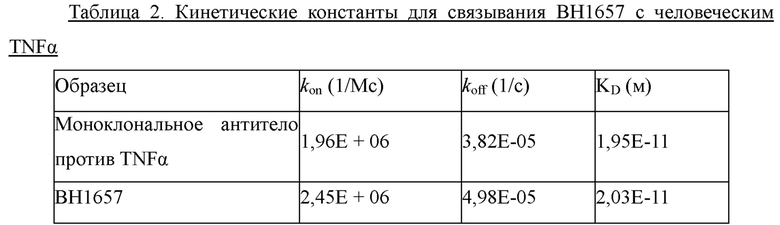
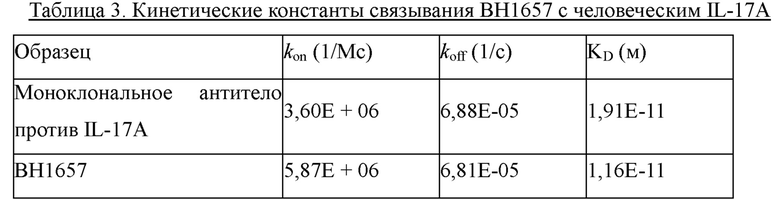
Кинетические константы ассоциации гетеродимерного антитела против TNFα/против IL-17A (ВН1657) с его антигенами TNFα и IL-17A определяли с использованием прибора Biacore X100. В приборе использовалась оптическая технология поверхностного плазмонного резонанса для выявления ассоциации и диссоциации между связанными с биочипом молекулами, которыми он покрыт, и молекулами, подлежащими выявлению. Основной используемый расходный материал представлял собой чип Protein A (GE Healthcare, 29-1275-57). Экспериментальная процедура кратко описана следующим образом: образцы ВН1657 и контрольные образцы (моноклональное антитело против TNFα и моноклональное антитело против IL-17A), человеческий TNFα и человеческий IL-17A разводили соответственно в 1×HBS-EP + раствор (10 мМ HEPES, 150 мМ NaCl, 3 мМ EDTA, 0,05% поверхностно-активное вещество Р20, рН 7,4). Во время фазы захвата-связывания 1 мкг/мл образца ВН1657 или контрольного образца инжектировали со скоростью 10 мкл/мин в течение 60 секунд; во время фазы связывания различные концентрации человеческого TNFα и растворителя в качестве контроля (1×HBS-EP + раствор) соответственно инжектировали со скоростью 30 мкл/мин в течение 120 секунд, или различные концентрации человеческого IL-17А и растворителя в качестве контроля инжектировали со скоростью 30 мкл/мин в течение 60 секунд, соответственно; во время фазы диссоциации 1×HBS-EP + раствор инжектировали со скоростью 10 мкл/мин в течение 1800 секунд. Условия регенерации представляли собой 10 мМ раствор соли глицина, рН 1,5. Кинетические константы ассоциации и кинетические константы диссоциации аналитически рассчитывали с использованием контрольного программного обеспечения Biacore Х100.
Кинетические константы ассоциации, кинетические константы диссоциации и равновесные константы диссоциации для ВН1657, человеческого TNFα и человеческого IL-17A представлены в Таблицах 2 и 3, соответственно. Результаты демонстрируют, что гетеродимер против TNFα/против IL-17A сохраняет антигенсвязывающую активность, согласующуюся с активностью родительского моноклонального антитела.
Связывающую способность гетеродимерного антитела ВН1657 против TNFα/против IL-17A в отношении одиночного антигена различных видов определяли при помощи твердофазного иммуноферментного анализа (ELISA).
Подробные процедуры представляют собой следующие: рекомбинантный человеческий TNFα, обезьяний TNFα, человеческий IL-17A или обезьяний IL-17A (все приобретены в Sino Biological, P.R. China) наносили на лунки 96-луночного планшета для ELISA с высокой адсорбцией с использованием карбонатного буферного раствора с рН 9,6 с покрывающей концентрацией 1 мкг/мл, 100 мкл на лунку. Покрывание осуществляли при 4°С в течение ночи. Планшет 5 раз промывали PBST (физиологическим раствором, забуференным фосфатом, с твином). Лунки блокировали 300 мкл на лунку PBST, содержащим 1% BSA (бычий сывороточный альбумин), и инкубировали в течение 1 часа при 25°С и 5 раз промывали PBST. Образцы ВН1657 (последовательно разбавленные PBST, содержащим 1% BSA) и контроль добавляли в количестве 100 мкл на лунку и инкубировали при 25°С в течение 1 часа. Лунки 5 раз промывали PBST. Затем меченное пероксидазой хрена антитело против человеческого IgG (Chemicon, кат. #АР309Р), разбавленное 1:10000 в PBST, содержащем 1% BS (бычью сыворотку) добавляли в количестве 100 мкл на лунку, и инкубировали при 25°С в течение 1 часа. Лунки 5 раз промывали PBST. Хромогенный субстрат ТМВ (тетраметилбензидин) добавляли в количестве 100 мкл на лунку и давали развиться окрашиванию в течение 10 минут при комнатной температуре. Развитие окрашивания останавливали путем добавления 1М H2SO4 в количестве 100 мкл на лунку. Поглощение при 450 нм считывали на ридере для микропланшетов.
Способности ВН1657 связываться с TNFα различных видов и IL-17A различных видов представлены в Таблице 4. Гетеродимер против TNFα/против IL-17A обладает хорошими связывающими способностями с человеческим TNFα, обезьяньим TNFα, человеческим IL-17A и обезьяньим IL-17A, и демонстрирует активности, похожие на активности родительских моноклональных антител.


Пример 8. Нейтрализующая активность гетеродимерного антитела против TNFα/против IL-17A in vitro
Человеческий фибробласт крайней плоти HFF-1 может секретировать серии цитокинов и хемокинов после стимулирования TNFα или IL-17A, и используется для измерения нейтрализующей активности гетеродимерного антитела против TNFα/против IL-17A BH1657 в отношении его мишеней.
Нейтрализующая TNFα активность: образец ВН1657 и контрольный образец последовательно разбавляли в полной среде DMEM (среда Игла, модифицированная Дульбекко) (GIBCO, кат. #11995-073), содержащей 15% FBS (фетальная бычья сыворотка) (Hyclone, кат. #SH 30084.03) в количестве 50 мкл на лунку и добавляли в планшет для клеточной культуры. Человеческий TNFα в концентрации 2 нг/мл (конечная концентрация 0,5 нг/мл), разбавленный в той же самой полной среде, затем добавляли в планшет для клеточной культуры в количестве 50 мкл на лунку и инкубировали в течение 1 часа при 37°С в инкубаторе в атмосфере 5% СО2. Клетки HFF-1 (АТСС (Американская коллекция типовых культур), кат. #SCRC-1041) затем ресуспендировали в полной среде и высевали в лунки 96-луночного планшета для клеточной культуры с плотностью 5000 клеток на лунку в количестве 100 мкл на лунку. Клетки инкубировали в течение 24 часов при 37°С в инкубаторе в атмосфере 5% CO2. После инкубирования планшет для клеточной культуры центрифугировали при 250 g в течение 5 минут, отбирали культуральный супернатант и измеряли уровень человеческого IL-6 с использованием набора ELISA для анализа человеческого IL-6 (R & D systems, продукт # S6050) в соответствии с его инструкциями. Как показано на Фиг. 9А, ВН1657 существенно ингибировал вызванную TNFα секрецию IL-6, демонстрируя хорошую нейтрализующую TNFα активность, несколько более слабую, чем активность бивалентного родительского моноклонального антитела против TNFα.
Нейтрализующая IL-17A активность: образец ВН1657 и контрольный образец последовательно разбавляли в полной среде DMEM (GIBCO, кат. #11995-073), содержащей 15% FBS (Hyclone, кат. #SH 30084.03) в количестве 50 мкл на лунку и добавляли в планшет для клеточной культуры. Человеческий IL-17A в концентрации 20 нг/мл (конечная концентрация 5 нг/мл), разбавленный в той же самой полной среде, затем добавляли в планшет для клеточной культуры в количестве 50 мкл на лунку и инкубировали в течение 1 часа при 37°С в инкубаторе в атмосфере 5% CO2. Клетки HFF-1 затем ресуспендировали в полной среде и высевали в лунки 96-луночного планшета для клеточной культуры с плотностью 5000 клеток на лунку в количестве 100 мкл на лунку. Клетки инкубировали в течение 24 часов при 37°С в инкубаторе в атмосфере 5% CO2. После инкубирования планшет для клеточной культуры центрифугировали при 250g в течение 5 минут, отбирали культуральный супернатант и измеряли уровень человеческого IL-6 с использованием набора ELISA для анализа человеческого IL-6 (R&D systems, продукт # S6050) в соответствии с его инструкциями. Как показано на Фиг. 9В, ВН1657 значительно ингибировал вызванную IL-17A секрецию IL-6, демонстрируя хорошую активность, нейтрализующую IL-17A, несколько более слабую, чем активность его бивалентного родительского моноклонального антитела против IL-17A.
TNFα и IL-17A имеют синергический эффект в отношении клеток HFF-1. Определение нейтрализующей активности в присутствии как TNFα, так и IL-17A: образец ВН1657 и контрольный образец последовательно разбавляли в полной среде DMEM (GIBCO, кат. #11995-073), содержащей 15% FBS (Hyclone, кат. #SH30084.03) в количестве 50 мкл на лунку, и добавляли в планшет для клеточной культуры. Человеческий TNFα в концентрации 2 нг/мл (конечная концентрация 0,5 нг/мл) и человеческий IL-17A в концентрации 10 нг/мл (конечная концентрация 2,5 нг/мл), разбавленные в той же самой полной среде, добавляли в лунки планшета для клеточной культуры, 50 мкл на лунку, и инкубировали в течение 1 часа при 37°С в инкубаторе в атмосфере 5% СО2. Клетки HFF-1 затем ресуспендировали в полной среде и высевали в лунки 96-луночного планшета для клеточной культуры с плотностью 5000 клеток на лунку в количестве 100 мкл на лунку. Клетки инкубировали в течение 24 часов при 37°С в инкубаторе в атмосфере 5% СО2. После инкубирования планшет для клеточной культуры центрифугировали при 250g в течение 5 минут, отбирали культуральный супернатант и измеряли уровень человеческого IL-6 с использованием набора ELISA для анализа человеческого IL-6 (R&D systems, продукт # S6050) в соответствии с его инструкциями. Как показано на Фиг. 9С, ВН1657 значительно ингибировал синергически индуцированную TNFα и IL-17A секрецию IL-6 в отношении HFF-1 и даже демонстрировал полное ингибирование IL-6 при высоких концентрациях, превосходящее ингибирование для бивалентного родительского моноклонального антитела.
Пример 9. Активность против TNFα гетеродимерного антитела против TNFα/против IL-17A зависит от присутствия или отсутствия IL-17A
Эффекты IL-17A в отношении блокирующей TNFα/TNFR2 активности гетеродимерного антитела против TNFα/против IL-17A ВН1657 определяли посредством ELISA. Подробные процедуры представляли собой следующие: рекомбинантный человеческий TNFα (приобретенный в Sino Biological, P.R. China) наносили на лунки 96-луночного планшета для ELISA с высокой адсорбцией с использованием карбонатного буферного раствора с рН 9,6 с покрывающей концентрацией 1 мкг/мл в количестве 100 мкл на нунку. Покрывание осуществляли при 4°С в течение ночи. Лунки 5 раз промывали PBST. Лунки блокировали 300 мкл на лунку PBST, содержащим 1% BSA, и инкубировали в течение 1 часа при 25°С и 5 раз промывали PBST. Добавляли образцы ВН1657 (последовательно разбавленные PBST, содержащим 1% BSA) и контроль 25 мкл, человеческий IL-17А (приобретенный в Sino Biological, P.R. China) 25 мкл (16 мкл/мл, конечная концентрация 4 мкг/мл), меченный биотином TNFR2-Fc (приобретенный в Sino Biological, P.R. China) 50 мкл (0,3 мкг/мл, конечная концентрация 0,15 мкг/мл) и инкубировали при 25°С в течение 1 часа. Лунки 5 раз промывали PBST. Затем меченный пероксидазой хрена стрептавидин (BD, кат. #554066), разбавленный 1:10000 в PBST, содержащем 1% BSA, добавляли в количестве 100 мкл на лунку и инкубировали при 25°С в течение 1 часа. Лунки 5 раз промывали PBST. Хромогенный субстрат ТМВ добавляли в количестве 100 мкл на лунку и давали развиться окрашиванию в течение 10 минут при комнатной температуре. Развитие окрашивания останавливали путем добавления 1М H2SO4 в количестве 100 мкл на лунку. Поглощение при 450 нм считывали на ридере для микропланшетов. Как показано на Фиг. 10А, в отсутствие IL-17А блокирующая TNFα/TNFR2 активность уменьшалась по сравнению с родительским моноклональным антителом; в присутствии IL-17A указанная активность увеличивалась по сравнению с активностью родительского моноклонального антитела. IL-17A не оказывал влияния на блокирующую TNFα/TNFR2 активность родительского моноклонального антитела против TNFα.
Эффект IL-17A в отношении нейтрализующей TNFα активности гетеродимерного антитела против TNFα/против IL-17A ВН1657 определяли с использованием клеток L-929 (приобретенных в Basic Medical Cell Center, the Institute of Basic Medical Sciences, Chinese Academy of Medical Sciences). Подробные процедуры представляли собой следующие: полная среда для клеток L-929 представляла собой среду MEM (GIBCO, кат. #10370-021), содержащую 10% FBS (Hyclone, кат. #SH 30084.03). Клетки L-929 ресуспендировали в полной среде и высевали в лунки 96-луночного планшета для клеточной культуры с плотностью 15000 клеток на лунку в количестве 100 мкл на лунку. Клетки инкубировали в течение ночи при 37°С в инкубаторе в атмосфере 5% СО2. Культуральный супернатант отбирали и образец ВН1657 и контрольный образец последовательно разбавляли в полной среде, содержащей 2 нг/мл человеческого TNFα и 1 мкг/мл актиномицина D, 100 мкл на лунку, и добавляли в лунки планшета для клеточной культуры. Клетки инкубировали в течение еще 24 часов при 37°С в инкубаторе в атмосфере 5% СО2. По окончании инкубирования в каждую лунку планшета для клеточной культуры для измерения жизнеспособности клеток добавляли 20 мкл MTS (CellTiter 96 Aqueous One Solution, Promega, кат. #G358B). Результаты представлены на Фиг. 10 В. Нейтрализующая TNFα активность части против TNFα гетеродимерного биспецифического антитела против TNFα/против IL-17A значительно увеличивалась в присутствии IL-17A по сравнению с отсутствием IL-17A. Эта разница в активности биспецифического антитела против TNFα/против IL-17А свидетельствует о его более сильной нейтрализующей TNFα активности в фокальном сайте с высокими уровнями IL-17A, тогда как оно демонстрирует более слабую нейтрализующую TNFα активность в системе кровообращения с низкими уровнями IL-17А, таким образом, свидетельствуя о том, что биспецифическое антитело может эффективно лечить заболевания при сохранении низких токсических и побочных эффектов.
Пример 10. Нейтрализующая активность in vivo гетеродимерного антитела против TNFα/против IL-17A
Самок мышей BALB/c в возрасте 6-8 недель, приобретенных в Beijing HFK Bioscience, Co., Ltd., использовали в качестве экспериментального материала. После одной недели, в течение которой мыши акклиматизировались к окружающей среде, их произвольным образом разделяли на группы, где каждая группа содержала по 6 мышей. Каждой группе путем внутривенной инъекции разовой дозы вводили гетеродимерное антитело против TNFα/IL-17A ВН1657, моноклональное антитело против TNFα, моноклональное антитело против IL-17A и комбинацию моноклонального антитела против TNFα и моноклонального антитела против IL-17A при трех уровнях доз (0,1 мг/кг, 1 мг/кг, 10 мг/кг для моноклональных антител, 0,2 мг/кг, 2 мг/кг, 20 мг/кг для биспецифического антитела), соответственно. Через час после введения подкожно инъецировали человеческий TNFα и IL-17A, 0,2 мкг TNFα и 20 мкг IL-17A на мышь. Через 2 часа кровь отбирали из глазной орбиты без антикоагуляции и образец крови оставляли при комнатной температуре в течение от 30 минут до 1 часа. После сворачивания образец крови центрифугировали при 3000 об./мин в течение 10 минут для получения образца сыворотки крови. Концентрацию мышиного CXCL1 в сыворотке крови определяли с использованием набора ELISA mouse CXCL1 ELISA kit (RayBiotech, кат. #ELM-KC) в соответствии с его инструкциями.
Как показано на Фиг. 11, ВН1657 значительно ингибировало синергически стимулируемую TNFα и IL-17A секрецию CXCL1 у мышей и даже демонстрировало полное ингибирование CXCL1 при высоких концентрациях, которое было более сильным, чем ингибирование его бивалентным родительским моноклональным антителом.
Пример 11. Активность связывания с мишенью гетеродимерного антитела против мышиного TNFα/против мышиного IL-17A
Связывающие способности гетеродимерного антитела против мышиного TNFα/против мышиного IL-17A (то есть ВН1654) с одним антигеном различных видов определяли посредством твердофазного иммуноферментного анализа (ELISA). Подробные процедуры представляли собой следующие: рекомбинантный мышиный TNFα, крысиный TNFα, мышиный IL-17A и крысиный IL-17A (все приобретены в Sino Biological, P.R. China) наносили на лунки 96-луночного планшета для ELISA с высокой адсорбцией с использованием карбонатного буферного раствора с рН 9,6 с покрывающей концентрацией 1 мкг/мл и с покрывающим количеством 100 мкл на лунку. Покрывание осуществляли при 4°С в течение ночи. Планшет 5 раз промывали PBST. Лунки блокировали 300 мкл на лунку PBST, содержащим 1% BSA, и инкубировали в течение 1 часа при 25°С и 5 раз промывали PBST. Образцы ВН1654 (последовательно разбавленные PBST, содержащим 1% BSA) и контроли (mAb против мышиного TNFα и mAb против мышиного IL-17A), добавляли в количестве 100 мкл на лунку и инкубировали при 25°С в течение 1 часа. Лунки 5 раз промывали PBST. Затем меченное пероксидазой хрена антитело против человеческого IgG (Chemicon, кат. #АР309Р), разбавленное 1:10000 в PBST, содержащем 1% BSA, добавляли в количестве 100 мкл на лунку и инкубировали при 25°С в течение 1 часа. Лунки 5 раз промывали PBST. Хромогенный субстрат ТМВ добавляли в количестве 100 мкл на лунку и давали развиться окрашиванию в течение 10 минут при комнатной температуре. Развитие окрашивания останавливали путем добавления 1М H2SO4 в количестве 100 мкл на лунку. Поглощение при 450 нм считывали на ридере для микропланшетов.
Способности ВН1654 связываться с TNFα различных видов и IL-17A различных видов представлены в таблице 5. Гетеродимер против мышиного TNFα/против мышиного IL-17A обладает хорошими связывающими способностями с мышиным TNFα и мышиным IL-17A, и имеет активности, похожие на активности родительских моноклональных антител. Он не связывается с крысиным TNFα и слабо связывается с крысиным IL-17А.

Пример 12. Фармакодинамические исследования гетеродимерного антитела против мышиного TNFα/против мышиного IL-17A в модели индуцированного коллагеном II типа мышиного артрита (mCIA)
Модель мышиного CIA лучшим образом имитирует ревматоидные заболевания у людей и предупреждает лечебный эффект лекарственного средства в отношении ревматоидных заболеваний у людей, и широко применяется для исследования патогенеза ревматоидного артрита и скрининга терапевтических лекарственных средств. Самцов мышей DBA1/J в возрасте 8 недель (приобретенных в Shanghai SLAC Laboratory Animal Co., Ltd) отбирали в качестве экспериментальных животных. Животных адаптировали к условиям окружающей среды в течение недели. Затем 5 мышей произвольным образом отбирали в качестве мышей "наивных" контрольных мышей и оставшихся использовали для построения модели мышиного CIA. Модель CIA получали после первичных и бустерных иммунизаций. Первичную иммунизацию осуществляли путем внутрикожной инъекции в основание хвоста мыши эмульсии, образованной 70 мкг бычьего коллагена II типа (Chondrex, кат. #20022), смешанной с полным адьювантном Фрейнда (Sigma-Aldrich, кат. #F5881). Через три недели осуществляли бустерную иммунизацию. Бустерную иммунизацию осуществляли путем внутрикожной инъекции в спину мыши эмульсии, образованной 70 мкг бычьего коллагена II типа, смешанного с неполным адьювантом Фрейнда (Sigma-Aldrich, кат. #F5506). После бустерной иммунизации мышей разделяли на группы (по 8 мышей в каждой группе) после обнаружения клинических симптомов артрита, таких как покраснение и отек конечностей, обследовали задние и передние лапы мышей.
Каждой группе в мышиной модели CIA отдельно последовательно вводили следующие агенты: носитель лекарственного средства (PBS), моноклональное антитело против мышиного TNFα (70 нмоль/кг), моноклональное антитело против мышиного IL-17А (70 нмоль/кг), комбинацию моноклонального антитела против мышиного TNFα и моноклонального антитела против мышиного IL-17A (70 нмоль/кг + 70 нмоль/кг), и гетеродимерного антитела против мышиного TNFα/против мышиного IL-17A ВН1654 (70 нмоль/кг, 140 нмоль/кг) один раз через сутки путем внутрибрюшинной инъекции в общей сложности 7 раз. После введения массу тела определяли один раз через сутки, регистрировали патологические изменения в четырех лапах, и оценивали тяжесть артрита: 0 - отсутствие наблюдаемого покраснения и отека, 1 - эритема и легкий отек, ограничивающийся голеностопным суставом или суставом предплюсны, 2 - эритема и легкий отек от голеностопного сустава до сустава предплюсны, 3 - эритема и умеренный отек от голеностопного сустава до плюсневого сустава, 4 - эритема и тяжелый отек от голеностопа до лап, включая межфаланговые суставы, или анкилоз четырех конечностей. Всем конечностям мышей были присвоены оценки воспаления, и максимальная оценка для каждой мыши составляла 16.
Как показано на Фиг. 12, мыши из "наивной" контрольной группы не демонстрировали воспалительный ответ, значительный воспалительный ответ был обнаружен у мышей в модели в группе, которой вводили носитель, с быстрым увеличением индекса артрита. Оценки артрита у мышей в мышиной модели CIA в группе, которой вводили гетеродимерное антитело против мышиного TNFα/против мышиного IL-17A ВН1654, значительно подавлялись, демонстрируя более хороший эффект облегчения воспаления по сравнению с моноклональным антителом против TNFα и моноклональным антителом против IL-17A.
Пример 13. Фармакодинамические исследования гетеродимерного антитела против мышиного TNFα/против мышиного IL-17A в модели индуцированного глюкозо-6-фосфат изомеразой артрита у мышей (mGPI)
Модель GPI у мышей создавали путем иммунизации мышей глюкозо-6-фосфат изомеразой (GPI) или ее пептидным фрагментом 325-339 (GPI325-339) Эта модель, представляющая собой животную модель, разработанную в последние годы, может лучшим образом имитировать ревматоидные заболевания человека и подходит для исследования патогенеза ревматоидного артрита и скрининга терапевтических лекарственных средств. Самцов мышей DBA1/J в возрасте 8 недель (приобретенных в Shanghai SLAC Laboratory Animal Co., Ltd) отбирали в качестве экспериментальных животных. Мышей адаптировали к условиям окружающей среды в течение недели. Затем 5 мышей произвольным образом отбирали в качестве "наивных" контрольных мышей и оставшихся использовали для создания модели GPI у мышей. Модель GPI получали путем однократной иммунизации. Иммунизацию осуществляли путем внутрикожной инъекции в основание хвоста мыши эмульсии, образованной 100 мкг GPI325-339 (синтезированной химической группой BEIJING HANMI PHARMACEUTICAL СО., аминокислотной последовательности IWYINCFGCETHAML (SEQ ID NO: 19)), смешанной с полным адъювантом Фрейнда (Sigma-Aldrich, кат. #F5881). Коклюшный токсин (Merck, кат. #516560) внутрибрюшинно инъецировали в 1 сутки (сутки иммунизации) и 3 сутки иммунизации. В 5 сутки после иммунизации мышей произвольным образом разделяли на группы, по 8 мышей в каждой группе.
Каждой группе мышей в модели GPI профилактически вводили следующие агенты, соответственно: носитель для лекарственного средства (PBS), моноклональное антитело против мышиного TNFα (35 нмоль/кг), моноклональное антитело против мышиного IL-17A (35 нмоль/кг), комбинацию моноклонального антитела против мышиного TNFα и моноклонального антитела против мышиного IL-17A (35 нмоль/кг + 35 нмоль/кг), и гетеродимерное антитело против мышиного TNFα/против мышиного IL-17А ВН1654 (35 нмоль/кг, 70 нмоль/кг) один раз через сутки посредством внутрибрюшинной инъекции в общей сложности 7 раз. После введения определяли массу тела один раз в сутки, наблюдали патологические изменения в четырех лапах, и оценивали тяжесть артрита: 0 - отсутствие наблюдаемого покраснения и отека, 1 - эритема и легкий отек, ограничивающийся голеностопным суставом или суставом предплюсны, 2 - эритема и легкий отек от голеностопного сустава до сустава предплюсны, 3 - эритема и умеренный отек от голеностопного сустава до плюсневого сустава, 4 - эритема и тяжелый отек от голеностопа до лап, включая межфаланговые суставы, или анкилоз четырех конечностей. Всем конечностям мышей были присвоены оценки воспаления, и максимальная оценка для каждой мыши составила 16 баллов.
Как показано на Фиг. 13, мыши из "наивной" контрольной группы не демонстрировали воспалительный ответ, значительный воспалительный ответ обнаружен в мышиной модели GPI в группе, которой вводили носитель, и гетеродимерное антитело против мышиного TNFα/против мышиного IL-17A ВН1654 демонстрировало хорошие противовоспалительные эффекты при 35 нмоль/кг и 70 нмоль/кг и демонстрировало зависимость от дозы. Эффект облегчения воспаления ВН1654 был более сильным, чем таковой моноклонального антитела против мышиного TNFα и моноклонального антитела против мышиного IL-17A.
Пример 14. Фармакодинамические исследования гетеродимерного антитела против мышиного TNFα/против мышиного IL-17A в модели индуцированного зимозаном псориатрического артрита (PsA) у мышей SKG
Модель псориатрического артрита у мышей создавали путем иммунизации мышей SKG зимозаном (глюканом). Эта модель, представляющая собой животную модель, разработанную в последние годы, имитирует спондилоартрит у людей (разновидность иммунных заболеваний, включающих анкилозирующий спондилит, псориатрический артрит и тому подобное). В настоящем Примере эту модель использовали для оценки терапевтических лекарственных средств для лечения псориатрического артрита. Самок мышей SKG/Jcl в возрасте от 9 до 10 недель (приобретенных в CLEA, Japan) отбирали в качестве экспериментальных животных. Животных адаптировали к условиям окружающей среды в течение недели. Затем 4 мышей произвольным образом отбирали в качестве "наивных" контрольных мышей и оставшихся мышей использовали для создания модели PsA у мышей. Модель PsA у мышей получали путем однократной иммунизации. Иммунизацию осуществляли путем внутрибрюшинной инъекции мышам 3 мг зимозана (приобретенного в Sigma-Alrich, кат. #Z4250) в буфере PBS. В 12 сутки после иммунизации мышей произвольным образом распределяли по группам, по 8 мышей в каждой группе.
Каждой группе в мышиной модели PsA профилактически вводили следующие агенты, соответственно: носитель для лекарственного средства (PBS), моноклональное антитело против мышиного TNFα (35 нмоль/кг), моноклональное антитело против мышиного IL-17A (35 нмоль/кг), гетеродимерное антитело против мышиного TNFα/против мышиного IL-17A ВН1654 (70 нмоль/кг) два раза в неделю путем внутрибрюшинной инъекции в общей сложности 8 раз. После введения определяли массу тела дважды в неделю, наблюдали патологические изменения четырех лап и оценивали тяжесть артрита: 0 - отсутствие аномальных явлений, таких как опухание суставов или лапы. 0,1 - красные и опухшие лапы, 0,1 для одной лапы. 0,5 - легкое опухание голеностопного сустава, первое проявление возникало на латеральной стороне голеностопного сустава. 1 - явное опухание голеностопного сустава. 1,5 - оценка степени, явное опухание голеностопного сустава и тенденция распространения на лапы, и степень опухания явно была больше 1 и меньше 2. 2 - умеренное опухание голеностопного сустава, опухание распространяется на лапы, но не на суставы стопы. 2,5 - оценка степени, степень опухания значительно больше 2, но не до суставов стопы. 3 - тяжелое опухание от лодыжки до лап. Самая высокая степень тяжести опухания суставов оценивалась как 3, что, как правило, сопровождалось тяжелым опуханием лап. Эта система оценок оценивает отдельно опухание суставов и опухание лапы, причем опухание суставов накладывалась на степень опухания 0,5, а оценка для лап составляла 0,1 для лапы. Оценку образовывали как сумму оценки опухания сустава и оценки опухания лапы.
Как показано на Фиг. 14, мыши из "наивной" контрольной группы не демонстрировали воспалительный ответ, причем значительный воспалительный ответ был обнаружен в модели мышей PsA в группе, которой вводили носитель, с симптомами псориаза и псориатрического артрита, и гетеродимерное антитело против мышиного TNFα/против мышиного IL-17A ВН1654 демонстрировало хорошие противовоспалительные эффекты при 70 нмоль/кг, тогда как моноклональное антитело против мышиного TNFα и моноклональное антитело против мышиного IL-17A по существу не оказывали противовоспалительного эффекта в этой модели.
Пример 15. Индуцирующие апоптоз эффекты гетеродимерного антитела против TNFα/против IL-17A в отношении клеток, экспрессируюших трансмембранный TNFα
Апоптоз иммунных клеток, экспрессирующих трансмембранный TNFα, может быть индуцирован сигналом снаружи-внутрь, который опосредован трансмембранным TNFα, после связывания антагониста TNFα с трансмембранным TNFα, и этот апоптоз ассоциирован со сниженной защитой хозяина, вызванной антагонистом TNFα. Индуцирующий апоптоз эффект Humira® сильнее индуцирующего апоптоз эффекта Enbrel®, и риск инфекции после введения Humira® также выше, чем для Enbrel®. Этот пример относится к выявлению индуцирующего апоптоз эффекта гетеродимерного антитела против TNFα/протв IL-17A ВН1657. Конкретный процесс осуществления является следующим: в соответствии со ссылкой (Arthritis & Rheumatism, 2008, 58(5): 1248-1257), клеточную линию, экспрессирующую трансмембранный ТNFальфа, конструировали на основе клеток Jurkat (приобретенных в Basic Medical Cell Center, the Institute of Basic Medical Sciences, Chinese Academy of Medical Sciences) и названных Jurkat/tmTNFα, и культивированных в среде RPMI 1640 (GIBCO, кат. #22400-089), содержащей 10% FBS (Hyclone, кат. #SH30084.03). В сутки эксперимента клетки Jurkat/tmTNFα в экспоненциальной фазе собирали, ресуспенировали в среде RPMI 1640, содержащей 2% FBS, и высевали в лунки 12-луночного планшета для клеточной культуры, 400000 клеток на лунку, 1 мл на лунку. Тестируемые образцы последовательно разбавляли в среде RPMI 1640, содержащей 2% FBS, и добавляли в лунки 12-луночного планшета для клеточной культуры, 1 мл на лунку. После 24 часов совместного инкубирования клетки собирали и окрашивали набором для тестирования апоптоза (Sigma-Alrich, кат. #APOAF-50TST) в соответствии инструкциями в наборе. Клетки затем анализировали в отношении апоптоза посредством проточной цитометрии.
Как продемонстрировано в Таблице 6, данные свидетельствовали о том, что Humira® индуцировал более сильный апоптотический эффект в отношении клеток Jurkat/tmTNFα, возможно, вследствие того, что антитело против TNFα Humira® является бивалентным и способно перекрестно связывать различные трансмембранные TNFα, индуцируя более сильный апоптотический сигнал извне-внутрь. Тем не менее, часть против TNFα гетеродимерного антитела против TNFα/против IL-17A ВН1657 является моновалентной, и индуцирующий апоптоз эффект является более слабым и сравним с эффектом Enbrel®. Таким образом, можно сделать предположение о том, что, по сравнению с Humira®, гетеродимерные антитела против TNFα/против IL-17A могут иметь меньший ингибирующий эффект в отношении резистентности хозяина, и, таким образом, может иметь меньший риск инфекции.

--->
Перечень последовательностей
<110> BEIJING HANMI PHARMACEUTICAL CO.,
<120> ANTI-TNFα/ANTI-IL-17A NATURAL ANTIBODY STRUCTURE-LIKE
HETERODIMERIC BISPECIFIC ANTIBODY, AND PREPARATION METHOD
THEREOF
<130> LZ1805868CN01
<160> 19
<170> PatentIn version 3.3
<210> 1
<211> 321
<212> DNA
<213> artificial
<220>
<223> вариабельная область легкой цепи антитела против человеческого
TNFα
<400> 1
gacatccaga tgacccaatc cccttcctcc ctcagcgcga gcgtcggaga cagggtgaca 60
atcacctgca gggcctccca gggaatccgg aactatctcg cctggtatca gcagaagccc 120
ggcaaggccc ccaagctgct gatctacgct gccagcacac tccaatccgg cgtgccttcc 180
aggttctccg gaagcggatc cggcaccgac ttcaccctca ccatttccag cctgcagccc 240
gaagacgtcg ccacctacta ctgccagcgg tacaacaggg ccccctacac cttcggccaa 300
ggcaccaagg tcgagatcaa g 321
<210> 2
<211> 107
<212> PRT
<213> artificial
<220>
<223> вариабельная область легкой цепи антитела против человеческого
TNFα
<400> 2
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Gln Arg Tyr Asn Arg Ala Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 3
<211> 321
<212> DNA
<213> artificial
<220>
<223> константная область легкой цепи антитела против человеческого
TNFα
<400> 3
aggaccgtgg ccgcccccag cgtgttcatc ttccctccct ccgacgagca gctgaagagc 60
ggcacagcca gcgtcgtgtg cctgctcaac aacttctacc ccagggaagc caaggtgcag 120
tggaaggtgg acaacgccct gcagtccggc aacagccagg agagcgtgac cgaacaggac 180
agcaaggaca gcacctacag cctgagctcc accctcaccc tgtccaaggc cgactacgag 240
aagcataagg tgtacgcctg cgaagtgacc catcagggcc tgtccagccc cgtgacaaag 300
tccttcaaca ggggcgaatg c 321
<210> 4
<211> 107
<212> PRT
<213> artificial
<220>
<223> константная область легкой цепи антитела против человеческого
TNFα
<400> 4
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 5
<211> 363
<212> DNA
<213> artificial
<220>
<223> вариабельная область тяжелой цепи антитела против человеческого
TNFα
<400> 5
gaggtgcagc tggtggaatc cggaggagga ctggtccaac ctggcaggtc cctcaggctc 60
tcctgtgctg ccagcggctt taccttcgac gattacgcta tgcattgggt gcggcaagcc 120
cctggcaaag gactggaatg ggtgagcgcc attacctgga actccggcca catcgactac 180
gccgactccg tggagggccg gtttaccatt agccgggaca acgccaagaa ctccctgtac 240
ctgcagatga acagcctgag ggctgaggac accgctgtgt actactgcgc caaggtgagc 300
tacctgtcca cagccagcag cctggattac tggggccagg gcaccctggt gacagtcagc 360
agc 363
<210> 6
<211> 121
<212> PRT
<213> artificial
<220>
<223> вариабельная область тяжелой цепи антитела против человеческого
TNFα
<400> 6
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Thr Trp Asn Ser Gly His Ile Asp Tyr Ala Asp Ser Val
50 55 60
Glu Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Val Ser Tyr Leu Ser Thr Ala Ser Ser Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 7
<211> 990
<212> DNA
<213> artificial
<220>
<223> константная область тяжелой цепи антитела против человеческого
TNFα
<400> 7
gctagcacaa aaggaccttc cgtgtttcca ctggcaccct ctagtaagag tacttcagga 60
ggaaccgcag cactgggatg tctggtgaag gactacttcc cagagcccgt caccgtgtct 120
tggaacagtg gagcactgac ctccggggtc catacatttc ctgccgtgct gcagtcatcc 180
ggtctgtata gcctgagctc tgtggtcaca gtcccaagtt catccctggg cacccagaca 240
tacatctgca acgtgaatca caaaccttcc aatactaagg tcgacaagaa agtggaaccc 300
aagtcctgcg ataagaccca cacatgccct ccctgtcctg ctcccgaact gctgggagga 360
ccctccgtct tcctgttccc ccccaagccc aaagacacac tgatgatcag caggacccct 420
gaagtgacct gcgtggtcgt ggacgtgagc cacgaggacc ccgaggtcaa gtttaactgg 480
tacgtggacg gcgtggaggt ccacaacgcc aagaccaagc ccagggagga gcagtacaac 540
agcacctaca gggtcgtgtc cgtgctgacc gtgctccacc aagattggct caacggcaag 600
gagtataagt gcaaagtcag caacaaggcc ctccccgccc ccatcgagaa aaccatcagc 660
aaggccaagg gccaaccgcg ggaacctcaa gtgtataccc tccctcccag ccgggatgag 720
ctgaccaaga accaagtctc cctcttgtgc ctggtcaagg gattctaccc ttccgacatt 780
gccgtcgaat gggagagcaa tggccagccc gagaacaact acaagacaac cccccccgtc 840
ctgcgcagcg acggatcctt cttcctgtac tccaagctca ccgtggacaa gagccggtgg 900
caacagggca acgtgttctc ctgtagcgtg atgcacgaag ccctccacaa ccactatacc 960
cagaagagcc tgagcctcag ccccggcaaa 990
<210> 8
<211> 330
<212> PRT
<213> artificial
<220>
<223> константная область тяжелой цепи антитела против человеческого
TNFα
<400> 8
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
225 230 235 240
Leu Thr Lys Asn Gln Val Ser Leu Leu Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Arg Ser Asp Gly Ser Phe Phe
275 280 285
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
325 330
<210> 9
<211> 333
<212> DNA
<213> artificial
<220>
<223> вариабельная область легкой цепи антитела против человеческого
IL-17
<400> 9
atcatcgtca tgacccagtc ccccctgtcc ctgcctgtga cactgggcca gcctgcctcc 60
atctcctgca ggtcctccca gagcctggtg cacagcaacg gcaacaccta cctgcactgg 120
tatcaacaga ggcctggcca gagccctagg ctgctgatct acaaggtgta caaccggttc 180
tccggcgtgc ctgacaggtt ctccggcagc ggttctggca ccgacttcac cctgaagatc 240
tccagggtgg aggccgagga tgtgggcgtg tacttctgca gccagtccac ccacttccct 300
accttcggcc agggcaccag gctggagatc aag 333
<210> 10
<211> 111
<212> PRT
<213> artificial
<220>
<223> вариабельная область легкой цепи антитела против человеческого
IL-17
<400> 10
Ile Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu His Trp Tyr Gln Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Tyr Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Phe Cys Ser Gln Ser
85 90 95
Thr His Phe Pro Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105 110
<210> 11
<211> 360
<212> DNA
<213> artificial
<220>
<223> вариабельная область тяжелой цепи антитела против человеческого
IL-17
<400> 11
caggtgcagg tgcaggaatc cggccctgga ctggtgaagc cctccgagac cctgtccctg 60
acctgtaccg tgtccggcaa ctccatcacc tcctactacg cctggaactg gatcaggcag 120
cctcccggaa agggcctgga gtggatgggc tacatcacct actccggcac cacctcctac 180
aacccttccc tgaagagccg gatcaccatc agcgtggaca cctccaagaa ccagttctcc 240
ctgaaactgt cctccgtgac agccgccgat accgccgtgt actactgcgc ccgggaggag 300
tacgacgaca tctacgccgt ggactactgg ggccagggca cactggtgac cgtgtcctcc 360
<210> 12
<211> 120
<212> PRT
<213> artificial
<220>
<223> вариабельная область тяжелой цепи антитела против человеческого
IL-17
<400> 12
Gln Val Gln Val Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Asn Ser Ile Thr Ser Tyr
20 25 30
Tyr Ala Trp Asn Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Met Gly Tyr Ile Thr Tyr Ser Gly Thr Thr Ser Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Ile Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Tyr Asp Asp Ile Tyr Ala Val Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 13
<211> 990
<212> DNA
<213> artificial
<220>
<223> константная область тяжелой цепи антитела против человеческого
IL-17
<400> 13
gctagcacaa aaggaccttc cgtgtttcca ctggcaccct ctagtaagag tacttcagga 60
ggaaccgcag cactgggatg tctggtgaag gactacttcc cagagcccgt caccgtgtct 120
tggaacagtg gagcactgac ctccggggtc catacatttc ctgccgtgct gcagtcatcc 180
ggtctgtata gcctgagctc tgtggtcaca gtcccaagtt catccctggg cacccagaca 240
tacatctgca acgtgaatca caaaccttcc aatactaagg tcgacaagaa agtggaaccc 300
aagtcctgcg ataagaccca cacatgcccc ccttgtcctg cccctgaact gctcggaggc 360
cctagcgtgt tcctcttccc tcccaaaccc aaggacaccc tcatgatctc caggacccct 420
gaggtgacct gcgtcgtggt ggacgtcagc cacgaggacc ccgaggtgaa gttcaactgg 480
tacgtggacg gcgtcgaggt ccacaacgcc aagacaaagc ccagggagga acagtacaac 540
agcacctaca gggtggtcag cgtgctgacc gtgctgcacc aggattggct caacggcaag 600
gagtacaagt gcaaagtctc caacaaggcc ctgcccgccc ccatcgagaa gaccatctcc 660
aaggctaagg gacagcccag ggagccccaa gtgtacaccg agcctcccag ccgggatgag 720
ctgaccaaga accaagtctc cctcacctgc ctggtcaagg gattctaccc ttccgacatt 780
gccgtcgaat gggagagcaa tggccagccc gagaacaact acaagacaac cccccccgtc 840
ctggatagcg acggatcctt cttcctgctc tccgtgctca ccgtcgacaa gagcagatgg 900
cagcagggca acgtgttcag ctgtagcgtg atgcacgagg ccctgcacaa ccactacacc 960
cagaagagcc tgtccctcag ccccggcaag 990
<210> 14
<211> 330
<212> PRT
<213> artificial
<220>
<223> константная область тяжелой цепи антитела против человеческого
IL-17
<400> 14
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Glu Pro Pro Ser Arg Asp Glu
225 230 235 240
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Leu Ser Val Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
325 330
<210> 15
<211> 321
<212> DNA
<213> artificial
<220>
<223> вариабельная область легкой цепи антитела против человеческого
IL-17A
<400> 15
gacatccaga tgacacagtc ccccagcttc ctgagcgcta gcgtgggaga gagggtgacc 60
ctgagctgca aggccagcca gaacatcaac aagtacctgg actggttcca gcagaagctg 120
ggcgaagccc ccaagctgct gatctacaac gccgacaacc tccataccgg cattcccagc 180
aggttcagcg gctccggctc cttcagcgac ttcatcctga ccatcagcag cctgcagccc 240
gaggatgacg ccacctactt ctgcctgcag agggaatcct ggccttacac cttcggcgcc 300
ggcaccaagc tggaactgaa g 321
<210> 16
<211> 107
<212> PRT
<213> artificial
<220>
<223> вариабельная область легкой цепи антитела против человеческого
IL-17A
<400> 16
Asp Ile Gln Met Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly
1 5 10 15
Glu Arg Val Thr Leu Ser Cys Lys Ala Ser Gln Asn Ile Asn Lys Tyr
20 25 30
Leu Asp Trp Phe Gln Gln Lys Leu Gly Glu Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Asn Ala Asp Asn Leu His Thr Gly Ile Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Phe Ser Asp Phe Ile Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Asp Ala Thr Tyr Phe Cys Leu Gln Arg Glu Ser Trp Pro Tyr
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 17
<211> 366
<212> DNA
<213> artificial
<220>
<223> вариабельная область тяжелой цепи антитела против человеческого
IL-17A
<400> 17
caggtgcaac tgaaggagag cggccccgga ctggtgcaac cttcccaaac actcagcctc 60
acctgtaccg tctccggatt ctccctgacc aactattacg tccactgggt cagacagcct 120
cccggcaagg gactggagtg gatgggaggc gtgtggaatg acggcgacac ctcctacaac 180
agcgtcctca ggagcagact gagcattacc agagacacca gcaagagcca ggtcctcctc 240
aagatgtcct ccctccagac agaagacacc gccacctatt actgcgccag ggaaggcagg 300
gaaggcttcg tcggctacta tgtgatggat gcttggggcc ctggagctag cgtgacagtg 360
agctcc 366
<210> 18
<211> 122
<212> PRT
<213> artificial
<220>
<223> вариабельная область тяжелой цепи антитела против человеческого
IL-17A
<400> 18
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Gln Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Asn Tyr
20 25 30
Tyr Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Gly Val Trp Asn Asp Gly Asp Thr Ser Tyr Asn Ser Val Leu Arg
50 55 60
Ser Arg Leu Ser Ile Thr Arg Asp Thr Ser Lys Ser Gln Val Leu Leu
65 70 75 80
Lys Met Ser Ser Leu Gln Thr Glu Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Glu Gly Arg Glu Gly Phe Val Gly Tyr Tyr Val Met Asp Ala Trp
100 105 110
Gly Pro Gly Ala Ser Val Thr Val Ser Ser
115 120
<210> 19
<211> 15
<212> PRT
<213> artificial
<220>
<223> GPI325-339
<400> 19
Ile Trp Tyr Ile Asn Cys Phe Gly Cys Glu Thr His Ala Met Leu
1 5 10 15
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛО ПРОТИВ IL-17A И ЕГО ПРИМЕНЕНИЕ | 2019 |
|
RU2816204C2 |
| АНТИТЕЛО ПРОТИВ TNFR2 И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2793165C1 |
| АНТИТЕЛА ПРОТИВ VSIG4 ЧЕЛОВЕКА И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2776638C1 |
| АНТИТЕЛА ПРОТИВ CD40 И ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2796413C2 |
| АНТИТЕЛО ПРОТИВ IL-5, ЕГО АНТИГЕНСВЯЗЫВАЮЩИЙ ФРАГМЕНТ И ЕГО МЕДИЦИНСКОЕ ПРИМЕНЕНИЕ | 2018 |
|
RU2772716C2 |
| АНТИТЕЛО ПРОТИВ CD147 | 2018 |
|
RU2785293C2 |
| АНТИТЕЛА ПРОТИВ TNFRSF9 И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2812200C2 |
| АНТИТЕЛА ПРОТИВ ЛИГАНДА 1 ПРОГРАММИРУЕМОЙ ГИБЕЛИ И ИХ ПРИМЕНЕНИЯ | 2020 |
|
RU2786235C1 |
| БИСПЕЦИФИЧНОЕ АНТИТЕЛО ПРОТИВ PD-L1/ПРОТИВ 4-1ВВ В ГЕТЕРОДИМЕРНОЙ ФОРМЕ, ПОДОБНОЕ ПО СТРУКТУРЕ ПРИРОДНОМУ АНТИТЕЛУ, И ЕГО ПОЛУЧЕНИЕ | 2022 |
|
RU2825838C1 |
| БИСПЕЦИФИЧЕСКОЕ АНТИТЕЛО ПРОТИВ CD3E/BCMA И ЕГО ПРИМЕНЕНИЕ | 2019 |
|
RU2800164C2 |
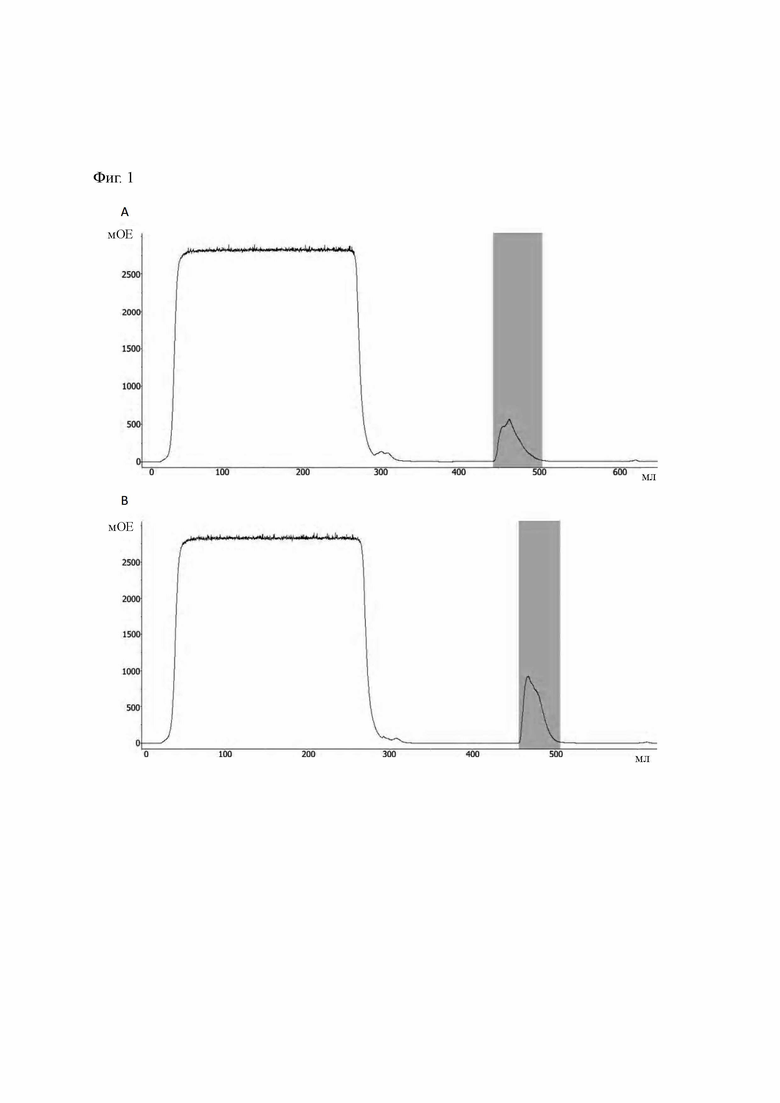
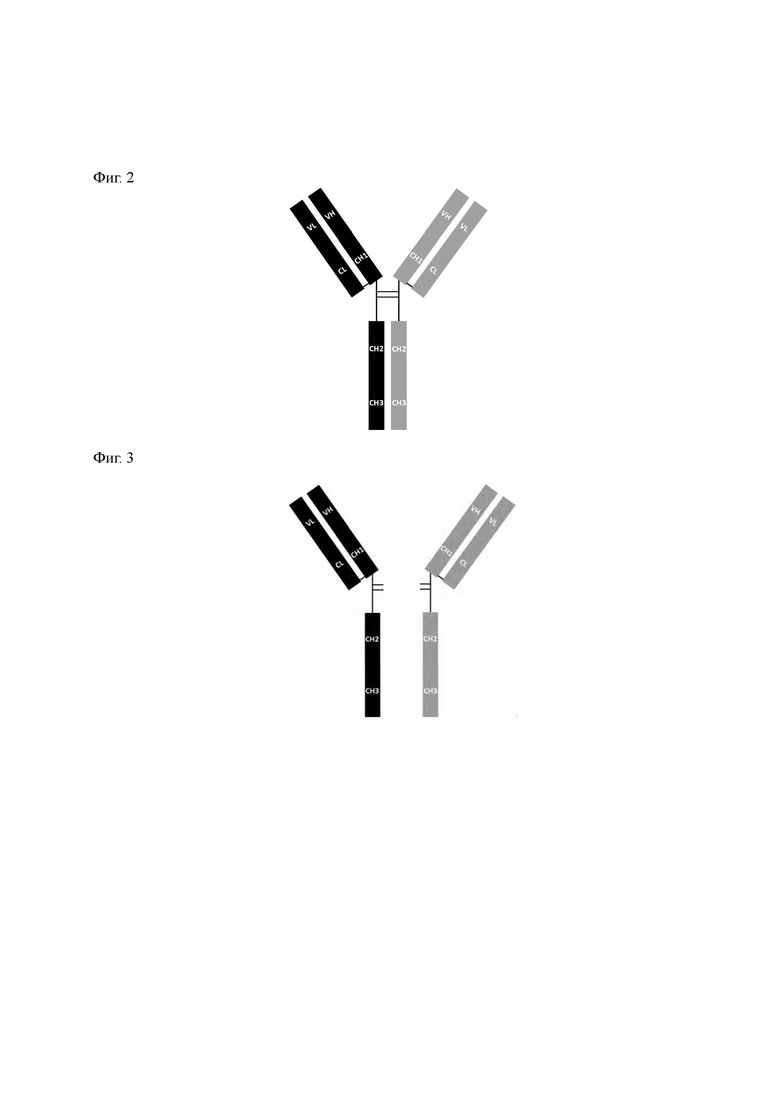
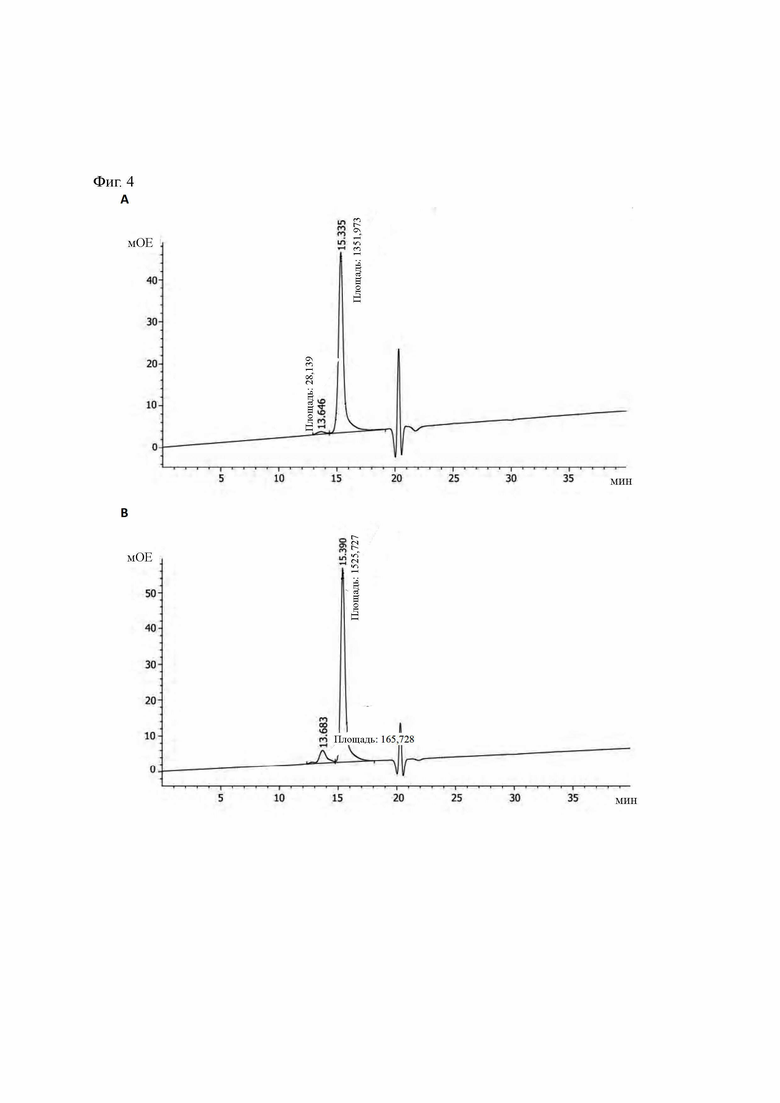


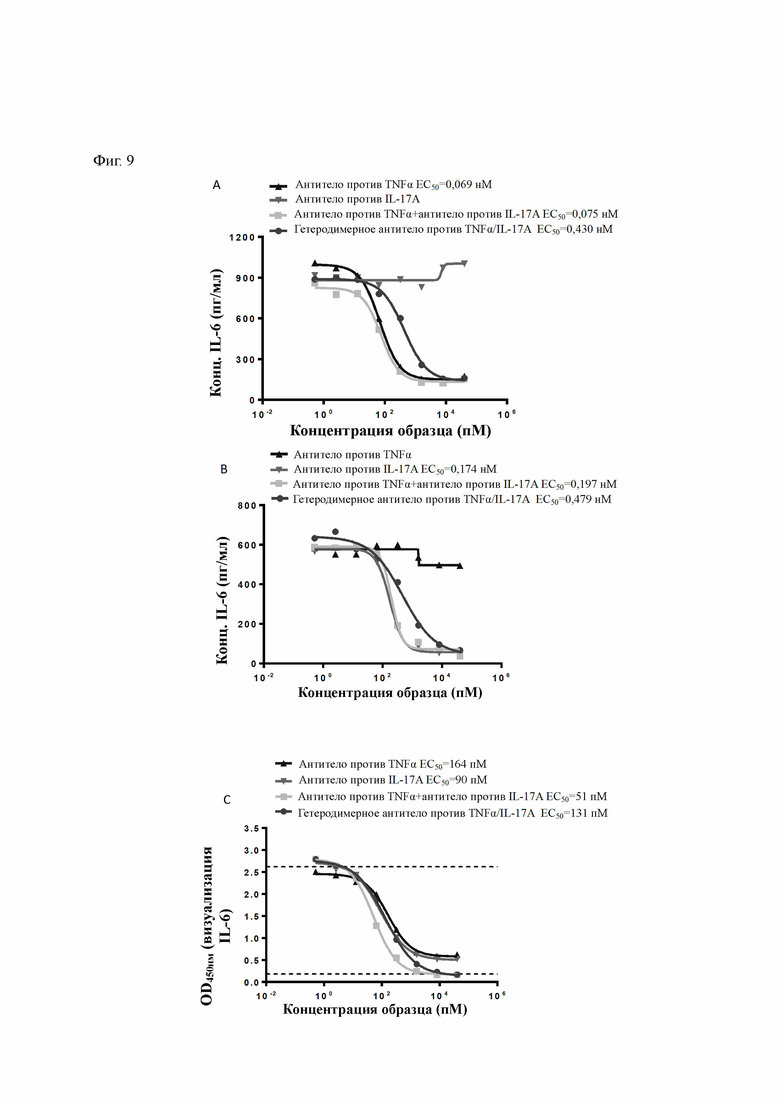

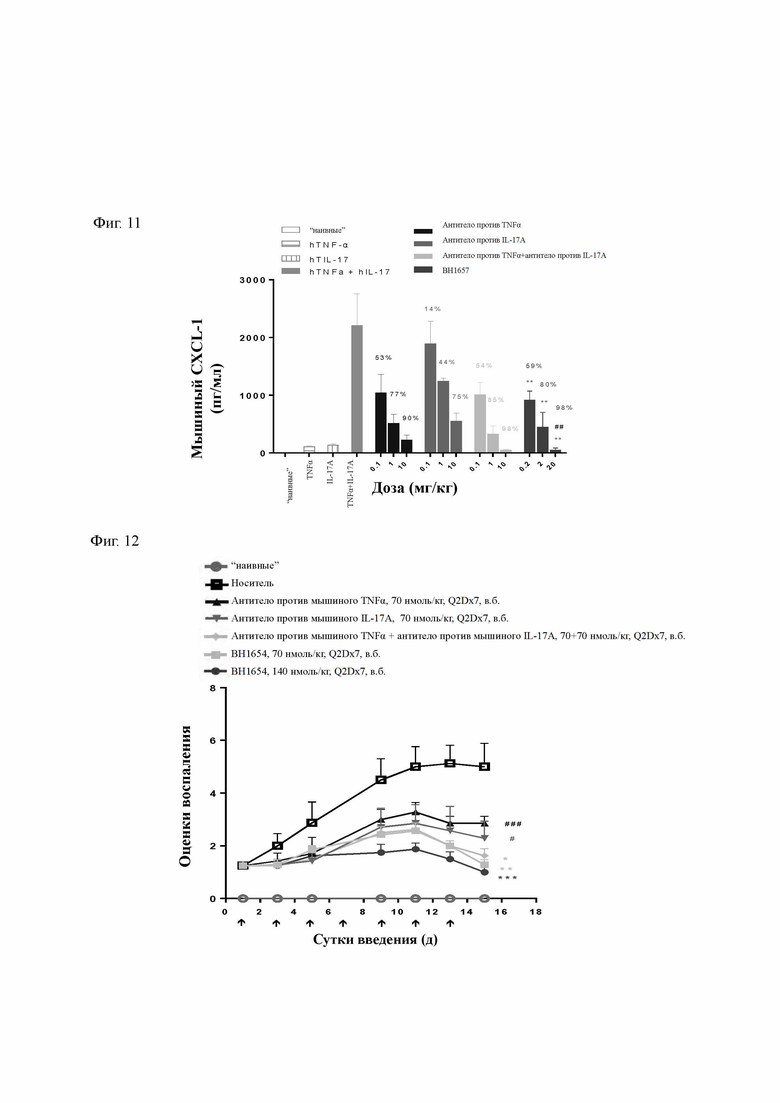
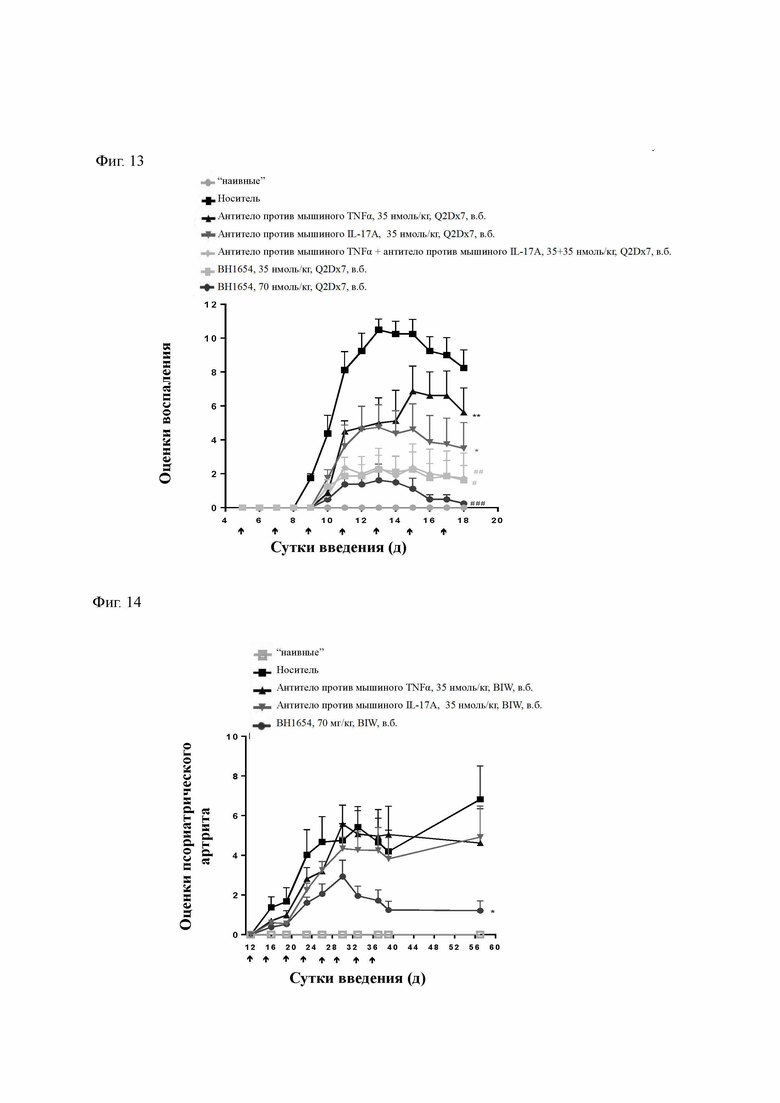
Изобретение относится к области биотехнологии, конкретно к получению гетеродимерного биспецифического антитела, и может быть использовано для предупреждения или лечения связанных с TNFα и IL-17A заболеваний. Полученное способом восстановления-окисления гетеродимерное биспецифическое антитело состоит из двух частей: 1) TNFα антигенсвязывающая область и первая цепь Fc и 2) IL-17A антигенсвязывающая область и вторая цепь Fc. Изобретение позволяет одновременно блокировать сигнальные пути TNFα и IL-17А. 7 н. и 19 з.п. ф-лы, 14 ил., 6 табл., 15 пр.
1. Гетеродимерное биспецифическое антитело, содержащее первую цепь Fc, и вторую цепь Fc, и первую антигенсвязывающую функциональную область, способную специфически связываться с TNFα, и вторую антигенсвязывающую функциональную область, способную специфически связываться с IL-17A;
где как первая цепь Fc, так и вторая цепь Fc представляют собой фрагменты Fc иммуноглобулина G, содержащие аминокислотные замены, и вместе образуют гетеродимер, который может связываться с рецептором Fc;
где первая цепь Fc и вторая цепь Fc связаны с первой и второй антигенсвязывающими функциональными областями соответственно посредством ковалентной связи или линкера;
где либо первая цепь Fc, либо вторая цепь Fc имеет аминокислотные замены T366L и D399R, а другая цепь имеет аминокислотные замены L351E, Y407L и K409V, где положения аминокислот пронумерованы в соответствии с системой нумерации Kabat EU;
где первая антигенсвязывающая функциональная область содержит аминокислотные последовательности SEQ ID NO: 2 и 6, а вторая антигенсвязывающая функциональная область содержит аминокислотные последовательности SEQ ID NO: 10 и 12; и
где гетеродимерное биспецифическое антитело образовано молекулами половины антител против TNFα и против IL-17A, каждая из которых содержит молекулы половины антител либо против TNFα, либо против IL-17A, посредством образования дисульфидных связей между ними.
2. Гетеродимерное биспецифическое антитело по п. 1, где как первая антигенсвязывающая функциональная область, так и вторая антигенсвязывающая функциональная область выбраны из группы, состоящей из фрагмента Fab, фрагмента scFv, фрагмента вариабельного домена Fv и фрагмента вариабельной области тяжелой цепи VHH антитела из тяжелых цепей.
3. Гетеродимерное биспецифическое антитело по п. 1 или 2, где как первая антигенсвязывающая функциональная область, так и вторая антигенсвязывающая функциональная область представляют собой фрагменты Fab.
4. Гетеродимерное биспецифическое антитело по п. 1 или 2, где одна из первой антигенсвязывающей функциональной области и второй антигенсвязывающей функциональной области представляет собой фрагмент Fab, а другая представляет собой фрагмент scFv.
5. Гетеродимерное биспецифическое антитело по п. 3, где фрагменты Fab содержат вариабельную область первой тяжелой цепи и вариабельную область второй тяжелой цепи, которые отличаются друг от друга, и вариабельную область первой легкой цепи и вариабельную область второй легкой цепи, которые отличаются друг от друга.
6. Гетеродимерное биспецифическое антитело по любому из пп. 1-5, где первая цепь Fc и первая антигенсвязывающая функциональная область, ковалентно связанная с ней, и вторая цепь Fc и вторая антигенсвязывающая функциональная область, ковалентно связанная с ней, образуют гомодимер в растворе в присутствии восстановителя и в отсутствие любых других полипептидов, отличающихся от первой цепи Fc и первой антигенсвязывающей функциональной области, ковалентно связанной с ней, и второй цепи Fc и второй антигенсвязывающей функциональной области, ковалентно связанной с ней, в массовом отношении менее 50% относительно всех полипептидных цепей.
7. Гетеродимерное биспецифическое антитело по п. 1, где молекула половины антитела против TNFα содержит аминокислотные последовательности SEQ ID NO: 4 и 8.
8. Гетеродимерное биспецифическое антитело по п. 1, где молекула половины антитела против IL-17A содержит аминокислотные последовательности SEQ ID NO: 4 и 14.
9. Выделенный полинуклеотид, кодирующий гетеродимерное биспецифическое антитело по любому из пп. 1-8.
10. Выделенный полинуклеотид по п. 9, где нуклеотидные последовательности, кодирующие аминокислотные последовательности первой антигенсвязывающей функциональной области, выбраны из группы, состоящей из: SEQ ID NO: 1 и 5.
11. Выделенный полинуклеотид по п. 9, где нуклеотидные последовательности, кодирующие аминокислотные последовательности второй антигенсвязывающей функциональной области, выбраны из группы, состоящей из: SEQ ID NO: 9 и 11.
12. Выделенный полинуклеотид по п. 10, где нуклеотидные последовательности, кодирующие аминокислотные последовательности первой антигенсвязывающей функциональной области, дополнительно выбраны из группы, состоящей из: SEQ ID NO: 3 и 7.
13. Выделенный полинуклеотид по п. 11, где нуклеотидные последовательности, кодирующие аминокислотные последовательности второй антигенсвязывающей функциональной области, дополнительно выбраны из группы, состоящей из: SEQ ID NO: 3 и 13.
14. Рекомбинантный экспрессионный вектор, содержащий выделенный полинуклеотид по любому из пп. 9-13.
15. Рекомбинантный экспрессионный вектор по п. 14, представляющий собой плазмидный вектор X0GC, модифицированный на основе pCDNA.
16. Клетка-хозяин, содержащая выделенный полинуклеотид по любому из пп. 9-13 или рекомбинантный экспрессионный вектор по п. 14 или 15.
17. Клетка-хозяин по п. 16, выбранная из группы, состоящей из эмбриональной клетки почки человека HEK293 или клетки HEK293T, клетки HEK293E и клетки HEK293F, имеющих происхождение от клетки HEK293; клетки яичника китайского хомячка CHO или клетки CHO-S, клетки CHO-dhfr, клетки CHO/DG44 и клетки ExpiCHO, имеющих происхождение от клетки CHO; Escherichia coli или Escherichia coli BL21, BL21 (DE3), Rosetta, Origami, имеющих происхождение от Escherichia coli; дрожжей или Pichia pastoris, Saccharomyces cerevisiae, Kluyveromyces lactis и Hansenula polymorpha, имеющих происхождение от дрожжей; клетки насекомого или клетки High 5 и клетки SF 9, имеющих происхождение от клетки насекомого; растительной клетки; клетки молочной железы млекопитающего, соматической клетки млекопитающего.
18. Фармацевтическая композиция, способная одновременно блокировать сигнальные пути TNFα и IL-17A, содержащая эффективное количество гетеродимерного биспецифического антитела по любому из пп. 1-8, или выделенного полинуклеотида по любому из пп. 9-13, или рекомбинантного экспрессионного вектора по п. 14 или 15, или клетки-хозяина по п. 16 или 17, и фармацевтически приемлемый носитель.
19. Способ получения гетеродимерного биспецифического антитела по любому из пп. 1-8, включающий стадии:
1) экспрессирования выделенного полинуклеотида по любому из пп. 9-13 или рекомбинантного экспрессионного вектора по п. 14 или 15 соответственно в клетке-хозяине;
2) восстановления каждого белка, соответственно экспрессированного в клетках-хозяевах; и
3) смешивания восстановленных белков и затем окисления смеси.
20. Способ по п. 19, где клетка-хозяин выбрана из группы, состоящей из эмбриональной клетки почки человека HEK293 или клетки HEK293T, клетки HEK293E и клетки HEK293F, имеющих происхождение от клетки HEK293; клетки яичника китайского хомячка CHO или клетки CHO-S, клетки CHO-dhfr, клетки CHO/DG44 и клетки ExpiCHO, имеющих происхождение от клетки CHO; Escherichia coli или Escherichia coli BL21, BL21 (DE3), Rosetta, Origami, имеющих происхождение от Escherichia coli; дрожжей или Pichia pastoris, Saccharomyces cerevisiae, Kluyveromyces lactis и Hansenula polymorpha, имеющих происхождение от дрожжей; клетки насекомого или клетки High 5 и клетки SF 9, имеющих происхождение от клетки насекомого; растительной клетки; клетки молочной железы млекопитающего, соматической клетки млекопитающего.
21. Способ по п. 19 или 20, где стадия восстановления включает: 1) проведение реакции восстановления в присутствии восстановителя, выбранного из группы, состоящей из 2-меркаптоэтиламина, дитиотреитола, трис(2-карбоксиэтил)фосфина или их химических производных; 2) удаление восстановителя.
22. Способ по любому из пп. 19-21, где стадия окисления представляет собой окисление воздухом или реакцию окисления в присутствии окислителя, выбранного из группы, состоящей из L-дегидроаскорбиновой кислоты или ее химических производных.
23. Способ по любому из пп. 19-22, дополнительно включающий стадию выделения и очистки.
24. Применение гетеродимерного биспецифического антитела по любому из пп.1-8 в изготовлении лекарственного средства для предупреждения или лечения связанных с TNFα и IL-17A заболеваний у субъекта.
25. Применение по п. 24, где субъект представляет собой млекопитающее, предпочтительно субъекта-человека.
26. Применение по п. 24, где заболевание выбрано из группы, состоящей из ревматоидного артрита, остеоартрита, псориатического артрита, анкилозирующего спондилита, подагрического артрита, ювенильного ревматоидного артрита и гнойного артрита.
| WO 2017132457 A1, 03.08.2017 | |||
| WO 2013002362 A1, 03.01.2013 | |||
| НЕДОРУБОВ А | |||
| А | |||
| и др | |||
| Печь для сжигания твердых и жидких нечистот | 1920 |
|
SU17A1 |
| Профилактика, диагностика, лечение, 2016, т | |||
| Устройство для электрической сигнализации | 1918 |
|
SU16A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
2022-10-18—Публикация
2019-11-05—Подача