Изобретение относится к области биотехнологии и фармацевтической промышленности и представляет собой новый способ получения двуспиральной рибонуклеиновой кислоты (дсРНК) из биомассы дрожжей Saccharomyces cerevisiae и может быть использовано в фармацевтике и биотехнологии для производства противоинфекционных и иммуномодулирующих препаратов.
Природные двуспиральные РНК (дсРНК) являются одними из важнейших медиаторов, обеспечивающих индукцию интерферона (IFN) в ответ на вирусную инфекцию в организме [1], при этом дсРНК вызывают индукцию всех типов интерферона, включая интерферон-дельта, обладают противовирусным действием в отношении различных видов вирусов. Таким образом, с точки зрения терапевтического потенциала дсРНК являются перспективным объектом для создания на их основе противовирусных, антибактериальных, противовоспалительных и противоопухолевых препаратов, а также средств для повышения неспецифической защитной реакции и снижения восприимчивости организма к действию патогенных агентов различной природы [2]. Источниками дсРНК могут являться РНК-содержащие вирусы растений и животных, а также некоторые микромицеты и дрожжи, в частности, так называемые «киллерные» штаммы вида Saccharomyces cerevisiae [3].
Несмотря на большой интерес к природной дсРНК, описанные в уровне техники способы ее получения недостаточно эффективны и требуют совершенствования.
Из уровня техники известен способ выделения дсРНК из клеток дрожжей, который заключается в последовательном применении 2-этилгексановой кислоты и додецилсульфата натрия при оптимальном температурном режиме для разрушения клеток Saccharomyces cerevisiae с последующим дробным фракционированием экстрагированных нуклеиновых кислот хлористым литием и дополнительной депротеинизации конечного продукта [4].
Также известен способ получения дсРНК из клеток дрожжей, охарактеризованный следующими стадиями: суспендирование клеток в буфере при 25оС при перемешивании в течение 60 мин; добавление хлороформа до 25% и перемешивание в течение 30 мин; центрифугирование; сбор водной фазы. Для получения препарата суммарной РНК для осаждения была выбрана концентрация соли 3,5 М. Полученный высаливанием 3,5 М NaCl, осадок дважды промывали 3,5 М раствором соли и растворяли в воде. Раствор осветляли центрифугированием и фильтровали, проводили осаждение РНК этанолом до концентрации 60%. Сформировавшийся осадок отделяли центрифугированием и промывали 60%-ным этанолом и лиофильно высушивали [5].
Недостатками указанных способов является низкие выход и чистота целевого продукта (дсРНК) в следствии использования исключительно химических реагентов для выделения РНК из клеток дрожжей.
Известен способ получения дсРНК из киллерных штаммов дрожжей Saccharomyces cerevisiae ВКПМ Y-448, который включает выделение из экстракта клеток двуспиральной РНК двойным фракционированием нуклеиновых кислот хлористым литием (1 этап: добавляют литий хлористый до конечной концентрации 2 М в целевом растворе; 2 этап: добавляют литий хлористый до концентрации 4 М в целевом растворе), очистку двуспиральной РНК хлороформом или смесью хлороформа с изоамиловым спиртом, выделение целевого продукта этанолом [6].
Также известен способ получения двуспиральной РНК (дсРНК) из клеток дрожжей Saccharomyces cerevisiae штамма ВКПМ Y-448 [7], характеризующийся тем, что включает следующие стадии: клетки дрожжей разрушают в буфере. Далее проводят концентрирование дсРНК из надосадочной жидкости в 7-8%-ном растворе ПЭГ 6000 с последующим центрифугированием и растворением полученного осажденного концентрата в воде; отделение дсРНК осуществляют в 2 моль/л растворе хлорида лития с последующим центрифугированием смеси и сбором водной фазы; осаждение дсРНК из водной фазы проводят в 3,5 моль/л растворе хлорида лития с последующим центрифугированием с получением осадка и растворением его в воде, а окончательную очистку и осаждение дсРНК из раствора осуществляют 55% раствором этанола.
Недостатки указанного способа состоят в том, что при разрушении клеточных стенок используется исключительно химический способ без применения дополнительной стадии механической обработки клеток, при этом температура инкубирования на стадии разрушения клеток не меняется и всегда постоянна (что выражается в снижении выхода целевого продукта). Период концентрирования РНК из надосадочной жидкости непродолжительный (что также характерно и для стадии отделения высокополимерной РНК от дсРНК) и не предполагает использование этанола в качестве концентрирующего агента. Помимо этого, стадия фракционирования предполагает всего один этап (т.е. снижается качество очистки дсРНК от низкомолекулярных примесей), аналогично стадия итогового осаждения дсРНК из раствора включает этап осаждения этанолом только в конкретной концентрации – 55%, что также сказывается на выходе и чистоте целевого продукта. Таким образом, все вышеуказанные недостатки данного способа могут снижать выход и чистоту целевого продукта – дсРНК.
Задачей настоящего изобретения является получение дсРНК из клеток киллерного штамма дрожжей Saccharomyces cerevisiae с увеличенными выходом и чистотой целевого продукта.
Техническим результатом является создание комплексного способа получения дсРНК с увеличенными выходом и чистотой целевого продукта (дсРНК) в среднем примерно в 2 раза.
Ниже приведены термины, которые используются в описании настоящего изобретения. Если не указано иное, все технические и специальные термины, использованные в описании, имеют общепринятое в данной области техники значение.
Термин «двуспиральная РНК (дсРНК)» в контексте настоящего изобретения характеризует молекулу РНК, состоящую из двух комплементарных цепей.
Термин «высокополимерная РНК» (впРНК) в контексте настоящего изобретения характеризует все возможные отличные от дсРНК виды молекул РНК (например, мРНК, тРНК и др).
«Суммарная РНК» в контексте настоящего изобретения – это суммарное количество всей полученной РНК в процессе выделения дсРНК из клеток киллерных дрожжей Saccharomyces cerevisiae, которая может включать, как высокополимерную РНК и двуспиральную РНК.
Термин «биомасса» в контексте настоящего изобретения относится к совокупной массе клеток киллерного штамма дрожжей Saccharomyces cerevisiae, отделенных в процессе центрифугирования от супернатанта культуральной жидкости, полученной в результате культивирования, в том числе, в качалочных колбах или биореакторах. (например, при культивировании батарейным способом).
Термин «одноатомный спирт» в контексте настоящего изобретения относится к спиртам, в составе молекулы которых содержится одна гидроксильная группа (например, метанол, этанол, пропанол и т.п.).
Термин «прецепитация» относится к процессу осаждения РНК одноатомным спиртом, в том числе, не ограничиваясь указанным, этанолом. Способ широко используется для очистки и концентрирования молекул нуклеиновых кислот. Эффект достигается за счет добавления соли и спирта в раствор, содержащий РНК. В присутствии соли (в частности, одновалентных катионов, таких как, например, ионы натрия (Na+)) спирты эффективно осаждает нуклеиновые кислоты.
Термин «фракционирование» в рамках настоящего изобретения характеризует процесс очистки осадка дсРНК от примесей (в основном высокополимерных РНК и ДНК, белков).
Термин «ресуспендирование» относится к процессу растворения осадка, полученного в результате центрифугирования после отделения от супернатаната, в определенном объеме указанного раствора.
Термин «депротеинизация» относится к процессу удаления белковых примесей путем их осаждения, в рамках настоящего изобретения, например, не ограничиваясь указанным, хлороформом, этанолом, ацетоном, ацетонитрилом или метанолом.
В контексте настоящего изобретения «96 % раствор одноатомного спирта» означает водно-спиртовой раствор с относительным содержанием одноатомного спирта от 95,1 % до 96,9 % (или об., или об/об %) от общего объема водного-спиртового раствора.
Термин «об. %» в контексте настоящего изобретения означает объёмную концентрацию (долю) некоторого жидкого вещества в растворителе (т.е. соотношение объема растворенного вещества к объему раствора, выраженное в процентах - об. %).
В контексте настоящего изобретения термин «пн» означает количество комплементарных пар нуклеотидов.
Поставленная задача решается, а заявленный технический результат достигается за счет нового способа получения двуспиральной РНК из клеток дрожжей киллерного штамма Saccharomyces cerevisiae, характеризующегося тем, что клетки дрожжей подвергают разрушению, центрифугируют, отделяют надосадочную жидкость и прецепитируют суммарную РНК, осадок отделяют и при перемешивании добавляют воду и хлорид натрия, отстаивают и центрифугируют, в полученный супернатант добавляют одноатомный спирт, чтобы его концентрация составила 40 об. % в целевом растворе, инкубируют и центрифугируют, к осадку при перемешивании добавляют буферный раствор и фракционируют раствором лития хлорида в две последовательные стадии: на первой стадии добавляют раствор хлорида лития до его концентрации в суспензии 2 М, на второй стадии до его концентрации в суспензии 4 М, полученную суспензию центрифугируют для отделения осадка и повторяют последовательное фракционирование раствором лития хлорида в две стадии, полученную суспензию центрифугируют и ресуспендируют в буферном растворе, далее дважды проводят депротеинизацию хлороформом и осаждают дсРНК из суспензии раствором одноатомного спирта до достижения его концентрации в целевом растворе 75 об. %, полученный осадок дважды промывают 96 об. % раствором одноатомного спирта.
Одним из вариантов исполнения настоящего изобретения является способ получения дсРНК из клеток дрожжей киллерного штамма Saccharomyces cerevisiae, в котором используют дрожжи киллерного штамма Saccharomyces cerevisiae ВКПМ Y448.
Поставленная задача решается, а заявленный технический результат достигается за счет нового способа получения двуспиральной РНК из клеток дрожжей киллерного штамма Saccharomyces cerevisiae ВКПМ Y448, характеризующегося тем, что клетки дрожжей подвергают разрушению, центрифугируют, отделяют надосадочную жидкость и прецепитируют суммарную РНК, осадок отделяют и при перемешивании добавляют воду и хлорид натрия, отстаивают и центрифугируют, в полученный супернатант добавляют одноатомный спирт, чтобы его концентрация составила 40 об. % в целевом растворе, инкубируют и центрифугируют, к осадку при перемешивании добавляют буферный раствор и фракционируют раствором лития хлорида в две последовательные стадии: на первой стадии добавляют раствор хлорида лития до его концентрации в суспензии 2 М, на второй стадии до его концентрации в суспензии 4 М, полученную суспензию центрифугируют для отделения осадка и повторяют последовательное фракционирование раствором лития хлорида в две стадии, полученную суспензию центрифугируют и ресуспендируют в буферном растворе, далее дважды проводят депротеинизацию хлороформом и осаждают дсРНК из суспензии раствором одноатомного спирта до достижения его концентрации в целевом растворе 75 об. %, полученный осадок дважды промывают 96 об. % раствором одноатомного спирта.
Поставленная задача решается, а заявленный технический результат достигается за счет нового способа получения двуспиральной РНК из клеток дрожжей киллерного штамма Saccharomyces cerevisiae ВКПМ Y448, характеризующегося тем, что клетки дрожжей подвергают разрушению, центрифугируют, отделяют надосадочную жидкость и прецепитируют суммарную РНК, осадок отделяют и при перемешивании добавляют воду и хлорид натрия, отстаивают и центрифугируют, в полученный супернатант добавляют одноатомный спирт, чтобы его концентрация составила 40 об. % в целевом растворе, инкубируют и центрифугируют, к осадку при перемешивании добавляют буферный раствор и фракционируют раствором лития хлорида в две последовательные стадии: на первой стадии добавляют раствор хлорида лития до его концентрации в суспензии 2 М, на второй стадии до его концентрации в суспензии 4 М, полученную суспензию центрифугируют для отделения осадка и повторяют последовательное фракционирование раствором лития хлорида в две стадии, полученную суспензию центрифугируют и ресуспендируют в буферном растворе, далее дважды проводят депротеинизацию хлороформом и осаждают дсРНК из суспензии раствором одноатомного спирта до достижения его концентрации в целевом растворе 75 об. %, полученный осадок дважды промывают 96 % раствором одноатомного спирта.
Поставленная задача решается, а заявленный технический результат достигается за счет нового способа получения двуспиральной рибонуклеиновой кислоты (дсРНК) из клеток дрожжей киллерного штамма Saccharomyces cerevisiae ВКПМ Y448, характеризующегося тем, что клетки дрожжей подвергают разрушению, центрифугируют, отделяют надосадочную жидкость и прецепитируют суммарную РНК, осадок отделяют и при перемешивании добавляют воду и хлорид натрия, отстаивают и центрифугируют, в полученный супернатант добавляют одноатомный спирт, чтобы его концентрация составила 40 об. % в целевом растворе, инкубируют и центрифугируют, к осадку при перемешивании добавляют буферный раствор и фракционируют раствором лития хлорида в две последовательные стадии: на первой стадии добавляют раствор хлорида лития до достижения его концентрации в суспензии 2 М, на второй стадии до достижения его концентрации в суспензии 4 М, полученную суспензию центрифугируют для отделения осадка и повторяют последовательное фракционирование растворами лития хлорида в две стадии, полученную суспензию центрифугируют и ресуспендируют в буферном растворе, далее дважды проводят депротеинизацию хлороформом в соотношении целевой раствор: хлороформ от 1:2 до 1:10 по объему и осаждают дсРНК из суспензии раствором одноатомного спирта до достижения его концентрации в целевом растворе 75 об. %, полученный осадок дважды промывают 96 об. % раствором одноатомного спирта.
Поставленная задача решается, а заявленный технический результат достигается за счет нового способа получения двуспиральной рибонуклеиновой кислоты (дсРНК) из клеток дрожжей киллерного штамма Saccharomyces cerevisiae ВКПМ Y448, характеризующегося тем, что клетки дрожжей подвергают разрушению, центрифугируют, отделяют надосадочную жидкость и прецепитируют суммарную РНК, осадок отделяют и при перемешивании добавляют воду и хлорид натрия, отстаивают и центрифугируют, в полученный супернатант добавляют одноатомный спирт, чтобы его концентрация составила 40 об. % в целевом растворе, инкубируют и центрифугируют, к осадку при перемешивании добавляют буферный раствор и фракционируют раствором лития хлорида в две последовательные стадии: на первой стадии добавляют раствор хлорида лития до достижения его концентрации в суспензии 2 М, на второй стадии до достижения его концентрации в суспензии 4 М, полученную суспензию центрифугируют для отделения осадка и повторяют последовательное фракционирование растворами лития хлорида в две стадии, полученную суспензию центрифугируют и ресуспендируют в буферном растворе, далее дважды проводят депротеинизацию хлороформом в соотношении целевой раствор: хлороформ от 1:2 до 1:10 по объему и осаждают дсРНК из суспензии раствором одноатомного спирта до достижения его концентрации в целевом растворе 75 об. %, полученный осадок дважды промывают 96 % раствором одноатомного спирта.
Поставленная задача решается, а заявленный технический результат достигается за счет нового способа получения двуспиральной рибонуклеиновой кислоты (дсРНК) из клеток дрожжей киллерного штамма Saccharomyces cerevisiae ВКПМ Y448, характеризующегося тем, что клетки дрожжей подвергают разрушению, центрифугируют, отделяют надосадочную жидкость и прецепитируют суммарную РНК, осадок отделяют и при перемешивании добавляют воду и хлорид натрия, отстаивают и центрифугируют, в полученный супернатант добавляют одноатомный спирт, чтобы его концентрация составила 40 об. % в целевом растворе, инкубируют и центрифугируют, к осадку при перемешивании добавляют буферный раствор и фракционируют раствором лития хлорида в две последовательные стадии: на первой стадии добавляют раствор хлорида лития до достижения его концентрации в суспензии 2 М, на второй стадии до достижения его концентрации в суспензии 4 М, полученную суспензию центрифугируют для отделения осадка и повторяют последовательное фракционирование растворами лития хлорида в две стадии, полученную суспензию центрифугируют и ресуспендируют в буферном растворе, далее дважды проводят депротеинизацию хлороформом в соотношении целевой раствор: хлороформ от 1:2 до 1:10 по объему и осаждают дсРНК из суспензии раствором одноатомного спирта до достижения его концентрации в целевом растворе 75 об. %, полученный осадок дважды промывают 96 % раствором одноатомного спирта.
Поставленная задача решается, а заявленный технический результат достигается за счет нового способа получения двуспиральной рибонуклеиновой кислоты (дсРНК) из клеток дрожжей киллерного штамма Saccharomyces cerevisiae ВКПМ Y448, характеризующегося тем, что клетки дрожжей подвергают разрушению, центрифугируют, отделяют надосадочную жидкость и прецепитируют суммарную РНК, осадок отделяют и при перемешивании добавляют воду и хлорид натрия, отстаивают и центрифугируют, в полученный супернатант добавляют одноатомный спирт, чтобы его концентрация составила 40 % в целевом растворе, инкубируют и центрифугируют, к осадку при перемешивании добавляют буферный раствор и фракционируют раствором лития хлорида в две последовательные стадии: на первой стадии добавляют раствор хлорида лития до достижения его концентрации в суспензии 2 М, на второй стадии до достижения его концентрации в суспензии 4 М, полученную суспензию центрифугируют для отделения осадка и повторяют последовательное фракционирование растворами лития хлорида в две стадии, полученную суспензию центрифугируют и ресуспендируют в буферном растворе, далее дважды проводят депротеинизацию хлороформом в соотношении целевой раствор: хлороформ от 1:2 до 1:10 по объему и осаждают дсРНК из суспензии раствором одноатомного спирта до достижения его концентрации в целевом растворе 75 %, полученный осадок дважды промывают 96 % раствором одноатомного спирта.
Одним из вариантов исполнения настоящего изобретения является способ получения дсРНК из клеток дрожжей киллерного штамма Saccharomyces cerevisiae, в котором одноатомный спирт представляет собой метанол, этанол, пропанол, изопропанол, бутанол или изобутанол.
Более предпочтительно в способе получения дсРНК по настоящему изобретению используют в качестве одноатомного спирта этанол.
Одним из вариантов исполнения настоящего изобретения является способ получения дсРНК из клеток дрожжей киллерного штамма Saccharomyces cerevisiae, в котором одноатомный спирт представляет собой этанол концентрацией 96 об. %.
Одним из вариантов исполнения настоящего изобретения является способ получения дсРНК из клеток дрожжей киллерного штамма Saccharomyces cerevisiae, в котором одноатомный спирт представляет собой этанол концентрацией 96 %.
Одним из вариантов исполнения настоящего изобретения является способ получения дсРНК из клеток дрожжей киллерного штамма Saccharomyces cerevisiae, в котором хлорид натрия добавляют до достижения его концентрации 2,0 М в целевом растворе.
Более предпочтительно депротеинизацию проводят хлороформом в соотношении целевой раствор (раствор, содержащий дсРНК) : хлороформ 1:2 по объему.
Одним из вариантов исполнения настоящего изобретения является способ получения дсРНК из клеток дрожжей киллерного штамма Saccharomyces cerevisiae, в котором используют водный раствор хлорида лития с концентрацией 8-10 М.
Более предпочтительно в способе по настоящему изобретению используют раствор хлорида лития с концентрацией 8 М.
Одним из вариантов исполнения настоящего изобретения является способ получения дсРНК из клеток дрожжей киллерного штамма Saccharomyces cerevisiae, в котором полученную дсРНК лиофильно высушивают.
Краткое описание чертежей.
Настоящее изобретение дополнительно проиллюстрировано посредством Фиг. 1 и Фиг. 2.
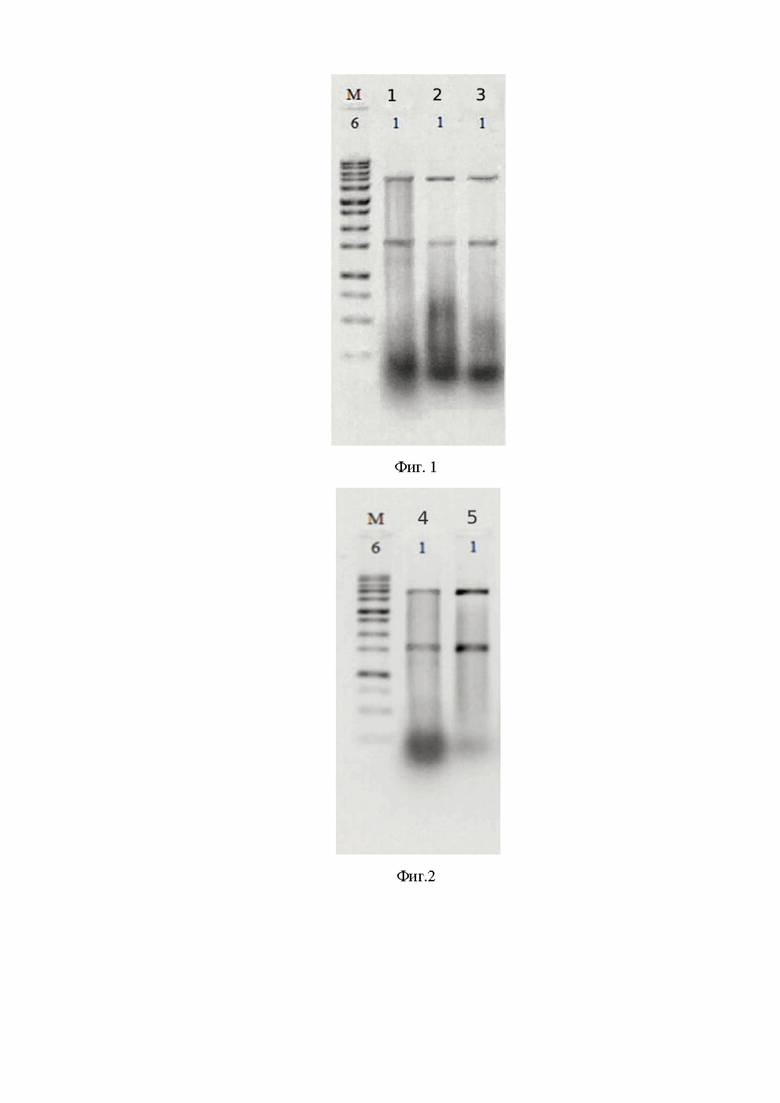
На Фиг.1 изображена электрофореграмма образцов дсРНК, полученных путем реализации способа 1, способа 2 и способа 5:
М – маркер молекулярной массы (маркер молекулярного веса ДНК, содержащий 13 фрагментов от 250 до 10000 п.н. (фрагменты: 250, 500, 750, 1000, 1500, 2000, 2500, 3000, 4000, 5000, 6000, 8000, 10000 п.н.);
1 – образец, полученный способом 1;
2 – образец, полученный способом 2;
3 – образец, полученный способом 5.
На Фиг. 2 изображена электрофореграмма образцов дсРНК, полученных путем реализации способов 3 и 4:
М – маркер молекулярной массы (маркер молекулярного веса ДНК, содержащий 13 фрагментов от 250 до 10000 п.н. (фрагменты: 250, 500, 750, 1000, 1500, 2000, 2500, 3000, 4000, 5000, 6000, 8000, 10000 п.н.);М – маркер молекулярной массы (маркер молекулярного веса ДНК, содержащий 13 фрагментов от 250 до 10000 п.н. (фрагменты: 250, 500, 750, 1000, 1500, 2000, 2500, 3000, 4000, 5000, 6000, 8000, 10000 п.н.);
4 – образец, полученный способом 4;
5 – образец, полученный способом 3.
Подробное описание изобретения. Раскрытие сущности изобретения.
Предложенный в рамках настоящего изобретения способ получения дсРНК из клеток дрожжей киллерного штамма Saccharomyces cerevisiae, например, из ВКПМ Y-448, по одному из вариантов исполнения настоящего изобретения предусматривает следующие этапы.
Клетки дрожжей киллерного штамма Saccharomyces cerevisiae ВКПМ Y-448 подвергают разрушению (механическому и/или химическому и/или ферментативному), суспензию центрифугируют, отделяют надосадочную жидкость и прецепитируют суммарную РНК. После чего осадок отделяют и при перемешивании смешивают с водой очищенной до достижения значений оптической плотности при 260 нм до 180±20 о.е./мл. Суспензию перемешивают до получения однородности в течение 6-10 ч, затем добавляют хлорид натрия до достижения его концентрации в целевом растворе 2,0 М. Раствор перемешивают, охлаждают до 5-2оС и инкубируют при этой температуре не менее 12 ч. Далее суспензию центрифугируют и определяют наличие зоны дсРНК в супернатанте.
Полученный в результате супернатант, содержащий фракцию дсРНК, собирают и отбирают пробу для определения оптической плотности при 260 нм, которая должна соответствовать значению 55±5 е.о.п. После чего в супернатант, содержащий фракцию дсРНК, добавляют одноатомный спирт, в том числе, не ограничиваясь указанным, метиловый, этиловый, пропиловый, бутиловый, изобутиловый, с концентрацией 90-96 % до достижения его концентрации в целевом растворе 40-45 об. %. Полученную суспензию перемешивают, охлаждают до 5±2 °С и отстаивают в течение не менее 12 часов.
Сформировавшийся осадок отделяют с помощью, например, центрифугирования, после чего к осадку добавляют буферный раствор ((рН = 7,20 ± 0,05) со следующим составом: натрия хлорид – 100-300 мМ; ЭДТА – 0,5-4,0 мМ; трис(оксиметил)аминометан – 30-150 мМ). Полученную суспензию перемешивают до полного растворения осадка в течение 6,0-9,0 ч. Оптическая плотность полученного раствора дсРНК должна составлять 120±30 е.о.п. при 260 нм.
Далее в приготовленный раствор дсРНК добавляют такой объем 8 М раствора хлорида лития, чтобы концентрация хлорида лития в полученной суспензии составила 2 М. Полученную суспензию перемешивают, охлаждают до 5±2 °С и отстаивают при установленной температуре не менее 12 часов. Полученную суспензию центрифугируют для отделения супернатанта.
К супернатанту, полученному на предыдущей стадии, загружают такой объем 8 М раствор хлорида лития, чтобы концентрация хлорида лития в полученной суспензии составляла 4 М. Полученный раствор перемешивают до получения однородной суспензии, охлаждают до 5±2 °С и отстаивают при установленной температуре в течение не менее 12 часов. Далее суспензию центрифугируют для отделения осадка. Супернатант утилизируют.
Полученный осадок отправляют на повторные стадии фракционирования 2 М и 4 М хлоридом лития. В полученном супернатанте измеряют оптическую плотность при 260 нм, которая должна соответствовать значению 8,0±5 е.о.п.
Полученный по окончании центрифугирования осадок дсРНК растворяют в буфере ((рН = 7,20± 0,05) следующего состава: натрия хлорид – 70 мМ; ЭДТА – 1мМ). Далее перемешивают полученную суспензию до гомогенного состояния в течение 2,0-4,0 ч. К полученной суспензии дсРНК добавляют хлороформ в объемном соотношении целевой раствор дсРНК : хлороформ от 1:2 до 1:10 и перемешивают до получения суспензии белого цвета в течение 15-45 мин. Полученную суспензию отстаивают при 5±2 °С в течение 1 часа.
После отстаивания отбирают водную верхнюю фракцию. Затем проводят повторный процесс депротеинизации раствора дсРНК при аналогичных условиях. После отстаивания отбирают водную верхнюю фракцию и измеряют оптическую плотность полученной фракции при 260 нм, которая должна соответствовать значению 75±10 е.о.п.
Далее к раствору дсРНК загружают одноатомный спирт, например, не ограничиваясь указанным, метиловый, этиловый, пропиловый, бутиловый, изобутиловый, концентрацией 96 % до концентрации его в целевом растворе 75 об. %, охлаждают до 5±2 °С и отстаивают при данной температуре в течение не менее 12 часов.
По окончании отстаивания суспензию центрифугируют. К полученному спиртовому осадку дсРНК добавляют одноатомный спирт, например, не ограничиваясь указанным, метиловый, этиловый, пропиловый, бутиловый или изобутиловый, в концентрации 96 % и перемешивают полученную суспензию. Затем суспензию центрифугируют. Данную процедуру промывки одноатомным спиртом проводят дважды.
Далее полученный спиртовой осадок растворяют в воде, например, не ограничиваясь указанным, очищенной, инъекционной, до полного растворения осадка. Измеряют рН и оптическую плотность раствора при 260 нм, значение которой должно соответствовать 90±10 е.о.п. В случае, если оптическая плотность раствора больше данного значения, то значение оптической плотности в растворе доводят до заданного диапазона с помощью воды, например, не ограничиваясь указанным, очищенной, инъекционной.
Полученный водный раствор дсРНК с предыдущей стадии подвергают фильтрации с целью удаления взвешенных частиц и мутности и лиофильно высушивают.
Список литературы.
1. Isaque João da Silva de Faria, Roenick Proveti Olmo, Emanuele Guimarães Silva, and João Trindade Marques.Journal of Interferon & Cytokine Research.May 2013.239-253.http://doi.org/10.1089/jir.2013.0026.
2. Yoneyama, Mitsutoshi and Takashi Fujita. “Recognition of viral nucleic acids in innate immunity.” Reviews in Medical Virology 20 (2010): n. pag.
3. Даниленко, Е. Д., Белкина, А. О., Сысоева, Г. М. (2019). Создание лекарственных препаратов на основе высокополимерных двуспиральных РНК для противовирусной и противоопухолевой терапии. Биомедицинская химия, 65(4), 282.
4. Краснопольский Ю. М.: Фармацевтическая биотехнология: Производство биологически активных веществ: учеб. пособие: в 2 ч. – Ч. 2 / Ю. М. Краснопольский, Н. Ф. Клещев. – Харьков: НТУ «ХПИ», 2013. – 47 с.
5. Шевченко З.А., Телегина Ю.В., Лебедев Л.Р. Способ получения препаратов на основе рнк // Актуальные проблемы гуманитарных и естественных наук. 2017. №8-2.
6. Патент РФ № 2302464.
7. Патент РФ № 2558256.
Далее приводятся примеры осуществления изобретения, которые иллюстрируют изобретение, но не охватывают все возможные варианты его осуществления и не ограничивают изобретение.
Специалисту в данной области очевидно, что возможны и другие частные варианты осуществления изобретения.
Пример 1. Получение дсРНК из клеток дрожжей Saccharomyces cerevisiae.
Клетки дрожжей киллерного штамма Saccharomyces cerevisiae ВКПМ Y-448 подвергали разрушению, суспензию центрифугировали, отделяли надосадочную жидкость и прецепитировали суммарную РНК.
В частном случае исполнения настоящего изобретения биомассу дрожжей киллерного штамма Saccharomyces cerevisiae ВКПМ Y-448 суспендировали в буферном растворе (состав рН = 7,00±0,05, состав: натрий сернокислый – 100 мМ; ЭДТА – 5 мМ; калий фосфорнокислый однозамещенный – 40 мМ; калия хлорид – 350 мМ; SDS – 5 мМ) до гомогенного состояния. Далее при постоянном перемешивании полученную суспензию нагревали до 30±1оС и добавляли ферментный препарат, содержащий зимолиазу, и 1 % раствор SDS. Суспензию перемешивали и инкубировали при указанной температуре 2 часа при перемешивании. Далее суспензию охлаждали до 18±1 оС и гомогенизировали при высоком давлении (1400 бар). Полученную суспензию центрифугировали. Далее проводили этап осаждения одноатомным спиртом, например, 96 % этиловым спиртом.
После чего осадок отделяли и при перемешивании смешивали с водой очищенной в количестве 3,33 л воды очищенной на 1,0 кг осадка до достижения значений оптической плотности при 260 нм до 180±20 о.е./мл. Далее суспензию перемешивали при температуре 18,0±1 оС до получения однородности в течение 6-10 ч, затем доводили объем суспензии водой очищенной до объема, равному двукратному количеству очищенной воды, используемой ранее, перемешивали в течение 15 мин.
К полученной суспензии добавляли взвешенный на весах хлорид натрия до достижения его концентрации в целевом растворе 2,0 М. Суспензию перемешивали до полного растворения в течение 20-30 мин и охлаждали до 4оС. Охлажденную суспензию инкубировали при этой температуре 12 ч. Далее суспензию центрифугировали при 15000 об/мин и определяют наличие зоны дсРНК в супернатанте. Полученный осадок сливали.
Полученный в результате супернатант, содержащий фракцию дсРНК, собирали и отбирали пробу для определения оптической плотности при 260 нм. Оптическая плотность соответствовала значению 55,0 е.о.п. Далее к супернатанту добавляли 96 % этиловый спирт (или другой одноатомный спирт, например, не ограничиваясь указанным, метанол, пропанол, изопропанол, бутанол или изобутанол) до достижения его концентрации в целевом растворе 40 об. %. Полученную суспензию перемешивали в течение 15 мин, охлаждали до 4±1 °С и отстаивали в течение 12 часов.
Сформировавшийся осадок отделяли с помощью центрифугирования, после чего к осадку добавляли буферный раствор ((рН = 7,20 ± 0,05) состав: натрия хлорид – 150 мМ; ЭДТА – 1,0 мМ; трис(оксиметил)аминометан – 50 мМ). Полученную суспензию перемешивали до полного растворения осадка в течение 6,0 ч. Оптическая плотность полученного раствора дсРНК составляла примерно 120 е.о.п. при 260 нм.
Далее в приготовленный раствор дсРНК приливали 8 М раствор хлорида лития до достижения его концентрации в полученной суспензии 2 М, то есть в объемном соотношении раствор дсРНК (целевой раствор) : 8 М раствор хлорида лития = 1,000 : 3,333. Полученную суспензию перемешивали в течение 15 мин, охлаждали до 4±1 °С и отстаивали при установленной температуре 12 часов. Полученную суспензию центрифугировали при 8000 об/мин для отделения супернатанта.
К супернатанту, полученному на предыдущей стадии, загружали 8 М раствор хлорида лития до достижения его концентрации в полученной суспензии 4 М, то есть в объемном соотношении раствор дсРНК : 8 М раствор хлорида лития = 1 : 0,5. Полученный раствор перемешивали до получения однородной суспензии в течение 15 минут, охлаждали до 4±1 °С и отстаивали при установленной температуре в течение 12 часов. Далее суспензию центрифугировали при 8000 об/мин для отделения осадка. Супернатант утилизировали.
Полученный осадок отправляли на повторные стадии фракционирования 2 М и 4 М хлоридом лития. Для этого к осадку добавляли буферный раствор ((рН = 7,20 ± 0,05) состав: натрия хлорид – 150 мМ; ЭДТА – 1,0 мМ; трис(оксиметил)аминометан – 50 мМ). Полученную суспензию перемешивали до полного растворения осадка в течение 4,0 ч. Оптическая плотность полученного раствора дсРНК составляла примерно 80 е.о.п. при 260 нм.
Далее в приготовленный раствор дсРНК приливали 8 М раствор хлорида лития до достижения его концентрации в полученной суспензии 2 М, то есть в объемном соотношении раствор дсРНК : 8 М раствор хлорида лития = 1,000 : 3,333. Полученную суспензию перемешивали в течение 15 мин, охлаждали до 4±1 °С и отстаивали при установленной температуре 12 часов. Полученную суспензию центрифугировали при 10000 об/мин для отделения супернатанта. Оптическая плотность полученного раствора дсРНК составляла примерно 40 е.о.п. при 260 нм.
К супернатанту, полученному на предыдущей стадии, загружали 8 М раствор хлорида лития до достижения его концентрации в полученной суспензии 4 М, то есть в объемном соотношении раствор дсРНК (целевой раствор) : 8 М раствор хлорида лития = 1 : 0,5. Полученный раствор перемешивали до получения однородной суспензии в течение 15 минут, охлаждали до 4±1 °С и отстаивали при установленной температуре в течение 12 часов. Далее суспензию центрифугировали при 10000 об/мин для отделения осадка. Оптическая плотность полученного супернатанта составляла примерно 8,0 е.о.п. при 260 нм.
Полученный по окончании центрифугирования осадок дсРНК растворяли в буфере ((рН = 7,20± 0,05) состав: натрия хлорид – 70 мМ; ЭДТА – 1мМ) и перемешивали полученную суспензию до гомогенного состояния в течение 2,0 ч. К полученной суспензии дсРНК добавляли хлороформ в соотношении раствор дсРНК (целевой раствор) : хлороформ от 1:2 до 1:10 по объему (в частном случае, в соотношении раствор дсРНК (целевой раствор) : хлороформ 1:2 по объему) и перемешивали до получения суспензии белого цвета в течение 15 мин. Полученную суспензию отстаивали при 4±1 °С в течение 1 часа.
После отстаивания отбирали водную верхнюю фракцию и проводили повторный процесс депротеинизации раствора дсРНК при аналогичных условиях. После отстаивания отбирали водную верхнюю фракцию и измеряли оптическую плотность полученной фракции при 260 нм. Оптическая плотность соответствовала значению 75±10 е.о.п. Нижнюю фазу (отработанный хлороформ) отправляли на утилизацию.
Далее к раствору дсРНК загружали 96 % этиловый спирт (или другой одноатомный спирт, например, не ограничиваясь указанным, метанол, пропанол, изопропанол, бутанол или изобутанол) до достижения его концентрации в целевом растворе 75 об. %, охлаждали до 4±1 °С и отстаивали при данной температуре в течение 12 часов.
По окончании отстаивания суспензию центрифугировали при 10000 об/мин. К полученному спиртовому осадку дсРНК добавляли 96 % этиловый спирт (или другой одноатомный спирт, например, не ограничиваясь указанным, метанол, пропанол, изопропанол, бутанол или изобутанол) в соотношении осадок : 96 % этиловый спирт = 1 г : 10 мл и перемешивали полученную суспензию в течение 10 мин. Затем суспензию центрифугировали при 10000 об/мин.
К полученному спиртовому осадку повторно добавляли 96 об. % этиловый спирт (или другой одноатомный спирт, например, не ограничиваясь указанным, метанол, пропанол, изопропанол, бутанол или изобутанол) в соотношении осадок : 96 об. % этиловый спирт = 1 г : 10 мл и подвергали промывке при аналогичных условиях.
Далее полученный спиртовой осадок растворяли в воде инъекционной до полного растворения осадка. РН полученного раствора составлял примерно 7,0, оптическую плотность доводили до примерно 90±10 е.о.п. при длине волны 260 нм.
Полученный водный раствор дсРНК с предыдущей стадии подвергали фильтрации с целью удаления взвешенных частиц и мутности, и лиофильно высушивали.
Идентификацию дсРНК проводили методами электрофореза в агарозном геле и высокоэффективной жидкостной хроматографии (ВЭЖХ). На электрофореграммах фиксировались полосы с четко очерченными границами. Высокая контрастность полос была обусловлена высокой степенью взаимодействия дсРНК с интеркалирующим агентом – бромистым этидием. Высокая степень интеркалирования прямо свидетельствует о двуспиральной структуре молекулы.
Пример 2. Изучение влияния различных условий в способах получения дсРНК из клеток киллерных дрожжей Saccharomyces cerevisiae на выход дсРНК.
Для изучения влияния различных условий в способах получения дсРНК из клеток киллерных дрожжей Saccharomyces cerevisiae на выход дсРНК авторы изобретения проделали ряд экспериментов по получению и выделению дсРНК различными способами. Результаты исследований представлены в таблице 1.
В способах получения дсРНК из киллерных дрожжей Saccharomyces cerevisiae согласно таблице 1 анализировали влияние различных условий фракционирования, депротеинизации и осаждения дсРНК на выход и чистоту целевого продукта, при этом разрушение клеток дрожжей в способах 1-5 осуществляли одним и тем же методом (механическим и/или химическим, и/или ферментативным).
Для проведения каждого из экспериментов, описанных в таблице 1, использовали по 6 кг биомассы киллерных дрожжей Saccharomyces cerevisiae ВКПМ Y-448, полученных с одного процесса ферментации. Для оценки сходимости результатов эксперименты проводили по 3 раза. Все целевые продукты, полученные по завершении экспериментов, лиофилизировали при одинаковых условиях. Количественное содержание и чистоту дсРНК в лиофилизатах оценивали методом эксклюзионной ВЭЖХ в пересчете на безводный и свободный от остаточных органических растворителей лиофилизат. Для определения количественного содержания примесного белка в лиофилизате (в пересчете на безводный и свободный от остаточных органических растворителей лиофилизат) использовали метод Лоури.
Таблица 1. Сравнение выхода и чистоты дсРНК, полученной различными способами.
Депротеинизация: хлороформом в соотношении целевой раствор дсРНК : хлороформ 1:1 по объему;
Осаждение дсРНК: из водной фазы двумя объемами этанола (или др одноатомного спирта)
Фракционирование: двойное фракционирование раствором LiCl до достижения его концентрации 2 М в целевом растворе и затем до достижения его концентрации 3,5 М в целевом растворе;
Осаждение дсРНК: в 55 об. % растворе этанола (или др одноатомного спирта)
(способ по настоящему изобретению)
Фракционирование: двойное фракционирование раствором LiCl до достижения его концентрации 2 М в целевом растворе и затем до достижения его концентрации 4 М в целевом растворе (двукратный повтор каждой стадии);
Депротеинизация: хлороформом в соотношении целевой раствор дсРНК : хлороформ от 1:2 до 1:10 по объему (2 раза);
Осаждение дсРНК: этанол (или др одноатомный спирт) до достижения его концентрации в целевом растворе 75 об. %
Фракционирование: двойное фракционирование раствором LiCl до достижения его концентрации 2М в целевом растворе и затем до достижения его концентрации 4М в целевом растворе (двукратный повтор каждой стадии);
Депротеинизация хлороформом в соотношении целевой раствор дсРНК : хлороформ от 1:2 до 1:10 по объему (2 раза);
Осаждение дсРНК: этанол (или др одноатомный спирт) до его концентрации в целевом растворе 75 об. %
Фракционирование: двойное фракционирование раствором LiCl до достижения его концентрации 2 М в целевом растворе и затем до достижения его концентрации 4 М в целевом растворе (двукратный повтор каждой стадии);
Депротеинизация: хлороформом в соотношении целевой раствор дсРНК : хлороформ от 1:2 до 1:10 по объему (2 раза);
Осаждение дсРНК: этанол (или др одноатомный спирт) до достижения его концентрации в целевом растворе 35 об. %
Дополнительно проводили идентификацию дсРНК, полученной способами 1-5, методами высокоэффективной жидкостной хроматографии (ВЭЖХ) и электрофореза в агарозном геле.
Результаты электрофоретических методов исследования представлены на Фиг. 1 и Фиг. 2.
На электрофореграмме дсРНК, полученной способом по настоящему изобретению (3 способ), были различимы две яркие контрастные полосы, соответствующие дсРНК (интервал значений от 4700 до 5300 пн, от 1400 до 1800 пн). Высокая контрастность полос обусловлена высокой степенью взаимодействия указанных соединений с интеркалирующим агентом – бромистым этидием. Высокая степень интеркалирования прямо свидетельствует о двуспиральной структуре молекулы. Яркость полос, соответствующих дсРНК, на электрофореграммах дсРНК, полученных способами 1-2, 4-5, была существеннее ниже, что свидетельствует о низком содержании дсРНК, при этом фиксировалось наличие впРНК (диапазон молекулярно- массового распределения впРНК начинался от десятков пн до примерно 1000 пн).
Целевой продукт, содержащий дсРНК, полученный способом 1, имел в своем составе значительное количество примесей и других нуклеиновых кислот, в т.ч. впРНК (примерно 50 %). Стадия депротеинизации не привела к значительному увеличению выхода продукта, который составил 135-177 мг на 1 кг биомассы клеток дрожжей.
Целевой продукт, содержащий дсРНК, полученный способом 2, содержал самое высокое содержание примесных белков (примерно 30 %), по сравнению со всеми остальными целевыми продуктами, полученными способами 1, 3-5, вследствие отсутствия отдельной стадии депротеинизации состава, а также примесей впРНК (примерно 30%), которые оставались в составе после осаждения раствором полиэтиленгликоля.
Целевой продукт, содержащий дсРНК, полученный способом 3, содержал следовые количества примесных белков и иных нуклеиновых кислот (в том числе высокополимерных РНК), при этом выход препарата дсРНК составил от 324 до 376 мг на 1 кг биомассы дрожжей.
В способах 4-5 варьировали концентрациями одноатомного спирта (в частности, этанола) при осаждении дсРНК. Выход и чистота целевых продуктов, полученных способами 4-5, были выше, чем в способах 1, 2. Количество примесных белков фиксировалось в районе 3-5 %, впРНК примерно 20 %, что существенно больше, чем в целевом продукте дсРНК, полученном способом по настоящему изобретению (3 способ).
Следовательно, предложенный способ получения дсРНК по настоящему изобретению за счет проведения нескольких этапов осаждения дсРНК одноатомным спиртом определенной концентрации, последовательных этапов очистки (две серии дробного фракционирования LiCl) и депротеинизации определенным объемом хлороформа позволяет значительно увеличить чистоту и выход целевого продукта в среднем примерно в 2 раза.
Таким образом, предложенный по настоящему изобретению способ получения дсРНК из клеток киллерного штамма дрожжей Saccharomyces cerevisiae позволяет получить целевой продукт с увеличенным выходом и чистотой.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ СУММАРНОЙ РНК ИЗ БИОМАССЫ КЛЕТОК ДРОЖЖЕЙ SACCHAROMYCES CEREVISIAE | 2022 |
|
RU2781832C1 |
| НОВЫЙ КИЛЛЕРНЫЙ ШТАММ ДРОЖЖЕЙ SACCHAROMYCES CEREVISIAE | 2022 |
|
RU2790685C1 |
| Новое применение природных двуспиральных РНК для лечения и/или профилактики вирусных инфекций | 2022 |
|
RU2781903C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДВУСПИРАЛЬНОЙ РИБОНУКЛЕИНОВОЙ КИСЛОТЫ (дсРНК) ИЗ КЛЕТОК ДРОЖЖЕЙ Saccharomyces cerevisiae | 2014 |
|
RU2558256C1 |
| Способ получения биологически активных компонентов из клеток дрожжей Saccharomyces cerevisiae и лечебное средство на их основе | 2018 |
|
RU2722731C2 |
| СПОСОБ ПОЛУЧЕНИЯ ДВУСПИРАЛЬНОЙ РИБОНУКЛЕИНОВОЙ КИСЛОТЫ | 2003 |
|
RU2302464C2 |
| Способ получения препаратов, обладающих адъювантными свойствами, при комплексной переработке киллерных дрожжей Saccharomyces cerevisiae | 2023 |
|
RU2836349C1 |
| ЛИПОСОМАЛЬНЫЙ ИНДУКТОР ИНТЕРФЕРОНА | 2004 |
|
RU2306936C2 |
| ИНДУКТОР ИНТЕРФЕРОНА ПРОЛОНГИРОВАННОГО ДЕЙСТВИЯ | 1999 |
|
RU2172631C2 |
| Способ фракционирования нуклеиновых кислот | 1989 |
|
SU1692986A1 |
Изобретение относится к области биотехнологии и фармацевтической промышленности. Предложен способ получения двуспиральной рибонуклеиновой кислоты (дсРНК) из клеток дрожжей киллерного штамма Saccharomyces cerevisiae ВКПМ Y448. Способ предусматривает разрушение клеток дрожжей, центрифугирование, отделение надосадочной жидкости и прецепитацию суммарной РНК. Полученный осадок отделяют и при перемешивании добавляют воду и хлорид натрия, отстаивают и центрифугируют. В полученный супернатант добавляют одноатомный спирт, чтобы его концентрация составила 40 об.% в целевом растворе, инкубируют и центрифугируют. К осадку при перемешивании добавляют буферный раствор и фракционируют раствором лития хлорида в две последовательные стадии: на первой стадии добавляют раствор хлорида лития до достижения его концентрации в суспензии 2 М, на второй стадии до достижения его концентрации в суспензии 4 М, полученную суспензию центрифугируют для отделения осадка и повторяют последовательное фракционирование растворами лития хлорида в две стадии. Полученную суспензию центрифугируют и ресуспендируют в буферном растворе, далее дважды проводят депротеинизацию хлороформом в соотношении целевой раствор : хлороформ от 1:2 до 1:10 по объему и осаждают дсРНК из суспензии раствором одноатомного спирта до достижения его концентрации в целевом растворе 75 об.%, полученный осадок дважды промывают 96% раствором одноатомного спирта. Изобретение обеспечивает достижение высокого выхода и чистоты целевого продукта дсРНК. 7 з.п. ф-лы, 2 ил., 1 табл., 2 пр.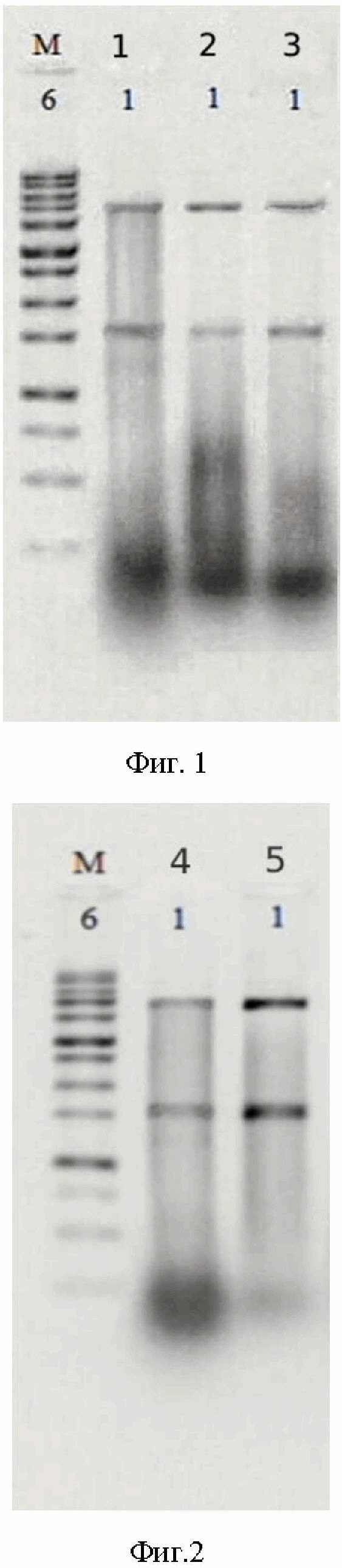
1. Способ получения двуспиральной рибонуклеиновой кислоты (дсРНК) из клеток дрожжей киллерного штамма Saccharomyces cerevisiae ВКПМ Y448, характеризующийся тем, что клетки дрожжей подвергают разрушению, центрифугируют, отделяют надосадочную жидкость и прецепитируют суммарную РНК, осадок отделяют и при перемешивании добавляют воду и хлорид натрия, отстаивают и центрифугируют, в полученный супернатант добавляют одноатомный спирт, чтобы его концентрация составила 40 об.% в целевом растворе, инкубируют и центрифугируют, к осадку при перемешивании добавляют буферный раствор и фракционируют раствором лития хлорида в две последовательные стадии: на первой стадии добавляют раствор хлорида лития до достижения его концентрации в суспензии 2 М, на второй стадии до достижения его концентрации в суспензии 4 М, полученную суспензию центрифугируют для отделения осадка и повторяют последовательное фракционирование растворами лития хлорида в две стадии, полученную суспензию центрифугируют и ресуспендируют в буферном растворе, далее дважды проводят депротеинизацию хлороформом в соотношении целевой раствор : хлороформ от 1:2 до 1:10 по объему и осаждают дсРНК из суспензии раствором одноатомного спирта до достижения его концентрации в целевом растворе 75 об.%, полученный осадок дважды промывают 96% раствором одноатомного спирта.
2. Способ получения по п. 1, в котором одноатомный спирт представляет собой метанол, этанол, пропанол, изопропанол, бутанол или изобутанол.
3. Способ получения по п. 2, в котором одноатомный спирт представляет собой этанол.
4. Способ получения по п. 3, в котором одноатомный спирт представляет собой 96% этанол.
5. Способ по п. 1, в котором хлорид натрия добавляют до его концентрации 2,0 М в целевом растворе.
6. Способ по п. 1, в котором депротеинизацию проводят хлороформом в соотношении целевой раствор : хлороформ 1:2 по объему.
7. Способ по п. 1, в котором используют водный раствор хлорида лития с концентрацией 8 М.
8. Способ по п. 1, отличающийся тем, что полученный дсРНК лиофильно высушивают.
| СПОСОБ ПОЛУЧЕНИЯ ДВУСПИРАЛЬНОЙ РИБОНУКЛЕИНОВОЙ КИСЛОТЫ (дсРНК) ИЗ КЛЕТОК ДРОЖЖЕЙ Saccharomyces cerevisiae | 2014 |
|
RU2558256C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДВУСПИРАЛЬНОЙ РИБОНУКЛЕИНОВОЙ КИСЛОТЫ | 2003 |
|
RU2302464C2 |
| Шевченко З.А | |||
| и др | |||
| Способ получения препаратов на основе РНК | |||
| Актуальные проблемы гуманитарных и естественных наук, 2017, 8-2, С.9-13 | |||
| Способ получения биологически активных компонентов из клеток дрожжей Saccharomyces cerevisiae и лечебное средство на их основе | 2018 |
|
RU2722731C2 |
| СПОСОБ ПОЛУЧЕНИЯ РИБОНУКЛЕИНОВОЙ КИСЛОТЫ | 1996 |
|
RU2103365C1 |
| Способ получения высокополимерной РНК из дрожжей | 1979 |
|
SU936701A1 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОПОЛИМЕРНОЙ РНК ИЗ ОТРАБОТАННЫХ ПИВНЫХ ДРОЖЖЕЙ | 2010 |
|
RU2435862C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОПОЛИМЕРНОЙ РНК ИЗ СУХИХ ПЕКАРСКИХ ДРОЖЖЕЙ | 2009 |
|
RU2403288C1 |
| СПОСОБ ВЫДЕЛЕНИЯ НУКЛЕИНОВЫХ КИСЛОТ | 2014 |
|
RU2584346C2 |
Авторы
Даты
2022-10-18—Публикация
2022-08-19—Подача