Изобретение относится к медицине, а именно к акушерству и гинекологии, и может быть использовано для оценки эффективности лечения внутривенными иммуноглобулинами у пациенток с привычным невынашиванием и циркуляцией антифосфолипидных антител.
Научные исследования указывают на взаимосвязь и общность механизмов развития гестационной патологии. Изменения в организме женщины начинаются с момента формирования и функционирования фетоплацентарного комплекса. Эволюционно сложившийся гемохориальный тип плацентации обеспечивает необходимую тесную взаимосвязь между организмом матери и плода для гармоничного и своевременного развития всех систем последнего. Данный тип плацентации с ранних сроков задействует все слои спиральных артерий, включая сосудистый эндотелий. Местная реакция на контакт двух генетически различных тканей может сопровождаться гиперактивацией защитных систем беременной и формировать специфический ответ на эти процессы, что, несомненно, может повлечь осложнения, изначально связанные с процессом плацентации.
Ни один орган не может сравниться с плацентой по разнообразию своих функций, потому что она выполняет действия всех основных систем органов, в то время как они дифференцируются и созревают у плода. Плацента также обладает основными эндокринными действиями, которые модулируют физиологию и метаболизм матери и обеспечивают безопасную и защитную среду, в которой может развиваться плод. Эффективность плацентарного обмена определяется сложным взаимодействием между ростом плаценты, экспрессией белка-переносчика, скоростью плацентарного кровотока, градиентами трансмембранной концентрации и метаболическими потребностями тканей плаценты. Это взаимодействие организуется материнскими, плацентарными и фетальными гормонами и при благоприятных условиях обеспечивает адекватное снабжение плода без чрезмерного истощения материнских резервов [Graham J. Burton and Abigail L. Fowden. The placenta: a multifaceted, transient organ. Philos Trans R Soc Lond B Biol Sci. 2015 Mar 5 DOI: 10.1098/rstb.2014.0066].
В случае нарушения маточно-плацентарных и плодово-плацентарных взаимоотношений формируется плацентарная недостаточность, которая представляет собой клинико-морфологический симптомокомплекс с острым или хроническим течением, возникающий в результате сочетанной реакции плода и плаценты на различные нарушения состояния материнского организма. Плацентарная недостаточность является самым распространенным осложнением в акушерской практике, встречается с частотой около 30 % [Ailamazyan E.K. Obstetrics: national guidelines / E.K. Ailamazyan, V.I. Kulakov, V.E. Radzinsky, G.M. Saveliev. - M.: GEOTAR - Media, 2014].
Формирование плацентарной недостаточности в 5-10% беременностей осложняются ограничением роста плода, которое характеризуется неспособностью плода достичь своего внутреннего потенциала роста. Нарушение внутриутробного развития плода служит риском неонатальной смертности, перинатальной заболеваемости и неблагоприятными долгосрочными последствиями, такими, как нарушение формирования и созревания центральной нервной системы, сердечно-сосудистыми, эндокринными и метаболическими заболеваниями [Romy E Bezemer, Mirthe H Schoots , Albertus Timmer. Altered Levels of Decidual Immune Cell Subsets in Fetal Growth Restriction, Stillbirth, and Placental Pathology. Frontiers in Immunology 2020 Aug 20 (11). DOI: 10.3389/fimmu.2020.01898].
Ограничение роста плода продолжает оставаться ведущей причиной предотвратимого мертворождения и негативных неврологических исходов у детей, а также преждевременных родов по медицинским показаниям со стороны плода. Изучение и выявление патогенеза как ранней, так и поздней задержки роста плода, особенно обусловленную плацентарной патологией, может дать представление о целенаправленном лечении, которое сохранит функцию плаценты [Melanie C. Audette, John C. Kingdom. Screening for fetal growth restriction and placental insufficiency. Semin Fetal Neonatal Med 2018 Apr; 23 (2) DOI: 10.1016/j.siny.2017.11.004].
Адекватное функционирование в системе «мать-плацента-плод» во многом определяется полноценным становлением кровотока, а также васкуло- и ангиогенезом. Васкулогенез – это образование новых кровеносных сосудов из мезодермальных клеток-предшественников эндотелиальных клеток (гемангиобластов), которое начинается в конце 3-й недели гестации [Rosen L.S. VEGF-targeted therapy: therapeutic potential and recent advances. Oncologist. 2005;10:382–391. DOI: 10.1634/theoncologist.10-6-382], тогда как ангиогенез связан с образованием сосудов из уже существующих структур за счет механизмов элонгации, инвагинации и капиллярного почкования [Соколов Д.И. Васкулогенез и ангиогенез в развитии плаценты. Журнал акушерства и женских болезней. 2007;56 (3):129–133].
Одним из значимых и достаточно изученных заболеваний в акушерской практике, оказывающих прямое повреждающее действие на гемодинамику фето-плацентарного комплекса является антифосфолипидный синдром (далее - АФС). АФС это аутоиммунное заболевание, характеризующееся развитием сосудистых тромбозов (артериальных и венозных) и/или акушерской патологии при наличии постоянно циркулирующих антифосфолипидных антител (антител к кардиолипину, далее – АФА), волчаночного антикоагулянта и антител к β2-гликопротеину-1, определенных у пациента два и более раз с интервалом не менее 12 недель [Miyakis S. International consensus statement on an update of the classification criteria for definite antiphospholipid syndrome (APS) / S. Miyakis, M.D. Lockshin, T. Atsumi et al. // J. Thromb. Haemost. - 2006. - Vol. 4. - № 2. - P. 295–306]. Кроме того, антифосфолипидные антитела многосторонне влияют на процессы трофобластической инвазии и фибриноидного моделировния сосудов с момента установления маточно-плацентарного кровотока.
Так у женщин с повышенным уровнем АФА при гистологическом исследовании плаценты отмечают: плацентарные инфаркты, децидуальное воспаление, увеличение числа синцитиальных почек, нарушение ремоделирования сосудистого русла, уменьшение васкулосинцитиальных мембран и отложение продуктов активации системы комплемента C4d [Viall C.A. Histopathology in the placentae of women with antiphospholipid antibodies: A systematic review of the literature / C.A. Viall, L.W. Chamley // Autoimmun. Rev. - 2015. - Vol. 14. - № 5. - P. 446–71].
Причиной развития акушерских осложнений при АФС длительное время считалось непосредственное образование тромбов в материнско-плацентарном кровотоке, однако тромбообразованием невозможно объяснить все гистопатологические процессы, обнаруживаемые в плацентах женщин с АФС [Viall C.A. Histopathology in the placentae of women with antiphospholipid antibodies: A systematic review of the literature / C.A. Viall, L.W. Chamley // Autoimmun. Rev. - 2015. - Vol. 14. - № 5. - P. 446–71] и создало предпосылки для выявления иных значимых факторов развития патологических процессов на границе матери и плода.
Одним из таких факторов стал белок кисспептин – важнейший элемент репродуктивной системы человека. Пептид отвечает за начало полового созревания в пубертатный период и регулирует эндокринные функции на последующих этапах жизни человека. Также кисспептины участвуют в поддержании гомеостаза организма (Mead EJ, Maguire JJ, et al, 2007).
Кисспептин был открыт американскими учеными в 1996 году при изучении злокачественных меланом, и изначально определялся как ген-супрессор метастаз, но позже был обнаружен и в некоторых, не относящихся к онкогенным, опухолях молочной железы (Lee JH, Miele ME, et al, 1996; Ikeguchi и др, 2003). Лишь в 2001 году после того, как из плаценты человека были выделены три биологически активных пептида, продукта расщепления препрокисспептина KiSS1 (предшественника кисспептина) длина которого составляет 138 аминокислотных остатков: KP-54, KP-13 и KP-10, эти соединения были названы кисспептинами. Первоначально ученые выделили самый большой фрагмент кисспептин-54 (КР-54), обладающий антиметастатическим потенциалом в клетках меланомы человека и мыши и получивший название метастин (Kotani et al., 2001; Ohtaki et al., 2001; Strausberg RL, Feingold EA, Grouse LH, et al., 2002.
Свое биологическое влияние на органы и ткани кисспептин реализует через рецептор к кисспептину – KiSS1R, состоящий из 398 аминокислот, принадлежит к обширному семейству трансмембранных рецепторов и связан с гетеротримерным G-белком, в состав которого входит активирующая фосфолипазу С альфа-субъединица (Bockaert, J. and Pin, J.P., 1999; Pankov YA, 2015). KiSS1R также известен под названиями GPR54, AXOR12, CPPB1, HH8 или hOT7T17, и локализуется в мембране клеток (Kotani M, Detheux M, Vandenbogaerde A, et al., 2001). Мембранные рецепторы KiSS1R были идентифицированы на клетках иммунной системы, включая моноциты. У человека KiSS1R расположен в пятом экзоне хромосомы 19. Хромосомная локализация препрокисспептина и KiSS1R других биологических объектов отражена (Pankov YA, 2015; Mead EJ, Maguire JJ, et al, 2007).
Группами авторов (Shirasaki et al, 2001, Sanchez-Carbayo et al, 2003) было установлено, что кисспептин выступают не только в качестве ингибиторов метастазирования меланомы, но и как регуляторы метастатического потенциала в различных раковых образованиях. Установлены различия в уровнях кисспептина и KISS1R в нативных раковых клетках доброкачественной и злокачественной опухолей. Большинство полученных данных свидетельствуют о снижении экспрессии кисспептина в метастазирующих образованиях, при этом имеются сведения о полном отсутствии кисспептина в метастазах. Корреляция морфологических стадий опухолей с уровнем экспрессии кисспептина показала, что количество белка снижается по мере прогрессирования рака. Высокий уровень экспрессии был обнаружен в доброкачественных образованиях, а также в радиальной фазе роста опухоли. На более поздних стадиях наблюдалось снижение уровня экспрессии (Ikeguchi и др, 2003; Sanchez-Carbayo и др, 2003). Помимо антираковых свойств, исследователи утверждают, что кисспептины отвечают за необходимую активность и выработку клеток гипофиза, управляющего уровнями лютеинизирующего и фолликулостимулирующего гормонов, от которых зависит зачатие.
Наиболее высокая экспрессия кисспептинов была обнаружена в поджелудочной железе, плаценте, спинном мозге, что указывает на роль белков в регуляции эндокринных функций. Данная гипотеза была убедительно доказана в опытах по стимуляции секреции окситоцина у крыс после введения кисспептинов. Меньший уровень экспрессии выявлен в лейкоцитах периферической крови, почках, легких, печени плода, желудке, тонкой кишке, семенниках, селезенке, тимусе, надпочечниках и лимфатических узлах. В мозге взрослого человека экспрессия выявлена в верхних лобных извилинах, хвостатых ядрах, базальных ядрах (в основании переднего мозга), поясной извилине, мосте, гиппокампе, миндалинах, а также в гипофизе и гипоталамусе (Kotani M, Detheux M, Vandenbogaerde A, et al., 2001).
Гипоталамическая система кисспептин/KISS1R – основной фактор в центральной регуляции гонадотропина в период полового созревания и во взрослой жизни. Рецептор к кисспептинам также возможно вовлечен в регуляцию инвазии трофобласта, которая генерируется самим трофобластом. Анализ путей передачи, активируемых рецептором, выявил связь между фосфолипазой-С и внутриклеточным высвобождением кальция (Ca2+) через токсин-нечувствительные G(q)-белки коклюша (Kotani M, Detheux M, Vandenbogaerde A, et al., 2001).
Методами количественной PCR и микрочипирования было установлено, что у человека самый высокий уровень экспрессии препрокисспептина и KISS1R наблюдается в клетках трофобласта (Janneau и др., 2002; Bilban и др., 2004). При использовании лазерной захватывающей микродиссекции кисспептин и KISS1R были обнаружены в ворсинчатом цитотрофобласте. Изменение уровня кисспептина на протяжении всей беременности и его экспрессия в вышеупомянутых клетках указывают на участие данного белка в плацентации. Поэтому предполагается, что измененная плацентарная экспрессия препрокисспептина и / или KISS1R может быть связана с аномальной плацентацией. и, как итог, развитием преэклампсии (ПЭ). Дополнительным подтверждением этого является наблюдение более низких концентраций циркулирующего препрокисспептина в образцах сыворотки в начале второго триместра у женщин, у которых впоследствии развивается ПЭ и задержка внутриутробного роста (Armstrong et al. 2009). Установлено, что помимо антиметастатических свойств, кисспептин супрессируют миграцию клеток трофобласта, что связывают с подавлением ММР-2 и ММР-9 активности.
Повышенный уровень экспрессии KiSS1R в плаценте наблюдается на 7-9 неделях беременности. Степень экспрессии этого белка повышена как в ранней плаценте, так и при пузырном заносе (трофобластическая болезнь), и понижена в клетках хориокарциномы Уровень экспрессии KISS1R значительно выше в первом триместре беременности, чем на последующих сроках гестации, что предполагает его участие в различных эндокринных/паракринных механизмах (Mead EJ, Maguire JJ, et al, 2007, Траль Т.Г.).
Помимо экспрессии кисспептин-54 в цитотрофобласте ворсин хориона, обнаруженной на уровне мРНК методом иммуногистохимического окрашивания, найдена кисспептин-54-подобная иммунореактивность в синцитиотрофобласте ворсин, которые отвечают за секрецию пептидов в кровоток матери (Mead EJ, Maguire JJ, et al, 2007).
Исследование KISS1R и кисспептина в сосудистой сети показало дискретную локализацию KISS1R в кровеносных сосудах, подверженных атеросклерозу, а также обнаружило мощное сосудосуживающее действие пептида (EJ Mead, JJ Maguire, RE Kuc and AP Davenport).
В плазме крови человека обнаружен белок кисспептин-54 в концентрациях приблизительно 1 fmol/ml, который характерен как для мужчин, так и для женщин. Измерения уровня кисспептин -54 на протяжении беременности показали количественное увеличение данного белка в 1000 раз в третьем триместре, по сравнению с его уровнем в период первого триместра беременности, что указывает на значимый синтез кисспептина плацентой. Уровень кисспептин -54 возвращался к обычному значению уже на 5-й день после родов.
Кисспептин детектируется в периферической крови только во время беременности и является важным регулятором функций моноцитов в этот период. Выявлено, что кисспептин в концентрации, соответствующей III триместру беременности, стимулирует фагоцитарную активность моноцитов и во всех исследуемых концентрациях повышает продукцию активных форм кислорода в реакции спонтанной и стимулированной люминолзависимой хемилюминесценции. Показано, что кисспептин в концентрации, соответствующей II триместру беременности, понижает активность внутриклеточной миелопероксидазы (МПО) моноцитов, повышая при этом активность секреторной МПО и липополисахарида индуцированной индоламин-2,3-диоксигеназы (Горбунова О.Л., 2013).
Особенно это актуально для гормонов. Кисспептин, продуцируемый плацентой во время беременности в системный кровоток матери, обладает иммуномодулирующим действием за счет клеток иммунной системы, экспрессирующих для него специфические мембранные рецепторы (Friedman Zoey, 2013).
Показано, что кисспептин в концентрациях, характерных для I-III триместров беременности, усиливает формирование Treg-лимфоцитов (CD4+FOXP3+CTLA-4+ GITR+) из TGF-ß1-примированных CD4+Т-лимфоцитов, повышая продукцию IL-10 CD4+T-лимфоцитами женщин. Одновременно кисспептин снижает уровень Тh17-клеток и секрецию IL-17A СD4+ Т-лимфоцитами. В концентрации, соответствующей II триместру беременности, гормон достоверно усиливает липополисахаридиндуцируемую активность IDO моноцитами. Таким образом, кисспептин является новым, ранее не учитываемым фактором формирования иммунологической толерантности в период физиологически протекающей беременности (Горбунова О.Л., Ширшев С.В., 2014).
Проблема невынашивания беременности при иммунологической патологии, а также ассоциированных с ними высоких рисков тромбоэмболических осложнений, является одной из наиболее актуальных в современной репродуктивной медицине.
На сегодняшний день не сформулированы единые терапевтические рекомендации для осуществления иммунотерапии АФС при ведении беременности. В прошлом веке иммунотерапия АФС проводилась с помощью метода иммунносупрессии (глюкокортикоидами).
Теоретическим обоснованием применения глюкокортикоидов является их противовоспалительная активность и снижение уровня АФА при их применении. Однако в работе Lockshin M (1989) представлены данные о неэффективности преднизолона у пациенток с синдромом потери плода и АФС, а также данные об угрозе здоровью для матери и плода при его применении. Наличие многочисленных побочных эффектов у глюкортикоидов переключило внимание ученых в сторону разработки методов иммуномодуляции, например, с помощью внутривенных иммуноглобулинов (ВВИГ) (Prednisone does not prevent recurrent fetal death in women with antiphospholipid antibody. Lockshin MD, Druzin ML, Qamar T.Am J Obstet Gynecol. 1989 Feb; 160(2):439-43.)
В акушерско-гинекологической практике для лечения женщин с АФС ВВИГ был впервые предложен к применению в 1992 году как альтернатива глюкортикоидам. К настоящему времени они стали препаратами выбора при лечении антифосфолипидного синдрома у беременных женщин. На данный момент нет установленных критериев оценки эффективности лечения ВВИГ беременных.
В послеродовой период проводится рутинное гистологическое исследование плаценты необходимое для выявления хронической или острой плацентарной недостаточности, стадии компенсаторных механизмов, а также выявления инфекционного поражения плаценты. Однако гистологическое исследование не позволяет достоверно оценить эффективность лечения внутривенными иммуноглобулинами у пациенток с привычным невынашиванием и циркуляцией антифосфолипидных антител на молекулярном уровне, что требует проведения дополнительных высокотехнологичных методов диагностики.
В клинической практике иммуногистохимические исследование для оценки эффективности терапии антифосфолипидного синдрома не проводится.
Предложенная методика имеет особое значение для обоснования терапии пациенток с привычным невынашиванием и АФА в период беременности. Применение предлагаемого способа оценки эффективности лечения ВВИГ беременных в практическом здравоохранении позволит акушерам-гинекологам получить данные для разработки персонифицированного подхода при реабилитации женщин в послеродовом периоде, а также для предгравидарной подготовки к следующей беременности с целью снижения рисков развития акушерских осложнений.
Задачей предлагаемого способа является обеспечение точной и достоверной оценки эффективности лечения внутривенными иммуноглобулинами у пациенток c привычным невынашиванием и циркуляцией антифосфолипидных антител.
Техническим результатом заявляемого способа является расширение арсенала морфологических диагностических средств оценки эффективности лечения внутривенными иммуноглобулинами у пациенток c привычным невынашиванием и циркуляцией антифосфолипидных антител.
Заявляемый технический результат достигается тем, что при иммуногистохимическом исследовании плаценты определяют площадь экспрессии кисспептина (KISS) и его рецептора (KISS1R). При значении относительной площади экспрессии кисспептина равном 35% или более подтверждают эффективность лечения внутривенными иммуноглобулинами у пациенток c привычным невынашиванием и циркуляцией антифосфолипидных антител.
Новизна изобретения заключается в том, что для оценки эффективности лечения внутривенными иммуноглобулинами у пациенток c привычным невынашиванием и циркуляцией антифосфолипидных антител впервые определяют экспрессию кисспептина и его рецептора в виллезном дереве плаценты.
Гистологическое и иммуногистохимическое исследование проводилось в лаборатории иммуногистохимии ФГБНУ «НИИ АГиР им. Д.О. Отта. Иммуногистохимическое исследование проводили на парафиновых срезах толщиной 5 мкм, которые помещали на предметные стекла, покрытые пленкой из поли-L-лизина. Для проведения иммуногистохимической реакции использовали стандартный одноэтапный протокол с демаскировкой антигена (высокотемпературной обработкой ткани) в 0,01 М цитратном буфере рН 6.0. В качестве системы визуализации использовали abcamMouseandRabbitSpecific HRP Plus (ABC) Detection IHC Kit (RTU)[ab93697].
Иммуногистохимический метод исследования включал: количественную и качественную оценку экспрессии кисспептина (KISS) и его рецептора (KISS1R). Антитела использованы в стандартном разведении в соответствии с рекомендациями фирмы производителя.
Количественную оценку результатов иммуногистохимической реакции проводили на микрофотографиях, полученных с помощью системы фиксации микроскопических изображений, состоящей из микроскопа Olympus BX46 и программного обеспечения «CellSens 47 Entry». Из фотосъемки исключались поля зрения, содержащие дефекты ткани, дефекты окрашивания и артефакты. Фотосъемку производили на увеличении 400× (окуляр 10×, объектив 40×), в режиме Photo, время экспозиции 1/38 с, чувствительность камеры – максимальная, размер изображения 2080×1544 пикселей, графический формат изображения JPEG (normal). Долю занимаемой экспрессии изучаемого маркера рассчитывали с помощью программы «VideotestMorphology 5.2».
В каждом срезе в 5 полях зрения оценивали следующие показатели:
оптическую плотность экспрессии являющегося базовым параметром программы «VideotestMorphology 5.2» и относительную площадь экспрессии – вычисляли как отношение площади иммунопозитивных клеток к общей площади препарата: после чего вычислялись средние величины исследуемых показателей.
Сущность заявляемого способа поясняется следующими примерами.
Пример 1.
Пациентка У., 36 лет. В анамнезе – неразвивающаяся беременность 8/9 недель, неразвивающаяся беременность 9/10 недель, самопроизвольный выкидыш при сроке 14 недель. Данная беременность IV, самостоятельная.
Обратилась при сроке 8/9 недель. По данным обследования – выявлен положительный волчаночный антикоагулянт (1,45), гипергомоцистеинемия.
Диагноз: Беременность 8/9 недель. Носительство волчаночного антикоагулянта. Привычное невынашивание. Отягощенный гинекологический анамнез.
Проводилось лечение внутривенными иммуноглобулинами – 3 курса: в 8/9 недель, 16 недель, 24 недели: 5%-100 мл внутривенно медленно 3 раза с интервалом 5 дней. За время течения беременности неоднократно госпитализировалась в отделение патологии беременности с целью контроля показателей гемостаза, фетометрии, допплерометрии. Данных за хроническую плацентарную недостаточность при беременности не получено.
При сроке 38 5/7 недель самостоятельно вступила в роды. Роды велись под постоянным кардиомониторным наблюдение за состоянием плода. Родился мальчик массой 3760 грамм, длиной 54 см с оценкой по шкале Апгар 8/9 баллов. Роды проведены через естественные родовые пути. Через 10 минут самостоятельно отделилась плацента и выделился послед, без дефектов плацентарной ткани. Кровопотеря составила 270 мл. Послед был направлен на гистологическое и иммуногистохимическое исследование.
Результаты гистологического исследования выявили соответствие строения плаценты сроку гестации с умеренно выраженными циркуляторными нарушениями и равномерным распределением компенсаторных механизмов.
Площадь экспрессии маркера вычисляли как отношение площади иммунопозитивных клеток к общей площади препарата (таблица 1):

Данные иммуногистохимического исследования площади экспрессии кисспептина и его рецептора представлены в таблице 1 и 2.
Таблица 1.
Площадь экспрессии кисспептина в виллезном дереве плаценты
Площадь экспрессии кисспептина в препарате составила 54,12%.
Таблица 2
Площадь экспрессии рецептора кисспептина (KISS1R) в виллезном дереве плаценты
Площадь экспрессии рецептора KISS1R в препарате составила 28,637% (Таблица 2).
Площадь экспрессии кисспептина более 35% указывает на эффективность применения терапии иммуноглобулинами.
Пример 2.
Пациентка С., 39 лет. В анамнезе – 1 срочные роды в 18 лет (2000 г.) без осложнений, в 2013 году – преждевременная отслойка нормально расположенной плаценты при сроке 22/23 недели, антенатальная гибель плода, кровотечение. В 2015 г. – неразвивающаяся беременность 8 недель. В 2016 году – срочные роды в 38/39 недель, при беременности обследовалась, учитывая наличие титра антител к аннексину V, волчаночного антикоагулянта, был проведен курс внутривенных иммуноглобулинов. Данная беременность V, самостоятельная. Обратилась при сроке 7 недель. При обследовании выявлены антитела к аннексину V в титре 16,03 Ед/мл. Учитывая наличие высокого титра антител к аннексину V, отягощенный акушерский анамнез, проведено лечение внутривенными иммуноглобулинами – 3 курса: в 8/9 недель, 16 недель, 24 недели: 5%-100 мл внутривенно медленно 3 раза с интервалом 5 дней. При сроке 9 недель выявлен гестационный сахарный диабет, с 20 недель начата инсулинотерапия. Неоднократно госпитализировалась с целью контроля за показателями свертывающей системы крови, коррекции углеводного обмена, установки разгрузочного акушерского пессария, а также проведения антибактериальной терапии в связи с бактериурией и обострением хронического гайморита.
Поступила для планового родоразрешения при сроке 38 недель с диагнозом: Беременность 38 0/7 недель. Истмико-цервикальная недостаточность. Акушерский разгрузочный пессарий удален 12.11.19. Рубец на матке после 2-х операций кесарева сечения. Хронический гайморит, обострение от 21.10.19. Пункция верхнечелюстных пазух от 24.10. и 29.10.19. Антифосфолипидный синдром. Гипергомоцистеинемия. Гестационный сахарный диабет (инсулинотерапия с 20 недель). Диффузно-дистрофическое заболевание позвоночника, вертебро-цервикогенные краниалгии, грыжеобразование C5-C6, C6-C7. Отягощенный акушерско-гинекологический анамнез (преждевременная отслойка нормально расположенной плаценты в 22/23 недели, экстренное кесарево сечение).
Родоразрешена путем операции кесарева сечения, родился мальчик массой 3700 грамм, длиной 53 см с оценкой по шкале Апгар 8/9 баллов. Кровопотеря составила 870 мл.
Плацента отправлена на гистологическое и иммуногистохимическое исследование.
Результаты гистологического исследования выявили соответствие строения плаценты сроку гестации со слабо выраженными циркуляторными нарушениями и равномерным распределением компенсаторных и приспособительных механизмов.
Данные иммуногистохимического исследования площади экспрессии кисспептина представлены в таблице 3.
Таблица 3.
Площадь экспрессии кисспептина в виллезном дереве плаценты
Площадь экспрессии KISS в препарате составила 39,027%.
Данные об экспрессии рецептора кисспептина представлены в таблице 4
Таблица 4.
Площадь экспрессии рецептора кисспептина (KISS1R) в виллезном дереве плаценты
Площадь экспрессии рецептора KISS1R в препарате составила 34,706%.
Площадь экспрессии кисспептина более 35% указывает на эффективность применения терапии иммуноглобулинами.
Пример 3.
Пациентка О., 32 лет. В анамнезе В анамнезе — 1 неразвивающаяся беременность 8/9 недель, 2 самопроизвольных выкидыша при сроке 15 недель и 6 недель. Данная беременность IV, самостоятельная. Обратилась при сроке 7/8 недель. При обследовании выявлен высокий титр волчаночного антикоагулянта (1,38), гипергомоцистеинемия. Проводилось лечение внутривенными иммуноглобулинами – 3 курса: в 8/9 недель, 16 недель, 24 недели: 5%-100 мл внутривенно медленно 3 раза с интервалом 5 дней. За время течения беременности неоднократно госпитализировалась в отделение патологии беременности с целью контроля показателей гемостаза, фетометрии, допплерометрии. Данных за хроническую плацентарную недостаточность при беременности не получено.
При сроке 39 0/7 недель самостоятельно вступила в роды. Роды велись под постоянным кардиомониторным наблюдение за состоянием плода. Родилась девочка массой 3230 грамм, длиной 51 см с оценкой по шкале Апгар 8/9 баллов. Роды проведены через естественные родовые пути. Через 5 минут самостоятельно отделилась плацента и выделился послед, без дефектов плацентарной ткани. Кровопотеря составила 280 мл. Послед был направлен на гистологическое и иммуногистохимическое исследование.
Результаты гистологического исследования выявили соответствие строения плаценты сроку гестации с умеренно выраженными циркуляторными нарушениями и равномерным распределением компенсаторных и приспособительных механизмов.
Данные иммуногистохимического исследования площади экспрессии кисспептина представлены в таблице 5.
Таблица 5.
Площадь экспрессии кисспептина (KISS1) в виллезном дереве плаценты
Площадь экспрессии KISS1 в препарате составила 41,394%.
Данные об экспрессии рецептора кисспептина представлены в таблице 6
Таблица 6.
Площадь экспрессии кисспептина (KISS1) в виллезном дереве плаценты
Площадь экспрессии рецепторов KISS1R в препарате составила 25,430%.
Площадь экспрессии кисспептина более 35% указывает на эффективность применения терапии иммуноглобулинами.
Пример 4.
Пациентка У., 34 лет. В анамнезе В анамнезе — 1 неразвивающаяся беременность 7/8 недель, 2 самопроизвольных выкидыша при сроке 13 недель и 9 недель. Данная беременность IV, самостоятельная. Обратилась при сроке 9 недель. При обследовании выявлен высокий титр волчаночного антикоагулянта (1,65), гипергомоцистеинемия. Проведена терапия внутривенными иммуноглобулинами – 1 курс в 9 недель: 5%-100 мл внутривенно медленно 3 раза с интервалом 5 дней. От предложенного дальнейшего лечения внутривенными иммуноглобулинами пациентка категорически отказалась. При сроке 25 недель выявлено нарушение гемодинамики I степени. По данным ультразвукового исследования – признаки асимметричной формы гипотрофии плода. За время течения беременности неоднократно госпитализировалась в отделение патологии беременности с целью контроля показателей гемостаза, фетометрии, допплерометрии. Получала терапию, улучшающую маточно-плацентарный кровоток, терапию угрожающих преждевременных родов, при сроке 28 недель проведена профилактика респираторного дистресс синдрома плода.
При сроке 36 0/7 недель самостоятельно вступила в роды. Роды велись под постоянным кардиомониторным наблюдение за состоянием плода. В связи с появлением признаков начавшейся гипоксии плода по данным кардиотокографии, родоразрешена оперативным путем в экстренном порядке. Родилась недоношенная гипотрофичная девочка массой 2030 грамм, длиной 48 см с оценкой по шкале Апгар 7/8 баллов. Кровопотеря составила 580 мл. Послед был направлен на гистологическое и иммуногистохимическое исследование.
Результаты гистологического исследования выявили несоответствие строения плаценты сроку гестации с выраженными циркуляторными нарушениями.
Данные иммуногистохимического исследования площади экспрессии кисспептина представлены в таблице 7.
Таблица 7.
Площадь экспрессии кисспептина в виллезном дереве плаценты
Площадь экспрессии кисспептина в препарате составила 19,230%.
Данные об экспрессии рецептора кисспептина представлены в таблице 8
Таблица 8.
Площадь экспрессии кисспептина в виллезном дереве плаценты
Площадь экспрессии рецепторов KISS1R в препарате составила 13,071%.
Таким образом, площадь экспрессии кисспептина менее 35% указывает на неэффективность применения терапии иммуноглобулинами при неполном курсе лечения.
Изобретение относится к медицине, а именно к акушерству и гинекологии, и может быть использовано для оценки эффективности лечения внутривенными иммуноглобулинами у пациенток с привычным невынашиванием и циркуляцией антифосфолипидных антител. Путем иммуногистохимического исследования плаценты определяют экспрессию кисспептина (KISS). Производят определение относительной площади экспрессии KISS, которое рассчитывают по формуле 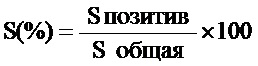 , где S(%) - относительная площадь экспрессии KISS, S позитив – значение площади иммунопозитивных клеток KISS; S общая – значение площади препарата. При значении относительной площади экспрессии KISS равном 35% и более подтверждают эффективность лечения. Способ обеспечивает возможность обеспечения точной и достоверной оценки эффективности лечения внутривенными иммуноглобулинами у пациенток c привычным невынашиванием и циркуляцией антифосфолипидных антител за счет определения экспрессии KISS при иммуногистохимическом исследовании плаценты. 8 табл., 4 пр.
, где S(%) - относительная площадь экспрессии KISS, S позитив – значение площади иммунопозитивных клеток KISS; S общая – значение площади препарата. При значении относительной площади экспрессии KISS равном 35% и более подтверждают эффективность лечения. Способ обеспечивает возможность обеспечения точной и достоверной оценки эффективности лечения внутривенными иммуноглобулинами у пациенток c привычным невынашиванием и циркуляцией антифосфолипидных антител за счет определения экспрессии KISS при иммуногистохимическом исследовании плаценты. 8 табл., 4 пр.
Способ оценки эффективности лечения внутривенными иммуноглобулинами у пациенток с привычным невынашиванием и циркуляцией антифосфолипидных антител, отличающийся тем, что путем иммуногистохимического исследования плаценты определяют экспрессию кисспептина (KISS), производят определение относительной площади экспрессии KISS, которое рассчитывают по формуле
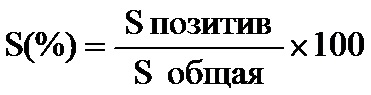 ,
,
где S(%) - относительная площадь экспрессии KISS,
S позитив - значение площади иммунопозитивных клеток KISS;
S общая - значение площади препарата;
и при значении относительной площади экспрессии KISS равном 35% и более подтверждают эффективность лечения.
| WO 2021032973 A1, 25.02.2021 | |||
| WO 2004026333 A1, 01.04.2004 | |||
| ТРАЛЬ Т.Г | |||
| Морфологические и иммуногистохимические особенности неразвивающейся беременности I триместра | |||
| Автореф | |||
| диссер | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| JAYASENA C.N | |||
| et al | |||
| Reduced levels of plasma Kisspeptin during the antenatal booking visit are associated with increased risk of miscarriage | |||
Авторы
Даты
2022-11-08—Публикация
2021-11-14—Подача