Изобретение относится к медицине, а именно к акушерству и гинекологии, и может быть использовано для оценки эффективности лечения внутривенными иммуноглобулинами у пациенток с привычным невынашиванием и циркуляцией антифосфолипидных антител.
В настоящее время около 15–20% всех наступивших беременностей заканчивается неудачно – беременность либо не развивается, либо прерывается (самопроизвольный выкидыш). Считается, что у здоровой пары может встречаться не более 3 случаев невынашивания беременности на сроках до 20 недель беременности, и это не требует какого-либо лечения. Однако при превышении этого порога состояние уже называют привычным невынашиванием беременности (ПНБ), или привычным выкидышем. Существует мнение, что этот диагноз должен ставиться уже после 2 произошедших выкидышей, поскольку вероятность последующего невынашивания беременности после 2-го и 3-го выкидышей схожа. Частота ПНБ в популяции составляет 2% всех беременностей. Риск повторного невынашивания после 2 выкидышей составляет 24%, после 3 - 30%, после 4 – 40% (Сидельникова В.М., Сухих Г.Т. Невынашивание беременности. М.: Мед. информ. агентство, 2010).
Привычное невынашивание беременности – широко распространенная и до сих пор до конца нерешенная проблема. Причины ПНБ разнообразны: инфекционно-воспалительные заболевания органов малого таза, нарушения в системе гемостаза (наследственная тромбофилия, нарушения фолатного цикла и пр.), аутоиммуная патология, хромосомные анеуплоидии, эндокринные нарушения, истмико-цервикальная недостаточность и др.
Проблема невынашивания беременности при аутоиммунной патологии, а также ассоциированных с ней высоких рисков тромбоэмболических осложнений, является одной из наиболее актуальных в современной репродуктивной медицине.
Заболеваемость аутоиммунной патологией неуклонно растет и достигает в популяции 7,6–9,4%, причем преимущественно среди лиц репродуктивного возраста, что придает им социально-экономическую значимость. Наибольшую роль среди аутоиммунных заболеваний в отношении репродуктивных потерь имеет антифосфолипидный синдром (АФС). Беременность при первичном АФС осложняется преэклампсией у 2%-8% женщин, плацентарной недостаточностью у 11%, преждевременными родами у 28%, внутриутробной гибелью плода у 7%. При вторичном АФС, возникшем на фоне другого аутоиммунного заболевания – системной красной волчанки, риски акушерских осложнений многократно возрастают. Риск преэклампсии при этом увеличивается и составляет от 32% до 50%, а преждевременных родов от 32% до 65%. Но наибольшее значение АФС имеет в отношении невынашивания беременности, являясь причиной привычного невынашивания у 7%-42% женщин (Шаповалова Е.А. Привычное невынашивание беременности при наличии циркулирующих антифосфолипидных антител (клиника, диагностика, лечение): Автореф. дисс. канд. мед. наук. – Санкт-Петербург. – 2001).
С 2006 года диагноз АФС устанавливается в соответствии с Международными критериями, принятыми в Сиднее в 2006 (Sydney Consensus Workshop, Sydney, 2006) (Miyakis S. International consensus statement on an update of the classification criteria for definite antiphospholipid syndrome (APS) / S. Miyakis, M.D. Lockshin, T. Atsumi et al. // J. Thromb. Haemost. - 2006. - Vol. 4. - № 2. - P. 295–306).
Лабораторными критериями признаны:
- положительный лабораторный тест на волчаночный антикоагулянт (ВА), обнаруженный в плазме два или более раз, с промежутком между исследованиями не менее 12 недель, с помощью комплекса из скринингового, подтверждающего и корректирующего коагулогических тестов в соответствии с требованиями Международного общества изучения тромбозов и гемостаза;
- обнаружение антител к кардиолипину классов IgG и/или IgM в сыворотке или плазме в среднем или высоком титре (т.е. >40 GPL или MPL, или более 99ого перцентиля здоровой популяции), повторно обнаруженные через не менее чем 12 недель, выявленные с помощью стандартизованной тест системы для иммуноферментного анализа (ИФА);
- обнаружение антител к β2-гликопротеину-1 классов IgG и/или IgM в сыворотке или плазме в титре более 99ого перцентиль здоровой популяции, выявленные не менее 2 раз с интервалом 12 недель с помощью стандартизованной ИФА- тест системы.
Клиническими критериями АФС признаны:
1. Сосудистый тромбоз: один или несколько эпизодов артериального, венозного или тромбоза мелких сосудов (за исключением поверхностных вен голени) в любой ткани или органе, подтвержденный с помощью КТ/МРТ, доплеровского исследования или морфологически. При гистологическом исследовании тромбоз не должен сочетаться с воспалительными изменениями стенки сосуда;
2. Патология беременности:
- одна или более неясная смерть морфологически нормального плода старше 10 недель беременности, с нормальной морфологией по данным ультразвукового исследования (УЗИ) или прямого обследования плода;
- одни или более преждевременные роды морфологически нормальным новорожденным до 34 недель гестации вследствие эклампсии, тяжелой преэклампсии или плацентарной недостаточности;
- три и более необъяснимых спонтанных выкидышей до 10 недель беременности после исключения анатомических, гормональных и генетических причин невынашивания.
Достаточно часто имеются клинические критерии АФС, но нет лабораторных, либо выявляются так называемые «неклассические» аутоантитела – например, к аннексину V, фосфатидилсерину, фосфатидилэтаноламину, протромбину.
Антифосфолипидные антитела (АФА) представляют собой семейство гетерогенных ауто- и аллоиммунных иммуноглобулинов: IgG, IgM и IgA, направленных против фосфолипидов (ФЛ) плазматической мембраны клеток.
Патогенез практически всех клинических проявлений АФС, включая акушерские осложнения, универсален и осуществляется через нарушение микроциркуляции, гемостаза и патологию сосудистой стенки. АФА способны опосредованно повреждать мембрану эндотелия, нарушая баланс в звене естественных антикоагулянтов и ингибиторов свертывания, и провоцировать гиперкоагуляцию.
Причиной развития акушерских осложнений при АФС длительное время считалось непосредственное образование тромбов в материнско-плацентарном кровотоке, однако тромбообразованием невозможно объяснить все гистопатологические процессы, обнаруживаемые в плацентах женщин с АФС. Так, например, на культуре клеток эндометрия человека, прокультивированном с поликлональными β2-гликопротеинзависимыми IgG, выделенными из крови пациенток с АФС, обнаружено, что АФА ингибируют процессы ангиогенеза в эндометрии благодаря снижению выработки сосудистого эндотелиального фактора роста VEGF (англ. Vascular endothelial growth factor).
Еще одним возможным патогенетическим механизмом в развитии репродуктивных потерь при АФС можно назвать разрушение «аннексинового щита» на поверхности клеток трофобласта. В процессе дифференцировки трофобласта одновременно с экстернализацией фосфолипидов (ФЛ) происходит выработка естественного антикоагулянта аннексина V. Он покрывает ФЛ по типу ковра, оказывая местный антикоагулянтный эффект, что препятствует тромбообразованию во время беременности. АФА в присутствии β2 гликопротеина -1 нарушают локальную антикоагулянтную активность аннексина V, вытесняя его с поверхности трофобласта, в результате чего анионные фосфолипиды начинают свободно контактировать с плазмой крови, что приводит к запуску коагуляционного каскада (Макацария А.Д. Патогенетическое значение антифосфолипидных антител / А.Д. Макацария, В.О. Бицадзе, Д.Х. Хизроева, Н.А. и др. // Практическая медицина. - 2012. - № 5 (60). С. 9-21).
В исследованиях данной тематики было показано, что у женщин с наследственной предрасположенностью к повышенному тромбообразованию при наличии повышенного титра аутоиммунных антител беременность протекает с угрозой прерывания в 77,7% случаев. При этом чаще обнаруживаются маркеры антифосфолипидного синдрома: волчаночный антикоагулянт (32%) и антитела к аннексину V (20,5%). (Rand J.H., Wu X.X., Quinn A.S., Taatjes D.J. Resistance to annexin A5 anticoagulant activity: a thrombogenic mechanism for the antiphospholipid syndrome. – Department of Pathology, Montefiore Medical Center, Albert Einstein College of Medicine, Bronx, N. Y., USA // Lupus. – 2008, Oct. – № 17 (10). – Р. 922–930.). Другими исследователями четкой зависимости между повышенными показателями антител к аннексину V и неблагоприятными исходами гестации не прослежено, поэтому окончательное суждение о значении аннексина V в развитии осложнений и исходах беременности можно будет сделать по мере накоплений результатов дальнейших исследований. (Милованов А.П., Долженко Т.А., Давтян Е.Л. Морфологическая диагностика и патогенез неразвивающейся беременности при антифосфолипидном синдроме // Архив патологии. – 2005. – № 1. – С. 9–13., Bruggeman C. CMV is involved in vascular pathology // Amer. Heart. J. – 2007. – Vol. 138. – № 5. – Р. 473–475.)
В 1994 г. появилась первая публикация Rand J. и соавт., в которой главной причиной акушерских осложнений у женщин с АФС предлагалось считать дефект плацентарного антикоагулянтного протеина – аннексин V. После этого в многочисленных работах была показана важная роль антител к аннексину V в развитии тромбозов. При этом АФА блокируют транспорт аннексина V на поверхность апикальной мембраны трофобласта и удаляют аннексин V с поверхности трофобласта с его последующим протеолитическим разрушением (Reduction of annexin-V (placental anticoagulant protein-I) on placental villi of women with antiphospholipid antibodies and recurrent spontaneous abortion. Rand JH, Wu XX, Guller S, Gil J, Guha A, Scher J, Lockwood CJ.Am J Obstet Gynecol. 1994 Dec;171(6):1566-72.).
Профилактика и лечение АФС представляют сложную проблему. Это обусловлено неоднородностью патогенетических механизмов, полиморфизмом клинических проявлений, а также отсутствием достоверных клинических и лабораторных показателей, позволяющих прогнозировать рецидивирование тромботических нарушений. Не существует общепринятых международных стандартов лечения, а предлагаемые рекомендации основаны главным образом на результатах открытых испытаний лекарственных препаратов или ретроспективного анализа исходов заболевания.
Лечение глюкокортикоидами и цитотоксическими препаратами при АФС, как правило, неэффективно, за исключением ситуаций, когда целесообразность их назначения продиктована активностью основного заболевания (например, системной красной волчанки).
Ведение больных с АФС (как и с другими тромбофилиями) основывается на назначении антикоагулянтов непрямого действия и антиагрегантов (в первую очередь низких доз ацетилсалициловой кислоты – АСК). Это связано прежде всего с тем, что для АФС характерен высокий риск повторных тромбозов, значительно превосходящий таковой при идиопатических венозных тромбозах. Полагают, что большинство больных АФС с тромбозами нуждаются в профилактической антиагрегантной и/или антикоагулянтной терапии в течение длительного времени, а иногда и пожизненно. Кроме того, риск первичных и повторных тромбозов при АФС необходимо снижать путем влияния на такие корригируемые факторы риска, как гиперлипидемия, артериальная гипертензия, гипергомоцистеинемия, малоподвижный образ жизни, курение, прием оральных контрацептивов и др.
Стандартом профилактики рецидивирующих потерь плода являются малые дозы АСК, которые рекомендуется принимать до, в течение беременности и после рождения ребенка (по крайней мере, в течение 6 месяцев). Во время беременности малые дозы АСК желательно комбинировать с препаратами низкомолекулярного гепарина.
В настоящее время не существует единых терапевтических рекомендаций в отношении иммунотерапии АФС при ведении беременности. До начала 90-х годов с этой целью наиболее широко применялись методы иммунносупрессии (глюкокортикоидами). Теоретическим обоснованием применения глюкокортикоидов является их противовоспалительная активность и снижение уровня АФА при их применении. Однако в 1989 Lockshin M. публикует данные о неэффективности преднизолона у пациенток с синдромом потери плода и АФС, а также данные об угрозе здоровью для матери и плода при его применении. Наличие многочисленных побочных эффектов у глюкортикоидов переключило внимание ученых в сторону разработки методов иммуномодуляции, например, с помощью внутривенных иммуноглобулинов (ВВИГ) (Prednisone does not prevent recurrent fetal death in women with antiphospholipid antibody. Lockshin MD, Druzin ML, Qamar T.Am J Obstet Gynecol. 1989 Feb;160 (2):439-43.).
В акушерско-гинекологической практике для лечения женщин с АФС ВВИГ был впервые предложен к применению в 1992 году как альтернатива глюкортикоидам. К настоящему времени они стали препаратами выбора при лечении антифосфолипидного синдрома у беременных женщин, а также внутриутробной цитомегаловирусной инфекции.
Механизм действия ВВИГ сложен и многосторонен. Эффективность больших доз ВВИГ при заболеваниях, в основе которых ведущую роль выполняют аутоантитела, основана на насыщении FcRn (неонатальный рецептор Fc), что приводит к увеличению катаболизма IgG, в том числе и аутоантител. Одним из важных свойств ВВИГ является защита эндотелия сосудов от повреждающего действия различных факторов, приводящих к развитию претромботического состояния. При терапии внутривенными иммуноглобулинами, за счет использования больших доз биопрепарата, создается высокая концентрация иммуноглобулинов в кровотоке, благодаря чему происходит подавление провоспалительной и прокоагулянтной активности эндотелиальных клеток, снижение экспрессии молекул адгезии P-selectin, ICAM-1, в результате чего происходит сдерживание лейкоцитарной инфильтрации тканей и предотвращение дальнейшего прогрессирования патологического процесса, приводящего к повышенной тромбогенности сосудистой стенки. Однако, несмотря на широкое применение ВВИГ, исследователи так и не пришли к единому мнению о механизмах их действия (Bleeker W. K., Teeling J. L., Hack C. E. Accelerated autoantibody clearance by intravenous immunoglobulin therapy: studies in experimental models to determine the magnitude and time course of the effect // Blood. — 2001. — Vol. 98, N 10. — P. 3136–3142).
Иммуномодулирующая терапия ВВИГ с целью коррекции иммунного ответа у больных с системными и аутоиммунными заболеваниями относится к числу наименее изученных областей. АФС на настоящий момент не включен в список показаний по применению ВВИГ и находится за пределами инструкций «off–label», так как проведенные исследования не дают однозначных клинических данных о позитивном влиянии препарата при данной патологии. Однако ВВИГ в последние несколько лет получили широкое распространение в терапии АФС при беременности, особенно в комплексной терапии АФС рефрактерного к стандартной терапии, при катастрофическом АФС.
До настоящего времени не представлялось возможным оценить эффективность проведенного лечения внутривенными иммуноглобулинами у пациенток c привычным невынашиванием и циркуляцией антифосфолипидных антител.
Задачей предлагаемого способа является обеспечение точной и достоверной оценки эффективности лечения внутривенными иммуноглобулинами у пациенток c привычным невынашиванием и циркуляцией антифосфолипидных антител.
Техническим результатом заявляемого способа является расширение арсенала морфологических диагностических средств оценки эффективности лечения внутривенными иммуноглобулинами у пациенток c привычным невынашиванием и циркуляцией антифосфолипидных антител.
Заявляемый технический результат достигается тем, что при иммуногистохимическом исследовании плаценты определяют относительную площадь экспрессии аннексина V. При значении относительной площади экспрессии аннексина V равном 15 % или более подтверждают эффективность лечения внутривенными иммуноглобулинами у пациенток c привычным невынашиванием и циркуляцией антифосфолипидных антител.
Новизна изобретения заключается в том, что для оценки эффективности лечения внутривенными иммуноглобулинами у пациенток c привычным невынашиванием и циркуляцией антифосфолипидных антител впервые определяют относительную площадь экспрессии аннексина V.
Аннекcин V относится к эндотелиальным факторам и является мембранным белком с молекулярной массой 35кД, который представлен, главным образом, в эндотелии клеток и плаценте. Основной функцией аннексина V является участие в процессе свертывания крови посредством мощной антикоагулянтной способности. Такой антикоагулянтный эффект объясняется возможностью белков вытеснять протеины коагуляции с фосфолипидных поверхностей. Антитромботическое действие его базируется на способности образовывать двухмерные кластеры на поверхности клеток. При этом молекулы аннексина V образуют на поверхности трофобласта межмолекулярные комплексы с множеством соединений по типу «щита», формирование которого играет тромборегуляторную роль в области контакта с кровеносными сосудами. Связывание аннексинa V с апикальной поверхностью синцитиотрофобласта является ключевым моментом для поддержания кровотока в плаценте и выживания плода.
Иммуногистохимическое исследование проводилось в лаборатории иммуногистохимии ФГБНУ «НИИ АГиР им. Д.О. Отта. Иммуногистохимическое исследование проводили на парафиновых срезах толщиной 5 мкм, которые помещали на предметные стекла, покрытые пленкой из поли-L-лизина. Для проведения иммуногистохимической реакции использовали стандартный одноэтапный протокол с демаскировкой антигена (высокотемпературной обработкой ткани) в 0,01 М цитратном буфере рН 6.0. В качестве системы визуализации использовали abcamMouseandRabbitSpecific HRP Plus (ABC) Detection IHC Kit (RTU)[ab93697].
Иммуногистохимический метод исследования включал: количественную и качественную оценку экспрессии антикоагулянтного протеина аннексина V. Антитела использованы в стандартном разведении в соответствии с рекомендациями фирмы производителя.
Количественную оценку результатов иммуногистохимической реакции проводили на микрофотографиях, полученных с помощью системы фиксации микроскопических изображений, состоящей из микроскопа Olympus BX46 и программного обеспечения «CellSens 47 Entry». Из фотосъемки исключались поля зрения, содержащие дефекты ткани, дефекты окрашивания и артефакты. Фотосъемку производили на увеличении 400× (окуляр 10×, объектив 40×), в режиме Photo, время экспозиции 1/38 с, чувствительность камеры – максимальная, размер изображения 2080×1544 пикселей, графический формат изображения JPEG (normal). Долю занимаемой экспрессии изучаемого маркера рассчитывали с помощью программы «VideotestMorphology 5.2».
В каждом срезе в 5 полях зрения оценивали следующие показатели:
– оптическую плотность экспрессии – величина вычислялась автоматически в соответствии с законом Бугера-Ламберта-Бера; использование показателя, так называемой «оптической плотности экспрессии», являющегося базовым параметром программы «VideotestMorphology 5.2». Для анализа оптических параметров микрофотографий, является приемлемым, поскольку измерения осуществляются по аналогии со спектрофотометрическим анализом;
– относительную площадь экспрессии – вычисляли как отношение площади иммунопозитивных клеток к общей площади препарата:
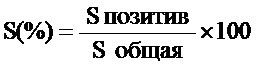
Где S% - относительная площадь экспрессии Аннексина V;
S позитив – значение площади иммунопозитивных клеток;
S общая – значение площади препарата.
После чего вычислялись средние величины исследуемых показателей.
Сущность заявляемого способа поясняется следующими примерами.
Пример 1.
Пациентка Р., 33 лет. В анамнезе – неразвивающаяся беременность 8/9 недель, самопроизвольный выкидыш 16 недель. Данная беременность III, самостоятельная.
Обратилась при сроке 8/9 недель. По данным обследования – выявлен положительный волчаночный антикоагулянт (1,33), гипергомоцистеинемия. Проводилось лечение внутривенными иммуноглобулинами – 3 курса: в 8/9 недель, 16 недель, 24 недели: 5%-100 мл внутривенно медленно 3 раза с интервалом 5 дней. За время течения беременности неоднократно госпитализировалась в отделение патологии беременности с целью контроля показателей гемостаза, фетометрии, допплерометрии, проведения антибактериальной терапии с учетом бактериурии. Данных за хроническую плацентарную недостаточность при беременности не получено.
При сроке 38 0/7 недель самостоятельно вступила в роды. Роды велись под постоянным кардиомониторным наблюдение за состоянием плода. Родилась девочка массой 3640 грамм, длиной 55 см с оценкой по шкале Апгар 8/9 баллов. Роды проведены через естественные родовые пути. Через 10 минут самостоятельно отделилась плацента и выделился послед, без дефектов плацентарной ткани. Кровопотеря составила 250 мл. Послед был направлен на гистологическое исследование, а также участок плаценты 3х3 см был вырезан и направлен на иммуногистохимическое исследование.
Относительная площадь экспрессии аннексина V в препарате составила 30,753%.
Эффективность лечения внутривенными иммуноглобулинами подтверждена морфологически.
Пример 2.
Пациентка С., 39 лет. В анамнезе – 1 срочные роды в 18 лет без осложнений, в 2013 г. – преждевременная отслойка нормально расположенной плаценты при сроке 22/23 недели, антенатальная гибель плода, кровотечение. В 2015 г. – неразвивающаяся беременность 8 недель. В 2016 г. – срочные роды в 38/39 недель, при беременности обследовалась, учитывая наличие титра антител к аннексину V, волчаночного антикоагулянта, был проведен курс внутривенных иммуноглобулинов. Данная беременность V, самостоятельная. Обратилась при сроке 7 недель. При обследовании выявлены антитела к аннексину V в титре 16,03 Ед/мл. Учитывая наличие высокого титра антител к аннексину V, отягощенный акушерский анамнез, проведено лечение внутривенными иммуноглобулинами – 3 курса: в 8/9 недель, 16 недель, 24 недели: 5%-100 мл внутривенно медленно 3 раза с интервалом 5 дней. При сроке 9 недель выявлен гестационный сахарный диабет, с 20 недель начата инсулинотерапия. Неоднократно госпитализировалась с целью контроля за показателями свертывающей системы крови, коррекции углеводного обмена, установки разгрузочного акушерского пессария, а также проведения антибактериальной терапии в связи с бактериурией и обострением хронического гайморита.
Поступила для планового родоразрешения при сроке 38 недель с диагнозом: Беременность 38 0/7 недель. Истмико-цервикальная недостаточность. Акушерский разгрузочный пессарий (удален 12.11.19). Рубец на матке после 2-х операций кесарева сечения. Хронический гайморит, обострение от 21.10.19. Пункция верхнечелюстных пазух от 24.10. и 29.10.19. АФС. Гипергомоцистеинемия. Гестационный сахарный диабет (инсулинотерапия с 20 недель). Диффузно-дистрофическое заболевание позвоночника, вертебро-цервикогенные краниалгии, грыжеобразование C5-C6, C6-C7. Отягощенный акушерско-гинекологический анамнез (преждевременная отслойка нормально расположенной плаценты в 22/23 недели, экстренное кесарево сечение).
Родоразрешена путем операции кесарева сечения, родился мальчик массой 3700 грамм, длиной 53 см с оценкой по шкале Апгар 8/9 баллов. Кровопотеря составила 870 мл.
Плацента располагалась по задней стенке, удалена рукой, отправлена на гистологическое и иммуногистохимическое исследование.
Относительная площадь экспрессии аннексина V в препарате составила 22,522%.
Эффективность лечения внутривенными иммуноглобулинами подтверждена морфологически.
Пример 3.
Пациентка К., 33 лет. В анамнезе — 1 неразвивающаяся беременность 6/7 недель, 2 самопроизвольных выкидыша при сроке 14 недель и 5 недель. Данная беременность IV, самостоятельная. Обратилась при сроке 7/8 недель. При обследовании выявлен высокий титр волчаночного антикоагулянта (1,38), гипергомоцистеинемия. Проводилось лечение внутривенными иммуноглобулинами – 3 курса: в 8/9 недель, 16 недель, 24 недели: 5%-100 мл внутривенно медленно 3 раза с интервалом 5 дней. За время течения беременности неоднократно госпитализировалась в отделение патологии беременности с целью контроля показателей гемостаза, фетометрии, допплерометрии. Данных за хроническую плацентарную недостаточность при беременности не получено.
При сроке 38 3/7 недель самостоятельно вступила в роды. Роды велись под постоянным кардиомониторным наблюдение за состоянием плода. Родилась девочка массой 3150 грамм, длиной 50 см с оценкой по шкале Апгар 8/9 баллов. Роды проведены через естественные родовые пути. Через 5 минут самостоятельно отделилась плацента и выделился послед, без дефектов плацентарной ткани. Кровопотеря составила 280 мл. Послед был направлен на гистологическое исследование, а также участок плаценты 3х3 см был вырезан и направлен на иммуногистохимическое исследование.
Относительная площадь экспрессии аннексина V в препарате составила 17,357%.
Эффективность лечения внутривенными иммуноглобулинами подтверждена морфологически.
Приведенные примеры показывают целесообразность проведенного лечения и подтверждают его эффективность заявленным способом.
Изобретение относится к медицине, а именно к акушерству и гинекологии. Способ подтверждения эффективности лечения внутривенными иммуноглобулинами у пациенток с привычным невынашиванием и циркуляцией антифосфолипидных антител включает иммуногистохимическое исследование плаценты путем определения относительной площади экспрессии аннексина V, равной 15% и более, которую рассчитывают по формуле: 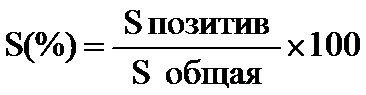 , где S% - относительная площадь экспрессии аннексина V; S позитив – значение площади иммунопозитивных клеток; S общая – значение площади препарата. Изобретение обеспечивает расширение арсенала средств определенного назначения. 2 з.п. ф-лы, 3 пр.
, где S% - относительная площадь экспрессии аннексина V; S позитив – значение площади иммунопозитивных клеток; S общая – значение площади препарата. Изобретение обеспечивает расширение арсенала средств определенного назначения. 2 з.п. ф-лы, 3 пр.
1. Способ подтверждения эффективности лечения внутривенными иммуноглобулинами у пациенток с привычным невынашиванием и циркуляцией антифосфолипидных антител, включающий иммуногистохимическое исследование плаценты путем определения относительной площади экспрессии аннексина V, равной 15% и более, которую рассчитывают по формуле:
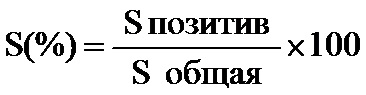 , где S% - относительная площадь экспрессии аннексина V; S позитив – значение площади иммунопозитивных клеток; S общая – значение площади препарата.
, где S% - относительная площадь экспрессии аннексина V; S позитив – значение площади иммунопозитивных клеток; S общая – значение площади препарата.
2. Способ по п.1, в котором за S позитив принимают значение площади иммунопозитивных клеток, представляющих собой значение площади окрашенного препарата на парафиновом срезе в результате воздействия на него реактива к аннексину V, в результате проведения иммуногистохимического исследования.
3. Способ по п.1, в котором за S общая принимают значение площади препарата, представляющего собой общую площадь парафинового среза, нанесенного на предметные стекла для воздействия на него реактива к аннексину V, в результате проведения иммуногистохимического исследования.
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЦИТОПРОТЕКТИВНОГО ЭФФЕКТА ИММУНОГЛОБУЛИНОВ ДЛЯ ВНУТРИВЕННОГО ВВЕДЕНИЯ ПРИ ТЕРАПИИ ЖЕНЩИН С ПРИВЫЧНЫМ НЕВЫНАШИВАНИЕМ БЕРЕМЕННОСТИ И ДИАГНОСТИРОВАННЫМ АНТИФОСФОЛИПИДНЫМ СИНДРОМОМ | 2014 |
|
RU2548754C1 |
| WO 2021032973 A1, 25.02.2021 | |||
| Макацария А.Д | |||
| Патогенетическое значение антифосфолипидных антител // Практическая медицина | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| - N | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| С | |||
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| ШПИГЕЛЬ А.С | |||
| Доказательная медицина // "Арнебия", 2004, с.40-43, 47-49. | |||
Авторы
Даты
2022-06-29—Публикация
2021-06-23—Подача