Изобретение относится к медицине, в частности к акушерству и гинекологии, и может быть использовано для прогнозирования риска развития хронической плацентарной недостаточности при сроке беременности 6-8 недель у женщин с циркуляцией АФА (антифосфолипидных антител) и отягощенным акушерским анамнезом.
Известен способ диагностики хронической плацентарной недостаточности (Патент на изобретение №2313765).
Недостатком данного способа является срок его применения - III триместр беременности. Несмотря на то, что формирование плаценты заканчивается в сроке 20-24 недели, диагностика хронической плацентарной недостаточности на таком сроке может привести к несвоевременному назначению соответствующей терапии.
Известен способ прогнозирования хронической плацентарной недостаточности на ранних сроках гестации (Патент на изобретение №2361522).
Недостатком данного способа является ограниченность условий применения, данное изобретение может быть реализовано лишь с учетом того, что из анамнеза определяют параметры состояния пациентки в период становления менструальной функции, перенесенные инфекционные заболевания в детстве и заболевания, передающиеся половым путем в репродуктивном возрасте, определяют диагностические коэффициенты и при сумме диагностических коэффициентов >0 диагностируют высокую вероятность развития хронической плацентарной недостаточности, а при сумме диагностических коэффициентов <0 диагностируют низкую вероятность развития хронической плацентарной недостаточности.
Ввиду недостаточной информативности оценочных показателей для осуществления данного способа, например перенесенные заболевания, передающиеся половым путем в репродуктивном возрасте, грипп, ОРВИ, кольпит, данный способ очевидно недостаточно точен в результатах прогнозирования хронической плацентарной недостаточности на ранних сроках гестации. В данном изобретении учтены не все коморбидные состояния (например, хроническая артериальная гипертензия, ожирение, наличие аутоиммунных заболеваний и др.), что, в свою очередь, влияет на точность прогнозирования хронической плацентарной недостаточности.
Задачей предложенного изобретения является повышение точности прогнозирования развития хронической плацентарной недостаточности при сроке беременности 6-8 недель у женщин с циркуляцией АФА и отягощенным акушерским анамнезом.
Техническим результатом изобретения является расширение арсенала средств специфичного и точного прогнозирования риска развития хронической плацентарной недостаточности у женщин с циркуляцией АФА и отягощенным акушерским анамнезом при сроке беременности 6-8 недель.
Указанный технический результат достигается тем, что при сроке беременности 6-8 недель у женщин с циркуляцией АФА и отягощенным акушерским анамнезом определяют наличие в крови растворимой fms-подобной тирозинкиназы (sFlt), затем определяют плацентарный фактор роста (PlGF), эндоглин, экспрессию CD11b на тромбоцитарно-моноцитарных комплексах, экспрессию CD40 на тромбоцитарно-моноцитарных комплексах, антитела (AT) к β2-гликопротеину (β2ГП), далее рассчитывают риск развития хронической плацентарной недостаточности в процентах по следующей формуле:
Р=1/(1+е-z)×1000%;
где Р - риск развития хронической плацентарной недостаточности (%);
Z - уравнение регрессии;
е - снование натуральных логарифмов;
z=-251,166-2,143XsFlt/PlGF+0,496ХЭндоглин+2,723XCD11b-7,878XCD40+3,492XAT к β2гп;
где XsFlt/PlGF - соотношение sFlt/PlGF, определенное в крови пациенток в сроке 6-8 недель беременности;
ХЭндоглин - уровень эндоглина в крови в сроке 6-8 недель;
XCD11b экспрессия CD11b (%) на тромбоцитарно-моноцитарных комплексах в сроке 6-8 недель;
XCD40 - экспрессия CD40 (%) на тромбоцитарно-моноцитарных комплексах в сроке 6-8 недель;
ХАТ к β2ГП - уровень AT к β2ГП (U/ml) в крови в сроке 6-8 недель.
При Р=50% и выше прогнозируют высокий риск развития хронической плацентарной недостаточности, при Р=49% и менее прогнозируют низкий риск развития хронической плацентарной недостаточности.
Новизна изобретения заключается в том, что впервые предложен способ, с помощью которого возможно прогнозирование риска развития хронической плацентарной недостаточности при сроке беременности 6-8 недель у женщин с циркуляцией АФА и отягощенным акушерским анамнезом, для реализации которого в качестве предикторов определяется уровень растворимой fms-подобной тирозинкиназы (sFlt) в крови, плацентарного фактора роста (PlGF), эндоглина, экспрессия CD11b и CD40 на тромбоцитарно-моноцитарных комплексах, уровень антител (AT) кβ2-гликопротеину (β2ГП) в крови пациенток.
На основании результатов наблюдения течения беременности пациенток с циркуляцией АФА и отягощенным акушерским анамнезом, была разработана прогностическая модель для определения вероятности ХПН в зависимости от соотношения sFlt/PlGF, эндоглина, CD11b на тромбоцитарно-моноцитарных комплексах, CD40 на тромбоцитарно-моноцитарных комплексах, AT к β2-гликопротеину методом бинарной логистической регрессии. Число наблюдений составило 52.
В Табл. 1 представлены Характеристики связи предикторов модели с вероятностью выявления ХПН. В Табл. 2 представлены Пороговые значения логистической функции Р.
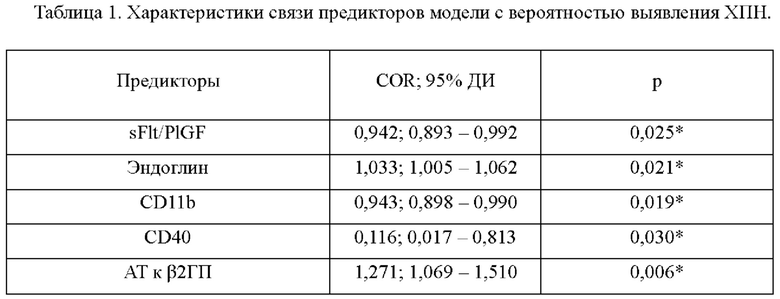

Полученная регрессионная модель является статистически значимой (р<0,001). Исходя из значения коэффициента детерминации Найджелкерка, модель объясняет 100,0% наблюдаемой дисперсии ХПН.
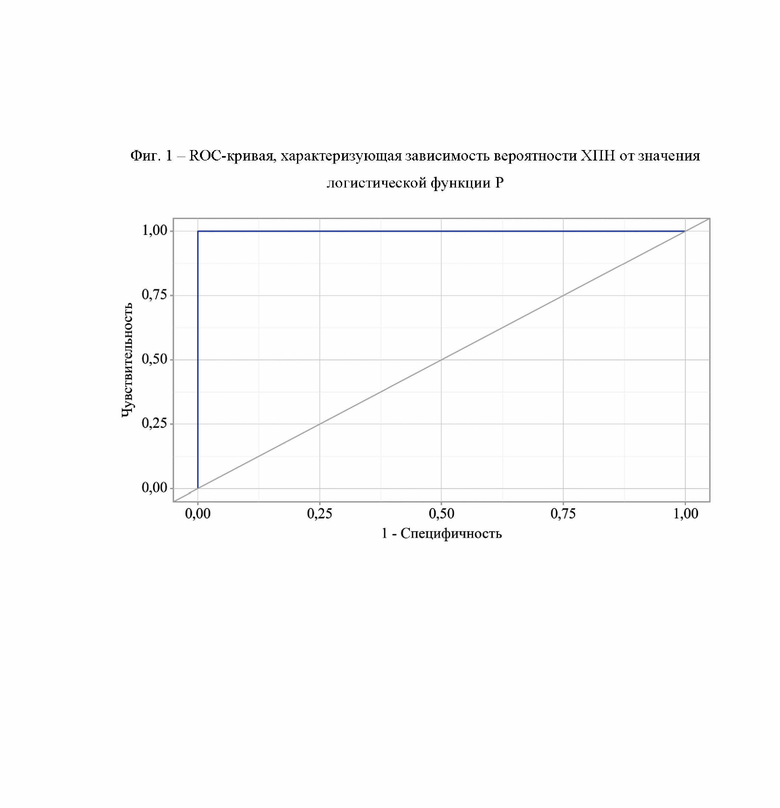
При оценке зависимости вероятности хронической плацентарной недостаточности от значения логистической функции Р с помощью ROC-анализа была получена ROC-кривая (Фиг. 1).
Площадь под ROC-кривой составила 1,000±0,000 с 95% ДИ: 1,000-1,000. Полученная модель была статистически значимой (р<0,001).
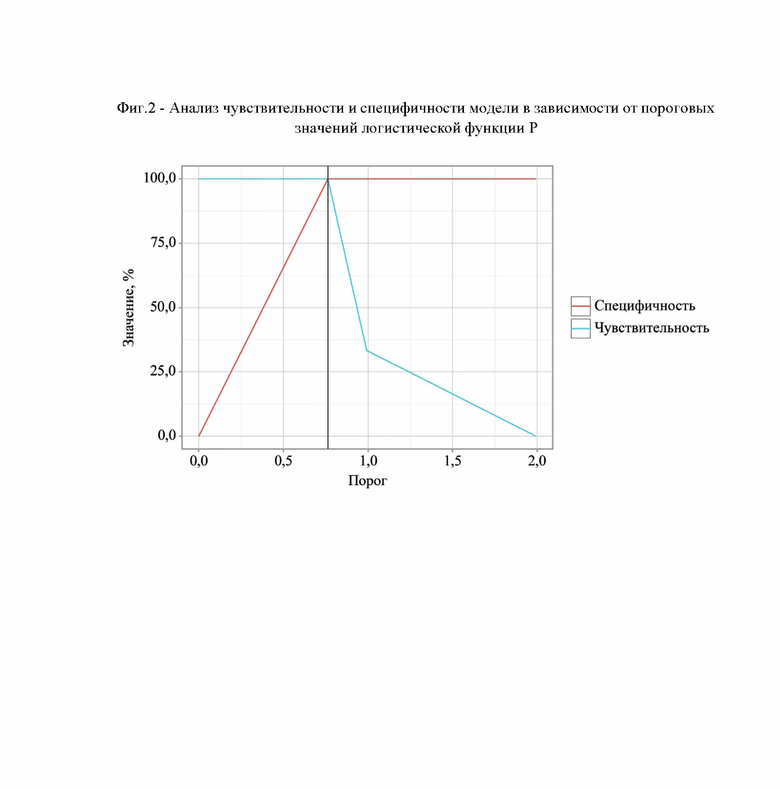
Пороговое значение логистической функции Р в точке cut-off, которому соответствовало наивысшее значение индекса Юдена, составило 0,762. Хроническая плацентарная недостаточность прогнозировалось при значении логистической функции Р выше данной величины или равном ей. Чувствительность и специфичность модели составили 100,0% и 100,0%, соответственно (Фиг. 2).
Краткое описание чертежей
На Фиг. 1 представлена ROC-кривая, характеризующая зависимость вероятности ХПН от значения логистической функции Р, полученная с помощью ROC-анализа.
На Фиг. 2 представлен анализ чувствительности и специфичности модели в зависимости от пороговых значений логистической функции Р.
Способ осуществляется следующим образом:
У пациенток с циркуляцией диагностических титров АФА (критериальных и некритериальных) и отягощенным акушерским анамнезом, то есть у которых в анамнезе зафиксировано:
- потеря/потери плода,
- тяжелая преэклампсия,
- преждевременная отслойка нормально расположенной плаценты,
- синдром задержки роста плода,
- невынашивания беременности/тей, в т.ч. после вспомогательных репродуктивных технологий,
- кровотечения после родов, абортов, преждевременных родов;
при сроке беременности 6-8 недель, определяют наличие в крови растворимой fms-подобной тирозинкиназы (sFlt), затем определяют плацентарный фактор роста (PlGF), эндоглин, CD11b на тромбоцитарно-моноцитарных комплексах, CD40 на тромбоцитарно-моноцитарных комплексах, антитела (AT) к β2-гликопротеину
Определение наличия в крови растворимой fins-подобной тирозинкиназы (sFlt)
Fms-подобная тирозинкиназа (sFlt) является растворимой формой васкулярного эндотелиального фактора роста (VEGF) рецептора 1, которая активно участвует в регуляции ангиогенеза. sFlt действует как «ловушка» для VEGF, предотвращая его связывание с мембранными рецепторами на эндотелиальных клетках, тем самым модулируя ангиогенез и сосудистую проницаемость. В контексте акушерства, повышенные уровни sFlt ассоциируются с патогенезом преэклампсии, заболеванием, характеризующимся высоким артериальным давлением и нарушением функции других органов у беременных.
Содержание sFlt (пг/мл) в сыворотке периферической крови определяют методом электрохемилюминесцентного анализа с использованием коммерческих тест-систем Elecsys sFlt фирмы Roche Diagnostics GmbH (Германия) на автоматическом иммунохимическом анализаторе Cobas е411 (Япония).
К 20 мкл образца сыворотки крови пациента добавляется одновременно биотинилированное моноклональное антитело, специфичное к sFlt и специфичное к sFlt моноклональное антитело, меченное рутениевым комплексом. После инкубации в течение 9 минут при 370°С добавляются микрочастицы, покрытые стрептавидином. Образовавшиеся в результате первой инкубации комплексы связываются с микрочастицами посредством взаимодействия биотина и стрептавидина. Далее реакционная смесь забирается в измерительную ячейку, где микрочастицы оседают на поверхность электрода в результате магнитного взаимодействия. Затем с помощью промывающих растворов удаляются не связавшиеся вещества. Далее приложенное к электроду напряжение вызывает хемилюминесцентную эмиссию, которая измеряется фотоумножителем. Результаты исследования оценивали количественным способом с помощью 2 точечной калибровочной кривой и референсной калибровочной кривой, данные которой предоставлены производителем в штрих-коде к реагенту.
Определение наличия в крови плацентарного фактора роста (PlGF)
Плацентарный фактор роста (PlGF) представляет собой белок, который также участвует в регуляции ангиогенеза и взаимодействует с VEGF и его рецепторами. PlGF способствует росту и выживаемости эндотелиальных клеток, а также стимулирует васкуляризацию плаценты. Уровни PlGF снижаются при преэклампсии, что делает его потенциальным маркером для раннего выявления и мониторинга этого состояния.
Содержание PlGF (пг/мл) в сыворотке периферической крови определяют методом электрохемилюминесцентного анализа с использованием коммерческих тест-систем «Elecsys PlGF» фирмы Roche Diagnostics GmbH (Германия) на автоматическом иммунохимическом анализаторе Cobas е411 (Япония).
К 20 мкл образца сыворотки крови пациента добавляется одновременно биотинилированное моноклональное антитело, специфичное к PlGF и специфичное к PlGF моноклональное антитело, меченное рутениевым комплексом. После инкубации в течение 9 минут при 370°С добавляются микрочастицы, покрытые стрептавидином. Образовавшиеся в результате первой инкубации комплексы связываются с микрочастицами посредством взаимодействия биотина и стрептавидина. Далее реакционная смесь забирается в измерительную ячейку, где микрочастицы оседают на поверхность электрода в результате магнитного взаимодействия. Затем с помощью промывающих растворов удаляются не связавшиеся вещества. Далее приложенное к электроду напряжение вызывает хемилюминесцентную эмиссию, которая измеряется фотоумножителем. Результаты исследования оценивали количественным способом с помощью 2 точечной калибровочной кривой и референсной калибровочной кривой, данные которой предоставлены производителем в штрих-коде к реагенту.
Определение наличия в крови эндоглина
Эндоглин является акцессорным рецептором для трансформирующего фактора роста-бета (TGF-β) и играет ключевую роль в ангиогенезе и развитии сердечно-сосудистой системы. Эндоглин экспрессируется на поверхности эндотелиальных клеток и участвует в модуляции сигналов TGF-β, влияющих на пролиферацию и миграцию эндотелиальных клеток. Повышенные уровни растворимого эндоглина ассоциируются с преэклампсией, указывая на его потенциальное значение как биомаркера для диагностики и прогнозирования этого состояния.
Определение концентрации эндоглина в сыворотке периферической крови определяют методом твердофазного иммуноферментного анализа (ИФА). Для этого на лунки микропланшета сорбируют моноклональные антитела к эндоглину в течение 18 часов при +40°С. Далее вносят по 100 мкл образцов сывороток пациенток, инкубируют при 37±20°С в течение 1 часа, отмывали 3 раза моющим буфером и добавляют по 100 мкл антител к эндоглину конъюгированных с пероксидазой хрена, инкубируют 45 минут при 37±20°С, отмывают 3 раза моющим буфером и добавляли по 100 мкл субстратно-хромогенного раствора, содержащего тетраметилбензидин и перекись водорода. Планшет инкубируют в течение 5 минут в темноте. Ферментативную реакцию останавливают внесением в лунки по 50 мкл «стоп»-реагента. Учет результатов анализа проводят инструментально путем измерения оптической плотности на автоматическом фотометре для микропланшет серии EL×808 производства BioTek Instruments Inc. (США) при длине волны 450 нм.
Определение наличия в крови CD11b на тромбоцитарно-моноцитарных комплексах
CD11b на тромбоцитарно-моноцитарных комплексах относится к молекулам адгезии, которые играют ключевую роль в воспалительных процессах и иммунном ответе. CD11b является субъединицей интегрина Мас-1 (также известного как αМβ2 или CD11b/CD18), который экспрессируется на поверхности моноцитов, нейтрофилов, и некоторых подтипов лимфоцитов. Этот рецептор способствует адгезии лейкоцитов к эндотелию, их миграции через сосудистую стенку в очаг воспаления, а также фагоцитозу и активацию клеток иммунной системы.
Тромбоцитарно-моноцитарные комплексы представляют собой агрегаты, состоящие из тромбоцитов и моноцитов, которые образуются в кровотоке. Формирование этих комплексов является частью нормального иммунного ответа, способствующего регуляции воспаления и восстановления тканей. Однако их чрезмерная активация и агрегация могут привести к патологическим состояниям, включая атеросклероз, тромбоз и другие сердечнососудистые заболевания. CD11b на тромбоцитарно-моноцитарных комплексах способствует их взаимодействию с компонентами сосудистого эндотелия, участвуя в их рекрутировании и активации в местах воспаления или травмы. Изучение роли CD11b и тромбоцитарно-моноцитарных комплексов в различных патологических процессах может предоставить важную информацию для разработки новых терапевтических стратегий, направленных на уменьшение воспаления и предотвращение связанных с ним заболеваний.
Для определения наличия в крови CD11b венозную кровь забирают в вакутейнер с цитратом натрия (первые 3-5 мл крови не использовали). В течение 10-15 мин после взятия к 100 мкл цельной крови добавляют антитела к CD45, CD14, CD41a и другим поверхностным антигенам моноцитов и тромбоцитов, в том числе CD11b и CD40. Инкубируют 20 мин при комнатной температуре в темноте. Лизируют эритроциты, добавляя лизирующий раствор BD FACS Lysing Solution. Центрифугируют (~300 g, 5 мин), отбирают излишек надосадочной жидкости, оставляя в пробирке ~400 мкл. Анализируют на FACS, гейтируя по SSC и CD45 (моноцитарный гейт). Моноциты гейтируют по CD14/CD41a, считая события CD14+CD41a+ тромбоцитарно-моноцитарными комплексами, а события CD14+CD41a- свободными моноцитами.
В случае необходимости предварительной фиксации используют вариант: сразу же после забора крови 0,5 мл цельной крови смешивают с равным объемом однократного раствора BD Cell Fix (конечная концентрация параформальдегида - 0,5%). Через 20-30 мин отбирают 100 мкл., добавляют антитела к CD45, CD14, CD41a и другим поверхностным антигенам моноцитов и тромбоцитов, в том числе CD11b и CD40. Инкубируют 20 мин при комнатной температуре в темноте. Лизируют эритроциты, добавляя лизирующий раствор BD FACS Lysing Solution. Центрифугируют (~300 g, 5 мин), отбирают излишек надосадочной жидкости, оставляя в пробирке ~400 мкл. Анализируют на FACS, гейтируя по SSC и CD45 (моноцитарный гейт). Моноциты гейтируют по CD14/CD41a, считая события CD14+CD41a+ тромбоцитарно-моноцитарными комплексами, а события CD14+CD41a- свободными моноцитами.
Определение наличия в крови CD40 на тромбоцитарно-моноцитарных комплексах.
CD40 на тромбоцитарно-моноцитарных комплексах относится к рецептору на поверхности клеток, который играет важную роль в регуляции иммунного ответа, включая активацию и дифференциацию В-лимфоцитов, а также в воспалительных процессах. CD40 является членом семейства рецепторов фактора некроза опухолей (TNF-рецепторов) и экспрессируется на многих типах клеток, в том числе на моноцитах, дендритных клетках, В-лимфоцитах, а также на тромбоцитах.
Тромбоцитарно-моноцитарные комплексы, содержащие CD40, могут способствовать атерогенезу и другим патологическим процессам за счет усиления воспалительного ответа и способствования агрегации тромбоцитов и моноцитов. Экспрессия CD40 на этих комплексах позволяет моноцитам взаимодействовать с CD40L (лигандом CD40), который может быть выражен на поверхности других иммунных клеток, включая активированные Т-лимфоциты и тромбоциты. Это взаимодействие играет ключевую роль в активации моноцитов и их последующей трансформации в пенные клетки в атеросклеротических бляшках, а также в высвобождении провоспалительных цитокинов и других медиаторов воспаления.
Активация CD40-CD40L пути на тромбоцитарно-моноцитарных комплексах может также участвовать в усилении коагуляционного каскада, способствуя образованию тромбов и развитию тромботических осложнений. В контексте сердечно-сосудистых заболеваний, взаимодействие CD40-CD40L может служить потенциальной мишенью для терапевтического вмешательства, направленного на снижение воспалительного ответа и предотвращение атеросклероза и связанных с ним осложнений.
Таким образом, CD40 на тромбоцитарно-моноцитарных комплексах представляет собой важный молекулярный механизм, участвующий в регуляции воспалительных процессов и иммунного ответа, особенно в контексте сердечно-сосудистых заболеваний. Исследования в этой области могут способствовать разработке новых подходов к лечению и для профилактики атеросклероза и других воспалительных заболеваний.
Для определения наличия в крови CD40 венозную кровь забирают в вакутейнер с цитратом натрия (первые 3-5 мл крови не использовали). В течение 10-15 мин после взятия к 100 мкл цельной крови добавляют антитела к CD45, CD14, CD41a и другим поверхностным антигенам моноцитов и тромбоцитов, в том числе CD11b и CD40. Инкубируют 20 мин при комнатной температуре в темноте. Лизируют эритроциты, добавляя лизирующий раствор BD FACS Lysing Solution. Центрифугируют (~300 g, 5 мин), отбирают излишек надосадочной жидкости, оставляя в пробирке ~400 мкл. Анализируют на FACS, гейтируя по SSC и CD45 (моноцитарный гейт). Моноциты гейтируют по CD14/CD41a, считая события CD14+CD41a+ тромбоцитарно-моноцитарными комплексами, а события CD14+CD41a- свободными моноцитами.
В случае необходимости предварительной фиксации используют вариант: сразу же после забора крови 0,5 мл цельной крови смешивают с равным объемом однократного раствора BD Cell Fix (конечная концентрация параформальдегида - 0,5%). Через 20-30 мин отбирают 100 мкл., добавляют антитела к CD45, CD14, CD41a и другим поверхностным антигенам моноцитов и тромбоцитов, в том числе CD11b и CD40. Инкубируют 20 мин при комнатной температуре в темноте. Лизируют эритроциты, добавляя лизирующий раствор BD FACS Lysing Solution. Центрифугируют (~300 g, 5 мин), отбирают излишек надосадочной жидкости, оставляя в пробирке ~400 мкл. Анализируют на FACS, гейтируя по SSC и CD45 (моноцитарный гейт). Моноциты гейтируют по CD14/CD41a, считая события CD14+CD41a+ тромбоцитарно-моноцитарными комплексами, а события CD14+CD41a- свободными моноцитами.
Определение наличия в крови AT к β2-гликопротеину
Антитела к β2 - гликопротеину являются классом аутоантител, которые играют роль в патогенезе аутоиммунных заболеваний, таких как антифосфолипидный синдром (АФС). АФС ассоциируется с повышенным риском тромбоза, потери беременности и других осложнений во время беременности. Антитела к β2 - гликопротеину могут взаимодействовать с фосфолипидами, присутствующими на поверхности клеток, способствуя формированию тромбов и нарушению нормальной функции плаценты.
В сыворотках периферической крови содержание AT к β2-гликопротеину определяют методом твердофазного иммуноферментного анализа (ИФА) с использованием коммерческих тест-систем фирмы Orgentec Diagnostika GmbH (Германия). При постановке исследований использовали стандартные образцы для построения калибровочной кривой и контрольные образцы. Учет результатов анализа проводили инструментально путем измерения оптической плотности на автоматическом спектрофотометре для микропланшет серии EL×808 производства BioTek Instruments Inc. (США) при длине волны 450 нм. Результаты исследования оценивали в соответствии с рекомендациями производителя.
Далее рассчитывают риск развития хронической плацентарной недостаточности в процентах по следующей формуле:
P=1/(1+e-z)×100%
Способ подтверждается следующими клиническими примерами:
Пример 1. Повторнородящая 28 лет с антенатальной гибелью плода в сроке 23 недели беременности в анамнезе, 1 неразвивающейся беременностью при сроке 8 недель, высоким уровнем волчаночного антикоагулянта (ВА) в крови (1,34). При обследовании в сроке 7 недель беременности определялись показатели в крови:
• Соотношение sFlt/PlGF - 29,758,
• Эндоглин (нг/мл) - 556,7,
• экспрессия CD11b (%) на тромбоцитарно-моноцитарных комплексах - 10,2,
• экспрессия CD40 (%) на тромбоцитарно-моноцитарных комплексах - 0,9,
• уровень AT к β2ГП (U/ml) - 5,712.
Рассчитывалось значение Z:
z=-251,166-2,143×29,758+0,496×556,7+2,723×10,2-7,878×0,9+3,492×5,712=1,816 Рассчитывалось значение e-z=0,1627.
Рассчитывают вероятность развития хронической плацентарной недостаточности при последующей беременности:
P=1/(1+e-z)×100%=86%
У пациентки развилась хроническая плацентарная недостаточность - гемодинамические нарушения I степени (в обеих маточных артериях) при сроке 34 недели. Роды путем экстренной операции кесарева сечения в 35 недель в связи с началом родовой деятельности и рубцом на матке после малого кесарева сечения, родилась девочка 2370/47 с оценкой по Апгар 7 баллов. По данным гистологического исследования плаценты - ХПН, компенсированная стадия.
Таким образом, значение Р указывает на высокий риск хронической плацентарной недостаточности, что и подтвердилось при наблюдении за течением беременности.
Пример 2. Повторнородящая 41 года с антенатальной гибелью плода в сроке 25 недель беременности в анамнезе, 1 неразвивающейся беременностью при сроке 10 недель, высоким уровнем ВА в крови (1,30). При обследовании в сроке 7 недель беременности определялись показатели в крови:
• Соотношение sFlt/PlGF - 146,97,
• Эндоглин (нг/мл) – 943,
• экспрессия CD11b (%) на тромбоцитарно-моноцитарных комплексах - 21,8,
• экспрессия CD40 (%) на тромбоцитарно-моноцитарных комплексах - 0,8,
• уровень AT к β2ГП (U/ml) - 3,2.
Рассчитывают значение Z:
z=-251,166-2,143×146,97+0,496×943+2,723×21,8-7,878×0,8+3,492×3,2=3,362
Рассчитывалось значение e-z=0,035.
Рассчитывают вероятность развития хронической плацентарной недостаточности при последующей беременности:
Р=1/(1+е-z)×100%=96,6%
У пациентки развилась хроническая плацентарная недостаточность - задержка роста плода выявлена при сроке 33 недели. Роды путем экстренной операции кесарева сечения при сроке 37 2/7 недель, родилась живая доношенная девочка массой 2470 грамм, длиной 49 см, с оценкой по Апгар 8 баллов. По данным гистологического исследования плаценты - ХПН, субкомпенсированная стадия.
Таким образом, значение Р указывает на высокий риск хронической плацентарной недостаточности, что и подтвердилось при анализе исхода беременности.
Пример 3. Первородящая 34 лет, в анамнезе, 1 неразвивающаяся беременность при сроке 10 недель, 1 самопроизвольный выкидыш при сроке 6 недель, высоким уровнем AT к кардиолипину - 14,3 U/ml. При обследовании в сроке 8 недель беременности определялись показатели в крови:
• Соотношение sFlt/PlGF - 24,5,
• Эндоглин (нг/мл) – 509,
• экспрессия CD11b (%) на тромбоцитарно-моноцитарных комплексах - 9,2,
• экспрессия CD40 (%) на тромбоцитарно-моноцитарных комплексах - 3,02,
• уровень AT к β2ГП (U/ml) - 14,3.
Рассчитывают значение Z:
z=-251,166-2,143×24,5+0,496×509+2,723×9,2-7,878×3,02+3,492×14,3=0,0005
Рассчитывалось значение e-z=1,04.
Рассчитывают вероятность развития хронической плацентарной недостаточности при последующей беременности:
Р=1/(1+е-z)×100%=49,0%
У пациентки беременность протекала без осложнений, признаков плацентарной недостаточности не было выявлено. Роды через естественные родовые пути в 39 5/7 недель, родился живой доношенный мальчик 3530 грамм, длиной 51 см, с оценкой по Апгар 8 баллов. По данным гистологического исследования плаценты - нормопластический тип строения плаценты.
Таким образом, значение Р указывает на низкий риск хронической плацентарной недостаточности, что и подтвердилось при анализе исхода беременности.
Таким образом, использование предложенного способа позволяет осуществить прогнозирование риска развития хронической плацентарной недостаточности при сроке беременности 6-8 недель у женщин с циркуляцией АФА и отягощенным акушерским анамнезом. Раннее выявление столь опасного заболевания дает возможность для своевременного начала профилактических и терапевтических мероприятий, направленных на предотвращение развития ХПН. Использование комплексного подхода, включающего определение в крови ряда маркеров (растворимой fins-подобной тирозинкиназы (sFlt), плацентарного фактора роста (PlGF), эндоглина, CD11b на тромбоцитарно-моноцитарных комплексах, CD40 на тромбоцитарно-моноцитарных комплексах, антител к р2-гликопротеину), позволяет достичь высокой точности прогнозирования риска развития ХПН. Регрессионная модель, разработанная на основе клинических наблюдений и предикторов, демонстрирует статистическую значимость и способна объяснить 100% наблюдаемой дисперсии ХПН, что подтверждает эффективность и надежность метода. Предложенный способ открывает новые перспективы для профилактики и патогенетически обоснованной терапии ХПН, что может значительно улучшить исходы беременности у женщин с высоким риском развития данного состояния.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования риска развития хронической плацентарной недостаточности при сроке беременности 16-18 недель у женщин с циркуляцией АФА и отягощенным акушерским анамнезом | 2024 |
|
RU2830350C1 |
| Способ прогнозирования риска развития хронической плацентарной недостаточности на этапе планирования беременности | 2024 |
|
RU2831480C1 |
| Способ оценки эффективности лечения внутривенными иммуноглобулинами у пациенток с привычным невынашиванием и циркуляцией антифосфолипидных антител | 2021 |
|
RU2783003C1 |
| Способ оценки эффективности лечения внутривенными иммуноглобулинами у пациенток с привычным невынашиванием и циркуляцией антифосфолипидных антител | 2021 |
|
RU2786456C1 |
| Способ оценки эффективности лечения внутривенными иммуноглобулинами у пациенток с привычным невынашиванием и циркуляцией антифосфолипидных антител | 2021 |
|
RU2775311C1 |
| СПОСОБ ФУНКЦИОНАЛЬНОЙ И КОЛИЧЕСТВЕННОЙ ОЦЕНКИ ТРОМБОЦИТАРНО-МОНОЦИТАРНЫХ КОМПЛЕКСОВ В ОБРАЗЦАХ ЦЕЛЬНОЙ ПЕРИФЕРИЧЕСКОЙ КРОВИ | 2020 |
|
RU2762820C1 |
| СПОСОБ ВЫБОРА ТАКТИКИ ВЕДЕНИЯ БЕРЕМЕННЫХ С ПЛАЦЕНТАРНОЙ НЕДОСТАТОЧНОСТЬЮ И СИНДРОМОМ ЗАДЕРЖКИ РОСТА ПЛОДА /СЗРП/ | 2015 |
|
RU2595884C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ПРЕЭКЛАМПСИИ У БЕРЕМЕННЫХ С САХАРНЫМ ДИАБЕТОМ 2 ТИПА | 2022 |
|
RU2800716C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ПРЕЭКЛАМПСИИ У БЕРЕМЕННЫХ С САХАРНЫМ ДИАБЕТОМ 1 ТИПА | 2022 |
|
RU2800717C1 |
| СПОСОБ ДИАГНОСТИКИ ХРОНИЧЕСКОЙ ПЛАЦЕНТАРНОЙ НЕДОСТАТОЧНОСТИ | 2006 |
|
RU2313795C1 |
Изобретение относится к области медицины, в частности к акушерству и гинекологии, и может быть использовано для прогнозирования риска развития хронической плацентарной недостаточности при сроке беременности 6-8 недель у женщин с циркуляцией АФА (антифосфолипидных антител) и отягощенным акушерским анамнезом. Определяют наличие в крови растворимой fms-подобной тирозинкиназы (sFlt), плацентарного фактора роста (PlGF), эндоглина, CD11b на тромбоцитарно-моноцитарных комплексах, CD40 на тромбоцитарно-моноцитарных комплексах, антител к β2-гликопротеину. Далее рассчитывают риск развития хронической плацентарной недостаточности по формуле. При P≥50% прогнозируют высокий риск развития, а при Р≤49% - низкий риск развития заболевания. Способ позволяет осуществить прогнозирование развития хронической плацентарной недостаточности за счет оценки комплекса наиболее значимых показателей. 2 ил., 2 табл., 3 пр.
Способ прогнозирования риска развития хронической плацентарной недостаточности при сроке беременности 6-8 недель у женщин с циркуляцией АФА и отягощенным акушерским анамнезом, включающий определение наличия в крови растворимой fms-подобной тирозанкиназы (sFlt), плацентарного фактора роста (PlGF), эндоглина, CD11b на тромбоцитарно-моноцитарных комплексах, CD40 на тромбоцитарно-моноцитарных комплексах, антител (АТ) к β2-гликопротеину (β2ГП), далее рассчитывают риск развития хронической плацентарной недостаточности в процентах по следующей формуле:
P = 1 / (1 + e-z) × 100%;
Где Р - риск развития хронической плацентарной недостаточности (%);
Z - уравнение регрессии;
е - снование натуральных логарифмов;
z = -251,166 - 2,143XsFlt/PlGF + 0,496XЭндоглин + 2,723XCD11b - 7,878XCD40 + 3,492XАТ к β2ГП;
где XsFlt/PlGF - соотношение sFlt/PlGF, определенное в крови пациенток в сроке 6-8 недель беременности;
XЭндоглин - уровень эндоглина в крови в сроке 6-8 недель;
XCD11b - экспрессия CD11b (%) на тромбоцитарно-моноцитарных комплексах в сроке 6-8 недель;
XCD40 - экспрессия CD40 (%) на тромбоцитарно-моноцитарных комплексах в сроке 6-8 недель;
XАТ к β2ГП - уровень АТ к β2ГП (U/ml) в крови в сроке 6-8 недель;
при P=50% и выше прогнозируют высокий риск развития хронической плацентарной недостаточности, при P=49% и менее прогнозируют низкий риск развития хронической плацентарной недостаточности.
| СПОСОБ ВЫБОРА ТАКТИКИ ВЕДЕНИЯ БЕРЕМЕННЫХ С ПЛАЦЕНТАРНОЙ НЕДОСТАТОЧНОСТЬЮ И СИНДРОМОМ ЗАДЕРЖКИ РОСТА ПЛОДА /СЗРП/ | 2015 |
|
RU2595884C1 |
| СПОСОБ ОЦЕНКИ РИСКА РАЗВИТИЯ И ПРЕДРАСПОЛОЖЕННОСТИ К РАЗВИТИЮ ПАТОЛОГИИ, АССОЦИИРОВАННОЙ С ПРИСУТСТВИЕМ АУТОАНТИТЕЛ ПРОТИВ EPCR | 2005 |
|
RU2375716C2 |
| ТЕТЕЛЮТИНА Ф.К | |||
| и др | |||
| Показатели обмена гликопротеинов у беременных женщин с плацентарной недостаточностью на фоне преэклампсии | |||
| Современные проблемы науки и образования | |||
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| Приспособление для увеличения сцепной силы тяги паровозов и других повозок | 1919 |
|
SU355A1 |
| СИДОРКИНА А.Г | |||
| и др | |||
| Современные методы диагностики хронической плацентарной недостаточности | |||
Авторы
Даты
2024-11-18—Публикация
2024-03-31—Подача