Изобретение относится к медицине, в частности к акушерству и гинекологии, и может быть использовано для прогнозирования риска развития хронической плацентарной недостаточности на этапе планирования беременности.
Хроническая плацентарная недостаточность (ХПН) - это прогрессирующее ухудшение функции плаценты с нарушением дыхательной, трофической и метаболической активности, приводящее к декомпенсации и задержке роста плода [Плацента-ассоциированные осложнения беременности: влияние полиморфизма rs4065 гена урокиназы / Д.Б. Ревина, А.В. Балацкий, Е.Б. Ларина [et al.] // Вопросы гинекологии, акушерства и перинатологии. - 2021. - Vol. 20. - № 1. - P. 5-10; Wardiner J.E. Placental insufficiency / J.E. Wardiner, S. Ambati // StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing. - 2023].
Данное заболевание связано с нарушением формирования плаценты на ранних сроках беременности и ее ангиогенеза на более поздних сроках. При этом местные плацентарные нарушения нередко сочетаются с системными: повышением системного сосудистого сопротивления, эндотелиальной дисфункцией и активацией системы свертывания крови [NationalProgram N. H. B. P. E. et al. Report of the National High Blood Pressure Education Program Working Group on High Blood Pressure in Pregnancy / NationalProgram N. H. B. P. E. et al. // American Journal of Obstetrics and Gynecology. - 2000. - Vol. 1. - № 183. - P. s1-s22] / Уменьшение диаметра маточных артерии снижает перфузию плаценты. [Effect of altitude on uterine artery blood flow during normal pregnancy / S. Zamudio, S. K. Palmer, T. Droma [et al.] // Journal of Applied Physiology. - 1995. - Vol. 79. - № 1. - P. 7-14]. Связанная с плацентарной недостаточностью хроническая гипоксия играет ключевую роль в формировании задержки роста плода.
ХПН - клинический синдром, обусловленный морфофункциональными изменениями в плаценте и нарушениями компенсаторно-приспособительных механизмов, обеспечивающих нормальный рост и развитие плода, а также адаптацию организма женщины к беременности.
Плацентарная недостаточность представляет собой результат сложной реакции плода и плаценты на различные патологические состояния материнского организма и проявляется в комплексе нарушений транспортной, трофической, эндокринной и метаболической функций плаценты, лежащих в основе патологии плода и новорожденного. Проблема профилактики и прогнозирования ХПН является чрезвычайно актуальной. Несмотря на профилактику и применение различной терапии, к сожалению, до сих пор не удалось добиться снижения частоты развития задержки развития плода. Это объясняет стремление исследователей к эффективному прогнозированию ХПН, начиная с I триместра беременности, и выделению группы женщин высокого риска с целью раннего принятия необходимых мер для улучшения плацентации и предотвращения частоты развития плацента-ассоциированных заболеваний.
Известен способ прогнозирования хронической плацентарной недостаточности на ранних сроках гестации (Патент на изобретение №2361522).
Недостатком данного способа является ограниченность условий применения, данное изобретение может быть реализовано лишь при ранних сроках гестации, что, в свою очередь, может быть неинформативно при назначении профилактирующей терапии на этапе предгравидарной подготовки и на этапе установления факта наступления беременности.
Задачей предложенного изобретения является повышение точности прогнозирования развития ХПН у женщин до наступления беременности.
Техническим результатом изобретения является расширение арсенала средств прогнозирования риска развития хронической плацентарной недостаточности у женщин до наступления беременности.
Указанный технический результат достигается тем, что у женщин на этапе планирования беременности оценивают наличие в крови диагностических титров критериальных и некритериальных антифосфолипидных антител (далее, АФА), определяют количество В-лимфоцитов и NK-клеток, далее рассчитывают риск развития хронической плацентарной недостаточности в процентах по следующей формуле:
P = 1 / (1 + e-z) × 100%;
Где Р - риск развития хронической плацентарной недостаточности (%);
Z - уравнение регрессии;
е - снование натуральных логарифмов;
z = -4,529 - 1,092 X Диагностические титры АФА + 0,003 XNK-клетки + 0,330 XВ-лимфоциты (CD19+);
где X Диагностические титры АФА - Диагностические титры АФА (0 - Без АФА, 1 - Диагностические титры АФА);
XNK-клетки - NK-клетки (%);
XВ-лимфоциты (CD19+) - В-лимфоциты (CD19+) (%)
При P=33,6% и выше прогнозируют высокий риск развития хронической плацентарной недостаточности, при P=33,0% и менее прогнозируют низкий риск развития хронической плацентарной недостаточности.
Новизна изобретения заключается в том, впервые предложен способ, с помощью которого возможно прогнозирование риска развития хронической плацентарной недостаточности до наступления беременности у женщин, для реализации которого в качестве предикторов оценивается наличие в крови диагностических титров критериальных и некритериальных АФА, а также количество NK-клеток и В-лимфоцитов в периферической крови.
На основании результатов наблюдения течения беременности пациенток с отягощенным акушерским анамнезом, была разработана прогностическая модель для определения вероятности развития ХПН в зависимости от диагностических титров АФА (критериальных и некритериальных), В-лимфоцитов (CD19+), NK-клеток методом бинарной логистической регрессии. Число наблюдений составило 48. В Табл. 1 представлена клиническая характеристика обследованных пациенток, принявших участие в исследовании. В Табл. 2 представлен анамнез обследованных пациенток, принявших участие в исследовании. В Табл. 3 представлены исходы беременностей у обследованных пациенток, принявших участие в исследовании.
Таблица 1
Таблица 2
(Доверительный интервал)
(критериальных и некритериальных)
Таблица 3
Полученная регрессионная модель является статистически значимой (p < 0,001). Исходя из значения коэффициента детерминации Найджелкерка, модель объясняет 50,7% наблюдаемой дисперсии ХПН.
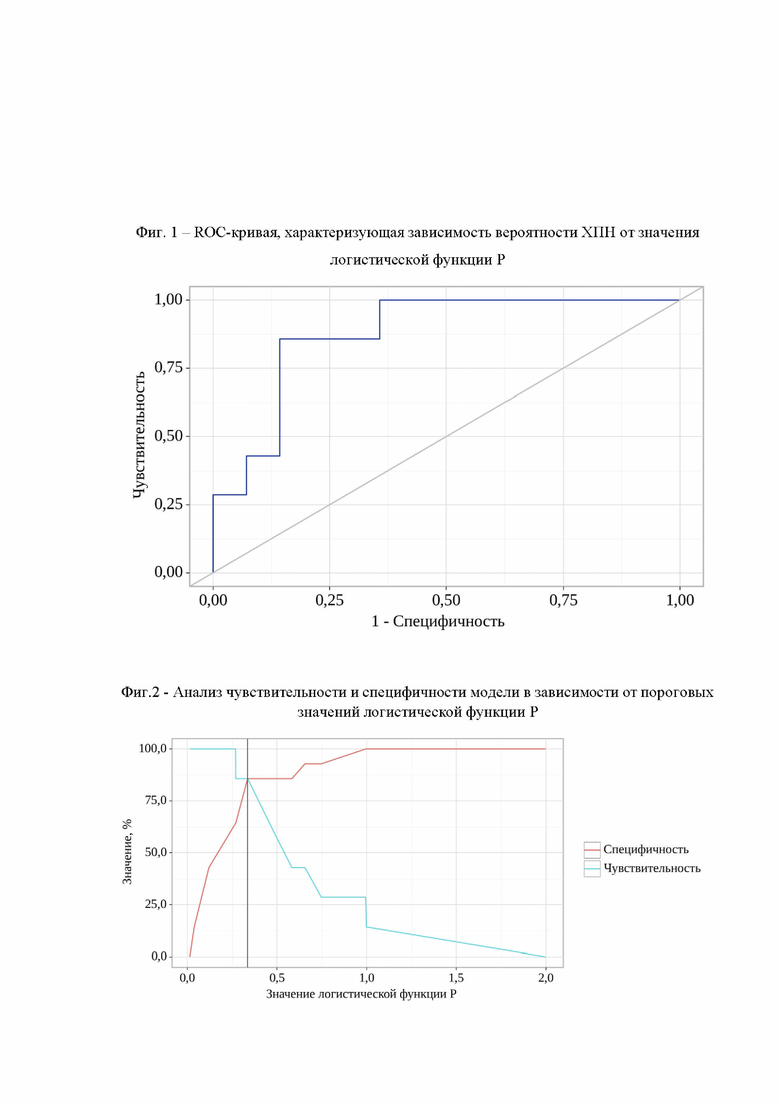
При оценке зависимости вероятности хронической плацентарной недостаточности от значения логистической функции P с помощью ROC-анализа была получена ROC -кривая (Фиг.1).
Площадь под ROC-кривой составила 0,878 ± 0,064 с 95% ДИ: 0,752 - 1,000. Полученная модель была статистически значимой (p < 0,001).
Пороговое значение логистической функции P в точке cut-off, которому соответствовало наивысшее значение индекса Юдена, составило 0,336. Хроническая плацентарная недостаточность прогнозировалось при значении логистической функции P выше данной величины или равном ей. Чувствительность и специфичность модели составили 85,7% и 85,7%, соответственно (Фиг. 2).
Краткое описание чертежей
На Фиг. 1 представлена ROC-кривая, характеризующая зависимость вероятности ХПН от значения логистической функции P, полученная с помощью ROC-анализа.
На Фиг. 2 представлен Анализ чувствительности и специфичности модели в зависимости от пороговых значений логистической функции P.
Способ осуществляется следующим образом:
У пациенток с отягощенным акушерским анамнезом, то есть у которых в анамнезе зафиксировано:
-потеря/потери плода,
-тяжелая преэклампсия,
-преждевременная отслойка нормально расположенной плаценты,
-синдром задержки роста плода,
-невынашивания беременности/тей, в т.ч. после вспомогательных репродуктивных технологий,
-кровотечения после родов, абортов, преждевременных родов;
до беременности оценивают наличие в крови диагностических титров критериальных и некритериальных антифосфолипидных антител, а также положительного лабораторного теста на волчаночный антикоагулянт, определяют количество В-лимфоцитов и NK-клеток в периферической крови.
Для определения и оценки наличия в крови диагностических титров антифосфолипидных (АФА) антител используют иммуноферментный анализ (ИФА) с применением твердофазных тест-систем (полистиролового планшета) для иммобилизации антигенов. Метод ИФА основан на связывании АФА в исследуемом образце с поверхностью полистиролового планшета, покрытого неподвижной фазой. В результате этого образуется комплекс антиген-антитело, который выявляют с помощью фермента пероксидазы. Пероксидаза расщепляет специфический хромогенный субстрат, вызывая изменение цвета, интенсивность которого определяется фотометрическим методом при длине волны 450 нм.
Научный комитет по стандартизации Международного общества тромбозов и гемостаза (Scientific Standardization Committee of the International Society of Thrombosis and Haemostasis) в 2014 г. представил рекомендации по выявлению АФА с помощью твердофазных тест-систем. В сыворотках периферической крови содержание антител IgG/IgM к кардиолипину, фосфатидилсерину, фосфатидилинозитолу, фосфатидиловой кислоте, бета2-гликопротеину-I, аннексину 5, протромбину определяли методом твердофазного иммуноферментного анализа (ИФА) с использованием коммерческих тест-систем фирмы Orgentec Diagnostika GmbH (Германия).
При постановке исследований используют стандартные образцы для построения калибровочной кривой и контрольные образцы.
Учет результатов анализа проводят инструментально путем измерения оптической плотности на автоматическом спектрофотометре для микропланшет серии EL×808 производства BioTek Instruments Inc. (США) при длине волны 450 нм. Результаты исследования оценивают в соответствии с рекомендациями производителя.
Антифосфолипидные антитела (АФА) представляют собой гетерогенную группу аутоантител, направленных против комплексов, содержащих фосфолипиды и белки, в кровеносной системе. Они играют ключевую роль в патогенезе антифосфолипидного синдрома (АФС), характеризующегося тромбозами, осложнениями беременности и другими клиническими проявлениями. АФА делятся на критериальные и некритериальные в зависимости от их роли в диагностических критериях АФС, принятых в 2006 году в Сиднее (Международные критерии для установки диагноза АФС, Sydney Consensus Workshop, Sydney, 2006).
В настоящем изобретении в качестве критериальных антифосфолипидных антител учитывают наличие:
- антител к кардиолипину (aCL);
- антител к β2-гликопротеину I (aβ2GPI);
- волчаночного антикоагулянта (LA).
В качестве некритериальных антифосфолипидных антител оценивают наличие:
- антител к фосфатидилсерину/протромбиновому комплексу;
- антител к фосфатидилэтаноламину;
- антител к протромбину;
- антител к аннексину V;
- антител к хорионическому гонадотропину человека (ХГЧ);
- антител к фосфатидиловой кислоте;
- антинуклеарный фактор;
- антител к двуспиральной ДНК.
Определение и дальнейшее оценивание положительного лабораторного теста на волчаночный антикоагулянт (ВА) основано на способности присутствующих в плазме пациента АФА удлинять время свертывания крови. Выявление волчаночного антикоагулянта проводят на основании рекомендаций Международного общества по изучению тромбозов и гемостаза (ISTH) по выявлению волчаночного антикоагулянта. Для верификации волчаночного коагулянта применяют специальные коагуляционные тесты, среди которых основными являются тест с разбавленным ядом гадюки Рассела и активированное частичное тромбопластиновое время (АЧТВ). Стандартная процедура детекции волчаночного антикоагулянта включает скрининговые и подтверждающие тесты. Результаты тестов интерпретируют в соответствии с рекомендациями ISTH как положительные или отрицательные на основании расчета нормализованного отношения скринингового и подтверждающего тестов.
Определение количества В-лимфоцитов и NK-клеток определяет иммунный статус пациентки. Для этого используют методику определения субпопуляций лимфоцитов.
Для анализа используют периферическую кровь, взятую в пробирки с антикоагулянтом (гепарин). На следующем этапе 50 мкл крови переносят в содержащие стандартное количество флуоресцентных микрочастиц и проводят инкубацию лимфоцитов крови со смесью моноклональных антител, конъюгированных с флуорохромами: анти-CD3-FITC, анти-CD16-PE, анти-CD56-PE, анти-CD45-PerCP-Cy5.5, анти-CD4-PE-Cy7, анти-CD19- APC, анти-CD8-APC-Cy7, взятой в количестве 20 мкл. Инкубацию проводят в течение 15 мин при комнатной температуре в темноте. Затем к образцам добавляют 450 мкл лизирующего раствора и инкубируют в течение 15 мин при комнатной температуре в темноте. Затем проточной цитометрией определяют количество дифференцировочных антигенов (CD3, CD4, CD8, CD19 и CD16+56).
После проведения измерений определяют относительное содержание Т-лимфоцитов, В-лимфоцитов и NK-клеток в % к общему количеству лимфоцитов, а также рассчитывают их абсолютное содержание в 1 мкл крови исходя из анализа концентрации флуоресцентных микрочастиц.
Далее рассчитывают риск развития хронической плацентарной недостаточности в процентах по следующей формуле:
P = 1 / (1 + e-z) × 100%
Способ подтверждается следующими клиническими примерами:
Пример 1. Беременная с антенатальной гибелью плода в анамнезе, высоким уровнем ВА в крови (1,30), титры АФА - в пределах референсных значений, субпопуляционный состав лимфоцитов периферической крови:
• В-лимфоциты (CD19+) - 10,2%
• NK-клетки 13,4%
Рассчитывают значение Z:
Z=-4,529 - 1,092×1 + 0,003×13,4 + 0,330×10,2 = -4,529 - 1,092 + 0,040 + 3,366 = -2,220
Рассчитывают значение e-z=0,109.
Рассчитывают вероятность развития хронической плацентарной недостаточности при последующей беременности
Р=1/(1+e-z) × 100% = 90,17%
У пациентки развилась хроническая плацентарная недостаточность - гемодинамические нарушения I степени (в правой маточной артерии) при сроке 35 недель. Роды через естественные родовые пути в 38 недель, родилась девочка 3050/52 с оценкой по Апгар 8 баллов.
Таким образом, значение P указывает на высокий риск хронической плацентарной недостаточности, что и подтвердилось при наблюдении за течением беременности.
Пример 2. Пациентка с 4 самопроизвольными выкидышами в анамнезе при сроках 7-10 недель. При обследовании на этапе планирования беременности выявлено:
• нормальный уровень ВА в крови (1,08)
• повышение уровня АТ к аннексину 5 (12,4 отн ед/мл)
• В-лимфоциты (CD19+) - 32,83%
• NK-клетки 4,1%
Рассчитывают значение Z:
Z=-4,529 - 1,092×1 + 0,003×4,1 + 0,330×32,83 = -4,529 - 1,092 + 0,012 + 10,834 = 5,225
Рассчитывают значение e-z=0,0054.
Рассчитывают вероятность развития хронической плацентарной недостаточности при последующей беременности
Р=1/(1+e-z) × 100%= 99,46%
У пациентки развилась хроническая плацентарная недостаточность - задержка роста плода выявлена при сроке 32 недели. Роды путем экстренной операции кесарева сечения при сроке 37 1/7 недель, родилась живая доношенная девочка массой 2380 грамм, длиной 48 см, с оценкой по Апгар 8 баллов.
Таким образом, значение P указывает на высокий риск хронической плацентарной недостаточности, что и подтвердилось при анализе исхода беременности.
Пример 3. Пациентка с 2 неразвивающимися беременностями при сроках 7-8 недель. При обследовании на этапе планирования беременности выявлено:
• нормальный уровень ВА в крови (1,08)
• нормальный титр АФА в крови
• В-лимфоциты (CD19+) - 4%
• NK-клетки 16%
Рассчитывают значение Z:
Z=-4,529 - 1,092×0 + 0,003×16 + 0,330×4 = -4,529 + 0,048 + 1,32 = -3,161
Рассчитывают значение e-z=23,59.
Рассчитывают вероятность развития хронической плацентарной недостаточности при последующей беременности
Р=1/(1+e-z) × 100% = 4,07%
У пациентки беременность протекала без осложнений, родоразрешена в сроке 38 2/7 недель путем экстренной операции кесарева сечения в связи с излитием околоплодных вод и наличием рубца на матке. Родилась живая доношенная девочка массой 3280 грамм, длиной 50 см, с оценкой по Апгар 8 баллов.
Таким образом, значение P указывает на низкий риск хронической плацентарной недостаточности, что и подтвердилось при оценке исхода беременности.
Таким образом, использование предложенного способа позволяет осуществить прогнозирование риска развития хронической плацентарной недостаточности на этапе планирования беременности.
Осуществление данного способа позволяет сформировать группу высокого риска по развитию тяжелого осложнения беременности и осуществить меры по профилактике хронической плацентарной недостаточности.
Изобретение относится к медицине, в частности к акушерству и гинекологии, и может быть использовано для прогнозирования риска развития хронической плацентарной недостаточности на этапе планирования беременности. Определяют наличие в крови диагностических титров критериальных и некритериальных антифосфолипидных антител, количества B-лимфоцитов и NK-клеток. Далее рассчитывают риск развития хронической плацентарной недостаточности. При P=30,0% и менее прогнозируют низкий риск развития хронической плацентарной недостаточности. Способ позволяет осуществить прогнозирование риска развития хронической плацентарной недостаточности на этапе планирования беременности, сформировать группу высокого риска по развитию тяжелого осложнения беременности и осуществить меры по профилактике хронической плацентарной недостаточности. 2 з.п. ф-лы, 2 ил., 3 пр.
1. Способ прогнозирования риска развития хронической плацентарной недостаточности на этапе планирования беременности, включающий определение наличия в крови диагностических титров критериальных и некритериальных антифосфолипидных антител (АФА), определение количества В-лимфоцитов и NK-клеток в периферической крови, далее рассчитывают риск развития хронической плацентарной недостаточности в процентах по следующей формуле:
P = 1 / (1 + e-z) × 100%;
Где Р - риск развития хронической плацентарной недостаточности (%);
Z - уравнение регрессии;
е - снование натуральных логарифмов;
z = -4,529 - 1,092 X Диагностические титры АФА + 0,003 XNK-клетки + 0,330 XВ-лимфоциты (CD19+);
где X Диагностические титры АФА - Диагностические титры АФА (0 - Без АФА, 1 - Диагностические титры АФА);
XNK-клетки - NK-клетки (%);
XВ-лимфоциты (CD19+) - В-лимфоциты (CD19+) (%)
При P=33,6% и выше прогнозируют высокий риск развития хронической плацентарной недостаточности, при P=30,0% и менее прогнозируют низкий риск развития хронической плацентарной недостаточности.
2. Способ по п.1, отличающийся тем, что в качестве диагностических титров критериальных антифосфолипидных антител оценивают наличие:
- антител к кардиолипину (aCL);
- антител к β2-гликопротеину I (aβ2GPI);
- волчаночного антикоагулянта (LA).
3. Способ по п.1, отличающийся тем, что в качестве диагностических титров некритериальных антифосфолипидных антител оценивают наличие:
- антител к фосфатидилсерину/протромбиновому комплексу;
- антител к фосфатидилэтаноламину;
- антител к протромбину;
- антител к аннексину V;
- антител к хорионическому гонадотропину человека (ХГЧ);
- антител к фосфатидиловой кислоте;
- антинуклеарный фактор;
- антител к двуспиральной ДНК.
| СПОСОБ ОЦЕНКИ РИСКА НЕВЫНАШИВАНИЯ БЕРЕМЕННОСТИ У ЖЕНЩИН С ПРИВЫЧНЫМ НЕВЫНАШИВАНИЕМ | 2017 |
|
RU2657433C1 |
| Способ прогнозирования репродуктивных потерь в сроке до 22 недель беременности у женщин с угрожающим выкидышем и привычным невынашиванием в анамнезе | 2020 |
|
RU2746033C1 |
| ДОЛГОВА Ю.С | |||
| и др | |||
| встречаемость антифосфолипидных антител при наличии отягощенного акушерско-гинекологичекого анамнеза и отягощенного тромботичекого анамнеза | |||
| Акушерство и гинекология Санкт-Петербурга | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| БАГДАСАРОВА Ю.С | |||
| и др | |||
| Частота плацента-ассоциированных осложнений при | |||
Авторы
Даты
2024-12-09—Публикация
2024-02-16—Подача