Изобретение относится к медицине, в частности к акушерству и гинекологии, и может быть использовано для прогнозирования риска развития хронической плацентарной недостаточности при сроке беременности 16-18 недель у женщин с циркуляцией АФА (антифосфолипидных антител) и отягощенным акушерским анамнезом.
Известен Способ диагностики хронической плацентарной недостаточности (патент на изобретение №2313795), в котором с целью повышения точности диагностики ХПН осуществляют определение в крови беременных женщин фактора роста плаценты и термостабильной щелочной фосфатазы, дополнительно производят определение содержания лимфоцитов, экспрессирующих специализированный рецептор сигналов индукции апоптоза - Fas-антиген (СД95+), и концентрацию фактора некроза опухоли альфа (ФНОα) и при изменении этих показателей по сравнению с нормой диагностируют хроническую плацентарную недостаточность и степень ее тяжести. Недостатком данного способа является отсутствие указания срока беременности, на котором данный способ может быть применен. Примеры, отраженные в описательной части, указывают на применение способа в III триместре беременности, что может привести к несвоевременной диагностике ХПН ввиду изменения показателей, указанных в формуле, с течением срока беременности.
Задачей предложенного изобретения является повышение точности прогнозирования развития хронической плацентарной недостаточности при сроке беременности 16-18 недель у женщин с циркуляцией АФА и отягощенным акушерским анамнезом.
Техническим результатом изобретения является расширение арсенала средств специфичного и точного прогнозирования риска развития хронической плацентарной недостаточности у женщин с циркуляцией АФА и отягощенным акушерским анамнезом при сроке беременности 16-18 недель.
Указанный технический результат достигается тем, что при сроке беременности 16-18 недель у женщин с циркуляцией АФА и отягощенным акушерским анамнезом, включающий измерение уровня Д-димера, определенного в крови пациенток в сроке 16-18 недель, измерение уровня антитромбина III (AT III), определенного в крови беременных в сроке 16-18 недель, а также включающий значения полученных измерений уровня растворимой fms-подобной тирозинкиназы (sFlt), определенной в крови пациенток в сроке 6-8 недель, и включающий значения полученных измерений уровня плацентарного фактора роста (P1GF), определенного в крови беременных в сроке 6-8 недель, далее рассчитывают риск развития хронической плацентарной недостаточности в процентах по следующей формуле:
Р = 1 / (1 + e z) × 100%
z = -10,152 - 0,006ХД.димер + 0,127ХАТ III - 0,012XsF1t/P1GF;
где Р – вероятность развития хронической плацентарной недостаточности;
z – уравнение регрессии;
е – основание натуральных логарифмов;
ХД.димер – уровень Д-димера (нг/мл), определенный в крови пациенток в сроке 16-18 недель беременности;
ХАТ III – уровень AT III (%), определенный в крови пациенток в сроке 16-18 недель беременности;
XSF1t/P1GF – соотношение sF1t/P1GF, определенное в крови пациенток в сроке 6-8 недель беременности;
при Р, равном 32,2% и выше, прогнозируют высокий риск развития хронической плацентарной недостаточности, при Р, равном 32,1% и менее, прогнозируют низкий риск развития хронической плацентарной недостаточности.
Новизна изобретения заключается в том, что впервые предложен способ, с помощью которого возможно прогнозирование риска развития хронической плацентарной недостаточности при сроке беременности 16-18 недель у женщин с циркуляцией АФА и отягощенным акушерским анамнезом, для реализации которого в качестве предикторов определяется уровень Д-димера, уровень антитромбина III, уровень растворимой fms-подобной тирозинкиназы (sFlt), плацентарного фактора роста (P1GF), в крови пациенток.
На основании результатов наблюдения за течением беременности пациенток с циркуляцией АФА и отягощенным акушерским анамнезом, была разработана прогностическая модель для определения вероятности ХПН в зависимости от уровня Д-димера, антитромбина III, определенных в крови пациенток при сроке 16-18 недель и соотношения sF1t/P1GF, определенного в сроке 6-8 недель, методом бинарной логистической регрессии. Число наблюдений составило 156.
В Табл. 1 представлены характеристики связи предикторов модели с вероятностью выявления ХПН. В Табл. 2 представлены пороговые значения логистической функции Р.
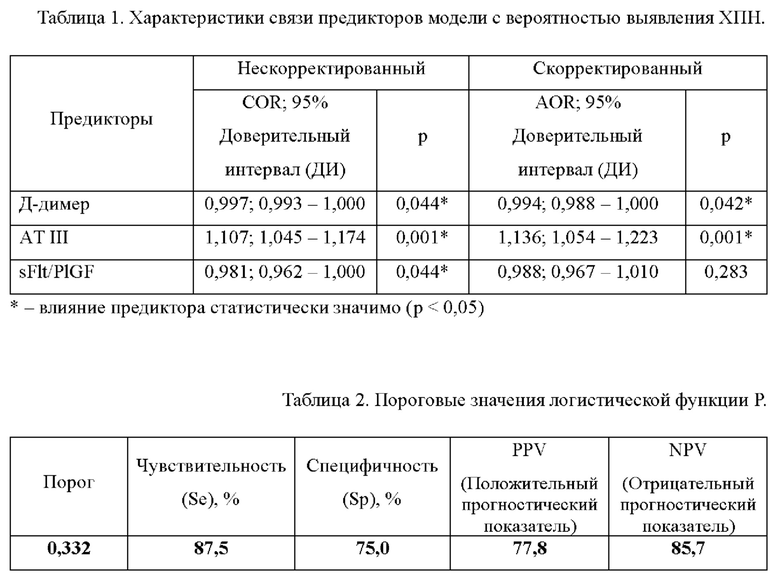
Полученная регрессионная модель является статистически значимой (р < 0,001). Исходя из значения коэффициента детерминации Найджелкерка, модель объясняет 56,5% наблюдаемой дисперсии ХПН.
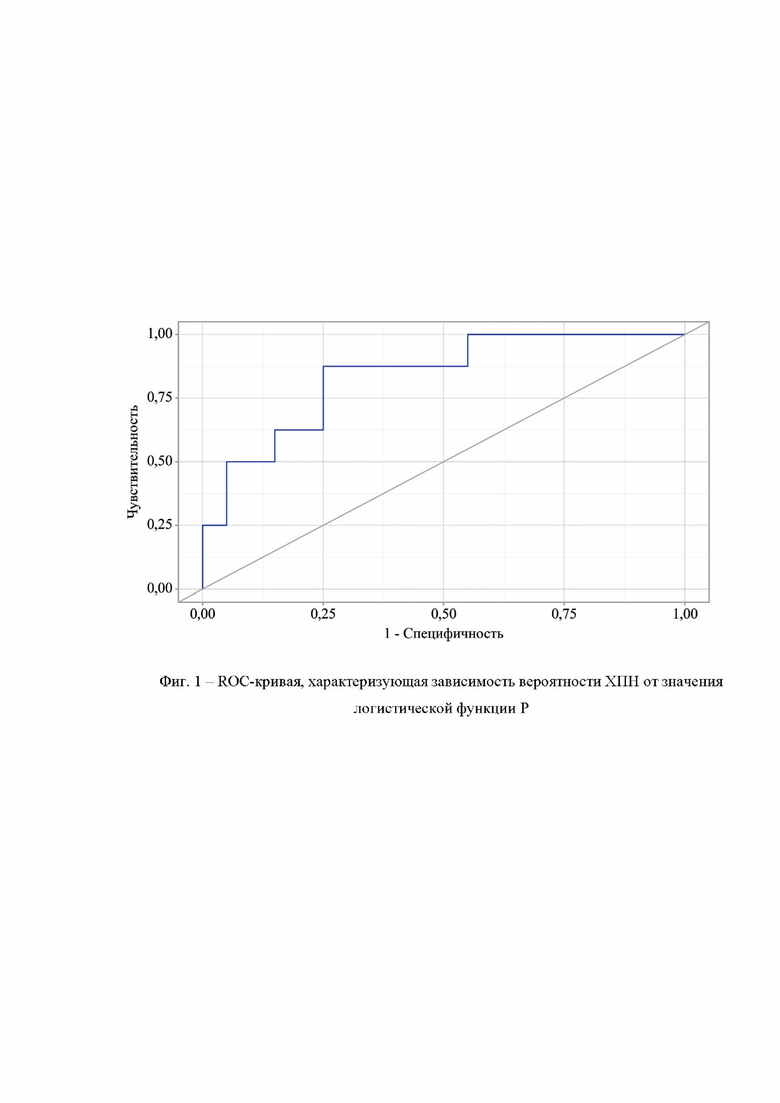
При оценке зависимости вероятности хронической плацентарной недостаточности от значения логистической функции Р с помощью ROC-анализа была получена следующая кривая (Фиг. 1).
Площадь под ROC-кривой составила 0,838 ± 0,067 с 95% ДИ: 0,707 - 0,968.
Полученная модель была статистически значимой (р < 0,001).
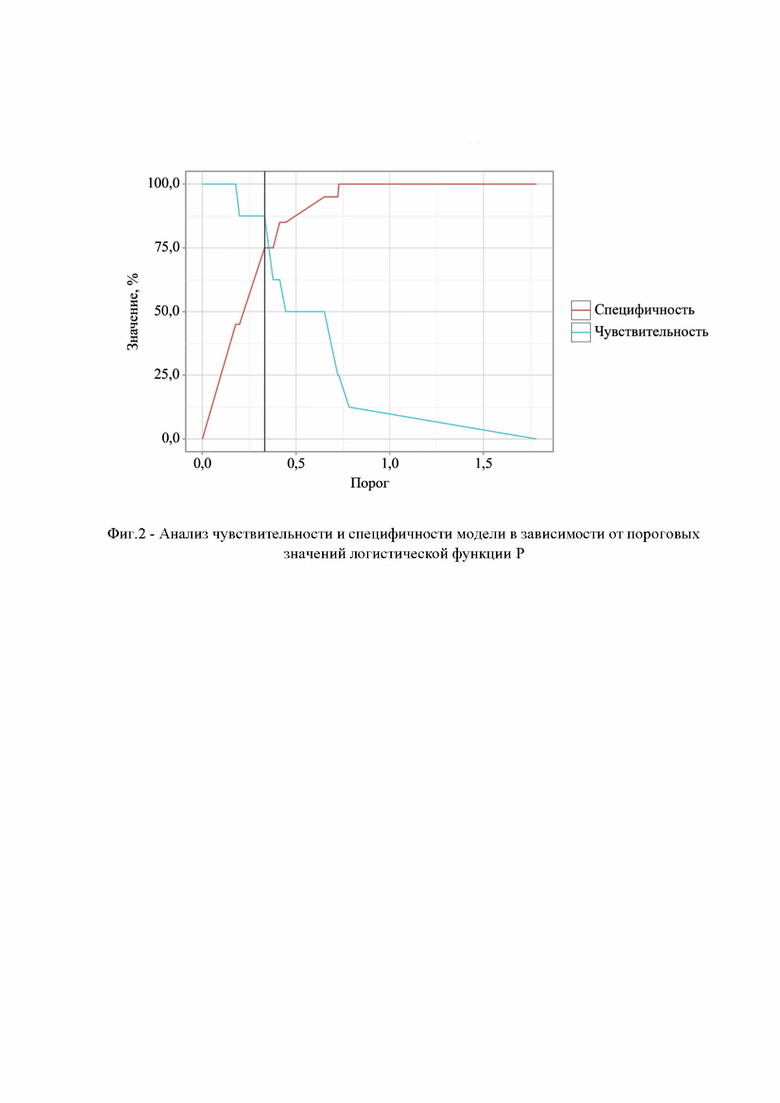
Пороговое значение логистической функции Р в точке cut-off, которому соответствовало наивысшее значение индекса Юдена, составило 0,332. Хроническая плацентарная недостаточность прогнозировалась при значении логистической функции Р выше данной величины или равном ей. Чувствительность и специфичность модели составили 87,5% и 75,0%, соответственно (Фиг. 2).
Разработанная прогностическая модель исследует взаимосвязь между уровнем Д-димера, антитромбина III при сроке беременности 16-18 недель и соотношением sF1t/P1GF, измеренным на ранних сроках беременности (6-8 недель) и вероятностью развития хронической плацентарной недостаточности (ХПН).
Таким образом, данная модель предоставляет ценные направления для клинической практики, позволяя своевременно идентифицировать беременных женщин с высоким риском развития ХПН и принимать необходимые профилактические меры.
Краткое описание чертежей
На Фиг. 1 представлена ROC-кривая, характеризующая зависимость вероятности ХПН от значения логистической функции Р, полученная с помощью ROC-анализа.
На Фиг. 2 представлен Анализ чувствительности и специфичности модели в зависимости от пороговых значений логистической функции Р.
Способ осуществляется следующим образом:
У пациенток с циркуляцией диагностических титров АФА (критериальных и некритериальных) и отягощенным акушерским анамнезом, то есть у которых в анамнезе зафиксировано:
-потеря/потери плода,
-тяжелая преэклампсия,
-преждевременная отслойка нормально расположенной плаценты (ПОНРП),
-синдром задержки роста плода,
-невынашивания беременности/тей, в т.ч. после вспомогательных репродуктивных технологий,
-кровотечения после родов, абортов, преждевременных родов;
при сроке беременности 16-18 недель осуществляют измерение уровня Д-димера, определенного в крови пациенток в сроке 16-18 недель, измеряют уровень антитромбина III (AT III), определенного в крови беременных в сроке 16-18 недель, а также включают значения полученных измерений уровня растворимой fms-подобной тирозинкиназы (sFlt), определенной в крови пациенток в сроке 6-8 недель, и включают значения полученных измерений уровня плацентарного фактора роста (P1GF), определенного в крови беременных в сроке 6-8 недель.
Определение наличия в крови растворимой fms-подобной тирозинкиназы (sFlt).
Fms-подобная тирозинкиназа (sFlt) является растворимой формой васкулярного эндотелиального фактора роста (VEGF) рецептора 1, которая активно участвует в регуляции ангиогенеза. sFlt действует как «ловушка» для VEGF, предотвращая его связывание с мембранными рецепторами на эндотелиальных клетках, тем самым модулируя ангиогенез и сосудистую проницаемость. В контексте акушерства, повышенные уровни sFlt ассоциируются с патогенезом преэклампсии, заболеванием, характеризующимся высоким артериальным давлением и нарушением функции других органов у беременных.
Содержание sFlt (пг/мл) в сыворотке периферической крови определяют методом электрохемилюминесцентного анализа с использованием коммерческих тест-систем Elecsys sFlt фирмы Roche Diagnostics GmbH (Германия) на автоматическом иммунохимическом анализаторе Cobas е411 (Япония). К 20 мкл образца сыворотки крови пациента добавляется одновременно биотинилированное моноклональное антитело, специфичное к sFlt и специфичное к sFlt моноклональное антитело, меченное рутениевым комплексом. После инкубации в течение 9 минут при 37°С добавляются микрочастицы, покрытые стрептавидином. Образовавшиеся в результате первой инкубации комплексы связываются с микрочастицами посредством взаимодействия биотина и стрептавидина. Далее реакционная смесь забирается в измерительную ячейку, где микрочастицы оседают на поверхность электрода в результате магнитного взаимодействия. Затем с помощью промывающих растворов удаляются не связавшиеся вещества. Далее приложенное к электроду напряжение вызывает хемилюминесцентную эмиссию, которая измеряется фотоумножителем. Результаты исследования оценивали количественным способом с помощью 2-точечной калибровочной кривой и референсной калибровочной кривой, данные которой предоставлены производителем в штрих-коде к реагенту.
Определение наличия в крови плацентарного фактора роста (P1GF).
Плацентарный фактор роста (PIGF) представляет собой белок, который также участвует в регуляции ангиогенеза и взаимодействует с VEGF и его рецепторами. P1GF способствует росту и выживаемости эндотелиальных клеток, а также стимулирует васкуляризацию плаценты. Уровни P1GF снижаются при преэклампсии, что делает его потенциальным маркером для раннего выявления и мониторинга этого состояния.
Содержание PIGF (пг/мл) в сыворотке периферической крови определяют методом электрохемилюминесцентного анализа с использованием коммерческих тест-систем «Elecsys PIGF» фирмы Roche Diagnostics GmbH (Германия) на автоматическом иммунохимическом анализаторе Cobas е411 (Япония). К 20 мкл образца сыворотки крови пациента добавляется одновременно биотинилированное моноклональное антитело, специфичное к PIGF и специфичное к PIGF моноклональное антитело, меченное рутениевым комплексом. После инкубации в течение 9 минут при 37°С добавляются микрочастицы, покрытые стрептавидином. Образовавшиеся в результате первой инкубации комплексы связываются с микрочастицами посредством взаимодействия биотина и стрептавидина. Далее реакционная смесь забирается в измерительную ячейку, где микрочастицы оседают на поверхность электрода в результате магнитного взаимодействия. Затем с помощью промывающих растворов удаляются не связавшиеся вещества. Далее приложенное к электроду напряжение вызывает хемилюминесцентную эмиссию, которая измеряется фотоумножителем. Результаты исследования оценивали количественным способом с помощью 2 точечной калибровочной кривой и референсной калибровочной кривой, данные которой предоставлены производителем в штрих-коде к реагенту.
Определение наличия в крови Д-димера и AT III осуществляется оптическим методом на автоматическом коагулометре модели ACL-200 производства компании Instrumentation Laboratory (Испания) с реактивами HemosIL (Италия) согласно инструкции.
Далее рассчитывают риск развития хронической плацентарной недостаточности в процентах по следующей формуле:
P = l / (l + e z) × 100%
Способ подтверждается следующими клиническими примерами:
Пример 1
Повторнородящая 29 лет с антенатальной гибелью плода в сроке 25 недели беременности в анамнезе, 1 неразвивающейся беременностью при сроке 7 недель, высоким уровнем волчаночного антикоагулянта (ВА) в крови (1,32).
При обследовании в сроке 7 недель беременности определялись показатели в крови:
Соотношение sFlt/ P1GF - 31,458.
При обследовании в сроке 17 недель беременности определялись показатели в крови:
уровень Д-димера в крови (нг/мл) - 745;
уровень ATIII (%) - 92,0;
Р = 1 / (1 + e z) × 100%
Z = -10,152 - 0,006ХД-димер + 0,127ХAT III - 0,012XsF1t/P1GfF
Рассчитывают значение Z:
z=-10,152-0,006×745+0,127×92-0,012×31,458 = -10,152-4,47+11,684-0,377 = -3,315
Рассчитывают значение e z=0,0363.
Рассчитывают вероятность развития хронической плацентарной недостаточности при последующей беременности:
P=l/(l+e z) ×100% = 96,5%
У пациентки развилась хроническая плацентарная недостаточность - гемодинамические нарушения I степени (в правой маточной артерии) при сроке 30 недель. Роды путем экстренной операции кесарева сечения в 35 недель в связи с началом родовой деятельности и рубцом на матке после кесарева сечения, родилась девочка 2260/45 с оценкой по Апгар 7 баллов. По данным гистологического исследования плаценты - ХПН, субкомпенсированная стадия.
Таким образом, значение Р указывает на высокий риск хронической плацентарной недостаточности, что и подтвердилось при наблюдении за течением беременности.
Пример 2
Повторнобеременная первородящая 34 лет с 1 неразвивающейся беременностью при сроке 8 недель и 1 самопроизвольным выкидышем при сроке 7 недель, высоким уровнем ВА в крови (1,29), диагностическим тиром AT к аннексину 5 - 9,129.
При обследовании в сроке 7 недель беременности определялись показатели в крови:
Соотношение sFlt/ P1GF - 24,329
При обследовании в сроке 17 недель беременности определялись показатели в крови:
уровень Д-димера в крови (нг/мл) - 239;
уровень АТIII (%) - 115,0
Р = 1 / (1 + e z) × 100%
z = -10,152 - 0,006ХД.димер + 0,127ХАТ III - 0,012XsF1t/P1GF
Рассчитывают значение Z:
z = -10,152-0,006×239+0,127×115-0,012×24,329 = -10,152-1,434+14,605-0,292 = 2,727
Рассчитывают значение e z=15,287
Рассчитывают вероятность развития хронической плацентарной недостаточности при последующей беременности:
P=l/(l+e z) × 100% = 6,13%
У пациентки беременность протекала без осложнений, признаков плацентарной недостаточности не было выявлено. Роды через естественные родовые пути в 39 5/7 недель, родился живой доношенный мальчик 3470 грамм, длиной 52 см, с оценкой по Апгар 8 баллов. По данным гистологического исследования плаценты - нормопластический тип строения плаценты.
Таким образом, значение Р указывает на низкий риск хронической плацентарной недостаточности, что и подтвердилось при анализе исхода беременности.
Пример 3
Повторнородящая 39 лет с ПОНРП в анамнезе при сроке 29 недель беременности в анамнезе, кровотечением, высоким уровнем AT к кардиолипину - 15,239 в крови.
При обследовании в сроке 8 недель беременности определялись показатели в крови:
Соотношение sFlt/ P1GF - 36,294.
При обследовании в сроке 16 недель беременности определялись показатели в крови:
Уровень Д-димера в крови (нг/мл) - 325
уровень АТШ (%) - 100,0
Р = 1 / (1+e z) × 100%
z = -10,152 - 0,006Хд.димер + 0,127ХAT III - 0,012Xsf1t>P1GF;
Рассчитывают значение Z:
z = -10,152 - 0,006×325+0,127×100-0,012×36,294 = -10,152-1,95+12,7-0,435 = 0,163
Рассчитывают значение e z=l,177
Рассчитывают вероятность развития хронической плацентарной недостаточности при последующей беременности
P=l/(l+e z) × 100% = 45,9%
У пациентки развилась хроническая плацентарная недостаточность - гемодинамические нарушения I степени (в правой маточной артерии) при сроке 32 недели. Роды через естественные родовые пути в 37/38 недель, родилась девочка 2800/47 с оценкой по Апгар 8 баллов. По данным гистологического исследования плаценты - ХПН, компенсированная стадия.
Таким образом, значение Р указывает на высокий риск хронической плацентарной недостаточности, что и подтвердилось при наблюдении за течением беременности.
Таким образом, использование предложенного способа позволяет осуществить прогнозирование риска развития хронической плацентарной недостаточности при сроке беременности 16-18 недель у женщин с циркуляцией АФА и отягощенным акушерским анамнезом. Своевременное выявление данного заболевания, учитывая факторы антиогинеза (sFlt/PIGF), а также учитывая существенное влияние системы гемостаза, позволяет своевременно начать профилактические и терапевтические мероприятия, направленные на профилактику развития ХПН.
Использование комплексного подхода, включающего определение в крови ряда маркеров (растворимой fms-подобной тирозинкиназы (sFlt), плацентарного фактора роста (P1GF), Д-димера, антитромбина III), позволяет достичь высокой точности прогнозирования риска развития ХПН.
Регрессионная модель, разработанная на основе клинических наблюдений и предикторов, демонстрирует статистическую значимость и способна объяснить 56,5% наблюдаемой дисперсии ХПН, что подтверждает эффективность и надежность способа. Предложенный способ предлагает новые возможности для профилактики и патогенетически обоснованной терапии хронической плацентарной недостаточности, что может оказать положительное влияние на исходы беременности у женщин с высоким риском развития данного состояния.
Изобретение относится к медицине, а именно к акушерству и гинекологии, и может быть использовано для прогнозирования риска развития хронической плацентарной недостаточности при сроке беременности 16-18 недель у женщин с циркуляцией антифосфолипидных антител (АФА) и отягощенным акушерским анамнезом. Осуществляют измерение уровня Д-димера в крови пациенток в сроке 16-18 недель, измерение уровня антитромбина III (АТ III) в крови беременных в сроке 16-18 недель. Также включают значения полученных измерений уровня растворимой fms-подобной тирозинкиназы (sFlt), определенной в крови пациенток в сроке 6-8 недель и значения полученных измерений уровня плацентарного фактора роста (PlGF), определенного в крови беременных в сроке 6-8 недель. Рассчитывают риск развития хронической плацентарной недостаточности в процентах по следующей формуле: P = 1 / (1 + e z) × 100%; z = -10,152 - 0,006XД-димер + 0,127XАТ III - 0,012XsFlt/PlGF; где P – вероятность развития хронической плацентарной недостаточности; z – уравнение регрессии; е – основание натуральных логарифмов; XД-димер – уровень Д-димера (нг/мл), определенный в крови пациенток в сроке 16-18 недель беременности; XАТ III – уровень АТ III (%), определенный в крови пациенток в сроке 16-18 недель беременности; XsFlt/PlGF – соотношение sFlt/PlGF, определенное в крови пациенток в сроке 6-8 недель беременности. При P, равном 32,2% и выше, прогнозируют высокий риск развития хронической плацентарной недостаточности. При P, равном 32,1% и менее, прогнозируют низкий риск развития хронической плацентарной недостаточности. Способ обеспечивает возможность повышения специфичности и точности прогнозирования риска развития хронической плацентарной недостаточности у женщин с циркуляцией АФА и отягощенным акушерским анамнезом при сроке беременности 16-18 недель за счет измерения уровня Д-димера и антитромбина III в крови пациенток при сроке беременности 16-18 недель и измерения уровня растворимой fms-подобной тирозинкиназы sFlt и плацентарного фактора роста P1GF в крови пациенток в сроке 6-8 недель. 2 ил., 2 табл., 3 пр.
Способ прогнозирования риска развития хронической плацентарной недостаточности при сроке беременности 16-18 недель у женщин с циркуляцией антифосфолипидных антител (АФА) и отягощенным акушерским анамнезом, включающий измерение уровня Д-димера, определенного в крови пациенток в сроке 16-18 недель, измерение уровня антитромбина III (АТ III), определенного в крови беременных в сроке 16-18 недель, а также включающий значения полученных измерений уровня растворимой fms-подобной тирозинкиназы (sFlt), определенной в крови пациенток в сроке 6-8 недель, и включающий значения полученных измерений уровня плацентарного фактора роста (PlGF), определенного в крови беременных в сроке 6-8 недель, далее рассчитывают риск развития хронической плацентарной недостаточности в процентах по следующей формуле:
P = 1 / (1 + e z) × 100%
z = -10,152 - 0,006XД-димер + 0,127XАТ III - 0,012XsFlt/PlGF;
где P – вероятность развития хронической плацентарной недостаточности;
Z – уравнение регрессии;
е – основание натуральных логарифмов;
XД-димер – уровень Д-димера (нг/мл), определенный в крови пациенток в сроке 16-18 недель беременности;
XАТ III – уровень АТ III (%), определенный в крови пациенток в сроке 16-18 недель беременности;
XsFlt/PlGF – соотношение sFlt/PlGF, определенное в крови пациенток в сроке 6-8 недель беременности;
при P, равном 32,2% и выше, прогнозируют высокий риск развития хронической плацентарной недостаточности, при P, равном 32,1% и менее, прогнозируют низкий риск развития хронической плацентарной недостаточности.
| СПОСОБ РЕТРОСПЕКТИВНОЙ (ПОСЛЕРОДОВОЙ) ЭКСПРЕСС-ДИАГНОСТИКИ ПЛАЦЕНТАРНОЙ НЕДОСТАТОЧНОСТИ ДЛЯ ВЫЯВЛЕНИЯ ГРУППЫ НОВОРОЖДЕННЫХ ВЫСОКОГО РИСКА РАЗВИТИЯ ПАТОЛОГИИ В НЕОНАТАЛЬНЫЙ ПЕРИОД И ПЕРИОД НОВОРОЖДЕННОСТИ | 2007 |
|
RU2361213C2 |
| RU 2008102818 A, 24.01.2008 | |||
| Способ прогнозирования течения беременности и родов у женщин с сочетанием ожирения и тромбофилии | 2020 |
|
RU2751415C1 |
| WO 2005076000 A1, 18.08.2005 | |||
| АРСЛАНБЕКОВА М.О | |||
| Сравнительная оценка эффективности различных режимов терапии у женщин с антифосфолипидным синдромом и отягощенным акушерским анамнезом | |||
| Дисс., Москва, 2021, стр | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| БАГДАСАРОВА Ю.С | |||
| и др | |||
| Частота | |||
Авторы
Даты
2024-11-18—Публикация
2024-05-22—Подача