Изобретение относится к технологии получения и использования в производстве фотокатализаторов для разложения органических веществ и загрязнителей при очистке воды, воздуха и в других фотохимических процессах, в газовых и оптических сенсорах.
Известен катализатор на основе гидроксильных групп кобальта состава Co3(Si2O5)2(OH)2 в виде низкокристаллических цветкоподобных кристаллов для каталитического разложения углеводородов с большой площадью поверхности и его способ получения из неорганических соединений (нитрата кобальта и силиката натрия при мольном отношении 3:8) в присутствии минерализатора хлорида аммония и аммиака, осуществляемый в гидротермальных условиях при 90°С с выдержкой в течение 12 часов, отделение осадка центрифугированием, промывку водой и этанолом и сушку в течение 12 часов. Показана высокая степень разложения 11-ти органических соединений в присутствии сульфатных радикалов, получаемых при активации пероксимоносульфата калия (2KHSO5⋅3KHSO4⋅K2SO4) кобальтом из CoSiOx https://doi.org/10.1016/j.apcatb.2019.118238.
Недостатками известного катализатора являются необходимость дополнительного введения при разложении органических загрязнителей серосодержащих реагентов в качестве окислителей, а также необходимость использования достаточно большого количества катализатора, что может приводить к вымыванию токсичного металла в присутствии органических веществ (красителей), способных образовывать устойчивые комплексы, и загрязнять растворы.
Известен катализатор для разложения летучих органических соединений, содержащий одноатомный кобальт на основе аморфного оксида кремния и способ его получения, который включает следующие стадии: смешивание и растворение цетилтриметиламмоний бромида и мочевины, добавление циклогексана и н-пентанола для получения смешанного растворителя; добавление ортосиликата этила, соли кобальта и соли алюминия к смешанному растворителю и равномерное перемешивание; гидротермальную обработку при температуре 110-150°С в течение 5-7 часов; последующее прокаливание при температуре 450-650°С в течение 4-6 часов (патент CN 113244920; МПК B01D 53/44, B01D 53/78, B01D 53/86, B01J 21/08, B01J 23/75, B01J 35/00, B01J 37/00, B01J 37/10; 2022 год).
Недостатками известного катализатора являются использование большого количества органических соединений в процессе его получения; необходимость дополнительной стадии прокаливания для полного удаления органических веществ, используемых в синтезе (остатков тетраэтоксисилана и др.), а также из прекурсора катализатора, содержащего прикрепленный к поверхности порообразователь катионы гексадецилтриметиламмония, при этом повышенная температуры прокалки приводит к образованию Co3O4 и, соответственно, агрегации равномерно распределенного кобальта в матрице оксида кремния, что снижает активность катализатора; необходимость дополнительного введения персульфатных соединений в процессе разложения летучих органических соединений, поскольку процесс разложения осуществляется в персульфатном растворе.
Известен фотокатализатор на основе TiO2/SiO2 в матрице силикагеля с размером гранул 0,1+ см и размером фотокаталитически активных частиц 15-20 нм и способ получения смешанного фотокатализатора, включающий на первом этапе получение активных частиц анатаза в гидротермальных условиях из оксисульфата титана и силиката натрия по пероксидной методике в автоклаве при 180°С в течение 24 часов с последующими центрифугированием, отмывкой дистиллированной водой до отрицательной реакции на противоионы исходных солей и сушкой при 60°С в течение 24 часов, на втором этапе - получение золя кремниевой кислоты путем пропускания раствора силиката натрия через катионит КУ-2-8 и введение фотоактивного оксида титана с обработкой смеси УЗ частотой 60 Гц в течение 90 минут, а на третьем этапе - гранулирование путем прикапывания смеси в иммерсионное масло на 24 часа, отмывку от масла и сушку до постоянной массы при 100°С. (RU 2760442, МПК B01J 21/06; B01J 37/03; C01G 23/053; C02F 1/30, 2021)(прототип).
Недостатками известного катализатора являются многостадийность и длительность способа его получения, необходимость использования дополнительного оборудования, образование большого количества промывных вод.
Таким образом, перед авторами стояла задача разработать состав фотокатализатора для разложения органических соединений, обеспечивающего расширение номенклатуры используемых в настоящее время фотокатализаторов, причем который может быть получен технологически простым и надежным способом.
Поставленная задача решена в предлагаемом составе фотокатализатора, содержащего матрицу на основе аморфного диоксида кремния и равномерно распределенного в матрице активного компонента, который в качестве активного компонента содержит гидроксосиликат кобальта состава Co3(Si2O5)2(OH)2 при следующем соотношении компонентов, мас.%: гидроксосиликат кобальта - 0,2÷3,0; аморфный диоксид кремния - 97,0÷99,8.
Поставленная задача также решена в предлагаемом способе получения фотокатализатора, содержащего матрицу на основе аморфного диоксида кремния и равномерно распределенного в матрице гидроксосиликата кобальта, включающем получение исходной смеси гидратированного кремнезема в растворе формиата кобальта Co(HCOO)2⋅2H2O при содержании (в пересчете на Со) в мольном отношении Co:SiO2=(0,001-0,01):1, в присутствии хлорида аммония в количестве 0,1-0,2 мас.% от общей массы смеси и аммиака в количестве 1-2 мас.% от общей массы, гидротермальную обработку исходной смеси в автоклаве при температуре 90-95°С в течение 10-12 часов, c последующим отделением осадка центрифугированием, промывкой до нейтральной реакции дистиллированной водой и сушкой при температуре 100-300°С в течение 3-4 часов.
В настоящее время из патентной и научно-технической литературы не известен фотокатализатор, содержащий матрицу на основе аморфного диоксида кремния и равномерно распределенного в матрице гидроксосиликата кальция в качестве активного компонента, а также способ получения катализатора в предлагаемых условиях.
Предлагаемый катализатор характеризуется низким содержанием активного компонента и проявляет фотокаталитическую активность в течение не менее 3-х циклов без деградации и вымывания кобальта из матрицы SiO2, обладает высокой удельной площадью поверхности. Циклическая стабильность является одним из наиболее важных факторов для оценки катализатора, включая структурную стабильность и возможность повторного использования без деградации.
Экспериментальные исследования, проведенные авторами, позволили сделать вывод, что фотокатализатор на основе оксида кремния, содержащий гидроксосиликат кобальта Co3(Si2O5)2(OH)2 в количестве 0,2-3,0 мас.% может быть получен простым и технологичным способом путем гидротермального синтеза с использованием гидратированного кремнезема и раствора формиата кобальта при мольном отношении (в пересчете на Со) Co:Si=(0,001-0,01):1 в предлагаемых условиях, что обеспечивает сохранение высокодисперсной структуры матрицы оксида кремния и образование на поверхности высокодисперсных частиц оксида кремния дополнительно частиц гидроксосиликата кобальта, обладающего в свою очередь за счет наличия ионов кобальта(2+) фотокаталитической активностью в отношении бензолсодержащих углеводородов.
Авторами экспериментально установлено, что существенным в процессе получения фотокатализатора на основе матрицы оксида кремния, содержащего гидроксосиликат кобальта Co3(Si2O5)2(OH)2, является соблюдение заявляемых параметров процесса. Так, при уменьшении мольного отношения Co:Si менее 0,001 в исходной смеси, снижении температуры гидротермальной обработки ниже температуры 90°С и продолжительности менее 10 часов наблюдается снижение содержания гидроксосиликата кобальта, что приводит к снижению фотокаталитической активности. Увеличение мольного отношения Co:Si более 0,1, температуры выше 95°С и продолжительности обработки более 12 часов не влияет на фотокаталитические свойства, приводит к перерасходу ресурсов (реактивов и электроэнергии) и является нецелесообразным.
Кроме того, необходимо отметить, что при получении фотокатализатора на основе оксида кремния, содержащего гидроксосиликат кобальта Co3(Si2O5)2(OH)2, необходимо обеспечить высокую удельную площадь поверхности, поскольку именно она обеспечивает наибольшую площадь контакта между фотокаталитическим материалом и растворенными углеводородными загрязнителями в растворе. При этом равномерное распределение по всей развитой поверхности прочно удерживаемого кобальта в виде нерастворимого гидроксосиликата Co3(Si2O5)2(OH)2 обеспечивает доступность активных центров, отвечающих за каталитическую активность. Гидротермальный процесс в предлагаемых мягких (не более 95°С) условиях обеспечивает получение равномерного распределения и прочного удерживания нерастворимого гидроксосиликата Co3(Si2O5)2(OH)2 во всем объеме матрицы аморфного высокодисперсного оксида кремния.
Предлагаемый фотокатализатор может быть получен следующим образом. Получают исходную смесь гидратированного кремнезема в растворе формиата кобальта Co(HCOO)2⋅2H2O при содержании (в пересчете на Со) в мольном отношении Co:SiO2=(0,001-0,01):1, в присутствии хлорида аммония в количестве 0,1-0,2 мас.% от общей массы смеси и аммиака в количестве 1-2 мас.% от общей массы, осуществляют гидротермальную обработку исходной смеси в автоклаве при температуре 90-95°С в течение 10-12 часов, c последующим отделением осадка центрифугированием со скоростью 3500 об/мин в течение 10 минут, промывают дистиллированной водой и сушат при температуре 100-300°С в течение 3-4 часов. Фотокаталитическая активность оценивалась по скорости окисления n-дигидроксибензола (гидрохинона) под воздействием УФ-излучения (λ=253 нм). Аттестацию полученных продуктов проводили методами рентгеноструктурного и химического анализов, ИК-спектроскопии, сканирующей электронной микроскопии и измерением удельной площади поверхности методом Брунауэра-Эммета-Теллера (БЭТ) при адсорбции азота. Данные РФА показывают наличие рентгеноаморфного гало высокодисперсного кремнезема и отсутствие кристаллических фаз силикатов и оксидов кобальта. Данные ИК-спектроскопии показывают проявление колебаний Co-O и смещение валентных колебаний тетраэдра SiO4 вследствие образования связей Co-O-Si в области 1020 см-1, что подтверждает образование гидроксосиликата кобальта. По данным СЭМ продукт представляет агломерированный тонкодисперсный порошок с округлой формой частиц, заданное содержание кобальта подтверждено химическим анализом. Величины удельной площади поверхности материалов составляют 150-250 м2/г, что характеризует развитую поверхность.
На фиг. 1 приведена морфология частиц Co3(Si2O5)2(OH)2/SiO2.
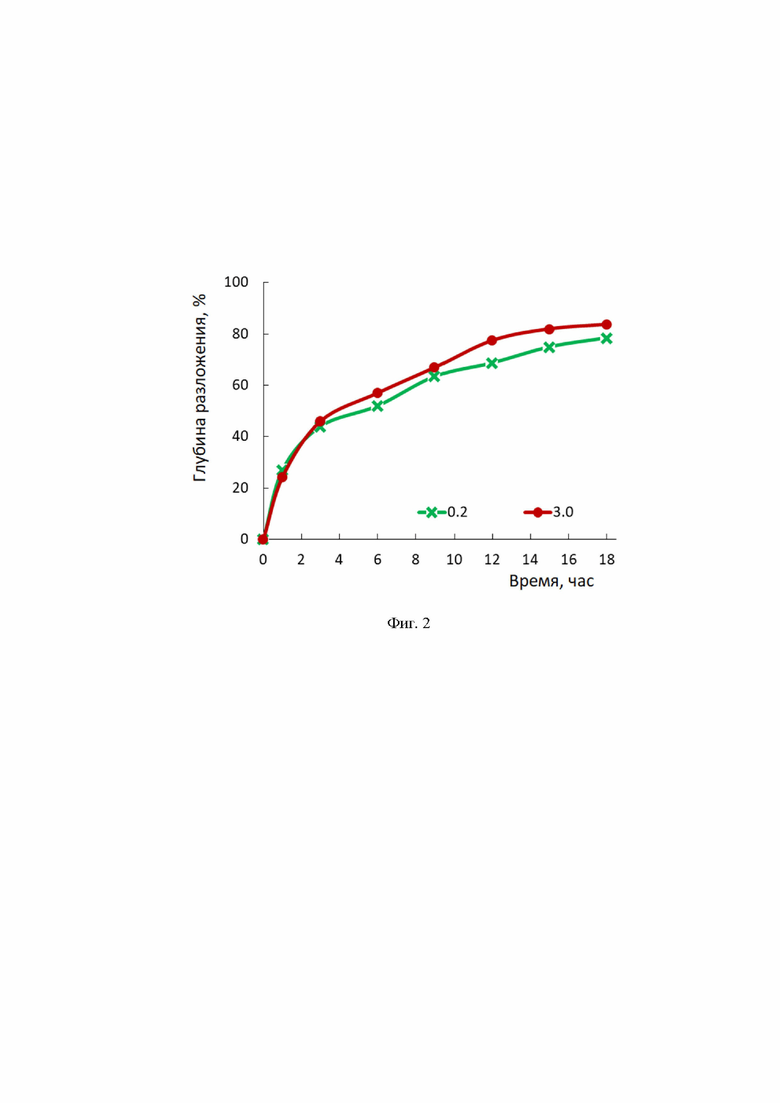
На фиг. 2 приведены зависимости глубины разложения п-дигидроксибензола в присутствии фотокатализаторов Co3(Si2O5)2(OH)2/SiO2 от продолжительности облучения.
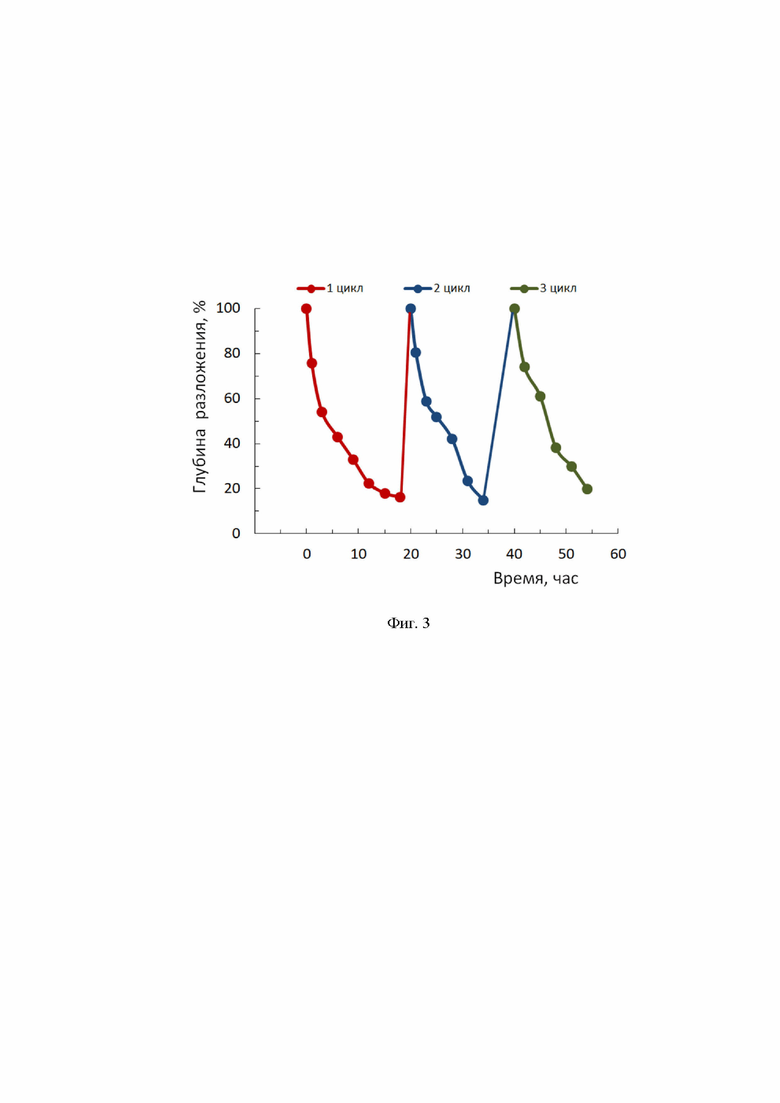
На фиг. 3 приведена зависимость глубины разложения п-дигидроксибензола в трех циклах повторения измерений за 18 часов облучения для образца по примеру 1 с содержанием 3,0 мас.% Co3(Si2O5)2(OH)2.
Получение предлагаемого фотокатализатора иллюстрируется следующими примерами.
Пример 1. Берут 4 г гидратированного диоксида кремния с содержанием 10% SiO2 и переносят в объем 40 мл дистиллированной воды, вводят 0,05 г хлорида аммония, что составляет 0,1 мас.% от общей массы, 1 мл аммиака, что составляет 2 мас.% от общей массы, и 0,0150 г формиата кобальта Со(HCOO)2⋅2H2O, что соответствует мольному соотношению (в пересчете на Со) Co:Si=0,01:1. Смесь помещают в автоклав и выдерживают при 90°С в течение 10 часов, после охлаждения центрифугируют и промывают осадок до нейтральной реакции и сушат при 100°С в течение 10 часов. Получают рентгеноаморфный продукт в виде светло-голубого порошка с содержанием 3,0 мас.% Co3(Si2O5)2(OH)2 и величиной удельной поверхности 150 м2/г (см. фиг. 1). Фотокаталитические свойства оценивали по скорости окисления п-дигидроксибензола (гидрохинона) в ультрафиолетовом свете (λ=253 нм). Глубина разложения п-дигидроксибензола составляет 84% за 18 часов облучения (см. фиг. 2).
Трехкратное повторение измерений для новых порций растворов п-дигидроксибензола свидетельствует о проявлении фотокаталитической активности при циклировании измерений с одним и тем же образцом после его отделения из предшествующего раствора (см. фиг. 3).
Пример 2. Берут 4 г гидратированного диоксида кремния с содержанием 10% SiO2 и переносят в объем 50 мл дистиллированной воды, вводят 0,1 г хлорида аммония, что составляет 0,2 мас.% от общей массы, 0,5 мл аммиака, что составляет 1 мас.% от общей массы, и 0,0010 г формиата кобальта Co(HCOO)2⋅2H2O, что соответствует мольному соотношению (в пересчете на Со) Co:Si=0,001:1 Смесь помещают в автоклав и выдерживают при 95°С в течение 12 часов, после охлаждения центрифугируют и промывают осадок до нейтральной реакции и сушат при 300°С. Получают рентгеноаморфный продукт в виде светло-голубого порошка с содержанием 0,2 мас.% Co3(Si2O5)2(OH)2 и величиной удельной поверхности 250 м2/г. Глубина разложения п-дигидроксибензола составляет 79% в течение 18 часов облучения (см. фиг. 2).
В таблице приведены данные по фотокаталитической активности (глубина разложения) в отношении п-дигидроксибензола фотокатализаторов с различным содержанием гидроксосиликата кобальта Co3(Si2O5)2(OH)2 в матрице на основе аморфного диоксида в сравнении с холостым опытом без использования фотокатализатора. Все составы фотокатализатора материалы проявляют сопоставимую высокую активность, свидетельствующую об эффективном разложении п-дигидроксибензола в течение 18 часов УФ-облучения.
Таким образом, авторами предлагается фотокатализатор, полученный простым технологически способом, обеспечивающий расширение номенклатуры фотокатализаторов для разложения углеводородов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ФОТОКАТАЛИЗАТОРА SnO | 2013 |
|
RU2538203C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФОТОКАТАЛИЗАТОРА НА ОСНОВЕ МЕХАНОАКТИВИРОВАННОГО ПОРОШКА ОКСИДА ЦИНКА | 2016 |
|
RU2627496C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФОТОКАТАЛИТИЧЕСКИХ КОМПОЗИТОВ СФЕРИЧЕСКОЙ СЛОИСТОЙ СТРУКТУРЫ ДЛЯ ОЧИСТКИ ВОДНЫХ ОБЪЕКТОВ И ФОТОКАТАЛИТИЧЕСКИЕ КОМПОЗИТЫ TiO2-Ag-SiO2, ПОЛУЧЕННЫЕ СПОСОБОМ | 2023 |
|
RU2829728C1 |
| Способ приготовления металл-нанесенного катализатора для процесса фотокаталитического окисления монооксида углерода | 2016 |
|
RU2637120C1 |
| Композитный материал для фотокатализатора и способ его получения | 2020 |
|
RU2748372C1 |
| Способ получения фотокатализатора на основе диоксида титана, допированного скандием | 2019 |
|
RU2709506C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФОТОКАТАЛИТИЧЕСКОГО СОРБИРУЮЩЕГО ТКАНЕВОГО МАТЕРИАЛА | 2014 |
|
RU2559506C1 |
| СПОСОБ ПОЛУЧЕНИЯ КРИСТАЛЛИЧЕСКОГО ДИОКСИДА ТИТАНА В СТРУКТУРНОЙ МОДИФИКАЦИИ АНАТАЗ | 2014 |
|
RU2575026C1 |
| Каталитическая композиция на основе оксидных соединений титана и алюминия и ее применение | 2021 |
|
RU2775472C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФОТОКАТАЛИЗАТОРА ИЗ ПОРОШКА ОКСИДА ЦИНКА МАССОВОГО ПРОИЗВОДСТВА | 2019 |
|
RU2733474C1 |

Изобретение относится к технологии получения и использования в производстве фотокатализаторов для разложения органических веществ и загрязнителей при очистке воды, воздуха и в других фотохимических процессах, в газовых и оптических сенсорах. Предлагаемый фотокатализатор содержит матрицу на основе аморфного диоксида кремния и равномерно распределенный в матрице активный компонент, в качестве которого фотокатализатор содержит гидроксосиликат кобальта состава Co3(Si2O5)2(OH)2. При этом соотношение компонентов в фотокатализаторе составляет, мас.%: гидроксосиликат кобальта - 0,2-3,0; аморфный диоксид кремния - 97,0-99,8. Также изобретение относится к способу получения предлагаемого фотокатализатора. Технический результат - разработка состава фотокатализатора для разложения органических соединений, обеспечивающего расширение номенклатуры используемых в настоящее время фотокатализаторов, при этом фотокатализатор может быть получен технологически простым и надежным способом. 2 н.п. ф-лы, 3 ил., 1 табл., 2 пр.
1. Фотокатализатор, содержащий матрицу на основе аморфного диоксида кремния и равномерно распределенного в матрице активного компонента, отличающийся тем, что в качестве активного компонента он содержит гидроксосиликат кобальта состава Co3(Si2O5)2(OH)2 при следующем соотношении компонентов, мас.%: гидроксосиликат кобальта – 0,2–3,0; аморфный диоксид кремния – 97,0–99,8.
2. Способ получения фотокатализатора, содержащего матрицу на основе аморфного диоксида кремния и равномерно распределенного в матрице гидроксосиликата кобальта по п. 1, включающий получение исходной смеси гидратированного кремнезема в растворе формиата кобальта Co(HCOO)2·2H2O при содержании (в пересчете на Со) в мольном отношении Co: SiO2 = (0,001–0,01) : 1, в присутствии хлорида аммония в количестве 0,1–0,2 мас.% от общей массы смеси и аммиака в количестве 1–2 мас.% от общей массы, гидротермальную обработку исходной смеси в автоклаве при температуре 90-95°С в течение 10-12 часов, c последующим отделением осадка центрифугированием, промывкой дистиллированной водой и сушкой при температуре 100-300°С в течение 3–4 часов.
| Способ получения смешанного фотокатализатора на основе оксида титана | 2021 |
|
RU2760442C1 |
| CN 113244920 B, 12.07.2022 | |||
| СПОСОБ ПОЛУЧЕНИЯ ТЕРМОСТАБИЛЬНОГО ФОТОКАТАЛИЗАТОРА НА ОСНОВЕ ДИОКСИДА ТИТАНА | 2014 |
|
RU2563239C1 |
| Zhong-Shuai Zhu et al., Preforming Abundant Surface Cobalt Hydroxyl Groups on Low Crystalline Flowerlike Co3(Si2O5)2(OH)2 for Enhancing Catalytic Degradation Performances with a Critical Nonradical Reaction | |||
| Applied Catalysis B: Environmental, 2020, 261:118238. | |||
Авторы
Даты
2022-11-23—Публикация
2022-08-22—Подача