Область техники
Настоящее изобретение имеет отношение к области адоптивной терапии. Настоящее изобретение обеспечивает иммунные клетки, дефектные по Suv39h1 c повышенной выживаемостью, потенциалом восстановления и фенотипом центральной памяти после адоптивного переноса.
Введение
Адоптивная T-клеточная терапия (ATCT) с использованием T-клеток, оснащенных T-клеточными рецепторами (TCR) и химерными антигенными рецепторами (CAR), демонстрирует весьма обнадеживающую активность в отношении нескольких злокачественных опухолей на начальных этапах клинических исследований, проводимых в ряде институтов (Kershaw MH, Westwood JA, Darcy PK. Nat Rev Cancer. 2013; 13:525–541).
Перспективность тематики связана с тем, что эффективное приживление и долгосрочная персистенция терапевтических T-клеток коррелирует с положительными терапевтическими эффектами. В некоторых доклинических исследованиях было показано, что наивные и дифференцировавшиеся в первых рядах T-клетки обладают повышенной способностью к длительной персистенции (Berger C et al., J Clin Invest. 2008; 118:294–305; Hinrichs CS et al., Proc Natl Acad Sci. 2009; 106:17469–17474; Tanel A et al., Expert Rev Vaccines. 2009; 8(3):299–312) и могут вызывать сильные противоопухолевые ответы (Gattinoni L et al., J Clin Investig. 2005; 115:1616–1626; Lugli E et al. J Clin Invest. 2013; 123:594–599). Кроме того, повышенная персистентность адоптивно перенесенных клеток, по-видимому, зависит от получения популяций Т-клеток центральной памяти (TCM) (Powell DJ et al., Blood. 2005; 105(1):241–50; Huang J, Khong HT et al. J Immunother. 2005; 28:258–267).
Обычно устойчивый перенос генов в клинических условиях осуществляется путем использования гамма ретровирусных векторов, для того, чтобы трансдуцировать поликлональные T-клетки CAR (смотри, например, Guest RD et al., Cancer Immunol Immunother. 2014;63:133–145) и TCR (смотри, в частности, Johnson LA et al., Blood. 2009;114(3):535–46) при этом у пациентов с приживленными CAR T-клетками, не наблюдалось неблагоприятных симптомов в отношении безопасности применения этих сконструированных клеток в течение более чем 10 лет (Scholler J et al., Sci Transl Med. 2012;4:132ra153).
Для эффективной трансдукции с использованием ретровирусных или лентивирусных векторов, первичные T-клетки должны быть активно пролиферирующими (Stacchini A et al., Leuk Res. 1999; 23:127–136), что в большинстве случаев достигается при помощи митогенной стимуляции покоящихся первичных T-клеток.
Однако, после активации T-клетки развиваются необратимым линейныс путем в эффекторный (TE) фенотип (Mahnke YD et al., Eur J Immunol. 2013; 43:2797–2809; Farber DL. Semin Immunol. 2009; 21:84-91). Митогенная активация для ретровирусной или лентивирусной трансдукции, следовательно, запускает дифференцировку T-клеток из наивных в сторону TE-фенотипа. В сочетании с протоколами культивирования ex-vivo с целью увеличения количества трансдуцированных T-клеток до количества, необходимого для клинического применения (около 109–1011), T-клетки «направляются» в сторону более дифференцированного фенотипа, который является недостаточно оптимальным для персистенции в целом.
Таким образом, в то время как адоптивная T-клеточная терапия, включая основанную на CAR T-клеточную терапию, в течение последних нескольких лет демонстрирует заметные терапевтические успехи, в частности при лечении некоторых гематологических раков, эффективность показана только в отношении незначительного числа типов рака крови и некоторых типов солидных опухолей. Предполагается, что низкая эффективность лечения может являться результатом ограниченной выживаемости T-клеток после адоптивного переноса.
Следовательно, в данной области техники, сохраняется потребность в модифицированных или сконструированных T-клетках, демонстрирующих усиленный фенотип центральной памяти и увеличенную выживаемость после адоптивного переноса. В частности, сохраняется необходимость в предоставлении иммунных клеток, в первую очередь T-клеток, пригодных для использования в адоптивной терапии, которая оказывает существенное содействие эффективной и широкомасштабной противоопухолевой терапии.
Раскрытие изобретения
В ходе данной работы изобретатели неожиданно обнаружили, что T-клетки дефективные по Suv39h1 несут улучшенный фенотип центральной памяти и обладают повышенной выживаемостью после адоптивного переноса. В частности, изобретатели показали, что T-клетки дефективные по Suv39h1 накапливаются и с повышенной эффективностью перепрограммируются в долгоживущие центральные T-клетки памяти, экспрессирующие и CD44 и CD62L. В связи с этим, настоящее изобретение имеет отношение к модифицированным или сконструированным иммунным клеткам, в первую очередь модифицированным T-клеткам, в которых Suv39h1 является инактивированным.
Указанные модифицированные или сконструированные иммунные клетки вызывают большой интерес в отношении их использования в адоптивной терапии. Таким образом, настоящее изобретение в частности имеет отношение к сконструированной или модифицированной иммунной клетке дефективной по Suv39h1, при этом предпочтительно иммунная клетка дополнительно содержит генетически сконструированный антигенный рецептор, который специфически связывается с антигеном-мишенью.
Как правило, сконструированная иммунная клетка по изобретению представляет собой T-клетку или NK-клетку, а именно CD4+ или CD8+ T-клетку. Предпочтительные клетки могут быть выбраны из TN клеток, TSCM, TCM или TEM клеток или их комбинации.
Также, в большинстве случаев сконструированная иммунная клетка выделяется из субъекта. Предпочтительно, указанный субъект страдает от рака или имеет риск развития рака.
Антиген-мишень, с которым специфически связывается генетически сконструированный антигенный рецептор, предпочтительно экспрессируется на раковых клетках и/или является универсальным опухолевым антигеном.
Генетически сконструированный антигенный рецептор может быть химерным антигенным рецептором (CAR), содержащим внеклеточный антигенраспознающий домен, который специфически связывается с антигеном-мишенью. Генетически сконструированный антигенный рецептор также может быть T-клеточным рецептором (TCR).
Предпочтительно, активность и/или экспрессия Suv39h1 в указанной сконструированной иммунной клетке селективно ингибируется или блокируется. В одном варианте осуществления указанная сконструированная иммунная клетка экспрессирует нуклеиновую кислоту Suv39h1, кодирующую нефункциональный белок Suv39h1.
Настоящее изобретение также имеет отношение к способу продуцирования генетически сконструированной иммунной клетки, включающему стадию, заключающуюся в ингибировании экспресии и/или активности Suv39h1 в иммунной клетке; и необязательно стадию, заключающуюся во введении в иммунную клетку генетически сконструированного антигенного рецептора, который специфически связывается с антигеном-мишенью.
Предпочтительно, ингибирование активности и/или экспрессии Suv39h1 включает, по меньшей мере, контактирование или приведение в контакт клетки с веществом, ингибирующим экспрессию и/или активность Suv39h1, и/или разрушение гена Suv39h1. Указанное вещество или агент может быть выбран из низкомолекулярных ингибиторов; производных антител, аптамеров, молекул нуклеиновых кислот, которые блокируют транскрипцию или трансляцию, или агентов, редактирующих геном.
Настоящее изобретение также имеет отношение к сконструированной иммунной клетке, как описано в этом документе, или композиции, содержащей указанную сконструированную иммунную клетку, для использования в адоптивной клеточной терапии, в особенности адоптивной терапии рака.
Подробное описание
Определения
Термин "антитело" в данном описании используется в самом широком смысле и включает поликлональные и моноклональные антитела, включая интактные антитела и функциональные (антиген-связывающие) фрагменты антител, включая антигенсвязывающие фрагменты (Fab), F(ab')2 фрагменты, Fab' фрагменты, Fv фрагменты, рекомбинантные IgG (rlgG) фрагменты, способные специфически связываться с антигеном вариабельные области тяжелой цепи (VH), , фрагменты одноцепочечных антител, включая одноцепочечные вариабельные фрагменты (scFv) и фрагменты типа однодоменных антител (например, sdAb, sdFv, нанотело). Термин включает генетически сконструированные и/или иным образом модифицированные формы иммуноглобулинов, такие как интратела, пептитела, химерные антитела, полностью человеческие антитела, гуманизированные антитела и гетероконъюгатные антитела, мультиспецифические, например, биспецифические, антитела, диатела, триатела и тетратела, тандемные ди-scFv, тандемные три-scFv. Если не указано иное, термин "антитело" следует понимать как включающий функциональные фрагменты антител. Термин также рассматривает интактные или полноразмерные антитела, включая антитела из любого класса или подкласса, включая IgG и его подклассы IgM, IgE, IgA и IgD.
"Фрагмент антитела" относится к отличной от интактного антитела молекуле, содержащей часть интактного антитела, которая связывается с тем-же антигеном, с которым связывается интактное антитело. Примеры фрагментов антител включают, но не ограничиваются этим, Fv, Fab, Fab', Fab'-SH, F(ab')2; диатела; линейные антитела; вариабельные области (VH) тяжелой цепи, молекулы одноцепочечных антител, такие как scFvs и одиночные VH однодоменных антител; и мультиспецифические антитела, образованные из фрагментов антител. В отдельных вариантах осуществления антитела являются фрагментами одноцепочечного антитела, содержащими вариабельную область тяжелой цепи и/или вариабельную область легкой цепи, такими как scFvs.
“Однодоменные антитела” представляют собой фрагменты антител, содержащие весь или часть вариабельного домена тяжелой цепи или весь или часть вариабельного домена легкой цепи антитела. В некоторых вариантах осуществления однодоменное антитело является человеческим однодоменным антителом.
При использовании в описании "репрессия" экспрессии гена имеет отношение к подавлению или уменьшению экспрессии одного или более продуктов генов, кодируемых данным геном в клетке, по сравнению с уровнем экспрессии продукта гена при отсутствии репрессии. Характерные продукты гена включают мРНК и белковые продукты, кодированные данным геном. Репрессия в некоторых случаях является временной или обратимой, а в других случаях является постоянной. Репрессия в некоторых случаях является репрессией функционального или полноразмерного белка или мРНК, несмотря на тот факт, что может продуцироваться усеченный или нефункциональный продукт. В некоторых вариантах осуществления в данном документе активность или функция гена, в противоположность экспрессии, репрессируется. Репрессия гена обычно вызывается искусственными способами, т.е., путем добавления или введения соединения, молекулы, комплекса или композиции, и/или путем разрушения гена или ассоциированной с данным геном нуклеиновой кислоты, например, на уровне ДНК. Типичные методы репрессии гена включают сайленсинг, нокдаун, нокаут и/или методы разрушения генов, такие как редактирование генома. Примеры включают антисмысловые технологии, такие как основанные на РНКi, siРНК, shРНК и/или рибозимах, что в большинстве случаев приводит к временному уменьшению экспрессии, а также методы генной инженерии, которые приводят к инактивации или разрушению гена-мишени, например, путем введения разрывов и/или гомологичной рекомбинации.
При использовании в описании "разрушение" гена имеет отношение к изменению в последовательности гена на уровне ДНК. Примеры включают инсерции, мутации и делеции. Разрушение в большинстве случаев приводит к репрессии и/или полному отсутствию экспрессии нормального продукта или продукта "дикого типа", кодируемого этим геном. Типичными примерами такого разрушения генов являются инсерции, сдвиг рамки считывания или миссенс-мутации, делеции, нокин и нокаут гена или части гена, включая делеции целого гена. Такие разрушения могут происходить в кодирующем участке, например, в одном или более экзонах, что приводит к неспособности продуцировать полноразмерный продукт, функциональный продукт или любой продукт, например, при помощи инсерции стоп-кодона. Такие разрушения также могут осуществляться посредством разрушений в промоторе или энхансере или другом участке, затрагивающем активацию транскрипции, в целях предотвращения транскрипции гена. Разрушение гена включает направленное воздействие на ген, включая инактивацию гена-мишени путем гомологичной рекомбинации.
Клетки изобретения
Клетки согласно изобретению в большинстве случаев являются эукариотическими клетками, такими как клетки млекопитающих (также называемые в настоящем изобретении животными клетками), например, человеческие клетки.
Конкретнее, клетки изобретения происходят из крови, костного мозга, лимфы или лимфоидных органов (в частности, тимуса) и являются клетками иммунной системы (т.е., иммунными клетками), такими как клетки врожденного или приобретенного иммунитета, например, миелоидные или лимфоидные клетки, включая лимфоциты, обычно T-клетки и/или NK-клетки.
В частности, клетки согласно изобретению предпочтительно являются лимфоцитами, включая T-клетки, B-клетки и NK-клетки.
Клетки согласно изобретению также могут быть иммунными клетками-предшественниками, такими как лимфоидные клетки-предшественники и более предпочтительно клетки-предшественники T-клеток.
Предшественники T-клеток обычно экспрессируют ряд консенсусных маркеров, включая CD44, CD117, CD135 и Sca-1, смотри также Petrie HT, Kincade PW. Many roads, one destination for T cell progenitors. The Journal of Experimental Medicine. 2005;202(1):11-13.
Клетки в большинстве случаев являются первичными клетками, как например клетки, изолированные непосредственно из субъекта и/или изолированные из субъекта и замороженные.
По отношению к субъекту, подлежащему лечению, клетки изобретения могут быть аллогенными и/или аутологичными.
В некоторых вариантах осуществления клетки включают одну или более субпопуляций T-клеток или клеток других типов, такие как полные T-клеточные популяции, CD4+ клетки, CD8+ клетки и их субпопуляции, например, популяции, определяемые функцией, состоянием активации, зрелостью, потенциалом для дифференцировки, распространения и рециркуляции, локализацией и/или возможностями к персистенции, специфичностью к антигену, типом антигенного рецептора, присутствием в конкретном органе или компартменте, профилем секреции маркера или цитокина и/или степенью дифференцировки.
К числу подтипов и субпопуляций Т-клеток и/или CD4+ и/или CD8+ T-клеток относятся наивные T (TN) клетки, эффекторные T-клетки (TEFF), T-клетки памяти и их подтипы, такие как стволовые T-клетки памяти (TSCM), Т-клетки центральной памяти (TCM), T-клетки эффекторной памяти (TEM) или терминально-дифференцированные T-клетки эффекторной памяти, инфильтрующие опухоль лимфоциты (TIL), незрелые T-клетки, зрелые T-клетки, хелперные T-клетки, цитотоксические Т-клетки, мукозальные инвариантные T-клетки (MAIT), природного происхождения и адаптивно регулируемые T-клетки (Treg), хелперные Т-клетки, такие как TH1 клетки, TH2 клетки, TH3 клетки, TH17 клетки, TH9 клетки, TH22 клетки, фолликулярные хелперные T-клетки, альфа/бета T-клетки и дельта/гамма T-клетки. Предпочтительно, клетки согласно изобретению являются TEFF клетками со свойствами стволовых/клеток памяти и повышенной способностью к воспроизведению, возникшей вследствие ингибирования Suv39h1, а также TN клетками, TSCM, TCM, TEM клетками и их комбинациями.
В некоторых вариантах осуществления одна или более T-клеточных популяций обогащается или обедняется клетками, которые являются положительными по или экспрессируют высокие уровни одного или более определенных маркеров, таких как поверхностные маркеры, или которые являются отрицательными по или экспрессируют относительно низкие уровни одного или более маркеров. В некоторых случаях такими маркерами являются маркеры, отсутствующие или экспрессирующиеся на относительно низких уровнях на некоторых популяциях T-клеток (таких как, клетки, не являющиеся клетками памяти), но которые присутствуют или экспрессируются на относительно высоких уровнях на некоторых других популяциях T-клеток (таких как клетки памяти). В одном варианте осуществления клетки (такие как CD8+ клетки или T-клетки, например, CD3+ клетки) обогащаются (т.е., положительно отбираются на основе) клетками, которые являются положительными или экспрессирующими высокие уровни поверхностных CD117, CD135, CD45RO, CCR7, CD28, CD27, CD44, CD127 и/или CD62L, и/или истощаются в отношении (например, отрицательно отбираются на основе) клеток, которые являются положительными или экспрессируют высокие уровни поверхностного CD45RA. В некоторых вариантах осуществления клетки обогащаются или истощаются в отношении клеток, положительных или экспрессирующих высокие уровни поверхностных CD122, CD95, CD25, CD27 и/или IL7-Ra (CD127). В некоторых образцах CD8+ T-клетки обогащаются клетками, положительными по CD45RO (или отрицательными по CD45RA) и по CD62L.
Например, согласно изобретению клетки могут включать популяцию CD4+ T-клеток и/или субпопуляцию CD8+ T-клеток, например, субпопуляцию, обогащенную клетками центральной памяти (TCM). Альтернативно, клетки могут быть другими типами лимфоцитов, включая клетки-натуральные киллеры (NK), MAIT клетки, природные лимфоидные клетки (ILCs) и B клетки.
Клетки и композиции (смеси), содержащие клетки для инженерии, согласно изобретению изолируются из образца, а именно, из биологического образца, например, полученного от или происходящего от субъекта. В большинстве случаев субъект нуждается в клеточной терапии (адоптивной клеточной терапии) и/или является субъектом, получающим клеточную терапию. Субъект предпочтительно является млекопитающим, а именно человеком. В одном варианте осуществления изобретения у субъекта имеется злокачественное заболевание.
Образцы включают ткань, жидкость и другие образцы, взятые непосредственно от субъекта, а также образцы, возникающие в результате одного или более этапов обработки, таких как выделение, центрифугирование, генетическая инженерия (например, трансдукция с использованием вирусного вектора), промывка и/или инкубация. Биологический образец может быть образцом, полученным непосредственно из биологического источника или образцом, который подвергается обработке. Биологический образец включает, но не ограничивается этим, жидкости организма, такие как кровь, плазма, сыворотка, спинно-мозговая жидкость, синовиальная жидкость, моча и пот, образцы тканей и органов, включая обработанные образцы, полученные из них. Предпочтительно, образец, из которого получены или изолированы клетки, является кровью или образцом, полученным из крови, или является или происходит из продукта афереза или лейкафереза. Характерные примеры включают цельную кровь, мононуклеарные клетки периферической крови (PBMC), лейкоциты, костный мозг, тимус, образцы биопсии тканей, опухоль, лейкемию, лимфому, лимфатический узел, ассоциированную с кишечником лимфоидную ткань, лимфоидную ткань слизистых оболочек, поджелудочную железу, другие лимфоидные ткани и/или клетки, происходящие из них. Образцы включают в контексте клеточной терапии (обычно адоптивной клеточной терапии) образцы от аутологичных и аллогенных источников.
В некоторых вариантах осуществления клетки происходят из клеточных линий, например, линий T-клеток. Клетки также могут быть получены из ксеногенного источника, такого как мышь, крыса, примат, не являющийся человеком, или свинья. Предпочтительно, клетки являются человеческими.
Клетки, дефектные по Suv39h1
При использовании в описании термин "Suv39h1" или "H3K9-гистон метилтрансфераза Suv39h1" имеет свое общее значение в данной области техники и относится к гистон метилтрансферазе "гомологу 1 супрессора мозаичности 3-9 (Drosophila)", который специфически триметилирует остаток Lys-9 гистона H3 с использованием монометилированного H3-Lys-9 в качестве субстрата (смотри также Aagaard L, Laible G, Selenko P, Schmid M, Dorn R, Schotta G, Kuhfittig S, Wolf A, Lebersorger A, Singh PB, Reuter G, Jenuwein T (Jun 1999). "Functional mammalian homologues of the Drosophila PEV-modifier Su(var)3-9 encode centromere-associated proteins which complex with the heterochromatin component M3 1". EMBO J 1 8 (7): 1923-38.). Указанная гистон-метилтрансфераза также известна как MG44, KMT1A, SUV39H, SUV39H1, гистон-лизин N-метилтрансфераза SUV39H1, H3-K9-HMTаза 1, OTTHUMP00000024298, гомолог 1 Su(var)3-9, лизин N-метилтрансфераза 1A, гистон H3-K9 метилтрансфераза 1, гомолог 3-9 эффекта положения мозаичного типа, гистон-лизин N-метилтрансфераза или H3 лизин-9 специфичный 1. Человеческая Suv39h1 метилтрансфераза обозначается O43463 в UNIPROT и кодируется геном Suv39h1, локализованным на хромосоме x (ген ID: 6839 в NCBI). Термин Suv39h1 согласно изобретению также рассматривает все ортологи SUV39H1, такие как SU(VAR)3-9.
При использовании в описании выражение “дефектная по Suv39h1” согласно настоящему изобретению имеет отношение к ингибированию или блокированию активности Suv39h1 (т.е., метилированию Lys-9 гистона H3 при помощи H3K9-гистон-метилтрансферазы) в клетке согласно изобретению.
“Ингибирование активности Suv39h1” согласно изобретению имеет отношение к уменьшению активности Suv39h1, по меньшей мере, на 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95% или 99% или более по сравнению с активностью или уровнем неингибированного белка Suv39h1. Преимущественно ингибирование активности Suv39h1 ведет к отсутствию в клетке обнаружимой существенной активности Suv39h1.
Ингибирование активности Suv39h1 также может достигаться путем подавления экспрессии гена Suv39h1 или путем разрушения гена Suv39h1. Согласно изобретению указанная репрессия уменьшает экспрессию Suv39h1 в клетке, в частности, в иммунной клетке изобретения, по меньшей мере, на 50, 60, 70, 80, 90 или 95% относительно такой же клетки, продуцированной при помощи данного способа при отсутствии репрессии. Разрушение гена также может приводить к уменьшенной экспрессии белка Suv39h1 или к экспрессии нефункционального белка Suv39h1.
Под “нефункциональным” Suv39h1 белком подразумевается белок с пониженной активностью или отсутствием обнаружимой активности, как описано выше.
Таким образом, ингибиторы активности Suv39h1 в клетке согласно изобретению могут быть выбраны из числа любого соединения или природного вещества, не обладающего способностью к ингибированию метилирования Lys-9 гистона H3 при помощи H3K9-гистон метилтрансферазы, или ингибирующего экспрессию гена H3K9-гистон метилтрансферазы SUV39H1.
Ингибирование Suv39h1 в иммунной клетке согласно настоящему изобретению может быть стабильным и необратимым или временным или обратимым. Предпочтительно, однако, что ингибирование Suv39h1 является стабильным и необратимым. Ингибирование Suv39h1 в клетке может достигаться до или после инъекции клетки намеченному пациенту, как описано ниже.
Генетически сконструированные клетки согласно изобретению
В некоторых вариантах осуществления клетки содержат одну или более нуклеиновых кислот, введенных при помощи генной инженерии, которые кодируют один или более антигенных рецепторов.
Как правило, нуклеиновые кислоты являются гетерологичными, (т.е., например, такими, которые обычно не обнаруживаются в клетке, будучи сконструированными, и/или в организме, из которого такая клетка происходит). В некоторых вариантах осуществления нуклеиновые кислоты не являются кислотами природного происхождения, включая химерные комбинации нуклеиновых кислот, кодирующих различные домены из нескольких разных типов клеток.
К числу антигенных рецепторов согласно изобретению относятся генетически сконструированные T-клеточные рецепторы (TCR) и их компоненты, а также функциональные не-TCR антигенные рецепторы, такие как химерные антигенные рецепторы (CAR).
Химерные антигенные рецепторы (CAR)
В некоторых вариантах осуществления сконструированные антигенные рецепторы включают химерные антигенные рецепторы (CAR), включая активирующие или стимулирующие CAR, костимулирующие CAR (смотри WO2014/055668) и/или ингибирующие CAR (iCAR, смотри Fedorov et al., Sci. Transl. Medicine, 5(215) (December, 2013)).
Химерные антигенные рецепторы (CAR) (также известные как химерные иммунорецепторы, химерные T-клеточные рецепторы, искусственные T-клеточные рецепторы) являются сконструированными рецепторами, которые «пересаживают» произвольно выбранную специфичность на иммунную эффекторную клетку (T-клетку). Как правило, эти рецепторы используются для «пересаживания» специфичности моноклонального антитела на T-клетку вместе с перенесением их кодирующей последовательности, осуществляемым с использованием ретровирусных векторов.
CAR в большинстве случаев включают внеклеточный антиген-связывающий (или лиганд-связывающий) домен, соединенный с одним или более внутриклеточными сигнальными компонентами, в некоторых аспектах через посредство линкеров и/или трансмембранного домена(ов). Такие молекулы обычно имитируют или приблизительно соответствуют сигналу, использующему природный антигенный рецептор, сигналу, использующему такой рецептор в комбинации с костимулирующим рецептором, и/или сигналу, использующему костимулирующий рецептор в отдельности.
В некоторых вариантах осуществления CAR конструируется со специфичностью к конкретному антигену (или маркеру или лиганду), такому как антиген, экспрессируемый на определенном типе клеток, на который нацеливается адоптивная терапия, например, онкомаркер. Таким образом, CAR в большинстве случаев содержит на своем внеклеточном участке одну или более антигенсвязывающих молекул, таких как один или более антигенсвязывающих фрагментов, доменов или участков, или один или более вариабельных доменов антитела и/или молекул антитела.
Молекулы, используемые для связывания с антигеном, относятся к трем основным категориям, или к фрагментам одноцепочного антитела (scFvs), происходящим от антител, или к Fab’s, выбранным из библиотек, или к природным лигандам, которые задействуют свой родственный рецептор (для CAR первого поколения). Удачные примеры в каждой из этих категорий приводятся в Sadelain M, Brentjens R, Riviere I. The basic principles of chimeric antigen receptor (CAR) design. Cancer discovery. 2013; 3(4):388-398 (смотри в частности таблицу 1) и включаются в настоящую заявку. Обычно используются scFv’s, происходящие из мышиных иммуноглобулинов, поскольку их можно легко получить из хорошо охарактеризованных моноклональных антител.
Обычно, CAR включает антигенсвязывающий участок или участки молекулы антитела, такие как фрагмент одноцепочечного антитела (scFv), происходящий из вариабельного участка тяжелой цепи (VH) и вариабельного участка легкой цепи (VL) моноклонального антитела (mAb).
В некоторых вариантах осуществления CAR содержит домен тяжелой цепи антитела, который специфически связывается с антигеном, например, онкомаркером или поверхностным антигеном клетки или болезни, подлежащей лечению, такой как опухолевая клетка или раковая клетка, например, таким как любой из антигенов-мишеней, описанных в этом документе или известных в данной области техники.
В некоторых вариантах осуществления CAR содержит антитело или антигенсвязывающий фрагмент (например, scFv), специфически распознающий антиген, такой как интактный антиген, экспрессированный на поверхности клетки.
В некоторых вариантах осуществления CAR содержит TCR-подобное антитело, такое как антитело или антигенсвязывающий фрагмент (например, scFv), который специфически распознает внутриклеточный антиген, например, опухоль-ассоциированный антиген, презентируемый на клеточной поверхности в виде MHC-пептидного комплекса. В некоторых вариантах осуществления антитело или его антигенсвязывающий участок, распознающий MHC-пептидный комплекс, может экспрессироваться на клетках как часть рекомбинантного рецептора, такого как антигенный рецептор. К числу антигенных рецепторов относятся функциональные не-TCR антигенные рецепторы, такие как химерные антигенные рецепторы (CAR). В большинстве случаев CAR, содержащий антитело или антигенсвязывающий фрагмент, демонстрирующий TCR-подобную специфичность, направленный против пептид-MHC-комплексов, также может называться TCR-подобным CAR.
В некоторых аспектах компонент антигенспецифического связывания или распознавания соединяется с одним или более трансмембранными и внутриклеточными сигнальными доменами. В некоторых вариантах осуществления CAR включает трансмембранный домен, соединенный с внеклеточным доменом CAR. В одном варианте осуществления используется трансмембранный домен, который в природных условиях связан с одним из доменов в CAR. В некоторых случаях трансмембранный домен выбирают или модифицируют путем замены аминокислоты, для того, чтобы избежать связывания таких доменов с трансмембранными доменами тех же самых или других белков на поверхностях мембран, чтобы свести к минимуму взаимодействия с другими членами рецепторного комплекса.
Трансмембранный домен в некоторых вариантах осуществления происходит или из естественного или из искусственного источника. В том случае, когда источник является природным, домен может происходить от какого-либо мембраносвязанного или трансмембранного белка. Трансмембранные участки включают участки, происходящие из (т.е. содержат, по меньшей мере, трансмембранный участок(и)) альфа, бета или дзета цепи T-клеточного рецептора, CD28, CD3 эпсилон, CD45, CD4, CD5, CDS, CD9, CD 16, CD22, CD33, CD37, CD64, CD80, CD86, CD 134, CD137, CD 154). Трансмембранный домен также может быть синтетическим.
В некоторых вариантах осуществления присутствует короткий олиго- или полипептидный линкер, например, линкер в интервале от 2 до 10 аминокислот в длину, образующий связь между трансмембранным доменом и цитоплазматическим сигнальным доменом CAR.
В большинстве случаев CAR включает, по меньшей мере, один внутриклеточный сигнальный компонент или компоненты. Первое поколение CAR обычно имело внутриклеточный домен из CD3 ζ-цепи, который является первичным передатчиком сигналов от эндогенных TCR. Второе поколение CAR в большинстве случаев дополнительно содержит внутриклеточные сигнальные домены из разных костимулирующих белковых рецепторов (например, CD28, 41BB, ICOS) в цитоплазматическом концевом сегменте CAR, чтобы обеспечить дополнительные сигналы к T-клетке. Доклинические испытания показали, что второе поколение улучшает противоопухолевую активность T-клеток. В последнее время третье поколение CAR объединяет несколько сигнальных доменов, таких как CD3z-CD28-41BB или CD3z-CD28-OX40, для увеличения эффективности.
Например, CAR может включать внутриклеточный компонент TCR комплекса, такой как TCR CD3+ цепь, который опосредует T-клеточную активацию и цитотоксичность, например, CD3 дзета цепь. Таким образом, в некоторых аспектах антигенсвязывающая молекула связывается с одним или более модулями сигнальной системы клетки. В некоторых вариантах осуществления клеточные сигнальные модули включают CD3 трансмембранный домен, CD3 внутриклеточные сигнальные домены и/или другие CD трансмембранные домены. Кроме того, CAR может дополнительно включать часть одной или более дополнительных молекул, таких как Fc рецептор γ, CD8, CD4, CD25 или CD16.
В некоторых вариантах осуществления после лигирования CAR, цитоплазматический домен или внутриклеточный сигнальный домен CAR активирует, по меньшей мере, одну из нормальных эффекторных функций или ответов соответствующей не созданной инженерным путем иммунной клетки (обычно T-клетки). Например, CAR может индуцировать функцию T-клетки, такую как цитолитическая активность или T-хелперная активность, секреция цитокинов или других факторов.
В некоторых вариантах осуществления внутриклеточный сигнальный домен(ы) включает цитоплазматические последовательности T-клеточного рецептора (TCR), и в некоторых аспектах также те из корецепторов, которые в природной среде функционируют совместно с таким рецептором, чтобы инициировать сигнальную трансдукцию после взаимодействия с антигенным рецептором, и/или любое производное или вариант таких молекул, и/или любую искусственную последовательность, которая обладает аналогичной функциональной способностью.
T-клеточная активация в некоторых аспектах описывается как активация, опосредуемая двумя классами цитоплазматических сигнальных последовательностей: теми, которые инициируют антиген-зависимую первичную активацию за счет использования TCR (первичные цитоплазматические сигнальные последовательности), и теми, которые действуют антиген-независимым образом, чтобы обеспечить вторичный или костимулирующий сигнал (вторичные цитоплазматические сигнальные последовательности). В некоторых аспектах CAR включает один или оба из таких сигнальных компонентов.
В некоторых аспектах CAR включает первичную цитоплазматическую сигнальную последовательность, которая регулирует первичную активацию TCR комплекса или стимулирующим или ингибирующим образом. Первичные цитоплазматические сигнальные последовательности, действующие стимулирующим образом, могут содержать сигнальные мотивы, которые известны как иммунорецепторные тирозиновые активирующие мотивы или ITAM. Примеры ITAM, содержащих первичные цитоплазматические сигнальные последовательности, включают полученные из TCR дзета, FcR гамма, FcR бета, CD3 гамма, CD3 дельта, CD3 эпсилон, CDS, CD22, CD79a, CD79b и CD66d. В некоторых вариантах осуществления цитоплазматическая сигнальная молекула(ы) в CAR содержит(ат) цитоплазматический сигнальный домен, его участок или последовательность, происходящую из CD3 дзета.
CAR также может включать сигнальный домен и/или трансмембранный участок костимулирующего рецептора, такой как CD28, 4-1BB, OX40, DAP10 и ICOS. В некоторых аспектах один и тот же CAR включает и активирующие и костимулирующие компоненты; альтернативно, активирующий домен предоставляется одним CAR, в то время как костимулирующий компонент предоставляется другим CAR, распознающим другой антиген.
CAR или другой антигенный рецептор также может быть ингибирующим CAR (например, iCAR) и включать внутриклеточные компоненты, которые ослабляют или подавляют ответ, например, иммунный ответ. Примерами таких внутриклеточных сигнальных компонентов являются те, которые обнаружены на молекулах иммунных контрольных точек, включая PD-1, CTLA4, LAG3, BTLA, OX2R, TIM-3, TIGIT, LAIR-1, PGE2 рецепторы, EP2/4 аденозиновые рецепторы, включая A2AR. В некоторых аспектах сконструированная клетка содержит ингибирующий CAR, включающий сигнальный домен такой ингибирующей молекулы или происходящий из такой ингибирующей молекулы, такой, что он служит для ослабления ответа. Например, такие CAR используются для того, чтобы уменьшить вероятность нецелевых эффектов, когда антиген распознаваемый активирующим рецептором, например, CAR, также экспрессируется, или может также экспрессироваться, на поверхности нормальных клеток.
TCR
В некоторых вариантах осуществления генетически сконструированные антигенные рецепторы включают рекомбинантные T-клеточные рецепторы (TCR) и/или TCR, клонированные из Т-клеток природного происхождения.
"T-клеточный рецептор" или "TCR" имеет отношение к молекуле, содержащей вариабельные a и β цепи (также известные как TCRa и TCRβ, соответственно) или вариабельные γ и δ цепи (также известные как TCRγ и TCRδ, соответственно), и которая является способной к специфическому связыванию с антигенным пептидом, связанным с MHC рецептором. В некоторых вариантах осуществления TCR находится в αβ форме. Как правило, TCR, существующие в αβ и γδ формах, обычно являются структурно схожими, однако экспрессирующие их T-клетки могут иметь различные анатомические местоположения или функции. TCR может быть обнаружен на поверхности клетки или в растворимой форме. Как правило, TCR обнаруживается на поверхности T-клеток (или T-лимфоцитов), где он обычно отвечает за распознавание антигенов, связанных с молекулами главного комплекса гистосовместимости (MHC). В некоторых вариантах осуществления TCR также может содержать константный домен, трансмембранный домен и/или короткий цитоплазматический концевой сегмент (смотри, например, Janeway et ah, Immunobiology: The Immune System in Health and Disease, 3 rd Ed., Current Biology Publications, p. 4:33, 1997). Например, в некоторых аспектах каждая цепь TCR может содержать один N-концевой вариабельный домен иммуноглобулина, один константный домен иммуноглобулина, трансмембранный участок и короткий цитоплазматический концевой сегмент на C-концевом участке. В некоторых вариантах осуществления TCR ассоциируется с инвариантными белками CD3 комплекса, вовлеченными в опосредование сигнальной трансдукции. Если не указано иное, термин "TCR" следует рассматривать как включающий функциональные фрагменты TCR. Термин также включает интактные или полноразмерные TCR, включая TCR в αβ форме или γδ форме.
Таким образом, для целей данного документа ссылка на TCR включает любой TCR или функциональный фрагмент, такой как антигенсвязывающий участок TCR, который связывается со специфическим антигенным пептидом, связанным на MHC молекуле, т.е. MHC-пептидный комплекс. Термины "антигенсвязывающий участок" или антигенсвязывающий фрагмент" TCR, которые могут использоваться взаимозаменяемым образом, имеют отношение к молекуле, которая содержит участок структурных доменов TCR, но которая связывается с антигеном (например, MHC-пептидный комплекс), с которым связывается целый TCR. В некоторых случаях антигенсвязывающий участок содержит вариабельные домены TCR, такие как вариабельная цепь и вариабельная β цепь TCR, достаточные для формирования сайта связывания для связывания со специфическим MHC-пептидным комплексом, как правило, такие, как для случаев, когда каждая цепь содержит три определяющие комплементарность области.
В некоторых вариантах осуществления вариабельные домены TCR цепей соединяются с образованием петель или определяющих комплементарность областей (CDR) аналогично иммуноглобулинам, которые обеспечивают распознавание антигена и определяют специфичность пептида путем формирования сайта связывания TCR молекулы и определяют специфичность пептида. Обычно, подобно иммуноглобулинам, CDR разделяются каркасными областями (FR) (смотри, например, Jores et al., Pwc. Nat'lAcad. Sci. U.S.A. 87:9138, 1990; Chothia et al., EMBO J. 7:3745, 1988; смотри также Lefranc et al., Dev. Comp. Immunol. 27:55, 2003). В некоторых вариантах осуществления CDR3 является главным CDR, ответственным за распознавание процессированного антигена, хотя показано, что CDR1 альфа цепи также взаимодействует с N-концевой областью антигенного пептида, в то время как CDR1 бета цепи взаимодействует с C-концевой областью пептида. Полагают, что CDR2 распознает MHC молекулу. В некоторых вариантах осуществления вариабельная область β-цепи может содержать дополнительный участок гипервариабельности (HV4).
В некоторых вариантах осуществления TCR цепи содержат константный домен. Например, подобно иммуноглобулинам, внеклеточный участок TCR цепей (например, a-цепи, β-цепи) может содержать два домена иммуноглобулина, вариабельный домен (например, Va или Vp; как правило, аминокислоты 1 - 116 согласно Kabat-нумерации Kabat et al., "Sequences of Proteins of Immunological Interest, US Dept. Health and Human Services, Public Health Service National Institutes of Health, 1991, 5th ed.) на N-конце, и один константный домен (например, константный домен a-цепи или Ca, как правило, аминокислоты 117 - 259 согласно Kabat, константный домен β-цепи или Cp, как правило, аминокислоты 117 - 295 согласно Kabat) расположенные рядом с клеточной мембраной. Например, в некоторых случаях внеклеточный участок TCR, сформированный двумя цепями, содержит два мембрано-проксимальных константных домена и два мембрано-дистальных вариабельных домена, содержащих CDR. Константный домен TCR домена содержит короткие связывающие последовательности, в которых остаток цистеина образует дисульфидную связь, образуя соединение между двумя цепями. В некоторых вариантах осуществления TCR может иметь дополнительный остаток цистеина в каждой из a и β цепей, так что TCR содержит две дисульфидные связи в константных доменах.
В некоторых вариантах осуществления TCR цепи могут содержать трансмембранный домен. В некоторых вариантах осуществления трансмембранный домен заряжен положительно. В некоторых случаях TCR цепи содержат цитоплазматический концевой сегмент. В некоторых случаях структура позволяет TCR соединяться с другими молекулами, подобными CD3. Например, TCR содержащие константные домены с трансмембранным участком могут фиксировать белок в клеточной мембране и соединяться с инвариантными субъединицами CD3 сигнального аппарата или комплекса.
Как правило, CD3 представляет собой мультибелковый комплекс, который может обладать тремя различными цепями (γ, δ и ε) у млекопитающих и ζ-цепью. Например, у млекопитающих данный комплекс может содержать CD3y цепь, CD35 цепь, две CD3s цепи и гомодимер из CD3ζ цепей. CD3y, CD35 и CD3s цепи являются близкородственными белками клеточной поверхности семейства иммуноглобулинов, содержащих единственный домен иммуноглобулина. Трансмембранные участки CD3y, CD35 и CD3s цепей заряжены отрицательно, что является свойством, позволяющим этим цепям соединяться с положительно заряженными цепями T-клеточного рецептора. Каждый из внутриклеточных «хвостов» CD3y, CD35 и CD3s цепей содержит один консервативный мотив, известный как иммунорецепторный тирозиновый активирующий мотив или ITAM, тогда как каждая CD3ζ цепь имеет три. Как правило, ITAM вовлечены в сигнальную способность TCR комплекса. Эти вспомогательные молекулы имеют отрицательно заряженные трансмембранные участки и играют роль в распространении сигнала от TCR в клетку. CD3- и ζ-цепи вместе с TCR формируют то, что называется T-клеточным рецепторным комплексом.
В некоторых вариантах осуществления TCR может быть гетеродимером из двух цепей a и β (или необязательно γ и δ) или он может быть одноцепочечной TCR конструкцией. В некоторых вариантах осуществления TCR представляет собой гетеродимер, содержащий две разных цепи (a и β цепи или γ и δ цепи), которые связаны, например, при помощи дисульфидной связи или дисульфидных связей.
Характерные антигенные рецепторы, включая CAR и рекомбинантные TCR, а также способы конструирования и введения данных рецепторов в клетки, включают те, которые описаны, например, в публикациях международных патентных заявок № WO200014257, WO2013126726, WO2012/129514, WO2014031687, WO2013/166321, WO2013/071154, WO2013/123061 публикациях патентных заявок США № US2002131960, US2013287748, US20130149337, патентах США №: 6,451,995, 7,446,190, 8,252,592, 8,339,645, 8,398,282, 7,446,179, 6,410,319, 7,070,995, 7,265,209, 7,354,762, 7,446,191, 8,324,353 и 8,479,118, и Европейской патентной заявке № EP2537416, и/или те, которые описаны Sadelain et al., Cancer Discov. 2013 April; 3(4): 388-398; Davila et al. (2013) PLoS ONE 8(4): e61338; Turtle et al., Curr. Opin. Immunol., 2012 October; 24(5): 633-39; Wu et al., Cancer, 2012 March 18(2): 160-75. В некоторых аспектах генетически сконструированные антигенные рецепторы включают CAR, описанные в патенте США №: 7,446,190, и те, которые описаны в публикации международной патентной заявки № WO/2014055668 Al.
Антигены
К числу антигенов, на которые нацелены генетически сконструированные антигенные рецепторы, относятся те, которые экспрессируются в связи с болезнью, состоянием или типом клеток, на которые необходимо нацеливаться посредством адоптивной клеточной терапии. К числу таких болезней и состояний относятся пролиферативные, неопластические и злокачественные болезни и нарушения, в частности, разные виды рака.
Рак может быть солидным раком или “опухолью жидких тканей”, таким как раки, затрагивающие кровь, костный мозг и лимфоидную систему, также известные как опухоли гематопоэтических и лимфоидных тканей, которые включают в первую очередь лейкоз и лимфому. Опухоли жидких тканей включают, например, острую миелоцитарную лейкемию (AML), хронический миелолейкоз (CML), острый лимфоцитарный лейкоз (ALL) и хронический лимфоцитарный лейкоз (CLL) (включая различные лимфомы, такие как лимфома из клеток мантийной зоны, неходжкинская лимфома (NHL), аденома, плоскоклеточная карцинома, карцинома гортани, карцинома желчного пузыря и желчного протока, раки сетчатки глаза, такие как ретинобластома).
В частности, солидные раки включают виды рака, поражающие один из органов, выбранный из группы, состоящей из толстой кишки, прямой кишки, кожи, эндометрия, легких (включая немелкоклеточную карциному легких), матку, кости (такие как остеосаркома, хондросаркома, саркома Юинга, фибросаркома, гигантоклеточная опухоль, адамантинома и хордома), печени, почки, пищевода, желудка, мочевого пузыря, поджелудочной железы, шейки матки, мозга (такие как менингиома, глиобластома, низкодифференцированная астроцитома, олигодендроцитома, опухоли гипофиза, шваннома и метастатический рак мозга), яичника, молочной железы, области головы и шеи, яичка, предстательной железы и щитовидной железы.
Предпочтительно, рак согласно изобретению является раком, поражающим кровь, костный мозг и лимфоидную систему, как описано выше. В большинстве случаев рак является или связан с множественной миеломой.
Болезни согласно изобретению также включают инфекционные белозни или состояния, такие как, но без ограничения, вирусные, ретровирусные, бактериальные и протозойные инфекции, иммунодефицитное состояние, цитомегаловирус (CMV), вирус эпштейна-Барр (EBV), аденовирус, BK полиомавирус; аутоиммунные или воспалительные болезни или состояния, такие как артрит, например, ревматоидный артрит (RA), диабет I типа, системная красная волчанка (SLE), воспалительная болезнь кишечника, псориаз, склеродерма, аутоиммунное заболевание щитовидной железы, заболевание Грейвса, болезнь Крона, множественный склероз, астма и/или болезнь или состояние, связанное с трансплантатом.
В некоторых вариантах осуществления антиген представляет собой полипептид. В некоторых вариантах осуществления он является углеводом или другой молекулой. В некоторых вариантах осуществления антиген селективно экспрессируется или сверхэкспрессируется на клетках, имеющих отношение к болезни или состоянию, например, на опухолевых клетках или патогенных клетках, по сравнению с нормальными или нецелевыми клетками или тканями. В других вариантах осуществления антиген экспрессируется на нормальных клетках и/или экспрессируется на сконструированных клетках. В некоторых вариантах осуществления с целью улучшения специфичности и/или эффективности используется многоцелевой подход и/или стратегия разрушения гена, как указано в этом документе.
В некоторых вариантах осуществления антиген представляет собой универсальный опухолевый антиген. Термин "универсальный опухолевый антиген" относится к иммуногенной молекуле, такой как белок, который обычно экспрессируется на более высоком уровне в опухолевых клетках, чем в неопухолевых клетках, и также экспрессируется в опухолях различных органов. В некоторых вариантах осуществления универсальный опухолевый антиген экспрессируется больше чем у 30%, 40%, 50%, 60%, 70%, 75%, 80%, 85%, 90% или более раков человека. В некоторых вариантах осуществления универсальный опухолевый антиген экспрессируется, по меньшей мере, в трех, по меньшей мере, четырех, по меньшей мере, пяти, по меньшей мере, шести, по меньшей мере, семи, по меньшей мере, восьми или больше разных типов опухолей. В некоторых случаях универсальный опухолевый антиген может экспрессироваться в неопухолевых клетках, таких как нормальные клетки, но на более низких уровнях, чем он экспрессируется в опухолевых клетках. В некоторых случаях универсальный опухолевый антиген не экспрессируется во всех неопухолевых клетках, например, не экспрессируется в нормальных клетках. Характерные универсальные опухолевые антигены включают, например, человеческая обратная транскриптаза теломеразы (hTERT), сурвивин, мышиный двойной микробелок 2 гомолог (MDM2), цитохром P450 1B1 (CYP1B), HER2/neu, ген 1 (WT1) опухоли Вильмса, ливин, альфафетопротеин (AFP), карциноэмбриональный антиген (CEA), муцин 16 (MUC16), MUC1, простата-специфический мембранный антиген (PSMA), p53 или циклин (Dl). Пептидные эпитопы опухолевых антигенов, включая универсальные опухолевые антигены, известны в данной области техники и в некоторых аспектах могут использоваться, чтобы получить MHC-рестриктированные антигенные рецепторы, такие как TCR или TCR-подобные CAR (смотри, например, опубликованную PCT заявку № WO2011009173 или WO2012135854 и опубликованную США заявку № US20140065708).
В некоторых аспектах антиген экспрессируется на фоне множественной миеломы, такой как CD38, CD138,и/или CS-1. другие характерные антигены множественной миеломы включают CD56, TIM-3, CD33, CD123 и/или CD44. Антитела или антигенсвязывающие фрагменты, направленные против таких антигенов, известны и включают, например, описанные в патентах США № 8,153,765; 8,603477, 8,008,450; опубликованной заявке США № US20120189622; и опубликованных международных PCT заявках № WO2006099875, WO2009080829 или WO2012092612. В некоторых вариантах осуществления такие антитела или их антигенсвязывающие фрагменты (например, scFv) могут использоваться для получения CAR.
В некоторых вариантах осуществления антиген может быть антигеном, который экспрессируется или повышенно активен в раковых или опухолевых клетках, но который может также экспрессироваться в иммунной клетке, такой как находящаяся в покое или активированная T-клетка. Например, в некоторых случаях экспрессия hTERT, сурвивина и других универсальных опухолевых антигенов присутствует в лимфоцитах, включая активированные T-лимфоциты (смотри, например, Weng et al. (1996) J Exp. Med., 183:2471-2479; Hathcock et al. (1998) J Immunol, 160:5702-5706; Liu et al. (1999) Proc. Natl Acad Sci., 96:5147-5152; Turksma et al. (2013) Journal of Translational Medicine, 11: 152). Аналогично, в некоторых случаях CD38 и другие опухолевые антигены также могут экспрессироваться в иммунных клетках, таких как T-клетки, например, активируются в активированных T-клетках. Например, в некоторых аспектах CD38 является известным маркером T-клеточной активации.
В некоторых вариантах осуществления, предоставленных в описании, иммунная клетка, такая как T-клетка, может быть сконструирована с целью подавления или разрушения гена, кодирующего антиген в иммунной клетке с тем расчетом, чтобы экспрессированный генетически сконструированный антигенный рецептор не связывался специфически с антигеном в условиях его экспрессии на самой иммунной клетке. Таким образом, в некоторых аспектах это может способствовать предотвращению ненаправленных действий, таких как связывание сконструированных иммунных клеток с самими собой, которое может уменьшить эффективность сконструированных иммунных клеток, например, в отношении адоптивной клеточной терапии.
В некоторых вариантах осуществления, например, в случае ингибирующих CAR, мишенью является нецелевой маркер, например, антиген, неэкспрессированный на нездоровой клетке или клетке, на которую следует нацелиться, но который экспрессируется на нормальной или на непораженной болезнью клетке, которая также экспрессирует болезнь-специфическую мишень, на которую нацеливание осуществляется с помощью активирующего или стимулирующего рецептора в той же самой сконструированной клетке. Примерами таких антигенов являются MHC молекулы, такие как молекулы I класса MHC, например, в связи с лечением болезней или состояний, при которых снижается количество таких молекул, но они остаются экспрессированными в нецелевых клетках.
В некоторых вариантах осуществления сконструированные иммунные клетки могут содержать антиген, который нацеливается на один или больше других антигенов. В некоторых вариантах осуществления один или более других антигенов является опухолевым антигеном или онкомаркером. Другой антиген, на который нацеливаются при помощи антигенных рецепторов на предоставленных иммунных клетках, может в некоторых вариантах осуществления включать орфанный тирозинкиназный рецептор ROR1, tEGFR, Her2, Ll-CAM, CD19, CD20, CD22, мезотелин, CEA, поверхностный антиген гепатита B, антифолатный рецептор, CD23, CD24, CD30, CD33, CD38, CD44, EGFR, EGP-2, EGP-4, EPHa2, ErbB2, 3 или 4, FBP, эмбриональный рецептор, GD2, GD3, HMW-MAA, IL-22R-альфа, IL-13R-альфа2, kdr, каппа легкая цепь, антиген Leу, молекула клеточной адгезии Ll, MAGE-A1, мезотелин, MUC1, MUC16, PSCA, NKG2D лиганды, NY-ESO-1, MART-1, gplOO, раково-эмбриональный антиген, ROR1, TAG72, VEGF-R2, карциноэмбриональный антиген (CEA), простатаспецифический антиген, PSMA, Her2/neu, рецептор эстрогена, рецептор прогестерона, эфрин B2, CD 123, CS-1, c-Met, GD-2, и MAGE A3, CE7, антиген 1 опухоли Вильмса (WT-1), циклин, такой как циклин Al (CCNA1), и/или биотинилированные молекулы, и/или молекулы, экспрессированные HIV, HCV, HBV или другими патогенами.
В некоторых вариантах осуществления CAR связывает патоген-специфический антиген. В некоторых вариантах осуществления CAR является специфическим в отношении вирусных антигенов (таких как HIV, HCV, HBV и т.д.), бактериальных антигенов и/или паразитарных антигенов.
В некоторых вариантах осуществления клетки изобретения являются генетически сконструированными, чтобы экспрессировать два или более генетически сконструированных рецепторов на клетке, каждый из которых распознает иной антиген и, как правило, включает отличный от других внутриклеточный сигнальный компонент. Такие многоцелевые стратегии описаны, например, в Международной патентной заявке, Публикация №: WO 2014055668 Al (описывает комбинацию активирующих и костимулирующих CAR, например, нацеленных на два разных антигена, присутствующих индивидуально на нецелевых, например, нормальных клетках, но присутствующих вместе только на клетках, имеющих отношение к болезни или состоянию, которое необходимо лечить) и Fedorov et al., Sci. Transl. Medicine, 5(215) (December, 2013) (описывает клетки, экспрессирующие активирующий и ингибирующий CAR, например, те, в которых активированный CAR связывается с одним антигеном, экспрессированным как на нормальных или на непораженных болезнью клетках, так и на клетках, имеющих отношение к болезни или состоянию, которое необходимо лечить, и ингибирующий CAR связывается с другим антигеном, экспрессированным только на нормальных клетках или клетках, которые не подлежат лечению).
В некоторых случаях сверхэкспрессия стимулирующего фактора (например, лимфокина или цитокина) может быть токсичной для субъекта. Таким образом, в некоторых случаях сконструированные клетки включают сегменты генов, которые обусловливают восприимчивость клеток к негативной селекции in vivo, например, после введения в адоптивной иммунотерапии. Например, в некоторых аспектах клетки конструируют так, что они могут быть ликвидированы в результате изменения in vivo состояния пациента, которому они вводятся. Негативно селектируемый фенотип может возникать в результате инсерции гена, который придает свойство чувствителности к введенному агенту, например, соединению. Негативно селектируемые гены включают ген тимидинкиназы вируса Herpes simplex I типа (HSV-I TK) (Wigler et al., Cell II:223, 1977), который придает свойство чувствительности к ганцикловиру; ген клеточной гипоксантин фосфорибозилтрансферазы (HPRT), ген клеточной аденин фосфорибозилтрансферазы (APRT), бактериальной цитозиндезаминазы (Mullen et al., Proc. Natl. Acad. Sci. USA. 89:33 (1992)).
В других вариантах осуществления изобретения клетки, например, T-клетки, не конструируют так, чтобы экспрессировать рекомбинантные рецепторы, но вместо этого включают антигенные рецепторы природного происхождения, специфичные в отношении желательных антигенов, такие как опухоль инфильтрирующие лимфоциты и/или T-клетки, культивированные in vitro или ex vivo, например, в ходе стадии(стадий) инкубации, чтобы способствовать размножению клеток, обладающих определенной специфичностью к антигену. Например, в некоторых вариантах осуществления клетки для адоптивной клеточной терапии получают путем изолирования опухоль-специфических T-клеток, например, аутологичных инфильтрирующих опухоль лимфоцитов (TIL). Прямое нацеливание на опухоли человека с использованием аутологичных инфильтрирующих опухоль лимфоцитов может в некоторых случаях опосредовать регрессию опухоли (смотри Rosenberg SA, et al.(1988) N Engl J Med. 319: 1676-1680). В некоторых вариантах осуществления лимфоциты выделяют из удаленных опухолей. В некоторых вариантах осуществления такие лимфоциты выращиваются in vitro. В некоторых вариантах осуществления такие лимфоциты культивируют с лимфокинами (например, IL-2). В некоторых вариантах осуществления такие лимфоциты опосредуют специфический лизис аутологичных опухолевых клеток, но не аллогенной опухоли или аутологичных нормальных клеток.
К числу дополнительных нуклеиновых кислот, например, генов для внедрения, относятся те, которые улучшают эффективность терапии, например, способствуя жизнеспособности и/или функции «перенесенных» клеток; гены, обеспечивающие генетический маркер для селекции и/или оценки клеток, такой как оценка in vivo выживаемости и локализации; гены, улучшающие безопасность, например, делая клетку восприимчивой к отрицательной селекции in vivo, как описано Lupton S. D. et al., Mol. and Cell Biol., 11:6 (1991); и Riddell et al., Human Gene Therapy 3:319-338 (1992); смотри также публикации PCT/US91/08442 и PCT/US94/05601 Lupton et al., описывающие использование бифункциональных селектируемых гибридных генов, происходящих в результате соединения доминантного позитивного селективного маркера с негативным селективным маркером. Смотри, например, Riddell et al., патент США № 6,040,177, столбцы 14-17.
Способ получения клеток согласно изобретению
Настоящее изобретение также имеет отношение к способу получения модифицированной или сконструированной иммунной клетки, включающему стадию, заключающуюся в ингибировании экспрессии и/или активности Suv39h1 в иммунной клетке.
Предпочтительно, способ получения клеток согласно изобретению дополнительно включает стадию, заключающуюся во введеннии в указанные иммунные клетки генетически сконструированного антигенного рецептора, который специфически связывается с целевым антигеном.
Ингибирование экспрессии и/или активности Suv39h1 и введение генетически сконструированного антигенного рецептора, который специфически связывается с целевым антигеном, в иммунную клетку может осуществляться одновременно или последовательно в любом порядке.
Ингибирование Suv39h1
Согласно изобретению сконструированная иммунная клетка может контактировать, по меньшей мере, с одним агентом, который ингибирует или блокирует экспрессию и/или активность Suv39h1.
Указанный агент может быть выбран из низкомолекулярных ингибиторов; производных антител, таких как интратела, нанотела или аффитела, которые, как правило, блокируют или ингибируют экспрессию или активность Suv39h1; аптамеров, которые обычно блокируют или ингибируют экспрессию или активность Suv39h1; молекул нуклеиновых кислот, которые блокируют транскрипцию или трансляцию, таких как антисмысловые молекулы, комплементарные к Suv39h1; РНК интерферирующие агенты (такие как малые интерферирующие РНК (siРНК), малые шпилькообразные РНК (shРНК), микроРНК (miРНК) или piwiРНК (piРНК); рибозимы или комбинации этого.
По меньшей мере, один агент может также быть экзогенной нуклеиновой кислотой, содержащей a) сконструированную направляющую РНК из неприродной системы CRISPR (короткие палиндромные повторы, регулярно расположенныеи группами ), которая гибридизируется с геномной нуклеиновокислотной последовательностью Suv39h1 и/или b) нуклеотидную последовательность, кодирующую белок CRISPR (обычно белок Cas9 типа-II), при этом необязательно клетки являются трансгенными для экспрессии белка Cas9. Агент также может быть белком типа цинковых пальцев (ZFN) или TAL белком.
Термин "небольшая органическая молекула" имеет отношение к молекуле размера, сопоставимого с органическими молекулами, обычно используемыми в фармацевтических препаратах. Термин исключает биологические макромолекулы (например, белки, нуклеиновые кислоты и т.д.). Размер предпочтительных небольших органических молекул колеблется в пределах примерно около 5000 Да, более предпочтительно около 2000 Да и наиболее предпочтительно около 1000 Да.
В отдельном варианте осуществления ингибитор H3K9-гистон метилтрансферазы SUV39H1 представляет собой кетоцин (CAS 28097-03-2), как описано Greiner D, Bonaldi T, Eskeland R, Roemer E, Imhof A. “Identification of a specific inhibitor of the histon methyltransferase SU(VAR)3-9”. Nat Chem Biol. 2005 Aug;l(3): 143-5.; Weber, H. P., et al, “The molecular structure and absolute configuration of chaetocin”, Acta Cryst, B28, 2945-2951 (1972); Udagawa, S., et al, “The production of chaetoglobosins, sterigmatocystin, O-methylsterigmatocystin, and chaetocin by Chaetomium spp. and related fungi”, Can. J. microbiol, 25, 170-177 (1979); и Gardiner, D. M., et al, “The epipolythiodioxopiperazine (ETP) class of fungal toxins: distribution, mode of action, functions and biosynthesis”, Microbiol, 151, 1021-1032 (2005). Например, кетоцин является коммерчески доступным от компании Sigma Aldrich.
Ингибитор Suv39h1 также может быть ETP69 (Rac-(3S,6S,7S,8aS)-6-(бензо[d][1,3]диоксол-5-ил)-2,3,7-триметил-1,4-диоксогексагидро-6H-3,8a-эпидитиопиррол[1,2-a]пиразин-7-карбонитрил)ом, рацемическим аналогом эпидитиодикетопиперазина алкалоида кетоцина A (смотри WO2014066435, а также смотри Baumann M, Dieskau AP, Loertscher BM, et al. Tricyclic Analogues of Epidithiodioxopiperazine Alkaloids with Promising In Vitro and In Vivo Antitumor Activity. Chemical science (Royal Society of Chemistry : 2010). 2015;6:4451-4457 и Snigdha S, Prieto GA, Petrosyan A, et al. H3K9me3 Inhibition Improves Memory, Promotes Spine Formation, and Increases BDNF Levels in the Aged Hippocampus. The Journal of Neuroscience. 2016;36(12):3611-3622).
Ингибирующая активность соединения может быть определена с помощью различных методов, как описано в Greiner D. Et al. Nat Chem Biol. 2005 Aug;l(3): 143-5 или Eskeland, R. et al. Biochemistry 43, 3740-3749 (2004).
Ингибирование Suv39h1 в клетке может быть достигнуто до или после инъекции намеченному пациенту. В отдельном варианте осуществления ингибирование, как определено ранее, осуществляется in vivo после введения клетки субъекту. Как правило, Suv39h1 ингибитор, как определено в описании, может включаться в композицию, содержащую данную клетку. Suv39h1 также может быть введен отдельно до, одновременно или после введения клетки(ок) субъекту.
Как правило, ингибирование Suv39h1 согласно изобретению может достигаться при помощи инкубации клетки согласно изобретению с композицией, содержащей, по меньшей мере, один фармакологический ингибитор, как описано ранее. Ингибитор включается во время размножения противоопухолевых T-клеток in vitro, таким образом, модифицируя их воспроизведение, выживаемость и терапевтичекую эффективность после адоптивного переноса.
Ингибирование Suv39h1 в клетке согласно изобретению может достигаться с помощью интрател. Интратела являются антителами, которые связываются внутриклеточно с их антигеном, после того, как они были продуцированы в той же самой клетке (например, смотри обзор Marschall AL, Dübel S and Böldicke T “Specific in vivo knockdown of protein function by intrabodies”, MAbs. 2015;7(6):1010-35. Также смотри Van Impe K, Bethuyne J, Cool S, Impens F, Ruano-Gallego D, De Wever O, Vanloo B, Van Troys M, Lambein K, Boucherie C, et al. “A nanobody targeting the F-actin capping protein CapG restrains breast cancer metastasis”. Breast Cancer Res 2013; 15:R116; Hyland S, Beerli RR, Barbas CF, Hynes NE, Wels W. “Generation and functional characterization of intracellular antibodies interacting with the kinase domain of human EGF receptor. Oncogene 2003; 22:1557-67”; Lobato MN, Rabbitts TH. “Intracellular antibodies and challenges facing their use as therapeutic agents”. Trends Mol Med 2003; 9:390-6, and Donini M, Morea V, Desiderio A, Pashkoulov D, Villani ME, Tramontano A, Benvenuto E. “Engineering stable cytoplasmic intrabodies with designed specificity”. J Mol Biol. 2003 Jul 4;330(2):323-32.).
Интратела можно получить путем клонирования соответствующей кДНК из имеющегося клона гибридомы или еще удобнее, новые scFvs/Fabs могут быть отобраны c помощью методов индикации in vitro, такого как фаговый дисплей, который обеспечивает необходимый ген, кодирующий антитело, с самого начала и дает возможность более подробного предварительного проектирования специфичности антитела. В дополнение к этому, может использоваться бактериальный дисплей, дрожжевой дисплей, дисплей поверхности клетки млекопитающего и рибосомный дисплей. Однако, наиболее часто используемой системой дисплея in vitro для селекции специфических антител является фаговый дисплей. В процедуре, называемой пэннингом (селекция аффинности), рекомбинантные фаговые антитела отбирают путем инкубации репертуара фаговых антител с антигеном. Это процесс повторяется несколько раз, что приводит к обогащенному репертуару антител, содержащему специфические связывающиеся с антигеном молекулы к едва ли не любой возможной мишени. На сегодняшний день in vitro собранные библиотеки рекомбинантных человеческих антител уже дали тысячи новых фрагментов рекомбинантных антител. Следует отметить, что предварительное условие для нокдауна специфического белка при помощи цитоплазматического интратела заключается в том, что антиген нейтрализуется/инактивируется в результате связывания антитела. Для получения подходящих антител имеется пять разных подходов: 1) In vivo селекция функциональных антител в эукариотах, таких как дрожжи, и в прокариотах, таких как E.coli (антиген-зависимый и независимый); 2) получение гибридных белков антитела для улучшения стабильности в цитозоле; 3) использование специальных «каркасов» улучшения стабильности в цитозоле (например, путем «пересадки» CDR или введения синтетических CDR в устойчивые каркасные участки антитела); 4) использование однодоменных антител для улучшенной стабильности в цитозоле; и 5) селекция стабильных интрател, лишенных дисульфидной связи. Эти подходы, в частности, подробно описаны в Marschall, A. L et al., mAbs 2015, как указано выше.
Наиболее часто используемым форматом для интрател является scFv, который состоит из H- и L-цепи вариабельного домена антитела (VH и VL), удерживаемых вместе при помощи короткой, гибкой линкерной последовательности (часто (Gly4Ser)3), чтобы избежать необходимости разделять экспрессию и сборку 2 цепей антитела полной молекулы IgG или Fab молекулы. Альтернативно, используется Fab формат, содержащий дополнительно C1 домен тяжелой цепи и константную область легкой. Недавно был описан новый возможный формат для интрател, scFab. scFab формат обеспечивает более легкое субклонирование доступных Fab генов во внутриклеточный вектор экспрессии, но еще остается выяснить, предоставляет ли это какое-либо преимущество по сравнению с общепризнанным scFv форматом. В дополнение к scFv и Fab в качестве интрател используются биспецифические форматы. Биспецифическое Tie-2 x VEGFR-2 антитело, нацеленное на ER, продемонстрировало увеличенное время полужизни по сравнению с моноспецифическими антителами-аналогами. Биспецифическое трансмембранное интратело разрабатывается как специальный формат для одновременного распознавания внутри- и внеклеточных эпитопов эпидермального фактора роста, объединяя разные свойства родственных моноспецифических антител, т.е., ингибирование аутофосфорилирования и связывание лиганда.
Другим форматом интратела, особенно подходящим для цитоплазматической экспрессии, являются однодоменные антитела (также называемые нанотелами), полученные от верблюдовых или состоящие из одного человеческого VH домена или человеческого VL домена. Эти однодоменные антитела зачастую обладают преимущественными характеристиками, например, высокой устойчивостью; хорошей растворимостью; удобством клонирования библиотеки и селекции; высоким выходом экспрессии в E.coli и дрожжах.
Ген интратела может экспрессироваться внутри клетки-мишени после трансфекции экспрессирующей плазмиды или вирусной трансдукции при помощи рекомбинантного вируса. Как правило, выбор имеет целью предоставление трансфекции интратела и уровней продуцирования. Успешную трансфекцию и последующее продуцирование интратела можно проанализировать путем детекции продуцированного антитела с помощью иммуноблотинга, а, для оценки правильного взаимодействия интратело/антиген может использоваться коиммунопреципитация из экстрактов HEK 293 клеток, временно котрансфицированных соответствующим антигеном и плазмидами, экспрессирующими интратело.
Ингибирование Suv39h1 в клетке согласно изобретению также может осуществляться с использованием аптамеров, ингибирующих или блокирующих экспрессию или активность Suv39h1. Аптамеры представляют собой класс молекул, представляющих альтернативу антителам, если иметь в виду молекулярное распознавание. Аптамеры представляют собой олигонуклеотидную (ДНК или РНК) или олигопептидную последовательности со способностью распознавать фактически любой класс молекул-мишеней с высокой аффинностью и специфичностью.
Олигонуклеотидные аптамеры могут быть изолированы с помощью систематической эволюции лигандов экспоненциальным обогащением (SELEX) из библиотеки случайных последовательностей, как описано в Tuerk C. и Gold L., 1990. Библиотеку случайных последовательностей получают путем комбинаторного химического синтеза ДНК. В этой библиотеке каждый член является линейным олигомером, в конечном итоге химически модифицированным, уникальной последовательности. Возможные модификации, применение и преимущества этого класса молекул рассмотрены в Jayasena S.D., 1999.
Пептидные аптамеры состоят из конформационно фиксированного вариабельного участка антитела, представленного на белковой платформе, такой как тиоредоксин A E. coli, которые отбирают из комбинаторных библиотек с помощью двух гибридных методов (Colas P, Cohen B, Jessen T, Grishina I, McCoy J, Brent R. “Genetic selection of peptide aptamers that recognize and inhibit cyclin-dependent kinase 2”. Nature. 1996 Apr 11;380(6574):548-50).
Ингибирование Suv39h1 в клетке согласно изобретению также может осуществляться с помощью молекул аффител. Аффитела представляют собой небольшие белки, созданные для связывания с большим количеством целевых белков или пептидов с высокой аффинностью, имитирующих моноклональные антитела, и являются, следовательно, членами семейства миметиков антител (смотри обзор Löfblom J, Feldwisch J, Tolmachev V, Carlsson J,  , Frejd FY. Affibody molecules: engineered proteins for therapeutic, diagnostic and biotechnological applications. FEBS Lett. 2010 Jun 18;584(12):2670-80). Молекулы аффител основаны на сконструированном варианте (Z домен) B-домена в иммуноглобулин-связывающих областях стафилококкового белка A, теоретически со специфичностью связывания с любой имеющейся мишенью. Библиотеки молекул аффител, как правило, создаются путем комбинаторной рандомизации 13 аминокислотных положений в спирали один и два, которые содержат первичную Fc-связывающую поверхность Z-домена. Обычно библиотеки представлены на фагах, с последующим биопэннингом против желательных мишеней. В случае, если аффинность первого увеличивается, созревание аффинности приводит обычно к улучшенному связыванию и может достигаться путем либо перетасовки спирали или выравнивания последовательности в сочетании с направленным комбинаторным мутагенезом. Вновь идентифицированные молекулы с их измененной связывающей поверхностью обычно сохраняют исходную спиральную структуру, а также высокую устойчивость, тем не менее, сообщалось об уникальных исключениях с интересными свойствами. Благодаря их небольшому размеру и свойствам быстрого свертывания, молекулы аффител могут быть получены методами химического пептидного синтеза.
, Frejd FY. Affibody molecules: engineered proteins for therapeutic, diagnostic and biotechnological applications. FEBS Lett. 2010 Jun 18;584(12):2670-80). Молекулы аффител основаны на сконструированном варианте (Z домен) B-домена в иммуноглобулин-связывающих областях стафилококкового белка A, теоретически со специфичностью связывания с любой имеющейся мишенью. Библиотеки молекул аффител, как правило, создаются путем комбинаторной рандомизации 13 аминокислотных положений в спирали один и два, которые содержат первичную Fc-связывающую поверхность Z-домена. Обычно библиотеки представлены на фагах, с последующим биопэннингом против желательных мишеней. В случае, если аффинность первого увеличивается, созревание аффинности приводит обычно к улучшенному связыванию и может достигаться путем либо перетасовки спирали или выравнивания последовательности в сочетании с направленным комбинаторным мутагенезом. Вновь идентифицированные молекулы с их измененной связывающей поверхностью обычно сохраняют исходную спиральную структуру, а также высокую устойчивость, тем не менее, сообщалось об уникальных исключениях с интересными свойствами. Благодаря их небольшому размеру и свойствам быстрого свертывания, молекулы аффител могут быть получены методами химического пептидного синтеза.
В других вариантах осуществления изобретения ингибирование активности Suv39h1 может осуществляться с помощью репрессии/суппрессии гена путем нокдауна гена с использованием РНК интерференции (РНКi), например, малой интерферирующей РНК (siРНК), короткой шпилечной РНК (shРНК) или рибозимов. Технология siРНК включает технологию, основанную на РНКi, использующих двухцепочечные РНК молекулы, имеющие последовательность, гомологичную с нуклеотидной последовательностью мРНК, которая транскрибируется с гена, и последовательность, комплементарную с нуклеотидной последовательностью. В большинстве случаев siРНК является гомологичной/комплементарной с одним участком мРНК, который транскрибируется с гена, или может быть siРНК, включающей множество молекул РНК, которые являются гомологичными/комплементарными с разными участками.
Антисмысловые олигонуклеотиды, включая антисмысловые РНК молекулы и антисмысловые ДНК молекулы, действуют таким образом, что непосредственно блокируют трансляцию H3K9-гистон метилтрансферазы Suv39h1, таким образом, предотвращая трансляцию белка или увеличивая деградацию мРНК, таким образом, уменьшая уровень H3K9-гистон метилтрансферазы SUV39H1 и, таким образом, ее активность в клетке. Например, антисмысловые олигонуклеотиды, по меньшей мере, примерно из 15 оснований и комплементарные уникальным участкам мРНК последовательности транскрипта, кодирующей H3K9-гистон метилтрансферазу SUV39H1, могут быть синтезированы, например, при помощи общепринятых фосфодиэфирных методов, и введены, например, путем внутривенной инъекции или инфузии. Способы применения антисмысловых технологий для специфичного ингибирования экспрессии генов, последовательность которых известна, хорошо известны в данной области техники (смотри, например, патенты США № 6,566,135; 6,566, 131; 6,365,354; 6,410,323; 6,107,091; 6,046,321 и 5,981,732).
"РНК интерферирующий агент" при использовании в описании определяется как какой-либо агент, который вмешивается в или ингибирует экспрессию биомаркерного гена-мишени путем РНК-интерференции (РНКi). Подобные РНК интерферирующие агенты включают, но не ограничиваются этим, молекулы нуклеиновых кислот, включая молекулы РНК, которые являются гомологичными с геном-мишенью изобретения (например, Suv39h1), или его фрагментом, малые интерферирующие РНК (siРНК) и небольшие молекулы, которые препятствуют или ингибируют экспрессию целевой нуклеиновой кислоты при помощи РНК интерференции (РНКi).
Малые интерферирующие РНК (siРНК) также могут функционировать как ингибиторы экспрессии для использования в настоящем изобретении. Экспрессия гена H3K9-гистон метилтрансферазы SUV39H1 может быть уменьшена путем контактирования субъекта или клетки c небольшой двухцепочечной РНК (dsРНК) или вектором или конструкцией, вызывающей продуцирование небольшой двухцепочечной РНК, так что экспрессия гена H3K9-гистон метилтрансферазы SUV39H1 специфически ингибируется (т.е. РНК интерференция или РНКi). Методы селекции подходящего dsРНК или dsРНК-кодирующего вектора хорошо известны в данной области техники для генов, последовательности которых известны (смотри, например, Tuschl, T. et al. (1999); Elbashir, S. M. et al. (2001); Hannon, GJ. (2002); McManus, MT. et al. (2002); Brummelkamp, TR. et al. (2002); патенты США № 6,573,099 и 6,506,559; и международные патентные публикации № WO 01/36646, WO 99/32619 и WO 01/68836). Все или часть фосфодиэфирных связей siРНК изобретения предпочтительно являются защищенными. Эта защита, как правило, осуществляется химическим путем с помощью методов, известных в данной области техники. Фосфодиэфирные связи могут быть защищены, например, тиоловой или аминной функциональной группой или с помощью фенильной группы. 5'- и/или 3'- концы siРНК изобретения являются также преимущественно защищенными, например, с использованием способов, описанных выше для защиты фосфодиэфирных связей. Последовательности siРНК преимущественно содержат, по меньшей мере, двенадцать смежных динуклеотидов или их производных.
При использовании в описании термин "производные siРНК" в отношении настоящих нуклеиновокислотных последовательностей относится к нуклеиновой кислоте, имеющей процент идентичности, по меньшей мере, 90% с эритропоэтином или его фрагментом, предпочтительно, по меньшей мере, 95%, например, по меньшей мере, 98%, и более предпочтительно, по меньшей мере, 98%.
При использовании в описании выражение "процент идентичности" между двумя нуклеиновокислотными последовательностями означает процент одинаковости между двумя сравниваемыми последовательностями, полученными путем лучшего выравнивания указанных последовательностей, этот процент является чисто статистическим и различия между этими двумя последовательностями являются случайным образом распределенными по последовательностям нуклеиновых кислот. При использовании в описании "самое лучшее выравнивание" или "оптимальное выравнивание" означает выравнивание, для которого определенный процент идентичности (смотри ниже) является самым высоким. Сравнение последовательности между двумя нуклеиновокислотными последовательностями обычно осуществляется путем сравнения этих последовательностей, которые были предварительно выравнены в соответствии с самым лучшим выравниванием; это сравнение осуществляется по сегментам сравнения, для того, чтобы идентифицировать и сличить локальные участки сходства. Лучшее выравнивание последовательностей для проведения сравнения может быть реализовано, кроме способа вручную, путем использования общего алгоритма поиска гомологии, разработанного SMITH и WATERMAN (Ad. App. Math., vol.2, p:482, 1981), путем использования алгоритма поиска локальной гомологии, разработанного NEDDLEMAN и WUNSCH (J. Mol. Biol, vol.48, p:443, 1970), путем использования метода подобия, разработанного PEARSON и LIPMAN (Proc. Natl. Acd. Sci. USA, vol.85, p:2444, 1988), путем использования компьютерного программного обеспечения с применением подобных алгоритмов (GAP, BESTFIT, BLAST P, BLAST N, FASTA, TFASTA в комплекте программного обеспечения Wisconsin Genetics, Genetics Computer Group, 575 Science Dr., Madison, WI USA), путем использования MUSCLE алгоритмов множественного выравнивания (Edgar, Robert C, Nucleic Acids Research, vol. 32, p: 1792, 2004). Для получения самого лучшего локального выравнивания предпочтительным является использование программного обеспечения BLAST. Процент идентичности между двумя последовательностями нуклеиновых кислот определяется путем сравнения этих двух оптимально выравненных последовательностей. Для того, чтобы получить оптимальное выравнивание между этими двумя последовательностями, следует учесть, что нуклеиновокислотные последовательности могут содержать инсерции или делеции относительно эталонной последовательности. Процент идентичности вычисляется путем определения количества идентичных положений между этими двумя последовательностями, делением этого числа на общее количество сравниваемых положений и умножением полученного результата на 100, чтобы получить процент идентичности между этими двумя последовательностями.
shРНК (короткие шпилечные РНК) также могут функционировать в качестве ингибиторов экспрессии при использовании в настоящем изобретении. shРНК в большинстве случаев состоят из короткой (например, 19-25 нуклеотидов) антисмысловой цепи, за которой следует петля из 5-9 нуклеотидов, и аналогичной смысловой последовательности. Альтернативно, смысловая последовательность может идти впереди петлеобразной структуры, за которой следует антисмысловая цепь.
Рибозимы также могут функционировать как ингибиторы экспрессии при использовании в настоящем изобретении. Рибозимы представляют собой молекулы ферментативной РНК, способные катализировать специфическое расщепление РНК. Механизм действия рибозимов затрагивает специфичную гибридизацию последовательности молекулы рибозима с комплементарной целевой РНК с последующим эндонуклеолитическим расщеплением. Таким образом, сконструированные шпилькообразные или утолщенные (в виде головки молота) мотивы молекул рибозимов, которые специфически и эффективно катализируют эндонуклеотическое расщепление мРНК последовательностей H3K9-гистон метилтрансферазы SUV39H1, используются в рамках настоящего изобретения. Сайты расщепления специфическими рибозимами в какой-либо потенциальной РНК-мишени первоначально устанавливаются путем сканирования молекулы-мишени на предмет наличия сайтов расщепления рибозимами, которые, как правило, включают следующие последовательности GUA, GUU и GUC. После идентификации короткие РНК последовательности примерно между 15 и 20 рибонуклеотидами, соответствующие участку гена-мишени, содержащему сайт расщепления, подлежат оценке в отношении предсказанных особенностей структуры, такой как вторичная структура, которая может привести олигонуклеотидную последовательность в непригодное состояние.
И антисмысловые олигонуклеотиды и рибозимы, подходящие в качестве ингибиторов экспрессии, можно получить известными способами. Эти способы включают методы химического синтеза, такие как, например, твердофазный фосфорамидитный химический синтез. Альтернативно, молекулы антисмысловых РНК могут быть получены путем in vitro или in vivo транскрипции последовательностей ДНК, кодирующих молекулу РНК. Такие последовательности ДНК могут быть «внедрены» в самые разные векторы, которые включают в себя подходящие промоторы РНК полимеразы, такие как T7 или SP6 промоторы полимеразы. С целью увеличения внутриклеточной стабильности и времени полужизни в олигонуклеотиды изобретения могут вводиться различные модификации. Возможные модификации включают, но не ограничиваются этим, добавление фланкирующих последовательностей рибонуклеотидов или дезоксирибонуклеотидов на 5' и/или 3' концах молекулы, или использование фосфоротиоатных или 2'-0-метил, а не фосфодиэстеразных связей, в пределах олигонуклеотидного остова.
Антисмысловые олигонуклеотиды, siРНК, shРНК и рибозимы изобретения могут доставляться in vivo отдельно или вместе с вектором. В широком смысле "вектор" является каким-либо носителем, способным обеспечить перенос антисмыслового олигонуклеотида, siРНК, shРНК или рибозимной нуклеиновой кислоты в клетки и предпочтительно клетки, экспрессирующие H3K9-гистон метилтрансферазу SUV39H1. Предпочтительно, вектор транспортирует нуклеиновую кислоту в клетку снижая степень деградации относительно степени деградации, которая происходила бы при отсутствии вектора. В общем, векторы, пригодные для изобретения, включают, но не ограничиваются этим, плазмиды, фагмиды, вирусы, другие носители, происходящие из вирусных или бактериальных источников, которые управляются посредством инсерции или введения антисмыслового олигонуклеотида, siРНК, shРНК или последовательностей рибозимной нуклеиновой кислоты. Вирусные векторы являются предпочтительным типом вектора и включают, но не ограничиваются этим, нуклеиновокислотные последовательности из следующих вирусов: ретровирусов, таких как вирус мышиного лейкоза Молони, вирус саркомы мышей Харви, вирус опухоли молочной железы мышей и вирус саркомы Рауса; аденовирус; аденоассоциированный вирус; вирусы SV40 типа; полиомавирусы; вирус Эпштейна-Барр; вирус папилломы; герпес вирус; вирус осповакцины; полиовирус и R A вирус, такой как ретровирус. Могут использоваться другие векторы, не упомянутые, но известные в данной области техники.
Предпочтительные вирусные векторы основываются на нецитопатических эукариотических вирусах, в которых второстепенные гены заменяются нужными генами. Нецитопатические вирусы включают ретровирусы (например, лентивирус), жизненный цикл которых затрагивает обратную транскрипцию вирусной геномной РНК в ДНК с последующей интеграцией провируса в клеточную ДНК хозяина. Ретровирусы допущены к испытаниям по поводу применения в генной терапии человека. Наиболее подходящими являются такие ретровирусы, которые дефектны по репликации (т.е. способны направлять синтез желательных белков, но неспособны к выработке инфекционной частицы). Подобные генетически измененные ретровирусные векторы экспрессии обычно используются для высокоэффективной трансдукции генов in vivo. Стандартные протоколы для получения ретровирусов, дефектных по репликации (включая этапы введения экзогенного генетического материала в плазмиду, трансфекции линий упаковывающих клеток плазмидой, выработки рекомбинантных ретровирусов линией упаковывающих клеток, сбор вирусных частиц из среды для культивирования тканей и инфицирование клетки-мишени вирусными частицами), предоставляются в Kriegler, 1990 и Murry, 1991).
Предпочтительными вирусами для определенных режимов использования являются аденовирусы и аденоассоциированные (AAV) вирусы, которые представляют собой двухцепочечные ДНК вирусы, которые уже допущены к применению в генной терапии человека. В настоящее время известны 12 разных AAV серотипов (AAV1 - 12), каждый с разным тропизмом к ткани (Wu, Z Mol Ther 2006; 14:316-27). Рекомбинантные AAVs происходят от зависимых парвовирусов AAV2 (Choi, VW J Virol 2005; 79:6801-07). Аденоассоциированный вирус типа 1-12 может быть сконструирован так, чтобы быть лишенным репликации и способным инфицировать широкий спектр типов и видов клеток (Wu, Z Mol Ther 2006; 14:316-27). Он кроме того имеет преимущества, такие как устойчивость к нагреванию и растворимости в липидах; высокая частота трансдукции в клетках различных линий дифференцировки, включая гемопоэтические клетки; и отсутствие ингибирования суперинфекции, тем самым обеспечивая некоторое количество серий трансдукций. Сообщается, что аденоассоциированный вирус может интегрироваться в клеточную ДНК человека сайт-специфичным образом, тем самым минимизируя возможность инсерционного мутагенеза и вариабельность свойств экспрессии введенного гена ретровирусной инфекции. В дополнение к этому, инфекции аденоассоциированным вирусом существуют в культуре ткани в течение более чем 100 пассажей при отсутствии селективного давления, что означает, что геномная интеграция, опосредованная аденоассоциированным вирусом, является относительно устойчивым событием. Аденоассоциированный вирус также может функционировать в экстрахромосомном режиме.
Другие векторы включают плазмидные векторы. Плазмидные векторы подробно описаны и хорошо известны специалистам в данной области техники. Смотри, например, Sambrook et al, 1989. В течение последних нескольких лет плазмидные векторы используются в качестве ДНК вакцин для доставки антиген-кодирующих генов в клетки in vivo. Они исключительно подходят для этого, потому что они не вызывают таких же опасений по поводу безопасности как многие из вирусных векторов. Эти плазмиды, однако, имея промотор, совместимый с клеткой-хозяином, могут экспрессировать пептид с гена, функционально закодированного в плазмиде. Некоторые широко используемые плазмиды включают pBR322, pUC18, pUC19, pRC/CMV, SV40 и pBlueScript. Другие плазмиды хорошо известны специалистам в данной области техники. Кроме того, плазмиды могут быть специально сконструированы с использованием рестрикционных ферментов и реакций лигирования для удаления и добавления специфических фрагментов ДНК. Плазмиды могут доставляться с помощью ряда парентеральных, мукозальных и местных способов. Например, ДНК плазмида может быть введена внутримышечным, внутрикожным, подкожным путем или другими путями. Она также может вводиться при помощи интраназальных спреев или капель, ректальных суппозиториев и перорально. Она также может вводиться в эпидермис или поверхность слизистой оболочки при помощи генной пушки. Плазмиды могут предоставляться в водном растворе, могут быть высушены на золотых частицах или предоставляться в сочетании с другой системой доставки ДНК, включая, но не ограничиваясь этим, липосомы, дендримеры, кохлеарные средства доставки и микрокапсулирование.
Антисмысловой олигонуклеотид, siРНК, shРНК или последовательность рибозимной нуклеиновой кислоты согласно изобретению находится обычно под контролем гетерологичного регуляторного элемента, например, гетерологичного промотора. Промотор может быть специфичным в отношении глиальных клеток Мюллера, клеток микроглии, эндотелиальных клеток, перицитов и астроцитов. Например, специфическая экспрессия в глиальных клетках Мюллера может быть получена за счет использования подходящего промотора гена глутамин синтетазы. Промотор также может быть, для примера, вирусным промотором, таким как CMV промотор или какие-либо искусственные промоторы.
Репрессия или разрушение гена Suv39h1
Ингибирование Suv39h1 в клетке согласно изобретению также может осуществляться путем репрессии или разрушения гена Suv39h1, например, делеции, такой как делеция целого гена, экзона или участка и/или замещение экзогенной последовательностью, и/или мутации, например, сдвига рамки считывания или миссенс-мутации в гене, как правило, в экзоне гена. В некоторых вариантах осуществления после введения в ген преждевременного стоп-кодона происходит разрушение, приводящее к тому, что белок Suv39h1 не экспрессируется или является нефункциональным. Разрушение в большинстве случаев осуществляется на уровне ДНК. Разрушение обычно является долговременным, необратимым или не временным.
В некоторых вариантах осуществления разрушение гена или репрессия осуществляется при помощи агентов, редактирующих геном, таких как ДНК-нацеленные молекулы, например, ДНК-связывающий белок или ДНК-связывающая нуклеиновая кислота или комплекс, соединение или композиция, содержащая вышеукзанное, которое специфически связывается или гибридизируется с геном. В некоторых вариантах осуществления нацеленная на ДНК молекула содержит ДНК-связывающий домен, например, ДНК-связывающий домен белка «цинковый палец» (ZFP), ДНК-связывающий домен белка-подобного активатору транскрипции (TAL) или TAL эффектора (TALE), ДНК-связывающий домен CRISPR (короткие палиндромные повторы, регулярно расположенные группами ), или ДНК-связывающий домен мегануклеазы.
Связывающие домены систем «цинкового пальца», TALE и CRISPR могут быть "сконструированы" так, чтобы связываться с предопределенной нуклеотидной последовательностью.
В некоторых вариантах осуществления нацеленная на ДНК молекула, комплекс или комбинация содержит ДНК-связывающую молекулу и один или более дополнительных доменов, таких как эффекторный домен, для оказания содействия репрессии или разрушению гена. Например, в некоторых вариантах осуществления разрушение гена осуществляется гибридными белками, которые содержат ДНК-связывающие белки и гетерологичный регулятороный домен или его функциональный фрагмент.
В большинстве случав дополнительным доменом является нуклеазный домен. Таким образом, в некоторых вариантах осуществления разрушение гена осуществляется при помощи редактирования гена или генома с использованием сконструированных белков, таких как нуклеазы и нуклеаз-содержащие комплексы или гибридные белки, состоящие из последовательность-специфических ДНК-связывающих доменов, соединенных с или образующих комплекс с неспецифическими ДНК-расщепляющими молекулами, такими как нуклеазы.
Эти нацеленные химерные нуклеазы или нуклеаз-содержащие комплексы осуществляют точные генетические модификации, индуцируя целевые двухцепочечные разрывы или одноцепочечные разрывы, стимулирующие механизмы клеточной репарации ДНК, включая способствующее ошибкам негомологичное соединение концов (NHEJ) и репарацию, направляемую гомологией (HDR). В некоторых вариантах осуществления нуклеаза представляет собой эндонуклеазу, такую как цинк-пальцевая нуклеаза (ZFN), TALE нуклеаза (TALEN), РНК-управляемая эндонуклеаза (RGEN), такая как CRISPR-ассоциированный (Cas) белок, или мегануклеазу. Такие системы хорошо известны в данной области техники (смотри, например, патент США № 8,697,359; Sander и Joung (2014) Nat. Biotech. 32:347-355; Hale et al. (2009) Cell 139:945-956; Karginov и Hannon (2010) Mol. Cell 37:7; патентные публикации США 2014/0087426 и 2012/0178169; Boch et al. (2011) Nat. Biotech. 29: 135-136; Boch et al. (2009) Science 326: 1509-1512; Moscou и Bogdanove (2009) Science 326: 1501; Weber et al. (2011) PLoS One 6:el9722; Li et al. (2011) Nucl. Acids Res. 39:6315-6325; Zhang et al. (201 1) Nat. Biotech. 29: 149-153; Miller et a/. (2011) Nat. Biotech. 29: 143-148; Lin et al. (2014) Nucl. Acids Res. 42:e47). Подобные генетические стратегии могут использовать системы конститутивной экспрессии или системы индуцибельной экспрессии согласно хорошо известным в данной области техники методам.
ZFP и ZFN; TAL, TALE и TALEN
В некоторых вариантах осуществления -нацеленная на ДНК молекула включает ДНК-связывающий белок, такой как один или более белок «цинковый палец» (ZFP) или белок, подобный активатору транскрипции (TAL), соединенный с эффекторным белком, таким как эндонуклеаза. Примеры включают ZFN, TALE и TALEN. Смотри Lloyd et al., Frontiers in Immunology, 4(221), 1-7 (2013).
В некоторых вариантах осуществления нацеленная на ДНК молекула содержит один или более белков «цинковый палец» (ZFP) или их доменов, которые связываются с ДНК последовательность-специфичным образом. ZFP или его домен является белком или доменом в пределах более крупного белка, который связывается с ДНК последовательность-специфичным образом за счет использования одного или более участков «цинковый палец» аминокислотной последовательности в пределах связывающего домена, структура которого стабилизируется за счет координации с ионом цинка. Как правило, специфичность последовательности ZFP может быть изменена внесением замен аминокислот в четырех положениях (-1, 2, 3 и 6) на распознающей спирали «цинковых пальцев». Таким образом, в некоторых вариантах осуществления ZFP или ZFP-содержащая молекула является молекулой неприродного происхождения, например, является сконструированной для связывания с выбранным сайтом-мишенью. Смотри, например, Beerli et al. (2002) Nature Biotechnol. 20: 135-141; Pabo et al. (2001) Ann. Rev. Biochem. 70:313-340; Isalan et al. (2001) Nature Biotechnol. 19:656-660; Segal et al. (2001) Curr. Opin. Biotechnol. 12:632-637; Choo et al. (2000) Curr. Opin. Struct. Biol. 10:411-416.
В некоторых вариантах осуществления нацеленная на ДНК молекула представляет собой или содержит ДНК-связывающий домен «цинкового пальца», соединенный с ДНК-ращепляющим доменом, с образованием цинк-пальцевой нуклеазы (ZFN). В некоторых вариантах осуществления гибридные белки содержат домен расщепления (или домен полурасщепления), по меньшей мере, из одного рестрикционного фермента типа IIS и один или более цинк-пальцевых связывающих доменов, которые могут быть или могут не быть сконструированными. В некоторых вариантах осуществления домен расщепления происходит из рестрикционной эндонуклеазы Fok I типа IIS. Смотри, например, патенты США № 5,356,802; 5,436,150 и 5,487,994; а также Li et al. (1992) Proc. Natl. Acad. Sci. USA 89:4275-4279; Li et al. (1993) Proc. Natl. Acad. Sci. USA 90:2764-2768; Kim et al. (1994a) Proc. Natl. Acad. Sci. USA 91:883-887; Kim et al. (1994b) J. Biol. Chem. 269:31,978-31,982.
В некоторых аспектах ZFN эффективно вызывает двухцепочечный разрыв (DSB), например, в заранее определенном месте в кодирующей области целевого гена (т.е. Suv39h1). Типичные целевые области гена включают экзоны, области, кодирующие N-концевые участки, первый экзон, второй экзон и области промотора или энхансера. В некоторых вариантах осуществления временная экспрессия ZFN способствует высокоэффективному и долговременному разрушению целевого гена в сконструированных клетках. В частности, в некоторых вариантах осуществления доставка ZFN приводит к долговременному разрушению гена с эффективностью, превышающей 50%. Многие ген-специфичные «цинковые пальцы» являются коммерчески доступными. Например, компания Sangamo Biosciences (Ричмонд, Калифорния, США) разработала платформу (CompoZr) для конструирования «цинковых пальцев» в партнерстве с Sigma-Aldrich (Сент-Луис, Миссури, США), предоставив исследователям возможность в целом избежать разработки и валидации «цинковых пальцев» и предоставив специфически нацеленные «цинковые пальцы» для тысяч белков. Gaj et al., Trends in Biotechnology, 2013, 31(7), 397-405. В некоторых вариантах осуществления используются коммерчески доступные «цинковые пальцы», являющиеся индивидуальной разработкой. (Смотри, например, каталожные номера Sigma-Aldrich CSTZFND, CSTZFN, CTI1-1KT и PZD0020).
В некоторых вариантах осуществления нацеленная на ДНК молекула содержит природный или сконструированный (неприродного происхождения) ДНК-связывающий домен белка, подобного активатору транскрипции (TAL), такой как в белке-эффекторе, подобном активатору транскрипции (TALE), смотри, например, патентную публикацию США № 20110301073. В некоторых вариантах осуществления молекула является ДНК-связывающей эндонуклеазой, такой как TALE-нуклеаза (TALEN). В некоторых аспектах TALEN является гибридным белком, содержащим ДНК-связывающий домен, происходящий от TALE и нуклеазный каталитический домен для расщепления целевой нуклеиновокислотной последовательности. В некоторых вариантах осуществления TALE ДНК-связывающий домен сконструирован для связывания с целевой последовательностью в пределах гена, кодирующего антиген-мишень и/или иммуносупрессорную молекулу. Например, в некоторых аспектах TALE ДНК-связывающий домен может нацеливаться на CD38 и/или аденозиновый рецептор, такой как A2AR.
В некоторых вариантах осуществления TALEN распознает и расщепляет целевую последовательность в гене. В некоторых аспектах расщепление ДНК приводит к двухцепочечным разрывам. В некоторых аспектах разрывы стимулируют скорость гомологичной рекомбинации или негомологичного соединения концов (NHEJ). В целом, NHEJ является неполноценным процессом репарации, который часто приводит к изменениям в последовательности ДНК в месте расщепления. В некоторых аспектах механизмы репарации вовлекают соединение двух оставшихся концов ДНК посредством прямого повторного лигирования (Critchlow и Jackson, Trends Biochem Sci. 1998 Oct;23(10):394-8) или посредством, так называемого соединения концов, опосредованного микрогомологией. В некоторых вариантах осуществления репарация посредством NHEJ приводит к небольшим инсерциям или делециям и может использоваться для разрушения гена и, тем самым, репрессии гена. В некоторых вариантах осуществления модификация может быть заменой, делецией или инсерцией, по меньшей мере, одного нуклеотида. В некоторых аспектах клетки, в которых происходит случай мутагенеза, индуцированный расщеплением, т.е. случай мутагенеза следует за NHEJ-событием, можно идентифицировать и/или отобрать с помощью хорошо известных в данной области техники методов.
TALE повторы можно собрать, чтобы специфически нацеливаться на ген Suv39h1. (Gaj et al., Trends in Biotechnology, 2013, 31(7), 397-405). Создана библиотека TALEN, нацеленных на 18740 генов, кодирующих человеческие белки (Kim et al., Nature Biotechnology. 31, 251-258 (2013)). Наборы TALE, сконструированных по специальному заказу, коммерчески доступны от компаний Cellectis Bioresearch (Париж, Франция), Transposagen Biopharmaceuticals (Лексингтон, Кентукки, США) и Life Technologies (Гранд-Айленд, Нью-Йорк, США). В частности, TALEN, нацеленные на CD38, коммерчески доступны (смотри Gencopoeia, каталожные номера HTN222870-1, HTN222870-2 и HTN222870-3, доступны в интернет-пространстве на сайте www. genecopoeia.com/product/search/detail.php?prt=26&cid=&key=HTN222870). Типичные молекулы описаны, например, в патентных публикациях США № US 2014/0120622 и 2013/0315884.
В некоторых вариантах осуществления TALEN вводятся как трансгены, кодированные одним или более плазмидными векторами. В некоторых аспектах плазмидный вектор может содержать селективный маркер, обеспечивающий идентификацию и/или селекцию клеток, которые получили указанный вектор.
RGEN (CRISPR/Cas системы)
Репрессия гена может осуществляться при помощи одной или более ДНК-связывающих нуклеиновых кислот, например, разрушение с помощью РНК-направляемой эндонуклеазы (RGEN) или другой вид разрушения при помощи другой РНК-направляемой эффекторной молекулы. Например, в некоторых вариантах осуществления репрессия гена может осуществляться при помощи CRISPR (короткие полиндромные повторы, регулярно расположенные группами ) и CRISPR-ассоциированных белков. Смотри Sander and Joung, Nature Biotechnology, 32(4): 347-355.
В общем, "CRISPR система" в совокупности имеет отношение к транскриптам и другим элементам, вовлеченным в экспрессию или управление активностью CRISPR- ассоциированных ("Cas") генов, включающих последовательности, кодирующие Cas ген, tracr (транс-активирующая CRISPR) последовательность (например, tracrRNA или активная неполная tracrRNA), tracr-mate последовательность (включающую "прямой повтор" и tracrRNA-процессированный неполный прямой повтор применительно к эндогенной CRISPR системе), направляющую последовательность (также называемую "спейсер" применительно к эндогенной CRISPR системе) и/или другие последовательности и транскипты из CRISPR локуса.
Как правило, CRISPR/Cas нуклеаза или CRISPR/Cas нуклеазная система включает некодирующую РНК молекулу (направляющую) РНК, которая последовательность-специфически связывается с ДНК, и CRISPR белок с нуклеазной функциональностью (например, два нуклеазных домена). Один или более элементов CRISPR системы может происходить из типа I, типа II или типа III CRISPR системы, такой как Cas нуклеаза. Предпочтительно, CRISPR белок является cas ферментом, таким как сas9. Cas ферменты хорошо известны в данной области; например, аминокислотную последовательность белка Cas9 из S. pyogenes можно найти в базе данных SwissProt под учетным номером Q99ZW2. В некоторых вариантах осуществления Cas нуклеаза и gRNA вводятся в клетку. В некоторых вариантах осуществления CRISPR система индуцирует DSB в сайте-мишени, с последующими разрывами, как обсуждалось в этом документе. В других вариантах осуществления Cas9 варианты, считающиеся "никазами", могут использоваться, чтобы разрезать одну цепь в сайте-мишени. Спаренные никазы также могут использоваться, например, с целью улучшения специфичности, при этом каждая управляется парой разных gRNA нацеливающих последовательностей. В следующих вариантах осуществления каталитически неактивная Cas9 может быть соединена с гетерологичным эффекторным доменом, таким как транскрипционный репрессор, чтобы влиять на экспрессию гена.
В общем, CRISPR система характеризуется элементами, которые способствуют формированию CRISPR комплекса в месте целевой последовательности. Как правило, в контексте формирования CRISPR комплекса "целевая последовательность" в большинстве случаев относится к последовательности, к которой комплементарна создаваемая направляющая последовательность, где гибридизация между целевой последовательностью и направляющей последовательностью способствует формированию CRISPR комплекса. Полная комплементарность не является обязательной, в том случае, если существует достаточная комплементарность, чтобы вызвать гибридизацию и способствовать формированию CRISPR комплекса. Целевая последовательность может содержать любой полинуклеотид, такой как ДНК или РНК полинуклеотиды. В частности, последовательность или матрица, которая может использоваться для рекомбинации в целевом локусе, содержащем целевые последовательности, называется "матрица редактирования" или "полинуклеотид редактирования" или " последовательность редактирования". В некоторых аспектах экзогенная полинуклеотидная матрица может называться матрицей редактирования. В некоторых аспектах рекомбинация является гомологичной рекомбинацией.
В некоторых вариантах осуществления один или более векторов, управляющих экспрессией одного или нескольких элементов CRISPR системы, вводятся в клетку таким образом, чтобы экспрессия элементов CRISPR системы управляла формированием CRISPR комплекса в одном или более сайтах-мишенях. Например, фермент Cas, направляющая последовательность связанная с tracr-mate последовательностью, и tracr последовательность, каждая может быть функционально связана с отдельными регуляторными элементами на разных векторах. Альтернативно, два или более элементов, экспрессированных с одного и того же или с разных регуляторных элементов, могут объединяться в одном векторе, где один или более дополнительных векторов обеспечивают любые компоненты CRISPR системы, не включенные в первый вектор. В некоторых вариантах осуществления элементы системы CRISPR, которые объединяются в одном векторе, могут располагаться в любой подходящей ориентации. В некоторых вариантах осуществления фермент CRISPR, направляющая последовательность, tracr mate последовательность и tracr последовательность являются функционально связанными с промотором и экспрессируются с одного и того же промотора. В некоторых вариантах осуществления вектор содержит регуляторный элемент, функционально связанный с кодирующей фермент последовательностью, кодирующей CRISPR фермент, такой как Cas белок.
В некоторых вариантах осуществления CRISPR фермент доставляется в клетку в комбинации с направляющей последовательностью (и необязательно образует с ней комплекс). В большинстве случаев CRISPR/Cas9 технология может использоваться для нокдауна экспрессии гена Suv39h1 в сконструированных клетках. Например, нуклеаза Cas9 и направляющая РНК, специфическая к Suv39h1 гену, могут вводиться в клетки, например, при помощи лентивирусных векторов доставки или с помощью любого из ряда известных способов доставки или носителей для переноса в клетки, такого как любой из целого ряда известных методов или носителей для доставки Cas9 молекул и направляющих РНК (также смотри ниже).
Доставка нуклеиновых кислот, кодирующих молекулы и комплексы, разрушающие ген.
В некоторых вариантах осуществления нуклеиновая кислота, кодирующая нацеленную на ДНК молекулу, комплекс или комбинацию, вводится или интродуцируется в клетку. Как правило, методы переноса гена на вирусной или невирусной основе могут использоваться для введения нуклеиновых кислот, кодирующих компоненты CRISPR, ZFP, ZFN, TALE и/или TALEN системы, в клетки в культуре.
В некоторых вариантах осуществления полипептиды синтезируются in situ в клетке в результате введения в клетку полинуклеотидов, кодирующих полипептиды. В некоторых аспектах полипептиды могут продуцироваться вне клетки и затем вводиться в нее.
Способы введения полинуклеотидной конструкции в животные клетки хорошо известны и включают, в качестве неограничивающих примеров, методы стабильной трансформации, согласно которым полинуклеотидная конструкция интегрируется в геном клетки, методы транзиентной трансформации, согласно которым полинуклеотидная конструкция не интегрируется в геном клетки, и способы, опосредованные вирусом.
В некоторых вариантах осуществления полинуклеотиды могут быть введены в клетку, например, при помощи рекомбинантных вирусных векторов (например, ретровирусов, аденовирусов), липосом и тому подобного. Методы транзиентной трансформации включают микроинъекцию, электропорацию или бомбардировку частицами. Нуклеиновая кислота вводится в форме вектора экспрессии. Предпочтительно, вектор экспрессии является ретровирусным вектором экспрессии, аденовирусным вектором экспрессии, ДНК плазмидным вектором экспрессии или AAV вектором экспрессии.
Методы невирусной доставки нуклеиновых кислот включают липофекцию, нуклеофекцию, микроинъекцию, биолистику, виросомы, липосомы, иммунолипосомы, конъюгаты поликатион или липид:нуклеиновая кислота, «оголенную» ДНКзахват поглощение ДНК. Липофекция описана, например, в патентах США № 5,049,386, 4,946,787 и 4,897,355) и реагенты для липофекции доступны в продаже (например, Transfectam™ и Lipofectin™). Катионные и нейтральные липиды, подходящие для эффективной рецептор-распознающей липофекции полинуклеотидов, включают те, которые упомянуты в Feigner, WO 91/17424; WO 91/16024. Доставка может происходить в клетки (например, in vitro или ex vivo введение) или ткани-мишени (например, in vivo введение).
Системы для переноса генов на основе РНК или ДНК вирусов включают ретровирусные, лентивирусные, аденовирусные векторы, векторы на основе аденоассоциированного и вирусов herpes simplex.
Обзор методов генной терапии смотри в Anderson, Science 256:808-813 (1992); Nabel & Feigner, TIBTECH 11:211-217 (1993); Mitani & Caskey, TIBTECH 11: 162-166 (1993); Dillon. TIBTECH 11: 167-175 (1993); Miller, Nature 357:455-460 (1992); Van Brunt, Biotechnology 6(10): 1149-1154 (1988); Vigne, Restorative Neurology и Neuroscience 8:35-36 (1995); Kremer & Perricaudet, British Medical Bulletin 51(1):31-44 (1995); Haddada et al., in Current Topics in Microbiology и Immunology Doerfler и Bohm (eds) (1995); и Yu et al., Gene Therapy 1: 13-26 (1994).
Ген-репортер, включающий, но без ограничения, глутатион-5-трансферазу (GST), пероксидазу хрена (HRP), хлорамфениколацетилтрансферазу (CAT), бета-галактозидазу, бета-глюкуронидазу, люциферазу, зеленый флуоресцентный белок (GFP), HcRed, DsRed, голубой флуоресцентный белок (CFP), желтый флуоресцентный белок (YFP) и автофлуоресцирующие белки, включая синий флуоресцентный белок (BFP), может быть «введен» в клетку, чтобы кодировать продукт гена, который служит маркером, с помощью которого можно измерить изменение или модификацию экспрессии продукта гена.
Получение клеток
Выделение клеток включает одну или более стадий получения и/или не основанных на аффинности стадий отделения согласно хорошо известным в данной области техники методам. В некоторых примерах клетки промывают, центрифугируют и/или инкубируют в присутствии одного или более реагентов, например, для удаления нежелательных компонентов, обогащения желательных компонентов, лизиса или удаления клеток, восприимчивых к отдельным реагентам. В некоторых примерах клетки разделяют, исходя из одного или более свойств, таких как плотность, свойство адгезивности, размер, чувствительность и/или резистентность к определенным компонентам.
В некоторых вариантах осуществления получение клеток включает стадии замораживания, например, криосохранение, клеток или до или после выделения, инкубации и/или конструирования. В определенных аспектах может использоваться любой из целого ряда известных растворов для замораживания и параметров замораживания.
В большинстве случаев клетки инкубируют до или на фоне генетической инженерии и/или ингибирования Suv39h1.
Стадии инкубации могут включать культивирование, инкубацию, стимулирование, активацию, экспансию и/или размножение.
Ингибирование Suv39h1 согласно изобретению также может достигаться in vivo после инъекции клеток намеченным пациентам. В большинстве случаев ингибирование suv39h1 осуществляется с использованием фармакологических ингибиторов, как было описано ранее.
Ингибирование Suv39h1 согласно описанному ранее методу также может осуществляться в течение стадий стимуляции, активации и/или экспансии. Например, PBMC, или очищенные T-клетки, или очищенные NK-клетки, или очищенные лимфоидные предшественники размножаются in vitro в присутствии фармакологических ингибиторов Suv39h1 до адоптивного переноса пациентам. В некоторых вариантах осуществления композиции или клетки инкубируют в присутствии стимулирующих условий или стимулирующего агента. Такие условия включают условия, созданные для того, чтобы вызвать пролиферацию, экспансию, активацию и/или выживаемость клеток в популяции, чтобы имитировать антигенную стимуляцию и/или подготовить клетки для генной инженерии, такой как введение генетически сконструированного антигенного рецептора.
Условия инкубации могут включать одно или более из числа определенных сред, температуры, содержания кислорода, содержания диоксида углерода, времени, веществ, например, питательных веществ, аминокислот, антибиотиков, ионов и/или стимулирующих факторов, таких как цитокины, хемокины, антигены, партнеры по связыванию, гибридные белки, рекомбинантные растворимые рецепторы и любые другие средства, созданные для активирования клеток.
В некоторых вариантах осуществления стимулирующие условия или агенты включают один или более агентов, например, лиганд, который способен активировать внутриклеточный сигнальный домен TCR комплекса. В некоторых аспектах агент «включает» или инициирует TCR/CD3 внутриклеточный сигнальный каскад в T-клетке. Такие агенты могут включать антитела, такие как антитела, специфические к TCR компоненту и/или костимулирующему рецептору, например, анти-CD3, анти-CD28, например, связанные с твердой подложкой, такой как гранула, и/или один или более цитокинов. Необязательно, метод экспансии может дополнительно включать стадию добавления анти-CD3 и/или анти-CD28 антитела в культуральную среду (например, в концентрации, по меньшей мере, около 0,5 нг/мл). В некоторых вариантах осуществления стимулирующий агент включает IL-2 и/или IL-15, например, при концентрации IL-2, по меньшей мере, около 10 единиц/мл.
В некоторых аспектах инкубация проводится в соответствии с методиками, описанными в патенте США № 6,040,1 77 Riddell et al., Klebanoff et al., J Immunother. 2012; 35(9): 651-660, Terakura et al., Blood. 2012; 1:72-82, и/или Wang et al. J Immunother. 2012,35(9):689-701.
В некоторых вариантах осуществления T-клетки выращивают, добавляя в культуру инициирующие питающие клетки, такие как неделящиеся мононуклеарные клетки периферической крови (PBMC), (например, так, что получающаяся в результате популяция клеток содержит, по меньшей мере, около 5, 10, 20, или 40 или более PBMC питающих клеток для каждого T-лимфоцита в первоначальной популяции, которая должна быть увеличена); и инкубируя культуру (например, в течение времени, достаточного для увеличения количества T-клеток). В некоторых аспектах неделящиеся питающие клетки могут содержать гамма-облученные PBMC питающие клетки. В некоторых вариантах осуществления PBMC облучают гамма-лучами в интервале примерно 3000 до 3600 рад, чтобы предотвратить деление клеток. В некоторых аспектах питающие клетки добавляют в культуральную среду до внесения популяций T-клеток.
В некоторых вариантах осуществления стимулирущие условия включают температуру, подходящую для роста человеческих T-лимфоцитов, например, по меньшей мере, около 25 градусов Цельсия, как правило, по меньшей мере, около 30 градусов и в основном при или около 37 градусов Цельсия. Необязательно, инкубация может дополнительно включать добавление неделящихся EBV-трансформированных лимфобластоидных клеток (LCL) в качестве питающих клеток. LCL могут быть облучены гамма-лучами в пределах примерно от 6000 до 10,000 рад. LCL питающие клетки в некоторых аспектах предоставляются в любом подходящем количестве, так что отношение LCL питающих клеток к исходным T-лимфоцитам составляет, по меньшей мере, около 10: 1.
В других вариантах осуществления антиген-специфические Т-клетки, такие как антиген-специфические CD4+ и/или CD8+ T-клетки, получают путем стимулирования наивных или антиген-специфических T-лимфоцитов антигеном. Например, линии или клоны антиген-специфических Т-клеток к антигенам цитомегаловируса можно получить путем изолирования T-клеток от инфицированных субъектов и стимулирования клеток in vitro тем же самым антигеном.
В некоторых аспектах способы включают оценку экспрессии одного или более маркеров на поверхности сконструированной клетки или конструируемой клетки. В одном варианте осуществления способы включают оценку поверхностной экспрессии одного или более целевых антигенов (например, антигена, распознаваемого генетически сконструированным антигенным рецептором), на которые должна быть нацелена адоптивная клеточная терапия, например, при помощи методов обнаружения на основе аффинности, таких как проточная цитометрия.
Векторы и способы для генетической инженерии клетки
В некоторых аспектах генетическая инженерия включает введение нуклеиновой кислоты, кодирующей генетически сконструированный компонент или другой компонент для введения в клетку, такой как компонент, кодирующий разрушающие ген белок или нуклеиновую кислоту.
В общем, для конструирования CAR в иммунных клетках (например, T-клетках) необходимо культивирование клеток, чтобы сделать возможными трансдукцию и экспансию. Для трансдукции может использоваться целый ряд методов, однако требуется устойчивый перенос генов, чтобы обеспечить долговременную экспрессию CAR в растущим посредством клональной экспансии и персистирующих сконструированных клетках.
В некоторых вариантах осуществления перенос гена осуществляется сначала путем стимулирования роста клеток, например, роста T-клеток, пролиферации и/или активации, с последующей трансдукцией активированных клеток и размножением в культуре до количеств, достаточных для клинического применения.
Различные способы введения генетически сконструированных компонентов, например, антигенных рецепторов, например, CAR, хорошо известны и могут использоваться вместе с предоставленными методами и композициями. К типичным способам относятся методы переноса нуклеиновых кислот, кодирующих рецепторы, включая перенос при помощи вирусов, например, ретровирусов или лентивирусов, трансдукцию, транспозоны и электропорацию.
В некоторых вариантах осуществления рекомбинантные нуклеиновые кислоты «переносят» в клетки при помощи рекомбинантных частиц патогенных вирусов, таких как, например, векторы, происходящие от вируса обезьяны 40 (SV40), аденовируса, аденоассоциированного вируса (AAV). В некоторых вариантах осуществления рекомбинантные нуклеиновые кислоты «переносят» в T-клетки при помощи рекомбинантных лентивирусных векторов или ретровирусных векторов, таких как гамма-ретровирусные векторы (смотри, например, Koste et al. (2014) Gene Therapy 2014 Apr 3.; Carlens et al. (2000) Exp Hematol 28(10): 1137-46; Alonso-Camino et al. (2013) Mol Ther Nucl Acids 2, e93; Park et al., Trends Biotechnol. 2011 November; 29(11): 550-557.
В некоторых вариантах осуществления ретровирусный вектор имеет длинный концевой повтор (LTR), например, ретровирусный вектор, производный от вируса мышиного лейкоза Молони (MoMLV), миелопролиферативного вируса саркомы (MPSV), вируса эмбриональных стволовых клеток мышей (MESV), вируса мышиных стволовых клеток (MSCV), вируса некроза селезенки (SFFV) или аденоассоциированного вируса (AAV). Большинство ретровирусных векторов происходит от мышиных ретровирусов. В некоторых вариантах осуществления ретровирусы включают те, которые происходят из какого-либо источника, птичьего или млекопитающих. Ретровирусы в большинстве случаев являются амфотропными, что означает, что они способны инфицировать клетки-хозяина нескольких видов, включая человека. В одном варианте осуществления ген, который должен экспрессироваться, помещают в ретровирусную gag, pol и/или env последовательности. Описан целый ряд иллюстративных ретровирусных систем (например, патенты США № 5,219,740; 6,207,453; 5,219,740; Miller and Rosman (1989) BioTechniques 7:980-990; Miller, A. D. (1990) Human Gene Therapy 1:5-14; Scarpa et al. (1991) Virology 180:849-852; Burns et al. (1993) Proc. Natl. Acad. Sci. USA 90:8033-8037; и Boris-Lawrie и Temin (1993) Cur. Opin. Genet. Develop. 3: 102-109.
Методы лентивирусной трансдукции также хорошо известны. Типичные методы описаны, например, в Wang et al. (2012) J. Immunother. 35(9): 689-701; Cooper et al. (2003) Blood. 101: 1637-1644; Verhoeyen et al. (2009) Methods Mol Biol. 506: 97-114; и Cavalieri et al. (2003) Blood. 102(2): 497-505.
В некоторых вариантах осуществления рекомбинантные нуклеиновые кислоты «переносят» в T-клетки при помощи электропорации (смотри, например, Chicaybam et al, (2013) PLoS ONE 8(3): e60298 и Van Tedeloo et al. (2000) Gene Therapy 7(16): 1431-1437). В некоторых вариантах осуществления рекомбинантные нуклеиновые кислоты «переносят» в T-клетки при помощи транспозиции (смотри, например, Manuri et al. (2010) Hum Gene Ther 21(4): 427-437; Sharma et al. (2013) Molec Ther Nucl Acids 2, e74; и Huang et al. (2009) Methods Mol Biol 506: 115-126). Другие методы внесения и экспрессирования генетического материала в иммунных клетках включают трансфекцию фосфатом кальция (например, как описано в Current Protocols in Molecular Biology, John Wiley & Sons, New York. N.Y.), слияние протопластов, трансфекцию, опосредованную катионными липосомами; бомбардировку микрочастицами вольфрама (Johnston, Nature, 346: 776-777 (1990)); и копреципитацию ДНК фосфатом стронция (Brash et al., Mol. Cell Biol., 7: 2031-2034 (1987)).
Другие подходы и векторы для переноса генетически сконструированных нуклеиновых кислот, кодирующих генетически сконструированные продукты, описаны, например, в международной патентной заявке, публикация № WO2014055668, и патенте США № 7,446,190.
Композиция изобретения
Настоящее изобретение также имеет отношение к композициям, содержащим клетки, описанные в этом документе и/или полученные при помощи предлагаемых способов. В большинстве случаев указанные композиции являются фармацевтическими композициями и составами для введения, например, при адоптивной клеточной терапии.
Фармацевтическая композиция изобретения обычно содержит, по меньшей мере, одну сконструированную иммунную клетку изобретения и фармацевтически приемлемый носитель.
При использовании в описании фраза "фармацевтически приемлемый носитель" включает физраствор, растворители, дисперсионные среды, покрытия, антибактериальные и противогрибковые средства, изотонические средства и вещества, замедляющие абсорбцию, и тому подобное, совместимое с фармацевтическим применением. Кроме того, в состав композиции могут быть введены дополнительные активные соединения. В некоторых аспектах выбор носителя в фармацевтической композиции определяется отчасти определенным сконструированным CAR или TCR, вектором или клетками, экспрессирующими CAR или TCR, а также конкретным способом, используемым для введения вектора или клетки-хозяина, экспрессирующей CAR. Соответственно, существует целый ряд подходящих составов. Например, фармацевтическая композиция может содержать консервирующие вещества. Подходящие консервирующие вещества могут включать, например, метилпарабен, пропилпарабен, бензоат натрия и хлорид бензалкония. В некоторых аспектах используется смесь двух или более консервирующих веществ. Консервирующее вещество или их смесь обычно присутствуют в количестве примерно от 0,0001 до 2% от веса всей композиции.
Фармацевтическая композиция составляется так, чтобы быть совместимой с предполагаемым способом введения.
Терапевтические методы
Настоящее изобретение также имеет отношение к клеткам, как определено ранее, и их использованию в адоптивной терапии (а именно, адоптивной T-клеточной терапии), обычно при лечении рака у субъекта, нуждающегося в этом.
«Лечение" при использовании в описании определяется как применение или введение клеток согласно изобретению или композиции, содержащей клетки, пациенту, нуждающемуся в этом, с целью исправления, излечивания, облегчения, снятия, преобразования, изменения, устранения, улучшения или воздействия на болезнь, такую как рак, или любой симптом болезни (например, рака). В частности, термины "лечить" или "лечение" имеет отношение к уменьшению или облегчению, по меньшей мере, одного неблагоприятного клинического симптома, связанного с болезнью, такой как рак, например, боли, отечности, низкого содержания форменных элементов крови и т.д.
В отношении лечения рака термин "лечить" или "лечение" также имеет отношение к замедлению или устранению неконтролируемого размножения неоплатических клеток, т.е. сокращению в объеме существующих опухолей и/или остановке роста опухоли. Термин "лечить" или "лечение" также имеет отношение к индукции апоптоза в раковых или опухолевых клетках у субъекта.
Субъектом изобретения (т.е. пациентом) является млекопитающее, в большинстве случаев примат, например, человек. В некоторых вариантах осуществления примат представляет собой обезьяну или человекообразную обезьяну. Субъект может быть мужчиной или женщиной и может быть любого подходящего возраста, включая детей, подростков, молодых людей, взрослых людей и лиц старческого возраста. В некоторых вариантах осуществления субъект является млекопитающим, не являющимся приматом, например, грызуном. В некоторых примерах пациент или субъект представляет собой валидизированную животную модель болезни для изучения адоптивной клеточной терапии и/или для оценки последствий токсичности, таких как синдром высвобождения цитокинов (CRS). В некоторых вариантах осуществления изобретения у указанного субъекта имеется рак, субъект имеет риск развития рака или субъект находится в состоянии ремиссии рака.
Рак может быть солидным раком или “опухолью жидких тканей”, таким как раки, затрагивающие кровь, костный мозг и лимфоидную систему, также известные как опухоли гематопоэтических и лимфоидных тканей, которые включают в первую очередь лейкоз и лимфому. Опухоли жидких тканей включают, например, острую миелоцитарную лейкемию (AML), хронический миелолейкоз (CML), острый лимфоцитарный лейкоз (ALL) и хронический лимфоцитарный лейкоз (CLL) (включая различные лимфомы, такие как лимфома из клеток мантийной зоны, неходжкинская лимфома (NHL), аденома, плоскоклеточная карцинома, карцинома гортани, карцинома желчного пузыря и желчного протока, раки сетчатки глаза, такие как ретинобластома).
В частности, солидные раки включают виды рака, поражающие один из органов, выбранный из группы, состоящей из толстой кишки, прямой кишки, кожи, эндометрия, легких (включая немелкоклеточную карциному легких), матку, кости (такие как остеосаркома, хондросаркома, саркома Юинга, фибросаркома, гигантоклеточная опухоль, адамантинома и хордома), печени, почки, пищевода, желудка, мочевого пузыря, поджелудочной железы, шейки матки, мозга (такие как менингиома, глиобластома, низкодифференцированная астроцитома, олигодендроцитома, опухоли гипофиза, шваннома и метастатический рак мозга), яичника, молочной железы, области головы и шеи, яичка, предстательной железы и щитовидной железы.
Преимущественно, рак согласно изобретению является раком, поражающим кровь, костный мозг и лимфоидную систему, как описано выше. В большинстве случаев рак является или связан с множественной миеломой.
В некоторых вариантах осуществления субъект страдает от или имеет риск развития инфекционной болезни или состояния, такого как, но без ограничения, вирусные, ретровирусные, бактериальные и протозойные инфекции, иммунодефицитное состояние, цитомегаловирус (CMV), вирус эпштейна-Барр (EBV), аденовирус, BK полиомавирус. В некоторых вариантах осуществления болезнь или состояние является аутоиммунным или воспалительным заболеванием или состоянием, таким как артрит, например, ревматоидный артрит (RA), диабет I типа, системная красная волчанка (SLE), воспалительная болезнь кишечника, псориаз, склеродерма, аутоиммунное заболевание щитовидной железы, заболевание Грейвса, болезнь Крона, множественный склероз, астма и/или болезнь или состояние, связанное с трансплантатом.
Настоящее изобретение имеет отношение к способу лечения и, в частности, к адоптивной клеточной терапии, предпочтительно адоптивной T-клеточной терапии, включающей введение субъекту, нуждающемуся в этом, ранее описанной композиции.
В некоторых вариантах осуществления клетки или композиции вводятся субъекту, например, субъекту, имеющему рак или имеющему риск развития рака или любой другой болезни, как упомянуто выше. В некоторых аспектах данные способы тем самым лечат, например, способствуют улучшению одного или более симптомов болезни или состояния, например, применительно к раку, путем уменьшения массы опухоли, экспрессирующей антиген, распознаваемый сконструированной клеткой.
Способы введения клеток для адоптивной клеточной терапии известны и могут использоваться вместе с предоставленными способами и композициями. Способы адоптивной T-клеточной терапии описаны, например, в опубликованной патентной заявке США № 2003/0170238 Gruenberg et al; патенте США № 4,690,915 Rosenberg; Rosenberg (2011) Nat Rev Clin Oncol. 8(10):577-85). Смотри, например, Themeli et al. (2013) Nat Biotechnol. 31(10): 928-933; Tsukahara et al. (2013) Biochem Biophys Res Commun 438(1): 84-9; Davila et al. (2013) PLoS ONE 8(4): e61338.
В некоторых вариантах осуществления клеточная терапия, например, адоптивная клеточная терапия, например, адоптивная Т-клеточная терапия, осуществляется при помощи аутологичного переноса, при котором клетки изолируют и/или подготавливают иным способом от субъекта, который предназначается для получения клеточной терапии, или из образца, полученного от такого субъекта. Таким образом, в некоторых аспектах клетки получают от субъекта, например, пациента, нуждающегося в лечении, и клетки, после изолирования и обработки вводятся тому же самому субъекту.
В некоторых вариантах осуществления клеточная терапия, например, адоптивная клеточная терапия, например, адоптивная Т-клеточная терапия, осуществляется посредством аллогенного переноса, при котором клетки выделяют и/или иным способом получают от субъекта, который не является субъектом, который должен получить или который в конечном итоге получает клеточную терапию, например, первый субъект. В таких вариантах осуществления клетки затем вводятся другому субъекту, например, второму субъекту, того же самого вида. В некоторых вариантах осуществления первый и второй субъекты являются генетически идентичными. В некоторых вариантах осуществления первый и второй субъекты являются генетически сходными. В некоторых вариантах осуществления второй субъект экспрессирует тот же самый HLA класс или супертип, как и первый субъект.
Введение, по меньшей мере, одной клетки согласно изобретению субъекту, нуждающемуся в этом, может объединяться с одним или более дополнительными терапевтическими средствами или применяться на фоне другого терапевтического воздействия, или одновременно или последовательно в любом порядке. В некоторых ситуациях клетки вводятся совместно с другим видом лечения достаточно близко по времени, так что клеточные популяции усиливают действие одного или более дополнительных терапевтических средств, или наоборот. В некоторых вариантах осуществления клеточные популяции вводятся перед введением одного или более дополнительных терапевтических средств. В некоторых вариантах осуществления клеточные популяции вводятся после одного или более дополнительных терапевтических средств.
Применительно к лечению рака, комбинированное лечение рака может включать, но не ограничивается этим, химиотерапевтические средства, гормоны, анти-ангиогенные средства, радиомеченые соединения, иммунотерапию, хирургическое вмешательство, криотерапию и/или лучевую терапию.
Иммунотерапия включает, но не ограничивается этим, модуляторы иммунных контрольных точек (т.е. ингибиторы и/или агонисты), моноклональные антитела, противораковые вакцины.
Предпочтительно, введение клетки при адоптивной T-клеточной терапии согласно изобретению объединяется с введением модуляторов иммунных контрольных точек. Наиболее предпочтительно, модуляторы иммунных контрольных точек содержат анти-PD-1 и/или анти-PDL-1 ингибиторы.
Настоящее изобретение также имеет отношение к применению композиции, содержащей сконструированную иммунную клетку, описанную в этом документе, для производства медикамента, предназначенного для лечения рака, инфекционной болезни или состояния, аутоиммунной болезни или состояния, или воспалительной болезни или состояния у субъекта.
Подписи к фигурам
Фигура 1: Количество CD8+ T-клеток центральной памяти увеличивается у Suv39h1-дефицитных мышей. A. Характерные FACS-диаграммы гейтированных CD8+ T-клеток селезенки. B. Процент CD8+ T-клеток центральной памяти был измерен в разных гематопоэтических компартментах (черные кружки, Suv39h1 KO; белые кружки: однопометники дикого типа).
Фигура 2: Характеристика стволовости и памяти в эндогенных антиген-специфических Suv39h1 KO CD8+ T-клетках. Suv39h1-дефицитные Kb-OVA+ CD8+ T-клетки имеют профиль генной экспрессии, подобный стволовым клеткам и клеткам памяти. Показан анализ обогащения групп генов (GSEA).
Фигура 3: Повышенная выживаемость и самообновление Suv39h1 дефицитных CD8T клеток. A. Постановка эксперимента, демонстрирующая перенос конгенных CD45.2 Kb-OVA пентамеров+ CD8+ T-клеток, изолированных от WT и Suv39h1 KO LM-OVA инфицированных мышей, наивным CD45.1 мышам-реципиентам (1: сортировка субпопуляций CD8+ T и перенос (D0); 2: анализ самообновления и дифференцировки (D40-44). Через 40 дней после адоптивного переноса наивных мышей-реципиентов заражали LM-OVA, а через 4 дня после этого Kb-OVA пентамеры+ CD8+ T-клетки анализировали с помощью FACS. B. Показаны характерные FACS-диаграммы донорных и реципиентных CD8+ T-клеток. C. Было измерено общее количество восстановленных CD8+ T-клеток. Результаты объединяют данные, полученные из двух независимых экспериментов.
Фиг. 4: Suv39h1 дефицитные CD8+ OT-1 клетки контролируют рост опухоли. (A) Обработанные IL-2/OVA Suv39h1-KO CD45.2 OT-1 и клетки дикого типа из однопометников WT «перенесли» i.v. мыши-реципиенту с опухолью через 7 дней после инокуляции и вводили внутрибрюшинно анти-PD-1 антитело (Bio X Cell, RMP-14). Кривые роста опухоли у обработанных IL-2/OVA однопометников WT (B) и Suv39h1-KO OT-1 клетками (C), адоптивно «перенесенными» реципиентной мыши-опухоленосителю.
Результаты
Материалы и методы:
Мышей одного помета и Suv39h1 -KO мышей инфицировали i.v. 5x103 CFU и через 40 дней заражали 2x106 CFU рекомбинантной Listeria monocytogenes, экспрессирующей OVA (LM-OVA, происходящий от штамма дикого типа 140403s). Бактерии выращивали в TSB среде (BD Bioscience) до ранней логарифмической фазы и их рост оценивали с помощью фотометра при OD600. Наивные, dump- CD44high Kb-OVA+ CD8+ T-клетки и родственные субпопуляции сортировали с помощью FACS. Для анализа каждой субпопуляции мы получали 3 или 4 биологических повтора. РНК экстрагировали, используя набор Rneasy Micro Kit (QUIGEN) в соответствии с протоколом производителя. Была включена обработка ДНКазой на колонке (QUIGEN). Для каждого режима использовали РНК, чтобы синтезировать кДНК согласно стандартному аффиметрическому протоколу. Меченую ДНК гибридизировали на Affymetrix mouse Gene 2.1 ST, и обрабатывали на приборе Affymetrix GeneTitan.
Результаты микроматричного анализа:
Данные микроматричного анализа были обработаны в R (версия 3.0.0) с использованием пакета от Bioconductor. Использовали файлы с исходной информацией CEL, и анализ контроля качества проводили при помощи пакета ArrayQualityMetrics. Первичные данные предварительно обрабатывали с использованием RMA метода, доступного в пакете oligo. Пробы без маркировки были удалены из анализа. Умеренные t-критерии определяли при помощи пакета limma, и p-значения корректировали при помощи многократного тестирования с помощью метода Бенджамини-Хохберга. Наконец, мы считали значение статистически значимым, если скорректированное p-значение составляло меньше чем 5%.
Анализ обогащенности групп генов. Анализ обогащенности групп генов (GSEA) осуществили с использованием гена с иммунологическими показателями (C7) и C2 (рекомендованный) из набора генов из базы данных Molecular Signatures DataBase (MSigDB база данных v5.1, http://software.broadinstitute.org/gsea/msigdb/index.jsp). GMT файл был загружен вместе с информацией о символах генов. GCT файл состоял всего из 41345 проб и был импортирован в GSEA. GSEA проходил с использованием стандартных параметров, за исключением нескольких перестановок (n = 10000). BubbleGUM анализ был выполнен, как описывалось ранее.
Анализ роста опухоли с Suv39h1 дефицитными CD8+ OT-1 клетками проводили, как описано далее:
Целую селезенку и лимфатический узел от самца Suv39h1-KO CD45.2 OT-1 (специфичный для OVA257-264 пептида SIINFEKL в контексте H2-Kb MHC класс I) и мышей одного помета дикого типа культивировали в полной среде (RPMI 1640 с добавлением 10% FBS, пенициллин-стрептомицина и L-глутамина) в течение 3 дней и затем активировали с использованием 100UI/мл IL-2 и 1 мкг/мл OVA257-264 пептида в течение еще 3 дней.
С целью инокуляции опухоли 1x106 клеток лимфомы EL4-OVA инъецировали подкожно в правый бок самца мыши CD45.1/C57BL/6 и через 7 дней мышам вводили i.v. 2x106 IL-2/OVA, обработанных Suv39h1-KO CD45.2 OT-1, или клетки дикого типа от однопометного животного.
Мышам внутрибрюшинно вводили анти-PD1 (Bio X Cell, RMP-14) в дозе 7,5мг/кг веса тела два раза в неделю в течение 2 недель. Рост опухоли измеряли с помощью штангенциркуля.
Результаты:
1) Наши результаты показали, что в клеточной популяции, полученной от Suv39h1-KO мышей, ранние предшественники с “подобным стволовой клетке” фенотипом накапливаются и перепрограммируются с повышенной эффективностью в долгоживущие T-клетки центральной памяти, экспрессирующие и CD44 и CD62L, по сравнению с клеточной популяцией, полученной от мышей дикого типа. Как проиллюстрировано на Фигуре 1, пропорция и количество T-клеток центральной памяти (экспрессирующих как CD44, так и CD62L) увеличены у Suv39h1-дефектных мышей.
2) Для того, чтобы понять механизм этого особого фенотипа, использовали транскриптомный анализ:
Мышей дикого типа и мышей, дефицитных по Suv39h1, иммунизировали при помощи OVA-экспрессирующих Listeria m., и OVA-специфические T-клетки изолировали на 7 День после иммунизации, используя сортировку при помощи проточной цитометрии.
После аффиметрического анализа клеток мы обнаружили, что эффекторные T-клетки из Suv39h1 экспрессируют более высокие уровни мРНК, кодирующих белки, имеющие отношение к стволовым клеткам (профиль, подобный стволовой клетке памяти CD8+ T (86 генов): Abcb1a Irf8 Rest Abcb1b Jarid2 Rif1 Alpl Kat6a Rnf138 Antxr2 Klf4 Rras Arl4c Ldha Sall4 Atr Ldhb Satb1 Baalc Ldhc Setbp1 Basp1 Ldhd Setdb1 Bcl6 Lect1 Skil Bub1 Lpin1 Smarcad1 Ccr7 Ly6a Sox2 Ccr9 Ly6e Spon1 Cd27 Map3k8 Stat3 Cxcr6 Mapk12 Tbx3 Dock9 Mcm3ap Tcf3 Dusp9 Mcoln2 Tcl1 Eomes Myc Tdgf1 Esrrb Nanog Tert Evl Ncor2 Tigit Fas Nr0b1 Tnfaip2 Fgf2 Nr1d2 Tnfrsf1b Fut4 P2ry14 Traf1 Gzmk Pax6 Traf4 Hand1 Pcgf2 Trib2 Hesx1 Plekha5 Txnip Ier3 Podxl Zfp42 Il2rb Pou5f1 Zfx Il7r Pou6f1 Zic3 Irf4 Prkce).
Мы сделали вывод, что OVA-специфические T-клетки из Suv39h1-дефицитных мышей, стимулированных после инфицирования Listeria m., экспрессируют профиль мРНК, подобный “стволовой клетке”.
3) CD8+ T клетки, дефицитные по Suv39h1, демонстрируют повышенную выживаемость и самообновление in vivo.
Конгенные CD45.2 Kb-OVA пентамеры+ CD8+ T клетки, изолированные из мышей WT и мышей, инфицированных Suv39h1 KO LM-OVA, были перенесены наивным мышам-реципиентам CD45.1. Через 40 дней после адоптивного переноса наивных мышей-реципиентов стимулировали LM-OVA, и через 4 дня Kb-OVA пентамеры+ CD8+ T клетки анализировали при помощи FACS.
Результаты продемонстрировали (Фигура 3), что Suv39h1-дефицитная клетка экспрессирует повышенные уровни “подобного стволовой клетке” профиля. Они также лучше выживают и более эффективно восстанавливают популяцию у мышей дикого типа после адоптивного переноса.
4) CD8+ OT-1 клетки, дефицитные по Suv39h1, контролируют рост опухоли in vivo
Фигуры 4 B и C показывают, что у мышей с адоптивно перенесенными Suv39h1-KO OT-1 клетками и обработанных анти-PD1 моноклональным антителом рост опухоли контролировался лучше, чем у мышей, получивших сходное лечение, но с использованием WT OT-1 клеток. Следует отметить, на 30 день после инъекции опухоли у 4 из 5 мышей с перенесенным WT OT-1 был отмечен рост опухоли, по сравнению только с 1 из 5 мышей, которым вводили Suv39h1-KO OT-1 клетки.
Заключение
Отсутствие Suv39h1 активности в CD8+ T-клетках связано с улучшенной противоопухолевой эффективностью терапевтического подхода на основе адоптивного Т-клеточного переноса.

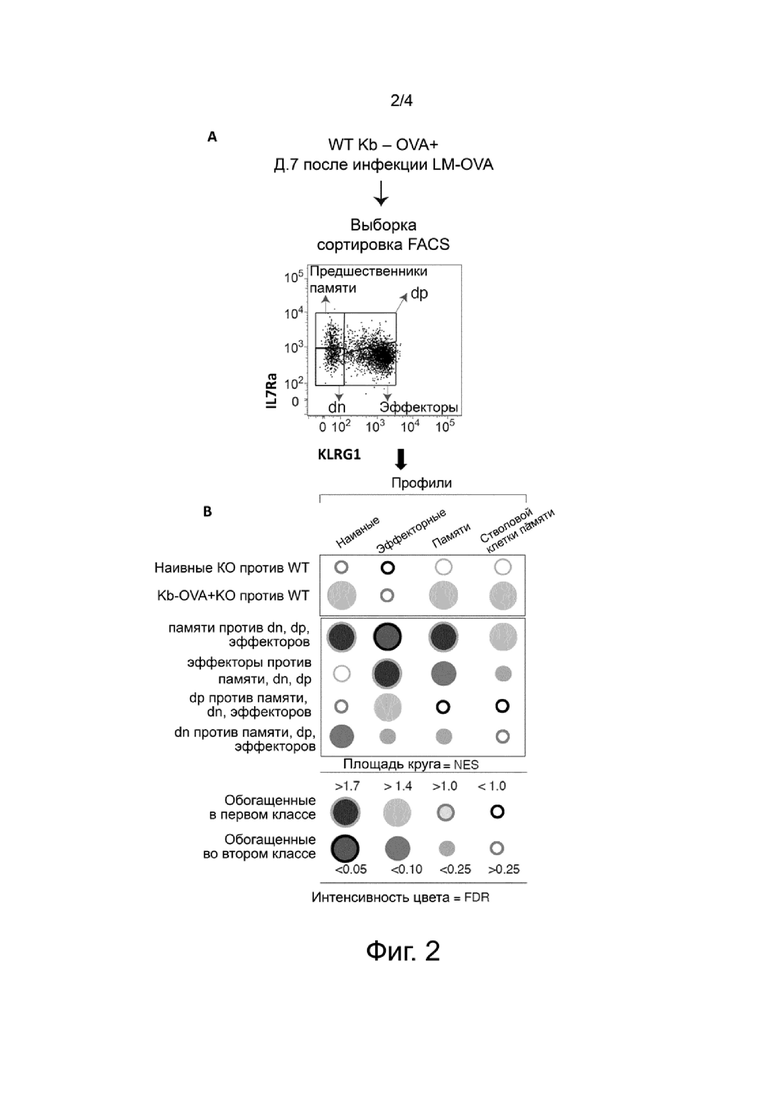
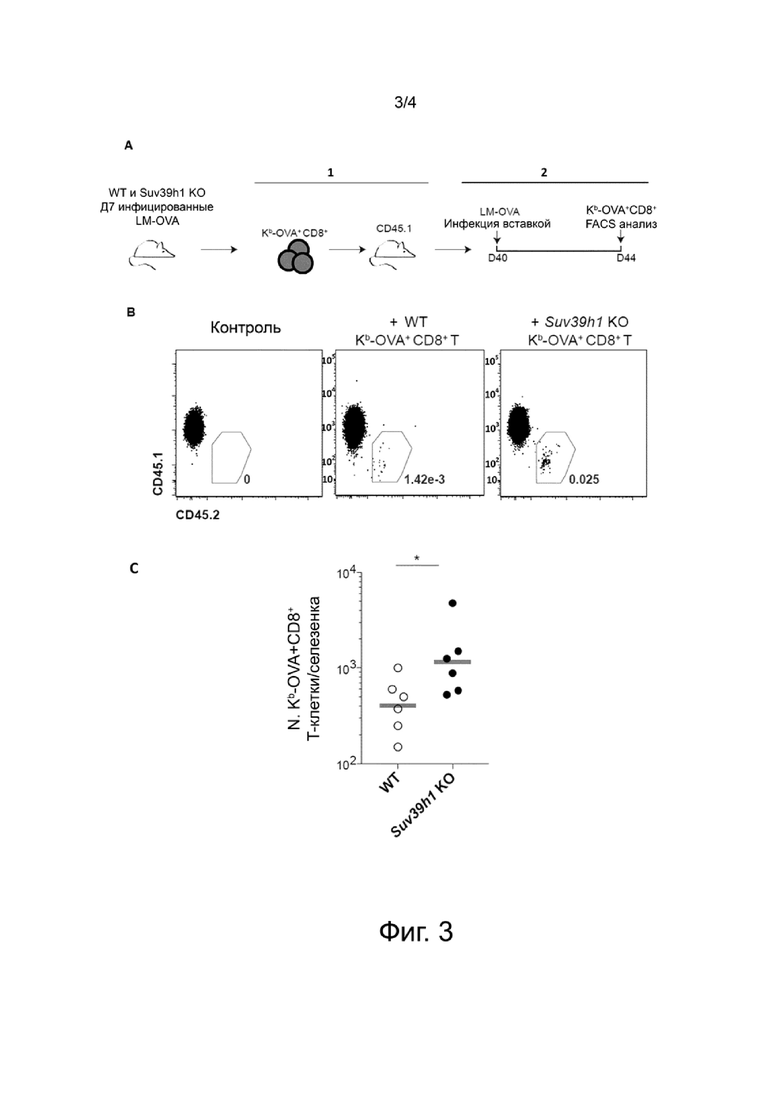
Группа изобретений относится к биотехнологии. Представлены: сконструированная иммунная клетка, где указанная иммунная клетка выбрана из Т клеток, NK клеток и их предшественников, которая является дефектной по Suv39h1 и ее применение. Кроме того, представлен способ получения генетически сконструированной иммунной клетки, дефектной по Suv39h1, где способ включает стадию ингибирования экспрессии и/или активности Suv39h1 в T клетке, NK клетке или их предшественнике, так что получившаяся сконструированная T клетка, NK клетка или их предшественник имеют повышенную выживаемость, а также раскрыта фармацевтическая композиция для адоптивной клеточной терапии, содержащая по меньшей мере одну сконструированную клетку, дефектную по Suv39h1. Изобретение позволяет использовать его в адоптивной терапии, в первую очередь для эффективного лечения рака. 4 н. и 21 з.п. ф-лы, 4 ил.
1. Сконструированная иммунная клетка, где указанная иммунная клетка выбрана из Т клеток, NK клеток и их предшественников, которая является дефектной по Suv39h1 и имеет повышенную выживаемость по сравнению с клеткой, не дефектной по Suv39h1.
2. Сконструированная иммунная клетка по п. 1, которая дополнительно содержит генетически сконструированный антигенный рецептор, специфически связывающийся с антигеном-мишенью.
3. Сконструированная иммунная клетка по п. 1 или 2, которая представляет собой T-клетку или ее предшественник.
4. Сконструированная иммунная клетка по любому из пп. 1-3, которая представляет собой CD4+ T-клетку или CD8+ T-клетку.
5. Сконструированная иммунная клетка по любому из пп. 1-4, которая извлекается из субъекта.
6. Сконструированная иммунная клетка по п. 5, при этом субъект страдает от рака или имеет риск развития рака.
7. Сконструированная иммунная клетка по любому из пп. 1-6, которая содержит два или более генетически сконструированных рецепторов, где каждый рецептор распознает иной антиген.
8. Сконструированная иммунная клетка по любому из пп. 1-7, при этом активность и/или экспрессия Suv39h1 в указанной сконструированной иммунной клетке селективно ингибируется или блокируется.
9. Сконструированная иммунная клетка по любому из пп. 1-8, где ген Suv39h1 репрессирован или разрушен делецией гена, экзона или участка, заменой экзогенной последовательностью и/или в гене содержится мутация сдвига рамки считывания или миссенс-мутация.
10. Сконструированная иммунная клетка по любому из пп. 1-9, при этом указанная сконструированная иммунная клетка экспрессирует нуклеиновую кислоту Suv39h1, кодирующую нефункциональный белок Suv39h1.
11. Сконструированная иммунная клетка по любому из пп. 2-10, где антиген-мишень экспрессируется на раковых клетках и/или является универсальным опухолевым антигеном.
12. Сконструированная иммунная клетка по любому из пп. 2-11, в которой генетически сконструированный антигенный рецептор является химерным антигенным рецептором (CAR), или T-клеточным рецептором (TCR).
13. Сконструированная иммунная клетка по любому из пп. 2-12, где указанный генетически сконструированный антигенный рецептор является химерным антигенным рецептором CAR который содержит (a) первичную цитоплазматическую сигнальную последовательность и/или вторичную цитоплазматическую сигнальную последовательность содержащую внутриклеточный домен из дзета цепи CD3, FcR гамма, FcR бета, CD3 гамма, CD3 дельта, CD3 эпсилон, CDS, CD22, CD79a, CD79b и/или CD66d.
14. Сконструированная иммунная клетка по п. 13, где CAR содержит костимулирующий домен из 4-1BB, CD28, ICOS, OX40 или DAP10.
15. Сконструированная иммунная клетка по п. 13 или 14, где генетически сконструированный антигенный рецептор является CAR, который содержит (a) внутриклеточный сигнальный домен из дзета цепи CD3, (b) один или несколько костимулирующих доменов из 4-1BB, CD28, ICOS, OX40 or DAP10, и (c) вариабельную область тяжелой цепи антитела и/или вариабельную область легкой цепи антитела.
16. Способ получения генетически сконструированной иммунной клетки, дефектной по Suv39h1, где способ включает стадию ингибирования экспрессии и/или активности Suv39h1 в T клетке, NK клетке или их предшественнике; так что получившаяся сконструированная T клетка, NK клетка или их предшественник имеют повышенную выживаемость.
17. Способ получения генетически сконструированной иммунной клетки, дефектной по Suv39h1 по п.16, который также включает стадию введения в указанную генетически сконструированную иммунную клетку, дефектную по Suv39h1, генетически сконструированного антигенного рецептора, специфически связывающегося с антигеном-мишенью.
18. Способ получения генетически сконструированной иммунной клетки, дефектной по Suv39h1 по любому из пп. 16, 17, согласно которому ингибирование экспрессии и/или активности Suv39h1 включает приведение в контакт данной клетки, по меньшей мере, с одним агентом, ингибирующим экспрессию и/или активность Suv39h1 и/или разрушающим ген Suv39h1.
19. Способ получения генетически сконструированной иммунной клетки, дефектной по Suv39h1 по п. 18, согласно которому агент выбирают из низкомолекулярных ингибиторов; производных антител, необязательно интрател, нанотел или аффител, аптамеров, молекул нуклеиновых кислот, блокирующих транскрипцию или трансляцию: малых интерферирующих РНК (миРНК), коротких шпилечных РНК (кшРНК), микро РНК (микроРНК), или piwiРНК (пиРНК); антисмысловых нуклеотидов; рибозимов, или агентов, редактирующих ген.
20. Фармацевтическая композиция для адоптивной клеточной терапии, содержащая по меньшей мере одну сконструированную клетку, дефектную по Suv39h1 согласно любому из пп. 1-15 или по меньшей мере одну генетически сконструированную иммунную клетку, дефектную по Suv39h1, полученную способом по любому из пп. 16-19, и фармацевтически приемлемый носитель.
21. Применение сконструированной иммунной клетки, дефектной по Suv39h1, по любому из пп. 1-15 или генетически сконструированной иммунной клетки дефектной по Suv39h1, полученной в способе по любому из пп. 16-19 или композиции по п. 20, в адоптивной клеточной терапии.
22. Применение по п. 21, где иммунная клетка является аутологичной или алогенной.
23. Применение по п. 21 или 22 где сконструированная иммунная клетка, дефектная по Suv39h1, по любому из пп. 1-15, или полученная в способе по любому из пп. 16-19, или композиции по п. 20 применяются в лечении рака.
24. Применение по п. 23, где сконструированная иммунная клетка, дефектная по Suv39h1, по любому из пп. 1-15, или полученная в способе по любому из пп. 16-19, или композиции по п. 20 применяются в комбинации со вторым противораковым терапевтическим агентом.
25. Применение по п. 24, где второй противораковый терапевтический агент является ингибитором иммунной контрольной точки.
| WO 2013050405 A1 11.04.2013 | |||
| ВИСЯЧИЙ СЕКРЕТНЫЙ БУКВЕННЫЙ ЗАМОК БЕЗ ДУЖКИ, ОТКРЫВАЕМЫЙ С КЛЮЧЕМ И БЕЗ КЛЮЧА | 1923 |
|
SU1036A1 |
| Машина для разделения сыпучих материалов и размещения их в приемники | 0 |
|
SU82A1 |
| YU WAKABAYASHI et al.: "Histone | |||
Авторы
Даты
2022-11-28—Публикация
2018-06-20—Подача