Изобретение относится к элементу аккумуляторной батареи, содержащему электролит на основе SO2.
Элементы аккумуляторной батареи имеют большое значение для многих областей техники. Часто они находят применение в тех случаях, когда требуются лишь небольшие элементы аккумуляторной батареи с относительно низкой силой тока, как, например, при пользовании мобильными телефонами. Однако наряду с этим отмечается также повышенный спрос и на более крупные элементы аккумуляторной батареи, предназначенные для высокоэнергетического применения, причем сверхбольшое накопление энергии в виде аккумуляторных элементов для электрического привода автомобилей имеет особое значение.
Важным требованием к таким элементам аккумуляторной батареи является высокая плотность энергии. Это означает, что элемент аккумуляторной батареи должен обладать по возможности большой электрической энергией в расчете на единицу веса и объема. В этом случае литий в качестве активного металла оказался особенно предпочтительным. Активным металлом элемента аккумуляторной батареи называют металл, ионы которого во время зарядки или разрядки элемента перемещаются в электролите в направлении к отрицательному или положительному электроду, участвуя там в электрохимических процессах. Эти электрохимические процессы приводят к непосредственной или косвенной отдаче электронов в наружную электрическую цепь или к поступлению электронов из наружной электрической цепи. Элементы аккумуляторной батареи с литием в качестве активного металла называются также литий-ионными элементами. Плотность энергии в таких литий-ионных элементах может быть повышена либо за счет увеличения удельной емкости электродов, либо за счет повышения напряжения элемента.
Как положительный, так и отрицательный электроды литий-ионных элементов выполнены в виде электродов включения. Под понятием «электрод включения» в смысле настоящего изобретения подразумеваются электроды, содержащие кристаллическую структуру, в которую ионы активного материала при эксплуатации литий-ионного элемента внедряются и из которой они выходят. Это значит, что электродные процессы могут протекать не только на поверхности электродов, но и внутри кристаллической структуры.
Во время зарядки литий-ионного элемента ионы активного металла выходят из положительного электрода и проникают в отрицательный электрод. При разрядке литий-ионного элемента процесс происходит обратный.
Электролит является также важным функциональным элементом любого элемента аккумуляторной батареи. В нем содержатся в большинстве случаев растворитель или смесь растворителей и, по меньшей мере, одна проводящая соль. Например, твердые электролиты или ионные жидкости не содержат растворители, а только проводящую соль, увеличивающую электропроводность электролита. Электролит контактирует с положительным и отрицательным электродами элемента аккумуляторной батареи. По меньшей мере, один ион проводящей соли (анион или катион) обладает внутри электролита такой подвижностью, что в результате ионной проводимости может происходить необходимый для функционирования элемента аккумуляторной батареи перенос зарядов между электродами. Начиная с определенного верхнего напряжения элемента аккумуляторного батареи, электролит электрохимически разлагается вследствие окисления. Этот процесс часто приводит к необратимому разрушению компонентов электролита и следовательно к выходу из строя элемента аккумуляторной батареи. Также и восстановительные процессы способны вызывать разложение электролита, начиная с определенного нижнего напряжения элемента. Для предупреждения этих процессов положительный и отрицательный электроды выбираются с таким расчетом, чтобы напряжение элемента было ниже или выше напряжения разложения электролита. Таким образом электролит определяет диапазон напряжения, в пределах которого элемент аккумуляторной батареи может обратимо эксплуатироваться, т.е. многократно заряжаться и разряжаться.
Известные из уровня техники литий-ионные элементы содержат электролит, состоящий из органического растворителя или смеси органических растворителей и растворенной в нем проводящей соли. Такая проводящая соль представляет собой соль лития, как, например, гексафторфосфат лития (LiPF6). Смесь растворителей может содержать, например, этиленкарбонат (ЭК). Электролит LP57, имеющий состав 1 М LiPF6 в среде ЭК: ЭМК (этилметилкарбонат) 3:7 (ЕС:ЕМС), представляет собой пример такого электролита. Из-за наличия органического растворителя или смеси органических растворителей этот тип литий-ионных элементов называется также органическими литий-ионными элементами.
Отрицательный электрод таких органических литий-ионных элементов состоит из углеродного покрытия, нанесенного на разрядный элемент из меди. Разрядный элемент создает электропроводящее подключение углеродного покрытия к наружной электрической цепи. Положительный электрод состоит из оксида литии-кобальта (LiCoO2), нанесенного на разрядный элемент из алюминия. Оба электрода имеют толщину, как правило, менее 100 пм и поэтому очень тонкие.
Издавна известно, что непроизвольная перезарядка органических литий-ионных элементов ведет к необратимому разложению компонентов электролита. При этом происходит окислительное разложение органического растворителя и/или проводящей соли на поверхности положительного электрода. Образующееся при этом разложении тепло реакции и возникающие газообразные продукты служат причиной последующего, так называемого «теплового пробоя» и возникающего вследствие этого разрушения органического литий-ионного элемента. В подавляющем большинстве протоколов зарядки таких литий-ионных элементов напряжение элемента фигурирует в качестве индикатора окончания зарядки. При этом аварии вследствие теплового пробоя особенно вероятны в случае применения комплекта многоэлементных батарей, в которых множество органических литий-ионных элементов с не совпадающей емкостью соединены последовательно.
Поэтому органические литий-ионные элементы проблематичны в отношении их стойкости и долгосрочной эксплуатационной надежности. Риски относительно надежности обусловлены также, в частности, горючестью органического растворителя или смеси органических растворителей. Если органический литий-ионный элемент воспламеняется или даже взрывается, то органический растворитель электролита создает горючий материал. Для предупреждения таких рисков в отношении надежности необходимы дополнительные меры. К ним относятся, в частности, очень точная регулировка процессов зарядки и разрядки органического литий-ионного элемента, а также оптимизированная конструкция аккумуляторной батареи. Кроме того в органическом литий-ионном элементе содержатся компоненты, которые при непреднамеренном повышении температуры плавятся и могут заливать органический литий-ионный элемент расплавленным полимером. В результате исключается последующее не контролируемое повышение температуры. Однако эти меры вызывают увеличение производственных затрат при изготовлении органического литий-ионного элемента, а также увеличение объема и веса. Кроме того эти меры снижают плотность энергии органического литий-ионного элемента.
Другой недостаток органических литий-ионных элементов состоит в том, что вероятные, образующиеся в присутствии остаточных количеств воды продукты гидролиза ведут себя очень агрессивно по отношению к компонентам элемента аккумуляторной батареи. Так, например, при часто применяемой в органических элементах проводящей соли LiPF6 образуется в результате реакции со следами воды очень реакционноспособный, агрессивный фтористый водород (HF). Вследствие этого при изготовлении таких элементов аккумуляторной батареи с органическим электролитом необходимо следить за минимизацией содержащейся в электролите и компонентах элемента остаточной воды. Поэтому производство часто ведется в дорогостоящих сушильных камерах с экстремально низкой влажностью воздуха. Описанные выше проблемы, касающиеся стойкости и длительной эксплуатационной надежности, имеют особенно большое значение при разработке органических литий-ионных элементов, обладающих, во-первых, очень хорошими показателями электрической энергии и мощности и, во-вторых, очень высокой эксплуатационной надежностью и долговечностью, в частности, очень большим числом полезных циклов зарядки и разрядки.
Для повышения плотности энергии ораганических литий-ионных элементов в уровне техники испытывали новые катодные материалы, т.е. новые активные материалы для положительных электродов, которые могут подвергатьмся циклам с более высоким конечным напряжением зарядки, т.е. с более высоким верхним потенциалом. Такими активными материалами выступают, например, оксиды лития-никеля-марганца-кобальта, сокращенно NMC. Об этом сообщается в публикации: “Oxygen Release and Its Effect on the Cycling Stability of LiNixMnyCozO2 (NMC) Cathode Materials for Li-Ion Batteries'' Roland Jung; Michael Metzger; Fillppo Maglla; Christoph Stinner and Hubert A. Gasteigera. Journal of The Electrochemical Society, 164 (7) M361-M377 (2017)
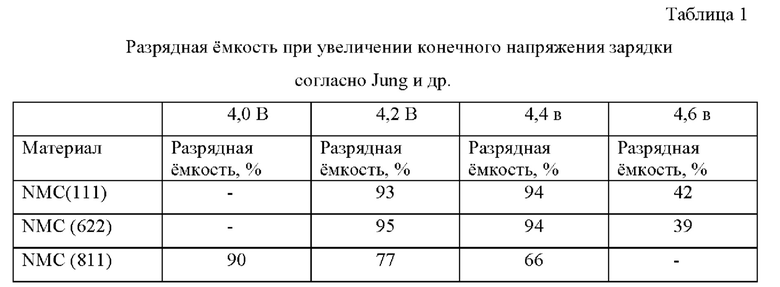
Эта публикация Jung и др. ниже обозначена как (VI). Jung и др. сообщили в (VI) об испытании разных материалов NMC с составом NMC(xyz). Строчные буквы в скобках (xyz) являются индексами х, у, z соединения LiNixMnyCozO2. В источнике (VI) три разных катодных материала NMC подвергались циклам в органическом литий-ионном элементе с описанным ранее электролитом LP57 (1 М LiPF6 в ЭК (этилкарбонат): ЭМК (этил метил карбонат) (ЕС:ЕМС)=3:7) при разных напряжениях зарядки. Под напряженинем зарядки имеется в виду напряжение тока, до которого отдельный аккумуляторный элемент или аккумуляторная батарея с несколькими аккумуляторными элементами заряжается зарядным устройством. Часто аккумуляторные батареи заряжают при определенной силе тока до определенного верхнего потенциала, т.е. до конечного напряжения заряда. Соответствующий верхний потенциал поддерживается до тех пор, пока зарядный ток не снизится до определенного значения. В (Д1) было проведено 300 циклов зарядки / разрядки. В приведенной ниже таблице 1 указано в % снижение разрядной емкости на 5-м цикла по сравнению с 300-ым циклом.
Из таблицы 1 следует, что при использовании материалов NMC (111) и NMC (622) происходит резкое падение емкости при проведении циклов с применением конечного напряжения заряда 4,6 В, поскольку достигаются лишь 42% или 39% от первоначальной емкости. Материал NMC (811) подвергали циклам только до достижения 4,4 В, причем отмечено также постоянное снижение емкости при повышении конечного напряжения зарядки. На основании (Д1) можно поэтому заключить, что органические литий-ионные элементы с катодными материалами NMC могут подвергаться циклам даже при более высоком верхнем потенциале. Правда, недостаток проявляется в том, что при этом происходит нежелательно большое снижение емкости.
Известное из уровня техники усовершенствование предусматривает применение электролита на основе диоксида серы (SO2) вместо органического электролита для элементов аккумуляторных батарей. Элемент аккумуляторной батареи, содержащий электролит на основе SO2, обладают в числе прочего высокой ионной проводимостью. Под понятием «электролит на основе SO2» следует понимать в смысле настоящего изобретения такой электролит, в котором SO2 содержится не только в качестве добавки при низкой концентрации, но также в котором подвижность ионов проводящей соли, содержащейся в электролите и вызывающей перенос зарядов, обеспечивается, по меньшей мере, частично, большей частью или даже полностью благодаря SO2. Следовательно SO2 служит в качестве растворителя для проводящей соли. Эта проводящая соль может образовывать с газообразным SO2 сольватный комплекс, причем SO2 связывается и давление пара заметно падает по сравнению с чистым SO2. Образуются электролиты с низким давлением пара. Такие электролиты на основе SO2 обладают по сравнению с описанным выше органическим электролитом преимуществом, выражающимся в негорючести. Риски относительно надежности, вызываемые горючестью электролита, в результате этого могут быть исключены.
Например, в ЕР 1201004 В1 (ниже V2) показан электролит на основе SO2 с составом LiAlCl4 * SO2 в сочетании с положительным электродом из UCoO2. Для избежания вызывающих нарушения реакций разложения при перезарядке элемента аккумуляторной батареи, начиная с верхнего потенциала 4,1-4,2 В, как, например, нежелательное выделение хлора (Cl2) из тетрахлоралюмината лития (LiAlCl4), в (V2) предложено применение дополнительной соли.
Также в источнике ЕР 2534719 В1 (ниже V3) раскрыт электролит на основе SO2 с применением в числе прочего LiAlCl4 в качестве проводящей соли. Это соединение LiAlCl4 образует вместе с SO2, например, комплексы формулы LiAlCl4 * 1,5 моль SO2 или LiAlCl4 *6 моль SO2. В качестве положительного электрода в (V3) применяется фосфат лития-железа (LiFePO4). (LiFePO4) обладает меньшим конечным напряжением заряда (3,7 В) по сравнению с LiCoO2 (4,2 В). Проблема, связанная с нежелательными реакциями перезарядки, в этом элементе аккумуляторной батареи отсутствует, поскольку не достигается вредный для электролита верхний потенциал 4,1 В.
Недостаток, который, в числе прочего, присущ и данному электролиту на основе SO2, заключается в том, что возможные, образующиеся в присутствии остаточной воды продукты гидролиза реагируют с компонентами элемента аккумуляторной батареи и вследствие этого возникают нежелательные побочные продукты. Вследствие этого при изготовлении таких элементов аккумуляторной батареи с электролитом на основе SO2 необходимо следить за минимизацией остаточной воды, содержащейся в электролите и компонентах элемента.
Другая присущая электролитам на основе SO2 проблема заключается в том, что многие, в частности, известные по органическим литий-ионовым элементам, проводящие соли не растворимы в среде SO2.
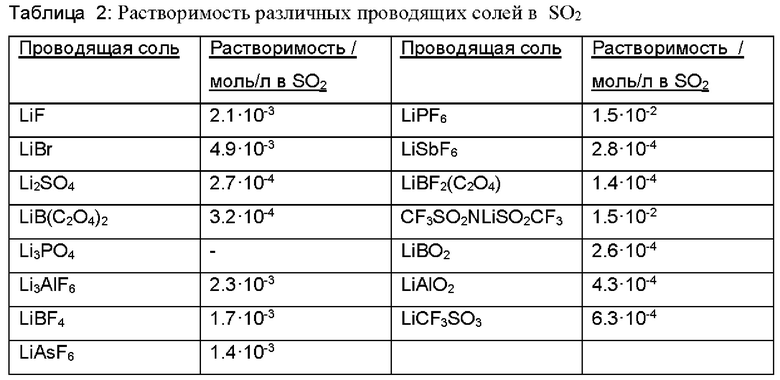
Измерения показали, что SO2 является плохим растворителем для многих проводящих солей, таких, как фторид лития (LiF), бромид лития (LiBr), сульфат лития (Li2SO4), бис(оксалат)борат лития (LiBOB), гексафторарсенат лития (LiAsF6), тетрафторборат лития (LiBF4), трилитийгексафторалюминат (LisAlF6), гексафторалюминат лития (LiSbFe), дифтор(оксалат)борат лития (UBF2C2O4), бис(трифторметансульфонил)имид лития (LiTFSI), метаборат лития (LiBO2), алюминат лития (LiAlO2), трифлат лития (LiCF3SO3) и хлорсульфонат лития (LiSO3Cl).
Равстворимость этих проводящих солей в SO2 составляет около 102-104 моль/л (см. табл.2). При таких низких концентрациях соли можно руководствоваться тем, что в любом случае происходит лишь малая растворимость, не являющаяся достаточной для эффективной эксплуатации элемента аккумуляторной батареи.
Для дополнительного улучшения возможностей применений и свойств элементов аккумуляторных батарей, содержащих электролит на основе SO2, в основу настоящего изобретения положена задача создания элемента аккумуляторной батареи с электролитом на основе SO2, который, по сравнению с известными из уровня техники элементами аккумуляторной батареи:
- имеет широкий электрохимический диапазон, вследствие чего отсутствует окислительное разложение электролита на положительном электроде;
- содержит на отрицательном электроде устойчивый покровный слой, при этом емкость этого слоя низкая и при последующей эксплуатации не происходит восстановительного разложения электролита на отрицательном электроде;
- содержит электролит на основе SO2, обладающий хорошей растворяющей способностью для проводящих солей, и следовательно служит хорошим проводником ионов и электронным изолятором, что упрощает перенос ионов и ограничивает до минимума саморазряд;
- содержит электролит на основе SO2, который инертен по отношению к другим компонентам элемента аккумуляторной батареи, таким, как сепараторы, материалы электродов и упаковочные материалы элементов;
- является устойчивым к другим неправомерным воздействиям, таким, как электрические, механические или термические;
- содержит электролит на основе SO2, характеризующийся повышенной стойкостью к остаточным количествам воды в компонентах элементов аккумуляторной батареи;
- обладает улучшенными рабочими электрическими характеристиками, в частности, высокой энергетической плотностью;
- имеет улучшенную способность к перезарядке и глубокому разряду, а также меньший саморазряд и
- характеризуется повышенным сроком службы, в частности, большим числом циклов зарядки и разрядки.
Такие элементы аккумуляторной батареи должны обладать, в частности, очень хорошими показателями электрической энергии и рабочими характеристиками, высокой эксплуатационной надежностью и долговечностью, в частности, большим числом полезных циклов зарядки и разрядки без разложения электролита в процессе эксплуатации элементов аккумуляторной батареи.
Данная цель достигается выполнением элемента аккумуляторной батареи с признаками пункта 1 формулы изобретения. В пунктах 2-30 формулы изобретения описаны предпочтительные варианты развития эле мента аккумуляторной батареи согласно изобретению.
Элемент аккумуляторной батареи согласно изобретению содержит активный металл, по меньшей мере, один положительный электрод, по меньшей мере, один отрицательный электрод, корпус и электролит. Положительный электрод выполнен в виде высоковольтного электрода. Электролит основан на SO2 и содержит, по меньшей мере, одну первую проводящую соль. Эта соль отвечает формуле (1):
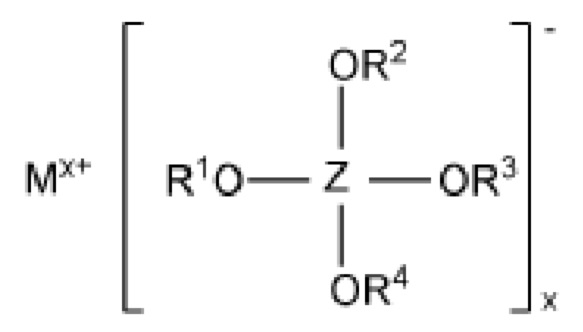
В формуле (I) означают : М - металл, выбранный из группы, состоящей из: щелочных металлов, щелочноземельных металлов, цинка и алюминия, х - целое число от 1 до 3. Заместители R1, R2, R3 и R4, независимо друг от друга, выбраны из группы, состоящей из C1-C10 алкила, C2-C10 алкенила, C2-C10 алкинила, C3-C10 циклоалкила, C6-C14 арила и C5-C14 гетероарила.
Центральный атом Z означает алюминий или бор.
Под понятим «высоковольтный электрод» подразумеваются в смысле настоящего изобретения электроды, заряжаемые, по меньшей мере, до верхнего потенциала, 4,0 В.
Предпочтительны высоковольтные электроды, заряжаемые, по меньшей мере, до верхнего потенциала 4,4 В, предпочтительно, по меньшей мере, до верхнего потенциала 4,8
В, предпочтительно, по меньшней мере, до верхнего потенциала 5,2 В, предпочтительно, по меньшей мере, до верхнего потенциала 5,6 В, особо предпочтительно, по меньшей мере, до верхнего потенциала 6,0 В в элементе аккумуляторной батареи согласно изобретению. При этом верхний потенциал соответствует конечному напряжению зарядки, до которого аккумуляторный элемент или аккумуляторная батарея из нескольких элементов заряжаются посредством зарядного устройства. Выполненные согласно изобретению элементы аккумукляторной батареи с высоковольтными электродами могут иметь напряжение элемента, равное, по меньшей мере, 4,0 В, предпочтительно, по меньшей мере,
4,4 В, предпочтительно, по меньшей мере, 4,8 В, предпочтительно, по меньшей мере, 5,2 В, предпочтительно, по меньшей мере, 5,6 В, особо предпочтительно, по меньшей мере, 6,0 В.
Электролит, применяемый в выполненном согласно изобретению элементе аккумуляторной батареи и основанный на SO2, содержит SO2 как добавку не только в незначительной концентрации, но также и в концентрациях, при которых обеспечивается подвижность ионов первой проводящей соли, содержащейся в электролите и обеспечивающей перенос ионов, по меньшей мере, частично, большей частью или даже полностью посредством SO2. Первая проводящая соль растворена в электролите и обладает в нем очень хорошей растворимостью. Вместе с газообразным SO2 она способна образовывать жидкий сольватный комплекс, в котором SO2 связывается. В этом случае давление пара жидкого сольватного комплекса заметно снижается по сравнению с чистым SO2, и образуются электролиты с низким давлением пара. Однако в объем изобретения входит и то, что при получении электролита согласно изобретению, в зависимости от химической структуры первой проводящей соли формулы (I), может не происходить снижения давления пара. В таком случае предпочтительно, чтобы получение электролита согласно изобретению велось при низкой температуре или под давлением. В электролите могут также содержаться несколько проводящих солей формулы (I), различающихся своей химической структурой.
Понятие «C1-С10 алкил» включает согласно настоящего изобретения линейные или разветвленные насыщенные углеводородные группы, содержащие от одного до десяти атомов углерода. Сюда относятся, в частности, метил, этил, n-пропил, изопропил, п-бутил, втор, бутил, изо-бутил, трет, бутил, n-пентил, изо-пентил, 2,2-диметилпропил, п-гексил, изо-гексил, 2-этилгексил, n-гептил, изо-гептил, n-октил, изо-октил, п-нонил, n-децил и др.
Понятие «С2-С10 алкенил» включает согласно настоящего изобретения ненасыщенные линейные или разветвленные углеводородные группы, содержащие от двух до десяти атомов углерода, причем углеводородные группы имеют, по меньшей мере, одну двойную связь С-С. Сюда относятся, в частности, этенил, 1-пропенил, 2-пропенил, 1-н-бутенил, 2-н-бутенил, изо-бутенил, 1-пентенил, 1-гексенил, 1-гептенил, 1-октенил, 1-ноненил, 1-деценил и др.
Понятие «С2-С10 алкинил» включает согласно настоящего изобретения ненасыщенные линейные или разветвленные углеводородные группы, содержащие от двух до десяти атомов углерода, причем углеводородные группы имеют, по меньшей мере, одну тройную связь С-С. Сюда относятся, в частности, этинил, 1-пропинил, 2-пропинил, 1-н-бутинил, 2-н-бутинил, изо-бутинил, 1-пентинил, 1-гексинил, 1-гептинил, 1-октинил, 1-нонинил, 1-децинил и др.
Понятие «С3-С10 циклоалкил» включает согласно настоящего изобретения циклические насыщенные углеводородные группы, содержащие от трех до десяти атомов углерода. Сюда относятся, в частности, циклопропил, циклобутил, циклопентил, циклогексил, циклогепсил, циклогексил, циклононил и циклодеканил.
Понятие «С6-С14 арил» включает согласно настоящего изобретения ароматические углеводородные группы, содержащие от шести до четырнадцати кольцевых атомов углерода. Сюда относятся, в частности, фенил (группа C6H5), нафтил (группа С10Н7) и антрацил (группа С14Н9).
Понятие «С5-С14 гетероарил» включает согласно настоящего изобретения ароматические углеводородные группы, содержащие от пяти до четырнадцати кольцевых углеродных атомов, в которых, по меньшей мере, один атом углеводорода заменен или замещен атомом азота, кислорода или серы. Сюда относятся, в частности, пирролил, фуранил, тиофенил, пирридинил, пиранил, тиопиранил и др. Все упомянутые выше углеводородные группы связаны через атом кислорода с центральным атомом согласно формуле (I).
Элемент аккумуляторной батареи с таким электролитом имеет то преимущество по сравнению с элементами аккумуляторной батареи с электролитами, известными из предшествующего уровня техники, что содержащаяся в нем первая проводящая соль обладает повышенной стойкостью к окислению и вследствие этого по существу не подвержена разложению при повышенных напряжениях элемента. Этот электролит устойчив к окислению предпочтительно, по меньшей мере, при верхнем потенциале до 4,0 В, предпочтительно, по меньшей мере, при верхнем потенциале до 4,2 В, предпочтительно, по меньшей мере, при верхнем потенциале до 4,4 В, предпочтительно, по меньшей мере, при верхнем потенциале до 4,6 В, предпочтительно, по меньшей мере, при верхнем потенциале до 4,8 В, особо предпочтительно, в частности, при верхнем потенциале до 5,0 В. Таким образом при использовании такого электролита в элементе аккумуляторной батареи происходит лишь незначительное разложение или даже не происходит разложения электролита в пределах рабочего потенциала, т.е. в диапазоне между конечным напряжением заряда и конечным напряжением разряда обоих электродов элемента аккумуляторной батареи. В результате элементы аккумуляторной батареи могут иметь конечное напряжение заряда, равное, по меньшей мере, 4,0 В, предпочтительно равное, по меньшей мере, 4,4 В, предпочтительно равное, по меньшей мере, 4,8 В, предпочтительно равное, по меньшей мере, 5,2 В, предпочтительно равное, по меньшей мере, 5,6 В, особо предпочтительно равное, по меньшей мере, 6,0 В. Срок службы элемента аккумуляторной батареи с таким электролитом заметно возрос по сравнению с элементом аккумуляторной батареи с известным из уровня техники электролитом.
Кроме того элемент аккумуляторной батареи с таким электролитом обладает стойкостью к низким температурам. При температуре, например, -40°С, может еще происходить разряжение 61% заряженной емкости. Электропроводность электролита при низких температурах остается достаточной для эксплуатации элемента аккумуляторной батареи. Кроме того элемент аккумуляторной батареи с таким электролитом обладает повышенной стойкостью к остаточным количествам воды. Если в электролите еще содержатся незначительные остатки воды (в диапазоне нескольких частей на миллион), то электролит или первая проводящая соль образует с водой, по сравнению с известными из уровня техники электролитами на основе SO2, продукты гидролиза, являющиеся заметно менее агрессивными по отношению к компонентам элемента. Вследствие этого отсутствие воды в электролите играет менее значительную роль по сравнению с электролитами на основе SO2, известными из уровня техники. Эти преимущества электролита согласно изобретению преобладают над недостатком, вызываемым тем фактом, что первая проводящая соль формулы (I) имеет анионы значительно большего размера по сравнению с известными из уровня техники проводящими солями. Такой увеличенный размер анионов обуславливает, по сравнению с электропроводностью LiAlCl4., более низкую электропроводность первой проводящей соли формулы (I).
Положительный электрод.
Ниже описаны предпочтительные варианты развития элемента аккумуляторной батареи согласно изобретению применительно к положительному электроду.
Положительный электрод согласно изобретению выполнен в виде высоковольтного электрода. Согласно предпочтительному варианту развития элемента аккумуляторной батареи по изобретению высоковольтный электрод содержит, по меньшей мере, один активный материал. Этот активный материал способен накапливать ионы активного металла, отдавать их при эксплуатации элемента аккумуляторной батареи и снова их принимать.Согласно предпочтительному варианту выполнения согласно изобретению элемента аккумуляторной батареи высоковольтный электрод содержит, по меньшей мере, одно интеркалярное соединение. Под понятием «интеркалярное соединение» имеется в виду в смысле настоящего изобретения подгруппа описанных выше материалов включения. Такое интеркалярное соединение действует как основная матрица с вакансиями, связанными между собой. В эти вакансии могут диффундировать ионы активного металла в процессе разрядки элемента аккумуляторной батареи и оставаться внедренными. В рамках такого внедрения ионов активного металла в основной матрице происходят лишь незначительные или вообще не происходят структурные изменения.
Согласно другому предпочтительному варианту развития выполненного согласно изобретению элемента аккумуляторной батареи активный материал содержит, по меньшей мере, одно соединение состава AxM'yM"zOa, где:
А по меньшей мере, один металл, выбираемый из группы, состоящей из щелочных металлов, щелочноземельных металлов, цинка или алюминия,
- M' по меньшей мере, один металл, выбираемый из группы, состоящей из элементов: Ti, V, Cr, Mn, Fe, Co, Ni, Cu, Zn;
- M" по меньшей мере, один элемент, выбиранемый из группы, состоящей из элементов групп 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16 Периодичнеской системы элементов;
- х, у независимо друг от друга, числа более 0;
- z число более или равное 0;
- а число более 0,
А означает предпочтительно литий, т.е. соединение может иметь состав: LixM'yM''zOa.
Индексы у, z в составе AxM'yM''zOa относятся к совокупности металлов и элементов, обозначаемых посредством М', М''. Если, например, М' означает два металла М'1 и М'2, то будет действительно для индекса у: y=y1+у2, при этом y1 и у2 являются индексами металлов М'1 и М'2. Индексы х, у, z, а должны выбираться так, чтобы внутри состава обеспечивалась нейтральность заряда. Примерами соединений, в которых А означает литий, М' означает два металла, являются оксиды лития-никеля-марганца-кобальта состава LixNiy1Mny2CozO2, где M'1=Ni, М'2=Mn и М''=Со. Примерами соединений, в которых z=0, которые следовательно не содержат другой металл или элемент М'', являются оксиды лития-кобальта LixCoyOa. Если, например, М'' включает в себя два элемента, во-первых, металл в виде М''1 и, во-вторых, фосфор в виде М''2, то будет действительно для индекса z: z=z1+z2, причем z1 и z2 являются индексами металла М''1 и фосфора (М''2). Индексы х, у, z, а должны и в этом случае выбираться так, чтобы внутри состава достигалась нейтральность заряда. Примерами соединений, у которых означают А - литий, М'' - металл М''1 и фосфор М''2, являются фосфаты лития-железа-марганца LixFeyFz1Sz2O4, где M-Fe. М''1=Mn, М''2=Р и z2=1.
В другом составе М'' может включать в себя два неметалла, например, фтор в виде М''1 и серу в виде М''2. Примерами таких соединений являются сульфаты лития-железа-фтора LixFeyFz1Sz2O4, где М-Fe, Mm1=F, М''2=Р.
Соединение состава AxM'yM''zOa может иметь химическую структуру шпинели, слоистого оксида или полианионного соединения.
Согласно предпочтительному варианту развития выполненного согласно изобретению элемента аккумуляторной батареи предусмотрено, что соединение имеет состав LixM'yM''zOa, в котором означают: А - литий, М' - металлы никель и марганец, М'' -кобальт. В этом составе формулы LixNiy1Mny2CozOa х, y1 и у2, независимо друг от друга, означают числа более 0, z означает число более или равное 0, а означает число более 0. Здесь речь идет преимущественно о составах формулы LixNiy1Mny2CozO2 (NMC), т.е. об оксидах лития-никеля-марганца-кобальта, имеющих химическую структуру слоистых оксидов. Примерами таких активных материалов из оксида лития-никеля-марганца-кобальта являются LiNi1/3Mn1/3Co1/3O2 (NMC111), LiNi0.2Co0.2O2 (NMC622) и LiNi0.8Mn0.1Co0.1O2 (NMC811). Другие соединения из оксида лития-никеля-марганца-кобальта могут иметь состав LiNi0.5Mn0.3Co0.2O2, LiNi0.5Mn0.25Co0.25O2, LiNi0.52Mn0.32Co0.16O2, LiNi0.55Mn0.30Co0.15O2, LiNi0.58Mn0.14Co0.28O2, LiNi0.64Mn0.18Co0.18O2, LiNi0.65Mn0.27Co0.08O2, LiNi0.7Mn0.2Co0.1O2, LiNi0.7Mn0.15Co0.15O2, LiNi0.72Mn0.10Co0.18O2, LiNi0.76Mn0.14Co0.10O2, LiNi0.86Mn0.04Co0.10O2, LiNi0.90Mn0.05Co0.05O2, LiNi0.95Mn0.025Co0.025O2 или их комбинацию. Из этих соединений могут быть изготовлены высоковольные электроды для элементов аккумуляторной батареи с напряжением элемента свыше 4,6 В.
Согласно другому предпочтительному варианту развития выполненного согласно изобретению элемента аккумуляторной батареи предусмотрено, что соединение состава LixM'yM''zOa представляет собой оксид металла, богатый литием и марганцем. Эти оксиды металлов также называются оксидными материалами, богатыми литием и марганцем, и могут иметь формулу LixMnyM''zOa. Также эти оксиды металлов LixMnyM''zOa могут иметь химическую структуру слоистых оксидов. Это значит, что в таком случае М' означает в приведенной выше формуле LixM'yM''zOa металл марганец (Мп). Здесь индекс х означает число, которое больше или равно 1, индекс у означает число, которое больше индекса z или больше суммы индексов z1+z2+z3 и т.д.. Если, например, М'' означает два металла М''1 и М''2. где индексы z1 и z2 (например, Li1.2Mn0.525Ni0.175Co0.1O2, где M''1=Ni, z1=0.175 and М''2=Со z2=0.1), то действительно для индекса у: y>z1+z2. Индекс z является числом, которое больше или равно 0, индекс а является числом, которое больше 0. Индексы х, у, z, а должны выбираться так, чтобы внутри состава достигалась нейтральность заряда. Оксиды металлов, богатых содержанием лития и марганца, могут быть также описаны формулой mLi2MnO3(1-m)LiM'O2, где 0<m<1. Примерами таких соединений служат Li1.2Mn0.525Ni0.175Co0.1O2, Li1.2Mn0.6Ni0.2O2, Li1.16 Mn0.61Ni0.15Co0.16O2 or Li1.2Ni0.13Co0.13Mn0.54O2. Эти оксиды металлов LixMnyM''zOa and mLi2MnO3⋅(1-m)LiM'O2 могут иметь химическую структуру слоистых оксидов.
Согласно предпочтительному варианту развития выполненного согласно изобретению элемента аккумуляторной батареи предусмотрено, что состав имеет формулу AxM'yM''zO4. Это значит, что в этом случае в приведенной выше формуле AxM'yM''zOa а имеет величину 4. Эти соединения имеют структуру шпинели. Эти структуры шпинели являются интеркалярными соединениями. Например, могут означать: А - литий, М' -кобальт, М'' - марганец. В этом случае активным материалом выступает оксид лития-кобальта-марганца (LiCoMnO4). С примененеим LiCoMnO4 могут изготавливаться высоковольтные электроды для выполненных согласно изобретению элементов аккумуляторной батареи с напряжением элемента свыше 4,6 В. В этом LiCoMnO4 предпочтительно не содержится Mn3+. Согласно предпочтительному варианту развития выполненного согласно изобретению элемента аккумуляторной батареи соединение имеет следовательно состав AxM'yM''zOa, где означают А - литий, М' - марганец и М'' - кобальт. Индексы х, у, z равны предпочтительно 1, а равно предпочтительно 4, в связи с чем этим предпочтительным соединением является LiMnCoO4.
Согласно другому примеру могут означать М' - никель, М'' - марганец. В этом случае активным материалом выступает оксид лития-никеля-марганца (LiNiMnO4). Молярные доли обоих металлов М' и М'' могут варьироваться. Например, оксид лития-никеля-марганца может иметь состав LiNi0.5Mn1.5O4.
Согласно другому предпочтительному варианту выполнения согласно изобретению элемента аккумуляторной батареи высоковольтный электрод содержит в качестве активного материала, по меньшей мере, один активный материал в виде способного к превращению соединения. Под понятием ''способное к превращению соединение'' следует понимать согласно настоящего изобретения материал, у которого во время электрохимической активности, т.е. во время зарядки и разрядки элемента аккумуляторной батареи, нарушаются и вновь создаются химические связи, образующие другие материалы. Во время поглощения или отдачи ионов активного металла в матрице способного к превращению соединения происходят структурные изменения.
Во время поглощения активного металла, например, лития или натрия, способные к превращению соединения проходят через твердофазную окислительно-восстановительную реакцию, во время которой изменяется кристаллическая структура материала. Это сопровождается разрывом и рекомбинацией химических связей. Полностью обратимые реакции способных к превращению соединений могут быть описаны, например, следующим образом:
Тип А: 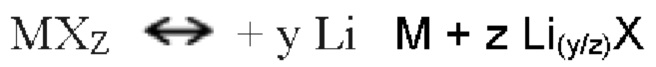
Тип В: 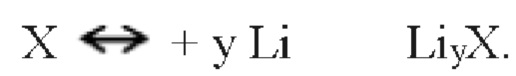
Примерами способных к превращению соединений служат: FeF2, FeF3, CoF2, CuF2, NiF2, BiF3, FeCl3, FeCl2, CoCl2, NiCl2, CuCl2, AgCl, LiCl, S, Li2S, Se, Li2Se, Те, I и Lil.
Согласно предпочтительному варианту развития соединение имеет состав LixM'yM''1z1M''2z2O4, в котором М''2 означает фосфор, z2 равно 1. Соединение состава LixM'yM''1M''1z1PO4 представляет собой так называемые металлические фосфаты лития. Эти металлические фосфаты лития могут иметь химическую структуру полианионного соединения. В частности, это соединение имеет состав LixFeyMnz1PO4. Примерами металлических фосфатов лития служат фосфаты лития-железа (LiFePO4) или фосфаты лития-железа-марганца (Li(FeyMnz)PO4). Примером фосфата лития-железа-марганца является фосфат состава Li(Fe0.3Mn0.7)PO4. Также металлические фосфаты лития других составов могут применяться в приготовленном согласно изобретению элементе аккумулятиорной батареи.
Согласно другому варианту развития выполненного согласно изобретению элемента аккумуляторной батареи предусмотрено, что высоковольтный электрод содержит, по меньшей мере, одно соединение металла. Это соединение металла выбирается из группы, состоящей из оксида металла, галогенида металла или фосфата металла. Предпочтительно металлом этого соединения является переходный металл с порядковым номером от 22 до 28 Периодической системы элементов, в частности, кобальт, никель или железо.
Согласно другому предпочтительному варианту развития выполненного согласно изобретению элемента аккумуляторной батареи предусмотрено, что высоковольтный электрод содержит, по меньшей мере, одно соединение металла, имеющее химическую структуру шпинели, слоистого оксида, способного к превращению соединения или полианионного соединения.
Также изобретением предусмотрено, что высоковольтный электрод содержит в качестве активного материала, по меньшей мере, одно из описанных соединений или их комбинацию. Под комбинацией соединений понимается высоковольтный электрод, содержащий, по меньшей мере, два из описанных материалов.
Согласно предпочтительному варианту развития выполненного согласно изобретению элемента аккумуляторной батареи предусмотрено, что высоковольтный электрод содержит разрядный элемент. Это означает, что в высоковольтном электроде помимо активного материала предусмотрен также разрядный элемент. Этот разрядный элемент предназначен для того, чтобы можно было обеспечить необходимое электронопроводящее подключение активного материала положительного электрода. Для этого разрядный элемент контактирует с активным материалом, участвующим в реакции на положительном электроде.
Этот разрядный элемент выполнен плоским в виде тонкого металлического листа или тонкой металлической фольги. Предпочтительно тонкая металлическая фольга имеет дырчатую или сетчатую структуру. Плоский разрядный элемент может состоять также из полимерной пленки с металлическим покрытием. Такие металлические покрытия имеют толщину в диапазоне от 0,1 до 20 пм. Активный материал положительного электрода наносится предпочтительно на поверхность тонкого металлического листа, тонкой металлической фольги или полимерной пленки с металлическом покрытием. Нанесение активного материала может производиться на лицевую и/или оборотную сторону плоского разрядного элемента. Подобные плоские разрядные элементы имеют толщину в диапазоне от 5 до 50 пм. Предпочтительно толщина плоского разрядного элемента составляет от 10 до 30 пм. При использовании плоских разрядных элементов общая толщина высоковольтного электрода может составить, по меньшей мере, 20 пм, предпочтительно, по меньшей мере, 40 пм, особо предпочтительно, по меньшей мере, 60 пм. Максимальная толщина составляет не более 200 пм, предпочтительно не более 150 пм, особо предпочтительно не более 100 пм. Поверхностно-удельная емкость положительного электрода, отнесенная к покрытию на одной стороне, составляет при использовании плоского разрядного элемента преимущественно, по меньшей мере, 0,5 мА.ч/см2, причем в этой последовательности предпочтительными являются следующие показатели: 1 мА.ч/см2, 3 мА.ч/см2, 5 мА.ч/см2, 10 мА.ч/см2, 15 мА.ч/см2, 20 мА.ч/см2.
Кроме того присутствует возможность того, что разрядный элемент может быть выполнен трехмерным в виде пористой металлической структуры, в частности, в виде металлической пены. Трехмерная пористая металлическая структура настолько пориста, что активный материал положительного электрода может внедряться в поры металлической структуры. Количеством внедрившегося или нанесенного активного материала определяется заряд положительного электрода. Если разрядный элемент выполнен трехмерным в виде пористой металлической структуры, в частности, в виде металлической пены, тогда толщина высоковольтного электрода составит преимущественно, по меньшей мере, 0,2 мм, предпочтительно, по меньшей мере, 0,3 мм, преимущественно, по меньшей мере, 0,4 мм, преимущественно, по меньшей мере, 0,5 мм, особо предпочтительно, по меньшей мере, 0,6 мм. Согласно другому предпочтительному варианту выполнения предусмотрено, что поверхностно-удельная емкость положительного электрода составляет при использовании трехмерного разрядного элемента, в частности, в виде металлической пены, предпочтительно, по меньшей мере, 2,5 мА.ч/см2, причем в этой последовательности предпочтительны следующие показатели: 5 мА.ч/см2, 15 мА.ч/см2, 25 мА.ч/см2, 35 мА.ч/см2, 45 мА.ч/см2, 55 мА.ч/см2, 65 мА.ч/см2, 75 мА.ч/см2. Если разрядный элемент выполнен трехмерным в виде пористой металлической структуры, в частности, в виде металлической пены, то количество активного материала положительного электрода, т.е. заряд электрода, в соотнесении с его поверхностью, составляет, по меньшей мере, 10 мг/см2, предпочтительно, по меньшей мере, 20 мг/см2, предпочтительно, по меньше мере, 40 мг/см2, предпочтительно, по меньшей мере, 60 мг/см2, предпочтительно, по меньшей мере, 80 мг/см2, особо предпочтительно, по меньшей мере, 100 мг/см2. Такой заряд положительного электрода положительно сказывается на процесс зарядки и разрядки элемента аккумуляторной батареи.
Согласно другому варианту развития выполненного согласно изобретеню элемента аккумуляторной батареи высоковольтный электрод содержит, по меньшей мере, одно связующее. Этим связующим является предпочтительно фторированное связующее, в частности, поливинилиденфторид и/или тройной сополимер, состоящий из тетрафторэтилена, гексафторпропилена и винилиденфторида. Однако возможно и связующее, состоящее из одного полимера, образованного мономерными структурными звеньями сопряженной карбоновой кислоты, или из соли щелочного металла, соли щелочноземельного металла иди соли аммония сопряженной карбоновой кислоты или их комбинаций. Также связующее может состоять из полимера на основе мономерных звеньев стирола и бутадиена. Кроме того связующее может происходить из группы карбоксиметилцеллюлоз. Связующее присутствует в положительном электроде преимущественно при концентрации не более 20 вес.%, предпочтительно не более 15 вес.%, предпочтительно не более 10 вес.%, предпочтительно не более 7 вес.%, предпочтительно не более 5 вес.%, особо предпочтительно не более 2 вес.%, от общего веса положительного электрода.
Электролит.
Ниже описаны предпочтительные варианты развития элемента аккумуляторной батареи применительно к электролиту на основе SO2.
Согласно предпочтительному варианту выполнения элемента аккумуляторной батареи заместители R1, R2, R3, R4 первой проводящей соли выбраны независимо друг от друга из группы, состоящей из:
- C1-С6 алкила; предпочтительно С2-С4 алкила; особо предпочтительно алкильных групп 2-пропил, метил и этил;
- С2-С6 алкенила; предпочтительно С2-С4 алкенила; особо предпочтительно алкенильных групп этенил и пропенил;
- С2-С6 алкинила; предпочтительно С2-С4 алкинила;
- С3-С6 циклоалкила;
- фенила,
- С5-С7 гетероарила.
В случае этого предпочтительного варианта выполнения электролита на основе SO2 понятие ''C1-C6 алкил'' означает линейные или разветвленные насыщенные углеводородные группы, содержащие от одного до шести атомов углерода, в частности, метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изобутил, трет-бутил, н-пентил, изопентил, 2,2-диметилпропил, н-гексил и изогексил. С2-С4 алкилы являются предпочтительными. Особенно предпочтительны С2-С4 алкилы 2-пропил, метил и этил.
В случае предпочтительного варианта выполнения электролита на основе SO2, понятие «С2-С6 алкенил» означает ненасыщенные линейные или разветвленные углеводородные группы, содержащие от двух до шести атомов углерода, при этом указанные углеводородные группы имеют по меньшей мере одну двойную связь С-С. Они включают, в частности, этенил, 1-пропенил, 2-пропенил, 1-н-бутенил, 2-н-бутенил, изобутенил, 1-пентенил и 1-гексенил, при этом С2-С4 алкенилы являются предпочтительными. Особенно предпочтительны этенил и 1-пропенил.
В случае этого предпочтительного варианта выполнения электролита на основе SO2, понятие «С2-С6 алкинил» означает ненасыщенные линейные или разветвленные углеводородные группы, содержащие от двух до шести атомов углерода, при этом указанные углеводородные группы имеют по меньшей мере одну тройную связь С-С. Они включают, в частности, этинил, 1-пропинил, 2-пропинил, 1-н-бутинил, 2-н-бутинил, изобутинил, 1-пентинил и 1-гексинил. Предпочтительными из них являются С2-С4 алкинилы.
В случае этого предпочтительного варианта выполнения электролита на основе SO2, понятие «С3-С6 циклоалкил» означает циклические насыщенные углеводородные группы, содержащие от трех до шести атомов углерода. Они включают, в частности, циклопропил, циклобутил, циклопентил и циклогексил.
В случае этого предпочтительного варианта выполнения электролита на основе SO2, понятие «С5-С7 гетероарил» означает фенил и нафтил.
В целях увеличения растворимости первой проводящей соли в электролите на основе SO2 заместители R1, R2, R3, R4 являются замещенными в другом предпочтительном варианте выполнения элемента аккумуляторной батареи, по меньшей мере, одним атомом фтора и/или, по меньшей мере, одной химической группой, причем эта группа выбирается из группы, состоящей из С1-С4 алкила, С2-С4 алкенила, С2-С4 алкинила, фенила и бензила. Химические группы С2-С4 алкил, С2-С4 алкенил, С2-С4 алкинил, фенил, и бензил обладают теми же свойствами или химическими структурами, что и описанные ранее углеводородные группы. В этой связи понятие «замещенный» означает, что отдельные атомы или группы атомов заместителей R1, R2, R3, R4 заменены атомом фтора и/или указанной химической группой.
Особенно большая растворимость первой проводящей соли в электролите на основе SO2 может достигаться в результате того, что, по меньшей мере, один из заместителей R1, R2, R3, R4 будет являться группой CF3 или группой OSO2CF3.
В другом предпочтительном варианте развития элемента аккумуляторной батареи первая проводящая соль выбирается из группы, состоящей из:
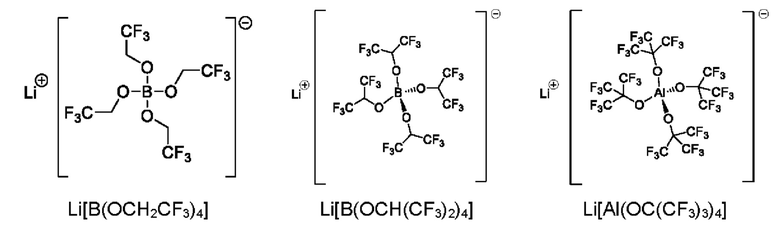
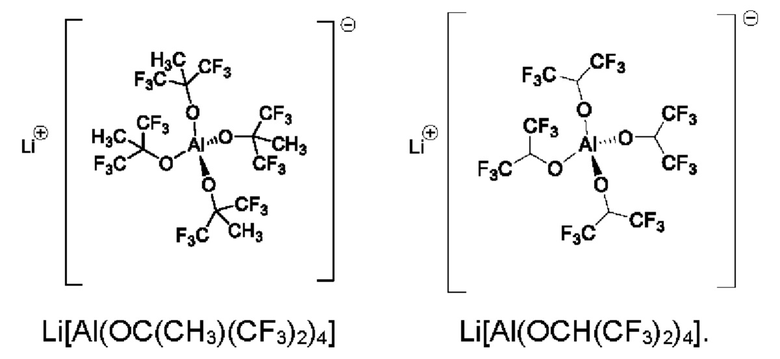
Для приведения электропроводности и/или других свойств электролита в соответствие с требуемым показателем электролит содержит, согласно предпочтительному варианту выполнения элемента аккумуляторной батареи по изобретению, по меньшей мере, одну вторую проводящую соль, отличающуюся от первой проводящей соли формулы (I). Это означает, что электролит может содержать кроме первой проводящей соли, также и вторую или вторые проводящие соли, которые по своему химическому составу и химической структуре отличаются от первой проводящей соли.
В другом предпочтительном варианте выполнения элемента аккумуляторной батареи согласно изобретению вторая проводящая соль, является соединением щелочного металла, в частности, соединением лития. Соединение щелочного металла или лития выбирается из группы, состоящей из алюмината, галогенида, оксалата, бората, фосфата, арсената и галлата. Предпочтительно второй проводящей солью является тетрагалогеноалюминат лития, в частности, LiAlCl4.
Кроме того, согласно другому предпочтительному варианту выполнения элемента аккумуляторной батареи по изобретению в электролите содержится, по меньшей мере, одна добавка. Эта добавка предпочтительно выбирается из группы, состоящей из виниленкарбоната и его производных, винилэтиленкарбоната и его производных, метилэтиленкарбоната и его производных, (бис-оксилат)бората лития, дифтор(оксалат)бората лития, тетрафтор(оксалат)фосфата лития, оксалата лития, 2-винилпиридина, 4-винил пиридина, циклических экзометиленкарбонатов, сультонов, циклических и ациклических сульфонатов, ациклических сульфитов, циклических и ациклических сульфинатов, органических сложных эфиров неорганических кислот, ациклических и циклических алканов, которые (ациклические и циклические алканы) имеют точку кипения при давлении 1 ат, по меньшей мере, 36°С, ароматических соединений, галогенизированных циклических и ациклических сульфонилимидов, галогенизированных циклических и ациклических сложных эфиров фосфата, галогенизированных циклических и ациклических фосфинов, галогенизированных циклических и ациклических фосфитов, галогенизированных циклических и ациклических фосфазенов, галогенизированных циклических и ациклических силиламинов, галогенизированных циклических и ациклических сложных эфиров, галогенизированных циклических и ациклических амидов, галогенизированных циклических и ациклических ангидридов и галогенизированных органических гетероциклов.
В еще одном предпочтительном варианте развития элемента аккумуляторной батареи электролит имеет следующий состав в соотнесении к общему весу электролита:
(i) 5-99,4 вес.% диоксида серы,
(ii) 0,6-95 вес.% первой проводящей соли,
(iii) 0-25 вес.% второй проводящей соли,
(iv) 0-10 вес.% добавки.
Как уже упоминалось выше, в электролите могут содержаться не только одна первая проводящая соль формулы (1) и одна вторая проводящая соль, но также и несколько первых проводящих солей формулы (1) и несколько вторых проводящих солей. Приведенные выше процентные доли содержат в себе в последнем случае также несколько первых и несколько вторых проводящих солей. Концентрация первой проводящей соли составляет от 0,01 до 10 моль/л, предпочтительно от 0,05 до 10 моль/л, предпочтительно от 0,1 до 6 моль/л, особо предпочтительно от 0,2 до 3,5 моль/л, от общего объема электролита.
Другим предпочтительным вариантом развития элемента аккумуляторной батареи, согласно изобретению, предусмотрено, что в электролите содержится, по меньшей мере, 0,1 моль SO2, предпочтительно, по меньшей мере, 1 моль SO2, предпочтительно, по меньшей мере, 5 моль SO2, предпочтительно, по меньшей мере, 10 моль SO2, особо предпочтительно, по меньшей мере, 20 моль SO2, на 1 моль проводящей соли. В электролите могут также содержаться очень большие молярные доли SO2, при этом предпочтительный верхний предел может составлять 2600 моль на 1 моль проводящей соли, причем в этой последовательности являются предпочтительными верхние пределы: 1500, 1000, 500 и 100 моль SO2 на 1 моль проводящей соли. Понятие «на 1 моль проводящей соли» относится при этом ко всем проводящим солям, содержащимся в электролите. Электролиты на основе SO2 с таким соотношением концентраций между SO2 и проводящей солью имеют то преимущество, что они по сравнению с известными из уровня техники электролитами, которые основаны, например, на смеси органических растворителей, могут растворять большее количество проводящей соли. В рамках изобретения неожиданно установили, что электролит с относительно низкой концентрацией проводящей соли, несмотря на связанное с этим повышенное давление пара, является предпочтительным, в частности, в связи с его стойкостью на протяжении многих циклов зарядки и разрядки элемента аккумуляторной батареи. Концентрация SO2 в электролите влияет на его электропроводность. Следовательно посредством выбора концентрации SO2 можно приводить в соответствие электропроводность электролита с запланированным применением элемента аккумуляторной батареи с таким электролитом.
Общее содержание SO2 и первой проводящей соли может составлять более 50 вес.% от веса электролита, предпочтительно более 60 вес.%, предпочтительно более 70 вес.%, предпочтительно более 80 вес.%, предпочтительно более 85 вес.%, предпочтительно более 90 вес.%, предпочтительно более 95 вес.%, предпочтительно более 99 вес.%.
В электролите может содержаться, по меньшей мере, 5 вес.% SO2 от общего количества содержащегося в элементе аккумуляторной батареи электролита, причем предпочтительными являются показатели 20 вес.%, 40 вес.%. и 60 вес.% SO2. Электролит может также содержать до 95 вес.% SO2, причем в этом ряду предпочтительными являются максимальные значения 80 вес.% и 90 вес.% SO2.
В рамках изобретения предусмотрено, что в электролите содержится предпочтительно лишь незначительная процентная доля, по меньшей мере, одного органического растворителя или он совсем не содержится. Предпочтительно доля органического растворителя в электролите, например, в виде одного растворителя или смеси из нескольких растворителей, может составлять не более 50 вес.% от веса электролита. Особо предпочтительны меньшие доли, составляющие не более 40 вес.%, не более 30 вес.%, не более 20 вес.%, не более 15 вес.%, не более 10 вес.%, не более 5 вес.% или не более 1 вес.% от веса электролита. Также предпочтителен электролит без содержания органических растворителей. Вследствие присутствия лишь незначительной доли органических растворителей или даже их полного отсутствия электролит является либо слабо горючим, либо вообще не горючим. Это повышает эксплуатационную надежность элемента аккумуляторной батареи, в котором применяется такой электролит на основе SO2. Особо предпочтителен электролит на основе SO2, не содержащий по существу органических растворителей.
Согласно предпочтительному варианту развития элемента аккумуляторной батареи электролит, в соотнесении к общему весу состава, имеет следующий состав:
(i) 5-99,4 вес.% диоксида серы,
(ii) 0,6-95 вес.% первой проводящей соли,
(iii) 0-25 вес.% второй проводящей соли,
(iv) 0-10 вес.% добавки,
(v) 0-50 вес.% органического растворителя.
Активный металл.
Ниже описаны предпочтительные варианты развития элемента аккумуляторной батареи согласно изобретению применительно к активному металлу.
Согласно предпочтительному варианту развития элемента аккумуляторной батареи активным металлом выступают:
- щелочной металл, в частности, литий или натрий,
- щелочноземельный металл, в частности, кальций,
- металл из группы 12 Периодической системы элементов, в частности, цинк, или
- алюминий.
Отрицательный электрод.
Ниже приводятся предпочтительные варианты развития элемента аккумуляторной батареи согласно изобретению применительно к отрицательному электроду.
Согласно предпочтительному варианту развития элемента аккумуляторной батареи предусмотрено, что отрицательный электрод является электродом включения. Этот электрод содержит материал включения в качестве активного материала, в который ионы активного металла внедряются во время зарядки элемента аккумуляторной батареи и из которого ионы активного металла выходят при разрядке элемента аккумуляторной батареи. Это значит, что электродные процессы могут протекать не только на поверхности отрицательного электрода, но также и внутри него. Если, например, применяется проводящая соль на основе лития, то ионы лития во время зарядки элемента аккумуляторной батареи могут внедряться в материал включения, а во время разрядки элемента аккумуляторной батареи из него выходить. Предпочтительно отрицательный электрод содержит в качестве активного материала или материала внедрения углерод, в частности, в виде графита. Также изобретением предусмотрено, что углерод применяется в виде природного графита (так называемого стимулятора коагуляции или имеющего округлую форму), синтетического графита (мезофазного графита), графитизированных мезокарбоновых микрогранул (МСМВ) вместе с графитом с углеродным покрытием или аморфным углеродом.
Согласно другому предпочтительному варианту развития элемента аккумуляторной батареи по изобретению отрицательный электрод содержит интеркалярные литиевые анод но-активные материалы без содержания углерода, например, титанаты лития (например, Li4Ti5O12).
Согласно предпочтительному варианту развития элемента аккумуляторной батареи предусмотрено, что отрицательный электрод содержит образующие с литием сплав анод но-активные материалы. Ими являются, например, накапливающие литий металлы и сплавы металлов (например, Si, Ge, Sn, SnCoxCy, SnSix и др.), а также оксиды накапливающих литий металлов и сплавов металлов (например, SnOx, SiOx, оксидные стекла Sn, Si и др.).
Согласно предпочтительному варианту развития элемента аккумуляторной батареи по изобретению отрицательный электрод содержит конверсионные анодно-активные материалы. Этими конверсионными анодно-активными материалами могут быть, например, оксиды переходных металлов в виде оксида марганца (MnOx), оксида железа (FeOx), оксида кобальта (СоОх), оксида никеля (NiOx), оксида меди ((CuOx) или гидриды металлов в виде гидрида магния (MgH2), гидрида титана (TiH2), гидрида алюминия (AlH3), а также троичные гидриды на основе бора, алюминия, магния, и др.
Согласно предпочтительному варианту развития элемента аккумуляторной батареи по изобретению отрицательный электрод содержит металл, в частности, металлический литий.
Согласно предпочтительному варианту развития элемента аккумуляторной батареи по изобретении предусмотрено, что отрицательный электрод выполнен пористым, причем пористость составляет предпочтительно не более 50%, предпочтительно не более 45%, предпочтительно не более 40%, предпочтительно не более 35%, предпочтительно не более 30%, предпочтительно не более 20%, особо предпочтительно не более 10%. Пористость -это объем пустот от общего объема отрицательного электрода, причем объем пустот образован так называемыми порами или пустыми пространствами. Данная пористость обеспечивает увеличение внутренней поверхности отрицательного электрода. Кроме того пористость снижает плотность отрицательного электрода, а следовательно и его вес. Отдельные поры отрицательного электрода могут заполняться электролитом в процессе эксплуатации преимущественно полностью.
Согласно другому предпочтительному варианту развития элемента аккумуляторной батареи по изобретению предусмотрено, что отрицательный электрод имеет разрядный элемент. Это означает, что отрицательный электрод содержит наряду с активным материалом или материалом внедрения также разрядный элемент. Этот разрядный элемент предназначен для обеспечения необходимой электронной проводимости на месте подключения активного материала отрицательного электрода. Для этого разрядный элемент контактирует с активным материалом, участвующим в протекающей на отрицательном электроде реакции. Такой разрядный элемент может быть выполнен плоским в виде тонкого металлического листа или тонкой металлической фольги. Тонкая металлическая фольга имеет предпочтительно дырчатую или сетчатую структуру. Плоский разрядный элемент может также состоять из полимерной пленки с металлическим покрытием. Толщина таких металлических покрытий составляет от 0,1 до 20 пм. Активный материал отрицательного электрода наносится предпочтительно на поверхность тонкого металлического листа, тонкой металлической фольги или полимерной пленки с металлическим покрытием. Активный материал может наноситься на лицевую и/или оборотную сторону плоского разрядного элемента. Такие плоские разрядные элементы имеют толщину в диапазоне от 5 до 50 пм. Предпочтительна толщина плоского разрядного элемента в диапазоне от 10 до 30 пм. При использовании плоских разрядных элементов общая толщина отрицательного электрода может составлять, по меньшей мере, 20 пм, предпочтительно, по меньшей мере, 40 пм, особо предпочтительно, по меньшей мере, 60 пм. Максимальная толщина составляет не более 200 пм, предпочтительно не более 150 пм, особо предпочтительно не более 100 пм. Поверхностно-удельная емкость отрицательного электрода, отнесенная к покрытию на одной стороне, составляет при использовании плоского разрядного элемента преимущественно, по меньшей мере, 0,5 мА.ч/см2, при этом при данной последовательности предпочтительными являются показатели: 1 мА. ч/см2, 3 мА.ч/см2, 5 мА.ч/см2, 10 мА.ч/см2, 15 мА.ч/см2, 20 м.ч/см2.
Кроме того присутствует возможность того, что разрядный элемент может быть выполнен трехмерным в виде пористой металлической структуры, в частности, в виде металлической пены. При этом понятие «трехмерная пористая металлическая структура» означает любую состоящую из металла структуру, располагающуюся не только подобно тонкому металлическому листу или металлической фольге по длине и ширине плоского электрода, но и по его толщине. Трехмерная пористая металлическая структура настолько пориста, что активный материал отрицательного электрода может внедряться в поры металлической структуры. Количеством внедрившегося или нанесенного активного материала определяется заряд отрицательного электрода. Если разрядный элемент выполнен трехмерным в виде пористой металлической структуры, в частности, в виде металлической пены, тогда толщина отрицательного электрода составит предпочтительно, по меньшей мере, 0,2 мм, предпочтительно, по меньшей мере, 0,3 мм, предпочтительно, по меньшей мере, 0,4 мм, предпочтительно, по меньшей мере, 0,5 мм, особо предпочтительно, по меньшей мере, 0,6 мм. В этом случае толщина электродов заметно больше по сравнению с отрицательными электродами, применяемыми в органических литий-ионных элементах аккумуляторной батареи. Согласно другому предпочтительному варианту выполнения предусмотрено, что поверхностно-удельная емкость отрицательного электрода составляет при использовании трехмерного разрядного элемента, в частности, в виде металлической пены, предпочтительно, по меньшей мере, 2,5 мА.ч/см2, причем в этой последовательности предпочтительны следующие показатели: 5 мА.ч/см2, 15 мА.ч/см2, 25 мА.ч/см2, 35 мА.ч/см2, 45 мА.ч/см2, 55 мА.ч/см2, 65 мА.ч/см2, 75 мА.ч/см2. Если разрядный элемент выполнен трехмерным в виде пористой металлической структуры, в частности, в виде металлической пены, то количество активного материала отрицательного электрода, т.е. заряд электрода, в соотнесении с его поверхностью, составляет, по меньшей мере, 10 мг/см2, предпочтительно, по меньшей мере, 20 мг/см2, предпочтительно, по меньше мере, 40 мг/см2, предпочтительно, по меньшей мере, 60 мг/см2, предпочтительно, по меньшей мере, 80 мг/см2, особо предпочтительно, по меньшей мере, 100 мг/см2. Такой заряд отрицательного электрода положительно сказывается на процесс зарядки и разрядки элемента аккумуляторной батареи.
Согласно другому варианту развития элемента аккумуляторной батареи по изобретению отрицательный электрод содержит, по меньшей мере, одно связующее. Этим связующим является предпочтительно фторированное связующее, в частности, поливинилиденфторид и/или тройной сополимер, состоящий из тетрафторэтилена, гексафторпропилена и винилиденфторида. Однако возможно и связующее, состоящее из одного полимера, образованного мономерными структурными звеньями сопряженной карбоновой кислоты, или из соли щелочного металла, соли щелочноземельного металла иди соли аммония сопряженной карбоновой кислоты или их комбинаций. Также связующее может состоять из полимера на основе мономерных звеньев стирола и бутадиена. Кроме того связующее может происходить из группы карбоксиметил-целлюлоз. Связующее присутствует в отрицательном электроде преимущественно при концентрации не более 20 вес.%, предпочтительно не более 15 вес.%, предпочтительно не более 10 вес.%, предпочтительно не более 7 вес.%, предпочтительно не более 5 вес.% особо предпочтительно не более 2 вес.%, от общего веса отрицательного электрода.
Согласно предпочтительному варианту развития элемента аккумуляторной батареи по изобретению отрицательный электрод содержит, по меньшей мере, одну электропроводящую добавку. Электропроводящая добавка должна иметь предпочтительно незначительный вес, высокую химическую стойкость и большую удельную поверхность. Примерами электропроводящих добавок могут служить углеродный порошок (газовая сажа, Супер Р, ацетиленовая сажа), углеродные волокна (углеродные нанотрубки, углеродные нановолокна), тонкодисперсные графиты и графен (нанолисты).
Структура элемента аккумуляторной батареи.
Ниже приводятся предпочтительные варианты развития элемента аккумуляторной батареи согласно изобретению применительно к его структуре.
Для дальнейшего улучшения функции элемента аккумуляторной батареи элемент аккумуляторной батареи согласно изобретению содержит несколько отрицательных и несколько положительных электродов, которые попеременно уложены в стопку внутри корпуса. При этом положительные и отрицательные электроды электрически разделены между собой сепараторами.
Сепаратор может состоять из нетканого материала, мембраны, тканого материала, трикотажного материала, органического материала, неорганического материала или их комбинаций. Органические сепараторы могут быть выполнены из незамещенных полиолефинов (например, полипропилена или полиэтилена), частично или полностью галогензамещенных полиолефинов (например, частично или полностью фторзамещенных, в частности, поливинилиденфторида (ПВДФ), этилентетрафторэтилена (ЭТФЭ), политетрафторэтилена (ПТФЭ), сложных полиэфиров, полиамидов или полисульфонов. Сепараторами, которые включают комбинацию из органических и неорганических материалов, являются, например, текстильные материалы из стекловолокон, в которых стекловолокна снабжены соответствующим полимерным покрытием. Указанное покрытие предпочтительно содержит фторсодержащий полимер, такой, как политетрафторэтилен (ПТФЭ), этилентетрафторэтилен (ЭТФЭ), перфторэтилен-пропилен (ФЭП), тройной полимер тетрафторэтилена, гексафторэтилена и винилиденфторида (ТГВ), перфторалкосиполимер (ПФА), аминосилан, полипропилен или полиэтилен (ПЭ). Сепаратор также может быть сложен в корпусе элемента аккумуляторной батареи, например, в виде так называемой «Z-образной складки». При такой Z-образной складке полосовой сепаратор загибается Z-образно через электроды или вокруг них. Более того, сепаратор также может быть выполнен в виде разделительной бумаги.
В рамках изобретения сепаратор может быть выполнен в виде оболочки, при этом каждый положительный и отрицательный электрод закрыт оболочкой. Оболочка может состоять из нетканого материала, мембраны, ткани, трикотажа, органического материала, неорганического материала или их комбинаций.
Оболочка положительного электрода обеспечивает равномерное перемещение и распределение ионов в элементе аккумуляторной батареи. Чем равномернее распределение ионов, в частности, в отрицательном электроде, тем больше возможная зарядка отрицательного электрода активным материалом и следовательно полезная емкость элемента аккумуляторной батареи. Одновременно исключаются риски, которые могут быть связаны с неравномерной зарядкой и результирующим отсюда отделением активного металла. Эти преимущества достигаются прежде всего в том случае, когда положительные электроды элемента аккумуляторной батареи закрыты оболочкой.
Размеры поверхности электродов и оболочки могут согласовываться между собой таким образом, чтобы наружные размеры оболочки и наружные размеры не закрытых электродов совпали, по меньшей мере, по одному размеру.
Размер поверхности оболочки может предпочтительно превышать размер поверхности электрода. В таком случае оболочка выходит за пределы электрода. Поэтому оба покрывающих электрод с обеих сторон слоя оболочки могут быть соединены между собой по краю положительного электрода краевой связью.
Согласно другому предпочтительному варианту выполнения элемента аккумуляторной батареи отрицательные электроды имеют оболочку, положительные электроды же оболочки не имеют.
Другие оптимальные свойства изобретения описаны и объяснены подробнее ниже со ссылкой на чертежи, примеры и эксперименты:
фиг. 1 показывает первый пример выполнения элемента аккумуляторной батареи согласно изобретению в поперечном сечении;
фиг. 2 показывает полученный с помощью электронного микроскопа снимок трехмерной пористой структуры металлической пены согласно первому примеру выполнения на фиг. 1 в виде подробного изображения;
фиг. 3 показывает второй пример выполнения элемента аккумуляторной батареи согласно изобретению в поперечном сечении;
фиг. 4 показывает деталь второго примера выполнения на фиг. 3;
фиг. 5 показывает третий пример выполнения элемента аккумуляторной батареи согласно изобретению в разобранном виде;
фиг. 6 показывает разрядную емкость, как функцию числа циклов испытуемых целых элементов аккумуляторной батареи, содержащих оксид лития-никеля-марганца-кобальта (НМК) состава LiNi0.6Mn0.2Co0.2O2 (НМК622) and LiNi0.8Mn0.1Co0.1O2 (НМК811) в качестве активного материала положительного электрода;
фиг. 7 показывает разрядную емкость, как функцию числа циклов испытуемых целых элементов аккумуляторной батареи, содержащих оксид лития-кобальта LiCoO2 (ЛКО) в качестве активного материала положительного электрода, при этом контрольный испытуемый целый элемент заполнен контрольным электролитом, испытуемый целый элемент заполнен электролитом 1;
фиг. 8 показывает разрядную емкость, как функцию числа циклов испытуемого целого элемента аккумуляторной батареи, содержащего оксид лития-никеля-марганца-кобальта (НМК) состава LiNi0.6Mn0.2Co0.2O2 (НМК622) в качестве активного материала положительного электрода, при этом контрольный испытуемый целый элемент аккумуляторной батареи заполнен контрольным электролитом, испытуемый целый элемент аккумуляторной батареи согласно изобретению заполнен электролитом 1;
фиг. 9 показывает кривую потенциала (в Вольтах), как функцию зарядки в процентах испытуемого целого элемента аккумуляторной батареи с применением фосфата лития-железа LiFePO4 (ЛЖФ) в качестве активного материала положительного электрода, при этом конечное напряжение заряда составляет 5 В;
фиг. 10 показывает разрядную емкость, как функцию числа циклов испытуемых целых элементов аккумуляторной батареи, содержащих фосфат лития-железа LiFePO4 (ЛЖФ) в качестве активного материала положительного электрода, при этом конечное напряжение заряда постепенно повышали с 4,5 до 5,0 В;
фиг. 11 показывает разрядную емкость, как функцию числа циклов испытуемого целого элемента аккумуляторной батареи с применением фосфата лития-железа-марганца Li(Fe0.3Mn0.7)PO4 в качестве активного материала положительного электрода, причем конечное напряжение зарядки составляло 4,5 В;
фиг. 12 показывает разрядную емкость, как функцию числа циклов испытуемого целого элемента аккумуляторной батареи с применением оксида металла состава Li1.16Mn0.61Ni0.15Co0.16O2 в качестве активного материала положительного электрода, при этом конечное напряжение зарядки составляло 4,8 В;
фиг. 13 показывает кривую потенциала (в Вольтах), как функцию процентной зарядки при циклах 1 и 2 с оксидом металла состава Li1.16Mn0.61Ni0.15Co0.16O2 в качестве активного материала положительного электрода;
фиг. 14 показывает кривую потенциала (в Вольтах), как функцию емкости при циклах 1 и 2 испытуемого элемента с оксидом лития-никеля-марганца состава LiNi0.5Mn1.5O4 в качестве активного материала положительного электрода;
фиг. 15 показывает потенциал (в Вольтах) трех испытуемых целых элементов аккумуляторной батареи, заполненных электролитами 1, 2 и контрольным электролитом из примера 1, при зарядке отрицательного электрода, как функцию емкости, соотнесенной с теоретической емкостью отрицательного электрода, во время образования покровного слоя на отрицательном электроде;
фиг. 16 показывает кривую потенциала при разрядке (в Вольтах), как функцию процентной зарядки трех испытуемых целых элементов аккумуляторной батареи, заполненных электролитами 1, 3, 4 из примера 2 и содержавших оксид лития-никеля-марганца-кобальта (НМК) в качестве активного электродного материала;
фиг. 17 показывает электропроводность (в мС/см) электролита 1 из примера 2 в зависимости от концентрации соединения 1;
фиг. 18 показывает электропроводность (в мС/см) электролита 3 из примера 2 в зависимости от концентрации соединения 3;
фиг. 19 показывает электропроводность (в мС/см) электролита 4 из примера 2 в зависимости от концентрации соединения 4.
На фиг. 1 представлен первый пример выполнения элемента 2 аккумуляторной батареи согласно изобретению в поперечном сечении. Элемент 2 аккумуляторной батареи выполнен в виде призматического элемента и содержит в числе прочего корпус 1. Этим корпусом 1 охватывается электродное устройство 3, состоящее из трех положительных электродов 4 и четырех отрицательных электродов 5. Положительные 4 и отрицательные 5 электроды расположены в электродном устройстве 3 в виде стопки с чередованием. Положительный электрод 4 в этом примере осуществления выполнен в виде высоковольтного электрода. Однако корпус 1 может вместить и большее количество положительных электродов 4 в виде высоковольтных электродов и/или отрицательных электродов 5. В целом предпочтительно, чтобы количество отрицательных электродов 5 было на единицу больше количества положительных электродов 4. Это связано с тем, что наружные торцевые поверхности электродной стопки образуются поверхностями отрицательных электродов 5. Электроды 4, 5 через свои выводы 6, 7 соединены с соответствующими соединительными контактами 9, 10 элемента 2 аккумуляторной батареи. Элемент 2 заполнен электролитом на основе SO2 таким образом, что электролит по возможности полностью проникает во все поры или пустоты, в частности, внутрь электродов 4, 5. На фиг. 1 электролит не показан. В данном примере выполнения положительные электроды 4 содержат интеркалярное соединение в качестве активного материала. Под интеркалярным соединением имеется в виду LiCoMnO4 со структурой шпинели.
В данном примере выполнения электроды 4, 5 являются плоскими, т.е. в виде слоев толщиной, которая незначительна по отношению к их поверхностной протяженности. Соответственно они разделены между собой сепаратором 11. Корпус 1 элемента 2 аккумуляторной батареи выполнен по существу прямоугольной формы, причем электроды 4, 5 и показанные в сечении стенки корпуса 1 расположены перпендикулярно плоскости чертежа и выполнены преимущественно прямыми и ровными. Однако элемент 2 аккумуляторной батареи может быть также выполнен витым, у которого электроды состоят из тонких слоев, намотанных вместе с материалом сепаратора. Сепараторы 11, во-первых, разделяют положительные 4 и отрицательные 5 электроды пространственно и электрически и, во-вторых, являются проницаемыми, в числе прочего, для ионов активного металла. Таким образом создаются большие электрохимически активные поверхности, обеспечивающие соответственно большой выход тока.
Кроме того электроды 4, 5 имеют разрядный элемент, предназначенный для обеспечения электронной проводимости подключения активного материала соответствующего электрода. Этот разрядный элемент контактирует с активным материалом, участвующим в реакции на соответствующем электроде 4, 5 (на фиг. 1 не показан). Разрядный элемент выполнен в виде пористой металлической пены 18. Металлическая пена 18 располагается по толщине электродов 4, 5. Активный материал положительных электродов 4 и отрицательных электродов 5 проникает в поры этой металлической пены 18, равномерно заполняя ее поры по всей толще структуры металла. Для повышения механической прочности положительные электроды 4 содержат связующее. Под этим связующим имеется в виду фторполимер. Отрицательные электроды 5 содержат в качестве активного материала углерод в виде материала внедрения, пригодного для поглощения ионов лития. Структура отрицательного электрода 5 аналогична структуре положительного электрода 4.
На фиг. 2 приведен выполненный под электронным микроскопом снимок трехмерной пористой структуры металлической пены 18 из первого примера выполнения на фиг. 1. Посредством указанного масштаба можно определить, что диаметр пор Р составляет в среднем свыше 100 пм, т.е. является относительно большим. Под этой металлической пеной имеется в виду металлическая пена из никеля.
На фиг. 3 приведен второй пример выполнения элемента 20 аккумуляторной батареи согласно изобретению в поперечном сечении. Этот второй пример выполнения отличается от первого на фиг. 1 тем, что электродное устройство содержит один положительный электрод 23 и два отрицательных электрода 22. Соответственно они разделены между собой сепараторами 21 и закрыты корпусом 28. Положительный электрод 23 содержит разрядный элемент 26 в виде плоской металлической фольги, на которую нанесен с обеих сторон активный материал 24 положительного электрода 23. Отрицательные электроды 22 также имеют разрядный элемент 27 в виде плоской металлической фольги, на которую с обеих сторон нанесен активный материал 25 отрицательного электрода 22. В качестве альтернативы плоские разрядные элементы краевых электродов, т.е. электродов, замыкающих электродную стопку, могут иметь только одностороннее покрытие активным материалом. Не покрытая сторона обращена к стенке корпуса 28. Электроды 22, 23 через свои выводы 29, 30 подключены к соответствующим соединительным контактам 31, 32 элемента 20 аккумуляторной батареи.
На фиг. 4 показана плоская металлическая фольга, которая используется в качестве разрядного элемента 26, 27 для положительных электродов 23 и отрицательных электродов 22 во втором примере выполнения на фиг. 3. Эта металлическая фольга имеет дырчатую или сетчатую структуру при толщине 20 пм.
На фиг. 5 приведен третий пример выполнения элемента 40 аккумуляторной батареи согласно изобретению в разобранном виде. Этот третий пример выполнения отличается от двух ранее рассмотренных примеров выполнения тем, что положительный электрод 44 закрыт оболочкой 13. При этом поверхностная протяженность оболочки 13 превышает поверхностную протяженность положительного электрода 44, граница 14 которого на фиг. 5 показана пунктирной линией. Два покрывающих с обеих сторон положительный электрод 44 слоя 15, 16 оболочки 13 соединены между собой на оборотном крае положительного электрода 44 краевой связью 17. Оба отрицательных электрода 45 оболочкой не закрыты. Электроды 44 и 45 могут контактировать через свои выводы 46, 47.
Пример 1: Приготовление контрольного электролита.
Используемый в описываемых ниже примерах контрольный электролит был приготовлен способом, раскрытым в описании изобретения к патенту ЕР 2954588 В1 (ниже V4). Сначала сушили хлорид лития (LiCl) в вакууме при 120°С в течение трех суток. Алюминиевые частицы (Al) сушили в вакууме в течение двух суток при 450°С. LiCl, хлорид алюминия (AlCl3) и Al смешали между собой в мольном соотношении AlCl3:LiCl:Al=1:1,06:0,35 в стеклянном сосуде с отверстием для выхода газа. Затем эту смесь постепенно термически обрабатывали до получения солевого расплава. После охлаждения фильтровали образовавшийся солевой расплав, охладили до комнатной температуры и подвели SO2 для достижения требуемого молярного соотношения между SO2 и LiAlCl4. Полученный при этом контрольный электролит имел состав LiAlCl4 × SO2, причем х зависел от подведенного количества SO2.
Пример 2. Приготовление электролита на основе SO2 для элемента аккумуляторной батареи в четырех примерах выполнения 1, 2, 3 и 4.
Для описываемых ниже экспериментов в четырех примерах выполнения 1, 2, 3 и 4 были приготовлены электролиты на основе SO2 (ниже обозначены как электролиты 1, 2, 3 и 4). Сначала для этого были приготовлены четыре разных первых проводящих соли по формуле (1) с применением способа, описанного в следующих источниках информации [V5], [V6] и [V7]:
[V5] „I. Krossing, Chem. Eur. J. 2001, 7, 490;
[V6] С.М. Иванова и др.., Chem. Eur. J. 2001, 7, 503;
[V7] Tsujioka и др., J. Electrochem. Soc., 2004, 151, A1418''
Эти четыре разных первых проводящих соли формулы (1) обозначены ниже как соединения 1, 2, 3 и 4. Они происходят из группы полифторалкоксиалюминатов и приготовлены по следующему уравнению реакции на основе LiAlH4 и соответствующего спирта R-ОН в гексане, где R1=R2=R3=R4.
Гексан

В результате образовались следующие, приведенные ниже соединения 1, 2, 3, 4 с суммарными и структурными формулами:
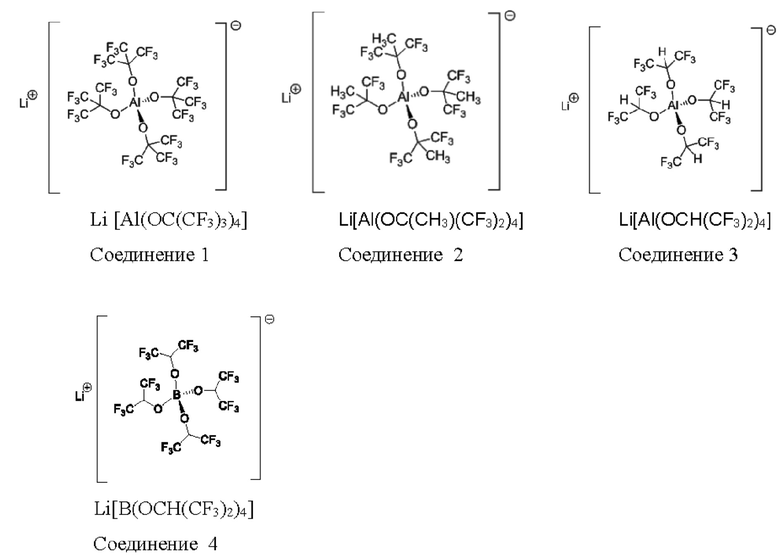
Для очистки соединения 1, 2, 3, 4 сначала подвергли перекристаллизации. В результате из первой проводящей соли были удалены остатки реагента LiAlH4, поскольку этот реагент вероятно может вызывать образование искры при взаимодействии с возможно присутствующими следами воды в SO2. Затем последовало растворение соединений 1, 2, 3, 4 в SO2. При этом отмечено, что соединения 1, 2, 3, 4 хорошо растворимы в SO2. Приготовление электролитов 1, 2, 3 и 4 проводилось при низкой температуре или под давлением в соответствии с приведенными ниже технологическими операциями 1-4:
1) помещение соответствующего соединения 1, 2, 3, 4 в напорную колбу со стояком,
2) вакуумирование напорной колбы,
3) впуск жидкого SO2,
4) повтор операций 2+3, пока не будет введено целевое количество SO2.
Концентрация соединений 1, 2, 3, 4 в электролитах 1, 2, 3, 4 составила 0,6 моль/л (количество вещества на 1 л электролита), если в описании эксперимента не указано иное. При использовании электролитов 1, 2, 3, 4 и контрольного электролита проводились описанные ниже эксперименты.
Пример 3. Изготовление испытуемых целых элементов аккумуляторной батареи.
Применявшиеся в описанных ниже экспериментах испытуемые целые элементы аккумуляторной батареи представляли собой элементы аккумуляторной батареи с двумя отрицательными электродами и одним положительным электродом, которые были разделены сепаратором. Положительные электроды содержали активный материал, активатор проводимости и связующее. Отрицательные электроды содержали графит в качестве активного материала, а также связующее. Как указано в описании эксперимента, отрицательные электроды могут содержать электропроводящую добавку. Активный материал положительного электрода указан в описании соответствующего эксперимента. Разрядный элемент положительных и отрицательных электродов состоял из никеля. В числе прочего целью исследований было подтверждение возможности применения разных активных материалов для положительного электрода в элементе аккумуляторной батареи согласно изобретению с высоким верхним (зарядным) потенциалом. В таблице 3 указано, какие активные материалы высоковольтного электрода исследовались и какие верхние потенциалы при этом применялись.
Испытуемые целые элементы аккумуляторной батареи были заполнены необходимым для экспериментов электролитом, т.е. либо контрольным электролитом, либо электролитами 1, 2, 3, 4.
Для каждого эксперимента было изготовлено несколько, т.е. от 2 до 4, идентичных испытуемых целых элементов аккумуляторной батареи. Полученные в ходе экспериментов результаты являются соответственно усредненными значениями, полученными на основе замеренных величин для идентичных испытуемых целых элементов аккумуляторной батареи.

Пример 4. Измерения испытуемых целых элементов аккумуляторной батареи.
При измерениях испытуемых целых элементов аккумуляторной батареи определяли, например, разрядную емкость через число циклов. Для этого испытуемые целые элементы аккумуляторной батареи заряжали при определенной силе зарядного тока до достижения определенного верхнего потенциала. Соответствующий определенный верхний потенциал выдерживался в течении столь длительного времени, пока зарядный ток не снижался до определенной величины. Затем проводилась разрядка при определенной силе разрядного тока до достижения определенного разрядного потенциала. При таком методе зарядки речь идет о так называемой зарядке I/U (сила тока / напряжение тока). В зависимости от требуемого числа цикла этот процесс может повторяться. Верхние потенциалы или разрядный потенциал и соответствующая сила тока при зарядке или разрядке указаны в описании экспериментов. Показатель, до которого должен снижаться зарядный ток при экспериментах, описан. Понятие «верхний потенциал» используется как синоним для понятий «зарядный потенциал», «зарядное напряжение», «конечное напряжение зарядки» и «верхний предел потенциала». Эти понятия означают напряжение / потенциал, до которого аккумуляторный элемент или батарея заряжаются с помощью зарядного устройства. Предпочтительно зарядка батареи ведется при норме тока С/2 и температуре 22°С. При скорости зарядки или разрядки 1С номинальная емкость элемента аккумуляторной батареи по определению заряжается или разряжается в течение одного часа. В соответствии с этим скорость зарядки С/2 означает время зарядки, равное 2 часам.
Понятие «потенциал разрядки» используется как синоним для понятия «нижнее напряжение» Этим обозначается напряжение / потенциал, до которого элемент аккумуляторной батареи или батарея разряжаются с помощью зарядного устройства. Предпочтительно разрядка элементов аккумуляторной батареи проводится при норме тока С/2 и температуре 22°С. Разрядная емкость выводится из разрядного тока и времени, при котором выполняются критерии окончания разрядки. Средние показатели разрядной емкости выражаются в процентах от номинальной емкости, которая часто нормируется как максимальная емкость, достигаемая при соответствующем испытании. Номинальную емкость получают вычитанием из теоретической емкости положительного электрода той емкости, которая была израсходована на первом цикле, служащим для образования покровного слоя на отрицательном электроде. Этот покровный слой формируется при первой зарядке испытуемого целого элемента аккумуляторной батареи на отрицательном электроде. При этом образовании покровного слоя невосполнимо расходуются ионы лития, вследствие чего соответствующий испытуемый целый элемент аккумуляторной батареи располагает меньшей, достигаемой при отдельном цикле емкостью при последующих циклах.
Эксперимент 1. Испытуемые целые элементы аккумуляторной батареи с оксидом лития-никеля-марганца-кобальта (НМК) состава LiNi0.6Mn0.2Co0.2O2 (НМК 622) и LiNi0.8Mn0.1Co0.1O2 (НМК 811) в качестве активного электродного материала.
С применением положительных электродов из оксида лития-никеля-марганца-кобальта состава LiNi0.6Mn0.2Co0.2O2 (НМК 622) and LiNi0.8Mn0.1Co0.1O2 (НМК 811) в качестве активных электродных материалов проводился экспертимент с испытуемыми целыми элементами аккумулятоной батареи согласно примеру 3. Соединения состава НМК в элементе аккумуляторной батареи с соответствующим электролитом могут заряжаться до высоких значений протенциала и снова разряжаться. Испытуемые целые элементы аккумуляторной батареи были заполнены описанным в примере 2 электролитом 1.
Испытуемые целые элементы аккумуляторной батареи содержали высоковольтные электроды с соединением НМК622, в одном испытуемом целом элементе аккумуляторной батареи был применен НМК 811 в качестве активного высоковольтного катодного материала.
Для определения разрядной емкости (см. пример 4) испытуемые целые элементы аккумуляторной батареи заряжали током силой 50 мА до достижения разных высоких потенциалов. Соответствующий высокий потенциал выдерживался до тех пор, пока зарядный ток не снижался до 40 мА. Затем следовала разрядка током силой 50 мА до потенциала разрядки 2,5 В. Верхние потенциалы составили для трех испытуемых целых элементов аккумуляторной батареи НМК 622: 4,4 В, 4,6 В и 5,0 В. Верхний потенциал для испытуемого целого элемента аккумуляторной батареи НМК 811 составил 4,6 В.
На фиг. 6 приведены средние показатели разрядной емкости четырех испытуемых целых элементов аккумуляторной батареи, как функции числа циклов. Средние показатели разрядной емкости выражены в процентах от номинальной емкости.
Кривая разрядной емкости четырех испытуемых целых элементов аккумуляторной батареи имеет равномерную, слегка пологую характеристику. Снижение емкости несколько больше у тех испытуемых целых элементов аккумуляторной батареи, циклы которых проводились при более высоком потенциале.
В упомянутой выше публикации (VI) из уровня техники приведено описание подобных экспериментов с органическими литий-ионными элементами, имевшими катоды НМК и органический электролит LP57 состава 1 М LiPF6 при соотношении этиленкарбонат: этилметилкарбонат (ЭК: ЭМК)=3:7. В таблице 4 приводится сравнение результатов эксперимента 1 с результатами эксперимента из (VI).
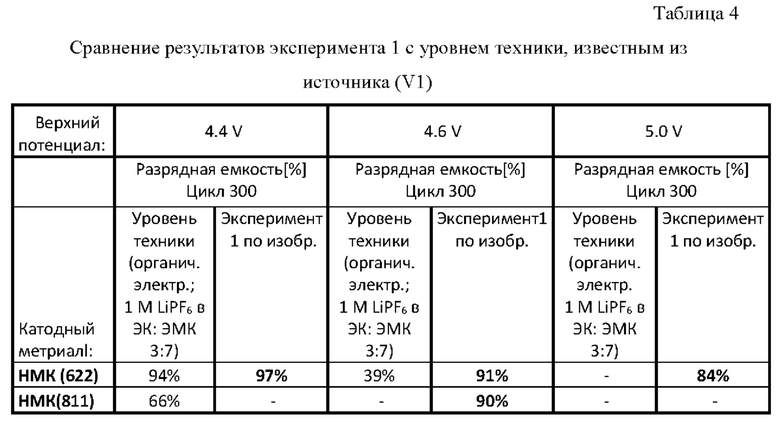
При сравнении с уровнем техники становятся очевидными превосходные свойства элементов аккумуляторной батареи согласно изобретению. Катодный материал НМК(622) в известных из уровня техники элементах аккумуляторной батареи показал при верхнем потенциале 4,4 В на 300-м цикле разрядную емкость, равную только 94%, а при верхнем потенциале 4,6 В - разрядную емкость только 39%. По сравнению с этим элемент согласно изобретению с катодным материадлом НМК(622) показал при 4,4 В - разрядную емкость 97% на 300-м цикле, при 4,6 В разрядную емкость 91% и при очень высоком потенциале, 5,0 В, даже 84%.
Катодный материал НМК(811) при проводившихся в уровне техники замерах показал при верхнем потенциале 4,4 В разрядную емкость 66% на 300-ом цикле. Тот же материал в элементе аккумуляторной батареи согласно изобретению показал при верхнем потенциале 4,6 В все еще высокую разрядную емкость, 90%.
Эксперимент 2. Испытуемые целые элементы аккумуляторной батареи с оксидом лития-кобальта LiCoO2 (ЛКО) в качестве активного материала.
При последующем эксперименте было изготовлено два испытуемых целых элемента аккумуляторной батареи согласно примеру 3. Активный материал положительных электродов (катодов) состоял из оксида лития-кобальта (ЛКО). Первый испытуемый целый элемент аккумуляторной батареи заполнили для этого эксперимента 2 контрольным электролитом согласно примеру 1. Электролит имел состав LiAlCl4 * 6 SO2. Второй испытуемый целый элемент аккумуляторной батареи заполнили описанным в примере 2 электролитом 1. Для опредения разрядной емкости (см. пример 4) испытуемые целые элементы аккумуляторной батареи подвергали циклам в соответствии с описанием эксперимента 1. Верхний потенциал элементов аккумуляторной батареи с контрольным электролитом составил 4,2 В, потенциал элементов согласно изобретению - 4,4 В. На фиг. 7 приведены средние показатели разрядной емкости двух испытуемых целых элементов аккумуляторной батареи, как функции числа циклов. Эти средние показатели разрядной емкости выражены в процентах от номинальной емкости. Кривые разрядной емкости двух испытуемых целых элементов аккумуляторной батареи имели совершенно разную характеристику.
Разрядная емкость испытуемого целого элемента аккумуляторной батареи с контрольным электролитом начинает возрастать с 45-го цикла и резко падать с 55-го цикла до тех пор, пока на 80-м цикле емкость не составит 50%. Такой испытуемый целый элемент акакумуляторной батареи оказывается необратимо поврежденным. Элемент аккумуляторной батареи, содержащий комбинацию из электрода с оксидом лития-кобальта в качестве активного материала и контрольного электролита, при высоком потенциале 4,2 В является неустойчивым.
Элемент согласно изобретению показал очень стойкую характеристику разрядной емкости. После 200 циклов все еще сохранялась емкость в размере 97%. При измерениях пришлось сделать перерыв между 125-м и 126-м циклами в связи с техническим обслуждиванием прибора. Показатели емкости после перерыва возросла на 2%, вследствие чего кривая разрядной емкости на этом месте имела локальный максимум.
Эксперимент 3. Испытуемые целые элементы аккумуляторной батареи с оксидом лития-никеля-марганца-кобальта (НМК) состава LiNi0.6Mn0.2Co0.2O2 (НМК 622) в качестве активного электродного материала.
Эксперимент 2 повторили с применением оксида лития-никеля-марганца-кобальта (НМК) состава LiNi0.6Mn0.2Co0.2O2 (НМК 622) в качестве активного материала положительных электродов (катодов). Снова было изготовлено два испытуемых целых элемента аккумулятиорной батареи согласно примеру 3. Первый испытуемый целый элемент апккумуляторной батареи заполнили контрольным электролитом согласно примеру 1. Электролит имел состав LiAlCl4 * 6 SO2. Второй испытуемый целый элемент аккумуляторной батареи был заполнен описанным в примере 2 электролитом 1. Для определения разрядной емкости (см. пример 4) испытуемые целые элементы аккумуляторной батареи подвергались циклам в соответствии с описанием эксперимента 1. Верхний потенциал первого испытуемого целого элемента аккумуляторной батареи с контрольным электролитом составил 4,2 В, тот же потенциал второго испытуемого целого элемента аккумуляторной батареи составил 4,4 В.
На фиг. 8 приведены средние показатели разрядной емкости этих двух испытуемых целых элементов аакакумуляторной батареи, как функции числа циклов. Средние показатели разрядной емкости выражены в процентах от номинальной емкости. Также и здесь кривые разрядной емкости обоих испытуемых целых элементов аккумуляторной батареи имели совершенно разную характеристику.
Разрядная емкость первого испытуемого целого элемента аккумуляторной батареи с контрольным электролитом после начальных колебаний начинает неуклонно падать, начиная с 75-го цикла. На 130-ом цикле достигается емкость, равная всего лишь 86%. Первый испытуемый целый элемент аккумуляторной батареи оказывается невосполнимо поврежденным. Элемент аккумуляторной батареи, содержащий комбинацию из электрода с оксидом лития-никеля-марганца-кобальта (НМК) состава LiNi0.6Mn0.2Co0.2O2 (НМК 622) в качестве активного материала и контрольного электролита, при высоком потенциале 4,2 В не устойчив.
Второй испытуемый целый элемент аккумуляторной батареи показал очень устойчивую характеристику разрядной емкости. На 200-м цикле сохранялась все еще емкость 97%.
Эксперимент 4. Испытуемые целые элементы аккумуляторной батареи с фосфатом лития-железа LiFePO4 (ЛЖФ) в качестве активного электродного материала.
Был изготовлен испытуемый целый элемент аккумуляторной батареи согласно примеру 3 с фосфатом лития-железа LiFePO4 (ЛЖФ) в качестве активного электродного материала положительного электрода. Испытуемый целый элемент аккумуляторной батареи заполнили описанным в примере 2 электролитом 1.
На фиг. 9 показана кривая потенциала на первом цикле (в Вольтах) над горизонтальной линией заряда в процентах, соотнесенного с максимальным зарядом испытуемого целого элемента аккумуляторной батареи. Испытуемый целый элемент аккумуляторной батареи заряжали током силой 50 мА до достижения верхнего потенциала 5 В. Потенциал выдерживали до тех пор, пока зарядный ток не снижался до 40 мА. Затем проводилась разрядка при силе тока 50 мА до достижения разрядного потенциала 2,5 В.
Эксперимент, касающийся зарядки / разрядки, снова повторили, но с тем отличием, что пороговый верхний потенциал или конечное напряжение зарядки увеличили с 4,5 В до 5,0 В при шаге 0,1 В (штриховая линия). По каждому потенциалу проводилось 5 циклов. На фиг. 10 показана разрядная емкость (сплошная линия) и соответствующий потенциал зарядки (верхний потенциал, штриховая линия).
Полученная разрядная емкость почти идентична для каждого потенциала зарядки и составила 99%. Это означает, что полученная разрядная емкость не зависит от потенциала зарядки. Следовательно повышенный потенциал зарядки не вызывает нежелательных реакций, таких, как, например, разложение электродов или невосполнимое разрушение активного материала ЛЖФ.
Эксперимент 5. Испытуемый целый элемент аккумуляторной батареи с фосфатом лития-железа-марганца Li(Fe0.3Mn0.7)PO4 в качестве активного электродного материала.
В целях испытания фосфатов лития и других металлов в другом эксперименте был изготовлен испытуемый целый элемент аккумулятиорной батареи согласно примеру 3. Активный материал положитиельных электродов (катодов) состоял из фосфата лития-железа-марганца Li(Fe0.3Mn0.7)PO4.
Испытуемый целый элемент аккумуляторной батареи заполнили описанным в примере 2 электролитом 1. Для определения разрядной емкости (см. пример 4) подвергли циклам испытуемый целый элемент аккумуляторной батареи в соответствии с описанием эксперимента 1. Верхний потенциал испытуемого целого элемента аккумуляторной батареи составлял 4,5 В.
На фиг. 11 приведены средние значения разрядной емкости испытуемого целого элемента аккумуляторной батареи, как функции числа циклов. Эти средние значения разрядной емкости выражены в процентах от номинальной емкости. Испытуемый целый элемент аккумуляторной батареи показал очень устойчивую характеристику разрядной емкости. На 200-м цикле емкость получили, равной 97%.
Эксперимент 6. Испытуемый целый элемент аккумуляторной батареи с оксидом маталла состава Li1.16Mn0.61Ni0.15Co0.16O2 в качестве активного материала.
В целях испытания богатого содержанием лития и марганца оксида металла в качестве активного электродного материала был изготовлен испытуемый целый элемент аккумулятиорной батареи согласно примеру 3. Активный материал положитиельных электродов (катодов) состоял из оксида металла состава Li1.16Mn0.61Ni0.15Co0.16O2, богатого содержанием лития и марганца. Испытуемый целый элемент аккумуляторной батареи заполнили описанным в примере 2 электролитом 1. Для определения разрядной емкости (см. пример 4) испытуемый целый элемент аккумуляторной батареи заряжали током силой 100 мА до верхнего потенциала 4,8 В. Верхний потенциал выдерживали до тех пор, пока зарядный ток не снижался до 40 мА. Затем следовала разрядка с применением тока силой 100 мА до достижения потенциала разрядки 2,0 В.
На фиг. 12 приведены средние значения для разрядной емкости испытуемого целого элемента аккумуляторной батареи, как функции числа циклов. Эти средние значения разрядной емкости выражены в процентах от номинальной емкости. Испытуемый целый элемент аккумуляторной батареи показал очень устойчивую характеристику разрядной емкости. На 100-м цикле емкость все еще сохраняется, равной 90%. На фиг. 13 показана кривая потенциала в Вольтах при циклах 1 и 2 испытуемого целого элемента аккумуляторной батареи с оксидом металла, богатого содержанием лития и марганца. На первом цикле оксид металла активировали, в результате чего обеспечилась типичная для данного материала высокая удельная емкость. Кривая потенциала показана над горизонталью процентной зарядки, соотнесенной с максимальной зарядкой испытуемого целого элемента аккумуляторной батареи. Этот элемент заряжали током силой 100 мА до достижения верхнего потенциала 4,8 В. Потенциал выдерживали до тех пор, пока зарядный ток не снижался до 40 мА. Затем следовала разрядка током силой 100 мА до потенциала разрядки 2,0 В. Кривая потенциала при цикле 1 четко указывает на иную характеристику, чем кривая при цикле 2. Это объясняется известными из литературы структурными изменениями материала. При этом процессе происходят необратимые изменения материала, вследствие чего при активации на первом цикле происходит потеря активных ионов лития. Снова в решетку могут внедриться только менее 90% ионов лития. На фиг. 13 отчетливо видно, что на втором цикле происходит повторное внедрение в количестве более 90% и следовательно невосполнимые потери заметно меньше, чем описано в литературе. На втором цикле особенно проявляется высокая стойкость потенциала электролита, настолько, что как будто при высоком конечном напряжении зарядки 4,8 В происходит почти полное внедрение ионов лития на втором цикле.
Эксперимент 7. Испытуемые целые элементы аккумуляторной батареи с оксидом лития-никеля-марганца состава LiNi0.5Mn1.5O4 в качестве активного электродного материала.
Для испытания оксида металла со структурой шпинели в качестве активного материала в другом эксперименте был изготовлен испытуемый целый элемент аккумулятиорной батареи с тремя электродами (рабочий электрод, противоэлектрод, электрод сравнения). Активный материал положительного электрода (катода) состоял из оксида металла состава LiNi0.5Mn1.5O4 Противоэлектрод и электрод сравнения были изготовлены из металлического лития. Испытуемый целый элемент аккумуляторной батареи был заполнен электролитом 1, описанным в примере 2..
На фиг. 14 показана кривая потенциала при циклах 1 и 2 в Вольтах, как функции емкости. Испытуемый целый элемент аккумуляторной батареи заряжали при скорости зарядки 0, 1 С до верхнего потенциала 5 В. Затем следовала разрядка при скорости разрядки 0, 1 С до потенциала разрядки 3,5 В. При обоих циклах отмечена устойчивая зарядно-разрядная характеристика несмотря на высокий конечный потенциал зарядки 5 В. На первом цикле достигнута высокая емкость, составившая 154 мА.ч/г. На втором цикле емкость незначительно снизилась.
Эксперимент 8. Исследование электролитов 1, 3 и 4.
Для исследования электролитов 1, 3 и 4 проводились разные эксперименты. Во-первых, выявляли емкость покровного слоя для электролитов 1, 3 и контрольного электролита и, во-вторых, определяли разрядную емкость в электролитах 1, 3 и 4.
Для определения емкости покровного слоя три испытуемых целых элемента аккумуляторной батареи были заполнены описанными в примере 2 электролитами 1 и 3 и описанным в примере 1 контрольным электролитом. Все три испытуемых целых элемента аккумуляторной батареи содержали фосфат лития-железа в качестве активного материала положительного электрода.
На фиг. 15 показан потенциал в Вольтах испытуемых целых элементов аккумуляторной батареи при зарядке отрицательного электрода, как функция емкости, соотнесенной с теоретической емкостью отрицательного электрода. Две изображенных кривых показывают усредненные результаты соответственно нескольких экспериментов с применением описанных ранее испытуемых целых элементов аккумуляторной батареи. Сначала испытуемые целые элементы аккумуляторной батареи заряжали током 15 мА до тех пор, пока емкость не достигла 125 мА.ч (Qlad). Затем следовала разрядка испытуемых целых элементов аккумуляторной батареи током 15 мА до достижения потенциала 2,5 В. При этом определяли разрядную емкость (Qent).
Емкость в процентах от теоретической, израсходованная на образование покровного слоя на отрицательном электроде, рассчитьывалась по следующей формуле:
емкость покровного слоя=(Qlad (125mAh) - Qent (x mAh)) / QNEL
Qnel означает теоретическую емкость использованного отрицательного электрода. Теоретическая емкость была рассчитана в случае с графитом равной 372 мА.ч/г. Абсолютные потери емкости составили 7,58% или 11,51% для электролитов 1 и 3, 6,85% для контрольного электролита. Емкость для образования покровного слоя при использовании обоих электролитов согласно изобретению была несколько выше, чем при контрольном электролите. Показатели абсолютных потерь емкости в диапазоне 7,5% - 11,5% являются хорошим результатом в сочетании с возможностью использования высоковольтных электродов до 5 Вольт.
Для проведения экспериментов по разрядке три испытуемых целых элемента аккумуляторной батареи согласно примеру 3 заполнили описанными в примере 2 электролитами 1, 3 и 4. В испытуемых целых элементах аккумуляторной батареи активным материалом положительного электрода служил оксид лития-никеля-марганца-кобальта (НМК). Для определения разрядной емкости (см. пример 4) испытуемые целые элементы аккумуляторной батареи заряжали током силой 15 мА до достижения емкости 125 мА.ч. Затем следовала разрядка с применением тока силой 15 мА до достижения потенциала разрядки 2,5 В.
На фиг. 16 показана кривая потенциала во время разрядки над горизонталью процентной разрядки (% от максимальной зарядки (разрядки). Все испытуемые целые элементы аккумуляторной батареи имели пологую кривую разрядки, которая необходима для надлежащей работы элемента аккумуляторной батареи.
Эксперимент 9. Определение электропроводности электролитов 1, 3 и 4.
Для определения электропроводности были приготовлены электролиты 1,3 и 4 с разной концентрацией соединений 1, 3 и 4. По каждой концентрации разных соединений определяли электропроводность электролитов посредством кондуктивного метода измерения. При этом после термостатирования двухэлектродный датчик выдерживали с возможностью контакта в растворе и измеряли в диапазоне 0-50 мС/см. При измерениях следили за тем, чтобы датчик мог взаимодействовать с электролитным раствором, содержащим SO2.
На фиг. 17 показана электропроводность электролита 1 в зависимости от концентрации соединения 1. Здесь можно видеть максимальное значение электропроводности при концентрации соединения 1, равной 0,6-0,7 моль/л, составляющее около 37,9 мС/см. По сравнению с этим известные их уровня техники органические электролиты, например, LP30 (LP30 (1 М LiPF6 / ЭК-ЭМК (1:1 по весу)) имеют электропроводность, составляющую только около 10 мС/см. На фигурах 18 (электролит 3) и 19 (электролит 4) приведены определенные при разной концентроации показатели электропроводности электролитов 3 и 4.
По электролиту 4 получили не более 18 мС/см при концентрации проводящей соли 1 моль/л. Электролит 3 характеризовался максимальной электропроводностью 0,5 мС/см при концентрации проводящей соли 0,6 моль/л. Хотя электролит 3 показал меньшую электропроводность, зарядка и разрядка испытуемого целого элемента аккумуляторной батареи, как и в эксперименте 4, совершенно возможны.
Эксперимент 10. Низкотемпературные свойства.
Для определения низкотемпературных свойств электролита 1 в сравнении с контрольным электролитом было изготовлено в соответствии с примером 3 два испытуемых целых элемента аккумуляторной батареи. Один испытуемый целый элемент аккумуляторной батареи заполнили контрольным электролитом состава LiAlCl4 * 6SO2, другой испытуемый целый элемент - электролитом 1. Испытуемый целый элемент аккумуляторной батареи с контрольным электролитом содержал фосфат лития-железа (ЛЖФ) в качестве активного материала, испытуемый целый элемент аккумуляторной батареи с электролитом 1 содержал оксид лития-никеля-марганца-кобальта (НМК) в качестве активного материала положительного электрода. Испытуемые целые элементы аккумуляторной батареи заряжали при 20°С до 3,6 В (ЛЖФ) или 4,4 В (НМК) и снова разряжали при соответствующей исследуемой температуре до 2,5 В. Полученная при 20°С разрядная емкость была оценена равной 100%. Температуру во время разрядки понижали на температурный шаг 10 К. Полученную разрядную емкость описали в % от разрядной емкости при 20°С. Поскольку низкотемпературная разрядка почти не зависит от применяемых активных материалов положительного и отрицательного электродов, то результаты могут быть перенесены на любые комбинации активных материалов. В таблице 5 приведены результаты.
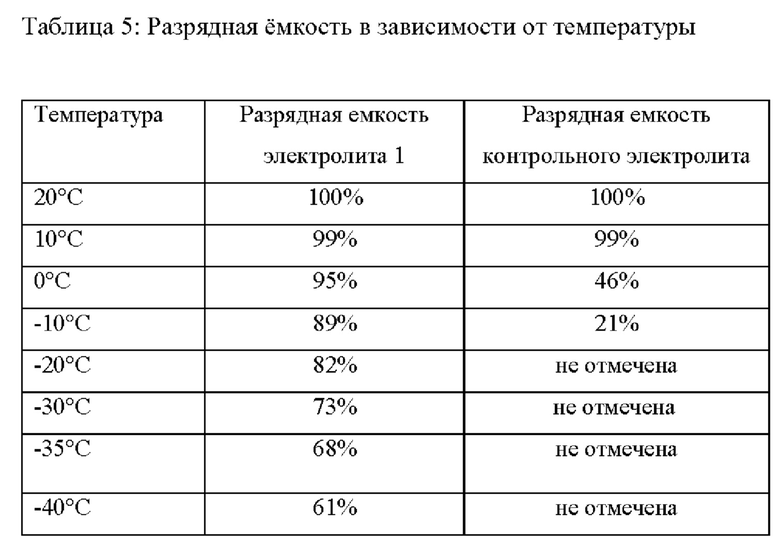
Испытуемый целый элемент аккумуляторной батареи с электролитом 1 показал очень хорошие низкотемпературные свойства. При -20°С емкость составляла все еще 82%, при -30°С все еще 73%. Даже при температуре -40°С разрядная емкость составляла 61%. В противоположность этому испытуемый целый элемент аккумуляторной батареи с контрольным электролитом показал способность к разрядке только до -10°С. При этом достигнута емкость 21%. При более низких температурах испытуемый целый элемент
| название | год | авторы | номер документа |
|---|---|---|---|
| ЭЛЕМЕНТ АККУМУЛЯТОРНОЙ БАТАРЕИ | 2020 |
|
RU2788178C1 |
| ЭЛЕМЕНТ АККУМУЛЯТОРНОЙ БАТАРЕИ | 2020 |
|
RU2787017C1 |
| ЭЛЕМЕНТ АККУМУЛЯТОРНОЙ БАТАРЕИ | 2020 |
|
RU2772791C1 |
| ЭЛЕКТРОЛИТ НА ОСНОВЕ SO2 ДЛЯ ЭЛЕМЕНТА АККУМУЛЯТОРНОЙ БАТАРЕИ И ЭЛЕМЕНТ АККУМУЛЯТОРНОЙ БАТАРЕИ | 2022 |
|
RU2814179C1 |
| ЭЛЕМЕНТ АККУМУЛЯТОРНОЙ БАТАРЕИ | 2020 |
|
RU2784564C1 |
| ЭЛЕКТРОЛИТ ДЛЯ ЭЛЕКТРОХИМИЧЕСКОГО ЭЛЕМЕНТА АККУМУЛЯТОРНОЙ БАТАРЕИ И СОДЕРЖАЩИЙ ЭЛЕКТРОЛИТ ЭЛЕМЕНТ АККУМУЛЯТОРНОЙ БАТАРЕИ | 2013 |
|
RU2629556C2 |
| Элемент аккумуляторной батареи | 2020 |
|
RU2786511C1 |
| Электролит на основе SO2 для элемента аккумуляторной батареи и элемент аккумуляторной батареи | 2020 |
|
RU2772790C1 |
| ПЕРЕЗАРЯЖАЕМЫЙ ЭЛЕМЕНТ АККУМУЛЯТОРНОЙ БАТАРЕИ | 2007 |
|
RU2438212C2 |
| ПЕРЕЗАРЯЖАЕМЫЙ ЭЛЕКТРОХИМИЧЕСКИЙ ЭЛЕМЕНТ | 2011 |
|
RU2569328C2 |
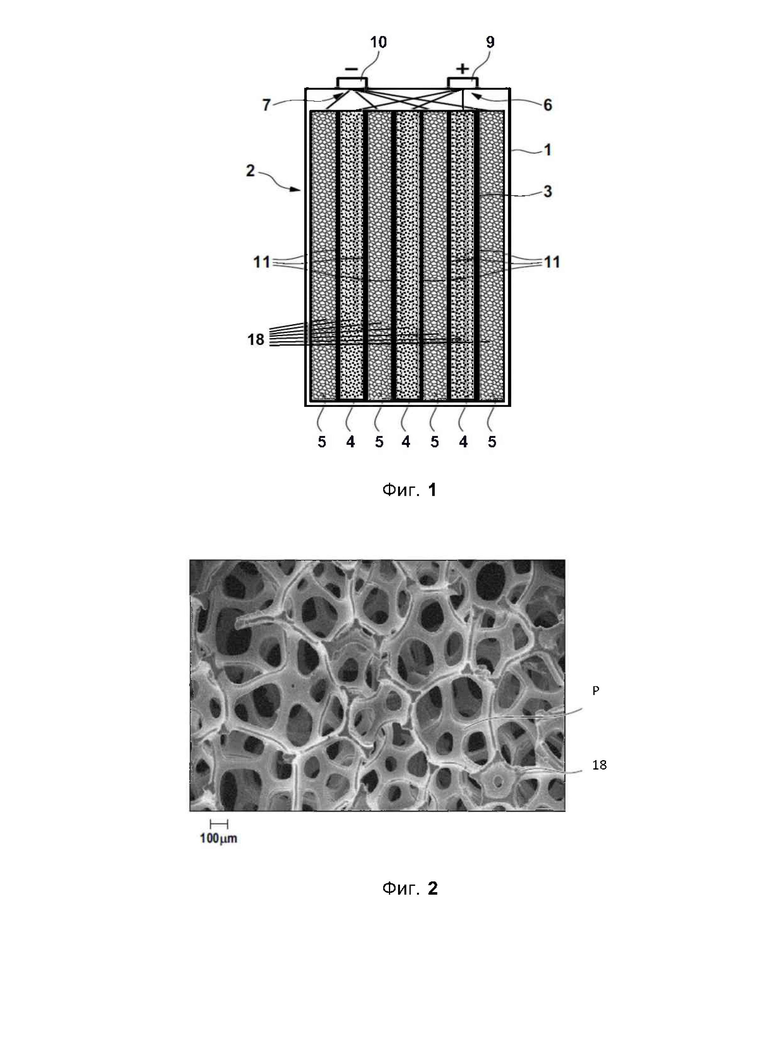
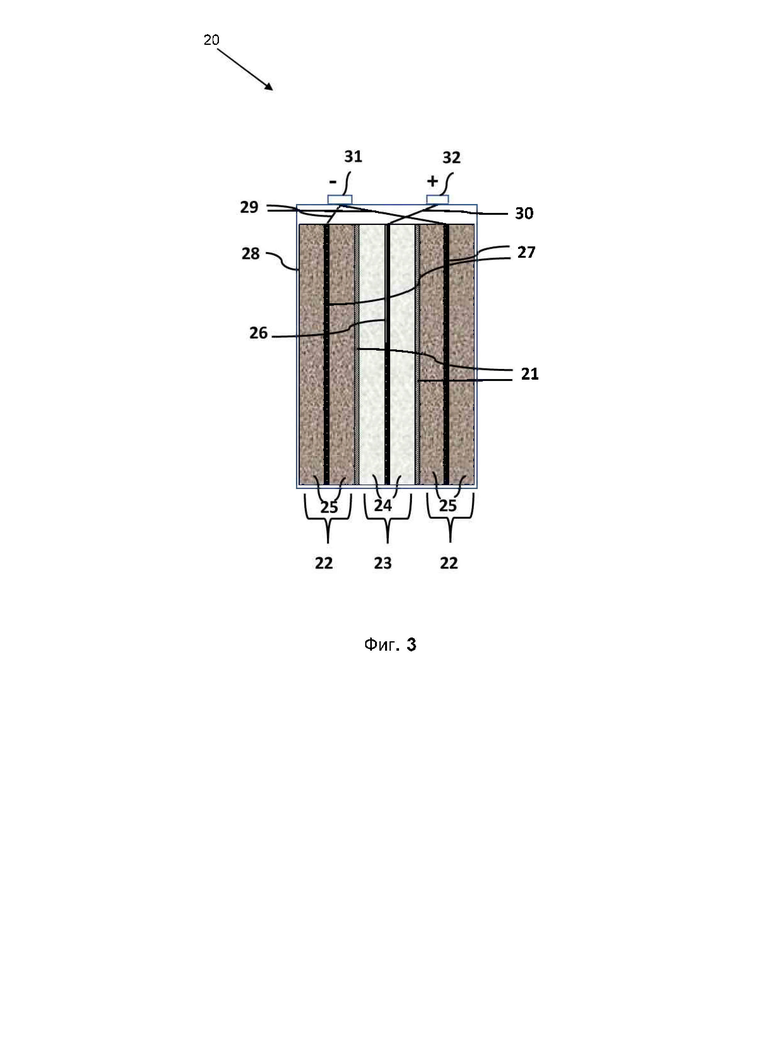

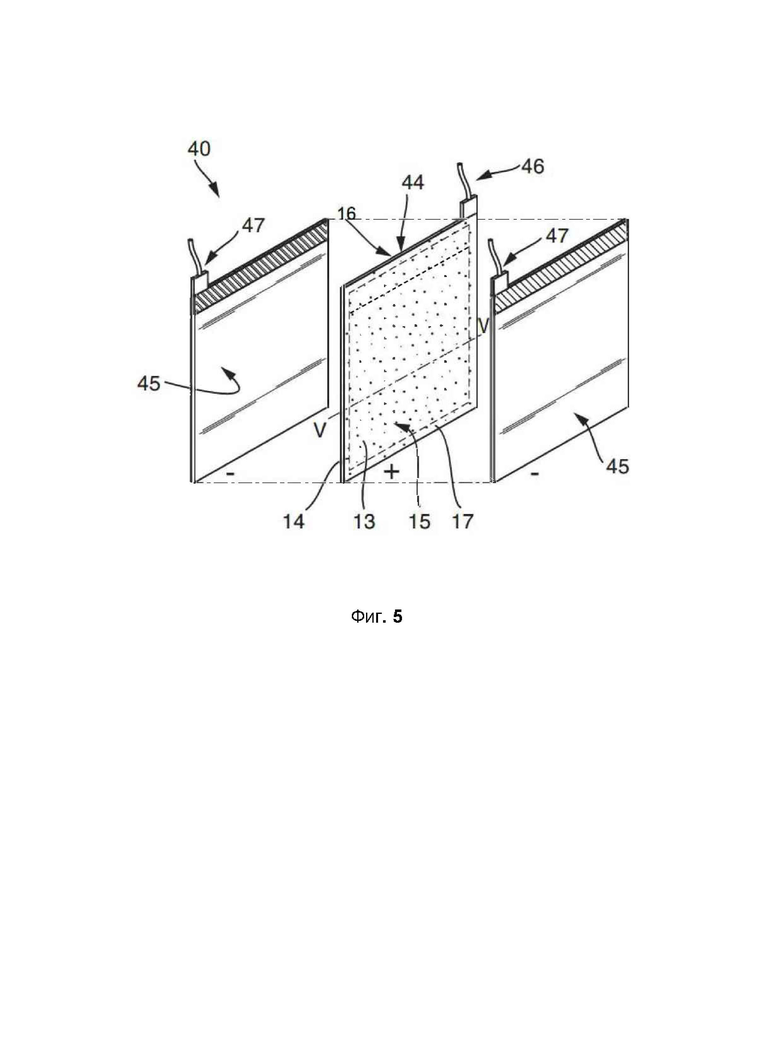
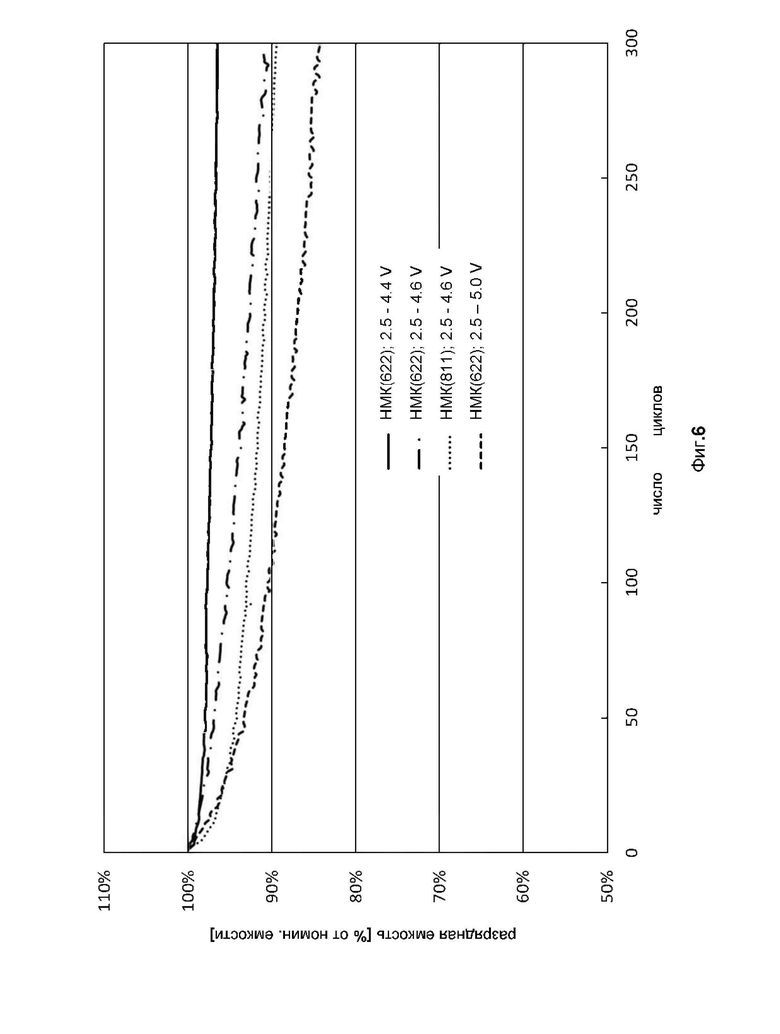
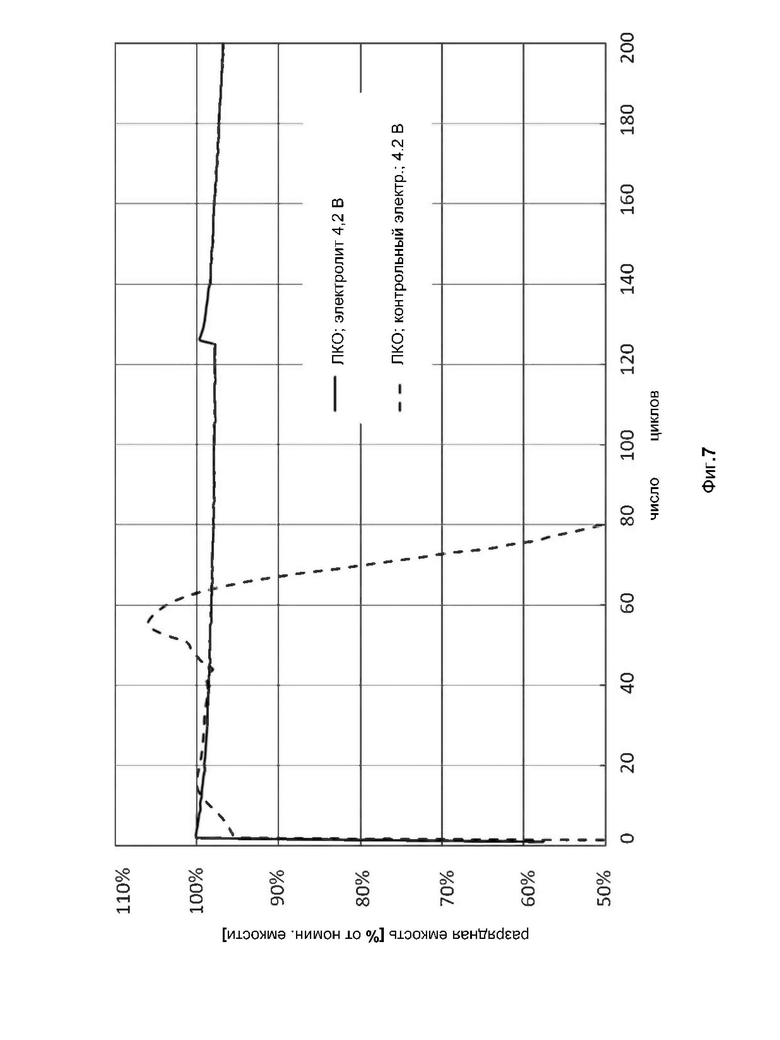
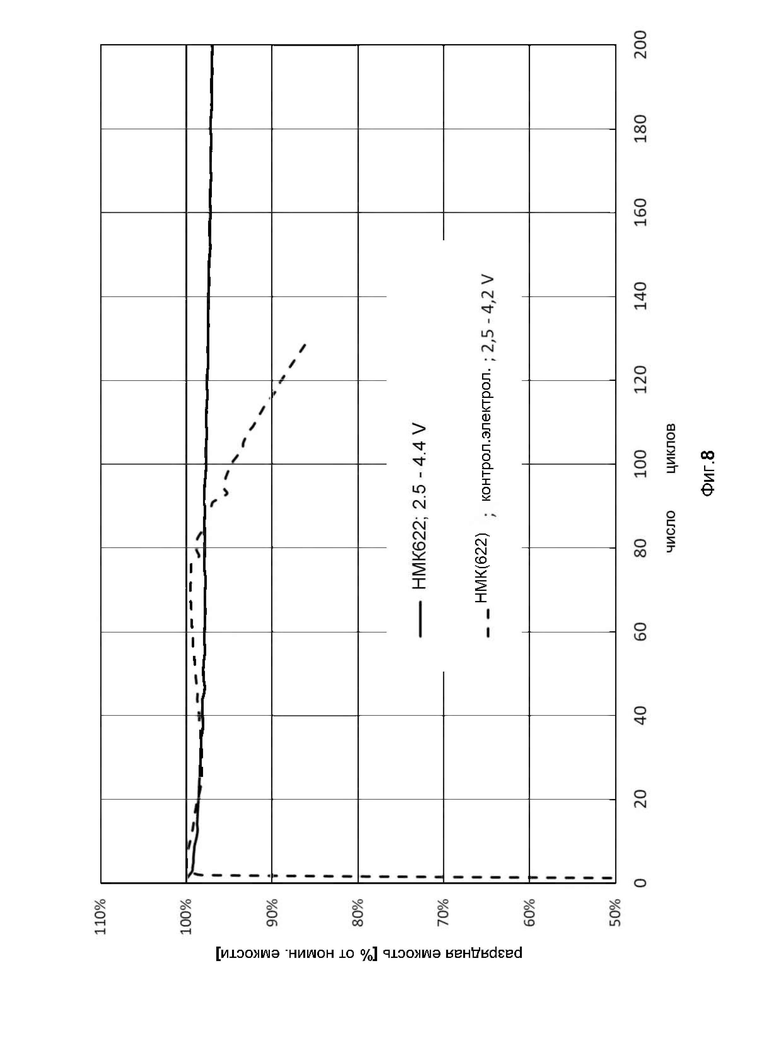
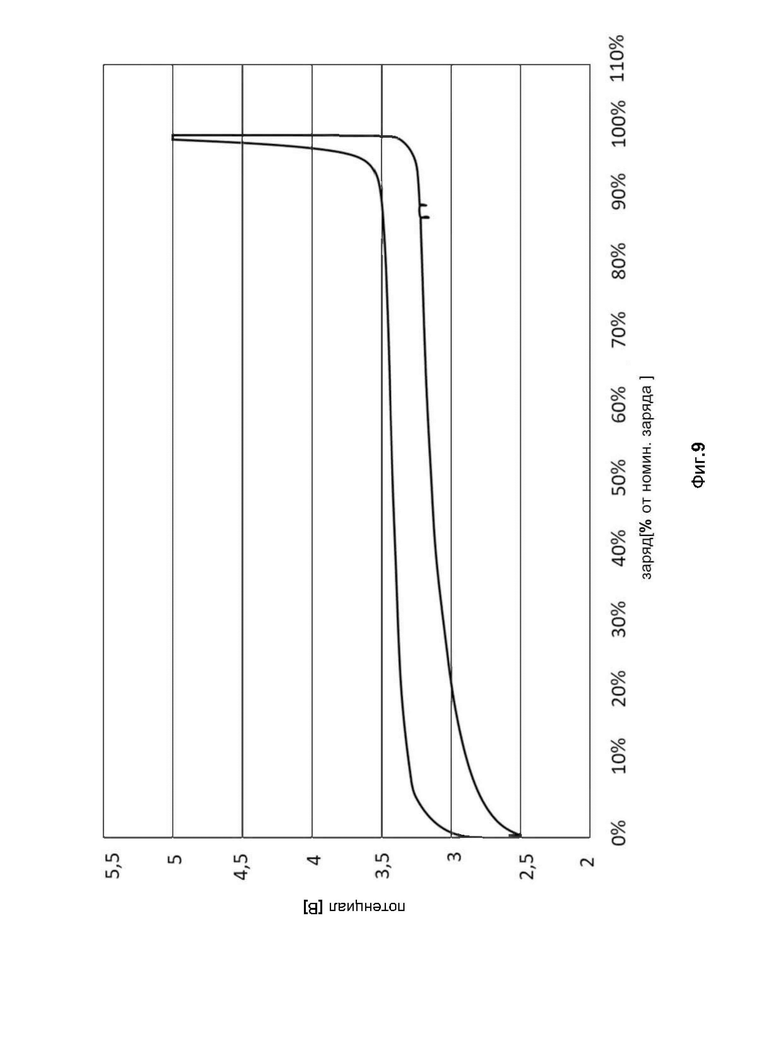
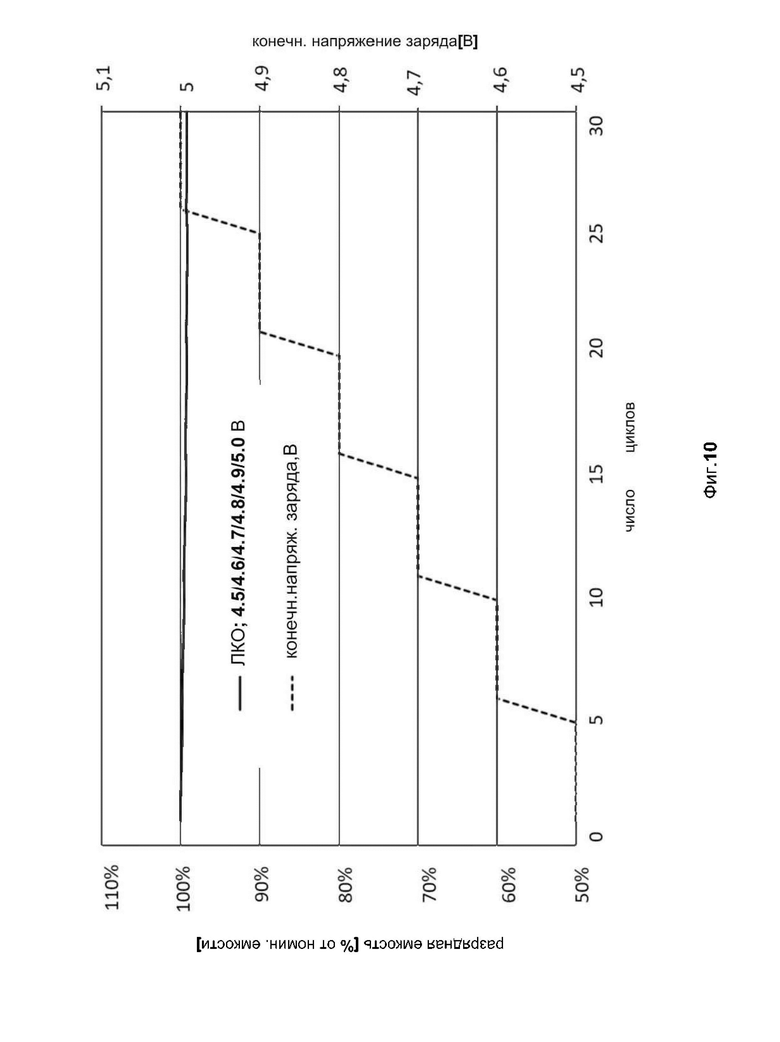
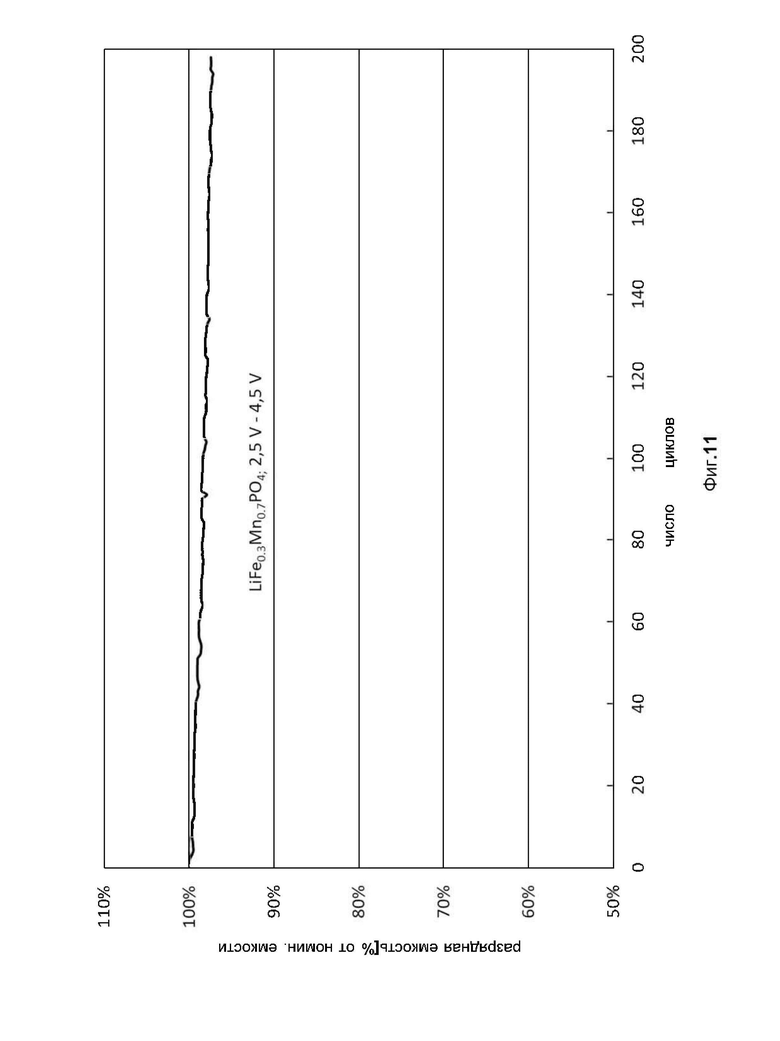
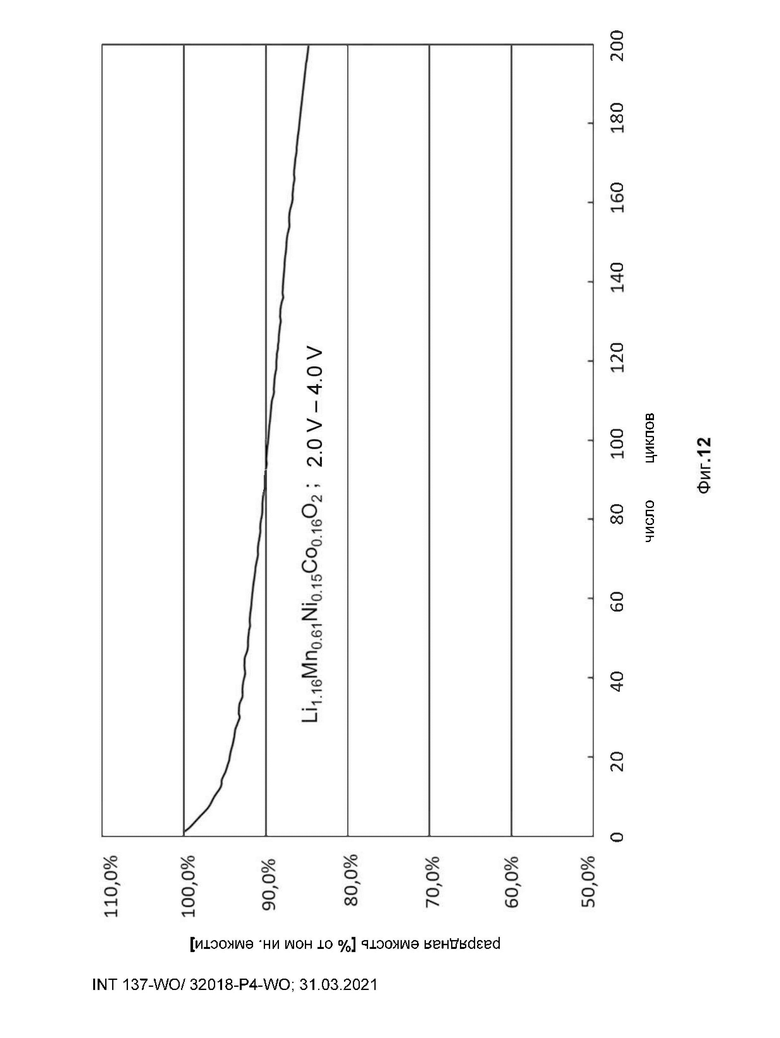
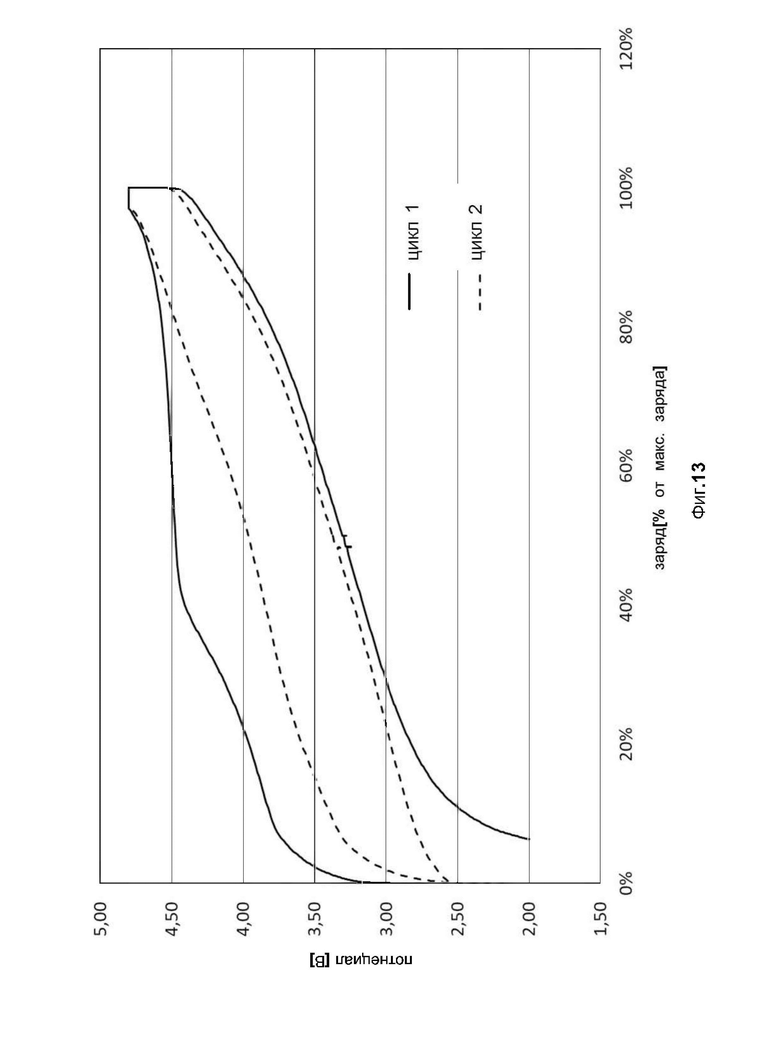
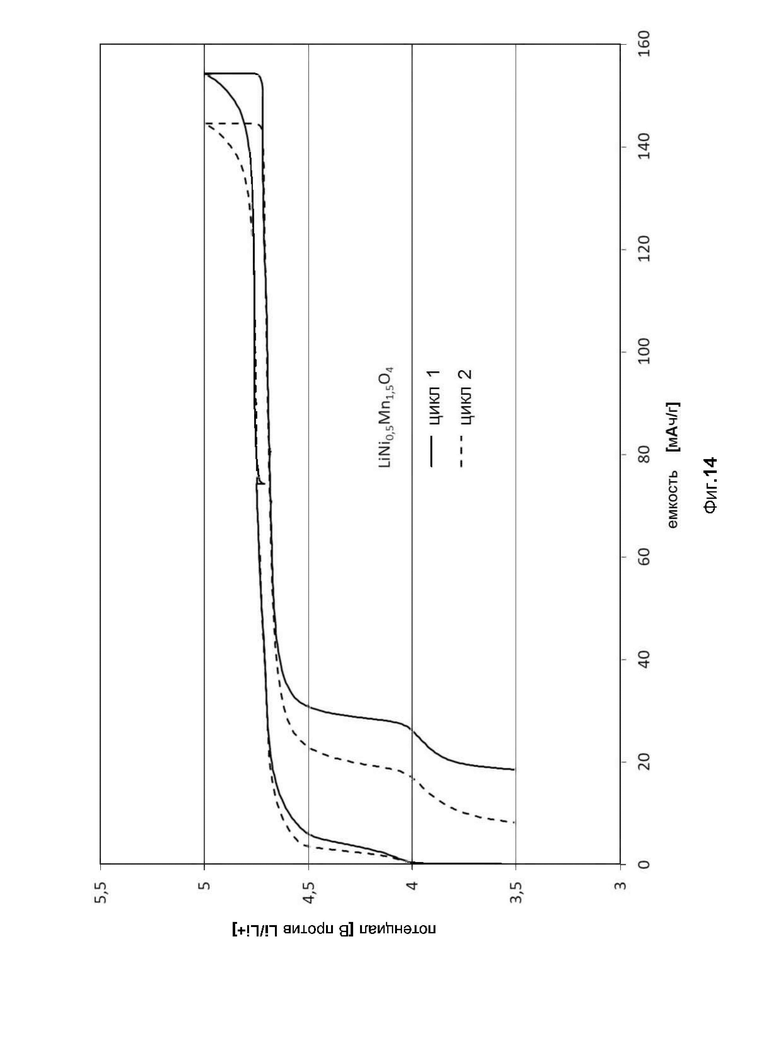
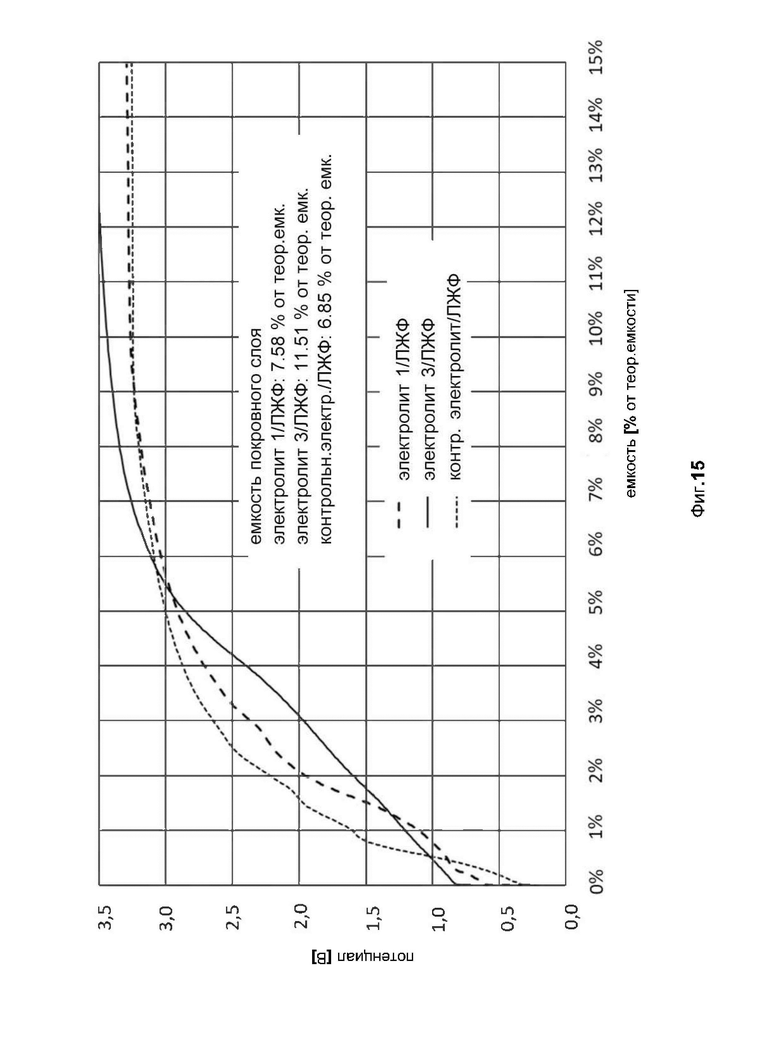
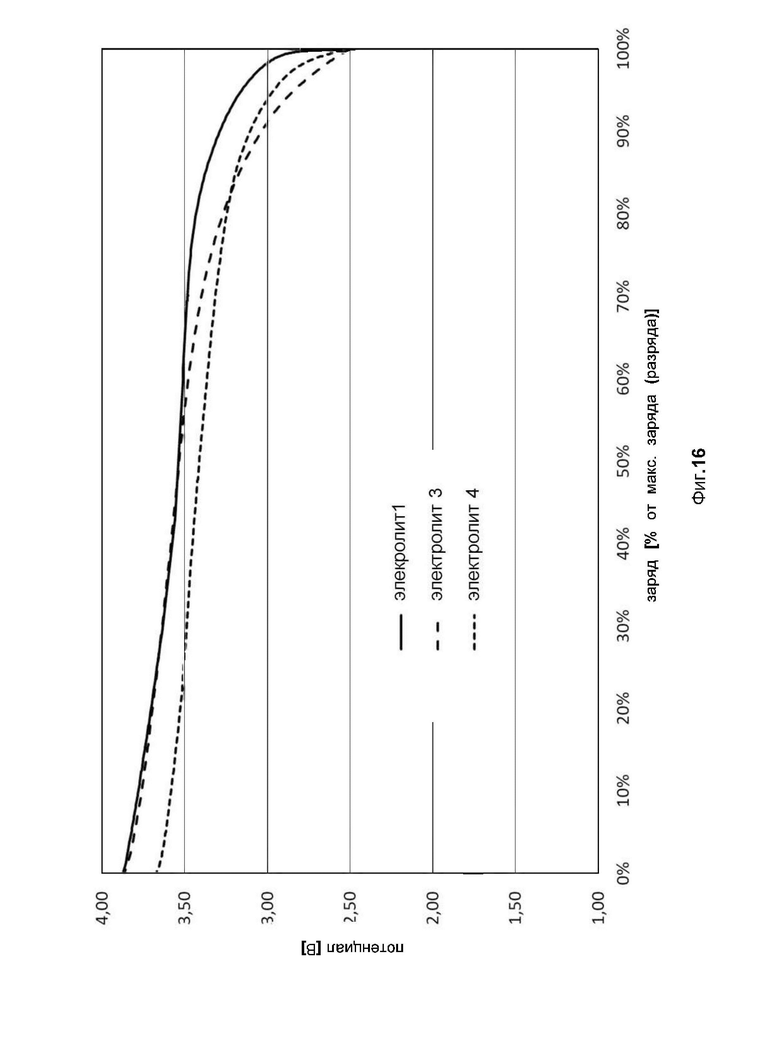
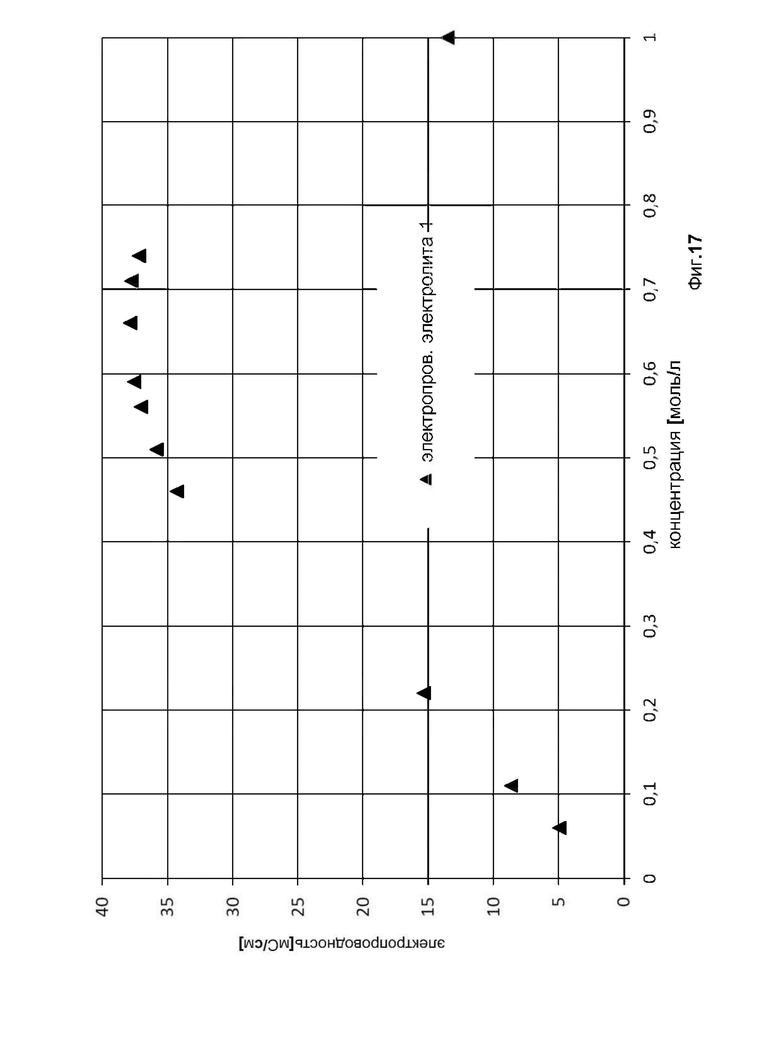
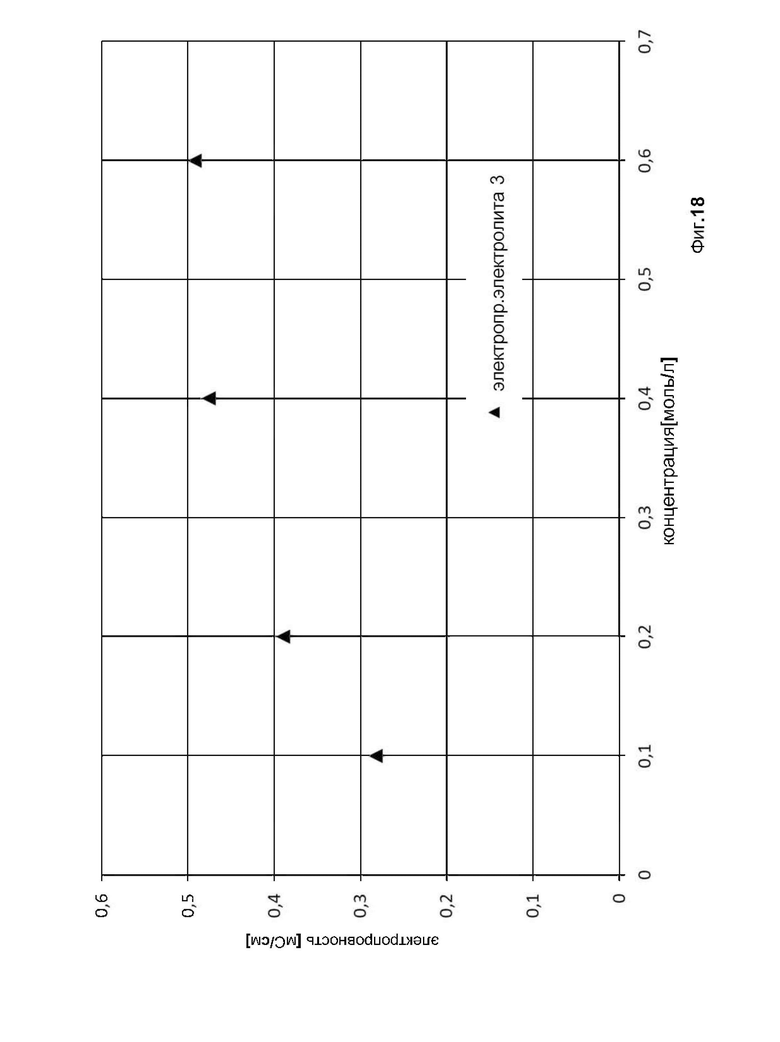
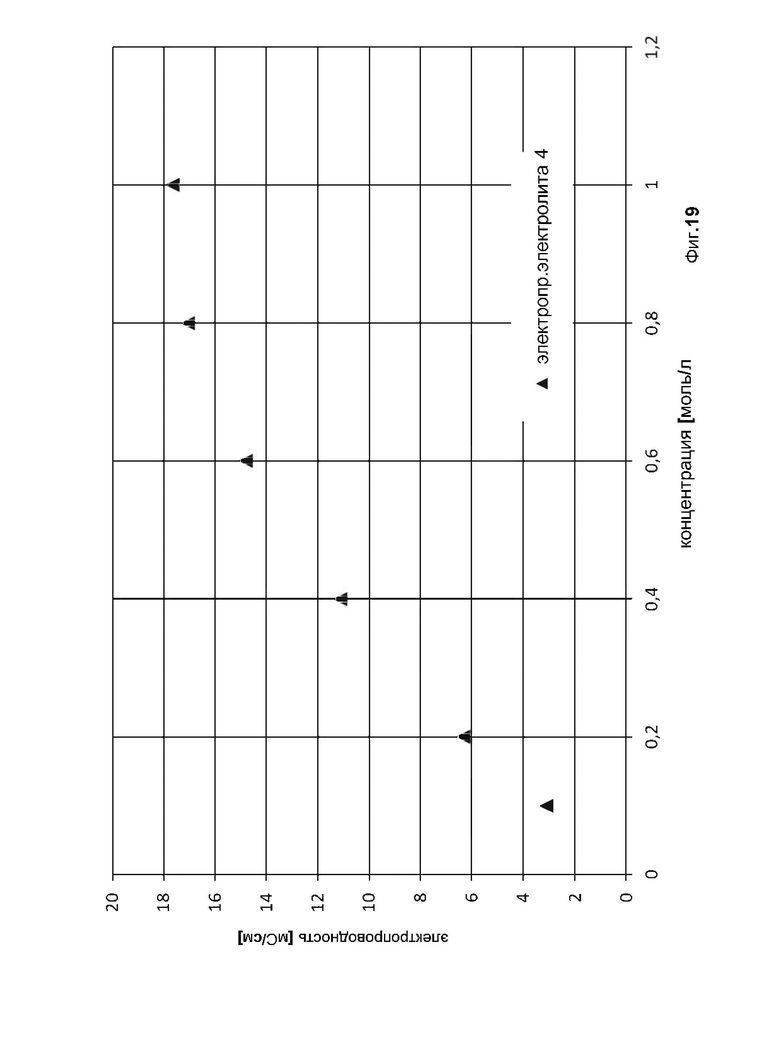
Изобретение относится к области электротехники, а именно к элементу аккумуляторной батареи с электролитом на основе SO2. Повышение надежности и срока службы аккумуляторной батареи при высокой разрядной емкости и цикличности является техническим результатом изобретения, который достигается за счет того, что элемент (2, 20, 40) аккумуляторной батареи содержит активный металл, по меньшей мере один положительный электрод (4, 23, 44), по меньшей мере один отрицательный электрод (5, 22, 45), корпус (1, 28) и электролит, при этом положительный электрод (4, 23, 44) выполнен в виде высоковольтного электрода, электролит основан на SO2 и содержит по меньшей мере одну первую проводящую соль формулы (1)
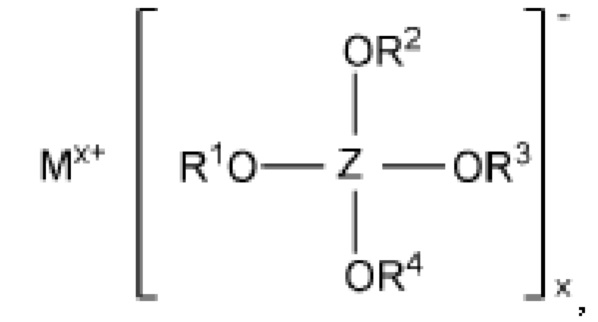
где: М - металл, выбранный из группы, состоящей из щелочных металлов, щелочноземельных металлов, металлов из группы 12 Периодической системы элементов и алюминия; х - целое число от 1 до 3; заместители R1, R2, R3 и R4 выбраны независимо друг от друга из группы, состоящей из C1-C10 алкила, С2-С10 алкенила, С2-С10 алкинила, С3-С10 циклоалкила, С6-С14 арила и С5-С14 гетероарила; Z означает алюминий или бор. 29 з.п. ф-лы, 19 ил., 5 табл., 10 пр.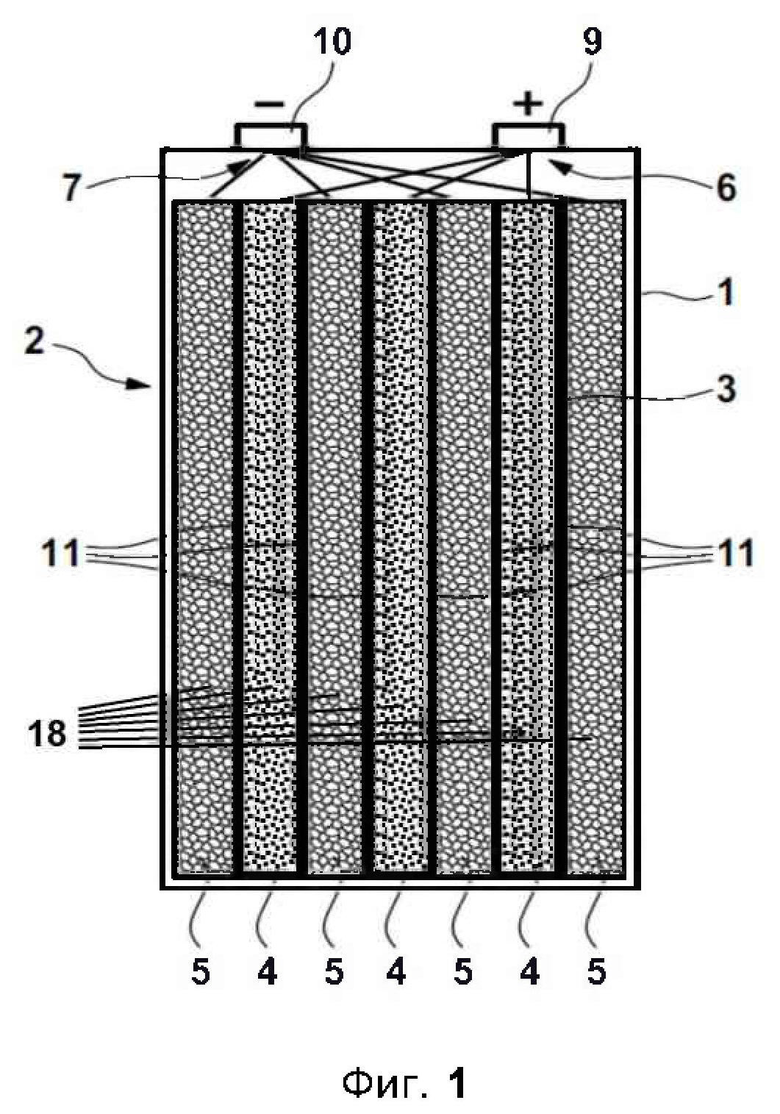
1. Элемент (2, 20, 40) аккумуляторной батареи, содержащий активный металл, по меньшей мере один положительный электрод (4, 23, 44), по меньшей мере один отрицательный электрод (5, 22, 45), корпус (1, 28) и электролит,
при этом положительный электрод (4, 23, 44) выполнен в виде высоковольтного электрода, электролит основан на SO2 и содержит по меньшей мере одну первую проводящую соль формулы (1):
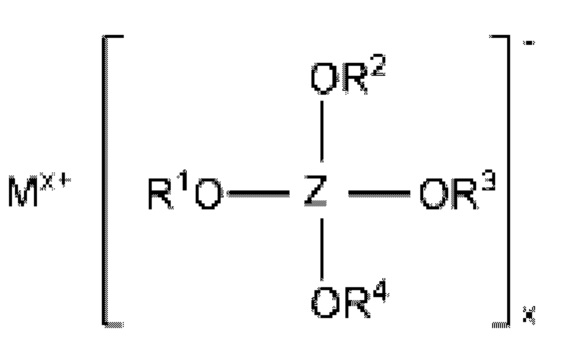
в которой означают:
- М - металл, выбранный из группы, состоящей из щелочных металлов, щелочноземельных металлов, цинка и алюминия;
- х - целое число от 1 до 3;
- заместители R1, R2, R3 и R4 выбраны независимо друг от друга из группы, состоящей из C1-С10 алкила, С2-С10 алкенила, С2-С10 алкинила, С3-С10 циклоалкила, С6-С14 арила и С5-С14 гетероарила,
- Z - алюминий или бор.
2. Элемент (2, 20, 40) аккумуляторной батареи по п. 1, в котором высоковольтный электрод (4, 23, 44) может заряжаться до достижения верхнего потенциала, равного по меньшей мере 4,4 В, предпочтительно равного по меньшей мере 4,8 В, предпочтительно равного по меньшей мере 5,2 В, предпочтительно равного по меньшей мере 5,6 В, особо предпочтительно равного по меньшей мере 6,0 В.
3. Элемент (2, 20, 40) аккумуляторной батареи по любому из предыдущих пунктов, в котором высоковольтный электрод (4, 23, 44) содержит в качестве активного материала по меньшей мере одно соединение предпочтительно следующего состава:
AxM'yM''zOa, где означают:
- А - по меньшей мере один металл, выбираемый из группы, состоящей из щелочных металлов, щелочноземельных металлов, цинка или алюминия,
- М' - по меньшей мере один металл, выбираемый из группы, состоящей из элементов М, V, Cr, Mn, Fe, Со, Bi, Cu, Zn,
- М'' - по меньшей мере один элемент, выбираемый из группы, состоящей из элементов групп 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 и 16 Периодической системы элементов,
- х, у - независимо друг от друга числа более 0,
- z - число более или равное 0,
- а - число более 0.
4. Элемент (2, 20, 40) аккумуляторной батареи по п. 3, в котором соединение имеет состав AxM'yM''zOa, где означают: А - литий, М' - марганец, М'' - кобальт, при этом х, у, z предпочтительно равны 1, а предпочтительно равно 4.
5. Элемент (2, 20, 40) аккумуляторной батареи по п. 3 или 4, в котором соединение имеет состав LixM'yM"zOa, в котором означают: М' - никель и марганец, М'' - кобальт.
6. Элемент (2, 20, 40) аккумуляторной батареи по п. 5, в котором соединение имеет состав LixNiy1Mny2CozOa, где х, y1, у2 независимо друг от друга означают числа более 0, z означает число более или равное 0, а означает число более 0.
7. Элемент (2, 20, 40) аккумуляторной батареи по п. 6, в котором соединение имеет состав LiNi0.33Мn0.33Со0.33O2, LiNi0.5Mn0.3Co0.2O2, LiNi0.5Mn0.25Co0.25O2, LiNi0.52Mn0.32Co0.16O2, LiNi0.55Mn0.30Co0.15O2, LiNi0.58Mn0.14Co0.28O2, LiNi0.6Mn0.2Co0.2O2, LiNi0.64Mn0.18Co0.18O2, LiNi0.65Mn0.27Co0.08O2, LiNi0.7Mn0.2Co0.1O2, LiNi0.7Mn0.15Co0.15O2, LiNi0.72Mn0.10Co0.18O2, LiNi0.76Mn0.14Co0.10O2, LiNi0.8Mn0.1Co0.1O2, LiNi0.86Mn0.04Co0.10O2, LiNi0.90Mn0.05Co0.05O2, LiNi0.95Mn0.025Co0.025O2 или их комбинации.
8. Элемент (2, 20, 40) аккумуляторной батареи по п. 3, в котором соединение имеет состав AxMnyM''zOa, где х - число более или равное 1, у - число, превышающее число z.
9. Элемент (2, 20, 40) аккумуляторной батареи по п. 8, в котором соединение имеет состав AxMnyM''zOa, где означают: А - литий, М'' - никель и/или кобальт, при этом соединение предпочтительно имеет состав Li1.2Mn0.525Ni0.175Co0.1O2, Lil.2Mn0.6Ni0.2O2, Li1.16Mn0.61Ni0.15Co0,16O2 или Li1.2Mn0.54Ni0.13Co0.13O2.
10. Элемент (2, 20, 40) аккумуляторной батареи по п. 3, в котором соединение имеет состав AxM'yM''1z1M"2z2O4, при этом М''2 означает фосфор, z2 равно 1.
11. Элемент (2, 20, 40) аккумуляторной батареи по п. 10, в котором соединение имеет состав AxM'yM''1z1M''2z2О4, где означают А - литий, М' - железо, М"1 - марганец, М"2 - фосфор, z2 равно 1, при этом соединение предпочтительно имеет состав Li(Fe0.3Mn0.7)PО4.
12. Элемент (2, 20, 40) аккумуляторной батареи по любому из предыдущих пунктов, в котором заместители R1, R2, R3, R4 первой проводящей соли выбраны независимо друг от друга из группы, состоящей из:
- C1-C6 алкила, предпочтительно С2-С4 алкила, особо предпочтительно алкильных групп 2-пропил, метил, этил;
- С2-С6 алкенила, предпочтительно С2-С4 алкинила, особо предпочтительно алкенильных групп этенил и пропенил;
- С2-С6 алкинила, предпочтительно С2-С4 алкинила;
- С3-С6 циклоалкила;
- фенила;
- С5-С7 гетероарила.
13. Элемент (2, 20, 40) аккумуляторной батареи по любому из предыдущих пунктов, в котором по меньшей мере один из заместителей R1, R2, R3, R4 первой проводящей соли замещен по меньшей мере одним атомом фтора и/или по меньшей мере одной химической группой, при этом химическая группа выбирается из группы, состоящей из C1-C4 алкила, С2-С4 алкенила, С2-С4 алкинила, фенила и бензила.
14. Элемент (2, 20, 40) аккумуляторной батареи по любому из предыдущих пунктов, в котором по меньшей мере один из заместителей R1, R2, R3, R4 первой проводящей соли является группой СF3 или группой OSO2CF3.
15. Элемент (2, 20, 40) аккумуляторной батареи по любому из предыдущих пунктов, в котором первая проводящая соль выбирается из группы, состоящей из:
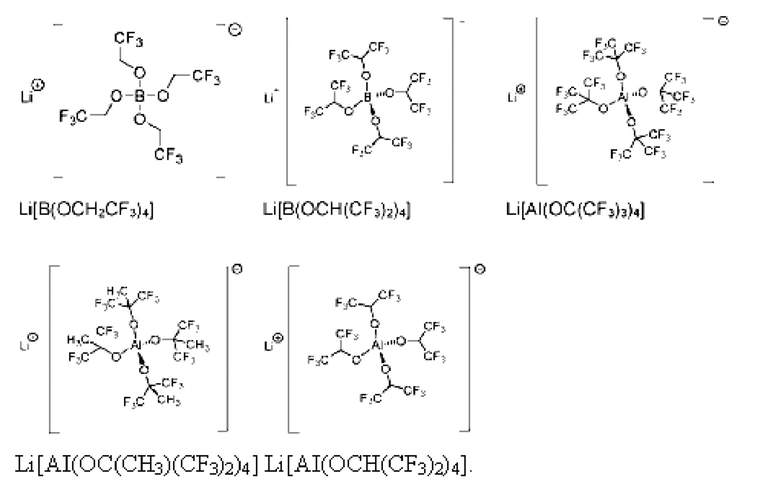
16. Элемент (2, 20, 40) аккумуляторной батареи по любому из предыдущих пунктов, в котором электролит содержит по меньшей мере одну вторую проводящую соль, отличающуюся от первой проводящей соли формулы (1).
17. Элемент (2, 20, 40) аккумуляторной батареи по п. 16, в котором вторая проводящая соль электролита является соединением щелочного металла, в частности соединением лития, выбираемым из группы, состоящей из алюмината, галогенида, оксалата, бората, фосфата, арсената и галлата.
18. Элемент (2, 20, 40) аккумуляторной батареи по п. 16 или 17, в котором второй проводящей солью электролита является тетрагалогеналюминат лития, в частности тетрахлоралюминат лития.
19. Элемент (2, 20, 40) аккумуляторной батареи по любому из предыдущих пунктов, в котором электролит содержит по меньшей мере одну добавку.
20. Элемент (2, 20, 40) аккумуляторной батареи по п. 19, в котором добавка для электролита выбирается из группы, состоящей из виниленкарбоната и его производных, винилэтиленкарбоната и его производных, метилэтиленкарбоната и его производных, (бис-оксилат)бората лития, дифтор(оксалат)бората лития, тетрафтор(оксалат)фосфата лития, оксалата лития, 2-винилпиридина, 4-винилпиридина, циклических экзометиленкарбонатов, сультонов, циклических и ациклических сульфонатов, ациклических сульфитов, циклических и ациклических сульфинатов, органических сложных эфиров неорганических кислот, ациклических и циклических алканов, которые (ациклические и циклические алканы) имеют точку кипения при давлении 1 атм по меньшей мере 36°С, ароматических соединений, галогенизированных циклических и ациклических сульфонилимидов, галогенизированных циклических и ациклических сложных эфиров фосфата, галогенизированных циклических и ациклических фосфинов, галогенизированных циклических и ациклических фосфитов, галогенизированных циклических и ациклических фосфазенов, галогенизированных циклических и ациклических силиламинов, галогенизированных циклических и ациклических сложных эфиров, галогенизированных циклических и ациклических амидов, галогенизированных циклических и ациклических ангидридов и галогенизированных органических гетероциклов.
21. Элемент (2, 20, 40) аккумуляторной батареи по любому из предыдущих пунктов, в котором электролит имеет следующий состав, соотнесенный с общим весом электролита:
(i) 5-99,4 вес. % диоксида серы,
(ii) 0,6-95 вес. % первой проводящей соли,
(iii) 0-25 вес. % второй проводящей соли,
(iv) 0-10 вес. % добавки.
22. Элемент (2, 20, 40) аккумуляторной батареи по любому из предыдущих пунктов, в котором концентрация первой проводящей соли составляет от 0,01 до 10 моль/л, предпочтительно от 0,05 до 10 моль/л, предпочтительно от 0,1 до 6 моль/л, особо предпочтительно от 0,2 до 3,5 моль/л, от общего объема электролита.
23. Элемент (2, 20, 40) аккумуляторной батареи по любому из предыдущих пунктов, в котором электролит содержит по меньшей мере 0,1 моль SO2, предпочтительно по меньшей мере 1 моль SO2, предпочтительно по меньшей мере 5 моль SO2, предпочтительно по меньшей мере 10 моль SO2, особо предпочтительно по меньшей мере 20 моль SO2, на 1 моль проводящей соли.
24. Элемент (2, 20, 40) аккумуляторной батареи по любому из предыдущих пунктов, в котором активным металлом являются:
- щелочной металл, в частности литий или натрий,
- щелочноземельный металл, в частности кальций,
- цинк или
- алюминий.
25. Элемент (2, 20, 40) аккумуляторной батареи по любому из предыдущих пунктов, в котором отрицательным электродом (5, 22) является электрод внедрения, содержащий в качестве активного материала преимущественно углерод, в частности, в виде графита.
26. Элемент (2, 20, 40) аккумуляторной батареи по любому из предыдущих пунктов, в котором высоковольтный электрод (4, 23, 44) содержит по меньшей мере одно соединение металла, выбираемое из группы, состоящей из оксида металла, галогенида металла и фосфата металла, причем металлом металлического соединения является предпочтительно переходной металл с порядковым номером от 22 до 28 Периодической системы элементов, в частности кобальт, никель, марганец или железо.
27. Элемент (2, 20, 40) аккумуляторной батареи по любому из предыдущих пунктов, в котором высоковольтный электрод содержит по меньшей мере одно соединение металла, имеющее химическую структуру шпинели, слоистого оксида, способного к превращению соединения или полианионного соединения.
28. Элемент (2, 20, 40) аккумуляторной батареи по любому из предыдущих пунктов, в котором высоковольтный электрод (4, 23, 44) и/или отрицательный электрод (5, 22, 45) содержат разрядный элемент (26, 27), выполненный преимущественно
- либо плоским в виде металлического листа или металлической фольги,
- либо трехмерным в виде пористой металлической структуры, в частности металлической пены (18).
29. Элемент (2, 20, 40) аккумуляторной батареи по любому из предыдущих пунктов, в котором высоковольтный электрод (4, 23, 44) и/или отрицательный электрод (5, 22, 45) содержат по меньшей мере одно связующее, предпочтительно фторированное связующее, в частности поливинилиденфторид, и/или тройной сополимер, состоящий из тетрафторэтилена, гексафторпропилена и винилиденфтортида,
или связующее из полимера, образованного мономерными структурными звеньями сопряженной карбоновой кислоты, или солью щелочного металла, щелочноземельного металла или аммония этой сопряженной карбоновой кислоты или их комбинацией,
или связующее из полимера, основанного на мономерных структурных звеньях стирола и бутадиена, или связующее из группы карбоксиметилцеллюлоз,
при этом связующее присутствует предпочтительно при концентрации не более 20 вес. %, предпочтительно не более 15 вес. %, предпочтительно не более 10 вес. %, предпочтительно не более 7 вес. %, предпочтительно не более 5 вес. %, особо предпочтительно не более 2 вес. %, от общего веса положительного электрода.
30. Элемент (2, 20, 40) аккумуляторной батареи по любому из предыдущих пунктов, в котором содержатся несколько отрицательных электродов (5, 22, 45) и по меньшей мере один или предпочтительно несколько положительных электродов (4, 23, 44) в виде высоковольтных электродов, которые, перемежаясь, расположены в виде стопки внутри корпуса (1, 28), причем высоковольтные (4, 23, 44) и отрицательные (5, 22, 45) электроды предпочтительно разделены электрически между собой сепараторами (11, 21, 13).
| СПОСОБ ДИАГНОСТИКИ РЕАЛЬНОЙ СТРУКТУРЫ КРИСТАЛЛОВ | 2013 |
|
RU2534719C1 |
| НОЖНИЦЫ ДЛЯ РЕЗКИ ЛИСТОВОГО ПРОКАТА | 2007 |
|
RU2360772C1 |
| ИОННЫЕ ЖИДКОСТИ II | 2001 |
|
RU2272043C2 |
| Устройство для очистки труб | 1983 |
|
SU1201004A1 |
| JP 2008277001 A, 13.11.2008 | |||
| JP 2003007334 A, 10.01.2003. | |||
Авторы
Даты
2022-12-23—Публикация
2020-07-30—Подача