Изобретение относится к медицине, а именно к экспериментальной офтальмологии, и может быть использовано для моделирования нейродегенеративных процессов в глазу с целью разработки новых способов их диагностики и лечения.
Нейродегенеративные процессы в сетчатке являются причиной необратимого снижения зрения при многих широко распространенных глазных болезнях, таких как возрастная макулодистрофия, глаукома, диабетическая ретинопатия и др. Нейродегенеративные процессы в сетчатке развиваются при нейродегенеративных заболеваниях центральной нервной системы, таких, например, как болезнь Альцгеймера и болезнь Паркинсона (Ashok A, Singh Ν, Chaudhary S, Bellamkonda V, Kritikos AE, Wise AS, Rana N, McDonald D, Ayyagari R. Retinal degeneration and Alzheimer's disease: an evolving link. International Journal of Molecular Sciences. 2020;21(19):7290; Chen PJ, Wan L, Lai JN, Chen CS, Chen JJ, Yen WM, Chiu LT, Ни КС, Tien PT, Lin HJ. Increased risk of Parkinson's disease among patients with age-related macular degeneration. BMC Ophthalmol. 2021;21(1):426). В основе дегенерации нервных клеток сетчатки и мозга лежат общие механизмы - это стресс эндоплазматического ретикулума, митохондриальная дисфункция, образование неправильно свернутых белков и их конгломератов, нейровоспаление (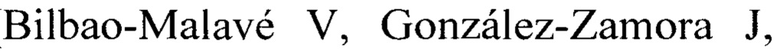 de la Puente Μ, Recalde S, Fernandez-Robredo Ρ, Hernandez Μ, Lay ana AG, Saenz de Viteri M. Mitochondrial dysfunction and endoplasmic reticulum stress in age related macular degeneration, role in pathophysiology, and possible new therapeutic strategies. Antioxidants (Basel). 2021; 10(8): 1170). Клинические признаки этих патологий выявляются на стадии далеко зашедшего процесса необратимой гибели нервных клеток, и сами заболевания, несмотря на имеющиеся достижения в терапии, очень трудно поддается лечению. Нарушение нервной регуляции в переднем сегменте глаза также является результатом локальных и системных нейродегенеративных процессов и сопровождает и/или является причиной глазных заболеваний. Поэтому проблема раннего выявления и разработка методов лечения как системных, так и глазных нейродегенеративных процессов является весьма актуальной. Моделирование нейродегенеративного процесса необходимо для изучения молекулярных механизмов развития нейродегенерации, разработки патогенетически обоснованных методов лечения, поиска биомаркеров для раннего прогноза.
de la Puente Μ, Recalde S, Fernandez-Robredo Ρ, Hernandez Μ, Lay ana AG, Saenz de Viteri M. Mitochondrial dysfunction and endoplasmic reticulum stress in age related macular degeneration, role in pathophysiology, and possible new therapeutic strategies. Antioxidants (Basel). 2021; 10(8): 1170). Клинические признаки этих патологий выявляются на стадии далеко зашедшего процесса необратимой гибели нервных клеток, и сами заболевания, несмотря на имеющиеся достижения в терапии, очень трудно поддается лечению. Нарушение нервной регуляции в переднем сегменте глаза также является результатом локальных и системных нейродегенеративных процессов и сопровождает и/или является причиной глазных заболеваний. Поэтому проблема раннего выявления и разработка методов лечения как системных, так и глазных нейродегенеративных процессов является весьма актуальной. Моделирование нейродегенеративного процесса необходимо для изучения молекулярных механизмов развития нейродегенерации, разработки патогенетически обоснованных методов лечения, поиска биомаркеров для раннего прогноза.
Нейродегенеративные процессы в сетчатке глаза часто воспроизводятся путем повышения внутриглазного давления, моделирования диабета, с помощью хирургических вмешательств и других методов, которые вызывают системные изменения в организме или сопровождаются травматическим воздействием на ткани глаза. Использование именно локального введения нейротоксина позволяет прицельно воздействовать на нервные клетки. В отличие от широко применяемого для моделирования болезни Паркинсона нейротоксина - 1-метил-4-фенил-1,2,3,6-тетрагидропиридина (МФТП), проникающего через гистогематические барьеры и поэтому быстро выводящегося из глаза, после интравитреального введения, нейротоксин 6-OHDA не проходит через эти барьеры и позволяет создавать необходимую концентрацию. 6-OHDA является высоко окисляемым аналогом дофамина, который захватывается транспортером дофамина, что позволяет ему поступать в катехоламинергические нейроны, где он оказывает нейротоксичесое действие. Предполагается 3 механизма нейротоксического действия 6-OHDA: 1) внутриклеточное или внеклеточное самоокисление 6-OHDA, которое способствует образованию перекиси водорода и супероксидных и гидроксильных радикалов, 2) образование перекиси водорода под действием моноаминоксидазы и 3) прямое ингибирование комплекса в митохондриальной дыхательной цепи.
Генерируемый 6-OHDA окислительный стресс в нервных клетках приводит как к нейровоспалению, так и к гибели клеток путем апоптоза.
Известны способы моделирования нейродегенерации сетчатки у кроликов путем интравитреального введения 6-OHDA, при этом используют очень широкий диапазон доз 6-OHDA - от 60 мкг до 2000 мкг, показана высокая зависимость производимого эффекта от введенной дозы (Olivier Ρ, Jolicoeur FB, Lafond G, Drumheller AL, Brunette JR. Dose related effects of 6-OHDA on rabbit retinal dopamine concentrations and ERG B-wave amplitudes. Brain Res Bull. 1986 May;16(5):751-3. doi: 10.1016/0361-9230(86)90148-6. PMID: 3091194; Moro F, Scapagnini U, Gorgone G, Reina R, Scaletta S, Drago F. Chronic degeneration of aminergic nerve endings and blood-aqueous barrier. Albrecht Von Graefes Arch Klin Exp Ophthalmol. 1979 Feb 8;209(4):225-30. doi: 10.1007/BF00419056. PMID: 218472.). В работе Olivier и соавт., было показано, что при дозе 6-OHDA 60 мкг изменений амплитуды В-волны ЭРГ или концентраций дофамина и его основных метаболитов в сетчатке не происходит, при дозе 1200 мкг наблюдается полное угасание ERG и почти полное исчезновение этих метаболитов. При промежуточной дозе 300 мкг 6-OHDA были получены значительные увеличения амплитуд В-волн и снижение концентраций дофамина и его метаболитов в сетчатке. Эти результаты демонстрируют, что селективное снижение дофамина сетчатки и его метаболитов может быть получено при однократном интравитреальном введении 300 мкг 6-OHDA, которая была выбрана ими для дальнейших исследований.
Ближайшим аналогом предлагаемого способа является способ того же назначения, включающий однократное интравитреальное введение кроликам 300 мкг 6-OHDA в 300 мкл раствора 0,9% хлористого натрия, содержащего аскорбиновую кислоту в концентрации 0,5% (Oliver Ρ, Jolicoeur FB, Lafond G, Drumheller A, Brunette JR. Effects of retinal dopamine depletion on the rabbit electroretinogram. Doc Ophthalmol. 1987 Aug;66(4):359-71. doi: 10.1007/BF00213664. PMID: 3123188). Аскорбиновая кислота необходима для стабилизации 6-OHDA. Авторами было показано значительное и прогрессирующее снижение концентраций дофамина и его основных метаболитов в сетчатке, при этом концентрации норадреналина, серотонина и 5-гидроксииндолуксусной кислоты не изменялись, что свидетельствовало о специфическом нейротоксическом действии 6-OHDA на дофаминергические нейроны сетчатки. Однако доза, превышающая 200 мкг, помимо воздействия на нейроны, может оказывать достаточно выраженное токсическое действие на другие клеточные структуры. Авторы работы вводили в стекловидное тело препарат в очень большом объеме - 300 мкл, что может вызвать большие изменения гидро- и гемодинамики глаза, а также метаболических процессов только за счет механического воздействия. Кроме того, в качестве контроля был использован парный глаз, однако учитывая существование взаимодействий между парными глазами, обусловленных сложным комплексом нейрогуморальных механизмов, приводящих к реакции парного глаза на нарушения в другом глазу, использование парного глаза в качестве контроля не корректно.
Задачей предлагаемого изобретения явилось создание адекватной модели нейродегенерации сетчатки при отсутствии негативного воздействия нейротоксина.
Техническим результатом предлагаемого изобретения является получение хорошо воспроизводимого и обратимого нейродегенеративного процесса в глазу у кролика.
Технический результат достигается за счет интравитреального введения 6-OHDA дважды с интервалом 2 часа по 100 мкг в растворе объемом 50 мкл.
Выбор предложенного нами режима интравитреального введения 6-OHDA основан на том, что доза менее 100 мкг не дает выраженных изменений (ОКТ, ВГД, содержание дофамина), тогда как введение 6-OHDA по 100 мкг дважды через 2 часа позволяет получить необходимый эффект. Кроме того, двукратное введение позволяет одномоментно вводить меньшую дозу в меньшем объеме, в то время как интравитреальное введение большего объема жидкости оказывает негативное действие на структуры глаза и на внутриглазное давление.
В исследование были включены 12 кроликов породы Шиншилла весом 2-2,5 кг. Первой опытной группе (6 кроликов, 12 глаз) проводили двукратные интравитреальные инъекции нейротоксина 6-OHDA с интервалом 2 часа в оба глаза по 100 мкг 6-OHDA в 50 мкл NaCl 0,9%, содержащего аскорбиновую кислоту в концентрации 0,5%. Второй контрольной группе кроликов (6 кроликов, 12 глаз) вводили интравитреально двухкратно с интервалом 2 часа по 50 мкл NaCl 0,9%, содержащего аскорбиновую кислоту в концентрации 0,5%, в оба глаза.
Проводили измерение внутриглазного давления (ВГД) с помощью автоматического тонометра (Tonovet, Финляндия) до и после введения нейротоксина в течение 3-х недель. За состоянием сетчатки наблюдали с помощью оптической когерентной томографии (ОКТ) (Heidelberg Engineering, Германия) до введения нейротоксина, на 10-й и 20-й день. Методом ОКТ оценивали морфометрические параметры центральной области сетчатки под зоной выхода зрительного нерва: среднюю толщину сетчатки, толщину отдельных слоев сетчатки. Во внутриглазной жидкости и в гомогенате сетчатки проводили определение концентрации дофамина методом ИФА с использованием наборов фирмы Cloud-Clone Corp., США, измерения проводили на фотометре «Synergy МХ» («BioTek», США).
В контрольной группе после интравитреальной инъекции в течение всего периода наблюдения ВГД оставалось повышенным на 4-6 мм.рт.ст.по сравнению с исходным, что можно объяснить воздействием введенного раствора. В опытной группе ВГД на 1 сутки оставалось на уровне нормы и достоверно снизилось на 7 сутки относительно исходного уровня и по сравнению с контрольной группой (р<0,006), далее на 20 сутки ВГД возрастало, достигая уровня, превышающего контрольный, и на 21 сутки снижалось до уровня контроля (чертеж - изменение ВГД (мм рт. ст.) после интравитреального введения 6-OHDA (опыт) и физраствора (контроль). Снижение уровня ВГД в первую неделю после введения 6-OHDA по сравнению с контролем связано с действием этого нейротоксина, вызывающего симпатэктомию в переднем отделе глаза (Hoyle С.Н., Pintor J. J., Diadenosine tetraphosphate protects sympathetic terminals from 6-hydroxydopamine-induced degeneration in the eye, Acta Physiol 2010, 199, 205-210doi: 10.1111/j. 1748-1716.2010.02089.x, p.205 - 210). Об этом свидетельствуют наши данные о снижении содержания дофамина в внутриглазной жидкости и сетчатке через 10 дней после введения 6-OHDA. Во внутриглазной жидкости содержание дофамина в опытных глазах составляло 0,018±0,004 пг/мг, в контрольных 0,113±0,03 пг/мг (р<0,01), в сетчатке опытных глаз - 0,05±0,009 пг/мг, в контрольных 0,103±0,0127 пг/мл (р<0,001). В других исследованиях интравитреальное введение 6-OHDA в более высоких дозах сопровождалось более длительным снижением ВГД, а в малых дозах (60 мкг) не оказывало влияния на ВГД. В нашем исследовании показано, что двухкратное введение нейротоксина по 100 мкг вызывает сначала снижение ВГД, затем постепенное его увеличение, превосходящее контрольный уровень на 20 сутки и к 21 суткам ВГД снижение до контрольных значений.
Снижение содержания дофамина во внутриглазной жидкости и изменение ВГД свидетельствуют о том, что интравитреальное введение 6-OHDA в предложенном режиме позволяет создать адекватную модель для изучения заболеваний, вызывающих глазную симпатическую дизавтономию.
По данным ОКТ-исследования у кроликов на 10-й день после интравитреального введения нейротоксина выявлены нейродегенеративные изменения в сетчатке. Происходит утолщение сетчатки в среднем на 15-20%. Обнаружено утолщение внутреннего плексиформного слоя на 10-30% и внутреннего ядерного слоя, где присутствуют дофаминергические амакриновые клетки, в среднем в 1,5 раза. На 20-е сутки происходил постепенный возврат и восстановление прежнего вида и размера слоев сетчатки. В контрольной группе достоверных изменений структуры и размера слоев сетчатки не обнаружено.
Таким образом, предлагаемый режим интравитреального введения 6-OHDA двукратно по 100 мкг в 50 мкл раствора NaCl 0,9%, содержащего аскорбиновую кислоту в концентрации 0,5%, позволяет воспроизвести модель нейродегенеративного процесса в глазу у кроликов, сопровождающегося снижением содержания дофамина во внутриглазной жидкости и сетчатке, обратимым снижением ВГД вследствие снижения активности симпатической иннервации (симпатэктомии) и обратимыми изменениями в сетчатке, отражающими начало нейродегенеративных процессов. Эта модель может быть использована для разработки новых методов лечения нейродегенеративных процессов в глазу и для поиска биомаркеров для их раннего прогноза.
Способ осуществляют следующим образом.
Кролику интравитреально вводят нейротоксин 6-OHDA в растворе 0,9% хлористого натрия, содержащего аскорбиновую кислоту в концентрации 0,5%. При этом 6-OHDA вводят дважды с интервалом 2 часа по 100 мкг в растворе объемом 50 мкл.
Примеры.
Пример. 1. Изменение ОКТ и уровня ВГД у кролика №1 (OS) до и после введения 6-OHDA на 10, 20 сутки. Изменение ОКТ кролика №1 (OS). 

У опытного кролика №1 (OS) после введения 6-OHDA на 10-й день обнаружены значительные изменения в структуре сетчатки: утолщение сетчатки на 21%, значительное утолщение, на 35%, внутреннего плексиформного слоя и утолщение внутреннего ядерного слоя (отечные проявления как результат нейровоспаления) в 2 раза от исходного уровня. На 20-е сутки толщина сетчатки, внутреннего плексиформного и ядерного слоя приближалась к исходному уровню.
Изменение ВГД в виде снижения в течение 10 суток, а на 20 сутки -подъем указывает на временную "химическую симпатэктомию" (нарушение передачи нервного импульса по локальной симпатической системе, в связи с повреждением дофаминергических нейронов) в переднем отделе глаза, в результате чего развивается нарушение гидродинамики глаза, приводящее к отдаленному повышению ВГД.
Таким образом, обнаруженные изменения на 10 сутки в сетчатке кролика №1 (OS) указывают на нейродегенеративные процессы в сетчатке. При этом нейровоспалительный процесс, выявленный во внутреннем плексиформном и ядерном слое связан со специфическим повреждающим воздействием нейротоксина 6-OHDA на находящиеся в нем дофаминергические амакриновые клетки.
Пример.2. ОКТ кролика №4 (OS) до введения NaCl 0,9%, содержащего аскорбиновую кислоту с концентрацией 0,5% и после на 10-20 сутки. Изменение ОКТ кролика №4 (OS).

У кролика №4 (OS) после введения NaCl 0,9%, содержащего аскорбиновую кислоту с концентрацией 0,5% на 10-й день обнаружено незначительное утолщение сетчатки (отечные проявления), при этом толщина внутреннего плексиформного и ядерного слоя не изменялась, в отличие от опытного кролика. Остальные слои также оставались без значительных изменений. На 20-й день толщина сетчатки возвращалась к исходному уровню.
Повышение уровня ВГД на протяжении 10 суток с постепенным снижением к 20 дню указывает на возможное механическое влияние дополнительно интравитреально введенного объема раствора NaCl 0,9%, содержащего 0,5% аскорбиновую кислоту, имеющего кислый рН.
Таким образом, обнаруженные незначительные кратковременные изменения в сетчатке на 10 сутки у кролика №4 (OS) указывают на отсутствие нейродегенеративных процессов и наличие незначительного воспалительного процесса в сетчатке, вероятно, связанного с ответной реакцией на введение физраствора, содержащей аскорбиновую кислоту.
Полученные данные позволяют рассматривать интравитреальное двухкратное введение нейротоксина 6-OHDA кроликам в дозе по 100 мкг дважды с интервалом 2 часа как адекватную модель для изучения раннего нейродегенеративного процесса в сетчатке и заболеваний, вызывающих глазную симпатическую дизавтономию. В перспективе данную модель предлагается использовать с целью выявления ранних биомаркеров нейродегенеративных заболеваний глаза, разработки новых методов лечения.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ лечения нейродегенеративного процесса в глазу в эксперименте | 2023 |
|
RU2794835C1 |
| Способ прогнозирования развития нейродегенеративных заболеваний, в основе патогенеза которых лежит гамма-синуклеинопатия | 2018 |
|
RU2703430C1 |
| Способ коррекции нейротрофильных изменений у пациентов с первичной открытоугольной глаукомой, перенесших коронавирусную инфекцию | 2023 |
|
RU2814770C1 |
| Способ выявления активного деструктивного процесса в сетчатке в эксперименте | 2021 |
|
RU2768588C1 |
| Способ оценки риска прогрессирования первичной открытоугольной глаукомы | 2023 |
|
RU2799582C1 |
| Способ лечения пролиферативных процессов заднего отрезка глаза | 2018 |
|
RU2684927C1 |
| СРЕДСТВО ДЛЯ СНИЖЕНИЯ ВНУТРИГЛАЗНОГО ДАВЛЕНИЯ И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2022 |
|
RU2815996C1 |
| Способ лечения морфометрических изменений макулярной области при полиморбидных соматических состояниях | 2016 |
|
RU2622759C1 |
| СПОСОБ ЛЕЧЕНИЯ ОККЛЮЗИИ ЦЕНТРАЛЬНОЙ ВЕНЫ СЕТЧАТКИ И ЕЕ ВЕТВЕЙ | 2015 |
|
RU2603318C1 |
| Способ изучения биологического действия потенциальных биомедицинских клеточных продуктов на основе клеток человека при субретинальной ксеногенной трансплантации в эксперименте | 2024 |
|
RU2830558C1 |
Изобретение относится к медицине, а именно к экспериментальной офтальмологии, и может быть использовано для моделирования нейродегенеративных процессов в глазу. Для этого проводят интравитреальное введение кролику нейротоксина 6-OHDA в растворе 0,9% хлористого натрия, содержащего аскорбиновую кислоту в концентрации 0,5%. При этом 6-OHDA вводят дважды с интервалом 2 часа по 100 мкг в растворе объемом 50 мкл. Изобретение обеспечивает получение хорошо воспроизводимого и обратимого нейродегенеративного процесса в глазу у кролика. 1 ил., 2 пр.
Способ моделирования нейродегенеративного процесса в сетчатке, включающий интравитреальное введение кролику нейротоксина 6-OHDA в растворе 0,9% хлористого натрия, содержащего аскорбиновую кислоту в концентрации 0,5%, отличающийся тем, что 6-OHDA вводят дважды с интервалом 2 часа по 100 мкг в растворе объемом 50 мкл.
| СПОСОБ МОДЕЛИРОВАНИЯ ПРОЛИФЕРАТИВНОЙ ВИТРЕОРЕТИНОПАТИИ У КРЫС | 2014 |
|
RU2563368C1 |
| Способ моделирования атрофии ретинального пигментного эпителия | 2019 |
|
RU2727000C1 |
| MARROCCO E | |||
| et al | |||
| α-synuclein overexpression in the retina leads to vision impairment and degeneration of dopaminergic amacrine cells / Scientific Reports, 2020, 10:9619, 10 pages | |||
| OLIVIER P | |||
| et al | |||
| Effects of retinal dopamine depletion on the rabbit electroretinogram / Documenta | |||
Авторы
Даты
2023-01-09—Публикация
2022-06-03—Подача