Изобретение относится к вариантам рекомбинантных плазмидных ДНК, содержащим полноразмерную ДНК-копию генома вируса Сендай и гены структурных белков нуклеокапсида N, Р и вирусной полимеразы L, и может быть использовано в биотехнологии, в частности, в генетической инженерии для конструирования рекомбинантных вариантов вируса Сендай штамма Москва, содержащих встройки трансгенов противоопухолевых белков или протективно-значимых антигенов патогенных агентов, с целью разработки на их основе противоопухолевых лекарственных средств и векторных вакцин против инфекционных заболеваний.
Вирус Сендай, также известный как вирус парагриппа мышей 1 типа, или гемагглютинирующий японский вирус, принадлежит к роду Respirovirus семейства Paramyxoviridae. Геном вируса представлен минус цепью РНК длиной 15384 нуклеотида и содержит шесть генов, кодирующих белки [Beaty, 2017; Zainutdinov, 2016] [1, 2]. Из них два гена кодируют поверхностные гликопротеины HN (гемагглютинин-нейраминидаза) и F (белок слияния), три кодируют нуклеокапсидные белки N (нуклеопротеин), Р (фосфопротеин) и L (полимераза), и один - негликозилированный внутренний матриксный белок М. Вирус Сендай вызывает легко передающуюся инфекцию дыхательных путей у мышей, хомяков, морских свинок, крыс и иногда - у свиней. Вирус Сендай способен распространяться как воздушно-капельным путем, так и при непосредственном контакте. Его можно обнаружить в колониях мышей по всему миру, но считается, что он непатогенен для людей [Matveeva, 2015] [3]. Очевидная безопасность вируса и многообещающие данные доклинических и начальных клинических исследований свидетельствуют, что вирус Сендай является перспективным кандидатом для создания на его основе векторных вакцин и противоопухолевых препаратов [Russell, 2021; Matveeva, 2015] [4, 3].
В мировой практике вакцинные и противораковые свойства вируса Сендай исследуются уже более 20 лет. Живой немодифицированный вирус Сендай использовали в виде капель в нос взрослым и детям для оценки иммуногенности по отношению к вирусу человеческого парагриппа 1-го типа. Результаты первой фазы клинических испытаний показали, что вирус Сендай не вызывал существенных побочных эффектов ни у взрослых, ни у детей, но эффективно индуцировал перекрестный иммунный ответ против вируса парагриппа человека 1-го типа [Adderson, 2015] [5]. Также первую фазу клинических испытаний успешно прошла вакцина SeVRSV, которая представляет собой рекомбинантный вирус Сендай, несущий встройку трансгена белка слияния респираторно-синцитиального вируса человека [Huang, 2021] [6]. Это фактически дивакцина, которая защищает против парагриппа человека I типа за счет векторной составляющей (вирус Сендай) и против респираторно-синцитиального вируса человека за счет экспрессии трансгена протективно-значимого белка слияния этого вируса. Исследование, проведенное на взрослом контингенте, показало безопасность и иммуногенность вакцины SeVRSV. Результаты стимулируют дальнейшие исследования SeVRSV в группах детей, которые наиболее часто подвержены инфекциям - мишеням данной вакцины.
Разработка векторной вакцины против ВИЧ-инфекции на основе вируса Сендай, находится на втором этапе клинических испытаний. Эта вакцина представляет собой рекомбинантный вирус Сендай, экспрессирующий трансген gag-белка ВИЧ-1. У людей она вызывает мощную индукцию Т-клеточного ответа и продукцию специфических нейтрализующих антител к белку gag в режиме прайм-буст [Nyombayire, 2017] [7].
Успешно прошла доклинические исследования интраназальная вакцина на основе рекомбинантного вируса Сендай SeV-MPV-Ft, который несет встройку трансгена усеченного белка слияния F метапневмовируса человека (hMPV). Инфекции, вызванные hMPV, представляют серьезный риск для здоровья детей раннего возраста, особенно в случае преждевременных родов. Лицензированной вакцины не существует, и нет стандартного лечения инфекций hMPV кроме поддерживающей терапии. Вакцина SeV-MPV-Ft индуцирует образование вируснейтрализующих антител и 100%-ную защиту от заражения hMPV в чувствительной модели хлопковых крыс [Russell, 2017] [8].
Таким образом, вирус Сендай является перспективным вектором для создания вакцин, особенно для респираторных вирусных инфекций. Его основным преимуществом по сравнению с другими векторными кандидатами является способность, не вызывая заболевания, реплицироваться в клетках бронхиального эпителия человека, а также в некоторых категориях дендритных клеток. Рекомбинантный вирус Сендай способен доставить и в клетки бронхиального эпителия человека, и в его дендритные клетки как чужеродные вирусные антигены, так и продукт своего репликационного цикла, а именно двухцепочечную РНК, которая является мощным патоген-ассоциированным паттерном, индуцирующим иммунную реакцию организма [Зайчук, 2020] [9].
В ряде работ было показано, что вирус Сендай, как природные штаммы, так и рекомбинантные варианты, может интенсивно распространяться в опухолевых клетках и уничтожать их, не затрагивая окружающие их нормальные клетки [Matveeva, 2015; Zimmermann, 2014] [10, 11]. Такое действие вируса часто приводит к ингибированию роста опухолей у модельных животных. Среди протестированных ксенотрансплантационных моделей опухолей человека были клетки фибросаркомы, панкреатической эпителиоидной карциномы и клетки рака толстой кишки [Kinoh, 2004] [12]. Также на мышиных моделях с применением рекомбинантного вируса Сендай, экспрессирующего трансген интерлейкина-2, было продемонстрировано существенное подавление роста опухоли, и даже полное рассасывание сформировавшихся опухолей мозга [Iwadate, 2005] [13]. Сходные результаты были получены с рекомбинантным вирусом Сендай, содержащим встройку трансгена интерферона-бета, в случае ксенотрансплантации мышам клеток саркомы и рака простаты человека [Kinoh, 2008; Tatsuta, 2009] [14, 15]. На крысиных ксенотрансплантационных моделях было показано, что рекомбинантный вирус Сендай с высокой эффективностью уничтожает человеческие опухоли меланомы, гепатоцеллюлярного рака, нейробластомы, плоскоклеточного рака и рака простаты [Yonemitsu, 2008] [16]. Противоопухолевая эффективность вируса Сендай была продемонстрирована на сингенных мышиных моделях [Tanaka, 2019] [17], причем было показано, что даже после УФО-инактивации препараты вируса Сендай эффективны против карциномы толстой кишки [Kurooka, 2007; Kawano, 2007] [18, 19], мочевого пузыря [Kawano, 2008] [20] и карцином почки [Fujihara, 2008] [21]. Эффективность УФО-инактивированного вируса Сендай была также показана на мышиной ксенотрансплантационной модели человеческого рака простаты [Hui, 2014] [22]. Во всех указанных исследованиях вирус Сендай приводил к полной регрессии опухолей или к серьезному подавлению их роста. Препарат УФО-инактивированного вируса Сендай прошел также I/IIa фазу клинических испытаний при внутриопухолевом введении пациентам с прогрессирующей меланомой стадии IIIC или IV с метастазами в коже или лимфе. Полные или частичные ответы наблюдались примерно в половине леченных случаев [Kiyohara, 2020] [23].
Мы работаем с уникальным по своим характеристикам российским штаммом Москва вируса Сендай [Zainutdinov, 2016] [2], который в ряде случайных клинических исследований в России продемонстрировал хороший противоопухолевый потенциал. В начале и середине 1990-х годов под руководством В.М. Сенина в клиниках Москвы и Санкт-Петербурга штамм Москва вируса Сендай был использован для лечения больных-добровольцев, имеющих разнообразные карциномы третьей и четвертой стадии заболевания. У ряда больных были отмечены длительные ремиссии заболевания, даже в случаях, когда опухоли были признаны неоперабельными и вирус использовали в качестве монотерапии. В некоторых случаях наблюдалось рассасывание первичных опухолей и метастазов, исчезали все обьективные и субъективные признаки онкологического заболевания. Иногда отсутствие признаков заболевания отмечались и спустя 5-10 и более лет после одного или двух курсов терапии вирусом Сендай [Matveeva, 2015] [24]. Краткие истории болезни этих больных приведены в тексте опубликованного патента [Сенин, 2014] [25]. Опубликованы также данные по полной или частичной ремиссии тучноклеточных раковых опухолей (мастоцитом) у собак при внутриопухолевых инъекциях вируса Сендай штамма Москва [Ilyinskaya, 2018] [26].
Первичная нуклеотидная последовательность штамма Москва была определена с участием авторов подаваемого изобретения и депонирована в базу данных «GenBank» под номером КР717417.1. Эта последовательность легла в основу создания набора рекомбинантных плазмидных ДНК для получения рекомбинантных вариантов вируса Сендай штамма Москва. Набор включает пять плазмидных конструкций, содержащих: (1) полноразмерную ДНК-копию генома вируса с сайтом для встройки трансгенов в 3'-некодирующую лидерную последовательность, расположенную перед геном N; (2) полноразмерную ДНК-копию генома вируса с сайтом для встройки трансгенов между генами Р и М; (3) ген N; (4) ген Р; (5) ген L. Экспрессия генов N (нуклеопротеин), Р (фосфопротеин) и L (полимераза) является необходимым элементом оживления рекомбинантных вариантов вируса; они обеспечивают упаковку и последующую репликацию геномной РНК, которая транскрибируется с плазмид, содержащих ее полногеномную ДНК-копию.
Наиболее близким к заявляемому изобретению (прототипом) является патент US9637758B2 [Hurwitz, 2018] [27]. В прототипе описаны рекомбинантные плазмидные ДНК, с помощью которых авторы конструировали рекомбинантные варианты вируса Сендай штамма Enders, несущие встройку репортерного трансгена люциферазы и некоторых других трансгенов в межгенные промежутки Р-М, M-F и F-HN генома вируса. Уникальные сайты распознавания NotI были клонированы в межгенные соединения Р-М, M-F и F-HN плазмиды вирусного генома PSEV на основе Эндерса с использованием сайтов клонирования, описанных ранее [Tokusumi et al. 2002, Virus Res 86: 33-38]. Ген люциферазы светлячка был амплифицирован методом ПЦР с использованием базового вектора pGL3 (Promega) и пары праймеров, помеченных ASCI, субклонированных в плазмиду-челнок, содержащую межгенный переход вируса Сендай и фланкирующие сайты рестрикции NotI [Токусуми и др. 2002, Virus Res 86: 33-38], а затем подклонирован в уникальный сайт NotI каждой из плазмид вирусного генома PSEV. В плазмиде PSEV-luc(M-F) начальный сигнал перед белком F был изменен с AGGGATAAAG (SEQ. ID. №: 19) на AGGGTGAAAG (SEQ.ID. №: 20) с использованием набора для мутагенеза, направленного на сайт QuikChange ™ (Stratagene Corp). Рекомбинантные SEV были извлечены из плазмид генома PSEV, как описано ранее [Zhan et al. 2008, Вакцина 26: 3480-3488].
Однако используемый набор плазмид не обеспечивает достаточную широту возможностей конструирования рекомбинантных вариантов вирусов Сендай вследствие наличия единственного уникального сайта NotI.
Техническим результатом заявляемого изобретения является расширение возможности конструирования рекомбинантных вариантов вируса Сендай с заданными свойствами за счет использования для встройки трансгенов полилинкер, содержащий несколько уникальных сайтов рестрикции (BsiWI, NruI, ClaI, AscI, BssHII), не встречающихся в геноме вируса Сендай штамма Москва.
Указанный технический результат достигается созданием первого варианта набора рекомбинантных плазмидных ДНК для получения рекомбинантных вирусов Сендай штамма Москва, включающий четыре плазмидных конструкций:
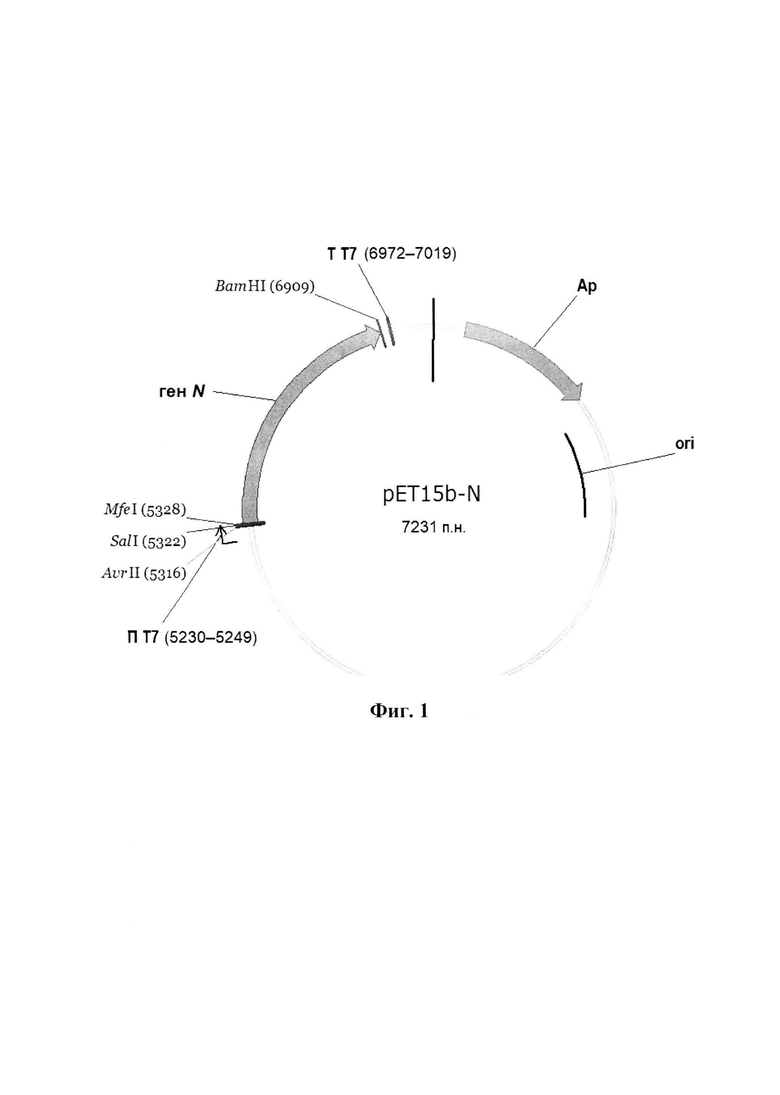
- первую плазмидную конструкцию pET15b-N, представленную на физической и генетической карте на фиг. 1, обеспечивающую экспрессию гена N, кодирующего нуклеопротеин вируса Сендай штамма Москва в трансформированных клетках эукариот, продуцирующих РНК-полимеразу фага Т7, имеющую последовательность SEQ ID No.: 1, размер 7231 п. н. и молекулярную массу 4,8 мегадальтон и состоящую из BamHI-NcoI векторного фрагмента плазмиды pET15b (5638 п. н.), включающего участок начала репликации ori, ген бета-лактамазы, придающей устойчивость к ампициллину, промотор и терминатор РНК-полимеразы фага Т7, между которыми встроен ген N (позиции нуклеотидов 120-1694, GenBank: КР717417.1), фланкированный модифицированной последовательностью 5'-CCTAGGGTCGACCAATTG, содержащей сайты рестриктаз AvrII (вместо NcoI в позиции 5316 п. н. исходной плазмиды pET15b), SalI и MfeI;
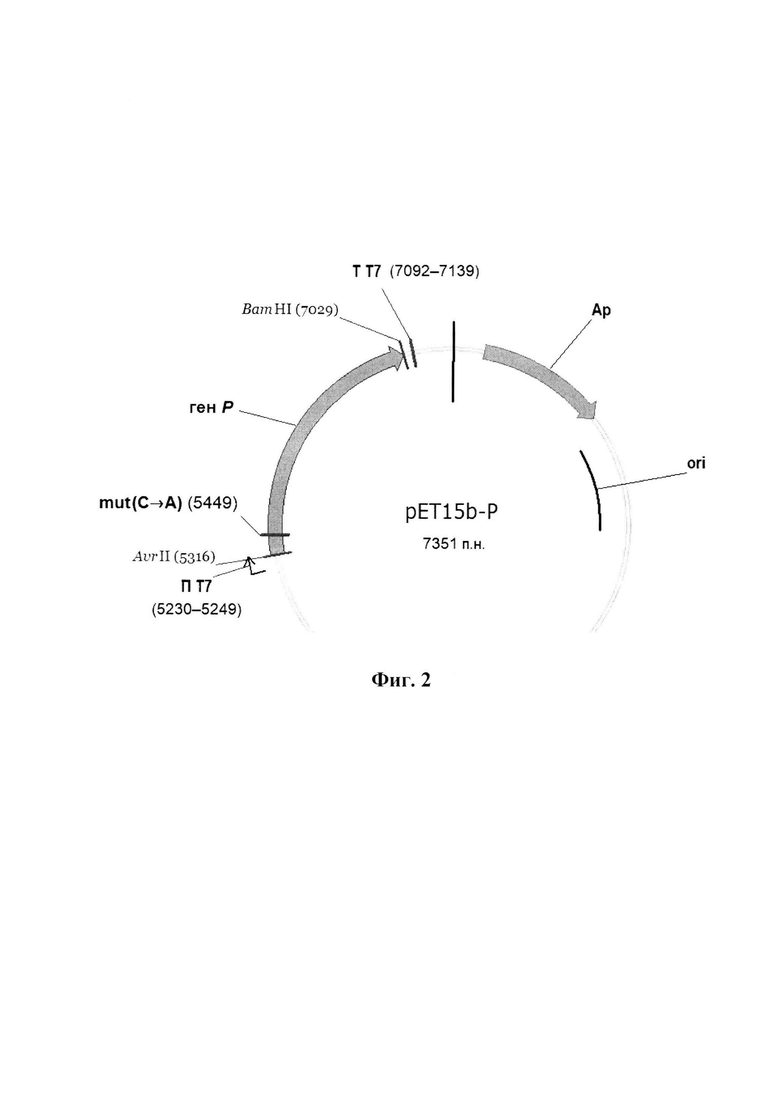
- вторую плазмидную конструкцию pET15b-Р, представленную на физической и генетической карте на фиг. 2, обеспечивающую экспрессию гена Р, кодирующего фосфопротеин вируса Сендай штамма Москва, в трансформированных клетках эукариот, продуцирующих РНК-полимеразу фага Т7, имеющую последовательность SEQ ID No.: 2, размер 7351 п. н. и молекулярную массу 4,9 мегадальтон и состоящую из BamHI-Ncol векторного фрагмента плазмиды pET15b (5638 п. н.), включающего участок начала репликации ori, ген бета-лактамазы, придающей устойчивость к ампициллину, промотор и терминатор РНК-полимеразы фага Т7, между которыми встроен ген Р (позиции нуклеотидов 1844-3550 с заменой С→А в позиции 1972 для удаления альтернативной рамки считывания, GenBank: КР717417.1), фланкированный последовательностью 5'-CCTAGG (сайт рестриктазы Avr II в позиции 5316 п. н.);
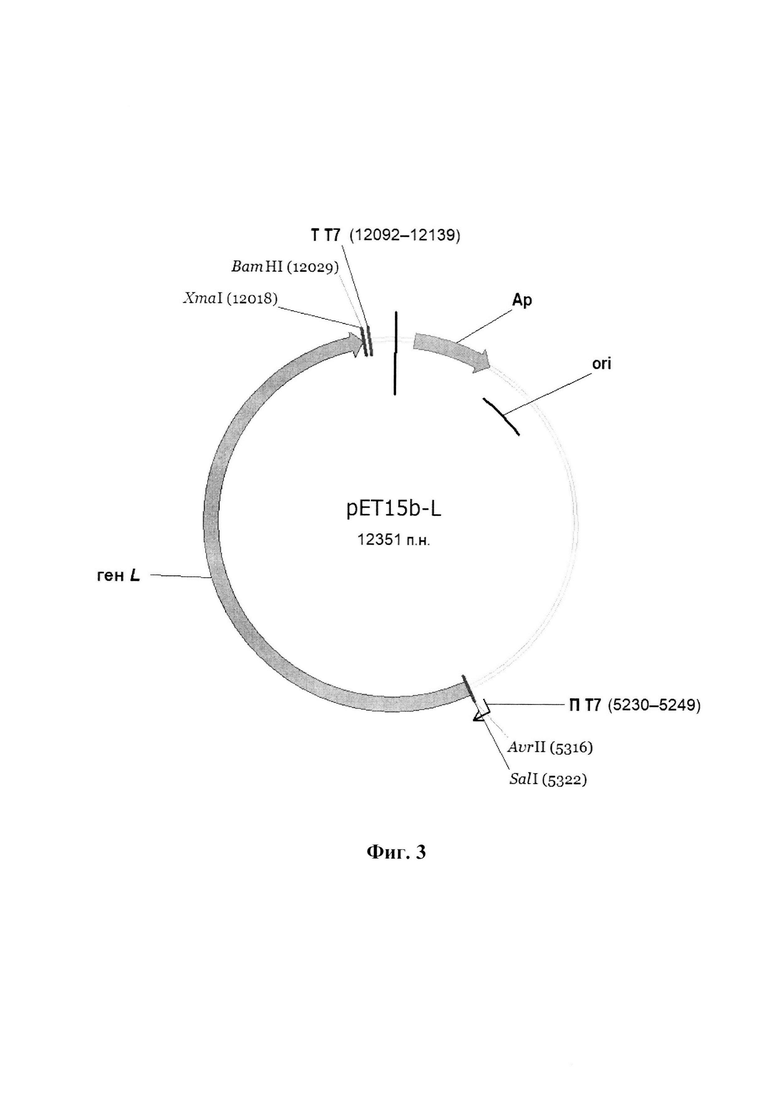
- третью плазмидную конструкцию pET15b-L, представленную на физической и генетической карте на фиг. 3, обеспечивающую экспрессию гена I, кодирующего полимеразу вируса Сендай штамма Москва, в трансформированных клетках эукариот, продуцирующих РНК-полимеразу фага Т7, имеющую последовательность SEQ ID No.: 3, размер 12351 п. н. и молекулярную массу 8,2 мегадальтон и состоящую из BamHI-NcoI векторного фрагмента плазмиды pET15b (5638 п. н.), включающего участок начала репликации ori, ген бета-лактамазы, придающей устойчивость к ампициллину, промотор и терминатор РНК-полимеразы фага Т7, между которыми встроен ген L (позиции нуклеотидов 8556-15245, GenBank: КР717417.1), фланкированный последовательностями 5'-CCTAGGGTCGAC (сайт рестриктаз Avr II и SaiI) и CCCGGGCTCGA-3', содержащей сайт рестриктазы XmaI;
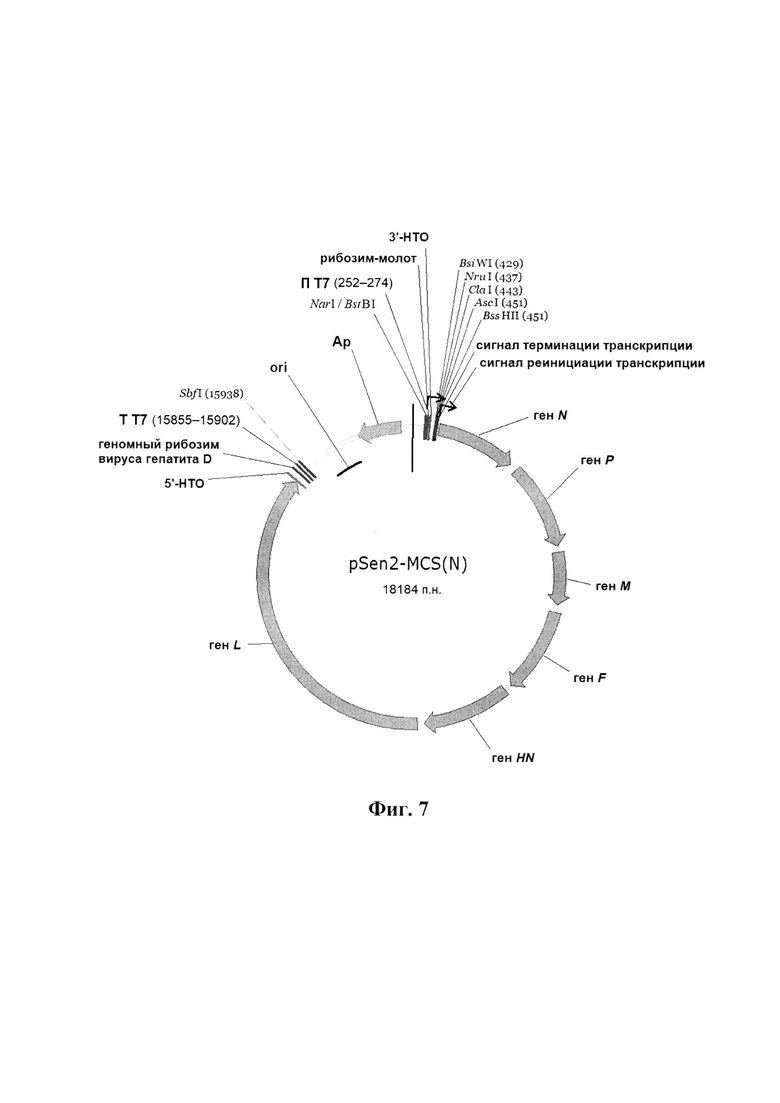
- четвертую плазмидную конструкцию pSen2-MCS(N), представленную на физической и генетической карте на фиг. 7, обеспечивающую транскрипцию геномной рекомбинантной РНК вируса Сендай штамма Москва со встройкой трансгенов перед геном N в трансформированных клетках эукариот, продуцирующих РНК-полимеразу фага Т7, имеющую последовательность SEQ ID No.: 4, размер 18184 п. н. и молекулярную массу 12 мегадальтон и состоящую из SbfI-NarI векторного фрагмента плазмиды pUC 19 (2483 п. н.), включающего участок начала репликации ori, ген бета-лактамазы, придающей устойчивость к ампициллину, и встройки, в которой последовательно расположены: промотор РНК-полимеразы фага Т7, рибозим-молот, копия ДНК 3'-НТО генома вируса Сендай штамма Москва (позиции нуклеотидов 1-104, GenBank: КР717417.1), полилинкер для встройки трансгенов, включающий пять уникальных сайтов для эндонуклеаз рестрикции BsiWI, NruI, ClaI, AscI, BssHII, сигнал терминации транскрипции трансгена, сигнал реинициации транскрипции последующего гена для РНК-полимеразы вируса Сендай, ген N (позиции нуклеотидов 120-1694, GenBank: КР717417.1), ген Р (позиции нуклеотидов 1844-3550, GenBank: КР717417.1), ген М (позиции нуклеотидов 3669-4715, GenBank: КР717417.1), ген F (позиции нуклеотидов 4866-6563, GenBank: КР717417.1), ген HN (позиции нуклеотидов 6693-8420, GenBank: КР717417.1), ген L (позиции нуклеотидов 8556-15245, GenBank: КР717417.1), копия ДНК 5'-НТО генома вируса Сендай штамма Москва (позиции нуклеотидов 15312-15384, GenBank: КР717417.1), геномный рибозим вируса гепатита D, терминатор РНК-полимеразы фага Т7.
Указанный технический результат достигается также созданием второго варианта набора рекомбинантных плазмидных ДНК для получения рекомбинантных вирусов Сендай штамма Москва, включающий четыре плазмидных конструкций:
- первую плазмидную конструкцию pET15b-N, представленную на физической и генетической карте на фиг. 1, обеспечивающую экспрессию гена N, кодирующего нуклеопротеин вируса Сендай штамма Москва в трансформированных клетках эукариот, продуцирующих РНК-полимеразу фага Т7, имеющую последовательность SEQ ID No.: 1, размер 7231 п. н. и молекулярную массу 4,8 мегадальтон и состоящую из BamHI-Ncol векторного фрагмента плазмиды pET15b (5638 п. н.), включающего участок начала репликации ori, ген бета-лактамазы, придающей устойчивость к ампициллину, промотор и терминатор РНК-полимеразы фага Т7, между которыми встроен ген N (позиции нуклеотидов 120-1694, GenBank: КР717417.1), фланкированный модифицированной последовательностью 5'-CCTAGGGTCGACCAATTG, содержащей сайты рестриктаз AvrII (вместо NcoI в позиции 5316 п. н. исходной плазмиды pET15b), SaiI и MfeI;
- вторую плазмидную конструкцию pET15b-Р, представленную на физической и генетической карте на фиг. 2, обеспечивающую экспрессию гена Р, кодирующего фосфопротеин вируса Сендай штамма Москва, в трансформированных клетках эукариот, продуцирующих РНК-полимеразу фага Т7, имеющую последовательность SEQ ID No.: 2 размер 7351 п. н. и молекулярную массу 4,9 мегадальтон и состоящую из BamHI-NcoI векторного фрагмента плазмиды pET15b (5638 п. н.), включающего участок начала репликации ori, ген бета-лактамазы, придающей устойчивость к ампициллину, промотор и терминатор РНК-полимеразы фага Т7, между которыми встроен ген Р (позиции нуклеотидов 1844-3550 с заменой С→А в позиции 1972 для удаления альтернативной рамки считывания, GenBank: КР717417.1), фланкированный последовательностью 5'-CCTAGG (сайт рестриктазы Avr II в позиции 5316 п. н.);
- третью плазмидную конструкцию pET15b-L, представленную на физической и генетической карте на фиг. 3, обеспечивающую экспрессию гена L, кодирующего полимеразу вируса Сендай штамма Москва, в трансформированных клетках эукариот, продуцирующих РНК-полимеразу фага Т7, имеющую последовательность SEQ ID No.: 3, размер 12351 п. н. и молекулярную массу 8,2 мегадальтон и состоящую из BamHI-NcoI векторного фрагмента плазмиды pET15b (5638 п. н.), включающего участок начала репликации ori, ген бета-лактамазы, придающей устойчивость к ампициллину, промотор и терминатор РНК-полимеразы фага Т7, между которыми встроен ген L (позиции нуклеотидов 8556-15245, GenBank: КР717417.1), фланкированный последовательностями 5'-CCTAGGGTCGAC (сайт рестриктаз Avr II и SaiI) и CCCGGGCTCGA-3', содержащей сайт рестриктазы XmaI;
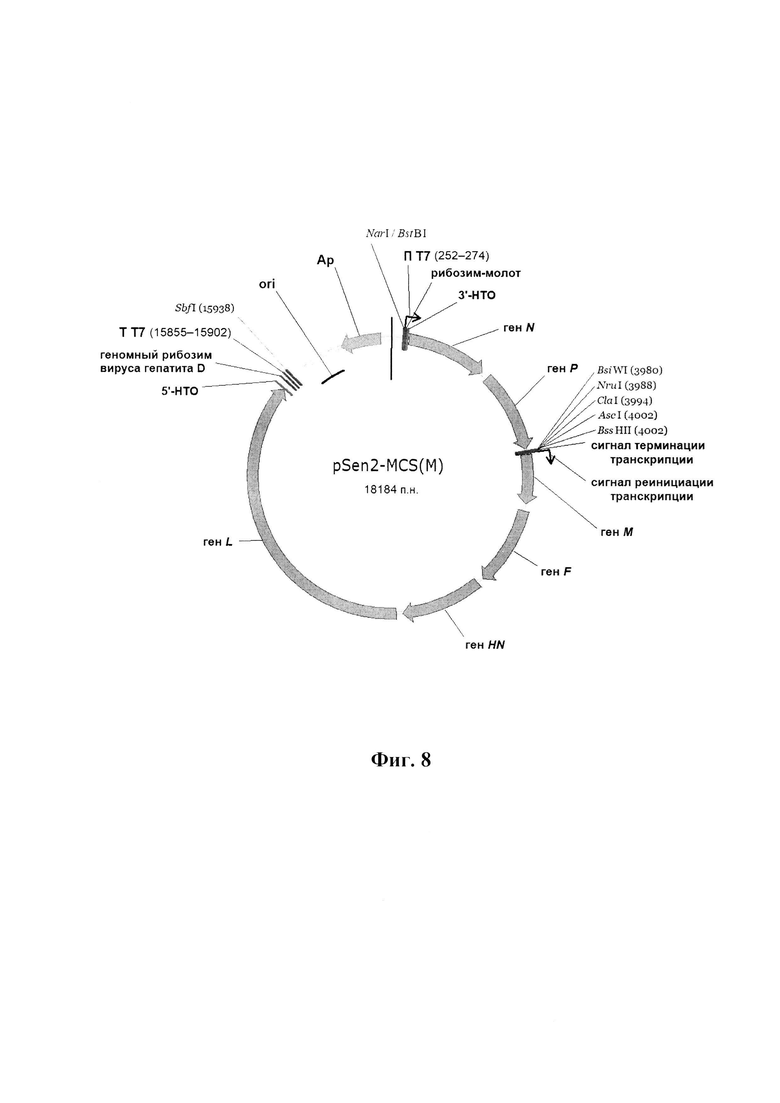
- четвертую плазмидную конструкцию pSen2-MCS(M), представленную на физической и генетической карте на фиг. 8, обеспечивающую транскрипцию геномной рекомбинантной РНК вируса Сендай штамма Москва со встройкой трансгенов перед геном М в трансформированных клетках эукариот, продуцирующих РНК-полимеразу фага Т7, имеющую последовательность SEQ ID No.: 5, размер 18184 п. н. и молекулярную массу 12 мегадальтон и состоящую из SbfI-NarI векторного фрагмента плазмиды pUC19 (2483 п. н.), включающего участок начала репликации ori, ген бета-лактамазы, придающей устойчивость к ампициллину, и встройки, в которой последовательно расположены: промотор РНК-полимеразы фага Т7, рибозим-молот, копия ДНК 3'-НТО генома вируса Сендай штамма Москва (позиции нуклеотидов 1-104, GenBank: КР717417.1), ген N (позиции нуклеотидов 120-1694, GenBank: КР717417.1), ген Р (позиции нуклеотидов 1844-3550, GenBank: КР717417.1), полилинкер для встройки трансгенов, включающий пять уникальных сайтов для эндонуклеаз рестрикции BsiWI, NruI, ClaI, AscI, BssHII, сигнал терминации транскрипции трансгена, сигнал реинициации транскрипции последующего гена для РНК-полимеразы вируса Сендай, ген М (позиции нуклеотидов 3669-4715, GenBank: КР717417.1), ген F (позиции нуклеотидов 4866-6563, GenBank: КР717417.1), ген HN (позиции нуклеотидов 6693-8420, GenBank: КР717417.1), ген L (позиции нуклеотидов 8556-15245, GenBank: КР717417.1), копия ДНК 5'-НТО генома вируса Сендай штамма Москва (позиции нуклеотидов 15312-15384, GenBank: КР717417.1), геномный рибозим вируса гепатита D, терминатор РНК-полимеразы фага Т7.
Преимущество заявляемого изобретения состоит, прежде всего, в использовании российского штамма Москва вируса Сендай, обладающего высокой природной онколитической активностью. Во-вторых, для встройки трансгенов мы ввели полилинкер, содержащий несколько уникальных сайтов рестрикции (BsiWI, NruI, ClaI, AscI, BssHII), в отличие от единственного NotI сайта прототипа. Введение дополнительных сайтов, не встречающихся в геноме вируса Сендай штамма Москва, расширяет возможности конструирования рекомбинантных вариантов вируса. Для получения рекомбинантных векторных вакцин на основе вируса Сендай, в отличие от прототипа, мы создали рекомбинантную плазмидную ДНК pSen2-MCS(N), которая обеспечивает встройку трансгенов в 3'-нетранслируемую область генома вируса Сендай штамма Москва, расположенную перед геном N. Позиция трансгена в этом районе обеспечивает максимальный уровень продукции белка вследствие наличия 3'>5' градиента уровня экспрессии генов в геноме парамиксовирусов [Makowska, 2020] [28]. Высокий уровень продукции протективно-значимых белков-иммуногенов в вакцинных конструктах обеспечит большую эффективность иммунного ответа и защиту от соответствующего патогена. Еще одна созданная нами рекомбинантная плазмидная ДНК pSen2-MCS(M) обеспечивает встройку трансгенов перед геном М в геномном промежутке Р-М генома вируса Сендай штамма Москва Этот район лучше использовать для встройки трансгенов биологически-активных белков в онколитических рекомбинантных вариантах вируса Сендай, для осуществления функциональной активности которых не требуется высокий уровень экспрессии трансгена и которые часто обладают токсичностью для клеток (гены онкотоксических белков, например).
Технической задачей изобретения является получение набора из четырех рекомбинантных плазмидных ДНК, три из которых экспрессируют гены N, P и L вируса Сендай штамма Москва (вспомогательные плазмиды), а четвертая содержит полногеномную копию ДНК геномной РНК вируса Сендай штамма Москва, в которую введены структурные элементы для встройки и экспрессии трансгенов в 3'-нетранслируемой области (НТО) вирусного генома, расположенной перед геном N (первый вариант четвертой плазмиды) или между генами Р и М (второй вариант четвертой плазмиды). Полученный набор плазмид обеспечивает оживление рекомбинантных вариантов вируса Сендай штамма Москва, которое мы подтвердили на примере модельного трансгена зеленого флюоресцентного белка EGFP.
Поставленная задача решается путем введения в плазмиду pET15b (Sigma-Aldrich, Cat. No. 69661-3; база данных SnapGene snapgene.com) [29] ДНК-копий фрагментов генома вируса Сендай штамма Москва, соответствующих генам N, Р и L, под контроль высокоэффективного промотора РНК-полимеразы фага Т7 с получением плазмид pET15b-N (Фиг. 1), pET15b-Р (Фиг. 2) и pET15b-L (Фиг. 3) (Пример 1). Сборка полногеномной копии ДНК вируса Сендай штамма Москва осуществляется в плазмиде pUC19 (база данных SnapGene snapgene.com) [30] в 6 этапов с получением промежуточной плазмиды pSen2 (Фиг. 5, пример 2). Транскрипция геномной РНК вируса Сендай осуществляется с плазмидной ДНК pSen2 высокопроизводительной РНК-полимеразой фага Т7. Точность размера генома вируса Сендай в процессе транскрипции вирусной РНК на матрице pSen2 контролируется рибозимами типа молот [Beaty et al, 2017] [1] и вируса гепатита D [Leyrer, 1998] [31], встроенными по 5'- и 3'-концам геномной кДНК соответственно. Необходимость контроля длины РНК объясняется тем, что у генома вируса Сендай, как и у всех парамиксовирусов, есть необычное свойство: он подчиняется «правилу шести» и имеет полигексамерную длину (6n+0), что затрудняет рекомбинацию и обеспечивает высокую стабильность РНК-геномов парамиксовирусов в природе [Matsumoto, 2018] [32]. Для встройки трансгенов в две области генома в плазмиду pSen2 введена одинаковая инсерция: полилинкер с уникальными сайтами для крупнощепящих эндонуклеаз рестрикции BsiWI, NruI, ClaI, AscI, BssHII, за которым следует сигнал терминации транскрипции трансгена и сигнал реинициации для транскрипции последующего гена (Фиг. 6). В результате были получены рекомбинантные плазмидные ДНК: pSen2-MCS(N) для встройки трансгенов перед геном N (Фиг. 7) и pSen2-MCS(M) для встройки трансгенов между генами Р и М(Фиг. 8).
В качестве тестового трансгена для проверки «работоспособности» созданного набора рекомбинантных плазмидных ДНК для получения (оживления) рекомбинантных вариантов вируса Сендай был использован ген зеленого флюоресцентного белка EGFP (позиции 679-1398, база данных SnapGene snapgene.com [33]. Получены два рекомбинантных варианта вируса Сендай штамма Москва: Sen2-EGFP(N) со встройкой трансгена EGFP перед геном N и Sen2-EGFP(M) со встройкой трансгена EGFP между генами Р и М (Фиг. 9).
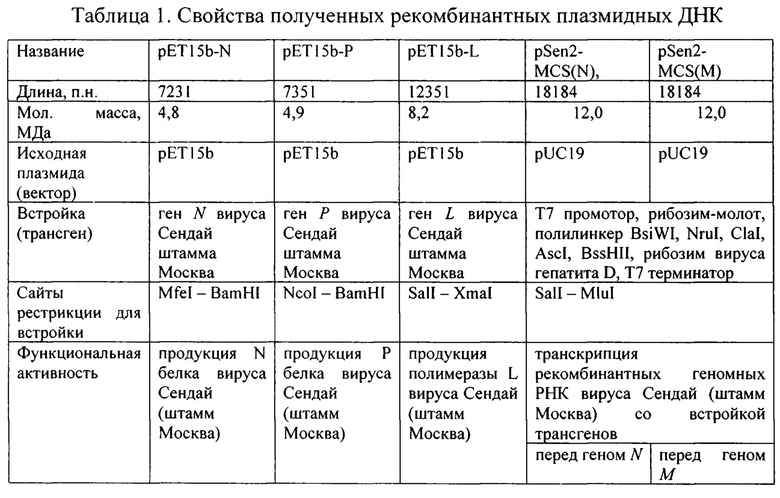
Физические карты рекомбинантных плазмидных ДНК pET15b-N, pET15b-P, pET15b-L, pSen2-MCS(N) и pSen2-MCS(M), являющихся предметом изобретения, представлены на Фиг. 1, 2, 3, 7 и 8, соответственно. Свойства полученных рекомбинантных плазмидных ДНК представлены в таблице 1 выше.
Общие свойства плазмид:
- содержат участок начала репликации (ori);
- содержат в качестве генетического маркера ген bla β-лактамазы, определяющий устойчивость трансформированных клеток Е. coli к ампициллину (Ар);
- содержат промотор РНК-полимеразы фага Т7 (П Т7), с которого начинается транскрипция мРНК генов N, Р и L или геномных РНК вируса Сендай штамма Москва;
-содержат терминатор РНК-полимеразы фага Т7 (Т Т7), на котором заканчивается транскрипция РНК.
Изобретение иллюстрируется следующими графическими материалами. Фиг. 1. Физическая карта рекомбинантной плазмидной ДНК pET15b-N. Вертикальная черта в верхней части плазмидной ДНК обозначает начало отсчета п. н. (нуклеотид №1). В скобках приведены позиции нуклеотидов в плазмидной ДНК, соответствующие обозначенным элементам конструкта. Ori
- участок начала репликации; Ар - ген bla β-лактамазы. П Т7 - промотор РНК-полимеразы фага Т7 (направление транскрипции указано стрелкой). Т Т7 - терминатор РНК-полимеразы фага Т7.
Фиг. 2. Физическая карта рекомбинантной плазмидной ДНК pET15b-Р. Вертикальная черта в верхней части плазмидной ДНК обозначает начало отсчета п. н. (нуклеотид №1). В скобках приведены позиции нуклеотидов в плазмидной ДНК, соответствующие обозначенным элементам конструкта. Ori - участок начала репликации; Ар - ген bla β-лактамазы. П Т7 - промотор РНК-полимеразы фага Т7 (направление транскрипции указано стрелкой). Т Т7 - терминатор РНК-полимеразы фага Т7.
Фиг.3. Физическая карта рекомбинантной плазмидной ДНК pET15b-L. Вертикальная черта в верхней части плазмидной ДНК обозначает начало отсчета п. н. (нуклеотид №1). В скобках приведены позиции нуклеотидов в плазмидной ДНК, соответствующие обозначенным элементам конструкта. Ori - участок начала репликации; Ар - ген bla β-лактамазы. П Т7 - промотор РНК-полимеразы фага Т7 (направление транскрипции указано стрелкой). Т Т7 - терминатор РНК-полимеразы фага Т7.
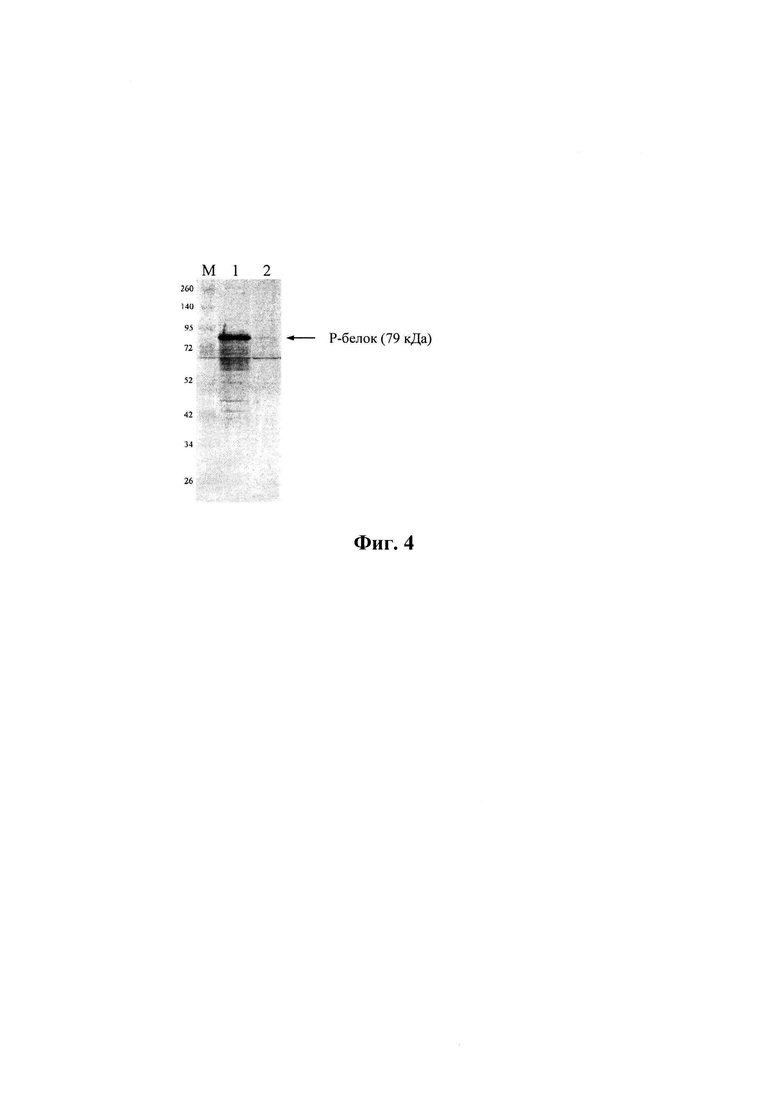
Фиг. 4. Выявление белка Р вируса Сендай в лизатах клеток 293-Т7, трансформированных плазмидой pET15b-Р. Лизаты клеток готовили через 48 часов после трансформации 2 мкг ДНК pET15b-Р с реагентом Lipofectamine™ LTX Plus (Invitrogen, Cat. 15338). Для лизиса клеток использовали RIPA (Sigma, Cat. R0278). 1 - лизат 293-Т7+pET15b-P; 2 - лизат 293-Т7 (отрицательный контроль). М - маркер молекулярных масс (Thermo Scientific, Cat. 26634). В качестве первичных антител использовали иммунную сыворотку овцы (1:5000). В качестве вторичных антител использовали конъюгат с щелочной фосфатазой anti-sheep IgG осла (1:5000) (Sigma, А5187).
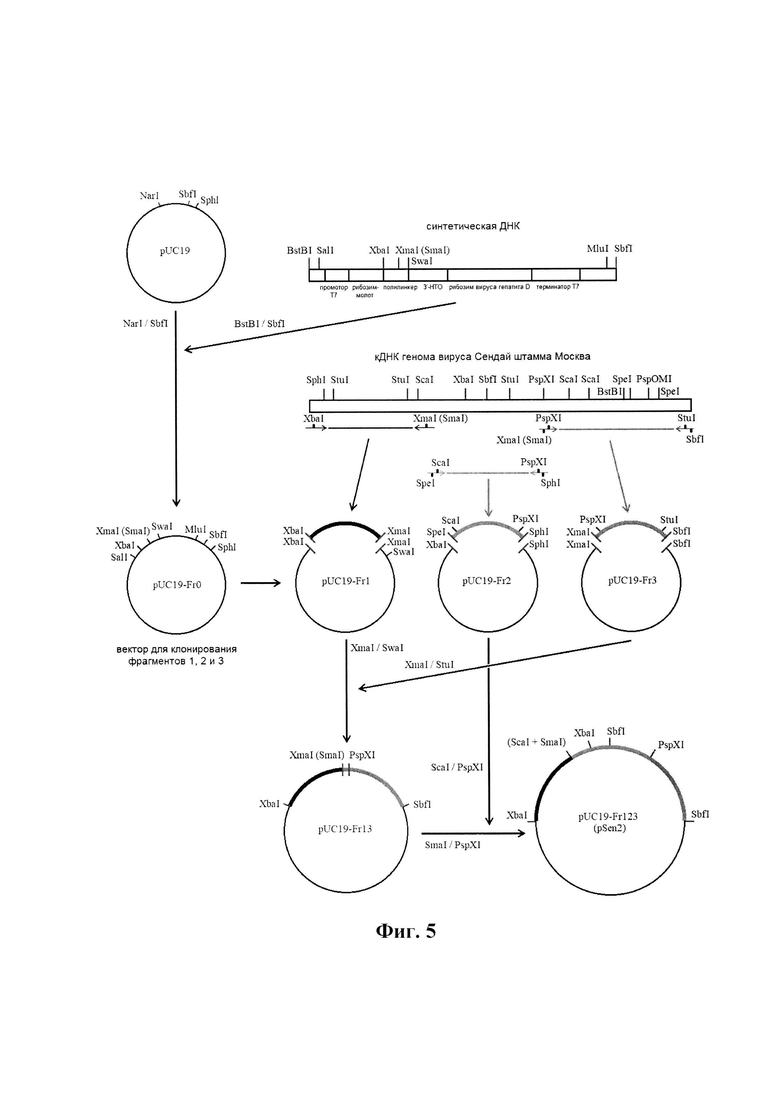
Фиг. 5. Схема сборки промежуточной плазмидной ДНК pSen2, содержащей ДНК-копию геномной РНК вируса Сендай штамма Москва. Сборка включает 6 этапов. 1 этап: получение плазмиды pUC19-FrO, содержащей синтетически полученный ДНК-фрагмент с 3'-НТО генома вируса, регуляторными последовательностями (промотор, терминатор, рибозимы) и полилинкер; 2-4 этапы: на основе pUC19-Fr0 получаются 3 плазмиды pUC19-Fr1, pUC19-Fr2 и pUC19-Fr3, содержащие 3 фрагмента генома вируса Сендай; 5-6 этапы: объединение трех клонированных фрагментов генома в единую полноразмерную цепь ДНК.
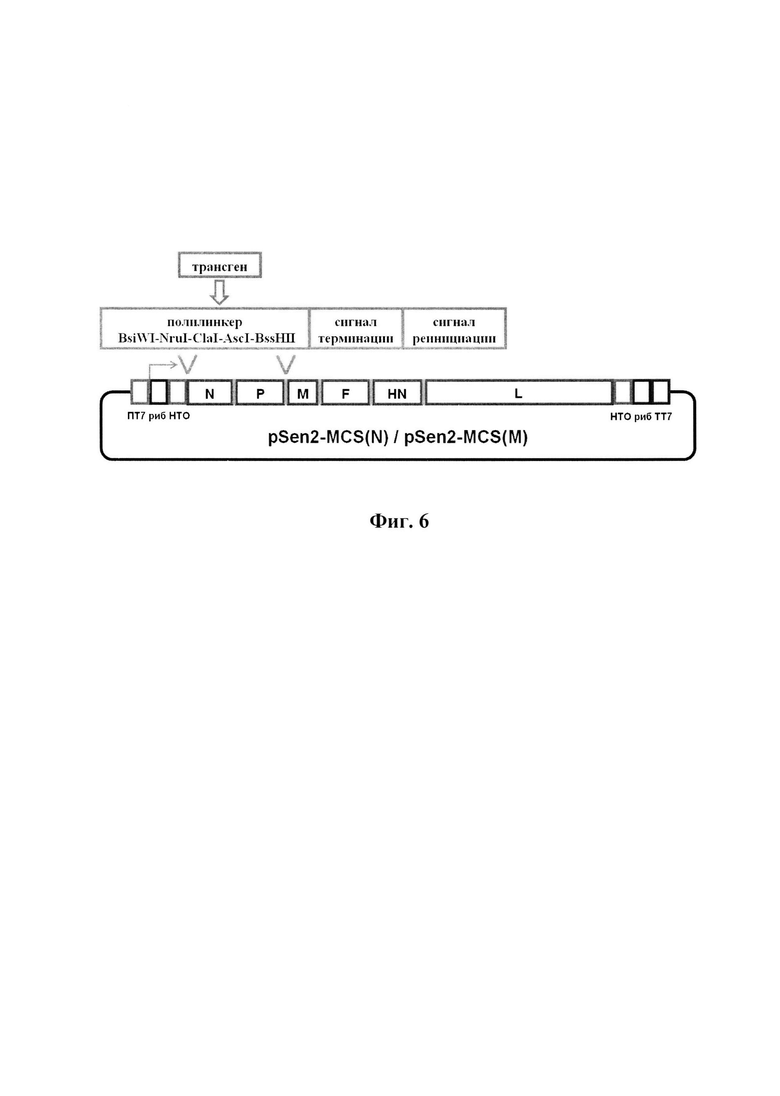
Фиг. 6. Схема рекомбинантного генома вируса Сендай штамма Москва с введением трансгенов в две области генома: перед геном N и перед геном М. Синтез геномной РНК рекомбинантных штаммов вируса Сендай осуществляется с плазмидной ДНК под контролем РНК-полимеразы фага Т7 - указано стрелкой. ПТ7 - промотор, ТТ7 - терминатор РНК-полимеразы фага Т7. Точность размера генома контролируется рибозимами, встроенными по концам геномной РНК (риб). Для встройки трансгенов в две области генома введена одинаковая инсерция: полилинкер с уникальными сайтами для крупнощепящих эндонуклеаз рестрикции, за полилинкером введен сигнал терминации транскрипции трансгена и сигнал реинициации для транскрипции последующего гена.
Фиг. 7. Физическая карта рекомбинантной плазмидной ДНК pSen2-MCS(N). Вертикальная черта в верхней части плазмидной ДНК обозначает начало отсчета п. н. (нуклеотид №1). В скобках приведены позиции нуклеотидов в плазмидной ДНК, соответствующие обозначенным элементам конструкта. Ori - участок начала репликации; Ар - ген bla β-лактамазы. П Т7 - промотор РНК-полимеразы фага Т7. Т Т7 - терминатор РНК-полимеразы фага Т7. Стрелками указано направление транскрипции.
Фиг. 8. Физическая карта рекомбинантной плазмидной ДНК pSen2-MCS(M). Вертикальная черта в верхней части плазмидной ДНК обозначает начало отсчета п. н. (нуклеотид №1). В скобках приведены позиции нуклеотидов в плазмидной ДНК, соответствующие обозначенным элементам конструкта. Ori - участок начала репликации; Ар - ген bla β-лактамазы. П Т7 - промотор РНК-полимеразы фага Т7. Т Т7 - терминатор РНК-полимеразы фага Т7. Стрелками указано направление транскрипции.
Фиг. 9. Оживление рекомбинантных вариантов Sen2-EGFP(N) и Sen2-EGFP(M) вируса Сендай штамма Москва. (А) Клетки 293-Т7, трансфицированные смесью плазмид pET15b-N, pET15b-P, pET15b-L и pSen2 (контроль автофлюоресценции - нет зеленого свечения); (Б) клетки 293-Т7, трансформированные плазмидой pEGFP-N1 (Пример 3) (положительный контроль - все клетки флюоресцируют); (В) интактные клетки 293-Т7 (отрицательный контроль); (Г) клетки 293-Т7, трансфицированные смесью плазмид pET15b-N, pET15b-P, pET15b-L и pSen2-EGFP(N) (флюоресцирующие клетки содержат оживленный рекомбинантный вирус Sen2-EGFP(N); (Д) клетки 293-Т7, трансфицированные смесью плазмид pET15b-N, pET15b-P, pET15b-L и pSen2-EGFP(M) (флюоресцирующие клетки содержат оживленный рекомбинантный вирус Sen2-EGFP(M). Визуализация клеток проведена на микроскопе «Axiovert» 40 CFL ZEISS с использованием светофильтров для зеленой люминесценции. 20Х увеличение.
Ниже приведены примеры получения заявляемых плазмидных конструкций.
Пример 1. Конструирование вспомогательных плазмид pET15b-N, pET15b-P и pET15b-L (Фиг. 1-4).
Все три вспомогательные плазмиды сконструированы по одной схеме на основе плазмиды pET15b [29], в которой экспрессия трансгенов осуществляется под контролем промотора высокоэффективной РНК-полимеразы фага Т7. Этапы конструирования плазмид следующие:
Этап 1. Из плазмидной ДНК pET15b с использованием эндонуклеаз Nco I и BamH I вырезали фрагмент 70 п. н. (позиции 389-320, база данных SnapGene snapgene.com) [29], вместо которого по тем же сайтам рестрикции NcoI и BamH I встраивали синтетически полученный фрагмент ДНК (ООО «Биосинтез», г. Новосибирск) следующей структуры:
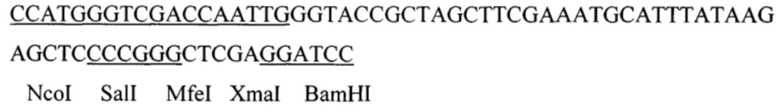
Синтетический фрагмент ДНК для встройки в плазмиду pET15b был рассчитан таким образом, чтобы он содержал уникальные сайты рестрикции (подчеркнуты), которых нет ни в плазмиде pET15b, ни в генах N, Р и L вируса Сендай штамма Москва. Полученную плазмиду обозначили pET15b1.

Этап 2. Гены N, Р и L получали методом ОТ-ПЦР с использованием геномной РНК вируса Сендай штамма Москва в качестве матрицы и в качестве праймеров следующие олигонуклеотиды, представленные в таблице 2.
В результате были получены ДНК-копии генов N, Р и L вируса Сендай, которые рестриктазно-лигазным методом встраивали в плазмиду pET15b1 по соответствующим сайтам рестрикции с получением промежуточных плазмид pET15b-N1, pET15b-Р1 и pET15b-L1. Структуру полученных плазмид подтверждали секвенированием.
Этап 3. С целью оптимизации синтеза белков N, Р и L во вспомогательных плазмидах был проведен сайт-направленный мутагенез плазмид pET15b-N1, pET15b-Р1 и pET15b-L1 с использованием набора реактивов QC Lightning Multi (Agilent Technologies, Cat. 210516-5, USA). В результате мутагенеза были сделаны следующие изменения:
- в плазмиде pET15b-Р1 была произведена синонимичная замена С → А в 129-й позиции гена Р, при этом кодон TCG (сер) альтернативной рамки считывания (ген С) заменился на стоп-кодон TAG, что обеспечивает синтез только одного белкового продукта гена Р - полноразмерного Р белка [Leyrer, 1998] [31];
- так как перед встройкой каждого гена в плазмидах pET15b-N1, pET15b-Р1, pET15b-L1 находится сайт рестрикции Nco I (CCATGG), содержащий ATG-кодон, необходимо было внести в него замену для того, чтобы трансляция не могла начинаться с альтернативного старт-кодона. Последовательность CCATGG была заменена сайт-направленным мутагенезом на CCTAGG (сайт рестриктазы Avr II).
Олигонуклеотиды, использованные для коррекции структуры плазмид методом сайт-направленного мутагенеза, представлены в таблице 3 ниже:
Плазмиды после сайт-направленного мутагенеза (целевые) назвали соответственно pET15b-N, pET15b-P, pET15b-L (Фиг. 1-3).

Анализ экспрессии встроенных генов, проведенный на примере плазмиды pET15b-Р (Фиг. 4), показал высокий уровень продукции вспомогательных белков в культуре трансформированных клеток 293-Т7, конститутивно продуцирующих РНК-полимеразу фага Т7 (культура клеток 293-Т7 любезно предоставлена Кулемзиным С.В., ИМКБ СО РАН). Как следует из Фиг. 4, в лизатах клеток 293-Т7, трансфицированных плазмидой pET15b-Р, выявляется полноразмерный Р-белок вируса Сендай в виде мажорной полосы с молекулярной массой 79 кДа.
Пример 2. Получение плазмид pSen2-MCS(N) и pSen2-MCS(M), содержащих полногеномные копии вирусной ДНК (Фиг. 5-8).
Сборку копии ДНК геномной РНК вируса Сендай штамма Москва осуществляли в плазмиде pUC 19 в 6 этапов.
Этап 1. В плазмиду pUC19 по сайтам NarI/BstI-SbfI встраивали синтетически полученный фрагмент ДНК (ООО «Биосинтез», г. Новосибирск), содержащий промотор РНК-полимеразы фага Т7 [Beaty, 2017] [1], фрагмент рибозима-молот [Beaty, 2017] [1], полилинкер, фрагмент ДНК-копии 3'-НТО генома вируса Сендай (позиции 15345-15384, GenBank Acc. КР717417), геномный рибозим вируса гепатита D [Perrotta, 1991] [34], терминатор РНК-полимеразы фага Т7 (позиции 260-213, база данных SnapGene snapgene.com) [29].
Структура синтетического фрагмента ДНК:

В результате получили плазмиду pUC19-Fr0 (Фиг. 5).
Этапы 2-4. Получение плазмид pUC19-Fr1, pUC19-Fr2 и pUC19-Fr3. Для сборки полногеномной последовательности геном вируса Сендай штамм Москва был разбит in silico на 3 стыкующихся фрагмента в направлении 5'→3': Fr1 - позиции 1-5128 п. н., GenBank Асс. КР717417; Fr2 - позиции 5129-9432 п. н., GenBank Асс. КР717417; Fr3 - позиции 9425-15384 п. н., GenBank Асс. КР717417. Позиции фрагментов были выбраны так, чтобы они не содержали сайтов рестрикции, используемых при их клонировании в плазмиду pUC19-Fr0, что позволяет собрать их воедино в этой плазмиде. Рассчитанные фрагменты получали методом ОТ-ПЦР с использованием в качестве матрицы РНК вируса Сендай штамма Москва и следующих пар праймеров: для фрагмента 1 (клонирование по сайтам рестриктаз XbaI - XmaI)
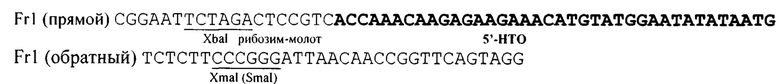
В состав прямого праймера Fr1, кроме сайта рестриктазы XbaI, введена последовательность рибозима-молота и 5'-НТО генома вируса Сендай штамм Москва.
для фрагмента 2 (клонирование по сайтам рестриктаз SpeI - SphI)
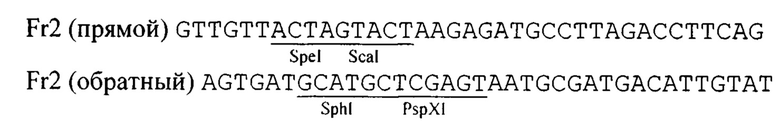
для фрагмента 3 (клонирование по сайтам рестриктаз XmaI-SbfI)
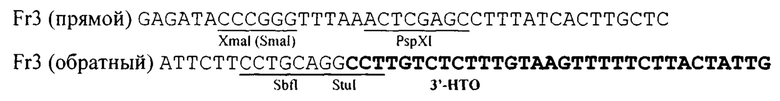
В плазмиду pUC19-Fr0 рестриктазно-лигазным методом встраивали три фрагмента генома вируса Сендай, полученных после ОТ-ПЦР, соответственно по сайтам рестрикции XbaI-XmaI, XbaI/Spel-SphI, XmaI-SbfI и получили три плазмиды: pUC19-Fr1, pUC19-Fr2, pUC19-Fr3 (Фиг. 5). Структуру полученных плазмид подтверждали секвенированием.
Этапы 5-6. Сборка плазмиды pSen2. На 5 этапе в плазмиду pUC19-Fr1 по сайтам XmaI-SwaI переносили фрагмент XmaI-StuI из плазмиды pUC19-Fr3, в результате чего получили плазмиду pUC19-Fr13 (Фиг. 5). На этапе 6 в плазмиду pUC19-Fr13 по сайтам SmaI-PspXI переносили фрагмент ScaI-PspXI из плазмиды pUC19-Fr3 с получением плазмиды pSen2. Структуру генома вируса Сендай штамма Москва в плазмиде pSen2 подтверждали секвенированием.
Для конструирования рекомбинантных вариантов вируса Сендай штамм Москва, несущих в своем геноме встройку чужеродных генов (трансгенов), необходимо получить плазмиду, аналогичную pSen2, но имеющую в местах встройки полилинкер из уникальных сайтов рестрикции (multiple cloning site - MCS). В качестве мест для встройки полилинкера использовали две области: перед геном N (3'-НТО) и перед геном М (межгенный промежуток Р-М). После полилинкера (MCS) в районы встройки должны быть также введены сигнальные последовательности терминации и реинициации транскрипции РНК-полимеразы вируса Сендай, чтобы обеспечить жизнеспособность рекомбинантного варианта вируса. Расчетные схемы плазмид pSen2-MCS(N) и pSen2-MCS(M) для конструирования рекомбинантных вариантов вируса Сендай штамма Москва, представлены на Фиг. 6. Поскольку оба района для встройки трансгенов расположены в плазмиде pUC19-Fr1 (Фиг. 5), все генно-инженерные процедуры по получению плазмид pSen2-MCS(N) и pSen2-MCS(M) удобнее проводить именно с плазмидой pUC19-Fr1 (7913 п. н.), чем с существенно большей по размеру pSen2 (18118 п. н.).
Проведенный in silico анализ структуры генома вируса Сендай штамма Москва в плазмиде pSen2 показал, что в состав полилинкера могут быть введены такие уникальные сайты рестриктаз, как BsiWI, NruI, ClaI, AscI, BssHII. Встройка полилинкера и сигнальных последовательностей перед геном TV (MCS(N)) и перед геном М (MCS(M)) может быть проведена с использованием рестриктаз PspOMI-BsiWI и MluI-PspOMI в соответствующие районы плазмиды pUC19-Fr1 после их сайт-направленного мутагенеза. Для проведения сайт-направленного мутагенеза были рассчитаны следующие олигонуклеотиды:
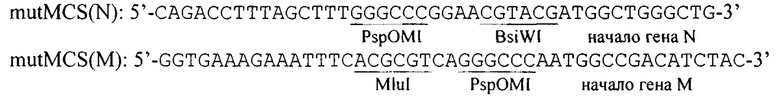
Сайт-направленный мутагенез проводили, как и в Примере 1, с использованием набора реактивов QC Lightning Multi (Agilent Technologies, Cat. 210516-5, USA). Пошаговая схема сайт-направленного мутагенеза и последующей встройки полилинкера и сигнальных последовательностей перед генами N и М в плазмиде pUC19-Fr1 приведена ниже:
Получение плазмиды pUC19-Fr1-MCS(N) (модифицированный участок)
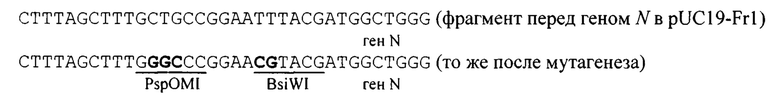
Далее по сайтам рестрикции PspOMI и BsiWI был встроен синтетический фрагмент ДНК:

После встройки этого фрагмента ДНК задействованные сайты рестрикции PspOMI и BsiWI в плазмиде pUC19-Fr1-MCS(N) нивелируются:

Получение плазмиды pUC19-Fr1-MCS(M) (модифицированный участок)
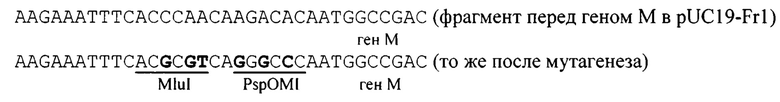
Далее по сайтам рестрикции MluI и PspOMI был встроен синтетический фрагмент ДНК:
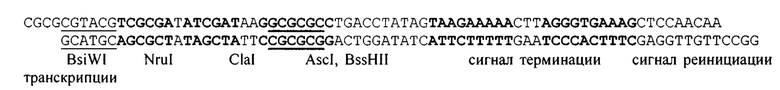
После встройки этого фрагмента ДНК задействованные сайты рестрикции MluI и PspOMI в плазмиде pUC19-Fr1-MCS(M) нивелируются:

Плазмида pUC19-Fr1-MCS(N) использовалась для сборки плазмиды pSen2-MCS(N), содержащей полногеномную ДНК копию вируса Сендай штамма Москва, в соответствии с вышеописанными Этапами 5-6 сборки плазмиды pSen2 (вместо плазмиды pUC19-Fr1). Аналогично использовалась плазмида pUC19-Fr1-MCS(M) для сборки геномной плазмиды pSen2-MCS(M). Структуры рекомбинантных плазмидных ДНК pSen2-MCS(N) и pSen2-MCS(M) представлены на Фиг. 7 и 8, соответственно.
Пример 3. Конструирование рекомбинантных вариантов вируса Сендай штамм Москва, содержащих встройку модельного трансгена EGFP (Фиг. 9).
Трансген EGFP получали методом ПНР с использованием в качестве матрицы плазмиды pEGFP-N1 [33] и олигонуклеотидных праймеров:

Встройку трансгена EGFP проводили рестриктазно-лигазным методом в полилинкер плазмид pSen2-MCS(N) и pSen2-MCS(M) по сайтам рестриктаз BsiWI и BssHII. В результате были получены геномные плазмиды pSen2-EGFP(N) и pSen2-EGFP(M).
Для оживления рекомбинантных вариантов вируса Сендай штамм Москва использовали культуру клеток 293-Т7, продуцирующую РНК-полимеразу фага Т7 (можно использовать любую культуру клеток эукариот, рекомбинантную или трансформированную, которая продуцирует РНК-полимеразу фага Т7). 80%-ный монослой клеток 293-Т7, выращенный в 6-ти луночном планшете, инфицировали вирусом MVA-T7 с множественностью 10 инфекционных единиц/клетка и через час трансфицировали смесью плазмидных ДНК (по 5 мкг каждой) с реагентом Lipofectamine™ LTX Plus (Invitrogen, Cat. 15338).
Использовали два типа смеси:
1) геномная плазмида pSen2-EGFP(N) + три вспомогательных плазмиды pET15b-N, pET15b-P и pET15b-L;
2) геномная плазмида pSen2-EGFP(M) + три вспомогательных плазмиды pET15b-N, pET15b-P и pET15b-L;
Для контроля оживления немодифицированного вируса Сендай использовали смесь плазмид pSen2, pET15b-N, pET15b-P и pET15b-L (Фиг. 9А). Для контроля EGFP флюоресценции использовали плазмиду pEGFP-N1 [33]. В плазмиде pEGFP-N1 ген EGFP экспрессируется под контролем CMV промотора независимо от наличия в клетках РНК-полимеразы фага Т7 и индуцирует интенсивную флюоресценцию трансформированных клеток (Фиг. 9Б).
Через 48 часов инкубации (37°С, 5% СО2) трансфицированные клетки анализировали на микроскопе «Axiovert» 40 CFL ZEISS с использованием светофильтров для зеленой люминесценции. Как следует из Фиг. 9А, в клетках, трансфицированных смесью плазмид pET15b-N, pET15b-P, pET15b-L и pSen2, наблюдается характерный для вируса Сендай цитопатический эффект (округлившиеся клетки, синцитии) в световом поле, но отсутствует флюоресценция. Наличие цитопатического эффекта свидетельствует об оживлении вируса Сендай штамма Москва с геномной плазмиды pSen2. На Фиг. 9 В представлены интактные нетрансфицированные клетки 293-Т7 (отрицательный контроль). Как следует из сравнения Фиг. 9Г и Фиг. 9Д, сконструированный нами набор рекомбинантных плазмидных ДНК обеспечивает создание рекомбинантных вариантов вируса Сендай штамма Москва, при этом уровень экспрессии трансгена рекомбинантом Sen2-EGFP(N) выше (более интенсивная флюоресценция), чем рекомбинантом Sen2-EGFP(M), что соответствует высказанным нами ранее предположениям о зависимости уровня экспрессии трансгена от близости к 3'-концу генома.
Таким образом, заявляемое техническое решение позволяет получать рекомбинантные варианты вируса Сендай штамма Москва со встройкой и экспрессией трансгенов в 3'-нетранслируемой области генома перед геном N и в межгенном промежутке Р-М перед геном М. В качестве трансгенов могут быть использованы противоопухолевые белки или протективно-значимые антигены патогенных агентов, с целью разработки на их основе противоопухолевых лекарственных средств и векторных вакцин против инфекционных заболеваний.
Источники научно-технической и патентной информации
1. Beaty S.M. et al. Efficient and robust Paramyxoviridae reverse genetics systems // mSphere. - 2017. - Vol.2. - No. 2. - e00376-16. Doi: 10.1128/mSphere.00376-16.
2. Zainutdinov S.S. et al. Complete genome sequence of Sendai virus oncolytic strain Moscow. // Genome Announcements. - 2016. - Vol.4. - No. 4. - e00818-16. Doi: 10.1128/genomeA.00818-16.
3. Matveeva O.V. et al. Mechanisms of oncolysis by paramyxovirus Sendai. // Acta Naturae. - 2015. - Vol.7. - No. 2. - P. 6-16. PMID: 26085940.
4. Russell C.J., Hurwitz J.L. Sendai virus-vectored vaccines that express envelope glycoproteins of respiratory viruses. // Viruses. - 2021. - Vol.13. No. 6: 1023. Doi: 10.3390/V13061023.
5. Adderson E. et al. Safety and immunogenicity of an intranasal Sendai virus-based human parainfluenza virus type 1 vaccine in 3- to 6-year-old children. // Clinical and Vaccine Immunology. - 2015. - V. 22. - No. 3. Doi: 10.1128/CVI.00618-14
6. Huang F.S. et al. Safety and immunogenicity of an intranasal Sendai virus-based vaccine for human parainfluenza virus type I and respiratory syncytial virus (SeVRSV) in adults. // Hum. Vaccin. Immunother. - 2021. - Vol.17. - No. 2. - P. 554-559. Doi: 10.1080/21645515.2020.1779517.
7. Nyombaire J. et al. First-in-human evaluation of the safety and immunogenicity of an intranasally administered replication-competent Sendai virus-vectored HIV type 1 Gag vaccine: induction of potent T-cell or antibody responses in prime-boost regimens. // J. Infect. Dis. - 2017. - Vol.215. - No. 1. - P 95-104. Doi: 10.1093/infdis/iiw500.
8. Russell C.J. et al. A Sendai virus recombinant vaccine expressing a gene for truncated human metapneumovirus (hMPV) fusion protein protects cotton rats from hMPV challenge. // Virology. - 2017. - Vol.509. - P. 60-66. Doi: 10.1016/i.virol.2017.05.021.
9. Зайчук T.A. и др. Проблемы создания вакцин против бетакоронавирусов: антителозависимое усиление инфекции и вирус Сендай как возможный вакцинный вектор // Молекулярная биология. - 2020. - Т. 54. - №6. - С.922-938. https://doi.Org/l0.31857/S0026898420060154.
10. Matveeva O.V. et al. Oncolysis by paramyxoviruses: multiple mechanisms contribute to therapeutic efficiency. // Mol. Ther. Oncolytics. - 2015. - Vol.2: 15011. doi: 10.1038/mto.2015.11.
11. Zimmermann M. et al. Attenuated and protease-profile modified Sendai virus vectors as a new tool for virotherapy of solid tumors. // Plos One. - 2014. - Vol.9. -No. 3. e90508. Doi: 10.137l/iournal.pone.0090508.
12. Kinoh H. et al. Generation of a recombinant Sendai virus that is selectively activated and lyses human tumor cells expressing matrix metalloproteinases.// Gene Ther.-2004. - Vol.11.-P. 1137-1145. Doi:: 10.1038/si.gt.3302272..
13. Iwadate Y. et al. Recombinant Sendai virus vector induces complete remission of established brain tumors through efficient interleukin-2 gene transfer in vaccinated rats. // Clin. Cancer. Res. - 2005. - Vol.11. - No. 10. - P. 3821-3827. Doi: 10.1158/1078-0432.CCR-04-1485.
14. Kinoh H. and Inoue M. New cancer therapy using genetically-engineered oncolytic Sendai virus vector. // Front. Biosci. - 2008. - Vol.13. - P. 2327-2334. Doi: 10.2741/2847.
15. Tatsuta K. et al. Complete elimination of established neuroblastoma by synergistic action of gamma-irradiation and DCs treated with rSeV expressing interferon-beta gene. // Gene Ther. - 2009. - Vol.16. - P. 240-251. Doi: 10.1038/gt.2008.161
16. Yonemitsu Y. et al. Immunostimulatory virotherapy using recombinant Sendai virus as a new cancer therapeutic regimen. // Front Biosci. - 2008. - Vol.13. - P. 1892-1898. Doi: 10.2741/2809.
17. Tanaka Y. et al. Oncolytic Sendai virus-induced tumor-specific immunoresponses suppress "simulated metastasis" of squamous cell carcinoma in an immunocompetent mouse model". // Head & Neck. - 2019. - Vol.41. - No. 6. - P. 1676-1686. Doi:10.1002/hed.25642.
18. Kurooka M. and Kaneda Y. Inactivated Sendai virus particles eradicate tumors by inducing immune responses through blocking regulatory T cells. // Cancer Res. -2007. Vol.67. No. 1. - P. 227-236. Doi: 10.1158/0008-5472.CAN-06-1615.
19. Kawano H. et al. A new therapy for highly effective tumor eradication using HVJ-E combined with chemotherapy. // BMC Medicine. - 2007. - Vol.5: 28. Doi: 10.1186/1741-7015-5-28
20. Kawano H. et al. New potential therapy for orthotopic bladder carcinoma by combining HVJ envelope with doxorubicin. Cancer Chemother. Pharmacol. // 2008. - Vol.61. - No. 6. - P. 973-978. Doi: 10.1007/s00280-007-0553-1.
21. Fujihara A. et al. Intratumoral injection of inactivated Sendai virus particles elicits strong antitumor activity by enhancing local CXCL10 expression and systemic NK cell activation. // Cancer Immunol. Immunother. - 2008. - Vol.57. -No. 1. - P. 73-84. Doi: 10.1007/s00262-007-0351-y.
22. Hui G. et al. Induction of apoptosis in hormone-resistant human prostate cancer PC3 cells by inactivated Sendai virus. // Biomed. Environ. Sci. - 2014. - Vol.27. -No. 7. - P. 506-514. Doi: 10.3967/bes2014.082.
23. Kiyohara E. et al. Intratumoral injection of hemagglutinating virus of Japan-envelope vector yielded an antitumor effect for advanced melanoma: a phase I/IIa clinical study. // Cancer Immunology, Immunotherapy. - 2020. - Vol.69. - P. 1131-1140. Doi: 10.1007/s00262-020-02509-8.
24. Matveeva O.V. et al. Oncolysis by paramyxoviruses: preclinical and clinical studies. // Mol. Ther. Oncolytics. - 2015. - Vol.2: 150017. Doi: 10.1038/mto.2015.17.
25. Сенин В. и др. Метод иммунотерапии онкологических заболеваний и фармацевтические композиции на основе вируса Сендай. // РФ патент №2519763. Опубликован 26.06.2014. Бюл. №17.
26. Ilyinskaya G.V. et al. Oncolytic Sendai Virus Therapy of Canine Mast Cell Tumors (A Pilot Study).// Front. Vet. Sci. - 2018. - Vol.5: 116. Doi: 10.3389/fvets.2018.00116.
27. Hurwitz J.L. at al. Modified Sendai virus vaccine and imaging vector. Patent US9637758B2. - 2018.
28. Makowska D.O. et al. Engineering of live chimeric vaccines against human metapneumovirus. // Pathogens. - 2020. - Vol.9. - No. 2:135. Doi: 10.3390/pathogens9020135.
29. https://www.snapgene.com/resources/plasmid-files/?set=pet_and_duet_vectors_(novagen) &plasmid=pET-15b
30. https://www.snapgene.com/resources/plasmid-files/?set=basic_cloning_vectors& plasmid=pUC19
31. Leyrer S. et al. Rapid and efficient recovery of Sendai virus from cDNA: factors influencing recombinant virus rescue. // J. Virol. Methods. - 1998. - Vol.75. - No. 1. - P. 47-58. Doi: 10.1016/s0166-0934(98)00095-0.
32. Matsumoto Y. et al. The control of paramyxovirus genome hexamer length and mRNA editing. // RNA. - 2018. - Vol.24. - P. 461-467. Doi: 10.1261/rna.065243.117
33. https://www.snapgene.com/resources/plasmid-files/?set=fluorescent_protein_genes_and_plasmids&plasmid=pEGFP-N1
34. Perrotta A.T. and Been M.D. A pseudoknot-like structure required for efficient self-cleavage of hepatitis delta virus RNA. // Nature. - 1991. - Vol.350. - No. 6317. - P. 434-436. Doi: 10.1038/350434a0.
| название | год | авторы | номер документа |
|---|---|---|---|
| Рекомбинантный штамм Sen-Sdelta(M) вируса Сендай, продуцирующий S белок SARS-CoV-2 и используемый для получения интраназальной вакцины против COVID-19 | 2024 |
|
RU2837536C1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pGEM-Puro-DS-Apo, СОДЕРЖАЩАЯ СИНТЕТИЧЕСКИЙ ГЕН АПОПТИНА, ФЛАНКИРОВАННЫЙ ПОСЛЕДОВАТЕЛЬНОСТЯМИ ГЕНОМА ВИРУСА ОСПОВАКЦИНЫ ИЗ РАЙОНА C10L-C12L, И РЕКОМБИНАНТНЫЙ ШТАММ VVdGF-ApoS24/2 ВИРУСА ОСПОВАКЦИНЫ, ПРОДУЦИРУЮЩИЙ АПОПТИН | 2012 |
|
RU2492238C1 |
| СИСТЕМЫ ЭКСПРЕССИИ РНК РЕКОМБИНАНТНОГО ВИРУСА НЬЮКАСЛСКОЙ БОЛЕЗНИ И ВАКЦИНЫ | 1999 |
|
RU2270864C2 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pBi101-IL18, КОДИРУЮЩАЯ СИНТЕЗ ИНТЕРЛЕЙКИНА-18 ЧЕЛОВЕКА В ТРАНСГЕННЫХ РАСТЕНИЯХ | 2005 |
|
RU2302460C1 |
| Рекомбинантный штамм VV-mNIS-NS1 вируса осповакцины, продуцирующий симпортер йодида натрия мышей mNIS и белок NS1 парвовируса крыс H-1 для тераностики злокачественных опухолей | 2023 |
|
RU2819082C1 |
| РЕКОМБИНАНТНЫЙ ШТАММ VV-GMCSF-Lact ВИРУСА ОСПОВАКЦИНЫ, ОБЛАДАЮЩИЙ ОНКОЛИТИЧЕСКОЙ АКТИВНОСТЬЮ И ПРОДУЦИРУЮЩИЙ ГРАНУЛОЦИТАРНО-МАКРОФАГАЛЬНЫЙ КОЛОНИЕСТИМУЛИРУЮЩИЙ ФАКТОР ЧЕЛОВЕКА И ОНКОТОКСИЧЕСКИЙ БЕЛОК ЛАКТАПТИН | 2015 |
|
RU2604187C1 |
| Генетическая конструкция для экспрессии генов mNG_CD4-CXCR4, рекомбинантная плазмида rVSV_mNG_CD4-CXCR4 и рекомбинантный штамм вируса везикулярного стоматита rVSV_mNG_CD4-CXCR4, обеспечивающий таргетный виролизис клеток, экспонирующих на своей поверхности белки gp120/gp 41 ВИЧ-1 тропности X4 | 2021 |
|
RU2768032C1 |
| РЕКОМБИНАНТНЫЙ ШТАММ VV-GMCSF-S1/3 ВИРУСА ОСПОВАКЦИНЫ, ПРОДУЦИРУЮЩИЙ СЕКРЕТИРУЕМЫЙ ГРАНУЛОЦИТАРНО-МАКРОФАГАЛЬНЫЙ КОЛОНИЕСТИМУЛИРУЮЩИЙ ФАКТОР ЧЕЛОВЕКА | 2013 |
|
RU2565544C2 |
| Способ получения рекомбинантного вируса везикулярного стоматита | 2022 |
|
RU2807751C1 |
| ШТАММ РЕКОМБИНАНТНОГО ВИРУСА ОСПОВАКЦИНЫ, ЭКСРЕССИРУЮЩИЙ СТРУКТУРНЫЕ БЕЛКИ ВИРУСА ВЕНЕСУЭЛЬСКОГО ЭНЦЕФАЛОМИЕЛИТА ЛОШАДЕЙ И ПРИГОДНЫЙ ДЛЯ ПРОИЗВОДСТВА ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1993 |
|
RU2091489C1 |
























Изобретение относится к биотехнологии. Представлен набор рекомбинантных плазмидных ДНК для получения рекомбинантных вирусов Сендай штамма Москва. Изобретение относится к рекомбинантным плазмидным ДНК, содержащим полноразмерную ДНК-копию генома вируса Сендай штамма Москва и гены структурных белков нуклеокапсида N, фосфопротеина Р и вирусной полимеразы L, и может быть использовано в биотехнологии, в частности в генетической инженерии для конструирования рекомбинантных вариантов вируса Сендай штамма Москва, содержащих встройки трансгенов противоопухолевых белков или протективно-значимых антигенов патогенных агентов, с целью разработки на их основе противоопухолевых лекарственных средств и векторных вакцин против инфекционных заболеваний. Структурный элемент включает полилинкер из пяти уникальных сайтов для крупнощепящих эндонуклеаз рестрикции BsiWI, NruI, ClaI, AscI, BssHII, за которым следует сигнал терминации транскрипции трансгена и сигнал реинициации транскрипции последующего гена для РНК-полимеразы вируса Сендай. Экспрессия генов N, Р и L вируса Сендай штамма Москва так же, как и синтез геномных РНК рекомбинантных штаммов вируса Сендай, осуществляется с соответствующих плазмидных ДНК под контролем полимеразы фага Т7. Точность размера геномных РНК контролируется рибозимами, встроенными по ее 3' и 5' концам. Техническим результатом изобретения является получение 3-х рекомбинантных плазмидных ДНК, экспрессирующих гены N, Р и L вируса Сендай штамма Москва (вспомогательные плазмиды pET15b-N, pET15b-P, pET15b-L), а также двух плазмид с полноразмерными копиями ДНК геномной РНК вируса Сендай штамм Москва (GenBank Асc. КР717417.1), содержащих структурный элемент для встройки и экспрессии трансгенов в 3'-нетранслируемой области вирусного генома (плазмида pSen2-MSC(N)) и между генами Р и М (pSen2-MCS(M)). Набор из трех вспомогательных плазмид и геномной плазмиды pSen2-MSC(N) обеспечивает создание рекомбинантных вариантов вируса Сендай штамма Москва с высоким уровнем экспрессии трансгенов. А набор из тех же вспомогательных плазмид и геномной плазмиды pSen2-MSC(M) обеспечивает создание рекомбинантных вариантов вируса Сендай штамма Москва со средним уровнем экспрессии трансгенов. Верификация заявляемого набора рекомбинантных плазмидных ДНК была проведена на примере модельного трансгена зеленого флюоресцентного белка EGFP. 2 н.п. ф-лы, 9 ил., 3 табл., 3 пр.
1. Набор рекомбинантных плазмидных ДНК для получения рекомбинантных вирусов Сендай штамма Москва, включающий четыре плазмидные конструкции:
- первую плазмидную конструкцию pET15b-N, представленную на физической и генетической карте на фиг. 1, обеспечивающую экспрессию гена N, кодирующего нуклеопротеин вируса Сендай штамма Москва в трансформированных клетках эукариот, продуцирующих РНК-полимеразу фага Т7, имеющую последовательность SEQ ID No.: 1, размер 7231 п. н. и молекулярную массу 4,8 мегадальтон и состоящую из BamHI-NcoI векторного фрагмента плазмиды pET15b, включающего участок начала репликации ori, ген бета-лактамазы, придающей устойчивость к ампициллину, промотор и терминатор РНК-полимеразы фага Т7, между которыми встроен ген N, фланкированный модифицированной последовательностью 5'-CCTAGGGTCGACCAATTG, содержащей сайты рестриктаз AvrII, SalI и MfeI;
- вторую плазмидную конструкцию pET15b-Р, представленную на физической и генетической карте на фиг. 2, обеспечивающую экспрессию гена Р, кодирующего фосфопротеин вируса Сендай штамма Москва, в трансформированных клетках эукариот, продуцирующих РНК-полимеразу фага Т7, имеющую последовательность SEQ ID No.: 2, размер 7351 п. н. и молекулярную массу 4,9 мегадальтон и состоящую из BamHI-NcoI векторного фрагмента плазмиды pET15b, включающего участок начала репликации ori, ген бета-лактамазы, придающей устойчивость к ампициллину, промотор и терминатор РНК-полимеразы фага Т7, между которыми встроен ген Р, фланкированный последовательностью 5'-CCTAGG;
- третью плазмидную конструкцию pET15b-L, представленную на физической и генетической карте на фиг. 3, обеспечивающую экспрессию гена L, кодирующего полимеразу вируса Сендай штамма Москва, в трансформированных клетках эукариот, продуцирующих РНК-полимеразу фага Т7, имеющую последовательность SEQ ID No.: 3, размер 12351 п. н. и молекулярную массу 8,2 мегадальтон и состоящую из BamHI-NcoI векторного фрагмента плазмиды pET15b, включающего участок начала репликации ori, ген бета-лактамазы, придающей устойчивость к ампициллину, промотор и терминатор РНК-полимеразы фага Т7, между которыми встроен ген L, фланкированный последовательностями 5'-CCTAGGGTCGAC и CCCGGGCTCGA-3', содержащей сайт рестриктазы XmaI;
- четвертую плазмидную конструкцию pSen2-MCS(N), представленную на физической и генетической карте на фиг. 7, обеспечивающую транскрипцию геномной рекомбинантной РНК вируса Сендай штамма Москва со встройкой трансгенов перед геном N в трансформированных клетках эукариот, продуцирующих РНК-полимеразу фага Т7, имеющую последовательность SEQ ID No.: 4, размер 18184 п. н. и молекулярную массу 12 мегадальтон и состоящую из SbfI-NarI векторного фрагмента плазмиды pUC 19, включающего участок начала репликации ori, ген бета-лактамазы, придающей устойчивость к ампициллину, и встройки, в которой последовательно расположены: промотор РНК-полимеразы фага Т7, рибозим-молот, копия ДНК 3'-НТО генома вируса Сендай штамма Москва, полилинкер для встройки трансгенов, включающий пять уникальных сайтов для эндонуклеаз рестрикции BsiWI, NruI, ClaI, AscI, BssHII, сигнал терминации транскрипции трансгена, сигнал реинициации транскрипции последующего гена для РНК-полимеразы вируса Сендай, ген N, ген Р, ген М, ген F, ген HN, ген L, копия ДНК 5'-НТО генома вируса Сендай штамма Москва, геномный рибозим вируса гепатита D, терминатор РНК-полимеразы фага Т7.
2. Набор рекомбинантных плазмидных ДНК для получения рекомбинантных вирусов Сендай штамма Москва, включающий четыре плазмидные конструкции:
- первую плазмидную конструкцию pET15b-N, представленную на физической и генетической карте на фиг. 1, обеспечивающую экспрессию гена N, кодирующего нуклеопротеин вируса Сендай штамма Москва в трансформированных клетках эукариот, продуцирующих РНК-полимеразу фага Т7, имеющую последовательность SEQ ID No.: 1, размер 7231 п. н. и молекулярную массу 4,8 мегадальтон и состоящую из BamHI-NcoI векторного фрагмента плазмиды pET15b, включающего участок начала репликации ori, ген бета-лактамазы, придающей устойчивость к ампициллину, промотор и терминатор РНК-полимеразы фага Т7, между которыми встроен ген N, фланкированный модифицированной последовательностью 5'-CCTAGGGTCGACCAATTG, содержащей сайты рестриктаз AvrII, SalI и MfeI;
- вторую плазмидную конструкцию pET15b-Р, представленную на физической и генетической карте на фиг. 2, обеспечивающую экспрессию гена Р, кодирующего фосфопротеин вируса Сендай штамма Москва, в трансформированных клетках эукариот, продуцирующих РНК-полимеразу фага Т7, имеющую последовательность SEQ ID No.: 2 размер 7351 п. н. и молекулярную массу 4,9 мегадальтон и состоящую из BamHI-NcoI векторного фрагмента плазмиды pET15b, включающего участок начала репликации ori, ген бета-лактамазы, придающей устойчивость к ампициллину, промотор и терминатор РНК-полимеразы фага Т7, между которыми встроен ген Р, фланкированный последовательностью 5'-CCTAGG;
- третью плазмидную конструкцию pET15b-L, представленную на физической и генетической карте на фиг. 3, обеспечивающую экспрессию гена L, кодирующего полимеразу вируса Сендай штамма Москва, в трансформированных клетках эукариот, продуцирующих РНК-полимеразу фага Т7, имеющую последовательность SEQ ID No.: 3, размер 12351 п. н. и молекулярную массу 8,2 мегадальтон и состоящую из BamHI-NcoI векторного фрагмента плазмиды pET15b, включающего участок начала репликации ori, ген бета-лактамазы, придающей устойчивость к ампициллину, промотор и терминатор РНК-полимеразы фага Т7, между которыми встроен ген L, фланкированный последовательностями 5' -CCTAGGGTCGAC и CCCGGGCTCGA-3', содержащей сайт рестриктазы XmaI;
- четвертую плазмидную конструкцию pSen2-MCS(M), представленную на физической и генетической карте на фиг. 8, обеспечивающую транскрипцию геномной рекомбинантной РНК вируса Сендай штамма Москва со встройкой трансгенов перед геном М в трансформированных клетках эукариот, продуцирующих РНК-полимеразу фага Т7, имеющую последовательность SEQ ID No.: 5, размер 18184 п. н. и молекулярную массу 12 мегадальтон и состоящую из SbfI-NarI векторного фрагмента плазмиды pUC19, включающего участок начала репликации ori, ген бета-лактамазы, придающей устойчивость к ампициллину, и встройки, в которой последовательно расположены: промотор РНК-полимеразы фага Т7, рибозим-молот, копия ДНК 3'-НТО генома вируса Сендай штамма Москва, ген N, ген Р, полилинкер для встройки трансгенов, включающий пять уникальных сайтов для эндонуклеаз рестрикции BsiWI, NruI, ClaI, AscI, BssHII, сигнал терминации транскрипции трансгена, сигнал реинициации транскрипции последующего гена для РНК-полимеразы вируса Сендай, ген М, ген F, ген HN, ген L, копия ДНК 5'-НТО генома вируса Сендай штамма Москва, геномный рибозим вируса гепатита D, терминатор РНК-полимеразы фага Т7.
| US 8741650 B2, 15.09.2020 | |||
| Способ терапии метастатического рака с использованием вируса Сендай | 2017 |
|
RU2662916C1 |
| РЕЖИМЫ ПРАЙМ-БУСТ, ВКЛЮЧАЮЩИЕ ВВЕДЕНИЕ ПО МЕНЬШЕЙ МЕРЕ ОДНОЙ КОНСТРУКЦИИ мРНК | 2016 |
|
RU2742993C2 |
Авторы
Даты
2023-01-12—Публикация
2021-12-09—Подача