Изобретение относится к химии кремнийорганических соединений, конкретно к способу получения силанолов, силоксанолов и алкоксиланолов из соответствующих гидросиланов.
Силанолы, особенно силоксанолы, являются востребованными кремнийорганическими соединениями и применяются в качестве реагентов в реакции Хияма-Денмарка для создания С-С-связей [Denmark S.E. and Ambrosi А. Org. Process Res. Dev., 2015,19 (8), 982; Nakao Y. and Hiyama T. Chem. Soc. Rev., 2011, 40, 4893], для получения силоксановых композитов холодного отверждения (в том числе коммерчески реализуемого двухкомпонентного герметика Виксинт ПК-68), мягких резин и гидрофобных покрытий [Cervantes J., Zarraga R. and Salazar-Hernandez C. Appl. Organomet. Chem., 2012, 26, 157]; а также органосилоксановых структур заданной архитектуры [Lang Н. and Luhmann В. Adv. Mater., 2001, 13 (20), 1523; Majoral J.-P. and Caminade A.-M. Chem. Rev., 1999, 99, 845; Coupar P.I., Jaffres P.A. and Morris R.E. Dalton Trans., 1999, 13, 2183], что позволяет настраивать их физико-химические свойства (термо- и морозостойкость, гидрофобность, механические, реологические и изоляционные параметры). Три(трет-бутокси)силанол используется для осаждения наноламинатных слоев аморфного диоксида кремния; трет-бутилдиметилсиланол является инициатором полимеризации 1,2-бензолдикарбоксальдегида [DiLauro А.М., Robbins J.S., Phillips S.T. Macromolecules, 2013, 46 (8), 2963] и этиленоксида [Soula О., Guyot A. Langmuir, 1999, 15 (23), 7956].
Известны способы получения силанолов, в которых используется гидролиз хлор- или алкоксисиланов. Однако такие способы очень неудобны с технологической точки зрения, так как для их реализации необходим строгий контроль условий реакции, в частности значения рН реакционной среды: при несоблюдении требуемых условий силанолы легко конденсируются, что приводит к значительному снижению выхода целевых продуктов [Rochow E.G., Gilliam W.F. J. Am. Chem. Soc, 1941, 63, 798; Sauer R.O. J. Am. Chem. Soc, 1944, 66, 1707; Tyler L.J. Am. Chem. Soc, 1955, 77, 770; Sieburth S.M., Mu W. J. Org. Chem., 1993, 58, 7584; Hirabayashi K., Mori A., Hiyama T. Tetrahedron Lett., 1997, 38, 461].
Известны способы получения силанолов, в которых используют окисление гидросиланов с преобразованием связи Si-H в связь Si-OH. В таких способах в качестве окислителей применяют соли серебра (I) [Duffaut N., Calas R., Mac J.-С.Bull. Chem. Soc. Fr., 1959, 1971], гидропероксиды [Sommer L.H., Ulland L.A., Parker G.A. J. Am. Chem. Soc, 1972, 94, 3469; Nagai Y., Honda K., Migita T. J. Organomet. Chem., 1967, 8, 372; Арзуманян A.B., Музафаров A.M., Гончарова И.К., Калинина A.A. Патент РФ 2633351 (2017)], перманганаты [Lickiss P.D., Lucas R. J. Organomet. Chem., 1995, 521, 229], диоксираны [Adam W., Mello R., Curci R. Angew. Chem., 1990, 102, 916; Kawakami Y., Sakuma Y., Wakuda Т., Nakai Т., Shirasaka M., Kabe Y. Organometallics, 2010, 29, 3281-3288], оксид осмия [Valliant-Saunders К., Gunn E., Shelton G.R., Hrovat D.A., Borden W.T., Mayer J.M. Inorg. Chem., 2007, 46, 5212], оксазиридины [Cavicchioli M., Montanari V., Resnati G. Tetrahedron Lett., 1994, 35, 6329], озон [Spialter L., Austin J.D. Inorg. Chem., 1966, 5, 1975; Spialter L., Austin J.D. J. Am. Chem. Soc, 1965, 87, 4406; Spialter L., Pazdernik L., Bernstein S., Swansiger W.A., Buell G.R., Freeburger M.E. J. Am. Chem Soc, 1971, 93, 5682; Ouellette R.J., Marks D.L. J. Organomet. Chem., 1968, 11, 407] и перекись водорода в присутствии органических катализаторов [Limnios D., Kokotos C.G. ACS Catal., 2013, 3 (10), 2239-2243]. Известны способы гидролитического окисления гидросиланов, катализируемые солями и комплексами таких металлов, как Rh, Ir, Ru, Ag, Cu, Cr, Re, Pt и Au [Shi M., Nicholas K.M. J. Chem. Research, 1997, 400-401; Lee Y., Seomoon D., Kim S., Han H., Chang S., Lee P.H. J. Org. Chem., 2004, 69, 1741; Garces K., Fernandez-Alvarez F.J., Polo V., Lalrempuia R., Perez-Torrente J.J., Oro L.A. Chem. Cat. Chem., 2014, 6, 1691-1697; Aliaga-Lavrijsen M., Iglesias M., Cebollada A., Garces K., Garcia N., Sanz Miguel P.J., Fernandez-Alvarez F.J., Perez-Torrente J.J., Oro L.A. Organometallics, 2015, 34 (11), 2378-2385; Lee M., Ко S., Chang S. J. Am. Chem. Soc, 2000, 122, 12011-12012; Mori K., Tano M., Mizugaki Т., Ebitani K., Kaneda K. New J. Chem., 2002, 26, 1536-1538; Choi E., Lee C, Na Y., Chang S. Org. Lett., 2002, 4, 2369-2371; Mitsudome Т., Arita S., Mori H., Mizugaki Т., Jitsukawa K., Kaneda K. Angew. Chem., 2008, 120, 8056-8058; Schubert U., Lorenz C. Inorg. Chem., 1997, 36, 1258-1259; Motokura K., Kashiwame D., Miyaji A., Baba T. Org. Lett., 2012, 14 (10), 2642-2645].
Недостатками описанных способов являются: ограниченная применимость (они не позволяют получать силокси- и алкоксисиланолы или их круг ограничен 1-2 примерами); зачастую достаточно жесткие условия осуществления, приводящие к конденсации образующихся силанолов и, следовательно, к снижению их выхода; в ряде случаев использование дорогих или токсичных реагентов; коммерческая недоступность, сложный синтез и дороговизна многих используемых катализаторов; образование эквивалентного количества продукта восстановления окислителя, затрудняющего выделение целевого продукта.
Для решения указанных проблем нужно было разработать способ, соответствующий следующим требованиям: недорогая, коммерчески доступная и нетоксичная (или малотоксичная) окислительная система; мягкие условия процесса, сводящие к минимуму образование побочных продуктов конденсации; легкое выделение целевых силанолов с высоким выходом; применимость к силанам не только с C-Si-, но и с C-O-Si- и Si-O-Si-связями.
В последние годы получило развитие аэробное окисление органических соединений с преобразованием связей С-Н в С-ОН в присутствии комбинации металло- и органокатализаторов [Zhang С., Huang Z., Lu J., Luo N. and Wang F. J. Am. Chem. Soc, 2018, 140 (6), 2032; Gaster E., Kozuch S. and Pappo D. Angew. Chem., 2017, 129, 1]. (Отметим, что кислород является доступным и экологичным окислителем, не образующим токсичных побочных продуктов.)
В дальнейшем данный способ был расширен на получение силанолов из гидросиланов, осуществляемое при нагревании в атмосфере кислорода с использованием каталитической системы, состоящей из N-гидроксифталимида (NHPI) и ацетата меди или кобальта [Arzumanyan A.V., Goncharova I.K., Novikov R.A., Milenin S.A, Boldyrev K.L., Solyev P.N., Muzafarov A.M. Green Chemistry, 2018, 20 (7), 1467-1471]. Так, для получения бис(триметилсилокси)метилсиланола указанным способом перемешивают смесь 67,5 ммоль бис(триметилсилокси)метилсилана, 13,5 ммоль N-гидроксифталимида, 0,675 ммоль ацетата меди в 150 мл ацетонитрила при 60 С в течение 8 ч в потоке кислорода. Выход бис(триметилсилокси)метилсиланола составляет 70%. Аналогично из соответствующих гидросиланов получают (триметилсилокси)метилфенилсиланол с выходом 20% и бис(триметилсилокси)фенилсиланол с выходом 35%.
Данный способ наиболее близок к заявляемому способу по существенным признакам, поэтому и был выбран в качестве прототипа. Недостатками способа являются: большая продолжительность реакции (10-24 ч), низкие селективность (образование значительного количества продуктов конденсации) и выходы (20-70% для низкомолекулярных силанолов) целевых продуктов; невозможность получения алкоксисиланолов (алкоксигруппа гидролизуется в указанных условиях).
Задачей изобретения является разработка способа получения силанолов окислением гидросиланов кислородом, позволяющего получать силанолы как с C-Si, так и с C-O-Si и Si-O-Si-связями, а также обеспечивающего высокий выход целевого продукта в мягких условиях при небольшой продолжительности процесса.
Задача решается заявляемым способом получения силанолов R1R2R3SiOH из гидросиланов R1R2R3SiH, где каждый из заместителей R1, R2 и R3 независимо обозначает фенил, C1-С3-алкил, C1-С4-алкокси, силокси, включающим окисление гидросилана кислородом при атмосферном давлении в присутствии каталитических количеств N-гидроксисукцинимида и соли кобальта (И) при нагревании в апротонном органическом растворителе.
В общем виде заявляемый способ может быть представлен следующей схемой:
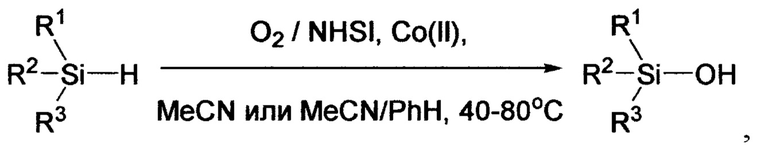
где R1, R2 и R3 независимо обозначают фенил, C1-С3-алкил, силокси, С1-С4-алкокси.
В отличие от прототипа, где в основном используют NHPI/Cu(II)-комбинацию катализаторов, в предлагаемом способе в качестве катализаторов используют MNSI/Со(II)-комбинацию. При этом выход целевых продуктов выше, а продолжительность синтеза (чаще всего 1-2 ч) меньше, чем в способе-прототипе (10-24 ч). Например, заявляемый способ позволяет получить (триметилсилокси)метилфенилсиланол с выходом 96% и бис(триметилсилокси)фенилсиланол с выходом 98%, что соответственно на 76 и 63% выше, чем в способе-прототипе.
Заявляемый способ позволяет синтезировать три(трет-бутокси)силанол, используемый для осаждения наноламинатных слоев диоксида кремния, из стабильного и доступного три(трет-бутокси)силана с выходом 96%. Альтернативный способ использует в качестве прекурсора малостабильный три(трет-бутокси)хлорсилан, сопровождается образованием токсичного хлористого водорода и характеризуется более низким выходом три(трет-бутокси)силанола [Docherty S.R., Estes D.P., Coperet С. Helv. Chim. Acta, 2018, 101 (3), e1700298].
В качестве окислителя используют кислород из баллона с объемным содержанием О2 85-95% или атмосферный воздух с объемным содержанием О2 20-23%. Использование атмосферного воздуха ожидаемо приводит к снижению выхода целевых продуктов, даже несмотря на проведение реакции в течение более длительного времени (примеры 3 и 13, 4 и 14, 36 и 38, 61 и 62).
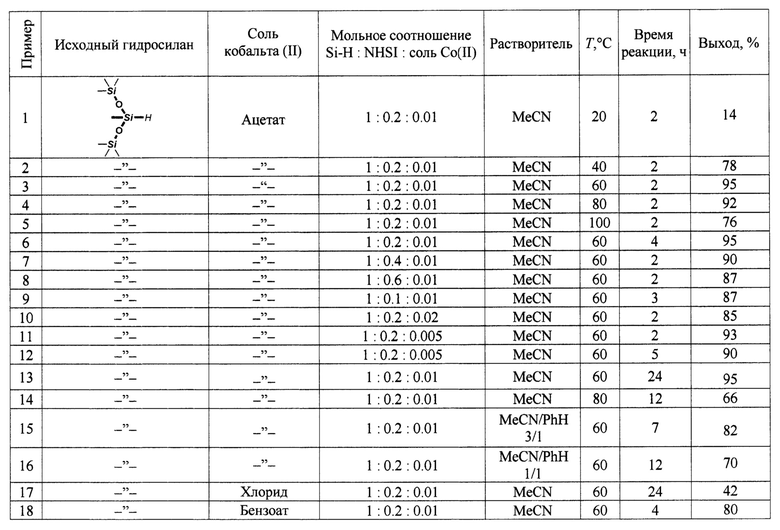
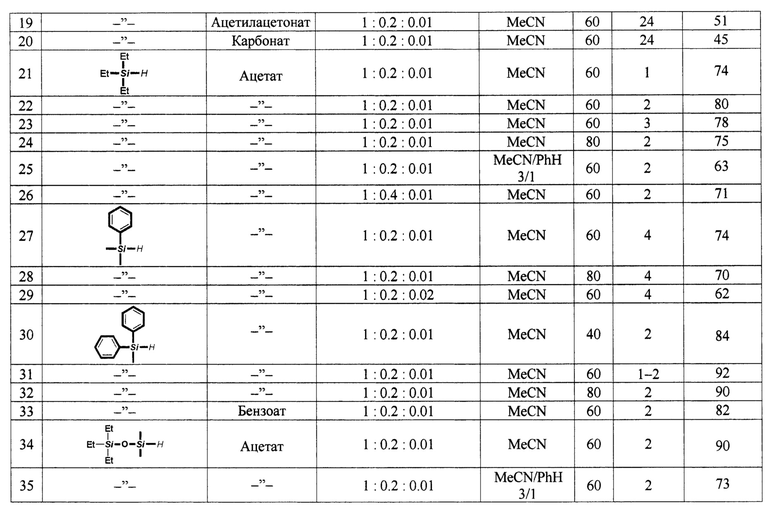
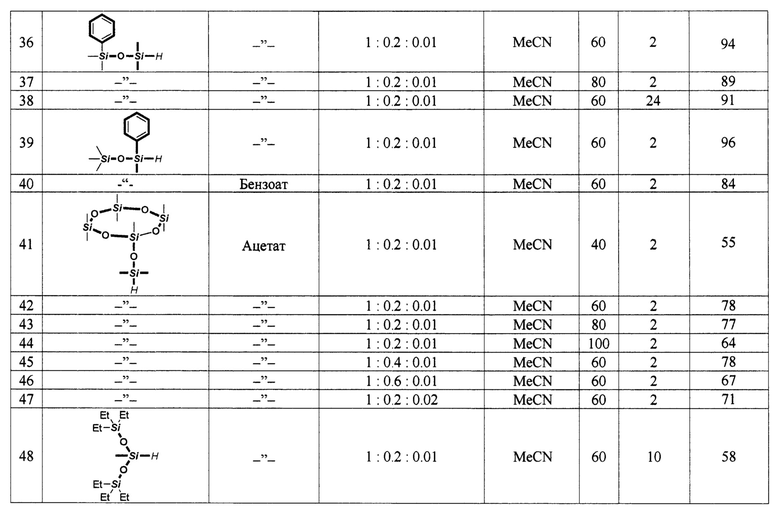
Мольное соотношение гидросилан : N-гидроксисукцинимид : соль кобальта (II) составляет 1:(0,1-0,6):(0,005-0,02), предпочтительно 1:0,2:0,01, что подтверждено многочисленными примерами (см. таблицу).
В качестве соли двухвалентного кобальта можно использовать ацетат, хлорид, бензоат, ацетилацетонат и карбонат, однако всегда использование ацетата Со (II) приводит к большим выходам целевых продуктов при меньшей продолжительности процесса окисления (примеры 3 и 17-20, 39 и 40).
Окисление осуществляют при температуре 40-80°С, предпочтительно при 60°С (примеры 2-4, 22 и 24, 27 и 28, 30-32, 36 и 37,42 и 43, 53 и 54, 57 и 58, 71 и 72). При температуре ниже 40°С выход целевого продукта снижается более чем на 60% (примеры 1 и 2), повышение температуры до 100°С приводит к снижению выхода на 13-16% (примеры 4 и 5,43 и 44).
Большинство исследованных моногидросиланов окисляется в силанолы с высокими выходами в течение 1-2 ч. Увеличение продолжительности реакции либо не сказывается на выходе (примеры 3, 6 и 13, 70 и 72), либо, в редких случаях (48 и 49, 64 и 65, 67 и 68), приводит к его повышению, либо, чаще всего, сопровождается его понижением (примеры 11 и 13, 36 и 38, 52 и 53, 56 и 57, 61 и 62), что, видимо, обусловлено конденсацией силанольных продуктов со временем.
В качестве апротонного органического растворителя используют ацетонитрил, бензол или их смеси. В рассмотренных в настоящем изобретении примерах с увеличением содержания бензола выход целевых продуктов снижается (сравни примеры 6 и 15, 16,22 и 25, 34 и 35).
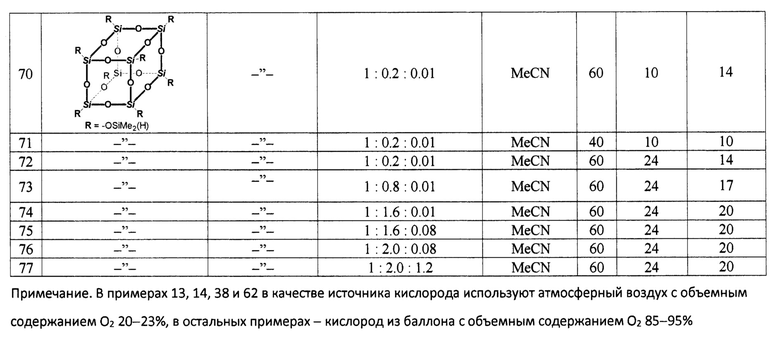
Дигидросиланы с атомами водорода при одном атоме кремния или полигидросиланы, содержащие несколько моногидросилильных фрагментов в молекуле, окисляются с трудом: выход целевых продуктов не превышает 20% (примеры 67-69, 70, 72-77).
Техническим результатом изобретения является способ получения силанолов окислением гидросиланов кислородом, обеспечивающий повышение выхода целевых продуктов и сокращение продолжительности реакции за счет использования новой доступной каталитической системы.
Все используемые гидросиланы, соли кобальта, N-гидроксисукцинимид и растворители являются коммерчески доступными реагентами и поставляются компаниями Acros Organics, Sigma Aldrich (Merk), ABCR Chemicals, TCI Chemicals. Источником кислорода чистоты 85-95% служит баллон со сжатым кислородом.
Изобретение иллюстрируется 77 примерами, результаты которых представлены в таблице.
Пример 1. Получение бис(триметилсилокси)метилсиланола
Смесь 40 г (180 ммоль) бис(триметилсилокси)метилсилана, 4,14 г (36 ммоль) N-гидроксисукцинимида, 0,45 г (1,8 ммоль) ацетата кобальта и 400 мл ацетонитрила продувают кислородом в течение 1-5 мин, после чего перемешивают при 60 С в течение 2 ч в атмосфере кислорода (1 атм) на магнитной мешалке. Растворитель отгоняют на роторном испарителе (200 мбар, 40 С), остаток взбалтывают в 150 мл гексана (продукт растворяется в гексане, компоненты каталитической системы - нет) и фильтруют через тонкий слой целита (Celite 545). Затем отгоняют гексан на роторном испарителе (300 мбар, 40°С) и получают 40,7 г (95%) бис(триметилсилокси)метилсиланола.
Строение продукта подтверждено с помощью комплекса физико-химических методов анализа, включая ЯМР- и ИК-спектроскопию, а также масс-спектрометрию.
Примеры 2-77, представленные в таблице, осуществляют по методике, аналогичной описанной в примере 1.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ СИЛАНОЛОВ ИЗ ГИДРОСИЛАНОВ | 2016 |
|
RU2633351C1 |
| Pt-СОДЕРЖАЩАЯ РЕГЕНЕРИРУЕМАЯ КАТАЛИТИЧЕСКАЯ СИСТЕМА И СПОСОБ ГИДРОСИЛИЛИРОВАНИЯ НЕПРЕДЕЛЬНЫХ СОЕДИНЕНИЙ С ЕЁ ИСПОЛЬЗОВАНИЕМ | 2023 |
|
RU2806031C1 |
| КАТАЛИТИЧЕСКАЯ СИСТЕМА И СПОСОБ ГИДРОСИЛИЛИРОВАНИЯ НЕПРЕДЕЛЬНЫХ СОЕДИНЕНИЙ С ЕЁ ИСПОЛЬЗОВАНИЕМ | 2024 |
|
RU2840134C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛОВЫХ ЭФИРОВ БЕНЗОЙНОЙ КИСЛОТЫ | 2011 |
|
RU2481324C2 |
| Катализатор и способ получения высших 2-кетонов С5-С10 | 2022 |
|
RU2790246C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-БЕНЗИЛИДЕНБЕНЗИЛАМИНА | 2012 |
|
RU2496770C2 |
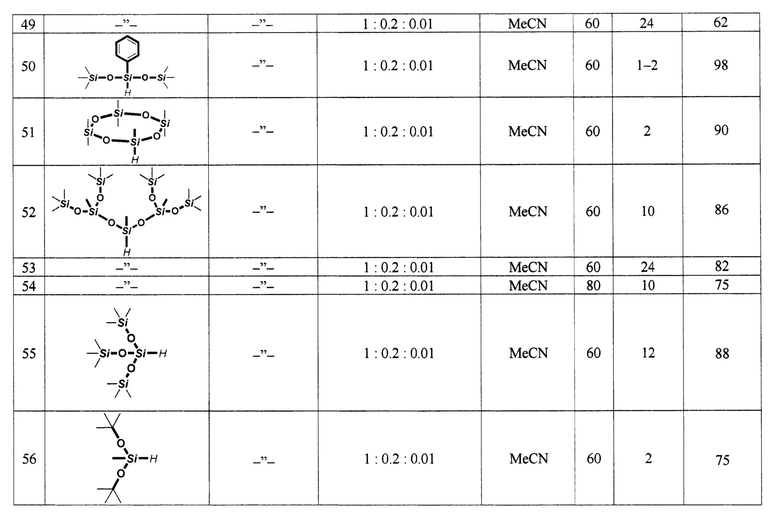
| СПОСОБ ПОЛУЧЕНИЯ МОНО- И ДИГИДРОКСИПОЛИФТОРБЕНЗОЛОВ | 2013 |
|
RU2536872C1 |
| Способ получения эфиров пиперидин-4,4-дикарбоновых кислот | 2021 |
|
RU2765464C1 |
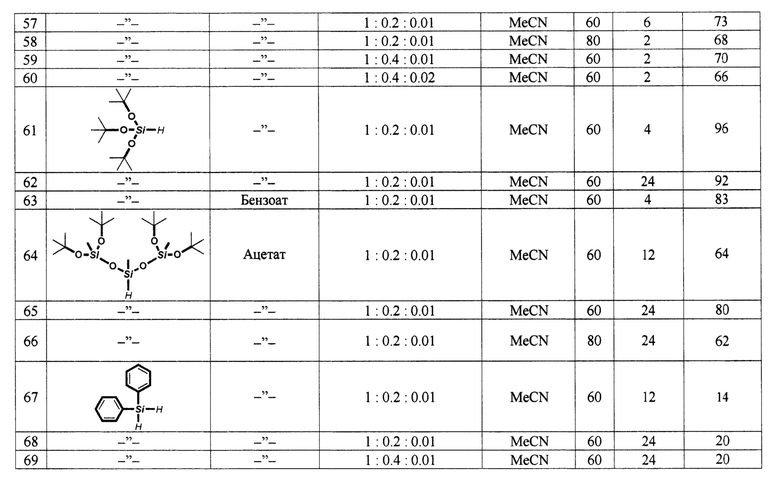
| СПОСОБ ПОЛУЧЕНИЯ ФЕНИЛЗАМЕЩЕННОГО ГЕТЕРОЦИКЛИЧЕСКОГО ПРОИЗВОДНОГО ПОСРЕДСТВОМ СОЧЕТАНИЯ С ИСПОЛЬЗОВАНИЕМ ПЕРЕХОДНОГО МЕТАЛЛА В КАЧЕСТВЕ КАТАЛИЗАТОРА | 2010 |
|
RU2510393C9 |
| СПОСОБ ПОЛУЧЕНИЯ БИЯДЕРНЫХ 3,4,5-ТРИАРИЛ-1,2-ДИФОСФАЦИКЛОПЕНТАДИЕНИДНЫХ КОМПЛЕКСОВ МАРГАНЦА | 2013 |
|
RU2515559C1 |
Изобретение относится к химии кремнийорганических соединений, конкретно к способу получения силанолов, силоксанолов и алкоксиланолов, которые являются востребованными кремнийорганическими соединениями. Предложен способ получения силанолов R1R2R3SiOH из гидросиланов R1R2R3SiH, где каждый из заместителей Rl, R2 и R3 независимо обозначает фенил, C1-С3-алкил, С1-С4-алкокси, силокси, включающий окисление гидросилана кислородом при атмосферном давлении в присутствии N-гидроксисукцинимида и соли кобальта (II) в ацетонитриле или его смеси с бензолом при 40-80°С. Мольное соотношение гидросилан: N-гидроксисукцинимид соль кобальта (II) предпочтительно составляет 1:0,2:0,01. В качестве соли кобальта (II) предпочтительно использовать ацетат. Технический результат - способ получения силанолов окислением гидросиланов кислородом, обеспечивающий повышение выхода целевых продуктов и сокращение продолжительности реакции за счет использования новой доступной каталитической системы. 4 з.п. ф-лы, 1 табл., 77 пр.
1. Способ получения силанолов R1R2R3SiOH из гидросиланов R1R2R3SiH, где каждый из заместителей R1, R2 и R3 независимо обозначает фенил, C1-С3-алкил, С1-С4-алкокси, силокси, включающий окисление гидросилана кислородом при атмосферном давлении в присутствии каталитических количеств N-гидроксисукцинимида и соли кобальта (II) при нагревании в апротонном органическом растворителе.
2. Способ по п. 1, в котором мольное соотношение гидросилан : N-гидроксисукцинимид : соль кобальта (II) составляет 1:(0,1-0,6):(0,005-0,02), предпочтительно 1:0,2:0,01.
3. Способ по п. 1 или 2, в котором в качестве соли кобальта (II) используют ацетат, хлорид, бензоат, ацетилацетонат, карбонат, предпочтительно ацетат.
4. Способ по любому из пп. 1-3, в котором в качестве апротонного органического растворителя используют ацетонитрил или его смеси с бензолом.
5. Способ по любому из пп. 1-4, в котором окисление проводят при температуре от 40 до 80°С, предпочтительно при 60°С.
| Arzumanyan, Ashot V., et al | |||
| "Aerobic Co or Cu/NHPI-catalyzed oxidation of hydride siloxanes: synthesis of siloxanols." Green Chemistry, 2018, vol.20, No.7, pp.1467-1471 | |||
| СПОСОБ ПОЛУЧЕНИЯ СИЛАНОЛОВ ИЗ ГИДРОСИЛАНОВ | 2016 |
|
RU2633351C1 |
| Jeon, Mina, Junghoon Han, and Jaiwook Park | |||
| "Catalytic synthesis of silanols from hydrosilanes and applications." ACS Catalysis, 2012, vol.2, | |||
Авторы
Даты
2023-01-31—Публикация
2022-08-04—Подача