Изобретение относится к области криобиологии, а именно к составам компонентов криопротекторов - веществ, защищающих живые объекты от повреждающего действия замораживания.
Одной из важнейших проблем, связанных с хранением и трансплантацией клеток и органов, является сохранение жизнеспособности биоматериала вне организма. Опыт по применению существующих в настоящее время криопротекторов для замораживания биоматериала показывает, что задача получения нетоксичного криопротектора остается нерешенной.
Основные повреждения клеток биоматериала происходят на этапах его консервации и расконсервации за счет обезвоживания, образования внеклеточных и внутриклеточных кристаллов льда и токсичности криопротекторов. Положение осложняется тем, что часто химические соединения, обладающие наиболее выраженными криопротекторными свойствами, одновременно проявляют значительную токсичность на клеточном и организменном уровнях. Итог отмывания размороженных клеток от криопротекторов, используемых в современной клинической практике, не удовлетворяет исследователей [Polge С., Smith A.U., Parkes A.S. // Nature, 1949, 164(10), 666; Rasmussen. D.H., Mackenzie A.P. // Nature, 1968, 220(12), 1315; Elliott G.D., Wang S., Fuller B.J. // Cryobiology, 2017, 76, 74-91].
В обзоре [Kostyaev A.A., Martusevich A.K., Andreev A.A. // Nauchnoe Obozrenie. Meditsinskie Nauki, 2016, 6, 54-74], посвященном токсичности криопротекторов, говорится о том, что к настоящему времени в качестве перспективных криопротекторов апробировано больше 120 веществ, принадлежащих к разным классам химических соединений. Однако ни одно соединение и ни один водный раствор какого-либо соединения не используется без добавок разного назначения, как правило, применяемых для уменьшения токсичности криопротектора и повышения его вязкости, способствующей переходу в стеклообразное состояние с минимально возможным эффектом кристаллизации.
На сегодняшний день на кривых нагревания всех известных классических криопротекторов наряду с эффектом стеклования всегда присутствует эффект кристаллизации и плавления в большей или меньшей степени. Это наглядно продемонстрировано в работе [Zinchenko A.V., Bobrova E.N. // Dopovidi Natsional'noi Akademii Nauk Ukraini, 2010, 12, 166- 170], посвященной исследованию фазовых переходов и стеклования в системах, содержащих плазму кордовой крови и водные растворы криопротекторов, широко используемых в криобиологии, таких как 1,2-пропандиол, глицерин и диметилсульфоксид, в температурном диапазоне от -196 до +10°С. Результаты этого исследования показали, что уменьшение интенсивности нежелательных эффектов (кристаллизации и плавления) в присутствии плазмы обусловлено наличием в системе биологических компонентов, существенно влияющих на состояние воды в растворе. Выводы этой работы свидетельствует о том, что совместное присутствие в системе криопротектора и биологического компонента (который сам обладает протекторными свойствами), не защищают от процесса кристаллизации, а только уменьшают величину его эффекта.
В качестве веществ, перспективных для использования в консервации биоматериала, рассматривают водно-солевые стеклообразующие системы с ионами металлов, жизненно важными для организма человека. В частности, в работе [Кириленко И.А. Винокуров Α.Α., Данилов В.П. и др.// Журн. неорган, химии, 2020, 65(7), 903-906] продемонстрирована возможность успешной подготовки спермы человека к гипотермическому способу хранения (+4°С) с использованием нетоксичного стеклообразующего водного раствора ацетатов магния, кальция и цинка. Раствор показал высокую протекторную эффективность в качестве благоприятной среды, замедляющей метаболизм для клеток спермы. В то же время, неизвестно, как такая многокомпонентная система проявит себя в условиях криозаморозки.
Критерием криопротекторной способности стеклообразующего вещества может служить стабильность стекла к кристаллизации [Кириленко И.А. Водно-электролитные стеклообразующие системы. М.: Красанд, 2016. 256 с.] - отсутствие процесса кристаллизации в ходе нагревания стекла от температур жидкого азота до комнатной температуры (на кривой нагревания стекла присутствует только эффект Tg).
Техническим результатом изобретения является разработка состава композиций нетоксичных стеклообразующих систем, обладающих стабильностью к кристаллизации.
Технический результат достигается тем, что предложен криопротектор биоматериала на основе стеклообразующего водного раствора ацетата магния, содержащий 40 масс. % Mg(CH3COO)2 и 60 масс. % Н2О.
Авторами настоящего изобретения впервые на основании экспериментальных исследований предложен состав водного раствора ацетата магния, отвечающий техническому результату изобретения. В связи с тем, что данное изобретение в своем роде является пионерским, оно не имеет близких аналогов.
Предлагаемый состав стабилен к кристаллизации в диапазоне температур от -140 до +40°С, при этом известно, что водные растворы ацетата магния нетоксичны и широко используются в фармакологии и медицине [Ranade V.V., Somberg J.C. // Am. J. Ther., 2001, 8(5), 345-357].
Изобретение проиллюстрировано следующей фигурой.
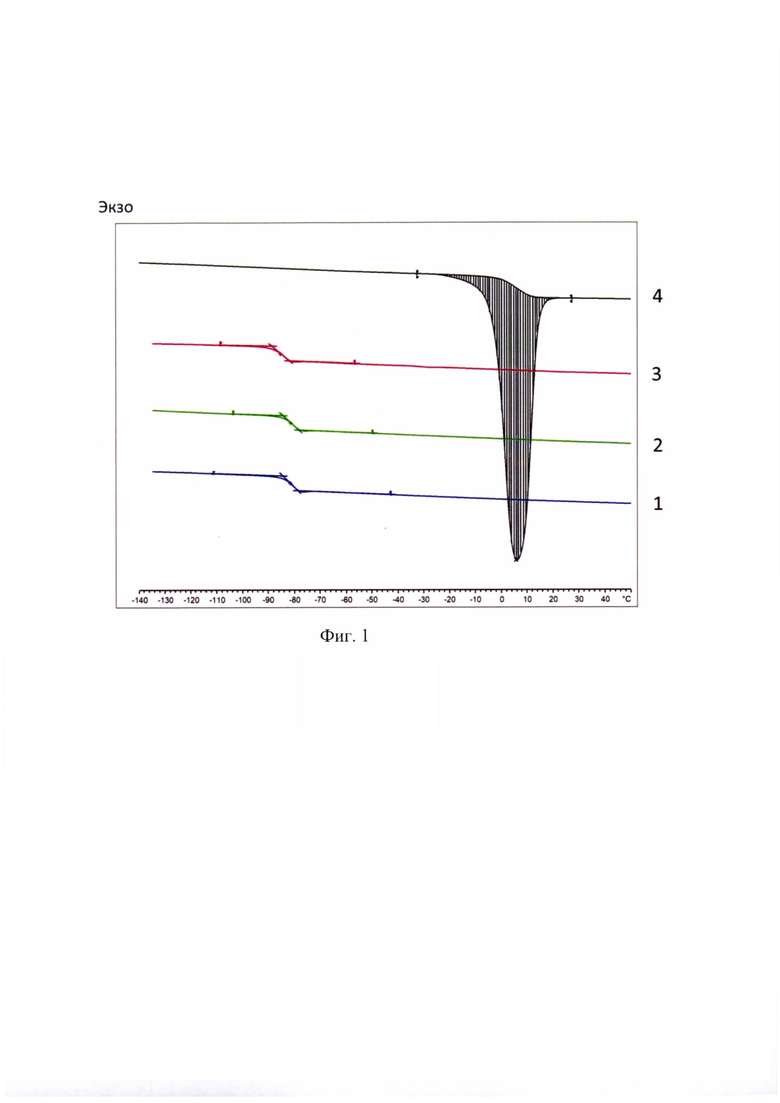
Фиг. 1. Термоаналитические кривые стеклообразующих составов (кривая 1 - состав по изобретению (40 масс. % Mg(CH3COO)2 и 60 масс. % H2O, Tg=-84.75°С), кривая 2 - состав по изобретению в смеси с белком куриного яйца (10 масс. %, Tg=-84.58°С), кривая 3 - состав по изобретению в смеси с белком куриного яйца (30 масс. %, Tg=-88.70°С), и термограмма плавления белка (кривая 4) с большим эндоэффектом плавления Тпл=-3.67°С.
Ниже приведены примеры иллюстрирующие, но не ограничивающие предложенное изобретение.
Пример 1. Получение стеклообразующего водного раствора ацетата магния.
Использовали соль состава Mg(CH3COO)2⋅4H2O марки «ч.д.а». Готовили водный раствор ацетата магния с концентрацией 30 масс. % и проводили его испарение до требуемого состава в открытом контейнере (с контролем массы) при температуре 60°С в течение 30 минут.Полученный раствор переносили в прозрачную стеклянную ампулу и затем замораживали в жидком азоте. Наблюдение за изменением прозрачности образца (отсутствие прозрачности - эффект кристаллизации) в ходе естественного нагревания от температур жидкого азота до комнатной температуры проводили визуально по методике [Angell С.А., Sare E.J. // J. Chem. Phys., 1970, 52(3), 1058] и с помощью дифференциальной сканирующей калориметрии (ДСК).
Пример 2. Проверка криопротекторной способности предлагаемого состава стеклообразующего водного раствора ацетата магния.
В качестве модельного биоматериала использовали белок свежего диетического куриного яйца. В белке куриного яйца содержатся практически все незаменимые аминокислоты. Такой белок представляет собой бесцветное желеобразное вещество, которое хорошо растворяется в воде [Abeyrathne H.Y., Lee D.U. // Poultry Science, 2013, 92, 3292-3299] При охлаждении в жидком азоте белок куриного яйца кристаллизуется с образованием белой массы, а при возвращении к комнатной температуре снова становился прозрачным.
При смешивании белка куриного яйца со стеклообразующим водным раствором ацетата магния состава 40 масс. % Mg(CH3COO)2 и 60 масс. % H2O образовывалась прозрачная слегка опалесцирующая заметно вязкая жидкость. При охлаждении в жидком азоте эта жидкость застывала в прозрачное стекло. При естественном нагревании от температуры жидкого азота до комнатной происходил постепенный переход от твердого состояния (стекло) к жидкому (изначальному) без кристаллизации. Так происходило и при 10, и при 30 процентном содержании белка. На кривых нагревания предлагаемого состава и составов с белком куриного яйца присутствует только эффект Tg (Фиг. 1).
Для чистого белка куриного яйца, который при охлаждении в жидком азоте кристаллизуется (внешне твердое вещество белого цвета) на кривой нагревания присутствует эффект плавления кристаллического белка (Фиг. 1). Таким образом, белок куриного яйца, который по своей природе при температуре жидкого азота кристаллизуется, при взаимодействии с предлагаемым составом теряет свою индивидуальность и находится под защитой криопротектора стабильного кристаллизации.
Следует отметить и такой важный фактор, который учитывается при криоконсервации биоматериалов, как скорость охлаждения и отогревания, влияющий на качество процесса [Mazur Р. // Science, 1970, 168(3934), 939-949]. Для стеклообразующих водно-солевых растворов, в т.ч. ацетата магния, такой проблемы не существует - скорость охлаждения и нагревания зависит только от массы раствора и при массе от 2-3 г составляет 7-10 град/сек. Это является еще одним преимуществом предлагаемого криопротектора на основе стеклообразующего водного раствора ацетата магния.
Таким образом, приведенные данные убедительно свидетельствуют о том, что предлагаемый стеклообразующий водно-солевой раствор состава 40 масс. % Mg(CH3COO)2 - 60 масс. % H2O обладает всеми необходимыми для криопротектора свойствами - стабильностью к кристаллизации, отсутствием токсичности и независимостью качества процесса консервации и расконсервации от скорости охлаждения и отогревания, соответственно.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ криоконсервации эмбрионов кур | 1985 |
|
SU1343357A1 |
| Способ получения мультипотентных стромальных клеток из криозамороженных тканей фетоплацентарного комплекса | 2015 |
|
RU2610132C1 |
| СПОСОБ ДЛИТЕЛЬНОГО ХРАНЕНИЯ ЕСТЕСТВЕННЫХ СИМБИОТИЧЕСКИХ АССОЦИАЦИЙ МИКРООРГАНИЗМОВ ЧЕЛОВЕКА И ЖИВОТНЫХ. | 1998 |
|
RU2123044C1 |
| СПОСОБ КРИОКОНСЕРВАЦИИ СПЕРМЫ ЧЕЛОВЕКА | 2003 |
|
RU2257710C2 |
| СПОСОБ ПОДБОРА КРИОПРОТЕКТОРОВ ДЛЯ КРИОКОНСЕРВАЦИИ БИОЛОГИЧЕСКИХ ОБРАЗЦОВ (ВАРИАНТЫ) | 2002 |
|
RU2236466C2 |
| Криопротектор для цельной крови при низкотемпературной заморозке | 2024 |
|
RU2837538C1 |
| Средство защиты кожи от холодового повреждения | 2018 |
|
RU2678188C1 |
| СИНТЕТИЧЕСКАЯ СРЕДА ДЛЯ РАЗБАВЛЕНИЯ И ЗАМОРАЖИВАНИЯ СПЕРМЫ БАРАНОВ | 2000 |
|
RU2198622C2 |
| СПОСОБ КРИОСОХРАНЕНИЯ МОРСКИХ МИКРОВОДОРОСЛЕЙ | 2012 |
|
RU2496318C1 |
| КОМБИНИРОВАННЫЙ КРИОПРОТЕКТОР "ДИМЕТИЛСУЛЬФОКСИД/РЕОПОЛИГЛЮКИН" ДЛЯ КРИОКОНСЕРВАЦИИ СТВОЛОВЫХ КЛЕТОК И СПОСОБ ИХ КРИОКОНСЕРВАЦИИ ДЛЯ КЛИНИЧЕСКОГО ПРИМЕНЕНИЯ | 2014 |
|
RU2563117C1 |
Изобретение относится к области криобиологии, а именно к составам криопротекторов. Предложен криопротектор биоматериала на основе стеклообразующего водного раствора ацетата магния, содержащий 40 масс. % Mg(CH3COO)2 и 60 масс. % H2O. Предлагаемый криопротектор биоматериала является нетоксичным, обладает стабильностью к кристаллизации. 1 ил., 2 пр.
Криопротектор биоматериала на основе стеклообразующего водного раствора ацетата магния, содержащий 40 масс. % Mg(CH3COO)2 и 60 масс. % H2O.
| СРЕДА ДЛЯ ХРАНЕНИЯ КЛЕТОК | 2006 |
|
RU2396748C2 |
| WO 2018065491 A1, 12.04.2018 | |||
| АНДРЕЕВ В.И | |||
| "Разработка и совершенствование способа криоконсервации спермы водоплавающих птиц", автореферат диссертации по биологии, Харьков, 1983 г., DOI: https://earthpapers.net/razrabotka-i-sovershenstvovanie-sposoba-kriokonservatsii-spermy-vodoplavayuschih-ptits. | |||
Авторы
Даты
2023-02-28—Публикация
2022-08-03—Подача