Изобретение относится к области медицины, в частности, к иммунологии и инфектологии и может использоваться для прогнозирования тяжелого течения геморрагической лихорадки с почечным синдромом в ранние периоды заболевания.
Геморрагическая лихорадка с почечным синдромом (ГЛПС) - острое вирусное природно-очаговое заболевание, характеризующееся системным поражением мелких сосудов, геморрагическим диатезом, гемодинамическими расстройствами и своеобразным поражением почек по типу острого интерстициального нефрита с развитием острой почечной недостаточности [1, 2].
ГЛПС распространена по всему миру и относится к группе инфекционных заболеваний с наивысшим приоритетом для эпиднадзора и эпидемиологических исследований [3]. В Российской Федерации ГЛПС по уровню заболеваемости занимает первое место среди природно-очаговых болезней [4], при этом природные очаги на территории России характеризуются высокой эпидемической активностью и являются одними из самых напряженных в мире [5].
Возбудителями ГЛПС являются хантавирусы, относящиеся к категории одноцепочечных РНК-содержащих вирусов и принадлежащие к отряду Bunyavirales [6]. На территории России встречается ГЛПС, этиологически связанная с 6 типами хантавирусов: Puumala, Hantaan, Seоul, Amur, Dobrava, Sochi [1, 7]. На территории Среднего Поволжья, где проводилось данное исследование, встречается только тип Puumala [8], а основным природным резервуаром является европейская рыжая полевка [9]. В последние годы описано несколько новых видов хозяев-резервуаров, несущих хантавирусы, кроме того, участились сообщения о случаях с тяжелым или атипичным клиническим течением [3].
Особенности тропизма хантавирусов к клеткам человека определяет их проникновение, в первую очередь, в клетки эндотелия системы кровотока и моноцитов/макрофагов [10], в связи с чем можно предполагать, что именно эти клеточные мишени определяют распространение возбудителя геморрагической лихорадки с почечным синдромом по организму без необходимости миграции в барьерные ткани, а также его способность оказывать воздействие на иммунные процессы. В результате при ГЛПС развивается системное воспаление, сопровождающееся "цитокиновым штормом" и другими иммунными нарушениями [11], что определяет летальность при данном инфекционном заболевании, колеблющуюся от 1% до 40% [1, 12].
Поражение вирусом эндотелия сосудов усугубляется присоединением уже в начале болезни нарушений со стороны системы гемостаза и приводит к развитию диссеминированного внутрисосудистого свертывания крови (ДВС-синдрома) [13]. При этом для тяжелого течения заболевания характерна выраженная тромбоцитопения [14]. Немалое значение в развитии тяжелого течения ГЛПС придается поражению почек, которое проявляется острой почечной недостаточностью и сопровождается олигоурией вплоть до полной анурии, протеинурии, креатининемии [14]. Так, анализ результатов биопсии почек больных при данном заболевании показал, что у таких пациентов в значительной степени страдает тубуло-интерстициальная ткань [15] в связи нарушением под влиянием вирусного возбудителя экспрессии белка ZO-1, определяющего плотные межклеточные контакты, максимальную приближенность клеток почечных клубочков друг к другу и их "сшивание" между собой. Падение экспрессии этого белка приводит к значительным нарушениям структуры и функции почечных тканей [16].
Все эти патогенетические особенности вызывают особый интерес исследователей с точки зрения попыток прогнозировать тяжелое течение заболевания в процессе его ранней диагностики [13, 17], что очень важно для предотвращения в дальнейшем тяжелых осложнений и летальных исходов [18, 19]. Указанная проблема приобретает особое значение и в связи с тем, что, по оценке современных исследователей, эффективной специфической терапии ГЛПС пока не существует, а состояние вакцинопрофилактики оставляет желать лучшего [19, 20].
В настоящее время показано, что тяжесть заболевания может быть связана с уровнями различных биомаркеров, которые могут служить прогностическими показателями. Было обнаружено, что биологические маркеры, такие как интерлейкин-6, пентраксин-3, идоламин-2,3-диоксигеназа, растворимый рецептор активатора плазминогена урокиназного типа и GATA-3, коррелируют с тяжестью течения ГЛПС [21, 22, 23]. С-реактивный белок и прокальцитонин используются, в частности, для различения бактериальных и вирусных инфекций и обычно обнаруживаются в высоких уровнях у пациентов с системными бактериальными инфекциями, но имеют также прогностическое значение и у пациентов с ГЛПС [24, 25]. Параллельно в острой фазе ГЛПС у пациентов обнаруживаются типовые лабораторные сдвиги, такие как анемия, лейкоцитоз, тромбоцитопения, протеинурия, гематурия, повышение активности печеночных ферментов и креатинина в сыворотке крови [26]. Высокий уровень лейкоцитов в сыворотке крови, азота мочевины крови (АМК), креатининфосфокиназы (КФК), С-реактивного белка (СРБ), протромбинового времени (ПВ), активированного частичного тромбопластинового времени (аЧТВ), D-димера и МНО (Международное нормализованное отношение) являются прогностическими факторами, повышающими риск смертности при ГЛПС [27]. Глюкозурия встречается относительно редко, но при ее наличии можно предсказать более тяжелое течение заболевания у пациентов с острой Puumala-инфекцией [28].
Еще одним неспецифическим маркером, связанным с прогнозом геморрагических лихорадок, в том числе ГЛПС, является High Mobility Group Box 1 (HMGB1) [26]. HMGB1 представляет собой негистоновый нуклеосомный белок, который связывает и изгибает ДНК. Он действует как фактор ядерного ремоделирования [29, 30]. Высокие уровни HMGB1 при вирусных инфекциях коррелировали с повышенной проницаемостью сосудов, интенсивностью симптомов и частотой вторичной инфекции [31, 32].
При описании иммунологических признаков тяжелого течения ГЛПС обращается внимание на низкий уровень ТФР-β в сыворотке крови на ранней стадии хантавирусной инфекции [33], что косвенно свидетельствует о снижении секреторной функции регуляторных Т-клеток, хотя вопрос об их как протективной роли, так и нежелательных проявлений функции при тяжелом течении ГЛПС еще не решен [34, 35]. Описана также генетически детерминированная низкая продукция ФНО-альфа, которая была связана с некоторыми параметрами, свидетельствующими о более тяжелом клиническом течении хантавирусной инфекции Puumala у людей, возможно, за счет нарушения активации ФНО-альфа-зависимых противовирусных механизмов, что, в свою очередь, способно привести к снижению элиминация хантавируса [36].
При идентификации биологических маркеров тяжелого течения ГЛПС определенный интерес представляют специфические иммунные механизмы, вызывающие тромбоцитопению. Недавно было показано, что специфичный для остановки клеточной пролиферации белок 6 (Gas6) и рецепторы ТАМ (Tyro3, Axl и Mer) играют важную роль в иммунной регуляции, а высокие уровни Gas6 в плазме могут предсказывать тяжесть заболевания [37]. К иммунным биомаркерам относится и CD163 как рецептор поглотителя гемоглобина для гаптоглобин-гемоглобиновых комплексов, который экспрессируется моноцитами/макрофагами и часто выделяется в виде растворимого CD163 в ответ на воспалительные стимулы. Сообщается, что этот рецептор-мусорщик ослабляет воспалительную реакцию, а высокие уровни растворимого CD163 в плазме, которые, как считается, отражают общий уровень экспрессии CD163 и могут служить предикторами тяжести заболевания [38]. В то же время необходимо подчеркнуть, что эффективность указанных маркеров установлена при ГЛПС, вызванной вирусом Hantaan.
В отечественной патентной базе содержится изобретение, рекомендующее в острую стадию болезни одновременное проведение транскраниальной допплерографии и ультразвукового дуплексного сканирования с регистрацией кровотоков в бассейнах средней мозговой артерии и почечной артерии и последующим расчетом церебрально-ренального показателя. При значении этого показателя больше 0,9 прогнозируют возможность развития сосудистой патологии мозга в реконвалесцентном периоде, а при значении меньше 0,9 данная патология не развивается [39].
Запатентован способ, включающий определение уровня простагландина Е2 в плазме крови больного геморрагической лихорадкой с почечным синдромом. Его снижение до 18,19 - 26,18 пг/мл оценивают как тяжелую степень течения, снижение уровня до 29,84 - 57,25 пг/мл - как среднетяжелую, а снижение уровня до 100,0 - 113,0 пг/мл - как легкую степень тяжести течения заболевания [40].
Для оценки тяжести течения ГЛПС проводят определение уровня конечных стабильных метаболитов оксида азота (NOx) в цельной крови. При его значении от 39,6 до 86,0 мкмоль/л регистрируют среднетяжелую форму ГЛПС, при значении NOx от 86,7 до 141,5 мкмоль/л - тяжелую форму заболевания, а от 88,2 до 128,6 мкмоль/л на фоне выраженной клинической картины - как осложненное течение заболевания [41].
Сущность еще одного изобретения заключается в том, что исследуют кровь больного тяжелой формой ГЛПС в олигоурическом периоде, определяют липидный индекс в нейтрофильных лейкоцитах и при показателе 237±2,01 в указанном периоде прогнозируют летальный исход, а показатель выше 310±1,53 предполагает выздоровление [42].
Для прогноза риска развития тяжелой формы ГЛПС из лимфоцитов периферической венозной крови выделяют ДНК, проводят ПЦР анализ полиморфных локусов CYP1A1 и GSTP1. При обнаружении гетерозиготного генотипа AG гена GSTP1 или комбинации генотипов 1A2C/AG генов CYP1A1 и GSTP1 прогнозируют высокий риск развития тяжелой формы ГЛПС [43].
Существует также способ оценки тяжести течения ГЛПС, включающий определение маркера дисфункции эндотелия сосудов в крови, где в плазме крови в качестве маркера дисфункции эндотелия сосудов определяют концентрацию антигена ингибитора активаторов плазминогена 1 типа (ИАП-1) в лихорадочный период болезни. Значение концентрации антигена ИАП-1 от 341,2 до 570,0 нг/мл оценивают как показатель среднетяжелой формы заболевания, от 240,4 до 320,1 нг/мл - тяжелой формы заболевания без осложнений, от 138,3 до 75,5 нг/мл - как предиктор тяжелой формы заболевания с осложненным течением [44].
Предложена оценка тяжести геморрагической лихорадки с почечным синдромом по содержанию циркулирующих иммунных комплексов (ЦИК) в крови. Среднетяжелая форма геморрагической лихорадки с почечным синдромом определяется повышением уровня ЦИК до 6,4-10,0×104/л. Признаком тяжелой формы заболевания без осложнений служит повышение уровня ЦИК до 10,7-14,6×104/л. Тяжелая форма геморрагической лихорадки с почечным синдромом и осложнениями связана с повышением уровня ЦИК до 14,9-21,0×104/л на фоне выраженной клинической картины [45].
Прототипом данного изобретения может служить способ прогнозирования тяжести геморрагической лихорадки с почечным синдромом путем проведения общего и биохимического исследования крови с определением гематокрита, относительного содержания сегментоядерных и палочкоядерных лейкоцитов и моноцитов, концентрации креатинина и С-реактивного белка. Вычисляют значения дискриминантных функций классификации степеней тяжести ГЛПС по формулам:
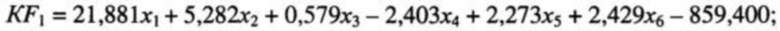
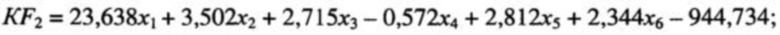
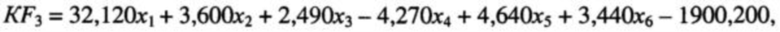
где KF1 - значение функции классификации легкой формы ГЛПС; KF2 - значение функции классификации среднетяжелой формы ГЛПС; KF3 - значение функции классификации тяжелой формы ГЛПС; x1 - гематокрит, %; х2 - относительное содержание сегментоядерных лейкоцитов, %; х3 - относительное содержание палочкоядерных лейкоцитов, %; x4 - относительное содержание моноцитов, %; x5 - концентрация креатинина, мкмоль/л; x6 - концентрация C-реактивного белка, мг/л.
Общность прототипа с заявляемым изобретением заключается в оценке тяжести течения ГЛПС на основе не единичных параметров, а с точки зрения интегрального подхода с учетом целой совокупности лабораторных данных, обработанных методом статистического анализа. В то же время особенностью заявляемого изобретения является ориентация не только на общепринятые лабораторные показатели, но и учет иммунной реакции на патологический процесс, а также иной способ статистической обработки полученных данных.
Целью настоящего изобретения служила разработка способа раннего прогнозирования риска развития тяжелого течения геморрагической лихорадки с почечным синдромом на основе широкого спектра лабораторных данных, включая иммунологические показатели.
Для получения технического результата были проведены сравнительные исследования крови 65 больных ГЛПС, проходивших стационарное лечение в клинике инфекционных болезней ФГБОУ ВО СамГМУ Минздрава России, среди которых у 53 человек (81,5%) заболевание, начиная с олигоурического периода, приобретало среднетяжелое течение, а у 12 человек (18,5%) - тяжелое. Всем проводилось определение величин рутинных лабораторных показателей (клинический и биохимический анализ крови и мочи), осуществлялось фенотипирование лимфоцитов крови путем оригинального подбора моноклональных антител для использования метода проточной цитофлуориметрии на приборе BD FACSCanto II (Becton Dickinson, США) после автоматизированной пробоподготовки цельной крови с помощью станции автоматической пробоподготовки BD FACS Sample Prep Assistant II (Becton Dickinson, США), а также устанавливался цитокиновый профиль плазмы крови методом иммуноферментного анализа с использованием микропланшетного ридера «Dynex MRX II» (Dynex technologies, USA) в соответствии с инструкциями по применению приборов, реактивов и моноклональных антител. Лабораторные исследования выполнялись в лихорадочный период ГЛПС (первый-пятый дни болезни), то есть до появления патогномоничных симптомов заболевания. Результаты анализировались путем статистического сравнения данных больных, у которых впоследствии заболевание принимало либо среднетяжелый, либо тяжелый характер. Статистическая обработка данных проводилась на основе пакета статистических программ SPSS, версия 21.
Результаты определения и статистического анализа полученных данных с учетом тяжести течения ГЛПС в лихорадочный период заболевания представлены в таблице 1 и на рисунке 1, при этом на рисунке показаны проценты отклонения показателей при тяжелом течении ГЛПС от показателей при среднетяжелом течении. В результате анализа были отобраны показатели, показывающие достоверность различий между группами с разной перспективой развития тяжелого течения. К их числу принадлежат:
- % моноцитов среди лейкоцитов крови;
- активность аланинаминотрансферазы (АЛТ) в крови;
- активность аспартатаминотрансферазы (АСТ) в крови;
- уровень мочевины крови;
- уровень креатинина крови;
- содержание белка в моче;
- количество лейкоцитов в моче;
- количество выщелоченных эритроцитов в моче;
- относительное число Т-хелперов (CD3+CD4+) в крови;
- относительное и абсолютное число цитотоксических Т-лимфоцитов (CD3+CD8+) в крови;
- относительное и абсолютное число цитотоксических Т-лимфоцитов, экспрессирующих активирующие NKG2D рецепторы (CD3+CD8+CD314+) в крови;
- относительное и абсолютное число регуляторных Т-клеток, экспрессирующих молекулы CD8 (СD3+CD8+FoxP3+), в крови;
- уровень ИЛ-6 в крови;
- уровень ИЛ-1β в крови.
Все эти 17 показателей были использованы в качестве независимых переменных для проведения регрессионного анализа, в ходе которого зависимой переменной выступала тяжесть заболевания, а принципом отбора показателей – их исследование в лихорадочный период ГЛПС. В результате было получено уравнение линейной регрессии следующего вида:
ПКТТ ГЛПС = 2,015 + 0,072 * [АЛТ] + 0,516 * [мочевина] + 0,364 * [СD3+CD8+CD314+] - 0,381 * [CD3+CD8+FoxP3+],
где ПКТТ ГЛПС - прогностический критерий тяжелого течения геморрагической лихорадки с почечным синдромом, * - знак умножения, АЛТ - активность аланинаминотрансферазы в крови в ЕД/л, мочевина - уровень мочевины в крови в ммоль/л, СD3+CD8+CD314+ – процент СD3+CD8+CD314+ Т-клеток среди лимфоцитов крови, CD3+CD8+FoxP3+ – процент CD3+CD8+FoxP3+ клеток среди лимфоцитов крови.
Как следует из полученной формулы, из 17 использованных параметров статистической программой было отобрано только 4 показателя, которые и вошли в состав уравнения регрессии для расчета прогностического критерия тяжести течения ГЛПС (ПКТТ). Подставляя в уравнение числовые значения каждого показателя у конкретного больного в лихорадочный период заболевания (первые 3-5 суток от начала появления симптомов), получается числовое значение ПКТТ для данного больного.
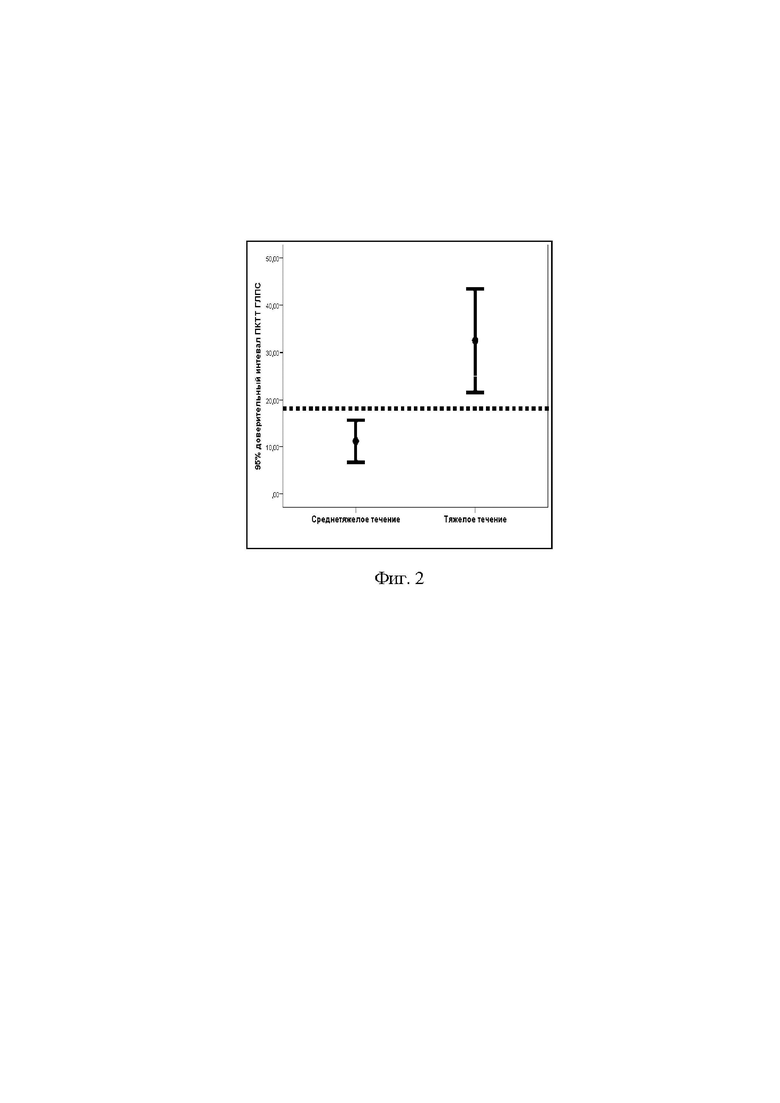
Чтобы определить критериальные значения ПКТТ ГЛПС, при которых тяжелое течение заболевания становится наиболее вероятным, проводилось сравнение 95%-ных доверительных интервалов этого коэффициента при среднетяжелом и тяжелом течении. Прогностическая значимость такого сравнения устанавливалась путем построения ROC-кривой, отражающей соотношение чувствительности и специфичности теста в форме линейной регрессии. Количественным выражением прогностической значимости в этих случаях служит площадь под ROC-кривой (AUC). При значениях AUC ≤ 0,5 тест как прогностически значимый не рассматривается, при значениях AUC 0,6-0,7 прогностическую значимость принято считать умеренной, при величинах 0,71-0,8 - тест высоко значим, а выше 0,8 - его значимость очень высокая при максимальных значениях AUC = 1,0 [46, 47]. 95%-ные доверительные интервалы критерия ПКТТ ГЛПС при среднетяжелом и тяжелом течении заболевания с обозначением прогностического критерия и ROC-кривая прогностической значимости теста представлены на рисунке 2.
Как следует из графика разграничительная величина для 95% доверительных интервалов ПКТТ у больных со среднетяжелым и тяжелым течением геморрагической лихорадки с почечным синдромом составляет 19.
Иными словами, при ПКТТ ГЛПС выше/равно 19 у больного можно констатировать риск тяжелого течения заболевания. Прогностическая значимость ПКТТ ГЛПС очень велика, поскольку при построении ROC-кривой AUC составляет 1,0, то есть соответствует максимальному значению площади под ROC-кривой.
Способ иллюстрируется следующими рисунками:
Фиг. 1. Проценты отклонения лабораторных показателей при тяжелом течении ГЛПС от показателей при среднетяжелом течении в лихорадочный период заболевания.
Фиг. 2. 95% доверительные интервалы прогностического критерия тяжелого течения геморрагической лихорадки с почечным синдромом (ПКТТ ГЛПС) в лихорадочный период при среднетяжелом и тяжелом течении.
Фиг. 3. ROC-кривая прогностического значения ПКТТ ГЛПС для определения риска тяжелого течения ГЛПС в лихорадочный период.
Таблица 1 содержит результаты определения и статистического анализа лабораторных данных в лихорадочный период ГЛПС в соответствии с развитием впоследствии среднетяжелого или тяжелого течения заболевания.
Предлагаемый способ иллюстрируется следующими примерами.
Пример 1. Больной А., 60 лет, поступил в клинику инфекционных болезней на 4-й день заболевания с диагнозом «Геморрагическая лихорадка с почечным синдромом». Проживает в частном доме и не отрицает возможность контакта с биологическими выделениями мышей.
При поступлении предъявлял жалобы на общую слабость, головную боль, тошноту, сухость во рту, боль в пояснице, снижение количества мочи. При поступлении отмечена гиперемия лица, инъекция сосудов склер, положительный симптом Пастернацкого.
При исследовании мочи было отмечено падение суточного диуреза до 250 мл при удельном весе 1002, наличии белка до 5,0 г/л, выщелоченных эритроцитов до 10 в поле зрения; лейкоциты по Нечипоренко 8750×106/л, эритроциты по Нечипоренко 1250×106/л.
Клинический анализ крови: эритроциты 5,36×1012/л; гемоглобин 156 г/л; тромбоциты 67,0×103/л; лейкоциты 7,4×109/л; нейтрофильные гранулоциты 69%; лимфоциты 24,4%; моноциты 6,6%; СОЭ 15 мм/ч.
Биохимический анализ крови: мочевина 19,7 ммоль/л; креатинин 402 ммоль/л; общий белок 61,1 г/л; альбумин 36,7 г/л; общий билирубин 9,8 ммоль/л; холестерин 3,2 ммоль/л; аланинаминотрансфераза 25 ЕД/л; аспартатаминотрансфераза 28,8 ЕД/л; щелочная фосфатаза 46,7 ЕД/л; креатининфосфокиназа 66,6 ЕД/л; глюкоза 7,7 г/л; С-реактивный белок 89,2 мг/л; натрий 141,7 ммоль/л; калий 4,7 ммоль/л; хлориды 100,9 ммоль/л.
Реакция непрямой иммунофлуоресценции (РНИФ) с парными сыворотками: 1:256 и 1:1024 (нарастание титра в 4 раза).
Фенотипирование лимфоцитов крови: CD19+ 9% и 0,1×109/л; СD3+ 82% и 1,4×109/л; CD3+CD4+ 37,7% и 0,64×109/л; CD3+CD8+ 45,2% и 0,77×109/л; CD3+CD8+CD314+ 35,8% и 0,59×109/л; СD3+CD4+FoxP3+ 8,8% и 0,9×109/л; СD3+CD8+FoxP3+ 10,8% и 0,15×109/л; СD16+CD56+ 17,1% и 0,17×109/л; CD16+CD56+CD314+ 11,8% и 0,12×109/л.
Цитокиновый профиль плазмы крови: ИЛ-1β 3,3 пг/мл; ИЛ-4 1,6 пг/мл; ИЛ-6 24,5 пг/мл; ИЛ-10 182,7 пг/мл; ИЛ-12 149 пг/мл; ФНОα 3,8 пг/мл; ФНОβ 452,2 пг/мл; ИФНγ 834,6 пг/мл.
По совокупности клинико-лабораторных данных у больного А. в лихорадочный период заболевания была диагностирована ГЛПС средней тяжести. Однако, определение прогностического критерия тяжелого течения (ПКТТ ГЛПС) показало, что его величина составляла 22,9 (>19), что свидетельствовало о риске развития тяжелого течения ГЛПС.
Дальнейшее наблюдение больного А. показало, что в олигоурический период заболевания у него развилась тяжелая острая почечная недостаточность, сопровождавшаяся выраженной азотемией (мочевина 42,6 ммоль/л, креатинин 898,4 ммоль/л), что было расценено как показание к применению гемодиализа, то есть прогноз тяжелого течения заболевания в данном случае подтвердился. После одного сеанса гемодиализа состояние больного улучшилось и на 31-й день от начала заболевания пациент был выписан на амбулаторное лечение в удовлетворительном состоянии.
Пример 2. Больной Д., 39 лет, поступил в клинику инфекционных болезней на 3-й день заболевания с диагнозом «Геморрагическая лихорадка с почечным синдромом». Сбор эпидемического анамнеза показал, что больной часто выезжает в сельскую местность на рыбалку, что создает условия для возможного контакта с грызунами.
Жалобы на головную боль, нарушения зрения, сухость во рту, тошноту, однократную рвоту, боль в пояснице. Объективное исследование выявило гиперемию и отечность лица, инъекцию сосудов склер, жесткость дыхания, слабоположительный симптом Пастернацкого.
При клиническом анализе мочи в момент поступления в стационар установлено снижение суточного диуреза до 300 мл, удельный вес составлял 1002, белок 1,5 г/л, свежие и выщелоченные эритроциты до 25 в поле зрения.
Клинический анализ крови: эритроциты 5,46×1012/л; гемоглобин 208 г/л; тромбоциты 33,0×103/л; лейкоциты 7,3×109/л; нейтрофильные гранулоциты 81,8%; лимфоциты 14,8%; моноциты 3,4%; СОЭ 21 мм/ч.
Биохимический анализ крови: мочевина 16,7 ммоль/л; креатинин 172,2 ммоль/л; общий белок 66,3 г/л; альбумин 36,5 г/л; общий билирубин 7,3 ммоль/л; холестерин 3,8 ммоль/л; аланинаминотрансфераза 29 ЕД/л; аспартатаминотрансфераза 35,8 ЕД/л; лактатдегидрогеназа 731 ЕД/л; креатинфосфокиназа 140 ЕД/л; глюкоза 6,7 г/л; С-реактивный белок 250 мг/л; натрий 135,7 ммоль/л; калий 3,6 ммоль/л; хлориды 99,3 ммоль/л.
Реакция непрямой иммунофлуоресценции (РНИФ) с парными сыворотками: 1:64 и 1:512 (нарастание титра в 8 раз).
Фенотипирование лимфоцитов крови: CD19+ 9% и 0,1×109/л; СD3+ 64,5% и 1,35×109/л; CD3+CD4+ 30,8% и 0,65×109/л; CD3+CD8+ 31,7% и 0,65×109/л; CD3+CD8+CD314+ 22,1% и 0,51×109/л; СD3+CD4+FoxP3+ 8% и 0,17×109/л; СD3+CD8+FoxP3+ 9% и 0,19×109/л; СD16+CD56+ 28,5% и 0,6×109/л; CD16+CD56+CD314+ 16% и 0,34×109/л.
Цитокиновый профиль плазмы крови: ИЛ-1β 2,6 пг/мл; ИЛ-4 1,8 пг/мл; ИЛ-6 20,4 пг/мл; ИЛ-10 645,2 пг/мл; ИЛ-12 125 пг/мл; ФНОα 3,2 пг/мл; ФНОβ 468,2 пг/мл; ИФНγ 885,6 пг/мл.
По совокупности клинико-лабораторных данных у больного Д. в лихорадочный период заболевания была диагностирована ГЛПС средней тяжести. Определение прогностического критерия тяжелого течения (ПКТТ ГЛПС) показало, что его величина составляла 17,3 (<19), что исключало риск развития тяжелого течения ГЛПС. Стационарное наблюдение больного Д. в последующие периоды развития заболевания полностью подтвердило, что заболевание имело среднетяжелое течение и не сопровождалось развитием каких-либо осложнений. На 19-й день заболевания больной был выписан в удовлетворительном состоянии для диспансерного наблюдения.
Литература:
1. Валишин, Д.А. Геморрагическая лихорадка с почечным синдромом у взрослых. Клинические рекомендации [Текст] / Д.А. Валишин, Р.Т. Мурзабаева, В.А. Иванис и др. // Некоммерческое партнерство «Национальное научное общество инфекционистов». - 2016. - 74 с.
2. Хунафина Д.Х. Геморрагическая лихорадка с почечным синдромом. Обзор литературы [Текст] / Д.Х. Хунафина, Д.А. Валишин, Л.Р. Шайхуллина, А.Т. Галиева // Международный журнал экспериментального образования. - 2014. – № 8-1. – С. 14-17.
3. Krautkramer, E. Old World hantaviruses: aspects of pathogenesis and clinical course of acute renal failure [Text] / E. Krautkramer, M.Zeier // Virus Res. – 2014. – Vol. 187. – P. 59-64.
4. Tkachenko, E.A. Hemorrhagic fever with renal syndrome, Russia [Text] / E.A.Tkachenko, A.A.Ishmukhametov, T.K.Dzagurova et al. // Emerg Infect Dis. – 2019. – Vol. 25 (12). – P. 2325-2328.
5. Валишин Д.А. Геморрагическая лихорадка с почечным синдромом: клиника, диагностика и лечение: учебное пособие для врачей [Текст] / Д.А. Валишин, Р.Т. Мурзабаева, А.П. Мамон и др. // Уфа, Изд-во ГБОУ ВПО БГМУ Минздравсоцразвития России. - 2012. - 51 с.
6. Klingstrom, J. Innate and adaptive immune responses against human Puumala virus infection: immunopathogenesis and suggestions for novel treatment strategies for severe hantavirus-associated syndromes [Text] / J.Klingstrom, А.Smed-Sörensen, K.T.Maleki et al. // J Intern Med. - 2019. - Vol. 285, N 5. - P. 510-523.
7. Морозов В.Г. Клинические особенности геморрагической лихорадки с почечным синдромом в России [Текст] / В.Г. Морозов, А.А. Ишмухаметов, Т.К. Дзагурова, Е.А. Ткаченко // Инфекционные болезни, 2017. - № 5. - С. 156-161.
8. Митрофанова Н.Н. Анализ клинико-эпидемиологических и эпизоотических особенностей заболеваемости геморрагической лихорадкой с почечным синдромом на территории Пензенской области [Текст] / Н.Н. Митрофанова, В.Л. Мельников, Н.Ф. Золина, Е.Д. Скороходова // Известия высших учебных заведений. Поволжский регион. Медицинские науки. – 2009. – №3 (11). – С. 109-116.
9. Алехин Е.К. Геморрагическая лихорадка с почечным синдромом [Текст] / Е.К. Алехин, Ф.Х. Камилов, Д.Х. Хунафина и др. // Медицинский вестник Башкортостана. - 2013. - № 5. - С. 24-31.
10. Connor, S.D. Regulated portals of entry into the cells [Text] / S.D. Connor, S.L. Schimid // Nature. - 2003. - Vol. 422, N 6927. - P. 37-44.
11. Wang, P.Z. Elevated serum concentrations of inflammatory cytokines and chemokines in patients with haemorrhagic fever with renal syndrome [Text] / P.Z. Wang, Z.D. Li, H.T. Yu et al. // J Int Med Res. - 2012. - Vol. 40, N 2. - P. 648-656.
12. Kruger, D.H. Hantaviruses-Globally emerging pathogens [Text] / D.H. Krüger, L.T. Figueiredo, J.W. Song, B. Klempa // J Clin Virol, 2015. - Vol. 64. - P. 128–136.
13. Jiang, H. Hemorrhagic fever with renal syndrome: pathogenesis and clinical picture [Text] / H.Jiang, H.Du, L.M.Wang et al. // Front Cell Infect Microbiol. - 2016. - Vol. 6. - P. 1-14.
14. Latus, J. Severe thrombocytopenia in hantavirus-induced nephropathia epidemica [Text] / J.Latus, D.Kitterer, S.Segerer et al. // Infection. – 2015. – Vol. 43, N 1. – P. 83-87.
15. Taylor, S.L. Endothelial cell permeability during hantavirus infection involves factor XII-dependent increased activation of the kallikrein–kinin system [Text] / S.L.Taylor, V.Wahl-Jensen, A.M.Copeland et al. // PLoS Pathog, 2013. - Vol. 9, N 7. - P. e1003470.
16. Krautkrаmer, E. Pathogenic old world hantaviruses infect renal glomerular and tubular cells and induce disassembling of cell-to-cell contacts [Text] / E.Krautkrämer, S.Grouls, N.Stein et al. // J Virol. - 2011. - Vol. 85, N 19. - P. 9811-9823.
17. Koivula, T.T. Regulatory T cell response correlates with the severity of human hantavirus infection [Text] / T.T.Koivula, A.Tuulasvaara, L.Hetemäki et al. // J Infec, 2014. - Vol. 68, N 4. - P. 387-394.
18. Lebecque, O. Puumala hantavirus: an imaging review [Text] / O. Lebecque, M.Dupont // Acta Radiol. – 2020. – Vol. 61, N 8. – P. 1072-1079.
19. Du, H. Clinical characteristics and outcomes in critical patients with hemorrhagic fever with renal syndrome [Text] / H.Du, P.-Z.Wang, J.Li et al. // BMC Infect Dis. – 2014. – Vol. 14. – P. 191.
20. Jiang, D.B. Hantavirus Gc induces long-term immune protection via LAMP-targeting DNA vaccine strategy [Text] / D.B.Jiang, J.P.Zhang, L.F.Cheng et al. // Antiviral Res, 2018. - Vol. 150. - P. 174-182.
21. Outinen, T.K. High activity of indoleamine 2,3-dioxygenase is associated with renal insufficiency in Puumala hantavirus induced nephropathia epidemica [Text] / T.K.Outinen, S.Makela, I.O.Ala-Houhala et al. // J Med Virol, 2011. – Vol. 83, N 4. – P. 731–737.
22. Outinen, T.K. High pentraxin-3 plasma levels associate with thrombocytopenia in acute Puumala hantavirus-induced nephropathia epidemica [Text] / T.K.Outinen, S.Makel, H.Huhtala et al. // Eur J Clin Microbiol Infect Dis: official publication of the European Society of Clinical Microbiology, 2012. – Vol. 31, N 6. – P. 957–963.
23. Outinen, T.K. Plasma levels of soluble urokinase-type plasminogen activator receptor associate with the clinical severity of acute puumala hantavirus infection [Text] / T.K. Outinen, L. Tervo, S. Makela et al. // PloS one, 2013. – Vol. 8, N 8. - e71335.
24. Jereb, M. Procalcitonin in hantavirus infections [Text] / M. Jereb, N.K. Lunacek, T. Kotar et al. // Scand J Clin Lab Invest, 2011. – Vol. 71, N 4. – P. 287–291.
25. Yilmaz G, Koksal I, Topbas M, Yilmaz H, Aksoy F (2010) The effectiveness of routine laboratory findings in determining disease severity in patients with Crimean-Congo hemorrhagic fever: severity prediction criteria [Text] / G. Yilmaz, I. Koksal, M. Topbas et al. // J Clin Virol, 2010. – Vol. 47, N 4. – P. 361–365.
26. Resman Rus, K. HMGB1 is a potential biomarker for severe viral hemorrhagic fevers [Text] / K. Resman Rus, L. Fajs, M. Korva, T. Avšič-Županc // PLoS Negl Trop Dis, 2016. – Vol. 10, N 6. - e0004804.
27. Kaya, S. Prognostic factors in hantavirus infections [Text] / S. Kaya // Mikrobiyol Bul, 2014. – Vol. 48, N 1. – P. 179-187.
28. Tietavainen, J. Glucosuria predicts the severity of puumala hantavirus infection [Text] / J. Tietavainen, P. Mantula, T. Outinen et al. // Kidney Int Rep, 2019. – Vol. 4, N 9. – P. 1296-1303.
29. Bianchi, M.E. HMG proteins: dynamic players in gene regulation and differentiation [Text] / M.E. Bianchi, A. Agresti // Curr Opin Genet Dev, 2005. – Vol. 15, N 5. – P. 496–506.
30. Stros, M. HMGB proteins: interactions with DNA and chromatin [Text] / M. Stros // Biochim Biophys Acta, 2010. – Vol. 1799, N 1-2. – P. 101–113.
31. Allonso, D. Elevated serum levels of high mobility group box 1 (HMGB1) protein in dengue-infected patients are associated with disease symptoms and secondary infection [Text] / D. Allonso, F.S. Belgrano, N. Calzada et al. // J Clin Virol, 2012. – Vol. 55, N 3. – P. 214–219.
32. Allonso, D. High mobility group box 1 protein as an auxiliary biomarker for dengue diagnosis [Text] / D. Allonso, S. Vazquez, M.G. Guzman, R. Mohana-Borges // Am J Trop Med Hyg, 2013. – Vol. 88, N 3. – P. 506–509.
33. Sadeghi, M. Association of low serum TGF-β level in hantavirus infected patients with severe disease [Text] / M. Sadeghi, I. Lahdou, J. Ettinger et al. // BMC Immunol, 2015. – Vol. 16. – P. 19.
34. Иванов, М.Ф. Иммунный ответ при геморрагической лихорадке с почечным синдромом различной степени тяжести [Teкст] / М.Ф. Иванов, Е.П. Ефратова, И.П. Балмасова // Аллергология и иммунология. - 2017. - Т. 18, № 3. - С. 147-151.
35. Koivula, T.-T. Regulatory T cell response correlates with the severity of human hantavirus infection [Text] / T.-T. Koivula, A. Tuulasvaara, I. Hetemaki et al. // J Infect, 2014. – Vol. 68, N 4. – P. 387-394.
36. Maes, P. Tumor necrosis factor-alpha genetic predisposing factors can influence clinical severity in nephropathia epidemica [Text] / P. Maes, J. Clement, P.H.P. Groeneveld et al. // Viral Immunol Summer, 2006. – Vol. 19, N 3. – P. 558-564.
37. Zhang, C. Elevated plasma growth arrest-specific 6 protein levels are associated with the severity of disease during Hantaan virus infection in humans [Text] / C. Zhang, K. Tang, Y. Zhang et al. // Viral Immunol, 2017. – Vol. 30, N 5. – P. 330-335.
38. Zhang, Y. Soluble scavenger receptor CD163 is associated with severe acute kidney injury in patients with Hantaan virus infection [Text] / Y. Zhang, Y. Ma, C. Zhang et al. // Viral Immunol, 2015. – Vol. 28, N 4. – P. 241-246.
Таблица 1.
лабораторного
исследования
показатели
тяжелого течения
средней
тяжести
анализ
крови
анализ
крови
крови
мочи
клеток/поле зрения
лимфоцитов
крови
лимфоцитов
крови
109 клеток/л
109 клеток/л
109 клеток/л
109 клеток/л
плазмы
крови
Примечание: р - вероятность различий в группе больных ГЛПС разной степени тяжести, серым цветом обозначена достоверность различий по критерию Манна-Уитни при р <0,05.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОГНОЗИРОВАНИЯ СТЕПЕНИ ТЯЖЕСТИ ТЕЧЕНИЯ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ С ПОЧЕЧНЫМ СИНДРОМОМ ПО ПОКАЗАТЕЛЮ C-РЕАКТИВНОГО БЕЛКА | 2024 |
|
RU2828321C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЯЖЕСТИ ТЕЧЕНИЯ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ С ПОЧЕЧНЫМ СИНДРОМОМ | 2024 |
|
RU2838792C1 |
| СПОСОБ ЛЕЧЕНИЯ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ С ПОЧЕЧНЫМ СИНДРОМОМ | 2000 |
|
RU2181046C2 |
| СПОСОБ ЛЕЧЕНИЯ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ С ПОЧЕЧНЫМ СИНДРОМОМ | 2002 |
|
RU2228196C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ОСЛОЖНЕНИЙ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ С ПОЧЕЧНЫМ СИНДРОМОМ В НАЧАЛЬНЫЙ ПЕРИОД ЗАБОЛЕВАНИЯ | 2010 |
|
RU2433407C1 |
| СПОСОБ ОЦЕНКИ ТЯЖЕСТИ ТЕЧЕНИЯ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ С ПОЧЕЧНЫМ СИНДРОМОМ | 2009 |
|
RU2392858C1 |
| СПОСОБ ЛЕЧЕНИЯ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ С ПОЧЕЧНЫМ СИНДРОМОМ СРЕДНЕТЯЖЕЛОЙ И ТЯЖЕЛОЙ ФОРМ | 2005 |
|
RU2289456C1 |
| СПОСОБ ОЦЕНКИ ТЯЖЕСТИ ТЕЧЕНИЯ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ С ПОЧЕЧНЫМ СИНДРОМОМ | 2003 |
|
RU2245552C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ЗАБОЛЕВАНИЯ, ВЫЗЫВАЕМОГО ВИРУСОМ ХАНТААН - ВОЗБУДИТЕЛЕМ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ С ПОЧЕЧНЫМ СИНДРОМОМ, НА ЭКСПЕРИМЕНТАЛЬНОМ ЖИВОТНОМ | 2005 |
|
RU2294563C2 |
| N-Ацилгидразон фенхона с фрагментом эпоксиизоиндола, используемый в качестве ингибитора репродукции вируса Хантаан | 2020 |
|
RU2733472C1 |

Изобретение относится к медицине, а именно к иммунологии и инфектологии, и может быть использовано для прогнозирования тяжелого течения геморрагической лихорадки с почечным синдромом на ранних этапах заболевания. Проводят определение в сыворотке крови больного геморрагической лихорадкой с почечным синдромом на первой неделе заболевания уровня мочевины и активности аланинаминотрансферазы (АЛТ), а также процента Т-клеток с фенотипами CD3+CD8+CD314+ и СD3+CD8+FoxP3+ среди лимфоцитов (CD45+) крови. На основе указанных показателей вычисляют прогностический критерий тяжелого течения заболевания (ПКТТ ГЛПС) по формуле: ПКТТ ГЛПС = 2,015 + 0,072 * [АЛТ] + 0,516 * [мочевина] + 0,364 * [СD3+CD8+CD314+] - 0,381 * [CD3+CD8+FoxP3+]. При значениях ПКТТ ГЛПС выше 19 прогнозируют развитие тяжелого течения геморрагической лихорадки с почечным синдромом. Способ обеспечивает возможность раннего прогнозирования риска развития тяжелого течения геморрагической лихорадки с почечным синдромом за счет определения широкого спектра лабораторных данных, включая иммунологические показатели. 3 ил., 1 табл., 2 пр.
Способ прогнозирования тяжелого течения геморрагической лихорадки с почечным синдромом на ранних этапах заболевания, включающий определение в сыворотке крови больного геморрагической лихорадкой с почечным синдромом на первой неделе заболевания уровня мочевины и активности аланинаминотрансферазы (АЛТ), а также процента Т-клеток с фенотипами CD3+CD8+CD314+ и СD3+CD8+FoxP3+ среди лимфоцитов (CD45+) крови, характеризующийся тем, что на основе указанных показателей вычисляют прогностический критерий тяжелого течения заболевания (ПКТТ ГЛПС) по формуле: ПКТТ ГЛПС = 2,015 + 0,072 * [АЛТ] + 0,516 * [мочевина] + 0,364 * [СD3+CD8+CD314+] - 0,381 * [CD3+CD8+FoxP3+], и при значениях ПКТТ ГЛПС выше 19 прогнозируют развитие тяжелого течения геморрагической лихорадки с почечным синдромом.
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЯЖЕСТИ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ С ПОЧЕЧНЫМ СИНДРОМОМ | 2019 |
|
RU2688691C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЯЖЕСТИ КЛИНИЧЕСКОГО ТЕЧЕНИЯ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ С ПОЧЕЧНЫМ СИНДРОМОМ (ГЛПС) | 2003 |
|
RU2239186C1 |
| СПОСОБ ОЦЕНКИ ТЯЖЕСТИ ТЕЧЕНИЯ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ С ПОЧЕЧНЫМ СИНДРОМОМ | 2009 |
|
RU2392858C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ОСЛОЖНЕНИЙ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ С ПОЧЕЧНЫМ СИНДРОМОМ В НАЧАЛЬНЫЙ ПЕРИОД ЗАБОЛЕВАНИЯ | 2010 |
|
RU2433407C1 |
| ИВАНОВ М.Ф | |||
| и др | |||
| Иммунопатогенетические особенности и прогностические критерии тяжелого течения геморрагической лихорадки с почечным синдромом // Вестник Российского университета дружбы народов | |||
| Серия: Медицина | |||
| Способ восстановления спиралей из вольфрамовой проволоки для электрических ламп накаливания, наполненных газом | 1924 |
|
SU2020A1 |
Авторы
Даты
2023-02-28—Публикация
2022-06-20—Подача