Область техники, к которой относится изобретение
Настоящее изобретение относится к аденоассоциированному вирусу (AAV), содержащему вставку по меньшей мере 6-8 аминокислот между позициями, соответствующими позициям 587 и 588 последовательности SEQ ID NO: 1. Также предложены AAV по настоящему изобретению для применения в качестве лекарственного средства и фармацевтические композиции, содержащие AAV по настоящему изобретению. Кроме того, настоящее изобретение относится к применению AAV по настоящему изобретению in vitro для трансдукции ядра клеток сетчатки. Изобретение также относится к способу скрининга вставочной последовательности, а также к пептиду, получаемому способом скрининга. Также предложены наборы, содержащие AAV по настоящему изобретению.
Уровень техники
Векторы на основе рекомбинантных аденоассоциированных вирусов (AAV) оказались очень подходящей системой доставки для эффективного и долгосрочного переноса генов в клетки сетчатки (Boye et al. (2013) “A comprehensive review of retinal gene therapy” Molecular therapy, 21 (2013) 509-519 and Trapani et al. (2014) “Vector platforms for gene therapy of inherited retinopathies” Prog Retin Eye Res). AAV - это непатогенные вирусы, которые относятся к семейству парвовирусов и роду Dependovirus и реплицируются только в присутствии адено-, папиллома- или герпесвирусов (Nathwani et al. (2014) “Long-term safety and efficacy of factor IX gene therapy in hemophilia B” N Engl J Med, 371 (2014) 1994-2004) и обладают геномом, представленным одноцепочечной ДНК длиной около 5 кб (Trapani et al. (2014) “Vector platforms for gene therapy of inherited retinopathies” Prog Retin Eye Res.).
AAV были широко исследованы в отношении безопасности и долгосрочной экспрессии трансгенов на моделях крупных животных, обезьянах и, в ряде исследований, на людях (MacLaren et al. (2014) “Retinal gene therapy in patients with choroideremia: initial findings from a phase 1/2 clinical trial” Lancet 383, 1129-1137, Maguire et al. (2008) “Safety and efficacy of gene transfer for Leber's congenital amaurosis” N Engl J Med, 358 2240-2248, Simonelliet al. (2010) ”Gene therapy for Leber's congenital amaurosis is safe and effective through 1.5 years after vector administration” Molecular therapy: the journal of the American Society of Gene Therapy 18, 643-650, Nathwani et al. (2014) “Long-term safety and efficacy of factor IX gene therapy in hemophilia B” N Engl J Med 371, 1994-2004).
AAV являются предпочтительными векторами переноса генов для терапии с дополнениями генов (также терапии с аугментацией генами). Терапия с дополнениями генов является привлекательным подходом для лечения наследственных заболеваний, направленным на восстановление недостаточной или нарушенной функции гена вследствие патогенной мутации. Цель состоит в том, чтобы восстановить нормальную физиологическую функцию пораженного типа клеток и/или ингибировать или задержать дегенеративные процессы путем дополнения функции гена.
Генная терапия направлена на восстановление недостаточной или нарушенной функции генов вследствие патогенной мутации. Этот подход особенно привлекателен для лечения рецидивирующих наследственных заболеваний, когда аберрантные транскрипты или белки, как ожидается, не будут мешать лечению. Цель состоит в том, чтобы остановить или предотвратить дегенеративный процесс и восстановить регулярную физиологическую функцию пораженного типа клеток или тканей путем дополнения нормальной функции генов в достаточном количестве и в нужном месте.
Хотя AAV показывают некоторую степень распространения в тканях и организмах (Le Guiner et al. (2011) “Biodistribution and shedding of AAV vectors” Methods in molecular biology 807, 339-359), при большинстве терапевтических подходов, в частности в генной терапии в области офтальмологии, они, как правило, требуют местного применения. Для трансдукции фоторецепторов или клеток пигментного эпителия сетчатки (RPE) частицы AAV вводят в субретинальное пространство (т.е. в полость, которая образуется после введения жидкостей между RPE и фоторецепторами) (Mühlfriedel et al. (2013) “Optimized technique for subretinal injections in mice” Methods in molecular biology 935, 343-349, Ochakovski et al. (2017) “Retinal Gene Therapy: Surgical Vector Delivery in the Translation to Clinical Trials.” Front Neurosci 11:174).
Структурно AAV представляют собой небольшие (25 нм) вирусы без оболочки с икосаэдрическим капсидом. Встречающиеся в природе или рекомбинантные варианты AAV (также серотипы AAV), отличающиеся составом и структурой своего капсидного белка (cap), обладают различным тропизмом, т.е. способностью трансфицировать различные типы клеток (сетчатки) (Boye et al. (2013) “A comprehensive review of retinal gene therapy” Molecular therapy 21 509-519 and Trapani et al. (2014) “Vector platforms for gene therapy of inherited retinopathies” Prog Retin Eye Res). В сочетании с повсеместно активными промоторами этот тропизм определяет участок экспрессии генов. При этом в комбинации со специфичными для типа клеток промоторами степень сайт-специфичности (т.е. экспрессии трансгена только в палочковых или колбочковых фоторецепторах) определяется комбинацией тропизма серотипа AAV и специфичности промотора (Schön et al. (2015) “Retinal gene delivery by adeno-associated virus (AAV) vectors: Strategies and applications” European journal of pharmaceutics and biopharmaceutics). Введение AAV в стекловидное тело глаза приводит к трансдукции клеток внутренней сетчатки, главным образом ганглиозных клеток и глиальных клеток Мюллера (Trapani et al. (2014) “Vector platforms for gene therapy of inherited retinopathies” Prog Retin Eye Res).
Ни один из встречающихся в природе серотипов AAV не способен трансфицировать фоторецепторы при введении в стекловидное тело из-за физического барьера на внутренней пограничной мембране (ILM) или отсутствия соответствующих рецепторов на ILM.
Необходимым предварительным условием для успешных подходов к проведению генной терапии является эффективная и длительная экспрессия трансгенов в клетках-мишенях с минимальной нецелевой экспрессией и наименьшими возможными побочными эффектами. Несмотря на то, что имеющиеся векторы AAV представляют собой ценные инструменты доставки генов, по-прежнему существует большая потребность в разработке усовершенствованных AAV.
Для обеспечения направленной доставки к фоторецепторам AAV необходимо вводить в субретинальное пространство. Эта крайне инвазивная хирургическая процедура приводит к отслоению сетчатки от RPE. Отслоение сетчатки обычно носит временный характер, и сетчатка восстанавливается без каких-либо серьезных или долгосрочных вредных последствий для функции и морфологии сетчатки. Однако риск побочных эффектов вследствие субретинальной инъекции может быть повышен в дегенерированной сетчатке и/или если отслоение затрагивает фовеомакулярную область. Поэтому необходимы улучшенные векторы AAV, в частности в отношении биодоступности, пути доставки и специфичности клеток-мишеней.
Таким образом, по-прежнему существует необходимость в дальнейшей разработке усовершенствованных векторов AAV. В настоящей заявке мы описываем новый AAV, который получен в результате отбора in vivo с улучшенными характеристиками для переноса генов в клетки сетчатки и особенно в клетки фоторецепторов.
Раскрытие изобретения
Настоящее изобретение соответствует этой потребности, как описано в настоящем документе, а также в примерах, на чертежах и в формуле изобретения.
Настоящее изобретение относится к аденоассоциированному вирусу (AAV), содержащему
вставку по меньшей мере 6-8 аминокислот между позициями, соответствующими позициям 587 и 588 последовательности SEQ ID NO: 1; при этом вставочная последовательность между N-концом и C-концом имеет формулу I:
X1A-X1B-X2-X3-X4-X5-X6-X7 (формула I)
в которой X5 выбрана из P (Pro), L (Leu) и V (Val);
в которой X7 - это R (Arg);
в которой X1A, X1B, X2, X3, X4, X6 независимо являются любой аминокислотой;
в которой X1A и/или X1B независимо необязательно отсутствуют или присутствуют,
или
в которой X5 выбрана из S (Ser) и T (Thr);
в которой X7 - это S (Ser);
в которой X1A, X1B, X2, X3, X4, X6 независимо являются любой аминокислотой;
в которой X1A и/или X1B независимо необязательно отсутствуют или присутствуют,
или
в которой X5 выбрана из A (Ala) и Q (Gln);
в которой X7 - это A (Ala);
в которой X1A, X1B, X2, X3, X4, X6 независимо являются любой аминокислотой;
в которой X1A и/или X1B независимо необязательно отсутствуют или присутствуют,
в которой вирусная ДНК AAV присутствует в ядерных экстрактах сетчатки мыши через 24 часа после внутривенного введения AAV в хвостовую вену мыши линии C57-Bl6J и
в которой вирусная ДНК AAV присутствует в MAC-сортированных палочках с использованием магнитных микроносителей, покрытых антителами к CD73, и/или FACS-сортированных колбочках, при этом колбочки экспрессируют eGFP и являются FACS-сортированными на основе их экспрессии eGFP, через 24 часа после внутривенного введения AAV в хвостовую вену мыши линии C57-Bl6J для сортировки палочек и в хвостовую вену мыши RG-eGFP линии R685933 для сортировки колбочек.
Кроме того, настоящее изобретение относится к AAV по настоящему изобретению для применения в качестве лекарственного средства.
Дополнительно настоящее изобретение относится к AAV по настоящему изобретению для применения в лечении поражения фоторецепторных клеток.
Настоящее изобретение также относится к фармацевтической композиции, содержащей AAV по настоящему изобретению.
Настоящее изобретение также относится к применению AAV по настоящему изобретению in vitro для трансдукции ядра клеток сетчатки.
Также настоящее изобретение относится к способу скрининга вставочной последовательности, который включает в себя
i) внутривенное введение библиотеки AAV, в которой каждый AAV содержит вставочную последовательность, субъекту;
ii) выделение вирусной ДНК AAV из ядерных экстрактов сетчатки глаза;
iii) субклонирование выделенной вирусной ДНК AAV во вторую библиотеку AAV;
iv) внутривенное введение второй библиотеки AAV, полученной на этапе iii), субъекту;
v) выделение вирусной ДНК AAV из палочковых или колбочковых фоторецепторов;
vi) определение последовательности вставочной последовательности,
получение, тем самым, вставочной последовательности.
Настоящее изобретение дополнительно относится к пептиду (вставочной последовательности), получаемому методом скрининга по настоящему изобретению.
Настоящее изобретение также относится к набору, содержащему AAV по настоящему изобретению.
Краткое описание чертежей
На фигурах представлены:
Фиг. 1: пептидные вставки из всей сетчатки.
Могли быть идентифицированы следующие новые AAV с перечисленными пептидными вставками в позиции 587 VP1 AAV2, наделенные способностью направленной доставки к клеткам сетчатки и переноса их генома в ядро клеток сетчатки в течение 24 часов после внутривенной доставки (перечислены только варианты с 2 или более ридами NGS, варианты с более чем 20 ридами NGS выделены “жирным” шрифтом).
Фиг. 2: пептидные вставки из палочковых фоторецепторов.
Дополнительно могли быть идентифицированы следующие новые AAV с перечисленными пептидными вставками в позиции 587 VP1 AAV2, наделенные способностью направленной доставки к палочковым фоторецепторам в течение 24 часов после внутривенной доставки (перечислены только пептиды с 2 или более ридами NGS, варианты с более чем 20 ридами NGS выделены “жирным” шрифтом).
Фиг. 3: пептидные вставки из колбочковых фоторецепторов.
Наконец могли быть идентифицированы следующие новые AAV с перечисленными пептидными вставками в позиции 587 VP1 AAV2, наделенные способностью направленной доставки к колбочковым фоторецепторам в течение 24 часов после внутривенной доставки (перечислены только пептиды с 2 или более ридами NGS, варианты с более чем 20 ридами NGS выделены “жирным” шрифтом).
Фиг. 4: Идентифицированные пептидные вставки с мотивами RGD, RGS или NGR.
Некоторые из идентифицированных AAV содержали предполагаемые мотивы связывания интегрина, такие как RGD, RGS или NGR, в своей вставочной последовательности. Эти вставочные последовательности представлены на Фиг. 4.
Фиг. 5: Пептидные вставки, идентифицированные в более чем одной популяции тканей/клеток. Показано количество ридов NGS в каждом эксперименте. Несколько AAV были обнаружены в более чем одном эксперименте. Эти перекрывающиеся AAV, содержащие указанные вставочные последовательности, с соответствующими номерами ридов NGS, представлены на Фиг. 5.
Фиг. 6: Репрезентативные изображения конфокальной сканирующей лазерной офтальмоскопии (cSLO) in vivo, показывающие аутофлуоресценцию eGFP на глазном дне 10-недельных мышей линии C57-BL6J через 2 недели после однократного введения в стекловидное тело 1 мкл (содержащего приблизительно 2 × 10E9 векторных геномов) вирусной суспензии AAV-sc-CMV-eGFP, упакованной с одним из новых вариантов AAV2 (вставочные последовательности пептида приведены вверху каждого изображения). Наблюдалась сильная аутофлуоресценция eGFP (серый цвет) в нескольких типах клеток сетчатки и на большой площади сетчатки.
Фиг. 7: Репрезентативные изображения конфокальной сканирующей микроскопии, показывающие флуоресценцию eGFP в поперечных срезах сетчатки у 11-недельных мышей линии C57-BL6J через 3 недели после однократного введения в стекловидное тело 1 мкл (содержащего приблизительно 2 × 10E9 векторных геномов) вирусной суспензии AAV-sc-CMV-eGFP, упакованной с одним из новых вариантов AAV2 (вставочные последовательности пептидов приведены вверху каждого изображения). Сильная флуоресценция eGFP (серый цвет) в различных типах клеток сетчатки и слоях и по всей площади поперечного среза сетчатки наблюдалась для вариантов «NNPTPSR» (см. общий вид на верхней панели и крупный план на нижней левой панели) и «GLSPPTR» (только крупный план показан на нижней правой панели). В частности, многие внутренние сегменты фоторецепторов (is) и клеточные тела в пределах внешнего ядерного слоя (onl) были eGFP-положительными, inl, внутренний ядерный слой; gcl, слой ганглиозных клеток. Шкала показывает 100 мкм на верхней панели и 25 мкм на нижней панели.
Фиг. 8: Репрезентативные изображения конфокальной сканирующей микроскопии, показывающие флуоресценцию eGFP в поперечных срезах сетчатки у 11-недельных мышей линии C57-BL6J через 3 недели после однократного введения в субретинальное пространство ((верние панеи) или в стекловидное тело (нижние панели) 1 мкл (содержащего приблизительно 2 × 10E9 векторных геномов) вирусной суспензии AAV-sc-CMV-eGFP, упакованной с одним из новых вариантов AAV2 (вставочные последовательности пептидов приведены вверху каждого изображения). Наблюдалась сильная флуоресценция eGFP (серый цвет) в различных типах и слоях клеток сетчатки. В частности, многие внутренние сегменты фоторецепторов (is) и клеточные тела в пределах внешнего ядерного слоя (onl) были eGFP-положительными. После введения в субретинальное пространство сильная флуоресценция eGFP наблюдалась также в клетках пигментного эпителия сетчатки (rpe). inl, внутренний ядерный слой; gcl, слой ганглиозных клеток. Шкала показывает 25 пм.
Фиг. 9: (А) Репрезентативные изображения конфокальной сканирующей лазерной офтальмоскопии (cSLO) in vivo, показывающие аутофлуоресценцию eGFP на глазном дне 2-месячных мышей линии C57-BL6J через 1, 2 и 3 недели после однократного введения в стекловидное тело (WPI) 1 мкл (содержащего приблизительно 2 × 10E9 векторных геномов) вирусной суспензии AAV-sc-CMV-eGFP, упакованной с одним из новых вариантов AAV (GLSPPTR или NNPTPSR; вставочные последовательности пептида приведены вверху каждого изображения). Наблюдалась сильная аутофлуоресценция eGFP (серый цвет) в нескольких типах клеток сетчатки и на большой площади сетчатки. Все изображения были получены с использованием одинаковых настроек лазера и детектора.
(B) Репрезентативные изображения конфокальной сканирующей микроскопии, показывающие иммуносигнал, полученный в присутствии антител к eGFP (серый цвет) в поперечных срезах сетчатки от 2 месячных мышей линии C57-BL6J через 3 недели после однократного введения в стекловидное тело (WPI) 1 мкл (содержащего приблизительно 2 × 10E9 векторных геномов) вирусной суспензии AAV-sc-CMV-eGFP, упакованной с AAV или с одним из новых вариантов AAV2 (GLSPPTR или NNPTPSR; вставочные последовательности пептидов приведены вверху каждого изображения). Сильный иммуносигнал eGFP (серый цвет) в различных типах и слоях клеток сетчатки наблюдался для новых вариантов GLSPPTR и NNPTPSR, соответственно. Напротив, AAV2 приводил к более слабой маркировке редких клеток. Все изображения были получены с использованием одинаковых настроек лазера и детектора. В частности, многие клеточные тела фоторецепторов в пределах внешнего ядерного слоя (onl) были eGFP-положительными, inl, внутренний ядерный слой; gcl, слой ганглиозных клеток.
Фиг. 10: Репрезентативные обзорные изображения конфокальной сканирующей микроскопии, показывающие иммуносигнал, полученный в присутствии антител к eGFP (верхние панели, серый цвет) в поперечных срезах сетчатки от 2 месячных мышей линии C57-BL6J через 3 недели после однократного введения в стекловидное тело (WPI) 1 мкл (содержащего приблизительно 2 × 10E9 векторных геномов) вирусной суспензии AAV-sc-CMV-eGFP, упакованной с AAV или с одним из новых вариантов AAV2 (GLSPPTR или NNPTPSR; вставочные последовательности пептидов приведены вверху каждого изображения). Сильный иммуносигнал eGFP (серый цвет) в различных типах и слоях клеток сетчатки и во всем поперечном срезе сетчатки наблюдался для новых вариантов GLSPPTR и NNPTPSR, соответственно. Напротив, AAV2 приводил к более слабой маркировке в меньшей области сетчатки. Все изображения были получены с использованием одинаковых настроек лазера и детектора. Соответствующие изображения ядерных клеток с окрашиванием красителем Hoechst 33342 (серый цвет) показаны под каждым изображением eGFP.
Фиг. 11: Эффективность трансдукции векторов AAV в клетках 661w. (А) Репрезентативные эпифлуоресцентные изображения из 661w клеточных культур через 48 часов после трансдукции с MOI 100000 AAV-sc-CMV-eGFP, упакованной с AAV2, 7m8 или одним из новых вариантов AAV (GLSPPTR или NNPTPSR; вставочные последовательности пептидов приведены вверху каждого изображения). (B) График, показывающий относительную интенсивность eGFP в %, измеренную с помощью FACS в нетрансфицированных культурах клеток 661w и в культурах клеток 661w через 48 часов после трансдукции с MOI 100 000 AAV-sc-CMV-eGFP в присутствии AAV2, 7m8 или одним из новых вариантов AAV (GLSPPTR или NNPTPSR; вставочные последовательности пептидов приведены вверху каждого изображения).
Фиг. 12: Репрезентативные изображения конфокальной сканирующей микроскопии, показывающие конусную экспрессию фоторецепторов eGFP на поперечных срезах сетчатки у 10-недельных мышей линии C57-BL6J через 6 недель после однократного введения в стекловидное тело 1 мкл (содержащего приблизительно 2 × 10E9 векторных геномов) вирусной суспензии ss-mSWS-eGFP, упакованной с новым капсидом AAV2 «GLSPPTR». AAV-ss-mSWS-eGFP стимулирует экспрессию eGFP под контролем промотора опсина мыши S. Наблюдался сильный иммуносигнал антител к eGFP (серый цвет) в колбочковых фоторецепторах. Количественное определение двойного мечения колбочковым аррестином в качестве колбочкового маркера показала, что 78,7 ± 3,1 % (n = 4) положительных по колбочковому аррестину колбочек были положительными по eGFP. OS/IS, внешний и внутренний сегменты. ONL, внешний ядерный слой. INL, внутренний ядерный слой. OPL, внешний плексиформный слой.
Фиг. 13: Репрезентативные изображения конфокальной сканирующей микроскопии, показывающие AAV-опосредованную экспрессию eGFP в эксплантатах сетчатки человека через девять дней in vitro (DIV) после трансдукции с 1 × 10E11 vg (вирусных геномов) sc-CMV-eGFP, упакованной с одним из новых AAV2 (вставочные последовательности пептидов приведены вверху каждого изображения). Наблюдалась сильная нативная флуоресценция eGFP (серый цвет) в различных типах и слоях клеток сетчатки. В частности, многие внутренние сегменты фоторецепторов (is) и клеточные тела в пределах внешнего ядерного слоя (onl) были eGFP-положительными. IS, внутренние сегменты. ONL, внешний ядерный слой. INL, внутренний ядерный слой. ONL, внутренний ядерный слой. GCL, слой ганглиозных клеток.
Фиг. 14: Репрезентативные измерения фотопического мерцания ERG у 3-месячной мыши с дефицитом Cnga3 через 2 месяца после однократного введения в стекловидное тело 1 мкл (содержащего приблизительно 1 × 10E10 vg (вирусных геномов) ss-mSWS-mCnga3-WPRE (Michalakis et al. (2010) Restoration of Cone Vision in the CNGA3-/- Mouse Model of Congenital Complete Lack of Cone Photoreceptor Function Mol Ther.: 2057-2063), упакованной с новым капсидным GLSPPTR AAV2. Показаны следы от обработанного глаза (черный цвет) и необработанного контрольного глаза (серый пунктир) при 3,1 log cd сек/м2 и указанной частоте.
Фиг. 15: Репрезентативные изображения конфокальной сканирующей микроскопии, показывающие экспрессию колбочкового фоторецептора белка CNGA3 на поперечных срезах сетчатки у 3-месячной мыши с дефицитом Cnga3 через 2 месяца после однократного введения в стекловидное тело 1 мкл (содержащего приблизительно 1 × 10E10 vg (вирусных геномов) ss-mSWS-mCnga3-WPRE (Michalakis et al. (2010) Restoration of Cone Vision in the CNGA3-/- Mouse Model of Congenital Complete Lack of Cone Photoreceptor Function Mol Ther.: 2057-2063), упакованной с новым капсидным GLSPPTR AAV2. Сильный иммуносигнал антител к CNGA3 обнаружен в положительных на арахисовый агглютинин (PNA) колбочковых фоторецепторах. os, внешние сегменты. onl, внешний ядерный слой. inl, внутренний ядерный слой. gcl, слой ганглиозных клеток.
Фиг. 16: Репрезентативные измерения скотопического однократного испарения ERG у 3-месячных мышей с дефицитом Cngb1 через 2 после однократного введения в стекловидное тело 1 мкл (содержащего приблизительно 1 × 10E10 vg (вирусных геномов) ss-mRho-mCngb1-sv40 (Koch et al. 2012) Gene therapy restores vision and delays degeneration in the CNGB1-/- mouse model of retinitis pigmentosa. Hum Mol Genet.: 4486-4496), упакованной с новым капсидным «NNPTPSR» AAV2. Показаны следы от обработанного глаза (черный цвет) и необработанного контрольного глаза (серый пунктир) при указанной яркости светового стимула.
Осуществление изобретения
Современные изобретатели нашли новые капсиды AAV с новыми пептидными вставками, которые очень ценны для всех исследований, направленных на эффективную трансдукцию типов клеток сетчатки и, в частности, фоторецепторов. Кроме того, эти новые варианты капсидов AAV позволяют преодолевать естественные барьеры для трансдукции типов клеток сетчатки (и, в частности, фоторецепторов) из интравитреальных или системных компартментов (отделов).
Тот факт, что AAV по настоящему изобретению являются особенно полезными, также является результатом специального процесса селекции. Процесс селекции включает в себя два или даже три раунда селекции, которые должен пройти AAV по настоящему изобретению. Во-первых, была представлена библиотека отображения пептидов AAV, аналогичная описанной в работе Perabo et al. (2003) “In vitro selection of viral vectors with modified tropism: the adeno-associated virus display.” Molecular Therapy, Vol. 8, No. 1. В частности, для построения плазмиды pWt.oen кассета промотора/энхансера HCMV и открытая рамка считывания GFP в плазмиде pEGFPC-1 (Clontech, Palo Alto, штат Калифорния) были заменены кодирующим AAV-2 фрагментом генома дикого типа плазмиды pUC-AV2 (Girod et al. (1999) “Genetic capsid modifications allow efficient re-targeting of adeno-associated virus type 2. Nat. Med. 5: 1052-1056). Фрагмент ДНК, кодирующий аминокислоты AAAstopA и сайты рестрикции NotI и AscI, был вставлен между аминокислотными позициями 587 и 588 методом ПЦР-мутагенеза. Для получения библиотеки плазмид AAV (Библиотека № 1) был синтезирован пул одноцепочечных молекул ДНК в виде 5'-TTGGCGCGCCGCVNNVNNVNNVNNVNNVNNVNNGGCGGCCGCTTTTTTCCTTGA-3' (нижняя нить; SEQ ID NO. 2) с последующей очисткой методом ВЭЖХ (Metabion GmbH, Мартинсрид, Германия). Для синтеза двухцепочечных молекул использовали праймер 5'-CTCAAGGAAAAAAGC-3' (SEQ ID NO. 3). Молекулы дцДНК клонировали в не очень большой фрагмент NotI-AscI плазмиды pWt.oen.
Библиотека № 1 была электропорирована в DH5α штамма Escherichia coli с помощью генного генератора импульсов (Bio-Rad, Hercules, штат Калифорния), и амплифицированная ДНК была очищена. Эффективность трансформации контролировали путем культивирования аликвот образца. ДНК более чем 20 клонов контролировали путем секвенирования с праймером 5'-ATGTCCGTCCGTGTGTGG-3' (SEQ ID No. 4). Проанализированные последовательности не показали никакой гомологии, что указывает на полную рандомизацию вставленной последовательности.
Для производства вирусов 15 чашек Петри 150 мм с клетками HEK293 при 80% конфлюентности были котрансфецированы 37,5 мкг ДНК. Для производства библиотеки AAV библиотеку №1 и плазмиду pXX6 (полученную, как описано в J. Samulski, Chapel Hill, NC; Xiao, Li and Samulski (1998) “Production of high-titer recombinant adeno-associated virus vectors in the absence of helper adenovirus.” J. Virol. 72: 2224-2232) котрансфецировали в молярном соотношении 1:1 в клетках HEK293. Через 48 ч клетки собирали и осаждали центрифугированием. Клетки ресуспендировали в 150 мм NaCl, 50 мм Tris-HCl (рН 8,5), несколько раз замораживали-размораживали и обрабатывали бензоназой (50 ЕД/мл) в течение 30 мин при температуре 37°C. Клеточный дебрис удаляли центрифугированием, а супернатант загружали на градиент йодиксанола и центрифугировали со скоростью 69000 об/мин в течение 1 ч при температуре 18°C, как описано (Zolotukhin et al. (1999) “Recombinant adeno-associated virus purification using novel methods improves infectious titer and yield. Gene Ther. 6: 973-985). Затем вирионы собирали из 40% йодиксанольной фазы и титровали методом дот-блот гибридизации ДНК с помощью rep зонда (Girod et al. (1999) “Genetic capsid modifications allow efficient re-targeting of adeno-associated virus type 2. Nat. Med. 5: 1052-1056). Эта процедура привела к созданию библиотеки № 1.
Как описано выше, библиотека отображения пептидов AAV была упакована в клетки HEK293 с последующим соединением гено- и фенотипов (как описано в PCT/EP2008/004366). Последнее необходимо для обеспечения того, чтобы геном кодировал пептид, который отображается на капсиде. Кроме того, библиотека AAV была лишена мутантов, связывающихся с HSPG через пептидную последовательность, которая была вставлена, чтобы свести к минимуму присутствие AAV, несущего вторичные высокоаффинные участки связывания для HSPG (Sallach et al. (2014) “Tropism-modified AAV vectors overcome barriers to successful cutaneous therapy. Mol. Ther. 22:929-39).
В раунде 1 селекции живые взрослые мыши C57BL/6J получали в хвостовую вену однократную инъекцию 100 мкл, содержащую приблизительно 8×10^10 векторных геномов (vg) библиотеки отображения пептидов AAV № 1. Через 24 часа мышей усыпляли путем цервикальной дислокации и делали проптоз глазного яблока, слегка сдавливая заднюю часть, близко к зрительному нерву, изогнутым пинцетом Dumont № 7 (Fine Science Tools, Хайдельберг). Роговицу рассекали вдоль экватора острым лезвием. Затем сетчатку отделяли от пигментного эпителия сетчатки (RPE) и, осторожно потянув пинцет вверх, удаляли из оставшейся ткани глаза вместе с хрусталиком и стекловидным телом. После промывки ткани в ледяном 0,1 М фосфатном буфере (PB) и удаления хрусталика и любых оставшихся клеток RPE пинцетом две сетчатки каждой мыши объединяли и переносили в пробирку Эппендорфа, глубоко замораживали в жидком азоте и хранили при температуре -80°C для дальнейшего использования. Ядра были выделены (чтобы гарантировать, что анализировалась только ядерная ДНК) из всей сетчатки с помощью набора для фракционирования субклеточного белкового комплекса для тканей (Subcellular Protein Fractionation Kit for Tissues, Thermo Fischer Scientific, #87790). Ядерная ДНК была выделена с помощью набора DNeasy Blood & Tissue Kit (Qiagen, #69504) и далее проанализирована путем секвенирования с помощью системы секвенирования Roche 454 для выявления геномов AAV с использованием специфических методов количественного определения, нацеленных на ДНК библиотеки AAV. Впоследствии вирусная ДНК вокруг места инъекции амплифицировали с помощью ПЦР с праймерами 5'-GTATCTACCAACCTCCAGAGAG-3' (SEQ ID NO. 5) and 5'-GTGTTGACATCTGCGGTAGC-3' (SEQ ID NO. 6) и клонировали по сайтам NotI-AscI в плазмиду pWt.oen генерируя, таким образом, пул плазмид.
Для получения библиотеки AAV № 2 15 чашек Петри 150 мм с 293 клетками при 80% конфлюентности были котрансфецированы в молярном соотношении 1:1 37,5 мкг пула плазмидной ДНК, полученного из раунда 1 селекции, и плазмиды pXX6. Через 48 ч клетки собирали и осаждали центрифугированием. Клетки ресуспендировали в 150 мм NaCl, 50 мм Tris-HCl (рН 8,5), несколько раз замораживали-размораживали и обрабатывали бензоназой (50 ЕД/мл) в течение 30 мин при температуре 37°C. Клеточный дебрис удаляли центрифугированием, а супернатант загружали на градиент йодиксанола и центрифугировали со скоростью 69000 об/мин в течение 1 ч при температуре 18°C, как описано (Zolotukhin et al. (1999) “Recombinant adeno-associated virus purification using novel methods improves infectious titer and yield. Gene Ther. 6: 973-985). Затем вирионы собирали из 40% йодиксанольной фазы и титровали методом дот-блот гибридизации ДНК с помощью rep или gfp зонда (Girod et al. (1999) “Genetic capsid modifications allow efficient re-targeting of adeno-associated virus type 2. Nat. Med. 5: 1052-1056). Эта процедура привела к созданию библиотеки № 2.
Библиотека № 2 была соединена по схеме «фенотип-генотип» (как описано в PCT/EP2008/004366), титрована и подвергнута новому раунду селекции in vivo. В частности, взрослые живые мыши C57BL/6J получали в хвостовую вену однократную инъекцию 50 мкл, содержащую приблизительно 5 × 10^11 vg. Последующие этапы раунда 2 селекции были выполнены так, как описано для раунда 1 селекции, в результате чего был получен новый пул плазмид, используемый для генерации библиотеки № 3.
Для получения библиотеки AAV № 3 15 чашек Петри 150 мм с 293 клетками при 80% конфлюентности были котрансфецированы в молярном соотношении 1:1 37,5 мкг пула плазмидной ДНК, полученного из отборного раунда 1, и плазмиды pXX6. Через 48 ч клетки собирали и осаждали центрифугированием. Клетки ресуспендировали в 150 мм NaCl, 50 мм Tris-HCl (рН 8,5), несколько раз замораживали-размораживали и обрабатывали бензоназой (50 ЕД/мл) в течение 30 мин при температуре 37°C. Клеточный дебрис удаляли центрифугированием, а супернатант загружали на градиент йодиксанола и центрифугировали со скоростью 69000 об/мин в течение 1 ч при температуре 18°C, как описано (Zolotukhin et al. (1999) “Recombinant adeno-associated virus purification using novel methods improves infectious titer and yield. Gene Ther. 6: 973-985). Затем вирионы собирали из 40% йодиксанольной фазы и титровали методом дот-блот гибридизации ДНК с помощью зонда rep или gfp (Girod et al. (1999) “Genetic capsid modifications allow efficient re-targeting of adeno-associated virus type 2. Nat. Med. 5: 1052-1056). Эта процедура привела к созданию библиотеки № 3.
В раунде 3а селекции живые взрослые мыши C57BL/6J получали в хвостовую вену однократную инъекцию 100 мкл, содержащую прибл. 5 × 10^11 vg (вирусных геномов) библиотеки отображения пептидов AAV № 3. Через 24 часа сетчатку выделяли, используя процедуру, описанную для селекционных раундов 1 и 2, за исключением того, что объединенные сетчатки не замораживали, а немедленно обрабатывали для выделения палочковых фоторецепторов. В частности, была проведена диссоциация папаина, как описано в работе Feodorova et al. (2015) “Quick and reliable method for retina dissociation and separation of rod photoreceptor perikarya from adult mice.” MethodsX 2: 39-46, и палочки были выделены методом MACS-сортировки на основе антител к CD73, как описано в работе Eberle et al. (2014) “Subretinal transplantation of MACS purified photoreceptor precursor cells into the adult mouse retina.” J Vis Exp 84:e50932. Ядра палочек были выделены (чтобы гарантировать, что анализировалась только ядерная ДНК) из MACS-сортированных палочек с помощью набора для фракционирования субклеточного белкового комплекса для тканей (Subcellular Protein Fractionation Kit for Tissues, Thermo Fischer Scientific, #87790). Ядерную ДНК выделяли с помощью набора DNeasy Blood & Tissue Kit (Qiagen, #69504). Секвенирование с помощью системы секвенирования Roche 454 было проведено для определения вставленных пептидных последовательностей, наиболее часто встречающихся в палочках.
В селекционном раунде 3b живые взрослые мыши RG-eGFP (Fei et al. (2003) “Development of the cone photoreceptor mosaic in the mouse retina revealed by fluorescent cones in transgenic mice.” Mol Vision 9: 31-42), экспрессирующие усиленный зеленый флуоресцентный белок (eGFP) в колбочковых фоторецепторах, получали в хвостовую вену однократную инъекцию 100 мкл, содержащую приблизительно 5 × 10^11 vg (вирусных геномов) библиотеки отображения пептидов AAV № 3. Через 24 часа сетчатку выделяли, используя процедуру, описанную для селекционных раундов 1 и 2, за исключением того, что объединенные сетчатки не замораживали, а немедленно обрабатывали для выделения колбочковых фоторецепторов. В частности, была проведена диссоциация папаина, как описано в работе Feodorova et al. (2015) “Quick and reliable method for retina dissociation and separation of rod photoreceptor perikarya from adult mice.” MethodsX 2: 39-46, и колбочки были подвергнуты FACS-сортировке (маркер eGFP), как описано в работе Becirovic et al. (2016) In Vivo Analysis of Disease-Associated Point Mutations Unveils Profound Differences in mRNA Splicing of Peripherin-2 in Rod and Cone Photoreceptors.” PLOS Genetics 12(1):e1005811. Ядра колбочек были выделены (чтобы гарантировать, что анализировалась только ядерная ДНК) из FACS-сортированных колбочек с помощью набора для фракционирования субклеточного белкового комплекса для тканей (Subcellular Protein Fractionation Kit for Tissues, Thermo Fischer Scientific, #87790). Ядерную ДНК выделяли с помощью набора DNeasy Blood & Tissue Kit (Qiagen, #69504). Секвенирование с помощью системы секвенирования Roche 454 было проведено для определения вставленных пептидных последовательностей, наиболее часто встречающихся в колбочках.
Для генерации новых хелперных плазмид-для производства векторов AAV с новыми вариантными капсидами были синтезированы (Eurofins Genomics GmbH, Эберсберг, Германия) синтетические одноцепочечные олиго-ДНК, кодирующие верхнюю (5'-CGCGGCCGCANNNNNNNNNNNNNNNNNNNNNGCCG-3') (SEQ ID NO. 7) и нижнюю (5'-CGCGCGGCNNNNNNNNNNNNNNNNNNNNNTGCGGC-3') (SEQ ID NO. 8) нити, кодирующие выбранные вставочные последовательности, полученные в предыдущих селекционных раундах, фланкированные 2-3 аланинами с обоих концах, затем гибридизированы для создания двухцепочечных олиго-ДНК, фланкированных липкими концами Mlul-Ascl, затем денатурированы и лигированы в сайты рестрикции Mlul-Ascl с транс-плазмидой AAV pRC99 (Nickiin et al. (2001) “Efficient and selective AAV2-mediated gene transfer directed to human vascular endothelial cells” Molecular therapy: the journal of the American Society of Gene Therapy 4, 174-181 и Girod et al. (1999) “Genetic capsid modifications allow efficient re-targeting of adeno-associated virus type 2” Nature medicine 5, 1052-1056), экспрессирующей гены Rep и Cap AAV2, что приводит к генерации открытой рамки считывания VP1-3 AAV2 с предполагаемыми пептидными вставками в положении, соответствующем аминокислоте 587 VP1. Вставка последовательности разрушает сайты Mlul / Ascl и создает новый сайт EagI , который может быть использован для скрининга правильных клонов. Правильная последовательность полученных плазмид была верифицирована стандартным секвенированием с использованием праймера 5'-ctttgggaagcaaggctcag-3' (SEQ ID NO. 9).
Эти модифицированные плазмиды pRC99 были использованы для получения частиц AAV с требуемой новой модификацией капсида AAV для биологических испытаний. Производство AAV осуществляли по стандартным методикам, описанным в работе Michalakis et al. (2010) “Restoration of cone vision in the CNGA3-/- mouse model of congenital complete lack of cone photoreceptor function, Molecular therapy: the journal of the American Society of Gene Therapy 18, 2057-2063 and Becirovic et al. (2016) “AAV Vectors for FRET-Based Analysis of Protein-Protein Interactions in Photoreceptor Outer Segments.” Front Neurosci 10:356. Самокомплементарную (sc) цис-плазмиду AAV, содержащую экспрессионную кассету CMV-eGFP (AAV-sc-CMV-eGFP) (Hacker et al. (2005) “Adeno-associated virus serotypes 1 to 5 mediated tumor cell directed gene transfer and improvement of transduction efficiency.” J Gene Med 7(11):1429-38), использовали в качестве цис-плазмиды.
Для получения капсидных модифицированных вариантов AAV 15 чашек Петри 150 мм с 293 клетками при 80% конфлюентности были котрансфицированы в молярном соотношении 1:1 37,5 мкг модифицированных плазмид pRC99, 37,5 мкг плазмид pXX6 и 37,5 мкг плазмид AAV-sc-CMV-eGFP. Через 48 ч клетки собирали и осаждали центрифугированием. Клетки ресуспендировали в 150 мм NaCl, 50 мм Tris-HCl (рН 8,5), несколько раз замораживали-размораживали и обрабатывали бензоназой (50 ЕД/мл) в течение 30 мин при температуре 37°C. Клеточный дебрис удаляли центрифугированием, а супернатант загружали на градиент йодиксанола и центрифугировали со скоростью 69000 об/мин в течение 1 ч при температуре 18°C, как описано (Zolotukhin et al. (1999) “Recombinant adeno-associated virus purification using novel methods improves infectious titer and yield. Gene Ther. 6: 973-985). Вирионы затем собирали из фазы 40% иодиксанола, повторно помещенной в фосфатно-солевой буфер (PBS), с использованием центробежных фильтрующих элементов Amicon Ultra-4, 100 кДа (Millipore), и титры геномных частиц определяли с помощью qПЦР (LightCycler System, Roche Diagnostics, Мангейм, Германия) с использованием специфических праймеров инвертированных концевых повторов (ITR) (D'Costa et al. (2016) “Practical utilization of recombinant AAV vector reference standards: focus on vector genomes titration by free ITR qPCR.” Mol Ther Methods Clin Dev. 5:16019).
В результате были получены хелперные плазмиды AAV для производства векторов капсидных вариантов AAV с высокой эффективностью трансдукции фоторецепторов сетчатки. Наличие специфического генома, кодирующего модифицированный капсид AAV в клетке-мишени (например, колбочковый фоторецептор) через 24 часа после внутривенного введения, указывает на то, что эти частные модификации капсида позволяют преодолеть следующие биологические барьеры:
1. Обход иммунной системы хозяина;
2. Обход системного клиренса;
3. Барьер эндотелиальных клеток кровеносных сосудов и барьер сетчатка-кровь (RBB);
4. Внутри сетчатки: выход из кровеносных сосудов сетчатки и диффузия в ткани сетчатки;
5. Если предполагается поступление из хориоидальных кровеносных сосудов: перенос через мембрану Бруха, барьер пигментных эпителиальных клеток сетчатки и внеклеточный матрикс фоторецепторов и, возможно, через наружную ограничивающую мембрану с окончательным попаданием в клетки фоторецептора. Если входной путь представляет собой наружный сегмент фоторецептора, то необходимо также преодолеть связующую ресничку;
6. Если предполагается поступление из витреальных кровеносных сосудов: перенос через внутреннюю ограничивающую мембрану, слой ганглиозных клеток, внутренний плексиформный слой, внутренний ядерный слой, внешний плексиформный слой с окончательным попаданием в фоторецепторы с их синаптических концов;
7. При попадании в клетку частицы AAV должны пройти через систему эндолизосомальных везикул и, покинув ее, раскрыть и перенести свой геном через ядерную мембрану в клеточное ядро;
8. Тем самым, обнаружение специфических геномов AAV при скрининге в ядрах клеток-мишеней позволяет предположить, что все эти барьеры должны были быть успешно преодолены.
Дополнительно библиотеки были подвергнуты деплеции для связывания гепарина. Это имеет особое значение, поскольку предполагается, что трансдукция клеток сетчатки и, в частности, фоторецепторов обычно требует связывания гепарина. Путем использования гепарин-связывающих деплецированных библиотек, специально отобранных для новых AAV, которые, скорее всего, используют различные механизмы поступления и переноса клеток по сравнению со стандартными AAV и ранее созданными AAV.
Как упомянуто выше, новые капсиды имеют большое значение для всех видов применений, направленных на эффективную трансдукцию клеток сетчатки. Это может быть в живом животном или в культуре ткани эксплантата, или в культуре клеток. Кроме того, это можно использовать для доклинических исследований или для клинических применений, таких как генная терапия в области офтальмологии. Кроме того, виды применения не ограничиваются экспрессией генов, но могут также включать в себя нокдаун генов с использованием технологии siRNA (shRNA) или редактирование генов с помощью, например, нуклеаз, таких как цинковый палец, TALEN или CAS9/CRISPR системы. Наконец, новые AAV также полезны в качестве грузовой системы для других молекул, включая, но не ограничиваясь, ДНК, РНК, пептиды, белки, химические соединения.
Настоящее изобретение относится к аденоассоциированному вирусу (AAV), содержащему вставку по меньшей мере 6-8 аминокислот между позициями, соответствующими позициям 587 и 588 последовательности SEQ ID NO: 1; при этом вставочная последовательность между N-концом и C-концом имеет формулу I:
X1A-X1B-X2-X3-X4-X5-X6-X7 (формула I)
в которой X5 выбрана из P (Pro), L (Leu) и V (Val);
в которой X7 - это R (Arg);
в которой X1A, X1B, X2, X3, X4, X6 независимо являются любой аминокислотой;
в которой X1A и/или X1B независимо необязательно отсутствуют или присутствуют,
или
в которой X5 выбрана из S (Ser) и T (Thr);
в которой X7 - это S (Ser);
в которой X1A, X1B, X2, X3, X4, X6 независимо являются любой аминокислотой;
в которой X1A и/или X1B независимо необязательно отсутствуют или присутствуют,
или
в которой X5 выбрана из A (Ala) и Q (Gln);
в которой X7 - это A (Ala);
в которой X1A, X1B, X2, X3, X4, X6 независимо являются любой аминокислотой;
в которой X1A и/или X1B независимо необязательно отсутствуют или присутствуют,
в которой вирусная ДНК AAV присутствует в ядерных экстрактах сетчатки мыши через 24 часа после внутривенного введения AAV в хвостовую вену мыши линии C57-Bl6J, и
в которой вирусная ДНК AAV присутствует в MAC-сортированных палочках с использованием магнитных микроносителей, покрытых антителами к CD73, и/или FACS-сортированных колбочках, при этом колбочки экспрессируют eGFP и являются FACS-сортированными на основе их экспрессии eGFP, через 24 часа после внутривенного введения AAV в хвостовую вену мыши линии C57-Bl6J для сортировки палочек и в хвостовую вену мыши RG-eGFP линии R685933 для сортировки колбочек.
Аденоассоциированный вирус (AAV) по настоящему изобретению может использоваться для обозначения любого AAV как такового или его части, например, вирусного капсида, вирусного генома и т.п. Термин «AAV» также охватывает все подтипы, как встречающиеся в природе, так и рекомбинантные формы, а также их варианты.
Не имеющие ограничительного характера примеры AAV включают в себя AAV тип 1 (AAV-1), AAV тип 2 (AAV-2), AAV тип 3 (AAV-3), AAV тип 3B (AAV-3B), AAV тип 4 (AAV-4), AAV тип 5 (AAV-5), AAV тип 6 (AAV-6), AAV тип 7 (AAV-7), AAV тип 8 (AAV-8), AAV9, AAV10, AAV11, AAV12, AAV13, rh10, птичий AAV, бычий (крупного рогатого скота) AAV, псовый AAV, лошадиный AAV, приматный AAV, неприматный AAV и овечий AAV. «Приматный AAV» относится к AAV, который инфицирует приматов, «неприматный AAV» относится к AAV, который инфицирует неприматных млекопитающих, «бычий (крупного рогатого скота) AAV» относится к AAV, который инфицирует жвачных млекопитающих и т.д.
В частности, описанные в настоящей заявке эксперименты проводили с модифицированными капсидами AAV2. Однако другие капсиды AAV (из других AAV, описанных в настоящем документе) также переносят пептидные вставки в соответствующие капсидные позиции (Michelfelder et al. (2011) “Peptide ligands incorporated into the threefold spike capsid domain to re-direct gene transduction of AAV8 and AAV9 in vivo” PloS one 6, e23101).
Поэтому пептидные вставки (вставочные последовательности, описанные в настоящей заявке) могут быть перенесены на другие известные капсиды AAV, например, на любой из капсидов любого из AAV, описанных в настоящей заявке, или, например, на AAV8, AAV9, AAV7 или AAV5. Эти AAV могут иметь более высокую эффективность и более широкие профили трансдукции в сетчатке по сравнению с AAV2.
Кроме того, вставки капсидного пептида AAV могут
сочетаться с мутациями капсидного тирозина, треонина и серина (Petrs-Silva et al. (2009) “High-efficiency transduction of the mouse retina by tyrosine-
mutant AAV serotype vectors” Molecular therapy: the journal of the American Society of Gene Therapy 17, 463-471 and Zhong et al. (2008) “Next generation of adeno-associated virus 2 vectors: point mutations in tyrosines lead to high-efficiency transduction at lower doses” Proceedings of the National Academy of Sciences of the United States of America, 105, 7827-7832) для снижения протеасомно-опосредованной деградации и повышения эффективности трансдукции.
AAV может быть AAV2.
Кроме того, AAV может быть природного происхождения (дикий тип AAV), вариантным или рекомбинантным AAV. Под «природным» («природного происхождения») или «диким типом» AAV подразумевается любой аденоассоциированный вирус или его производное, содержащие вирусные белки, такие как вирусный капсид, который состоит из вирусных (капсидных) белков, встречающихся в природе. Таким образом, AAV по настоящему изобретению может быть природного происхождения, содержащим только вставочную последовательность, как описано в настоящей заявке, между позициями, соответствующими позициям 587 и 588 SEQ ID NO: 1.
Под «вариантом AAV» или «вариантным AAV» подразумевается включение вирусной частицы AAV, содержащей вариант или мутант белка AAV, такого как мутантный белок AAV. Примеры вариантных белков AAV включают белки AAV, содержащие по меньшей мере одно отличие аминокислот (например, замещение аминокислоты, вставка аминокислоты, делеция аминокислоты) от соответствующего родительского белка AAV, т. е. белка AAV, из которого он был получен, белка AAV дикого типа и т.д., при этом вариантный белок AAV не состоит из аминокислотной последовательности, присутствующей в природном AAV. Например, такие вариантные AAV могут содержать мутацию в капсидном белке VP3 в дополнение к вставочной последовательности по настоящему изобретению.
Помимо структурного отличия, т.е. на уровне последовательности, от соответствующего родительского AAV, вариантный AAV может отличаться от соответствующего родительского AAV функционально. Иными словами, вариантный капсидный белок, содержащий по меньшей мере одно аминокислотное отличие от соответствующего родительского капсидного белка AAV, может придавать вариантному AAV функциональные характеристики, которыми не обладает соответствующий родительский AAV. Например, вариант AAV может отличаться клеточным тропизмом, т.е. аффинностью и/или способностью заражать определенный тип клеток, например, вариант AAV может связываться с клеткой, например, с клеткой сетчатки, с более высокой (или более низкой) аффинностью, чем родительский AAV, и/или заражать/трансфицировать клетку, например, клетку сетчатки, с более высокой (или более низкой) эффективностью, чем родительский AAV, так что одним и тем же титром вирусных частиц трансфицируется/инфицируется больше (или меньше) клеток клеточной популяции. В качестве второго примера вариант AAV может иметь большую (или меньшую) аффинность к антителам, вырабатываемым животным-хозяином, например, вариант AAV может связываться с большей (или меньшей) аффинностью с нейтрализующими антителами и выводиться из питающих тканей в большей (или меньшей) степени. Таким образом, AAV по настоящему изобретению может быть мутантным (вариантным) AAV, содержащим вставочную последовательность, как описано в настоящей заявке, между позициями, соответствующими позициям 587 и 588 SEQ ID NO: 1.
Под «рекомбинантным AAV» или «rAAV» подразумевается включение любого AAV, который содержит гетерологичную полинуклеотидную последовательность в своем вирусном геноме. В общем случае гетерологичный полинуклеотид фланкирован по меньшей мере одной и, как правило, двумя инвертированными концевыми повторами (ITR) природного или вариантного AAV. Термин «вектор rAAV» включает в себя как частицы векторов rAAV, так и плазмиды векторов rAAV. Вирусным вектором, как описано в настоящей заявке, также является rAAV. Так, например, rAAV, который включает в себя гетерологичные полинуклеотидные последовательности, может быть rAAV, который включает нуклеотидные последовательности, как правило, не включенные в AAV дикого типа, например, трансген (например, кодирующие РНК полинуклеотидные последовательности, не относящиеся к AAV, белок-кодирующие полинуклеотидные последовательности, не относящиеся к AAV), промоторную последовательность, не относящуюся к AAV, поли-аденилированную последовательность, не относящуюся к AAV, и т.д.
Такие рекомбинантные векторы AAV известны из области техники, и специалисту в области техники также известен способ создания таких рекомбинантных AAV.
«Векторный геном rAAV» или «геном rAAV» - это геном AAV (т.е. вДНК), который содержит одну или несколько гетерологичных нуклеотидных последовательностей. Векторы rAAV обычно могут требовать только концевых повторов (TR) для генерации вируса. Все остальные вирусные последовательности считаются расходными и могут поступать при переносе (Muzyczka, (1992) Curr Topics Microbiol. Immunol. 158:97). Как правило, векторный геном rAAV сохраняет только одну или несколько последовательностей TR, чтобы максимизировать размер трансгена, который может быть эффективно упакован вектором/капсидом. Структурные и неструктурные кодирующие белок последовательности могут быть получены при переносе (например, из вектора, такого как плазмида, или путем стабильной интеграции последовательностей в упаковочную клетку). В вариантах осуществления изобретения векторный геном rAAV содержит по меньшей мере одну последовательность TR (например, последовательность TR AAV), необязательно две TR (например, две TR AAV), которые обычно находятся на 5' и 3' концах векторного генома и фланкируют гетерологичную нуклеиновую кислоту, но не обязательно должны быть смежными с ней. TR могут быть одинаковыми или отличаться друг от друга.
Термин «концевой повтор» или «TR» включает в себя любой вирусный концевой повтор или синтетическую последовательность, которая образует шпилечную структуру и функционирует как инвертированный концевой повтор (т.е. опосредует желаемые функции, такие как репликация, упаковка вируса, интеграция и/или восстановление провируса и т.п.). TR может быть TR AAV или TR не-AAV. Например, последовательность TR не-AAV, такая как последовательность других парвовирусов (например, псовый парвовирус (CPV), мышиный парвовирус (MVM), человеческий парвовирус B-19) или любая другая подходящая вирусная последовательность (например, шпилечная SV40, которая служит источником репликации SV40), может быть использована в качестве TR, которая может быть дополнительно модифицирована путем усечения, замены, делеции, вставки и/или добавления. Кроме того, TR может быть частично или полностью синтетическим, таким как «двойная последовательность D», как описано в патенте США № 5,478,745, Samulski et al.
«Концевой повтор AAV» или «TR AAV» может быть из любого AAV включая без ограничения серотипы 1, 2, 3, 3B, 4, 5, 6, 7, 8, 9, 10, 11, 12 или 13 или любой другой AAV, известный сейчас или ставший известным позднее. Концевой повтор AAV не должен иметь нативную последовательность концевых повторов (например, нативная последовательность TR AAV может быть изменена путем вставки, делеции, усечения и/или миссенс-мутаций), если концевой повтор опосредует желаемые функции, например, репликацию, упаковку вируса, интеграцию и/или восстановление провируса и т.п. Вирусные векторы по изобретению могут дополнительно быть «направленными» вирусными векторами (например, имеющими направленный тропизм) и/или «гибридным» парвовирусом (т.е. в котором вирусные TR и вирусный капсид происходят от разных парвовирусов), как описано в международной публикации WO 00/28004 и у Chao et al., (2000) Molecular Therapy 2:619.
Также под термином «рекомбинантный AAV» понимаются AAV, которые включают в себя, например, только капсид AAV и несут внутри капсида неполинуклеотидный груз, такой как белок, полипептид или другая молекула, в дополнение к его геному или вместо его генома. Например, капсид может содержать нуклеиновую кислоту, которая гетерологична геному, связанному с AAV. Также предполагается, что капсид нес нуклеиновую кислоту, которая является гетерологичной (нуклеиновая кислота, не относящаяся к AAV). Способ производства таких рекомбинантных AAV, описан, например, в US9610354B2 или WO1996000587 A1.
Капсидный белок по настоящему изобретению относится к капсидному белку AAV. Как правило, капсид AAV состоит из 60 капсидных белковых субъединиц VP1, VP2 и VP3, которые расположены в икосаэдрической симметрии обычно в соотношении 1:1:10 или 1:1:20. Сообщалось, что VP2 и VP3 имеют решающее значение для правильной сборки вириона. Однако недавно было показано, что VP2 не требуется для полного образования вирусных частиц и эффективной инфекционности, а также показано, что VP2 может переносить большие вставки на своем N-конце, в то время как VP1 не может, вероятно, из-за присутствия домена PLA2. Примечательно, что N-конец VP1 секвестирован внутри зрелого капсида. Он может содержать фосфолипаза А2-подобную область и гипотетические клеточные сигналы внутриядерной локализации. Таким образом, капсидный белок может содержать капсидный белок VP1 по настоящему изобретению и дополнительно один или оба капсидных белка VP2 и/или VP3 AAV.
Последовательности для капсидного белка VP1, VP2 и VP3 известны специалисту в области техники. Также предусмотрены варианты любого из VP1, VP2 и VP3, при условии, что они еще способны собирать капсид (см. также таблицу 1 в настоящем документе, в которой приводятся некоторые последовательности). Методы анализа способности сборки капсида также известны специалисту в области техники и, например, описаны в Sonntag et al. (2011) “The Assembly-Activating Protein Promotes Capsid Assembly of Different Adeno-Associated Virus Serotypes” J Virol. 85(23): 12686-12697.
«Вариант» капсидного белка по настоящему изобретению включает капсидный белок, содержащий мутацию. Мутация может присутствовать в отношении любой последовательности капсида. Например, мутация может присутствовать в отношении любой из последовательностей, указанных в таблице 1, если она приводит к мутации капсидного белка. Такие мутации могут включать одну или несколько точечных мутаций, таких как 1, 2, 5, 10, 15, 20, 50 или больше точечных мутаций. Вариант может также содержать вставки (добавление одного или нескольких нуклеотидов к ДНК/РНК или добавление одной или нескольких аминокислот в определенный капсидный белок, такой как VP1, VP2 и/или VP3), такие как 1, 2, 3, 5, 6 или больше вставок. Как точечные мутации, так и вставки могут быть выбраны в соответствии с общими правилами, известными из уровня техники, которые не могут оказывать влияния на активность аминокислотной последовательности по сравнению, например, с аминокислотной последовательностью SEQ ID NO: 1.
Вариант может также включать делецию основания нуклеиновой кислоты или аминокислоты, приводящую к образованию капсидного белка с уменьшенным количеством аминокислот. Таким образом, полипептид может содержать делецию 1, 2, 3, 4, 5, 10, 20, 30 или больше аминокислотных остатков по сравнению с его последовательностью дикого типа, например, любой из последовательностей, как показано в таблице 1. Настоящее изобретение также охватывает делеции более чем 1, 2, 3, 4, 10, 20, 30, 40, 50, 60, 70, 80, 90, 100, 200, 300 или более оснований нуклеиновой кислоты по сравнению с молекулой нуклеиновой кислоты, показанной в таблице 1. Однако этот вариант может по-прежнему обладать теми же функциональными свойствами, что и любой из полипептидов или молекул нуклеиновых кислот, изображенных в таблице 1.
Учитывая, что описанные в настоящей заявке варианты капсидных белков (полипептиды, молекулы нуклеиновых кислот) также охвачены настоящим изобретением, настоящее изобретение также охватывает капсидные последовательности нуклеиновых кислот или полипептидные последовательности, которые имеют идентичность последовательности: 80 %, 85 %, 90 %, 95 %, 97 %, 99 % или 100 % с любым из полипептидов/молекул нуклеиновых кислот, указанных в таблице 1.
Так, рекомбинантный AAV, несущий полипептид, белок или молекулу, может содержать капсидные белки VP1, VP3 и/или VP2 в качестве единственных белков AAV, присутствующих в этом векторе.
Таким образом, AAV по настоящему изобретению может быть рекомбинантным AAV, содержащим вставочную последовательность, как описано в настоящей заявке, между позициями, соответствующими позициям 587 и 588 SEQ ID NO: 1.
Также предполагается, что AAV включает в себя или имеет последовательность, имеющую идентичность последовательности по меньшей мере 70 %, 75 %, 80 %, 85 %, 90 %, 95 %, 97 %, 99 % или 100 % с естественным AAV типа 1 (AAV-1), AAV типа 2 (AAV-2), AAV типа 3 (AAV-3), AAV3B, AAV типа 4 (AAV-4), AAV типа 5 (AAV-5), AAV типа 6 (AAV-6), AAV типа 7 (AAV-7), AAV типа 8 (AAV-8), AAV9, AAV10, AAV11, AAV12, rh10, птичьим AAV, бычьим (крупного рогатого скота) AAV, псовым AAV, лошадиным AAV, приматным AAV, неприматным AAV и овечьим AAV. Также предполагается, что АВ имеет идентичность последовательности по меньшей мере 70 %, 75 %, 80 %, 85 %, 90 %, 95 %, 97 %, 99 % или 100 % с последовательностями, указанными в таблице 1.
Термин «полипептид» в контексте настоящей заявки означает пептид, белок или полипептид, который используется взаимозаменяемым и который охватывает аминокислотные цепи заданной длины, в которых аминокислотные остатки связаны ковалентными пептидными связями. Полипептиды могут содержать аминокислоты из числа 20 кодируемых генами аминокислот. Они известны специалистам в данной области техники. Также сюда входят аминокислоты, отличные от 20 кодируемых генами аминокислот, а именно не встречающиеся в природе аминокислоты. Примеры таких не встречающихся в природе аминокислот включают D-аминокислоты, гомо-аминокислоты, N-метил аминокислоты, альфа-метил аминокислоты, бета (гомо)-аминокислоты, гамма-аминокислоты, спираль/поворот стабилизирующие мотивы, модификации остова (например, пептоиды). Также предусмотрены необычные аминокислоты, которые встречаются в природе и известны специалистам в данной области техники. Примеры включают селеноцистеин, гидроксипролин (Hyp), бета-аланин, цитруллин (Cit), орнитин (Orn), норлейцин (Nle), 3-нитротирозин, нитроаргинин, пироглутаминовую кислоту (Pyr). Таким образом, термин «полипептид» может также включать аминокислотные последовательности, содержащие аминокислоту не из числа 20 кодируемых генами аминокислот. Он может, например, содержать одну или несколько необычных аминокислот, встречающихся в природе, и/или одну или несколько аминокислот, не встречающихся в природе.
Термин «полипептид» также относится к модификациям полипептида и не исключает их. Такие модификации известны специалистам в области техники и, например, перечислены в WO 2010/093784.
Что касается термина «молекула нуклеиновой кислоты», то в контексте настоящего изобретения он охватывает любую молекулу нуклеиновой кислоты, имеющую нуклеотидную последовательность оснований, включающих в себя пуриновые и пиримидиновые основания, которые входят в состав указанной молекулы нуклеиновой кислоты, причем указанные основания представляют собой первичную структуру молекулы нуклеиновой кислоты. Последовательности нуклеиновых кислот могут включать ДНК, кДНК, геномную ДНК, РНК, как кодирующие, так и антисмысловые нити. Полинуклеотид по настоящему изобретению может быть составлен из любого полирибонуклеотида или полидеоксрибонуклеотида, который может быть немодифицированной РНК или ДНК, или модифицированной РНК, или ДНК.
ДНК и РНК могут быть подвергнуты различным модификациям; таким образом, термин «молекулы нуклеиновых кислот» может охватывать химически, ферментативно или метаболически модифицированные формы. «Модифицированные» основания включают, например, тритилированные основания и необычные основания, такие как инозин.
В соответствии с настоящим изобретением термин «идентичная» или «процентная идентичность» в контексте двух или более молекул нуклеиновых кислот или аминокислотных последовательностей относится к двум или более последовательностям или подпоследовательностям, которые являются одинаковыми или которые имеют определенный процент аминокислотных остатков или нуклеотидов, которые являются одинаковыми (например, по меньшей мере 95 %, 96 %, 97 %, 98 % или 99 % идентичность), при сравнении и выравнивании для максимального соответствия над окном сравнения или над обозначенной областью, измеренной с помощью алгоритма сравнения последовательностей, известного из уровня техники, или путем ручного выравнивания и визуального контроля. Последовательности, имеющие, например, от 80 % до 95 % или более идентичность последовательности, считаются по существу идентичными. Такое определение также применимо к комплементу тестовой последовательности. Специалистам в данной области техники известен способ определения процентной идентичности последовательностей с использованием, например, алгоритмов, основанных на компьютерной программе CLUSTALW (Thompson Nucl. Acids Res. 2 (1994), 4673-4680) или FASTDB (Brutlag Comp. App. Biosci. 6 (1990), 237-245), как известно из уровня техники.
Специалистам в области техники также доступны алгоритмы BLAST и BLAST 2.0 (Altschul Nucl. Acids Res. 25 (1977), 3389-3402). Программа BLASTN для последовательностей нуклеиновых кислот использует по умолчанию размер слова (W) 28, порог ожидания (E) 10, оценку соответствия/несоответствия 1, -2, линейную зависимость цены делеции в последующих итерациях и сравнение обеих нитей. Для аминокислотных последовательностей программа BLASTP использует по умолчанию размер слова (W) 6 и порог ожидания (E) 10, цены делеции в последующих итерациях Existence: 11 и Extension: 1. Кроме того, может быть использована матрица замен BLOSUM62 (Henikoff Proc. Natl. Acad. Sci., USA, 89, (1989), 10915).
Например, можно использовать BLAST2. 0, что расшифровывается как «Basic Local Alignment Search Tool» (средство поиска основного локального выравнивания) (Altschul, Nucl. Acids Res. 25 (1997), 3389-3402; Altschul, J. Mol. Evol. 36 (1993), 290-300; Altschul, J. Mol. Biol. 215 (1990), 403-410), для поиска локальных выравниваний последовательностей.
AAV по настоящему изобретению имеют вставку по меньшей мере 6-8 аминокислот между позициями, соответствующими позициям 587 и 588 SEQ ID NO: 1. Вставочная последовательность может содержать 6 аминокислот. Вставочная последовательность может также содержать 7 аминокислот. Вставочная последовательность может содержать 8 аминокислот. Таким образом, предусматривается также AAV, содержащий вставочную последовательность, как описано в настоящей заявке, в котором отсутствует X1A и присутствует X1B или в котором отсутствует X1B и присутствует X1A.
Вставочная последовательность между N-концом и C-концом имеет формулу I: X1A-X1B-X2-X3-X4-X5-X6-X7 (формула I). В этой формуле Х5 может быть выбрана из P (Pro), L (Leu) и V (Val), при этом X7 может быть R (Arg); X1A, X1B, X2, X3, X4, X6 могут независимо быть любой аминокислотой и X1A и/или X1B могут независимо необязательно отсутствовать или присутствовать, при этом вирусная ДНК AAV необязательно присутствует в ядерных экстрактах сетчатки мыши через 24 часа после введения AAV в хвостовую вену мыши C57-Bl6J.
Таким образом, настоящее изобретение также относится к аденоассоциированному вирусу (AAV), содержащему
вставку по меньшей мере 6-8 аминокислот между позициями, соответствующими позициям 587 и 588 последовательности SEQ ID NO: 1 (вставочная последовательность), причем вставочная последовательность между N-концом и C-концом имеет формулу I:
X1A-X1B-X2-X3-X4-X5-X6-X7 (формула I),
в которой X5 выбрана из P (Pro), L (Leu) и V (Val);
в которой X7 - это R (Arg);
в которой X1A, X1B, X2, X3, X4, X6 независимо являются любой аминокислотой;
в которой X1A и/или X1B независимо необязательно отсутствуют или присутствуют, причем вирусная ДНК AAV необязательно присутствует в ядерных экстрактах сетчатки мыши через 24 после внутривенного введения AAV в хвостовую вену мыши линии C57-Bl6J.
Аналогичным образом настоящее изобретение относится к капсидному белку VP1 аденоассоциированного вируса (AAV), при этом VP1 AAV содержит вставку по меньшей мере 6-8 аминокислот между позициями, соответствующими позициям 587 и 588 последовательности SEQ ID NO: 1 (вставочная последовательность), причем вставочная последовательность между N-концом и C-концом имеет формулу I:
X1A-X1B-X2-X3-X4-X5-X6-X7 (формула I),
в которой X5 выбрана из P (Pro), L (Leu) и V (Val);
в которой X7 - это R (Arg);
в которой X1A, X1B, X2, X3, X4, X6 независимо являются любой аминокислотой;
в которой X1A и/или X1B независимо необязательно отсутствуют или присутствуют.
В частности, в AAV или в VP1 AAV капсидном белке X5 может быть P (Pro). Альтернативно X5 может быть L (Leu). Альтернативно X5 может быть V (Val). Дополнительно или в качестве альтернативы X1A и/или X1B могут быть выбраны из G, S, N, V и P, предпочтительно X1A и/или X1B является N. Дополнительно или в качестве альтернативы X2 может быть выбрана из L, S и N, предпочтительно X2 может быть S. Дополнительно или в качестве альтернативы X3 может быть выбрана из S, P, T, Q. X3 может быть выбрана из S и P. Дополнительно или в качестве альтернативы X4 может быть выбрана из P, G, S, A и T, предпочтительно X4 может быть S. Дополнительно или в качестве альтернативы X6 может быть выбрана из T, P, N, Q и S, предпочтительно X6 может быть P. Таким образом, AAV или капсидный белок VP1 AAV по настоящему изобретению может включать в себя вставочную последовательность GLSPPTR (SEQ ID NO. 10), SSPGLPR (SEQ ID NO. 11), NSTSVNR (SEQ ID NO. 12), VSSSLQR (SEQ ID NO. 13), PNQAPPR (SEQ ID NO. 14) или NNPTPSR (SEQ ID NO: 15), как описано в настоящей заявке.
Альтернативно в формуле I X5 может быть выбрана из S (Ser) и T (Thr); X7 может быть S (Ser); X1A, X1B, X2, X3, X4, X6 могут независимо быть любой аминокислотой и X1A и/или X1B могут независимо необязательно отсутствовать или присутствовать.
Таким образом, настоящее изобретение также относится к аденоассоциированному вирусу (AAV), содержащему
вставку по меньшей мере 6-8 аминокислот между позициями, соответствующими позициям 587 и 588 последовательности SEQ ID NO: 1; при этом вставочная последовательность между N-концом и C-концом имеет формулу I:
X1A-X1B-X2-X3-X4-X5-X6-X7 (формула I),
в которой X5 выбрана из S (Ser) и T (Thr);
в которой X7 - это S (Ser);
в которой X1A, X1B, X2, X3, X4, X6 независимо являются любой аминокислотой;
в которой X1A и/или X1B независимо необязательно отсутствуют или присутствуют, причем вирусная ДНК AAV необязательно присутствует в ядерных экстрактах сетчатки мыши через 24 после внутривенного введения AAV в хвостовую вену мыши линии C57-Bl6J.
Аналогичным образом настоящее изобретение также относится к капсидному белку VP1 аденоассоциированного вируса (AAV), при этом VP1 AAV содержит
вставку по меньшей мере 6-8 аминокислот между позициями, соответствующими позициям 587 и 588 последовательности SEQ ID NO: 1; при этом вставочная последовательность между N-концом и C-концом имеет формулу I:
X1A-X1B-X2-X3-X4-X5-X6-X7 (формула I),
в которой X5 выбрана из S (Ser) и T (Thr);
в которой X7 - это S (Ser);
в которой X1A, X1B, X2, X3, X4, X6 независимо являются любой аминокислотой;
в которой X1A и/или X1B независимо необязательно отсутствуют или присутствуют.
В частности, в AAV или в VP1 AAV капсидном белке X5 может быть S (Ser). Альтернативно X5 может быть T (Thr). Дополнительно или в качестве альтернативы X1A и/или X1B может быть выбрана из G, R, H и S. Дополнительно или в качестве альтернативы X2 может быть выбрана из A, S и Q, предпочтительно, X2 может быть A. Дополнительно или в качестве альтернативы X3 может быть выбрана из H, N и A, предпочтительно X3 может быть N. Дополнительно или в качестве альтернативы X4 может быть выбрана из R, Q и D, предпочтительно X4 может быть R. Дополнительно или в качестве альтернативы X6 может быть выбрана из R, S и D, предпочтительно X6 может быть D.
Таким образом, AAV или капсидный белок VP1 AAV по настоящему изобретению может также включать в себя последовательность вставки GAHRSDS (SEQ ID NO. 16), RANQTSS (SEQ ID NO. 17), HSARTDS (SEQ ID NO. 18) или SQNDSRS (SEQ ID NO. 19).
Альтернативно в формуле I X5 может быть выбрана из A (Ala) и Q (Gln); X7 может быть A (Ala); X1A, X1B, X2, X3, X4, X6 могут независимо быть любой аминокислотой и X1A и/или X1B могут независимо необязательно отсутствовать или присутствовать.
Таким образом, настоящее изобретение также относится к аденоассоциированному вирусу (AAV), содержащему
вставку по меньшей мере 6-8 аминокислот между позициями, соответствующими позициям 587 и 588 последовательности SEQ ID NO: 1; при этом вставочная последовательность между N-концом и C-концом имеет формулу I:
X1A-X1B-X2-X3-X4-X5-X6-X7 (формула I),
в которой X5 выбрана из A (Ala) и Q (Gln);
в которой X7 - это A (Ala);
в которой X1A, X1B, X2, X3, X4, X6 независимо являются любой аминокислотой;
в которой X1A и/или X1B независимо необязательно отсутствуют или присутствуют, причем вирусная ДНК AAV необязательно присутствует в ядерных экстрактах сетчатки мыши через 24 после внутривенного введения AAV в хвостовую вену мыши линии C57-Bl6J.
Аналогичным образом настоящее изобретение также относится к капсидному белку VP1 аденоассоциированного вируса (AAV), при этом VP1 AAV содержит
вставку по меньшей мере 6-8 аминокислот между позициями, соответствующими позициям 587 и 588 последовательности SEQ ID NO: 1; при этом вставочная последовательность между N-концом и C-концом имеет формулу I:
X1A-X1B-X2-X3-X4-X5-X6-X7 (формула I),
в которой X5 выбрана из A (Ala) и Q (Gln);
в которой X7 - это A (Ala);
в которой X1A, X1B, X2, X3, X4, X6 независимо являются любой аминокислотой;
в которой X1A и/или X1B независимо необязательно отсутствуют или присутствуют.
В частности, в AAV или в VP1 AAV капсидном белке X5 может быть A (Ala). Альтернативно X5 может быть Q (Gln). Дополнительно или в качестве альтернативы X1A и/или X1B может быть выбрана из N и R. Дополнительно или в качестве альтернативы X2 может быть выбрана из S и G. Дополнительно или в качестве альтернативы X3 может быть выбрана из R и S. Дополнительно или в качестве альтернативы X4 может быть выбрана из P и L. Дополнительно или в качестве альтернативы X6 может быть выбрана из A и N.
Таким образом, AAV или капсидный белок VP1 AAV по настоящему изобретению может также включать в себя последовательность вставки NSRPAAA (SEQ ID NO. 20) или RGSLQNA (SEQ ID NO. 21).
Вставка по меньшей мере 6-8 аминокислот присутствует между позициями, соответствующими позициям 587 и 588 SEQ ID NO: 1. Термин «позиция» в контексте настоящего изобретения означает положение любой аминокислоты в аминокислотной последовательности SEQ ID NO. 1. Примечательно, что SEQ ID NO. 1 соответствует белку VP1 капсида AAV2.
Термин «соответствующий» в контексте настоящего изобретения также предусматривает, что позиция определяется не только числом предшествующих нуклеотидов/аминокислот. Позиция данного нуклеотида в соответствии с настоящим изобретением, который может быть замещен, может меняться вследствие делеций или дополнительных нуклеотидов в другом месте в капсидном белке VP1 AAV (мутантном, рекомбинантном или дикого типе), включая промотор и/или любые другие регуляторные последовательности или ген (включая экзоны и интроны). Аналогичным образом позиция данной аминокислоты в соответствии с настоящим изобретением, которая может быть замещена, может меняться вследствие делеции или добавлении аминокислот в другом месте в капсидном белке VP1 AAV (мутантном или дикого типа).
Таким образом, под «соответствующей позицией» в соответствии с настоящим изобретением предпочтительно понимать, что аминокислоты могут отличаться по указанному числу, но все же могут иметь сходные соседние нуклеотиды/аминокислоты. Термин «соответствующая позиция» также включает в себя упомянутые аминокислоты, которые могут быть замещены, удалены или добавлены. В частности, специалист в области техники может при выравнивании эталонной последовательности SEQ ID No: 1 с представляющей интерес аминокислотной последовательностью, например, проверить представляющую интерес последовательность на наличие мотива GNRQ (позиции 586-589 SEQ ID NO. 1; SEQ ID NO. 22) при поиске положения аминокислоты, указанного в настоящей заявке (т.е. позиции, соответствующей позиции 587 и 588 аминокислотной последовательности, показанной в SEQ ID No: 1).
Для того чтобы определить, соответствует ли аминокислотный остаток в данной аминокислотной последовательности (мутантной или дикого типа) определенному положению в аминокислотной последовательности SEQ ID No: 1, специалист в данной области техники может использовать средства и методы, хорошо известные из уровня техники, например, выравнивания, либо вручную, либо с помощью компьютерных программ, таких как BLAST2.0, что расшифровывается как «Basic Local Alignment Search Tool» (средство поиска основного локального выравнивания) или ClustalW, либо любой другой подходящей программы для генерации линейных последовательностей.
Также предполагается, что вставочная последовательность фланкирована одной или несколькими гибкими аминокислотами на одном или обоих концах вставочной последовательности. Гибкие аминокислоты позволяют соседним белковым доменам свободно перемещаться относительно друг друга. Под выражением «гибкая аминокислота» следует понимать любую гибкую аминокислоту. Специалисту в данной области техники известно, какие аминокислоты являются гибкими, а какие - менее гибкими.
«Гибкая аминокислота» в контексте настоящего изобретения может быть выбрана из A (Ala), L (Leu), G (Gly), S (Ser) и T (Thr). Гибкая аминокислота также может быть выбрана из G (Gly), S (Ser) и A (Ala). Гибкой аминокислотой также может быть Ala.
Вставочная последовательность может быть фланкирована на одном или обоих концах любым количеством гибких аминокислот. Например, вставочная последовательность может быть фланкирована на одном или обоих концах 1, 2, 3, 4, 5, 6, 7, 8, 9 или более гибкими аминокислотами.
Также включены капсидные белки AAV или VP1 AAV по настоящему изобретению, в которых вставочная последовательность между N-концом и C-концом имеет формулу II:
L3-L2-L1-X1A-X1B-X2-X3-X4-X5-X6-X7-L4-L5-L6 (формула II)
в которой L1, L2, L3, L4, L5 и L6 независимо является гибкой аминокислотой и
в которой L1, L2, L3, L4, L5 и L6 независимо необязательно отсутствует или присутствует.
Также предполагается, что дополнительно L1, L2, L3, L4, L5 и L6 независимо выбраны из A (Ala), L (Leu), G (Gly), S (Ser) и T (Thr). Кроме того, предполагается, что во вставочной последовательности, описанной в настоящей заявке, одна из X1A и X1B присутствует, а другая из X1A и X1B отсутствует, и что в формуле (II) присутствуют все из L1, L2, L3, L4 и L5, а при этом L6 отсутствует.
Таким образом, вставочная последовательность, включающая в себя гибкие аминокислоты, может иметь длину от 7 до 14 аминокислот. Так, вставочная последовательность, включающая гибкие аминокислоты, может иметь длину 7, 8, 9, 10, 11, 12, 13, или 14 аминокислот. Однако в присутствии более гибких аминокислот вставочная последовательность, включающая гибкие аминокислоты, может также иметь длину 15, 16, 17, 18, 19, 20 или более аминокислот.
Также предполагается, что AAV или капсидный белок VP1 AAV по настоящему изобретению содержит вставочную последовательность, описанную в настоящей заявке, в которой X1A, и/или X1B, и/или X2 и/или X3 является/являются кислой аминокислотой. Дополнительно или в качестве альтернативы вставочная последовательность, описанная в настоящей заявке, не содержит аминокислоту E (глутамат).
«Кислая аминокислота» в контексте настоящего изобретения относится к аминокислотам D (Asp) и E (глутамат).
Дополнительно или в качестве альтернативы вставочная последовательность, описанная в настоящей заявке, может содержать 1, 2, 3 или 4 кислые аминокислоты. Например, вставочная последовательность может содержать одну кислую аминокислоту. Аминокислотой может быть D (Asp).
Кроме того, предполагается, что AAV или капсидный белок VP1 AAV по настоящему изобретению содержит вставочную последовательность, описанную в настоящей заявке, в которой одна из X1A и X1B присутствует, а другая из X1A и X1B отсутствует и в которой X2 не является основной или кислой аминокислотой.
В контексте настоящего изобретения «основная аминокислота» - это любая из K (Lys), R (Arg) и H (His).
Также предполагается, что AAV или капсидный белок VP1 AAV по настоящему изобретению содержит вставочную последовательность, описанную в настоящей заявке, которая не содержит K (Lys) или H (His) в любой позиции. Также предполагается, что вставочная последовательность содержит R (Arg) в качестве единственной основной аминокислоты. Кроме того, вставочная последовательность может содержать D (Asp) в качестве единственной кислой аминокислоты.
Также предполагается, что AAV или капсидный белок VP1 AAV по настоящему изобретению содержит вставочную последовательность, описанную в настоящей заявке, в которой X1A, и/или X1B, и/или X2, и/или X3, и/или X4 , и/или X6 не является гидрофобной ароматической аминокислотой.
«Гидрофобная аминокислота» в контексте настоящего изобретения является аминокислотой, выбранной из F (Phe), W (Trp) или Y (Tyr).
Также предполагается, что AAV или капсидный белок VP1 AAV по настоящему изобретению содержит вставочную последовательность, описанную в настоящей заявке, которая не содержит гидрофобной аминокислоты.
Кроме того, предполагается, что AAV или капсидный белок VP1 AAV по настоящему изобретению содержит вставочную последовательность, описанную в настоящей заявке, которая не содержит ни одну из аминокислот F (Phe), W (Trp), Y (Tyr), K (Lys), E (Glu), C (Cys), M (Met), I (Ile) и H (His).
Кроме того, предполагается, что AAV или капсидный белок VP1 AAV по настоящему изобретению содержит вставочную последовательность, описанную в настоящей заявке, в которой X1A или X1B - это специальная аминокислота, гидрофобная алифатическая аминокислота или полярная аминокислота с незаряженной боковой группой.
«Специальная аминокислота» в контексте настоящего изобретения включает в себя C (Cys), G (Gly) и P (Pro).
«Гидрофобная алифатическая аминокислота» в контексте настоящего изобретения включает в себя A (Ala), L (Leu), V (Val) и I (Ile).
«Полярная аминокислота с незаряженной боковой группой» в контексте настоящего изобретения включает в себя S (Ser), T (Thr), N (Asn) и Q (Gln).
Так, во вставочной последовательности, описанной в настоящей заявке, X1A и/или X1B могут быть выбраны из A, L, V, I, S, T, N, Q, C, P и G. Во вставочной последовательности, описанной в настоящей заявке, X1A и/или X1B также могут быть выбраны из G, P и N. Во вставочной последовательности, описанной в настоящей заявке, X1A и/или X1B также могут быть выбраны из G, N, S и A.
Во вставочной последовательности, описанной в настоящей заявке, X1A и/или X1B также могут быть любой аминокислотой, помимо L, K, D, E, I, C, M, F, W, Y. Во вставочной последовательности, описанной в настоящей заявке, X1A и/или X1B также могут быть любой аминокислотой.
Дополнительно или в качестве альтернативы AAV или капсидный белок VP1 AAV по настоящему изобретению содержит вставочную последовательность, описанную в настоящей заявке, в которой X2 может быть гидрофобной алифатической аминокислотой или полярной аминокислотой с незаряженной боковой группой. Так, во вставочной последовательности, описанной в настоящей заявке, X2 может быть выбрана из S, T, N, Q, A, L, V и I. X2 может быть также выбрана из N и L. Во вставочной последовательности, описанной в настоящей заявке, X2 может быть также выбрана из L, N, S и A. X2 также может быть любой аминокислотой. Во вставочной последовательности, описанной в настоящей заявке, X2 также может быть любой аминокислотой, помимо D, E, I, C, M, F, W и Y.
Дополнительно или в качестве альтернативы AAV или капсидный белок VP1 AAV по настоящему изобретению содержит вставочную последовательность, описанную в настоящей заявке, в которой X3 может быть выбрана из гидрофобной алифатической аминокислоты или специальной аминокислоты, или полярной аминокислоты с незаряженной боковой группой. Так, во вставочной последовательности, описанной в настоящей заявке, X3 может быть выбрана из A, L, V, I, S, T, N, Q, C, G и P. Во вставочной последовательности, описанной в настоящей заявке, X3 может быть также выбрана из S, Q и P. Во вставочной последовательности, описанной в настоящей заявке, X3 может быть также выбрана из P, S, G и A. X3 может быть также P. Во вставочной последовательности, описанной в настоящей заявке, X3 может быть также любой аминокислотой. Во вставочной последовательности, описанной в настоящей заявке, X3 может быть также любой аминокислотой, помимо L, E, I, C, M, F, W и Y.
Дополнительно или в качестве альтернативы AAV или капсидный белок VP1 AAV по настоящему изобретению содержит вставочную последовательность, описанную в настоящей заявке, в которой X4 может быть гидрофобной алифатической аминокислотой или основной или кислой аминокислотой, или специальной аминокислотой, или полярной аминокислотой с незаряженной боковой группой. Так, во вставочной последовательности, описанной в настоящей заявке, X4 может быть выбрана из K, R, H, D, E, S, T, N, Q, A, V, I, L, C, G и P. Во вставочной последовательности, описанной в настоящей заявке, X4 может быть также выбрана из P, A и T. Во вставочной последовательности, описанной в настоящей заявке, X4 может быть также выбрана из P, T, S и G. Во вставочной последовательности, описанной в настоящей заявке, X4 может быть выбрана из P или T. Во вставочной последовательности, описанной в настоящей заявке, X4 может быть P. X4 может быть T. Во вставочной последовательности, описанной в настоящей заявке, X4 может быть также любой аминокислотой, помимо L, E, I, C, M, F, W и Y.
Дополнительно или в качестве альтернативы AAV или капсидный белок VP1 AAV по настоящему изобретению содержит вставочную последовательность, описанную в настоящей заявке, в которой X6 может быть кислой аминокислотой, основной аминокислотой, полярной аминокислотой с незаряженной боковой группой или специальной аминокислотой. Так, во вставочной последовательности, описанной в настоящей заявке, X6 может быть выбрана из K, R, H, D, E, S, T, N, Q, A, C, G и P. Во вставочной последовательности, описанной в настоящей заявке, X6 может быть также выбрана из T, P и S. X6 может быть также выбрана из S, T, P и A. Во вставочной последовательности, описанной в настоящей заявке, X6 может быть также выбрана из S, T, P и A. X6 может быть также выбрана из S или T. Во вставочной последовательности, описанной в настоящей заявке, X6 может быть S. Во вставочной последовательности, описанной в настоящей заявке, X6 может быть T.
Таким образом, AAV или капсидный белок VP1 AAV по настоящему изобретению может также включать в себя последовательность вставки, описанную в настоящей заявке, в которой одна из X1A и X1B присутствует, а другая из X1A и X1B отсутствует и
в котором X1A или X1B выбрана из A, L, V, I, S, T, N, Q, C, P и G, предпочтительно X1A или X1B выбрана из G, P и N, и/или
в котором X2 выбрана из S, T, N, Q, A, L, V и I, предпочтительно X2 выбрана из N и L, и/или
в котором X3 выбрана из A, L, V, I, S, T, N, Q, C, G и P, предпочтительно X3 выбрана из S, Q и P, и/или
в котором X4 выбрана из K, R, H, D, E, S, T, N, Q, A, V, I, L, C, G и P, предпочтительно X4 выбрана из P, A и T, и/или
в котором X6 выбрана из K, R, H, D, E, S, T, N, Q, A, C, G и P, предпочтительно X6 выбрана из T, P и S.
AAV по настоящему изобретению способен трансфицировать/трансдуцировать клетки сетчатки. Так, в результате использования AAV по настоящему изобретению вирусная ДНК AAV может присутствовать в ядерных экстрактах сетчатки мыши через 24 часа после введения AAV в хвостовую вену мыши C57-Bl6J (также указанной в настоящей заявке как C57BL/6J). Мышей можно приобрести в Charles River (http://www.criver.com/products-services/basic-research/find-a-model/jax-mice-strain-c57bl-6j?loc=DE ).
Инбредный штамм C57BL/6J был получен доктором CC Little в результате спаривания самки 57 с самцом 52, выведенных Miss Abbie Lathrop's stock. Таким же образом были получены штаммы C57L и C57BR.
Специалисту в области техники известен генотип этой линии мышей, а также то, где можно получить такой штамм мыши. Специалисту в области техники также известны различия между субштаммами, как описано, например, в Mekasa et al. (2009) “Genetic differences among C57BL/6 Substrains” Exp. Anim. 58(2), 141-149.
Эта линия мышей коммерчески доступна и может быть получена, например, от лабораторий Charles River или Janvier.
В частности, максимум 8×10E10 геномных частиц библиотеки AAV № 1, как описано в настоящей заявке, вводят в хвостовую вену 4-недельных мышей C57-BL6J. Через 24 часа после введения в хвостовую вену отбирают ткань сетчатки, как это подробно описано в настоящей заявке. После этого геном AAV, обладающий способностью проникать в ядро клеток сетчатки в течение 24 часов после внутривенного введения, амплифицируют при помощи ПЦР, как это подробно описано в настоящей заявке.
Также предполагается, что в AAV по настоящему изобретению присутствует вирусная ДНК AAV в ядерных экстрактах сетчатки мыши через 24 часа после введения AAV в хвостовую вену мыши C57-Bl6J (C57/BL6J) и что после определения вставочной последовательности (селекционный раунд 1) и субклонирования обнаруженной вставочной последовательности в дополнительном AAV вирусная ДНК дополнительного AAV присутствует в ядерных экстрактах сетчатки мыши через 24 часа после введения AAV в хвостовую вену мыши C57-Bl6J (C57/BL6J) (селекционный раунд 2). Во втором селекционном раунде используют ту же процедуру, что описана в настоящей заявке для первого селекционного раунда, а также в примерах.
Для обнаружения вирусной ДНК в колбочках сначала вирус, полученный в селекционном раунде 1 и 2, как описано в настоящей заявке, вводят в хвостовую вену 4-недельной мыши C57BL6J или мыши RG-eGFP линии R685933, как описано в настоящей заявке.
Не более 5 х 10^11 геномных частиц, полученных во втором селекционном раунде, как описано в настоящей заявке, вводят в хвостовую вену 4-недельной мыши C57BL6J или мыши RG-eGFP линии R685933, как описано в настоящей заявке.
Мыши RG-eGFP (линии R685933) описаны Fei and Hughes (2001) “Transgenic expression of the jellyfish green fluorescent protein in the cone photoreceptors of the mouse.” Vis Neurosci. 18(4):615-23. Мышей RG-eGFP (линии R685933) можно приобрести в MMRRC (https://www.mmrrc.org/catalog/sds.php?mmrrc_id=43).
Для обнаружения вирусной ДНК в палочках через 24 часа после инъекции мышей усыпляли путем цервикальной дислокации и делали проптоз глазного яблока, слегка сдавливая заднюю часть, близко к зрительному нерву, изогнутым пинцетом Dumont № 7 (Fine Science Tools, Хайдельберг). Роговицу рассекали вдоль экватора острым лезвием. Затем сетчатку отделяли от пигментного эпителия сетчатки (RPE) и, осторожно потянув пинцет вверх, удаляли из оставшейся ткани глаза вместе с хрусталиком и стекловидным телом. После промывки ткани в ледяном 0,1 М фосфатном буфере (PB) и удаления хрусталика и любых оставшихся клеток RPE пинцетом две сетчатки каждой мыши объединяли, переносили в пробирку Эппендорфа и немедленно обрабатывали для выделения палочковых фоторецепторов. В частности, была проведена диссоциация папаина, как описано в Feodorova et al. (2015) “Quick and reliable method for retina dissociation and separation of rod photoreceptor perikarya from adult mice.” MethodsX 2: 39-46, и палочки были выделены методом MACS-сортировки на основе антител к CD73, как описано в Eberle et al. (2014) “Subretinal transplantation of MACS purified photoreceptor precursor cells into the adult mouse retina.” J Vis Exp 84:e50932. Ядра палочек были выделены (чтобы гарантировать, что анализировалась только ядерная ДНК) из MACS-сортированных палочек с помощью набора для фракционирования субклеточного белкового комплекса для тканей (Subcellular Protein Fractionation Kit for Tissues, Thermo Fischer Scientific, #87790). Ядерную ДНК выделяли с помощью набора DNeasy Blood & Tissue Kit (Qiagen, #69504). Секвенирование с помощью системы секвенирования Roche 454 было проведено для определения вставленных пептидных последовательностей, наиболее часто встречающихся в палочках. Дополнительно или в качестве альтернативы AAV или капсидный белок VP1 AAV по настоящему изобретению является таким, что вирусная ДНК AAV присутствует в палочках, MAC-сортированных с использованием магнитных носителей, покрытых антителами к CD73, и/или FACS-сортированных колбочках, при этом колбочки экспрессируют eGFP и являются FACS-сортированными на основе их экспрессии eGFP, через 24 часа после введения AAV в хвостовую вену мыши C57BL/6J.
Для обнаружения вирусной ДНК AAV в колбочках через 24 часа после инъекции мышей усыпляли путем цервикальной дислокации и делали проптоз глазного яблока, слегка сдавливая заднюю часть, близко к зрительному нерву, изогнутым пинцетом Dumont № 7 (Fine Science Tools, Хайдельберг). Роговицу рассекали вдоль экватора острым лезвием. Затем сетчатку отделяли от пигментного эпителия сетчатки (RPE) и, осторожно потянув пинцет вверх, удаляли из оставшейся ткани глаза вместе с хрусталиком и стекловидным телом. После промывки ткани в ледяном 0,1 М фосфатном буфере (PB) и удаления хрусталика и любых оставшихся клеток RPE пинцетом две сетчатки каждой мыши объединяли, переносили в пробирку Эппендорфа и немедленно обрабатывали для выделения колбочковых фоторецепторов. В частности, была проведена диссоциация папаина, как описано в Feodorova et al. (2015) “Quick and reliable method for retina dissociation and separation of rod photoreceptor perikarya from adult mice.” MethodsX 2: 39-46, и колбочки были подвергнуты FACS-сортировке (маркер eGFP), как описано в Becirovic et al. (2016) In Vivo Analysis of Disease-Associated Point Mutations Unveils Profound Differences in mRNA Splicing of Peripherin-2 in Rod and Cone Photoreceptors.” PLOS Genetics 12(1):e1005811. Ядра колбочек были выделены (чтобы гарантировать, что анализировалась только ядерная ДНК) из FACS-сортированных колбочек с помощью набора для фракционирования субклеточного белкового комплекса для тканей (Subcellular Protein Fractionation Kit for Tissues, Thermo Fischer Scientific, #87790). Ядерную ДНК выделяли с помощью набора DNeasy Blood & Tissue Kit (Qiagen, #69504). Секвенирование с помощью системы секвенирования Roche 454 было проведено для определения вставленных пептидных последовательностей, наиболее часто встречающихся в колбочках.
Колбочковые фоторецепторы подвергают FAC-сортировке на основе флуоресценции eGFP от мышей RG-eGFP линии R685933, как описано в настоящей заявке. Затем вирусную ДНК выделяют из сортированных палочковых и колбочковых фоторецепторов и секвенируют с помощью секвенирования следующего поколения (NGS).
Настоящее изобретение также относится к капсиду AAV, содержащему капсидный белок VP1 AAV по настоящему изобретению.
Настоящее изобретение также относится к вирусному вектору, содержащему капсид AAV по настоящему изобретению и трансген, молекулу или полипептид, в котором нуклеиновая кислота, молекула или полипептид заключены в капсид AAV. Нуклеиновая кислота, молекула или полипептид необязательно обеспечивают лечебный эффект.
Настоящее изобретение также относится к применению AAV или вирусного вектора по настоящему изобретению в качестве лекарственного средства. Настоящее изобретение также относится к применению AAV или вирусного вектора по настоящему изобретению в терапии.
Для этих целей AAV по настоящему изобретению может служить в качестве грузовой системы для других молекул. Не имеющими ограничительного характера примерами таких молекул являются ДНК, РНК, пептиды, белки или химические соединения. Таким образом, AAV, используемый для терапии или используемый в фармацевтической композиции, как описано в настоящей заявке, может быть рекомбинантным AAV, как описано в настоящей заявке. Такой AAV может включать в себя трансген.
Трансген может кодировать продукт, который полезен в биологии и медицине, такой как белки, пептиды, РНК, ферменты или каталитические РНК. Желательные молекулы РНК включают кшРНК (shRNA, т.е. малые РНК, образующие шпильки, или короткие РНК, образующие шпильки), тРНК (tRNA, транспортные РНК), дцРНК (dsRNA, двухцепочечные РНК), рибосомные РНК, каталитические РНК и антисмысловые РНК. Одним из примеров полезной последовательности РНК является последовательность, которая подавляет экспрессию целевой последовательности нуклеиновых кислот в обработанном субъекте.
Описанный в настоящей заявке rAAV или вирусный вектор может содержать трансген, такой как миниген. Миниген может быть составлен, как минимум, из гетерологичной последовательности нуклеиновых кислот (трансген), как описано в настоящей заявке, и ее регуляторных последовательностей, а также 5' и 3' инвертированных концевых повторов (ITR) AAV. Именно этот миниген может быть упакован в капсидный белок и доставлен в выбранную клетку-мишень (целевую).
Трансген может быть, например, последовательностью нуклеиновых кислот, гетерологичной к векторным последовательностям, фланкирующим трансген, который кодирует полипептид, белок или другой продукт, представляющий интерес. Кодирующая последовательность нуклеиновых кислот может быть функционально связана с регуляторными компонентами таким образом, чтобы обеспечить транскрипцию, трансляцию и/или экспрессию трансгена в клетке-мишени. Гетерологичная последовательность нуклеиновых кислот (трансген) может быть получена из любого организма. AAV или вирусный вектор может содержать один или несколько трансгенов.
Состав трансгенной последовательности будет зависеть от того, как будет использоваться полученный вектор. Например, трансген выбирают для обеспечения оптогенетической терапии. В оптогенетической терапии искусственные фоторецепторы строят путем доставки генов активируемых светом каналов или насосов к выжившим типам клеток в оставшемся контуре сетчатки. Это особенно полезно для пациентов, у которых утрачена значительная часть фоторецепторной функции, но биполярный клеточный контур ганглиозных клеток и зрительного нерва остается интактным (неповрежденным). В одном варианте осуществления гетерологичная последовательность нуклеиновых кислот (трансген) может быть опсином. Опсиновая последовательность может быть получена из любого подходящего одноклеточного или многоклеточного организма, включая человека, водоросли и бактерии. Опсин может быть, например, родопсином, фотопсином, опсином длиной/средней волны (L/M) (красный/зеленый) или опсином короткой волны (S) (синий). В другом варианте осуществления опсин является канальным родопсином или гало-родопсином.
Трансген также может быть выбран для применения в терапии с аугментацией генами, т.е. для обеспечения замещающей копии отсутствующего или дефектного гена. Трансген может быть легко выбран специалистом в данной области техники для обеспечения необходимого замещающего гена. В одном варианте осуществления отсутствующий/дефектный ген связан с офтальмологическим нарушением. Трансгеном также может быть YX, GRM6, TRPM1L или GPR179, а офтальмологическим нарушением - врожденная стабильная никталопия. См., например, Zeitz et al, Am J Hum Genet. 2013 Jan 10;92(l):67-75.
Трансген также может быть выбран для применения в генной супрессивной терапии (с подавлением генов), т.е. экспрессия одного или нескольких нативных генов прерывается или подавляется на транскрипционном или трансляционном уровнях. Это может быть достигнуто, например, с помощью короткой шпилечной РНК (кшРНК) или других методов, хорошо известных в данной области техники. См., например, Sun et al, Int J Cancer. 2010 Feb l;126(3):764-74 and O'Reilly M, et al. Am J Hum Genet. 2007 Jul;81(l): 127-35. Трансген может быть легко выбран специалистом в данной области техники в зависимости от гена, транскрипцию которого требуется подавить.
Трансген может содержать более одного трансгена. Это может быть достигнуто с помощью одного вектора, несущего две или более гетерологичных последовательностей, или с использованием двух или более AAV или вирусных векторов, каждый из которых несет одну или более гетерологичных последовательностей.
AAV или вирусный вектор также может быть использован для супрессии генов (или нокдауна) и совместной терапии с аугментацией генами. При совместной терапии с нокдауном/ аугментацией дефектная копия интересующего гена выключается и включается немутированная копия. Это может быть достигнуто с помощью двух или более совместно вводимых векторов. См. Millington-Ward et al, Molecular Therapy, April 2011, 19(4): 642- 649. Трансгены могут быть легко выбраны специалистом в данной области техники в зависимости от желаемого результата.
Трансген может быть выбран для использования в терапии с коррекцией генов. Это может быть достигнуто с помощью, например, индуцированного цинк-пальцевой нуклеазой (ZFN) двухцепочечного разрыва ДНК в сочетании с экзогенным субстратом донора ДНК, а также систем TALEN или CAS9/CRISPR в сочетании с экзогенным субстратом донора РНК. См,. например, Ellis et al. (2013) “Zinc-finger nuclease-mediated gene correction using single AAV vector transduction and enhancement by Food and Drug Administration-approved drugs” Gene Ther. 20(1):35-42 и Singh, Braddick, Dhar (2017) 'Exploring the potential of genome editing CRISPR-Cas9 technology.' Gene; 599, pp. 1-18. Трансгены могут быть легко выбраны специалистом в данной области техники в зависимости от желаемого результата. Например, Cas9 и несколько рРНК могут быть упакованы в отдельные векторы AAV, увеличивая общую емкость упаковки, но требуя очистки и коинфекции двух AAV.
Трансген может содержать или состоять из репортерных последовательностей, которые при экспрессии производят обнаруживаемый сигнал. Такие репортерные последовательности включают, помимо прочего, последовательности ДНК, кодирующие β-лактамазу, β-галактозидазу (LacZ), щелочную фосфатазу, тимидинкиназу, зеленый флуоресцентный белок (GFP), красный флуоресцентный белок (RFP), хлорамфениколацетилтрансферазу (CAT), люциферазу, мембраносвязанные белки, включая, например, CD2, CD4, CD8, белок гемагглютинина гриппа и другие хорошо известные из уровня техники, к которым существуют или могут быть обычными способами продуцированы направленные на них высокоаффинные антитела, а также белки слияния, содержащие мембраносвязанный белок, соответствующим образом слитый с доменом антигенной метки из, среди прочего, гемагглютинина или Myc.
Эти кодирующие последовательности, описанные в настоящей заявки, при связи с регуляторными элементами, которые стимулируют их экспрессию, могут обеспечивать сигналы, обнаруживаемые обычными средствами, включая ферментативные, рентгенографические, колориметрические, флуоресцентные или другие спектрографические анализы, флуоресцентные активирующие анализы клеточного сортинга и иммунологические анализы, включая твердофазный иммуноферментный анализ (ELISA), радиоиммуноанализ (RIA) и иммуногистохимию. Например, в случаях, когда маркерной последовательностью является ген LacZ, присутствие вектора, несущего сигнал, обнаруживается с помощью анализа активности бета-галактозидазы. В случаях, когда трансген представляет собой зеленый флуоресцентный белок или люциферазу, вектор, несущий сигнал, может быть измерен визуально по цвету или светопродукции в люминометре.
Трансген может быть использован для коррекции или улучшения недостатков генов (как в рассмотренных выше применениях), которые могут включать недостатки, при которых нормальные гены экспрессируются на менее, чем нормальные, уровнях, или недостатки, при которых продукт функционального гена не экспрессируется. Предпочтительный тип трансгенной последовательности кодирует терапевтический белок или полипептид, который экспрессируется в клетке-мишени.
Изобретение также включает в себя применение нескольких трансгенов, например, для коррекции или улучшения дефекта гена, вызванного белком из многих субъединиц. В определенных ситуациях для кодирования каждой субъединицы белка или для кодирования различных пептидов или белков может использоваться разный/другой трансген. Это желательно, когда размер ДНК, кодирующей белковую субъединицу, велик. Для того чтобы клетка производила белок из многих субъединиц, клетка инфицируется рекомбинантным вирусом, содержащим каждую из различных субъединиц. В качестве альтернативы различные субъединицы белка могут быть закодированы одним и тем же трансгеном. В этом случае один трансген включает в себя ДНК, кодирующую каждую из субъединиц, причем ДНК для каждой субъединицы разделена внутренним сайтом связывания рибозимы (IRES). Это желательно, когда размер ДНК, кодирующей каждую из субъединиц, невелик, например, общий размер ДНК, кодирующей эти субъединицы и IRES, составляет менее пяти килобаз.
Регуляторные последовательности включают обычные управляющие элементы, которые могут быть функционально связаны с трансгеном таким образом, чтобы обеспечить его транскрипцию, трансляцию и/или экспрессию в клетке, трансфицированной вектором или инфицированной вирусом, полученным, как описано в настоящей заявке. В контексте настоящей заявки, «функционально связанные» последовательности включают в себя как управляющие последовательности экспрессии, смежные с интересующим геном, так и управляющие последовательности экспрессии, которые действуют при переносе или на расстоянии, контролируя интересующий ген.
Управляющие последовательности экспрессии в контексте настоящего изобретения могут включать соответствующие последовательности инициации и терминации транскрипции, последовательности промоторов и энхансеров; эффективные сигналы обработки РНК, такие как сигналы сплайсинга и полиаденилирования (polyA); последовательности, стабилизирующие цитоплазматическую мРНК (mRNA); последовательности, повышающие эффективность трансляции (т.е. консенсусная последовательность Козака); последовательности, повышающие стабильность белка, и, при желании, последовательности, повышающие секрецию кодируемого продукта. Большое количество управляющих последовательностей экспрессии, включая промоторы, известно из уровня техники и может быть использовано.
Регуляторные последовательности, полезные в AAV по настоящему изобретению, могут также содержать интрон, желательно расположенный между последовательностью промотора/энхансера и геном. Одна желательная интронная последовательность получена из SV-40 и представляет собой мини-интронный донор сплайсированного фрагмента/акцептор сплайсированного фрагмента 100 bp, обозначаемый как SD-SA. Другая подходящая последовательность включает в себя посттранскрипционный элемент вируса гепатита сурков (см., например, L. Wang and I. Verma, 1999 Proc. Natl. Acad. Sci., USA, 96:3906-3910). Сигналы PolyA могут быть получены от многих подходящих видов, включая, без ограничения, SV-40, человека и крупного рогатого скота.
Другим регуляторным компонентом AAV по настоящему изобретению, является внутренний сайт связывания рибосомы (IRES). Последовательность IRES или другие подходящие системы могут быть использованы для получения более чем одного полипептида из одного транскрипта гена. IRES (или другая подходящая последовательность) используется для получения белка, содержащего более одной полипептидной цепи, или для экспрессии двух различных белков из одной и той же клетки или внутри нее. Примером IRES является внутренняя последовательность связывания рибосомы вируса полиомиелита (полиовируса), которая поддерживает экспрессию трансгена в фоторецепторах, RPE и ганглиозных клетках. Предпочтительно, чтобы IRES располагался в положении 3' относительно трансгена в векторе rAAV.
AAV по настоящему изобретению может содержать промотор (или функциональный фрагмент промотора). Выбор промотора, который будет использоваться в AAV, может быть сделан из широкого числа конститутивных или индуцибельных промоторов, которые могут экспрессировать выбранный трансген в желаемой клетке-мишени. Клетка-мишень может быть фоторецепторной клеткой. Промотор может быть получен от любого вида, включая человека. Желательно, чтобы промотор был «клеточным». Термин «клеточный» означает, что конкретный промотор, выбранный для рекомбинантного вектора, может направлять экспрессию выбранного трансгена в конкретной клетке или глазном типе клеток. Полезные промоторы включают, помимо прочего, палочковый промотор опсина (RHO), красно-зеленый промотор опсина, синий промотор опсина, промотор cGMP-фосфодиэстеразы, промотор SWS (синий промотор коротковолнового чувствительного (SWS) опсина), мышиный промотор опсина (Beltran et al 2010, упомянуто выше), промотор родопсина (Mussolino et al, Gene Ther, July 2011, 18(7):637-45); альфа-субъединица колбочкового трансдуцина (Morrissey et al, BMC Dev, Biol, Jan 2011, 11:3); промотор колбочкового аррестина (ARR3) (Kahle NA et al., Hum Gene Ther Clin Dev, September 2018, 29(3):121-131), промотор бета-фосфодиэстеразы (PDE); промотор пигментного ретинита (RP1) (Nicord et al, J. Gene Med, Dec 2007, 9(12): 1015-23); промотор NXNL2/NXNL 1 (Lambard et al, PLoS One, Oct. 2010, 5(10):el3025), промотор RPE65; медленный промотор/промотор перифирина 2 (Rds/perph2) дегенерации сетчатки (Cai et al, Exp Eye Res. 2010 Aug;91(2): 186-94); промотор VMD2 (Achi et al, Human Gene Therapy, 2009 (20:31- 9)) и промотор ABCA4.
Выбор этих и других общих векторных и регуляторных элементов стандартен, и доступны многие подобные последовательности. См., например, Sambrook et al, и ссылки в ней, например, на страницах 3.18-3.26 и 16.17-16.27, а также Ausubel et al., Current Protocols in Molecular Biology, John Wiley & Sons, New York, 1989). Конечно, не все векторы и управляющие последовательности экспрессии будут одинаково хорошо функционировать в плане экспрессии всех трансгенов, как описано в настоящей заявке. Однако специалист в данной области техники может сделать выбор между этими и другими управляющими последовательностями экспрессии, не выходя за рамки данного изобретения.
Как правило, терапия или лечение, или профилактика заболевания включает введение млекопитающему субъекту, нуждающемуся в этом, эффективного количества композиции, содержащей rAAV или вирусный вектор по настоящему изобретению, например, несущий последовательность нуклеиновых кислот, кодирующую трансген, или его фрагмент, под контролем регуляторных последовательностей, которые экспрессируют продукт гена в клетках глаза субъекта, и необязательно дополнительно фармацевтически приемлемый носитель.
Настоящее изобретение также относится к фармацевтической композиции, содержащей AAV или вирусный вектор, как описано в настоящей заявке. Такие фармацевтические композиции могут дополнительно содержать носитель, предпочтительно фармацевтически приемлемый носитель. Фармацевтическая композиция может быть в форме инъекционного раствора. Инъекционные растворы или суспензии могут быть составлены в соответствии с известным уровнем техники с использованием подходящих нетоксичных, фармацевтически приемлемых разбавителей или растворителей, таких как маннит, 1,3-бутандиол, вода, раствор Рингера или изотонический раствор хлорида натрия, или подходящих диспергирующих или смачивающих и суспендирующих агентов, таких как стерильные, легкие, нелетучие масла, включая синтетические моно - или диглицериды, и жирные кислоты, включая олеиновую кислоту.
Для инъекционных составов фармацевтические композиции могут находиться в лиофилизированном порошке в смеси с подходящими эксципиентами в подходящем флаконе или пробирке. Перед применением в клинике лекарственные средства могут быть восстановлены путем растворения лиофилизированного порошка в подходящей системе растворителей с образованием композиции, пригодной для внутривенного или внутримышечного введения, или для субретинального, интравитреального или субконъюнктивального введения.
Также предусматривается, что фармацевтическая композиция по настоящему изобретению изготавливается/вводится в виде глазных капель.
AAV по настоящему изобретению или фармацевтическая композиция по настоящему изобретению может быть введен(а) в терапевтически эффективном количестве. «Терапевтически эффективное количество» в отношении AAV может варьироваться в зависимости от факторов, включая, без ограничения, стабильность активного вещества в организме пациента, тяжесть состояний, подлежащих облегчению, общую массу тела пациента, способ введения, легкость всасывания, распределения и выведения активного вещества организмом, возраст и чувствительность пациента, побочные эффекты и тому подобное, как это будет очевидно для специалиста в области техники. Количество введения может быть скорректирован по мере изменения различных факторов с течением времени.
В принципе, AAV/фармацевтическая композиция по настоящему изобретению может быть введен(а) любым подходящим способом. AAV по настоящему изобретению, например, содержащий желаемый трансген для применения в фоторецепторных клетках-мишенях, может быть в составе фармацевтической композиции, предназначенной для субретинальной или интравитреальной инъекции. Другие формы введения, которые могут быть полезны в описанных в настоящей заявке способах, включают, без ограничения, прямую доставку к желаемому органу (например, к глазу, например, глазные капли), пероральный, ингаляционный, интраназальный, интратрахеальный, внутривенный, внутримышечный, подкожный, интрадермальный и другие исходные пути введения. При желании пути введения могут быть скомбинированы.
Кроме того, может быть желательно проводить неинвазивную визуализацию сетчатки и функциональные исследования для выявления областей специфических глазных клеток, на которые должна быть нацелена терапия.
AAV может быть введен субъекту в физиологически приемлемом носителе, как описано в настоящей заявке. Концентрация AAV в фармацевтической композиции или при введении может составлять от 10E8 до 10E12 общих векторных геномов на мкл, предпочтительно от 6×10E8 до 6×10E9 на мкл. AAV можно также вводить в концентрации около 10E9 векторных геномов на мкл.
AAV по настоящему изобретению можно вводить отдельно или в комбинации с другими видами лечения. Таким образом, фармацевтическая композиция может также дополнительно или в качестве альтернативы содержать одно или более дополнительных активных ингредиентов.
Фармацевтическую композиция/AAV для применения по изобретению можно вводить субъекту. AAV и фармацевтические композиции, описанные в настоящей заявке, применимы как в терапии человека, так и в ветеринарии. Субъектом может быть млекопитающее или птица. Примеры подходящих млекопитающих включают, без ограничения, мышь, крысу, корову, козу, овцу, свинью, собаку, кошку, лошадь, морскую свинку, собаку, хомяка, норку, тюленя, кита, верблюда, шимпанзе, макаку-резуса и человека, причем предпочтение отдается человеку. Примеры некоторых подходящих птиц включают, без ограничения, индейку, курицу, гуся, утку, чирок, крякву, скворца, шилохвость, чайку, лебедя, цесарку или водоплавающую дичь. Фармацевтическая композиция может дополнительно содержать фармацевтически приемлемый носитель.
Настоящее изобретение также относится к применению AAV по настоящему изобретению в лечении поражения фоторецепторных клеток. В этих вариантах осуществления AAV (например, rAAV) или вирусный вектор может содержать гетерологичную нуклеиновую кислоту, кодирующую терапевтический полипептид, терапевтическую нуклеиновую кислоту, терапевтический белок/полипептид или терапевтическую молекулу.
Настоящее изобретение также относится к способу лечения субъекта (например, предпочтительно субъекта, нуждающегося в нем), включающим в себя введение AAV по настоящему изобретению. Предпочтительно, чтобы AAV вводили в терапевтически эффективном количестве.
AAV по настоящему изобретению также может быть использован в диагностическом методе in vitro. Таким образом, настоящее изобретение также относится к способу диагностики, включающему в себя контакт AAV по настоящему изобретению с образцом, полученным от субъекта.
Настоящее изобретение также относится к производству лекарственного средства, содержащего AAV по настоящему изобретению.
Настоящее изобретение также относится к препарату, содержащему AAV по настоящему изобретению.
Гетерологичная нуклеиновая кислота может находиться под контролем промоторной последовательности, которая экспрессируется в сетчатке. Гетерологичная нуклеиновая кислота может быть функционально связана с промотором, подходящим для экспрессии терапевтического полипептида или терапевтической нуклеиновой кислоты в одном или нескольких типах клеток сетчатки, таких как палочки и колбочки. Например, промотором может быть промотор родопсинкиназы (RK), промотор опсина, промотор цитомегаловируса (CMV), промотор β-актина птиц (CBA).
AAV по настоящему изобретению может содержать гетерологичную нуклеиновую кислоту для доставки гетерологичной нуклеиновой кислоты к фоторецепторным клеткам субъекта.
Гетерологичная нуклеиновая кислота, терапевтическая нуклеиновая кислота, терапевтический белок/полипептид или терапевтическая молекула могут быть использованы для лечения офтальмологического нарушения, выбранного из группы, состоящей из: аутосомно-рецессивной тяжелой дегенерации сетчатки с ранним началом (врожденный амавроз Лебера), врожденной ахроматопсии, болезни Штаргардта, болезни Беста, болезни Дойна, колбочковой дистрофии, пигментной дистрофии сетчатки, сцепленного с Х-хромосомой ретиношизиса, синдрома Ашера, атрофической возрастной макулярной дегенерации, неоваскулярной ВДМ (AMD), диабетической макулопатии, пролиферативной диабетической ретинопатии (ПДР), кистозного макулярного отека, центральной серозной ретинопатии, отслоения сетчатки, внутриглазного воспаления, глаукомы и заднего увеита.
Поражение фоторецепторных клеток, описанное в настоящей заявке, может быть любым заболеванием, затрагивающим фоторецепторные клетки, такие как палочки и/или колбочки. Не имеющие ограничительного характера примеры заболеваний, затрагивающих фоторецепторные клетки, включают в себя слепоту, ахроматопсию, возрастную макулярную дегенерацию, дегенерацию сетчатки, дистрофию сетчатки, пигментную дистрофию сетчатки, колбочковую дистрофия, палочковую дистрофию, дальтонизм, дегенерацию желтого пятна (макулярную дегенерацию), никталопию, ретиношизис, хороидеремию, диабетическую ретинопатию, наследственную нейропатию зрительного нерва, болезнь Огучи типа I, белоточечный ретинит (RPA), прогрессирующую атрофию сетчатки (PRA), белоточечное глазное дно (FA) или врожденную стабильную никталопию (CSNB).
Настоящее изобретение также относится к применению AAV или вирусного вектора по настоящему изобретению in vitro для трансдукции ядра клеток сетчатки.
Настоящее изобретение также относится к способу скрининга вставочной последовательности, который включает в себя
i) внутривенное введение библиотеки AAV, в которой каждый AAV содержит вставочную последовательность, субъекту;
ii) выделение вирусной ДНК AAV из ядерных экстрактов сетчатки глаза;
iii) определение последовательности вставочной последовательности,
получение, тем самым, вставочной последовательности.
Настоящее изобретение также относится к способу скрининга вставочной последовательности, который включает в себя:
i) внутривенное введение библиотеки AAV, в которой каждый AAV содержит вставочную последовательность, субъекту;
ii) выделение вирусной ДНК AAV из ядерных экстрактов сетчатки глаза;
iii) субклонирование выделенной вирусной ДНК AAV во вторую библиотеку AAV;
iv) внутривенное введение второй библиотеки AAV, полученной на этапе iii), субъекту;
v) выделение вирусной ДНК AAV из палочковых или колбочковых фоторецепторов;
vi) определение последовательности вставочной последовательности,
получение, тем самым, вставочной последовательности.
В способе скрининга вставочной последовательности по настоящему изобретению шаги i), ii) и iii) могут быть выполнены повторно.
Библиотека AAV представляет собой вирусную библиотеку, как описано в настоящей заявке. Субклонирование выполняли, как описано в настоящей заявке.
Настоящее изобретение также относится к пептиду (вставочной последовательности), получаемому способом скрининга, как описано в настоящей заявке.
Настоящее изобретение также относится к набору, содержащему AAV по настоящему изобретению или фармацевтическую композицию по настоящему изобретению. Набор может дополнительно содержать один или несколько из следующих компонентов:
(i) буфер(ы);
(ii) олигонуклеотид(ы);
(iii) активные ингредиенты;
(iv) шприцы, подходящие для интравитреальной инъекции (в стекловидное тело).
Настоящее изобретение также относится к набору, содержащему AAV по настоящему изобретению или фармацевтическую композицию по настоящему изобретению. Набор может дополнительно содержать один или несколько из следующих компонентов:
(i) буфер(ы);
(ii) олигонуклеотид(ы);
(iii) активные ингредиенты;
(iv) контейнер, подходящий для глазных капель.
Настоящее изобретение также относится к шприцу, подходящему для интравитреальной инъекции, содержащему раствор с AAV или вирусным вектором по настоящему изобретению или фармацевтическую композицию по настоящему изобретению.
Настоящее изобретение также обеспечивает способ получения AAV по настоящему изобретению. Например, AAV может быть получен путем культивирования клетки-хозяина, которая содержит последовательность нуклеиновых кислот, кодирующую капсидный белок AAV, как описано в настоящей заявке, или его фрагмент; функциональный rep ген; составленный из, как минимум, инвертированных концевых повторов (ITR) AAV и необязательно гетерологичной последовательности нуклеиновых кислот, кодирующей желательный трансген; и достаточные хелперные функции, обеспечивающие возможность упаковки в капсидный белок AAV. Компоненты, необходимые для культивирования в клетке-хозяине для упаковки AAV в капсид AAV, могут быть доставлены в клетку-хозяин при переносе. Альтернативно любой один или более из требуемых компонентов (например, rep последовательности, cap последовательности и/или хелперные функции) может быть обеспечен стабильной клеткой-хозяином, полученной с использованием методов, известных специалистам в данной области, и содержащей один или более из требуемых компонентов.
Удобнее, чтобы такая стабильная клетка-хозяин содержала необходимые компоненты под контролем индуцибельного промотора. Однако необходимые компоненты могут находиться под контролем конститутивного промотора. В настоящей заявке приведены примеры подходящих индуцибельных и конститутивных промоторов. В еще одном варианте осуществления изобретения выбранная стабильная клетка-хозяин может содержать выбранный(е) компонент(ы) под контролем конститутивного промотора и другой(ие) выбранный(е) компонент(ы) под контролем одного или нескольких индуцибельных промоторов. Например, может быть получена стабильная клетка-хозяин из клеток HEK293 (которые содержат хелперные функции El под контролем конститутивного промотора), но которая содержит при этом rep и/или cap белки под контролем индуцибельных промоторов. При этом специалист в области техники может создать другие стабильные клетки-хозяева.
Последовательности rep, последовательности cap и хелперные функции, необходимые для получения rAAV, описанного в настоящей заявке, могут быть доставлены в пакующую клетку-хозяина в виде любого генетического элемента, который передает переносимые на нем последовательности. Выбранный генетический элемент может быть доставлен любым подходящим способом, включая описанный в настоящей заявке. Способы, используемые для построения любого варианта осуществления настоящего изобретения, известны специалистам в области обработки нуклеиновых кислот и включают генную инженерию, рекомбинантную инженерию и синтетические способы. См., например, Sambrook et al, Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Press, Cold Spring Harbor, NY. Аналогичным образом способы генерации вирионов rAAV хорошо известны, и выбор подходящего способа не является ограничением для настоящего изобретения. См., например, K. Fisher et al, 1993 J. Virol, 70:520-532 и патент US 5,478,745, среди прочих источников.
Настоящее изобретение дополнительно характеризуется следующими элементами:
1. Аденоассоциированный вирус (AAV), содержащий
вставку по меньшей мере 6-8 аминокислот между позициями, соответствующими позициям 587 и 588 последовательности SEQ ID NO: 1; при этом вставочная последовательность между N-концом и C-концом имеет формулу I:
X1A-X1B-X2-X3-X4-X5-X6-X7 (формула I)
в которой X5 выбрана из P (Pro), L (Leu) и V (Val);
в которой X7 - это R (Arg);
в которой X1A, X1B, X2, X3, X4, X6 независимо являются любой аминокислотой;
в которой X1A и/или X1B независимо необязательно отсутствуют или присутствуют,
или
в которой X5 выбрана из S (Ser) и T (Thr);
в которой X7 - это S (Ser);
в которой X1A, X1B, X2, X3, X4, X6 независимо являются любой аминокислотой;
в которой X1A и/или X1B независимо необязательно отсутствуют или присутствуют,
или
в которой X5 выбрана из A (Ala) и Q (Gln);
в которой X7 - это A (Ala);
в которой X1A, X1B, X2, X3, X4, X6 независимо являются любой аминокислотой;
в которой X1A и/или X1B независимо необязательно отсутствуют или присутствуют,
в которой вирусная ДНК AAV присутствует в ядерных экстрактах сетчатки мыши через 24 часа после внутривенного введения AAV в хвостовую вену мыши линии C57-Bl6J, и
в которой вирусная ДНК AAV присутствует в MAC-сортированных палочках с использованием магнитных микроносителей, покрытых антителами к CD73, и/или FACS-сортированных колбочках, при этом колбочки экспрессируют eGFP и являются FACS-сортированными на основе их экспрессии eGFP, через 24 часа после внутривенного введения AAV в хвостовую вену мыши линии C57-Bl6J для сортировки палочек и в хвостовую вену мыши RG-eGFP линии R685933 для сортировки колбочек.
2. Аденоассоциированный вирус (AAV), содержащий
вставку по меньшей мере 6-8 аминокислот между позициями, соответствующими позициям 587 и 588 последовательности SEQ ID NO: 1 (вставочная последовательность); при этом вставочная последовательность между N-концом и C-концом имеет формулу I:
X1A-X1B-X2-X3-X4-X5-X6-X7 (формула I),
в которой X5 выбрана из P (Pro), L (Leu) и V (Val);
в которой X7 - это R (Arg);
в которой X1A, X1B, X2, X3, X4, X6 независимо являются любой аминокислотой;
в которой X1A и/или X1B независимо необязательно отсутствуют или присутствуют, в которой вирусная ДНК AAV необязательно присутствует в ядерных экстрактах сетчатки мыши через 24 часа после внутривенного введения AAV в хвостовую вену мыши линии C57-Bl6J.
3. Аденоассоциированный вирус (AAV), содержащий
вставку по меньшей мере 6-8 аминокислот между позициями, соответствующими позициям 587 и 588 последовательности SEQ ID NO: 1; при этом вставочная последовательность между N-концом и C-концом имеет формулу I:
X1A-X1B-X2-X3-X4-X5-X6-X7 (формула I),
в которой X5 выбрана из S (Ser) и T (Thr);
в которой X7 - это S (Ser);
в которой X1A, X1B, X2, X3, X4, X6 независимо являются любой аминокислотой;
в которой X1A и/или X1B независимо необязательно отсутствуют или присутствуют, в которой вирусная ДНК AAV необязательно присутствует в ядерных экстрактах сетчатки мыши через 24 часа после внутривенного введения AAV в хвостовую вену мыши линии C57-Bl6J.
4. Аденоассоциированный вирус (AAV), содержащий
вставку по меньшей мере 6-8 аминокислот между позициями, соответствующими позициям 587 и 588 последовательности SEQ ID NO: 1; при этом вставочная последовательность между N-концом и C-концом имеет формулу I:
X1A-X1B-X2-X3-X4-X5-X6-X7 (формула I),
в которой X5 выбрана из A (Ala) и Q (Gln);
в которой X7 - это A (Ala);
в которой X1A, X1B, X2, X3, X4, X6 независимо являются любой аминокислотой;
в которой X1A и/или X1B независимо необязательно отсутствуют или присутствуют, в которой вирусная ДНК AAV необязательно присутствует в ядерных экстрактах сетчатки мыши через 24 часа после внутривенного введения AAV в хвостовую вену мыши линии C57-Bl6J.
5. Капсидный белок VP1 аденоассоциированного вируса (AAV), содержащий
вставку по меньшей мере 6-8 аминокислот между позициями, соответствующими позициям 587 и 588 последовательности SEQ ID NO: 1 (вставочная последовательность), при этом вставочная последовательность между N-концом и C-концом имеет формулу I:
X1A-X1B-X2-X3-X4-X5-X6-X7 (формула I),
в которой X5 выбрана из P (Pro), L (Leu) и V (Val);
в которой X7 - это R (Arg);
в которой X1A, X1B, X2, X3, X4, X6 независимо являются любой аминокислотой;
в которой X1A и/или X1B независимо необязательно отсутствуют или присутствуют.
6. Капсидный белок VP1 аденоассоциированного вируса (AAV), содержащий
вставку по меньшей мере 6-8 аминокислот между позициями, соответствующими позициям 587 и 588 последовательности SEQ ID NO: 1, при этом вставочная последовательность между N-концом и C-концом имеет формулу I:
X1A-X1B-X2-X3-X4-X5-X6-X7 (формула I),
в которой X5 выбрана из S (Ser) и T (Thr);
в которой X7 - это S (Ser);
в которой X1A, X1B, X2, X3, X4, X6 независимо являются любой аминокислотой;
в которой X1A и/или X1B независимо необязательно отсутствуют или присутствуют.
7. Капсидный белок VP1 аденоассоциированного вируса (AAV), содержащий
вставку по меньшей мере 6-8 аминокислот между позициями, соответствующими позициям 587 и 588 последовательности SEQ ID NO: 1, при этом вставочная последовательность между N-концом и C-концом имеет формулу I:
X1A-X1B-X2-X3-X4-X5-X6-X7 (формула I),
в которой X5 выбрана из A (Ala) и Q (Gln);
в которой X7 - это A (Ala);
в которой X1A, X1B, X2, X3, X4, X6 независимо являются любой аминокислотой;
в которой X1A и/или X1B независимо необязательно отсутствуют или присутствуют.
8. Капсидный белок AAV или AAV2 по любому из пп. 1-7, в котором X1A отсутствует, а X1B присутствует, или X1B отсутствует, а X1A присутствует.
9. Капсидный белок AAV или VP1 AAV по любому из пп. 1-8, в котором вставочная последовательность между N-концом и C-концом имеет формулу II:
L3-L2-L1-X1A-X1B-X2-X3-X4-X5-X6-X7-L4-L5-L6 (формула II)
в которой L - это гибкая аминокислота и
в которой L1, L2, L3, L4, L5 и L6 независимо выбраны из Ala, Leu, Gly, Ser и Thr, и
в которой L1, L2, L3, L4, L5 и L6 независимо необязательно отсутствуют или присутствуют.
10. Капсидный белок AAV или VP1 AAV по одному из предыдущих пунктов, в котором одна из X1A и X1B присутствует, а другая из X1A и X1B отсутствует, и
в котором присутствуют все L1, L2, L3, L4 и L5, а L6 отсутствует.
11. Капсидный белок AAV или AAV2 по любому из предыдущих пунктов, в котором X1A, и/или X1B, и/или X2 и/или X3 не является кислой аминокислотой.
12. Капсидный белок AAV или VP1 AAV по одному из предыдущих пунктов, в котором одна из X1A и X1B присутствует, а другая из X1A и X1B отсутствует, и в котором X2 не является основной или кислой аминокислотой.
13. Капсидный белок AAV или VP1 AAV по одному из предыдущих пунктов, в котором X1A, и/или X1B, и/или X2, и/или X3, и/или X4, и/или X6 не является гидрофобной ароматической аминокислотой.
14. Капсидный белок AAV или VP1 AAV по одному из предыдущих пунктов, в котором одна из X1A и X1B присутствует, а другая из X1A и X1B отсутствует, и
в котором X1A или X1B выбрана из A, L, V, I, S, T, N, Q, C, P и G, предпочтительно X1A или X1B выбрана из G, P и N, и/или
в котором X2 выбрана из S, T, N, Q, A, L, V и I, предпочтительно X2 выбрана из N и L, и/или
в котором X3 выбрана из A, L, V, I, S, T, N, Q, C, G и P, предпочтительно X3 выбрана из S, Q и P, и/или
в котором X4 выбрана из K, R, H, D, E, S, T, N, Q, A, V, I, L, C, G и P, предпочтительно X4 выбрана из P, A и T, и/или
в котором X6 выбрана из K, R, H, D, E, S, T, N, Q, A, C, G и P, предпочтительно X6 выбрана из T, P и S.
15. Капсидный белок AAV или VP1 AAV по любому из предыдущих пунктов для применения в качестве лекарственного средства/лечения заболевания.
16. AAV по любому из предыдущих пунктов для применения в лечении поражения фоторецепторных клеток.
17. Капсид AAV, содержащий капсидный белок VP1 AAV по любому из предыдущих пунктов и необязательно дополнительно содержащий один или несколько капсидных белков AAV VP2 и/или VP3.
18. Вирусный вектор, содержащий капсид AAV по п. 17 и трансген, молекулу или полипептид, в котором нуклеиновая кислота, молекула или полипептид заключены в капсид AAV.
19. Фармацевтическая композиция, содержащая AAV или вирусный вектор по любому из предыдущих пунктов.
20. In vitro применение AAV или вирусного вектора по любому из пп. 1-18 для трансдукции ядра клеток сетчатки.
21. Способ скрининга вставочной последовательности, который включает в себя
i) внутривенное введение библиотеки AAV, в которой каждый AAV содержит вставочную последовательность, субъекту;
ii) выделение вирусной ДНК AAV из ядерных экстрактов сетчатки;
iii) субклонирование выделенной вирусной ДНК AAV во вторую библиотеку AAV;
iv) внутривенное введение второй библиотеки AAV, полученной на этапе iii), субъекту;
v) выделение вирусной ДНК из палочковых или колбочковых фоторецепторов;
vi) определение последовательности вставочной последовательности,
получение, тем самым, вставочной последовательности.
22. Пептид (вставочная последовательность), получаемый способом по п. 21.
23. Набор, содержащий AAV или вирусный вектор по любому из пп. 1-18.
24. Вирусный вектор по любому из предыдущих пунктов для применения в качестве лекарственного средства/лечения заболевания.
25. Вирусный вектор по любому из предыдущих пунктов для применения в лечении поражения фоторецепторных клеток.
Геномные последовательности и белковые последовательности VP1 различных AAV, как описано в настоящей заявке.
Таблица 1. Геномные последовательности и белковые последовательности VP1 различных AAV
(полный геном)
(полный геном)
Последовательности, используемые в настоящем изобретении.
Таблица 2. Последовательности, описанные в настоящей заявке
CAPSD_AAV2S Капсидный белок VP1 OS = аденоассо-циирован-ный вирус 2 (изолят Srivastava/1982) GN=VP1 PE=1 SV=2
Последнее изменение: 5 апреля 2011 г. - в. 2
(позиции 487 и 488 выделены в приведенной выше последовательности)
GGCGGCCGCTTTTTTCCTTGA-3'
где V = A, или C, или G и
N = A, или C, или G, или T.
Этот выбор нуклеиновых оснований направлен на уменьшение возможности генерирования стоп-последовательностей.
где N = A, или C, или G, или T.
где N = A, или C, или G, или T.
ПРИМЕРЫ
Следующие примеры иллюстрируют изобретение. Эти примеры не ограничивают объем данного изобретения. Примеры приведены в целях иллюстрации, и настоящее изобретение ограничено только формулой изобретения.
Пример 1: Новые капсиды AAV
Мы провели выбор дисплея пептида AAV для идентификации AAV с улучшенной направленной доставкой к клеткам сетчатки. Мы использовали AAV-библиотеку мутантов, отображающих 7-мерные рандомные пептиды (иногда также 6-мерные и 8-мерные) в аминокислотном положении 587 капсидного белка VP1 AAV2 (Perabo et al. (2003)” In vitro selection of viral vectors with modified tropism: the adeno-associated virus display, Molecular therapy: the journal of the American Society of Gene Therapy 8, 151-157). Вставленные пептиды фланкированы 2-3 дополнительными «гибкими» аминокислотами (например, аланином) на обоих концах (N-конце и C-конце). Аминокислотное положение 587 расположено на кончике пика на оси тройной симметрии капсида (Xie et al. (2002) “The atomic structure of adeno-associated virus (AAV-2), a vector for human gene therapy” Proceedings of the National Academy of Sciences of the United States of America 99, 10405-10410) и в пределах участка связывания гепаринсульфатного протеогликана (HSPG) (Opie et al. (2003) “Identification of amino acid residues in the capsid proteins of adeno-associated virus type 2 that contribute to heparin sulfate proteoglycan binding, Journal of virology 77, 6995-7006 и Kern et al. (2003) “Identification of a heparin-binding motif on adeno-associated virus type 2 capsids” Journal of virology 77, 11072-11081).
Введение 7-mers в эту открытую позицию облегчает связывание с рецепторами вставленных пептидов и нарушает первичный рецептор-связывающий мотив для HSPG (Perabo et al. (2006) “Heparan sulfate proteoglycan binding properties of adeno-associated virus retargeting mutants and consequences for their in vivo tropism” Journal of virology, 80, 7265-7269), который имеет важное значение в подходах, направленных на перенаправление вирусного тропизма. Кроме того, библиотека AAV была лишена мутантов, связывающихся с HSPG через пептидную последовательность, которая была вставлена (Perabo et al. (2006) “Heparan sulfate proteoglycan binding properties of adeno-associated virus retargeting mutants and consequences for their in vivo tropism” Journal of virology, 80, 7265-7269), чтобы свести к минимуму присутствие AAV, несущего вторичные высокоаффинные сайты связывания для HSPG (Sallach et al. (2014) “Tropism-modified AAV vectors overcome barriers to successful cutaneous therapy” Molecular therapy: the journal of the American Society of Gene Therapy 22, 929-939). 8×10E10 геномных частиц этой библиотеки AAV (библиотеки №1) были введены в хвостовую вену 4-недельных мышей C57-BL6J. Через 24 часа собирали ткань сетчатки и выделяли вирусную ДНК из ядерных экстрактов сетчатки. Геном AAV, обладающий способностью проникать в ядро клеток сетчатки в течение 24 часов после внутривенного введения, был амплифицирован с помощью ПЦР и использован для генерации второй библиотеки AAV, содержащей 7-мерные вставки, выбранные из первого раунда. Затем в хвостовую вену 4-недельных мышей C57-BL6J вводили 8×10E10 геномных частиц из второй библиотеки AAV (библиотеки №2). Через 24 часа собирали ткань сетчатки (без RPE или дополнительной ткани сетчатки) и выделяли вирусную ДНК из ядерных экстрактов сетчатки. После амплификации на основе ПЦР была создана последовательность ДНК, кодирующая 7-мерный AAV, и сформирована третья библиотека AAV с этими 7-мерными вставками. Затем 8×10E10 геномных частиц третьей библиотеки AAV (библиотека № 3) вводили в хвостовую вену 4-недельных мышей C57-BL6J или RG-eGFP линии R685933 (Fei and Hughes (2001) “Transgenic expression of the jellyfish green fluorescent protein in the cone photoreceptors of the mouse” Visual neuroscience 18, 615-623), экспрессирующих eGFP в колбочковых фоторецепторах. Через 24 часа палочковые фоторецепторы были подвергнуты MAC-сортировке с использованием магнитных микроносителей, покрытых антителами к CD73 (Eberle et al. (2011) “integration of transplanted CD73-positive photoreceptor precursors into adult mouse retina” Investigative ophthalmology & visual science 52, 6462-6471), а колбочковые фоторецепторы были подвергнуты FAC-сортировке на основе флуоресценции eGFP (Fei and Hughes (2001) “Transgenic expression of the jellyfish green fluorescent protein in the cone photoreceptors of the mouse” Visual neuroscience 18, 615-623). Затем вирусную ДНК выделяли из сортированных палочковых и колбочковых фоторецепторов и секвенируют с помощью секвенирования следующего поколения (NGS). Могли быть идентифицированы следующие новые AAV с перечисленными пептидными вставками в позиции 587 VP1 AAV2, наделенные способностью направленной доставки к клеткам сетчатки и переноса их генома в ядро клеток сетчатки в течение 24 часов после внутривенной доставки (перечислены только варианты с 2 или более ридами NGS, варианты с более чем 20 ридами NGS выделены “жирным” шрифтом) (см. Фиг. 1).
Кроме того, могли быть идентифицированы следующие новые AAV с перечисленными пептидными вставками в позиции 587 VP1 AAV2, наделенные способностью направленной доставки к палочковым фоторецепторам в течение 24 часов после внутривенной доставки (перечислены только пептиды с 2 или более ридами NGS, варианты с более чем 20 ридами NGS выделены “жирным” шрифтом) (см. Фиг. 2).
Наконец, могли быть идентифицированы следующие новые AAV с перечисленными пептидными вставками в позиции 587 VP1 AAV2, наделенные способностью направленной доставки к колбочковым фоторецепторам в течение 24 часов после внутривенной доставки (перечислены только пептиды с 2 или более ридами NGS, AAV с более чем 20 ридами NGS выделены “жирным” шрифтом) (см. Фиг. 3).
Некоторые из идентифицированных вариантов содержали предполагаемые мотивы связывания интегрина, такие как RGD, RGS или NGR. Эти AAV, несущие указанные вставочные последовательности, приведены на Фиг. 4.
Несколько AAV были обнаружены более чем в одном эксперименте. Эти перекрывающиеся AAV с соответствующими номерами ридов NGS, представлены на Фиг. 5. Примечательно, что для последовательности «RGSLQNA» указано, что число ридов NGS со всей сетчатки будет равно 0. Однако это ошибка. Причина этого заключается в том, что риды NGS обнаруживаются для палочек и колбочек. Эти данные могут быть получены только в том случае, если вставочная последовательность была предварительно выбрана в селекционных раундах 1 и 2 - особенностью обоих селекционных раундов является то, что ДНК обнаруживается в сетчатке. Таким образом, эта вставочная последовательность должна была быть обнаружена в сетчатке и раннее.
Пример 2: Биологическое тестирование новых капсидов AAV
Синтетические олиго-ДНК, кодирующие выбранные пептидные варианты, фланкированные 2-3 аланинами с обоих концов, были вставлены в сайты рестрикции Asel / Mlul транс-плазмиды pRC99 AAV (Nickiin et al. (2001) “Efficient and selective AAV2-mediated gene transfer directed to human vascular endothelial cells, Molecular therapy: the journal of the American Society of Gene Therapy 4, 174-181 and Girod et al. (1999) “Genetic capsid modifications allow efficient re-targeting of adeno-associated virus type 2”, Nature medicine 5, 1052-1056), экспрессирующей гены Rep и Cap AAV2, что приводит к генерации открытой рамки считывания VP1-3 AAV2 с предполагаемыми пептидными вставками в положении, соответствующем аминокислоте 587 VP1. Эти модифицированные плазмиды pRC99 были использованы для получения частиц AAV с новыми вариантами капсида AAV для биологических испытаний. Производство AAV осуществляли по стандартным методикам, описанным в Michalakis et al. (2010) “Restoration of cone vision in the CNGA3-/- mouse model of congenital complete lack of cone photoreceptor function, Molecular therapy: the journal of the American Society of Gene Therapy, 18, 2057-2063. Для упаковки использовали самокомплементарную (sc) цис-плазмиду AAV, содержащую экспрессионную кассету CMV-eGFP (AAV-sc-CMV-eGFP). Такие частицы AAV (общие векторные геномы 6×10E8 - 6×10E9) затем вводили в стекловидное тело (интравитреальная инъекция 1 pi суспензии AAV) взрослых мышей дикого типа C56-BL6/J, а затем мышей исследовали с помощью флуоресцентной микроскопии глазного дна in vivo (конфокальная сканирующая лазерная офтальмоскопия). Затем глаза были удалены, а глазные ванночки обработаны для гистологического анализа, флуоресцентной визуализации eGFP и иммуногистохимии. Полученные результаты показаны на Фиг. 6-9.
Серотипированные векторы AAV2 дикого типа показывают только ограниченную эффективность трансдукции при поступлении в субретинальное пространство или стекловидное тело (Lebherz et al. (2008) “Novel AAV serotypes for improved ocular gene transfer” The journal of gene medicine 10, 375-382, Auricchio et al. (2001) “ Exchange of surface proteins impacts on viral vector cellular specificity and transduction characteristics: the retina as a model” Hum Mol Genet, 10, 3075-3081, Hellstrom et al. (2009) “Cellular tropism and transduction properties of seven adeno-associated viral vector serotypes in adult retina after intravitreal injection, Gene therapy 16, 521-532). В частности, AAV2 трансфицирует преимущественно клетки пигментного эпителия сетчатки (RPE) из субретинального пространства (Auricchio et al. (2001) “Exchange of surface proteins impacts on viral vector cellular specificity and transduction characteristics: the retina as a model” Hum Mol Genet 10, 3075-3081 and Trapani et al. (2014) “Vector platforms for gene therapy of inherited retinopathies” Prog Retin Eye Res.). Из интравитреального компартмента AAV2 трансфицирует преимущественно глиальные клетки Мюллера и ганглионарные клетки сетчатки (Auricchio et al. (2001) “Exchange of surface proteins impacts on viral vector cellular specificity and transduction characteristics: the retina as a model” Hum Mol Genet 10, 3075-3081 and Trapani et al. (2014) “Vector platforms for gene therapy of inherited retinopathies” Prog Retin Eye Res.).
Примеры интравитреальной трансдукции (при введении в стекловидное тело) см. на Фиг. 2а в Hellstrom et al. (2009) “Cellular tropism and transduction properties of seven adeno-associated viral vector serotypes in adult retina after intravitreal injection, Gene therapy 16, 521-532 или на Фиг. 4a в Auricchio et al. (2001) “Exchange of surface proteins impacts on viral vector cellular specificity and transduction characteristics: the retina as a model” Hum Mol Genet 10, 3075-3081. Примеры трансдукции при введении в субретинальное пространство см. на Фиг. 4 в Lebherz et al. (2008) “Novel AAV serotypes for improved ocular gene transfer” The journal of gene medicine 10, 375-382.
Описанные здесь специфические модификации заметно изменили тропизм и динамику трансдукции наших новых вариантов капсид AAV, которые теперь способны очень эффективно трансфицировать различные типы клеток сетчатки из субретинального и интравитреального компартментов/простанств (см. Фиг. 6-10). Что более важно, новый AAV очень эффективно трансфицирует палочковые и колбочковые фоторецепторы из субретинального и/или интравитреального компартмента. В заключение следует отметить, что биологическое тестирование выбранных новых вариантов капсидов AAV предполагает заметно измененную динамику трансдукции, индуцируемую нашими новыми пептидными вставками, что будет очень полезно для любого рода экспериментов, направленных на эффективную и высокоуровневую трансдукцию специфических типов клеток сетчатки в доклинических исследованиях или для разработки методов лечения глазных заболеваний на основе переноса генов (например, генная терапии в области офтальмологии). В комбинации с клеточными специфическими промоторами (например, колбочковым или палочковым промотором) новые варианты капсида AAV позволят преодолеть естественные барьеры для трансдукции и направленной доставки специфических типов клеток после системного применения или после введения в субретинальное пространство или стекловидное тело.
Эффективность трансдукции наших новых вариантов капсида AAV была дополнительно охарактеризована в иммортализованной линии клеток колбочковых фоторецепторов 661w (Tan et al. (2004) “Expression of cone-photoreceptor-specific antigens in a cell line derived from retinal tumors in transgenic mice.” Investigative Ophthalmology & Visual Science 45 764-768). Для этого 661w, выращенные при приблизительно 60% конфлюэнтности, были инфицированы при множественной инфекции (MOI) 100 000 вирусных геномов на клетку либо новыми капсидами AAV, диким типом AAV2, либо рекомбинантным вариантом 7m8 AAV2 (Dalkara et al. (2013) “In vivo-directed evolution of a new adeno-associated virus for therapeutic outer retinal gene delivery from the vitreous.” Science Translational Medicine, 5(189) 189ra76), а именно LALGETTRP (SEQ ID NO. 23), экспрессирующим eGFP под контролем промотора CMV. Через 48 часов флуоресценцию eGFP определяли с помощью эпифлуоресцентной микроскопии (система флуоресцентной визуализации клеток EVOS FL cell imaging system, Thermo Fisher Scientific). Затем клетки фиксировали в течение 15 минут 4% параформальдегидом в фосфатно-солевом буфере (PBS), промывали и ресуспендировали в PBS для анализа на сигнал eGFP методом проточной цитометрии (FACSCantoII system, BD Bioscience). Новые варианты капсида AAV «NNPTPSR» и «GLSPPTR» показали превосходную эффективность трансдукции лунок 661w по сравнению с AAV2 или 7m8. Полученные результаты показаны на Фиг. 11.
Все эксперименты до сих пор проводились с модифицированными капсидами AAV2. Однако другие капсиды AAV также переносят пептидные вставки в соответствующие капсидные позиции (Michelfelder et al. (2011) “Peptide ligands incorporated into the threefold spike capsid domain to re-direct gene transduction of AAV8 and AAV9 in vivo” PloS one, 6, e23101), поэтому наши новые пептидные вставки могут быть перенесены на другой известный капсид AAV, например, в AAV8, AAV9, AAV7 или AAV5, которые, как известно, имеют более высокую эффективность и более широкие профили трансдукции в сетчатке по сравнению с AAV2. Кроме того, новые вставки капсидного пептида AAV могут быть скомбинированы с мутациями капсидного тирозина, треонина и серина (Petrs-Silva et al. (2009) “High-efficiency transduction of the mouse retina by tyrosine-mutant AAV serotype vectors” Molecular therapy: the journal of the American Society of Gene Therapy 17, 463-471 and Zhong et al. (2008) “Next generation of adeno-associated virus 2 vectors: point mutations in tyrosines lead to high-efficiency transduction at lower doses” Proceedings of the National Academy of Sciences of the United States of America, 105, 7827-7832) для снижения протеасомно-опосредованной деградации и повышения эффективности трансдукции.
Пример 3: Поперечные срезы сетчатки
Чтобы показать, что описанные здесь векторы AAV действительно трансфицируют фоторецепторы, капсид AAV2 «GLSPPTR» был введен (интравитреально) в стекловидное тело живых мышей. В частности, однократная интравитреальная инъекция 1 мкл (содержащего приблизительно 2 векторных генома 10Е9) вирусной суспензии ss-mSWS-eGFP, упакованной с капсидом «GLSPPTR» AAV2 (см. также пример 2), была применена к 10-недельным мышам C57-BL6J. AAV-ss-mSWS-eGFP стимулирует экспрессию eGFP под контролем промотора SWS мыши. Экспрессия GFP была проанализирована через 6 недель после этого. В этой связи из области фоторецепторов глаза были получены изображения конфокальной сканирующей микроскопии. Как видно из Фиг. 12, eGFP могут быть обнаружены в поперечных срезах сетчатки из колбочковых фоторецепторов. В этом случае наблюдался сильный иммуносигнал антител к eGFP (серый цвет) в колбочковых фоторецепторах. Количественное определение двойного мечения колбочковым аррестином в качестве колбочкового маркера показала, что 78,7 ± 3,1 % (n = 4) положительных по колбочковому аррестину колбочек были положительными по eGFP. Таким образом, этот эксперимент показывает, что AAV нацелен на фоторецепторы.
Пример 4: Эксплантаты человека
Чтобы проанализировать, будут ли векторы AAV, описанные в примерах 1 и 2, также трансфицировать человеческие фоторецепторные клетки, были проанализированы эксплантаты человека. Ткани сетчатки человека, полученные после смерти, культивировали фоторецепторной стороной вниз по ранее опубликованным методикам (Fradot M et al. May 2011 Gene therapy in ophthalmology: validation on cultured retinal cells and explants from postmortem human eyes. Human gene therapy. 22(5):587-93). Эксплантат ткани сетчатки человека трансфицировали в день 0 путем нанесения 1 × 10E11 vg (вирусных геномов) sc-CMV-eGFP, упакованных с одним из новых капсидов «GLSPPTR» или «NNPTPSR» AAV2, на витреальную сторону сетчатки и культивировали в течение девяти дней in vitro (DIV). На DIV 9 питательную среду удаляли, а ткань фиксировали 4% параформальдегидом в фосфатно-солевом буфере и затем обрабатывали для изготовления криосрезов и нативной флуоресцентной визуализации eGFP с использованием конфокальной микроскопии.
На Фиг. 13 представлены репрезентативные изображения конфокальной сканирующей микроскопии, показывающие AAV-опосредованную экспрессию eGFP в эксплантатах сетчатки человека (вставочные последовательности капсидных пептидов приведены вверху каждого изображения). Примечательно, что наблюдалась сильная нативная флуоресценция eGFP (серый цвет) в различных типах и слоях клеток сетчатки. В частности, многие внутренние сегменты фоторецепторов (is) и клеточные тела в пределах внешнего ядерного слоя (onl) были eGFP-положительными. IS, внутренние сегменты. ONL, внешний ядерный слой. INL, внутренний ядерный слой. ONL, внутренний ядерный слой. GCL, слой ганглиозных клеток.
Пример 5: Измерения ERG (экспрессия трансгена в колбочках)
Чтобы проанализировать, являются ли векторы AAV, полученные в примерах 1 и 2, также эффективными при переносе трансгена в фоторецепторную клетку, были проведены измерения ERG. Электроретинограмма (ERG) - это диагностическое исследование, известное специалисту в области техники, по измерению электрической активности, генерируемой нервными клетками (нейронами) и клетками, отличными от нейронов, в сетчатке в ответ на световой стимул. Электрическая реакция является результатом потенциала сетчатки, создаваемого световыми изменениями в потоке трансретинальных ионов, в первую очередь натрия и калия.
Для этого эксперимента были использованы мыши с дефицитом Cnga3 (CNGA3-/-), которые имеют врожденно нефункциональный колбочковый фоторецептор из-за генетической делеции в CNGA3-субъединице управляемого циклическими нуклеотидами (CNG) канала колбочкового фоторецептора. Векторы AAV в примере 2 способны стимулировать экспрессию комплементарной ДНК мыши CNGA3 под контролем синего промотора (коротковолнового чувствительного, SWS) опсина (ss-mSWS-mCnga3-WPRE) в направлении колбочек. Эта методика также описана в Michalakis et al. (2010) Restoration of Cone Vision in the CNGA3-/- Mouse Model of Congenital Complete Lack of Cone Photoreceptor Function Mol Ther.: 2057-2063. AAV2 был упакован с капсидом «GLSPPTR», как описано в примере 2. Приблизительно 1 × 10E10 vg (вирусных геномов) AAV частиц были доставлены интравитреально у 4-недельных мышей с дефицитом Cnga3.
В частности, измерение ERG проводили через 2 месяца после однократной интравитреальной инъекции 1 мкл (содержащего приблизительно 1 × 10E10 vg (вирусных геномов) ss-mSWS-mCnga3-WPRE). Репрезентативные измерения фотопического мерцания ERG приведены на Фиг. 14. Показаны следы от обработанного глаза (черный цвет) и необработанного контрольного глаза (серый пунктир) при стимуле 3,1 log cd сек/м2 и указанной частоте.
У мышей с дефицитом Cnga3, получающих вектор AAV, содержащий трансген, наблюдается увеличение амплитуды. Увеличение амплитуды указывает на улучшение функции колбочковой системы в фотопических условиях, в то время как необработанные мыши с дефицитом Cnga3 не реагируют на световую стимуляцию (Michalakis et al. (2010) Restoration of Cone Vision in the CNGA3-/- Mouse Model of Congenital Complete Lack of Cone Photoreceptor Function Mol Ther.: 2057-2063).
После измерения ERG обработанные и необработанные контрольные глаза собирали и обрабатывали для иммуногистологического анализа экспрессии белка CNGA3, как описано в Michalakis et al. (2010) Restoration of Cone Vision in the CNGA3-/- Mouse Model of Congenital Complete Lack of Cone Photoreceptor Function Mol Ther.: 2057-2063.
Репрезентативные данные приведены на Фиг. 15. В частности, представлены изображения конфокальной сканирующей микроскопии, показывающие экспрессию колбочкового фоторецептора белка CNGA3 на поперечных срезах сетчатки у 3-месячной мыши с дефицитом Cnga3 через 2 месяца после однократной интравитреальной инъекции 1 мкл (содержащего приблизительно 1 × 10E10 vg (вирусных геномов) ss-mSWS-mCnga3-WPRE (см. Michalakis et al. 2010, уже упомянутую в тексте настоящей заявки), упакованных с новым капсидом «GLSPPTR» AAV2. Сильный иммуносигнал антител к CNGA3 обнаружен в положительных на арахисовый агглютинин (PNA) колбочковых фоторецепторах. os, внешние сегменты. onl, внешний ядерный слой. inl, внутренний ядерный слой. gcl, слой ганглиозных клеток.
Пример 6: Измерения ERG (экспрессия трансгена в палочках)
Аналогично примеру 5 на Фиг. 16 представлены репрезентативные измерения скотопического однократного испарения ERG у 3-месячных мышей с дефицитом Cnga3 через 2 месяца после однократной интравитреальной инъекции 1 мкл (содержащего приблизительно 1 × 10E10 vg (вирусных геномов) ss-mRho-mCngb1-sv40 (Koch et al. 2012) Gene therapy restores vision and delays degeneration in the CNGB1-/- mouse model of retinitis pigmentosa. Hum Mol Genet.: 4486-4496), упакованной с новым капсидным «NNPTPSR» AAV2. Показаны следы от обработанного глаза (черный цвет) и необработанного контрольного глаза (серый пунктир) при указанной яркости светового стимула.
Следует отметить, что в контексте настоящей заявки формы единственного числа включают формы во множественном числе, если только контекст явно не указывает на иное. Так, например, ссылка на «реагент» включает в себя один или несколько таких различных реагентов, а ссылка на «способ» включает в себя ссылку на эквивалентные этапы и способы, известные специалистам в данной области техники, которые могут быть изменены или заменены способами, описанными в настоящей заявке.
Кроме того, подразумевается, что слово «приблизительно» в контексте настоящей заявки, когда речь идет об измеримом значении, таком как длина полинуклеотидной или полипептидной последовательности, доза, время, температура и т.п., охватывает вариации ± 20%, ± 10%, ± 5%, ± 1 %, ± 0 5%, или даже ± 0,1% от указанного значения. Кроме того, в контексте настоящего изобретения, «и/или» относится и охватывает все возможные комбинации одного или нескольких связанных перечисленных элементов, а также отсутствие комбинаций при интерпретации в альтернативном варианте («или»).
Если контекст не указывает на иное, то предполагается, что различные признаки изобретения, описанные в настоящей заявке, могут быть использованы в любой комбинации.
Кроме того, настоящее изобретение также предусматривает, что в некоторых вариантах осуществления изобретения любой признак или комбинация признаков, изложенных в настоящей заявке, могут быть исключены или опущены.
Все публикации и патенты, упомянутые в настоящем описании, включены посредством ссылки в полном объеме. Если материал, включенный в качестве ссылки, противоречит или не согласуется с данным описанием, описание заменяет любой такой материал.
Если не указано иное, термин «по меньшей мере», предшествующий серии элементов, следует понимать, как относящийся к каждому элементу в серии. Специалисты в данной области техники распознают или смогут установить, используя не более чем обычные эксперименты, множество эквивалентов конкретных вариантов осуществления изобретения, описанных в настоящей заявке. Подразумевается, что настоящее изобретение охватывает такие эквиваленты.
В данном описании и в формуле изобретения далее по тексту, если контекст не требует иного, слово «содержит» и такие варианты, как «включает в себя» и «содержащий», подразумевают включение указанного целого числа или шага, или группы целых чисел или шагов, но не исключение любого другого целого числа или шага или группы целых чисел или шагов. В контексте настоящей заявки термин «содержащий» может быть заменен термином «включающий в себя» или в некоторых случаях термином «обладающий/имеющий».
В контексте настоящей заявки «состоящий из» исключает любой элемент, этап или ингредиент, не указанный в элементе формулы изобретения. В контексте настоящей заявки «по существу состоящий из» не исключает материалы или этапы, которые не оказывают существенного влияния на основные и новые характеристики формулы изобретения.
В каждом случае в контексте настоящей заявки любой из терминов «содержащий», «по существу состоящий из» и «состоящий из» может быть заменен любым из двух других терминов.
В тексте данного описания цитируются несколько документов. Каждый из документов, цитируемых в настоящей заявке (включая все патенты, заявки на выдачу патентов, научные публикации, спецификации производителя, инструкции и т.д.), выше или ниже по тексту, настоящим включены посредством ссылки в полном объеме. Ничто в настоящем документе не должно быть истолковано как признание того, что изобретение не имеет права предшествовать такому раскрытию в силу предшествующего изобретения.
ССЫЛКИ
Altschul Nucl. Acids Res. 25 (1977), 3389-3402.
Altschul, J. Mol. Evol. 36 (1993), 290-300.
Altschul, J. Mol. Biol. 215 (1990), 403-410.
Auricchio et al. (2001) “Exchange of surface proteins impacts on viral vector cellular specificity and transduction characteristics: the retina as a model” Hum Mol Genet, 10, 3075-3081.
Ausubel et al., Current Protocols in Molecular Biology, John Wiley & Sons, New York, 1989.
Becirovic et al. (2016) In Vivo Analysis of Disease-Associated Point Mutations Unveils Profound Differences in mRNA Splicing of Peripherin-2 in Rod and Cone Photoreceptors.” PLOS Genetics 12(1):e1005811.
Becirovic et al. (2016) “AAV Vectors for FRET-Based Analysis of Protein-Protein Interactions in Photoreceptor Outer Segments.” Front Neurosci 10:356.
Boye et al. (2013) “A comprehensive review of retinal gene therapy”
Molecular therapy, 21 509-519.
Brutlag Comp. App. Biosci. 6 (1990), 237-245 et al, Exp Eye Res. 2010 Aug;91(2): 186-94.
Chao et ai., (2000) Molecular Therapy 2:619.
Dalkara et al. (2013) “In vivo-directed evolution of a new adeno-associated virus for therapeutic outer retinal gene delivery from the vitreous.” Science Translational Medicine, 5(189) 189ra76.
D'Costa et al. (2016) “Practical utilization of recombinant AAV vector reference standards: focus on vector genomes titration by free ITR qPCR.” Mol Ther Methods Clin Dev. 5:16019.
Eberle et al. (2011) “integration of transplanted CD73-positive photoreceptor precursors into adult mouse retina, Investigative ophthalmology & visual science, 52, 6462-6471.
Eberle et al. (2014) “Subretinal transplantation of MACS purified photoreceptor precursor cells into the adult mouse retina.” J Vis Exp 84:e50932.
Ellis et al. (2013) “Zinc-finger nuclease-mediated gene correction using single AAV vector transduction and enhancement by Food and Drug Administration-approved drugs” Gene Ther. 20(1):35-42.
Fei and Hughes (2001) “Transgenic expression of the jellyfish green fluorescent protein in the cone photoreceptors of the mouse” Visual neuroscience, 18, 615-623.
Fisher et al, 1993 J. Virol, 70:520-532.
Fei et al. (2003) “Development of the cone photoreceptor mosaic in the mouse retina revealed by fluorescent cones in transgenic mice.” Mol Vision 9:31-42
Feodorova et al. (2015) “Quick and reliable method for retina dissociation and separation of rod photoreceptor perikarya from adult mice.” MethodsX 2:39-46
Fradot M et al. May 2011 Gene therapy in ophthalmology: validation on cultured retinal cells and explants from postmortem human eyes. Human gene therapy. 22(5):587-93
Girod et al. (1999) “Genetic capsid modifications allow efficient re-targeting of adeno-associated virus type 2. Nat. Med. 5: 1052-1056
Hacker et al. (2005) “Adeno-associated virus serotypes 1 to 5 mediated tumor cell directed gene transfer and improvement of transduction efficiency.” J Gene Med 7(11):1429-38
Hellstrom et al. (2009) “Cellular tropism and transduction properties of seven adeno-associated viral vector serotypes in adultretina after intravitreal injection, Gene therapy, 16, 521-532.
Henikoff Proc. Natl. Acad. Sci., USA, 89, (1989), 10915
Kern et al. (2003) “Identification of a heparin-binding motif on adeno-associated virus type 2 capsids” Journal of virology, 77, 11072-11081
Kahle NA et al., Hum Gene Ther Clin Dev, September 2018, 29(3):121-131
Koch et al. (2012) Gene therapy restores vision and delays degeneration in the CNGB1-/- mouse model of retinitis pigmentosa. Hum Mol Genet.: 4486-4496
Kotterman and Schaffer (2014) “Engineering adeno-associated viruses for clinical gene therapy” Nat Rev Genet, 15, 445-451
Lambard et al, PLoS One, Oct. 2010, 5(10):el3025.
Lebherz et al. (2008) “Novel AAV serotypes for improved ocular gene transfer” The journal of gene medicine, 10, 375-382.
Le Guiner et al. (2011) “Biodistribution and shedding of AAV vectors” Methods in molecular biology 807, 339-359.
MacLaren et al. (2014) “Retinal gene therapy in patients with choroideremia: initial findings from a phase 1/2 clinical trial” Lancet, 383, 1129-1137.
Maguire et al. (2008) “Safety and efficacy of gene transfer for Leber's congenital amaurosis, N Engl J Med, 358 2240-2248.
Mekasa et al. (2009) “Genetic differences among C57BL/6 Substrains” Exp. Anim. 58(2), 141-149.
Michalakis et al. (2010) Restoration of Cone Vision in the CNGA3-/- Mouse Model of Congenital Complete Lack of Cone Photoreceptor Function Mol Ther.: 2057-2063
Michelfelder et al. (2011) “Peptide ligands incorporated into the threefold spike capsid domain to re-direct gene transduction of AAV8 and AAV9 in vivo” PloS one, 6, e23101.
Millington-Ward et al., Molecular Therapy, April 2011, 19(4): 642- 649.
Mussolino et al., Gene Ther, July 2011, 18(7):637-45).
Muzyczka, (1992) Curr Topics Microbiol. Immunol. 158:97
Morrissey et al., BMC Dev, Biol, Jan 2011, 11 :3.
Mühlfriedel et al. (2013) “Optimized technique for subretinal injections in mice” Methods in molecular biology, 935, 343-349.
Nathwani et al. (2014) “Long-term safety and efficacy of factor IX gene therapy in hemophilia B” N Engl J Med, 371 (2014) 1994-2004.
Nicord et al., J. Gene Med, Dec 2007, 9(12): 1015-23.
Nickiin et al. (2001) “Efficient and selective AAV2-mediated gene transfer directed to human vascular endothelial cells” Molecular therapy: the journal of the American Society of Gene Therapy 4, 174-181
Ochakovski et al. (2017) “Retinal Gene Therapy: Surgical Vector Delivery in the Translation to Clinical Trials.” Front Neurosci 11:174
Opie et al. (2003) “Identification of amino acid residues in the capsid proteins of adeno-associated virus type 2 that contribute to heparin sulfate proteoglycan binding, Journal of virology, 77, 6995-7006.
O'Reilly M, et al. Am J Hum Genet. 2007 Jul;81(l): 127-35.
Perabo et al. (2003)” In vitro selection of viral vectors with modified tropism: the adeno-associated virus display, Molecular therapy: the journal of the American Society of Gene Therapy, 8, 151-157.
Perabo et al. (2006) “Heparan sulfate proteoglycan binding properties of adeno-associated virus retargeting mutants and consequences for their in vivo tropism” Journal of virology, 80, 7265-7269.
Sallach et al. (2014) “Tropism-modified AAV vectors overcome barriers to successful cutaneous therapy” Molecular therapy: the journal of the American Society of Gene Therapy, 22, 929-939.
Sambrook et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Press, Cold Spring Harbor, NY.
J. Samulski, Chapel Hill, NC; Xiao, Li and Samulski (1998) “Production of high-titer recombinant adeno-associated virus vectors in the absence of helper adenovirus.” J. Virol. 72: 2224-2232.
Schön et al. (2015) “Retinal gene delivery by adeno-associated virus (AAV) vectors:Strategies and applications” European journal of pharmaceutics and biopharmaceutics.
Simonelli et al. (2010) “Gene therapy for Leber's congenital amaurosis is safe and effective through 1.5 years after vector administration” Molecular therapy: the journal of the American Society of Gene Therapy, 18 (2010) 643-650.
Sonntag et al. (2011) “The Assembly-Activating Protein Promotes Capsid Assembly of Different Adeno-Associated Virus Serotypes” J Virol. 85(23): 12686-12697.
Sun et al, Int J Cancer. 2010 Feb l;126(3):764-74.
Tan et al. (2004) “Expression of cone-photoreceptor-specific antigens in a cell line derived from retinal tumors in transgenic mice.” Investigative Ophthalmology & Visual Science 45 764-768.
Thompson Nucl. Acids Res. 2 (1994), 4673-4680.
Trapani et al. (2014) “Vector platforms for gene therapy of inherited retinopathies” Prog Retin Eye Res.
Wang and I. Verma, 1999 Proc. Natl. Acad. Sci., USA, 96:3906-3910.
Xiao, Li and Samulski (1998) “Production of high-titer recombinant adeno-associated virus vectors in the absence of helper adenovirus.” J. Virol. 72: 2224-2232.
Xie et al. (2002) “The atomic structure of adeno-associated virus (AAV-2), a vector for human gene therapy” Proceedings of the National Academy of Sciences of the United States of America, 99 10405-10410.
Zhong (2008) “Tyrosine-phosphorylation of AAV2 vectors and its consequences on viral intracellular trafficking and transgene expression” Virology, 381, 194-202.
Petrs-Silva et al. (2009) “High-efficiency transduction of the mouse retina by tyrosine-mutant AAV serotype vectors” Molecular therapy: the journal of the American Society of Gene Therapy, 17, 463-471.
Zeitz et al, Am J Hum Genet. 2013 Jan 10;92(l):67-75.
Zhong et al. (2008) “Next generation of adeno-associated virus 2 vectors: point mutations in tyrosines lead to high-efficiency transduction at lower doses” Proceedings of the National Academy of Sciences of the United States of America, 105, 7827-7832.
Zolotukhin et al. (1999) “Recombinant adeno-associated virus purification using novel methods improves infectious titer and yield. Gene Ther. 6: 973-985.
US 5,478,745
PCT/EP2008/004366
US 9610354 B2
WO 1996/000587 A1
WO 2010/093784
WO 00/28004.
| название | год | авторы | номер документа |
|---|---|---|---|
| ВИРИОНЫ АДЕНОАССОЦИИРОВАННОГО ВИРУСА С ВАРИАНТНЫМ КАПСИДОМ И СПОСОБЫ ИХ ИСПОЛЬЗОВАНИЯ | 2017 |
|
RU2742724C1 |
| ВИРИОНЫ АДЕНОАССОЦИИРОВАННОГО ВИРУСА С ВАРИАНТНЫМ КАПСИДОМ И СПОСОБЫ ИХ ИСПОЛЬЗОВАНИЯ | 2012 |
|
RU2611202C2 |
| РЕКОМБИНАНТНЫЕ ВИРУСНЫЕ ВЕКТОРЫ С МОДИФИЦИРОВАННЫМ ТРОПИЗМОМ И ПУТИ ИХ ПРИМЕНЕНИЯ ДЛЯ НАЦЕЛЕННОГО ВВЕДЕНИЯ ГЕНЕТИЧЕСКОГО МАТЕРИАЛА В КЛЕТКИ ЧЕЛОВЕКА | 2018 |
|
RU2809246C2 |
| СПОСОБЫ ВЫЯВЛЕНИЯ AAV | 2017 |
|
RU2771622C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ НАРУШЕНИЙ И ЗАБОЛЕВАНИЙ, СВЯЗАННЫХ С RDH12 | 2017 |
|
RU2764920C2 |
| Повышение тканеспецифической доставки генов путем модификации капсида | 2019 |
|
RU2801217C2 |
| ВЕКТОР АДЕНОАССОЦИИРОВАННОГО ВИРУСА | 2015 |
|
RU2743382C2 |
| АДЕНОАССОЦИИРОВАННЫЕ ВИРУСНЫЕ ВЕКТОРЫ ДЛЯ ЛЕЧЕНИЯ МИОЦИЛИНОВОЙ (MYOC) ГЛАУКОМЫ | 2015 |
|
RU2746991C2 |
| Вектор, способ лечения хороидермии, способ селективной экспрессии полинуклеотида | 2014 |
|
RU2723101C2 |
| КОМПОЗИЦИЯ И СПОСОБЫ ВЫСОКОЭФФЕКТИВНОГО ПЕРЕНОСА ГЕНОВ С ПОМОЩЬЮ ВАРИАНТОВ КАПСИДА AAV | 2013 |
|
RU2683497C2 |















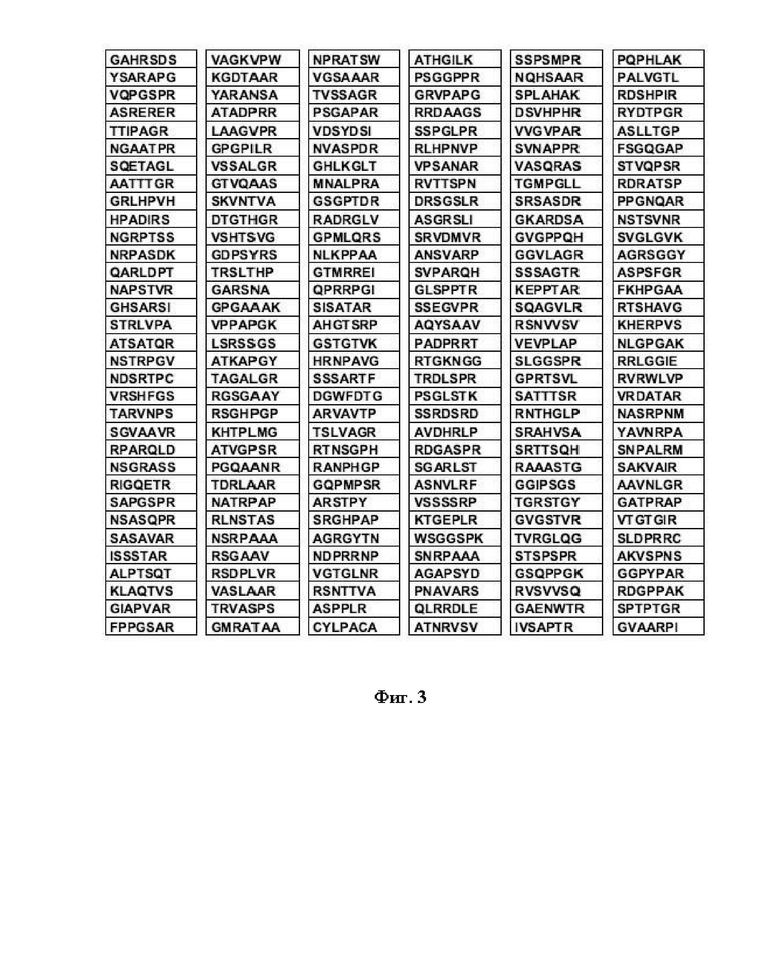


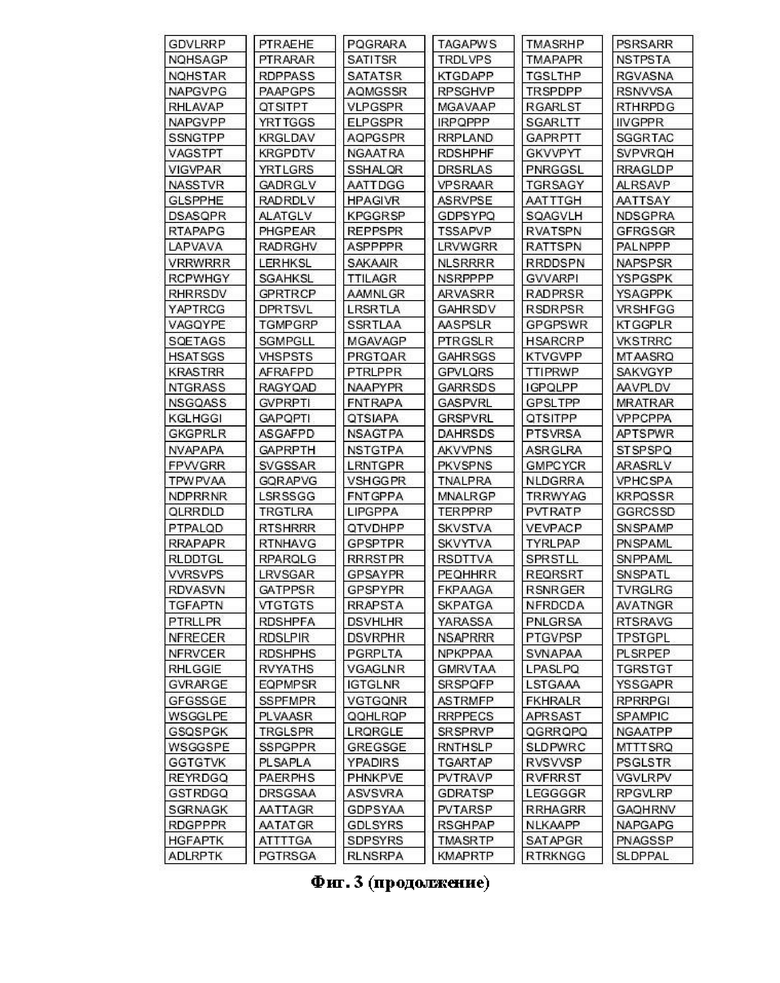

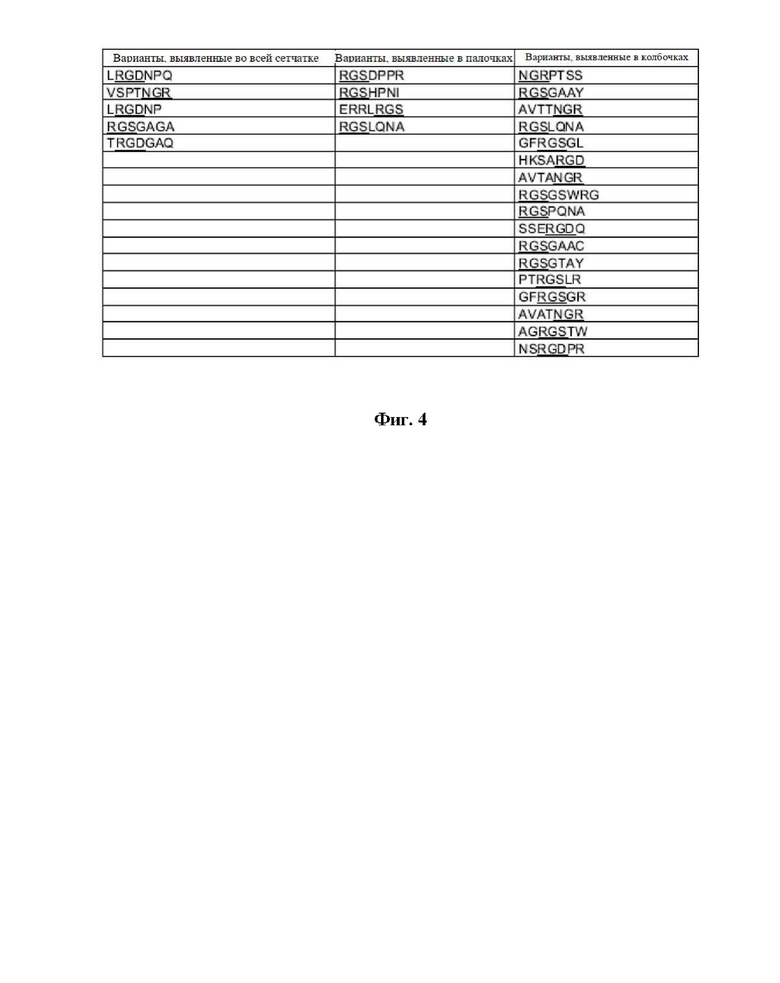
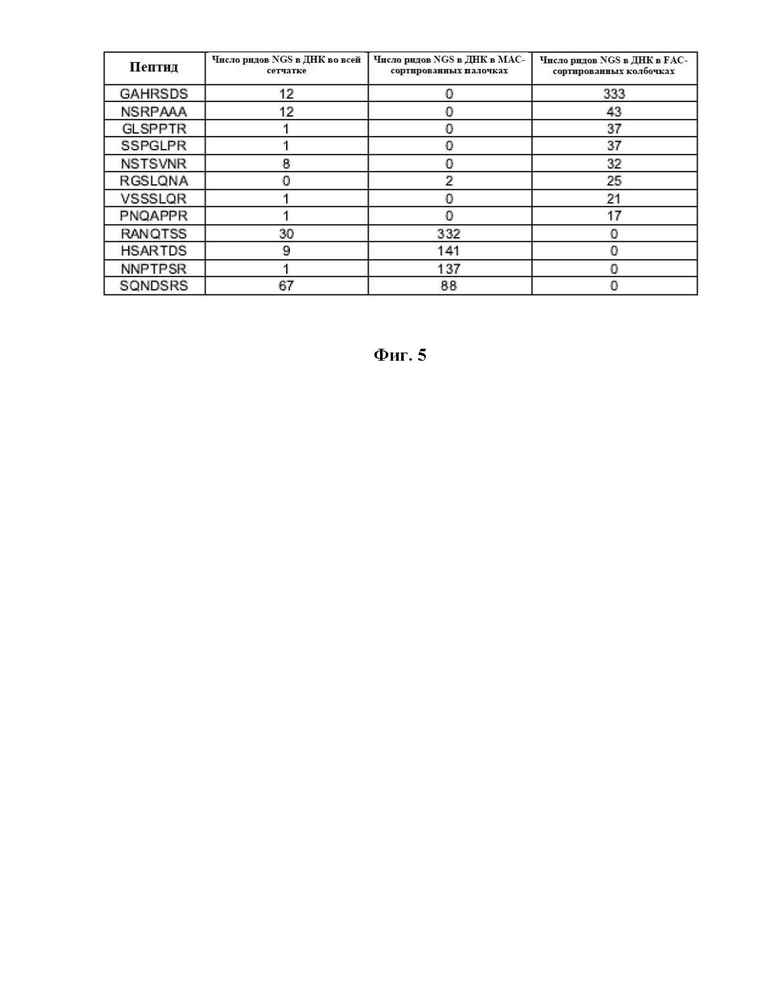
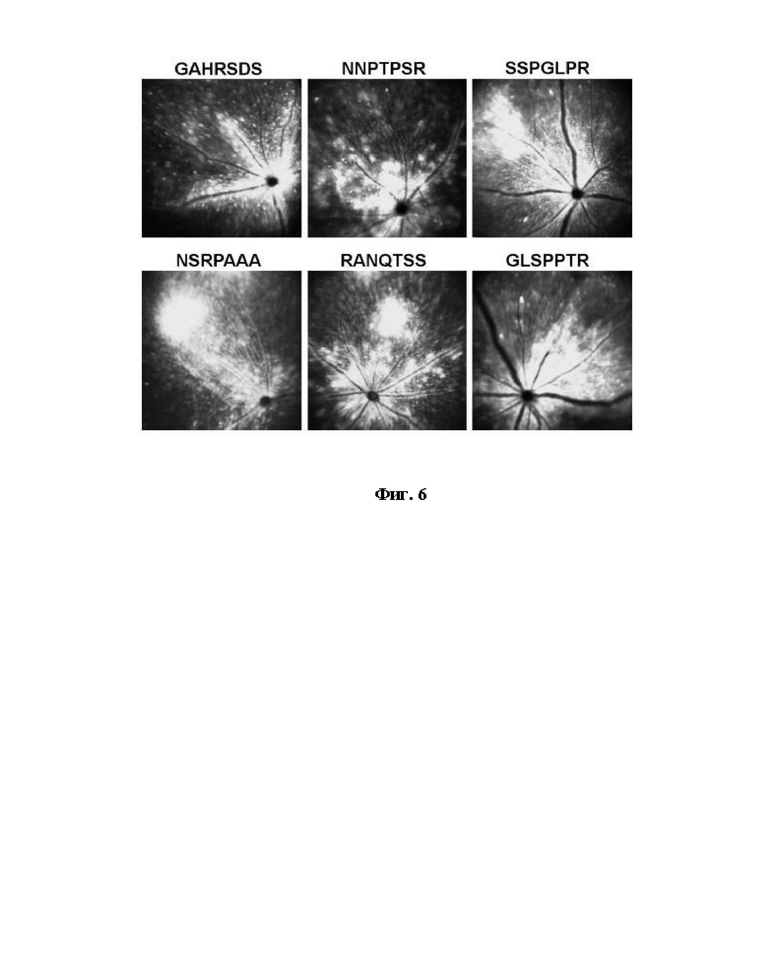
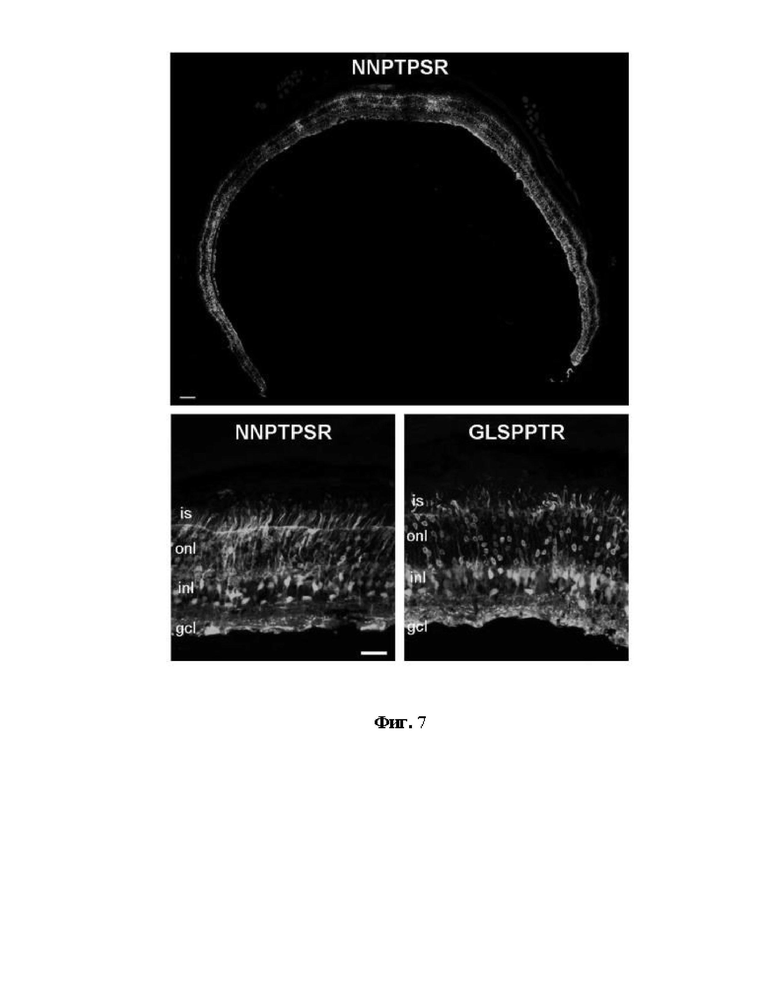
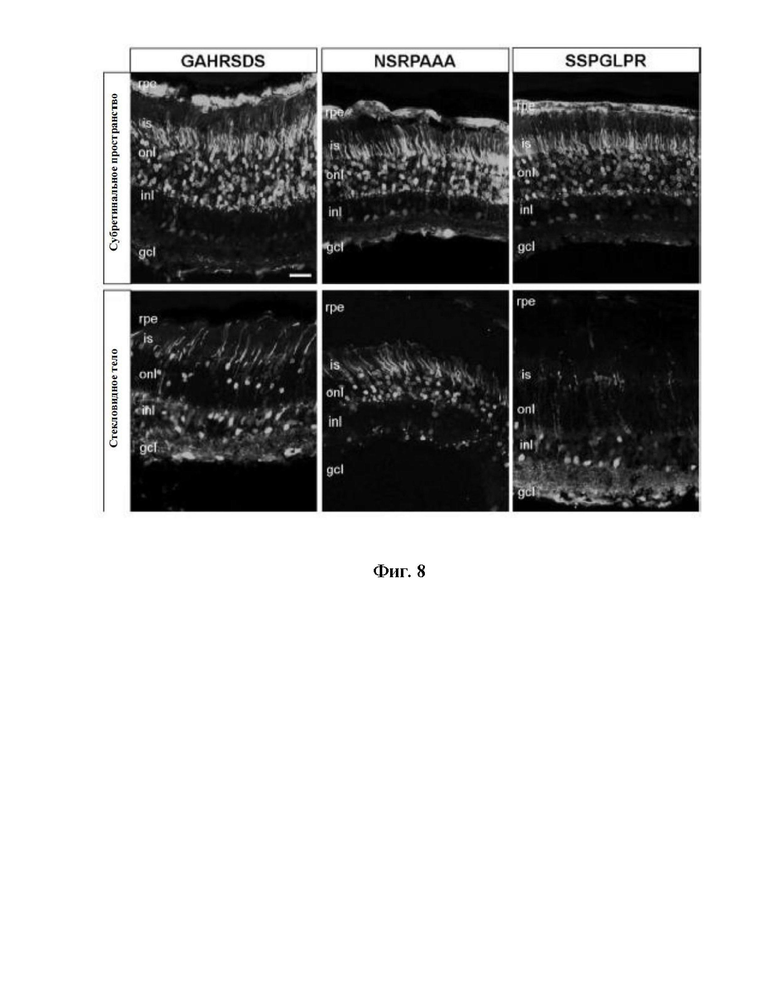
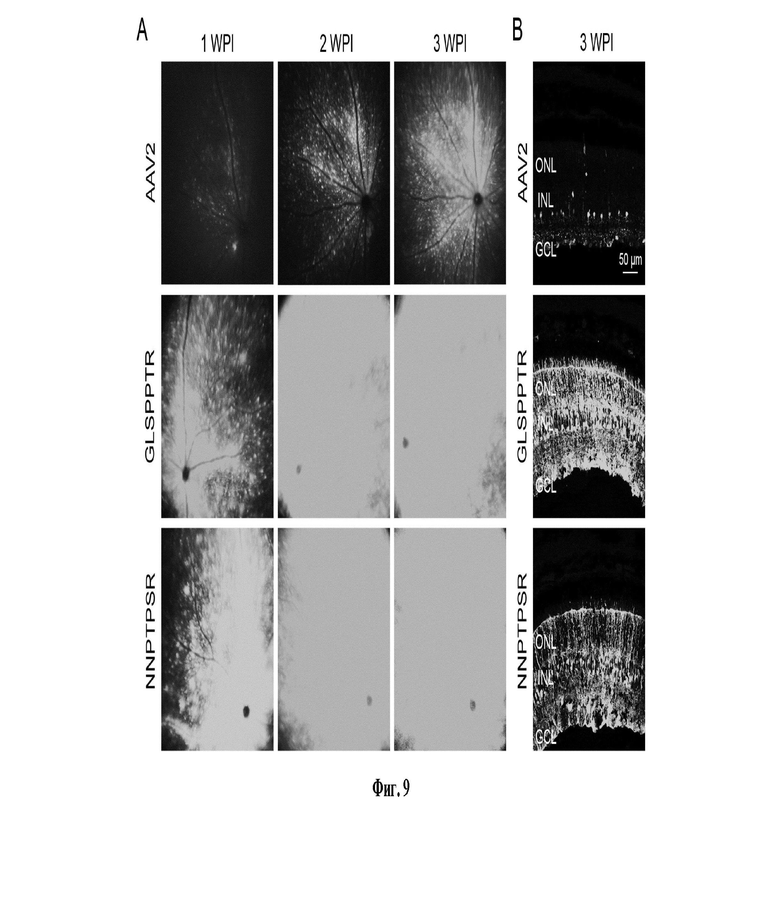
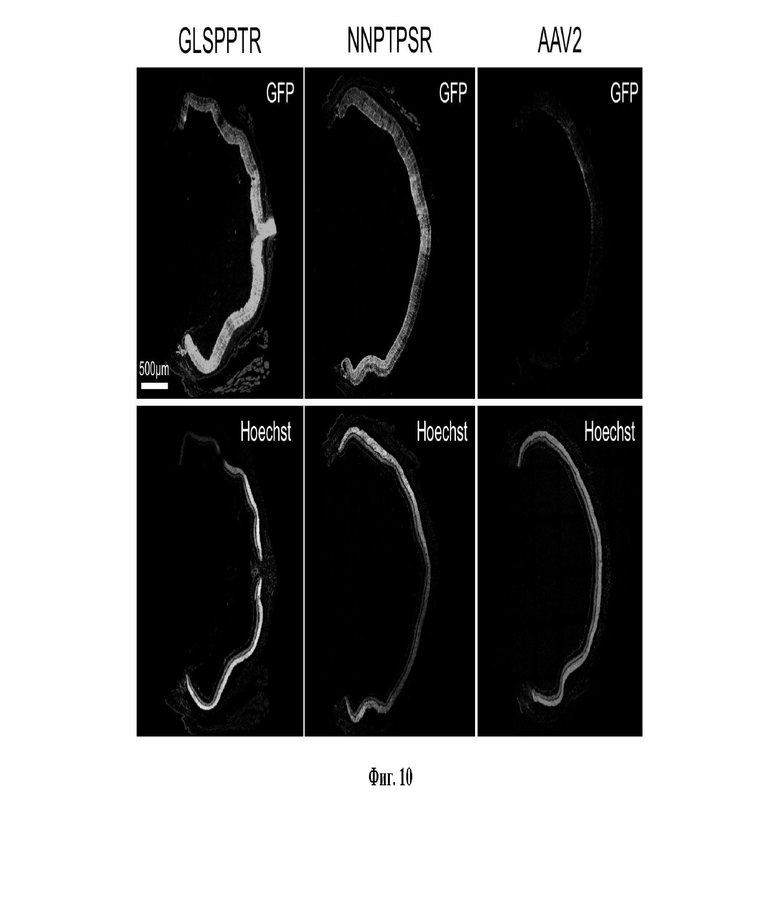
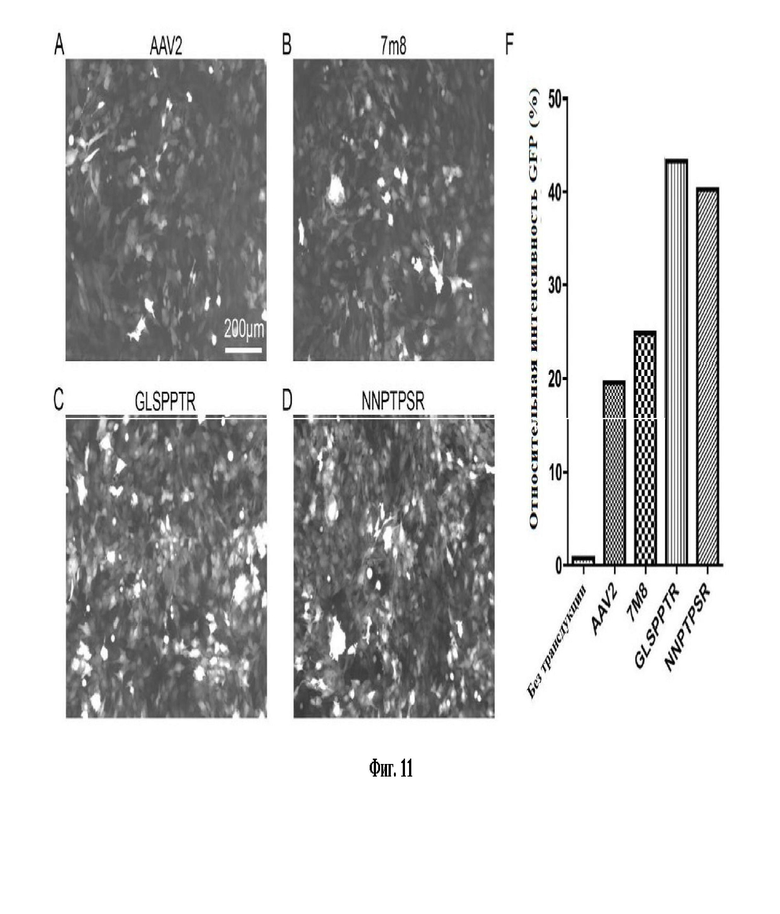
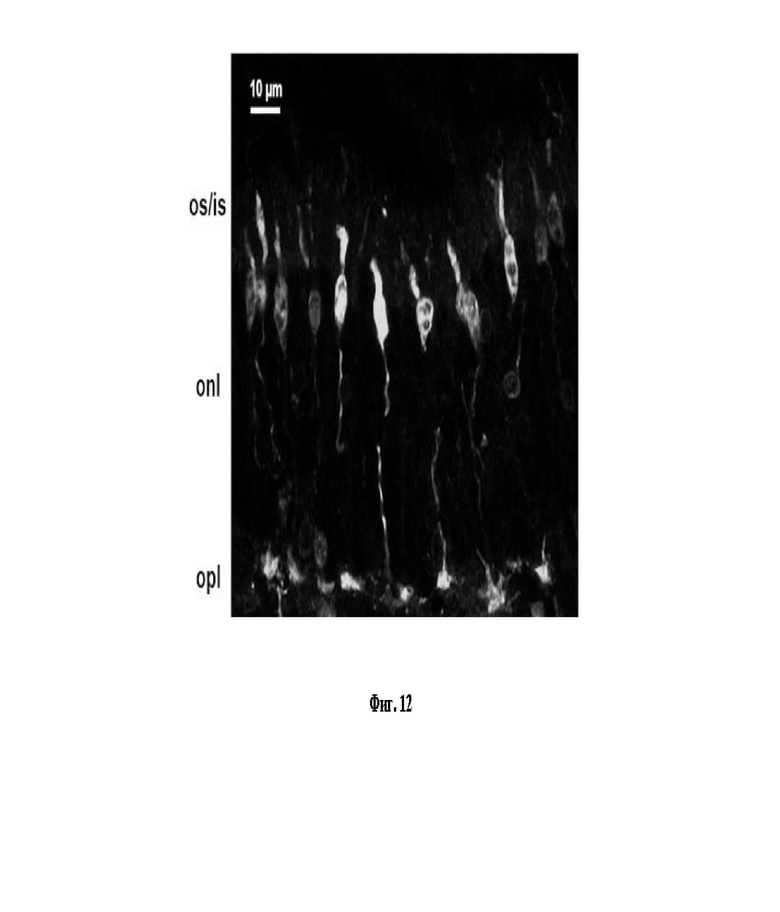
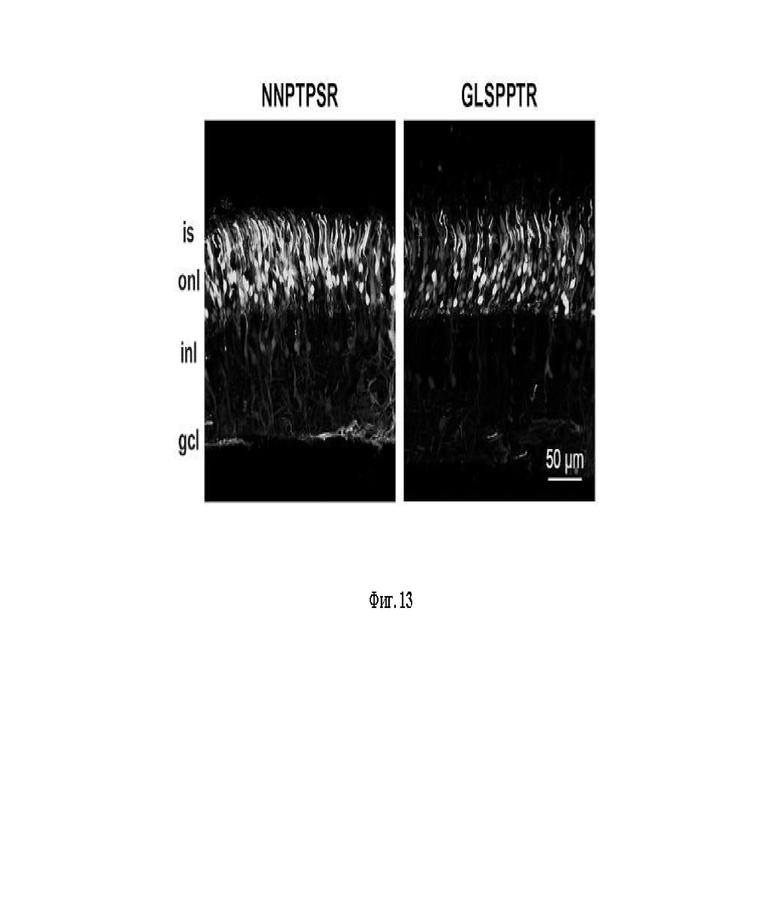


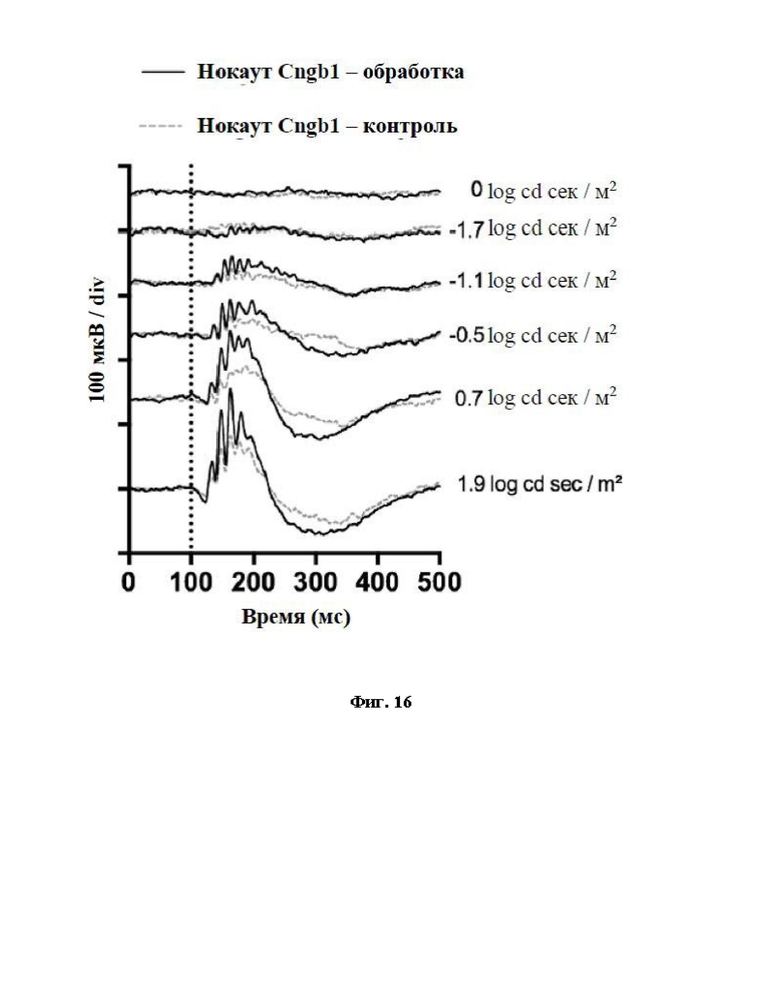
Изобретение относится к области биотехнологии. Описана группа изобретений, включающая аденоассоциированный вирус (AAV) для трансдукции клеток сетчатки, фармацевтическую композицию для переноса генов в клетки сетчатки, применение AAV для лечения поражения фоторецепторных клеток, применение in vitro AAV для трансдукции ядра клеток сетчатки и набор для переноса генов в клетки сетчатки. Изобретение расширяет арсенал средств для трансдукции клеток сетчатки. 5 н. и 9 з.п. ф-лы, 16 ил., 2 табл., 6 пр.
1. Аденоассоциированный вирус (AAV) для трансдукции клеток сетчатки, содержащий
вставочную последовательность, включающую по меньшей мере 6-8 аминокислот между позициями, соответствующими позициям 587 и 588 последовательности SEQ ID NO: 1; причем вставочная последовательность между N-концом и C-концом имеет формулу I:
X1A-X1B-X2-X3-X4-X5-X6-X7 (формула I)
в которой X5 выбрана из P (Pro), L (Leu) и V (Val);
в которой X7 - это R (Arg);
в которой X1A, X1B, X2, X3, X4, X6 независимо являются любой аминокислотой;
в которой X1A и/или X1B независимо необязательно отсутствуют или присутствуют,
или
в которой X5 выбрана из S (Ser) и T (Thr);
в которой X7 - это S (Ser);
в которой X1A, X1B, X2, X3, X4, X6 независимо являются любой аминокислотой;
в которой X1A и/или X1B независимо необязательно отсутствуют или присутствуют,
или
в которой X5 выбрана из A (Ala) и Q (Gln);
в которой X7 - это A (Ala);
в которой X1A, X1B, X2, X3, X4, X6 независимо являются любой аминокислотой;
в которой X1A и/или X1B независимо необязательно отсутствуют или присутствуют.
2. AAV по п. 1, в котором X1A отсутствует, а X1B присутствует или в котором что X1B отсутствует, а X1A присутствует.
3. AAV по п. 1 или 2, в котором вставочная последовательность фланкирована на одном или обоих своих концах одной или несколькими гибкими аминокислотами (L).
4. AAV по п. 3, в котором вставочная последовательность между N-концом и C-концом имеет формулу II:
L3-L2-L1-X1A-X1B-X2-X3-X4-X5-X6-X7-L4-L5-L6 (формула II),
в которой L1, L2, L3, L4, L5 и L6 независимо выбраны из Ala, Gly и Ser, и
в которой L1, L2, L3, L4, L5 и L6 независимо отсутствуют или присутствуют.
5. AAV по п. 4, в котором одна из X1A и X1B присутствует, а другая из X1A и X1B отсутствует, и
в котором все L1, L2, L3, L4 и L5 присутствуют и в котором L6 отсутствует.
6. AAV по любому из предыдущих пунктов, в котором X1A и/или X1B, и/или X2 и/или X3 не является кислой аминокислотой.
7. AAV по любому из предыдущих пунктов, в котором одна из X1A и X1B присутствует, а другая из X1A и X1B отсутствует и в котором X2 не является основной или кислой аминокислотой.
8. AAV по любому из предыдущих пунктов, в котором X1A, и/или X1B, и/или X2, и/или X3, и/или X4, и/или X6 не является гидрофобной ароматической аминокислотой.
9. AAV по любому из предыдущих пунктов, в котором одна из X1A и X1B присутствует, а другая из X1A и X1B отсутствует, и
в котором X1A или X1B выбрана из A, L, V, I, S, T, N, Q, C, P и G, предпочтительно X1A или X1B выбрана из G, P и N, и/или
в котором X2 выбрана из S, T, N, Q, A, L, V и I, предпочтительно X2 выбрана из N и L, и/или
в котором X3 выбрана из A, L, V, I, S, T, N, Q, C, G и P, предпочтительно X3 выбрана из S, Q и P, и/или
в котором X4 выбрана из K, R, H, D, E, S, T, N, Q, A, V, I, L, C, G и P, предпочтительно X4 выбрана из P, A и T, и/или
в котором X6 выбрана из K, R, H, D, E, S, T, N, Q, A, C, G и P, предпочтительно X6 выбрана из T, P и S.
10. AAV по любому из предыдущих пунктов, в котором вирусная ДНК AAV присутствует в ядерных экстрактах сетчатки мыши через 24 часа после внутривенного введения AAV в хвостовую вену мыши линии C57-Bl6J, и
в котором вирусная ДНК AAV присутствует в MAC-сортированных палочках с использованием магнитных микроносителей, покрытых антителами к CD73, и/или FACS-сортированных колбочках, причем колбочки экспрессируют eGFP и являются FACS-сортированными на основе их экспрессии eGFP, через 24 часа после внутривенного введения AAV в хвостовую вену мыши линии C57-Bl6J для сортировки палочек и в хвостовую вену мыши RG-eGFP линии R685933 для сортировки колбочек.
11. Фармацевтическая композиция для переноса генов в клетки сетчатки, содержащая AAV по любому из пп. 1–10 в терапевтически эффективном количестве и фармацевтически приемлемый носитель.
12. Применение AAV по любому из предыдущих пунктов для лечения поражения фоторецепторных клеток.
13. Применение in vitro AAV по любому из пп. 1-10 для трансдукции ядра клеток сетчатки.
14. Набор для переноса генов в клетки сетчатки, содержащий AAV по любому из пп. 1-10, причем указанный набор дополнительно содержит один или несколько из следующих компонентов: (i) буфер(ы); (ii) олигонуклеотид(ы); (iii) контейнер, подходящий для глазных капель, или шприц(ы), подходящие для интравитреальной инъекции.
| ГЕННАЯ ТЕРАПИЯ НЕЙРОДЕГЕНЕРАТИВНЫХ НАРУШЕНИЙ | 2010 |
|
RU2603740C2 |
| WO 2014186579 A1 20.11.2014 | |||
| WO 2015062516 A1 07.05.2015 | |||
| WO 2012145601 A2 26.10.2012 | |||
| AAV ВЕКТОРЫ С УСОВЕРШЕНСТВОВАННЫМИ Rep-КОДИРУЮЩИМИ ПОСЛЕДОВАТЕЛЬНОСТЯМИ, ИСПОЛЬЗУЕМЫМИ В СИСТЕМАХ ПРОДУКЦИИ НА ОСНОВЕ КЛЕТОК НАСЕКОМЫХ | 2007 |
|
RU2457252C2 |
| T.K | |||
| Park, et al., Intravitreal delivery of AAV8 retinoschisin results in cell type-specific gene expression and retinal rescue in the Rs1-KO mouse | |||
| Gene Therapy, 2009, 16(7), 916-926 | |||
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
Авторы
Даты
2023-03-29—Публикация
2018-10-16—Подача