Изобретение относится к физиологически активным производным гетероциклической природы, конкретно – к 2-замещенным производным 5-(гетеро)алкил-6-гидроксипиримидин-4(1H)-она, которые могут быть использованы в качестве действующих начал лекарственных препаратов, обладающих анксиолитическими свойствами.
В настоящее время известен ряд соединений различной химической структуры, которые являются активными началами анксиолитических средств [Машковский, М. Д. Лекарственные средства / М. Д. Машковский. – 16-е изд., перераб., испр. и доп. – М.: Новая волна: Издатель Умеренков, 2020. – Разд.4 (Гл. 1). – С.77-83.]. В число таковых входит и оригинальный отечественный препарат – Фенибут, сочетающий анксиолитические действие с ноотропными свойствами и обладающий относительно низкой острой токсичностью.
Тем не менее, при использовании этого препарата в высоких дозах, особенно – в течение длительного времени, может развиваться токсичное поражение печени, сопровождающееся жировой дистрофией этого органа. Это явление связано, в первую очередь с тем, что метаболизм Фенибута ((2RS)-4-амино-2-фенилбутановой кислоты) сопровождается гидроксилированием положения 4 ароматического ядра, что дает значительную нагрузку на системы микросомального окисления. Ввиду того, что Фенибут применяется в довольно высоких разовых и суточных дозах, этот побочный эффект может играть важную роль, как фактор, ограничивающий применение этого препарата.
Задачей предлагаемого изобретения является разработка новых функциональных производных ряда пиримидина, не содержащих в своей структуре ароматических, ненасыщенных или галогеналифатических заместителей, как вероятных маркеров гепатотоксичности, потенциально пригодных для использования в качестве действующих начал анксиолитических препаратов.
Техническим результатом является расширение номенклатуры соединений, оказывающих анксиолитическое действие.
Технический результат достигается при применении 2-замещенных 5-(гетеро)алкил-6-гидроксипиримидин-4(1Н)-онов общей формулы:
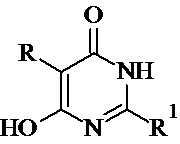 ,
,
где R=i-Pr, s-Pen, i-Pen, MeSCH2CH2, R1=SCH2CH2N(CH3)2, SCH2CH2N(CH3СH2)2, SCH2CH2N(СH2)4, SCH2CH2N(СH2)5, SCH2CH2SCH3, тиоморфолин-4-ил,
или их солянокислых солей в качестве действующих начал лекарственных препаратов, обладающих анксиолитическими свойствами.
Проявление заявленными соединениями анксиолитических свойств может быть связано с их влиянием на рецепторы ГАМК (ввиду структурного родства с производными 5,5-диалкил-2-тиобарбитуровой кислоты) [Катцунг, Б. Г. Базисная и клиническая фармакология. В 2-х т. Т.1. / Б. Г. Катцунг – М.-СПб.: Бином-Невский Диалект, 1998. – 598 с.], мелатонина (ввиду структурного сродства с производными 5-алкил-6-гидроксипиримидин-4(1H)-она, обладающих таким действием) [Virtual discovery of melatonin receptor ligands to modulate circadian rhythms / T. Che, V. Cherezov, M. L. Dubocovich, G. C. Glatfelter, X. Huang, J. J. Irwin, L. C. Johansson, A. J. Jones, H. J. Kang, T. Kenakin, J. K. McCorvy, Y. S. Moroz, B. L. Roth, O. Savych, S. Slocum, B. Stauch, R. M. Stein // Nature. – 2021. – Vol. 579, No. 7800. – P. 609-614.], [Заявка WO2021041702, МПК A61P25/20, A61P25/24, C07C15/12. – 04.03.2021г.], гистамина (ввиду структурного сродства с Нордимапритом) [Nordimaprit, homodimaprit, clobenpropit and imetit: affinities for H3 binding sites and potencies in a functional H3 receptor model / M. Kathmann, E. Schlicker, M. Detzner, H. Timmerman // Naunyn-Schmiedeberg's Archives of Pharmacology. – 1993. - Vol. 348, No. 5. – P. 498-503. – DOI: 10.1007/BF00173209], σ-рецепторы (ввиду структурного сродства с Афобазолом) [Interaction of Afobazole with Sigma-1 Receptors in the Mouse Brain / E. V. Abramova, M. V. Voronin, S. B. Seredenin // Pharmaceutical Chemistry Journal. – 2015. - Vol. 49, No. 1. – P. 7-9. – DOI: 10.1007/s11094-015-1212-1], а также прямого активирующего влияния на процессы гликолиза.
Заявляемые структурные аналоги изотиобарбамина, проявляющие анксиолитические свойства представлены в таблице 1.
Таблица 1.
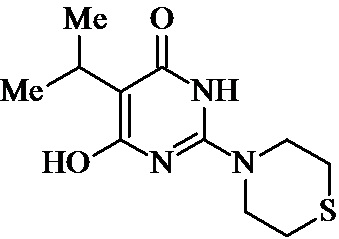
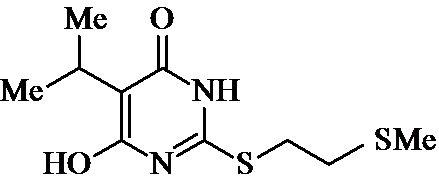
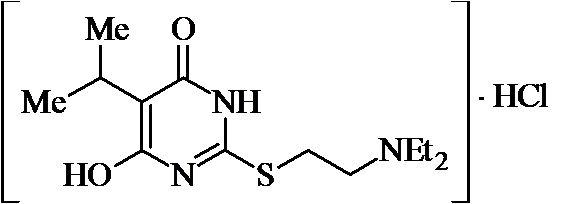
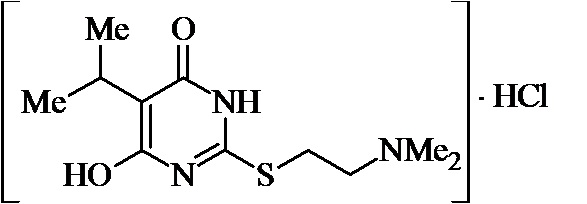
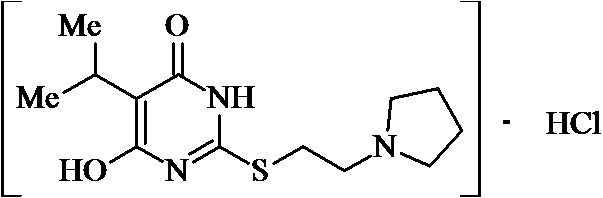
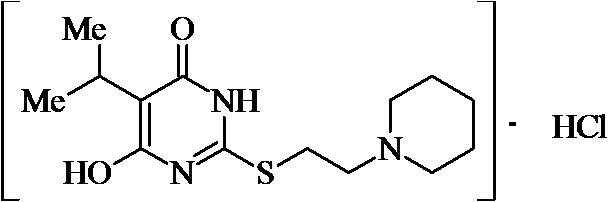
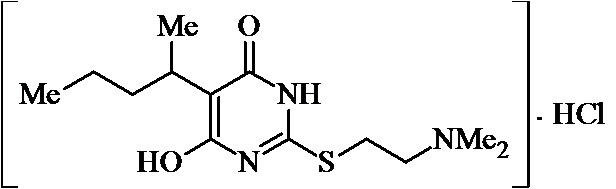
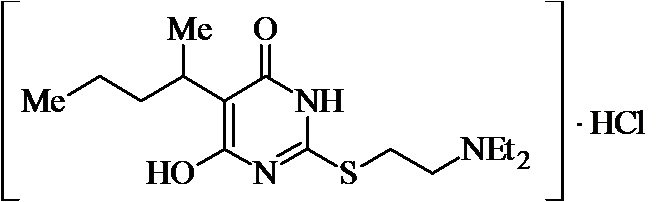
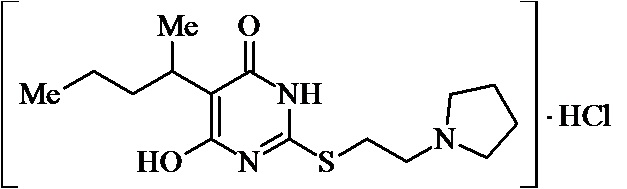
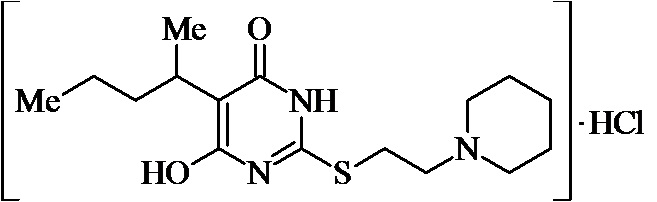
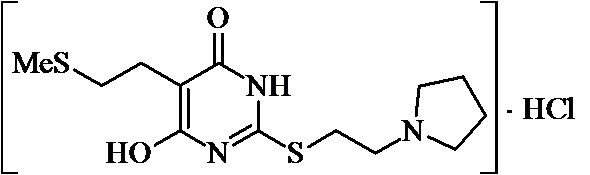
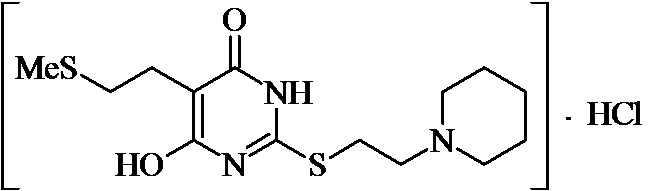
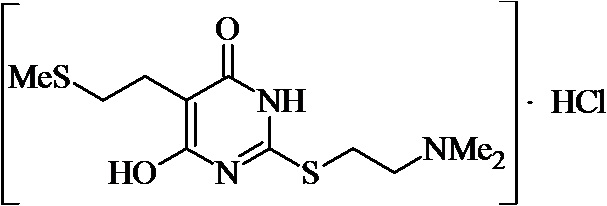
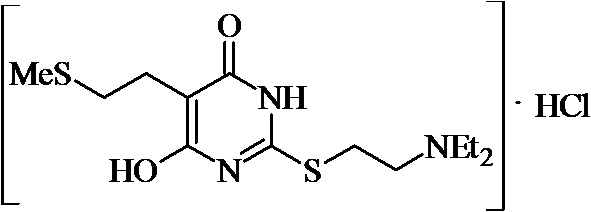
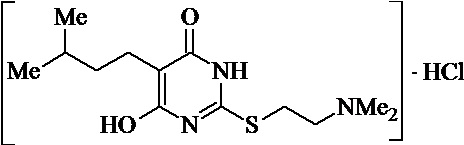
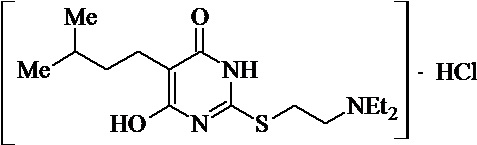
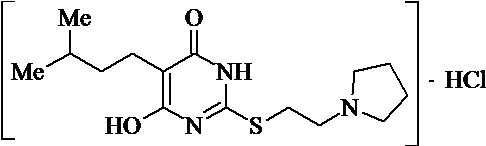
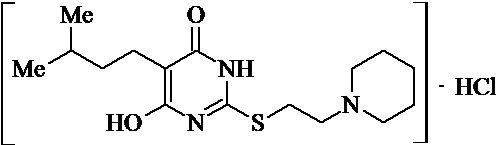
Заявленные соединения 1, 2 были получены в соответствие с методами, описанными ранее [Синтез и биологические свойства новых структурных аналогов изотиобарбамина / И. А. Новаков, Д.С. Шейкин, Е. А. Ручко, Л. Л. Брунилина, А. А. Вернигора, Н. А. Салыкин, О. В. Вострикова, В. В. Чапуркин, М. Б. Навроцкий, Д. В. Куркин, Д. А. Бакулин, М. Ю. Воронцов, Л. А. Саблина, Н. С. Ковалев, И. Н. Тюренков // Известия Академии наук. Серия химическая. – 2021. - № 11. – С. 2220-2226], а синтез соединений 3-12 осуществлялся в соответствии с методикой, представленной в статье Региоспецифичное S-аминоалкилирование 5-замещенных производных 6-гидрокси-2-тиоурацила в синтезе структурных аналогов изотиобарбамина / И. А. Новаков, Д. С. Шейкин, В. В. Чапуркин, М. Б. Навроцкий, Б. Д. Кореньков, И. А. Кириллов, П. П. Дешевов, О. В. Вострикова, Л. Л. Брунилина // Известия Академии наук. Серия химическая. – 2021. – № 5. – C. 943-948.
Синтез новых веществ этого ряда (13-18) был выполнен согласно следующему общему методу: насыщенный раствор соответствующего гидрохлорида N-(2-хлорэтил)амина в i-PrOH обрабатывали эквимолярным количеством свежеприготовленного раствора i-PrONa в i-PrOH при перемешивании и поддержании температуры ниже +5°C. Полученную суспензию фильтровали, и полученный таким образом прозрачный фильтрат добавляли по каплям к насыщенному раствору соответствующего 5-замещенного-6-гидрокси-2-тиоурацила в абсолютном i-PrOH. Полученную смесь кипятили при перемешивании c защитой от влаги в течение периода времени, необходимого для полного расхода исходного материала (ВЭЖХ-контроль). Затем реакционную смесь медленно охлаждали в холодильнике. В нескольких случаях происходило осаждение значительного количества осадка целевого вещества, которое отфильтровывалось. Фильтрат упаривали при пониженном давлении, а твердый остаток перекристаллизовывали из соответствующего растворителя. Первый и второй сорта целевого соединения смешивали вместе и перекристаллизовывали до постоянной температуры плавления. Если реакционный раствор оставался прозрачным после полного превращения исходного материала, его полностью выпаривали в вакууме, а остаток обесцвечивали и очищали путем перекристаллизации с использованием активированного угля.
Солянокислая соль 2-{[2-(диметиламино)этил]сульфанил}-6-гидрокси-5-[2-метилсульфанил)этил]пиримидин-4(3Н)-она (13).
Белые кристаллы; выход = 45 %; т.пл. = 226.7-227.2 °C. 1H ЯМР (DMSO-d6, δ, м.д., J/Гц): 3.67 (с, 2H), 3.35-3.37 (м, 4H), 2.81 (с, 7H), 2.51-2.55 (м, 4H), 2.05 (с, 3H). 13C ЯМР (D2O, δ, м.д.): 169.90, 159.71, 101.22, 59.30, 45.75, 34.43, 27.24, 24.48, 17.05. Масс-спектр: найдено 290.0991 m/z [M + H]+; вычислено для C11H20N3O2S2+ (m/z) 290.0998. Элементный анализ: найдено (%) C, 42.15; H, 6.96; Cl, 10.04; N, 11.49; S, 19.38; вычислено для C13H26ClN3O3S2 (с C2H5OH) (%) C, 41.98; H, 7.05; Cl, 9.53; N, 11.30; S, 17.24.
Солянокислая соль 2-{[2-(диэтиламино)этил]сульфанил}-6-гидрокси-5-[2-(метилсульфанил)этил]пиримидин-4(3H)-она (14).
Белые кристаллы; выход = 44 %; т.пл. = 197.3-198.9 °C. 1H ЯМР (DMSO-d6, δ, м.д., J/Гц): 3.68 (с, 2H), 3.31-3.39 (м, 4H), 3.14-3.19 (м, 4H), 2.51-2.55 (м, 4H), 2.04 (с, 3H), 1.19 (т, 7H, J = 7.2). 13C ЯМР (D2O, δ, м.д.): 169.52, 160.01, 101.47, 53.63, 50.68, 34.38, 26.94, 24.38, 17.06, 10.98. Масс-спектр: найдено (m/z) 318.1304 [M + H]+; вычислено для C13H24N3O2S2+ (m/z) 318.1311. Элементный анализ: найдено (%) C, 44.11; H, 6.87; Cl, 9.94; N, 11.91; S, 18.05; вычислено для C13H24ClN3O2S2 (%) C, 44.12; H, 6.84; Cl, 10.02; N, 11.87; S, 18.12.
Солянокислая соль 2-{[2-(диметиламино)этил]сульфанил}-6-гидрокси-5-(3-метилбутил)пиримидин-4(3Н)-она (15).
Белые кристаллы; выход = 49 %; т.пл. = 256.7-257.2 °C. 1H ЯМР (DMSO-d6, δ, м.д., J/Гц): 3.67 (с, 2H), 3.36 (т, 4H, J = 4.5), 2.81 (с, 7H), 2.24 (т, 2H, J = 7.8), 1.44 (сеп, 1H, J = 6.6), 1.22-1.26 (м, 2H), 0.85 (д, 6H, J = 6.6). 13C ЯМР (D2O, δ, м.д.): 169.31, 158.66, 103.94, 59.12, 45.62, 39.27, 30.23, 27.06, 24.51, 22.70. Масс-спектр: найдено (m/z) 286.1584 [M + H]+; вычислено для C13H24N3O2S+ (m/z) 286.1590. Элементный анализ: найдено (%) C, 48.36; H, 7.52; Cl, 10.97; N, 12.88; S, 9.90; вычислено для C13H24ClN3O2S (%): C, 48.51; H, 7.52; Cl, 11.01; N, 13.06; S, 9.96.
Солянокислая соль 2-{[2-(диэтиламино)этил]сульфанил}-6-гидрокси-5-(3-метилбутил)пиримидин-4(3Н)-она (16).
Белые кристаллы; выход = 52 %; т.пл. = 179.5-180.5 °C. 1H ЯМР (DMSO-d6, δ, м.д., J/Гц): 3.68 (с, 2H), 3.29-3.38 (м, 4H), 3.16 (кв, 4H, J = 7.2), 2.24 (т, 2H, J = 7.8), 1.45 (сеп, 1H, J = 6.6), 1.22-1.26 (м, 2H), 1.19 (т, 7H, J = 7.2), 0.85 (д, 6H, J = 6.7). 13C NMR (D2O, δ, м.д.): 166.21, 155.57, 100.79, 50.53, 47.38, 36.13, 27.05, 23.72, 21.35, 19.55, 7.66. Масс-спектр: найдено (m/z) 314.1897 [M + H]+; вычислено для C15H28N3O2S+ (m/z) 314.1903. Элементный анализ: найдено (%) C, 51.43; H, 8.06; Cl, 10.11; N, 11.94; S, 9.18; вычислено для C15H28ClN3O2S (%): C, 51.49; H, 8.07; Cl, 10.13; N, 12.01; S, 9.16.
Солянокислая соль 6-гидрокси-5-(3-метилбутил)-2-{[2-(пирролидин-1-ил)этил]сульфанил}пиримидин-4(3Н)-она (17).
Белые кристаллы; выход = 58 %; т.пл. = 242.3-242.7 °C. 1H ЯМР (DMSO-d6, δ, м.д., J/Гц): 3.67 (с, 2H), 3.32-3.44 (м, 4H), 2.24 (т, 2H, J = 7.8), 1.93 (уш. с, 9H), 1.45 (сеп, 1H, J = 6.6), 1.21-1.26 (м, 2H), 0.85 (д, 6H, J = 6.6). 13C ЯМР (D2O, δ, м.д.): 166.28, 158.02, 101.13, 54.30, 36.42, 27.40, 25.31, 22.50, 21.68, 19.83. Масс-спектр: найдено (m/z) 312.1740 [M + H]+; вычислено для C15H26N3O2S+ (m/z) 312.1746. Элементный анализ; найдено (%) C, 51.72; H, 7.57; Cl, 10.18; N, 11.98; S, 9.08; вычислено для C15H26ClN3O2S (%) C, 51.79; H, 7.53; Cl, 10.19; N, 12.08; S, 9.22.
Солянокислая соль 6-гидрокси-5-(3-метилбутил)-2-{[2-(пиперидин-1-ил)этил]сульфанил}пиримидин-4(3Н)-она (18).
Белые кристаллы; выход = 46 %; т.пл. = 242.4-243.2 °C. 1H ЯМР (DMSO-d6, δ, м.д., J/Гц): 3.67 (с, 2H), 3.29-3.39 (м, 4H), 2.24 (т, 2H, J = 7.8), 1.73 (уш. с, 11H), 1.45 (сеп, 1H, J = 6.7), 1.22-1.26 (м, 2H), 0.85 (д, 6H, J = 6.6). 13C ЯМР (D2O, δ, м.д.): 167.17, 158.93, 103.81, 58.49, 39.31, 30.28, 25.36, 24.56, 23.68, 22.73. Масс-спектр: найдено (m/z) 326.1897 [M + H]+; вычислено для C16H27N3O2S+ (m/z) 326.1903. Элементный анализ: найдено (%) C, 53.00; H, 7.72; Cl, 9.66; N, 11.60; S, 9.02; вычислено для C16H28ClN3O2S (%) C, 53.10; H, 7.80; Cl, 9.79; N, 11.61; S, 8.86.
Исследование анксиолитических свойств заявленных соединений были выполнены на крысах линии Вистар.
Анксиолитические свойства в скрининге изучались в тестах открытое поле (ОП) и приподнятый крестообразный лабиринт (ПКЛ) в сравнении с фенибутом.
Скрининговые исследования производных барбитуровой кислоты проводились в равных дозах 3 мг/кг. Препарат сравнения (Фенибут) вводили в дозе 25 мг/кг. Все вещества вводили перорально через желудочный зонд за 60 минут до тестирования. Статистическая обработка данных производилась по критерию Краскелла-Уоллиса с постобработкой критерием Данна.
Суммированные данные о поведении животных в открытом поле, приподнятом крестообразном лабиринте представлены в таблице 2.
Таблица 2.
Из представленных данных видно, что в приведенных экспериментах полученные соединения проявляют активность сопоставимую с Фенибутом, оказывают выраженное анксиолитическое действие в тестах «Приподнятый крестообразный лабиринт», что проявилось в большем количестве переходов между рукавами, более длительном пребывании в открытых рукавах, большем числе стоек и свешиваний с открытых рукавов, при этом действуя в дозе примерно в 8 раз ниже таковой для Фенибута.
Таким образом, заявленные 2-замещенные 5-(гетеро)алкил-6-гидроксипиримидин-4(1H)-оны или их солянокислые соли, обладающие анксиолитической активностью, позволяют расширить номенклатуру соединений, оказывающих анксиолитическое действие.
| название | год | авторы | номер документа |
|---|---|---|---|
| 2-Замещенные 5-(гетеро)алкил-6-гидроксипиримидин-4(1H)-оны, обладающие ноотропной активностью | 2022 |
|
RU2793806C1 |
| 2-Замещенные 5-(гетеро)алкил-6-гидроксипиримидин-4(1H)-оны, обладающие антидепрессантной активностью | 2021 |
|
RU2792888C1 |
| ГИБРИДНЫЕ СОЕДИНЕНИЯ НА ОСНОВЕ ФУРАН-2(3Н)-ОНА И ХРОМЕН-4(4Н)-ТИОНА, ОБЛАДАЮЩИЕ АНТИБАКТЕРИАЛЬНОЙ АКТИВНОСТЬЮ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2024 |
|
RU2830172C1 |
| Способ получения 2-амино-4-арил-6-гексил-7-гидрокси-4H-хромен-3-карбонитрилов | 2022 |
|
RU2802631C1 |
| Способ получения изотиобарбамина | 2020 |
|
RU2744470C1 |
| Способ получения 4-арилзамещенных 7-гидрокси-6'-фенил-5',6'-дигидро-1'Н-спиро[хроман-2,4'-пиримидин]-2'(3'H)-онов | 2023 |
|
RU2818006C1 |
| Способ получения 4-арилзамещенных 8-гидрокси-5,10а-диметил-1,3,4,10а-тетрагидро-2Н-хромено[2.3-d]пиримидин-2-онов(тионов) | 2023 |
|
RU2821110C1 |
| Способ получения замещенных O-алкилированных гексагидро-2H-хромено[4,3-d]пиримидин-2,5(1H)-дионов | 2022 |
|
RU2796532C1 |
| Противотуберкулезное средство на основе 4'-гидрокси-1'-(2-гидроксифенил)-3'-ацил-спиро[бензо[b][1,4]тиазин-2,2'-пиррол]-3,5'(1'H,4H)-дионов | 2023 |
|
RU2806097C1 |
| Азопроизводные аминофенолов, обладающие способностью ингибировать образование конечных продуктов гликирования | 2024 |
|
RU2839138C1 |
Изобретение относится к фармацевтике, а именно к применению 2-замещенных 5-(гетеро)алкил-6-гидроксипиримидин-4(1Н)-онов общей формулы 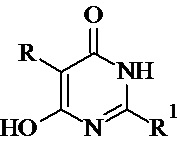 ,
,
где R=i-Pr, s-Pen, i-Pen, MeSCH2CH2, R1=SCH2CH2N(CH3)2, SCH2CH2N(CH3СH2)2, SCH2CH2N(СH2)4, SCH2CH2N(СH2)5, SCH2CH2SCH3, тиоморфолин-4-ил, или их солянокислых солей в качестве действующих начал лекарственных препаратов, обладающих анксиолитической активностью. Технический результат: эффективное анксиолитическое действие. 2 табл.
Применение 2-замещенных 5-(гетеро)алкил-6-гидроксипиримидин-4(1Н)-онов общей формулы:
 ,
,
где
R=i-Pr, s-Pen, i-Pen, MeSCH2CH2,
R1=SCH2CH2N(CH3)2, SCH2CH2N(CH3СH2)2, SCH2CH2N(СH2)4, SCH2CH2N(СH2)5, SCH2CH2SCH3, тиоморфолин-4-ил,
или их солянокислых солей в качестве действующих начал лекарственных препаратов, обладающих анксиолитическими свойствами.
| Novakov, I.A., и др | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Деревянный торцевой шкив | 1922 |
|
SU70A1 |
| Аппарат для гашения извести | 1931 |
|
SU27324A1 |
| WO 2015200619 A1, 30.12.2015 | |||
| Рентгеновская трубка | 1926 |
|
SU6942A1 |
Авторы
Даты
2023-04-04—Публикация
2021-12-03—Подача