Изобретение относится к способу получения N,N-диметил-4-бифениламина и его производных.
Бифенильный фрагмент часто встречается в составе различных лекарственных структур, среди них препараты, обладающие противоамебным, противогрибковым, противоинфекционным, антигиперхолестеринемическим (снижающим уровень холистерина в крови), антигиперлипопротеинемическим (снижающим уровень липопротеинов, осуществляющих перенос жиров в различных тканях организма), фасциолицидным (применимым в лечении фасциолеза - вирусного поражения печени, заболевание характеризуется лихорадкой, крапивницей, тошнотой, желтухой, болями в правом подреберье, увеличением размеров печени), противоревматическим, обезболивающим, противовоспалительным, антитромботическим и антиаритмическим действием [1].
На сегодняшний день используется множество методик каталитического кросс-сочетания для получения N,N-диметил-4-бифениламина и его производных, ставших классическими, а именно реакции Сузуки-Мияура [2-6], Кумада [7-9], Негиши [9-14], модификация Нигеши [15] и Гомбердта-Бахмана [15-17], Хайяма [18-20].
Последняя реакция осуществляется между ароматическими галогенидами и арил-триметилсиланами под действием комплексов палладия. Металлический катализатор и органосилан активируются фторидом калия [18]. Реакция протекает в среде пропиленгликоля при температуре 100°С в течение 12 часов. Несмотря на высокий выход целевого продукта (>95%), существенными недостатками данной реакции является высокая себестоимость палладиевого катализатора и арил-триметилсилана, токсичность фторида калия (ПДК 2 мг/л), необходимость проведения реакции при высокой температуре (100°С), длительность синтетической процедуры (12 ч).
Наиболее близким является способ получения бифенилов и их производных [15], включающий взаимодействие диазосоединения в растворе спирта. Получение целевого продукта осуществляется через взаимодействие фторборида фенилдиазония и реактива Гриньяра. Методика синтеза предполагает последовательное добавление рутениевого катализатора, хлорида никеля, соль диазония в раствор этанола. Параллельно получают цинк дифенил перемешиванием 2 часа в тетрагидрофуране реактива Гриньяра, бромида цинка (в соотношении 2:1) и бромида лития для поддержания нейтральной рН-среды во избежание разрушения реактива. По окончании реакции растворитель удаляют, остаток разбавляют толуолом, полученный раствор смешивают со спиртовым, переносят в светоизлучающую пробирку, которую затем запечатывают в тефлоне и действуют светодиодом, инициирующим образование арильного радикала под катализом рутениевого комплекса на борфторид арилдиазония и фенильного радикала взаимодействием дихлорида никеля и цинкдифенила. Выделение целевого продукта осуществляют разбавлением реакционной смеси водой с последующей экстракцией этилацетатом. Органический слой высушивают над сульфатом натрия, промывают насыщенным раствором хлорида натрия, концентрируют под вакуумом. Последующее элюирование смесью этилацетат : гексан (30%:5%) на хроматографической колонке дает чистый бифенил белого цвета с выходом 73%. Недостатком является высокая себестоимость рутениевого и никелевого катализаторов, многостадийность синтеза (получение дифенилцинка, затем - целевого продукта) и длительность химического процесса (перемешивание реакционной смеси с реактивом Гриньяра, бромидами лития и цинка 2 часа, инициирующее облучение), наряду с необходимостью в сооружении сложных химических установок - для вакуумной перегонки, чтобы удалить тетрагидрофуран, и светодиодного излучения, потери целевого продукта при его экстракции с последующим высушиванием и промыванием органического слоя. Более того, длительность очистки реакционной смеси на хроматографической колонке приводит к утечке растворителей, необходимость в соблюдении точности при добавлении компонентов реакционной смеси, приготовлении элюента (этилацетат : гексан 30%:5%).
Цель изобретения - разработка простой эффективной методики синтеза N,N-диметил-4-бифениламина и его производных.
Техническим результатом является относительно низкая себестоимость реактивов, отсутствие необходимости использования катализаторов и оснований, упрощение способа получения N,N-диметил-4-бифениламина и его производных с одновременным сокращением времени протекания реакции.
Технический результат достигается, что способ получения N,N-диметил-4-бифениламина и его производных общей формулы (R1)Ph-Ph(R2)-N(CH3)2, где R1 - Н, n-СООСН3, R2 - Н, о-СН3 включает взаимодействие N,N-диметиламино-фенилдиазенил-арила, тетрацианоэтилена и метанола под действием ультразвука при частоте 90-100 Гц, температуре 35-40°С. В зависимости от выбранного диазосоединения время реакции варьируется от двух до десяти минут.
Сущность изобретения состоит во взаимодействии N,N-диметиламино-фенилдиазениларила, тетрацианоэтилена и метанола под действием ультразвука при частоте 90-100 Гц, температуре 35-40°С в течении 2-10 минут. Целевой продукт, выпавший в осадок, отфильтровывают на фильтре Шота, промывают холодным этилацетатом.
Схема взаимодействия N,N-диметиламино-фенилдиазениларила с тетрацианоэтиленом в среде метанола под действием ультразвука:
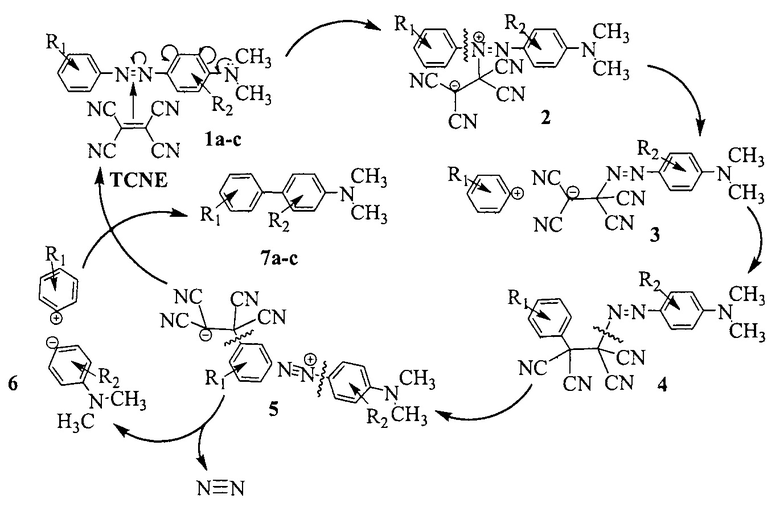
где
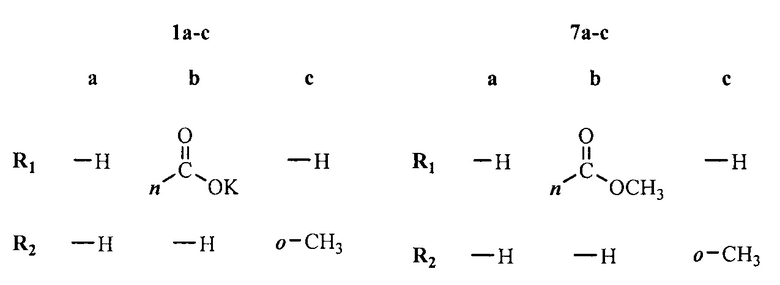
Для получения используют следующие соединения: диметиланилин (ГОСТ 5855-78), о-метилдиметиланилин (ГОСТ 30188-97), анилин (ГОСТ 5819-78), парааминобензоат калия (ГОСТ 5354-79), нитрит натрия (ГОСТ 19906-74), тетрафторборную кислоту (ГОСТ 2567-89), метанол (ГОСТ 2222-95), тетрацианоэтилен (Acros Organics).
О-Метилдиметиланилин, парааминобензоат калия были приобретены у коммерческих поставщиков и использовались без дальнейшей очистки. Тетрацианоэтилен был предварительно перекристаллизован из диоксана, метанол перегнан при температуре 64°С, диметиланилин - под вакуумом при температуре 150°С, анилин - под вакуумом при температуре 130°С. Протекание реакции и чистоту продуктов контролируют методом ТСХ на пластинах Sorbfil (пятна визуализировались в УФ-свете, при обработке парами йода или при нагревании). Температуры плавления и разложения определены на приборе Optimelt МРА100. ИК-спектры записаны на спектрометре ФСМ-1202 с преобразованием Фурье для образцов, диспергированных в нуйоле. Спектры ЯМР 1Н и 13С записаны в ДМСО-d6 с внутренним стандартом ТМС на спектрометре Bruker AVANCE400 WB при рабочей частоте 400,13 МГц для 1Н и 100,61 МГц для 13С.
Бензендиазоний и 4-Калийкарбоксибензендиазоний синтезированы по общей методике [21]: для этого анилин или парааминобензоат калия (76 ммоль) добавляют к перемешанному раствору тетрафторборной кислоты (48% по массе) и воды (20 см3), раствор помещают на ледяную баню и перемешивают, добавляя по каплям холодный водный раствор нитрита натрия (76 ммоль) в воде (5 см3), реакционную смесь перемешивают по мере повышения температуры до комнатной температуры, затем фильтруют при пониженном давлении для отделения осадка, который промывают разбавленным водным раствором тетрафторборной кислоты, этанола и диэтилового эфира, затем сушат под вакуумом. Продукт очищают растворением в ацетоне с последующим осаждением диэтиловым эфиром.
(Е)-N,N-Диметил-4-(фенилдиазенил)анилин 1а, калий (Е)-4-((4-(диметиламино)фенил)диазенил)бензоат 1b, (Е)-N,N,3-триметил-4-(фенилдиазенил)анилин 1с были получены по общей методике [22]: к ледяному раствору соответствующего арила (диметиланилина или о-метилдиметиланилина) (0,02 моль) в этаноле (25 мл), содержащему каталитическое количество ацетата натрия (0,5 г), на ледяной бане добавляют холодный раствор фторборида арилдиазония (0,02 моль) по каплям при непрерывном перемешивании при 0°С. После завершения реакции, раствор перемешивают в течение дополнительных 30 минут при комнатной температуре. Осажденный твердый материал отфильтровывают, сушат и перекристаллизовывают из этанола.
Ниже приведены примеры осуществления изобретения.
Пример 1. Синтез N,N-диметил-[1,1'-бифенил]-4-амина (7а).
К 0,88 г (0,0039 моль) (Е)-N,N-Диметил-4-(фенилдиазенил)анилина 1а, растворенному в метаноле, прибавляют 0,50 г (0,0039 моль) тетрацианоэтилена. Реакционную смесь помещают в ультразвуковой реактор, при частоте 90-100 Гц температуре 35°С на 2 минуты, после чего наблюдают выпадение целевого продукта. Осадок отфильтровывают на фильтре Шотта, промывают холодным этилацетатом. Выход 84% (0,65 г), т.пл. 117°С [23]. ЯМР 1Н δ, м.д, J, Гц (ДМСО-d6): 7.83 - 7.73 (m, 4Н, (СН12,8,6,4)4, 7.55 - 7.47 (m, 2Н, (СН3,1)2), 6.86 - 6.79 (m, 2Н, (СН11,9)2), 3.17 - 2.87 (s, 6Н, N(CH3)2). ЯМР 13С м. д., (ДМСО-d6): 152.56 (С5), 152.44 (С7), 142.59 (С10), 129.65 (СН2), 129.28 ((СН12,8,6,4)4), 124.80 ((СН3,1)2), 121.86 ((СН9,11)2), 56.55 (С17), 49.84 (СН33,16), 38.93 (N(CH3)2). Масс, m/z: Выч. C14H15N: 197.1265 (100%) [М]+. Найдено, С 84.32; Н 7.80; N 7.41. C14H15N. Вычислено, %: С 85.24; Н 7.66; N 7.10.
Пример 2. Синтез метил 4'-(диметиламино)-[1,1'-бифенил]-4-карбоксилата (7b).
К 1,21 г (0,0039 моль) калий (Е)-4-((4-(диметиламино)фенил)диазенил)бензоата 1b, растворенному в метаноле, прибавляют 0,50 г (0,0039 моль) тетрацианоэтилена. Реакционную смесь помещают в ультразвуковой реактор, при частоте 90-100 Гц температуре 40°С на 5 минут, после чего наблюдают выпадение целевого продукта. Осадок отфильтровывают на фильтре Шотта, промывают холодным этилацетатом. Выход 57% (0,57 г), т.пл. 215°С [24]. ЯМР 1Н δ, м.д., J, Гц (ДМСО-d6): 8.20 - 7.95 (m, 2Н, (СН3,1)2), 7.89 - 7.67 (m, 4Н, (СН14,10,6.4)4), 7.35 (d, J=0.7 Hz, 1Н, СН20), 6.84 (dd, J=9.3, 2.0 Hz, 2H, (CH13,11)2), 3.42 (s, 3H, OCH3), 3.17 - 2.96 (m, 6H, N(CH3)2). ЯМР 13C м.д., (ДМСО-d6): 169.88 (C=O), 16 7.26 (С12), 152.95 (С9), 142.72 (С5), 130.70 (С2), 130.43 ((С14,10,6,4)4), 125.21 ((СН3,1)2), 121.60 ((СН18,11)2), 56.56 (СН20), 49.84 (ОСН3), 38.93 (N(CH3)2). Масс, m/z: Выч. C16H17NO2: 255.1298 (100%) [М]+. Найдено, С 74.98; Н 6.65; N 5.33. C16H17NO2. Вычислено, %: С 75.27; Н 6.71; N 5.49.
Пример 3. Синтез N,N-диметил-2-метил-[1,1'-бифенил]-4-амина (7с).
К 0,93 г (0,0039 моль) (Е)-N,N,3-триметил-4-(фенилдиазенил)анилина 1с, растворенному в метаноле, прибавляют 0,50 г (0,0039 моль) тетрацианоэтилена. Реакционную смесь помещают в ультразвуковой реактор, при частоте 90-100 Гц температуре 40°С перемешивают 2 раза по 5 минут, после чего наблюдают выпадение целевого продукта. Осадок отфильтровают на фильтре Шотта, промывают холодным этилацетатом. Выход 60% (0,49 г), т.пл. 162°С. ЯМР 1Н δ, м.д., J, Гц (ДМСО-d6): 7.75 (t, J=1.7 Hz, 1Н, СН8), 7.74 (t, J=1.5 Hz, 1H, CH12), 7.61 (dd, J=5.4, 1.9 Hz, 1H, CH4), 7.53 -7.47 (m, 2H, (CH11,9)2), 7.42 - 7.36 (m, 1H, CH10), 6.73 (d, J=2.9 Hz, 1H, CH3), 6.70 (s, 1H, CH1), 3.64 (s, 3H, OCH3), 3.07 (s, 6H, N(CH3)2), 2.61 (s, 3Н, СН3). ЯМР 13C м.д., (ДМСО-d6): 169.91 (C=O), 153.12 (С2), 140.26 (С7), 139.05 (С6), 132.27 (С5), 129.64 (СН1), 129.32((СН12-8)4), 129.13 (СН13), 123.02 (СН2), 56.50 (ОСН3), 49.85 (СН3), 17.91 (N(CH3)2). Масс, m/z: Выч. C15H17N: 211.1453 (100.0%) [М]+. Найдено, С 85.14; Н 9.21; N 6.85. C15H17N. Вычислено, %: С 85.26; Н 8.11; N 6.63.
Таким образом, для синтеза бифенильных структур разработан новый упрощенный способ получения целевых продуктов с хорошими выходами, не требует дорогостоящих реактивов, использования катализаторов и оснований значительно снижает продолжительность процесса за счет действия ультразвука.
ЦИТИРОВАННЫЕ ДОКУМЕНТЫ
[1] Horton, D.A., Bourne, G.Т., & Smythe, M.L. (2003). The Combinatorial Synthesis of Bicyclic Privileged Structures or Privileged Substructures. Chemical Reviews, 103(3), 893-930. doi:10.1021/cr020033s
[2] Sawamura, M., Arashima, J., & Iwai, T. (2018). A Polystyrene-Cross-Linking Tricyclohexylphosphine: Synthesis, Characterization and Applications to Pd-Catalyzed Cross-Coupling Reactions of Aryl Chlorides. Chemistry - An Asian Journal. doi: 10.1002/asia.201801651
[3] Lim, Т., Ryoo, J. Y., Jang, M., & Han, M. S. (2021). Ligand-free Suzuki-Miyaura cross-coupling with low Pd content: rapid development by a fluorescence-based high-throughput screening method. Organic & Biomolecular Chemistry, 19(5), 1009-1016. doi:10.1039/d0ob02359k
[4] Seo, Т., Ishiyama, Т., Kubota, K., & Ito, H. (2019). Solid-State Suzuki-Miyaura Cross-Coupling Reactions: Olefin-Accelerated C-C Coupling Using Mechanochemistry. Chemical Science. doi:10.1039/c9sc02185j
[5] Wang, G., Meng, M., Deng, L., Cheng, K., & Qi, C. (2017). Denitrogenative Pd/Cu-catalyzed Suzuki-type Cross-coupling of Aryltrifluoroborates with Arylhydrazine Hydrochlorides in Water under Room Temperature. Applied Organometallic Chemistry, 32(3), e4203. doi:10.1002/aoc.4203
[6] Asghar, S., Tailor, S.В., Elorriaga, D., & Bedford, R.B. (2017). Cobalt-Catalyzed Suzuki Biaryl Coupling of Aryl Halides. Angewandte Chemie International Edition, 56(51), 16367-16370. doi:10.1002/anie.201710053
[7] Wang, Z.-X., & Zhang, X.-Q. (2013). Amido Pincer Nickel Catalyzed Kumada Cross-Coupling of Aryl, Heteroaryl, and Vinyl Chlorides. Synlett, 24(16), 2081-2084. doi:10.1055/s-0033-1339653
[8] Guo, W.-J., & Wang, Z.-X. (2013). Cross-Coupling of ArX with ArMgBr Catalyzed by N-Heterocyclic Carbene-Based Nickel Complexes. The Journal of Organic Chemistry, 78(3), 1054-1061. doi:10.1021/jo302425x
[9] Wu, D., & Wang, Z.-X. (2014). P,N,N-Pincer nickel-catalyzed cross-coupling of aryl fluorides and chlorides. Organic & Biomolecular Chemistry, 12(33), 6414. doi:10.1039/c4ob01041h
[10] Yang, X., & Wang, Z.-X. (2014). Mono- and Dinuclear Pincer Nickel Catalyzed Activation and Transformation of C-Cl, C-N, and C-O Bonds. Organometallics, 33(20), 5863- 5873. doi:10.1021/om500452c
[11] Yamamoto, K., Otsuka, S., Nogi, K., & Yorimitsu, H. (2017). Nickel-Catalyzed Cross-Coupling Reaction of Aryl Sulfoxides with Arylzinc Reagents: When the Leaving Group is an Oxidant. ACS Catalysis, 7(11), 7623-7628. doi:10.1021/acscatal.7b02347
[12] Tao, J.-L., & Wang, Z.-X. (2015). Pincer-Nickel-Catalyzed Cross-Coupling of Aryl Sulfamates with Arylzinc Chlorides. European Journal of Organic Chemistry, 2015(29), 6534-6540. doi:10.1002/ejoc.201500987
[13] Xie, L.-G., & Wang, Z.-X. (2011). Nickel-Catalyzed Cross-Coupling of Aryltrimethylammonium Iodides with Organozinc Reagents. Angewandte Chemie International Edition, 50(21), 4901-904. doi:10.1002/anie.201100683
[14] Dai, W.-C, Yang, В., Xu, S.-H., & Wang, Z.-X. (2021). Nickel-Catalyzed Cross-Coupling of Aryl 2-Pyridyl Ethers with Organozinc Reagents: Removal of the Directing Group via Cleavage of the Carbon-Oxygen Bonds. The Journal of Organic Chemistry, 86(3), 2235-2243. doi:10.1021/acs.joc.0c02389
[15] Wang, L., & Liu, G. (2019). One-pot Negishi cross-coupling reaction of aryldiazonium salts via Ni catalysis induced by visible-light. Catalysis Communications, 105785. doi:10.1016/j.catcom.2019.105785
[16] Milanesi, S., Fagnoni, M., & Albini, A. (2005). (Sensitized) Photolysis of Diazonium Salts as a Mild General Method for the Generation of Aryl Cations. Chemoselectivity of the Singlet and Triplet 4-Substituted Phenyl Cations. The Journal of Organic Chemistry, 70(2), 603-610. doi:10.1021/jo048413w
[17] Kapoor, R., Chawla, R., & Yadav, L. D. S. (2019). Visible-light-mediated Gomberg-Bachmann reaction: an efficient photocatalytic approach to 2-aminobiphenyls. Tetrahedron Letters.doi: 10.1016/j.tetlet.2019.02.022
[18] Ichii, S., Hamasaka, G., & Uozumi, Y. (2019). The Hiyama Cross-Coupling Reaction at Parts Per Million Levels of Pd: In Situ Formation of Highly Active Spirosilicates in Glycol Solvents. Chemistry-An Asian Journal. doi:10.1002/asia.201901155
[19] Ju, J., Nam, H., Jung, H. M., & Lee, S. (2006). Palladium-catalyzed cross-coupling of trimethoxysilylbenzene with aryl bromides and chlorides using phosphite ligands. Tetrahedron Letters, 47(49), 8673-8678. doi: 10.1016/j.tetlet.2006.10.017
[20] Gordillo, A., de Jesus, E., & Lopez-Mardomingo, C. (2006). C-C Coupling Reactions of Aryl Bromides and Arylsiloxanes in Water Catalyzed by Palladium Complexes of Phosphanes Modified with Crown Ethers. Organic Letters, 8(16), 3517-3520. doi:10.1021/ol061221y
[21] Canning, P. S. J., McCrudden, K., Maskill, H., & Sexton, B. (1999). Rates and mechanisms of the thermal solvolytic decomposition of arenediazonium ions. Journal of the Chemical Society, Perkin Transactions 2, (12), 2735-2740. doi:10.1039/a905567c
[22] Abu-Melha, S. (2012). Synthesis, antimicrobial evaluation and spectroscopic characterization of novel imidazolone, triazole and triazinone derivatives. Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, 96, 898-905. doi:10.1016/j.saa.2012.04.068
[23] Stibingerova, I., Voltrova, S., Kocova, S., Lindale, M., & Srogl, J. (2015). Modular Approach to Heterogenous Catalysis. Manipulation of Cross-Coupling Catalyst Activity. Organic Letters, 18(2), 312-315. doi:10.1021/acs.orglett.5b03480
[24] Amatore, M., & Gosmini, C. (2008). Efficient Cobalt-Catalyzed Formation of Unsymmetrical Biaryl Compounds and Its Application in the Synthesis of a Sartan Intermediate. Angewandte Chemie International Edition, 47(11), 2089-2092. doi:10.1002/anie.200704402.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ИНГИБИТОРА АКТИВИН-РЕЦЕПТОРОПОДОБНОЙ КИНАЗЫ | 2020 |
|
RU2826600C1 |
| Способ получения пирроло[3,4-с]хинолинов | 2022 |
|
RU2802332C1 |
| Способ получения 1-(3-(триметоксисилил)пропил)-1H-имидазола | 2023 |
|
RU2805918C1 |
| Способ получения 5-амино-N-метил-3,4-дицианопиразола | 2022 |
|
RU2785675C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЦЕТИЛЕНОВЫХ КЕТОНОВ | 2017 |
|
RU2641697C1 |
| Способ получения транс-миртановой кислоты | 2022 |
|
RU2794756C1 |
| Способ получения производного неокупроина | 2022 |
|
RU2799334C1 |
| Способ получения пара-терфенила сцинцилляционного качества | 2021 |
|
RU2767518C1 |
| Способ получения 1,2-диарилэтан-1,2-дионов | 2024 |
|
RU2841326C1 |
| МЕЧЕННЫЕ ТРИТИЕМ N-ФЕНИЛХИНОЛИНИЕВЫЕ И ХИНАЛЬДИНИЕВЫЕ СОЛИ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2006 |
|
RU2320647C1 |
Изобретение относится к способу получения N,N-диметил-4-бифениламина и его производных общей формулы (R1)Ph-Ph(R2)-N(CH3)2, где R1 - H, n-СООСН3, R2 - H, o-СН3. Способ заключается во взаимодействии N,N-диметиламинофенилдиазениларила общей формулы (R1)Ph-N=N-Ph(R2)-N(CH3)2, где R1 - Н, n-СООСН3, R2 - Н, o-СН3, тетрацианоэтилена и метанола под действием ультразвука при частоте 90-100 Гц и температуре 35-40°С. Техническим результатом является использование доступных недорогих реактивов, отсутствие катализаторов и оснований, одностадийность и сокращение времени реакции. 3 пр.
Способ получения N,N-диметил-4-бифениламина и его производных общей формулы (R1)Ph-Ph(R2)-N(CH3)2, где R1 - Н, n-СООСН3, R2 - Н, o-СН3, включающий взаимодействие N,N-диметиламинофенилдиазениларила общей формулы (R1)Ph-N=N-Ph(R2)-N(CH3)2, где R1 - Н, n-СООСН3, R2 - Н, o-СН3, тетрацианоэтилена и метанола под действием ультразвука при частоте 90-100 Гц и температуре 35-40°С.
| WANG L | |||
| ET AL, One-pot Negishi cross-coupling reaction of aryldiazonium salts via Ni catalysis induced by visible-light, CATALYSIS COMMUNICATIONS, 2019, 105785; doi:10.1016/j.catcom.2019.105785 | |||
| CANNING P | |||
| S | |||
| J | |||
| ET AL, Rates and mechanisms of the thermal solvolytic decomposition of arenediazonium ions, JOURNAL OF THE CHEMICAL SOCIETY, PERKIN |
Авторы
Даты
2023-04-11—Публикация
2022-11-01—Подача