Предлагаемое изобретение относится к области органической химии, в частности, к новому способу получения 1,2-диарилэтан-1,2-дионов общей формулы 1:

1,2-Диарилэтан-1,2-дионовый фрагмент является основным структурным элементом в соединениях, выделенных из растений семейства Leguminosae, и проявляющих различную биологическую активность (Worayuthakarn R., Boonya-Udtayan S., Ruchirawat S., Thasana N. Total synthesis of unsymmetrical benzils, scandione and calophione A. // Eur. J. Org. Chem., 2014, 12, 2496-2507. doi: 10.1002/ejoc.201301722; Richter M. J. R., Schneider M., Brandstatter M., et al. Total Synthesis of (-)-Mitrephorone A. // J. Am. Chem. Soc., 2018, 140(48), 16704-16710. doi: 10.1021/jacs.8b09685), включая антимикробную (Li W., Asada Y., Yoshikawa T. Antimicrobial flavonoids from Glycyrrhiza glabra hairy root cultures. // Planta Med., 1998, 64(8), 746-747. doi: 10.1055/s-2006-957571), антибактериальную, гипертензивную, антирадикальную (Mahabusarakam W., Deachathai S., Phongpaichit S., Jansakul C., Taylor W. C. // Phytochemistry, 2004, 65, 1185-1189. doi: 10.1016/j.phytochem.2004.03.006; Johns S. R., Lamberton J. A., Sioumis A. A., Willing R. I. New alkaloids from Cryptocarya pleurosperma (Lauraceae): The structures of cryptopleuridine and cryptopleurospermine. // Aust. J. Chem., 1970, 23, 353-361. doi: 10.1071/CH9700353) активность, ингибирование карбоксилэстераз млекопитающих (Hyatt J. L., Stacy V., Wadkins R. M., et al. Inhibition of carboxylesterases by benzil (diphenylethane-1,2-dione) and heterocyclic analogues is dependent upon the aromaticity of the ring and the flexibility of the dione moiety. // J. Med. Chem., 2005, 48(17), 5543-5550. doi: 10.1021/jm0504196), а также цитотоксичность (Ganapaty S., Srilakshmi G. V. K., Pannakal S. T., et al. Cytotoxic benzil and coumestan derivatives from Tephrosia calophylla. // Phytochemistry, 2009, 70, 95-99. doi: 10.1016/j.phytochem.2008.10.009). Кроме того, 1,2-диарилэтан-1,2-дионы являются прекурсорами для получения лекарственных препаратов (Машковский М. Д., Лекарственные средства. - М.: Медицина, 1987. - Т. 1. - 624 с.; Крыльский Д. В., Сливкин А. И., Гетероциклические лекарственные вещества. Учебное пособие по фармацевтической химии, 2007, с. 93;), высокотермостойких полимеров - полихиноксалинов (Фрейзер А. Г., Высокотермостойкие полимеры. - М.: Химия, 1971. - С. 181-183) и лигандов, таких как диолы (Babudri F., Fiandanese V., Marchese G., Punzi A. A direct access to α-diones from oxalyl chloride. // Tet. Lett., 1995, 36(40), 7305-7308. doi: 10.1016/0040-4039(95)01471-S), N-гетероциклических карбенов (NHC) (Singh S. K., Saibaba V., Ravikumar V., et al. Synthesis and biological evaluation of 2,3-diarylpyrazines and quinoxalines as selective COX-2 inhibitors// Bioorg. Med. Chem., 2004, 12(8), 1881-1893. doi: 10.1016/j.bmc.2004.01.033; Kong L., Meng J., Tian W., Liu J., Hu X., Zhi-Hong Jiang, Zhang W., Li Y., Bai L.- P. I2-Catalyzed carbonylation of α-methylene ketones to synthesize 1,2-diaryl diketones and antiviral quinoxalines in one pot. // ACS Omega, 2022, 7(1), 1380-1394. doi: 10.1021/acsomega.1c06017) и диаминов (De Luca L., Mezzetti A. Base-free asymmetric transfer hydrogenation of 1,2-di- and monoketones catalyzed by a (NH)2P2-macrocyclic Iron(II) hydride. // Angew.Chem. 2017, 56(39), 11949-11953. doi: 10.1002/anie.201706261), широко использующихся в процессах синтеза полимеров (Dove A. P., Li H., Pratt R. C., et al. Stereoselective polymerization of rac- and meso-lactide catalyzed by sterically encumbered N-heterocyclic carbenes. // Chem. Comm. 2006, (27), 2881-2883. doi: 10.1039/b601393g) и в качестве фотоинициаторов при отверждении полимерных сеток (Guo L., Gao H., Guan Q., et al. Systematic investigation of ligand substitution effects in cyclophane-based nickel(II) and palladium(II) olefin polymerization catalysts (1). // Organometallics 2012, 31(17), 6054-6062. doi: 10.1021/om300380b). Наиболее простой стратегией получения 1,2-диарилэтан-1,2-дионов является прямое окисление ацетиленов. Известен способ (Shen D., Wang H., Zheng Y., Zhu X., et al. Catalyst-free and transition-metal-free approach to 1,2-diketones via aerobic alkyne oxidation. // J. Org. Chem. 2021, 86(7), 5354-5361. doi: 10.1021/acs.joc.0c03010) получения 1,2-диарилэтан-1,2-дионов окислением диарил- и арилалкилзамещенных ацетиленов персульфатом калия K2S2O8 и кислородом воздуха из баллона без использования катализаторов, при нагревании при 60°С в водно-ацетонитрильной среде (2:1) в течение 8 ч.
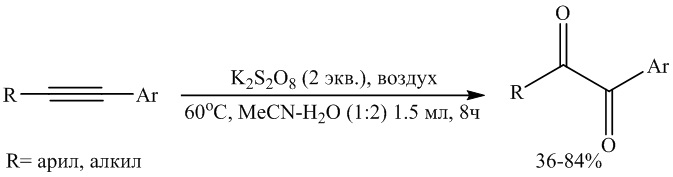
Известным способом могут быть получены 1,2-диарилэтан-1,2-дионы общей формулы 1. Недостатком известного метода является использование дорогостоящих исходных соединений - арилацетиленов.
Известен способ (Alterman J. L., Vang D. X., Stroud M. R., Halverson L. J., Kraus G. A. Ozonolysis of alkynes - a flexible route to alpha-diketones: Synthesis of AI-2. // Org. Lett. 2020, 22(19), 7424-7426. doi: 10.1021/acs.orglett.0c02182) получения 1,2-диарилэтан-1,2-дионов озонолизом дизамещенных ацетиленов в смеси метиленхлорида и ацетона в соотношении 1:1 при температуре -78°C. Побочные озониды гасили PPh3.
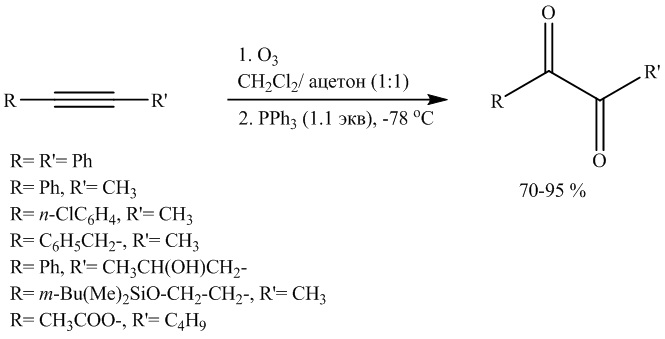
Известным способом могут быть получены 1,2-диарилэтан-1,2-дионы общей формулы 1. Недостатками известного метода являются использование дорогостоящих исходных соединений - арилацетиленов и необходимость проведения реакций при низкой температуре (- 78°С).
Известен способ (Xu N., Gu D. W., Dong Y. S., Yi F. P., et al. Copper-catalyzed synthesis of 1,2-diketones via oxidation of alkynes. // Tetr. Lett. 2015, 56(12), 1517-1519. doi: 10.1016/j.tetlet.2015.01.195) получения 1,2-диарилэтан-1,2-дионов окислением диарилзамещенных ацетиленов с помощью Na2S2O8 на воздухе в присутствии катализатора CuI в ДМСО в течение 24 ч при температуре 140°С.

Известным способом могут быть получены 1,2-диарилэтан-1,2-дионы общей формулы 1. Недостатками известного метода являются использование дорогостоящих исходных соединений, высокая температура 140°С и большая продолжительность проведения реакции (24 ч).
Известен способ (Joo C., Kang S., Kim S. M., Han H., Yang J. W. Oxidation of benzoins to benzils using sodium hydride. // Tetrahedron Letters, 2010, 51(46), 6006-6007. doi: 10.1016/j.tetlet.2010.09.028) получения 1,2-диарилэтан-1,2-дионов взаимодействием ацилоинов, синтезированных кипячением спиртового раствора соответствующих альдегидов в водном растворе цианида натрия при 80°С, с 2-х кратным избытком гидрида натрия:
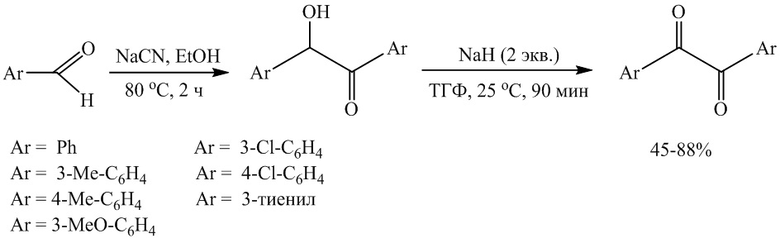
Известным способом могут быть получены 1,2-диарилэтан-1,2-дионы общей формулы 1. Основным недостатком этого способа является двухстадийность процесса, необходимость синтеза исходных соединений с применением токсичного цианида натрия на первой стадии реакции.
Известен способ (Kong L., Meng J., Tian W., Liu J., et al. I2-Catalyzed carbonylation of α-methylene ketones to synthesize 1,2-diaryl diketones and antiviral quinoxalines in one pot. // ACS Omega 2022, 7(1), 1380-1394. doi: 10.1021/acsomega.1c06017) получения 1,2-диарилэтан-1,2-дионов окислительным карбонилированием ароматических α-метиленкетонов с помощью системы реагентов 10 мол% I2 - 3 эквивалента т-BuOOH в N,N-диметилформамиде при температуре 100 °С в течение 5 ч.
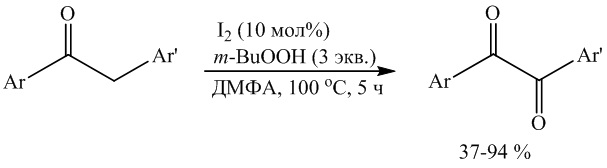
Известным способом могут быть получены 1,2-диарилэтан-1,2-дионы общей формулы 1. Недостатком известного метода является необходимость предварительного синтеза α-метиленкетонов и проведения реакции при температуре 100°С.
Известен способ (Хафизова Л.О., Шайбакова М.Г., Чобанов Н.М., Джемилев У.М. Патент РФ RU 2624673 C2, 10.07.2017) получения бензила взаимодействием метилового эфира бензойной кислоты (МЭБК) с этилалюминийдихлоридом (EtAlCl2) в присутствии Mg и катализатора Cp2TiCl2, взятых в мольном соотношении МЭБК:EtAlCl2:Mg:Cp2TiCl2 = 10:20-40:20:0.8-1.2, предпочтительно 10:30:20:1. Реакцию проводят в тетрагидрофуране в атмосфере аргона при температуре 60°С и атмосферном давлении. Время реакции 4-8 ч, предпочтительно 6 ч. Выход целевого продукта составляет 64-90 %.
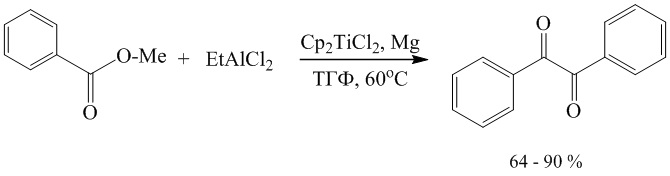
Известным способом могут быть получены 1,2-диарилэтан-1,2-дионы общей формулы 1. Недостатком способа является использование пожароопасного EtAlCl2.
Задачей настоящего изобретения является разработка эффективного однореакторного способа получения 1,2-диарилэтан-1,2-дионов общей формулы 1 на основе использования доступных сложных эфиров, бис(циклопентадиенил)цирконий дихлорида Cp2ZrCl2, металлического магния и пожаробезопасного триметилхлорсилана Me3SiCl.
Сущность заявляемого способа заключается в каталитическом синтезе 1,2-диарилэтан-1,2-дионов (1) из эфиров ароматических кислот ArCOOR, таких как н-бутилбензоат, метилтолуоат и этилнафтоат, в присутствии магния, катализатора Cp2ZrCl2 (10 мол%) и триметилхлорсилана (Me3SiCl), взятых в мольном соотношении [ArCOOR]: [Mg] : [Cp2ZrCl2] : [Me3SiCl] = 1:(1-4):(0.08-0.12):(3-8), предпочтительно 1:2:0.1:4. Реакцию проводят в тетрагидрофуране в атмосфере аргона при температуре 50 °С и атмосферном давлении в течение 6 ч. Предлагаемый способ позволяет получать 1,2-диарилэтан-1,2-дионы (1) с выходом 81-87 % при использовании предпочтительных соотношений реагентов и времени реакции.
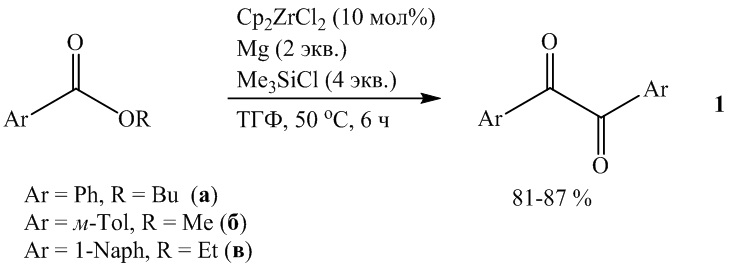
Проведение указанной реакции в присутствии реагента Me3SiCl, взятого в количестве более 4 экв., например, 6 экв., или Mg в количестве более 2 экв., например, 4 экв., снижает селективность реакции и не приводит к увеличению выхода образующихся 1,2-диарилэтан-1,2-дионов (1) (84 % и 82 % в случае реакции с н-бутилбензоатом). Использование 8 экв. Me3SiCl и 4 экв. Mg не приводит к существенному увеличению выхода 1,2-диарилэтан-1,2-дионов (1) (85 % в случае реакции с н-бутилбензоатом). Проведение указанной реакции в присутствии реагента Me3SiCl, взятого в количестве менее 4 экв., например, 3 экв., или Mg в количестве менее 2 экв., например, 1 экв., снижает конверсию сложного эфира и приводит к снижению выхода образующихся 1,2-диарилэтан-1,2-дионов (1) (до 75 % и 72 %, соответственно, в случае реакции с н-бутилбензоатом). Увеличение количества катализатора Cp2ZrCl2 до 0.12 ммолей не оказывает существенного влияния на скорость реакции и выход целевого продукта (1). Уменьшение количества катализатора до 0.08 ммолей снижает выход целевого продукта (1) (с 87 % до 81 % в случае реакции с н-бутилбензоатом), что связано, возможно, со снижением концентрации каталитически активных центров в реакционной массе. В отсутствии Me3SiCl или Mg реакция не проходит. В случае замены реагента Me3SiCl на AlCl3 и при соотношении реагентов [ArCOOR]: [Mg] : [Cp2ZrCl2] : [AlCl3] = 1:2:0.1:4 образуется трудно анализируемая смесь соединений. Реакции проводили при температуре 50 °С в течение 6 ч. При более высокой температуре (например, 70°С) увеличиваются энергозатраты на проведение процесса, при более низкой температуре (40°С) снижается скорость реакции и выход целевого продукта 1 (с 87% до 78 % в случае реакции с н-бутилбензоатом). При уменьшении времени проведения реакции с 6 ч до 4 ч наблюдается не полная конверсия сложного эфира, что приводит к снижению выхода образующихся 1,2-диарилэтан-1,2-дионов (1) (до 69% в случае реакции с н-бутилбензоатом).
Целевой продукт 1 образуется только с участием эфиров ароматических кислот, магния и Me3SiCl в тетрагидрофуране.
Существенные отличия предлагаемого способа:
Известные способы получения 1,2-диарилэтан-1,2-дионов основаны на реакциях некаталитического и каталитического окисления дорогостоящих арилацетиленов, ацелоинов и α-метиленкетонов. Реакции проводятся при высокой (140 °С) или при низкой (-78°С) температуре в течение длительного времени (24 ч). Один известный способ базируется на использовании эфиров ароматических кислот, магния, пожароопасного этилалюминийдихлорида (EtAlCl2) и катализатора Cp2TiCl2.
Предлагаемый каталитический способ, базируется на использовании коммерчески доступного пожаробезопасного Me3SiCl и катализатора Cp2ZrCl2.
Предлагаемый способ обладает следующими преимуществами:
В отличие от известного способа предлагаемый способ подразумевает использование удобного в практическом применении Me3SiCl, что позволяет снизить пожароопасность, связанную с применением EtAlCl2 и получать с высокими выходами 1,2-диарилэтан-1,2-дионы общей формулы 1.
Способ поясняется следующими примерами:
ПРИМЕР. В стеклянный реактор, установленный на магнитной мешалке в атмосфере сухого аргона, при охлаждении в ледяной бане последовательно помещали 0.048 г Mg (2 ммоль, порошок), 0.0292 г Cp2ZrCl2 (0.1 ммоль), 5 мл ТГФ и 0.51 мл Me3SiCl (4 ммоль). Реакционную смесь перемешивали 30 минут. Далее в реакционную смесь добавляли 0.18 мл н-бутилбензоата (1 ммоль) и перемешивали при 50 °С в течение 6 ч. Реакционную массу охлаждали до комнатной температуры и обрабатывали 2%-ным водным раствором NaHCO3. Продукты реакции экстрагировали диэтиловым эфиром и сушили над прокаленным MgSO4. Растворитель упаривали на роторном испарителе и 1,2-дифенилэтан-1,2-дион (1а) выделяли колоночной хроматографией (силикагель L, 180/250 μ; элюент - гексан:этилацетат (100:1)). Выход 87 %. Rf (гексан: этилацетат, 100:1) 0.65. Структуру выделенных соединений устанавливали анализом спектров ЯМР 13С и 1Н.
Спектральные характеристики 1,2-дифенилэтан-1,2-диона (1а):
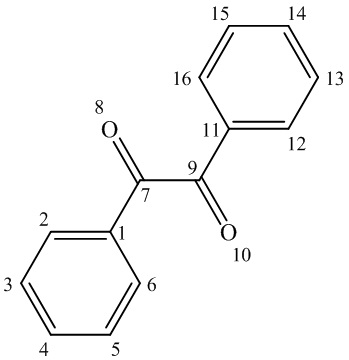
Спектр ЯМР 1Н, CDCl3, δ, м.д.: 7.53 (т, J=7.8 Гц, 4Н, С3,5,13,15Н), 7.68 (т, J=7.5 Гц, 2Н, С4,14Н), 8.00 (д, J=7.5 Гц, 4Н, С2,6,12,16Н).
Другие примеры, подтверждающие способ, приведены в таблице.
Таблица. Влияние условий реакции на выход 1,2-диарилэтан-1,2-дионов.*
сложный эфир
[R'COOR'']: [Mg] : [Zr] : [Me3SiCl]
°С
час
2
3
4
5
6
7
8
9
10
11
12
14
15
PhCOOBu
PhCOOBu
PhCOOBu
PhCOOBu
PhCOOBu
PhCOOBu
PhCOOBu
PhCOOBu
PhCOOBu
PhCOOBu
PhCOOBu
м-TolCOOMe
1-NaphCOOEt
1:2:0.1:6
1:4:0.1:4
1:4:0.1:8
1:2:0.1:3
1:1:0.1:4
1:2:0.12:4
1:2:0.08:4
1:2:0.1:4
1:2:0.1:4
1:2:0.1:4
1:2:0.1:4
1:2:0.1:4
1:2:0.1:4
50
50
50
50
50
50
50
70
40
50
50
50
50
6
6
6
6
6
6
6
6
6
4
8
6
6
84
82
85
75
72
87
81
86
78
69
87
85
81
* Реакции проводили в тетрагидрофуране.
Спектральные характеристики 1,2-ди-(м-толил)этан-1,2-диона (1б):
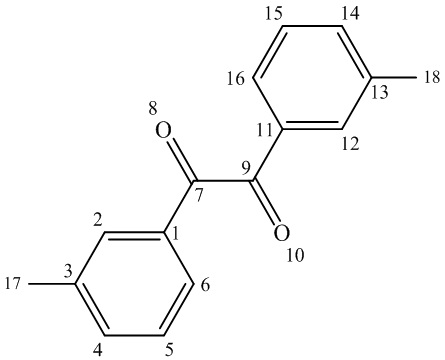
Спектр ЯМР 13С, CDCl3, δ, м.д.: 21.27 (С17,18), 127.24 (С6,16), 128.95 (С5,15), 130.22 (С2,12), 133.07 (С1,11), 135.77 (С4,14), 139.02 (С3,13), 195.03 (С7,9).
Спектральные характеристики 1,2-ди-(1-нафтил)этан-1,2-диона (1в):

Спектр ЯМР 13С, CDCl3, δ, м.д.: 124.63 (С7,21), 126.21 (С3,17), 127.24 (С8,22), 128.94 (С9,23), 129.12 (С6,20), 129.55 (С2,16), 131.33 (С1,15), 134.29 (С4,18), 135.22 (С10,24), 135.94 (С5,19), 197.10 (С11,13).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ БЕНЗИЛА | 2015 |
|
RU2624673C2 |
| Способ получения N,N-диметил-4-бифениламина и его производных | 2022 |
|
RU2794095C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ФЕНИЛ-1-БОРАСПИРОАЛКАНОВ | 2022 |
|
RU2800048C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА ДЛЯ ПОЛУЧЕНИЯ 3-АЦЕТИЛГЕПТАН-2,6-ДИОНА И СПОСОБ ПОЛУЧЕНИЯ 3-АЦЕТИЛГЕПТАН-2,6-ДИОНА С ИСПОЛЬЗОВАНИЕМ ПОЛУЧЕННОГО КАТАЛИЗАТОРА | 2012 |
|
RU2494810C1 |
| СПОСОБ ПОЛУЧЕНИЯ 3-АЛКИЛ-3-МЕТИЛ-1-ФЕНИЛ-3-ОЛОВ | 2014 |
|
RU2596878C2 |
| ДИСПИРОИНДОЛИНОНЫ НА ОСНОВЕ РОДАНИНОВ КАК ИНГИБИТОРЫ Р53-MDM2 БЕЛОК-БЕЛКОВОГО ВЗАИМОДЕЙСТВИЯ | 2019 |
|
RU2730286C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,2-ДИАЛКИЛБОРИРАНОВ | 2017 |
|
RU2688195C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3-ДИАЛКИЛ-1,4-ДИЦИКЛОПРОПИЛ-1,4-БУТАНДИОНОВ | 2014 |
|
RU2565789C1 |
| Способ получения дигалогенпроизводного 1,2,3,4-тетрагидропиридо- или пиридо[1,2-а]бензимидазол-6,9-диона | 2023 |
|
RU2828349C1 |
| СПОСОБ ПОЛУЧЕНИЯ α-[(ПЕНТАН-2,4-ДИОН-3-ИЛ)МЕТОКСИ]-ω-[(ПЕНТАН-2,4-ДИОН-3-ИЛ)МЕТИЛСУЛЬФАНИЛ]АЛКАНОВ | 2014 |
|
RU2605450C2 |
Изобретение относится к способу получения 1,2-диарилэтан-1,2-дионов общей формулы 1:

из сложных эфиров ароматических кислот, в присутствии катализатора, порошка магния, в тетрагидрофуране, в атмосфере аргона, при атмосферном давлении, согласно изобретению в качестве катализатора используют Cp2ZrCl2, в качестве сложных эфиров ароматических кислот соединения ArCOОR, где Ar = Ph, R = н-Bu, Ar = м-толил, R = Me, Ar = 1-нафтил, R = Et, реакцию проводят в присутствии триметилхлорсилана (Me3SiCl), при мольном соотношении ArCOОR:Mg:Zr:Me3SiCl = 1:(1-4):(0.08-0.12):(3-8), при 50 °С, в течение 6 ч. Технический результат: разработан новый способ получения 1,2-диарилэтан-1,2-дионов (1) из эфиров ароматических кислот в присутствии магния, катализатора и триметилхлорсилана, который позволяет снизить пожароопасность, связанную с применением EtAlСl2, и получать 1,2-диарилэтан-1,2-дионы (1) с выходом 81-87%. 1 табл., 16 пр.
Способ получения 1,2-диарилэтан-1,2-дионов общей формулы 1:
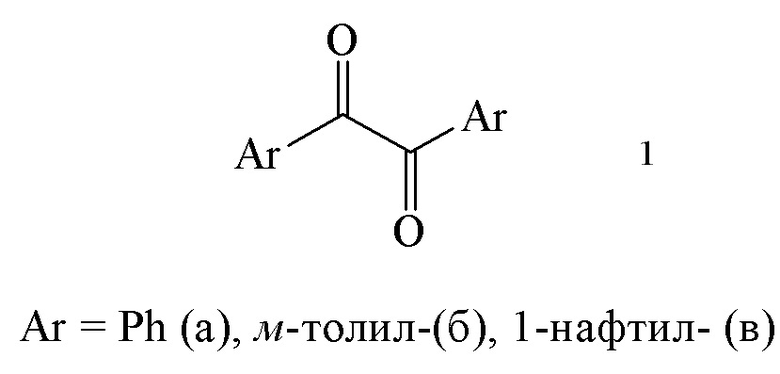
из сложных эфиров ароматических кислот, в присутствии катализатора, порошка магния, в тетрагидрофуране, в атмосфере аргона, при атмосферном давлении, отличающийся тем, что в качестве катализатора используют Cp2ZrCl2, в качестве сложных эфиров ароматических кислот соединения ArCOОR, где Ar = Ph, R = н-Bu; Ar = м-толил, R = Me; Ar = 1-нафтил, R = Et, реакцию проводят в присутствии триметилхлорсилана (Me3SiCl), при мольном соотношении ArCOОR:Mg:Zr:Me3SiCl = 1:(1-4):(0.08-0.12):(3-8), при 50 °С, в течение 6 ч.
| СПОСОБ ПОЛУЧЕНИЯ ДИАРИЛЭТАНОВ | 0 |
|
SU387956A1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАРИЛМЕТАНА ИЛИ ЕГО ПРОИЗВОДНЫХ | 1998 |
|
RU2182896C2 |
| CN 107556183 B, 03.05.2022 | |||
| Kashimura S | |||
| et al | |||
| Cathodic coupling of aliphatic esters | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Топка с качающимися колосниковыми элементами | 1921 |
|
SU1995A1 |
| - Т | |||
| Коридорная многокамерная вагонеточная углевыжигательная печь | 1921 |
|
SU36A1 |
| Прибор с двумя призмами | 1917 |
|
SU27A1 |
| - С | |||
| Автоматический прибор для продажи разных изделий в плитках или коробках | 1925 |
|
SU4805A1 |
| СПОСОБ ПОЛУЧЕНИЯ ТРЕТИЧНЫХ СПИРТОВ РЕАКЦИЕЙ АРИЛОЛЕФИНОВ С AlCl3 И КЕТОНАМИ ПОД ДЕЙСТВИЕМ КАТАЛИЗАТОРА Cp2ZrCl2 | 2023 |
|
RU2813640C1 |
Авторы
Даты
2025-06-06—Публикация
2024-12-24—Подача