РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Данная заявка испрашивает приоритет по одному или более 35 U.S.C. 119(a)-119(d) индийской патентной заявки No. 1418/DEL/2015, поданной 19 мая 2015, содержание обеих заявок включено в настоящее изобретение с помощью ссылки во всей своей полноте.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ НАСТОЯЩЕЕ ИЗОБРЕТЕНИЕ
[0002] Настоящее изобретение относится к области нанотехнологии и противораковой терапии. В частности, настоящее изобретение относится к получению конъюгированных с липидами платиновых соединений, и дополнительно относится к способам получения конъюгированных с липидами платиновых соединений с высокой чистотой и хорошими выходами. Настоящее изобретение также относится к наночастицам, содержащим конъюгированные с липидами платиновые соединения с высокой эффективностью загрузки лекарственного средства для применения в химиотерапии, и способам получения указанных наночастиц.
УРОВЕНЬ ТЕХНИКИ
[0003] Платиновые химиотерапевтические агенты применяют в качестве терапии первой линии в более чем 70% всех случаев рака. Цисплатина подвергается быстрому превращению в цис-[Pt(NH3)2Cl(OH2)]+ и цис-[Pt(NH3)2(OH2)]2+, приводя в результате к почечной токсичности. Кроме того, гидратация карбоплатины и оксалиплатины является в значительной степени медленной, приводя в результате к сниженной эффективности. В последние годы был достигнут значительный прогресс, когда Dhar et al. (PNAS, 2008, 105, 17356) разработали платиновый (IV) комплекс (c,t,c-[Pt(NH3)2(O2CCH2CH2CH2CH2CH3)2Cl2], который является достаточно гидрофобным для инкапсулирования в PLGA-b-PEG наночастицы. Однако, в данном случае, пролекарство должно быть внутриклеточно превращено в цисплатину. Более того, альтернативные стратегии на основе конъюгирования платины с полимерами (например, комплекс полиамидоаминового дендримера и платины) приводили в результате к 200-550 кратному снижению токсичности по сравнению со свободной цисплатиной. Это было результатом сильных связей, образованных между полимером и платиной (J. Pharm. Sci., 2009, 98, 2299). Другой пример представляет собой AP5280, платину, соединенную с N-(2-гидроксипропил)метакриламидным сополимером, который является менее эффективным, чем карбоплатина. Здесь, платина удерживается хелатирующим агентом на основе аминомалоновой кислоты, соединенным с COOH-концевым глицином тетрапептидного спейсера (Clin. Can. Res., 2004, 10, 3386; Eur. J. Can., 2004, 40, 291). Кроме того, WO 2010/091192 A2 (Sengupta et al.) описывает биосовместимые конъюгированные полимерные наночастицы, содержащие сополимерный остов, некоторое количество боковых цепей, ковалентно присоединенных к указанному остову, и некоторое количество платинового соединения, диссоциируемо присоединенного к указанному остову.
[0004] Липидный молекулярный остов оксалиплатины, цисплатины и карбоплатины представляет собой интересную область исследований для разработки противораковых лекарственных средств, из-за его способности образовывать наночастицы и обеспечивать улучшенные эффекты проникновения и удержания (EPR). Однако, сообщения о конъюгированных с липидами платиновых лекарственных средствах чрезвычайно редки. Это обусловлено проблемами, связанными со способами получения с низкими выходами и сложностью очистки данных соединений. Достижение хороших выходов реакций конденсации (комплексообразлвания) липида и платины остается сложным из-за большой разницы в растворимости между липидными лигандами и платиновыми предшественниками. Содержащие липиды лиганды являются более растворимыми в органических растворителях, тогда как платиновые предшественники лучше растворяются в воде. Для увеличения растворимости реагентов, смеси органических и водных растворителей применяют в большинстве из сообщаемых реакций комплексообразования, особенно если липид является нерастворимым в воде (например, холестерин, смотри таблицу 1, ссылку 1). Тем не менее, данная проблема с растворимостью приводит в результате к неполному протеканию реакций. Таким образом, очистка целевого платинового комплекса от непрореагировавших исходных соединений становится трудной. Данные реакции также страдают от недостатков, таких как сложные многостадийные способы (смотри таблицу 1, ссылку 3), высокие температуры реакций (смотри таблицу 1, ссылки 2, 3) и усложненные способы обработки (смотри таблицу 1, ссылка 2) и т.д.
Таблица 1: Сравнительное исследование сообщаемых в литературе способов получения конъюгированных с липидами платиновых комплексов
(0C)
(en=этилендиамин)
[0005] Известно, что дополнительная очистка Pt соединений для получения продукта, который удовлетворяет требованиям Управления по продовольствию и лекарствам США (FDA), представляет собой сложный и проблематичный процесс. Очистка конечных конъюгированных с липидами платиновых активных фармацевтических ингредиентов (API) является проблематичной, поскольку их трудно кристаллизовать из-за их большого размера и амфифильных свойств. Pt(IV)-пептидные конъюгаты очищают обращенно-фазовой высокоэффективной жидкостной хроматографией (HPLC); однако конечная чистота по ВЭЖХ аналитическим способам не сообщалась (Mukhopadhyay, S. et al., Bioconjug. Chem., 19, 39-49 (2008)). Для нескольких других случаев, сообщалось, что Pt(IV) комплексы разлагаются на колонке, и их нельзя очистить (Saouma, C. T., Synthetic strategies to improve the cytotoxicity of platinum-based cancer therapeutics. 1-78 (2005) at <http://dspace.mit.edu/handle/1721,1/36279#files-area>). Аналогично, для другого способа, приведенного для очистки Pt(II) комплексов, не показана конечная чистота по ВЭЖХ (Tromp, R. et al., Bioorg. Med. Chem. Lett., 14, 4273-6 (2004)). Сообщалось о проблемах с очисткой Pt(II) соединений, особенно соединений, содержащих азотсодержащие лиганды (Roberts, J. D., Inorg. Chim. Acta, 153, 123-127 (1988)). В данном случае, продукт после очистки был биологически менее активным.
[0006] Настоящее изобретение относится к преодолению данных недостатков предшествующего уровня техники и обеспечивает улучшенный способ получения, получая достаточно высокую чистоту неочищенных конъюгированных с липидами платиновых соединений (API) с высокими выходами. Определенные аспекты настоящего изобретения также обеспечивают надежный способ препаративной ВЭЖХ для очистки конъюгированных с липидами платиновых соединений. Определенные аспекты настоящего изобретения обеспечивают стабильные, эффективные и безопасные наноплатинаты для химиотерапии рака.
СУЩНОСТЬ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
[0007] Настоящее изобретение относится к синтетическим стратегиям для получения конъюгированных с липидами платиновых соединений. Один аспект настоящего изобретения относится к способу получения конъюгированного с липидами платинового соединения, где способ включает: реакцию растворимой в воде соли липида с растворимым в воде платиновым соединением в по существу водном растворе, получая конъюгированное с липидами платиновое соединение в виде осадка. Другой аспект относится к способу дополнительной очистки конъюгированного с липидами платинового соединения, применяя ВЭЖХ. Другой аспект относится к способу получения наночастиц, содержащих описанные конъюгированные с липидами платиновые соединения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0008] Для того чтобы настоящее изобретение можно было бы более легко понять и осуществлять на практике, ссылки далее будут делаться на примерные варианты осуществления, как показано ссылкой на прилагаемые фигуры. Фигуры вместе с подробным описанием ниже включены и образуют часть настоящего изобретения и служат для дополнительной иллюстрации вариантов осуществления и объяснения различных принципов и преимуществ согласно настоящему изобретению.
[0009] Фигура 1 показывает ВЭЖХ профиль соединения 26 (RT: 10,93 мин) на C18 колонке перед промывкой водой/ацетоном. Чистота соединения составляет 82%. Подвижная фаза: 100% метанол. Детекция: 210нм, УФ.
[0010] Фигура 2 показывает ВЭЖХ профиль соединения 26 (RT: 11,2 мин) на C18 колонке после промывки водой/ацетоном. Чистота соединения составляет 90%. Подвижная фаза: 100% метанол. Детекция: 210нм, УФ.
[0011] Фигура 3 показывает примерный аналитический профиль соединения 25 после ВЭЖХ очистки. Чистота составляет >99,5%. Чистоту рассчитывали после наложения спектра холостого раствора (не показан).
[0012] Фигура 4 показывает примерный аналитический профиль соединения 27 после ВЭЖХ очистки. Чистота составляет 99,5%. Чистоту рассчитывали после наложения спектра холостого раствора (не показан).
[0013] Фигура 5 показывает примерный аналитический профиль соединения 28 после ВЭЖХ очистки. Чистота составляет 99%. Чистоту рассчитывали после наложения спектра холостого раствора (не показан).
[0014] Фигуры 6A и 6B показывают примерный аналитический профиль соединения 25 после ВЭЖХ очистки. Чистота составляет 98,5% на C18 колонке (фигура 6A), но ~100% на амино колонке (фигура 6B), подтверждая разложение соединения на C18 колонке. Данные результаты придают значение выбору способа анализа на чистоту.
[0015] Фигуры 7A и 7B показывает примерный аналитический профиль соединения 27 после ВЭЖХ очистки. Чистота составляет 59% на C18 колонке (фигура 7A), но 98% на амино колонке (фигура 7B), подтверждая разложение соединения на C18 колонке. Данные результаты придают значение выбору способа анализа на чистоту.
[0016] Фигура 8 показывает ДРС гистограмму супрамолекулярного состава соединения 25.
[0017] Фигура 9 показывает изображения трансмиссионного электронного микроскопа (TEM) наночастиц, содержащих конъюгированные с липидами платиновые соединения согласно настоящему изобретению. Наночастицы показаны при различном увеличении, как можно видеть на измерительной линейке на каждом изображении.
[0018] Фигура 10 показывает изображение с помощью крио-трансмиссионного электронного микроскопа (Cryo-TEM) наночастиц, содержащих конъюгированные с липидами платиновые соединения согласно одному варианту осуществления настоящего изобретения.
[0019] Фигура 11 показывает ДРС гистограмму супрамолекулярного состава соединения 25 с диолеоилфосфатидилэтаноламином (DOPE).
[0020] Фигура 12 показывает, что содержащий DOPE состав соединения 25 (IO-125) имеет большую эффективность, чем составы без DOPE в A549 и DU145 клеточных линиях.
[0021] Фигура 13 показывает ВЭЖХ профиль промежуточного соединения Im-06 перед образованием соли с HCl. Как можно видеть, чистота Im-06 перед образованием соли с HCl составляла 91%.
[0022] Фигура 14 показывает ВЭЖХ профиль промежуточного соединения Im-06 после образования соли с HCl и обессоливания. Как можно видеть, чистота Im-06 после образования соли с HCl и обессоливания увеличивалась до 96,7%.
[0023] Фигура 15 показывает ВЭЖХ профиль соединения 25 после кристаллизации и после двух суспендирований.
[0024] Фигура 16 показывает порошковые рентгеновские 2θ дифрактограммы твердых веществ, извлеченных после успешного скрининга условий кристаллизации неочищенного соединения 25.
[0025] Фигура 17 показывает порошковые рентгеновские 2θ дифрактограммы твердых веществ после температурного циклирования.
[0026] Фигура 18 показывает микроснимки микроскопии в поляризованном свете кристаллического материала, полученные из метанол:дихлорметан (10:90%об/об) с затравкой.
[0027] Фигура 19 показывает порошковые рентгеновские 2θ дифрактограммы твердых веществ после температурного циклирования при концентрации приблизительно 150 мг/мл.
[0028] Фигуры 20 и 21 показывают порошковые рентгеновские 2θ дифрактограммы твердых веществ после температурного циклирования, гептан применяли в качестве антирастворителя.
[0029] Фигура 22 показывает порошковые рентгеновские 2θ дифрактограммы твердых веществ, полученных кристаллизацией при охлаждении.
[0030] Фигура 23 показывает микроснимки микроскопии в поляризованном свете высушенных твердых веществ.
[0031] Фигура 24 представляет собой ВЭЖХ хроматограмму 2 после кристаллизации охлаждением.
[0032] Фигура 25 показывает порошковые рентгеновские 2θ дифрактограммы высушенных твердых веществ.
[0033] Фигура 26 показывает микроснимки микроскопии в поляризованном свете высушенных твердых веществ.
[0034] Фигура 27 представляет собой ВЭЖХ хроматограмму твердых веществ, выделенных, применяя метанол:дихлорметан (20:80%об/об).
[0035] Фигура 28 показывает порошковые рентгеновские 2θ дифрактограммы высушенных твердых веществ.
[0036] Фигура 29 показывает микроснимки микроскопии в поляризованном свете высушенных твердых веществ.
[0037] Фигура 30 представляет собой ВЭЖХ хроматограмму твердых веществ, выделенных, применяя метанол:дихлорметан (20:80%об/об), с гептаном в качестве антирастворителя.
ПОДРОБНОЕ ОПИСАНИЕ
[0038] Настоящее изобретение относится к способу простой и экономичной липидной функционализации платиновых соединений, которые образуют достаточно чистые конъюгированные с липидами платиновое соединение с высоким выходом из самой реакционной смеси. После образования, немедленное осаждение конъюгированного с липидами платинового соединения термодинамически направляет реакцию в сторону комплексообразования, таким образом приводя к большим выходам. Другие преимущества определенных примерных вариантов осуществления описанного способа включают мягкие условия реакций, так что реакция может завершаться при комнатной температуре и давлении в одну атмосферу в пределах нескольких часов. В определенных примерных вариантах осуществления, воду применяют в качестве единственного растворителя. В определенных примерных вариантах осуществления, конъюгированное с липидами платиновое соединение осаждают из реакционной смеси, получая неочищенный продукт с≥50%,≥60%,≥70%,≥80% или≥90% выходом, или с выходом в диапазоне 70%-90%. В определенных примерных вариантах осуществления, конъюгированное с липидами платиновое соединение имеет чистоту неочищенного продукта≥50%,≥60%,≥70%,≥80% или≥90%. В определенных примерных вариантах осуществления, неочищенные продукты, затем, очищают, применяя полупрепаративную или препаративную высокоэффективную жидкостную хроматографию (ВЭЖХ), до чистоты >99,5%, удовлетворяя требованиям Управления по контролю за продуктами и лекарствами США.
[0039] Определенные примерные варианты осуществления настоящего изобретения обеспечивают способ получения конъюгированного с липидами платинового соединения, где способ включает: реакцию растворимой в воде соли липида с растворимым в воде платиновым соединением в по существу водном растворе, получая конъюгированное с липидами платиновое соединение в виде осадка. Определенные примерные варианты осуществления дополнительно включают стадию фильтрования или центрифугирования реакционной смеси, отделяя осадок от по существу водного раствора, и необязательно стадию промывки осадка водой. Не желая быть связанными теорией, описанные способы обеспечивают продукт, который осаждается, поскольку он является нерастворимым в водном растворе, тогда как реагенты остаются в растворе, таким образом, обеспечивая удобную очистку продукта простым фильтрованием или центрифугированием реакционной смеси.
[0040] Определенные примерные варианты осуществления дополнительно включают стадию очистки конъюгированного с липидами платинового соединения, применяя ВЭЖХ. ВЭЖХ применяют для дополнительного увеличения чистоты конъюгированного с липидами платинового соединения до >99,5% согласно указаниям FDA. ВЭЖХ способы вначале оптимизируют на аналитической колонке, и затем переносят на больший масштаб на препаративной колонке, получая граммовые количества конъюгированного с липидами платинового соединения с чистотой≥99,5%. ВЭЖХ способы, описанные в настоящем изобретении (смотри примеры ниже), являются очень надежными и независимыми от начальной чистоты конъюгированного с липидами платинового соединения. Соединения с начальной чистотой 20-90% успешно очищают, применяя описанные способы. Способ ВЭЖХ очистки также дает большие выходы (например, ≥50%,≥60%,≥70%,≥80% или≥90% для различных функционализированных липидами платиновых соединений). Конъюгированные с липидами платиновые соединения трудно очистить перекристаллизацией, но способы ВЭЖХ очистки, описанные в настоящем изобретении, успешно преодолевают данную проблему.
[0041] В определенных примерных вариантах осуществления в способе очистки ВЭЖХ применяют препаративную обращено-фазовую колонку. В определенных примерных вариантах осуществления, колонка содержит NH2 стационарную фазу, Phenyl стационарную фазу или C18 стационарную фазу. В определенных примерных вариантах осуществления, колонка содержит NH2 или Phenyl в качестве стационарной фазы, и конъюгированное с липидами платиновое соединение элюируют, применяя градиентный способ. В определенных примерных вариантах осуществления, градиентный способ включает элюирование подвижной фазой, содержащей смесь воды и метанола, где элюирование начинают смесью, содержащей большой процент воды и линейно увеличивают с течением времени до смеси, содержащей большой процент метанола. В определенных примерных вариантах осуществления колонка содержит C18 в качестве стационарной фазы, и конъюгированное с липидами платиновое соединение элюируют, применяя изократический способ. В определенных примерных вариантах осуществления, изократический способ включает элюирование подвижной фазой, содержащей 98% метанола и 2% воды.
[0042] Термин ʺпо существу водный растворʺ определяют как раствор, содержащий в основном воду, например, по меньшей мере, 90% воды, по меньшей мере, 95% воды, по меньшей мере, 98% воды, по меньшей мере, 99% воды и 100% воды. По меньшей мере, 99% воды может включать любое количество воды 99% или более и вплоть до 100%, например 99,3% воды, 99,5% воды, 99,8% воды, 99,9% воды и 100% воды.
[0043] В определенных примерных вариантах осуществления растворимая в воде соль липида и растворимое в воде платиновое соединение реагируют при комнатной температуре. Термин ʺкомнатная температураʺ применяют в общепринятом смысле, в том смысле, что внешний нагревающий или охлаждающий элемент не применяют для данной реакции. Комнатная температура может включать температуры в диапазоне, например 10°C-40°C, 20°C-30°C, 22°C-28°C и приблизительно 25°C. В определенных примерных вариантах осуществления растворимая в воде соль липида и растворимое в воде платиновое соединение реагируют при давлении в одну атмосферу. Давление в одну атмосферу может включать величину в пределах диапазона, например 790-650 мм рт.ст., 780-690 мм рт.ст., 770-730 мм рт.ст. и приблизительно 760 мм рт.ст.
[0044] В определенных примерных вариантах осуществления растворимую в воде соль липида выбирают из группы, состоящей из: литиевой соли, натриевой соли, калиевой соли, рубидиевой соли, цезиевой соли, магниевой соли, кальциевой соли, стронциевой соли, бариевой соли и любой их комбинации. В некоторых вариантах осуществления, растворимую в воде соль липида можно обеспечивать реакцией липида с основанием, выбранным из группы, состоящей из: LiOH, NaOH, KOH, RbOH, CsOH, Mg(OH)2, Ca(OH)2, Sr(OH)2, Ba(OH)2 и любой их комбинации.
[0045] В некоторых вариантах осуществления, растворимая в воде соль липида может представлять собой соль кислоты. Кислота для получения соли кислоты может представлять собой неорганическую или органическую кислоту. Примеры неорганических кислот для получения растворимой в воде соли липида включают, но не ограничиваются, трифторуксусную кислоту (TFA), уксусную кислоту, антраниловую кислоту, бензолсульфоновую кислоту, бензойную кислоту, камфорсульфоновую кислоту, коричную кислоту, лимонную кислоту, циклопентанпропионовую кислоту, этансульфоновую кислоту, муравьиную кислоту, фумаровую кислоту, 1,2-этандисульфоновую кислоту, 2-гидроксиэтансульфоновую кислоту, 2-нафталинсульфоновую кислоту, 3-фенилпропионовую кислоту, 4-метилбицикло[2.2.2]окт-2-ен-1-карбоновую кислоту, 4,4'-мефениленбис(3-гидрокси-2-ен-1-карбоновую кислоту), глюкогептоновую кислоту, глюконовую кислоту, глутамовую кислоту, гликолевую кислоту, гептановую кислоту, гидроксинафтойную кислоту, молочную кислоту, лаурилсерную кислоту, малеиновую кислоту, яблочную кислоту, малоновую кислоту, миндальную кислоту, метансульфоновую кислоту, муконовую кислоту, нафталинсульфоновую кислоту, о-(4-гидроксибензоил)бензойную кислоту, щавелевую кислоту, п-хлорбензолсульфоновую кислоту, пропионовую кислоту, п-толуолсульфоновую кислоту, пировиноградную кислоту, салициловую кислоту, стеариновую кислота, янтарную кислоту, сульфаниловую кислоту, винную кислоту, трет-бутилуксусную кислоту, трифторуксусную кислоту, триметилуксусную кислоту и подобные. Примеры неорганических кислот для получения растворимой в воде соли липида включают, но не ограничиваются, хлористоводородную кислоту, бромистоводородную кислоту, перхлорную кислоту, азотную кислоту, тиоциановую кислоту, серную кислоту, фосфорную кислоту и подобные.
[0046] В некоторых вариантах осуществления различных аспектов, описанных в настоящем изобретении, платиновая молекула представляет собой соединение платины (II) или платины (IV). В некоторых вариантах осуществления, соединение платины (II) выбирают из группы, состоящей из DACH-платины, цисплатины, оксалиплатины, карбоплатины, параплатины, сартраплатины и их различных комбинаций. В некоторых вариантах осуществления, соединение, содержащее платину, представляет содой соединение Pt(II), соединение Pt(IV) или платиновое соединение, содержащие галогенид. В предпочтительном варианте осуществления, платиновые соединения представляют собой оксалиплатину.
[0047] Термин "липид" применяют в общепринятом смысле, и он включает соединения различной длины цепи, начиная с такой короткой как приблизительно 2 атома углерода вплоть до 28 атомов углерода. Кроме того, соединения может быть насыщенным или ненасыщенным и с нормальными или разветвленными цепями или в виде неконденсированных или конденсированных кольцевых структур. Примеры липидов включают, но не ограничиваются, жиры, воски, стеролы, стероиды, желчные кислоты, жирорастворимые витамины (такие как A, D, E и K), моноглицериды, диглицериды, фосфолипиды, гликолипиды, сульфолипиды, аминолипиды, хромолипиды (липохромы), глицерофосфолипиды, сфинголипиды, преноллипиды, сахаролипиды, поликетиды и жирные кислоты.
[0048] Без ограничений липид можно выбрать из группы, состоящей из стерольных липидов, жирных кислот, жирных спиртов, глицеролипидов (например, моноглицеридов, диглицеридов и триглицеридов), фосфолипидов, глицерофосфолипидов, сфинголипидов, преноллипидов, сахаролипидов, поликетидов и любой их комбинации. Липид может представлять собой полиненасыщенную жирную кислоту или спирт. Термин "полиненасыщенная жирная кислотаʺ или "полиненасыщенный жирный спирт", как применяют в настоящем изобретении, обозначает жирную кислоту или спирт с двумя или более углерод-углеродными двойными связями в его углеводородной цепи. Липид может также представлять собой сильно ненасыщенную жирную кислоту или спирт. Термин "сильно полиненасыщенная жирная кислотаʺ или "сильно полиненасыщенный жирный спирт", как применяют в настоящем изобретении, обозначает жирную кислоту или спирт, содержащие, по меньшей мере, 18 атомов углерода и, по меньшей мере, 3 двойные связи. Липид может представлять собой омега-3 жирную кислоту. Термин "омега-3 жирная кислота", как применяют в настоящем изобретении, обозначает полиненасыщенную жирную кислоту, чья первая двойная связь находится по третьей углерод-углеродной связи от конца, противоположного карбоксильной группе.
[0049] В некоторых вариантах осуществления, липид можно выбрать из группы, состоящей из дикаприлата/дикапрата 1,3-пропандиола; 10-ундеценовой кислоты; 1-дотриаконтанола; 1-гептакозанола; 1-нонакозанола; 2-этилгексанола; андростанов; арахидной кислоты; арахидоновой кислоты; арахидилового спирта; бегеновой кислоты; бегенилового спирта; Capmul MCM C10; каприновой кислоты; капринового спирта; каприлового спирта; каприловой кислоты; эфира каприловой/каприновой кислоты и насыщенного жирного спирта C12-C18; каприловых/каприновых триглицеридов; церамидфосфорилхолина (сфингомиелина, SPH); церамидфосфорилэтаноламина (сфингомиелина, Cer-PE); церамидфосфорилглицерина; церопластовой кислоты; церотовой кислоты; церилового спирта; цетеарилового спирта; цетета-10; цетилового спирта; холанов; холестанов; холестерина; цис-11-эйкозеновой кислоты; цис-11-октадеценовой кислоты; цис-13-докозеновой кислоты; клуитилового спирта; коэнзима Q10 (CoQ10); дигомо-γ-линоленовой кислоты; докозагексановой кислоты; яичного лецитина; эйкозапентаеновой кислоты; эйкозеновой кислоты; элаидиновой кислоты; элаидолиноленилового спирта; элаидолинолеилового спирта; элаидилового спирта; эруковой кислоты; эруцилового спирта; эстранов; дистеарата этиленгликоля (EGDS); геддовой кислоты; гедиллового спирта; дистеарата глицерина (тип I) EP (прецирол ATO 5); трикаприлата/капрата глицерина; трикаприлата/капрата глицерина (CAPTEX® 355 EP/NF); монокаприлата глицерина (Capmul MCM C8 EP); триацетата глицерина; трикаприлата галицерина; трикаприлата/капрата/лаурата глицерина; трикаприлата/трикапрата глицерина; трипальмитата глицерина (трипальмитин); хенатриаконтиловой кислоты; геникозилового спирта; генэйкозановой кислоты; гептакозиловой кислоты; гептадекановой кислоты; гептадецилового спирта; гексатриаконтиловой кислоты; изостеариновой кислоты; изостеарилового спирта; лацериновой кислоты; лауриновой кислоты; лаурилового спирта; лигноцериновой кислоты; лигноцерилового спирта; линоэлаидиновой кислоты; линоленовой кислоты; линоленилового спирта; линолеилового спирта; маргариновой кислоты; мидовой кислоты; мелиссиновой кислоты; мелиссилового спирта; монтановой кислоты; монтанилового спирта; мирицилового спирта; миристиновой кислоты; миристолеиновой кислоты; миристилового спирта; неодекановой кислоты; неогептановой кислоты; неононановой кислоты; ацетэруковой кислоты; нонакозиловой кислоты; нонадецилового спирта; нонадециловой кислоты; нонадециловой кислоты; олеиновой кислоты; олеилового спирта; пальмитиновой кислоты; пальмитолеиновой кислоты; пальмитолеилового спирта; пеларгоновой кислоты; пералгонового спирта; пентакозиловой кислоты; пентадецилового спирта; пентадециловой кислоты; фосфатидной кислоты (фосфатидат, PA); фосфатидилхолина (лецитин, PC); фосфатидилэтаноламина (цефалин, PE); фосфатидилинозитола (PI); бисфосфата фосфатидилинозитола (PIP2); фосфата фосфатидилинозитола (PIP); трифосфата фосфатидилинозитола (PIP3); фосфатидилсерина (PS); полиглицерин-6-дистеарата; прегнанов; дикапрата пропиленгликоля; дикаприлокапрата пропиленгликоля; дикаприлокапрата пропиленгликоля; псилластеариновой кислоты; рициноленовой кислоты; рицинолеилового спирта; сапиеновой кислоты; соевого лецитина; стериновой кислоты; стеаридоновой кислоты; стеарилового спирта; трикозановой кислоты; тридецилового спирта; тридекановой кислоты; триолеина; ундецилового спирта; ундециленовой кислоты; ундециловой кислоты; вакценовой кислоты; α-линоленовой кислоты; γ-линоленовой кислоты; соли 10-ундеценовой кислоты, адапалена, арахиновой кислоты, арахидоновой кислоты, бегеновой кислоты, масляной кислоты, каприновой кислоты, каприловой кислоты, церотовой кислоты, цис-11-эйкозеновой кислоты, цис-11-октадеценовой кислоты, цис-13-докозеновой кислоты, докозагексановой кислоты, эйкозапентавой кислоты, элаидиновой кислоты, эруковой кислоты, генэйкозановой кислоты, гептакозиловой кислоты, гептадекановой кислоты, изостеариновой кислоты, лауриновой кислоты, лигноцериновой кислоты, линоэладиновой кислоты, линолевой кислоты, монтановой кислоты, миристиновой кислоты, миристолевой кислоты, неодекановой кислоты, неогептановой кислоты, неононановой кислоты, неадециловой кислоты, олеиновой кислоты, пальмитиновой кислоты, пальмитолевой кислоты, пеларгоновой кислоты, пентакозиловой кислоты, пентадециловой кислоты, ретинолевой кислоты (например, рецинолеата цинка), сапиевой кислоты, стеариновой кислоты, трикозиловой кислоты, тридециловой кислоты, ундециленовой кислоты, ундециловой кислоты, вакценовой кислоты, валериановой кислоты, α-линоленовой кислоты, γ-линоленовой кислоты; и любых их комбинаций.
[0050] В определенных примерных вариантах осуществления липид представляет собой холестерин или его производные. В некоторых вариантах осуществления липид представляет собой α-токоферол.
[0051] В определенных примерных вариантах осуществления растворимая в воде соль липида дополнительно содержит линкер, ковалентно присоединенный к липиду. Как применяют в настоящем изобретении, термин ʺлинкерʺ обозначает органическую группу, которая может соединять части соединения. Линкеры обычно включают непосредственную связь с атомом, таким как кислород или сера, фрагменты, такие как NR1, C(O), C(O)NH, C(O)O, NHC(O)O, OC(O)O, SO, SO2, SO2NH или цепи атомов, такие как замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, арилалкил, арилалкенил, арилалкинил, гетероарилалкил, гетероарилалкенил, гетероарилалкинил, гетероциклилалкил, гетероциклилалкенил, гетероциклилалкинил, арил, гетероарил, гетероциклил, циклоалкил, циклоалкенил, алкиларилалкил, алкиларилалкенил, алкиларилалкинил, алкениларилалкил, алкениларилалкенил, алкениларилалкинил, алкиниларилалкил, алкиниларилалкенил, алкиниларилалкинил, алкилгетероарилалкил, алкилгетероарилалкенил, алкилгетероарилалкинил, алкенилгетероарилалкил, алкенилгетероарилалкенил, алкенилгетероарилалкинил, алкинилгетероарилалкил, алкинилгетероарилалкенил, алкинилгетероарилалкинил, алкилгетероциклилалкил, алкилгетероциклилалкенил, алкилгетероциклилалкинил, алкенилгетероциклилалкил, алкенилгетероциклилалкенил, алкенилгетероциклилалкинил, алкинилгетероциклилалкил, алкинилгетероциклилалкенил, алкинилгетероциклилалкинил, алкиларил, алкениларил, алкиниларил, алкилгетероарил, алкенилгетероарил, алкинилгетероарил, где один или более метиленов можно прерывать или терминировать O, S, S(O), SO2, NR1, C(O), C(O)NH, C(O)O, NHC(O)O, OC(O)O, SO2NH, расщепляемые линкерные группы, замещенный или незамещенный арил, замещенный или незамещенный гетероарил, замещенный или незамещенный гетероциклил; где R1 представляет собой водород, ацил, является алифатическим или замещенным алифатическим.
[0052] В определенных примерных вариантах осуществления, линкер, ковалентно соединенный с липидом, представлен формулой I:
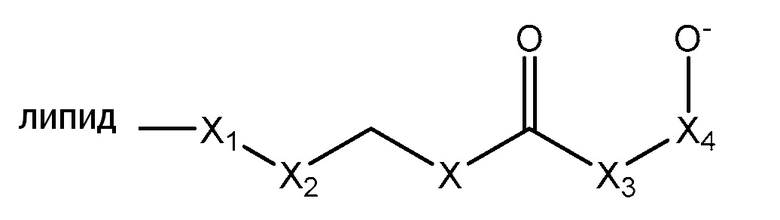
Где:
X представляет собой NH;
X1 выбирают из группы, состоящей из COOH, CONH2, O-(CH2)n-OH, NH2 и OH;
X2 представляет собой (CH2)n или CO;
X3 выбирают из группы, состоящей из (CH2)n, CH2-NH и C4H8;
X4 представляет собой CO или -CH-CH3;
и где n= 0-2.
[0053] В определенных примерных вариантах осуществления, линкер, ковалентно соединенный с липидом, представлен, формулой II:
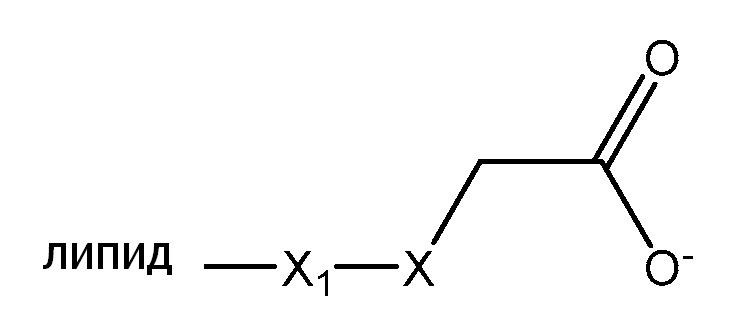
Где:
X представляет собой NH или N-CH2COO-;
X1 выбирают из группы, состоящей из -(CH2)nOH, -(CH2)nNHCOOH, -(CH2)nCONH(CH2)nOH, (CH2)nO(CH2)nOH, (CH2)nC=O, -(CH2)nNHCO(CH2)nOH и (CH2)n-COOH; где n= 0-2.
[0054] В определенных примерных вариантах осуществления, линкер, ковалентно соединенный с липидом, представлен, формулой III:
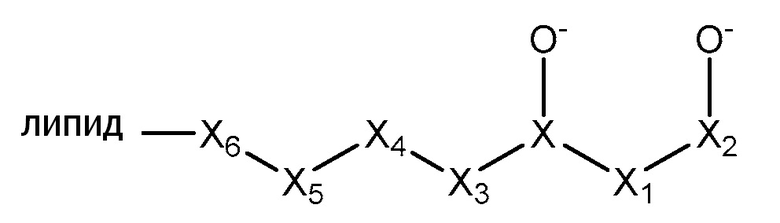
Где:
X выбирают из группы, состоящей из S+, C, S+=O, N+H и P=O;
X1 выбирают из группы, состоящей из -CH, -CH2 и -CH2O;
X2 представляет собой C=O;
X3 представляет собой CH, CH2 или O; и
X4, X5, X6 представляет собой -CH2O или O.
[0055] В определенных примерных вариантах осуществления, линкер, ковалентно соединенный с липидом, представлен, формулой IV:
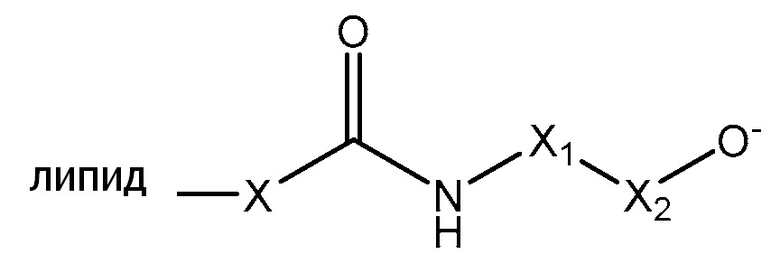
Где:
X представляет CH2OH;
X1 представляет собой (CH2)n, где n=0-2; и
X2 представляет собой C=O.
[0056] В некоторых вариантах осуществления, линкер представляет собой разветвленный линкер. Место разветвления разветвленного линкера может представлять собой, по меньшей мере, трехвалентный, но может представлять собой четырехвалентный, пятивалентный или шестивалентный атом, или группу, представляющую данные множественные валентности. В некоторых вариантах осуществления, место разветвления представляет собой -N, -N(Q)-C, -O-C, -S-C, -SS-C, -C(O)N(Q)-C, -OC(O)N(Q)-C, -N(Q)C(O)-C или -N(Q)C(O)O-C; где Q независимо для каждого появления представляет собой H или необязательно замещенный алкил. В некоторых вариантах осуществления место разветвления представляет собой глицерин или его производное.
[0057] Расщепляемая линкерная группа представляет собой отщепляемую линкерную группу, которая является достаточно стабильной вне клетки, но после проникновения в клетку, расщепляется, высвобождая две части, удерживающие линкер вместе. В предпочтительном варианте осуществления расщепляемая линкерная группа расщепляется, по меньшей мере, в 10 раз или более, предпочтительно, по меньшей мере, в 100 раз быстрее в целевой клетке или при первых заданных условиях (которые можно, например, выбрать для имитации или репрезентации внутриклеточных условий), чем в крови или сыворотке субъекта, или при вторых заданных условиях (которые можно, например, выбрать для имитации или репрезентации условий, обнаруживаемых в крови или сыворотке).
[0058] Отщепляемые линкерные группы подвержены действию расщепляющих агентов, например, pH, окислительно-восстановительному потенциалу или присутствию деструктивных молекул. Обычно, расщепляющие агенты более преобладают или обнаруживаются в больших концентрациях или при больших активностях внутри клеток, чем в сыворотке или крови. Примеры данных деструктивных агентов включают: окислительно-восстановительные агенты, которые выбирают для конкретных субстратов или которые не обладают субстратной специфичностью, включая, например, окисляющие или восстанавливающие ферменты или восстанавливающие агенты, такие как меркаптаны, присутствующие в клетках, которые могут расщеплять окислительно-восстановительно отщепляемую линкерную группу восстановлением; эстеразы; амидазы; эндосомы или агенты, которые могут создавать кислое окружение, например, агенты, которые обеспечивают pH пять или ниже; ферменты, которые могут гидролизовать или разрушать кислотно отщепляемую линкерную группу действием в качестве обычной кислоты, пептидазы (который могут быть специфичными к субстрату) и протеазы и фосфатазы.
[0059] Линкер может включать отщепляемую линкерную группу, которая расщепляется конкретным ферментом. Тип расщепляемой линкерной группы, введенной в линкер, может зависеть от целевой клетки. Например, лиганды, направленные на печень, могут быть соединены с катионными липидами через линкер, который содержит эфирную группу. Клетки печени являются богатыми эстеразами и, следовательно, линкер будет расщепляться более эффективно в клетках печени, чем в типах клеток, которые не являются богатыми эстеразами. Другие типы клеток, богатые эстеразами, включают клетки легких, кору почек и семенник. Линкеры, которые содержат пептидные связи, можно применять, когда типы целевых клеток богаты пептидазами, такие как клетки печени и синовиоциты.
[0060] В некоторых вариантах осуществления расщепляемая линкерная группа расщепляется, по меньшей мере, в 1,25, 1,5, 1,75, 2, 3, 4, 5, 10, 25, 50 или 100 раз быстрее в клетках (или в условиях in vitro, выбранных для имитации внутриклеточных условий) по сравнению с кровью или сывороткой (или в условиях in vitro, выбранных для имитации внеклеточных условий). В некоторых вариантах осуществления, расщепляемая линкерная группа расщепляется менее чем на 90%, 80%, 70%, 60%, 50%, 40%, 30%, 20%, 10%, 5% или 1% в крови (в условиях in vitro, выбранных для имитации внеклеточных условий) по сравнению со случаем в клетке (в условиях in vitro, выбранных для имитации внутриклеточных условий).
[0061] Примеры расщепляемых линкерных групп включают, но не ограничиваются, окислительно-восстановительно отщепляемые линкерные группы (например, -S-S- и -C(R)2-S-S-, где R представляет собой H или C1-C6 алкил и, по меньшей мере, один R представляет собой C1-C6 алкил, такой как CH3 или CH2CH3); фосфатные отщепляемые линкерные группы (например, -O-P(O)(OR)-O-, -O-P(S)(OR)-O-, -O-P(S)(SR)-O-, -S-P(O)(OR)-O-, -O-P(O)(OR)-S-, -S-P(O)(OR)-S-, -O-P(S)(ORk)-S-, -S-P(S)(OR)-O-, -O-P(O)(R)-O-, -O-P(S)(R)-O-, -S-P(O)(R)-O-, -S-P(S)(R)-O-, -S-P(O)(R)-S-, -O-P(S)( R)-S-, -O-P(O)(OH)-O-, -O-P(S)(OH)-O-, -O-P(S)(SH)-O-, -S-P(O)(OH)-O-, -O-P(O)(OH)-S-, -S-P(O)(OH)-S-, -O-P(S)(OH)-S-, -S-P(S)(OH)-O-, -O-P(O)(H)-O-, -O-P(S)(H)-O-, -S-P(O)(H)-O-, -S-P(S)(H)-O-, -S-P(O)(H)-S- и -O-P(S)(H)-S-, где R представляет собой необязательно замещенный линейный или разветвленный C1-C10 алкил); кислотнорасщепляемые линкерные группы (например, гидразоны, эфиры и эфиры аминокислот, -C=NN- и -OC(O)-); эфирные отщепляемые линкерные группы (например, -C(O)O-); пептидные отщепляемые линкерные группы (например, линкерные группы, расщепляемые ферментами, такими как пептидазы и протеазы, в клетках, например, -NHCHRAC(O)NHCHRBC(O)-, где RA и RB представляют собой R группы двух соседних аминокислот). Пептидная расщепляемая линкерная группа содержит две или более аминокислот. В некоторых вариантах осуществления пептидный расщепляемый линкер содержит аминокислотную последовательность, которая представляет собой субстрат для пептидазы или протеазы, обнаруживаемых в клетках.
[0062] В некоторых вариантах осуществления, кислотнорасщепляемая линкерная группа является расщепляемой в кислом окружении с pH приблизительно 6,5 или ниже (например, приблизительно 6,5, 6,0, 5,5, 5,0 или ниже), или агентами, таким как ферменты, которые могут действовать как обычные кислоты.
[0063] Линкеры согласно настоящему изобретению включают молекулы, содержащие две или более углеродные молекулы, такие как, например, этилендиамин, этиленгликоль, глицин, бета-аланин и полиэтиленгликоль (PEG) молекулярного веса от приблизительно 44 до приблизительно 200 кДа. Кроме того, из настоящего изобретения ясно, что платиновый фрагмент и/или липид можно модифицировать так, чтобы они содержали функциональные группы для соединения с молекулой линкера.
[0064] В некоторых вариантах осуществления различных аспектов, описанных в настоящем изобретении, линкер представляет собой -X-CH2-X2-X1-, где X представляет собой NH; X1 представляет собой C(O)O, C(O)NH, O(CH2)-O, NH или O; X2 представляет собой (CH2)n или C(O); и n равен 0, 1, 2, 3, 4 или 5.
[0065] В некоторых других вариантах осуществления, линкер представляет собой -(CH2)nO-, -(CH2)nNHC(O)O-, -(CH2)nOC(O)NH-, - (CH2)nC(O)NH(CH2)mO-, - (CH2)nO(CH2)mO-, - (CH2)nO(O)-, -(CH2)nNHC(O)(CH2)mO- или -(CH2)nC(O)O-; и n и m независимо равны 0, 1, 2, 3, 4 или 5.
[0066] В еще некоторых других вариантах осуществления, линкер представляет собой -X3-X4X5-X6-, где X3 представляет собой CH, CH2, или O; и X4, X5 и X6 независимо являются одинаковыми или различными и представляют собой -CH2O- или O.
[0067] В еще некоторых других вариантах осуществления, линкер представляет собой -CH2O-.
[0068] В некоторых вариантах осуществления, линкер выбирают из группы, состоящей из связи, -O-, NHCH2CH2NHC(O)-, -NHCH2CH2NHC(O)O-, -NHCH2CH2-, -NHCH2CH2O-, -NHCH2C(O)-, -NHCH2C(O)O-, -NHCH2C(O)OCH2CH2CH2-, -NHCH2C(O)OCH2CH2CH2O-, -NHCH2C(O)NH-, -CH2CH2-, -CH2CH2O-, -CH2CH2NHC(O)-, -CH2CH2NHC(O)O-, -CH2CH2O-, -CH2C(O)NHCH2CH2-, -CH2C(O)NHCH2CH2O-, -CH2CH2OCH2CH2-, -CH2CH2OCH2CH2O-, -CH2C(O) -, -CH2C(O)O-, -CH2CH2CH2-, --CH2CH2CH2O-, =CH-CH=CH2-, =CH-CH=CHCH2O-, -CH=CHCH2-, -CH=CHCH2O-, -OCH2CH2O-, -CH2-, -CH2O-, -NHC(O)CH2-, -NHC(O)CH2O-, -C(O)CH2-, -C(O)CH2O-, -OC(O)CH2-, -OC(O)CH2O-, -C(O)CH2CH2C(O)NHCH2CH2-, -OC(O)CH2CH2C(O)NHCH2CH2-, -C(O)CH2CH2C(O)NHCH2CH2O-, -OC(O)CH2CH2C(O)NHCH2CH2O-, -C(O)CH2CH2C(O)NHCH2CH2NHC(O)-, -OC(O)CH2CH2C(O)NHCH2CH2NHC(O)-, -C(O)CH2CH2C(O)NHCH2CH2NHC(O)O-, -OC(O)CH2CH2C(O)NHCH2CH2NHC(O)O- и любых их комбинаций.
[0069] В определенных примерных вариантах осуществления, растворимую в воде соль липида можно обеспечивать реакцией липида или линкера, ковалентно присоединенного к липиду, с основанием, выбранным из группы, состоящей из: LiOH, NaOH, KOH, RbOH, CsOH, Mg(OH)2, Ca(OH)2, Sr(OH)2, Ba(OH)2 и любой их комбинации. В некоторых вариантах осуществления, липид или линкер, ковалентно соединенный с липидом, реагирует с LiOH, давая растворимую в воде соль липида.
[0070] В определенных примерных вариантах осуществления, растворимое в воде платиновое соединение представлено формулой V:
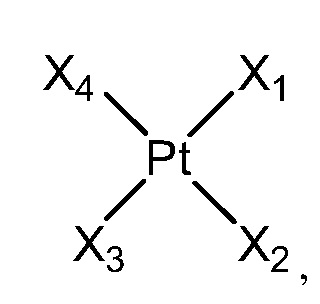
где
[0071] X1, X2, X3 и X4 независимо выбраны из группы, состоящей из галогенида, алкила, амино, алкиламино, диалкиламино, гидроксила, H2O, алкокси, тиола, тиоалкила, O-ацила и любых их комбинаций.
[0072] X1 и X2 могут представлять собой монодентатные или бидентатные лиганды. В некоторых вариантах осуществления, X1 и X2 представляют собой амино, например, NH3 или диаминоциклогексил (DACH). В некоторых вариантах осуществления, каждый X3 и X4 представляет собой H2O. В определенных примерных вариантах осуществления растворимое в воде платиновое соединение обеспечивают реакцией платинового соединения формулы V, где X1 и X2 включают бидентатный аминолиганд, и каждый X3 и X4 включает галогенид, с AgNO3 и H2O. В некоторых вариантах осуществления данной стадии, X1 и X2 представляют собой DACH, и каждый X3 и X4 представляет собой Cl.
[0073] Описанные способы настоящего изобретения можно применять для получения различных конъюгированных с липидами платиновых соединений. В определенных примерных вариантах осуществления конъюгированное с липидами платиновое соединение представлено формулой V:

где
X1, X2, X3 и X4 независимо выбраны из группы, состоящей из галогенида, алкила, амино, алкиламино, диалкиламино, гидроксила, алкокси, тиола, тиоалкила, O-ацила и любых их комбинаций.
[0074] В некоторых вариантах осуществления, конъюгированные с липидами платиновые соединения, описанные в настоящем изобретении, представлены формулой (VI):
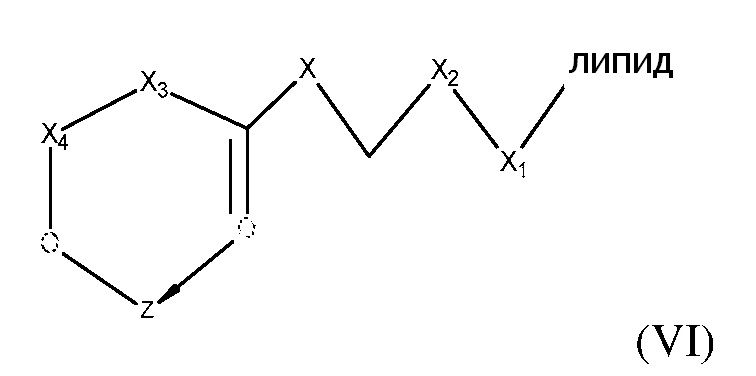
где
X представляет собой NH;
X1 выбран из группы, состоящей из COOH, CONH2, O-(CH2)n-OH, NH2 и OH;
X2 представляет собой (CH2)n или CO;
X3 выбран из группы, состоящей (CH2)n, CH2-NH и C4H8;
X4 представляет собой CO или -CH-CH3;
Z представляет собой платиновое соединение согласно формуле V, где платина образует часть кольца формулы VI; и
n равен 0, 1 или 2.
[0075] В некоторых других вариантах осуществления конъюгированные с липидами платиновые соединения, описанные в настоящем изобретении, представлены формулой (VII):
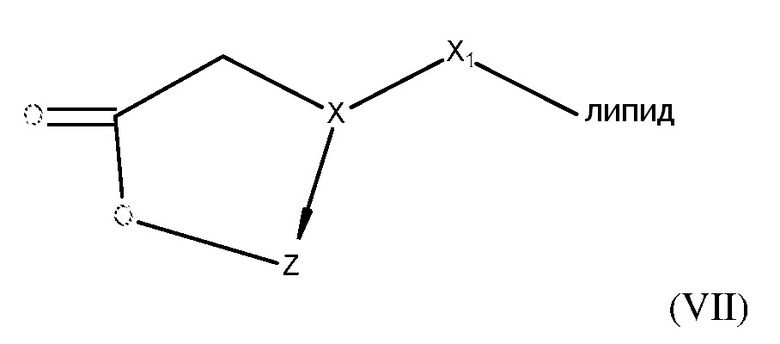
где
X представляет собой NH или N-CH2COO-;
X1 выбран из группы, состоящей -(CH2)nOH, -(CH2)nNHCOOH, -(CH2)nCONH(CH2)nOH, (CH2)nO(CH2)nOH, (CH2)nC=O, -(CH2)nNHCO(CH2)nOH и (CH2)n-COOH;
Z представляет собой платиновое соединение согласно формуле V, где платина образует часть кольца формулы VII; и
n равен 0, 1 или 2.
[0076] В некоторых вариантах осуществления, конъюгированные с липидами платиновые соединения, описанные в настоящем изобретении, представлены формулой (VIII):
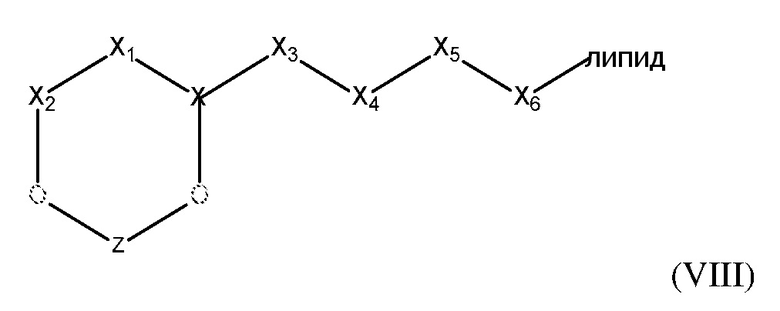
где
X выбран из группы, состоящей S+, C, S+=O, N+H и P=O;
X1 выбран из группы, состоящей -CH, -CH2 и -CH2O;
X2 представляет собой C=O;
X3 выбран из CH, CH2 или O;
X4, X5, X6 выбран из -CH2O или O
Z представляет собой платиновое соединение согласно формуле V, где платина образует часть кольца формулы VIII.
[0077] В некоторых вариантах осуществления, конъюгированные с липидами платиновые соединения, описанные в настоящем изобретении, представлены формулой (IX):
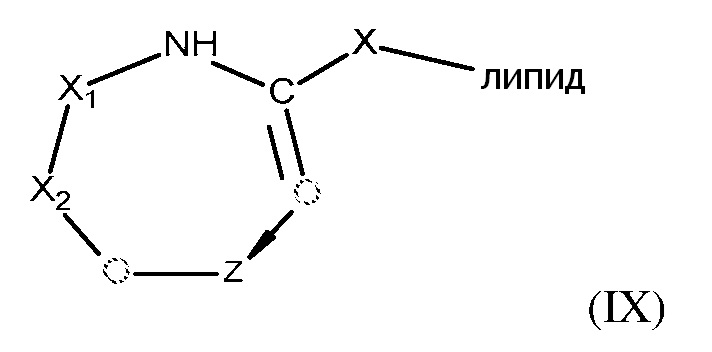
где
X представляет CH2OH;
X1 представляет собой (CH2)n;
X2 представляет собой C=O;
Z представляет собой платиновое соединение согласно формуле V, где платина образует часть кольца формулы IX; и
n равен 0, 1 или 2.
[0078] Примеры соединений формулы (VI) включают, но не ограничиваются, следующие соединения: все соединения формулы (VI) содержат нитратный (NO3-) противоион, который не показан на фигурах.
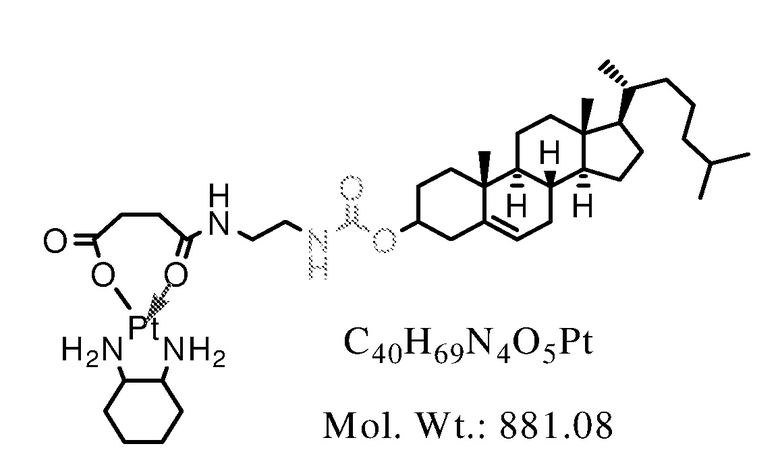
Соединение 1
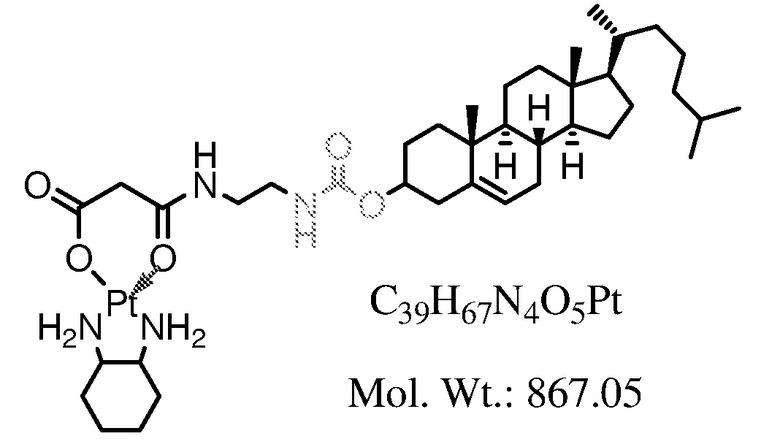
Соединение 2
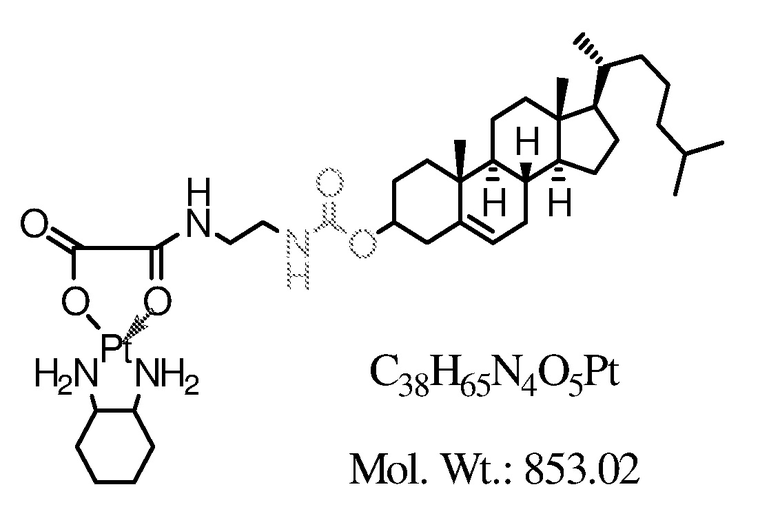
Соединение 3
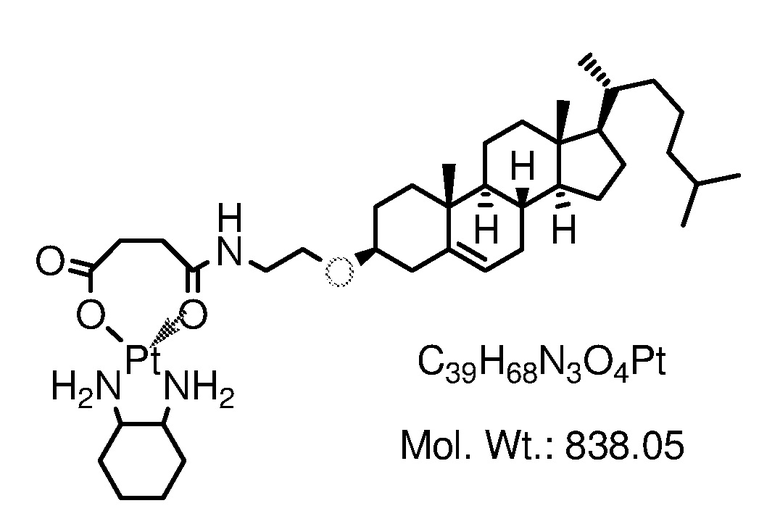
Соединение 4
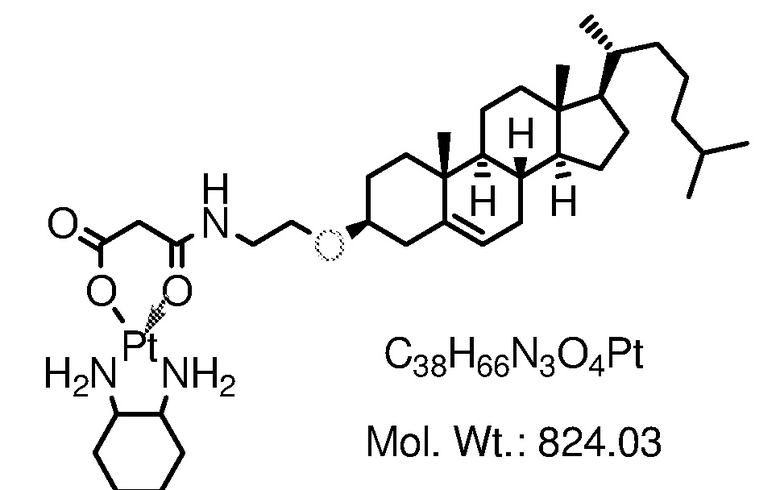
Соединение 5
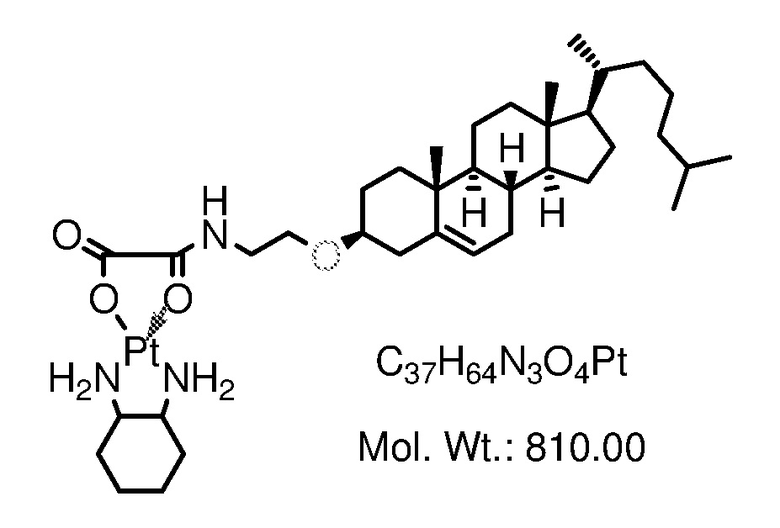
Соединение 6
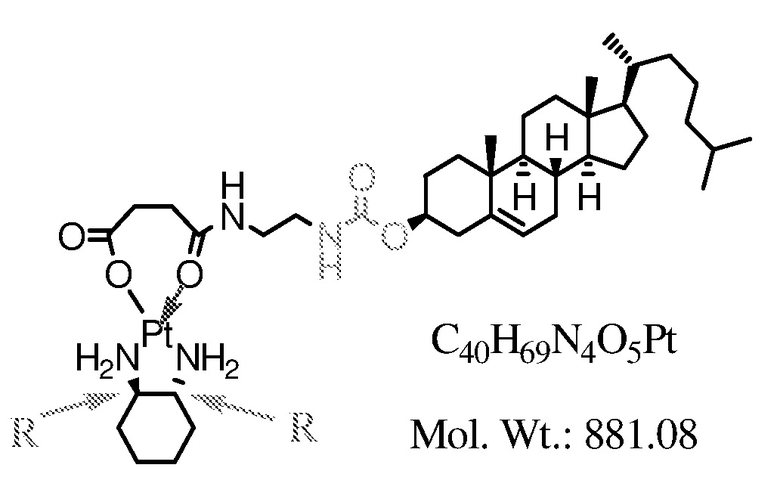
Соединение 7
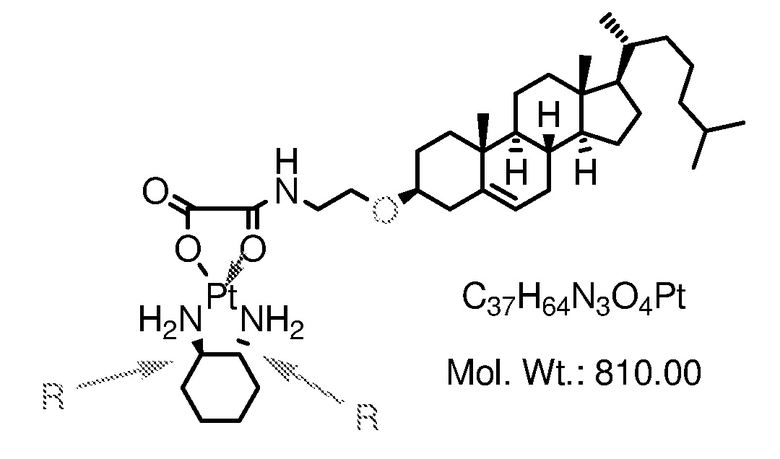
Соединение 8
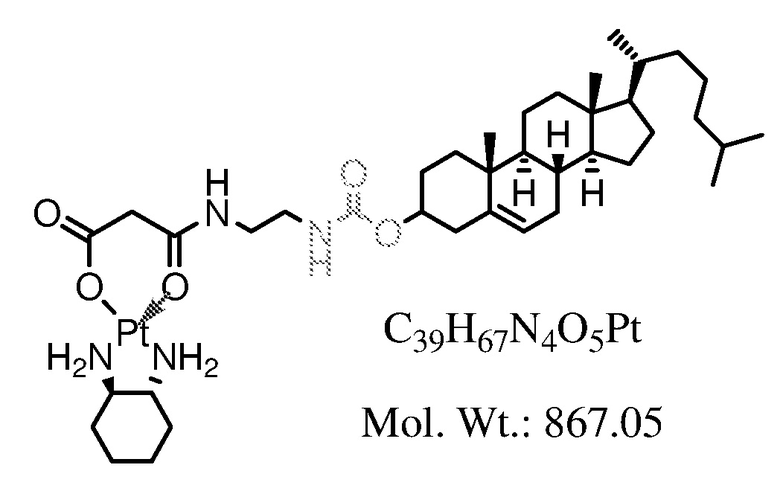
Соединение 9
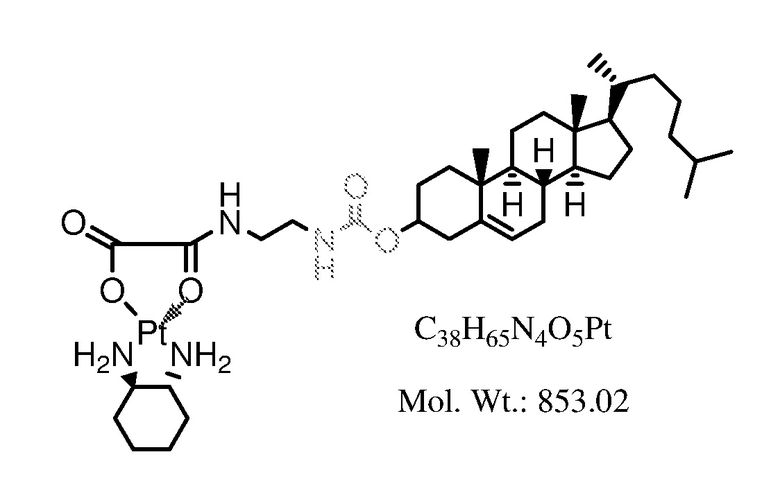
Соединение 10
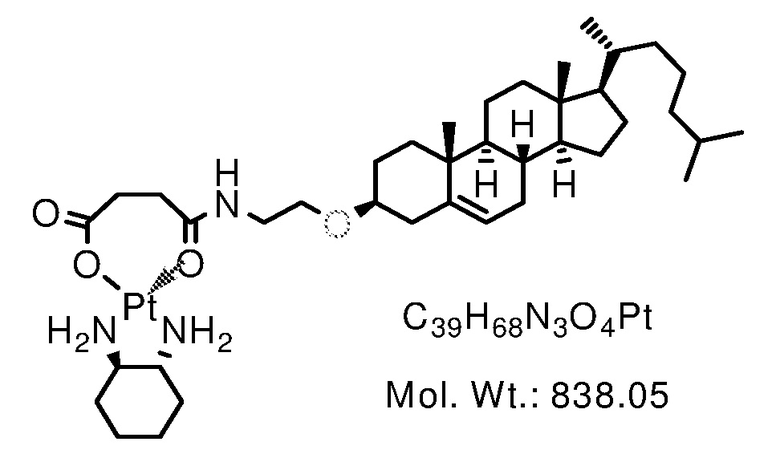
Соединение 11
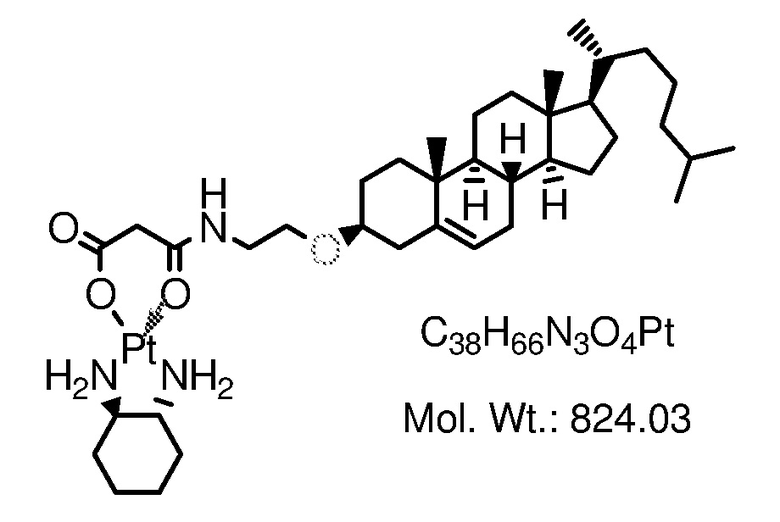
Соединение 12
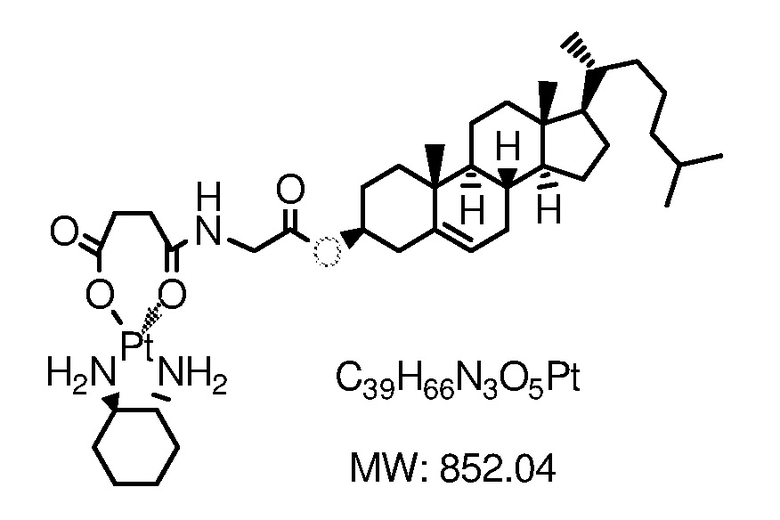
Соединение 13
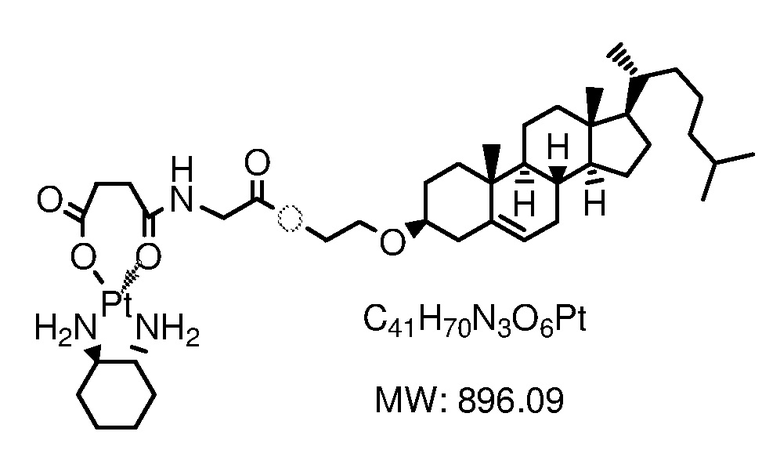
Соединение 14
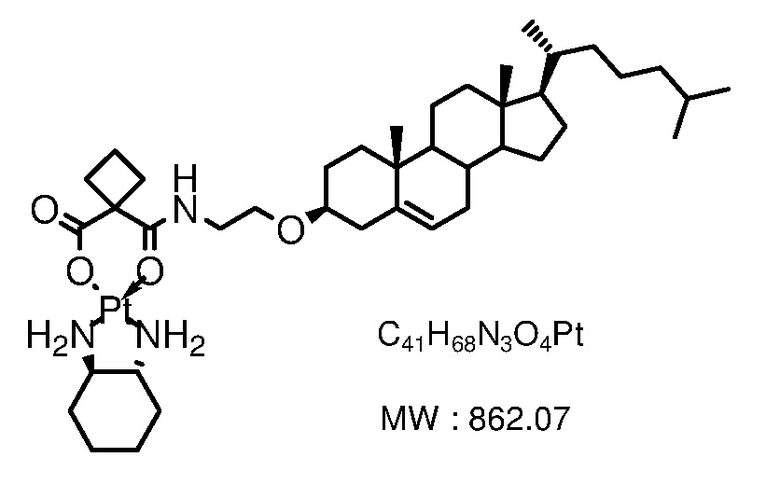
Соединение 15
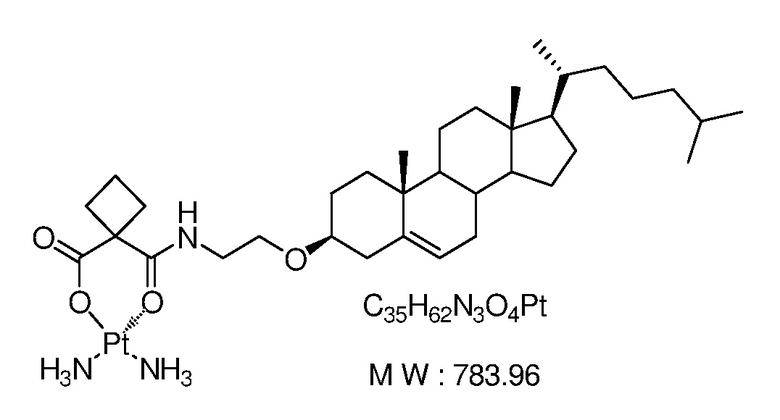
Соединение 16
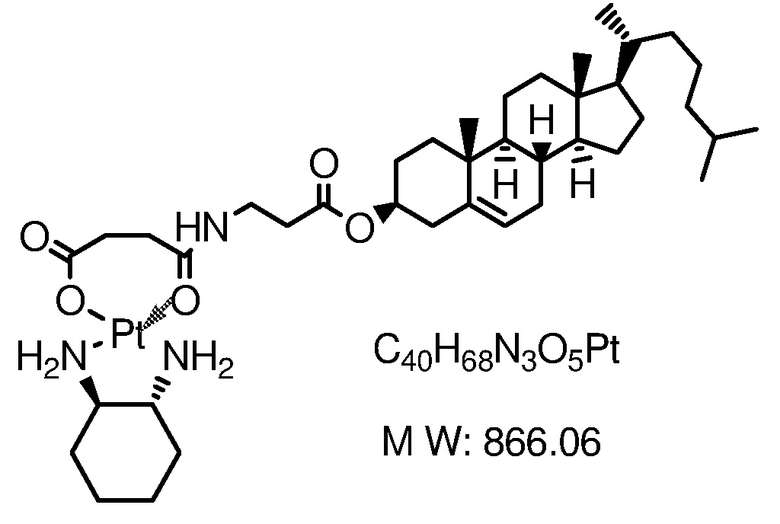
Соединение 17

Соединение 18
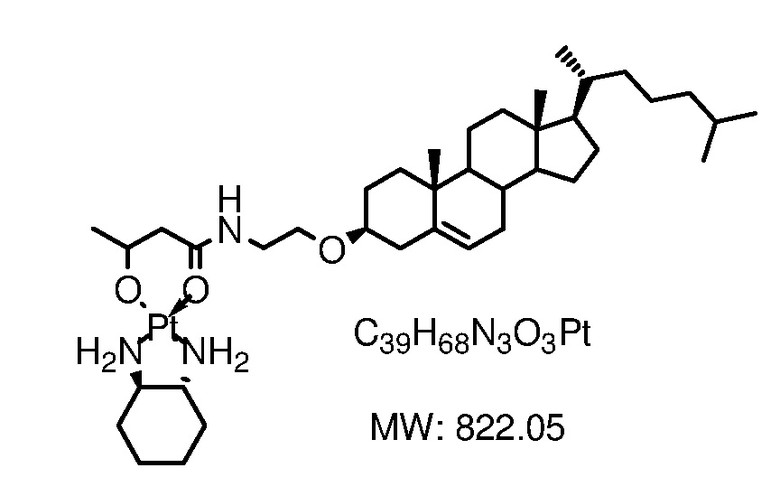
Соединение 19
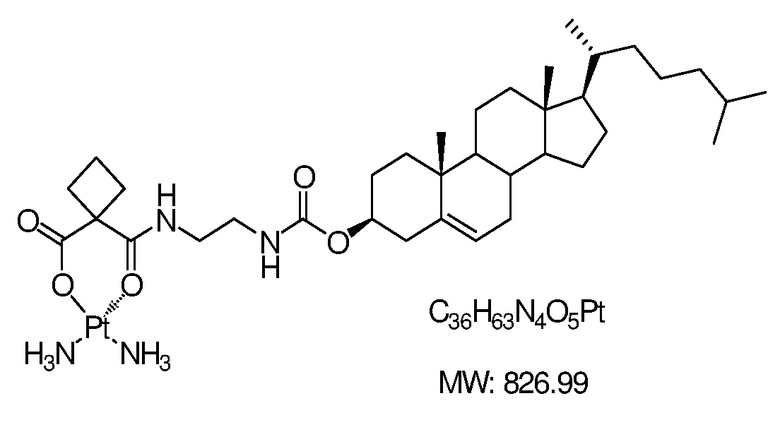
Соединение 20
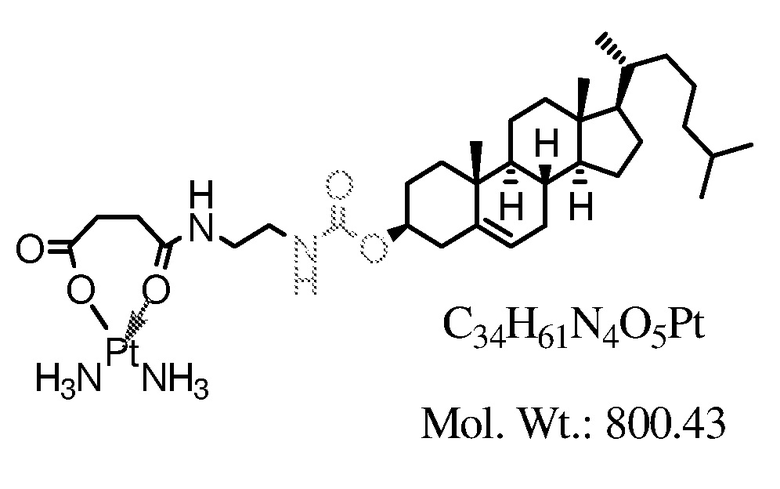
Соединение 21
[0079] Примеры соединений формулы (VII) включают, но не ограничиваются, следующие соединения:
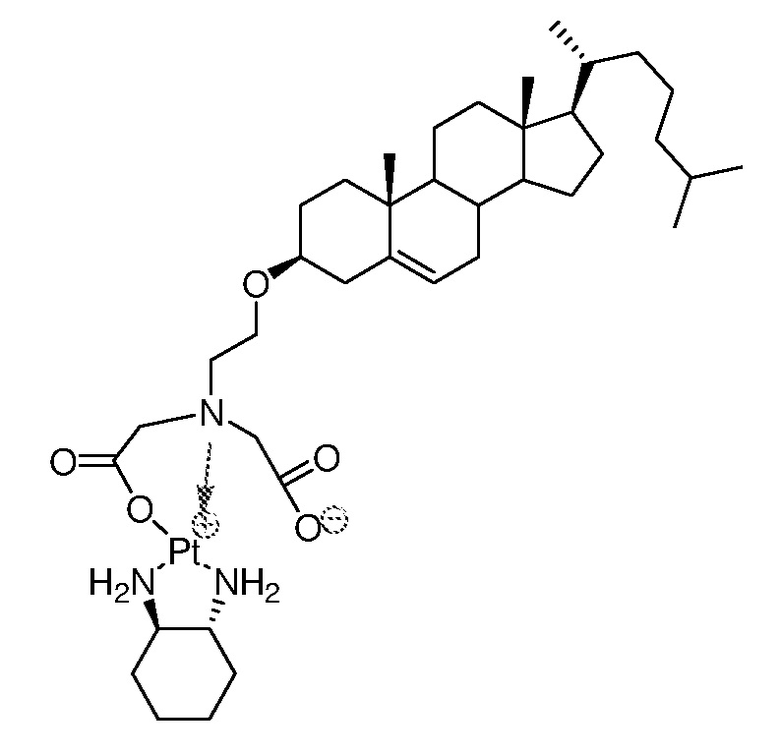
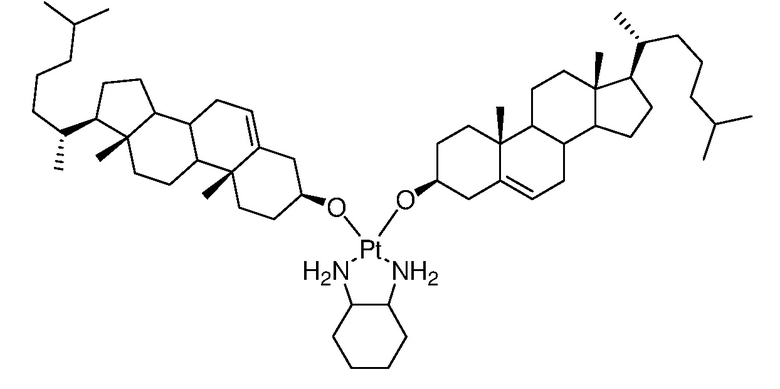
Соединение 25
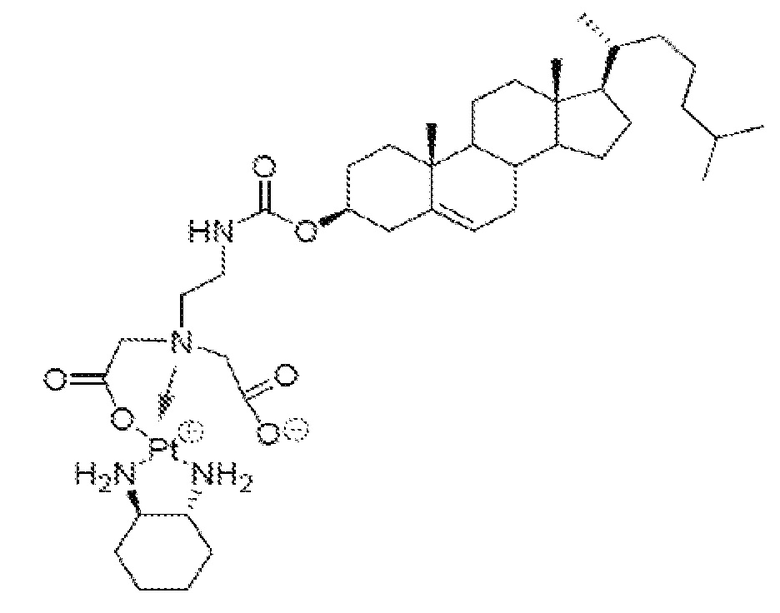
Соединение 26
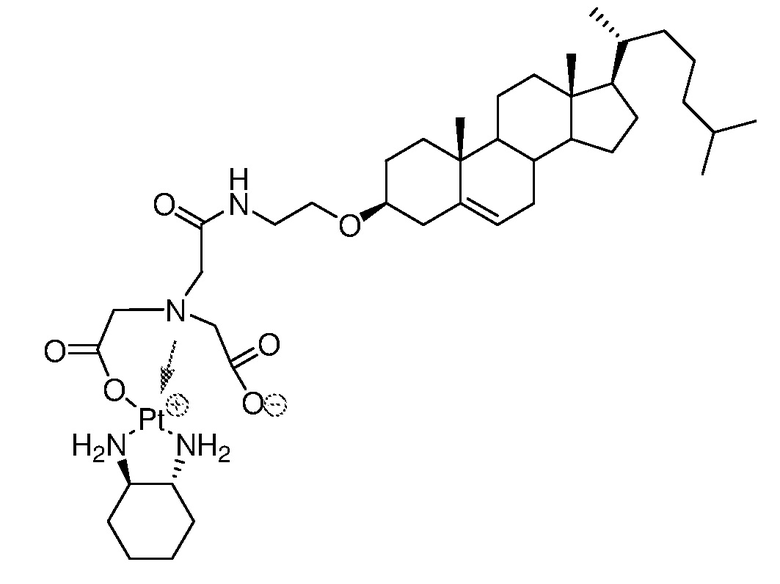
Соединение 27
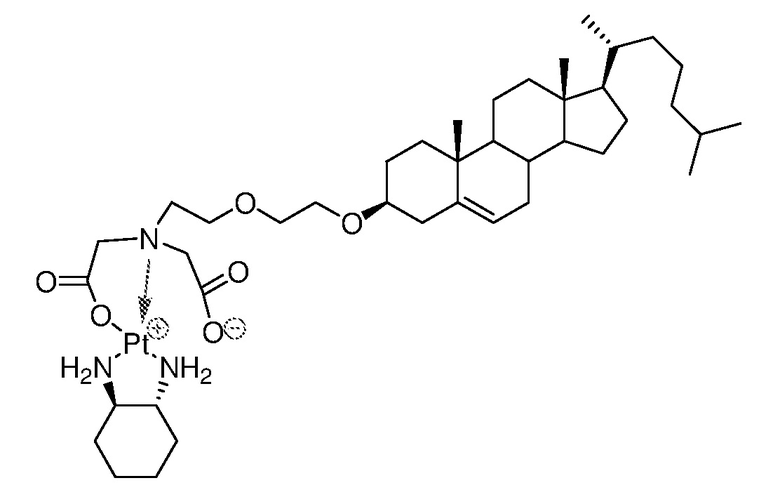
Соединение 28
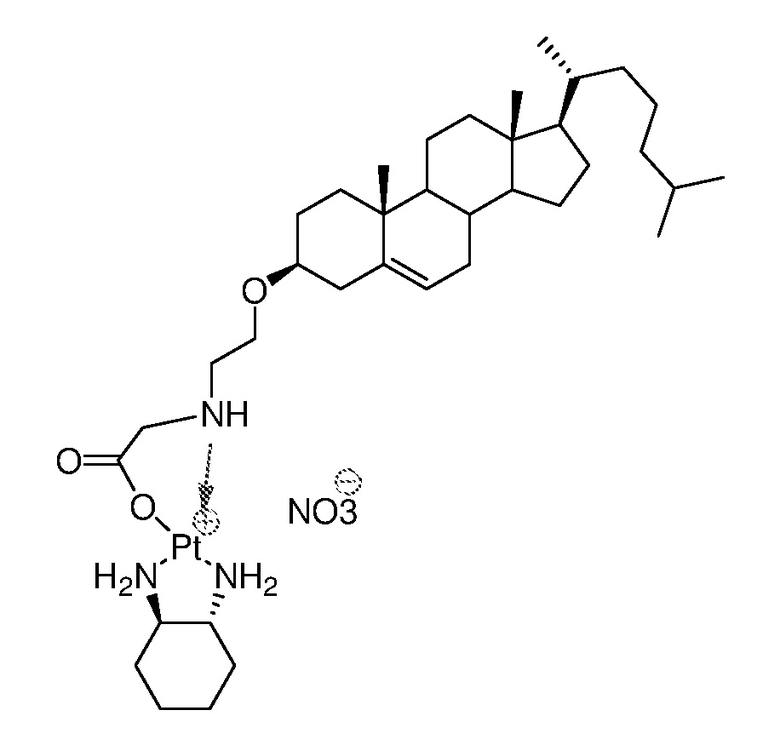
Соединение 29
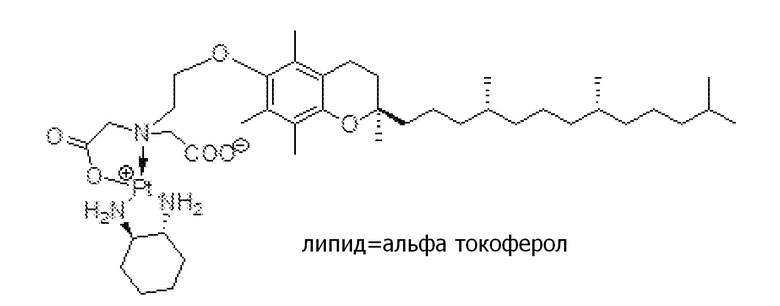
Соединение 38
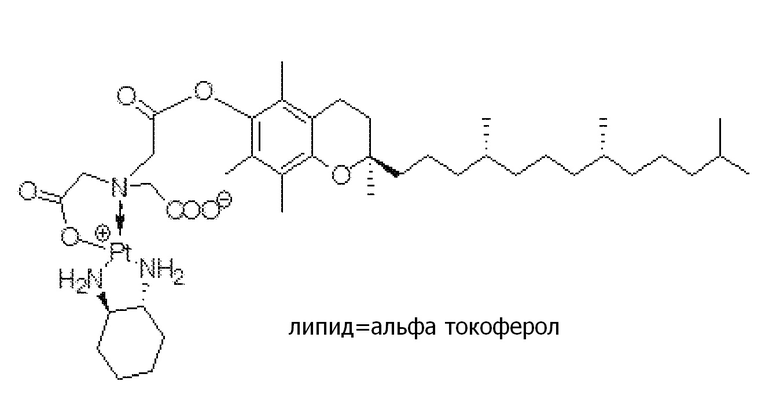
Соединение 39
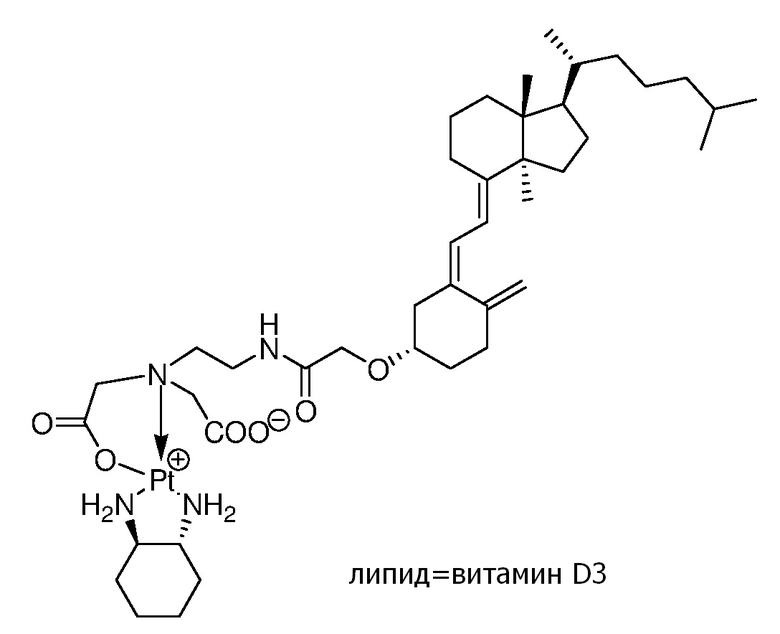
Соединение 40
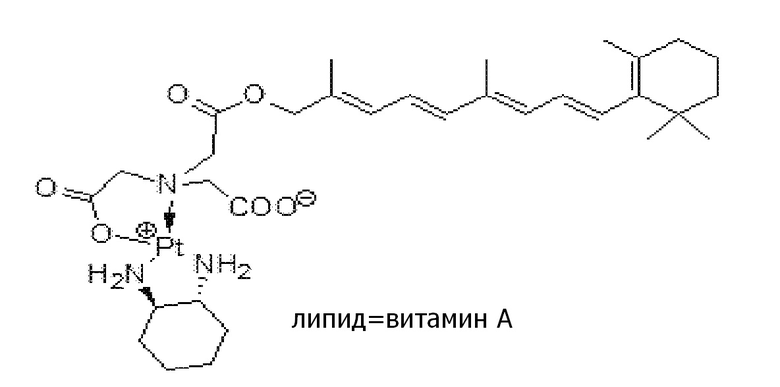
Соединение 41
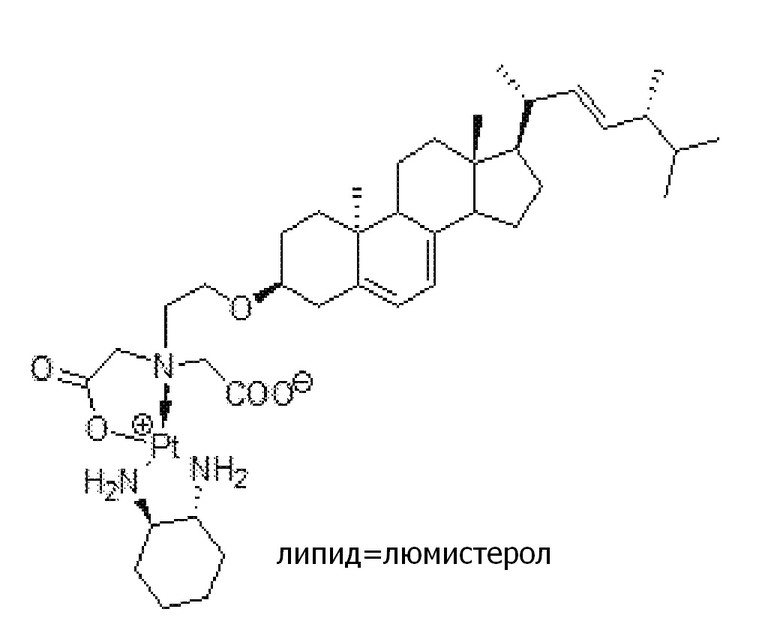
Соединение 42
[0080] Примеры соединений формулы (VIII) включают, но не ограничиваются, следующие соединения:
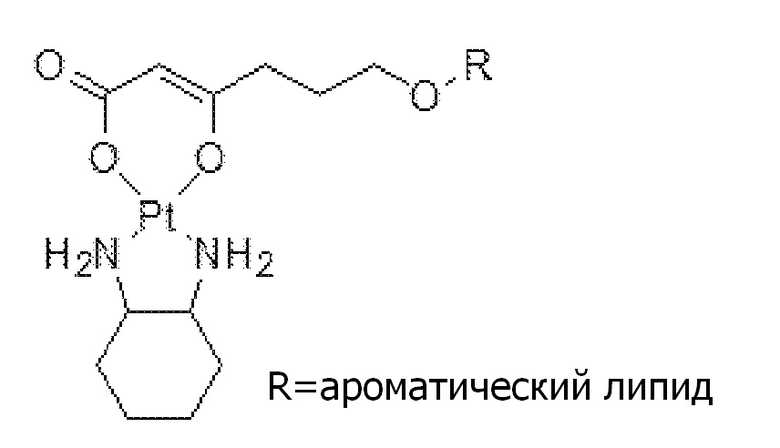
Соединение 66
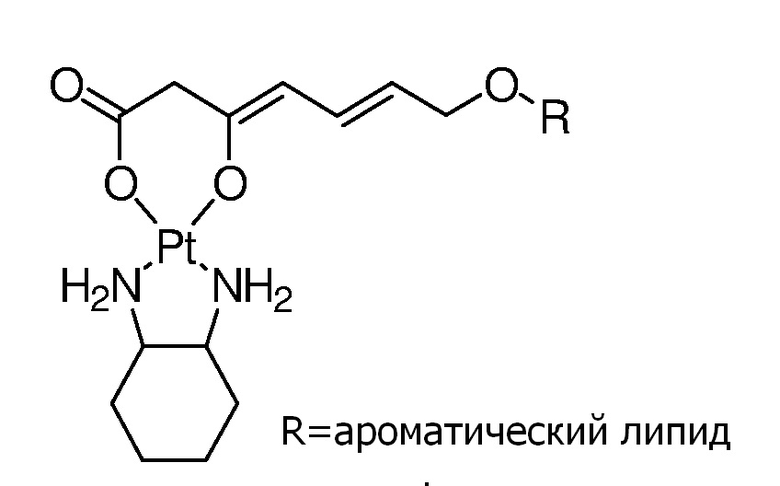
Соединение 67
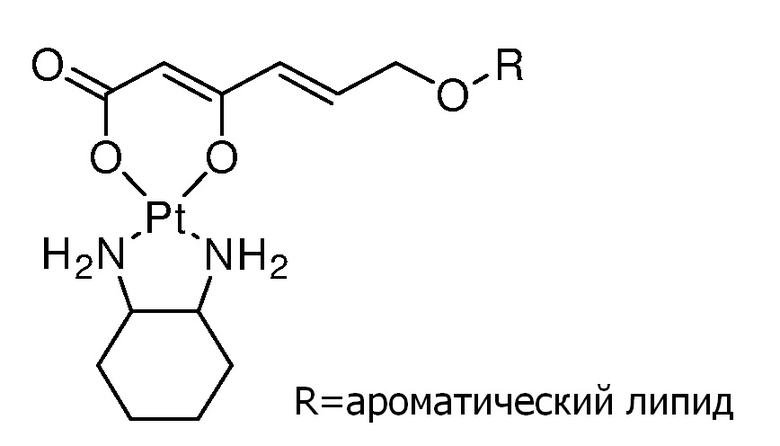
Соединение 68
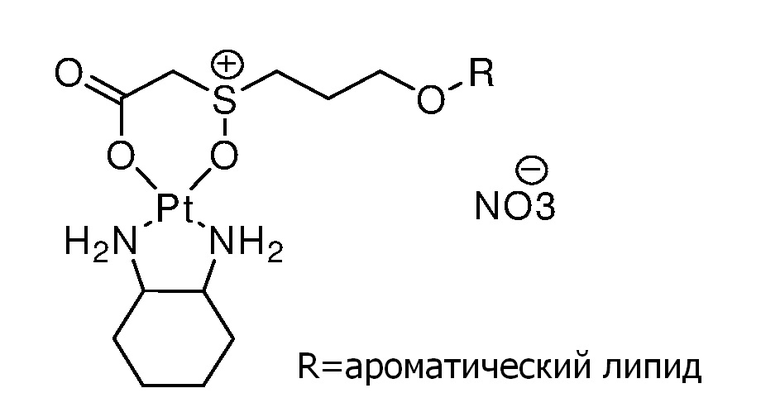
Соединение 69
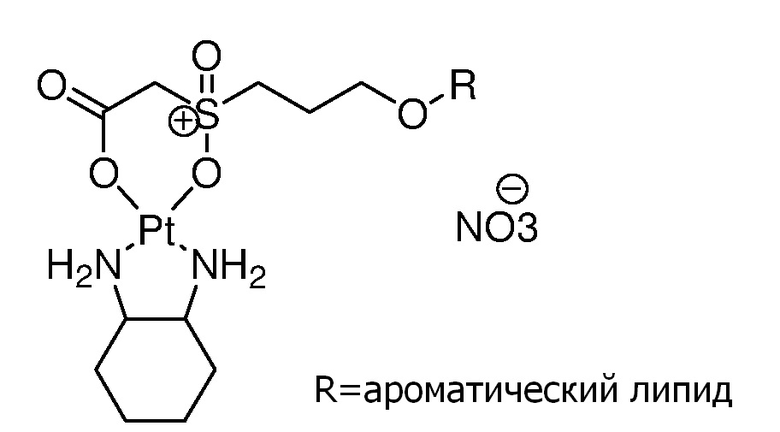
Соединение 70
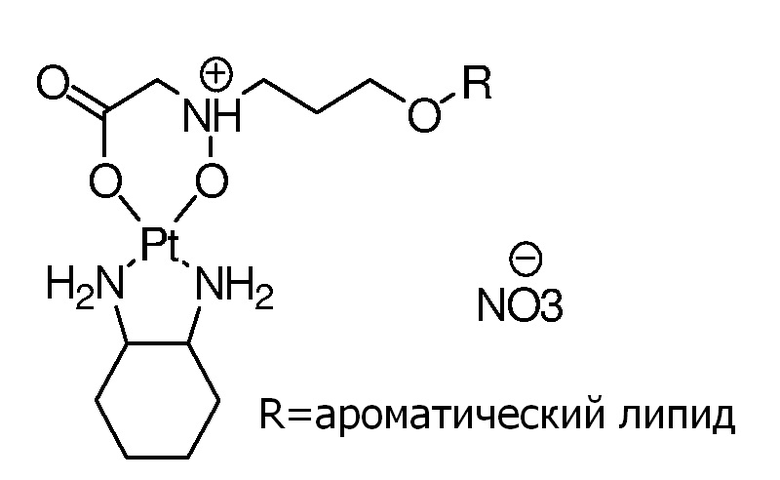
Соединение 72
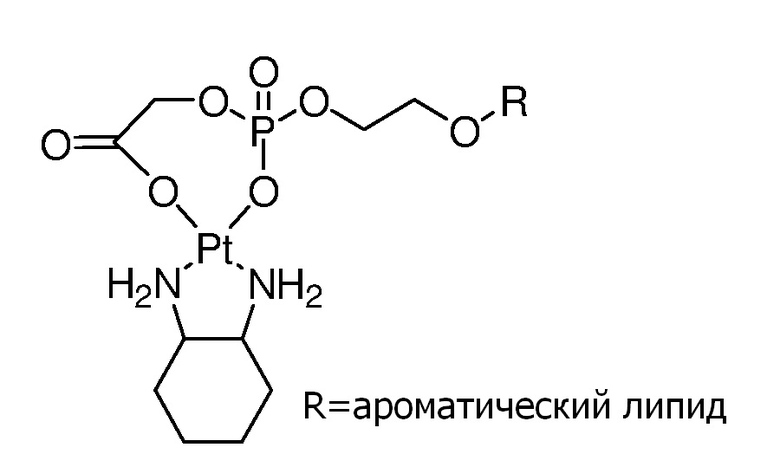
Соединение 71
[0081] Примеры соединений формулы (IX) включают, но не ограничиваются, следующие соединения:
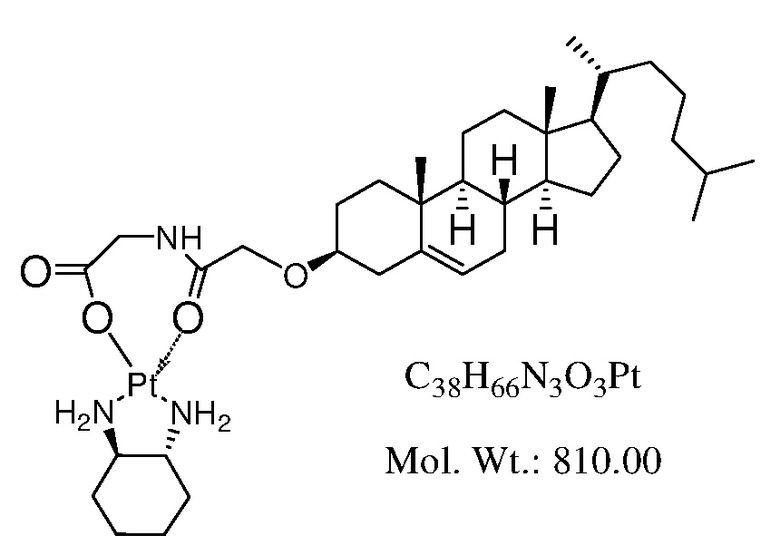
Соединение 22
[0082] Описание также относится к следующим соединениям:
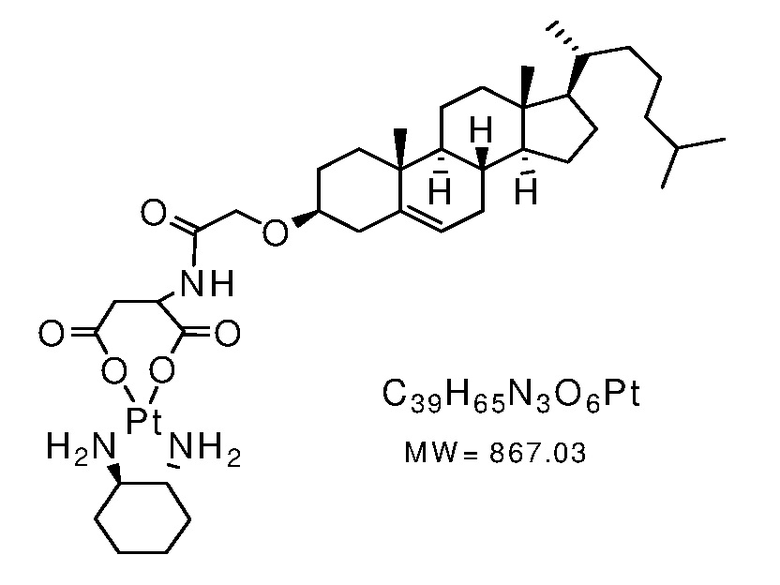
Соединение 23
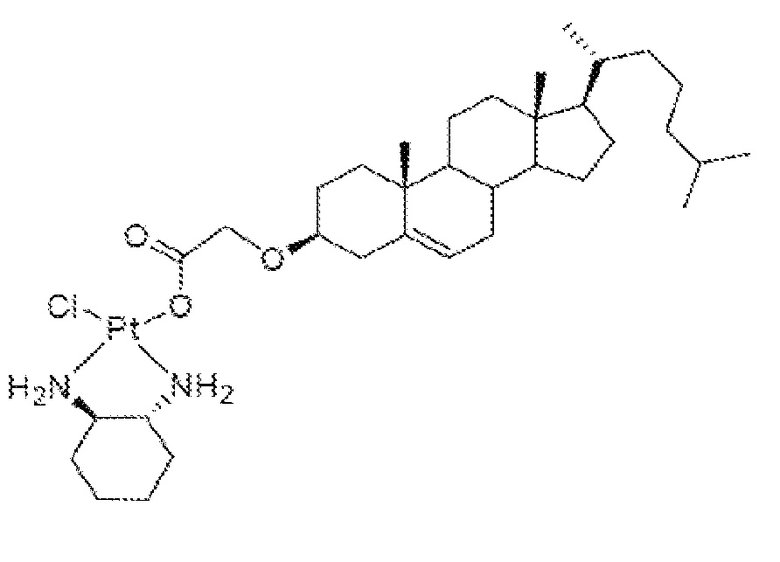
Соединение 30
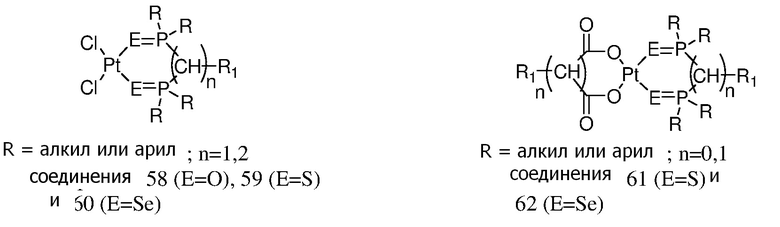
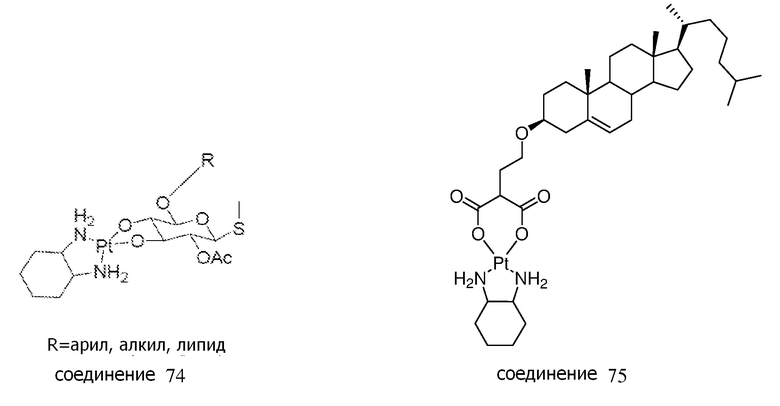
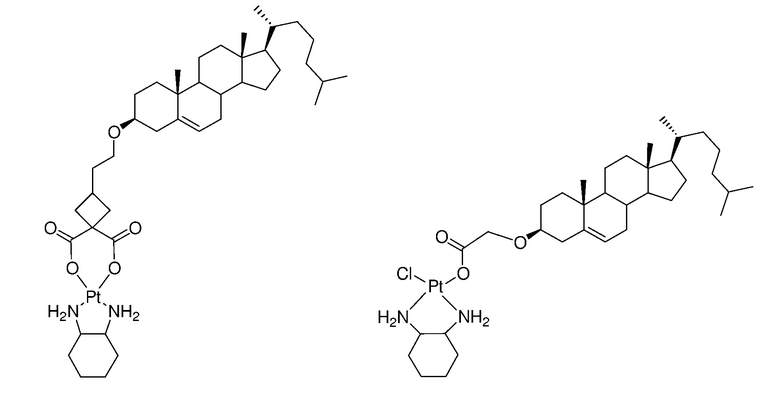
[0083] В некоторых вариантах осуществления различных аспектов, описанных в настоящем изобретении, платиновое соединение формулы (V) выбрано из группы, состоящей соединений 43-65 и 73-85 и соединения 95. В предпочтительном варианте осуществления, Pt соединение представляет собой DACH-Pt.
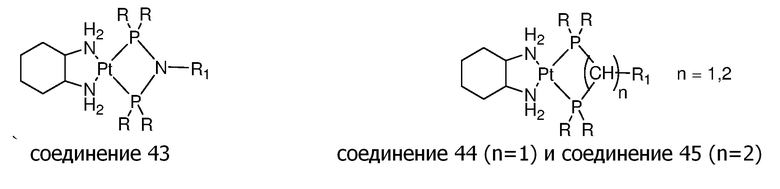
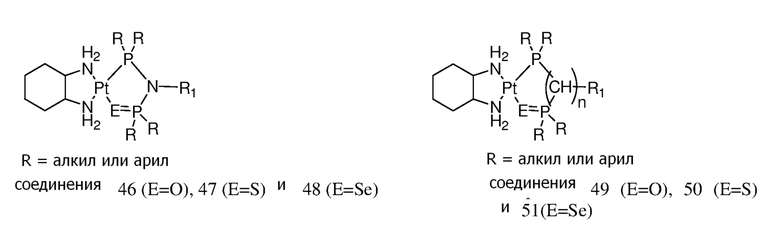
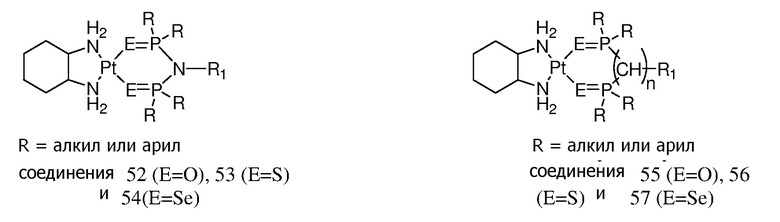

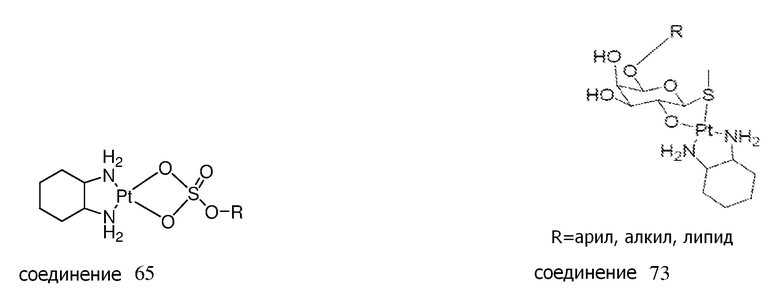
Соединение 76 Соединение 77
Соединение 79
[0084] В приведенных выше соединениях R1 представляет собой -линкер-липид, и n равен 1, если не определяют иначе.
[0085] Некоторые примерные варианты осуществления настоящего изобретения обеспечивают наночастицы, содержащие описанные конъюгированные с липидами платиновые соединения, и способы получения указанных наночастиц. Описанные способы эффективно обеспечивают высокую эффективность инкапсулирования, высокую степень загрузки лекарственного средства, равномерный размер и высокую стабильность. В определенных примерных вариантах осуществления описывают способы для получения стабильных лиофилизированных пегилированных амфифильных супрамолекулярных самосборок состава соединения 25 с высокой эффективностью загрузки лекарственного средства для применения в химиотерапии. Для прояснения характеристик настоящего изобретения, некоторые примеры его осуществления с различными мол.% активных и неактивных фармацевтических ингредиентов описаны ниже в примерах. Ясно, что хотя примеры описывают составы, содержащие соединение 25, любое конъюгированное с липидами платиновое соединение, описанное в настоящем изобретении, можно замещать, получая наночастицы настоящего изобретения.
[0086] В определенных примерных вариантах осуществления, описан способ получения наночастиц, где способ включает: смешение платинового соединения, содержащего платиновую часть, и липида, соединенного с указанной платиновой частью, с солипидом в присутствии растворителя, получая наночастицу. В определенных примерных вариантах осуществления, платиновое соединение получают согласно способам, описанным в настоящем изобретении. В определенных примерных вариантах осуществления, растворитель выбран из группы, включающей хлороформ, метанол, дихлорметан, этанол и любые их комбинации. В определенных примерных вариантах осуществления, солипид выбирают из группы, состоящей из соевого фосфатидилхолина (полностью гидрогенизированный), 1,2-дистеароил-sn-глицеро-3-Фосфоэтаноламин-N-[метокси(полиэтиленгликоля)-2000], диолеоилфосфатидилхолина (DOPC), DSPE-PEG-OMe, диолеоилфосфатидилэтаноламина (DOPE), дипальмиоилфосфатидилхолина (DPPC) и любой их комбинации. В определенных примерных вариантах осуществления, способ получения наночастицы дополнительно включает стадии сушки, выдерживания и необязательного добавления стабилизатора. В определенных примерных вариантах осуществления, стабилизатор выбирают из группы, состоящей из DSPE-PEG-OMe, DSPE-PEG-NH2, PEG, неорганической соли, углевода и любых их комбинаций. В определенных примерных вариантах осуществления, неорганическую соль выбирают из группы, состоящей из хлорида аммония, хлорида калия, хлорида натрия, гидрофосфата динатрия, дигидрофосфата натрия и любой их комбинации. В определенных примерных вариантах осуществления, углевод выбирают из группы, состоящей из глюкозы, декстрозы, сахарозы, трегалозы, маннитола, лактозы и любых их комбинаций. В определенных примерных вариантах осуществления, солипиды включают соевый фосфатидилхолин (гидрогенизированный) (HSPC) и 1,2-дистеароил-sn-глицеро-3-фосфоэтаноламин-N-[метокси(полиэтиленгликоль)-2000] (DSPE-PEG2000). В определенных примерных вариантах осуществления, мол.% соотношение платинового соединения (Pt) и солипидов (Pt:HSPC:DSPE-PEG2000) составляет приблизительно 30-32:55-60:4-5, или от приблизительно 30:55:4 до приблизительно 32:60:5. В определенных примерных вариантах осуществления, мол.% соотношение платинового соединения (Pt) и солипидов (Pt:HSPC:DSPE-PEG2000) составляет приблизительно 4-5:30-32:55-60, или от приблизительно 4:30:55 до приблизительно 5:32:60. В определенных примерных вариантах осуществления, солипиды включают соевый фосфатидилхолин (гидрогенизированный) (HSPC), холестерин (CHOL) и 1,2-дистеароил-sn-глицеро-3-фосфоэтаноламин-N-[метокси(полиэтиленгликоль)-2000] (DSPE-PEG2000). В определенных примерных вариантах осуществления, мол.% соотношение платинового соединения (Pt) и солипидов (Pt:HSPC:CHOL:DSPE-PEG2000) составляет приблизительно 20-35:60-70:3-15:1-5, или от приблизительно 20:60:3:1 до приблизительно 35:70:15:5. В определенных примерных вариантах осуществления, мол.% соотношение платинового соединения (Pt) и солипидов (Pt:HSPC:CHOL:DSPE-PEG2000) составляет приблизительно 1-5:20-35:60-70:3-15, или от приблизительно 1:20:60:3:1 до приблизительно 5:35:70:15. В некоторых вариантах осуществления, мол.% соотношение HSPC:CHOL:Pt:DSPE-PEG2000 составляет 55:3:38:4 мол.%.
[0087] В определенных примерных вариантах осуществления солипид представляет собой DOPE. Мол.% платинового соединения (Pt) и DOPE липида могут находиться в диапазоне 20-35:30-50. В определенных вариантах осуществления, мол. % платинового соединения (Pt) и DOPE липида могут находиться в диапазоне 22,5-27,5:35-50. В вариантах осуществления мол.% платинового соединения (Pt) и DOPE липида составляет приблизительно 40:25. В определенных примерных вариантах осуществления солипиды включают DOPE, соевый фосфатидилхолин (гидрогенизированный) (HSPC), холестерин (CHOL) и 1,2-дистеароил-sn-глицеро-3-фосфоэтаноламин-N-[метокси(полиэтиленгликоль)-2000] (DSPE-PEG2000). В некоторых вариантах осуществления солипиды представляют собой DOPE и HSPC, и мол.% соотношение DOPE и HSPC составляет приблизительно 30-50:25-35 или от приблизительно 30:25 до приблизительно 50:35. В некоторых вариантах осуществления, солипиды представляют собой DOPE и холестерин, и мол.% соотношение DOPE к холестерину составляет приблизительно 30-50:1-5 или от приблизительно 30:1 до приблизительно 50:5. В некоторых вариантах осуществления, солипиды представляют собой DOPE и DSPE-PEG2000, и мол.% соотношение DOPE к DSPE-PEG2000 составляет приблизительно 30-50:1-10, от приблизительно 30:1 до 50:4. В определенных примерных вариантах осуществления, мол.% соотношение платинового соединения (Pt) и солипидов (Pt:DOPE:HSPC:CHOL:DSPE-PEG2000) составляет приблизительно 20-40:30-50:25-35:3-15:1-5. В одном варианте осуществления, Pt:DOPE:HSPC:CHOL:DSPE-PEG2000 мол.% соотношение составляет приблизительно 25:40:28:3:4.
[0088] Определенные примерные варианты осуществления относятся к получению серии платиновых наночастиц, где диаминоциклогексил-Pt (DACH-Pt) содержит монокарбоксилированную ковалентную связь через карбоновую кислоту и координационную связь с амидным кислородом. Применяют дикарбонильные молекулы (дикарбоновые кислоты), такие как янтарная кислота, малоновая кислота и щавелевая кислота, которые в итоге образуют семи, шести и пяти членные кольца с платиной (II), соответственно. Линкер между платиновым кольцом и холестерином помогает образованию связей, выбранных из группы, включающий карбаматную связь (соединения 1, 2, 3), эфирную связь (соединения 6, 4, 5) или подобные или любые их комбинации. Следовательно, некоторые из вариантов осуществления настоящего изобретения относятся к соединениям, представленным общим остовом: липид-линкер-дикарбонил. Данные молекулы применяют для образования комплексов платиновых соединений, таких как DACH-Pt, оксалиплатина, цисплатина, карбены, содержащие платину, или других платинатов и платиновых соединений, через ковалентные и/или координационные связи.
[0089] В одном варианте осуществления настоящего изобретения также обеспечивают несколько вариантов платиновых соединений, такие как рацематы, диастереомеры и подобные (например, соединения 1-6).
[0090] В одном варианте осуществления настоящего изобретения можно применять любую молекулу, которая содержит две карбонильные группы. В одном варианте осуществления дикарбонильная молекула представляет собой дикарбоновую кислоту, такую как, например, янтарная кислота, малоновая кислота или щавелевая кислота.
[0091] Описание также относится к частицам, содержащим одно или более из платиновых соединений, описанных в настоящем изобретении. Обычно частица, описанная в настоящем изобретении, может быть любой формы, например, сферической, стержневой, эллиптической, цилиндрической, в виде капсулы или диска; и данные частицы могут образовывать часть сети или агрегата.
[0092] В некоторых вариантах осуществления, частица представляет собой микрочастицу или наночастицу. Как применяют в настоящем изобретении, термин ʺмикрочастица" относится к частице, имеющей размер частиц от приблизительно 1 мкм до приблизительно 1000 мкм. Как применяют в настоящем изобретении, термин ʺнаночастица" относится к частице, имеющей размер частиц от приблизительно 0,1 нм до приблизительно 1000 нм. Обычно, частицы имеют любой размер от нм до миллиметров. В некоторых вариантах осуществления частицы могут иметь средний диаметр в диапазоне от приблизительно 5 нм до приблизительно 5000 нм. В некоторых вариантах осуществления частицы имеют средний диаметр от приблизительно 50 нм до приблизительно 2500 нм, от приблизительно 100 нм до приблизительно 2000 нм, от приблизительно 150 нм до приблизительно 1700 нм, от приблизительно 200 нм до приблизительно 1500 нм, или приблизительно 260 нм. В некоторых вариантах осуществления, частицы имеют средний диаметр от приблизительно 30 нм до приблизительно 150 нм или от приблизительно 50 нм до приблизительно 250 нм. В некоторых вариантах осуществления частицы имеют средний диаметр от приблизительно 100 нм до приблизительно 1000 нм, от приблизительно 200 нм до приблизительно 800 нм, от приблизительно 200 нм до приблизительно 700 нм или от приблизительно 300 нм до приблизительно 700 нм.
[0093] В некоторых вариантах осуществления, частица имеет средний размер от приблизительно 50 до приблизительно 1000 нм. В следующем варианте осуществления, наночастицы настоящего изобретения находятся в диапазоне приблизительно 50 до приблизительно 500 нм. В другом варианте осуществления, наночастицы настоящего изобретения находятся в диапазоне приблизительно 50 до приблизительно 200 нм. В одном варианте осуществления, частица имеет размер приблизительно 50 до приблизительно 100 нм.
[0094] Специалисту в данной области техники ясно, что частицы обычно имеют распределение размеров частиц в районе указанного ʺразмераʺ. Если не указано иначе, термин ʺразмер частицʺ, как применяют в настоящем изобретении, относится к виду распределения частиц по размерам, т.е., величине, появляющейся наиболее часто в распределении частиц. Способы измерения размера частиц являются известными специалисту в данной области техники, например, динамическим рассеянием света (таким как корреляционная спектроскопия, лазерная дифракция, малоугловое лазерное светорассеяние (LALLS) и среднеугловое лазерное светорассеяние (MALLS)), методом затенения частиц (таким как способ анализа по Коултеру), или другими способами (такими как реология и световая или электронная микроскопия).
[0095] В некоторых вариантах осуществления, частицы могут быть по существу сферическими. Под ʺпо существу сферическиеʺ предполагается то, что отношение длин самой длинной к самой короткой перпендикулярных осей поперечного сечения частицы является меньшим, чем или равным приблизительно 1,5. По существу сферические не требует линии симметрии. Кроме того, частицы могут иметь текстурированную поверхность, такую как линии или углубления или выпуклости, которые имеют малый масштаб по сравнению с общим размером частицы и, тем не менее, быть по существу сферическими. В некоторых вариантах осуществления отношение длин самой длинной и самой короткой осей частицы является меньшим чем или равным приблизительно 1,5, является меньшим чем или равным приблизительно 1,45, является меньшим чем или равным приблизительно 1,4, является меньшим чем или равным приблизительно 1,35, является меньшим чем или равным приблизительно 1,30ё является меньшим чем или равным приблизительно 1,25ё является меньшим чем или равным приблизительно 1,20ё является меньшим чем или равным приблизительно 1,15 является меньшим чем или равным приблизительно 1,1. Не желая быть связанными теорией, поверхностный контакт поддерживают в частицах, которые являются по существу сферическими, что сводит к минимуму нежелательную агломерацию частиц при хранении. Многие кристаллы или пластинки имеют плоскую поверхность, которая может обеспечить большие площади поверхности контакта, когда агломерация может возникать за счет ионных или неионных взаимодействий. Сфера обеспечивает контакт на меньшей площади.
[0096] В некоторых вариантах осуществления частицы имеют по существу одинаковый размер частиц. Частицы, имеющие широкое распределение частиц, где присутствуют относительно большие и маленькие частицы, обеспечивают заполнение более мелких частиц в промежутках между большими частицами, посредством этого создавая новые поверхности контакта. Широкое распределение частиц может приводить в результате к большим сферам созданием многих возможностей контакта для связывания агломератов. Частицы, описанные в настоящем изобретении, находятся в пределах узкого распределения частиц, посредством этого сводя к минимуму возможность контактной агломерации. Под ʺузким распределением частицʺ предполагается, что распределение размеров частиц, которое имеет отношение объемного диаметра 90 процентов небольших сферических частиц к объемному диаметру 10 процентов, является меньшим чем или равным 5. В некоторых вариантах осуществления, объемный диаметр 90 процентов небольших сферических частиц к объемному диаметру 10 процентов является меньшим чем или равным 4,5, является меньшим чем или равным 4, является меньшим чем или равным 3,5, является меньшим чем или равным 3, является меньшим чем или равным 2,5, является меньшим чем или равным 2, является меньшим чем или равным 1,5, является меньшим чем или равным 1,45, является меньшим чем или равным 1,40, является меньшим чем или равным 1,35, является меньшим чем или равным 1,3, является меньшим чем или равным 1,25, является меньшим чем или равным 1,20, является меньшим чем или равным 1,15 или является меньшим чем или равным 1,1.
[0097] Геометрическое стандартное отклонение (GSD) можно также применять для указания узкого распределения частиц. Расчеты GSD включают определение эффективного предельного диаметра (ECD) при кумулятивных процентах, меньших чем 15,9% и 84,1%. GSD является равным квадратному корню отношения ECD, меньшему чем 84,17%, к ECD, меньшему чем 15,9%. GSD имеет узкое распределение размеров при GSD<2,5. В некоторых вариантах осуществления, GSD является меньшим чем 2, меньшим чем 1,75 или меньшим чем 1,5. В одном варианте осуществления, GSD является меньшим чем 1,8.
[0098] В добавление к платиновым соединениям, описанным в настоящем изобретении, частица может содержать солипиды и/стабилизаторы. Дополнительные липиды можно включать в частицы для ряда целей, таких как предотвращение окисления липидов, стабилизации бислоя, снижение агрегации в процессе образования или присоединение лигандов к поверхности частиц. Может присутствовать любое количество дополнительных липидов и/или других компонентов, включая амфипатические, нейтральные, катионные, анионные липиды, и липиды с программируемым слиянием. Данные липиды и/или компоненты можно применять отдельно или в комбинации. Один или более компонентов частицы могут содержать лиганд, например, адресно взаимодействующий лиганд.
[0099] В некоторых вариантах осуществления частица дополнительно содержит фосфолипид. Без ограничений, фосфолипиды могут быть природного происхождения, такие как яичный желток или фосфолипиды соевых бобов, или синтетического или полусинтетического происхождения. Фосфолипиды могут быть частично очищены или фракционированы так, чтобы содержать чистые фракции или смеси фосфатидилхолинов, фосфатидилхолинов с определенными ацильными группами, содержащими 6-22 атома углерода, фосфатидилэтаноламинов, фосфатидилинозитолов, фосфатидной кислоты, фосфатидилсеринов, сфингомиелина или фосфатидилглицеринов. Подходящие фосфолипиды включают, но не ограничиваются, фосфатидилхолин, фосфатидилглицерин, лецитин, β,γ-дипальмитоил-α-лецитин, сфингомиелин, фосфатидилсерин, фосфатидную кислоту, хлорид N-(2,3-ди(9-(Z)-октадеценилокси))-проп-1-ил-N,N,N-триметиламмония, фосфатидилэтаноламин, лизолецитин, лизофосфатидилэтаноламин, фосфатидилинозитол, цефалин, кардиолипин, цереброзиды, дицетилфосфат, диолеоилфосфатидилхолин, дипальмитоилфосфатидилхолин, дипальмитоилфосфатидилглицерин, диолеоилфосфатидилглицерин, пальмитоилолеоилфосфатидилхолин, дистеароилфосфатидилхолин, стеароилпальмитоилфосфатидилхолин, дипальмитоилфосфатидилэтаноламин, ди-стеароилфосфатидилэтаноламин, ди-миристлилфосфатидилсерин, ди-олеилфосфатидилхолин, димиристоилфосфатидилхолин (DMPC), диолеоилфосфатидилэтаноламин (DOPE), пальмитоилолеоилфосфатидилхолин (POPC), яичный фосфатидилхолин (EPC), дистеароилфосфатидилхолин (DSPC), диолеоилфосфатидилхолин (DOPC), дипальмитоилфосфатидилхолин (DPPC), диолеоилфосфатидилглицерин (DOPG), дипальмитоилфосфатидилглицерин (DPPG), фосфатидилэтаноламин (POPE), диолеоилфосфатидилэтаноламин 4-(N-малеимидометил)-циклогексан-1-карбоксилат (DOPE-mal), 1-стеароил-2-олеоилфосфатидилхолин (SOPC), 1,2-дистеароил-sn-глицил-3-фосфоэтаноламин (DSPE) и любые их комбинации. Можно также применять несодержащие фосфор липиды. Они включают, например, стеариламин, додециламин, ацетилпальмитат, амиды жирных кислот и подобные. Можно также применять другие несодержащие фосфор соединения, такие как сфинголипиды, семейство гликосфинголипидов, диацилглицерины и β-ацилоксикислоты.
[00100] В некоторых вариантах осуществления, фосфолипид в частице выбирают из группы, состоящей из 1,2-дидеканоил-sn-глицеро-3-фосфохолина; 1,2-диэрукоил-sn-глицеро-3-фосфата (натриевой соли); 1,2-диэрукоил-sn-глицеро-3-фосфохолина; 1,2-диэрукоил-sn-глицеро-3-фосфоэтаноламина; 1,2-диэрукоил-sn-глицеро-3[фосфо-rac-(1-глицерина) (натриевой соли); 1,2-дилинолеоил-sn-глицеро-3-фосфохолина; 1,2-дилауроил-sn-глицеро-3-фосфата (натриевой соли); 1,2-дилауроил-sn-глицеро-3-фосфохолина; 1,2-дилауроил-sn-глицеро-3-фосфоэтаноламина; 1,2-дилауроил-sn-глицеро-3[фосфо-rac-(1-глицерина) (натриевой соли); 1,2-дилауроил-sn-глицеро-3[фосфо-rac-(1-глицерина) (аммониевой соли); 1,2-дилауроил-sn-глицеро-3-фосфосерина (натриевой соли); 1,2-димиристоил-sn-глицеро-3-фосфата (натриевой соли); 1,2-димиристоил-sn-глицеро-3-фосфохолина; 1,2-димиристоил-sn-глицеро-3-фосфоэтаноламина; 1,2-димиристоил-sn-глицеро-3[фосфо-rac-(1-глицерина) (натриевой соли); 1,2-димиристоил-sn-глицеро-3[фосфо-rac-(1-глицерина) (аммониевой соли); 1,2-димиристоил-sn-глицеро-3[фосфо-rac-(1-глицерина) (натриевой/аммониевой соли); 1,2-димиристоил-sn-глицеро-3-фосфосерина (натриевой соли); 1,2-диолеоил-sn-глицеро-3-фосфата (натриевой соли); 1,2-диолеоил-sn-глицеро-3-фосфохолина; 1,2-диолеоил-sn-глицеро-3-фосфоэтаноламина; 1,2-диолеоил-sn-глицеро-3[фосфо-rac-(1-глицерина) (натриевой соли); 1,2-диолеоил-sn-глицеро-3-фосфосерина (натриевой соли); 1,2-дипальмитоил-sn-глицеро-3-фосфата (натриевой соли); 1,2-дипальмитоил-sn-глицеро-3-фосфохолина; 1,2-дипальмитоил-sn-глицеро-3-фосфоэтаноламина; 1,2-дипальмитоил-sn-глицеро-3[фосфо-rac-(1-глицерина) (натриевой соли); 1,2-дипальмитоил-sn-глицеро-3[фосфо-rac-(1-глицерина) (аммониевой соли); 1,2-дипальмитоил-sn-глицеро-3-фосфосерина (натриевой соли); 1,2-дистеароил-sn-глицеро-3-фосфата (натриевой соли); 1,2-дистеароил-sn-глицеро-3-фосфохолина; 1,2-дистеароил-sn-глицеро-3-фосфоэтаноламина; 1,2-дистеароил-sn-глицеро-3[фосфо-rac-(1-глицерина) (натриевой соли); 1,2-дистеароил-sn-глицеро-3[фосфо-rac-(1-глицерина) (аммониевой соли); 1,2-дистеароил-sn-глицеро-3-фосфосерина (натриевой соли); яичного PC; гидрогенизированного яичного PC; гидрогенизированного соевого PC; 1-миристоил-sn-глицеро-3-фосфохолина; 1-пальмитоил-sn-глицеро-3-фосфохолина; 1-стеароил-sn-глицеро-3-фосфохолина; 1-миристоил-2-пальмитоил-sn-глицеро-3-фосфохолина; 1-миристоил-2-стеароил-sn-глицеро-3-фосфохолина; 1-пальмитоил-2-миристоил-sn-глицеро-3-фосфохолина; 1-пальмитоил-2-олеоил-sn-глицеро-3-фосфохолина; 1-пальмитоил-2-олеоил-sn-глицеро-3-фосфоэтаноламина; 1-пальмитоил-2-олеоил-sn-глицеро-3[фосфо-rac-(1-глицерина)] (натриевой соли); 1-пальмитоил-2-стеароил-sn-глицеро-3-фосфохолина; 1-стеароил-2-миристоил-sn-глицеро-3-фосфохолина; 1-стеароил-2-олеоил-sn-глицеро-3-фосфохолина; и 1-стеароил-2-пальмитоил-sn-глицеро-3-фосфохолина. В некоторых вариантах осуществления фосфолипид представляет собой SPOC, яичный PC или гидрогенизированный соевый PC (HSPC). В одном варианте осуществления фосфолипид в композиции представляет собой HSPC. В некоторых вариантах осуществления липид представляет собой DOPE.
[00101] В некоторых вариантах осуществления частица дополнительно содержит полиэтиленгликоль (PEG). PEG можно включать в частицу как есть или конъюгированным с компонентом, присутствующим в частице. Например, PEG можно конъюгировать с платиновым соединением или компонентом солипид/стабилизатор частицы. В некоторых вариантах осуществления, PEG конъюгируют с солипидным компонентом частицы. Без ограничений, PEG можно конъюгировать с любым солипидом. Например, конъюгируемый с PEG солипид можно выбрать из группы, состоящей из конъюгируемых с PEG диацилглицеринов и диалкилглицеринов, конъюгируемого с PEG фосфатидилэтаноламина, конъюгируемой с PEG фосфатидной кислоты, конъюгируемых с PEG церамидов (смотри патент США No. 5885613), конъюгируемых с PEG диалкиламинов, конъюгируемых с PEG 1,2-диацилоксипропан-3-аминов и конъюгируемого с PEG 1,2-дистеароил-sn-глицил-3-фосфоэтаноламина (DSPE), и любых их комбинаций. В некоторых вариантах осуществления конъюгируемый с PEG липид представляет собой 1,2-дистеароил-sn-глицил-3-фосфоэтаноламин-N-[амино(полиэтиленгликоль)-2000] (DSPE-PEG2000).
[00102] В некоторых вариантах осуществления частица дополнительно содержит поверхностно-активное вещество. Поверхностно-активные вещества находят широкое применение в составах, таких как эмульсии (включая микроэмульсии) и липосомы. Самый распространенный способ классификации и ранжирования свойств многих различных типов поверхностно-активных веществ, и природных и синентических, основан на применении гидролипидного баланса (HLB). Свойства гидрофильных групп (также известных как ʺголовкаʺ) относится к самому приемлемому средству категоризации различных поверхностно-активных веществ, применяемых в составах (Rieger, in Pharmaceutical Dosage Forms, Marcel Dekker, Inc., New York, N.Y., 1988, p. 285).
[00103] Если молекула поверхностно-активного вещества не является ионизированной, его классифицируют как неионное поверхностно-активное вещество. Неионные поверхностно-активные вещества находят широкое применение в фармацевтических и косметических продуктах и являются пригодными в широком диапазоне величин pH. В общем, их величины HLB находятся в диапазоне от 2 до приблизительно 18, в зависимости от их структуры. Неионные поверхностно-активные вещества включают неионные эфиры, такие как эфиры этиленгликоля, эфиры пропиленгликоля, эфиры глицерина, эфиры полиглицерина, эфиры сорбитана, эфиры сахарозы и этоксилированные эфиры. Неионные алканоламины и эфиры, такие как этоксилаты жирных спиртов, пропоксилированные спирты и этоксилированные/пропоксилированные блочные полимеры также включены в данный класс. Полиоксиэтиленовые поверхностно-активные вещества являются самыми популярными членами класса неионных поверхностно-активных веществ.
[00104] Если молекула поверхностно-активного вещества несет отрицательный заряд при растворении или диспергировании в воде, поверхностно-активное вещество классифицируют как анионное. Анионные поверхностно-активные вещества включают карбоксилаты, такие как мыла, ациллактилаты, ациламиды аминокислот, эфиры серной кислоты, такие как алкилсульфаты и этоксилированные алкилсульфаты, сульфонаты, такие как алкилбензолсульфонаты, ацилизетионаты, ацилтаураты и сульфосукцинаты, и фосфаты. Самые важные члены класса анионных поверхностно-активных веществ представляют собой алкилсульфаты и мыла.
[00105] Если молекула поверхностно-активного вещества несет положительный заряд при растворении или диспергировании в воде, поверхностно-активное вещество классифицируют как катионное. Катионные поверхностно-активные вещества включают четвертичные аммониевые соли и этоксилированные амины. Четвертичные аммониевой соли представляют собой самые применяемые члены данного класса.
[00106] Если молекула поверхностно-активного вещества обладает способностью нести или положительный или отрицательный заряд, поверхностно-активное вещество классифицируют как амфотерное. Амфотерные поверхностно-активные вещества включают производные акриловой кислоты, замещенные алкиламиды, N-алкилбетаины и фосфатиды.
[00107] Применение поверхностно-активных веществ в лекарственных продуктах, составах и в эмульсиях является освященным (Rieger, в Pharmaceutical Dosage Forms, Marcel Dekker, Inc., New York, N.Y., 1988, p. 285).
[00108] В некоторых вариантах осуществления, частица может дополнительно содержать катионный липид. Примеры катионных липидов включают, но не ограничиваются, хлорид N,N-диолеил-N,N-диметиламмония (DODAC), бромид N,N-дистеарил-N,N-диметиламмония (DDAB), хлорид N-(1-(2,3-диолеоилокси)пропил)-N,N,N-триметиламмония (DOTAP), хлорид N-(1-(2,3-диолеилокси)пропил)-N,N,N-триметиламмония (DOTMA), N,N-диметил-2,3-диолеилокси)пропиламин (DODMA), 1,2-дилинолеилокси-N,N-диметиламинопропан (DLinDMA), 1,2-дилиноленилокси-N,N-диметиламинопропан (DLenDMA), 1,2-дилинолеилкарбамоилокси-3-диметиламинопропан (DLin-C-DAP), 1,2-дилинолеилокси-3-(диметиламино)ацетоксипропан (DLin-DAC), 1,2-дилинолеилокси-3-морфолинопропан (DLin-MA), 1,2-дилинолеоил-3-диметиламинопропан (DLinDAP), 1,2-дилинолеилтио-3-диметиламинопропан (DLin-S-DMA), 1-линолеоил-2-линолеилокси-3-диметиламинопропан (DLin-2-DMAP), хлоридную соль 1,2-дилинолеилокси-3-триметиламинопропана (DLin-TMA.C1), хлоридную соль 1,2-дилинолеоил-3-триметиламинопропана (DLin-TAP.C1), 1,2-дилинолеилокси-3-(N-метилпиперазино)пропан (DLin-MPZ) или 3-(N,N-дилинолеиламино)-1,2-пропандиол (DLinAP), 3-(N,N-диолеиламино)-1,2-пропандиол (DOAP), 1,2-дилинолеилоксо-3-(2-N,N-диметиламино)этоксипропан (DLin-EG-DMA), 1,2-дилиноленилокси-N,N-диметиламинопропан (DLinDMA), 2,2-дилинолеил-4-диметиламинометил-[1,3]-диоксолан (DLin-K-DMA) или его аналоги, (3aR,5s,6aS)-N,N-диметил-2,2-ди((9Z,12Z)-октадека-9,12-диенил)тетрагидро-3aH-циклопента[d][1,3]диоксол-5-амин (ALN100), (6Z,9Z,28Z,31Z)-гептатриаконта-6,9,28,31-тетраен-19-ил 4-(диметиламино)бутаноат (MC3), 1,1′-(2-(4-(2-((2-(бис(2-гидроксидодецил)амино)этил)(2-гидроксидодецил)амино)этил)пиперазин-1-ил)этилазанедиил)дидодекан-2-ол (Tech Gi) или их смесь.
[00109] В некоторых вариантах осуществления частица дополнительно содержит некатионный липид. Некатионный липид может представлять собой анионный липид или нейтральный липид, включая, но не ограничиваясь, дистеароилфосфатидилхолин (DSPC), диолеоилфосфатидилхолин (DOPC), дипальмитоилфосфатидилхолин (DPPC), диолеоилфосфатидилглицерин (DOPG), дипальмитоилфосфатидилглицерин (DPPG), диолеоилфосфатидилэтаноламин (DOPE), пальмитоилолеоилфосфатидилхолин (POPC), пальмитоилолеоилфосфатидилэтаноламин (POPE), диолеоилфосфатидилэтаноламин 4-(N-малеимидометил)циклогексан-1-карбоксилат (DOPE-mal), дипальмитоилфосфатидилэтаноламин (DPPE), димиристоилфосфоэтаноламин (DMPE), дистеароилфосфатидилэтаноламин (DSPE), 16-O-монометил PE, 16-O-диметил PE, 18-1-транс PE, 1-стеароил-2-олеоил-фосфатидилэтаноламин (SOPE), холестерин или их смесь.
[00110] Конъюгированные липиды, которые ингибируют агрегацию частиц, можно также включать в частицы, описанные в настоящем изобретении. Данные липиды включают, но не ограничиваются, полиэтиленгликоль (PEG)-липид, включая, без ограничения, PEG-диацилглицерин (DAG), PEG-диалкилоксипропил (DAA), PEG-фосфолипид, PEG-церамид (Cer) или их смесь. PEG-DAA конъюгат может представлять собой, например, PEG-дилаурилоксипропил (C12), PEG-димиристилоксипропил (C14), PEG-дипальмитилоксипропил (C16) или PEG-дистеарилоксипропил (C18). Конъюгированный липид, который препятствует агрегации частиц, может составлять от 0,01 мол. % до приблизительно 20 мол. % или приблизительно 2 мол. % всех липидов, присутствующих в частице.
[00111] В некоторых вариантах осуществления частица имеет форму липосомы, везикулы или эмульсии. Как применяют в настоящем изобретении, термин ʺлипосомаʺ включает любое пространство, окруженное липидным слоем. Липосомы могут иметь одну или более липидных мембран. Липосомы можно характеризовать типом мембраны и размером. Небольшие моноламеллярные везикулы (SUV) имеют одну мембрану и обычно имеют диаметр в диапазоне от 0,02 до 0,05 мкм; большие моноламеллярные везикулы (LUVS) является обычно большими чем 0,05 мкм. Олиголамеллярные большие везикулы и многослойные везикулы имеют множество обычно концентрических мембранных слоев и обычно являются большими чем 0,1 мкм. Липосомы с несколькими неконцентрическими мембранами, т.е., несколько небольших везикул содержится в большой везикуле, называют мультивезикулярными везикулами.
[00112] Для того чтобы образовать липосому, молекулы липидов содержат удлиненные неполярные (гидрофобные) части и полярные (гидрофильные) части. Гидрофобные и гидрофильные части молекулы предпочтительно располагаются на двух концах удлиненной молекулярной структуры. Когда данные липиды диспергируют в воде, они самопроизвольно образуют бислойные мембраны, называемые ламеллами. Ламеллы состоят из двух монослойных листов липидных молекул, причем их неполярные (гидрофобные) поверхности смотрят друг на друга, и их полярные (гидрофильные) поверхности повернуты в водную среду. Мембраны, образованные липидами, включают часть водной фазы способом, аналогичным способу, которым клеточная мембрана окружает содержимое клетки. Таким образом, бислой липосомы сходен с клеточной мембраной без белковых компонентов, присутствующих в клеточной мембране.
[00113] Липосомную композицию можно получить рядом способов, которые являются известными в данной области техники. Смотри, например, патент США No. 4235871, No. 4897355 и No. 5171678; опубликованные PCT заявки WO 96/14057 и WO 96/37194; Felgner, P. L. et al., Proc. Natl. Acad. Sci., USA (1987) 8:7413-7417, Bangham, et al. M. Mol. Biol. (1965) 23:238, Olson, et al. Biochim. Biophys. Acta (1979) 557:9, Szoka, et al. Proc. Natl. Acad. Sci. (1978) 75: 4194, Mayhew, et al. Biochim. Biophys. Acta (1984) 775:169, Kim, et al. Biochim. Biophys. Acta (1983) 728:339 и Fukunaga, et al. Endocrinol. (1984) 115:757, содержание всех из которых включено в настоящее изобретение с помощью ссылки во всей своей полноте.
[00114] Липосомы можно получить так, чтобы они имели по существу гомогенные размеры в выбранном диапазоне размеров. Один эффективный способ установления размеров включает продавливание водной суспензии липосом через серию поликарбонатных мембран, имеющих выбранный равномерный размер пор; размер пор мембраны будет приблизительно соответствовать наибольшему размеру липосом, полученных продавливанием через данную мембрану. Смотри, например, патент США No. 4737323, содержание которого включено в настоящее изобретение с помощью ссылки во всей своей полноте.
[00115] Не желая быть связанными теорией, наночастицы, описанные в настоящем изобретении, обладают большим поглощением платины раковыми клетками относительно цисплатины и оксалиплатины. В некоторых вариантах осуществления, наночастицы, описанные в настоящем изобретении, обладают приблизительно 25%, приблизительно 50%, приблизительно 75%, приблизительно 1-кратным, приблизительно 5-кратным, приблизительно 10-кратным, приблизительно 15-кратным, приблизительно 20-кратным, приблизительно 25-кратным или более поглощением платины раковыми клетками относительно цисплатины или оксалиплатины при эквивалентной дозе.
[00116] Кроме того, наночастицы, описанные в настоящем изобретении, также обеспечивают высокое накопление платины в ткани, такой как, но не ограничиваясь, опухоли, относительно цисплатины и оксалиплатины при дозировании одинаковых количеств. Например, наночастицы, описанные в настоящем изобретении, обеспечивают приблизительно 25%, приблизительно 50%, приблизительно 75%, приблизительно 1-кратное, приблизительно 5-кратное, приблизительно 10-кратное, приблизительно 15-кратное, приблизительно 20-кратное, приблизительно 25-кратное или более накопление в ткани платины относительно цисплатины или оксалиплатины при дозировании одинаковых количеств.
Определения
[00117] Для удобства, определенные термины, применяемые в настоящем изобретении, в описании, примерах и формуле изобретения, собраны далее. Если не указано иначе или подразумевается по контексту, следующие термины и фразы включают значения, приведенные ниже. Если в явной форме не указано иначе или очевидно из контекста, термины и фразы ниже не исключают значение, которое термин или фраза приобрела на предшествующем уровне техники, к которому она относится. Определения обеспечивают для того, чтобы способствовать описанию конкретных вариантов осуществления, и не предполагаются ограничивающими заявленное настоящее изобретение, поскольку объем настоящего изобретения ограничен только формулой изобретения. Кроме того, если иначе не требуется по контексту, единичные формы должны включать множественные формы, и множественные термины должны включать единичные.
[00118] Если не определяют иначе, все технические и научные термины, применяемые в настоящем изобретении, имеют те же значения, как термины, обычно известные специалисту в данной области техники, к которой относится настоящее изобретение. Хотя любые известные способы, устройства и материалы можно применять при осуществлении на практике или тестировании настоящего изобретения, способы, устройства и материалы, в этой связи, описаны в настоящем изобретении.
[00119] Как применяют в настоящем изобретении термин ʺвключаяʺ или ʺвключаетʺ применяют со ссылкой на композиции, способы и их соответствующий компонент (компоненты), которые являются существенными для настоящего изобретения, в то же время открытые для включения неуказанных элементов, важны они или нет.
[00120] Как применяют в настоящем изобретении термин "состоящий по существу из" относится к элементам, требуемым для указанного варианта осуществления. Термин обеспечивает наличие элементов, которые материально не влияют на основу и новизну или функциональную характеристику (характеристики) данного варианта осуществления настоящего изобретения.
[00121] Единичные формы ʺa,ʺ ʺan,ʺ и ʺtheʺ включают множественные референты, если контекст явно не указывает иначе. Аналогично, слово ʺилиʺ предполагается включающим ʺиʺ, если контекст явно не указывает иначе.
[00122] Исключая текущие примеры или когда указано иначе, все числа, выражающие количества ингредиентов или условия реакций, применяемые в настоящем изобретении, следует понимать как модифицированные во всех случаях термином ʺприблизительно.ʺ Термин ʺприблизительноʺ при применении в сочетании с процентами может обозначать±1% величины, на которую ссылаются. Например, приблизительно 100 обозначает от 99 до 101.
[00123] Хотя способы и материалы, аналогичные или эквивалентные способам и материалам, описанным в настоящем изобретении, можно применять при осуществлении на практике или тестировании настоящего описания, подходящие способы и материалы описаны ниже. Термин ʺвключаетʺ обозначает ʺвключаетʺ. Сокращение, ʺe.g.ʺ получено от латинского exempli gratia, и его применяют в настоящем изобретении для обозначения неограничивающего примера. Таким образом, сокращение ʺнапримерʺ является синонимом термина ʺнапримерʺ.
[00124] Термин ʺзамещенныйʺ, предшествует ли ему термин ʺнеобязательноʺ или нет, относится к замещению водородного радикала в указанной структуре радикалом указанного заместителя. Когда более одной позиции в любой указанной структуре можно замещать более чем одним заместителем, выбранным из указанной группы, заместитель может быть одинаковым или отличным в различных положениях. Как применяют в настоящем изобретении, термин ʺзамещенныйʺ предполагается включающим все допустимые заместители органических соединений. В широком аспекте, допустимые заместители включают ациклические и циклические, разветвленные и неразветвленные, карбоциклические и гетероциклические, ароматические и неароматические заместители органических соединений. Гетероатомы, такие как азот, могут содержать заместители водорода и/или любые допустимые заместители органических соединений, описанных в настоящем изобретении, которые удовлетворяют валентности гетероатомов.
[00125] Описание вариантов осуществления настоящего описания не предполагается исчерпывающим или ограничивающим настоящее изобретение точной описанной формой. Тогда как конкретные варианты осуществления и примеры настоящего изобретения описаны в настоящем изобретении с целью иллюстрации, различные эквивалентные модификации являются возможными в пределах объема настоящего изобретения, как ясно специалисту в данной области техники. Например, когда стадии способа или функции присутствуют в указанном порядке, альтернативные варианты осуществления могут осуществлять функции в отличном порядке, или функции можно осуществлять по существу одновременно. Идеи настоящего изобретения, относящиеся к настоящему изобретению, можно применять для других процедур или способов, при необходимости. Различные варианты осуществления, описанные в настоящем изобретении, можно комбинировать для обеспечения дополнительных вариантов осуществления. Аспекты описания можно изменять, при необходимости, применяя композиции, функции и концепции ссылок выше и заявку, обеспечивая еще дополнительные варианты осуществления настоящего изобретения. Данные и другие изменения можно вносить в настоящее изобретение в свете подробного описания. Все данные модификации предполагаются включенными в объем прилагаемой формулы изобретения.
[00126] Конкретные элементы любого из описанных вариантов осуществления можно комбинировать или заменять элементами из других вариантов осуществления. Более того, тогда как преимущества, связанные с определенными вариантами осуществления настоящего изобретения, описаны в контексте данных вариантов осуществления, другие варианты осуществления могут также обладать данными преимуществами, и не все варианты осуществления обязательно проявляют данные преимущества, попадая в пределы объема настоящего изобретения.
ПРИМЕРЫ
[00127] Следующие примеры иллюстрируют некоторые варианты осуществления и аспекты настоящего изобретения. Специалисту в данной области техники ясно, что различные модификации, дополнения, замены и подобные, можно осуществлять, не изменяя сущность или объем настоящего изобретения, и данные модификации и варианты включены в пределы объема настоящего изобретения, как определено в формуле изобретения, которая следует ниже. Следующие примеры не ограничивают настоящее изобретение любым способом.
Пример 1: схематическое изображение примерного способа получения
Схема 1
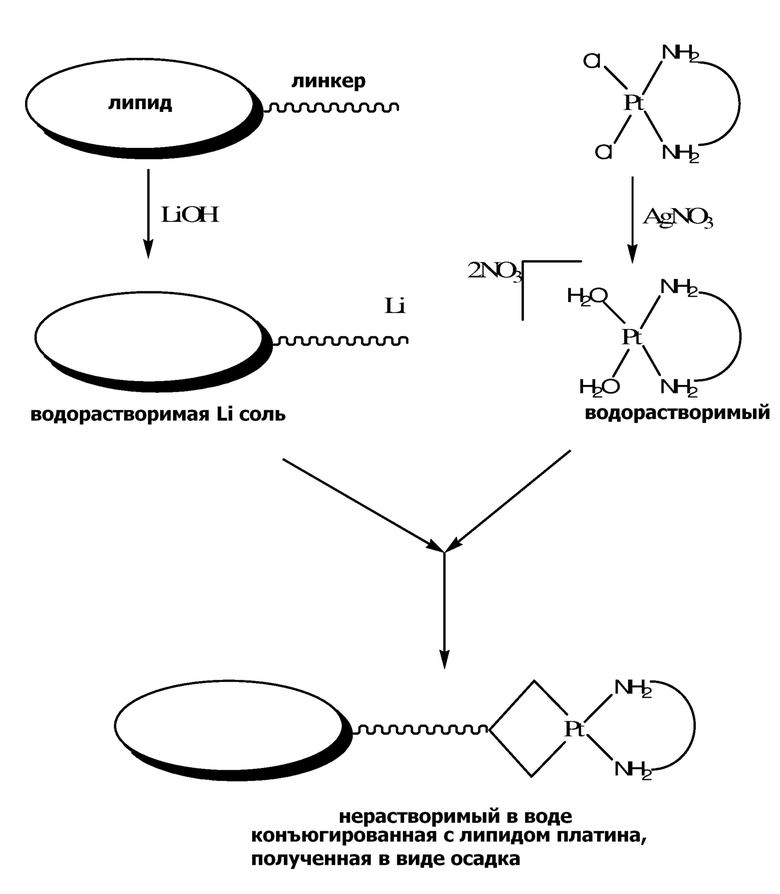
[00128] Аналогичные способы применяли для получения соединений 25-28 и других конъюгированных с липидами платиновых соединений. Данные примерные способы хорошо работали для всех соединений. Включение дополнительных стадий промывки способствовало увеличению чистоты соединения 26 вплоть до 93% (таблица 2).
Таблица 2: выходы и чистота соединений, полученных, применяя варианты осуществления настоящего изобретения
[00129] Фигура 1 показывает ВЭЖХ профиль соединения 26 перед промывкой водой и ацетоном, и фигура 2 показывает ВЭЖХ профиль соединения 26 после промывки водой и ацетоном. Она представляет собой максимальную чистоту, достигаемую промывкой.
[00130] Подробные способы для получения примеров соединений выше описаны в международной патентной заявке PCT/US2014/042339, опубликованной как WO/2014/201376, которая включена в настоящее изобретение с помощью ссылки.
Пример 2: улучшенные способы получения промежуточного соединения 6 соединения 25
[00131] Многостадийный синтез соединения 25 можно найти в WO/2014/201376. Снижение количества стадий получения лиганда могло бы способствовать увеличению выхода соединения 25 (API). Способ ссылки включает шесть стадий для получения промежуточного соединения 6, тогда как способы, описанные в настоящем изобретении, будут требовать две стадии для получения данного промежуточного соединения. Суммарный выход промежуточного соединения 6 составляет 13% в способе ссылки (схема 1). Значительное увеличение выхода промежуточного соединения 6 наблюдали (50%) в новом способе (схема 5).
Схема 2: предшествующие стадии получения соединения 25
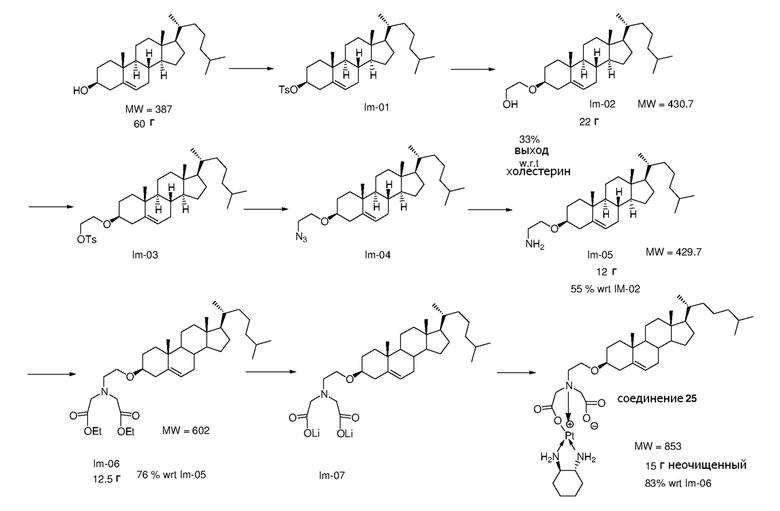
Схема 3A. способ 1 для получения промежуточного соединения 6 с меньшим количеством стадий
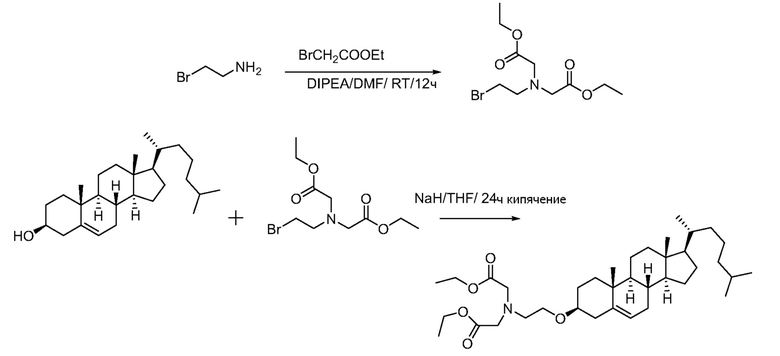
Схема 3B. способ 1B для получения промежуточного соединения 6
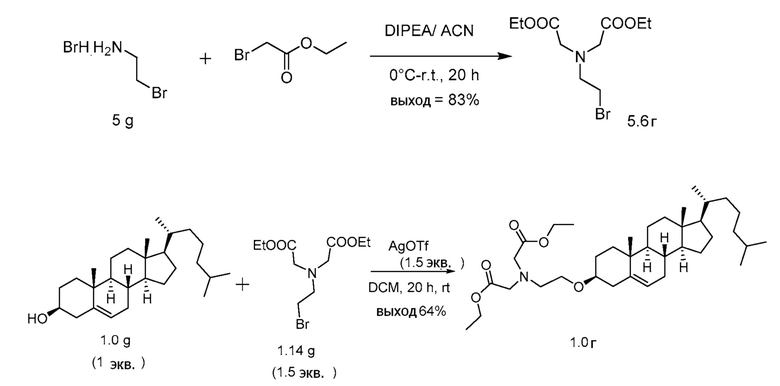
[00132] Экспериментальные подробности для способа 1B (схема 3B): гидробромидную соль 2-бромэтиламина (5,0 г, 25 ммоль) добавляли порциями к смеси бромэтилацетата (8,6 мл, 75 ммоль), DIPEA (17,5 мл, 100 ммоль) и 30 мл сухого ацетонитрила при 0°C. Смесь перемешивали при комнатной температуре в течение 20 часов, и затем фильтровали и концентрировали на роторном испарителе. Колоночную хроматографию проводили (элюируя этилацетатом:гексаном=1:3), получая 5,6 г (77%) третичного бромдиэфирамина.
[00133] К раствору холестерина (1,0 г, 2,59 ммоль) в безводном CH2Cl2 (свежеперегнанный) (15 мл) при 25 °C перемешивали при комнатной температуре в атмосфере N2 в течение 10 минут. Затем, добавляли AgOTf (1,0 г, 3,88 ммоль), и перемешивание продолжали в течение 10 минут. Затем, раствор третичного бромдиэфирамина (1,14 г, 3,88 ммоль) в 5 мл DCM прикапывали к реакционной смеси по каплям. После перемешивания в течение 20 часов при комнатной температуре, смесь нейтрализовали Et3N и разбавляли хлороформом и фильтровали. Его концентрировали и очищали колоночной хроматографией (этилацетат/гексан). выход=1,0 г (64%).
Схема 4. альтернативный способ 2 для получения промежуточного соединения 6
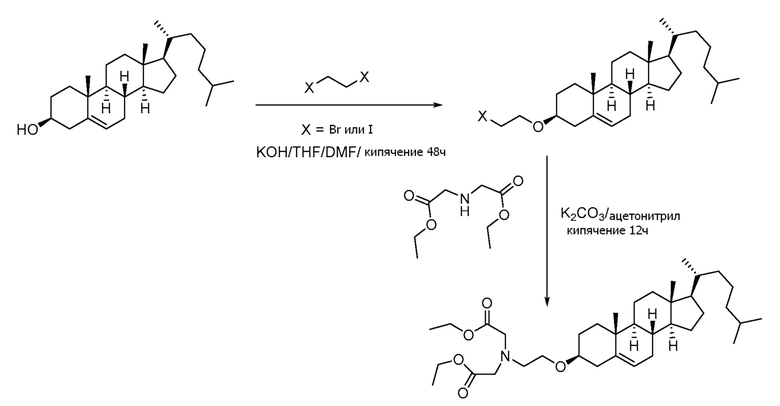
Схема 5. Альтернативный способ 3 для получения промежуточного соединения 6
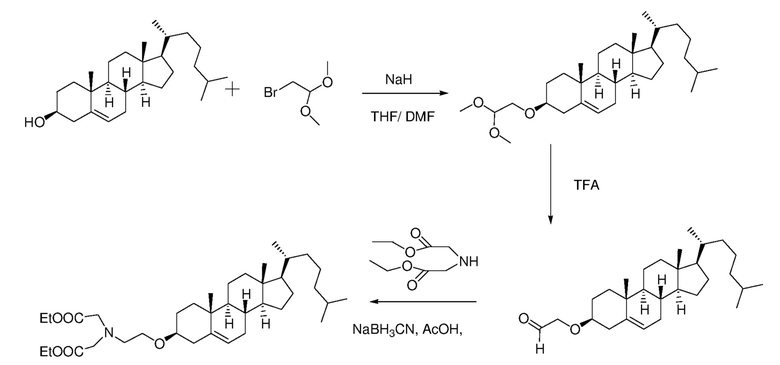
Экспериментальные подробности для способа 3 (схема 5):
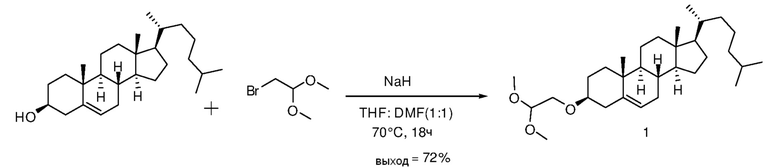
[00134] Экспериментальный способ: холестерин (10 г, 25,86 ммоль) растворяли в 100 мл сухого DMF/ THF(1:1) и добавляли 60% гидрид натрия (вес/вес) в минеральном масле (6,2 г, 155,17 ммоль), с последующим перемешиванием в течение 10 мин. 2-Бром-1,1-диметоксиэтан (9,2 мл, 78 ммоль) добавляли по каплям, и реакционную смесь перемешивали при 70˚C при кипячении с обратным холодильником в течение 18 часов. Реакционную смесь охлаждали и гасили добавлением воды. Органический слой экстрагировали этилацетатом, промывали несколько раз водой, сушили над Na2SO4, фильтровали и концентрировали, и продукт реакции очищали флэш-хроматографией на силикагеле в 3% EtOAc/гексан. выход=8,8 г (72%).
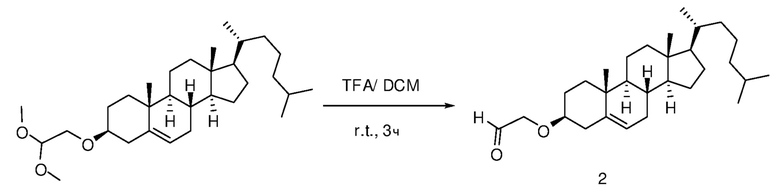
[00135] Экспериментальный способ: TFA (2 мл) добавляли к раствору соединения 1 (0,350 г, 0,737 ммоль) в 2 мл DCM, и смесь перемешивали при комнатной температуре в течение 3 часов. Смесь нейтрализовали 1 N NaOH, экстрагировали дважды DCM и сушили над сульфатом натрия, фильтровали и концентрировали, затем применяли непосредственно в следующей стадии.
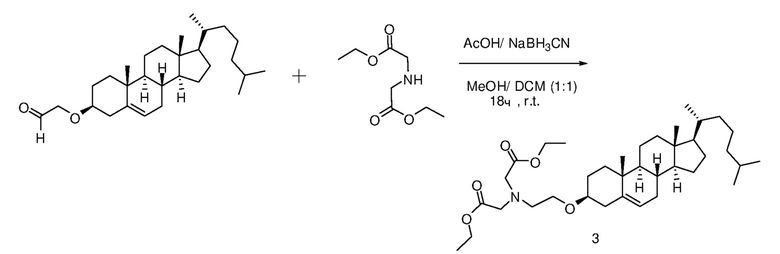
[00136] Экспериментальный способ: соединение 2 растворяли в 3,2 мл смеси MeOH:DCM (1:1), содержащей диэтилиминодиацетат (0,161 мл, 0,9 ммоль), последовательно добавляли AcOH (0,214 мл, 3,74 ммоль) и NaBH3CN (0,093 г, 1,48 ммоль). Смесь перемешивали в течение 18 часов при комнатной температуре, разбавляли EtOAc, промывали дважды NaHCO3 и водой, сушили над Na2SO4, фильтровали и концентрировали. Неочищенный продукт очищали колоночной флэш-хроматографией на силикагеле, применяя систему EtOAc/гексан. выход=72%.
Схема 6. альтернативный способ 4 для получения промежуточного соединения 6
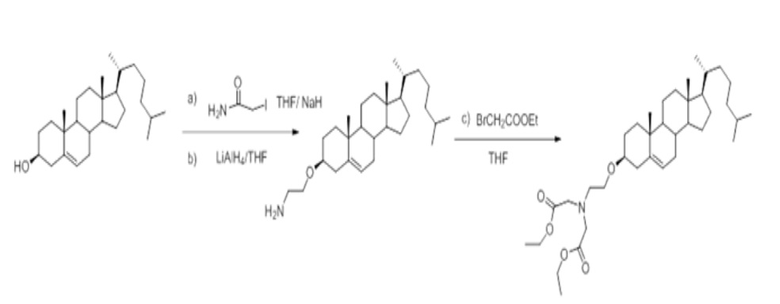
Схема 7. Альтернативный способ 5 для получения промежуточного соединения 6
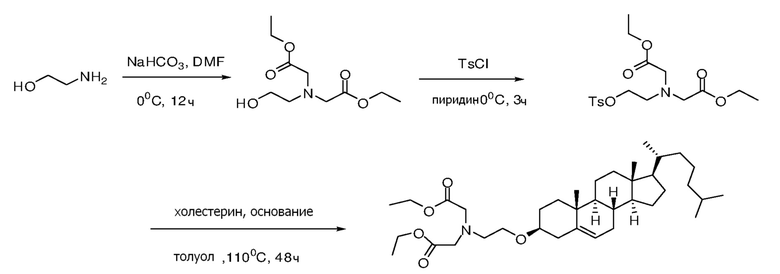
Пример 3: ВЭЖХ очистка и анализ
[00137] Затем, конъюгированные с липидами платиновые соединения настоящего изобретения можно очищать препаративной обращено-фазовой ВЭЖХ. Соединения можно очищать на колонке, содержащей C18 стационарную фазу, NH2 стационарную фазу или Phenyl стационарную фазу. Обнаружено, что некоторые соединения являются нестабильными на C18, C8, циано и PFP стационарных фазах, приводя в результате к неправильной оценке чистоты. Следовательно, оценку чистоты осуществляют или на NH2 колонке или Phenyl колонке, на которых соединение, как было установлено, являлось стабильным.
[00138] Очистка на C18 колонке включает изократический способ с подвижной фазой, содержащей 98% метанола и 2% воды. Контролировали УФ поглощение при 210 нм. Пик соединения собирали, объединяли, и растворитель удаляли упариванием и лиофилизацией, получая соединение с чистотой >99,5% в виде порошка.
[00139] Очистка на NH2 или Phenyl колонке включает градиентный способ, начинающийся с большего процента воды, линейно изменяясь с течением времени до большего процента метанола. Контролировали УФ поглощение при 210 нм. Пик соединения собирали, объединяли, и растворитель удаляли упариванием и лиофилизацией, получая соединение с чистотой >99,5% в виде порошка.
[00140] Аналитический способ для оценки чистоты осуществляют, применяя NH2 или Phenyl стационарную фазу. Соединение растворяют в метаноле (>1 мг/мл). Анализ осуществляют с градиентом вода/метанол и УФ/PDA детектором при 210 нм. Чистоту измеряют расчетом процента площади пика соединения относительно суммарной площади пиков. Для учета ложных пиков, анализ осуществляют после наложения хроматограммы введения чистого метанола.
[00141] Фигура 3 показывает аналитический профиль соединения 25 после ВЭЖХ очистки. Фигуры 6A и 6B показывают сравнение ВЭЖХ профилей соединения 25 на C18 и NH2 колонках. Фигура 4 показывает аналитический профиль соединения 27 после ВЭЖХ очистки. Фигуры 7A и 7B показывают сравнение ВЭЖХ профилей соединения 27 на C18 и NH2 колонках. Фигура 5 показывает аналитический профиль соединения 28 после ВЭЖХ очистки.
Пример 4: способ получения наночастиц, содержащих соединение 25
[00142] Соевый фосфатидилхолин (полностью гидрогенизированный, HSPC), холестерин (CHOL), соединение 25 и 1,2-дистеароил-sn-глицеро-3-фосфоэтаноламин-N-[амино(полиэтиленгликоль)-2000] (DSPE-PEG2000), взятые при 55:3:38:4 мол.% соотношениях, растворяли в смеси DCM/MeOH (1:1, об/об). Все липидные растворы гомогенно смешивали в круглодонной колбе, органический растворитель упаривали на роторном испарителе, и липидную пленку выдерживали при высоком вакууме в течение 4-5 часов. Затем, тонкую пленку гидратировали добавлением к ней 40 мл 5% раствора лактозы, и вращали в роторной водяной бане в течение 1,0 часа при 65°C. Затем, гидратированные супрамолекулы последовательно экструдировали через мембраны с 400 нм, 200 нм и 100 нм размером пор (Whatman® фильтры), поддерживаемые держателем для фильтров, 10 раз, применяя LIPEXTM экструдер (100 мл), соединенный с циркулирующей водяной баней при 65°C. Измерение с помощью атомно-абсорбционного спектрометра (AAS) Pt показало, что конечный Pt-эквивалент данного состава составляет 2,33 мг/мл, и эффективность инкапсулирования в % составляет 32,7 мол. % соединения 25.
[00143] Приведенный выше супрамолекулярный состав лиофилизировали (5% раствор лактозы применяли в качестве криопротектора) в течение 16-20 часов. Образовавшийся затем белый порошок перерастворяли добавлением требуемого количества стерильной воды для инъекции. ДРС исследование данного растворенного супрамолекулярного состава показало размер, PDI, поверхностный потенциал супрамолекул, аналогичные тем, которые были до лиофилизации.
Пример 5: способ получения флуоресцентных наночастиц, содержащих соединение 25
[00144] HSPC, CHOL, соединение 25, DSPE-PEG2000 и Liss Rhod PE (флуоресцентный краситель), взятые в мол.% соотношениях 61,02:3,55:31,32:3,55:0,56, растворяли в смеси DCM/MeOH (1:1, об/об). Все растворы липидов смешивали гомогенно в круглодонной колбе (обернутой алюминиевой фольгой), и органический растворитель упаривали на роторном испарителе. Затем, тонкую пленку гидратировали добавлением к ней 2,5 мл 5% раствора лактозы и вращали в водяной роторной бане в течение 1,0 часа при 65°C. Затем, гидратированные супрамолекулы последовательно экструдировали через мембраны с 400 нм, 200 нм и 100 нм размером пор (Whatman® фильтры), поддерживаемые держателем для фильтров, 10 раз, применяя LIPEXTM экструдер (10 мл), соединенный с баней с циркулирующей водой при 65°C. Измерение атомно-абсорбционным спектрометром (AAS) Pt показало, что конечный Pt-эквивалент данного состава составляет 1,2 мг/мл, и % эффективность инкапсулирования составляет 25 мол.% соединения 25.
[00145] Приведенный выше супрамолекулярный состав лиофилизировали (5% раствора лактозы применяли в качестве криопротектора) в течение 16-20 часов. Образовавший после этого белый порошок перерастворяли добавлением требуемого объема стерильной воды для инъекции. ДРС исследование данного перерастворенного супрамолеклярного состава показало размер, PDI, поверхностный потенциал супрамолекул, аналогичные тем, что были до лиофилизации.
Пример 6: способ получения наночастиц, содержащих соединение 25
[00146] HSPC, CHOL, соединение 25 и DSPE-PEG2000, взятые в мол.% соотношениях 65,57:10,93:21,86:1,64 растворяли в смеси DCM/MeOH (1:1, об/об). Все растворы липидов смешивали гомогенно в круглодонной колбе, и органический растворитель упаривали на роторном испарителе. Затем, тонкую пленку гидратировали добавлением к ней 4 мл 5% раствора лактозы, и вращали в водяной роторной бане в течение 1,0 часа при 65°C. Затем, гидратированные супрамолекулы последовательно экструдировали через мембраны с 400 нм, 200 нм и 100 нм размером пор (Whatman® фильтры) при 65°C, поддерживаемые держателем для фильтров, 11 раз, применяя Avanti экструдер (1 мл), помещенный над горячей плиткой. Супрамолекулярный состав, полученный экструдированием, пропускали через Sephadex G-25 (PD-10) колонку для обессоливания, уравновешанную 5% раствором сахарозы, и собирали различные фракции. Фракции, содержащие супрамолекулы, объединяли и концентрировали до конечного объема 3 мл, применяя фильтровальную центрифугу (Amicon Ultra, 30 кДа) при 3000 g в течение 15 мин. Измерение атомно-абсорбционным спектрометром (AAS) Pt показало, что конечный Pt-эквивалент данного состава составляет 0,43 мг/мл, и % эффективность инкапсулирования составляет 12,8 мол.% соединения 25.
[00147] Приведенный выше супрамолекулярный состав лиофилизировали (5% раствор сахарозы применяли в качестве криопротектора) в течение 16-20 часов. Образовавший после этого белый порошок перерастворяли добавлением требуемого объема стерильной воды для инъекции. ДРС исследование данного перерастворенного супрамолеклярного состава показало размер, PDI, поверхностный потенциал супрамолекул, аналогичные тем, что были до лиофилизации.
Пример 7: способ получения наночастиц, содержащих соединение 25
[00148] HSPC, CHOL, соединение 25, DSPE-PEG2000, взятые в мол.% соотношении 62,54:3,24:32,45:1,77 в стеклянной пробирке, растворяли в смеси DCM/MeOH (1:1, об/об). 4 мл 5% раствора лактозы помещали в грушевидную колбу, и медленно добавляли в нее органическую фазу. Смесь аккуратно встряхивали в течение 1 минуты. Органический растворитель удаляли продувкой N2 через роторный испаритель при 65°C в течение 1 часа, получая в результате вязкую суспензию. Ее обрабатывали ультразвуком 5 циклов, применяя ультразвуковой диспергатор для проб. Затем, гидратированные супрамолекулы последовательно экструдировали через мембраны с размером пор 400 нм, 200 нм и 80 нм (Whatman® фильтры) при 65°C, поддерживаемые держателем для фильтров, 9 раз, применяя Avanti экструдер (1 мл), помещенный над горячей плиткой. Измерение с помощью атомно-абсорбционного спектрометра (AAS) Pt показало, что конечный Pt-эквивалент данного состава составляет 1,56 мг/мл, и % эффективность инкапсулирования составляет 19 мол.% соединения 25.
[00149] Приведенный выше супрамолекулярный состав лиофилизировали (5% раствора лактозы применяли в качестве криопротектора) в течение 16-20 часов. Образовавший после этого белый порошок перерастворяли добавлением требуемого объема стерильной воды для инъекции. ДРС исследование данного перерастворенного супрамолеклярного состава показало размер, PDI, поверхностный потенциал супрамолекул, аналогичные тем, что были до лиофилизации.
Пример 8: получение характеристик супрамолекулярного состава соединения 25
[00150] Получение характеристик супрамолекулярного состава динамическим рассеянием света ДРС (ДРС): кумулятивный размер частиц состава, полученного в примере 7, измеряли способом динамического рассеяния света, применяя Zetasizer Nano ZS90 (Malvern, UK). 50 мкл состав разбавляли до 1 мл, применяя DI воду, и измерение проводили при угле рассеяния 90 градусов при 25°C, получая распределение среднего размера частиц. ДРС гистограмма примерного состава показана на фигуре 8. Как видно из фигуры 8, средний размер частиц находится в диапазоне от приблизительно 40 нм до приблизительно 300 нм. Изображения, полученные трансмиссионным электронным микроскопом (TEM), наночастиц, содержащих конъюгированные с липидами платиновые соединения, согласно одному варианту осуществления настоящего изобретения показаны на фигуре 9. Наночастицы показаны при различном увеличении, как можно видеть из шкалы масштаба на каждом изображении. Зета-потенциал также измеряли, применяя тот же прибор, Zetasizer ZS90. Результаты измерений зета-потенциала приведены в таблице 3.
Таблица 3: ДРС данные (из примеров 29-37)
[00151] Атомно-абсорбционная спектроскопия (AAS): Pt-эквивалент в составе определяли количественно, применяя измерение с помощью атомно-абсорбционного спектрометра (AAS). Результаты AAS приведены в таблице 4.
Таблица 4: AAS данные (из примеров 29-37)
[00152] Стабильность примерного супрамолекулярного состава определяли и приводили в таблице 5.
[00153] Анализ на стабильность соединения 25 (IO-125, пример 47):
Условия исследования на стабильность: ICH Q1 A (R2) испытание на стабильность новых лекарственных веществ и продуктов
Ускоренное исследование: (6 месяцев)
Таблица 5: данные по стабильности соединения 25 (IO-125, пример 47)
Пример 9: Способ получения чувствительных к pH наночастиц, содержащих соединение 25 и DOPE в качестве липидного компонента
[00154] Известно, что DOPE образует чувствительный к pH супрамолекулярный состав (Pharmacy и Pharmacology 2007, 59, 469). Не желая быть связанными теорией, следующие факторы являются ответственными за чувствительность к pH DOPE: 1) протонируемая кислотная группа; 2) низкая температура перехода; и 3) присутствие двойной связи в алкильных цепях.
[00155] Способ: 1,2-диолеоил-sn-глицеро-3-фосфоэтаноламин (DOPE), гидрогенизированный соевый PC (HSPC), холестерин, соединение 25 и 1,2-дистеароил-sn-глицеро-3-фосфоэтаноламин-N-[амино(полиэтиленгликоль)-2000] (DSPE-PEG2000), взятые в мол.% соотношениях 40:28:3:25:4 (суммарная концентрация фосфолипидов была равна 19,7 мМ), растворяли в смеси CHCl3/MeOH (1:1, об/об). В таблице приведены липидные композиции различных составов, полученных в данном примере.
Таблица 6: различие в липидной композиции составов соединения 25 в присутствии и отсутствии DOPE
[00156] Все липидные растворы смешивали гомогенно в круглодонной колбе, органический растворитель упаривали на роторном испарителе, и липидные пленки выдерживали при высоком вакууме в течение 4-5 часов (Experimental Biology и Medicine 2012; 237: 973-984, International Journal of Nanomedicine 2012:7 5259-5269&Journal of Liposome Research, 2011; 21(1): 60-69). Затем, тонкую пленку гидратировали добавлением к ней 5% раствора лактозы, и вращали в роторной водяной бане в течение 1,0 часа при 65°C. Затем, гидратированный супрамолекулярный состав последовательно экструдировали через мембраны с размером пор 400 нм, 200 нм и 100 нм (Whatman® фильтры), поддерживаемые держателем для фильтров, 10 раз, применяя LIPEXTM экструдер (10 мл), соединенный с баней с циркулирующей водой при 65°C. Измерение с помощью атомно-абсорбционного спектрометра (AAS) Pt показало, что конечный Pt-эквивалент данного состава составляет 1,13 мг/мл.
[00157] Приведенный выше супрамолекулярный состав лиофилизировали (5% раствора лактозы применяли в качестве криопротектора) в течение 12-15 часов. Образовавший после этого белый порошок перерастворяли добавлением требуемого объема milliQ вода и измеряли ДРС. ДРС гистограмму можно видеть на фигуре 11, и данные приведены в таблице 7.
Таблица 7: сводка ДРС данных для примерного состава, содержащего DOPE
[00158] Определяли эффективность состава, содержащего DOPE. Как видно на фигуре 12 и приведено в таблице 8, состав, содержащий DOPE, показал относительно лучшую эффективность в A549 и DU145 клеточных линиях, чем аналогичный состав, несодержащий DOPE.
Таблица 8: эффективность состава, содержащего DOPE, в A549 и DU145 клеточных линиях
Пример 10: улучшенный способ получения промежуточного соединения 6 (Im-06)
[00159] Чистота промежуточного соединения 6 (Im-06), полученного применяя схему получения 3, показанную в примере 2, изменялась в пределах 88-92%. Желательно увеличить чистота до требуемой спецификации 95%. Это достигалось получением кислотной соли промежуточного соединения Im-06, с последующим обессоливанием, как показано на схеме 8.
СХЕМА 8
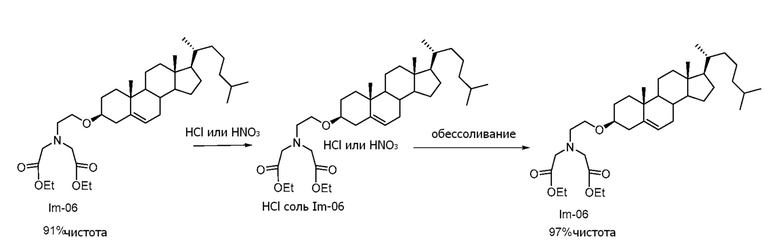
[00160] Стадия 1: получение солей с HCl или HNO3 при масштабе 10 г: к Im-06 (10,0 г, 91% чистота, показанная на фигуре 13) в EtOAc (90 мл) при комнатной температуре добавляли 5 N HCl или HNO3/EtOAc (30 мл). Смесь нагревали и перемешивали в течение 30 минут. Белый осадок фильтровали. Остаток на фильтре промывали холодным EtOAc, сушили, получая Im-06-HCl или HNO3 соль (8 г, 80% выход, ВЭЖХ 96,0%) в виде белого твердого остатка.
[00161] Перекристаллизация: смесь Im-06-HCl или HNO3 соли (8 г) в EtOAc/EtOH (50 мл/8 мл) нагревали до 80°C при встряхивании (до растворения). Раствор охлаждали до комнатной температуры в течение 2 часов без встряхивания. Осадок собирали фильтрованием, промывали EtOAc, получая Im-06-HCl или HNO3 (кристаллический) (5-6 г, ВЭЖХ 97%) в виде белого твердого остатка.
[00162] Стадия 2: обессоливание Im-06.HCl или Im-06.HNO3: к смеси Im-06.HCl или Im-06.HNO3 (100 мг) в EtOAc (10 мл) добавляли NaHCO3 (2 мл, водный насыщенный). Смесь перемешивали 10 минут, потом разделяли. Органический слой сушили над Na2SO4 и концентрировали, получая Im-06 (70-80 мг, 80-90% выход, ВЭЖХ чистота при 210 нм для Im-06, извлеченного из HCl соли, составляла 96,7%, фигура 14) в виде бесцветного масла.
[00163] Хотя предпочтительные варианты осуществления показаны и описаны подробно в настоящем изобретении, специалисту в данной области техники ясно, что различные модификации, дополнения, замены и подобные можно вносить, не выходя за пределы сущности настоящего изобретения и, следовательно, их считают включенными в объем настоящего изобретения, как определено в формуле изобретения, которая следует далее. Кроме того, в тех случая, когда это еще не показано, специалисту в данной области техники ясно, что любой из различных вариантов осуществления, описанных и проиллюстрированных в настоящем изобретении, можно дополнительно модифицировать так, чтобы включить признаки, показанные в любом из других вариантов осуществления, описанных в настоящем изобретении.
Пример 11: улучшенный способ получения Im-07
[00164] Получение Im-07 осуществляли с некоторыми небольшими изменениями, относящимися к обработке, относительно ранее описанного способа. Как показано на схеме 9, LiOH добавляют до достижения полного превращения (требуется приблизительно 2,1 экв.). Обработку проводили без экстракции дихлорметаном, и получали прозрачный продукт.
Схема 9
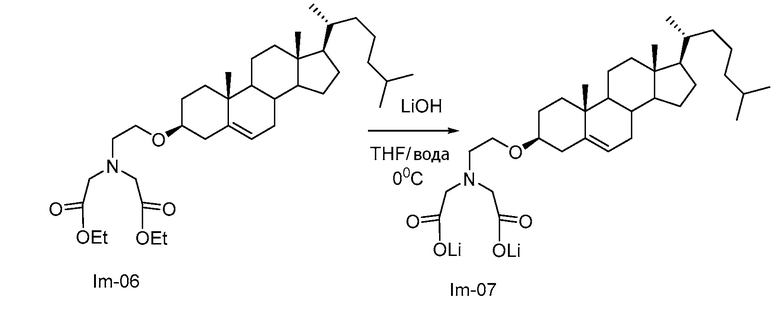
Пример 12: получение соединения 25
[00165] Цель настоящего исследования заключалась в получении соединения 25 (COMP 25), подходящего для токсикологических исследований, с чистотой приблизительно 97%, но без колоночной хроматографии. В связи с этим, в добавление к кристаллизации, осуществляли некоторые дополнения с целью облегчения выделения. В первоначальных испытаниях, два раствора Im-07 и Im-08 смешивали вместе согласно способу, и немедленно образовывался осадок (схема 10).
Схема 10
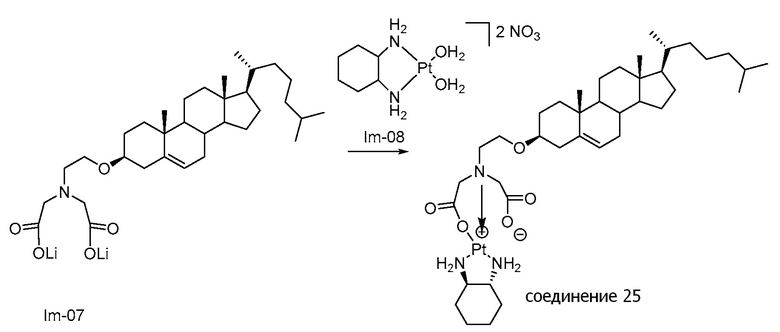
[00166] Однако фильтрование не было эффективным, поскольку твердого остатка не оставалось на фильтре. В связи с этим, в конечных испытаниях удаляли воду, получая остаток. Затем, выделенный продукт кристаллизовали в смеси DCM/метанол и суспендировали в смеси вода/ацетон. Неочищенный остаток содержал большое количество NO3 (приблизительно 11%) перед кристаллизацией. Это легко объяснимо тем фактом, что продукт выделяли без промывки, и количество воды в реакции было недостаточным для его удаления. Получали две суспензии, и нитраты восстанавливали. Чистота конечного API составляла приблизительно 97%. В таблице 9 показаны стадии последовательной очистки неочищенного соединения 25.
Таблица 9: аналитические результаты пошаговой очистки соединения 25
NO3: 11,2%
NO3: 7,6%
NO3: 0,99%
NO3: 0,45%
[00167] Реакции осуществляли с максимум 20 г Im-06, и 97% соединение 25 получали с выходом 57%. Реакционный способ можно комфортно осуществлять в кг масштабе. ВЭЖХ хроматограмма соединения 25 после кристаллизации и после двух суспендирований показана на фигуре 15, и результаты пиков фигуры 15 показаны в таблице 10.
Таблица 10: результаты пиков фигуры 15
Пример 13. Кристаллизация соединения 25
[00168] Для увеличения чистоты соединения 25, определяли набор условий, который приводил в результате к кристаллизации соединения 25 (COMP 25) и обеспечивал явное повышение чистоты. В процессе данной программы работы, ряд аморфных твердых остаток получали для ряда систем растворителей. PXRD и PLM анализ показывает, что твердый остаток, полученный в процессе некоторых из исследований на кристаллизацию, кристаллизовался самопроизвольно.
[00169] Последовательные стадии для анализа неочищенного образца (например, пример 12, чистоту 94%) были следующими:
1) Скрининг на кристаллизацию неочищенного соединения 25 с отобранными растворителями (опыты с 20 мг)
2) Кристаллизация с затравкой при охлаждении неочищенного соединения 25 (опыты с 20 мг)
3) Кристаллизация при охлаждении неочищенного соединения 25 (опыты с 20 мг)
4) Кристаллизация с антирастворителем/охлаждением неочищенного соединения 25 (опыты с 20 мг и 50 мг)
5) Кристаллизация при охлаждении неочищенного соединения 25 (200-250 мг масштаб)
6) Кристаллизация с затравкой при охлаждении неочищенного соединения 25 (опыт с 250 мг)
7) Кристаллизация с затравкой, антирастворителем и при охлаждении неочищенного соединения 25 (опыт с 140-150 мг)
[00170] Первоначально, серию растворителей и смесь растворителей скринировали для отбора подходящих растворителей для способа кристаллизации. Как показано в таблице, смесь спиртов, таких как метанол/этанол, и хлороформ/дихлорметан представляют собой подходящие смеси растворителей для способа кристаллизации.
Таблица 11: сводка данных по растворимости соединения 25 в чистых растворителях и смесях
[00171] Скрининг условий кристаллизации неочищенного соединения 25 для отобранных растворителей: скрининг условий кристаллизации для неочищенного соединения 25 (COMP 25) осуществляли, применяя смесь растворителей метанол:дихлорметан и этанол:дихлорметан. Материал, выделенный в каждом из экспериментов после температурного циклирования, анализировали XRPD, и результаты приведены в таблице 12. Кристаллическое соединение 25 получали, применяя системы растворителей метанол:дихлорметан (20:80% об/об) и (10:90% об/об). Все другие системы растворителей метанол:дихлорметан и этанол:дихлорметан давали аморфный материал. Порошковые рентгеновские 2θ дифрактограммы твердых веществ, извлеченных в результате успешного скрининга условий кристаллизации неочищенного соединения 25, показаны на фигуре 16.
Таблица 12: скрининг условий кристаллизации для неочищенного соединения 25
Кристаллизация с затравкой при охлаждении неочищенного соединения 25
[00172] Общий способ: приблизительно 20 мг неочищенного соединения 25 взвешивали в 2 мл стеклянной пробирке, и 100 мкл соответствующей системы растворителей добавляли к экспериментам при приблизительно 25°C. Все растворители сушили над предварительно высушенными 3 Ǻ молекулярными ситами (при необходимости) перед применением. Небольшое количество кристаллического соединения 25 добавляли в качестве затравки к экспериментам. Эксперименты нагревали до 40°C. Эксперименты охлаждали до 5°C при приблизительно 0,11°C/минута. Эксперименты перемешивали при 5°C в течение 3 дней, и температуру циклически изменяли от 5°C до 40°C при 0,2°C/минута в течение ночи (приблизительно 18 часов). В экспериментах, в которых наблюдали твердый материал, твердый материал выделяли, применяя центрифугу при температуре окружающей среды (приблизительно 22°C) и анализировали XRPD. В таблице 13 приведены системы растворителей, применяемые для кристаллизации с затравкой при охлаждении неочищенного соединения 25.
Таблица 13: системы растворителей для кристаллизации с затравкой при охлаждении неочищенного соединения 25
[00173] Единственные экспериментальные условия, которые давали повторяющуюся кристаллическую форму, представляли собой метанол:дихлорметан (10:90%об/об). Смесь метанол:дихлорметан (20:90%об/об) давала слабо кристаллический материал. Все смеси этанол:дихлорметан и метанол:дихлорметан (30:70%об/об) давали аморфный материал. Фигура 17 показывает порошковые рентгеновские 2θ дифрактограммы твердых веществ после температурного циклирования, и фигура 18 показывает микроснимки микроскопии в поляризованном свете кристаллического материала, полученного в смеси метанол:дихлорметан (10:90%об/об) с затравкой.
Кристаллизация при охлаждении неочищенного соединения 25 (опыты с 20 мг)
[00174] Общий способ: неочищенное соединение 25 взвешивали в 2 мл пробирках для образцов, и известную аликвоту растворителя добавляли при приблизительно 25°C. Перемешивали при 25°C. Охлаждали с 25°C до 5°C при приблизительно 0,11°C/минута. Перемешивали при 5°C в течение 3 часов. Температуру циклически изменяли от 5°C до 40°C при приблизительно 0,2 °C/минута. В экспериментах, в которых образовывался твердый материал, твердые вещества выделяли при 25°C, применяя центрифугу, и анализировали XRPD. В таблице 14 приведены условия, применяемые для кристаллизации при охлаждении, и в таблице 15 приведены условия для кристаллизации при охлаждении в двойном масштабе. В таблицах 16 и 17 приведены результаты и наблюдения для исследований кристаллизации при охлаждении. Порошковые рентгеновские 2θ дифрактограммы примерных твердых веществ после температурного циклирования при концентрации приблизительно 150 мг/мл показаны на фигуре 19.
Таблица 14: условия кристаллизации при охлаждении
Таблица 15: условия кристаллизации при охлаждении в двойном масштабе
Таблица 16: сводка результатов и наблюдений для кристаллизации при охлаждении
Таблица 17: сводка результатов и наблюдений для кристаллизации при охлаждении
(% об/об)
Кристаллизация с антирастворителем при охлаждении неочищенного соединения 25
[00175] Общий способ: приблизительно 50 мг неочищенного соединения 25 взвешивали в 2 мл пробирке для образцов, и подходящее количество соответствующего растворителя добавляли при приблизительно 25°C. Соответствующий антирастворитель добавляли в подходящую пробирку в 25NL аликвоты при приблизительно 25°C. Эксперименты охлаждали с 25°C до 5°C при приблизительно 0,11°C/минуту. Перемешивали при 5°C в течение 3 часов. Эксперименты подвергали температурному циклированию от 5°C до 40°C при приблизительно 0,2 °C/минута в течение ночи (приблизительно 18 часов). В экспериментах, в которых образовывалась негустая суспензия или истинный раствор, добавляли к экспериментам дополнительное количество антирастворителя при приблизительно 25°C. Эксперименты охлаждали с 25°C до 5°C при приблизительно 0,11°C/минута. Перемешивали при 5°C в течение 3 часов. Эксперименты подвергали температурному циклированию в течение ночи от 5°C до 40°C при приблизительно 0,2 °C/минута в течение ночи (приблизительно 18 часов). В экспериментах, в которых наблюдали твердый материал, твердые вещества выделяли при температуре окружающей среды (приблизительно 22°C), применяя центрифугу, и анализировали XRPD. Затем, образцы, которые выделяли, сушили в вакууме при температуре окружающей среды в течение ночи, применяя 2-метил THF в качестве антирастворителя. Кристаллизация приводила в результате к образованию гелеобразного материала, применяя смеси растворителей метанол:дихлорметан и систему растворителей этанол:дихлорметан (30:70% об/об). Применяя гептан в качестве антирастворителя, кристаллический материал наблюдали, применяя большинство из систем растворителей. Как показано в таблицах 18 и 19, применяя ацетонитрил в качестве антирастворителя, частично кристаллический материал наблюдали, применяя большинство из систем растворителей. Порошковые рентгеновские 2θ дифрактограммы твердых веществ после температурного циклирования при применении гептана в качестве антирастворителя показаны на фигурах 20 и 21.
Таблица 18: наблюдения и результаты кристаллизации при добавлении антирастворителя и при охлаждении
дихлорметан (30:70)
дихлорметан (20:80)
дихлорметан (10:90)
дихлорметан (30:70)
дихлорметан (20:80)
дихлорметан (10:90)
дихлорметан (30:70)
дихлорметан (20:80)
дихлорметан (10:90)
Таблица 19: наблюдения и результаты для кристаллизации с добавлением антирастворителя при охлаждении
Кристаллизации при охлаждении неочищенного соединения 25 (200-250 мг масштаб)
[00176] Общий способ: соответствующую массу неочищенного соединения 25 взвешивали в 20 мл пробирке для образцов, и подходящий объем соответствующей системы растворителей добавляли при приблизительно 25°C, растворяя образец. Эксперименты охлаждали до 5°C при приблизительно 0,1°C/мин. Перемешивали при 5°C в течение 2 часов. Температуру циклично изменяли от 5°C до 40°C. Нагревали до 40°C в течение 2 часов (приблизительно 0,3°C/минута). Перемешивали при 40°C в течение 2 часов. Охлаждали до 5°C в течение 2 часов (приблизительно 0,3°C/минута). Перемешивали при 5°C в течение 2 часов. Образцы выделяли при температуре окружающей среды (приблизительно 22°C) фильтрованием через воронку Бюхнера в вакууме, применяя бумажный фильтр Ватмана No. 1, затем сушили в вакууме при температуре окружающей среды в течение ночи (приблизительно 18 часов). Затем, твердый материал анализировали XRPD и PLM. Результаты приведены в таблице 20 и показаны на фигурах 22 и 23. ВЭЖХ хроматограмма примерной кристаллизации при охлаждении 2 показана на фигуре 24.
Таблица 20: наблюдения и результаты для кристаллизации при охлаждении
(% об/об)
Кристаллизация с затравкой при охлаждении неочищенного соединения 25 (250 мг масштаб)
[00177] Общий способ: соответствующую массу неочищенного соединения 25 взвешивали в 20 мл пробирке для образцов, и подходящий объем соответствующей системы растворителей добавляли при приблизительно 25°C, растворяя образец. Кристаллическое соединение 25 добавляли к экспериментам в качестве затравки. Эксперименты охлаждали до 5°C при приблизительно 0,1°C/мин. Перемешивали при 5°C в течение 2 часов. Температура циклически изменяли с 5°C до 40°C. Нагревали до 40°C в течение 2 часов (приблизительно 0,3°C/минута). Перемешивали при 40°C в течение 2 часов. Охлаждали до 5°C в течение 2 часов (приблизительно 0,3°C/минута). Перемешивали при 5°C в течение 2 часов. Образцы выделяли при температуре окружающей среды (приблизительно 22°C) фильтрования через воронку Бюхнера в вакууме, применяя бумажный фильтр Ватмана No. 1, затем сушили в вакууме при температуре окружающей среды в течение ночи (приблизительно 18 часов). Затем, твердый материал анализировали XRPD и PLM. Результаты приведены в таблице 21 и показаны на фигурах 25 и 26.
[00178] Смесь растворителей метанол:дихлорметан (10:90%об/об). Концентрация 160 мг/мл. Полученный материал был кристаллическим и имел чистоту 96,65% по ВЭЖХ. Рассчитанный выход для данного эксперимента составлял 36%. Смесь растворителей метанол:дихлорметан (20:80%об/об). Концентрация 190 мг/мл. Полученный материал был кристаллическим и имел чистоту 96,21% по ВЭЖХ (фигура 27). Рассчитанный выход для данного эксперимента составлял 41%.
Таблица 21: Условия для кристаллизации с затравкой при охлаждении
Кристаллизации с добавлением затравки и антирастворителя при охлаждении
[00179] Общий способ: приблизительно 250 мг неочищенного соединения 25 взвешивали в 20 мл пробирке для образцов, и подходящий объем соответствующей системы растворителей добавляли при приблизительно 25°, растворяя IO-125. Гептан добавляли в качестве антирастворителя в 250NL аликвотах. Суммарно 1 мл гептана добавляли в каждом эксперименте. В эксперименты вносили затравку, применяя кристаллическое соединение 25. Эксперименты перемешивали при 25°C в течение приблизительно 1 часа, и затем охлаждали до 5°C при приблизительно 0,1°C/минута. Перемешивали при 5°C в течение 2 часов. Температура циклически изменяли с 5°C до 40°C. Нагревали до 40°C в течение 2 часов (приблизительно 0,3°C/минута). Перемешивали при 40°C в течение 2 часов. Охлаждали до 5°C в течение 2 часов (приблизительно 0,3°C/минута). Перемешивали при 5°C в течение 2 часов. Эксперименты выделяли при температуре окружающей среды (приблизительно 22°C) фильтрованием через воронку Бюхнера в вакууме, применяя бумажный фильтр Ватмана no 1, и затем сушили в вакууме при температуре окружающей среды в течение ночи (приблизительно 18 часов). Затем, твердый материал анализировали XRPD (фигура 28) и PLM (фигура 29). Комбинацию всех трех техник применяли для наблюдения, есть ли любое различие в материале, полученном в системах растворителей, и также для наблюдения, найдены ли лучшие условия кристаллизации. Осуществляли расчеты выходов, и они приведены в таблице 22. ВЭЖХ хроматограмма выделенного твердого вещества, применяя метанол:дихлорметан (20:80%об/об) с гептаном в качестве антирастворителя, показана на фигуре 30.
Таблица 22: экспериментальные наблюдения кристаллизации с добавлением затравки и антирастворителя при охлаждении
[00180] Все патенты и другие публикации; включая литературные ссылки, выданные патенты, опубликованные патентные заявки и одновременно заявленные патентные заявки; цитируемые в данной заявке, включены явным образом в настоящее изобретение с помощью ссылки с целью описания и раскрытия, например, методологии, описанной в данных публикациях, которую можно применять в сочетании с технологией, описанной в настоящем изобретении. Данные публикации приведены только для их раскрытия перед датой подачи настоящей заявки. Ничто, в этой связи, не следует рассматривать как допущение того, что изобретатели уполномочены датировать задним числом настоящее изобретение посредством предшествующего изобретения или для любых других причин. Все заявления относительно даты или репрезентации относительно содержимого данных документов основаны на информации, доступной заявителям, и не отражают любого допущения относительно корректности дат или содержания данных документов.
Ясно, что настоящее изобретение не ограничивается конкретной методологией, протоколами и реагентами, и т.д., описанными в настоящем изобретении и, как таковые, они могут изменяться. Терминология, применяемая в настоящем изобретении, приведена только с целью описания конкретных вариантов осуществления, и не предполагается ограничивающей объем настоящего изобретения, который определяется единственно формулой изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЕДИНЕНИЯ НА ОСНОВЕ ПЛАТИНЫ И ЛИПИДОВ И НАНОЧАСТИЦЫ | 2014 |
|
RU2737735C2 |
| СОЕДИНЕНИЯ НА ОСНОВЕ ПЛАТИНЫ И ЛИПИДОВ И НАНОЧАСТИЦЫ | 2014 |
|
RU2679896C2 |
| СОЕДИНЕНИЯ ДЛЯ НАЦЕЛЕННОЙ ДОСТАВКИ ЛЕКАРСТВЕННОГО СРЕДСТВА И УСИЛЕНИЯ АКТИВНОСТИ siPHK | 2012 |
|
RU2632888C2 |
| ЛИПИДНОЕ СОЕДИНЕНИЕ И КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ | 2021 |
|
RU2825571C1 |
| КАТИОННЫЕ ЭМУЛЬСИИ "МАСЛО-В-ВОДЕ" | 2011 |
|
RU2625546C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ АНИОННОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО, И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2016 |
|
RU2721558C2 |
| АМИНОКИСЛОТЫ-ЛИПИДЫ | 2013 |
|
RU2670618C2 |
| УЛУЧШЕННЫЙ СПОСОБ ПОЛУЧЕНИЯ ЛИПИДНЫХ НАНОЧАСТИЦ, ЗАГРУЖЕННЫХ мРНК | 2020 |
|
RU2832672C2 |
| НУКЛЕИНОВЫЕ КИСЛОТЫ ДЛЯ ИНГИБИРОВАНИЯ ЭКСПРЕССИИ ГЕНА-МИШЕНИ, СОДЕРЖАЩИЕ ФОСФОДИТИОАТНЫЕ СВЯЗИ | 2018 |
|
RU2812806C2 |
| ПОКРЫТИЕ ДЛЯ ИНТРАЛЮМИНАЛЬНОГО РАСШИРЯЮЩЕГОСЯ КАТЕТЕРА, ОБЕСПЕЧИВАЮЩЕЕ КОНТАКТНЫЙ ПЕРЕНОС МИКРОРЕЗЕРВУАРОВ С ЛЕКАРСТВЕННЫМ СРЕДСТВОМ | 2019 |
|
RU2820776C2 |

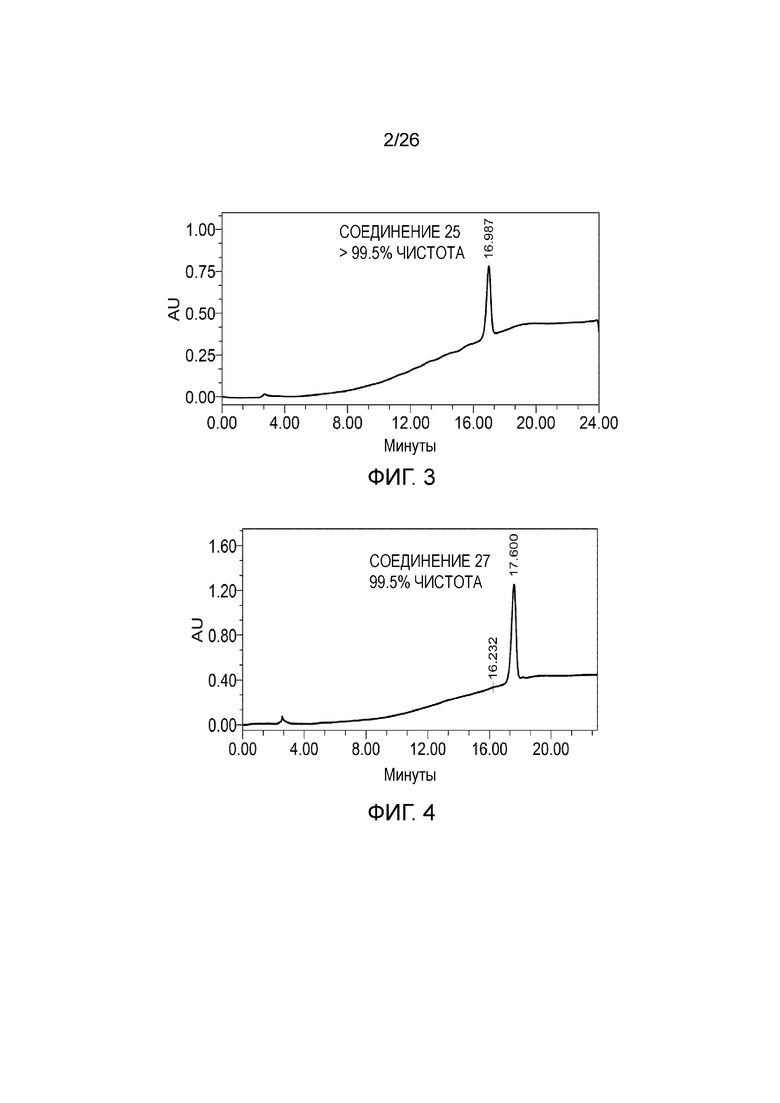
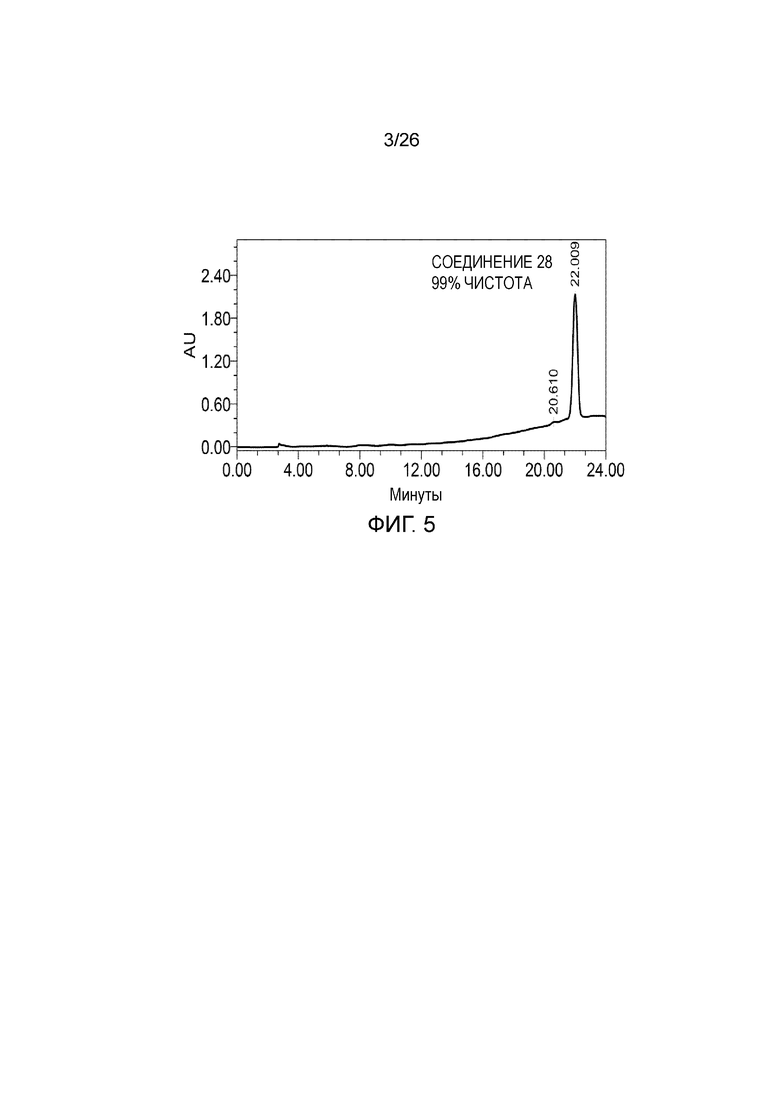
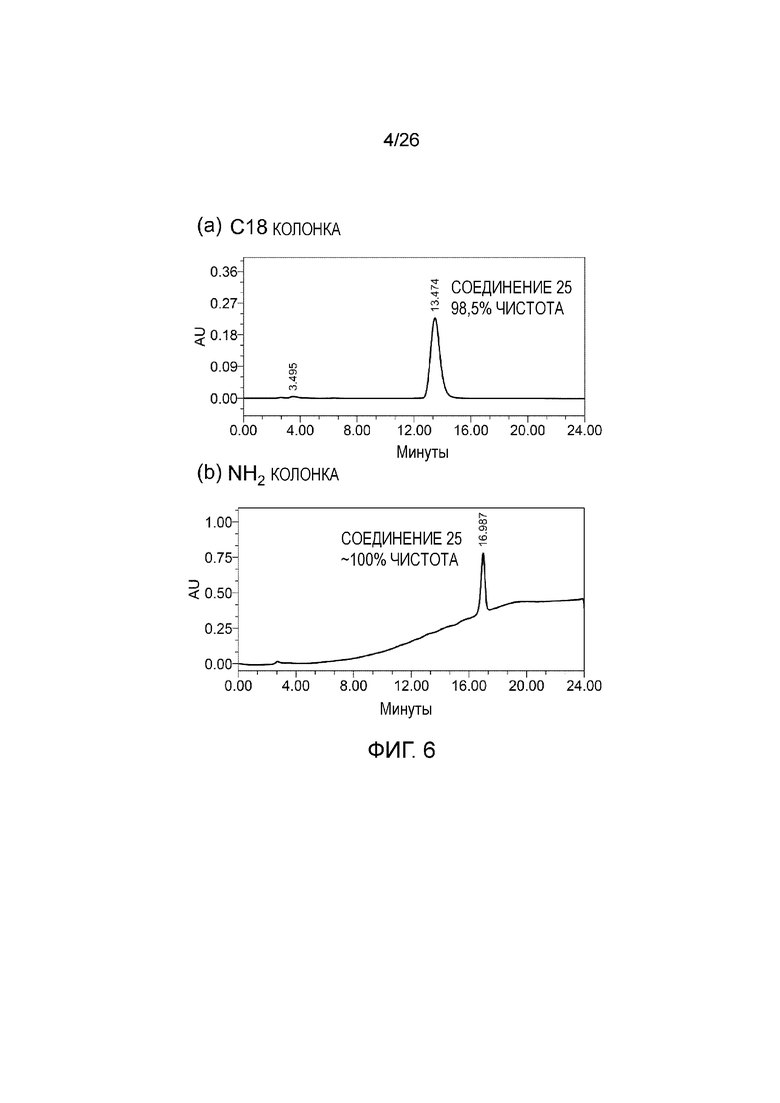
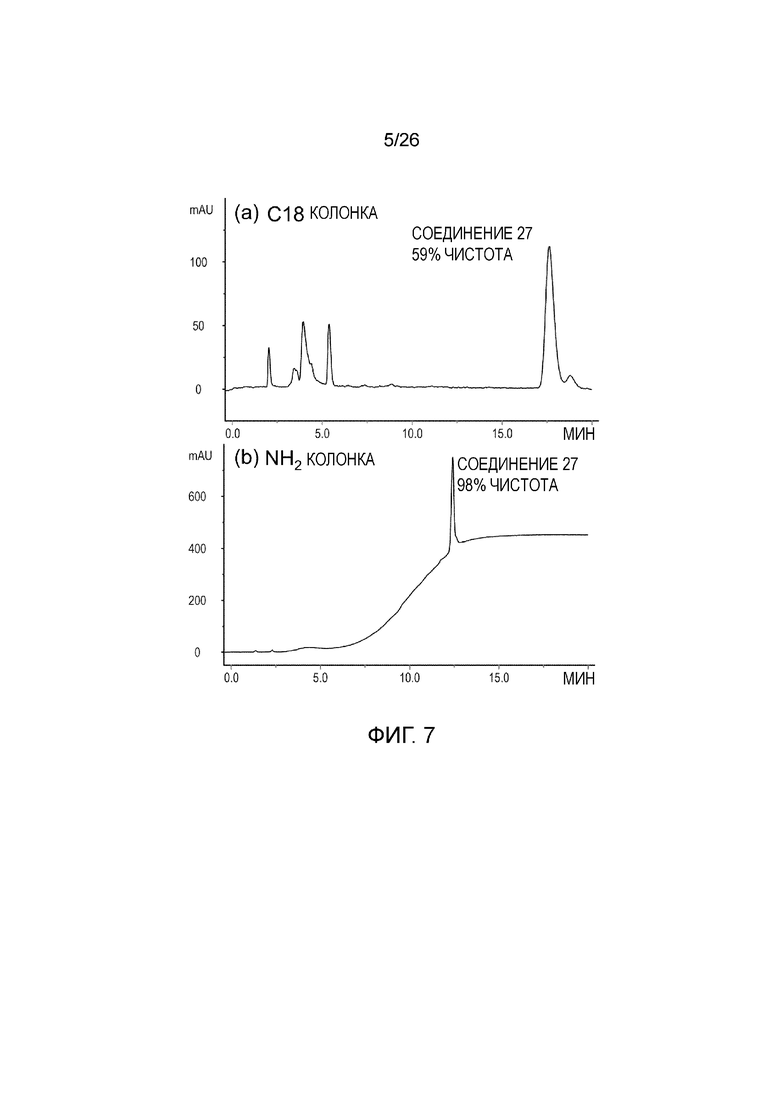
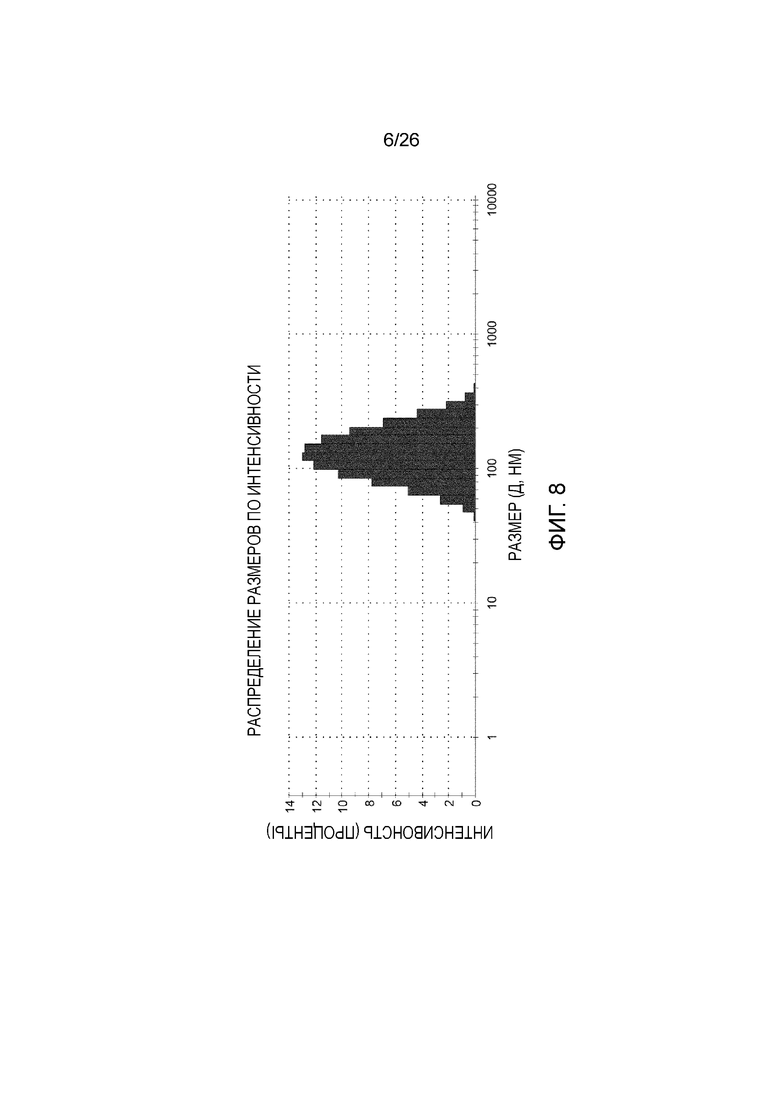
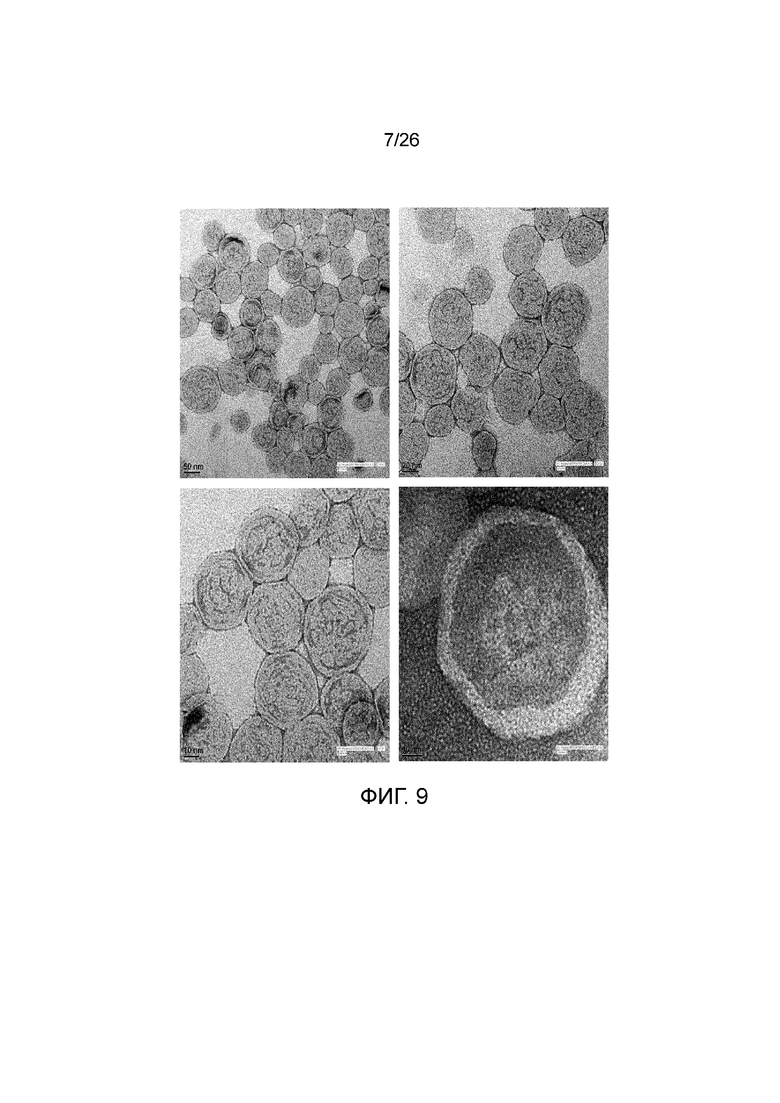

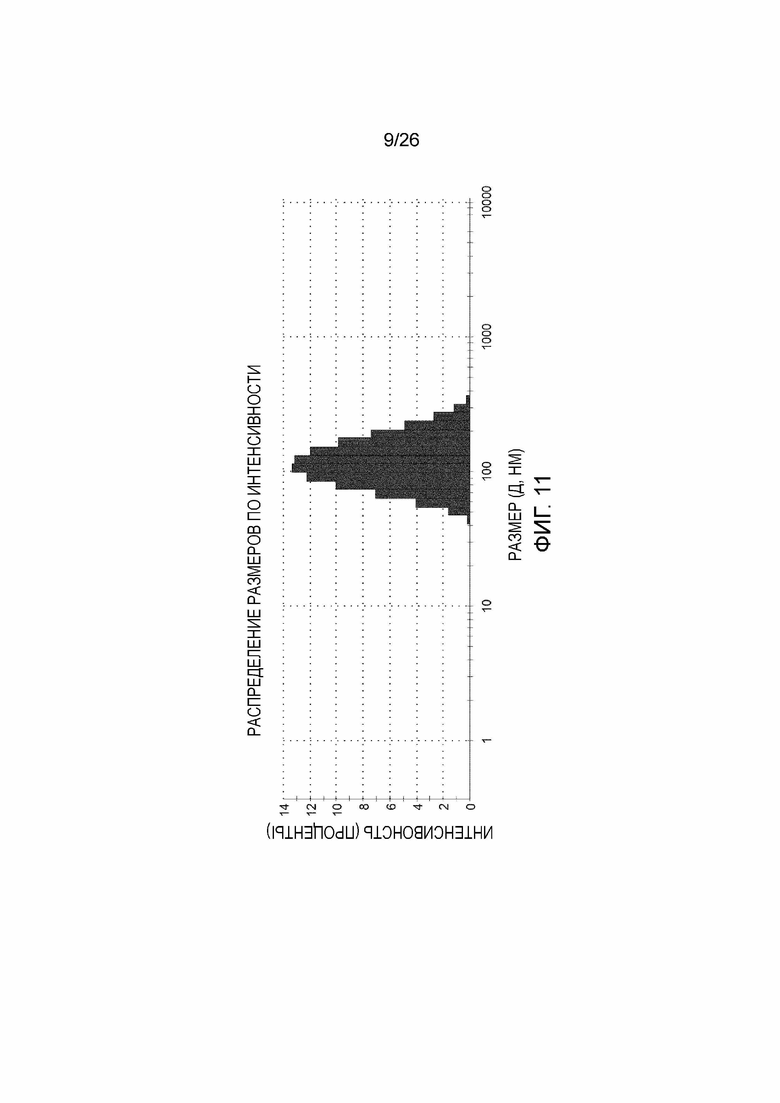
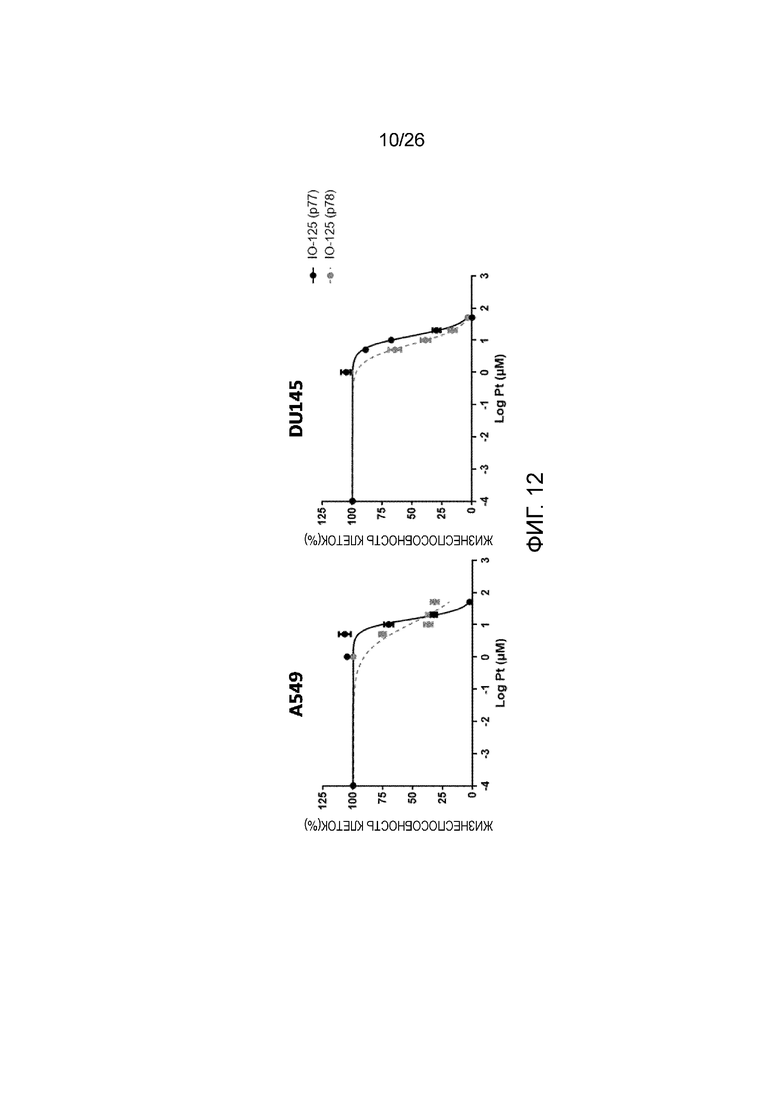
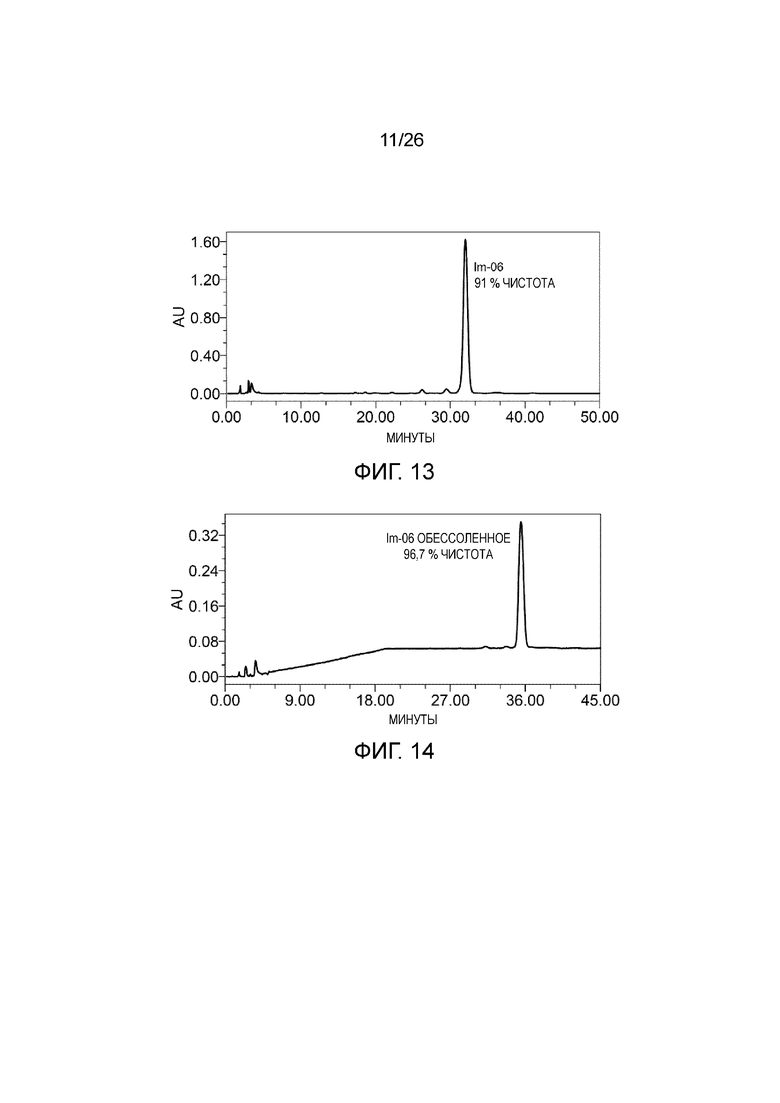
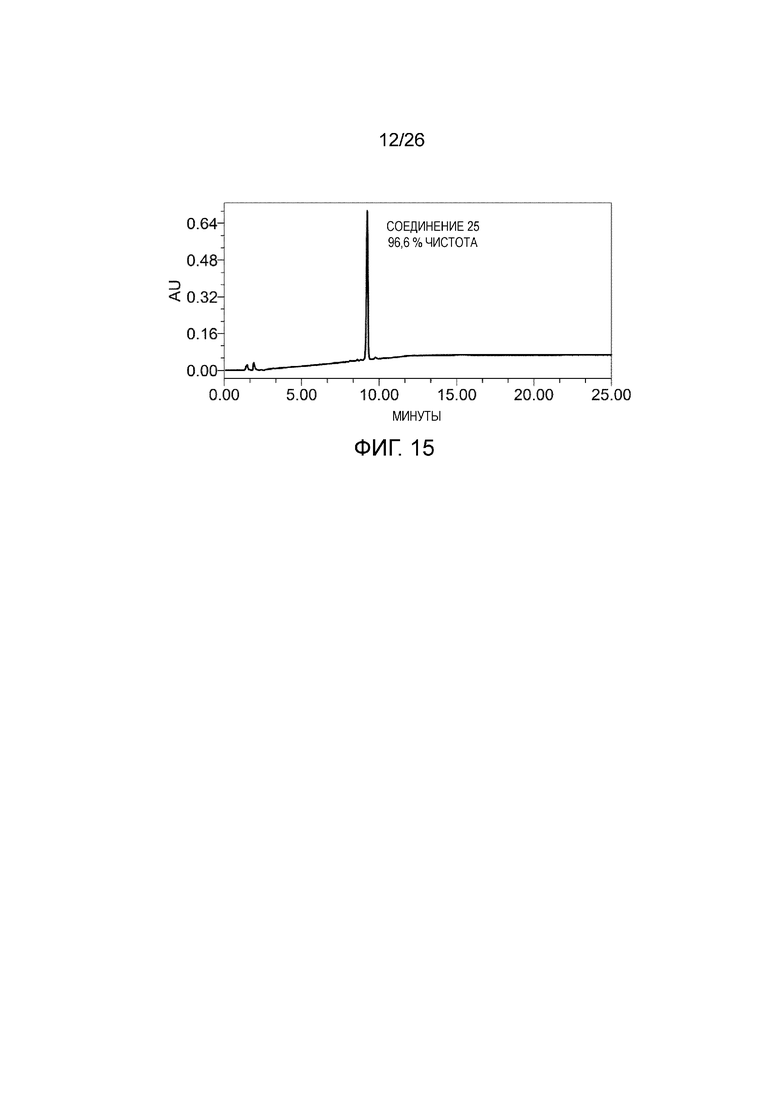
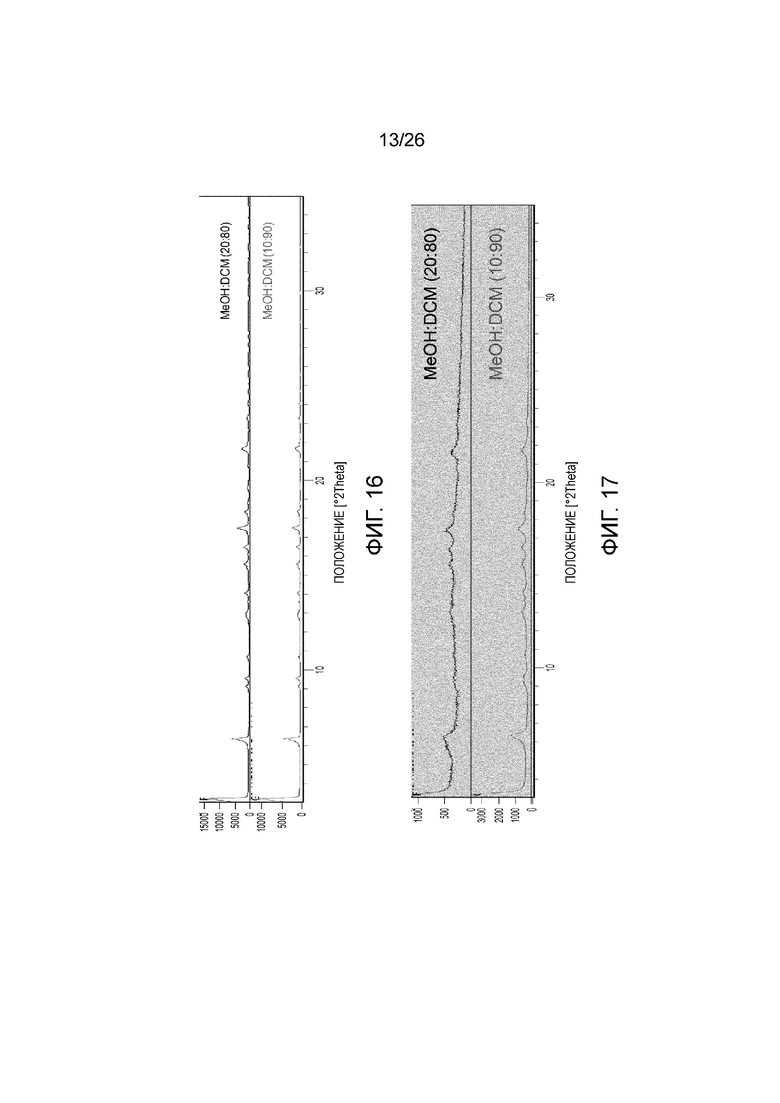
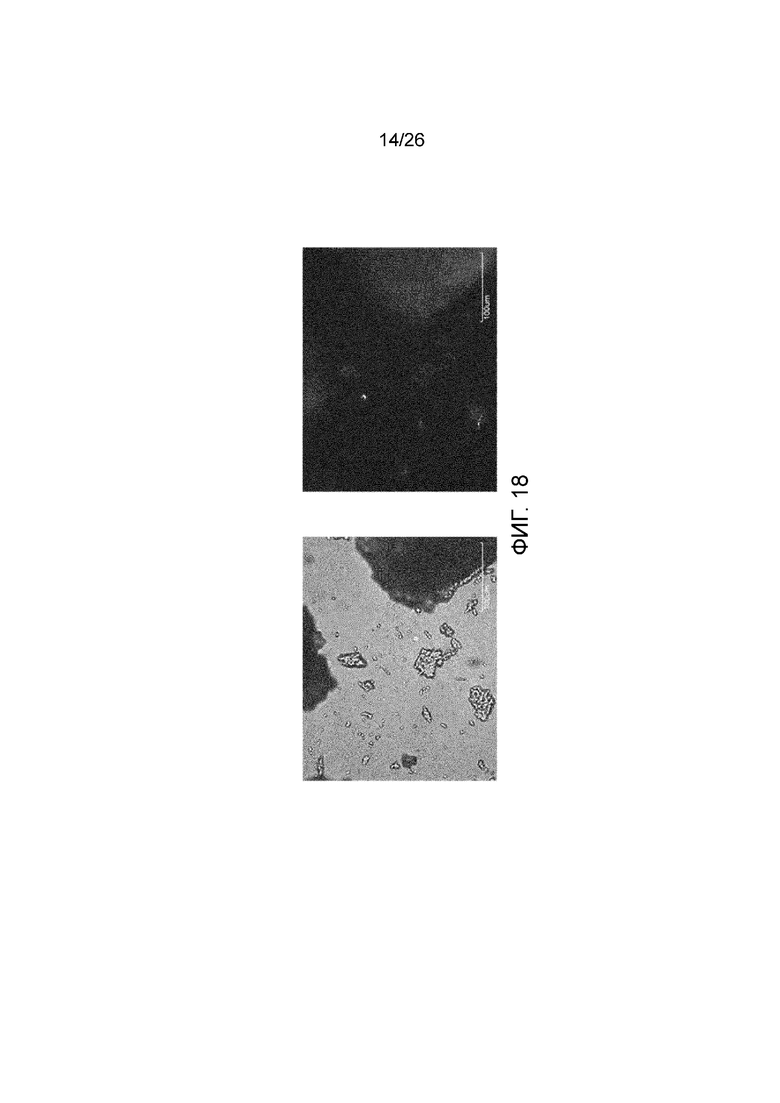
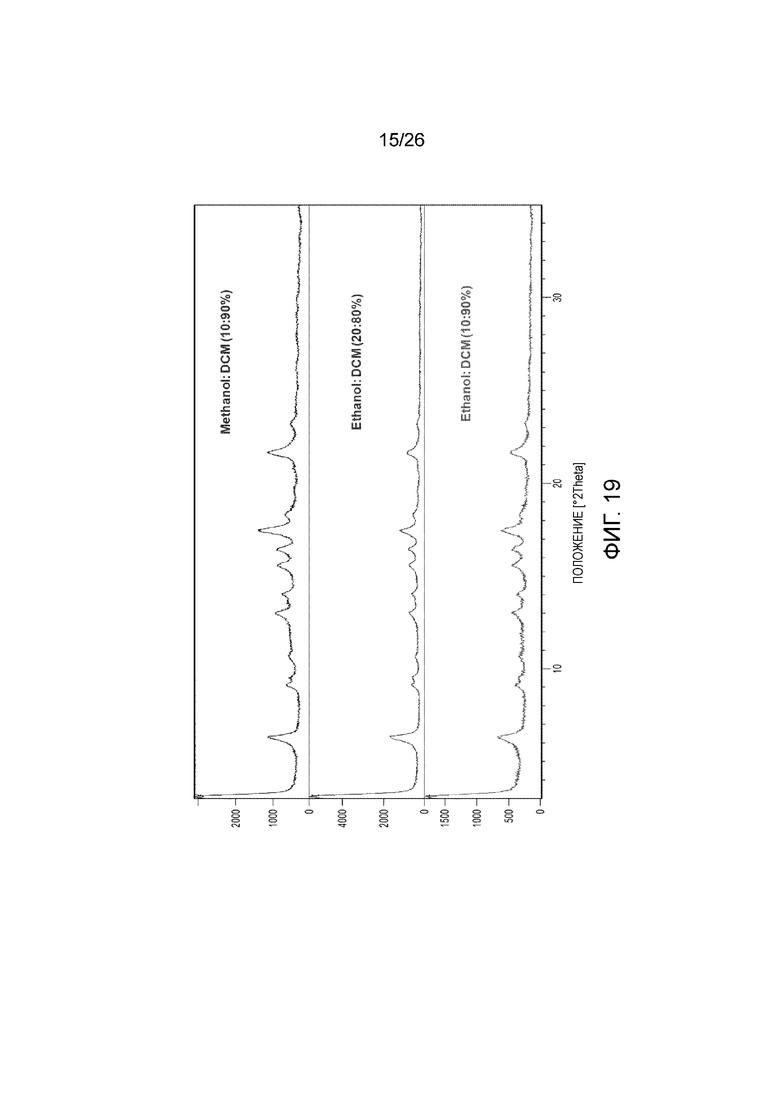
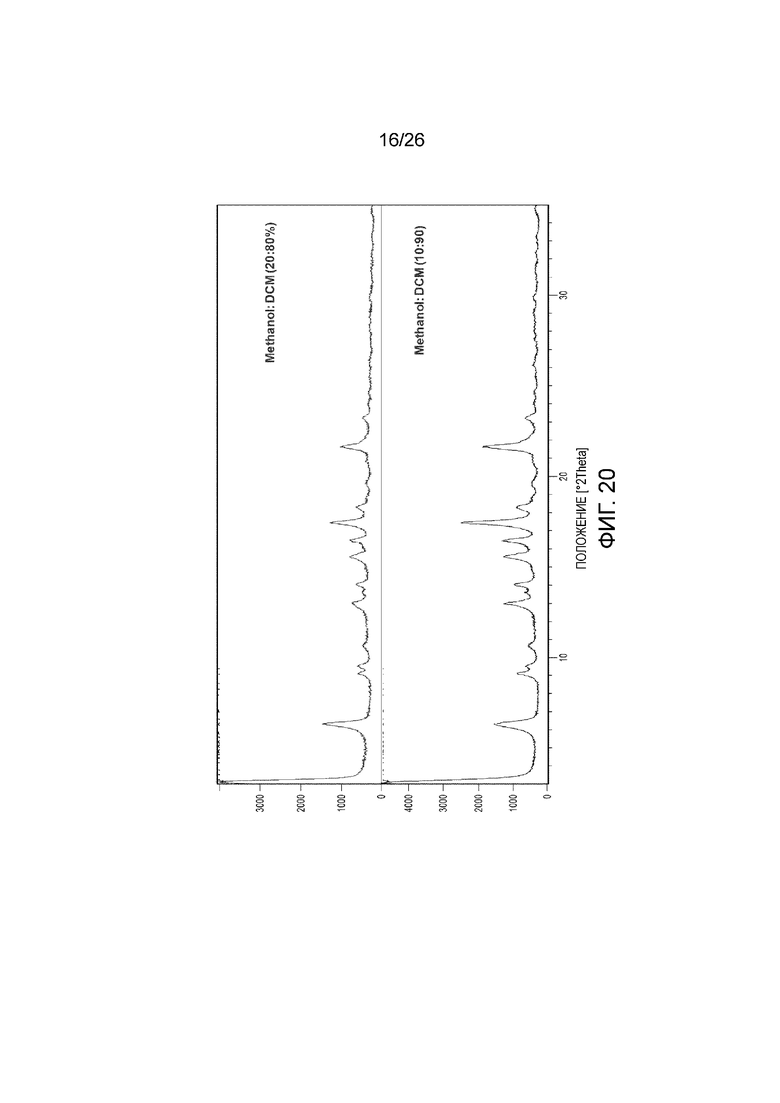
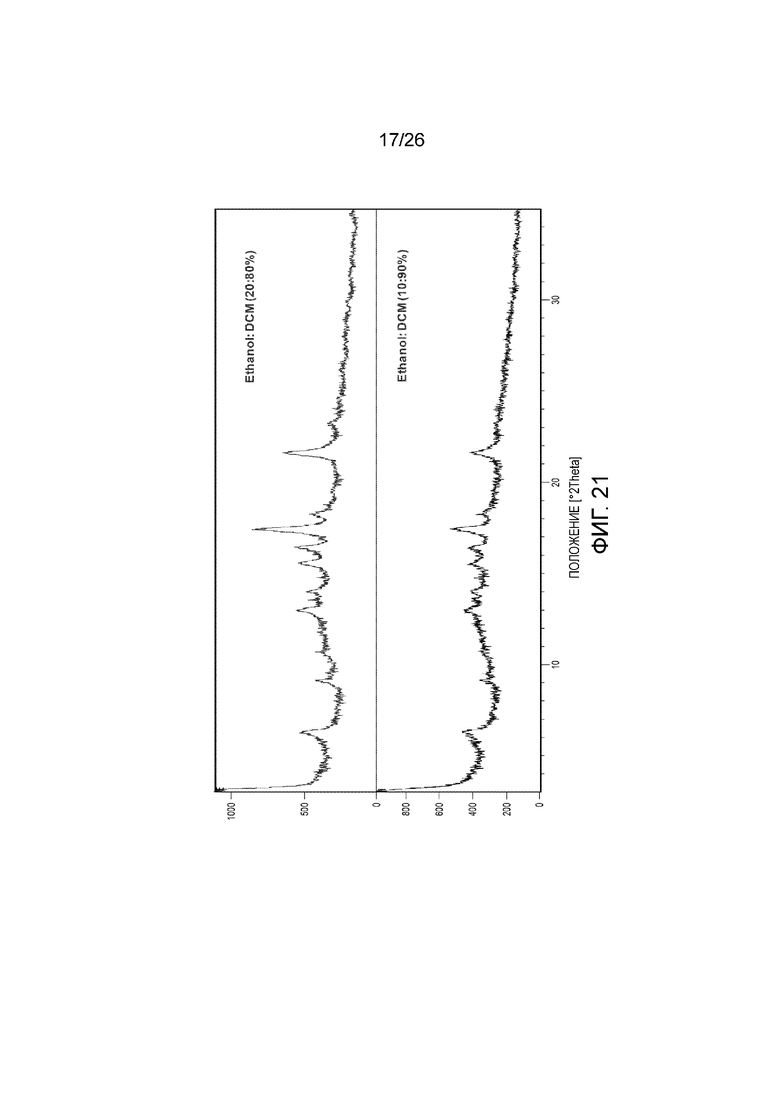
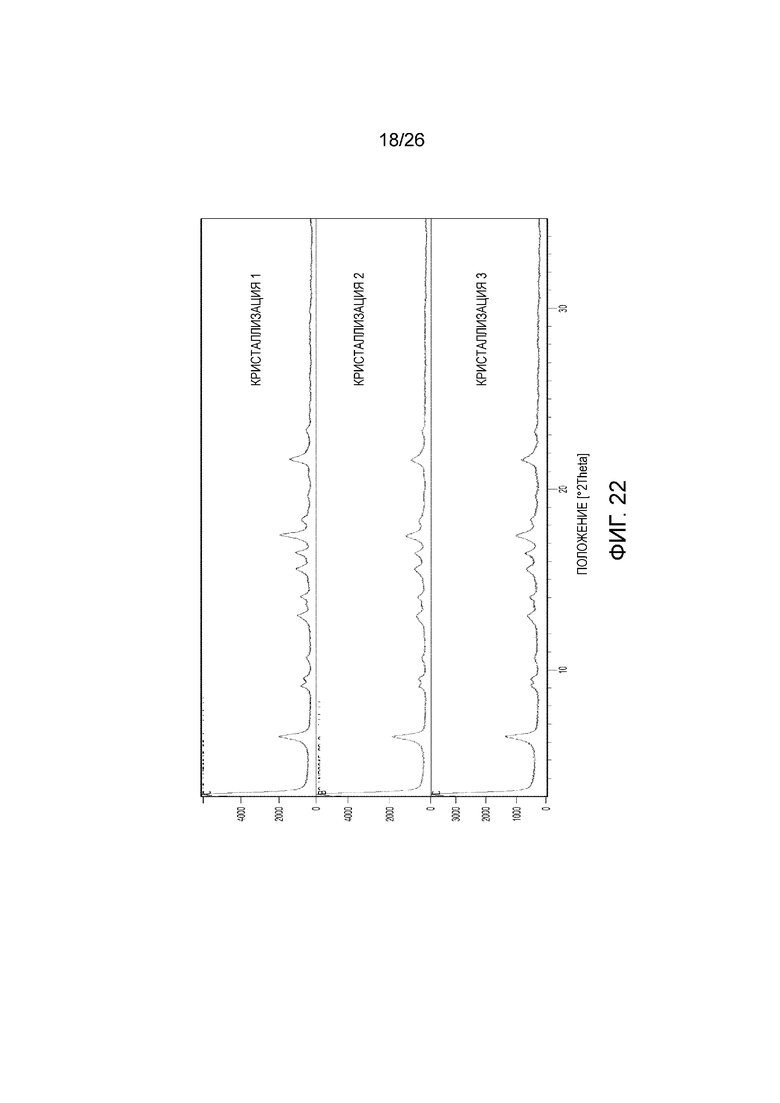
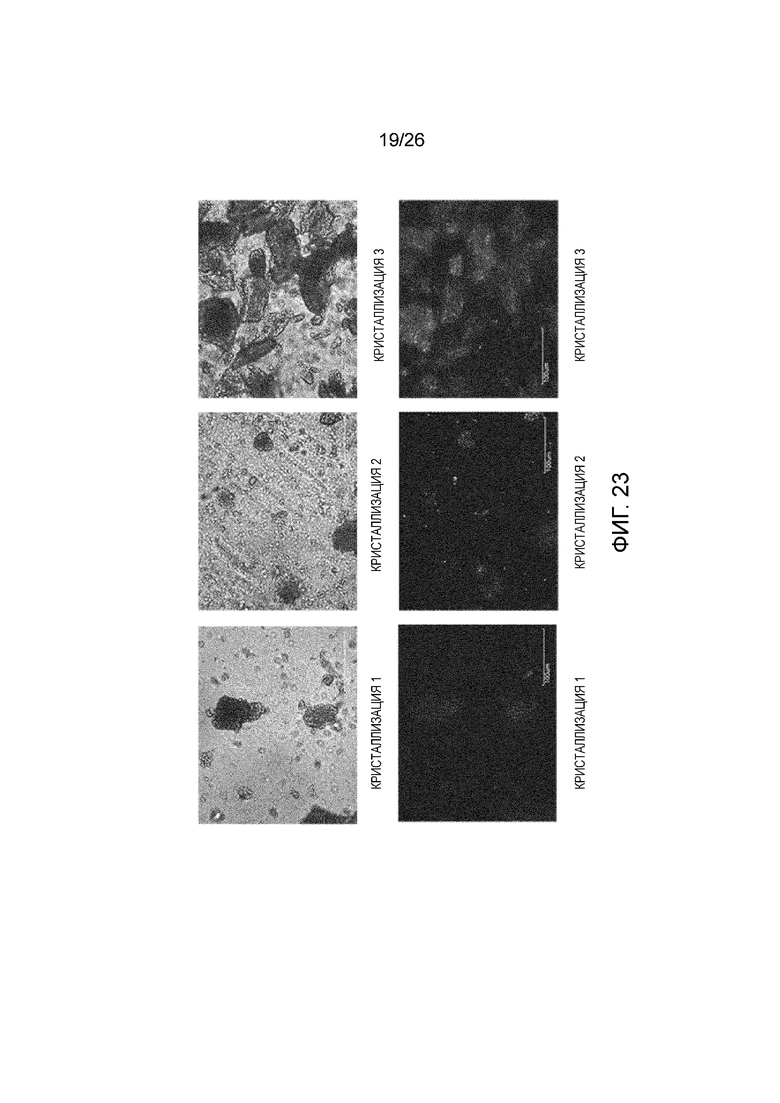

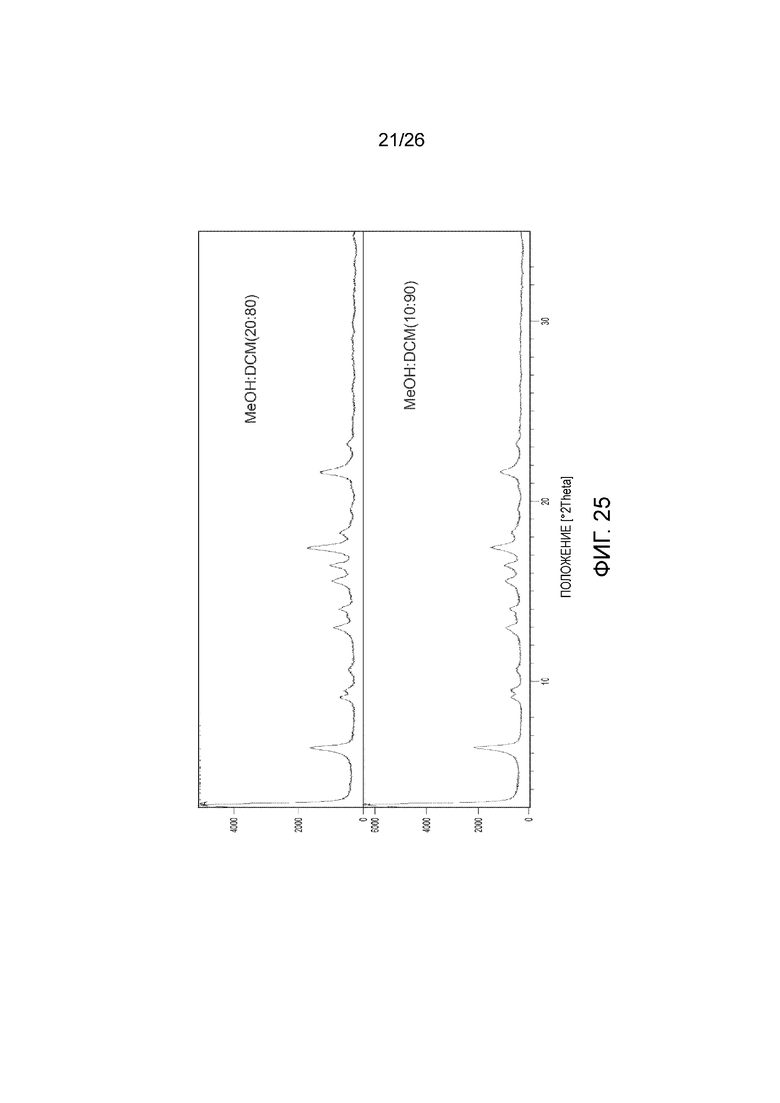
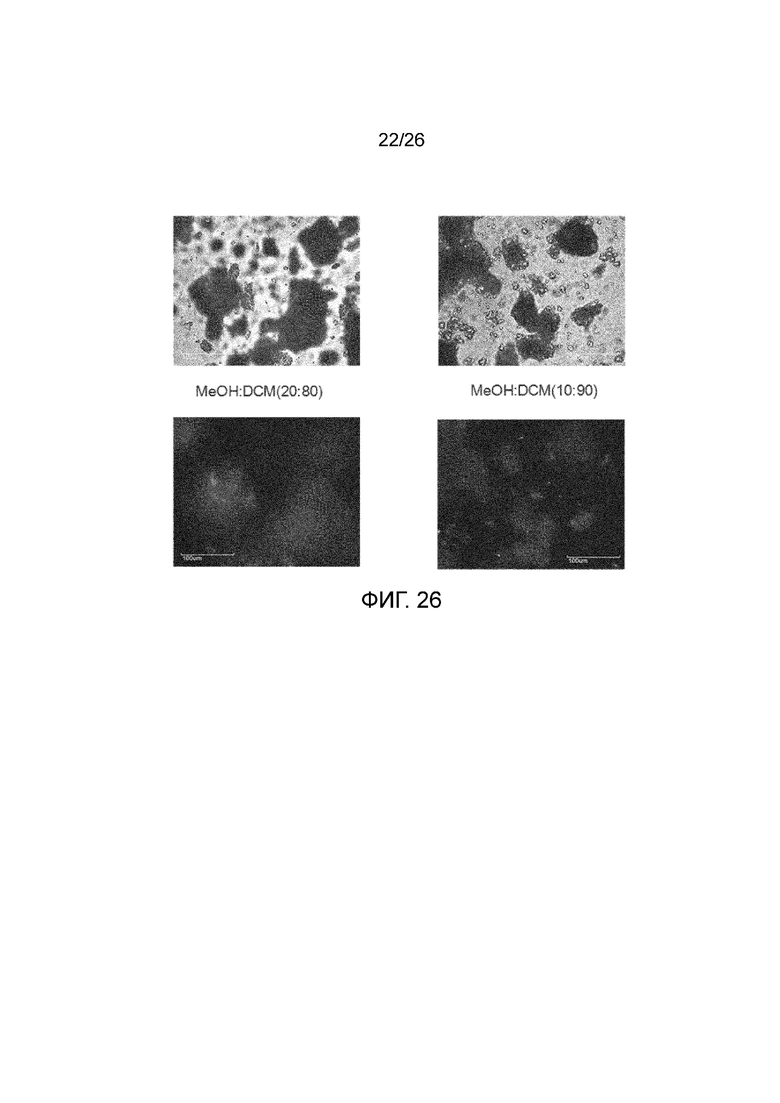

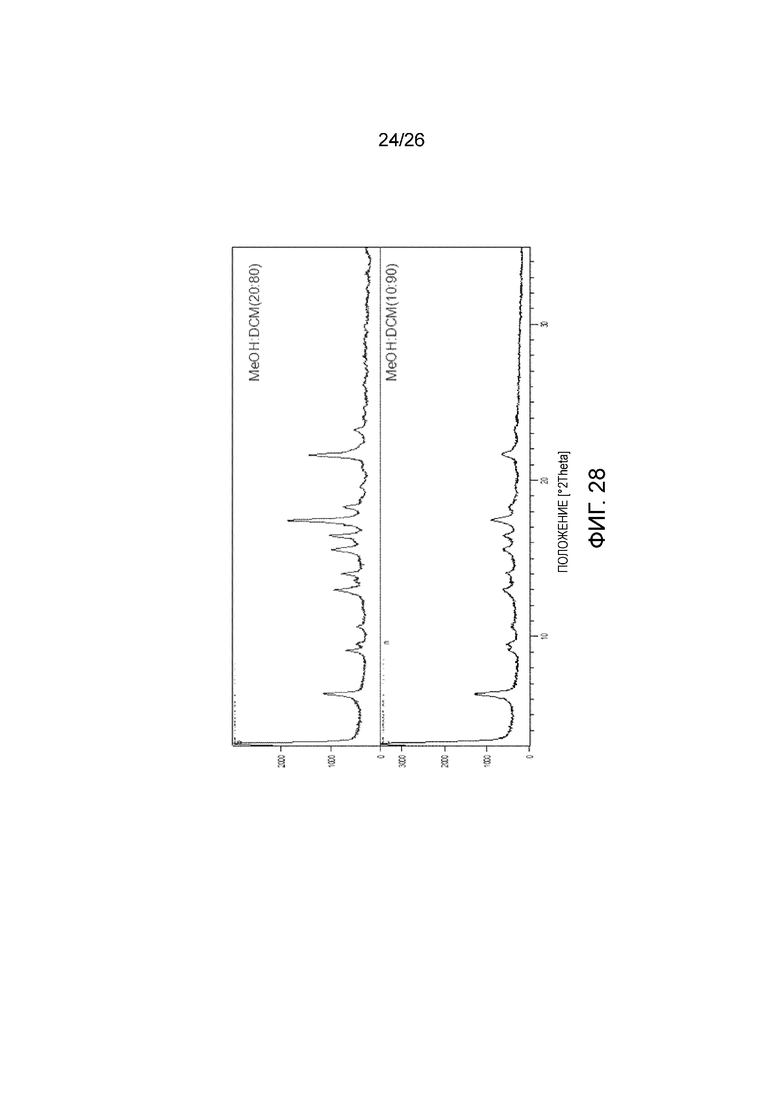
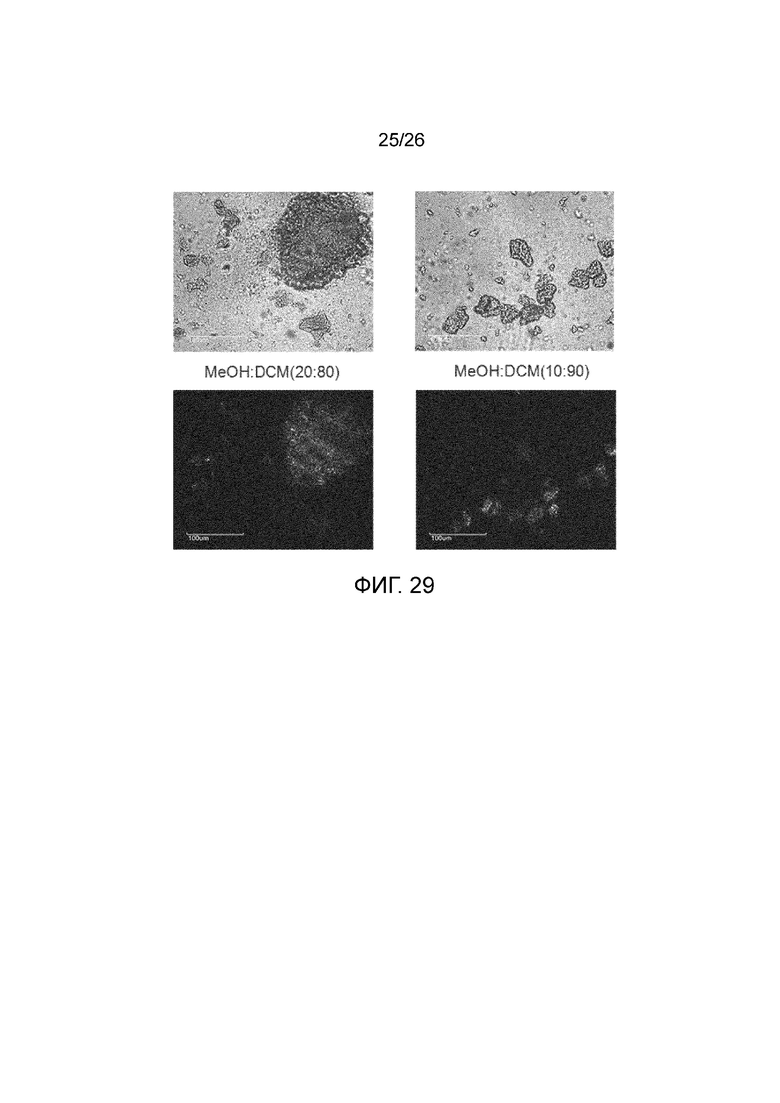

Настоящее изобретение относится к области нанотехнологии и противораковых лекарственных средств, а именно к способу получения конъюгированного с липидами платинового соединения. Способ включает: реакцию растворимой в воде соли липида с растворимым в воде платиновым соединением в по существу водном растворе, получая конъюгированное с липидами платиновое соединение в виде осадка, где растворимая в воде соль липида содержит соединение формулы II, где X представляет собой NH или N-CH2COO-, X1 выбран из группы, состоящей из -(CH2)nO-, -(CH2)nNHCOO-, -(CH2)nCONH(CH2)nO-, -(CH2)nO(CH2)nO-, -(CH2)nC(O)-, -(CH2)nNHCO(CH2)nO- и -(CH2)nCOO-, n представляет собой 0-2. Получение растворимой в воде соли липида формулы II состоит из: a. ковалентного соединения линкера с липидом формулы II; и b. реакции линкера, ковалентно соединенного с липидом, с основанием, которое представляет собой LiOH, NaOH, KOH, RbOH, CsOH, Mg(OH)2, Ca(OH)2, Sr(OH)2, Ba(OH)2, кислотой, такой как трифторуксусная кислота (TFA), или любой их комбинацией. Также предложены способ получения наночастицы и композиции для применения в химиотерапии. Предложенный способ обеспечивает выход >50% и чистоту >70% для конъюгированного с липидами платинового соединения. 3 н. и 41 з.п. ф-лы, 30 ил., 22 табл., 13 пр.
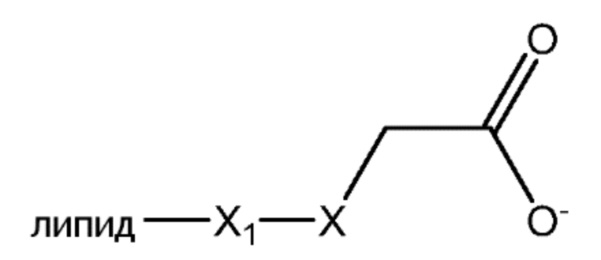 (формула II)
(формула II)
1. Способ получения конъюгированного с липидами платинового соединения, включающий:
реакцию растворимой в воде соли липида с растворимым в воде платиновым соединением в по существу водном растворе, получая конъюгированное с липидами платиновое соединение в виде осадка;
где растворимая в воде соль липида содержит соединение формулы II:
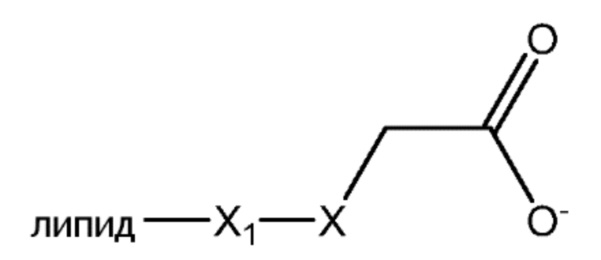 (формула II)
(формула II)
где
X представляет собой NH или N-CH2COO-,
X1 выбран из группы, состоящей из -(CH2)nO-, -(CH2)nNHCOO-, -(CH2)nCONH(CH2)nO-, -(CH2)nO(CH2)nO-, -(CH2)nC(O)-, -(CH2)nNHCO(CH2)nO- и -(CH2)nCOO-; и
n представляет собой 0-2,
характеризующийся тем, что получение растворимой в воде соли липида формулы II состоит из:
a. ковалентного соединения линкера с липидом формулы II; и
b. реакции линкера, ковалентно соединенного с липидом, с основанием, которое представляет собой LiOH, NaOH, KOH, RbOH, CsOH, Mg(OH)2, Ca(OH)2, Sr(OH)2, Ba(OH)2, кислотой, такой как трифторуксусная кислота (TFA), или любой их комбинацией, получая растворимую в воде соль липида формулы II;
где способ обеспечивает выход >50% для конъюгированного с липидами платинового соединения; и
где способ обеспечивает чистоту >70% для конъюгированного с липидами платинового соединения.
2. Способ по п. 1, дополнительно включающий стадию:
фильтрования или центрифугирования реакционной смеси, отделяя осадок от по существу водного раствора, и необязательно промывки осадка водой.
3. Способ по п. 1 или 2, дополнительно включающий стадию:
очистки конъюгированного с липидами платинового соединения, применяя ВЭЖХ.
4. Способ по любому из пп. 1-3, где чистоту конъюгированного с липидами платинового соединения определяют, применяя аналитическую ВЭЖХ на NH2, C18 или Phenyl колонке.
5. Способ по п. 3, где в ВЭЖХ очистке применяют препаративную обращено-фазовую колонку.
6. Способ по п. 5, где колонка содержит NH2 стационарную фазу, Phenyl стационарную фазу или C18 стационарную фазу.
7. Способ по любому из пп. 4-6, где колонка содержит NH2 или Phenyl стационарную фазу, и конъюгированное с липидами платиновое соединение элюируют, применяя градиентный способ.
8. Способ по п. 7, где градиентный способ включает элюирование подвижной фазой, содержащей смесь воды и метанола, где элюирование начинают смесью, содержащей большой процент воды и линейно изменяют со временем до смеси, имеющей большой процент метанола.
9. Способ по любому одному из пп. 4-6, где колонка содержит C18, и конъюгированное с липидами платиновое соединение элюируют, применяя изократический способ.
10. Способ по п. 9, где изократический способ включает элюирование подвижной фазой, содержащей 98% метанола и 2% воды.
11. Способ по любому из пп. 3-10, где стадия ВЭЖХ очистки обеспечивает чистоту >99,5% для конъюгированного с липидами платинового соединения.
12. Способ по любому из пп. 1-11, где способ обеспечивает выход >70% для конъюгированного с липидами платинового соединения.
13. Способ по любому из пп. 1-12, где по существу водный раствор содержит, по меньшей мере, 90% воды.
14. Способ по любому из пп. 1-12, где по существу водный раствор содержит, по меньшей мере, 95% воды.
15. Способ по любому из пп. 1-12, где по существу водный раствор содержит, по меньшей мере, 98% воды.
16. Способ по любому из пп. 1-12, где по существу водный раствор содержит, по меньшей мере, 99% воды.
17. Способ по любому из пп. 1-12, где по существу водный раствор содержит 100% воды.
18. Способ по любому из пп. 1-17, где реакцию проводят при комнатной температуре и при давлении приблизительно в одну атмосферу.
19. Способ по любому из пп. 1-18, где растворимая в воде соль липида представляет собой литиевую соль, натриевую соль, калиевую соль, рубидиевую соль, цезиевую соль, магниевую соль, кальциевую соль, стронциевую соль, бариевую соль, соль трифторуксусной кислоты (TFA) или любую их комбинацию.
20. Способ по любому из пп. 1-19, где растворимая в воде соль липида содержит липид, который представляет собой жир, воск, стерол, стероид, желчную кислоту(ы), жирорастворимый витамин, моноглицерид, диглицерид, фосфолипид, гликолипид, сульфолипид, аминолипид, хромолипид, глицерофосфолипид, сфинголипид, преноллипид, сахаролипид, поликетид, жирную кислоту или любую их комбинацию.
21. Способ по п. 20, где липид представляет собой холестерин или его производное.
22. Способ по п. 20, где липид представляет собой α-токоферол.
23. Способ по любому из пп. 1-22, где растворимое в воде платиновое соединение представляет собой формулу V:
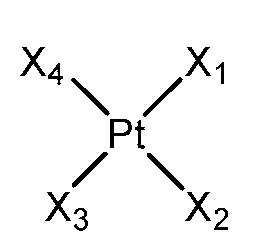 (V)
(V)
где
X1, X2, X3 и X4 независимо представляют собой галогенид, алкил, амин, алкиламин, диалкиламин, гидроксил, H2O, алкокси, тиол, тиоалкил, O-ацил или любую(ые) их комбинацию(и).
24. Способ по п. 23, где X1 и X2 представляют собой монодентатные или бидентатные лиганды.
25. Способ по п. 23 или 24, где X1 и X2 представляют собой амино.
26. Способ по любому из пп. 23-25, где X1 и X2 представляют собой диаминоциклогексил (DACH).
27. Способ по любому из пп. 23-26, где каждый X3 и X4 представляет собой H2O.
28. Способ по любому из пп. 23-27, где растворимое в воде платиновое соединение обеспечивают реакцией платинового соединения формулы V, где X1 и X2 содержит бидентатный аминолиганд, и каждый X3 и X4 содержит галогенид, с AgNO3 и H2O.
29. Способ по п. 28, где X1 и X2 представляют собой DACH, и каждый X3 и X4 представляет собой Cl.
30. Способ получения наночастицы, где способ включает:
смешение конъюгированного с липидом платинового соединения, полученного способом по любому одному из пп. 1-29, с солипидом в присутствии растворителя, получая наночастицу.
31. Способ по п. 30, где растворитель представляет собой хлороформ, метанол, дихлорметан, этанол или любую(ые) их комбинацию(и).
32. Способ по п. 30 или 31, где солипид представляет собой полностью гидрогенизированный соевый фосфатидилхолин (HSPC), аммониевую соль 1,2-дистеароил-sn-глицеро-3-фосфоэтаноламина-N-[метокси(полиэтиленгликоля)-2000] (DSPE-PEG2000), диолеоилфосфатидилхолин (DOPC), 1,2-дистеароил-sn-глицеро-3-фосфоэтаноламин (DSPE)-PEG-OMe, диолеоилфосфатидилэтаноламин (DOPE), дипальмитоилфосфатидилхолин (DPPC) или любую(ые) их комбинацию(и).
33. Способ по любому из пп. 30-32, где способ дополнительно включает стадии сушки, выдерживания и необязательного добавления стабилизатора.
34. Способ по п. 33, где стабилизатор представляет собой 1,2-дистеароил-sn-глицеро-3-фосфоэтаноламин (DSPE)-PEG-OMe, 1,2-дистеароил-sn-глицеро-3-фосфоэтаноламин (DSPE)-PEG-NH2, PEG, неорганическую соль, углевод или любую(ые) их комбинацию(и).
35. Способ по п. 34, где неорганическую соль представляет собой хлорид аммония, хлорид калия, хлорид натрия, гидрофосфат динатрия, дигидрофосфат натрия или любую их комбинацию(и).
36. Способ по п. 34, где углевод представляет собой глюкозу, декстрозу, сахарозу, трегалозу, маннитол, лактозу или любую(ые) их комбинацию(и).
37. Способ по любому из пп. 30-36, где солипиды включают гидрогенизированный соевый фосфатидилхолин и аммониевую соль 1,2-дистеароил-sn-глицеро-3-фосфоэтаноламин-N-[метокси(полиэтиленгликоля)-2000].
38. Способ по п. 30 или 37, где мол.% соотношение платинового соединения и солипидов составляет от 30:55:4 до 38:57:5.
39. Способ по любому из пп. 30-36, где солипиды включают гидрогенизированный соевый фосфатидилхолин, холестерин и аммониевую соль 1,2-дистеароил-sn-глицеро-3-фосфоэтаноламин-N-[метокси(полиэтиленгликоль)-2000].
40. Способ по п. 39, где мол.% соотношение платиновое соединение : HSPC : холестерин : аммониевая соль DSPE-PEG2000 представляет собой от 20:60:3:1 до приблизительно 35:70:15:5.
41. Композиция для применения в химиотерапии, содержащая конъюгированное с липидом платиновое соединение, полученное способом по любому одному из пп. 1-29, и DOPE.
42. Композиция по п. 41, где мол.% соотношение платинового соединения и DOPE составляет от приблизительно 20:30 до приблизительно 30:50.
43. Способ по п. 1, где конъюгированное с липидом платиновое соединение представляет собой конъюгированное с холестерином платиновое соединение, и конъюгированное с холестерином платиновое соединение получают
реакцией растворимой в воде соли холестерина с растворимым в воде платиновым соединением по существу в водном растворе, получая конъюгированное с холестерином платиновое соединение в виде осадка;
где растворимую в воде соль холестерина получают
a. реакцией холестерина или холестеринового производного с соединением, которое представляет собой:
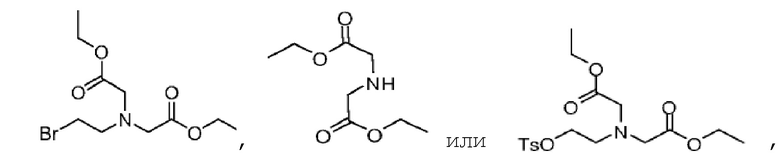
для получения
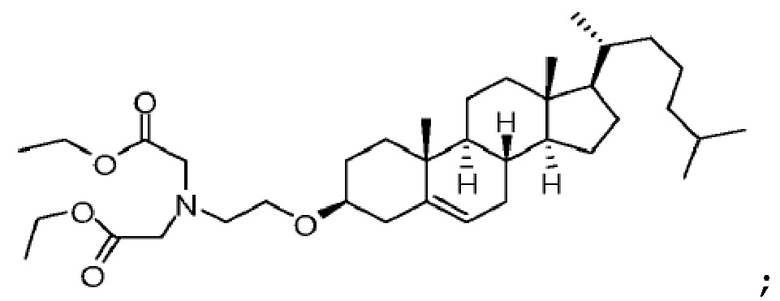 и
и
b. реакцией продукта, полученного на стадии a), с основанием, которое представляет собой LiOH, NaOH, KOH, RbOH, CsOH, Mg(OH)2, Ca(OH)2, Sr(OH)2, Ba(OH)2, кислотой, такой как трифторуксусная кислота (TFA), или любой их комбинацией, для получения растворимой в воде соли холестерина.
44. Способ по п. 1, где конъюгированное с липидами соединение платины представляет собой:
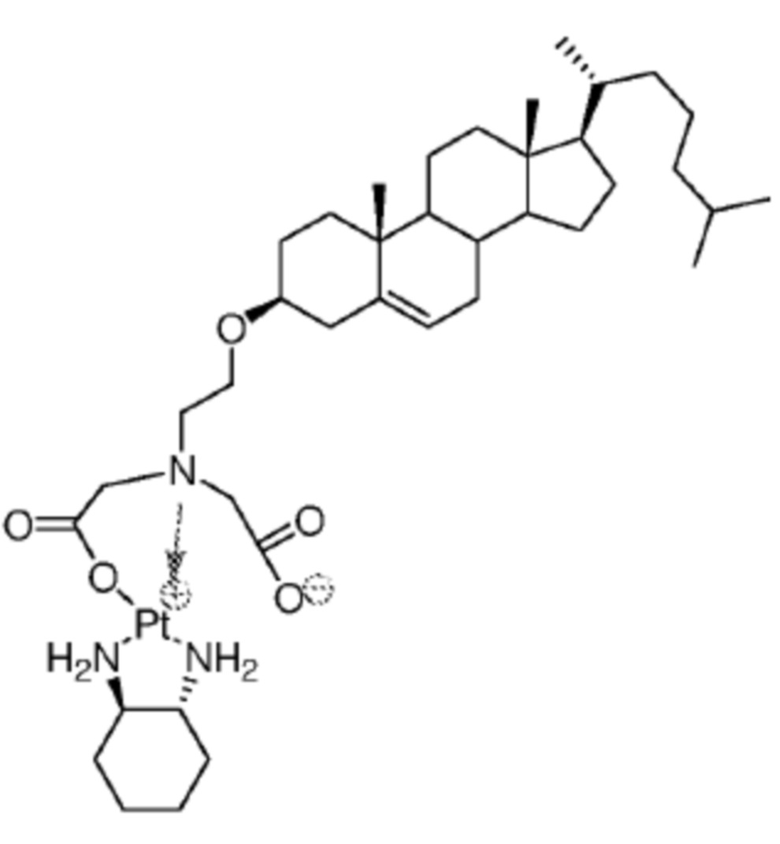
| WO 2014201376 A2, 18.12.2014 | |||
| WO 2014199352 A2, 18.12.2014 | |||
| WO 2010091192 A2, 12.08.2010 | |||
| SENGUPTA P | |||
| et al, Cholesterol-tethered platinum II - based supramolecular nanoparticle increases antitumor efficacy and reduces nephrotoxicity, Proceedings of the national academy of sciences, 2012, v | |||
| Шкив для канатной передачи | 1920 |
|
SU109A1 |
| Видоизменение прибора с двумя приемами для рассматривания проекционные увеличенных и удаленных от зрителя стереограмм | 1919 |
|
SU28A1 |
| Ртутный выпрямитель | 1927 |
|
SU11294A1 |
| ПЛАТИНОВЫЕ ФАРМАЦЕВТИЧЕСКИЕ СРЕДСТВА | 1990 |
|
RU2074861C1 |
Авторы
Даты
2023-05-02—Публикация
2016-05-18—Подача