Область техники, к которой относится изобретение
Настоящее изобретение относится к стабильным белкам F RSV и иммуногенным композициям, содержащим их, а также к способам применения иммуногенных композиций и композиций, содержащих белки F RSV.
Перекрестная ссылка на родственные заявки
Данная заявка заявляет приоритет на основании предварительной заявки на патент США № 62/623184, поданной 29 января 2018 г., содержание которой в полном объеме включено здесь посредством ссылки.
Представление списка последовательностей, поданного в электронном виде
Список последовательностей в настоящей заявке представляется в электронном виде через EFS-Web в виде списка последовательностей в формате ASCII с названием файла «24566WOPCT-SEQLIST-18JAN2019.TXT», с датой создания 18 января 2019 г. и размером 167 КБ. Данный список последовательностей, представленный через EFS-Web, является частью заявки и в полном объеме включен здесь посредством ссылки.
Уровень техники
Респираторно-синцитиальный вирус (RSV) является членом семейства пневмовирусов. Инфекция, вызванная RSV, представляет основную причину инфекции нижних дыхательных путей у детей младшего возраста и у пожилых людей (> 65 лет). В настоящее время отсутствует лицензированная вакцина, и терапевтические возможности ограничены.
Оболочка RSV содержит три поверхностных гликопротеина: F, G и SH. Белки G и F являются защитными антигенами и мишенями нейтрализующих антител. Однако F-белок является более консервативным среди штаммов и типов RSV (A и B). F RSV представляет собой вирусный слитый белок типа I, который структурно перестраивается из метастабильной формы «до слияния» в высокостабильную форму «после слияния». Несмотря на то, что мишени для нейтрализующих моноклональных антител находятся в конформации белка F «после слияния», ответная выработка нейтрализующих Ab в первую очередь нацелена на конформацию белка F «до слияния» у людей, естественно инфицированных RSV (Magro M et al., Proc. Natl. Acad. Sci. USA; 109(8): 3089-94, 2012; Ngwuta J.O. et al., Sci. Transl. Med., 2015; 7(309): 309ra162). Следовательно, сконструированный белок F RSV, стабилизированный в его конформации «до слияния», является привлекательной стратегией для разработки вакцинных антигенов F RSV. Например, ранее было показано, что рекомбинантный тример F RSV, включающий замены «DS-Cav1» (155C, 290C, 190F и 207L), индуцирует нейтрализующий иммунный ответ на животных моделях, который сильнее, чем ответ, наблюдаемый для белка F в конформации «после слияния» на основе иммуногенов F RSV (McLellan et al., Science, 342: 592-598, 2013). Здесь описаны новые антигены RSV, которые являются еще более стабильными в форме «до слияния», представляющей интерес.
Сущность изобретения
Настоящее изобретение относится к рекомбинантному тримеру F респираторно-синцитиального вируса (RSV), содержащему: три рекомбинантных пептида F RSV, каждый из которых содержит делецию аминокислот в положениях 98-146 F RSV дикого типа и линкер из восьми-четырнадцати аминокислот между аминокислотными положениями 97 и 147 F RSV дикого типа, где рекомбинантные F-пептиды содержат следующие модификации для стабилизации рекомбинантного тримера F RSV в конформации «до слияния»: (i) аминокислотные замены 190F и 207L, (ii) аминокислотные замены 155C и 290C, и одно (или более) из: (a) аминокислотных замен 486C и 490C; (b) аминокислотных замен 180C и 186C; (c) аминокислотных замен 486C и 489C; (d) аминокислотные замен 512C и 513C; (е) аминокислотной замены 505С; и (f) делеции аминокислот 482-513 F RSV дикого типа. В одном варианте осуществления каждый пептид F RSV дополнительно содержит на С-конце делецию трансмембранного домена и цистоплазматического домена F RSV дикого типа (например, содержит на С-конце делецию аминокислот 525-574 F RSV дикого типа). В дополнительном варианте осуществления каждый пептид F RSV содержит делецию аминокислот 514-574 F RSV дикого типа.
В одном варианте осуществления рекомбинантного тримера F RSV каждый из рекомбинантных F-пептидов дополнительно содержит последовательность фолдона на С-конце каждого пептида. В дополнительном варианте осуществления последовательность домена фолдона начинается у С-конца пептида и заменяет трансмембранный домен и цитоплазматический домен F RSV дикого типа (например, домен фолдона заменяет аминокислоты 525-574 F RSV). В дополнительном варианте осуществления последовательность домена фолдона начинается после аминокислотного положения 513 F RSV дикого типа (т.е. последовательность фолдона заменяет аминокислоты 514-574 F RSV дикого типа). В еще одном варианте осуществления, когда пептиды F RSV содержат дополнительную делецию аминокислот 482-513 F RSV дикого типа, то последовательность домена фолдона начинается после аминокислотного положения 481 F RSV дикого типа (см., например, SEQ ID NO: 44). В некоторых вариантах осуществления последовательность фолдона содержит SEQ ID NO: 8.
В одном варианте осуществления тримера F RSV каждый из рекомбинантных F-пептидов содержит аминокислотные замены 190F и 207L, аминокислотные замены 155C и 290C, аминокислотные замены 486C и 490C и делецию аминокислот 514-574 F RSV дикого типа. В одном варианте осуществления каждый рекомбинантный F-пептид дополнительно содержит ненативную внутрипептидную дисульфидную связь между цистеинами, введенными аминокислотными заменами 155C и 290C. В еще одном варианте осуществления тример F RSV содержит одну или несколько ненативных межпептидных дисульфидных связей между цистеинами, введенными аминокислотными заменами 486C и 490C. В дополнительном варианте осуществления С-конец каждого из рекомбинантных пептидов F RSV содержит последовательность домена фолдона. В еще одном варианте осуществления последовательность домена фолдона содержит SEQ ID NO: 8.
В одном варианте осуществления тримера F RSV каждый из рекомбинантных F-пептидов содержит аминокислотные замены 190F и 207L, аминокислотные замены 155C и 290C, аминокислотные замены 180C и 186C и делецию аминокислот 514-574 F RSV дикого типа. В одном варианте осуществления каждый рекомбинантный пептид F RSV дополнительно содержит ненативную внутрипептидную дисульфидную связь между цистеинами, введенными аминокислотными заменами 155C и 290C, и/или ненативную внутрипептидную дисульфидную связь между цистеинами, введенными аминокислотными заменами 190C и 186C. В дополнительном варианте осуществления С-конец каждого из рекомбинантных пептидов F RSV содержит последовательность домена фолдона. В еще одном варианте осуществления последовательность домена фолдона содержит SEQ ID NO: 8.
В одном варианте осуществления рекомбинантного тримера F RSV каждый из рекомбинантных F-пептидов содержит аминокислотные замены 190F и 207L, аминокислотные замены 155C и 290C, аминокислотные замены 486C и 489C и делецию аминокислот 514-574 из F RSV дикого типа. В одном варианте осуществления каждый рекомбинантный пептид F RSV дополнительно содержит ненативную внутрипептидную дисульфидную связь между цистеинами, введенными аминокислотными заменами 155C и 290C. В еще одном варианте осуществления тример F RSV содержит ненативную межпептидную дисульфидную связь между цистеинами, введенными аминокислотными заменами 486C и 489C. В дополнительном варианте осуществления С-конец каждого из рекомбинантных пептидов F RSV содержит последовательность домена фолдона. В еще одном варианте осуществления последовательность домена фолдона содержит SEQ ID NO: 8.
В одном варианте осуществления тримера RSV каждый из рекомбинантных F-пептидов содержит аминокислотные замены 190F и 207L, аминокислотные замены 155C и 290C, аминокислотные замены 512C и 513C и делецию аминокислот 514-574 F RSV дикого типа. В одном варианте осуществления каждый рекомбинантный пептид F RSV дополнительно содержит ненативную внутрипептидную дисульфидную связь между цистеинами, введенными аминокислотными заменами 155C и 290C. В еще одном варианте осуществления тример F RSV содержит ненативную межпептидную дисульфидную связь между цистеинами, введенными аминокислотными заменами 512C и 513C. В дополнительном варианте осуществления С-конец каждого из рекомбинантных пептидов F RSV содержит последовательность домена фолдона. В еще одном варианте осуществления последовательность домена фолдона содержит SEQ ID NO: 8.
В одном варианте осуществления рекомбинантного тримера F RSV каждый из рекомбинантных F-пептидов содержит аминокислотные замены 190F и 207L, аминокислотные замены 155C и 290C, аминокислотную замену 505C и делецию аминокислот 514-574 F RSV дикого типа. В еще одном варианте осуществления каждый рекомбинантный пептид F RSV дополнительно содержит ненативную внутрипептидную дисульфидную связь между цистеинами, введенными аминокислотными заменами 155C и 290C. В дополнительном варианте осуществления С-конец каждого из рекомбинантных пептидов F RSV содержит последовательность домена фолдона. В еще одном варианте осуществления последовательность домена фолдона содержит SEQ ID NO: 8.
В одном варианте осуществления рекомбинантного тримера F RSV каждый из рекомбинантных F-пептидов содержит аминокислотные замены 190F и 207L, аминокислотные замены 155C и 290C и делецию аминокислот 482-513 F RSV дикого типа, а также делецию аминокислот 514-574 F RSV дикого типа. В одном варианте осуществления каждый рекомбинантный пептид F RSV дополнительно содержит ненативную внутрипептидную дисульфидную связь между цистеинами, введенными аминокислотными заменами 155C и 290C. В дополнительном варианте осуществления С-конец каждого из рекомбинантных пептидов F RSV содержит последовательность домена фолдона. В еще одном варианте осуществления последовательность домена фолдона содержит SEQ ID NO: 8.
В одном варианте осуществления линкер имеет длину из восьми (8), десяти (10), двенадцати (12) или четырнадцати (14) аминокислот. В одном варианте осуществления линкер содержит аминокислотную последовательность, представленную в SEQ ID NO: 46. В еще одном варианте осуществления линкер имеет аминокислотную последовательность, представленную в любой из SEQ ID NO: 1, 2, 3 или 4.
В одном варианте осуществления каждый из рекомбинантных F-пептидов тримера F RSV содержит, состоит по существу из или состоит из зрелой аминокислотной последовательности, представленной в SEQ ID NO: 22. В одном варианте осуществления рекомбинантные F-пептиды каждого тримера F RSV содержат, состоят по существу из или состоят из зрелой аминокислотной последовательности, представленной в SEQ ID NO: 24. В одном варианте осуществления рекомбинантные F-пептиды каждого тримера F RSV содержат, состоят по существу из или состоят из зрелой аминокислотной последовательности, представленной в SEQ ID NO 26. В одном варианте осуществления рекомбинантные F-пептиды каждого тримера F RSV содержат, состоят по существу из или состоят из зрелой аминокислотной последовательности, представленной в SEQ ID NO 28. В одном варианте осуществления рекомбинантные F-пептиды каждого тримера F RSV содержат, состоят по существу из или состоят из зрелой аминокислотной последовательности, представленной в SEQ ID NO: 30. В одном варианте осуществления рекомбинантные F-пептиды каждого тримера F RSV содержат, состоят по существу из или состоят из зрелой аминокислотной последовательности, представленной в SEQ ID NO: 44.
Настоящее изобретение также относится к иммуногенной композиции RSV, содержащей рекомбинантный тример (RSV) F респираторно-синцитиального вируса, содержащий три рекомбинантных пептида F RSV, каждый из которых содержит делецию аминокислот в положениях 98-146 F RSV дикого типа и линкер из восьми-четырнадцати аминокислот между аминокислотными положениями 97 и 147 F RSV дикого типа, где рекомбинантные F-пептиды включают следующие модификации для стабилизации рекомбинантного тримера F RSV в конформации «до слияния»: (i) аминокислотные замены 190F и 207L, (ii) аминокислотные замены 155C и 290C и одно (или более) из (a) аминокислотных замен 486C и 490C; (b) аминокислотных замен 180C и 186C; (c) аминокислотных замен 486C и 489C; (d) аминокислотных замен 512C и 513C; (е) аминокислотной замены 505С; и (f) делеции аминокислот 482-513 F RSV дикого типа. В одном варианте осуществления каждый пептид F RSV дополнительно содержит на С-конце делецию трансмембранного домена и цистоплазматического домена F RSV дикого типа (например, содержит на С-конце делецию аминокислот 525-574 F RSV дикого типа). В дополнительном варианте осуществления каждый пептид F RSV содержит делецию аминокислот 514-574 F RSV дикого типа.
В одном варианте осуществления иммуногенной композиции каждый из рекомбинантных F-пептидов дополнительно содержит последовательность фолдона на С-конце каждого пептида. В дополнительном варианте осуществления последовательность домена фолдона начинается после аминокислотного положения 513 F RSV дикого типа (т.е. последовательность фолдона заменяет аминокислоты 514-574 F RSV дикого типа). В еще одном варианте осуществления, когда пептиды F RSV содержат дополнительную делецию аминокислот 482-513 F RSV дикого типа, то последовательность домена фолдона начинается после аминокислотного положения 481 F RSV дикого типа (см., например, SEQ ID NO: 44). В некоторых вариантах осуществления последовательность фолдона содержит SEQ ID NO: 8.
В одном варианте осуществления иммуногенной композиции тример F RSV представляет любой из тримеров RSV, описанных здесь. В еще одном варианте иммуногенной композиции рекомбинантные F-пептиды каждого тримера F RSV содержат, состоят по существу из или состоят из зрелой аминокислотной последовательности, представленной в любой из SEQ ID NO: 22, 24, 26, 28, 30 и 44.
Настоящее изобретение также относится к пептиду RSV, который включает делецию аминокислот в положениях 98-146 F RSV дикого типа и линкер из восьми-четырнадцати аминокислот между положениями 97 и 147 F RSV дикого типа, и дополнительные модификации для стабилизации рекомбинантного тримера F RSV, содержащего три таких рекомбинантных пептида RSV в конформации «до слияния». Такие дополнительные модификации в одноцепочечном пептиде RSV включают: (i) аминокислотные замены 190F и 207L, (ii) аминокислотные замены 155C и 290C и одно (или более) из (a) аминокислотных замен 486C и 490C; (b) аминокислотных замен 180C и 186C; (c) аминокислотных замен 486C и 489C; (d) аминокислотных замен 512C и 513C; (е) аминокислотной замены 505С; и (f) делецию аминокислот 482-513 F RSV дикого типа. В одном варианте осуществления пептид F RSV дополнительно содержит на С-конце делецию трансмембранного домена и цистоплазматического домена F RSV дикого типа (например, содержит на С-конце делецию аминокислот 525-574 F RSV дикого типа). В дополнительном варианте осуществления пептид F RSV включает делецию аминокислот 514-574 F RSV дикого типа.
В одном варианте осуществления пептид F RSV дополнительно содержит последовательность фолдона на С-конце. В дополнительном варианте осуществления последовательность домена фолдона начинается после аминокислотного положения 513 F RSV дикого типа (т.е. последовательность фолдона заменяет аминокислоты 514-574 RSV-F дикого типа). В еще одном варианте осуществления, когда пептид F RSV содержит дополнительную делецию аминокислот 482-513 F RSV дикого типа, то последовательность домена фолдона начинается после аминокислотного положения 482 F RSV дикого типа (см., например, SEQ ID NO: 44). В некоторых вариантах осуществления последовательность фолдона содержит SEQ ID NO: 8.
В одном варианте осуществления пептид F RSV содержит аминокислотные замены 190F и 207L, аминокислотные замены 155C и 290C, аминокислотные замены 486C и 490C и делецию аминокислот 514-574 F RSV дикого типа. В еще одном варианте осуществления пептид F RSV дополнительно содержит ненативную внутрипептидную дисульфидную связь между цистеинами, введенными аминокислотными заменами 155С и 290С. В дополнительном варианте осуществления С-конец пептида F RSV содержит последовательность домена фолдона. В еще одном варианте осуществления последовательность домена фолдона содержит SEQ ID NO: 8.
В одном варианте осуществления пептид F RSV включает аминокислотные замены 190F и 207L, аминокислотные замены 155C и 290C, аминокислотные замены 180C и 186C и делецию аминокислот 514-574 F RSV дикого типа. В еще одном варианте осуществления пептид F RSV дополнительно содержит ненативную внутрипептидную дисульфидную связь между цистеинами, введенными аминокислотными заменами 155С и 290С, и/или ненативную внутрипептидную дисульфидную связь между цистеинами, введенными аминокислотными заменами 190С и 186С. В дополнительном варианте осуществления С-конец пептида F RSV содержит последовательность домена фолдона. В еще одном варианте осуществления последовательность домена фолдона содержит SEQ ID NO: 8.
В одном варианте осуществления пептид F RSV содержит аминокислотные замены 190F и 207L, аминокислотные замены 155C и 290C, аминокислотные замены 486C и 489C и делецию аминокислот 514-574 F RSV дикого типа. В еще одном варианте осуществления пептид F RSV дополнительно содержит ненативную внутрипептидную дисульфидную связь между цистеинами, введенными аминокислотными заменами при 155С и 290С. В дополнительном варианте осуществления С-конец пептида F RSV содержит последовательность домена фолдона. В еще одном варианте осуществления последовательность домена фолдона содержит SEQ ID NO: 8.
В одном варианте осуществления пептид F RSV включает аминокислотные замены 190F и 207L, аминокислотные замены 155C и 290C, аминокислотные замены 512C и 513C и делецию аминокислот 514-574 F RSV дикого типа. В еще одном варианте осуществления пептид F RSV дополнительно содержит ненативную внутрипептидную дисульфидную связь между цистеинами, введенными аминокислотными заменами при 155С и 290С. В дополнительном варианте осуществления С-конец пептида F RSV содержит последовательность домена фолдона. В еще одном варианте осуществления последовательность домена фолдона содержит SEQ ID NO: 8.
В одном варианте осуществления пептид F RSV содержит аминокислотные замены 190F и 207L, аминокислотные замены 155C и 290C, аминокислотную замену 505C и делецию аминокислот 514-574 F RSV дикого типа. В еще одном варианте осуществления пептид F RSV дополнительно содержит ненативную внутрипептидную дисульфидную связь между цистеинами, введенными аминокислотными заменами 155С и 290С. В дополнительном варианте осуществления С-конец пептида F RSV содержит последовательность домена фолдона. В еще одном варианте осуществления последовательность домена фолдона содержит SEQ ID NO: 8.
В одном варианте осуществления пептид F RSV включает аминокислотные замены 190F и 207L, аминокислотные замены 155C и 290C и делецию аминокислот 482-513 F RSV дикого типа, а также делецию аминокислот 514-574 F RSV дикого типа. В одном варианте осуществления пептид F RSV дополнительно содержит ненативную внутрипептидную дисульфидную связь между цистеинами, введенными аминокислотными заменами 155C и 290C. В дополнительном варианте осуществления каждый С-конец каждого пептида F RSV содержит последовательность домена фолдона. В еще одном варианте осуществления последовательность домена фолдона содержит SEQ ID NO: 8.
В одном варианте осуществления линкер имеет длину из восьми (8), десяти (10), двенадцати (12) или четырнадцати (14) аминокислот. В одном варианте осуществления линкер содержит аминокислотную последовательность, представленную в SEQ ID NO: 46. В еще одном варианте осуществления линкер имеет аминокислотную последовательность, представленную в любой из SEQ ID NO: 1, 2, 3 или 4.
В одном варианте осуществления пептид F RSV содержит, состоит по существу из или состоит из зрелой аминокислотной последовательности, представленной в SEQ ID NO: 22. В одном варианте осуществления пептид F RSV содержит, состоит по существу из или состоит из зрелой аминокислотной последовательности, представленной в SEQ ID NO: 24. В одном варианте осуществления пептид F RSV содержит, состоит по существу из или состоит из зрелой аминокислотной последовательности, представленной в SEQ ID NO 26. В одном варианте осуществления пептид F RSV содержит, состоит по существу из или состоит из зрелой аминокислотной последовательности, представленной в SEQ ID NO 28. В одном варианте осуществления пептид F RSV содержит, состоит по существу из или состоит из зрелой аминокислотной последовательности, представленной в SEQ ID NO: 30. В одном варианте осуществления пептид F RSV содержит, состоит по существу из или состоит из зрелой аминокислотной последовательности, представленной в SEQ ID NO: 44.
В одном варианте осуществления пептид RSV при получении рекомбинантно образует тример F RSV, как здесь описано.
Настоящее изобретение также обеспечивает выделенную молекулу нуклеиновой кислоты, кодирующую одноцепочечный пептид RSV, как здесь описано. В одном варианте осуществления выделенная молекула нуклеиновой кислоты представляет молекулу ДНК. Настоящее изобретение дополнительно обеспечивает вектор, содержащий указанную молекулу нуклеиновой кислоты.
Настоящее изобретение также обеспечивает способ получения рекомбинантного тримера (RSV) F респираторно-синцитиального вируса, как здесь описано, где указанный способ включает (i) экспрессию молекулы нуклеиновой кислоты или вектора, каждый из которых описан выше, и (ii) очистку рекомбинантного тримера F RSV, полученного из них.
Настоящее изобретение также относится к молекулам антител, включающим полноразмерные антитела и производные антител, направленные против тримера F RSV, описанного здесь, или против пептидов F RSV, описанных здесь.
В некоторых вариантах иммуногенную композицию формулируют с адъювантом. В одном варианте адъювант представляет адъювант на основе соединения алюминия. В некоторых вариантах осуществления адъювант на основе соединения алюминия представляет MAA или MAPA.
В некоторых вариантах осуществления рекомбинантный тример F RSV или пептиды F RSV, каждый из которых здесь описан, формулируют в виде липидной наночастицы (LNP), содержащей катионный липид, ПЭГ-модифицированный липид, стерол и некатионный липид.
Некоторые варианты осуществления настоящего изобретения обеспечивают способы индукции F RSV-специфического иммунного ответа у субъекта, включающие введение субъекту любой из иммуногенных композиций, описанных здесь, или рекомбинантных тримеров F RSV, описанных здесь, в количестве, эффективном для получения F RSV-специфического иммунного ответа. В некоторых вариантах осуществления антигенспецифический иммунный ответ включает Т-клеточный ответ или В-клеточный ответ.
В некоторых вариантах осуществления способ включает введение субъекту однократной дозы (без бустер-дозы) иммуногенной композиции или тримера F RSV, как здесь описано. В еще одном варианте осуществления способ дополнительно включает введение субъекту второй (бустер) дозы иммуногенной композиции или тримера F RSV, как здесь описано. В еще одном варианте осуществления способ дополнительно включает введение, по меньшей мере, одной бустер-дозы тримера F RSV или иммуногенной композиции RSV. Могут быть введены дополнительные дозы.
В некоторых вариантах осуществления иммуногенную композицию RSV или тример F RSV вводят субъекту внутрикожной инъекцией, внутримышечной инъекцией или интраназальным введением. В некоторых вариантах осуществления вакцину против RSV вводят субъекту внутримышечной инъекцией.
В некоторых вариантах осуществления тример F RSV или иммуногенная композиция придает иммунитет субъекту против RSV в течение 1 или 2 лет. В некоторых вариантах осуществления тример F RSV или иммуногенная композиция придает иммунитет субъекту против RSV в течение более 2 лет, более 3 лет, более 4 лет или в течение 5-10 лет. В одном варианте иммуногенную композицию вводят в виде вакцины ежегодно.
В некоторых вариантах возраст субъекта составляет примерно 5 лет или младше. Например, субъект может находиться в возрасте примерно от 1 года до примерно 5 лет (например, примерно 1, 2, 3, 4 или 5 лет) или в возрасте примерно от 6 месяцев до примерно 1 года (например, примерно 6, 7, 8, 9, 10, 11 или 12 месяцев). В некоторых вариантах осуществления возраст субъект составляет примерно 12 месяцев или младше (например, 12, 11, 10, 9, 8, 7, 6, 5, 4, 3, 2 месяца или 1 месяц). В некоторых вариантах возраст субъекта составляет примерно 6 месяцев или младше.
В некоторых вариантах субъект был рожден в срок (например, примерно на 37-42 неделе беременности). В некоторых вариантах субъект был рожден преждевременно, например, примерно на 36 неделе беременности или раньше (например, примерно на 36, 35, 34, 33, 32, 31, 30, 29, 28, 27, 26 или 25 неделе). Например, субъект, возможно, родился примерно на 32 неделе беременности или раньше. В некоторых вариантах субъект был рожден преждевременно между примерно 32 и примерно 36 неделями беременности. Таким субъектам вакцину можно вводить в более старшем возрасте, например, в возрасте примерно от 6 месяцев до примерно 5 лет или старше.
В некоторых вариантах осуществления субъект представляет собой молодого человека в возрасте примерно от 20 лет до примерно 50 лет (например, в возрасте примерно 20, 25, 30, 35, 40, 45 или 50 лет).
В некоторых вариантах осуществления субъект представляет собой пожилого субъекта в возрасте примерно 50-60 лет, 60 лет, примерно 70 лет или старше, 80 лет или старше, 90 лет или старше (например, примерно в возрасте 60, 65, 70, 75, 80, 85 или 90 лет). В некоторых вариантах осуществления субъект страдает иммунодефицитом (например, имеет иммунное расстройство или аутоиммунное заболевание).
В некоторых вариантах осуществления субъект-женщина беременна, когда ей вводят иммуногенную композицию RSV. В некоторых вариантах осуществления у субъекта имеет место хроническое заболевание легких, такое как хроническая обструктивная болезнь легких (ХОБЛ) или астма.
В некоторых вариантах осуществления субъект подвергался воздействию RSV, заражен (имеет) инфекцию RSV или подвергается риску заражения RSV.
Детали различных вариантов осуществления изобретения изложены в нижеприведенном описании. Другие признаки, объекты и преимущества раскрытия будут очевидны из описания и формулы изобретения.
Краткое описание фигур
Вышеуказанные и другие цели, признаки и преимущества будут очевидны из последующего описания конкретных вариантов осуществления изобретения, как показано на прилагаемых фигурах, на которых одинаковые ссылочные признаки относятся к одним и тем же частям в разных видах. Фигуры не обязательно выполнены в масштабе, вместо этого акцент делается на иллюстрации принципов различных вариантов осуществления изобретения.
На фиг.1А и 1В показано связывание свежесобранных клеточных культуральных супернатантов (supe) на сутки 7 после трансфекции LZF40 (DS-Cav1 с линкером из 8 аминокислот) (фиг. 1А) или тех, которые хранили при 4°С в течение 8 суток (фиг. 1В) с моноклональными антителами D25 и Synagis® (паливизумабом).
На фиг.2A-2F показано связывание свежесобранных клеточных культуральных супернатантов (supe) на сутки 3 после трансфекции LZF55(F55), LZF56(F56) и LZF57(F57) (DS-Cav1 с линкером из 10, 12 или 14 аминокислот соответственно; фиг.2А, 2В и 2С соответственно) или тех, которые хранили при 4°С в течение 7 суток (фиг. 2D, 2E и 2F соответственно) с D25 и Synagis® (паливизумабом).
На фиг.3 приведены результаты вестерн-блоттинга с анти-F RSV сывороткой для одноцепочечных мутантов RSV LZF55, LZF56 и LZF57 в сравнении с DS-Cav1.
На фиг.4А-4С показано связывание свежесобранных клеточных культуральных супернатантов DS-Cav1 (фиг. 4А), LZF57 (фиг. 4В) или LZF111 (фиг. 4С) с моноклональными антителами D25 и 4D7, как определено методом ELISA. На фиг. 4D показаны очищенные DS-Cav1, F57 и F111, анализированные с помощью SDS-PAGE в восстанавливающих (R) и невосстанавливающих (NR) условиях.
На фиг.5А и 5В приведены CD спектры LZF111 и DS-Cav1 соответственно.
На фиг. 6 приведены результаты анализа вторичной структуры посредством реконструкции CD спектров (от 185 до 260 нм) DS-Cav1 и LZF111 с использованием с использованием искусственной нейронной сети с обучением для CD спектров белков с разрешенной трехмерной структурой.
На фиг.7 показана термостабильность очищенных LZF111 и DS-Cav1, анализированных с помощью дифференциальной сканирующей флуориметрии (DSF).
На фиг.8А-8Е показана долговременная стабильность очищенного белка DS-Cav1 или LZF111, хранившегося в замороженном виде или при 4°С в течение 1 (фиг. 8А-8С), 2 (фиг. 8D) или 3 (фиг. 8Е) месяцев, по оценке связывания с D25, 4D7 и Synagis® (паливизумабом) в анализе связывания ELISA.
На фиг.9A и 9B показаны титры ED10 ELISA сывороток мышей PD2 против F-белка в конформации «до слияния» (фиг. 9A) и титры нейтрализации сыворотки мышей PD2 против штамма RSV Long (фиг. 9B). Горизонтальная пунктирная линия обозначает предел детектирования. Данные показывают, что LZF111 индуцировал сходные уровни нейтрализующих антител с DS-Cav1 в разных дозах.
На фиг.10 приведена принципиальная схема LZF111 (вверху), DS-Cav1 (в центре) и LZF57 (внизу).
На фиг.11 представлены титры сывороточных нейтрализующих антител (индивидуальные значения NT50 и GMT с доверительными интервалами 95%) против RSV A, индуцированные у хлопковых крыс мРНК-вакцинами и контрольными составами.
На фиг.12 представлены титры сывороточных антител в конкурентном ELISA (индивидуальные значения IT50 и GMT с 95% доверительными интервалами) для D25 (сайт Ø), паливизумаба (сайт II) и 4D7 (сайт I), измеренных на сутки 56 (4 недели PD2).
На фиг.13 показано содержание RSV в легких и носовой полости после заражения хлопковых крыс RSV A.
На фиг.14 представлены титры сывороточных нейтрализующих антител (индивидуальные значения NT50 и GMT с доверительными интервалами 95%) против RSV A, индуцированных у африканских зеленых мартышек мРНК-вакцинами и контрольными составами.
На фиг.15 представлены титры сывороточных антител в конкурентном ELISA (индивидуальные значения IT50 и GMT с 95% доверительными интервалами) для D25 (сайт Ø), паливизумаба (сайт II) и 4D7 (сайт I), измеренных на неделе 10 (2 недели PD3).
На фиг.16A-16C показано содержание RSV в бронхоальвеолярном лаваже (BAL) после заражения AGM. На фиг. 16А представлена иммунизация в высокой дозе. На фиг. 16В представлена иммунизация в низкой дозе. На фиг. 16 C показана площадь под кривой.
На фиг.17А-17С показано содержание RSV в мазках из носовой полости после заражения AGM. На фиг. 17А представлена иммунизация в высокой дозе. На фиг. 17В представлена иммунизация в низкой дозе. На фиг. 17 C показана площадь под кривой.
На фиг.18 приведены титры сывороточных нейтрализующих антител (индивидуальные значения NT50 и GMT с доверительными интервалами 95%) против RSV A, индуцированных у опытных африканских зеленых мартышек мРНК-вакцинами и контрольными составами..
На фиг.19 приведены титры сывороточных антител в конкурентном ELISA (индивидуальные значения IT50 и GMT с 95% доверительными интервалами) для D25 (сайт Ø), паливизумаба (сайт II) и 4D7 (сайт I), измеренных на неделе 10 (2 недели PD3).
Подробное описание изобретения
Белок F RSV представляет собой слитый гликопротеин I типа, который является довольно консервативным среди клинических изолятов, включая антигенные подгруппы RSV-A и RSV-B. Белок F переходит между состоянием «до слияния» и более стабильным состоянием «после слияния», тем самым облегчая проникновение в клетки-мишени. Гликопротеин F RSV первоначально синтезируется в виде белка-предшественника F0. F RSV0 превращается в тример, который активируется расщеплением фурином с превращением в зрелый белок «до слияния», содержащий субъединицы F1 и F2 (Bolt, et al., Virus Res., 68:25, 2000). Белок F RSV, стабилизированный в конформации «до слияния», вызывает высокий нейтрализующий иммунный ответ на животных моделях, чем ответ, который наблюдается с белком F RSV, стабилизированным в конформации «после слияния» (McLellan et al., Science, 342: 592-598, 2013). Таким образом, стабилизированные белки F RSV «до слияния» являются хорошими кандидатами для включения в вакцину против RSV. Растворимые эктодомены RSV, стабилизированные в конформации «до слияния», были получены ранее, включающие замены «DS-Cav1». См. WO 2014/160463A1 и WO 2017/172890A1, содержание каждой из которых включено здесь посредством ссылки.
Ранее было показано, что стабилизированный конструкт с формой «до слияния» F RSV, DS-Cav1, претерпевает конформационные изменения и образует промежуточные структуры при длительном хранении при 4°C (Flynn JA et al., PLoS ONE, 2016; 11 (10): e0164789). Долговременная стабильность при 4°C или выше является желательным свойством для субъединичного вакцинного антигена F RSV. Здесь описаны дополнительные модификации на основе структуры для дальнейшего повышения стабильности тримера F RSV в конформации «до слияния». Такие конструкты обладают повышенной стабильностью при 4°C по сравнению с DS-Cav1, сохраняя при этом иммуногенность.
Термины «слитый белок RSV» и «белок F RSV», используемые здесь, относятся к гликопротеину оболочки RSV, который способствует слиянию вирусных и клеточных мембран. В природе белок F RSV синтезируется в виде одного полипептидного предшественника, обозначаемого F0, который включает сигнальный пептид, который направляет локализацию в эндоплазматический ретикулум, где сигнальный пептид отщепляется. Оставшиеся остатки F0 олигомеризуются с образованием тримера и подвергаются протеолитическому процессированию протеазой с двумя консервативными последовательностями расщепления фурином с образованием двух фрагментов, F1 и F2, связанных дисульфидной связью. В природе три пептида F2-F1 олигомеризуются в тример с образованием зрелого белка F, который принимает метастабильную конформацию «до слияния» и может претерпевать изменение конформации с превращением в конформацию «после слияния».
«Трансмембранный домен F RSV» соответствует трансмембранному домену F RSV дикого типа (т.е. аминокислотам 525-550 из SEQ ID NO: 10).
«Цитоплазматический домен F RSV» или «цитоплазматический хвост F RSV» соответствует цитоплазматическому хвостовому домену F RSV дикого типа (т.е. аминокислотам 551-574 SEQ ID NO: 10).
«Антитело D25» или «D25» в контексте настоящего описания описывает нейтрализующее антитело, которое специфически связывается с пептидами F RSV с конформацией «до слияния». Это антитело описано в публикации заявки на патент США № 2010/0239593, полное содержание которой включено здесь посредством ссылки.
«Одноцепочечные мутанты RSV» относятся к белку F RSV, который был модифицирован таким образом, что он не включает сайты расщепления фурином, так что, когда в клетках продуцируется одноцепочечный мутант RSV, то пептид F0 не расщепляется на отдельные цепи F1 и F2. Неограничивающий пример одноцепочечного мутанта RSV включает положение 97 полипептида F2, связанного с положением 97-147 пептида F1 гибким линкером, для генерирования одноцепочечного мутанта RSV.
Замены «DS-CAV1»; «DS-Cav1», каждая из которых используется в настоящем документе, относятся к генетическим модификациям белка F RSV, который содержит замены «DS» 155C и 290C, для введения ненативной дисульфидной связи между цистеинами, введенными заменами (такими как как замены S155C и S290C) и замены «Cav1», которые включают аминокислотные замены, заполняющие полость 190F и 207L (такие как S190F и V207L). DS-Cav1 описана в WO 2014/160463, полное содержание которой включено здесь посредством ссылки.
Термины «домен фолдона» или «фолдон», каждый из которых используется здесь, относится к домену тримеризации фибритина бактериофага Т4, который содержит аминокислотную последовательность, которая естественным образом образует тримерную структуру. В некоторых примерах последовательность белка F RSV модифицирована так, чтобы она содержала домен фолдона. В других примерах одноцепочечные мутанты RSV содержат домен фолдона. Пример тримеризации домена фолдона включает аминокислотную последовательность, представленную в SEQ ID NO: 8.
В данном контексте «сигнальный пептид» или «сигнальная последовательность» представляют собой короткие аминокислотные последовательности, которые направляют вновь синтезированные секреторные или мембранные белки к мембранам и через них и, таким образом, универсально контролируют поступление большинства белков как у эукариот, так и прокариот на секреторный путь. В результате процессинга в эндоплазматическом ретикулуме образуются зрелые белки, в которых сигнальный пептид отщепляется от белков-предшественников. Как здесь указано, «зрелая аминокислотная последовательность» не содержит сигнального пептида. Зрелая аминокислотная последовательность одноцепочечных мутантов RSV не содержит сигнального пептида. Кроме того, тример RSV, который состоит из трех зрелых одноцепочечных мутантов RSV, не содержит сигнальной пептидной последовательности.
Как здесь используется, термин «замена», «аминокислотная замена» или «вариант замены» применительно к полипептидам означает таковые, которые имеют по меньшей мере один аминокислотный остаток в нативной или исходной последовательности, удаленный и замененный на другую аминокислоту, вставленную на его место в том же положении. Замены могут быть единичными, когда только одна аминокислота в молекуле была заменена, или они могут быть множественными, где две или более (например, 3, 4 или 5) аминокислоты были заменены в одной и той же молекуле. Например, как здесь используется, ссылка на замену «155C» в белке F RSV или одноцепочечном мутанте F RSV относится к одноцепочечному белку F RSV, имеющему остаток цистеина в положении 155, где этот остаток цистеина был заменен на соответствующий нативный остаток в положении 155 в белке F RSV. В качестве ссылки, SEQ ID NO: 10 является референсной последовательностью в отношении положения замены. Например, замена «S155C» представляет замену S в положении 155 SEQ ID NO: 10 на C.
«Выделенные» полипептиды или полинуклеотиды, по меньшей мере, частично не содержат других биологических молекул из клеток или клеточных культур, в которых они продуцируются. Такие биологические молекулы включают другие нуклеиновые кислоты, белки, липиды, углеводы или другой материал, такой как клеточный дебрис и культуральную среду. Кроме того, они могут, по меньшей мере, частично не содержать компонентов экспрессионной системы, таких как биологические молекулы из клетки-хозяина или ее культуральной среды. Как правило, термин «выделенный» не предназначен для обозначения полного отсутствия таких биологических молекул или отсутствия воды, буферов или солей или компонентов фармацевтического состава, который включает полипептиды или полинуклеотиды.
«Вариант полипептида» представляет собой молекулу, которая отличается по своей аминокислотной последовательности относительно нативной последовательности или референсной последовательности. Варианты аминокислотной последовательности могут иметь замены, делеции, вставки или комбинацию любых двух или трех из вышеуказанных в определенных положениях в аминокислотной последовательности по сравнению с нативной последовательностью или референсной последовательностью. Обычно варианты обладают по меньшей мере 50% идентичностью относительно нативной последовательности или референсной последовательности. В некоторых вариантах варианты имеют, по меньшей мере, 80% идентичность или, по меньшей мере, 90% идентичность с нативной последовательностью или референсной последовательностью.
Под «аналогами» понимаются варианты полипептидов, которые отличаются одной или несколькими аминокислотными изменениями, например, заменами, добавлениями или делециями аминокислотных остатков, которые все еще сохраняют одно или более свойств родительского или исходного полипептида.
Настоящее изобретение обеспечивает несколько типов композиций на основе полинуклеотидов или полипептидов, включая варианты и производные. К ним относятся, например, замещающие, инсерционные, делеционные и ковалентные варианты и производные. Термин «производное» является синонимом термина «вариант» и, как правило, относится к молекуле, которая была модифицирована и/или изменена каким-либо образом относительно референсной молекулы или исходной молекулы.
Как таковые, полинуклеотиды, кодирующие пептиды или полипептиды, содержащие замены, вставки и/или добавления, делеции и ковалентные модификации относительно референсных последовательностей, в частности полипептидных последовательностей, раскрытых здесь, включаются в объем настоящего раскрытия. Например, последовательности меток или аминокислоты, такие как один или более лизинов, могут быть добавлены к пептидным последовательностям (например, на N-конце или С-конце). Последовательности меток можно использовать для детектирования, очистки или установления локализации пептидов. Лизины можно использовать для повышения растворимости пептидов или для обеспечения биотинилирования. Альтернативно, аминокислотные остатки, расположенные в карбокси- и аминоконцевых областях аминокислотной последовательности пептида или белка, могут быть необязательно делецированы с обеспечением усеченных последовательностей. Некоторые аминокислоты (например, С-концевые остатки или N-концевые остатки) альтернативно могут быть делецированы в зависимости от применения последовательности, например, экспрессии последовательности в виде части большей последовательности, которая является растворимой или связанной с твердой подложкой.
Как здесь используется, термин «консервативная аминокислотная замена» относится к аминокислотной замене, которая обычно присутствует в последовательности, на другую аминокислоту аналогичного размера, заряда или полярности. Примеры консервативных замен включают замену неполярного (гидрофобного) остатка, такого как остаток изолейцина, валина и лейцина, на другой неполярный остаток. Аналогично, примеры консервативных замен включают замену одного полярного (гидрофильного) остатка на другой, такой как выбранный между аргинином и лизином, между глутамином и аспарагином и между глицином и серином. Кроме того, замена основного остатка, такого как лизин, аргинин или гистидин, на другой основный, или замена одного кислого остатка, такого как аспарагиновая кислота или глутаминовая кислота, на другой кислый остаток являются дополнительными примерами консервативных замен. Примеры неконсервативных замен включают замену неполярного (гидрофобного) аминокислотного остатка, такого как остаток изолейцина, валина, лейцина, аланина, метионина, на полярный (гидрофильный) остаток, такой как остаток цистеина, глутамина, глутаминовой кислоты или лизина, и/или полярный остаток на неполярный остаток.
Как здесь используется, термин «домен» относится к мотиву полипептида, имеющему одну или несколько идентифицируемых структурных или функциональных характеристик или свойств (например, связывающую способность, служащую сайтом для белок-белковых взаимодействий).
Как здесь используется, термин «сайт» применительно к полипептидам как он относится вариантам осуществления на основе аминокислот, используется в качестве синонима «аминокислотный остаток» и «боковая цепь аминокислоты». Как здесь используется, термин «сайт» применительно к полинуклеотидам как относится к вариантам осуществления, основанным на нуклеотидах, используется в качестве синонима «нуклеотид». Сайт представляет собой положение в пептиде или полипептиде или полинуклеотиде, которое может быть модифицировано, подвергнуто манипулироваию, изменено, дериватизировано или подвергнуто варьированию в молекулах на основе полипептида или на основе полинуклеотида.
Как здесь используется, термины «концы» или «конец» при ссылке на полипептиды или полинуклеотиды относятся к концу полипептида или полинуклеотида соответственно. Такой конец не ограничивается только первым или конечным сайтом полипептида или полинуклеотида, а может включать дополнительные аминокислоты или нуклеотиды в концевых областях. Молекулы на основе полипептидов могут быть охарактеризованы как имеющие как N-конец (оканчивающийся аминокислотой со свободной аминогруппой (NH2)), так и C-конец (оканчивающийся аминокислотой со свободной карбоксильной группой (COOH)). В некоторых случаях белки состоят из множества полипептидных цепей, соединенных дисульфидными связями или нековалентными силами (мультимеры, олигомеры). Эти белки имеют несколько N- и C-концов. Альтернативно, концы полипептидов могут быть модифицированы таким образом, чтобы они начинались или заканчивались, в зависимости от конкретного случая, группой не на основе полипептидов, такой как органический конъюгат.
Специалисты в данной области понимают, что белковые фрагменты, функциональные белковые домены и гомологичные белки также рассматриваются в качестве находящихся в объеме полипептидов, представляющих интерес. Например, здесь обеспечивается любой белковый фрагмент (имеется в виду полипептидная последовательность, которая, по меньшей мере, на один аминокислотный остаток короче референсной полипептидной последовательности, но в остальном идентичная) референсного белка, имеющий длину 10, 20, 30, 40, 50, 60, 70, 80, 90, 100 или более 100 аминокислот. В еще одном примере любой белок, который включает участок из 20, 30, 40, 50 или 100 (смежных) аминокислот, на 40%, 50%, 60%, 70%, 80%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентичный любой из последовательностей, описанных здесь, можно использовать в соответствии с изобретением. В некоторых вариантах осуществления полипептид включает 2, 3, 4, 5, 6, 7, 8, 9, 10 или более мутаций, как показано в любой из последовательностей, представленных здесь или упомянутых здесь. В еще одном примере любой белок, который включает участок из 20, 30, 40, 50 или 100 аминокислот, который более чем на 80%, 90%, 95% или 100% идентичен любой из последовательностей, описанных здесь, где белок имеет участок из 5, 10, 15, 20, 25 или 30 аминокислот, который менее чем на 80%, 75%, 70%, от 65% до 60% идентичен любой из последовательностей, описанных здесь, можно использовать в соответствии с раскрытием.
Полипептидные или полинуклеотидные молекулы по настоящему изобретению могут иметь определенную степень сходства или идентичности последовательностей с референсными молекулами (например, референсными полипептидами или референсными полинуклеотидами), например, с описанными в данной области молекулами (например, генно-инженерными или сконструированными молекулами или молекулами дикого типа). Термин «идентичность», как известно в данной области, относится к взаимосвязи между последовательностями двух или более полипептидов или полинуклеотидов, которая определяется сравнением последовательностей. В данной области под идентичностью также подразумевается степень родства между двумя последовательностями, определяемая по числу совпадений между участками из двух или более аминокислотных остатков или остатков нуклеиновых кислот. Идентичность определяет процент идентичных совпадений между меньшей из двух или более последовательностей выравниванием с гэпами (если они есть), с использованием конкретной математической модели или компьютерной программы (например, «алгоритмов»). Идентичность родственных пептидов можно легко рассчитать известными способами. Термин «% идентичности» применительно к полипептидным или полинуклеотидным последовательностям определяется как процент остатков (аминокислотных остатков или остатков нуклеиновых кислот) в аминокислотной последовательности-кандидате или последовательности-кандидате нуклеиновой кислоты, которые идентичны остаткам в аминокислотной последовательности или последовательности нуклеиновой кислоты второй последовательности после выравнивания последовательностей и введения гэпов, если необходимо, для достижения максимального процента идентичности. Методы и компьютерные программы для выравнивания хорошо известны в данной области. Идентичность зависит от расчета процента идентичности, но может различаться по значению за счет гэпов и штрафов, введенных в расчет. Как правило, варианты конкретного полинуклеотида или полипептида имеют, по меньшей мере, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92% 93%, 94%, 95%, 96%, 97%, 98%, 99%, но менее чем 100% идентичность последовательности с конкретным референсным полинуклеотидом или полипептидом, как определено программами выравнивания последовательностей и параметрами, описанными здесь и известными специалистам в данной области техники. Такие инструменты для выравнивания включают инструменты из алгоритма BLAST (Stephen F. Altschul et al. (1997), «Gapped BLAST and PSI-BLAST: a new generation of protein database search programs», Nucleic Acids Res. 25:3389-3402). Другой популярный метод локального выравнивания основан на алгоритме Смита-Ватермана (Smith, T.F. & Waterman, M.S. (1981), «Identification of common molecular subsequences», J. Mol. Biol. 147:195-197). Общим методом глобального выравнивания, основанным на динамическом программировании, является алгоритм Нидлмана-Вунша (Needleman, SB & Wunsch, CD (1970), «A general method applicable to the search for similarities in the amino acid sequences of two proteins», J. Mol. Biol., 48:443-453). Совсем недавно был разработан быстрый алгоритм оптимального глобального выравнивания последовательностей (FOGSAA), который предположительно проводит глобальное выравнивание последовательностей нуклеотидов и белков быстрее, чем другие оптимальные методы глобального выравнивания, включая алгоритм Нидлмана-Вунша. Другие инструменты описаны здесь, в частности, при определении термина «идентичность» ниже.
Как здесь используется, термин «гомология» относится к общему родству между полимерными молекулами, например, между молекулами нуклеиновой кислоты (например, молекулами ДНК) и/или между молекулами полипептида. Полимерные молекулы (например, молекулы нуклеиновой кислоты (например, молекулы ДНК) и/или молекулы полипептида), которые имеют пороговый уровень сходства или идентичности, определяемый выравниванием совпадающих остатков, называются гомологичными. Гомология представляет качественный термин, который описывает отношения между молекулами и может основываться на количественном сходстве или идентичности. Сходство или идентичность представляют количественный термин, который определяет степень совпадения последовательностей между двумя сравниваемыми последовательностями. В некоторых вариантах осуществления полимерные молекулы считаются «гомологичными» друг другу, если их последовательности имеют по меньшей мере 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичность или сходство. Термин «гомологичный» обязательно относится к сравнению по меньшей мере двух последовательностей (полинуклеотидных или полипептидных последовательностей). Две полинуклеотидные последовательности считаются гомологичными, если полипептиды, которые они кодируют, составляют, по меньшей мере, 50%, 60%, 70%, 80%, 90%, 95% или даже 99% по меньшей мере одного участка, по меньшей мере, из 20 аминокислот. В некоторых вариантах осуществления гомологичные полинуклеотидные последовательности характеризуются способностью кодировать участок по меньшей мере из 4-5 уникально указанных аминокислот. Для полинуклеотидных последовательностей длиной менее 60 нуклеотидов гомология определяется способностью кодировать участок, по меньшей мере, из 4-5 уникально указанных аминокислот. Две белковые последовательности считаются гомологичными, если белки, по меньшей мере, на 50, 60, 70, 80 или 90% идентичны, по меньшей мере, по одному участку, по меньшей мере, из 20 аминокислот.
Гомология подразумевает, что сравниваемые последовательности разошлись в эволюционном процессе из общего источника происхождения. Термин «гомолог» относится к первой аминокислотной последовательности или последовательности нуклеиновой кислоты (например, последовательности гена (ДНК или РНК) или последовательности белка), которая связана со второй аминокислотной последовательностью или последовательностью нуклеиновой кислоты по происхождению от общей наследственной последовательности. Термин «гомолог» может применяться к отношению между генами и/или белками, разделенным в результате видообразования, или к отношению между генами и/или белками, разделенными в случае генетической дубликации. «Ортологи» представляют гены (или белки) у разных видов, которые произошли от общего наследственного гена (или белка) посредством видообразования. Как правило, ортологи сохраняют ту же функцию в ходе эволюции. «Паралоги» представляют гены (или белки), связанные дубликацией в геноме. Ортологи сохраняют ту же функцию в ходе эволюции, в то время как паралоги развивают новые функции, даже если они связаны с исходной.
Термин «идентичность» относится к общему родству между полимерными молекулами, например, между полинуклеотидными молекулами (например, молекулами ДНК) и/или между полипептидными молекулами. Например, вычисление процентной идентичности двух последовательностей полинуклеиновой кислоты может быть выполнено выравниванием двух последовательностей в цлях оптимального сравнения (например, могут быть введены гэпы в одной или обеих первой и второй последовательностях нуклеиновой кислоты для оптимального выравнивания и неидентичные последовательности могут не учитываться для целей сравнения). В некоторых вариантах осуществления длина последовательности, выравненной для целей сравнения, составляет по меньшей мере 30%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90%, при минимум 95% или 100% от длины референсной последовательности. Затем сравнивают нуклеотиды в соответствующих нуклеотидных положениях. Когда положение в первой последовательности занято тем же нуклеотидом, что и соответствующее положение во второй последовательности, то молекулы идентичны по этому положению. Процент идентичности между двумя последовательностями является функцией числа идентичных положений, совместно используемых последовательностями, с учетом количества гэпов и длины каждого гэпа, которые необходимо ввести для оптимального выравнивания двух последовательностей. Сравнение последовательностей и определение процента идентичности между двумя последовательностями может быть выполнено с использованием математического алгоритма. Например, процент идентичности между двумя последовательностями нуклеиновых кислот может быть определен с использованием методов, таких как методы, описанные в монографиях Computational Molecular Biology, Lesk, A. M., ed., Oxford University Press, New York, 1988; Biocomputing: Informatics and Genome Projects, Smith, D. W., ed., Academic Press, New York, 1993; Sequence Analysis in Molecular Biology, von Heinje, G., Academic Press, 1987; Computer Analysis of Sequence Data, Part I, Griffin, A. M., и Griffin, H. G., eds., Humana Press, New Jersey, 1994; и Sequence Analysis Primer, Gribskov, M. and Devereux, J., eds., M Stockton Press, New York, 1991; каждый источник включен здесь посредством ссылки. Например, процент идентичности между двумя последовательностями нуклеиновых кислот может быть определен с использованием алгоритма Мейерса и Миллера (CABIOS, 1989, 4: 11-17), который был включен в программу ALIGN (версия 2.0) с использованием таблицы остаточных весов РАМ120, штрафом за длину гэпа, равным 12, и штрафом за гэп, равным 4. Процент идентичности между двумя последовательностями нуклеиновой кислоты можно, в качестве альтернативы, определить с использованием программы GAP в программном пакете GCG с использованием матрицы NWSgapdna.CMP. Методы, обычно используемые для определения процента идентичности между последовательностями, включают, не ограничиваясь этим, методы, раскрытые в публикации Carillo H. and Lipman D., SIAM J. Applied Math., 48: 1073 (1988); которая включена здесь посредством ссылки. Методы определения систематизированы в общедоступных компьютерных программах. Примеры компьютерного программного обеспечения для определения гомологии между двумя последовательностями включают, не ограничиваясь этим, пакет программ GCG, Devereux, J. и др., Nucleic Acids Research, 12, 387 (1984)), BLASTP, BLASTN и FASTA Altschul, SF et al., J. Molec. Biol., 215, 403 (1990)).
Липидные наночастицы
Как здесь используется, термин «липидная наночастица» или «LNP» относится к любой липидной композиции, которую можно использовать для доставки продукта, включая, не ограничиваясь этим, липосомы или везикулы, где водный объем инкапсулирован амфипатическими липидными бислоями (например, одиночным, однослойным или множественным, многослойным) или, в других вариантах осуществления, где липиды покрывают внутреннюю полость, содержащую профилактический продукт, или липидные агрегаты или мицеллы, где инкапсулированный в липид терапевтический продукт находится в относительно неупорядоченной липидной смеси. За исключением отмеченных случаев, отсутствует необходимость включать в липидную наночастицу антигенный полипептид, и ее можно использовать для доставки продукта в одной и той же композиции.
Как здесь используется, термин «полиамин» означает соединения, имеющие две или более аминогрупп. Примеры включают путресцин, кадаверин, спермидин и спермин.
Если не указано иное, то мол.% относится к молярному проценту от общего количества липидов. Обычно LNP композиций по изобретению состоят из одного или нескольких катионных липидов (включая ионизируемые катионные липиды) и одного или нескольких поли(этиленгликоль)-липидов(PEG-липид). В определенных вариантах осуществления LNP дополнительно содержат один или несколько некатионных липидов. Один или несколько некатионных липидов могут включать фосфолипид, производное фосфолипида, стерол, жирную кислоту или их комбинацию.
Катионные липиды и ионизируемые катионные липиды, подходящие для LNP, описаны здесь. Ионизируемые катионные липиды характеризуются слабой основностью их липидных головных групп, что влияет на поверхностный заряд липида рН-зависимым образом, делая их положительно заряженными при кислом рН, но близкими к нейтральному заряду при физиологическом рН. Катионные липиды характеризуются моновалентным или поливалентным катионным зарядом на своих головных группах, что делает их положительно заряженными при нейтральном рН. В некоторых вариантах осуществления катионный и ионизируемый липид способен образовывать комплексы с гидрофильными биологически активными молекулами с образованием гидрофобного комплекса, который разделяется на органическую фазу двухфазной водно-органической системы. Полагается, что как моновалентные, так и поливалентные катионные липиды можно использовать для образования гидрофобных комплексов с биологически активными молекулами.
В некоторых вариантах осуществления катионные и ионизируемые катионные липиды для использования в образовании LNP включают, не ограничиваясь этим, хлорид N, N-диолеил-N, N-диметиламмония («DODAC»); хлорид N-(2,3-диолеилокси)пропил)-N, N,N-триметиламмония («DOTMA»); бромид N, N-дистеарил-N, N-диметиламмония («DDAB»); хлорид N-(2,3-диолеилокси)пропил)-N, N,N-триметиламмония («DOTAP»); 1,2-бис(олеоилокси)-3-(триметиламмонио)пропан («DOTAP»); 3-(N-(N',N'-диметиламиноэтан)-карбамоил)холестерин («DC-Chol»); дигептадециламидоглицилспермидин («DHGS») и бромид N-(1,2-димиристилоксипроп-3-ил)-N, N-диметил-N-гидроксиэтиламмония («DMRIE»). Кроме того, имеется ряд коммерческих препаратов катионных липидов, а также других компонентов, которые можно использовать в настоящем изобретении. К ним относятся, например, LIPOFECTIN® (коммерчески доступные катионные липидные наночастицы, содержащие DOTMA и 1,2-диолеоил-sn-3-фосфоэтаноламин («DOPE») производства GIBCOBRL, Гранд-Айленд, N.Y., США); и LIPOFECTAMINE® (коммерчески доступные катионные липидные наночастицы, содержащие трифторацетат N-(1-(2,3-диолеилокси)пропил)-N-(2-(сперминкарбоксамидо)этил)-N, N-диметиламмония («DOSPA») и («DOPE») производства (GIBCOBRL). Следующие липиды являются катионными и имеют положительный заряд при рН ниже физиологического: DODAP, DODMA, DMDMA, 1,2-дилинолеилокси-N, N-диметиламинопропан (DLinDMA), 4-(2,2-диокта)-9,12-диенил-[1,3]диоксолан-4-илметил)диметиламин, DLinKDMA (WO 2009/132131 A1), DLin-K-C2-DMA (WO2010/042877), DLin-M-C3-DMA (WO2010/146740 и/или WO2010/105209), DLin-MC3-DMA (гептатриаконта-6,9,28,31-тетраен-19-ил 4-(диметиламино)бутаноат; Jayaraman et al., 2012, Angew. Chem. Int. Ed. Engl. 51: 8529-8533), 2-{4-[(3β)-холест-5-ен-3-илокси]бутокси}-N, N-диметил-3-[(9Z,12Z)-октадека-9,12-диенилоксил]пропан-1-амин) (CLinDMA) и тому подобное. Другие катионные липиды, подходящие для использования в изобретении, включают, например, катионные липиды, описанные в патентах США № 5208036, 5264618, 5279833 и 5283185, а также в публикациях патентных заявок США № 2008/0085870 и 2008/0057080. Другие катионные липиды, подходящие для использования в изобретении, включают, например, липиды E0001-E0118 или E0119-E0180, как раскрыто в таблице 6 (страницы 112-139) международной публикации патентной заявки № WO2011/076807 (которая также раскрывает способы получения и способы применения этих катионных липидов).
В некоторых вариантах осуществления катионный липид включает любое соединение из DLinDMA; DlinKC2DMA; Dlin-МС3-DMA; CLinDMA; S-octyl CLinDMA;
(2S)-1-{7-[(3β)-холест-5-ен-3-илокси]гептилокси}-3-[(4Z)-дек-4-ен-1-илокси]-N, N диметилпропан-2-амин;
(2R)-1-{4-[(3β)-холест-5-ен-3-илокси]бутокси}-3-[(4Z)-дек-4-ен-1-илокси]-N, N диметилпропан-2-амин;
1-[(2R)-1-{4-[(3β)-холест-5-ен-3-илокси]бутокси}-3-(октилокси)пропан-2-ил]гуанидин;
1-[(2R)-1-{7-[(3β)-холест-5-ен-3-илокси]гептилокси}-N, N-диметил-3-[(9Z,12Z)-октадека-9,12-диен-1-илокси]пропан-2-амин;
1-[(2R)-1-{4-[(3β)-холест-5-ен-3-илокси]бутокси}-N, N-диметил-3-[(9Z,12Z)-октадека-9,12-диен-1-илокси]пропан-2-амин;
(2S)-1-({6-[(3β))-холест-5-ен-3-илокси]гексил}окси)-N, N-диметил-3-[(9Z)-октадека-9-ен-1-илокси]пропан-2-амин;
(3β)-3-[6-{[(2S)-3-[(9Z)-октадека-9-ен-1-илокси]-2-(пирролидин-1-ил)пропил]окси}гексил)окси]холест-5-ен;
(2R)-1-{4-[(3β)-холест-5-ен-3-илокси]бутокси}-3-(октилокси)пропан-2-амин;
(2R)-1-({8-[(3β)-холест-5-ен-3-илокси]октил}окси)-N, N-диметил-3-(пентилокси)пропан-2-амин;
(2R)-1-({8-[(3β)-холест-5-ен-3-илокси]октил}окси)-3-(гептилокси)-N, N-диметилпропан-2-амин;
(2R)-1-({8-[(3β)-холест-5-ен-3-илокси]октил}окси)-N, N-диметил-3-[(2Z)пент-2-ен-1-илокси]пропан-2-амин;
(2S)-1-бутокси-3-({8-[(3β)-холест-5-ен-3-илокси]октил}окси)-N, N-диметилпропан-2-амин;
(2S-1-({8-[(3β)-холест-5-ен-3-илокси]октил}окси)-3-[2,2,3,3,4,4,5,5,6,6,7,7,8,8,9,9-гексадекафторнонил)окси]-N, N-диметилпропан-2-амин;
2-амино-2-{[(9Z,12Z)-октадека-9,12-диен-1-илокси]метил}пропан-1,3-диол;
2-амино-3-((9-(((3S,10R,13R)-10,13-диметил-17-(6-метилгептан-2-ил)-2,3,4,7,8,9,10,11,12,13,14,15,16,17-тетрадекагидро-1Н-циклопента[а]фенантрен-3-ил)окси)нонил)окси)-2-((((9Z,12Z)-октадека-9,12-диен-1-ил)окси)метил)пропан-1-ол;
2-амино-3-((6-(((3S,10R,13R)-10,13-диметил-17-(6-метилгептан-2-ил)-2,3,4,7,8,9,10,11,12,13,14,15,16,17-тетрагидро-1Н-циклопента[а]фенантрен-3-ил)окси)гексил)окси)-2-((((Z)-октадек-9-ен-1-ил)окси)метил)пропан-1-ол;
(20Z,23Z)-N, N-диметилнонакоза-20,23-диен-10-амин;
(17Z,20Z)-N, N-диметилгексакоза-17,20-диен-9-амин;
(16Z,19Z)-N, N-диметилпентакоза-16,19-диен-8-амин;
(13Z,16Z)-N, N-диметилдокоза-13,16-диен-5-амин;
(12Z,15Z)-N, N-диметилгеникоза-12,15-диен-4-амин;
(14Z,17Z)-N, N-диметилтрикоза-14,17-диен-6-амин;
(15Z,18Z)-N, N-диметилтетракоза-15,18-диен-7-амин;
(18Z,21Z)-N, N-диметилгептакоза-18,21-диен-10-амин;
(15Z,18Z)-N, N-диметилтетракоза-15,18-диен-5-амин;
(14Z,17Z)-N, N-диметилтрикоза-14,17-диен-4-амин;
(19Z,22Z)-N, N-диметилоктакоза-19,22-диен-9-амин;
(18Z,21Z)-N, N-диметилгептакоза-18,21-диен-8-амин;
(17Z,20Z)-N, N-диметилгексакоза-17,20-диен-7-амин;
(16Z,19Z)-N, N-диметилпентакоза-16,19-диен-6-амин;
(22Z,25Z)-N, N-диметилгентриаконта-22,25-диен-10-амин;
(21Z,24Z)-N, N-диметилтриаконта-21,24-диен-9-амин;
(18Z)-N, N-диметилгептакоз-18-ен-10-амин;
(17Z)-N, N-диметилгексакоз-17-ен-9-амин;
(19Z,22Z)-N, N-диметилоктакоза-19,22-диен-7-амин;
N, N-диметилгептакозан-10-амин;
(20Z,23Z)-N-этил-N-метилнонакоза-20,23-диен-10-амин;
1-[(11Z,14Z)-1-нониликоза-11,14-диен-1-ил]-пирролидин;
(20Z)-N, N-диметилгептакоз-20-ен-10-амин;
(15Z)-N, N-диметилгептакоз-15-ен-10-амин;
(14Z)-N, N-диметилнонакоз-14-ен-10-амин;
(17Z)-N, N-диметилнонакоз-17-ен-10-амин;
(24Z)-N, N-диметилтритриаконт-24-ен-10-амин;
(20Z)-N, N-диметилнонакоз-20-ен-10-амин;
(22Z)-N, N-диметилгентриаконт-22-ен-10-амин;
(16Z)-N, N-диметилпентакоз-16-ен-8-амин;
(12Z,15Z)-N, N-диметил-2-нонилгеникоза-12,15-диен-1-амин;
(13Z,16Z)-N, N-диметил-3-нонилдокоза-13,16-диен-1-амин;
N, N-диметил-1-[(1S,2R)-2-октилциклопропил]гептадекан-8-амин;
1-[(1S,2R)-2-гексилциклопропил]-N, N-диметилнонадекан-10-амин;
N, N-диметил-1-[(1S,2R)-2-октилциклопропил]нонадекан-10-амин;
N, N-диметил-21-[(1S,2R)-2-октилциклопропил]геникозан-10-амин;
N, N-диметил-1-[(1S,2S)-2-{[(1R,2R)-2-пентилциклопропил]метил}циклопропил]нонадекан-10-амин;
N, N-диметил-1-[(1S,2R)-2-октилциклопропил]гексадекан-8-амин;
N, N-диметил-1-[(1R,2S)-2-ундецилциклопропил]тетрадекан-5-амин;
N, N-диметил-3-{7-[(1S,2R)-2-октилциклопропил]гептил}додекан-1-амин;
1-[(1R,2S)-2-гептилциклопропил]-N, N-диметилоктадекан-9-амин;
1-[(1S,2R)-2-децилциклопропил]-N, N-диметилпентадекан-6-амин;
N, N-диметил-1-[(1S,2R)-2-октилциклопропил]пентадекан-8-амин; и
(11E,20Z,23Z)-N, N-диметилнонакоза-11,20,23-триен-10-амин;
или его фармацевтически приемлемую соль, или стереоизомер любого из вышеуказанного.
В некоторых аспектах этого варианта осуществления изобретения LNP содержат один или более из следующих ионизируемых катионных липидов: DLinDMA, DlinKC2DMA, DLin-MC3-DMA, CLinDMA или S-Octyl CLinDMA (см. публикацию международной патентной заявки № WO2010/021865). В еще одних аспектах этого варианта осуществления изобретения LNP содержат один или более из следующих ионизируемых катионных липидов: (13Z,16Z)-N, N-диметил-3-нонилдокоза-13,16-диен-1-амин или N, N-диметил-1-[(1S,2R)-2-октилциклопропил]гексадекан-8-амин, каждый из которых описан в PCT/US2011/0523238, опубликованной как WO 2012/040184, которая в полном объеме включена здесь посредством ссылки.
В некоторых аспектах этого варианта осуществления изобретения ионизируемый катионный липид может включать липид, описанный в международной патентной заявке WO 2017/049245, которая в полном объеме включена здесь посредством ссылки.
В определенных аспектах этого варианта осуществления изобретения LNP включают один или более ионизируемых катионных липидов, описанных в публикации международной патентной заявки № WO2011/022460 А1, или любую фармацевтически приемлемую соль или стереоизомер любого из соединений или солей, описанных в ней.
Когда структуры одного и того же строения различаются по пространственному расположению определенных атомов или групп, то они являются стереоизомерами, и соображения, которые важны при анализе их взаимосвязей, являются топологическими. Если взаимосвязь между двумя стереоизомерами такая же, как у объекта и его неналагающегося зеркального отражения, то эти две структуры являются энантиомерными, и каждая структура называется хиральной. Стереоизомеры также включают диастереомеры, цис-транс-изомеры и конформационные изомеры. Диастереоизомеры могут быть хиральными или ахиральными и не являются зеркальными отражениями друг друга. Цис-транс-изомеры различаются только положениями атомов относительно указанной плоскости в тех случаях, когда эти атомы являются или считаются таковыми, как если бы они были частями жесткой структуры. Конформационные изомеры представляют собой изомеры, которые могут превращаться друг в друга вращением вокруг формально одинарных связей. Примеры таких конформационных изомеров включают конформации циклогексана с конформерами типа кресла и типа лодки, углеводы, конформации линейных алканов с заторможенными, заслоненными конфомерами и гош-конформерами и т. д. См. J. Org. Chem., 35, 2849 (1970).
Многие органические соединения находятся в оптически активных формах, способных вращать плоскость плоско-поляризованного света. При описании оптически активного соединения префиксы D и L или R и S используются для обозначения абсолютной конфигурации молекулы относительно ее хирального центра(ов). Префиксы d и l или (+) и (-) используются для указания направления вращения соединением плоско-поляризованного света, где (-) или l означает, что соединение является левовращающим. Соединение с префиксом (+) или d является правовращающим. Для данной химической структуры эти стереоизомеры являются идентичными, если не считать, что они являются неналагающимися зеркальными отражениями друг друга. Смесь энантиомеров часто называют энантиомерной смесью. Смесь энантиомеров в соотношении 50:50 называется рацемической смесью. Многие из катионных липидов, описанных здесь, могут иметь один или несколько хиральных центров и, следовательно, могут существовать в разных энантиомерных формах. При желании хиральный углерод может быть обозначен звездочкой (*). Когда связи с хиральным углеродом изображены в формулах изобретения в виде прямых линий, то подразумевается, что обе конфигурации (R) и (S) хирального углерода и, следовательно энантиомеры и их смеси, включаются в формулу. Как используется в данной области техники, когда требуется указать абсолютную конфигурацию относительно хирального углерода, то одна из связей с хиральным углеродом может быть изображена в виде клина (связи с атомами над плоскостью), а другая может быть изображена в виде серии или клина из коротких параллельных линий (связей с атомами ниже плоскости). Систему Кана-Ингольда-Прелога можно использовать для отнесения (R) или (S) конфигурации хиральному углероду.
Когда катионные липиды по настоящему изобретению содержат один хиральный центр, то соединения находятся в двух энантиомерных формах, и настоящее изобретение включает как энантиомеры, так и смеси энантиомеров, такие как конкретная смесь 50:50, называемая рацемической смесью. Энантиомеры можно разделить способами, известными специалистам в данной области, такими как получение диастереоизомерных солей, которые можно разделить, например, кристаллизацией (см. «CRC Handbook of Optical Resolutions via Diastereomeric Salt Formation», David Kozma (CRC Press, 2001)); получение диастереоизомерных производных или комплексов, которые можно разделить, например, кристаллизацией, газожидкостной или жидкостной хроматографией; селективное взаимодействие одного энантиомера с энантиомер-специфическим реагентом, например ферментативная этерификация; или газожидкостной или жидкостной хроматографией в хиральной среде, например, на хиральном носителе, например диоксиде кремния со связанным хиральным лигандом, или в присутствии хирального растворителя. Должно быть понятно, что, когда требуемый энантиомер превращают в другую химическую молекулу с помощью одной из процедур разделения, описанных выше, то требуется дополнительная стадия для высвобождения требуемой энантиомерной формы. Альтернативно, конкретные энантиомеры можно синтезировать асимметрическим синтезом с использованием оптически активных реагентов, субстратов, катализаторов или растворителей или превратить один энантиомер в другой путем асимметрического превращения.
Обозначение конкретной абсолютной конфигурации на хиральном углероде катионных липидов, описанных здесь, понимается как означающее, что указанная энантиомерная форма соединений находится в энантиомерном избытке (ее) или, другими словами, по существу не содержит другого энантиомера. Например, "R" формы соединений по существу не содержат "S" форм соединений и, таким образом, находятся в энантиомерном избытке "S" форм. Напротив, "S" формы соединений по существу не содержат "R" форм соединений и, таким образом, находятся в энантиомерном избытке "R" форм. Как здесь используется, термин «энантиомерный избыток» представляет присутствие определенного энантиомера в количестве более 50%. В конкретном варианте осуществления, когда указана конкретная абсолютная конфигурация, то энантиомерный избыток изображенных соединений составляет, по меньшей мере, примерно 90%.
Когда катионный липид, описанный здесь, содержит два или более хиральных атома углерода, то он может иметь более двух оптических изомеров и может существовать в диастереоизомерных формах. Например, когда имеется два хиральных атома углерода, то соединение может иметь до 4 оптических изомеров и 2 пары энантиомеров (((S, S)/(R, R) и (R, S)/(S, R)). Пары энантиомеров (например, (S, S)/(R, R)) являются стереоизомерами зеркального отображения друг друга. Стереоизомеры, которые не являются зеркальными отображениями (например, (S, S) и (R, S)), представляют диастереомеры. Диастереоизомерные пары можно разделить способами, известными специалистам в данной области, например хроматографией или кристаллизацией, и отдельные энантиомеры в каждой паре могут быть разделены, как описано выше. LNP, описанные здесь, включают каждый диастереоизомер таких катионных липидов и их смеси.
LNP также могут содержать любую комбинацию двух или более катионных липидов, описанных здесь. В определенных аспектах катионный липид обычно составляет от примерно 0,1 до примерно 99,9 мол.% от общего количества липида, присутствующего в указанной частице. В некоторых аспектах катионный липид может составлять примерно от 80 до примерно 99,9% мол.%. В еще одних аспектах катионный липид составляет примерно от 2% до примерно 70%, примерно от 5% до примерно 50%, примерно от 10% до примерно 45%, примерно от 20% до примерно 99,8%, примерно от 30% до примерно 70%, примерно от 34% до примерно 59%, примерно от 20% до примерно 40% или примерно от 30% до примерно 40% (в мол.%) от общего количества липидов, присутствующих в указанной частице.
LNP, описанные здесь, могут дополнительно содержать некатионный липид, который может представлять любой из множества нейтральных незаряженных, цвиттер-ионных или анионных липидов, способных образовывать стабильный комплекс. Предпочтительно они являются нейтральными, хотя они могут быть отрицательно заряженными. Примеры некатионных липидов, используемых здесь, включают связанные с фосфолипидами вещества, такие как природные фосфолипиды, синтетические производные фосфолипидов, жирные кислоты, стеролы и их комбинации. Природные фосфолипиды включают фосфатидилхолин (PC), фосфатидилэтаноламин (PE) и фосфатидилглицерин (PG), фосфатидилсерин (PS), фосфатидилинозит (PI), фосфатидную кислоту (фосфатидат) (PA), дипальмитоилфосфатидилхолин, моноацилфосфатидилхолин (lyso PC), 1-пальмитоил-2-олеоил-sn-глицеро-3-фосфохолин (POPC), N-ацил-PE, фосфоинозитиды и фосфосфинголипиды. Производные фосфолипидов включают фосфатидную кислоту (DMPA, DPPA, DSPA), фосфатидилхолин (DDPC, DLPC, DMPC, DPPC, DSPC, DOPC, POPC, DEPC), фосфатидилглицерин (DMPG, DPPG, DSPG, POPG), фосфатидилэтаноламин (DMPE, DPPE, DSPE, DOPE) и фосфатидилсерин (DOPS). Жирные кислоты включают пальмитиновую кислоту (С14:0), стеариновую кислоту (С18:0), олеиновую кислоту (С18:1), линолевую кислоту (С18:2), линоленовую кислоту (С18:3) и арахидоновую кислоту (С20:4), С20:0, С22:0 и летицин.
В некоторых вариантах осуществления LPN, описанных здесь, некатионный липид выбран из лецитина, фосфатидилэтаноламина, лизолецитина, лизофосфатидилэтаноламина, фосфатидилсерина, фосфатидилинозита, сфингомиелина, цефалина, кардиолипина, фосфатидной кислоты, цереброзидов, диацетилфосфата, дистеароилфосфатидилхолина (DSPC), диолеилфосфатидилхолина (DOPC), дипальмитоилфосфатидилхолина (DPPC), диолеилфосфатидилглицерина (DOPG), дипальмитоилфосфатидилглицерина (DPPG), диолеоил-фосфатидилэтаноламина (DOPE), пальмитоилолеилфосфатидилхолина (POPC), пальмитоилолеилфосфатидилэтаноламина (POPE) и диолеоил-фосфатидилэтаноламин-4-(N-малеимидометил)циклогексан-1-карбоксилата (DOPE-mal). Некатионные липиды также включают стеролы, такие как холестерин, стигмастерол или стигмастанол. Холестерин известен в данной области. См. публикации заявок на патент США: 2006/0240554 и 2008/0020058. В определенных вариантах осуществления LNP включает комбинацию фосфолипида и стерола.
Некатионный липид, если он присутствует, обычно составляет примерно от 0,1% до примерно 65%, примерно от 2% до примерно 65%, примерно от 10% до примерно 65% или примерно от 25% до примерно 65%, при выражении в молярных процентах от общего количества липида, присутствующего в LNP. LNP, описанные здесь, дополнительно включают конъюгат полиэтиленгликоля (PEG)-липида («PEG-липид»), который используется в качестве компонента, стабилизирующего бислой. Липидный компонент ПЭГ-липида может представлять любой некатионный липид, описанный выше, включая природные фосфолипиды, синтетические производные фосфолипидов, жирные кислоты, стеролы и их комбинации. В некоторых вариантах осуществления LNP, описанных здесь, ПЭГ-липиды включают ПЭГ, связанный с диалкилоксипропилами (PEG-DAA), описанный, например, в публикации международной патентной заявки № WO 05/026372, ПЭГ, связанной с диацилглицерином (PEG-DAG), описанный, например, в публикациях заявок на патент США № 20030077829 и 2005008689; ПЭГ, связанный с фосфатидилэтаноламином (PE) (PEG-PE), или ПЭГ, конъюгированный с 1,2-ди-О-гексадецил-sn-глицеридом (PEG-DSG), или любую их смесь (см., например, патент США № 5885613).
В одном варианте осуществления конъюгат PEG-DAG представляет собой конъюгат дилаурилглицерина (C12)-ПЭГ, конъюгат ПЭГ-димиристилглицерина (C14), конъюгат ПЭГ-дипальмитоилглицерина (C16), конъюгат ПЭГ-дилаурилгликамида (C12), конъюгат ПЭГ-димиритилгликамида (C14), конъюгат ПЭГ-дипальмитоилгликамида (C16) или ПЭГ-дистерилгликамида (C18). Специалисты в данной области легко поймут, что другие диацилглицерины могут быть использованы в конъюгатах PEG-DAG.
В некоторых вариантах осуществления ПЭГ-липиды включают, не ограничиваясь этим, ПЭГ-димиристолглицерин (PEG-DMG), ПЭГ-дистерилглицерин (PEG-DSG), ПЭГ-дипальметолеил, ПЭГ-диолеил, ПЭГ-дистеарил, ПЭГ-диацилгликамид (PEG-DAG), ПЭГ-дипальмитоилфосфатидилэтаноламин (PEG-DPPE) и ПЭГ-1,2-димиристилоксилпропил-3-амин (PEG-c-DMA).
В некоторых вариантах осуществления ПЭГ-липид представляет ПЭГ, связанный с димиристоилглицерином (PEG-DMG), например, как описано в публикации Abrams et al., 2010, Molecular Therapy 18 (1): 171, и публикациях патентной заявки США № 2006/0240554 и US 2008/0020058, включая, например, 2KPEG/PEG200-DMG.
В некоторых вариантах осуществления ПЭГ-липид, такой как ПЭГ-DAG, ПЭГ-холестерин, ПЭГ-DMB включает полиэтиленгликоль, имеющий среднюю молекулярную массу в диапазоне примерно от 500 дальтон до примерно 10000 дальтон, примерно от 750 дальтон до примерно 5000 дальтон, примерно от 1000 дальтон до примерно 5000 дальтон, примерно от 1500 дальтон до примерно 3000 дальтон или примерно 2000 дальтон. В некоторых вариантах осуществления ПЭГ-липид включает ПЭГ400, ПЭГ1500, ПЭГ2000 или ПЭГ5000.
Ацильные группы в любом из липидов, описанных выше, предпочтительно представляют собой ацильные группы, происходящие из жирных кислот, содержащих примерно от 10 до примерно 24 атомов углерода. В одном варианте осуществления ацильная группа представляет лауроил, миристоил, пальмитоил, стеароил или олеоил.
Конъюгат ПЭГ-липид обычно составляет примерно от 0,1% до примерно 15%, примерно от 0,5% до примерно 20%, примерно от 1,5% до примерно 18%, примерно от 4% до примерно 15%, примерно от 5% до примерно 12%, примерно от 1% до примерно 4% или примерно 2%, при выражении в мол.% от общего количества липида, присутствующего в указанной частице.
В некоторых вариантах осуществления изобретения LNP содержат один или более катионных липидов, холестерин и 1,2-димиристоил-sn-глицерин, метоксиполиэтиленгликоль (PEG-DMG).
В некоторых вариантах осуществления изобретения LNP содержат один или более катионных липидов, холестерин, 1,2-дистеароил-sn-глицеро-3-фосфохолин (DSPC) и 1,2-димиристоил-sn-глицерин, метоксиполиэтиленгликоль (PEG-DMG).
В некоторых вариантах осуществления изобретения LNP содержат липидные соединения, объединенные в следующих молярных соотношениях:
катионный липид (20-99,8 мол.%)
некатионный липид (0,1-65 мол.%) И
PEG-DMG (0,1-20 мол.%).
В некоторых вариантах осуществления изобретения LNP содержат липидные соединения, объединенные в следующих молярных соотношениях:
катионный липид (30-70 мол.%)
некатионный липид (20-65 мол.%) и
PEG-DMG (1-15 мол.%).
В некоторых аспектах этого варианта осуществления некатионный липид представляет собой холестерин.
Типичные LNP могут включать катионный липид/холестерин/PEG-DMG в следующих молярных соотношениях: 58/30/10.
В некоторых аспектах этого варианта осуществления некатионный липид представляет собой холестерин и DSPC. Типичные LNP могут включать катионный липид/холестерин/DSPC/PEG-DMG в следующих молярных соотношениях: 59/30/10/1; 58/30/10/2; 43/41/15/1; 42/41/15/2; 40/48/10/2; 39/41/19/1; 38/41/19/2; 34/41/24/1 и 33/41/24/2.
Приготовление LNP
LNP можно получить, например, с помощью процесса быстрого осаждения, который включает микросмешивание липидных компонентов, растворенных в этаноле, с водным раствором с использованием смесительного аппарата с ограниченным объемом, такого как Т-микросмеситель с ограниченным объемом, вихревой смеситель с несколькими патрубками (MIVM), или микрожидкостные смесители, как описано ниже. Раствор липидов содержит один или более катионных липидов, один или более некатионных липидов (например, DSPC), PEG-DMG и, необязательно, холестерин в определенных молярных соотношениях в этаноле. Водный раствор состоит из забуференного солевого раствора цитрата натрия или ацетата натрия с рН в диапазоне 2-6, предпочтительно 3,5-5,5. Два раствора нагревают до температуры в диапазоне 25°С-45°С, предпочтительно 30°С-40°С, и затем смешивают в смесителе с ограниченным объемом, тем самым мгновенно получая LNP. Когда используется T-микросмеситель с ограниченным объемом, то T-микросмеситель имеет внутренний диаметр (ID) в диапазоне от 0,25 до 1,0 мм. Спиртовые и водные растворы поступают на вход Т-микросмесителя с используемых программируемых шприцевых насосов и с общей скоростью потока 10-600 мл/мин. Спиртовые и водные растворы объединяются в смесителе с ограниченным объемом в соотношении от 1:1 до 1:3 об./об., но предпочтительно от 1:1,1 до 1:2,3. Комбинация объемной фракции этанола, скоростей потока раствора реагента и ID патрубков Т-микросмесителя, используемых на этой стадии смешивания, позволяет контролировать размер частиц LNP от 30 до 300 нм. Полученную суспензию LNP дважды разбавляют буфером с более высоким pH в диапазоне 6-8 в последовательном многостадийном поточном процессе смешивания. Для первого разбавления суспензию LNP смешивают с забуференным раствором при более высоком рН (рН 6-7,5) с соотношением смешивания в диапазоне от 1:1 до 1:3 об./об., но предпочтительно 1:2 об./об. Этот забуференный раствор имеет температуру в диапазоне 15-40°С, препочтительно 30-40°С. Полученную суспензию LNP дополнительно смешивают с забуференным раствором при более высоком рН, например 6-8, и с соотношением смешивания в диапазоне от 1:1 до 1:3 об./об., но предпочтительно на 1:2 об./об. Этот более поздний забуференный раствор имеет температуру в диапазоне 15-40°С, предпочтительно 16-25°С. Смешанные LNP выдерживают от 30 мин до 2 ч перед стадией анионообменной фильтрации. Температура во время периода инкубации находится в диапазоне 15-40°С, предпочтительно 30-40°С. После инкубации суспензию LNP фильтруют через 0,8 мкм фильтр, включая стадию анионообменного разделения. В этом процессе используются трубки с ID от 1 мм до 5 мм и скорость потока от 10 до 2000 мл/мин. LNP концентрируют и подвергают диафильтрации посредством процесса ультрафильтрации, где спирт удаляют и буфер заменяют на конечный буферный раствор, такой как забуференный фосфатом физиологический раствор или буферную систему, подходящую для криоконсервации (например, содержащую сахарозу, трегалозу или их комбинации). В процессе ультрафильтрации используется формат фильтрации в тангенциальном потоке (TFF). В этом процессе используется мембрана с диапазоном отсечения по номинальной молекулярной массе от 30 до 500 кДа, предпочтительно 100 кДа. Формат мембраны может представлять кассету из полого волокна или плоского листа. Процессы TFF с надлежащим отсечением по молекулярной массе удерживают LNP в ретентате, а фильтрат или пермеат содержат спирт и конечные буферные отходы. Процесс TFF представляет собой многостадийный процесс с начальной концентрацией до концентрации липидов 20-30 мг/мл. После концентрирования суспензию LNP подвергают диафильтрации против конечного буфера (например, забуференного фосфатом солевого раствора (PBS) с рН 7-8, 10 мМ Трис, 140 мМ NaCl с рН 7-8 или 10 мМ Трис, 70 мМ NaCl, 5 мас.% сахарозы, с рН 7-8) с 5-20 объемами для удаления спирта и проведения замены на буфер. Затем материал концентрируется дополнительно в 1-3 раза посредством ультрафильтрации. Заключительными стадиями процесса получения LNP являются стерилизующая фильтрация концентрированного раствора LNP в подходящий контейнер в асептических условиях. Стерилизующую фильтрацию проводят, пропуская раствор LNP через предфильтр (Acropak 500 PES 0,45/0,8 мкм капсула) и фильтр для снижения биологической нагрузки (Acropak 500 PES 0,2/0,8 мкм капсула). После фильтрации продукт LNP, разлитый во флаконы, хранят в подходящих условиях хранения (2°C-8°C или -20°C, если состав подлежит замороживанию).
В некоторых вариантах осуществления LNP в композициях, обеспеченных здесь, имеют средний геометрический диаметр, который составляет менее 1000 нм. В некоторых вариантах осуществления LNP имеют средний геометрический диаметр, который больше 50 нм, но меньше 500 нм. В некоторых вариантах осуществления средний геометрический диаметр популяции LNP составляет примерно 60 нм, 75 нм, 100 нм, 125 нм, 150 нм, 175 нм, 200 нм, 225 нм, 250 нм, 275 нм, 300 нм, 325 нм, 350 нм, 375 нм, 400 нм, 425 нм, 450 нм или 475 нм. В некоторых вариантах осуществления средний геометрический диаметр составляет 100-400 нм, 100-300 нм, 100-250 нм или 100-200 нм. В некоторых вариантах осуществления средний геометрический диаметр составляет 60-400 нм, 60-350 нм, 60-300 нм, 60-250 нм или 60-200 нм. В некоторых вариантах осуществления средний геометрический диаметр составляет 75-250 нм. В некоторых вариантах осуществления 30%, 40%, 50%, 60%, 70%, 80%, 90% или более LNP из популяции LNP имеют диаметр менее 500 нм. В некоторых вариантах осуществления 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или более LNP из популяции LNP имеют диаметр более 50 нм, но менее 500 нм. В некоторых вариантах осуществления 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или более LNP из популяции LNP имеют диаметр примерно 60 нм, 75 нм, 100 нм, 125 нм, 150 нм, 175 нм, 200 нм, 225 нм, 250 нм, 275 нм, 300 нм, 325 нм, 350 нм, 375 нм, 400 нм, 425 нм, 450 нм или 475 нм. В некоторых вариантах осуществления 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или более LNP из популяции LNP имеют диаметр 100-400 нм, 100-300 нм, 100-250 нм или 100-200 нм. В некоторых вариантах осуществления 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или более LNP из популяции LNP имеют диаметр, который находится в диапазоне 60-400 нм, 60-350 нм, 60-300 нм, 60-250 нм или 60-200 нм.
В конкретном варианте осуществления размер LNP составляет примерно от 1 до 1000 нм, предпочтительно примерно от 10 до 500 нм, более предпочтительно примерно от 100 до 300 нм и предпочтительно 100 нм.
Нуклеиновые кислоты/полинуклеотиды
ДНК по настоящему изобретению в некоторых вариантах осуществления кодон-оптимизирована. Способы кодон-оптимизации известны в данной области техники и могут использоваться, как описано здесь. Кодон-оптимизацию в некоторых вариантах осуществления можно использовать для приведения в соответствии частот кодонов в организмах-мишенях и организмах-хозяевах для обеспечения надлежащего фолдинга; смещения GC-содержания для увеличения стабильности мРНК или уменьшения образования вторичных структур; минимизации тандемных повторов кодонов или оснований, которые могут нарушать конструирование или экспрессию генов; модификации областей транскрипционного и трансляционного контроля; инсерции или делеции последовательности транспорта белков; делеции/добавления сайтов посттрансляционной модификации в кодированном белке (например, сайтов гликозилирования); добавления, делеции или перестановки белковых доменов; инсерции или делеции сайтов рестрикции; модификации сайтов связывания рибосомы и сайтов деградации мРНК; корректировки скорости трансляции, чтобы позволить различным доменам белка правильно складываться; или уменьшения или устранения проблемы образования вторичных структур внутри полинуклеотида. Инструменты, алгоритмы и наборы для кодон-оптимизации известны в данной области техники. Неограничивающие примеры включают наборы GeneArt (Life Technologies), DNA2.0 (Menlo Park CA) и/или запатентованные методы. В некоторых вариантах осуществления последовательность открытой рамки считывания (ORF) оптимизируется с использованием алгоритмов оптимизации.
В некоторых вариантах осуществления кодон-оптимизированная последовательность имеет идентичность последовательности менее чем 95%, идентичность последовательности менее чем 90%, идентичность последовательности менее чем 85%, идентичность последовательности менее чем 80% или идентичность последовательности менее чем 75% с встречающейся в природе или последовательностью дикого типа.
В некоторых вариантах осуществления кодон-оптимизированная последовательность имеет от 65% до 85% (например, примерно от 67% до примерно 85% или примерно от 67% до примерно 80%) идентичность последовательности с встречающейся в природе последовательностью или последовательностью дикого типа. В некоторых вариантах кодон-оптимизированная последовательность имеет от 65% до 75% или примерно 80% идентичность последовательности с встречающейся в природе последовательностью или последовательностью дикого типа.
Способы лечения
В настоящем документе обеспечиваются композиции (например, фармацевтические композиции), способы, наборы и реагенты для профилактики и/или лечения RSV у людей и других млекопитающих. Вакцины против вируса RSV можно использовать в качестве терапевтических или профилактических агентов. Они могут быть использованы в медицине для профилактики и/или лечения инфекционных заболеваний. В примерных аспектах иммуногенные композиции RSV по настоящему изобретению используются в качестве вакцин для обеспечения профилактической защиты от вируса RSV. Профилактическая защита от вируса RSV может быть достигнута после введения вакцины против RSV по настоящему изобретению. Вакцины можно вводить один, два, три, четыре или более раз. Возможно, хотя и менее желательно, вводить вакцину инфицированному человеку для достижения терапевтического ответа. В этом случае может потребоваться скорректировать соответствующим образом дозировку.
В некоторых вариантах осуществления иммуногенные композиции RSV по настоящему изобретению можно использовать в качестве способа профилактики инфекции, вызванной RSV, у субъекта, где способ включает введение указанному субъекту по меньшей мере одной иммуногенной композиции RSV, описанной здесь. В некоторых вариантах осуществления иммуногенные композиции RSV по настоящему изобретению можно использовать в качестве способа лечения инфекции, вызванной RSV, у субъекта, где способ включает введение указанному субъекту по меньшей мере одной иммуногенной композиции RSV, описанной здесь. В некоторых вариантах осуществления иммуногенные композиции RSV по настоящему изобретению могут использоваться в качестве способа снижения частоты возникновения RSV у субъекта, где способ включает введение указанному субъекту по меньшей мере одной иммуногенной композиции RSV, описанной здесь. В некоторых вариантах осуществления иммуногенную композицию RSV по настоящему изобретению можно использовать в качестве способа ингибирования распространения RSV от первого субъекта, инфицированного RSV, второму субъекту, не инфицированному RSV, где способ включает введение, по меньшей мере, одному из указанного первого субъекта и указанного второго субъекта по меньшей мере одной иммуногенной композиции RSV, описанной здесь.
В аспектах изобретения обеспечивается способ индукции иммунного ответа у субъекта против RSV. Способ включает введение субъекту иммуногенной композиции RSV, описанной здесь, тем самым индуцируя у субъекта иммунный ответ, специфичный к RSV.
Профилактически эффективная доза представляет терапевтически эффективную дозу, которая предупреждает заражение вирусом на клинически приемлемом уровне. В некоторых вариантах осуществления терапевтически эффективной дозой является доза, указанная на вкладыше для вакцины в упаковке.
Терапевтические и профилактические композиции
В настоящем документе обеспечиваются композиции (например, фармацевтические композиции), способы, наборы и реагенты для профилактики, лечения или диагностики RSV, например, у людей и других млекопитающих. Иммуногенные композиции RSV, включая вакцины, можно использовать в качестве терапевтических или профилактических агентов. Они могут быть использованы в медицине для профилактики и/или лечения инфекционных заболеваний. В некоторых вариантах осуществления иммуногенные композиции RSV по настоящему изобретению можно использовать для лечения RSV.
Иммуногенные композиции RSV, включая вакцины против RSV, можно вводить профилактически или терапевтически в виде части схемы активной иммунизации здоровым людям или на ранних стадиях инфекции во время инкубационного периода или во время активной инфекции после появления симптомов. В некоторых вариантах осуществления количество вакцины по настоящему изобретению, обеспеченное клетке, ткани или субъекту, может представлять количество, эффективное для иммунопрофилактики.
Иммуногенные композиции RSV, включая вакцины против RSV, можно вводить с другими профилактическими или терапевтическими соединениями. В качестве неограничивающего примера, профилактическое или терапевтическое соединение может представлять собой адъювант или бустер-компонент. Как здесь используется, применительно к профилактической композиции, такой как вакцина, термин «бустер-компонент» относится к дополнительному введению профилактической (вакцинной) композиции. Бустер (или бустер-компонент) можно вводить после более раннего введения профилактической композиции. Время введения между начальным введением профилактической композиции и бустер-компонента может составлять, не ограничиваясь этим, 1 мин, 2 мин, 3 мин, 4 мин, 5 мин, 6 мин, 7 мин, 8 мин, 9 мин, 10 мин, 15 мин, 20 мин, 35 мин, 40 мин, 45 мин, 50 мин, 55 мин, 1 ч, 2 ч, 3 ч, 4 ч, 5 ч, 6 ч, 7 ч, 8 ч, 9 ч , 10 ч, 11 ч, 12 ч, 13 ч, 14 ч, 15 ч, 16 ч, 17 ч, 18 ч, 19 ч, 20 ч, 21 ч, 22 ч, 23 ч, 1 сутки, 36 ч, 2 суток, 3 суток, 4 суток, 5 суток, 6 суток, 1 неделю, 10 суток, 2 недели, 3 недели, 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 1 год, 18 месяцев, 2 года, 3 года, 4 года, 5 лет, 6 лет, 7 лет, 8 лет, 9 лет, 10 лет, 11 лет, 12 лет, 13 лет , 14 лет, 15 лет, 16 лет, 17 лет, 18 лет, 19 лет, 20 лет, 25 лет, 30 лет, 35 лет, 40 лет, 45 лет, 50 лет, 55 лет, 60 лет, 65 лет, 70 лет, 75 лет, 80 лет, 85 лет, 90 лет, 95 лет или более 99 лет. В некоторых вариантах осуществления время введения между начальным введением профилактической композиции и бустер-компонента может составлять, не ограничиваясь этим, 1 неделю, 2 недели, 3 недели, 1 месяц, 2 месяца, 3 месяца, 6 месяцев или 1 год.
В некоторых вариантах осуществления иммуногенные композиции RSV, включая вакцины против RSV, можно вводить внутримышечно, внутрикожно или интраназально, аналогично введению инактивированных вакцин, известных в данной области. В некоторых вариантах осуществления иммуногенные композиции RSV, включая вакцины против RSV, вводят внутримышечно.
Иммуногенные композиции RSV, включая вакцины против RSV, можно использовать в различных ситуациях в зависимости от распространенности инфекции или степени или уровня неудовлетворенных медицинских потребностей. Вакцины обладают превосходными свойствами в том смысле, что они продуцируют гораздо более высокие титры антител и вызывают реакции раньше, чем коммерчески доступные противовирусные агенты/композиции.
В настоящем документе обеспечиваются фармацевтические композиции, включающие иммуногенные композиции RSV, необязательно в комбинации с одним или более фармацевтически приемлемыми эксципиентами.
Иммуногенные композиции RSV, которые включают вакцины против RSV, можно формулировать или вводить самостоятельно или в сочетании с одним или более другими компонентами. Например, такие композиции могут содержать другие компоненты, включая, не ограничиваясь этим, адъюванты.
В некоторых вариантах осуществления иммуногенные композиции RSV не включают адъювант (т.е. они не содержат адъюванта).
Было давно установлено, что соединения алюминия стимулируют иммунную реакцию против совместно вводимых антигенов. Вакцинные составы по настоящему изобретению адсорбированы на алюминиевом адъюванте. Предпочтительно, чтобы алюминиевый адъювант в композициях по настоящему изобретению не находился в форме осадка алюминия. Вакцины, осажденные на алюминии, могут усиливать иммунную реакцию в отношении антигена-мишени, но при этом являются высоко гетерогенными составами и не позволяют получить сопоставимые результаты (см. публикацию Lindblad E.B. Immunology and Cell Biology 82:497-505 (2004)). В отличие от этого вакцины, адсорбированные на соединении алюминия, могут быть стандартизированы, что является важной характеристикой вакцинных составов, предназначенных для введения человеку. Кроме того, считается, что физическая адсорбция требуемого антигена на алюминиевом адъюванте имеет важное значение для функционирования адъюванта, вероятно, благодаря более медленному распространению от места инъекции или более эффективному поглощению антигена антигенпрезентирующими клетками.
Адъювант на основе соединений алюминия по настоящему изобретению может находиться в форме гидроксида алюминия (Al(OH)3), фосфата алюминия (AlPO4), гидроксифосфата алюминия, аморфного сульфата гидроксифосфата алюминия (AAHS) или так называемых «квасцов» (KA1(S04)⋅12H20) (см. Klein et al., Klein et al, Analysis of aluminium hydroxyphosphate vaccine adjuvants by (27)A1 MAS NMR., J. Pharm. Sci. 89(3): 311-21 (2000)). В примерных вариантах осуществления изобретения адъювант на основе алюминия представляет гидроксифосфат алюминия или AAHS. Соотношение фосфата и алюминия в алюминиевом адъюванте может составлять от 0 до 1,3. В предпочтительных вариантах осуществления этого аспекта изобретения соотношение фосфата к алюминию находится в диапазоне от 0,1 до 0,70. В особенно предпочтительных вариантах осуществления соотношение фосфата к алюминию находится в диапазоне от 0,2 до 0,50. MAPA представляет водную суспензию гидроксифосфата алюминия. MAPA получают смешиванием хлорида алюминия и фосфата натрия в объемном соотношении 1:1 для осаждения гидроксифосфата алюминия. После процесса смешивания материал уменьшают в размере с помощью смесителя с высоким сдвиговым усилием для достижения целевого размера частиц агрегата в диапазоне 2-8 мкм. Затем продукт подвергают диафильтрации против физиологического раствора и стерилизуют паром. См., например, публикацию международной патентной заявки № WO2013/078102.
В некоторых вариантах осуществления изобретения адъювант на основе соединения алюминия находится в форме AAHS (взаимозаменяемо относится здесь к «алюминиевому адъюванту Merck (MAA)»). MAA несет нулевой заряд при нейтральном pH, в то время как AlOH несет общий положительный заряд, в то время как AlPO4 обычно несет общий отрицательный заряд при нейтральном pH.
Специалист в данной области может определить оптимальную дозу адъюванта на основе соединения алюминия, которая является одновременно безопасной и эффективной в усилении иммунного ответа на целевые антигенные полипептиды. Для ознакомления с профилем безопасности алюминия, а также количества алюминия, включенного в вакцины, лицензированные FDA, см. Baylor et al., Vaccine 20: S18-S23 (2002). Как правило, эффективная и безопасная доза алюминиевого адъюванта варьируется от 150 до 600 мкг/дозу (концентрация от 300 до 1200 мкг/мл). В конкретных вариантах осуществления составов и композиций по настоящему изобретению содержится 200-300 мкг алюминиевого адъюванта на дозу вакцины. В альтернативных вариантах осуществления составов и композиций по настоящему изобретению количество алюминиевого адъюванта составляет 300-500 мкг на дозу вакцины.
Иммуногенные композиции RSV, включая вакцины против RSV, можно формулировать или вводить в комбинации с одним или более фармацевтически приемлемыми эксципиентами. В некоторых вариантах осуществления композиции содержат, по меньшей мере, одно дополнительное активное вещество, например, такое как терапевтически активное вещество, профилактически активное вещество или их комбинацию. Композиции могут быть стерильными, апирогенными или как стерильными, так и апирогенными. Общие принципы формуляции и/или производства фармацевтических агентов, таких как вакцинные композиции, можно найти, например, в монографии Remington: The Science and Practice of Pharmacy, 21-е изд., Lippincott Williams & Wilkins, 2005 (в полном объеме включена здесь посреством ссылки). В некоторых вариантах осуществления иммуногенные композиции RSV, включая вакцины против RSV, вводят людям, пациентам-людям или субъектам.
Составы иммуногенных композиций RSV, описанные здесь, можно приготовить любым способом, известным или разработанным в будущем в области фармакологии. Как правило, такие способы приготовления включают стадию объединения активного ингредиента (например, полипептида или полинуклеотида) с эксципиентом и/или одним или более другими вспомогательными ингредиентами, и затем, при необходимости и/или если желательно, разделение, придание формы и/или упаковку продукта в желаемую разовую или мультидозовую единицу.
Относительные количества активного ингредиента, фармацевтически приемлемого эксципиента и/или любых дополнительных ингредиентов в фармацевтической композиции в соответствии с настоящим изобретением будут варьироваться в зависимости от идентичности, размера и/или состояния субъекта, которого лечат, и, кроме того, в зависимости от пути, которым должна вводиться композиция. Например, композиция может содержать от 0,1 до 100%, например, от 0,5 до 50%, от 1 до 30%, от 5 до 80%, по меньшей мере, 80% (мас./мас.) активного ингредиента.
Способы введения вакцин
Иммуногенные композиции RSV, включая вакцины против RSV, можно вводить любым путем, который приводит к терапевтически эффективному результату. Они включают, не ограничиваясь этим, внутрикожное, внутримышечное, интраназальное и/или подкожное введение. Настоящее раскрытие обеспечивает способы, включающие введение композиций субъекту, нуждающемуся в этом. Точное требуемое количество будет варьироваться от субъекта к субъекту в зависимости от вида, возраста и общего состояния здоровья субъекта, тяжести заболевания, конкретной композиции, способа ее введения, механизма ее действия и тому подобное. Иммуногенные композиции RSV обычно формулируют в разовой лекарственной форме для простоты введения и однородности дозировки. Понятно, однако, что решение о суммарном суточном применении вакцинных композиций будет приниматься лечащим врачом по результатам тщательной клинической оценки. Конкретный терапевтически эффективный, профилактически эффективный или подходящий уровень дозы для визуализации для любого конкретного пациента будет зависеть от множества факторов, включая расстройство, подлежащее лечению, и тяжесть расстройства; активность конкретного используемого соединения; конкретный используемый состав; возраст, масса тела, общее состояние здоровья, пол и рацион пациента; время введения, способ введения и скорость выведения конкретного используемого соединения; продолжительность лечения; лекарственные средства, используемые в комбинации или одновременно с конкретным применяемым соединением; и подобные факторы, хорошо известные в медицине.
В некоторых вариантах осуществления иммуногенные композиции RSV можно вводить в дозах, достаточных для доставки от 0,0001 мг/кг до 100 мг/кг, от 0,001 мг/кг до 0,05 мг/кг, от 0,005 мг/кг до 0,05 мг/кг, 0,001 мг/кг до 0,005 мг/кг, от 0,05 до 0,5 мг/кг, от 0,01 до 50 мг/кг, от 0,1 до 40 мг/кг, от 0,5 до 30 мг/кг, 0,01 мг/кг. до 10 мг/кг, от 0,1 мг/кг до 10 мг/кг или от 1 мг/кг до 25 мг/кг массы тела субъекта в сутки, один или несколько раз в день, в неделю, в месяц и т. д. для получения желаемого терапевтического, диагностического, профилактического или визуального эффекта. В типичных вариантах осуществления иммуногенные композиции RSV в виде вакцин можно вводить в дозах, достаточных для доставки от 0,0005 до 0,01 мг/кг, например, примерно от 0,0005 до примерно 0,0075 мг/кг, например, примерно 0,0005 мг/кг, примерно 0,001 мг/кг, примерно 0,002 мг/кг, примерно 0,003 мг/кг, примерно 0,004 мг/кг или примерно 0,005 мг/кг.
В некоторых вариантах осуществления иммуногенные композиции RSV можно вводить один или два (или более) раза в дозах, достаточных для доставки от 0,025 мг/кг до 0,250 мг/кг, от 0,025 мг/кг до 0,500 мг/кг, от 0,025 мг/кг до 0,750 мг/кг или от 0,025 до 1,0 мг/кг.
Иммуногенная фармацевтическая композиция RSV, описанная здесь, может быть формулирована в лекарственной форме, описанной здесь, такой как лекарственная форма для интраназального, интратрахеального или инъекционного введения (например, для внутривенного, внутриглазного, интравитреального, внутримышечного, внутрикожного, интракардиального, внутрибрюшинного, интраназального и подкожного введения).
Настоящее изобретение не ограничивается в своем применении деталями конструирования и расположения компонентов, изложенными в последующем описании или иллюстрированными на чертежах. Изобретение допускает другие варианты осуществления и может быть применено на практике или выполнено различными способами. Кроме того, фразеология и терминология, используемые в данном документе, предназначены для целей описания и не должны рассматриваться как ограничивающие. Использование «включающий», «содержащий» или «имеющий», «входящий в состав», «вовлекающий» и их варианты в настоящем документе подразумевает включение элементов, перечисленных после и их эквивалентов, а также дополнительных элементов.
Примеры
Пример 1: получение одноцепочечных мутантов, содержащих фрагменты F1 и F2, соединенные пептидным линкером
Полипептид F RSV дикого типа расщепляется на фрагменты F1 и F2 фурин-протеазой хозяина после трансляции. Для оценки одноцепочечных мутантов RSV, которые не расщепляются фурином и которые остаются в виде одного полипептида, аминокислоты 98-146 WT RSV (где эти аминокислоты включают сайты расщепления фурином, пептид р27 и часть слитого пептида) заменяли гибким аминокислотным линкером различной длины (8-14 аминокислот) на фоне стабилизирующих мутаций «до слияния» DS-Cav1 (S155C, S190F, V207L и S290C) (McLellan et al. 2013). У этих мутантов домен тримеризации фабритина фага Т4 (фолдон) был присоединен к С-концу эктодомена F RSV, за которым следовал сайт расщепления протеазой и метка для очистки. Последовательности мутантного F RSV кодон-оптимизировали для использования кодонов млекопитающих, клонировали в экспрессионный вектор и транзиентно трансфектировали в суспензионную культуру клеток Expi293 (Life Technologies). Клеточные культуральные супернатанты собирали на сутки 3-7 после трансфекции плазмидой для оценки связывания этих мутантов с различными антителами против F RSV. Вкратце, 96-луночные планшеты, покрытые Ni-NTA (Thermo Scientific), покрывали клеточными культуральными супернатантами в течение 1 ч при комнатной температуре. Несвязанные сайты блокировали добавлением 2% (об./об.) бычьего сывороточного альбумина (BSA) в PBS и инкубацией в течение 1 ч при комнатной температуре. Планшеты промывали PBS, содержащим 0,05% (об./об.) Твина™ 20 (полисорбата 20) (PBS-T), и инкубировали с серийными разведениями антител (D25 или Synagis® (паливизумаб)) при комнатной температуре в течение 1 ч. Планшеты снова промывали PBS-T и инкубировали в течение 1 ч при комнатной температуре с вторичным козьим антителом против человеческого IgG, конъюгированным с HRG (Thermo Fisher) в разведении 1:2000. После дополнительного промывания PBS-T и быстрого ополаскивания ddH2O добавляли субстрат Super AquaBlue ELISA (eBiosience), и планшет сразу анализировали на ридере при 405 нм в течение 5 мин. Для каждой лунки рассчитывали mOD/мин.
На фиг. 1А и 1В показано связывание свежесобранных культуральных клеточных супернатантов после трансфекции на сутки 7 с конструктом 40а (DS-Cav1 с линкером из 8 аа) (фиг. 1А) или образцов супернатантов, которые хранили при 4°С в течение 8 суток (фиг. 1В), с моноклональными антителами D25 и Synagis® (паливизумаб). Мутант LZF40a демонстрировал низкое специфическое связывание с mAb D25, специфического для формы «до слияния». Связывание с паливизумабом (который реагирует как с формой F «до слияния», так и с формой F «после слияния») было высоким, что свидетельствует о том, что мутант хорошо экспрессировался. На фиг. 2А и 2В показано связывание свежесобранных клеточных культуральных супернатантов с LZF55a, LZF56a и LZF57a на сутки 3 после трансфекции (DS-Cav1 с линкером из 10, 12 или 14 аминокислот соответственно; фиг. 2А, 2В, 2С соответственно) или образцов, которые хранили при 4°C в течение 7 суток (фиг. 2D, 2E и 2F соответственно), с D25 и паливизумабом. Все три мутанта хорошо экспрессировались, основываясь на реактивности с паливизумабом. Среди этих мутантов LZF57a (DS-Cav1 с линкером из 14 аминокислот) демонстрировал самое высокое специфическое для формы «до слияния» связывание с mAb D25 и сохранял связывание с D25 после 7 суток хранения при 4°C.
В дополнение к ELISA клеточные культуральные супернатанты, собранные на различные временные точки после трансфекции, анализировали с помощью вестерн-блоттинга с антисывороткой против F RSV. Супернатанты обрабатывали загрузочным буфером SDS с восстановителем (Life Technologies), наносили на гель для электрофореза и затем переносили электропереносом на нитроцеллюлозные мембраны (Life Technologies). Мембраны блокировали в течение ночи при 4°С блокатором для блоттинга (BioRad) в 1X TBST (забуференном Трис-буфером солевом растворе+Твин). Мембраны инкубировали с поликлональными сыворотками морских свинок против эктодомена белка F RSV дикого типа (Sino Biological), и затем с АР-конъюгированным вторичным козьим антителом против IgG морской свинки (Santa Cruz Biotechnology). Одноцепочечные мутанты RSV LZF55a, LZF56a и LZF57a показали достоверно более высокие уровни экспрессии по сравнению с исходным DS-Cav1 (фиг.3). DS-Cav1 появлялся на геле в виде двух полос: верхняя полоса представляет нерасщепленный F-белок, и нижняя полоса представляет фрагмент F1, расщепленный фурином. Одноцепочечные мутанты RSV LZF55, LZF56 и LZF57 появились в виде единственной преобладающей полосы на геле, представляющей нерасщепленный F.
Пример 2: дополнительные стабилизирующие мутации
Моноклональное антитело 4D7, которое реагирует с антигенным сайтом I на F-белке в конформации RSV «после слияния», можно использовать для оценки стабильности структуры F «до слияния» (Flynn et al. 2016). Свежесобранные клеточные культуральные супернатанты с DS-Cav1 или конструктами LZF57a оценивали с помощью ELISA на связывание с D25 и 4D7 (фиг. 4C). Несмотря на то, что конструкт LZF57a сохранил способность к связыванию с D25, что указывает на его конформацию «до слияния», он, по-видимому, демонстрирует повышенное связывание с 4D7 по сравнению с исходным конструктом DS-Cav1, свидетельствуя о том, что при введении одноцепочечного линкера могут иметь место тонкие конформационные изменения. Для дальнейшей стабилизации одноцепочечного мутантного конструкта RSV LZF57a проводили конструирование на основе структуры для получения вариантов с мутациями дисульфидной связи; мутациями заполнения полости; и/или мутациями дестабилизации конформации «после слияния». В частности, модель дисульфидного мутанта D486C/D489C, основанная на кристаллической структуре белка F «до слияния», предполагает, что межмолекулярная дисульфидная связь в пределах 3,8 Å может помочь в дальнейшей стабилизации конформации «до слияния» (данные не показаны). Выбранные мутации объединяли с мутациями LZF57a и оценивали с использованием mAb D25 и 4D7, специфичных для формы «до слияния», как описано выше. Мутант LZF 111a (который соответствует LZF57a с мутацией D486C/D489C) проявлял пониженное связывание с 4D7 по сравнению с конструком LZF57a, позволяя предположить, что он может принимать в большей степени конформацию «до слияния» (фиг. 4B, 4C и 4D). На фиг. 10 представлена схема конструктов LZF111 и LZF57.
В целях дополнительной характеристики мутанта LZF111, белки F RSV (DS-Cav1 и LZF111a) очищали от культуральных супернатантов с помощью ранее описанного метода в модификации (McLellan 2013). Вкратце, His-меченые белки очищали с использованием хроматографии на Ni-сефарозе (GE Healthcare). Метки удаляли расщеплением в течение ночи тромбином. Расщепление проводили во время диализа для снижения концентрации имидазола. Для удаления коэлюирующих примесей и нерасщепленного F-белка, образцы подвергали второй стадии хроматографии на Ni-сефарозе. F-белки дополнительно очищали гель-хроматографией (Superdex 200, GE Healthcare) и хранили в буфере из 50 мМ HEPES, рН 7,5, 300 мМ NaCl. Проводили анализ SDS-PAGE в восстанавливающих и невосстанавливающих условиях для оценки образования дисульфидных связей (фиг. 4D). Вкратце, образцы очищенного белка обрабатывали загрузочным буфером SDS с или без восстановителя (Life Technologies), нагревали при 95°C в течение 2-3 мин и наносили на гель для электрофореза NuPAGE (Invitrogen). Гели окрашивали окрашивающим раствором Gel Code Blue (Pierce) и отмывали избыток красителя водой. В восстанавливающих условиях DS-Cav1 появлялся в виде двух полос на геле, представляющих расщепленные фрагменты F1 и F2, как и ожидалось. В невосстанавливающих условиях DS-Cav1 появлялся в основном в виде полосы, соответствующей примерно 50 кДа, представляющей один расщепленный фрагмент F1 и один фрагмент F2, удерживаемые вместе нативными дисульфидными связями. Как и ожидалось, одноцепочечный мутант RSV, LZF57 появлялся на геле в основном в виде полосы, соответствующей нерасщепленномй мономеру F0, при любом условии электрофореза. Изменение подвижности LZF57 в восстанавливающих и невосстанавливающих условиях, скорее всего, является результатом потери компактности в восстанавливающих условиях, что приводит к увеличению кажущейся молекулярной массы. Одноцепочечный мутант RSV, LZF111 также появлялся в основном в виде полосы нерасщепленного мономера F0 на геле в восстанавливающих условиях. В невосстанавливающих условиях, хотя имели место две субдоминантные нижние полосы, соответствующие 50 кДа и 100 кДа, согласующиеся с мономерной и димерной формами, доминирующая полоса LZF111 смещалась вверх примерно к 150 кДа, что согласуется с молекулярной массой тримера. Поскольку мутации D486C/D489C были единственным различием между конструками LZF57 и LZF111, то эти данные свидетельствуют о том, что сконструированная межмолекулярная дисульфидная связь действительно образуется в большинстве молекул LZF111.
Пример 3: исследования стабильности LZF111
Для анализа вторичных структур очищенных белков F RSV, получали спектры кругового дихроизма («CD») на спектрометре Chirascan (Applied Photophysics LtD, UK). Образцы анализировали после замены буфера на 10 мМ Na2HPO4 с использованием спин-колонок Zeba (Pierce) и последующего разведения 1:2 в 10 мМ Na2HPO4, что давало конечную концентрацию белка 3,9 мкМ и 4,4 мкМ для DsCav-1 и LZF111 соответственно. CD спектры записывали в неразбавленном виде с использованием кварцевой кюветы с длиной пути 0,5 мм. Контроль температуры устанавливали на 20°C. Ширина полосы была установлена на 1 нм. Точки данных между 185 и 260 нм получали с интервалами 1 нм со временем отбора образцов в 5 с на временную точку. Спектр образца и буфера получали после 10 мин уравновешивания температуры, используя три технических повтора, соответственно. Средние спектры буфера вычитали из спектров образцов. Результирующие точки данных сглаживали с помощью алгоритма Савицкого-Голея (порядок полинома 2, две точки данных слева и справа) с использованием пакета программ Origin Pro 7.5 SR7 (Origin Lab Corporation). CD спектры DS-Cav1 и LZF 111 были практически идентичными (фиг.5А и 5В). Вторичные структуры дополнительно анализировали реконструкцией CD спектров (от 185 до 260 нм) с использованием искусственной нейронной сети с обучением для CD спектров белков с разрешенной трехмерной структурой (программное обеспечение CDNN: нейронная сеть для кругового дихроизма) (фиг. 6), указывая на то, что модификации LZF111 не приводила к значительным изменениям во вторичных структурах F-белка в конформации «до слияния».
Дифференциальный сканирующий флуориметрический анализ (DSF) проводили с белками DS-Cav1 и LZF111 для оценки их стабильности. Растворы белка DS-Cav1 (0,27-35 мкМ) в буфере из 50 мМ HEPES, 300 мМ NaCl при рН 7,5 готовили серийным разведением. Сигнал флуоресценции каждого образца белка в объеме 85 мкл в микрокварцевой кювете с длиной оптического пути 3×3 мм (Thermo Fisher) регистрировали с использованием флуориметра Cary Eclipse, оборудованного регулятором температуры Cary (Agilent Technologies, CA). Собственную флуоресценцию белка регистрировали при 330 нм и 350 нм. Длину волны возбуждения устанавливали на 280 нм с шириной щели 10 нм. Ширина эмиссионной щели была установлена равной 2,5 нм. Напряжение фотоумножителя регулировали перед каждым измерением до значений между 500 В и 800 В для максимизации сигнала флуоресценции. Эксперименты по термическому разворачиванию белков проводили с использованием температурного изменения 1°С/мин от 20°С до 95°С с шагом 0,5°С. Образец уравновешивали при начальной температуре в течение 1 мин, и сигналы флуоресценции усредняли для каждой точки данных в течение 1,5 с. Многоячеистый держатель позволял анализировать до 4 образцов одновременно. Необработанные данные экспортировали для дальнейшей обработки с помощью Origin Pro®7.5 SR7 для получения кривых плавления интенсивности флуоресценции как функции температуры. Кривые плавления сглаживали (полиномиальный порядок=1, количество точек=12), и центры пиков первого производного с отношением между 350 нм и 330 нм использовали в качестве температур плавления (Tm). Данные нормализовали по наибольшей интенсивности сигнала для сравнения различных образцов белка или концентраций белка. DS-Cav1 имеет две переходные средние точки (60,85±1,98°C и 80,7± 0,93°C), которые представлены в виде среднего значения, полученного из всех концентраций белка, анализированных для одного и того же типа образца (Flynn et al. 2016) (фиг. 7). Для LZF111 представленную Tm (~81°C) получали из одной концентрации 15 мкМ (фиг. 7). Отсутствие более низкой Tm при ~60,85°C и более узкий пик для более высокой Tm при ~81°C свидетельствует о том, что LZF111 обладает улучшенной стабильностью по сравнению с DS-Cav1.
Долговременная стабильность при 4°С или выше является желательным признаком для субъединичного вакцинного антигена. Для оценки долговременной стабильности DS-Cav1 ранее использовали анализ связывания с антителами D25 и 4D7, а также биофизические анализы. Полученные данные показали, что при длительном хранении при 4°C DS-Cav1 претерпевает конформационные изменения, принимая альтернативные структуры, которые приобретают способность связываться с 4D7 (Flynn et al. 2016). Для оценки долговременной стабильности LZF111, очищенный белок DS-Cav1 или конструкт LZF111 хранили в замороженном виде или при 4°С в течение 1, 2 или 3 месяцев и оценивали с использованием D25, 4D7 и паливизумаба в анализе связывания ELISA. Вкратце, очищенные белки разбавляли до концентрации 1 мкг/мл PBS и вносили в 96-луночный планшет для постановки ELISA (NUNC) на ночь при 4°C. Несвязанные сайты блокировали добавлением 2% (об./об.) бычьего сывороточного альбумина (BSA) в PBS и инкубацией в течение 1 ч при комнатной температуре. Планшеты промывали PBS, содержащим 0,05% (об./об.) Твин® 20 (полисорбат 20) (PBS-T), и инкубировали с серийными разведениями антител (D25 или паливизумаба) при комнатной температуре в течение 1 ч. Планшеты снова промывали PBS-T и инкубировали в течение 1 ч при комнатной температуре с вторичным козьим антителом против человеческого IgG (для D25 и паливизумаба) или вторичным антителом против мышиного IgG, конъюгированным с HRP (Thermo Fisher) в разведении 1:2000. После дополнительного промывания PBS-T и быстрого ополаскивания ddH2O добавляли субстрат Super AquaBlue ELISA (eBiosience), и планшет сразу анализировали на ридере при 405 нм в течение 5 мин. Для каждой лунки рассчитывали mOD/мин. На фиг. 8А, 8В и 8С показано, что после хранения в течение 1 месяца при 4°С, в то время как реактивность D25 и паливизумаба сохранялась для обоих конструктов, было обнаружено достоверное увеличение связывания 4D7 с DS-Cav1, но не с улучшенным LZF111. Кроме того, не наблюдали повышенного связывания 4D7 с LZF111 после хранения в течение 2 и 3 месяцев при 4°C (фиг. 8D и 8E), свидетельствуя о том, что долговременная стабильность LZF111 превосходит DS-Cav1.
Пример 4: исследование иммуногенности
Исследование иммуногенности на мышах проводили для сравнения иммуногенности субъединичных вакцин DS-Cav1 и LZF111. Опытными животными были самки мышей BALB/c, полученные из питомника Charles River Laboratories. 10 мышей на группу иммунизировали дважды тремя различными дозами (2 мкг, 0,4 мкг и 0,2 мкг) очищенных белков DS-Cav1 или LZF 111a с адъювантами на основе алюминия на неделе 0 и 3. Образцы крови отбирали через 2 недели после каждой иммунизации и сыворотки анализировали. Для определения титров антител, связывающихся с F-белком в конформации «до слияния», микротитрационные планшеты immulon 12HB (NUNC) покрывали из расчета 2 мкг/мл очищенным рекомбинантным белком F RSV DS-Cav1 и инкубировали при 4°С в течение ночи. Затем планшеты промывали и блокировали в течение 1 ч PBS-T, содержащим 3% обезжиренного молока (блокирующий буфер) при комнатной температуре. Готовили 4-кратные серийные разведения испытуемых образцов в блокирующем буфере (начиная с разведения 1:50), переносили в планшеты, покрытые F RSV, и инкубировали в течение 2 ч при комнатной температуре. После трех промываний PBS-T в планшеты добавляли вторичное антитело против мышиного IgG, конъюгированное с HRP (Invitrogen) в разведении 1:3000 в блокирующем буфере, и инкубировали еще в течение 1 ч. Планшеты снова промывали и окрашивание развивали SuperBlu Turbo TMB (Virolabs) в темноте. Реакцию останавливали через 5 мин и измеряли оптическую плотность при 450 нм на планшетном ридере VersaMax ELISA (Molecular Devices). Титры ED10 в ELISA, которые указывали на эффективное разведение образца сыворотки, дающее 10% от максимального сигнала, определяли с помощью построения четырехпараметрической кривой с использованием программного обеспечения GraphPad Prism 7. На фиг. 9А показаны титры ED10 ELISA на F-белок в форме «до слияния» после введения дозы 2. Нижняя горизонтальная пунктирная линия обозначает предел детектирования. Полученные данные показали, что LZF111 индуцировал сходные уровни антител против F-белка в конформации «до слияния» по сравнению с DS-Cav1 в разных дозах.
Анализ нейтрализации также проводили на мышиной сыворотке, которую обрабатывали при 56°С в течение 30 мин для инактивации комплемента перед тестированием. Готовили двухкратные серийные разведения образцов сыворотки в EMEM, содержащей 2% FBS, начиная с разведения 1:4. Разбавленную сыворотку вносили в двух повторностях в 96-луночные планшеты и смешивали со штаммом RSV Long (100 БОЕ/мл) в общем объеме 100 мкл. Смесь образцов вируса и сыворотки инкубировали в течение 1 ч при 37°С в атмосфере с 5% СО2. После инкубации добавляли клетки Hep-2 в концентрации 1,5×104 клеток на лунку. Планшеты инкубировали в течение 3 суток при 37°С с 5% СО2. Затем клетки промывали и фиксировали 80% ацетоном в течение 15 мин. Затем клетки, инфицированные RSV, иммуноокрашивали. Вкратце, F RSV- и N-специфические моноклональные антитела добавляли в опытные планшеты с фиксированными клетками и инкубировали в течение 1 ч при комнатной температуре. После промывания добавляли биотинилированные козьи антимышиный IgG антитела и инкубировали в течение 1 ч. Планшеты снова промыли и проявляли с помощью двухканальной системы детектирования в ближнем инфракрасном свете (NID). Инфракрасный краситель-стрептавидин для детектирования RSV-специфического сигнала и два красителя клеток для нормализации анализа добавляли в 96-луночные планшеты и инкубировали в течение 1 ч в темноте. Планшеты промывали, высушивали в темноте в течение 20 мин и анализировали на автоматической системе визуализации Licor Aerius1, используя лазер 700 channel для нормализации клеток и лазер 800 channel для детектирования RSV-специфического сигнала. Рассчитывали соотношения 800/700, и определяли титры нейтрализующих антител в сыворотке (IC50) с помощью построения четырехпараметрической кривой программным обеспечением GraphPad Prism 7. Сывороточные титры нейтрализации PD2 сыворотки против штамма RSV Long показаны на фиг. 9В. Нижняя горизонтальная пунктирная линия обозначает предел детектирования. Данные показали, что LZF111 индуцировал сходные уровни нейтрализующих антител с DS-Cav1 в разных дозах.
Пример 5: исследование иммуногенности на хлопковых крысах
В данном примере проводили опыты для тестирования иммуногенности и эффективности вакцин мРНК/LNP на модели хлопковых крыс, зараженных RSV. Более конкретно, использовали самок хлопковых крыс Sigmodon hispidus, и иммунизацию начинали в возрасте 6-7 недель. Готовили используемые мРНК-вакцины и формулировали в виде липидных наночастиц. мРНК-вакцины, тестированные в этом исследовании, включали:
MRK-04 мембраносвязанный DS-Cav1 (стабилизированный F-белок в конформации «до слияния»)
MRK-04_nopolyA_3mut мембраносвязанный DS-Cav1 (стабилизированный F-белок в конформации «до слияния»)
mVRC-1 (v2) мембраносвязанные одноцепочечные sc9 mDS-Cav1, A149C, Y458C (стабилизированный F-белок в конформации «до слияния»)
MLZF-111 мембраносвязанные одноцепочечные mDS-Cav1, D486C, D489C (стабилизированный F-белок в конформации «до слияния»)
Группы из 8 хлопковых крыс иммунизировали внутримышечно 100 мкл вакцины с введением по 50 мкл в каждую четырехглавую мышцу бедра. Группы вакцинировали следующими вакцинами:
Животных иммунизировали на сутки 0 и сутки 28 эксперимента. На сутки 28 и 56 дни у каждого животного отбирали образцы крови и использовали для серологических анализов. На сутки 56 хлопковым крысам вводили интраназально 1×105,5 БОЕ RSV A2. Через четыре дня после инокуляции животных подвергали эвтаназии ингаляцией CO2 и извлекали легкие (левые доли) и носовые раковины и гомогенизировали в 10 объемах сбалансированного солевого раствора Хенкса (Lonza), содержащего SPG, на влажном льду. Образцы осветляли центрифугированием при 2000 об/мин в течение 10 мин, аликвотировали, быстро замораживали и сразу хранили в замороженном виде при -70°С.
Анализ нейтрализации RSV:
Сыворотку хлопковых крыс от каждого животного оценивали на нейтрализацию RSV-A (штамм Long) с использованием следующих процедур:
1. Все образцы сывороток инактивировали нагреванием, помещая их на сухую баню-термостат, установленную на 56°C, на 30 мин. Затем опытные образцы и контрольные сыворотки разбавляли 1:3 разбавителем для вируса (2% FBS в EMEM), и образцы в двух повторностях добавляли в планшет для анализа и готовили серийные разведения.
2. Стоковый раствор вируса RSV-Long извлекали из морозильной камеры и быстро размораживали на водяной бане при 37°С. Вирусы разбавляли до 2000 БОЕ/мл разбавителем для вируса.
3. 50 мкл разведенного вируса вносили в каждую лунку 96-луночного планшета, за исключением одного ряда с клетками, который использовали в качестве контроля «без вируса».
4. Клетки HEp-2 трипсинизировали, промывали, ресуспендировали при 1,5×105 клеток/мл разбавителем для вируса и 100 мл суспендированных клеток вносили в каждую лунку 96-луночного планшета. Затем планшеты инкубировали в течение 72 ч при 37°С, в атмосфере с 5% СО2.
5. После 72-ч инкубации клетки промывали PBS и фиксировали, используя 80% ацетон, растворенный в PBS, в течение 10-20 мин при 16-24°C. Фиксатор удаляли и планшеты высушивали на воздухе.
6. Затем планшеты тщательно промывали PBS+0,05% Твина. Моноклональные антитела для детектирования, 143-F3-1B8 и 34C9, разбавляли до концентрации 2,5 мкг/мл разбавителем для анализа (1% BSA-PBS-0,1% Твина), и 50 мкл разведенных антител добавляли в каждую лунку 96 планшета. Затем планшеты инкубировали во влажной камере при 16-24°С в течение 60-75 мин на лабораторной качалке.
7. После инкубации планшеты тщательно промывали.
8. Биотинилированные лошадиные антимышиный IgG антитела разбавляли 1:200 разбавителем для анализа и добавляли в каждую лунку 96-луночного планшета. Планшеты инкубировали, как указано выше, и промывали.
9. Смесь из стрептавидина IRDye 800CW (конечное разведение 1:1000), Sapphire 700 (разведение 1:1000) и 5 мМ раствора DRAQ5 (разведение 1:10000) готовили в разбавителе для анализа и 50 мл смеси добавляли в каждую лунку 96-луночного планшета. Планшеты инкубировали, как описано выше, в темноте, промывали и оставляли сушиться на воздухе.
10. Затем планшеты анализировали с использованием Aerius Imager. Затем рассчитывали титры сывороточных нейтрализующих антител с использованием 4-параметрической кривой с использованием Graphpad Prism.
Титры, определенные после введения дозы 1 (сутки 28) и после введения дозы 2 (сутки 56), показаны на фиг. 11. Было обнаружено, что титры нейтрализующих антител индуцировались в зависимости от дозы для всех мРНК-вакцин. Все мРНК-вакцины приводили к увеличению титров после второй дозы независимо от тестированной дозы. Как mVRC-1 (v2), так и mLZF111 индуцировали более высокие титры, чем MRK-04 и MRK-04_nopolyA_3mut, демонстрируя высокие или сходные сывороточные титры нейтрализующих антител в 5 раз более низкой дозе.
Конкурентный анализ alphaLISA
Охарактеризовали иммунный ответ на специфические эпитопы белка F RSV для нейтрализующих антител. Антигенный сайт II является сайтом связывания с паливизумабом, моноклональным антителом, разработанным для профилактики инфекции нижних дыхательных путей RSV у младенцев и детей младшего возраста с повышенным риском заражения. Антигенный сайт Ø является сайтом связывания с более сильными нейтрализующими антителами, выработка которых индуцируется естественной инфекцией RSV. Кроме того, создали антитело (4D7), которое нацелено на сайт I эпитоп антитела (4D7), отсутствующий в конформации «до слияния». Следовательно, в отличие от D25, выявление 4D7-конкурентных антител может свидетельствовать о генерации F-подобных белков в конформации «после слияния» in vivo. Конкурентный анализ alphaLISA был разработан для характеристики ответа антигенного сайта Ø, антигенного сайта I и антигенного сайта II на различные вакцины на основе мРНК.
Для измерения титров конкурентных антител, 10 мкл образцов, серийно разбавленных в буфере HiBlock (PerkinElmer), помещали в 384-луночный планшет для постановки alphaLISA. Разбавленные образцы смешивали с 5 мкл акцепторных гранул AlphaLISA (100 мкг/мл), которые ранее были конъюгированы со стабилизированным белком F RSV в конформациии «до слияния» (DS-Cav1) или белком F RSV в конформации «после слияния» (F RSV wt). После 30-мин инкубации при комнатной температуре в каждую лунку добавляли 10 мкл биотинилированного антитела D25, паливизумаба или 4D7, разведенного в буфере HiBlock. Еще через 30 мин инкубации в каждую лунку добавляли 25 мкл донорных гранул, покрытых стрептавидином (20 мкг/мл) в буфере HiBlock и инкубировали в течение 30 мин в темноте. Затем планшет анализировали на EnVision_Alpha (детектирование при 615 нм).
Титры конкурентных антител паливизумаба, D25 и 4D7, измеренные на сутки 56 (4 недели PD2), представлены на фиг. 12. Данные конкурентного анализа выявили, что mVRC-1(v2) индуцировал более низкие уровни конкурентных антител 4D7 для белка F «после слияния», тогда как титры D25 «до слияния» и титры паливизумаба не изменялись. Такой различный профиль конкуренции коррелирует с мРНК mVRC-1 (v2), экспрессирующей более стабилизированный белок «до слияния», чем MRK-04_nopolyA_3mut и mLZF-111.
C. Результаты заражения хлопковых крыс
Процедуры измерения титров RSV в гомогенатах легких и носовой полости у хлопковых крыс описаны ниже. Гомогенаты легких и носовой полости осветляли центрифугированием и разбавляли 1:10 и 1:100 в EMEM. Конфлюэнтные монослои HEp-2 инфицировали в двух повторностях из расчета 50 мкл на лунку, начиная с неразбавленных (чистых) образцов и затем разбавленных гомогенатов в 24-луночных планшетах. После инкубации в течение часа при 37°C в термостате с 5% CO2, лунки покрывали 0,75% метилцеллюлозной средой и планшеты выдерживали в термостате при 37°C. После 4 суток инкубации покровный слой удаляли и клетки фиксировали 0,1% кристаллическим фиолетовым красителем в течение одного часа, затем промывали и высушивали на воздухе. Подсчитывали число бляшек и титры вируса выражали в бляшкообразующих единицах на грамм ткани.
Для оценки опосредованной вакциной защиты вирусные титры измеряли в легких и носовой полости через 5 суток после заражения. Все мРНК-вакцины обеспечивали полную защиту в легких, а mVRC-1 (v2) и mLZF111 демонстрировали улучшенную защиту в носовой полости, демонстрируя высокую или сходную эффективность с MRK-04 и MRK-04_nopolyA_3mut, в 5 раз меньшей дозе (фиг. 13).
Пример 6: оценка иммуногенности и эффективности на африканских зеленых мартышках
В данном примере проводили анализы для оценки иммуногенности и эффективности мРНК/LNP вакцин на модели заражения RSV африканских зеленых мартышек.
Более конкретно, использовали взрослых самцов и самок африканских зеленых мартышек с массой тела от 1,6 до 2,65 кг, которые, как было подтверждено по титру нейтрализующих антител, являются RSV-отрицательные. Готовили используемые мРНК-вакцины и формулировали в виде липидных наночастиц. мРНК-вакцины, тестированные в данном исследовании, включали:
MRK-04_nopolyA_3mut мембраносвязанный DS-Cav1 (стабилизированный F-белок в конформации «до слияния»)
mVRC-1 (v2) мембраносвязанные одноцепочечные sc9 mDS-Cav1, A149C, Y458C (стабилизированный F-белок в конформации «до слияния»)
MLZF-111 мембраносвязанные одноцепочечные mDS-Cav1, D486C, D489C (стабилизированный F-белок в конформации «до слияния»)
Группы из 4 африканских зеленых мартышек иммунизировали внутримышечно 500 мкл вакцины с введением в одну четырехглавую мышцу бедра. Группы были вакцинированы следующими вакцинами, как показано в таблице 1.
Составы вакцин, тестированных на иммуногенность на африканских зеленых мартышках
Животных иммунизировали на сутки 0, сутки 28 и сутки 56 эксперимента. На сутки 0, 14, 28, 42, 56 и 70 у каждого животного отбирали образцы крови и использовали для серологических анализов. На сутки 70 африканским зеленым мартышкам интраназально вводили 1×105,5 БОЕ RSV A2. Мазки из носоглотки собирали на сутки 1-14 после заражения, и образцы бронхоальвеолярного лаважа собирали на сутки 3, 5, 7, 9, 12 и 14 после заражения для тестирования на репликацию вируса.
А. Анализ нейтрализации RSV:
Сыворотки обезьян от каждого животного оценивали на нейтрализацию RSV-A (штамм Long), как описано выше. Титры NT50, определенные после введения дозы 1 и после введения дозы 2, показаны на фиг. 14. Видно, что титры возрастали после введения каждой дозы во всех группах, получавших мРНК-вакцины. GMT, полученные с помощью мРНК-вакцин на неделе 10 (через 2 недели после введения дозы 3), были на 1-2 порядка выше, чем у животных, получавших RSV A2, в зависимости от дозы и тестированной мРНК. Образцы сыворотки от животных, иммунизированных mVRC-1 (v2), демонстрировали самые высокие титры нейтрализации, показывая в 5 раз более высокую активность по сравнению с MRK-04_nopolyA_3mut.
В. Конкурентный ELISA
Титры в конкурентном анализе ELISA определяли для паливизумаба, D25 и 4D7 для характеристики ответа антигенного сайта Ø, антигенного сайта I и антигенного сайта II на различные вакцины на основе мРНК, как описано выше.
Титры конкурентных антител паливизумаба, D25 и 4D7, измеренные на неделе 10 (2 недели PD3), представлены на фиг.15. Данные конкурентного анализа выявили, что mVRC-1(v2) индуцировал более низкие уровни конкурентных антител 4D7 на F-белок в конформации «после слияния», в то время как титры D25 на белок в конформации «до слияния» и титры паливизумаба не изменялись. Такой разный профиль конкуренции коррелирует с мРНК mVRC-1 (v2), экспрессирующей более стабилизированный белок с конформацией «до слияния», чем MRK-04_nopolyA_3mut и mLZF-111.
C. Результаты заражения африканских зеленых мартышек
Как описано выше, для оценки эффективности вакцины африканским зеленым мартышкам вводили интраназально 1×105,5 БОЕ RSV A2 на сутки 70 после вакцинации, и отбирали мазки из носоглотки и бронхоальвеолярный лаваж после заражения для определения наличия вируса.
Для измерения титров RSV в образцах бронхоальвеолярного лаважа от африканских зеленых мартышек, использовали анализ вирусных бляшек для измерения титров вируса, как описано ниже. Вкратце, образцы разбавляли и вносили в двух повторностях в 24-луночные планшеты, содержащие конфлюентные монослои клеток HEp-2. Планшеты инкубировали при 37°С в течение одного часа. После инкубации в течение одного часа инокулят образца аспирировали и добавляли 1 мл покровного слоя, содержащего 0,75% метилцеллюлозы. Планшеты инкубировали при 37°С в течение 5 суток. После 5-дневной инкубации клетки фиксировали и окрашивали раствором кристаллического фиолетового/глутаральдегида. Подсчитывали число бляшек и титры выражали в БОЕ/мл. Анализ содержания вируса в жидкости бронхоальвеолярного лаважа (BAL) (фиг.16А-16С) показал, что только mVRC-1 (v2) (25 мкг) обеспечивает полную защиту в легких и обеспечивает лучшую защиту в более низкой дозе (5 мкг).
Для измерения титров RSV в носоглоточных мазках африканских зеленых мартышек, проводили анализ RSV с использованием ОТ-кПЦР для выявления RSV A следующим образом:
1) Оборудование и материалы:
А. Оборудование
1. Система для ПЦР в режиме реального времени Stratagene Mx3005P и программное обеспечение MxPro
2. Центрифуга Jouan GR422 или эквивалентная
3. Носители Jouan Plate или эквивалентные
В. Реагенты
1. Набор Quantitect® Probe Rt-PCR (1000), номер по каталогу 204445
2. Сверхчистая вода, не содержащая ДНКаз и протеаз Molecular Biology, 5 Prime, номер по каталогу 2900136
3. Буфер ТЕ, 10 мМ Трис, 1 мМ ЭДТА, рН 8,0, Fisher Bioreagents, номер по каталогу BP2473-100
4. Вирусные праймеры: прямой и обратный праймеры RSV A, Sigma custom, очищенные ВЭЖХ. Стоки праймеров восстанавливали до 100 мкМ сверхчистой водой и хранили при -20°С
5. Зонд с двойной меткой RSV, Sigma custom, очищенный ВЭЖХ. Стоки зондов восстанавливали до 100 мкМ буфером ТЕ и хранили при -20°С в защищенном от света месте
6. Стандарт RSV получали внутри компании и хранили при -20°C. Стандарты для анализа получали конструированием пар праймеров для гена N RSV A. Длина продукта для стандарта RSV A составляет 885 п.н. ОТ-ПЦР QIAGEN OneStep использовали для получения этого стандарта.
7. Набор для очистки общей вирусной нуклеиновой кислоты Promega, Maxwell® 16 (продукт № AS1150)
C. Поставки
1. Stratagene оптические крышки для реакционных пробирок в стрипах по 8 шт, номер по каталогу 401425
2. Stratagene Mx3000P 96-луночные планшеты, с ободком, номер по каталогу 401334
3. Наконечники с фильтром ART
2) Реакции ОТ-ПЦР и настройка
А. Подготовка полной смеси мастер-микс для ПЦР
1. Готовят полную смесь мастер-микс, следуя инструкциям ниже, для конечного реакционного объема 50 мкл. В следующей таблице приведен объем на лунку. Конечная концентрация праймеров составляет 300 нМ, и конечная концентрация зонда составляет 200 нМ.
2. Добавляют 45 мкл полной смеси мастер-микс в каждую лунку. Накрывают планшет крышкой и обертывают алюминиевой фольгой для защиты от света.
B. Построение стандартной кривой
1. Стандарт извлекают из морозильной камеры с температурой -20°C.
2. Разводят стандарты до конечных концентраций от 1ed копий/5 мкл до 1 копия/5 мкл, используя 10-кратные разведения.
C. Подготовка образцов
1. Образцы мазка из носоглотки и бронхоальвеолярного лаважа готовят для реакции ОТ-ПЦР с использованием набора для очистки общей вирусной нуклеиновой кислоты Maxwell® 16 (Promega, номер продукта AS1150).
2. 200 мкл образца извлекают в соответствии с протоколом изготовителя и элюируют в 50 мкл для использования в реакциях ПЦР.
D. Добавления к образцам
1. Добавляют 5 мкл отобранных образцов в соответствующие лунки. После добавления образцов лунки с образцами тщательно накрывают крышкой перед добавлением стандартов для построения кривых.
2. Добавляют 5 мкл разбавленного стандарта в соответствующие лунки и накрывают крышкой.
3. Добавляют 5 мкл сверхчистой воды в лунки контроля без матрицы (NTC).
4. Завертывают планшеты в алюминиевую фольгу и переносят планшеты в центрифугу.
5. Планшеты центрифугируют в течение 2 мин при 100 об/мин для полного осаждения образцов или смеси мастер-микс, включая остатки, которые могут находиться по бокам лунки.
6. Планшеты завертывают в алюминиевую фольгу и переносят на прибор Stratagene.
E. термоциклер: Stratagene MX 3005P
1. Планшеты помещают в Stratagene Mx3005P и устанавливают профиль термических условий:
2. Анализ результатов с использованием программного обеспечения Stratagene Mx3005p.
Среднее число копий РНК, обнаруженное в образцах из носовой полости, представлено на фиг. 17А-17С. Защитный эффект всех вакцин на основе мРНК был менее выражен в носовой полости, но вновь mVRC-1(v2) продемонстрировал в 5 раз более высокую эффективность по сравнению с MRK-04_nopolyA_3mut.
Пример 6: иммуногенность у африканских зеленых мартышек, зараженных RSV
Иммуногенность мРНК-вакцин, формулированных в LNP, тестировали на африканских зеленых мартышках, зараженных RSV.
Для исследования были отобраны здоровые взрослые африканские зеленые мартышки обоего пола (n=4 или 5 на группу) с массой тела в диапазоне от 2,85 до 4,65 кг, которые как было подтверждено по результатам ELISA и титрам нейтрализующих антител, являются серопозитивные по RSV. Пул животных, отобранных для этого исследования, экспериментально заражали RSV в предыдущих экспериментах и распределяли по опытным группам на основе их титров нейтрализации RSV до настоящего исследования, так что у всех групп были одинаковые значения GMT в начале исследования. Опытные животные с заражением RSV обеспечивают модель ответов иммунной памяти на вакцинацию, которая может отражать ответы, ожидаемые у серопозитивных взрослых людей, с пояснением, что ответ антител у AGM после воздействия RSV более смещен на эпитопы F-белка «до слияния», чем у иммунный репертуар человека.
Однократную дозу вакцины вводили каждому животному на неделе 0 внутримышечно (в/в). В дизайн исследования также включали контрольную группу, получающую только PBS. Вакцины вводили, как показано в таблице 2. После вакцинации за животными ежедневно наблюдали в отношении любых изменений в месте инокуляции или других изменений в активности или кормовых привычках, которые могли указывать на неблагоприятную реакцию на вакцину, но ничего не было отмечено. Образцы сыворотки собирали для определения титров нейтрализующих RSV антител, а также титров конкурентых антител паливизумаба (сайт II), D25 (сайт Ø) и 4D7 (сайт I).
Составы вакцин, тестированных на иммуногенность у серопозитивных на RSV африканских зеленых мартышек
Титры NT50 у отдельных животных измеряли в образцах сыворотки, собранных в начале опыта и через 2 недели после вакцинации, с использованием методов, описанных выше, и результаты приведены на фиг. 18. Было установлено, что все вакцины являются высокоиммуногенными, что было продемонстрировано увеличением уровней сывороточных антител, связывающих белки F RSV (на F RSV как «до слияния», так и «после слияния», данные не показаны) и увеличением уровней сывороточных нейтрализующих антител. mVRC-1 (v2) индуцировал самое высокое увеличение титров нейтрализующих антител (> 100 раз в самой высокой дозе) и проявлял аналогичную эффективность в 5 раз более низкой дозе по сравнению с MRK-04_nopolyA_3mut. Аналогично, mLZF-111 также продемонстрировал повышенную активность по сравнению с MRK-04_nopolyA_3mut. В контрольной группе с PBS повышения титров не наблюдали.
Для оценки качества бустер-ответов у вакцинированных животных, определяли титры конкурентных антител паливизумаба (сайт II), D25 (сайт Ø) и 4D7 (сайт I) в сыворотке, собранной через 2 недели после вакцинации (фиг. 19). Как описано выше, антигенный сайт II является эпитопом нейтрализации, обнаруженным как в конформации F-белка «до слияния», так и в конформации «после слияния», сайт Ø представляет собой эпитоп специфической нейтрализации «до слияния», а 4D7 представляет собой эпитоп, специфичный для формы «после слияния». За счет исходного иммунного смещения к конформации «после слияния» у AGM, зараженных RSV, отсутствуют определяемые титры конкурентных антител D25 до иммунизации. Однако все три мРНК антигена индуцировали высокие титры конкурентных антител D25, демонстрируя, что у AGM действительно индуцируется иммунный ответ на антигенный сайт Ø после заражения RSV, который может быть усилен иммунизацией. Повышение титров конкурентных антител D25 после иммунизации mVRC-1(v2) было самым высоким (> 450 раз) и он снова демонстрировал аналогичную эффективность в 5 раз более низкой дозе, чем MRK-04_nopolyA_3mut. В отличие от наивных животных (хлопковых крыс и AGM), наблюдали высокий рост 4D7/F-специфических антител на белок в конформации «после слияния» у AGM, зараженных RSM, в группе mVRC-1(v2), демонстрируя, что исходный пул антител может определять профиль эпитоп-специфических антител после иммунизации. Поскольку считается, что пул В-клеток памяти в результате естественной инфекции RSV у людей сильно смещен в сторону конформации «до слияния», предполагается, что иммунизация mVRC-1(v2) людей будет усиливать выработку преимущественно антител против этих эпитопов, которые, как известно, обладают более сильной нейтрализующей активностью, что приводит к повышению эффективности по сравнению с MRK-04_nopolyA_3mut.
Последовательность аминокислотных линкеров, сайт расщепления TEV, сайт расщепления тромбином и Strep-метка
Антигенные полипептидные последовательности
последовательность содержит линкер из 8 аминокислот (выделен жирным шрифтом и подчеркнут), замены DS-Cav1 (S155C, S290C, S190F и V207L) и С-концевой фолдон (выделен жирным шрифтом)
последовательность содержит линкер из 8 аминокислот (выделен жирным шрифтом и подчеркнут), замены DS-Cav1 (S155C, S290C, S190F и V207L), С-концевой фолдон (выделен жирным шрифтом), линкер GG (подчеркнут), сайт расщепления тромбином, His-метку, линкер SA (подчеркнут) и strep-метку
последовательность содержит линкер из 10 аминокислот (выделен жирным и подчеркнут), замены DS-Cav1 (S155C, S290C, S190F и V207L) и С-концевой фолдон (выделен жирным шрифтом)
последовательность содержит линкер из 10 аминокислот (выделен жирным шрифтом и подчеркнут), замены DS-Cav1 (S155C, S290C, S190F и V207L), С-концевой фолдон (выделен жирным шрифтом), линкер GG (подчеркнут), сайт расщепления тромбином, His-метку, линкер SA (подчеркнут) и strep-метку
последовательность содержит линкер из 12 аминокислот (выделен жирным шрифтом и подчеркнут), замены DS-Cav1 (S155C, S290C, S190F и V207L) и С-концевой фолдон (выделен жирным шрифтом)
последовательность содержит линкер из 12 аминокислот (выделен жирным шрифтом и подчеркнут), замены DS-Cav1 (S155C, S290C, S190F и V207L), С-концевой фолдон (выделен жирным шрифтом), линкер GG (подчеркнут), сайт расщепления тромбином, His-метку, линкер SA (подчеркнут) и strep-метку
последовательность содержит линкер из 14 аминокислот (выделен жирным шрифтом и подчеркнут), замены DS-Cav1 (S155C, S290C, S190F и V207L) и С-концевой фолдон (выделен жирным шрифтом)
последовательность содержит линкер из 14 аминокислот (выделен жирным шрифтом и подчеркнут), замены DS-Cav1 (S155C, S290C, S190F и V207L), С-концевой фолдон (выделен жирным шрифтом), линкер GG (подчеркнут), сайт расщепления тромбина, His-метку, линкер SA (подчеркнут) и strep-метку
последовательность содержит линкер из 14 аминокислот (выделен жирным шрифтом и подчеркнут), замены DS-Cav1 (S155C, S290C, S190F и V207L), дополнительные мутации S180C и S186C (выделены жирным шрифтом, курсивом и подчеркнуты) и С-концевой фолдон (выделен жирным шрифтом)
последовательность содержит линкер из 14 аминокислот (выделен жирным шрифтом и подчеркнут), замены DS-Cav1 (S155C, S290C, S190F и V207L), дополнительные мутации S180C и S186C (выделены жирным шрифтом, курсивом и подчеркнуты) и С-концевой фолдон (выделен жирным шрифтом), и линкер GG (подчеркнут), сайт расщепления тромбином, His-метку, линкер SA (подчеркнут) и strep-метку
последовательность содержит линкер из 14 аминокислот (выделен жирным шрифтом и подчеркнут), замены DS-Cav1 (S155C, S290C, S190F и V207L), дополнительные мутации D486C и A490C (выделены жирным шрифтом, курсивом и подчеркнуты) и С-концевой фолдон (выделен жирным шрифтом)
последовательность содержит линкер из 14 аминокислот (выделен жирным шрифтом и подчеркнут), замены DS-Cav1 (S155C, S290C, S190F и V207L), дополнительные мутации D486C и A490C (выделены жирным шрифтом, курсивом и подчеркнуты), С-концевой фолдон (выделен жирным шрифтом), и линкер GG (подчеркнут), сайт расщепления тромбином, His-метку, линкер SA (подчеркнут) и strep-метку
последовательность содержит линкер из 14 аминокислот (выделен жирным шрифтом и подчеркнут), замены DS-Cav1 (S155C, S290C, S190F и V207L), дополнительные мутации D486C и D489C (выделены жирным шрифтом, курсивом и подчеркнуты) и С-концевой фолдон (выделен жирным шрифтом)
последовательность содержит линкер из 14 аминокислот (выделен жирным шрифтом и подчеркнут), замены DS-Cav1 (S155C, S290C, S190F и V207L), дополнительные мутации D486C и D489C (выделены жирным шрифтом, курсивом и подчеркнуты), С-концевой фолдон (выделен жирным шрифтом), GG линкер (подчеркнут), сайт расщепления тромбином, His-метку, линкер SA (подчеркнут) и strep-метку
последовательность содержит линкер из 14 аминокислот (выделен жирным шрифтом и подчеркнут), замены DS-Cav1 (S155C, S290C, S190F и V207L), дополнительные мутации L512C и L513C (выделены жирным шрифтом, курсивом и подчеркнуты) и С-концевой фолдон (выделен жирным шрифтом)
последовательность содержит линкер из 14 аминокислот (выделен жирным шрифтом и подчеркнут), замены DS-Cav1 (S155C, S290C, S190F и V207L), дополнительные мутации L512C и L513C (выделены жирным шрифтом, курсивом и подчеркнуты), С-концевой фолдон (выделен жирным шрифтом), и линкер GG (подчеркнут), сайт расщепления тромбином, His-метку, линкер SA (подчеркнут) и strep-метку
последовательность содержит линкер из 14 аминокислот (выделен жирным шрифтом и подчеркнут), замены DS-Cav1 (S155C, S290C, S190F и V207L), дополнительную мутацию F505C (выделена жирным шрифтом, курсивом и подчеркнута) и c-концевой фолдон (выделен жирным шрифтом)
последовательность содержит линкер из 14 аминокислот (выделен жирным шрифтом и подчеркнут), замены DS-Cav1 (S155C, S290C, S190F и V207L), дополнительную мутацию F505C (выделена жирным шрифтом, курсивом и подчеркнута), С-концевой фолдон (выделен жирным шрифтом), линкер GG (подчеркнут), сайт расщепления тромбином, His-метку, линкер SA (подчеркнут) и strep-метку
последовательность содержит замены DS-Cav1 (S155C, S290C, S190F и V207L) и дополнительные замены S180C и S186C (выделены жирным шрифтом, курсивом и подчеркнуты) и С-концевой фолдон (выделен жирным шрифтом)
последовательность содержит замены DS-Cav1 (S155C, S290C, S190F и V207L) и дополнительные замены S180C и S186C (выделены жирным шрифтом, курсивом и подчеркнуты), С-концевой фолдон (выделен жирным шрифтом), линкер GG (подчеркнут), сайт расщепления тромбином, His-метку, линкер SA (подчеркнут) и strep-метку
последовательность содержит замены DS-Cav1 (S155C, S290C, S190F и V207L) и дополнительные замены D486C и A490C (выделены жирным шрифтом, курсивом и подчеркнуты) и С-концевой фолдон (выделен жирным шрифтом)
последовательность содержит замены DS-Cav1 (S155C, S290C, S190F и V207L), дополнительные замены D486C и A490C (выделены жирным шрифтом, курсивом и подчеркнуты) и С-концевой фолдон (выделен жирным шрифтом), линкер GG (подчеркнут), сайт расщепления тромбином, His-метку, линкер SA (подчеркнут) и strep-метку
последовательность содержит замены DS-Cav1 (S155C, S290C, S190F и V207L) и дополнительные замены D486C и D489C (выделены жирным шрифтом, курсивом и подчеркнуты) и С-концевой фолдон (выделен жирным шрифтом)
последовательность содержит замены DS-Cav1 (S155C, S290C, S190F и V207L), дополнительные замены D486C и D489C (выделены жирным шрифтом, курсивом и подчеркнуты) и С-концевой фолдон (выделен жирным шрифтом), линкер GG (подчеркнут), сайт расщепления тромбином, His-метку, линкер SA (подчеркнут) и strep-метку
последовательность содержит замены DS-Cav1 (S155C, S290C, S190F и V207L) и дополнительные замены L512C и L513 (выделены жирным шрифтом, курсивом и подчеркнуты) и c-концевой фолдон (выделен жирным шрифтом)
последовательность содержит замены DS-Cav1 (S155C, S290C, S190F и V207L), дополнительные замены L512C и L513C (выделены жирным шрифтом, курсивом и подчеркнуты), С-концевой фолдон (выделен жирным шрифтом), линкер GG (подчеркнут), сайт расщепления тромбином, His-метку, линкер SA (подчеркнут) и strep-метку
последовательность содержит замены DS-Cav1 (S155C, S290C, S190F и V207L) и дополнительную замену F505C (выделена жирным шрифтом, курсивом и подчеркнута) и С-концевой фолдон (выделен жирным шрифтом)
последовательность содержит замены DS-Cav1 (S155C, S290C, S190F и V207L), дополнительную замену F505C (выделена жирным шрифтом, курсивом и подчеркнута), С-концевой фолдон (выделен жирным шрифтом), линкер (подчеркнут), сайт расщепления тромбином, His-метку, линкер (подчеркнут) и strep-метку
последовательность содержит замены DS-Cav1 (S155C, S290C, S190F и V207L) и дополнительную делецию домена HRB, соответствующего аминокислотам 482-513, и С-концевой фолдон (выделен жирным шрифтом)
последовательность содержит замены DS-Cav1 (S155C, S290C, S190F и V207L), дополнительную делецию домена HRB, соответствующего аминокислотам 482-513, С-концевой фолдон (выделен жирным шрифтом), линкер (подчеркнут), сайт расщепления тромбином, His-метку, линкер (подчеркнут) и strep-метку
Специалисты в данной области техники распознают или смогут установить, используя не более чем обычное экспериментирование, множество эквивалентов конкретных вариантов осуществления раскрытия, описанных здесь. Такие эквиваленты предназначены для охвата следующей формулой изобретения.
Все ссылки, включая патентные документы, раскрытые здесь, в полном объеме включены здесь посредством ссылки.
--->
Список последовательностей
<110> Merck Sharp & Dohme Corp.
Zhang, Lan
Fridman, Arthur
Durr, Eberhard
Bett, Andrew
<120> Стабилизированные белки RSV F и их применения
<130> 24566
<150> 62/623,184
<151> 2018-01-29
<160> 49
<170> PatentIn version 3.5
<210> 1
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Аминокислотный линкер
<400> 1
Gly Gly Gly Ser Gly Gly Gly Ser
1 5
<210> 2
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Аминокислотный линкер
<400> 2
Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly
1 5 10
<210> 3
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Аминокислотный линкер
<400> 3
Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser
1 5 10
<210> 4
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Аминокислотный линкер
<400> 4
Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Ser
1 5 10
<210> 5
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> TEV Cleavage Site
<400> 5
Glu Asn Leu Tyr Phe Gln Ser
1 5
<210> 6
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Strep Tag
<400> 6
Trp Ser His Pro Gln Phe Glu Lys
1 5
<210> 7
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Сайт расщепления тромбином
<400> 7
Leu Val Pro Arg Gly Ser
1 5
<210> 8
<211> 31
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Фолдон
<400> 8
Ser Ala Ile Gly Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln Ala
1 5 10 15
Tyr Val Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu
20 25 30
<210> 9
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Сигнальная последовательность
<400> 9
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly
20 25
<210> 10
<211> 574
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Референсная последовательность RSV F
<400> 10
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gln Ser Thr Pro Pro Thr Asn Asn Arg Ala Arg Arg Glu Leu Pro
100 105 110
Arg Phe Met Asn Tyr Thr Leu Asn Asn Ala Lys Lys Thr Asn Val Thr
115 120 125
Leu Ser Lys Lys Arg Lys Arg Arg Phe Leu Gly Phe Leu Leu Gly Val
130 135 140
Gly Ser Ala Ile Ala Ser Gly Val Ala Val Ser Lys Val Leu His Leu
145 150 155 160
Glu Gly Glu Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys
165 170 175
Ala Val Val Ser Leu Ser Asn Gly Val Ser Val Leu Thr Ser Lys Val
180 185 190
Leu Asp Leu Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Val Asn
195 200 205
Lys Gln Ser Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln
210 215 220
Gln Lys Asn Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn
225 230 235 240
Ala Gly Val Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu
245 250 255
Leu Leu Ser Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys
260 265 270
Leu Met Ser Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile
275 280 285
Met Ser Ile Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro
290 295 300
Leu Tyr Gly Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro
305 310 315 320
Leu Cys Thr Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg
325 330 335
Thr Asp Arg Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe
340 345 350
Pro Gln Ala Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp
355 360 365
Thr Met Asn Ser Leu Thr Leu Pro Ser Glu Ile Asn Leu Cys Asn Val
370 375 380
Asp Ile Phe Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr
385 390 395 400
Asp Val Ser Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys
405 410 415
Tyr Gly Lys Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile
420 425 430
Lys Thr Phe Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Met Asp
435 440 445
Thr Val Ser Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly
450 455 460
Lys Ser Leu Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro
465 470 475 480
Leu Val Phe Pro Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn
485 490 495
Glu Lys Ile Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Leu
500 505 510
Leu His Asn Val Asn Ala Gly Lys Ser Thr Thr Asn Ile Met Ile Thr
515 520 525
Thr Ile Ile Ile Val Ile Ile Val Ile Leu Leu Ser Leu Ile Ala Val
530 535 540
Gly Leu Leu Leu Tyr Cys Lys Ala Arg Ser Thr Pro Val Thr Leu Ser
545 550 555 560
Lys Asp Gln Leu Ser Gly Ile Asn Asn Ile Ala Phe Ser Asn
565 570
<210> 11
<211> 556
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 11
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gln Ser Thr Pro Ala Thr Asn Asn Arg Ala Arg Arg Glu Leu Pro
100 105 110
Arg Phe Met Asn Tyr Thr Leu Asn Asn Ala Lys Lys Thr Asn Val Thr
115 120 125
Leu Ser Lys Lys Arg Lys Arg Arg Phe Leu Gly Phe Leu Leu Gly Val
130 135 140
Gly Ser Ala Ile Ala Ser Gly Val Ala Val Ser Lys Val Leu His Leu
145 150 155 160
Glu Gly Glu Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys
165 170 175
Ala Val Val Ser Leu Ser Asn Gly Val Ser Val Leu Thr Ser Lys Val
180 185 190
Leu Asp Leu Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Val Asn
195 200 205
Lys Gln Ser Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln
210 215 220
Gln Lys Asn Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn
225 230 235 240
Ala Gly Val Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu
245 250 255
Leu Leu Ser Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys
260 265 270
Leu Met Ser Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile
275 280 285
Met Ser Ile Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro
290 295 300
Leu Tyr Gly Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro
305 310 315 320
Leu Cys Thr Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg
325 330 335
Thr Asp Arg Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe
340 345 350
Pro Gln Ala Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp
355 360 365
Thr Met Asn Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val
370 375 380
Asp Ile Phe Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr
385 390 395 400
Asp Val Ser Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys
405 410 415
Tyr Gly Lys Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile
420 425 430
Lys Thr Phe Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp
435 440 445
Thr Val Ser Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly
450 455 460
Lys Ser Leu Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro
465 470 475 480
Leu Val Phe Pro Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn
485 490 495
Glu Lys Ile Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Leu
500 505 510
Leu His Asn Val Asn Ala Gly Lys Ser Thr Thr Asn Ile Met Ile Thr
515 520 525
Thr Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln Ala Tyr Val Arg
530 535 540
Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu
545 550 555
<210> 12
<211> 605
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 12
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gln Ser Thr Pro Ala Thr Asn Asn Arg Ala Arg Arg Glu Leu Pro
100 105 110
Arg Phe Met Asn Tyr Thr Leu Asn Asn Ala Lys Lys Thr Asn Val Thr
115 120 125
Leu Ser Lys Lys Arg Lys Arg Arg Phe Leu Gly Phe Leu Leu Gly Val
130 135 140
Gly Ser Ala Ile Ala Ser Gly Val Ala Val Ser Lys Val Leu His Leu
145 150 155 160
Glu Gly Glu Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys
165 170 175
Ala Val Val Ser Leu Ser Asn Gly Val Ser Val Leu Thr Ser Lys Val
180 185 190
Leu Asp Leu Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Val Asn
195 200 205
Lys Gln Ser Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln
210 215 220
Gln Lys Asn Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn
225 230 235 240
Ala Gly Val Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu
245 250 255
Leu Leu Ser Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys
260 265 270
Leu Met Ser Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile
275 280 285
Met Ser Ile Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro
290 295 300
Leu Tyr Gly Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro
305 310 315 320
Leu Cys Thr Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg
325 330 335
Thr Asp Arg Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe
340 345 350
Pro Gln Ala Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp
355 360 365
Thr Met Asn Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val
370 375 380
Asp Ile Phe Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr
385 390 395 400
Asp Val Ser Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys
405 410 415
Tyr Gly Lys Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile
420 425 430
Lys Thr Phe Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp
435 440 445
Thr Val Ser Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly
450 455 460
Lys Ser Leu Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro
465 470 475 480
Leu Val Phe Pro Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn
485 490 495
Glu Lys Ile Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Leu
500 505 510
Leu His Asn Val Asn Ala Gly Lys Ser Thr Thr Asn Ile Met Ile Thr
515 520 525
Thr Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln Ala Tyr Val Arg
530 535 540
Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu Glu Asn Leu Tyr
545 550 555 560
Phe Gln Ser Trp Ser His Pro Gln Phe Glu Lys Gly Gly Gly Ser Gly
565 570 575
Gly Gly Ser Gly Gly Gly Ser Trp Ser His Pro Gln Phe Glu Lys Gly
580 585 590
Ser Gly Ser Gly Ser His His His His His His His His
595 600 605
<210> 13
<211> 544
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 13
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gln Ser Thr Pro Ala Thr Asn Asn Arg Ala Arg Arg Glu Leu Pro
100 105 110
Arg Phe Met Asn Tyr Thr Leu Asn Asn Ala Lys Lys Thr Asn Val Thr
115 120 125
Leu Ser Lys Lys Arg Lys Arg Arg Phe Leu Gly Phe Leu Leu Gly Val
130 135 140
Gly Ser Ala Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu
145 150 155 160
Glu Gly Glu Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys
165 170 175
Ala Val Val Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val
180 185 190
Leu Asp Leu Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn
195 200 205
Lys Gln Ser Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln
210 215 220
Gln Lys Asn Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn
225 230 235 240
Ala Gly Val Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu
245 250 255
Leu Leu Ser Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys
260 265 270
Leu Met Ser Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile
275 280 285
Met Cys Ile Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro
290 295 300
Leu Tyr Gly Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro
305 310 315 320
Leu Cys Thr Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg
325 330 335
Thr Asp Arg Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe
340 345 350
Pro Gln Ala Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp
355 360 365
Thr Met Asn Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val
370 375 380
Asp Ile Phe Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr
385 390 395 400
Asp Val Ser Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys
405 410 415
Tyr Gly Lys Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile
420 425 430
Lys Thr Phe Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp
435 440 445
Thr Val Ser Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly
450 455 460
Lys Ser Leu Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro
465 470 475 480
Leu Val Phe Pro Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn
485 490 495
Glu Lys Ile Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Leu
500 505 510
Leu Ser Ala Ile Gly Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln
515 520 525
Ala Tyr Val Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu
530 535 540
<210> 14
<211> 503
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 14
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gly Gly Gly Ser Gly Gly Gly Ser Ala Ile Ala Ser Gly Val Ala
100 105 110
Val Cys Lys Val Leu His Leu Glu Gly Glu Val Asn Lys Ile Lys Ser
115 120 125
Ala Leu Leu Ser Thr Asn Lys Ala Val Val Ser Leu Ser Asn Gly Val
130 135 140
Ser Val Leu Thr Phe Lys Val Leu Asp Leu Lys Asn Tyr Ile Asp Lys
145 150 155 160
Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser Cys Ser Ile Ser Asn Ile
165 170 175
Glu Thr Val Ile Glu Phe Gln Gln Lys Asn Asn Arg Leu Leu Glu Ile
180 185 190
Thr Arg Glu Phe Ser Val Asn Ala Gly Val Thr Thr Pro Val Ser Thr
195 200 205
Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser Leu Ile Asn Asp Met Pro
210 215 220
Ile Thr Asn Asp Gln Lys Lys Leu Met Ser Asn Asn Val Gln Ile Val
225 230 235 240
Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile Ile Lys Glu Glu Val Leu
245 250 255
Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly Val Ile Asp Thr Pro Cys
260 265 270
Trp Lys Leu His Thr Ser Pro Leu Cys Thr Thr Asn Thr Lys Glu Gly
275 280 285
Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg Gly Trp Tyr Cys Asp Asn
290 295 300
Ala Gly Ser Val Ser Phe Phe Pro Gln Ala Glu Thr Cys Lys Val Gln
305 310 315 320
Ser Asn Arg Val Phe Cys Asp Thr Met Asn Ser Leu Thr Leu Pro Ser
325 330 335
Glu Val Asn Leu Cys Asn Val Asp Ile Phe Asn Pro Lys Tyr Asp Cys
340 345 350
Lys Ile Met Thr Ser Lys Thr Asp Val Ser Ser Ser Val Ile Thr Ser
355 360 365
Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys Thr Lys Cys Thr Ala Ser
370 375 380
Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe Ser Asn Gly Cys Asp Tyr
385 390 395 400
Val Ser Asn Lys Gly Val Asp Thr Val Ser Val Gly Asn Thr Leu Tyr
405 410 415
Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu Tyr Val Lys Gly Glu Pro
420 425 430
Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe Pro Ser Asp Glu Phe Asp
435 440 445
Ala Ser Ile Ser Gln Val Asn Glu Lys Ile Asn Gln Ser Leu Ala Phe
450 455 460
Ile Arg Lys Ser Asp Glu Leu Leu Ser Ala Ile Gly Gly Tyr Ile Pro
465 470 475 480
Glu Ala Pro Arg Asp Gly Gln Ala Tyr Val Arg Lys Asp Gly Glu Trp
485 490 495
Val Leu Leu Ser Thr Phe Leu
500
<210> 15
<211> 527
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 15
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gly Gly Gly Ser Gly Gly Gly Ser Ala Ile Ala Ser Gly Val Ala
100 105 110
Val Cys Lys Val Leu His Leu Glu Gly Glu Val Asn Lys Ile Lys Ser
115 120 125
Ala Leu Leu Ser Thr Asn Lys Ala Val Val Ser Leu Ser Asn Gly Val
130 135 140
Ser Val Leu Thr Phe Lys Val Leu Asp Leu Lys Asn Tyr Ile Asp Lys
145 150 155 160
Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser Cys Ser Ile Ser Asn Ile
165 170 175
Glu Thr Val Ile Glu Phe Gln Gln Lys Asn Asn Arg Leu Leu Glu Ile
180 185 190
Thr Arg Glu Phe Ser Val Asn Ala Gly Val Thr Thr Pro Val Ser Thr
195 200 205
Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser Leu Ile Asn Asp Met Pro
210 215 220
Ile Thr Asn Asp Gln Lys Lys Leu Met Ser Asn Asn Val Gln Ile Val
225 230 235 240
Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile Ile Lys Glu Glu Val Leu
245 250 255
Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly Val Ile Asp Thr Pro Cys
260 265 270
Trp Lys Leu His Thr Ser Pro Leu Cys Thr Thr Asn Thr Lys Glu Gly
275 280 285
Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg Gly Trp Tyr Cys Asp Asn
290 295 300
Ala Gly Ser Val Ser Phe Phe Pro Gln Ala Glu Thr Cys Lys Val Gln
305 310 315 320
Ser Asn Arg Val Phe Cys Asp Thr Met Asn Ser Leu Thr Leu Pro Ser
325 330 335
Glu Val Asn Leu Cys Asn Val Asp Ile Phe Asn Pro Lys Tyr Asp Cys
340 345 350
Lys Ile Met Thr Ser Lys Thr Asp Val Ser Ser Ser Val Ile Thr Ser
355 360 365
Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys Thr Lys Cys Thr Ala Ser
370 375 380
Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe Ser Asn Gly Cys Asp Tyr
385 390 395 400
Val Ser Asn Lys Gly Val Asp Thr Val Ser Val Gly Asn Thr Leu Tyr
405 410 415
Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu Tyr Val Lys Gly Glu Pro
420 425 430
Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe Pro Ser Asp Glu Phe Asp
435 440 445
Ala Ser Ile Ser Gln Val Asn Glu Lys Ile Asn Gln Ser Leu Ala Phe
450 455 460
Ile Arg Lys Ser Asp Glu Leu Leu Ser Ala Ile Gly Gly Tyr Ile Pro
465 470 475 480
Glu Ala Pro Arg Asp Gly Gln Ala Tyr Val Arg Lys Asp Gly Glu Trp
485 490 495
Val Leu Leu Ser Thr Phe Leu Gly Gly Leu Val Pro Arg Gly Ser His
500 505 510
His His His His His Ser Ala Trp Ser His Pro Gln Phe Glu Lys
515 520 525
<210> 16
<211> 505
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 16
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Ala Ile Ala Ser Gly
100 105 110
Val Ala Val Cys Lys Val Leu His Leu Glu Gly Glu Val Asn Lys Ile
115 120 125
Lys Ser Ala Leu Leu Ser Thr Asn Lys Ala Val Val Ser Leu Ser Asn
130 135 140
Gly Val Ser Val Leu Thr Phe Lys Val Leu Asp Leu Lys Asn Tyr Ile
145 150 155 160
Asp Lys Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser Cys Ser Ile Ser
165 170 175
Asn Ile Glu Thr Val Ile Glu Phe Gln Gln Lys Asn Asn Arg Leu Leu
180 185 190
Glu Ile Thr Arg Glu Phe Ser Val Asn Ala Gly Val Thr Thr Pro Val
195 200 205
Ser Thr Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser Leu Ile Asn Asp
210 215 220
Met Pro Ile Thr Asn Asp Gln Lys Lys Leu Met Ser Asn Asn Val Gln
225 230 235 240
Ile Val Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile Ile Lys Glu Glu
245 250 255
Val Leu Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly Val Ile Asp Thr
260 265 270
Pro Cys Trp Lys Leu His Thr Ser Pro Leu Cys Thr Thr Asn Thr Lys
275 280 285
Glu Gly Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg Gly Trp Tyr Cys
290 295 300
Asp Asn Ala Gly Ser Val Ser Phe Phe Pro Gln Ala Glu Thr Cys Lys
305 310 315 320
Val Gln Ser Asn Arg Val Phe Cys Asp Thr Met Asn Ser Leu Thr Leu
325 330 335
Pro Ser Glu Val Asn Leu Cys Asn Val Asp Ile Phe Asn Pro Lys Tyr
340 345 350
Asp Cys Lys Ile Met Thr Ser Lys Thr Asp Val Ser Ser Ser Val Ile
355 360 365
Thr Ser Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys Thr Lys Cys Thr
370 375 380
Ala Ser Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe Ser Asn Gly Cys
385 390 395 400
Asp Tyr Val Ser Asn Lys Gly Val Asp Thr Val Ser Val Gly Asn Thr
405 410 415
Leu Tyr Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu Tyr Val Lys Gly
420 425 430
Glu Pro Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe Pro Ser Asp Glu
435 440 445
Phe Asp Ala Ser Ile Ser Gln Val Asn Glu Lys Ile Asn Gln Ser Leu
450 455 460
Ala Phe Ile Arg Lys Ser Asp Glu Leu Leu Ser Ala Ile Gly Gly Tyr
465 470 475 480
Ile Pro Glu Ala Pro Arg Asp Gly Gln Ala Tyr Val Arg Lys Asp Gly
485 490 495
Glu Trp Val Leu Leu Ser Thr Phe Leu
500 505
<210> 17
<211> 529
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 17
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Ala Ile Ala Ser Gly
100 105 110
Val Ala Val Cys Lys Val Leu His Leu Glu Gly Glu Val Asn Lys Ile
115 120 125
Lys Ser Ala Leu Leu Ser Thr Asn Lys Ala Val Val Ser Leu Ser Asn
130 135 140
Gly Val Ser Val Leu Thr Phe Lys Val Leu Asp Leu Lys Asn Tyr Ile
145 150 155 160
Asp Lys Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser Cys Ser Ile Ser
165 170 175
Asn Ile Glu Thr Val Ile Glu Phe Gln Gln Lys Asn Asn Arg Leu Leu
180 185 190
Glu Ile Thr Arg Glu Phe Ser Val Asn Ala Gly Val Thr Thr Pro Val
195 200 205
Ser Thr Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser Leu Ile Asn Asp
210 215 220
Met Pro Ile Thr Asn Asp Gln Lys Lys Leu Met Ser Asn Asn Val Gln
225 230 235 240
Ile Val Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile Ile Lys Glu Glu
245 250 255
Val Leu Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly Val Ile Asp Thr
260 265 270
Pro Cys Trp Lys Leu His Thr Ser Pro Leu Cys Thr Thr Asn Thr Lys
275 280 285
Glu Gly Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg Gly Trp Tyr Cys
290 295 300
Asp Asn Ala Gly Ser Val Ser Phe Phe Pro Gln Ala Glu Thr Cys Lys
305 310 315 320
Val Gln Ser Asn Arg Val Phe Cys Asp Thr Met Asn Ser Leu Thr Leu
325 330 335
Pro Ser Glu Val Asn Leu Cys Asn Val Asp Ile Phe Asn Pro Lys Tyr
340 345 350
Asp Cys Lys Ile Met Thr Ser Lys Thr Asp Val Ser Ser Ser Val Ile
355 360 365
Thr Ser Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys Thr Lys Cys Thr
370 375 380
Ala Ser Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe Ser Asn Gly Cys
385 390 395 400
Asp Tyr Val Ser Asn Lys Gly Val Asp Thr Val Ser Val Gly Asn Thr
405 410 415
Leu Tyr Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu Tyr Val Lys Gly
420 425 430
Glu Pro Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe Pro Ser Asp Glu
435 440 445
Phe Asp Ala Ser Ile Ser Gln Val Asn Glu Lys Ile Asn Gln Ser Leu
450 455 460
Ala Phe Ile Arg Lys Ser Asp Glu Leu Leu Ser Ala Ile Gly Gly Tyr
465 470 475 480
Ile Pro Glu Ala Pro Arg Asp Gly Gln Ala Tyr Val Arg Lys Asp Gly
485 490 495
Glu Trp Val Leu Leu Ser Thr Phe Leu Gly Gly Leu Val Pro Arg Gly
500 505 510
Ser His His His His His His Ser Ala Trp Ser His Pro Gln Phe Glu
515 520 525
Lys
<210> 18
<211> 507
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 18
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Ala Ile Ala
100 105 110
Ser Gly Val Ala Val Cys Lys Val Leu His Leu Glu Gly Glu Val Asn
115 120 125
Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys Ala Val Val Ser Leu
130 135 140
Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val Leu Asp Leu Lys Asn
145 150 155 160
Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser Cys Ser
165 170 175
Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln Gln Lys Asn Asn Arg
180 185 190
Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn Ala Gly Val Thr Thr
195 200 205
Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser Leu Ile
210 215 220
Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys Leu Met Ser Asn Asn
225 230 235 240
Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile Ile Lys
245 250 255
Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly Val Ile
260 265 270
Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro Leu Cys Thr Thr Asn
275 280 285
Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg Gly Trp
290 295 300
Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe Pro Gln Ala Glu Thr
305 310 315 320
Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp Thr Met Asn Ser Leu
325 330 335
Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val Asp Ile Phe Asn Pro
340 345 350
Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr Asp Val Ser Ser Ser
355 360 365
Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys Thr Lys
370 375 380
Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe Ser Asn
385 390 395 400
Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp Thr Val Ser Val Gly
405 410 415
Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu Tyr Val
420 425 430
Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe Pro Ser
435 440 445
Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn Glu Lys Ile Asn Gln
450 455 460
Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Leu Leu Ser Ala Ile Gly
465 470 475 480
Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln Ala Tyr Val Arg Lys
485 490 495
Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu
500 505
<210> 19
<211> 531
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 19
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Ala Ile Ala
100 105 110
Ser Gly Val Ala Val Cys Lys Val Leu His Leu Glu Gly Glu Val Asn
115 120 125
Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys Ala Val Val Ser Leu
130 135 140
Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val Leu Asp Leu Lys Asn
145 150 155 160
Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser Cys Ser
165 170 175
Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln Gln Lys Asn Asn Arg
180 185 190
Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn Ala Gly Val Thr Thr
195 200 205
Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser Leu Ile
210 215 220
Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys Leu Met Ser Asn Asn
225 230 235 240
Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile Ile Lys
245 250 255
Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly Val Ile
260 265 270
Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro Leu Cys Thr Thr Asn
275 280 285
Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg Gly Trp
290 295 300
Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe Pro Gln Ala Glu Thr
305 310 315 320
Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp Thr Met Asn Ser Leu
325 330 335
Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val Asp Ile Phe Asn Pro
340 345 350
Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr Asp Val Ser Ser Ser
355 360 365
Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys Thr Lys
370 375 380
Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe Ser Asn
385 390 395 400
Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp Thr Val Ser Val Gly
405 410 415
Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu Tyr Val
420 425 430
Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe Pro Ser
435 440 445
Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn Glu Lys Ile Asn Gln
450 455 460
Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Leu Leu Ser Ala Ile Gly
465 470 475 480
Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln Ala Tyr Val Arg Lys
485 490 495
Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu Gly Gly Leu Val Pro
500 505 510
Arg Gly Ser His His His His His His Ser Ala Trp Ser His Pro Gln
515 520 525
Phe Glu Lys
530
<210> 20
<211> 509
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 20
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Ser Ala
100 105 110
Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu Glu Gly Glu
115 120 125
Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys Ala Val Val
130 135 140
Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val Leu Asp Leu
145 150 155 160
Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser
165 170 175
Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln Gln Lys Asn
180 185 190
Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn Ala Gly Val
195 200 205
Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser
210 215 220
Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys Leu Met Ser
225 230 235 240
Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile
245 250 255
Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly
260 265 270
Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro Leu Cys Thr
275 280 285
Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg
290 295 300
Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe Pro Gln Ala
305 310 315 320
Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp Thr Met Asn
325 330 335
Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val Asp Ile Phe
340 345 350
Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr Asp Val Ser
355 360 365
Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys
370 375 380
Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe
385 390 395 400
Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp Thr Val Ser
405 410 415
Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu
420 425 430
Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe
435 440 445
Pro Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn Glu Lys Ile
450 455 460
Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Leu Leu Ser Ala
465 470 475 480
Ile Gly Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln Ala Tyr Val
485 490 495
Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu
500 505
<210> 21
<211> 533
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 21
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Ser Ala
100 105 110
Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu Glu Gly Glu
115 120 125
Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys Ala Val Val
130 135 140
Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val Leu Asp Leu
145 150 155 160
Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser
165 170 175
Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln Gln Lys Asn
180 185 190
Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn Ala Gly Val
195 200 205
Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser
210 215 220
Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys Leu Met Ser
225 230 235 240
Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile
245 250 255
Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly
260 265 270
Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro Leu Cys Thr
275 280 285
Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg
290 295 300
Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe Pro Gln Ala
305 310 315 320
Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp Thr Met Asn
325 330 335
Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val Asp Ile Phe
340 345 350
Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr Asp Val Ser
355 360 365
Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys
370 375 380
Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe
385 390 395 400
Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp Thr Val Ser
405 410 415
Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu
420 425 430
Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe
435 440 445
Pro Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn Glu Lys Ile
450 455 460
Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Leu Leu Ser Ala
465 470 475 480
Ile Gly Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln Ala Tyr Val
485 490 495
Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu Gly Gly Leu
500 505 510
Val Pro Arg Gly Ser His His His His His His Ser Ala Trp Ser His
515 520 525
Pro Gln Phe Glu Lys
530
<210> 22
<211> 509
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 22
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Ser Ala
100 105 110
Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu Glu Gly Glu
115 120 125
Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys Ala Val Val
130 135 140
Cys Leu Ser Asn Gly Val Cys Val Leu Thr Phe Lys Val Leu Asp Leu
145 150 155 160
Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser
165 170 175
Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln Gln Lys Asn
180 185 190
Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn Ala Gly Val
195 200 205
Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser
210 215 220
Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys Leu Met Ser
225 230 235 240
Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile
245 250 255
Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly
260 265 270
Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro Leu Cys Thr
275 280 285
Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg
290 295 300
Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe Pro Gln Ala
305 310 315 320
Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp Thr Met Asn
325 330 335
Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val Asp Ile Phe
340 345 350
Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr Asp Val Ser
355 360 365
Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys
370 375 380
Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe
385 390 395 400
Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp Thr Val Ser
405 410 415
Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu
420 425 430
Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe
435 440 445
Pro Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn Glu Lys Ile
450 455 460
Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Leu Leu Ser Ala
465 470 475 480
Ile Gly Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln Ala Tyr Val
485 490 495
Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu
500 505
<210> 23
<211> 533
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 23
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Ser Ala
100 105 110
Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu Glu Gly Glu
115 120 125
Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys Ala Val Val
130 135 140
Cys Leu Ser Asn Gly Val Cys Val Leu Thr Phe Lys Val Leu Asp Leu
145 150 155 160
Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser
165 170 175
Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln Gln Lys Asn
180 185 190
Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn Ala Gly Val
195 200 205
Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser
210 215 220
Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys Leu Met Ser
225 230 235 240
Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile
245 250 255
Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly
260 265 270
Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro Leu Cys Thr
275 280 285
Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg
290 295 300
Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe Pro Gln Ala
305 310 315 320
Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp Thr Met Asn
325 330 335
Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val Asp Ile Phe
340 345 350
Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr Asp Val Ser
355 360 365
Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys
370 375 380
Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe
385 390 395 400
Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp Thr Val Ser
405 410 415
Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu
420 425 430
Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe
435 440 445
Pro Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn Glu Lys Ile
450 455 460
Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Leu Leu Ser Ala
465 470 475 480
Ile Gly Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln Ala Tyr Val
485 490 495
Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu Gly Gly Leu
500 505 510
Val Pro Arg Gly Ser His His His His His His Ser Ala Trp Ser His
515 520 525
Pro Gln Phe Glu Lys
530
<210> 24
<211> 509
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 24
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Ser Ala
100 105 110
Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu Glu Gly Glu
115 120 125
Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys Ala Val Val
130 135 140
Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val Leu Asp Leu
145 150 155 160
Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser
165 170 175
Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln Gln Lys Asn
180 185 190
Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn Ala Gly Val
195 200 205
Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser
210 215 220
Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys Leu Met Ser
225 230 235 240
Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile
245 250 255
Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly
260 265 270
Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro Leu Cys Thr
275 280 285
Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg
290 295 300
Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe Pro Gln Ala
305 310 315 320
Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp Thr Met Asn
325 330 335
Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val Asp Ile Phe
340 345 350
Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr Asp Val Ser
355 360 365
Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys
370 375 380
Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe
385 390 395 400
Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp Thr Val Ser
405 410 415
Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu
420 425 430
Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe
435 440 445
Pro Ser Cys Glu Phe Asp Cys Ser Ile Ser Gln Val Asn Glu Lys Ile
450 455 460
Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Leu Leu Ser Ala
465 470 475 480
Ile Gly Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln Ala Tyr Val
485 490 495
Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu
500 505
<210> 25
<211> 533
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 25
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Ser Ala
100 105 110
Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu Glu Gly Glu
115 120 125
Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys Ala Val Val
130 135 140
Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val Leu Asp Leu
145 150 155 160
Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser
165 170 175
Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln Gln Lys Asn
180 185 190
Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn Ala Gly Val
195 200 205
Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser
210 215 220
Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys Leu Met Ser
225 230 235 240
Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile
245 250 255
Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly
260 265 270
Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro Leu Cys Thr
275 280 285
Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg
290 295 300
Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe Pro Gln Ala
305 310 315 320
Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp Thr Met Asn
325 330 335
Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val Asp Ile Phe
340 345 350
Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr Asp Val Ser
355 360 365
Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys
370 375 380
Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe
385 390 395 400
Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp Thr Val Ser
405 410 415
Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu
420 425 430
Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe
435 440 445
Pro Ser Cys Glu Phe Asp Cys Ser Ile Ser Gln Val Asn Glu Lys Ile
450 455 460
Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Leu Leu Ser Ala
465 470 475 480
Ile Gly Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln Ala Tyr Val
485 490 495
Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu Gly Gly Leu
500 505 510
Val Pro Arg Gly Ser His His His His His His Ser Ala Trp Ser His
515 520 525
Pro Gln Phe Glu Lys
530
<210> 26
<211> 509
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 26
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Ser Ala
100 105 110
Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu Glu Gly Glu
115 120 125
Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys Ala Val Val
130 135 140
Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val Leu Asp Leu
145 150 155 160
Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser
165 170 175
Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln Gln Lys Asn
180 185 190
Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn Ala Gly Val
195 200 205
Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser
210 215 220
Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys Leu Met Ser
225 230 235 240
Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile
245 250 255
Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly
260 265 270
Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro Leu Cys Thr
275 280 285
Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg
290 295 300
Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe Pro Gln Ala
305 310 315 320
Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp Thr Met Asn
325 330 335
Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val Asp Ile Phe
340 345 350
Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr Asp Val Ser
355 360 365
Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys
370 375 380
Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe
385 390 395 400
Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp Thr Val Ser
405 410 415
Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu
420 425 430
Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe
435 440 445
Pro Ser Cys Glu Phe Cys Ala Ser Ile Ser Gln Val Asn Glu Lys Ile
450 455 460
Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Leu Leu Ser Ala
465 470 475 480
Ile Gly Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln Ala Tyr Val
485 490 495
Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu
500 505
<210> 27
<211> 533
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 27
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Ser Ala
100 105 110
Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu Glu Gly Glu
115 120 125
Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys Ala Val Val
130 135 140
Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val Leu Asp Leu
145 150 155 160
Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser
165 170 175
Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln Gln Lys Asn
180 185 190
Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn Ala Gly Val
195 200 205
Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser
210 215 220
Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys Leu Met Ser
225 230 235 240
Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile
245 250 255
Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly
260 265 270
Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro Leu Cys Thr
275 280 285
Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg
290 295 300
Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe Pro Gln Ala
305 310 315 320
Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp Thr Met Asn
325 330 335
Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val Asp Ile Phe
340 345 350
Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr Asp Val Ser
355 360 365
Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys
370 375 380
Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe
385 390 395 400
Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp Thr Val Ser
405 410 415
Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu
420 425 430
Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe
435 440 445
Pro Ser Cys Glu Phe Cys Ala Ser Ile Ser Gln Val Asn Glu Lys Ile
450 455 460
Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Leu Leu Ser Ala
465 470 475 480
Ile Gly Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln Ala Tyr Val
485 490 495
Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu Gly Gly Leu
500 505 510
Val Pro Arg Gly Ser His His His His His His Ser Ala Trp Ser His
515 520 525
Pro Gln Phe Glu Lys
530
<210> 28
<211> 509
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 28
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Ser Ala
100 105 110
Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu Glu Gly Glu
115 120 125
Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys Ala Val Val
130 135 140
Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val Leu Asp Leu
145 150 155 160
Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser
165 170 175
Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln Gln Lys Asn
180 185 190
Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn Ala Gly Val
195 200 205
Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser
210 215 220
Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys Leu Met Ser
225 230 235 240
Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile
245 250 255
Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly
260 265 270
Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro Leu Cys Thr
275 280 285
Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg
290 295 300
Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe Pro Gln Ala
305 310 315 320
Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp Thr Met Asn
325 330 335
Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val Asp Ile Phe
340 345 350
Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr Asp Val Ser
355 360 365
Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys
370 375 380
Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe
385 390 395 400
Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp Thr Val Ser
405 410 415
Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu
420 425 430
Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe
435 440 445
Pro Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn Glu Lys Ile
450 455 460
Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Cys Cys Ser Ala
465 470 475 480
Ile Gly Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln Ala Tyr Val
485 490 495
Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu
500 505
<210> 29
<211> 533
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 29
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Ser Ala
100 105 110
Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu Glu Gly Glu
115 120 125
Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys Ala Val Val
130 135 140
Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val Leu Asp Leu
145 150 155 160
Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser
165 170 175
Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln Gln Lys Asn
180 185 190
Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn Ala Gly Val
195 200 205
Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser
210 215 220
Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys Leu Met Ser
225 230 235 240
Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile
245 250 255
Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly
260 265 270
Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro Leu Cys Thr
275 280 285
Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg
290 295 300
Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe Pro Gln Ala
305 310 315 320
Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp Thr Met Asn
325 330 335
Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val Asp Ile Phe
340 345 350
Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr Asp Val Ser
355 360 365
Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys
370 375 380
Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe
385 390 395 400
Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp Thr Val Ser
405 410 415
Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu
420 425 430
Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe
435 440 445
Pro Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn Glu Lys Ile
450 455 460
Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Cys Cys Ser Ala
465 470 475 480
Ile Gly Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln Ala Tyr Val
485 490 495
Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu Gly Gly Leu
500 505 510
Val Pro Arg Gly Ser His His His His His His Ser Ala Trp Ser His
515 520 525
Pro Gln Phe Glu Lys
530
<210> 30
<211> 509
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 30
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Ser Ala
100 105 110
Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu Glu Gly Glu
115 120 125
Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys Ala Val Val
130 135 140
Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val Leu Asp Leu
145 150 155 160
Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser
165 170 175
Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln Gln Lys Asn
180 185 190
Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn Ala Gly Val
195 200 205
Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser
210 215 220
Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys Leu Met Ser
225 230 235 240
Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile
245 250 255
Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly
260 265 270
Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro Leu Cys Thr
275 280 285
Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg
290 295 300
Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe Pro Gln Ala
305 310 315 320
Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp Thr Met Asn
325 330 335
Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val Asp Ile Phe
340 345 350
Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr Asp Val Ser
355 360 365
Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys
370 375 380
Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe
385 390 395 400
Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp Thr Val Ser
405 410 415
Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu
420 425 430
Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe
435 440 445
Pro Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn Glu Lys Ile
450 455 460
Asn Gln Ser Leu Ala Cys Ile Arg Lys Ser Asp Glu Leu Leu Ser Ala
465 470 475 480
Ile Gly Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln Ala Tyr Val
485 490 495
Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu
500 505
<210> 31
<211> 533
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 31
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Ser Ala
100 105 110
Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu Glu Gly Glu
115 120 125
Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys Ala Val Val
130 135 140
Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val Leu Asp Leu
145 150 155 160
Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser
165 170 175
Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln Gln Lys Asn
180 185 190
Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn Ala Gly Val
195 200 205
Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser
210 215 220
Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys Leu Met Ser
225 230 235 240
Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile
245 250 255
Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly
260 265 270
Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro Leu Cys Thr
275 280 285
Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg
290 295 300
Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe Pro Gln Ala
305 310 315 320
Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp Thr Met Asn
325 330 335
Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val Asp Ile Phe
340 345 350
Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr Asp Val Ser
355 360 365
Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys
370 375 380
Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe
385 390 395 400
Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp Thr Val Ser
405 410 415
Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu
420 425 430
Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe
435 440 445
Pro Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn Glu Lys Ile
450 455 460
Asn Gln Ser Leu Ala Cys Ile Arg Lys Ser Asp Glu Leu Leu Ser Ala
465 470 475 480
Ile Gly Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln Ala Tyr Val
485 490 495
Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu Gly Gly Leu
500 505 510
Val Pro Arg Gly Ser His His His His His His Ser Ala Trp Ser His
515 520 525
Pro Gln Phe Glu Lys
530
<210> 32
<211> 544
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 32
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gln Ser Thr Pro Ala Thr Asn Asn Arg Ala Arg Arg Glu Leu Pro
100 105 110
Arg Phe Met Asn Tyr Thr Leu Asn Asn Ala Lys Lys Thr Asn Val Thr
115 120 125
Leu Ser Lys Lys Arg Lys Arg Arg Phe Leu Gly Phe Leu Leu Gly Val
130 135 140
Gly Ser Ala Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu
145 150 155 160
Glu Gly Glu Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys
165 170 175
Ala Val Val Cys Leu Ser Asn Gly Val Cys Val Leu Thr Phe Lys Val
180 185 190
Leu Asp Leu Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn
195 200 205
Lys Gln Ser Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln
210 215 220
Gln Lys Asn Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn
225 230 235 240
Ala Gly Val Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu
245 250 255
Leu Leu Ser Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys
260 265 270
Leu Met Ser Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile
275 280 285
Met Cys Ile Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro
290 295 300
Leu Tyr Gly Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro
305 310 315 320
Leu Cys Thr Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg
325 330 335
Thr Asp Arg Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe
340 345 350
Pro Gln Ala Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp
355 360 365
Thr Met Asn Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val
370 375 380
Asp Ile Phe Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr
385 390 395 400
Asp Val Ser Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys
405 410 415
Tyr Gly Lys Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile
420 425 430
Lys Thr Phe Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp
435 440 445
Thr Val Ser Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly
450 455 460
Lys Ser Leu Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro
465 470 475 480
Leu Val Phe Pro Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn
485 490 495
Glu Lys Ile Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Leu
500 505 510
Leu Ser Ala Ile Gly Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln
515 520 525
Ala Tyr Val Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu
530 535 540
<210> 33
<211> 568
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 33
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gln Ser Thr Pro Ala Thr Asn Asn Arg Ala Arg Arg Glu Leu Pro
100 105 110
Arg Phe Met Asn Tyr Thr Leu Asn Asn Ala Lys Lys Thr Asn Val Thr
115 120 125
Leu Ser Lys Lys Arg Lys Arg Arg Phe Leu Gly Phe Leu Leu Gly Val
130 135 140
Gly Ser Ala Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu
145 150 155 160
Glu Gly Glu Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys
165 170 175
Ala Val Val Cys Leu Ser Asn Gly Val Cys Val Leu Thr Phe Lys Val
180 185 190
Leu Asp Leu Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn
195 200 205
Lys Gln Ser Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln
210 215 220
Gln Lys Asn Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn
225 230 235 240
Ala Gly Val Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu
245 250 255
Leu Leu Ser Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys
260 265 270
Leu Met Ser Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile
275 280 285
Met Cys Ile Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro
290 295 300
Leu Tyr Gly Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro
305 310 315 320
Leu Cys Thr Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg
325 330 335
Thr Asp Arg Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe
340 345 350
Pro Gln Ala Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp
355 360 365
Thr Met Asn Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val
370 375 380
Asp Ile Phe Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr
385 390 395 400
Asp Val Ser Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys
405 410 415
Tyr Gly Lys Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile
420 425 430
Lys Thr Phe Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp
435 440 445
Thr Val Ser Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly
450 455 460
Lys Ser Leu Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro
465 470 475 480
Leu Val Phe Pro Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn
485 490 495
Glu Lys Ile Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Leu
500 505 510
Leu Ser Ala Ile Gly Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln
515 520 525
Ala Tyr Val Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu
530 535 540
Gly Gly Leu Val Pro Arg Gly Ser His His His His His His Ser Ala
545 550 555 560
Trp Ser His Pro Gln Phe Glu Lys
565
<210> 34
<211> 544
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 34
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gln Ser Thr Pro Ala Thr Asn Asn Arg Ala Arg Arg Glu Leu Pro
100 105 110
Arg Phe Met Asn Tyr Thr Leu Asn Asn Ala Lys Lys Thr Asn Val Thr
115 120 125
Leu Ser Lys Lys Arg Lys Arg Arg Phe Leu Gly Phe Leu Leu Gly Val
130 135 140
Gly Ser Ala Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu
145 150 155 160
Glu Gly Glu Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys
165 170 175
Ala Val Val Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val
180 185 190
Leu Asp Leu Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn
195 200 205
Lys Gln Ser Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln
210 215 220
Gln Lys Asn Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn
225 230 235 240
Ala Gly Val Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu
245 250 255
Leu Leu Ser Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys
260 265 270
Leu Met Ser Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile
275 280 285
Met Cys Ile Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro
290 295 300
Leu Tyr Gly Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro
305 310 315 320
Leu Cys Thr Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg
325 330 335
Thr Asp Arg Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe
340 345 350
Pro Gln Ala Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp
355 360 365
Thr Met Asn Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val
370 375 380
Asp Ile Phe Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr
385 390 395 400
Asp Val Ser Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys
405 410 415
Tyr Gly Lys Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile
420 425 430
Lys Thr Phe Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp
435 440 445
Thr Val Ser Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly
450 455 460
Lys Ser Leu Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro
465 470 475 480
Leu Val Phe Pro Ser Cys Glu Phe Asp Cys Ser Ile Ser Gln Val Asn
485 490 495
Glu Lys Ile Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Leu
500 505 510
Leu Ser Ala Ile Gly Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln
515 520 525
Ala Tyr Val Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu
530 535 540
<210> 35
<211> 568
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 35
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gln Ser Thr Pro Ala Thr Asn Asn Arg Ala Arg Arg Glu Leu Pro
100 105 110
Arg Phe Met Asn Tyr Thr Leu Asn Asn Ala Lys Lys Thr Asn Val Thr
115 120 125
Leu Ser Lys Lys Arg Lys Arg Arg Phe Leu Gly Phe Leu Leu Gly Val
130 135 140
Gly Ser Ala Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu
145 150 155 160
Glu Gly Glu Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys
165 170 175
Ala Val Val Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val
180 185 190
Leu Asp Leu Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn
195 200 205
Lys Gln Ser Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln
210 215 220
Gln Lys Asn Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn
225 230 235 240
Ala Gly Val Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu
245 250 255
Leu Leu Ser Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys
260 265 270
Leu Met Ser Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile
275 280 285
Met Cys Ile Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro
290 295 300
Leu Tyr Gly Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro
305 310 315 320
Leu Cys Thr Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg
325 330 335
Thr Asp Arg Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe
340 345 350
Pro Gln Ala Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp
355 360 365
Thr Met Asn Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val
370 375 380
Asp Ile Phe Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr
385 390 395 400
Asp Val Ser Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys
405 410 415
Tyr Gly Lys Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile
420 425 430
Lys Thr Phe Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp
435 440 445
Thr Val Ser Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly
450 455 460
Lys Ser Leu Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro
465 470 475 480
Leu Val Phe Pro Ser Cys Glu Phe Asp Cys Ser Ile Ser Gln Val Asn
485 490 495
Glu Lys Ile Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Leu
500 505 510
Leu Ser Ala Ile Gly Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln
515 520 525
Ala Tyr Val Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu
530 535 540
Gly Gly Leu Val Pro Arg Gly Ser His His His His His His Ser Ala
545 550 555 560
Trp Ser His Pro Gln Phe Glu Lys
565
<210> 36
<211> 544
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 36
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gln Ser Thr Pro Ala Thr Asn Asn Arg Ala Arg Arg Glu Leu Pro
100 105 110
Arg Phe Met Asn Tyr Thr Leu Asn Asn Ala Lys Lys Thr Asn Val Thr
115 120 125
Leu Ser Lys Lys Arg Lys Arg Arg Phe Leu Gly Phe Leu Leu Gly Val
130 135 140
Gly Ser Ala Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu
145 150 155 160
Glu Gly Glu Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys
165 170 175
Ala Val Val Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val
180 185 190
Leu Asp Leu Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn
195 200 205
Lys Gln Ser Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln
210 215 220
Gln Lys Asn Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn
225 230 235 240
Ala Gly Val Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu
245 250 255
Leu Leu Ser Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys
260 265 270
Leu Met Ser Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile
275 280 285
Met Cys Ile Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro
290 295 300
Leu Tyr Gly Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro
305 310 315 320
Leu Cys Thr Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg
325 330 335
Thr Asp Arg Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe
340 345 350
Pro Gln Ala Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp
355 360 365
Thr Met Asn Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val
370 375 380
Asp Ile Phe Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr
385 390 395 400
Asp Val Ser Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys
405 410 415
Tyr Gly Lys Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile
420 425 430
Lys Thr Phe Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp
435 440 445
Thr Val Ser Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly
450 455 460
Lys Ser Leu Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro
465 470 475 480
Leu Val Phe Pro Ser Cys Glu Phe Cys Ala Ser Ile Ser Gln Val Asn
485 490 495
Glu Lys Ile Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Leu
500 505 510
Leu Ser Ala Ile Gly Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln
515 520 525
Ala Tyr Val Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu
530 535 540
<210> 37
<211> 568
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 37
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gln Ser Thr Pro Ala Thr Asn Asn Arg Ala Arg Arg Glu Leu Pro
100 105 110
Arg Phe Met Asn Tyr Thr Leu Asn Asn Ala Lys Lys Thr Asn Val Thr
115 120 125
Leu Ser Lys Lys Arg Lys Arg Arg Phe Leu Gly Phe Leu Leu Gly Val
130 135 140
Gly Ser Ala Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu
145 150 155 160
Glu Gly Glu Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys
165 170 175
Ala Val Val Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val
180 185 190
Leu Asp Leu Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn
195 200 205
Lys Gln Ser Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln
210 215 220
Gln Lys Asn Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn
225 230 235 240
Ala Gly Val Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu
245 250 255
Leu Leu Ser Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys
260 265 270
Leu Met Ser Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile
275 280 285
Met Cys Ile Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro
290 295 300
Leu Tyr Gly Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro
305 310 315 320
Leu Cys Thr Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg
325 330 335
Thr Asp Arg Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe
340 345 350
Pro Gln Ala Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp
355 360 365
Thr Met Asn Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val
370 375 380
Asp Ile Phe Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr
385 390 395 400
Asp Val Ser Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys
405 410 415
Tyr Gly Lys Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile
420 425 430
Lys Thr Phe Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp
435 440 445
Thr Val Ser Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly
450 455 460
Lys Ser Leu Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro
465 470 475 480
Leu Val Phe Pro Ser Cys Glu Phe Cys Ala Ser Ile Ser Gln Val Asn
485 490 495
Glu Lys Ile Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Leu
500 505 510
Leu Ser Ala Ile Gly Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln
515 520 525
Ala Tyr Val Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu
530 535 540
Gly Gly Leu Val Pro Arg Gly Ser His His His His His His Ser Ala
545 550 555 560
Trp Ser His Pro Gln Phe Glu Lys
565
<210> 38
<211> 544
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 38
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gln Ser Thr Pro Ala Thr Asn Asn Arg Ala Arg Arg Glu Leu Pro
100 105 110
Arg Phe Met Asn Tyr Thr Leu Asn Asn Ala Lys Lys Thr Asn Val Thr
115 120 125
Leu Ser Lys Lys Arg Lys Arg Arg Phe Leu Gly Phe Leu Leu Gly Val
130 135 140
Gly Ser Ala Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu
145 150 155 160
Glu Gly Glu Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys
165 170 175
Ala Val Val Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val
180 185 190
Leu Asp Leu Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn
195 200 205
Lys Gln Ser Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln
210 215 220
Gln Lys Asn Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn
225 230 235 240
Ala Gly Val Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu
245 250 255
Leu Leu Ser Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys
260 265 270
Leu Met Ser Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile
275 280 285
Met Cys Ile Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro
290 295 300
Leu Tyr Gly Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro
305 310 315 320
Leu Cys Thr Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg
325 330 335
Thr Asp Arg Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe
340 345 350
Pro Gln Ala Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp
355 360 365
Thr Met Asn Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val
370 375 380
Asp Ile Phe Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr
385 390 395 400
Asp Val Ser Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys
405 410 415
Tyr Gly Lys Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile
420 425 430
Lys Thr Phe Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp
435 440 445
Thr Val Ser Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly
450 455 460
Lys Ser Leu Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro
465 470 475 480
Leu Val Phe Pro Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn
485 490 495
Glu Lys Ile Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Cys
500 505 510
Cys Ser Ala Ile Gly Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln
515 520 525
Ala Tyr Val Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu
530 535 540
<210> 39
<211> 568
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 39
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gln Ser Thr Pro Ala Thr Asn Asn Arg Ala Arg Arg Glu Leu Pro
100 105 110
Arg Phe Met Asn Tyr Thr Leu Asn Asn Ala Lys Lys Thr Asn Val Thr
115 120 125
Leu Ser Lys Lys Arg Lys Arg Arg Phe Leu Gly Phe Leu Leu Gly Val
130 135 140
Gly Ser Ala Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu
145 150 155 160
Glu Gly Glu Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys
165 170 175
Ala Val Val Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val
180 185 190
Leu Asp Leu Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn
195 200 205
Lys Gln Ser Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln
210 215 220
Gln Lys Asn Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn
225 230 235 240
Ala Gly Val Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu
245 250 255
Leu Leu Ser Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys
260 265 270
Leu Met Ser Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile
275 280 285
Met Cys Ile Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro
290 295 300
Leu Tyr Gly Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro
305 310 315 320
Leu Cys Thr Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg
325 330 335
Thr Asp Arg Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe
340 345 350
Pro Gln Ala Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp
355 360 365
Thr Met Asn Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val
370 375 380
Asp Ile Phe Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr
385 390 395 400
Asp Val Ser Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys
405 410 415
Tyr Gly Lys Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile
420 425 430
Lys Thr Phe Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp
435 440 445
Thr Val Ser Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly
450 455 460
Lys Ser Leu Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro
465 470 475 480
Leu Val Phe Pro Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn
485 490 495
Glu Lys Ile Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Cys
500 505 510
Cys Ser Ala Ile Gly Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln
515 520 525
Ala Tyr Val Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu
530 535 540
Gly Gly Leu Val Pro Arg Gly Ser His His His His His His Ser Ala
545 550 555 560
Trp Ser His Pro Gln Phe Glu Lys
565
<210> 40
<211> 544
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 40
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gln Ser Thr Pro Ala Thr Asn Asn Arg Ala Arg Arg Glu Leu Pro
100 105 110
Arg Phe Met Asn Tyr Thr Leu Asn Asn Ala Lys Lys Thr Asn Val Thr
115 120 125
Leu Ser Lys Lys Arg Lys Arg Arg Phe Leu Gly Phe Leu Leu Gly Val
130 135 140
Gly Ser Ala Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu
145 150 155 160
Glu Gly Glu Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys
165 170 175
Ala Val Val Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val
180 185 190
Leu Asp Leu Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn
195 200 205
Lys Gln Ser Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln
210 215 220
Gln Lys Asn Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn
225 230 235 240
Ala Gly Val Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu
245 250 255
Leu Leu Ser Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys
260 265 270
Leu Met Ser Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile
275 280 285
Met Cys Ile Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro
290 295 300
Leu Tyr Gly Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro
305 310 315 320
Leu Cys Thr Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg
325 330 335
Thr Asp Arg Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe
340 345 350
Pro Gln Ala Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp
355 360 365
Thr Met Asn Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val
370 375 380
Asp Ile Phe Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr
385 390 395 400
Asp Val Ser Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys
405 410 415
Tyr Gly Lys Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile
420 425 430
Lys Thr Phe Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp
435 440 445
Thr Val Ser Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly
450 455 460
Lys Ser Leu Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro
465 470 475 480
Leu Val Phe Pro Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn
485 490 495
Glu Lys Ile Asn Gln Ser Leu Ala Cys Ile Arg Lys Ser Asp Glu Leu
500 505 510
Leu Ser Ala Ile Gly Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln
515 520 525
Ala Tyr Val Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu
530 535 540
<210> 41
<211> 568
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 41
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gln Ser Thr Pro Ala Thr Asn Asn Arg Ala Arg Arg Glu Leu Pro
100 105 110
Arg Phe Met Asn Tyr Thr Leu Asn Asn Ala Lys Lys Thr Asn Val Thr
115 120 125
Leu Ser Lys Lys Arg Lys Arg Arg Phe Leu Gly Phe Leu Leu Gly Val
130 135 140
Gly Ser Ala Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu
145 150 155 160
Glu Gly Glu Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys
165 170 175
Ala Val Val Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val
180 185 190
Leu Asp Leu Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn
195 200 205
Lys Gln Ser Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln
210 215 220
Gln Lys Asn Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn
225 230 235 240
Ala Gly Val Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu
245 250 255
Leu Leu Ser Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys
260 265 270
Leu Met Ser Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile
275 280 285
Met Cys Ile Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro
290 295 300
Leu Tyr Gly Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro
305 310 315 320
Leu Cys Thr Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg
325 330 335
Thr Asp Arg Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe
340 345 350
Pro Gln Ala Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp
355 360 365
Thr Met Asn Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val
370 375 380
Asp Ile Phe Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr
385 390 395 400
Asp Val Ser Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys
405 410 415
Tyr Gly Lys Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile
420 425 430
Lys Thr Phe Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp
435 440 445
Thr Val Ser Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly
450 455 460
Lys Ser Leu Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro
465 470 475 480
Leu Val Phe Pro Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn
485 490 495
Glu Lys Ile Asn Gln Ser Leu Ala Cys Ile Arg Lys Ser Asp Glu Leu
500 505 510
Leu Ser Ala Ile Gly Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln
515 520 525
Ala Tyr Val Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu
530 535 540
Gly Gly Leu Val Pro Arg Gly Ser His His His His His His Ser Ala
545 550 555 560
Trp Ser His Pro Gln Phe Glu Lys
565
<210> 42
<211> 512
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 42
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gln Ser Thr Pro Ala Thr Asn Asn Arg Ala Arg Arg Glu Leu Pro
100 105 110
Arg Phe Met Asn Tyr Thr Leu Asn Asn Ala Lys Lys Thr Asn Val Thr
115 120 125
Leu Ser Lys Lys Arg Lys Arg Arg Phe Leu Gly Phe Leu Leu Gly Val
130 135 140
Gly Ser Ala Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu
145 150 155 160
Glu Gly Glu Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys
165 170 175
Ala Val Val Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val
180 185 190
Leu Asp Leu Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn
195 200 205
Lys Gln Ser Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln
210 215 220
Gln Lys Asn Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn
225 230 235 240
Ala Gly Val Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu
245 250 255
Leu Leu Ser Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys
260 265 270
Leu Met Ser Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile
275 280 285
Met Cys Ile Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro
290 295 300
Leu Tyr Gly Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro
305 310 315 320
Leu Cys Thr Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg
325 330 335
Thr Asp Arg Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe
340 345 350
Pro Gln Ala Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp
355 360 365
Thr Met Asn Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val
370 375 380
Asp Ile Phe Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr
385 390 395 400
Asp Val Ser Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys
405 410 415
Tyr Gly Lys Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile
420 425 430
Lys Thr Phe Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp
435 440 445
Thr Val Ser Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly
450 455 460
Lys Ser Leu Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro
465 470 475 480
Leu Ser Ala Ile Gly Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln
485 490 495
Ala Tyr Val Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu
500 505 510
<210> 43
<211> 536
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 43
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gln Ser Thr Pro Ala Thr Asn Asn Arg Ala Arg Arg Glu Leu Pro
100 105 110
Arg Phe Met Asn Tyr Thr Leu Asn Asn Ala Lys Lys Thr Asn Val Thr
115 120 125
Leu Ser Lys Lys Arg Lys Arg Arg Phe Leu Gly Phe Leu Leu Gly Val
130 135 140
Gly Ser Ala Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu
145 150 155 160
Glu Gly Glu Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys
165 170 175
Ala Val Val Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val
180 185 190
Leu Asp Leu Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn
195 200 205
Lys Gln Ser Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln
210 215 220
Gln Lys Asn Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn
225 230 235 240
Ala Gly Val Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu
245 250 255
Leu Leu Ser Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys
260 265 270
Leu Met Ser Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile
275 280 285
Met Cys Ile Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro
290 295 300
Leu Tyr Gly Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro
305 310 315 320
Leu Cys Thr Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg
325 330 335
Thr Asp Arg Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe
340 345 350
Pro Gln Ala Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp
355 360 365
Thr Met Asn Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val
370 375 380
Asp Ile Phe Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr
385 390 395 400
Asp Val Ser Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys
405 410 415
Tyr Gly Lys Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile
420 425 430
Lys Thr Phe Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp
435 440 445
Thr Val Ser Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly
450 455 460
Lys Ser Leu Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro
465 470 475 480
Leu Ser Ala Ile Gly Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln
485 490 495
Ala Tyr Val Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu
500 505 510
Gly Gly Leu Val Pro Arg Gly Ser His His His His His His Ser Ala
515 520 525
Trp Ser His Pro Gln Phe Glu Lys
530 535
<210> 44
<211> 477
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 44
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Ser Ala
100 105 110
Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu Glu Gly Glu
115 120 125
Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys Ala Val Val
130 135 140
Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val Leu Asp Leu
145 150 155 160
Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser
165 170 175
Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln Gln Lys Asn
180 185 190
Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn Ala Gly Val
195 200 205
Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser
210 215 220
Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys Leu Met Ser
225 230 235 240
Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile
245 250 255
Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly
260 265 270
Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro Leu Cys Thr
275 280 285
Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg
290 295 300
Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe Pro Gln Ala
305 310 315 320
Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp Thr Met Asn
325 330 335
Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val Asp Ile Phe
340 345 350
Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr Asp Val Ser
355 360 365
Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys
370 375 380
Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe
385 390 395 400
Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp Thr Val Ser
405 410 415
Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu
420 425 430
Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro Leu Ser Ala
435 440 445
Ile Gly Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln Ala Tyr Val
450 455 460
Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu
465 470 475
<210> 45
<211> 501
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пептидный конструкт
<400> 45
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Ser Ala
100 105 110
Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu Glu Gly Glu
115 120 125
Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys Ala Val Val
130 135 140
Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val Leu Asp Leu
145 150 155 160
Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser
165 170 175
Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln Gln Lys Asn
180 185 190
Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn Ala Gly Val
195 200 205
Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser
210 215 220
Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys Leu Met Ser
225 230 235 240
Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile
245 250 255
Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly
260 265 270
Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro Leu Cys Thr
275 280 285
Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg
290 295 300
Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe Pro Gln Ala
305 310 315 320
Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp Thr Met Asn
325 330 335
Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val Asp Ile Phe
340 345 350
Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr Asp Val Ser
355 360 365
Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys
370 375 380
Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe
385 390 395 400
Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp Thr Val Ser
405 410 415
Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu
420 425 430
Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro Leu Ser Ala
435 440 445
Ile Gly Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln Ala Tyr Val
450 455 460
Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu Gly Gly Leu
465 470 475 480
Val Pro Arg Gly Ser His His His His His His Ser Ala Trp Ser His
485 490 495
Pro Gln Phe Glu Lys
500
<210> 46
<211> 25
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 46
ctcaatttcc tcacttctcc agtgt 25
<210> 47
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 47
cttgattcct cggtgtacct ctgt 24
<210> 48
<211> 25
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 48
tcccattatg cctaggccag cagca 25
<210> 49
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Аминокислотный линкер
<400> 1
Gly Gly Gly Ser
1
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| МУТАНТНЫЙ БЕЛОК F RSV И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2807742C1 |
| САМОСОБИРАЮЩИЕСЯ НАНОСТРУКТУРНЫЕ ВАКЦИНЫ | 2019 |
|
RU2811439C2 |
| МУТАНТЫ БЕЛКА F RSV | 2016 |
|
RU2788403C2 |
| АНТИГЕННЫЕ ПОЛИПЕПТИДЫ НА ОСНОВЕ ПОСЛЕДОВАТЕЛЬНОСТИ РЕСПИРАТОРНО-СИНЦИТИАЛЬНОГО ВИРУСА | 2019 |
|
RU2807992C2 |
| МУТАНТЫ БЕЛКА F RSV | 2016 |
|
RU2723039C2 |
| БЕЛКИ RSV В ПРЕДШЕСТВУЮЩЕЙ СЛИЯНИЮ КОНФОРМАЦИИ И ИХ ПРИМЕНЕНИЕ | 2014 |
|
RU2761631C2 |
| ИММУНОГЛОБУЛИН С ОДНИМ ВАРИАБЕЛЬНЫМ ДОМЕНОМ ПРОТИВ F-БЕЛКА PCB | 2016 |
|
RU2730671C2 |
| КОМПОЗИЦИИ ГЕМАГГЛЮТИНИНА ГРИППА С ГЕТЕРОЛОГИЧНЫМИ ЭПИТОПАМИ И/ИЛИ ИЗМЕНЕННЫМИ САЙТАМИ РАСЩЕПЛЕНИЯ ПРИ СОЗРЕВАНИИ | 2017 |
|
RU2769406C2 |
| СКОНСТРУИРОВАННЫЕ МУЛЬТИСПЕЦИФИЧЕСКИЕ АНТИТЕЛА И ДРУГИЕ МУЛЬТИМЕРНЫЕ БЕЛКИ С АСИММЕТРИЧНЫМИ МУТАЦИЯМИ В ОБЛАСТИ CH2-CH3 | 2018 |
|
RU2804031C2 |
| МУЛЬТИВАЛЕНТНЫЕ PD-L1-СВЯЗЫВАЮЩИЕ СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ | 2020 |
|
RU2816646C2 |
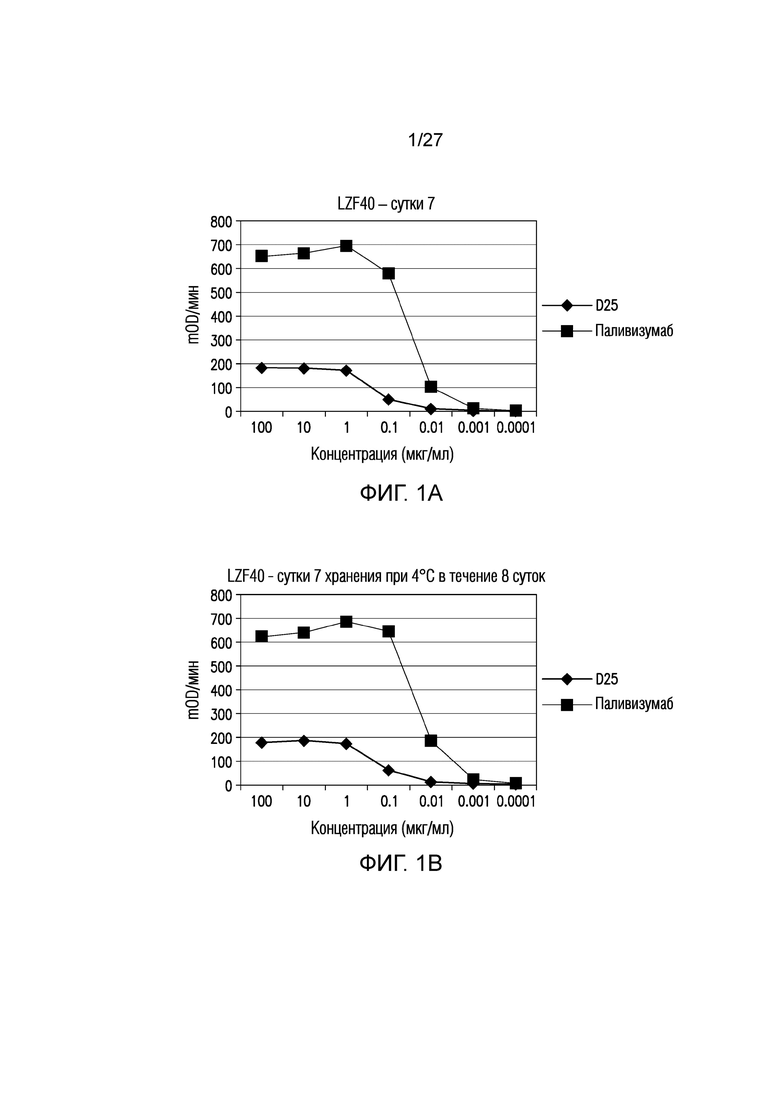
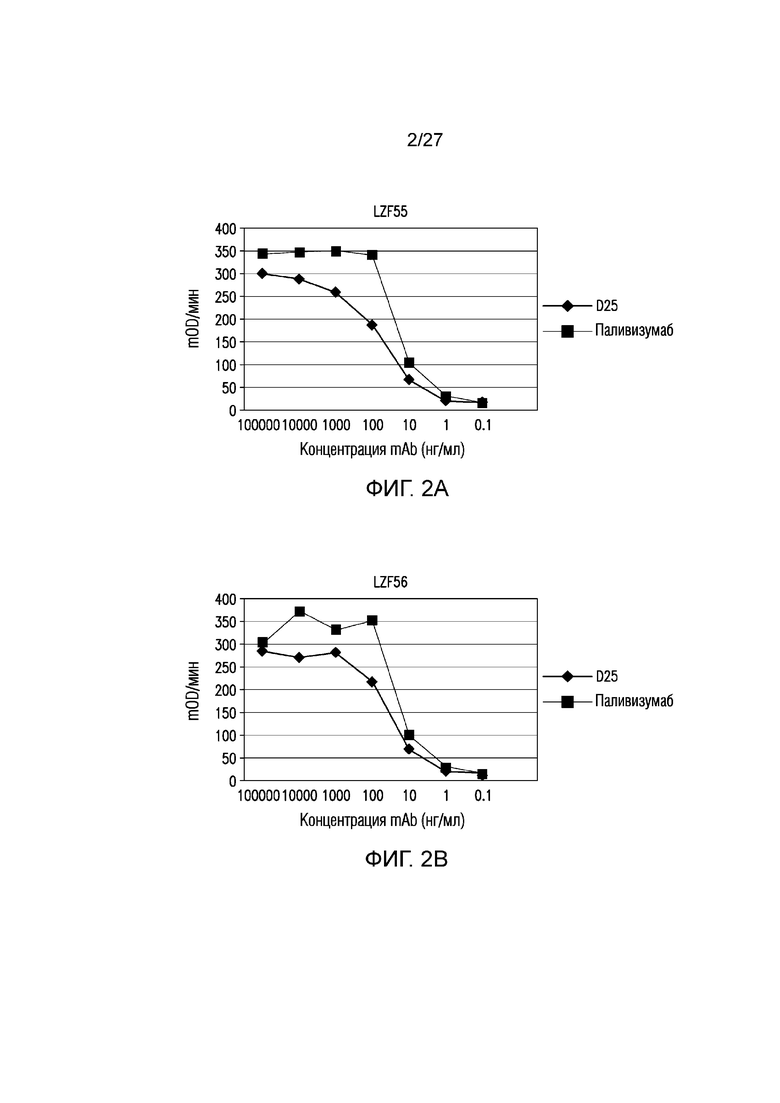
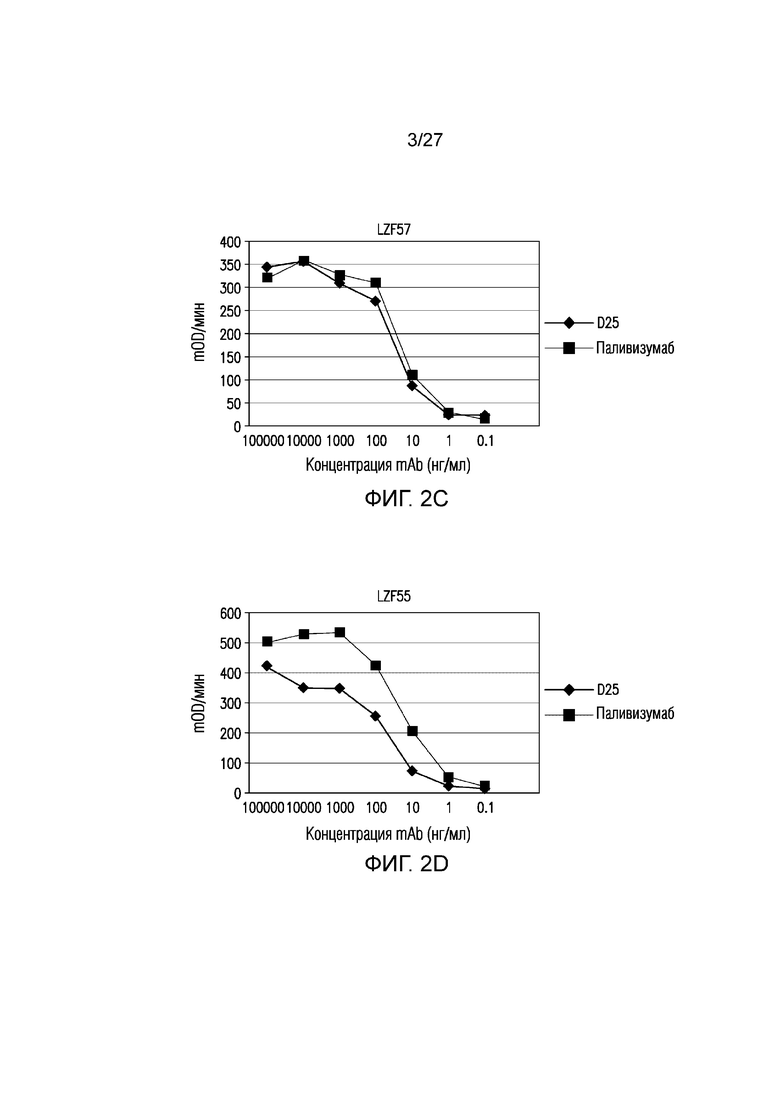
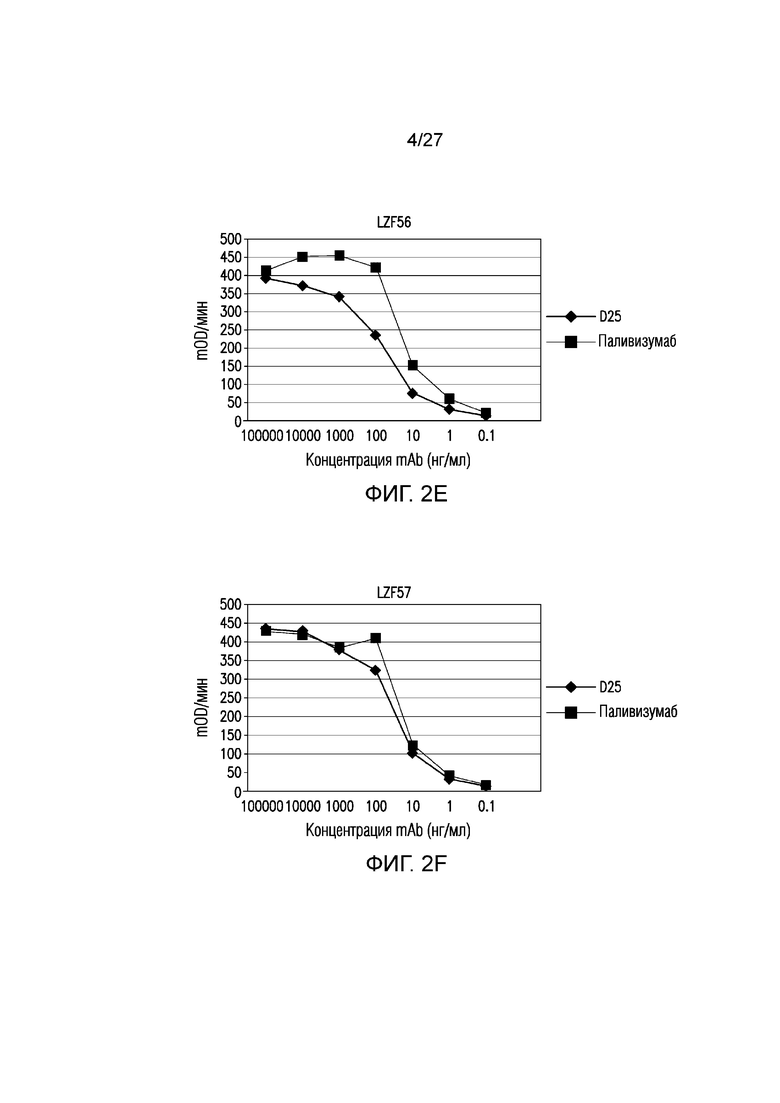

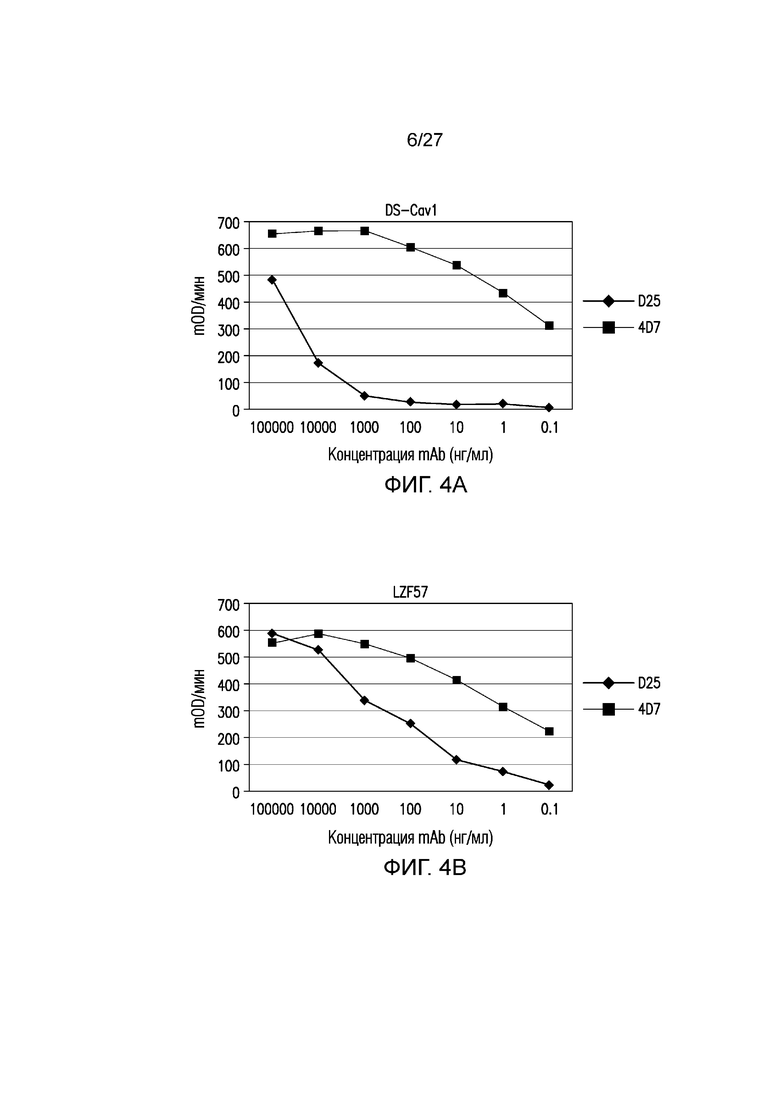
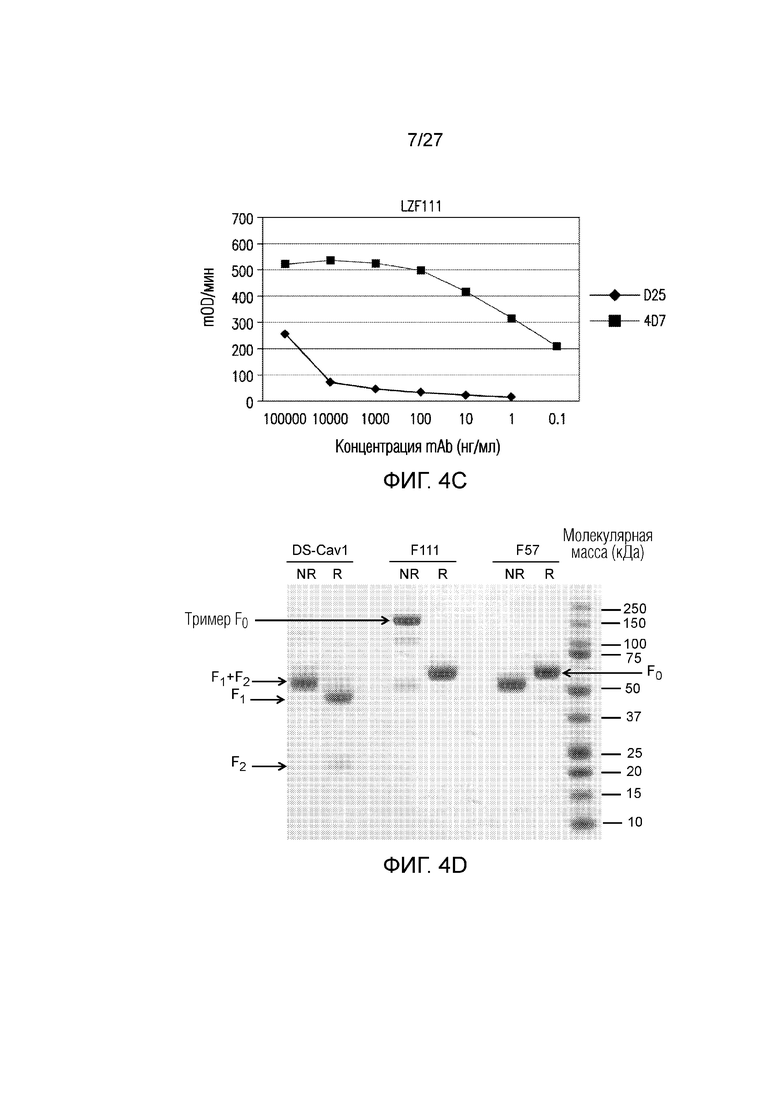
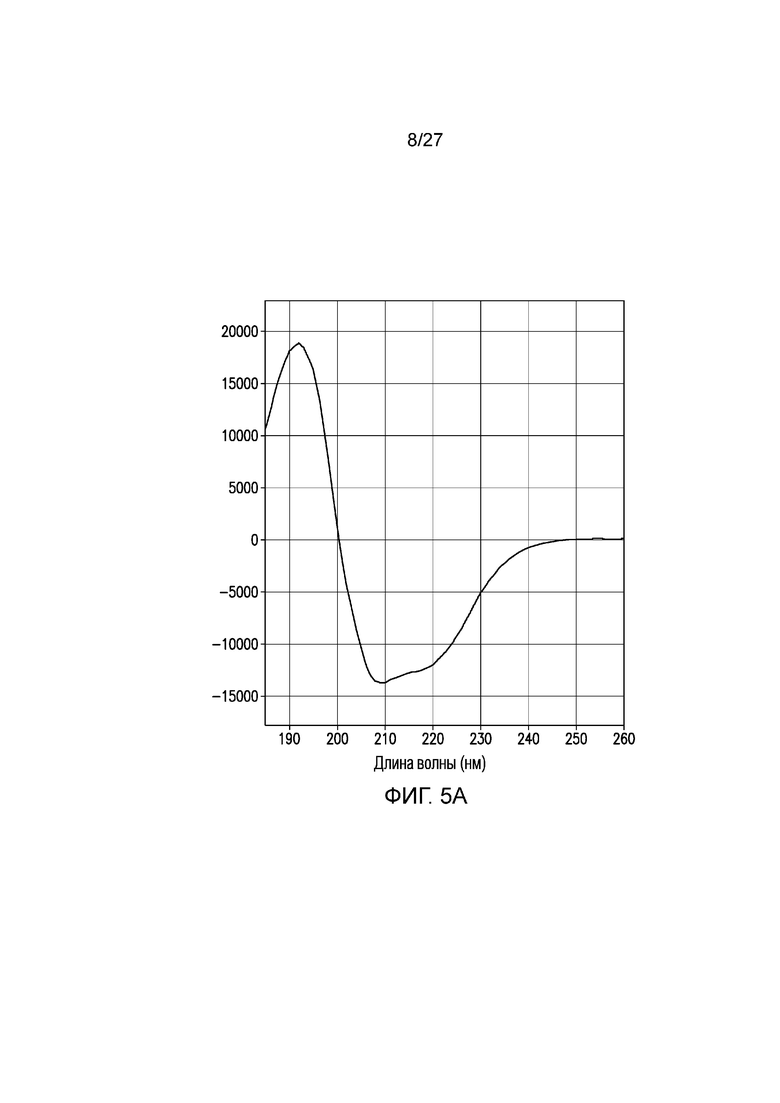
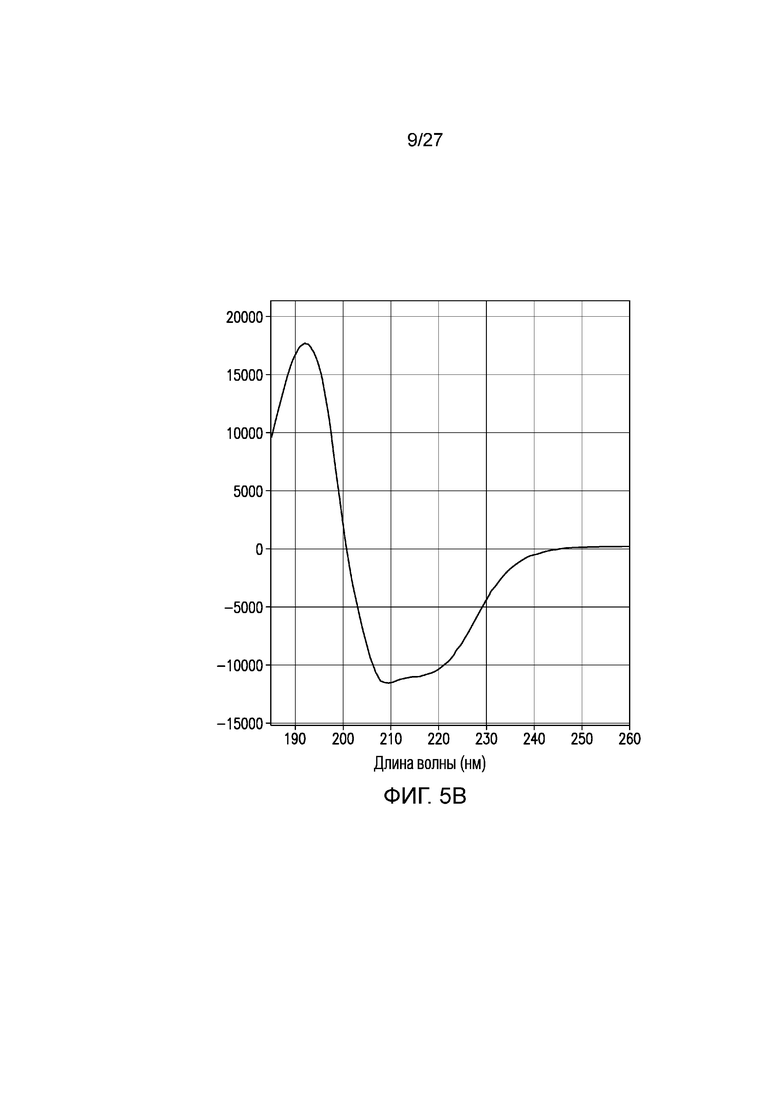
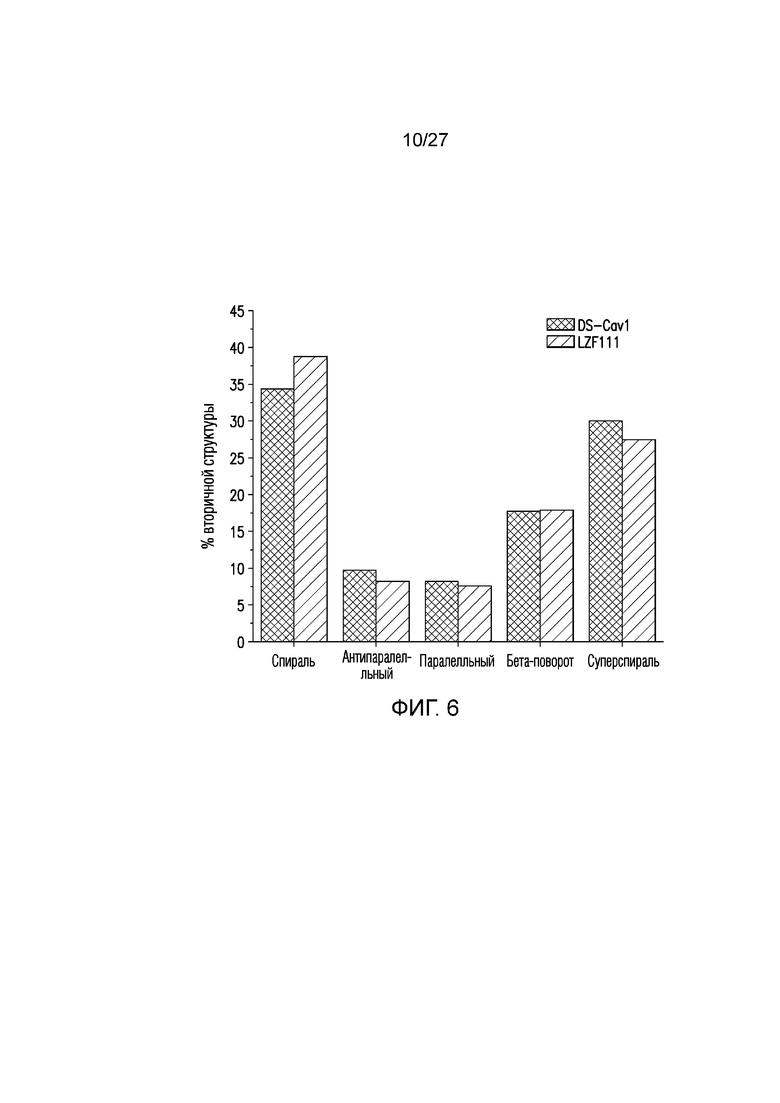
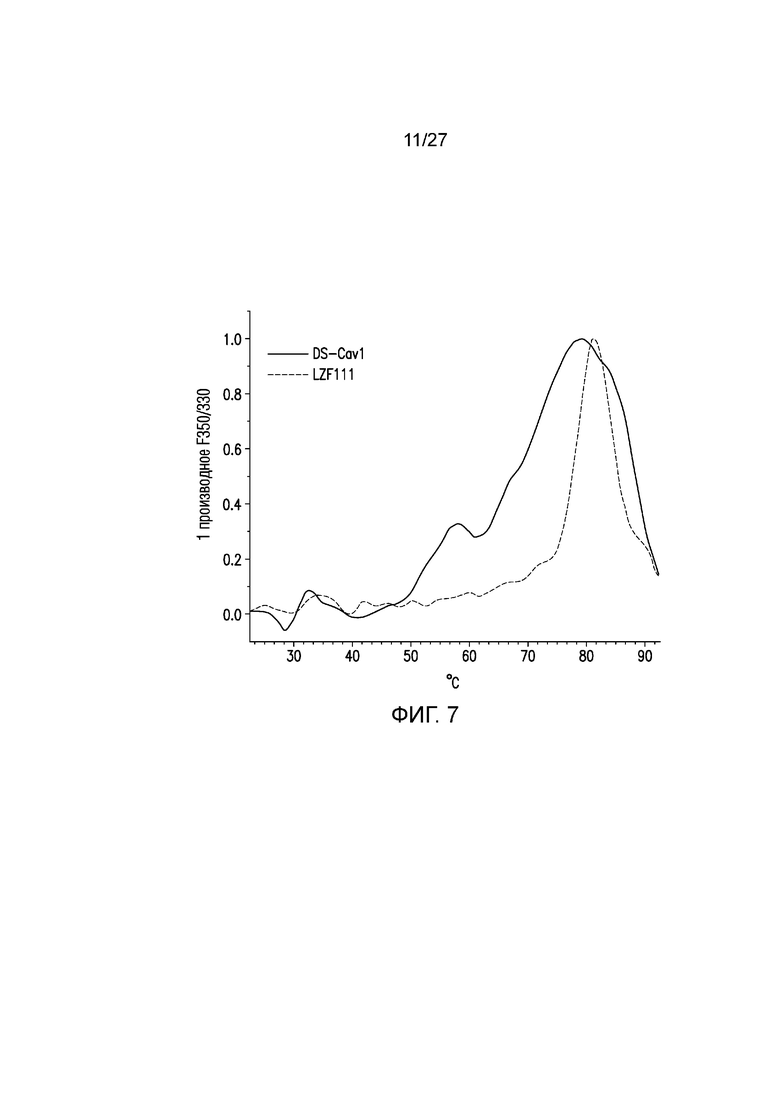
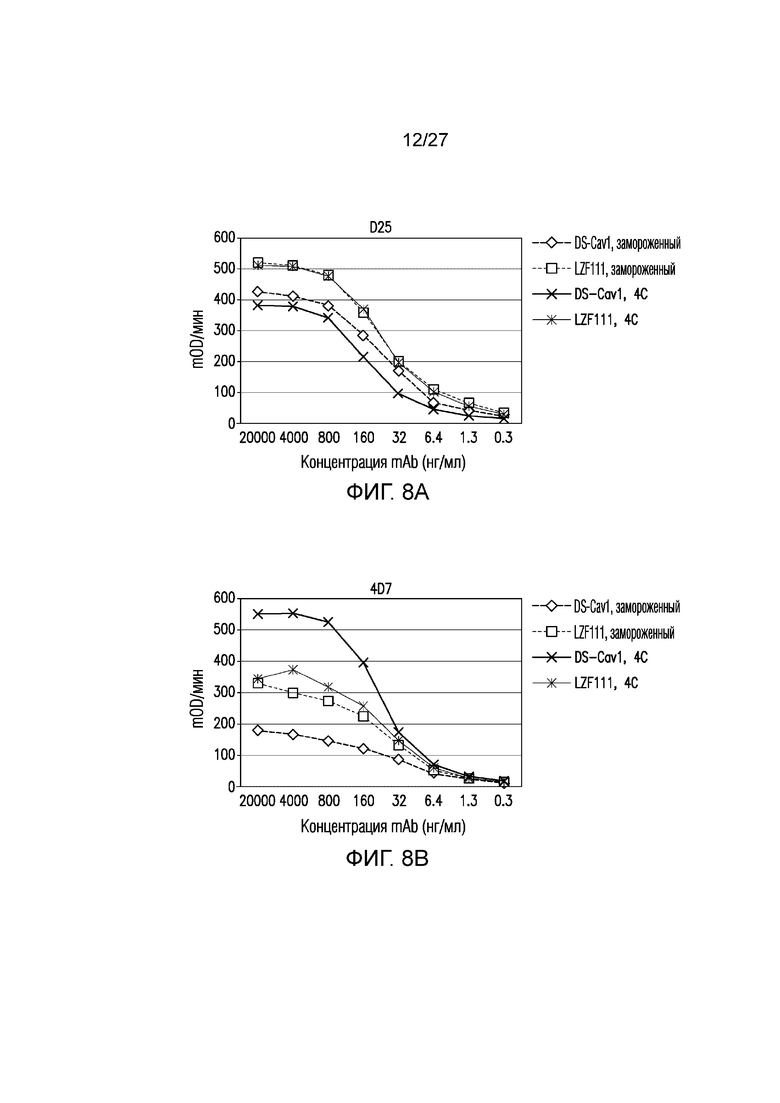
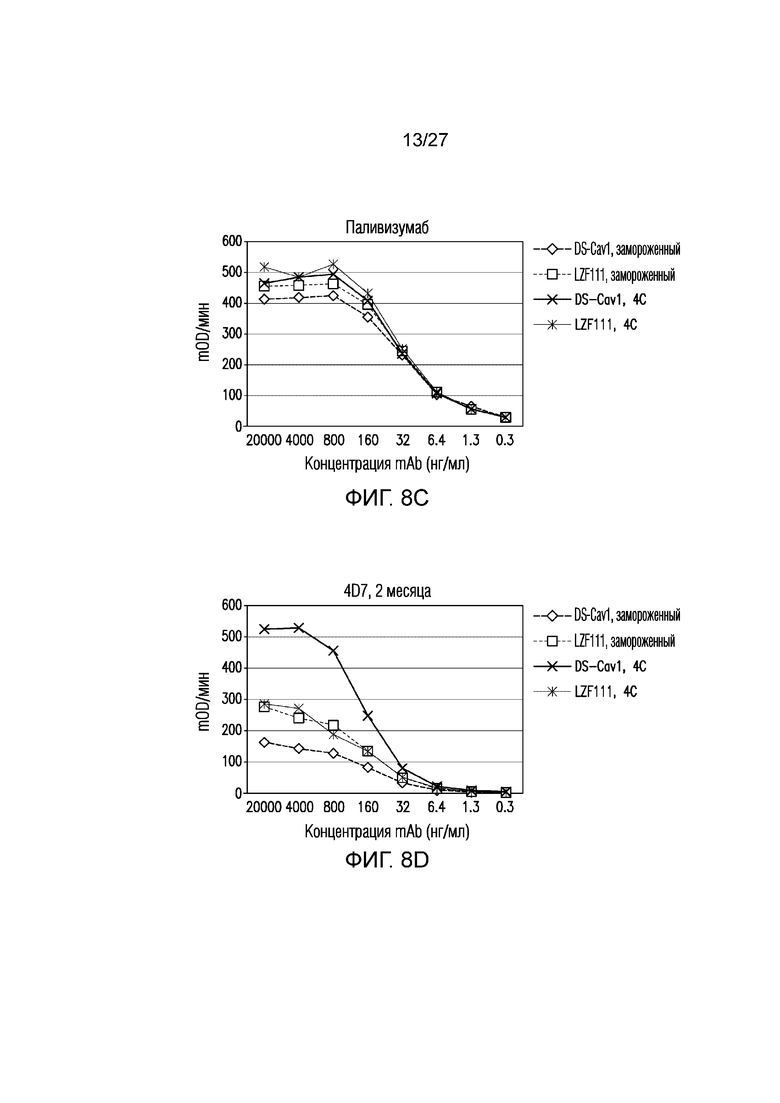
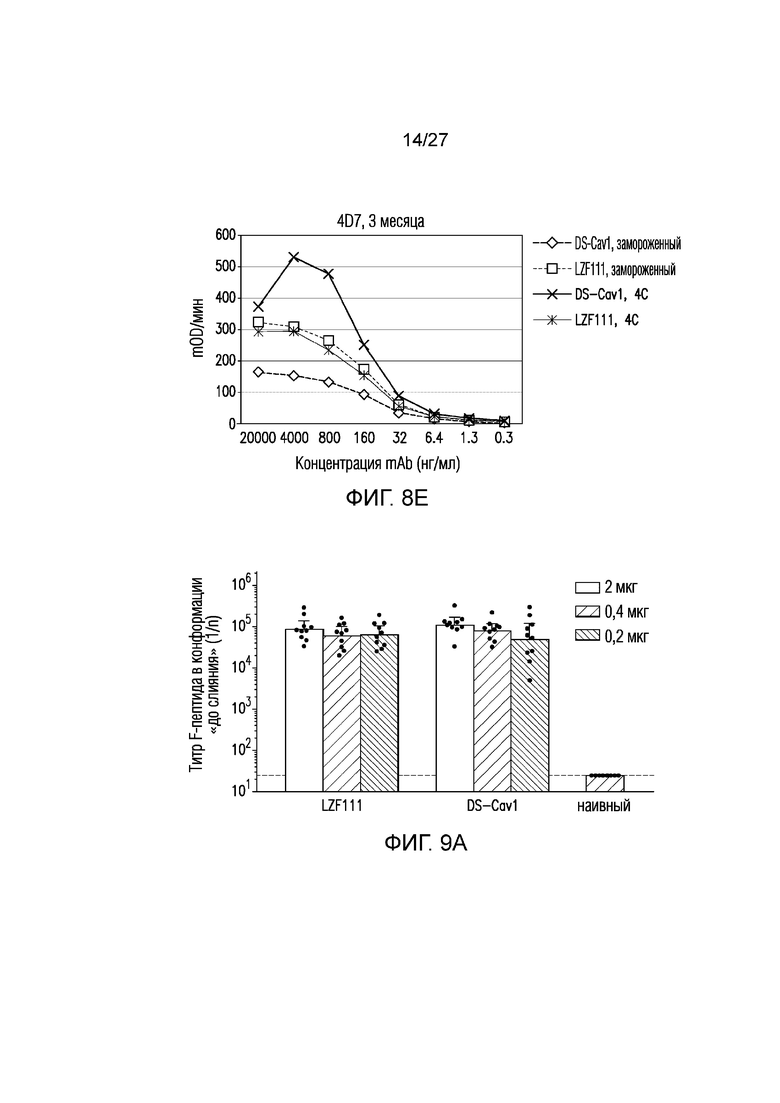
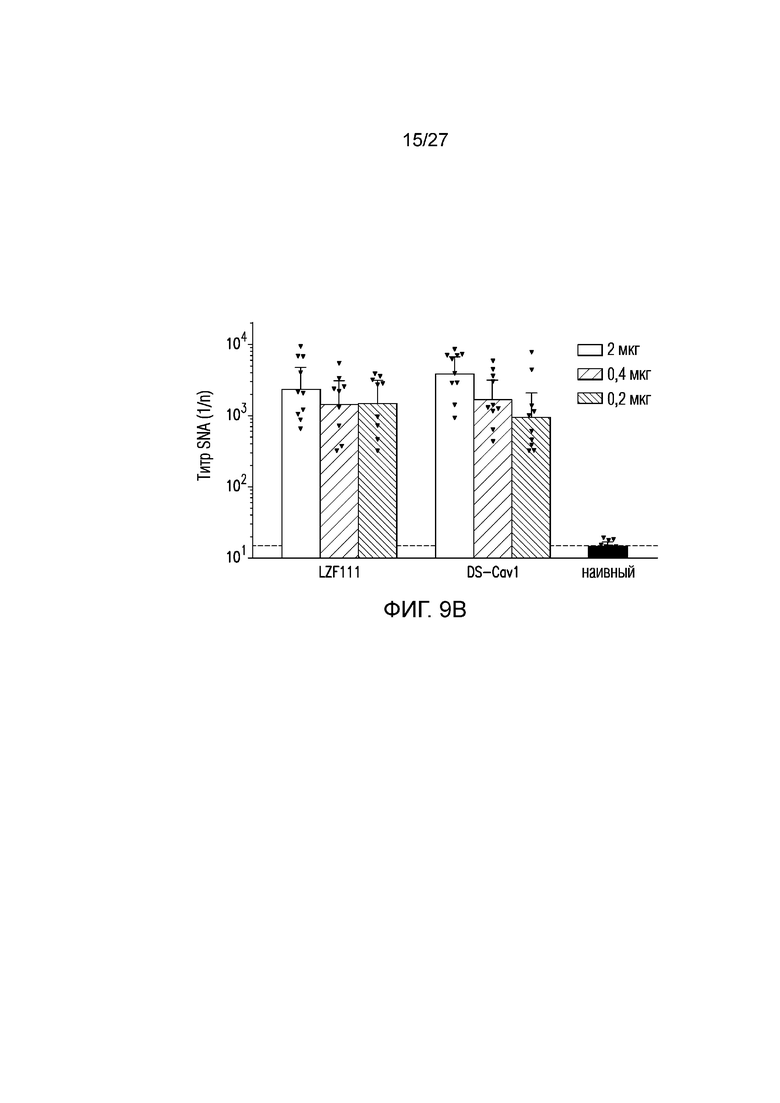
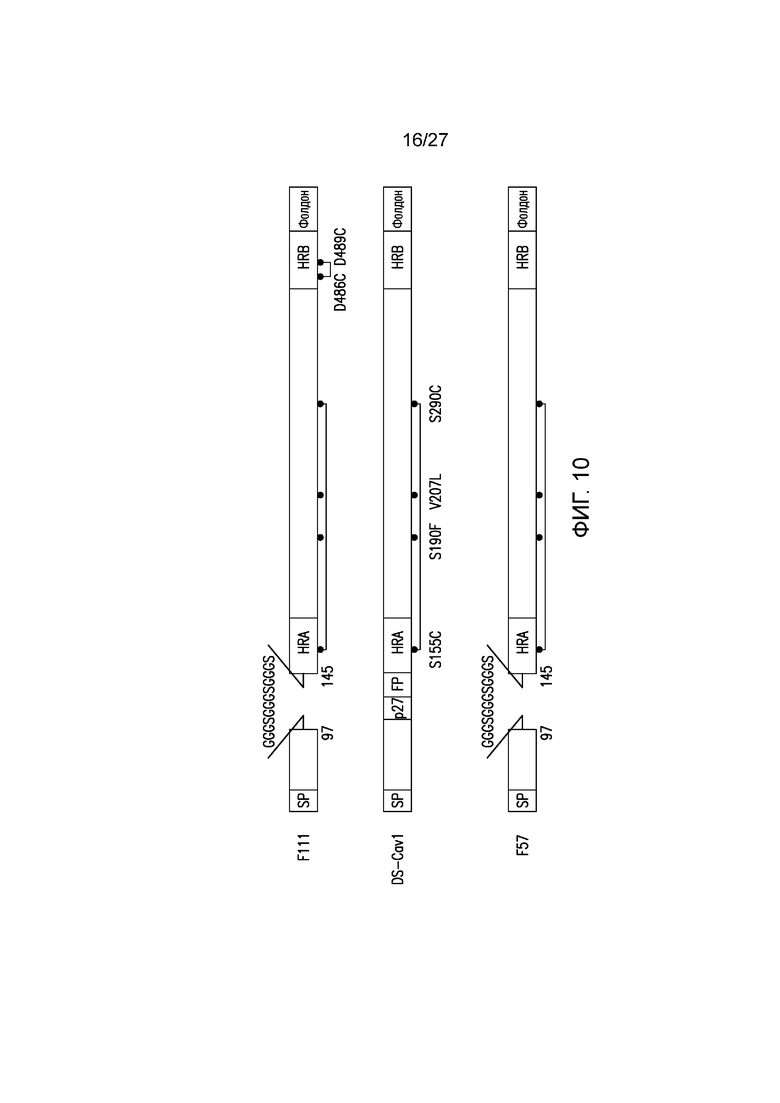
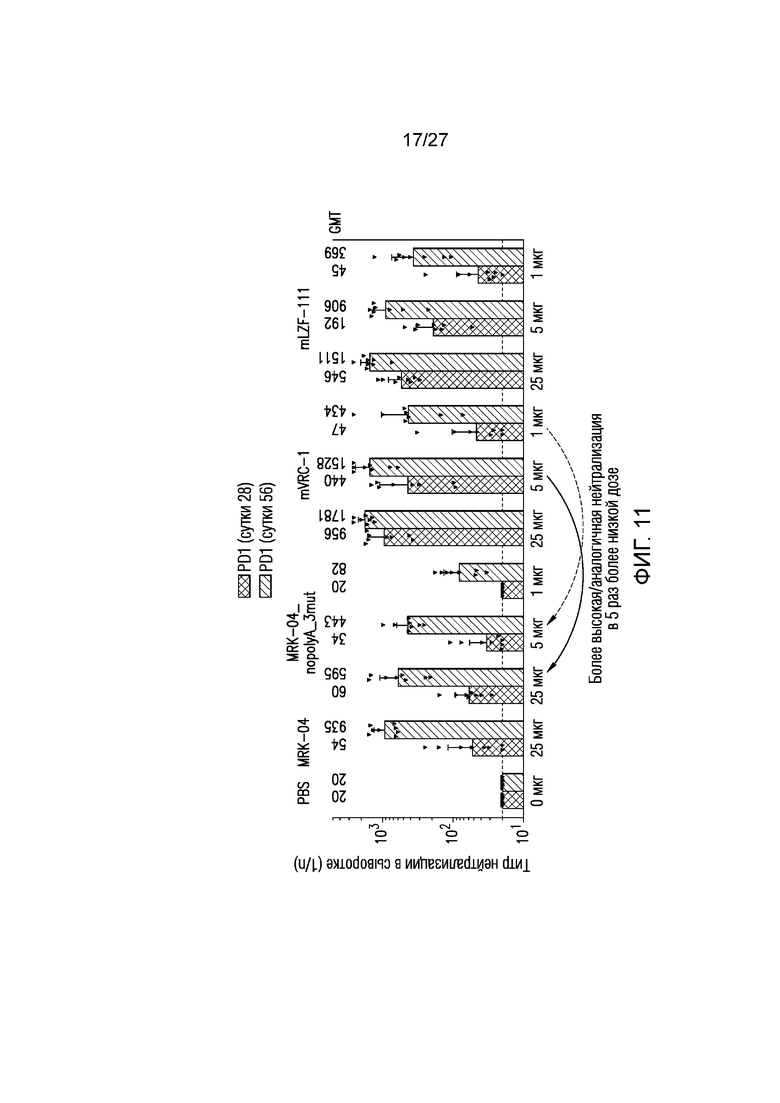
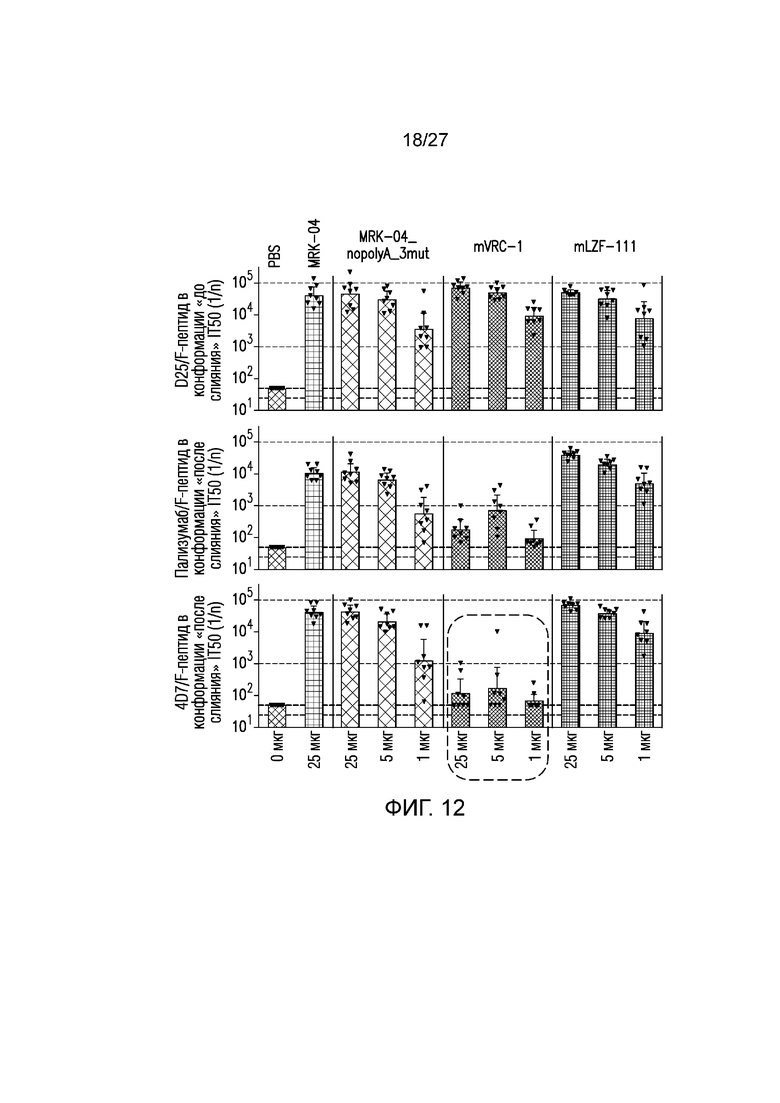
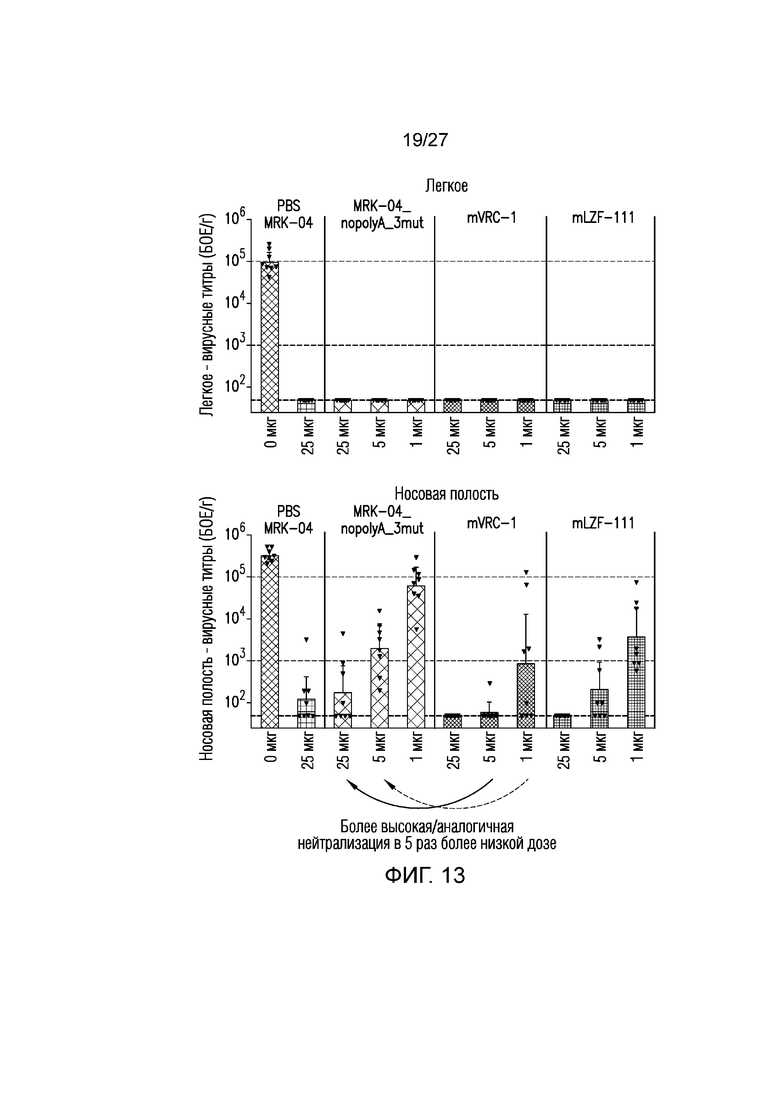



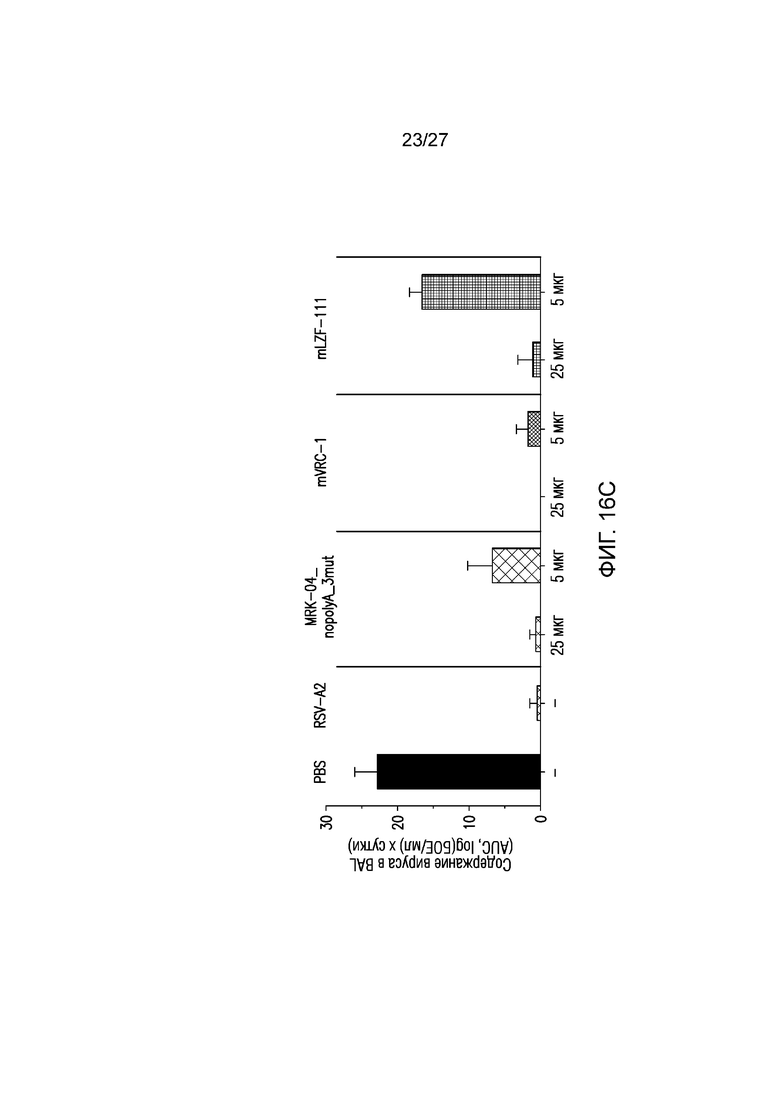
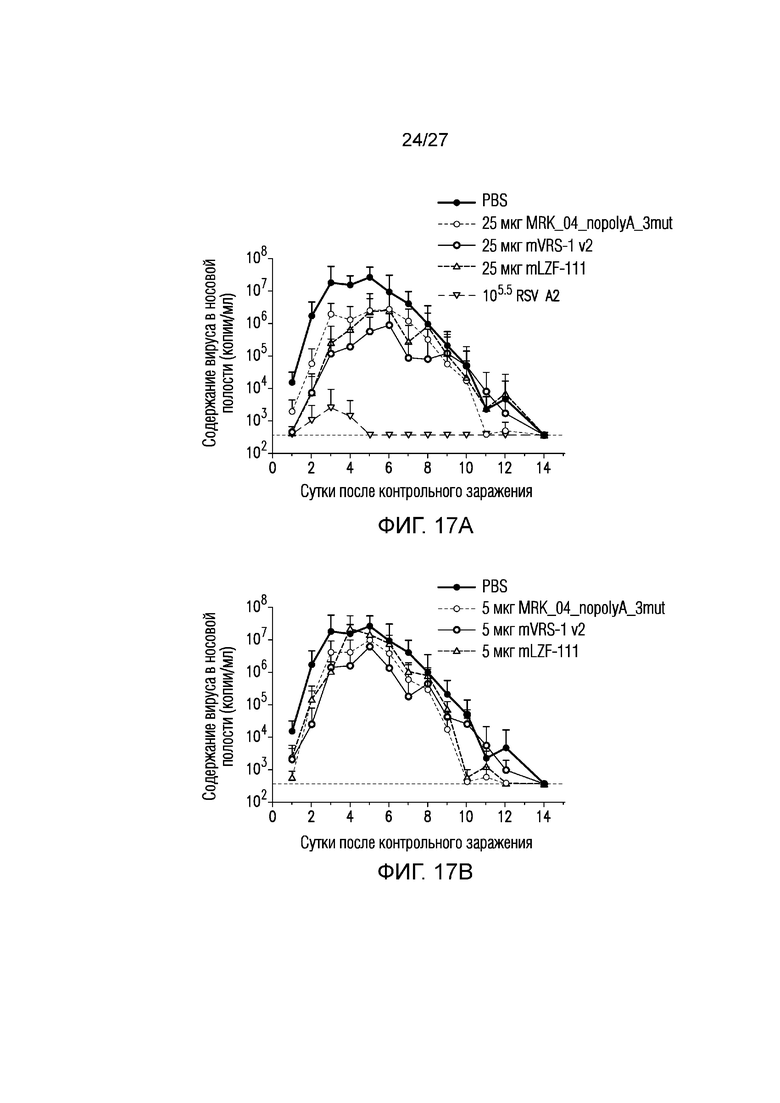
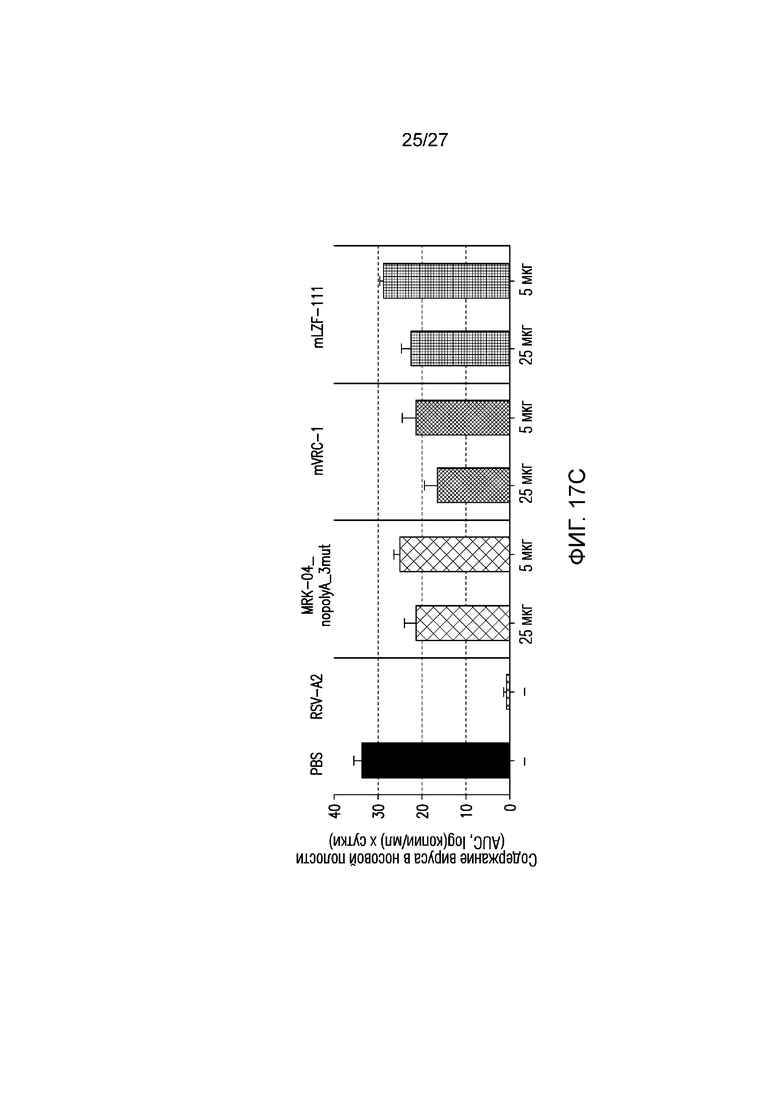
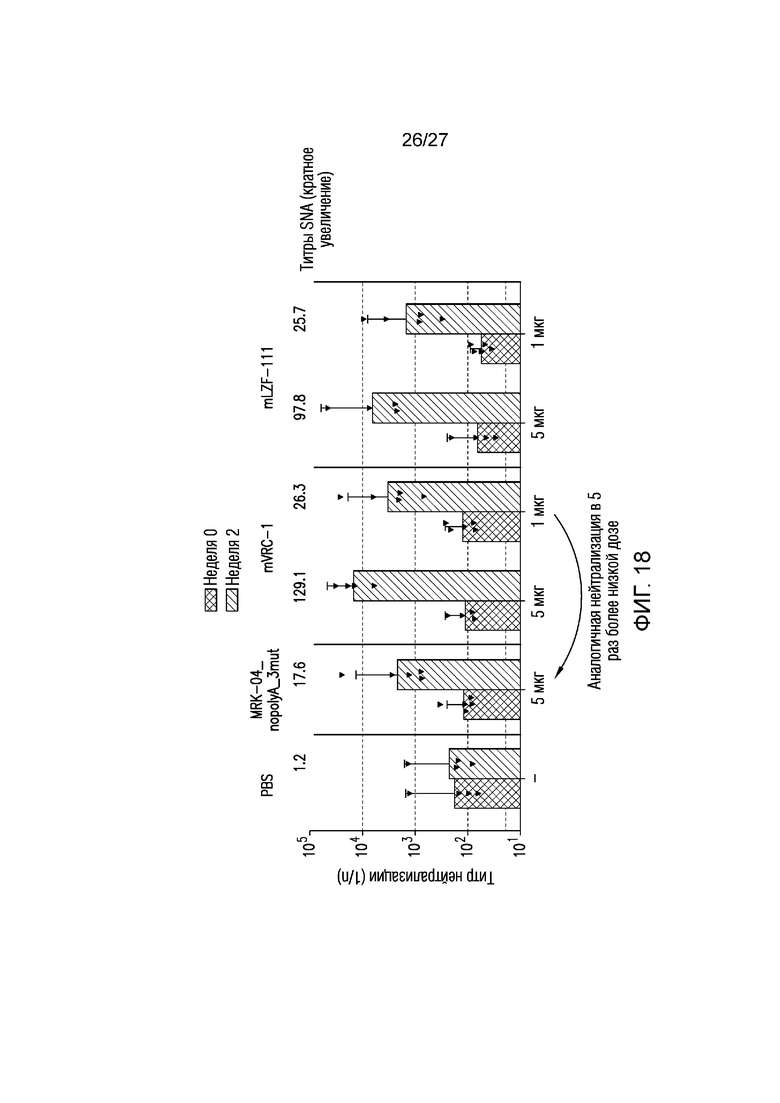
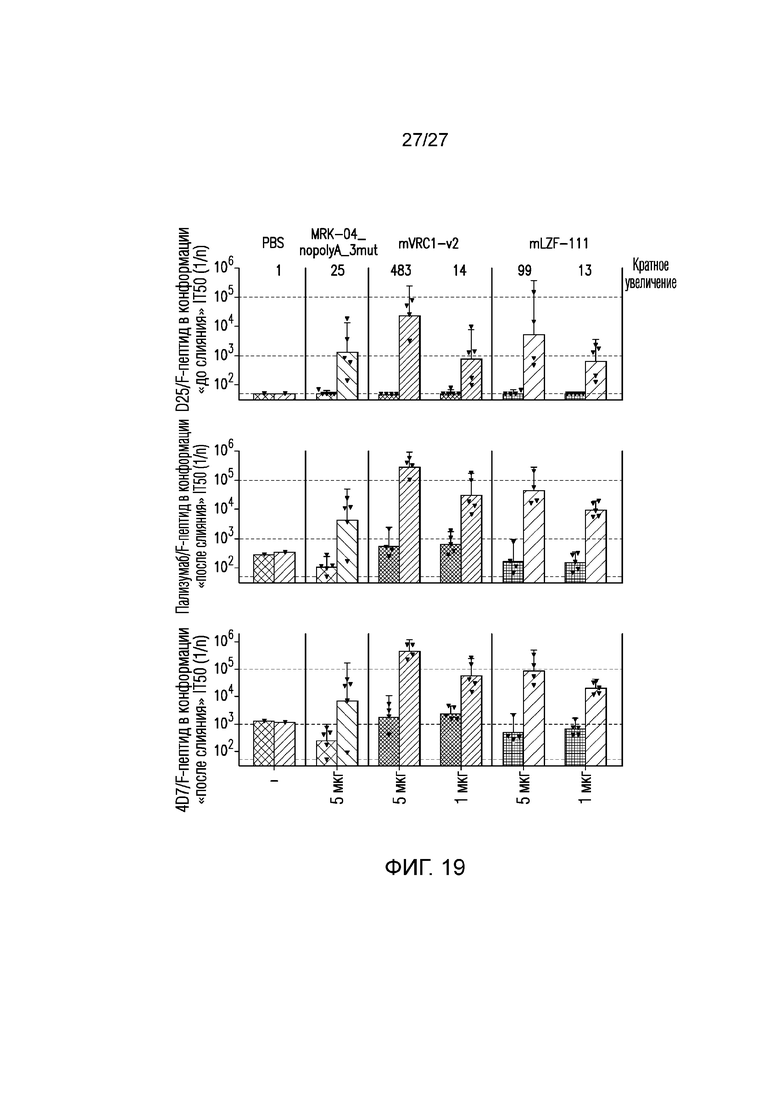
Изобретение относится к области биотехнологии, конкретно к получению тримера белка F респираторно-синцитиального вируса (RSV), и может быть использовано в медицине для индукции иммунного ответа на антиген RSV. Рекомбинантным путем получают белок F RSV, содержащий гибкий линкер вместо сайта расщепления протеазой и мутации в аминокислотной последовательности, придающие большую стабильность белку в конформации «до слияния». Изобретение позволяет получить тример белка F RSV, отличающийся большей стабильностью в конформации «до слияния». 5 н. и 20 з.п. ф-лы, 19 ил., 4 табл., 6 пр.
1. Рекомбинантный тример белка F респираторно-синцитиального вируса (RSV) для получения иммунного ответа на белок F RSV у субъекта, содержащий аминокислотную последовательность, представленную в любой из SEQ ID NO: 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 44 или 45.
2. Иммуногенная композиция RSV для индукции иммунного ответа на антиген RSV, содержащая рекомбинантный тример белка F RSV по п.1 в эффективном количестве и фармацевтически приемлемый эксципиент.
3. Иммуногенная композиция по п.2, формулированная для индукции антигенспецифического иммунного ответа, направленного против рекомбинантного тримера F RSV или рекомбинантного пептида F RSV.
4. Иммуногенная композиция по любому из п.2 или 3, которая формулирована с адъювантом.
5. Иммуногенная композиция по п.4, где адъювант представляет адъювант на основе соединения алюминия.
6. Иммуногенная композиция по п.5, где адъювант на основе соединения алюминия представляет собой аморфный сульфат гидроксифосфата алюминия или водную суспензию гидроксифосфата алюминия.
7. Иммуногенная композиция по п.2, дополнительно содержащая липидную наночастицу, содержащую один или более катионных липидов и поли(этиленгликоль)-липид (PEG-липид).
8. Иммуногенная композиция по п.7, где один или более катионных липидов представляют ионизируемые катионные липиды.
9. Иммуногенная композиция по п.8, где ионизируемые катионные липиды выбраны из DLinDMA; DlinKC2DMA; Dlin-МС3-DMA; CLinDMA; S-Octyl CLinDMA;
(2S)-1-{7-[(3β)-холест-5-ен-3-илокси]гептилокси}-3-[(4Z)-дек-4-ен-1-илокси]-N, N диметилпропан-2-амина;
(2R)-1-{4-[(3β)-холест-5-ен-3-илокси]бутокси}-3-[(4Z)-дек-4-ен-1-илокси]-N, N диметилпропан-2-амина;
1-[(2R)-1-{4-[(3β)-холест-5-ен-3-илокси]бутокси}-3-(октилокси)пропан-2-ил]гуанидина;
1-[(2R)-1-{7-[(3β)-холест-5-ен-3-илокси]гептилокси}-N, N-диметил-3-[(9Z,12Z)-октадека-9,12-диен-1-илокси]пропан-2-амина;
1-[(2R)-1-{4-[(3β)-холест-5-ен-3-илокси]бутокси}-N, N-диметил-3-[(9Z,12Z)-октадека-9,12-диен-1-илокси]пропан-2-амина;
(2S)-1-({6-[(3β))-холест-5-ен-3-илокси]гексил}окси)-N, N-диметил-3-[(9Z)-октадек-9-ен-1-илокси]пропан-2-амина;
(3β)-3-[6-{[(2S)-3-[(9Z)-октадек-9-ен-1-илокси]-2-(пирролидин-1-ил)пропил]окси}гексил)окси]холест-5-ена;
(2R)-1-{4-[(3β)-холест-5-ен-3-илокси]бутокси}-3-(октилокси)пропан-2-амина;
(2R)-1-({8-[(3β)-холест-5-ен-3-илокси]октил}окси)-N, N-диметил-3-(пентилокси)пропан-2-амина;
(2R)-1-({8-[(3β)-холест-5-ен-3-илокси]октил}окси)-3-(гептилокси)-N, N-диметилпропан-2-амина;
(2R)-1-({8-[(3β)-холест-5-ен-3-илокси]октил}окси)-N, N-диметил-3-[(2Z)пент-2-ен-1-илокси]пропан-2-амина;
(2S)-1-бутокси-3-({8-[(3β)-холест-5-ен-3-илокси]октил}окси)-N, N-диметилпропан-2-амина;
(2S-1-({8-[(3β)-холест-5-ен-3-илокси]октил}окси)-3-[2,2,3,3,4,4,5,5,6,6,7,7,8,8,9,9-гексадекафторнонил)окси]-N, N-диметилпропан-2-амина;
2-амино-2-{[(9Z,12Z)-октадека-9,12-диен-1-илокси]метил}пропан-1,3-диола;
2-амино-3-((9-(((3S,10R,13R)-10,13-диметил-17-(6-метилгептан-2-ил)-2,3,4,7,8,9,10,11,12,13,14,15,16,17-тетрадекагидро-1Н-циклопента[а]фенантрен-3-ил)окси)нонил)окси)-2 -((((9Z,12Z)-октадека-9,12-диен-1-ил)окси)метил)пропан-1-ола;
2-амино-3-((6-(((3S,10R,13R)-10,13-диметил-17-(6-метилгептан-2-ил)-2,3,4,7,8,9,10,11,12,13,14,15,16,17-тетрагидро-1Н-циклопента[а]фенантрен-3-ил)окси)гексил)окси)-2-((((Z)-октадек-9-ен-1-ил)окси)метил)пропан-1-ола;
(20Z,23Z)-N, N-диметилнонакоза-20,23-диен-10-амина;
(17Z,20Z)-N, N-диметилгексакоза-17,20-диен-9-амина;
(16Z,19Z)-N, N-диметилпентакоза-16,19-диен-8-амина;
(13Z,16Z)-N, N-диметилдокоза-13,16-диен-5-амина;
(12Z,15Z)-N, N-диметилгеникоза-12,15-диен-4-амина;
(14Z,17Z)-N, N-диметилтрикоза-14,17-диен-6-амина;
(15Z,18Z)-N, N-диметилтетракоза-15,18-диен-7-амина;
(18Z,21Z)-N, N-диметилгептакоза-18,21-диен-10-амина;
(15Z,18Z)-N, N-диметилтетракоза-15,18-диен-5-амина;
(14Z,17Z)-N, N-диметилтрикоза-14,17-диен-4-амина;
(19Z,22Z)-N, N-диметилоктакоза-19,22-диен-9-амина;
(18Z,21Z)-N, N-диметилгептакоза-18,21-диен-8-амина;
(17Z,20Z)-N, N-диметилгексакоза-17,20-диен-7-амина;
(16Z,19Z)-N, N-диметилпентакоза-16,19-диен-6-амина;
(22Z,25Z)-N, N-диметилгентриаконта-22,25-диен-10-амина;
(21Z,24Z)-N, N-диметилтриаконта-21,24-диен-9-амина;
(18Z)-N, N-диметилгептакоз-18-ен-10-амина;
(17Z)-N, N-диметилгексакоз-17-ен-9-амина;
(19Z,22Z)-N, N-диметилоктакоза-19,22-диен-7-амина;
N, N-диметилгептакозан-10-амина;
(20Z,23Z)-N-этил-N-метилнонакоза-20,23-диен-10-амина;
1-[(11Z,14Z)-1-нониликоза-11,14-диен-1-ил]-пирролидина;
(20Z)-N, N-диметилгептакоз-20-ен-10-амина;
(15Z)-N, N-диметилгептакоз-15-ен-10-амина;
(14Z)-N, N-диметилнонакоз-14-ен-10-амина;
(17Z)-N, N-диметилнонакоз-17-ен-10-амина;
(24Z)-N, N-диметилтритриаконт-24-ен-10-амина;
(20Z)-N, N-диметилнонакоз-20-ен-10-амина;
(22Z)-N, N-диметилгентриаконт-22-ен-10-амина;
(16Z)-N, N-диметилпентакоз-16-ен-8-амина;
(12Z,15Z)-N, N-диметил-2-нонилгеникоза-12,15-диен-1-амина;
(13Z,16Z)-N, N-диметил-3-нонилдокоза-13,16-диен-1-амина;
N, N-диметил-1-[(1S,2R)-2-октилциклопропил]гептадекан-8-амина;
1-[(1S,2R)-2-гексилциклопропил]-N, N-диметилнонадекан-10-амина;
N, N-диметил-1-[(1S,2R)-2-октилциклопропил]нонадекан-10-амина;
N, N-диметил-21-[(1S,2R)-2-октилциклопропил]геникозан-10-амина;
N, N-диметил-1-[(1S,2S)-2-{[(1R,2R)-2-пентилциклопропил]метил}циклопропил]нонадекан-10-амина;
N, N-диметил-1-[(1S,2R)-2-октилциклопропил]гексадекан-8-амина;
N, N-диметил-1-[(1R,2S)-2-ундецилциклопропил]тетрадекан-5-амина;
N, N-диметил-3-{7-[(1S,2R)-2-октилциклопропил]гептил} додекан-1-амина;
1-[(1R,2S)-2-гептилциклопропил]-N, N-диметилоктадекан-9-амина;
1-[(1S,2R)-2-децилциклопропил]-N, N-диметилпентадекан-6-амина;
N, N-диметил-1-[(1S,2R)-2-октилциклопропил]пентадекан-8-амина; и
(11E,20Z,23Z)-N, N-диметилнонакоза-11,20,23-триен-10-амина;
или фармацевтически приемлемой соли, или стереоизомера любого из вышеуказанного.
10. Иммуногенная композиция по п.9, где ионизируемые катионные липиды выбраны из группы, состоящей из (2S)-1-({6-[(3β))-холест-5-ен-3-илокси]гексил}окси)-N, N-диметил-3-[(9Z)-октадек-9-ен-1-илокси]пропан-2-амина; (13Z,16Z)-N, N-диметил-3-нонилдокоза-13,16-диен-1-амина и N, N-диметил-1-[(1S,2R)-2-октилциклопропил]гептадекан-8-амина; или фармацевтически приемлемой соли, или стереоизомера любого из вышеуказанного.
11. Иммуногенная композиция по п.10, которая содержит 30-75 мол.% ионизируемого катионного липида и 0,1-20 мол.% ПЭГ-липида.
12. Иммуногенная композиция по любому из пп.7-11, дополнительно включающая один или более некатионных липидов, выбранных из фосфолипида, производного фосфолипида, жирной кислоты, стерола или их комбинации.
13. Иммуногенная композиция по п.12, где стерол представляет холестерин, стигмастерол или стигмастанол.
14. Иммуногенная композиция по п.12, где фосфолипид выбран из фосфатидилсерина, 1,2-дистеароил-sn-глицеро-3-фосфохолина (DSPC), 1,2-дипальмитолеоил-sn-глицеро-3-фосфохолина, 1,2-димиристоил-sn-глицеро-3-фосфохолина (DMPC), дилауроилфосфатидилхолина (DLPC), 1,2-диейкозеноил-sn-глицеро-3-фосфохолина и 1,2-диолеоил-sn-глицеро-3-фосфохолина (DOPC).
15. Иммуногенная композиция по любому из пп.8-14, где ПЭГ-липид представляет 1,2-димиристоил-sn-глицерин- метоксиполиэтиленгликоль (PEG-DMG), ПЭГ-дистерилглицерин (PEG-DSG), ПЭГ-дипальметолеил, ПЭГ-диолеил, ПЭГ-дистеарил, ПЭГ-диацилгликамид (PEG-DAG), ПЭГ-дипальмитоилфосфатидилэтаноламин (PEG-DPPE) или ПЭГ-1,2-димиристилоксилпропил-3-амин (PEG-c-DMA).
16. Иммуногенная композиция по любому из пп.12-15, которая содержит 20-99,8 мол.% ионизируемых катионных липидов, 0,1-65 мол.% некатионных липидов и 0,1-20 мол.% ПЭГ-липида.
17. Иммуногенная композиция по п.16, где некатионные липиды включают смесь холестерина и DSPC.
18. Иммуногенная композиция по п.12, которая содержит 34-59 мол.% ионизируемых катионных липидов, выбранных из группы, состоящей из (2S)-1-({6-[(3β))-холест-5-ен-3-илокси]гексил}окси)-N, N-диметил-3-[(9Z)-октадек-9-ен-1-илокси]пропан-2-амина; (13Z,16Z)-N, N-диметил-3-нонилдокоза-13,16-диен-1-амина; и N, N-диметил-1-[(1S,2R)-2-октилциклопропил]гептадекан-8-амина, 30-48 мол.% холестерина, 10-24% DSPC и 1-2 мол.% PEG-DMG.
19. Способ получения иммунного ответа на белок F RSV у субъекта, где способ включает введение субъекту эффективного количества тримера белка F RSV по п.1.
20. Способ по п.19, где субъекту вводят однократную дозу тримера белка F RSV.
21. Способ по п.19, где субъекту вводят по меньшей мере одну бустер-дозу тримера белка F RSV.
22. Способ по любому из пп.19-21, где тример белка F RSV вводят субъекту внутрикожной инъекцией или внутримышечной инъекцией.
23. Способ по любому из пп.19-22, где субъект подвергался воздействию вируса RSV, где субъект инфицирован вирусом RSV или где субъект подвергается риску заражения вирусом RSV.
24. Применение тримера белка F RSV по п.1 в способе индукции иммунного ответа на белок F RSV у субъекта, где способ включает введение субъекту тримера белка F RSV в количестве, эффективном для получения антигенспецифического иммунного ответа у субъекта.
25. Применение тримера белка F RSV по п.1 в производстве лекарственного средства для применения в способе индукции иммунного ответа на белок F RSV у субъекта, где способ включает введение субъекту тримера белка F RSV в количестве, эффективном для получения антигенспецифического иммунного ответа у субъекта.
| WO 2017172890 A1, 05.10.2017 | |||
| WO 2017109629 А1, 29.06.2017 | |||
| RU 2012105308 А, 20.08.2013 | |||
| CHEN X | |||
| et al., Fusion protein linkers: property, design and functionality, Advanced drug delivery reviews, 2013, v | |||
| Разборное приспособление для накатки на рельсы сошедших с них колес подвижного состава | 1920 |
|
SU65A1 |
| MAEDA Y | |||
| et al., Engineering of functional chimeric protein G-Vargula Luciferase, Analytical biochemistry, 1997, v | |||
Авторы
Даты
2023-05-03—Публикация
2019-01-24—Подача