ПЕРЕКРЕСТНАЯ ССЫЛКА
[0001] Настоящая заявка испрашивает приоритет согласно предварительным заявкам на патент США под номерами 62/636757, дата подачи 28 февраля 2018 г., и 62/724721, дата подачи 30 августа 2018 г., каждая из которых полностью включена в настоящий документ посредством ссылки.
ОПИСАНИЕ ТЕКСТОВОГО ФАЙЛА, ПРЕДСТАВЛЕННОГО В ЭЛЕКТРОННОМ ВИДЕ
[0002] Эта заявка подана в электронном виде через EFS-Web и включает в себя перечень последовательностей, представленный в электронном виде в формате .txt. Файл .txt, содержащий список последовательностей, имеет название «ICVX_001_02WO_SeqList_ST25.txt», создан 27 февраля 2019 г. и имеет размер ~373 килобайт.
ОБЛАСТЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
[0003] Настоящее изобретение в целом относится к вакцинам и способам их применения. В частности, настоящее изобретение относится к вакцинам на основе наноструктур, способным вызывать иммунные ответы на антигены, такие как антигенные белки различных инфекционных агентов, включая бактерии, вирусы и паразиты.
УРОВЕНЬ ТЕХНИКИ ОТНОСИТЕЛЬНО ИЗОБРЕТЕНИЯ
[0004] Вакцинация - это метод лечения, используемый для предотвращения или уменьшения тяжести инфекции различными инфекционными агентами, включая бактерии, вирусы и паразиты. Разработка новых вакцин имеет важные коммерческие последствия и последствия для общественного здравоохранения. В частности, болезнь Лайма, коклюш, вирус герпеса, ортомиксовирус, парамиксовирус, пневмовирус, филовирус, флавивирус, реовирус, ретровирус и малярия являются инфекционными агентами, вакцины против которых уже существуют, разрабатываются или желательны.
[0005] Субъединичные вакцины - это вакцины, состоящие из изолированных антигенов, обычно белков, рекомбинантно экспрессируемых в бактериальных клетках, клетках насекомых или клетках млекопитающих-хозяев. Обычно антигенный компонент субъединичной вакцины выбран из белков инфекционного агента, которые, как показали наблюдения, вызывают естественный иммунный ответ при инфекции, хотя в некоторых случаях можно применять другие компоненты инфекционного агента. Типичные антигены для применения в субъединичных вакцинах включают белок, экспрессируемый на поверхности целевого инфекционного агента, например, экспрессируемые на поверхности гликопротеины оболочки вирусов. Предпочтительно антиген является мишенью для нейтрализующих антител. Более предпочтительно, антиген является мишенью для нейтрализующих антител широкого спектра действия, то есть иммунный ответ на антиген обеспечивает иммунитет против множества штаммов инфекционного агента. В некоторых случаях гликаны, N-связанные или O-связанные с субъединичной вакциной, также могут быть важны для вакцинации, либо за счет их вклада в эпитоп антигена, либо благодаря тому, что они направляют иммунный ответ на определенные эпитопы антигена за счет стерических затруднений. Иммунный ответ, который возникает в ответ на вакцинацию, может представлять собой непосредственный ответ на сам белок, на гликан или одновременно на белок и связанные гликаны. Субъединичные вакцины обладают различными преимуществами, в том числе не содержат живых патогенов, что устраняет опасения по поводу инфицирования пациента вакциной; они могут быть разработаны с использованием стандартных методов генной инженерии; они более однородны, чем другие формы вакцины; и они могут производиться в стандартизированных системах продукции экспрессии рекомбинантных белков с использованием хорошо описанных систем экспрессии. В некоторых случаях антиген может быть сконструирован методами генной инженерии, чтобы способствовать образованию желаемых антител, таких как нейтрализующие антитела или нейтрализующие антитела широкого спектра действия. В частности, структурная информация об интересующем антигене, полученная с помощью рентгеновской кристаллографии, электронной микроскопии или экспериментов с ядерным магнитным резонансом, может использоваться для управления рациональным дизайном субъединичных вакцин.
[0006] Известным ограничением субъединичных вакцин является то, что вызываемый ими иммунный ответ иногда может быть слабее, чем иммунный ответ на другие типы вакцин, такие как цельные вирусные, живые или живые аттенуированные вакцины. Авторы настоящего изобретения обнаружили и в данном документе раскрывают, что вакцины на основе наноструктур могут обладать преимуществами субъединичных вакцин при одновременном повышении эффективности и широты иммунного ответа, индуцированного вакциной, посредством поливалентного экспонирования антигена в симметрично упорядоченных структурах. Вакцины на основе наноструктур - это одна из форм «вакцины на основе наночастиц». В настоящем описании вакцины на основе наноструктур отличаются от вакцин на основе наночастиц, поскольку термин вакцина на основе наночастиц использовался в данной области для обозначения вакцин на основе белков или гликопротеинов (см., Например, патент США № US 9441019), полимеризованных липосом (см., например, Патент США №7285289), мицелл поверхностно-активного вещества ( см., например, опубликованный Патент США № US 2004/0038406 A1) и синтетических биоразлагаемых частиц (см., например, Патент США № US 8323696). Вакцинация на основе наноструктур представляет собой парадигму вакцинации со значительными коммерческими последствиями и последствиями для общественного здравоохранения. Таким образом, существует потребность в вакцинах на основе наноструктур и способах их применения для того чтобы вызывать иммунные ответы на инфекционные агенты, такие как бактерии, вирусы и паразиты; и для предотвращения или уменьшения серьезности инфекции, вызванной инфекционным агентом, включая, например, и без ограничения, болезнь Лайма, коклюш, вирус герпеса, ортомиксовирус, парамиксовирус, пневмовирус, филовирус, флавивирус, реовирус, ретровирус, менингококк и малярию.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0007] В настоящем документе описаны наноструктуры, вакцины, способы их применения и способы получения указанных наноструктур.
[0008] В одном аспекте настоящего изобретения предложены наноструктуры, содержащие первое множество полипептидов, причем первое множество полипептидов расположено в соответствии с по меньшей мере одним оператором симметрии; наноструктура содержит первое множество антигенов; каждый из первого множества антигенов имеет проксимальный конец и дистальный конец; и каждый из проксимальных концов антигенов присоединен к элементу первого множества полипептидов.
[0009] В другом аспекте настоящего изобретения предложены вакцины, содержащие любую из наноструктур согласно настоящему изобретению, причем указанная вакцина способна вызывать нейтрализующий ответ антител на инфекционный агент. В одном из вариантов реализации вакцина представлена в виде фармацевтической композиции.
[0010] В другом аспекте настоящего изобретения предложены способы создания иммунитета к инфекционному агенту у субъекта, включающие введение любой из вакцин согласно настоящему изобретению.
[0011] В другом аспекте настоящего изобретения предложены способы получения любой из наноструктур согласно настоящему изобретению путем сборки in vitro компонента, очищенного (выделенного) из одной или нескольких рекомбинантных систем экспрессии. В другом аспекте настоящего изобретения предложены способы получения любой из наноструктур согласно настоящему изобретению путем совместной экспрессии всех компонентов в рекомбинантной системе экспрессии с получением наноструктуры, и очистку указанной наноструктуры.
[0012] В одном из вариантов реализации наноструктур согласно настоящему изобретению наноструктура дополнительно содержит второе множество полипептидов, причем второе множество полипептидов присоединено к первому множеству полипептидов. В одном из вариантов реализации наноструктура дополнительно содержит второе множество антигенов. В одном из вариантов реализации наноструктура дополнительно содержит второе множество антигенов, причем каждый из второго множества вторых антигенов имеет проксимальный конец и дистальный конец, и каждый проксимальный конец вторых антигенов присоединен к элементу второго множества полипептидов; и, необязательно, проксимальные концы антигенов представляют собой N-концы антигенов или C-концы антигенов.
[0013] В одном из вариантов реализации наноструктур согласно настоящему изобретению множество антигенов представляет собой множество антигенных белков или их антигенных фрагментов. В одном из вариантов реализации антигенный белок наноструктуры выбран из SEQ ID NO: 52-88 и 90-113 или их варианта; или антигенный белок по меньшей мере на 75, 80, 85, 90, 95 или 99% идентичен полипептиду, выбранному из SEQ ID NO: 52-88 и 90-97; или антигенный белок представляет собой любой из следующих: Env ВИЧ, РСВ F, грипп HA, gp350 ВЭБ, gB ЦМВ, UL128 ЦМВ, UL130 ЦМВ, UL131A ЦМВ, gH ЦМВ, gL ЦМВ, возбудитель болезни Лайма OspA, токсин коклюша, денге E, S вируса SARS , S вируса MERS, GP заирского эболавируса , GP Суданского эболавируса, Марбургский вирус GP, вирус Ханта Gn, вирус Ханта Gc, поверхностный антиген HepB, корь H, домен оболочки III вируса Зика, малярия CSP, малярия Pfs25, fHbp менингококка В, NadA менингококка В, NHBA менингококка В, вирус Нипах F, вирус Нипах G, ротавирус VP4, ротавирус VP8*, F МПВч, G МПВч, F вируса паротита или HN вируса паротита 8.
[0014] В одном из вариантов реализации наноструктура выполнена с возможностью экспонирования (дисплея) целевого эпитопа антигена; и, необязательно, целевой эпитоп доступен для антитела, как определено в настоящем документе ниже. В любом варианте реализации, в котором наноструктура содержит множество антигенных белков, наноструктуры, необязательно, выполнена с возможностью вызывать иммунный ответ на первое множество антигенных белков, причем иммунный ответ предпочтительно направлен на целевой эпитоп антигенного белка. В вариантах реализации настоящего изобретения целевой эпитоп является консервативным, представляет собой эпитоп для нейтрализующих антител, представляет собой эпитоп для перекрестно-реактивных антител или представляет собой эпитоп для нейтрализующего антитела широкого спектра действия.
[0015] В одном из вариантов реализации наноструктур согласно настоящему изобретению множество антигенов включает по меньшей мере одну мутацию, выбранную из группы, состоящей из мутации, стабилизирующей интерфейс (участок взаимодействия), комплементарных мутаций цистеина, которые дают возможность образования дисульфидной связи, делеции петли, добавления сайта N-связанного гликозилирования, удаления сайта N-связанного гликозилирования, мутации, разрушающей эпитоп, и мутации, создающей эпитоп. В одном из вариантов реализации множество антигенов включает антигенный олигосахарид.
[0016] В одном из вариантов реализации вакцин согласно настоящему изобретению ответ нейтрализующих антител защищает от инфекции инфекционным агентом. В одном из вариантов реализации ответ нейтрализующих антител представляет собой нейтрализующий ответ широкого спектра действия против различных штаммов инфекционного агента. В одном из вариантов реализации инфекционным агентом является любой из следующих: болезнь Лайма, коклюш, вирус герпеса, ортомиксовирус, парамиксовирус, пневмовирус, филовирус, флавивирус, реовирус, ретровирус, менингококк или малярия. В одном из вариантов реализации инфекционный агент представляет собой вирус, выбранный из следующих: ВИЧ, РСВ (RSV, респираторно-сцинциляционный вирус), грипп, ВЭБ, ЦМВ, денге, вирус тяжелого острого респираторного синдрома (SARS), вирус ближневосточного респираторного синдрома (MERS), вирус Эбола, вирус Марбург, вирус Ханта, гепатит В, ВПЧ, корь, вирус Нипах, ротавирус, метапневмовирус, вирус парагриппа и вирус Зика. В одном из вариантов реализации инфекционным агентом является болезнь Лайма или коклюш. В одном из вариантов реализации инфекционным агентом является малярия. В одном из вариантов реализации инфекционным агентом является менингококк.
[0017] В одном из вариантов реализации способов создания иммунитета согласно настоящему изобретению способ дополнительно включает введение адъюванта. В одном из вариантов реализации способ дополнительно включает повторное введение вакцины. В одном из вариантов реализации способ дополнительно включает введение второй вакцины, выбранной из следующих: вакцина на основе наночастиц, вакцина на основе белка, живая вакцина, живая аттенуированная вакцина, вакцина с цельным возбудителем, вакцина ДНК или вакцина РНК; и, возможно, первая вакцина является первичной, а вторая вакцина является бустерной, или, возможно, вторая вакцина является первичной, а первая вакцина является бустерной. В одном из вариантов реализации способ индуцирует направленное созревание аффинности. В одном из вариантов реализации способ приводит к нейтрализующему иммунному ответу широкого спектра действия.
[0018] В одном из вариантов реализации способов получения любой из наноструктур согласно настоящему изобретению способ обеспечивает сборку наноструктуры in vitro путем последовательной или непоследовательной экспрессии первого множества полипептидов в первой рекомбинантной системе экспрессии, экспрессии первого множества антигенов во второй рекомбинантной системе экспрессии, очистки первого множества полипептидов, очистки первого множества антигенов, при условии, что экспрессия каждого компонента предшествует очистке этого компонента; и затем смешивания первого множества полипептидов и первого множества антигенов; тем самым обеспечивают создание наноструктуры.
[0019] В одном из вариантов реализации способов получения наноструктуры способ реализует сборку наноструктуры in vitro путем последовательной или непоследовательной экспрессии первого множества полипептидов в первой рекомбинантной системе экспрессии, экспрессии первого множества антигенов во второй рекомбинантной экспрессии, экспрессии второго множества полипептидов в третьей рекомбинантной системе экспрессии, очистки первого множества полипептидов, очистки первого множества антигенов, очистки второго множества полипептидов, при условии, что экспрессия каждого компонента предшествует очистке этого компонента; и смешивания первого множества полипептидов, первого множества антигенов и второго множества полипептидов; благодаря чему обеспечивают создание наноструктуры. Необязательно, первая рекомбинантная система экспрессии и вторая рекомбинантная система экспрессии являются одинаковыми, и первое множество полипептидов и первое множество антигенов очищают вместе.
[0020] В одном из вариантов реализации способов получения наноструктуры способ включает экспрессию первого множества полипептидов и первого множества антигенов в одной рекомбинантной системе экспрессии с образованием наноструктуры, и очистку указанной наноструктуры. В одном из вариантов реализации способ включает экспрессию первого множества полипептидов, первого множества антигенов и второго множества полипептидов в единой рекомбинантной системе экспрессии с образованием наноструктуры, и очистку указанной наноструктуры. В одном из вариантов реализации, необязательно, первое множество полипептидов и первое множество антигенов кодируют одной открытой рамкой считывания; и необязательно, одна открытая рамка считывания кодирует слитый белок полипептида и антигена; и, необязательно, одна открытая рамка считывания кодирует саморасщепляющийся пептид.
[0021] Абзацы выше не предназначены для определения каждого аспекта изобретения, а дополнительные аспекты описаны в других разделах, таких как Подробное описание. Предполагается, что весь документ связан как единое раскрытие, и следует понимать, что предусмотрены все комбинации признаков согласно настоящему описанию, даже если комбинация функций не встречается вместе в одном предложении, или абзаце, или разделе настоящего документа. Изобретение включает в качестве дополнительного аспекта все варианты реализации, более узкие по объему в любом отношении, по сравнению с вариантами, определенными конкретными абзацами выше. Например, если определенные аспекты изобретения описаны как род, следует понимать, что каждый член рода является индивидуальным аспектом изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
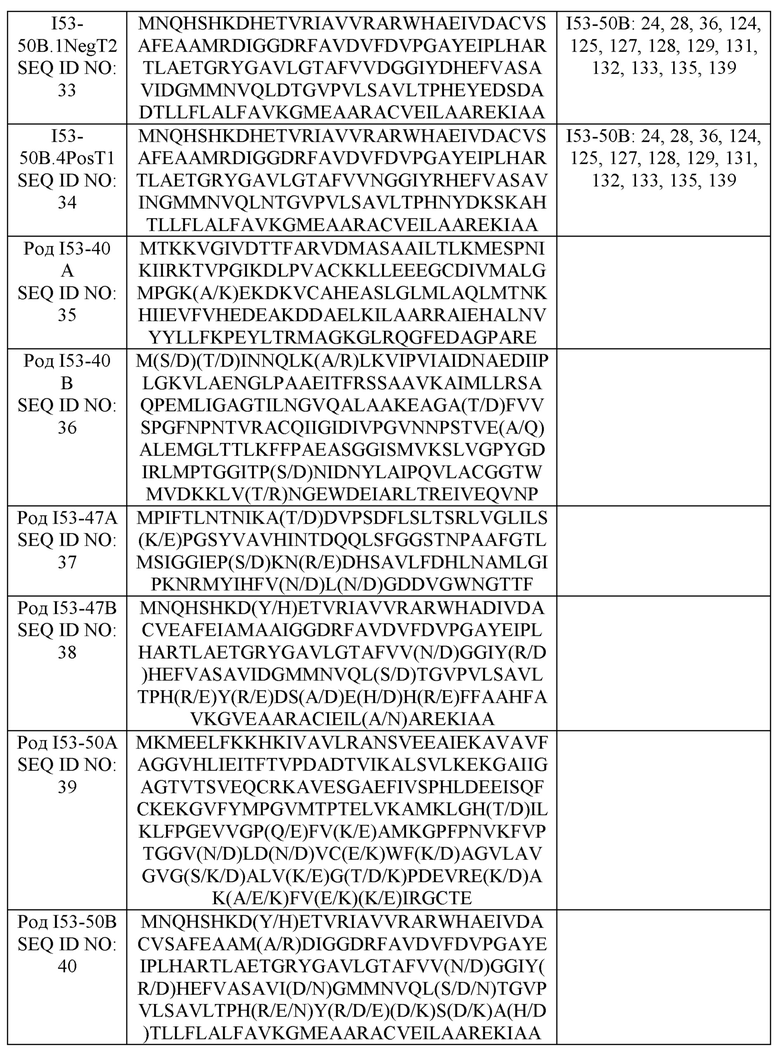
[0022] На Фиг. 1A показана схематическая диаграмма получения несущих антиген наноструктур путем сборки in vitro. Два компонента или строительных блока данной наноструктуры могут быть экспрессированы и очищены по отдельности, что позволяет начать сборку наноструктуры путем смешивания очищенных компонентов in vitro, такой способ называют сборкой in vitro. В некоторых вариантах реализации два компонента наноструктуры могут быть экспрессированы в разных хозяевах экспрессии (например, в клетках человека HEK293F или бактериальных клетках E. coli). На рисунке схематически изображена сборка 120-субъединичной наноструктуры, содержащей 20 тримерных антигенов (60 антигенных субъединиц), посредством сборки in vitro тримерного гибридного белка антиген-наноструктура, продуцируемого в клетках HEK293F, и пентамерного белка наноструктуры, продуцируемого в E. coli.
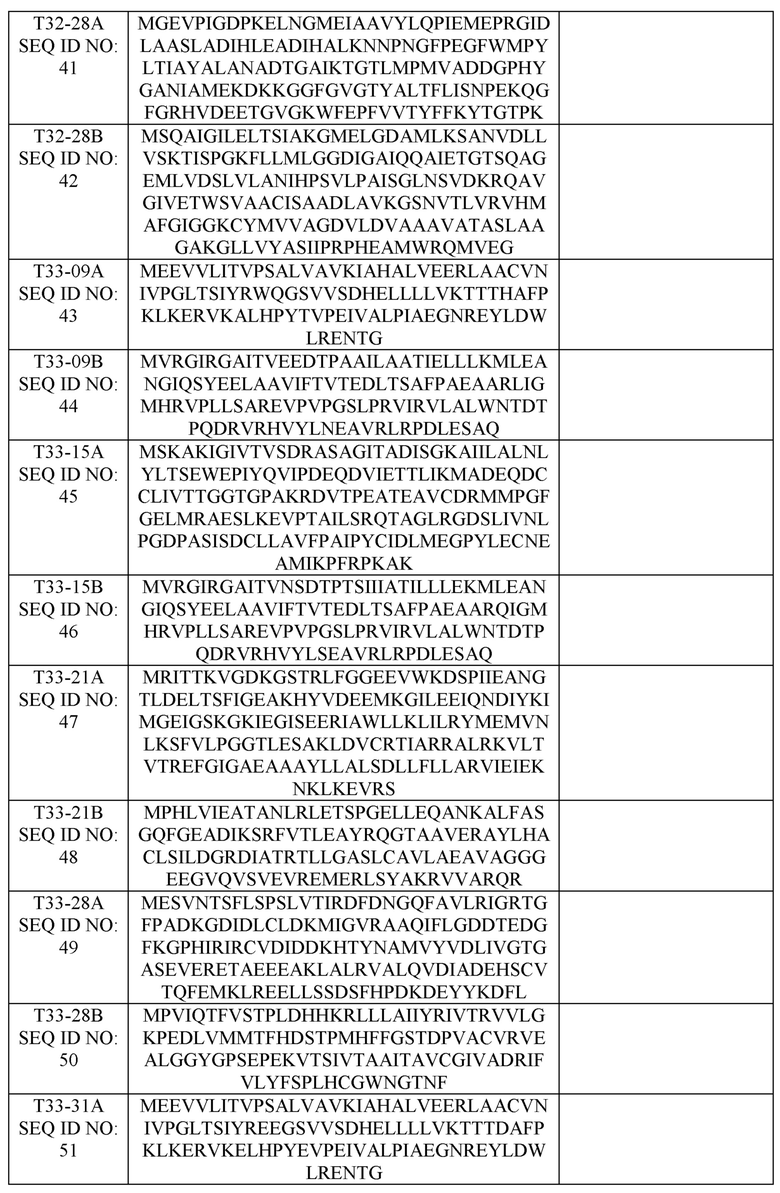
[0023] На Фиг. 1B показан пример архитектуры наноструктур.
[0024] На Фиг. 2A-2C показаны графики, иллюстрирующие обнаружение секретируемых гибридных белков DS-Cav1 (фиг. 2A), DS-Cav1-фолдон-T33-31A (Фиг. 2B) и DS-Cav1-T33-31A (Фиг. 2C) в супернатантах культур тканей. Анализы ELISA были выполнены на супернатантах культур тканей из клеток, экспрессирующих DS-Cav1 (вверху), DS-Cav-l-фолдон-T33-31A/T33-31B (внизу слева) и DS-Cav-1-T33-31A/T33-31B (внизу справа). Четыре различных моноклональных антитела, которые связывают РСВ F, использовали для оценки присутствия DS-Cav1 или гибридных белков DS-Cav1 в супернатантах. Результаты подтверждают секрецию белков, содержащих правильно свернутый антиген РСВ F.
[0025] На Фиг. 3 показана эксклюзионная хроматография DS-Cav1-I53-50A. Белок, очищенный из супернатантов тканевых культур с помощью аффинной хроматографии с иммобилизованным металлом, наносили на колонку для эксклюзионной хроматографии Superose 6 10/300 GL. Белок элюировался как один монодисперсный вид.
[0026] На Фиг. 4 показана эксклюзионная хроматография собранных in vitro наноструктур DS-Cav1-I53-50. Очищенные белки DS-Cav1-I53-50A и I53-50B.4PT1 смешивали в молярном соотношении приблизительно 1:1, инкубировали в течение ночи при 4°C, а затем наносили на колонку для эксклюзионной хроматографии Sephacryl S-500 16/60 HR. Собранная наноструктура элюировалась в виде единственного монодисперсного пика около 65 мл, в то время как избыток тримерного компонента DS-Cav1-I53-50A элюировался около 90 мл.
[0027] На Фиг. 5 показана электронная микрофотография с негативным окрашиванием и двумерные средние по классам наноструктур DS-Cav1-I53-50, собранных in vitro. Собранные in vitro наноструктуры DS-Cav1-I53-50, очищенные с помощью эксклюзионной хроматографии, были визуализированы с помощью электронной микроскопии с негативным окрашиванием (вверху). Усреднение многих наноструктур дало двумерные средние по классам (внизу), которые показывают, что часть I53-50 наноструктур высоко упорядочена и согласована, в то время как точное трехмерное положение экспонируемого антигена незначительно варьируется из-за гибкой природы линкера между доменами DS-Cav1 и I53-50A гибридного белка DS-Cav1-I53-50A.
[0028] На ФИГ. 6A-6C показан ряд графиков, отражающих антигенность наноструктур DS-Cav1-I53-50. Анализ очищенных наноструктур DS-Cav1-I53-50 с помощью ELISA (фиг. 6A) с использованием четырех моноклональных антител, специфичных к РСВ F, включая специфические к конформации до слияния антитела MPE8, D25 и RSD5, показал, что антиген DS-Cav1 свернут правильно и поддерживается в состоянии перед слиянием при поливалентном экспонировании на наноструктурах DS-Cav1-I53-50. Это открытие было подтверждено измерениями поверхностного плазмонного резонанса с использованием множества антител, специфичных к РСВ F, которые, по сравнению с тримерным DS-Cav1 (Фиг. 6C), также позволили предположить, что мультивалентное экспонирование DS-Cav1 (Фиг. 6B) приводит к эффекту авидности, который уменьшает скорость диссоциации антител.
[0029] Фиг. 7 представляет собой график, изображающий титры DS-Cav1-специфических сывороточных антител от мышей, иммунизированных наноструктурами DS-Cav1-I53-50. Группы мышей иммунизировали наноструктурами I53-50 без дополнительного антигена, тримерными наноструктурами DS-Cav1 или I53-50, несущими антиген DS-Cav1 с валентностью 33%, 66% или 100%. Титры сывороточных антител, специфичных к DS-Cav1, измеряли с помощью ELISA на планшетах, покрытых DS-Cav1. Титры сывороточных антител для каждой мыши нанесены на график в виде кружков, а среднее геометрическое значение в каждой группе показано горизонтальной линией и представлено численно внизу.
[0030] Фиг. 8 представляет собой график, изображающий нейтрализующую активность сыворотки, вызванную иммунизацией наноструктурами DS-Cav1-I53-50. Группы мышей иммунизировали наноструктурами I53-50 без дополнительного антигена, тримерными наноструктурами DS-Cav1 или I53-50, несущими антиген DS-Cav1 с валентностью 33%, 66% или 100%. Титры нейтрализации для каждой мыши нанесены на график в виде кружков, а среднее геометрическое значение в каждой группе показано в виде горизонтальной линии.
[0031] Фиг. 9A-9B представляют собой графики, изображающие иммуногенность в иммунной системе приматов, вызванную иммунизацией наноструктурами DS-Cav1-фолдон-I53-50. Макакам-резус вводили наноструктуры DS-Cav1-фолдон-I53-50 внутримышечно на 0 и 4 неделе либо со свободным тримером DS-Cav1, либо с наноструктурами DS-Cav1-фолдон-I53-50, демонстрирующими DS-Cav1 со 100% валентностью. В обоих случаях доза антигена DS-Cav1 составляла 50 мкг, а иммуногены были приготовлены с MF59-подобным адъювантом SWE на основе сквалена в эмульсии типа масло-в-воде. Сыворотки, полученные от животных на 6-й и 16-й неделях, оценивали на титры антител к DS-Cav1 (Фиг. 9A) и титры нейтрализующих РСВ антител (Фиг. 9A).
[0032] Фиг. 10 представляет собой график, изображающий физическую стабильность DS-Cav1 при слиянии с I53-50A и/или при дальнейшей сборке в икосаэдрическую наноструктуру. Образцы наноструктур тримерного DS-Cav1, тримерного DS-Cav1-фолдон-I53-50A и DS-Cav1-фолдон-I53-50, содержащих эквивалентные концентрации (50 нМ) DS-Cav1, были разделены на четыре аликвоты и инкубированы при 20, 50, 70 или 80°C в течение 1 часа. После охлаждения до комнатной температуры связывание D25 анализировали с помощью поверхностного плазмонного резонанса (ППР).
[0033] Фиг. 11A-11J представляют собой графики, отражающие физическую стабильность наноструктур. Химическая денатурация в гидрохлориде гуанидина (GdnHCl), отслеживаемая по собственной флуоресценции триптофана, была использована в качестве второго, независимого от антител метода оценки физической стабильности тримерного DS-Cav1 (Фиг. 1A и Фиг. 1B), DS-Cav1-фолдон-I53-50A (Фиг. 1C и Фиг. 1D), DS-Cav1-фолдон-I53-50 (Фиг. 1E и Фиг. 1F), I53-50 (Фиг. 1G и Фиг. 1H) и I53-50A (Фиг. 1I и Фиг. 11J). Эти данные указывают на превосходную физическую стабильность антигена DS-Cav1 при генетическом слиянии с компонентом наноструктуры I53-50A.
ПОДРОБНОЕ ОПИСАНИЕ
[0034] Настоящее изобретение относится к наноструктурам и вакцинам на основе наноструктур. Некоторые наноструктуры согласно настоящему изобретению содержат антигены, способные вызывать иммунные ответы на инфекционные агенты, такие как бактерии, вирусы и паразиты. Некоторые вакцины согласно настоящему изобретению полезны для предотвращения или уменьшения тяжести инфекции, вызванной инфекционным агентом, включая, например, без ограничения, болезнь Лайма, коклюш, вирус герпеса, ортомиксовирус, парамиксовирус, пневмовирус, филовирус, флавивирус, реовирус, ретровирус, менингококк и малярию. Антигены могут быть присоединены к сердцевине наноструктуры либо нековалентно, либо ковалентно, в том числе в виде слитого белка, или другими способами, описанными в настоящем документе. Мультимерные антигены, необязательно, могут экспонироваться вдоль оси симметрии наноструктуры. Также предложены белки и молекулы нуклеиновых кислот, кодирующие такие белки, составы и способы применения.
[0035] Перед дальнейшим описанием настоящего изобретения следует понимать, что это изобретение не ограничено конкретными описанными вариантами реализации, поскольку они, конечно, могут варьироваться. Также следует понимать, что используемая здесь терминология предназначена только для описания конкретных вариантов реализации и не предназначена для ограничения, поскольку объем настоящего изобретения будет ограничен только формулой изобретения.
1. Обзор наноструктур
[0036] Наноструктуры согласно настоящему изобретению могут содержать мультимерные белковые сборки, выполненные с возможностью экспонирования антигенов или антигенных фрагментов. Наноструктуры согласно настоящему изобретению содержат по меньшей мере первое множество полипептидов. Первое множество полипептидов может быть получено из встречающейся в природе белковой последовательности путем замены по меньшей мере одного аминокислотного остатка или путем добавления на N- или C-конце одного или нескольких остатков. В некоторых случаях первое множество полипептидов включает последовательность гена, определенную de novo вычислительными методами. Указанное первое множество полипептидов может образовывать всю наноструктуру; или наноструктура может содержать один или несколько дополнительных полипептидов, так что наноструктура включает два, три, четыре, пять, шесть, семь или более множеств полипептидов. В некоторых случаях первое множество будет образовывать тримеры, связанные вращательной симметрией 3 порядка, а второе множество будет образовывать пентамеры, связанные вращательной симметрией 5 порядка. Вместе указанные одно или несколько множеств полипептидов могут быть расположены так, что элементы каждого множества полипептидов связаны друг с другом операторами симметрии. Общий вычислительный способ конструирования самособирающихся белковых материалов, включающий симметричную стыковку (докинг) строительных блоков белка в целевой симметричной архитектуре, раскрыт в патентной публикации США № US 2015/0356240 A1.
[0037] «Ядро» наноструктуры используется здесь для описания центральной части наноструктуры, которая связывает вместе антигены или антигенные фрагменты, экспонируемые наноструктурой. В одном из вариантов реализации ядро и экспонируемые антигены представляют собой один и тот же полипептид, что означает, что сами антигены способны к самосборке в наноструктуру. Преимущество разработки антигенов, способных к самосборке, состоит в том, что вся наноструктура затем действует как антигенный компонент вакцины. Но в одном из вариантов реализации ядра наноструктур согласно настоящему изобретению представляют собой общие платформы, выполненные с возможностью экспонирования любого из различных антигенов, которые можно выбрать для включения в вакцину. Преимущество разработки ядра как общей платформы состоит в том, что одно или несколько множеств полипептидов, составляющих ядро, можно сконструировать и оптимизировать заранее, а затем применить к различным антигенам. Следует понимать, что в некоторых случаях один и тот же полипептид может образовывать часть «ядра», а затем выходить наружу либо как адаптер для присоединения антигена, либо как сам антиген (т.е. гибридный белок с антигеном). В вариантах реализации настоящего изобретения антиген представляет собой белок, гликопротеин или олигосахарид инфекционного агента.
[0038] В некоторых случаях самосборке может дополнительно стимулироваться мультимеризацией антигена, даже если ядро в отсутствие антигена может быть независимо способным к самосборке. Это может иметь место, например, когда гомотримерный антиген (такой как gp140 ВИЧ, HA гриппа или белок РСВ F) является антигеном или одним из нескольких антигенов, экспонируемых на частице. В некоторых случаях тримерный антиген, расположенный вдоль оси 3 порядка наноструктуры, способствует правильной укладке и стабильности конформации антигена и делает самосборку наноструктуры кооперативным процессом, в котором антиген должным образом тримеризируется частично из-за его экспонирования на оси 3 порядка ядра наноструктуры, и наноструктура стабилизируется в собранной форме, по крайней мере частично, за счет нековалентных или ковалентных взаимодействий между тримерными звеньями. В некоторых случаях введение мутаций в антиген или компоненты наноструктуры может, необязательно, дополнительно стабилизировать сборку, в частности, если остатки цистеина находятся в положении для создания внутримолекулярных дисульфидных связей. В некоторых примерах димерный, тримерный, тетрамерный, пентамерный или гексамерный антиген экспонируется на ядре, сконструированном так, чтобы иметь совпадающую оси симметрии 2 порядка, 3 порядка, 4 порядка, 5 порядка или 6 порядка, так что ядро способствует расположению мультимерного антигена с нативной симметрией антигена.
2. Различные неограничительные примеры наноструктур
[0039] Неограничительный пример варианта реализации показан на фиг. 1А, где изображен белок РСВ F, генетически слитый с компонентом (первым множеством полипептидов) наноструктуры, который рекомбинантно экспрессируется в клетках 293F; вместе со сборкой пентамерного белка (второе множество полипептидов), которое рекомбинантно экспрессируется в клетках E. coli, эти два множества полипептидов самособираются в наноструктуру («искусственную иммуногенную наночастицу»), демонстрирующую 20 тримеров F-белка вокруг икосаэдрического ядра. В этом варианте реализации ядро имеет общую конструкцию. Как поясняется ниже, в других вариантах реализации белок F РСВ заменен другим белком другого антигена, таким как тримерный гликопротеин другого вируса. В некоторых вариантах реализации наноструктура включает тримерные гликопротеины ВИЧ-1, ВИЧ-2, ВЭБ, ЦМВ, РСВ, гриппа, вируса Эбола, марбургского вируса, денге, SARS, MERS, вируса Ханта или вируса Зика. В некоторых вариантах реализации наноструктура содержит тримерные гликопротеины вирусов, которые эволюционно родственны или идентичны последовательности любых из этих типичных вирусов, включая, без ограничения, вирус герпеса, ортомиксовирус, парамиксовирус, пневмовирус, филовирус, флавивирус, реовирус или ретровирус. В одном из вариантов реализации наноструктура включает внеклеточный домен или домены трансмембранного белка или гликопротеина или их антигенный фрагмент. В некоторых вариантах реализации наноструктура содержит антигенные белки или фрагменты белка или антигенные олигосахариды бактериального патогена, включая, в числе прочего, Neisseria meningitides (также известный как «менингококк»), Haemophilus influenzae типа B, Streptococcus pneumonia и Listeria monocytogenes.
[0040] Тримерные антигены, которые можно использовать с этой или подобными наноструктурами, в некоторых случаях, без ограничения, представляют собой gp140 ВИЧ, HA гриппа, белок E денге или sGP вируса Эбола. Когда используются другие тримерные антигены, они, необязательно, могут быть размещены на оси симметрии 3 порядка наноструктуры. В некоторых случаях выбранный антиген является мономерным и, тем не менее, расположен на оси 3 порядка. Таким образом, наноструктура, изображенная на фиг. 1A способна экспонировать 20 тримерных антигенов или 60 мономерных антигенов. Дополнительно или в качестве альтернативы, пентамерные комплексы наноструктуры используют для экспонирования 12 пентамерных антигенов или 70 мономерных антигенов. В одном из вариантов реализации наноструктура содержит 20 копий тримерного антигена и 12 копий пентамерного антигена.
2.1 Ядра наноструктуры
[0041] Другие возможные расположения полипептидов согласно настоящему изобретению показаны на фиг. 1B. В некоторых вариантах реализации наноструктура выполнена с возможностью экспонирования до 8 тримеров; 8 тримеров и 12 димеров; 6 тетрамеров и 12 димеров; 6 тетрамеров и 8 тримеров; 20 тримеров и 30 димеров; 4 тримеров и 6 димеров; 4 первых тримеров и 4 вторых тримеров, или 8 тримеров; 12 пентамеров и 20 тримеров; или 12 пентамеров и 30 димеров; или 4 тримеров. В некоторых случаях одна из осей симметрии не используется для экспонирования антигена, таким образом, в некоторых вариантах осуществления наноструктура адаптирована для экспонирования до 8 тримеров; 12 димеров; 6 тетрамеров; 20 тримеров; 30 димеров; 4 тримеров; 6 димеров; 8 тримеров; или 12 пентамеров. В некоторых случаях экспонируются мономерные антигены, и, таким образом, наноструктура выполнена с возможностью экспонирования до 12, 24, 60 или 70 мономерных антигенов. В некоторых случаях наноструктура включает смешанное множество полипептидов, так что в остальном идентичные полипептиды ядра наноструктуры экпонируют разные антигены или не несут антигена. Таким образом, в зависимости от соотношения полипептидов, наноструктура в некоторых случаях выполнена с возможностью экспонирования от 1 до 130 антигенов (например, на частице I52), где каждый из экспонируемых антигенов может быть одинаковым или они могут быть разными элементами смешанной популяции. пропорционально любому выбранному соотношению. Антигены можно совместно экспрессировать в рекомбинантной системе экспрессии и они могут самоорганизовываться перед очисткой. Альтернативно, антигены можно экспрессировать отдельно, а затем смешивать вместе либо до, либо после очистки от экспрессирующего хозяина и связанных загрязнителей. В различных вариантах реализации экспонируют 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или более антигенов. Неограничительные иллюстративные наноструктуры представлены в Bale et al. Science 353: 389-94 (2016); Heinze et al. J. Phys. Chem B. 120: 5945-5952 (2016); King et al. Nature 510: 103-108 (2014); и King et al. Science 336: 1171-71 (2012).
2.2. Смешанные наноструктуры
[0042] В некоторых вариантах реализации наноструктура экспонирует два или более антигенов из одного и того же организма, например, без ограничения gp140 ВИЧ и gp41 ВИЧ; или GP1 и GP2 вируса Эбола; или белки кори H и F; или gB ЦМВ и UL128 ЦМВ, UL130, UL131A, gH (UL75) и gL (UL115), на одной наноструктуре. В некоторых случаях наноструктура экспонирует два антигенных белка или гликопротеина, которые образуются в результате посттранскрипционного расщепления, такого как расщепление белка F РСВили белка HA гриппа протеазами, эндогенными для рекомбинантной системы экспрессии, или протеазами, поставляемыми экзогенно.
[0043] В некоторых случаях наноструктура выполнена с возможностью экспонирования одного и того же антигена из двух или более различных штаммов патогенного организма. В неограничительных примерах одна и та же наноструктура экспонирует смешанные популяции гомотримерных белковых антигенов или смешанные гетеротримеры белковых антигенов из разных штаммов инфекционного агента. В одном варианте реализации наноструктура экспонирует белки HA гриппа A H1N1 и белки гриппа A H3N2. В одном варианте реализации наноструктура экспонирует белки HA вируса гриппа A и вируса гриппа B. В одном варианте реализации белки gp140 из различных штаммов ВИЧ экспонируются на одной наноструктуре. Два, три, четыре, пять или шесть штаммов ВИЧ могут экспонироваться одной и той же наноструктурой. Не ограничиваясь теорией, преимущество такой смешанной наноструктуры состоит в том, что она способствует возникновению перекрестно-реактивных иммунных ответов или нейтрализующих иммунных ответов широкого спектра действия. В некоторых случаях вакцина на основе наноструктур согласно настоящему изобретению является универсальной вакциной против гриппа. В некоторых случаях вакцина на основе наноструктур согласно настоящему изобретению представляет собой вакцину против ВИЧ. В некоторых случаях вакцина на основе наноструктур согласно настоящему изобретению обеспечивает длительную защиту от ВИЧ. В некоторых случаях вакцина на основе наноструктур согласно настоящему изобретению обеспечивает длительную защиту от гриппа. В одном варианте реализации наноструктура выполнена с возможностью экспонирования белков E вируса Денге типа 1, типа 2, типа 3 и типа 4. В одном из вариантов реализации вакцина на основе наноструктур содержит наноструктуры, которые индивидуально экспонируют белок E каждого из типов вируса Денге типа 1, типа 2, типа 3 и типа 4. В одном варианте реализации вакцина на основе наноструктур согласно настоящему изобретению обеспечивает иммунитет к вирусу Денге без повышенного риска геморрагической лихорадки Денге или шокового синдрома Денге.
[0044] При создании смешанных наноструктур может быть выгодно обеспечить гомомеризацию специфическим для штамма образом, а не допускать гетеродимеризацию, так что, например, все белки HA вируса гриппа A H1N1 экспонируются на одной оси 3 порядка частицы T33, тогда как все H3N2 Белки НА гриппа A экспонируются на другой оси 3 порядка частицы Т33. Это может быть достигнуто путем использования наноструктуры, содержащей два или более множества полипептидов, в качестве ядра наноструктуры, при этом каждое множество полипептидов присоединено к разному антигену. Альтернативно, наноструктура может быть сконструирована с использованием одной или нескольких мутаций, нарушающих симметрию, таких как мутации типа «выступ в лунку» или внутримолекулярные дисульфидные мутации, которые предотвращают образование тримеров между различными антигенами. В этом случае наноструктура экспонирует мультимерные антигены из разных штаммов в симметрично эквивалентных позициях на наноструктуре, но каждая позиция в наноструктуре занята гомомерами из одного и того же штамма, с лишь незначительной долей гетеромерных антигенов между штаммами. В некоторых случаях сам антиген может быть генетически модифицирован для предотвращения межштаммовой гетеродимеризации. В одном из вариантов реализации наноструктура выполнена с возможностью предотвращения гетеромизации двух антигенных белков с консервативной структурой, но с различной антигенностью, таких как, например, белок HA от гриппа H1N1 Калифорнии 2009 года и белок HA от гриппа H1N1 Новой Каледонии 1999 года. Кроме того, когда создают смешанные наноструктуры и антигены экспонируются как гибридные (слитые) белки, наноструктура будет включать три или более разных белка, так как гибридные белки будут иметь одинаковые (или эквивалентные) домены, используемые для формирования ядра наноструктуры с разными антигенными доменами, по одному для каждого антигена, экспонируемого на наноструктуре.
2.3. Условия присоединения
[0045] Наноструктуры согласно настоящему изобретению экспонируют антигены различными способами, в том числе в виде слияния генов или другими способами, описанными в настоящем документе. Используемый здесь термин «присоединенный к» означает любые известные в данной области техники средства, вызывающие ассоциацию двух полипептидов. Связь может быть прямой или опосредованной, обратимой или необратимой, слабой или сильной, ковалентной или нековалентной, а также селективной или неселективной.
[0046] В некоторых вариантах реализации присоединение обеспечивают с помощью генной инженерии для создания слияния N- или C-конца антигена с одним из множества полипептидов, составляющих наноструктуру. Таким образом, наноструктура может состоять или состоять по существу из одного, двух, трех, четырех, пяти, шести, семи, восьми, девяти или десяти множеств полипептидов, экспонирующих один, два, три, четыре, пять, шесть, семь, восемь, девять или десять множеств антигенов, причем по меньшей мере один из множества антигенов генетически слит по меньшей мере с одним из множества полипептидов. В некоторых случаях наноструктура состоит по существу из одного множества полипептидов, способных к самосборке и содержащих множество генетически слитых с указанными полипептидами антигенов. В некоторых случаях наноструктура состоит, по существу, из первого множества полипептидов, содержащих множество антигенов, генетически слитых с указанными полипептидами; и второго множества полипептидов, способных к совместной сборке в двухкомпонентную наноструктуру, причем одно множество полипептидов связывает антиген с наноструктурой, а другое множество полипептидов способствует самосборке наноструктуры.
[0047] В некоторых вариантах реализации присоединение обеспечивают при помощи посттрансляционного ковалентного присоединения между одним или более множеством полипептидов и одним или более множеством антигенов. В некоторых случаях химическое сшивание используют для неспецифического присоединения антигена к полипептиду наноструктуры. В некоторых случаях химическое сшивание используют для специфического присоединения антигена к полипептиду наноструктуры. В данной области техники известны различные специфические и неспецифические химические методы сшивания, такие как клик-химия и другие методы. В общем, любая химия сшивания, используемая для связывания двух белков, может быть адаптирована для использования в наноструктурах согласно настоящему изобретению. В частности, могут быть использованы химические методы, используемые для создания иммуноконъюгатов или конъюгатов антитело-лекарственное средство. В некоторых случаях конъюгат антиген-наноструктура (ANC) создают с использованием расщепляемого или нерасщепляемого линкера. Процессы и способы конъюгации антигенов с носителями представлены, например, в патентной публикации США. № US 2008/0145373 A1. В одном из вариантов реализации антиген представляет собой полисахарид. В некоторых случаях антиген представляет собой полисахарид, а наноструктура действует как гаптен. В одном из вариантов реализации антиген-мишень представляет собой белок, и конъюгацию антигена-мишени с полисахаридом используют для усиления иммунного ответа. Способы получения конъюгатов белок-полисахарид представлены, например, в патенте США №6248334. Конъюгация белков с полисахаридами в некоторых случаях превращает полисахарид из слабо иммуногенного Т-клеточно-независимого антигена в Т-клеточно-зависимый антиген, который привлекает помощь Т-клеток и, таким образом, стимулирует усиленные иммунные ответы. См. J.M. Cruse, et al. (Редакторы), Conjugate Vaccines (Конъюгированные вакцины), Karger, Basel (1989); и R.W. Ellis, et al. (Редакторы), Development and Clinical Uses of Haemophilus B Conjugate Vaccines (Разработка и клиническое использование конъюгированных вакцин против гемофильной инфекции B), Marcel Dekker, New York (1994).
[0048] В одном варианте реализации присоединение обеспечивают посредством нековалентного присоединения между одним или несколькими множествами полипептидов и одним или несколькими множествами антигена. В некоторых случаях конструируют антиген так, чтобы он был заряжен отрицательно, по крайней мере, на одной поверхности, а полипептид конструируют так, чтобы он был заряжен положительно, по крайней мере, на одной поверхности, или положительно и отрицательно заряжены, соответственно. Это способствует межмолекулярной ассоциации между антигеном и полипептидами наноструктуры за счет электростатической силы. В некоторых случаях комплементарность формы используют, чтобы вызвать связывание антигена с наноструктурой. Взаимодополняемость форм может существовать заранее или являться рационально разработанной. В некоторых случаях для достижения присоединения используют компьютерный дизайн интерфейсов белок-белок. В одном из вариантов реализации антиген помечен биотином, а полипептид содержит стрептавидин, или наоборот. В одном из вариантов реализации стрептавидин экспонируют путем слияния генов или иным образом в виде тетрамера на оси 4 порядка наноструктуры, а меченный биотином антиген является мономерным, димерным или тетрамерным, что позволяет обеспечить связывание с наноструктурой в конфигурации, подходящей для нативной мультимеризации антигена. В некоторых случаях для захвата антигена используется адаптер на основе белка. В некоторых случаях полипептид слит с белком, способным связывать комплементарный белок, который слит с антигеном. В одном из вариантов реализации полипептид слит с белком ротавируса VP6, который образует тример, а антиген слит на N-конце с N-концевым пептидом VP7 ротавируса, что позволяет связывать тример антигена с наноструктурой. См. Chen et al. Molecular interactions in rotavirus assembly and uncoating seen by high-resolution cryo-EM (Молекулярные взаимодействия в сборке ротавируса и снятии оболочки, наблюдаемые с помощью крио-ЭМ высокого разрешения), PNAS 2009 Июнь, 106 (26) 10644-10648.
[0049] В одном из вариантов реализации каждый из первого множества антигенных белков имеет проксимальный конец и дистальный конец, и каждый из проксимальных концов антигенных белков присоединен к элементу первого множества полипептидов. Таким образом, дистальный конец антигенного белка определяют как часть антигена, наиболее удаленную от центра наноструктуры. В одном из вариантов реализации антигенный белок содержит целевой эпитоп, и наноструктура выполнена с возможностью экспонирования целевого эпитопа. В некоторых случаях антигенный белок может содержать более одного целевого эпитопа, и наноструктура выполнена с возможностью экспонирования каждого из целевых эпитопов. Эпитопы, постепенно приближающиеся к дистальному концу, в некоторых случаях (не ограничиваясь теорией) преимущественно доступны для иммунной системы. Дистальный конец антигенного белка может быть его N-концом, его C-концом или ни одним из концов. Таким образом, в зависимости от того, как антигенный белок присоединен к наноструктуре, антигенный белок может экспонироваться в любой ориентации. В некоторых случаях антигенный белок экспонируется таким образом, что один или несколько известных эпитопов ориентированы в направлении к дистальному концу антигенного белка, так что эти эпитопы предпочтительно доступны для иммунной системы. В некоторых случаях ориентация повторяет ориентацию вирусного белка по отношению к вирусу. Таким образом, в случае HA гриппа антигенный белок HA может быть ориентирован так, что сайт связывания рецептора находится на дистальном конце белка, аналогично ориентации HA в цельном вирусе; или, альтернативно, белок НА гриппа может быть ориентирован таким образом, что стволовой эпитоп предпочтительно доступен для иммунной системы. Выбор ориентации может направить иммунную систему на тот или иной эпитоп. В этом примере иммунный ответ на грипп может быть направлен на сайт связывания рецептора или на ствол путем выбора ориентации. Точно так же ориентация других антигенов может влиять на иммунный ответ. В некоторых вариантах реализации ориентация антигена приводит к иммунному ответу, нацеленному на предпочтительный эпитоп. В случае ВИЧ антигенный белок в некоторых вариантах реализации представляет собой белок Env ВИЧ-1 или ВИЧ-2 или их антигенный фрагмент. Ориентация Env или его фрагмента в некоторых случаях повторяет ориентацию белка Env относительно вируса ВИЧ, так что проксимальный конец является проксимальным к мембране концом белка Env или его фрагмента. В некоторых случаях предпочтительный эпитоп выбран из группы, состоящей из сайта связывания CD4 (CD4bs); протеогликанового фрагмента V2 на вершине тримера Env; протеогликанового фрагмента V3 на высокоманнозном участке Env; проксимально-внешней области мембраны (MPER) трансмембранного домена Env; и интерфейса gp120-gp41 со слитым пептидом или без него. В некоторых случаях предпочтение эпитопа контролируют другими способами, такими как размещение гликанов на наноструктуре путем добавления или вычитания N-связанного мотива последовательности гликана NX- [T/S] в заранее определенных положениях в аминокислотной последовательности любого из полипептидов наноструктуры, входящих в аминокислотную последовательность антигена. В некоторых случаях эпитопы, обнаруженные на промежуточных расстояниях от проксимального до дистального конца, будут предпочтительнее эпитопов, расположенных более дистально, в зависимости от различных соображений, включая, без ограничения, общую геометрию наноструктуры, гидрофобность поверхности, поверхностный заряд и конкурентное связывание белков, эндогенно присутствующих у субъекта, или белков, экзогенно предоставленных в вакцинной композиции. Настоящее раскрытие охватывает все известные способы рационального конструирования белковой структуры, и вышеизложенное не предназначено для ограничения.
2.4. Последовательности наноструктурных полипептидов
[0050] Одно или несколько множеств полипептидов согласно настоящему изобретению могут иметь любую из различных аминокислотных последовательностей. В патентной публикации США № US 2015/0356240 A1 описаны различные методы конструирования наноструктур. Как раскрыто в патентной публикации США № US 2016/0122392 A1 и в международной патентной публикации № WO 2014/124301 A1, изолированные полипептиды SEQ ID NO: 1-51 были разработаны с учетом их способности к самосборке в пары с образованием наноструктур, таких как икосаэдрические наноструктуры. Дизайн включал в себя разработку подходящих интерфейсных остатков для каждого члена полипептидной пары, которые могут быть собраны для формирования наноструктуры. Образованные таким образом наноструктуры включают симметрично повторяющиеся, неприродные, нековалентные границы раздела полипептид-полипептид, которые ориентируют первую сборку и вторую сборку в наноструктуру, например, с икосаэдрической симметрией. Таким образом, в одном варианте реализации первый и второй полипептиды выбраны из группы, состоящей из SEQ ID NO: 1-51. В каждом случае N-концевой остаток метионина является необязательным.
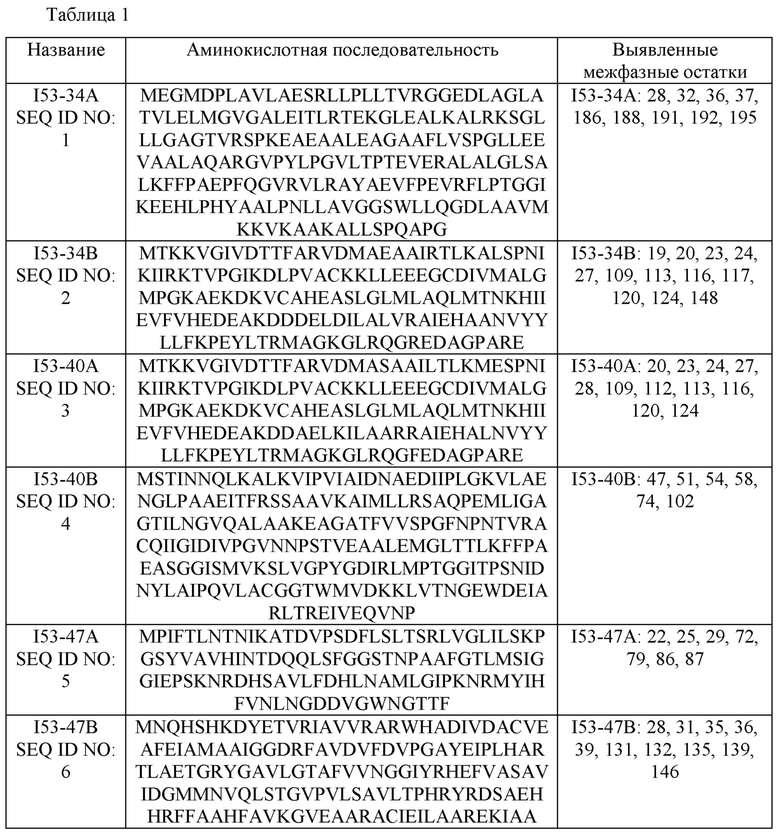
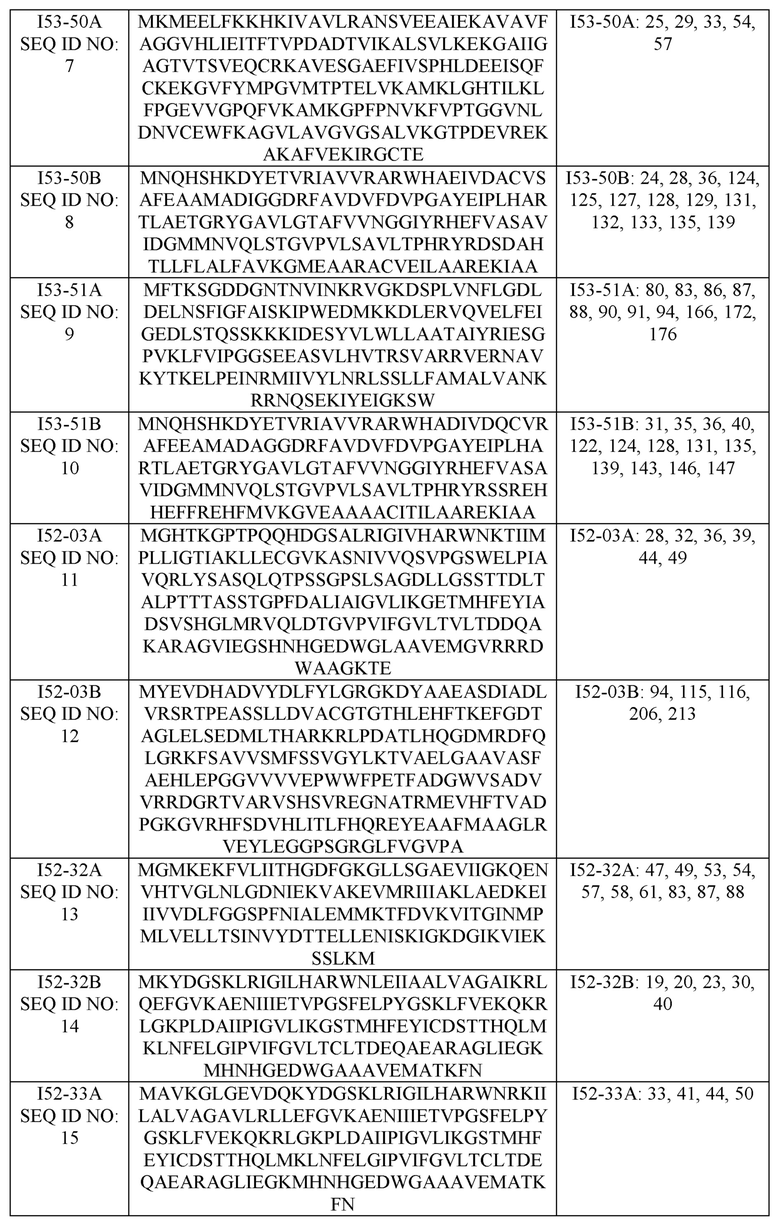
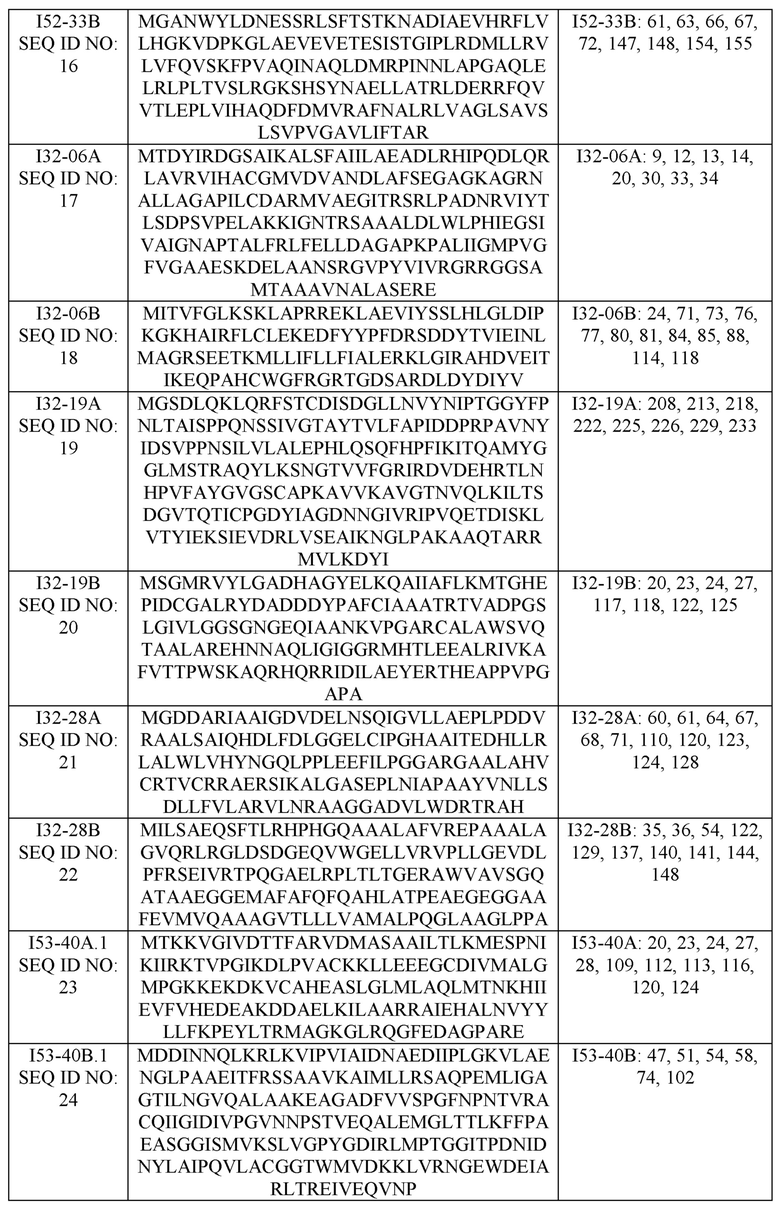
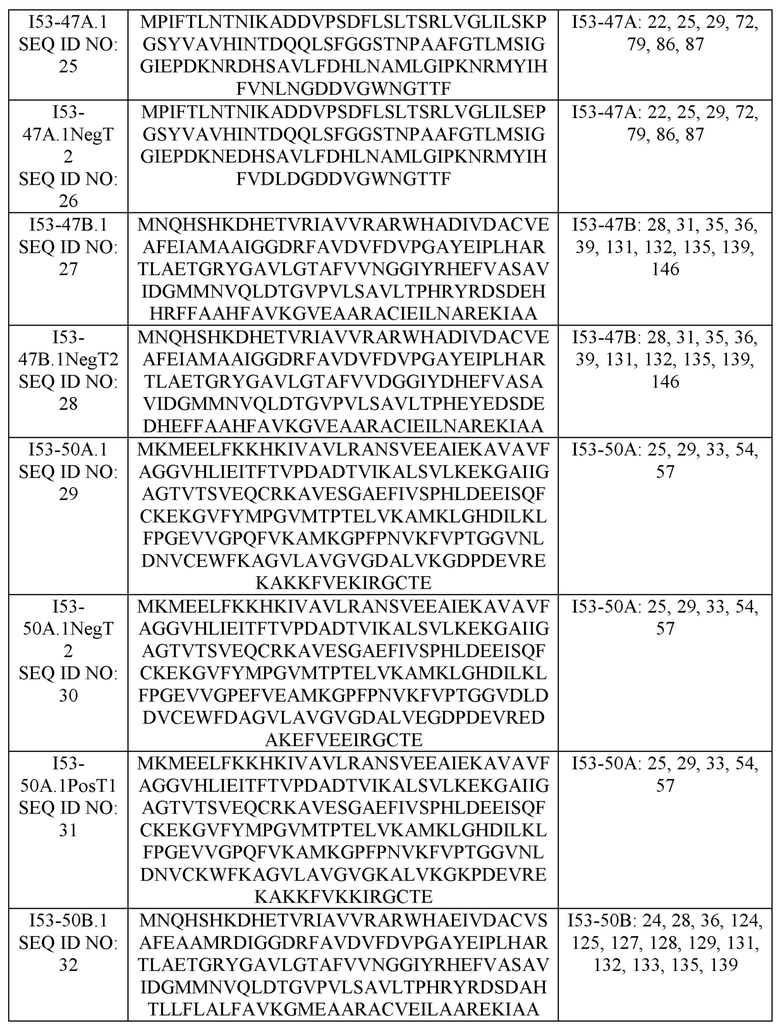
[0051] В таблице 1 представлена аминокислотная последовательность первого и второго полипептидов из вариантов реализации настоящего изобретения. В каждом случае пары последовательностей образуют икосаэдр I53. В правом столбце Таблицы 1 указаны номера остатков в каждом примерном полипептиде, который был идентифицирован как присутствующий на границе раздела полученных собранных наноструктур (то есть: «идентифицированные остатки границы раздела»). Как можно видеть, количество интерфейсных остатков для типичных полипептидов SEQ ID NO: 1-34 находится в диапазоне 4-13. В различных вариантах реализации первый и второй полипептиды содержат аминокислотную последовательность, которая по меньшей мере на 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична по длине и идентична по крайней мере в 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12 или 13 позициях интерфейса (в зависимости от числа интерфейсных остатков для данного полипептида) аминокислотной последовательности полипептида, выбранного из группы, состоящей из SEQ ID NO: 1-34. SEQ ID NO: 35-51 представляют собой другие аминокислотные последовательности первого и второго полипептидов из вариантов реализации настоящего изобретения. В других вариантах реализации первый и второй полипептиды содержат аминокислотную последовательность, которая по меньшей мере на 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична по длине и идентична по крайней мере на 20%, 25%, 33%, 40%, 50%, 60%, 70%, 75%, 80%, 90% или 100% идентифицированных положений области взаимодействия аминокислотной последовательности полипептида, выбранного из группы, состоящей из SEQ ID NO: 1-51.
[0052] Как и в случае с белками в целом, ожидается, что полипептиды будут допускать некоторые вариации в разработанной последовательности без нарушения последующей сборки в наноструктуры: особенно, когда такое изменение включает консервативные аминокислотные замены. Используемый здесь термин «консервативная аминокислотная замена» означает, что: гидрофобные аминокислоты (Ala, Cys, Gly, Pro, Met, Val, Ile, Leu) могут быть заменены только другими гидрофобными аминокислотами; гидрофобные аминокислоты с объемными боковыми цепями (Phe, Tyr, Trp) могут быть заменены только другими гидрофобными аминокислотами с объемными боковыми цепями; аминокислоты с положительно заряженными боковыми цепями (Arg, His, Lys) могут быть заменены только другими аминокислотами с положительно заряженными боковыми цепями; аминокислоты с отрицательно заряженными боковыми цепями (Asp, Glu) могут быть заменены только другими аминокислотами с отрицательно заряженными боковыми цепями; и аминокислоты с полярными незаряженными боковыми цепями (Ser, Thr, Asn, Gln) могут быть заменены только другими аминокислотами с полярными незаряженными боковыми цепями.
[0053] В различных вариантах реализации наноструктуры согласно настоящему изобретению первые полипептиды и вторые полипептиды содержат полипептиды с аминокислотной последовательностью, выбранной из следующих пар, или их модифицированных версий (то есть: допустимые модификации, раскрытые для полипептидов согласно настоящему изобретению: изолированные полипептиды, содержащие аминокислотную последовательность, которая по меньшей мере на 75% идентична по своей длине и/или идентична по меньшей мере в одном идентифицированном положении области взаимодействия аминокислотной последовательности, указанной при помощи номера последовательности SEQ ID NO.):
SEQ ID NO: 1 и SEQ ID NO: 2 (I53-34A и I53-34B);
SEQ ID NO: 3 и SEQ ID NO: 4 (I53-40A и I53-40B);
SEQ ID NO: 3 и SEQ ID NO: 24 (I53-40A и I53-40B.1);
SEQ ID NO: 23 и SEQ ID NO: 4 (I53-40A.1 и I53-40B);
SEQ ID NO: 35 и SEQ ID NO: 36 (род I53-40A и род I53-40B);
SEQ ID NO: 5 и SEQ ID NO: 6 (I53-47A и I53-47B);
SEQ ID NO: 5 и SEQ ID NO: 27 (I53-47A и I53-47B.1);
SEQ ID NO: 5 и SEQ ID NO: 28 (I53-47A и I53-47B.1NegT2);
SEQ ID NO: 25 и SEQ ID NO: 6 (I53-47A.1 и I53-47B);
SEQ ID NO: 25 и SEQ ID NO: 27 (I53-47A.1 и I53-47B.1);
SEQ ID NO: 25 и SEQ ID NO: 28 (I53-47A.1 и I53-47B.1NegT2);
SEQ ID NO: 26 и SEQ ID NO: 6 (I53-47A.1NegT2 и I53-47B);
SEQ ID NO: 26 и SEQ ID NO: 27 (I53-47A.1NegT2 и I53-47B.1);
SEQ ID NO: 26 и SEQ ID NO: 28 (I53-47A.1NegT2 и I53-47B.1NegT2);
SEQ ID NO: 37 и SEQ ID NO: 38 (род I53-47A и род I53-47B);
SEQ ID NO: 7 и SEQ ID NO: 8 (I53-50A и I53-50B);
SEQ ID NO: 7 и SEQ ID NO: 32 (I53-50A и I53-50B.1);
SEQ ID NO: 7 и SEQ ID NO: 33 (I53-50A и I53-50B.1NegT2);
SEQ ID NO: 7 и SEQ ID NO: 34 (I53-50A и I53-50B.4PosT1);
SEQ ID NO: 29 и SEQ ID NO: 8 (I53-50A.1 и I53-50B);
SEQ ID NO: 29 и SEQ ID NO: 32 (I53-50A.1 и I53-50B.1);
SEQ ID NO: 29 и SEQ ID NO: 33 (I53-50A.1 и I53-50B.1NegT2);
SEQ ID NO: 29 и SEQ ID NO: 34 (I53-50A.1 и I53-50B.4PosT1);
SEQ ID NO: 30 и SEQ ID NO: 8 (I53-50A.1NegT2 и I53-50B);
SEQ ID NO: 30 и SEQ ID NO: 32 (I53-50A.1NegT2 и I53-50B.1);
SEQ ID NO: 30 и SEQ ID NO: 33 (I53-50A.1NegT2 и I53-50B.1NegT2);
SEQ ID NO: 30 и SEQ ID NO: 34 (I53-50A.1NegT2 и I53-50B.4PosT1);
SEQ ID NO: 31 и SEQ ID NO: 8 (I53-50A.1PosT1 и I53-50B);
SEQ ID NO: 31 и SEQ ID NO: 32 (I53-50A.1PosT1 и I53-50B.1);
SEQ ID NO: 31 и SEQ ID NO: 33 (I53-50A.1PosT1 и I53-50B.1NegT2);
SEQ ID NO: 31 и SEQ ID NO: 34 (I53-50A.1PosT1 и I53-50B.4PosT1);
SEQ ID NO: 39 и SEQ ID NO: 40 (род I53-50A и род I53-50B);
SEQ ID NO: 9 и SEQ ID NO: 10 (I53-51A и I53-51B);
SEQ ID NO: 11 и SEQ ID NO: 12 (I52-03A и I52-03B);
SEQ ID NO: 13 и SEQ ID NO: 14 (I52-32A и I52-32B);
SEQ ID NO: 15 и SEQ ID NO: 16 (I52-33A и I52-33B)
SEQ ID NO: 17 и SEQ ID NO: 18 (I32-06A и I32-06B);
SEQ ID NO: 19 и SEQ ID NO: 20 (I32-19A и I32-19B);
SEQ ID NO: 21 и SEQ ID NO: 22 (I32-28A и I32-28B);
SEQ ID NO: 23 и SEQ ID NO: 24 (I53-40A.1 и I53-40B.1);
SEQ ID NO: 41 и SEQ ID NO: 42 (T32-28A и T32-28B);
SEQ ID NO: 43 и SEQ ID NO: 44 (T33-09A и T33-09B);
SEQ ID NO: 45 и SEQ ID NO: 46 (T33-15A и T33-15B);
SEQ ID NO: 47 и SEQ ID NO: 48 (T33-21A и T33-21B);
SEQ ID NO: 49 и SEQ ID NO: 50 (T33-28A и T32-28B); и
SEQ ID NO: 51 и SEQ ID NO: 44 (T33-31A и T33-09B (также известная как T33-31B))
[0054] В одном варианте реализации один или несколько белков или их антигенных фрагментов экспрессируются как гибридный белок с первым и/или вторым полипептидом. В указанных вариантах реализации один или несколько белков или их антигенных фрагментов присутствуют на N-конце гибридного белка, тогда указанная конфигурация может способствовать презентации одного или нескольких белков или их антигенных фрагментов на внешней стороне наноструктуры. Предпочтение присутствию белка на N-конце гибридного белка происходит всякий раз, когда местоположение С-конца белков находится на проксимальном конце белка. В указанных вариантах реализации один или несколько белков или их антигенных фрагментов присутствуют на С-конце гибридного белка, тогда указанная конфигурация может способствовать представлению одного или нескольких белков или их антигенных фрагментов на внешней стороне наноструктуры. Предпочтение присутствию белка на С-конце гибридного белка происходит всякий раз, когда N-конец белков находится на проксимальном конце белка.
[0055] Неограничительные примеры наноструктур, применимых в вакцинах согласно настоящему изобретению, включают примеры, раскрытые в патенте США №9630994 и предварительной заявке на патент США №62/481331, которые полностью включены в настоящий документ посредством ссылок.
3. Антигены
[0056] Согласно настоящему изобретению предложены вакцины на основе наноструктур против любых из различных известных бактерий, вирусов или паразитов, имеющих отношение к болезням человека или животных. В частности, настоящее изобретение относится к вакцинам против болезни Лайма, коклюша, вируса герпеса, ортомиксовируса, парамиксовируса, пневмовируса, филовируса, флавивируса, реовируса, ретровируса, малярии, вирусного менингита, грибкового менингита и бактериального менингита, включая Neisseria meningitides (также известный как «менингококк»), Haemophilus influenzae типа B, Streptococcus pneumonia и Listeria monocytogenes. Для каждого из этих организмов известны антигены (белки или полисахариды), способные вызывать защитные иммунные ответы. Настоящее изобретение относится к включению любого из указанных антигенов, особенно антигенных белков, в вакцины на основе наноструктур. Рекомендации, в частности, доступны на основании исследований иммунного ответа на инфекцию или вакцинацию, таких как выделение связывающих или нейтрализующих антител, генетический анализ последовательности антигена, структурные исследования антигенных белков и антител и, в частности, клинический и ветеринарный опыт с субъединичными вакцинами. С небольшими ограничениями любая известная субъединичная вакцина может быть адаптирована для использования с наноструктурами согласно настоящему изобретению путем использования представленных выше модальностей экспонированиия. В некоторых вариантах реализации вакцины на основе наноструктур согласно настоящему изобретению содержат олигосахарид (например, менингококковый олигосахарид), конъюгированный непосредственно или через промежуточный белок (например, дифтерийный анатоксин, столбнячный анатоксин или CRM197) с наноструктурой. В некоторых вариантах реализации вакцины на основе наноструктур согласно настоящему изобретению содержат антигены или антигенные фрагменты из списка, приведенного в таблице 2.
ТАБЛИЦА 2
Неограничительный список антигенов
[0057] В некоторых вариантах реализации антиген представляет собой антигенный белок, выбранный из полипептида SEQ ID NO: 52-88 и 90-113 или его варианта, как представлено в таблице 3.
ТАБЛИЦА 3
Неограничительный список антигенных последовательностей
gp160
MRVKGIKKNYQHWWRGGIMLLGMLMICSSAEKLWVTVYYGVPVWKEATTTLFCASDAKAQNPEMHNIWATHACVPTDPNPQEVILKNLTEEFNMWKNNMVEQMHEDIISLWDQSLKPCVKLTPLCVTLNCTNAESLNCTATNGTNNCSASTKPMEEMKNCSFNITTSVQDKKQQEYALFYKLDIIPIDNNENDLNNTNYTSYRLISCNTSVITQACPKITFEPIPIHYCAPAGFAILKCKDKRFNGTGPCKNVSTVQCTHGIRPVVSTQLLLNGSLAEEGVVLRSENFTDNAKNIIVQLKDPVNITCTRPNNNTRKSITIGPGRAFYATGQVIGDIRKAHCDLNGTEWDNALKQIVEELRKQYGNNITIFNSSSGGDPEIVMHSFNCGGEFFYCNTAQLFNSTWLFNSTWNSTERLGNDTERTNDTITLPCKIKQVINMWQTVGKAMYAPPIRGLIRCSSNITGLILTRDGSGNTTGNETFRPGGGNMKDNWRSELYKYKVVKIEPLGVAPTRAKRRVVQREKRAAGLGALFLGFLGMAGSTMGAASLTLTVQARQLLSGIVQQQNNLLRAIEAQQHLLQLTVWGIKQLQARVLAVERYLRDQQLLGIWGCSGKLICTTTVPWNASWSNKSLDNIWENMTWMQWEKEIDNYTDVIYKLLEESQNQQEKNEQELLELDKWASLWNWFDITRWLWYIKIFIMIVGGLVGLRIVFAVLSIVNRVRQGYSPLSFQTLFPAPRGPDRPEGTEEGGGERGRDSSDRSAHGFLALIWGDLWSLCLFSYRRLRDLLLIAARIVELLGRRGWEVLKYWWSLLQYWSQELKKSAVSLLNATAIAVAEGTDRIIEIVQRAGRAIIHIPRRIRQGAERALL
gp120
LWVTVYYGVPVWKEATTTLFCASDAKAQNPEMHNIWATHACVPTDPNPQEVILKNLTEEFNMWKNNMVEQMHEDIISLWDQSLKPCVKLTPLCVTLNCTNAESLNCTATNGTNNCSASTKPMEEMKNCSFNITTSVQDKKQQEYALFYKLDIIPIDNNENDLNNTNYTSYRLISCNTSVITQACPKITFEPIPIHYCAPAGFAILKCKDKRFNGTGPCKNVSTVQCTHGIRPVVSTQLLLNGSLAEEGVVLRSENFTDNAKNIIVQLKDPVNITCTRPNNNTRKSITIGPGRAFYATGQVIGDIRKAHCDLNGTEWDNALKQIVEELRKQYGNNITIFNSSSGGDPEIVMHSFNCGGEFFYCNTAQLFNSTWLFNSTWNSTERLGNDTERTNDTITLPCKIKQVINMWQTVGKAMYAPPIRGLIRCSSNITGLILTRDGSGNTTGNETFRPGGGNMKDNWRSELYKYKVVKIEPLGVAPTRAKRRVVQREKR
gp41
MGAASLTLTVQARQLLSGIVQQQNNLLRAIEAQQHLLQLTVWGIKQLQARVLAVERYLRDQQLLGIWGCSGKLICTTTVPWNASWSNKSLDNIWENMTWMQWEKEIDNYTDVIYKLLEESQNQQEKNEQELLELDKWASLWNWFDITRWLWYIKIFIMIVGGLVGLRIVFAVLSIVNRVRQGYSPLSFQTL
MPER
ELDKWASLWNWFDITRWLWYIK
Белок F
MELPILKTNAITTILAAVTLCFASSQNITEEFYQSTCSAVSKGYLSALRTGWYTSVITIELSNIKENKCNGTDAKVKLIKQELDKYKNAVTELQLLMQSTPAANNRARRELPRFMNYTLNNTKNNNVTLSKKRKRRFLGFLLGVGSAIASGIAVSKVLHLEGEVNKIKNALLSTNKAVVSLSNGVSVLTSKVLDLKNYIDKQLLPIVNKQSCSISNIETVIEFQQKNNRLLEITREFSVNAGVTTPVSTYMLTNSELLSLINDMPITNDQKKLMSNNVQIVRQQSYSIMSIIKEEVLAYVVQLPLYGVIDTPCWKLHTSPLCTTNTKEGSNICLTRTDRGWYCDNAGSVSFFPQAETCKVQSNRVFCDTMNSLTLPSEVNLCNIDIFNPKYDCKIMTSKTDVSSSVITSLGAIVSCYGKTKCTASNKNRGIIKTFSNGCDYVSNKGVDTVSVGNTLYYVNKQEGKSLYVKGEPIINFYDPLVFPSDEFDASISQVNEKINQSLAFIRKSDELLHNVNVGKSTTNIMITTIIIVIIVILLLLIAVGLFLYCKARSTPVTLSKDQLSGINNIAFSN
HA
MKAILVVLLYTFATANADTLCIGYHANNSTDTVDTVLEKNVTVTHSVNLLEDKHNGKLCKLRGVAPLHLGKCNIAGWILGNPECESLSTASSWSYIVETPSSDNGTCYPGDFIDYEELREQLSSVSSFERFEIFPKTSSWPNHDSNKGVTAACPHAGAKSFYKNLIWLVKKGNSYPKLSKSYINDKGKEVLVLWGIHHPSTSADQQSLYQNADAYVFVGSSRYSKKFKPEIAIRPKVRDQEGRMNYYWTLVEPGDKITFEATGNLVVPRYAFAMERNAGSGIIISDTPVHDCNTTCQTPKGAINTSLPFQNIHPITIGKCPKYVKSTKLRLATGLRNIPSIQSRGLFGAIAGFIEGGWTGMVDGWYGYHHQNEQGSGYAADLKSTQNAIDEITNKVNSVIEKMNTQFTAVGKEFNHLEKRIENLNKKVDDGFLDIWTYNAELLVLLENERTLDYHDSNVKNLYEKVRSQLKNNAKEIGNGCFEFYHKCDNTCMESVKNGTYDYPKYSEEAKLNREEIDGVKLESTRIYQILAIYSTVASSLVLVVSLGAISFWMCSNGSLQCRICI
HA
MKAIIVLLMVVTSNADRICTGITSSNSPHVVKTATQGEVNVTGVIPLTTTPTKSYFANLKGTKTRGKLCPDCLNCTDLDVALGRPMCVGTTPSAKASILHEVRPVTSGCFPIMHDRTKIRQLANLLRGYENIRLSTQNVIDAEKAPGGPYRLGTSGSCPNATSKSGFFATMAWAVPKDNNKNATNPLTVEVPYICAEGEDQITVWGFHSDNKTQMKNLYGDSNPQKFTSSANGVTTHYVSQIGGFPDQTEDGGLPQSGRIVVDYMMQKPGKTGTIVYQRGVLLPQKVWCASGRSKVIKGSLPLIGEADCLHEKYGGLNKSKPYYTGEHAKAIGNCPIWVKTPLKLANGTKYRPPAKLLKERGFFGAIAGFLEGGWEGMIAGWHGYTSHGAHGVAVAADLKSTQEAINKITKNLNSLSELEVKNLQRLSGAMDELHNEILELDEKVDDLRADTISSQIELAVLLSNEGIINSEDEHLLALERKLKKMLGPSAVDIGNGCFETKHKCNQTCLDRIAAGTFNAGEFSLPTFDSLNITAASLNDDGLDNHTILLYYSTAASSLAVTLMLAIFIVYMVSRDNVSCSICL
гликопротеин 350/220 (gp350)
MEAALLVCQYTIQSLIHLTGEDPGFFNVEIPEFPFYPTCNVCTADVNVTINFDVGGKKHQLDLDFGQLTPHTKAVYQPRGAFGGSENATNLFLLELLGAGELALTMRSKKLPINVTTGEEQQVSLESVDVYFQDVFGTMWCHHAEMQNPVYLIPETVPYIKWDNCNSTNITAVVRAQGLDVTLPLSLPTSAQDSNFSVKTEMLGNEIDIECIMEDGEISQVLPGDNKFNITCSGYESHVPSGGILTSTSPVATPIPGTGYAYSLRLTPRPVSRFLGNNSILYVFYSGNGPKASGGDYCIQSNIVFSDEIPASQDMPTNTTDITYVGDNATYSVPMVTSEDANSPNVTVTAFWAWPNNTETDFKCKWTLTSGTPSGCENISGAFASNRTFDITVSGLGTAPKTLIITRTATNATTTTHKVIFSKAPESTTTSPTLNTTGFADPNTTTGLPSSTHVPTNLTAPASTGPTVSTADVTSPTPAGTTSGASPVTPSPSPWDNGTESKAPDMTSSTSPVTTPTPNATSPTPAVTTPTPNATSPTPAVTTPTPNATSPTLGKTSPTSAVTTPTPNATSPTLGKTSPTSAVTTPTPNATSPTLGKTSPTSAVTTPTPNATGPTVGETSPQANATNHTLGGTSPTPVVTSQPKNATSAVTTGQHNITSSSTSSMSLRPSSNPETLSPSTSDNSTSHMPLLTSAHPTGGENITQVTPASISTHHVSTSSPAPRPGTTSQASGPGNSSTSTKPGEVNVTKGTPPQNATSPQAPSGQKTAVPTVTSTGGKANSTTGGKHTTGHGARTSTEPTTDYGGDSTTPRPRYNATTYLPPSTSSKLRPRWTFTSPPVTTAQATVPVPPTSQPRFSNLSMLVLQWASLAVLTLLLLLVMADCAFRRNLSTSHTYTTPPYDDAETYV
gB
MESRIWCLVVCVNLCIVCLGAAVSSSSTSHATSSTHNGSHTSRTTSAQTRSVYSQHVTSSEAVSHRANETIYNTTLKYGDVVGVNTTKYPYRVCSMAQGTDLIRFERNIICTSMKPINEDLDEGIMVVYKRNIVAHTFKVRVYQKVLTFRRSYAYIYTTYLLGSNTEYVAPPMWEIHHINKFAQCYSSYSRVIGGTVFVAYHRDSYENKTMQLIPDDYSNTHSTRYVTVKDQWHSRGSTWLYRETCNLNCMLTITTARSKYPYHFFATSTGDVVYISPFYNGTNRNASYFGENADKFFIFPNYTIVSDFGRPNAAPETHRLVAFLERADSVISWDIQDEKNVTCQLTFWEASERTIRSEAEDSYHFSSAKMTATFLSKKQEVNMSDSALDCVRDEAINKLQQIFNTSYNQTYEKYGNVSVFETSGGLVVFWQGIKQKSLVELERLANRSSLNITHRTRRSTSDNNTTHLSSMESVHNLVYAQLQFTYDTLRGYINRALAQIAEAWCVDQRRTLEVFKELSKINPSAILSAIYNKPIAARFMGDVLGLASCVTINQTSVKVLRDMNVKESPGRCYSRPVVIFNFANSSYVQYGQLGEDNEILLGNHRTEECQLPSLKIFIAGNSAYEYVDYLFKRMIDLSSISTVDSMIALDIDPLENTDFRVLELYSQKELRSSNVFDLEEIMREFNSYKQRVKYVEDKVVDPLPPYLKGLDDLMSGLGAAGKAVGVAIGAVGGAVASVVEGVATFLKNPFGAFTIILVAIAVVIITYLIYTRQRRLCTQPLQNLFPYLVSADGTTVTSGSTKDTSLQAPPSYEESVYNSGRKGPGPPSSDASTAAPPYTNEQAYQMLLALARLDAEQRAQQNGTDSLDGQTGTQDKGQKPNLLDRLRHRKNGYRHLKDSDEEENV
UL128
MSPKDLTPFLTTLWLLLGHSRVPRVRAEECCEFINVNHPPERCYDFKMCNRFTVALRCPDGEVCYSPEKTAEIRGIVTTMTHSLTRQVVHNKLTSCNYNPLYLEADGRIRCGKVNDKAQYLLGAAGSVPYRWINLEYDKITRIVGLDQYLESVKKHKRLDVCRAKMGYMLQ
UL130
MLRLLLRHHFHCLLLCAVWATPCLASPWSTLTANQNPSPPWSKLTYSKPHDAATFYCPFLYPSPPRSPLQFSGFQRVSTGPECRNETLYLLYNREGQTLVERSSTWVKKVIWYLSGRNQTILQRMPRTASKPSDGNVQISVEDAKIFGAHMVPKQTKLLRFVVNDGTRYQMCVMKLESWAHVFRDYSVSFQVRLTFTEANNQTYTFCTHPNLIV
UL131A
MRLCRVWLSVCLCAVVLGQCQRETAEKNDYYRVPHYWDACSRALPDQTRYKYVEQLVDLTLNYHYDASHGLDNFDVLKRINVTEVSLLISDFRRQNRRGGTNKRTTFNAAGSLAPHARSLEFSVRLFAN
gH (UL75)
MRPGLPPYLTVFTVYLLSHLPSQRYGADAASEALDPHAFHLLLNTYGRPIRFLRENTTQCTYNSSLRNSTVVRENAISFNFFQSYNQYYVFHMPRCLFAGPLAEQFLNQVDLTETLERYQQRLNTYALVSKDLASYRSFSQQLKAQDSLGQQPTTVPPPIDLSIPHVWMPPQTTPHDWKGSHTTSGLHRPHFNQTCILFDGHDLLFSTVTPCLHQGFYLMDELRYVKITLTEDFFVVTVSIDDDTPMLLIFGHLPRVLFKAPYQRDNFILRQTEKHELLVLVKKAQLNRHSYLKDSDFLDAALDFNYLDLSALLRNSFHRYAVDVLKSGRCQMLDRRTVEMAFAYALALFAAARQEEAGTEISIPRALDRQAALLQIQEFMITCLSQTPPRTTLLLYPTAVDLAKRALWTPDQITDITSLVRLVYILSKQNQQHLIPQWALRQIADFALQLHKTHLASFLSAFARQELYLMGSLVHSMLVHTTERREIFIVETGLCSLAELSHFTQLLAHPHHEYLSDLYTPCSSSGRRDHSLERLTRLFPDATVPATVPAALSILSTMQPSTLETFPDLFCLPLGESFSALTVSEHVSYVVTNQYLIKGISYPVSTTVVGQSLIITQTDSQTKCELTRNMHTTHSITAALNISLENCAFCQSALLEYDDTQGVINIMYMHDSDDVLFALDPYNEVVVSSPRTHYLMLLKNGTVLEVTDVVVDATDSRLLMMSVYALSAIIGIYLLYRMLKTC
gL (UL115)
MCRRPDCGFSFSPGPVVLLWCCLLLPIVSSVAVSVAPTAAEKVPAECPELTRRCLLGEVFQGDKYESWLRPLVNVTRRDGPLSQLIRYRPVTPEAANSVLLDDAFLDTLALLYNNPDQLRALLTLLSSDTAPRWMTVMRGYSECGDGSPAVYTCVDDLCRGYDLTRLSYGRSIFTEHVLGFELVPPSLFNVVVAIRNEATRTNRAVRLPVSTAAAPEGITLFYGLYNAVKEFCLRHQLDPPLLRHLDKYYAGLPPELKQTRVNLPAHSRYGPQAVDAR
Белок А внешней поверхности (OspA)
MKKYLLGIGLILALIACKQNVSSLDEKNSVSVDVPGGMKVLVSKEKNKDGKYDLMATVDNVDLKGTSDKNNGSGILEGVKADKSKVKLTVADDLSKTTLEVLKEDGTVVSRKVTSKDKSTTEAKFNEKGELSEKTMTRANGTTLEYSQMTNEDNAAKAVETLKNGIKFEGNLASGKTAVEIKEGTVTLKREIDKNGKVTVSLNDTASGSKKTASWQESTSTLTISANSKKTKDLVFLTNGTITVQNYDSAGTKLEGSAAEIKKLDELKNALR
Субъединицы 1-5 коклюшного токсина (КТ)
MRCTRAIRQTARTGWLTWLAILAVTAPVTSPAWADDPPATVYRYDSRPPEDVFQNGFTAWGNNDNVLDHLTGRSCQVGSSNSAFVSTSSSRRYTEVYLEHRMQEAVEAERAGRGTGHFIGYIYEVRADNNFYGAASSYFEYVDTYGDNAGRILAGALATYQSEYLAHRRIPPENIRRVTRVYHNGITGETTTTEYSNARYVSQQTRANPNPYTSRRSVASIVGTLVRMAPVIGACMARQAESSEAMAAWSERAGEAMVLVYYESIAYSF
Белок оболочки E
MRCVGIGNRDFVEGLSGATWVDVVLEHGSCVTTMAKDKPTLDIELLKTEVTNPAVLRKLCIEAKISNTTTDSRCPTQGEATLVEEQDTNFVCRRTFVDRGWGNGCGLFGKGSLITCAKFKCVTKLEGKIVQYENLKYSVIVTVHTGDQHQVGNETTEHGTTATITPQAPTSEIQLTDYGALTLDCSPRTGLDFNEMVLLTMEKKSWLVHKQWFLDLPLPWTSGASTSQETWNRQDLLVTFKTAHAKKQEVVVLGSQEGAMHTALTGATEIQTSGTTTIFAGHLKCRLKMDKLTLKGMSYVMCTGSFKLEKEVAETQHGTVLVQVKYEGTDAPCKIPFSSQDEKGVTQNGRLITANPIVTDKEKPVNIEAEPPFGESYIVVGAGEKALKLSWFKKGSSIGKMFEATARGARRMAILGDTAWDFGSIGGVFTSVGKLIHQIFGTAYGVLFSGVSWTMKIGIGILLTWLGLNSRSTSLSMTCIAVGMVTLYLGVMVQA
Гликопротеин шиповидных отростков (S)
MFIFLLFLTLTSGSDLDRCTTFDDVQAPNYTQHTSSMRGVYYPDEIFRSDTLYLTQDLFLPFYSNVTGFHTINHTFGNPVIPFKDGIYFAATEKSNVVRGWVFGSTMNNKSQSVIIINNSTNVVIRACNFELCDNPFFAVSKPMGTQTHTMIFDNAFNCTFEYISDAFSLDVSEKSGNFKHLREFVFKNKDGFLYVYKGYQPIDVVRDLPSGFNTLKPIFKLPLGINITNFRAILTAFSPAQDIWGTSAAAYFVGYLKPTTFMLKYDENGTITDAVDCSQNPLAELKCSVKSFEIDKGIYQTSNFRVVPSGDVVRFPNITNLCPFGEVFNATKFPSVYAWERKKISNCVADYSVLYNSTFFSTFKCYGVSATKLNDLCFSNVYADSFVVKGDDVRQIAPGQTGVIADYNYKLPDDFMGCVLAWNTRNIDATSTGNYNYKYRYLRHGKLRPFERDISNVPFSPDGKPCTPPALNCYWPLNDYGFYTTTGIGYQPYRVVVLSFELLNAPATVCGPKLSTDLIKNQCVNFNFNGLTGTGVLTPSSKRFQPFQQFGRDVSDFTDSVRDPKTSEILDISPCSFGGVSVITPGTNASSEVAVLYQDVNCTDVSTAIHADQLTPAWRIYSTGNNVFQTQAGCLIGAEHVDTSYECDIPIGAGICASYHTVSLLRSTSQKSIVAYTMSLGADSSIAYSNNTIAIPTNFSISITTEVMPVSMAKTSVDCNMYICGDSTECANLLLQYGSFCTQLNRALSGIAAEQDRNTREVFAQVKQMYKTPTLKYFGGFNFSQILPDPLKPTKRSFIEDLLFNKVTLADAGFMKQYGECLGDINARDLICAQKFNGLTVLPPLLTDDMIAAYTAALVSGTATAGWTFGAGAALQIPFAMQMAYRFNGIGVTQNVLYENQKQIANQFNKAISQIQESLTTTSTALGKLQDVVNQNAQALNTLVKQLSSNFGAISSVLNDILSRLDKVEAEVQIDRLITGRLQSLQTYVTQQLIRAAEIRASANLAATKMSECVLGQSKRVDFCGKGYHLMSFPQAAPHGVVFLHVTYVPSQERNFTTAPAICHEGKAYFPREGVFVFNGTSWFITQRNFFSPQIITTDNTFVSGNCDVVIGIINNTVYDPLQPELDSFKEELDKYFKNHTSPDVDLGDISGINASVVNIQKEIDRLNEVAKNLNESLIDLQELGKYEQYIKWPWYVWLGFIAGLIAIVMVTILLCCMTSCCSCLKGACSCGSCCKFDEDDSEPVLKGVKLHYT
Гликопротеин шиповидных отростков (S)
MIHSVFLLMFLLTPTESYVDVGPDSIKSACIEVDIQQTFFDKTWPRPIDVSKADGIIYPQGRTYSNITITYQGLFPYQGDHGDMYVYSAGHATGTTPQKLFVANYSQDVKQFANGFVVRIGAAANSTGTVIISPSTSATIRKIYPAFMLGSSVGNFSDGKMGRFFNHTLVLLPDGCGTLLRAFYCILEPRSGNHCPAGNSYTSFATYHTPATDCSDGNYNRNASLNSFKEYFNLRNCTFMYTYNITEDEILEWFGITQTAQGVHLFSSRYVDLYGGNMFQFATLPVYDTIKYYSIIPHSIRSIQSDRKAWAAFYVYKLQPLTFLLDFSVDGYIRRAIDCGFNDLSQLHCSYESFDVESGVYSVSSFEAKPSGSVVEQAEGVECDFSPLLSGTPPQVYNFKRLVFTNCNYNLTKLLSLFSVNDFTCSQISPAAIASNCYSSLILDYFSYPLSMKSDLSVSSAGPISQFNYKQSFSNPTCLILATVPHNLTTITKPLKYSYINKCSRLLSDDRTEVPQLVNANQYSPCVSIVPSTVWEDGDYYRKQLSPLEGGGWLVASGSTVAMTEQLQMGFGITVQYGTDTNSVCPKLEFANDTKIASQLGNCVEYSLYGVSGRGVFQNCTAVGVRQQRFVYDAYQNLVGYYSDDGNYYCLRACVSVPVSVIYDKETKTHATLFGSVACEHISSTMSQYSRSTRSMLKRRDSTYGPLQTPVGCVLGLVNSSLFVEDCKLPLGQSLCALPDTPSTLTPRSVRSVPGEMRLASIAFNHPIQVDQLNSSYFKLSIPTNFSFGVTQEYIQTTIQKVTVDCKQYVCNGFQKCEQLLREYGQFCSKINQALHGANLRQDDSVRNLFASVKSSQSSPIIPGFGGDFNLTLLEPVSISTGSRSARSAIEDLLFDKVTIADPGYMQGYDDCMQQGPASARDLICAQYVAGYKVLPPLMDVNMEAAYTSSLLGSIAGVGWTAGLSSFAAIPFAQSIFYRLNGVGITQQVLSENQKLIANKFNQALGAMQTGFTTTNEAFHKVQDAVNNNAQALSKLASELSNTFGAISASIGDIIQRLDVLEQDAQIDRLINGRLTTLNAFVAQQLVRSESAALSAQLAKDKVNECVKAQSKRSGFCGQGTHIVSFVVNAPNGLYFMHVGYYPSNHIEVVSAYGLCDAANPTNCIAPVNGYFIKTNNTRIVDEWSYTGSSFYAPEPITSLNTKYVAPQVTYQNISTNLPPPLLGNSTGIDFQDELDEFFKNVSTSIPNFGSLTQINTTLLDLTYEMLSLQQVVKALNESYIDLKELGNYTYYNKWPWYIWLGFIAGLVALALCVFFILCCTGCGTNCMGKLKCNRCCDRYEEYDLEPHKVHVH
GP
MGVTGILQLPRDRFKRTSFFLWVIILFQRTFSIPLGVIHNSTLQVSDVDKLVCRDKLSSTNQLRSVGLNLEGNGVATDVPSATKRWGFRSGVPPKVVNYEAGEWAENCYNLEIKKPDGSECLPAAPDGIRGFPRCRYVHKVSGTGPCAGDFAFHKEGAFFLYDRLASTVIYRGTTFAEGVVAFLILPQAKKDFFSSHPLREPVNATEDPSSGYYSTTIRYQATGFGTNETEYLFEVDNLTYVQLESRFTPQFLLQLNETIYTSGKRSNTTGKLIWKVNPEIDTTIGEWAFWETKKNLTRKIRSEELSFTVVSNGAKNISGQSPARTSSDPGTNTTTEDHKIMASENSSAMVQVHSQGREAAVSHLTTLATISTSPQSLTTKPGPDNSTHNTPVYKLDISEATQVEQHHRRTDNDSTASDTPSATTAAGPPKAENTNTSKSTDFLDPATTTSPQNHSETAGNNNTHHQDTGEESASSGKLGLITNTIAGVAGLITGGRRTRREAIVNAQPKCNPNLHYWTTQDEGAAIGLAWIPYFGPAAEGIYIEGLMHNQDGLICGLRQLANETTQALQLFLRATTELRTFSILNRKAIDFLLQRWGGTCHILGPDCCIEPHDWTKNITDKIDQIIHDFVDKTLPDQGDNDNWWTGWRQWIPAGIGVTGVIIAVIALFCICKFVF
GP
MKTTCFLISLILIQGTKNLPILEIASNNQPQNVDSVCSGTLQKTEDVHLMGFTLSGQKVADSPLEASKRWAFRTGVPPKNVEYTEGEEAKTCYNISVTDPSGKSLLLDPPTNIRDYPKCKTIHHIQGQNPHAQGIALHLWGAFFLYDRIASTTMYRGKVFTEGNIAAMIVNKTVHKMIFSRQGQGYRHMNLTSTNKYWTSSNGTQTNDTGCFGALQEYNSTKNQTCAPSKIPPPLPTARPEIKLTSTPTDATKLNTTDPSSDDEDLATSGSGSGEREPHTTSDAVTKQGLSSTMPPTPSPQPSTPQQGGNNTNHSQDAVTELDKNNTTAQPSMPPHNTTTISTNNTSKHNFSTLSAPLQNTTNDNTQSTITENEQTSAPSITTLPPTGNPTTAKSTSSKKGPATTAPNTTNEHFTSPPPTPSSTAQHLVYFRRKRSILWREGDMFPFLDGLINAPIDFDPVPNTKTIFDESSSSGASAEEDQHASPNISLTLSYFPNINENTAYSGENENDCDAELRIWSVQEDDLAAGLSWIPFFGPGIEGLYTAVLIKNQNNLVCRLRRLANQTAKSLELLLRVTTEERTFSLINRHAIDFLLTRWGGTCKVLGPDCCIGIEDLSKNISEQIDQIKKDEQKEGTGWGLGGKWWTSDWGVLTNLGILLLLSIAVLIALSCICRIFTKYIG
Гликопротеин оболочки Gn
LRNVYDMKIECPHTVSFGENSVIGYVELPPVPLADTAQMVPESSCNMDNHQSLNTITKYTQVSWRGKADQSQSSQNSFETVSTEVDLKGTCVLKHKMVEESYRSRKSVTCYDLSCNSTYCKPTLYMIVPIHACNMMKSCLIALGPYRVQVVYERSYCMTGVLIEGKCFVPDQSVVSIIKHGIFDIASVHIVCFFVAVKGNTYKIFEQVKKSFESTCNDTENKVQGYYICIVGGNSAPIYVPTLDDFRSMEAFTGIFRSPHGEDHDLAGEEIASYSIVGPANAKVPHSASSDTLSLIAYSGIPSYSSLSILTSSTEAKHVFSPGLFPKLNHTNCDKSAIPLIWTGMIDLPGYYEAVHPCTVFCVLSGPGASCEAFSEGGIFNITSPMCLVSKQNRFRLTEQQVNFVCQRVDMDIVVYCNGQRKVILTKTLVIGQCIYTITSLFSLLPGVAHSIAVELCVPGFHGWATAALLVTFCFGWVLIPAITFIILTVLKFIANIFHTSNQENRLKSVLRKIKEEFEKTKGSMVCDVCKYECETYKELKAHGVSCPQSQCPYCFTHCEPTEAAFQAHYKVCQVTHRFRDDLKKTVTPQNFTPGCYRTLNLFRYKSRCYIFTMWIFLLVLESILWAASA
Гликопротеин оболочки Gc
SETPLTPVWNDNAHGVGSVPMHTDLELDFSLTSSSKYTYRRKLTNPLEEAQSIDLHIEIEEQTIGVDVHALGHWFDGRLNLKTSFHCYGACTKYEYPWHTAKCHYERDYQYETSWGCNPSDCPGVGTGCTACGLYLDQLKPVGSAYKIITIRYSRRVCVQFGEENLCKIIDMNDCFVSRHVKVCIIGTVSKFSQGDTLLFFGPLEGGGLIFKHWCTSTCQFGDPGDIMSPRDKGFLCPEFPGSFRKKCNFATTPICEYDGNMVSGYKKVMATIDSFQSFNTSTMHFTDERIEWKDPDGMLRDHINILVTKDIDFDNLGENPCKIGLQTSSIEGAWGSGVGFTLTCLVSLTECPTFLTSIKACDKAICYGAESVTLTRGQNTVKVSGKGGHSGSTFRCCHGEDCSQIGLHAAAPHLDKVNGISEIENSKVYDDGAPQCGIKCWFVKSGEWISGIFSGNWIVLIVLCVFLLFSLVLLSILCPVRKHKKS
Поверхностный антиген HepB (HBs)
MENITSGFLGPLLVLQAGFFLLTKILTIPQSLNSWWTSLSFLGGNTVCLGQNSQSPTSNHSPTSCPPTCPGYRWMCLRRFIIFLFILLLCLIFLLVLLDYQGMLPVCPLIPGSSTTSTGPCRTCKTPAQGTSMYPSCCCTKPSDGNCTCIPIPSSWAFGKFLWEWASARFSWLSLIVPFVQWFVGLSPTVWLSVIWMMWYWGPSLYSILSPFLPLLPIFFCLWVYI
Белок H
MSPQRDRINAFYKDNPHPKGSRIVINREHLMIDRPYVLLAVLFVMFLSLIGLLAIAGIRLHRAAIYTAEIHKSLSTNLDVTNSIEHQVKDVLTPLFKIIGDEVGLRTPQRFTDLVKFISDKIKFLNPDREYDFRDLTWCINPPERIKLDYDQYCADVAAEELMNALVNSTLLETRTTNQFLAVSKGNCSGPTTIRGQFSNMSLSLLDLYLGRGYNVSSIVTMTSQGMYGGTYLVEKPNLSSKRSELSQLSMYRVFEVGVIRNPGLGAPVFHMTNYLEQPVSNDLSNCMVALGELKLAALCHGEDSITIPYQGSGKGVSFQLVKLGVWKSPTDMQSWVPLSTDDPVIDRLYLSSHRGVIADNQAKWAVPTTRTDDKLRMETCFQQACKGKIQALCENPEWAPLKDNRIPSYGVLSVDLSLTVELKIKIASGFGPLITHGSGMDLYKSNHNNVYWLTIPPMKNLALGVINTLEWIPRFKVSPYLFNVPIKEAGEDCHAPTYLPAEVDGDVKLSSNLVILPGQDLQYVLATYDTSRVEHAVVYYVYSPSRSFSYFYPFRLPIKGVPIELQVECFTWDQKLWCRHFCVLADSESGGHITHSGMEGMGVSCTVTREDGTNRR
Белок F
MGLKVNVSAIFMAVLLTLQTPTGQIHWGNLSKIGVVGIGSASYKVMTRSSHQSLVIKLMPNITLLNNCTRVEIAEYRRLLRTVLEPIRDALNAMTQNIRPVQSVASSRRHKRFAGVVLAGAALGVATAAQITAGIALHQSMLNSQAIDNLRASLETTNQAIEAIRQAGQEMILAVQGVQDYINNELIPSMNQLSCDLIGQKLGLKLLRYYTEILSLFGPSLRDPISAEISIQALSYALGGDINKVLEKLGYSGGDLLGILESRGIKARITHVDTESYFIVLSIAYPTLSEIKGVIVHRLEGVSYNIGSQEWYTTVPKYVATQGYLISNFDESSCTFMPEGTVCSQNALYPMSPLLQECLRGSTKSCARTLVSGSFGNRFILSQGNLIANCASILCKCYTTGTIINQDPDKILTYIAADHCPVVEVNGVTIQVGSRRYPDAVYLHRIDLGPPISLERLDVGTNLGNAIAKLEDAKELLESSDQILRSMKGLSSTSIVYILIAVCLGGLIGIPALICCCRGRCNKKGEQVGMSRPGLKPDLTGTSKSYVRSL
Домен оболочки вируса Зика III (ZEDIII)
IRCIGVSNRDFVEGMSGGTWVDVVLEHGGCVTVMAQDKPTVDIELVTTTVSNMAEVRSYCYEASISDMASDSRCPTQGEAYLDKQSDTQYVCKRTLVDRGWGNGCGLFGKGSLVTCAKFTCSKKMTGKSIQPENLEYRIMLSVHGSQHSGMIGYETDEDRAKVEVTPNSPRAEATLGGFGSLGLDCEPRTGLDFSDLYYLTMNNKHWLVHKEWFHDIPLPWHAGADTGTPHWNNKEALVEFKDAHAKRQTVVVLGSQEGAVHTALAGALEAEMDGAKGRLFSGHLKCRLKMDKLRLKGVSYSLCTAAFTFTKVPAETLHGTVTVEVQYAGTDGPCKIPVQMAVDMQTLTPVGRLITANPVITESTENSKMMLELDPPFGDSYIVIGVGDKKITHHWHRSGSTIGKAFEATVRGAKRMAVLGDTAWDFGSVGGVFNSLGKGIHQIFGAAFKSLFGGMSWFSQILIGTLLVWLGLNTKNGSISLTCLALGGVMIFLSTAVSA
белок циркумспорозоита (CSP)
MKNFILLAVSSILLVDLFPTHCGHNVDLSKAINLNGVNFNNVDASSLGAAHVGQSASRGRGLGENPDDEEGDAKKKKDGKKAEPKNPRENKLKQPGDRADGQPAGDRADGQPAGDRADGQPAGDRAAGQPAGDRADGQPAGDRADGQPAGDRADGQPAGDRADGQPAGDRAAGQPAGDRAAGQPAGDRADGQPAGDRAAGQPAGDRADGQPAGDRAAGQPAGDRADGQPAGDRAAGQPAGDRAAGQPAGDRAAGQPAGDRAAGQPAGNGAGGQAAGGNAGGGQGQNNEGANAPNEKSVKEYLDKVRATVGTEWTPCSVTCGVGVRVRRRVNAANKKPEDLTLNDLETDVCTMDKCAGIFNVVSNSLGLVILLVLALFN
Белок F
MVVILDKRCYCNLLILILMISECSVGILHYEKLSKIGLVKGVTRKYKIKSNPLTKDIVIKMIPNVSNMSQCTGSVMENYKTRLNGILTPIKGALEIYKNNTHDLVGDVRLAGVIMAGVAIGIATAAQITAGVALYEAMKNADNINKLKSSIESTNEAVVKLQETAEKTVYVLTALQDYINTNLVPTIDKISCKQTELSLDLALSKYLSDLLFVFGPNLQDPVSNSMTIQAISQAFGGNYETLLRTLGYATEDFDDLLESDSITGQIIYVDLSSYYIIVRVYFPILTEIQQAYIQELLPVSFNNDNSEWISIVPNFILVRNTLISNIEIGFCLITKRSVICNQDYATPMTNNMRECLTGSTEKCPRELVVSSHVPRFALSNGVLFANCISVTCQCQTTGRAISQSGEQTLLMIDNTTCPTAVLGNVIISLGKYLGSVNYNSEGIAIGPPVFTDKVDISSQISSMNQSLQQSKDYIKEAQRLLDTVNPSLISMLSMIILYVLSIASLCIGLITFISFIIVEKKRNTYSRLEDRRVRPTSSGDLYYIGT
G белок
MPAENKKVRFENTTSDKGKIPSKVIKSYYGTMDIKKINEGLLDSKILSAFNTVIALLGSIVIIVMNIMIIQNYTRSTDNQAVIKDALQGIQQQIKGLADKIGTEIGPKVSLIDTSSTITIPANIGLLGSKISQSTASINENVNEKCKFTLPPLKIHECNISCPNPLPFREYRPQTEGVSNLVGLPNNICLQKTSNQILKPKLISYTLPVVGQSGTCITDPLLAMDEGYFAYSHLERIGSCSRGVSKQRIIGVGEVLDRGDEVPSLFMTNVWTPPNPNTVYHCSAVYNNEFYYVLCAVSTVGDPILNSTYWSGSLMMTRLAVKPKSNGGGYNQHQLALRSIEKGRYDKVMPYGPSGIKQGDTLYFPAVGFLVRTEFKYNDSNCPITKCQYSKPENCRLSMGIRPNSHYILRSGLLKYNLSDGENPKVVFIEISDQRLSIGSPSKIYDSLGQPVFYQASFSWDTMIKFGDVLTVNPLVVNWRNNTVISRPGQSQCPRFNTCPEICWEGVYNDAFLIDRINWISAGVFLDSNQTAENPVFTVFKDNEILYRAQLASEDTNAQKTITNCFLLKNKIWCISLVEIYDTGDNVIRPKLFAVKIPEQCT
Белок VP4
MASLIYRQLLTNSYSVDLHDEIEQIGSEKTQNVTINPSPFAQTRYAPVNWGHGEINDSTTVEPILDGPYQPTTFTPPNDYWILINSNTNGVVYESTNNSDFWTAVVAIEPHVNPVDRQYTIFGESKQFNVSNDSNKWKFLEMFRSSSQNEFYNRRTLTSDTRFVGILKYGGRVWTFHGETPRATTDSSSTANLNNISITIHSEFYIIPRSQESKCNEYINNGLPPIQNTRNVVPLPLSSRSIQYKRAQVNEDIIVSKTSLWKEMQYNRDIIIRFKFGNSIVKMGGLGYKWSEISYKAANYQYNYLRDGEQVTAHTTCSVNGVNNFSYNGGSLPTDFGISRYEVIKENSYVYVDYWDDSKAFRNMVYVRSLAANLNSVKCTGGSYNFSIPVGAWPVMNGGAVSLHFAGVTLSTQFTDFVSLNSLRFRFSLTVDEPPFSILRTRTVNLYGLPAANPNNGNEYYEISGRFSLIYLVPTNDDYQTPIMNSVTVRQDLERQLTDLREEFNSLSQEIAMAQLIDLALLPLDMFSMFSGIKSTIDLTKSMATSVMKKFRKSKLATSISEMTNSLSDAASSASRNVSIRSNLSAISNWTNVSNDVSNVTNSLNDISTQTSTISKKFRLKEMITQTEGMSFDDISAAVLKTKIDMSTQIGKNTLPDIVTEASEKFIPKRSYRILKDDEVMEINTEGKFFAYKINTFDEVPFDVNKFAELVTDSPVISAIIDFKTLKNLNDNYGITRTEALNLIKSNPNMLRNFINQNNPIIRNRIEQLILQCKL
Белок VP8
MASLIYRQLLTNSYSVDLHDEIEQIGSEKTQNVTINPSPFAQTRYAPVNWGHGEINDSTTVEPILDGPYQPTTFTPPNDYWILINSNTNGVVYESTNNSDFWTAVVAIEPHVNPVDRQYTIFGESKQFNVSNDSNKWKFLEMFRSSSQNEFYNRRTLTSDTRFVGILKYGGRVWTFHGETPRATTDSSSTANLNNISITIHSEFYIIPRSQESKCNEYINNGLPPIQNTR
Белок F
MSWKVVIIFSLLITPQHGLKESYLEESCSTITEGYLSVLRTGWYTNVFTLEVGDVENLTCSDGPSLIKTELDLTKSALRELKTVSADQLAREEQIENPRQSRFVLGAIALGVATAAAVTAGVAIAKTIRLESEVTAIKNALKTTNEAVSTLGNGVRVLATAVRELKDFVSKNLTRAINKNKCDIDDLKMAVSFSQFNRRFLNVVRQFSDNAGITPAISLDLMTDAELARAVSNMPTSAGQIKLMLENRAMVRRKGFGILIGVYGSSVIYMVQLPIFGVIDTPCWIVKAAPSCSGKKGNYACLLREDQGWYCQNAGSTVYYPNEKDCETRGDHVFCDTAAGINVAEQSKECNINISTTNYPCKVSTGRHPISMVALSPLGALVACYKGVSCSIGSNRVGIIKQLNKGCSYITNQDADTVTIDNTVYQLSKVEGEQHVIKGRPVSSSFDPIKFPEDQFNVALDQVFENIENSQALVDQSNRILSSAEKGNTGFIIVIILIAVLGSSMILVSIFIIIKKTKKPTGAPPELSGVTNNGFIPHS
G белок
MEVKVENIRAIDMLKARVKNRVARSKCFKNASLILIGITTLSIALNIYLIINYTIQKTSSESEHHTSSPPTESNKEASTISTDNPDINPNSQHPTQQSTENPTLNPAASVSPSETEPASTPDTTNRLSSVDRSTAQPSESRTKTKPTVHTRNNPSTASSTQSPPRATTKAIRRATTFRMSSTGKRPTTTSVQSDSSTTTQNHEETGSANPQASVSTMQN
Белок F
MQKSEILFLIYSSLLLSSSLCQIPVDKLSNVGVIINEGKLLKIAGSYESRYIVLSLVPSIDLEDGCGTTQIIQYKNLLNRLLIPLKDALDLQESLITITNDTTVTNDNPQSRFFGAVIGTIALGVATAAQITAGIALAEAREARKDIALIKDSIIKTHNSVELIQRGIGEQIIALKTLQDFVNNEIRPAIGELRCETTALKLGIKLTQHYSELATAFSSNLGTIGEKSLTLQALSSLYSANITEILSTIKKDKSDIYDIIYTEQVKGTVIDVDLEKYMVTLLVKIPILSEIPGVLIYRASSISYNIEGEEWHVAIPNYIINKASSLGGADVTNCIESRLAYICPRDPTQLIPDNQQKCILGDVSKCPVTKVINNLVPKFAFINGGVVANCIASTCTCGTNRIPVNQDRSRGVTFLTYTNCGLIGINGIELYANKRGRDTTWGNQIIKVGPAVSIRPVDISLNLASATNFLEESKIELMKAKAIISAVGGWHNTESTQIIIIIIVCILIIIICGILYYLYRVRRLLVMINSTHNSPVNTYTLESRMRNPYIGNNSN
Белок HN
MEDYSNLSLKSIPKRTCRIIFRTATILGICTLIVLCSSILHEIIHLDVSSGLMDSDDSQQGIIQPIIESLKSLIALANQILYNVAIIIPLKIDSIETVIFSALKDMHTGSMSNTNCTPGNLLLHDAAYINGINKFLVLKSYNGTPKYGPLLNIPSFIPSATSPNGCTRIPSFSLIKTHWCYTHNVMLGDCLDFTTSNQYLAMGIIQQSAAAFPIFRTMKTIYLSDGINRKSCSVTAIPGGCVLYCYVATRSEKEDYATTDLAELRLAFYYYNDTFIERVISLPNTTGQWATINPAVGSGIYHLGFILFPVYGGLISGTPSYNKQSSRYFIPKHPNITCAGNSSEQAAAARSSYVIRYHSNRLIQSAVLICPLSDMHTARCNLVMFNNSQVMMGAEGRLYVIDNNLYYYQRSSSWWSASLFYRINTDFSKGIPPIIEAQWVPSYQVPRPGVMPCNATSFCPANCITGVYADVWPLNDPEPTSQNALNPNYRFAGAFLRNESNRTNPTFYTASASALLNTTGFNNTNHKAAYTSSTCFKNTGTQKIYCLIIIEMGSSLLGEFQIIPFLRELIP
Поверхностный антиген pfs25
MNKLYSLFLFLFIQLSIKYNNAKVTVDTVCKRGFLIQMSGHLECKCENDLVLVNEETCEEKVLKCDEKTVNKPCGDFSKCIKIDGNPVSYACKCNLGYDMVNNVCIPNECKNVTCGNGKCILDTSNPVKTGVCSCNIGKVPNVQDQNKCSKDGETKCSLKCLKENETCKAVDGIYKCDCKDGFIIDNESSICTAFSAYNILNLSIMFILFSVCFFIM
fHbp
MNRTAFCCLSLTTALILTACSSGGGGVAADIGAGLADALTAPLDHKDKGLQSLTLDQSVRKNEKLKLAAQGAEKTYGNGDSLNTGKLKNDKVSRFDFIRQIEVDGQLITLESGEFQVYKQSHSALTAFQTEQIQDSEHSGKMVAKRQFRIGDIAGEHTSFDKLPEGGRATYRGTAFGSDDAGGKLTYTIDFAAKQGNGKIEHLKSPELNVDLAAADIKPDGKRHAVISGSVLYNQAEKGSYSLGIFGGKAQEVAGSAEVKTVNGIRHIGLAAKQ
NadA
MQTAARRSFDYDMPLIQTPTSACQIRQAWAKVADTPDRETAGRLKDEIKALLKETNAVLVAHYYVDPLIQDLALETGGCVGDSLEMARFGAEHEAGTLVVAGVRFMGESAKILCPEKTVLMPDLEAECSLDLGCPEEAFSAFCDQHPDRTVVVYANTSAAVKARADWVVTSSVALEIVSYLKSRGEKLIWGPDRHLGDYIRRETGADMLLWQGSCIVHNEFKGQELAALKAEHPDAVVLVHPESPQSVIELGDVVGSTSKLLKAAVSRPEKKFIVATDLGILHEMQKQAPDKQFIAAPTAGNGGSCKSCAFCPWMAMNSLGGIKYALTSGHNEILLDRKLGEAAKLPLQRMLDFAAGLKRGDVFNGMGPA
NHBA
MFKRSVIAMACIFALSACGGGGGGSPDVKSADTLSKPAAPVVSEKETEAKEDAPQAGSQGQGAPSAQGGQDMAAVSEENTGNGGAAATDKPKNEDEGAQNDMPQNAADTDSLTPNHTPASNMPAGNMENQAPDAGESEQPANQPDMANTADGMQGDDPSAGGENAGNTAAQGTNQAENNQTAGSQNPASSTNPSATNSGGDFGRTNVGNSVVIDGPSQNITLTHCKGDSCSGNNFLDEEVQLKSEFEKLSDADKISNYKKDGKNDGKNDKFVGLVADSVQMKGINQYIIFYKPKPTSFARFRRSARSRRSLPAEMPLIPVNQADTLIVDGEAVSLTGHSGNIFAPEGNYRYLTYGAEKLPGGSYALRVQGEPSKGEMLAGTAVYNGEVLHFHTENGRPSPSRGRFAAKVDFGSKSVDGIIDSGDGLHMGTQKFKAAIDGNGFKGTWTENGGGDVSGKFYGPAGEEVAGKYSYRPTDAEKGGFGVFAGKKEQD
4. Сборочные домены и линкеры
[0058] В одном варианте реализации наноструктура содержит тримерный узел. Сборка тримеров включает область взаимодействия белок-белок, которая индуцирует самоассоциацию трех копий первых полипептидов с образованием тримерных строительных блоков. Каждая копия первых полипептидов дополнительно содержит открытую область взаимодействия, которая взаимодействует с дополнительной открытой областью взаимодействия на втором сборочном домене. Как описано в King et al. (Nature 510, 103-108, 2014), Bale et al. (Science 353, 389-394, 2016) и патентных публикациях WO 2014124301 A1 и US 20160122392 A1, комплементарная белок-белковая область взаимодействия между тримерным доменом сборки и вторым доменом сборки управляет сборкой множественных копий домена сборки тримера и второго домена сборки в целевую наноструктуру. В некоторых вариантах реализации каждая копия тримерных доменов сборки наноструктуры несет антигенные белки или их антигенный фрагмент в виде генетического слияния; эти наноструктуры экспонируют белки с полной валентностью. В других вариантах реализации наноструктуры согласно настоящему изобретению содержат одну или несколько копий тримерных сборочных доменов, несущих антигенные белки или их антигенные фрагменты в виде генетических слияний, а также один или несколько тримерных сборочных доменов, которые не несут антигенные белки в виде генетических слияний; эти наноструктуры экспонируют белки F с частичной валентностью. Тримерный домен сборки может представлять собой любую полипептидную последовательность, которая образует тример и взаимодействует со вторым доменом сборки, чтобы управлять сборкой целевой наноструктуры. В некоторых вариантах реализации наноструктура содержит первый и второй полипептиды, выбранные из полипептидов, раскрытых в US 20130274441 A1, US 2015/0356240 A1, US 2016/0122392 A1, WO 2018/187325 A1, каждый из которых полностью включен в настоящее описание посредством ссылки.
[0059] В наноструктурах согласно настоящему изобретению антигенный белок и ядро наноструктуры могут быть генетически слиты, так что они оба присутствуют в одном полипептиде. Предпочтительно, связь между белком и ядром наноструктуры позволяет экспонировать белок или его антигенный фрагмент на внешней стороне наноструктуры. Таким образом, точка соединения с ядром наноструктуры должна находиться на внешней стороне ядра сформированной наноструктуры. Как будет понятно специалистам в данной области техники, для связывания белков или их антигенных фрагментов и ядра наноструктуры можно использовать большое количество полипептидных последовательностей. Эти полипептидные последовательности называются линкерами. Может быть использован любой подходящий линкер; отсутствуют требования к аминокислотной последовательности, подходящей в качестве линкера. Не требуется, чтобы линкер навязывал жесткую относительную ориентацию белка или его антигенного фрагмента к сердцевине наноструктуры, кроме того, чтобы белок или его антигенный фрагмент могли экспонироваться на внешней стороне наноструктуры. В некоторых вариантах реализации линкер включает дополнительные домены тримеризации (например, домен фолдон фибритина Т4), которые способствуют стабилизации тримерной формы белка F.
>Домен фолдон фибритина Т4 (необязательно в линкерной области) GYIPEAPRDGQAYVRKDGEWVLLSTFL (SEQ ID NO: 89)
[0060] В некоторых вариантах реализации линкер может содержать линкер Gly-Ser (т.е. линкер, состоящий из остатков глицина и серина) любой подходящей длины. В некоторых вариантах реализации линкер Gly-Ser может содержать 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или более аминокислот в длину. В некоторых вариантах реализации линкер Gly-Ser может содержать или состоять из аминокислотной последовательности GSGGSGSGSGGSGSG, GGSGGSGS или GSGGSGSG.
5. Сборка наноструктур
[0061] В некоторых вариантах реализации один или несколько очищенных образцов множества полипептидов для использования при формировании наноструктуры смешивают в приблизительно эквимолярном молярном соотношении в водных условиях. Полипептиды взаимодействуют друг с другом, чтобы управлять сборкой целевой наноструктуры. Успешная сборка целевой наноструктуры может быть подтверждена путем анализа реакции сборки in vitro обычными биохимическими или биофизическими методами, используемыми для оценки физического размера белков или белковых сборок, включая, помимо прочего, эксклюзионную хроматографию, нативный (неденатурирующий) гель-электрофорез, динамическое рассеяние света, многоугловое рассеяние света, аналитическое ультрацентрифугирование, электронную микроскопию с негативным окрашиванием, криоэлектронную микроскопию или рентгеновскую кристаллографию. При необходимости собранная наноструктура может быть очищена от других видов или молекул, присутствующих в реакции сборки in vitro, с использованием препаративных методов, обычно используемых для выделения белков по их физическому размеру, включая, помимо прочего, эксклюзионную хроматографию, препаративное ультрацентрифугирование, фильтрацию в тангенциальном потоке или препаративный гель-электрофорез. Присутствие антигенного белка в наноструктуре можно оценить методами, обычно используемыми для определения идентичности белковых молекул в водных растворах, включая, помимо прочего, SDS-PAGE, масс-спектрометрию, секвенирование белка или аминокислотный анализ. Доступность белка на внешней стороне частицы, а также его конформацию или антигенность можно оценить методами, обычно используемыми для обнаружения присутствия и конформации антигена, включая, помимо прочего, связывание моноклональными антителами, конформационно-специфическими моноклональными антителами или антисыворотками, специфичными к антигену.
[0062] В других вариантах реализации наноструктуры согласно настоящему изобретению содержат два или более отдельных первых полипептида, несущих разные антигенные белки в виде генетических слияний; указанные наноструктуры совместно экспонируют несколько разных белков на одной наноструктуре. Такие мультиантигенные наноструктуры получают путем выполнения сборки in vitro со смесями первых полипептидов, в которых каждый первый полипептид несет один из двух или более отдельных белков в виде генетического слияния. Доля каждого первого полипептида в смеси определяет среднюю валентность каждого антигенного белка в полученных наноструктурах. Присутствие и среднюю валентность каждого первого полипептида, несущего белок, в данном образце можно оценить с помощью количественного анализа, используя описанные выше методы для оценки присутствия антигенных белков в полновалентных наноструктурах.
[0063] В различных вариантах реализации наноструктуры имеют диаметр от около 20 нанометров (нм) до около 40 нм, с внутренними просветами от около 15 до около 32 нм в поперечнике и размером пор в белковых оболочках от около 1 до около 14 нм в самом длинном измерении.
[0064] В одном варианте реализации наноструктура имеет икосаэдрическую симметрию. В этом варианте реализации наноструктура может содержать 60 копий первого полипептида и 60 копий второго полипептида. В одном таком варианте реализации количество идентичных первых полипептидов в каждой первой сборке отличается от количества идентичных вторых полипептидов в каждой второй сборке. Например, в одном варианте реализации наноструктура содержит двенадцать первых сборок и двадцать вторых сборок; в этом варианте реализации каждая первая сборка может, например, включать пять копий идентичного первого полипептида, и каждая вторая сборка может, например, включать три копии идентичного второго полипептида. В другом варианте реализации наноструктура содержит двенадцать первых сборок и тридцать вторых сборок; в этом варианте осуществления каждая первая сборка может, например, содержать пять копий идентичного первого полипептида, и каждая вторая сборка может, например, содержать две копии идентичного второго полипептида. В дополнительном варианте реализации наноструктура включает двадцать первых сборок и тридцать вторых сборок; в этом варианте осуществления каждая первая сборка может, например, включать три копии идентичного первого полипептида, и каждая вторая сборка может, например, содержать две копии идентичного второго полипептида. Все эти варианты реализации способны формировать синтетические наноматериалы с правильной икосаэдрической симметрией.
[0065] В различных дополнительных вариантах реализации олигомерные состояния первого и второго полипептидов следующие:
I53-34A: тример + I53-34B: пентамер;
I53-40A: пентамер + I53-40B: тример;
I53-47A: тример + I53-47B: пентамер;
I53-50A: тример + I53-50B: пентамер;
I53-51A: тример + I53-51B: пентамер;
I32-06A: димер + I32-06B: тример;
I32-19A: тример + I32-19B: димер;
I32-28A: тример + I32-28B: димер;
I52-03A: пентамер + I52-03B: димер;
I52-32A: димер + I52-32B: пентамер; и
I52-33A: пентамер + I52-33B: димер
6. Нуклеиновые кислоты
[0066] В другом аспекте настоящего изобретения предложены изолированные (выделенные) нуклеиновые кислоты, кодирующие гибридный белок согласно настоящему изобретению. Изолированная последовательность нуклеиновой кислоты может содержать РНК или ДНК. Используемый здесь термин «изолированные нуклеиновые кислоты» означает те, которые были удалены из их нормальных окружающих последовательностей нуклеиновых кислот в геноме или в последовательностях кДНК. Такие рекомбинантные последовательности нуклеиновых кислот могут содержать дополнительные последовательности, подходящие для содействия экспрессии и/или очистке кодируемого белка, включая, не ограничиваясь перечисленным, последовательности полиА, модифицированные последовательности Козак и последовательности, кодирующие эпитопные метки, сигналы экспорта и сигналы секреции, сигналы ядерной локализации и сигналы локализации в плазматической мембране. Специалистам в данной области будет очевидно, на основании представленных здесь идей, какие последовательности нуклеиновых кислот будут кодировать белки согласно настоящему изобретению.
[0067] В дополнительном аспекте настоящего изобретения предложены рекомбинантные векторы экспрессии, содержащие рекомбинантную нуклеиновую кислоту согласно любому из вариантов реализации или комбинации вариантов реализации настоящего изобретения, функционально связанную с подходящей регуляторной последовательностью. «Рекомбинантный вектор экспрессии» включает векторы, функционально связывающие кодирующую область нуклеиновой кислоты или ген с любыми регуляторными последовательностями, способными осуществлять экспрессию продукта гена. «Регуляторные последовательности», функционально связанные с последовательностями нуклеиновых кислот согласно настоящему изобретению, представляют собой последовательности нуклеиновых кислот, способные осуществлять экспрессию молекул нуклеиновых кислот. Регуляторные последовательности не обязательно должны быть смежными с последовательностями нуклеиновых кислот при условии, что они выполняют функцию управления их экспрессией. Таким образом, например, между последовательностью промотора и последовательностями нуклеиновых кислот могут присутствовать промежуточные нетранслированные, но транскрибированные последовательности, и последовательность промотора по-прежнему может считаться «функционально связанной» с кодирующей последовательностью. Другие такие регуляторные последовательности включают, не ограничиваясь перечисленным, сигналы полиаденилирования, сигналы терминации и сайты связывания рибосомы. Такие векторы экспрессии могут быть любого типа, включая, не ограничиваясь перечисленным, плазмидные и вирусные векторы экспрессии. Контрольная последовательность, используемая для управления экспрессией описанных последовательностей нуклеиновых кислот в системе млекопитающих, может быть конститутивной (управляемой любым из множества промоторов, включая, помимо прочего, CMV, SV40, RSV, актин, EF) или индуцибельной (управляемой с помощью любого из ряда индуцибельных промоторов, включая, помимо прочего, тетрациклин, экдизон, стероид-зависимые). Конструирование векторов экспрессии для использования при трансфекции прокариотических клеток также хорошо известно в данной области и, таким образом, может быть выполнено стандартными методами. (См., например, Sambrook, Fritsch и Maniatis, в: Molecular Cloning, A Laboratory Manual (Молекулярное клонирование: лабораторное руководство.), Cold Spring Harbor Laboratory Press, 1989; Gene Transfer and Expression Protocols (Протоколы переноса и экспрессии генов.), стр. 109-128, ред. EJ Murray, The Humana Press Inc., Clifton, N.J.) и каталог Ambion 1998 (Ambion, Austin, TX). Вектор экспрессии может иметь возможность реплицироваться в организмах-хозяевах либо в виде эписомы, либо путем встраивания в хромосомную ДНК хозяина. В предпочтительном варианте реализации вектор экспрессии включает плазмиду. Однако настоящее изобретение предназначено для включения других векторов экспрессии, которые выполняют эквивалентные функции, таких как вирусные векторы.
[0068] В еще одном аспекте настоящего изобретения предложены рекомбинантные клетки-хозяева, содержащие рекомбинантные векторы экспрессии, раскрытые в настоящем документе, где клетки-хозяева могут быть прокариотическими либо эукариотическими, такими как клетки млекопитающих. Клетки могут быть временно или стабильно трансфицированы. Такая трансфекция векторов экспрессии в прокариотические и эукариотические клетки может быть осуществлена с помощью любого метода, известного в данной области, включая, помимо прочего, стандартные бактериальные трансформации, соосаждение с фосфатом кальция, электропорацию или опосредованные липосомами, опосредованные декстраном DEAE, опосредованные поликатионом или опосредованные вирусами виды трансфекции. (См., например, Molecular Cloning: A Laboratory Manual (Sambrook, et al., 1989, Cold Spring Harbor Laboratory Press; Culture of Animal Cells: A Manual of Basic Technique (Культура клеток животных: руководство по основной методике.), 2-е изд. (R.I. Freshney, 1987, Liss, Inc. New York, NY). Способ получения полипептида согласно настоящему изобретению является дополнительной частью настоящего изобретения. Способ включает стадии (а) культивирования хозяина в соответствии с указанным аспектом настоящего изобретения в условиях, способствующих экспрессии полипептида, и (б) необязательно, выделения экспрессированного полипептида.
7. Вакцины и введение
[0069] Согласно настоящему изобретению также предложены вакцины, содержащие описанные в настоящем документе наноструктуры. Такие композиции можно использовать для выработки антител у млекопитающего (например, человека). Композиции вакцин согласно настоящему изобретению обычно включают фармацевтически приемлемый носитель, и подробное обсуждение таких носителей доступно в Remington: The Science and Practice of Pharmacy (Теория и практика фармацевтики).
[0070] PH композиции обычно составляет от примерно 4,5 до примерно 11, например от примерно 5 до примерно 11, от примерно 5,5 до примерно 11, от примерно 6 до примерно 11, от примерно 5 до примерно 10,5, от примерно 5,5 до примерно 10,5, от примерно 6 до примерно 10,5, от примерно 5 до примерно 10, от примерно 5,5 до примерно 10, от примерно 6 до примерно 10, от примерно 5 до примерно 9,5, от примерно 5,5 до примерно 9,5, от примерно 6 до примерно 9,5, от примерно 5 до примерно 9, от примерно 5,5 до примерно 9, от примерно 6 до примерно 9, от примерно 5 до примерно 8,5, от примерно 5,5 до примерно 8,5, от примерно 6 до примерно 8,5, от примерно 5 до примерно 8, от примерно 5,5 до примерно 8, от примерно 6 до примерно 8, примерно 4,5, примерно 5, примерно 5,5, примерно 6, примерно 6,5, примерно 7, примерно 7,5, примерно 8, примерно 8,5, примерно 9, примерно 9,5, примерно 10, примерно 10,5, примерно 11 и т.д. Стабильный рН можно поддерживать с помощью буферного агента, например трис-буфера, цитратного буфера, фосфатного буфера или гистидинового буфера. Таким образом, композиция обычно включает буферный агент.
[0071] Композиция может быть стерильной и/или апирогенной. Композиции могут быть изотоничными по отношению к человеку.
[0072] Композиция вакцины содержит иммунологически эффективное количество ее антигена (антигенов). «Иммунологически эффективное количество» - это количество, которое при введении субъекту эффективно для индукции ответа антител против антигена. Это количество может варьироваться в зависимости от здоровья и физического состояния человека, подлежащего лечению, его возраста, способности иммунной системы человека синтезировать антитела, желаемой степени защиты, состава вакцины, оценки лечащим врачом медицинской ситуации и других соответствующих факторов. Ожидается, что это количество будет находиться в относительно широком диапазоне, который можно определить с помощью обычных испытаний. Содержание антигена в композициях согласно настоящему изобретению обычно выражается в единицах массы белка на дозу. Может быть полезна доза 10-500 мкг (например, 50 мкг) на антиген.
[0073] Композиции вакцины могут включать иммунологический адъювант. Примеры адъювантов включают следующее: 1. минеральные композиции; 2. масляные эмульсии; 3. составы сапонина; 4. виросомы и вирусоподобные частицы; 5. бактериальные или микробные производные; 6. биоадгезивы и мукоадгезивы; 7. липосомы; 8. составы простого эфира полиоксиэтилена и сложного эфира полиоксиэтилена; 9. полифосфазен (pcpp); 10. мурамиловые пептиды; 11. соединения имидазохинолона; 12. тиосемикарбазоновые соединения; 13. соединения триптантрина; 14. иммуномодуляторы человека; 15. липопептиды; 16. бензонафтиридины; 17. микрочастицы; 18. иммуностимулирующий полинуклеотид (такой как РНК или ДНК; например, cpg-содержащие олигонуклеотиды).
[0074] Например, композиция может включать адъювант на основе соли алюминия, эмульсию типа масло-в-воде (например, эмульсию типа масло-в-воде, содержащую сквален, такой как MF59 или AS03), агонист TLR7 (такой как имидазохинолин или имиквимод) или комбинацию указанных вариантов. Подходящие соли алюминия включают гидроксиды (например, оксигидроксиды), фосфаты (например, гидроксифосфаты, ортофосфаты) (например, см. Главы 8 и 9 Vaccine Design... (1995) под ред. Powell & Newman. ISBN: 030644867X. Plenum) или их смеси. Соли могут иметь любую подходящую форму (например, гелевую, кристаллическую, аморфную и т.д.), примером которой является адсорбция антигена на соли. Концентрация Al+++ в композиции для введения пациенту может составлять менее 5 мг/мл, например <4 мг/мл, <3 мг/мл, <2 мг/мл, <1 мг/мл и т.д. Предпочтительный диапазон составляет от 0,3 до 1 мг/мл. Предпочтительно, максимум 0,85 мг/дозу. Адъюванты на основе гидроксида алюминия и фосфата алюминия подходят для использования согласно настоящему изобретению.
[0075] Примеры адъювантов включают, но не ограничиваются ими, адъювант, адъюмер, микрочастицы альбумин-гепарин, водорослевой глюкан, альгаммулин, квасцы, состав антигена, адъювант AS-2, аутологичные дендритные клетки, аутологичные PBMC, Avridine™, B7-2, BAK, BAY R1005, бупивакаин, бупивакаин-HCl, BWZL, кальцитриол, кальцийфосфатный гель, пептиды CCR5, CFA, холотоксин (CT) и субъединица холерного токсина B (CTB), соединение D-субъединицы D холерного токсина-белок A белок, CpG, CRL1005, цитокинсодержащие липосомы, D-мурапальмитин, DDA, DHEA, дифтерийный токсоид, DL-PGL, DMPC, DMPG, комплекс DOC/Alum, оспа птиц, полный адъювант Фрейнда, гамма-инулин, адъювант Gerbu, GM-CSF, GMDP, hGM-CSF, hIL-12 (N222L), hTNF-alpha, IFA, IFN-gamma в pcDNA3, ДНК IL-12, плазмида IL-12, плазмида IL-12/GMCSF (Sykes), IL-2 в pcDNA3, плазмида IL-2/Ig, белок IL-2/Ig, IL-4, IL-4 в pcDNA3, Imiquimod, ImmTher™, иммунолипосомы, содержащие антитела к костимулирующим молекулам, интерферон-гамма, интерлейкин-1 бета, интерлейки n-12, интерлейкин-2, интерлейкин-7, ISCOM(s)™, Iscoprep 7.0.3™, гемоцианин лимфы улитки, липидный адъювант, липосомы, локсорибин, LT (R192G), LT-OA или пероральный адъювант LT, LT-R192G, LTK63, LTK72, MF59, MONTANIDE ISA 51, MONTANIDE ISA 720, MPL TM, MPL-SE, MTP-PE, MTP-PE липосомы, мураметид, мурапальмитин, NAGO, нКТ нативный холерный токсин, неионные поверхностно-активные везикулы, нетоксичный мутант E1 12K холерного токсина mCT-E112K, метиловый эфир п-гидроксибензойной кислоты, pCIL-10, pCIL12, pCMVmCAT1, pCMVN, Peptomer-NP, Pleuran, PLG, PLGA, PGAonic и L121, Plur, PMMA, PODDS™, Poly rA: Poly rU, Полисорбат 80, кохлеаты белков, QS-21, Quadri A сапонин, Quil-A, Rehydragel HPA, Rehydragel LV, RIBI, Ribilike адъювантная система (MPL, TMD, CWS), S -28463, SAF-1, пептид Sclavo, протеолипосомы Сендай, липидные матрицы, содержащие Сендай, Span 85, Specol, сквалан 1, сквален 2, стеарилтирозин, столбнячный анатоксин (TT), Theramide™, треонилмурамилдипептид (TMDP), Ty Частицы и липосомы Уолтера Рида. Выбор адъюванта зависит от пациента, которого лечат. Предпочтительно использовать фармацевтически приемлемый адъювант.
[0076] Один подходящий иммунологический адъювант включает соединение формулы (I), определенное в WO 2011/027222, или его фармацевтически приемлемую соль, адсорбированную на соли алюминия. Можно использовать многие дополнительные адъюванты, включая любые из адъювантов, раскрытых в Powell & Newman (1995).
[0077] Композиции могут включать противомикробное средство, особенно когда они упакованы в формате множественных доз. Противомикробные средства, такие как тиомерсал и 2-феноксиэтанол, обычно содержатся в вакцинах, но иногда может быть желательно использовать консервант, не содержащий ртути, или вообще не использовать консервант.
[0078] Композиции могут содержать детергент, например, полисорбат, такой как полисорбат 80. Детергенты обычно присутствуют в небольших количествах, например, <0,01%.
[0079] Композиции могут включать соли натрия (например, хлорид натрия) для придания тоничности. Типичная концентрация NaCl составляет 10±2 мг/мл, например около 9 мг/мл.
[0080] В некоторых вариантах реализаци буферный агент в составе композиции вакцины представляет собой трис-буфер, гистидиновый буфер, фосфатный буфер, цитратный буфер или ацетатный буфер. Композиция также может включать лиопротектор, например, сахарозу, сорбит или трегалозу. В отдельных вариантах реализации композиция включает консервант, например, бензалкония хлорид, бензетоний, хлоргексидин, фенол, м-крезол, бензиловый спирт, метилпарабен, пропилпарабен, хлорбутанол, о-крезол, п-крезол, хлоркрезол, нитрат фенилртути, тимеросал, бензойную кислоту и различные смеси указанных соединений. В других вариантах реализации композиция включает объемообразующий агент, такой как глицин. В других вариантах реализации композиция включает поверхностно-активное вещество, например, полисорбат-20, полисорбат-40, полисорбат-60, полисорбат-65, полисорбат-80, полисорбат-85, полоксамер-188, сорбитанмонолаурат, сорбитанмонопальмитат, сорбитанмоностеарат, сорбитанмоноолеат, сорбитантрилаурат, сорбитантристеарат, сорбитантриолеат или комбинацию указанных соединений. Композиция также может включать агент, регулирующий тоничность, например, соединение, делающее состав по существу изотоничным или изоосмотичным крови человека. Примеры агентов, регулирующих тоничность, включают сахарозу, сорбит, глицин, метионин, маннит, декстрозу, инозит, хлорид натрия, аргинин и гидрохлорид аргинина. В других вариантах реализации фармацевтическая композиция дополнительно включает стабилизатор, например, молекулу, которая по существу предотвращает или уменьшает химическую и/или физическую нестабильность наноструктуры в лиофилизированной или жидкой форме. Примеры стабилизаторов включают сахарозу, сорбит, глицин, инозит, хлорид натрия, метионин, аргинин и гидрохлорид аргинина.
[0081] В другом аспекте настоящего изобретения предложен способ индукции иммунного ответа против инфекционного агента, включающий введение субъекту, нуждающемуся в этом, иммунологически эффективного количества иммуногенной композиции, описанной в данном документе, которая содержит описанную наноструктуру.
[0082] В некоторых вариантах реализации иммунный ответ включает выработку нейтрализующих антител против инфекционного агента. В некоторых вариантах реализации нейтрализующие антитела не зависят от комплемента.
[0083] Иммунный ответ может включать гуморальный иммунный ответ, клеточно-опосредованный иммунный ответ или и то, и другое. В некоторых вариантах реализации иммунный ответ индуцируется против каждого доставленного антигенного белка. Клеточно-опосредованный иммунный ответ может включать ответ хелперных Т-клеток (Th), ответ цитотоксических Т-клеток (CTL) CD8+ или оба этих ответа. В некоторых вариантах реализации иммунный ответ включает гуморальный иммунный ответ, и антитела представляют собой нейтрализующие антитела. Нейтрализующие антитела блокируют вирусное заражение клеток. Вирусы поражают эпителиальные клетки, а также клетки фибробластов. В некоторых вариантах реализации иммунный ответ снижает или предотвращает инфицирование обоих типов клеток. Ответы нейтрализующих антител могут быть зависимыми от комплемента или независимыми от комплемента. В некоторых вариантах реализации ответ нейтрализующих антител не зависит от комплемента. В некоторых вариантах реализации нейтрализующий ответ антител является перекрестной нейтрализацией; т.е. антитело, генерируемое против введенной композиции, нейтрализует вирус штамма, отличного от штамма, используемого в композиции.
[0084] Полезной мерой эффективности антител в данной области является «титр нейтрализации 50%». Для определения титра нейтрализации 50% сыворотку иммунизированных животных разводят, чтобы оценить, насколько разбавленной сывороткой может быть сохранена способность блокировать проникновение 50% вирусов в клетки. Например, титр 700 означает, что сыворотка сохранила способность нейтрализовать 50% вируса после 700-кратного разбавления. Таким образом, более высокие титры указывают на более сильные ответы нейтрализующих антител. В некоторых вариантах реализации этот титр находится в диапазоне, имеющем нижний предел примерно 200, примерно 400, примерно 600, примерно 800, примерно 1000, примерно 1500, примерно 2000, примерно 2500, примерно 3000, примерно 3500, примерно 4000, примерно 4500, примерно 5000, примерно 5500, примерно 6000, примерно 6500 или примерно 7000. Диапазон титра нейтрализации 50% может иметь верхний предел примерно 400, примерно 600, примерно 800, примерно 1000, примерно 1500, примерно 2000, примерно 2500, примерно 3000, примерно 3500, примерно 4000, примерно 4500, примерно 5000, примерно 5500, примерно 6000, примерно 6500, примерно 7000, примерно 8000, примерно 9000, примерно 10000, примерно 11000, примерно 12000, примерно 13000, примерно 14000, примерно 15000, примерно 16000, примерно 17000, примерно 18000, примерно 19000, примерно 20000, примерно 21000, примерно 22000, примерно 23000, примерно 24000, примерно 25000, примерно 26000, примерно 27000, примерно 28000, примерно 29000 или примерно 30000. Например, титр нейтрализации 50% может составлять от примерно 3000 до примерно 25000. «Примерно» означает плюс или минус 10% от указанного значения.
[0085] Композиции согласно настоящему изобретению обычно вводят непосредственно субъекту. Непосредственную доставку можно осуществлять при помощи парентеральной инъекции (например, подкожно, внутрибрюшинно, внутривенно, внутримышечно или в интерстициальное пространство ткани) или любым другим подходящим путем. Например, можно использовать внутримышечное введение, например, в бедро или плечо. Инъекцию можно осуществлять с помощью иглы (например, иглы для подкожных инъекций), но альтернативно можно использовать инъекцию без иглы. Типичный объем внутримышечной дозы составляет 0,5 мл.
[0086] Дозировку можно осуществлять в однократном режиме или в многократном режиме. Множественные дозы можно использовать в режиме первичной иммунизации и/или в режиме бустерной иммунизации. В режиме множественных доз различные дозы можно вводить одним и тем же или разными путями, например, парентеральная первичная и мукозальная бустерная, мукозальная первичная и парентеральная бустерная и т.д. Множественные дозы обычно будут вводить с интервалом не менее 1 недели (например, около 2 недель, около 3 недель, около 4 недель, около 6 недель, около 8 недель, около 10 недель, около 12 недель, около 16 недель и т.д.).
[0087] Субъектом может быть животное, предпочтительно позвоночное, более предпочтительно млекопитающее. Типичный субъект включает, например, человека, корову, свинью, курицу, кошку или собаку, так как инфекционные агенты, описанные в данном документе, могут быть проблематичными для широкого круга видов. Если вакцина предназначена для профилактического использования, человек предпочтительно является ребенком (например, дошкольник или младенец), подростком или взрослым; если вакцина предназначена для терапевтического использования, человек предпочтительно является подростком или взрослым. Вакцина, предназначенная для детей, также может вводиться взрослым, например, для оценки безопасности, дозировки, иммуногенности и т.д.
[0088] Вакцины согласно настоящему изобретению могут быть профилактическими (т.е. для предотвращения заболевания) или терапевтическими (т.е. для уменьшения или устранения симптомов заболевания). Термин «профилактический» может рассматриваться как уменьшение тяжести или предотвращение возникновения определенного состояния. Во избежание сомнений термин профилактическая вакцина может также относиться к вакцинам, которые улучшают эффекты будущей инфекции, например, уменьшая тяжесть или продолжительность такой инфекции.
[0089] Выделенные и/или очищенные наноструктуры, описанные в настоящем документе, можно вводить отдельно или в качестве первичной или бустерной вакцины в смешанных режимах, таких как первичная РНК с последующим бустерным белком. Преимущества стратегии первичная РНК /бустерный белок по сравнению со стратегией первичный белок /бустерный белок включают, например, повышенные титры антител, более сбалансированный профиль подтипа IgG1: IgG2a, индукцию TH1-типа CD4+ T-клеточно-опосредованного иммунного ответа, подобного ответу вирусных частиц, и снижение выработки ненейтрализующих антител. Первичная РНК может повышать иммуногенность композиций независимо от того, содержат ли они адъювант или нет.
[0090] В стратегии первичная РНК / бустерный белок РНК и белок направлены на один и тот же антиген-мишень. Примеры подходящих способов доставки РНК включают вирусоподобные частицы репликона (VRP), РНК альфавируса, репликоны, инкапсулированные в липидные наночастицы (LNP), или составы с РНК, такие как репликоны в составах с катионными наноэмульсиями (CNE). Подходящие катионные наноэмульсии типа масло-в-воде раскрыты в WO 2012/006380, например, содержащие масляное ядро (например, включающее сквален) и катионный липид (например, DOTAP, DMTAP, DSTAP, DC-холестерин и т.д.).
[0091] В некоторых вариантах реализации молекула РНК инкапсулирована, связана или адсорбирована на катионном липиде, липосоме, кохлеате, виросоме, иммуностимулирующем комплексе, микрочастице, микросфере, наносфере, однослойном пузырьке, многослойном пузырьке, эмульсии типа масло-в-воде, эмульсии типа вода-в-масле, эмульсоме, поликатионном пептиде, катионной наноэмульсии или комбинации указанных вариантов.
[0092] Также в настоящем документе представлены наборы для введения нуклеиновой кислоты (например, РНК), очищенных белков и очищенных наноструктур, описанных в данном документе, и инструкции по применению. Согласно настоящему изобретению также предложено устройство для доставки, предварительно заполненное композицией или вакциной, описанной в данном документе.
[0093] Описанные в настоящем документе фармацевтические композиции можно вводить в сочетании с одним или несколькими дополнительными терапевтическими агентами. Дополнительные терапевтические агенты могут включать, без ограничения, антибиотики или антибактериальные агенты, противорвотные агенты, противогрибковые агенты, противовоспалительные агенты, противовирусные агенты, иммуномодулирующие агенты, цитокины, антидепрессанты, гормоны, алкилирующие агенты, антиметаболиты, противоопухолевые антибиотики, антимитотические агенты, ингибиторы топоизомеразы, цитостатические агенты, противоинвазионные агенты, антиангиогенные агенты, ингибиторы функции фактора роста, ингибиторы репликации вируса, ингибиторы вирусных ферментов, противоопухолевые агенты, альфа-интерфероны, бета-интерферон, рибавирин, гормоны и другие модуляторы толл-подобного рецептора, иммуноглобулины (Ig) и антитела, модулирующие функцию Ig (например, анти-IgE (омализумаб)).
[0094] В некоторых вариантах реализации описанные в настоящем документе композиции можно использовать в качестве лекарственного средства, например, для использования для индукции или усиления иммунного ответа у субъекта, который в этом нуждается, такого как млекопитающее.
[0095] В некоторых вариантах реализации описанные в настоящем документе композиции могут быть использованы при производстве лекарственного средства для индукции или усиления иммунного ответа у субъекта, нуждающегося в этом, такого как млекопитающее.
[0096] Один из способов проверки эффективности терапевтического лечения включает мониторинг инфекции, вызванной инфекционным агентом, после введения композиций или вакцин, описанных в данном документе. Один из способов проверки эффективности профилактического лечения включает в себя мониторинг иммунных ответов, системный (например, мониторинг уровня продукции IgG1 и IgG2a) и/или слизистой оболочки (например, мониторинг уровня продукции IgA), против антигена. Как правило, антиген-специфические реакции сывороточных антител определяют после иммунизации, но до заражения, тогда как антиген-специфические ответы антител слизистой оболочки определяют после иммунизации и после заражения.
8. Терминология
[0097] Все публикации и патенты, упомянутые в данном документе, включены в настоящее описание посредством ссылки во всей своей полноте, как если бы каждая отдельная публикация или патент были специально и индивидуально указаны для включения посредством ссылки. В случае конфликта настоящая заявка, включая любые определения в данном документе, будет иметь преимущественную силу. Однако упоминание любых ссылок, статей, публикаций, патентов, патентных публикаций и патентных заявок, цитируемых здесь, не является и не должно восприниматься как подтверждение или любая форма предположения, что они составляют действительный предшествующий уровень техники или являются частью общих знаний в любой стране мира.
[0098] В рамках данной заявки, если не указано иное, используемые методы можно найти в любой из нескольких хорошо известных ссылок, таких как: Molecular Cloning: A Laboratory Manual (Sambrook, et al., 1989, Cold Spring Harbor Laboratory Press), Gene Expression Technology (Технология экспрессии генов) (Methods in Enzymology, Vol. 185, edited by D. Goeddel, 1991. Academic Press, San Diego, CA), "Guide to Protein Purification" (Руководство по очистке белков) в Methods in Enzymology (M.P. Deutshcer, ред., (1990) Academic Press, Inc.); PCR Protocols: A Guide to Methods and Applications (Протоколы ПЦР: руководство по методам и применениям) (Innis, et al. 1990. Academic Press, San Diego, CA), Culture of Animal Cells: A Manual of Basic Technique, 2-е изд. (RI. Freshney. 1987 Liss, Inc. New York, NY), Gene Transfer and Expression Protocols, стр. 109-128, ред. E.J. Murray, The Humana Press Inc., Clifton, NJ.), и каталог Ambion 1998 (Ambion, Austin, TX).
[0099] В настоящем описании любой диапазон концентраций, процентный диапазон, диапазон соотношений или целочисленный диапазон следует понимать как включающий значение любого целого числа в указанном диапазоне и, при необходимости, его доли (например, одну десятую и одну сотую от целого числа), если не указано иное. Термин «примерно», непосредственно предшествующий числу или цифре, означает, что число или числовое значение находятся в диапазоне плюс или минус 10%. Следует понимать, что используемые здесь термины единственного числа относятся к «одному или нескольким» из перечисленных компонентов, если не указано иное. Использование альтернативы (например, «или») следует понимать как означающее одну, обе или любую их комбинацию. Термин «и/или» следует понимать как означающий одну или обе альтернативы. В контексте настоящего описания термины «включать» и «содержать» используются как синонимы.
[00100] Заголовки разделов, используемые здесь, предназначены только для организационных целей и не должны толковаться как ограничивающие описанный предмет.
[00101] Если специально не определено иное, следующие термины и фразы, которые являются общими для различных вариантов осуществления, раскрытых в данном документе, определены следующим образом:
[00102] Используемый здесь термин «белок» относится к белку или гликопротеину.
[00103] Используемый здесь термин «иммуногенный» относится к способности конкретного белка или его конкретной области вызывать иммунный ответ на конкретный белок или на белки, содержащие аминокислотную последовательность, имеющую высокую степень идентичности с конкретным белком. Согласно настоящему изобретению, два белка с высокой степенью идентичности имеют аминокислотные последовательности, которые по меньшей мере, на 80% идентичны, по меньшей мере на 85% идентичны, по меньшей мере на 87% идентичны, по меньшей мере на 90% идентичны, по меньшей мере на 92% идентичны, по меньшей мере на 94% идентичны, не менее чем на 96% идентичны, не менее чем на 98% идентичны или не менее чем на 99% идентичны.
[00104] В контексте настоящего описания иммунный ответ на вакцину или наноструктуру по настоящему изобретению представляет собой развитие у субъекта гуморального и/или клеточного иммунного ответа на антигенный белок, присутствующий в вакцине. Для целей настоящего раскрытия «гуморальный иммунный ответ» относится к иммунному ответу, опосредованному молекулами антител, включая секреторные (IgA) или молекулы IgG, в то время как «клеточный иммунный ответ» опосредуется Т-лимфоцитами и/или другими белыми кровяными клетками. Один важный аспект клеточного иммунитета включает антигенспецифический ответ цитолитических Т-клеток («CTL»). CTL обладают специфичностью к пептидным антигенам, которые представлены в ассоциации с белками, кодируемыми главным комплексом гистосовместимости (MHC), и экспрессируются на поверхности клеток. CTL помогают индуцировать и способствовать разрушению внутриклеточных микробов или лизису клеток, инфицированных такими микробами. Другой аспект клеточного иммунитета включает антигенспецифический ответ хелперных Т-клеток. Хелперные Т-клетки помогают стимулировать функцию и фокусировать активность неспецифических эффекторных клеток против клеток, экспонирующих пептидные антигены в ассоциации с молекулами MHC на своей поверхности. Клеточный иммунный ответ также относится к продукции цитокинов, хемокинов и других подобных молекул, продуцируемых активированными Т-клетками и/или другими лейкоцитами, включая те, которые происходят из Т-клеток CD4+ и CD8+.
[00105] Таким образом, иммунологический ответ может быть ответом, который стимулирует CTL и/или продукцию или активацию хелперных Т-клеток. Также может быть стимулировано производство хемокинов и/или цитокинов. Вакцина также может вызывать иммунный ответ, опосредованный антителами. Следовательно, иммунологический ответ может включать в себя один или несколько из следующих эффектов: продукция антител (например, IgA или IgG) B-клетками; и/или активация супрессорных, цитотоксических или хелперных Т-клеток и/или Т-клеток, специфически направленных на белок гемагглютинин, присутствующий в вакцине. Эти ответы могут служить для нейтрализации инфекционности и/или опосредовать антитело-комплемент или антитело-зависимую клеточную цитотоксичность (ADCC) для обеспечения защиты иммунизированного индивидуума. Такие ответы можно определить с помощью стандартных иммуноанализов и анализов нейтрализации, хорошо известных в данной области техники.
[00106] Используемый здесь термин «антитело» включает интактные молекулы, а также их функциональные фрагменты, такие как Fab, F (ab') 2, Fv, scFv, dsFv, или однодоменные молекулы, такие как VH и VL, которые способны специфически связываться к эпитопу антигена. Термин «антитело» охватывает рецепторы B-клеток. Термин «антитело» также включает антитела верблюдовых.
[00107] В контексте описания вирусов нейтрализующие антитела - это антитела, которые не позволяют вирусу завершить один цикл репликации. Как определено в данном документе, один цикл репликации относится к жизненному циклу вируса, начиная с присоединения вируса к клетке-хозяину и заканчивая отпочкованием вновь образованного вируса из клетки-хозяина. Этот жизненный цикл включает, без ограничения, этапы присоединения к клетке, проникновения в клетку, расщепления и перестройки вирусных белков, слияния вирусной мембраны с эндосомальной мембраной, высвобождения вирусных рибонуклеопротеидов в цитоплазму, образования новых вирусных частиц и отпочкование вирусных частиц от мембраны клетки-хозяина.
[00108] В данном контексте нейтрализующие антитела широкого спектра действия представляют собой антитела, которые нейтрализуют более одного типа, подтипа и/или штамма бактерий, вирусов или паразитов. Например, нейтрализующие антитела широкого спектра действия против белка HA гриппа из вируса гриппа типа A, могут нейтрализовать вирус типа B или типа C. В качестве дополнительного примера нейтрализующие антитела широкого спектра действия против белка НА гриппа из вируса гриппа I группы, могут нейтрализовать вирус группы 2. В качестве дополнительного примера, нейтрализующие антитела широкого спектра действия против белка НА из одного подтипа или штамма вируса, могут нейтрализовать другой подтип или штамм вируса. Например, нейтрализующие антитела широкого спектра действия против белка НА из вируса гриппа H1, могут нейтрализовать вирусы одного или нескольких подтипов, выбранных из группы, состоящей из H2, H3, H4, H5, H6, H7, H8, H8, H10, H11, H12, H13, H14, H15 или H16.
[00109] Что касается антигенов, специалистам в данной области техники понятно, что антигенные белки из разных штаммов могут иметь разную длину из-за мутаций (вставок, делеций) в белке. Таким образом, ссылка на соответствующую область относится к области других белков, которая идентична или почти идентична (например, идентична по меньшей мере на 95%, идентична по меньшей мере на 98% или идентична по меньшей мере на 99%) по последовательности, структуре и/или функции в сравниваемом регионе. Например, что касается эпитопа белка, соответствующая область в соответствующем белке из другого штамма организма может не иметь одинаковых номеров остатков, но будет иметь аналогичную или почти идентичную последовательность и будет выполнять ту же функцию. Чтобы лучше прояснить сравнение последовательностей между штаммами, специалисты в этой области техники используют системы нумерации, которые связывают положения аминокислот с эталонной последовательностью. Таким образом, соответствующие аминокислотные остатки в антигенных белках из разных штаммов могут не иметь одинакового числа остатков по отношению к их расстоянию от N-концевой аминокислоты белка. Использование таких систем нумерации понятно специалистам в данной области техники.
[00110] Согласно настоящему изобретению домен тримеризации представляет собой серию аминокислот, которые при соединении (также называемом слиянием) с белком или пептидом позволяют слитому белку взаимодействовать с другими слитыми белками, содержащими домен тримеризации, благодаря чему формируется тримерная структура. В настоящем изобретении можно использовать любой известный домен тримеризации. Примеры доменов тримеризации включают, но не ограничиваются ими, домен тримеризации gp41 ВИЧ-1, домен тримеризации gp41 SIV, домен тримеризации gp-2 вируса Эбола, домен тримеризации gp-21 HTLV-1, домен тримеризации фибритина Т4. (т.е. фолдон), домен тримеризации фактора транскрипции теплового шока дрожжей и домен тримеризации коллагена человека.
[00111] В данном контексте вариант относится к белку или молекуле нуклеиновой кислоты, последовательность которых подобна, но не идентична эталонной последовательности, где активность вариантного белка (или белка, кодируемого вариантной молекулой нуклеиновой кислоты) существенно не изменяется. Эти вариации в последовательности могут быть встречающимися в природе вариациями или они могут быть разработаны с использованием техники генной инженерии, известной специалистам в данной области техники. Примеры таких методов можно найти в Sambrook J, Fritsch E F, Maniatis T et al., in Molecular Cloning-A Laboratory Manual, 2nd Edition, Cold Spring Harbor Laboratory Press, 1989, pp. 9.31-9.57), или в Current Protocols in Molecular Biology (Современные протоколы молекулярной биологии), John Wiley & Sons, N.Y. (1989), 6.3.1-6.3.6, оба из которых полностью включены в настоящий документ посредством ссылки.
[00112] Что касается вариантов, любой тип изменения последовательности аминокислоты или нуклеиновой кислоты допустим до тех пор, пока полученный вариантный белок сохраняет способность вызывать нейтрализующие антитела против вируса гриппа. Примеры таких вариаций включают, но не ограничиваются ими, делеции, вставки, замены и их комбинации. Например, что касается белков, специалистам в данной области хорошо понятно, что одна или несколько (например, 2, 3, 4, 5, 6, 7, 8, 9 или 10) аминокислот часто могут быть удалены из амино- и/или карбоксиконцевых концов белка без значительного влияния на активность этого белка. Аналогично, одна или несколько (например, 2, 3, 4, 5, 6, 7, 8, 9 или 10) аминокислот часто могут быть вставлены в белок без значительного влияния на активность белка.
[00113] Как отмечалось, вариантные белки согласно настоящему изобретению могут содержать аминокислотные замены по сравнению с описанными здесь наноструктурными белками-антигенами. Допускается любая аминокислотная замена, если на активность белка не оказывается существенного влияния. В этом отношении в данной области техники принято во внимание, что аминокислоты можно классифицировать по группам на основе их физических свойств. Примеры таких групп включают, без ограничения, заряженные аминокислоты, незаряженные аминокислоты, полярные незаряженные аминокислоты и гидрофобные аминокислоты. Предпочтительными вариантами, содержащими замены, являются те, в которых аминокислота заменена аминокислотой из той же группы. Такие замены называются консервативными заменами.
[00114] В данном контексте аминокислотные остатки сокращены следующим образом: аланин (Ala; A), аспарагин (Asn; N), аспарагиновая кислота (Asp; D), аргинин (Arg; R), цистеин (Cys; C), глутаминовая кислота. кислота (Glu; E), глутамин (Gln; Q), глицин (Gly; G), гистидин (His; H), изолейцин (Ile; I), лейцин (Leu; L), лизин (Lys; K), метионин (Met; M), фенилаланин (Phe; F), пролин (Pro; P), серин (Ser; S), треонин (Thr; T), триптофан (Trp; W), тирозин (Tyr; Y) и валин (Val; В). Используемый здесь термин «примерно» означает +/-5% приведенного параметра.
[00115] Встречающиеся в природе остатки можно разделить на классы на основе общих свойств боковой цепи: 1) гидрофобные: Met, Ala, Val, Leu, Ile; 2) нейтральные гидрофильные: Cys, Ser, Thr; 3) кислые: Asp, Glu; 4) основные: Asn, Gln, His, Lys, Arg; 5) остатки, влияющие на ориентацию цепи: Gly, Pro; и 6) ароматические: Trp, Tyr, Phe. Например, неконсервативные замены могут включать замену члена одного из этих классов членом другого класса.
[00116] При замене аминокислот можно учитывать индекс гидрофобности аминокислот. Каждой аминокислоте присвоен индекс гидрофобности на основании ее гидрофобности и характеристик заряда. Индексы гидрофобности: изолейцин (+4,5); валин (+4,2); лейцин (+3,8); фенилаланин (+2,8); цистеин/цистин (+2,5); метионин (+1,9); аланин (+1,8); глицин (-0,4); треонин (-0,7); серин (-0,8); триптофан (-0,9); тирозин (-1,3); пролин (-1,6); гистидин (-3,2); глутамат (-3,5); глутамин (-3,5); аспартат (-3,5); аспарагин (-3,5); лизин (-3,9); и аргинин (-4,5). Важность индекса гидрофобности аминокислоты в придании интерактивной биологической функции белку обычно понятна в данной области техники (Kyte et al., 1982, J. Mol. Biol. 157: 105-31). Известно, что некоторые аминокислоты могут быть заменены другими аминокислотами, имеющими аналогичный индекс или балл гидрофобности, и все же сохранять аналогичную биологическую активность. При внесении изменений, основанных на индексе гидрофобности, замены аминокислот, индексы гидрофобности которых находятся в пределах ± 2, являются предпочтительными, те, которые находятся в пределах ± 1, особенно предпочтительны, а те, которые находятся в пределах ± 0,5, еще более предпочтительны.
[00117] В данной области техники также понятно, что замена подобных аминокислот может быть эффективно произведена на основе гидрофильности, в частности, когда созданный таким образом биологически функционально эквивалентный белок или пептид предназначен для использования в иммунологическом изобретении, как в настоящем случае. Наибольшая локальная средняя гидрофильность белка, определяемая гидрофильностью соседних с ним аминокислот, коррелирует с его иммуногенностью и антигенностью, то есть с биологическим свойством белка. Указанным аминокислотным остаткам были присвоены следующие значения гидрофильности: аргинин (+3,0); лизин (+3,0); аспартат (+3,0±1); глутамат (+3,0±1); серин (+0,3); аспарагин (+0,2); глутамин (+0,2); глицин (0); треонин (-0,4); пролин (-0,5±1); аланин (-0,5); гистидин (-0,5); цистеин (-1,0); метионин (-1,3); валин (-1,5); лейцин (-1,8); изолейцин (-1,8); тирозин (-2,3); фенилаланин (-2,5); и триптофан (-3,4). При внесении изменений, основанных на аналогичных значениях гидрофильности, замены аминокислот, значения гидрофильности которых находятся в пределах ± 2, являются предпочтительными, те, которые находятся в пределах ± 1, особенно предпочтительными, и те, которые находятся в пределах ± 0,5, даже более предпочтительными. Можно также идентифицировать эпитопы из первичных аминокислотных последовательностей на основе гидрофильности.
[00118] Желаемые аминокислотные замены (консервативные или неконсервативные) могут быть определены специалистом в данной области техники в то время, когда такие замены желательны. Например, аминокислотные замены можно использовать для идентификации важных остатков белка НА или для увеличения или уменьшения иммуногенности, растворимости или стабильности белков НА, описанных в данном документе. Примеры аминокислотных замен показаны ниже в таблице 4.
ТАБЛИЦА 4
Аминокислотные замены
[00119] В контексте настоящего описания фраза «существенно влияет на активность белка» относится к снижению активности белка по меньшей мере на 10%, по меньшей мере на 20%, по меньшей мере на 30%, по меньшей мере на 40% или по меньшей мере на 50%. Что касается настоящего изобретения, указанную активность можно измерить, например, как способность белка вызывать нейтрализующие антитела против вируса. Такую активность можно измерить путем измерения титра указанных антител против вируса или путем измерения количества типов, подтипов или штаммов, нейтрализованных вызванными антителами. Способы определения титров антител и способы проведения анализов нейтрализации вирусов известны специалистам в данной области техники. В дополнение к активности, описанной выше, другие активности, которые можно измерить, включают способность агглютинировать красные кровяные тельца и сродство связывания белка с клеткой. Способы измерения такой активности известны специалистам в данной области техники.
[00120] В данном контексте гибридный белок представляет собой рекомбинантный белок, содержащий аминокислотную последовательность по меньшей мере из двух неродственных белков, которые были соединены вместе посредством пептидной связи с образованием единого белка. Неродственные аминокислотные последовательности могут быть соединены непосредственно друг с другом или могут быть соединены с использованием линкерной последовательности. В данном контексте белки не являются родственными между собой, если их аминокислотные последовательности обычно не обнаруживаются соединенными посредством пептидной связи в их естественной среде (средах) (например, внутри клетки). Например, аминокислотные последовательности мономерных субъединиц, составляющих полипептид, и аминокислотные последовательности антигенных белков обычно не обнаруживаются соединенными вместе посредством пептидной связи.
[00121] Термины индивидуум, субъект и пациент хорошо известны в данной области техники и используются здесь взаимозаменяемо для обозначения любого человека или другого животного, восприимчивого к инфекции. Примеры включают, без ограничения, людей и других приматов, включая обезьян, таких как шимпанзе и другие виды человекообразных обезьян и обезьян; сельскохозяйственных животных, таких как крупный рогатый скот, овцы, свиньи, тюлени, козы и лошади; домашние млекопитающие, такие как собаки и кошки; лабораторные животные, включая грызунов, таких как мыши, крысы и морские свинки; птицы, включая домашних, диких и диких птиц, таких как куры, индейки и другие куриные птицы, утки, гуси и т.п. Сами по себе термины индивидуум, субъект и пациент не обозначают конкретный возраст, пол, расу и т.п. Таким образом, предполагается, что люди любого возраста, будь то мужчины или женщины, охвачены настоящим раскрытием и включают, без ограничения, пожилых людей, взрослых, детей, новорожденных, младенцев и детей дошкольного возраста. Аналогичным образом, способы настоящего раскрытия могут применяться к любой расе, включая, например, европеоидов (белые), афроамериканцы (черные), коренных американцев, коренных гавайцев, испаноязычных, латиноамериканцев, азиатов и европейцев.
[00122] В данном контексте вакцинированный субъект - это субъект, которому была введена вакцина, предназначенная для обеспечения защитного действия против бактерий, вирусов или паразитов.
[00123] Используемые здесь термины «воздействовать», «воздействие» и т.п. указывают на то, что субъект вступил в контакт с человеком или животным, которое, как известно, инфицировано бактериями, вирусом или паразитом.
[00124] Публикации, обсуждаемые в данном документе, предоставляются исключительно для их раскрытия до даты подачи настоящей заявки. Ничто в данном документе не должно быть истолковано как признание того, что настоящее раскрытие не имеет права датировать такую публикацию более ранней датой в силу предшествующего раскрытия. Кроме того, указанные даты публикации могут отличаться от фактических дат публикации, которые могут потребовать независимого подтверждения.
[00125] Если не указано иное, все технические и научные термины, используемые в данном документе, имеют то же значение, которое обычно понимается специалистом в области техники, к которой относится настоящее изобретение. Хотя любые способы и материалы, подобные или эквивалентные описанным в настоящем документе, также могут быть использованы на практике или при тестировании настоящего изобретения, в настоящем документе описаны предпочтительные способы и материалы. Все публикации, упомянутые в настоящем документе, включены в него посредством ссылки для раскрытия и описания способов и/или материалов, в связи с которыми цитируются указанные публикации.
[00126] Понятно, что определенные признаки изобретения, которые для ясности описаны в контексте отдельных вариантов реализации, также могут быть предоставлены в комбинации в одном варианте реализации. И наоборот, различные признаки изобретения, которые для краткости описаны в контексте одного варианта реализации, также могут быть предоставлены отдельно или в любой подходящей подкомбинации. Все комбинации вариантов реализации конкретно охвачены настоящим раскрытием и раскрыты в настоящем документе, как если бы каждая комбинация была раскрыта отдельно и явно. Кроме того, все подкомбинации также конкретно охвачены настоящим раскрытием и раскрыты в настоящем документе так же, как если бы каждая такая подкомбинация была отдельно и явно раскрыта в настоящем документе.
[00127] Изобретение дополнительно описано в следующих примерах, которые не ограничивают объем раскрытия, описанный в формуле изобретения.
9. Примеры
9.1. Пример 1. Респираторно-синцитиальный вирус (РСВ)
9.1.1. Последовательности
[00128] В вариантах реализации настоящего раскрытия белок F РСВ присутствует в виде гибридного белка с первым полипептидом, и используется линкер, последовательность белок F-линкер может включать следующее:

[00129] В различных дополнительных вариантах реализации первые полипептиды содержат или состоят из первых полипептидов, имеющих последовательность, выбранную из следующего (необязательные остатки в скобках):
> DS-Cav1-фолдон-T33-31A (SEQ ID NO: 91)
(MELLILKANVIATILTAVTFCFASS) QNITEEFYQSTCSAVSKGYLSALRTGWYTSVITIELSNIKENKCNGTDAKVKLIKQELDKYKNAVTELQLLMQSTPATNNRARRELPRFMNYTLNNAKKTNVTLSKKRKRRFLGFLLGVGSAIASGVAVCKVLHLEGEVNKIKSALLSTNKAVVSLSNGVSVLTFKVLDLKNYIDKQLLPILNKQSCSISNIETVIEFQQKNNRLLEITREFSVNAGVTTPVSTYMLTNSELLSLINDMPITNDQKKLMSNNVQIVRQQSYSIMCIIKEEVLAYVVQLPLYGVIDTPCWKLHTSPLCTTNTKEGSNICLTRTDRGWYCDNAGSVSFFPQAETCKVQSNRVFCDTMNSLTLPSEVNLCNVDIFNPKYDCKIMTSKTDVSSSVITSLGAIVSCYGKTKCTASNKNRGIIKTFSNGCDYVSNKGVDTVSVGNTLYYVNKQEGKSLYVKGEPIINFYDPLVFPSDEFDASISQVNEKINQSLAFIR (KSDELL) GYIPEAPRDGQAYVRKDGEWVLLSTFLGGSMEEVVLITVPSALVAVKIAHALVEERLAACVNIVPGLTSIYREEGSVVSDHELLLLVKTTTDAFPKLKERVKELHPYEVPEIVALPIAEGNREYLDWLRENTG
> DS-Cav1-T33-31A (SEQ ID NO: 92)
(MELLILKANVIATILTAVTFCFASS) QNITEEFYQSTCSAVSKGYLSALRTGWYTSVITIELSNIKENKCNGTDAKVKLIKQELDKYKNAVTELQLLMQSTPATNNRARRELPRFMNYTLNNAKKTNVTLSKKRKRRFLGFLLGVGSAIASGVAVCKVLHLEGEVNKIKSALLSTNKAVVSLSNGVSVLTFKVLDLKNYIDKQLLPILNKQSCSISNIETVIEFQQKNNRLLEITREFSVNAGVTTPVSTYMLTNSELLSLINDMPITNDQKKLMSNNVQIVRQQSYSIMCIIKEEVLAYVVQLPLYGVIDTPCWKLHTSPLCTTNTKEGSNICLTRTDRGWYCDNAGSVSFFPQAETCKVQSNRVFCDTMNSLTLPSEVNLCNVDIFNPKYDCKIMTSKTDVSSSVITSLGAIVSCYGKTKCTASNKNRGIIKTFSNGCDYVSNKGVDTVSVGNTLYYVNKQEGKSLYVKGEPIINFYDPLVFPSDEFDASISQVNEKINQSLAFIR (KSDELL) GGSMEEVVLITVPSALVAVKIAHALVEERLAACVNIVPGLTSIYREEGSVVSDHELLLLVKTTTDAFPKLKERVKELHPYEVPEIVALPIAEGNREYLDWLRENTG
> DS-Cav1-фолдон-T33-15B (SEQ ID NO: 93)
(MELLILKANVIATILTAVTFCFASS) QNITEEFYQSTCSAVSKGYLSALRTGWYTSVITIELSNIKENKCNGTDAKVKLIKQELDKYKNAVTELQLLMQSTPATNNRARRELPRFMNYTLNNAKKTNVTLSKKRKRRFLGFLLGVGSAIASGVAVCKVLHLEGEVNKIKSALLSTNKAVVSLSNGVSVLTFKVLDLKNYIDKQLLPILNKQSCSISNIETVIEFQQKNNRLLEITREFSVNAGVTTPVSTYMLTNSELLSLINDMPITNDQKKLMSNNVQIVRQQSYSIMCIIKEEVLAYVVQLPLYGVIDTPCWKLHTSPLCTTNTKEGSNICLTRTDRGWYCDNAGSVSFFPQAETCKVQSNRVFCDTMNSLTLPSEVNLCNVDIFNPKYDCKIMTSKTDVSSSVITSLGAIVSCYGKTKCTASNKNRGIIKTFSNGCDYVSNKGVDTVSVGNTLYYVNKQEGKSLYVKGEPIINFYDPLVFPSDEFDASISQVNEKINQSLAFIR (KSDELL) GYIPEAPRDGQAYVRKDGEWVLLSTFLGGSMVRGIRGAITVNSDTPTSIIIATILLLEKMLEANGIQSYEELAAVIFTVTEDLTSAFPAEAARQIGMHRVPLLSAREVPVPGSLPRVIRVLALWNTDTPQDRVRHVYLSEAVRLRPDLESAQ
> DS-Cav1-T33-15B (SEQ ID NO: 94)
(MELLILKANVIATILTAVTFCFASS) QNITEEFYQSTCSAVSKGYLSALRTGWYTSVITIELSNIKENKCNGTDAKVKLIKQELDKYKNAVTELQLLMQSTPATNNRARRELPRFMNYTLNNAKKTNVTLSKKRKRRFLGFLLGVGSAIASGVAVCKVLHLEGEVNKIKSALLSTNKAVVSLSNGVSVLTFKVLDLKNYIDKQLLPILNKQSCSISNIETVIEFQQKNNRLLEITREFSVNAGVTTPVSTYMLTNSELLSLINDMPITNDQKKLMSNNVQIVRQQSYSIMCIIKEEVLAYVVQLPLYGVIDTPCWKLHTSPLCTTNTKEGSNICLTRTDRGWYCDNAGSVSFFPQAETCKVQSNRVFCDTMNSLTLPSEVNLCNVDIFNPKYDCKIMTSKTDVSSSVITSLGAIVSCYGKTKCTASNKNRGIIKTFSNGCDYVSNKGVDTVSVGNTLYYVNKQEGKSLYVKGEPIINFYDPLVFPSDEFDASISQVNEKINQSLAFIR (KSDELL) GGSMVRGIRGAITVNSDTPTSIIIATILLLEKMLEANGIQSYEELAAVIFTVTEDLTSAFPAEAARQIGMHRVPLLSAREVPVPGSLPRVIRVLALWNTDTPQDRVRHVYLSEAVRLRPDLESAQ


> DS-Cav1-I32-28A (SEQ ID NO: 97)
(MELLILKANAITTILTAVTFCFASG) QNITEEFYQSTCSAVSKGYLSALRTGWYTSVITIELSNIKENKCNGTDAKVKLIKQELDKYKNAVTELQLLMQSTPATNNRARRELPRFMNYTLNNAKKTNVTLSKKRKRRFLGFLLGVGSAIASGVAVCKVLHLEGEVNKIKSALLSTNKAVVSLSNGVSVLTFKVLDLKNYIDKQLLPILNKQSCSISNIETVIEFQQKNNRLLEITREFSVNAGVTTPVSTYMLTNSELLSLINDMPITNDQKKLMSNNVQIVRQQSYSIMCIIKEEVLAYVVQLPLYGVIDTPCWKLHTSPLCTTNTKEGSNICLTRTDRGWYCDNAGSVSFFPQAETCKVQSNRVFCDTMNSLTLPSEVNLCNVDIFNPKYDCKIMTSKTDVSSSVITSLGAIVSCYGKTKCTASNKNRGIIKTFSNGCDYVSNKGVDTVSVGNTLYYVNKQEGKSLYVKGEPIINFYDPLVFPSDEFDASISQVNEKINQSLAFIR (KSDELL) GGSGGSGSDDARIAAIGDVDELNSQIGVLLAEPLPDDVRAALSAIQHDLFDLGGELCIPGHAAITEDHLLRLALWLVHYNGQLPPLEEFILPGGARGAALAHVCRTVCRRAERSIKALGASEPLNIAPAAYVNLLSDLLFVLARVLNRAAGGADVLWDRTRAH
>DS-Cav1-Tr-фолдон-T33-31A (SEQ ID NO: 101)
QNITEEFYQSTCSAVSKGYLSALRTGWYTSVITIELSNIKENKCNGTDAKVKLIKQELDKYKNAVTELQLLMQSTPATNNRARRELPRFMNYTLNNAKKTNVTLSKKRKRRFLGFLLGVGSAIASGVAVCKVLHLEGEVNKIKSALLSTNKAVVSLSNGVSVLTFKVLDLKNYIDKQLLPILNKQSCSISNIETVIEFQQKNNRLLEITREFSVNAGVTTPVSTYMLTNSELLSLINDMPITNDQKKLMSNNVQIVRQQSYSIMCIIKEEVLAYVVQLPLYGVIDTPCWKLHTSPLCTTNTKEGSNICLTRTDRGWYCDNAGSVSFFPQAETCKVQSNRVFCDTMNSLTLPSEVNLCNVDIFNPKYDCKIMTSKTDVSSSVITSLGAIVSCYGKTKCTASNKNRGIIKTFSNGCDYVSNKGVDTVSVGNTLYYVNKQEGKSLYVKGEPIINFYDPLVFPSDEFDASISQVNEKINQSLAFIRGYIPEAPRDGQAYVRKDGEWVLLSTFLGGSMEEVVLITVPSALVAVKIAHALVEERLAACVNIVPGLTSIYREEGSVVSDHELLLLVKTTTDAFPKLKERVKELHPYEVPEIVALPIAEGNREYLDWLRENTG
>DS-Cav1-Tr-T33-31A (SEQ ID NO: 102)
QNITEEFYQSTCSAVSKGYLSALRTGWYTSVITIELSNIKENKCNGTDAKVKLIKQELDKYKNAVTELQLLMQSTPATNNRARRELPRFMNYTLNNAKKTNVTLSKKRKRRFLGFLLGVGSAIASGVAVCKVLHLEGEVNKIKSALLSTNKAVVSLSNGVSVLTFKVLDLKNYIDKQLLPILNKQSCSISNIETVIEFQQKNNRLLEITREFSVNAGVTTPVSTYMLTNSELLSLINDMPITNDQKKLMSNNVQIVRQQSYSIMCIIKEEVLAYVVQLPLYGVIDTPCWKLHTSPLCTTNTKEGSNICLTRTDRGWYCDNAGSVSFFPQAETCKVQSNRVFCDTMNSLTLPSEVNLCNVDIFNPKYDCKIMTSKTDVSSSVITSLGAIVSCYGKTKCTASNKNRGIIKTFSNGCDYVSNKGVDTVSVGNTLYYVNKQEGKSLYVKGEPIINFYDPLVFPSDEFDASISQVNEKINQSLAFIRGGSMEEVVLITVPSALVAVKIAHALVEERLAACVNIVPGLTSIYREEGSVVSDHELLLLVKTTTDAFPKLKERVKELHPYEVPEIVALPIAEGNREYLDWLRENTG
>DS-Cav1-Tr-фолдон-T33-15B (SEQ ID NO: 103)
QNITEEFYQSTCSAVSKGYLSALRTGWYTSVITIELSNIKENKCNGTDAKVKLIKQELDKYKNAVTELQLLMQSTPATNNRARRELPRFMNYTLNNAKKTNVTLSKKRKRRFLGFLLGVGSAIASGVAVCKVLHLEGEVNKIKSALLSTNKAVVSLSNGVSVLTFKVLDLKNYIDKQLLPILNKQSCSISNIETVIEFQQKNNRLLEITREFSVNAGVTTPVSTYMLTNSELLSLINDMPITNDQKKLMSNNVQIVRQQSYSIMCIIKEEVLAYVVQLPLYGVIDTPCWKLHTSPLCTTNTKEGSNICLTRTDRGWYCDNAGSVSFFPQAETCKVQSNRVFCDTMNSLTLPSEVNLCNVDIFNPKYDCKIMTSKTDVSSSVITSLGAIVSCYGKTKCTASNKNRGIIKTFSNGCDYVSNKGVDTVSVGNTLYYVNKQEGKSLYVKGEPIINFYDPLVFPSDEFDASISQVNEKINQSLAFIRGYIPEAPRDGQAYVRKDGEWVLLSTFLGGSMVRGIRGAITVNSDTPTSIIIATILLLEKMLEANGIQSYEELAAVIFTVTEDLTSAFPAEAARQIGMHRVPLLSAREVPVPGSLPRVIRVLALWNTDTPQDRVRHVYLSEAVRLRPDLESAQ
>DS-Cav1-Tr-T33-15B (SEQ ID NO: 104)
QNITEEFYQSTCSAVSKGYLSALRTGWYTSVITIELSNIKENKCNGTDAKVKLIKQELDKYKNAVTELQLLMQSTPATNNRARRELPRFMNYTLNNAKKTNVTLSKKRKRRFLGFLLGVGSAIASGVAVCKVLHLEGEVNKIKSALLSTNKAVVSLSNGVSVLTFKVLDLKNYIDKQLLPILNKQSCSISNIETVIEFQQKNNRLLEITREFSVNAGVTTPVSTYMLTNSELLSLINDMPITNDQKKLMSNNVQIVRQQSYSIMCIIKEEVLAYVVQLPLYGVIDTPCWKLHTSPLCTTNTKEGSNICLTRTDRGWYCDNAGSVSFFPQAETCKVQSNRVFCDTMNSLTLPSEVNLCNVDIFNPKYDCKIMTSKTDVSSSVITSLGAIVSCYGKTKCTASNKNRGIIKTFSNGCDYVSNKGVDTVSVGNTLYYVNKQEGKSLYVKGEPIINFYDPLVFPSDEFDASISQVNEKINQSLAFIRGGSMVRGIRGAITVNSDTPTSIIIATILLLEKMLEANGIQSYEELAAVIFTVTEDLTSAFPAEAARQIGMHRVPLLSAREVPVPGSLPRVIRVLALWNTDTPQDRVRHVYLSEAVRLRPDLESAQ
>DS-Cav1-Tr-фолдон-I53-50A (SEQ ID NO: 105)
QNITEEFYQSTCSAVSKGYLSALRTGWYTSVITIELSNIKENKCNGTDAKVKLIKQELDKYKNAVTELQLLMQSTPATNNRARRELPRFMNYTLNNAKKTNVTLSKKRKRRFLGFLLGVGSAIASGVAVCKVLHLEGEVNKIKSALLSTNKAVVSLSNGVSVLTFKVLDLKNYIDKQLLPILNKQSCSISNIETVIEFQQKNNRLLEITREFSVNAGVTTPVSTYMLTNSELLSLINDMPITNDQKKLMSNNVQIVRQQSYSIMCIIKEEVLAYVVQLPLYGVIDTPCWKLHTSPLCTTNTKEGSNICLTRTDRGWYCDNAGSVSFFPQAETCKVQSNRVFCDTMNSLTLPSEVNLCNVDIFNPKYDCKIMTSKTDVSSSVITSLGAIVSCYGKTKCTASNKNRGIIKTFSNGCDYVSNKGVDTVSVGNTLYYVNKQEGKSLYVKGEPIINFYDPLVFPSDEFDASISQVNEKINQSLAFIRGYIPEAPRDGQAYVRKDGEWVLLSTFLGSGSHHHHHHHHGGSGGSGSEKAAKAEEAARKMEELFKKHKIVAVLRANSVEEAIEKAVAVFAGGVHLIEITFTVPDADTVIKALSVLKEKGAIIGAGTVTSVEQCRKAVESGAEFIVSPHLDEEISQFCKEKGVFYMPGVMTPTELVKAMKLGHTILKLFPGEVVGPQFVKAMKGPFPNVKFVPTGGVNLDNVCEWFKAGVLAVGVGSALVKGTPDEVREKAKAFVEKIRGCTE
>DS-Cav1-Tr-I53-50A (SEQ ID NO: 106)
QNITEEFYQSTCSAVSKGYLSALRTGWYTSVITIELSNIKENKCNGTDAKVKLIKQELDKYKNAVTELQLLMQSTPATNNRARRELPRFMNYTLNNAKKTNVTLSKKRKRRFLGFLLGVGSAIASGVAVCKVLHLEGEVNKIKSALLSTNKAVVSLSNGVSVLTFKVLDLKNYIDKQLLPILNKQSCSISNIETVIEFQQKNNRLLEITREFSVNAGVTTPVSTYMLTNSELLSLINDMPITNDQKKLMSNNVQIVRQQSYSIMCIIKEEVLAYVVQLPLYGVIDTPCWKLHTSPLCTTNTKEGSNICLTRTDRGWYCDNAGSVSFFPQAETCKVQSNRVFCDTMNSLTLPSEVNLCNVDIFNPKYDCKIMTSKTDVSSSVITSLGAIVSCYGKTKCTASNKNRGIIKTFSNGCDYVSNKGVDTVSVGNTLYYVNKQEGKSLYVKGEPIINFYDPLVFPSDEFDASISQVNEKINQSLAFIRGGSGGSGSEKAAKAEEAARKMEELFKKHKIVAVLRANSVEEAIEKAVAVFAGGVHLIEITFTVPDADTVIKALSVLKEKGAIIGAGTVTSVEQCRKAVESGAEFIVSPHLDEEISQFCKEKGVFYMPGVMTPTELVKAMKLGHTILKLFPGEVVGPQFVKAMKGPFPNVKFVPTGGVNLDNVCEWFKAGVLAVGVGSALVKGTPDEVREKAKAFVEKIRGCTE
>DS-Cav1-Tr-I32-28A (SEQ ID NO: 107)
QNITEEFYQSTCSAVSKGYLSALRTGWYTSVITIELSNIKENKCNGTDAKVKLIKQELDKYKNAVTELQLLMQSTPATNNRARRELPRFMNYTLNNAKKTNVTLSKKRKRRFLGFLLGVGSAIASGVAVCKVLHLEGEVNKIKSALLSTNKAVVSLSNGVSVLTFKVLDLKNYIDKQLLPILNKQSCSISNIETVIEFQQKNNRLLEITREFSVNAGVTTPVSTYMLTNSELLSLINDMPITNDQKKLMSNNVQIVRQQSYSIMCIIKEEVLAYVVQLPLYGVIDTPCWKLHTSPLCTTNTKEGSNICLTRTDRGWYCDNAGSVSFFPQAETCKVQSNRVFCDTMNSLTLPSEVNLCNVDIFNPKYDCKIMTSKTDVSSSVITSLGAIVSCYGKTKCTASNKNRGIIKTFSNGCDYVSNKGVDTVSVGNTLYYVNKQEGKSLYVKGEPIINFYDPLVFPSDEFDASISQVNEKINQSLAFIRGGSGGSGSDDARIAAIGDVDELNSQIGVLLAEPLPDDVRAALSAIQHDLFDLGGELCIPGHAAITEDHLLRLALWLVHYNGQLPPLEEFILPGGARGAALAHVCRTVCRRAERSIKALGASEPLNIAPAAYVNLLSDLLFVLARVLNRAAGGADVLWDRTRAH
9.1.2. Способы
Экспрессия и скрининг тримерных строительных блоков, содержащих белок F и тримерный домен сборки.
[00130] Оптимизированные по кодонам человека последовательности тримерных строительных блоков, содержащие слияния DS-Cav1 или не содержащие их, были заказаны в Genscript. Строительные блоки для однокомпонентных наноструктур (например, I3-01) были клонированы в вектор pcDNA3.1 (ThermoFisher Scientific), содержащий один промотор CMV, в то время как строительные блоки для двухкомпонентных наноструктур (например, I53-50) были клонированы в вектор pBudCE4.1 (ThermoFisher Scientific), содержащий промоторы CMV и EF-1α. Рекомбинантные белки экспрессировали временной трансфекцией клеток Expi293F (ThermoFisher Scientific) с использованием полиэтиленимина (PEI). Культуры клеток собирали центрифугированием через пять дней после трансфекции. Секретированные белки анализировали с помощью ELISA, используя либо прямое покрытие клеточных супернатантов, либо сэндвич-ELISA. Вкратце, 96-луночные планшеты MaxiSorp (Nunc) покрывали клеточным супернатантом для прямого ELISA или мышиным моноклональным антителом к гистидиновой метке (ThermoFisher Scientific) для сэндвич-ELISA. Секретированные белки детектировали с использованием моноклональных антител к паливизумабу человека, MPE8, RSD5 и D25. Трансфицированные клетки Expi293F фиксировали и пермеабилизировали с помощью BD cytofix/cytoperm (BD Biosciences), инкубировали с человеческими моноклональными антителами к паливизумабу, MPE8 и D25, и окрашивали конъюгированными с Alexa Fluor 647 антителами к IgG человека (Jackson ImmunoResearch). Окрашенные клетки подсчитывали с помощью проточного цитометра FACS Fortessa (BD Biosciences). Анализ проводили с помощью программного обеспечения FlowJo. Клеточные линии обычно тестировали на заражение микоплазмами.
Экспрессия и очистка DS-Cav1-I53-50A
[00131] Лентивирус получали путем временной трансфекции клеток 293Т (АТСС) с использованием линейного полиэтиленимина 25 кДа (ПЭИ; Polysciences). Вкратце, 4×106 клеток высевали на чашки для тканевых культур размером 10 см. Через 24 часа 3 мкг psPAX2, 1,5 мкг pMD2G (плазмиды Addgene №12260 и №12259 соответственно) и 6 мкг лентивирусной векторной плазмиды смешивали в 500 мкл разбавителя (5 мМ HEPES, 150 мМ NaCl, pH = 7,05) и 42 мкл ПЭИ (1 мг/мл) и инкубировали в течение 15 мин. Затем в чашку по каплям добавляли комплекс ДНК/ПЭИ. Лентивирус собирали через 48 часов после трансфекции и концентрировали в 100 раз низкоскоростным центрифугированием при 8000 g в течение 18 часов. Трансдукцию линии клеток-мишеней проводили во встряхиваемых колбах объемом 125 мл, содержащих 10×106 клеток в 10 мл питательной среды. В колбу добавляли 100 мкл 100-кратного лентивируса и клетки инкубировали при встряхивании (225 об./мин) при 37°C в 8% CO2 в течение 4-6 часов. Через 4-6 часов во встряхиваемую колбу добавляли 20 мл среды для выращивания.
[00132] Трансдуцированные клетки разбавляли через день до плотности 1×106 клеток/мл до достижения конечного объема культуры 4 л. Среду собирали через 17 дней полной инкубации после измерения конечной концентрации клеток (~5×106 клеток/мл) и жизнеспособности (~90% жизнеспособности). Супернатант культуры собирали при помощи низкоскоростного центрифугирования для удаления клеток из супернатанта. NaCl и NaN3 добавляли до конечных концентраций 250 мМ и 0,02% соответственно. Супернатант загружали на одну колонку HisTrap FF Crude объемом 5 мл (GE Healthsciences) со скоростью 5 мл/мин с помощью AKTA Pure (GE Healthsciences). Элюирование никелем применяли на колонке HiLoad 16/600 Superdex 200 пг (GE Healthsciences) для дальнейшей очистки целевого белка с помощью эксклюзионной хроматографии. Целевой белок, очищенный методом эксклюзионной хроматографии, мгновенно замораживали в жидком азоте и хранили при -80°C.
Сборка in vitro наноструктур, несущих DS-Cav1
[00133] Частицы со 100% валентностью (20 тримеров DS-Cav1 на икосаэдрическую наноструктуру) получали путем смешивания тримеров DS-Cav1-фолдон-I53-50A и пентамеров I53-50B.4PT1 в концентрации 50 мкМ каждый и инкубирования при качании в течение ночи при 4°C. В некоторых случаях собранные наноструктуры очищали от избыточных компонентов, оставшихся в реакции сборки in vitro, с использованием колонки GE Sephacryl S-500 HR 16/60 в буфере, содержащем 25 мМ Трис pH 8, 250 мМ NaCl, 5% глицерина. Нагрузку образца и фракции эксклюзионной хроматографии анализировали с помощью SDS-PAGE в присутствии и в отсутствии восстанавливающего агента. Пиковые фракции объединяли, концентрировали с использованием центробежного фильтра GE Vivaspin 20 30 кДа MWCO и количественно оценивали с помощью спектрофотометра Agilent 8454.
[00134] Частицы с валентностью 66% (~14 тримеров DS-Cav1 на икосаэдрическую наноструктуру) получали смешиванием тримеров DS-Cav1-фолдон-I53-50A, тримеров I53-50A и пентамеров I53-50B.4PosT1 в концентрации 50, 25 и 75 мкМ соответственно. Частицы с 33% валентностью (-7 тримеров DS-Cav1 на икосаэдрическую наноструктуру) получали смешиванием тримеров DS-Cav1-фолдон-I53-50A, тримеров I53-50A и пентамеров I53-50B.4PosT1 в концентрации 25, 50 и 75 мкМ соответственно. Реакции сборки in vitro оставляли для инкубирования при качании в течение ночи при 4°C. В некоторых случаях собранные наноструктуры очищали от избыточных компонентов, оставшихся в реакции сборки in vitro, с использованием колонки GE Sephacryl S-500 HR 16/60 в буфере, содержащем 25 мМ Трис pH 8, 250 мМ NaCl, 5% глицерина. Нагрузку образца и фракции эксклюзионной хроматографии анализировали с помощью SDS-PAGE в присутствии и в отсутствии восстанавливающего агента. Пиковые фракции объединяли, концентрировали с использованием центробежного фильтра GE Vivaspin 20 30 кДа MWCO и количественно определяли с помощью спектрофотометра Agilent 8454 после центрифугирования при ~21000 g в течение 10 минут при 4°C. Затем образцы переносили в криогенные пробирки аликвотами по 1 мл в концентрации 1,1 мг/мл для частиц с валентностью 33% и 0,6 мг/мл для частиц с валентностью 66%, мгновенно замораживали в жидком азоте и хранили при -80°C.
Электронная микроскопия наноструктур с DS-Cav1
[00135] Образцы готовили для негативного окрашивания ЭМ путем разбавления до 0,01 мг/мл с использованием 25 мМ Трис pH 8, 250 мМ NaCl, 5% глицерина, и 3,5 мкл инкубировали на медной решетке с угольным покрытием с тлеющим разрядом в течение 20 секунд перед блоттингом, удаляя жидкость с помощью куска фильтровальной бумаги Whatman №1. Через несколько секунд после удаления образца капля пятна 3,5 мкл (2% масс./об. уранилформиата) была отложена и немедленно подвергнута блоттингу, а затем был проведен второй цикл окрашивания/блоттинга.
Спектрополяриметрия кругового дихроизма (КД)
[00136] Спектры КД белков F (0,5 мг мл-1) регистрировали на спектрополяриметре Chirascan (Applied Photophysics) в диапазоне длин волн от 195 до 260 нм при ширине полосы 1 нм, размере шага 0,5 нм и 1 с на шаг. Спектры в далекой ультрафиолетовой области требовали в среднем трех сканирований и вычитались из холостых спектров, выполненных с буфером. Температурную денатурацию контролировали, выполняя сканирование с интервалом в 1°C после уравновешивания в течение 1 мин при каждой температуре. Данные были подогнаны к простой кривой первого порядка. Значения ΔA222 представлены на оси y как процент от значений, зарегистрированных при 20°C.
Иммуноферментный анализ (ELISA)
[00137] Для тестирования специфического связывания антитела или сывороток, 96-луночные MaxiSorp планшеты (Nunc) покрывали серийными разведениями супернатантов культуры тканей из клеток, экспрессирующих тримерные строительные блоки, содержащие F белки и тримерный домен сборки, или 2 мкг мл-1 следующих очищенных белков: Ds-Cav1 с фолдоном, Ds-Cav1, слитый с тримерным первым полипептидом, или наноструктуры, экспонирующие DS-Cav1. Планшеты блокировали 1% бычьим сывороточным альбумином (BSA) и инкубировали с титрованными антителами (D25, MPE8, паливизумаб, RSD5) или мышиной сывороткой, а затем с AP-конъюгированными козьими антителами к IgG человека (Southern Biotech, 2040-04) или козьими антителами к IgG мыши (Southern Biotech, 1030-04). Затем планшеты промывали буфером PBS (Gibco, Invitrogen), добавляли 0,05% Твин-20 и субстрат (p-NPP, Sigma), и планшеты считывали при 405 нм.
Поверхностный плазмонный резонанс (ППР)
[00138] Эксперименты проводили при 25°C на приборе ProteON XPR-36 (Bio-Rad Laboratories) в буфере PBS (Gibco, Invitrogen), 0,05% Твин-20. MAb D25 иммобилизовали на поверхности сенсорного чипа GLM посредством аминового связывания при 1000 единиц отклика (RU), и пустую поверхность без белка создавали в идентичных условиях связывания для использования в качестве сравнения. Моноклональные антитела (D25, MPE8, паливизумаб и 131-2a) вводили со скоростью 100 мкл/мин при концентрациях 50 нМ в различных каналах сенсора. Данные обрабатывали с помощью программного обеспечения Proteon и подвергали двойной проверке путем вычитания пустой поверхности и инъекции только буфера перед локальной подгонкой данных.
Вакцинация и серологический анализ
[00139] Самки мышей BALB/c в возрасте 6-9 недель были получены от Harlan Laboratories Inc. Все процедуры выполняли в соответствии с руководящими принципами Швейцарского федерального ветеринарного управления и после получения местного этического разрешения. Мышей иммунизировали внутрибрюшинно 100 мкл состава иммуногена на 0, 14 и 28 день. Прайминговую инфекцию в день 0 проводили агонистом лиганда TLR9 мыши (ODN 1668, InvivoGen). У мышей брали кровь на 10, 20 и 40 день, и титры антиген- и сайт-специфичных IgG измеряли в сыворотке с помощью ELISA. Нейтрализующие титры также определяли на клетках HEp-2, как описано ниже.
Анализ нейтрализации вирусов и микроскопический анализ
[00140] Сливающиеся слои клеток HEp-2 в 96-луночных планшетах с плоским дном инфицировали фиксированным количеством респираторно-синцитиального вируса человека с зеленым флуоресцентным белком (штамм RSV A2, Vira Tree # R121) при MOI 1. Через 48 часов после инфицирования клетки окрашивали Hoechst (Sigma # H6024) и получали изображения с помощью системы биовизуализации BD Pathway. Процент инфицированных клеток автоматически рассчитывали в программе BD AttoVision. Число инфицированных клеток наносили на график в виде кривых зависимости отклика от дозы путем нанесения относительного количества инфицированных клеток в зависимости от разведений антител.
Стабильность наноструктур, несущих DS-Cav1
[00141] Физическую стабильность конформации до слияния сконструированного белка DS-Cav1-фолдон-I53-50 оценивали путем инкубации белка при различных концентрациях в блоке для ПЦР с обогерваемой крышкой при 80°C в течение 1 часа. Остаточную конформацию перед слиянием оценивали путем прямого покрытия белка и ELISA со специфическим для предварительного слияния антителом D25.
Статистический анализ
[00142] Никакие статистические методы не использовались для предварительного определения размера выборки. Данные анализировали с помощью Prism 6 (программное обеспечение GraphPad) с использованием двустороннего непараметрического U-критерия Манна-Уитни при сравнении двух групп или теста Краскалла-Уоллиса (и посттеста Данна) при сравнении трех или более групп.
9.1.3. Результаты
Тримерные строительные блоки, содержащие белок F и тримерный домен сборки
[00143] Было обнаружено, что несколько тримерных строительных блоков, каждый из которых содержит белок F, генетически слитый с тримерным сборочным доменом, секретируются из клеток HEK293F с их белками F в хорошо свернутой конформации перед слиянием, о чем судили по связыванию специфичных для конформации перед слиянием моноклональных антител в анализах ELISA. На Фиг. 2 показан пример данных ELISA при анализе супернатанта клеток HEK293F, экспрессирующих DS-Cav1-фолдон, DS-Cav1-фолдон-T33-31A и DS-Cav1-T33-31A. Несколько других тримерных строительных блоков давали детектируемую секрецию хорошо свернутых, в конформации перед слиянием, F-белков.
Экспрессия и очистка DS-Cav1-фолдон-I53-50A
[00144] Лентивирусный вектор, кодирующий DS-Cav1-фолдон-I53-50A, использовали для трансдукции клеток HEK293F для крупномасштабной экспрессии. Секретируемый белок очищали из супернатантов тканевых культур с помощью аффинной хроматографии с иммобилизованным металлом и эксклюзионной хроматографии. Эксклюзионная хроматограмма (фиг. 3) показала, что очищенный белок образовывал один монодисперсный вид.
Экспрессия и очистка I53-50B.4PT1
[00145] I53-50B.4PT1, пентамерный белок, содержащий второй домен сборки, который взаимодействует с тримерным доменом сборки в I53-50A или DS-Cav1-фолдон-I53-50A, для управления сборкой наноструктур на основе икосаэдра I53-50, очищали, как описано в Bale et al. и в патентной публикации US 20160122392 A1.
Сборка in vitro и характеристика наноструктур I53-50, несущих DS-Cav1
[00146] I53-50 представляет собой двухкомпонентную наноструктуру из 120 субъединиц с икосаэдрической симметрией, включающую 20 тримерных (I53-50A) и 12 пентамерных (I53-50B) строительных блоков, как недавно описано Bale et al. N-конец I53-50A обнажен на внешней стороне наноструктуры I53-50, что делает возможным экспонирование антигенов на внешней стороне наноструктуры посредством генетического слияния с N-концом I53-530A. Очищенные DS-Cav1-фолдон-I53-50A и I53-50B.4PT1 были собраны in vitro с образованием икосаэдрических наноструктур из 120 субъединиц, демонстрирующих различные количества DS-Cav1 на внешней стороне наноструктуры, путем смешивания двух очищенных белков в различных молярных соотношениях. В отдельных препаратах наноструктуры, экспонирующие DS-Cav1 с валентностями 100% (20 тримеров), 66% (~14 тримеров) и 33% (~7 тримеров), получали, как описано выше. Виды, присутствующие в реакциях сборки in vitro после инкубации в течение ночи, оценивали с помощью нескольких методик, включая эксклюзионную хроматографию - многоугловое рассеяние света (SEC-MALS), динамическое рассеяние света и УФ/видимую спектроскопию. Собранные 120-субъединичные наноструктуры очищали в реакциях сборки in vitro с использованием эксклюзионной хроматографии (пример хроматограммы, полученной с использованием наноструктур со 100% валентностью, представлен на фиг. 4). Очищенные наноструктуры характеризовали с помощью электронной микроскопии с негативным окрашиванием, которая выявила поля монодиперсных частиц, в которых DS-Cav1 был четко виден в виде шипов, выступающих наружу из ядра икосаэдрической сборки I53-50 (представлен пример микрофотографии, полученной с использованием частиц со 100% валентностью на фиг. 5). Анализы ELISA с использованием моноклональных антител, специфичных к конформации перед слиянием, подтвердили, что DS-Cav1, экспонируемый таким образом на внешней стороне наноструктуры, был хорошо сложен и антигенно не затронут (фиг. 6). Эксперименты по поверхностному плазмонному резонансу, оценивающие кинетику связывания моноклональных антител, показали, что диссоциация антитела из наноструктур DS-Cav1-фолдон-I53-50 со 100% валентностью происходила медленнее, чем из тримеров DS-Cav1-фолдон, вероятно, из-за эффектов авидности, происходящих от поливалентного представления DS-Cav1 на внешней стороне наноструктуры (фиг. 6). Вместе указанные эксперименты подтвердили, что наноструктуры DS-Cav1-фолдон-I53-50 образуют монодисперсные икосаэдрические наноструктуры, которые демонстрируют хорошо свернутые, антигенно не затронутые тримеры DS-Cav1 на своей внешней стороне. Эти данные побудили к проведению экспериментов по оценке применимости наноструктур DS-Cav1-фолдон-I53-50 в качестве иммуногенов для индукции гуморальных иммунных ответов против DS-Cav1 у животных.
Иммуногенность наноструктур DS-Cav1-фолдон-I53-50
[00147] Наноструктуры DS-Cav1-фолдон-I53-50, демонстрирующие DS-Cav1 с валентностью 33%, 66% и 100%, вводили мышам с использованием стратегии первичного бустинга, как описано выше. Дополнительным группам мышей вводили тримерный DS-Cav1-фолдон в качестве эталона для гуморального иммунного ответа, индуцированного против DS-Cav1 наноструктурами или наноструктурами I53-50, в которых отсутствует экспонируемый DS-Cav1 в качестве отрицательного контроля для специфического отклика DS-Cav1. ELISA-анализы сыворотки, выделенной у мышей в определенные моменты времени после инъекций, использовали для измерения титров специфических антител к DS-Cav1, присутствующих в сыворотках получивших инъекции животных (фиг. 7). Как и ожидалось, сыворотка от животных, которым инъецировали наноструктуры I53-50 без экспонируемого DS-Cav1, не содержала антител, специфичных к DS-Cav1. Тримерный DS-Cav1-фолдон индуцировал DS-Cav1-специфические антитела в соответствии с предыдущими результатами (McClellan et al.). Все наноструктуры DS-Cav1 с валентностью 33%, 66% и 100% индуцировали более высокие титры антител к DS-Cav1, чем тримерный DS-Cav1-фолдон, причем титры антител возрастали с увеличением валентности DS-Cav1. Титры, специфичные для DS-Cav1, были в среднем примерно в 2,5 раза выше у мышей, которым вводили наноструктуры DS-Cav1-фолдон-I53-50 со 100% валентностью, по сравнению с DS-Cav1. Полученные результаты демонстрируют, что иммуногены, в которых белки парамиксовируса F мультивалентно экспонируются на самособирающихся белковых наноструктурах, могут вызывать более высокие гуморальные иммунные ответы при введении животным.
[00148] Сыворотки мышей, которым инъецировали серию иммуногенов, описанных выше, также оценивали на присутствие титров нейтрализующих антител с использованием стандартного анализа нейтрализации в клетках HEp-2 (фиг. 8). Тенденция титров сывороточных нейтрализующих антител сильно коррелировала с тенденцией, наблюдаемой в титрах антител, специфичных к DS-Cav1. Сыворотки животных, которым инъецировали наноструктуры I53-50 без экспонируемого DS-Cav1, не нейтрализовали вирус, что согласуется с отсутствием в этих сыворотках антител, специфичных к DS-Cav1. Сыворотки животных, которым вводили тримерный DS-Cav-l-фолдон, нейтрализовывали вирус со средним титром (1/ID50) 3030. Наноструктуры DS-Cav1-I53-50 с валентностью 33%, 66% и 100% индуцировали более высокие титры нейтрализующих антител, чем тримерный DS-Cav1-фолдон, со средними титрами 9400, 20 000 и 30 500 соответственно. Эти результаты демонстрируют, что более высокий ответ, вызванный иммуногенами, в которых белки парамиксовируса F мультивалентно экспонированы на самособирающихся белковых наноструктурах, приводит к более эффективной нейтрализации вируса.
Физическая стабилизация DS-Cav1 путем слияния с I53-50A
[00149] Учитывая ключевые антигенные свойства белка F перед слиянием, мы использовали два ортогональных подхода для измерения физической стабильности DS-Cav1 при слиянии с I53-50A и/или при дальнейшей сборке в икосаэдрическую наноструктуру. В первом тесте измеряли сохранение связывания со специфичным для конформации перед слиянием mAb (D25), после термического стресса, подход, который ранее использовался для характеристики стабильности белка F перед слиянием (McLellan et al.2013; Joyce et al.2016; Krarup et al. 2015). Образцы наноструктур тримерного DS-Cav1, тримерного DS-Cav1-I53-50A и DS-Cav1-I53-50, содержащих эквивалентные концентрации (50 нМ) DS-Cav1, были разделены на четыре аликвоты и инкубированы при 20, 50, 70 или 80°C в течение 1 часа. После охлаждения до комнатной температуры связывание D25 анализировали с помощью поверхностного плазмонного резонанса (ППР). Было обнаружено, что все образцы связывали D25 эквивалентно при 20 и 50°C, но теряли большую часть своей реактивности к D25 через 1 час при 80°C, как ранее сообщалось для DS-Cav1 (McLellan et al. 2013; Joyce et al. 2016) (Фиг. 10). Интересно, что хотя D25 также не мог связывать тримерный DS-Cav1, инкубированный при 70°C в течение 1 часа, тримерные DS-Cav1-I53-50A и наноструктуры DS-Cav1-I53-50 сохраняли 50 и 80% своих соответствующих сигналов связывания (Фиг. 10). Хотя поливалентная природа наноструктур DS-Cav1 - I53-50 затрудняет прямое количественное сравнение с тримерным DS-Cav1, эти результаты показывают, что генетическое слияние с тримером I53-50A дополнительно стабилизирует конформацию перед слиянием DS-Cav1, и предполагают, что это повышенная стабильность сохраняется в контексте собранной наноструктуры иммуногена.
[00150] В качестве второго, независимого от антител метода для оценки физической стабильности, использовали химическую денатурацию в гидрохлориде гуанидина (GdnHCl), контролируемую по собственной флуоресценции триптофана. Анализ испускания флуоресценции DS-Cav1, инкубированного в 0-6,5 М GdnHCl, показал, что белок претерпевает два слегка различных перехода: один между 0,25 и 2,25 М GdnHCl, а другой - между 2,25 и 5,75 М (фиг. 11A-11J). Напротив, для тримерного DS-Cav1 - I53-50A очевиден только один переход, происходящий между 2,25 и 6,25 М GdnHCl (фиг. 11A-11J). В настоящее время неясно, отсутствует ли переход при более низком [GdnHCl] для DS-Cav1 в тримерном DS-Cav1-I53-50A или просто сдвинут на более высокий [GdnHCl]. Однако очевидно, что нативная конформация DS-Cav1 стабилизируется генетическим слиянием с тримером I53-50A, что соответствует результатам, полученным при измерении связывания D25 после термического стресса. Сравнение данных для наноструктуры DS-Cav1 - I53-50 и одной наноструктуры I53-50 (без слитого DS-Cav1) показало, что стабилизация сохраняется при сборке с икосаэдрической наноструктурой (Фиг. 11A-11J). Источником этого эффекта, вероятно, является чрезвычайная стабильность тримера I53-50A. I53-50A происходит от альдолазы KDPG гипертермофильной бактерии T. maritima и начинает проявлять изменения флуоресценции только при очень высоких (≥5,75 M) концентрациях GdnHCl (фиг. 11A-11J).
[00151] Были получены дополнительные конструкции для оценки количества повторов GS и необходимости в стабилизационном домене, таком как фрагмент фолдон.
[00152] Информация о последовательности
> RSV_F-10 (SEQ ID NO: 108)
QNITEEFYQSTCSAVSKGYLSALRTGWYTSVITIELSNIKENKCNGTDAKVKLIKQELDKYKNAVTELQLLMQSTPATNNRARRFLGFLLGVGSAIASGVAVCKVLHLEGEVNKIKSALLSTNKAVVSLSNGVSVLTFKVLDLKNYIDKQLLPILNKQSCSISNIETVIEFQQKNNRLLEITREFSVNAGVTTPVSTYMLTNSELLSLINDMPITNDQKKLMSNNVQIVRQQSYSIMCIIKEEVLAYVVQLPLYGVIDTPCWKLHTSPLCTTNTKEGSNICLTRTDRGWYCDNAGSVSFFPQAETCKVQSNRVFCDTMNSLTLPSEVNLCNVDIFNPKYDCKIMTSKTDVSSSVITSLGAIVSCYGKTKCTASNKNRGIIKTFSNGCDYVSNKGVDTVSVGNTLYYVNKQEGKSLYVKGEPIINFYDPLVFPSDEFDASISQVNEKINQSLAFIRGSGGSGSGEKAAKAEEAARKMEELFKKHKIVAVLRANSVEEAIEKAVAVFAGGVHLIEITFTVPDADTVIKALSVLKEKGAIIGAGTVTSVEQCRKAVESGAEFIVSPHLDEEISQFCKEKGVFYMPGVMTPTELVKAMKLGHTILKLFPGEVVGPQFVKAMKGPFPNVKFVPTGGVNLDNVCEWFKAGVLAVGVGSALVKGTPDEVREKAKAFVEKIRGCTE
> RSV_F-11 (SEQ ID NO: 109)
QNITEEFYQSTCSAVSKGYLSALRTGWYTSVITIELSNIKENKCNGTDAKVKLIKQELDKYKNAVTELQLLMQSTPATNNRARRFLGFLLGVGSAIASGVAVCKVLHLEGEVNKIKSALLSTNKAVVSLSNGVSVLTFKVLDLKNYIDKQLLPILNKQSCSISNIETVIEFQQKNNRLLEITREFSVNAGVTTPVSTYMLTNSELLSLINDMPITNDQKKLMSNNVQIVRQQSYSIMCIIKEEVLAYVVQLPLYGVIDTPCWKLHTSPLCTTNTKEGSNICLTRTDRGWYCDNAGSVSFFPQAETCKVQSNRVFCDTMNSLTLPSEVNLCNVDIFNPKYDCKIMTSKTDVSSSVITSLGAIVSCYGKTKCTASNKNRGIIKTFSNGCDYVSNKGVDTVSVGNTLYYVNKQEGKSLYVKGEPIINFYDPLVFPSDEFDASISQVNEKINQSLAFIRGSGGSGSGSGGSEKAAKAEEAARKMEELFKKHKIVAVLRANSVEEAIEKAVAVFAGGVHLIEITFTVPDADTVIKALSVLKEKGAIIGAGTVTSVEQCRKAVESGAEFIVSPHLDEEISQFCKEKGVFYMPGVMTPTELVKAMKLGHTILKLFPGEVVGPQFVKAMKGPFPNVKFVPTGGVNLDNVCEWFKAGVLAVGVGSALVKGTPDEVREKAKAFVEKIRGCTE
> RSV_F-12 (SEQ ID NO: 110)
QNITEEFYQSTCSAVSKGYLSALRTGWYTSVITIELSNIKENKCNGTDAKVKLIKQELDKYKNAVTELQLLMQSTPATNNRARRFLGFLLGVGSAIASGVAVCKVLHLEGEVNKIKSALLSTNKAVVSLSNGVSVLTFKVLDLKNYIDKQLLPILNKQSCSISNIETVIEFQQKNNRLLEITREFSVNAGVTTPVSTYMLTNSELLSLINDMPITNDQKKLMSNNVQIVRQQSYSIMCIIKEEVLAYVVQLPLYGVIDTPCWKLHTSPLCTTNTKEGSNICLTRTDRGWYCDNAGSVSFFPQAETCKVQSNRVFCDTMNSLTLPSEVNLCNVDIFNPKYDCKIMTSKTDVSSSVITSLGAIVSCYGKTKCTASNKNRGIIKTFSNGCDYVSNKGVDTVSVGNTLYYVNKQEGKSLYVKGEPIINFYDPLVFPSDEFDASISQVNEKINQSLAFIRGSGGSGSGSGGSGSGGEKAAKAEEAARKMEELFKKHKIVAVLRANSVEEAIEKAVAVFAGGVHLIEITFTVPDADTVIKALSVLKEKGAIIGAGTVTSVEQCRKAVESGAEFIVSPHLDEEISQFCKEKGVFYMPGVMTPTELVKAMKLGHTILKLFPGEVVGPQFVKAMKGPFPNVKFVPTGGVNLDNVCEWFKAGVLAVGVGSALVKGTPDEVREKAKAFVEKIRGCTE
> RSV_F-13 (SEQ ID NO: 111)
QNITEEFYQSTCSAVSKGYLSALRTGWYTSVITIELSNIKENKCNGTDAKVKLIKQELDKYKNAVTELQLLMQSTPATNNRARRFLGFLLGVGSAIASGVAVCKVLHLEGEVNKIKSALLSTNKAVVSLSNGVSVLTFKVLDLKNYIDKQLLPILNKQSCSISNIETVIEFQQKNNRLLEITREFSVNAGVTTPVSTYMLTNSELLSLINDMPITNDQKKLMSNNVQIVRQQSYSIMCIIKEEVLAYVVQLPLYGVIDTPCWKLHTSPLCTTNTKEGSNICLTRTDRGWYCDNAGSVSFFPQAETCKVQSNRVFCDTMNSLTLPSEVNLCNVDIFNPKYDCKIMTSKTDVSSSVITSLGAIVSCYGKTKCTASNKNRGIIKTFSNGCDYVSNKGVDTVSVGNTLYYVNKQEGKSLYVKGEPIINFYDPLVFPSDEFDASISQVNEKINQSLAFIRGSGGSGSGSGEKAAKAEEAARKMEELFKKHKIVAVLRANSVEEAIEKAVAVFAGGVHLIEITFTVPDADTVIKALSVLKEKGAIIGAGTVTSVEQCRKAVESGAEFIVSPHLDEEISQFCKEKGVFYMPGVMTPTELVKAMKLGHTILKLFPGEVVGPQFVKAMKGPFPNVKFVPTGGVNLDNVCEWFKAGVLAVGVGSALVKGTPDEVREKAKAFVEKIRGCTE
> RSV_F-14 (SEQ ID NO: 112)
QNITEEFYQSTCSAVSKGYLSALRTGWYTSVITIELSNIKENKCNGTDAKVKLIKQELDKYKNAVTELQLLMQSTPATNNRARRFLGFLLGVGSAIASGVAVCKVLHLEGEVNKIKSALLSTNKAVVSLSNGVSVLTFKVLDLKNYIDKQLLPILNKQSCSISNIETVIEFQQKNNRLLEITREFSVNAGVTTPVSTYMLTNSELLSLINDMPITNDQKKLMSNNVQIVRQQSYSIMCIIKEEVLAYVVQLPLYGVIDTPCWKLHTSPLCTTNTKEGSNICLTRTDRGWYCDNAGSVSFFPQAETCKVQSNRVFCDTMNSLTLPSEVNLCNVDIFNPKYDCKIMTSKTDVSSSVITSLGAIVSCYGKTKCTASNKNRGIIKTFSNGCDYVSNKGVDTVSVGNTLYYVNKQEGKSLYVKGEPIINFYDPLVFPSDEFDASISQVNEKINQSLAFIRGYIPEAPRDGQAYVRKDGEWVLLSTFLGSGGSGSGSGGSGSGEKAAKAEEAARKMEELFKKHKIVAVLRANSVEEAIEKAVAVFAGGVHLIEITFTVPDADTVIKALSVLKEKGAIIGAGTVTSVEQCRKAVESGAEFIVSPHLDEEISQFCKEKGVFYMPGVMTPTELVKAMKLGHTILKLFPGEVVGPQFVKAMKGPFPNVKFVPTGGVNLDNVCEWFKAGVLAVGVGSALVKGTPDEVREKAKAFVEKIRGCTE
> RSV_F-15 (SEQ ID NO: 113)
QNITEEFYQSTCSAVSKGYLSALRTGWYTSVITIELSNIKENKCNGTDAKVKLIKQELDKYKNAVTELQLLMQSTPATNNRARRFLGFLLGVGSAIASGVAVCKVLHLEGEVNKIKSALLSTNKAVVSLSNGVSVLTFKVLDLKNYIDKQLLPILNKQSCSISNIETVIEFQQKNNRLLEITREFSVNAGVTTPVSTYMLTNSELLSLINDMPITNDQKKLMSNNVQIVRQQSYSIMCIIKEEVLAYVVQLPLYGVIDTPCWKLHTSPLCTTNTKEGSNICLTRTDRGWYCDNAGSVSFFPQAETCKVQSNRVFCDTMNSLTLPSEVNLCNVDIFNPKYDCKIMTSKTDVSSSVITSLGAIVSCYGKTKCTASNKNRGIIKTFSNGCDYVSNKGVDTVSVGNTLYYVNKQEGKSLYVKGEPIINFYDPLVFPSDEFDASISQVNEKINQSLAFIRGYIPEAPRDGQAYVRKDGEWVLLSTFLGSGGSGSGSGGSGSGGSSGSEKAAKAEEAARKMEELFKKHKIVAVLRANSVEEAIEKAVAVFAGGVHLIEITFTVPDADTVIKALSVLKEKGAIIGAGTVTSVEQCRKAVESGAEFIVSPHLDEEISQFCKEKGVFYMPGVMTPTELVKAMKLGHTILKLFPGEVVGPQFVKAMKGPFPNVKFVPTGGVNLDNVCEWFKAGVLAVGVGSALVKGTPDEVREKAKAFVEKIRGCTE
[00153] Исследования были основаны на выходе экспрессии при небольшой временной трансфекции. Плазмиды, способные экспрессировать соответствующие конструкции, трансформировали в клетки NEB 5α E.coli и отбирали на чашках с агаром LB + карбенициллин. 1 мл культур получали инокуляцией TB-среды бактериальной колонией и повторным отбором при 50 мкг/мл карбенициллина. Набор Qiagen Mini Prep использовали для очистки плазмиды от культур E. coli в соответствии с протоколом производителя. Клетки Expi293F™ (ThermoFisher) культивировали в экспрессионной среде Expi293™ (ThermoFisher) с добавлением пенициллина (100 ед./мл) и стрептомицина (100 мкг/мл) при 8% CO2, 37°C и встряхивании 125 об./мин.
[00154] За день до трансфекции клетки высевали с концентрацией 2E6 клеток/мл. В день трансфекции клетки подсчитывали на приборе Countess II (ThermoFisher) с трипановым синим для определения жизнеспособности клеток. Концентрацию клеток доводили до 2,5E6 клеток/мл, и клетки помещали в необработанные 12-луночные планшеты (Corning) в объемах 1 мл. 1 мкг плазмиды ДНК трансфицировали на каждую лунку, используя Expifectamine™ (ThermoFisher), следуя инструкциям производителя. Энхансеры, компоненты набора для трансфекции Expifectamine™ компании ThermoFisher, добавляли через 18 часов после трансфекции. Культуры объемом 1 мл собирали через 5 дней после трансфекции, и клетки осаждали из супернатанта центрифугированием при 1500 g в течение 5 минут при 4°C. Супернатанты фильтровали через фильтр 0,45 мкМ с мембраной ПВДФ.
[00155] Отфильтрованные супернатанты, содержащие конструкции DS-Cav1 - I53-50A, денатурировали и кипятили в течение 10 минут при 95°C в течение 10 минут в 2-кратном буфере Лэммли с 2-меркаптоэтанолом. При помощи SDS-PAGE разделяли фракции образца, которые затем переносили на нитроцеллюлозную мембрану и зондировали паливизумабом, а затем вторичным антителом человека, конъюгированным с HRP. Блот был визуализирован с использованием субстрата для блоттинга Clarity Western ECL (Bio-Rad).
[00156] Отфильтрованные супернатанты, содержащие конструкции DS-Cav1 - I53-50A, связывали с 96-луночными планшетами Nunc MaxiSorp в серии двукратных разведений. Специфическое к конформации перед слиянием антитело D25 использовали для обнаружения DS-Cav1-I53-50A, а затем вторичное антитело человека, конъюгированное с HRP. Выход белка определяли колориметрически через субстрат ТМВ, и оптическую плотность регистрировали при 450 нм.
[00157] Выходы экспрессии и связывание mAb D25, специфичного для предварительного слияния (данные не показаны), указывают на то, что все конструкции хорошо экспрессируются и находятся в конформации до слияния. Как известно специалистам в данной области, гетерологичный домен тримеризации (например, фолдон) обычно требуется для правильной экспрессии и укладки в конформации перед слиянием F-конструкций. Полученные результаты показывают, что компонент наноструктуры I53-50A может поддерживать экспрессию и правильную укладку DS-Cav1 без использования домена тримеризации, такого как фолдон. Связывание D25 с этими конструкциями предполагает, что они антигенно интактны и, как ожидается, будут вызывать сильные иммунные ответы, включая нейтрализующие антитела, аналогично наноструктурам, содержащим слитый полипептид DS-Cav1-фолдон-I53-50.
9.2. Пример 2: Цитомегаловирус (ЦМВ)
[00158] Белковые вакцины против ЦМВ описаны, например, в патентной публикации США № US 2016/0159864 A1 и US 2017/0369532 A1; Международной патентной публикации № WO 2016/092460 A3; и Kirchmeier al. Экспрессия оболочечной вирусоподобной частицы антигена гликопротеина B цитомегаловируса человека индуцирует антитела с сильной и широкой нейтрализующей активностью. Clin Vaccine Immunol. 2014; 21 (2): 174-80. Гомотримерный комплекс gB, тримерный комплекс gH/gL/gO или пентамерный комплекс gH/gL/pUL128/pUL130/pUL131A считаются тремя основными мишенями для вакцинации против ЦМВ.
[00159] Первая из этих мишеней, gB, образует тримерную структуру, которая включает несколько гидрофобных поверхностей. С-конец внеклеточного домена gB расположен проксимальнее трансмембранной области и лежит около оси 3 порядка молекулы. См. Chandramouli et al. Structure of HCMV glycoprotein B in the postfusion conformation bound to a neutralizing human antibody (Структура гликопротеина B HCMV в конформации после слияния, связанного с нейтрализующим антителом человека). Nat Commun. 2015 Sep 14; 6: 8176. За счет замены линкера трансмембранной области gB белок gB ЦМВ на N-конце связывается с наноструктурой, имеющей свободный N-конец на или около оси 3 порядка наноструктуры. Полученная наноструктура имеет на своей поверхности 20 копий тримера gB и эффективно вызывает иммунный ответ на gB ЦМВ. Мутации в белке gB, описанные в публикации международного патента № WO 2016/092460 A3, улучшают растворимость и иммуногенность вакцины на основе наноструктур.
[00160] Вторая из этих мишеней, тримерный комплекс gH/gL/gO, и третья из этих мишеней, пентамерный gH/gL/pUL128/pUL130/pUL131A, образуются в результате взаимоисключающих взаимодействий гликопротеинов оболочки gH/gL с gO или pUL128/pUL130/pUL131A. См. Ciferri et al. Structural and biochemical studies of HCMV gH/gL/gO and Pentamer reveal mutually exclusive cell entry complexes. Proc. Natl. Acad. Sci. U.S.A. 112, 1767-1772 (2015). Компонент gH нацелен на антитела, нейтрализующие инфекцию как фибробластов, так и эндотелиальных/эпителиальных клеток. Область UL содержит сайты связывания для потенциально нейтрализующих антител инфекции эпителиальных и эндотелиальных клеток.
[00161] Компонент gH экспрессируется в виде слияния гена с наноструктурным полипептидом, и совместно экспрессируются либо gL/gO, либо gL/pUL128/pUL130/pUL131A. Экспрессированные белки самоорганизуются в вакцины на основе наноструктур gH/gL/gO или gH/gL/pUL128/pUL130/pUL131A соответственно. Экспрессию и правильную укладку наноструктуры оценивают путем связывания антитела MSL-109 или его Fab-фрагмента с наноструктурой. Правильную укладку и антигенность пентамерного комплекса оценивают с использованием антител и Fab-фрагментов, описанных в Chandramouli et al. Structural basis for potent antibody-mediated neutralization of human cytomegalovirus (Структурная основа мощной опосредованной антителами нейтрализации цитомегаловируса человека) Sci. Immunol. 2, eaan1457 (2017).
9.3. Пример 3: вирус Эпштейна-Барра (ВЭБ)
[00162] Вирус Эпштейна-Барра (ВЭБ) представляет собой серьезную глобальную проблему здравоохранения. Хотя указанный вирус связан с инфекционным мононуклеозом и ~200000 раковых заболеваний ежегодно во всем мире, вакцина отсутствует. Основной мишенью иммунитета является гликопротеин ВЭБ 350/220 (gp350), который опосредует присоединение к В-клеткам через рецептор комплемента 2 (CR2/CD21). См. Kanekiyo et al. Rational Design of an Epstein-Barr Virus Vaccine Targeting the Receptor-Binding Site. (Рациональный дизайн вакцины против вируса Эпштейна-Барра, нацеленной на центр связывания с рецептором) Cell 162(5): 1090-1100 (2015). Эктодомен gp350 или фрагмент D123 gp350 экспрессируется в виде слияния гена с полипептидами наноструктуры в виде N-концевого или C-концевого слияния. Полученные в результате слияния генов экспрессируются, собираются и превращаются в вакцины на основе наноструктур. Антигенность определяют с использованием моноклональных антител 72A1 и 2L10.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> University of Washington
King, Neil
Baker, David
Stewart, Lance
<120> САМОCОБИРАЮЩИЕСЯ НАНОСТРУКТУРНЫЕ ВАКЦИНЫ
<130> ICVX-001/02WO 333041-2012
<150> US 62/724,721
<151> 2018-08-30
<150> US 62/636,757
<151> 2018-02-28
<160> 113
<170> PatentIn, версия 3.5
<210> 1
<211> 207
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 1
Met Glu Gly Met Asp Pro Leu Ala Val Leu Ala Glu Ser Arg Leu Leu
1 5 10 15
Pro Leu Leu Thr Val Arg Gly Gly Glu Asp Leu Ala Gly Leu Ala Thr
20 25 30
Val Leu Glu Leu Met Gly Val Gly Ala Leu Glu Ile Thr Leu Arg Thr
35 40 45
Glu Lys Gly Leu Glu Ala Leu Lys Ala Leu Arg Lys Ser Gly Leu Leu
50 55 60
Leu Gly Ala Gly Thr Val Arg Ser Pro Lys Glu Ala Glu Ala Ala Leu
65 70 75 80
Glu Ala Gly Ala Ala Phe Leu Val Ser Pro Gly Leu Leu Glu Glu Val
85 90 95
Ala Ala Leu Ala Gln Ala Arg Gly Val Pro Tyr Leu Pro Gly Val Leu
100 105 110
Thr Pro Thr Glu Val Glu Arg Ala Leu Ala Leu Gly Leu Ser Ala Leu
115 120 125
Lys Phe Phe Pro Ala Glu Pro Phe Gln Gly Val Arg Val Leu Arg Ala
130 135 140
Tyr Ala Glu Val Phe Pro Glu Val Arg Phe Leu Pro Thr Gly Gly Ile
145 150 155 160
Lys Glu Glu His Leu Pro His Tyr Ala Ala Leu Pro Asn Leu Leu Ala
165 170 175
Val Gly Gly Ser Trp Leu Leu Gln Gly Asp Leu Ala Ala Val Met Lys
180 185 190
Lys Val Lys Ala Ala Lys Ala Leu Leu Ser Pro Gln Ala Pro Gly
195 200 205
<210> 2
<211> 156
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 2
Met Thr Lys Lys Val Gly Ile Val Asp Thr Thr Phe Ala Arg Val Asp
1 5 10 15
Met Ala Glu Ala Ala Ile Arg Thr Leu Lys Ala Leu Ser Pro Asn Ile
20 25 30
Lys Ile Ile Arg Lys Thr Val Pro Gly Ile Lys Asp Leu Pro Val Ala
35 40 45
Cys Lys Lys Leu Leu Glu Glu Glu Gly Cys Asp Ile Val Met Ala Leu
50 55 60
Gly Met Pro Gly Lys Ala Glu Lys Asp Lys Val Cys Ala His Glu Ala
65 70 75 80
Ser Leu Gly Leu Met Leu Ala Gln Leu Met Thr Asn Lys His Ile Ile
85 90 95
Glu Val Phe Val His Glu Asp Glu Ala Lys Asp Asp Asp Glu Leu Asp
100 105 110
Ile Leu Ala Leu Val Arg Ala Ile Glu His Ala Ala Asn Val Tyr Tyr
115 120 125
Leu Leu Phe Lys Pro Glu Tyr Leu Thr Arg Met Ala Gly Lys Gly Leu
130 135 140
Arg Gln Gly Arg Glu Asp Ala Gly Pro Ala Arg Glu
145 150 155
<210> 3
<211> 156
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 3
Met Thr Lys Lys Val Gly Ile Val Asp Thr Thr Phe Ala Arg Val Asp
1 5 10 15
Met Ala Ser Ala Ala Ile Leu Thr Leu Lys Met Glu Ser Pro Asn Ile
20 25 30
Lys Ile Ile Arg Lys Thr Val Pro Gly Ile Lys Asp Leu Pro Val Ala
35 40 45
Cys Lys Lys Leu Leu Glu Glu Glu Gly Cys Asp Ile Val Met Ala Leu
50 55 60
Gly Met Pro Gly Lys Ala Glu Lys Asp Lys Val Cys Ala His Glu Ala
65 70 75 80
Ser Leu Gly Leu Met Leu Ala Gln Leu Met Thr Asn Lys His Ile Ile
85 90 95
Glu Val Phe Val His Glu Asp Glu Ala Lys Asp Asp Ala Glu Leu Lys
100 105 110
Ile Leu Ala Ala Arg Arg Ala Ile Glu His Ala Leu Asn Val Tyr Tyr
115 120 125
Leu Leu Phe Lys Pro Glu Tyr Leu Thr Arg Met Ala Gly Lys Gly Leu
130 135 140
Arg Gln Gly Phe Glu Asp Ala Gly Pro Ala Arg Glu
145 150 155
<210> 4
<211> 209
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 4
Met Ser Thr Ile Asn Asn Gln Leu Lys Ala Leu Lys Val Ile Pro Val
1 5 10 15
Ile Ala Ile Asp Asn Ala Glu Asp Ile Ile Pro Leu Gly Lys Val Leu
20 25 30
Ala Glu Asn Gly Leu Pro Ala Ala Glu Ile Thr Phe Arg Ser Ser Ala
35 40 45
Ala Val Lys Ala Ile Met Leu Leu Arg Ser Ala Gln Pro Glu Met Leu
50 55 60
Ile Gly Ala Gly Thr Ile Leu Asn Gly Val Gln Ala Leu Ala Ala Lys
65 70 75 80
Glu Ala Gly Ala Thr Phe Val Val Ser Pro Gly Phe Asn Pro Asn Thr
85 90 95
Val Arg Ala Cys Gln Ile Ile Gly Ile Asp Ile Val Pro Gly Val Asn
100 105 110
Asn Pro Ser Thr Val Glu Ala Ala Leu Glu Met Gly Leu Thr Thr Leu
115 120 125
Lys Phe Phe Pro Ala Glu Ala Ser Gly Gly Ile Ser Met Val Lys Ser
130 135 140
Leu Val Gly Pro Tyr Gly Asp Ile Arg Leu Met Pro Thr Gly Gly Ile
145 150 155 160
Thr Pro Ser Asn Ile Asp Asn Tyr Leu Ala Ile Pro Gln Val Leu Ala
165 170 175
Cys Gly Gly Thr Trp Met Val Asp Lys Lys Leu Val Thr Asn Gly Glu
180 185 190
Trp Asp Glu Ile Ala Arg Leu Thr Arg Glu Ile Val Glu Gln Val Asn
195 200 205
Pro
<210> 5
<211> 114
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 5
Met Pro Ile Phe Thr Leu Asn Thr Asn Ile Lys Ala Thr Asp Val Pro
1 5 10 15
Ser Asp Phe Leu Ser Leu Thr Ser Arg Leu Val Gly Leu Ile Leu Ser
20 25 30
Lys Pro Gly Ser Tyr Val Ala Val His Ile Asn Thr Asp Gln Gln Leu
35 40 45
Ser Phe Gly Gly Ser Thr Asn Pro Ala Ala Phe Gly Thr Leu Met Ser
50 55 60
Ile Gly Gly Ile Glu Pro Ser Lys Asn Arg Asp His Ser Ala Val Leu
65 70 75 80
Phe Asp His Leu Asn Ala Met Leu Gly Ile Pro Lys Asn Arg Met Tyr
85 90 95
Ile His Phe Val Asn Leu Asn Gly Asp Asp Val Gly Trp Asn Gly Thr
100 105 110
Thr Phe
<210> 6
<211> 157
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 6
Met Asn Gln His Ser His Lys Asp Tyr Glu Thr Val Arg Ile Ala Val
1 5 10 15
Val Arg Ala Arg Trp His Ala Asp Ile Val Asp Ala Cys Val Glu Ala
20 25 30
Phe Glu Ile Ala Met Ala Ala Ile Gly Gly Asp Arg Phe Ala Val Asp
35 40 45
Val Phe Asp Val Pro Gly Ala Tyr Glu Ile Pro Leu His Ala Arg Thr
50 55 60
Leu Ala Glu Thr Gly Arg Tyr Gly Ala Val Leu Gly Thr Ala Phe Val
65 70 75 80
Val Asn Gly Gly Ile Tyr Arg His Glu Phe Val Ala Ser Ala Val Ile
85 90 95
Asp Gly Met Met Asn Val Gln Leu Ser Thr Gly Val Pro Val Leu Ser
100 105 110
Ala Val Leu Thr Pro His Arg Tyr Arg Asp Ser Ala Glu His His Arg
115 120 125
Phe Phe Ala Ala His Phe Ala Val Lys Gly Val Glu Ala Ala Arg Ala
130 135 140
Cys Ile Glu Ile Leu Ala Ala Arg Glu Lys Ile Ala Ala
145 150 155
<210> 7
<211> 205
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 7
Met Lys Met Glu Glu Leu Phe Lys Lys His Lys Ile Val Ala Val Leu
1 5 10 15
Arg Ala Asn Ser Val Glu Glu Ala Ile Glu Lys Ala Val Ala Val Phe
20 25 30
Ala Gly Gly Val His Leu Ile Glu Ile Thr Phe Thr Val Pro Asp Ala
35 40 45
Asp Thr Val Ile Lys Ala Leu Ser Val Leu Lys Glu Lys Gly Ala Ile
50 55 60
Ile Gly Ala Gly Thr Val Thr Ser Val Glu Gln Cys Arg Lys Ala Val
65 70 75 80
Glu Ser Gly Ala Glu Phe Ile Val Ser Pro His Leu Asp Glu Glu Ile
85 90 95
Ser Gln Phe Cys Lys Glu Lys Gly Val Phe Tyr Met Pro Gly Val Met
100 105 110
Thr Pro Thr Glu Leu Val Lys Ala Met Lys Leu Gly His Thr Ile Leu
115 120 125
Lys Leu Phe Pro Gly Glu Val Val Gly Pro Gln Phe Val Lys Ala Met
130 135 140
Lys Gly Pro Phe Pro Asn Val Lys Phe Val Pro Thr Gly Gly Val Asn
145 150 155 160
Leu Asp Asn Val Cys Glu Trp Phe Lys Ala Gly Val Leu Ala Val Gly
165 170 175
Val Gly Ser Ala Leu Val Lys Gly Thr Pro Asp Glu Val Arg Glu Lys
180 185 190
Ala Lys Ala Phe Val Glu Lys Ile Arg Gly Cys Thr Glu
195 200 205
<210> 8
<211> 157
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 8
Met Asn Gln His Ser His Lys Asp Tyr Glu Thr Val Arg Ile Ala Val
1 5 10 15
Val Arg Ala Arg Trp His Ala Glu Ile Val Asp Ala Cys Val Ser Ala
20 25 30
Phe Glu Ala Ala Met Ala Asp Ile Gly Gly Asp Arg Phe Ala Val Asp
35 40 45
Val Phe Asp Val Pro Gly Ala Tyr Glu Ile Pro Leu His Ala Arg Thr
50 55 60
Leu Ala Glu Thr Gly Arg Tyr Gly Ala Val Leu Gly Thr Ala Phe Val
65 70 75 80
Val Asn Gly Gly Ile Tyr Arg His Glu Phe Val Ala Ser Ala Val Ile
85 90 95
Asp Gly Met Met Asn Val Gln Leu Ser Thr Gly Val Pro Val Leu Ser
100 105 110
Ala Val Leu Thr Pro His Arg Tyr Arg Asp Ser Asp Ala His Thr Leu
115 120 125
Leu Phe Leu Ala Leu Phe Ala Val Lys Gly Met Glu Ala Ala Arg Ala
130 135 140
Cys Val Glu Ile Leu Ala Ala Arg Glu Lys Ile Ala Ala
145 150 155
<210> 9
<211> 177
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 9
Met Phe Thr Lys Ser Gly Asp Asp Gly Asn Thr Asn Val Ile Asn Lys
1 5 10 15
Arg Val Gly Lys Asp Ser Pro Leu Val Asn Phe Leu Gly Asp Leu Asp
20 25 30
Glu Leu Asn Ser Phe Ile Gly Phe Ala Ile Ser Lys Ile Pro Trp Glu
35 40 45
Asp Met Lys Lys Asp Leu Glu Arg Val Gln Val Glu Leu Phe Glu Ile
50 55 60
Gly Glu Asp Leu Ser Thr Gln Ser Ser Lys Lys Lys Ile Asp Glu Ser
65 70 75 80
Tyr Val Leu Trp Leu Leu Ala Ala Thr Ala Ile Tyr Arg Ile Glu Ser
85 90 95
Gly Pro Val Lys Leu Phe Val Ile Pro Gly Gly Ser Glu Glu Ala Ser
100 105 110
Val Leu His Val Thr Arg Ser Val Ala Arg Arg Val Glu Arg Asn Ala
115 120 125
Val Lys Tyr Thr Lys Glu Leu Pro Glu Ile Asn Arg Met Ile Ile Val
130 135 140
Tyr Leu Asn Arg Leu Ser Ser Leu Leu Phe Ala Met Ala Leu Val Ala
145 150 155 160
Asn Lys Arg Arg Asn Gln Ser Glu Lys Ile Tyr Glu Ile Gly Lys Ser
165 170 175
Trp
<210> 10
<211> 157
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 10
Met Asn Gln His Ser His Lys Asp Tyr Glu Thr Val Arg Ile Ala Val
1 5 10 15
Val Arg Ala Arg Trp His Ala Asp Ile Val Asp Gln Cys Val Arg Ala
20 25 30
Phe Glu Glu Ala Met Ala Asp Ala Gly Gly Asp Arg Phe Ala Val Asp
35 40 45
Val Phe Asp Val Pro Gly Ala Tyr Glu Ile Pro Leu His Ala Arg Thr
50 55 60
Leu Ala Glu Thr Gly Arg Tyr Gly Ala Val Leu Gly Thr Ala Phe Val
65 70 75 80
Val Asn Gly Gly Ile Tyr Arg His Glu Phe Val Ala Ser Ala Val Ile
85 90 95
Asp Gly Met Met Asn Val Gln Leu Ser Thr Gly Val Pro Val Leu Ser
100 105 110
Ala Val Leu Thr Pro His Arg Tyr Arg Ser Ser Arg Glu His His Glu
115 120 125
Phe Phe Arg Glu His Phe Met Val Lys Gly Val Glu Ala Ala Ala Ala
130 135 140
Cys Ile Thr Ile Leu Ala Ala Arg Glu Lys Ile Ala Ala
145 150 155
<210> 11
<211> 201
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 11
Met Gly His Thr Lys Gly Pro Thr Pro Gln Gln His Asp Gly Ser Ala
1 5 10 15
Leu Arg Ile Gly Ile Val His Ala Arg Trp Asn Lys Thr Ile Ile Met
20 25 30
Pro Leu Leu Ile Gly Thr Ile Ala Lys Leu Leu Glu Cys Gly Val Lys
35 40 45
Ala Ser Asn Ile Val Val Gln Ser Val Pro Gly Ser Trp Glu Leu Pro
50 55 60
Ile Ala Val Gln Arg Leu Tyr Ser Ala Ser Gln Leu Gln Thr Pro Ser
65 70 75 80
Ser Gly Pro Ser Leu Ser Ala Gly Asp Leu Leu Gly Ser Ser Thr Thr
85 90 95
Asp Leu Thr Ala Leu Pro Thr Thr Thr Ala Ser Ser Thr Gly Pro Phe
100 105 110
Asp Ala Leu Ile Ala Ile Gly Val Leu Ile Lys Gly Glu Thr Met His
115 120 125
Phe Glu Tyr Ile Ala Asp Ser Val Ser His Gly Leu Met Arg Val Gln
130 135 140
Leu Asp Thr Gly Val Pro Val Ile Phe Gly Val Leu Thr Val Leu Thr
145 150 155 160
Asp Asp Gln Ala Lys Ala Arg Ala Gly Val Ile Glu Gly Ser His Asn
165 170 175
His Gly Glu Asp Trp Gly Leu Ala Ala Val Glu Met Gly Val Arg Arg
180 185 190
Arg Asp Trp Ala Ala Gly Lys Thr Glu
195 200
<210> 12
<211> 237
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 12
Met Tyr Glu Val Asp His Ala Asp Val Tyr Asp Leu Phe Tyr Leu Gly
1 5 10 15
Arg Gly Lys Asp Tyr Ala Ala Glu Ala Ser Asp Ile Ala Asp Leu Val
20 25 30
Arg Ser Arg Thr Pro Glu Ala Ser Ser Leu Leu Asp Val Ala Cys Gly
35 40 45
Thr Gly Thr His Leu Glu His Phe Thr Lys Glu Phe Gly Asp Thr Ala
50 55 60
Gly Leu Glu Leu Ser Glu Asp Met Leu Thr His Ala Arg Lys Arg Leu
65 70 75 80
Pro Asp Ala Thr Leu His Gln Gly Asp Met Arg Asp Phe Gln Leu Gly
85 90 95
Arg Lys Phe Ser Ala Val Val Ser Met Phe Ser Ser Val Gly Tyr Leu
100 105 110
Lys Thr Val Ala Glu Leu Gly Ala Ala Val Ala Ser Phe Ala Glu His
115 120 125
Leu Glu Pro Gly Gly Val Val Val Val Glu Pro Trp Trp Phe Pro Glu
130 135 140
Thr Phe Ala Asp Gly Trp Val Ser Ala Asp Val Val Arg Arg Asp Gly
145 150 155 160
Arg Thr Val Ala Arg Val Ser His Ser Val Arg Glu Gly Asn Ala Thr
165 170 175
Arg Met Glu Val His Phe Thr Val Ala Asp Pro Gly Lys Gly Val Arg
180 185 190
His Phe Ser Asp Val His Leu Ile Thr Leu Phe His Gln Arg Glu Tyr
195 200 205
Glu Ala Ala Phe Met Ala Ala Gly Leu Arg Val Glu Tyr Leu Glu Gly
210 215 220
Gly Pro Ser Gly Arg Gly Leu Phe Val Gly Val Pro Ala
225 230 235
<210> 13
<211> 138
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 13
Met Gly Met Lys Glu Lys Phe Val Leu Ile Ile Thr His Gly Asp Phe
1 5 10 15
Gly Lys Gly Leu Leu Ser Gly Ala Glu Val Ile Ile Gly Lys Gln Glu
20 25 30
Asn Val His Thr Val Gly Leu Asn Leu Gly Asp Asn Ile Glu Lys Val
35 40 45
Ala Lys Glu Val Met Arg Ile Ile Ile Ala Lys Leu Ala Glu Asp Lys
50 55 60
Glu Ile Ile Ile Val Val Asp Leu Phe Gly Gly Ser Pro Phe Asn Ile
65 70 75 80
Ala Leu Glu Met Met Lys Thr Phe Asp Val Lys Val Ile Thr Gly Ile
85 90 95
Asn Met Pro Met Leu Val Glu Leu Leu Thr Ser Ile Asn Val Tyr Asp
100 105 110
Thr Thr Glu Leu Leu Glu Asn Ile Ser Lys Ile Gly Lys Asp Gly Ile
115 120 125
Lys Val Ile Glu Lys Ser Ser Leu Lys Met
130 135
<210> 14
<211> 154
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 14
Met Lys Tyr Asp Gly Ser Lys Leu Arg Ile Gly Ile Leu His Ala Arg
1 5 10 15
Trp Asn Leu Glu Ile Ile Ala Ala Leu Val Ala Gly Ala Ile Lys Arg
20 25 30
Leu Gln Glu Phe Gly Val Lys Ala Glu Asn Ile Ile Ile Glu Thr Val
35 40 45
Pro Gly Ser Phe Glu Leu Pro Tyr Gly Ser Lys Leu Phe Val Glu Lys
50 55 60
Gln Lys Arg Leu Gly Lys Pro Leu Asp Ala Ile Ile Pro Ile Gly Val
65 70 75 80
Leu Ile Lys Gly Ser Thr Met His Phe Glu Tyr Ile Cys Asp Ser Thr
85 90 95
Thr His Gln Leu Met Lys Leu Asn Phe Glu Leu Gly Ile Pro Val Ile
100 105 110
Phe Gly Val Leu Thr Cys Leu Thr Asp Glu Gln Ala Glu Ala Arg Ala
115 120 125
Gly Leu Ile Glu Gly Lys Met His Asn His Gly Glu Asp Trp Gly Ala
130 135 140
Ala Ala Val Glu Met Ala Thr Lys Phe Asn
145 150
<210> 15
<211> 164
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 15
Met Ala Val Lys Gly Leu Gly Glu Val Asp Gln Lys Tyr Asp Gly Ser
1 5 10 15
Lys Leu Arg Ile Gly Ile Leu His Ala Arg Trp Asn Arg Lys Ile Ile
20 25 30
Leu Ala Leu Val Ala Gly Ala Val Leu Arg Leu Leu Glu Phe Gly Val
35 40 45
Lys Ala Glu Asn Ile Ile Ile Glu Thr Val Pro Gly Ser Phe Glu Leu
50 55 60
Pro Tyr Gly Ser Lys Leu Phe Val Glu Lys Gln Lys Arg Leu Gly Lys
65 70 75 80
Pro Leu Asp Ala Ile Ile Pro Ile Gly Val Leu Ile Lys Gly Ser Thr
85 90 95
Met His Phe Glu Tyr Ile Cys Asp Ser Thr Thr His Gln Leu Met Lys
100 105 110
Leu Asn Phe Glu Leu Gly Ile Pro Val Ile Phe Gly Val Leu Thr Cys
115 120 125
Leu Thr Asp Glu Gln Ala Glu Ala Arg Ala Gly Leu Ile Glu Gly Lys
130 135 140
Met His Asn His Gly Glu Asp Trp Gly Ala Ala Ala Val Glu Met Ala
145 150 155 160
Thr Lys Phe Asn
<210> 16
<211> 175
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 16
Met Gly Ala Asn Trp Tyr Leu Asp Asn Glu Ser Ser Arg Leu Ser Phe
1 5 10 15
Thr Ser Thr Lys Asn Ala Asp Ile Ala Glu Val His Arg Phe Leu Val
20 25 30
Leu His Gly Lys Val Asp Pro Lys Gly Leu Ala Glu Val Glu Val Glu
35 40 45
Thr Glu Ser Ile Ser Thr Gly Ile Pro Leu Arg Asp Met Leu Leu Arg
50 55 60
Val Leu Val Phe Gln Val Ser Lys Phe Pro Val Ala Gln Ile Asn Ala
65 70 75 80
Gln Leu Asp Met Arg Pro Ile Asn Asn Leu Ala Pro Gly Ala Gln Leu
85 90 95
Glu Leu Arg Leu Pro Leu Thr Val Ser Leu Arg Gly Lys Ser His Ser
100 105 110
Tyr Asn Ala Glu Leu Leu Ala Thr Arg Leu Asp Glu Arg Arg Phe Gln
115 120 125
Val Val Thr Leu Glu Pro Leu Val Ile His Ala Gln Asp Phe Asp Met
130 135 140
Val Arg Ala Phe Asn Ala Leu Arg Leu Val Ala Gly Leu Ser Ala Val
145 150 155 160
Ser Leu Ser Val Pro Val Gly Ala Val Leu Ile Phe Thr Ala Arg
165 170 175
<210> 17
<211> 208
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 17
Met Thr Asp Tyr Ile Arg Asp Gly Ser Ala Ile Lys Ala Leu Ser Phe
1 5 10 15
Ala Ile Ile Leu Ala Glu Ala Asp Leu Arg His Ile Pro Gln Asp Leu
20 25 30
Gln Arg Leu Ala Val Arg Val Ile His Ala Cys Gly Met Val Asp Val
35 40 45
Ala Asn Asp Leu Ala Phe Ser Glu Gly Ala Gly Lys Ala Gly Arg Asn
50 55 60
Ala Leu Leu Ala Gly Ala Pro Ile Leu Cys Asp Ala Arg Met Val Ala
65 70 75 80
Glu Gly Ile Thr Arg Ser Arg Leu Pro Ala Asp Asn Arg Val Ile Tyr
85 90 95
Thr Leu Ser Asp Pro Ser Val Pro Glu Leu Ala Lys Lys Ile Gly Asn
100 105 110
Thr Arg Ser Ala Ala Ala Leu Asp Leu Trp Leu Pro His Ile Glu Gly
115 120 125
Ser Ile Val Ala Ile Gly Asn Ala Pro Thr Ala Leu Phe Arg Leu Phe
130 135 140
Glu Leu Leu Asp Ala Gly Ala Pro Lys Pro Ala Leu Ile Ile Gly Met
145 150 155 160
Pro Val Gly Phe Val Gly Ala Ala Glu Ser Lys Asp Glu Leu Ala Ala
165 170 175
Asn Ser Arg Gly Val Pro Tyr Val Ile Val Arg Gly Arg Arg Gly Gly
180 185 190
Ser Ala Met Thr Ala Ala Ala Val Asn Ala Leu Ala Ser Glu Arg Glu
195 200 205
<210> 18
<211> 128
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 18
Met Ile Thr Val Phe Gly Leu Lys Ser Lys Leu Ala Pro Arg Arg Glu
1 5 10 15
Lys Leu Ala Glu Val Ile Tyr Ser Ser Leu His Leu Gly Leu Asp Ile
20 25 30
Pro Lys Gly Lys His Ala Ile Arg Phe Leu Cys Leu Glu Lys Glu Asp
35 40 45
Phe Tyr Tyr Pro Phe Asp Arg Ser Asp Asp Tyr Thr Val Ile Glu Ile
50 55 60
Asn Leu Met Ala Gly Arg Ser Glu Glu Thr Lys Met Leu Leu Ile Phe
65 70 75 80
Leu Leu Phe Ile Ala Leu Glu Arg Lys Leu Gly Ile Arg Ala His Asp
85 90 95
Val Glu Ile Thr Ile Lys Glu Gln Pro Ala His Cys Trp Gly Phe Arg
100 105 110
Gly Arg Thr Gly Asp Ser Ala Arg Asp Leu Asp Tyr Asp Ile Tyr Val
115 120 125
<210> 19
<211> 235
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 19
Met Gly Ser Asp Leu Gln Lys Leu Gln Arg Phe Ser Thr Cys Asp Ile
1 5 10 15
Ser Asp Gly Leu Leu Asn Val Tyr Asn Ile Pro Thr Gly Gly Tyr Phe
20 25 30
Pro Asn Leu Thr Ala Ile Ser Pro Pro Gln Asn Ser Ser Ile Val Gly
35 40 45
Thr Ala Tyr Thr Val Leu Phe Ala Pro Ile Asp Asp Pro Arg Pro Ala
50 55 60
Val Asn Tyr Ile Asp Ser Val Pro Pro Asn Ser Ile Leu Val Leu Ala
65 70 75 80
Leu Glu Pro His Leu Gln Ser Gln Phe His Pro Phe Ile Lys Ile Thr
85 90 95
Gln Ala Met Tyr Gly Gly Leu Met Ser Thr Arg Ala Gln Tyr Leu Lys
100 105 110
Ser Asn Gly Thr Val Val Phe Gly Arg Ile Arg Asp Val Asp Glu His
115 120 125
Arg Thr Leu Asn His Pro Val Phe Ala Tyr Gly Val Gly Ser Cys Ala
130 135 140
Pro Lys Ala Val Val Lys Ala Val Gly Thr Asn Val Gln Leu Lys Ile
145 150 155 160
Leu Thr Ser Asp Gly Val Thr Gln Thr Ile Cys Pro Gly Asp Tyr Ile
165 170 175
Ala Gly Asp Asn Asn Gly Ile Val Arg Ile Pro Val Gln Glu Thr Asp
180 185 190
Ile Ser Lys Leu Val Thr Tyr Ile Glu Lys Ser Ile Glu Val Asp Arg
195 200 205
Leu Val Ser Glu Ala Ile Lys Asn Gly Leu Pro Ala Lys Ala Ala Gln
210 215 220
Thr Ala Arg Arg Met Val Leu Lys Asp Tyr Ile
225 230 235
<210> 20
<211> 162
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 20
Met Ser Gly Met Arg Val Tyr Leu Gly Ala Asp His Ala Gly Tyr Glu
1 5 10 15
Leu Lys Gln Ala Ile Ile Ala Phe Leu Lys Met Thr Gly His Glu Pro
20 25 30
Ile Asp Cys Gly Ala Leu Arg Tyr Asp Ala Asp Asp Asp Tyr Pro Ala
35 40 45
Phe Cys Ile Ala Ala Ala Thr Arg Thr Val Ala Asp Pro Gly Ser Leu
50 55 60
Gly Ile Val Leu Gly Gly Ser Gly Asn Gly Glu Gln Ile Ala Ala Asn
65 70 75 80
Lys Val Pro Gly Ala Arg Cys Ala Leu Ala Trp Ser Val Gln Thr Ala
85 90 95
Ala Leu Ala Arg Glu His Asn Asn Ala Gln Leu Ile Gly Ile Gly Gly
100 105 110
Arg Met His Thr Leu Glu Glu Ala Leu Arg Ile Val Lys Ala Phe Val
115 120 125
Thr Thr Pro Trp Ser Lys Ala Gln Arg His Gln Arg Arg Ile Asp Ile
130 135 140
Leu Ala Glu Tyr Glu Arg Thr His Glu Ala Pro Pro Val Pro Gly Ala
145 150 155 160
Pro Ala
<210> 21
<211> 157
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 21
Met Gly Asp Asp Ala Arg Ile Ala Ala Ile Gly Asp Val Asp Glu Leu
1 5 10 15
Asn Ser Gln Ile Gly Val Leu Leu Ala Glu Pro Leu Pro Asp Asp Val
20 25 30
Arg Ala Ala Leu Ser Ala Ile Gln His Asp Leu Phe Asp Leu Gly Gly
35 40 45
Glu Leu Cys Ile Pro Gly His Ala Ala Ile Thr Glu Asp His Leu Leu
50 55 60
Arg Leu Ala Leu Trp Leu Val His Tyr Asn Gly Gln Leu Pro Pro Leu
65 70 75 80
Glu Glu Phe Ile Leu Pro Gly Gly Ala Arg Gly Ala Ala Leu Ala His
85 90 95
Val Cys Arg Thr Val Cys Arg Arg Ala Glu Arg Ser Ile Lys Ala Leu
100 105 110
Gly Ala Ser Glu Pro Leu Asn Ile Ala Pro Ala Ala Tyr Val Asn Leu
115 120 125
Leu Ser Asp Leu Leu Phe Val Leu Ala Arg Val Leu Asn Arg Ala Ala
130 135 140
Gly Gly Ala Asp Val Leu Trp Asp Arg Thr Arg Ala His
145 150 155
<210> 22
<211> 157
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 22
Met Ile Leu Ser Ala Glu Gln Ser Phe Thr Leu Arg His Pro His Gly
1 5 10 15
Gln Ala Ala Ala Leu Ala Phe Val Arg Glu Pro Ala Ala Ala Leu Ala
20 25 30
Gly Val Gln Arg Leu Arg Gly Leu Asp Ser Asp Gly Glu Gln Val Trp
35 40 45
Gly Glu Leu Leu Val Arg Val Pro Leu Leu Gly Glu Val Asp Leu Pro
50 55 60
Phe Arg Ser Glu Ile Val Arg Thr Pro Gln Gly Ala Glu Leu Arg Pro
65 70 75 80
Leu Thr Leu Thr Gly Glu Arg Ala Trp Val Ala Val Ser Gly Gln Ala
85 90 95
Thr Ala Ala Glu Gly Gly Glu Met Ala Phe Ala Phe Gln Phe Gln Ala
100 105 110
His Leu Ala Thr Pro Glu Ala Glu Gly Glu Gly Gly Ala Ala Phe Glu
115 120 125
Val Met Val Gln Ala Ala Ala Gly Val Thr Leu Leu Leu Val Ala Met
130 135 140
Ala Leu Pro Gln Gly Leu Ala Ala Gly Leu Pro Pro Ala
145 150 155
<210> 23
<211> 156
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 23
Met Thr Lys Lys Val Gly Ile Val Asp Thr Thr Phe Ala Arg Val Asp
1 5 10 15
Met Ala Ser Ala Ala Ile Leu Thr Leu Lys Met Glu Ser Pro Asn Ile
20 25 30
Lys Ile Ile Arg Lys Thr Val Pro Gly Ile Lys Asp Leu Pro Val Ala
35 40 45
Cys Lys Lys Leu Leu Glu Glu Glu Gly Cys Asp Ile Val Met Ala Leu
50 55 60
Gly Met Pro Gly Lys Lys Glu Lys Asp Lys Val Cys Ala His Glu Ala
65 70 75 80
Ser Leu Gly Leu Met Leu Ala Gln Leu Met Thr Asn Lys His Ile Ile
85 90 95
Glu Val Phe Val His Glu Asp Glu Ala Lys Asp Asp Ala Glu Leu Lys
100 105 110
Ile Leu Ala Ala Arg Arg Ala Ile Glu His Ala Leu Asn Val Tyr Tyr
115 120 125
Leu Leu Phe Lys Pro Glu Tyr Leu Thr Arg Met Ala Gly Lys Gly Leu
130 135 140
Arg Gln Gly Phe Glu Asp Ala Gly Pro Ala Arg Glu
145 150 155
<210> 24
<211> 209
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 24
Met Asp Asp Ile Asn Asn Gln Leu Lys Arg Leu Lys Val Ile Pro Val
1 5 10 15
Ile Ala Ile Asp Asn Ala Glu Asp Ile Ile Pro Leu Gly Lys Val Leu
20 25 30
Ala Glu Asn Gly Leu Pro Ala Ala Glu Ile Thr Phe Arg Ser Ser Ala
35 40 45
Ala Val Lys Ala Ile Met Leu Leu Arg Ser Ala Gln Pro Glu Met Leu
50 55 60
Ile Gly Ala Gly Thr Ile Leu Asn Gly Val Gln Ala Leu Ala Ala Lys
65 70 75 80
Glu Ala Gly Ala Asp Phe Val Val Ser Pro Gly Phe Asn Pro Asn Thr
85 90 95
Val Arg Ala Cys Gln Ile Ile Gly Ile Asp Ile Val Pro Gly Val Asn
100 105 110
Asn Pro Ser Thr Val Glu Gln Ala Leu Glu Met Gly Leu Thr Thr Leu
115 120 125
Lys Phe Phe Pro Ala Glu Ala Ser Gly Gly Ile Ser Met Val Lys Ser
130 135 140
Leu Val Gly Pro Tyr Gly Asp Ile Arg Leu Met Pro Thr Gly Gly Ile
145 150 155 160
Thr Pro Asp Asn Ile Asp Asn Tyr Leu Ala Ile Pro Gln Val Leu Ala
165 170 175
Cys Gly Gly Thr Trp Met Val Asp Lys Lys Leu Val Arg Asn Gly Glu
180 185 190
Trp Asp Glu Ile Ala Arg Leu Thr Arg Glu Ile Val Glu Gln Val Asn
195 200 205
Pro
<210> 25
<211> 114
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 25
Met Pro Ile Phe Thr Leu Asn Thr Asn Ile Lys Ala Asp Asp Val Pro
1 5 10 15
Ser Asp Phe Leu Ser Leu Thr Ser Arg Leu Val Gly Leu Ile Leu Ser
20 25 30
Lys Pro Gly Ser Tyr Val Ala Val His Ile Asn Thr Asp Gln Gln Leu
35 40 45
Ser Phe Gly Gly Ser Thr Asn Pro Ala Ala Phe Gly Thr Leu Met Ser
50 55 60
Ile Gly Gly Ile Glu Pro Asp Lys Asn Arg Asp His Ser Ala Val Leu
65 70 75 80
Phe Asp His Leu Asn Ala Met Leu Gly Ile Pro Lys Asn Arg Met Tyr
85 90 95
Ile His Phe Val Asn Leu Asn Gly Asp Asp Val Gly Trp Asn Gly Thr
100 105 110
Thr Phe
<210> 26
<211> 114
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 26
Met Pro Ile Phe Thr Leu Asn Thr Asn Ile Lys Ala Asp Asp Val Pro
1 5 10 15
Ser Asp Phe Leu Ser Leu Thr Ser Arg Leu Val Gly Leu Ile Leu Ser
20 25 30
Glu Pro Gly Ser Tyr Val Ala Val His Ile Asn Thr Asp Gln Gln Leu
35 40 45
Ser Phe Gly Gly Ser Thr Asn Pro Ala Ala Phe Gly Thr Leu Met Ser
50 55 60
Ile Gly Gly Ile Glu Pro Asp Lys Asn Glu Asp His Ser Ala Val Leu
65 70 75 80
Phe Asp His Leu Asn Ala Met Leu Gly Ile Pro Lys Asn Arg Met Tyr
85 90 95
Ile His Phe Val Asp Leu Asp Gly Asp Asp Val Gly Trp Asn Gly Thr
100 105 110
Thr Phe
<210> 27
<211> 157
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 27
Met Asn Gln His Ser His Lys Asp His Glu Thr Val Arg Ile Ala Val
1 5 10 15
Val Arg Ala Arg Trp His Ala Asp Ile Val Asp Ala Cys Val Glu Ala
20 25 30
Phe Glu Ile Ala Met Ala Ala Ile Gly Gly Asp Arg Phe Ala Val Asp
35 40 45
Val Phe Asp Val Pro Gly Ala Tyr Glu Ile Pro Leu His Ala Arg Thr
50 55 60
Leu Ala Glu Thr Gly Arg Tyr Gly Ala Val Leu Gly Thr Ala Phe Val
65 70 75 80
Val Asn Gly Gly Ile Tyr Arg His Glu Phe Val Ala Ser Ala Val Ile
85 90 95
Asp Gly Met Met Asn Val Gln Leu Asp Thr Gly Val Pro Val Leu Ser
100 105 110
Ala Val Leu Thr Pro His Arg Tyr Arg Asp Ser Asp Glu His His Arg
115 120 125
Phe Phe Ala Ala His Phe Ala Val Lys Gly Val Glu Ala Ala Arg Ala
130 135 140
Cys Ile Glu Ile Leu Asn Ala Arg Glu Lys Ile Ala Ala
145 150 155
<210> 28
<211> 157
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 28
Met Asn Gln His Ser His Lys Asp His Glu Thr Val Arg Ile Ala Val
1 5 10 15
Val Arg Ala Arg Trp His Ala Asp Ile Val Asp Ala Cys Val Glu Ala
20 25 30
Phe Glu Ile Ala Met Ala Ala Ile Gly Gly Asp Arg Phe Ala Val Asp
35 40 45
Val Phe Asp Val Pro Gly Ala Tyr Glu Ile Pro Leu His Ala Arg Thr
50 55 60
Leu Ala Glu Thr Gly Arg Tyr Gly Ala Val Leu Gly Thr Ala Phe Val
65 70 75 80
Val Asp Gly Gly Ile Tyr Asp His Glu Phe Val Ala Ser Ala Val Ile
85 90 95
Asp Gly Met Met Asn Val Gln Leu Asp Thr Gly Val Pro Val Leu Ser
100 105 110
Ala Val Leu Thr Pro His Glu Tyr Glu Asp Ser Asp Glu Asp His Glu
115 120 125
Phe Phe Ala Ala His Phe Ala Val Lys Gly Val Glu Ala Ala Arg Ala
130 135 140
Cys Ile Glu Ile Leu Asn Ala Arg Glu Lys Ile Ala Ala
145 150 155
<210> 29
<211> 205
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 29
Met Lys Met Glu Glu Leu Phe Lys Lys His Lys Ile Val Ala Val Leu
1 5 10 15
Arg Ala Asn Ser Val Glu Glu Ala Ile Glu Lys Ala Val Ala Val Phe
20 25 30
Ala Gly Gly Val His Leu Ile Glu Ile Thr Phe Thr Val Pro Asp Ala
35 40 45
Asp Thr Val Ile Lys Ala Leu Ser Val Leu Lys Glu Lys Gly Ala Ile
50 55 60
Ile Gly Ala Gly Thr Val Thr Ser Val Glu Gln Cys Arg Lys Ala Val
65 70 75 80
Glu Ser Gly Ala Glu Phe Ile Val Ser Pro His Leu Asp Glu Glu Ile
85 90 95
Ser Gln Phe Cys Lys Glu Lys Gly Val Phe Tyr Met Pro Gly Val Met
100 105 110
Thr Pro Thr Glu Leu Val Lys Ala Met Lys Leu Gly His Asp Ile Leu
115 120 125
Lys Leu Phe Pro Gly Glu Val Val Gly Pro Gln Phe Val Lys Ala Met
130 135 140
Lys Gly Pro Phe Pro Asn Val Lys Phe Val Pro Thr Gly Gly Val Asn
145 150 155 160
Leu Asp Asn Val Cys Glu Trp Phe Lys Ala Gly Val Leu Ala Val Gly
165 170 175
Val Gly Asp Ala Leu Val Lys Gly Asp Pro Asp Glu Val Arg Glu Lys
180 185 190
Ala Lys Lys Phe Val Glu Lys Ile Arg Gly Cys Thr Glu
195 200 205
<210> 30
<211> 205
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 30
Met Lys Met Glu Glu Leu Phe Lys Lys His Lys Ile Val Ala Val Leu
1 5 10 15
Arg Ala Asn Ser Val Glu Glu Ala Ile Glu Lys Ala Val Ala Val Phe
20 25 30
Ala Gly Gly Val His Leu Ile Glu Ile Thr Phe Thr Val Pro Asp Ala
35 40 45
Asp Thr Val Ile Lys Ala Leu Ser Val Leu Lys Glu Lys Gly Ala Ile
50 55 60
Ile Gly Ala Gly Thr Val Thr Ser Val Glu Gln Cys Arg Lys Ala Val
65 70 75 80
Glu Ser Gly Ala Glu Phe Ile Val Ser Pro His Leu Asp Glu Glu Ile
85 90 95
Ser Gln Phe Cys Lys Glu Lys Gly Val Phe Tyr Met Pro Gly Val Met
100 105 110
Thr Pro Thr Glu Leu Val Lys Ala Met Lys Leu Gly His Asp Ile Leu
115 120 125
Lys Leu Phe Pro Gly Glu Val Val Gly Pro Glu Phe Val Glu Ala Met
130 135 140
Lys Gly Pro Phe Pro Asn Val Lys Phe Val Pro Thr Gly Gly Val Asp
145 150 155 160
Leu Asp Asp Val Cys Glu Trp Phe Asp Ala Gly Val Leu Ala Val Gly
165 170 175
Val Gly Asp Ala Leu Val Glu Gly Asp Pro Asp Glu Val Arg Glu Asp
180 185 190
Ala Lys Glu Phe Val Glu Glu Ile Arg Gly Cys Thr Glu
195 200 205
<210> 31
<211> 205
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 31
Met Lys Met Glu Glu Leu Phe Lys Lys His Lys Ile Val Ala Val Leu
1 5 10 15
Arg Ala Asn Ser Val Glu Glu Ala Ile Glu Lys Ala Val Ala Val Phe
20 25 30
Ala Gly Gly Val His Leu Ile Glu Ile Thr Phe Thr Val Pro Asp Ala
35 40 45
Asp Thr Val Ile Lys Ala Leu Ser Val Leu Lys Glu Lys Gly Ala Ile
50 55 60
Ile Gly Ala Gly Thr Val Thr Ser Val Glu Gln Cys Arg Lys Ala Val
65 70 75 80
Glu Ser Gly Ala Glu Phe Ile Val Ser Pro His Leu Asp Glu Glu Ile
85 90 95
Ser Gln Phe Cys Lys Glu Lys Gly Val Phe Tyr Met Pro Gly Val Met
100 105 110
Thr Pro Thr Glu Leu Val Lys Ala Met Lys Leu Gly His Asp Ile Leu
115 120 125
Lys Leu Phe Pro Gly Glu Val Val Gly Pro Gln Phe Val Lys Ala Met
130 135 140
Lys Gly Pro Phe Pro Asn Val Lys Phe Val Pro Thr Gly Gly Val Asn
145 150 155 160
Leu Asp Asn Val Cys Lys Trp Phe Lys Ala Gly Val Leu Ala Val Gly
165 170 175
Val Gly Lys Ala Leu Val Lys Gly Lys Pro Asp Glu Val Arg Glu Lys
180 185 190
Ala Lys Lys Phe Val Lys Lys Ile Arg Gly Cys Thr Glu
195 200 205
<210> 32
<211> 157
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 32
Met Asn Gln His Ser His Lys Asp His Glu Thr Val Arg Ile Ala Val
1 5 10 15
Val Arg Ala Arg Trp His Ala Glu Ile Val Asp Ala Cys Val Ser Ala
20 25 30
Phe Glu Ala Ala Met Arg Asp Ile Gly Gly Asp Arg Phe Ala Val Asp
35 40 45
Val Phe Asp Val Pro Gly Ala Tyr Glu Ile Pro Leu His Ala Arg Thr
50 55 60
Leu Ala Glu Thr Gly Arg Tyr Gly Ala Val Leu Gly Thr Ala Phe Val
65 70 75 80
Val Asn Gly Gly Ile Tyr Arg His Glu Phe Val Ala Ser Ala Val Ile
85 90 95
Asp Gly Met Met Asn Val Gln Leu Asp Thr Gly Val Pro Val Leu Ser
100 105 110
Ala Val Leu Thr Pro His Arg Tyr Arg Asp Ser Asp Ala His Thr Leu
115 120 125
Leu Phe Leu Ala Leu Phe Ala Val Lys Gly Met Glu Ala Ala Arg Ala
130 135 140
Cys Val Glu Ile Leu Ala Ala Arg Glu Lys Ile Ala Ala
145 150 155
<210> 33
<211> 157
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 33
Met Asn Gln His Ser His Lys Asp His Glu Thr Val Arg Ile Ala Val
1 5 10 15
Val Arg Ala Arg Trp His Ala Glu Ile Val Asp Ala Cys Val Ser Ala
20 25 30
Phe Glu Ala Ala Met Arg Asp Ile Gly Gly Asp Arg Phe Ala Val Asp
35 40 45
Val Phe Asp Val Pro Gly Ala Tyr Glu Ile Pro Leu His Ala Arg Thr
50 55 60
Leu Ala Glu Thr Gly Arg Tyr Gly Ala Val Leu Gly Thr Ala Phe Val
65 70 75 80
Val Asp Gly Gly Ile Tyr Asp His Glu Phe Val Ala Ser Ala Val Ile
85 90 95
Asp Gly Met Met Asn Val Gln Leu Asp Thr Gly Val Pro Val Leu Ser
100 105 110
Ala Val Leu Thr Pro His Glu Tyr Glu Asp Ser Asp Ala Asp Thr Leu
115 120 125
Leu Phe Leu Ala Leu Phe Ala Val Lys Gly Met Glu Ala Ala Arg Ala
130 135 140
Cys Val Glu Ile Leu Ala Ala Arg Glu Lys Ile Ala Ala
145 150 155
<210> 34
<211> 157
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 34
Met Asn Gln His Ser His Lys Asp His Glu Thr Val Arg Ile Ala Val
1 5 10 15
Val Arg Ala Arg Trp His Ala Glu Ile Val Asp Ala Cys Val Ser Ala
20 25 30
Phe Glu Ala Ala Met Arg Asp Ile Gly Gly Asp Arg Phe Ala Val Asp
35 40 45
Val Phe Asp Val Pro Gly Ala Tyr Glu Ile Pro Leu His Ala Arg Thr
50 55 60
Leu Ala Glu Thr Gly Arg Tyr Gly Ala Val Leu Gly Thr Ala Phe Val
65 70 75 80
Val Asn Gly Gly Ile Tyr Arg His Glu Phe Val Ala Ser Ala Val Ile
85 90 95
Asn Gly Met Met Asn Val Gln Leu Asn Thr Gly Val Pro Val Leu Ser
100 105 110
Ala Val Leu Thr Pro His Asn Tyr Asp Lys Ser Lys Ala His Thr Leu
115 120 125
Leu Phe Leu Ala Leu Phe Ala Val Lys Gly Met Glu Ala Ala Arg Ala
130 135 140
Cys Val Glu Ile Leu Ala Ala Arg Glu Lys Ile Ala Ala
145 150 155
<210> 35
<211> 156
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<220>
<221> разн_признаки
<222> (70)..(70)
<223> Xaa представляет собой Ala или Lys
<400> 35
Met Thr Lys Lys Val Gly Ile Val Asp Thr Thr Phe Ala Arg Val Asp
1 5 10 15
Met Ala Ser Ala Ala Ile Leu Thr Leu Lys Met Glu Ser Pro Asn Ile
20 25 30
Lys Ile Ile Arg Lys Thr Val Pro Gly Ile Lys Asp Leu Pro Val Ala
35 40 45
Cys Lys Lys Leu Leu Glu Glu Glu Gly Cys Asp Ile Val Met Ala Leu
50 55 60
Gly Met Pro Gly Lys Xaa Glu Lys Asp Lys Val Cys Ala His Glu Ala
65 70 75 80
Ser Leu Gly Leu Met Leu Ala Gln Leu Met Thr Asn Lys His Ile Ile
85 90 95
Glu Val Phe Val His Glu Asp Glu Ala Lys Asp Asp Ala Glu Leu Lys
100 105 110
Ile Leu Ala Ala Arg Arg Ala Ile Glu His Ala Leu Asn Val Tyr Tyr
115 120 125
Leu Leu Phe Lys Pro Glu Tyr Leu Thr Arg Met Ala Gly Lys Gly Leu
130 135 140
Arg Gln Gly Phe Glu Asp Ala Gly Pro Ala Arg Glu
145 150 155
<210> 36
<211> 209
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<220>
<221> разн_признаки
<222> (2)..(2)
<223> Xaa представляет собой Ser или Asp
<220>
<221> разн_признаки
<222> (3)..(3)
<223> Xaa представляет собой Thr или Asp
<220>
<221> разн_признаки
<222> (10)..(10)
<223> Xaa представляет собой Ala или Arg
<220>
<221> разн_признаки
<222> (85)..(85)
<223> Xaa представляет собой Thr или Asp
<220>
<221> разн_признаки
<222> (119)..(119)
<223> Xaa представляет собой Ala или Gln
<220>
<221> разн_признаки
<222> (163)..(163)
<223> Xaa представляет собой Ser или Asp
<220>
<221> разн_признаки
<222> (189)..(189)
<223> Xaa представляет собой Thr или Arg
<400> 36
Met Xaa Xaa Ile Asn Asn Gln Leu Lys Xaa Leu Lys Val Ile Pro Val
1 5 10 15
Ile Ala Ile Asp Asn Ala Glu Asp Ile Ile Pro Leu Gly Lys Val Leu
20 25 30
Ala Glu Asn Gly Leu Pro Ala Ala Glu Ile Thr Phe Arg Ser Ser Ala
35 40 45
Ala Val Lys Ala Ile Met Leu Leu Arg Ser Ala Gln Pro Glu Met Leu
50 55 60
Ile Gly Ala Gly Thr Ile Leu Asn Gly Val Gln Ala Leu Ala Ala Lys
65 70 75 80
Glu Ala Gly Ala Xaa Phe Val Val Ser Pro Gly Phe Asn Pro Asn Thr
85 90 95
Val Arg Ala Cys Gln Ile Ile Gly Ile Asp Ile Val Pro Gly Val Asn
100 105 110
Asn Pro Ser Thr Val Glu Xaa Ala Leu Glu Met Gly Leu Thr Thr Leu
115 120 125
Lys Phe Phe Pro Ala Glu Ala Ser Gly Gly Ile Ser Met Val Lys Ser
130 135 140
Leu Val Gly Pro Tyr Gly Asp Ile Arg Leu Met Pro Thr Gly Gly Ile
145 150 155 160
Thr Pro Xaa Asn Ile Asp Asn Tyr Leu Ala Ile Pro Gln Val Leu Ala
165 170 175
Cys Gly Gly Thr Trp Met Val Asp Lys Lys Leu Val Xaa Asn Gly Glu
180 185 190
Trp Asp Glu Ile Ala Arg Leu Thr Arg Glu Ile Val Glu Gln Val Asn
195 200 205
Pro
<210> 37
<211> 114
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<220>
<221> разн_признаки
<222> (13)..(13)
<223> Xaa представляет собой Thr или Asp
<220>
<221> разн_признаки
<222> (33)..(33)
<223> Xaa представляет собой Lys или Glu
<220>
<221> разн_признаки
<222> (71)..(71)
<223> Xaa представляет собой Ser или Asp
<220>
<221> разн_признаки
<222> (74)..(74)
<223> Xaa представляет собой Arg или Glu
<220>
<221> разн_признаки
<222> (101)..(101)
<223> Xaa представляет собой Asn или Asp
<220>
<221> разн_признаки
<222> (103)..(103)
<223> Xaa представляет собой Asn или Asp
<400> 37
Met Pro Ile Phe Thr Leu Asn Thr Asn Ile Lys Ala Xaa Asp Val Pro
1 5 10 15
Ser Asp Phe Leu Ser Leu Thr Ser Arg Leu Val Gly Leu Ile Leu Ser
20 25 30
Xaa Pro Gly Ser Tyr Val Ala Val His Ile Asn Thr Asp Gln Gln Leu
35 40 45
Ser Phe Gly Gly Ser Thr Asn Pro Ala Ala Phe Gly Thr Leu Met Ser
50 55 60
Ile Gly Gly Ile Glu Pro Xaa Lys Asn Xaa Asp His Ser Ala Val Leu
65 70 75 80
Phe Asp His Leu Asn Ala Met Leu Gly Ile Pro Lys Asn Arg Met Tyr
85 90 95
Ile His Phe Val Xaa Leu Xaa Gly Asp Asp Val Gly Trp Asn Gly Thr
100 105 110
Thr Phe
<210> 38
<211> 157
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<220>
<221> разн_признаки
<222> (9)..(9)
<223> Xaa представляет собой Tyr или His
<220>
<221> разн_признаки
<222> (82)..(82)
<223> Xaa представляет собой Asn или Asp
<220>
<221> разн_признаки
<222> (87)..(87)
<223> Xaa представляет собой Arg или Asp
<220>
<221> разн_признаки
<222> (105)..(105)
<223> Xaa представляет собой Ser или Asp
<220>
<221> разн_признаки
<222> (119)..(119)
<223> Xaa представляет собой Arg или Glu
<220>
<221> разн_признаки
<222> (121)..(121)
<223> Xaa представляет собой Arg или Glu
<220>
<221> разн_признаки
<222> (124)..(124)
<223> Xaa представляет собой Ala или Asp
<220>
<221> разн_признаки
<222> (126)..(126)
<223> Xaa представляет собой His или Asp
<220>
<221> разн_признаки
<222> (128)..(128)
<223> Xaa представляет собой Arg или Glu
<220>
<221> разн_признаки
<222> (150)..(150)
<223> Xaa представляет собой Ala или Asn
<400> 38
Met Asn Gln His Ser His Lys Asp Xaa Glu Thr Val Arg Ile Ala Val
1 5 10 15
Val Arg Ala Arg Trp His Ala Asp Ile Val Asp Ala Cys Val Glu Ala
20 25 30
Phe Glu Ile Ala Met Ala Ala Ile Gly Gly Asp Arg Phe Ala Val Asp
35 40 45
Val Phe Asp Val Pro Gly Ala Tyr Glu Ile Pro Leu His Ala Arg Thr
50 55 60
Leu Ala Glu Thr Gly Arg Tyr Gly Ala Val Leu Gly Thr Ala Phe Val
65 70 75 80
Val Xaa Gly Gly Ile Tyr Xaa His Glu Phe Val Ala Ser Ala Val Ile
85 90 95
Asp Gly Met Met Asn Val Gln Leu Xaa Thr Gly Val Pro Val Leu Ser
100 105 110
Ala Val Leu Thr Pro His Xaa Tyr Xaa Asp Ser Xaa Glu Xaa His Xaa
115 120 125
Phe Phe Ala Ala His Phe Ala Val Lys Gly Val Glu Ala Ala Arg Ala
130 135 140
Cys Ile Glu Ile Leu Xaa Ala Arg Glu Lys Ile Ala Ala
145 150 155
<210> 39
<211> 205
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<220>
<221> разн_признаки
<222> (126)..(126)
<223> Xaa представляет собой Thr или Asp
<220>
<221> разн_признаки
<222> (139)..(139)
<223> Xaa представляет собой Gln или Glu
<220>
<221> разн_признаки
<222> (142)..(142)
<223> Xaa представляет собой Lys или Glu
<220>
<221> разн_признаки
<222> (160)..(160)
<223> Xaa представляет собой Asn или Asp
<220>
<221> разн_признаки
<222> (163)..(163)
<223> Xaa представляет собой Asn или Asp
<220>
<221> разн_признаки
<222> (166)..(166)
<223> Xaa представляет собой Glu или Lys
<220>
<221> разн_признаки
<222> (169)..(169)
<223> Xaa представляет собой Lys или Asp
<220>
<221> разн_признаки
<222> (179)..(179)
<223> Xaa представляет собой Ser, Lys или Asp
<220>
<221> разн_признаки
<222> (183)..(183)
<223> Xaa представляет собой Lys или Glu
<220>
<221> разн_признаки
<222> (185)..(185)
<223> Xaa представляет собой Thr, Asp или Lys
<220>
<221> разн_признаки
<222> (192)..(192)
<223> Xaa представляет собой Lys или Asp
<220>
<221> разн_признаки
<222> (195)..(195)
<223> Xaa представляет собой Ala, Glu или Lys
<220>
<221> разн_признаки
<222> (198)..(198)
<223> Xaa представляет собой Glu или Lys
<220>
<221> разн_признаки
<222> (199)..(199)
<223> Xaa представляет собой Lys или Glu
<400> 39
Met Lys Met Glu Glu Leu Phe Lys Lys His Lys Ile Val Ala Val Leu
1 5 10 15
Arg Ala Asn Ser Val Glu Glu Ala Ile Glu Lys Ala Val Ala Val Phe
20 25 30
Ala Gly Gly Val His Leu Ile Glu Ile Thr Phe Thr Val Pro Asp Ala
35 40 45
Asp Thr Val Ile Lys Ala Leu Ser Val Leu Lys Glu Lys Gly Ala Ile
50 55 60
Ile Gly Ala Gly Thr Val Thr Ser Val Glu Gln Cys Arg Lys Ala Val
65 70 75 80
Glu Ser Gly Ala Glu Phe Ile Val Ser Pro His Leu Asp Glu Glu Ile
85 90 95
Ser Gln Phe Cys Lys Glu Lys Gly Val Phe Tyr Met Pro Gly Val Met
100 105 110
Thr Pro Thr Glu Leu Val Lys Ala Met Lys Leu Gly His Xaa Ile Leu
115 120 125
Lys Leu Phe Pro Gly Glu Val Val Gly Pro Xaa Phe Val Xaa Ala Met
130 135 140
Lys Gly Pro Phe Pro Asn Val Lys Phe Val Pro Thr Gly Gly Val Xaa
145 150 155 160
Leu Asp Xaa Val Cys Xaa Trp Phe Xaa Ala Gly Val Leu Ala Val Gly
165 170 175
Val Gly Xaa Ala Leu Val Xaa Gly Xaa Pro Asp Glu Val Arg Glu Xaa
180 185 190
Ala Lys Xaa Phe Val Xaa Xaa Ile Arg Gly Cys Thr Glu
195 200 205
<210> 40
<211> 157
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<220>
<221> разн_признаки
<222> (9)..(9)
<223> Xaa представляет собой Tyr или His
<220>
<221> разн_признаки
<222> (38)..(38)
<223> Xaa представляет собой Ala или Arg
<220>
<221> разн_признаки
<222> (82)..(82)
<223> Xaa представляет собой Asn или Asp
<220>
<221> разн_признаки
<222> (87)..(87)
<223> Xaa представляет собой Arg или Asp
<220>
<221> разн_признаки
<222> (97)..(97)
<223> Xaa представляет собой Asp или Asn
<220>
<221> разн_признаки
<222> (105)..(105)
<223> Xaa представляет собой Ser, Asp или Asn
<220>
<221> разн_признаки
<222> (119)..(119)
<223> Xaa представляет собой Arg, Glu или Asn
<220>
<221> разн_признаки
<222> (121)..(121)
<223> Xaa представляет собой Arg, Asp или Glu
<220>
<221> разн_признаки
<222> (122)..(122)
<223> Xaa представляет собой Asp или Lys
<220>
<221> разн_признаки
<222> (124)..(124)
<223> Xaa представляет собой Asp или Lys
<220>
<221> разн_признаки
<222> (126)..(126)
<223> Xaa представляет собой His или Asp
<400> 40
Met Asn Gln His Ser His Lys Asp Xaa Glu Thr Val Arg Ile Ala Val
1 5 10 15
Val Arg Ala Arg Trp His Ala Glu Ile Val Asp Ala Cys Val Ser Ala
20 25 30
Phe Glu Ala Ala Met Xaa Asp Ile Gly Gly Asp Arg Phe Ala Val Asp
35 40 45
Val Phe Asp Val Pro Gly Ala Tyr Glu Ile Pro Leu His Ala Arg Thr
50 55 60
Leu Ala Glu Thr Gly Arg Tyr Gly Ala Val Leu Gly Thr Ala Phe Val
65 70 75 80
Val Xaa Gly Gly Ile Tyr Xaa His Glu Phe Val Ala Ser Ala Val Ile
85 90 95
Xaa Gly Met Met Asn Val Gln Leu Xaa Thr Gly Val Pro Val Leu Ser
100 105 110
Ala Val Leu Thr Pro His Xaa Tyr Xaa Xaa Ser Xaa Ala Xaa Thr Leu
115 120 125
Leu Phe Leu Ala Leu Phe Ala Val Lys Gly Met Glu Ala Ala Arg Ala
130 135 140
Cys Val Glu Ile Leu Ala Ala Arg Glu Lys Ile Ala Ala
145 150 155
<210> 41
<211> 159
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 41
Met Gly Glu Val Pro Ile Gly Asp Pro Lys Glu Leu Asn Gly Met Glu
1 5 10 15
Ile Ala Ala Val Tyr Leu Gln Pro Ile Glu Met Glu Pro Arg Gly Ile
20 25 30
Asp Leu Ala Ala Ser Leu Ala Asp Ile His Leu Glu Ala Asp Ile His
35 40 45
Ala Leu Lys Asn Asn Pro Asn Gly Phe Pro Glu Gly Phe Trp Met Pro
50 55 60
Tyr Leu Thr Ile Ala Tyr Ala Leu Ala Asn Ala Asp Thr Gly Ala Ile
65 70 75 80
Lys Thr Gly Thr Leu Met Pro Met Val Ala Asp Asp Gly Pro His Tyr
85 90 95
Gly Ala Asn Ile Ala Met Glu Lys Asp Lys Lys Gly Gly Phe Gly Val
100 105 110
Gly Thr Tyr Ala Leu Thr Phe Leu Ile Ser Asn Pro Glu Lys Gln Gly
115 120 125
Phe Gly Arg His Val Asp Glu Glu Thr Gly Val Gly Lys Trp Phe Glu
130 135 140
Pro Phe Val Val Thr Tyr Phe Phe Lys Tyr Thr Gly Thr Pro Lys
145 150 155
<210> 42
<211> 184
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 42
Met Ser Gln Ala Ile Gly Ile Leu Glu Leu Thr Ser Ile Ala Lys Gly
1 5 10 15
Met Glu Leu Gly Asp Ala Met Leu Lys Ser Ala Asn Val Asp Leu Leu
20 25 30
Val Ser Lys Thr Ile Ser Pro Gly Lys Phe Leu Leu Met Leu Gly Gly
35 40 45
Asp Ile Gly Ala Ile Gln Gln Ala Ile Glu Thr Gly Thr Ser Gln Ala
50 55 60
Gly Glu Met Leu Val Asp Ser Leu Val Leu Ala Asn Ile His Pro Ser
65 70 75 80
Val Leu Pro Ala Ile Ser Gly Leu Asn Ser Val Asp Lys Arg Gln Ala
85 90 95
Val Gly Ile Val Glu Thr Trp Ser Val Ala Ala Cys Ile Ser Ala Ala
100 105 110
Asp Leu Ala Val Lys Gly Ser Asn Val Thr Leu Val Arg Val His Met
115 120 125
Ala Phe Gly Ile Gly Gly Lys Cys Tyr Met Val Val Ala Gly Asp Val
130 135 140
Leu Asp Val Ala Ala Ala Val Ala Thr Ala Ser Leu Ala Ala Gly Ala
145 150 155 160
Lys Gly Leu Leu Val Tyr Ala Ser Ile Ile Pro Arg Pro His Glu Ala
165 170 175
Met Trp Arg Gln Met Val Glu Gly
180
<210> 43
<211> 103
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 43
Met Glu Glu Val Val Leu Ile Thr Val Pro Ser Ala Leu Val Ala Val
1 5 10 15
Lys Ile Ala His Ala Leu Val Glu Glu Arg Leu Ala Ala Cys Val Asn
20 25 30
Ile Val Pro Gly Leu Thr Ser Ile Tyr Arg Trp Gln Gly Ser Val Val
35 40 45
Ser Asp His Glu Leu Leu Leu Leu Val Lys Thr Thr Thr His Ala Phe
50 55 60
Pro Lys Leu Lys Glu Arg Val Lys Ala Leu His Pro Tyr Thr Val Pro
65 70 75 80
Glu Ile Val Ala Leu Pro Ile Ala Glu Gly Asn Arg Glu Tyr Leu Asp
85 90 95
Trp Leu Arg Glu Asn Thr Gly
100
<210> 44
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 44
Met Val Arg Gly Ile Arg Gly Ala Ile Thr Val Glu Glu Asp Thr Pro
1 5 10 15
Ala Ala Ile Leu Ala Ala Thr Ile Glu Leu Leu Leu Lys Met Leu Glu
20 25 30
Ala Asn Gly Ile Gln Ser Tyr Glu Glu Leu Ala Ala Val Ile Phe Thr
35 40 45
Val Thr Glu Asp Leu Thr Ser Ala Phe Pro Ala Glu Ala Ala Arg Leu
50 55 60
Ile Gly Met His Arg Val Pro Leu Leu Ser Ala Arg Glu Val Pro Val
65 70 75 80
Pro Gly Ser Leu Pro Arg Val Ile Arg Val Leu Ala Leu Trp Asn Thr
85 90 95
Asp Thr Pro Gln Asp Arg Val Arg His Val Tyr Leu Asn Glu Ala Val
100 105 110
Arg Leu Arg Pro Asp Leu Glu Ser Ala Gln
115 120
<210> 45
<211> 177
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 45
Met Ser Lys Ala Lys Ile Gly Ile Val Thr Val Ser Asp Arg Ala Ser
1 5 10 15
Ala Gly Ile Thr Ala Asp Ile Ser Gly Lys Ala Ile Ile Leu Ala Leu
20 25 30
Asn Leu Tyr Leu Thr Ser Glu Trp Glu Pro Ile Tyr Gln Val Ile Pro
35 40 45
Asp Glu Gln Asp Val Ile Glu Thr Thr Leu Ile Lys Met Ala Asp Glu
50 55 60
Gln Asp Cys Cys Leu Ile Val Thr Thr Gly Gly Thr Gly Pro Ala Lys
65 70 75 80
Arg Asp Val Thr Pro Glu Ala Thr Glu Ala Val Cys Asp Arg Met Met
85 90 95
Pro Gly Phe Gly Glu Leu Met Arg Ala Glu Ser Leu Lys Glu Val Pro
100 105 110
Thr Ala Ile Leu Ser Arg Gln Thr Ala Gly Leu Arg Gly Asp Ser Leu
115 120 125
Ile Val Asn Leu Pro Gly Asp Pro Ala Ser Ile Ser Asp Cys Leu Leu
130 135 140
Ala Val Phe Pro Ala Ile Pro Tyr Cys Ile Asp Leu Met Glu Gly Pro
145 150 155 160
Tyr Leu Glu Cys Asn Glu Ala Met Ile Lys Pro Phe Arg Pro Lys Ala
165 170 175
Lys
<210> 46
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 46
Met Val Arg Gly Ile Arg Gly Ala Ile Thr Val Asn Ser Asp Thr Pro
1 5 10 15
Thr Ser Ile Ile Ile Ala Thr Ile Leu Leu Leu Glu Lys Met Leu Glu
20 25 30
Ala Asn Gly Ile Gln Ser Tyr Glu Glu Leu Ala Ala Val Ile Phe Thr
35 40 45
Val Thr Glu Asp Leu Thr Ser Ala Phe Pro Ala Glu Ala Ala Arg Gln
50 55 60
Ile Gly Met His Arg Val Pro Leu Leu Ser Ala Arg Glu Val Pro Val
65 70 75 80
Pro Gly Ser Leu Pro Arg Val Ile Arg Val Leu Ala Leu Trp Asn Thr
85 90 95
Asp Thr Pro Gln Asp Arg Val Arg His Val Tyr Leu Ser Glu Ala Val
100 105 110
Arg Leu Arg Pro Asp Leu Glu Ser Ala Gln
115 120
<210> 47
<211> 172
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 47
Met Arg Ile Thr Thr Lys Val Gly Asp Lys Gly Ser Thr Arg Leu Phe
1 5 10 15
Gly Gly Glu Glu Val Trp Lys Asp Ser Pro Ile Ile Glu Ala Asn Gly
20 25 30
Thr Leu Asp Glu Leu Thr Ser Phe Ile Gly Glu Ala Lys His Tyr Val
35 40 45
Asp Glu Glu Met Lys Gly Ile Leu Glu Glu Ile Gln Asn Asp Ile Tyr
50 55 60
Lys Ile Met Gly Glu Ile Gly Ser Lys Gly Lys Ile Glu Gly Ile Ser
65 70 75 80
Glu Glu Arg Ile Ala Trp Leu Leu Lys Leu Ile Leu Arg Tyr Met Glu
85 90 95
Met Val Asn Leu Lys Ser Phe Val Leu Pro Gly Gly Thr Leu Glu Ser
100 105 110
Ala Lys Leu Asp Val Cys Arg Thr Ile Ala Arg Arg Ala Leu Arg Lys
115 120 125
Val Leu Thr Val Thr Arg Glu Phe Gly Ile Gly Ala Glu Ala Ala Ala
130 135 140
Tyr Leu Leu Ala Leu Ser Asp Leu Leu Phe Leu Leu Ala Arg Val Ile
145 150 155 160
Glu Ile Glu Lys Asn Lys Leu Lys Glu Val Arg Ser
165 170
<210> 48
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 48
Met Pro His Leu Val Ile Glu Ala Thr Ala Asn Leu Arg Leu Glu Thr
1 5 10 15
Ser Pro Gly Glu Leu Leu Glu Gln Ala Asn Lys Ala Leu Phe Ala Ser
20 25 30
Gly Gln Phe Gly Glu Ala Asp Ile Lys Ser Arg Phe Val Thr Leu Glu
35 40 45
Ala Tyr Arg Gln Gly Thr Ala Ala Val Glu Arg Ala Tyr Leu His Ala
50 55 60
Cys Leu Ser Ile Leu Asp Gly Arg Asp Ile Ala Thr Arg Thr Leu Leu
65 70 75 80
Gly Ala Ser Leu Cys Ala Val Leu Ala Glu Ala Val Ala Gly Gly Gly
85 90 95
Glu Glu Gly Val Gln Val Ser Val Glu Val Arg Glu Met Glu Arg Leu
100 105 110
Ser Tyr Ala Lys Arg Val Val Ala Arg Gln Arg
115 120
<210> 49
<211> 158
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 49
Met Glu Ser Val Asn Thr Ser Phe Leu Ser Pro Ser Leu Val Thr Ile
1 5 10 15
Arg Asp Phe Asp Asn Gly Gln Phe Ala Val Leu Arg Ile Gly Arg Thr
20 25 30
Gly Phe Pro Ala Asp Lys Gly Asp Ile Asp Leu Cys Leu Asp Lys Met
35 40 45
Ile Gly Val Arg Ala Ala Gln Ile Phe Leu Gly Asp Asp Thr Glu Asp
50 55 60
Gly Phe Lys Gly Pro His Ile Arg Ile Arg Cys Val Asp Ile Asp Asp
65 70 75 80
Lys His Thr Tyr Asn Ala Met Val Tyr Val Asp Leu Ile Val Gly Thr
85 90 95
Gly Ala Ser Glu Val Glu Arg Glu Thr Ala Glu Glu Glu Ala Lys Leu
100 105 110
Ala Leu Arg Val Ala Leu Gln Val Asp Ile Ala Asp Glu His Ser Cys
115 120 125
Val Thr Gln Phe Glu Met Lys Leu Arg Glu Glu Leu Leu Ser Ser Asp
130 135 140
Ser Phe His Pro Asp Lys Asp Glu Tyr Tyr Lys Asp Phe Leu
145 150 155
<210> 50
<211> 113
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 50
Met Pro Val Ile Gln Thr Phe Val Ser Thr Pro Leu Asp His His Lys
1 5 10 15
Arg Leu Leu Leu Ala Ile Ile Tyr Arg Ile Val Thr Arg Val Val Leu
20 25 30
Gly Lys Pro Glu Asp Leu Val Met Met Thr Phe His Asp Ser Thr Pro
35 40 45
Met His Phe Phe Gly Ser Thr Asp Pro Val Ala Cys Val Arg Val Glu
50 55 60
Ala Leu Gly Gly Tyr Gly Pro Ser Glu Pro Glu Lys Val Thr Ser Ile
65 70 75 80
Val Thr Ala Ala Ile Thr Ala Val Cys Gly Ile Val Ala Asp Arg Ile
85 90 95
Phe Val Leu Tyr Phe Ser Pro Leu His Cys Gly Trp Asn Gly Thr Asn
100 105 110
Phe
<210> 51
<211> 103
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный наноструктурный полипептид
<400> 51
Met Glu Glu Val Val Leu Ile Thr Val Pro Ser Ala Leu Val Ala Val
1 5 10 15
Lys Ile Ala His Ala Leu Val Glu Glu Arg Leu Ala Ala Cys Val Asn
20 25 30
Ile Val Pro Gly Leu Thr Ser Ile Tyr Arg Glu Glu Gly Ser Val Val
35 40 45
Ser Asp His Glu Leu Leu Leu Leu Val Lys Thr Thr Thr Asp Ala Phe
50 55 60
Pro Lys Leu Lys Glu Arg Val Lys Glu Leu His Pro Tyr Glu Val Pro
65 70 75 80
Glu Ile Val Ala Leu Pro Ile Ala Glu Gly Asn Arg Glu Tyr Leu Asp
85 90 95
Trp Leu Arg Glu Asn Thr Gly
100
<210> 52
<211> 869
<212> БЕЛОК
<213> вирус иммунодефицита человека 1
<400> 52
Met Arg Val Lys Gly Ile Lys Lys Asn Tyr Gln His Trp Trp Arg Gly
1 5 10 15
Gly Ile Met Leu Leu Gly Met Leu Met Ile Cys Ser Ser Ala Glu Lys
20 25 30
Leu Trp Val Thr Val Tyr Tyr Gly Val Pro Val Trp Lys Glu Ala Thr
35 40 45
Thr Thr Leu Phe Cys Ala Ser Asp Ala Lys Ala Gln Asn Pro Glu Met
50 55 60
His Asn Ile Trp Ala Thr His Ala Cys Val Pro Thr Asp Pro Asn Pro
65 70 75 80
Gln Glu Val Ile Leu Lys Asn Leu Thr Glu Glu Phe Asn Met Trp Lys
85 90 95
Asn Asn Met Val Glu Gln Met His Glu Asp Ile Ile Ser Leu Trp Asp
100 105 110
Gln Ser Leu Lys Pro Cys Val Lys Leu Thr Pro Leu Cys Val Thr Leu
115 120 125
Asn Cys Thr Asn Ala Glu Ser Leu Asn Cys Thr Ala Thr Asn Gly Thr
130 135 140
Asn Asn Cys Ser Ala Ser Thr Lys Pro Met Glu Glu Met Lys Asn Cys
145 150 155 160
Ser Phe Asn Ile Thr Thr Ser Val Gln Asp Lys Lys Gln Gln Glu Tyr
165 170 175
Ala Leu Phe Tyr Lys Leu Asp Ile Ile Pro Ile Asp Asn Asn Glu Asn
180 185 190
Asp Leu Asn Asn Thr Asn Tyr Thr Ser Tyr Arg Leu Ile Ser Cys Asn
195 200 205
Thr Ser Val Ile Thr Gln Ala Cys Pro Lys Ile Thr Phe Glu Pro Ile
210 215 220
Pro Ile His Tyr Cys Ala Pro Ala Gly Phe Ala Ile Leu Lys Cys Lys
225 230 235 240
Asp Lys Arg Phe Asn Gly Thr Gly Pro Cys Lys Asn Val Ser Thr Val
245 250 255
Gln Cys Thr His Gly Ile Arg Pro Val Val Ser Thr Gln Leu Leu Leu
260 265 270
Asn Gly Ser Leu Ala Glu Glu Gly Val Val Leu Arg Ser Glu Asn Phe
275 280 285
Thr Asp Asn Ala Lys Asn Ile Ile Val Gln Leu Lys Asp Pro Val Asn
290 295 300
Ile Thr Cys Thr Arg Pro Asn Asn Asn Thr Arg Lys Ser Ile Thr Ile
305 310 315 320
Gly Pro Gly Arg Ala Phe Tyr Ala Thr Gly Gln Val Ile Gly Asp Ile
325 330 335
Arg Lys Ala His Cys Asp Leu Asn Gly Thr Glu Trp Asp Asn Ala Leu
340 345 350
Lys Gln Ile Val Glu Glu Leu Arg Lys Gln Tyr Gly Asn Asn Ile Thr
355 360 365
Ile Phe Asn Ser Ser Ser Gly Gly Asp Pro Glu Ile Val Met His Ser
370 375 380
Phe Asn Cys Gly Gly Glu Phe Phe Tyr Cys Asn Thr Ala Gln Leu Phe
385 390 395 400
Asn Ser Thr Trp Leu Phe Asn Ser Thr Trp Asn Ser Thr Glu Arg Leu
405 410 415
Gly Asn Asp Thr Glu Arg Thr Asn Asp Thr Ile Thr Leu Pro Cys Lys
420 425 430
Ile Lys Gln Val Ile Asn Met Trp Gln Thr Val Gly Lys Ala Met Tyr
435 440 445
Ala Pro Pro Ile Arg Gly Leu Ile Arg Cys Ser Ser Asn Ile Thr Gly
450 455 460
Leu Ile Leu Thr Arg Asp Gly Ser Gly Asn Thr Thr Gly Asn Glu Thr
465 470 475 480
Phe Arg Pro Gly Gly Gly Asn Met Lys Asp Asn Trp Arg Ser Glu Leu
485 490 495
Tyr Lys Tyr Lys Val Val Lys Ile Glu Pro Leu Gly Val Ala Pro Thr
500 505 510
Arg Ala Lys Arg Arg Val Val Gln Arg Glu Lys Arg Ala Ala Gly Leu
515 520 525
Gly Ala Leu Phe Leu Gly Phe Leu Gly Met Ala Gly Ser Thr Met Gly
530 535 540
Ala Ala Ser Leu Thr Leu Thr Val Gln Ala Arg Gln Leu Leu Ser Gly
545 550 555 560
Ile Val Gln Gln Gln Asn Asn Leu Leu Arg Ala Ile Glu Ala Gln Gln
565 570 575
His Leu Leu Gln Leu Thr Val Trp Gly Ile Lys Gln Leu Gln Ala Arg
580 585 590
Val Leu Ala Val Glu Arg Tyr Leu Arg Asp Gln Gln Leu Leu Gly Ile
595 600 605
Trp Gly Cys Ser Gly Lys Leu Ile Cys Thr Thr Thr Val Pro Trp Asn
610 615 620
Ala Ser Trp Ser Asn Lys Ser Leu Asp Asn Ile Trp Glu Asn Met Thr
625 630 635 640
Trp Met Gln Trp Glu Lys Glu Ile Asp Asn Tyr Thr Asp Val Ile Tyr
645 650 655
Lys Leu Leu Glu Glu Ser Gln Asn Gln Gln Glu Lys Asn Glu Gln Glu
660 665 670
Leu Leu Glu Leu Asp Lys Trp Ala Ser Leu Trp Asn Trp Phe Asp Ile
675 680 685
Thr Arg Trp Leu Trp Tyr Ile Lys Ile Phe Ile Met Ile Val Gly Gly
690 695 700
Leu Val Gly Leu Arg Ile Val Phe Ala Val Leu Ser Ile Val Asn Arg
705 710 715 720
Val Arg Gln Gly Tyr Ser Pro Leu Ser Phe Gln Thr Leu Phe Pro Ala
725 730 735
Pro Arg Gly Pro Asp Arg Pro Glu Gly Thr Glu Glu Gly Gly Gly Glu
740 745 750
Arg Gly Arg Asp Ser Ser Asp Arg Ser Ala His Gly Phe Leu Ala Leu
755 760 765
Ile Trp Gly Asp Leu Trp Ser Leu Cys Leu Phe Ser Tyr Arg Arg Leu
770 775 780
Arg Asp Leu Leu Leu Ile Ala Ala Arg Ile Val Glu Leu Leu Gly Arg
785 790 795 800
Arg Gly Trp Glu Val Leu Lys Tyr Trp Trp Ser Leu Leu Gln Tyr Trp
805 810 815
Ser Gln Glu Leu Lys Lys Ser Ala Val Ser Leu Leu Asn Ala Thr Ala
820 825 830
Ile Ala Val Ala Glu Gly Thr Asp Arg Ile Ile Glu Ile Val Gln Arg
835 840 845
Ala Gly Arg Ala Ile Ile His Ile Pro Arg Arg Ile Arg Gln Gly Ala
850 855 860
Glu Arg Ala Leu Leu
865
<210> 53
<211> 492
<212> БЕЛОК
<213> вирус иммунодефицита человека 1
<400> 53
Leu Trp Val Thr Val Tyr Tyr Gly Val Pro Val Trp Lys Glu Ala Thr
1 5 10 15
Thr Thr Leu Phe Cys Ala Ser Asp Ala Lys Ala Gln Asn Pro Glu Met
20 25 30
His Asn Ile Trp Ala Thr His Ala Cys Val Pro Thr Asp Pro Asn Pro
35 40 45
Gln Glu Val Ile Leu Lys Asn Leu Thr Glu Glu Phe Asn Met Trp Lys
50 55 60
Asn Asn Met Val Glu Gln Met His Glu Asp Ile Ile Ser Leu Trp Asp
65 70 75 80
Gln Ser Leu Lys Pro Cys Val Lys Leu Thr Pro Leu Cys Val Thr Leu
85 90 95
Asn Cys Thr Asn Ala Glu Ser Leu Asn Cys Thr Ala Thr Asn Gly Thr
100 105 110
Asn Asn Cys Ser Ala Ser Thr Lys Pro Met Glu Glu Met Lys Asn Cys
115 120 125
Ser Phe Asn Ile Thr Thr Ser Val Gln Asp Lys Lys Gln Gln Glu Tyr
130 135 140
Ala Leu Phe Tyr Lys Leu Asp Ile Ile Pro Ile Asp Asn Asn Glu Asn
145 150 155 160
Asp Leu Asn Asn Thr Asn Tyr Thr Ser Tyr Arg Leu Ile Ser Cys Asn
165 170 175
Thr Ser Val Ile Thr Gln Ala Cys Pro Lys Ile Thr Phe Glu Pro Ile
180 185 190
Pro Ile His Tyr Cys Ala Pro Ala Gly Phe Ala Ile Leu Lys Cys Lys
195 200 205
Asp Lys Arg Phe Asn Gly Thr Gly Pro Cys Lys Asn Val Ser Thr Val
210 215 220
Gln Cys Thr His Gly Ile Arg Pro Val Val Ser Thr Gln Leu Leu Leu
225 230 235 240
Asn Gly Ser Leu Ala Glu Glu Gly Val Val Leu Arg Ser Glu Asn Phe
245 250 255
Thr Asp Asn Ala Lys Asn Ile Ile Val Gln Leu Lys Asp Pro Val Asn
260 265 270
Ile Thr Cys Thr Arg Pro Asn Asn Asn Thr Arg Lys Ser Ile Thr Ile
275 280 285
Gly Pro Gly Arg Ala Phe Tyr Ala Thr Gly Gln Val Ile Gly Asp Ile
290 295 300
Arg Lys Ala His Cys Asp Leu Asn Gly Thr Glu Trp Asp Asn Ala Leu
305 310 315 320
Lys Gln Ile Val Glu Glu Leu Arg Lys Gln Tyr Gly Asn Asn Ile Thr
325 330 335
Ile Phe Asn Ser Ser Ser Gly Gly Asp Pro Glu Ile Val Met His Ser
340 345 350
Phe Asn Cys Gly Gly Glu Phe Phe Tyr Cys Asn Thr Ala Gln Leu Phe
355 360 365
Asn Ser Thr Trp Leu Phe Asn Ser Thr Trp Asn Ser Thr Glu Arg Leu
370 375 380
Gly Asn Asp Thr Glu Arg Thr Asn Asp Thr Ile Thr Leu Pro Cys Lys
385 390 395 400
Ile Lys Gln Val Ile Asn Met Trp Gln Thr Val Gly Lys Ala Met Tyr
405 410 415
Ala Pro Pro Ile Arg Gly Leu Ile Arg Cys Ser Ser Asn Ile Thr Gly
420 425 430
Leu Ile Leu Thr Arg Asp Gly Ser Gly Asn Thr Thr Gly Asn Glu Thr
435 440 445
Phe Arg Pro Gly Gly Gly Asn Met Lys Asp Asn Trp Arg Ser Glu Leu
450 455 460
Tyr Lys Tyr Lys Val Val Lys Ile Glu Pro Leu Gly Val Ala Pro Thr
465 470 475 480
Arg Ala Lys Arg Arg Val Val Gln Arg Glu Lys Arg
485 490
<210> 54
<211> 191
<212> БЕЛОК
<213> вирус иммунодефицита человека 1
<400> 54
Met Gly Ala Ala Ser Leu Thr Leu Thr Val Gln Ala Arg Gln Leu Leu
1 5 10 15
Ser Gly Ile Val Gln Gln Gln Asn Asn Leu Leu Arg Ala Ile Glu Ala
20 25 30
Gln Gln His Leu Leu Gln Leu Thr Val Trp Gly Ile Lys Gln Leu Gln
35 40 45
Ala Arg Val Leu Ala Val Glu Arg Tyr Leu Arg Asp Gln Gln Leu Leu
50 55 60
Gly Ile Trp Gly Cys Ser Gly Lys Leu Ile Cys Thr Thr Thr Val Pro
65 70 75 80
Trp Asn Ala Ser Trp Ser Asn Lys Ser Leu Asp Asn Ile Trp Glu Asn
85 90 95
Met Thr Trp Met Gln Trp Glu Lys Glu Ile Asp Asn Tyr Thr Asp Val
100 105 110
Ile Tyr Lys Leu Leu Glu Glu Ser Gln Asn Gln Gln Glu Lys Asn Glu
115 120 125
Gln Glu Leu Leu Glu Leu Asp Lys Trp Ala Ser Leu Trp Asn Trp Phe
130 135 140
Asp Ile Thr Arg Trp Leu Trp Tyr Ile Lys Ile Phe Ile Met Ile Val
145 150 155 160
Gly Gly Leu Val Gly Leu Arg Ile Val Phe Ala Val Leu Ser Ile Val
165 170 175
Asn Arg Val Arg Gln Gly Tyr Ser Pro Leu Ser Phe Gln Thr Leu
180 185 190
<210> 55
<211> 22
<212> БЕЛОК
<213> вирус иммунодефицита человека 1
<400> 55
Glu Leu Asp Lys Trp Ala Ser Leu Trp Asn Trp Phe Asp Ile Thr Arg
1 5 10 15
Trp Leu Trp Tyr Ile Lys
20
<210> 56
<211> 574
<212> БЕЛОК
<213> респираторно-сцинтилляционный вирус, тип A
<400> 56
Met Glu Leu Pro Ile Leu Lys Thr Asn Ala Ile Thr Thr Ile Leu Ala
1 5 10 15
Ala Val Thr Leu Cys Phe Ala Ser Ser Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gln Ser Thr Pro Ala Ala Asn Asn Arg Ala Arg Arg Glu Leu Pro
100 105 110
Arg Phe Met Asn Tyr Thr Leu Asn Asn Thr Lys Asn Asn Asn Val Thr
115 120 125
Leu Ser Lys Lys Arg Lys Arg Arg Phe Leu Gly Phe Leu Leu Gly Val
130 135 140
Gly Ser Ala Ile Ala Ser Gly Ile Ala Val Ser Lys Val Leu His Leu
145 150 155 160
Glu Gly Glu Val Asn Lys Ile Lys Asn Ala Leu Leu Ser Thr Asn Lys
165 170 175
Ala Val Val Ser Leu Ser Asn Gly Val Ser Val Leu Thr Ser Lys Val
180 185 190
Leu Asp Leu Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Val Asn
195 200 205
Lys Gln Ser Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln
210 215 220
Gln Lys Asn Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn
225 230 235 240
Ala Gly Val Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu
245 250 255
Leu Leu Ser Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys
260 265 270
Leu Met Ser Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile
275 280 285
Met Ser Ile Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro
290 295 300
Leu Tyr Gly Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro
305 310 315 320
Leu Cys Thr Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg
325 330 335
Thr Asp Arg Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe
340 345 350
Pro Gln Ala Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp
355 360 365
Thr Met Asn Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Ile
370 375 380
Asp Ile Phe Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr
385 390 395 400
Asp Val Ser Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys
405 410 415
Tyr Gly Lys Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile
420 425 430
Lys Thr Phe Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp
435 440 445
Thr Val Ser Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly
450 455 460
Lys Ser Leu Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro
465 470 475 480
Leu Val Phe Pro Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn
485 490 495
Glu Lys Ile Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Leu
500 505 510
Leu His Asn Val Asn Val Gly Lys Ser Thr Thr Asn Ile Met Ile Thr
515 520 525
Thr Ile Ile Ile Val Ile Ile Val Ile Leu Leu Leu Leu Ile Ala Val
530 535 540
Gly Leu Phe Leu Tyr Cys Lys Ala Arg Ser Thr Pro Val Thr Leu Ser
545 550 555 560
Lys Asp Gln Leu Ser Gly Ile Asn Asn Ile Ala Phe Ser Asn
565 570
<210> 57
<211> 566
<212> БЕЛОК
<213> Вирус гриппа А
<400> 57
Met Lys Ala Ile Leu Val Val Leu Leu Tyr Thr Phe Ala Thr Ala Asn
1 5 10 15
Ala Asp Thr Leu Cys Ile Gly Tyr His Ala Asn Asn Ser Thr Asp Thr
20 25 30
Val Asp Thr Val Leu Glu Lys Asn Val Thr Val Thr His Ser Val Asn
35 40 45
Leu Leu Glu Asp Lys His Asn Gly Lys Leu Cys Lys Leu Arg Gly Val
50 55 60
Ala Pro Leu His Leu Gly Lys Cys Asn Ile Ala Gly Trp Ile Leu Gly
65 70 75 80
Asn Pro Glu Cys Glu Ser Leu Ser Thr Ala Ser Ser Trp Ser Tyr Ile
85 90 95
Val Glu Thr Pro Ser Ser Asp Asn Gly Thr Cys Tyr Pro Gly Asp Phe
100 105 110
Ile Asp Tyr Glu Glu Leu Arg Glu Gln Leu Ser Ser Val Ser Ser Phe
115 120 125
Glu Arg Phe Glu Ile Phe Pro Lys Thr Ser Ser Trp Pro Asn His Asp
130 135 140
Ser Asn Lys Gly Val Thr Ala Ala Cys Pro His Ala Gly Ala Lys Ser
145 150 155 160
Phe Tyr Lys Asn Leu Ile Trp Leu Val Lys Lys Gly Asn Ser Tyr Pro
165 170 175
Lys Leu Ser Lys Ser Tyr Ile Asn Asp Lys Gly Lys Glu Val Leu Val
180 185 190
Leu Trp Gly Ile His His Pro Ser Thr Ser Ala Asp Gln Gln Ser Leu
195 200 205
Tyr Gln Asn Ala Asp Ala Tyr Val Phe Val Gly Ser Ser Arg Tyr Ser
210 215 220
Lys Lys Phe Lys Pro Glu Ile Ala Ile Arg Pro Lys Val Arg Asp Gln
225 230 235 240
Glu Gly Arg Met Asn Tyr Tyr Trp Thr Leu Val Glu Pro Gly Asp Lys
245 250 255
Ile Thr Phe Glu Ala Thr Gly Asn Leu Val Val Pro Arg Tyr Ala Phe
260 265 270
Ala Met Glu Arg Asn Ala Gly Ser Gly Ile Ile Ile Ser Asp Thr Pro
275 280 285
Val His Asp Cys Asn Thr Thr Cys Gln Thr Pro Lys Gly Ala Ile Asn
290 295 300
Thr Ser Leu Pro Phe Gln Asn Ile His Pro Ile Thr Ile Gly Lys Cys
305 310 315 320
Pro Lys Tyr Val Lys Ser Thr Lys Leu Arg Leu Ala Thr Gly Leu Arg
325 330 335
Asn Ile Pro Ser Ile Gln Ser Arg Gly Leu Phe Gly Ala Ile Ala Gly
340 345 350
Phe Ile Glu Gly Gly Trp Thr Gly Met Val Asp Gly Trp Tyr Gly Tyr
355 360 365
His His Gln Asn Glu Gln Gly Ser Gly Tyr Ala Ala Asp Leu Lys Ser
370 375 380
Thr Gln Asn Ala Ile Asp Glu Ile Thr Asn Lys Val Asn Ser Val Ile
385 390 395 400
Glu Lys Met Asn Thr Gln Phe Thr Ala Val Gly Lys Glu Phe Asn His
405 410 415
Leu Glu Lys Arg Ile Glu Asn Leu Asn Lys Lys Val Asp Asp Gly Phe
420 425 430
Leu Asp Ile Trp Thr Tyr Asn Ala Glu Leu Leu Val Leu Leu Glu Asn
435 440 445
Glu Arg Thr Leu Asp Tyr His Asp Ser Asn Val Lys Asn Leu Tyr Glu
450 455 460
Lys Val Arg Ser Gln Leu Lys Asn Asn Ala Lys Glu Ile Gly Asn Gly
465 470 475 480
Cys Phe Glu Phe Tyr His Lys Cys Asp Asn Thr Cys Met Glu Ser Val
485 490 495
Lys Asn Gly Thr Tyr Asp Tyr Pro Lys Tyr Ser Glu Glu Ala Lys Leu
500 505 510
Asn Arg Glu Glu Ile Asp Gly Val Lys Leu Glu Ser Thr Arg Ile Tyr
515 520 525
Gln Ile Leu Ala Ile Tyr Ser Thr Val Ala Ser Ser Leu Val Leu Val
530 535 540
Val Ser Leu Gly Ala Ile Ser Phe Trp Met Cys Ser Asn Gly Ser Leu
545 550 555 560
Gln Cys Arg Ile Cys Ile
565
<210> 58
<211> 584
<212> БЕЛОК
<213> Вирус гриппа В
<400> 58
Met Lys Ala Ile Ile Val Leu Leu Met Val Val Thr Ser Asn Ala Asp
1 5 10 15
Arg Ile Cys Thr Gly Ile Thr Ser Ser Asn Ser Pro His Val Val Lys
20 25 30
Thr Ala Thr Gln Gly Glu Val Asn Val Thr Gly Val Ile Pro Leu Thr
35 40 45
Thr Thr Pro Thr Lys Ser Tyr Phe Ala Asn Leu Lys Gly Thr Lys Thr
50 55 60
Arg Gly Lys Leu Cys Pro Asp Cys Leu Asn Cys Thr Asp Leu Asp Val
65 70 75 80
Ala Leu Gly Arg Pro Met Cys Val Gly Thr Thr Pro Ser Ala Lys Ala
85 90 95
Ser Ile Leu His Glu Val Arg Pro Val Thr Ser Gly Cys Phe Pro Ile
100 105 110
Met His Asp Arg Thr Lys Ile Arg Gln Leu Ala Asn Leu Leu Arg Gly
115 120 125
Tyr Glu Asn Ile Arg Leu Ser Thr Gln Asn Val Ile Asp Ala Glu Lys
130 135 140
Ala Pro Gly Gly Pro Tyr Arg Leu Gly Thr Ser Gly Ser Cys Pro Asn
145 150 155 160
Ala Thr Ser Lys Ser Gly Phe Phe Ala Thr Met Ala Trp Ala Val Pro
165 170 175
Lys Asp Asn Asn Lys Asn Ala Thr Asn Pro Leu Thr Val Glu Val Pro
180 185 190
Tyr Ile Cys Ala Glu Gly Glu Asp Gln Ile Thr Val Trp Gly Phe His
195 200 205
Ser Asp Asn Lys Thr Gln Met Lys Asn Leu Tyr Gly Asp Ser Asn Pro
210 215 220
Gln Lys Phe Thr Ser Ser Ala Asn Gly Val Thr Thr His Tyr Val Ser
225 230 235 240
Gln Ile Gly Gly Phe Pro Asp Gln Thr Glu Asp Gly Gly Leu Pro Gln
245 250 255
Ser Gly Arg Ile Val Val Asp Tyr Met Met Gln Lys Pro Gly Lys Thr
260 265 270
Gly Thr Ile Val Tyr Gln Arg Gly Val Leu Leu Pro Gln Lys Val Trp
275 280 285
Cys Ala Ser Gly Arg Ser Lys Val Ile Lys Gly Ser Leu Pro Leu Ile
290 295 300
Gly Glu Ala Asp Cys Leu His Glu Lys Tyr Gly Gly Leu Asn Lys Ser
305 310 315 320
Lys Pro Tyr Tyr Thr Gly Glu His Ala Lys Ala Ile Gly Asn Cys Pro
325 330 335
Ile Trp Val Lys Thr Pro Leu Lys Leu Ala Asn Gly Thr Lys Tyr Arg
340 345 350
Pro Pro Ala Lys Leu Leu Lys Glu Arg Gly Phe Phe Gly Ala Ile Ala
355 360 365
Gly Phe Leu Glu Gly Gly Trp Glu Gly Met Ile Ala Gly Trp His Gly
370 375 380
Tyr Thr Ser His Gly Ala His Gly Val Ala Val Ala Ala Asp Leu Lys
385 390 395 400
Ser Thr Gln Glu Ala Ile Asn Lys Ile Thr Lys Asn Leu Asn Ser Leu
405 410 415
Ser Glu Leu Glu Val Lys Asn Leu Gln Arg Leu Ser Gly Ala Met Asp
420 425 430
Glu Leu His Asn Glu Ile Leu Glu Leu Asp Glu Lys Val Asp Asp Leu
435 440 445
Arg Ala Asp Thr Ile Ser Ser Gln Ile Glu Leu Ala Val Leu Leu Ser
450 455 460
Asn Glu Gly Ile Ile Asn Ser Glu Asp Glu His Leu Leu Ala Leu Glu
465 470 475 480
Arg Lys Leu Lys Lys Met Leu Gly Pro Ser Ala Val Asp Ile Gly Asn
485 490 495
Gly Cys Phe Glu Thr Lys His Lys Cys Asn Gln Thr Cys Leu Asp Arg
500 505 510
Ile Ala Ala Gly Thr Phe Asn Ala Gly Glu Phe Ser Leu Pro Thr Phe
515 520 525
Asp Ser Leu Asn Ile Thr Ala Ala Ser Leu Asn Asp Asp Gly Leu Asp
530 535 540
Asn His Thr Ile Leu Leu Tyr Tyr Ser Thr Ala Ala Ser Ser Leu Ala
545 550 555 560
Val Thr Leu Met Leu Ala Ile Phe Ile Val Tyr Met Val Ser Arg Asp
565 570 575
Asn Val Ser Cys Ser Ile Cys Leu
580
<210> 59
<211> 907
<212> БЕЛОК
<213> Вирус Эпштейна-Барр
<400> 59
Met Glu Ala Ala Leu Leu Val Cys Gln Tyr Thr Ile Gln Ser Leu Ile
1 5 10 15
His Leu Thr Gly Glu Asp Pro Gly Phe Phe Asn Val Glu Ile Pro Glu
20 25 30
Phe Pro Phe Tyr Pro Thr Cys Asn Val Cys Thr Ala Asp Val Asn Val
35 40 45
Thr Ile Asn Phe Asp Val Gly Gly Lys Lys His Gln Leu Asp Leu Asp
50 55 60
Phe Gly Gln Leu Thr Pro His Thr Lys Ala Val Tyr Gln Pro Arg Gly
65 70 75 80
Ala Phe Gly Gly Ser Glu Asn Ala Thr Asn Leu Phe Leu Leu Glu Leu
85 90 95
Leu Gly Ala Gly Glu Leu Ala Leu Thr Met Arg Ser Lys Lys Leu Pro
100 105 110
Ile Asn Val Thr Thr Gly Glu Glu Gln Gln Val Ser Leu Glu Ser Val
115 120 125
Asp Val Tyr Phe Gln Asp Val Phe Gly Thr Met Trp Cys His His Ala
130 135 140
Glu Met Gln Asn Pro Val Tyr Leu Ile Pro Glu Thr Val Pro Tyr Ile
145 150 155 160
Lys Trp Asp Asn Cys Asn Ser Thr Asn Ile Thr Ala Val Val Arg Ala
165 170 175
Gln Gly Leu Asp Val Thr Leu Pro Leu Ser Leu Pro Thr Ser Ala Gln
180 185 190
Asp Ser Asn Phe Ser Val Lys Thr Glu Met Leu Gly Asn Glu Ile Asp
195 200 205
Ile Glu Cys Ile Met Glu Asp Gly Glu Ile Ser Gln Val Leu Pro Gly
210 215 220
Asp Asn Lys Phe Asn Ile Thr Cys Ser Gly Tyr Glu Ser His Val Pro
225 230 235 240
Ser Gly Gly Ile Leu Thr Ser Thr Ser Pro Val Ala Thr Pro Ile Pro
245 250 255
Gly Thr Gly Tyr Ala Tyr Ser Leu Arg Leu Thr Pro Arg Pro Val Ser
260 265 270
Arg Phe Leu Gly Asn Asn Ser Ile Leu Tyr Val Phe Tyr Ser Gly Asn
275 280 285
Gly Pro Lys Ala Ser Gly Gly Asp Tyr Cys Ile Gln Ser Asn Ile Val
290 295 300
Phe Ser Asp Glu Ile Pro Ala Ser Gln Asp Met Pro Thr Asn Thr Thr
305 310 315 320
Asp Ile Thr Tyr Val Gly Asp Asn Ala Thr Tyr Ser Val Pro Met Val
325 330 335
Thr Ser Glu Asp Ala Asn Ser Pro Asn Val Thr Val Thr Ala Phe Trp
340 345 350
Ala Trp Pro Asn Asn Thr Glu Thr Asp Phe Lys Cys Lys Trp Thr Leu
355 360 365
Thr Ser Gly Thr Pro Ser Gly Cys Glu Asn Ile Ser Gly Ala Phe Ala
370 375 380
Ser Asn Arg Thr Phe Asp Ile Thr Val Ser Gly Leu Gly Thr Ala Pro
385 390 395 400
Lys Thr Leu Ile Ile Thr Arg Thr Ala Thr Asn Ala Thr Thr Thr Thr
405 410 415
His Lys Val Ile Phe Ser Lys Ala Pro Glu Ser Thr Thr Thr Ser Pro
420 425 430
Thr Leu Asn Thr Thr Gly Phe Ala Asp Pro Asn Thr Thr Thr Gly Leu
435 440 445
Pro Ser Ser Thr His Val Pro Thr Asn Leu Thr Ala Pro Ala Ser Thr
450 455 460
Gly Pro Thr Val Ser Thr Ala Asp Val Thr Ser Pro Thr Pro Ala Gly
465 470 475 480
Thr Thr Ser Gly Ala Ser Pro Val Thr Pro Ser Pro Ser Pro Trp Asp
485 490 495
Asn Gly Thr Glu Ser Lys Ala Pro Asp Met Thr Ser Ser Thr Ser Pro
500 505 510
Val Thr Thr Pro Thr Pro Asn Ala Thr Ser Pro Thr Pro Ala Val Thr
515 520 525
Thr Pro Thr Pro Asn Ala Thr Ser Pro Thr Pro Ala Val Thr Thr Pro
530 535 540
Thr Pro Asn Ala Thr Ser Pro Thr Leu Gly Lys Thr Ser Pro Thr Ser
545 550 555 560
Ala Val Thr Thr Pro Thr Pro Asn Ala Thr Ser Pro Thr Leu Gly Lys
565 570 575
Thr Ser Pro Thr Ser Ala Val Thr Thr Pro Thr Pro Asn Ala Thr Ser
580 585 590
Pro Thr Leu Gly Lys Thr Ser Pro Thr Ser Ala Val Thr Thr Pro Thr
595 600 605
Pro Asn Ala Thr Gly Pro Thr Val Gly Glu Thr Ser Pro Gln Ala Asn
610 615 620
Ala Thr Asn His Thr Leu Gly Gly Thr Ser Pro Thr Pro Val Val Thr
625 630 635 640
Ser Gln Pro Lys Asn Ala Thr Ser Ala Val Thr Thr Gly Gln His Asn
645 650 655
Ile Thr Ser Ser Ser Thr Ser Ser Met Ser Leu Arg Pro Ser Ser Asn
660 665 670
Pro Glu Thr Leu Ser Pro Ser Thr Ser Asp Asn Ser Thr Ser His Met
675 680 685
Pro Leu Leu Thr Ser Ala His Pro Thr Gly Gly Glu Asn Ile Thr Gln
690 695 700
Val Thr Pro Ala Ser Ile Ser Thr His His Val Ser Thr Ser Ser Pro
705 710 715 720
Ala Pro Arg Pro Gly Thr Thr Ser Gln Ala Ser Gly Pro Gly Asn Ser
725 730 735
Ser Thr Ser Thr Lys Pro Gly Glu Val Asn Val Thr Lys Gly Thr Pro
740 745 750
Pro Gln Asn Ala Thr Ser Pro Gln Ala Pro Ser Gly Gln Lys Thr Ala
755 760 765
Val Pro Thr Val Thr Ser Thr Gly Gly Lys Ala Asn Ser Thr Thr Gly
770 775 780
Gly Lys His Thr Thr Gly His Gly Ala Arg Thr Ser Thr Glu Pro Thr
785 790 795 800
Thr Asp Tyr Gly Gly Asp Ser Thr Thr Pro Arg Pro Arg Tyr Asn Ala
805 810 815
Thr Thr Tyr Leu Pro Pro Ser Thr Ser Ser Lys Leu Arg Pro Arg Trp
820 825 830
Thr Phe Thr Ser Pro Pro Val Thr Thr Ala Gln Ala Thr Val Pro Val
835 840 845
Pro Pro Thr Ser Gln Pro Arg Phe Ser Asn Leu Ser Met Leu Val Leu
850 855 860
Gln Trp Ala Ser Leu Ala Val Leu Thr Leu Leu Leu Leu Leu Val Met
865 870 875 880
Ala Asp Cys Ala Phe Arg Arg Asn Leu Ser Thr Ser His Thr Tyr Thr
885 890 895
Thr Pro Pro Tyr Asp Asp Ala Glu Thr Tyr Val
900 905
<210> 60
<211> 906
<212> БЕЛОК
<213> Цитомегаловирус человека
<400> 60
Met Glu Ser Arg Ile Trp Cys Leu Val Val Cys Val Asn Leu Cys Ile
1 5 10 15
Val Cys Leu Gly Ala Ala Val Ser Ser Ser Ser Thr Ser His Ala Thr
20 25 30
Ser Ser Thr His Asn Gly Ser His Thr Ser Arg Thr Thr Ser Ala Gln
35 40 45
Thr Arg Ser Val Tyr Ser Gln His Val Thr Ser Ser Glu Ala Val Ser
50 55 60
His Arg Ala Asn Glu Thr Ile Tyr Asn Thr Thr Leu Lys Tyr Gly Asp
65 70 75 80
Val Val Gly Val Asn Thr Thr Lys Tyr Pro Tyr Arg Val Cys Ser Met
85 90 95
Ala Gln Gly Thr Asp Leu Ile Arg Phe Glu Arg Asn Ile Ile Cys Thr
100 105 110
Ser Met Lys Pro Ile Asn Glu Asp Leu Asp Glu Gly Ile Met Val Val
115 120 125
Tyr Lys Arg Asn Ile Val Ala His Thr Phe Lys Val Arg Val Tyr Gln
130 135 140
Lys Val Leu Thr Phe Arg Arg Ser Tyr Ala Tyr Ile Tyr Thr Thr Tyr
145 150 155 160
Leu Leu Gly Ser Asn Thr Glu Tyr Val Ala Pro Pro Met Trp Glu Ile
165 170 175
His His Ile Asn Lys Phe Ala Gln Cys Tyr Ser Ser Tyr Ser Arg Val
180 185 190
Ile Gly Gly Thr Val Phe Val Ala Tyr His Arg Asp Ser Tyr Glu Asn
195 200 205
Lys Thr Met Gln Leu Ile Pro Asp Asp Tyr Ser Asn Thr His Ser Thr
210 215 220
Arg Tyr Val Thr Val Lys Asp Gln Trp His Ser Arg Gly Ser Thr Trp
225 230 235 240
Leu Tyr Arg Glu Thr Cys Asn Leu Asn Cys Met Leu Thr Ile Thr Thr
245 250 255
Ala Arg Ser Lys Tyr Pro Tyr His Phe Phe Ala Thr Ser Thr Gly Asp
260 265 270
Val Val Tyr Ile Ser Pro Phe Tyr Asn Gly Thr Asn Arg Asn Ala Ser
275 280 285
Tyr Phe Gly Glu Asn Ala Asp Lys Phe Phe Ile Phe Pro Asn Tyr Thr
290 295 300
Ile Val Ser Asp Phe Gly Arg Pro Asn Ala Ala Pro Glu Thr His Arg
305 310 315 320
Leu Val Ala Phe Leu Glu Arg Ala Asp Ser Val Ile Ser Trp Asp Ile
325 330 335
Gln Asp Glu Lys Asn Val Thr Cys Gln Leu Thr Phe Trp Glu Ala Ser
340 345 350
Glu Arg Thr Ile Arg Ser Glu Ala Glu Asp Ser Tyr His Phe Ser Ser
355 360 365
Ala Lys Met Thr Ala Thr Phe Leu Ser Lys Lys Gln Glu Val Asn Met
370 375 380
Ser Asp Ser Ala Leu Asp Cys Val Arg Asp Glu Ala Ile Asn Lys Leu
385 390 395 400
Gln Gln Ile Phe Asn Thr Ser Tyr Asn Gln Thr Tyr Glu Lys Tyr Gly
405 410 415
Asn Val Ser Val Phe Glu Thr Ser Gly Gly Leu Val Val Phe Trp Gln
420 425 430
Gly Ile Lys Gln Lys Ser Leu Val Glu Leu Glu Arg Leu Ala Asn Arg
435 440 445
Ser Ser Leu Asn Ile Thr His Arg Thr Arg Arg Ser Thr Ser Asp Asn
450 455 460
Asn Thr Thr His Leu Ser Ser Met Glu Ser Val His Asn Leu Val Tyr
465 470 475 480
Ala Gln Leu Gln Phe Thr Tyr Asp Thr Leu Arg Gly Tyr Ile Asn Arg
485 490 495
Ala Leu Ala Gln Ile Ala Glu Ala Trp Cys Val Asp Gln Arg Arg Thr
500 505 510
Leu Glu Val Phe Lys Glu Leu Ser Lys Ile Asn Pro Ser Ala Ile Leu
515 520 525
Ser Ala Ile Tyr Asn Lys Pro Ile Ala Ala Arg Phe Met Gly Asp Val
530 535 540
Leu Gly Leu Ala Ser Cys Val Thr Ile Asn Gln Thr Ser Val Lys Val
545 550 555 560
Leu Arg Asp Met Asn Val Lys Glu Ser Pro Gly Arg Cys Tyr Ser Arg
565 570 575
Pro Val Val Ile Phe Asn Phe Ala Asn Ser Ser Tyr Val Gln Tyr Gly
580 585 590
Gln Leu Gly Glu Asp Asn Glu Ile Leu Leu Gly Asn His Arg Thr Glu
595 600 605
Glu Cys Gln Leu Pro Ser Leu Lys Ile Phe Ile Ala Gly Asn Ser Ala
610 615 620
Tyr Glu Tyr Val Asp Tyr Leu Phe Lys Arg Met Ile Asp Leu Ser Ser
625 630 635 640
Ile Ser Thr Val Asp Ser Met Ile Ala Leu Asp Ile Asp Pro Leu Glu
645 650 655
Asn Thr Asp Phe Arg Val Leu Glu Leu Tyr Ser Gln Lys Glu Leu Arg
660 665 670
Ser Ser Asn Val Phe Asp Leu Glu Glu Ile Met Arg Glu Phe Asn Ser
675 680 685
Tyr Lys Gln Arg Val Lys Tyr Val Glu Asp Lys Val Val Asp Pro Leu
690 695 700
Pro Pro Tyr Leu Lys Gly Leu Asp Asp Leu Met Ser Gly Leu Gly Ala
705 710 715 720
Ala Gly Lys Ala Val Gly Val Ala Ile Gly Ala Val Gly Gly Ala Val
725 730 735
Ala Ser Val Val Glu Gly Val Ala Thr Phe Leu Lys Asn Pro Phe Gly
740 745 750
Ala Phe Thr Ile Ile Leu Val Ala Ile Ala Val Val Ile Ile Thr Tyr
755 760 765
Leu Ile Tyr Thr Arg Gln Arg Arg Leu Cys Thr Gln Pro Leu Gln Asn
770 775 780
Leu Phe Pro Tyr Leu Val Ser Ala Asp Gly Thr Thr Val Thr Ser Gly
785 790 795 800
Ser Thr Lys Asp Thr Ser Leu Gln Ala Pro Pro Ser Tyr Glu Glu Ser
805 810 815
Val Tyr Asn Ser Gly Arg Lys Gly Pro Gly Pro Pro Ser Ser Asp Ala
820 825 830
Ser Thr Ala Ala Pro Pro Tyr Thr Asn Glu Gln Ala Tyr Gln Met Leu
835 840 845
Leu Ala Leu Ala Arg Leu Asp Ala Glu Gln Arg Ala Gln Gln Asn Gly
850 855 860
Thr Asp Ser Leu Asp Gly Gln Thr Gly Thr Gln Asp Lys Gly Gln Lys
865 870 875 880
Pro Asn Leu Leu Asp Arg Leu Arg His Arg Lys Asn Gly Tyr Arg His
885 890 895
Leu Lys Asp Ser Asp Glu Glu Glu Asn Val
900 905
<210> 61
<211> 171
<212> БЕЛОК
<213> Цитомегаловирус человека
<400> 61
Met Ser Pro Lys Asp Leu Thr Pro Phe Leu Thr Thr Leu Trp Leu Leu
1 5 10 15
Leu Gly His Ser Arg Val Pro Arg Val Arg Ala Glu Glu Cys Cys Glu
20 25 30
Phe Ile Asn Val Asn His Pro Pro Glu Arg Cys Tyr Asp Phe Lys Met
35 40 45
Cys Asn Arg Phe Thr Val Ala Leu Arg Cys Pro Asp Gly Glu Val Cys
50 55 60
Tyr Ser Pro Glu Lys Thr Ala Glu Ile Arg Gly Ile Val Thr Thr Met
65 70 75 80
Thr His Ser Leu Thr Arg Gln Val Val His Asn Lys Leu Thr Ser Cys
85 90 95
Asn Tyr Asn Pro Leu Tyr Leu Glu Ala Asp Gly Arg Ile Arg Cys Gly
100 105 110
Lys Val Asn Asp Lys Ala Gln Tyr Leu Leu Gly Ala Ala Gly Ser Val
115 120 125
Pro Tyr Arg Trp Ile Asn Leu Glu Tyr Asp Lys Ile Thr Arg Ile Val
130 135 140
Gly Leu Asp Gln Tyr Leu Glu Ser Val Lys Lys His Lys Arg Leu Asp
145 150 155 160
Val Cys Arg Ala Lys Met Gly Tyr Met Leu Gln
165 170
<210> 62
<211> 214
<212> БЕЛОК
<213> Цитомегаловирус человека
<400> 62
Met Leu Arg Leu Leu Leu Arg His His Phe His Cys Leu Leu Leu Cys
1 5 10 15
Ala Val Trp Ala Thr Pro Cys Leu Ala Ser Pro Trp Ser Thr Leu Thr
20 25 30
Ala Asn Gln Asn Pro Ser Pro Pro Trp Ser Lys Leu Thr Tyr Ser Lys
35 40 45
Pro His Asp Ala Ala Thr Phe Tyr Cys Pro Phe Leu Tyr Pro Ser Pro
50 55 60
Pro Arg Ser Pro Leu Gln Phe Ser Gly Phe Gln Arg Val Ser Thr Gly
65 70 75 80
Pro Glu Cys Arg Asn Glu Thr Leu Tyr Leu Leu Tyr Asn Arg Glu Gly
85 90 95
Gln Thr Leu Val Glu Arg Ser Ser Thr Trp Val Lys Lys Val Ile Trp
100 105 110
Tyr Leu Ser Gly Arg Asn Gln Thr Ile Leu Gln Arg Met Pro Arg Thr
115 120 125
Ala Ser Lys Pro Ser Asp Gly Asn Val Gln Ile Ser Val Glu Asp Ala
130 135 140
Lys Ile Phe Gly Ala His Met Val Pro Lys Gln Thr Lys Leu Leu Arg
145 150 155 160
Phe Val Val Asn Asp Gly Thr Arg Tyr Gln Met Cys Val Met Lys Leu
165 170 175
Glu Ser Trp Ala His Val Phe Arg Asp Tyr Ser Val Ser Phe Gln Val
180 185 190
Arg Leu Thr Phe Thr Glu Ala Asn Asn Gln Thr Tyr Thr Phe Cys Thr
195 200 205
His Pro Asn Leu Ile Val
210
<210> 63
<211> 129
<212> БЕЛОК
<213> Цитомегаловирус человека
<400> 63
Met Arg Leu Cys Arg Val Trp Leu Ser Val Cys Leu Cys Ala Val Val
1 5 10 15
Leu Gly Gln Cys Gln Arg Glu Thr Ala Glu Lys Asn Asp Tyr Tyr Arg
20 25 30
Val Pro His Tyr Trp Asp Ala Cys Ser Arg Ala Leu Pro Asp Gln Thr
35 40 45
Arg Tyr Lys Tyr Val Glu Gln Leu Val Asp Leu Thr Leu Asn Tyr His
50 55 60
Tyr Asp Ala Ser His Gly Leu Asp Asn Phe Asp Val Leu Lys Arg Ile
65 70 75 80
Asn Val Thr Glu Val Ser Leu Leu Ile Ser Asp Phe Arg Arg Gln Asn
85 90 95
Arg Arg Gly Gly Thr Asn Lys Arg Thr Thr Phe Asn Ala Ala Gly Ser
100 105 110
Leu Ala Pro His Ala Arg Ser Leu Glu Phe Ser Val Arg Leu Phe Ala
115 120 125
Asn
<210> 64
<211> 743
<212> БЕЛОК
<213> Цитомегаловирус человека
<400> 64
Met Arg Pro Gly Leu Pro Pro Tyr Leu Thr Val Phe Thr Val Tyr Leu
1 5 10 15
Leu Ser His Leu Pro Ser Gln Arg Tyr Gly Ala Asp Ala Ala Ser Glu
20 25 30
Ala Leu Asp Pro His Ala Phe His Leu Leu Leu Asn Thr Tyr Gly Arg
35 40 45
Pro Ile Arg Phe Leu Arg Glu Asn Thr Thr Gln Cys Thr Tyr Asn Ser
50 55 60
Ser Leu Arg Asn Ser Thr Val Val Arg Glu Asn Ala Ile Ser Phe Asn
65 70 75 80
Phe Phe Gln Ser Tyr Asn Gln Tyr Tyr Val Phe His Met Pro Arg Cys
85 90 95
Leu Phe Ala Gly Pro Leu Ala Glu Gln Phe Leu Asn Gln Val Asp Leu
100 105 110
Thr Glu Thr Leu Glu Arg Tyr Gln Gln Arg Leu Asn Thr Tyr Ala Leu
115 120 125
Val Ser Lys Asp Leu Ala Ser Tyr Arg Ser Phe Ser Gln Gln Leu Lys
130 135 140
Ala Gln Asp Ser Leu Gly Gln Gln Pro Thr Thr Val Pro Pro Pro Ile
145 150 155 160
Asp Leu Ser Ile Pro His Val Trp Met Pro Pro Gln Thr Thr Pro His
165 170 175
Asp Trp Lys Gly Ser His Thr Thr Ser Gly Leu His Arg Pro His Phe
180 185 190
Asn Gln Thr Cys Ile Leu Phe Asp Gly His Asp Leu Leu Phe Ser Thr
195 200 205
Val Thr Pro Cys Leu His Gln Gly Phe Tyr Leu Met Asp Glu Leu Arg
210 215 220
Tyr Val Lys Ile Thr Leu Thr Glu Asp Phe Phe Val Val Thr Val Ser
225 230 235 240
Ile Asp Asp Asp Thr Pro Met Leu Leu Ile Phe Gly His Leu Pro Arg
245 250 255
Val Leu Phe Lys Ala Pro Tyr Gln Arg Asp Asn Phe Ile Leu Arg Gln
260 265 270
Thr Glu Lys His Glu Leu Leu Val Leu Val Lys Lys Ala Gln Leu Asn
275 280 285
Arg His Ser Tyr Leu Lys Asp Ser Asp Phe Leu Asp Ala Ala Leu Asp
290 295 300
Phe Asn Tyr Leu Asp Leu Ser Ala Leu Leu Arg Asn Ser Phe His Arg
305 310 315 320
Tyr Ala Val Asp Val Leu Lys Ser Gly Arg Cys Gln Met Leu Asp Arg
325 330 335
Arg Thr Val Glu Met Ala Phe Ala Tyr Ala Leu Ala Leu Phe Ala Ala
340 345 350
Ala Arg Gln Glu Glu Ala Gly Thr Glu Ile Ser Ile Pro Arg Ala Leu
355 360 365
Asp Arg Gln Ala Ala Leu Leu Gln Ile Gln Glu Phe Met Ile Thr Cys
370 375 380
Leu Ser Gln Thr Pro Pro Arg Thr Thr Leu Leu Leu Tyr Pro Thr Ala
385 390 395 400
Val Asp Leu Ala Lys Arg Ala Leu Trp Thr Pro Asp Gln Ile Thr Asp
405 410 415
Ile Thr Ser Leu Val Arg Leu Val Tyr Ile Leu Ser Lys Gln Asn Gln
420 425 430
Gln His Leu Ile Pro Gln Trp Ala Leu Arg Gln Ile Ala Asp Phe Ala
435 440 445
Leu Gln Leu His Lys Thr His Leu Ala Ser Phe Leu Ser Ala Phe Ala
450 455 460
Arg Gln Glu Leu Tyr Leu Met Gly Ser Leu Val His Ser Met Leu Val
465 470 475 480
His Thr Thr Glu Arg Arg Glu Ile Phe Ile Val Glu Thr Gly Leu Cys
485 490 495
Ser Leu Ala Glu Leu Ser His Phe Thr Gln Leu Leu Ala His Pro His
500 505 510
His Glu Tyr Leu Ser Asp Leu Tyr Thr Pro Cys Ser Ser Ser Gly Arg
515 520 525
Arg Asp His Ser Leu Glu Arg Leu Thr Arg Leu Phe Pro Asp Ala Thr
530 535 540
Val Pro Ala Thr Val Pro Ala Ala Leu Ser Ile Leu Ser Thr Met Gln
545 550 555 560
Pro Ser Thr Leu Glu Thr Phe Pro Asp Leu Phe Cys Leu Pro Leu Gly
565 570 575
Glu Ser Phe Ser Ala Leu Thr Val Ser Glu His Val Ser Tyr Val Val
580 585 590
Thr Asn Gln Tyr Leu Ile Lys Gly Ile Ser Tyr Pro Val Ser Thr Thr
595 600 605
Val Val Gly Gln Ser Leu Ile Ile Thr Gln Thr Asp Ser Gln Thr Lys
610 615 620
Cys Glu Leu Thr Arg Asn Met His Thr Thr His Ser Ile Thr Ala Ala
625 630 635 640
Leu Asn Ile Ser Leu Glu Asn Cys Ala Phe Cys Gln Ser Ala Leu Leu
645 650 655
Glu Tyr Asp Asp Thr Gln Gly Val Ile Asn Ile Met Tyr Met His Asp
660 665 670
Ser Asp Asp Val Leu Phe Ala Leu Asp Pro Tyr Asn Glu Val Val Val
675 680 685
Ser Ser Pro Arg Thr His Tyr Leu Met Leu Leu Lys Asn Gly Thr Val
690 695 700
Leu Glu Val Thr Asp Val Val Val Asp Ala Thr Asp Ser Arg Leu Leu
705 710 715 720
Met Met Ser Val Tyr Ala Leu Ser Ala Ile Ile Gly Ile Tyr Leu Leu
725 730 735
Tyr Arg Met Leu Lys Thr Cys
740
<210> 65
<211> 278
<212> БЕЛОК
<213> Цитомегаловирус человека
<400> 65
Met Cys Arg Arg Pro Asp Cys Gly Phe Ser Phe Ser Pro Gly Pro Val
1 5 10 15
Val Leu Leu Trp Cys Cys Leu Leu Leu Pro Ile Val Ser Ser Val Ala
20 25 30
Val Ser Val Ala Pro Thr Ala Ala Glu Lys Val Pro Ala Glu Cys Pro
35 40 45
Glu Leu Thr Arg Arg Cys Leu Leu Gly Glu Val Phe Gln Gly Asp Lys
50 55 60
Tyr Glu Ser Trp Leu Arg Pro Leu Val Asn Val Thr Arg Arg Asp Gly
65 70 75 80
Pro Leu Ser Gln Leu Ile Arg Tyr Arg Pro Val Thr Pro Glu Ala Ala
85 90 95
Asn Ser Val Leu Leu Asp Asp Ala Phe Leu Asp Thr Leu Ala Leu Leu
100 105 110
Tyr Asn Asn Pro Asp Gln Leu Arg Ala Leu Leu Thr Leu Leu Ser Ser
115 120 125
Asp Thr Ala Pro Arg Trp Met Thr Val Met Arg Gly Tyr Ser Glu Cys
130 135 140
Gly Asp Gly Ser Pro Ala Val Tyr Thr Cys Val Asp Asp Leu Cys Arg
145 150 155 160
Gly Tyr Asp Leu Thr Arg Leu Ser Tyr Gly Arg Ser Ile Phe Thr Glu
165 170 175
His Val Leu Gly Phe Glu Leu Val Pro Pro Ser Leu Phe Asn Val Val
180 185 190
Val Ala Ile Arg Asn Glu Ala Thr Arg Thr Asn Arg Ala Val Arg Leu
195 200 205
Pro Val Ser Thr Ala Ala Ala Pro Glu Gly Ile Thr Leu Phe Tyr Gly
210 215 220
Leu Tyr Asn Ala Val Lys Glu Phe Cys Leu Arg His Gln Leu Asp Pro
225 230 235 240
Pro Leu Leu Arg His Leu Asp Lys Tyr Tyr Ala Gly Leu Pro Pro Glu
245 250 255
Leu Lys Gln Thr Arg Val Asn Leu Pro Ala His Ser Arg Tyr Gly Pro
260 265 270
Gln Ala Val Asp Ala Arg
275
<210> 66
<211> 272
<212> БЕЛОК
<213> Borreliella burgdorferi
<400> 66
Met Lys Lys Tyr Leu Leu Gly Ile Gly Leu Ile Leu Ala Leu Ile Ala
1 5 10 15
Cys Lys Gln Asn Val Ser Ser Leu Asp Glu Lys Asn Ser Val Ser Val
20 25 30
Asp Val Pro Gly Gly Met Lys Val Leu Val Ser Lys Glu Lys Asn Lys
35 40 45
Asp Gly Lys Tyr Asp Leu Met Ala Thr Val Asp Asn Val Asp Leu Lys
50 55 60
Gly Thr Ser Asp Lys Asn Asn Gly Ser Gly Ile Leu Glu Gly Val Lys
65 70 75 80
Ala Asp Lys Ser Lys Val Lys Leu Thr Val Ala Asp Asp Leu Ser Lys
85 90 95
Thr Thr Leu Glu Val Leu Lys Glu Asp Gly Thr Val Val Ser Arg Lys
100 105 110
Val Thr Ser Lys Asp Lys Ser Thr Thr Glu Ala Lys Phe Asn Glu Lys
115 120 125
Gly Glu Leu Ser Glu Lys Thr Met Thr Arg Ala Asn Gly Thr Thr Leu
130 135 140
Glu Tyr Ser Gln Met Thr Asn Glu Asp Asn Ala Ala Lys Ala Val Glu
145 150 155 160
Thr Leu Lys Asn Gly Ile Lys Phe Glu Gly Asn Leu Ala Ser Gly Lys
165 170 175
Thr Ala Val Glu Ile Lys Glu Gly Thr Val Thr Leu Lys Arg Glu Ile
180 185 190
Asp Lys Asn Gly Lys Val Thr Val Ser Leu Asn Asp Thr Ala Ser Gly
195 200 205
Ser Lys Lys Thr Ala Ser Trp Gln Glu Ser Thr Ser Thr Leu Thr Ile
210 215 220
Ser Ala Asn Ser Lys Lys Thr Lys Asp Leu Val Phe Leu Thr Asn Gly
225 230 235 240
Thr Ile Thr Val Gln Asn Tyr Asp Ser Ala Gly Thr Lys Leu Glu Gly
245 250 255
Ser Ala Ala Glu Ile Lys Lys Leu Asp Glu Leu Lys Asn Ala Leu Arg
260 265 270
<210> 67
<211> 269
<212> БЕЛОК
<213> Bordetella pertussis
<400> 67
Met Arg Cys Thr Arg Ala Ile Arg Gln Thr Ala Arg Thr Gly Trp Leu
1 5 10 15
Thr Trp Leu Ala Ile Leu Ala Val Thr Ala Pro Val Thr Ser Pro Ala
20 25 30
Trp Ala Asp Asp Pro Pro Ala Thr Val Tyr Arg Tyr Asp Ser Arg Pro
35 40 45
Pro Glu Asp Val Phe Gln Asn Gly Phe Thr Ala Trp Gly Asn Asn Asp
50 55 60
Asn Val Leu Asp His Leu Thr Gly Arg Ser Cys Gln Val Gly Ser Ser
65 70 75 80
Asn Ser Ala Phe Val Ser Thr Ser Ser Ser Arg Arg Tyr Thr Glu Val
85 90 95
Tyr Leu Glu His Arg Met Gln Glu Ala Val Glu Ala Glu Arg Ala Gly
100 105 110
Arg Gly Thr Gly His Phe Ile Gly Tyr Ile Tyr Glu Val Arg Ala Asp
115 120 125
Asn Asn Phe Tyr Gly Ala Ala Ser Ser Tyr Phe Glu Tyr Val Asp Thr
130 135 140
Tyr Gly Asp Asn Ala Gly Arg Ile Leu Ala Gly Ala Leu Ala Thr Tyr
145 150 155 160
Gln Ser Glu Tyr Leu Ala His Arg Arg Ile Pro Pro Glu Asn Ile Arg
165 170 175
Arg Val Thr Arg Val Tyr His Asn Gly Ile Thr Gly Glu Thr Thr Thr
180 185 190
Thr Glu Tyr Ser Asn Ala Arg Tyr Val Ser Gln Gln Thr Arg Ala Asn
195 200 205
Pro Asn Pro Tyr Thr Ser Arg Arg Ser Val Ala Ser Ile Val Gly Thr
210 215 220
Leu Val Arg Met Ala Pro Val Ile Gly Ala Cys Met Ala Arg Gln Ala
225 230 235 240
Glu Ser Ser Glu Ala Met Ala Ala Trp Ser Glu Arg Ala Gly Glu Ala
245 250 255
Met Val Leu Val Tyr Tyr Glu Ser Ile Ala Tyr Ser Phe
260 265
<210> 68
<211> 495
<212> БЕЛОК
<213> Вирус Денге
<400> 68
Met Arg Cys Val Gly Ile Gly Asn Arg Asp Phe Val Glu Gly Leu Ser
1 5 10 15
Gly Ala Thr Trp Val Asp Val Val Leu Glu His Gly Ser Cys Val Thr
20 25 30
Thr Met Ala Lys Asp Lys Pro Thr Leu Asp Ile Glu Leu Leu Lys Thr
35 40 45
Glu Val Thr Asn Pro Ala Val Leu Arg Lys Leu Cys Ile Glu Ala Lys
50 55 60
Ile Ser Asn Thr Thr Thr Asp Ser Arg Cys Pro Thr Gln Gly Glu Ala
65 70 75 80
Thr Leu Val Glu Glu Gln Asp Thr Asn Phe Val Cys Arg Arg Thr Phe
85 90 95
Val Asp Arg Gly Trp Gly Asn Gly Cys Gly Leu Phe Gly Lys Gly Ser
100 105 110
Leu Ile Thr Cys Ala Lys Phe Lys Cys Val Thr Lys Leu Glu Gly Lys
115 120 125
Ile Val Gln Tyr Glu Asn Leu Lys Tyr Ser Val Ile Val Thr Val His
130 135 140
Thr Gly Asp Gln His Gln Val Gly Asn Glu Thr Thr Glu His Gly Thr
145 150 155 160
Thr Ala Thr Ile Thr Pro Gln Ala Pro Thr Ser Glu Ile Gln Leu Thr
165 170 175
Asp Tyr Gly Ala Leu Thr Leu Asp Cys Ser Pro Arg Thr Gly Leu Asp
180 185 190
Phe Asn Glu Met Val Leu Leu Thr Met Glu Lys Lys Ser Trp Leu Val
195 200 205
His Lys Gln Trp Phe Leu Asp Leu Pro Leu Pro Trp Thr Ser Gly Ala
210 215 220
Ser Thr Ser Gln Glu Thr Trp Asn Arg Gln Asp Leu Leu Val Thr Phe
225 230 235 240
Lys Thr Ala His Ala Lys Lys Gln Glu Val Val Val Leu Gly Ser Gln
245 250 255
Glu Gly Ala Met His Thr Ala Leu Thr Gly Ala Thr Glu Ile Gln Thr
260 265 270
Ser Gly Thr Thr Thr Ile Phe Ala Gly His Leu Lys Cys Arg Leu Lys
275 280 285
Met Asp Lys Leu Thr Leu Lys Gly Met Ser Tyr Val Met Cys Thr Gly
290 295 300
Ser Phe Lys Leu Glu Lys Glu Val Ala Glu Thr Gln His Gly Thr Val
305 310 315 320
Leu Val Gln Val Lys Tyr Glu Gly Thr Asp Ala Pro Cys Lys Ile Pro
325 330 335
Phe Ser Ser Gln Asp Glu Lys Gly Val Thr Gln Asn Gly Arg Leu Ile
340 345 350
Thr Ala Asn Pro Ile Val Thr Asp Lys Glu Lys Pro Val Asn Ile Glu
355 360 365
Ala Glu Pro Pro Phe Gly Glu Ser Tyr Ile Val Val Gly Ala Gly Glu
370 375 380
Lys Ala Leu Lys Leu Ser Trp Phe Lys Lys Gly Ser Ser Ile Gly Lys
385 390 395 400
Met Phe Glu Ala Thr Ala Arg Gly Ala Arg Arg Met Ala Ile Leu Gly
405 410 415
Asp Thr Ala Trp Asp Phe Gly Ser Ile Gly Gly Val Phe Thr Ser Val
420 425 430
Gly Lys Leu Ile His Gln Ile Phe Gly Thr Ala Tyr Gly Val Leu Phe
435 440 445
Ser Gly Val Ser Trp Thr Met Lys Ile Gly Ile Gly Ile Leu Leu Thr
450 455 460
Trp Leu Gly Leu Asn Ser Arg Ser Thr Ser Leu Ser Met Thr Cys Ile
465 470 475 480
Ala Val Gly Met Val Thr Leu Tyr Leu Gly Val Met Val Gln Ala
485 490 495
<210> 69
<211> 1255
<212> БЕЛОК
<213> Короновирус SARS человека
<400> 69
Met Phe Ile Phe Leu Leu Phe Leu Thr Leu Thr Ser Gly Ser Asp Leu
1 5 10 15
Asp Arg Cys Thr Thr Phe Asp Asp Val Gln Ala Pro Asn Tyr Thr Gln
20 25 30
His Thr Ser Ser Met Arg Gly Val Tyr Tyr Pro Asp Glu Ile Phe Arg
35 40 45
Ser Asp Thr Leu Tyr Leu Thr Gln Asp Leu Phe Leu Pro Phe Tyr Ser
50 55 60
Asn Val Thr Gly Phe His Thr Ile Asn His Thr Phe Gly Asn Pro Val
65 70 75 80
Ile Pro Phe Lys Asp Gly Ile Tyr Phe Ala Ala Thr Glu Lys Ser Asn
85 90 95
Val Val Arg Gly Trp Val Phe Gly Ser Thr Met Asn Asn Lys Ser Gln
100 105 110
Ser Val Ile Ile Ile Asn Asn Ser Thr Asn Val Val Ile Arg Ala Cys
115 120 125
Asn Phe Glu Leu Cys Asp Asn Pro Phe Phe Ala Val Ser Lys Pro Met
130 135 140
Gly Thr Gln Thr His Thr Met Ile Phe Asp Asn Ala Phe Asn Cys Thr
145 150 155 160
Phe Glu Tyr Ile Ser Asp Ala Phe Ser Leu Asp Val Ser Glu Lys Ser
165 170 175
Gly Asn Phe Lys His Leu Arg Glu Phe Val Phe Lys Asn Lys Asp Gly
180 185 190
Phe Leu Tyr Val Tyr Lys Gly Tyr Gln Pro Ile Asp Val Val Arg Asp
195 200 205
Leu Pro Ser Gly Phe Asn Thr Leu Lys Pro Ile Phe Lys Leu Pro Leu
210 215 220
Gly Ile Asn Ile Thr Asn Phe Arg Ala Ile Leu Thr Ala Phe Ser Pro
225 230 235 240
Ala Gln Asp Ile Trp Gly Thr Ser Ala Ala Ala Tyr Phe Val Gly Tyr
245 250 255
Leu Lys Pro Thr Thr Phe Met Leu Lys Tyr Asp Glu Asn Gly Thr Ile
260 265 270
Thr Asp Ala Val Asp Cys Ser Gln Asn Pro Leu Ala Glu Leu Lys Cys
275 280 285
Ser Val Lys Ser Phe Glu Ile Asp Lys Gly Ile Tyr Gln Thr Ser Asn
290 295 300
Phe Arg Val Val Pro Ser Gly Asp Val Val Arg Phe Pro Asn Ile Thr
305 310 315 320
Asn Leu Cys Pro Phe Gly Glu Val Phe Asn Ala Thr Lys Phe Pro Ser
325 330 335
Val Tyr Ala Trp Glu Arg Lys Lys Ile Ser Asn Cys Val Ala Asp Tyr
340 345 350
Ser Val Leu Tyr Asn Ser Thr Phe Phe Ser Thr Phe Lys Cys Tyr Gly
355 360 365
Val Ser Ala Thr Lys Leu Asn Asp Leu Cys Phe Ser Asn Val Tyr Ala
370 375 380
Asp Ser Phe Val Val Lys Gly Asp Asp Val Arg Gln Ile Ala Pro Gly
385 390 395 400
Gln Thr Gly Val Ile Ala Asp Tyr Asn Tyr Lys Leu Pro Asp Asp Phe
405 410 415
Met Gly Cys Val Leu Ala Trp Asn Thr Arg Asn Ile Asp Ala Thr Ser
420 425 430
Thr Gly Asn Tyr Asn Tyr Lys Tyr Arg Tyr Leu Arg His Gly Lys Leu
435 440 445
Arg Pro Phe Glu Arg Asp Ile Ser Asn Val Pro Phe Ser Pro Asp Gly
450 455 460
Lys Pro Cys Thr Pro Pro Ala Leu Asn Cys Tyr Trp Pro Leu Asn Asp
465 470 475 480
Tyr Gly Phe Tyr Thr Thr Thr Gly Ile Gly Tyr Gln Pro Tyr Arg Val
485 490 495
Val Val Leu Ser Phe Glu Leu Leu Asn Ala Pro Ala Thr Val Cys Gly
500 505 510
Pro Lys Leu Ser Thr Asp Leu Ile Lys Asn Gln Cys Val Asn Phe Asn
515 520 525
Phe Asn Gly Leu Thr Gly Thr Gly Val Leu Thr Pro Ser Ser Lys Arg
530 535 540
Phe Gln Pro Phe Gln Gln Phe Gly Arg Asp Val Ser Asp Phe Thr Asp
545 550 555 560
Ser Val Arg Asp Pro Lys Thr Ser Glu Ile Leu Asp Ile Ser Pro Cys
565 570 575
Ser Phe Gly Gly Val Ser Val Ile Thr Pro Gly Thr Asn Ala Ser Ser
580 585 590
Glu Val Ala Val Leu Tyr Gln Asp Val Asn Cys Thr Asp Val Ser Thr
595 600 605
Ala Ile His Ala Asp Gln Leu Thr Pro Ala Trp Arg Ile Tyr Ser Thr
610 615 620
Gly Asn Asn Val Phe Gln Thr Gln Ala Gly Cys Leu Ile Gly Ala Glu
625 630 635 640
His Val Asp Thr Ser Tyr Glu Cys Asp Ile Pro Ile Gly Ala Gly Ile
645 650 655
Cys Ala Ser Tyr His Thr Val Ser Leu Leu Arg Ser Thr Ser Gln Lys
660 665 670
Ser Ile Val Ala Tyr Thr Met Ser Leu Gly Ala Asp Ser Ser Ile Ala
675 680 685
Tyr Ser Asn Asn Thr Ile Ala Ile Pro Thr Asn Phe Ser Ile Ser Ile
690 695 700
Thr Thr Glu Val Met Pro Val Ser Met Ala Lys Thr Ser Val Asp Cys
705 710 715 720
Asn Met Tyr Ile Cys Gly Asp Ser Thr Glu Cys Ala Asn Leu Leu Leu
725 730 735
Gln Tyr Gly Ser Phe Cys Thr Gln Leu Asn Arg Ala Leu Ser Gly Ile
740 745 750
Ala Ala Glu Gln Asp Arg Asn Thr Arg Glu Val Phe Ala Gln Val Lys
755 760 765
Gln Met Tyr Lys Thr Pro Thr Leu Lys Tyr Phe Gly Gly Phe Asn Phe
770 775 780
Ser Gln Ile Leu Pro Asp Pro Leu Lys Pro Thr Lys Arg Ser Phe Ile
785 790 795 800
Glu Asp Leu Leu Phe Asn Lys Val Thr Leu Ala Asp Ala Gly Phe Met
805 810 815
Lys Gln Tyr Gly Glu Cys Leu Gly Asp Ile Asn Ala Arg Asp Leu Ile
820 825 830
Cys Ala Gln Lys Phe Asn Gly Leu Thr Val Leu Pro Pro Leu Leu Thr
835 840 845
Asp Asp Met Ile Ala Ala Tyr Thr Ala Ala Leu Val Ser Gly Thr Ala
850 855 860
Thr Ala Gly Trp Thr Phe Gly Ala Gly Ala Ala Leu Gln Ile Pro Phe
865 870 875 880
Ala Met Gln Met Ala Tyr Arg Phe Asn Gly Ile Gly Val Thr Gln Asn
885 890 895
Val Leu Tyr Glu Asn Gln Lys Gln Ile Ala Asn Gln Phe Asn Lys Ala
900 905 910
Ile Ser Gln Ile Gln Glu Ser Leu Thr Thr Thr Ser Thr Ala Leu Gly
915 920 925
Lys Leu Gln Asp Val Val Asn Gln Asn Ala Gln Ala Leu Asn Thr Leu
930 935 940
Val Lys Gln Leu Ser Ser Asn Phe Gly Ala Ile Ser Ser Val Leu Asn
945 950 955 960
Asp Ile Leu Ser Arg Leu Asp Lys Val Glu Ala Glu Val Gln Ile Asp
965 970 975
Arg Leu Ile Thr Gly Arg Leu Gln Ser Leu Gln Thr Tyr Val Thr Gln
980 985 990
Gln Leu Ile Arg Ala Ala Glu Ile Arg Ala Ser Ala Asn Leu Ala Ala
995 1000 1005
Thr Lys Met Ser Glu Cys Val Leu Gly Gln Ser Lys Arg Val Asp
1010 1015 1020
Phe Cys Gly Lys Gly Tyr His Leu Met Ser Phe Pro Gln Ala Ala
1025 1030 1035
Pro His Gly Val Val Phe Leu His Val Thr Tyr Val Pro Ser Gln
1040 1045 1050
Glu Arg Asn Phe Thr Thr Ala Pro Ala Ile Cys His Glu Gly Lys
1055 1060 1065
Ala Tyr Phe Pro Arg Glu Gly Val Phe Val Phe Asn Gly Thr Ser
1070 1075 1080
Trp Phe Ile Thr Gln Arg Asn Phe Phe Ser Pro Gln Ile Ile Thr
1085 1090 1095
Thr Asp Asn Thr Phe Val Ser Gly Asn Cys Asp Val Val Ile Gly
1100 1105 1110
Ile Ile Asn Asn Thr Val Tyr Asp Pro Leu Gln Pro Glu Leu Asp
1115 1120 1125
Ser Phe Lys Glu Glu Leu Asp Lys Tyr Phe Lys Asn His Thr Ser
1130 1135 1140
Pro Asp Val Asp Leu Gly Asp Ile Ser Gly Ile Asn Ala Ser Val
1145 1150 1155
Val Asn Ile Gln Lys Glu Ile Asp Arg Leu Asn Glu Val Ala Lys
1160 1165 1170
Asn Leu Asn Glu Ser Leu Ile Asp Leu Gln Glu Leu Gly Lys Tyr
1175 1180 1185
Glu Gln Tyr Ile Lys Trp Pro Trp Tyr Val Trp Leu Gly Phe Ile
1190 1195 1200
Ala Gly Leu Ile Ala Ile Val Met Val Thr Ile Leu Leu Cys Cys
1205 1210 1215
Met Thr Ser Cys Cys Ser Cys Leu Lys Gly Ala Cys Ser Cys Gly
1220 1225 1230
Ser Cys Cys Lys Phe Asp Glu Asp Asp Ser Glu Pro Val Leu Lys
1235 1240 1245
Gly Val Lys Leu His Tyr Thr
1250 1255
<210> 70
<211> 1353
<212> БЕЛОК
<213> вирус ближневосточного респираторного синдрома (MERS)
<400> 70
Met Ile His Ser Val Phe Leu Leu Met Phe Leu Leu Thr Pro Thr Glu
1 5 10 15
Ser Tyr Val Asp Val Gly Pro Asp Ser Ile Lys Ser Ala Cys Ile Glu
20 25 30
Val Asp Ile Gln Gln Thr Phe Phe Asp Lys Thr Trp Pro Arg Pro Ile
35 40 45
Asp Val Ser Lys Ala Asp Gly Ile Ile Tyr Pro Gln Gly Arg Thr Tyr
50 55 60
Ser Asn Ile Thr Ile Thr Tyr Gln Gly Leu Phe Pro Tyr Gln Gly Asp
65 70 75 80
His Gly Asp Met Tyr Val Tyr Ser Ala Gly His Ala Thr Gly Thr Thr
85 90 95
Pro Gln Lys Leu Phe Val Ala Asn Tyr Ser Gln Asp Val Lys Gln Phe
100 105 110
Ala Asn Gly Phe Val Val Arg Ile Gly Ala Ala Ala Asn Ser Thr Gly
115 120 125
Thr Val Ile Ile Ser Pro Ser Thr Ser Ala Thr Ile Arg Lys Ile Tyr
130 135 140
Pro Ala Phe Met Leu Gly Ser Ser Val Gly Asn Phe Ser Asp Gly Lys
145 150 155 160
Met Gly Arg Phe Phe Asn His Thr Leu Val Leu Leu Pro Asp Gly Cys
165 170 175
Gly Thr Leu Leu Arg Ala Phe Tyr Cys Ile Leu Glu Pro Arg Ser Gly
180 185 190
Asn His Cys Pro Ala Gly Asn Ser Tyr Thr Ser Phe Ala Thr Tyr His
195 200 205
Thr Pro Ala Thr Asp Cys Ser Asp Gly Asn Tyr Asn Arg Asn Ala Ser
210 215 220
Leu Asn Ser Phe Lys Glu Tyr Phe Asn Leu Arg Asn Cys Thr Phe Met
225 230 235 240
Tyr Thr Tyr Asn Ile Thr Glu Asp Glu Ile Leu Glu Trp Phe Gly Ile
245 250 255
Thr Gln Thr Ala Gln Gly Val His Leu Phe Ser Ser Arg Tyr Val Asp
260 265 270
Leu Tyr Gly Gly Asn Met Phe Gln Phe Ala Thr Leu Pro Val Tyr Asp
275 280 285
Thr Ile Lys Tyr Tyr Ser Ile Ile Pro His Ser Ile Arg Ser Ile Gln
290 295 300
Ser Asp Arg Lys Ala Trp Ala Ala Phe Tyr Val Tyr Lys Leu Gln Pro
305 310 315 320
Leu Thr Phe Leu Leu Asp Phe Ser Val Asp Gly Tyr Ile Arg Arg Ala
325 330 335
Ile Asp Cys Gly Phe Asn Asp Leu Ser Gln Leu His Cys Ser Tyr Glu
340 345 350
Ser Phe Asp Val Glu Ser Gly Val Tyr Ser Val Ser Ser Phe Glu Ala
355 360 365
Lys Pro Ser Gly Ser Val Val Glu Gln Ala Glu Gly Val Glu Cys Asp
370 375 380
Phe Ser Pro Leu Leu Ser Gly Thr Pro Pro Gln Val Tyr Asn Phe Lys
385 390 395 400
Arg Leu Val Phe Thr Asn Cys Asn Tyr Asn Leu Thr Lys Leu Leu Ser
405 410 415
Leu Phe Ser Val Asn Asp Phe Thr Cys Ser Gln Ile Ser Pro Ala Ala
420 425 430
Ile Ala Ser Asn Cys Tyr Ser Ser Leu Ile Leu Asp Tyr Phe Ser Tyr
435 440 445
Pro Leu Ser Met Lys Ser Asp Leu Ser Val Ser Ser Ala Gly Pro Ile
450 455 460
Ser Gln Phe Asn Tyr Lys Gln Ser Phe Ser Asn Pro Thr Cys Leu Ile
465 470 475 480
Leu Ala Thr Val Pro His Asn Leu Thr Thr Ile Thr Lys Pro Leu Lys
485 490 495
Tyr Ser Tyr Ile Asn Lys Cys Ser Arg Leu Leu Ser Asp Asp Arg Thr
500 505 510
Glu Val Pro Gln Leu Val Asn Ala Asn Gln Tyr Ser Pro Cys Val Ser
515 520 525
Ile Val Pro Ser Thr Val Trp Glu Asp Gly Asp Tyr Tyr Arg Lys Gln
530 535 540
Leu Ser Pro Leu Glu Gly Gly Gly Trp Leu Val Ala Ser Gly Ser Thr
545 550 555 560
Val Ala Met Thr Glu Gln Leu Gln Met Gly Phe Gly Ile Thr Val Gln
565 570 575
Tyr Gly Thr Asp Thr Asn Ser Val Cys Pro Lys Leu Glu Phe Ala Asn
580 585 590
Asp Thr Lys Ile Ala Ser Gln Leu Gly Asn Cys Val Glu Tyr Ser Leu
595 600 605
Tyr Gly Val Ser Gly Arg Gly Val Phe Gln Asn Cys Thr Ala Val Gly
610 615 620
Val Arg Gln Gln Arg Phe Val Tyr Asp Ala Tyr Gln Asn Leu Val Gly
625 630 635 640
Tyr Tyr Ser Asp Asp Gly Asn Tyr Tyr Cys Leu Arg Ala Cys Val Ser
645 650 655
Val Pro Val Ser Val Ile Tyr Asp Lys Glu Thr Lys Thr His Ala Thr
660 665 670
Leu Phe Gly Ser Val Ala Cys Glu His Ile Ser Ser Thr Met Ser Gln
675 680 685
Tyr Ser Arg Ser Thr Arg Ser Met Leu Lys Arg Arg Asp Ser Thr Tyr
690 695 700
Gly Pro Leu Gln Thr Pro Val Gly Cys Val Leu Gly Leu Val Asn Ser
705 710 715 720
Ser Leu Phe Val Glu Asp Cys Lys Leu Pro Leu Gly Gln Ser Leu Cys
725 730 735
Ala Leu Pro Asp Thr Pro Ser Thr Leu Thr Pro Arg Ser Val Arg Ser
740 745 750
Val Pro Gly Glu Met Arg Leu Ala Ser Ile Ala Phe Asn His Pro Ile
755 760 765
Gln Val Asp Gln Leu Asn Ser Ser Tyr Phe Lys Leu Ser Ile Pro Thr
770 775 780
Asn Phe Ser Phe Gly Val Thr Gln Glu Tyr Ile Gln Thr Thr Ile Gln
785 790 795 800
Lys Val Thr Val Asp Cys Lys Gln Tyr Val Cys Asn Gly Phe Gln Lys
805 810 815
Cys Glu Gln Leu Leu Arg Glu Tyr Gly Gln Phe Cys Ser Lys Ile Asn
820 825 830
Gln Ala Leu His Gly Ala Asn Leu Arg Gln Asp Asp Ser Val Arg Asn
835 840 845
Leu Phe Ala Ser Val Lys Ser Ser Gln Ser Ser Pro Ile Ile Pro Gly
850 855 860
Phe Gly Gly Asp Phe Asn Leu Thr Leu Leu Glu Pro Val Ser Ile Ser
865 870 875 880
Thr Gly Ser Arg Ser Ala Arg Ser Ala Ile Glu Asp Leu Leu Phe Asp
885 890 895
Lys Val Thr Ile Ala Asp Pro Gly Tyr Met Gln Gly Tyr Asp Asp Cys
900 905 910
Met Gln Gln Gly Pro Ala Ser Ala Arg Asp Leu Ile Cys Ala Gln Tyr
915 920 925
Val Ala Gly Tyr Lys Val Leu Pro Pro Leu Met Asp Val Asn Met Glu
930 935 940
Ala Ala Tyr Thr Ser Ser Leu Leu Gly Ser Ile Ala Gly Val Gly Trp
945 950 955 960
Thr Ala Gly Leu Ser Ser Phe Ala Ala Ile Pro Phe Ala Gln Ser Ile
965 970 975
Phe Tyr Arg Leu Asn Gly Val Gly Ile Thr Gln Gln Val Leu Ser Glu
980 985 990
Asn Gln Lys Leu Ile Ala Asn Lys Phe Asn Gln Ala Leu Gly Ala Met
995 1000 1005
Gln Thr Gly Phe Thr Thr Thr Asn Glu Ala Phe His Lys Val Gln
1010 1015 1020
Asp Ala Val Asn Asn Asn Ala Gln Ala Leu Ser Lys Leu Ala Ser
1025 1030 1035
Glu Leu Ser Asn Thr Phe Gly Ala Ile Ser Ala Ser Ile Gly Asp
1040 1045 1050
Ile Ile Gln Arg Leu Asp Val Leu Glu Gln Asp Ala Gln Ile Asp
1055 1060 1065
Arg Leu Ile Asn Gly Arg Leu Thr Thr Leu Asn Ala Phe Val Ala
1070 1075 1080
Gln Gln Leu Val Arg Ser Glu Ser Ala Ala Leu Ser Ala Gln Leu
1085 1090 1095
Ala Lys Asp Lys Val Asn Glu Cys Val Lys Ala Gln Ser Lys Arg
1100 1105 1110
Ser Gly Phe Cys Gly Gln Gly Thr His Ile Val Ser Phe Val Val
1115 1120 1125
Asn Ala Pro Asn Gly Leu Tyr Phe Met His Val Gly Tyr Tyr Pro
1130 1135 1140
Ser Asn His Ile Glu Val Val Ser Ala Tyr Gly Leu Cys Asp Ala
1145 1150 1155
Ala Asn Pro Thr Asn Cys Ile Ala Pro Val Asn Gly Tyr Phe Ile
1160 1165 1170
Lys Thr Asn Asn Thr Arg Ile Val Asp Glu Trp Ser Tyr Thr Gly
1175 1180 1185
Ser Ser Phe Tyr Ala Pro Glu Pro Ile Thr Ser Leu Asn Thr Lys
1190 1195 1200
Tyr Val Ala Pro Gln Val Thr Tyr Gln Asn Ile Ser Thr Asn Leu
1205 1210 1215
Pro Pro Pro Leu Leu Gly Asn Ser Thr Gly Ile Asp Phe Gln Asp
1220 1225 1230
Glu Leu Asp Glu Phe Phe Lys Asn Val Ser Thr Ser Ile Pro Asn
1235 1240 1245
Phe Gly Ser Leu Thr Gln Ile Asn Thr Thr Leu Leu Asp Leu Thr
1250 1255 1260
Tyr Glu Met Leu Ser Leu Gln Gln Val Val Lys Ala Leu Asn Glu
1265 1270 1275
Ser Tyr Ile Asp Leu Lys Glu Leu Gly Asn Tyr Thr Tyr Tyr Asn
1280 1285 1290
Lys Trp Pro Trp Tyr Ile Trp Leu Gly Phe Ile Ala Gly Leu Val
1295 1300 1305
Ala Leu Ala Leu Cys Val Phe Phe Ile Leu Cys Cys Thr Gly Cys
1310 1315 1320
Gly Thr Asn Cys Met Gly Lys Leu Lys Cys Asn Arg Cys Cys Asp
1325 1330 1335
Arg Tyr Glu Glu Tyr Asp Leu Glu Pro His Lys Val His Val His
1340 1345 1350
<210> 71
<211> 676
<212> БЕЛОК
<213> Заирский эболавирус
<400> 71
Met Gly Val Thr Gly Ile Leu Gln Leu Pro Arg Asp Arg Phe Lys Arg
1 5 10 15
Thr Ser Phe Phe Leu Trp Val Ile Ile Leu Phe Gln Arg Thr Phe Ser
20 25 30
Ile Pro Leu Gly Val Ile His Asn Ser Thr Leu Gln Val Ser Asp Val
35 40 45
Asp Lys Leu Val Cys Arg Asp Lys Leu Ser Ser Thr Asn Gln Leu Arg
50 55 60
Ser Val Gly Leu Asn Leu Glu Gly Asn Gly Val Ala Thr Asp Val Pro
65 70 75 80
Ser Ala Thr Lys Arg Trp Gly Phe Arg Ser Gly Val Pro Pro Lys Val
85 90 95
Val Asn Tyr Glu Ala Gly Glu Trp Ala Glu Asn Cys Tyr Asn Leu Glu
100 105 110
Ile Lys Lys Pro Asp Gly Ser Glu Cys Leu Pro Ala Ala Pro Asp Gly
115 120 125
Ile Arg Gly Phe Pro Arg Cys Arg Tyr Val His Lys Val Ser Gly Thr
130 135 140
Gly Pro Cys Ala Gly Asp Phe Ala Phe His Lys Glu Gly Ala Phe Phe
145 150 155 160
Leu Tyr Asp Arg Leu Ala Ser Thr Val Ile Tyr Arg Gly Thr Thr Phe
165 170 175
Ala Glu Gly Val Val Ala Phe Leu Ile Leu Pro Gln Ala Lys Lys Asp
180 185 190
Phe Phe Ser Ser His Pro Leu Arg Glu Pro Val Asn Ala Thr Glu Asp
195 200 205
Pro Ser Ser Gly Tyr Tyr Ser Thr Thr Ile Arg Tyr Gln Ala Thr Gly
210 215 220
Phe Gly Thr Asn Glu Thr Glu Tyr Leu Phe Glu Val Asp Asn Leu Thr
225 230 235 240
Tyr Val Gln Leu Glu Ser Arg Phe Thr Pro Gln Phe Leu Leu Gln Leu
245 250 255
Asn Glu Thr Ile Tyr Thr Ser Gly Lys Arg Ser Asn Thr Thr Gly Lys
260 265 270
Leu Ile Trp Lys Val Asn Pro Glu Ile Asp Thr Thr Ile Gly Glu Trp
275 280 285
Ala Phe Trp Glu Thr Lys Lys Asn Leu Thr Arg Lys Ile Arg Ser Glu
290 295 300
Glu Leu Ser Phe Thr Val Val Ser Asn Gly Ala Lys Asn Ile Ser Gly
305 310 315 320
Gln Ser Pro Ala Arg Thr Ser Ser Asp Pro Gly Thr Asn Thr Thr Thr
325 330 335
Glu Asp His Lys Ile Met Ala Ser Glu Asn Ser Ser Ala Met Val Gln
340 345 350
Val His Ser Gln Gly Arg Glu Ala Ala Val Ser His Leu Thr Thr Leu
355 360 365
Ala Thr Ile Ser Thr Ser Pro Gln Ser Leu Thr Thr Lys Pro Gly Pro
370 375 380
Asp Asn Ser Thr His Asn Thr Pro Val Tyr Lys Leu Asp Ile Ser Glu
385 390 395 400
Ala Thr Gln Val Glu Gln His His Arg Arg Thr Asp Asn Asp Ser Thr
405 410 415
Ala Ser Asp Thr Pro Ser Ala Thr Thr Ala Ala Gly Pro Pro Lys Ala
420 425 430
Glu Asn Thr Asn Thr Ser Lys Ser Thr Asp Phe Leu Asp Pro Ala Thr
435 440 445
Thr Thr Ser Pro Gln Asn His Ser Glu Thr Ala Gly Asn Asn Asn Thr
450 455 460
His His Gln Asp Thr Gly Glu Glu Ser Ala Ser Ser Gly Lys Leu Gly
465 470 475 480
Leu Ile Thr Asn Thr Ile Ala Gly Val Ala Gly Leu Ile Thr Gly Gly
485 490 495
Arg Arg Thr Arg Arg Glu Ala Ile Val Asn Ala Gln Pro Lys Cys Asn
500 505 510
Pro Asn Leu His Tyr Trp Thr Thr Gln Asp Glu Gly Ala Ala Ile Gly
515 520 525
Leu Ala Trp Ile Pro Tyr Phe Gly Pro Ala Ala Glu Gly Ile Tyr Ile
530 535 540
Glu Gly Leu Met His Asn Gln Asp Gly Leu Ile Cys Gly Leu Arg Gln
545 550 555 560
Leu Ala Asn Glu Thr Thr Gln Ala Leu Gln Leu Phe Leu Arg Ala Thr
565 570 575
Thr Glu Leu Arg Thr Phe Ser Ile Leu Asn Arg Lys Ala Ile Asp Phe
580 585 590
Leu Leu Gln Arg Trp Gly Gly Thr Cys His Ile Leu Gly Pro Asp Cys
595 600 605
Cys Ile Glu Pro His Asp Trp Thr Lys Asn Ile Thr Asp Lys Ile Asp
610 615 620
Gln Ile Ile His Asp Phe Val Asp Lys Thr Leu Pro Asp Gln Gly Asp
625 630 635 640
Asn Asp Asn Trp Trp Thr Gly Trp Arg Gln Trp Ile Pro Ala Gly Ile
645 650 655
Gly Val Thr Gly Val Ile Ile Ala Val Ile Ala Leu Phe Cys Ile Cys
660 665 670
Lys Phe Val Phe
675
<210> 72
<211> 681
<212> БЕЛОК
<213> марбургский вирус озера Виктория
<400> 72
Met Lys Thr Thr Cys Phe Leu Ile Ser Leu Ile Leu Ile Gln Gly Thr
1 5 10 15
Lys Asn Leu Pro Ile Leu Glu Ile Ala Ser Asn Asn Gln Pro Gln Asn
20 25 30
Val Asp Ser Val Cys Ser Gly Thr Leu Gln Lys Thr Glu Asp Val His
35 40 45
Leu Met Gly Phe Thr Leu Ser Gly Gln Lys Val Ala Asp Ser Pro Leu
50 55 60
Glu Ala Ser Lys Arg Trp Ala Phe Arg Thr Gly Val Pro Pro Lys Asn
65 70 75 80
Val Glu Tyr Thr Glu Gly Glu Glu Ala Lys Thr Cys Tyr Asn Ile Ser
85 90 95
Val Thr Asp Pro Ser Gly Lys Ser Leu Leu Leu Asp Pro Pro Thr Asn
100 105 110
Ile Arg Asp Tyr Pro Lys Cys Lys Thr Ile His His Ile Gln Gly Gln
115 120 125
Asn Pro His Ala Gln Gly Ile Ala Leu His Leu Trp Gly Ala Phe Phe
130 135 140
Leu Tyr Asp Arg Ile Ala Ser Thr Thr Met Tyr Arg Gly Lys Val Phe
145 150 155 160
Thr Glu Gly Asn Ile Ala Ala Met Ile Val Asn Lys Thr Val His Lys
165 170 175
Met Ile Phe Ser Arg Gln Gly Gln Gly Tyr Arg His Met Asn Leu Thr
180 185 190
Ser Thr Asn Lys Tyr Trp Thr Ser Ser Asn Gly Thr Gln Thr Asn Asp
195 200 205
Thr Gly Cys Phe Gly Ala Leu Gln Glu Tyr Asn Ser Thr Lys Asn Gln
210 215 220
Thr Cys Ala Pro Ser Lys Ile Pro Pro Pro Leu Pro Thr Ala Arg Pro
225 230 235 240
Glu Ile Lys Leu Thr Ser Thr Pro Thr Asp Ala Thr Lys Leu Asn Thr
245 250 255
Thr Asp Pro Ser Ser Asp Asp Glu Asp Leu Ala Thr Ser Gly Ser Gly
260 265 270
Ser Gly Glu Arg Glu Pro His Thr Thr Ser Asp Ala Val Thr Lys Gln
275 280 285
Gly Leu Ser Ser Thr Met Pro Pro Thr Pro Ser Pro Gln Pro Ser Thr
290 295 300
Pro Gln Gln Gly Gly Asn Asn Thr Asn His Ser Gln Asp Ala Val Thr
305 310 315 320
Glu Leu Asp Lys Asn Asn Thr Thr Ala Gln Pro Ser Met Pro Pro His
325 330 335
Asn Thr Thr Thr Ile Ser Thr Asn Asn Thr Ser Lys His Asn Phe Ser
340 345 350
Thr Leu Ser Ala Pro Leu Gln Asn Thr Thr Asn Asp Asn Thr Gln Ser
355 360 365
Thr Ile Thr Glu Asn Glu Gln Thr Ser Ala Pro Ser Ile Thr Thr Leu
370 375 380
Pro Pro Thr Gly Asn Pro Thr Thr Ala Lys Ser Thr Ser Ser Lys Lys
385 390 395 400
Gly Pro Ala Thr Thr Ala Pro Asn Thr Thr Asn Glu His Phe Thr Ser
405 410 415
Pro Pro Pro Thr Pro Ser Ser Thr Ala Gln His Leu Val Tyr Phe Arg
420 425 430
Arg Lys Arg Ser Ile Leu Trp Arg Glu Gly Asp Met Phe Pro Phe Leu
435 440 445
Asp Gly Leu Ile Asn Ala Pro Ile Asp Phe Asp Pro Val Pro Asn Thr
450 455 460
Lys Thr Ile Phe Asp Glu Ser Ser Ser Ser Gly Ala Ser Ala Glu Glu
465 470 475 480
Asp Gln His Ala Ser Pro Asn Ile Ser Leu Thr Leu Ser Tyr Phe Pro
485 490 495
Asn Ile Asn Glu Asn Thr Ala Tyr Ser Gly Glu Asn Glu Asn Asp Cys
500 505 510
Asp Ala Glu Leu Arg Ile Trp Ser Val Gln Glu Asp Asp Leu Ala Ala
515 520 525
Gly Leu Ser Trp Ile Pro Phe Phe Gly Pro Gly Ile Glu Gly Leu Tyr
530 535 540
Thr Ala Val Leu Ile Lys Asn Gln Asn Asn Leu Val Cys Arg Leu Arg
545 550 555 560
Arg Leu Ala Asn Gln Thr Ala Lys Ser Leu Glu Leu Leu Leu Arg Val
565 570 575
Thr Thr Glu Glu Arg Thr Phe Ser Leu Ile Asn Arg His Ala Ile Asp
580 585 590
Phe Leu Leu Thr Arg Trp Gly Gly Thr Cys Lys Val Leu Gly Pro Asp
595 600 605
Cys Cys Ile Gly Ile Glu Asp Leu Ser Lys Asn Ile Ser Glu Gln Ile
610 615 620
Asp Gln Ile Lys Lys Asp Glu Gln Lys Glu Gly Thr Gly Trp Gly Leu
625 630 635 640
Gly Gly Lys Trp Trp Thr Ser Asp Trp Gly Val Leu Thr Asn Leu Gly
645 650 655
Ile Leu Leu Leu Leu Ser Ile Ala Val Leu Ile Ala Leu Ser Cys Ile
660 665 670
Cys Arg Ile Phe Thr Lys Tyr Ile Gly
675 680
<210> 73
<211> 630
<212> БЕЛОК
<213> вирус Ханта
<400> 73
Leu Arg Asn Val Tyr Asp Met Lys Ile Glu Cys Pro His Thr Val Ser
1 5 10 15
Phe Gly Glu Asn Ser Val Ile Gly Tyr Val Glu Leu Pro Pro Val Pro
20 25 30
Leu Ala Asp Thr Ala Gln Met Val Pro Glu Ser Ser Cys Asn Met Asp
35 40 45
Asn His Gln Ser Leu Asn Thr Ile Thr Lys Tyr Thr Gln Val Ser Trp
50 55 60
Arg Gly Lys Ala Asp Gln Ser Gln Ser Ser Gln Asn Ser Phe Glu Thr
65 70 75 80
Val Ser Thr Glu Val Asp Leu Lys Gly Thr Cys Val Leu Lys His Lys
85 90 95
Met Val Glu Glu Ser Tyr Arg Ser Arg Lys Ser Val Thr Cys Tyr Asp
100 105 110
Leu Ser Cys Asn Ser Thr Tyr Cys Lys Pro Thr Leu Tyr Met Ile Val
115 120 125
Pro Ile His Ala Cys Asn Met Met Lys Ser Cys Leu Ile Ala Leu Gly
130 135 140
Pro Tyr Arg Val Gln Val Val Tyr Glu Arg Ser Tyr Cys Met Thr Gly
145 150 155 160
Val Leu Ile Glu Gly Lys Cys Phe Val Pro Asp Gln Ser Val Val Ser
165 170 175
Ile Ile Lys His Gly Ile Phe Asp Ile Ala Ser Val His Ile Val Cys
180 185 190
Phe Phe Val Ala Val Lys Gly Asn Thr Tyr Lys Ile Phe Glu Gln Val
195 200 205
Lys Lys Ser Phe Glu Ser Thr Cys Asn Asp Thr Glu Asn Lys Val Gln
210 215 220
Gly Tyr Tyr Ile Cys Ile Val Gly Gly Asn Ser Ala Pro Ile Tyr Val
225 230 235 240
Pro Thr Leu Asp Asp Phe Arg Ser Met Glu Ala Phe Thr Gly Ile Phe
245 250 255
Arg Ser Pro His Gly Glu Asp His Asp Leu Ala Gly Glu Glu Ile Ala
260 265 270
Ser Tyr Ser Ile Val Gly Pro Ala Asn Ala Lys Val Pro His Ser Ala
275 280 285
Ser Ser Asp Thr Leu Ser Leu Ile Ala Tyr Ser Gly Ile Pro Ser Tyr
290 295 300
Ser Ser Leu Ser Ile Leu Thr Ser Ser Thr Glu Ala Lys His Val Phe
305 310 315 320
Ser Pro Gly Leu Phe Pro Lys Leu Asn His Thr Asn Cys Asp Lys Ser
325 330 335
Ala Ile Pro Leu Ile Trp Thr Gly Met Ile Asp Leu Pro Gly Tyr Tyr
340 345 350
Glu Ala Val His Pro Cys Thr Val Phe Cys Val Leu Ser Gly Pro Gly
355 360 365
Ala Ser Cys Glu Ala Phe Ser Glu Gly Gly Ile Phe Asn Ile Thr Ser
370 375 380
Pro Met Cys Leu Val Ser Lys Gln Asn Arg Phe Arg Leu Thr Glu Gln
385 390 395 400
Gln Val Asn Phe Val Cys Gln Arg Val Asp Met Asp Ile Val Val Tyr
405 410 415
Cys Asn Gly Gln Arg Lys Val Ile Leu Thr Lys Thr Leu Val Ile Gly
420 425 430
Gln Cys Ile Tyr Thr Ile Thr Ser Leu Phe Ser Leu Leu Pro Gly Val
435 440 445
Ala His Ser Ile Ala Val Glu Leu Cys Val Pro Gly Phe His Gly Trp
450 455 460
Ala Thr Ala Ala Leu Leu Val Thr Phe Cys Phe Gly Trp Val Leu Ile
465 470 475 480
Pro Ala Ile Thr Phe Ile Ile Leu Thr Val Leu Lys Phe Ile Ala Asn
485 490 495
Ile Phe His Thr Ser Asn Gln Glu Asn Arg Leu Lys Ser Val Leu Arg
500 505 510
Lys Ile Lys Glu Glu Phe Glu Lys Thr Lys Gly Ser Met Val Cys Asp
515 520 525
Val Cys Lys Tyr Glu Cys Glu Thr Tyr Lys Glu Leu Lys Ala His Gly
530 535 540
Val Ser Cys Pro Gln Ser Gln Cys Pro Tyr Cys Phe Thr His Cys Glu
545 550 555 560
Pro Thr Glu Ala Ala Phe Gln Ala His Tyr Lys Val Cys Gln Val Thr
565 570 575
His Arg Phe Arg Asp Asp Leu Lys Lys Thr Val Thr Pro Gln Asn Phe
580 585 590
Thr Pro Gly Cys Tyr Arg Thr Leu Asn Leu Phe Arg Tyr Lys Ser Arg
595 600 605
Cys Tyr Ile Phe Thr Met Trp Ile Phe Leu Leu Val Leu Glu Ser Ile
610 615 620
Leu Trp Ala Ala Ser Ala
625 630
<210> 74
<211> 487
<212> БЕЛОК
<213> вирус Ханта
<400> 74
Ser Glu Thr Pro Leu Thr Pro Val Trp Asn Asp Asn Ala His Gly Val
1 5 10 15
Gly Ser Val Pro Met His Thr Asp Leu Glu Leu Asp Phe Ser Leu Thr
20 25 30
Ser Ser Ser Lys Tyr Thr Tyr Arg Arg Lys Leu Thr Asn Pro Leu Glu
35 40 45
Glu Ala Gln Ser Ile Asp Leu His Ile Glu Ile Glu Glu Gln Thr Ile
50 55 60
Gly Val Asp Val His Ala Leu Gly His Trp Phe Asp Gly Arg Leu Asn
65 70 75 80
Leu Lys Thr Ser Phe His Cys Tyr Gly Ala Cys Thr Lys Tyr Glu Tyr
85 90 95
Pro Trp His Thr Ala Lys Cys His Tyr Glu Arg Asp Tyr Gln Tyr Glu
100 105 110
Thr Ser Trp Gly Cys Asn Pro Ser Asp Cys Pro Gly Val Gly Thr Gly
115 120 125
Cys Thr Ala Cys Gly Leu Tyr Leu Asp Gln Leu Lys Pro Val Gly Ser
130 135 140
Ala Tyr Lys Ile Ile Thr Ile Arg Tyr Ser Arg Arg Val Cys Val Gln
145 150 155 160
Phe Gly Glu Glu Asn Leu Cys Lys Ile Ile Asp Met Asn Asp Cys Phe
165 170 175
Val Ser Arg His Val Lys Val Cys Ile Ile Gly Thr Val Ser Lys Phe
180 185 190
Ser Gln Gly Asp Thr Leu Leu Phe Phe Gly Pro Leu Glu Gly Gly Gly
195 200 205
Leu Ile Phe Lys His Trp Cys Thr Ser Thr Cys Gln Phe Gly Asp Pro
210 215 220
Gly Asp Ile Met Ser Pro Arg Asp Lys Gly Phe Leu Cys Pro Glu Phe
225 230 235 240
Pro Gly Ser Phe Arg Lys Lys Cys Asn Phe Ala Thr Thr Pro Ile Cys
245 250 255
Glu Tyr Asp Gly Asn Met Val Ser Gly Tyr Lys Lys Val Met Ala Thr
260 265 270
Ile Asp Ser Phe Gln Ser Phe Asn Thr Ser Thr Met His Phe Thr Asp
275 280 285
Glu Arg Ile Glu Trp Lys Asp Pro Asp Gly Met Leu Arg Asp His Ile
290 295 300
Asn Ile Leu Val Thr Lys Asp Ile Asp Phe Asp Asn Leu Gly Glu Asn
305 310 315 320
Pro Cys Lys Ile Gly Leu Gln Thr Ser Ser Ile Glu Gly Ala Trp Gly
325 330 335
Ser Gly Val Gly Phe Thr Leu Thr Cys Leu Val Ser Leu Thr Glu Cys
340 345 350
Pro Thr Phe Leu Thr Ser Ile Lys Ala Cys Asp Lys Ala Ile Cys Tyr
355 360 365
Gly Ala Glu Ser Val Thr Leu Thr Arg Gly Gln Asn Thr Val Lys Val
370 375 380
Ser Gly Lys Gly Gly His Ser Gly Ser Thr Phe Arg Cys Cys His Gly
385 390 395 400
Glu Asp Cys Ser Gln Ile Gly Leu His Ala Ala Ala Pro His Leu Asp
405 410 415
Lys Val Asn Gly Ile Ser Glu Ile Glu Asn Ser Lys Val Tyr Asp Asp
420 425 430
Gly Ala Pro Gln Cys Gly Ile Lys Cys Trp Phe Val Lys Ser Gly Glu
435 440 445
Trp Ile Ser Gly Ile Phe Ser Gly Asn Trp Ile Val Leu Ile Val Leu
450 455 460
Cys Val Phe Leu Leu Phe Ser Leu Val Leu Leu Ser Ile Leu Cys Pro
465 470 475 480
Val Arg Lys His Lys Lys Ser
485
<210> 75
<211> 226
<212> БЕЛОК
<213> Гепатит В
<400> 75
Met Glu Asn Ile Thr Ser Gly Phe Leu Gly Pro Leu Leu Val Leu Gln
1 5 10 15
Ala Gly Phe Phe Leu Leu Thr Lys Ile Leu Thr Ile Pro Gln Ser Leu
20 25 30
Asn Ser Trp Trp Thr Ser Leu Ser Phe Leu Gly Gly Asn Thr Val Cys
35 40 45
Leu Gly Gln Asn Ser Gln Ser Pro Thr Ser Asn His Ser Pro Thr Ser
50 55 60
Cys Pro Pro Thr Cys Pro Gly Tyr Arg Trp Met Cys Leu Arg Arg Phe
65 70 75 80
Ile Ile Phe Leu Phe Ile Leu Leu Leu Cys Leu Ile Phe Leu Leu Val
85 90 95
Leu Leu Asp Tyr Gln Gly Met Leu Pro Val Cys Pro Leu Ile Pro Gly
100 105 110
Ser Ser Thr Thr Ser Thr Gly Pro Cys Arg Thr Cys Lys Thr Pro Ala
115 120 125
Gln Gly Thr Ser Met Tyr Pro Ser Cys Cys Cys Thr Lys Pro Ser Asp
130 135 140
Gly Asn Cys Thr Cys Ile Pro Ile Pro Ser Ser Trp Ala Phe Gly Lys
145 150 155 160
Phe Leu Trp Glu Trp Ala Ser Ala Arg Phe Ser Trp Leu Ser Leu Ile
165 170 175
Val Pro Phe Val Gln Trp Phe Val Gly Leu Ser Pro Thr Val Trp Leu
180 185 190
Ser Val Ile Trp Met Met Trp Tyr Trp Gly Pro Ser Leu Tyr Ser Ile
195 200 205
Leu Ser Pro Phe Leu Pro Leu Leu Pro Ile Phe Phe Cys Leu Trp Val
210 215 220
Tyr Ile
225
<210> 76
<211> 617
<212> БЕЛОК
<213> вирус кори
<400> 76
Met Ser Pro Gln Arg Asp Arg Ile Asn Ala Phe Tyr Lys Asp Asn Pro
1 5 10 15
His Pro Lys Gly Ser Arg Ile Val Ile Asn Arg Glu His Leu Met Ile
20 25 30
Asp Arg Pro Tyr Val Leu Leu Ala Val Leu Phe Val Met Phe Leu Ser
35 40 45
Leu Ile Gly Leu Leu Ala Ile Ala Gly Ile Arg Leu His Arg Ala Ala
50 55 60
Ile Tyr Thr Ala Glu Ile His Lys Ser Leu Ser Thr Asn Leu Asp Val
65 70 75 80
Thr Asn Ser Ile Glu His Gln Val Lys Asp Val Leu Thr Pro Leu Phe
85 90 95
Lys Ile Ile Gly Asp Glu Val Gly Leu Arg Thr Pro Gln Arg Phe Thr
100 105 110
Asp Leu Val Lys Phe Ile Ser Asp Lys Ile Lys Phe Leu Asn Pro Asp
115 120 125
Arg Glu Tyr Asp Phe Arg Asp Leu Thr Trp Cys Ile Asn Pro Pro Glu
130 135 140
Arg Ile Lys Leu Asp Tyr Asp Gln Tyr Cys Ala Asp Val Ala Ala Glu
145 150 155 160
Glu Leu Met Asn Ala Leu Val Asn Ser Thr Leu Leu Glu Thr Arg Thr
165 170 175
Thr Asn Gln Phe Leu Ala Val Ser Lys Gly Asn Cys Ser Gly Pro Thr
180 185 190
Thr Ile Arg Gly Gln Phe Ser Asn Met Ser Leu Ser Leu Leu Asp Leu
195 200 205
Tyr Leu Gly Arg Gly Tyr Asn Val Ser Ser Ile Val Thr Met Thr Ser
210 215 220
Gln Gly Met Tyr Gly Gly Thr Tyr Leu Val Glu Lys Pro Asn Leu Ser
225 230 235 240
Ser Lys Arg Ser Glu Leu Ser Gln Leu Ser Met Tyr Arg Val Phe Glu
245 250 255
Val Gly Val Ile Arg Asn Pro Gly Leu Gly Ala Pro Val Phe His Met
260 265 270
Thr Asn Tyr Leu Glu Gln Pro Val Ser Asn Asp Leu Ser Asn Cys Met
275 280 285
Val Ala Leu Gly Glu Leu Lys Leu Ala Ala Leu Cys His Gly Glu Asp
290 295 300
Ser Ile Thr Ile Pro Tyr Gln Gly Ser Gly Lys Gly Val Ser Phe Gln
305 310 315 320
Leu Val Lys Leu Gly Val Trp Lys Ser Pro Thr Asp Met Gln Ser Trp
325 330 335
Val Pro Leu Ser Thr Asp Asp Pro Val Ile Asp Arg Leu Tyr Leu Ser
340 345 350
Ser His Arg Gly Val Ile Ala Asp Asn Gln Ala Lys Trp Ala Val Pro
355 360 365
Thr Thr Arg Thr Asp Asp Lys Leu Arg Met Glu Thr Cys Phe Gln Gln
370 375 380
Ala Cys Lys Gly Lys Ile Gln Ala Leu Cys Glu Asn Pro Glu Trp Ala
385 390 395 400
Pro Leu Lys Asp Asn Arg Ile Pro Ser Tyr Gly Val Leu Ser Val Asp
405 410 415
Leu Ser Leu Thr Val Glu Leu Lys Ile Lys Ile Ala Ser Gly Phe Gly
420 425 430
Pro Leu Ile Thr His Gly Ser Gly Met Asp Leu Tyr Lys Ser Asn His
435 440 445
Asn Asn Val Tyr Trp Leu Thr Ile Pro Pro Met Lys Asn Leu Ala Leu
450 455 460
Gly Val Ile Asn Thr Leu Glu Trp Ile Pro Arg Phe Lys Val Ser Pro
465 470 475 480
Tyr Leu Phe Asn Val Pro Ile Lys Glu Ala Gly Glu Asp Cys His Ala
485 490 495
Pro Thr Tyr Leu Pro Ala Glu Val Asp Gly Asp Val Lys Leu Ser Ser
500 505 510
Asn Leu Val Ile Leu Pro Gly Gln Asp Leu Gln Tyr Val Leu Ala Thr
515 520 525
Tyr Asp Thr Ser Arg Val Glu His Ala Val Val Tyr Tyr Val Tyr Ser
530 535 540
Pro Ser Arg Ser Phe Ser Tyr Phe Tyr Pro Phe Arg Leu Pro Ile Lys
545 550 555 560
Gly Val Pro Ile Glu Leu Gln Val Glu Cys Phe Thr Trp Asp Gln Lys
565 570 575
Leu Trp Cys Arg His Phe Cys Val Leu Ala Asp Ser Glu Ser Gly Gly
580 585 590
His Ile Thr His Ser Gly Met Glu Gly Met Gly Val Ser Cys Thr Val
595 600 605
Thr Arg Glu Asp Gly Thr Asn Arg Arg
610 615
<210> 77
<211> 550
<212> БЕЛОК
<213> вирус кори
<400> 77
Met Gly Leu Lys Val Asn Val Ser Ala Ile Phe Met Ala Val Leu Leu
1 5 10 15
Thr Leu Gln Thr Pro Thr Gly Gln Ile His Trp Gly Asn Leu Ser Lys
20 25 30
Ile Gly Val Val Gly Ile Gly Ser Ala Ser Tyr Lys Val Met Thr Arg
35 40 45
Ser Ser His Gln Ser Leu Val Ile Lys Leu Met Pro Asn Ile Thr Leu
50 55 60
Leu Asn Asn Cys Thr Arg Val Glu Ile Ala Glu Tyr Arg Arg Leu Leu
65 70 75 80
Arg Thr Val Leu Glu Pro Ile Arg Asp Ala Leu Asn Ala Met Thr Gln
85 90 95
Asn Ile Arg Pro Val Gln Ser Val Ala Ser Ser Arg Arg His Lys Arg
100 105 110
Phe Ala Gly Val Val Leu Ala Gly Ala Ala Leu Gly Val Ala Thr Ala
115 120 125
Ala Gln Ile Thr Ala Gly Ile Ala Leu His Gln Ser Met Leu Asn Ser
130 135 140
Gln Ala Ile Asp Asn Leu Arg Ala Ser Leu Glu Thr Thr Asn Gln Ala
145 150 155 160
Ile Glu Ala Ile Arg Gln Ala Gly Gln Glu Met Ile Leu Ala Val Gln
165 170 175
Gly Val Gln Asp Tyr Ile Asn Asn Glu Leu Ile Pro Ser Met Asn Gln
180 185 190
Leu Ser Cys Asp Leu Ile Gly Gln Lys Leu Gly Leu Lys Leu Leu Arg
195 200 205
Tyr Tyr Thr Glu Ile Leu Ser Leu Phe Gly Pro Ser Leu Arg Asp Pro
210 215 220
Ile Ser Ala Glu Ile Ser Ile Gln Ala Leu Ser Tyr Ala Leu Gly Gly
225 230 235 240
Asp Ile Asn Lys Val Leu Glu Lys Leu Gly Tyr Ser Gly Gly Asp Leu
245 250 255
Leu Gly Ile Leu Glu Ser Arg Gly Ile Lys Ala Arg Ile Thr His Val
260 265 270
Asp Thr Glu Ser Tyr Phe Ile Val Leu Ser Ile Ala Tyr Pro Thr Leu
275 280 285
Ser Glu Ile Lys Gly Val Ile Val His Arg Leu Glu Gly Val Ser Tyr
290 295 300
Asn Ile Gly Ser Gln Glu Trp Tyr Thr Thr Val Pro Lys Tyr Val Ala
305 310 315 320
Thr Gln Gly Tyr Leu Ile Ser Asn Phe Asp Glu Ser Ser Cys Thr Phe
325 330 335
Met Pro Glu Gly Thr Val Cys Ser Gln Asn Ala Leu Tyr Pro Met Ser
340 345 350
Pro Leu Leu Gln Glu Cys Leu Arg Gly Ser Thr Lys Ser Cys Ala Arg
355 360 365
Thr Leu Val Ser Gly Ser Phe Gly Asn Arg Phe Ile Leu Ser Gln Gly
370 375 380
Asn Leu Ile Ala Asn Cys Ala Ser Ile Leu Cys Lys Cys Tyr Thr Thr
385 390 395 400
Gly Thr Ile Ile Asn Gln Asp Pro Asp Lys Ile Leu Thr Tyr Ile Ala
405 410 415
Ala Asp His Cys Pro Val Val Glu Val Asn Gly Val Thr Ile Gln Val
420 425 430
Gly Ser Arg Arg Tyr Pro Asp Ala Val Tyr Leu His Arg Ile Asp Leu
435 440 445
Gly Pro Pro Ile Ser Leu Glu Arg Leu Asp Val Gly Thr Asn Leu Gly
450 455 460
Asn Ala Ile Ala Lys Leu Glu Asp Ala Lys Glu Leu Leu Glu Ser Ser
465 470 475 480
Asp Gln Ile Leu Arg Ser Met Lys Gly Leu Ser Ser Thr Ser Ile Val
485 490 495
Tyr Ile Leu Ile Ala Val Cys Leu Gly Gly Leu Ile Gly Ile Pro Ala
500 505 510
Leu Ile Cys Cys Cys Arg Gly Arg Cys Asn Lys Lys Gly Glu Gln Val
515 520 525
Gly Met Ser Arg Pro Gly Leu Lys Pro Asp Leu Thr Gly Thr Ser Lys
530 535 540
Ser Tyr Val Arg Ser Leu
545 550
<210> 78
<211> 500
<212> БЕЛОК
<213> вирус Зика
<400> 78
Ile Arg Cys Ile Gly Val Ser Asn Arg Asp Phe Val Glu Gly Met Ser
1 5 10 15
Gly Gly Thr Trp Val Asp Val Val Leu Glu His Gly Gly Cys Val Thr
20 25 30
Val Met Ala Gln Asp Lys Pro Thr Val Asp Ile Glu Leu Val Thr Thr
35 40 45
Thr Val Ser Asn Met Ala Glu Val Arg Ser Tyr Cys Tyr Glu Ala Ser
50 55 60
Ile Ser Asp Met Ala Ser Asp Ser Arg Cys Pro Thr Gln Gly Glu Ala
65 70 75 80
Tyr Leu Asp Lys Gln Ser Asp Thr Gln Tyr Val Cys Lys Arg Thr Leu
85 90 95
Val Asp Arg Gly Trp Gly Asn Gly Cys Gly Leu Phe Gly Lys Gly Ser
100 105 110
Leu Val Thr Cys Ala Lys Phe Thr Cys Ser Lys Lys Met Thr Gly Lys
115 120 125
Ser Ile Gln Pro Glu Asn Leu Glu Tyr Arg Ile Met Leu Ser Val His
130 135 140
Gly Ser Gln His Ser Gly Met Ile Gly Tyr Glu Thr Asp Glu Asp Arg
145 150 155 160
Ala Lys Val Glu Val Thr Pro Asn Ser Pro Arg Ala Glu Ala Thr Leu
165 170 175
Gly Gly Phe Gly Ser Leu Gly Leu Asp Cys Glu Pro Arg Thr Gly Leu
180 185 190
Asp Phe Ser Asp Leu Tyr Tyr Leu Thr Met Asn Asn Lys His Trp Leu
195 200 205
Val His Lys Glu Trp Phe His Asp Ile Pro Leu Pro Trp His Ala Gly
210 215 220
Ala Asp Thr Gly Thr Pro His Trp Asn Asn Lys Glu Ala Leu Val Glu
225 230 235 240
Phe Lys Asp Ala His Ala Lys Arg Gln Thr Val Val Val Leu Gly Ser
245 250 255
Gln Glu Gly Ala Val His Thr Ala Leu Ala Gly Ala Leu Glu Ala Glu
260 265 270
Met Asp Gly Ala Lys Gly Arg Leu Phe Ser Gly His Leu Lys Cys Arg
275 280 285
Leu Lys Met Asp Lys Leu Arg Leu Lys Gly Val Ser Tyr Ser Leu Cys
290 295 300
Thr Ala Ala Phe Thr Phe Thr Lys Val Pro Ala Glu Thr Leu His Gly
305 310 315 320
Thr Val Thr Val Glu Val Gln Tyr Ala Gly Thr Asp Gly Pro Cys Lys
325 330 335
Ile Pro Val Gln Met Ala Val Asp Met Gln Thr Leu Thr Pro Val Gly
340 345 350
Arg Leu Ile Thr Ala Asn Pro Val Ile Thr Glu Ser Thr Glu Asn Ser
355 360 365
Lys Met Met Leu Glu Leu Asp Pro Pro Phe Gly Asp Ser Tyr Ile Val
370 375 380
Ile Gly Val Gly Asp Lys Lys Ile Thr His His Trp His Arg Ser Gly
385 390 395 400
Ser Thr Ile Gly Lys Ala Phe Glu Ala Thr Val Arg Gly Ala Lys Arg
405 410 415
Met Ala Val Leu Gly Asp Thr Ala Trp Asp Phe Gly Ser Val Gly Gly
420 425 430
Val Phe Asn Ser Leu Gly Lys Gly Ile His Gln Ile Phe Gly Ala Ala
435 440 445
Phe Lys Ser Leu Phe Gly Gly Met Ser Trp Phe Ser Gln Ile Leu Ile
450 455 460
Gly Thr Leu Leu Val Trp Leu Gly Leu Asn Thr Lys Asn Gly Ser Ile
465 470 475 480
Ser Leu Thr Cys Leu Ala Leu Gly Gly Val Met Ile Phe Leu Ser Thr
485 490 495
Ala Val Ser Ala
500
<210> 79
<211> 378
<212> БЕЛОК
<213> Plasmodium vivax
<400> 79
Met Lys Asn Phe Ile Leu Leu Ala Val Ser Ser Ile Leu Leu Val Asp
1 5 10 15
Leu Phe Pro Thr His Cys Gly His Asn Val Asp Leu Ser Lys Ala Ile
20 25 30
Asn Leu Asn Gly Val Asn Phe Asn Asn Val Asp Ala Ser Ser Leu Gly
35 40 45
Ala Ala His Val Gly Gln Ser Ala Ser Arg Gly Arg Gly Leu Gly Glu
50 55 60
Asn Pro Asp Asp Glu Glu Gly Asp Ala Lys Lys Lys Lys Asp Gly Lys
65 70 75 80
Lys Ala Glu Pro Lys Asn Pro Arg Glu Asn Lys Leu Lys Gln Pro Gly
85 90 95
Asp Arg Ala Asp Gly Gln Pro Ala Gly Asp Arg Ala Asp Gly Gln Pro
100 105 110
Ala Gly Asp Arg Ala Asp Gly Gln Pro Ala Gly Asp Arg Ala Ala Gly
115 120 125
Gln Pro Ala Gly Asp Arg Ala Asp Gly Gln Pro Ala Gly Asp Arg Ala
130 135 140
Asp Gly Gln Pro Ala Gly Asp Arg Ala Asp Gly Gln Pro Ala Gly Asp
145 150 155 160
Arg Ala Asp Gly Gln Pro Ala Gly Asp Arg Ala Ala Gly Gln Pro Ala
165 170 175
Gly Asp Arg Ala Ala Gly Gln Pro Ala Gly Asp Arg Ala Asp Gly Gln
180 185 190
Pro Ala Gly Asp Arg Ala Ala Gly Gln Pro Ala Gly Asp Arg Ala Asp
195 200 205
Gly Gln Pro Ala Gly Asp Arg Ala Ala Gly Gln Pro Ala Gly Asp Arg
210 215 220
Ala Asp Gly Gln Pro Ala Gly Asp Arg Ala Ala Gly Gln Pro Ala Gly
225 230 235 240
Asp Arg Ala Ala Gly Gln Pro Ala Gly Asp Arg Ala Ala Gly Gln Pro
245 250 255
Ala Gly Asp Arg Ala Ala Gly Gln Pro Ala Gly Asn Gly Ala Gly Gly
260 265 270
Gln Ala Ala Gly Gly Asn Ala Gly Gly Gly Gln Gly Gln Asn Asn Glu
275 280 285
Gly Ala Asn Ala Pro Asn Glu Lys Ser Val Lys Glu Tyr Leu Asp Lys
290 295 300
Val Arg Ala Thr Val Gly Thr Glu Trp Thr Pro Cys Ser Val Thr Cys
305 310 315 320
Gly Val Gly Val Arg Val Arg Arg Arg Val Asn Ala Ala Asn Lys Lys
325 330 335
Pro Glu Asp Leu Thr Leu Asn Asp Leu Glu Thr Asp Val Cys Thr Met
340 345 350
Asp Lys Cys Ala Gly Ile Phe Asn Val Val Ser Asn Ser Leu Gly Leu
355 360 365
Val Ile Leu Leu Val Leu Ala Leu Phe Asn
370 375
<210> 80
<211> 546
<212> БЕЛОК
<213> Вирус Нипах
<400> 80
Met Val Val Ile Leu Asp Lys Arg Cys Tyr Cys Asn Leu Leu Ile Leu
1 5 10 15
Ile Leu Met Ile Ser Glu Cys Ser Val Gly Ile Leu His Tyr Glu Lys
20 25 30
Leu Ser Lys Ile Gly Leu Val Lys Gly Val Thr Arg Lys Tyr Lys Ile
35 40 45
Lys Ser Asn Pro Leu Thr Lys Asp Ile Val Ile Lys Met Ile Pro Asn
50 55 60
Val Ser Asn Met Ser Gln Cys Thr Gly Ser Val Met Glu Asn Tyr Lys
65 70 75 80
Thr Arg Leu Asn Gly Ile Leu Thr Pro Ile Lys Gly Ala Leu Glu Ile
85 90 95
Tyr Lys Asn Asn Thr His Asp Leu Val Gly Asp Val Arg Leu Ala Gly
100 105 110
Val Ile Met Ala Gly Val Ala Ile Gly Ile Ala Thr Ala Ala Gln Ile
115 120 125
Thr Ala Gly Val Ala Leu Tyr Glu Ala Met Lys Asn Ala Asp Asn Ile
130 135 140
Asn Lys Leu Lys Ser Ser Ile Glu Ser Thr Asn Glu Ala Val Val Lys
145 150 155 160
Leu Gln Glu Thr Ala Glu Lys Thr Val Tyr Val Leu Thr Ala Leu Gln
165 170 175
Asp Tyr Ile Asn Thr Asn Leu Val Pro Thr Ile Asp Lys Ile Ser Cys
180 185 190
Lys Gln Thr Glu Leu Ser Leu Asp Leu Ala Leu Ser Lys Tyr Leu Ser
195 200 205
Asp Leu Leu Phe Val Phe Gly Pro Asn Leu Gln Asp Pro Val Ser Asn
210 215 220
Ser Met Thr Ile Gln Ala Ile Ser Gln Ala Phe Gly Gly Asn Tyr Glu
225 230 235 240
Thr Leu Leu Arg Thr Leu Gly Tyr Ala Thr Glu Asp Phe Asp Asp Leu
245 250 255
Leu Glu Ser Asp Ser Ile Thr Gly Gln Ile Ile Tyr Val Asp Leu Ser
260 265 270
Ser Tyr Tyr Ile Ile Val Arg Val Tyr Phe Pro Ile Leu Thr Glu Ile
275 280 285
Gln Gln Ala Tyr Ile Gln Glu Leu Leu Pro Val Ser Phe Asn Asn Asp
290 295 300
Asn Ser Glu Trp Ile Ser Ile Val Pro Asn Phe Ile Leu Val Arg Asn
305 310 315 320
Thr Leu Ile Ser Asn Ile Glu Ile Gly Phe Cys Leu Ile Thr Lys Arg
325 330 335
Ser Val Ile Cys Asn Gln Asp Tyr Ala Thr Pro Met Thr Asn Asn Met
340 345 350
Arg Glu Cys Leu Thr Gly Ser Thr Glu Lys Cys Pro Arg Glu Leu Val
355 360 365
Val Ser Ser His Val Pro Arg Phe Ala Leu Ser Asn Gly Val Leu Phe
370 375 380
Ala Asn Cys Ile Ser Val Thr Cys Gln Cys Gln Thr Thr Gly Arg Ala
385 390 395 400
Ile Ser Gln Ser Gly Glu Gln Thr Leu Leu Met Ile Asp Asn Thr Thr
405 410 415
Cys Pro Thr Ala Val Leu Gly Asn Val Ile Ile Ser Leu Gly Lys Tyr
420 425 430
Leu Gly Ser Val Asn Tyr Asn Ser Glu Gly Ile Ala Ile Gly Pro Pro
435 440 445
Val Phe Thr Asp Lys Val Asp Ile Ser Ser Gln Ile Ser Ser Met Asn
450 455 460
Gln Ser Leu Gln Gln Ser Lys Asp Tyr Ile Lys Glu Ala Gln Arg Leu
465 470 475 480
Leu Asp Thr Val Asn Pro Ser Leu Ile Ser Met Leu Ser Met Ile Ile
485 490 495
Leu Tyr Val Leu Ser Ile Ala Ser Leu Cys Ile Gly Leu Ile Thr Phe
500 505 510
Ile Ser Phe Ile Ile Val Glu Lys Lys Arg Asn Thr Tyr Ser Arg Leu
515 520 525
Glu Asp Arg Arg Val Arg Pro Thr Ser Ser Gly Asp Leu Tyr Tyr Ile
530 535 540
Gly Thr
545
<210> 81
<211> 602
<212> БЕЛОК
<213> Вирус Нипах
<400> 81
Met Pro Ala Glu Asn Lys Lys Val Arg Phe Glu Asn Thr Thr Ser Asp
1 5 10 15
Lys Gly Lys Ile Pro Ser Lys Val Ile Lys Ser Tyr Tyr Gly Thr Met
20 25 30
Asp Ile Lys Lys Ile Asn Glu Gly Leu Leu Asp Ser Lys Ile Leu Ser
35 40 45
Ala Phe Asn Thr Val Ile Ala Leu Leu Gly Ser Ile Val Ile Ile Val
50 55 60
Met Asn Ile Met Ile Ile Gln Asn Tyr Thr Arg Ser Thr Asp Asn Gln
65 70 75 80
Ala Val Ile Lys Asp Ala Leu Gln Gly Ile Gln Gln Gln Ile Lys Gly
85 90 95
Leu Ala Asp Lys Ile Gly Thr Glu Ile Gly Pro Lys Val Ser Leu Ile
100 105 110
Asp Thr Ser Ser Thr Ile Thr Ile Pro Ala Asn Ile Gly Leu Leu Gly
115 120 125
Ser Lys Ile Ser Gln Ser Thr Ala Ser Ile Asn Glu Asn Val Asn Glu
130 135 140
Lys Cys Lys Phe Thr Leu Pro Pro Leu Lys Ile His Glu Cys Asn Ile
145 150 155 160
Ser Cys Pro Asn Pro Leu Pro Phe Arg Glu Tyr Arg Pro Gln Thr Glu
165 170 175
Gly Val Ser Asn Leu Val Gly Leu Pro Asn Asn Ile Cys Leu Gln Lys
180 185 190
Thr Ser Asn Gln Ile Leu Lys Pro Lys Leu Ile Ser Tyr Thr Leu Pro
195 200 205
Val Val Gly Gln Ser Gly Thr Cys Ile Thr Asp Pro Leu Leu Ala Met
210 215 220
Asp Glu Gly Tyr Phe Ala Tyr Ser His Leu Glu Arg Ile Gly Ser Cys
225 230 235 240
Ser Arg Gly Val Ser Lys Gln Arg Ile Ile Gly Val Gly Glu Val Leu
245 250 255
Asp Arg Gly Asp Glu Val Pro Ser Leu Phe Met Thr Asn Val Trp Thr
260 265 270
Pro Pro Asn Pro Asn Thr Val Tyr His Cys Ser Ala Val Tyr Asn Asn
275 280 285
Glu Phe Tyr Tyr Val Leu Cys Ala Val Ser Thr Val Gly Asp Pro Ile
290 295 300
Leu Asn Ser Thr Tyr Trp Ser Gly Ser Leu Met Met Thr Arg Leu Ala
305 310 315 320
Val Lys Pro Lys Ser Asn Gly Gly Gly Tyr Asn Gln His Gln Leu Ala
325 330 335
Leu Arg Ser Ile Glu Lys Gly Arg Tyr Asp Lys Val Met Pro Tyr Gly
340 345 350
Pro Ser Gly Ile Lys Gln Gly Asp Thr Leu Tyr Phe Pro Ala Val Gly
355 360 365
Phe Leu Val Arg Thr Glu Phe Lys Tyr Asn Asp Ser Asn Cys Pro Ile
370 375 380
Thr Lys Cys Gln Tyr Ser Lys Pro Glu Asn Cys Arg Leu Ser Met Gly
385 390 395 400
Ile Arg Pro Asn Ser His Tyr Ile Leu Arg Ser Gly Leu Leu Lys Tyr
405 410 415
Asn Leu Ser Asp Gly Glu Asn Pro Lys Val Val Phe Ile Glu Ile Ser
420 425 430
Asp Gln Arg Leu Ser Ile Gly Ser Pro Ser Lys Ile Tyr Asp Ser Leu
435 440 445
Gly Gln Pro Val Phe Tyr Gln Ala Ser Phe Ser Trp Asp Thr Met Ile
450 455 460
Lys Phe Gly Asp Val Leu Thr Val Asn Pro Leu Val Val Asn Trp Arg
465 470 475 480
Asn Asn Thr Val Ile Ser Arg Pro Gly Gln Ser Gln Cys Pro Arg Phe
485 490 495
Asn Thr Cys Pro Glu Ile Cys Trp Glu Gly Val Tyr Asn Asp Ala Phe
500 505 510
Leu Ile Asp Arg Ile Asn Trp Ile Ser Ala Gly Val Phe Leu Asp Ser
515 520 525
Asn Gln Thr Ala Glu Asn Pro Val Phe Thr Val Phe Lys Asp Asn Glu
530 535 540
Ile Leu Tyr Arg Ala Gln Leu Ala Ser Glu Asp Thr Asn Ala Gln Lys
545 550 555 560
Thr Ile Thr Asn Cys Phe Leu Leu Lys Asn Lys Ile Trp Cys Ile Ser
565 570 575
Leu Val Glu Ile Tyr Asp Thr Gly Asp Asn Val Ile Arg Pro Lys Leu
580 585 590
Phe Ala Val Lys Ile Pro Glu Gln Cys Thr
595 600
<210> 82
<211> 775
<212> БЕЛОК
<213> Ротавирус A
<400> 82
Met Ala Ser Leu Ile Tyr Arg Gln Leu Leu Thr Asn Ser Tyr Ser Val
1 5 10 15
Asp Leu His Asp Glu Ile Glu Gln Ile Gly Ser Glu Lys Thr Gln Asn
20 25 30
Val Thr Ile Asn Pro Ser Pro Phe Ala Gln Thr Arg Tyr Ala Pro Val
35 40 45
Asn Trp Gly His Gly Glu Ile Asn Asp Ser Thr Thr Val Glu Pro Ile
50 55 60
Leu Asp Gly Pro Tyr Gln Pro Thr Thr Phe Thr Pro Pro Asn Asp Tyr
65 70 75 80
Trp Ile Leu Ile Asn Ser Asn Thr Asn Gly Val Val Tyr Glu Ser Thr
85 90 95
Asn Asn Ser Asp Phe Trp Thr Ala Val Val Ala Ile Glu Pro His Val
100 105 110
Asn Pro Val Asp Arg Gln Tyr Thr Ile Phe Gly Glu Ser Lys Gln Phe
115 120 125
Asn Val Ser Asn Asp Ser Asn Lys Trp Lys Phe Leu Glu Met Phe Arg
130 135 140
Ser Ser Ser Gln Asn Glu Phe Tyr Asn Arg Arg Thr Leu Thr Ser Asp
145 150 155 160
Thr Arg Phe Val Gly Ile Leu Lys Tyr Gly Gly Arg Val Trp Thr Phe
165 170 175
His Gly Glu Thr Pro Arg Ala Thr Thr Asp Ser Ser Ser Thr Ala Asn
180 185 190
Leu Asn Asn Ile Ser Ile Thr Ile His Ser Glu Phe Tyr Ile Ile Pro
195 200 205
Arg Ser Gln Glu Ser Lys Cys Asn Glu Tyr Ile Asn Asn Gly Leu Pro
210 215 220
Pro Ile Gln Asn Thr Arg Asn Val Val Pro Leu Pro Leu Ser Ser Arg
225 230 235 240
Ser Ile Gln Tyr Lys Arg Ala Gln Val Asn Glu Asp Ile Ile Val Ser
245 250 255
Lys Thr Ser Leu Trp Lys Glu Met Gln Tyr Asn Arg Asp Ile Ile Ile
260 265 270
Arg Phe Lys Phe Gly Asn Ser Ile Val Lys Met Gly Gly Leu Gly Tyr
275 280 285
Lys Trp Ser Glu Ile Ser Tyr Lys Ala Ala Asn Tyr Gln Tyr Asn Tyr
290 295 300
Leu Arg Asp Gly Glu Gln Val Thr Ala His Thr Thr Cys Ser Val Asn
305 310 315 320
Gly Val Asn Asn Phe Ser Tyr Asn Gly Gly Ser Leu Pro Thr Asp Phe
325 330 335
Gly Ile Ser Arg Tyr Glu Val Ile Lys Glu Asn Ser Tyr Val Tyr Val
340 345 350
Asp Tyr Trp Asp Asp Ser Lys Ala Phe Arg Asn Met Val Tyr Val Arg
355 360 365
Ser Leu Ala Ala Asn Leu Asn Ser Val Lys Cys Thr Gly Gly Ser Tyr
370 375 380
Asn Phe Ser Ile Pro Val Gly Ala Trp Pro Val Met Asn Gly Gly Ala
385 390 395 400
Val Ser Leu His Phe Ala Gly Val Thr Leu Ser Thr Gln Phe Thr Asp
405 410 415
Phe Val Ser Leu Asn Ser Leu Arg Phe Arg Phe Ser Leu Thr Val Asp
420 425 430
Glu Pro Pro Phe Ser Ile Leu Arg Thr Arg Thr Val Asn Leu Tyr Gly
435 440 445
Leu Pro Ala Ala Asn Pro Asn Asn Gly Asn Glu Tyr Tyr Glu Ile Ser
450 455 460
Gly Arg Phe Ser Leu Ile Tyr Leu Val Pro Thr Asn Asp Asp Tyr Gln
465 470 475 480
Thr Pro Ile Met Asn Ser Val Thr Val Arg Gln Asp Leu Glu Arg Gln
485 490 495
Leu Thr Asp Leu Arg Glu Glu Phe Asn Ser Leu Ser Gln Glu Ile Ala
500 505 510
Met Ala Gln Leu Ile Asp Leu Ala Leu Leu Pro Leu Asp Met Phe Ser
515 520 525
Met Phe Ser Gly Ile Lys Ser Thr Ile Asp Leu Thr Lys Ser Met Ala
530 535 540
Thr Ser Val Met Lys Lys Phe Arg Lys Ser Lys Leu Ala Thr Ser Ile
545 550 555 560
Ser Glu Met Thr Asn Ser Leu Ser Asp Ala Ala Ser Ser Ala Ser Arg
565 570 575
Asn Val Ser Ile Arg Ser Asn Leu Ser Ala Ile Ser Asn Trp Thr Asn
580 585 590
Val Ser Asn Asp Val Ser Asn Val Thr Asn Ser Leu Asn Asp Ile Ser
595 600 605
Thr Gln Thr Ser Thr Ile Ser Lys Lys Phe Arg Leu Lys Glu Met Ile
610 615 620
Thr Gln Thr Glu Gly Met Ser Phe Asp Asp Ile Ser Ala Ala Val Leu
625 630 635 640
Lys Thr Lys Ile Asp Met Ser Thr Gln Ile Gly Lys Asn Thr Leu Pro
645 650 655
Asp Ile Val Thr Glu Ala Ser Glu Lys Phe Ile Pro Lys Arg Ser Tyr
660 665 670
Arg Ile Leu Lys Asp Asp Glu Val Met Glu Ile Asn Thr Glu Gly Lys
675 680 685
Phe Phe Ala Tyr Lys Ile Asn Thr Phe Asp Glu Val Pro Phe Asp Val
690 695 700
Asn Lys Phe Ala Glu Leu Val Thr Asp Ser Pro Val Ile Ser Ala Ile
705 710 715 720
Ile Asp Phe Lys Thr Leu Lys Asn Leu Asn Asp Asn Tyr Gly Ile Thr
725 730 735
Arg Thr Glu Ala Leu Asn Leu Ile Lys Ser Asn Pro Asn Met Leu Arg
740 745 750
Asn Phe Ile Asn Gln Asn Asn Pro Ile Ile Arg Asn Arg Ile Glu Gln
755 760 765
Leu Ile Leu Gln Cys Lys Leu
770 775
<210> 83
<211> 230
<212> БЕЛОК
<213> Ротавирус A
<400> 83
Met Ala Ser Leu Ile Tyr Arg Gln Leu Leu Thr Asn Ser Tyr Ser Val
1 5 10 15
Asp Leu His Asp Glu Ile Glu Gln Ile Gly Ser Glu Lys Thr Gln Asn
20 25 30
Val Thr Ile Asn Pro Ser Pro Phe Ala Gln Thr Arg Tyr Ala Pro Val
35 40 45
Asn Trp Gly His Gly Glu Ile Asn Asp Ser Thr Thr Val Glu Pro Ile
50 55 60
Leu Asp Gly Pro Tyr Gln Pro Thr Thr Phe Thr Pro Pro Asn Asp Tyr
65 70 75 80
Trp Ile Leu Ile Asn Ser Asn Thr Asn Gly Val Val Tyr Glu Ser Thr
85 90 95
Asn Asn Ser Asp Phe Trp Thr Ala Val Val Ala Ile Glu Pro His Val
100 105 110
Asn Pro Val Asp Arg Gln Tyr Thr Ile Phe Gly Glu Ser Lys Gln Phe
115 120 125
Asn Val Ser Asn Asp Ser Asn Lys Trp Lys Phe Leu Glu Met Phe Arg
130 135 140
Ser Ser Ser Gln Asn Glu Phe Tyr Asn Arg Arg Thr Leu Thr Ser Asp
145 150 155 160
Thr Arg Phe Val Gly Ile Leu Lys Tyr Gly Gly Arg Val Trp Thr Phe
165 170 175
His Gly Glu Thr Pro Arg Ala Thr Thr Asp Ser Ser Ser Thr Ala Asn
180 185 190
Leu Asn Asn Ile Ser Ile Thr Ile His Ser Glu Phe Tyr Ile Ile Pro
195 200 205
Arg Ser Gln Glu Ser Lys Cys Asn Glu Tyr Ile Asn Asn Gly Leu Pro
210 215 220
Pro Ile Gln Asn Thr Arg
225 230
<210> 84
<211> 539
<212> БЕЛОК
<213> Метапневмовирус человека
<400> 84
Met Ser Trp Lys Val Val Ile Ile Phe Ser Leu Leu Ile Thr Pro Gln
1 5 10 15
His Gly Leu Lys Glu Ser Tyr Leu Glu Glu Ser Cys Ser Thr Ile Thr
20 25 30
Glu Gly Tyr Leu Ser Val Leu Arg Thr Gly Trp Tyr Thr Asn Val Phe
35 40 45
Thr Leu Glu Val Gly Asp Val Glu Asn Leu Thr Cys Ser Asp Gly Pro
50 55 60
Ser Leu Ile Lys Thr Glu Leu Asp Leu Thr Lys Ser Ala Leu Arg Glu
65 70 75 80
Leu Lys Thr Val Ser Ala Asp Gln Leu Ala Arg Glu Glu Gln Ile Glu
85 90 95
Asn Pro Arg Gln Ser Arg Phe Val Leu Gly Ala Ile Ala Leu Gly Val
100 105 110
Ala Thr Ala Ala Ala Val Thr Ala Gly Val Ala Ile Ala Lys Thr Ile
115 120 125
Arg Leu Glu Ser Glu Val Thr Ala Ile Lys Asn Ala Leu Lys Thr Thr
130 135 140
Asn Glu Ala Val Ser Thr Leu Gly Asn Gly Val Arg Val Leu Ala Thr
145 150 155 160
Ala Val Arg Glu Leu Lys Asp Phe Val Ser Lys Asn Leu Thr Arg Ala
165 170 175
Ile Asn Lys Asn Lys Cys Asp Ile Asp Asp Leu Lys Met Ala Val Ser
180 185 190
Phe Ser Gln Phe Asn Arg Arg Phe Leu Asn Val Val Arg Gln Phe Ser
195 200 205
Asp Asn Ala Gly Ile Thr Pro Ala Ile Ser Leu Asp Leu Met Thr Asp
210 215 220
Ala Glu Leu Ala Arg Ala Val Ser Asn Met Pro Thr Ser Ala Gly Gln
225 230 235 240
Ile Lys Leu Met Leu Glu Asn Arg Ala Met Val Arg Arg Lys Gly Phe
245 250 255
Gly Ile Leu Ile Gly Val Tyr Gly Ser Ser Val Ile Tyr Met Val Gln
260 265 270
Leu Pro Ile Phe Gly Val Ile Asp Thr Pro Cys Trp Ile Val Lys Ala
275 280 285
Ala Pro Ser Cys Ser Gly Lys Lys Gly Asn Tyr Ala Cys Leu Leu Arg
290 295 300
Glu Asp Gln Gly Trp Tyr Cys Gln Asn Ala Gly Ser Thr Val Tyr Tyr
305 310 315 320
Pro Asn Glu Lys Asp Cys Glu Thr Arg Gly Asp His Val Phe Cys Asp
325 330 335
Thr Ala Ala Gly Ile Asn Val Ala Glu Gln Ser Lys Glu Cys Asn Ile
340 345 350
Asn Ile Ser Thr Thr Asn Tyr Pro Cys Lys Val Ser Thr Gly Arg His
355 360 365
Pro Ile Ser Met Val Ala Leu Ser Pro Leu Gly Ala Leu Val Ala Cys
370 375 380
Tyr Lys Gly Val Ser Cys Ser Ile Gly Ser Asn Arg Val Gly Ile Ile
385 390 395 400
Lys Gln Leu Asn Lys Gly Cys Ser Tyr Ile Thr Asn Gln Asp Ala Asp
405 410 415
Thr Val Thr Ile Asp Asn Thr Val Tyr Gln Leu Ser Lys Val Glu Gly
420 425 430
Glu Gln His Val Ile Lys Gly Arg Pro Val Ser Ser Ser Phe Asp Pro
435 440 445
Ile Lys Phe Pro Glu Asp Gln Phe Asn Val Ala Leu Asp Gln Val Phe
450 455 460
Glu Asn Ile Glu Asn Ser Gln Ala Leu Val Asp Gln Ser Asn Arg Ile
465 470 475 480
Leu Ser Ser Ala Glu Lys Gly Asn Thr Gly Phe Ile Ile Val Ile Ile
485 490 495
Leu Ile Ala Val Leu Gly Ser Ser Met Ile Leu Val Ser Ile Phe Ile
500 505 510
Ile Ile Lys Lys Thr Lys Lys Pro Thr Gly Ala Pro Pro Glu Leu Ser
515 520 525
Gly Val Thr Asn Asn Gly Phe Ile Pro His Ser
530 535
<210> 85
<211> 219
<212> БЕЛОК
<213> Метапневмовирус человека
<400> 85
Met Glu Val Lys Val Glu Asn Ile Arg Ala Ile Asp Met Leu Lys Ala
1 5 10 15
Arg Val Lys Asn Arg Val Ala Arg Ser Lys Cys Phe Lys Asn Ala Ser
20 25 30
Leu Ile Leu Ile Gly Ile Thr Thr Leu Ser Ile Ala Leu Asn Ile Tyr
35 40 45
Leu Ile Ile Asn Tyr Thr Ile Gln Lys Thr Ser Ser Glu Ser Glu His
50 55 60
His Thr Ser Ser Pro Pro Thr Glu Ser Asn Lys Glu Ala Ser Thr Ile
65 70 75 80
Ser Thr Asp Asn Pro Asp Ile Asn Pro Asn Ser Gln His Pro Thr Gln
85 90 95
Gln Ser Thr Glu Asn Pro Thr Leu Asn Pro Ala Ala Ser Val Ser Pro
100 105 110
Ser Glu Thr Glu Pro Ala Ser Thr Pro Asp Thr Thr Asn Arg Leu Ser
115 120 125
Ser Val Asp Arg Ser Thr Ala Gln Pro Ser Glu Ser Arg Thr Lys Thr
130 135 140
Lys Pro Thr Val His Thr Arg Asn Asn Pro Ser Thr Ala Ser Ser Thr
145 150 155 160
Gln Ser Pro Pro Arg Ala Thr Thr Lys Ala Ile Arg Arg Ala Thr Thr
165 170 175
Phe Arg Met Ser Ser Thr Gly Lys Arg Pro Thr Thr Thr Ser Val Gln
180 185 190
Ser Asp Ser Ser Thr Thr Thr Gln Asn His Glu Glu Thr Gly Ser Ala
195 200 205
Asn Pro Gln Ala Ser Val Ser Thr Met Gln Asn
210 215
<210> 86
<211> 555
<212> БЕЛОК
<213> вирус парагриппа человека
<400> 86
Met Gln Lys Ser Glu Ile Leu Phe Leu Ile Tyr Ser Ser Leu Leu Leu
1 5 10 15
Ser Ser Ser Leu Cys Gln Ile Pro Val Asp Lys Leu Ser Asn Val Gly
20 25 30
Val Ile Ile Asn Glu Gly Lys Leu Leu Lys Ile Ala Gly Ser Tyr Glu
35 40 45
Ser Arg Tyr Ile Val Leu Ser Leu Val Pro Ser Ile Asp Leu Glu Asp
50 55 60
Gly Cys Gly Thr Thr Gln Ile Ile Gln Tyr Lys Asn Leu Leu Asn Arg
65 70 75 80
Leu Leu Ile Pro Leu Lys Asp Ala Leu Asp Leu Gln Glu Ser Leu Ile
85 90 95
Thr Ile Thr Asn Asp Thr Thr Val Thr Asn Asp Asn Pro Gln Ser Arg
100 105 110
Phe Phe Gly Ala Val Ile Gly Thr Ile Ala Leu Gly Val Ala Thr Ala
115 120 125
Ala Gln Ile Thr Ala Gly Ile Ala Leu Ala Glu Ala Arg Glu Ala Arg
130 135 140
Lys Asp Ile Ala Leu Ile Lys Asp Ser Ile Ile Lys Thr His Asn Ser
145 150 155 160
Val Glu Leu Ile Gln Arg Gly Ile Gly Glu Gln Ile Ile Ala Leu Lys
165 170 175
Thr Leu Gln Asp Phe Val Asn Asn Glu Ile Arg Pro Ala Ile Gly Glu
180 185 190
Leu Arg Cys Glu Thr Thr Ala Leu Lys Leu Gly Ile Lys Leu Thr Gln
195 200 205
His Tyr Ser Glu Leu Ala Thr Ala Phe Ser Ser Asn Leu Gly Thr Ile
210 215 220
Gly Glu Lys Ser Leu Thr Leu Gln Ala Leu Ser Ser Leu Tyr Ser Ala
225 230 235 240
Asn Ile Thr Glu Ile Leu Ser Thr Ile Lys Lys Asp Lys Ser Asp Ile
245 250 255
Tyr Asp Ile Ile Tyr Thr Glu Gln Val Lys Gly Thr Val Ile Asp Val
260 265 270
Asp Leu Glu Lys Tyr Met Val Thr Leu Leu Val Lys Ile Pro Ile Leu
275 280 285
Ser Glu Ile Pro Gly Val Leu Ile Tyr Arg Ala Ser Ser Ile Ser Tyr
290 295 300
Asn Ile Glu Gly Glu Glu Trp His Val Ala Ile Pro Asn Tyr Ile Ile
305 310 315 320
Asn Lys Ala Ser Ser Leu Gly Gly Ala Asp Val Thr Asn Cys Ile Glu
325 330 335
Ser Arg Leu Ala Tyr Ile Cys Pro Arg Asp Pro Thr Gln Leu Ile Pro
340 345 350
Asp Asn Gln Gln Lys Cys Ile Leu Gly Asp Val Ser Lys Cys Pro Val
355 360 365
Thr Lys Val Ile Asn Asn Leu Val Pro Lys Phe Ala Phe Ile Asn Gly
370 375 380
Gly Val Val Ala Asn Cys Ile Ala Ser Thr Cys Thr Cys Gly Thr Asn
385 390 395 400
Arg Ile Pro Val Asn Gln Asp Arg Ser Arg Gly Val Thr Phe Leu Thr
405 410 415
Tyr Thr Asn Cys Gly Leu Ile Gly Ile Asn Gly Ile Glu Leu Tyr Ala
420 425 430
Asn Lys Arg Gly Arg Asp Thr Thr Trp Gly Asn Gln Ile Ile Lys Val
435 440 445
Gly Pro Ala Val Ser Ile Arg Pro Val Asp Ile Ser Leu Asn Leu Ala
450 455 460
Ser Ala Thr Asn Phe Leu Glu Glu Ser Lys Ile Glu Leu Met Lys Ala
465 470 475 480
Lys Ala Ile Ile Ser Ala Val Gly Gly Trp His Asn Thr Glu Ser Thr
485 490 495
Gln Ile Ile Ile Ile Ile Ile Val Cys Ile Leu Ile Ile Ile Ile Cys
500 505 510
Gly Ile Leu Tyr Tyr Leu Tyr Arg Val Arg Arg Leu Leu Val Met Ile
515 520 525
Asn Ser Thr His Asn Ser Pro Val Asn Thr Tyr Thr Leu Glu Ser Arg
530 535 540
Met Arg Asn Pro Tyr Ile Gly Asn Asn Ser Asn
545 550 555
<210> 87
<211> 571
<212> БЕЛОК
<213> вирус парагриппа человека
<400> 87
Met Glu Asp Tyr Ser Asn Leu Ser Leu Lys Ser Ile Pro Lys Arg Thr
1 5 10 15
Cys Arg Ile Ile Phe Arg Thr Ala Thr Ile Leu Gly Ile Cys Thr Leu
20 25 30
Ile Val Leu Cys Ser Ser Ile Leu His Glu Ile Ile His Leu Asp Val
35 40 45
Ser Ser Gly Leu Met Asp Ser Asp Asp Ser Gln Gln Gly Ile Ile Gln
50 55 60
Pro Ile Ile Glu Ser Leu Lys Ser Leu Ile Ala Leu Ala Asn Gln Ile
65 70 75 80
Leu Tyr Asn Val Ala Ile Ile Ile Pro Leu Lys Ile Asp Ser Ile Glu
85 90 95
Thr Val Ile Phe Ser Ala Leu Lys Asp Met His Thr Gly Ser Met Ser
100 105 110
Asn Thr Asn Cys Thr Pro Gly Asn Leu Leu Leu His Asp Ala Ala Tyr
115 120 125
Ile Asn Gly Ile Asn Lys Phe Leu Val Leu Lys Ser Tyr Asn Gly Thr
130 135 140
Pro Lys Tyr Gly Pro Leu Leu Asn Ile Pro Ser Phe Ile Pro Ser Ala
145 150 155 160
Thr Ser Pro Asn Gly Cys Thr Arg Ile Pro Ser Phe Ser Leu Ile Lys
165 170 175
Thr His Trp Cys Tyr Thr His Asn Val Met Leu Gly Asp Cys Leu Asp
180 185 190
Phe Thr Thr Ser Asn Gln Tyr Leu Ala Met Gly Ile Ile Gln Gln Ser
195 200 205
Ala Ala Ala Phe Pro Ile Phe Arg Thr Met Lys Thr Ile Tyr Leu Ser
210 215 220
Asp Gly Ile Asn Arg Lys Ser Cys Ser Val Thr Ala Ile Pro Gly Gly
225 230 235 240
Cys Val Leu Tyr Cys Tyr Val Ala Thr Arg Ser Glu Lys Glu Asp Tyr
245 250 255
Ala Thr Thr Asp Leu Ala Glu Leu Arg Leu Ala Phe Tyr Tyr Tyr Asn
260 265 270
Asp Thr Phe Ile Glu Arg Val Ile Ser Leu Pro Asn Thr Thr Gly Gln
275 280 285
Trp Ala Thr Ile Asn Pro Ala Val Gly Ser Gly Ile Tyr His Leu Gly
290 295 300
Phe Ile Leu Phe Pro Val Tyr Gly Gly Leu Ile Ser Gly Thr Pro Ser
305 310 315 320
Tyr Asn Lys Gln Ser Ser Arg Tyr Phe Ile Pro Lys His Pro Asn Ile
325 330 335
Thr Cys Ala Gly Asn Ser Ser Glu Gln Ala Ala Ala Ala Arg Ser Ser
340 345 350
Tyr Val Ile Arg Tyr His Ser Asn Arg Leu Ile Gln Ser Ala Val Leu
355 360 365
Ile Cys Pro Leu Ser Asp Met His Thr Ala Arg Cys Asn Leu Val Met
370 375 380
Phe Asn Asn Ser Gln Val Met Met Gly Ala Glu Gly Arg Leu Tyr Val
385 390 395 400
Ile Asp Asn Asn Leu Tyr Tyr Tyr Gln Arg Ser Ser Ser Trp Trp Ser
405 410 415
Ala Ser Leu Phe Tyr Arg Ile Asn Thr Asp Phe Ser Lys Gly Ile Pro
420 425 430
Pro Ile Ile Glu Ala Gln Trp Val Pro Ser Tyr Gln Val Pro Arg Pro
435 440 445
Gly Val Met Pro Cys Asn Ala Thr Ser Phe Cys Pro Ala Asn Cys Ile
450 455 460
Thr Gly Val Tyr Ala Asp Val Trp Pro Leu Asn Asp Pro Glu Pro Thr
465 470 475 480
Ser Gln Asn Ala Leu Asn Pro Asn Tyr Arg Phe Ala Gly Ala Phe Leu
485 490 495
Arg Asn Glu Ser Asn Arg Thr Asn Pro Thr Phe Tyr Thr Ala Ser Ala
500 505 510
Ser Ala Leu Leu Asn Thr Thr Gly Phe Asn Asn Thr Asn His Lys Ala
515 520 525
Ala Tyr Thr Ser Ser Thr Cys Phe Lys Asn Thr Gly Thr Gln Lys Ile
530 535 540
Tyr Cys Leu Ile Ile Ile Glu Met Gly Ser Ser Leu Leu Gly Glu Phe
545 550 555 560
Gln Ile Ile Pro Phe Leu Arg Glu Leu Ile Pro
565 570
<210> 88
<211> 217
<212> БЕЛОК
<213> Plasmodium falciparum
<400> 88
Met Asn Lys Leu Tyr Ser Leu Phe Leu Phe Leu Phe Ile Gln Leu Ser
1 5 10 15
Ile Lys Tyr Asn Asn Ala Lys Val Thr Val Asp Thr Val Cys Lys Arg
20 25 30
Gly Phe Leu Ile Gln Met Ser Gly His Leu Glu Cys Lys Cys Glu Asn
35 40 45
Asp Leu Val Leu Val Asn Glu Glu Thr Cys Glu Glu Lys Val Leu Lys
50 55 60
Cys Asp Glu Lys Thr Val Asn Lys Pro Cys Gly Asp Phe Ser Lys Cys
65 70 75 80
Ile Lys Ile Asp Gly Asn Pro Val Ser Tyr Ala Cys Lys Cys Asn Leu
85 90 95
Gly Tyr Asp Met Val Asn Asn Val Cys Ile Pro Asn Glu Cys Lys Asn
100 105 110
Val Thr Cys Gly Asn Gly Lys Cys Ile Leu Asp Thr Ser Asn Pro Val
115 120 125
Lys Thr Gly Val Cys Ser Cys Asn Ile Gly Lys Val Pro Asn Val Gln
130 135 140
Asp Gln Asn Lys Cys Ser Lys Asp Gly Glu Thr Lys Cys Ser Leu Lys
145 150 155 160
Cys Leu Lys Glu Asn Glu Thr Cys Lys Ala Val Asp Gly Ile Tyr Lys
165 170 175
Cys Asp Cys Lys Asp Gly Phe Ile Ile Asp Asn Glu Ser Ser Ile Cys
180 185 190
Thr Ala Phe Ser Ala Tyr Asn Ile Leu Asn Leu Ser Ile Met Phe Ile
195 200 205
Leu Phe Ser Val Cys Phe Phe Ile Met
210 215
<210> 89
<211> 27
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен фолдон фибритина Т4
<400> 89
Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln Ala Tyr Val Arg Lys
1 5 10 15
Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu
20 25
<210> 90
<211> 540
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный антиген
реапираторно-сцинциляционного вируса
<400> 90
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gln Ser Thr Pro Ala Thr Asn Asn Arg Ala Arg Arg Glu Leu Pro
100 105 110
Arg Phe Met Asn Tyr Thr Leu Asn Asn Ala Lys Lys Thr Asn Val Thr
115 120 125
Leu Ser Lys Lys Arg Lys Arg Arg Phe Leu Gly Phe Leu Leu Gly Val
130 135 140
Gly Ser Ala Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu
145 150 155 160
Glu Gly Glu Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys
165 170 175
Ala Val Val Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val
180 185 190
Leu Asp Leu Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn
195 200 205
Lys Gln Ser Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln
210 215 220
Gln Lys Asn Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn
225 230 235 240
Ala Gly Val Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu
245 250 255
Leu Leu Ser Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys
260 265 270
Leu Met Ser Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile
275 280 285
Met Cys Ile Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro
290 295 300
Leu Tyr Gly Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro
305 310 315 320
Leu Cys Thr Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg
325 330 335
Thr Asp Arg Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe
340 345 350
Pro Gln Ala Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp
355 360 365
Thr Met Asn Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val
370 375 380
Asp Ile Phe Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr
385 390 395 400
Asp Val Ser Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys
405 410 415
Tyr Gly Lys Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile
420 425 430
Lys Thr Phe Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp
435 440 445
Thr Val Ser Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly
450 455 460
Lys Ser Leu Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro
465 470 475 480
Leu Val Phe Pro Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn
485 490 495
Glu Lys Ile Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Leu
500 505 510
Leu Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln Ala Tyr Val Arg
515 520 525
Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu
530 535 540
<210> 91
<211> 646
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный антиген
реапираторно-сцинциляционного вируса
<400> 91
Met Glu Leu Leu Ile Leu Lys Ala Asn Val Ile Ala Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Ser Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gln Ser Thr Pro Ala Thr Asn Asn Arg Ala Arg Arg Glu Leu Pro
100 105 110
Arg Phe Met Asn Tyr Thr Leu Asn Asn Ala Lys Lys Thr Asn Val Thr
115 120 125
Leu Ser Lys Lys Arg Lys Arg Arg Phe Leu Gly Phe Leu Leu Gly Val
130 135 140
Gly Ser Ala Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu
145 150 155 160
Glu Gly Glu Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys
165 170 175
Ala Val Val Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val
180 185 190
Leu Asp Leu Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn
195 200 205
Lys Gln Ser Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln
210 215 220
Gln Lys Asn Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn
225 230 235 240
Ala Gly Val Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu
245 250 255
Leu Leu Ser Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys
260 265 270
Leu Met Ser Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile
275 280 285
Met Cys Ile Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro
290 295 300
Leu Tyr Gly Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro
305 310 315 320
Leu Cys Thr Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg
325 330 335
Thr Asp Arg Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe
340 345 350
Pro Gln Ala Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp
355 360 365
Thr Met Asn Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val
370 375 380
Asp Ile Phe Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr
385 390 395 400
Asp Val Ser Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys
405 410 415
Tyr Gly Lys Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile
420 425 430
Lys Thr Phe Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp
435 440 445
Thr Val Ser Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly
450 455 460
Lys Ser Leu Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro
465 470 475 480
Leu Val Phe Pro Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn
485 490 495
Glu Lys Ile Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Leu
500 505 510
Leu Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln Ala Tyr Val Arg
515 520 525
Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu Gly Gly Ser Met
530 535 540
Glu Glu Val Val Leu Ile Thr Val Pro Ser Ala Leu Val Ala Val Lys
545 550 555 560
Ile Ala His Ala Leu Val Glu Glu Arg Leu Ala Ala Cys Val Asn Ile
565 570 575
Val Pro Gly Leu Thr Ser Ile Tyr Arg Glu Glu Gly Ser Val Val Ser
580 585 590
Asp His Glu Leu Leu Leu Leu Val Lys Thr Thr Thr Asp Ala Phe Pro
595 600 605
Lys Leu Lys Glu Arg Val Lys Glu Leu His Pro Tyr Glu Val Pro Glu
610 615 620
Ile Val Ala Leu Pro Ile Ala Glu Gly Asn Arg Glu Tyr Leu Asp Trp
625 630 635 640
Leu Arg Glu Asn Thr Gly
645
<210> 92
<211> 619
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный антиген
реапираторно-сцинциляционного вируса
<400> 92
Met Glu Leu Leu Ile Leu Lys Ala Asn Val Ile Ala Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Ser Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gln Ser Thr Pro Ala Thr Asn Asn Arg Ala Arg Arg Glu Leu Pro
100 105 110
Arg Phe Met Asn Tyr Thr Leu Asn Asn Ala Lys Lys Thr Asn Val Thr
115 120 125
Leu Ser Lys Lys Arg Lys Arg Arg Phe Leu Gly Phe Leu Leu Gly Val
130 135 140
Gly Ser Ala Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu
145 150 155 160
Glu Gly Glu Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys
165 170 175
Ala Val Val Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val
180 185 190
Leu Asp Leu Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn
195 200 205
Lys Gln Ser Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln
210 215 220
Gln Lys Asn Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn
225 230 235 240
Ala Gly Val Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu
245 250 255
Leu Leu Ser Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys
260 265 270
Leu Met Ser Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile
275 280 285
Met Cys Ile Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro
290 295 300
Leu Tyr Gly Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro
305 310 315 320
Leu Cys Thr Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg
325 330 335
Thr Asp Arg Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe
340 345 350
Pro Gln Ala Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp
355 360 365
Thr Met Asn Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val
370 375 380
Asp Ile Phe Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr
385 390 395 400
Asp Val Ser Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys
405 410 415
Tyr Gly Lys Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile
420 425 430
Lys Thr Phe Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp
435 440 445
Thr Val Ser Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly
450 455 460
Lys Ser Leu Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro
465 470 475 480
Leu Val Phe Pro Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn
485 490 495
Glu Lys Ile Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Leu
500 505 510
Leu Gly Gly Ser Met Glu Glu Val Val Leu Ile Thr Val Pro Ser Ala
515 520 525
Leu Val Ala Val Lys Ile Ala His Ala Leu Val Glu Glu Arg Leu Ala
530 535 540
Ala Cys Val Asn Ile Val Pro Gly Leu Thr Ser Ile Tyr Arg Glu Glu
545 550 555 560
Gly Ser Val Val Ser Asp His Glu Leu Leu Leu Leu Val Lys Thr Thr
565 570 575
Thr Asp Ala Phe Pro Lys Leu Lys Glu Arg Val Lys Glu Leu His Pro
580 585 590
Tyr Glu Val Pro Glu Ile Val Ala Leu Pro Ile Ala Glu Gly Asn Arg
595 600 605
Glu Tyr Leu Asp Trp Leu Arg Glu Asn Thr Gly
610 615
<210> 93
<211> 665
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный антиген
реапираторно-сцинциляционного вируса
<400> 93
Met Glu Leu Leu Ile Leu Lys Ala Asn Val Ile Ala Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Ser Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gln Ser Thr Pro Ala Thr Asn Asn Arg Ala Arg Arg Glu Leu Pro
100 105 110
Arg Phe Met Asn Tyr Thr Leu Asn Asn Ala Lys Lys Thr Asn Val Thr
115 120 125
Leu Ser Lys Lys Arg Lys Arg Arg Phe Leu Gly Phe Leu Leu Gly Val
130 135 140
Gly Ser Ala Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu
145 150 155 160
Glu Gly Glu Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys
165 170 175
Ala Val Val Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val
180 185 190
Leu Asp Leu Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn
195 200 205
Lys Gln Ser Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln
210 215 220
Gln Lys Asn Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn
225 230 235 240
Ala Gly Val Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu
245 250 255
Leu Leu Ser Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys
260 265 270
Leu Met Ser Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile
275 280 285
Met Cys Ile Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro
290 295 300
Leu Tyr Gly Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro
305 310 315 320
Leu Cys Thr Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg
325 330 335
Thr Asp Arg Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe
340 345 350
Pro Gln Ala Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp
355 360 365
Thr Met Asn Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val
370 375 380
Asp Ile Phe Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr
385 390 395 400
Asp Val Ser Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys
405 410 415
Tyr Gly Lys Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile
420 425 430
Lys Thr Phe Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp
435 440 445
Thr Val Ser Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly
450 455 460
Lys Ser Leu Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro
465 470 475 480
Leu Val Phe Pro Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn
485 490 495
Glu Lys Ile Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Leu
500 505 510
Leu Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln Ala Tyr Val Arg
515 520 525
Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu Gly Gly Ser Met
530 535 540
Val Arg Gly Ile Arg Gly Ala Ile Thr Val Asn Ser Asp Thr Pro Thr
545 550 555 560
Ser Ile Ile Ile Ala Thr Ile Leu Leu Leu Glu Lys Met Leu Glu Ala
565 570 575
Asn Gly Ile Gln Ser Tyr Glu Glu Leu Ala Ala Val Ile Phe Thr Val
580 585 590
Thr Glu Asp Leu Thr Ser Ala Phe Pro Ala Glu Ala Ala Arg Gln Ile
595 600 605
Gly Met His Arg Val Pro Leu Leu Ser Ala Arg Glu Val Pro Val Pro
610 615 620
Gly Ser Leu Pro Arg Val Ile Arg Val Leu Ala Leu Trp Asn Thr Asp
625 630 635 640
Thr Pro Gln Asp Arg Val Arg His Val Tyr Leu Ser Glu Ala Val Arg
645 650 655
Leu Arg Pro Asp Leu Glu Ser Ala Gln
660 665
<210> 94
<211> 638
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный антиген
реапираторно-сцинциляционного вируса
<400> 94
Met Glu Leu Leu Ile Leu Lys Ala Asn Val Ile Ala Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Ser Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gln Ser Thr Pro Ala Thr Asn Asn Arg Ala Arg Arg Glu Leu Pro
100 105 110
Arg Phe Met Asn Tyr Thr Leu Asn Asn Ala Lys Lys Thr Asn Val Thr
115 120 125
Leu Ser Lys Lys Arg Lys Arg Arg Phe Leu Gly Phe Leu Leu Gly Val
130 135 140
Gly Ser Ala Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu
145 150 155 160
Glu Gly Glu Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys
165 170 175
Ala Val Val Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val
180 185 190
Leu Asp Leu Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn
195 200 205
Lys Gln Ser Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln
210 215 220
Gln Lys Asn Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn
225 230 235 240
Ala Gly Val Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu
245 250 255
Leu Leu Ser Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys
260 265 270
Leu Met Ser Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile
275 280 285
Met Cys Ile Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro
290 295 300
Leu Tyr Gly Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro
305 310 315 320
Leu Cys Thr Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg
325 330 335
Thr Asp Arg Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe
340 345 350
Pro Gln Ala Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp
355 360 365
Thr Met Asn Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val
370 375 380
Asp Ile Phe Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr
385 390 395 400
Asp Val Ser Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys
405 410 415
Tyr Gly Lys Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile
420 425 430
Lys Thr Phe Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp
435 440 445
Thr Val Ser Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly
450 455 460
Lys Ser Leu Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro
465 470 475 480
Leu Val Phe Pro Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn
485 490 495
Glu Lys Ile Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Leu
500 505 510
Leu Gly Gly Ser Met Val Arg Gly Ile Arg Gly Ala Ile Thr Val Asn
515 520 525
Ser Asp Thr Pro Thr Ser Ile Ile Ile Ala Thr Ile Leu Leu Leu Glu
530 535 540
Lys Met Leu Glu Ala Asn Gly Ile Gln Ser Tyr Glu Glu Leu Ala Ala
545 550 555 560
Val Ile Phe Thr Val Thr Glu Asp Leu Thr Ser Ala Phe Pro Ala Glu
565 570 575
Ala Ala Arg Gln Ile Gly Met His Arg Val Pro Leu Leu Ser Ala Arg
580 585 590
Glu Val Pro Val Pro Gly Ser Leu Pro Arg Val Ile Arg Val Leu Ala
595 600 605
Leu Trp Asn Thr Asp Thr Pro Gln Asp Arg Val Arg His Val Tyr Leu
610 615 620
Ser Glu Ala Val Arg Leu Arg Pro Asp Leu Glu Ser Ala Gln
625 630 635
<210> 95
<211> 769
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный антиген
реапираторно-сцинциляционного вируса
<400> 95
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gln Ser Thr Pro Ala Thr Asn Asn Arg Ala Arg Arg Glu Leu Pro
100 105 110
Arg Phe Met Asn Tyr Thr Leu Asn Asn Ala Lys Lys Thr Asn Val Thr
115 120 125
Leu Ser Lys Lys Arg Lys Arg Arg Phe Leu Gly Phe Leu Leu Gly Val
130 135 140
Gly Ser Ala Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu
145 150 155 160
Glu Gly Glu Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys
165 170 175
Ala Val Val Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val
180 185 190
Leu Asp Leu Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn
195 200 205
Lys Gln Ser Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln
210 215 220
Gln Lys Asn Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn
225 230 235 240
Ala Gly Val Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu
245 250 255
Leu Leu Ser Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys
260 265 270
Leu Met Ser Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile
275 280 285
Met Cys Ile Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro
290 295 300
Leu Tyr Gly Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro
305 310 315 320
Leu Cys Thr Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg
325 330 335
Thr Asp Arg Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe
340 345 350
Pro Gln Ala Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp
355 360 365
Thr Met Asn Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val
370 375 380
Asp Ile Phe Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr
385 390 395 400
Asp Val Ser Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys
405 410 415
Tyr Gly Lys Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile
420 425 430
Lys Thr Phe Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp
435 440 445
Thr Val Ser Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly
450 455 460
Lys Ser Leu Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro
465 470 475 480
Leu Val Phe Pro Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn
485 490 495
Glu Lys Ile Asn Gln Ser Leu Ala Phe Ile Arg Gly Tyr Ile Pro Glu
500 505 510
Ala Pro Arg Asp Gly Gln Ala Tyr Val Arg Lys Asp Gly Glu Trp Val
515 520 525
Leu Leu Ser Thr Phe Leu Gly Ser Gly Ser His His His His His His
530 535 540
His His Gly Gly Ser Gly Gly Ser Gly Ser Glu Lys Ala Ala Lys Ala
545 550 555 560
Glu Glu Ala Ala Arg Lys Met Glu Glu Leu Phe Lys Lys His Lys Ile
565 570 575
Val Ala Val Leu Arg Ala Asn Ser Val Glu Glu Ala Ile Glu Lys Ala
580 585 590
Val Ala Val Phe Ala Gly Gly Val His Leu Ile Glu Ile Thr Phe Thr
595 600 605
Val Pro Asp Ala Asp Thr Val Ile Lys Ala Leu Ser Val Leu Lys Glu
610 615 620
Lys Gly Ala Ile Ile Gly Ala Gly Thr Val Thr Ser Val Glu Gln Cys
625 630 635 640
Arg Lys Ala Val Glu Ser Gly Ala Glu Phe Ile Val Ser Pro His Leu
645 650 655
Asp Glu Glu Ile Ser Gln Phe Cys Lys Glu Lys Gly Val Phe Tyr Met
660 665 670
Pro Gly Val Met Thr Pro Thr Glu Leu Val Lys Ala Met Lys Leu Gly
675 680 685
His Thr Ile Leu Lys Leu Phe Pro Gly Glu Val Val Gly Pro Gln Phe
690 695 700
Val Lys Ala Met Lys Gly Pro Phe Pro Asn Val Lys Phe Val Pro Thr
705 710 715 720
Gly Gly Val Asn Leu Asp Asn Val Cys Glu Trp Phe Lys Ala Gly Val
725 730 735
Leu Ala Val Gly Val Gly Ser Ala Leu Val Lys Gly Thr Pro Asp Glu
740 745 750
Val Arg Glu Lys Ala Lys Ala Phe Val Glu Lys Ile Arg Gly Cys Thr
755 760 765
Glu
<210> 96
<211> 730
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный антиген
реапираторно-сцинциляционного вируса
<400> 96
Met Glu Leu Leu Ile Leu Lys Ala Asn Val Ile Ala Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Ser Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gln Ser Thr Pro Ala Thr Asn Asn Arg Ala Arg Arg Glu Leu Pro
100 105 110
Arg Phe Met Asn Tyr Thr Leu Asn Asn Ala Lys Lys Thr Asn Val Thr
115 120 125
Leu Ser Lys Lys Arg Lys Arg Arg Phe Leu Gly Phe Leu Leu Gly Val
130 135 140
Gly Ser Ala Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu
145 150 155 160
Glu Gly Glu Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys
165 170 175
Ala Val Val Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val
180 185 190
Leu Asp Leu Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn
195 200 205
Lys Gln Ser Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln
210 215 220
Gln Lys Asn Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn
225 230 235 240
Ala Gly Val Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu
245 250 255
Leu Leu Ser Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys
260 265 270
Leu Met Ser Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile
275 280 285
Met Cys Ile Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro
290 295 300
Leu Tyr Gly Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro
305 310 315 320
Leu Cys Thr Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg
325 330 335
Thr Asp Arg Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe
340 345 350
Pro Gln Ala Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp
355 360 365
Thr Met Asn Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val
370 375 380
Asp Ile Phe Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr
385 390 395 400
Asp Val Ser Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys
405 410 415
Tyr Gly Lys Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile
420 425 430
Lys Thr Phe Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp
435 440 445
Thr Val Ser Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly
450 455 460
Lys Ser Leu Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro
465 470 475 480
Leu Val Phe Pro Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn
485 490 495
Glu Lys Ile Asn Gln Ser Leu Ala Phe Ile Arg Gly Gly Ser Gly Gly
500 505 510
Ser Gly Ser Glu Lys Ala Ala Lys Ala Glu Glu Ala Ala Arg Lys Met
515 520 525
Glu Glu Leu Phe Lys Lys His Lys Ile Val Ala Val Leu Arg Ala Asn
530 535 540
Ser Val Glu Glu Ala Ile Glu Lys Ala Val Ala Val Phe Ala Gly Gly
545 550 555 560
Val His Leu Ile Glu Ile Thr Phe Thr Val Pro Asp Ala Asp Thr Val
565 570 575
Ile Lys Ala Leu Ser Val Leu Lys Glu Lys Gly Ala Ile Ile Gly Ala
580 585 590
Gly Thr Val Thr Ser Val Glu Gln Cys Arg Lys Ala Val Glu Ser Gly
595 600 605
Ala Glu Phe Ile Val Ser Pro His Leu Asp Glu Glu Ile Ser Gln Phe
610 615 620
Cys Lys Glu Lys Gly Val Phe Tyr Met Pro Gly Val Met Thr Pro Thr
625 630 635 640
Glu Leu Val Lys Ala Met Lys Leu Gly His Thr Ile Leu Lys Leu Phe
645 650 655
Pro Gly Glu Val Val Gly Pro Gln Phe Val Lys Ala Met Lys Gly Pro
660 665 670
Phe Pro Asn Val Lys Phe Val Pro Thr Gly Gly Val Asn Leu Asp Asn
675 680 685
Val Cys Glu Trp Phe Lys Ala Gly Val Leu Ala Val Gly Val Gly Ser
690 695 700
Ala Leu Val Lys Gly Thr Pro Asp Glu Val Arg Glu Lys Ala Lys Ala
705 710 715 720
Phe Val Glu Lys Ile Arg Gly Cys Thr Glu
725 730
<210> 97
<211> 676
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный антиген
реапираторно-сцинциляционного вируса
<400> 97
Met Glu Leu Leu Ile Leu Lys Ala Asn Ala Ile Thr Thr Ile Leu Thr
1 5 10 15
Ala Val Thr Phe Cys Phe Ala Ser Gly Gln Asn Ile Thr Glu Glu Phe
20 25 30
Tyr Gln Ser Thr Cys Ser Ala Val Ser Lys Gly Tyr Leu Ser Ala Leu
35 40 45
Arg Thr Gly Trp Tyr Thr Ser Val Ile Thr Ile Glu Leu Ser Asn Ile
50 55 60
Lys Glu Asn Lys Cys Asn Gly Thr Asp Ala Lys Val Lys Leu Ile Lys
65 70 75 80
Gln Glu Leu Asp Lys Tyr Lys Asn Ala Val Thr Glu Leu Gln Leu Leu
85 90 95
Met Gln Ser Thr Pro Ala Thr Asn Asn Arg Ala Arg Arg Glu Leu Pro
100 105 110
Arg Phe Met Asn Tyr Thr Leu Asn Asn Ala Lys Lys Thr Asn Val Thr
115 120 125
Leu Ser Lys Lys Arg Lys Arg Arg Phe Leu Gly Phe Leu Leu Gly Val
130 135 140
Gly Ser Ala Ile Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu
145 150 155 160
Glu Gly Glu Val Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys
165 170 175
Ala Val Val Ser Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val
180 185 190
Leu Asp Leu Lys Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn
195 200 205
Lys Gln Ser Cys Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln
210 215 220
Gln Lys Asn Asn Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn
225 230 235 240
Ala Gly Val Thr Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu
245 250 255
Leu Leu Ser Leu Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys
260 265 270
Leu Met Ser Asn Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile
275 280 285
Met Cys Ile Ile Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro
290 295 300
Leu Tyr Gly Val Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro
305 310 315 320
Leu Cys Thr Thr Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg
325 330 335
Thr Asp Arg Gly Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe
340 345 350
Pro Gln Ala Glu Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp
355 360 365
Thr Met Asn Ser Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val
370 375 380
Asp Ile Phe Asn Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr
385 390 395 400
Asp Val Ser Ser Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys
405 410 415
Tyr Gly Lys Thr Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile
420 425 430
Lys Thr Phe Ser Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp
435 440 445
Thr Val Ser Val Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly
450 455 460
Lys Ser Leu Tyr Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro
465 470 475 480
Leu Val Phe Pro Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn
485 490 495
Glu Lys Ile Asn Gln Ser Leu Ala Phe Ile Arg Lys Ser Asp Glu Leu
500 505 510
Leu Gly Gly Ser Gly Gly Ser Gly Ser Asp Asp Ala Arg Ile Ala Ala
515 520 525
Ile Gly Asp Val Asp Glu Leu Asn Ser Gln Ile Gly Val Leu Leu Ala
530 535 540
Glu Pro Leu Pro Asp Asp Val Arg Ala Ala Leu Ser Ala Ile Gln His
545 550 555 560
Asp Leu Phe Asp Leu Gly Gly Glu Leu Cys Ile Pro Gly His Ala Ala
565 570 575
Ile Thr Glu Asp His Leu Leu Arg Leu Ala Leu Trp Leu Val His Tyr
580 585 590
Asn Gly Gln Leu Pro Pro Leu Glu Glu Phe Ile Leu Pro Gly Gly Ala
595 600 605
Arg Gly Ala Ala Leu Ala His Val Cys Arg Thr Val Cys Arg Arg Ala
610 615 620
Glu Arg Ser Ile Lys Ala Leu Gly Ala Ser Glu Pro Leu Asn Ile Ala
625 630 635 640
Pro Ala Ala Tyr Val Asn Leu Leu Ser Asp Leu Leu Phe Val Leu Ala
645 650 655
Arg Val Leu Asn Arg Ala Ala Gly Gly Ala Asp Val Leu Trp Asp Arg
660 665 670
Thr Arg Ala His
675
<210> 98
<211> 274
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 98
Met Asn Arg Thr Ala Phe Cys Cys Leu Ser Leu Thr Thr Ala Leu Ile
1 5 10 15
Leu Thr Ala Cys Ser Ser Gly Gly Gly Gly Val Ala Ala Asp Ile Gly
20 25 30
Ala Gly Leu Ala Asp Ala Leu Thr Ala Pro Leu Asp His Lys Asp Lys
35 40 45
Gly Leu Gln Ser Leu Thr Leu Asp Gln Ser Val Arg Lys Asn Glu Lys
50 55 60
Leu Lys Leu Ala Ala Gln Gly Ala Glu Lys Thr Tyr Gly Asn Gly Asp
65 70 75 80
Ser Leu Asn Thr Gly Lys Leu Lys Asn Asp Lys Val Ser Arg Phe Asp
85 90 95
Phe Ile Arg Gln Ile Glu Val Asp Gly Gln Leu Ile Thr Leu Glu Ser
100 105 110
Gly Glu Phe Gln Val Tyr Lys Gln Ser His Ser Ala Leu Thr Ala Phe
115 120 125
Gln Thr Glu Gln Ile Gln Asp Ser Glu His Ser Gly Lys Met Val Ala
130 135 140
Lys Arg Gln Phe Arg Ile Gly Asp Ile Ala Gly Glu His Thr Ser Phe
145 150 155 160
Asp Lys Leu Pro Glu Gly Gly Arg Ala Thr Tyr Arg Gly Thr Ala Phe
165 170 175
Gly Ser Asp Asp Ala Gly Gly Lys Leu Thr Tyr Thr Ile Asp Phe Ala
180 185 190
Ala Lys Gln Gly Asn Gly Lys Ile Glu His Leu Lys Ser Pro Glu Leu
195 200 205
Asn Val Asp Leu Ala Ala Ala Asp Ile Lys Pro Asp Gly Lys Arg His
210 215 220
Ala Val Ile Ser Gly Ser Val Leu Tyr Asn Gln Ala Glu Lys Gly Ser
225 230 235 240
Tyr Ser Leu Gly Ile Phe Gly Gly Lys Ala Gln Glu Val Ala Gly Ser
245 250 255
Ala Glu Val Lys Thr Val Asn Gly Ile Arg His Ile Gly Leu Ala Ala
260 265 270
Lys Gln
<210> 99
<211> 370
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 99
Met Gln Thr Ala Ala Arg Arg Ser Phe Asp Tyr Asp Met Pro Leu Ile
1 5 10 15
Gln Thr Pro Thr Ser Ala Cys Gln Ile Arg Gln Ala Trp Ala Lys Val
20 25 30
Ala Asp Thr Pro Asp Arg Glu Thr Ala Gly Arg Leu Lys Asp Glu Ile
35 40 45
Lys Ala Leu Leu Lys Glu Thr Asn Ala Val Leu Val Ala His Tyr Tyr
50 55 60
Val Asp Pro Leu Ile Gln Asp Leu Ala Leu Glu Thr Gly Gly Cys Val
65 70 75 80
Gly Asp Ser Leu Glu Met Ala Arg Phe Gly Ala Glu His Glu Ala Gly
85 90 95
Thr Leu Val Val Ala Gly Val Arg Phe Met Gly Glu Ser Ala Lys Ile
100 105 110
Leu Cys Pro Glu Lys Thr Val Leu Met Pro Asp Leu Glu Ala Glu Cys
115 120 125
Ser Leu Asp Leu Gly Cys Pro Glu Glu Ala Phe Ser Ala Phe Cys Asp
130 135 140
Gln His Pro Asp Arg Thr Val Val Val Tyr Ala Asn Thr Ser Ala Ala
145 150 155 160
Val Lys Ala Arg Ala Asp Trp Val Val Thr Ser Ser Val Ala Leu Glu
165 170 175
Ile Val Ser Tyr Leu Lys Ser Arg Gly Glu Lys Leu Ile Trp Gly Pro
180 185 190
Asp Arg His Leu Gly Asp Tyr Ile Arg Arg Glu Thr Gly Ala Asp Met
195 200 205
Leu Leu Trp Gln Gly Ser Cys Ile Val His Asn Glu Phe Lys Gly Gln
210 215 220
Glu Leu Ala Ala Leu Lys Ala Glu His Pro Asp Ala Val Val Leu Val
225 230 235 240
His Pro Glu Ser Pro Gln Ser Val Ile Glu Leu Gly Asp Val Val Gly
245 250 255
Ser Thr Ser Lys Leu Leu Lys Ala Ala Val Ser Arg Pro Glu Lys Lys
260 265 270
Phe Ile Val Ala Thr Asp Leu Gly Ile Leu His Glu Met Gln Lys Gln
275 280 285
Ala Pro Asp Lys Gln Phe Ile Ala Ala Pro Thr Ala Gly Asn Gly Gly
290 295 300
Ser Cys Lys Ser Cys Ala Phe Cys Pro Trp Met Ala Met Asn Ser Leu
305 310 315 320
Gly Gly Ile Lys Tyr Ala Leu Thr Ser Gly His Asn Glu Ile Leu Leu
325 330 335
Asp Arg Lys Leu Gly Glu Ala Ala Lys Leu Pro Leu Gln Arg Met Leu
340 345 350
Asp Phe Ala Ala Gly Leu Lys Arg Gly Asp Val Phe Asn Gly Met Gly
355 360 365
Pro Ala
370
<210> 100
<211> 492
<212> БЕЛОК
<213> Neisseria meningitidis
<400> 100
Met Phe Lys Arg Ser Val Ile Ala Met Ala Cys Ile Phe Ala Leu Ser
1 5 10 15
Ala Cys Gly Gly Gly Gly Gly Gly Ser Pro Asp Val Lys Ser Ala Asp
20 25 30
Thr Leu Ser Lys Pro Ala Ala Pro Val Val Ser Glu Lys Glu Thr Glu
35 40 45
Ala Lys Glu Asp Ala Pro Gln Ala Gly Ser Gln Gly Gln Gly Ala Pro
50 55 60
Ser Ala Gln Gly Gly Gln Asp Met Ala Ala Val Ser Glu Glu Asn Thr
65 70 75 80
Gly Asn Gly Gly Ala Ala Ala Thr Asp Lys Pro Lys Asn Glu Asp Glu
85 90 95
Gly Ala Gln Asn Asp Met Pro Gln Asn Ala Ala Asp Thr Asp Ser Leu
100 105 110
Thr Pro Asn His Thr Pro Ala Ser Asn Met Pro Ala Gly Asn Met Glu
115 120 125
Asn Gln Ala Pro Asp Ala Gly Glu Ser Glu Gln Pro Ala Asn Gln Pro
130 135 140
Asp Met Ala Asn Thr Ala Asp Gly Met Gln Gly Asp Asp Pro Ser Ala
145 150 155 160
Gly Gly Glu Asn Ala Gly Asn Thr Ala Ala Gln Gly Thr Asn Gln Ala
165 170 175
Glu Asn Asn Gln Thr Ala Gly Ser Gln Asn Pro Ala Ser Ser Thr Asn
180 185 190
Pro Ser Ala Thr Asn Ser Gly Gly Asp Phe Gly Arg Thr Asn Val Gly
195 200 205
Asn Ser Val Val Ile Asp Gly Pro Ser Gln Asn Ile Thr Leu Thr His
210 215 220
Cys Lys Gly Asp Ser Cys Ser Gly Asn Asn Phe Leu Asp Glu Glu Val
225 230 235 240
Gln Leu Lys Ser Glu Phe Glu Lys Leu Ser Asp Ala Asp Lys Ile Ser
245 250 255
Asn Tyr Lys Lys Asp Gly Lys Asn Asp Gly Lys Asn Asp Lys Phe Val
260 265 270
Gly Leu Val Ala Asp Ser Val Gln Met Lys Gly Ile Asn Gln Tyr Ile
275 280 285
Ile Phe Tyr Lys Pro Lys Pro Thr Ser Phe Ala Arg Phe Arg Arg Ser
290 295 300
Ala Arg Ser Arg Arg Ser Leu Pro Ala Glu Met Pro Leu Ile Pro Val
305 310 315 320
Asn Gln Ala Asp Thr Leu Ile Val Asp Gly Glu Ala Val Ser Leu Thr
325 330 335
Gly His Ser Gly Asn Ile Phe Ala Pro Glu Gly Asn Tyr Arg Tyr Leu
340 345 350
Thr Tyr Gly Ala Glu Lys Leu Pro Gly Gly Ser Tyr Ala Leu Arg Val
355 360 365
Gln Gly Glu Pro Ser Lys Gly Glu Met Leu Ala Gly Thr Ala Val Tyr
370 375 380
Asn Gly Glu Val Leu His Phe His Thr Glu Asn Gly Arg Pro Ser Pro
385 390 395 400
Ser Arg Gly Arg Phe Ala Ala Lys Val Asp Phe Gly Ser Lys Ser Val
405 410 415
Asp Gly Ile Ile Asp Ser Gly Asp Gly Leu His Met Gly Thr Gln Lys
420 425 430
Phe Lys Ala Ala Ile Asp Gly Asn Gly Phe Lys Gly Thr Trp Thr Glu
435 440 445
Asn Gly Gly Gly Asp Val Ser Gly Lys Phe Tyr Gly Pro Ala Gly Glu
450 455 460
Glu Val Ala Gly Lys Tyr Ser Tyr Arg Pro Thr Asp Ala Glu Lys Gly
465 470 475 480
Gly Phe Gly Val Phe Ala Gly Lys Lys Glu Gln Asp
485 490
<210> 101
<211> 615
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный антиген
реапираторно-сцинциляционного вируса
<400> 101
Gln Asn Ile Thr Glu Glu Phe Tyr Gln Ser Thr Cys Ser Ala Val Ser
1 5 10 15
Lys Gly Tyr Leu Ser Ala Leu Arg Thr Gly Trp Tyr Thr Ser Val Ile
20 25 30
Thr Ile Glu Leu Ser Asn Ile Lys Glu Asn Lys Cys Asn Gly Thr Asp
35 40 45
Ala Lys Val Lys Leu Ile Lys Gln Glu Leu Asp Lys Tyr Lys Asn Ala
50 55 60
Val Thr Glu Leu Gln Leu Leu Met Gln Ser Thr Pro Ala Thr Asn Asn
65 70 75 80
Arg Ala Arg Arg Glu Leu Pro Arg Phe Met Asn Tyr Thr Leu Asn Asn
85 90 95
Ala Lys Lys Thr Asn Val Thr Leu Ser Lys Lys Arg Lys Arg Arg Phe
100 105 110
Leu Gly Phe Leu Leu Gly Val Gly Ser Ala Ile Ala Ser Gly Val Ala
115 120 125
Val Cys Lys Val Leu His Leu Glu Gly Glu Val Asn Lys Ile Lys Ser
130 135 140
Ala Leu Leu Ser Thr Asn Lys Ala Val Val Ser Leu Ser Asn Gly Val
145 150 155 160
Ser Val Leu Thr Phe Lys Val Leu Asp Leu Lys Asn Tyr Ile Asp Lys
165 170 175
Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser Cys Ser Ile Ser Asn Ile
180 185 190
Glu Thr Val Ile Glu Phe Gln Gln Lys Asn Asn Arg Leu Leu Glu Ile
195 200 205
Thr Arg Glu Phe Ser Val Asn Ala Gly Val Thr Thr Pro Val Ser Thr
210 215 220
Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser Leu Ile Asn Asp Met Pro
225 230 235 240
Ile Thr Asn Asp Gln Lys Lys Leu Met Ser Asn Asn Val Gln Ile Val
245 250 255
Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile Ile Lys Glu Glu Val Leu
260 265 270
Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly Val Ile Asp Thr Pro Cys
275 280 285
Trp Lys Leu His Thr Ser Pro Leu Cys Thr Thr Asn Thr Lys Glu Gly
290 295 300
Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg Gly Trp Tyr Cys Asp Asn
305 310 315 320
Ala Gly Ser Val Ser Phe Phe Pro Gln Ala Glu Thr Cys Lys Val Gln
325 330 335
Ser Asn Arg Val Phe Cys Asp Thr Met Asn Ser Leu Thr Leu Pro Ser
340 345 350
Glu Val Asn Leu Cys Asn Val Asp Ile Phe Asn Pro Lys Tyr Asp Cys
355 360 365
Lys Ile Met Thr Ser Lys Thr Asp Val Ser Ser Ser Val Ile Thr Ser
370 375 380
Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys Thr Lys Cys Thr Ala Ser
385 390 395 400
Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe Ser Asn Gly Cys Asp Tyr
405 410 415
Val Ser Asn Lys Gly Val Asp Thr Val Ser Val Gly Asn Thr Leu Tyr
420 425 430
Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu Tyr Val Lys Gly Glu Pro
435 440 445
Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe Pro Ser Asp Glu Phe Asp
450 455 460
Ala Ser Ile Ser Gln Val Asn Glu Lys Ile Asn Gln Ser Leu Ala Phe
465 470 475 480
Ile Arg Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln Ala Tyr Val
485 490 495
Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu Gly Gly Ser
500 505 510
Met Glu Glu Val Val Leu Ile Thr Val Pro Ser Ala Leu Val Ala Val
515 520 525
Lys Ile Ala His Ala Leu Val Glu Glu Arg Leu Ala Ala Cys Val Asn
530 535 540
Ile Val Pro Gly Leu Thr Ser Ile Tyr Arg Glu Glu Gly Ser Val Val
545 550 555 560
Ser Asp His Glu Leu Leu Leu Leu Val Lys Thr Thr Thr Asp Ala Phe
565 570 575
Pro Lys Leu Lys Glu Arg Val Lys Glu Leu His Pro Tyr Glu Val Pro
580 585 590
Glu Ile Val Ala Leu Pro Ile Ala Glu Gly Asn Arg Glu Tyr Leu Asp
595 600 605
Trp Leu Arg Glu Asn Thr Gly
610 615
<210> 102
<211> 588
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный антиген
реапираторно-сцинциляционного вируса
<400> 102
Gln Asn Ile Thr Glu Glu Phe Tyr Gln Ser Thr Cys Ser Ala Val Ser
1 5 10 15
Lys Gly Tyr Leu Ser Ala Leu Arg Thr Gly Trp Tyr Thr Ser Val Ile
20 25 30
Thr Ile Glu Leu Ser Asn Ile Lys Glu Asn Lys Cys Asn Gly Thr Asp
35 40 45
Ala Lys Val Lys Leu Ile Lys Gln Glu Leu Asp Lys Tyr Lys Asn Ala
50 55 60
Val Thr Glu Leu Gln Leu Leu Met Gln Ser Thr Pro Ala Thr Asn Asn
65 70 75 80
Arg Ala Arg Arg Glu Leu Pro Arg Phe Met Asn Tyr Thr Leu Asn Asn
85 90 95
Ala Lys Lys Thr Asn Val Thr Leu Ser Lys Lys Arg Lys Arg Arg Phe
100 105 110
Leu Gly Phe Leu Leu Gly Val Gly Ser Ala Ile Ala Ser Gly Val Ala
115 120 125
Val Cys Lys Val Leu His Leu Glu Gly Glu Val Asn Lys Ile Lys Ser
130 135 140
Ala Leu Leu Ser Thr Asn Lys Ala Val Val Ser Leu Ser Asn Gly Val
145 150 155 160
Ser Val Leu Thr Phe Lys Val Leu Asp Leu Lys Asn Tyr Ile Asp Lys
165 170 175
Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser Cys Ser Ile Ser Asn Ile
180 185 190
Glu Thr Val Ile Glu Phe Gln Gln Lys Asn Asn Arg Leu Leu Glu Ile
195 200 205
Thr Arg Glu Phe Ser Val Asn Ala Gly Val Thr Thr Pro Val Ser Thr
210 215 220
Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser Leu Ile Asn Asp Met Pro
225 230 235 240
Ile Thr Asn Asp Gln Lys Lys Leu Met Ser Asn Asn Val Gln Ile Val
245 250 255
Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile Ile Lys Glu Glu Val Leu
260 265 270
Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly Val Ile Asp Thr Pro Cys
275 280 285
Trp Lys Leu His Thr Ser Pro Leu Cys Thr Thr Asn Thr Lys Glu Gly
290 295 300
Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg Gly Trp Tyr Cys Asp Asn
305 310 315 320
Ala Gly Ser Val Ser Phe Phe Pro Gln Ala Glu Thr Cys Lys Val Gln
325 330 335
Ser Asn Arg Val Phe Cys Asp Thr Met Asn Ser Leu Thr Leu Pro Ser
340 345 350
Glu Val Asn Leu Cys Asn Val Asp Ile Phe Asn Pro Lys Tyr Asp Cys
355 360 365
Lys Ile Met Thr Ser Lys Thr Asp Val Ser Ser Ser Val Ile Thr Ser
370 375 380
Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys Thr Lys Cys Thr Ala Ser
385 390 395 400
Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe Ser Asn Gly Cys Asp Tyr
405 410 415
Val Ser Asn Lys Gly Val Asp Thr Val Ser Val Gly Asn Thr Leu Tyr
420 425 430
Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu Tyr Val Lys Gly Glu Pro
435 440 445
Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe Pro Ser Asp Glu Phe Asp
450 455 460
Ala Ser Ile Ser Gln Val Asn Glu Lys Ile Asn Gln Ser Leu Ala Phe
465 470 475 480
Ile Arg Gly Gly Ser Met Glu Glu Val Val Leu Ile Thr Val Pro Ser
485 490 495
Ala Leu Val Ala Val Lys Ile Ala His Ala Leu Val Glu Glu Arg Leu
500 505 510
Ala Ala Cys Val Asn Ile Val Pro Gly Leu Thr Ser Ile Tyr Arg Glu
515 520 525
Glu Gly Ser Val Val Ser Asp His Glu Leu Leu Leu Leu Val Lys Thr
530 535 540
Thr Thr Asp Ala Phe Pro Lys Leu Lys Glu Arg Val Lys Glu Leu His
545 550 555 560
Pro Tyr Glu Val Pro Glu Ile Val Ala Leu Pro Ile Ala Glu Gly Asn
565 570 575
Arg Glu Tyr Leu Asp Trp Leu Arg Glu Asn Thr Gly
580 585
<210> 103
<211> 634
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный антиген
реапираторно-сцинциляционного вируса
<400> 103
Gln Asn Ile Thr Glu Glu Phe Tyr Gln Ser Thr Cys Ser Ala Val Ser
1 5 10 15
Lys Gly Tyr Leu Ser Ala Leu Arg Thr Gly Trp Tyr Thr Ser Val Ile
20 25 30
Thr Ile Glu Leu Ser Asn Ile Lys Glu Asn Lys Cys Asn Gly Thr Asp
35 40 45
Ala Lys Val Lys Leu Ile Lys Gln Glu Leu Asp Lys Tyr Lys Asn Ala
50 55 60
Val Thr Glu Leu Gln Leu Leu Met Gln Ser Thr Pro Ala Thr Asn Asn
65 70 75 80
Arg Ala Arg Arg Glu Leu Pro Arg Phe Met Asn Tyr Thr Leu Asn Asn
85 90 95
Ala Lys Lys Thr Asn Val Thr Leu Ser Lys Lys Arg Lys Arg Arg Phe
100 105 110
Leu Gly Phe Leu Leu Gly Val Gly Ser Ala Ile Ala Ser Gly Val Ala
115 120 125
Val Cys Lys Val Leu His Leu Glu Gly Glu Val Asn Lys Ile Lys Ser
130 135 140
Ala Leu Leu Ser Thr Asn Lys Ala Val Val Ser Leu Ser Asn Gly Val
145 150 155 160
Ser Val Leu Thr Phe Lys Val Leu Asp Leu Lys Asn Tyr Ile Asp Lys
165 170 175
Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser Cys Ser Ile Ser Asn Ile
180 185 190
Glu Thr Val Ile Glu Phe Gln Gln Lys Asn Asn Arg Leu Leu Glu Ile
195 200 205
Thr Arg Glu Phe Ser Val Asn Ala Gly Val Thr Thr Pro Val Ser Thr
210 215 220
Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser Leu Ile Asn Asp Met Pro
225 230 235 240
Ile Thr Asn Asp Gln Lys Lys Leu Met Ser Asn Asn Val Gln Ile Val
245 250 255
Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile Ile Lys Glu Glu Val Leu
260 265 270
Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly Val Ile Asp Thr Pro Cys
275 280 285
Trp Lys Leu His Thr Ser Pro Leu Cys Thr Thr Asn Thr Lys Glu Gly
290 295 300
Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg Gly Trp Tyr Cys Asp Asn
305 310 315 320
Ala Gly Ser Val Ser Phe Phe Pro Gln Ala Glu Thr Cys Lys Val Gln
325 330 335
Ser Asn Arg Val Phe Cys Asp Thr Met Asn Ser Leu Thr Leu Pro Ser
340 345 350
Glu Val Asn Leu Cys Asn Val Asp Ile Phe Asn Pro Lys Tyr Asp Cys
355 360 365
Lys Ile Met Thr Ser Lys Thr Asp Val Ser Ser Ser Val Ile Thr Ser
370 375 380
Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys Thr Lys Cys Thr Ala Ser
385 390 395 400
Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe Ser Asn Gly Cys Asp Tyr
405 410 415
Val Ser Asn Lys Gly Val Asp Thr Val Ser Val Gly Asn Thr Leu Tyr
420 425 430
Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu Tyr Val Lys Gly Glu Pro
435 440 445
Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe Pro Ser Asp Glu Phe Asp
450 455 460
Ala Ser Ile Ser Gln Val Asn Glu Lys Ile Asn Gln Ser Leu Ala Phe
465 470 475 480
Ile Arg Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln Ala Tyr Val
485 490 495
Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu Gly Gly Ser
500 505 510
Met Val Arg Gly Ile Arg Gly Ala Ile Thr Val Asn Ser Asp Thr Pro
515 520 525
Thr Ser Ile Ile Ile Ala Thr Ile Leu Leu Leu Glu Lys Met Leu Glu
530 535 540
Ala Asn Gly Ile Gln Ser Tyr Glu Glu Leu Ala Ala Val Ile Phe Thr
545 550 555 560
Val Thr Glu Asp Leu Thr Ser Ala Phe Pro Ala Glu Ala Ala Arg Gln
565 570 575
Ile Gly Met His Arg Val Pro Leu Leu Ser Ala Arg Glu Val Pro Val
580 585 590
Pro Gly Ser Leu Pro Arg Val Ile Arg Val Leu Ala Leu Trp Asn Thr
595 600 605
Asp Thr Pro Gln Asp Arg Val Arg His Val Tyr Leu Ser Glu Ala Val
610 615 620
Arg Leu Arg Pro Asp Leu Glu Ser Ala Gln
625 630
<210> 104
<211> 607
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный антиген
реапираторно-сцинциляционного вируса
<400> 104
Gln Asn Ile Thr Glu Glu Phe Tyr Gln Ser Thr Cys Ser Ala Val Ser
1 5 10 15
Lys Gly Tyr Leu Ser Ala Leu Arg Thr Gly Trp Tyr Thr Ser Val Ile
20 25 30
Thr Ile Glu Leu Ser Asn Ile Lys Glu Asn Lys Cys Asn Gly Thr Asp
35 40 45
Ala Lys Val Lys Leu Ile Lys Gln Glu Leu Asp Lys Tyr Lys Asn Ala
50 55 60
Val Thr Glu Leu Gln Leu Leu Met Gln Ser Thr Pro Ala Thr Asn Asn
65 70 75 80
Arg Ala Arg Arg Glu Leu Pro Arg Phe Met Asn Tyr Thr Leu Asn Asn
85 90 95
Ala Lys Lys Thr Asn Val Thr Leu Ser Lys Lys Arg Lys Arg Arg Phe
100 105 110
Leu Gly Phe Leu Leu Gly Val Gly Ser Ala Ile Ala Ser Gly Val Ala
115 120 125
Val Cys Lys Val Leu His Leu Glu Gly Glu Val Asn Lys Ile Lys Ser
130 135 140
Ala Leu Leu Ser Thr Asn Lys Ala Val Val Ser Leu Ser Asn Gly Val
145 150 155 160
Ser Val Leu Thr Phe Lys Val Leu Asp Leu Lys Asn Tyr Ile Asp Lys
165 170 175
Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser Cys Ser Ile Ser Asn Ile
180 185 190
Glu Thr Val Ile Glu Phe Gln Gln Lys Asn Asn Arg Leu Leu Glu Ile
195 200 205
Thr Arg Glu Phe Ser Val Asn Ala Gly Val Thr Thr Pro Val Ser Thr
210 215 220
Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser Leu Ile Asn Asp Met Pro
225 230 235 240
Ile Thr Asn Asp Gln Lys Lys Leu Met Ser Asn Asn Val Gln Ile Val
245 250 255
Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile Ile Lys Glu Glu Val Leu
260 265 270
Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly Val Ile Asp Thr Pro Cys
275 280 285
Trp Lys Leu His Thr Ser Pro Leu Cys Thr Thr Asn Thr Lys Glu Gly
290 295 300
Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg Gly Trp Tyr Cys Asp Asn
305 310 315 320
Ala Gly Ser Val Ser Phe Phe Pro Gln Ala Glu Thr Cys Lys Val Gln
325 330 335
Ser Asn Arg Val Phe Cys Asp Thr Met Asn Ser Leu Thr Leu Pro Ser
340 345 350
Glu Val Asn Leu Cys Asn Val Asp Ile Phe Asn Pro Lys Tyr Asp Cys
355 360 365
Lys Ile Met Thr Ser Lys Thr Asp Val Ser Ser Ser Val Ile Thr Ser
370 375 380
Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys Thr Lys Cys Thr Ala Ser
385 390 395 400
Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe Ser Asn Gly Cys Asp Tyr
405 410 415
Val Ser Asn Lys Gly Val Asp Thr Val Ser Val Gly Asn Thr Leu Tyr
420 425 430
Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu Tyr Val Lys Gly Glu Pro
435 440 445
Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe Pro Ser Asp Glu Phe Asp
450 455 460
Ala Ser Ile Ser Gln Val Asn Glu Lys Ile Asn Gln Ser Leu Ala Phe
465 470 475 480
Ile Arg Gly Gly Ser Met Val Arg Gly Ile Arg Gly Ala Ile Thr Val
485 490 495
Asn Ser Asp Thr Pro Thr Ser Ile Ile Ile Ala Thr Ile Leu Leu Leu
500 505 510
Glu Lys Met Leu Glu Ala Asn Gly Ile Gln Ser Tyr Glu Glu Leu Ala
515 520 525
Ala Val Ile Phe Thr Val Thr Glu Asp Leu Thr Ser Ala Phe Pro Ala
530 535 540
Glu Ala Ala Arg Gln Ile Gly Met His Arg Val Pro Leu Leu Ser Ala
545 550 555 560
Arg Glu Val Pro Val Pro Gly Ser Leu Pro Arg Val Ile Arg Val Leu
565 570 575
Ala Leu Trp Asn Thr Asp Thr Pro Gln Asp Arg Val Arg His Val Tyr
580 585 590
Leu Ser Glu Ala Val Arg Leu Arg Pro Asp Leu Glu Ser Ala Gln
595 600 605
<210> 105
<211> 744
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный антиген
реапираторно-сцинциляционного вируса
<400> 105
Gln Asn Ile Thr Glu Glu Phe Tyr Gln Ser Thr Cys Ser Ala Val Ser
1 5 10 15
Lys Gly Tyr Leu Ser Ala Leu Arg Thr Gly Trp Tyr Thr Ser Val Ile
20 25 30
Thr Ile Glu Leu Ser Asn Ile Lys Glu Asn Lys Cys Asn Gly Thr Asp
35 40 45
Ala Lys Val Lys Leu Ile Lys Gln Glu Leu Asp Lys Tyr Lys Asn Ala
50 55 60
Val Thr Glu Leu Gln Leu Leu Met Gln Ser Thr Pro Ala Thr Asn Asn
65 70 75 80
Arg Ala Arg Arg Glu Leu Pro Arg Phe Met Asn Tyr Thr Leu Asn Asn
85 90 95
Ala Lys Lys Thr Asn Val Thr Leu Ser Lys Lys Arg Lys Arg Arg Phe
100 105 110
Leu Gly Phe Leu Leu Gly Val Gly Ser Ala Ile Ala Ser Gly Val Ala
115 120 125
Val Cys Lys Val Leu His Leu Glu Gly Glu Val Asn Lys Ile Lys Ser
130 135 140
Ala Leu Leu Ser Thr Asn Lys Ala Val Val Ser Leu Ser Asn Gly Val
145 150 155 160
Ser Val Leu Thr Phe Lys Val Leu Asp Leu Lys Asn Tyr Ile Asp Lys
165 170 175
Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser Cys Ser Ile Ser Asn Ile
180 185 190
Glu Thr Val Ile Glu Phe Gln Gln Lys Asn Asn Arg Leu Leu Glu Ile
195 200 205
Thr Arg Glu Phe Ser Val Asn Ala Gly Val Thr Thr Pro Val Ser Thr
210 215 220
Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser Leu Ile Asn Asp Met Pro
225 230 235 240
Ile Thr Asn Asp Gln Lys Lys Leu Met Ser Asn Asn Val Gln Ile Val
245 250 255
Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile Ile Lys Glu Glu Val Leu
260 265 270
Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly Val Ile Asp Thr Pro Cys
275 280 285
Trp Lys Leu His Thr Ser Pro Leu Cys Thr Thr Asn Thr Lys Glu Gly
290 295 300
Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg Gly Trp Tyr Cys Asp Asn
305 310 315 320
Ala Gly Ser Val Ser Phe Phe Pro Gln Ala Glu Thr Cys Lys Val Gln
325 330 335
Ser Asn Arg Val Phe Cys Asp Thr Met Asn Ser Leu Thr Leu Pro Ser
340 345 350
Glu Val Asn Leu Cys Asn Val Asp Ile Phe Asn Pro Lys Tyr Asp Cys
355 360 365
Lys Ile Met Thr Ser Lys Thr Asp Val Ser Ser Ser Val Ile Thr Ser
370 375 380
Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys Thr Lys Cys Thr Ala Ser
385 390 395 400
Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe Ser Asn Gly Cys Asp Tyr
405 410 415
Val Ser Asn Lys Gly Val Asp Thr Val Ser Val Gly Asn Thr Leu Tyr
420 425 430
Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu Tyr Val Lys Gly Glu Pro
435 440 445
Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe Pro Ser Asp Glu Phe Asp
450 455 460
Ala Ser Ile Ser Gln Val Asn Glu Lys Ile Asn Gln Ser Leu Ala Phe
465 470 475 480
Ile Arg Gly Tyr Ile Pro Glu Ala Pro Arg Asp Gly Gln Ala Tyr Val
485 490 495
Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr Phe Leu Gly Ser Gly
500 505 510
Ser His His His His His His His His Gly Gly Ser Gly Gly Ser Gly
515 520 525
Ser Glu Lys Ala Ala Lys Ala Glu Glu Ala Ala Arg Lys Met Glu Glu
530 535 540
Leu Phe Lys Lys His Lys Ile Val Ala Val Leu Arg Ala Asn Ser Val
545 550 555 560
Glu Glu Ala Ile Glu Lys Ala Val Ala Val Phe Ala Gly Gly Val His
565 570 575
Leu Ile Glu Ile Thr Phe Thr Val Pro Asp Ala Asp Thr Val Ile Lys
580 585 590
Ala Leu Ser Val Leu Lys Glu Lys Gly Ala Ile Ile Gly Ala Gly Thr
595 600 605
Val Thr Ser Val Glu Gln Cys Arg Lys Ala Val Glu Ser Gly Ala Glu
610 615 620
Phe Ile Val Ser Pro His Leu Asp Glu Glu Ile Ser Gln Phe Cys Lys
625 630 635 640
Glu Lys Gly Val Phe Tyr Met Pro Gly Val Met Thr Pro Thr Glu Leu
645 650 655
Val Lys Ala Met Lys Leu Gly His Thr Ile Leu Lys Leu Phe Pro Gly
660 665 670
Glu Val Val Gly Pro Gln Phe Val Lys Ala Met Lys Gly Pro Phe Pro
675 680 685
Asn Val Lys Phe Val Pro Thr Gly Gly Val Asn Leu Asp Asn Val Cys
690 695 700
Glu Trp Phe Lys Ala Gly Val Leu Ala Val Gly Val Gly Ser Ala Leu
705 710 715 720
Val Lys Gly Thr Pro Asp Glu Val Arg Glu Lys Ala Lys Ala Phe Val
725 730 735
Glu Lys Ile Arg Gly Cys Thr Glu
740
<210> 106
<211> 705
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный антиген
реапираторно-сцинциляционного вируса
<400> 106
Gln Asn Ile Thr Glu Glu Phe Tyr Gln Ser Thr Cys Ser Ala Val Ser
1 5 10 15
Lys Gly Tyr Leu Ser Ala Leu Arg Thr Gly Trp Tyr Thr Ser Val Ile
20 25 30
Thr Ile Glu Leu Ser Asn Ile Lys Glu Asn Lys Cys Asn Gly Thr Asp
35 40 45
Ala Lys Val Lys Leu Ile Lys Gln Glu Leu Asp Lys Tyr Lys Asn Ala
50 55 60
Val Thr Glu Leu Gln Leu Leu Met Gln Ser Thr Pro Ala Thr Asn Asn
65 70 75 80
Arg Ala Arg Arg Glu Leu Pro Arg Phe Met Asn Tyr Thr Leu Asn Asn
85 90 95
Ala Lys Lys Thr Asn Val Thr Leu Ser Lys Lys Arg Lys Arg Arg Phe
100 105 110
Leu Gly Phe Leu Leu Gly Val Gly Ser Ala Ile Ala Ser Gly Val Ala
115 120 125
Val Cys Lys Val Leu His Leu Glu Gly Glu Val Asn Lys Ile Lys Ser
130 135 140
Ala Leu Leu Ser Thr Asn Lys Ala Val Val Ser Leu Ser Asn Gly Val
145 150 155 160
Ser Val Leu Thr Phe Lys Val Leu Asp Leu Lys Asn Tyr Ile Asp Lys
165 170 175
Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser Cys Ser Ile Ser Asn Ile
180 185 190
Glu Thr Val Ile Glu Phe Gln Gln Lys Asn Asn Arg Leu Leu Glu Ile
195 200 205
Thr Arg Glu Phe Ser Val Asn Ala Gly Val Thr Thr Pro Val Ser Thr
210 215 220
Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser Leu Ile Asn Asp Met Pro
225 230 235 240
Ile Thr Asn Asp Gln Lys Lys Leu Met Ser Asn Asn Val Gln Ile Val
245 250 255
Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile Ile Lys Glu Glu Val Leu
260 265 270
Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly Val Ile Asp Thr Pro Cys
275 280 285
Trp Lys Leu His Thr Ser Pro Leu Cys Thr Thr Asn Thr Lys Glu Gly
290 295 300
Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg Gly Trp Tyr Cys Asp Asn
305 310 315 320
Ala Gly Ser Val Ser Phe Phe Pro Gln Ala Glu Thr Cys Lys Val Gln
325 330 335
Ser Asn Arg Val Phe Cys Asp Thr Met Asn Ser Leu Thr Leu Pro Ser
340 345 350
Glu Val Asn Leu Cys Asn Val Asp Ile Phe Asn Pro Lys Tyr Asp Cys
355 360 365
Lys Ile Met Thr Ser Lys Thr Asp Val Ser Ser Ser Val Ile Thr Ser
370 375 380
Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys Thr Lys Cys Thr Ala Ser
385 390 395 400
Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe Ser Asn Gly Cys Asp Tyr
405 410 415
Val Ser Asn Lys Gly Val Asp Thr Val Ser Val Gly Asn Thr Leu Tyr
420 425 430
Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu Tyr Val Lys Gly Glu Pro
435 440 445
Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe Pro Ser Asp Glu Phe Asp
450 455 460
Ala Ser Ile Ser Gln Val Asn Glu Lys Ile Asn Gln Ser Leu Ala Phe
465 470 475 480
Ile Arg Gly Gly Ser Gly Gly Ser Gly Ser Glu Lys Ala Ala Lys Ala
485 490 495
Glu Glu Ala Ala Arg Lys Met Glu Glu Leu Phe Lys Lys His Lys Ile
500 505 510
Val Ala Val Leu Arg Ala Asn Ser Val Glu Glu Ala Ile Glu Lys Ala
515 520 525
Val Ala Val Phe Ala Gly Gly Val His Leu Ile Glu Ile Thr Phe Thr
530 535 540
Val Pro Asp Ala Asp Thr Val Ile Lys Ala Leu Ser Val Leu Lys Glu
545 550 555 560
Lys Gly Ala Ile Ile Gly Ala Gly Thr Val Thr Ser Val Glu Gln Cys
565 570 575
Arg Lys Ala Val Glu Ser Gly Ala Glu Phe Ile Val Ser Pro His Leu
580 585 590
Asp Glu Glu Ile Ser Gln Phe Cys Lys Glu Lys Gly Val Phe Tyr Met
595 600 605
Pro Gly Val Met Thr Pro Thr Glu Leu Val Lys Ala Met Lys Leu Gly
610 615 620
His Thr Ile Leu Lys Leu Phe Pro Gly Glu Val Val Gly Pro Gln Phe
625 630 635 640
Val Lys Ala Met Lys Gly Pro Phe Pro Asn Val Lys Phe Val Pro Thr
645 650 655
Gly Gly Val Asn Leu Asp Asn Val Cys Glu Trp Phe Lys Ala Gly Val
660 665 670
Leu Ala Val Gly Val Gly Ser Ala Leu Val Lys Gly Thr Pro Asp Glu
675 680 685
Val Arg Glu Lys Ala Lys Ala Phe Val Glu Lys Ile Arg Gly Cys Thr
690 695 700
Glu
705
<210> 107
<211> 645
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетически сконструированный антиген
реапираторно-сцинциляционного вируса
<400> 107
Gln Asn Ile Thr Glu Glu Phe Tyr Gln Ser Thr Cys Ser Ala Val Ser
1 5 10 15
Lys Gly Tyr Leu Ser Ala Leu Arg Thr Gly Trp Tyr Thr Ser Val Ile
20 25 30
Thr Ile Glu Leu Ser Asn Ile Lys Glu Asn Lys Cys Asn Gly Thr Asp
35 40 45
Ala Lys Val Lys Leu Ile Lys Gln Glu Leu Asp Lys Tyr Lys Asn Ala
50 55 60
Val Thr Glu Leu Gln Leu Leu Met Gln Ser Thr Pro Ala Thr Asn Asn
65 70 75 80
Arg Ala Arg Arg Glu Leu Pro Arg Phe Met Asn Tyr Thr Leu Asn Asn
85 90 95
Ala Lys Lys Thr Asn Val Thr Leu Ser Lys Lys Arg Lys Arg Arg Phe
100 105 110
Leu Gly Phe Leu Leu Gly Val Gly Ser Ala Ile Ala Ser Gly Val Ala
115 120 125
Val Cys Lys Val Leu His Leu Glu Gly Glu Val Asn Lys Ile Lys Ser
130 135 140
Ala Leu Leu Ser Thr Asn Lys Ala Val Val Ser Leu Ser Asn Gly Val
145 150 155 160
Ser Val Leu Thr Phe Lys Val Leu Asp Leu Lys Asn Tyr Ile Asp Lys
165 170 175
Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser Cys Ser Ile Ser Asn Ile
180 185 190
Glu Thr Val Ile Glu Phe Gln Gln Lys Asn Asn Arg Leu Leu Glu Ile
195 200 205
Thr Arg Glu Phe Ser Val Asn Ala Gly Val Thr Thr Pro Val Ser Thr
210 215 220
Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser Leu Ile Asn Asp Met Pro
225 230 235 240
Ile Thr Asn Asp Gln Lys Lys Leu Met Ser Asn Asn Val Gln Ile Val
245 250 255
Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile Ile Lys Glu Glu Val Leu
260 265 270
Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly Val Ile Asp Thr Pro Cys
275 280 285
Trp Lys Leu His Thr Ser Pro Leu Cys Thr Thr Asn Thr Lys Glu Gly
290 295 300
Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg Gly Trp Tyr Cys Asp Asn
305 310 315 320
Ala Gly Ser Val Ser Phe Phe Pro Gln Ala Glu Thr Cys Lys Val Gln
325 330 335
Ser Asn Arg Val Phe Cys Asp Thr Met Asn Ser Leu Thr Leu Pro Ser
340 345 350
Glu Val Asn Leu Cys Asn Val Asp Ile Phe Asn Pro Lys Tyr Asp Cys
355 360 365
Lys Ile Met Thr Ser Lys Thr Asp Val Ser Ser Ser Val Ile Thr Ser
370 375 380
Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys Thr Lys Cys Thr Ala Ser
385 390 395 400
Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe Ser Asn Gly Cys Asp Tyr
405 410 415
Val Ser Asn Lys Gly Val Asp Thr Val Ser Val Gly Asn Thr Leu Tyr
420 425 430
Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu Tyr Val Lys Gly Glu Pro
435 440 445
Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe Pro Ser Asp Glu Phe Asp
450 455 460
Ala Ser Ile Ser Gln Val Asn Glu Lys Ile Asn Gln Ser Leu Ala Phe
465 470 475 480
Ile Arg Gly Gly Ser Gly Gly Ser Gly Ser Asp Asp Ala Arg Ile Ala
485 490 495
Ala Ile Gly Asp Val Asp Glu Leu Asn Ser Gln Ile Gly Val Leu Leu
500 505 510
Ala Glu Pro Leu Pro Asp Asp Val Arg Ala Ala Leu Ser Ala Ile Gln
515 520 525
His Asp Leu Phe Asp Leu Gly Gly Glu Leu Cys Ile Pro Gly His Ala
530 535 540
Ala Ile Thr Glu Asp His Leu Leu Arg Leu Ala Leu Trp Leu Val His
545 550 555 560
Tyr Asn Gly Gln Leu Pro Pro Leu Glu Glu Phe Ile Leu Pro Gly Gly
565 570 575
Ala Arg Gly Ala Ala Leu Ala His Val Cys Arg Thr Val Cys Arg Arg
580 585 590
Ala Glu Arg Ser Ile Lys Ala Leu Gly Ala Ser Glu Pro Leu Asn Ile
595 600 605
Ala Pro Ala Ala Tyr Val Asn Leu Leu Ser Asp Leu Leu Phe Val Leu
610 615 620
Ala Arg Val Leu Asn Arg Ala Ala Gly Gly Ala Asp Val Leu Trp Asp
625 630 635 640
Arg Thr Arg Ala His
645
<210> 108
<211> 678
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> RSV F-10 DS-Cav1-8GS-HelExt-50A
<400> 108
Gln Asn Ile Thr Glu Glu Phe Tyr Gln Ser Thr Cys Ser Ala Val Ser
1 5 10 15
Lys Gly Tyr Leu Ser Ala Leu Arg Thr Gly Trp Tyr Thr Ser Val Ile
20 25 30
Thr Ile Glu Leu Ser Asn Ile Lys Glu Asn Lys Cys Asn Gly Thr Asp
35 40 45
Ala Lys Val Lys Leu Ile Lys Gln Glu Leu Asp Lys Tyr Lys Asn Ala
50 55 60
Val Thr Glu Leu Gln Leu Leu Met Gln Ser Thr Pro Ala Thr Asn Asn
65 70 75 80
Arg Ala Arg Arg Phe Leu Gly Phe Leu Leu Gly Val Gly Ser Ala Ile
85 90 95
Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu Glu Gly Glu Val
100 105 110
Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys Ala Val Val Ser
115 120 125
Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val Leu Asp Leu Lys
130 135 140
Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser Cys
145 150 155 160
Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln Gln Lys Asn Asn
165 170 175
Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn Ala Gly Val Thr
180 185 190
Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser Leu
195 200 205
Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys Leu Met Ser Asn
210 215 220
Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile Ile
225 230 235 240
Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly Val
245 250 255
Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro Leu Cys Thr Thr
260 265 270
Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg Gly
275 280 285
Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe Pro Gln Ala Glu
290 295 300
Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp Thr Met Asn Ser
305 310 315 320
Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val Asp Ile Phe Asn
325 330 335
Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr Asp Val Ser Ser
340 345 350
Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys Thr
355 360 365
Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe Ser
370 375 380
Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp Thr Val Ser Val
385 390 395 400
Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu Tyr
405 410 415
Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe Pro
420 425 430
Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn Glu Lys Ile Asn
435 440 445
Gln Ser Leu Ala Phe Ile Arg Gly Ser Gly Gly Ser Gly Ser Gly Glu
450 455 460
Lys Ala Ala Lys Ala Glu Glu Ala Ala Arg Lys Met Glu Glu Leu Phe
465 470 475 480
Lys Lys His Lys Ile Val Ala Val Leu Arg Ala Asn Ser Val Glu Glu
485 490 495
Ala Ile Glu Lys Ala Val Ala Val Phe Ala Gly Gly Val His Leu Ile
500 505 510
Glu Ile Thr Phe Thr Val Pro Asp Ala Asp Thr Val Ile Lys Ala Leu
515 520 525
Ser Val Leu Lys Glu Lys Gly Ala Ile Ile Gly Ala Gly Thr Val Thr
530 535 540
Ser Val Glu Gln Cys Arg Lys Ala Val Glu Ser Gly Ala Glu Phe Ile
545 550 555 560
Val Ser Pro His Leu Asp Glu Glu Ile Ser Gln Phe Cys Lys Glu Lys
565 570 575
Gly Val Phe Tyr Met Pro Gly Val Met Thr Pro Thr Glu Leu Val Lys
580 585 590
Ala Met Lys Leu Gly His Thr Ile Leu Lys Leu Phe Pro Gly Glu Val
595 600 605
Val Gly Pro Gln Phe Val Lys Ala Met Lys Gly Pro Phe Pro Asn Val
610 615 620
Lys Phe Val Pro Thr Gly Gly Val Asn Leu Asp Asn Val Cys Glu Trp
625 630 635 640
Phe Lys Ala Gly Val Leu Ala Val Gly Val Gly Ser Ala Leu Val Lys
645 650 655
Gly Thr Pro Asp Glu Val Arg Glu Lys Ala Lys Ala Phe Val Glu Lys
660 665 670
Ile Arg Gly Cys Thr Glu
675
<210> 109
<211> 682
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> RSV F-11 DS-Cav1-12GS-HelExt-50A
<400> 109
Gln Asn Ile Thr Glu Glu Phe Tyr Gln Ser Thr Cys Ser Ala Val Ser
1 5 10 15
Lys Gly Tyr Leu Ser Ala Leu Arg Thr Gly Trp Tyr Thr Ser Val Ile
20 25 30
Thr Ile Glu Leu Ser Asn Ile Lys Glu Asn Lys Cys Asn Gly Thr Asp
35 40 45
Ala Lys Val Lys Leu Ile Lys Gln Glu Leu Asp Lys Tyr Lys Asn Ala
50 55 60
Val Thr Glu Leu Gln Leu Leu Met Gln Ser Thr Pro Ala Thr Asn Asn
65 70 75 80
Arg Ala Arg Arg Phe Leu Gly Phe Leu Leu Gly Val Gly Ser Ala Ile
85 90 95
Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu Glu Gly Glu Val
100 105 110
Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys Ala Val Val Ser
115 120 125
Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val Leu Asp Leu Lys
130 135 140
Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser Cys
145 150 155 160
Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln Gln Lys Asn Asn
165 170 175
Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn Ala Gly Val Thr
180 185 190
Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser Leu
195 200 205
Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys Leu Met Ser Asn
210 215 220
Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile Ile
225 230 235 240
Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly Val
245 250 255
Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro Leu Cys Thr Thr
260 265 270
Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg Gly
275 280 285
Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe Pro Gln Ala Glu
290 295 300
Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp Thr Met Asn Ser
305 310 315 320
Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val Asp Ile Phe Asn
325 330 335
Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr Asp Val Ser Ser
340 345 350
Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys Thr
355 360 365
Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe Ser
370 375 380
Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp Thr Val Ser Val
385 390 395 400
Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu Tyr
405 410 415
Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe Pro
420 425 430
Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn Glu Lys Ile Asn
435 440 445
Gln Ser Leu Ala Phe Ile Arg Gly Ser Gly Gly Ser Gly Ser Gly Ser
450 455 460
Gly Gly Ser Glu Lys Ala Ala Lys Ala Glu Glu Ala Ala Arg Lys Met
465 470 475 480
Glu Glu Leu Phe Lys Lys His Lys Ile Val Ala Val Leu Arg Ala Asn
485 490 495
Ser Val Glu Glu Ala Ile Glu Lys Ala Val Ala Val Phe Ala Gly Gly
500 505 510
Val His Leu Ile Glu Ile Thr Phe Thr Val Pro Asp Ala Asp Thr Val
515 520 525
Ile Lys Ala Leu Ser Val Leu Lys Glu Lys Gly Ala Ile Ile Gly Ala
530 535 540
Gly Thr Val Thr Ser Val Glu Gln Cys Arg Lys Ala Val Glu Ser Gly
545 550 555 560
Ala Glu Phe Ile Val Ser Pro His Leu Asp Glu Glu Ile Ser Gln Phe
565 570 575
Cys Lys Glu Lys Gly Val Phe Tyr Met Pro Gly Val Met Thr Pro Thr
580 585 590
Glu Leu Val Lys Ala Met Lys Leu Gly His Thr Ile Leu Lys Leu Phe
595 600 605
Pro Gly Glu Val Val Gly Pro Gln Phe Val Lys Ala Met Lys Gly Pro
610 615 620
Phe Pro Asn Val Lys Phe Val Pro Thr Gly Gly Val Asn Leu Asp Asn
625 630 635 640
Val Cys Glu Trp Phe Lys Ala Gly Val Leu Ala Val Gly Val Gly Ser
645 650 655
Ala Leu Val Lys Gly Thr Pro Asp Glu Val Arg Glu Lys Ala Lys Ala
660 665 670
Phe Val Glu Lys Ile Arg Gly Cys Thr Glu
675 680
<210> 110
<211> 686
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> RSV F-12 DS-Cav1-16GS-HelExt-50A
<400> 110
Gln Asn Ile Thr Glu Glu Phe Tyr Gln Ser Thr Cys Ser Ala Val Ser
1 5 10 15
Lys Gly Tyr Leu Ser Ala Leu Arg Thr Gly Trp Tyr Thr Ser Val Ile
20 25 30
Thr Ile Glu Leu Ser Asn Ile Lys Glu Asn Lys Cys Asn Gly Thr Asp
35 40 45
Ala Lys Val Lys Leu Ile Lys Gln Glu Leu Asp Lys Tyr Lys Asn Ala
50 55 60
Val Thr Glu Leu Gln Leu Leu Met Gln Ser Thr Pro Ala Thr Asn Asn
65 70 75 80
Arg Ala Arg Arg Phe Leu Gly Phe Leu Leu Gly Val Gly Ser Ala Ile
85 90 95
Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu Glu Gly Glu Val
100 105 110
Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys Ala Val Val Ser
115 120 125
Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val Leu Asp Leu Lys
130 135 140
Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser Cys
145 150 155 160
Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln Gln Lys Asn Asn
165 170 175
Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn Ala Gly Val Thr
180 185 190
Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser Leu
195 200 205
Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys Leu Met Ser Asn
210 215 220
Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile Ile
225 230 235 240
Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly Val
245 250 255
Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro Leu Cys Thr Thr
260 265 270
Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg Gly
275 280 285
Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe Pro Gln Ala Glu
290 295 300
Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp Thr Met Asn Ser
305 310 315 320
Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val Asp Ile Phe Asn
325 330 335
Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr Asp Val Ser Ser
340 345 350
Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys Thr
355 360 365
Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe Ser
370 375 380
Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp Thr Val Ser Val
385 390 395 400
Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu Tyr
405 410 415
Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe Pro
420 425 430
Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn Glu Lys Ile Asn
435 440 445
Gln Ser Leu Ala Phe Ile Arg Gly Ser Gly Gly Ser Gly Ser Gly Ser
450 455 460
Gly Gly Ser Gly Ser Gly Gly Glu Lys Ala Ala Lys Ala Glu Glu Ala
465 470 475 480
Ala Arg Lys Met Glu Glu Leu Phe Lys Lys His Lys Ile Val Ala Val
485 490 495
Leu Arg Ala Asn Ser Val Glu Glu Ala Ile Glu Lys Ala Val Ala Val
500 505 510
Phe Ala Gly Gly Val His Leu Ile Glu Ile Thr Phe Thr Val Pro Asp
515 520 525
Ala Asp Thr Val Ile Lys Ala Leu Ser Val Leu Lys Glu Lys Gly Ala
530 535 540
Ile Ile Gly Ala Gly Thr Val Thr Ser Val Glu Gln Cys Arg Lys Ala
545 550 555 560
Val Glu Ser Gly Ala Glu Phe Ile Val Ser Pro His Leu Asp Glu Glu
565 570 575
Ile Ser Gln Phe Cys Lys Glu Lys Gly Val Phe Tyr Met Pro Gly Val
580 585 590
Met Thr Pro Thr Glu Leu Val Lys Ala Met Lys Leu Gly His Thr Ile
595 600 605
Leu Lys Leu Phe Pro Gly Glu Val Val Gly Pro Gln Phe Val Lys Ala
610 615 620
Met Lys Gly Pro Phe Pro Asn Val Lys Phe Val Pro Thr Gly Gly Val
625 630 635 640
Asn Leu Asp Asn Val Cys Glu Trp Phe Lys Ala Gly Val Leu Ala Val
645 650 655
Gly Val Gly Ser Ala Leu Val Lys Gly Thr Pro Asp Glu Val Arg Glu
660 665 670
Lys Ala Lys Ala Phe Val Glu Lys Ile Arg Gly Cys Thr Glu
675 680 685
<210> 111
<211> 680
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> RSV F-13 DS-Cav1-foldon-10GS-HelExt-50A
<400> 111
Gln Asn Ile Thr Glu Glu Phe Tyr Gln Ser Thr Cys Ser Ala Val Ser
1 5 10 15
Lys Gly Tyr Leu Ser Ala Leu Arg Thr Gly Trp Tyr Thr Ser Val Ile
20 25 30
Thr Ile Glu Leu Ser Asn Ile Lys Glu Asn Lys Cys Asn Gly Thr Asp
35 40 45
Ala Lys Val Lys Leu Ile Lys Gln Glu Leu Asp Lys Tyr Lys Asn Ala
50 55 60
Val Thr Glu Leu Gln Leu Leu Met Gln Ser Thr Pro Ala Thr Asn Asn
65 70 75 80
Arg Ala Arg Arg Phe Leu Gly Phe Leu Leu Gly Val Gly Ser Ala Ile
85 90 95
Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu Glu Gly Glu Val
100 105 110
Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys Ala Val Val Ser
115 120 125
Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val Leu Asp Leu Lys
130 135 140
Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser Cys
145 150 155 160
Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln Gln Lys Asn Asn
165 170 175
Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn Ala Gly Val Thr
180 185 190
Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser Leu
195 200 205
Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys Leu Met Ser Asn
210 215 220
Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile Ile
225 230 235 240
Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly Val
245 250 255
Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro Leu Cys Thr Thr
260 265 270
Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg Gly
275 280 285
Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe Pro Gln Ala Glu
290 295 300
Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp Thr Met Asn Ser
305 310 315 320
Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val Asp Ile Phe Asn
325 330 335
Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr Asp Val Ser Ser
340 345 350
Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys Thr
355 360 365
Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe Ser
370 375 380
Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp Thr Val Ser Val
385 390 395 400
Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu Tyr
405 410 415
Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe Pro
420 425 430
Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn Glu Lys Ile Asn
435 440 445
Gln Ser Leu Ala Phe Ile Arg Gly Ser Gly Gly Ser Gly Ser Gly Ser
450 455 460
Gly Glu Lys Ala Ala Lys Ala Glu Glu Ala Ala Arg Lys Met Glu Glu
465 470 475 480
Leu Phe Lys Lys His Lys Ile Val Ala Val Leu Arg Ala Asn Ser Val
485 490 495
Glu Glu Ala Ile Glu Lys Ala Val Ala Val Phe Ala Gly Gly Val His
500 505 510
Leu Ile Glu Ile Thr Phe Thr Val Pro Asp Ala Asp Thr Val Ile Lys
515 520 525
Ala Leu Ser Val Leu Lys Glu Lys Gly Ala Ile Ile Gly Ala Gly Thr
530 535 540
Val Thr Ser Val Glu Gln Cys Arg Lys Ala Val Glu Ser Gly Ala Glu
545 550 555 560
Phe Ile Val Ser Pro His Leu Asp Glu Glu Ile Ser Gln Phe Cys Lys
565 570 575
Glu Lys Gly Val Phe Tyr Met Pro Gly Val Met Thr Pro Thr Glu Leu
580 585 590
Val Lys Ala Met Lys Leu Gly His Thr Ile Leu Lys Leu Phe Pro Gly
595 600 605
Glu Val Val Gly Pro Gln Phe Val Lys Ala Met Lys Gly Pro Phe Pro
610 615 620
Asn Val Lys Phe Val Pro Thr Gly Gly Val Asn Leu Asp Asn Val Cys
625 630 635 640
Glu Trp Phe Lys Ala Gly Val Leu Ala Val Gly Val Gly Ser Ala Leu
645 650 655
Val Lys Gly Thr Pro Asp Glu Val Arg Glu Lys Ala Lys Ala Phe Val
660 665 670
Glu Lys Ile Arg Gly Cys Thr Glu
675 680
<210> 112
<211> 712
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> RSV_F-14 DS-Cav1-foldon-15GS-HelExt-50A
<400> 112
Gln Asn Ile Thr Glu Glu Phe Tyr Gln Ser Thr Cys Ser Ala Val Ser
1 5 10 15
Lys Gly Tyr Leu Ser Ala Leu Arg Thr Gly Trp Tyr Thr Ser Val Ile
20 25 30
Thr Ile Glu Leu Ser Asn Ile Lys Glu Asn Lys Cys Asn Gly Thr Asp
35 40 45
Ala Lys Val Lys Leu Ile Lys Gln Glu Leu Asp Lys Tyr Lys Asn Ala
50 55 60
Val Thr Glu Leu Gln Leu Leu Met Gln Ser Thr Pro Ala Thr Asn Asn
65 70 75 80
Arg Ala Arg Arg Phe Leu Gly Phe Leu Leu Gly Val Gly Ser Ala Ile
85 90 95
Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu Glu Gly Glu Val
100 105 110
Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys Ala Val Val Ser
115 120 125
Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val Leu Asp Leu Lys
130 135 140
Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser Cys
145 150 155 160
Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln Gln Lys Asn Asn
165 170 175
Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn Ala Gly Val Thr
180 185 190
Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser Leu
195 200 205
Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys Leu Met Ser Asn
210 215 220
Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile Ile
225 230 235 240
Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly Val
245 250 255
Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro Leu Cys Thr Thr
260 265 270
Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg Gly
275 280 285
Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe Pro Gln Ala Glu
290 295 300
Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp Thr Met Asn Ser
305 310 315 320
Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val Asp Ile Phe Asn
325 330 335
Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr Asp Val Ser Ser
340 345 350
Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys Thr
355 360 365
Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe Ser
370 375 380
Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp Thr Val Ser Val
385 390 395 400
Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu Tyr
405 410 415
Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe Pro
420 425 430
Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn Glu Lys Ile Asn
435 440 445
Gln Ser Leu Ala Phe Ile Arg Gly Tyr Ile Pro Glu Ala Pro Arg Asp
450 455 460
Gly Gln Ala Tyr Val Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr
465 470 475 480
Phe Leu Gly Ser Gly Gly Ser Gly Ser Gly Ser Gly Gly Ser Gly Ser
485 490 495
Gly Glu Lys Ala Ala Lys Ala Glu Glu Ala Ala Arg Lys Met Glu Glu
500 505 510
Leu Phe Lys Lys His Lys Ile Val Ala Val Leu Arg Ala Asn Ser Val
515 520 525
Glu Glu Ala Ile Glu Lys Ala Val Ala Val Phe Ala Gly Gly Val His
530 535 540
Leu Ile Glu Ile Thr Phe Thr Val Pro Asp Ala Asp Thr Val Ile Lys
545 550 555 560
Ala Leu Ser Val Leu Lys Glu Lys Gly Ala Ile Ile Gly Ala Gly Thr
565 570 575
Val Thr Ser Val Glu Gln Cys Arg Lys Ala Val Glu Ser Gly Ala Glu
580 585 590
Phe Ile Val Ser Pro His Leu Asp Glu Glu Ile Ser Gln Phe Cys Lys
595 600 605
Glu Lys Gly Val Phe Tyr Met Pro Gly Val Met Thr Pro Thr Glu Leu
610 615 620
Val Lys Ala Met Lys Leu Gly His Thr Ile Leu Lys Leu Phe Pro Gly
625 630 635 640
Glu Val Val Gly Pro Gln Phe Val Lys Ala Met Lys Gly Pro Phe Pro
645 650 655
Asn Val Lys Phe Val Pro Thr Gly Gly Val Asn Leu Asp Asn Val Cys
660 665 670
Glu Trp Phe Lys Ala Gly Val Leu Ala Val Gly Val Gly Ser Ala Leu
675 680 685
Val Lys Gly Thr Pro Asp Glu Val Arg Glu Lys Ala Lys Ala Phe Val
690 695 700
Glu Lys Ile Arg Gly Cys Thr Glu
705 710
<210> 113
<211> 717
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> RSV F-15 DS-Cav1-foldon-20GS-HelExt-50A
<400> 113
Gln Asn Ile Thr Glu Glu Phe Tyr Gln Ser Thr Cys Ser Ala Val Ser
1 5 10 15
Lys Gly Tyr Leu Ser Ala Leu Arg Thr Gly Trp Tyr Thr Ser Val Ile
20 25 30
Thr Ile Glu Leu Ser Asn Ile Lys Glu Asn Lys Cys Asn Gly Thr Asp
35 40 45
Ala Lys Val Lys Leu Ile Lys Gln Glu Leu Asp Lys Tyr Lys Asn Ala
50 55 60
Val Thr Glu Leu Gln Leu Leu Met Gln Ser Thr Pro Ala Thr Asn Asn
65 70 75 80
Arg Ala Arg Arg Phe Leu Gly Phe Leu Leu Gly Val Gly Ser Ala Ile
85 90 95
Ala Ser Gly Val Ala Val Cys Lys Val Leu His Leu Glu Gly Glu Val
100 105 110
Asn Lys Ile Lys Ser Ala Leu Leu Ser Thr Asn Lys Ala Val Val Ser
115 120 125
Leu Ser Asn Gly Val Ser Val Leu Thr Phe Lys Val Leu Asp Leu Lys
130 135 140
Asn Tyr Ile Asp Lys Gln Leu Leu Pro Ile Leu Asn Lys Gln Ser Cys
145 150 155 160
Ser Ile Ser Asn Ile Glu Thr Val Ile Glu Phe Gln Gln Lys Asn Asn
165 170 175
Arg Leu Leu Glu Ile Thr Arg Glu Phe Ser Val Asn Ala Gly Val Thr
180 185 190
Thr Pro Val Ser Thr Tyr Met Leu Thr Asn Ser Glu Leu Leu Ser Leu
195 200 205
Ile Asn Asp Met Pro Ile Thr Asn Asp Gln Lys Lys Leu Met Ser Asn
210 215 220
Asn Val Gln Ile Val Arg Gln Gln Ser Tyr Ser Ile Met Cys Ile Ile
225 230 235 240
Lys Glu Glu Val Leu Ala Tyr Val Val Gln Leu Pro Leu Tyr Gly Val
245 250 255
Ile Asp Thr Pro Cys Trp Lys Leu His Thr Ser Pro Leu Cys Thr Thr
260 265 270
Asn Thr Lys Glu Gly Ser Asn Ile Cys Leu Thr Arg Thr Asp Arg Gly
275 280 285
Trp Tyr Cys Asp Asn Ala Gly Ser Val Ser Phe Phe Pro Gln Ala Glu
290 295 300
Thr Cys Lys Val Gln Ser Asn Arg Val Phe Cys Asp Thr Met Asn Ser
305 310 315 320
Leu Thr Leu Pro Ser Glu Val Asn Leu Cys Asn Val Asp Ile Phe Asn
325 330 335
Pro Lys Tyr Asp Cys Lys Ile Met Thr Ser Lys Thr Asp Val Ser Ser
340 345 350
Ser Val Ile Thr Ser Leu Gly Ala Ile Val Ser Cys Tyr Gly Lys Thr
355 360 365
Lys Cys Thr Ala Ser Asn Lys Asn Arg Gly Ile Ile Lys Thr Phe Ser
370 375 380
Asn Gly Cys Asp Tyr Val Ser Asn Lys Gly Val Asp Thr Val Ser Val
385 390 395 400
Gly Asn Thr Leu Tyr Tyr Val Asn Lys Gln Glu Gly Lys Ser Leu Tyr
405 410 415
Val Lys Gly Glu Pro Ile Ile Asn Phe Tyr Asp Pro Leu Val Phe Pro
420 425 430
Ser Asp Glu Phe Asp Ala Ser Ile Ser Gln Val Asn Glu Lys Ile Asn
435 440 445
Gln Ser Leu Ala Phe Ile Arg Gly Tyr Ile Pro Glu Ala Pro Arg Asp
450 455 460
Gly Gln Ala Tyr Val Arg Lys Asp Gly Glu Trp Val Leu Leu Ser Thr
465 470 475 480
Phe Leu Gly Ser Gly Gly Ser Gly Ser Gly Ser Gly Gly Ser Gly Ser
485 490 495
Gly Gly Ser Ser Gly Ser Glu Lys Ala Ala Lys Ala Glu Glu Ala Ala
500 505 510
Arg Lys Met Glu Glu Leu Phe Lys Lys His Lys Ile Val Ala Val Leu
515 520 525
Arg Ala Asn Ser Val Glu Glu Ala Ile Glu Lys Ala Val Ala Val Phe
530 535 540
Ala Gly Gly Val His Leu Ile Glu Ile Thr Phe Thr Val Pro Asp Ala
545 550 555 560
Asp Thr Val Ile Lys Ala Leu Ser Val Leu Lys Glu Lys Gly Ala Ile
565 570 575
Ile Gly Ala Gly Thr Val Thr Ser Val Glu Gln Cys Arg Lys Ala Val
580 585 590
Glu Ser Gly Ala Glu Phe Ile Val Ser Pro His Leu Asp Glu Glu Ile
595 600 605
Ser Gln Phe Cys Lys Glu Lys Gly Val Phe Tyr Met Pro Gly Val Met
610 615 620
Thr Pro Thr Glu Leu Val Lys Ala Met Lys Leu Gly His Thr Ile Leu
625 630 635 640
Lys Leu Phe Pro Gly Glu Val Val Gly Pro Gln Phe Val Lys Ala Met
645 650 655
Lys Gly Pro Phe Pro Asn Val Lys Phe Val Pro Thr Gly Gly Val Asn
660 665 670
Leu Asp Asn Val Cys Glu Trp Phe Lys Ala Gly Val Leu Ala Val Gly
675 680 685
Val Gly Ser Ala Leu Val Lys Gly Thr Pro Asp Glu Val Arg Glu Lys
690 695 700
Ala Lys Ala Phe Val Glu Lys Ile Arg Gly Cys Thr Glu
705 710 715
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| СТАБИЛИЗИРОВАННЫЕ БЕЛКИ F RSV И ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2795459C2 |
| АНТИГЕННЫЕ ПОЛИПЕПТИДЫ НА ОСНОВЕ ПОСЛЕДОВАТЕЛЬНОСТИ РЕСПИРАТОРНО-СИНЦИТИАЛЬНОГО ВИРУСА | 2019 |
|
RU2807992C2 |
| ИММУНОГЛОБУЛИН С ОДНИМ ВАРИАБЕЛЬНЫМ ДОМЕНОМ ПРОТИВ F-БЕЛКА PCB | 2016 |
|
RU2730671C2 |
| МУТАНТНЫЙ БЕЛОК F RSV И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2807742C1 |
| БЕЛКИ RSV В ПРЕДШЕСТВУЮЩЕЙ СЛИЯНИЮ КОНФОРМАЦИИ И ИХ ПРИМЕНЕНИЕ | 2014 |
|
RU2761631C2 |
| Композиции для получения глюкозных сиропов | 2015 |
|
RU2706297C2 |
| МУТАНТЫ БЕЛКА F RSV | 2016 |
|
RU2788403C2 |
| МУТАНТЫ БЕЛКА F RSV | 2016 |
|
RU2723039C2 |
| ОПТИМИЗИРОВАННЫЙ ПОЛИПЕПТИД ДЛЯ СУБЪЕДИНИЧНОЙ ВАКЦИНЫ ПРОТИВ РЕОВИРУСА ПТИЦ | 2017 |
|
RU2742250C2 |
| МУТАНТЫ FIMH E. COLI И ИХ ПРИМЕНЕНИЕ | 2021 |
|
RU2831010C1 |
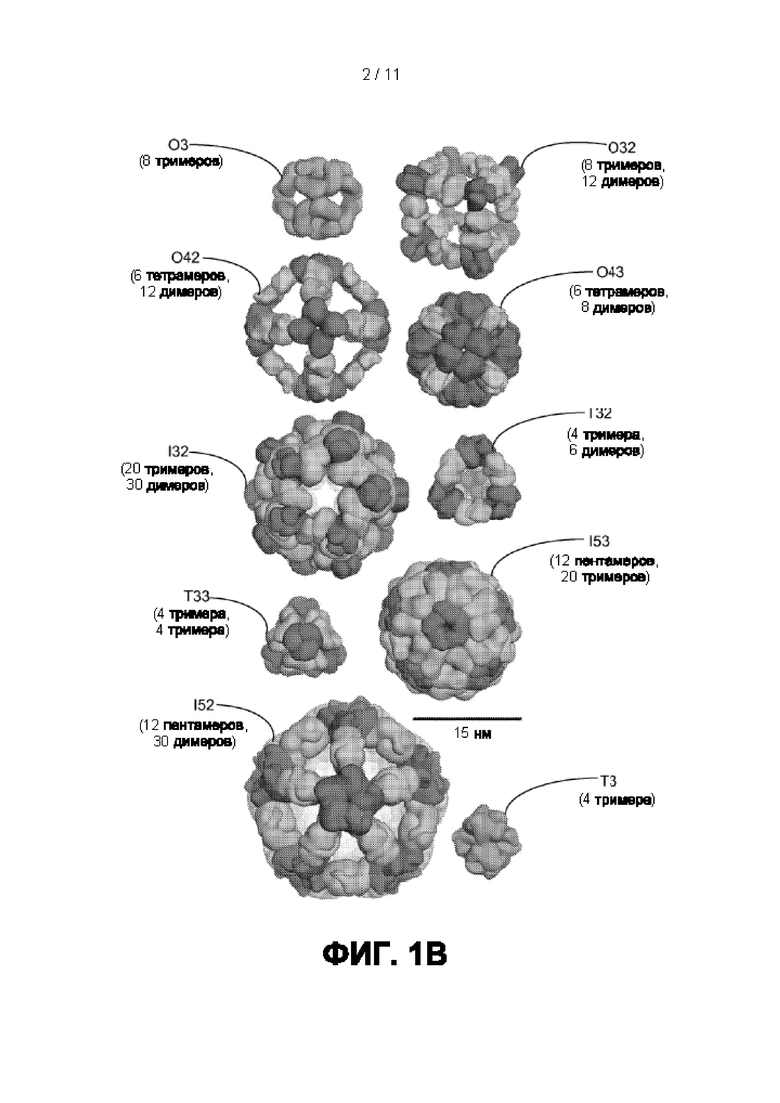
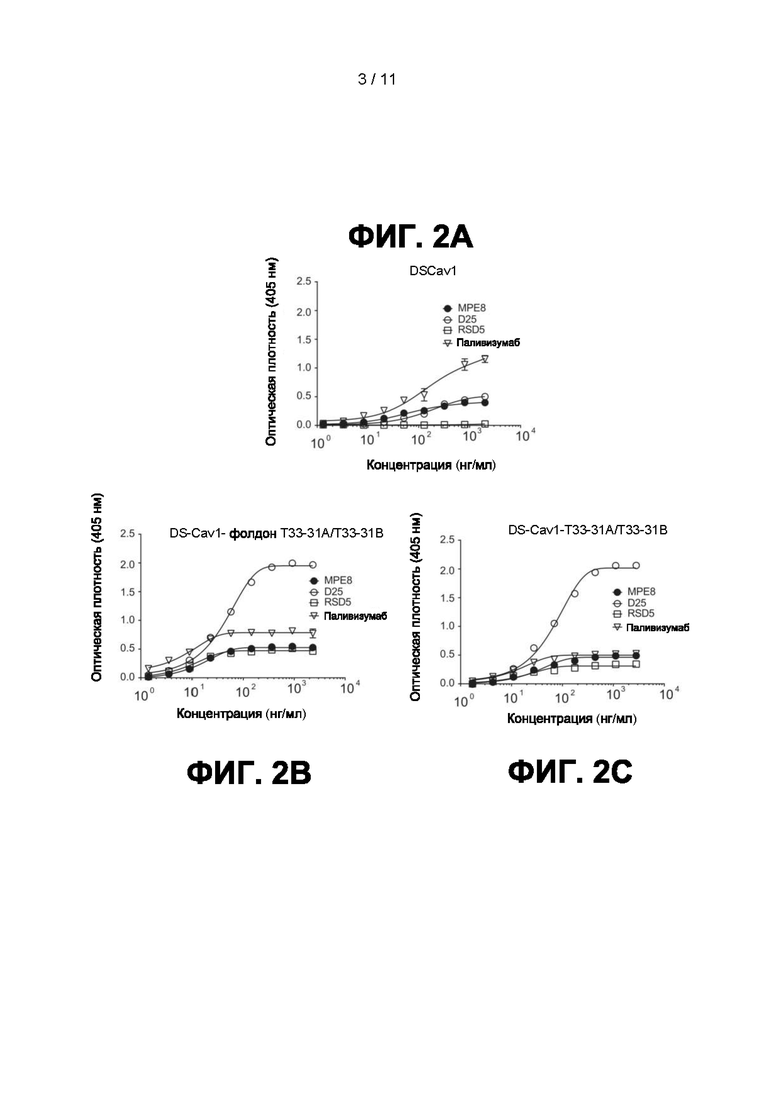
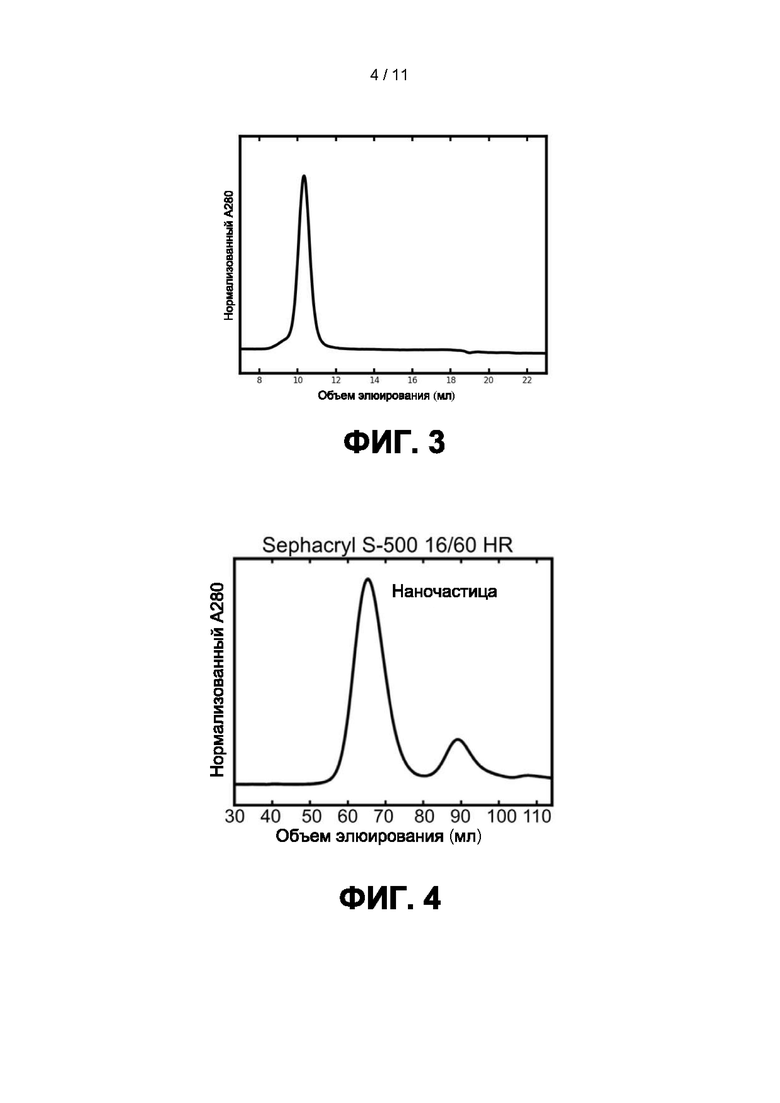

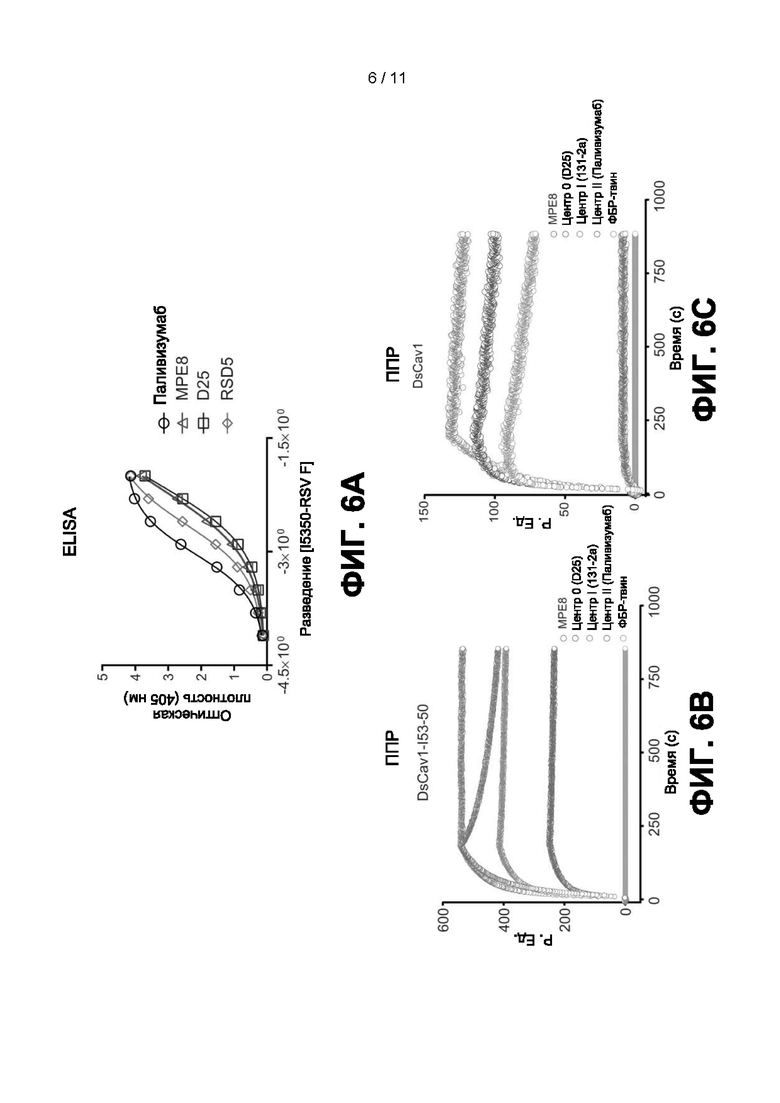
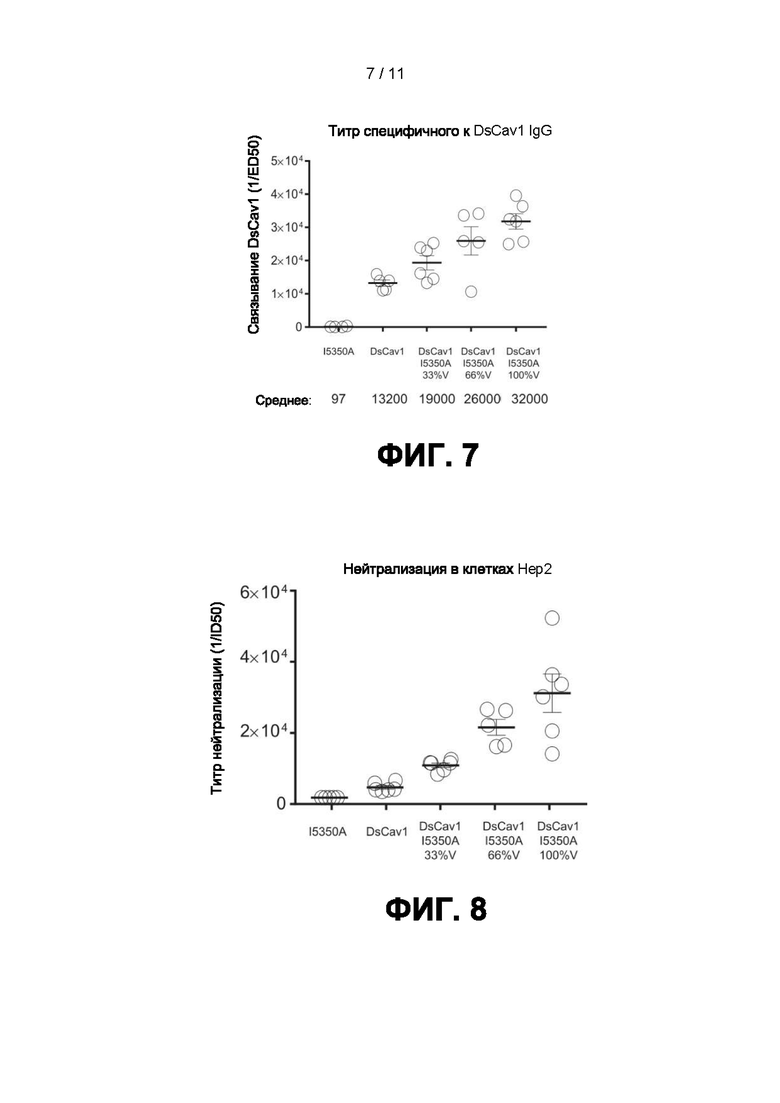
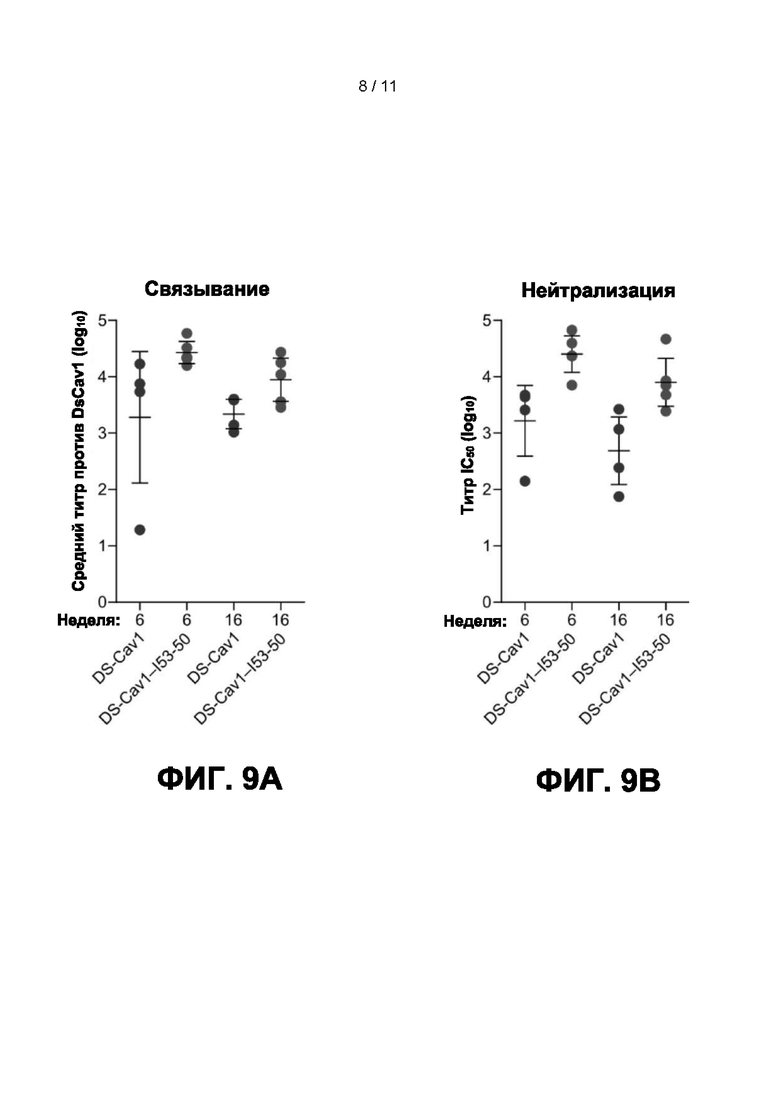
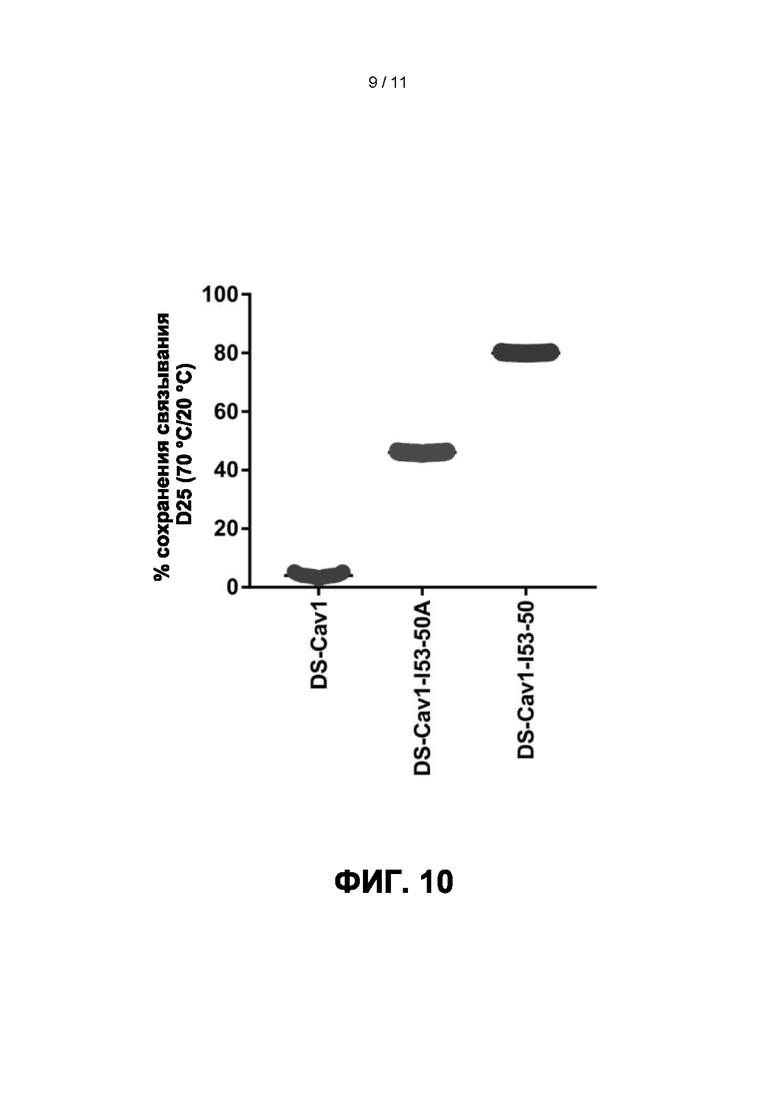
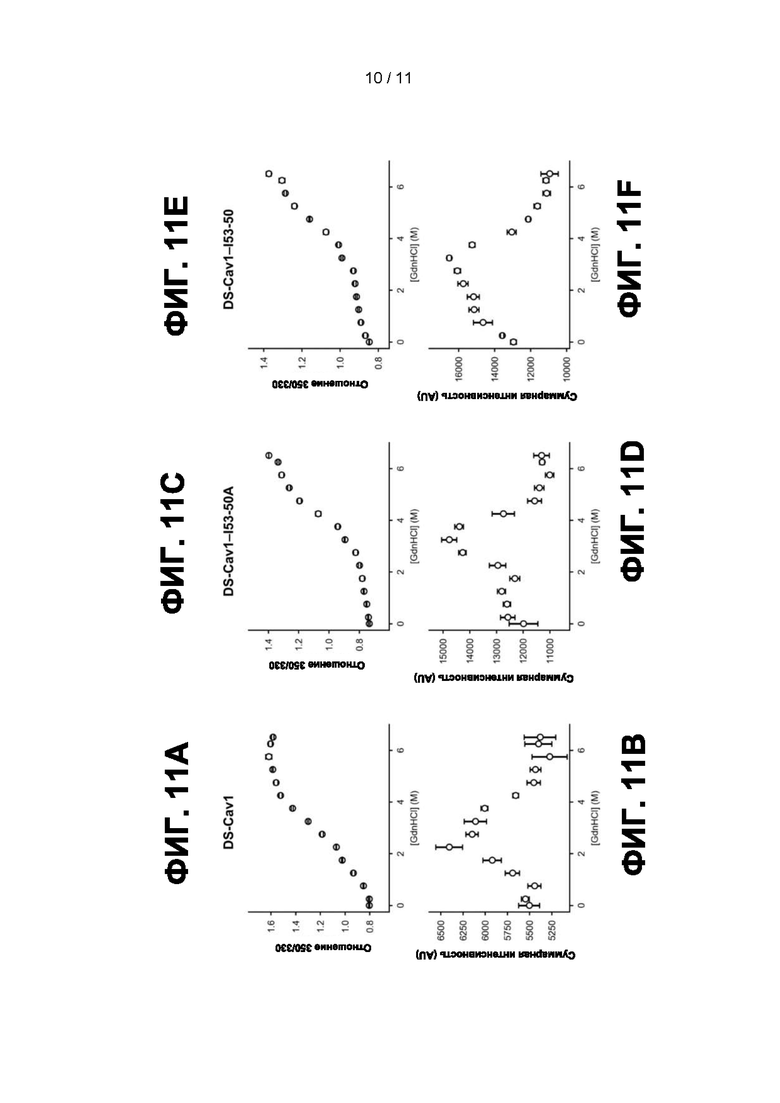
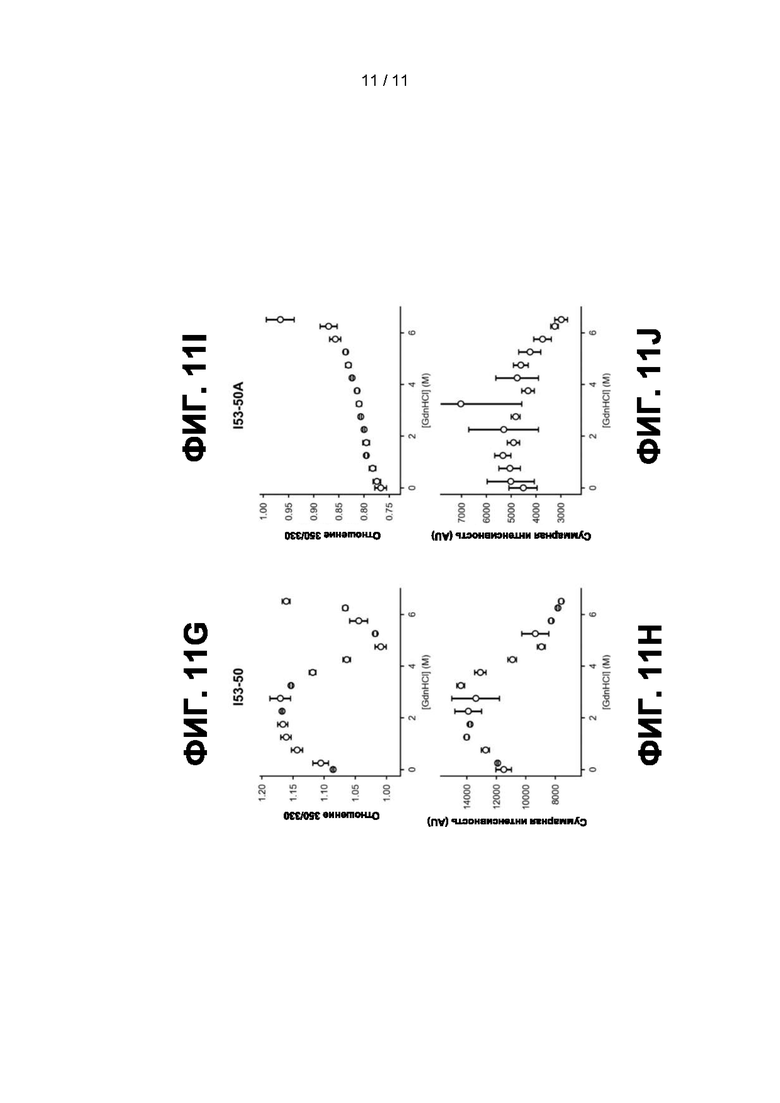
Изобретение относится к биотехнологии. Описана самособирающаяся икосаэдрическая белковая наноструктура для экспонирования антигенов HA вируса гриппа. Наноструктура содержит 20 тримерных сборок. Каждая сборка имеет симметрию 3 порядка, причем каждая тримерная сборка содержит 3 белка триммера. Каждый белок тримера содержит полипептид, состоящий из, в порядке от N- к C- концу, внеклеточного домена HA гриппа, полипептидного линкера и субъединицы тримера, содержащей полипептид, содержащий последовательность, которая по меньшей мере на 95% идентична аминокислотной последовательности, выбранной из SEQ ID NO: 7 или 29-31. Наноструктура также содержит 12 пентамерных сборок, имеющих симметрию 5 порядка. Причем каждая пентамерная сборка содержит 5 субъединиц пентамера, где каждая субъединица пентамера содержит полипептид, содержащий аминокислотную последовательность, которая по меньшей мере на 95% идентична аминокислотной последовательности, выбранной из SEQ ID NO: 8 или 32-34. Тримерные сборки и пентамерные сборки образуют икосаэдр. Внеклеточный домен HA гриппа содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична аминокислотной последовательности SEQ ID NO: 57. Кроме того, описана вакцина для обеспечения ответа нейтрализующих антител на грипп, содержащая указанную наноструктуру. Представлен способ создания иммунитета к гриппу у субъекта, включающий введение эффективного количества наноструктуры или вакцины. А также представлена фармацевтическая композиция, содержащая указанную вакцину и фармацевтически приемлемый адъювант. Изобретение расширяет арсенал средств для лечения гриппа. 4 н. и 15 з.п. ф-лы, 11 ил., 4 табл., 3 пр.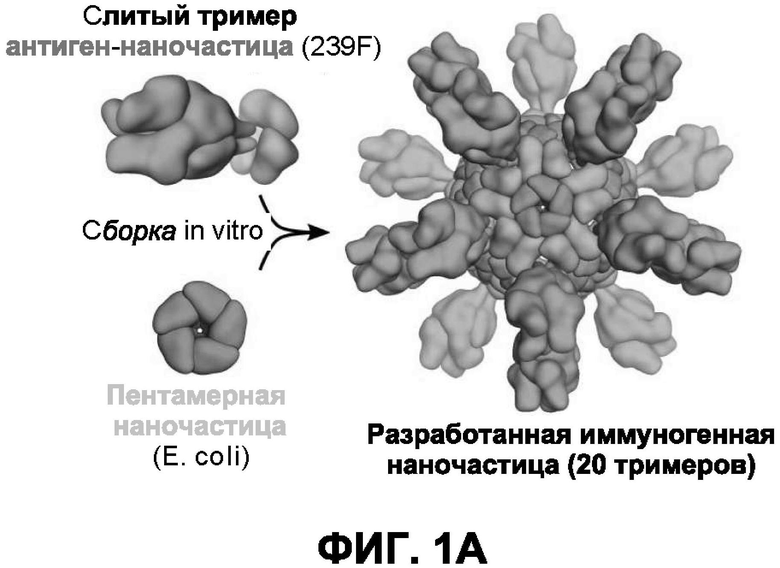
1. Самособирающаяся икосаэдрическая белковая наноструктура для экспонирования антигенов HA вируса гриппа, содержащая:
20 тримерных сборок, имеющих симметрию 3 порядка, причем каждая тримерная сборка содержит 3 белка тримера, где каждый белок тримера содержит полипептид, состоящий из, в порядке от N- к C- концу, внеклеточного домена HA гриппа, полипептидного линкера и субъединицы тримера, содержащей полипептид, содержащий аминокислотную последовательность, которая по меньшей мере на 95% идентична аминокислотной последовательности, выбранной из SEQ ID NO: 7 или 29-31; и
12 пентамерных сборок, имеющих симметрию 5 порядка, причем каждая пентамерная сборка содержит 5 субъединиц пентамера, где каждая субъединица пентамера содержит полипептид, содержащий аминокислотную последовательность, которая по меньшей мере на 95% идентична аминокислотной последовательности, выбранной из SEQ ID NO: 8 или 32-34;
где тримерные сборки и пентамерные сборки образуют икосаэдр; и при этом внеклеточный домен HA гриппа содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична аминокислотной последовательности SEQ ID NO: 57.
2. Наноструктура по п. 1, характеризующаяся тем, что каждый из внеклеточных доменов HA гриппа и субъединиц тримера независимо гомотримеризуются с образованием тримерных сборок.
3. Наноструктура по п. 1 или 2, характеризующаяся тем, что внеклеточные домены HA гриппа экспонированы на поверхности икосаэдра в виде тримеров.
4. Наноструктура по любому из пп. 1-3, характеризующаяся тем, что каждая субъединица тримера содержит интерфейсные остатки в аминокислотных положениях 25, 29, 33, 54 и 57 эталонной последовательности тримера, выбранной из SEQ ID NO: 7 или 29-31, причем каждая субъединица тримера идентична по меньшей мере в 1, 2, 3, 4 или 5 интерфейсных положениях полипептидной последовательности эталонной последовательности тримера,
причем каждая субъединица пентамера содержит интерфейсные остатки в аминокислотных положениях 24, 28, 36, 124, 125, 127, 128, 129, 131, 132, 133, 135 и 139 эталонной последовательности пентамера, выбранной из группы SEQ ID NO: 8 или 32-34, и при этом каждая субъединица пентамера идентична по меньшей мере в 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12 или 13 интерфейсных положениях полипептидной последовательности эталонной последовательности пентамера.
5. Наноструктура по любому из пп. 1-4, характеризующаяся тем, что полипептидный линкер содержит полипептидную последовательность, выбранную из GSGGSGSGSGGSGSG (SEQ ID NO: 114), GGSGGSGS (SEQ ID NO: 115) и GSGGSGSG (SEQ ID NO: 116).
6. Наноструктура по любому из пп. 1-5, характеризующаяся тем, что каждая субъединица тримера содержит аминокислотную последовательность, которая по меньшей мере на 95% идентична аминокислотной последовательности SEQ ID NO: 7.
7. Наноструктура по любому из пп. 1-6, характеризующаяся тем, что каждая субъединица пентамера содержит аминокислотную последовательность, которая по меньшей мере на 95% идентична аминокислотной последовательности SEQ ID NO: 34.
8. Наноструктура по любому из пп. 1-7, характеризующаяся тем, что внеклеточный домен HA гриппа содержит аминокислотную последовательность, которая по меньшей мере на 90% идентична аминокислотной последовательности SEQ ID NO: 57.
9. Наноструктура по любому из пп. 1-7, характеризующаяся тем, что внеклеточный домен HA гриппа содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична аминокислотной последовательности SEQ ID NO: 58.
10. Наноструктура по любому из пп. 1-7, характеризующаяся тем, что внеклеточный домен HA гриппа содержит аминокислотную последовательность, которая на 90% идентична аминокислотной последовательности SEQ ID NO: 58.
11. Наноструктура по любому из пп. 1-10, характеризующаяся тем, что каждая субъединица тримера содержит аминокислотную последовательность, которая по меньшей мере на 95% идентична аминокислотной последовательности SEQ ID NO: 7, и при этом каждая субъединица пентамера содержит аминокислотную последовательность, которая по меньшей мере на 95% идентична аминокислотной последовательности SEQ ID NO: 34.
12. Наноструктура по любому из пп. 1-10, характеризующаяся тем, что каждая субъединица тримера содержит аминокислотную последовательность, которая по меньшей мере на 95% идентична аминокислотной последовательности SEQ ID NO: 7, причем каждая субъединица пентамера содержит аминокислотную последовательность, которая по меньшей мере на 95% идентична аминокислотной последовательности SEQ ID NO: 34, и где внеклеточный домен HA гриппа содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична аминокислотной последовательности SEQ ID NO: 57.
13. Наноструктура по любому из пп. 1-10, характеризующаяся тем, что каждая субъединица тримера содержит аминокислотную последовательность, которая по меньшей мере на 95% идентична аминокислотной последовательности SEQ ID NO: 7, причем каждая субъединица пентамера содержит аминокислотную последовательность, которая по меньшей мере на 95% идентична аминокислотной последовательности SEQ ID NO: 34, и при этом внеклеточный домен HA гриппа содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична аминокислотной последовательности SEQ ID NO: 58.
14. Наноструктура по любому из пп. 1-10, характеризующаяся тем, что каждая субъединица тримера содержит аминокислотную последовательность, которая по меньшей мере на 99% идентична аминокислотной последовательности SEQ ID NO: 7, причем каждая субъединица пентамера содержит аминокислотную последовательность, которая по меньшей мере на 99% идентична аминокислотной последовательности SEQ ID NO: 34, и при этом внеклеточный домен HA гриппа содержит аминокислотную последовательность, которая по меньшей мере на 95% идентична аминокислотной последовательности SEQ ID NO: 57.
15. Наноструктура по любому из пп. 1-10, характеризующаяся тем, что каждая субъединица тримера содержит аминокислотную последовательность, соответствующую SEQ ID NO: 7, причем каждая субъединица пентамера содержит аминокислотную последовательность, соответствующую SEQ ID NO: 34, и при этом внеклеточный домен HA гриппа содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична аминокислотной последовательности SEQ ID NO: 57.
16. Наноструктура по любому из пп. 1-10, характеризующаяся тем, что каждая субъединица тримера содержит аминокислотную последовательность, соответствующую SEQ ID NO: 7, причем каждая субъединица пентамера содержит аминокислотную последовательность, соответствующую SEQ ID NO: 34, и при этом внеклеточный домен HA гриппа содержит аминокислотную последовательность, которая по меньшей мере на 85% идентична аминокислотной последовательности SEQ ID NO: 58.
17. Вакцина для обеспечения ответа нейтрализующих антител на грипп, содержащая наноструктуру по любому из пп. 1-16.
18. Способ создания иммунитета к гриппу у субъекта, включающий введение эффективного количества наноструктуры по любому из пп. 1-16 или вакцины по п. 17.
19. Фармацевтическая композиция, содержащая вакцину по п. 17 и фармацевтически приемлемый адъювант.
| US 9630994 B2, 25.04.2017 | |||
| US 2015356240 A1, 10.12.2015 | |||
| US 8969521 B2, 03.03.2015 | |||
| US 2015110825 A1, 23.04.2015 | |||
| GUO Q | |||
| et al, "Expression, purification and re folding of a self-assembling protein nanoparticle (SAPN) malaria vaccine", Methods, 01.05.2013, V | |||
| Способ получения молочной кислоты | 1922 |
|
SU60A1 |
| САМООРГАНИЗУЮЩИЕСЯ ПЕПТИДНЫЕ НАНОЧАСТИЦЫ, ПОЛЕЗНЫЕ В КАЧЕСТВЕ ВАКЦИН | 2009 |
|
RU2540871C2 |
| VOTTELER J | |||
| Et al, "Designed proteins | |||
Авторы
Даты
2024-01-11—Публикация
2019-02-28—Подача