Изобретение относится к медицине, радиологии, к составам и способам получения радиоактивных препаратов медицинского назначения, которые могут быть использованы для радионуклидной диагностики в онкологии.
В изобретении описан новый препарат и способ его получения для диагностики опухолей, экспрессирующих простатспецифический мембранный антиген (ПСМА), в частности рака предстательной железы (РПЖ). РПЖ занимает второе место в структуре заболеваемости и пятое в структуре смертности от онкологических заболеваний у мужчин [Torre LA, Bray F, Siegel RL et al. Global cancer statistics, 2012. CA: A Cancer J Clin. 2015;65(2):87-108]. Методы ядерной медицины занимают лидирующие позиции в стадировании, рестадировании, а также в выявлении рецидивов заболевания. ПЭТ-КТ с мечеными лигандами к ПСМА в настоящее время широко применяются в клинической практике. Превосходство ПЭТ-КТ с 68Ga-nCMA по диагностической точности над 18Р-холином и 11С-ацетатом отражено в статье [Lutje S, Heskamp S, Cornelissen AS et al. PSMA Ligands for Radionuclide Imaging and Therapy of Prostate Cancer: Clinical Status. Theranostics. 2015;5(12):1388- 401.].
В исследовании [Afshar-Oromieh A, Zechmann CM, Malcher A et al. Comparison of PET imaging with a (68)Ga-labelled PSMA ligand and (18)F-choline-based PET/CT for the diagnosis of recurrent prostate cancer. Eur J Nucl Med Mol Imaging. 2014;41(1):11-20] выполнено сравнение диагностической эффективности ПЭТ-КТ с 68Ga-nCMA и с 18Р-холином в определении локализации патологических очагов у 37 больных с биохимическим рецидивом РПЖ. Было продемонстрировано диагностическое превосходство 68Ga-nCMA над 18Р-холином в обнаружении метастазов РПЖ: 78 очагов у 32 пациентов против 56 очагов у 26 пациентов. Кроме того, оказалось, что различие в чувствительности ПЭТ-КТ с 68Ga-nCMA и с 18Р-холином значительно увеличивается при низких уровнях простатспецифического антигена (ПСА).
В статье [Von Eyben, F.E.; Picchio, М.; von Eyben, R.; Rhee, H.; Bauman, G. 68Ga-Labeled Prostate-specific Membrane Antigen Ligand Positron Emission Tomography/Computed Tomography for Prostate Cancer: A Systematic Review and Meta-analysis. Eur. Urol. Focus 2018, 4, 686-6934] приведен мета-анализ публикаций, посвященных информативности ПЭТ-КТ с 68Ga-nCMA у пациентов с злокачественным новообразованием предстательной железы. Чувствительность метода в выявлении первичного опухолевого очага составляла 70% и чувствительность в идентификации метастазов в лимфатические узлы всего 61%. Основными причинами низкой чувствительности ПЭТ-КТ с 68Ga-nCMA являются не только малые размеры опухолевого очага, но и низкая экспрессия ПСМА на мембранах опухолевых клеток примерно у 10% больных раком предстательной железы, резистентные к антиандрогенной терапии формы рака предстательной железы (например, нейроэндокринный рак) [Schwarzenboeck, S.M.; Rauscher, I.; Bluemel, С; Fendler,W.P.; Rowe, S.P.; Pomper, M.G.; Asfhar-Oromieh, A.; Herrmann, K.; Eiber, M. PSMA Ligands for PET Imaging of Prostate Cancer. J. Nucl. Med. 2017, 58, 1545-1552; Sheikhbahaei, S.; Afshar-Oromieh, A.; Eiber, M.; Solnes, L.B.; Javadi, M.S.; Ross, A.E.; Pienta, K.J.; Allaf, M.E.; Haberkorn, U.; Pomper, M.G.; et al. Pearls and pitfalls in clinical interpretation of prostate-specific membrane antigen (PSMA)-targeted PET imaging. Eur. J. Nucl. Med. Mol. Imaging 2017, 44, 2117-2136].
Новым шагом к повышению эффективности ПЭТ-диагностики рака предстательной железы стала разработка меченых соединений на основе гастрин-рилизинг пептида (ГРП), который также экспрессируется на клетках рака предстательной железы [Beer, М.; Montani, М.; Gerhardt, J.; Wild, P.J.; Hany, T.F.; Hermanns, Т.;  M.; Kristiansen, G. Profiling gastrin-releasing
M.; Kristiansen, G. Profiling gastrin-releasing
peptide receptor in prostate tissues: Clinical implications and molecular correlates. Prostate 2012, 72, 318-325]. В исследовании [Minamimoto, R.; Sonni, I.; Hancock, S.; Vasanawala, S.; Loening, A.; Gambhir, S.S.; Iagaru, A. Prospective Evaluation of 68Ga-RM2 PET/MRI in Patients with Biochemical Recurrence of Prostate Cancer and Negative Findings on Conventional Imaging. J. Nucl. Med. 2018, 59, 803-808] продемонстрирована высокая чувствительность меченого соединения, имеющего тропность к рецепторам ГРП в диагностике рака предстательной железы - 88%. В более раннем исследовании [Minamimoto, 2016], выполненном на малой когорте пациентов (7 пациентов), произведено прямое сопоставление результатов ПЭТ визуализации с мечеными ПСМА и ГРП. При этом не было обнаружено полной сопоставимости полученных результатов, что позволило сделать вывод о необходимости создания химического соединения, которое будет иметь аффинность одновременно к ПСМА и ГРП [Minamimoto, R.; Hancock, S.; Schneider, В.; Chin, F.T.; Jamali, M.; Loening, A.; Vasanawala, S.; Gambhir, S.S.; Iagaru, A. Pilot Comparison of 68Ga-RM2 PET and 68Ga-PSMA-11 PET in Patients with Biochemically Recurrent Prostate Cancer. J. Nucl. Med. 2016, 57, 557-562].
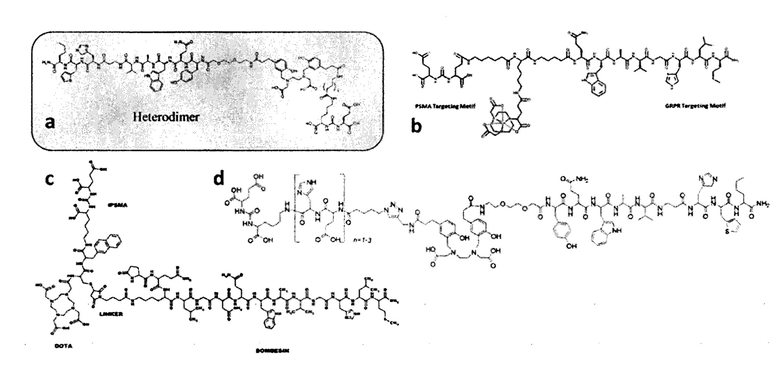
В последние годы появились публикации о разработке меченных изотопами химических соединений на основе лиганда к ПСМА и агониста к ГРП производного от бомбезина [Eder, М.; Schafer, М.; Bauder-Wust, U.; Haberkorn, U.; Eisenhut, М.; Корка, К. Preclinical evaluation of a bispecific low-molecular heterodimer targeting both PSMA and GRPR for improved PET imaging and therapy of prostate cancer. Prostate 2014, 74, 659-668; Bandari, R.P.; Jiang, Z.; Reynolds, T.S.; Bernskoetter, N.E.; Szczodroski, A.F.; Bassuner, K.J.; Kirkpatrick, D.L.; Rold, T.L.; Sieckman, G.L.; Hoffman, T.J.; et al. Synthesis and biological evaluation of copper-64 radiolabeled [DUPA-6-Ahx-(NODAGA)-5-Ava-BBN(7-14)NH2], a novel bivalent targeting vector having affhity for two distinct biomarkers (GRPr/PSMA) of prostate cancer. Nucl. Med. Biol. 2014, 41, 355-363; Mendoza-Figueroa, M.J.; Escudero-Castellanos, A.; Ramirez-Nava, G.J.; Ocampo-Garcia, B.E.; Santos-Cuevas, C.L.; Ferro-Flores, G.; Pedraza-Lopez, M.; Avila-Rodriguez, M.A. Preparation and preclinical evaluation of 68Ga-iPSMA-BN as a potential heterodimeric radiotracer for PET-imaging of prostate cancer. J. Radioanal. Nucl. Chem. 2018, 318, 2097-2105; Escudero-Castellanos, A.; Ocampo-Garcia, В.; Morales-Avila, E.; Luna-Gutierrez, M.; Isaac-Olive, K.; Ferro-Flores, G.; Santos-Cuevas, C. Synthesis and preclinical evaluation of the 177Lu-DOTA-PSMA(inhibitor)-Lys3-bombesin heterodimer designed as a radiotheranostic probe for prostate cancer. Nucl. Med. Commun. 2018, 40, 278-286; Liolios, C; Schafer, M.; Haberkorn, U.; Eder, M.; Корка, К. Novel Bispecific PSMA/GRPr Targeting Radioligands with Optimized Pharmacokinetics for Improved PET Imaging of Prostate Cancer. Bioconjugate Chem. 2016, 27, 737-751]: Химические соединения, нацеленные на ПСМА и ГРП на основе агонистов ГРП: а - Glu-urea-Lys(Ahx)-HBED-CC-BZH3; b - DUPA-6-Ahx-(NODAGA)-5-Ava-BBN(7-14)NH2; с - DOTA-PSMA(inhibitor)-Lys3-bombesin; d - HE0-HE3.
Тем не менее, существенным недостатком агонистов к ГРП является их сильная физиологическая активность и митогенность - индукция клеточного деления [Casanueva, F.F.; Perez, F.R.; Casabiell, X.; Camina, J.P.; Cai, R.Z.; Serially, A.V. Correlation between the effects of bombesin antagonists on cell proliferation and intracellular calcium concentration in Swiss 3T3 and HT-29 cell lines. Proc. Natl. Acad. Sci. USA 1996, 93, 1406-1411]. Кроме того, было продемонстрировано, что антагонисты ГРП имеют больше сайтов связывания с опухолевой клеткой, чем агонисты, что повышает захват радиофармацевтического препарата опухолевым узлом [Mansi, R.; Fleischmann, А.; Маске, H.R.; Reubi, J.C. Targeting GRPR in urological cancers-from basic research to clinical application. Nat. Rev. Urol. 2013, 10, 235-244; Varasteh, Z.; Velikyan, I.; Lindeberg, G.; Sorensen, J.; Larhed, M.; Sandstrom, M.; Selvaraju, R.K.; Malmberg, J.; Tolmachev, V.; Orlova, A. Synthesis and characterization of a high-affhity NOTA-conjugated bombesin antagonist for GRPR-targeted tumor imaging. Bioconjug. Chem. 2013, 24, 1144-1153].
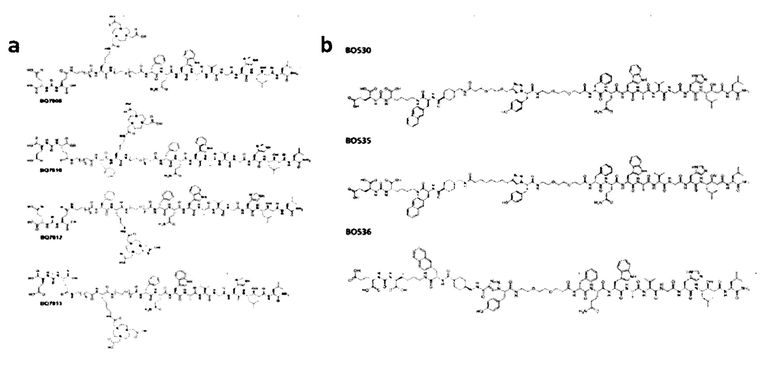
Известны также разработки новых радиофармацевтических препаратов, которые включают ПСМА-связывающий фрагмент [Kularatne, S.A.; Wang, K.; Santhapuram, Н.K.; Low, P.S. Prostate-specific membrane antigen targeted imaging and therapy of prostate cancer using a PSMA inhibitor as a homing ligand. Mol. Pharm. 2009, 6, 780-789] и антагонист ГРП - GRPR RM26 [Varasteh 2014], связанный через глутаминовую кислоту, несущую хелатор NOTA, для мечения радиометаллами или тирозин для радиогалогенирования [Abouzayed, A.; Yim, С.-В.; Mitran, В.; Rinne, S.S.; Tolmachev, V.; Larhed, М.; Rosenstrom, U.; Orlova, A. Synthesis and Preclinical Evaluation of Radio-Iodinated GRPR/PSMA Bispecific Heterodimers for the Theranostics Application in Prostate Cancer. Pharmaceutics 2019, 11, 358; Mitran, В.; Varasteh, Z.; Abouzayed, A.; Rinne, S.S.; Puuvuori, E.; De Rosa, M.; Larhed, M.; Tolmachev, V.; Orlova, A.; Rosenstrom, U. Bispecific GRPR-Antagonistic Anti-PSMA/GRPR Heterodimer for PET and SPECT Diagnostic Imaging of Prostate Cancer. Cancers 2019, 11, 1371; Lundmark F, Abouzayed A, Mitran B, Rinne SS, Varasteh Z, Larhed M, Tolmachev V, Rosenstrom U, Orlova A. Heterodimeric Radiotracer Targeting PSMA and GRPR for Imaging of Prostate Cancer-Optimization of the Affinity towards PSMA by Linker Modification in Murine Model. Pharmaceutics 2020, 12, 614]: химические соединения - лиганды к ПСМА и ГРП на основе агонистов ГРП. а. производные NOTA-DUPA-RM26: BQ7800, BQ7810, BQ7812, BQ7813; Ь. производные DUPA-X-triazolyl-Tyr-PEG2-RM26 (X=PEG2 (ВО530), (СН2) 8 (В0535), none (В0536).
Первое изученное меченое химическое соединение продемонстрировало специфическое связывание с обеими мишенями: ПСМА и ГРП, однако его сродство к ПСМА было в субмикромолярном диапазоне, что привело к низкому накоплению в опухолях, экспрессирующих только ПСМА [Mitran]. Далее, были синтезированы три аналога пептида BQ7800 [Lundmark], используя следующие две стратегии для повышения аффинности ПСМА связывающего домена:
1. Путем включения фенилаланина, предполагая, что его гидрофобная боковая цепь будет взаимодействовать с Phe546, и Тгр541 во входном тоннеле к месту связывания Glu-Ureido PSMA-связывающийего фрагмента [Barve, А.; Jin, W.; Cheng, К. Prostate cancer relevant antigens and enzymes for targeted drug delivery. J. Control. Release 2014, 187, 118-132; Корка, K.; Benesova, M.; Barinka, C; Haberkorn, U.; Babich, J. Glu-ureido-based inhibitors of prostate-specific membrane antigen: Lessons learned during the development of a novel class of low-molecular-weight theranostic radiotracers. J. Nucl. Med. 2017, 58, 17S-26S].
2. Путем увеличения длины ПЭТ-линкера, который не влияет на сродство к ГРП [Varasteh, Z.;  U.; Velikyan, I.; Mitran, В.; Altai, M.; Honarvar, H.; Sorensen, J.; Rosestedt, M.; Lindeberg, G.; Larhed, M.; et al. The effect of mini-PEG-based spacer length on binding and pharmacokinetic properties of a 68Ga-labeled NOTA-conjugated antagonistic analog of bombesin. Molecules 2014, 19, 10455-10472].
U.; Velikyan, I.; Mitran, В.; Altai, M.; Honarvar, H.; Sorensen, J.; Rosestedt, M.; Lindeberg, G.; Larhed, M.; et al. The effect of mini-PEG-based spacer length on binding and pharmacokinetic properties of a 68Ga-labeled NOTA-conjugated antagonistic analog of bombesin. Molecules 2014, 19, 10455-10472].
Известно синтезированное химическое соединение, которое является смесью пептида, и представляет последовательность аминокислот и химических модификаций: (3S,7S,21S,24S,36R,39S,42S,45S,48S,54S,57S,58S,62S)-54-((1H-imidazol-4-y1)methyl)-42-((1H-indol-3-y1)methyl)-39-(3-amino-3-oxopropyl)-21,36-dibenzyl-24-(4-(2-(4,7-bis(carboxymethyl)-1,4,7-triazonan-1-y1)acetamido)butyl)-62-carbamoyl-58-hydroxy-57-isobutyl-48-isopropyl-45,64-dimethyl-5,10,19,22,25,34,37,40,43,46,49,52,55,60-tetradecaoxo-29,32-dioxa-4,6,11,20,23,26,35,38,41,44,47,50,53,56,61-pentadecaazapentahexacontane-1,3,7-tricarboxylic acid. Согласно IUPAC (Медународный союз теоретической и прикладной химии) программа Chemdraw сгенерировала следующую аббревиатуру химического соединения: BQ7812.
Синтезированное химическое соединение BQ7812 с формулой:
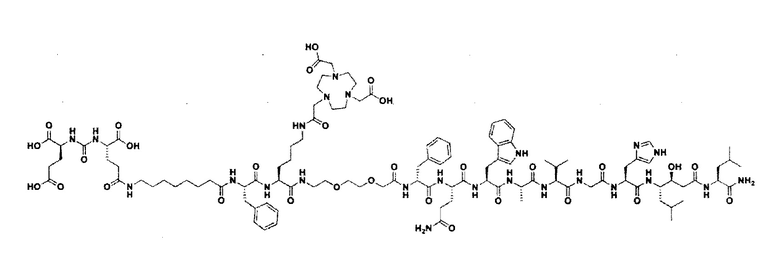
продемонстрировал 10-кратное повышение аффинности к ПСМА, в то время как сродство к ГРП не изменилось и было на низком наномолярном уровне.
Синтез химического соеднинения BQ7812.
Сокращения:
Fmoc - Фторенилметоксикарбонильная защитная группа
Boc - третбутилоксикарбонильная защитная группа
Trt - трифенилметильная защитная группа
Alloc - аллилоксикарбонильная защитная группа
Синтез проводят на твердой фазе смолы Rink Amide 4-метилбензгидриламин (МВНА) присоединением Fmoc-Лей-ОН к исходной смоле, и последующим наращиванием цепи путем последовательного добавления Fmoc-Ста-ОН, Fmoc-rHc(Trt)-OH, Fmoc-Гли-ОН, Fmoc-Вал-ОН, Fmoc-Ала-ОН, Fmoc-Tpn (Boc) -ОН, Fmoc-Глн (Trt) -ОН, Fmoc-D-Фен-ОН, Fmoc-020c-OH, Fmoc-Лиз(Alloc)-ОН, Fmoc-Фен-ОН, 8-(Fmoc-амино)октановой кислоты и (S)-5-(трет-бутокси)-4-(3-((S)-1,5-ди-трет-бутокси-1,5-диоксопентан-2-ил)уреидо)-5-оксопентановой кислоты.
Реакции присоединения проводят в диметилформамиде (ДМФ) с использованием этилциангидроксииминоацетата (Oxyma), N,N'-диизопропилкарбодиимида (DIC) и диизопропилэтиламина (DIPEA). Перед каждой стадией присоединения следующего вещества защитную группу Fmoc удаляют с помощью 20% раствора пиперидина в ДМФ. Защитная группа Alloc боковой цепи лизина удаляется путем добавления PhSiH3 и Pd (PPh3)4 в дихлорметане(ОСМ) с последующим присоединением NOTA-бис-третбутилового эфира. Отщепление от твердого носителя, а также удаление прочих защитных групп выполняют обработкой 5% HrO в трифторуксусной кислоте (TFA) в сочетании с тиоанизолом и триизопропилсиланом в качестве поглотителей. Использование Oxyma в сочетании с DIC более выгодно по сравнению с использованием связывающих реагентов на основе солей фосфония / амина / урония, таких как РуВОР, HBTU и HATU, из-за более низкой рацемизации, более высоких выходов, меньшей взрывоопасности и более низкой стоимости [A1-Warhi, T.I.; А1-Hazimi, Н.М.А.; El-Faham, A. Recent development in peptide coupling reagents. J. Saudi Chem. Soc. 2012, 16, 97-116, doi:10.1016/j.jscs.2010.12.006, Jad, Y.E.; Acosta, G.A.; Khattab, S.N.; De La Torre, B.G.; Govender, Т.; Kruger, H.G.; El-Faham, A.; Albericio, F. Peptide synthesis beyond DMF: THF and ACN as excellent and friendlier alternatives. Org. Biomol. Chem. 2015, 13, 2393-2398, doi:10.1039/c4ob02046d, Wehrstedt, K.D.; Wandrey, P.A.; Heitkamp, D. Explosive properties of 1-hydroxybenzotriazoles. J. Hazard. Mater. 2005, 126, 1-7, doi:10.1016/j.jhazmat.2005.05.044. Subiros-Funosas, R.; Prohens, R.; Barbas, R.; El-Faham, A.; Albericio, F. Oxyma: an efficient additive for peptide synthesis to replace the benzotriazole-based HOBt and HOAt with a lower risk of explosion. Chemistry 2009, 15, 9394-9403, doi:10.1002/CHEM.200900614.]. Это делает комбинацию Oxyma / DIC более рентабельной в использовании по сравнению с другими связующими реагентами на рынке для синтеза химического соединения BQ7812.
Полученное химическое соединение BQ7812, был мечен радиоизотопом 111In-111 для диагностики рака предстательной железы с помощью однофотонной эмиссионной компьютерной томографии [Fanny Lundmark, Ayman Abouzayed, Bogdan Mitran, Sara S. Rinne, Zohreh Varasteh, Mats Larhed, Vladimir Tolmachev, Ulrika Rosenstrom and Anna Orlova Heterodimeric Radiotracer Targeting PSMA and GRPR for Imaging of Prostate Cancer-Optimization of the Affinity towards PSMA by Linker Modification in Murine Model // Pharmaceutics. - 2020, 12, 614; doi:10.3390/pharmaceutics 12070614]. Он продемонстрировал наибольшую аффинность к ПСМА домену. Однако методика однофотонной эмиссионной компьютерной томографии имеет ряд недостатков, а именно относительно низкая разрешающая способность метода по сравнению с позитронной эмиссионной томографией (1 см) и длинный период полураспада изотопа (2,8047 сут).
Задачей заявляемого изобретения является создание нового радиофармацевтического препарата для диагностики рака предстательной железы методом позитронной эмиссионной томографии, позволяющего повысить эффективность диагностики.
Техническим результатом предлагаемого изобретения является повышение выявляемости рака предстательной железы и его метастазов в связи с высокой разрешающей способностью технологии позитронной эмиссионной томографии и снижение лучевой нагрузки на пациентов.
Изобретение поясняется следующими чертежами, где:
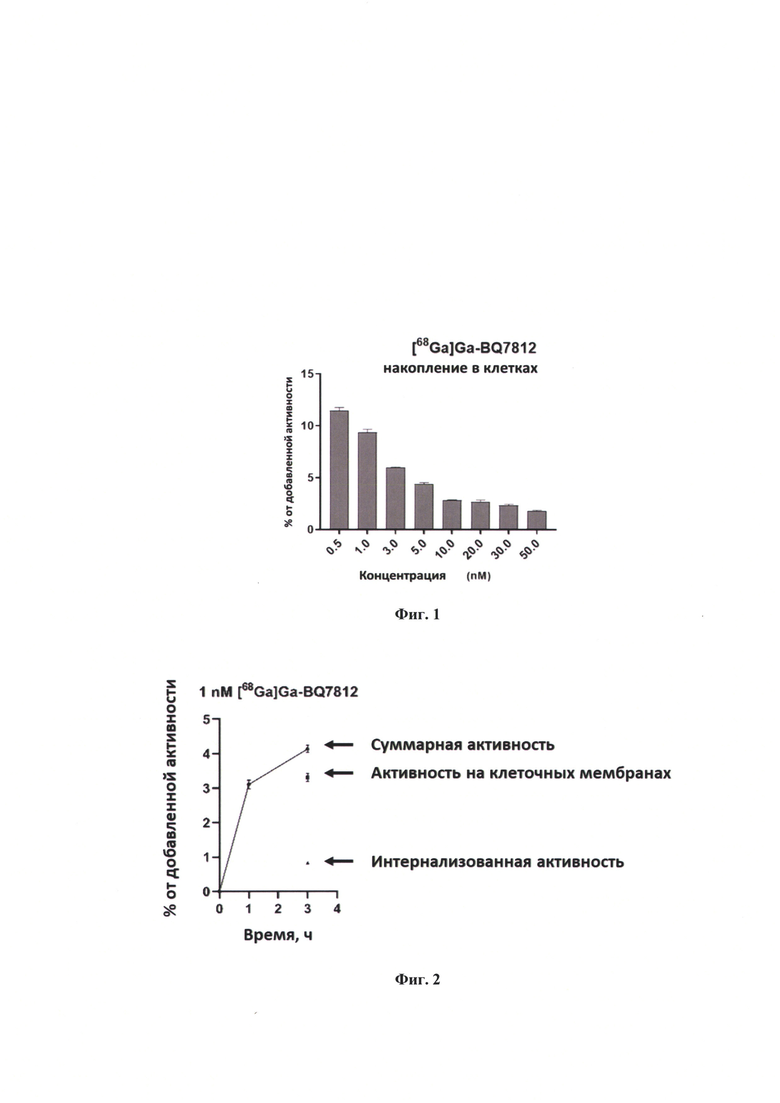
На фиг. 1 представлен график результатов определения специфичности нового химического соединения в эксперименте in vitro.
На фиг. 2 представлен график процесса связывания[68Ga]Ga-BQ7812 с РС-3pip клетками в зависимости от времени инкубации.
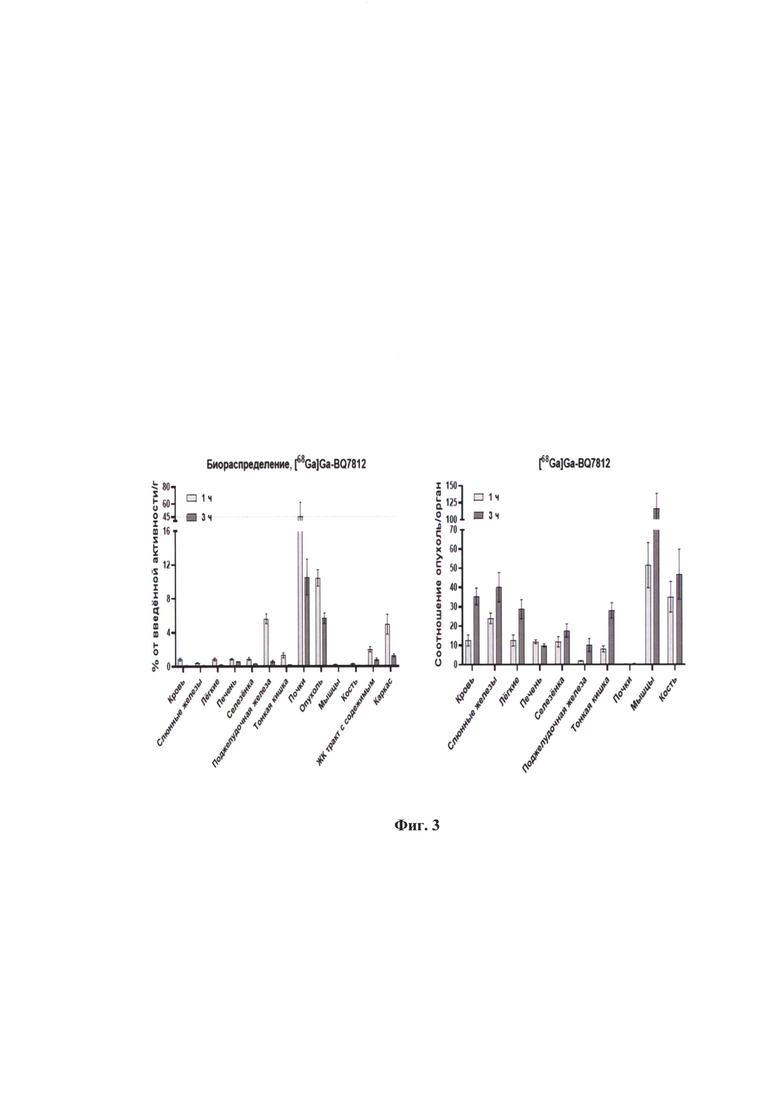
На фиг. 3 представлен график результатов измерений в эксперименте in vivo с мышами линейки Balb/c-nu/nu с PC-3pip опухолями: А - в зависимости от времени после инъекции заявляемого препарата; В - соотношение опухоль-ткань в мышах в зависимости от времени после инъекции заявляемого препарата.
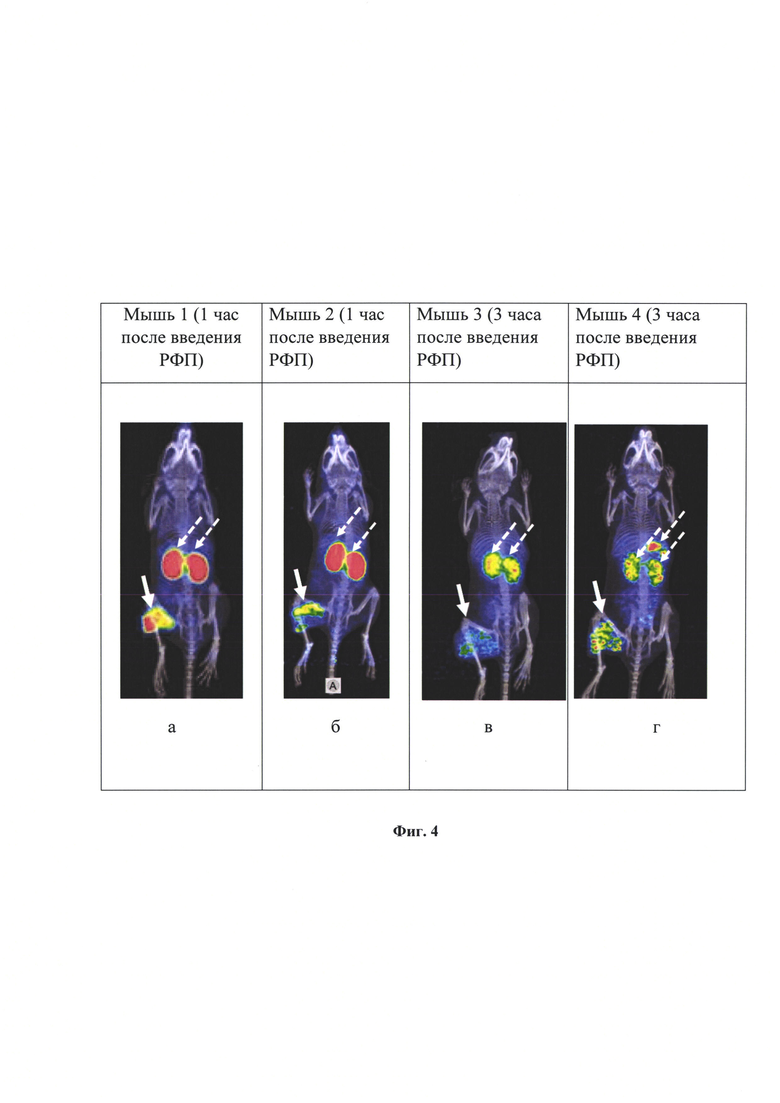
На фиг. 4 представлена РЕТ/СТ визуализация распределения в организме мышей линейки Balb/c-nu/nu с PC-3pip ксенографтами, экспрессирующими на поверхности рецепторы гастрин-рилизинг пептида и ПСМА через 1 и 3 часа после введения радиофармацевтического препарата. Стрелкой указана опухоль, стрелкой-пунктиром указано физиологическое накопление препарата в почках и поджелудочной железе - органах мишенях для лигандов к ПСМА и гастрин-рилизинг пептиду.
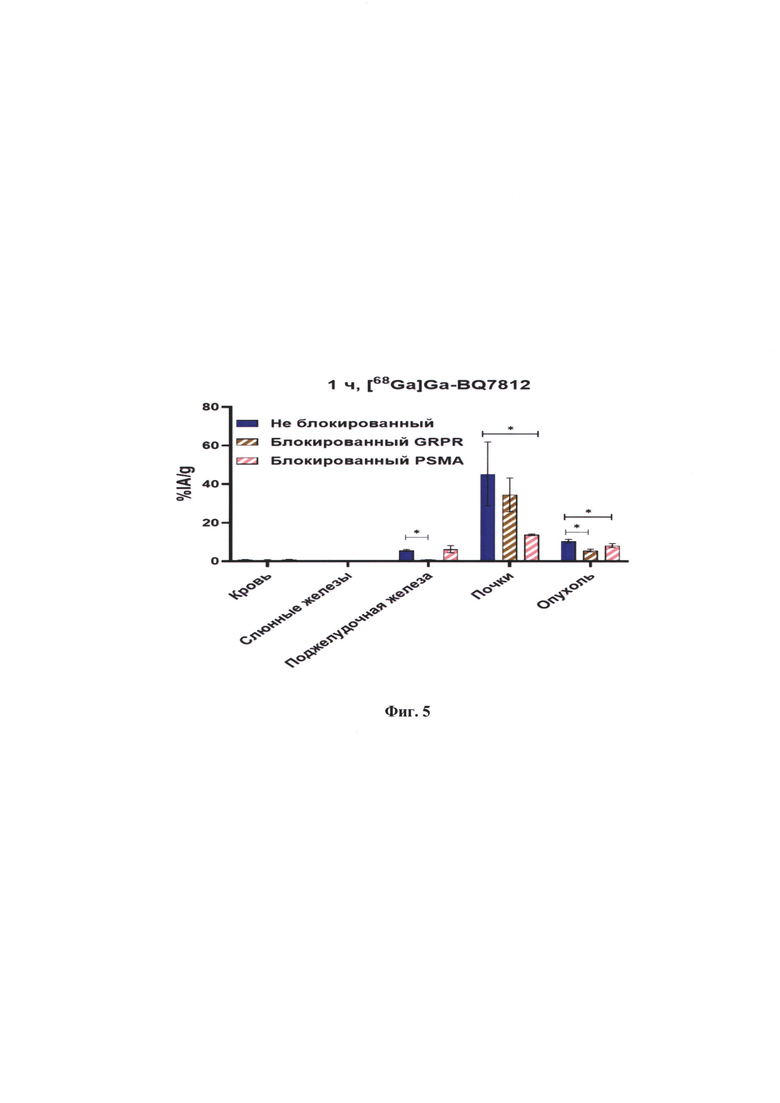
На фиг. 5 - представлен график результатов теста на in vivo специфичность.
Изобретение осуществляется следующим образом.
Включение позитрон-активного радионуклида 68Ga в заявляемое химическое соединение проводится автоматически с помощью устройства для синтеза радиофармпрепаратов на основе изотопа 68Ga (патент на ПМ РФ №199965, опул. 29.09.2020 г), позволяющего производить радиохимическую реакцию ионного обмена с радиоактивными металлами по разработанной программе для ЭВМ (Свидетельство №2020610097, Программа управления устройством для синтеза радиофармпрепаратов на основе изотопа 68Ga, опубл. 10.01.2020). Способ получения радиофармацевтического препарата заключается в мечении химического соединения с аффинностью к рецептору ГРП и ПСМА, нестабильным изотопом 68Ga, путем синтеза осуществляемого в два этапа:
- на первом этапе осуществляют элюирование генератора 68Ge/68Ga путем пропускания через колонку генератора 5 раствора HCl 0,1М, в дозировке 8 мл, последовательным пропусканием элюата, содержащего изотоп 68Ga, через картридж с нанесенными на него 5 г хлорида натрия в твердом агрегатном состоянии и через картридж конечной очистки для твердофазной экстракции по типу слабого анионного обмена с нанесенными на него 40-45 мг сорбента, картридж конечной очистки последовательно промывают 5М раствором NaCl и 1,3 мл дистиллированной воды, на выходе получают катион 3-х валентного 68Ga3+;
- на второй этапе, полученный раствор катиона 3-х валентного 68Ga3+, помещают в реактор 9, загруженный 0,65 мл 2М подкисленного ацетата натрия (рН 4,5) и 2 nMol раствора химического соединения с аффинностью к ПСМА и ГРП, смесь инкубируют в течение 12 минут при температуре 90°С, после чего реакционную смесь разбавляют 5 мл воды для инъекций.
Получен радиофармацевтический препарат для диагностики рака предстательной железы методом позитронной эмиссионной томографии, содержащий химическое соединение с аффинностью к гастрин-рилизинг пептиду (ГРП) и простатспецифическому мембранному антигену (ПСМА), общей формулы (1):
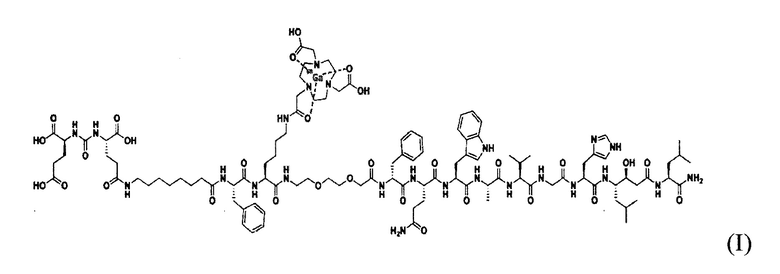
с радионуклидной меткой, в качестве которой используют позитрон-активный радионуклид 68Ga.
Заявляемое изобретение основано на результатах эксперимента, проведенного на лабораторных мышах, линейки Balb/c-nu/nu с опухолями РС-3pip ксенографтами.
Изобретение иллюстрируется примерами.
Пример 1. Характеристика нового соединения [68Ga]Ga-BQ7812 in vitro.
Специфичность заявляемого меченного химического соединения проверяли на клетках опухолях PC-3pip, имеющих экспрессию обоих рецепторов ПСМА и гастрин-рилизинг пептида. Концентрация раствора [68Ga]Ga-BQ7812 составляла - 40 пМ,
концентрация блокирующих растворов NOTA-PEG2-RM26 для блокировки рецепторов к гастрин-рилизинг пептиду ПСМА - 1 цМ. Меченное химическое соединение продемонстрировало специфическое связывание с обеими клеточными мишенями. С увеличение концентрации меченного химического соединения наблюдалось уменьшение относительного связывания его с клетками. Результаты представлены на фиг. 1.
Исследование связи [68Ga]Ga-BQ7812 с клетками PC-3pip опухоли изучалось в течение 3-х часов, характеризовалось быстрой кинетикой. В течение первого часа активность связанная с клетками достигла 75% от максимальной наблюдаемой при инкубации в течение3-х часов. Измерение инторнализованной активности, проведенное через 3 часа после начала инкубации, показало, что 25% активности ассоциированной с клетками было интернализованно. Полученные результаты показывают (фиг. 2), что меченное химическое соединение имеет быструю кинетику связывания необходимую для визуализирующего РФП с быстрым выведением. Относительно высокая степень интернализации препарата для молекулы с аффинностью к ПСМА и ГРП, также должно положительно влиять на удержание препарата в опухоли и повышать контраст.
Пример 2.
Характеристика нового npenapaTa[68Ga]Ga-BQ7812 in vivo:
Высокая диагностическая пригодность нового соединения [68Ga]Ga-BQ7812 была продемонстрирована при изучении его распределения в организме экспериментальных животных лабораторных мышей линейки Balb/c-nu/nu с PC-3pip опухолями ксенографтами. На фиг. 3 (А) представлено накопление радиофармацевтического препарата в опухоли и внутренних органах как % введенной активности на 1 г ткани. Отмечается высокий уровень накопления [68Ga]Ga-BQ7812 по сравнению с фоновой активностью. На фиг. 3 (В) показано высокое соотношение концентраций радиофармацевтического препарата в опухоли и окружающих органах и тканях, что свидетельствует о высоком качестве ПЭТ изображения опухоли.
Пример 3.
Характеристика нового препарата [68Ga]Ga-BQ7812 in vivo:
На фиг. 4 представлена визуализация накопления нового соединения [68Ga]Ga-BQ7812 в опухоли PC-3pip ксенографт, экспрессирующей на поверхности рецепторы гастрин-рилизинг пептида и ПСМА, у мышей линии Balb/c-nu/nu. После внутривенного введения радиофармацевтического препарата уже через 1 час отмечается его включение в опухолевую ткань с получением высококачественного ПЭТ изображения. Физиологическая аккумуляция РФП отмечена в почках и поджелудочной железе - органах, имеющих рецепторы к ПСМА (почки) и гастрин-рилизинг пептиду (поджелудочная железа). Через 3 часа после введения [68Ga]Ga-BQ7812 отмечается умеренное снижение накопления радиофармацевтического препарата в опухоли и почках. Тем не менее, сохраняется высокая контрастность изображения опухоли благодаря интернализации меченного вещества в клетках опухоли.
Характеризация in vivo:
Результаты теста на in vivo специфичность (фиг. 5). Поглощение активности в «неблокированной» группе (инъецированной 40 pmol меченого химического соединения с аффинностью к рецептору ГРП и ПСМА) сравнивали с захватом в группе, инъецированной совместно с 5 nmol связующего ПСМА (PSMA-617), и в группе, совместно инъецированной 5 nmol связующего ГРП (RM26).
Совместная инъекция обоих агентов приводит к значительному снижению поглощения активности в опухолях, совместная инъекция связующего вещества ПСМА значительно снижает поглощение активности в почках, органе с эндогенной экспрессией ПСМА, а совместная инъекция связующего вещества ГРП значительно снижает поглощение активности в поджелудочной железе, орган с эндогенной экспрессией ГРП.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ радионуклидной диагностики рака предстательной железы | 2021 |
|
RU2776234C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПЛЕКСА ПСМА-ТАРГЕТНОГО СОЕДИНЕНИЯ НА ОСНОВЕ МОЧЕВИНЫ Lu-PS-161 И КОМПЛЕКС | 2023 |
|
RU2808636C1 |
| Способ радионуклидной диагностики рака предстательной железы | 2024 |
|
RU2830406C1 |
| ПСМА-ТАРГЕТНОЕ СОЕДИНЕНИЕ И ЕГО КОМПЛЕКС С РАДИОНУКЛИДАМИ ДЛЯ ТЕРАНОСТИКИ ОПУХОЛЕЙ, ЭКСПРЕССИРУЮЩИХ ПСМА | 2022 |
|
RU2803734C1 |
| Способ диагностики злокачественных новообразований органов малого таза | 2024 |
|
RU2828567C1 |
| Лиофилизат на основе лигандов к простат-специфическому мембранному антигену (ПСМА) для приготовления радиофармацевтической композиции в форме раствора для инъекций для лечения рака предстательной железы, радиофармацевтическая композиция на ее основе для лечения рака предстательной железы и способ приготовления радиофармацевтической композиции | 2023 |
|
RU2817970C1 |
| КОМПЛЕКС ПРОИЗВОДНОГО МОЧЕВИНЫ С РАДИОНУКЛИДНОЙ МЕТКОЙ Tс ДЛЯ ДИАГНОСТИКИ ОПУХОЛЕЙ, ЭКСПРЕССИРУЮЩИХ ПРОСТАТСПЕЦИФИЧЕСКИЙ МЕМБРАННЫЙ АНТИГЕН, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2023 |
|
RU2825402C1 |
| Молекула общей структуры Y-Nic-F, способы получения, предшественники для её получения, а также применение в качестве действующего вещества в составе потенциального радиофармацевтического лекарственного препарата | 2021 |
|
RU2811181C2 |
| КОНЪЮГИРОВАННЫЕ БИСФОСФОНАТЫ ДЛЯ ДИАГНОСТИКИ И ТЕРАПИИ ЗАБОЛЕВАНИЙ КОСТЕЙ | 2015 |
|
RU2742660C2 |
| Лиганды PSMA для визуализации и эндорадиотерапии | 2018 |
|
RU2807076C2 |
Заявленная группа изобретений относится к области медицины, а именно к радиологии, и раскрывает радиофармацевтический препарат для диагностики рака предстательной железы методом позитронной эмиссионной томографии, содержащий химическое соединение с аффинностью к рецептору гастрин-рилизинг-пептид (ГРП) и простатспецифическому мембранному антигену (ПСМА), общей формулы (I), с радионуклидной меткой, в качестве которой используют позитрон-активный радионуклид 68Ga. Также раскрыт способ получения радиофармацевтического препарата. Техническим результатом группы изобретений является повышение выявляемости рака предстательной железы и его метастазов в связи с высокой разрешающей способностью технологии позитронной эмиссионной томографии и снижение лучевой нагрузки на пациентов. 2 н.п. ф-лы, 5 ил., 3 пр.
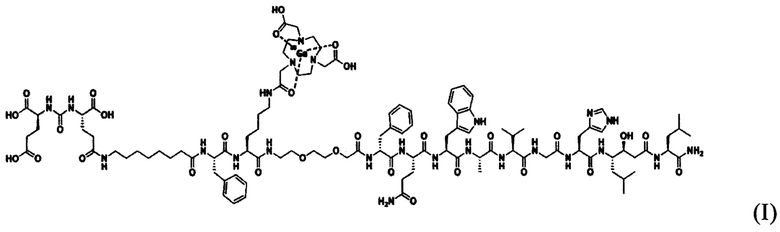
1. Радиофармацевтический препарат для диагностики рака предстательной железы методом позитронной эмиссионной томографии, содержащий химическое соединение с аффинностью к рецептору гастрин-рилизинг-пептид (ГРП) и простатспецифическому мембранному антигену (ПСМА), общей формулы (I)
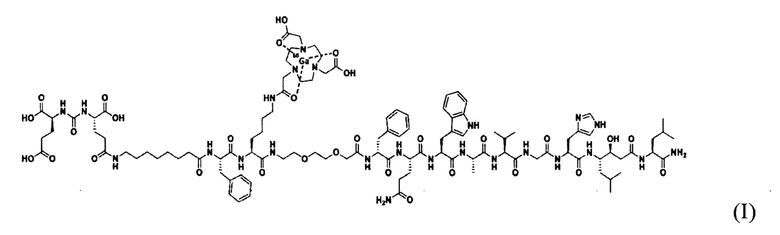
с радионуклидной меткой, в качестве которой используют позитрон-активный радионуклид 68Ga.
2. Способ получения радиофармацевтического препарата по п. 1, заключающийся в мечении химического соединения с аффинностью к рецептору ГРП и простатспецифическому мембранному антигену (ПСМА) позитрон-активным радионуклидом 68Ga путем синтеза, осуществляемого в два этапа:
- на первом этапе осуществляют элюирование генератора 68Ge/68Ga путем пропускания через колонку генератора раствора HCl 0,1М, в дозировке 8 мл, последовательным пропусканием элюата, содержащего изотоп 68Ga, через картридж с нанесенными на него 5 г хлорида натрия в твердом агрегатном состоянии и через картридж конечной очистки для твердофазной экстракции по типу слабого анионного обмена с нанесенными на него 40-45 мг сорбента, картридж конечной очистки последовательно промывают 5М раствором NaCl и 1,3 мл дистиллированной воды, на выходе получают катион 3-валентного 68Ga3+;
- на втором этапе полученный раствор катиона 3-валентного 68Ga3+ помещают в реактор, загруженный 0,65 мл 2М подкисленного ацетата натрия (рН 4,5) и 2nMol раствора химического соединения с аффинностью к рецептору ГРП и простатспецифическому мембранному антигену (ПСМА), смесь инкубируют в течение 12 минут при температуре 90°С, после чего реакционную смесь разбавляют 5 мл воды для инъекций.
| АНТАГОНИСТЫ GRPR ДЛЯ ОБНАРУЖЕНИЯ, ДИАГНОСТИКИ И ЛЕЧЕНИЯ GRPR-ПОЗИТИВНОГО ОНКОЛОГИЧЕСКОГО ЗАБОЛЕВАНИЯ | 2013 |
|
RU2693465C2 |
| FANNY LUNDMARK et al | |||
| Heterodimeric Radiotracer Targeting PSMA and GRPR for Imaging of Prostate Cancer-Optimization of the Affinity towards PSMA by Linker Modification in Murine Model | |||
| Pharmaceutics, 12 (7), 614, 2020, рр.1-15 | |||
| MITRAN, B | |||
| et al | |||
| Bispecific GRPR-Antagonistic Anti-PSMA/GRPR Heterodimer for PET and SPECT | |||
Авторы
Даты
2023-05-17—Публикация
2022-04-19—Подача