Изобретение относится к гидрометаллургии, а именно к переработке минерального и техногенного полиметаллического сульфидного сырья, содержащего цветные и благородные металлы.
По мере истощения типового сырья цветных металлов возникает необходимость вовлечения в переработку более бедных и трудно перерабатываемых руд и отходов производства. Ухудшение качества сырья заключается как в снижении количественного содержания металлов, так и в увеличении доли материалов с тонкой вкрапленностью сульфидов металлов друг в друге и в минералах пустой породы. Последнее определяет невозможность получения качественных монометаллических концентратов (медных, цинковых, свинцовых и т.д.). Получаемые полиметаллические концентраты характеризуются присутствием вредных примесей (мышьяк, сурьма и т.п.), которые усложняют переработку такого сырья традиционными пирометаллургическими процессами.
Известны пирометаллургические способы переработки полиметаллических сульфидных концентратов [SU 996491 A1, RU 2191210 C2], заключающиеся в их вариативной плавке с получением штейна. Главными недостатками данных способов являются высокие энергозатраты, большой объем цинксодержащих пылей и сложности переработки полиметаллического штейна.
Комбинированные методы переработки полиметаллического сульфидного сырья [RU 2607681 C1, WO 2012053614 A1] включают последовательные пиро- и гидрометаллургические процессы, первые из которых направлены на удаление из концентратов вредных летучих элементов (например, мышьяка), перевод ценных компонентов в легкорастворимые в кислотах формы. Однако использование пирометаллургических процессов сопровождается образованием труднорастворимых соединений (ферритов, силикатов цветных металлов), образованием сернистых газов и мышьяк содержащих пылей, что требует применения дорогого и сложного оборудования для их улавливания и переработки.
Гидрометаллургические методы переработки полиметаллического сульфидного сырья достаточно разнообразны. Известен способ выщелачивания тонкоизмельченного сульфидного сырья [RU 2339708] в растворе серной кислоты при 20-95°С. Для интенсификации процесса в пульпу добавляют окислитель - соли трехвалентного железа, перекись водорода и озон, используют ультразвуковое воздействие. Главным недостатком данного способа является большая длительность процесса выщелачивания (не менее 3-8 часов) и неудовлетворительная степень извлечения.
Автоклавные технологии позволяют интенсифицировать процессы выщелачивания, сократить их продолжительность до 1-2 часов. Например, способ [US4084961A] описывает автоклавное сернокислотное выщелачивание сульфидного концентрата в растворах серной кислоты с добавкой азотной кислоты в качестве катализатора процессов разложения сульфидов. В автоклавных условиях возможна регенерация азотной кислоты из образующегося NO. Применение данного способа сопровождается образованием элементной серы, что может приводить к снижению скорости растворения сульфидов из-за блокирования их поверхности пленкой серы. Последующее извлечение благородных металлов цианированием из нерастворенных остатков выщелачивания будет осложняться повышенным расходом реагентов и низким извлечением благородных металлов из-за присутствия на поверхности частиц элементной серы.
Применение азотнокислотных и нитратных растворов при выщелачивании сульфидов цветных металлов характеризуется высокими значениями окислительного потенциала, что выгодно отличает этот вариант от более распространенных серно- и солянокислых реагентов.
Например, ряд способов предлагают прямое растворение сульфидных материалов в растворах азотной кислоты с продувкой пульпы кислородом [CA 1117772 A] или оксидами азота (NO2, N2O4, N2O3) [US 4647307 A], с добавлением нитрата железа [SU 981413 A1], нитрит-ионов [SU1314692A1], а также в условиях избыточного давления [US 3793429 A]. В результате использования данных методов удается с высокой эффективностью перевести цветные металлы в раствор, тем самым обеспечивая вскрытие благородных металлов. Однако данные способы требуют повышенной концентрации азотной кислоты (не менее 100 г/л).
Наиболее близким к заявляемому по технической сути является способ переработки сульфидного материала, содержащего цветные металлы, [CN 110724816 B], включающий следующие стадии:
(1) приготовление пульпы, состоящей из воды и сульфидного материала с соотношением жидкого к твердому (Ж : Т) 10 : (4-6);
(2) добавление азотной кислоты и выщелачивание в герметичном реакторе при температуре 20-80°С и конечном pH раствора 0,5-4,0;
(3) регенерация азотной кислоты из диоксида азота, образующегося при разложении сульфидов, и возврат её на стадию выщелачивания.
Для регенерации азотной кислоты предложено использовать абсорбционную колонну.
Из описания примеров реализации способа-прототипа следует, что лучшие результаты достигаются при Ж : Т = 3 : 2, температуре 80°С, продолжительности 35 мин, конечном pH раствора 1-2, при которых степень разложения сульфидной руды составила 98,2 %. Основным недостатком прототипа является высокий удельный расход азотной кислоты.
В оптимальных условиях выделяющиеся из реактора оксиды азота улавливаются в абсорбционной колонне и регенерируются с получением азотной кислоты на 98,3 %. Вместе с тем, значительная часть азотной кислоты (нитрат-иона), задействуется на сольватацию железа и других металлов, растворяемых из реакционной массы. Эта доля кислоты выводится из оборота, теряется безвозвратно и расценивается как расходная часть. Практика показывает, что, несмотря на установку регенерационной системы, удельный расход азотной кислоты составляет не менее 0,7-1,5 кг (в пересчете на 100 % HNO3) на 1 кг полиметаллического концентрата. Этот негативный показатель увеличивается при стремлении ускорить процесс использованием более высоких начальных концентраций азотной кислоты. Другими словами, при больших скоростях процесса возрастает удельный расход азотной кислоты несмотря на высокую степень регенерации оксидов азота с получением оборотных выщелачивающих растворов.
Технической проблемой, на решение которой направлен предлагаемый способ, является высокий расход азотной кислоты при выщелачивании сульфидных руд и концентратов. Технический результат заключается в изменении реагентного режима.
Технический результат достигается в способе переработки полиметаллического сульфидного сырья, основанного на обработке растворами азотной кислоты и улавливанием нитрозных газов. В отличие от прототипа обработку растворами азотной кислоты ведут в присутствии катализатора, в качестве которого используют пиритный концентрат и оборотный раствор сульфата железа (III), при этом соотношение общей массы пирита и сульфидов цветных металлов в полиметаллическом сульфидном сырье составляет (0,5-1) : 1, а начальная концентрация ионов железа (III) в выщелачивающем растворе составляет 5-30 г/дм3. В качестве водного раствора сульфата железа (III) используют оборотный раствор, полученный при обработке предыдущей партии пиритного концентрата и полиметаллического сульфидного сырья с последующим улавливанием этим раствором нитрозных газов.
Процесс выщелачивания индивидуальных сульфидных минералов в азотнокислых растворах несколько отличается, например, растворение халькопирита (CuFeS2), ковеллина (CuS), халькозина (Cu2S) сопровождается образованием элементной серы, при разложении пирита (FeS2) сера окисляется преимущественно до сульфат-иона. Известно, что реакционная способность (скорость растворения) пирита и халькозина выше, чем у халькопирита и ковеллина, что отражается на значимо большем тепловом эффекте процесса [Prater J.D., Queneau P.B., Hudson T.J. Nitric acid route to processing copper concentrates // Society of Mining Engineers, AIME. 1973. Vol. 254 P. 117-254].
Имеются сведения, что совместное растворение двух сульфидов приводит к заметному ускорению процесса для одного и замедлению для другого минерала, что связано с их электродными потенциалами. Эти гальванические взаимодействия между сульфидами являются одним из важнейших электрохимических факторов, который управляет процессами растворения сульфидов в гидрометаллургических системах [Aziz A., Shafaei S.Z., Noaparast M., Karamoozian M. Galvanic Interaction between Chalcopyrite and Pyrite with Low Alloy and High Carbon Chromium Steel Ball // Journal of Chemistry. 2013. Vol. 2013. ID 817218.].
Установлен следующий ряд сульфидов в порядке возрастания их потенциалов: ZnS < PbS < Cu2S ≈ CuS < CuFeS2 < FeS2 [Луцик, В.И. Кинетика гидролитического и окислительного растворения сульфидов металлов: монография / В.И. Луцик, А.Е. Соболев. Тверь: ТГТУ, 2009. 140 с.]. Представленный ряд позволяет прогнозировать ускорение растворения одних минералов и замедление других: минералы с большим потенциалом будут ускорять растворение минералов с меньшим. Например, при совместном растворении халькопирита и пирита в сернокислых средах последний (потенциал пирита 0,63 В) будет выступать в качестве катода и его разложение будет тормозиться, в то время как поверхность халькопирита будет являться в данной системе анодом (потенциал 0,52 В) и растворяться с большей скоростью, чем в отсутствие пирита [Mehta A.P., Murr L.E. Fundamental studies of the contribution of galvanic interaction to acid-bacterial leaching of mixed metal sulfides // Hydrometallurgy. 1983. Vol. 9. № 3. P. 235-256]. Данный принцип взят за основу в процессе Galvanox, где выщелачивание сульфидного сырья цветных металлов осуществляется в сернокислых средах с добавкой пирита и кислорода [US7846233B2, US8795612B2]. Необходимо отметить, что материалов, содержащих правоустанавливающие сведения о растворении сульфидов в азотной кислоте в присутствии пирита не выявлено.
Электрохимический механизм окислительного растворения смеси сульфидов при азотнокислотном выщелачивании описывают следующими электродными процессами на примере пирита и халькопирита.
Реакция на катодном сульфиде (пирит):

Реакция на анодном сульфиде (халькопирит):

В соответствии с этой моделью при физическом контакте минеральных зерен пирита и халькопирита последний растворяется в первую очередь.
Частицы пирита, не контактирующие с халькопиритом, также подвергаются окислению
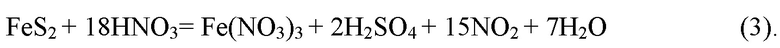
В соответствии с вышеизложенным, пирит, выступая в качестве катализатора, ускоряющего растворение хаклькопирита, с другой стороны, является источником дополнительного количества ионов Fe (III). Ионы Fe (III) выступают в роли окислителя и увеличивают скорость растворения сульфидов цветных металлов. Взаимодействие халькопирита и ионов трехвалентного железа можно представить следующей реакцией:
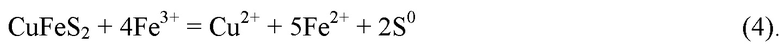
При высокой начальной концентрации азотной кислоты и соответствующем значении окислительно-восстановительного потенциала (ОВП) железо переходит в раствор преимущественно в виде катионов Fe3+. Этому способствуют вторичные процессы с участием оксидов азота:
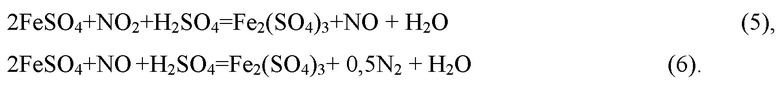
Характерно, что на завершающих стадиях процесса, когда концентрация свободной кислоты и ОВП снижается, железо переходит в раствор в форме Fe2+.
Пленка элементной серы, образующаяся на поверхности зерен халькопирита, вызывает диффузионные затруднения и замедляет скорость процесса. Установлено, что элементная сера в обсуждаемой системе растворяется с поверхности минерала за счет дополнительного окисления диоксидом азота (NO2):

Данная особенность в определяющей степени обуславливает протекание растворения в активном режиме, когда поверхность сульфидов не пассивируется пленками элементной серы. Кроме того, частицы золота в нерастворенном остатке также, в большей степени доступны для последующего выщелачивания.
Оксиды азота выступают в качестве окислителя при разложении сульфидов цинка, железа и т.д. Таким образом, при введении пирита в состав реакционной массы ускоряется процесс в целом и повышается степень целевого использования азотной кислоты на процессы разложения сульфидов и перевода элементной серы в сульфатную.
В ходе процесса и, особенно на начальной стадии, нитрозные газы, образуются в избытке, не успевают расходоваться на вторичные процессы (реакции 5 и 6), выделяются из реактора и улавливаются в абсорбционной колонне. Исследованиями установлено, что если улавливание нитрозных газов проводить растворами, содержащими Fe (II), то такое улавливание протекает быстрее и полнее.
Анализ совокупности процессов в обсуждаемой системе показывает, что отработанные растворы разложения сульфидных концентратов, содержащих соль Fe2(SO4)3, логично использовать при переработке новой порции концентратов, что позволит минимизировать расходы на дополнительные реагенты, в полной степени использовать окислительную способность диоксида азота.
В качестве источника пирита могут выступать низкокачественные золотосодержащие пиритные концентраты или пиритные хвосты обогащения, в которых содержание тонковкрапленного золота может достигать 1-4 г/т. Автономная переработка такого относительно бедного сырья для извлечения благородных металлов экономически не оправдана. Азотнокислое выщелачивание смеси позволит совместно перерабатывать сульфидное сырье цветных металлов и пиритные концентраты, выделять цветные металлы из растворов выщелачивания, а нерастворенные остатки направлять на выделение благородных металлов цианированием.
При обосновании рекомендуемых пределов отличительных признаков необходимо отметить, что положительный эффект присутствия пирита в реакционной смеси наблюдается только при соотношении пирит - сульфиды цветных металлов не менее 0,5:1. Большая доля низкокачественного пирита в смеси чем 1:1 экономически не оправдана. При относительно небольшой массе дополнительно извлекаемого золота дополнительный расход азотной кислоты не окупается.
Рекомендуемый диапазон содержания Fe (III) в выщелачивающих растворах также диктуется технологическими причинами. Позитивное влияние на скорость растворения наблюдается при содержании Fe (III) более 5 г/л, при содержании выше 30 г/л снижение удельного расхода азотной кислоты не происходит. В качестве оборотного источника Fe (III) предложено использовать часть ранее полученных растворов выщелачивания, использованных в качестве абсорбента нитрозных газов.
Таким образом, совокупность отличительных признаков предлагаемого способа:
- добавление пиритного концентрата при выщелачивании в соотношении пирит - сульфиды цветных металлов в полиметаллическом сульфидном сырье (0,5÷1): 1;
- введение солей Fe (III) в выщелачивающий раствор в количестве 5-30 г/л;
- частичное использование растворов в обороте
по сравнению с прототипом обеспечивают снижение удельных расходов азотной кислоты.
Примером реализации предлагаемого способа служат результаты следующих опытов.
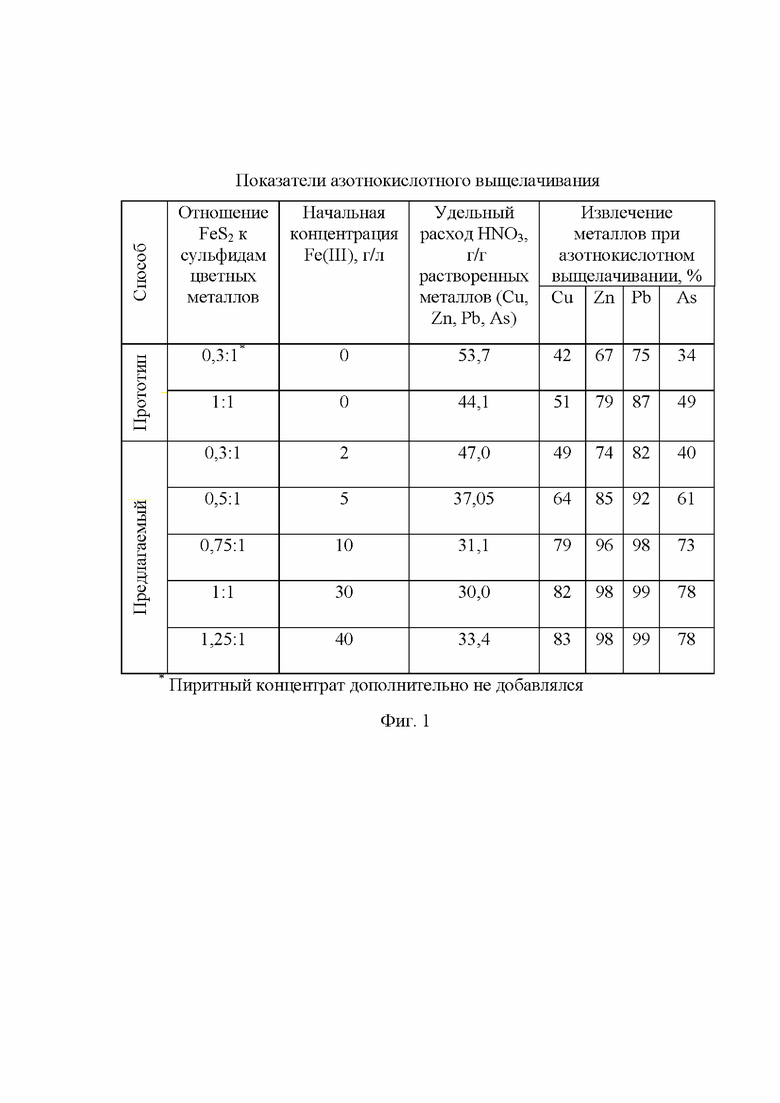
В качестве объекта исследований использовали сульфидный полиметаллический концентрат Учалинского месторождения с содержанием меди 18 %, цинка 4,8 %, мышьяка 3 %, свинца 2 %, железа 17 % (из них 8 % в пирите), золота 5 г/т, серебра 96 г/т, и пиритный концентрат с содержанием железа 34 %, золота 3 г/т. Естественное соотношение пирита к сульфидам цветных металлов в полиметаллическом концентрате составляло 0,3:1. Указанные сульфидные материалы были предварительно измельчены, просеяны, в экспериментах использовали фракцию 74-100 мкм. Навески полиметаллического концентрата распульповывали водой при Ж : Т = 3 : 2, добавляли требуемое количество азотной кислоты. В заданном количестве в полученную смесь добавляли катализаторы: раствор сульфата железа (III) и пиритные хвосты. В ходе выщелачивания поддерживали температуру пульпы при 80°С и pH на уровне 1,0, добавляя азотную кислоту при непрерывном контроле pH. Продолжительность выщелачивания составляла 20 минут. Пульпу после выщелачивания фильтровали, растворы анализировали методом атомно-абсорбционной спектрофотометрии на содержание меди, цинка, свинца, мышьяка, по результатам анализа оценивали степень извлечения металлов. Результаты азотнокислотного выщелачивания представлены в фиг. 1.
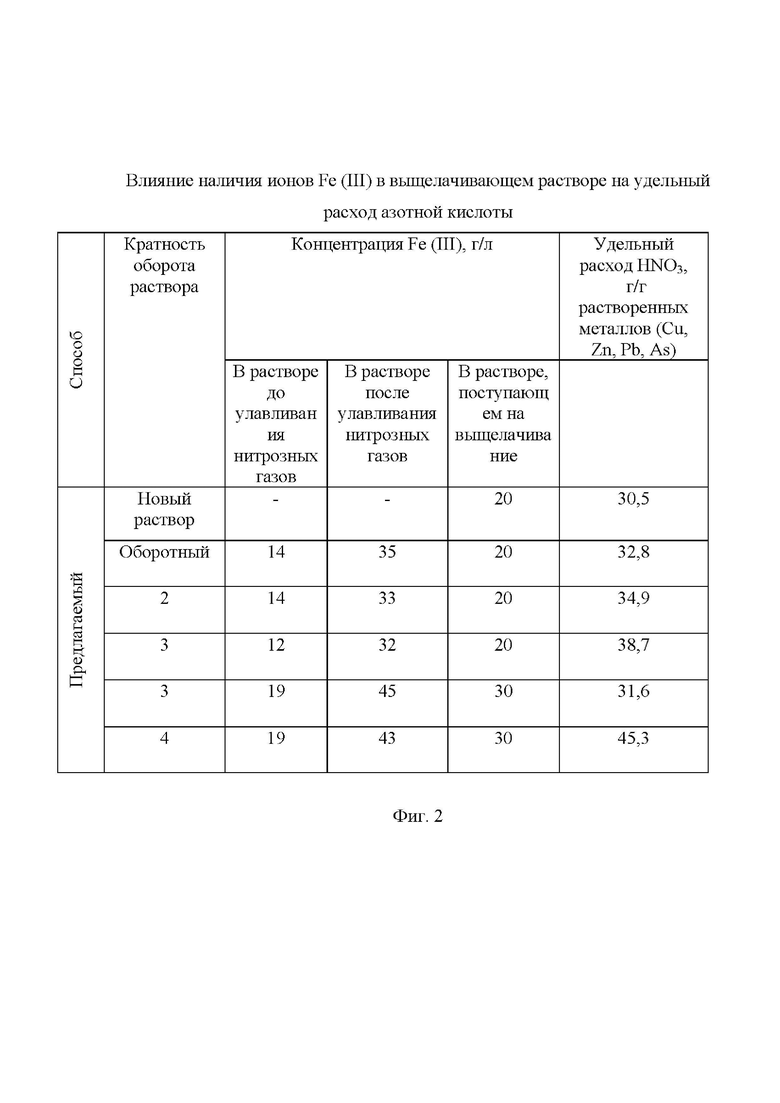
Дополнительно провели опыты, в которых часть растворов азотнокислого выщелачивания с содержанием Fe (II) 25- 30 г/л и Fe (III) до 20 г/л использовали для улавливания нитрозных газов при обработке новых навесок смеси пиритного и полиметаллического концентратов. Содержание Fe (III) в улавливающих растворах возрастало до 45 г/л и часть такого раствора использовали при подготовке выщелачивающего раствора с заданной концентрацией Fe (III). При необходимости добавляли реактив сульфата железа (III). Растворы использовали неоднократно. В данных опытах использовали соотношение масс пирита к массе сульфидов цветных металлов 1:1. Другие условия экспериментов аналогичны тем, что использовали в первой серии. Результаты данных экспериментов приведены на фиг. 2.
Для сравнения проведены опыты по условиям способа прототипа, то есть без использования предлагаемых катализаторов.
Сравнительный анализ технических решений, в том числе способа, представленного в качестве прототипа, и предлагаемого изобретения, позволяет сделать вывод, что именно совокупность заявленных признаков обеспечивает достижение необходимого технического результата. Реализация предложенного способа дает возможность снизить расход азотной кислоты в 1,8 раза и при сопоставимых условиях увеличить степень извлечения цветных металлов на 24-44 %.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОБОГАЩЕНИЯ ТЕХНОГЕННОГО МИНЕРАЛЬНОГО СЫРЬЯ ЦВЕТНЫХ МЕТАЛЛОВ | 2012 |
|
RU2480290C1 |
| Способ комплексной переработки пиритсодержащего сырья | 2016 |
|
RU2627835C2 |
| СПОСОБ ГИДРОМЕТАЛЛУРГИЧЕСКОЙ ПЕРЕРАБОТКИ СУЛЬФИДНЫХ КОНЦЕНТРАТОВ | 2007 |
|
RU2339706C1 |
| КУЧНОЕ БИОВЫЩЕЛАЧИВАНИЕ БЕДНОГО УПОРНОГО МИНЕРАЛЬНОГО СЫРЬЯ ПРИРОДНОГО И ТЕХНОГЕННОГО ПРОИСХОЖДЕНИЯ | 2017 |
|
RU2679724C1 |
| КОМБИНИРОВАННЫЙ СПОСОБ ПЕРЕРАБОТКИ ХВОСТОВ ОБОГАЩЕНИЯ ПОЛИМЕТАЛЛИЧЕСКИХ РУД | 1992 |
|
RU2044079C1 |
| СПОСОБ ВЫЩЕЛАЧИВАНИЯ МЕДНЫХ КОНЦЕНТРАТОВ | 2005 |
|
RU2373298C2 |
| Способ выщелачивания пиритсодержащего сырья | 2017 |
|
RU2651017C1 |
| КОМБИНИРОВАННЫЙ СПОСОБ ПЕРЕРАБОТКИ ХВОСТОВ ОБОГАЩЕНИЯ ПОЛИМЕТАЛЛИЧЕСКИХ РУД | 1998 |
|
RU2197547C2 |
| ИЗВЛЕЧЕНИЕ МЕТАЛЛОВ ИЗ СУЛЬФИДНЫХ МАТЕРИАЛОВ | 2003 |
|
RU2353679C2 |
| Способ комплексной переработки золотосодержащих сульфидных мышьяковистых концентратов | 2015 |
|
RU2632742C2 |
Изобретение относится к гидрометаллургии, а именно к переработке полиметаллического сульфидного сырья, содержащего цветные и благородные металлы. Полиметаллическое сульфидное сырьё цветных металлов выщелачивают в растворе азотной кислоты и улавливают нитрозные газы. Выщелачивание проводят в присутствии катализаторов, в качестве которых используют пиритный концентрат и водный раствор сульфата железа (III). Соотношение общей массы пирита и сульфидов цветных металлов в полиметаллическом сырье составляет (0,5-1):1, а начальная концентрация ионов железа (III) в растворе выщелачивания равна 5-30 г/дм3. Способ позволяет снизить расход азотной кислоты и повысить извлечение цветных металлов в раствор. 1 з.п. ф-лы, 2 ил.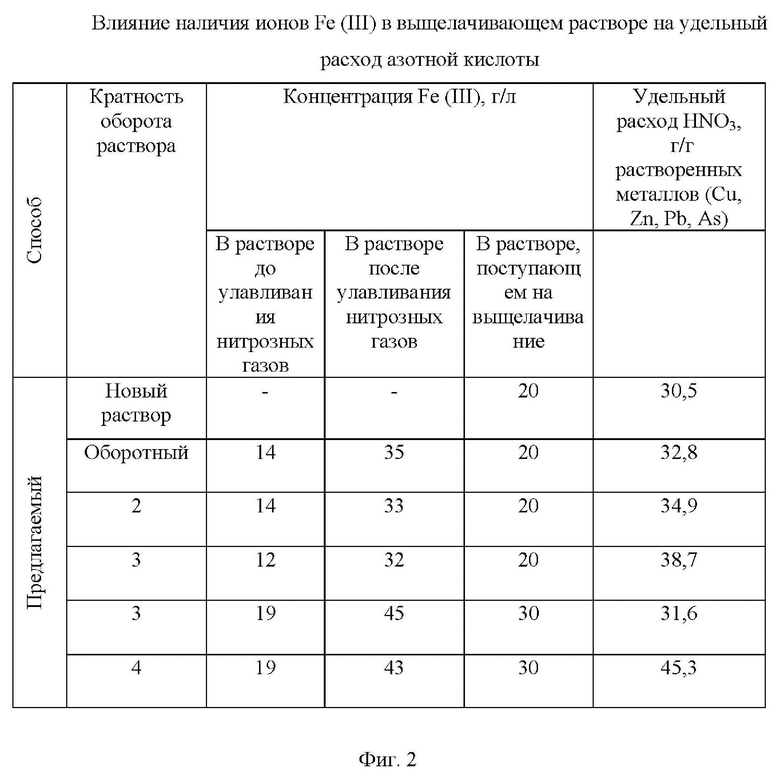
1. Способ переработки полиметаллического сульфидного сырья цветных металлов, включающий выщелачивание сырья в растворе азотной кислоты и улавливание нитрозных газов, отличающийся тем, что выщелачивание проводят в присутствии катализаторов, в качестве которых используют пиритный концентрат и водный раствор сульфата железа (III), при этом соотношение общей массы пирита и сульфидов цветных металлов в полиметаллическом сырье составляет (0,5-1):1, а начальная концентрация ионов железа (III) в растворе выщелачивания равна 5-30 г/дм3.
2. Способ по п.1, отличающийся тем, что в качестве раствора сульфата железа (III) используют оборотный раствор, полученный при обработке предыдущей партии смеси пиритного концентрата и полиметаллического сульфидного сырья с последующим улавливанием этим раствором нитрозных газов.
| CN 110724816 A, 24.01.2020 | |||
| СПОСОБ ВЫЩЕЛАЧИВАНИЯ ПОЛИМЕТАЛЛИЧЕСКОГО СЫРЬЯ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2003 |
|
RU2245378C1 |
| АВТОМАТИЧЕСКИЙ СТАНОК ТИПА ПАНТОГРАФА ДЛЯ ОБРАБОТКИ ФАСОННЫХ ПОВЕРХНОСТЕЙ | 1934 |
|
SU40129A1 |
| СПОСОБ ГИДРОМЕТАЛЛУРГИЧЕСКОГО ИЗВЛЕЧЕНИЯ МЕТАЛЛОВ ИЗ КОМПЛЕКСНЫХ РУД | 1995 |
|
RU2105824C1 |
| WO 2012053614 A1, 26.04.2012. | |||
Авторы
Даты
2023-05-22—Публикация
2022-09-20—Подача