ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] По данной заявке испрашивается преимущество предварительной заявки США № 62/521758, поданной 19 июня, 2017, описание которой полностью включено в настоящий документ посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
[0002] Данное раскрытие относится к композициям и способам модуляции уровней белка альфа-синуклеина посредством гена и белка FAF1 и к ингибиторам активности FAF1 в отношении модуляции уровня, или агрегации, или модификации альфа-синуклеина для лечения или предотвращения опосредованных альфа-синуклеином синуклеинопатий. Раскрытие включает соответствующие способы диагностики и способы лечения с использованием соединений, обладающих активностью в отношении модуляции количеств или активности FAF1.
УРОВЕНЬ ТЕХНИКИ
[0003] FAF1 представляет собой белок, связанный с рецептором апоптоза Fas и называемый Fas-ассоциированным фактором 1. FAF1 связывается с Fas при взаимодействии Fas с лигандом, называемым лигандом Fas (FasL), и способствует апоптозу. Таким образом, FAF1 является проапоптотическим белком. FAF1 имеет N-концевую 200-аминокислотную область, которая связывается с Fas (Ryu SW et al. 2003, Yu C et al. 2016). FAF1 затем активирует каспазу 8 и сигнальный путь апоптоза с помощью активирования каспазного каскада. FAF1 также активирует JNK и связывается с PARP1, и таким образом стимулирует сигнальный путь инициации некроза (Yu C et al. 2016). Однако в неактивированном состоянии FAF1 связан с HSP70 и поддерживается как неактивная форма (Kim HJ et al., 2005, Gao X et al., 2015). Сообщается, что FAF1 сверхэкспрессирован в посмертной ткани пациентов с болезнью Паркинсона (Betarbet R et al. 2008).
[0004] Синуклеинопатии представляют собой группу нейродегенеративных заболеваний, вызванных накоплением неправильно свернутого альфа-синуклеина и его агрегатов, таких как включения телец Леви (LB) или нейритов Леви (LN). Примеры включают болезнь Паркинсона (PD), деменцию с тельцами Леви (DLB) и множественную системную атрофию (MSA) (Spillantini MG и Goedert M 2000,  MJ et al. 2003).
MJ et al. 2003).
[0005] Альфа-синуклеин, имеющий название гена SNCA, представляет собой небольшой цитоплазматический белок массой 14 кДа, в основном расположенный в синаптических пузырьках в нейронных клетках, и выполняет функции активации сигнального пути и трансмиссии (Snead D. and Eliezer D., 2014). Белок состоит из трех доменов: N-концевого домена с амфипатическими спиралями, центрального домена с бета-листами гибкой конформации и С-концевого хвоста со многими кислотными остатками (Gallegos S et al. 2015). Известно, что белок существует в растворимой форме в виде мономера или тетрамера. Однако альфа-синуклеин складывается и агрегирует, образуя олигомеры и другие мультимеры, а также может по различным неясным причинам объединяться в фибриллярную структуру, называемую тельцем Леви и невритом Леви. Процесс включает С-концевой протеолиз, фосфорилирование по серину в положении 129, моноубиквитинирование и другие модификации (Sato H et al., 2013, Oueslati A, 2016). Причины неправильного сворачивания и агрегации альфа-синуклеина включают накопление белка из-за сверхэкспрессии белка путем генной мультипликации или снижения деградации или изменения свойств самого белка в результате мутации. Однако известны и другие негенетические причины, такие как токсины окружающей среды, клеточные стрессы, такие как клеточная токсичность, ER стресс и окислительный стресс (Rockenstein E et al. 2014, Ingelsson M, 2016). Кроме того, на уровень альфа-синуклеина и его агрегацию влияют полиморфные варианты локуса SNCA (Mata IF et al., 2010).
[0006] Токсичность неправильно свернутых мультимеров альфа-синуклеина и телец Леви была изучена и, возможно, связана с различными патогенными процессами, в частности с дисфункциями при мембранном транспорте, включая экзоцитоз, транспорт между ЭР и аппаратом Гольджи, стресс ЭР, гомеостаз Гольджи, эндоцитоз, аутофагию и окислительный стресс (Wang T and Hay JC 2016, Snead D et al. 2014). Кроме того, токсичность альфа-синуклеина также может включать митохондриальную токсичность и воспаление (Ingelsson M, 2016). Олигомеры альфа-синуклеина и тельца Леви могут вмешиваться в протеасомный путь и связаны с разрушением плазматической мембраны и образованием пор, которые приводят к активации апоптоза в клетках (Gallegos S et al. 2015).
[0007] «Синуклеинопатии» представляют собой группу нейродегенеративных расстройств, имеющих ряд клинических симптомов, таких как болезнь Паркинсона (PD), болезнь Паркинсона с деменцией (PDD), деменция с тельцами Леви (DLB), множественная системная атрофия (MSA), атипичный паркинсонизм, атипичная болезнь Паркинсона и чистая вегетативная недостаточность (PAF) (Spillantini MG and Goedert M 2000,  MJ 2003). Эти заболевания вызваны тельцами Леви или невритами Леви или агрегатами альфа-синуклеина в нейронах и глие. Клинически они характеризуются хроническим и прогрессирующим снижением двигательных, когнитивных и вегетативных функций в зависимости от распределения поражений.
MJ 2003). Эти заболевания вызваны тельцами Леви или невритами Леви или агрегатами альфа-синуклеина в нейронах и глие. Клинически они характеризуются хроническим и прогрессирующим снижением двигательных, когнитивных и вегетативных функций в зависимости от распределения поражений.
[0008] Болезнь Паркинсона является вторым наиболее распространенным нейродегенеративным заболеванием нашего времени (Feng LR et al. 2010), обычно рассматриваемым как двигательное расстройство. Патологическим признаком PD является избирательная прогрессирующая дегенерация и потеря дофаминергических нейронов в черной субстанции (SNc), особенно в компактной области черной субстанции (SNpc) (Luk KC et al. 2012) в среднем мозге, ответственном за нарушение движения. Однако симптомы часто сопровождаются появлением вегетативных, когнитивных и психиатрических проблем (Jankovic J 2008).
[0009] Другим отличительным признаком PD является наличие цитоплазматических включений, называемых тельцами Леви (LB) и нейритами Леви (LN) в дофаминергических нейронных клетках, которые наблюдаются в посмертных тканях более чем у 90 процентов пациентов с болезнью Паркинсона. Основным белковым компонентом LB является неправильно свернутый и агрегированный альфа-синуклеин (Angot E et al. 2012).
[0010] Считается, что некоторые генетические изменения, точечные мутации и генная мультипликация гена SNCA вызывают семейную болезнь Паркинсона (PD) или причинную реакцию для PD. Доминантное наследование этих генетических мутаций предполагает механизм усиления функции, такой как агрегация вследствие изменений свойств белка или повышенного уровня белка (Devine MJ et al. 2011, Appel-Cresswell S et al. 2013, Kasten M and Klein C 2013, Petrucci S et al. 2016). Определенные полиморфизмы в гене SNCA или мутации в области дистального энхансера могут усиливать его экспрессию и, следовательно, агрегацию, и, как сообщается, связаны с PD (Mata IF et al. 2010, Soldner F et al. 2016).
[0011] Помимо мутаций в гене SNCA многие мутации связаны с болезнью Паркинсона и связанными с ним синуклеинопатиями (Wang C-D and Chan P 2014, Kalinderi K et al. 2016, Federoff M 2015, Nussbaum R 2017). Предполагается, что некоторые из этих генов участвуют в процессинге альфа-синуклеина и его накоплении. Например, мутация в GBA (ген глюкоцереброзидазы) составляет 23% случаев деменции с тельцами Леви и 21% с PD (Sidransky E et al. 2009, Jesus S et al. 2016). Сообщалось, что мутанты GBA увеличивают накопление SNCA путем изменения процессинга альфа-синуклеина (Cullen V et al. 2011, Fernandes HJ 2016). Другими известными генами, которые связаны с этими заболеваниями, являются Parkin, LRRK2, DJ-1 и PINK1. Хотя роль этих генов в патогенезе паркинсонизма и других синуклеинопатий в значительной степени неизвестна, эти гены выполняют функции посттрансляционной модификации и процессинга белка, такие как убиквитинирование, мембранный трафик, аутофагия и свертывание белка, и сверхэкспрессия альфа-синуклеина происходит из-за мутаций в некоторых из этих генов (Walden H and Muqit MMK 2017, Galegos S 2015).
[0012] Деменция с тельцами Леви (DLB) является второй наиболее распространенной формой деменции, с клиническими симптомами прогрессирующего снижения когнитивных функций с деменцией и флуктуирующим познанием, в частности, с визуальной галлюцинацией. Посмертные ткани показывают многочисленные тельца Леви (LB) в коре головного мозга кроме в черной субстанции, и эти LB включают альфа-синуклеин (Gaser F et al. 2005, Goeder M et al. 2017).
[0013] Множественная системная атрофия (MSA) является фатальным нейродегенеративным заболеванием с симптомами вегетативной недостаточности, паркинсонизма и мозжечковой атаксии в различных комбинациях (Daniela Kuzdas-Wood et al. 2014). Она является редким заболеванием с распространенностью 1,9-4,9/100000 и выживаемостью 6-9 лет (Stefanova et al. 2009), и развивается у взрослых в среднем возрасте 57 лет. Что касается патологии, то наблюдаются широко распространенные цитоплазматические включения (GCI) в глие по всей ЦНС (Trojanowski JQ and Revesz T 2007), которые состоят из нитчатого альфа-синуклеина. Новыми предложенными критериями являются преобладающая атаксия мозжечка с преобладающими двигательными особенностями и нейропатологическая демонстрация альфа-синуклеин-положительных глиоплазитных включений ЦНС с нейродегенеративными изменениями в стриатонигральных или оливопонтоцеребеллярных структурах (Gilman S, 2008).
КРАТКОЕ ОПИСАНИЕ ФИГУР
[0014] На фигуре 1 проиллюстрирована сверхэкспрессия в клетках SH-SY5Y трансфецированного трансгена FAF1-FLAG.
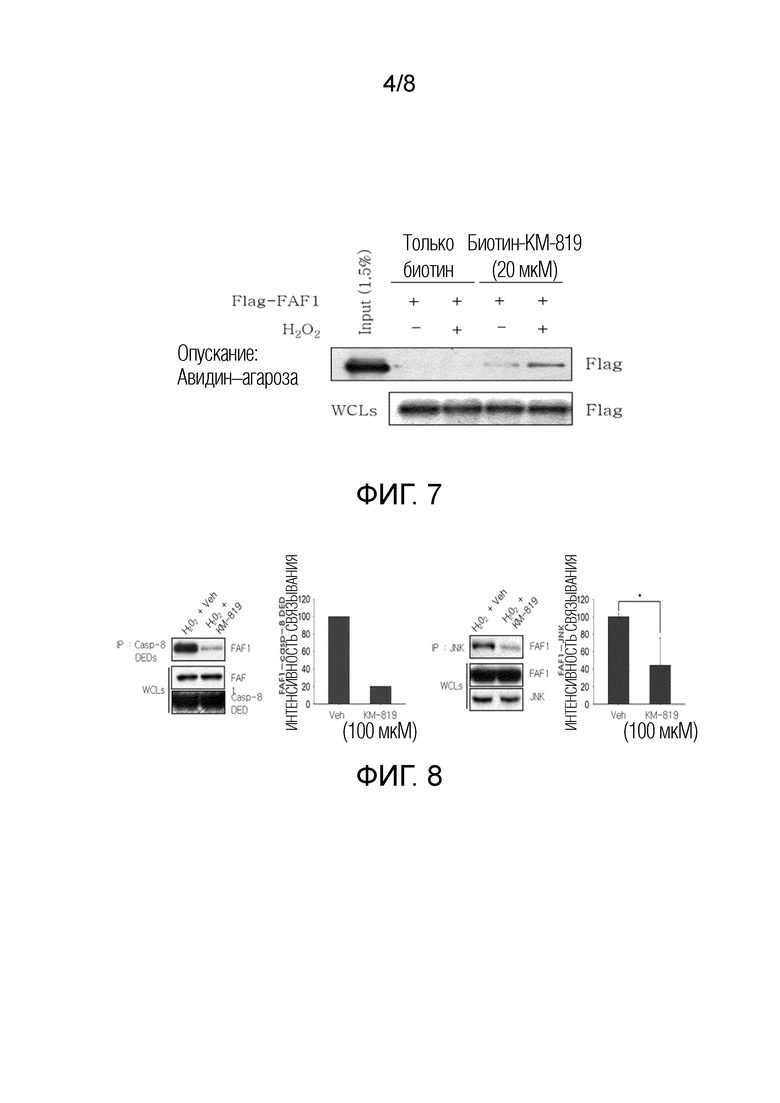
[0015] На фигуре 2 показана агрегация α-синуклеина в клетках SH-SY5Y, которые сверхэкспрессируют трансген FAF1-FLAG.
[0016] На фигурах 3A и 3B показано образование подобных тельцам Леви форм в клетках SH-SY5Y, сверхэкспрессирующих трансфецированный трансген FAF1-FLAG. На фигуре 3А показаны клетки, трансфецированные векторным контролем. На фиг.3В показаны клетки, трансфецированные трансгеном FAF1-FLAG. DAPI - окрашивание DAPI; α-syn - окрашивание анти-α-синуклеин антитела; Ps129-α-syn - окрашивание с окрашиванием анти-фосфорилированного α-синуклеина; объединенные - наложение трех изображений.
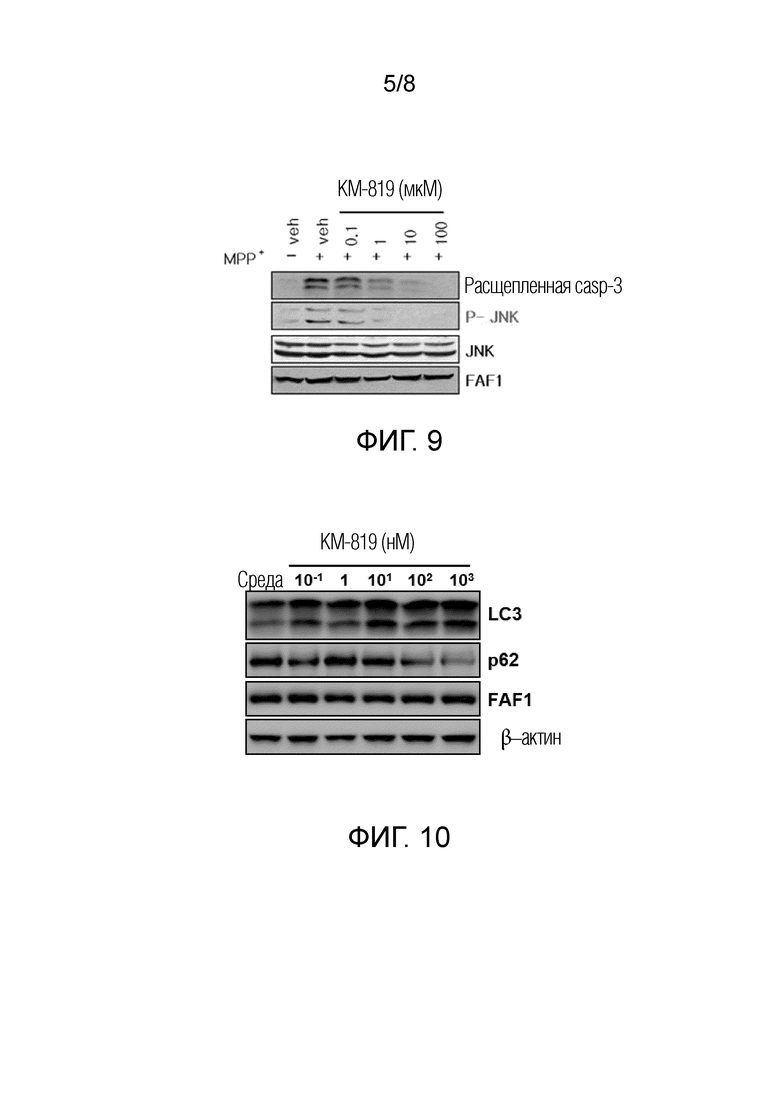
[0017] На фигуре 4 проиллюстрирована сверхэкспрессия FAF1 в среднем мозге мышей, имеющих FAF1-экспрессирующую аденовирусную конструкцию, микроинъецированную в ткань среднего мозга.
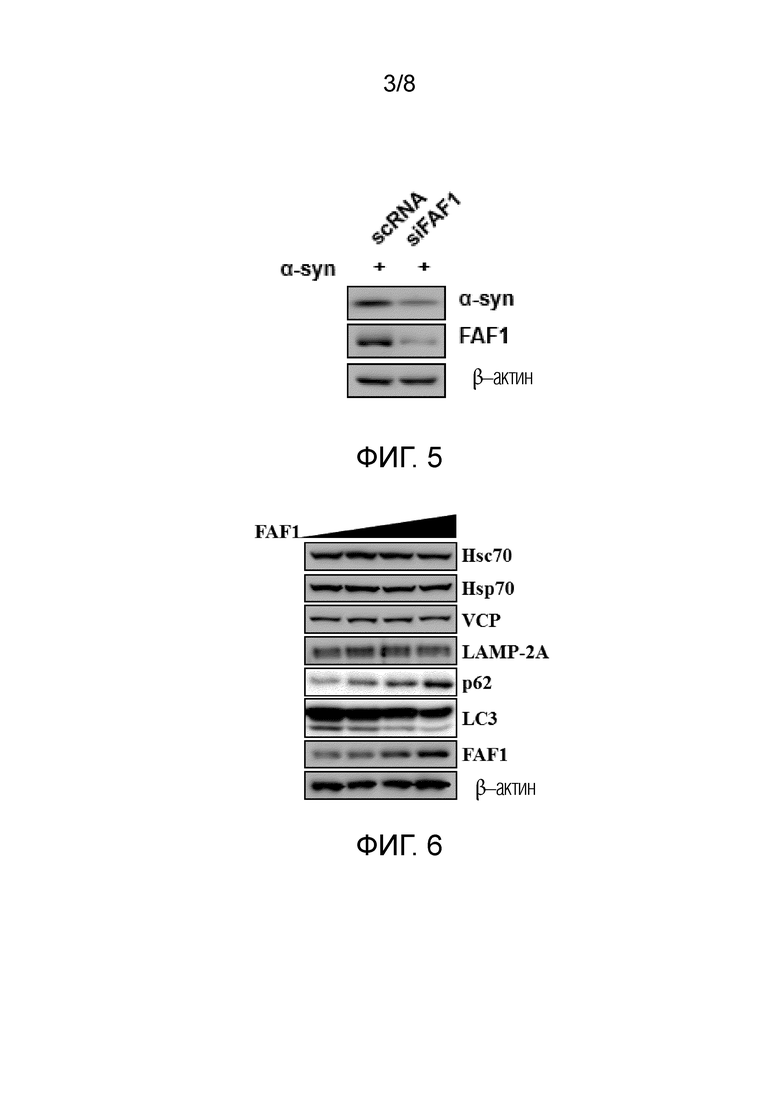
[0018] На фигуре 5 показано ослабление экспрессии FAF1 в клетках SH-SY5Y, ко-трансфецированных геном α-синуклеина и соответствующей siRNA.
[0019] На фигуре 6 показано изменения в экспрессии белка p62 и LC3 в клетках SH-SY5Y, трансфецированных геном FAF1.
[0020] На фигуре 7 показано связывание KM-819 с FAF1 в клетках, трансфецированных конструкцией FAF1-FLAG.
[0021] На фигуре 8 показано ингибирование образования FAF1-каспазы 8 и комплексов FAF1-JNK с помощью KM-819 в клеточных экстрактах.
[0022] На фигуре 9 показано ингибирование активности каспазы 8 в расщеплении каспазы 3 и фосфорилирования JNK с помощью KM-819 в клеточных экстрактах.
[0023] На фигуре 10 показано уменьшение количества белка p62 и увеличение количества белка LC3 в клетках SH-SY5Y, сверхэкспрессирующих FAF1 и обработанных KM-819.
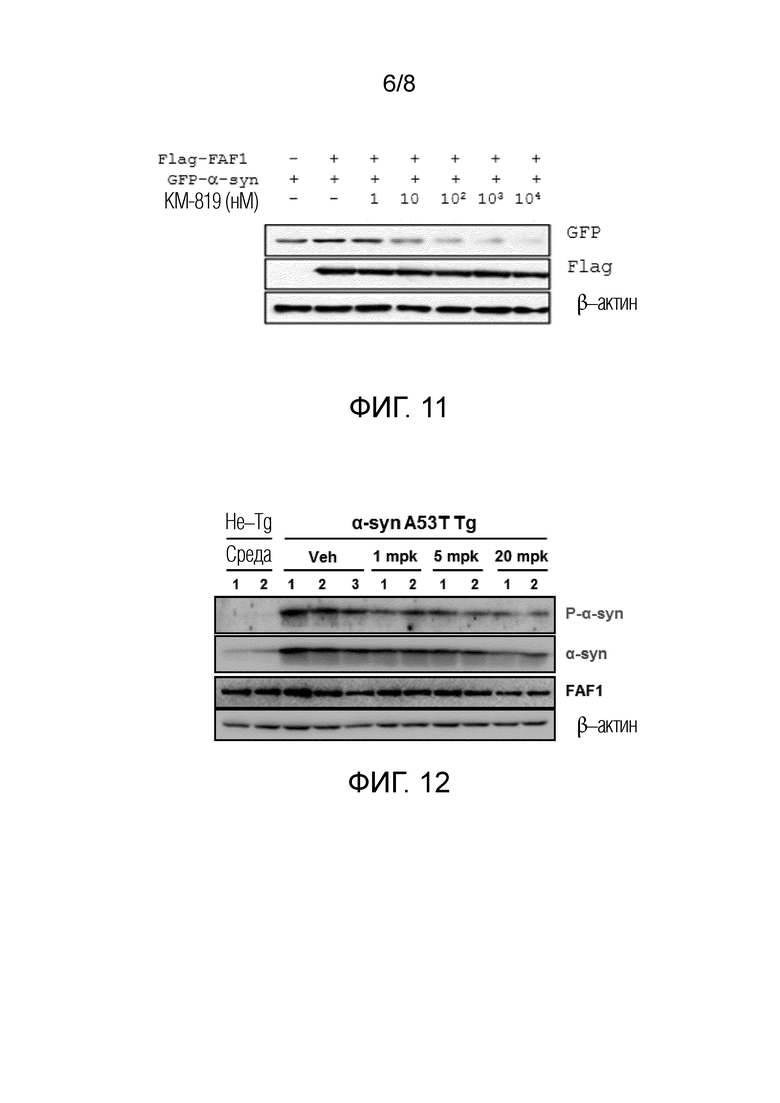
[0024] На фигуре 11 показано уменьшение белка α-синуклеина в клетках, ко-трансфецированных с экспрессирующей конструкцией FAF1-FLAG и экспрессирующей конструкцией α-синуклеина-GFP (зеленый флуоресцентный белок).
[0025] На фигуре 12 показано уменьшение количества α-синуклеина и количества S129 фосфорилированного α-синуклеина в ткани среднего мозга трансгенных мышей со сверхэкспрессией FAF1 после введения KM-819.
[0026] На фигуре 13 показано уменьшение количества α-синуклеина в гиппокампе у трансгенных мышей со сверхэкспрессией FAF1 после введения KM-819.
[0027] На фигуре 14 показано уменьшение количества α-синуклеина в коре головного мозга трансгенных мышей со сверхэкспрессией FAF1 после введения KM-819.
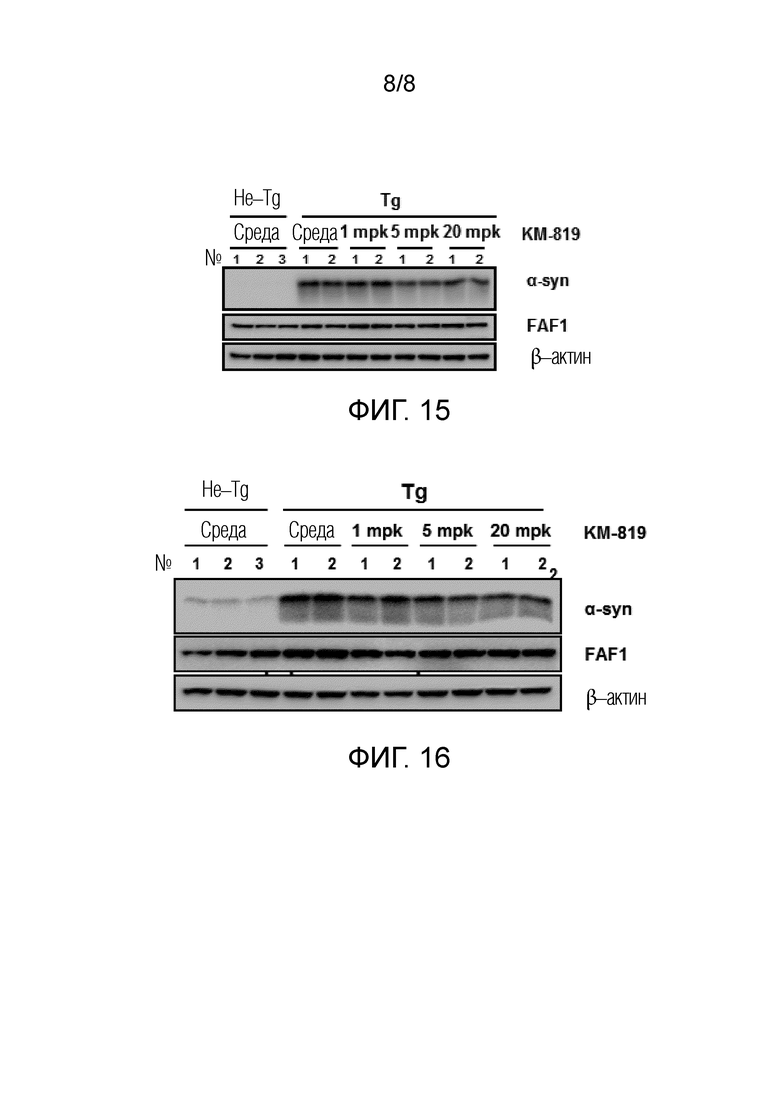
[0028] На фигуре 15 показано уменьшение количества α-синуклеина в мозжечке трансгенных мышей, сверхэкспрессирующих FAF1 после введения KM-819.
[0029] На фигуре 16 показано уменьшение количества α-синуклеина в полосатом теле трансгенных мышей, сверхэкспрессирующих FAF1 после введения KM-819.
ОПИСАНИЕ
[0030] Изобретение появилось благодаря неожиданному открытию, что FAF1 увеличивает накопление альфа-синуклеина в нейрональных клетках и его агрегацию. После этого исследования авторов подтвердили, что ингибитор FAF1 на основе производного аминопиразола действительно уменьшает накопление альфа-синуклеина в нейрональных клетках и его агрегацию. Изобретение также выявилось благодаря открытию того, что FAF1 ингибирует аутофагию посредством увеличения белка p62 и уменьшения LC3. И исследование авторов изобретения подтвердило, что ингибитор FAF1 на основе производного аминопиразола действительно инвертирует активность FAF1, усиливая аутофагию посредством уменьшения белка p62 и увеличения LC3. Эти результаты являются неожиданными, поскольку FAF1 является проапоптотическим белком, который способствует гибели клеток, а активность FAF1 в отношении аутофагии является новым открытием.
[0031] Данное изобретение относится к композициям и способам модуляции уровней белка альфа-синуклеина с помощью гена и белка FAF1 и к ингибиторам FAF1 для модуляции уровня или агрегации или модификации альфа-синуклеина для лечения или предотвращения опосредованных альфа-синуклеином синуклеинопатий. Изобретение включает соответствующие способы диагностики и способы лечения с использованием соединений, обладающих активностью в отношении модуляции уровней FAF1.
[0032] Настоящее изобретение в целом относится к композициям и способам использования антител, пептидов, нуклеиновых кислот, таких как аптамеры или антисмысловые нуклеиновые кислоты или siRNA или тому подобное, или небольших молекул, изменяющих экспрессию FAF1 или активность белка FAF1 в клетках человека, которые обеспечивают блокирование или замедление прогрессирование синуклеинопатий. Следовательно, предложены композиции и способы для обеспечения модифицированных последовательностей генов и измененной экспрессии белка и активностей FAF1, в которых затрагивается прогрессирование заболеваний. Описано также применение таких композиций и способов для обнаружения и количественного определения уровня альфа-синуклеина и/или характеристики формы синуклеина в образце для диагностических или прогностических целей.
[0033] Неожиданно, используя анализ на основе трансфецированных клеток, было обнаружено, что FAF1 повышает уровень альфа-синуклеина в клетках дозозависимым образом. Кроме того, повышенная экспрессия FAF1 у животных путем инфицирования рекомбинантным аденовирусом, экспрессирующим FAF1, повышает уровень альфа-синуклеина. Кроме того, снижение FAF1 за счет трансфекции RNAi ослабляет уровень альфа-синуклеина. Авторы обнаружили также, что FAF1 ингибирует аутофагию, увеличивая LC-3II и p62, что позволяет предположить, что альфа-синуклеин, по крайней мере частично, передается путями аутофагии в клетках in vitro и у животных.
[0034] Авторы изобретения разработали ингибитор FAF1 KM-819 (KR-88493, патент США 7939550, You SE et al., 2016, который включен посредством ссылки во всей своей полноте и для любых целей). В настоящем документе описывается, что соединение аминопиразола KM-819 с химическим названием 4-[2-(4-бромфенилсульфанил)ацетиламино]-1-фенэтил-1H-пиразол-3-карбоновая кислота является ингибитором FAF1. В настоящем документе описывается, что соединение аминопиразола KM-819 инвертирует эффекты сверхэкспрессии FAF1, уменьшая альфа-синуклеин в клетках и животных. Взятые в совокупности, эксперименты в примерах ниже показывают, что siRNA FAF1 или антисмысловые или связанные с ними генные конструкции, пептиды и антитела и небольшие молекулы, модулирующие FAF1, могут быть использованы для модуляции количеств альфа-синуклеина или состояния фосфорилирования и, таким образом, для лечения индуцированных альфа-синуклеином синуклеинопатий.
[0035] Один аспект настоящего изобретения относится к способу лечения заболевания или состояния, возникающего вследствие синуклеинопатий, включающий введение субъекту, имеющему симптомы или подверженному риску указанных синуклеинопатий, ингибитора активности FAF1 в отношении повышения количества альфа-синуклеина или регулирования количества LC-3 и p62 в клетках субъекта. Эффективное количество, которое вводят, представляет собой количество, которое снижает количество альфа-синуклеина или увеличивает количество LC-3 и/или снижает количество р62 в клетках субъекта, соответственно.
[0036] В некоторых вариантах осуществления этого способа ингибитор активности FAF1 может представлять собой аминопиразольное соединение формулы 1 или его фармацевтически приемлемую соль:
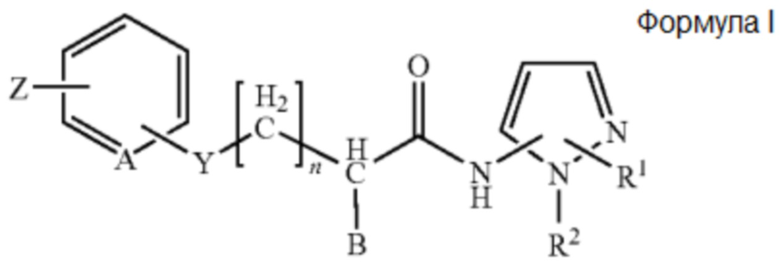 ,
,
где R1 представляет собой -CO2R3, -CH2OR3, -CONR3R4 или
 ,
,
где R3 и R4 независимо друг от друга представляют собой H или прямой, разветвленный или циклический C1-C6 алкил; R2 представляет собой -(CH2)2-фенил; B представляет собой H, фенил или C1-C3 алкил- или галогензамещенный фенил; n обозначает целое число от 0 до 2; Y представляет собой S, O, CH2, SO, SO2 или NR3R4, где R3 и R4 независимо друг от друга представляют собой H или прямой, разветвленный или циклический C1-C6 алкил; Z представляет собой H, галоген, OCH3, NO2, NH2 или прямой, разветвленный или циклический C1-C3 алкил; и A представляет собой CH или N.
[0037] В некоторых случаях аминопиразольное соединение может представлять собой 4-[2-(4-бромфенилсульфанил)ацетиламино]-1-фенэтил-1H-пиразол-3-карбоновую кислоту или ее сложный эфир или амид.
[0038] Другой аспект настоящего изобретения относится к способу лечения заболевания или состояния, возникающего вследствие синуклеинопатий, включающий введение субъекту, имеющему симптомы или подверженному риску указанных синуклеинопатий, такого количества соединения, связывающегося с белком FAF1, которое является эффективным для уменьшения количества α-синуклеина, который фосфорилируется по аминокислоте S129 в клетках указанного субъекта.
[0039] В некоторых вариантах осуществления этого аспекта ингибитор активности FAF1 может представлять собой аминопиразольное соединение формулы 1 или его фармацевтически приемлемую соль:
 ,
,
где R1 представляет собой -CO2R3, -CH2OR3, -CONR3R4 или
 ,
,
где R3 и R4 независимо друг от друга представляют собой H или прямой, разветвленный или циклический C1-C6 алкил; R2 представляет собой -(CH2)2-фенил; B представляет собой H, фенил или C1-C3 алкил- или галогензамещенный фенил; n обозначает целое число от 0 до 2; Y представляет собой S, O, CH2, SO, SO2 или NR3R4, где R3 и R4 независимо друг от друга представляют собой H или прямой, разветвленный или циклический C1-C6 алкил; Z представляет собой H, галоген, OCH3, NO2, NH2 или прямой, разветвленный или циклический C1-C3 алкил; и A представляет собой CH или N.
[0040] В некоторых случаях аминопиразольное соединение может представлять собой 4-[2-(4-бромфенилсульфанил)ацетиламино]-1-фенэтил-1H-пиразол-3-карбоновую кислоту или ее сложный эфир или амид.
[0041] В любом аспекте лечения по настоящему изобретению ингибитор FAF1 можно вводить перорально или путем инъекции в мозг или спинномозговую жидкость или кровь, или через кожу, или другими общепринятыми практическими методами, такими как имплантация мини-насоса. Наиболее удобным способом является такой, при котором соединение, связывающее FAF1, вводят перорально.
[0042] Производные аминопиразола по настоящему изобретению могут быть не только в форме их фармацевтически приемлемых солей, но также и в форме их сольватов, гидратов и энантиомеров, которые могут быть из них получены.
[0043] Фармацевтически приемлемые соли производных аминопиразола по настоящему изобретению включают кислотно-аддитивные соли, полученные из фармацевтически приемлемых свободных кислот. Свободные кислоты могут быть неорганическими или органическими. Примеры органических кислот включают лимонную кислоту, малеиновую кислоту, фумаровую кислоту, глюконовую кислоту, метансульфоновую кислоту, уксусную кислоту, гликолевую кислоту, янтарную кислоту, винную кислоту, 4-толуолсульфоновую кислоту, галактуроновую кислоту, эмбоновую кислоту, глутаминовую кислоту и аспарагиновую кислоту. Кроме того, в качестве неорганических кислот можно использовать хлористоводородную кислоту, бромистоводородную кислоту, серную кислоту, сернистую кислоту или фосфорную кислоту, предпочтительно, метансульфоновую кислоту и хлористоводородную кислоту.
[0044] Кислотно-аддитивные соли в соответствии с настоящим изобретением могут быть получены с использованием общепринятого способа, например, путем растворения производных аминопиразола формулы 1 в смешивающемся с водой органическом растворителе, таком как ацетон, метанол, этанол и ацетонитрил, добавления избытка органической кислоты или водного раствора неорганической кислоты для осаждения или кристаллизации солей, выпаривания растворителя или избыточных кислот из полученной смеси и сушки или фильтрования с отсосом осажденных солей. Производные аминопиразола по настоящему изобретению, их фармацевтически приемлемые соли и фармацевтическая композиция, содержащая их, могут быть клинически назначены в виде пероральных или не пероральных форм. Обычно их готовят в сочетании с разбавителем или вспомогательным веществом, таким как наполнитель, загуститель, связующее, смачиватель, разрыхлитель или поверхностно-активное вещество и т.д.
[0045] Твердые агенты, предназначенные для перорального введения, могут быть получены путем смешивания по меньшей мере одного производного аминопиразола по настоящему изобретению с по меньшей мере одним вспомогательным веществом, таким как крахмал, карбонат кальция, сахароза, лактоза или желатин. Кроме того, можно также добавить лубрикант, такой как стеарат магния, тальк и тому подобное.
[0046] Жидкие агенты, предназначенные для перорального введения, включают суспензии, растворы для внутреннего применения, эмульсии, сиропы и тому подобное. В дополнение к простому разбавителю, такому как вода или жидкий парафин, в жидких агентах для перорального введения соединения по настоящему изобретению могут использоваться различные вспомогательные вещества, такие как смачивающие агенты, подслащивающие вещества, ароматические вещества, консерванты и тому подобное.
[0047] Кроме того, соединение по настоящему изобретению можно вводить не пероральным путем. Для этого могут использоваться стерильные водные растворы, неводные растворители, суспензии, эмульсии, лиофильные агенты, суппозитории и тому подобное. Для неводных растворителей и суспензий могут быть подходящими инъецируемое растительное масло, такое как пропиленгликоль, полиэтиленгликоль или оливковое масло, и сложный эфир, такой как этилолат. Основы для суппозиториев включают витсол, макрогол, твин 61, какао-бумагу, лауриновую бумагу, глицерин и желатин.
[0048] В зависимости от состояния пациентов, включая возраст, массу тела, пол, путь введения, состояние здоровья и тяжесть заболевания, дозы введения людям производных аминопиразола по настоящему изобретению, их фармацевтически приемлемых солей и фармацевтической композиции, содержащей их, могут различаться. Обычно соединение по настоящему изобретению вводят в дозе от 0,1 до 1000 мг в день для взрослого человека весом 70 кг и, предпочтительно, в дозе от 1 до 500 мг в день. Соединение может быть введено в одной дозе или в разделенных дозах в день.
[0049] Аминопиразольное соединение 4-[2-(4-бром фенилсульфанил)ацетиламино]-1-фенэтил-1H-пиразол-3-карбоновой кислоты имеет EC50 1 нМ для модулирования уровней LC-3 и p62 в клетках и EC50 20 мкМ для уменьшения количества альфа-синуклеина в клетках. Соответственно, эффективное количество этого соединения для модулирования количества LC-3 и p62 в клетках ткани мозга является количеством, которое обеспечивает концентрацию по меньшей мере 0,5 нМ, предпочтительно, по меньшей мере 1 нМ, по меньшей мере 2 нМ, по меньшей мере 5 нМ или по меньшей мере 10 нМ в клетках ткани мозга, и эффективное количество этого соединения для уменьшения количества альфа-синуклеина в клетках ткани мозга является количеством, которое обеспечивает концентрацию по меньшей мере 10 нМ, предпочтительно, по меньшей мере 20 мМ, по меньшей мере 40 нМ, по меньшей мере 100 нМ или по меньшей мере 200 нМ в клетках ткани мозга.
[0050] Другой аспект изобретения относится к способу диагностики синуклеинопатии или оценки риска возникновения синуклеинопатии у субъекта, включающий измерение количества белка FAF1 или уровня активности FAF1 в отношении ингибирования аутофагии, опосредованной белками LC-3 и p62, в клетках субъекта или в образце, взятом у субъекта, где уровень активности или уровень белка FAF1 выше, чем у нормальных людей, что указывает на развитие синуклеинопатии или на риск развития у субъекта синуклеинопатии.
[0051] Другой аспект изобретения объединяет диагностику и лечение для предоставления способа лечения заболевания или состояния, возникающего вследствие синуклеинопатий у субъекта, включающий введение субъекту, у которого в клетках указанного субъекта выявляется количество белка FAF1 или уровень активности FAF1, ингибирующие аутофагию, опосредуемую белками LC-3 и p62 в клетках субъекта, выше, чем у нормальных людей, такого количества ингибитора активности FAF1 в отношении регулирования количеств LC-3 и p62, которое является эффективным для повышения количества LC3 и/или снижения количества p62 в клетках субъекта, или такого количества соединения, связывающегося с белком FAF1, которое является эффективным для уменьшения количества α-синуклеина, который фосфорилируется в аминокислоте S129 в клетках субъекта.
[00052] В некоторых вариантах осуществления этого аспекта изобретения, соединение, которое связывается с FAF1 или ингибирует активность FAF1 в отношении регулирования количеств LC-3 и p62, может представлять собой аминопиразольное соединение формулы 1 или его фармацевтически приемлемую соль:
 ,
,
где R1 представляет собой -CO2R3, -CH2OR3, -CONR3R4 или
 ,
,
где R3 и R4 независимо друг от друга представляют собой H или прямой, разветвленный или циклический C1-C6 алкил; R2 представляет собой -(CH2)2-фенил; B представляет собой H, фенил или C1-C3 алкил- или галогензамещенный фенил; n обозначает целое число от 0 до 2; Y представляет собой S, O, CH2, SO, SO2 или NR3R4, где R3 и R4 независимо друг от друга представляют собой H или прямой, разветвленный или циклический C1-C6 алкил; Z представляет собой H, галоген, OCH3, NO2, NH2 или прямой, разветвленный или циклический C1-C3 алкил; и A представляет собой CH или N.
[0053] Для определения уровней FAF1 и альфа-синуклеина у субъекта может быть взята спинномозговая жидкость (CSF). Для сбора образцов CSF для анализа FAF1 или альфа-синуклеина можно использовать временную выборку с помощью постоянного спинального катетера, например, как описано T.H. Langenickel et al., Br. J. Clin Pharmacol., vol. 81, pp. 878-890 (2016) (настоящим включено посредством ссылки во всей своей полноте).
[0054] ПРИМЕРЫ
1. Увеличение альфа-синуклеина с помощью FAF1 в клетках
FAF1 сверхэкспрессируется в клетках SH-SY5Y путем трансфекции геном FAF1, помеченным Flag. Сверхэкспрессия подтверждается вестерн-блоттингом клеточных экстрактов с использованием анти-Flag-антитела и анти-FAF1-антитела. Кроличье антитело против FAF1 приобретается у компании Proteintech, Chicago, IL, USA, кат. № 10271-1-АР. Клетки ко-трансфецировали геном альфа-синуклеина. Уровень альфа-синуклеина контролируется вестерн-блоттингом с использованием анти-альфа-синуклеин антитела. Со всей очевидностью и неожиданно уровень альфа-синуклеина повышается при сверхэкспрессии FAF1 (фигура 1). Обращается внимание на то, что уровень бета-актина используется в качестве внутреннего контроля. Обращается внимание на то, что в клетках существует определенный уровень эндогенного белка FAF1.
[0055] 2. Увеличение агрегированной формы альфа-синуклеина в клетках с помощью FAF1
FAF1 сверхэкспрессируется в клетках SH-SY5Y путем трансфекции геном FAF1, помеченным Flag. Клетки ко-трансфецировали геном альфа-синуклеина. Уровень агрегированной формы альфа-синуклеина контролируется вестерн-блоттингом с использованием анти-альфа-синуклеина антитела с длительным воздействием пленки. Со всей очевидностью и неожиданно уровень агрегированной формы альфа-синуклеина повышается при сверхэкспрессии FAF1 (фигура 2).
[0056] 3. Продукция подобной тельцам Леви формы альфа-синуклеина в клетках с помощью FAF1
FAF1 сверхэкспрессируется в клетках SH-SY5Y путем трансфекции геном FAF1, помеченным Flag. Клетки ко-трансфецировали геном альфа-синуклеина. LB-подобную форму альфа-синуклеина контролируют с помощью иммунофлуоресцентного окрашивания с использованием анти-альфа-синуклеин антитела. Со всей очевидностью и неожиданно, что LB-подобная форма альфа-синуклеина наблюдается при избыточной экспрессии FAF1 (фигура 3В вверху, стрелка-маркер). Однако LB-подобная форма не наблюдается при векторном контроле (фигура 3А вверху), демонстрируя, что FAF1 индуцирует LB-подобное образование.
[0057] Известно, что альфа-синуклеин фосфорилируется по остатку серина в положении 129, что является вероятным патологическим процессом, приводящим к выработке тельца Леви. Фосфорилированную форму альфа-синуклеина в положении 129 контролируют с помощью иммунофлуоресцентного окрашивания с использованием анти-Ps129-альфа-синуклеина антитела. Ясно, что фосфорилированная форма S129 альфа-синуклеина наблюдается, когда FAF1 сверхэкспрессируется в LM-подобной форме (фигура 3B внизу, стрелка-маркер). Тем не менее, это фосфорилирование не наблюдается с векторным контролем (фигура 3А внизу), демонстрируя, что FAF1 индуцирует фосфорилирование альфа-синуклеина по остатку серина в положении 129.
[0058] 4. Увеличение альфа-синуклеина у мышей с помощью FAF1
FAF1 сверхэкспрессируется у мышей путем инъекции стереотипа обычным способом с рекомбинантным аденовирусом, содержащим ген FAF1, в область среднего мозга. Сверхэкспрессия подтверждается вестерн-блоттингом экстрактов ткани среднего мозга с использованием анти-FAF1 антитела. Средний мозг представляет собой ткань, в которой имеются субстанциальные дофаминергические нейроны, которые, как известно, влияют на движение при синуклеинопатиях. Двум мышам инъецировали аденовирус FAF1, и две неинъецированные мыши использовались в качестве контроля. Уровень альфа-синуклеина контролируется вестерн-блоттингом с использованием анти-альфа-синуклеин антитела. Видно, что повышенный уровень альфа-синуклеина коррелирует со сверхэкспрессией FAF1 (фигура 4).
[0059] 5. Уменьшение альфа-синуклеина siRNA FAF1 в клетках
Экспрессия FAF1 ослабляется обработкой клеток SH-SY5Y siRNA (последовательность: GUGUUGUGGCACAAACCAU), и снижение уровня FAF подтверждается вестерн-блоттингом клеточных экстрактов с использованием анти-FAF1 антитела. Клетки ко-трансфецировали геном альфа-синуклеина. Уровень альфа-синуклеина контролируется вестерн-блоттингом с использованием анти-альфа-синуклеин антитела. Видно, что уровень альфа-синуклеина снижается при обработке siRNA FAF1 (фигура 5). С другой стороны, обработка контрольной siRNA (scRNA, вырожденная последовательность) не снижает уровень альфа-синуклеина.
[0060] 6. FAF1 является супрессором аутофагии
Известно, что альфа-синуклеин расщепляется в клетках различными путями, включая протеасому, аутофагию и аутофагию, опосредованную шапероном (Sampaio-Marques B and Ludovico P 2015). FAF1 сверхэкспрессируется путем трансфекции в клетках SH-SY5Y, и различные белки, участвующие в путях деградации белка, анализируют с помощью вестерн-блоттинга (фигура 6).
[0061] Как показано на фигуре 6, при сверхэкспрессии FAF1 белок p62 увеличивается, а LC3 уменьшается, что указывает на то, что FAF1 подавляет аутофагию. Необходимо отметить, что все остальные белки неизменны. Это изменение опосредует аутофагию, как описано (Sampaio-Marques B and Ludovico P, 2015). Эти данные демонстрируют, что FAF1 увеличивает альфа-синуклеин путем подавления пути аутофагии.
[0062] 7. KM-819 (KR-33493) является ингибитором FAF1
KM-819 (KR-33493, 4-[2-(4-бромфенилсульфанил)ацетиламино]-1-фенэтил-1H-пиразол-3-карбоновая кислота) представляет собой производное аминопиразола, описанное в предшествующем уровне техники для гибели ишемических клеток ингибитор (патент США № 7939550, Yoo SE et al. 2016). Ингибирование FAF1 KM-819 подтверждается связыванием KM-819 с FAF1, как описано и показано на фигуре 7). Кроме того, ингибирование FAF1 KM-819 подтверждается ингибированием нижестоящих мишеней FAF1 в клетках, включая белки пути апоптоза каспазы 8 и JAK (фигура 8). Соединение показало 70%-ное ингибирование апоптоза при 10 мкМ в анализах гибели ишемических клеток, вызванной дезоксиглюкозой апоптоз, опосредованный гипоксией (патент США № 7939550).
[0063] Связывание KM-819 с FAF1 подтверждается анализом выпадения в экстрактах клеток SH-SY6H с использованием меченного биотином KM-819, как описано (Yoo SE et al. 2016). Клетки трансфецируют с flag-меченным FAF1. Образовавшийся комплекс FAF1-KM-819 осаждают, используя покрытую авидином агарозу. Осажденный FAF1 в комплексе измеряют вестерн-блоттингом с использованием анти-Flag антитела. Очевидно, что FAF1 связывается с KM-819, когда клетки подвергаются стрессу перекисью водорода, и, таким образом, FAF1 активируется. Необходимо отметить, что общий уровень FAF1 в экстрактах целых клеток (WCL) измеряется в качестве контроля.
[0064] FAF1 активирует апоптотический стресс различными стимулами посредством активации каспазного каскада и некроза, как описано (Yu C et al. 2016). Прямыми мишенями для FAF1 в этих двух путях являются каспаза 8 и JNK, соответственно. И стадией этой активации является формирование этих комплексов с последующей активацией нижестоящих мишеней.
[0065] Ингибирование комплексообразования FAF1-каспаза 8 и FAF1-JNK с помощью KM-819 подтверждают обычными анализами на иммунопреципитацию с использованием каспаза 8 DED антитела и JNK антитела, а связанный и осажденный FAF1 измеряют с использованием вестерн-блоттинга, используя анти-FAF1 антитело. Ясно, что KM-819 эффективно ингибирует образование комплекса, ингибирование составляет около 80% при 0,1 мкМ (фигура 8).
[0066] Ингибирование активации каспазы 8 и JNK с помощью KM-819 подтверждается анализом расщепления субстрата каспазы 8, каспазы 3 и аутофосфорилирования JNK, соответственно (фигура 9). Клетки обрабатывают KM-819 различной концентрации, как указано, и уровни расщепленной каспазы 3 и аутофосфорилированной формы JNK измеряют вестерн-блоттингом, используя анти-каспаза 3 антитело и анти-фосфо-JNK антитело, соответственно. Видно, что KM-819 ингибирует активность активации каспазы 8 и JNK (фигура 9). IC50 активации каспазы 8 KM-819 составляет 0,73 мкМ, а IC50 активации JNK KM-819 составляет 0,25 мкМ.
[0067] 8. KM-819 усиливает аутофагию
Известно, что альфа-синуклеин расщепляется различными путями в клетках, в том числе посредством протеасом, аутофагии и опосредованной шапероном аутофагии (Sampaio-Marques B and Ludovico P, 2015). FAF1 подавляет аутофагию.
[0068] Для подтверждения того, что ингибитор FAF1 ингибирует активность FAF1-опосредованного подавления аутофагии, клетки SH-SY5Y со сверхэкспрессией FAF1 обрабатывают KM-819, как указано, и уровень LC3 и p62 измеряют вестерн-блоттингом (фигура 10). KM-819 уменьшает белок p62 и увеличивает LC3, демонстрируя, что KM-819 способствует пути аутофагии. EC50 для стимулирования аутофагии KM-819 составляет 1 нМ.
[0069] 9. Уменьшение альфа-синуклеина в клетках с помощью ингибитора FAF1
Для подтверждения того, что ингибитор FAF1 снижает уровень альфа-синуклеина в клетках, клетки SH-SY5Y обрабатывают ингибитором FAF1 KM-819 (KR-88493, патент США 7939550, Yoo SE et al. 2016). Клетки совместно трансфецируют генами, кодирующими FAF1, помеченными Flag, и альфа-синуклеином, помеченными GFP. Уровень альфа-синуклеина измеряют с помощью вестерн-блоттинга клеточных экстрактов с использованием анти-GFP антитела. Уровень FAF1 измеряют вестерн-блоттингом клеточных экстрактов с использованием анти-Flag антитела. Видно, что уровень альфа-синуклеина снижается при обработке ингибитором FAF1 (фигура 11). IC50 составляет 20 нМ, и ингибирование составляет более 95% при 10 мкМ. Это намного более высокая эффективность по сравнению с активностью ингибирования апоптоза, измеренной в предшествующем уровне техники, 70%-ное ингибирование при 10 мкМ. Необходимо отметить, что сам уровень FAF1 не изменяется при обработке ингибитором FAF1.
[0070] 10. Уменьшение альфа-синуклеина в среднем мозге у мышей с помощью ингибитора FAF1
Чтобы увидеть влияние ингибитора FAF1 на уровень альфа-синуклеина у животных, трансгенных мышей со сверхэкспрессией альфа-синуклеина обрабатывают ингибитором FAF1 KM-819. Трансгенные животные представляют собой мышиный штамм, который имеет мутантный ген человеческого альфа-синуклеина A53T под промотором гена Prion (семейный паркинсон, несущий человеческий синуклеин (Lee MK et al. 2002).
[0071] Мышам трехмесячного возраста перорально вводят КМ-819 в дозе 1, 5 и 10 мг/кг/день в течение 9 дней. Двух нетрансгенных мышей (не-Tg) используют в качестве контроля, а трем трансгенным мышам (альфа-syn A53T Tg) вводят только носитель без KM-819. И две мыши используются для каждого дозирования KM-819. Животных умерщвляют, а ткани среднего мозга выделяют и делают экстракты. Альфа-синуклеин, S129-фосфорилированную форму альфа-синуклеина и FAF1 измеряют вестерн-блоттингом с использованием анти-альфа-синуклеин антитела, P-альфа-syn антитела и FAF1 антитела, соответственно. Видно, что как уровень альфа-синуклеина, так и его фосфорилированной формы снижается при обработке ингибитором FAF1 KM-819, демонстрируя, что ингибитор FAF1 уменьшает накопление альфа-синуклеина у животных (фигура 12). Необходимо отметить, что сам уровень FAF1 не изменяется при обработке ингибитором FAF1. Необходимо отметить, что уровень бета-актина используется в качестве внутреннего контроля.
[0072] 11. Уменьшение альфа-синуклеина в гиппокампе у мышей с помощью ингибитора FAF1
Чтобы увидеть влияние ингибитора FAF1 на уровень альфа-синуклеина у животных, трансгенных мышей со сверхэкспрессией альфа-синуклеина обрабатывают ингибитором FAF1 KM-819. Трансгенные животные представляют собой мышиный штамм, который имеет мутантный ген человеческого альфа-синуклеина A53T под промотором гена Prion (семейный паркинсон, несущий человеческий синуклеин (Lee MK et al. 2002).
[0073] Мышам трехмесячного возраста перорально вводят КМ-819 в дозе 1, 5 и 10 мг/кг/день в течение 9 дней. Три нетрансгенных (не Tg) мыши используются в качестве контроля, и двум трансгенным мышам (альфа-syn A53T Tg) вводят только носитель без KM-819. И две мыши используются для каждого дозирования KM-819. Животных умерщвляют, а ткани гиппокампа выделяют и делают экстракты. Альфа-синуклеин и FAF1 измеряют вестерн-блоттингом с использованием анти-альфа-синуклеин антитела и FAF1 антитела, соответственно. Видно, что уровень альфа-синуклеина снижается при обработке ингибитором FAF1 KM-819, демонстрируя, что ингибитор FAF1 уменьшает накопление альфа-синуклеина у животных (фигура 13).
[0074] 12. Уменьшение альфа-синуклеина в коре головного мозга у мышей с помощью ингибитора FAF1
Чтобы увидеть влияние ингибитора FAF1 на уровень альфа-синуклеина у животных, трансгенных мышей со сверхэкспрессией альфа-синуклеина обрабатывают ингибитором FAF1 KM-819. Трансгенные животные представляют собой мышиный штамм, который имеет мутантный ген человеческого альфа-синуклеина A53T под промотором гена Prion (семейный паркинсон, несущий человеческий синуклеин (Lee MK
[0075] Мышам трехмесячного возраста вводят КМ-819 перорально в дозе 1, 5 и 10 мг/кг/день в течение 9 дней. Две нетрансгенные мыши (не-Tg) используются в качестве контроля, и двум трансгенным мышам (альфа-syn A53T Tg) вводят только носитель без KM-819. И две мыши используются для каждого дозирования KM-819. Животных забивают, а ткани коры головного мозга выделяют и делают экстракты. Альфа-синуклеин измеряют вестерн-блоттингом с использованием анти-альфа-синуклеин антитела. Видно, что уровень альфа-синуклеина снижается при обработке ингибитором FAF1 KM-819, демонстрируя, что ингибитор FAF1 уменьшает накопление альфа-синуклеина у животных (фигура 14).
[0076] 13. Уменьшение альфа-синуклеина в мозжечке у мышей с помощью ингибитора FAF1
Чтобы увидеть влияние ингибитора FAF1 на уровень альфа-синуклеина у животных, трансгенных мышей со сверхэкспрессией альфа-синуклеина обрабатывают ингибитором FAF1 KM-819. Трансгенные животные представляют собой мышиный штамм, который имеет мутантный ген человеческого альфа-синуклеина A53T под промотором гена Prion (семейный паркинсон, несущий человеческий синуклеин (Lee MK et al. 2002).
[0077] Мышам трехмесячного возраста вводят КМ-819 перорально в дозе 1, 5 и 10 мг/кг/день в течение 9 дней. Три нетрансгенных мыши (не-Tg) используют в качестве контроля, а двум трансгенным мышам (альфа-syn A53T Tg) вводят только носитель без KM-819. И две мыши используются для каждого дозирования KM-819. Животных умерщвляют, а ткани мозжечка выделяют и делают экстракты. Альфа-синуклеин и FAF1 измеряют вестерн-блоттингом с использованием анти-альфа-синуклеин антитела и FAF1 антитела, соответственно. Видно, что оба уровня альфа-синуклеина снижаются при обработке ингибитором FAF1 KM-819, демонстрируя, что ингибитор FAF1 уменьшает накопление альфа-синуклеина у животных (фигура 15).
[0078] 14. Уменьшение альфа-синуклеина в полосатом теле у мышей с помощью ингибитора FAF1
Чтобы увидеть влияние ингибитора FAF1 на уровень альфа-синуклеина у животных, трансгенных мышей со сверхэкспрессией альфа-синуклеина обрабатывают ингибитором FAF1 KM-819. Трансгенные животные представляют собой мышиный штамм, который имеет мутантный ген человеческого альфа-синуклеина A53T под промотором гена Prion (семейный паркинсон, несущий человеческий синуклеин (Lee MK et al. 2002).
[0079] Мышам трехмесячного возраста вводят КМ-819 перорально в дозе 1, 5 и 10 мг/кг/день в течение 9 дней. Три нетрансгенных (не Tg) мыши используются в качестве контроля, и двум трансгенным мышам (альфа-syn A53T Tg) вводят только носитель без KM-819. И две мыши используются для каждого дозирования KM-819. Животных умерщвляют, ткани полосатого тела выделяют и делают экстракты. Альфа-синуклеин и FAF1 измеряют вестерн-блоттингом с использованием анти-альфа-синуклеин антитела и FAF1 антитела, соответственно. Видно, что уровень альфа-синуклеина снижается при обработке ингибитором FAF1 KM-819, демонстрируя, что ингибитор FAF1 уменьшает накопление альфа-синуклеина у животных (фигура 16).
ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
[0080] Вариант осуществления изобретения 1: Способ лечения заболевания или состояния, возникающего вследствие синуклеинопатий, включающий введение субъекту, имеющему симптомы или подверженному риску указанных синуклеинопатий, эффективного количества ингибитора активности FAF1, повышающего количество альфа-синуклеина, или эффективного количества ингибитора активности FAF1 в отношении регулирования количеств LC-3 и p62.
[0081] Вариант осуществления изобретения 2: Способ по варианту осуществления изобретения 1, в котором ингибитор активности FAF1 представляет собой аминопиразольное соединение формулы 1 или его фармацевтически приемлемую соль:
 ,
,
где R1 представляет собой -CO2R3, -CH2OR3, -CONR3R4 или
 ,
,
где R3 и R4 независимо друг от друга представляют собой H или прямой, разветвленный или циклический C1-C6 алкил; R2 представляет собой -(CH2)2-фенил; B представляет собой H, фенил или C1-C3 алкил- или галогензамещенный фенил; n обозначает целое число от 0 до 2; Y представляет собой S, O, CH2, SO, SO2 или NR3R4, где R3 и R4 независимо друг от друга представляют собой H или прямой, разветвленный или циклический C1-C6 алкил; Z представляет собой H, галоген, OCH3, NO2, NH2 или прямой, разветвленный или циклический C1-C3 алкил; и A представляет собой CH или N.
[0082] Вариант осуществления изобретения 3: Способ по варианту осуществления изобретения 1, в котором аминопиразольное соединение представляет собой 4-[2-(4-бромфенилсульфанил)ацетиламино]-1-фенэтил-1H-пиразол-3-карбоновую кислоту или ее сложный эфир или амид.
[0083] Вариант осуществления изобретения 4: Способ лечения заболевания или состояния, возникающего вследствие синуклеинопатий, включающий введение субъекту, имеющему симптомы или подверженному риску возникновения указанных синуклеинопатий, такого количества соединения, связывающегося с белком FAF1, которое является эффективным для уменьшения количества α-синуклеина, который фосфорилируется по аминокислоте S129 в клетках указанного субъекта.
[0084] Вариант осуществления изобретения 5: Способ по варианту осуществления изобретения 4, в котором соединение, которое связывается с белком FAF1, представляет собой аминопиразольное соединение формулы 1 или его фармацевтически приемлемую соль:
 ,
,
где R1 представляет собой -CO2R3, -CH2OR3, -CONR3R4 или
 ,
,
где R3 и R4 независимо друг от друга представляют собой H или прямой, разветвленный или циклический C1-C6 алкил; R2 представляет собой -(CH2)2-фенил; B представляет собой H, фенил или C1-C3 алкил- или галогензамещенный фенил; n обозначает целое число от 0 до 2; Y представляет собой S, O, CH2, SO, SO2 или NR3R4, где R3 и R4 независимо друг от друга представляют собой H или прямой, разветвленный или циклический C1-C6 алкил; Z представляет собой H, галоген, OCH3, NO2, NH2 или прямой, разветвленный или циклический C1-C3 алкил; и A представляет собой CH или N.
[0085] Вариант осуществления изобретения 6: Способ по варианту осуществления изобретения 4, в котором аминопиразольное соединение представляет собой 4-[2-(4-бромфенилсульфанил)ацетиламино]-1-фенэтил-1H-пиразол-3-карбоновую кислоту или ее сложный эфир или амид.
[0086] Вариант осуществления изобретения 7: Способ по любому из вариантов осуществления изобретения от 1 до 3, в котором ингибитор FAF1 вводится перорально, или инъекцией в мозг или кровь, или через кожу.
[0087] Вариант осуществления изобретения 8: Способ по любому из вариантов осуществления изобретения от 4 до 6, в котором соединение, которое связывается с белком FAF1, вводится перорально, или инъекцией в мозг или кровь, или через кожу, или другими общеизвестными практическими способами, в которых FAF1-связывающее соединение вводится перорально.
[0088] Вариант осуществления изобретения 9: Способ диагностики синуклеинопатии или оценки риска возникновения синуклеинопатии у субъекта, включающий измерение активности FAF1 или уровня FAF1 в отношении ингибирования аутофагии, включая белки LC-3 и p62 в клетках субъекта или в любом другом образце от субъекта, где уровень активности или уровень белка FAF1 выше, чем у нормальных людей, что указывает на развитие синуклеинопатии или на риск развития у субъекта синуклеинопатии.
[0089] Вариант осуществления изобретения 10: Способ лечения у субъекта заболевания или состояния, возникающего вследствие синуклеинопатий, включающий введение субъекту, у которого проявляется в клетках указанного субъекта активность FAF1 или уровень FAF1 в отношении ингибирования аутофагии, опосредуемой белками LC-3 и p62 в клетках субъекта, где уровень активности или уровень белка FAF1 выше, чем у нормальных людей, что указывает на развитие синуклеинопатий или на риск развития у субъекта синуклеинопатий, такого количества соединения, связывающегося с белком FAF1, которое является эффективным для уменьшения количества α-синуклеина, который фосфорилируется по аминокислоте S129 в клетках указанного субъекта.
[0090] Вариант осуществления изобретения 11. Способ по варианту осуществления изобретения 10, в котором вводится аминопиразольное соединение формулы 1 или его фармацевтически приемлемая соль:

где R1 представляет собой -CO2R3, -CH2OR3, -CONR3R4 или

где R3 и R4 независимо друг от друга представляют собой H или прямой, разветвленный или циклический C1-C6 алкил; R2 представляет собой -(CH2)2-фенил; B представляет собой H, фенил или C1-C3 алкил- или галогензамещенный фенил; n обозначает целое число от 0 до 2; Y представляет собой S, O, CH2, SO, SO2 или NR3R4, где R3 и R4 независимо друг от друга представляют собой H или прямой, разветвленный или циклический C1-C6 алкил; Z представляет собой H, галоген, OCH3, NO2, NH2 или прямой, разветвленный или циклический C1-C3 алкил; и A представляет собой CH или N.
[0091] Вариант осуществления изобретения 12: Способ получения лекарственного средства, включающий смешивание аминопиразольного соединения формулы 1 или его фармацевтически приемлемой соли:
 ,
,
где R1 представляет собой -CO2R3, -CH2OR3, -CONR3R4 или
 ,
,
где R3 и R4 независимо друг от друга представляют собой H или прямой, разветвленный или циклический C1-C6 алкил; R2 представляет собой -(CH2)2-фенил; B представляет собой H, фенил или C1-C3 алкил- или галогензамещенный фенил; n обозначает целое число от 0 до 2; Y представляет собой S, O, CH2, SO, SO2 или NR3R4, где R3 и R4 независимо друг от друга представляют собой H или прямой, разветвленный или циклический C1-C6 алкил; Z представляет собой H, галоген, OCH3, NO2, NH2 или прямой, разветвленный или циклический C1-C3 алкил; и A представляет собой CH или N; и фармацевтически приемлемого носителя.
[0092] Вариант осуществления изобретения 13: Способ по варианту осуществления изобретения 12, где лекарственное средство предназначено для лечения у субъекта заболевания или состояния, возникающего вследствие синуклеинопатий.
[0093] Вариант осуществления изобретения 14: Применение аминопиразольного соединения формулы 1 или его фармацевтически приемлемой соли:
 ,
,
где R1 представляет собой -CO2R3, -CH2OR3, -CONR3R4 или
 ,
,
где R3 и R4 независимо друг от друга представляют собой H или прямой, разветвленный или циклический C1-C6 алкил; R2 представляет собой -(CH2)2-фенил; B представляет собой H, фенил или C1-C3 алкил- или галогензамещенный фенил; n обозначает целое число от 0 до 2; Y представляет собой S, O, CH2, SO, SO2 или NR3R4, где R3 и R4 независимо друг от друга представляют собой H или прямой, разветвленный или циклический C1-C6 алкил; Z представляет собой H, галоген, OCH3, NO2, NH2 или прямой, разветвленный или циклический C1-C3 алкил; для лечения у субъекта заболевания или состояния, возникающего вследствие синуклеинопатий.
[0094] Вариант осуществления изобретения 15: Применение по варианту осуществления изобретения 14, в котором аминопиразольное соединение является эффективным для ингибирования активности FAF1 в отношении повышения количества альфа-синуклеина в клетке субъекта или в клетке образца от субъекта, или является эффективным для повышения аутофагии, опосредованной белками LC-3 и p62, в клетке субъекта или в клетке образца от субъекта, или является эффективным для уменьшения количества α-синуклеина, который фосфорилируется по аминокислоте S129 в клетке субъекта или в клетке образца от субъекта.
ССЫЛОЧНАЯ ЛИТЕРАТУРА
Appel-Cresswell S, Vilarino-Guell C, Encarnacion M, Sherman H, Yu I, Shah B, Weir D, Thompson C, Szu-Tu C, Trinh J, Aasly JO, Rajput A, Rajput AH, Jon Stoessl A, Farrer MJ. 2013. Alpha-synuclein p.H50Q, a novel pathogenic mutation for Parkinson's disease. Mov. Disord. 28, 811-3.
Angot E, Steiner JA, Lema Tome CM, Ekstrom P, Mattsson B, Bjorklund A, Brundin P. 2012. Alpha-synuclein cell-to-cell transfer and seeding in grafted dopaminergic neurons in vivo. PloS ONE 7:e39465.
Betarbet R, Anderson LR, Gearing M, Hodges TR, Fritz JJ, Lah JJ, Levey AI. 2008. Fas-associated factor 1 and Parkinson's disease. Neurobiol. Dis. 31, 309-15.
Cullen V, Sardi SP, Ng J, Xu YH, Sun Y, Tomlinson JJ, Kolodziej P, Kahn I, Saftig P, Woulfe J, Rochet JC, Glicksman MA, Cheng SH, Grabowski GA, Shihabuddin LS, Schlossmacher MG. 2011. Acid β-glucosidase mutants linked to Gaucher disease, Parkinson disease, and Lewy body dementia alter α-synuclein processing. Ann. Neurol. 69, 940-53.
Devine MJ, Gwinn K, Singleton A, Hardy J. 2011. Parkinson's disease and α-synuclein expression. Mov. Disord. 26, 2160-8.
Federoff M, Schottlaender LV, Houlden H, and Singleton A. 2015 Multiple system atrophy: the application of genetics in understanding etiology. Clin. Auton. Res. 25, 19-36.
Feng LR, Federoff HJ, Vicini S, and Maguire-Zeiss KA. 2010. Alpha-synuclein mediates alterations in membrane conductance: a potential role for alpha-synuclein oligomers in cell vulnerability. Eur.J.Neurosci. 32, 10-17.
Fernandes HJ, Hartfield EM, Christian HC, Emmanoulidou E, Zheng Y, Booth H, Bogetofte H, Lang C, Ryan BJ, Sardi SP, Badger J, Vowles J, Evetts S, Tofaris GK, Vekrellis K, Talbot K, Hu MT, James W, Cowley SA, Wade-Martins R. 2016. ER stress and autophagic perturbations lead to elevated extracellular α-synuclein in GBA-N370S Parkinson's iPSC-derived dopamine neurons. Stem Cell Reports. 6, 342-56.
Gallegos S, Pacheco C, Peters C, Opazo CM2, Aguayo LG. 2015. Features of alpha-synuclein that could explain the progression and irreversibility of Parkinson's disease. Front Neurosci. 9, 59.
Gao X, Liu W, Huang L, Zhang T, Mei Z, Wang X, Gong J, Zhao Y, Xie F, Ma J, Qian L. 2015. HSP70 inhibits stress-induced cardiomyocyte apoptosis by competitively binding to FAF1. Cell Stress Chaperones. 20, 653-61.
Geser F, Wenning GK, Poewe W, McKeith I. 2005. How to diagnose dementia with Lewy bodies: state of the art. Mov. Disord. 12, S11-20.
Gilman S, Wenning GK, Low PA, Brooks DJ, Mathias CJ, Trojanowski JQ, Wood NW, Colosimo C, Durr A, Fowler CJ, Kaufmann H, Klockgether T, Lees A, Poewe W, Quinn N, Revesz T, Robertson D, Sandroni P, Seppi K, Vidailhet M. 2008. Second consensus statement on the diagnosis of multiple system atrophy. Neurology 71, 670-676.
Goedert M, Jakes R, and Spillantinib MG. 2017. The Synucleinopathies: twenty years on. J. Parkinsons Dis. 7, S51-S69.
Ingelsson M. 2016. Alpha-synuclein oligomers-neurotoxic molecules in Parkinson's Disease and other Lewy Body disorders. Frontiers in Neuroscience Volume10, Article408
Jankovic J. 2008. Parkinson’s disease: clinical features and diagnosis. J. Neurol. Neurosurg. Psychiatry 79, 368-376.
Jellinger KA. 2003. Neuropathological spectrum of synucleinopathies. Mov. Disord. 6, S2-12.
 , Huertas I, Bernal-Bernal I, Bonilla-Toribio M,
, Huertas I, Bernal-Bernal I, Bonilla-Toribio M,  MT,
MT,  ,
,  , Carrillo F,
, Carrillo F,  , Carballo M,
, Carballo M,  , Mir P. 2016. GBA variants Influence motor and non-motor features of Parkinson's disease. PLoS One. 11:e0167749.
, Mir P. 2016. GBA variants Influence motor and non-motor features of Parkinson's disease. PLoS One. 11:e0167749.
Kalinderi K, Bostantjopoulou S, Fidani L. 2016. The genetic background of Parkinson’s disease: current progress and future prospects. Acta Neurol. Scand. 134: 314-326.
Kasten M, Klein C. 2013. The many faces of alpha-synuclein mutations. Mov. Disord. 28, 697-701.
Kim HJ, Song EJ, Lee YS, Kim E, Lee KJ. 2005. Human Fas-associated factor 1 interacts with heat shock protein 70 and negatively regulates chaperone activity. J. Biol. Chem. 280, 8125-33.
Kuzdas-Wood D, Stefanova N, Jellinger KA, Seppi K, Schlossmacher MG, Poewe W, Wenning GK. 2014. Towards translational therapies for multiple system atrophy. Progress in Neurobiology 118, 19-35.
Lee MK, Stirling W, Xu Y, Xu X, Qui D, Mandir AS, Dawson TM, Copeland NG, Jenkins NA, Price DL. 2002. Human -synuclein-harboring familial Parkinson’s disease-linked Ala-53 Thr mutation causes neurodegenerative disease with alpha--synuclein aggregation in transgenic mice. PNAS 99, 8968-8973.
Langenickel, T.H., et al. 2016. The effect of LCZ696 (sacubitril/valsartan) on amyloid-β concentrations in cerebrospinal fluid in healthy subjects. Br. J. Clin Pharmacol. 81, 878-890.
Luk KC, Kehm V, Carroll J, Zhang B, O’Brien P, Trojanowski JQ, Lee VM. 2012. Pathological α-synuclein transmission initiates Parkinson-like neurodegeneration in nontransgenic mice. Science 338, 949-953.
 MJ, Tolosa E, Campdelacreu J. 2003. Clinical overview of the synucleinopathies. Mov. Disord. 6:S21-7.
MJ, Tolosa E, Campdelacreu J. 2003. Clinical overview of the synucleinopathies. Mov. Disord. 6:S21-7.
Mata IF, Shi M, Agarwal P, Chung KA, Edwards KL, Factor SA, Galasko DR, Ginghina C, Griffith A, Higgins DS, Kay DM, Kim H, Leverenz JB, Quinn JF, Roberts JW, Samii A, Snapinn KW, Tsuang DW, Yearout D, Zhang J, Payami H, Zabetian CP. 2010. SNCA variant associated with Parkinson disease and plasma -synuclein level. Arch Neurol. Nov;67(11):1350-6.
Nussbaum RL. 2017. Genetics of synucleinopathies. Cold Spring Harb Perspect Med. pii: a024109.
Oueslati A. 2016. Implication of alpha-synuclein phosphorylation at S129 in synucleinopathies: What have we learned in the last decade? J. Parkinsons Dis. 6, 39-51.
Petrucci S, Ginevrino M, Valente EM. 2016. Phenotypic spectrum of alpha-synuclein mutations: New insights from patients and cellular models. Parkinsonism Relat. Disord. 1:S16-20.
Rockenstein E, Nuber S, Overk CR, Ubhi K, Mante M, Patrick C, Adame A, Trejo-Morales M, Gerez J, Picotti P, Jensen PH, Campioni S, Riek R, Winkler J, Gage FH, Winner B, Masliah E. 2014. Accumulation of oligomer-prone a-synuclein exacerbates synaptic and neuronal degeneration in vivo. Brain 137, 1496-1513.
Ryu SW, Lee SJ, Park MY, Jun JI, Jung YK, Kim E. 2003. Fas-associated factor 1, FAF1, is a member of Fas death-inducing signaling complex. J. Biol. Chem. 278, 24003-10.
Sampaio-Marques B and Ludovico P. 2015. Sirtuins and proteolytic systems: implications for pathogenesis of synucleinopathies. Biomolecules 5, 735-757.
Sato, H, Kato, T, and Arawaka, S. 2013. The role of Ser129 phosphorylation of α synuclein in neurodegeneration of Parkinson’s disease: a review of in vivo models. Rev. Neurosci. 24,115-123.
Snead D, Eliezer D. 2014. Alpha-synuclein function and dysfunction on cellular membranes. Exp. Neurobiol. 23,292-313.
Spillantini MG, Schmidt ML, Lee VMY, Trojanowski JQ, Jakes R, and Goedert M. 1997. Alpha-synuclein in Lewy bodies. Nature, 388, 839-840.
Spillantini MG, Crowther RA, Jakes R, Hasegawa M, and Goedert M. 1998. Alpha-synuclein in filamentous inclusions of Parkinson’s disease and dementia with Lewy bodies. Proc Natl Acad Sci USA , 95, 6469-6473.
Spillantini MG, Goedert M. 2000. The alpha-synucleinopathies: Parkinson's disease, dementia with Lewy bodies, and multiple system atrophy. Ann N Y Acad Sci. 920, 16-27.
Stefanova N, Bucke P, Duerr S, Wenning GK. 2009. Multiple system atrophy: an update. Lancet Neurol. 8, 1172-1178.
Sul JW, Park MY, Shin J, Kim YR, Yoo SE, Kong YY, Kwon KS, Lee YH, Kim E. 2013. Accumulation of the parkin substrate, FAF1, plays a key role in the dopaminergic neurodegeneration. Hum. Mol. Genet. 2013 Apr 15;22(8):1558-73.
Sidransky E, Nalls MA, Aasly JO, Aharon-Peretz J, Annesi G, Barbosa ER, Bar-Shira A, Berg D, Bras J, Brice A, Chen CM, Clark LN, Condroyer C, De Marco EV,  , Eblan MJ, Fahn S, Farrer MJ, Fung HC, Gan-Or Z, Gasser T, Gershoni-Baruch R, Giladi N, Griffith A, Gurevich T, Januario C, Kropp P, Lang AE, Lee-Chen GJ, Lesage S, Marder K, Mata IF, Mirelman A, Mitsui J, Mizuta I, Nicoletti G, Oliveira C, Ottman R, Orr-Urtreger A, Pereira LV, Quattrone A, Rogaeva E, Rolfs A, Rosenbaum H, Rozenberg R, Samii A, Samaddar T, Schulte C, Sharma M, Singleton A, Spitz M, Tan EK, Tayebi N, Toda T, Troiano AR, Tsuji S, Wittstock M, Wolfsberg TG, Wu YR, Zabetian CP, Zhao Y, Ziegler SG. 2009. Multicenter analysis of glucocerebrosidase mutations in Parkinson’s disease. N. Engl. J. Med. 361, 1651-1661.
, Eblan MJ, Fahn S, Farrer MJ, Fung HC, Gan-Or Z, Gasser T, Gershoni-Baruch R, Giladi N, Griffith A, Gurevich T, Januario C, Kropp P, Lang AE, Lee-Chen GJ, Lesage S, Marder K, Mata IF, Mirelman A, Mitsui J, Mizuta I, Nicoletti G, Oliveira C, Ottman R, Orr-Urtreger A, Pereira LV, Quattrone A, Rogaeva E, Rolfs A, Rosenbaum H, Rozenberg R, Samii A, Samaddar T, Schulte C, Sharma M, Singleton A, Spitz M, Tan EK, Tayebi N, Toda T, Troiano AR, Tsuji S, Wittstock M, Wolfsberg TG, Wu YR, Zabetian CP, Zhao Y, Ziegler SG. 2009. Multicenter analysis of glucocerebrosidase mutations in Parkinson’s disease. N. Engl. J. Med. 361, 1651-1661.
Trojanowski JQ, Revesz T. 2007. Proposed neuropathological criteria for the post mortem diagnosis of multiple system atrophy. Neuropathol. Appl. Neurobiol. 33, 615-620.
Walden H, and Muqit MMK. 2017. Ubiquitin and Parkinson’s disease through the looking glass of genetics. Biochemical Journal 474, 1439-1451.
Soldner F, Stelzer Y, Shivalila CS, Abraham BJ, Latourelle JC, Barrasa MI, Goldmann J, Myers RH, Young RA, Jaenisch R. 2016. Parkinson-associated risk variant in distal enhancer of α-synuclein modulates target gene expression. Nature 533, 95-9.
Wang T, Hay JC. 2015. Alpha-synuclein toxicity in the early secretory pathway: How it drives neurodegeneration in Parkinsons disease. Frontiers in Neuroscience Volume 9, Article 433.
Wang C, Chan P. 2014. Clinicogenetics of Parkinson’s disease: a drawing but not completed picture. Neuroimmunol. Neuroinflammation 1, 115-126.
Yoo SE, Yu C, Jung S, Kim E, Kang NS. 2016. Design and synthesis of fluorescent and biotin tagged probes for the study of molecular actions of FAF1 inhibitor. Bioorg. Med. Chem. Lett. 26, 1169-72.
Yu C, Kim BS, Kim E. 2016. FAF1 mediates regulated necrosis through PARP1 activation upon oxidative stress leading to dopaminergic neurodegeneration. Cell Death Differ. 23, 1873-1885.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Kainos Medicine
<120> Модуляторы альфа-синуклеина
<130> 400514-20005
<140> PCT/IB2018/000766
<141> 2018-06-19
<160> 1
<170> PatentIn version 3.5
<210> 1
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> альфа-синуклеин антисмысловой РНК
<400> 1
guguuguggc acaaaccau 19
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛА, СВЯЗЫВАЮЩИЕСЯ С ПРОТОФИБРИЛЛАМИ, И ИХ ПРИМЕНЕНИЕ В МЕТОДАХ ТЕРАПИИ И ДИАГНОСТИКИ БОЛЕЗНИ ПАРКИНСОНА, ДЕМЕНЦИИ, АССОЦИИРОВАННОЙ С ОБРАЗОВАНИЕМ ДИФФУЗНЫХ ТЕЛЕЦ ЛЕВИ, И ДРУГИХ АЛЬФА-СИНУКЛЕИНОПАТИЙ | 2011 |
|
RU2555526C2 |
| Способ диагностики болезни Паркинсона с деменцией | 2024 |
|
RU2838286C1 |
| СОЕДИНЕНИЯ, КОМПОЗИЦИИ И СПОСОБЫ, ПРЕДНАЗНАЧЕННЫЕ ДЛЯ ЛЕЧЕНИЯ БЕТА-АМИЛОИДНЫХ ЗАБОЛЕВАНИЙ И СИНУКЛЕИНОПАТИЙ | 2009 |
|
RU2501792C2 |
| АНТИТЕЛА К АЛЬФА-СИНУКЛЕИНУ И ВАРИАНТЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2812765C2 |
| СРЕДСТВА, ПУТИ ПРИМЕНЕНИЯ И СПОСОБЫ ЛЕЧЕНИЯ СИНУКЛЕОПАТИИ | 2016 |
|
RU2765303C2 |
| АНТИТЕЛА ПРОТИВ АЛЬФА-СИНУКЛЕИНА | 2018 |
|
RU2787039C2 |
| НОВЫЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА ДЛЯ ИНГИБИРОВАНИЯ АГРЕГАЦИИ БЕЛКОВ, ВОВЛЕЧЕННЫХ В ЗАБОЛЕВАНИЯ, СВЯЗАННЫЕ С АГРЕГАЦИЕЙ БЕЛКОВ, И НЕЙРОДЕГЕНЕРАТИВНЫЕ ЗАБОЛЕВАНИЯ | 2009 |
|
RU2531915C2 |
| ГУМАНИЗИРОВАННЫЕ АНТИТЕЛА, КОТОРЫЕ РАСПОЗНАЮТ АЛЬФА-СИНУКЛЕИН | 2012 |
|
RU2575629C2 |
| ПРИМЕНЕНИЕ МИМЕОТОПОВ АЛЬФА-СИНУКЛЕИНОВЫХ ЭПИТОПОВ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, СВЯЗАННЫХ С ТЕЛЬЦАМИ ЛЕВИ | 2010 |
|
RU2532351C2 |
| ПЕПТИДНЫЕ ИММУНОГЕНЫ ИЗ С-ТЕРМИНАЛЬНОГО КОНЦА БЕЛКА АЛЬФА-СИНУКЛЕИНА И СОСТАВЫ НА ИХ ОСНОВЕ ДЛЯ ЛЕЧЕНИЯ СИНУКЛЕИНОПАТИЙ | 2018 |
|
RU2810774C2 |



Изобретение относится к применению аминопиразольного соединения 4-[2-(4-бромфенилсульфанил)ацетиламино]-1-фенэтил-1Н-пиразол-3-карбоновой кислоты или ее фармацевтически приемлемой соли или композиции указанного аминопиразольного соединения или его фармацевтически приемлемой соли для получения лекарственного средства для лечения или для лечения альфа-синуклеинопатии: вызванной тельцами Леви, невритами Леви или агрегатами α-синуклеина в нейронах и глие; или вызванной мутацией в гене альфа-синуклеина (SNCA); или опосредованной активностью FAF1 в отношении регулирования количеств LC-3 и р62, активностью FAF1 в отношении регулирования количества α-синуклеина, или опосредованной количеством агрегированного α-синуклеина, или опосредованной количеством α-синуклеина, который фосфорилируется по аминокислоте S129 в клетках указанного субъекта; или вызванной накоплением неправильно свернутого альфа синуклеина или накоплением агрегатов альфа-синуклеина в клетках указанного субъекта. Технический результат: эффективное лечение альфа-синуклеинопатии, вызванной указанными выше причинами. 2 н. и 6 з.п. ф-лы, 16 ил.
1. Применение аминопиразольного соединения 4-[2-(4-бромфенилсульфанил)ацетиламино]-1-фенэтил-1Н-пиразол-3-карбоновой кислоты или ее фармацевтически приемлемой соли или композиции указанного аминопиразольного соединения или его фармацевтически приемлемой соли;
для получения лекарственного средства для лечения альфа-синуклеинопатии:
вызванной тельцами Леви, невритами Леви или агрегатами α-синуклеина в нейронах и глие; или вызванной мутацией в гене альфа-синуклеина (SNCA); или
опосредованной активностью FAF1 в отношении регулирования количеств LC-3 и р62, активностью FAF1 в отношении регулирования количества α-синуклеина, или
опосредованной количеством агрегированного α-синуклеина, или
опосредованной количеством α-синуклеина, который фосфорилируется по аминокислоте S129 в клетках указанного субъекта; или
вызванной накоплением неправильно свернутого альфа-синуклеина или накоплением агрегатов альфа-синуклеина в клетках указанного субъекта.
2. Применение по п. 1, где аминопиразольное соединение или его фармацевтически приемлемая соль или композиция составлены для перорального введения, или для инъекции в мозг, или для инъекции в кровь.
3. Применение по п. 2, где состав обеспечивает от 1 до 10 мг/кг/сутки субъекту при введении.
4. Применение по любому из пп. 1-3, где альфа-синуклеинопатия представляет собой болезнь Паркинсона с деменцией (PDD), деменцию с тельцами Леви, множественную системную атрофию, атипичную болезнь Паркинсона и чистую вегетативную недостаточность.
5. Применение аминопиразольного соединения 4-[2-(4-бромфенилсульфанил)ацетиламино]-1-фенэтил-1Н-пиразол-3-карбоновой кислоты или ее фармацевтически приемлемой соли или композиции указанного аминопиразольного соединения или его фармацевтически приемлемой соли;
для лечения альфа-синуклеинопатии:
вызванной тельцами Леви, невритами Леви или агрегатами α-синуклеина в нейронах и глие; или вызванной мутацией в гене альфа-синуклеина (SNCA), или
опосредованной активностью FAF1 в отношении регулирования количеств LC-3 и р62, активностью FAF1 в отношении регулирования количества α-синуклеина, или
опосредованной количеством агрегированного α-синуклеина, или
опосредованной количеством α-синуклеина, который фосфорилируется по аминокислоте S129 в клетках указанного субъекта; или
вызванной накоплением неправильно свернутого альфа-синуклеина или накоплением агрегатов альфа-синуклеина в клетках указанного субъекта.
6. Применение по п. 5, где аминопиразольное соединение или его фармацевтически приемлемая соль или композиция составлены для перорального введения, или для инъекции в мозг, или для инъекции в кровь.
7. Применение по п. 6, где состав обеспечивает от 1 до 10 мг/кг/сутки субъекту при введении.
8. Применение по любому из пп. 5-7, где альфа-синуклеинопатия представляет собой болезнь Паркинсона с деменцией (PDD), деменцию с тельцами Леви, множественную системную атрофию, атипичную болезнь Паркинсона и чистую вегетативную недостаточность.
| WO 2008051047 A1, 02.05.2008 | |||
| Jeong, J.-W | |||
| et al | |||
| Способ наплавки твердых сплавов тина Вокар или Стеллит на рабочую часть инструмента для вращательного бурения | 1932 |
|
SU33493A1 |
| Горный компас | 0 |
|
SU81A1 |
| Betarbet, R | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2023-06-07—Публикация
2018-06-19—Подача