Изобретение относится к процессу и катализаторам селективного окисления аммиака до азота и может найти применение при использовании аммиака как источника альтернативного топлива.
С каждым годом человечество все больше нуждается в энергии. В настоящее время основными источниками энергии в промышленности и транспортной отрасли, по-прежнему, являются уголь, нефть и природный газ, сжигание которых приводит к выделению оксидов углерода, азота, углеводородов, оказывающих негативное влияние на климат и здоровье человека. Исключительно важно разрабатывать и внедрять новые технологии в области энергетики, промышленности и транспорта, исключающие выбросы углекислого газа в атмосферу. Как известно, водород обладает большим потенциалом в использовании его в качестве энергоносителя с перспективным применением в энергетических системах. Однако, проблемы, связанные с хранением, распределением и развертыванием инфраструктуры, препятствуют его полному внедрению. Исследования и разработки в области применения аммиака, а именно, в использовании его в качестве безуглеродного носителя водорода, представляют все больший интерес в связи с экономическими и промышленными потребностями в экологически чистых источниках энергии. Так, перспективным считается применение аммиака в виде альтернативного топлива, особенно в газовых турбинах, промышленных печах и двигателях внутреннего сгорания [H. Kobayashi, A. Hayakawa, K.D.K.A. Somarathne, E.C. Okafor, Proc. Combust. Inst. 37 (2019) 109-133].
Аммиак обладает более высокой объемной плотностью энергии, до трех раз превышающую плотность водорода. Также, в отличие от водорода, аммиак легко сжижается, его удобно хранить и транспортировать. С точки зрения безопасности аммиак имеет более высокие показатели по сравнению с другими видами топлива, используемыми при транспортировке, такими как водород, бензин и пропан, при соблюдении некоторых мер предосторожности.
Основной проблемой, сдерживающей использование аммиака в качестве топлива, является образование оксидов азота - NОx (NO2, NO, N2O). Решением этой проблемы может быть переход к селективному каталитическому сжиганию аммиака до азота и воды, что одновременно обеспечит снижение температуры воспламенения аммиачно-воздушной смеси, более высокой, чем у углеводородно-воздушных смесей.
Большинство работ по каталитическому окислению аммиака касается либо высокотемпературного окисления аммиака до оксида азота NO, поскольку этот процесс лежит в основе технологической схемы получения азотной кислоты [М.М. Караваев, В.М. Олевский. Справочник азотчика, 2-е изд. - М.: Химия, 1987. 464], либо низкотемпературного окисления примесей аммиака до азота в процессах обезвреживания газовых выхлопов и сточных выбросов от аммиака [CA 2679599C, B01J 23/42, 04.09.2008]. Имеются также работы по селективному каталитическому окислению аммиака до закиси азота, используемой в медицинских целях [RU 2214863, B01J 23/34, 27.10.2003]. Авторы большого количества работ отмечают более высокую реакционную способность в процессе окисления аммиака благородных металлов Pt, Pd, Ru, Ir, Au и Ag [Qiulin Zhang, Tengxiang Zhang, et al. Appl. Surf. Sci. 500 (2020) 144044:1-11], содержание которых колеблется в пределах 0.5-4 мас.% для металлов платиновой группы. Упоминаются менее дорогие катализаторы, содержащие 5-15 мас.% переходных (Cu, Мо, V) [S. Shrestha. Catal. Today 267(2016) 130-144] или благородных (Au и Ag) [Mingyue Lin, Baoxiang An, et al. ACS Catal. 9, 3 (2019) 1753-1756] металлов. В качестве носителей катализаторов обычно используются Al2O3, Nb2O5, TiO2 и цеолиты. Упоминаются также оксидные катализаторы на основе редкоземельных элементов Ce, Zr, Nd, La, допированные различными переходными элементами [Jongsik Kim, Dong Ho Kim, et al. Applied Surface Science 518 (2020) 146238].
Из уровня техники известны активные и селективные каталитические системы для низкотемпературного (200-300°С) окисления обедненных воздушно-аммиачных смесей до азота и воды, однако возможность использования этих систем в качестве катализаторов селективного сжигания аммиака в концентрированных аммиачно-воздушных смесях до азота (как энергетического топлива для теплотехники, например, горелочные устройства) не изучена. Во-первых, следует учесть концентрационный диапазон горения аммиака (от 16 до 25 об.% в воздухе) [Mingyue Lin, Baoxiang An, et al. ACS Catal. 9, 3 (2019) 1753-1756], где, скорее всего, количество топлива должно соответствовать количеству кислорода в воздухе, необходимому для его полного сгорания до азота, т.е вблизи стехиометрического состава - это около 22% NH3. Во-вторых, катализатор должен быть термостабильным в условиях горения (при температурах до 900°С), поскольку это экзотермическая реакция. В-третьих, катализатор должен быть селективным в широком диапазоне температур.
Поэтому задача изобретения - разработка эффективного катализатора для процесса селективного окисления аммиака до азота в широком ряду температур и концентраций аммиака для его использования в горелочных устройствах.
Задача решается применением катализатора, который представляет собой алюминат меди со структурой шпинели и оксид меди при их соотношениях от 0.1 до 100 в форме гранул и характеризуется величиной удельной поверхности 30-150 м2/г, средним размером пор 3-16 нм, прочностью гранул на раздавливание 20-80 кг/см2.
Задача решается также способом получения предлагаемого катализатора селективного окисления аммиака до азота в форме гранул, включающим гидротермальную обработку водной суспензии рентгеноаморфного продукта центробежно-термической активации гиббсита и нитрата меди при 150°С при соотношении Ж:Т = 3:1 с получением геля, его экструзионное формование и термообработку при температуре не ниже 450°С, в результате чего получают гранулированный катализатор - алюминат меди со структурой шпинели и оксид меди при фазовом соотношении от 0.1 до 100 с требуемыми структурными характеристиками.
Задача решается также способом проведения процесса селективного окисления аммиака до азота с использованием заявляемого катализатора или приготовленного заявляемым способом, причем при стехиометрическом соотношении аммиака и кислорода при температурах 550-900 °С обеспечивается выход азота не менее 97%, а при селективном окислении аммиака до азота в смеси с избытком кислорода при температурах 450-900 °С обеспечивается выход азота 70-80%.
Для сравнения выбраны известные промышленные катализаторы нанесенного типа AOK-78-22 (Pd/Al2O3) и ИК-42-1 (CuO/Al2O3), химический состав которых наиболее близко соответствует известным активным в низкотемпературном окислении обедненных аммиачно-воздушных смесей до азота изученным в литературе каталитическим системам [CA 2679599C, B01J 23/42, 04.09.2008].
Алюминат меди со структурой шпинели может быть приготовлен различными методами, такими как керамический [Yajie Liu, Shaojun Qing, et al. J. materials and aplications. 7:2 (2018) P. 82-89], соосаждение [Mimani T. J. Alloy Comp. (2001) 315:123-128] или золь-гель метод [M.Salavati-Niasari, F. Davar, M. Farhadi. J. Sol-Gel Sci. Technol. 51 (2009) 48-52]. Недостатком керамического метода приготовления является высокая температура и длительное время термообоработки исходных реагентов, что приводит к низким величинам удельной поверхности. «Мокрые» методы позволяют получать высокодисперсные сложные оксиды, однако они многостадийны и характеризуются наличием большого количества водных стоков.
Известен бессточный способ приготовления алюмината магния с высокой удельной поверхностью путем гидротермальной обработки водной суспензии продукта термоактивации гиббсита и нитрата магния с последующим прокаливанием продукта взаимодействие при 500-550°С [RU 2735668, C01F 7/16, 05.11.2020].
В предлагаемом изобретении алюминат меди получают гидротермальной обработкой водной суспензии продукта термоактивации гиббсита и нитрата меди с последующим прокаливанием продукта взаимодействия при 450-850°С. В качестве исходного алюминий-содержащего реагента используют рентгеноаморфный продукт центробежной термической активации гиббсита ЦТА-ГБ [RU 2237019, C01F 7/02, 27.09.2004]. В качестве исходного Cu-содержащего соединения используют трехводную соль азотнокислой меди Cu(NO3)2·3H2O, которую растворяют, получая водный раствор с необходимой концентрацией катионов меди.
Синтез катализатора проводят путем гидротермальной обработки водной суспензии ЦТА-ГБ и азотнокислой меди при 150°C в течение 4-х часов при мольном соотношении катионов в обрабатываемой суспензии Al/Cu=2, что соответствует стехиометрическому соотношению катионов в шпинели «нормального» состава CuAl2O4. Соотношение Ж/Т в суспензии составляет около 3, а величина pH водного раствора соли азотнокислой меди - 4.0÷4.2. После гидротермальной обработки образец представляет собой гель/пасту, который, не отмывая, подвергают экструзионному формованию, полученные экструдаты сушат при 110°C в течение 6 ч. Конечную термообработку проводят при температурах 450-850°C, в течение 4 ч в муфельной печи на воздухе, получая гранулы катализатора, содержащего алюминат меди и оксид меди, соотношение которых зависит от температуры прокаливания.
Каталитическую активность образцов в реакции окисления аммиака определяют для фракции 0.25-0.50 мм в установке с проточным реактором при температурах 250-900°С и времени контакта 0.18 с. Эксперименты проводят с использованием двух реакционных смесей, отличающихся соотношением аммиака и кислорода. В смеси с избытком кислорода соотношение NH3/O2 = 0.13 (2.1%NH3 в He, 15.5%O2 воздуха), а смесь, имеющая соотношение NH3/O2 = 1.54 (8.3%NH3, 5.4%O2 в Ar) близка к стехиометрической. Стехиометрическое соотношение при окислении аммиака до азота предполагает мольное соотношение NH3/O2 = 1.3 согласно реакции 4NH3 + 3O2 = 2N2 + 6H2O. Состав исходной газовой смеси и продуктов превращения определяют на входе и на выходе из реактора в режиме on-line при температуре 120°С с помощью ИК-фурье-спектрометра «ФТ-801».
Перед исследованиями активности катализаторов выполнены контрольные эксперименты по окислению аммиака в реакторе без катализатора (в присутствии кварцевого наполнителя, фракция 0.5-0.25мм) при разных температурах. В стехиометрической смеси (NH3/O2 = 1.5) гомогенная реакция окисления аммиака до N2 начинается при температурах выше 600°С и 100% конверсия аммиака достигается при 900°С.
Степень конверсии аммиака рассчитывают по формуле:
XNH3 , % = 100%* (CNH3 (разложившегося газа) / CNH3 (исходная конц. газа))
Селективность по продуктам реакции:
Si, % = 100% *(Ci ·ni / ƩCi ·ni)
Выход N2 :
YN2, % = 100% *(XNH3* SN2),
где Ci - концентрация (мол.%), ni - стехиометрический коэффициент.
Сущность изобретения иллюстрируется следующими примерами
Пример 1
Продукт термоактивации гиббсита (содержание аморфной фазы 95%, бемита -5%, ППП-~4%), измельченный до среднего размера частиц ~ 30 мкм (ППП= ~4%) помещают в реактор высокого давления, добавляют раствор нитрата меди с концентрацией 350 г/л Сu, (pH раствора соли составляет около 4.5) и при соотношении жидкой и твердой фаз Ж:Т=3:1, образующуюся суспензию перемешивают и выдерживают при 1500C в течение 4 ч. Полученный концентрированный гель/пасту формуют экструзией, получая экструдаты диаметром 4мм. Далее образцы сушат при 110°С и затем прокаливают при 450°С. Гранулы имеет удельную поверхность по БЭТ 142 м2/г, суммарный объем пор 0.28 см3/г и средний диаметр пор 3.6 нм. Фазовый состав образца после термообработки при 450°С соответствует смеси фаз шпинели СuAl2O4 (следы) и оксида меди CuO в соотношении 10:90 (СuAl2O4 / CuO ~0.1), прочность 20 кг/см2.
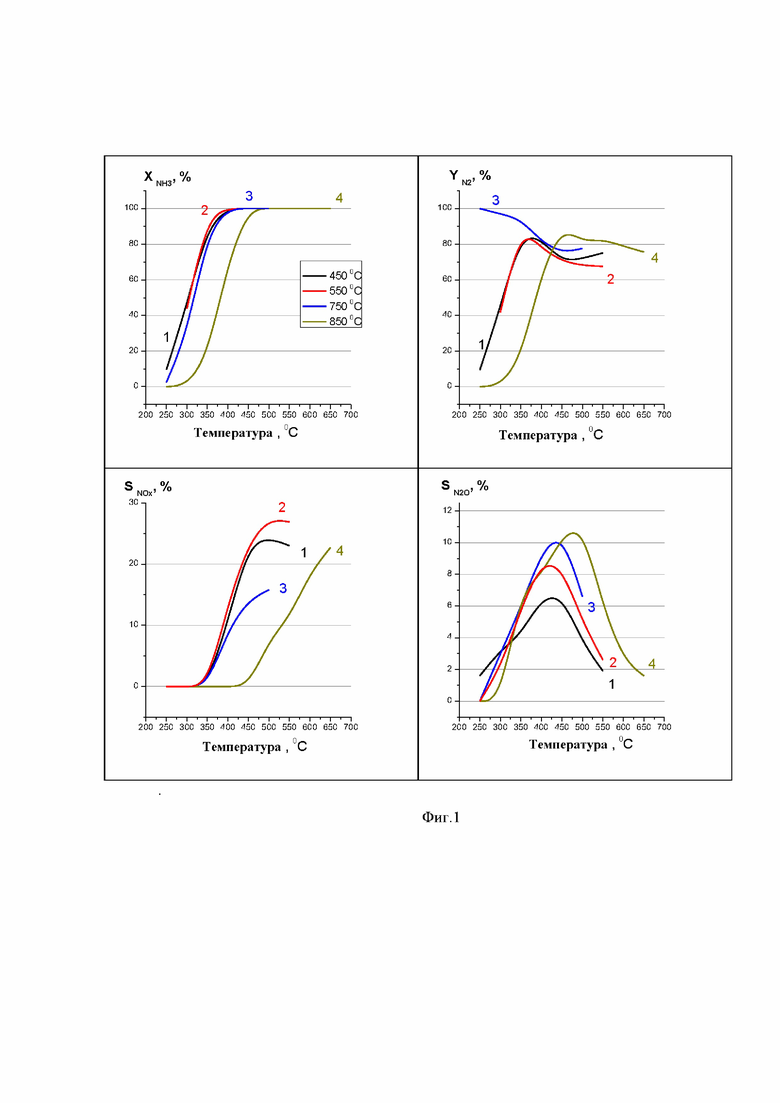
Результаты испытаний образцов катализатора в процессе селективного окисления аммиака в смеси с избытком кислорода в виде температурной зависимости конверсии NH3, выхода N2, селективностей NOx и N2O, представлены на Фиг.1, кривая 1. Испытания проведены для образцов, прокаленных при разных температурах; температуры прокаливания обозначены на рисунке: кривая 1- образец прокален при 450°С, кривая 2 - образец прокален при 550°С, кривая 3-образец прокален при 750°С, кривая 4-образец прокален при 850°С. Условия процесса: NH3/O2 = 0.13 (2.1%NH3 в He, 15.5%O2 воздуха), τ = 0.18 c (V кат.=0.2 мл).
Эксперименты показывают (фиг. 1, кривая 1), что при повышении температуры испытаний степень конверсии аммиака увеличивается и при температуре ~ 400°С достигается 100%-конверсия аммиака в реакционной смеси аммиака с избытком кислорода, при этом достигается и максимальный выход азота ~ 80%. При дальнейшем увеличении температуры испытаний до 900 °С выход азота снижается до 70% за счет увеличения селективности по NO. В стехиометрической смеси аммиака и кислорода при температуре 400°С также достигается полная конверсия аммиака при этом достигается максимальный выход азота ~ 97%, который при дальнейшем увеличении температуры испытаний практически не снижается.
Пример 2
Катализатор готовят аналогично примеру 1 с тем отличием, что экструдаты прокаливают при 550°С, при этом фазовый состав гранул образца не изменяется, увеличивается доля фазы шпинели до соотношения 40:6 (СuAl2O4 / CuO ~6,6), образец имеет удельную поверхность по БЭТ 87 м2/г, общий объем пор 0.23 см3/г и средний диаметр пор 0.38 нм, прочность 30 кг/см2.
Испытания катализатора в процессе селективного окисления аммиака в смеси с избытком кислорода проводят аналогично примеру 1 (фиг. 1, кривая 2).
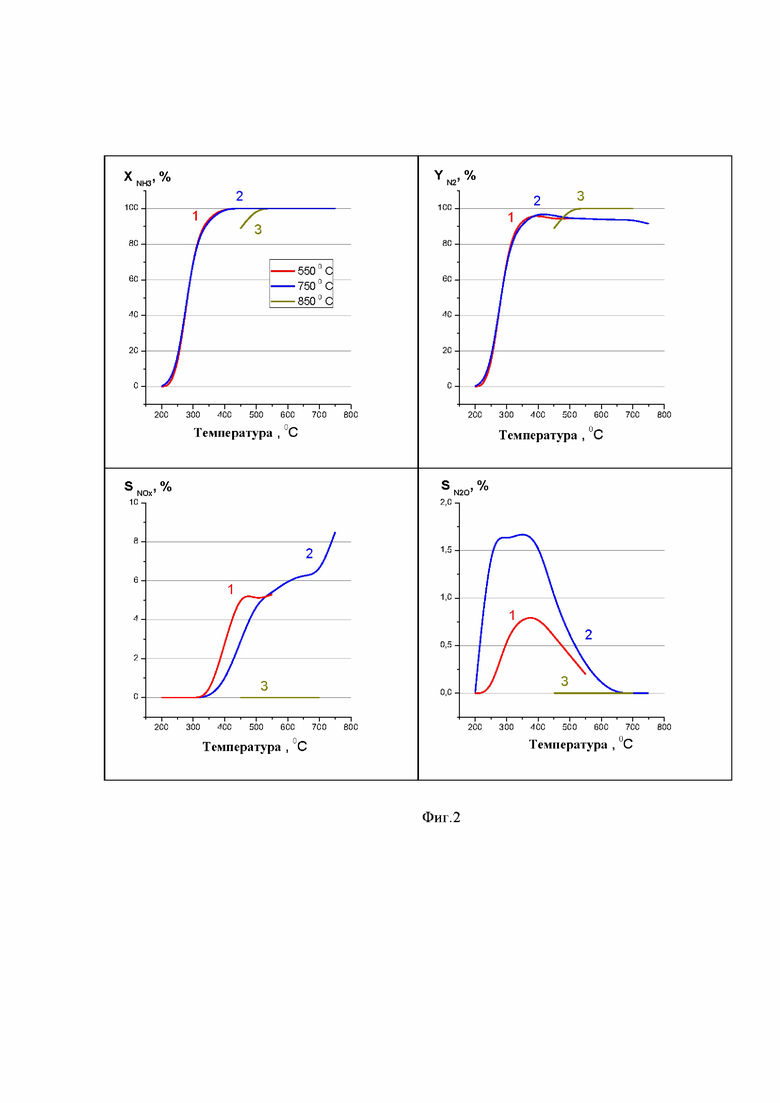
Результаты испытаний образцов катализатора в процессе селективного окисления аммиака в стехиометрической смеси в виде температурной зависимости конверсии NH3, выхода N2, селективностей NOx и N2O, представлены на Фиг.2, кривая 1. Условия процесса: NH3/O2 = 1.5 (8.3%NH3, 5.4%O2 в Ar), τ = 0.18 c (V кат.=0.2 мл).
Каталитические испытания в процессе селективного окисления аммиака показывают, что полная конверсия аммиака в реакционной смеси аммиака с избытком воздуха достигается при 400 °С при этом достигается максимальный выход азота ~80%. Повышение температуры испытаний до 900 °С снижает выход азота до ~ 70% за счет увеличения селективности по NO (фиг. 1, кривая 2). В стехиометрической смеси при температуре 400oС также достигается полная конверсия аммиака, и достигается 97% выход азота, который при повышении температуры испытаний практически не изменяется (фиг. 2, кривая 1).
Пример 3
Катализатор готовят аналогично примеру 1 с тем отличием, что экструдаты прокаливают при 750°С. После прокаливания при 750°С фазовый состав образца не изменяется, увеличивается доля фазы шпинели до соотношения 80:20 (СuAl2O4 / CuO = 4) образец имеет удельную поверхность по БЭТ 70 м2/г, общий объем пор 0.27 см3/г и средний диаметр пор 3.8 нм, прочность 50 кг/см2.
Испытания образцов катализатора в процессе селективного окисления аммиака в смеси с избытком кислорода проводят аналогично примеру 1 (фиг. 1, кривая 3), а в процессе селективного окисления аммиака в стехиометрической смеси аналогично примеру 2 (фиг. 2, кривая 2).
Каталитические испытания в процессе селективного окисления аммиака показывают, что полная конверсия аммиака в смеси с избытком воздуха достигается при 400°С при этом выход азота составляет ~ 80% и снижаться до ~ 70% при повышении температуры испытаний (фиг. 1, кривая 3). В стехиометрической смеси - при температуре 400°С также достигается полная конверсия аммиака, выход азота достигает ~ 97% и далее не изменяется при увеличении температуры испытаний (фиг. 2, кривая 2).
Пример 4
Катализатор готовят аналогично примеру 1 с тем отличием, что экструдаты прокаливают при 850°С. После прокаливания при 850°С доля фазы шпинели увеличивается почти до 100% (соотношение СuAl2O4 / CuO = 100), образец имеет удельную поверхность по БЭТ 31 м2/г, общий объем пор 0.21 см3/г и средний диаметр пор 15.6 нм. Прочность гранул на раздавливание по образующей составляет 80 кг/см2.
Испытания образцов катализатора в процессе селективного окисления аммиака в смеси с избытком кислорода проводят аналогично примеру 1 (фиг. 1, кривая 4), а в процессе селективного окисления аммиака в стехиометрической смеси аналогично примеру 2 (фиг. 2, кривая 3).
Полная конверсия аммиака в смеси аммиака с избытком воздуха достигается при ~ 500°С , а выход азота достигает 83%. С повышением температуры испытаний выход азота снижается до 80% (фиг. 1, кривая 4). В стехиометрической смеси полная конверсия аммиака достигается при 550 °С, при этом выход азота составляет 100% и не изменяется при увеличении температуры испытаний (фиг. 2, кривая 3).
Пример 5 - сравнительный
В качестве катализатора селективного окисления аммиака до азота испытан промышленный катализатор состава 0.11%Pd/Al2O3 (AOK-78-22). Катализатор активно окисляет аммиак и уже при температуре ~ 320°С достигается его 100% конверсия, при этом достигается и максимальный выход азота ~ 75%, существенно снижающийся при повышении температуры испытаний до 45% (при 550°С), что не удовлетворяет заявленным требованиям к катализатору сжигания аммиака.
Пример 6 - сравнительный
В качестве катализатора окисления аммиака до азота испытан промышленный катализатор ИК-42-1 состава 26%CuO/Al2O3. Катализатор активно окисляет аммиак и уже при температуре ~ 400°С достигается его 100% конверсия, при этом достигается и максимальный выход азота ~ 80%, снижающийся при повышении температуры испытаний до 70% (при 500°С), что не удовлетворяет заявленным требованиям к катализатору сжигания аммиака.
Таким образом, переход от стехиометрической смеси к смеси с избытком кислорода и повышение температуры испытаний в смеси с избытком кислорода способствуют снижению выхода азота для катализаторов, прокаленных при температуре менее 750°С. После термообработки при 850°С формируется катализатор, обеспечивающий 100% выход азота при окислении стехиометрической смеси при температурах испытаний выше 550°С, что удовлетворяет заявленным требованиям к катализатору сжигания аммиака.
Предлагаемый способ приготовления катализатора с использованием продукта термоактивации гиббсита обеспечивает получение катализатора без стадии осаждения и не требует носителя. Полученный продукт гидратации гранулируется методом экструзионного формования, причем форма, размер и текстура гранул могут быть оптимизирована в соответствии с требованиями процесса. Катализатор обеспечивает 100% конверсию аммиака при температурах выше 400°С и 100% выход азота при окислении стехиометрической смеси, его селективность не изменяется при повышении температуры испытаний.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ приготовления медьсодержащих цеолитов и их применение | 2020 |
|
RU2736265C1 |
| КАТАЛИЗАТОР ДЛЯ ПОЛУЧЕНИЯ ЗАКИСИ АЗОТА | 1996 |
|
RU2102135C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИЗОПРОПИЛОВОГО СПИРТА | 2022 |
|
RU2798625C1 |
| СПОСОБ КОМПЛЕКСНОЙ ОЧИСТКИ ГАЗОВЫХ ВЫБРОСОВ | 1996 |
|
RU2102124C1 |
| СПОСОБ ПРЯМОГО ВЫДЕЛЕНИЯ ЭЛЕМЕНТНОЙ СЕРЫ ИЗ СЕРОВОДОРОДСОДЕРЖАЩИХ ГАЗОВ И КАТАЛИЗАТОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1998 |
|
RU2142906C1 |
| КАТАЛИЗАТОР И СПОСОБ ПОЛУЧЕНИЯ ЗАКИСИ АЗОТА | 2002 |
|
RU2213615C1 |
| СПОСОБ ОЧИСТКИ ОТХОДЯЩИХ ГАЗОВ ОТ АММИАКА | 1992 |
|
RU2064816C1 |
| КАТАЛИЗАТОР ПОЛУЧЕНИЯ ЗАКИСИ АЗОТА И СПОСОБ | 2002 |
|
RU2214865C1 |
| КАТАЛИЗАТОР ДЛЯ АЛКИЛИРОВАНИЯ БЕНЗОЛА ПРОПИЛЕНОМ И СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ | 1995 |
|
RU2097129C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА ДЛЯ ПОЛУЧЕНИЯ ИЗОПРОПИЛОВОГО СПИРТА | 2022 |
|
RU2800947C1 |
Изобретение относится к каталитическим процессам селективного окисления аммиака до азота и может найти применение при использовании аммиака как источника альтернативного топлива. Предложен катализатор селективного окисления аммиака до азота, представляющий собой алюминат меди со структурой шпинели и CuO в соотношении фаз от 0.1 до 100 в форме гранул. При этом катализатор характеризуется величиной удельной поверхности 30-150 м2/г, средним размером пор 3-16 нм, прочностью гранул на раздавливание 20-80 кг/см2. Также раскрывается способ получения катализатора селективного окисления аммиака до азота и процесс селективного окисления аммиака до азота. Техническим результатом изобретения является разработка эффективного катализатора для процесса селективного окисления аммиака до азота в широком ряду температур и концентраций аммиака для его использования в горелочных устройствах. 3 н.п. ф-лы, 2 ил., 6 пр.
1. Катализатор селективного окисления аммиака до азота, представляющий собой алюминат меди со структурой шпинели и CuO в соотношении фаз от 0.1 до 100 в форме гранул, характеризующийся величиной удельной поверхности 30-150 м2/г и средним размером пор 3-16 нм, прочностью гранул на раздавливание 20-80 кг/см2.
2. Способ получения катализатора селективного окисления аммиака до азота в форме гранул, включающий гидротермальную обработку водной суспензии рентгеноаморфного продукта центробежно-термической активации гиббсита и нитрата меди при 150°С при соотношении Ж:Т = 3:1 с получением геля, его экструзионное формование и термообработку при температуре не ниже 450°С, при этом получают катализатор, представляющий собой алюминат меди со структурой шпинели и CuO в соотношении фаз от 0.1 до 100 в форме гранул, характеризующийся величиной удельной поверхности 30-150 м2/г и средним размером пор 3-16 нм, прочностью 20-80 кг/см2.
3. Процесс селективного окисления аммиака до азота с использованием катализатора по п.1 или приготовленного по п.2, при этом селективное окисление смеси со стехиометрическим соотношением аммиака и кислорода при температурах 550-900°С обеспечивает выход азота не менее 97%, а селективное окисление смеси с избытком кислорода при температурах 450-900°С обеспечивает выход азота 70-80%.
| M | |||
| JABŁONSKA et al | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| CATALYSIS COMMUNICATIONS | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| V | |||
| Прибор, автоматически записывающий пройденный путь | 1920 |
|
SU110A1 |
| P | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| ИНДИКАТОР ВРЕМЕНИ СКАНИРОВАНИЯ ЛУЧА | 2015 |
|
RU2679599C1 |
| КАТАЛИЗАТОР, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ И СПОСОБ ОКИСЛЕНИЯ АММИАКА | 2010 |
|
RU2430782C1 |
| F | |||
| GAO et al | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
Авторы
Даты
2023-06-14—Публикация
2022-10-18—Подача