ССЫЛКА НА СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
[0001] Полное содержание принятого в электронной форме списка последовательностей («4130_002PC08_SeqListing_ST25.txt», 122709 байт, созданного 31 мая 2019 г.), поданного вместе с заявкой, приведено в настоящем описании в качестве ссылки.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[0002] Настоящее изобретение относится к биспецифическим антителам, которые связываются с карциноэмбриональным антигеном CEACAM5 (CEA) человека и CD47 человека (биспецифическим антителам CEAxCD47). Кроме того, настоящее изобретение относится к полинуклеотидам, кодирующим такие биспецифические антитела, и к векторам и клеткам-хозяевам, содержащим такие полинуклеотиды. Изобретение, кроме того, относится к способам отбора и получения таких антител, и к способам применения таких антител в лечении заболеваний. Изобретение также относится к терапевтическому применению биспецифических антител CEAxCD47 в монотерапии и в комбинированной терапии, особенно с T-клеточными биспецифическими антителами (TCB) CEAxCD3 и/или ингибиторами PD-1 или PD-L1.
УРОВЕНЬ ТЕХНИКИ ДЛЯ ИЗОБРЕТЕНИЯ
[0003] Семейство CEA человека содержит 29 генов, из которых 18 экспрессируются: 7, принадлежащие к подгруппе CEA, и 11 - к подгруппе специфического для беременности гликопротеина. Считают, что члены подгруппы CEA имеют свойства клеточной адгезии. Считают, что CEA играют роль в врожденном иммунитете (Hammarström S., Semin Cancer Biol. 9(2):67-81 (1999)). Карциноэмбриональный антиген (CEA, CEACAM5 или CD66e; UniProtKB - P06731) является членом семейства родственных карциноэмбриональному антигену молекул клеточной адгезии (CEACAM) и опухолеассоциированным антигеном (Gold and Freedman, J Exp. Med., 121:439-462, 1965; Berinstein N. L., J Clin Oncol., 20:2197-2207, 2002). CEACAM6 (CD66c; UniProtKB - P40199) также принадлежит к семейству карциноэмбрионального антигена (CEA). Множество моноклональных антител получены против CEA для исследовательских целей, в качестве диагностических инструментов, и для терапевтических целей (см., например, WO2012117002 (полное содержание которой приведено в качестве ссылки), см. также Пример 8 f)). Растворимый CEA - в настоящем описании называемый также слущивающимся CEA или sCEA - представляет собой установленный маркер опухоли. Уровни в плазме пациентов с злокачественными опухолями могут, в некоторых случаях, подниматься выше 1000 нг/мл, в то время как концентрации в плазме у здоровых индивидуумов составляют ниже 10 нг/мл (например, в Sandler B. et al Anticancer Res 1999, 19(5B), 4229-33). Hao C., Zhang G. and L. in Progress in Molecular Biology and Translational Science (2019) опубликовано, что концентрации в плазме CEA между 100 и 250 нг/мл можно обнаружить у значительного % пациентов при раке поджелудочной железы, раке ободочной и прямой кишки, раке легкого и раке желудка. Такие высокие уровни особенно наблюдают, когда эти злокачественные опухоли являются местнораспространенными и/или метастазирующими. В соответствии с Wanebo et. al., New Eng. J. Med. (1978), 21% случаев рецидивирующего/метастазирующего рака толстого кишечника имеют sCEA выше 100 нг/мл. В Hohenberger et. al., Annals Surgery (1994) опубликовано для пациентов с колоректальными опухолями, стадией 4 по классификации Дьюка и метастазированием в печень, что 26% пациентов имеют sCEA выше 50 нг/мл. В Jurgensmerier et al Br. J. Cancer (2013) опубликовано в довольно больших исследованиях для нескольких сотен пациентов, страдающих метастазирующим колоректальным раком sCEA выше 225 нг/мл у 24%, соответственно, 25% из этих пациентов. Растворимый CEA может конкурировать за связывание с терапевтическими антителами против CEA с CEA на клетках опухолей, потенциально вызывая уменьшение эффективности антитела против CEA. Этого можно избегать, у большинства пациентов с злокачественными опухолями, например, у пациентов с колоректальным раком, с использованием антител против CEA с ограниченной перекрестной реакционной способностью по отношению к растворимому CEA, вплоть до концентраций в плазме sCEA 100-250 нг/мл
[0004] Мышиное моноклональное антитело PR1A3 получено посредством слияния клеток миеломы NS1 (P3/NS l/I-Ag-4-l) с клетками селезенки от мышей, иммунизированных нормальным колоректальным эпителием, в Richman P. I. and Bodmer W. F., Int. J. Cancer, 39:317-328, 1987 описано мышиное моноклональное антитело PR1A3. Эпитопное картирование PRl A3 показывает, что антитело нацелено на домен B3 и якорь GPI молекулы CEA (Durbin H. et al., Proc. Natl. Scad. Sci. USA, 91:4313-4317, 1994). Следовательно, антитело PR1A3 связывается в основном со связанным с мембраной CEA, а не с растворимой формой CEA, которую можно обнаружить в кровотоке пациентов с злокачественными опухолями. Эпитоп, связываемый PRl A3, представляет собой конформационный эпитоп, не линейный эпитоп (Stewart et al., Cancer Immunol Immunother, 47 (1999) 299-06). Гуманизированные антитела PRl A3 (hPRl A3) описаны, например, в Conaghhan P. J., et al., Br. J. Cancer, 98 (2008)1217-1225 и WO2012117002 (полное содержание которых приведено в настоящем описании в качестве ссылки).
[0005] Способ лечения злокачественной опухоли посредством комбинации антагониста оси PD-1 человека и биспецифического антитела против CEA/против CD3 упомянут в US20140242079 и WO2017118657 (полное содержание каждого из которых приведено в настоящем описании в качестве ссылки), и клинические результаты опубликованы в ASCO conference 2017 (Tabernero et al, J Clin Oncol 35, 2017 (suppl;abstr 3002)). Способ лечения опухолей посредством введения антагонистов иммунных контрольных точек, связывающих две или более различных мишени на пути иммунных контрольных точек, и перенаправляющего T-клетки средства, связывающегося с CEA и антигеном поверхности T-клетки, упомянут в WO2015112534. Конъюгат, состоящий из однодоменного антитела против CEACAM6 и уреазы, в настоящее время находится на клинических исследованиях (NCT02309892; WO2016116907). Антитело класса I, связывающееся с CEACAM5, CEACAM6 и гранулоцитами, упомянуто в US20110064653.
[0006] Антитело против CD3ɛ описанное на предшествующем уровне техники, представляет собой SP34 (Yang SJ, The Journal of Immunology (1986) 137; 1097-1100). SP34 вступает в реакцию с CD3 как приматов, так и человека. SP34 является доступным из BD Biosciences. Следующее антитело против CD3, описанное на предшествующем уровне техники, представляет собой UCHT-1 (см. WO2000041474). Следующее антитело против CD3, описанное на предшествующем уровне техники, представляет собой BC-3 (Fred Hutchinson Cancer Research Institute; использовано в исследованиях фазы I/II от GvHD, Anasetti et al., Transplantation 54: 844 (1992)). SP34 отличается от UCHT-1 и BC-3, тем, что SP-34 узнает эпитоп, присутствующий только на цепи ε CD3 (см. Salmeron et al., (1991) J. Immunol. 147: 3047), в то время как UCHT-1 и BC-3 узнают эпитоп, в котором участвуют обе цепи ε и γ. Антитела против CD3 описаны также в WO2007042261, WO2008119565, WO2008119566, WO2008119567, WO2010037836, WO2010037837, WO2010037838 и US8236308 (полное содержание каждой из которых приведено в настоящем описании в качестве ссылки). Биспецифическое антитело, содержащее связывающую часть, специфическую для CEA и связывающую часть, специфическую для CD3ε, описано в US20140242079A1 (полное содержание которой приведено в настоящем описании в качестве ссылки).
[0007] CD47 человека (UniProtKB - Q08722 (CD47_HUMAN; IAP) представляет собой трансмембранный белок, который связывается с лигандами тромбоспондином-1 (TSP-1) и регулирующим сигнал белком альфа (SIRPα; CD172a; UniProtKB P78324) и может действовать в качестве сигнала «не ешь меня» для иммунной системы, особенно для макрофагов. CD47 вовлечен в ряд клеточных процессов, включая апоптоз, пролиферацию, адгезию и миграцию. Кроме того, он играет ключевую роль в иммунных и ангиогенных ответах. CD47 сверхэкспрессирован в клетках различных опухолей. Антитела против CD47 описаны на предшествующем уровне техники, и некоторые из них находятся на клинических исследованиях в качестве лекарственных средств для лечения опухоли (Weiskopf K. European Journal of Cancer 76 (2017) 100-109; Huang Y et al., J Thorac Dis 2017;9(2):E168-E174. Антитела подкласса IgGl, которые связывают CD47, могут приводить к истощению тромбоцитов и к уменьшению гемоглобина эритроцитов RBC зависимым от Fc образом (см., например, US20140140989). Для исключения этого неблагоприятного эффекта, в WO2017196793 описана мутантная форма подкласса IgG4 антитела против CD47 (IgG4PE, с мутацией S228P, так же как с мутацией L235E, для уменьшения связывания FcyR). Такое антитело против CD47 с сильно уменьшенным связыванием с FcyR и эффекторной функцией не приводит к такому истощению тромбоцитов. Однодоменное биспецифическое антитело против CD47 и CD20 описано в von Bommel PE et al., Oncoimmunol. 7 (2018) e386361, и в Piccione EC et al. mAbs 7 (2015)946-956. Dheilly E. et al., Mol. Thera. 25 (2017) 523-533 (см. также WO2014087248) описано биспецифическое антитело против CD19 и CD47. Биспецифическое антитело против CD19 и CD47, содержащее общую тяжелую цепь из SEQ ID NO:5 и вариабельный домен легкой цепи VL из SEQ ID NO:10, описано в WO2014087248 (полное содержание которой приведено в настоящем описании в качестве ссылки).
[0008] FcRI (CD64) человека ограничен моноцитами/макрофагами и дендритными клетками (DC) и, индуцируемым образом экспрессируется на нейтрофилах и тучных клетках; hFc RIIA (CD32A) экспрессируется на всех миелоидных клетках, но не на лимфоцитах; hFc RIIB (CD32B) на высоком уровне экспрессируется только на циркулирующих B-клетках и базофилах (L. Cassard, F. Joensson, S. Arnaud, M. Daeron, J. Immunol.189 (2012(2995-3006), слабо экспрессируется на 20% моноцитов и 4% нейтрофилов, и экспрессируется на тканевых макрофагах и DC, но не на тучных клетках. hFc RIIC (CD32C) экспрессируется на клетках NK, моноцитах и нейтрофилах. hFc RIIIA (CD16A) экспрессируется на клетках NK и моноцитах/макрофагах; hFcRIIIB CD16B) экспрессируется на нейтрофилах и, как недавно показано, на подгруппах базофилов. Эти паттерны экспрессии подчеркивают, что hFc RIIA является единственным активирующим рецептором IgG, конститутивно экспрессируемым тучными клетками, базофилами, нейтрофилами и эозинофилами (Bruhns P., Blood 119 (2012) 5640). Виды биологической активности каждого подкласса IgG плохо известны. Рецепторы IgG (FcγR) являются поразительно многочисленными у человека. Они включают высокоаффинные и низкоаффинные рецепторы. Как высокоаффинные, так и низкоаффинные FcγR, связывают IgG-иммунные комплексы с высокой авидностью, но только высокоаффинные FcγR связывают мономерное IgG. Существует один высокоаффинный рецептор IgG у человека, hFcγRI (CD64), и два семейства низкоаффинных рецепторов IgG, hFcγ RIIA, IIB и IIC (CD32), и hFcγRIIIA и IIIB (CD16). hFcγRI и hFcγRIIIA представляют собой ассоциированные с FcγR активирующие рецепторы, hFcγRIIA и hFcγRIIC представляют собой однодоменные активирующие рецепторы, hFcγRIIB представляют собой однодоменные ингибирующие рецепторы, и hFcγRIIIB представляют собой заякоренные GPI рецепторы, функция которых неизвестна (Bruhns P. Blood 113 (2009) 3716). Несколько исследовательских групп показали, что антитела, лишенные 1,6-фукозы в гликозилировании на своей тяжелой цепи, имеют увеличенную аффинность связывания с рецептором FcγRIII и увеличенную активность ADCC (Shields, R. L., et al., (2002) J Biol. Chem. 277, 26733-26740.; (2002) J Biol. Chem. 8, 8). Кроме того, установлена корреляция между аффинностью связывания с рецептором FcγRIII и активностью ADCC (Okazaki, A., et al., (2004) J Mol. Biol. 336, 1239-1249; Dall'Ozzo, 2004). Молекула IgG несет два N-связанных олигосахарида в области Fc, один на каждой тяжелой цепи. Как любой гликопротеин, антитело образуется в форме популяции гликоформ, которые разделяют одинаковый полипептидный остов, но имеют различные олигосахариды, присоединенные к участкам гликозилирования. Олигосахариды, обычно обнаруживаемые в области Fc сывороточного IgG, принадлежат к комплексному двухантенному типу (Wormald et al., Biochemistry 36: 130-38 (1997), с низким уровнем терминальной сиаловой кислоты и разделенным надвое N-ацетилглюкозамином (GlcNAc), и различной степенью терминального галактозилирования и корового фукозилирования. Некоторые исследования позволяют предполагать, что минимальная углеводная структура, необходимая для связывания FcyR, лежит внутри олигосахаридного кора. Lund et al., J. Immunol. 157:4963-69 (1996). Антитела с уменьшенным содержанием фукозы в группах гликана, имеют более высокую активность антителозависимой клеточной цитотоксичности (ADCC), по сравнению с нормально фукозилированным антителом (Niwa R et al., Cancer Res, 64, 2127-33, 2004). Механизмом в основе увеличенной ADCC антитела с низким содержанием/отсутствием фукозы, является его увеличенная аффинность для FcγRIIIa (CD16). Линия клеток с нокаутом обоих аллелей гена, ответственного за добавление фукозы (α1,6-фукозилтрансферазы; FUT8), описана в US6946292, US7425446, US8067232 (полное содержание каждого из которых приведено в настоящем описании в качестве ссылки), и в http://www.potelligent.com. Сверхэкспрессия в клетках яичника китайского хомячка (CHO) β(1,4)-N-ацетилглюкозаминилтрансферазы III (GnTIII), гликозилтрансферазы, катализирующей образование разделенных надвое олигосахаридов, значительно увеличивает активность in vitro ADCC антител, продуцированных модифицированными клетками CHO. ( et al., Nature Biotechnol. 17:176-180 (1999), WO199954342, US20030175884 (полное содержание каждого из которых приведено в настоящем описании в качестве ссылки)). Мутации в домене Fc могут также изменять свойства связывания домена Fc с различными рецепторами Fc (WO2004063351, WO2004099249; WO2005018669, WO2005063815, WO2005110474, WO2005056759, WO2005092925, WO2005018572, WO2006019447, WO2006116260, WO2006023420-, WO2006047350, WO2006085967, WO2006105338, WO2007021841, WO2007008943, WO2007024249, WO2007041635, WO2007048077, WO2007044616, WO2007106707, WO2008022152, WO2008140603, WO2008036688, WO2008091798, WO2008091954, WO2008092117, WO2008098115, WO2008121160, WO2008150494, WO2010033736, WO2014113510 (полное содержание каждой из которых приведено в настоящем описании в качестве ссылки)).
et al., Nature Biotechnol. 17:176-180 (1999), WO199954342, US20030175884 (полное содержание каждого из которых приведено в настоящем описании в качестве ссылки)). Мутации в домене Fc могут также изменять свойства связывания домена Fc с различными рецепторами Fc (WO2004063351, WO2004099249; WO2005018669, WO2005063815, WO2005110474, WO2005056759, WO2005092925, WO2005018572, WO2006019447, WO2006116260, WO2006023420-, WO2006047350, WO2006085967, WO2006105338, WO2007021841, WO2007008943, WO2007024249, WO2007041635, WO2007048077, WO2007044616, WO2007106707, WO2008022152, WO2008140603, WO2008036688, WO2008091798, WO2008091954, WO2008092117, WO2008098115, WO2008121160, WO2008150494, WO2010033736, WO2014113510 (полное содержание каждой из которых приведено в настоящем описании в качестве ссылки)).
[0009] Значительный прогресс достигнут в лечении гематологических злокачественных новообразований. Это отличается от прогресса, достигнутого в лечении нескольких типов солидных опухолей на поздних стадиях. Выживаемость без прогрессирования (PFS) и общая выживаемость (OS) для этих типов опухолей на поздних стадиях, многие из которых достаточно частые, была до некоторой степени улучшена посредством новых схем химиотерапии в присутствии и в отсутствие моноклональных антител против, например, VEGFR или ERGFR, в качестве партнера для комбинации с химиотерапией. Однако, в последние годы для многих находящихся на поздних стадиях/метастазирующих солидных опухолей, прогресс терапии с использованием лекарственных средств был ограничен. Больше надежды возлагали на иммунотерапию злокачественных опухолей и получены определенные, но ограниченные, успехи. Опухоли развивают меры для защиты своих клеток от разрушения эффекторными T-клетками и другими иммуноцитами, подобными макрофагам. Иммунотерапия злокачественных опухолей в последнее десятилетие(десятилетия) определенно в некоторой степени сфокусирована и имеет успех в том, чтобы сделать T-клетки снова подходящими и перенаправлять их против клеток злокачественных опухолей. Наиболее многообещающими примерами являются ингибиторы/активаторы определенных иммунных контрольных точек. Например, показано, что ингибиторы контрольных точек, подобные антагонистам оси PD-1, повторно активируют эффекторные T-клетки для борьбы с солидными злокачественными опухолями. Однако, не все типы солидных опухолей являются отвечающими, и даже для отвечающих, часто менее 50% пациентов получают соответствующее преимущество, например, от лечения с использованием антитела против PD-1 или PD-L1.
[0010] Для адоптивной T-клеточной терапии с использованием CAR-T-клеток, а также терапии с использованием T-клеточных биспецифических антител, получены многообещающие клинические результаты при гематологических злокачественных новообразованиях. Однако, клинические исследования видов адоптивной T-клеточной терапии, например, CAR-T-клеток, при различных солидных опухолей, по большей части показали отсутствие ответа или только незначительную частоту ответа (например, Xu et. al. Expert Review of Anticancer Therapy 2017, 17, 1099-1106).
[0011] В US20140242079 и WO2017055389 (полное содержание каждой из которых приведено в настоящем описании в качестве ссылки) описаны T-клеточные биспецифические антитела CEAxCD3. Одно антитело из US20140242079 и одно из WO2017055389 оба находятся в клинической разработке (см. clinicaltrials.gov; RO6958688 в NCT3866239 и RO7172508 в NCT03539484). Эти T-клеточные биспецифические антитела связываются с различными эпитопами CEAxCD3 и имеют различную активность уничтожения клеток опухолей. Применительно к уничтожению клеток опухолей в анализе in vitro с использованием T-клеток человека, наиболее активные T-клеточные биспецифические антитела CEAxCD3, описанные в WO201705389, являются в 10-100 или более раз более активными, чем RO6958688/цибисатамаб (CEA-TCB).
[0012] До недавнего времени, результаты клинических исследований с использованием T-клеточных биспецифических антител TAA x CD3 (TAA=опухолеассоциированный антиген) у пациентов с солидными опухолями на поздних стадиях являлись разочаровывающими. Однако, результаты предварительной фазы 1 опубликованы в ASCO 2017 для T-клеточного биспецифического антитела CEAxCD3 CEA-TCB (RO6958688/цибисатамаба, см., например, Bacac et al Clin. Cancer Res., 22(13), 3286-97 (2016); и в US20140242079) показаны для пациентов с колоректальным раком на поздних стадиях, подвергаемых монотерапии, частичные ответы и стабильное заболевание (J.Tabernero et.al., J. Clin. Oncol. 35, 2017 (suppl. Abstr. 3002)). В клинически активных дозах, концентрации в плазме, например, 300 нМ, достигнуты для цибисатамаба. Больше случаев частичного ответа и стабильного заболевания возникало, когда CEA-TCB комбинировали с ингибирующим PD-L1 антителом. Эти данные показывают, что эффективности можно достигать для CEA-TCB в солидных опухолях на поздних стадиях. Однако, при использовании монотерапии, а также комбинации с ингибитором PD-L1, большинство пациентов все еще имели прогрессирование, и для пациентов с реакцией показаны, самое лучшее, частичные ответы и стабильное заболевание, но не достигнуто полных ответов. Одним способом для достижения лучших результатов может являться добавление к T-клеточным биспецифическим антителам не только ингибитора оси контрольных точек PD-1, но также добавление дополнительных ингибиторов или агонистов контрольных точек. Однако, до настоящего времени, насколько известно авторам настоящего изобретения, не существует доступных многообещающих клинических данных для такого комбинированного способа. Ограниченная доступность T-клеток внутри солидных опухолей на поздних стадиях определенно является важным механизмом, ограничивающим эффективность, достижимую с использованием T-клеточных биспецифических антител плюс ингибиторов оси PD-1 и/или других ингибиторов контрольных точек или агонистов для T-клеток.
[0013] Вместо добавления к комбинации T-клеточного биспецифического антитела и ингибитора оси PD-1 другого лекарственного средства, целью которого является перенацеливание T-клеток против клеток опухолей, для солидных опухолях на поздних стадиях, может являться более успешным добавление лекарственного средства, перенацеливающего на клетки опухолей других иммуноцитов, особенно макрофагов или макрофагов и естественных киллеров NK-клеток. Настоящее изобретение относится к биспецифическим антителам, перенацеливающим макрофаги, а также клетки NK, против экспрессирующих CEA солидных опухолей, в качестве монотерапии или в комбинации например, с T-клеточными биспецифическими антителами и/или ингибирующими PD-1/PD-L1 антителами.
[0014] Разочаровывающие результаты для CAR-T-клеток при солидных опухолях могут иметь простое объяснение - количества CAR-T-клеток, проникающих в солидную опухоль и распространяющихся в ней, просто являются недостаточными. Это определенно отличается от большинства гематологических злокачественных новообразований; CAR-T-клетки могут легко достигать клетки опухолей, что объясняет отличие высокой эффективности для этих злокачественных новообразований, по сравнению с разочаровывающей эффективностью для солидных опухолей. Кроме того, CAR-T-клетки могут быть сильно супрессированы микроокружением опухолей (TME), которое, в большинстве случаев, является сильно иммуносупрессивным.
[0015] Моноклональные антитела, а также биспецифические антитела, используемые в терапии, могут оказывать множество неблагоприятных эффектов. Важной проблемой токсичности является синдром высвобождения цитокинов (CRS), обнаруженный, например, при терапии алемтузумабом, муромонабом-CD3, ритуксимабом и биспецифическим антителом против CD19 x CD3 блинатумомабом. Обнаружено также, что лечение антителами против CD47 индуцирует образование увеличенных количеств провоспалительных цитокинов после опосредованного антителом против CD47 фагоцитоза (см., например, US20160144009). Известными неблагоприятными событиями для моноклональных антител против CD47 с Fc wt IgG1 являются увеличенный фагоцитоз/лизис эритроцитов RBC и активация тромбоцитов (см., например, на фигурах 8 и 10 фагоцитоз RBC и активацию тромбоцитов, индуцированные антителом против CD47 B6H12.2, несущим Fc wt IgG1).
[0016] Настоящее изобретение относится к биспецифическим антителам, специфически связывающимся с CEACAM5 человека и CD47 человека, предназначенным для лечения солидных опухолей. Эти биспецифические антитела сочетают высокую эффективность с низкой токсичностью, низкой иммуногенностью и благоприятными фармакокинетическими свойствами. Биспецифические антитела по настоящему изобретению индуцируют свои эффекты против клеток опухолей по большей части посредством оптимизированных ADCP (антителозависимого клеточного фагоцитоза) и ADCC (антителозависимой клеточной цитотоксичности), благодаря вовлечению иммуноцитов, особенно макрофагов и NK-клеток. Настоящее изобретение также относится к биспецифическим антителам, специфически связывающихся с CEACAM5 человека и CD47 человека, разработанным для комбинированного лечения с T-клеточными биспецифическими антителами CEAxCD3, подобными RO6958688, RO7172508 и другими T-клеточными биспецифическими антителами CEAxCD3, например, как описано ниже, и демонстрирующим фагоцитоз клеток опухолей, подобных MKN-45, в присутствии макрофагов человека.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0017] В одном варианте осуществления, изобретение относится к биспецифическому антителу (далее также названному как «Mab CEAxCD47» или «биспецифическое антитело CEAxCD47»), содержащему первую связывающую часть, специфически связывающуюся с CEACAM5 человека (далее также названным как «CEA»), и вторую связывающую часть, специфически связывающуюся с CD47 человека (далее также названным как «CD47»).
[0018] В одном варианте осуществления, изобретение относится к биспецифическому антителу, специфически связывающемуся с CEACAM5 человека и CD47 человека, отличающемуся тем, что область Fc подвергнута гликоинженерии, для получения уменьшенного количества остатков фукозы по сравнению с таким же, но не подвергнутым гликоинженерии биспецифическим антителом.
[0019] В одном варианте осуществления, настоящее изобретение относится к биспецифическому антителу, отличающемуся специфическим связыванием CEACAM5 и CEACAM6 человека в первой связывающей части, и с CD47 человека во второй связывающей части. В одном варианте осуществления изобретение относится к биспецифическому антителу CEAxCD47, специфически связывающемуся уравновешенным образом с CEACAM5 человека и CEACAM6 человека. В одном варианте осуществления, биспецифическое антитело отличается связыванием с человеческим рекомбинантным CEACAM5 и CEACAM6, отличающимся тем, что значения EC50 для связывания с CEACAM5 и CEACAM6 отличаются менее чем в 3 раза (уравновешенное связывание, связывание уравновешенным образом, см. таблицу 5). Связывание измеряют в ELISA на основе стрептавидина/биотина (см. пример 8f).
[0020] В одном варианте осуществления, настоящее изобретение относится к биспецифическому антителу, специфически связывающемуся с CEACAM5 и CEACAM6 человека в первой связывающей части и CD47 человека во второй связывающей части, отличающемуся
a) тем, что первая связывающая часть содержит вариабельную область тяжелой цепи, содержащую, в качестве CDR, CDRH1 из SEQ ID NO:25, CDRH2 из SEQ ID NO:26 и CDRH3 из SEQ ID NO:27, и вариабельную область легкой цепи, содержащую, в качестве CDR, CDRL1 из SEQ ID NO: 112, CDRL2 из SEQ ID NO: 113 и CDRL3 из SEQ ID NO: 114, и
b) тем, что вторая связывающая часть содержит вариабельную область тяжелой цепи, содержащую, в качестве CDR, CDRH1 из SEQ ID NO:25, CDRH2 из SEQ ID NO:26 и CDRH3 из SEQ ID NO:27, и вариабельную область легкой цепи, содержащую, в качестве CDR, CDRL1 из SEQ ID NO:28, CDRL2 из SEQ ID NO:29 и CDRL3 из SEQ ID NO:30.
[0021] В одном варианте осуществления, изобретение относится к биспецифическому антителу, специфически связывающемуся с CEACAM5 человека и CD47 человека, содержащему первую связывающую часть, специфически связывающуюся с CEACAM5 человека, и вторую связывающую часть, специфически связывающуюся с CD47 человека, отличающемуся тем, что первая связывающая часть связывается с Ig-подобным доменом V-типа CEACAM5 из аминокислот 35-144.
[0022] В одном варианте осуществления, изобретение относится к биспецифическому антителу, специфически связывающемуся с CEACAM5 человека и CD47 человека, содержащему первую связывающую часть, специфически связывающуюся с CEACAM5 человека, и вторую связывающую часть, специфически связывающуюся с CD47 человека, отличающемуся тем, что указанное биспецифическое антитело конкурирует с антителом против CEA SM3E, содержащим, в качестве доменов VK и VH, VK и VH из последовательностей SEQ ID NO:100 и 101, за связывание с CEACAM5.
[0023] В одном варианте осуществления, изобретение относится к биспецифическому антителу, специфически связывающемуся с CEACAM5 человека и CD47 человека, содержащему первую связывающую часть, специфически связывающуюся с CEACAM5 человека, и вторую связывающую часть, специфически связывающуюся с CD47 человека, отличающемуся тем, что указанное биспецифическое антитело не конкурирует с антителами против CEA SM3E, MEDI, содержащими, в качестве доменов VL и VH, VL и VH из последовательностей SEQ ID NO:102 и 103, лабетузумабом (Lab), содержащим, в качестве доменов VK и VH, VK и VH из последовательностей SEQ ID NO:110 и 111, SAR, содержащим, в качестве доменов VK и VH, VK и VH из последовательностей SEQ ID NO:104 и 105, T86.66, содержащим, в качестве доменов VK и VH, VK и VH из последовательностей SEQ ID NO:108 и 109, CH1A1A, содержащим, в качестве доменов VK и VH, VK и VH из последовательностей SEQ ID NO:106 и 107, за связывание с CEACAM5.
[0024] В одном варианте осуществления, изобретение относится к биспецифическому антителу, специфически связывающемуся с CEACAM5 человека и CD47 человека, содержащему первую связывающую часть, специфически связывающуюся с CEACAM5 человека, и вторую связывающую часть, специфически связывающуюся с CD47 человека, отличающемуся тем, что значение EC50 кривой показателей фагоцитоза посредством указанного биспецифического антитела лежит в диапазоне от 0,1- до 3-кратного значения E50 эталонного антитела K2AC22 в таких же экспериментальных условиях и в присутствии или в отсутствие 1 мг/мл IgG человека. В следующих вариантах осуществления, диапазон составляет 0,2-3,0, 0,3-3,0, 0,5-2,5 или 1,0-2,5. Значения EC50 для фагоцитоза измеряют как значения EC50 кривой показателей фагоцитоза (анализ фагоцитоза на основе визуализации, см. пример 9 и фигуру 12, и таблицу 3).
[0025] В одном варианте осуществления, изобретение относится к биспецифическому антителу, специфически связывающемуся с CEACAM5 человека и CD47 человека, содержащему первую связывающую часть, специфически связывающуюся с CEACAM5 человека, и вторую связывающую часть, специфически связывающуюся с CD47 человека, отличающемуся
тем, что в присутствии 1 мг/мл IgG человека, максимальный показатель фагоцитоза (см. пример 9,2; анализ на основе CellInsight™) указанного биспецифического антитела не уменьшается на 30% или более, по сравнению с максимальным показателем фагоцитоза, измеренным в таких же экспериментальных условиях, но без добавления IgG человека (см., например, фигуру 17).
[0026] В одном варианте осуществления, биспецифическое антитело отличается тем, что содержит первую связывающую часть, специфически связывающуюся с CEACAM5 человека, и вторую связывающую часть, специфически связывающуюся с CD47 человека, отличающиеся тем, что:
a) первая связывающая часть содержит вариабельную область тяжелой цепи, содержащую CDRH1 из SEQ ID NO:1, CDRH2 из SEQ ID NO:2 и CDRH3 из SEQ ID NO:3 и константный домен легкой цепи типа лямбда человека и из SEQ ID NO:13, и
вторая связывающая часть содержит вариабельную область тяжелой цепи, содержащую CDRH1 из SEQ ID NO:1, CDRH2 из SEQ ID NO:2 и CDRH3 из SEQ ID NO:3, и вариабельную область легкой цепи, содержащую CDRL1 из SEQ ID NO:7, CDRL2 из Ala Ala Ser, включенную в SEQ ID NO:8, и CDRL3 из SEQ ID NO:9, или
b) первая связывающая часть содержит вариабельную область тяжелой цепи, содержащую, в качестве CDR, CDRH1 из SEQ ID NO:25, CDRH2 из SEQ ID NO:26 и CDRH3 из SEQ ID NO:27 и константный домен легкой цепи типа лямбда человека и из SEQ ID NO:13, и вторая связывающая часть содержит вариабельную область тяжелой цепи, содержащую, в качестве CDR, CDRH1 из SEQ ID NO:25, CDRH2 из SEQ ID NO:26 и CDRH3 из SEQ ID NO:27, и вариабельную область легкой цепи, содержащую CDRL1 из SEQ ID NO:28, CDRL2 из SEQ ID NO:29 и CDRL3 из SEQ ID NO:30.
[0027] В одном варианте осуществления биспецифическое антитело отличается тем, что содержит первую связывающую часть, специфически связывающуюся с CEACAM5 человека, и вторую связывающую часть, специфически связывающуюся с CD47 человека, отличающиеся тем, что:
a) первая связывающая часть содержит вариабельную область тяжелой цепи, содержащую, в качестве CDR, CDRH1 из SEQ ID NO:25, CDRH2 из SEQ ID NO:26 и CDRH3 из SEQ ID NO:27, и вариабельную область легкой цепи, содержащую комбинацию из CDRL1, CDRL2 и CDRL3, выбранную из группы, состоящей из:
SEQ ID NO:31, 32 и 33; SEQ ID NO:34, 35 и 36, SEQ ID NO:37, 38 и 39, SEQ ID NO:40, 41 и 42, SEQ ID NO:43, 44 и 45, SEQ ID NO:46, 47 и 48, SEQ ID NO:49, 50 и 51, SEQ ID NO:52, 53 и 54, SEQ ID NO:55, 56 и 57, SEQ ID NO:58, 59 и 60, SEQ ID NO:61, 62 и 63, SEQ ID NO: 112, 113 и 114, и
b) вторая связывающая часть содержит вариабельную область тяжелой цепи, содержащую, в качестве CDR, CDRH1 из SEQ ID NO:25, CDRH2 из SEQ ID NO:26 и CDRH3 из SEQ ID NO:27, и вариабельную область легкой цепи, содержащую, в качестве CDR, CDRL1 из SEQ ID NO:28, CDRL2 из SEQ ID NO:29 и CDRL3 из SEQ ID NO:30.
[0028] В одном варианте осуществления, биспецифическое антитело отличается тем, что содержит в первой связывающей части, в качестве константного домена легкой цепи, константный домен типа лямбда человека из SEQ ID NO:13.
[0029] В одном варианте осуществления, биспецифическое антитело отличается тем, что содержит первую связывающую часть, специфически связывающуюся с CEACAM5 человека, и вторую связывающую часть, специфически связывающуюся с CD47 человека, отличающиеся тем, что:
a) первая связывающая часть содержит вариабельную область тяжелой цепи (VH) из SEQ ID NO:4 и вариабельную область легкой цепи, выбранную из группы VL, включенных в области VLCL, состоящей из:
SEQ ID NO:64, SEQ ID NO:65, SEQ ID NO:66, SEQ ID NO:67, SEQ ID NO:68, SEQ ID NO:69, SEQ ID NO:70, SEQ ID NO:71, SEQ ID NO:72, SEQ ID NO:73, SEQ ID NO:74 и SEQ ID NO:115, и
b) вторая связывающая часть содержит вариабельную область тяжелой цепи из SEQ ID NO:4 и вариабельную область легкой цепи из SEQ ID NO:10.
[0030] В одном варианте осуществления, биспецифическое антитело отличается тем, что содержит первую связывающую часть, специфически связывающуюся с CEACAM5 человека, и вторую связывающую часть, специфически связывающуюся с CD47 человека, отличающиеся тем, что:
a) первая связывающая часть содержит тяжелую цепь из SEQ ID NO:5 и легкую цепь, выбранную из группы, состоящей из:
SEQ ID NO:64, SEQ ID NO:65, SEQ ID NO:66, SEQ ID NO:67, SEQ ID NO:68, SEQ ID NO:69, SEQ ID NO:70, SEQ ID NO:71, SEQ ID NO:72, SEQ ID NO:73, SEQ ID NO:74 и SEQ ID NO:115
b) вторая связывающая часть содержит вариабельную область тяжелой цепи из SEQ ID NO:5 и вариабельную область легкой цепи из SEQ ID NO:11.
[0031] В одном варианте осуществления, биспецифическое антитело отличается тем, что является моновалентным для первой связывающей части и моновалентным для второй связывающей части.
[0032] В одном варианте осуществления, константные и вариабельные последовательности каркасной области являются человеческими.
[0033] В одном варианте осуществления, биспецифическое антитело отличается тем, что каждая из первой и второй связывающей части содержит тяжелую цепь иммуноглобулина и легкую цепь иммуноглобулина. В одном варианте осуществления, биспецифическое антитело отличается тем, что принадлежит к типу IgG1 человека. В одном варианте осуществления, биспецифическое антитело представляет собой полноразмерное антитело.
[0034] В одном варианте осуществления, биспецифическое антитело по изобретению отличается тем, что содержит первую связывающую часть, специфически связывающуюся с CEA, содержащую вариабельный домен легкой цепи каппа и константный домен легкой цепи лямбда и вторую связывающую часть, специфически связывающуюся с CD47, содержащую вариабельный домен легкой цепи каппа и константный домен легкой цепи каппа (биспецифическое антитело κλ, антитело κλ, типа 1).
[0035] В одном варианте осуществления биспецифическое антитело по изобретению отличается тем, что содержит первую связывающую часть, специфическую для CEA, содержащую вариабельный домен легкой цепи лямбда и константный домен легкой цепи лямбда и вторую связывающую часть, специфическую для CD47, содержащую вариабельный домен легкой цепи каппа и константный домен легкой цепи каппа (биспецифическое антитело κλ, антитело κλ, типа 2). В одном варианте осуществления, биспецифическое антитело по изобретению имеет формат полностью человеческого биспецифического IgG (особенно IgG1) и дополнительно, биспецифического антитела κλ типа 1 или типа 2.
[0036] В одном варианте осуществления, биспецифическое антитело по изобретению отличается тем, что представляет собой биспецифическое антитело κλ типа 1 или типа 2 и содержит общую тяжелую цепь (cHC).
[0037] В одном варианте осуществления, биспецифическое антитело отличается тем, что связывается с CD47 человека с аффинностью связывания 100 нМ - 600 нМ, в одном варианте осуществления, с аффинностью связывания 100 нМ - 500 нМ.
[0038] В одном варианте осуществления, биспецифическое антитело отличается тем, что связывается с клетками MKN-45 с значением EC50 1-200 нМ. В одном варианте осуществления, биспецифическое антитело отличается тем, что связывается с клетками MKN-45 с значением EC50 1-50 нМ. В одном варианте осуществления биспецифическое антитело отличается тем, что связывается с клетками MKN-45 с значением EC50 50-100 нМ. В одном варианте осуществления биспецифическое антитело отличается тем, что связывается с клетками MKN-45 с значением EC50 100-200 нМ.
[0039] В одном варианте осуществления, биспецифическое антитело по изобретению отличается тем, что максимальный достижимый показатель фагоцитоза для фагоцитоза клеток MKN-45 в присутствии макрофагов человека, посредством указанного биспецифического антитела, не уменьшается более чем на 20% в присутствии 5000 нг/мл растворимого CEA, по сравнению с показателем фагоцитоза, измеренным без растворимого CEA.
[0040] В одном варианте осуществления биспецифическое антитело по изобретению отличается тем, что EC50 для кривой показателей фагоцитоза клеток MKN-45 в присутствии макрофагов человека, посредством указанного биспецифического антитела, не сдвигается более чем в 4 раза в сторону более высоких концентраций в присутствии 200 нг/мл растворимого CEA, по сравнению с EC50, измеренной без растворимого CEA и/или что максимум кривой показателей фагоцитоза не уменьшается на 10% или более, 15% или более, или 20% или более, посредством добавления 200 нг/мл sCEA (см., например, фигуру 20B).
[0041] В одном варианте осуществления, биспецифическое антитело по изобретению отличается тем, что EC50 для кривой связывания с клетками MKN-45 указанного биспецифического антитела не сдвигается более чем в 2 раза в сторону более высоких концентраций в присутствии 200 нг/мл растворимого CEA, по сравнению с EC50, измеренной без растворимого CEA (см., например, фигуру 20A).
[0042] В одном варианте осуществления, биспецифическое антитело отличается тем, что не имеет перекрестной реакционной способности по отношению к CEACAM1 человека.
[0043] В одном варианте осуществления, биспецифическое антитело отличается тем, что связывается с CEACAM6 человека, экспрессированным на рекомбинантных клетках CHO CHO-K1 (ATCC® CCL-61™), с значением EC50 1-50 нМ (отрицательные по CEACAM6 клетки CHO трансфицируют вектором, содержащим кДНК CEACAM6 человека, для получения экспрессии белка CEACAM6).
[0044] В одном варианте осуществления, биспецифическое антитело по изобретению отличается тем, что моноклональное антитело, специфически связывающееся с CEACAM5 человека (далее также названное как MAB CEA), содержащее вариабельную область тяжелой цепи из SEQ ID NO:20 и вариабельную область легкой цепи из SEQ ID NO:21, в концентрации 300 нМ, не сдвигает EC50 кривой связывания биспецифического антитела по изобретению с клетками MKN-45 более чем в 3 раза, в одном варианте осуществления, в сторону более высоких концентраций. В одном варианте осуществления биспецифическое антитело по изобретению отличается тем, что биспецифическое антитело, специфически связывающееся с CEACAM5 человека и CD3ε (далее также названное как CEA-TCB), содержащее, в качестве тяжелых цепей, тяжелые цепи из SEQ ID NO:97 и 98 и, в качестве легких цепей, легкие цепи из SEQ ID NO: 96 и 99, в концентрации 300 нМ, не сдвигает EC50 кривой связывания биспецифического антитела по изобретению с клетками MKN-45 более чем в 3 раза, в одном варианте осуществления, в сторону более высоких концентраций. В таком случае, биспецифическое антитело по изобретению и CEA-TCB определяют как «не конкурентные» и считают способными связываться одновременно с CEA без значительных помех для связывания с указанным CEA.
[0045] В одном варианте осуществления, биспецифическое антитело по изобретению отличается тем, что биспецифическое антитело, специфически связывающееся с CEACAM5 человека и CD3ε (далее также названное как CEA-TCB1), содержащее, в качестве тяжелых и легких цепей, цепи аминокислотных последовательностей SEQ ID NO: 92-95, в концентрации 30 нМ, не сдвигает EC50 кривой связывания биспецифического антитела по изобретению с клетками MKN-45 более чем в 3 раза, в одном варианте осуществления, в сторону более высоких концентраций. В таком случае биспецифическое антитело по изобретению и CEA-TCB1 определяют как «не конкурентные» и считают способными связываться одновременно с CEA без значительных помех для связывания с указанным CEA. В таком случае, биспецифическое антитело по изобретению и MAB CEA, CEA-TCB и/или CEA-TCB1 определяют как «не конкурентные» и считают способными связываться одновременно с CEA без значительных помех для их связывания с указанным CEA.
[0046] В одном варианте осуществления, биспецифическое антитело по изобретению отличается тем, что биспецифическое антитело, специфически связывающееся с CEACAM5 человека и CD3ε (далее также названное как CEA-TCB1), содержащее, в качестве тяжелых и легких цепей, цепи аминокислотных последовательностей SEQ ID NO: 92-95, в концентрации 30 нМ, не сдвигает EC50 кривой показателей фагоцитоза, посредством биспецифического антитела по изобретению, клеток MKN-45 более чем в 3 раза, в одном варианте осуществления, в сторону более высоких концентраций. В таком случае, биспецифическое антитело по изобретению и CEA-TCB1 определяют как «не конкурентные» и считают способными связываться одновременно с CEA без значительных помех для их связывания с указанным CEA, и способными, таким образом, оказывать свой эффект на фагоцитоз (CEAxCD47) без помех, а также свой эффект на активацию T-клеток (CEAxTCB1) без помех, даже если терапевтические уровни обоих лекарственных средств одновременно присутствуют в ткани опухоли (см. фигуру 18).
[0047] В одном варианте осуществления, биспецифическое антитело по изобретению отличается тем, что биспецифическое антитело, специфически связывающееся с CEACAM5 человека и CD3ε (далее также названное как CEA-TCB), содержащее, в качестве тяжелых и легких цепей, цепи аминокислотных последовательностей SEQ ID NO: 96-99 в концентрации 300 нМ, не сдвигает EC50 кривой показателей фагоцитоза, посредством биспецифического антитела по изобретению, клеток MKN-45 более чем в 3 раза, в одном варианте осуществления, в сторону более высоких концентраций. В таком случае биспецифическое антитело по изобретению и CEA-TCB определяют как «не конкурентные» и считают способными связываться одновременно с CEA без значительных помех для их связывания с указанным CEA, и способными, таким образом, оказывать свой эффект на фагоцитоз (CEAxCD47) без помех, а также свой эффект на активацию T-клеток (CEA-TCB) без помех, даже если терапевтические уровни обоих лекарственных средств одновременно присутствуют в ткани опухоли (см. фигуру 18). Это облегчает комбинированную терапию CEA-TCB/TCB1 с CEAxCD47 по этому изобретению (см. фигуру 18).
[0048] Последовательности из SEQ ID NO 88-99 соответствуют US20140242079, соответственно, WO2017055389.
[0049] В одном варианте осуществления, для биспецифических антител CEAxCD47 по изобретению в комбинации с биспецифическими антителами CEAxCD3, подбными CEA-TCB и CEA-TCB1, показан по меньшей мере аддитивный или даже синергический % уничтожения клеток опухолей в анализе, включающем, например, клетки опухоли MKN-45 и макрофаги человека, и T-клетки, полученные от того же самого добровольного донора-человека (см. фигуры 19 A и B).
[0050] В одном варианте осуществления, биспецифическое антитело отличается тем, что содержит общую тяжелую цепь (cHC), в качестве тяжелой цепи первой связывающей части и в качестве тяжелой цепи второй связывающей части. В одном варианте осуществления, биспецифическое антитело отличается тем, что указанная общая тяжелая цепь каждой связывающей части содержит, в качестве CDR, CDRH1 из SEQ ID NO:1, CDRH2 из SEQ ID NO:2 и CDRH3 из SEQ ID NO:3, или CDRH1 из SEQ ID NO:25, CDRH2 из SEQ ID NO:26 и CDRH3 из SEQ ID NO:27. В одном варианте осуществления, биспецифическое антитело отличается тем, что указанная общая тяжелая цепь каждой связывающей части содержит, в качестве общего вариабельного тяжелого домена (cVH), SEQ ID NO:4. В одном варианте осуществления биспецифическое антитело по изобретению отличается тем, что содержит общую тяжелую цепь (cHC), выбранную из группы, состоящей из SEQ ID NO:5, SEQ ID NO:23 и SEQ ID NO:24. В одном варианте осуществления общая тяжелая цепь из SEQ ID NO:5 кодирована последовательностью нуклеиновой кислоты, показанной в SEQ ID NO:6.
[0051] В одном варианте осуществления, биспецифическое антитело по изобретению отличается тем, что содержит, в качестве второй связывающей части, специфической для CD47, общую тяжелую цепь, содержащую, в качестве CDR, CDRH1 из SEQ ID NO:1, CDRH2 из SEQ ID NO:2 и CDRH3 из SEQ ID NO:3, и легкую цепь (LC), содержащую, в качестве CDR, CDRL1 из SEQ ID NO:7, CDRL2 из Ala Ala Ser, включенную в SEQ ID NO:8, и CDRL3 из SEQ ID NO:9, или общую тяжелую цепь, содержащую, в качестве CDR, CDRH1 из SEQ ID NO:25, CDRH2 из SEQ ID NO:26 и CDRH3 из SEQ ID NO:27, и легкую цепь (LC), содержащую, в качестве CDR, CDRL1 из SEQ ID NO:28, CDRL2 из SEQ ID NO:29 и CDRL3 из SEQ ID NO:30.
[0052] В одном варианте осуществления, биспецифическое антитело по изобретению отличается тем, что содержит, в качестве второй связывающей части, тяжелую цепь, содержащую, в качестве вариабельного тяжелого домена (cVH), SEQ ID NO:4 и вариабельный легкий домен (VL) из SEQ ID NO:10.
[0053] В одном варианте осуществления, биспецифическое антитело по изобретению отличается тем, что содержит, в качестве второй связывающей части, тяжелую цепь (cHC), состоящую из SEQ ID NO:5, и легкую цепь (CL) из SEQ ID NO:11. В одном варианте осуществления, биспецифическое антитело по изобретению отличается тем, что содержит, в качестве второй связывающей части, тяжелую цепь (cHC), состоящую из SEQ ID NO:23, и легкую цепь (CL) из SEQ ID NO:11. В одном варианте осуществления, биспецифическое антитело по изобретению отличается тем, что содержит, в качестве второй связывающей части, тяжелую цепь (cHC), состоящую из SEQ ID NO:24, и легкую цепь (CL) из SEQ ID NO:11. В одном варианте осуществления, легкая цепь (LC) из SEQ ID NO:11 кодирована последовательностью нуклеиновой кислоты, показанной в SEQ ID NO:12.
[0054] В одном варианте осуществления, биспецифическое антитело отличается тем, что специфически связывается с CEA и содержит константный домен легкой цепи из SEQ ID NO:13.
[0055] В одном варианте осуществления, биспецифическое антитело по изобретению отличается тем, что ингибирует взаимодействие между CD47 на клетках MKN-45 с IC50 0,1-10 нМ. SIRPα (SIRPα, CD172a; UniProtKB P78324) используют в концентрации 200 нг/мл (меченный His растворимый SIRPальфа). Подробности анализа описаны в примере 8 (блокирующая SIRPα активность антител против CD47), и результаты показаны в таблице 2.
[0056] В одном варианте осуществления, биспецифическое антитело по изобретению отличается зависимым от концентрации фагоцитозом (ADCP) экспрессирующих CEA линий клеток опухолей, подобных клеткам MKN-45, макрофагами человека при EC50 биспецифического антитела ниже 10 нМ. ADCP измеряют по изобретению как показатель фагоцитоза (EC50 или максимум), посредством визуализации, обычно при соотношении E:T 1:3 (макрофаги человека;клетки-мишени (клетки опухолей); см., например, фиг. 12, 15 и 16). Результаты на фигуре 3B получены при E:T 1:1. Подробности анализа описаны в примере 9.2.
[0057] Для получения дополнительной информации, фагоцитоз (ADCP) экспрессирующих CEA линий клеток опухолей, подобных клеткам MKN-45, макрофагами человека при EC50 биспецифического антитела ниже 10 нМ. ADCP также можно измерять посредством проточной цитометрии при соотношении E:T, например, 3:1 (макрофаги человека;клетки-мишени (клетки опухолей); см., например, фиг.3A). Подробности анализа описаны в примере 9 (1. анализ ADCP на основе проточной цитометрии).
[0058] В одном варианте осуществления, биспецифическое антитело отличается тем, что специфически связывается с CEACAM5, но не конкурирует за связывание с CEACAM5 на клетках опухолей, подобных MKN-45, с MAB CEA, CEA-TCB и/или CEA-TCB1.
[0059] В одном варианте осуществления, биспецифическое антитело по изобретению отличается тем, что значение EC50 для связывания с клетками MKN-45 (EC50 между 1 и 200 нМ) увеличивается менее, чем в три раза, посредством добавления MAB CEA или CEA-TCB в концентрации 300 нМ, соответственно, посредством добавления CEA-TCB1 в концентрации 30 нМ (отсутствие конкуренции).
[0060] В одном варианте осуществления, для антител CEAxCD47 по изобретению показана в 100 или более раз более высокая EC50 для фагоцитоза RBC, по сравнению с EC50, измеренной в таком же анализе (пример 15) с использованием B6H12.2.
[0061] В одном варианте осуществления, для антител CEAxCD47 по изобретению (несущих Fc wt IgG1, в отсутствие или в присутствии афукозилирования) не показана значительная активация тромбоцитов в концентрациях вплоть до 200 мкг/мл (см. пример 15 и результаты, упомянутые в примере 15 для биспецифических антител CEAxCD47 K2AC5 и K2AC22).
[0062] В другом варианте осуществления, настоящее изобретение относится к биспецифическому антителу по изобретению, подвергнутого гликоинженерии для получения области Fc с модифицированными олигосахаридами. Неожиданно обнаружено, что такое подвергнутое гликоинженерии биспецифическое антитело по изобретению отличается по меньшей мере в 3 раза более низким значением EC50 для кривой показателей фагоцитоза, измеренным посредством анализа на основе визуализации), чем такое же, не подвергнутое гликоинженерии (исходное) биспецифическое антитело, при измерении в таких же экспериментальных условиях. В одном варианте осуществления, EC50 для показателя фагоцитоза составляет в 5-10 раз ниже или в 10-30 раз ниже). В одном варианте осуществления, область Fc модифицирована для получения уменьшенного количества остатков фукозы по сравнению с таким же, но не подвергнутым гликоинженерии биспецифическим антителом. В другом варианте осуществления, область Fc имеет увеличенную долю разделенных надвое олигосахаридов, по сравнению с не подвергнутым гликоинженерии биспецифическим антителом. В другом варианте осуществления, разделенные надвое олигосахариды, предпочтительно, представляют собой разделенный надвое комплекс. В другом варианте осуществления, подвергнутые гликоинженерии антигенсвязывающие молекулы по изобретению имеют увеличенную долю разделенных надвое, нефукозилированных олигосахаридов в области Fc указанного биспецифического антитела, по сравнению с не подвергнутым гликоинженерии биспецифическим антителом. Альтернативно, биспецифические антитела по изобретению могут иметь увеличенное соотношение остатков GIcNAc к остаткам фукозы в области Fc, по сравнению с не подвергнутым гликоинженерии биспецифическим антителом. В одном варианте осуществления, разделенные надвое, нефукозилированные олигосахариды преобладают в гибридной форме. Альтернативно, разделенные надвое, нефукозилированные олигосахариды преобладают комплексного типа.
[0063] В одном варианте осуществления, биспецифическое антитело по изобретению отличается тем, что 50%-100% N-связанных олигосахаридов в области Fc являются нефукозилированными.
[0064] В одном варианте осуществления, биспецифическое антитело отличается тем, что 50%-100% N-связанных олигосахаридов в области Fc являются разделенными надвое.
[0065] В одном варианте осуществления биспецифическое антитело отличается тем, что 80%-100% N-связанных олигосахаридов в области Fc являются разделенными надвое и нефукозилированными.
[0066] В одном варианте осуществления, биспецифическое антитело отличается тем, что кривая концентрации/ADCC (уменьшение EC50 или увеличение максимума ADCC (см. фигуры 13 и 14), индуцированной указанным подвергнутым гликоинженерии антителом, увеличена, по меньшей мере в 1,2 раза, по сравнению с ADCC, индуцированной таким же, но не подвергнутым гликоинженерии биспецифическим антителом. В одном варианте осуществления ADCC увеличена в 1,2-2,0 раза.
[0067] В одном варианте осуществления биспецифическое антитело отличается по меньшей мере в 3 раза более низким значением EC50 для кривой показателей фагоцитоза, измеренным посредством анализа на основе визуализации, по сравнению с таким же, но не подвергнутым гликоинженерии (исходным) биспецифическим антителом, при измерении в таких же экспериментальных условиях. В одном варианте осуществления, EC50 для показателя фагоцитоза составляет в 5-10 раз ниже или в 10-30 раз ниже
[0068] В одном варианте осуществления, биспецифическое антитело отличается тем, что максимальный показатель фагоцитоза, индуцированный указанным подвергнутым гликоинженерии антителом и измеренный посредством проточной цитометрии, увеличен по меньшей мере в 1,2 раза, по сравнению с максимальным показателем фагоцитоза, индуцированным таким же, но не подвергнутым гликоинженерии биспецифическим антителом. В одном варианте осуществления максимальный показатель фагоцитоза увеличен в 1,2-2,0 раза.
[0069] В одном варианте осуществления, биспецифическое антитело отличается тем, что максимальный показатель фагоцитоза, индуцированный указанным подвергнутым гликоинженерии антителом и измеренный посредством визуализации, увеличен по меньшей мере в 1,2 раза, по сравнению с максимальным показателем фагоцитоза, индуцированным таким же, но не подвергнутым гликоинженерии биспецифическим антителом. В одном варианте осуществления максимальный показатель фагоцитоза увеличен в 1,2-2,0 раза.
[0070] В одном варианте осуществления, биспецифическое антитело по изобретению отличается тем, что содержит одну, две или три аминокислотные замены в области Fc («аминокислотную замену в Fc») выбранные из группы, состоящей из одиночных замен S239D, I332E, G236A, двойных замен I332E и G236A, S239D и I332E, S239D и G236A, и тройной замены S329D и I332E и G236A.
[0071] В одном варианте осуществления, биспецифическое антитело по изобретению отличается тем, что содержит одну, две или три аминокислотные замены в области Fc, выбранные из группы, состоящей из одиночных замен S239D, I332E, G236A, двойных замен I332E и G236A, S239D и I332E, S239D и G236A, и тройной замены S329D и I332E и G236A, и область Fc, подвергнутую гликоинженерии для получения уменьшенного количества остатков фукозы по сравнению с таким же, но не подвергнутым гликоинженерии биспецифическим антителом.
[0072] В одном варианте осуществления, биспецифическое антитело, содержащее указанные замены в области Fc, отличается тем, что кривая концентрации/ADCC (уменьшение EC50 или увеличение максимума ADCC), индуцированная указанным антителом с аминокислотными заменами, увеличена по меньшей мере в 1,2 раза, по сравнению с ADCC, индуцированной указанным антителом, не содержащим указанных аминокислотных замен в области Fc. В одном варианте осуществления ADCC увеличена в 1,2-2,0 раза.
[0073] В одном варианте осуществления, биспецифическое антитело, содержащее указанные замены в области Fc, отличается по меньшей мере в 3 раза более низким значением EC50 для кривой показателей фагоцитоза, измеренным посредством анализа на основе визуализации, по сравнению с таким же (исходным) биспецифическим антителом, не содержащим указанных аминокислотных замен в области Fc, при измерении в таких же экспериментальных условиях. В одном варианте осуществления, EC50 для показателя фагоцитоза составляет в 5-10 раз ниже, или в 10-30 раз ниже
[0074] В одном варианте осуществления, биспецифическое антитело, содержащее указанные замены в области Fc, отличается тем, что определенный посредством проточной цитометрии максимальный фагоцитоз (ADCP), индуцированный указанным антителом с аминокислотными заменами, увеличен по меньшей мере в 1,2 раза, по сравнению с ADCP, индуцированным указанным антителом, не содержащим указанных аминокислотных замен в области Fc. В одном варианте осуществления ADCP увеличен в 1,2-2,0 раза. В одном варианте осуществления, биспецифическое антитело, содержащее указанные замены в области Fc, отличается тем, что определенный посредством визуализации максимальный показатель фагоцитоза, индуцированный указанным антителом с аминокислотными заменами, увеличен по меньшей мере в 1,2 раза, по сравнению с ADCP, индуцированным указанным антителом, не содержащим указанных аминокислотных замен в области Fc. В одном варианте осуществления ADCP увеличен в 1,2-2,0 раза.
[0075] В одном варианте осуществления, биспецифическое антитело по изобретению отличается тем, что 50%-100%, 60%-100%, 70%-100% или 80%-100% N-связанных олигосахаридов в области Fc являются нефукозилиированными. В одном варианте осуществления, биспецифическое антитело по изобретению отличается тем, что 50%-100%, 60%-100%, 70%-100% или 80%-100% N-связанных олигосахаридов в области Fc являются разделенными надвое. В одном варианте осуществления, биспецифическое антитело по изобретению отличается тем, что 50%-100%, 60%-100%, 70%-100% или 80%-100% N-связанных олигосахаридов в области Fc являются разделенными надвое, нефукозилированными.
[0076] В одном варианте осуществления, подвергнутое гликоинженерии биспецифическое антитело имеет увеличенные эффекторные функции, по сравнению с не подвергнутым гликоинженерии биспецифическим антителом, содержащим, в качестве общей тяжелой цепи, SEQ ID NO:5 (исходным биспецифическим антителом, продуцированным линией клеток CHO K1, CHO-K1 (ATCC® CCL-61™, в стандартных условиях, как определено ниже).
[0077] В одном варианте осуществления, биспецифическое антитело по изобретению отличается тем, что указанное подвергнутое гликоинженерии биспецифическое антитело имеет одну или несколько увеличенных эффекторных функций, таких как функции из группы, состоящей из увеличенной аффинности связывания с FcγR, увеличенного связывания с макрофагами (увеличенного антителозависимого клеточного фагоцитоза; ADCP), увеличенного связывания с клетками NK (увеличенной опосредованной антителом клеточной цитотоксичности; ADCC) и увеличенного связывания с моноцитами.
[0078] Концентрация/кривая показателей фагоцитоза, измеренная для моноклонального антитела против CD47 hu5F9-G4 (тестированного в клинических исследованиях с 2014 г., см., например, clintrial.gov), сильно уменьшается посредством добавления huIgG, добавленного в анализ в физиологических концентрациях 1 мг/мл (увеличение EC50 и уменьшение максимума кривой фагоцитоза, измеренного в анализе на основе визуализации, см., например, на фигуре 17).
[0079] Неожиданно, для антител CEAxCD47 по изобретению показан только небольшой сдвиг EC50, ниже чем в 3 раза, и отсутствие значительного уменьшения максимума концентрации/кривой показателей фагоцитоза при добавлении IgG человека (см. таблицу 4).
[0080] В одном варианте осуществления, антитела CEAxCD47 по изобретению отличаются тем, что добавление 1 мг /мл hu IgG в анализ фагоцитоза на основе визуализации вызывает уменьшение, менее чем в 0,9 раз, максимума концентрации/кривой показателей фагоцитоза, и/или сдвиг EC50, менее чем в 3 раза, в сторону более высоких концентраций (см. таблицу 4)
[0081] Дополнительный вариант осуществления изобретения представляет собой выделенный полинуклеотид, отличающийся кодированием биспецифического антитела по изобретению.
[0082] Дополнительный вариант осуществления изобретения представляет собой экспрессирующий вектор, содержащий полинуклеотид по изобретению.
[0083] Дополнительный вариант осуществления изобретения представляет собой клетку-хозяина, содержащую экспрессирующий вектор по изобретению.
[0084] Дополнительный вариант осуществления изобретения представляет собой способ получения биспецифического антитела по изобретению, отличающийся включением:
a) культивирования клетки-хозяина, содержащей экспрессирующий вектор, кодирующий указанное биспецифическое антитело, в условиях, обеспечивающих продукцию указанного антитела по изобретению, и
b) выделения указанного антитела, где указанное антитело является способным специфически связываться с CEA и CD47.
[0085] В одном варианте осуществления, изобретение отличается тем, что относится к способу продукции подвергнутого гликоинженерии биспецифического антитела по изобретению в клетке-хозяине, где указанный способ включает:
a) культивирование клетки-хозяина, подвергнутой гликоинженерии, для экспрессии по меньшей мере одной нуклеиновой кислоты, кодирующей полипептид, имеющий активность β(1,4)-N-ацетилглюкозаминилтрансферазы III, в условиях, обеспечивающих продукцию указанного биспецифического антитела по изобретению, и позволяющих модификацию олигосахаридов, присутствующих в области Fc указанного биспецифического антитела; и
b) выделение указанного подвергнутого гликоинженерии биспецифического антитела, где указанное подвергнутое гликоинженерии биспецифическое антитело является способным специфически связываться с CEA и CD47.
[0086] В одном варианте осуществления, изобретение отличается тем, что относится к способу продукции подвергнутого гликоинженерии биспецифического антитела в клетке-хозяине, где указанный способ включает:
a) культивирование клетки-хозяина, подвергнутой гликоинженерии, посредством направленного повреждения гена FUT8, в условиях, обеспечивающих продукцию указанного биспецифического антитела по изобретению, и позволяющих модификацию олигосахаридов, присутствующих в области Fc указанного биспецифического антитела, и
b) выделение указанного подвергнутого гликоинженерии биспецифического антитела, где указанное подвергнутое гликоинженерии биспецифическое антитело является способным специфически связываться с CEA и CD47.
[0087] В одном варианте осуществления, изобретение отличается тем, что относится к способу продукции Fc-замещенного биспецифического антитела по изобретению в клетке-хозяине, где указанный способ включает:
a) культивирование клетки-хозяина, содержащей экспрессирующий вектор, кодирующий Fc-замещенное, биспецифическое антитело по изобретению в условиях, обеспечивающих продукцию указанного биспецифического антитела, и
b) выделение указанного Fc-замещенного биспецифического антитела, где указанное биспецифическое антитело является способным специфически связываться с CEA и CD47.
[0088] Дополнительный вариант осуществления изобретения представляет собой способ индукции клеточного лизиса клетки опухоли, включающий приведение клетки опухоли в контакт с биспецифическим антителом по изобретению. Клетка опухоли представляет собой клетку опухоли человека, предпочтительно, в организме пациента.
[0089] Дополнительный вариант осуществления изобретения представляет собой способ по изобретению, отличающийся тем, что клетка опухоли представляет собой клетку колоректального рака, клетку NSCLC (немелкоклеточного рака легкого), клетку рака желудка, клетку рака поджелудочной железы, клетку рака молочной железы или другую клетку опухоли, экспрессирующую CEA.
[0090] Дополнительный вариант осуществления изобретения представляет собой способ лечения индивида, имеющего злокачественную опухоль, экспрессирующую CEA, включающий введение индивиду терапевтически эффективного количества биспецифического антитела по изобретению.
[0091] Дополнительный вариант осуществления изобретения представляет собой способ увеличения времени выживаемости индивида, имеющего злокачественную опухоль, экспрессирующую CEA, где указанный способ включает введение указанному индивиду терапевтически эффективного количества биспецифического антитела по изобретению.
[0092] Дополнительный вариант осуществления изобретения представляет собой способ по изобретению, отличающийся тем, что злокачественная опухоль представляет собой колоректальный рак, немелкоклеточный рак легкого (NSCLC), рак желудка, рак поджелудочной железы или молочной железы.
[0093] Дополнительный вариант осуществления изобретения представляет собой способ по изобретению, отличающийся тем, что биспецифическое антитело по изобретению вводят в комбинации с химиотерапией или радиотерапией индивиду-человеку.
[0094] Дополнительный вариант осуществления изобретения представляет собой способ лечения индивида, имеющего злокачественную опухоль, экспрессирующую CEA, включающий введение индивиду терапевтически эффективного количества биспецифического антитела по изобретению, отличающийся тем, что значение EC50 для фагоцитоза указанного биспецифического антитела лежит в диапазоне от 0,1- до 3-кратного значения E50 эталонного антитела K2AC22 в таких же экспериментальных условиях и в присутствии и/или в отсутствие 1 мг/мл IgG человека. В следующих вариантах осуществления диапазон составляет 0,2-3,0, 0,3-3,0, 0,5-2,5 или 1,0-2,5. В одном варианте осуществления биспецифическое антитело отличается тем, что связывается с CD47 человека с аффинностью связывания 100 нМ - 600 нМ, в одном варианте осуществления, с аффинностью связывания 100 нМ - 500 нМ.
[0095] Дополнительный вариант осуществления изобретения представляет собой применение биспецифического антитела по изобретению в способе лечения индивида, имеющего злокачественную опухоль, экспрессирующую CEA, включающем введение индивиду терапевтически эффективного количества биспецифического антитела по изобретению, отличающемся тем, что значение EC50 для фагоцитоза указанного биспецифического антитела лежит в диапазоне от 0,1- до 3-кратного значения E50 эталонного антитела K2AC22 в таких же экспериментальных условиях и в присутствии и/или в отсутствие 1 мг/мл IgG человека. В следующих вариантах осуществления, диапазон составляет 0,2-3,0, 0,3-3,0, 0,5-2,5 или 1,0-2,5. В одном варианте осуществления, биспецифическое антитело отличается тем, что связывается с CD47 человека с аффинностью связывания 100 нМ - 600 нМ, в одном варианте осуществления, с аффинностью связывания 100 нМ - 500 нМ.
[0096] Как можно видеть из фигур 13-17, на значения ADCC и ADCP/показателя фагоцитоза антител по изобретению не влияют или только до низкой степени влияют IgG человека в концентрации 1 мг/мл (1 мг/мл или даже более высокая концентрация IgG человека присутствует у большинства пациентов), в то время как для антитела против CD47 предшествующего уровня техники (hu5F9-G4), значения ADCC и ADCP сильно уменьшаются в присутствии 1 мг/мл IgG человека.
[0097] Дополнительный вариант осуществления изобретения представляет собой применение биспецифического антитела по изобретению в изготовлении лекарственного средства для лечения индивида, имеющего злокачественную опухоль, экспрессирующую CEA.
[0098] Дополнительный вариант осуществления изобретения представляет собой применение биспецифического антитела по изобретению в изготовлении лекарственного средства по изобретению, отличающееся тем, что злокачественная опухоль выбрана из группы, состоящей из колоректального рака, немелкоклеточного рака легкого (NSCLC), рака желудка, рака поджелудочной железы и рака молочной железы.
[0099] Дополнительный вариант осуществления изобретения представляет собой биспецифическое антитело по изобретению, для применения в одновременной, отдельной или последовательной комбинации с вторым биспецифическим антителом, содержащим третью связывающую часть, специфически связывающуюся с CEACAM5 человека, и четвертую связывающую часть, специфически связывающуюся с CD3ε человека, в лечении индивида, имеющего злокачественную опухоль, экспрессирующую CEA. Дополнительный вариант осуществления изобретения представляет собой биспецифическое антитело по изобретению, для применения в одновременной, отдельной или последовательной комбинации с вторым биспецифическим антителом, содержащим третью связывающую часть, специфически связывающуюся с CEACAM5 человека и четвертую связывающую часть, специфически связывающуюся с эпитопом CD3ε человека, где указанный эпитоп содержит аминокислотную последовательность из SEQ ID NO:22, в лечении индивида, имеющего злокачественную опухоль, экспрессирующую CEA.
[0100] Дополнительный вариант осуществления изобретения представляет собой биспецифическое антитело по изобретению, для применения в одновременной, отдельной или последовательной комбинации с CEA-TCB и/или CEA/TCB1 в лечении индивида, имеющего злокачественную опухоль, экспрессирующую CEA.
[0101] Дополнительный вариант осуществления изобретения представляет собой биспецифическое антитело по изобретению, для применения в одновременной, отдельной или последовательной комбинации с вторым биспецифическим антителом, содержащим третью связывающую часть, специфически связывающуюся с CEACAM5 человека, содержащую вариабельную область тяжелой цепи из SEQ ID NO:20 и вариабельную область легкой цепи из SEQ ID NO:21, и четвертую связывающую часть, специфически связывающуюся с эпитопом CD3ε человека, где указанный эпитоп содержит аминокислотную последовательность из SEQ ID NO:22, в лечении индивида, имеющего злокачественную опухоль, экспрессирующую CEA. Дополнительный вариант осуществления изобретения представляет собой биспецифическое антитело по изобретению, отличающееся тем, что не конкурирует с указанным вторым биспецифическим антителом для применения в одновременной, отдельной или последовательной комбинации с указанным вторым биспецифическим антителом в лечении индивида, имеющего злокачественную опухоль, экспрессирующую CEA.
[0102] Дополнительный вариант осуществления изобретения представляет собой биспецифическое антитело по изобретению, отличающееся тем, что не конкурирует с CEA-TCB или CEA-TCB1, для применения в одновременной, отдельной или последовательной комбинации с указанным CEA-TCB или CEA-TCB1 в лечении индивида, имеющего злокачественную опухоль, экспрессирующую CEA.
[0103] Дополнительный вариант осуществления изобретения представляет собой биспецифическое антитело по изобретению, отличающееся тем, что конкурирует с CEA-TCB или CEA-TCB1, для применения в одновременной, отдельной или последовательной комбинации с указанным CEA-TCB или CEA-TCB1 в лечении индивида, имеющего злокачественную опухоль, экспрессирующую CEA.
[0104] Дополнительный вариант осуществления изобретения представляет собой биспецифическое антитело по изобретению, для применения в одновременной, отдельной или последовательной комбинации с вторым биспецифическим антителом, содержащим третью связывающую часть, специфически связывающуюся с CEACAM5 человека, содержащую вариабельную область тяжелой цепи из SEQ ID NO:88 и вариабельную область легкой цепи из SEQ ID NO:89, и четвертую связывающую часть, специфически связывающуюся с CD3ε человека, содержащую вариабельную область тяжелой цепи из SEQ ID NO:90 и вариабельную область легкой цепи из SEQ ID NO:91.
[0105] Дополнительный вариант осуществления изобретения представляет собой биспецифическое антитело по изобретению, для применения по изобретению, отличающегося тем, что биспецифическое антитело по изобретению и второе биспецифическое антитело вводят указанному индивиду попеременно с интервалами 6-15 суток.
[0106] Дополнительный вариант осуществления изобретения представляет собой биспецифическое антитело по изобретению, для применения по изобретению, отличающегося тем, что биспецифическое антитело по изобретению и второе биспецифическое антитело вводят указанному индивиду одновременно с интервалами 6-15 суток.
[0107] Дополнительный вариант осуществления изобретения представляет собой первое биспецифическое антитело по изобретению, содержащее первую связывающую часть, специфически связывающуюся с CEACAM5 человека, и вторую связывающую часть, специфически связывающуюся с CD47 человека, для применения в одновременной, отдельной или последовательной комбинации в лечении индивида, имеющего злокачественную опухоль, экспрессирующую CEA, с вторым биспецифическим антителом, содержащим третью связывающую часть, специфически связывающуюся с CEACAM5 человека, содержащую вариабельную область тяжелой цепи из SEQ ID NO:20 и вариабельную область легкой цепи из SEQ ID NO:21, и четвертую связывающую часть, специфически связывающуюся с эпитопом CD3ε человека, содержащим аминокислотную последовательность из SEQ ID NO:22, в результате чего указанное второе биспецифическое антитело в концентрации 300 нМ не сдвигает значение EC50 кривой показателей фагоцитоза клеток MKN-45 посредством биспецифического антитела по изобретению более чем в 3 раза, в одном варианте осуществления, в сторону более высоких концентраций.
[0108] Дополнительный вариант осуществления изобретения представляет собой первое биспецифическое антитело по изобретению, содержащее первую связывающую часть, специфически связывающуюся с CEACAM5 человека, и вторую связывающую часть, специфически связывающуюся с CD47 человека, для применения в одновременной, отдельной или последовательной комбинации в лечении индивида, имеющего злокачественную опухоль, экспрессирующую CEA, с вторым биспецифическим антителом, содержащим третью связывающую часть, специфически связывающуюся с CEACAM5 человека, содержащую вариабельную область тяжелой цепи из SEQ ID NO:88 и вариабельную область легкой цепи из SEQ ID NO:89, и четвертую связывающую часть, специфически связывающуюся с CD3ε человека, содержащую вариабельную область тяжелой цепи из SEQ ID NO:90 и вариабельную область легкой цепи из SEQ ID NO:91, в результате чего указанное второе биспецифическое антитело в концентрации 30 нМ не сдвигает EC50 кривой связывания с клетками MKN-45 биспецифического антитела по изобретению более чем в 3 раза, в одном варианте осуществления, в сторону более высоких концентраций.
[0109] Дополнительный вариант осуществления изобретения представляет собой первое биспецифическое антитело по изобретению, для применения в одновременной, отдельной или последовательной комбинации в лечении индивида, имеющего злокачественную опухоль, экспрессирующую CEA, с CEA-TCB или CEA-TCB1, в результате чего указанное CEA-TCB в концентрации 300 нМ или CEA-TCB1 в концентрации 30 нМ не сдвигает EC50 кривой связывания с клетками MKN-45 биспецифического антитела по изобретению более чем в 3 раза, в одном варианте осуществления, в сторону более высоких концентраций.
[0110] Дополнительный вариант осуществления изобретения представляет собой первое биспецифическое антитело по изобретению, содержащее первую связывающую часть, специфически связывающуюся с CEACAM5 человека, и вторую связывающую часть, специфически связывающуюся с CD47 человека, по изобретению, для применения по изобретению, отличающегося тем, что указанная злокачественная опухоль представляет собой колоректальный рак, немелкоклеточный рак легкого (NSCLC), рак желудка, рак поджелудочной железы и рак молочной железы.
[0111] Дополнительный вариант осуществления изобретения представляет собой композицию, содержащую биспецифическое антитело по изобретению, отличающееся тем, что не конкурирует с указанным вторым биспецифическим антителом, как определено выше, для применения в лечении индивида, имеющего злокачественную опухоль, экспрессирующую CEA.
[0112] Дополнительный вариант осуществления изобретения представляет собой композицию, содержащую биспецифическое антитело по изобретению, отличающееся тем, что не конкурирует с вторым биспецифическим антителом, содержащим третью связывающую часть, специфически связывающуюся с CEACAM5 человека, содержащую вариабельную область тяжелой цепи из SEQ ID NO:20 и вариабельную область легкой цепи из SEQ ID NO:21, и четвертую связывающую часть, специфически связывающуюся с эпитопом CD3ε человека, содержащим аминокислотную последовательность из SEQ ID NO:22, для применения в лечении индивида, имеющего злокачественную опухоль, экспрессирующую CEA.
[0113] Дополнительный вариант осуществления изобретения представляет собой композицию, содержащую биспецифическое антитело по изобретению, отличающееся тем, что не конкурирует с вторым биспецифическим антителом, содержащим третью связывающую часть, специфически связывающуюся с CEACAM5 человека, содержащую вариабельную область тяжелой цепи из SEQ ID NO:88 и вариабельную область легкой цепи из SEQ ID NO:89, и четвертую связывающую часть, специфически связывающуюся с CD3ε человека, содержащую вариабельную область тяжелой цепи из SEQ ID NO:90 и вариабельную область легкой цепи из SEQ ID NO:91, для применения в лечении индивида, имеющего злокачественную опухоль, экспрессирующую CEA. Дополнительный вариант осуществления изобретения представляет собой композицию, содержащую биспецифическое антитело по изобретению, отличающееся тем, что не конкурирует с CEA-TCB и/или CEA-TCB1.
[0114] Дополнительный вариант осуществления изобретения представляет собой способ лечения пациента-человека, у которого диагностирована опухоль (злокачественная опухоль), особенно солидная опухоль, особенно солидная злокачественная опухоль, экспрессирующая CEA, особенно колоректальный рак, немелкоклеточный рак легкого (NSCLC), рак желудка, рак поджелудочной железы и рак молочной железы, включающий введение эффективного количества биспецифического антитела по изобретению и второго биспецифического антитела, как описано выше, против CEA и CD3 (в одном варианте осуществления CEA-TCB или CEA-TCB1), пациенту-человеку, включающий последовательно:
введение пациенту дозы 0,1-10 мг/кг, в следующем варианте осуществления, 0,5-10 мг/кг, в следующем варианте осуществления, 1-2 мг/кг, указанного второго антитела против CEAxCD3, например, еженедельно в течение 4-12 недель.
введение пациенту указанного второго антитела q1, q2w, q3w или, необязательно, q4w,
введение, после этих 4-12 недель и после дополнительных 2 или 3 или 4 периодов полувыведения указанного антитела против CEAxCD3, пациенту дозы 0,1-20 мг/кг антитела по изобретению,
введение пациенту указанного антитела по изобретению q1, q2w, q3w или, необязательно, q4w,
ожидание 2 или 3 или 4 периодов полувыведения указанного антитела по изобретению и затем
необязательно, повтор указанного цикла введения биспецифического антитела CEA x CD3, с последующим введением биспецифического антитела CEA x CD47 и необязательно, снова повтор этого цикла.
[0115] Этот «чередующийся» способ используют, если антитело по изобретению и второе биспецифическое антитело являются конкурентными.
[0116] В случае, когда указанное биспецифическое антитело CEA x CD3 и биспецифическое антитело CEA x CD47 по настоящему изобретению являются не конкурентными, два биспецифических антитела можно также вводить таким способом («одновременным способом»), что пациента подвергают воздействию терапевтически эффективных концентраций в плазме и ткани обоих биспецифических антител параллельно, например, посредством введения пациенту в приблизительно одно и то же время дозы 0,1-10 мг/кг, в следующем варианте осуществления, 0,5-10 мг/кг, в следующем варианте осуществления, 1-2 мг/кг, биспецифического антитела CEA x CD3 и 1-20 мг/кг биспецифического антитела CEA x CD47 по этому изобретению, с последующими одним или несколькими из этих комбинированных введений с частотой q1w или q2w, или q3w, или, необязательно, q4w.
[0117] Термин «Q1w» обозначает введение один раз в неделю; q2w обозначает введение каждые две недели и т.д.
[0118] Дополнительный вариант осуществления изобретения представляет собой фармацевтическую композицию, содержащую антитело по изобретению и фармацевтически приемлемый наполнитель или носитель.
[0119] Следующий предпочтительный вариант осуществления изобретения представляет собой фармацевтическую композицию, содержащую антитело по изобретению, для применения в качестве лекарственного средства.
[0120] Следующий предпочтительный вариант осуществления изобретения представляет собой фармацевтическую композицию, содержащую антитело по изобретению, для применения в качестве лекарственного средства в лечении нарушений с солидными опухолями.
[0121] Следующий предпочтительный вариант осуществления изобретения представляет собой фармацевтическую композицию, содержащую антитело по изобретению, для применения в качестве лекарственного средства в лечении колоректального рака, NSCLC (немелкоклеточного рака легкого), рака желудка, рака поджелудочной железы или рака молочной железы.
[0122] Дополнительный вариант осуществления изобретения представляет собой композицию, содержащую биспецифическое антитело по изобретению, для применения в одновременной, отдельной или последовательной комбинации в лечении индивида, имеющего злокачественную опухоль, экспрессирующую CEA, с вторым биспецифическим антителом, содержащим третью связывающую часть, специфически связывающуюся с CEACAM5 человека, содержащую вариабельную область тяжелой цепи из SEQ ID NO:20 и вариабельную область легкой цепи из SEQ ID NO:21, и четвертую связывающую часть, специфически связывающуюся с эпитопом CD3ε человека, содержащим аминокислотную последовательность из SEQ ID NO:22, в результате чего указанное второе биспецифическое антитело в концентрации 300 нМ не сдвигает EC50 кривой связывания с клетками MKN-45 биспецифического антитела по изобретению более чем в 3 раза, в одном варианте осуществления, в сторону более высоких концентраций.
[0123] Дополнительный вариант осуществления изобретения представляет собой композицию, содержащую биспецифическое антитело по изобретению, для применения в одновременной, отдельной или последовательной комбинации в лечении индивида, имеющего злокачественную опухоль, экспрессирующую CEA, с вторым биспецифическим антителом, содержащим третью связывающую часть, специфически связывающуюся с CEACAM5 человека, содержащую вариабельную область тяжелой цепи из SEQ ID NO:88 и вариабельную область легкой цепи из SEQ ID NO:89, и четвертую связывающую часть, специфически связывающуюся с CD3ε человека, содержащую вариабельную область тяжелой цепи из SEQ ID NO:90 и вариабельную область легкой цепи из SEQ ID NO:91, в результате чего указанное второе биспецифическое антитело в концентрации 30 нМ не сдвигает EC50 кривой связывания с клетками MKN-45 биспецифического антитела по изобретению более чем в 3 раза, в сторону более высоких концентраций.
[0124] Дополнительный вариант осуществления изобретения представляет собой композицию по изобретению, отличающуюся тем, что злокачественная опухоль представляет собой колоректальный рак, немелкоклеточный рак легкого (NSCLC), рак желудка, рак поджелудочной железы, или рак молочной железы.
[0125] Дополнительный вариант осуществления изобретения представляет собой применение антитела по изобретению для изготовления фармацевтической композиции.
[0126] Дополнительный вариант осуществления изобретения представляет собой применение антитела по изобретению и фармацевтически приемлемого наполнителя или носителя для изготовления фармацевтической композиции.
[0127] Дополнительный вариант осуществления изобретения представляет собой применение антитела по изобретению для изготовления лекарственного средства, в лечении нарушений с солидными опухолями.
[0128] Дополнительный вариант осуществления изобретения представляет собой применение антитела по изобретению в лечении колоректального рака, NSCLC (немелкоклеточного рака легкого), рака желудка, рака поджелудочной железы или рака молочной железы.
[0129] В другом аспекте, настоящее изобретению относится к способу индукции клеточного лизиса клетки опухоли, включающему приведение клетки опухоли в контакт с биспецифическим антителом из любого из вышеописанных вариантов осуществления. В некоторых вариантах осуществления, клетка опухоли представляет собой клетку колоректального рака, NSCLC (немелкоклеточного рака легкого), клетку рака желудка, клетку рака поджелудочной железы или клетку рака молочной железы.
[0130] В одном варианте осуществления, лизис клетки индуцируют посредством антителозависимого клеточного фагоцитоза и/или антителозависимой клеточной цитотоксичности биспецифического антитела.
[0131] В другом аспекте, настоящее изобретению относится к способу лечения индивида, имеющего злокачественную опухоль, аномально экспрессирующую CEA, включающему введение индивиду терапевтически эффективного количества биспецифического антитела из любого из вышеописанных вариантов осуществления.
[0132] В другом аспекте, настоящее изобретению относится к способу лечения индивида, имеющего злокачественную опухоль, аномально экспрессирующую CEA, включающему введение индивиду терапевтически эффективного количества биспецифического антитела из любого из вышеописанных вариантов осуществления в комбинации с биспецифическим антителом, связывающимся с CEA человека и CD3 человека. Если антитело CEAxCD47 и антитело CEAxCD3 являются конкурентными, они могут конкурировать за рецепторы CEA на поверхности клетки опухоли, и занятость и эффективность рецептора для каждого партнера в комбинации зависит от их аффинности связывания и их концентраций в плазме, и таким образом, является трудно предсказуемой, а также изменчивой с течением времени, если концентрации двух лекарственных средств имеют различное время полувыведения, соответственно выведению из организма. Таким образом, конкурентные биспецифические антитела CEAxCD3 и CEAxCD47 необходимо вводить последовательно (с чередованием). Если биспецифические антитела CEAxCD3 и CEAxCD47 являются не конкурентными или только минимально конкурентными, их можно вводить не только последовательно, но также параллельно (одновременно), что может действительно представлять собой преимущество, поскольку уничтожение клетки опухоли с использованием привлечения T-клеток посредством биспецифического антитела CEAxCD3 и, в то же самое время, с использованием привлечения макрофагов посредством биспецифического антитела CEAxCD47, является аддитивным или может являться даже синергическим, что означает, что эффективность увеличивается, если оба лекарственных средства вводят параллельно.
[0133] В другом аспекте, настоящее изобретению относится к способу увеличения времени выживаемости без прогрессирования и/или общей выживаемости индивида, имеющего злокачественную опухоль, аномально экспрессирующую CEA, где указанный способ включает введение указанному индивиду терапевтически эффективного количества биспецифического антитела из любого из вышеописанных вариантов осуществления. В одном варианте осуществления, злокачественная опухоль представляет собой колоректальный рак, немелкоклеточный рак легкого (NSCLC), рак желудка, рак поджелудочной железы или рак молочной железы, или другую злокачественную опухоль, экспрессирующую CEA.
[0134] В конкретных вариантах осуществления этих способов, биспецифическое антитело вводят в комбинации с химиотерапией или радиотерапией. В одном варианте осуществления, индивид представляет собой пациента, страдающего от колоректального рака или рака легкого, или рака желудка, или рака поджелудочной железы, или рака молочной железы, или другой злокачественной опухоли, экспрессирующей CEA.
[0135] В другом аспекте, настоящее изобретению относится к способу лечения индивида, имеющего злокачественную опухоль, аномально экспрессирующую CEA, включающему введение индивиду терапевтически эффективного количества биспецифического антитела из любого из вышеописанных вариантов осуществления в комбинации с биспецифическим антителом против CEA человека и CD3-эпсилон человека.
[0136] В другом аспекте, настоящее изобретению относится к способу увеличения времени выживаемости без прогрессирования и/или общей выживаемости индивида, имеющего злокачественную опухоль, аномально экспрессирующую CEA, где указанный способ включает введение указанному индивиду терапевтически эффективного количества биспецифического антитела из любого из вышеописанных вариантов осуществления. В одном варианте осуществления, злокачественная опухоль представляет собой колоректальный рак, немелкоклеточный рак легкого (NSCLC), рак желудка, рак поджелудочной железы или рак молочной железы.
[0137] В конкретных вариантах осуществления этих способов, биспецифическое антитело вводят в комбинации с химиотерапией или радиотерапией. В одном варианте осуществления, индивид представляет собой пациента с злокачественной опухолью с колоректальным раком или раком легкого, или раком желудка, или раком поджелудочной железы, или раком молочной железы, или другой экспрессирующей CEA злокачественной опухолью.
[0138] Другой вариант осуществления изобретения относится к применению биспецифического антитела по изобретению для любого из вышеописанных способов лечения. В одном варианте осуществления, злокачественная опухоль выбрана из группы, состоящей из колоректального рака, немелкоклеточного рака легкого (NSCLC), рака желудка, рака поджелудочной железы и рака молочной железы.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0139] На фигуре 1 показан общий молекулярный формат биспецифических антител CEAxCD47 по этому изобретению; структура полноразмерного IgG1 человека, неотличимая от моноклонального антитела IgG и без ак-мостиков для минимизации иммуногенности и образования антитела против лекарственного средства ADA; общая тяжелая цепь (см. список последовательностей); легкая цепь каппа (CL и VL) в связывающей CD47 части (см. список последовательностей); CL лямбда в связывающей CEA части (см. список последовательностей) и VL лямбда или каппа в связывающей CEA части (A); гликоинженерия (низкое содержание фукозы) Fc или мутация(мутации) ак, или и то, и другое, для увеличения ADCP и ADCC (B).
[0140] На фигуре 2 показано связывание биспецифического антителоа TAAxCD47 с клетками опухолей, несущими на поверхности TAA, так же как CD47. Связывание TAAxCD47 с EC50 между 1 и 50 нМ (сплошная линия, см. также на фигуре 11 кривые связывания различных антител CEAxCD47 по изобретению); пунктирной линией показан иллюстративный и схематичный потенциальный сдвиг кривой связывания посредством, например, растворимого CEA, конкретные данные см. на фигуре 20A, показывающей, например, влияние 200 нг/мл растворимого CEA на кривую связывания с клетками MKN-45 биспецифических антител CEAxCD47 по изобретению, подобно K2AC5 и 22.
[0141] На фигуре 3A показано зависимое от концентрации увеличение фагоцитоза (оцененное посредством проточной цитометрии и выраженное как % фагоцитоза) линии клеток рака поджелудочной железы человека HPAC (экспрессирует CEA и другие TAA, подобные мезотелину MSLN) с использованием биспецифического антитела TAAxCD47, несущего связывающее CD47 плечо по изобретению, соответствующего моновалентного антитела против CD47 и TAA, так же как высокоаффинного моноклонального антитела против TAA (MSLN), аматуксимаба. Все антитела несут части Fc IgG1 дикого типа. Для биспецифического антитела показан наивысший фагоцитоз.
[0142] На фигуре 3B показано зависимое от концентрации увеличение фагоцитоза (оцененное с использованием анализа CellInsight и выраженное как показатель фагоцитоза), индуцированного различными антителами; кривая 1: контрольное hIgG1, не связывающееся с TAA или CD47; кривая 2: биспецифическое антитело TAAxCD47 с Fc hIgG1 дикого типа; кривая 3: антитело против CD47 B6H12.2 с hIgG1 дикого типа; кривая 4: биспецифическое антитело TAAxCD47 с заменами ак DEA (S329D, I332E и G236A) в части Fc hIgG1. Наиболее сильный фагоцитоз достигнут с использованием TAAxCD47 с Fc с мутациями DEA.
[0143] На фигуре 4 показан пример кривых зависимости ADCC от дозы (оцененной с использованием анализа Cr51+ и выраженной как % специфического уничтожения) для различных биспецифических антител TAA x CD47 (TAA представляет собой мезотелин MSLN), всех несущих одинаковое связывающее CD47 плечо по этому изобретению, с использованием клеток злокачественных опухолей рака легкого NCI-H226 в качестве клеток-мишеней (PBMC добровольца-человека к клеткам опухолей 50:1). Для всех биспецифических антител показана более сильная ADCC, чем для высокоаффинного моноклонального антитела против TAA, аматуксимаба, mAb против MSLN.
[0144] На фигуре 5 показаны кривые зависимости ADCC от дозы (оцененной с использованием анализа Cr51+ и выраженной как % специфического уничтожения) для биспецифического антитела TAAxCD47 с Fc дикого типа, соответствующего биспецифического антитела TAAxCD47 с Fc, несущим мутации DEA, высокоаффинного моноклонального антитела против TAA (TAA на этой фигуре не представляет собой CEA), и контрольного антитела IgG1 человека; с использованием клеток злокачественных опухолей рака легкого NCI-H226 в качестве клеток-мишеней (эффектор к клеткам опухолей 50:1). Наиболее сильную ADCC наблюдали с использованием биспецифического антитела, несущего мутации DEA.
[0145] На фигуре 6 показано зависимое от концентрации блокирование связывания растворимого SIRPальфа с CD47, экспрессированным на клетках MKN-45, совместно экспрессирующих CEA (TAA), посредством биспецифического антитела TAAxCD47 (сплошная линия) и соответствующего моновалентного антитела против CD47 (пунктирная линия). Более высокая блокирующая активность биспецифического антитела обусловлена более сильным связыванием с клетками-мишенями и зависимым от совместного привлечения TAA блокированием CD47.
[0146] На фигуре 7A показано высвобождение цитокинов IFNγ и TNFα в цельной крови человека, инкубированной с 200 мкг/мл следующих антител: эрбитукс в качестве отрицательного контроля, антитело против CD52 кампат в качестве положительного контроля, и три биспецифических антитела, имеющие идентичные антигенсвязывающие области, но различные области Fc (слева направо): Fc IgG1 человека дикого типа, Fc IgG1 с мутациями DEA (S329D и I332E), Fc IgG1 с мутациями DE. biAb CD47lo и CD47lo относится к одному и тому же биспецифическому антителу CD47xTAA. Высвобождение IFNγ и TNFα, наблюдаемое с использованием биспецифического антитела, несущего мутации DEA, не выше, чем для биспецифического антитела с Fc дикого типа.
[0147] На фигуре 7B показано высвобождение цитокинов IL-6 и IL-8 в цельной крови человека, инкубированной с 200 мкг/мл следующих антител: эрбитукс в качестве отрицательного контроля, антитело против CD52 кампат в качестве положительного контроля, и три биспецифических антитела, имеющие идентичные антигенсвязывающие области, но различные области Fc (слева направо): Fc IgG1 человека дикого типа, Fc IgG1 с мутациями DEA, Fc IgG1 с мутациями DE. biAb CD47lo и CD47lo относится к одному и тому же биспецифическому антителу CD47xTAA. Высвобождение IL-6 и IL-8, наблюдаемое с использованием биспецифических антител, несущих мутации DE или DEA, не выше, чем для биспецифического антитела с Fc дикого типа.
[0148] На фигуре 8 показан зависимый от концентрации фагоцитоз эритроцитов (RBC), главный «антигензависимый слив» для моноклональных антител против CD47 (каждый RBC экспрессирует между 20000 и 25000 молекул CD47 на клеточной поверхности), индуцированный различными антителами: антителом huIgG1 против CD47 B6H12.12 с Fc дикого типа, биспецифическим антителом CD47xTAA с Fc дикого типа и таким же биспецифическим антителом CD47xTAA с Fc, несущим мутации DEA. Для B6H12 показан фагоцитоз RBC при концентрациях 10-100 нг/мл (приблизительно 0,07-0,7 нМ), в то время как для биспецифического антитела TAAxCD47 с Fc huIgG1 дикого типа не показан фагоцитоз RBC при концентрациях вплоть до 200000 нг/мл (приблизительно 1350 нМ); для такого же биспецифического антитела, но с частью Fc, несущей мутации DEA, показан увеличенный фагоцитоз RBC по сравнению с Fc дикого типа, при концентрациях выше 1000 нг/мл, (приблизительно 7 нМ), что все еще на 2-2,5 log выше, чем для антитела huIgG1 против CD47 B6H12.
[0149] На фигуре 9 показаны количества эритроцитов и количества тромбоцитов у нечеловекообразных приматов (NHP; яванские макаки), которым вводили четыре еженедельные iv инфузии либо контрольного антитела hIgG1, либо биспецифического антитела TAAxCD47 (30 мг/кг в течение первых двух недель и 100 мг/кг в течение последних двух недель). Значительного уменьшения гематологических показателей не наблюдали с использованием биспецифического антитела TAAxCD47, несмотря на высокую степень воздействия (концентрация в плазме биспецифического антитела TAAxCD47 в конце второго дозирования, при 30 мг/кг, составляла приблизительно 500 нМ).
[0150] На фигуре 10 показана активация тромбоцитов in vitro (оцененная посредством проточной цитометрии и выраженная как % экспрессии CD62P), индуцированная посредством инкубации цельной крови человека с антителами, как указано, в различных концентрациях (от 0 до 200 мкг/мл). В отличие от B6H12-hIgG1, которое индуцирует активацию тромбоцитов при 2 мкг/мл и выше, биспецифическое антитело TAAxCD47 с Fc IgG1 дикого типа не индуцирует активацию тромбоцитов, даже при наивысшей тестируемой концентрации (200 мкг/мл). Тестировали также биспецифические антитела CEAxCD47 K2AC5 и K2AC22, для вариантов с wtFc IgG1, так же как афукозилированных вариантов, не показана значимая активация тромбоцитов, вплоть до 20 мкг/мл (см. пример 15).
[0151] На фигуре 11A и B показано зависимое от концентрации связывание биспецифических антител CD47xCEA по изобретению, по сравнению с соответствующим моновалентным антителом против CD47. Связывание с клетками-мишенями (MKN-45), экспрессирующими CD47 и CEA, оценивали посредством FACS. На фигуре 11A показаны антитела, классифицированные в группу 1, связывание с клетками MKN-45 ингибировано посредством антитела SM3E не более чем на 80%; На фигуре 11B показаны антитела, классифицированные в группы 2, связывание с клетками MKN-45 не ингибировано посредством антител против CEA SM3E, MEDI, T84,66, SAR, Lab и CH1A1A (менее чем на 20%).
[0152] На фигуре 12 показано зависимое от концентрации увеличение фагоцитоза (оцененное посредством анализа CellInsight и выраженное как показатель фагоцитоза) клеток MKN-45, индуцированное различными биспецифическими антителами CD47xCEA в различных концентрациях (K2AC5, K2AC22, K2AC23, K2AC25, K2AC26, K2AC27, K2AC28 и K2AC29), по сравнению с соответствующим моновалентным антителом против CD47. 1 мг/мл hIgG (иммуноглобулина человека) добавляют в этом эксперименте для каждого тестированного антитела. Значения EC50 установленные в этом эксперименте, составляют между 0,2 и 20 мкг/мл, и максимальный показатель фагоцитоза (при 10 мкг/мл) лежит в диапазоне между 32,5% и 69% (см. в таблице 3 в разделе примеры обобщение данных для каждого индивидуального тестированного биспецифического антитела CD47xCEA).
[0153] На фигурах 13 и 14 показано зависимое от концентрации увеличение ADCC (оцененное с использованием анализа высвобождения LDH и выраженное как % специфического лизиса клеток злокачественных опухолей MKN45), индуцированное двумя выбранными биспецифическими антителами CD47xCEA (K2AC5 и K2AC22) по изобретению и соответствующим моновалентным антителом против CD47, несущими каждое часть Fc IgG1 дикого типа человека или афукозилированную часть Fc. Идентичный по последовательности аналог антитела против CD47 Hu5F9-G4 (5F9, несущее часть Fc IgG4 человека, описанное в US20160333093) анализировали для сравнения. Эксперименты проводили в отсутствие (фигура 13) или в присутствии (фигура 14) 1 мг/мл IgG человека. В обоих условиях эксперимента, варианты антитела с афукозилированным Fc индуцируют более высокую активность лизиса/уничтожения, по сравнению с соответствующими вариантами, несущими Fc дикого типа (в 5-9 раз более низкая EC50 для афукозилированных биспецифических антител K2AC5 и K2AC22, по сравнению с вариантом wt).
[0154] На фигуре 15 и фигуре 16 показано зависимое от концентрации увеличение фагоцитоза (оцененное с использованием анализа на основании визуализации CellInsight и выраженное как показатель фагоцитоза), индуцированное биспецифическими антителами CD47xCEA K2AC5 и K2AC22, несущими либо часть Fc IgG1 дикого типа человека, либо афукозилированную часть Fc. Соответствующее моновалентное антитело против CD47 (с Fc hIgG1 дикого типа) и идентичный по последовательности аналог антитела против CD47 Hu5F9-G4 (5F9) анализировали для сравнения. Эксперименты проводили либо в отсутствие (фигура 15), либо в присутствии (фигура 16) 1 мг/мл IgG человека. В обоих условиях эксперимента, для биспецифических вариантов антитела с афукозилированноеым Fc показана более высокая фагоцитирующая активность, по сравнению с соответствующими вариантами, несущими Fc дикого типа (в 3-10 раз более низкая EC50 для афукозилированных биспецифических антител K2AC5 и K2AC22, по сравнению с вариантом wt).
[0155] На фигуре 17 показано зависимое от концентрации увеличение фагоцитоза (оцененное с использованием анализа на основании визуализации (CellInsight) и выраженное как показатель фагоцитоза), индуцированное двумя выбранными биспецифическими антителами CD47xCEA, т.е. K2AC5 и K2AC22, в присутствии или в отсутствие 1 мг/мл IgG человека. Идентичный по последовательности аналог антитела против CD47 Hu5F9-G4 (5F9, несущее часть Fc IgG4 человека, описанное в US20160333093) анализировали для сравнения. Добавление 1 мг/мл IgG человека (то есть даже ниже физиологических концентраций IgG в плазме человека) слабо влияло на активность (т.е. EC50) биспецифических антител CD47xCEA, в то время как активность, обусловленная mAb 5F9, радикально нарушена (EC50 и максимальный фагоцитоз).
[0156] На фигуре 18 показан эффект перенацеливания T-клеток биспецифическими антителами CEA-TCB1 (30 нМ) и CEA-TCB (300 нМ) (биспецифические антитела CEAxCD3 CEA-TCB: RO6958688/цибисатамаб, см., например, Bacac et al Clin. Cancer Res., 22(13), 3286-97 (2016) и US20140242079; CEA-TCB1: из WO2017055389) на фагоцитоз (оцененный с использованием анализа на основании визуализации (CellInsight) и выраженный как показатель фагоцитоза), индуцированный биспецифическим антителом CEAxCD47 K2AC22. Перенацеливающие T-клетки биспецифические антитела, биспецифическое антитело CD47xCEA и соответствующее моновалентное антитело против CD47 тестировали отдельно для сравнения. Ни CEA-TCB, ни CEA-TCB1 не нарушало зависимую от концентрации активность K2AC22 при фагоцитозе.
[0157] На фигуре 19 показано уничтожение (оцененное посредством люминесценции и выраженное как % уничтожения) клеток злокачественной опухоли MKN45 в смешанном анализе (с добавленными PBMC и макрофагами, полученныеми от того же самого добровольного донора-человека) посредством 2 выбранных биспецифических антител CD47xCEA по изобретению (K2AC5 (фигура 19A) и K2AC22 (фигура 19B) в двух дозах (т.е. 0,37 мкг/мл или 1,1 мкг/мл), отдельно или в комбинации с CEA-TCB при 0,16 нМ или 0,8 нМ, и, по сравнению с CEA-TCB отдельно или с не относящимся к делу контрольным hIgG1. (A) По меньшей мере аддитивный эффект комбинации биспецифического антитела CEAxCD3 CEA-TCB (SEQ ID NO:96-99) и биспецифического антитела CEAxCD47 K2AC5; (B) По меньшей мере аддитивные эффекты также для CEA-TCB+K2AC22.
[0158] На фигуре 20 показаны зависимые от концентрации эффекты антител CEAxCD47 K2AC5 и 22 на связывание (20A) и фагоцитоз (20B) (оцененные с использованием анализа на основании визуализации (CellInsight) и выраженные как показатель фагоцитоза) в присутствии или в отсутствие 200 нг/мл слущивающегося CEA. Отсутствие значительного влияния 200 нг/мл растворимого CEA на кривые связывания обоих антител CEAxCD47. Отсутствие значительного эффекта растворимого CEA на максимальный фагоцитоз, EC50 сдвинуты менее чем в 4 раза.
[0159] На фигуре 21A показано зависимое от концентрации связывание биспецифических антител CD47xCEA по изобретению с клетками MKN-45, по сравнению с соответствующим моновалентным антителом против CD47 и с не относящимся к делу контрольным hIgG1. K2AC39 представляет собой биспецифическое антитело-кандидат CD47xCEA, имеющее перекрестную реакционную способность по отношению к CEACAM5 человека и CEACAM6 человека; в то время как K2AC22 не имеет перекрестной реакционной способности по отношению к CEACAM6. Связывание с клетками-мишенями (MKN-45) экспрессирующими CD47, CEACAM5 и CEACAM6, оценивали посредством FACS.
[0160] На фигуре 21B показано зависимое от концентрации увеличение фагоцитоза (оцененное посредством анализа на основе визуализации (CellInsight) и выраженное как показатель фагоцитоза) клеток MKN-45, индуцированного 2 различными биспецифическими антителами CD47xCEA (K2AC22 и K2AC39), по сравнению с соответствующим моновалентным антителом против CD47 и с не относящимся к делу контрольным hIgG1. K2AC39 представляет собой биспецифическое антитело-кандидат CD47xCEA, имеющее перекрестную реакционную способность по отношению к CEACAM5 человека и CEACAM6 человека; в то время как K2AC22 не имеет перекрестной реакционной способности по отношению к CEACAM6. 1 мг/мл IgG человека добавляют в этом эксперименте. Для K2AC39 показан более высокий фагоцитоз клеток MKN45 по сравнению с K2AC22.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0161] Термины используют в настоящем описании, как обычно используют в данной области, если иное не определено следующим образом.
[0162] В рамках изобретения, термин «антигенсвязывающая часть, связывающая часть» относится, в его самом широком смысле, к части антитела, которая специфически связывается с антигенной детерминантой, такой как CEA, CD47 и CD3.
[0163] Более конкретно, в рамках изобретения, связывающая часть, которая связывается со связанным с мембраной человеческим карциноэмбриональным антигеном (CEA, таким же как CEACAM5) или с CD47, специфически связывается с CEA или CD47, более конкретно, со связанным с клеточной поверхностью или мембраной CEA или CD47. Таким образом, каждая связывающая часть связывается либо с CEA, либо с CD47. Под «специфически связывающийся с, специфический для, связывающийся с» понимают, что связывание является избирательным для антигена, и его можно отличать от нежелательных или неспецифических взаимодействий. В некоторых вариантах осуществления, степень связывания антитела против мишени с неродственным, не являющимся мишенью белком, приблизительно в 10 раз, предпочтительно, в >100 раз меньше, чем связывание антитела с указанной мишенью, как измерено, например, посредством поверхностного плазмонного резонанса (SPR) например, Biacore®, твердофазного иммуноферментного анализа (ELISA) или проточной цитометрии (FACS). Мишени представляют собой белки, обсуждаемые в настоящем описании - например, CEA, CD47 и CD3ε. В одном варианте осуществления, связывающая CEA часть связывается дополнительно с CEACAM6.
[0164] «Специфически связывающийся с CEA, CD47, связывающийся с CEA, CD47, специфический для CEA, CD47», относится, в одном варианте осуществления, к антителу, например, биспецифическому антителу, способному к связыванию с мишенями CEA и CD47 с достаточной аффинностью, так что антитело можно использовать в качестве лекарственного средства при нацеливании на клетки опухолей, экспрессирующие CEA и CD47. Термин «связывание с клетками MKN-45 с значением EC50» относится к условиям анализа, при которых тестированные концентрации биспецифического антитела составляют между 0,1 и 1000 нМ, в присутствии антитела против CD47 B6H12.2 (ATCC® HB-9771™, также названного B6H12 в настоящем описании) в концентрации 300 нМ.
[0165] В одном варианте, осуществления биспецифическое антитело по изобретению связывается с CEACAM5 яванского макака так же как с CEACAM5 человека.
[0166] В рамках изобретения, термин «антитело» относится к антителу, содержащему две тяжелые цепи и две легкие цепи. В одном варианте осуществления, антитело представляет собой полноразмерное антитело. В рамках изобретения, термин «тяжелая цепь антитела» относится к тяжелой цепи антитела, состоящей из вариабельной области и константной области, как определено для полноразмерного антитела. В рамках изобретения, термин «легкая цепь антитела» относится к легкой цепи антитела, состоящей из вариабельной области и константной области, как определено для полноразмерного антитела.
[0167] Термин «полноразмерное антитело» обозначает антитело, состоящее из двух «полноразмерных тяжелых цепей антитела» и двух «полноразмерных легких цепей антитела». «Полноразмерная тяжелая цепь антитела» представляет собой полипептид, состоящий, в направлении от N-конца к C-концу, из вариабельного домена тяжелой цепи (VH) антитела, константного домена 1 тяжелой цепи (CH1) антитела, шарнирной области (HR) антитела, константного домена 2 тяжелой цепи (CH2) антитела и константного домена 3 тяжелой цепи (CH3) антитела, кратко обозначенный как VH-CH1-HR-CH2-CH3. «Полноразмерная легкая цепь антитела» представляет собой полипептид, состоящий, в направлении от N-конца к C-концу, из вариабельного домена легкой цепи (VL) антитела и константного домена легкой цепи (CL) антитела, кратко обозначенный как VL-CL. Константный домен легкой цепи (CL) антитела может представлять собой κ (каппа) или λ (лямбда). Два полноразмерных домена антитела связаны вместе межполипептидными дисульфидными связями между доменом CL и доменом CH1, и между шарнирными областями тяжелых цепей полноразмерных антител. Примеры типичных полноразмерных антител представляют собой природные антитела, подобные IgG (например, IgG 1 и IgG2), IgM, IgA, IgD и IgE. Полноразмерное антитело по изобретению принадлежит, в одном варианте осуществления, к типу IgG1 человека, в одном дополнительном варианте осуществления, содержащему одну или несколько аминокислотных замен в части Fc, как определено ниже, и/или подвергнутому гликоинженерии в Asn297. Полноразмерное антитело по изобретению содержит две связывающие части, каждая из которых сформирована парой VH и VL, одну, связывающуюся с CEA и другую, связывающуюся с CD47.
[0168] В рамках изобретения, «определяющая комплементарность область(области)» («CDR») описывают не являющиеся непрерывными участки связывания антигена (также известные как антигенсвязывающие области), обнаруженные внутри вариабельной области полипептидов как тяжелой, так и легкой цепи. CDR также обозначены как «гипервариабельные области», и этот термин используют в настоящем описании взаимозаменяемо с термином «CDR», применительно к частям вариабельной области, формирующим антигенсвязывающие области. Эта конкретная область описана в Kabat et al., U.S. Dept. of Health and Human Services, «Sequences of Proteins of Immunological Interest» (1983) и в Chothia et al., J. Mol. Biol. 196:901-917 (1987), содержание которых приведено в настоящем описании в качестве ссылки, где определения включают перекрывающиеся аминокислотные остатки или подгруппы аминокислотных остатков, при сравнении друг с другом. Определение областей FR-IMGT и CDR-IMGT IG и TR основано на «IMGT unique numbering for all IG and TR V-REGIONs of all species: interest for structure and evolution» (Lefranc, M.-P. et al., Dev. Comp. Immunol., 27, 55-77 (2003) и, для реаранжированных CDR3-IMGT и для FR4-IMGT, на «IMGT unique numbering for V-DOMAIN and V-LIKE-DOMAIN» (Lefranc, M.-P. et al., Dev. Comp. Immunol., 27, 55-77 (2003) ). Тем не менее, использование любого определения для обозначения CDR антитела или его вариантов предназначено для включения в объем термина, как определено и использовано в настоящем описании. Подходящие аминокислотные остатки, охватывающие CDR, как определено посредством IMGT и Kabat, указаны ниже в таблице списка последовательностей. Точные номера остатков, охватывающих конкретную CDR, могут меняться, в зависимости от последовательности и размера CDR. Специалист в данной области может общепринятым образом определять, какие остатки содержат конкретную CDR, с учетом аминокислотной последовательности вариабельной области антитела. В рамках изобретения, термин «содержащий CDRL1 из SEQ ID NO:x» обозначает то, что часть CDRL1 указанной вариабельной легкой цепи происходит из SEQ ID NO:x (содержащей, в качестве CDRL1, CDRL1 из SEQ ID NO:x). Это справедливо также для других CDR.
[0169] В рамках изобретения, термин «область Fc; домен Fc» относится к C-концевой области тяжелой цепи IgG; в случае антитела IgG1, C-концевая область содержит -CH2-CH3 (см. выше). Хотя границы области Fc тяжелой цепи IgG могут немного меняться, область Fc тяжелой цепи IgG человека обычно определяют как фрагмент от аминокислотного остатка в положении Cys226 до карбокси-конца.
[0170] Константные области хорошо известны на предшествующем уровне техники и описаны, например, в Kabat, E.A., (см., например, Johnson, G., and Wu, T.T., Nucleic Acids Res.28 (2000) 214-218; Kabat, E.A., et al, Proc. Natl. Acad. Sci. USA 72 (1975) 2785- 2788).
[0171] Термин «эпитоп» включает любую полипептидную детерминанту, способную к специфическому связыванию с антителом. В конкретных вариантах осуществления, «эпитоп» включает химически активные поверхностные группировки молекул, такие как аминокислоты, боковые цепи сахара, фосфорил или сульфонил, и, в конкретных вариантах осуществления, может иметь специфические характеристики трехмерной структуры, и/или специфические характеристики заряда. Эпитоп представляет собой область мишени, связываемую посредством антитела. В одном варианте осуществления, биспецифическое антитело по изобретению связывается с N-концевым доменом CEACAM5 (Ig-подобным доменом V-типа из аминокислот 35-144, UniProtKB - P06731). Локализацию связывания биспецифических антител CEAxCD47 с CEACAM5 получают посредством группировки эпитопов. При группировке эпитопов, антитела тестируют попарным комбинаторным способом, и антитела, конкурирующие за одну и ту же область связывания, группируют совместно в группы. Тестирование конкуренции проводят по настоящему изобретению с использованием антител против CEA, в соответствии с предшествующим уровнем техники и как описано в настоящем описании. В одном варианте осуществления, биспецифическое антитело по изобретению конкурирует за связывание с CEACAM5 с эталонным антителом SM3E (группа 1). В одном варианте осуществления, биспецифическое антитело по изобретению не конкурирует за связывание с CEACAM5 с эталонными антителами SM3E, MEDI, T84,66, SAR, Lab и CH1A1A (группа 2). Конкуренцию измеряют посредством анализа, в котором биотинилированный CEACAM5 человека в концентрации 0,5 мкг/мл иммобилизуют и инкубируют с 10 мкг/мл эталонного антитела. Антитела против CEACAM5, содержащие связывающую CEACAM5 часть биспецифического антитела CEAxCD47 по настоящему изобретению, добавляют при 0,2 мкг/мл на 1 час при комнатной температуре. Планшет промывают, и связавшиеся mAb против CEACAM5 детектируют.
[0172] В одном варианте осуществления биспецифическое антитело по изобретению связывается с доменом B3 и якорем GPI из CEACAM5. В одном варианте осуществления изобретения, антитело по изобретению связывается с таким же эпитопом, что и антитело против CEA (MAB CEA), которое содержит вариабельную область тяжелой цепи из SEQ ID NO:20 и вариабельную область легкой цепи из SEQ ID NO:21.
[0173] В рамках изобретения, термин «общая тяжелая цепь (cHC)» относится к полипептиду, состоящему, в направлении от N-конца к C-концу, из вариабельного домена тяжелой цепи (VH) антитела, константного домена 1 тяжелой цепи (CH1) антитела, шарнирной области (HR) антитела, константного домена 2 тяжелой цепи (CH2) антитела и константного домена 3 тяжелой цепи (CH3) антитела, кратко обозначенному как VH-CH1-HR-CH2-CH3. Общие тяжелые цепи, пригодные для биспецифических антител по изобретению, представляют собой тяжелые цепи антитела против CD47, как описано в WO2012023053, WO2013088259, WO2014087248 и WO2016156537 (полное содержание каждой из которых приведено в настоящем описании в качестве ссылки). В одном варианте осуществления, cHC биспецифического антитела по изобретению содержит, в качестве CDR легкой цепи, CDRL1 из SEQ ID NO:1, CDRL2 из SEQ ID NO:2 и CDRL3 из SEQ ID NO:3, и в качестве CDR тяжелой цепи, CDRH1 из SEQ ID NO:25, CDRH2 из SEQ ID NO:26 и CDRH3 из SEQ ID NO:27. В одном варианте осуществления, cHC биспецифического антитела по изобретению содержит, в качестве вариабельной области тяжелой цепи VH, область VH из SEQ ID NO:4. В одном варианте осуществления, cHC биспецифического антитела по изобретению происходит из SEQ ID NO:5. В одном варианте осуществления, антитело по изобретению представляет собой биспецифическое антитело κλ, содержащее cHC (антитело κλ).
[0174] «Антитело формата κλ позволяет аффинную очистку биспецифических антител, которые являются неотличимыми от стандартной молекулы IgG, и характеристики которых являются неотличимыми от стандартного моноклонального антитела (см., например, WO2013088259, WO2012023053), что обещает отсутствующий или низкий иммуногенный потенциал у пациентов.
[0175] Биспецифические антитела по изобретению, содержащие общую тяжелую цепь, можно получать, например, в соответствии с WO2012023053 (полное содержание которой приведено в настоящем описании в качестве ссылки). Способами, описанными в WO2012023053, получают биспецифические антитела, которые являются идентичными по структуре с иммуноглобулином человека. Этот тип молекулы состоит из двух копий уникального полипептида тяжелой цепи, первой вариабельной области легкой цепи, слитой с константным доменом каппа, и второй вариабельной области легкой цепи, слитой с константным доменом лямбда. Для одного участка связывания показана специфичность для CEA, и для другого участка показана специфичность для CD47, в который вносят вклад каждая из тяжелой и соответствующей легкой цепи. Вариабельные области легкой цепи могут принадлежать к семейству лямбда или каппа и являются, предпочтительно, слитыми с константными доменами лямбда и каппа, соответственно. Это является предпочтительным, чтобы избегать образования неприродных полипептидных стыков. Однако, является также возможным получение биспецифических антител по изобретению посредством слияния вариабельного домена легкой цепи каппа с константным доменом лямбда для первой специфичности или слияния вариабельного домена легкой цепи лямбда с константным доменом каппа для второй специфичности. Тогда другая легкая цепь всегда представляет собой полноразмерную каппа (VL и CL) или полноразмерную лямбда). Биспецифические антитела, описанные в WO 2012023053, представляют собой «антитела κλ». Это формат антитела κλ позволяет аффинную очистку биспецифического антитела, которое является неотличимым от стандартной молекулы IgG, с характеристиками, которые являются неотличимыми от стандартного моноклонального антитела, и, таким образом, обеспечивает преимущества по сравнению с предшествующими форматами, включающими, например, аминокислотные мостики или другие неприродные элементы.
[0176] Необходимой стадией способа является идентификация двух областей Fv антитела (каждая из которых состоит из вариабельного легкого домена и вариабельного тяжелого домена), имеющих различные антигенные специфичности, разделяющие один и тот же вариабельный домен тяжелой цепи. Описаны многочисленные способы получения моноклональных антител и их фрагментов. (см., например, Antibodies: A Laboratory Manual, Harlow E, and Lane D, 1988, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY). Полностью человеческие антитела представляют собой молекулы антител, в которых последовательность как легкой цепи, так и тяжелой цепи, включая CDR 1 и 2, происходят из человеческих генов. Область CDR3 может иметь человеческое происхождение или может быть сконструирована синтетическими способами. Такие антитела названы «человеческими антителами» или «полностью человеческими антителами». Человеческие моноклональные антитела можно получать с использованием способа триомы; способа гибридомы из B-клетки человека (см. Kozbor, et al., 1983 Immunol Today 4: 72); и способа гибридомы EBV для получения человеческих моноклональных антител (см. Cole, et al., 1985 In: Monoclonal Antibodies and Cancer Therapy, Alan R. Liss, Inc., pp. 77-96). Человеческие моноклональные антитела можно использовать и можно получать с использованием человеческих гибридом (см. Cote, et al., 1983. Proc Natl Acad Sci USA 80: 2026-2030) или посредством трансформации B-клеток человека вирусом Эпштейна-Барр in vitro (см. Cole, et al., выше).
[0177] В рамках изобретения, термин «CEA, CEACAM5» относится к карциноэмбриональному антигену человека (CEA, CEACAM-5 или CD66e; UniProtKB - P06731), который представляет собой гликопротеин поверхности клеток и опухолеассоциированный антиген (Gold and Freedman, J Exp. Med., 121:439-462, 1965; Berinstein NL, J Clin Oncol., 20:2197-2207, 2002). В рамках изобретения, термин «CEACAM6» относится к CEACAM6 человека (CD66c; UniProtKB - P40199), который также является членом семейства родственных карциноэмбриональному антигену молекул клеточной адгезии (CEACAM). В рамках изобретения, термин «CEACAM1» относится к CEACAM1 человека (UniProtKB - P13688 (CEAM1_HUMAN), который также является членом семейства родственных карциноэмбриональному антигену молекул клеточной адгезии (CEACAM). Дополнительную информацию и информацию о других членах семейства CEA можно обнаружить в http://www.uniprot.org.
[0178] В рамках изобретения, термин «MAB CEA» относится к моноклональному антителу, специфически связывающемуся с CEACAM5 человека, содержащему вариабельную область тяжелой цепи из SEQ ID NO:20 и вариабельную область легкой цепи из SEQ ID NO:21. В рамках изобретения, термин «MAB CEA1» относится к моноклональному антителу, специфически связывающемуся с CEACAM5 человека, содержащему вариабельную область тяжелой цепи из SEQ ID NO:88 и вариабельную область легкой цепи из SEQ ID NO:89. В одном варианте осуществления, биспецифическое антитело по изобретению является конкурентным с MAB CEA, MAB CEA1, CEA-TCB, или CEA-TCB1; в следующем варианте осуществления биспецифическое антитело по изобретению является не конкурентным с MAB CEA, MAB CEA1, CEA-TCB или CEA-TCB1. MAB CEA и указанные вариабельные цепи описаны в US20140242079 (SEQ ID NO:21 и 27 из US20140242079 (полное содержание которой приведено в настоящем описании в качестве ссылки)). Биспецифическое антитело против CEA x против CD3ε (CEA-TCB), содержащее VH и VL из MAB CEA, описано в Bacac et al Clin. Cancer Res., 22(13), 3286-97 (2016)). Дополнительное биспецифическое Mab CEAxCD3, содержащее VH и VL из MAB CEA1 (CEA-TCB1), описано в WO2017055389 как молекула B «2+1 IgG CrossFab, инвертированное» с модификациями заряда (обмен VH/VL в связывающем CD3 члене, модификация заряда в связывающем CEA члене, гуманизированный связывающий CEA член) (см. фигуру 3B и SEQ ID NO 34, 36-38 из WO2017055389 (полное содержание которой приведено в настоящем описании в качестве ссылки)). В рамках изобретения, в одном варианте осуществления, «биспецифическое антитело CEA x CD3» относится к антителу CEA-TCB или антителу CEA-TCB1.
[0179] В рамках изобретения, термины «специфическое связывание с CD47, связывание с CD47, связывающая CD47 часть» относятся, в контексте биспецифических антител по изобретению, к специфичности для CD47. CD47 представляет собой несколько раз пересекающий мембрану белок и содержит три внеклеточных домена (аминокислоты 19-141, 198-207 и 257-268; см. UniProtKB - Q08722). В рамках изобретения, термин «аффинность связывания для CD47» измеряют посредством SPR.
[0180] В одном варианте осуществления связывание биспецифического антитела по изобретению с CD47 происходит посредством одного или нескольких из указанных внеклеточных доменов. В одном варианте осуществления, биспецифические антитела по изобретению ингибируют взаимодействие между CD47 человека и SIRPα человека.
[0181] В рамках изобретения, термины «специфическое связывание с CEA, связывание с CEA, связывающая CEA часть» относятся, в контексте биспецифических антител по изобретению, к специфичности для CEACAM5 на поверхности клетки. Связывание с CEA (CEACAM5) на клетках, предпочтительно, измеряют с использованием клеток аденокарциномы желудка MKN-45, содержащих 200000-600000 копий CEA на клетку. Концентрацию антитела по изобретению меняют в соответствующем диапазоне, применительно к полученному в результате значению EC50 для связывания с клетками MKN-45, как определено выше. Биспецифические антитела по изобретению специфически связываются с таким связанным с клеточной мембраной CEACAM5 и не связываются или только минимально связываются, в следующем варианте осуществления, с растворимым CEACAM5, в концентрациях, подобных обнаруженным в крови/плазме пациентов, т.е., растворимый CEA, в таких концентрациях, не влияет или только минимально влияет на эффективность биспецифического антитела по изобретению. Это измеряют посредством влияния растворимого CEA на фагоцитоз клеток MKN-45 посредством биспецифических антител по этому изобретению, как описано.
[0182] В рамках изобретения, термин «связанный с мембраной CEA человека» относится к карциноэмбриональному антигену (CEA) человека, связанному с мембранной частью клетки или с поверхностью клетки, в частности, поверхностью клетки опухоли. Термин «связанный с мембраной CEA человека» может, в определенных условиях, относиться к CEA, который не является связанным с мембраной клетки, но который сконструирован таким образом, чтобы сохранять эпитоп связанного с мембраной CEA, с которым связывается антитело по изобретению.
[0183] В рамках изобретения, термин «отсутствие значительной перекрестной реакционной способности против растворимого CEACAM5, отсутствие связывания с растворимым CEACAM5» означает, в контексте биспецифических антител по изобретению, что для таких антител не показывают значительное связывание с растворимым CEACAM5, в частности, по сравнению со связанным с мембраной CEACAM5. Такое отсутствие связывания можно опосредованным образом определять по низкому влиянию растворимого CEA на активность фагоцитоза посредством биспецифического антитела в анализе фагоцитоза с использованием клеток MKN-45, как описано ниже, предпочтительно, в основанном на визуализации измерении показателя фагоцитоза, см. пример 9). Отсутствие значительной перекрестной реакционной способности против растворимого CEACAM5 означает, таким образом, что максимальный достижимый показатель фагоцитоза (типичные кривые концентрация-показатель фагоцитоза посредством биспецифического антитела CEAxCD47 и максимальный достижимый показатель фагоцитоза показаны, например, на фигурах 12, 15, 16, 17, 20A, анализ объяснен в примере 9.2) для фагоцитоза клеток MKN-45 в присутствии макрофагов человека, посредством указанного биспецифического антитела, не уменьшается более чем на 20%, если 200 нг/мл растворимого CEA добавляют в анализ фагоцитоза. Альтернативно, можно определять сдвиг EC50 для кривой концентрация - показатель фагоцитоза. Добавление 200 нг/мл растворимого CEA не может сдвигать эту EC50 более чем в 3 раза, в одном варианте осуществления, в сторону более высоких концентраций. Альтернативно, ожидают отсутствие влияния или минимальное влияние растворимого CEA на связывание биспецифического антитела по этому изобретению с CEA на клетках, посредством влияния растворимого CEA на кривую связывания, измеренного посредством проточной цитометрии (такая кривая связывания показана на фигуре 20B). Добавление 200 нг/мл растворимого CEA в анализ проточной цитометрии не может сдвигать кривую связывания, соответственно EC50, более чем в 3 раза, в одном варианте осуществления, в сторону более высоких концентраций
[0184] Термин «растворимый CEA, слущивающийся CEA, sCEA» относится к CEACAM5, который не является связанным или является отщепленным от мембраны клетки или поверхности клетки (например, поверхности клетки опухоли). Растворимый CEA можно, например, обнаружить в кровотоке индивида с злокачественной опухолью. Когда CEA слущивается с мембраны клетки, заключают, что якорь GPI разрушается, и CEACAM5 подвергается конформационному изменению, которое может предотвращать или по меньшей мере ослаблять связывание растворимого CEA с антителом по изобретению.
[0185] В рамках изобретения, термины «перекрестная реакционная способность против CEACAM6, специфическое связывание с CEACAM6, связывание с CEACAM6, связывающая CEACAM6 часть» означает, в контексте биспецифических антител по изобретению, что биспецифическое антитело по изобретению специфически узнает CEACAM5 и CEACAM6 на поверхности (мембране) клетки. В одном варианте осуществления, биспецифические антитела по изобретению являются специфически связывающимися с связанным с мембраной CEACAM6, по сравнению со связыванием с связанным с мембраной CEA. Степень занятости CEACAM5 для рецепторов CEACAM6 на поверхности клетки для данного биспецифического антитела по изобретению зависит от аффинности связывания с CEACAM5, соответственно, CEACAM6, и может быть легко рассчитана, если эта аффинность связывание измерена, например, посредством SPR.
[0186] В конкретных вариантах осуществления, антитело, которое специфически связывается с CEACAM5, не связывается с родственными карциноэмбриональному антигену белками клеточной адгезии, такими как CEACAM1, CEACAM3, CEACAM4, CEACAM6, CEACAM7 и CEACAM8. В конкретных вариантах осуществления, антитело, которое специфически связывается с CEACAM5, также связывается с CEACAM6 при сходной EC50.
[0187] В рамках изобретения, термины «отсутствие значительной перекрестной реакционной способности против CEACAM1 и/ или CEACAM3, CEACAM4, CEACAM6, CEACAM7 и CEACAM8, отсутствие связывания с указанным CEACAM» означает, в контексте биспецифических антител по изобретению, что для таких антител не показано какое-либо значительное связывание с указанным связанным с мембраной CEACAM при терапевтических концентрациях в плазме (1-1000 нМ), по сравнению со связанным с мембраной CEACAM5. Отсутствие связывания с CEACAM1 и/или CEACAM5, CEACAM6 и CEACAM8 можно определять посредством измерения, на основе проточной цитометрии, кривой связывания с рекомбинантными клетками CHO, экспрессирующими указанный CEACAM, и с CEACAM3 и/или CEACAM4 и CEACAM7, посредством измерения кривой связывания с рекомбинантными клетками PEAK, экспрессирующими указанный CEACAM, или посредством анализа ELISA, измеряющего связывание с рекомбинантными белками CEACAM. В рамках изобретения, термины «не связывается, отсутствие связывания с» соединением, упомянутым в настоящем описании (например, IgG человека), относится также к такому не относящемуся к делу связыванию или отсутствию перекрестной реакционной способности. Например, в ELISA, значения OD для таких неродственных соединений может являться приблизительно равным пределу детекции.
[0188] В рамках изобретения, термин «биспецифическое антитело, связывающееся с CEA человека и CD3 человека, Mab CEAxCD3» обозначает биспецифическое антитело, связывающееся с CEACAM5 человека и CD3ε. Такие антитела представляют собой, например, «CEA-TCB» и «CEA-TCB1». В рамках изобретения, «CEA-TCB» относится к биспецифическому антителу, связывающемуся с CEA и CD3, как описано в US20140242079 (полное содержание которой приведено в настоящем описании в качестве ссылки), как SEQ ID NO:1, 2, 21 и 22. Аминокислотные последовательности CEA-TCB также описаны как SEQ ID NO:96-99 по настоящему изобретению. В рамках изобретения «CEA-TCB1» относится к молекуле B в формате «2+1 IgG CrossFab, инвертированного», с модификациями заряда (обмен VH/VL в связывающем CD3 члене, модификация заряда в связывающем CEA члене, гуманизированный связывающий CEA член); фигура 3B, SEQ ID NO 34, 36-38 из WO2017055389 (полное содержание которой приведено в настоящем описании в качестве ссылки)). Аминокислотные последовательности CEA-TCB1 описаны как SEQ ID NO:92-95 по настоящему изобретению. Дополнительные Mab CEAxCD3 описаны в WO2007071426, WO2013012414, WO2015112534, WO2017118675, US20140242079 и WO2017055389 (полное содержание каждой из которых приведено в настоящем описании в качестве ссылки). Дополнительный Mab CEAxCD3 представляет собой RO6958688 (см., например, Bacac et al Clin. Cancer Res., 22(13), 3286-97 (2016). В одном варианте осуществления, указанное Mab CEAxCD3 является конкурентным и/или связывается с таким же эпитопом CEACAM5 человека, что и MAB CEA. В одном варианте осуществления указанное Mab CEAxCD3 является конкурентным и/или связывается с таким же эпитопом CEACAM5 человека, что и MAB CEA1.
[0189] В рамках изобретения «CD3 Mab, антитело против CD3» относится к CD3ε человека (UniProtKB - P07766 (CD3E_HUMAN). Термин «антитело против CD3ɛ, анти-CD3ɛ антитело» относится к антителу, специфически связывающемуся с CD3ɛ. В одном варианте осуществления, антитело против CD3ε специфически связывается с таким же эпитопом, что и антитело против CD3 SP34 (BD Biosciences, каталожный No.565983). В одном варианте осуществления, антитело против CD3ε специфически связывается с эпитопом CD3ε человека, содержащим аминокислотную последовательность из SEQ ID NO:22. В одном варианте осуществления, антитело против CD3ε специфически связывается с CD3ε человека и содержит вариабельную область тяжелой цепи из SEQ ID NO:90 и вариабельную область легкой цепи из SEQ ID NO:91.
[0190] В одном варианте осуществления, биспецифическое антитело по изобретению не конкурирует с CEA-TCB и/или CEA-TCB1 за связывание с CEA, какой представлен на клетках MKN-45. Таким образом CEA-TCB в концентрации 300 нМ (CEA-TCB) или 30 нМ (CEA-TCB1) не сдвигают EC50 кривой показателей фагоцитоза указанного биспецифического антитела по изобретению для клеток MKN-45 более чем в 3 раза, в одном варианте осуществления, в сторону более высоких концентраций.
[0191] 300 нМ представляет собой концентрацию, измеренную в плазме пациента при терапевтически эффективных дозах CEA-TCB ((J.Tabernero et.al., J. Clin. Oncol. 35, 2017 (suppl. Abstr. 3002)). CEA-TCB1 является в доклинических исследованиях приблизительно в 10-100 раз более активным, чем CEA-TCB (аффинность связывания, лизис клетки опухоли, WO2017055389), таким образом, сдвиг EC50 тестируют при 30 нМ.
[0192] Конкуренцию за связывание можно определять посредством измерения на основе проточной цитометрии кривой связывания с клетками MKN-45 и определения EC50 этой кривой связывания (см., например, на фигуре 2 и фигуре 11 такие кривые связывания). Отсутствие конкуренции означает, что EC50 сдвигается менее чем в 3 раза, в одном варианте осуществления, в сторону более высоких концентраций, если 300 нМ MAB CEA или CEA-TCB добавляют в анализ. 300 нМ представляет собой концентрацию в диапазоне терапевтически активных доз/концентраций в плазме биспецифического антитела CEA x CD3 (CEA-TCB) (J.Tabernero et.al., J. Clin. Oncol. 35, 2017 (suppl. Abstr. 3002)). Отсутствие конкуренции с MAB CEA1 или CEA-TCB1 означает, что EC50 сдвигается менее чем в 3 раза, если 30 нМ MAB CEA1, соответственно CEA-TCB1, добавляют в анализ.
[0193] Конкуренцию за связывание можно определять посредством измерения на основе проточной цитометрии кривой связывания с клетками MKN-45 и определения EC50 этой кривой связывания (см. на фигуре 2 и фигуре 11 такие кривые связывания). Отсутствие конкуренции означает, что EC50 изменяется менее чем в 3 раза, если 300 нМ MAB CEA или CEA-TCB добавляют в анализ. 300 нМ представляет собой концентрацию в диапазоне терапевтически активных доз/концентраций в плазме биспецифического антитела CEA x CD3 (CEA-TCB) (J.Tabernero et.al., J. Clin. Oncol. 35, 2017 (suppl. Abstr. 3002)).
[0194] Отсутствие конкуренции с MAB CEA1 или CEA-TCB1 означает, что EC50 изменяется менее чем в 3 раза, если 30 нМ MAB CEA1, соответственно CEA-TCB1, добавляют в анализ.
[0195] В рамках изобретения, термин «неконкурентные» означает, что второе антитело (MAB CEA, MAB CEA1 или биспецифическое антитело против CEAxCD3ε, подобное CEA-TCB или CEA-TCB1) в концентрации 300 нМ (MAB-CEA, CEA-TCB) или 30 нМ (MAB CEA1, CEA-TCB1) не сдвигает EC50 кривой связывания биспецифического антитела по изобретению с клетками MKN-45 более чем в 3 раза, в одном варианте осуществления, в сторону более высоких концентраций. В рамках изобретения, термин «конкурентные» означает, что второе антитело (MAB CEA, MAB CEA1 или биспецифическое антитело против CEAxCD3ε, подобное CEA-TCB или CEA-TCB1) в концентрации 300 нМ, соответственно 30 нМ (MAB CEA1 или CEA-TCB1) сдвигает EC50 кривой связывания биспецифического антитела по изобретению с клетками MKN-45 более чем в 3 раза, предпочтительно, более чем в 5 раз, в сторону более высоких концентраций.
[0196] В рамках изобретения, термин «определяющая комплементарность область» («CDR») описывает не являющиеся непрерывными участки связывания антигена (также известные как антигенсвязывающие области), обнаруженные в вариабельной области полипептидов как тяжелой, так и легкой цепей. CDR также обозначены как «гипервариабельные области», и этот термин используют в настоящем описании взаимозаменяемо с термином «CDR», применительно к частям вариабельной области, формирующим антигенсвязывающие области. Эта конкретная область определена в Kabat et al., U.S. Dept. of Health and Human Services, «Sequences of Proteins of Immunological Interest» (1983) и в Chothia et al., J. Mol. Biol. 196:901-917 (1987). В Kabat et al. определена также система нумерации для последовательностей вариабельного домена, применимая к любому антителу. Специалист в данной области может однозначно приписать эту систему «нумерации по Kabat» к любой последовательности вариабельного домена, вне зависимости от каких-либо экспериментальных данных помимо собственно последовательности. В рамках изобретения, «нумерация по Kabat» относится к системе нумерации, указанной в Kabat et al., U.S. Dept. of Health and Human Services, «Sequence of Proteins of Immunological Interest» (1983). Если не указано иное, ссылки на нумерацию положений конкретных аминокислотных остатков в биспецифическом антителе по изобретению приведены, в соответствии с системой нумерации Kabat.
[0197] В рамках изобретения, термин «ADCP» относится к антителозависимому опосредованному клетками фагоцитозу.
[0198] В рамках изобретения «фагоцитоз, значение EC50 для фагоцитоза, максимум фагоцитоза, показатель фагоцитоза» по изобретению относятся к фагоцитозу, измеренному с использованием клеток MKN-45 посредством «визуализации». Подходящий способ визуализации, с инкубацией при соотношении эффектора (макрофагов): мишени - клеток (опухоли), например, 1:1 или 1:3, и с использованием «показателя фагоцитоза» в качестве регистрируемых данных (определенного посредством визуализации ADCP»), описан в примере 9. На фигуре 3B показан максимальный достижимый показатель фагоцитоза, как определено в тестируемом диапазоне концентраций, от 0,1 или даже ниже до приблизительно 500 нМ биспецифических антител TAA x CD47. На фигурах 12, 15 и 16 показаны результаты ADCP для биспецифических антител по изобретению K2AC5 и K2AC22. В рамках изобретения, «фагоцитоз указанного биспецифического антитела» означает фагоцитоз, вызванный/индуцированный указанным антителом. Антитело K2AC22 содержит первую связывающую часть, специфически связывающуюся с CEACAM5 человека, и вторую связывающую часть, специфически связывающуюся с CD47 человека, при этом первая связывающая часть содержит тяжелую цепь из SEQ ID NO:5 и легкую цепь из SEQ ID NO:65, и таким образом, вторая связывающая часть содержит тяжелую цепь из SEQ ID NO:5 и легкую цепь из SEQ ID NO:11. Антитело K2AC5 содержит первую связывающую часть, специфически связывающуюся с CEACAM5 человека, и вторую связывающую часть, специфически связывающуюся с CD47 человека, при этом, первая связывающая часть содержит тяжелую цепь из SEQ ID NO:5 и легкую цепь из SEQ ID NO:64, и таким образом, вторая связывающая часть содержит тяжелую цепь из SEQ ID NO:5 и легкую цепь из SEQ ID NO:11. Антитела K2AC10, K2AC13 K2AC18, K2AC23, K2AC25, K2AC26, K2AC27, K2AC28, K2AC29 содержат одинаковые тяжелые цепи и легкую цепь второй связывающей части, но отличаются легкой цепью первой связывающей части (см. таблицу 1, список последовательностей).
[0199] Для получения дополнительной информации о фагоцитозе, в данной области, фагоцитоз можно также измерять способом на основе проточной цитометрии как % фагоцитоза (см. в примере 9 и на фигуре 3A зависимость % фагоцитоза от концентраций моновалентных антител TAA и CD47 и биспецифического антитела TAA x CD47) и при соотношении, например, 3 макрофага человека к 1 клетке-мишени/опухоли («определенный посредством проточной цитометрии ADCP»).
[0200] Термины «IgG человека, hIgG» относятся к коммерчески доступному гомогенному препарату иммуноглобулина IgG человека клинической квалификации (от компании Bio-rad.com), который не связывается специфически с CD47 и CEACAM5.
[0201] Антитела, продуцированные в клетках CHO, как правило, имеют комплексные двухантенные структуры с очень низким уровнем или отсутствием разделенного надвое-N-ацетилглюкозамина (разделенного надвое GlcNAc) и высокими уровнями корового фукозилирования. Сверхэкспрессию N-ацетилглюкозаминилтрансферазы III использовали для увеличения доли разделенного надвое GlcNAc, находящегося на антителах, для улучшения антителозависимой клеточной цитотоксичности (ADCC). Технологии РНКи и делеции гена также использовали для уменьшения уровня или исключения фукозы на антителах для чрезвычайного увеличения активности ADCC (Davis J. et al.; Biotechnol. Bioeng. 2001;74:288-294; Saba JA, et al.; Anal. Biochem. 2002;305:16-31; Kanda Y, et al.; J. Biotechnol. 2007;130:300-310; Mori K, et al.; Biotechnol. Bioeng. 2004;88:901-908).
[0202] В одном варианте осуществления, биспецифическое антитело по изобретению подвергнуто гликоинженерии. В одном варианте осуществления, подвергнутое гликоинженерии биспецифическое антитело по изобретению имеет увеличенную активность ADCC и/или ADCP (уменьшенную EC50 и/или более высокий максимум показателя фагоцитоза), по сравнению с биспецифическим антителом, содержащим часть Fc, включенную в SEQ ID NO:5 (исходным антителом), имеющим гликозилирование, в соответствии с продукцией в линии клеток CHO K1 (ATCC® CCL-61™), в стандартных условиях (флакон 1000 мл, температура 37ºC, pH 7,0, скорость мешалки 80 об/мин, минимальное содержание растворенного кислорода 30%; время культивирования 14 суток).
[0203] В более конкретном варианте осуществления, присутствует увеличение ADCC (уменьшение EC50 и/или увеличение максимума) в 1,2-2,0 или даже по меньшей мере в 2,0 раза, по сравнению с указанным исходным антителом (см., например, фигуры 13 и 14).
[0204] В более конкретном варианте осуществления, присутствует увеличение ADCP (уменьшение EC50 кривой показателей фагоцитоза) по меньшей мере в 3 или даже 5 раз, или более, по сравнению с указанным исходным антителом (см., например, фигуры 15 и 16).
[0205] В рамках изобретения, термин «полипептид, имеющий активность GnTIII, GnTIII», относится к полипептидам, способным катализировать добавление остатка N-ацетилглюкозамина (GlcNAc) в β-1-4-связи к β-связанному маннозиду из триманнозильного кора N-связанных олигосахаридов, например, β-l,4-маннозил-гликопротеин-4-ß-N-ацетилглюкозаминил-трансферазе (EC 2.4.1.144).
[0206] В рамках изобретения, термин «FUT8» относится к α1,6-фукозилтрансферазе (EC:2.4.1.68).
[0207] В рамках изобретения, термин «эффекторная функция, Fc-опосредованная клеточная цитотоксичность» относится к тем видам биологической активности, которые можно приписать области Fc (природной последовательности области Fc или варианту аминокислотной последовательности области Fc) антитела. Примеры эффекторных функций антитела включают, но без ограничения, аффинность связывания с рецептором Fc, антителозависимую клеточную цитотоксичность (ADCC), антителозависимый клеточный фагоцитоз (ADCP), секрецию цитокинов, опосредованное иммунными комплексами поглощение антигена антигенпредставляющими клетками, понижающую регуляцию рецепторов поверхности клеток и т.д. Такой иммунный механизм лежит в основе лизиса «клеток-мишеней» «человеческими иммуноэффекторными клетками».
[0208] В рамках изобретения, термин «подвергнутое гликоинженерии антитело» относится к биспецифическому антителу по изобретению, которое содержит уменьшенное количество фукозилированных и/или разделенных надвое олигосахаридов, присоединенных к области Fc указанного антитела, обычно, к аминокислоте Asn297, по сравнению с исходным антителом.
[0209] В рамках изобретения, термин «исходное антитело, исходное биспецифическое антитело», в контексте гликоинженерии, относится к биспецифическому антителу по изобретению, которое имеет такой же аминокислотный состав, что и подвергнутое гликоинженерии антитело, но не подвергнуто гликоинженерии. Для такого сравнения, исходное антитело и подвергнутое гликоинженерии антитело продуцируют в одинаковой клетке-хозяине, но в первом случае, в клетке-хозяине без гликоинженерии, и во втором случае, в такой же клетке-хозяине, но подвергнутой инженерии посредством направленного повреждения гена FUT8 или инженерии посредством экспрессии полинуклеотида, кодирующего полипептид, имеющий активность GnTIII, в стандартных условиях (см. выше).
[0210] В рамках изобретения, термин «человеческие иммуноэффекторные клетки» относится к популяции лейкоцитов, экспонирующих на своих поверхностях рецепторы Fc, посредством которых они связываются с областью Fc антигенсвязывающих молекул или слитых с Fc белков и осуществляют эффекторные функции. Такая популяция может включать, но без ограничения ими, мононуклеарные клетки периферической крови (PBMC) и/или клетки естественные киллеры (NK) и/или макрофаги.
[0211] В рамках изобретения, термин «увеличенная Fc-опосредованная клеточная цитотоксичность» определяют как увеличение количества «клеток-мишеней», лизируемых за данное время, при данной концентрации биспецифического антитела по изобретению, в среде, окружающей клетки-мишени, посредством механизма Fc-опосредованной клеточной цитотоксичности, определенной выше, и/или уменьшение концентрации биспецифического антитела по изобретению, в среде, окружающей клетки-мишени, необходимое для достижения лизиса данного количества «клеток-мишеней» за данное время, посредством механизма Fc-опосредованной клеточной цитотоксичности. Увеличение Fc-опосредованной клеточной цитотоксичности присутствует относительно клеточной цитотоксичности, опосредованной таким же биспецифическим антителом по изобретению продуцированным таким же типом клеток-хозяев, с использованием таких же стандартных условий, но не продуцированным клетками-хозяевами, подвергнутыми инженерии для получения измененного паттерна гликозилирования (например, для экспрессии гликозилтрансферазы, GnTIII, или других гликозилтрансфераз, или повреждения FUT8), способами, описанными в настоящем описании.
[0212] В рамках изобретения термин «экспрессирующий вектор» относится к одному или нескольким векторам, содержащим тяжелые и легкие цепи антитела по изобретению подходящим образом, как известно на предшествующем уровне техники.
[0213] В рамках изобретения «клетки-хозяева, подвергнутые инженерии посредством направленного повреждения гена FUT8», относится к клетки-хозяевам, способным экспрессировать антитело по изобретению и дополнительно подвергнутым гликоинженерии посредством направленного повреждения гена FUT8, как описано например, в US8067232, US7425446, US6946292 (полное содержание каждой из которых приведено в настоящем описании в качестве ссылки), и Yamane-Ohnuki N. et al., Biotech. Bioeng.; 87 (2004) 614-622. Антитело по изобретению, экспрессированное в такой клетке-хозяине, содержит область Fc, содержащую комплексные N-гликозид-связанные цепи сахаров, связанные с областью Fc, содержащие восстанавливающий конец, который содержит N-ацетилглюкозамин, где цепи сахаров не содержат фукозы, связанной с положением 6 N-ацетилглюкозамина на восстанавливающем конце цепей сахаров.
[0214] Настоящее изобретение, кроме того, относится к способу получения биспецифического антитела, в соответствии с настоящим изобретением, отличающегося отсутствием фукозилирования на 50%-100%, 60%-100%, 70%-100%, 80%-100% или 90%-100%, продуцированного клеткой-хозяином, включающему экспрессию в указанной клетке-хозяине нуклеиновой кислоты, кодирующей биспецифическое антитело по изобретению, и нуклеиновой кислоты, кодирующей полипептид с активностью гликозилтрансферазы, или вектора, содержащего такие нуклеиновые кислоты. Гены с активностью гликозилтрансферазы включают гены (l,4)-N-ацетилглюкозаминилтрансферазы III (GnTIII), a-манноидазы II (Manll), (l,4)-галактозилтрансферазы (GalT), (l,2)-N-ацетилглюкозаминилтрансферазы I (GnTI) и β(1,2)-N-ацетилглюкозаминилтрансферазы II (GnTII). В одном варианте осуществления, комбинацию генов с активностью гликозилтрансферазы экспрессируют в клетке-хозяине (например, GnTIII и Man II). Подобным образом, способ включает также экспрессию одного или нескольких полинуклеотида(полинуклеотидов), кодирующих биспецифическое антитело, в клетке-хозяине, в которой ген гликозилтрансферазы поврежден или иным образом инактивирован (например, в клетке-хозяине, в которой активность гена, кодирующего a-1-6-кор-фукозилтрансферазу, подвергнута нокауту). В другом варианте осуществления, биспецифические антитела по настоящему изобретению можно продуцировать в клетке-хозяине, дополнительно экспрессирующей полинуклеотид, кодирующий полипептид, имеющий активность GnTIII, для модификации паттерна гликозилирования. В конкретном варианте осуществления, полипептид, имеющий активность GnTIII, представляет собой слитый полипептид, содержащий домен локализации в аппарате Гольджи из располагающегося в аппарате Гольджи полипептида. В другом предпочтительном варианте осуществления, экспрессия биспецифических антител по настоящему изобретению в клетке-хозяине, экспрессирующей полинуклеотид, кодирующий полипептид, имеющий активность GnTIII, приводит к получению биспецифических антител с увеличенной аффинностью связывания с рецептором Fc и увеличенной эффекторной функцией.
[0215] Настоящее изобретение, кроме того, относится к способу получения биспецифического антитела, в соответствии с настоящим изобретением, отличающегося отсутствием фукозилирования на 50%-100%, 60%-100%, 70%-100%, 80%-100% или 90%-100%, продуцированного клеткой-хозяином, включающему экспрессию в указанной клетке-хозяине нуклеиновой кислоты, кодирующей биспецифическое антитело по изобретению и поврежденный ген FUT8.
[0216] В одном варианте осуществления, для биспецифических антител с измененным гликозилированием, продуцированных клетками-хозяевами по изобретению, показана увеличенная аффинность связывания с рецептором Fc и/или увеличенная эффекторная функция в результате модификации клетки-хозяина (например, посредством экспрессии гена гликозилтрансферазы). Предпочтительно, увеличенная аффинность связывания с рецептором Fc представляет собой увеличенное связывание с активирующим рецептором Fcγ, таким как рецептор FcγRIIIa.
[0217] В одном варианте осуществления, процент нефукозилированных олигосахаридов составляет 50%-100%, конкретно, 60%-100%, 70%-100% и более конкретно, 80%-100%. Нефукозилированные олигосахариды могут принадлежать к гибридному или комплексному типу. В другом варианте осуществления, биспецифическое антитело, продуцированное способами по изобретению, имеет увеличенную долю разделенных надвое олигосахаридов в области Fc, в результате модификации олигосахаридов способами по настоящему изобретению. В одном варианте осуществления, процент разделенных надвое олигосахаридов составляет 50%-100%, конкретно, 50%, 60%-70% и более конкретно, 80%. В особенно предпочтительном варианте осуществления, биспецифическое антитело, продуцированное посредством клеток-хозяев и способов по изобретению, имеет увеличенную долю разделенных надвое, нефукозилированных олигосахаридов в области Fc. Разделенные надвое, нефукозилированные олигосахариды могут являться либо гибридными, либо комплексными.
[0218] В рамках изобретения, термин «клетка-хозяин» включает любой вид клеточной системы, который можно подвергать инженерии для получения биспецифических антител по настоящему изобретению. В одном варианте осуществления, клетку-хозяина подвергают инженерии для обеспечения продукции антигенсвязывающей молекулы с моифицированными гликоформами. В конкретных вариантах осуществления, клетки-хозяева подвергают дополнительной манипуляции для экспрессии увеличенных уровней одного или нескольких полипептидов, имеющих активность GnTIII. Клетки-хозяева включают культивированные клетки, например, культивированные клетки млекопитающих, такие как клетки CHO (см. выше), клетки BHK, клетки NSO, клетки SP2/0, клетки миеломы YO, клетки миеломы мыши P3X63, клетки PER, клетки PER.C6 или клетки гибридомы, клетки дрожжей, клетки насекомых и клетки растений, помимо прочих, но также клетки, содержащиеся в трансгенном животном, трансгенном растении или культивированной ткани растения или животного. Клетки-хозяева для продукции подвергнутых гликоинженерии биспецифических антител по настоящему изобретению описаны например, в US6602684, US20040241817, US20030175884; и WO 2004065540. Биспецифические антитела по настоящему изобретению можно, альтернативно, подвергать гликоинженерии для получения уменьшенного количества остатков фукозы в области Fc, в соответствии со способами, описанными в US2003/0157108, EP1176195, WO2003084570, WO2003085119 и US2003/0115614, US2004/093621, US2004/110282, US2004/110704, US2004/132140 (полное содержание каждой из которых приведено в настоящем описании в качестве ссылки). Подвергнутые гликоинженерии биспецифические антитела по изобретению можно также получать в системах экспрессии, образующих модифицированные гликопротеины, таких как системы, описанные в WO2003/056914, WO2004/057002, и WO2004/024927 (полное содержание каждой из которых приведено в настоящем описании в качестве ссылки).
[0219] В следующем варианте осуществления изобретения, антитело по изобретению содержит одну или две, или три аминокислотные замены в области Fc («аминокислотную замену в Fc»), выбранные из группы, состоящей из одиночных замен S239D, I332E, G236A, двойных замен I332E и G236A, S239D и I332E («замена DE»), S239D и G236A, и тройной замены S329D и I332E и G236A («замена DEA»); (Richards JO, et al., Mol. Cancer Ther. 7 (2008) 2517-2527). Из-за различного подсчета тяжелой цепи, эти номера аминокислот могут отличаться на +/- одну, две или три аминокислоты, но с одинаковым сдвигом для всех трех. В случае тяжелой цепи из SEQ ID NO:5, присутствует сдвиг на одну аминокислоту, и S329D и I332E и G236A, таким образом, обозначает S328D и I331E и G235A. SEQ ID: NO:5 с заменой DE показана в SEQ ID NO:23, и SEQ ID: NO:5 с заменой DEA показана в SEQ ID NO:24. Активность ADCC и/или ADCP биспецифического антитела можно увеличивать посредством такой модификации аминокислоты из части Fc.
[0220] В рамках изобретения, термин «исходное антитело, исходное биспецифическое антитело», в контексте замены в Fc, относится к биспецифическому антителу по изобретению, которое имеет такой же аминокислотный состав, что и Fc-замещенное антитело, но без указанной замены(замен). Для такого сравнения, исходное антитело и Fc-замещенное антитело продуцируют - как в случае подвергнутых гликоинженерии антител - в такой же клетке-хозяине, в таких же условиях, но в первом случае, в клетке-хозяине без замены в Fc, и во втором случае, в такой же клетке-хозяине, но с такой заменой(заменами) в Fc. Полезная линия клеток-хозяев представляет собой, например, CHO-K1.
[0221] В рамках изобретения, термин «исходное антитело, исходное биспецифическое антитело», в контексте биспецифического антитела по изобретению, которое содержит замену в Fc и подвергнуто гликоинженерии, такое исходное антитело, таким образом, представляет собой соответствующее биспецифическое антитело, которое имеет такой же аминокислотный состав, что и Fc-замещенное антитело, но без указанной замены(замен), и не подвергнуто гликоинженерии.
[0222] В следующем варианте осуществления изобретения, активность ADCC и/или ADCP биспецифического антитела увеличена посредством аминокислотной замены в части Fc в комбинации с гликоинженерией части Fc, по сравнению с ADCC и/или ADCP соответствующего исходного антитела.
[0223] Изобретение относится, таким образом, в одном варианте осуществления, к биспецифическому антителу, специфически связывающемуся с CEACAM5 человека и CD47 человека, отличающемуся включением одной или двух, или трех аминокислотных замен в области Fc («аминокислотной замены в Fc»), выбранных из группы, состоящей из одиночных замен S239D, I332E, G236A, двойных замен I332E и G236A, S239D и I332E, тройных замен S329D и I332E и G236A, и имеющему отсутствие фукозилирования части Fc на 50%-100%, 60%-100%, 70%-100%, 80%-100% или 90%-100%.
[0224] В примере 9 описаны анализы, используемые для определения активности ADCC, а также активности ADCP
[0225] ADCC можно измерять посредством анализа ADCC in vitro следующим образом:
1) в анализе используют клетки-мишени, как известно, экспрессирующие CEA, узнаваемый связывающей CEA областью биспецифического антитела;
2) в анализе используют мононуклеарные клетки периферической крови (PBMC) человека, выделенные из крови случайным образом выбранного здорового человека, в качестве эффекторных клеток;
3) анализ проводят, в соответствии со следующим способом:
i) PBMC выделяют с использованием стандартных способов центрифугирования в градиенте плотности и суспендируют при 6,25×106 клеток/мл в культуральной среде RPMI;
ii) клетки-мишени выращивают посредством стандартных способов культивирования тканей, собирают в фазе экспоненциального роста с жизнеспособностью выше 90%, промывают в культуральной среде RPMI, метят с использованием 100 микроКюри 51Cr для 1×106 клеток, промывают дважды культуральной средой и ресуспендируют в культуральной среде при плотности 0,25×106 клеток/мл;
iii) 20 микролитров вышеуказанной конечной суспензии клеток-мишеней переносят в каждую лунку 96-луночного микропланшета для титрования;
iv) биспецифическое антитело серийно разводят от 4000 нг/мл до 0,12 нг/мл в культуральной среде, и 20 микролитров полученных растворов антитела добавляют к клеткам-мишеням в 96-луночном микропланшете для титрования, тестируя в трех повторах различные концентрации антитела, перекрывающие весь вышеуказанный диапазон концентраций;
v) для контроля максимального высвобождения (MR), в 3 дополнительные лунки в планшете, содержащие меченые клетки-мишени, вводят 50 микролитров 5% (об./об.) водного раствора неионного детергента (тритона, Sigma, St. Louis), вместо раствора биспецифического антитела (пункт iv выше);
vi) для контроля спонтанного высвобождения (SR), в 3 дополнительные лунки в планшете, содержащие меченые клетки-мишени, вводят 20 микролитров культуральной среды RPMI вместо раствора биспецифического антитела (пункт iv выше);
vii) затем 96-луночный микропланшет для титрования центрифугируют при 50 x g в течение 1 минуты и инкубируют в течение 1 часа при 4°C;
viii) 40 микролитров суспензии PBMC (пункт i выше) добавляют в каждую лунку для получения соотношения эффекторных клеток:клеток-мишеней (E:T) 50:1, и планшеты помещают в инкубатор в атмосферу 5% CO2 при 37°C на 4 часа;
ix) не содержащий клеток супернатант из каждой лунки собирают, и высвобожденную в эксперименте радиоактивность (ER) количественно оценивают с использованием счетчика гамма-излучения;
x) процент специфического лизиса рассчитывают для каждой концентрации биспецифического антитела, в соответствии с формулой (ER-MR)/(MR-SR) x 100, где ER представляет собой среднюю радиоактивность, количественно оцененную (см. пункт ix выше) для этой концентрации антитела, MR представляет собой среднюю радиоактивность, количественно оцененную (см. пункт ix выше) для контроля MR (см. пункт v выше), и SR представляет собой среднюю радиоактивность, количественно оцененную (см. пункт ix выше) для контроля SR (см. пункт vi выше);
[0226] В рамках изобретения «увеличенную ADCC» определяют как увеличение максимального процента специфического лизиса, наблюдаемого в пределах диапазона концентраций биспецифического антитела, тестированного выше, и/или уменьшение концентрации биспецифического антитела, необходимой для получения половины максимального процента специфического лизиса (EC50), наблюдаемого в пределах диапазона концентраций биспецифического антитела, тестированного выше. Увеличение ADCC присутствует относительно ADCC, измеренной с использованием вышеуказанного анализа, опосредованной таким же биспецифическим антителом, продуцированным таким же типом клеток-хозяев, с использованием таких же стандартных способов продукции, очистки, получения состава и хранения, но не продуцированным клетками-хозяевами, подвергнутыми инженерии для сверхэкспрессии GnTIII или клетками-хозяевами, подвергнутыми инженерии посредством направленного повреждения гена FUT8 («исходным антителом»). В случае аминокислотных замен в Fc, увеличение ADCC присутствует относительно ADCC, измеренной с использованием исходного биспецифического антитела, не несущего замены(замен). В случае биспецифического антитела, содержащего аминокислотные замены в части Fc и подвергнутого гликоинженерии, увеличение ADCC присутствует относительно ADCC, измеренной с использованием исходного, не подвергнутого гликоинженерии, биспецифического антитела, не несущего замены(замен).
Терапевтические применения и способы применения антигенсвязывающих молекул против CEA
[0227] Биспецифические антитела CEACAM x CD47 по изобретению являются оптимизированными для лечения солидных опухолей, в основном посредством опосредованного макрофагами фагоцитоза клеток опухолей, либо в монотерапии, либо в комбинированной терапии, особенно вместе с CEAxCD3 T-клеточным биспецифическим антителом, подобным CEA-TCB или CEA-TCB1, и/или антагонистом оси PD-1. Антитело по изобретению и T-клеточное биспецифическое антитело CEAxCD3 можно вводить, как описано ниже.
[0228] В конкретном варианте осуществления, заболевание, соответствующее солидной опухоли, представляет собой злокачественную опухоль, экспрессирующую или даже сверхэкспрессирующую CEA, включая, но без ограничения, группу из колоректальных опухолей, немелкоклеточных опухолей легкого, опухолей желудка, опухолей поджелудочной железы и опухолей молочной железы. В конкретном варианте осуществления, опухоль представляет собой колоректальную опухоль. Все терапевтические применения, способы применения, применения, комбинации и т.д., описанные в настоящем описании, представляют собой конкретные варианты осуществления для лечения этих опухолей/заболеваний.
[0229] Авторы настоящего изобретения выявили, что для антител по изобретению показан низкий потенциал или отсутствие потенциала образования ADA, соответственно, потери воздействия из-за нейтрализующего ADA, соответственно, потери эффективности.
[0230] В одном варианте осуществления, изобретение относится к способу лечения карцином (злокачественных опухолей, опухолей, например, карцином человека), особенно, экспрессирующих CEA опухолей, in vivo. Этот способ включает введение индивиду фармацевтически эффективного количества композиции, содержащей биспецифическое антитело по изобретению. Под «индивидом» понимают индивида-человека, в одном варианте осуществления, пациента. страдающего злокачественной опухолью/опухолью/карциномой.
[0231] Экспрессия CEA в различных видах опухолей обычно является очень высокой, особенно, в колоректальной карциноме, аденокарциноме поджелудочной железы, раке желудка, немелкоклеточном раке легкого, раке молочной железы, карциноме головы и шеи, раке матки и мочевого пузыря, среди прочих. В здоровом, нормальном гландулярном эпителии в желудочно-кишечном тракте, CEA в основном экспрессируется в поляризованном паттерне на апикальной поверхности клеток. Этот поляризованный паттерн экспрессии ограничивает доступность моно- или биспецифических антител против CEA, вводимых системно, и таким образом, потенциальную токсичность. Вместе с низкой аффинностью связывания CD47 антитела по изобретению, это приводит к отсутствующему или ограниченному фагоцитозу таких нормальных клеток посредством антитела по изобретению. Этот поляризованный паттерн экспрессии теряется в клетках злокачественных опухолей желудочно-кишечного тракта и других злокачественных опухолей. CEA равным образом экспрессируется по всей клеточной поверхности клеток злокачественных опухолей, что означает, что клетки злокачественных опухолей являются намного более доступными для антитела по изобретению, чем нормальные, здоровые клетки, и могут быть избирательно уничтожены посредством биспецифических антител CEAxCD47 по изобретению, соответственно, посредством комбинаций, упомянутых выше.
[0232] В одном варианте осуществления, биспецифические антитела по этому изобретению можно использовать в монотерапии для лечения солидных опухолей на поздних стадиях, в одном варианте осуществления, экспрессирующих CEA опухолей. В одном варианте осуществления биспецифическое антитело по изобретению используют в комбинации с Mab CEAxCD3 в одновременной, отдельной или последовательной комбинации. В одном варианте осуществления биспецифическое антитело по изобретению используют в комбинации с Mab CEAxCD3 и/или антагонистом оси PD-1 в одновременной, отдельной или последовательной комбинации. В одном варианте осуществления, биспецифическое антитело по изобретению используют в комбинации с антагонистом оси PD-1 в одновременной, отдельной или последовательной комбинации. Такие антагонисты оси PD-1 описаны, например, в WO2017118675. Такие комбинации атакуют солидную злокачественную опухоль посредством макрофагов и T-клеток. Два Mab CEAxCD3 находятся в клинической разработке (CEA-TCB и CEA-TCB1; см. clinicaltrials.gov; RO6958688 в NCT3866239 и RO7172508 в NCT03539484). MEDI-565 находился в клинической разработке, однако, активные клинические исследования невозможно идентифицировать в clinicaltrials.gov. В одном варианте осуществления, в качестве биспецифического антитела против CEA и CD3, используют антитело CEA-TCB или CEA-TCB1.
[0233] Связывающий CEA член, использованный в CEA-TCB, получен из антитела против CEA PR1A3 (см., например, EP2681244B1). Это антитело связывается с так называемым доменом B3 CEA. CEA-TCB имеет низкую нМ аффинность связывания с CEA, и для него показана эффективность в высоких дозах (между 40 и 600 мг на дозу и пациента; (см., например, J.Tabernero et.al., J. Clin. Oncol. 35, 2017 (suppl. Abstr. 3002)). В этих дозах, почти все мишени CEA на клеточных поверхностях заняты посредством CEA-TCB. Комбинация CEA-TCB или CEA-TCB1 и CEAxCD47 образует терапевтические уровни в плазме обоих лекарственных средств в одно и то же время и приводит к достижению наилучших результатов (аддитивных или даже синергических), если оба лекарственные средства являются неконкурентными за антиген CEA.
[0234] В рамках изобретения термины «комбинация, одновременная, отдельная или последовательное комбинация» антитела по изобретению и второго биспецифического антитела, связывание с CEA человека и CD3ε человека, относятся к любому введению двух антител (или трех антител, в случае комбинации антитела по изобретению, Mab CEAxCD3 и антагониста оси PD-1), либо отдельно, либо вместе, где два или три антитела вводят в качестве части подходящего режима дозирования, разработанного для получения преимущества комбинированной терапии, например, при отдельном, последовательном, одновременном, параллельном, распределенном в хронологическом порядке или чередующемся введении. Таким образом, два или три антитела можно вводить либо в качестве части одной и той же фармацевтической композиции, либо в отдельных фармацевтических композициях. Антитело по изобретению можно вводить до, во время или после введения второго биспецифического антитела, или в некоторой их комбинации. Когда антитело по изобретению вводят пациенту с повторяющимися интервалами, например, в ходе стандартного курса лечения, второе биспецифическое антитело можно вводить до, во время или после каждого введения антитела по изобретению или в некоторой их комбинации, или с различными интервалами, применительно к лечению с использованием антитела по изобретению, или в однократной дозе до, в любое время в ходе или после курса лечения с использованием антитела по изобретению. В одном варианте осуществления, антитело по изобретению и второе биспецифическое антитело вводят в чередующемся введении, в одном варианте осуществления, с интервалами 6-15 суток между введением антитела по изобретению и второго антитела. В таком чередующемся введении, первая доза может представлять собой антитело по изобретению или второе антитело.
[0235] Термин «антагонист оси PD-1» относится к антителу против PD-1 или антителу против PD-Ll. Антитела против PD-1 представляют собой например, пембролизумаб (кейтруда®, MK-3475), ниволумаб, пидилизумаб, ламбролизумаб, MEDI-0680, PDR001, и REGN2810. Антитела против PD-1 описаны например, в 5 WO200815671, WO2013173223, WO2015026634, US7521051, US8008449, US8354509, WO2009114335, WO2015026634, WO2008156712, WO2015026634, WO2003099196, WO2009101611, WO2010/027423, WO2010/027827, WO2010/027828, WO2008/156712 и WO2008/156712 (полное содержание каждой из которых приведено в настоящем описании в качестве ссылки).
[0236] Антитела против PD-Ll представляют собой, например, атезолизумаб, MDX-1 105, дурвалумаб и авелумаб. Антитела против PD-Ll представляют собой, например, описанные в WO2015026634, WO2013/019906, W02010077634, US8383796, WO2010077634, WO2007005874 и WO2016007235 (полное содержание каждой из которых приведено в настоящем описании в качестве ссылки).
[0237] Применительно к комбинированному введению антитела по изобретению и второго биспецифического антитела, оба соединения могут присутствовать в одной лекарственной форме или в отдельных лекарственных формах, например, в двух различных или идентичных лекарственных формах.
[0238] Если антитело по изобретению и второе антитело являются неконкурентными применительно к CEACAM5, в одном варианте осуществления, оба антитела, если желательно терапевту, можно вводить одновременно. Если антитело по изобретению и второе антитело являются конкурентными применительно к CEACAM5, в одном варианте осуществления, оба антитела вводят в чередующемся введении.
[0239] Антитело по изобретению можно, как правило, вводить пациенту в режиме дозирования, обеспечивающем наиболее эффективное лечение злокачественной опухоли (с точек зрения как эффективности, так и безопасности), от которой лечат пациента, как известно в данной области. Предпочтительно, клетки опухолей атакуют в одно и то же время посредством T-клеток и макрофагов, для достижения полного терапевтического потенциала этого способа, биспецифические антитела CEA-CD3 и CEAxCD47 должны являться неконкурентными, применительно к связыванию с CEA на клеточной поверхности.
[0240] Как обсуждали выше, количество введенного антитела и расписание введения антитела по изобретению может зависеть от типа (например, пола, возраста, массы) и состояния пациента, подвергаемого лечению, тяжести заболевания или состояния, подвергаемого лечению, и от способа введения. Например, антитело по изобретению и второе антитело можно вводить пациенту в дозах, лежащих в диапазоне от 0,1 до 100 мг/кг массы тела в сутки или в неделю, в однократной или дробных дозах, или посредством непрерывной инфузии. В одном варианте осуществления каждое из антитела по изобретению и второго антитела вводят пациенту в дозах, лежащих в диапазоне от 0,1 до 20 мг/кг. В некоторых случаях, уровни дозирования ниже нижнего предела вышеуказанного диапазона, могут являться адекватными, в то время как в других случаях еще большие дозы можно использовать без вызова какого-либо опасного побочного эффекта.
[0241] В рамках изобретения, термин «время полужизни антитела» относится к времени полужизни указанного антитела, как измерено в обычном фармакокинетическом анализе, например, как описано в примере 17. Антитело по изобретению и второе биспецифическое антитело против CEA и CD3 имеют период времени полувыведения 3-14 суток.
[0242] В другом аспекте, изобретение относится также к применению биспецифического антитела по изобретению в лечении заболевания, в частности, нарушений пролиферации клеток, при которых CEA экспрессируется, в частности, при которых CEA аномально экспрессируется (например, сверхэкспрессируется или экспрессируется с отличным паттерном на клеточной поверхности), по сравнению с нормальной тканью из того же типа клеток. Такие нарушения включают, но без ограничения, колоректальный рак, NSCLC (немелкоклеточный рак легкого), рак желудка, рак поджелудочной железы и рак молочной железы. Уровни экспрессии CEA можно определять способами, известными в данной области (например, посредством иммуногистохимического анализа, иммунофлуоресцентного анализа, иммуноферментного анализа, ELISA, проточной цитометрии, радиоиммунного анализа и т.д.).
[0243] В одном аспекте, биспецифические антитела по настоящему изобретению можно использовать для нацеливания на клетки, in vivo или in vitro экспрессирующие CEA. Биспецифические антитела по изобретению являются особенно полезными в предотвращении образования опухолей, уничтожении опухолей и ингибировании роста или метастазирования опухоли посредством индукции ADCP и ADCC клеток опухолей. Биспецифические антитела по изобретению можно использовать для лечения любой опухоли, экспрессирующей CEA. Конкретные злокачественные новообразования, которые можно лечить с использованием биспецифических антител по изобретению, включают, но без ограничения, колоректальный рак, немелкоклеточный рак легкого, рак желудка, рак поджелудочной железы и рак молочной железы.
[0244] Биспецифические антитела по изобретению вводят млекопитающему, предпочтительно, человеку, в фармацевтически приемлемой лекарственной форме, такой как обсуждаемые ниже, включая формы, которые можно вводить человеку внутривенно в форме болюса или посредством непрерывной инфузии в течение некоторого периода времени, посредством внутримышечного, внутрибрюшинного, интрацереброспинального, подкожного, интраартикулярного, внутрисуставного, интратекального, перорального, местного или ингаляционного способов. Биспецифические антитела по изобретению также подходящим образом вводят посредством внутриопухолевого, перитуморального, внутриочагового или периочагового способов для оказания местных, так же как системных терапевтических эффектов.
[0245] Для лечения заболевания, подходящая доза биспецифических антител по изобретению может зависеть от типа заболевания, подлежащего лечению, тяжести и течения заболевания, предшествующей терапии, анамнеза пациента и ответа на антитело, и решения лечащего терапевта. Биспецифическое антитело по изобретению подходящим образом вводят пациенту за один раз или на протяжении серий лечения. Настоящее изобретение относится к способу избирательного уничтожения клеток опухолей, экспрессирующих CEA.
[0246] Этот способ включает взаимодействие биспецифических антител по изобретению с указанными клетками опухолей. Эти клетки опухолей могут происходить из карциномы человека, включая колоректальную карциному, немелкоклеточную карциному легких (NSCLC), карциному желудка, карциному поджелудочной железы и карцинома молочной железы.
[0247] В другом аспекте изобретение относится к применению биспецифических антител по изобретению для изготовления лекарственного средства для лечения заболевания, связанного с аномальной экспрессией CEA. В конкретном варианте осуществления, заболевание представляет собой злокачественную опухоль, экспрессирующую или даже сверхэкспрессирующую CEA, включая, но без ограничения, колоректальную опухоль, немелкоклеточную опухоль легкого, опухоль желудка, опухоль поджелудочной железы и опухоль молочной железы. В конкретном варианте осуществления, опухоль представляет собой колоректальную опухоль.
Композиции, составы, дозы и способы введения
[0248] В одном аспекте, настоящее изобретение относится к фармацевтическим композициям, содержащим биспецифические антитела по настоящему изобретению и фармацевтически приемлемый носитель. Настоящее изобретение, кроме того, относится к применению таких фармацевтических композиций в способе лечения заболевания, такого как злокачественная опухоль, или в изготовлении лекарственного средства для лечения заболевания, такого как злокачественная опухоль. Конкретно, настоящее изобретение относится к способу лечения заболевания, и более конкретно, лечения злокачественной опухоли, включающему введение терапевтически эффективного количества фармацевтической композиции по изобретению.
[0249] В одном аспекте, настоящее изобретение относится к фармацевтическим композициям, комбинациям и способам для лечения карцином, опухолей человека, как определено выше. Например, изобретение относится к фармацевтическим композициям для применения в лечении карцином человека, содержащим фармацевтически эффективное количество антитела по настоящему изобретению и фармацевтически приемлемый носитель.
[0250] Композиции биспецифического антитела по изобретению можно вводить с использованием общепринятых способов введения, включая, но без ограничения, внутривенное, внутрибрюшинное, пероральное, внутрилимфатическое или прямое внутриопухолевое введение. Внутривенное введение или подкожное введение являются предпочтительными.
[0251] В одном аспекте изобретения, терапевтические составы, содержащие биспецифические антитела по изобретению, подготавливают для хранения посредством смешивания антитела, имеющего желательную степень чистоты, с необязательными фармацевтически приемлемыми носителями, наполнителями или стабилизаторами (Remington's Pharmaceutical Sciences 16th edition, Osol, A. Ed. (1980)), в форме лиофилизированных составов или жидких составов. Приемлемые носители, наполнители или стабилизаторы являются нетоксичными для реципиентов в используемых дозах и концентрациях. Составы, подлежащие использованию для введения in vivo, должны являться стерильными. Этого легко достичь фильтрацией через стерилизующие фильтрационные мембраны. Наиболее эффективный способ введения и режим дозирования для фармацевтических композиций по этому изобретению зависит от тяжести и течения заболевания, состояния пациента и ответа на лечение, и решения лечащего терапевта. Соответственно, дозы композиций могут представлять собой фиксированные дозы или могут быть адаптированы для индивидуального пациента, например, по массе тела. Тем не менее, эффективная доза композиций по этому изобретению, как правило, лежит в диапазоне от 0,1 до 20 мг/кг.
[0252] Биспецифические антитела по этому изобретению имеют молекулярную массу порядка 150 кДа на моль. Они несут, в одном варианте осуществления, часть Fc. Период времени полувыведения у пациентов лежит в диапазоне от 3 до 14 суток. Это время полужизни позволяет, но без ограничения, введение один раз в сутки, один раз в неделю, или один раз в каждые две недели.
[0253] Биспецифические антитела по настоящему изобретению и их соответствующее композиции могут находиться во множестве лекарственных форм, которые включают, но без ограничения, жидкие растворы или суспензии, таблетки, пилюли, порошки, суппозитории, полимерные микрокапсулы или микровезикулы, липосомы и пригодные для инъекции или инфузии растворы. Предпочтительная форма зависит от способа введения и терапевтического применения.
[0254] Композицию, содержащую биспецифическое антитело по настоящему изобретению, можно составлять, дозировать и вводить способом, согласующимся с надлежащей медицинской практикой. Факторы для учета в этом контексте включают конкретное заболевание или нарушение, подвергаемое лечению, конкретное млекопитающее, подвергаемое лечению, клиническое состояние индивидуального пациента, причину заболевания или нарушения, участок доставки средства, способ введения, расписание введения, и другие факторы, известные практикующему специалисту в области медицины.
Изделия
[0255] В другом аспекте, изобретение относится к изделию, содержащему материалы, которые можно использовать для лечения, предотвращения и/или диагностики нарушений, описанных выше. Изделие содержит контейнер и этикетку или листовку-вкладыш на контейнере, или приложенные к контейнеру. Подходящие контейнеры включают, например, флаконы, ампулы, шприцы, пакеты для IV раствора и т.д. Контейнеры могут быть изготовлены из множества материалов, таких как стекло или пластик. Контейнер содержит композицию, которая, самостоятельно или в комбинации с другой композицией, является эффективной для лечения, предотвращения и/или диагностики состояния, и может иметь стерильное отверстие для доступа (например, контейнер может представлять собой пакет или флакон с раствором для внутривенного введения, имеющий пробку, прокалываемую стерильной иглой для подкожных инъекций). По меньшей мере одно действующее вещество в композиции представляет собой биспецифическое антитело по изобретению. На этикетке или в листовке-вкладыше указано, что композицию используют для лечения выбранного состояния. Кроме того, изделие может содержать (a) первый контейнер с содержащейся в нем композицией, содержащей биспецифическое антитело по изобретению; и (b) второй контейнер с содержащейся в нем композицией, содержащей дополнительное цитотоксическое или иное лекарственное средство. Изделие, в этом варианте осуществления изобретения, может дополнительно содержать листовку-вкладыш, где указано, что композиции можно использовать для лечения конкретного состояния. Альтернативно или дополнительно, изделие может дополнительно содержать второй (или третий) контейнер, содержащий фармацевтически приемлемый буфер, такой как бактериостатическая вода для инъекций (BWFI), фосфатно-солевой буфер, раствор Рингера и раствор декстрозы. Он может дополнительно включать другие материалы, желательные с коммерческой и пользовательской точки зрения, включая другие буферы, разбавители, фильтры, иглы и шприцы.
ДОПОЛНИТЕЛЬНЫЕ ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
[0256] Ниже описаны варианты осуществления биспецифического антитела, специфически связывающегося с CEACAM5 человека и CD47 человека.
[0257] 1. Биспецифическое антитело, содержащее первую связывающую часть, специфически связывающуюся с CEACAM5 человека, и вторую связывающую часть, специфически связывающуюся с CD47 человека.
[0258] 2. Биспецифическое антитело, в соответствии с вариантом осуществления 1, отличающееся тем, что область Fc подвергнута гликоинженерии для получения уменьшенного количества остатков фукозы по сравнению с таким же, но не подвергнутым гликоинженерии, биспецифическим антителом.
[0259] 3. Биспецифическое антитело, в соответствии с вариантом осуществления 1 или 2, отличающееся тем, что первая связывающая часть связывается с Ig-подобным доменом V-типа CEACAM5 из аминокислот 35-144.
[0260] 4. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-3, отличающееся тем, что указанное биспецифическое антитело конкурирует с антителом SM3E за связывание с CEACAM5.
[0261] 5. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-3, отличающееся тем, что указанное биспецифическое антитело не конкурирует с антителами SM3E, MEDI, LAB, SAR, T86.66, CH1A1A.
[0262] 6. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-5, отличающееся тем, что значение EC50 для фагоцитоза посредством указанного биспецифического антитела лежит в диапазоне от 0,1- до 10-кратного значения E50 эталонного антитела K2AC22 в таких же экспериментальных условиях и в присутствии или в отсутствие 1 мг/мл IgG человека.
[0263] 7. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-6, отличающееся тем, что в присутствии 1 мг/мл IgG человека максимум показателя фагоцитоза, измеренный в анализе на основе визуализации, не уменьшается более чем на 30% по сравнению с фагоцитозом без IgG человека в таких же экспериментальных условиях.
[0264] 8. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-7, отличающееся тем, что является моновалентным для первой связывающей части и моновалентным для второй связывающей части.
[0265] 9. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-8, отличающееся тем, что каждая из первой и второй связывающей части содержит тяжелую цепь иммуноглобулина и легкую цепь иммуноглобулина.
[0266] 10. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-9, отличающееся тем, что принадлежит к типу IgG1 человека.
[0267] 11. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-10, отличающееся тем, что константные и вариабельные последовательности каркасной области являются человеческими или имеют человеческое происхождение.
[0268] 12. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-11, отличающееся тем, что биспецифическое антитело представляет собой полноразмерное антитело.
[0269] 13. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-12, отличающееся содержанием первой связывающей части, специфически связывающейся с CEACAM5 человека, содержащей вариабельный домен легкой цепи каппа и константный домен легкой цепи лямбда, и второй связывающей части, специфически связывающейся с CD47 человека, содержащей вариабельный домен легкой цепи каппа и константный домен легкой цепи каппа.
[0270] 14. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-12, отличающееся содержанием первой связывающей части, специфически связывающейся с CEACAM5 человека, содержащей вариабельный домен легкой цепи лямбда и константный домен легкой цепи лямбда, и второй связывающей части, специфически связывающейся с CD47 человека, содержащей вариабельный домен легкой цепи каппа и константный домен легкой цепи каппа.
[0271] 15. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 13 или 14, отличающееся содержанием общей тяжелой цепи.
[0272] 16. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-15, отличающееся
a) тем, что первая связывающая часть содержит вариабельную область тяжелой цепи, содержащую CDRH1 из SEQ ID NO:1, CDRH2 из SEQ ID NO:2 и CDRH3 из SEQ ID NO:3, и константный домен легкой цепи типа лямбда человека и из SEQ ID NO:13, и
тем, что вторая связывающая часть содержит вариабельную область тяжелой цепи, содержащую CDRH1 из SEQ ID NO:1, CDRH2 из SEQ ID NO:2 и CDRH3 из SEQ ID NO:3, и вариабельную область легкой цепи, содержащую CDRL1 из SEQ ID NO:7, CDRL2 из Ala Ala Ser, включенную в SEQ ID NO:8, и CDRL3 из SEQ ID NO:9, или
b) тем, что первая связывающая часть содержит вариабельную область тяжелой цепи, содержащую, в качестве CDR, CDRH1 из SEQ ID NO:25, CDRH2 из SEQ ID NO:26 и CDRH3 из SEQ ID NO:27, и константный домен легкой цепи типа лямбда человека и из SEQ ID NO:13, и тем, что вторая связывающая часть содержит вариабельную область тяжелой цепи, содержащую, в качестве CDR, CDRH1 из SEQ ID NO:25, CDRH2 из SEQ ID NO:26 и CDRH3 из SEQ ID NO:27, и вариабельную область легкой цепи, содержащую, в качестве CDR, CDRL1 из SEQ ID NO:28, CDRL2 из SEQ ID NO:29 и CDRL3 из SEQ ID NO:30.
[0273] 17. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-16, отличающееся содержанием первой связывающей части, специфически связывающейся с CEACAM5 человека, и второй связывающей части, специфически связывающейся с CD47 человека, отличающиеся
a) тем, что первая связывающая часть содержит вариабельную область тяжелой цепи, содержащую, в качестве CDR, CDRH1 из SEQ ID NO:25, CDRH2 из SEQ ID NO:26 и CDRH3 из SEQ ID NO:27, и вариабельную область легкой цепи, содержащую комбинацию из CDRL1, CDRL2 и CDRL3, выбранную из группы, состоящей из:
SEQ ID NO:31, 32 и 33; SEQ ID NO:34, 35 и 36, SEQ ID NO:37, 38 и 39, SEQ ID NO:40, 41 и 42, SEQ ID NO:43, 44 и 45, SEQ ID NO:46, 47 и 48, SEQ ID NO:49, 50 и 51, SEQ ID NO:52, 53 и 54, SEQ ID NO:55, 56 и 57, SEQ ID NO:58, 59 и 60, SEQ ID NO:61, 62 и 63, и SEQ ID NO: 112, 113 и 114, и
b) тем, что вторая связывающая часть содержит вариабельную область тяжелой цепи, содержащую, в качестве CDR, CDRH1 из SEQ ID NO:1, CDRH2 из SEQ ID NO:2 и CDRH3 из SEQ ID NO:3, и вариабельную область легкой цепи, содержащую, в качестве CDR, CDRL1 из SEQ ID NO:7, CDRL2 из Ala Ala Ser, включенную в SEQ ID NO:8, и CDRL3 из SEQ ID NO:9, или
тем, что вторая связывающая часть содержит вариабельную область тяжелой цепи, содержащую, в качестве CDR, CDRH1 из SEQ ID NO:25, CDRH2 из SEQ ID NO:26 и CDRH3 из SEQ ID NO:27, и вариабельную область легкой цепи, содержащую, в качестве CDR, CDRL1 из SEQ ID NO:28, CDRL2 из SEQ ID NO:29 и CDRL3 из SEQ ID NO:30, и необязательно, константный домен легкой цепи типа лямбда человека и из SEQ ID NO:13
[0274] 18. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-17, отличающееся содержанием первой связывающей части, специфически связывающейся с CEACAM5 человека, и второй связывающей части, специфически связывающейся с CD47 человека, отличающихся
a) тем, что первая связывающая часть содержит вариабельную область тяжелой цепи из SEQ ID NO:4 и вариабельную область легкой цепи, выбранную из группы VL, включенных в области VLCL, состоящей из:
SEQ ID NO:64, SEQ ID NO:65, SEQ ID NO:66, SEQ ID NO:67, SEQ ID NO:68, SEQ ID NO:69, SEQ ID NO:70, SEQ ID NO:71, SEQ ID NO:72, SEQ ID NO:73, SEQ ID NO:74 и SEQ ID NO:115, и
b) тем, что первая связывающая часть содержит вариабельную область тяжелой цепи из SEQ ID NO:4 и вариабельную область легкой цепи из SEQ ID NO:10.
[0275] 19. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-18, отличающееся содержанием первой связывающей части, специфически связывающейся с CEACAM5 человека, и второй связывающей части, специфически связывающейся с CD47 человека, отличающихся
a) тем, что первая связывающая часть содержит тяжелую цепь из SEQ ID NO:5 и легкую цепь, выбранную из группы, состоящей из:
SEQ ID NO:64, SEQ ID NO:65, SEQ ID NO:66, SEQ ID NO:67, SEQ ID NO:68, SEQ ID NO:69, SEQ ID NO:70, SEQ ID NO:71, SEQ ID NO:72, SEQ ID NO:73, SEQ ID NO:74 и SEQ ID NO:115, и
b) тем, что вторая связывающая часть содержит вариабельную область тяжелой цепи из SEQ ID NO:5 и вариабельную область легкой цепи из SEQ ID NO:11.
[0276] 20. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-19, отличающееся тем, что представляет собой полноразмерное биспецифическое антитело типа IgG1 человека и является моновалентным для первой связывающей части и моновалентным для второй связывающей части, и содержащее первую связывающую часть, специфически связывающуюся с CEACAM5 человека, содержащую вариабельный домен легкой цепи каппа и константный домен легкой цепи лямбда, и вторую связывающую часть, специфически связывающуюся с CD47 человека, содержащую вариабельный домен легкой цепи каппа и константный домен легкой цепи каппа, или содержащее первую связывающую часть, специфически связывающуюся с CEACAM5 человека, содержащую вариабельный домен легкой цепи лямбда и константный домен легкой цепи лямбда, и вторую связывающую часть, специфически связывающуюся с CD47 человека, содержащую вариабельный домен легкой цепи каппа и константный домен легкой цепи каппа.
[0277] 21. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-20, отличающееся связыванием с CD47 человека с аффинностью связывания 100 нМ - 600 нМ, предпочтительно 100-500 нМ.
[0278] 22. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-21, отличающееся связыванием с клетками MKN-45 с значением EC50 1-200 нМ.
[0279] 23. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-22, отличающееся связыванием с CD47 человека с аффинностью связывания 100 нМ - 500 нМ, и связыванием с клетками MKN-45 с значением EC50 1-200 нМ.
[0280] 24. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-23, отличающееся тем, что
a) EC50 для кривой показателей фагоцитоза клеток MKN-45 в присутствии макрофагов человека, посредством указанного биспецифического антитела, не сдвигается более чем в 4 раза в сторону более высоких концентраций в присутствии 200 нг/мл растворимого CEA, по сравнению с EC50, измеренной без растворимого CEA, и/или что максимум кривой показателей фагоцитоза не уменьшается на 10% или более, 15% или более, или 20% или более посредством добавления 200 нг/мл растворимого CEA, и/или
b) EC50 для кривой связывания с клетками MKN-45 указанного биспецифического антитела не сдвигается более чем в 2 раза в сторону более высоких концентраций в присутствии 200 нг/мл растворимого CEA, по сравнению с EC50, измеренной без растворимого CEA.
[0281] 25. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-24, отличающееся связыванием с человеческими рекомбинантными CEACAM5 и CEACAM6, при этом значения EC50 для связывания с рекомбинантным CEACAM5 и CEACAM6 отличаются менее чем в 3 раза.
[0282] 26. Биспецифическое антитело, в соответствии с вариантом осуществления 25, отличающееся
a) тем, что первая связывающая часть содержит вариабельную область тяжелой цепи, содержащую, в качестве CDR, CDRH1 из SEQ ID NO:25, CDRH2 из SEQ ID NO:26 и CDRH3 из SEQ ID NO:27, и вариабельную область легкой цепи, содержащую, в качестве CDR, CDRL1 из SEQ ID NO: 112, CDRL2 из SEQ ID NO: 113 и CDRL3 из SEQ ID NO: 114, и
b) тем, что вторая связывающая часть содержит вариабельную область тяжелой цепи, содержащую, в качестве CDR, CDRH1 из SEQ ID NO:25, CDRH2 из SEQ ID NO:26 и CDRH3 из SEQ ID NO:27, и вариабельную область легкой цепи, содержащую, в качестве CDR, CDRL1 из SEQ ID NO:28, CDRL2 из SEQ ID NO:29 и CDRL3 из SEQ ID NO:30.
[0283] 27. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-26, отличающееся тем, что биспецифическое антитело, специфически связывающееся с CEACAM5 человека и CD3ε, содержащее, в качестве тяжелых цепей, тяжелые цепи из SEQ ID NO:97 и 98 и, в качестве легких цепей, легкие цепи из SEQ ID NO: 96 и 99, в концентрации 300 нМ, не сдвигает EC50 кривой связывания биспецифического антитела по изобретению с клетками MKN-45 более чем в 3 раза, в одном варианте осуществления, в сторону более высоких концентраций.
[0284] 28. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-27, отличающееся тем, что биспецифическое антитело, специфически связывающееся с CEACAM5 человека и CD3ε (далее также названное как CEA-TCB1), содержащее, в качестве тяжелых и легких цепей, цепи аминокислотных последовательностей SEQ ID NO: 92-95 в концентрации 30 нМ, не сдвигает EC50 кривой связывания биспецифического антитела по изобретению с клетками MKN-45 более чем в 3 раза, в одном варианте осуществления, в сторону более высоких концентраций.
[0285] 29. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-28, отличающееся тем, что область Fc подвергнута гликоинженерии для получения уменьшенного количества остатков фукозы, по сравнению с соответствующим исходным биспецифическим антителом.
[0286] 30. Биспецифическое антитело, в соответствии с вариантом осуществления 29, отличающееся тем, что 50%-100% N-связанных олигосахаридов в области Fc являются нефукозилированными.
[0287] 31. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 29 или 30, отличающееся тем, что 50%-100% N-связанных олигосахаридов в области Fc являются разделенными надвое.
[0288] 32. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 29-31, отличающееся тем, что 80%-100% N-связанных олигосахаридов в области Fc являются разделенными надвое и нефукозилированными.
[0289] 33. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 29-32, отличающееся тем, что значение EC50 для ADCC и/или максимум ADCC, индуцированной указанным антителом, увеличены в 1,2-2,0 раза или по меньшей мере в 2,0 раза, и/или значение EC50 кривой показателей фагоцитоза уменьшено по меньшей мере в 1,2-2,0 раза или по меньшей мере в 2,0 раза, по сравнению с максимумом ADCC и/или значением EC50, индуцированными соответствующим исходным биспецифическим антителом.
[0290] 34. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 29-33, отличающееся тем, что определенный посредством визуализации максимум показателя фагоцитоза, индуцированного указанным антителом, увеличен по меньшей мере в 3 раза, и/или значение EC50 кривой показателей фагоцитоза уменьшено по меньшей мере в 3 раза или по меньшей мере в 5 раз, по сравнению с максимумом показателя фагоцитоза, соответственно, значением EC50, индуцированными соответствующим исходным биспецифическим антителом.
[0291] 35. Способ получения биспецифического антитела, в соответствии с любым из вариантов осуществления 29-34 и 30, отличающийся включением:
a) культивирования клетки-хозяина, подвергнутой инженерии для экспрессии по меньшей мере одной нуклеиновой кислоты, кодирующей полипептид, имеющий активность β(1,4)-N-ацетилглюкозаминилтрансферазы III, в условиях, обеспечивающих продукцию указанного биспецифического антитела, и позволяющих указанную модификацию гликоинженерии олигосахаридов, присутствующих в области Fc указанного биспецифического антитела; и
b) выделения указанного подвергнутого гликоинженерии биспецифического антитела, где указанное антитело является способным специфически связываться с CEACAM5 человека и CD47 человека.
[0292] 36. Способ получения биспецифического антитела, в соответствии с любым из вариантов осуществления 29-30 и 33-34, отличающийся включением:
a) культивирования клетки-хозяина, подвергнутой гликоинженерии, посредством направленного повреждения гена FUT8, в условиях, обеспечивающих продукцию указанного подвергнутого гликоинженерии биспецифического антитела по изобретению, и позволяющих указанную модификацию гликоинженерии олигосахаридов, присутствующих в области Fc указанного биспецифического антитела, и
b) выделения указанного подвергнутого гликоинженерии биспецифического антитела, где указанное антитело является способным специфически связываться с CEACAM5 человека и CD47 человека.
[0293] 37. Выделенный полинуклеотид, отличающийся кодированием биспецифического антитела, в соответствии с любым из вариантов осуществления 1-34.
[0294] 38. Вектор, содержащий полинуклеотид, в соответствии с вариантом осуществления 37.
[0295] 39. Клетка-хозяин, содержащая вектор, в соответствии с вариантом осуществления 38.
[0296] 40. Композиция, содержащая биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-34, и фармацевтически приемлемый носитель.
[0297] 41. Способ индукции клеточного лизиса клетки опухоли, включающий приведение клетки опухоли в контакт с биспецифическим антителом, в соответствии с любым из вариантов осуществления 1-34.
[0298] 42. Способ, в соответствии с вариантом осуществления 41, отличающийся тем, что клетка опухоли представляет собой клетку колоректального рака, NSCLC (немелкоклеточного рака легкого), клетку рака желудка, клетку рака поджелудочной железы, клетку рака молочной железы или другую клетку опухоли, экспрессирующую CEACAM5 человека.
[0299] 43. Способ лечения индивида, имеющего злокачественную опухоль, экспрессирующую CEA, включающий введение индивиду терапевтически эффективного количества биспецифического антитела, в соответствии с любым из вариантов осуществления 1-34.
[0300] 44. Способ увеличения времени выживаемости индивида, имеющего злокачественную опухоль, экспрессирующую CEA, где указанный способ включает введение указанному индивиду терапевтически эффективного количества биспецифического антитела, в соответствии с любым из вариантов осуществления 1-34.
[0301] 45. Способ, в соответствии с вариантом осуществления 43 или 44, отличающееся тем, что злокачественная опухоль представляет собой колоректальный рак, немелкоклеточный рак легкого (NSCLC), рак желудка, рак поджелудочной железы или рак молочной железы.
[0302] 46. Способ, в соответствии с любым из вариантов осуществления 43-45, отличающееся тем, что биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-34, вводят в комбинации с химиотерапией или радиотерапией индивиду-человеку.
[0303] 47. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-34, для применения в изготовлении лекарственного средства для лечения индивида, имеющего злокачественную опухоль, экспрессирующую CEA.
[0304] 48. Биспецифическое антитело для применения в соответствии с вариантом осуществления 47, отличающегося тем, что злокачественная опухоль выбрана из группы, состоящей из колоректального рака, немелкоклеточного рака легкого (NSCLC), рака желудка, рака поджелудочной железы и рака молочной железы.
[0305] 49. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-34, для применения в способе лечения индивида, имеющего злокачественную опухоль, экспрессирующую CEA, включающем введение индивиду терапевтически эффективного количества указанного биспецифического антитела, отличающегося тем, что значение EC50 для фагоцитоза указанного биспецифического антитела лежит в диапазоне от 0,1- до 10-кратного значения E50 эталонного антитела K2AC22, содержащего первую связывающую часть, специфически связывающуюся с CEACAM5 человека, и вторую связывающую часть, специфически связывающуюся с CD47 человека, при этом первая связывающая часть содержит тяжелую цепь из SEQ ID NO:5 и легкую цепь из SEQ ID NO:65, и тем, что вторая связывающая часть содержит тяжелую цепь из SEQ ID NO:5 и легкую цепь из SEQ ID NO:11, в таких же экспериментальных условиях и в присутствии и/или в отсутствие 1 мг/мл IgG человека.
[0306] 50. Первое биспецифическое антитело, содержащее первую связывающую часть, специфически связывающуюся с CEACAM5 человека, и вторую связывающую часть, специфически связывающуюся с CD47 человека, для применения в одновременной, отдельной или последовательной комбинации с вторым биспецифическим антителом, содержащим третью связывающую часть, специфически связывающуюся с CEACAM5 человека, и четвертую связывающую часть, специфически связывающуюся с CD3ε человека, в лечении индивида-человека, имеющего опухоль, экспрессирующую CEA.
[0307] 51. Первое биспецифическое антитело для применения в соответствии с вариантом осуществления 50, отличающееся тем, что указанная четвертая связывающая часть второго биспецифического антитела связывается с эпитопом CD3ε человека, содержащим аминокислотную последовательность из SEQ ID NO:22.
[0308] 52. Первое биспецифическое антитело для применения в соответствии с вариантом осуществления 50 или 51, отличающееся тем, что указанное второе антитело содержит, в качестве тяжелой и легкой цепей, цепи из SEQ ID NO:96-99, или содержит, в качестве тяжелой и легкой цепей, цепи аминокислотных последовательностей SEQ ID NO: 92-95, и что указанное второе антитело в концентрации 300 нМ или 30 нМ не сдвигает EC50 кривой связывания указанного первого биспецифического антитела с клетками MKN-45 более чем в 3 раза, в одном варианте осуществления, в сторону более высоких концентраций.
[0309] 53. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-34, для применения в одновременной, отдельной или последовательной комбинации с вторым биспецифическим антителом, содержащим, в качестве тяжелых и легких цепей, цепи из SEQ ID NO:96-99 или содержащим, в качестве тяжелых и легких цепей, цепи аминокислотных последовательностей SEQ ID NO: 92-95 в лечении индивида, имеющего злокачественную опухоль, экспрессирующую CEA.
[0310] 54. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-34 и 50-53, отличающееся тем, что не конкурирует с вторым биспецифическим антителом, содержащим, в качестве тяжелых и легких цепей, цепи из SEQ ID NO:96-99 или содержащим, в качестве тяжелых и легких цепей, цепи аминокислотных последовательностей SEQ ID NO: 92-95, для применения в одновременной, отдельной или последовательной комбинации с указанным вторым биспецифическим антителом в лечении индивида, имеющего злокачественную опухоль, экспрессирующую CEACAM5 человека.
[0311] 55. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-34 и 50-53, для применения в одновременной, отдельной или последовательной комбинации в лечении индивида, имеющего злокачественную опухоль, экспрессирующую CEACAM5 человека, с вторым биспецифическим антителом, содержащим a) третью связывающую часть, специфически связывающуюся с CEACAM5 человека, содержащую вариабельную область тяжелой цепи из SEQ ID NO:20 и вариабельную область легкой цепи из SEQ ID NO:21, и четвертую связывающую часть, специфически связывающуюся с эпитопом CD3ε человека, где указанный эпитоп содержит аминокислотную последовательность из SEQ ID NO:22 или b), в качестве тяжелых и легких цепей, цепи из SEQ ID NO:96-99 или, в качестве тяжелых и легких цепей, цепи аминокислотных последовательностей SEQ ID NO: 92-95 соответственно, в лечении индивида, имеющего злокачественную опухоль, экспрессирующую CEACAM5 человека, в результате чего указанное второе биспецифическое антитело в концентрации 300 нМ (SEQ ID NO:96-99) или 30 нМ (SEQ ID NO 92-95) не сдвигает EC50 кривой показателей фагоцитоза клеток MKN-45 биспецифического антитела, в соответствии с любым из вариантов осуществления 1-34 более чем в 3 раза, в сторону более высоких концентраций.
[0312] 56. Биспецифическое антитело для применения в соответствии с любым из вариантов осуществления 50-55, отличающееся тем, что указанная злокачественная опухоль представляет собой колоректальный рак, немелкоклеточный рак легкого (NSCLC), рак желудка, рак поджелудочной железы и рак молочной железы.
[0313] 57. Биспецифическое антитело для применения в соответствии с любым из вариантов осуществления 50-56, отличающееся тем, что биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-34, и второе биспецифическое антитело вводят указанному индивиду попеременно или одновременно с интервалами 6-15 суток.
[0314] 58. Композиция, содержащая биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-34, отличающееся отсутствием перекрестной реакционной способности с вторым биспецифическим антителом, содержащим a) третью связывающую часть, специфически связывающуюся с CEACAM5 человека, содержащую вариабельную область тяжелой цепи из SEQ ID NO:20 и вариабельную область легкой цепи из SEQ ID NO:21, и четвертую связывающую часть, специфически связывающуюся с эпитопом CD3ε человека, содержащим аминокислотную последовательность из SEQ ID NO:22, или b), в качестве тяжелых и легких цепей, цепи из SEQ ID NO:96-99 или, в качестве тяжелых и легких цепей, цепи аминокислотных последовательностей SEQ ID NO: 92-95, для применения в лечении индивида, имеющего злокачественную опухоль, экспрессирующую CEACAM5 человека.
[0315] 59. Композиция, содержащая биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-34, для применения в одновременной, отдельной или последовательной комбинации в лечении индивида, имеющего злокачественную опухоль, экспрессирующую CEACAM5 человека, с вторым биспецифическим антителом, содержащим a) третью связывающую часть, специфически связывающуюся с CEACAM5 человека, содержащую вариабельную область тяжелой цепи из SEQ ID NO:20 и вариабельную область легкой цепи из SEQ ID NO:21, и четвертую связывающую часть, специфически связывающуюся с эпитопом CD3ε человека, содержащим аминокислотную последовательность из SEQ ID NO:22, или b), в качестве тяжелых и легких цепей, цепи из SEQ ID NO:96-99 или, в качестве тяжелых и легких цепей, цепи аминокислотных последовательностей SEQ ID NO: 92-95, в результате чего указанное второе биспецифическое антитело в концентрации 300 нМ, соответственно 30 нМ (SEQ ID NO: 92-95), не сдвигает EC50 кривой показателей фагоцитоза клеток MKN-45 биспецифического антитела, в соответствии с любым из вариантов осуществления 1-34, более чем в 3 раза, в одном варианте осуществления, в сторону более высоких концентраций.
[0316] 60. Композиция, в соответствии с вариантом осуществления 58 или 59, отличающаяся тем, что злокачественная опухоль представляет собой колоректальный рак, немелкоклеточный рак легкого (NSCLC), рак желудка, рак поджелудочной железы и рак молочной железы.
[0317] 61. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-34, для применения в способе лечения индивида, имеющего злокачественную опухоль, экспрессирующую CEA, включающем введение индивиду терапевтически эффективного количества указанного биспецифического антитела.
[0318] 62. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 1-34, для применения в способе увеличения времени выживаемости индивида, имеющего злокачественную опухоль, экспрессирующую CEA, где указанный способ включает введение указанному индивиду терапевтически эффективного количества указанного биспецифического антитела.
[0319] 63. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 61 или 62, отличающееся тем, что указанное биспецифическое антитело вводят в комбинации с химиотерапией или радиотерапией индивиду-человеку.
[0320] 64. Биспецифическое антитело, в соответствии с любым из вариантов осуществления 60 или 62, отличающееся тем, что указанная злокачественная опухоль представляет собой колоректальный рак, немелкоклеточный рак легкого (NSCLC), рак желудка, рак поджелудочной железы или рак молочной железы.
Таблица 1: СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
[SEQ ID 36] ак TCB WO2017055389) и SEQ37
WO201705538
[SEQ ID 34])
(выступ, P329G LALA) [SEQ ID 37] ак TCB WO2017055389)
VH-CK FC, выступ P329G LALA
SEQ ID NO:92-95 относится к CEA-TCB1, и SEQ 96-99 относится к CEA-TCB.
Ala: аланин; Ser: серин
ПРИМЕРЫ
Пример 1 Клонирование, экспрессия и очистка CD47 человека
Клонирование
[0321] Последовательность, соответствующую внеклеточному домену CD47 человека (hCD47), амплифицируют из кДНК человека посредством полимеразной цепной реакции (ПЦР) с использованием специфических олигонуклеотидов. Продукт амплификации очищают в геле и клонируют в экспрессирующий вектор для млекопитающих pEAK8 (Edge Biosystems, Gaithersburg, Md.). Вектор дополнительно модифицируют для введения Avitag™ (Avidity, Denver Colo.) и гекса-гистидиновой метки на C-конце, позволяющей биотинилирование одиночного участка белка и очистку посредством IMAC (аффинной хроматографии с иммобилизованным ионом металла), соответственно. Конструкции подтверждают посредством секвенирования ДНК.
Экспрессия
[0322] Затем плазмидой трансфицируют клетки млекопитающих с использованием реагента для трансфекции на основе липосом, такого как липофектамин 2000 (Thermofisher Scientific). Стадия трансфекции требует только небольших количеств ДНК и клеток, как правило, 2×105 клеток и 2 мкг плазмидной ДНК на лунку, и трансфекцию проводят в 6-луночном планшете. Несмотря на то, что можно использовать различные линии клеток млекопитающих, в примерах, приведенных ниже, трансфицируют монослой эпителиальных клеток эмбриональной почки человека (клеток PEAK). Эти клетки стабильно экспрессируют ген EBNA-1, дополнительно поддерживая процесс эписомной репликации, являются полуадгерентными, и их можно выращивать в стандартных условиях культивирования клеток (5% CO2; 37°C в среде DMEM, дополненной 10% эмбриональной телячьей сывороткой). Через 24 час, клетки помещают в селективные условия посредством добавления среды, содержащей 0,5-2 мкг/мл пуромицина: клетки, несущие эписомный вектор, являются устойчивыми к этому антибиотику.
[0323] Через две-три недели после трансфекции, амплифицированные и отобранные клетки инъецировали в одноразовые биореакторы CELLine™ для стадии продукции. CELLine™ представляет собой двухкамерный биореактор, который можно использовать в стандартном инкубаторе для культивирования клеток. Меньшая камера (15 мл) содержит клетки и отделена от большей (один литр), содержащей среду камеры посредством полупроницаемой мембраны с порогом отсечения 10 кДа (Bruce et al. 2002, McDonald et al. 2005). Эта система позволяет диффузию питательных веществ, газов и побочных продуктов, в то же время сохраняя клетки и секретированные белки в меньшей камере. Культуру поддерживают в течение 7-10 суток перед сбором супернатанта. Поскольку среда содержит сыворотку, клетки сохраняют хорошую жизнеспособность, и несколько циклов продукции можно получать с использованием одних и тех же клеток и контейнеров.
Очистка
[0324] После сбора, культуральные супернатанты осветляют посредством центрифугирования. Затем супернатант дополняют 100 мМ имидазолом и наносят на Ni-NTA смолу для аффинной хроматографии (Qiagen). Относительно высокая концентрация имидазола минимизирует связывание контаминантов со смолой. После промывки колонки, белки элюируют при скорости потока 2 мл/мин с использованием 30 мл градиента имидазола (20-400 мМ имидазола) в хроматографической системе AKTA Prime (Amersham Pharmacia Biotech). Градиент элюции дополнительно улучшает чистоту рекомбинантного белка, но может быть заменен способом ступенчатой элюции, если хроматографическая система является недоступной. Элюированные фракции можно анализировать посредством SDS-PAGE или ELISA для определения содержания в них рекомбинантного белка. Представляющие интерес фракции пулируют и обессоливают на колонках Amicon 10KD (Millipore) уравновешенных фосфатно-солевым буфером или другим подходящим буфером. Затем обессоленные белки можно количественно оценивать с использованием различных способов, и их чистоту анализировать посредством SDS-PAGE. Рекомбинантный CD47 биотинилируют in vitro с использованием биотин-лигазы (Avidity, Denver Colo.), согласно инструкциям производителя. После обессоливания, уровень биотинилирования оценивают посредством анализов осаждения с использованием магнитных бусин со стрептавидином и анализа SDS-PAGE.
Пример 2 Клонирование, экспрессия и очистка членов семейства CEACAM человека
Клонирование
[0325] Последовательность, соответствующую полному внеклеточному домену (ECD) и доменам A3-B3 CEACAM5, синтезировали в Eurofins и Twist Bioscience. Эти синтетические гены субклонировали в экспрессирующий вектор для млекопитающих pEAK8 (Edge Biosystems, Gaithersburg, Md.). Векторы модифицировали для введения Avitag™ (Avidity, Denver Colo.) и любого из гекса-гистидиновой метки, области FC человека или области FC мыши на C-конце. Конструкции подтверждали посредством секвенирования ДНК. Очистку рекомбинантного растворимого белка проводили посредством IMAC (аффинной хроматографии с иммобилизованным ионом металла), аффинного матрикса FcXL или CaptureSelect™ IgG-Fc (ms) (Thermofisher Scientific).
[0326] Векторы, кодирующие полноразмерный вариант CEACAM человека 1, 3, 4, 5, 6, 7, 8, 18, 19, 20, 21 и CEACAM5 яванского макака, также получали для экспрессии на клеточной поверхности клеток PEAK и/или CHO. Растворимый, полноразмерный CEACAM16 человека также клонировали сходным образом.
Экспрессия и очистка
[0327] Экспрессию, очистку и биотинилирование вышеупомянутых рекомбинантных белков проводили, как подробно описано в примере 1.
Пример 3 Отбор посредством фагового дисплея Fv против CEACAM5 с использованием библиотек человеческих scFv, содержащих фиксированный вариабельный тяжелый домен
[0328] Общие способы конструирования и манипуляции для библиотек scFv человека, экспонированных на бактериофаге M13, описаны в Vaughan et al., (Nat. Biotech. 1996, 14:309-314), полное содержание которого, таким образом, приведено в качестве ссылки. Библиотеки для отбора и скрининга кодируют scFv, которые все разделяют одинаковый домен VH и имеют разнообразие единственно в домене VL. Способы получения библиотек с фиксированным VH и их использование для идентификации и сборки биспецифических антител описаны в US 2012/0184716 и WO 2012/023053, полное содержание каждой из которых, таким образом, приведено в качестве ссылки. Способы идентификации связывания scFv с CECAM5 человека описаны ниже.
Отбор с использованием белков
[0329] Аликвоты фаговых библиотек scFv (1012 БОЕ) блокируют с использованием PBS, содержащего 3% (масс./об.) обезжиренного молока, в течение одного часа при комнатной температуре в ротационном смесителе. Блокированный фаг отсеивают на магнитных бусинах со стрептавидином (Dynabeads™ M-280) в течение одного часа при комнатной температуре в ротационном смесителе. Отсеянный фаг инкубируют либо с 100 нМ биотинилированным CEACAM5 человека, либо с доменом A3-B3, связанными на магнитных бусинах со стрептавидином, в течение двух часов при комнатной температуре в ротационном смесителе. Бусины связывают с использованием магнитного штатива, с последующими пятью промывками с использованием PBS/0,1% Tween 20 и двумя промывками с использованием PBS. Фаг элюируют с использованием 100 нМ TEA в течение 30 минут при комнатной температуре в ротационном смесителе. Элюированный фаг и бусины нейтрализуют с использованием Трис-HCl 1M pH 7,4 и добавляют непосредственно к 10 мл находящихся в фазе экспоненциального роста клеток TG1, и инкубируют в течение одного часа при 37°C с медленным встряхиванием (90 об/мин). Аликвоту инфицированных TG1 серийно разводят для титрования выхода отбора. Остальные инфицированные TG1 центрифугируют при 3800 об/мин в течение 10 минут и ресуспендируют в 2 мл 2xTY, и распределяют по чашкам с 2xTYAG (средой 2xTY, содержащей 100 мкг/мл ампициллина и 2% глюкозы) с агаром Bioassay. После инкубации в течение ночи при 30°C, 10 мл 2xTY добавляют в чашки, и клетки соскребают с поверхности и переносят в 50 мл полипропиленовую пробирку. Раствор 50% глицерина добавляют к суспензии клеток для получения конечной концентрации 17% глицерина. Аликвоты после циклов отбора сохраняют при -80°C.
Выделение фага
[0330] 50 мкл суспензии клеток, полученных из предшествующих циклов отбора, добавляют к 50 мл 2xTYAG и выращивают при 37°C при встряхивании (240 об/мин) до достижения OD600 0,3-0,5. Затем культуру суперинфицируют с использованием 1,2×1011 фага-помощника M13K07 и инкубируют в течение одного часа при 37°C (90 об/мин). Среду меняют посредством центрифугирования клеток при 3800 об/мин в течение 10 минут, удаления среды и ресуспендирования осадка в 50 мл 2xTYAK (среды 2xTY, содержащей 100 мкг/мл ампициллина; 50 мкг/мл канамицина). Затем культуру выращивают в течение ночи при 30°C (240 об/мин). На следующие сутки, содержащий фаг супернатант используют для следующего цикла отбора.
Отборы на клеточной поверхности
[0331] Содержащие фаги супернатанты блокируют с использованием PBS, содержащего 3% (масс./об.) обезжиренного молока, в течение одного часа при комнатной температуре в ротационном смесителе. Затем блокированный фаг отсеивают в течение одного часа на MKN45 CEACAM5KO, которые не экспрессируют CEACAM5 человека. Отсеянный фаг инкубируют с 2×107 клеток MKN45, экспрессирующих CEACAM5 (блокированных в PBS 3% BSA 0,1% NaN3) в течение двух часов при комнатной температуре с осторожным встряхиванием. Клетки осаждают и промывают шесть раз с использованием PBS. Связанный фаг элюируют с использованием 76 мМ лимонной кислоты и встряхивания в течение 10 минут. После нейтрализации с использованием 1M Трис-HCl, pH 8, клетки добавляют непосредственно к 10 мл находящихся в фазе экспоненциального роста TG1 и инкубируют в течение одного часа при 37°C с медленным встряхиванием. Аликвоту инфицированных TG1 серийно разводят для титрования выхода отбора. Инфицированные TG1 центрифугируют при 3800 об/мин в течение 10 минут и ресуспендируют в 2 мл среды 2xTY, и распределяют по чашкам с 2xTYAG с агаром Bioassay. После инкубации в течение ночи при 30°C, 10 мл 2xTY добавляют в чашку, и клетки соскребают с поверхности и переносят в 50 мл полипропиленовую пробирку. Раствор 50% глицерина добавляют к суспензии клеток для получения конечной концентрации 17% глицерина. Аликвоты после циклов отбора сохраняют при -80°C.
Пример 4 Скрининг по связыванию/отсутствию связывания scFv с растворимыми CEACAM5, CEACAM6 и CEACAM1
Периплазматический препарат scFv для тестов связывания и функциональных тестов
[0332] Индивидуальные клоны инокулируют в микропланшет для титрования с глубокими лунками, содержащий 0,9 мл на лунку среды 2xTYAG (среды 2xTY, содержащей 100 мкг/мл ампициллина, 0,1% глюкозы) и выращивают при 37°C в течение 5-6 часов (240 об/мин). Затем 100 мкл на лунку 0,2 мМ IPTG в среде 2xTY добавляют для получения конечной концентрации 0,02 мМ IPTG. Планшет инкубируют в течение ночи при 30°C с встряхиванием при 240 об/мин. Планшет с глубокими лунками центрифугируют при 3200 об/мин в течение 10 минут при 4°C, и супернатант осторожно удаляют. Осадки ресуспендируют в 150 мкл буфера TES (50 мМ Трис-HCl (pH 8), 1 мМ ЭДТА (pH 8), 20% сахарозы, дополненного полным ингибитором протеаз, Roche). Гипотонический шок получают посредством добавления 150 мкл разведенного буфера TES (разведение 1:5 TES:вода) и инкубации на льду в течение 30 минут. Планшет центрифугируют при 4000 об/мин в течение 10 минут при 4°C для осаждения клеток и дебриса. Супернатанты осторожно переносят в другой микропланшет для титрования и сохраняют на льду для немедленного тестирования в функциональных анализах или анализах связывания.
Связывание
[0333] Скрининг scFv по связыванию с CEACAM5 тестируют в гомогенном анализе с использованием технологии CellInsightTM. Следующие реагенты смешивают в каждой лунке 384-луночного планшета с прозрачным дном (Corning): 30 мкл суспензии полистироловых бусин со стрептавидином (Polysciences; 3000 бусин/лунку), покрытых любым из биотинилированного CEACAM5, биотинилированного домена A3-B3 или биотинилированного NusA в качестве контрольного белка; 60 мкл блокированного периплазматического препарата scFv; 10 мкл буфера для детекции (PBS, содержащего антитело мыши против c-myc при 5 мкг/мл; антитело против Fc мыши с AlexaFluor® 647, разведенное 1:200). После перемешивания при 600 об/мин в течение 5 минут, 384-луночный планшет инкубируют при комнатной температуре и считывают через 2 часа на платформе для одновременного многопараметрического скрининга CellInsightTM CX5 (ThermoFisher Scientific). Клоны, экспрессирующие scFv, подающие специфический сигнал для CEACAM5, а не для NusA, отбирают для дальнейшего анализа или секвенирования.
[0334] Связывание с CEACAM1, CEACAM6 и другими CEACAM можно измерять таким же способом.
Секвенирование фаговых клонов
[0335] Отдельные клоны инокулируют в 96-луночный микропланшет для титрования с глубокими лунками, содержащий 1 мл среды LBAG (среды LB с 100 мкг/мл ампициллина и 2% глюкозы) на лунку и выращивают в течение ночи при 37°C, 240 об/мин. ДНК выделяют с использованием набора для выделения в минимасштабе Zyppy-96 Plasmid Miniprep (Zymo Research) и секвенируют.
Пример 5. Переформатирование кандидатов с фиксированным VH в IgG и временная экспрессия в клетках млекопитающих
[0336] После скрининга и секвенирования, scFv-кандидаты с желательными свойствами связывания переформатируют в IgG и экспрессируют посредством временной трансфекции в клетках PEAK. Последовательности VH и VL отобранных scFv амплифицируют с использованием специфических олигонуклеотидов и клонируют в экспрессирующий вектор, содержащий константные области тяжелой и легкой цепи, и конструкции подтверждают посредством секвенирования. Экспрессирующими векторами трансфицируют клетки млекопитающих с использованием липофектамина 2000 (Thermofisher Scientific), согласно инструкциям производителя. Кратко, 3,5×106 клеток PEAK культивируют в флаконах T75 в 25 мл культуральных сред, содержащих эмбриональную бычью сыворотку. Трансфицированные клетки культивируют в течение 5-6 суток при 37°C, продукцию IgG количественно оценивают посредством устройства OctetRED96. Супернатант собирают для очистки IgG на аффинной смоле FcXL (Thermofisher Scientific), согласно инструкциям производителя. Кратко, супернатанты от трансфицированных клеток инкубируют в течение ночи при 4°C с подходящим количеством смолы FcXL. После промывки смолы посредством PBS, образцы наносят на колонку Amicon Pro, и впоследствии, IgG элюируют в 50 мМ глицине pH3,5. Затем элюированную фракцию IgG подвергают диализу посредством Amicon 50 кДа против буфера гистидина NaCl pH6,0, и содержание IgG количественно оценивают по поглощению при 280 нм. Чистоту и целостность IgG подтверждают посредством биоанализатора от производителя Agilent (Agilent Technologies, Santa Clara, Calif., USA).
Пример 6 Характеризация антител против CEACAM5
a) Связывание антител против CEACAM5 с клетками, трансфицированными различными членами семейства CEACAM
[0337] Насколько известно авторам настоящего изобретения, специфичность моноклональных антител против CEACAM5 (mAb) можно показать посредством проточной цитометрии с использованием клеток PEAK и/или CHO, трансфицированных различными членами семейства CEACAM. Векторы, кодирующие полноразмерный вариант CEACAM человека 1, 3, 4, 5, 6, 7, 8, 18, 19, 20 и 21 и 20, используют для экспрессии этих белков на поверхности клеток PEAK и/или CHO, как описано в примере 2. Нетрансфицированные клетки PEAK и/или CHO используют в качестве отрицательного контроля. Клетки собирают, подсчитывают, проверяют жизнеспособность и ресуспендируют при 3×106 клеток/мл в буфере для FACS (PBS 2% BSA, 0,1% NaN3). 100 мкл суспензии клеток распределяют в 96-луночные планшеты с V-образным дном (3×105 клеток/лунку). Супернатант удаляют посредством центрифугирования в течение 3 минут при 4°C, 1300 об/мин, и клетки инкубируют в течение 15 минут при 4°C с увеличивающимися концентрациями антитела по изобретению. Антитела разводят в буфере для FACS, и диапазон концентраций составляет 30 пМ - 500 нМ. Клетки промывают дважды холодным буфером для FACS и повторно инкубируют в течение дополнительных 15 минут при 4°C с конъюгированным с PE (R-фикоэритрином) вторичным антителом мыши против Fc IgG человека (SouthernBiotech, предварительно разведенным 1:100 в буфере для FACS). Клетки промывают дважды холодным буфером для FACS и ресуспендируют в 300 мкл буфера для FACS с разведенным 1:1500 TOPRO-3 (Invitrogen). Флуоресценцию измеряют с использованием FACSCaliburTM (BD Biosciences). Кривые ответа связывания в зависимости от дозы подбирают с использованием программного обеспечения GraphPad Prism7. Таким же способом, можно характеризовать CEACAM1, CEACAM6 и другие CEACAM. Кратко, очищенные Mab инкубируют с клетками, экспрессирующими один из белков семейства CEACAM, при конечной концентрации 10 мкг/мл в течение 30 минут. После двух промывок, связанные антитела детектируют с использованием конъюгированного с Cy-5 вторичного антитела против Fc человека (BD biosciences).
[0338] Антитело по изобретению обнаруживают как не имеющее связывания с указанным CEACAM, если связанное антитело не детектируют посредством конъюгированного с PE вторичного антитела против Fc IgG человека.
b) Перекрестная реакционная способность антител против CEACAM5 по отношению к CEACAM5 яванского макака
[0339] Насколько известно авторам настоящего изобретения, перекрестную реакционную способность моноклональных антител против CEACAM5 по настоящему изобретению по отношению к CEACAM5 яванского макака можно тестировать посредством проточной цитометрии с использованием клеток PEAK CHO, трансфицированных вектором, экспрессирующим полноразмерный CEACAM5 яванского макака. Проточная цитометрия позволяет детекцию того, связывается ли указанное антитело с клетками PEAK CHO, экспрессирующими CEACAM5 яванского макака, или, если указанное антитело не связывается с клетками PEAK CHO, соответственно, отсутствия связывания с указанным CEACAM.
Пример 7 Экспрессия и очистка биспецифических антител, несущих легкую цепь лямбда и каппа
[0340] Одновременная экспрессия одной тяжелой цепи и двух легких цепей в одной и той же клетке может приводить к сборке трех различных антител. Одновременную экспрессию можно достигать различными способами, такими как трансфекция множеством векторов, экспрессирующих одну из цепей для совместной экспрессии, или с использованием векторов, управляющих экспрессией множества генов. Векторы, кодирующие различные антитела против CEACAM5, совместно трансфицируют с другим вектором, экспрессирующим тяжелую и легкую цепь антитела против CD47 Ka3 (SEQ ID NO:5 и 11), антитела против CD47, несущего такую же общую тяжелую цепь и описанного в US 2014/0303354. Альтернативно, две легкие цепи клонируют в вектор pNovi κHλ, полученный ранее, чтобы обеспечивать совместную экспрессию одной тяжелой цепи, одной легкой цепи каппа и одной легкой цепи лямбда, как описано в US 2012/0184716 и WO 2012/023053, полное содержание каждой из которых, таким образом, приведено в качестве ссылки. Экспрессией трех генов управляют посредством промоторов цитомегаловируса человека (hCMV), и вектор также содержит ген глутаминсинтетазы (GS), позволяющий отбор и получение стабильных линий клеток. Гены общей VH и VL IgG против CEACAM5 и IgG против CD47 клонируют в вектор pNovi κHλ, для временной экспрессии в клетках млекопитающих. Клетки Peak культивируют в подходящем флаконе с использованием подходящего количества клеток и объема культуральной среды (содержащей эмбриональную бычью сыворотку). Плазмидной ДНК трансфицируют клетки с использованием липофектамина 2000) согласно инструкциям производителя. Концентрацию антитела в супернатанте трансфицированных клеток измеряют в ходе продукции с использованием OctetRED96. В соответствии с концентрацией антитела, супернатанты собирают через 5-7 суток после трансфекции и осветляют посредством центрифугирования при 1300 g в течение 10 мин. Способ очистки состоит из трех аффинных стадий. Сначала, аффинный матрикс FcXL (Thermofisher Scientific) промывают с использованием PBS и затем добавляют в осветленный супернатант. После инкубации в течение ночи при +4°C, супернатанты центрифугируют при 2000 g в течение 10 мин, проскок сохраняют, и смолу промывают дважды с использованием PBS. Затем, смолу переносят в колонки Amicon Pro, и раствор, содержащий 50 мМ глицин при pH 3,0, используют для элюции. Несколько фракций элюции получают, пулируют и обессоливают против PBS с использованием модулей для фильтрации ультрацентрифугированием 50 кДа Amicon™ (Merck KGaA, Darmstadt, Germany). Элюированный продукт, содержащий тотальные IgG человека из супернатанта, количественно оценивают с использованием спектрофотометра Nanodrop (NanoDrop Technologies, Wilmington, Del.) и инкубируют в течение 15 мин при RT и 20 об/мин с подходящим объемом аффинного матрикса для отбора цепей каппа, Kappa select (GE Healthcare). Стадии инкубации, выделения смолы, элюции и обессоливания проводят, как описано ранее. Последнюю стадию аффинной очистки проводят с использованием аффинного матрикса для отбора Fab лямбда, lambda Fab select (GE Healthcare), с использованием такого же способа, как и для двух предшествующих стадий очистки. Конечный продукт количественно оценивают с использованием Nanodrop. Очищенные биспецифические антитела анализируют посредством электрофореза в денатурирующих и восстанавливающих условиях. Биоанализатор Agilent 2100 используют с набором Protein 80, как описано производителем (Agilent Technologies, Santa Clara, Calif., USA). 4 мкл очищенных образцов смешивают с буфером для образцов, дополненных дитиотреитолом (DTT; Sigma Aldrich, St. Louis, Mo.). Образцы нагревают при 95°C в течение 5 мин и затем наносят на чип.Все образцы тестируют по контаминации эндотоксином с использованием теста с лизатом амебоцитов мечехвоста (LAL; Charles River Laboratories, Wilmington, Mass.).
Пример 8: Характеризация моновалентных и биспецифических антител
a) Биспецифические антитела с двойным нацеливанием связываются с двумя различными антигенами на поверхности одной и той же клетки.
[0341] Насколько известно авторам настоящего изобретения, одновременное связывание двух плеч антитела с двумя антигенами на поверхности клетки (названное совместным привлечением) может приводить к аддитивному или синергическому увеличению аффинности благодаря механизму авидности. Следовательно, совместное привлечение обеспечивает высокую избирательность по отношению к клеткам, экспрессирующим оба антигена, по сравнению с клетками, экспрессирующими только один отдельный антиген. Кроме того, аффинность двух плеч биспецифического антитела для их соответствующих мишеней можно устанавливать таким образом, чтобы принципиально управлять связыванием с клетками-мишенями посредством одного из плеч антитела. Например, антитело κλ с двойным нацеливанием, состоящее из одного плеча, связывающегося с высокой аффинностью с CEACAM5 или с CEACAM5 и CEACAM6, и второго плеча, связывающегося с более низкой аффинностью с CD47 - однако, достаточной для ингибирования CD47/SIRPα при совместном привлечении CEACAM5 или CEACAM5 и CEACAM6 с CD47, должно позволять предпочтительное ингибирование CD47 в клетках злокачественной опухоли, по сравнению с нормальными клетками.
b) Измерение аффинности для CD47 человека
[0342] Насколько известно авторам настоящего изобретения, аффинность связывания антител по изобретению с CD47 человека можно оценивать посредством технологии поверхностного плазмонного резонанса с использованием устройства Biacore T200. Биотинилированный растворимый рекомбинантный белок CD47 человека можно связывать с покрытым стрептавидином сенсорным чипом (сенсорным чипом SA серий S). Затем серии концентраций тестируемого антитела можно инъецировать над поверхностью, с регенерацией поверхности между каждыми инъекциями.
[0343] Такие измерения проводили с использованием биспецифического антитела κλ CD19xCD47. Аффинность связывания, измеренная при повторяющихся определениях, составляла между 400 и 500 нМ. Связывающее CD47 плечо этого антитела является таким же, как связывающее CD47 плечо биспецифических антител CEAxCD47 по этому изобретению. Насколько известно авторам настоящего изобретения, в таких же экспериментах, проводимых с использованием биспецифических антител CEAxCD47 по изобретению, можно получать сходные результаты в пределах стандартного отклонения для таких экспериментов.
c) Активность блокирования SIRPα моновалентных и биспецифических антител для демонстрации совместного привлечения CEACAM5 и CD47 на поверхности клеток опухолей - мишеней
[0344] Насколько известно авторам настоящего изобретения, можно проводить другие серии экспериментов, которые могут обеспечивать доказательство совместного привлечения TAA (подобного CEACAM5) и CD47 на поверхности клетки-мишени, представляющие собой эксперименты, показывающие, что нейтрализация взаимодействия CD47-SIRPα посредством антител κλ CD47xCEACAM5, является зависимой от CEACAM5. В таких экспериментах, активность антител κλ CD47xCEACAM5 и соответствующих моновалентных антител можно тестировать в анализе ингибирования CD47-SIRPα. На фигуре 6 показаны результаты с использованием биспецифического антитела TAAxCD47 (TAA не представляет собой CEA), содержащего такое же связывающее CD47 плечо, что и биспецифические антитела по этому изобретению, по сравнению с соответствующим моновалентным антителом против CD47.
d) Активность блокирования SIRPα антител против CD47
[0345] Дизайн эксперимента для измерения данных активности ингибирования SIRPα, показанных для биспецифических антител по этому изобретению (результаты см. в таблице 2):
[0346] Детекцию связанного SIRPα в анализе на основе клеток, мониторирующем взаимодействие растворимого SIRPα с CD47 человека, экспрессированным на поверхности MKN45, используют для детекции активности блокирования. Эксперименты по зависимости ответа от дозы с использованием биспецифических антител по изобретению позволяют определение значения IC50.
[0347] Клетки злокачественной опухоли MKN45, экспрессирующие как CD47, так и CEACAM5, окрашивают с использованием CFSE фиолетового, чтобы позволить системе визуализации (CX5) детектировать клетки. Кратко, 3000 окрашенных клеток MKN45 на лунку рассевают в 384-луночный оптический планшет (Costar) и инкубируют в течение 50 минут с увеличенными концентрациями биспецифических антител по изобретению (1,9 пМ - 333 нМ, в четырех повторах). Затем, фиксированную концентрацию SIRPα—Fc мыши, предварительно смешанного со связанным с AF647 антителом против IgG-Fc мыши (Jackson Immunoresearch, разведенного 1:2000) добавляют при конечной концентрации 50 нг/мл. После инкубации, информацию для планшетов 3H30 получают с использованием системы для визуализации (CX5, Thermofisher), и сигналы флуоресценции, испускаемые детектированным связанным SIRPα, регистрируют посредством программного обеспечения, предназначенного для системы визуализации. Сигналы флуоресценции наносят на график, в соответствии с тестируемым диапазоном дозирования, и IC50 рассчитывают посредством программного обеспечения (Prism, Graphpad).
[0348] В таблице 2 показана активность нескольких биспецифических антител CEAxCD47 при ингибировании связывания CD47/SIRPα, имеющая диапазон IC50 от 0,22 нМ до 7 нМ.
e) Группировка эпитопов антител против CEACAM5 посредством конкуренции с эталонными антителами
[0349] Группировка эпитопов представляет собой конкурентный иммуноанализ, используемый для характеризации связывания антител по изобретению или например, связывания родственных антител против CEA (белка-мишени) из первой связывающей части. Получают конкурентный профиль блокирования связывания антитела с белком-мишенью, против антител, которые также связываются с этим белком-мишенью и для которых связываемый эпитоп уже установлен/опубликован. Конкуренция с одним из этих эталонных антител показывает, что антитело имеет такой же или близко локализованный эпитоп, и они «группируются» вместе. Способность mAb против CEACAM5, которые являются частью биспецифических антител по настоящему изобретению, к конкуренции с эталонными антителами против CEACAM5 тестируют посредством ELISA с рекомбинантным CEACAM5 человека, с использованием следующих эталонных антител, несущих область Fc мыши: SM3E, последовательности mAb, происходящие из SM3E, описанные в Патенте US20050147614A1, mAb, продуцированное с использованием стандартных способов; MEDI, mAb, происходящее из MEDI-565, описанное в Патенте WO2016036678A1; SAR, mAb, происходящее из Mab2_VLg5VHg2, описанное в Патенте EP3199552A1; CH1A1A, mAb, происходящее из CH1A1A-2F1, описанное в Патенте US20120251529 и в Klein et al in Oncoimmunology, 2017 Jan 11;6(3); гуманизированное mAb T84.66, происходящее из варианта 1, описанного в Патенте WO2017055389; mAb LAB, происходящее из hMN14, описанного в Патенте US 2002/0165360 A1. SM3E связывается, например, с более близкой к N-концу, отдаленной от клеточной мембраны, частью CEA, MEDI - со средней частью, и CH1A1A связывается близко с мембраной.
[0350] Биотинилированным CEACAM5 человека покрывают, при 0,5 мкг/мл, покрытый стрептавидином 96-луночный планшет, и инкубируют с 10 мкг/мл эталонных mAb или не имеющего отношения к делу mAb, несущих область Fc мыши, в течение 1 часа. mAb против CEACAM5 (как двухвалентные моноклональные антитела против CEA, а не как соответствующее биспецифические антитела CEAxCD47) добавляют при 0,2 мкг/мл на 1 час при комнатной температуре. Планшет промывают, и связанные mAb против CEACAM5 детектируют с использованием антитела против IgG человека(Fc)-HRP (Jackson ImmunoResearch). После промывки, планшет проявляют с использованием реагента Amplex красного. Сигнал флуоресценции измеряют в считывателе для планшетов Synergy HT (Biotek).
[0351] Результаты показаны в таблице 2. Группа 1 означает, что соответствующее антитело конкурирует с SM3E за связывание с CEACAM5. Группа 2 означает, что соответствующее антитело не конкурирует ни с каким из являющихся инструментами антител, упомянутых выше. Эксперименты по конкуренции для всех биспецифических антител CEAxCD47, перечисленных в таблице 2, проводили с использованием соответствующих двухвалентных моноклональных антител против CEA. В случае, когда связывание такого моноклонального антитела с CEACAM5 уменьшалось посредством соответствующего являющегося инструментом антитела на 80% или более, заключали, что биспецифическое антитело CEAxCD47 классифицировано как конкурирующее за связывание с являющимся инструментом антителом. Антитело CEAxCD47 идентифицируют как не конкурирующее с являющимся инструментом антителом, в случае, когда связывание соответствующего двухвалентного mAb против CEA с CEACAM5 уменьшается на 20% или менее, если сравнивают результаты с добавлением и без добавления являющегося инструментом антитела.
Группа 1: K2AC13, K2AC18, K2AC23, K2AC27, K2AC29
Группа 2: K2AC10, K2AC25, K2AC28, K2AC26
[0352] Результаты для характеризации групп, значения EC50 для связывания с CEA, активность ингибирования SIRPα и EC50, так же как максимальный показатель фагоцитоза для биспецифических антител по изобретению показаны в таблицах 2, 3 и 4
Таблица 2: Характеристики in vitro биспецифических антител CEAxCD47
# с использованием клеток злокачественной опухоли MKN45 CEA+
Таблица 3: Функциональная активность in vitro биспецифических антител CEAxCD47*
Таблица 4: EC50 и максимальный показатель фагоцитоза для двух биспецифических антител CD47xCEA в присутствии или в отсутствие 1 мг/мл hIgG1 с использованием клеток MKN45.
max.= максимум; максимальный показатель фагоцитоза, оцененный при 10 мкг/мл; # с использованием клеток злокачественной опухоли MKN45 CEA+
Таблица 5: EC50 для связывания с CEACAM5 человека или CEACAM6 человека посредством ELISA с использованием рекомбинантных белков.
f) Связывание антител против CEA с CEACAM5 человека и CEACAM6 человека
[0353] Биотинилированные рекомбинантные белки CEACAM5 человека или CEACAM6 связывают при 0,5 мкг/мл с покрытым стрептавидином 96-луночныйм микропланшетом. Планшет промывают и моноклональные двухвалентные антитела против CEA по настоящему изобретению добавляют в широком диапазоне концентраций (например, от 5×10-4 до 1 мкг/мл) , и инкубируют в течение 1 час. Планшет промывают и связанные антитела детектируют с использованием антитела против IgG человека(Fc)-HRP (Jackson ImmunoResearch). После промывки, планшет проявляют с использованием реагента Amplex Red (Molecular Probes). Сигнал флуоресценции измеряют в считывателе для планшетов Synergy HT (Biotek).
[0354] Результаты, полученные для моноклонального антитела AC39, содержатся в таблице 5; для этого антитела показано уравновешенное связывание с CEACAM5 и CEACAM6, что означает, что EC50 для связывания с CEACAM5 и CEACAM6 являются сходными (диапазон соотношения EC50 для связывания с CEACAM5 и связывания с CEACAM6 уравновешенных антител от 0,33 до 3). Антитела с соотношением вне этого диапазона рассматривают как неуравновешенные.
Пример 9: ADCC и ADCP, опосредованные биспецифическими антителами
a) ADCP и ADCC, опосредованные биспецифическими антителами TAAxCD47, являются зависимыми от TAA
[0355] Способность антител κλ с двойным нацеливанием TAAxCD47 к совместному привлечению CD47 и TAA приводит к значительному увеличению аффинности связывания с положительными по TAA клетками по сравнению с отрицательными по TAA клетками и зависимой от TAA нейтрализации взаимодействия CD47-SIRPα. Это, в свою очередь, можно переводить в эффективное и избирательное уничтожение клеток злокачественных опухолей, опосредованное антитела κλ CEAxCD47.
[0356] Результаты, как показано по экспериментам ADCP (анализ на основе проточной цитометрии), показанным на фигуре 3A, демонстрируют более высокую ADCP для биспецифического антитела TAAxCD47, по сравнению с соответствующим моновалентным антителом против TAA, так же как моновалентным антителом против CD47. На фигуре 4 показана более высокая ADCC (анализ на основе Cr51) четырех биспецифических антител TAAxCD47 (TAA представляет собой мезотелин MSLN), по сравнению с высокоаффинным моноклональным антителом против TAA аматуксимабом (TAA представляет собой MSLN) (используют клетки опухоли рака легкого NCI-H226, несущие MSLN).
b) анализ высвобождения Cr51+, измеренного с использованием антител TAAxCD47
[0357] Здоровые PBMC активировали в течение ночи при 37°C с использованием RPMI/10% инактивированной нагреванием FCS, дополненной 10 нг/мл рекомбинантного hIL-2. На следующие сутки, клетки-мишени (т.е., клетки злокачественных опухолей экспрессирующие TAA) инкубировали с 100 мкКи Cr51 (Perkin Elmer, 37°C, 1 час). После промывки, клетки подвергали опсонизации с использованием тестируемых антител (30 мин, 37°C). Нагруженные Cr51 клетки злокачественных опухолей затем смешивали с клетками PBMC для получения конечного соотношения 80:1 или 50:1 между эффекторными клетками (PBMC) и клетками-мишенями (экспрессирующими TAA клетками). Смесь клеток инкубировали в течение 4 час при 37°C перед центрифугированием в течение 10 мин при 1500 об/мин. Супернатант переносили в планшет LumaPlate (покрытый сцинтиллятором) и подсчитывали в γ-счетчике. Отрицательный контроль (спонтанное высвобождение Cr51), состоял из нагруженных Cr51 клеток-мишеней, инкубированных со средой в отсутствие эффекторных клеток. Контроль тотального лизиса состоял из нагруженных Cr51 клеток-мишеней, инкубированных с 5 мкл раствора для лизиса клеток (тритон X-100). Контроль неспецифического лизиса (фон) состоял из нагруженных Cr51 клеток-мишеней, инкубированных с эффекторными клетками, без Ab. Процент ADCC рассчитывали с использованием следующей формулы: % специфической ADCC=((количество импульсов в минуту (cpm) для образца - cpm для контроля неспецифического лизиса)/(cpm для контроля тотального лизиса - cpm для отрицательного контроля)) x 100%.
[0358] На фигуре 5 показаны результаты для ADCC (анализа на основе Cr 51) в эксперименте сравнения между вариантом Fc wt IgG1 против варианта Fc, кроме того, имеющего мутацию DEA, биспецифического антитела CD47xTAA (TAA не представляет собой CEA), несущего такое же плечо для CD47, что и антитела CEAxCD47 по изобретению. Также, показаны результаты для высокоаффинного двухвалентного mAb против TAA. За наивысшей ADCC биспецифического антитела TAAxCD47, несущего Fc IgG1 с мутациями DEA, следовало biAb CEAxCD47 с Fc IgG1 и двухвалентное mAb с Fc wt IgG1.
c) ADCC, измеренная посредством высвобождения LDH
[0359] ADCC биспецифических антител CEAxCD47 тестировали в следующем анализе:
[0360] Здоровые PBMC активировали в течение ночи при 37°C с использованием RPMI/10% инактивированной нагреванием FCS, дополненной 10 нг/мл рекомбинантного hIL-2. На следующие сутки, клетки-мишени (например, клетки злокачественной опухоли MKN45) подвергают опсонизации с использованием различных концентраций тестируемых антител. PBMC и опсонизированные клетки-мишени совместно инкубируют при соотношении эффектор/мишень 50/1 в круглодонных планшетах в течение 6 часов при 37°C в инкубаторе для культивирования клеток. После этой инкубации, супернатанты переносят в оптический плоскодонный планшет, и высвобождение LDH количественно оценивают с использованием коммерческого набора от Roche посредством измерения OD с использованием считывателя для микропланшетов. % специфического лизиса рассчитывают с использованием следующей формулы:
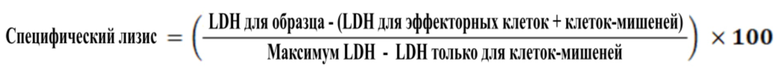
[0361] На фигуре 13 показаны результаты экспериментов сравнения между биспецифическими антителами по изобретению и их подвергнутыми гликоинженерии формами, и антителом 5F9. На фигуре 14 показаны результаты экспериментов сравнения между биспецифическими антителами по изобретению и их подвергнутыми гликоинженерии формами, и антителом 5F9, в присутствии 1 мг/мл иммуноглобулина (IgG) человека.
d) Анализ ADCP
[0362] Используют два способа. В способе на основе FACS, определяют процент фагоцитоза (представляющий собой процент макрофагов, поглотивших по меньшей мере одну клетку опухоли). На фигуре 3A показаны результаты, полученные с использованием этого анализа на основе FACS для антитела TAAxCD47, несущего связывающее CD47 плечо, также используемое в антителах CEAxCD47. С использованием способа на основе визуализации, в котором используют платформу для одновременного многопараметрического скрининга CellInsight CX5, определяют показатель фагоцитоза, определенный как среднее количество клеток-мишеней, поглощенных 100 макрофагами. На фигуре 3B показаны результаты, полученные с использованием биспецифического антитела TAAxCD47 (TAA не представляет собой CEA), несущего связывающее CD47 плечо из антитела CEAxCD47. На фигурах 12, 15, 16, 17, 18, 20B и 21B показаны результаты, полученные с использованием биспецифических антител CEAxCD47 по изобретению. На фигуре 15 показаны результаты экспериментов сравнения между биспецифическими антителами по изобретению и их подвергнутыми гликоинженерии формами, и антителом против CD47 5F9. На фигуре 16 показаны результаты экспериментов сравнения между биспецифическими антителами по изобретению и их подвергнутыми гликоинженерии формами, и антителом 5F9 в присутствии 1 мг/мл иммуноглобулина (IgG) человека, как обычно присутствует у пациентов. На фигуре 17 показаны результаты экспериментов сравнения между биспецифическими антителами по изобретению в присутствии или в отсутствие 1 мг/мл иммуноглобулина человека (huIgG, 1 мг/мл или даже выше, присутствует у пациентов). На фигуре 18 показаны кривые концентрации/показателей фагоцитоза для K2AC22 в присутствии или в отсутствие 30 нМ CEA-TCB1 или 300 нМ CEA-TCB.
e) Анализы фагоцитоза: 1. Анализ визуализации на основе платформы для одновременного многопараметрического скрининга CellInsight CX5 и 2. Анализ на основе проточной цитометрии
[0363] Получение макрофагов: мононуклеарные клетки периферической крови (PBMC) человека выделяют из лейкоцитарных пленок посредством градиента плотности фиколла. Макрофаги получают посредством культивирования PBMC в течение 7 суток в полной среде (RPMI 1640, 10% инактивированной нагреванием эмбриональной телячьей сыворотки [Invitrogen]), 2 мМ L-глутамин, 1 мМ пируват натрия, 10 мМ буфер HEPES, 25 мг/мл гентамицина (все из Sigma-Aldrich) и 50 мМ 2-меркаптоэтанол (Thermo Fisher Scientific) в присутствии 20 нг/мл макрофагального колониестимулирующего фактора (M-CSF) человека (PeproTech). Неадгерентные клетки впоследствии удаляют в фазе дифференцировки (сутки+1) посредством замены культуральной среды, и адгерентные клетки, представляющие собой макрофаги, открепляют с использованием буфера для диссоциации клеток (Sigma-Aldrich) и промывают в полной среде на сутки использования (сутки 8 или сутки 9) для эксперимента ADCP на основе цитометрии. Для ADCP на основе визуализации клеток, макрофаги открепляют на сутки 6 с использованием буфера для диссоциации клеток и рассевают при 30000 на лунку в 96-луночный оптический планшет (costar).
1. Анализ на основе CellInsight™
[0364] Макрофаги (окрашенные кальцеином красно-оранжевым), адгерентные к лункам микропланшета, совместно инкубируют с меченными кальцеином AM клетками опухолей - мишенями при соотношении эффектор:клетки-мишени 1:3 в течение 2,5 часов при 37 градусов C в присутствии различных концентраций подлежащего тестированию антитела. В конце периода инкубации, супернатанты заменяют на полную культуральную среду, и микропланшеты подвергают визуализации с использованием платформы для одновременного многопараметрического скрининга CellInsight™ CX5. 1500 макрофагов получают и анализируют на лунку. Фагоцитоз доказывают по двойным положительным событиям (макрофаг+клетка опухоли-мишень), и показатели фагоцитоза рассчитывают посредством программного обеспечения от производителя CellInsightTM.
[0365] Все результаты на фигурах 12, 15, 16, 17, 18, 20B и 21B, так же как значения EC50 и макс. показателя фагоцитоза, показанные в таблицах 3 и 4, получены с использованием клеток MKN-45, экспрессирующих CEA, и с использованием соотношения эффекторных клеток и мишеней/клеток опухоли 1:3. Данные на фигуре 3B получены с использованием клеток NCI-N87, несущих TAA (не являющийся CEA) и с использованием соотношения эффекторов и мишеней/клеток опухоли 1:1. Чем больше клеток опухолей предоставляют на макрофаг, тем выше ожидаемый показатель фагоцитоза, это, возможно, является основной причиной для в общем более низкого показателя фагоцитоза, а также фонового сигнала, показанных на фигуре 3 B для биспецифического антитела TAAxCD47 (TAA не представляет собой CEA), по сравнению с другими фигурами, показывающими результат для биспецифических антител по изобретению.
[0366] Все значения, диапазоны и т.п.для ADCP (фагоцитоза) по настоящему изобретению основаны на анализе на основе визуализации, если иное и явно не указано (данные на фигуре 3A получены с использованием анализа на основе проточной цитометрии).
2. Анализ ADCP на основе проточной цитометрии
[0367] Насколько известно авторам настоящего изобретения, ADCP можно также измерять способом, как описано следующим образом: макрофаги совместно инкубируют с меченными CSFE клетками опухолей-мишенями (например, клетками опухолей MKN-45, LS174T или HPAC) при соотношении эффектор:клетки-мишени например, 3:1, в течение 2,5 часов при 37 градусов C в присутствии различных концентраций подлежащего тестированию антитела. В конце периода инкубации, биотинилированное антитело против CD14 человека и Strep-Cy5 добавляют для мечения макрофагов. Затем клетки промывают и подвергают анализу проточной цитометрии. Фагоцитоз доказывают по двойным положительным событиям CD14+ и CFSE+. Процент фагоцитоза представляют как соотношение между двойными положительными событиями CD14+/CSFE+ и общим количеством клеток-мишеней, умноженное на 100. Данные на фигуре 3A получают с использованием клеток HPAC, несущих TAA (не являющийся CEA) и с использованием соотношения эффектора и мишеней/клеток опухолей 1:1. Использовали анализ на основе проточной цитометрии. Данные на фигуре 3B получены с использованием клеток NCI-N87, несущих TAA (не являющийся CEA) и с использованием соотношения эффектора и мишеней/клеток опухолей 1:1. Использовали анализ на основе визуализации.
Пример 10: Связывание CEAxCD47 и CEAxCD3 с клетками MNK-45; конкуренция за связывание с CEAxCD3
a) Связывание биспецифического антитела CD47xCEACAM5 тестируют например, на экспрессирующих CEA клетках аденокарциномы желудка человека (MKN-45, DSMZ ACC 409).
[0368] Клетки собирают, подсчитывают, проверяют жизнеспособность и ресуспендируют при 3×106 клеток/мл в буфере для FACS (PBS 2% BSA, 0,1% NaN3). 100 мкл суспензии клеток распределяют в 96-луночные планшеты с V-образным дном (3×105 клеток/лунку). Супернатант удаляют посредством центрифугирования в течение 3 минут при 4°C, 1300 об/мин. Затем увеличивающиеся концентрации антитела по изобретению добавляют в лунки и инкубируют в течение 15 минут при 4°C. Клетки промывают дважды холодным буфером для FACS и повторно инкубируют в течение дополнительных 15 минут при 4°C с конъюгированным с PE (R-фикоэритрином) вторичным антителом мыши против Fc IgG человека (SouthernBiotech, предварительно разведенным 1:100 в буфере для FACS). Клетки промывают дважды холодным буфером для FACS и ресуспендируют в 300 мкл буфера для FACS с разведенным 1:15000 SytoxBlue (Life Technologies). Флуоресценцию измеряют с использованием Cytoflex (Millipore). Кривые связывания и значения EC50 получают и рассчитывают с использованием программного обеспечения GraphPad Prism7. Таким же способом можно тестировать связывание MAB CEA или MAB CEA1 с клетками MKN-45. На фигуре 11 показаны кривые связывания нескольких биспецифических антител CEAxCD47 с клетками MKN-45.
b) Сдвиг кривой связывания антитела CEAxCD47 с положительной по CEA линии клеток опухоли (MKN-45) посредством добавления T-клеточного биспецифического антитела CEAxCD3.
[0369] Насколько известно авторам настоящего изобретения для экспериментов конкуренции биспецифического антитела CD47xCEACAM5 по изобретению и T-клеточных биспецифических антител CEAxCD3, подобных CEA-TCB или CEA-TCB1, связывание CEACAM5xCD47 с клетками MKN-45 можно определять, как описано выше, но в присутствии и в отсутствие добавления T-клеточного биспецифического антитела CEAxCD3, для исследования, является ли T-клеточное биспецифическое антитело CEAxCD3, в качестве партнера для комбинации для биспецифических антител CEAxCD47 по этому изобретению, конкурентным за связывание с CEA или нет.
Пример 11: Получение и очистка фукозилированных и афукозилированных биспецифических антител K2AC5 и K2AC22
[0370] Получение фукозилированных и афукозилированных биспецифических антител K2AC5 и K2AC22:
[0371] Пул CHO (один для K2AC5 и один для K2AC22) инокулируют при концентрации жизнеспособных клеток 0,3×106 клеток/мл в устройство Эрленмеера от Thomson с рабочим объемом 700 мл или 100 мл для получения фукозилированных и афукозилированных антител, соответственно. Со всеми пулами работают в течение 15 суток в режиме периодического культивирования с подпиткой с использованием CDACF среды CDCHO и в адаптированном режиме подпитки. Для получения афукозилированных антител, болюс 200 мкМ ингибитора фукозы (1,3,4-три-O-ацетил-2-дезокси-2-фтор-L-фукозы) добавляют на сутки 0, 5, 8 и 11 в ходе периодического процесса с подпиткой, на основании способа афукозилирования, описанного в Rillahan et al. Nature Chem. Biol. 2012 Jul;8(7):661-8 и основанного на EP2282773. Сбор супернатантов пулов K2AC5 и K2AC22, содержащих фукозилированные или афукозилированные антитела, проводят через 15 суток периодического культивирования с подпиткой. Сбор супернатантов пулов CHO осветляют с использованием системы для сбора клеток Sartoclear Dynamics® Lab V Cell Harvesting Sartorius (см. инструкции поставщика).
Очистка фукозилированных и афукозилированных биспецифических антител K2AC5 и K2AC22
[0372] Очистка фукозилированных и афукозилированных биспецифических антител K2AC5 и K2AC22 представляет собой способ очистки с тремя аффинными стадиями. Перед началом очистки, концентрацию антитела в супернатанте пулов K2AC5 и K2AC 22 измеряют с использованием OctetRED96 для использования колонок с подходящим объемом аффинного матрикса. Каждый осветленный супернатант пула CHO, содержащий фукозилированные или афукозилированные биспецифические антитела, наносят на колонку MabSelect SuRe (MSS) (GE Healthcare) без предшествующего доведения, для удаления основной части контаминантов культуры клеток. Затем элюат MSS обрабатывают посредством поддержания при низком pH для инактивации вирусов, и нейтрализуют при pH 6 с использованием Трис 1M pH9. Затем элюат MSS наносят на колонку LambdaFabSelect (LFS) (GE Healthcare) для удаления моноспецифических κ (моно-κ). Затем pH элюата LFS доводят до pH 6. LFS наносят на колонку Capto L (CL) (GE Healthcare) для удаления моноспецифических λ (моно-λ). pH элюата CL доводят перед хранением. Затем конечный материал концентрируют и подвергают диафильтрации в буфере для конечного состава, его концентрацию доводят с использованием Nanodrop. Фукозилированные и афукозилированные биспецифические антитела K2AC5 и K2AC22 аликвотируют и хранят при -80°C до доставки. Очищенные биспецифические антитела анализируют по размеру посредством электрофореза в денатурирующих и восстанавливающих условиях с помощью биоанализатора Agilent 2100 с использованием набора Protein 80, как описано производителем (Agilent Technologies, Santa Clara, Calif., USA). Уровень агрегации оценивают посредством эксклюзионной хроматографии (SEC-UPLC) с использованием системы ACQUITY UPLC H-Class Bio (Waters). Анализ вариантов заряда очищенных биспецифических антител осуществляют способом изоэлектрического фокусирования (IEF) с использованием системы для электрофореза Multiphor II (GE Healthcare). Относительное распределение N-связанных комплексных двухантенных гликоформ фукозилированных и афукозилированных антител K2AC5 и K2AC22 определяют с использованием способа высокопроизводительных чипов-CE в LabChip GXII Touch (Perkin Elmer). Все антитела тестируют по контаминации эндотоксином с использованием теста с лизатом амебоцитов мечехвоста (LAL; Charles River Laboratories, Wilmington, Mass). Для подвергнутого гликоинженерии K2AC5 показано 79,68% афукозилирования, и для подвергнутого гликоинженерии K2AC22 показано 89,13% афукозилирования.
[0373] Эти афукозилированные биспецифические антитела CEAxCD47 использовали для получения результатов, показанных на фигурах 13, 14, 15 и 16.
Пример 12: Экспрессия и очистка в FUT8(-) линии клеток
[0374] Альтернативно и, насколько известно авторам настоящего изобретения, афукозилированные биспецифические антитела по изобретению можно получать также в соответствии со следующим способом:
[0375] Материалы и способы находятся в соответствии с Naoko Yamane-Ohnuki et al., Biotech. Bioeng.; 87 (2004) 614-622.
Выделение кДНК FUT8 китайского хомяка
[0376] Тотальную РНК выделяют из клеток CHO/DG44 с использованием набора в минимасштабе RNeasy® Mini (Qiagen, Hilden, Germany) и подвергают обратной транскрипции с олиго-dT с использованием системы для синтеза первой цепи Superscript, для обратной транскрипции-полимеразной цепной реакции (RT-ПЦР) (Invitrogen, Carlsbad, CA). кДНК FUT8 китайского хомяка амплифицируют с одноцепочечных кДНК клеток CHO/DG44 посредством ПЦР с использованием праймеров 5V-GTCTGAAGCATTATGTGTTGAAGC-3V (SEQ ID NO:14) и 5V-GTGAGTACATTCATTGTACTGTG-3V (SEQ ID NO:15), сконструированных по кДНК FUT8 мыши (Hayashi, 2000; DNA Seq 11:91-96).
Конструкция для нацеливания на локус FUT8
[0377] Направленное повреждение гена FUT8 в клетках CHO/DG44 проводят с использованием двух векторов замещения, pKOFUT8Neo и pKOFUT8Puro. Фрагмент 9,0 т.п.о. гена FUT8, включающий первый кодирующий экзон, выделяют посредством скрининга E-геномной библиотеки клеток CHO-K1 (Stratagene, La Jolla, CA) с использованием кДНК FUT8 китайского хомяка в качестве зонда для получения нацеливающих конструкций. Фрагмент 234 п.о., содержащий участок инициации трансляции, заменяют кассетой гена устойчивости к неомицину (Neor) или кассетой гена устойчивости к пуромицину (Puror) из плазмиды pKOSelectNeo или pKOSelectPuro (Lexicon, TX), соответственно, фланкированных участками loxP. Кассету гена дифтерийного токсина (DT) из плазмиды pKOSelectDT (Lexicon) вставляют в гомологичную область 5V. Полученные нацеливающие конструкции, pKOFUT8Neo и pKOFUT8Puro, включают 1,5-т.п.о. гомологичную последовательность 5V и 5,3-т.п.о. гомологичную последовательность 3V. Перед трансфекцией, нацеливающие конструкции линеаризуют в уникальном участке SalI.
Трансфекция и скрининг продуктов гомологичной рекомбинации
[0378] Субконфлюэнтные клетки CHO/DG44 (1,6 106) подвергают электропорации с использованием 4 аг линеаризованной pKOFUT8Neo при 350 В и 250 аФ с использованием Bio-Rad GenePulser® II. После электропорации, трансфектанты отбирают с использованием 600 аг/мл G418 (Nacalai Tesque, Kyoto, Japan). Геномную ПЦР проводят в 96-луночных планшетов посредством модифицированного способа микроэкстракции, опубликованного ранее (Ramirez-Solis et al., 1992; Anal Biochem 201:331- 335.) с использованием следующих праймеров:
5V-TTGTGTGACTCTTAACTCTCAGAG-3V (SEQ ID NO:16) и 5V-GAGGCCACTTGTGTAGCGCCAAGTG-3V (SEQ ID NO:17).
[0379] Продукты гомологичной рекомбинации идентифицируют посредством фрагмента 1,7 т.п.о., полученного с использованием геномной ПЦР, и подтверждают посредством анализа Саузерн-блоттинга с использованием фрагмента 221 п.о., амплифицированного с использованием следующих праймеров:
5V-GTGAGTCCATGGCTGTCACTG-3V (SEQ ID NO:218) и 5V-CCTGACTTGGCTATTCTCAG-3V (SEQ ID NO:19).
[0380] Гемизиготный клон подвергают второму циклу гомологичной рекомбинации с использованием линеаризованной pKOFUT8Puro и отбора с лекарственным средством с использованием 15 аг/мл пуромицина (Sigma-Aldrich, St. Louis, MO), как описано ранее. Идентифицированные гомозиготные носители поврежденного гена подвергают электропорации с использованием экспрессирующего Cre-рекомбиназу вектора pBS185 (Invitrogen) для удаления кассет генов устойчивости к лекарственному средству из обоих аллелей FUT8.
Продукция моноклонального антитела FUT8(-) клетками
[0381] FUT8(-) линии клеток подвергают электропорации экспрессирующим вектором, кодирующим биспецифическое антитело по изобретению, и отбору в среде с отсутствием гипоксантина и тимидина. Конфлюэнтные трансфектанты культивируют в среде Ex-Cell® 301 (JRH Biosciences, Lenexa, KS) в течение 1 недели. Антитело очищают из культуральных супернатантов с использованием MabSelect™ (Amersham Biosciences, Piscataway, NJ). Дополнительные стадии очистки могут представлять собой анионо/катионообменную хроматографию, эксклюзионную хроматографию и особенно очистку с использованием смол, избирательных для каппа, лямбда, соответственно, как описано выше.
Пример 13: Противоопухолевая активность in vivo биспецифических антител
[0382] Насколько известно авторам настоящего изобретения, противоопухолевую активность биспецифического антитела по изобретению можно оценивать в моделях ксенотрансплантатов, например, посредством следующей модели: 1 или 2×106 положительных по CEA клеток опухолей, подобных клеткам MKN-45 или LS174T, имплантируют подкожно мышам NOD/SCID. Объемы опухолей измеряют 3 раза в неделю. После достижения трансплантатом опухоли приблизительно 0,1 см3, мышей случайным образом распределяют на группы (например, 4-6 мышей на группу), и начинают лечение антителом. В этом эксперименте можно, например, сравнивать эффект биспецифического антитела по изобретению и положительных контрольных Mab, например, антитело против CD47 Mab B6H12.2 инъецируют, например, i.v. каждую неделю до конца эксперимента (d25). Антитела вводят, например, при 50-1200 мкг на мышь на инъекцию.
[0383] Комбинации биспецифического антитела по этому изобретению с биспецифическим антителом CEAxCD3 можно тестировать в подходящей модели. Модели, в которых можно тестировать комбинацию антитела по изобретению вместе с MAB CEA, MAB CEA1 или CEA-TCB CEA-TCB1, описаны, например, в Bacac et al (Clin. Cancer Res., 22(13);3286-97;2016) и их также используют, особенно для комбинаторных исследований CEACAM5xCD47 и CEA-TCB или CEA-TCB1.
Пример 14: Высвобождение цитокинов, тестированное в цельной крови и PBMC из человеческой крови здоровых доноров-людей
[0384] Насколько известно авторам настоящего изобретения, анализ высвобождения цитокинов in vitro можно проводить с использованием цельной крови (WB CRA) с минимальным разведением тестируемыми антителами (95% об./об. крови), с представлением в водной фазе. Этот формат анализа считают более близко имитирующим внешнее окружение in vivo, содержащее факторы в физиологических концентрациях, которые могут влиять на механизмы высвобождения цитокинов. Однако, этот формат считают слабо прогностическим для опосредованного T-клеткой высвобождения цитокина (например, против CD28).
[0385] Анализ можно проводить также с использованием мононуклеарных клеток периферической крови (PBMC) от здоровых доноров-людей и с использованием представления иммобилизованного mAb (твердофазного, SP) для оценки опосредованного T-клеткой высвобождения цитокина (PBMC SP CRA). Этот формат анализа имитирует перекрестное связывание и высокую плотность представления mAb, которые могут встречаться in vivo (например, кластеризацию мишени посредством взаимодействия части Fc антитела с рецепторами Fcγ на других иммуноцитах или перекрестное связывание mAb антителами против лекарственного средства). Этот формат является прогностическим для опосредованного T-клеткой высвобождения цитокина.
[0386] Отрицательный контроль, так же как специфический положительный контроль, для каждого формата анализа можно тестировать параллельно с антителом TAAxCD47, подобным биспецифическому антителу CD47xCEA. См. фигуры 7A и B.
Пример 15: Связывание антитела с эритроцитами, фагоцитоз эритроцитов, и активация и агрегация тромбоцитов
Связывание цельной крови
[0387] Насколько известно авторам настоящего изобретения, образцы цельной крови человека, собранные от здоровых доноров, в цитрате, можно смешивать с 3 мкг/мл связанных с AF488 биспецифических антител CEA x CD47 по этому изобретению, B6H12.2 или антител для контроля изотипа и окрашивающих поверхность антител (антитела против hCD45 с PE-Cy7 и антитела против hCD41a с PE, только для тромбоцитов) в течение 30 мин при 4°C. После инкубации, цельную кровь разделяют на два образца: 5 мкл разводят и промывают в PBS для анализа эритроцитов, в то время как 150 мкл инкубируют с раствором для лизиса эритроцитов и промывают для анализа тромбоцитов. Информацию для образцов получают в устройстве CytoFLEX и анализируют с использованием программного обеспечения FlowJo для определения значений MFI.
Эритрофагоцитоз
[0388] Насколько известно авторам настоящего изобретения, эритроциты (RBC) человека можно выделять из цельной крови человека посредством центрифугирования при 300xg, промывать дважды в PBS, метить с использованием CFSE (сукцинимидилового сложного эфира карбоксифлуоресцеина) и предварительно инкубировать с тестируемым антителом в течение 1 часа при 37°C перед добавлением макрофагов. Меченные RBC можно культивировать с макрофагами человека в присутствии антитела по изобретению или контроля (несвязывающего антитела IgG1) в течение одного часа при соотношении мишени к эффектору 200:1. После культивирования, клетки окрашивают с использованием антитела против CD14-APC и анализируют посредством проточной цитометрии. Фагоцитоз оценивали количественно как процент CD14+ событий (макрофагов), являющихся также CFSE+ и поглотивших, таким образом, по меньшей мере один RBC (события отбирают в синглетах). Анализ фагоцитоза и FACS выполняют, как описано в примере 9, за исключением того, что эритроциты лизировали с использованием раствора для лизиса для FACS после окрашивания макрофагов.
[0389] На фигуре 8 показано, что фагоцитоз RBC для моноклонального антитела IgG1 против CD47 B6H12.2 является намного более активным, чем для биспецифических антител IgG1 κλ TAA x CD47 (не CEAxCD47), содержащих связывающее CD47 плечо из биспецифических антител CEA x CD47 по этому изобретению. Для биспецифического антитела TAA x CD47 с Fc дикого типа не показан фагоцитоз в тестируемом диапазоне концентраций, если Fc несет ак мутации DEA (S329D и I332E и G236A), фагоцитоз детектируют, но при более высоких концентрациях, чем для антитела B6H12.2.
Активация и агрегация тромбоцитов in vitro
[0390] В стандартном эксперименте проточной цитометрии, способность биспецифических антител TAAxCD47 и CEAxCD47 индуцировать активацию тромбоцитов человека в цельной крови семи здоровых доноров-людей измеряли посредством повышающей регуляции поверхностного маркера CD62P. Кратко, 5 мкл цельной крови инкубируют с 10 мкл каждого образца (полученного в 2X) в течение 15 минут при комнатной температуре. Каждое тестируемое антитело добавляют в различных концентрациях (0, 0,02, 0,2, 2, 20 и 200 мкг/мл). Аденозиндифосфат (АДФ) и антитело против CD9 (ALB6), включенные в качестве реагентов для положительного контроля, как известно, индуцирующих активацию тромбоцитов, добавляют в концентрации 10 мкМ и 10 мкг/мл, соответственно. Затем, 10 мкл антитела против CD41a-PE и 10 мкл антитела против CD62P-APC добавляли и инкубировали в течение 15 мин в темноте при комнатной температуре. Наконец, добавляли 500 мкл CellFix (BD Biosciences, разведенного 1/10 в воде), и 200 мкл каждого образца переносили в 96-луночный планшет с U-образным дном, подходящий для анализа в CytoFLEX. Тромбоциты идентифицируют посредством положительного окрашивания по CD41a-PE. Активацию тромбоцитов оценивают посредством экспрессии маркера CD62P.
[0391] На фигуре 10 показаны результаты, полученные для крови от семи доноров-добровольцев. Обнаружено, что ни моноклональное антитело против TAA, ни биспецифическое антитело TAAxCD47 не индуцировали значительную активацию тромбоцитов (оба с Fc wt IgG1). В отличие от этого, антитело против CD47 B6H12.2 с Fc wt IgG1 индуцировало активацию тромбоцитов, а также для TAAxCD47 biAb с Fc, несущим мутации DEA, показана активация тромбоцитов.
[0392] Также антитела CEAxCD47 K2AC5 и K2AC22 (в присутствии и в отсутствие афукозилирования) исследовали в диапазоне концентраций, как показано на фигуре 10, по активации тромбоцитов в цельной крови. В крови 6 из 7 доноров не наблюдали значительную активацию тромбоцитов, подобную показанной для TAAxCD47 на фигуре 10. Для одного донора уже для положительных контрольных средств показана необычная активация тромбоцитов и затем также некоторая активация тромбоцитов с использованием K2AC5 и 22. Результаты для этого одного донора исключали из-за необычной активации тромбоцитов.
[0393] Насколько известно авторам настоящего изобретения, потенциал для агрегации в присутствии биспецифического антитела CD47/CEA можно оценивать в богатой тромбоцитами плазме (PRP). PRP подвергают воздействию АДФ при 10 мкМ и 5 мкМ или тестируемых веществ при 200, 100, 20, 25 и 12,5 мкг/мл, так же как солевого раствора или контроля изотипа. Агрегацию тромбоцитов можно оценивать посредством стимуляции тромбоцитов (т.е., 10 мин) с использованием Thrombo-aggregometer TA 4V при постоянном перемешивании. Программное обеспечение Thrombosoft 1.6 (SD Innovation, Frouard, France) можно использовать для анализа данных.
Пример 16: Гематологическая оценка для яванского макака. Примеры
[0394] Насколько известно авторам настоящего изобретения, антитела с перекрестной реакционной способностью по отношению к яванскому макаку, можно тестировать in vivo у яванских макаков по любому эффекту на гематологические параметры (включая RBC и тромбоциты). Антитело по изобретению, например, вводят яванским макакам внутривенным способом, в дозах вплоть до 100 мг/кг, на еженедельной основе. Гематологические параметры, включая количества эритроцитов и тромбоцитов, мониторируют с течением времени и по сравнению с контрольными параметрами у обезьян (значениями до дозирования). Гематологические параметры определяют общепринятыми способами.
[0395] Результаты на фигуре 9 получены с использованием биспецифического антитела IgG1 κλ TAA x CD47 (не CEAxCD47), содержащего связывающее CD47 плечо из биспецифических антител CEA x CD47 по настоящему изобретению. Несмотря на повторяющееся дозирование в высоких дозах, не присутствует значительного различия между контрольными животными и подвергнутыми лечению животными, применительно к количествам RBC и количествам тромбоцитов. Это отличается от опубликованных результатов с использованием антитела против CD47 IgG4 hu5F9-G4 (Jie Liu et al (Open access article, PLOS ONE 10(9) September 2015)), показывающих зависимое от дозы уменьшение гемоглобина, начиная уже с однократных доз около 1 мг/кг. Формат IgG4 использовали для минимизации эффектов на эритроциты и тромбоциты, по сравнению с форматом IgG1. Несмотря на эти меры, даже уже при достаточно низких дозах 1 мг/кг и менее, зависимые от дозы уменьшения количеств, например, гемоглобина наблюдают у яванских макаков.
Пример 17: Определение фармакокинетических свойств у яванских макаков
[0396] Насколько известно авторам настоящего изобретения, в фармакокинетических исследованиях однократной дозы, животных можно случайным образом распределять на 2-5 групп лечения из n=2-4 обезьян на группу (включая самцов и самок). Животным вводят однократные IV дозы биспецифических антител по этому изобретению (инфузия в течение 15-30 минут). Дозы в группах лечения лежат в диапазоне от 0,01 мг/кг до 100 мг/кг. Объемы введения составляют вплоть до 5 мл/кг. Отборы крови проводят по расписанию, в соответствии с экспериментальным способом, в множестве временных точек, например, через 0,25, 1, 4, 8, 24, 48, 72, 96, 120, 168, 240, 336, 504 (сутки 22), 672 (сутки 29), 840 (сутки 36), 1008 (сутки 43), 1176 (сутки 50) и 1344 час (сутки 57) после внутривенного введения биспецифического антитела. Собирают образцы крови по приблизительно 2 мл на животное и временную точку. Концентрации антител измеряют либо в сыворотке, либо в плазме. Тест ELISA разрабатывают и подтверждают для измерения концентраций. Каждый образец измеряют в двух повторах.
[0397] По кривым концентрации в зависимости от времени, PK параметры, подобные Cмакс., выведению, периоду времени полувыведения, площади под кривой и т.д., можно определять с использованием стандартного в данной области программного обеспечения (Phoenix WinNonlin; некомпартментный анализ).
[0398] Ожидают, что периоды времени полувыведения биспецифических антител каппа-лямбда CEA x CD47 лежат в диапазоне 3-14 суток, предполагая q1w или q2w или q3w или q4w введения пациентам.
Пример 18: ADCP, опосредованный биспецифическими антителами, в присутствии слущивающегося CEA
[0399] Клетки MKN45, используемые в качестве клеток-мишеней, окрашивают с использованием кальцеина AM. Параллельно, концентрации тестируемых антител инкубируют или нет с фиксированной дозой (200 нг/мл) коммерческого слущивающегося CEA (BioRad). После этой инкубации, окрашенные MKN-45 подвергают опсонизации в течение 20 минут при комнатной температуре с использованием антител, предварительно смешанных со слущивающимся CEA. Затем макрофаги (окрашенные кальцеином красно-оранжевым), адгерентные к лункам микропланшета, совместно инкубируют с опсонизированными мечеными клетками опухолей-мишенями при соотношении эффектор:клетки-мишени 1:3 в течение 2,5 часов при 37°C. ADCP проводят в присутствии 1 мг/мл IgG человека. В конце периода инкубации, супернатанты заменяют на полную культуральную среду, и микропланшеты подвергают визуализации с использованием платформы для одновременного многопараметрического скрининга CellInsight™ CX5. 1500 макрофагов получают и анализируют на лунку. Фагоцитоз доказывают по двойным положительным событиям (макрофаг+поглощенная клетка опухоли-мишень), и показатели фагоцитоза рассчитывают посредством программного обеспечения от производителя CellInsightTM. Результаты показаны на фигуре 20B.
Пример 19: ADCP, опосредованный биспецифическими антителами, в присутствии CEA-TCB и CEA-TCB1
[0400] Меченные кальцеином AM клетки MKN45, используемые в качестве клеток-мишеней, предварительно инкубируют или нет с фиксированной дозой CEA-TCB (300 нМ) или CEA-TCB1 (30 нМ) в течение 20 мин при RT. После этой инкубации, различные концентрации тестируемого антитела добавляют в соответствующую лунку на 20 мин. Затем макрофаги (окрашенные кальцеином красно-оранжевым), адгерентные к лункам микропланшета, совместно инкубируют с опсонизированными мечеными клетками опухолей-мишенями при соотношении эффектор:клетки-мишени 1:3 в течение 2,5 часов при 37°C. ADCP проводят в присутствии 1 мг/мл hIgG человека. В конце периода инкубации, супернатанты заменяют на полную культуральную среду, и микропланшеты подвергают визуализации с использованием платформы для одновременного многопараметрического скрининга CellInsight™ CX5. 1500 макрофагов получают и анализируют на лунку. Фагоцитоз доказывают по двойным положительным событиям (макрофаг+поглощенная клетка опухоли-мишень), и показатели фагоцитоза рассчитывают посредством программного обеспечения от производителя CellInsightTM.
[0401] На фигуре 18 показано, что ни добавленное CEA-TCB, ни добавленное CEA-TCB1 не уменьшает фагоцитоз, индуцированный посредством K2AC22. Неожиданно, фагоцитоз K2AC22 даже немного увеличивался посредством добавления 30 нМ CEA-TCB1.
Пример 20: Анализ уничтожения посредством комбинации CD47xCEA и CEAxCD3
[0402] Мононуклеарные клетки периферической крови (PBMC) человека выделяли из лейкоцитарных пленок. Часть этих PBMC замораживали в среде для замораживания (90% FCS, 10% DMSO) (чтобы использовать в качестве источника T-клеток), и часть использовали для получения макрофагов (как объяснено в разделе фагоцитоз). Через 6 суток дифференцировки макрофагов, клетки рассевали в 96-луночные планшеты и инкубировали при 37°C. На сутки анализа (2 суток после рассева макрофагов), замороженные PBMC от соответствующего донора макрофагов размораживали и добавляли в планшеты с макрофагами. Клетки-мишени (MKN45, подвергнутые инженерии для экспрессии люциферазы) подвергали опсонизации с использованием комбинации антител, т.е. с использованием T-клеточного биспецифического антитела CEAxCD3 в определенных концентрациях вместе с определенных концентрациями биспецифического антитела CEAxCD47. Опсонизированные мишени добавляли в планшеты, содержащие макрофаги и аутологичные PBMC; и планшеты инкубировали при 37°C в течение 48 час. Через 48 час, половину среды из лунок удаляли, и раствор 2X люциферина добавляли в планшеты для получения конечной концентрации 150 мкг/мл. После 5 минут инкубации при RT, планшеты считывали с использованием Synergy NEO. Процент жизнеспособности рассчитывали посредством деления значения люминесценции (минус фон) на контроль, содержащий только клетки-мишени, и умножения на 100. Затем процент уничтожения экстраполировали посредством вычитания процента жизнеспособности из 100.
[0403] На фигурах 19A и B показаны результаты, полученные с использованием комбинаций CEA-TCB и K2AC5, и K2AC22 в различных концентрациях.
[0404] Полное содержание всех публикаций, патентов, патентных заявок, сайтов в интернет и номеров доступа/последовательностей в базах данных, включая как полинуклеотидные, так и полипептидные последовательности, процитированных в настоящем описании, таким образом, приведено в настоящем описании в качестве ссылки для всех целей, в такой же степени, как если было конкретно и индивидуально указано, что содержание каждой индивидуальной публикации, патента, патентной заявки, сайта в интернет или номера доступа/последовательности в базе данных приведено в качестве ссылки.
| название | год | авторы | номер документа |
|---|---|---|---|
| БИСПЕЦИФИЧЕСКИЕ АНТИТЕЛА ПРОТИВ CEACAM5 И CD3 | 2020 |
|
RU2827106C1 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ С УСТОЙЧИВОСТЬЮ К РАСТВОРИМОМУ СЕА | 2006 |
|
RU2426743C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ С УСТОЙЧИВОСТЬЮ К РАСТВОРИМОМУ СЕА | 2010 |
|
RU2573893C2 |
| ПОЛУЧЕНИЕ МУЛЬТИСПЕЦИФИЧЕСКИХ СМЕСЕЙ АНТИТЕЛ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2815826C2 |
| АНТИТЕЛА К РОДСТВЕННОЙ РАКОВО-ЭМБРИОНАЛЬНОМУ АНТИГЕНУ МОЛЕКУЛЕ КЛЕТОЧНОЙ АДГЕЗИИ (СЕАСАМ) | 2012 |
|
RU2650869C2 |
| АНТИТЕЛА, СПЕЦИФИЧНЫЕ К CD47 и PD-L1 | 2020 |
|
RU2779652C2 |
| Терапевтические антитела к CD47 | 2016 |
|
RU2748401C2 |
| Выделенное биспецифическое антитело, которое специфически связывается с CD47 и PD-L1 | 2021 |
|
RU2815823C2 |
| ГУМАНИЗИРОВАННЫЕ АНТИ-SIRPα АНТИТЕЛА | 2019 |
|
RU2812199C2 |
| АНТИ-SIRPα АНТИТЕЛА | 2018 |
|
RU2771174C2 |
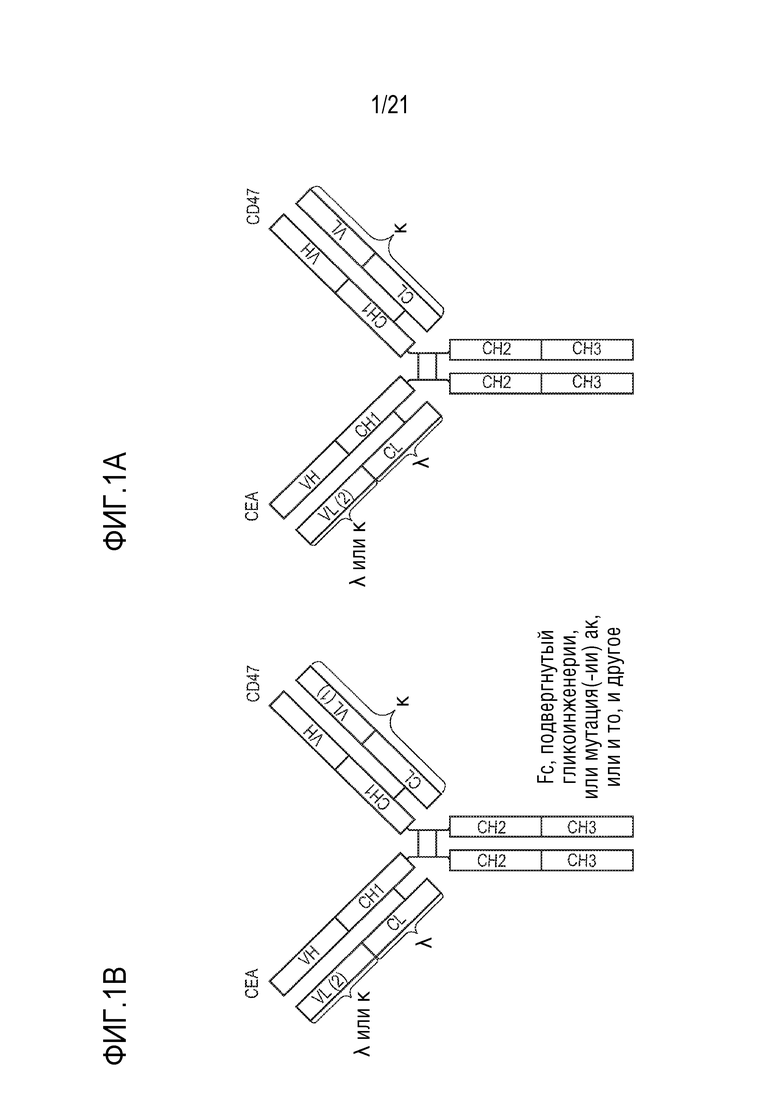
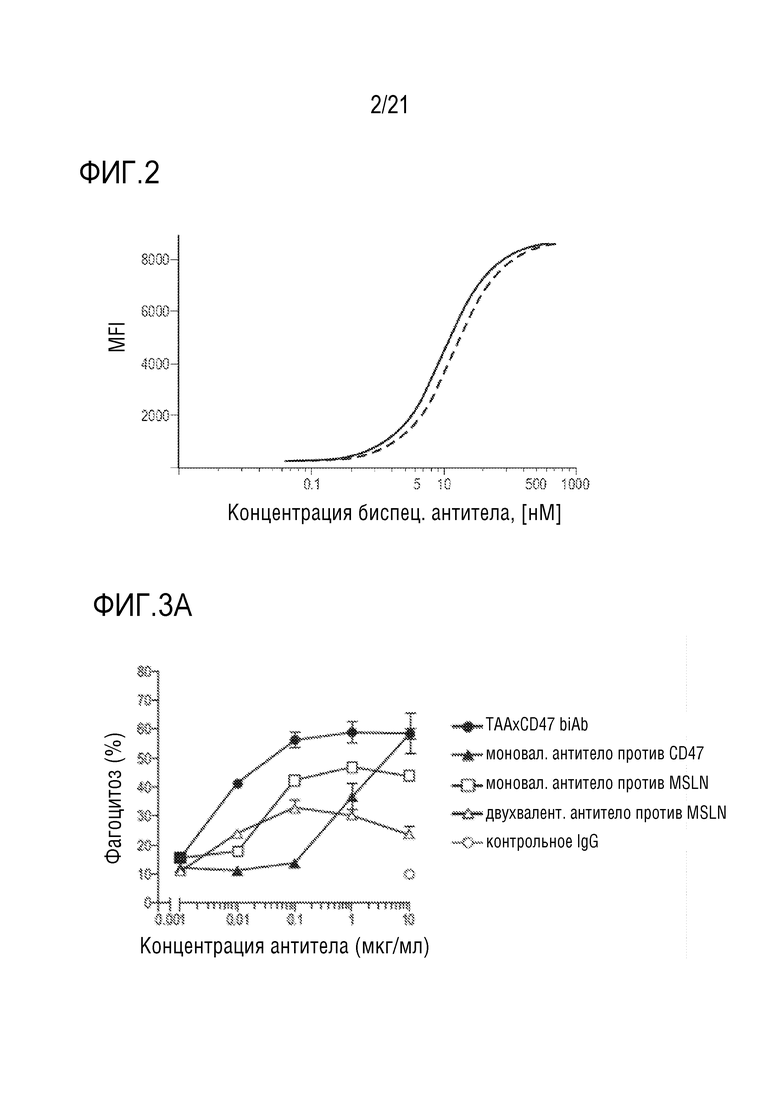
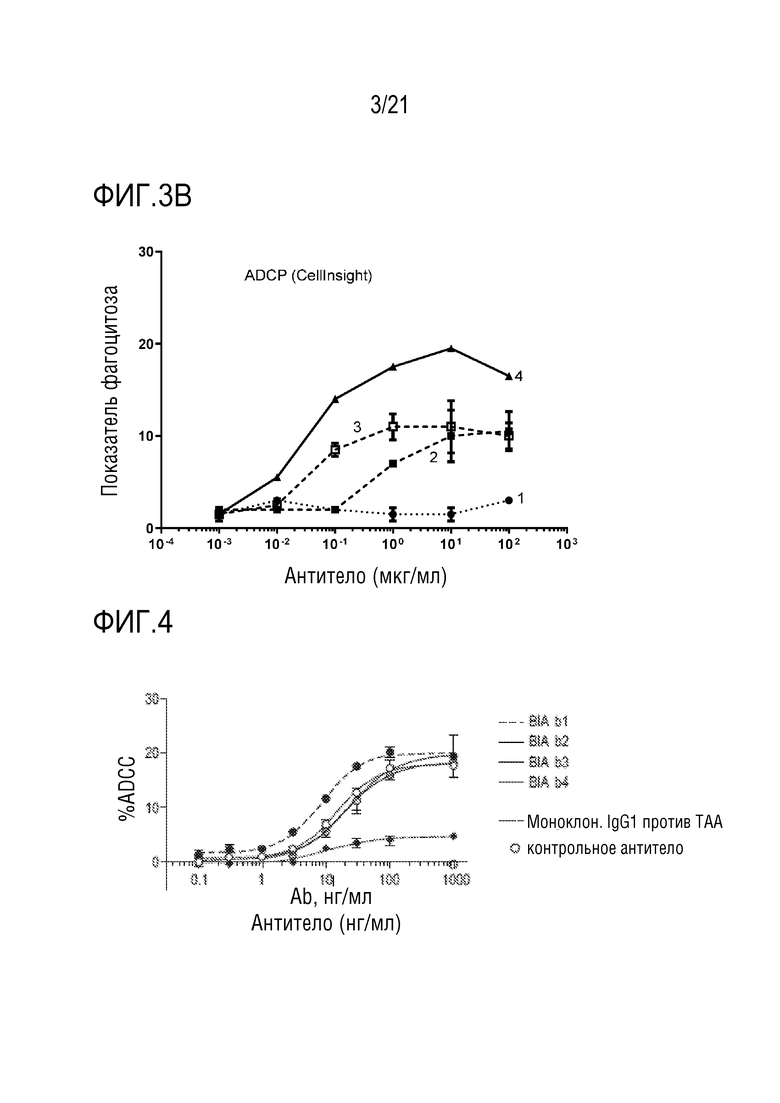
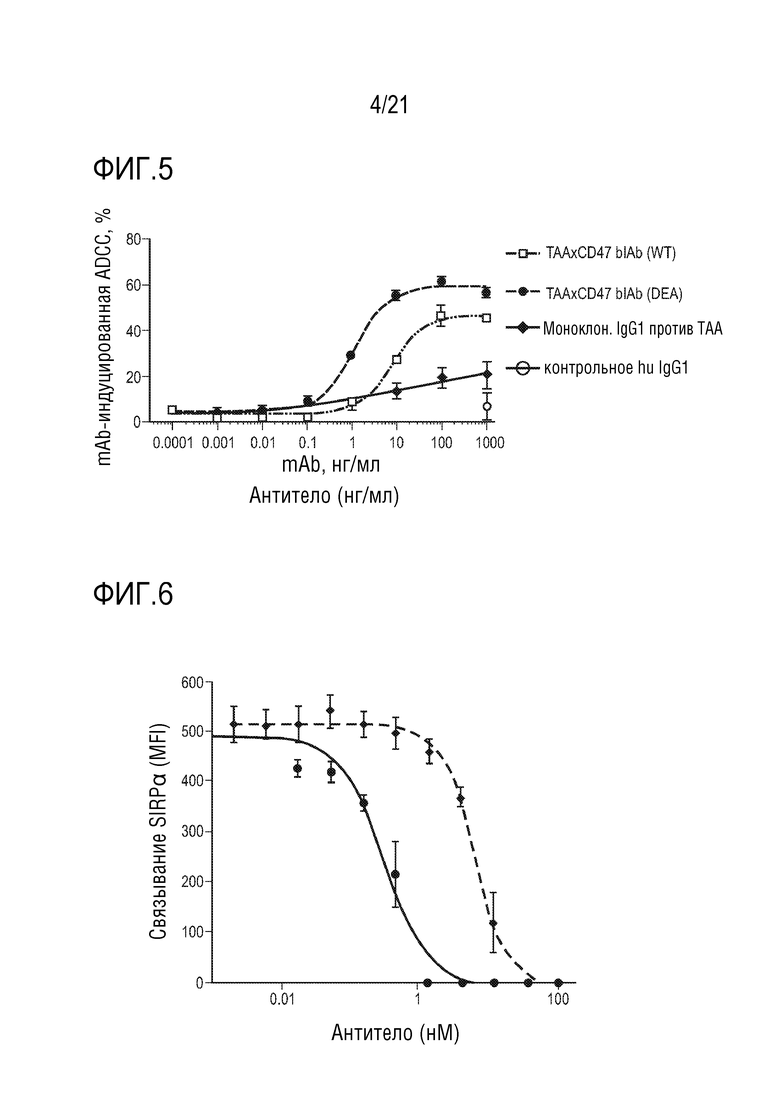
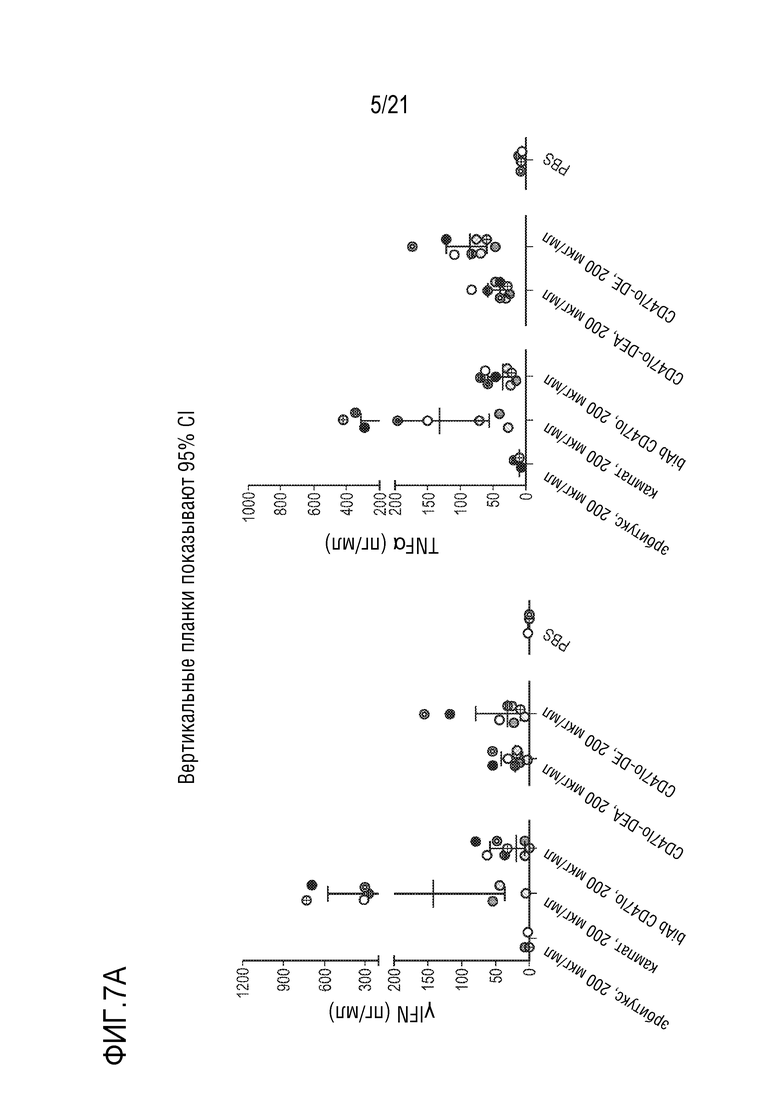

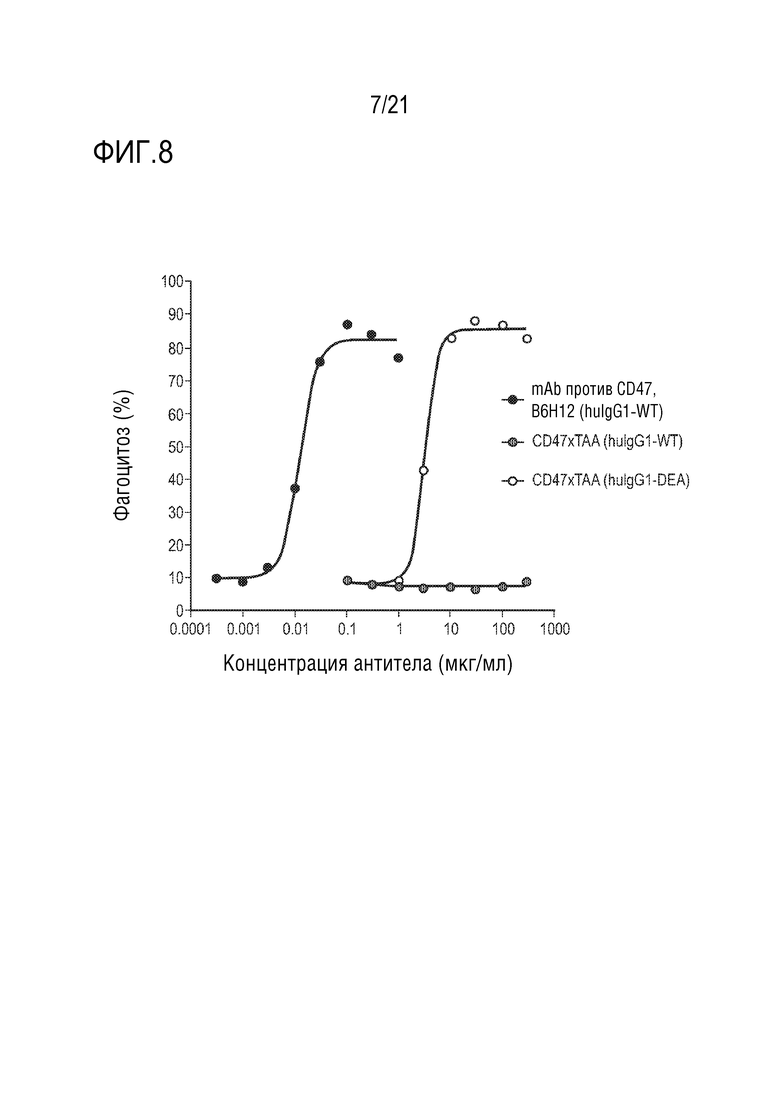
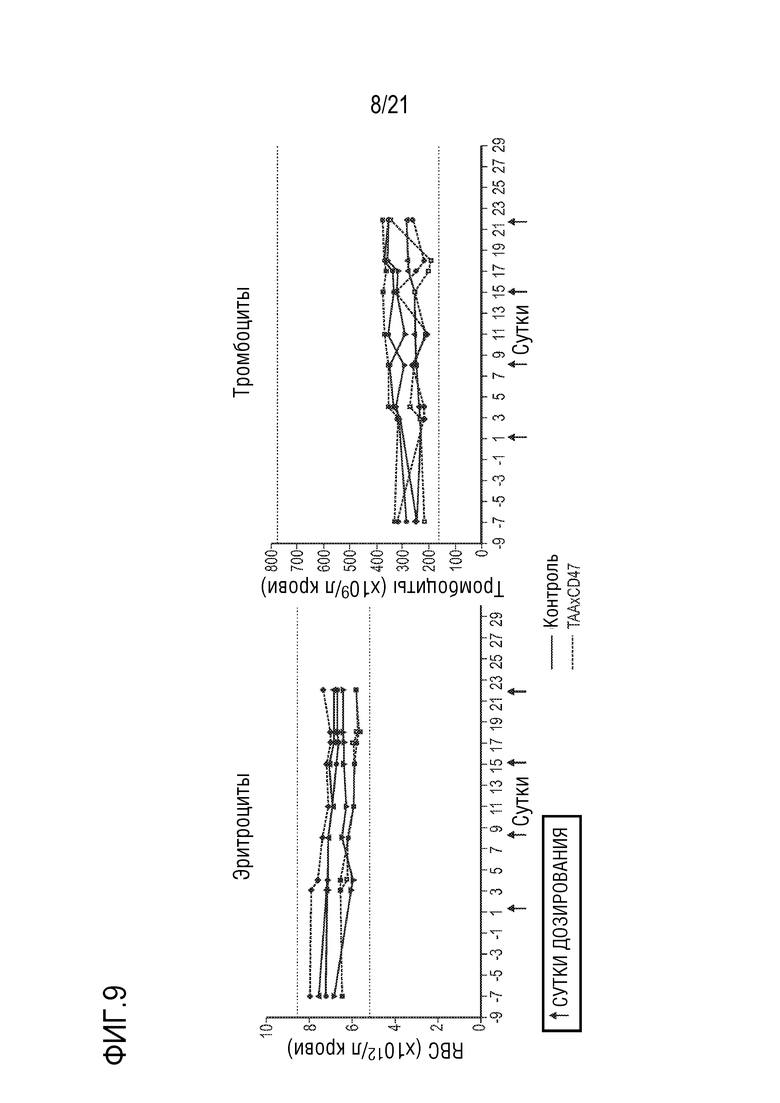
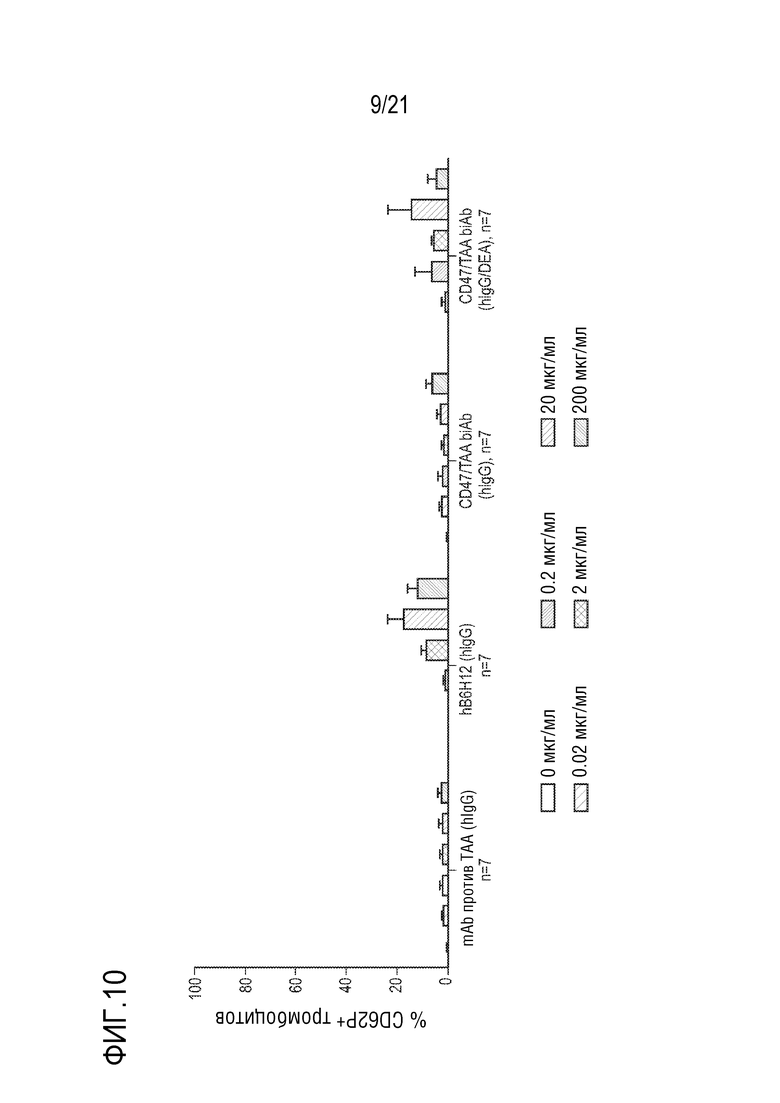
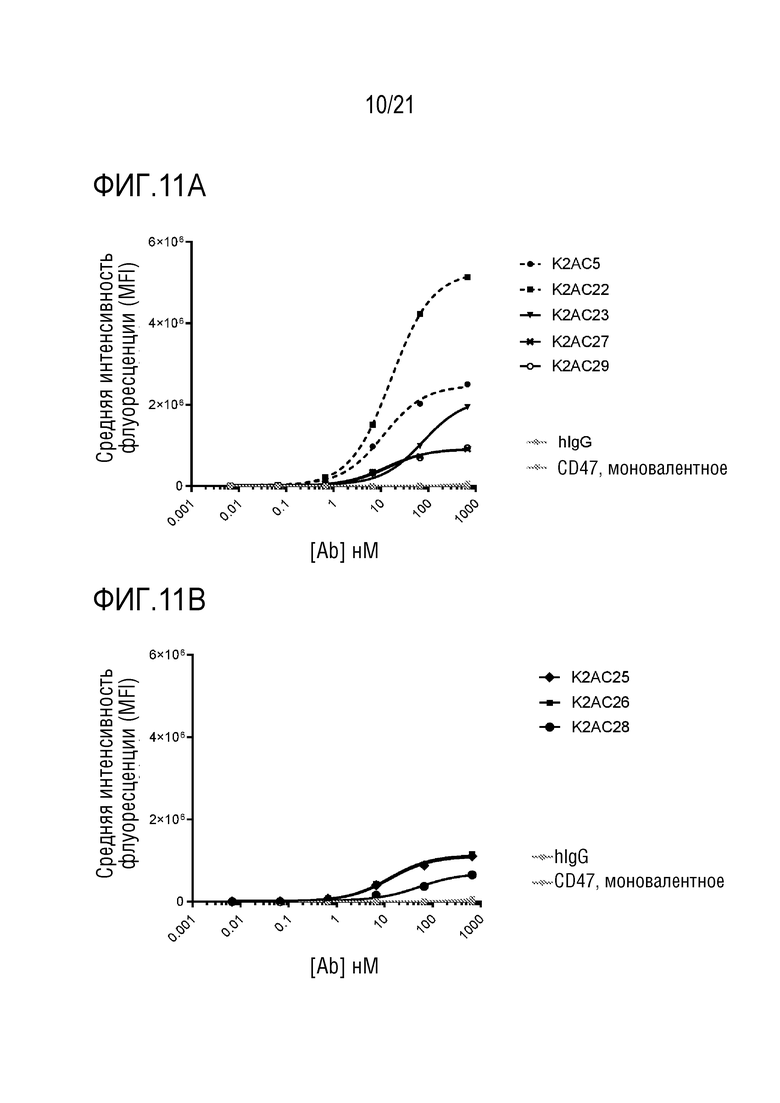
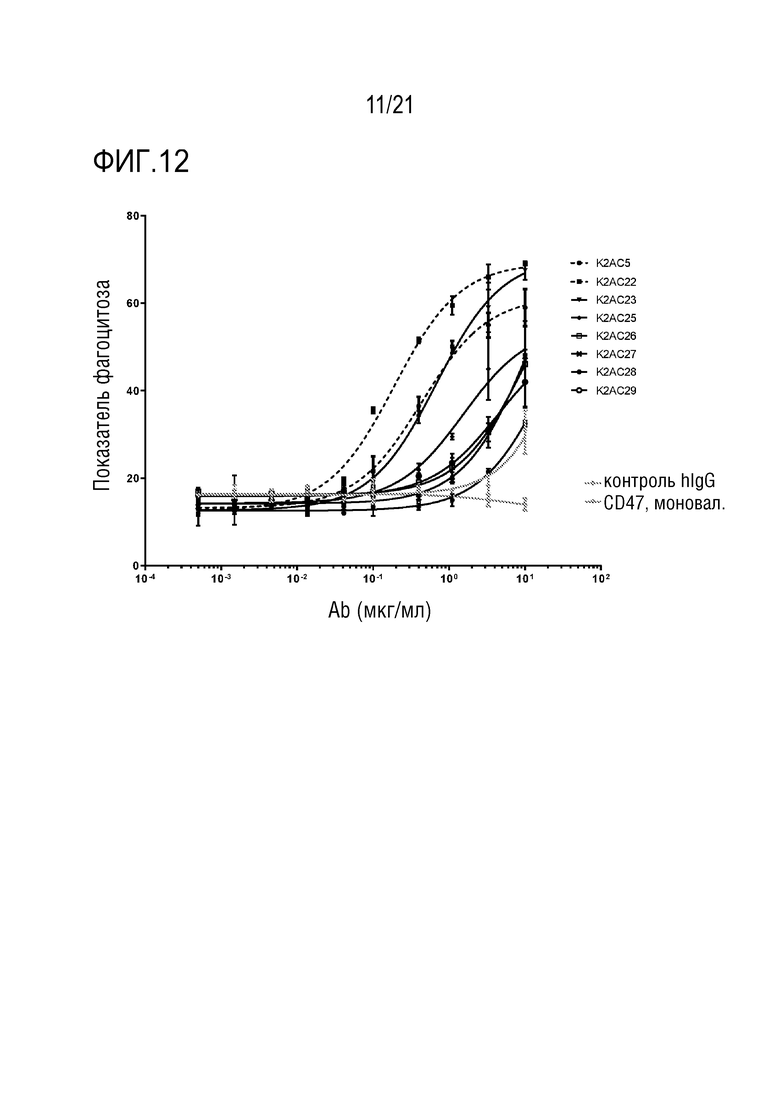
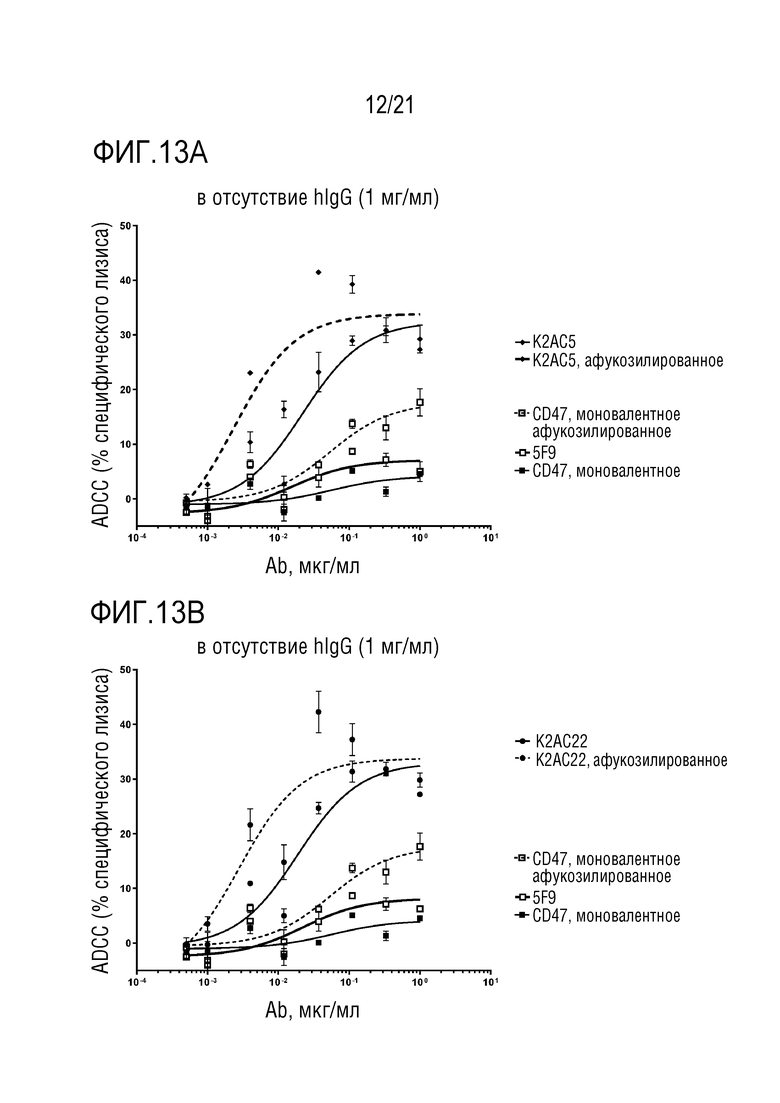
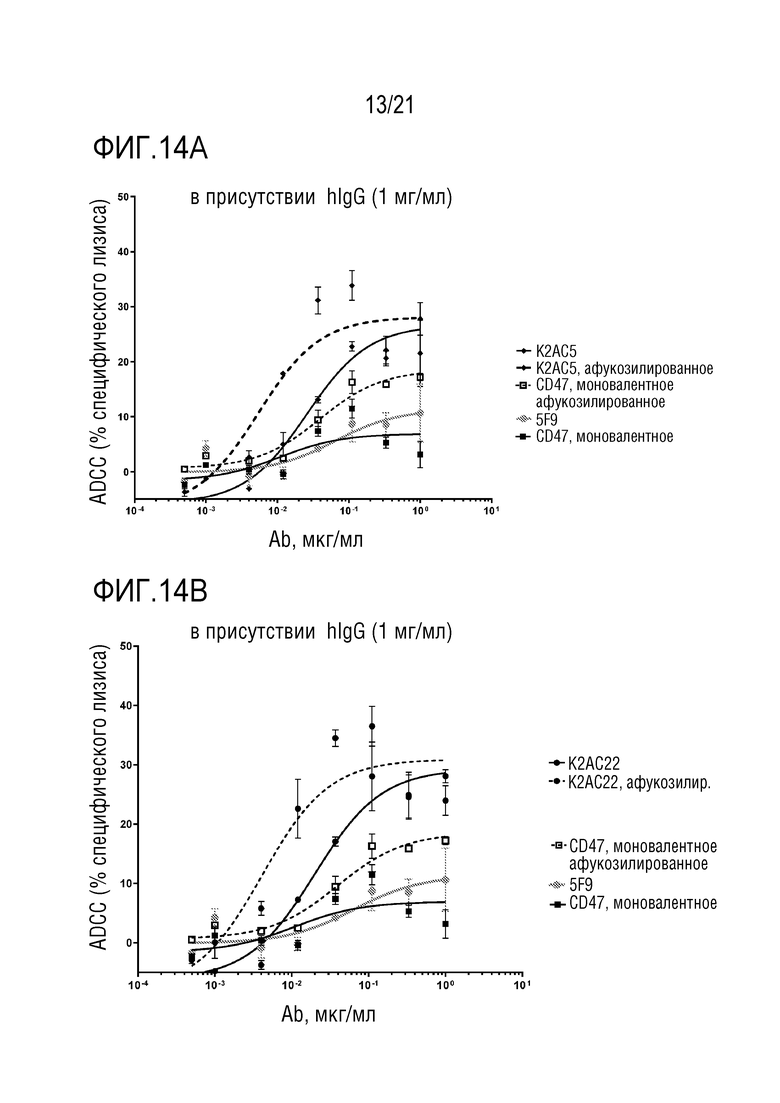
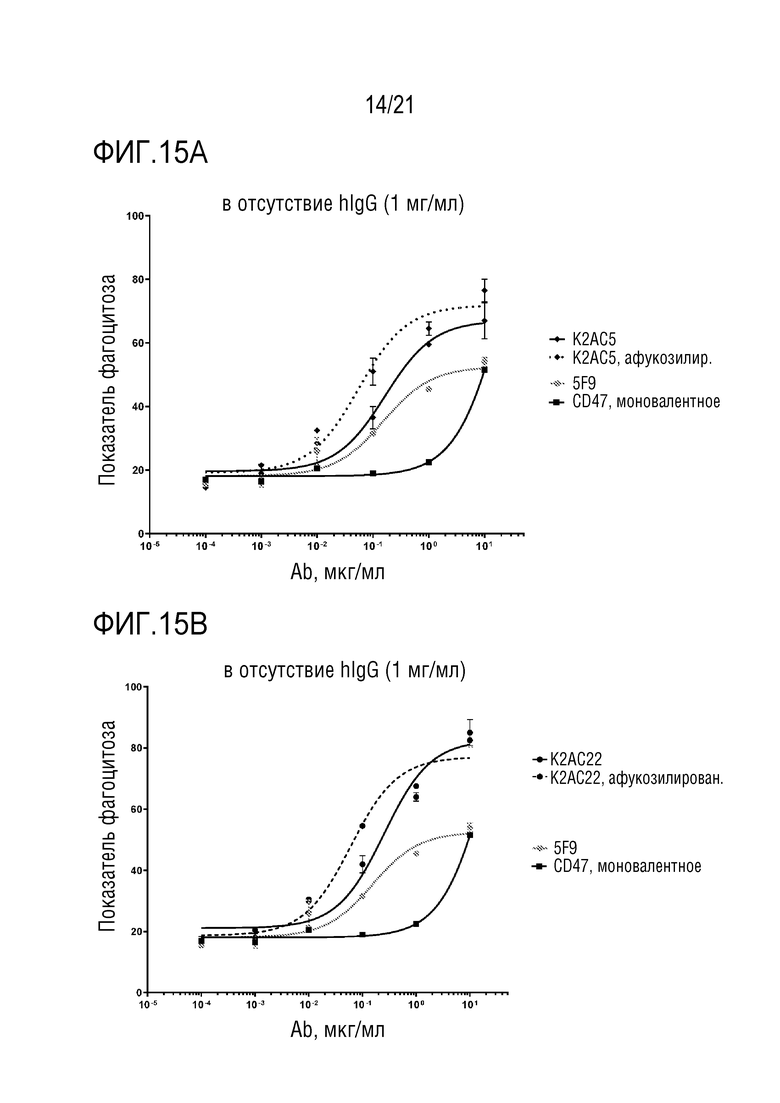

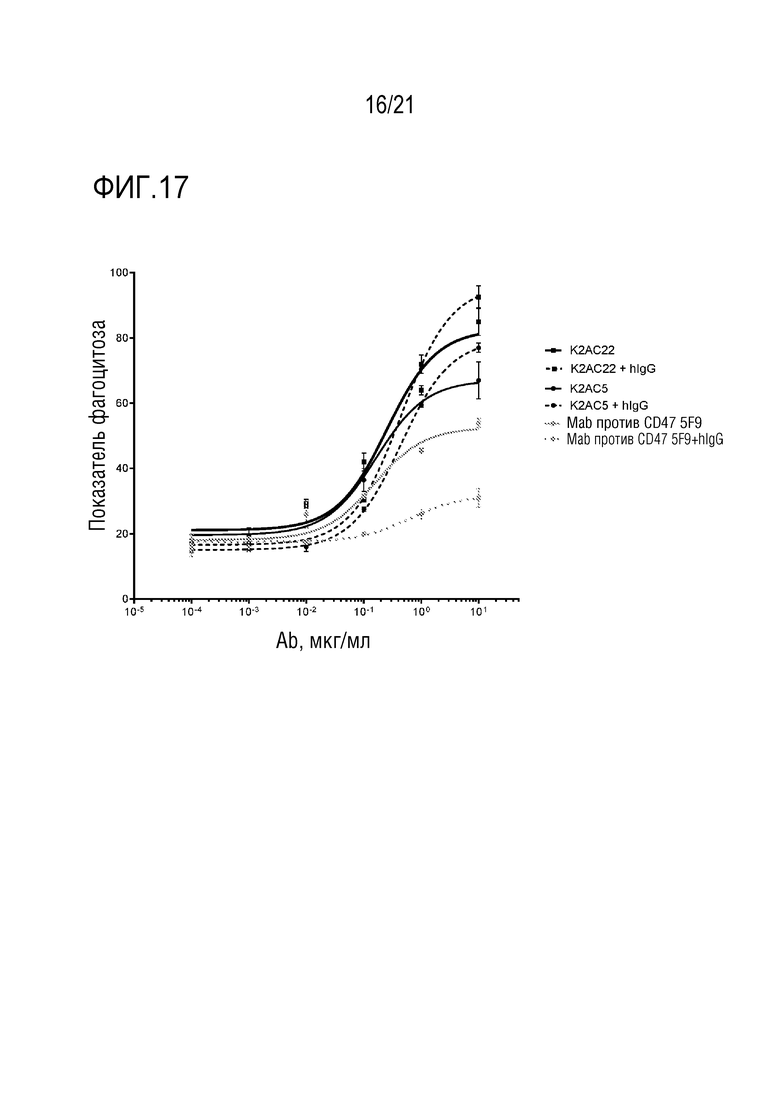
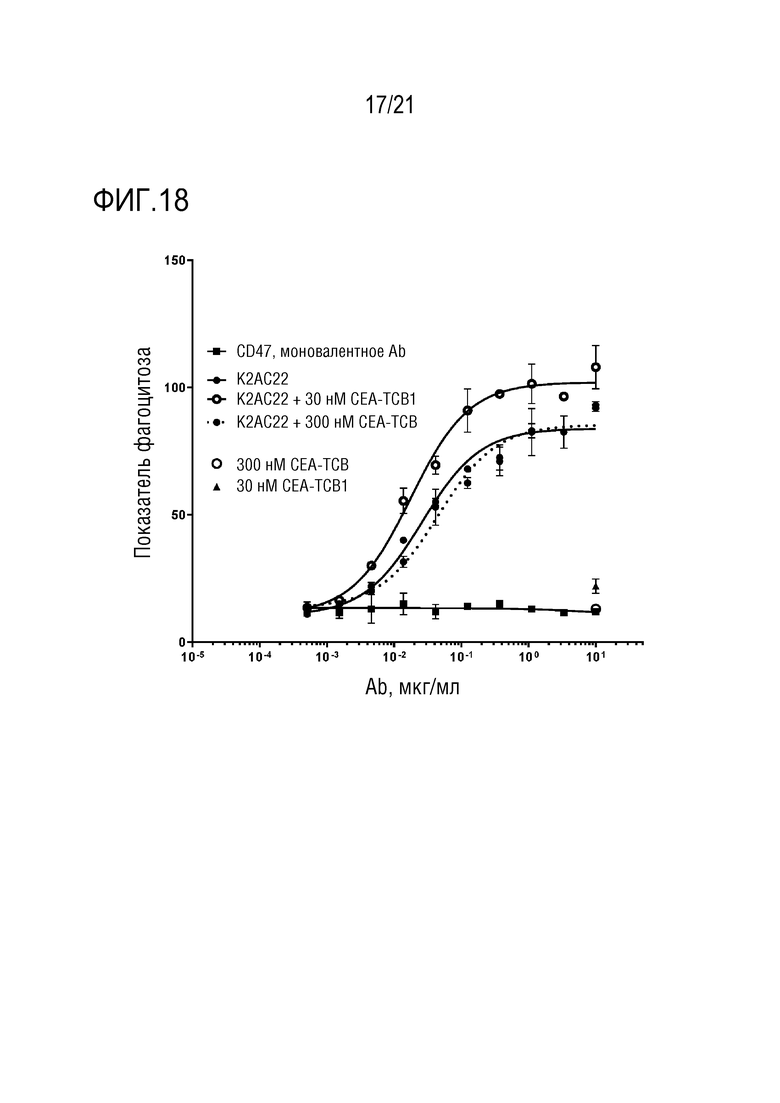
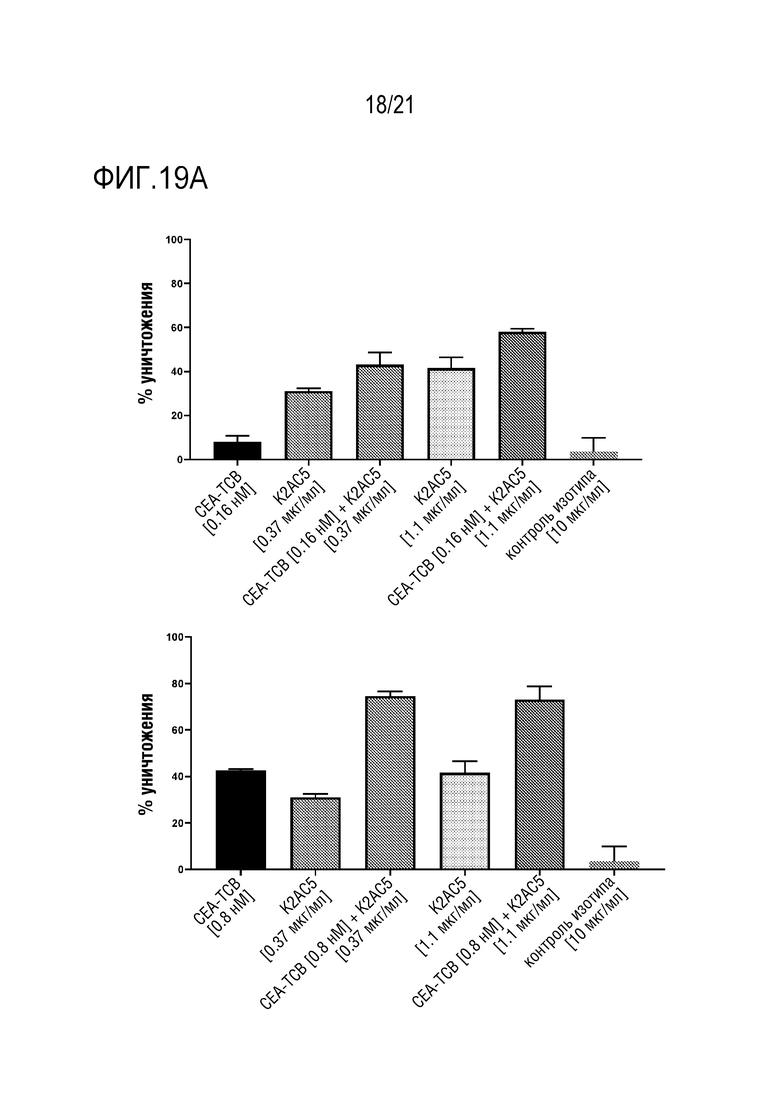
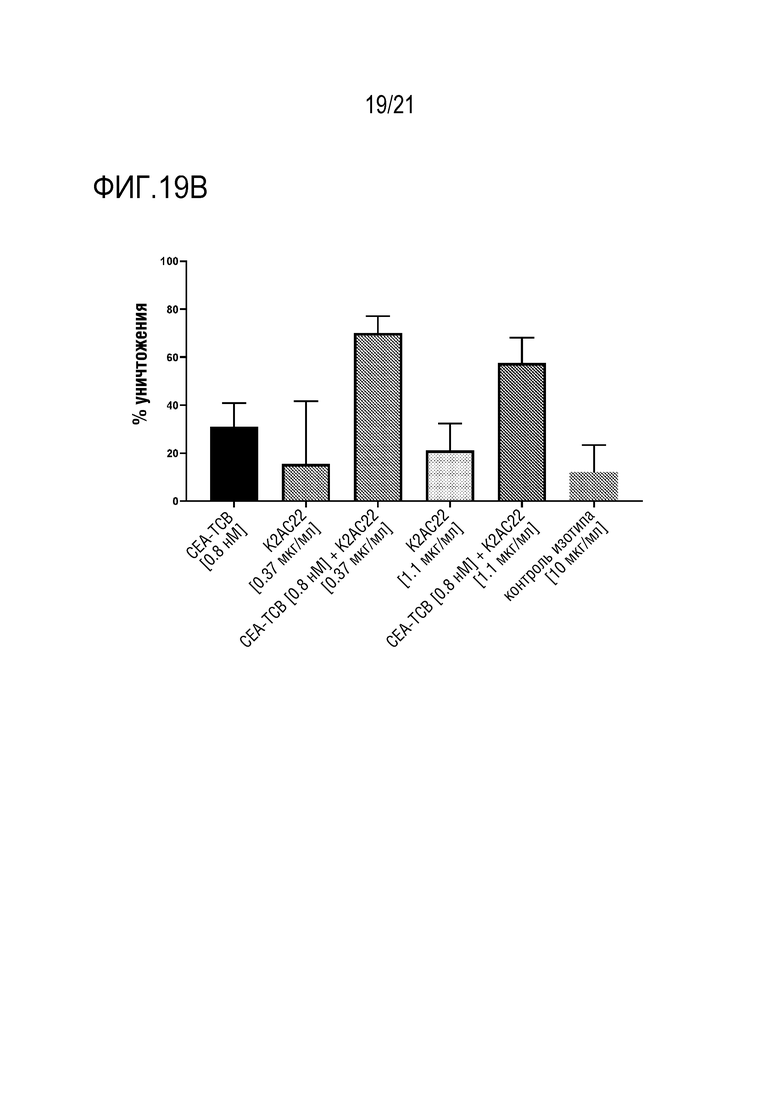
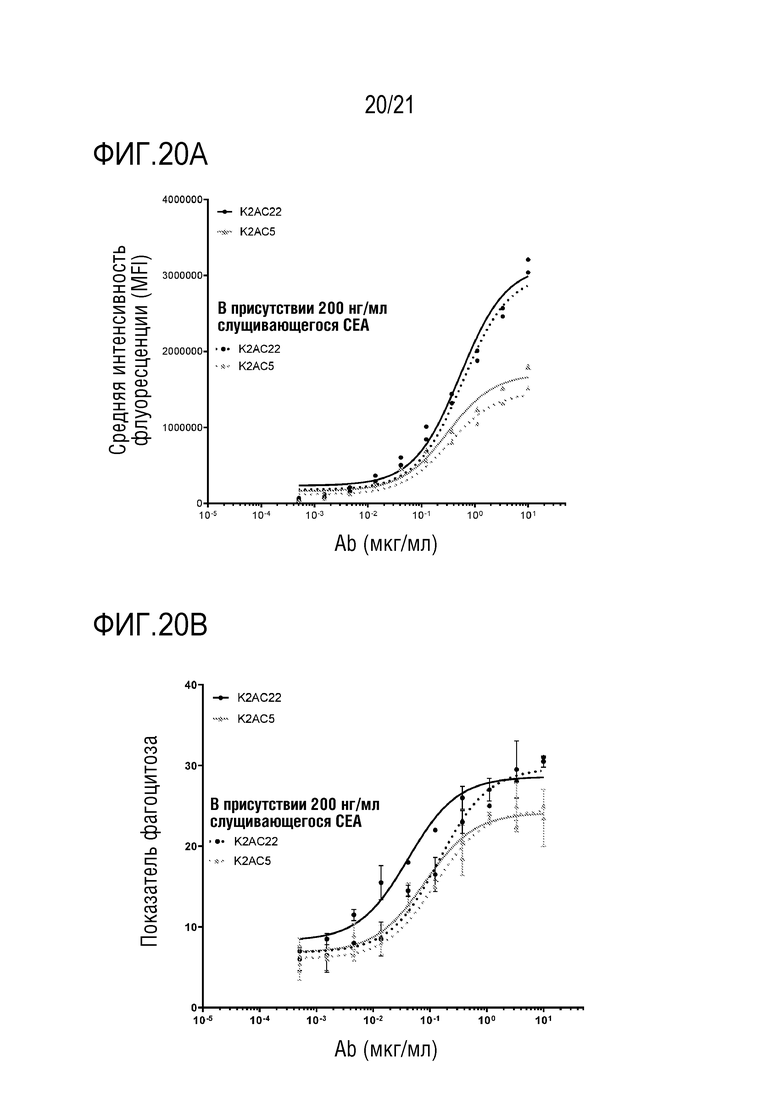
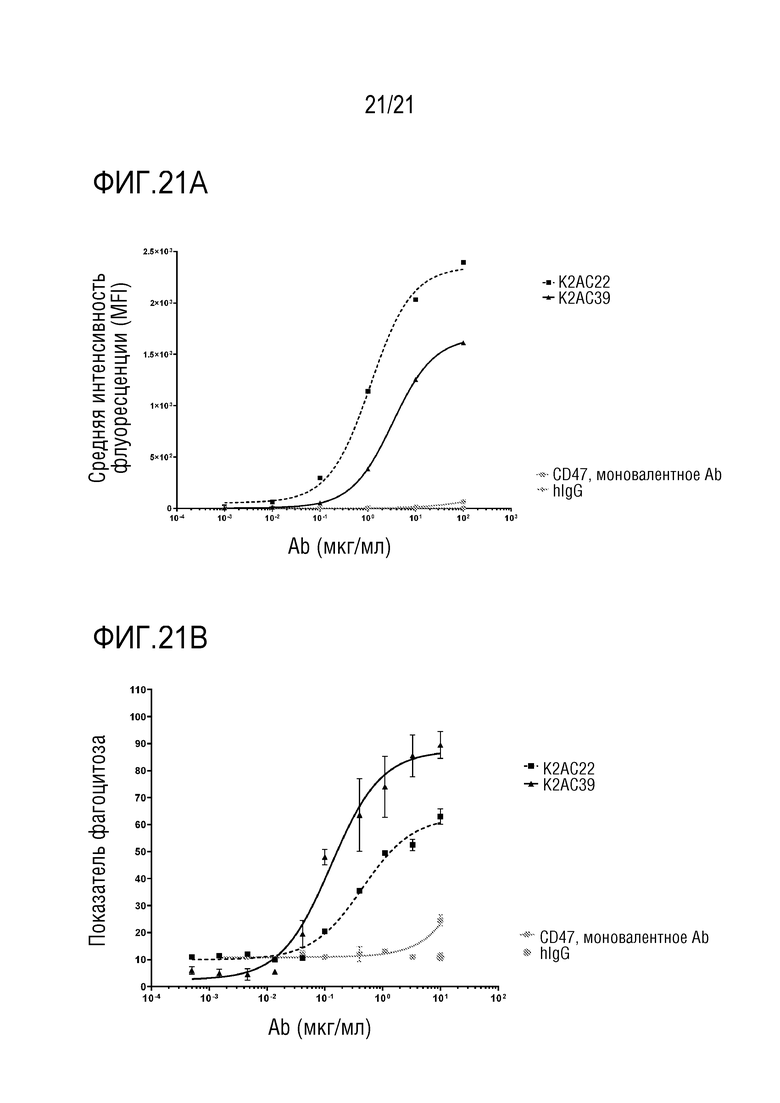
Группа изобретений относится к биотехнологии. Предложены биспецифическое антитело, связывающееся с карциноэмбриональным антигеном CEACAM5 человека и CD47 человека, способ получения биспецифического антитела, способ и фармацевтическая композиция для лечения рака, который экспрессирует CEACAM5. Биспецифические антитела сочетают высокую эффективность с низкой токсичностью, низкой иммуногенностью и благоприятными фармакокинетическими свойствами. 4 н. и 6 з.п. ф-лы, 21 ил., 20 пр.
1. Биспецифическое антитело, содержащее первую связывающую часть, специфически связывающуюся с СЕАСАМ5 человека, и вторую связывающую часть, специфически связывающуюся с CD47 человека, где
а) первая связывающая часть содержит
вариабельную область тяжелой цепи, содержащую в качестве CDR: CDRH1 SEQ ID NO: 25, CDRH2 SEQ ID NO: 26 и CDRH3 SEQ ID NO: 27, и
вариабельную область легкой цепи, содержащую комбинацию CDRL1, CDRL2 и CDRL3, выбранную из группы, состоящей из SEQ ID NO: 31, 32 и 33; SEQ ID NO: 34, 35 и 36; и
b) вторая связывающая часть содержит
вариабельную область тяжелой цепи, содержащую в качестве CDR: CDRH1 SEQ ID NO: 25, CDRH2 SEQ ID NO: 26 и CDRH3 SEQ ID NO: 27, и
вариабельную область легкой цепи, содержащую в качестве CDR CDRL1 SEQ ID NO: 28, CDRL2 SEQ ID NO: 29 и CDRL3 SEQ ID NO: 30.
2. Биспецифическое антитело по п.1, где
а) первая связывающая часть содержит вариабельную область тяжелой цепи (VH) SEQ ID NO: 4 и легкую цепь, выбранную из группы, состоящей из SEQ ID NO: 64 и SEQ ID NO: 65; и
b) вторая связывающая часть содержит тяжелую цепь SEQ ID NO: 4 и вариабельную область легкой цепи SEQ ID NO: 10.
3. Биспецифическое антитело по п.1, где
а) первая связывающая часть содержит тяжелую цепь SEQ ID NO: 5 и легкую цепь, выбранную из группы, состоящей из SEQ ID NO: 64 и SEQ ID NO: 65; и
b) вторая связывающая часть содержит тяжелую цепь SEQ ID NO: 5 и вариабельную область легкой цепи SEQ ID NO: 11.
4. Биспецифическое антитело по любому из пп.1-3,
где первая связывающая часть, специфичная в отношении CEACAM5, содержит вариабельный домен легкой цепи лямбда и константный домен легкой цепи лямбда, и
где вторая связывающая часть, специфичная в отношении CD47, содержит вариабельный домен легкой цепи каппа и константный домен легкой цепи каппа, или
где первая связывающая часть, специфически связывающаяся с CEACAM5, содержит вариабельный домен легкой цепи каппа и константный домен легкой цепи лямбда, и
где вторая связывающая часть, специфически связывающаяся с CD47, содержит вариабельный домен легкой цепи каппа и константный домен легкой цепи каппа.
5. Биспецифическое антитело по п.4, где каждая связывающая часть биспецифического антитела содержит общую тяжелую цепь (cHC).
6. Биспецифическое антитело по любому из пп.1-5, содержащее одну, две или три аминокислотные замены в Fc-области, выбранные из группы, состоящей из:
моно-замещенных S239D, I332E, G236A,
би-замещенных I332E и G236A, S239D и I332E, S239D и G236A, и
три-замещенных S329D и I332E и G236A.
7. Биспецифическое антитело по любому из пп.1-6 в одновременной, раздельной или последовательной комбинации со вторым биспецифическим антителом, содержащим третью связывающую часть, специфически связывающуюся с СЕАСАМ5 человека, и четвертую связывающую часть, специфически связывающуюся с CD3ε человека, в способе лечения рака, экспрессирующего СЕАСАМ5, у пациента.
8. Способ получения биспецифического антитела по любому из пп.1-6, включающий:
а) культивирование клетки-хозяина, содержащей вектор экспрессии, содержащий полинуклеотид, кодирующий биспецифическое антитело по любому из пп.1-6, в условиях, обеспечивающих продукцию биспецифического антитела, и
b) выделение биспецифического антитела.
9. Способ лечения рака, который экспрессирует CEACAM5, включающий введение биспецифического антитела по любому из пп.1-6 пациенту.
10. Фармацевтическая композиция для лечения рака, который экспрессирует CEACAM5, содержащая биспецифическое антитело по любому из пп.1-6 и фармацевтически приемлемый эксципиент или носитель.
| WO 2018098384 A1, 31.05.2018 | |||
| WO2014087248 A2, 12.06.2014 | |||
| WO 2017118675 A1, 13.07.2017 | |||
| DHEILLY E | |||
| ET AL | |||
| Способ очищения сернокислого глинозема от железа | 1920 |
|
SU47A1 |
| WEISKOPF K | |||
| Cancer immunotherapy targeting | |||
Авторы
Даты
2023-06-20—Публикация
2019-05-31—Подача