Область техники
Настоящее изобретение относится к области биотехнологии, а именно к антителам или их антигенсвязывающим фрагментам, а также их применению. Более конкретно, настоящее изобретение относится к антителам, которые специфически связываются с CD47 и PD-L1. Изобретение также относится к нуклеиновой кислоте, кодирующей данное антитело или его антигенсвязывающий фрагмент, вектору экспрессии, способу получения антитела и к применению указанных антител и композиций в терапии рака.
Уровень техники
Обеспечение двух отдельных сигналов к Т-клеткам представляет собой широко распространенную модель лимфоцитарной активации оставшихся Т-лимфоцитов антиген-презентирующими клетками (АРС). Данная модель полностью обеспечивает распознование своих и чужих, и иммунную толерантность. Первичный сигнал или антиген-специфичный сигнал передается через Т-клеточный рецептор (TCR) после распознавания чужеродного антигенного пептида, презентированного в контексте главного комплекса гистосовместимости (МНС). Второй или ко-стимулирующий сигнал доставляется Т-клеткам с помощью ко-стимулирующих молекул, экспрессированных на антиген-презентирующих клетках (АРС), и индуцирует Т-клетки для стимулирования клональной экспансии, секреции цитокинов и эффекторной функции. При отсутствии ко-стимуляции Т-клетки могут стать невосприимчивыми к антигенной стимуляции, они вызывают эффективный иммунный ответ, и далее это может приводить к истощению или устойчивости к чужеродным антигенам.
В двухсигнальной модели Т-клетки получают оба сигнала: как положительный, так и отрицательный вторичный ко-стимулирующий сигнал. Регуляция таких положительных и отрицательных сигналов является критической для максимизации защитной иммунной реакции хозяина, с поддержанием при этом иммунной устойчивости и предотвращением аутоиммунитета. Отрицательные вторичные сигналы, по-видимому, необходимы для индукции Т-клеточной устойчивости, в то время как положительные сигналы стимулируют Т-клеточную активацию. В то время как простая двухсигнальная модель всё ещё обеспечивает достоверное объяснение для наивных лимфоцитов, при этом иммунная реакция представляет собой динамичный процесс, и ко-стимулирующие сигналы к антиген-экспанированным Т-клеткам также могу обеспечиваться. Механизм ко-стимуляции представляет интерес с терапевтической точки зрения, так как было показано, что манипуляции с ко-стимулирующими сигналами обеспечивают средства либо усиления, либо терминации иммунного ответа. Недавно было обнаружено, что Т-клеточная дисфункция или анергия проявляется одновременно с индуцированной и стойкой экспрессией ингибирующего рецептора, полипептида 1 программируемой клеточной смерти (PD-1). В результате терапевтическая направленность PD-1 и других молекул, которые передают сигнал через взаимодействие с PD-1, таких как лиганд 1 программируемой смерти (PD-L1) и лиганд 2 программируемой смерти (PD-L2), является областью интенсивного интереса.
PD-L1 сверхэкспрессируется при множестве злокачественных новообразований и часто ассоциирован с неблагоприятным прогнозом. Интересно, что большинство опухолевых инфильтрующих Т-лимфоцитов с преобладанием экпрессируют PD-1, в отличие от Т-лимфоцитов в нормальных тканях и Т-лимфоцитов периферической крови, что выявляет положительную регуляцию PD-1 в отношении опухоль-реактивных Т-клеток и может способствовать пониженному иммунному ответу. Это может быть связано с применением сигнального пути PD-L1, опосредованного опухолевыми клетками, экспрессирующими PD-L1, и взаимодействующими с Т-клетками, экспрессирующими PD-1, с итоговым ослаблением Т-клеточной активации и уклонением от иммунного надзора. Таким образом, ингибирование PD-L1/PD-1 может усиливать CD8+ Т-клеточноопосредованное уничтожение опухолей.
Терапевтическая направленность PD-1 и других молекул, которые передают сигнал через взаимодействие с PD-1, таких как PD-L1 и PD-L2, является областью интенсивного интереса. Ингибировать сигналы PD-L1 предлагалось в качестве средств для усиления Т-клеточного иммунитета (например, противоопухолевого иммунитета) для лечения злокачественного новообразования и инфекции, включая как острую, так и хроническую инфекцию. Ингибиторы, блокирующие взаимодействие PD-L1 и PD-1, известны, помимо прочих источников, из документов W02001014557, W02002086083, W02007005874, W02010036959, W02010077634 и WO2011066389. Однако оптимального терапевтического средства, направленного на мишень по данному пути, ещё не коммерциализовали, и в этом заключается значительная нереализованная потребность медицины.
CD47 представляет собой гликопротеин клеточной поверхности, который связывается с SIRPα (иначе называемым как SHPS-1) и SIRPγ на соответствующих клетках. Это взаимодействие приводит к негативной регуляции функции иммунных клеток или может опосредовать клеточную адгезию и миграцию. Было предложено применение CD47 в качестве биологического препарата при лечении аутоиммунных нарушений (WO 1999/040940). В отличие от этого, имеется очень мало данных о возможном применении лигандов CD47, таких как SIRPα для аналогичных терапевтических целей. Одно из объяснений заключается в том, что имеет место повсеместная экспрессия CD47, которая может препятствовать применению связывающих CD47 полипептидов в качестве потенциальных лекарственных средств. Данные, опубликованные Yu с соавторами (J Invest Dermatol, 126, 2006, cc. 797-807) позволяют предположить, что слитый белок, состоящий из внеклеточных доменов SIRPα, слитых с Fc-доменом иммуноглобулина, может препятствовать миграции образовавшихся дентритных клеток (DC) из кожи в дренирующие лимфатические узлы у мышей и тем самым ослаблять (по меньшей мере частично) контактную гиперчувствительную реакцию (ответ) у мышей. Миграция и функции DC являются важными для иммунных или воспалительных ответов. В болезненном состоянии эти обостренные ответы DC могут приводить к поддержанию заболевания. Воздействие на миграцию патогенных DC из ткани в лимфоидные органы может является привлекательной возможностью для прекращения порочного цикла стимуляции аутоиммунных или воспалительных заболеваний.
CD47, также известен как интегрин-ассоциированный белок (IAP), антиген ОА3 рака яичников, Rh-ассоциированный антиген и MER6, представляет собой трансмембранный рецептор, несколько раз пронизывающий мембрану, и принадлежащий к суперсемейству иммуноглобулинов. Экспрессия и/или активность CD47 наблюдаются в ряде заболеваний и нарушений. Таким образом, существует потребность в терапиях, которые направленно воздействуют на CD47. Кроме того, по причине экспрессии CD47 на тромбоцитах, также существует потребность в терапиях, направленно воздействующих на CD47 (например, антителах), которые не вызывают значительных уровней истощения тромбоцитов, гемагглютинации, истощения красных телец и/или анемии при введении субъекту.
Известные антетела ингибирующие взаимодействие между CD47 и лигандом SIRPα описаны в следующих источниках: заявки WO2014123580, WO2013119714, WO2015191861, WO2011143624, WO/2014/093678, WO2017053423.
Также известны различные источники, описывающие мультиспецифические антитела, например, WO/2014/087248 описано биспецифическое антитело, которое специфично к CD47 и CD19, а в WO2016023001 описано биспецифическое антитело, которое специфично к CD47 и PD1. Однако ранее не было описано возможности создания и эффективного использования мультиспецифического антитела, которое специфически связывается с CD47 и PD-L1.
В связи с вышесказанным, актуальным является создание новых антител, которые эффективно связываются с CD47 и PD-L1.
Краткое описание изобретения
Настоящее изобретение относится к связывающим молекулам, например, антителам, направленным для связывания с CD47 и PD-L1. Такие антитела могут быть использованы для лечения заболевания или нарушения, опосредуемого CD47 и PD-L1.
В одном из аспектов настоящее изобретение относится к моноклональному антителу, которое специфически связывается с CD47 и PD-L1 и включает один сайт связывания с CD47, и по крайней мере один сайт связывания с PD-L1.
В некоторых вариантах антитело по настоящему изобретению представляет собой полноразмерное антитело или его антигенсвязывающий фрагмент.
В некоторых вариантах антитело по настоящему изобретению включает один или два сайта связывания с PD-L1.
В некоторых вариантах сайт связывания с CD47 антитела по настоящему изобретению ингибирует взаимодействие CD47 рецептора и SIRPα лиганда, и/или сайт связывания с PD-L1 ингибирует взаимодействие PD-L1 с PD-1 рецептором.
В некоторых вариантах сайт связывания c CD47 антитела по настоящему изобретению включает вариабельный домен тяжелой цепи, который содержит последовательности CDR1, CDR2, CDR3, где CDR1 представляет собой последовательность не менее чем на 80% гомологичную последовательности выбранной из следующей группы SEQ ID NO: 1 - 4, то есть CDR1 представляет собой последовательность, выбранную из группы SEQ ID NO: 1-4 или последовательность, выбранную из группы SEQ ID NO: 1-4 с 1 или 2 заменами. где CDR2 представляет собой последовательность не менее чем на 80% гомологичную последовательности выбранной из следующей группы SEQ ID NO: 6 - 15, то есть CDR2 представляет собой последовательность, выбранную из группу SEQ ID NO: 6 - 15 или последовательность, выбранную из группу SEQ ID NO: 6 - 15 с 1, 2, 3, 4 или 5 заменами. где CDR3 представляет собой последовательность не менее чем на 80% гомологичную последовательности выбранной из следующей группы SEQ ID NO: 17 – 20, то есть CDR3 представляет собой последовательность, выбранную из группы SEQ ID NO: 17 - 20 или последовательность, выбранную из группы SEQ ID NO: 17 - 20 с 1, 2 или 3 заменами.
В некоторых вариантах сайт связывания c CD47 антитела по настоящему изобретению включает вариабельный домен тяжелой цепи, который содержит последовательности CDR1, CDR2, CDR3, где CDR1 представляет собой последовательность, выбранную из следующей группы SEQ ID NO: 1 - 4, где CDR2 представляет собой последовательность, выбранную из следующей группы SEQ ID NO: 6 - 15, где CDR3 представляет собой последовательность, выбранную из следующей группы SEQ ID NO: 17 - 20.
В некоторых вариантах сайт связывания c CD47 антитела по настоящему изобретению включает вариабельный домен тяжелой цепи по п.4, и вариабельный домен легкой цепи, который содержит последовательности CDR1, CDR2, CDR3, где CDR1 представляет собой последовательность не менее чем на 80% гомологичную последовательности выбранной из следующей группы SEQ ID NO: 22 - 34, то есть CDR1 представляет собой последовательность, выбранную из группу SEQ ID NO: 22 - 34 или последовательность, выбранную из группу SEQ ID NO: 22 - 34 с 1 или 2 заменами, где CDR2 представляет собой последовательность не менее чем на 80% гомологичную последовательности выбранной из следующей группы SEQ ID NO: 36 - 48, то есть CDR2 представляет собой последовательность, выбранную из группу SEQ ID NO: 36 - 48 или последовательность, выбранную из группу SEQ ID NO: 36 - 48 с 1, 2 или 3 заменами, где CDR3 представляет собой последовательность не менее чем на 80% гомологичную последовательности выбранной из следующей группы SEQ ID NO: 50 – 64, то есть CDR3 представляет собой последовательность SEQ ID NO: 50 - 64 или последовательность, выбранную из группу SEQ ID NO: 50 - 64 с 1 или 2 заменами..
В некоторых вариантах сайт связывания c CD47 антитела по настоящему изобретению включает вариабельный домен тяжелой цепи по п.4, и вариабельный домен легкой цепи, который содержит последовательности CDR1, CDR2, CDR3, где CDR1 представляет собой последовательность, выбранную из следующей группы SEQ ID NO: 22 - 34, CDR2 представляет собой последовательность, выбранную из следующей группы SEQ ID NO: 36 - 48, CDR3 представляет собой последовательность, выбранную из следующей группы SEQ ID NO: 50 - 64.
В некоторых вариантах сайт связывания с CD47 антитела по настоящему изобретению включает вариабельный домен тяжелой цепи, который содержит последовательности гомологичные не менее чем на 90% последовательностям, выбранным из следующей группы SEQ ID NO: 66 - 88, и вариабельный домен легкой цепи, который содержит последовательности гомологичные не менее чем на 90% последовательностям, выбранным из следующей группы SEQ ID NO: 89 - 106.
В некоторых вариантах сайт связывания с CD47 антитела по настоящему изобретению включает вариабельный домен тяжелой цепи, который содержит последовательности, выбранные из следующей группы SEQ ID NO: 66 - 88, и вариабельный домен легкой цепи, который содержит последовательности, выбранные из следующей группы SEQ ID NO: 89 - 106.
В некоторых вариантах сайт связывания с PD-L1 антитела по настоящему изобретению включает вариабельный домен тяжелой цепи, который содержит последовательности гомологичные не менее чем на 80% следующим: SEQ ID NO: 5, SEQ ID NO: 16 и SEQ ID NO: 21, то есть содержит аминокислотные последовательности SEQ ID NO: 5, 16 и 21 или SEQ ID NO: 5 с 1 заменой, SEQ ID NO: 16 с 1, 2 или 3 заменами, SEQ ID NO: 21 с 1, 2 или 3 заменами, и вариабельный домен легкой цепи, который содержит последовательности гомологичные не менее чем на 80% следующим: SEQ ID NO: 35, SEQ ID NO: 49 и SEQ ID NO: 65, то есть содержит аминокислотные последовательности SEQ ID NO: 35, 49 и 65 или SEQ ID NO: 35 с 1, 2 или 3 заменами, SEQ ID NO: 49 с 1 заменой, SEQ ID NO: 65 с 1 или 2 заменами.
В некоторых вариантах сайт связывания с PD-L1 антитела по настоящему изобретению включает вариабельный домен тяжелой цепи, который содержит следующие последовательности: SEQ ID NO: 5, SEQ ID NO: 16 и SEQ ID NO: 21, и вариабельный домен легкой цепи, который содержит следующие последовательности: SEQ ID NO: 35, SEQ ID NO: 49 и SEQ ID NO: 65.
В некоторых вариантах сайт связывания с CD47 антитела по настоящему изобретению представляет собой Fab, scFv, scFab или изолированные монодомены VH или VHH.
В некоторых вариантах сайт связывания с PD-L1 антитела по настоящему изобретению представляет собой Fab, scFv, scFab или изолированные монодомены VH или VHH.
В некоторых вариантах антитело по настоящему изобретению характеризуется тем, что оно вызывает антитело-зависимую клеточную цитотоксичность, макрофаг-опосредованный фагоцитози/или опосредованную T-клетками цитотоксичность в отношении клеток, несущих на поверхности антигены CD47 и/или PD-L1.
В некоторых вариантах антитело по настоящему изобретению характеризуется тем, что оно содержит Fc-фрагмент по меньшей мере с одной мутацией или модификацией, которая повышает антитело-зависимую клеточно-опосредованную цитотоксичность (ADCC) по сравнению с тем же антителом без мутации или модификации.
В некоторых вариантах антитело по настоящему изобретению используется для применения в качестве лекарства для лечения рака.
В одном из аспектов настоящее изобретение относится к нуклеиновой кислоте, которая кодирует любое из антител, описанных выше.
В некоторых вариантах нуклеиновая кислота по настоящему изобретению представляет собой ДНК.
В одном из аспектов настоящее изобретение относится к экспрессионному вектору, который содержит нуклеиновую кислоту, описанную выше.
В одном из аспектов настоящее изобретение относится к способу получения клетки-хозяина для получения любого из антител описанных выше, который включает трансформирование клетки вектором по настоящему изобретению.
В одном из аспектов настоящее изобретение относится к клетке-хозяину для получения любого антитела из описанных выше, которая содержит нуклеиновую кислоту, описанную выше.
В одном из аспектов настоящее изобретение относится к способу получения любого антитела из описанных выше, который заключается в культивировании клетки-хозяина в культуральной среде в условиях, достаточных для получения указанного антитела, при необходимости, с последующим выделением и очисткой полученного антитела.
В одном из аспектов настоящее изобретение относится к фармацевтической композиция для профилактики или лечения заболевания или нарушения, опосредуемого PD-L1 и CD47, которая содержит любое антитело из описанных выше, в сочетании с одним или несколькими фармацевтически приемлемыми эксципиентами.
В некоторых вариантах фармацевтическая композиция по настоящему изобретению предназначена для профилактики или лечения заболевания или нарушения, опосредуемого PD-L1 и CD47, выбранного из группы: ПРГШ (плоскоклеточный рак головы и шеи), рак шейки матки, рак без выявленного первоисточника, глиобластома, рак пищевода, рак мочевого пузыря, ТНРМЖ (трижды негативный рак молочной железы), КРР (колоректальный рак), гепатоцеллюлярная карцинома, меланома, НМРЛ (Немелкоклеточный рак легкого), рак почки, рак яичника, MSI КРР (колоректальный рак с высокой микросателлитной нестабильностью), лейкоз (острый или миелобластный), лимфома, множественная миелома, рак молочной железы, рак предстательной железы, саркома, лимфома Ходжкина, T- и B-клеточном острый лимфобластный лейкоз, мелкоклеточный рак лёгкого, острый миелобластный лейкоз, рефрактерная В-клеточная неходжкинская лимфома, фолликулярная лимфома, В-клеточная лимфома маргинальной зоны, крупноклеточная В-клеточной диффузная лимфома, , рак поджелудочной железы, рак яичника, и миелодиспластический синдром высокого риска.
В одном из аспектов настоящее изобретение относится к способу лечения заболевания или нарушения, опосредованного PD-L1 и CD47, которое включает введение субъекту любого антитела из указанных выше или фармацевтической композиции по данному изобретению, нуждающемуся в таком лечении, в терапевтически эффективном количестве.
В некоторых вариантах способа лечения по настоящему изобретению заболевание или нарушение выбрано из группы: ПРГШ (плоскоклеточный рак головы и шеи), рак шейки матки, рак без выявленного первоисточника, глиобластома, рак пищевода, рак мочевого пузыря, ТНРМЖ (трижды негативный рак молочной железы), КРР (колоректальный рак), гепатоцеллюлярная карцинома, меланома, НМРЛ (Немелкоклеточный рак легкого), рак почки, рак яичника, MSI КРР (колоректальный рак с высокой микросателлитной нестабильностью), лейкоз (острый или миелобластный), лимфома, множественная миелома, рак молочной железы, , рак предстательной железы, рак мочевого пузыря, саркома, гепатоцеллюлярная карцинома, глиобластома, лимфома Ходжкина, T- и B-клеточном острый лимфобластный лейкоз, мелкоклеточный рак лёгкого, острый миелобластный лейкоз, рефрактерная В-клеточная неходжкинская лимфома, фолликулярная лимфома, В-клеточная лимфома маргинальной зоны, крупноклеточная В-клеточной диффузная лимфома, , рак поджелудочной железы, рак яичника, и миелодиспластический синдром высокого риска.
В одном из аспектов настоящее изобретение относится к способу ингибирования биологической активности PD-L1 и/или CD47 у субъекта, нуждающемуся в таком ингибировании, который включает введение субъекту эффективного количества любого антитела из указанных выше.
В одном из аспектов настоящее изобретение относится к применению любого из указанных выше антител или указанной выше фармацевтической композиции для лечения у субъекта, нуждающегося в таком лечении заболевания или нарушения, опосредуемого PD-L1 и CD47.
В некоторых вариантах применения антитела по настоящему изобретению заболевание или нарушение выбрано из группы: ПРГШ (плоскоклеточный рак головы и шеи), рак шейки матки, рак без выявленного первоисточника, глиобластома, рак пищевода, рак мочевого пузыря, ТНРМЖ (трижды негативный рак молочной железы), КРР (колоректальный рак), гепатоцеллюлярная карцинома, меланома, НМРЛ (Немелкоклеточный рак легкого), рак почки, рак яичника, MSI КРР (колоректальный рак с высокой микросателлитной нестабильностью), лейкоз (острый или миелобластный), лимфома, множественная миелома, рак молочной железы, рак предстательной железы, рак мочевого пузыря, саркома, гепатоцеллюлярная карцинома, глиобластома, лимфома Ходжкина, T- и B-клеточном острый лимфобластный лейкоз, мелкоклеточный рак лёгкого, острый миелобластный лейкоз, рефрактерная В-клеточная неходжкинская лимфома, фолликулярная лимфома, В-клеточная лимфома маргинальной зоны, крупноклеточная В-клеточной диффузная лимфома, рак поджелудочной железы, рак яичника, и миелодиспластический синдром высокого риска.
Краткое описание чертежей
Фиг. 1. Карта плазмиды для транзиентной продукции CD47-Fc человека в культуре CHO-K1 клеток млекопитающих.
Фиг. 2. SDS-гель-электрофорез в нередуцирующих условиях препарата CD47-Fc человека.
Фиг. 3. SDS-гель-электрофорез в редуцирующих условиях препарата контрольного anti-CD47 антитела B6H12
Фиг. 4. SDS-гель-электрофорез в нередуцирующих условиях препарата контрольного anti-CD47 антитела B6H12.
Фиг. 5. График ИФА поликлонального фага, несущих VHH фрагменты антител, специфически взаимодействующих с CD47 антигеном человека.
Фиг. 6. Схематичное представление доменной структуры anti-PD-L1/anti-CD47 биспецифических антител, где A – на основе anti-CD47 scFv фрагментов и B – на anti-CD47 VHH фрагментов. При этом PD-L1 связывающая часть представлена ввиде Fab фрагмента.
Фиг. 7. SDS-гель-электрофорез в нередуцирующих условиях препаратов anti-PD-L1/anti-CD47 биспецифических антител на основе anti-CD47 scFv фрагментов.
Фиг.8. SDS-гель-электрофорез в редуцирующих условиях препаратов anti-PD-L1/anti-CD47 биспецифических антител на основе anti-CD47 VHH фрагментов.
Фиг.9. Зависимость цитотоксического эффекта от концентрации исследуемых anti-PD-L1/anti-CD47 биспецифических антител.
Фиг. 10. Зависимость цитотоксического эффекта от концентрации исследуемых anti-PD-L1/anti-CD47 биспецифических антител.
Фиг. 11. Эффективность фагоцитоза клеток линии MDA-MB-231 макрофагами человека в присутствии anti-PD-L1/anti-CD47 биспецифических антител.
Фиг. 12. Зависимость уровня флуоресценции от концентрации anti-PD-L1/anti-CD47 биспецифических антител.
Фиг. 13. Зависимость уровня флуоресценции от концентрации anti-PD-L1/anti-CD47 биспецифических антител.
Фиг. 14. Зависимость уровня флуоресценции от концентрации anti-PD-L1/anti-CD47 биспецифических антител.
Фиг. 15. Зависимость уровня флуоресценции от концентрации anti-PD-L1/anti-CD47 биспецифических антител.
Фиг. 16. Анти-PD-L1 активность биспецифических анти-PD-L1/CD47 антител. По вертикальной оси показано отношение люминесценции лунок с исследуемыми анти-CD47/PD-L1 антителами к люминесценции лунок без добавления антител.
Фиг. 17. Гельфильтрационный профиль оценки агрегационной гомогенности anti-PD-L1/anti-CD47 биспецифического антитела.
Описание изобретения
Определения и общие методы
Если иное не определено в настоящем документе, научные и технические термины, используемые в связи с настоящим изобретением, будут иметь значения, которые обычно понятны специалистам в данной области.
Кроме того, если по контексту не требуется иное, термины в единственном числе включают в себя термины во множественном числе, и термины во множественном числе включают в себя термины в единственном числе. Как правило, используемая классификация и методы культивирования клеток, молекулярной биологии, иммунологии, микробиологии, генетики, аналитической химии, химии органического синтеза, медицинской и фармацевтической химии, а также гибридизации и химии белка и нуклеиновых кислот, описанные в настоящем документе, хорошо известны специалистам и широко применяются в данной области. Ферментативные реакции и способы очистки осуществляют в соответствии с инструкциями производителя, как это обычно осуществляется в данной области, или как описано в настоящем документе.
Определения, связанные с антителом
PD-L1 (лиганд 1 рецептора программируемой гибели клеток), также известный как кластер дифференцировки 274 (CD274) или гомолог 1 B7 (B7-H1), является трансмембранным белком 1 типа, массой 40кДа. Состоит из 3 доменов: внеклеточного, представленного Ig V и C-подобными доменами (220), трансмембранного (21) и внутриклеточного (31). Он играет важную роль в супрессии иммунной системы в период беременности, при пересадке чужеродной ткани, некоторых заболеваниях, например, при гепатите. В нормальных условиях, в ответ на собственные антигены, в лимфатических узлах и селезенке аккумулируется некоторое количество антиген-специфичных CD8+ Т-эффекторных клеток, с целью предотвращения аутоиммунного процесса, формируются PD-1/PD-L1 или B7-1/PD-L1 комплексы, это приводит к передаче ингибиторного сигнала, снижающего пролиферацию данных CD8+ T – клеток в лимфоузлах. Таким образом PD-1/PD-L-взаимодействие является одним из ключевых в развитии иммунной толерантности.
CD47, многократно пронизывающий мембрану трансмембранный рецептор, принадлежащий к суперсемейству иммуноглобулинов, взаимодействует с SIRPα (регулирующий сигналы белок α) на макрофагах и тем самым ослабляет фагоцитоз. Раковые клетки, у которых работает этот путь, избегают фагоцитоза. Поэтому терапевтическое воздействие на CD47 имеет широкое применение при различных раковых заболеваниях. Антитела к CD47 могут обладать способностью блокировать взаимодействие между CD47 и SIRPα, а могут не обладать такой способностью.
Термин «связывающая молекула» включает в себя антитела и иммуноглобулины.
Термин «антитело» или «иммуноглобулин» или «моноклональное антитело» или «биспецифическое антитело» или «мультиспецифическое антитело» (Ig), как использовано в данном описании, включает целое/полноразмерное антитело или любой антигенсвязывающий фрагмент (т.е. «антигенсвязывающую часть»). Кроме того, например, термины «антитело» или «иммуноглобулин» или «моноклональное антитело» включают любую комбинацию антиген-связывающих фрагментов, одной или более валентности и одной или более специфичности, и константных областей иммуноглобулинов и могут быть аналогичны по смыслу терминам «биспецифическое антитело» или «мультиспецифическое антитело». Кроме того, например, термины «антитело» или «иммуноглобулин» или «моноклональное антитело» включают любую комбинацию антиген-связывающих фрагментов и константных областей иммуноглобулинов, связанных и ковалентно или нековалентно с любым полипептидом любой природы. Кроме того, термин «антитело», например, относится к гликопротеину, содержащему по меньшей мере две тяжелые (H) цепи и две легкие (L) цепи, взаимосвязанные дисульфидными связями, или его антигенсвязывающей частью. Каждая тяжелая цепь содержит вариабельную область тяжелой цепи (сокращенно называемую в данном описании как VH) и константную область тяжелой цепи. Известно пять типов тяжелых цепей антител млекопитающих, которые обозначают греческими буквами: α, δ, ε, γ и µ. Присутствующий тип тяжелой цепи определяет класс антитела; указанные цепи обнаружены в антителах типа IgA, IgD, IgE, IgG и IgM соответственно. Различные тяжелые цепи отличаются по размеру и составу; α и γ содержат примерно 450 аминокислот, а µ и ε состоят примерно из 550 аминокислот. Каждая тяжелая цепь содержит две области, т.е. константную область и вариабельную область. Константная область является идентичной во всех антителах одного и того же изотипа, но отличается в антителах различного изотипа. Тяжелые цепи γ, α и δ содержат константную область, которая состоит из трех константных доменов CH1, СН2 и CH3 (выстроены в ряд) и шарнирной области, которая придает гибкость (Woof J., Burton D., Nat Rev Immunol 4, 2004, cc.89-99); тяжелые цепи µ и ε содержат константную область, которая состоит из четырех константных доменов CH1, СН2, CH3 и CH4. У млекопитающих известно только два типа легких цепей, которые обозначают как лямбда (λ) и каппа (κ). Каждая легкая цепь состоит из вариабельной области легкой цепи (сокращенно называемой в данном описании как VL) и константной области легкой цепи. Примерная длина легкой цепи составляет 211-217 аминокислот. Предпочтительно легкая цепь представляет собой легкую каппа (κ)-цепь, а константный домен CL предпочтительно представляет собой С-каппа (κ).
«Антитела» согласно изобретению могут представлять собой антитела любого класса (например, IgA, IgD, IgE, IgG и IgM, предпочтительно IgG) или подкласса (например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2, предпочтительно IgG1).
Области VH и VL могут быть дополнительно подразделены на области гипервариабельности, называемые определяющими комплементарность областями (CDR), разбросанные между областями, которые являются более консервативными, называемыми каркасными областями (FR). Каждая VH и VL состоит из трех CDR и четырех FR, расположенных от амино-конца к карбокси-концу в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4. Вариабельные области тяжелой и легкой цепей содержат домен связывания, который взаимодействует с антигеном. Константные области антител могут опосредовать связывание иммуноглобулина с тканями хозяина или факторами, включая различные клетки иммунной системы (например, эффекторными клетками), и первый компонент (Clq) классической системы комплемента.
Термин «антигенсвязывающая часть» антитела или «антигенсвязывающий фрагмент» (или просто «часть антитела» или «фрагмент антитела»), как использовано в данном описании, относится к одному или нескольким фрагментам антитела, которые сохраняют способность специфически связываться с антигеном. Было показано, что антигенсвязывающая функция антитела может выполняться фрагментами полноразмерного антитела. Примеры связывающих фрагментов, включенных в термин “антигенсвязывающая часть" антитела включают (i) Fab-фрагмент, одновалентный фрагмент, состоящий из доменов VL, VH, CL и CH 1; (ii) F(ab’)2-фрагмент, двухвалентный фрагмент, содержащий два Fab-фрагмента, связанных дисульфидным мостиком в шарнирной области; (iii) Fd- фрагмент, состоящий из доменов VH и CH 1; (iv) Fv-фрагмент, состоящий из доменов VL и VH в едином плече антитела, (v) dAb-фрагмент (Ward et al., (1989) Nature 341:544-546), который состоит из домена VH/VHH; и (vi) выделенная определяющая комплементарность область (CDR). Кроме того, две области Fv-фрагмента, VL и VH, кодируются разными генами, они могут быть соединены при помощи рекомбинантных способов с использованием синтетического линкера, который дает возможность получать их в виде единой белковой цепи, в которой области VL и VH спариваются с образованием одновалентных молекул (известных как одноцепочечный Fv (scFv); см., например, Bird et al. (1988) Science 242:423-426; и Huston et al. (1988) Proc. Natl. Acad. Sci. USA 85:5879-5883). Предполагается, что такие одноцепочечные молекулы также включены в термин «антигенсвязывающая часть» антитела. Такие фрагменты антител получают с использованием общепринятых способов, известных специалистам в данной области, и эти фрагменты подвергают скринингу таким же образом, как и интактные антитела.
Предпочтительно CDR антигенсвязывающего участка или весь антигенсвязывающий участок антител по изобретению имеет происхождение из мыши, ламы или донорской человеческой библиотеки или по существу человеческое происхождение с определенными аминокислотными остатками, измененными, например, замещенными разными аминокислотными остатками с тем, чтобы оптимизировать конкретные свойства антитела, например KD, koff, IC50, EC50, ED50. Предпочтительно каркасные участки антитела по изобретению имеют человеческое происхождение или по существу человеческое происхождение (по крайней мере на 80, 85, 90, 95, 96, 97, 98 или 99% человеческое происхождение).
В других вариантах осуществления антигенсвязывающий участок антитела по изобретению может происходить из других нечеловеческих видов, включая мышь, ламу, кролика, крысу или хомяка, но не ограничиваясь ими. Альтернативно, антигенсвязывающий участок может происходить из человеческих видов.
Термин «вариабельный» относится к тому факту, что определенные сегменты вариабельных доменов широко отличаются в последовательности среди антител. Домен V опосредует связывание антигена и определяет специфичность конкретного антитела к его конкретному антигену. Однако вариабельность неравномерно распределяется на участке вариабельных доменов из 110 аминокислот. Напротив, V области состоят из инвариантных фрагментов, называемых каркасными областями (FR) из 15-30 аминокислот, разделенных более короткими участками чрезвычайной вариабельности, называемых «гипервариабельными областями» или CDR. Каждый вариабельный домен нативных тяжелых и легких цепей содержит четыре FR, в основном принимающих конфигурацию бета-листов, связанных тремя гипервариабельными областями, которые образуют петли, связывающие, и в некоторых случаях являющиеся частью бета-складчатой структуры. Гипервариабельные области в каждой цепи удерживаются вместе в тесной близости с помощью FR и с гипервариабельными областями другой цепи вносят вклад в образование антигенсвязывающего сайта антител. Константные домены не принимают непосредственного участия в связывании антитела с антигеном, но проявляют различные эффекторные функции, такие как участие антитела в антителозависимой клеточной цитотоксичности (АЗКЦ, ADCC).
Термин «гипервариабельная область» по данному описанию относится к аминокислотным остаткам антитела, которые отвечают за связывание антигена. Обычно гипервариабельная область содержит аминокислотные остатки из «области, определяющей комплементарность» или «CDR», и/или такие остатки из «гипервариабельной петли».
В некоторых случаях может также быть предпочтительным изменение одного или более остатков аминокислот CDR-участков с целью повышения аффинности связывания с целевым эпитопом. Это известно, как «созревание аффиности» и в некоторых случаях может выполняться в связи с гуманизацией, например, в ситуациях, когда гуманизация антитела приводит к снижению специфичности или аффинности связывания, и не представляется возможным в достаточной степени улучшить специфичность или аффинность связывания с помощью только обратных мутаций. Различные методы созревания аффинности известны в данной области техники, например, способ in vitro сканирующего насыщающего мутагенеза, описанный Burks et al., Proc Natl Acad Sci USA, 94:412–417 (1997), и способ пошагового in vitro созревания аффинности, предложенный Wu et al., Proc Natl Acad Sci USA 95:6037 6042 (1998).
«Каркасные области» (FR) представляют собой остатки вариабельного домена, отличные от CDR остатков. Обычно каждый вариабельный домен имеет четыре FR, определяемые как FR1, FR2, FR3 и FR4. Если CDR определяются согласно Kabat, FR остатки легкой цепи локализуются, приблизительно, в области остатков 1-23 (LCFR1), 35-49 (LCFR2), 57-88 (LCFR3) и 98-107 (LCFR4), а остатки FR тяжелой цепи локализуются, приблизительно, в области остатков 1-30 (HCFR1), 36-49 (HCFR2), 66-94 (HCFR3) и 103- 113 (HCFR4) в тяжелой цепи. Если участки CDR содержат аминокислотные остатки из гипервариабельных петель, FR остатки легкой цепи локализуются, приблизительно, в остатках 1-25 (LCFR1), 33-49 (LCFR2), 53-90 (LCFR3) и 97-107 (LCFR4) в легкой цепи, а FR остатки тяжелой цепи локализуются, примерно, в остатках 1-25 (HCFRI), 33-52 (HCFR2), 56-95 (HCFR3) и 102-113 (HCFR4) в остатках тяжелой цепи. В некоторых примерах, когда CDR содержит аминокислоты как из CDR по Kabat, так и аминокислоты из гипервариабельной петли, FR соответствующим образом корректируются. Например, когда CDRH1 включает аминокислоты Н26-Н35, остатки FR1 тяжелой цепи находятся в положениях 1-25, а остатки FR2 находятся в положениях 36-49.
Антитело по данному изобретению, «которое связывает» целевой антиген, представляет собой антитело, которое связывает антиген с достаточной аффинностью так, что антитело можно применять в качестве диагностического и/или терапевтического агента при нацеливании на белок или клетку, или ткань, экспрессирующую антиген, и в незначительной степени перекрестно реагирует с другими белками. По данным аналитических методов: сортинга флуоресцентно-активированных клеток (FACS), радиоиммунопреципитации (RIA) или ИФА (ELISA), в таких вариантах изобретения степень связывания антитела с белком, не являющимся «мишенью» (с «нецелевым белком»), составляет менее 10% от связывания антитела с конкретным белком-мишенью. По отношению к связыванию антитела с молекулой-мишенью термин «специфическое связывание» или выражения «специфически связывается с» или «специфический к» конкретному полипептиду или эпитопу на конкретном полипептиде-мишени означает связывание, которое заметно (измеримо) отличается от неспецифического взаимодействия (например, в случае bH1-44 или bH1-81 неспецифическое взаимодействие представляет собой связывание с бычьим сывороточным альбумином, казеином, фетальной бычьей сывороткой или нейтравидином).
Специфическое связывание можно определять количественно, например, определяя связывание молекулы по сравнению со связыванием контрольной молекулы. Например, специфическое связывание можно определять конкурентной реакцией с другой молекулой, аналогичной мишени, например, с избытком немеченой мишени. В этом случае специфическое связывание указывается, если связывание меченой мишени с зондом конкурентно ингибируется избытком немеченой мишени. В данном описании термин «специфическое связывание» или выражения «специфически связывается с» или «специфический к» конкретному полипептиду или эпитопу на конкретном полипептиде-мишени можно характеризовать на примере молекулы, имеющей Kd к мишени по меньшей мере около 200 нМ, или же по меньшей мере около 150 нМ, или же по меньшей мере около 100 нМ, или же по меньшей мере около 60 нМ, или же по меньшей мере около 50 нМ, или же по меньшей мере около 40 нМ, или же по меньшей мере около 30 нМ, или же по меньшей мере около 20 нМ, или же по меньшей мере около 10 нМ, или же по меньшей мере около 8 нМ, или же по меньшей мере около 6 нМ, или же по меньшей мере около 4 нМ, или же по меньшей мере около 2 нМ, или же по меньшей мере около 1 нМ или выше. В одном варианте изобретения термин «специфическое связывание» относится к связыванию, при котором молекула связывается с конкретным полипептидом или эпитопом на конкретном полипептиде, практически не связываясь с каким-либо другим полипептидом или эпитопом на полипептиде.
Термин «Ka», как использовано в данном описании, относится к скорости ассоциации конкретного взаимодействия антитело-антиген, тогда как термин или «Kd» относится к скорости диссоциации конкретного взаимодействия антитело-антиген.
«Аффинность связывания» обычно относится к силе совокупных нековалентных взаимодействий между единичным сайтом связывания молекулы (например, антитела) и ее партнером по связыванию (например, антигеном). Если не указано иначе, «аффинность связывания» относится к внутренней (характерной, истинной) аффинности связывания, которая отражает 1:1 взаимодействие между членами пары связывания (например, антителом и антигеном). Аффинность молекулы Х к своему партнеру Y обычно можно представить константной диссоциации (Kd). Желательно, чтобы величина Kd составляла, примерно, 200 нМ, 150 нМ, 100 нМ, 60 нМ, 50 нМ, 40 нМ, 30 нМ, 20 нМ, 10 нМ, 8 нМ, 6 нМ, 4 нМ, 2 нМ, 1 нМ или менее. Аффинность можно измерять обычными методами, известными в уровне техники, включая методы по данному описанию. Низкоаффинные антитела обычно медленно связываются с антигеном и имеют тенденцию легко диссоциировать, тогда как высокоаффинные антитела обычно быстрее связывают антиген и имеют тенденцию дольше оставаться в связанном состоянии. В уровне техники известны различные методы измерения аффинности связывания, любой из этих методов можно использовать для целей настоящего изобретения.
В одном варианте изобретения «Kd» или «величину Kd» по данному изобретению измеряют методами поверхностного плазмонного резонанса на приборе BIAcore™-2000 или BIAcore™-3000 (BIAcore, Inc., Piscataway, NJ) при 25°С, используя чипы с иммобилизованным антигеном СМ5 при ~10 относительных единицах (единицах отклика, RU). Коротко говоря, биосенсорные чипы с карбоксиметилдекстраном (СМ5, BIAcore Inc.) активируют гидрохлоридом N-этил-N'-(3-диметиламинопропил)-карбодиимида (EDC) и N-гидроксисукцинимидом (NHS) в соответствии с инструкциями производителя. Антиген разводят 10 мМ раствором ацетата натрия, рН 4.8, до концентрации 5 мкг/мл (~0.2 мкМ), а затем вводят (инжекция) при скорости потока 5 мкл/минута до достижения, примерно, 10 относительных единиц (RU) связанного белка. После введения антигена вводят 1 М раствор этаноламина, чтобы блокировать непрореагировавшие группы. Для кинетических измерений двукратные серийные разведения Fab (например, от 0.78 нМ до 500 нМ) вводят в PBS с 0.05% Tween 20 (PBST) при 25°С при скорости потока, примерно, 25 мкл/мин. Величины скорости ассоциации (kon) и скорости диссоциации (koff) рассчитывают, применяя простую модель Ленгмюра для связывания один-плюс-один (BIAcore Evaluation Software версия 3.2), с помощью одновременного получения сенсограммы ассоциации и диссоциации. Константу равновесной диссоциации (Kd) рассчитывают, как отношение koff/kon. См., например, Chen, Y., et al., (1999) J. Mol. Biol. 293: 865-881. Если по данным вышеуказанного метода поверхностного плазмонного резонанса скорость ассоциации превышает 106 М-1 сек-1, тогда ее можно определять методом тушения флуоресценции, который измеряет увеличение или уменьшение интенсивности флуоресцентной эмиссии (возбуждение=295 нм; эмиссия (излучение)=340 нм, полоса 16 нм) при 25°С раствора антитела против антигена (Fab форма) с концентрацией 20 нМ в PBS, рН 7.2, в присутствии увеличивающихся концентраций антигена, измеряемых с помощью спектрометра, такого как спектрофотометр остановленного потока (Aviv Instruments) или спектрофотометр SLM-Aminco (ThermoSpectronie) серии 8000 с кюветой с перемешиванием.
Термин «koff» относится к константе скорости диссоциации конкретного взаимодействия связывающей молекулы и антигена. Константу скорости диссоциации koff можно измерить посредством биослойной интерферометрии, например, с помощью системы Octet™.
«Скорость ассоциации» («on-rate») или «kon» по данному изобретению можно также определять тем же самым описанным выше методом поверхностного плазмонного резонанса на приборе BIAcore™-2000 или BIAcore™-3000 (BIAcore, Inc., Piscataway, NJ) при 25°С, используя чипы с иммобилизованным антигеном СМ5 при ~10 относительных единицах (единицах отклика, RU). Коротко говоря, биосенсорные чипы с карбоксиметилдекстраном (СМ5, BIAcore Inc.) активируют гидрохлоридом N-этил-N'-(3-диметиламино пропил)-карбодиимида (EDC) и N-гидроксисукцинимидом (NHS) в соответствии с инструкциями производителя. Антиген разводят 10 мМ раствором ацетата натрия, рН 4.8, до концентрации 5 мкг/мл (~0.2 мкМ), а затем вводят (инжекция) при скорости потока 5 мкл/минута до достижения, примерно, 10 относительных единиц (RU) связанного белка. После введения антигена вводят 1 М раствор этаноламина, чтобы блокировать непрореагировавшие группы.
Если специально не указано иначе, выражения "биологически активный", и "биологическая активность", и "биологические характеристики", по отношению к полипептиду по данному изобретению, означают обладание способностью связываться с биологической молекулой.
Выражение «биологическая молекула» относится к нуклеиновой кислоте, белку, углеводу, липиду и их комбинации. В одном варианте изобретения биологическая молекула существует в природе.
Участки антител, такие как Fab- и F (аb ') 2-фрагменты, могут быть получены из целых антител с использованием традиционных методов, таких как папаиновый или пепсиновый гидролиз целых антител. Более того, антитела, части антител и молекулы иммуноадгезии могут быть получены с использованием стандартных методов рекомбинантной ДНК, например, как описано в настоящем документе.
Термин «рекомбинантное антитело» означает антитело, которое экспрессируется в клетке или клеточной линии, содержащей нуклеотидную последовательность (нуклеотидные последовательности), которая кодирует антитела, при этом указанная нуклеотидная последовательность (нуклеотидные последовательности) не ассоциирована с клеткой в природе.
Термин «вариантное» антитело, используемый в данном документе, относится к антителу, имеющему аминокислотную последовательность, которая отличается от аминокислотной последовательности его «родительского» антитела путем добавления, удаления и/или замены одного или более аминокислотных остатков относительно последовательности родительского антитела. В предпочтительном варианте осуществления изобретения вариантное антитело содержит по меньшей мере одно или более (например, от одного до двенадцати, например, два, три, четыре, пять, шесть, семь, восемь или девять, десять, одиннадцать или двенадцать; и в некоторых вариантах осуществления изобретения от одного до примерно десяти) добавлений, делеций и/или замен аминокислот относительно родительского антитела. В некоторых вариантах осуществления изобретение добавления, делеции и/или замены осуществляются на CDR-участках вариантного антитела. Идентичность или гомология по отношению к последовательности вариантного антитела определяется в настоящем документе как процент аминокислотных остатков в последовательности вариантного антитела, которые идентичны остаткам родительского антитела, после выравнивания последовательностей и введения гэпов, если это необходимо, для достижения максимального процента идентичности последовательности. Вариантное антитело сохраняет способность связываться с тем же антигеном, и предпочтительно эпитопом, с которым связывается родительское антитело, и в некоторых вариантах осуществления изобретения по меньшей мере одно свойство или биологическая активность превосходит аналогичные свойства родительского антитела. Например, вариантное антитело может иметь, например, более выраженную аффинность связывания, более длительный период полувыведения, более низкое значение ИК50 или повышенную способность подавлять биологическую активность антигена по сравнению с родительским антителом. Особый интерес в настоящем документе представляет вариантное антитело, показывающее биологическую активность, превышающую по меньшей мере в 2 раза (предпочтительно, по меньшей мере в 5 раз, 10 раз или 20 раз) биологическую активность родительского антитела.
Термин «биспецифичное антитело» означает антитело, содержащее антигенсвязывающий домен или антигенсвязывающие домены, которые способны к специфическому связыванию с двумя различными эпитопами на одной биологической молекуле или способны к специфическому связыванию с эпитопами на двух различных биологических молекулах. Биспецифичное антитело также упоминается в настоящем документе, как обладающее «двойной специфичностью» или как являющееся антителом с «двойной специфичностью».
Термин «химерное антитело» относится в широком смысле к антителу, которое содержит одну или более областей из одного антитела, и одну или более областей из одного или нескольких других антител, как правило, антитело, частично человеческого происхождения и частично нечеловеческого происхождения, то есть полученное частично из не относящегося к человеку животного, например, мыши, крысы или другого грызуна, или верблюдовых, таких как лама или альпака. Химерные антитела являются предпочтительными по сравнению с нечеловеческими антителами для того, чтобы снизить риск иммунного ответа, направленного против антител у человека, например, ответа, направленного против мышиных антител у человека в случае мышиного антитела. Примером типичного химерного антитела является то, в котором последовательности вариабельного участка являются мышиными, в то время как последовательности константного участка являются человеческими. В случае химерного антитела нечеловеческие части могут быть подвергнуты дальнейшему изменению с целью гуманизации антитела.
Термин «гуманизация» относится к факту, что когда антитело имеет полностью или частично нечеловеческое происхождение, например, антитело мыши или ламы, полученное при иммунизации мышей или лам, соответственно, с представляющим интерес антигеном, или является химерным антителом на основе такого антитела мыши или ламы, можно заменить некоторые аминокислоты, например, в каркасных областях и константных доменах тяжелой и легкой цепей, с тем чтобы избежать или свести к минимуму иммунный ответ у человека. Специфичность взаимодействия антитела с антигеном-мишенью присуща главным образом аминокислотным остаткам, расположенных в шести CDR-участках тяжелой и легкой цепи. Поэтому аминокислотные последовательности внутри CDR-участков, являются гораздо более вариабельными между отдельными антителами, по сравнению с последовательностями вне CDR-участков. Поскольку последовательности CDR участков отвечают за большинство антитело-антиген взаимодействий, можно экспрессировать рекомбинантные антитела, которые имитируют свойства специфического природного антитела, или в более общем плане какого-либо специфического антитела с данной аминокислотной последовательностью, например, путем конструирования экспрессионных векторов, которые экспрессируют последовательности CDR-участков из специфического антитела и каркасные последовательности другого антитела. В результате, можно «гуманизировать» нечеловеческое антитело и в значительной степени сохранить специфичность связывания и аффинность исходного антитела. Несмотря на то, что невозможно точно предсказать иммуногенность и тем самым иммунный ответ, направленный против антитела у человека на конкретное антитело, нечеловеческие антитела, как правило, более иммуногенны, чем человеческие антитела. Химерные антитела, у которых инородные (например, грызуна или верблюда) константные участки были заменены последовательностями человеческого происхождения, показали в целом более низкую иммуногенность, чем антитела полностью инородного происхождения, и существует тенденция использовать в терапевтических антителах гуманизированные или полностью человеческие антитела. Химерные антитела или другие антитела нечеловеческого происхождения, таким образом, могут быть гуманизированы, чтобы снизить риск иммунного ответа, направленного против антитела, у человека.
Для химерных антител, гуманизация обычно включает в себя модификацию каркасных участков последовательностей вариабельного участка. Аминокислотные остатки, которые являются частью участков, определяющих комплементарность (CDR участков), чаще всего не будут изменяться в связи с гуманизацией, хотя в некоторых случаях это может быть желательным, чтобы изменить отдельные аминокислотные остатки CDR-участка, например, чтобы удалить участок гликозилирования, участок дезамидирования, участок изомеризации аспартата или нежелательный остаток цистеина или метионина. N-связанное гликозилирование происходит путем присоединения олигосахаридной цепи к остатку аспарагина в трипептидной последовательности Asn-X-Ser или Asn-X-Thr, где Х может быть любой аминокислотой, кроме Pro. Удаление участка N-гликозилирования может быть достигнуто путем мутирования Asn или Ser/Thr остатка другим остатком, предпочтительно путем консервативной замены. Дезамидирование остатков аспарагина и глутамина может происходить в зависимости от таких факторов, как рН и обнажение поверхности. Остатки аспарагина особенно восприимчивы к дезамидированию, прежде всего, если они присутствуют в последовательности Asn-Gly, и в меньшей степени в других дипептидных последовательностях, таких как Asn-Ala. При наличии такого дезамидированного участка, например, Asn-Gly в последовательности CDR-участка, может быть предпочтительным удалить этот участок, как правило, путем консервативной замены для удаления одного из вовлеченных остатков.
В данной области техники известны многочисленные способы гуманизации последовательности антитела. Одним из наиболее часто используемых методов является трансплантация CDR-участков. Трансплантация CDR участка может быть основана на определениях CDR-участков по Kabat, хотя в более поздней публикации (Magdelaine-Beuzelin et al., Crit Rev.Oncol Hematol. 64:210 225 (2007)) предполагается, что определение по IMGT® (the international ImMunoGeneTics information system®, www.imgt.org) может улучшить результат гуманизации (см Lefranc et al., Dev. Comp Immunol. 27:55-77 (2003)). В некоторых случаях, трансплантация CDR-участка может уменьшить специфичность и аффинность связывания, и, следовательно, биологическую активность, в CDR трансплантированном нечеловеческом антителе, по сравнению с родительским антителом, из которого получены CDR-участки. Обратные мутации (иногда именуемые «ремонт каркасного участка»), могут применяться в выбранных положениях CDR трансплантированного антитела, как правило, в каркасных участках, для того, чтобы восстановить специфичность и аффинность связывания родительского антитела. Определение позиций для возможных обратных мутаций может быть выполнено с использованием информации, имеющейся в литературе и в базах данных антител. Аминокислотные остатки, которые являются кандидатами для обратных мутаций, как правило, расположены на поверхности молекулы антитела, в то время как остатки, которые углублены или имеют низкую степень обнажения поверхности обычно не будут подвержены изменениям. Метод гуманизации, альтернативный трансплантации CDR-участка и обратной мутации, представляет собой изменение поверхности, при котором неэкспонированные на поверхности остатки нечеловеческого происхождения, сохраняются, в то время как экспонированные на поверхности остатки изменяются в человеческие остатки.
Существует две технологии получения полностью человеческих антител: с использованием in vitro собранных фаговых библиотек или in vivo иммунизацией гуманизированных животных (мышей, крыс и т.д.).
Фаговый дисплей является первой и самой широко распространенной in vitro технологией для поиска антител. В 1985 году Смит обнаружил, что последовательности чужеродной ДНК могут быть клонированы в нитевидный бактериофаг M13 таким образом, что клонированные последовательности генов экспрессируются на поверхности фаговых частиц как слитые белки (Smith GP: Filamentous fusion phage: novel expression vectors that display cloned antigens on the virion surface. Science 1985, 228:1315-1317.). Таким образом, можно проводить селекцю интересующих нас слитых белков на основе их способности связывать другие белки. Это открытие было скомбинировано с методами ПЦР-амплификации, что позволило клонировать кДНК репертуар генов иммуноглобулинов для создания разнообразных фаговых библиотек, содержащих вариабельные домены, которые могут быть использованы для быстрого поиска мишень-специфичных моноклональных антител. Репертуар фаговых библиотек отражает репертуар антител B-лимфоцитов каждого человека или животного, кровь которого была использована при создании библиотеки. В 1995 году две статьи сообщили о создании генетически сконструированных мышей, которые экспрессировали полностью человеческие антитела, репертуар которых может быть соспоставим с полученным гибридомной технологией (Lonberg N, Taylor LD, Harding FA, Trounstine M, Higgins KM, Schramm SR, Kuo CC, Mashayekh R, Wymore K, McCabe JG et al.: Antigen-specific human antibodies from mice comprising four distinct genetic modifications. Nature 1994, 368:856-859). У этих животных были целенаправленно разрушены гены своих собственных эндогенных тяжелых и k легких цепей иммунноглобулинов и введены трансгены, представляющие собой сегменты генов тяжелых и k легких цепей человека. Оказалось, что репертуар генов человека может быть использован мышиной иммунной системой для создания высокоспецифичных и высокоаффинных антител к большему разнообразию антигенов. Несмотря на то, что трансгенные мыши экспрессируют B-клеточные рецепторы, которые по существу являются гибридными мышиных и человеческих (человеческий иммуноглобулин, мышиные Igα, Igβ и другие сигнальные молекулы), их B-клетки нормально развиваются и созревают.
В некоторых случаях может также быть предпочтительным изменение одного или более остатков аминокислот CDR-участков с целью повышения аффинности связывания с целевым эпитопом. Это известно, как «созревание аффинности» и в некоторых случаях может выполняться в связи с гуманизацией, например, в ситуациях, когда гуманизация антитела приводит к снижению специфичности или аффинности связывания, и не представляется возможным в достаточной степени улучшить специфичность или аффинность связывания с помощью только обратных мутаций. Различные методы созревания аффинности известны в данной области техники, например, способ in vitro сканирующего насыщающего мутагенеза, описанный Burks et al., Proc Natl Acad Sci USA, 94:412–417 (1997), и способ пошагового in vitro созревания аффинности, предложенный Wu et al., Proc Natl Acad Sci USA 95:6037 6042 (1998).
Термин «моноклональное антитело» или «mAb» относится к антителу, которое синтезировано и выделено отдельной клональной популяцией клеток. Клональная популяция может быть клональной популяцией иммортализованных клеток. В некоторых вариантах осуществления изобретения иммортализованные клетки в клональной популяции являются гибридными клетками, гибридомами, которые обычно получают путем слияния отдельных В-лимфоцитов от иммунизированных животных с отдельными клетками лимфоцитарной опухоли. Гибридомы представляют собой тип сконструированных клеток и не встречаются в природе.
«Нативные антитела» обычно являются гетеротетрамерными гликопротеидами с молекулярной массой примерно 150000 дальтон, состоящие из двух идентичных легких (L) цепей и двух идентичных тяжелых (H) цепей. Каждая легкая цепь связана с тяжелой цепью одной ковалентной дисульфидной связью, тогда как количество дисульфидных связей между тяжелыми цепями варьирует в разных изотипах иммуноглобулинов. Каждая тяжелая и легкая цепь также имеет равномерно расположенные внутрицепочечные дисульфидные мостики. Каждая тяжелая цепь имеет на одном конце вариабельный домен (VH), за которым следует несколько константных доменов. Каждая легкая цепь имеет вариабельный домен на одном конце (VL) и константный домен на другом конце. Константный домен легкой цепи выровнен с первым константным доменом тяжелой цепи, и вариабельный домен легкой цепи выровнен с вариабельным доменом тяжелой цепи. Полагают, что конкретные аминокислотные остатки образуют поверхность раздела между вариабельными доменами легкой цепи и тяжелой цепи.
Определение «выделенный» («изолированный»), применяемое для описания различных антител по данному описанию, означает антитело, идентифицированное и выделенное и/или регенерированное из клетки или клеточной культуры, в которой оно экспрессируется. Примеси (загрязняющие компоненты) из природной среды представляют собой материалы, которые, как правило, мешают диагностическому или терапевтическому применению полипептида, и могут включать ферменты, гормоны и другие белковые или небелковые растворенные вещества. В предпочтительных вариантах изобретения антитело очищают (1) до степени, достаточной для получения по меньшей мере 15 остатков N-концевой или внутренней аминокислотной последовательности, при использовании секвенатора с вращающейся стеклянной чашечкой (секвенатора Эдмана), или (2) до гомогенности методом SDS-PAGE в невосстанавливающих или восстанавливающих условиях с применением окрашивания Кумасси бриллиантовым голубым или, предпочтительно, серебром. Выделенное антитело включает антитела in situ внутри рекомбинантных клеток, так как по меньшей мере один компонент природной среды полипептида отсутствует. Обычно выделенный полипептид получают в результате по меньшей мере одной стадии очистки.
«Выделенная» молекула нуклеиновой кислоты представляет собой молекулу нуклеиновой кислоты, которая идентифицирована и отделена от по меньшей мере одной молекулы нуклеиновой кислоты-примеси, с которой она обычно связана в естественном источнике нуклеиновой кислоты антитела. Выделенная молекула нуклеиновой кислоты отличается от той формы или набора, в которых она находится в естественных условиях. Таким образом, выделенная молекула нуклеиновой кислоты отличается от молекулы нуклеиновой кислоты, существующей в клетках в естественных условиях. Однако выделенная молекула нуклеиновой кислоты включает молекулу нуклеиновой кислоты, находящуюся в клетках, в которых в норме происходит экспрессия антитела, например, в случае, если молекула нуклеиновой кислоты имеет локализацию в хромосоме, отличную от ее локализации в клетках в естественных условиях.
Термин «эпитоп» при использовании в данном документе относится к части (детерминанте) антигена, который специфически связывается со связывающей молекулой (например, и антитело или родственная молекула, такие как биспецифичная связывающая молекула). Эпитопные детерминанты обычно состоят из химически активных поверхностных групп молекул, таких как аминокислоты или углеводы, или боковые цепи сахаров, и, как правило, имеют специфические трехмерные структурные характеристики, а также специфические характеристики зарядов. Эпитоп может быть «линейным» или «конформационным». В линейном эпитопе, все точки взаимодействия между белком (например, антиген) и взаимодействующей молекулой (такой как антитело) происходит линейно вдоль первичной аминокислотной последовательности белка. В конформационном эпитопе, точки взаимодействия происходят через аминокислотные остатки на белке, отделенные друг от друга в первичной аминокислотной последовательности. Когда желаемый эпитоп антигена определен, можно генерировать антитела к этому эпитопу с использованием методик, хорошо известных в данной области техники. Кроме того, генерация и характеристика антител или других связывающих молекул могут пролить свет на информацию о желательных эпитопах. Основываясь на этой информации, можно затем конкурентно скринировать связывающие молекулы для связывания с теми же или аналогичными эпитопами, например, путем проведения исследований конкуренции, чтобы найти связывающие молекулы, которые конкурируют за связывание с антигеном.
Термин «пептидный линкер» в настоящем документе означает любой пептид с возможностью соединения доменов с длиной в зависимости от доменов, которые он связывает между собой, содержащий любую аминокислотную последовательность. Предпочтительно пептидный линкер имеет длину более 5 аминокислот и состоит из любого набора аминокислот, выбранного из G, A, S, P, E, T, D, K.
Термин «in vitro» относится к биологическому объекту, биологическому процессу или биологической реакции вне организма, смоделированному в искусственных условиях. Например, рост клеток in vitro должен пониматься как рост клеток в среде вне организма, например, в пробирке, культуральном флаконе или микропланшете.
Термин «IС50» (50% ингибирующая концентрация) относится к концентрациям препарата, при которых измеряемая активность или отклик, например, рост или пролиферация клеток, таких как опухолевые клетки, ингибируется на 50%. Значение IС50 может оцениваться c помощью соответствующих кривых зависимости ответа от логарифма дозы, с использованием специальных статистических программ для обработки кривых.
Термин GI50 (50% ингибирование роста) относится к концентрациям препарата, при которых пролиферация клеток, таких как опухолевые клетки, ингибируется на 50%.
Термин ED50 (EC50) (50% эффективная доза/концентрация) относится к концентрациям препарата, при которых измеряемый биологический эффект достигается на 50% (может включать цитотоксичность).
Понятие «эффекторная функция» антитела относится к видам биологической активности, связанным с Fс-областью (нативной последовательностью Fc-области или с вариантами аминокислотной последовательности Fc-области) антитела, и варьируют в зависимости от изотипа антитела. Примерами эффекторных функций антитела являются: Clq- связывание; комплементзависимая цитотоксичность; связывание Fc-рецептора; антитело-зависимая клеточно-опосредованная цитотоксичность (ADCC); фагоцитоз; понижающая регуляция рецепторов клеточной поверхности (например, В-клеточного рецептора, BCR) и В-клеточная активация.
«Антитело-зависимая клеточная цитотоксичность» или «ADCC» относится к опосредованному клетками ответу, при котором неспецифичные цитотоксические клетки, которые экспрессируют рецепторы Fc (FcR) (например, природные клетки-киллеры (NK), нейтрофилы и макрофаги), узнают связанное антитело на клетке-мишени и затем вызывают лизис клетки-мишени. Первичные клетки для опосредования ADCC, NK-клетки, экспрессируют только FcγRIII, тогда как моноциты экспрессируют FcγRI, FcγRII и FcγRIII. Экспрессия FcR на гематопоэтических клетках суммирована в таблице 3 на странице 464 в публикации Ravetch and Kinet, Annu. Rev. Immunol 9: 457-92 (1991). Чтобы оценить активность в ADCC представляющей интерес молекулы можно осуществить анализы ADCC in vitro, такие как анализы, описанные в патентах США № 5500362 или 5821337. Применимые эффекторные клетки для таких анализов включают мононуклеарные клетки периферической крови (PBMC) и природные клетки-киллеры (NK). Альтернативно или дополнительно ADCC-активность представляющей интерес молекулы можно оценить in vivo, например, в животной модели, такой как модель, описанная в Clynes et al. PNAS (USA) 95: 652-656 (1998).
«Эффекторными клетками человека» являются лейкоциты, которые экспрессируют один или несколько FcR и осуществляют эффекторные функции. Предпочтительно клетки экспрессируют, по меньшей мере, FcγRIII и осуществляют ADCC-эффекторную функцию. Примеры лейкоцитов человека, которые опосредуют ADCC, включают мононуклеарные клетки периферической крови (PBMC), природные клетки-киллеры (NK), моноциты, цитотоксические T-клетки и нейтрофилы; при этом предпочтительны PBMC и NK-клетки. Эффекторные клетки могут быть выделены из их природного источника, например, из крови или PBMC, как описано в настоящей публикации.
Термины «Fc-рецептор» и «FcR» используют для описания рецептора, который связывается с Fc-областью антитела. Предпочтительным FcR является FcR человека с нативной последовательностью. Кроме того, предпочтительным FcR является FcR, который связывает IgG-антитело (гамма-рецептор), и к предпочтительным рецепторам относятся рецепторы подклассов FcγRI, FcγRII (FcγRIIa и FcγRIIb), FcγRIII (FcγRIIIa и FcγRIIIb), включая различные аллели и альтернативно сплайсируемые формы указанных рецепторов. FcγRI проявляет высокую аффинность к IgG, тогда как FcγRII и FcγRIII проявляют более слабую аффинность. FcγRIIa и FcγRIIIa представляют собой активирующие FcγR, которые экспрессированы на моноцитах/макрофагах и моноцитах/макрофагах/естественных киллерных клетках, соответственно, и могут запускать цитотоксичность мишеней человека. Активирующий рецептор FcγRIIA содержит в своем цитоплазматическом домене основанный на тирозине мотив активации иммунорецептора (ITAM). Ингибирующий рецептор FcγRIIB содержит в своем цитоплазматическом домене основанный на тирозине мотив ингибирования иммунорецептора (ITIM) (см. обзор в Daëron, Annu. Rev. Immunol. 15: 203-234 (1997)). Обзор, посвященный FcR, представлен в Ravetch and Kinet, Annu. Rev. Immunol 9: 457-92 (1991). Другие FcR, включая FcR, которые будут идентифицированы в будущем, включены в настоящем описании в термин «FcR». Термин также включает неонатальный рецептор, FcRn, который отвечает за перенос материнских IgG в плод.
«Комплемент-зависимая цитотоксичность» или «CDC» относится к способности молекулы лизировать мишень в присутствии комплемента. Путь активации комплемента инициируется связыванием первого компонента системы комплемента (C1q) с молекулой (например, антителом) в комплексе со своим антигеном. Чтобы оценить активацию комплемента можно осуществить анализ CDC, например, как описано в Gazzano-Santoro et al., J. Immunol. Methods 202: 163 (1996).
Термин «идентичность» или «гомологичность» следует толковать как означающее процентное содержание остатков аминокислот в кандидатной последовательности, которые идентичны остаткам соответствующей последовательности, с которой ее сравнивают, после сравнения последовательностей и введения «брешей», если необходимо достичь максимального процента идентичности для полной последовательности и не учитывая любые консервативные замещения как часть идентичности последовательности. Ни N- или С-концевой удлиняющей, ни инсерционные сегменты не следует толковать как уменьшающие идентичность или гомологичность. Методы и компьютерные программы для сравнения хорошо известны. Идентичность последовательности можно определить, используя программное обеспечение для анализа последовательности (например, Sequence Analysis Software Package, Genetics Computer Group, University of Wisconsin Biotechnology Center, 1710 University Ave., Madison, WI 53705). Данное программное обеспечение подходит для подобных последовательностей путем определения степени гомологичности для разнообразных замещений, делеций (элиминирований) и других модификаций.
Фразу «гомологичный», что касается полипептидной последовательности антитела, следует толковать как антитело, проявляющее по крайней мере, 70%-ную, предпочтительно 80%-ную, более предпочтительно 90%-ную и наиболее предпочтительно 95%-ную идентичность последовательности относительно полипептидной последовательности. Термин в отношении последовательности нуклеиновой кислоты следует толковать как последовательность нуклеотидов, проявляющих, по крайней мере, 85%-ную, предпочтительно 90%-ную, более предпочтительно 95%-ную и наиболее предпочтительно 97%-ную идентичность последовательности относительно последовательности нуклеиновой кислоты.
Предлагается модификация(и) аминокислотных последовательностей антител, описанных в настоящей публикации. Например, может быть желательным улучшение аффинности связывания и/или других биологических свойств антитела. Варианты аминокислотной последовательности антитела получают введением соответствующих изменений нуклеотидов в нуклеиновую кислоту антитела или пептидным синтезом. Такие модификации включают, например, делеции, и/или инсерции, и/или замены остатков в аминокислотных последовательностях антитела. Осуществляют любое сочетание делеции, инсерции и замены, чтобы получить конечную конструкцию, при условии, что конечная конструкция обладает требуемыми характеристиками. Изменения аминокислот также могут изменять посттрансляционные процессы в антителе, такие как изменение количества или положения сайтов гликозилирования.
Вариант модификации аминокислотных последовательностей антител с помощью аминокислотных замен. Такой вариант представляет собой замену, по меньшей мере, одного аминокислотного остатка в молекуле антитела на другой остаток. Места, представляющие наибольший интерес для мутагенеза путем замен, включают гипервариабельные области или CDR, но также предполагаются изменения и в области FR или Fc. Консервативные замены показаны в таблице А под заголовком «предпочтительные замены». Если такие замены приводят к изменению биологической активности, то могут быть введены дополнительные существенные изменения, названные «примерами заменам» в таблице А, или изменения, дополнительно описанные ниже при описании классов аминокислот, и может быть проведен скрининг продуктов.
Термины «нуклеиновая кислота», «нуклеиновая последовательность» или «нуклеиновокислотная последовательность», «полинуклеотид», «олигонуклеотид», «полинуклеотидная последовательность» и «нуклеотидная последовательность», которые используются равнозначно в данном описании, обозначают четкую последовательность нуклеотидов, модифицированных или не модифицированных, определяющую фрагмент или участок нуклеиновой кислоты, содержащую или не содержащую неприродные нуклеотиды и являющуюся либо двухцепочечной ДНК или РНК, либо одноцепочечной ДНК или РНК, либо продуктами транскрипции указанных ДНК.
Здесь также следует упомянуть, что данное изобретение не относится к нуклеотидным последовательностям в их природной хромосомной среде, т.е. в природном состоянии. Последовательности данного изобретения были выделены и/или очищены, т.е. были взяты прямо или косвенно, например, путем копирования, при этом их среда была по меньшей мере частично модифицирована. Таким образом, также здесь следует подразумевать изолированные нуклеиновые кислоты, полученные путем генетической рекомбинации, например, с помощью принимающих клеток (клеток-хозяев), или полученные путем химического синтеза.
Ссылка на нуклеотидную последовательность охватывает его комплемент, если не указано иное. Таким образом, ссылка на нуклеиновую кислоту, имеющую определенную последовательность следует понимать, как охватывающие ее комплементарную цепь с ее комплементарной последовательностью.
Выражение «контролирующие последовательности» относится к последовательностям ДНК, необходимым для экспрессии функционально связанной кодирующей последовательности в определенном организме-хозяине. Пригодные для прокариот контролирующие последовательности представляют собой, например, промотор, необязательно оператор и сайт связывания рибосомы. Как известно, в эукариотических клетках присутствуют промоторы, сигналы полиаденилирования и энхансеры.
Нуклеиновая кислота «функционально связана», если она находится в функциональной связи с другой нуклеотидной последовательностью. Например, ДНК предпоследовательности или секреторной лидерной последовательности функционально связывают с ДНК полипептида, если он экспрессируется в виде предпротеина, который принимает участие в секреции полипептида; промотор или энхансер функционально связывают с кодирующей последовательностью, если он оказывает воздействие на транскрипцию последовательности; сайт связывания рибосомы функционально связывают с кодирующей последовательностью, если он расположен так, что может облегчать трансляцию. Как правило, «функционально связан» обозначает, что связанные последовательности ДНК являются смежными, а в случае секреторной лидерной последовательности являются смежными и находятся в фазе считывания. Однако энхансеры не обязательно должны быть смежными.
Термин «вектор» при использовании в настоящем документе означает молекулу нуклеиновой кислоты, способную транспортировать другую нуклеиновую кислоту, с которой она соединена. В некоторых вариантах осуществления изобретения вектор представляет собой плазмиду, т.е. кольцевую двухцепочечную часть ДНК, в которую могут быть лигированы дополнительные сегменты ДНК. В некоторых вариантах осуществления изобретения вектор представляет собой вирусный вектор, в котором дополнительные сегменты ДНК могут быть лигированы в вирусный геном. В некоторых вариантах осуществления изобретения векторы способны к автономной репликации в клетке-хозяине, в которую они введены (например, бактериальные векторы, имеющие бактериальный сайт инициации репликации и эписомные векторы млекопитающих). В других вариантах осуществления изобретения векторы (например, неэписомальные векторы млекопитающих) могут быть интегрированы в геном клетки-хозяина при введении в клетку-хозяина, и таким образом реплицируются вместе с геном хозяина. Более того, некоторые векторы способны направлять экспрессию генов, с которыми они функционально соединены. Такие векторы упоминаются в данном документе как «рекомбинантные экспрессирующие векторы» (или просто «экспрессирующие векторы»).
Термин «рекомбинантная клетка-хозяин» (или просто «клетка-хозяин») при использовании в данном документе означает клетку, в которую введен рекомбинантный экспрессионный вектор. Настоящее изобретение относится к клеткам-хозяевам, которые могут включать, например, вектор в соответствии с настоящим изобретением, описанным выше. Настоящее изобретение относится также к клеткам-хозяевам, которые включают, например, нуклеотидную последовательность, кодирующую тяжелую цепь или ее антигенсвязывающие части, нуклеотидную последовательность, кодирующую легкую цепь или ее антигенсвязывающие части, или обе из них, первого связывающего домена и/или второго связывающего домена связывающей молекулы по данному изобретению. Следует понимать, что «рекомбинантная клетка-хозяин» и «клетка-хозяин» означают не только конкретную заявленную клетку, но также и потомство такой клетки. Поскольку модификации могут проходить в последующих поколениях вследствие мутации или воздействий окружающей среды, такое потомство не может, на самом деле, быть идентичным родительской клетке, но такие клетки по-прежнему включены в объем термина «клетка-хозяин» при использовании в настоящем документе.
Термин «эксципиент» используется в данном документе для описания любого ингредиента, отличающегося от соединения(-ий) по данному изобретению.
«Фармацевтическая композиция» обозначает композицию, включающую в себя антитело согласно изобретению и, по крайней мере, один из компонентов, выбранных из группы, состоящей из фармацевтически приемлемых и фармакологически совместимых наполнителей, растворителей, разбавителей, носителей, вспомогательных, распределяющих и воспринимающих средств, средств доставки, таких как консерванты, стабилизаторы, наполнители, измельчители, увлажнители, эмульгаторы, суспендирующие агенты, загустители, подсластители, отдушки, ароматизаторы, антибактериальные агенты, фунгициды, лубриканты, регуляторы пролонгированной доставки, выбор и соотношение которых зависит от природы и способа назначения и дозировки. Примерами суспендирующих агентов являются этоксилированный изостеариловый спирт, полиоксиэтилен, сорбитол и сорбитовый эфир, микрокристаллическая целлюлоза, метагидроксид алюминия, бентонит, агар-агар и трагакант, а также смеси этих веществ. Защита от действия микроорганизмов может быть обеспечена с помощью разнообразных антибактериальных и противогрибковых агентов, например, таких как парабены, хлорбутанол, сорбиновая кислота и подобные им соединения. Композиция может включать также изотонические агенты, например, сахара, полиолы, хлористый натрий и им подобные. Пролонгированное действие композиции может быть обеспечено с помощью агентов, замедляющих абсорбцию активного начала, например, моностеарат алюминия и желатин. Примерами подходящих носителей, растворителей, разбавителей и средств доставки являются вода, этанол, полиспирты, а также их смеси, растительные масла (такие, как оливковое масло) и инъекционные органические сложные эфиры (такие, как этилолеат). Примерами наполнителей являются лактоза, молочный сахар, цитрат натрия, карбонат кальция, фосфат кальция и им подобные. Примерами измельчителей и распределяющих средств являются крахмал, альгиновая кислота и ее соли, силикаты. Примерами лубрикантов являются стеарат магния, лаурилсульфат натрия, тальк, а также полиэтиленгликоль с высоким молекулярным весом. Фармацевтическая композиция для перорального, сублингвального, трансдермального, внутриглазного, внутримышечного, внутривенного, подкожного, местного или ректального введения активного начала, одного или в комбинации с другим активным началом, может быть введена животным и людям в стандартной форме введения в виде смеси с традиционными фармацевтическими носителями. Пригодные стандартные формы введения включают пероральные формы, такие как таблетки, желатиновые капсулы, пилюли, порошки, гранулы, жевательные резинки и пероральные растворы или суспензии, сублингвальные и трансбуккальные формы введения, аэрозоли, имплантаты, местные, трансдермальные, подкожные, внутримышечные, внутривенные, интраназальные или внутриглазные формы введения и ректальные формы введения.
«Лекарственное средство (препарат)» - вещество (или смесь веществ в виде фармацевтической композиции) в виде таблеток, капсул, растворов, мазей и др. готовых форм, предназначенное для восстановления, исправления или изменения физиологических функций у человека и животных, а также для лечения и профилактики болезней, диагностики, анестезии, контрацепции, косметологии и прочего.
Термин «заболевание или нарушение, опосредованное CD47 и PD-L1», подразумевает все заболевания или нарушения, которые либо прямо, либо косвенно связаны с CD47 и PD-L1, включая этиологию, развитие, прогресс, персистентность или патологию заболевания или нарушения. «Лечить», «лечение» и «терапия» относятся к методу смягчения или устранения биологического расстройства и/или по меньшей мере одного из сопутствующих ему симптомов. Используемый в данном документе термин «облегчить» болезнь, заболевание или состояние, означает уменьшение тяжести и/или частоты возникновения симптомов заболевания, расстройства или состояния. Кроме того, содержащиеся в данном документе ссылки на «лечение» включает ссылки на лечебную, паллиативную и профилактическую терапию.
В одном аспекте субъект лечения или пациент является млекопитающим, предпочтительно человеческим субъектом. Вышеупомянутый субъект может быть мужского или женского пола любого возраста.
Термин «нарушение» означает любое состояние, которое можно улучшить в результате лечения по настоящему изобретению. В определение данного термина входят хронические и острые нарушения или заболевания, включающие в себя патологические состояния, которые вызывают предрасположенность млекопитающего к возникновению данного нарушения. Предпочтительным подлежащим лечению нарушением согласно изобретению, является рак.
Термины "рак" или "раковый" относятся к физиологическому состоянию или описывают физиологическое состояние у млекопитающих, которое, как правило, характеризуется нерегулируемым(/-ой) ростом/пролиферацией клеток. Это определение охватывает доброкачественные и злокачественные раковые заболевания. Примеры раковых заболеваний включают, но без ограничения, карциному, лимфому, бластому, саркому и лейкоз. Более конкретные примеры таких раковых заболеваний включают плоскоклеточный рак, мелкоклеточный рак легкого, немелкоклеточный рак легкого, аденокарциному легкого, плоскоклеточную карциному легкого, рак брюшины, печеночноклеточный рак, рак желудка, включая рак ЖКТ, рак поджелудочной железы, глиобластому, глиому, цервикальный рак, рак яичника, рак печени, рак мочевого пузыря, рак молочной железы, рак толстой кишки, колоректальный рак, карциному эндометрия и матки, карциному слюнных желез, рак почки (почечноклеточную карциному), рак предстательной железы (рак простаты), рак наружных женских половых органов, рак щитовидной железы, печеночную карциному, карциному анального канала, карциному пениса, меланому и различные типы рака головы и шеи.
Термины «иммунный ответ», «аутоиммунная реакция», «аутоиммунное воспаление» относятся, например, к действию лимфоцитов, антиген-представляющих клеток, фагоцитирующих клеток, гранулоцитов и растворимых макромолекул, вырабатываемых указанными клетками или клетками печени (включая антитела, цитокины и комплемент, образующиеся в результате селективного повреждения, разрушения или элиминации из человеческого организма инвазивных патогенов, клеток или тканей, инфицированных патогенами, раковых клеток или, в случаях аутоиммунитета или патологического воспаления, нормальных человеческих клеток или тканей).
«Терапевтически эффективным количеством» считается количество вводимого в процессе лечения терапевтического агента, которое избавит в определенной степени от одного или нескольких симптомов заболевания, по поводу которого проводится лечение.
Понятие «хроническое» применение относится к непрерывному (продолжительному) применению агента(ов) в противоположность острому (кратковременному) пути введения, так чтобы поддерживать первоначальное терапевтическое действие (активность) в течение длительного периода времени.
«Прерывистое» применение обозначает лечение, которое не осуществляют последовательно без перерывов, но которое скорее по своей природе является периодическим.
В настоящем описании и в последующей формуле изобретения, если контекстом не предусмотрено иное, слова «иметь», «включать» и «содержать» или их вариации, такие как «имеет», «имеющий», «включает», «включающий», «содержит» или «содержащий», следует понимать, как включение указанного целого или группы целых, но не исключение любого другого целого или группы целых.
Подробное описание изобретения
Антитело
Настоящее изобретение относится к антителам, которые связывают с CD47 и PD-L1.
В одном из вариантов осуществления настоящее изобретения антитело представляет собой полноразмерное антитело или его антигенсвязывающий фрагмент
В одном из вариантов осуществления настоящее изобретения антитело включает один или два сайта связывания с PD-L1.
В одном из вариантов осуществления настоящее изобретение сайт связывания с CD47 ингибирует взаимодействие CD47 рецептор и SIRPα лиганда, и/или сайт связывания с PD-L1 ингибирует взаимодействие PD-L1 с PD-1 рецептором.
В одном из вариантов осуществления настоящее изобретение относится к антителу, которое связывает CD47 и PD-L1, и сайт связывания с CD47 которого включает вариабельную область тяжелой цепи, содержащую:
(a) CDR1 с аминокислотной последовательностью по меньшей мере на 80% или 90% гомологичной или идентичной последовательности, выбранной из группы SEQ ID NO: 1 – 4, то есть CDR1 представляет собой последовательность, выбранную из группы SEQ ID NO: 1 - 4 или последовательность, выбранную из группы SEQ ID NO: 1 - 4 с 1 или 2 заменами;
(b) CDR2 с аминокислотной последовательностью по меньшей мере на 80%, 84%, 86%, 88%, 92% или 96% гомологичной или идентичной последовательности, выбранной из группы SEQ ID NO: 6 - 15, то есть CDR2 представляет собой последовательность SEQ ID NO: 6 - 15 или последовательность, выбранную из группу SEQ ID NO: 6 - 15 с 1, 2, 3, 4 или 5 заменами;
(c) CDR3 с аминокислотной последовательностью по меньшей мере на 80%, 85%, 86% 90%, 93% или 95%гомологичной или идентичной последовательности, выбранной из группы SEQ ID NO: 17 - 20, то есть CDR3 представляет собой последовательность, выбранную из группы SEQ ID NO: 17 - 20 или последовательность, выбранную из группы SEQ ID NO: 17 - 20 с 1, 2 или 3 заменами.
В одном из вариантов осуществления настоящее изобретение относится к антителу, которое связывает CD47 и PD-L1, и сайт связывания с CD47 которого включает вариабельную область тяжелой цепи, содержащую:
(d) CDR1 с аминокислотной последовательностью идентичной последовательности, выбранной из группы SEQ ID NO: 1 - 4;
(e) CDR2 с аминокислотной последовательностью идентичной последовательности, выбранной из группы SEQ ID NO: 6 - 15;
(f) CDR3 с аминокислотной последовательностью идентичной последовательности, выбранной из группы SEQ ID NO: 17 - 20.
В одном из вариантов осуществления настоящее изобретение относится к антителу, которое связывает CD47 и PD-L1, и включает сайт связывания с CD47 содержащий:
(a) вариабельную область тяжелой цепи, содержащую:
(i) CDR1 с аминокислотной последовательностью по меньшей мере на 80% или 90% гомологичной или идентичной последовательности, выбранной из группы SEQ ID NO: 1 – 4, то есть CDR1 представляет собой последовательность, выбранную из группы SEQ ID NO: 1 - 4 или последовательность, выбранную из группы SEQ ID NO: 1 - 4 с 1 или 2 заменами;
(ii) CDR2 с аминокислотной последовательностью по меньшей мере на 80%, 84%, 86%, 88%, 92% или 96% гомологичной или идентичной последовательности, выбранной из группы SEQ ID NO: 6 - 15, то есть CDR2 представляет собой последовательность SEQ ID NO: 6 - 15 или последовательность, выбранную из группы SEQ ID NO: 6 - 15 с 1, 2, 3, 4 или 5 заменами,
(iii) CDR3 с аминокислотной последовательностью по меньшей мере на 80%, 85%, 86%, 90%, 93% или 95% гомологичной или идентичной последовательности, выбранной из группы SEQ ID NO: 17 - 20, то есть CDR3 представляет собой последовательность, выбранную из группы SEQ ID NO: 17 - 20 или последовательность, выбранную из группы SEQ ID NO: 17 - 20 с 1, 2 или 3 заменами, и
(b) вариабельную область легкой цепи, содержащую:
(i) CDR1 с аминокислотной последовательностью по меньшей мере на 80% или 90%гомологичной или идентичной последовательности, выбранной из группы SEQ ID NO: 22 - 34, то есть CDR1 представляет собой последовательность, выбранную из группы SEQ ID NO: 22 - 34 или последовательность, выбранную из группы SEQ ID NO: 22 - 34 с 1 или 2 заменами,
(ii) CDR2 с аминокислотной последовательностью по меньшей мере на 80%, 87% или94%гомологичной или идентичной последовательности, выбранной из группы SEQ ID NO: 36 - 48, то есть CDR2 представляет собой последовательность, выбранную из группы SEQ ID NO: 36 - 48 или последовательность, выбранную из группы SEQ ID NO: 36 - 48 с 1, 2 или 3 заменами,
(iii) CDR3 с аминокислотной последовательностью по меньшей мере на 80%или 90% гомологичной или идентичной последовательности, выбранной из группы SEQ ID NO: 50 – 64, то есть CDR3 представляет собой последовательность, выбранную из группы SEQ ID NO: 50 - 64 или последовательность, выбранную из группы SEQ ID NO: 50 - 64 с 1 или 2 заменами.
В одном из вариантов осуществления настоящее изобретение относится к антителу, которое связывает CD47 и PD-L1, и включает сайт связывания с CD47 содержащий:
(a) вариабельную область тяжелой цепи, содержащую:
(i) CDR1 с аминокислотной последовательностью, выбранной из группы SEQ ID NO: 1 - 4,
(ii) CDR2 с аминокислотной последовательностью, выбранной из группы SEQ ID NO: 6 - 15,
(iii) CDR3 с аминокислотной последовательностью, выбранной из группы SEQ ID NO: 17 - 20, и
(b) вариабельную область легкой цепи, содержащую:
(i) CDR1 с аминокислотной последовательностью, выбранной из группы SEQ ID NO: 22 - 34,
(ii) CDR2 с аминокислотной последовательностью, выбранной из группы SEQ ID NO: 36 - 48,
(iii) CDR3 с аминокислотной последовательностью, выбранной из группы SEQ ID NO: 50 - 64.
В одном из вариантов осуществления настоящее изобретение относится к антителу, которое связывает CD47 и PD-L1, и включает сайт связывания с CD47 содержащий:
(a) вариабельную область тяжелой цепи с аминокислотной последовательностью по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологичной или идентичной последовательности, выбранной из группы SEQ ID NO: 66 - 88, и
(b) вариабельную область легкой цепи с аминокислотной последовательностью по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологичной или идентичной последовательности, выбранной из группы SEQ ID NO: 89 - 106.
В одном из вариантов осуществления настоящее изобретение относится к антителу, которое связывает CD47 и PD-L1, и включает сайт связывания с CD47 содержащий:
(a) вариабельную область тяжелой цепи с аминокислотной последовательностью, выбранной из группы SEQ ID NO: 66 - 88, и
(b) вариабельную область легкой цепи с аминокислотной последовательностью, выбранной из группы SEQ ID NO: 89 - 106.
В одном из вариантов осуществления настоящее изобретение относится к антителу, которое связывает CD47 и PD-L1, и включает сайт связывания с PD-L1 содержащий:
(a) вариабельную область тяжелой цепи, содержащую:
(i) CDR1 с аминокислотной последовательностью по меньшей мере на 80%гомологичной или идентичной последовательности SEQ ID NO: 5, то есть CDR1 представляет собой последовательность SEQ ID NO: 5 или последовательность SEQ ID NO: 5 с 1 заменой;
(ii) CDR2 с аминокислотной последовательностью по меньшей мере на 80%, 86% или 92% гомологичной или идентичной последовательности SEQ ID NO: 16, то есть CDR2 представляет собой последовательность SEQ ID NO: 16 или последовательность SEQ ID NO: 16 с 1, 2 или 3 заменами; (iii) CDR3 с аминокислотной последовательностью по меньшей мере на 80%, или 90% гомологичной или идентичной последовательности SEQ ID NO: 21, то есть CDR3 представляет собой последовательность SEQ ID NO: 21 или последовательность SEQ ID NO: 21 с 1 или 2 заменами, и
(b) вариабельную область легкой цепи, содержащую:
(i) CDR1 с аминокислотной последовательностью по меньшей мере на 80%, 86% или 83% гомологичной или идентичной последовательности SEQ ID NO: 35, то есть CDR1 представляет собой последовательность SEQ ID NO: 35 или последовательность SEQ ID NO: 35 с 1, 2 или 3 заменами;
(ii) CDR2 с аминокислотной последовательностью по меньшей мере на 80%% гомологичной или идентичной последовательности SEQ ID NO: 49, то есть CDR2 представляет собой последовательность SEQ ID NO: 49 или последовательность SEQ ID NO: 49 с 1 заменой;(iii) CDR3 с аминокислотной последовательностью по меньшей мере на 80% или 90% гомологичной или идентичной последовательности SEQ ID NO: 65, то есть CDR3 представляет собой последовательность SEQ ID NO: 65 или последовательность SEQ ID NO: 65 с 1 или 2 заменами.
В одном из вариантов осуществления настоящее изобретение относится к антителу, которое связывает CD47 и PD-L1, и включает сайт связывания с PD-L1 содержащий:
(a) вариабельную область тяжелой цепи, содержащую:
(i) CDR1 с аминокислотной последовательностью SEQ ID NO: 5,
(ii) CDR2 с аминокислотной последовательностью SEQ ID NO: 16,
(iii) CDR3 с аминокислотной последовательностью SEQ ID NO: 21, и
(b) вариабельную область легкой цепи, содержащую:
(i) CDR1 с аминокислотной последовательностью SEQ ID NO: 35,
(ii) CDR2 с аминокислотной последовательностью SEQ ID NO: 49,
(iii) CDR3 с аминокислотной последовательностью SEQ ID NO: 65.
В одном из вариантов осуществления настоящее изобретение относится к антителу, которое связывает CD47 и PD-L1, характеризуется тем, что сайт связывания с CD47 представляет собой Fab, scFv, scFab или изолированные монодомены VH или VHH.
В одном из вариантов осуществления настоящее изобретение относится к антителу, которое связывает CD47 и PD-L1, характеризуется тем, что сайт связывания с PD-L1 представляет собой Fab, scFv, scFab или изолированные монодомены VH или VHH.
В одном из вариантов осуществления настоящее изобретение относится к антителу, которое связывает CD47 и PD-L1, характеризуется тем, что оно вызывает антитело-зависимой клеточной цитотоксичностью, макрофаг-опосредованный фагоцитоз, комплемент-зависимую цитотоксичность и/или опосредованную T-клетками цитотоксичность в отношении клеток, несущих на поверхности антигены CD47 и/или PD-L1.
В одном из вариантов осуществления настоящее изобретение относится к антителу, которое связывает CD47 и PD-L1, характеризуется тем, что оно содержит Fc-фрагмент по меньшей мере с одной мутацией или модификацией, которая повышает антитело-зависимую клеточно-опосредованную цитотоксичность (ADCC) и/или комплемент-зависимую цитотоксичность (CDC) по сравнению с той же антитело без мутации или модификации.
Молекулы нуклеиновых кислот
Настоящее изобретение также относится к молекулам нуклеиновых кислот, и последовательностям, кодирующим антитело к CD47 и PD-L1 по данному изобретению, описанным в данном документе. В некоторых вариантах осуществления изобретения различные молекулы нуклеиновых кислот кодируют первый домен и второй домен аминокислотной последовательности антитела к CD47 и PD-L1. Там, где первый домен и/или второй домен содержит тяжелую цепь и легкую цепь, в некоторых вариантах осуществления изобретения различные нуклеиновые кислоты кодируют тяжелую цепь и аминокислотные последовательности легкой цепи. В других вариантах осуществления изобретения та же молекула нуклеиновой кислоты кодирует последовательность тяжелой цепи и легкой цепи. В определенных вариантах осуществления изобретения молекула нуклеиновой кислоты может кодировать любую комбинацию из аминокислотных последовательностей (например, последовательности тяжелой и легкой цепи) первого и второго домена. В конкретном варианте осуществления изобретения молекула нуклеиновой кислоты может кодировать аминокислотную последовательность первого связывающего домена и аминокислотную последовательность легкой цепи второго связывающего домена, необязательно включающей любую последовательность соединяющего их пептидного линкера. Ссылка на нуклеотидную последовательность, охватывает его комплемент, если не указано иное. Таким образом, ссылка на нуклеиновую кислоту, имеющую определенную последовательность следует понимать, как охватывающие ее комплементарную цепь с ее комплементарной последовательностью. Термин «полинуклеотид», упоминаемый в данном документе, означает полимерную форму нуклеотидов, по меньшей мере 10 оснований в длину, либо рибонуклеотидов, либо дезоксинуклеотидов или модифицированную форму любого типа нуклеотида. Термин включает в себя одно- и двухцепочечные формы.
В любом из указанных выше вариантах осуществления изобретения молекулы нуклеиновых кислот могут быть выделенными.
Молекула нуклеиновой кислоты по данному изобретению может быть выделена из любого источника, который продуцирует антитело к CD47 и PD-L1. В определенных вариантах осуществления изобретения молекула нуклеиновой кислоты данному изобретению может быть синтезирована, а не выделена.
В некоторых вариантах осуществления изобретения молекула нуклеиновой кислоты по данному изобретению может содержать нуклеотидную последовательность, кодирующую VH домен из первого или второго домена антитела по данному изобретению, соединенного в рамках считывания с нуклеотидной последовательности, кодирующей константный домен тяжелой цепи из любого источника. Аналогичным образом, молекула нуклеиновой кислоты по данному изобретению может содержать нуклеотидную последовательность, кодирующую VL домен из первой или второй области антитела по данному изобретению, объединенной в рамках считывания с нуклеотидной последовательностью, кодирующей константный домен легкой цепи из любого источника.
В еще одном аспекте настоящего изобретения молекулы нуклеиновой кислоты, кодирующие вариабельный домен тяжелой (VH) и/или легкой (VL) цепей первого или второго связывающего домена, могут «преобразовываться» по всей длине генов антитела. В одном варианте осуществления изобретения молекулы нуклеиновых кислот, кодирующие домены VH или VL преобразуются в гены антитела по всей длине путем вставки в экспрессионный вектор, уже кодирующей константные домены тяжелой цепи (СН) или легкой цепи (CL), соответственно, так что VH сегмент функционально соединен с CH сегментом(-ами) в векторе и/или VL сегмент оперативно соединен с CL сегментом в векторе. В другом варианте осуществления изобретения молекулы нуклеиновых кислот, кодирующие VH и/или VL домены преобразуются в гены по всей длине антитела путем соединения, например, лигирования, молекулы нуклеиновой кислоты, кодирующей VH и/или VL домены, к молекуле нуклеиновой кислоты, кодирующей CH и/или CL домены с использованием стандартных молекулярно-биологических методов. Молекулы нуклеиновых кислот, кодирующие по всей длине тяжелую и/или легкую цепи, могут затем экспрессироваться в клетке, в которую они были введены.
Молекулы нуклеиновой кислоты могут использоваться для экспрессии большого количества рекомбинантных антител к CD47 и PD-L1. Молекулы нуклеиновой кислоты могут использоваться для получения человеческих антител, гуманизированных антител, химерных антител, биспецифических антител, одноцепочечных антител, иммуноадгезинов, диател, мутировавших антител и производных антител, как описано в настоящем документе.
Вектор
В еще одном аспекте настоящее изобретение относится к вектору, подходящему для экспрессии любой из нуклеотидных последовательностей, описанных в настоящем документе.
Настоящее изобретение относится к векторам, содержащим молекулы нуклеиновых кислот, которые кодируют любую из аминокислотных последовательностей антител к CD47 и PD-L1 или их частей (например, последовательностей тяжелой цепи первого и/или тяжелой и/или легкой цепи второго связывающих доменов) как описано в настоящем документе. Настоящее изобретение далее относится к векторам, содержащим молекулы нуклеиновых кислот, кодирующих слитые белки, модифицированные антитела, фрагменты антител.
В другом варианте осуществления изобретения молекулы нуклеиновых кислот и векторы могут быть использованы для изготовления мутировавших антител к CD47 и PD-L1. Антитела могут мутировать в вариабельных доменах тяжелой и/или легкой цепей первого и/или тяжелой и/или легкой цепей второго связывающего домена, например, для изменения связывающей способности антител. Например, мутация может произойти в одном или нескольких CDR-участках, чтобы увеличить или уменьшить KD антител, чтобы увеличить или уменьшить koff или изменить специфичность связывания антитела в отношении FcRn. В другом варианте осуществления изобретения одной или более мутациям подвергнут аминокислотный остаток, который, как известно, изменен по сравнению с зародышевой линией в антителе, соответствующем первому или второму связывающему домену антитела к CD47 и PD-L1 по данному изобретению. Эти мутации могут быть сделаны в CDR-участке или каркасном участке вариабельного домена, или в константном домене. В предпочтительном варианте осуществления изобретения мутации произведены в вариабельном домене. В другом варианте осуществления изобретения одной или нескольким мутациям подвергнут аминокислотный остаток, который, как известно, изменен по сравнению с зародышевой линией в CDR-участке или каркасном участке вариабельного домена антитела по данному изобретению.
В некоторых вариантах осуществления изобретения, антитела к CD47 и PD-L1 по данному изобретению экспрессируются путем вставки ДНК, кодирующей частично или полностью последовательность первого и второго связывающего домена (например, последовательности тяжелой и легкой цепи, где связывающий домен содержит последовательности тяжелой и легкой цепи), полученный, как описано выше, в экспрессионных векторах таким образом, что гены функционально соединены с необходимыми последовательностями, контролирующими экспрессию, такими как транскрипционные и трансляционные контрольные последовательности. Экспрессионные векторы включают плазмиды, ретровирусы, аденовирусы, аденоассоциированные вирусы (AAV), вирусы растений, такие как вирус мозаики цветной капусты, вирусы табачной мозаики, космиды, YAC, EBV полученные эписомы и тому подобное. Молекулы ДНК могут быть лигированы в вектор таким образом, что последовательности, контролирующие транскрипцию и трансляцию в векторе, выполняют предусмотренную функцию регуляции транскрипции и трансляции ДНК. Экспрессионный вектор и последовательности контроля экспрессии могут быть выбраны таким образом, чтобы быть совместимыми с используемой экспрессирующей клеткой-хозяином. Молекулы ДНК, кодирующие частично или по всей длине последовательности первого и второго связывающих доменов (например, последовательности тяжелой и легкой цепи, где связывающий домен содержит последовательность тяжелой и легкой цепи) могут быть введены в отдельные векторы. В одном варианте осуществления изобретения любая комбинация указанных выше молекул ДНК вводится в тот же экспрессионный вектор. Молекулы ДНК могут быть введены в экспрессионный вектор стандартными способами (например, лигированием комплементарных сайтов рестрикции на фрагменте гена антитела и вектора или лигированием тупых концов, если сайты рестрикции отсутствуют).
Подходящим вектором является тот, который кодирует функционально законченные последовательности CH или CL человеческого иммуноглобулина с конструированием соответствующего места рестрикции так, что любая последовательность VH или VL может быть легко включена и экспрессирована, как описано выше. HC - и LC-кодирование генов в таких векторах может содержать интронные последовательности, что приводит к общему увеличению белковых продуктов антитела путем стабилизации, соответствующей мРНК. Интронные последовательности находятся в окружении сплайс-донора и сплайс-акцептора сайтов, которые определяют, где будет происходить сплайсинг РНК. Расположение интронных последовательностей может быть либо в вариабельных или константных участках цепей антитела, или как в вариабельных, так и константных участках, когда используются несколько интронов. Прекращение полиаденилирования и транскрипции может произойти вниз по ходу сайта нативной хромосомы кодируемых участков. Рекомбинантный экспрессионный вектор также может кодировать сигнальный пептид, который облегчает выработку цепочки антитела клеткой-хозяином. Ген цепочки антитела может быть клонирован в вектор таким образом, что сигнальный пептид соединен с рамкой считывания аминоконца цепи иммуноглобулина. Сигнальным пептидом может быть сигнальный пептид иммуноглобулина или гетерологичный сигнальный пептид (то есть, сигнальный пептид белка не иммуноглобулиновой природы).
Помимо цепочки генов антител, рекомбинантный экспрессионный вектор по данному изобретению может нести регулирующие последовательности, которые контролируют экспрессию генов цепи антител в клетке-хозяине. Специалистам в этой области будет понятно, что дизайн экспрессионного вектора, включая выбор регулирующих последовательностей, может зависеть от таких факторов, как селекция клетки-хозяина для трансформации, уровень экспрессии желаемого белка, и т.д. Предпочтительные регулирующие последовательности для экспрессирующей клетки-хозяина млекопитающих включают вирусные элементы обеспечивающие высокий уровень экспрессии белков в клетках млекопитающих, таких как промоторы и/или энхансеры, полученные из ретровирусной LTR, цитомегаловируса (CMV) (например, CMV промотора/энхансера), обезьяньего вируса 40 (SV40) (например, SV40 промотора/энхансера), аденовируса, (например, большого позднего промотора аденовируса (AdMLP)), вирус полиомы, а также сильных промоторов млекопитающих, таких как промотор нативных иммуноглобулинов или промотор актина. Для дальнейшего описания вирусных регулирующих элементов и их последовательностей см., например, патенты США 5,168,062, 4,510,245 and 4,968,615. Способы экспрессии связывающих молекул, таких как антитела растений, в том числе описание промоторов и векторов, а также трансформация растений, известны в данной области техники. См., например, патент США 6,517,529. Методы экспрессии полипептидов в бактериальных клетках или клетках грибов, например, дрожжевых клетках, также хорошо известны в данной области техники.
В дополнение к генам цепи антитела и регулирующим последовательностям, рекомбинантные векторы экспрессии изобретения могут нести дополнительные последовательности, такие как последовательности, которые регулируют репликацию вектора в клетках-хозяевах (например, точки начала репликации) и гены селектируемого маркера. Ген селектируемого маркера облегчает селекцию клеток-хозяев, в которые был введен вектор (см., например, патенты США 4,399,216, 4,634,665 и 5,179,017). Например, обычно ген селектируемого маркера придает устойчивость к лекарственным средствам, таким как G418, гигромицин или метотрексат, клетке-хозяину, в которую вектор введен. Например, гены селектируемого маркера включают ген дигидрофолат редуктазы (DHFR) (для использования в dhfr-клетках-хозяевах при селекции/амплификации метотрексата), ген нео (для селекции G418) и ген синтетазы глутамата.
Термин «последовательность контроля экспрессии», используемый в данном описании, означает полинуклеотидные последовательности, которые необходимы для воздействия на экспрессию и процессинг кодирующих последовательностей, к которым они лигированы. Контролирующие экспрессию последовательности включают соответствующие последовательности инициации транскрипции, терминации, промотора и энхансера; эффективные сигналы процессинга РНК, такие как сплайсинг и сигналы полиаденилирования; последовательности, которые стабилизируют цитоплазматическую мРНК; последовательности, которые повышают эффективность трансляции (т.е. консенсусная последовательность Козака); последовательности, которые повышают стабильность белка; и, при желании, последовательности, которые усиливают секрецию белка. Характер таких контролирующих последовательностей различается в зависимости от организма-хозяина; в прокариотах такие контролирующие последовательности, как правило, включают промотор, сайт связывания рибосомы, а также последовательности терминации транскрипции; в эукариотах, как правило, такие контролирующие последовательности включают промоторы и последовательности терминации транскрипции. Термин «контролирующие последовательности» включает, как минимум, все компоненты, наличие которых имеет важное значение для экспрессии и процессинга, и может также включать дополнительные компоненты, чье присутствие является полезным, например, лидирующие последовательности и последовательности слившихся клеток.
Клетки-хозяева
Дополнительный аспект настоящего изобретения относится к способам получения антител к CD47 и PD-L1 по данному изобретению. Один вариант осуществления изобретения относится к способу получения антител, как определено в настоящем документе, содержащему введение получение рекомбинантной клетки-хозяина, способной экспрессировать антитела, культивирование указанной клетки-хозяина в условиях, подходящих для экспрессии продукции антитела, и выделение полученного антитела. Антитело к CD47 и PD-L1, полученное такой экспрессией в таких рекомбинантных клетках-хозяевах упоминается в данном документе как «рекомбинантные антитела». Изобретение также относится к потомству клеток таких клеток-хозяев и антителам к CD47 и PD-L1, получаемым аналогично.
Молекулы нуклеиновой кислоты, кодирующие антитела к CD47 и PD-L1 по изобретению и векторы, содержащие эти молекулы нуклеиновой кислоты, могут быть использованы для трансфекции подходящего млекопитающего или его клетки, растения или его клетки, бактериальной или дрожжевой клетки-хозяина. Преобразование может происходить любым известным способом для введения полинуклеотидов в клетку-хозяина. Способы введения гетерологичных полинуклеотидов в клетки млекопитающих хорошо известны в данной области и включают декстран-опосредованную трансфекцию, трансфекцию комплексом нуклеиновой кислоты и позитивно заряженного полимера, трансфекцию преципитатом нуклеиновой кислоты и фосфата кальция, полибрен-опосредованную трансфекцию, слияние протопластов, трансфекцию инкапсулированными в липосомы полинуклеотидами и прямую микроинъекцию ДНК в ядра. В дополнение, молекулы нуклеиновых кислот могут быть введены в клетки млекопитающих вирусными векторами. Способы трансфекции клеток хорошо известны в данной области техники. См., например, патенты США, 4,399,216, 4,912,040, 4,740,461 и 4,959,455. Способы трансформации клеток растений хорошо известны в данной области, включая, например, Agrobacterium-опосредованную трансформацию, биолистическую трансформацию, прямую инъекцию, электропорацию и вирусную трансформацию. Методы трансформации клеток бактерий и дрожжей также хорошо известны в данной области.
Клеточные линии млекопитающих, используемые в качестве хозяев для трансформации, хорошо известны в данной области и включают множество иммортализованных доступных клеточных линий. К ним относятся, например, клетки яичников китайского хомячка (CHO), NS0 клетки, клетки SP2, HEK-293T клетки, 293 Фристайл клетки (Invitrogen), NIH-3T3 клетки, клетки HeLa, клетки почек хомячка (BHK), клетки почек африканских зеленых мартышек (COS), клетки гепатоцеллюлярной карциномы человека (например, Hep G2), A549 клетки и ряд других клеточных линий. Клеточные линии выбираются путем определения, какие клеточные линии имеют высокие уровни экспрессии и обеспечивают необходимые характеристики продуцируемого белка. Другими клеточными линиями, которые могут быть использованы, являются клеточные линии насекомых, такие как Sf9 или Sf21 клетки. Когда векторы рекомбинантной экспрессии, кодирующие антитела к CD47 и PD-L1, вводятся в клетки-хозяева млекопитающих, антитела продуцируются путем культивирования клеток-хозяев в течение времени, достаточного для экспрессии антител в клетках-хозяевах или, предпочтительнее, выделения антител в питательную среду, в которой выращиваются клетки-хозяева. Антитела к CD47 и PD-L1 могут быть выделены из питательной среды с использованием стандартных методов очистки белка. Клетки-хозяева растений, например, включают Nicotiana, Arabidopsis, ряску, кукурузу, пшеницу, картофель и т.д. Клетки бактерий хозяина включают виды E. coli и Streptomyces. Дрожжевые клетки-хозяева включают Schizosaccharomyces pombe, Saccharomyces cerevisiae и Pichia pastoris.
Кроме того, уровень продукции антител к CD47 и PD-L1 по данному изобретению из продуцирующей клеточной линии можно усилить с помощью ряда известных методов. Например, система экспрессии гена глутамин синтетазы (система GS) является достаточно распространенной для усиления экспрессии при определенных условиях. Система GS обсуждается в целом или частично в связи с патентами ЕР 0216846, 0256055, 0323997 и 0338841.
Вполне вероятно, что антитела к CD47 и PD-L1 различных клеточных линий или трансгенные животные будут отличаться друг от друга профилем гликозилирования. Однако все антитела к CD47 и PD-L1, кодируемые молекулами нуклеиновой кислоты, описанными в данном документе, или содержащими аминокислотные последовательности, приведенные в настоящем документе, являются частью данного изобретения, независимо от состояния гликозилирования связывающих молекул и в целом, независимо от наличия или отсутствия пост-трансляционных модификаций.
Получение антител
Изобретение относится также к способам и процессам получения антител к CD47 и PD-L1 и их антигенсвязывающих фрагментов.
Моноклональные антитела
Моноклональные антитела можно создавать, например, с помощью метода на основе гибридом, который впервые описан Kohler и др., Nature, 256, 1975, с. 495, или с помощью методов рекомбинантной ДНК (US 4816567).
При использовании метода на основе гибридом мышь или другое пригодное животное-хозяин, такое как хомячок, иммунизируют согласно описанной выше методике, для того, чтобы вызывать образование лимфоцитов, которые продуцируют или могут продуцировать антитела, обладающие способностью специфически связываться с белком, применяемым для иммунизации. Согласно другому варианту лимфоциты можно получать в результате иммунизации in vitro. После иммунизации лимфоциты выделяют и затем сливают с клеточной линией миеломы с помощью приемлемого связывающего агента, такого как полиэтиленгликоль, с получением клетки гибридомы.
Полученные таким образом клетки гибридомы высевают и выращивают в пригодной культуральной среде, которая предпочтительно содержит одно или несколько веществ, ингибирующих рост или выживание неслитых родительских клеток миеломы. Например, если родительские клетки миеломы не содержат фермента гипоксантингуанинфосфорибозилтрансферазы (HGPRT или HPRT), то культуральная среда для гибридом, как правило, должна включать гипоксантин, аминоптерин и тимидин (НАТ-среда), т.е. вещества, которые препятствуют росту клеток с дефицитом HGPRT.
Предпочтительными применяемые в качестве компонента для слияния клетками миеломы являются клетки, которые легко поддаются слиянию, поддерживают стабильный высокий уровень производства антител выбранными продуцирующими антитела клетками и чувствительны к избирательной среде, на которой происходит отбор несвязанных родительских клеток. Предпочтительными линиями клеток миелом являются линии мышиной миеломы, такие как созданные на основе мышиных линий опухолевых клеток линии МОРС-21 и МРС-11, которые можно получать из Salk Institite Cell Disrtibution Center, Сан-Диего, шт. Калифорния, США, и линии SP-2 или Х63- Ag8-653, которые можно получать из Американской коллекции типовых культур, Роквилл, шт. Мэриленд, США. Описано также применение линий клеток человеческой миеломы и гетеромиеломы типа «мышь-человек» для производства моноклональных антител (Kozbor, J. Immunol., 133, 1984, с. 3001).
Предпочтительно специфичность связывания моноклональных антител, полученных с использованием клеток гибридомы, определяют методом иммунопреципитации или с помощью анализа связывания in vitro, такого как радиоиммунный анализ (РИА) или твердофазный имммуноферментный анализ (ELISA).
Аффинность связывания моноклонального антитела можно, например, определять с помощью Скэтчард-анализа, описанного у Munson и др., Anal. Biochem., 107, 1980, с. 220.
После выявления клеток гибридомы, которые продуцируют антитела требуемой специфичности, аффинности и/или активности, клоны можно субклонировать с помощью метода лимитирующих разведений и выращивать стандартными методами. Пригодные для этой цели среды включают, например, среду DMEM или RPMI-1640. Кроме того, клетки гидрибомы можно выращивать in vivo в виде асцитных опухолей в организме животных, например, путем внутрибрюшинной (i.p.) инъекции клеток мышам.
Моноклональные антитела, секретируемые субклонами, можно отделять от культуральной среды, асцитной жидкости или сыворотки с помощью обычных методов очистки антител, например, аффинной хроматографией (например, с использованием протеин А- или протеин Q-сефарозы), или ионообменной хроматографии, хроматографии на гидроксилапатитах, гель-электрофореза, диализа и т.д.
ДНК, кодирующую моноклональные антитела, можно легко выделять и секвенировать с помощью общепринятых процедур (например, с использованием олигонуклеотидных зондов, которые обладают способностью специфически связываться с генами, кодирующими тяжелые и легкие цепи мышиных антител). В качестве предпочтительного источника такой ДНК служат клетки гибридомы. После выделения ДНК можно включать в экспрессионные векторы, которыми затем трансфектируют клетки-хозяева, такие как клетки Е. coli, обезьяньи COS- клетки, клетки яичника китайского хомячка (СНО) или клетки миеломы, которые без трансфекции не продуцируют белок антитела, что приводит к синтезу моноклональных антител в рекомбинантных клетках-хозяевах. Обзор статей о рекомбинантной экспрессии в бактериях ДНК, кодирующей антитело.
Согласно еще одному варианту осуществления изобретения моноклональные антитела или фрагменты антител можно выделять из фаговых библиотек антител, созданных с помощью методов, описанных у McCafferty и др., Nature, 348, 1990, cc. 552-554. У Clackson и др., Nature, 352, 1991, cc. 624- 628 и Marks и др., J. Mol. Biol., 222, 1991, cc. 581-597 описано выделение мышиных и человеческих антител соответственно с помощью фаговых библиотек. В последующих публикациях было описано производство высокоаффинных (нМ-диапазон) человеческих антител с помощью перестановки цепи (Marks и др., Bio/Technology, 10, 1992, cc. 779-783), а также комбинаторная инфекция и рекомбинация in vivo в качестве стратегии конструирования очень больших фаговых библиотек (Waterhouse и др., Nucl. Acids. Res., 21, 1991, cc. 2265-2266). Таким образом, эти методы представляют собой реальную альтернативу традиционным методам выделения моноклональных антител на основе гибридом моноклональных антител.
ДНК, кодирующую антитело, можно также модифицировать, например таким образом, чтобы получать химерные или слитые полипептиды антител, например, путем замены последовательностей константных областей тяжелой и легкой цепи (Сн и CL) на гомологичные мышиные последовательности (US 4816567 и Morrison и др., Proc. Natl. Acad. Sci. USA: 81, 1984, с. 6851) или с помощью ковалентного связывания кодирующей последовательности иммуноглобулина со всей или с частью кодирующей последовательности полипептида, не относящегося к иммуноглобулинам (гетерологичного полипептида). Не относящиеся к иммуноглобулинам полипептидные последовательности можно заменять на константные области антитела или заменять на вариабельные области антигенсвязывающего центра антитела, создавая химерное бивалентное антитело, которое содержит один антигенсвязывающий центр, обладающий специфичностью в отношении антигена, и другой антигенсвязывающий центр, обладающий специфичностью в отношении другого антигена.
Гуманизированные антитела
Методы создания «гуманизированных» антител животных, кроме человека, известны в данной области. Предпочтительно гуманизированное антитело имеет один или несколько встроенных в него аминокислотных остатков, полученных из источника, отличного от человека. Эти полученные из источника, отличного от человека, аминокислотные остатки часто называют «импортными» остатками, поскольку их обычно получают из «импортной» вариабельной области. Гуманизацию в целом можно осуществлять согласно методу Winter с соавторами (Jones и др., Nature, 321, 1986, сс. 522-525) путем замены последовательностей гипервариабельного участка на соответствующие последовательности человеческого антитела. Таким образом, «гуманизированные» антитела представляют собой химерные антитела (US 4816567), в которых участок, существенно меньший, чем интактная человеческая вариабельная область, заменен соответствующей последовательностью, полученной из видов кроме человека. На практике гуманизированные антитела представляют собой, как правило, человеческие антитела, в которых часть остатков гипервариабельного участка и возможно часть остатков FR заменены остатками из аналогичных участков антител грызунов.
Выбор человеческих вариабельных областей как легкой, так и тяжелой цепи, предназначенных для получения гуманизированных антител, очень важен для снижения антигенности и НАМА-ответа (человеческое антимышиное антитело), когда антитело предназначено для лечения человека. Согласно так называемому методу «наилучшего подбора» последовательность вариабельной области антитела грызунов подвергают скринингу относительно полной библиотеки известных последовательностей человеческих вариабельных областей. Человеческую последовательность V-области, которая наиболее близка к последовательности из организма грызунов, идентифицируют и внутри нее выбирают человеческий каркасный участок (FR), пригодный для применения в гуманизированном антителе (Sims и др., J. Immunol., 151, 1993, с. 2296). В другом методе используют определенный каркасный участок, полученный из консенсусной последовательности определенной подгруппы легких или тяжелых цепей всех человеческих антител. Один и тот же каркасный участок можно применять для нескольких различных гуманизированных антител (Carter и др., Proc. Natl. Acad. Sci. USA: 89, 1992, с. 4285).
Также важно, чтобы антитела были гуманизированы с сохранением высокой связывающей способности к антигену и других важных биологических свойств. Для решения этой задачи согласно предпочтительному способу гуманизированные антитела получают с помощью анализа родительских последовательностей и различных гуманизированных продуктов с использованием умозрительных трехмерных моделей родительских и гуманизированных последовательностей. Трехмерные модели иммуноглобулинов общедоступны и хорошо известны специалистам в данной области. Известны компьютерные программы, которые иллюстрируют и отображают возможные трехмерные конформационные структуры выбранных перспективных последовательностей иммуноглобулинов. Изучение этих изображений позволяет осуществлять анализ возможной роли остатков в функции перспективной последовательности иммуноглобулина, т.е. анализ остатков, которые влияют на способность перспективного иммуноглобулина связываться с антигеном. Таким путем можно выбирать остатки в FR и объединять с реципиентными и импортными последовательностями для достижения требуемых характеристик антитела, таких как повышенная аффинность к антигену(ам)-мишени(ням). Как правило, остатки гипервариабельного участка оказывают непосредственное и наиболее существенное влияние на связывание антигена.
Гуманизированное антитело может представлять собой фрагмент антитела, такой как Fab-фрагмент, необязательно конъюгированный с одним или несколькими цитотоксическим(ими) агентом(ами) для создания иммуноконъюгата. В альтернативном варианте гуманизированное антитело может представлять собой полноразмерное антитело, например, полноразмерное антитело в виде IgGl.
Человеческие антитела и методика, основанная на применении фаговой дисплейной библиотеки
В качестве альтернативы гуманизации можно получать человеческие антитела. Например, в настоящее время можно получать трансгенных животных (например, мышей), которые после иммунизации могут продуцировать полный спектр человеческих антител без производства эндогенного иммуноглобулина. Например, было описано, что гомозиготная делеция областей стыка гена тяжелой цепи антитела (Jн-сегмента) в организме химерных мышей и мышей с мутацией в зародышевой линии приводит к полному ингибированию производства эндогенного антитела. Перенос набора зародышевой линии гена человеческого иммуноглобулина в такую мутантную зародышевую линию мышей приводит к производству человеческих антител после контрольного заражения антигеном (US 5545806, 5569825, 5591669 (все на имя фирмы GenPharm); 5545807; и WO 97/17852).
В альтернативном варианте для получения человеческих антител и фрагментов антител in vitro из спектра генов вариабельной области (V) иммуноглобулина из организма иммунизированных доноров можно использовать фаговую дисплейную технологию (McCafferty и др., Nature, 348, 1990, сс. 552-554). Согласно этой методике гены V-области антитела клонируют в рамке считывания либо с основным, либо с минорным геном оболочечного белка нитчатого бактериофага, такого как М13 или fd, и презентируют в виде функциональных фрагментов антитела на поверхности фаговой частицы. Поскольку нитчатая частица содержит копию одноцепочечной ДНК фагового генома, селекции по признаку функциональных свойств антитела, также приводят к отбору гена, кодирующего антитело, которое обладает указанными свойствами. Таким образом, фаг имитирует некоторые свойства В-клетки. Фаговую презентацию можно осуществлять в различных форматах. Для фаговой презентации можно использовать различные источники сегментов V-генов. Clackson и др., Nature, 352, 1991, сс. 624-628 выделили различные наборы антител к оксазолону из небольшой произвольной комбинаторной библиотеки V-генов, полученной из селезенки иммунизированных мышей. Можно конструировать спектр V-генов, полученных из организма иммунизированных людей-доноров, и антитела к различному набору антигенов (включая аутоантигены) можно выделять в целом согласно методам, описанным у Marks и др., J. Mol. Biol., 222, 1991, cc. 581-597.
Как описано выше, человеческие антитела могут продуцироваться также in vitro активированными В-клетками (см. US 5567610 и 5229275).
Фрагменты антител
В определенных обстоятельствах целесообразно применять фрагменты антител, а не полные антитела. Меньший размер фрагментов способствует их быстрому клиренсу и может способствовать лучшему проникновению в плотные опухоли.
Для получения фрагментов антител разработаны различные методы. Традиционно эти фрагменты получали путем протеолитического расщепления интактных антител. Однако в настоящее время эти фрагменты можно получать непосредственно с помощью рекомбинантных клеток-хозяев. Fab-, Fv- и scFv-фрагменты антител можно экспрессировать и секретировать из Е. coli, что позволяет облегчать производство больших количеств указанных фрагментов. Фрагменты антител можно выделять из описанных выше фаговых библиотек антител. Согласно другому варианту Fab'-SH-фрагменты можно непосредственно выделять из Е. coli и химически сшивать с получением F(аb')2-фрагментов (Carter и др., Bio/Technology, 10, 1992, сс. 163-167). Согласно другому подходу F(аb')2 - фрагменты можно выделять непосредственно из культуры рекомбинантных клеток-хозяев. Fab- и F(аb')2-фрагмент с повышенным временем полужизни in vivo, в которых сохранены остатки эпитопсвязывающего рецептора, описаны в US 5869046.Специалистам в данной области должны быть очевидны другие методики получения фрагментов антител. В других вариантах осуществления изобретения выбранное антитело представляет собой одноцепочечный Fv- фрагмент (scFv) (см. WO 93/16185; US 5571894 и US США 5587458). Fv и sсFv представляют собой единственные виды с интактными связывающими сайтами, лишенные константных областей; в результате их можно применять для пониженного неспецифического связывания при применении in vivo. Слитые белки, несущие sсFv, можно конструировать для получения слияния эффекторного белка либо на N-, либо на С-конце sсFv. Фрагмент антитела может представлять собой также «линейное антитело», например, описанное в US 5641870. Такие фрагменты линейного антитела могут быть моноспецифическими или биспецифическими.
Мультиспецифические антитела
Мультицифические антитела представляют собой антитела, которые обладают специфичностью к связыванию с по крайней мере двумя различными эпитопами. Например, биспецифические антитела могут связываться с двумя различными эпитопами белка. Другие мультиспецифические антитела могут нести сайт связывания с CD47 и PD-L1 в сочетании с сайтом связывания другого белка. Биспецифические антитела можно получать в виде полноразмерных антител или фрагментов антител (например, F(аb')2-фрагментов биспецифических антител).
Методы создания мультиспецифических антител известны в данной области. Например, общепринятое получение полноразмерных биспецифических антител основано на совместной экспрессии двух пар тяжелых и легких цепей иммуноглобулина, где обе цепи имеют различную специфичность. Из-за случайного набора тяжелых и легких цепей иммуноглобулина, эти гибридомы (квадромы) потенциально могут продуцировать смесь из 10 различных молекул антител, из которых только одна имеет правильную биспецифическую структуру. Очистка правильной молекулы, которую обычно осуществляют в несколько стадий с помощью аффинной хроматографии, является довольно трудоемкой, а выход продукта - низким. Аналогичные процессы описаны в WO 93/08829.
Согласно другому подходу вариабельные области антитела с требуемой специфичностью связывания (антигенсвязывающие центры антитела) сливают с последовательностями константной области иммуноглобулина. Слияние предпочтительно осуществляют с константной областью тяжелой цепи Ig, которая включает по меньшей мере часть шарнирных СН2- и СНЗ-областей. Предпочтительно, чтобы по меньшей мере в одном из слияний присутствовала первая константная область тяжелой цепи (СН1), содержащая сайт, необходимый для связывания легкой цепи. ДНК, кодирующие слияния тяжелой цепи иммуноглобулина и при необходимости легкой цепи иммуноглобулина, встраивают в различные экспрессионные векторы и ими совместно трансфектируют приемлемый организм-хозяин. Это обеспечивает большую гибкость в подборе общих пропорций трех полипептидных фрагментов в вариантах, когда в конструкции используют неравные соотношения трех полипептидных цепей с целью оптимизации выходов. Однако можно также встраивать кодирующие последовательности в две или во все три полипептидные цепи в одном экспрессионном векторе, когда экспрессия по меньшей мере двух полипептидных цепей в равных пропорциях обеспечивает высокие выходы или, когда соотношения не имеют решающего значения.
В предпочтительном варианте осуществления указанного подхода биспецифические антитела представляют собой гибрид тяжелой цепи иммуноглобулина, обеспечивающий первую специфичность связывания в первом плече, и гибрид пары тяжелая цепь - легкая цепь иммуноглобулина (что обеспечивает вторую специфичность связывания) во втором плече. Было обнаружено, что эта асимметричная структура облегчает отделение требуемой биспецифической молекулы от нежелательных комбинаций цепей иммуноглобулинов, поскольку присутствие легкой цепи иммуноглобулина только в одной половине биспецифической молекулы облегчает разделение. Этот подход описан в WO 94/04690. Дополнительное подробное описание получения биспецифических антител см., например, Suresh и др., Methods in Enzymology, 121, 1986, c. 210.
Согласно следующему подходу, описанному в патенте US 5731168, можно сконструировать область контакта между парой молекул антител с целью повышения до максимального уровня процентного содержания гетеродимеров, которые получают из культуры рекомбинантных клеток. Предпочтительная область контакта включает по меньшей мере часть СНЗ-области. Согласно этому методу одну или несколько небольших аминокислот с боковыми цепями из области контакта первой молекулы антитела заменяют на молекулы с более крупными боковыми цепями (например, на тирозин или триптофан). Уравновешивающие «полости», идентичные или близкие по размеру большой(им) боковой(ым) цепи(ям) создают в области контакта второй молекулы антитела путем замены аминокислот с крупными боковыми цепями на аминокислоты с более мелкими боковыми цепями (например, на аланин или треонин). Это обеспечивает механизм, способствующий повышению выхода гетеродимера относительно других нежелательных конечных продуктов.
Биспецифические антитела включают перекрестносшитые антитела или «гетероконъюгаты». Например, одно из антител в гетероконъюгате может быть сшито с авидином, а другое с биотином. Такие антитела можно использовать, например, для направленного переноса клеток иммунной системы к нежелательным клеткам (US 4676980) и для лечения ВИЧ-инфекции (WO 91/00360, WO 92/200373 и ЕР 03089). Антитела-гетероконъюгаты можно создавать с помощью любого из обычных методов введения перекрестных сшивок. Приемлемые кросс-линкеры хорошо известны в данной области и описаны в US 4676980 наряду с различными методами введения перекрестных сшивок.
Методы получения биспецифических антител из фрагментов антител также описаны в литературе. Например, биспецифические антитела можно получать с помощью химического связывания. Brennan и др., Science, 229, 1985, с. 81 описали методику, согласно которой интактные антитела подвергают протеолитическому расщеплению, получая F(аb')2-фрагменты. Эти фрагменты восстанавливают в присутствии агента, образующего комплексы с дитиолом, такого как арсенит натрия, для стабилизации соседних дитиолов и предупреждения образования межмолекулярных дисульфидных связей. Полученные Fab'-фрагменты затем превращают в тионитробензоатное (TNB) производное. Одно из Fab'-TNB-производных затем повторно превращают в Fab'-тиол путем восстановления меркаптоэтиламином и смешивают с эквимолярным количеством другого Fab'-TNB-производного, получая биспецифическое антитело. Полученные биспецифические антитела можно применять в качестве агентов для избирательной иммобилизации ферментов.
Достигнутый в настоящее прогресс позволяет облегчать непосредственное выделение из Е. coli Fab'-SH-фрагментов, которые можно химически сшивать с образованием биспецифических антител. Shalaby и др., J. Exp. Med., 175, 1992, с. 217-225 описали получение F(аb')2-фрагмента молекулы полностью гуманизированного биспецифического антитела. Каждый Fab'-фрагмент по отдельности секретировался из Е. coli и его подвергали непосредственному химическому связыванию in vitro с получением биспецифического антитела. Полученное таким образом биспецифическое антитело обладало способностью связываться с клетками, для которых характерна сверхэкспрессия рецептора ЕrbВ2, и с обычными человеческими Т-клетками, а также стимулировать литическую активность человеческих цитотоксических лимфоцитов, мишенью которых является опухоль молочной железы человека.
Описаны также различные методы получения и выделения фрагментов биспецифических антител непосредственно из культуры рекомбинантных клеток. Например, биспецифические антитела получали с помощью лейциновых «застежек-молний» (Kostelny и др., J. Immunol., 148(5), 1992, сс. 1547-1553). Пептиды лейциновых «застежек-молний» из белков Fos и Jun связывали с Fab'-фрагментами двух различных антител путем генного слияния. Гомодимеры антител восстанавливали в шарнирной области с получением мономеров, а затем путем повторного окисления получали гетеродимеры антител. Этот метод можно применять также для получения гомодимеров антител. Технология на основе «двойных антител», описанная Hollinger и др., Proc. Natl. Acad. Sci. USA, 90, 1993, с. 6444-6448, представляет собой другой механизм получения фрагментов биспецифических антител. Фрагменты содержат VH-область, связанную с VL- областью линкером, который является слишком коротким, для того чтобы позволить произойти спариванию двух доменов одной и той же цепи. Таким образом, VH- и VL-области одного фрагмента должны спариваться с комплементарными VL- и VH-областями другого фрагмента, образуя тем самым два антигенсвязывающих центра. Описана также другая стратегия получения фрагментов биспецифических антител, основанная на применении одноцепочечных (Fv)- (sFv) димеров (см. Gruber и др., J. Immunol, 152, 1994, с. 5368).
Под объем изобретения подпадают также антитела, имеющие более двух валентностей. Например, можно получать триспецифические антитела.
Поливалентные антитела
Поливалентное антитело может интернализоваться (и/или диссимилироваться) клеткой, экспрессирующей антиген, с которым связывается антитело, быстрее, чем бивалентное антитело. Антитела, предлагаемые в настоящем изобретении, могут представлять собой поливалентные антитела (отличные от класса IgM) с тремя или большим количеством антигенсвяызвающих центров (например, тетравалентные антитела), которые можно легко получать путем рекомбинантной экспрессии нуклеиновой кислоты, кодирующей полипептидные цепи антитела. Поливалентное антитело может содержать димеризованный домен и три или большее количество антигенсвязывающих центров. Предпочтительный димеризованный домен содержит (или состоит из) Fc-фрагмент или шарнирную область. В таком случае антитело должно содержать Fc-фрагмент и три или большее количество антигенсвязывающих центров, расположенных на N-конце относительно Fc- фрагмента. Согласно настоящему описанию предпочтительное поливалентное антитело содержит (или состоит из) от 3 до примерно 8, но предпочтительно 4, антигенсвязывающих центров. Поливалентное антитело содержит по меньшей мере одну полипептидную цепь (и предпочтительно две полипептидные цепи), при этом полипептидная(ые) цепь(и) содержит(ат) две или большее количество вариабельных областей. Например, полипептидная(ые) цепь(и) может(ут) содержать VDl-(X1)n-VD2-(X2)n-Fc, где VD1 обозначает первую вариабельную область, VD2 обозначает вторую вариабельную область, Fc обозначает одну полипептидную цепь Fc-фрагмента, X1 и Х2 обозначают аминокислоту или полипептид и n обозначает 0 или 1. Например, полипептидная(ые) цепь(и) может(ут) содержать следующую цепь: VH-CH1-гибкий линкер-VH-CH1-Fc-фрагмент; или VH-CH1-VH-CH1-Fc-фрагмент. Поливалентное антитело, предлагаемое в настоящем изобретении, предпочтительно дополнительно содержит по меньшей мере 2 (и предпочтительно 4) полипептида вариабельной области легкой цепи. Поливалентное антитело, предлагаемое в настоящем изобретении, может, например, содержать от примерно 2 до примерно 8 полипептидов вариабельной области легкой цепи. В контексте настоящего описания подразумевается, что полипептиды вариабельной области легкой цепи содержат вариабельную область легкой цепи и необязательно дополнительно содержит CL-область.
Фармацевтические композиции
Другим аспектом изобретения является фармацевтическая композиция, содержащая в качестве активного ингредиента (или в качестве единственного активного ингредиента) антитело, которое специфично к CD47 и PD-L1. Фармацевтическая композиция может включать по меньшей мере одно антитело к CD47 и PD-L1 и/или одну или более дополнительных связывающих молекул (например, антител), которые нацелены на один или более соответствующих поверхностных рецепторов, как описано в данном документе. В некоторых вариантах осуществления изобретения композиции предназначены для улучшения, профилактики или лечения нарушений, которые опосредованы IgG.
«Фармацевтическая композиция» обозначает композицию, включающую в себя антитело к CD47 и PD-L1 согласно изобретению и, по крайней мере, один из компонентов, выбранных из группы, состоящей из фармацевтически приемлемых и фармакологически совместимых эксипиентов, таких как наполнители, растворители, разбавители, носители, вспомогательные, распределяющие, средства доставки, консерванты, стабилизаторы, эмульгаторы, суспендирующие агенты, загустители, регуляторы пролонгированной доставки, выбор и соотношение которых зависит от природы и способа назначения и дозировки. Фармацевтические композиции по настоящему изобретению и способы их изготовления будут бесспорно очевидными для специалистов в этой области. Производство фармацевтических композиций предпочтительно должно соответствовать требованиям GMP (надлежащей производственной практики). Композиция может включать буферную композицию, тонические агенты, стабилизаторы и солюбилизаторы. Пролонгированное действие композиции может быть обеспечено с помощью агентов, замедляющих абсорбцию активного фармацевтического ингредиента, например, моностеарат алюминия и желатин. Примерами подходящих носителей, растворителей, разбавителей и средств доставки являются вода, этанол, полиспирты, а также их смеси, масла и инъекционные органические сложные эфиры.
«Лекарственное средство (препарат)» – вещество или смесь веществ в виде фармацевтической композиции в виде таблеток, капсул, порошков, лиофилизатов, инъекций, инфузий, мазей и др. готовых форм, предназначенное для восстановления, исправления или изменения физиологических функций у человека и животных, а также для лечения и профилактики болезней, диагностики, анестезии, контрацепции, косметологии и прочего. Любой способ введения пептидов, белков или антител, принятый в данной области, может соответствующим образом использоваться для антитела к CD47 и PD-L1 по данному изобретению.
Термин «фармацевтически приемлемый» означает один или несколько совместимых жидких или твердых компонентов, которые подходят для введения млекопитающему, предпочтительно человеку.
Термин «эксципиент» или «вспомогательное вещество» используется в данном документе для описания любого компонента, отличающегося от ранее описанных по данному изобретению. Это вещества неорганического или органического происхождения, используемые в процессе производства, изготовления лекарственных препаратов для придания им необходимых физико-химических свойств.
Под термином «буфер», «буферная композиция», «буферный агент» понимается раствор, способный сохранять значение pH, благодаря взаимодействию кислотных и щелочных компонентов, входящих в его состав, который дает возможность препарату антитела к CD47 и PD-L1 проявлять устойчивость к изменениям рН. В общем случае, преимущественными являются значения рН фармацевтической композиции от 4,0 до 8,0. В качестве буферных агентов могут быть использованы, например, ацетатный, фосфатный, цитратный, гистидиновый, сукцинатный и т.п. буферные растворы, но, не ограничиваясь ими.
Термины «тонический агент», «осмолитик» или «осмотический агент» в том виде, как они здесь использованы, относятся к эксципиенту, который может подводить осмотическое давление жидкого препарата антитела. «Изотоничный» препарат представляет собой препарат, который имеет осмотическое давление, эквивалентное давлению человеческой крови. Изотоничные препараты обычно имеют осмотическое давление от примерно 250 до 350 мОсм/кг. В качестве изотоноческих агентов могут быть использованы полиолы, моно- и дисахара, аминокислоты, соли металлов, например, хлорид натрия, и т.п., но, не ограничиваясь ими.
Под «стабилизатором» понимается вспомогательное вещество или смесь двух и более вспомогательных веществ, которые обеспечивают физическую и/или химическую стабильность активного агента. В качестве стабилизаторов могут быть использованы аминокислоты, например, аргинин, гистидин, глицин, лизин, глутамин, пролин, но, не ограничиваясь ими; поверхностно-активные вещества, например полисорбат 20 (торговое наименование Tween 20), полисорбат 80 (торговое наименование Tween 80), полиэтилен-полипропилен гликоль и его кополимеры (торговые наименования Полоксамер (Poloxaner), Плуроник (Pluronic)), натрия додецилсульфат (SDS), но, не ограничиваясь ими; антиоксиданты, например метионин, ацетилцистеин, аскорбиновая кислота, монотиоглицерол, соли серистых кислот, и т.п., но не ограничиваясь ими; хелатирующие агенты, например этилендиаминтетрауксусная кислота (ЭДТА), диэтилентриаминпентауксусная кислота (ДТПА), цитрат натрия и т.п., но не ограничиваясь ими.
Фармацевтическая композиция является «стабильной», если активный агент сохраняет свою физическую стабильность и/или химическую стабильность и/или биологическую активность в течение заявленного срока годности при температуре хранения, например, при 2-8 ºС. Предпочтительно, чтобы активный агент сохранял и физическую, и химическую стабильность, а также биологическую активность. Период хранения выбирается на основании результатов исследования стабильности при ускоренном и естественном хранении.
Фармацевтическая композиция по данному изобретению может изготавливаться, упаковываться или широко продаваться в виде единичной стандартной дозы или множества единичных стандартных доз в виде готовой лекарственной формы. Используемый в данном документе термин «единичная стандартная доза» означает дискретное количество фармацевтической композиции, содержащей заранее определенное количество активного ингредиента. Количество активного ингредиента обычно равно дозировке активного ингредиента, который будет вводиться субъекту, или удобной части такой дозировки, например, половине или трети такой дозировки.
Фармацевтические композиции по настоящему изобретению, как правило, пригодны для парентерального введения в виде стерильных лекарственных средств, предназначенных для введения в организм человека с нарушением целостности кожных покровов или слизистых оболочек, минуя желудочно-кишечный тракт путем инъекций, инфузий или имплантации. Например, предполагается, что парентеральное введение включает, помимо прочего, подкожную, внутрибрюшинную, внутримышечную, внутривенную, внутриартериальную, интратекальную, внутрижелудочковую, интрауретральную, внутричерепную, внутрисуставнную, трансдермальную инъекцию или инфузи и почечные диализные инфузионные методики. Также предусмотрена региональная перфузия. Предпочтительные варианты осуществления изобретения включают внутривенный и подкожный пути. Любой способ введения пептидов или белков, принятый в данной области, может соответствующим образом использоваться для антитела к CD47 и PD-L1 по данному изобретению.
Инъекционные лекарственные средства могут быть изготовлены, упакованы или проданы в стандартной лекарственной форме, например, в ампулах, флаконах, полимерных контейнерах, преднаполненных шприцах, устройствах для автоинжекции, но не ограничиваясь ими. Лекарственные средства для парентерального введения включают, помимо прочего, суспензии, растворы, эмульсии в масляных или водных основах, пасты и тому подобное.
Еще одним вариантом осуществления изобретения является лекарственное средство для парентерального введения, где фармацевтическая композиция предоставлена в сухой форме, то есть, порошка или гранул для растворения в подходящем растворителе (например, стерильной апирогенной воде) перед введением. Такое лекарственное средство может быть получено, например, с помощью лиофилизации, т.е. процесса, известного в данной области техники как сушка из замороженного состояния, включающая в себя замораживание препарата и последующее удаление растворителя из замороженного содержимого.
Антитело к CD47 и PD-L1 по данному изобретению может также вводиться интраназально или ингаляционно, самостоятельно, в виде смеси с подходящим фармацевтически приемлемым наполнителем из ингалятора, такого как аэрозольный контейнер под давлением, помпа, спрей, распылитель) или небулайзер, в котором используется или не используется подходящий пропеллент, или в виде назальных капель или спрея.
Лекарственное средство для парентерального введения может быть немедленного или модифицированного высвобождения. Лекарственные средства с модифицированным высвобождением включают отсроченное, замедленное, пульсирующее, контролируемое, нацеленное и программируемое высвобождение.
Терапевтическое применение антитела к CD47 и PD-L1 по данному изобретению
В одном аспекте антитело к CD47 и PD-L1 по данному изобретению применяется в лечении нарушений, которые опосредованы CD47 и PD-L1, например заболевание или нарушение выбрано из группы: ПРГШ (плоскоклеточный рак головы и шеи), рак шейки матки, рак без выявленного первоисточника, глиобластома, рак пищевода, рак мочевого пузыря, ТНРМЖ (трижды негативный рак молочной железы), КРР (колоректальный рак), гепатоцеллюлярная карцинома, меланома, НМРЛ (немелкоклеточный рак легкого), рак почки, рак яичника, лимфома Ходжкина, MSI КРР (колоректальный рак с высокой микросателлитной нестабильностью), лейкоз (острый или хронический), неходжкинская лимфома, множественная миелома, миелодиспластический синдром.
В одном аспекте субъект лечения или пациент является млекопитающим, предпочтительно человеческим субъектом. Вышеупомянутый субъект может быть мужского или женского пола и любого возраста.
В случае опухоли (например, раковой опухоли) терапевтически эффективное количество антитела или фрагмента антитела (например, антитела или фрагмента антитела, которое специфически связывает к CD47 и PD-L1) может уменьшать число раковых клеток; уменьшать начальный размер опухоли; ингибировать (т.е. до некоторой степени замедлять и, предпочтительно, прекращать) инфильтрацию раковыми клетками периферических органов; ингибировать (т.е. до некоторой степени замедлять и, предпочтительно, прекращать) метастазирование опухоли; ингибировать, до некоторой степени, рост опухоли; и/или облегчать, до некоторой степени, один или более симптомов, обусловленных расстройством. Антитело или фрагмент антитела может, до некоторой степени, предупреждать рост и/или убивать имеющиеся раковые клетки, оно может вызывать цитостатический и/или цитотоксический эффект. При терапии рака эффективность in vivo можно определять, например, оценивая общую продолжительность жизни (OS), время до прогрессирования заболевания (ТТР), общую частоту ответа опухоли на лечение (ORR), продолжительность ответа (DR) и/или качество жизни.
Используемые в данном документе термины «совместное назначение», «совместно назначенный» и «в сочетании с» относящиеся к антителу к CD47 и PD-L1 с одним или более другими терапевтическими агентами, как предполагается, означают, сслылаются или включают:
1) одновременное введение такой комбинации антитела к CD47 и PD-L1 по данному изобретению и терапевтического агента пациенту, который нуждается в лечении, когда такие компоненты сформулированы вместе в одной лекарственной форме, из которой указанные компоненты высвобождаются практически одновременно указанному пациенту,
2) одновременное введение такой комбинации антитела к CD47 и PD-L1 по данному изобретению и терапевтического агента пациенту, который нуждается в лечении, когда такие компоненты сформулированы отдельно в разных лекарственных формах, введение которых происходит практически в одно и то же время указанному пациенту, после чего указанные компоненты высвобождаются практически одновременно указанному пациенту,
3) последовательное введение такой комбинации антитела к CD47 и PD-L1 по данному изобретению и терапевтического агента пациенту, который нуждается в лечении, когда такие компоненты сформулированы отдельно друг от друга в отдельных лекарственных формах, которые принимаются последовательно по времени указанным пациентом со значимым временным интервалом между каждым введением, после чего указанные компоненты высвобождаются в практически разное время указанному пациенту; а также
4) последовательное введение такой комбинации антитела к CD47 и PD-L1 по данному изобретению и терапевтического агента пациенту, который нуждается в лечении, когда такие компоненты сформулированы вместе в единый лекарственной форме, из которой высвобождение указанных компонентов происходит контролируемым образом, после чего они одновременно, последовательно или совместно высвобождаются в одно и то же время и/или разное время указанному пациенту, где каждая часть может быть введена одним или разными путями.
Антитело к CD47 и PD-L1 по данному изобретению могут назначаться без дополнительного терапевтического лечения, т.е. в качестве самостоятельной терапии. Кроме того, лечение антителом по данному изобретению может включать по меньшей мере одно дополнительное терапевтическое лечение (комбинированная терапия). В некоторых вариантах осуществления изобретения, антитело к CD47 и PD-L1 может вводиться совместно или быть сформулировано с другим медикаментом/препаратом для лечения рака.
Термин «цитотоксическое средство» в используемом в настоящем описании смысле относится к веществу, которое ингибирует или предотвращает функционирование клеток и/или вызывает разрушение клеток. Подразумевается, что термин включает радиоактивные изотопы (например, At211, I131, I125, Y90, Re186, Re188, Sm153, Bi212, P32 и радиоактивные изотопы Lu), химиотерапевтические средства и токсины, такие как низкомолекулярные токсины или ферментативно активные токсины, имеющие происхождение из бактерий, грибов, растений или животных, включая их фрагменты и/или варианты.
"Химиотерапевтическим средством" является химическое соединение, применимое для лечения злокачественной опухоли. Примеры химиотерапевтических средств включают алкилирующие агенты, такие как тиотепа и циклофосфамид (CYTOXAN®); алкилсульфонаты, такие как бусульфан, импросульфан и пипосульфан; азиридины, такие как бензодопа, карбохинон, метуредопа и уредопа; этиленимины и метилмеламины, включая алтретамин, триэтиленмеламин, триэтиленфосфорамид, триэтилентиофосфорамид и триметилмеламин; ацетогенины (например, буллатацин и буллатацинон); бета-лапахон; лапахол; колхицины; бетулиновую кислоту; камптотецин (включая синтетический аналог топотекан (HYCAMTIN®), CPT-11 (иринотекан, CAMPTOSAR®), ацетилкамптотецин, скополектин и 9-аминокамптотецин); бриостатин; каллистатин; CC-1065 (включая его синтетические аналоги адозелезин, карзелезин и бизелезин); подофиллотоксин; подофиллиновую кислоту; тенипозид; криптофицины (например, криптофицин 1 и криптофицин 8); доластатин; дуокармицин (включая синтетические аналоги KW-2189 и CB1-TM1); элеутеробин; панкратистатин; саркодиктиин; спонгистатин; азотистые иприты, такие как хлорамбуцил, хлорнафазин, холофосфамид, эстрамустин, ифосфамид, мехлорэтамин, гидрохлорид оксида мехлорэтамина, мелфалан, новембихин, фенестерин, преднимустин, трофосфамид, урамустин; нитрозомочевины, такие как кармустин, хлорозотоцин, фотемустин, ломустин, нимустин и ранимнустин; антибиотики, такие как энедииновые антибиотики (например, калихеамицин, например, калихеамицин гамма II и калихеамицин омега II (см., например, Agnew, Chem. Intl. Ed. Engl., 33: 183-186 (1994)); динемицин, включая динемицин A; эсперамицин; а также хромофор неокарциностатина и родственные хромофоры хромопротеинов - энедииновые антибиотики, аклациномизины, актиномицин, аутрамицин, азасерин, блеомицины, кактиномицин, карабицин, карминомицин, карзинофилин, хромомицины, дактиномицин, даунорубицин, деторубицин, 6-диазо-5-оксо-L-норлейцин, доксорубицин (включая ADRIAMICIN®, морфолинодоксорубицин, цианоморфолинодоксорубицин, 2-пирролинодоксорубицин, доксорубицино-HCl в инъецируемых липосомах (DOXOL®), липосомный доксорубицин TLC D-99 (MYOCET®), пегилированный липосомный доксорубицин (CAELYX®) и дезоксидоксорубицин), эпирубицин, эзорубицин, идарубицин, марцелломицин, митомицины, такие как митомицин C, микофеноловую кислоту, ногаламицин, оливомицины, пепломицин, потфиромицин, пуромицин, квеламицин, родорубицин, стрептонигрин, стрептозоцин, туберцидин, убенимекс, зиностатин, зорубицин; антиметаболиты, такие как метотрексат, гемцитабин (GEMZAR®), тегафур (UFTORAL®), капецитабин (XELODA®), эпотилон и 5-фторурацил (5-FU); аналоги фолиевой кислоты, такие как деноптерин, метотрексат, птероптерин, триметрексат; аналоги пурина, такие как флударабин, 6-меркаптопурин, тиамиприн, тиогуанин; аналоги пиримидина, такие как анцитабин, азацитидин, 6-азауридин, кармофур, цитарабин, дидезоксиуридин, доксифлуридин, эноцитабин, флоксуридин; средства, подавляющие функции надпочечников, такие как аминоглютетимид, митотан, трилостан; компенсатор фолиевой кислоты, такой как фолиновая кислота; ацеглатон; гликозид альдофосфамида; аминолевулиновую кислоту; энилурацил; амсакрин; бестрабуцил; бисантрен; эдатраксат; дефофамин; демеколцин; диазихон; элфорнитин; ацетат эллиптиния; этоглуцид; нитрат галлия; гидроксимочевину; лентинан; лонидаинин; майтанзиноиды, такие как майтанзин и ансамитоцины; митогуазон; митоксантрон; мопиданмол; нитраэрин; пентостатин; фенамет; пирарубицин; лозоксантрон; 2-этилгидразид; прокарбазин; полисахаридный комплекс PSK® (JHS Natural Products, Eugene, OR); разоксан; ризоксин; сизофиран; спирогерманий; тенуазоновую кислоту; триазиквон; 2,2',2"-трихлортриэтиламин; трихотецены (например, токсин T-2, верракурин A, роридин A и ангуидин); уретан; дакарбазин; манномустин; митобронитол; митолактол; пипоброман; гацитозин; арабинозид ("ara-C"); тиотепа; таксоид, например паклитаксел (TAXOL®), препарат паклитаксела на основе сконструированных связанных с альбумином наночастиц (ABRAXANETM) и доцетаксел (TAXOTERE®); хлорамбуцил; 6-тиогуанин; меркаптопурин; метотрексат; средства на основе платины, такие как цисплатин, оксалиплатин и карбоплатин; алкалоиды барвинка, которые предотвращают полимеризацию тубулина из образующихся микротрубочек, включая винбластин (VELBAN®), винкристин (ONCOVIN®), виндезин (ELDISINE®, FILDESIN®) и винорелбин (NAVELBINE®); этопозид (VP-16); ифосфамид; митоксантрон; лейковорин; новантрон; эдатрексат; дауномицин; аминоптерин; ибандронат; ингибитор топоизомеразы RFS 2000; дифторметилорнитин (DMFO); ретиноиды, такие как ретиноевая кислота, включая бексаротен (TARGRETIN®); бифосфонаты, такие как клодронат (например, BONEFOS® или OSTAC®), этидронат (DIDROCAL®), NE-58095, золедроновую кислоту/золедронат (ZOMETA®), алендронат (FOSAMAX®), памидронат (AREDIA®), тилудронат (SKELID®) или ризендронат (ACTONEL®); троксацитабин (1,3-диоксолановый нуклеозидный аналог цитозина); антисмысловые олигонуклеотиды, например, олигонуклеотиды, которые ингибируют экспрессию генов в путях передачи сигналов, вовлеченных в пролиферацию аберрантных клеток, таких как, например, PKC-альфа, Raf, H-Ras и рецептора эпидермального фактора роста (EGF-R); вакцины, такие как вакцина THERATOPE® и вакцины для генной терапии, например вакцина ALLOVECTIN®, вакцина LEUVECTIN® и вакцина VAXID®; ингибитор топоизомеразы 1 (например, LURTOTECAN®); rmRH (например, ABARELIX®); BAY439006 (сорафениб; Bayer); SU-11248 (Pfizer); перифосин, ингибитор ЦОГ-2 (например, целекоксиб или эторикоксиб), ингибитор протеосом (например, PS341); бортезомиб (VELCADE®); CCI-779; типифарниб (811577); орафениб, ABT510; ингибитор Bcl-2, такой как облимерсен натрия (GENASENSE®); пиксантрон; ингибиторы EGFR (см. определение ниже); ингибиторы тирозинкиназ (см. определение ниже); и фармацевтически приемлемые соли, кислоты или производные любого из указанных выше средств; а также сочетания двух или более указанных выше средств, такие как CHOP, сокращенное название комбинированной терапии циклофосфамидом, доксорубицином, винкристином и преднизолоном, и FOLFOX, сокращенное название схемы лечения оксалиплатином (ELOXATINTM) в сочетании с 5-FU и лейковорином.
Также в указанное определение включены противогормональные средства, которые действуют, регулируя или ингибируя действие гормонов на опухоли, такие как антиэстрогены со смешанным профилем агонист/антагонист, включая тамоксифен (NOLVADEX®), 4-гидрокситамоксифен, триоксифен, торемифен (FARESTON®); идоксифен, дролоксифен, ралоксифен (EVISTA®), триоксифен, кеоксифен и избирательные модуляторы рецепторов эстрогена (SERM), такие как SERM3; чистые антиэстрогены без агонистических свойств, такие как фулвестрант (FASLODEX®) и EM800 (такие средства могут блокировать димеризацию рецепторов эстрогена (ER), ингибировать связывание ДНК, усиливать метаболизм ER и/или снижать уровни ER); ингибиторы ароматазы, включая стероидные ингибиторы ароматазы, такие как форместан и эксеместан (AROMASIN®), и нестероидные ингибиторы ароматазы, такие как анастразол (ARIMIDEX®), летрозол (FEMARA®) и аминоглутетимид и другие ингибиторы ароматазы, включая ворозол (RIVISOR®), ацетат мегестрола (MEGASE®), фадрозол, имидазол; агонисты рилизинг-гормона лютеинизирующего гормона, включая лейпролид (LUPRON® и ELIGARD®), гозерелин, бузерелин и триптерелин; половые стероиды, включая прогестины, такие как ацетат мегестрола и ацетат медроксипрогестерона, эстрогены, такие как диэтилстилбестрол и премарин и андрогены/ретиноиды, такие как флуоксиместерон, полностью трансретиноевая кислота и фенретинид; онапристон; антипрогестероны; понижающие регуляторы рецепторов эстрогенов (ERD); антиандрогены, такие как флутамид, нилутамид и бикалутамид; тестолактон; и фармацевтически приемлемые соли, кислоты или производные любого из указанных выше средств; а также сочетания двух или более указанных выше средств.
Другими терапевтическими средствами, которые могут применяться в комбинации с антителами против CD47 и PD-L1 согласно изобретению могут быть ингибиторы функции фактора роста, например, такие ингибиторы включают антитела фактора роста и антитела рецептора фактора роста (например, анти-erbB2 антитело трастузумаб [Herceptin], анти-EGFR антитело панитумумаб, анти-erbB1 антитело цетуксимаб [Erbitux, C225] и любые антитела факторов роста или рецепторов фактора роста, раскрытые Stern et al. Critical reviews in oncology/haematology, 2005, Vol. 54, pp11-29); антиангиогенные агенты, такие как ингибирующие эффекты сосудистого эндотелиального фактора роста, [например, антитело против фактора роста сосудистых эндотелиальных клеток бевацизумаб (Avastin)], антитела против рецепторов сосудистого эндотелиального фактора роста, такие как анти-KDR антитела и анти-flt1 антитела; антисмысловые нуклеотиды, например, направленные на вышеперечисленные мишени, такие как ISIS 2503, анти-ras антисмысловые средства или G3139 (Genasense), анти-bcl2 антисмысловые средства; подходами генной терапии, включая, например, подходы с заменой аберрантных генов, таких как аберрантный p53 или аберрантный BRCA1 или BRCA2, GDEPT (ген-направленная ферментная пролекарственная терапия) подходы с использованием цитозиндеаминазы, тимидинкиназы или фермента бактериальной нитроредуктазы, и подходы, направленные на повышение толерантности пациента к химиотерапии или лучевой терапии, такие как генная терапия мультилекарственной резистентности; иммунотерапевтические подходы, включая, например, лечение Алемтузумабом (campath-1H), моноклональным антителом, направленным на CD52, или лечение антителами, направленными на CD22, ex vivo и in vivo подходы по повышению иммуногенности опухолевых клеток пациента, трансфекцию цитокинами, такими как интерлейкин 2, интерлейкин 4 или гранулоцит-макрофаг колониестимулирующий фактор, подходы, направленные на снижение анергии T-клеток, такие как лечение моноклональными антителами, ингибирующими функцию CTLA-4, подходы с использованием трансфицированных иммунных клеток, таких как цитокин-трансфицированные дендритные клетки, подходы с использованием цитокин-трансфицированных опухолевых клеточных линий и подходы, использующие анти-идиотипические антитела, адаптивный перенос T-клеток с использованием T-клеток, подвергнутых неспецифической активации или нацеленных на конкретный антиген, представляющий интерес, ex vivo; ингибиторы деградации белка, такие как ингибитор протеасом, такой как Велкейд (бортезомиб); биотерапевтические терапевтические подходы, например, использующие пептиды или белки (такие как антитела или растворимые конструкты внешних рецепторных доменов), которые секвестируют рецепторы лигандов, блокируют связывание лиганда с рецептором или ослабляют сигнализацию рецептора (например, вследствие повышенной деградации рецептора или сниженных уровней экспрессии).
Дозы и пути введения
Антитело к CD47 и PD-L1 по данному изобретению будет вводиться в количестве, эффективном для лечения состояния, о котором идет речь, т.е. в дозах и в течение периодов времени, необходимых для достижения желаемого результата. Терапевтически эффективное количество может изменяться в зависимости от таких факторов, как конкретное состояние, по поводу которого проводится лечение, возраста, пола и веса пациента, а также является ли введение антитела к CD47 и PD-L1 самостоятельным лечением или оно проводится в комбинации с одним или более дополнительных методов лечения.
Схемы приема лекарственных средств можно регулировать, чтобы обеспечить оптимальный желаемый ответ. Например, может быть введен один болюс, несколько разделенных доз могут быть введены в течение некоторого времени, или доза может быть пропорционально уменьшена или увеличена в зависимости от остроты терапевтической ситуации. Особенно полезным является изготовление парентеральных композиций в стандартной лекарственной форме для простоты введения и однородности дозирования. Стандартная лекарственная форма при использовании в данном документе, относится к физически дискретным единицам, пригодным в качестве единичных доз для пациентов/субъектов, подлежащих лечению; каждая единица содержит заданное количество активного соединения, рассчитанное для получения желаемого терапевтического эффекта в сочетании с требуемым фармацевтическим носителем. Спецификация для стандартных лекарственных форм по настоящему изобретению, как правило, диктуется и непосредственно зависит от (a) уникальных характеристик химиотерапевтического агента и конкретного терапевтического или профилактического эффекта, которые должны быть достигнуты, и (b) ограничений, присущих в технике составления такого активного соединения для лечения субъектов.
Таким образом, квалифицированным специалистам понятно, исходя из раскрытия, представленного в данном документе, что дозы и режим дозирования корректируются в соответствии со способами, хорошо известными в терапевтической области. Это означает, что может быть легко установлена максимально переносимая доза и может быть также определено эффективное количество, обеспечивающее обнаруживаемый терапевтический эффект для пациента, так же, как и требования к времени введения каждого агента для достижения видимого терапевтического эффекта для пациента. Таким образом, хотя некоторые дозы и схемы режима введения приведены в качестве примеров в данном документе, эти примеры никоим образом не ограничивают дозы и режимы введения, которые могут понадобиться для пациента в практике применения настоящего изобретения.
Следует отметить, что значения дозировки могут изменяться, в зависимости от типа и тяжести состояния, которое следует облегчить, и может включать одну или более доз. Кроме того, необходимо понимать, что для любого конкретного пациента, конкретные схемы введения должны быть скорректированы через некоторое время согласно индивидуальной потребности и на усмотрение медицинского работника, который осуществляет введение или контролирует введение композиций, и что диапазоны концентрации, приведенные в данном описании, приведены только в качестве примера и не предназначены для ограничения объема или практики заявленных композиций. Кроме того, режим дозирования с композициями по данному изобретению может быть основан на различных факторах, включая тип заболевания, возраст, вес, пол, состояние здоровья пациента, тяжесть состояния, путь введения и конкретное используемое антитело к CD47 и PD-L1. Таким образом, режим дозирования может широко варьироваться, но может определяться регулярно с помощью стандартных методов. Например, дозы могут быть скорректированы на основе фармакокинетических и фармакодинамических параметров, которые могут включать клинические эффекты, такие как токсические эффекты или лабораторные значения. Таким образом, настоящее изобретение охватывает индивидуальное повышение дозы, которое определяется квалифицированным специалистом. Определение необходимой дозы и режимы хорошо известны в соответствующей области техники и будут понятны специалисту в данной области после ознакомления с идеями, раскрытыми в данном документе.
Примеры подходящих способов введения предусмотрены выше.
Предполагается, что подходящая доза антитела к CD47 и PD-L1 по данному изобретению будет в диапазоне от 0,1-200 мг/кг, предпочтительно 0,1-100 мг/кг, в том числе около 0,5-50 мг/кг, например, около 1-20 мг/кг. Антитело к CD47 и PD-L1 может быть введена, например, в дозе по меньшей мере 0,25 мг/кг, например, по меньшей мере 0,5 мг/кг, в том числе не менее 1 мг/кг, например, по меньшей мере 1,5 мг/кг, например, также как не менее 2 мг/кг, например, по меньшей мере 3 мг/кг, в том числе по меньшей мере 4 мг/кг, например, по меньшей мере 5 мг/кг; и например вплоть до максимально 50 мг/кг, в том числе вплоть до максимально 30 мг/кг, например, вплоть до максимально 20 мг/кг, в том числе вплоть до максимально 15 мг/кг. Введение будет повторяться обычно в подходящие промежутки времени, например, раз в неделю, раз в две недели, один раз каждые три недели или один раз каждые четыре недели, и так долго, как будет сочтено целесообразным ответственным врачом, который может в некоторых случаях увеличить или уменьшить дозу при необходимости.
Изделие (продукты) и наборы
Следующим вариантом осуществления изобретения является изделие, которое содержит продукты, применяемые для лечения рака, например, ПРГШ, рака шейки матки, рака без выявленного первоисточника, глиобластомы, рака пищевода, рака мочевого пузыря, ТНРМЖ, КРР, гепатоцеллюлярной карциномы, меланомы, НМРЛ, рака почки, рака яичника, лимфомы Ходжкина, MSI КРР, лейкоз (острый или хронический), неходжкинская лимфома, множественная миелома, миелодиспластический синдром. Изделие представляет собой контейнер и этикетку или листовку-вкладыш в упаковке, которые размещены на контейнере или вложены в него. Приемлемыми контейнерами являются, например, банки, пузырьки, шприцы и т.д. Контейнеры можно изготавливать из различных материалов, таких как стекло или пластмасса. Контейнер содержит композицию, эффективную для лечения определенного состояния, и может иметь стерильный входной канал (например, контейнер может представлять собой пакет для внутривенного раствора или пузырек, снабженный пробкой, которую можно прокалывать с помощью иглы для подкожных инъекций). По меньшей мере одно действующее вещество в композиции представляет собой антитело к PD-L1, предлагаемое в изобретении. На этикетке или листовке-вкладыше в упаковке указано, что композицию применяют для лечения конкретного состояния. Этикетка или листовка-вкладыш в упаковке дополнительно должны содержать инструкции по введению композиции антитела пациенту.
Листовка-вкладыш в упаковке содержит обычные инструкции, которые включают в поступающие в продажу упаковки терапевтических продуктов, в том числе примерную информацию о показаниях, применении, дозе, пути введения, противопоказаниях и/или мерах предосторожности, касающихся применения таких терапевтических продуктов. В одном из вариантов осуществления изобретения на листовке-вкладыше в упаковке указано, что композицию применяют для лечения рака, например, ПРГШ, рака шейки матки, рака без выявленного первоисточника, глиобластомы, рака пищевода, рака мочевого пузыря, ТНРМЖ, КРР, гепатоцеллюлярной карциномы, меланомы, НМРЛ, рака почки, рака яичника, лимфомы Ходжкина, MSI КРР, лейкоз (острый или хронический), неходжкинская лимфома, множественная миелома, миелодиспластический синдром.
Кроме того, изделие может дополнительно содержать второй контейнер с фармацевтически приемлемым буфером, таким как бактериостатическая вода для инъекций (БСВИ), забуференный фосфатом физиологический раствор, раствор Рингера и раствор декстрозы. Кроме того, оно может включать другие продукты, необходимые с коммерческой точки зрения и с точки зрения потребителя, например, другие буферы, разбавители, фильтры, иглы и шприцы.
Изобретение относится также к наборам, которые можно применять для различных целей, например, для детектирования PD-L1 в тканях, клетках или жидкостях организма млекопитающего. Такой набор будет пригодным для скрининга ассоциированных с PD-L1 болезней. Набор включает специфический связывающий агент или антитело по изобретению и средства, указывающие на протекание реакции специфического связывающего агента или антитела с PD-L1, в случае его присутствия. В одном варианте воплощения антитело представляет собой моноклональное антитело. В одном варианте воплощения антитело, связывающее PD-L1, является меченым. В другом варианте воплощения антитело представляет собой немеченое первичное антитело, и набор дополнительно включает средства детектирования первичного антитела. В одном варианте воплощения средства детектирования включают меченое второе антитело, представляющее собой анти-иммуноглобулин. Антитело может быть меченым с помощью маркера, выбранного из группы, состоящей из флуорохрома, фермента, радионуклида и радионепрозрачного материала. Набор может представлять собой набор, который содержит антитела для выявления и количественной оценки PD-L1 in vitro, например, при осуществлении ELISA или Вестерн-блоттинга. Также, как и в случае изделия, набор содержит контейнер и этикетку или листовку-вкладыш в упаковке, расположенные на поверхности или внутри контейнера. Контейнер содержит композицию, которая включает по меньшей мере одно антитело к PD-L1, предлагаемое в изобретении. Дополнительные контейнеры могут содержать, например, разбавители и буферы, контрольные антитела. Этикетка или листовка-вкладыш в упаковке могут содержать описание композиции, а также инструкции по их применению in vitro или для целей диагностики.
Диагностическое использование и композиции
Антитело к CD47 и PD-L1 по настоящему изобретению также используются в диагностических процессах (например, in vitro, ex vivo). Например, антитело к CD47 и PD-L1 может использоваться для обнаружения или измерения уровня CD47 и/или PD-L1 в образцах, полученных от пациента (например, образец ткани или образец жидкости тела, такой как воспалительный экссудат, кровь, сыворотка крови, жидкость кишечника, слюна или моча). Подходящие методы обнаружения и измерения включают иммунологические методы, такие как проточная цитометрия, твердофазный иммуноферментный анализ (ИФА), хемилюминесцентный анализ, радиоиммуноанализ и иммуногистология. Изобретение далее включает наборы (например, диагностические наборы), содержащие антитела к CD47 и PD-L1, описанные в данном документе.
Примеры
Для наилучшего понимания изобретения приводятся следующие примеры. Эти примеры приведены только в иллюстративных целях и не должны толковаться как ограничивающие сферу применения изобретения в любой форме.
Все публикации, патенты и патентные заявки, указанные в этой спецификации включены в данный документ путем отсылки. Хотя вышеупомянутое изобретение было довольно подробно описано путем иллюстрации и примера в целях исключения двусмысленного толкования, специалистам в данной области на основе идей, раскрытых в данном изобретении, будет вполне понятно, что могут быть внесены определенные изменения и модификации без отклонения от сущности и объема прилагаемых вариантов осуществления изобретения.
Пример 1.
Продукция рекомбинантных антигенов и антител в суспензионной культуре клеток млекопитающих.
Последовательности экстраклеточных доменов человека CD47 (Leu19-Val134) и PD-L1 (Phe19-Arg238) (SEQ ID NO: 107-108) клонировали в плазмиду для наработки белка в клетках млекопитающих с тагом Fc (фиг. 1) по сайтам рестрикции SalI/NotI. Плазмиды нарабатывали в необходимых количествах в клетках E.Coli и очищали при помощи набора Qiagen.
Последовательности вариабельных доменов антитела к CD47 (B6H12, Stanford University, US20130142786) клонировали в плазмиды для наработки белка в формате IgG1 в клетках млекопитающих. Плазмиды нарабатывали в необходимых количествах в клетках E.Coli и очищали при помощи набора Qiagen.
Антитела и антигены продуцировали в клетках постоянной клеточной линии, полученной из клеток яичника китайского хомячка (линия CHO-T). Суспензионное культивирование осуществляли в колбах на орбитальном шейкере, с использованием бессывороточных сред производства компании Life Technologies Corporation и согласно инструкциям производителя. Для транзиентной экспрессии клетки в концентрации 2*106/мл трансфецировали с помощью линейного полиэтиленимина (например, ПЭИ «MAX», компания «Polysciences»). Соотношение ДНК/ПЭИ составляло 1:3/1:10. Через 5-7 дней после трансфекции культуральную среду центрифугировали при 2000 g в течение 20 минут и фильтровали через фильтр с размером пор 0,22 мкм. Целевые белки выделяли из культуральной жидкости с помощью аффинной хроматографии.
Рекомбинантные белки с Fc из культуральной жидкости выделяли и очищали, используя колонку для аффинной хроматографии с протеином А. Осветленную культуральную жидкость пропускали через колонку HiTrap rProtein A Sepharose FF объемом 5 мл (GE Healthcare), уравновешенную фосфатно-солевым буфером (ФСБ, pH 7,4). Затем колонку промывали 5 колоночными объемами ФСБ, чтобы вымыть неспецифически связывающие компоненты. Связанный антиген элюировали, используя 0,1 М глициновый буфер рН 3. Главный протеиновый пик элюции собирали и доводили его рН до нейтральности с помощью 1 М буфера Tris (рН 8). Все стадии проводили при скорости потока 110 см/ч. Далее белок переводили в ФСБ (pH 7,4) с помощью диализа, используя технологию SnakeSkin Dialysis Tubing, фильтровали (0,22 мкм), переносили в пробирки и хранили при -70°С.
Чистоту полученного раствора белка оценивали с помощью SDS-гель-электрофореза в 12% ПААГ нередуцирующих условиях Фиг 2.
Пример 2.
Получение полноразмерных антител.
Клонирование проводили по стандартной методике. Нарабатывали ПЦР-продукты, содержащие гены вариабельных доменов тяжелой и легкой цепей антител с праймерами содержащими сайты рестрикции. Вариабельный домен тяжелой цепи клонировали в вектор pEE-Hc IgG1 по сайтам рестрикции Sal1/Nhe1. Вариабельный домен легкой цепи клонировали в вектор pEE-CK по сайтам рестрикции Sal1/BsiW1. Полученные генетические конструкции передали на транзиентную наработку белков в клеточной линии CHO-T. Белки выделяли и очищали по стандартной методике путем аффинной хроматографии на бактериальном белке Protein A как описано в Примере 1. Электрофорез проводили в денатурирующем 12% ПААГ c добавлением меркаптоэтанола Фиг.3 и денатурирующем 8% ПААГ без добавлением меркаптоэтанола Фиг.4
Пример 3.
Создание наивной фаговой Fab-библиотеки человеческих антител MeganLibTM.
Суммарную РНК В-лимфоцитов из индивидуальных образцов крови более тысячи человеческих доноров выделяли с помощью набора RNeasy Mini Kit согласно предлагаемому протоколу (от QIAGEN). Концентрацию РНК определяли с помощью набора Nanovue (от GE Healthcare) и проверяли качество выделенной РНК с помощью электрофореза в 1,5%-ном агарозном геле.
Реакцию обратной транскрипции проводили с использованием набора MMLV RT kit (от Evrogen) согласно рекомендуемому протоколу с использованием обратной транскриптазы MMuLV и рандом-гексамерных олигонуклеотидов в качестве затравки.
Продукты обратной транскрипции использовали в качестве матрицы в двухступенчатой полимеразной цепной реакции для получения генов вариабельных доменов, фланкированных сайтами рестрикции, с использованием набора олигонуклеотидов по протоколам авторов [J Biol Chem. 1999 Jun 25; 274(26): 18218-30].
Полученный ДНК препарат VL-CK-VH (обрабатывали эндонуклеазами рестрикции NheI/Eco91I и лигировали в оригинальную фагмиду pH5. Продукты лигирования трансформировали в электрокомпетентные клетки штамма SS320 E.Coli, приготовленные согласно протоколам [Methods Enzymol. 2000;328: 333-63.]. Репертуар комбинаторной фаговой Fab-дисплейной библиотеки MeganLibTM составлял 1011 трансформантов. Препараты фага Fab-библиотек готовили согласно процедуре, описанной ранее [J Mol Biol. 1991 Dec 5;222(3): 581-97].
Пример 4.
Иммунизация ламы CD47 антигеном человека и создание фаговой дисплейной библиотеки фрагментов антител ламы.
Животное Lama Glama последовательно иммунизировали 5 раз путем подкожного введения антигенного материала, смешанного с равным объемом полного (при первой инъекции) или неполного (при остальных инъекциях) адъюванта Фрейнда. В качестве антигена использовали рекомбинантный белок CD47 человека, описанный в Примере 1 по 1 мг на 1 инъекцию. Инъекции антигенов проводили на следующих сроках: 0, 2, 4, 5, 8 недели. Взятие крови (50 мл) проводили через 5 дней после каждой инъекции, начиная с третьей. В качестве антикоагулянта применяли 3,8% цитрат натрия в соотношении 1:9. Отобранную кровь ламы разводили в 2 раза стерильным физиологическим раствором. 30 мл разбавленного раствора крови наслаивали на среду Lymphoprep™ (Axis-Shield, Norway) с плотностью 1,077 г/мл объемом 15 мл и проводили центрифугирование в течение 20 мин при 800g. Мононуклеарные клетки (лимфоциты и моноциты) отбирали из интерфазной зоны плазма/среда Lymphoprep, после чего промывали стерильным раствором PBS.
Полученный титр сывороточного иммуноглобулина против CD47, оцененный согласно стандартному протоколу, оказался не менее 1/100000, что является достаточным для приготовления библиотеки антител.
Суммарную РНК мононуклеарных клеток ламы выделяли с помощью набора RNeasy Mini Kit согласно предлагаемому протоколу (QIAGEN). Концентрацию РНК определяли с помощью Nanovue (GE Healthcare) и проверяли качество выделенной РНК с помощью электрофореза в 1,5%-ном агарозном геле.
Реакцию обратной транскрипции проводили с использованием набора MMLV RT kit (от Evrogen) согласно рекомендованному протоколу с использованием обратной транскриптазы MMuLV и рандом-гексамерных олигонуклеотидов в качестве затравки.
Продукты обратной транскрипции использовали в качестве матрицы в двухступенчатой полимеразной цепной реакции для получения генов монодоменов VHH, scFv или Fab фланкированных сайтами рестрикции, с использованием набора олигонуклеотидов и протоколам авторов [FASEB J. 2007 Nov;21(13):3490-8]. Полученный ДНК препарат генов VHH обрабатывали рестриктазами NcoI /NotI и лигировали в оригинальную фагмиду pscFv, аналогичной по всем элементам pHEN2, использованной в работе [FASEB J. 2007 Nov;21(13):3490-8]. Продукты лигирования трансформировали в электрокомпетентные клетки штамма SS320, полученные согласно протоколам [Methods Enzymol. 2000;328: 333-63.]. Репертуары библиотек на основе VHH составили 0,5-2*10E+8 независимых трансформантов. Репертуары библиотек на основе scFv и Fab составили 0,5-2*10E+9 и 1,2-2,5*10E+9 соответственно. Препарат фага библиотек был приготовлен согласно процедуре, описанной ранее [J Mol Biol. 1991 Dec 5;222(3): 581-97].
Пример 5
Селекция фаговых дисплейных-библиотек фрагментов антител
Специфичные фаговые антитела против CD47 были получены из фаговой Fab, VHH или scFv дисплейных библиотек (Примере 3, 4) путем стандартных селекционных процедур, описанных ранее [EMBO J. 1994 Jul 15;13(14):3245-60, Nat Biotechnol. 1996 Mar;14(3):309-14; J Mol Biol.1991 Dec 5;222(3): 581-97], но с использованием магнитных частиц и прибора KingFisher Flex, так как использование данной методики позволяет проводить параллельно до 96 различных схем и вариантов.
Человеческий биотинилированный антиген PD-L1 и CD47 (Fc, EPEA) направленно иммобилизовали на поверхность стрептавидиновых магнитных частиц (streptavidin magnetic beads, NEB) в концентрации 10 мкг/мл для первого раунда, 2 мкг/мл для второго, 0,4 и 0,2 мкг/мл для третьего и четвертого, соответственно. Антиген инкубировали с частицами в течение 1 часа при комнатной температуре на ротаторе. Далее частицы отмывали ФСБ (pH 7,4) и блокировали поверхность частиц раствором 2% обезжиренного молока или 1% БСА на ФСБ (pH 7,4) в течение 1 часа. Человеческую фаговую библиотеку MeganLibTM разводили в концентрации 2*10 13 фаговых частиц на мл в ФСБ (pH 7,4) с 2% обезжиренным молоком и нецелевым антигеном с тагом целевого антигена и преселектировали с магнитными частицами, не содержащими антиген на поверхности, для удаления неспецифически связывающихся фагов. IL-5Rα-покрытые магнитные частицы затем были инкубированы с MeganLibTM в течении 1-2 часов при комнатной температуре.
Несвязавшиеся фаги удаляли в ходе нескольких отмывок магнитных частиц раствором ФСБ (pH 7,4) с 0,1% Твин 20. Количество отмывок увеличивали от раунда к раунду (на 1-ом раунде 3 отмывок, на 2-ом − 9 и на 3-ем – 12, на 4-ом-15). Фаги, связавшиеся с антигеном на поверхности магнитных частиц, элюировали с частиц 100 мM раствором Gly-HCl (pH 2,2) в течение 15 мин при перемешивании, после элюции нейтрализовали раствор 1M TRIS-HCl (pH 7.6). Бактерии штамма Е. coli TG1 инфицировали фагами и нарабатывали в культуре, после чего выделяли их и использовали в следующем раунде селекции. После трех-четырех раундов из культуры Е. coli TG1 выделяли фагмидную ДНК согласно стандартному протоколу производителя (Qiagen). Обогащение библиотеки на целевые антигены и оценку присутствия неспецифически связывающихся фаговых частиц проводили при помощи иммуноферментного анализа поликлонального фага (ИФА).
Пример 6.
Иммуноферментный анализ поликлонального фага на специфические и неспецифические антигены.
Для проведения ИФА на высоко-сорбционные плашки (Greiner-Bio) иммобилизовали целевой антиген (CD47 и PD-L1) и нецелевой (с Fc-фьюжн белком). Белок добавляли в концентрации 1 и 5 мкг/мл соответственно, в 0,1 M NaHCO3 (pH 9.0) и титровали с шагом 2 до 7 разведения, после чего, герметично закрытые плашки инкубировали в течение ночи при +4°С. Все последующие этапы проводили по стандартному ИФА протоколу с использованием высокопроизводительной автоматизированной платформы на базе роботизированной системы Tecan Freedom EVO 200 (от Tecan). Для блокирования неспецифического связывания в лунки планшетов добавляли блокирующий буфер 2% обезжиренное молоко или 1% БСА на ФСБ (pH 7,4). Планшеты инкубировали в течение часа при комнатной температуре. После отмывок фосфатно-солевым буфером, содержащим Твин-20 (ФСБТ), добавляли по 50 мкл на лунку тестируемого поликлонального фага. После промывания добавляли (50 мкл/лунку) анти-M13 HRP-конъюгированного вторичного антитела (от Pierce-ThermoScientific) в соотношении 1:7500 в ФСТБ. После инкубации 50 минут при комнатной температуре планшеты отмывали ФСТБ три раза. Колориметрический сигнал развивали добавлением субстратного раствора (Н2О2-0,02% и ТМБ в CH3COONa рН5.5) на 10 минут, затем реакцию останавливали добавлением 1% серной кислоты (20 мкл). Цветовой сигнал измеряли при длине волны 450 нм, используя подходящий планшет-ридер Tecan-Sunrise (от Tecan).
После третьего и четвертого раунда селекции на целевом антигене проведенный ИФА анализ препарата поликлонального фага показал значительное обогащение Фиг. 5. Для реклонирования и дальнейшего скрининга отобрали библиотеки, у которых наблюдали превышение сигнала более чем в 5 раз на минимальном разведении фаговых библиотек на негомологичные контрольные антигены.
Пример 7.
Реклонирование генов фрагментов антител в экспрессионную плазмиду.
Реклонирование генов вариабельных доменов антител в экспрессионную плазмиду из фагмидного вектора после успешных раундов селекции осуществляли по стандартному протоколу с применением рестриктазно лигазного метода.
Полученный пул клонов, обогащенных VHH монодоменами или scFv, специфичных против CD47, был реклонирован в экспрессионную плазмиду pET-22 (Novagen) под контроль T7 промотора, содержащую дополнительно myc-tag и His6 tag последовательности на С- конце VHH. Гены Fab фрагментов для библиотек, содержащих обогащенные последовательности против CD47 антигена, были реклонированы в pLL4 экспрессионный вектор, под контролем lac промотора, и содержащий дополнительно myc-tag и His6 tag последовательности на С- конце CH1 домена тяжелой цепи.
В последующем экспрессионные вектора содержащие фрагменты антител, трансформировали в штамм E. coli Bl21(DE3)Gold (Stratagene) для наработки фрагментов антител путем секреции в культуральную среду и проведения сравнительного анализа аффинности вариабельных фрагментов антител из дисплейных библиотек к антигену методом ИФА с использованием технологической платформы Mabnext Flow Chart.
Пример 8.
Анализ специфического связывания scFv или VHH монодомена с CD47-Fc человека.
ИФА (ELISA) использовали для измерения связывания исследуемых специфических фрагментов антител, из Примера 4, с CD47-Fc человека. Для анализа специфического связывания лунки планшетов ELISA (от Nunc ImmunoMaxisorp) покрывали 50 мкл (0,5 мкг/мл в 1X покрывающем карбонатном буфере) CD47-Fc человека (Биокад), герметично закрывали и инкубировали в течение ночи при 4°С. Все последующие этапы проводили по стандартному ИФА протоколу с использованием высокопроизводительной автоматизированной платформы на базе роботизированных систем GenetixQ-pix2xt (от Molecular Device) и Tecan Freedom EVO 200 (от Tecan). Для блокирования неспецифического связывания добавляли блокирующий буфер BB (200 мкл 0,5% нежирного молока в PBS). Планшеты инкубировали на шейкере в течение часа при комнатной температуре. После отмывок PBS-Твином добавляли по 100 мкл на лунку тестируемого клеточного супернатанта, содержащего исследуемый фрагмент антитела. Планшеты снова инкубировали, встряхивая, один час при комнатной температуре, после чего каждую лунку планшетов пять раз промывали буфером PBS-Твин. После промывания добавляли (50 мкл/лунку) mouse анти-MYC IgG clone 9E10 (ThermoFisher Scientific) в соотношении 1:5000 в PBS-Твин. Планшеты встряхивали на ротационном шейкере (50 мин, комнатная температура) и промывали пять раз буфером PBS-Твин, как описано выше. После промывания добавляли (50 мкл/лунку) anti-mouse IgG HRP конъюгат (ThermoFisher Scientific) в соотношении 1:10000 в PBS-Твин. Планшеты встряхивали на ротационном шейкере (50 мин, комнатная температура) и промывали пять раз буфером PBS-Твин, как описано выше. Колориметрический сигнал развивали добавлением ТМВ (50 мкл/лунку) до насыщения (в среднем 10-12 мин), затем дальнейшее развитие останавливали добавлением стопового раствора (25 мкл/лунку, 1% серная кислота). Цветовой сигнал измеряли при длине волны 450 нм, используя подходящий планшет-ридер Tecan-Sunrise (от Tecan). Степень связывания антитела была пропорциональна продуцированию цветового сигнала. Клоны, у которых цветовой сигнал превышал фоновый более чем в 5 раз, были проверены в конкурентном ИФА анализе для выявления антагонистических специфических фрагментов антител, блокирующих взаимодействие SIRP-Fc лиганда (BIOCAD) и рецептора CD47-Fc человека в условиях аналогичных описываемым [WO2016048188 A8] и с пониженным в 4 раза сигналом относительно контроля, не содержащего анализируемые фрагменты антител.
В результате скрининга 2400 клонов было получено 265 клонов scFv и VHH с указанным 5-кратным превышением в сигнале над фоном. Из данной панели позитивных клонов было получено 27 антагонистических клонов способных блокировать взаимодействие SIRP-Fc лиганда (BIOCAD) и рецептора CD47-Fc человека. Нуклеотидная последовательность генов позитивных клонов была определена секвенированием по Сенгеру на приборе 3130xl Genetic Analyzer (Applied Biosystems). В качестве примера, было получено шесть клонов VHH монодоменов различных по последовательности более чем на 1 аминокислоту, но имеющих более 90% гомологии каждого из CDR участка друг с другом, что указывает на их происхождение от одного родительского клона путем in vivo матурации в иммунизированной ламе (Таблица1).
Таблица 1. Последовательности специфических CD47 связывающих VHH монодоменов с CD47 человека.
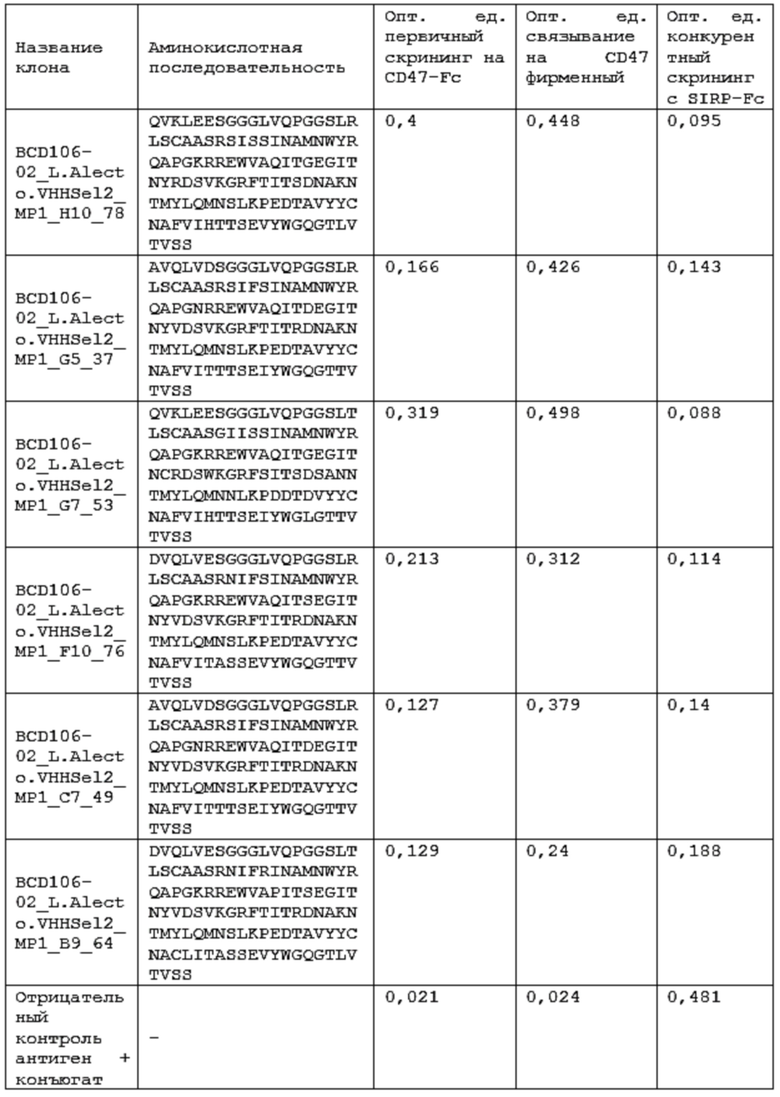
Пример 9.
Анализ специфического связывания Fab фрагментов с CD47-Fc человека.
Наработку Fab проводили по стандартной методике: бактериальные клетки трансформировали экспрессионными векторами, содержащими гены Fab, а последующее добавление индуктора, который запускает транскрипцию lac-оперона, в среду при культивировании полученных трансформантов вызывает экспрессию Fab.
Далее проводили ИФА с целью поиска Fab, связывающих CD47 человека.
В качестве позитивного контроля использовали B6H12 Fab с опубликованной последовательностью (см. пример 1). Для анализа специфического связывания лунки планшетов ELISA (high binding от Greiner bio one) покрывали 50 мкл CD47 Fc lama (0,2 мкг/мл в 1× карбонатном буфере), герметично закрывали и инкубировали в течение ночи при 4°С. Все последующие этапы проводили по стандартному протоколу ИФА с использованием высокопроизводительной автоматизированной платформы на базе роботизированных систем Genetix Qpix2xt (от Molecular Device) и Tecan Freedom EVO 200 (от Tecan). Для блокирования неспецифического связывания добавляли блокирующий буфер BB (200 мкл 0,5% нежирного молока в ФСБ). Планшеты инкубировали в течение часа при комнатной температуре. После отмывок ФСБ-Твином добавляли по 60 мкл на лунку тестируемого клеточного супернатанта, содержащего исследуемый Fab. Планшеты снова инкубировали один час при комнатной температуре, после чего каждую лунку планшетов три раза промывали буфером ФСБ-Твин. После промывания добавляли (50 мкл/лунку) анти-человеческого Fab HRP-конъюгированного вторичного антитела (от Pierce-ThermoScientific) в соотношении 1:7500 в ФСБ-Твин. Планшеты инкубировали 1 час при комнатной температуре и промывали три раза буфером ФСБ-Твин, как описано выше. Колориметрический сигнал развивали добавлением ТМВ (50 мкл/лунку) до насыщения (15 мин), затем дальнейшее развитие останавливали добавлением стопового раствора (25 мкл/лунку, 1% серная кислота). Цветовой сигнал измеряли при длине волны 450 нм, используя подходящий планшет-ридер Tecan-Sunrise (от Tecan). Степень связывания антитела была пропорциональна продуцированию цветового сигнала. Клоны, у которых цветовой сигнал превышал сигнал от контрольного антитела, проверяли в ИФА на неспецифическое связывание.
Пример 10.
Анализ неспецифического связывания Fab фрагментов с различными антигенами человека.
Целью вторичного скринига является отбор клонов, продуцирующих Fab, которые взаимодействуют с полноразмерным антигеном CD47 и не взаимодействуют с неспецифичными антигенами, а также конкурируют с лигандом (CD47) за связывание с SIRPa.
Для анализа неспецифического связывания исследуемых Fab-фрагментов с другими антигенами использовали ИФА (ELISA). Исследование проводили, как описано выше, но в качестве антигенов для иммобилизации использовали 3DHer3-H6E, INFα2b, PD-L1-Fc-lama (2,5 мкг/мл в 1× карбонатном буфере). В качестве контроля специфического связывания использовали CD47 FE и CD47 Fc lama (0,2 мкг/мл в 1× карбонатном буфере). Все последующие этапы проводили по стандартному протоколу ИФА с использованием высокопроизводительной автоматизированной платформы на базе роботизированных систем Genetix Qpix2xt (от Molecular Device) и Tecan Freedom EVO 200 (от Tecan).
Конкурентный ИФА (ELISA) использовали для проверки отобранных ранее специфичных Fab против CD47 человека на способность блокировать взаимодействие с рецептором SIRPa. В качестве позитивного контроля антагониста использовали Fab с опубликованной последовательностью (см. пример 1).
SIRPa иммобилизовали в лунках планшетов ELISA (high binding от Greiner bio one) по 50 мкл с концентрацией 0.5 мкг/мл в 1× карбонатном буфере и инкубировали в течение ночи при 4°С. Все последующие этапы проводили по стандартным ИФА протоколам с использованием высокопроизводительной автоматизированной платформы на базе роботизированных систем Genetix Qpix2xt (от Molecular Device) и Tecan Freedom EVO 200 (от Tecan). Для блокирования неспецифического связывания добавляли блокирующий буфер BB (200 мкл 0,5% нежирного молока в ФСБ). Планшеты инкубировали в течение часа при комнатной температуре.
Параллельно в несорбирующих планшетах смешивали в соотношении 1:1 клеточный супернатант, содержащий тестируемый Fab и CD47 Fc lama (в конечной концентрации 1 мкг/мл в ФСБ-Твин), инкубировали в течение 45 минут при комнатной температуре.
После отмывок от BB планшета, содержащего рецептор SIRPa, туда переносили смесь Fab и CD47 Fc lama, инкубировали в течение 45 минут при комнатной температуре. После чего каждую лунку планшетов три раза промывали буфером ФСБ-Твин, добавляли по 50 мкл/лунку анти-человеческого Fab HRP-конъюгированного вторичного антитела (от Pierce-ThermoScientific) в соотношении 1:7500 в ФСБ-Твин. Инкубировали 45 мин при комнатной температуре, после чего каждую лунку планшетов три раза промывали буфером ФСБ-Твин, как описано выше. Колориметрический сигнал развивали добавлением ТМВ (50 мкл/лунку) до насыщения (в среднем 15 мин), затем дальнейшее развитие останавливали добавлением стопового раствора (25 мкл/лунку, 1% серная кислота). Цветовой сигнал измеряли при длине волны 450 нм, используя подходящий планшет-ридер Tecan-Sunrise (от Tecan). Степень связывания Fab была обратно пропорциональна продуцированию цветового сигнала. Клоны, показавшие блокирование на уровне контрольного Fab антитела, отмечали как позитивные и использовали в дальнейших анализах. Гены вариабельных доменов позитивных клонов секвенировали, согласно стандартным протоколам на аппарате Applied Biosystems 3130 Genetic Analyzer (Applied Biosystems) и анализировали.
Пример 11.
Сравнительный скрининг анти-CD47 фрагментов антителпо кинетической константе диссоциации koff (kdis).
В качестве примера анализа кинетических параметров взаимодействия фрагментов антител, специфически связывающихся с рецептором CD47, провели измерение VHH фрагментов антител. Сравнительный скрининг по константе диссоциации (kdis) для VHH-фрагментов проводили с использованием прибора Octet Red 96 и аминореактивных биосенсоров ARG2 (Pall-ForteBio). Константы аффинности можно рассчитать, зная точную концентрацию белка в анализируемом растворе и, так как в качестве раствора белков были использованы среды роста клеток и концентрации белков не были измерены, то кандидаты сравнивали друг с другом по их константе диссоциации. Биосенсоры заранее регидратировали в течение часа в воде. После активации биосенсеров CD47-Fc в концентрации 10 мкг\мл в ацетатном буфере рН4 был неспецифически (по NH2 –группам) иммобилизован на поверхности биосенсора. Затем сенсоры погружались в лунки с клеточной средой роста со специфическими VHH (ориентировочно от 1 мкг VHH в 1 мл среды), где происходила ассоциация комплекса. После этого сенсоры погружались в буферный раствор, в котором и проходила последующая стадия диссоциации комплекса. В исследуемые образцы среды роста клеток E. Coli, содержащих анти-CD47 VHH-фрагменты, добавляли 1/10 объема 10x-рабочего буфера и перемешали. Анализ полученных кривых проводили с помощью программного обеспечения OctetDataAnalysis (версия 7.0) согласно стандартной процедуре с использованием модели взаимодействия 1:1.
Результаты koff-скрининга анти-CD47 VHH кандидатов представлены в Таблице 2. Продемонстрировано специфическое связывание всех VHH-фрагментов с CD47 человека, кандидат BCD106-02_L.Alecto.VHHSel2_MP1_C7_49 по преимущественному kdis был выбран для дальнейшей работы и реклонирования для получения биспецифических антител.
Таблица 2. Кинетические константы диссоциации VHH с CD47-Fc
Пример 12.
Получение конструкций и наработки ассиметричных биспецифических против CD47 и PD-L1 антител.
Последовательности всех вариабельных доменов оптимизированных scFv-фрагментов, также как и последовательности генов для синтеза дикого и мутантных вариантов вариабельного домена VHH кандидата BCD106-02-VHH_C7_49 (Таблица 3) и гены вариабельных доменов легких и тяжелых цепей anti-PD-L1 антитела (BCD135 -оригинальное антитело человека компании BIOCAD) получали de novo расчетом с использованием фирменных компьютерных алгоритмов и ПЦР-синтезом из олигонуклеотидов, полученных на на синтезаторах ASM-2000 (Новосибирск) оп стандартному протоколу [http://www.openwetware.org/wiki/DNA_Synthesis_from_Oligos]. Длинные гены scFv были наработаны из генов VH и VL двух этапной ПЦР-синтеза из одноцепочечных молекул ДНК. После ПЦР синтеза фракционированные на агарозном геле фрагменты ДНК были очищены на колонках QIAquick Gel Extraction Kit (Qiagen) Гены scFv и VHH лигированы индивидуально в плазмиду pEE-Fc(knob), тогда как вариабельные домен тяжелой цепи специфичного aPD-L1 антитела в pEE-Fc(hole) плазмиду. При этом pEE-Fc(knob) содержит Fc IgG1 человека с мутациями S354C+T366W и pEE-Fc(hole) содержит Fc IgG1 человека с мутациями Y349C+T366S+L368A, обеспечивающими гетеродимеризацию этих Fc частей друг с другом, при минимальной степени гомодимеризации [Nat Biotechnol. 1998 Jul;16(7):677-81.] при совместной транзиентной экспрессии в клетках CHO-EBNA с вариабельным доменом легкой цепи aPD-L1, аналогично клонированную в pEE-Clambda. После реакции безлигазного клонирования методом модифицированного LIC [Aslanidis C, de Jong PJ. Ligation-independent cloning of PCR products (LIC-PCR). Nucleic Acids Res. 1990;18:6069–6074]) ДНК трансформировали в E.coli. Корректные по последовательности конструкции pEE-Fc(knob)-scFv или pEE-Fc(knob)-VHH котрансфецировали с pEE-BCD135-VH-299P-HC-hole и pEE-BCD135-01 4LG VL hzau CL для получения так называемых ассиметричных биспецифических антител (см. фиг. 6). На данном рисунке представлены схематично модели ассиметричных биспецифических антител, А- на основе связывающих фрагментов anti-CD47 scFv и anti-PD-L1 Fab, Б- на основе связывающих фрагментов anti-CD47 VHH и anti-PD-L1 Fab. Полученные генетические конструкции были использованы в наработку белков в клеточной линии CHO-Т, согласно Примеру 2. Антитела после очистки были высокогомогенны по составу, продукционные выходы биспецифических антител варьировали от 60 до 260 мг/мл культуральной среды. На фиг. 7 приведены примеры очищенных биспецифических антител на основе anti-CD47 scFv фрагментов. На фиг. 8 приведены примеры очищенных биспецифических антител на основе anti-CD47 VHH фрагментов. Вариант антитела содержащий указанную в таб.3 VHH47Opt3 последовательность дал крайне низкий выход антитела и был исключен из дальнейших анализов.
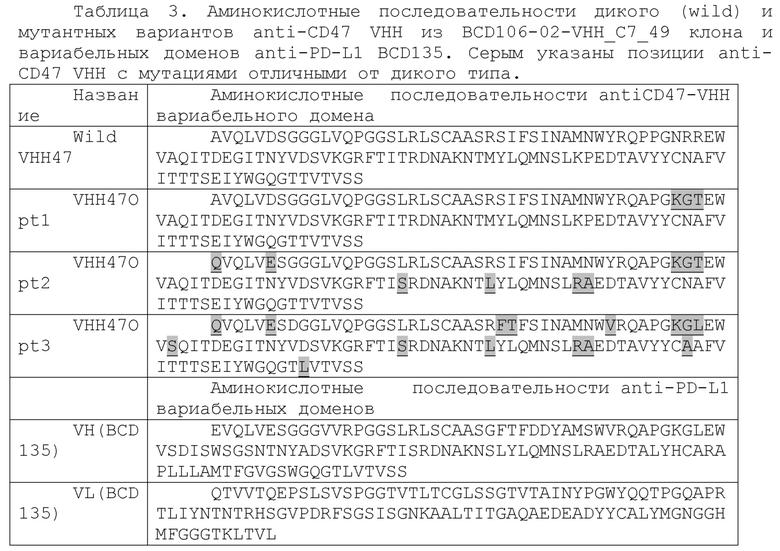
Пример 13.
Анализ взаимодействия anti-PD-L1/anti-CD47 биспецифических антител PD-L1 с антигенами PD-L1 и CD47 человека на приборе OctetRED96.
Анализ взаимодействия биспецифических антител PD-L1 с антигенами PD-L1 и CD47 человека проводили на приборе OctetRed 96 (Pall-ForteBio). Биосенсоры AR2G заранее были регидратированы в течение часа в mQ. После активации биосенсеров PD-L1-Fc или CD47-Fc в концентрации 25 мкг\мл в ацетатном буфере рН4 были неспецифически (по NH2 –группам) иммобилизованы на поверхности биосенсора. Затем сенсоры погружались в лунки с растворами anti-PD-L1/anti-CD47 антитела (10 мкг\мл). В этом растворе происходила ассоциация комплекса антитела и антигена. После этого сенсоры погружались в буферный раствор для последующей стадии диссоциации. Кривые связывания с вычетом базового сигнала анализировали с помощью программы Octet Data Analysis (версия 8.2) согласно стандартной процедуре с использованием модели взаимодействия 1:1.
Результаты анализов приведены в таблице 4. Таким образом можно заключить что антитела высокоаффинны, при этом аффиность к PD-L1 антигену в антителах такого формата составила нМ значения, тогда как аффиность к CD47 антигену имеет субнМ значения. Такое связывание считается достаточным для взаимодействия антитела с рецепторами на клетках мишени, для последующей проверки как in vitro так in vivo терапевтической активности.
Таблица 4. Кинетические константы диссоциации anti-CD47/anti-PD-L1 биспецифических антител.

Пример 14.
Анализ взаимодействий anti-PD-L1/anti-CD47 биспецифических антител с рецепторами CD47 и PD-L1 макаки циномолгус на приборе Forte Bio Octet RED 384.
Эксперименты по исследованию аффинности связывания антител к антигенам CD47 и PD-L1 животных проводили на приборе Forte Bio Octert RED 384. Антитела в концентрации 20 мкг/мл иммобилизовали на поверхность AR2G сенсоров (Forte Bio) по стандартному протоколу согласно инструкции производителя. Анализ проводили при 30°С c использованием ФСБ, содержащим 0,1% Твин-20 и 0,1% БСА в качестве рабочего буфера. После того как в буферном растворе прописывали базовую линию сенсоры погружали в лунки с раствором антигенов (CD47 животных и PD-L1) на 300 секунд, где происходила ассоциация комплекса. Затем детектировали диссоциацию комплекса в буферном растворе в течении 600 секунд.
Кривые связывания с вычетом базового сигнала анализировали с помощью программы Octet Data Analysis (версия 9.0) согласно стандартной процедуре с использованием модели взаимодействия 1:1 Global. Анти-CD47 антитела специфически связываются с антигенами макаки CD47 и PD-L1. Таблица 5 и Таблица 6.
Таблица 5. Кинетические значения взаимодействия антител к антигену макаки (CD-47).
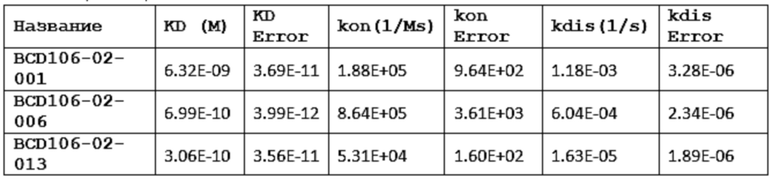
Таблица 6. Кинетические значения взаимодействия антител к антигену макаки (PD-L1).

Пример 15.
Анализ неспецифического связывания anti-PD-L1/anti-CD47 биспецифических антител с панелью антигенов на приборе Forte Bio Octet RED 384.
Эксперименты по исследованию неспецифического связывания проводили на панели неспецифичных антигенов с ГИС-тагом. Для измерения использовались биосенсоры Anti-hIgG Fc Capture (AHC) заранее регедратированые в течение 10 минут в ФСБ, содержащим 0,1% Твин-20 и 0,1% БСА в качестве рабочего буфера.
Антитела в концентрации 30 мкг/мл иммобилизовали на поверхность Anti-hIgG Fc Capture (AHC) сенсоров (Forte Bio). Анализ проводили при 30°С c использованием ФСБ, содержащим 0,1% Твин-20 и 0,1% БСА в качестве рабочего буфера. После того как в буферном растворе прописывали базовую линию, сенсоры погружали в лунки с раствором неспецифичных антигенов на 300 секунд, где происходила ассоциация комплекса. Затем детектировали диссоциацию комплекса в буферном растворе в течение 600 секунд.
Кривые связывания с вычетом базового сигнала анализировали с помощью программы Octet Data Analysis (версия 9.0) согласно стандартной процедуре с использованием модели взаимодействия 1:1 Global. anti-PD-L1/anti-CD47 биспецифических антител не связываются неспецифически с панелью антигенов.
Пример 16.
Анализ взаимодействия anti-PD-L1/anti-CD47 биспецифических антител с панелью FcγRIIIa на приборе Forte Bio Octet RED 384.
Эксперименты по исследованию аффинности антител к панели Fc-связывающих белков проводились на приборе Forte Bio Octert RED 384, с использованием стрептавидиновых (SAX) биосенсоров заранее гедратированых в течение 30 минут в ФСБ, содержащим 0,1% Твин-20 и 0,1% БСА.
Биотинилированные Fc-связывающие белки FcγRIIIa-F158 и FcγRIIIa-V158 с Ави-тагом в концентрации 5 мкг/мл в кинетическом буфере ФСБ, содержащим 0,1% Твин-20 и 0,1% БСА рН 7,4 иммобилизировали на поверхность стрептавидиновых (SAX) сенсоров, с фиксированием tRecLoad - время достижения сигнала уровня равного 0,4 нм. После того как в буферном растворе прописывали базовую линию сенсоры погружали в лунки с раствором антител на 60 секунд, где происходила ассоциация комплекса. Затем детектировали диссоциацию комплекса в буферном растворе в течение 150 секунд.
Кривые связывания с вычетом референсного сигнала анализировали с помощью программы Octet Data Analysis (версия 9.0) согласно стандартной процедуре с использованием модели взаимодействия 2:1 Global. anti-PD-L1/anti-CD47 биспецифических антител специфически связываются с Fc-связывающими белками FcγRIIIa-F158 и FcγRIIIa-V158. Таблица 7 (- и Таблица 8.
Таблица 7. Кинетические значения взаимодействия антител BCD-106(02-001, 03-006, 02-013) к FcγRIIIa-F158.
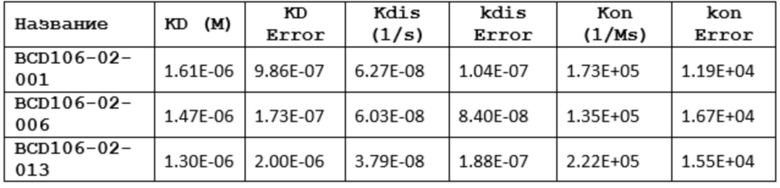
Таблица 8. Кинетические значения взаимодействия антител BCD-106(02-001, 03-006, 02-013) к FcγRIIIa-V158.
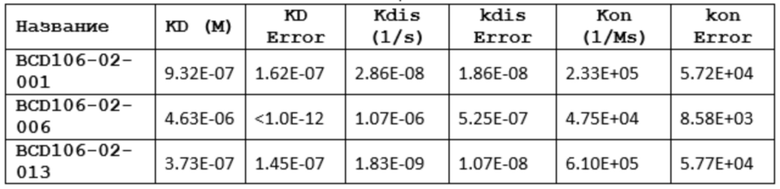
Пример 17.
Анализ взаимодействия anti-PD-L1/anti-CD47 биспецифических антител с FcRn на приборе Forte Bio Octet RED 384.
Эксперименты по исследованию аффинности антител к панели Fc-связывающих белков проводились на приборе Forte Bio Octert RED 384, с использованием стрептавидиновых (SAX) биосенсоров заранее гедратированых в течение 30 минут в ФСБ, содержащим 0,1% Твин-20 и 0,1% БСА.
Биотинилированный FcRn с Ави-тагом в концентрации 5 мкг/мл в кинетическом буфере ФСБ, содержащим 0,1% Твин-20 рН 6 иммобилизировали на поверхность стрептавидиновых (SAX) сенсоров, с фиксированием tRecLoad - время достижения сигнала уровня равного 0,4 нм. После того как в буферном растворе прописывали базовую линию сенсоры погружали в лунки с раствором антител в кинетическом буфере ФСБ, содержащим 0,1% Твин-20 рН 6 на 60 секунд, где происходила ассоциация комплекса. Затем детектировали диссоциацию комплекса в кинетическом буфере ФСБ, содержащим 0,1% Твин-20 и 0,1% БСА рН 7,4 в течение 150 секунд.
Кривые связывания с вычетом референсного сигнала анализировали с помощью программы Octet Data Analysis (версия 9.0) согласно стандартной процедуре с использованием модели взаимодействия 2:1 Global. anti-PD-L1/anti-CD47 биспецифических антител специфически связываются с FcRn. Таблица 9.
Таблица 9. Кинетические значения взаимодействия антител BCD-106(02-001, 03-006, 02-013) к FcRn.
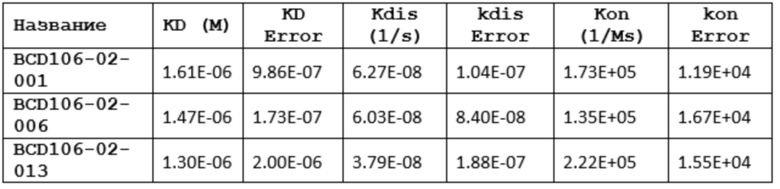
Пример 18.
Анализ способности anti-PD-L1/anti-CD47 биспецифических антител PD-L1 вызывать антитело-зависимую клеточную цитотоксичность на PD-L1 и CD47 позитивных клетках.
Для анализа ADCС (antibody-dependent cellular cytotoxicity – антитело-зависимая клеточная цитотоксичность) использовали клеточную линию MDA-MB-231, экспрессирующую на своей поверхности рецепторы PD-L1 и CD47, и мононуклеарные клетки периферической крови (PBMC).
Получение мононуклеарных клеток периферической крови
PBMC получали фракционированием клеток венозной крови здоровых доноров в градиенте плотности. После выделения клетки культивировали в среде RPMI-1640 c 10% FBS в концентрации 2-5×106 кл/мл 18-24 часов при 37°C 5% CO2.
Подготовка клеток-мишеней
Клетки MDA-MB-231 культивировали в среде DMEM с 10% FBS (фетальной бычьей сывороткой) при 37°C 5% CO2. Клетки снимали с поверхности пластика с помощью трипсина, ресуспендировали в DMEM с 10% FBS. Добавляли Кальцеин AM до концентрации 5 мкМ. Через 30 минут отмывали клетки дважды от избыточного Кальцеина АМ с помощью DMEM с 10% FBS. В среде DMEM с 10% FBS готовили суспензию клеток-мишеней с концентрацией 105кл/мл.
Подготовка разведений исследуемых антител
Все исследуемые антитела разводили средой DMEM с 10% FBS до концентрации 10 мкг/мл. Готовили ряд последовательных разведений с шагом 5. Концентрации исследуемых антител составили (нг/мл): 10000; 2000; 400; 80; 16; 3,2; 0,64; 0,128; 0,0256; 0.
Подготовка PBMC
Мононуклеарные лимфоциты собирали из флаконов. Центрифугировали при 200×g 5 минут. В среде DMEM с 10% FBS готовили суспензию клеток с концентрацией 5×106 кл/мл.
Проведение ADCС теста
В лунки 96-луночного планшета вносили по 50 мкл/лунку исследуемых антител. Добавляли в лунки с антителами по 100 мкл суспензии клеток-мишеней. Инкубировали планшет при 37°С 5% CO2 15-20 минут. Добавляли в лунки с антителами и клетками-мишенями по 50 мкл суспензии PBMC. В три лунки (контроль максимального лизиза – KL) вносили по 50 мкл среды DMEM с 10% FBS, 100 мкл суспензии клеток-мишеней и 50 мкл суспензии PBMC. Инкубировали планшет при 37°С 5% CO2 3,5-4 часа. За 30 минут до окончания инкубации в лунки KL вносили лизирующий буфер.
По окончании инкубации, планшеты центрифугировали при 200×g 10 минут. Надосадочную жидкость переносили в новые 96-луночные планшеты. Измеряли показания флуоресценции в относительных единицах флуоресценции при длине волны возбуждения/излучения 485/538 нм, используя планшетный флуориметр.
Эффективность ADCC рассчитывали по формуле:
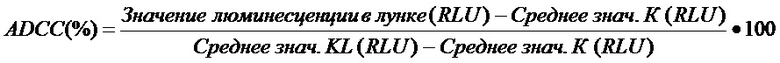 , где
, где
K - контроль спонтанного лизиса клеток-мишеней в присутствии эффекторных клеток (50 мкл/лунку среды DMEM с 10% FBS + 100мкл/лунка клеток-мишеней + 50 мкл/лунка PBMC)
KL - контроль максимального лизиса клеток-мишеней (50 мкл/лунку среды DMEM с 10% FBS + 100мкл/лунка клеток-мишеней + 50 мкл/лунка PBMCs + лизирующий буфер)
Данные экспериментов представлены на фиг. 9 и 10.
Согласно полученным данным, все антитела против CD47/PD-L1 имеют значения EC50, сопоставимые или превосходящие значение EC50 для контрольного воспроизведенного B6H12 моноспецифичяеского антитела против CD47.
Пример 19.
Сравнение активности anti-PD-L1/anti-CD47 биспецифических антител против CD47/PD-L1 в тесте на стимуляцию фагоцитоза макрофагальными клетками человека
Для анализа ADCP (Antibody-Dependent Cellular Phagocytosis – антитело-зависимый клеточный фагоцитоз) использовали клеточную линию MDA-MB-231, имеющую на своей поверхности рецепторы PD-L1 и CD47, и макрофагальные клетки человека.
Получение макрофагов человека
Мононуклеарные клетки периферической крови (PBMC) выделяли из венозной крови здоровых доноров разделением в градиенте плотности. С помощью набора для выделения фракции CD14-позитивных клеток человека (Miltenyi Biotec) выделили моноциты крови человека. В лунках 24-луночного планшета культивировали по 350 000 моноцитов на лунку в 700 мкл RPMI-1640 c 10% FBS, 100 нг/мл GM-CSF (Peprotech) при 37°C 5% CO2 3 суток. На 4 день культивирования сменили среду на новую по 700 мкл RPMI-1640 c 10% FBS, 100 нг/мл GM-CSF (Peprotech), 50 нг/мл IFNγ (Peprotech) и 10 нг/мл LPS (Sigma) на лунку, культивировали клетки при 37°С 5% CO2 еще 3 суток.
Подготовка клеток-мишеней
Клетки MDA-MB-231 культивировали в среде DMEM с 10% FBS (фетальной бычьей сывороткой) при 37°C 5% CO2. Клетки снимали с поверхности пластика с помощью трипсина и суспендировали в DMEM с 10% FBS. Добавляли Кальцеин AM до концентрации 5 мкМ. Через 30 минут отмывали клетки дважды от избыточного Кальцеина АМ с помощью DMEM с 10% FBS. В среде DMEM с 10% FBS готовили суспензию клеток-мишеней с концентрацией 105 кл/мл.
Проведение ADCP теста
Отобрали из лунок планшета с макрофагами среду, внесли в лунки по 500 мкл среды RPMI-1640 c 10% FBS и 20 мкг/мл исследуемых антител. Добавили в лунки по 500 мкл суспензии клеток-мишеней. Инкубировали планшет при 37°С 5% CO2 3 часа. После отобрали среду, сняли клетки с поверхности пластика с помощью реагента TrypLE Express, окрасили клетки флуоресцентно-меченными антителами против CD14. Анализировали суспензию окрашенных клеток на проточном цитофлюориметре.
Эффективность ADCP рассчитывали по формуле:
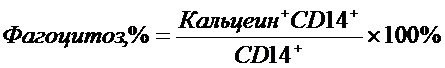 , где
, где
Кальцеин+CD14+ – количество CD14-позитивных клеток, содержащих окраску кальцеином
CD14+ – количество всех CD14-позитивных клеток
Результаты представлены на фиг. 11.
Согласно полученным данным, ряд антител против CD47/PD-L1 имеют эффективность стимуляции фагоцитоза клеток линии MDA-MB-231 макрофагами человека, сопоставимую с эффективностью контрольного воспроизведенного B6H12 моноспецифического антитела против CD47.
Пример 20.
Сравнение влияния кандидатов anti-PD-L1/anti-CD47 биспецифических антител на гемагглютинацию эритроцитов человека
Для анализа способности антител вызывать геммаглютинацию использовались эритроциты человека.
Приготовление суспензии эритроцитов
Произвели забор крови из вены здорового донора в вакуумную пробирку с гепарином. Перенесли 9мл крови в центрифужную пробирку на 50 мл. Кровь развели до 30 мл раствором DPBS без Ca2+ и Mg2+ комнатной температуры. Центрифугировали суспензию при 800g по 10 минут, надосадочную жидкость слили. Дважды повторили процедуру отмывки клеток с помощью DPBS без Ca2+ и Mg2+ и центрифугирования. Затем 300 мкл клеточного осадка ресуспендировали в 30 мл DPBS, в результате чего получили 1% суспензию эритроцитов.
Проведение теста на геммаглютинацию
Испытуемые антитела развели в DPBS до концентрации 20 мкг/мл. В 96 луночном круглодонном планшете смешали по 100 мкл разведений антител и суспензии эритроцитов. Инкубировали планшет в CO2-инкубаторе 16 часов при 37˚С. Учет результатов производили визуально по условной шкале 4 крестов. Достоверно-положительным считается результат от 2 крестов и выше. Результаты представлены в Таблице 10.
Таблица 10. Реакция геммаглютинации в присутствии антител против CD47/PD-L1. Символ – обозначает отсутствие агглютинации.
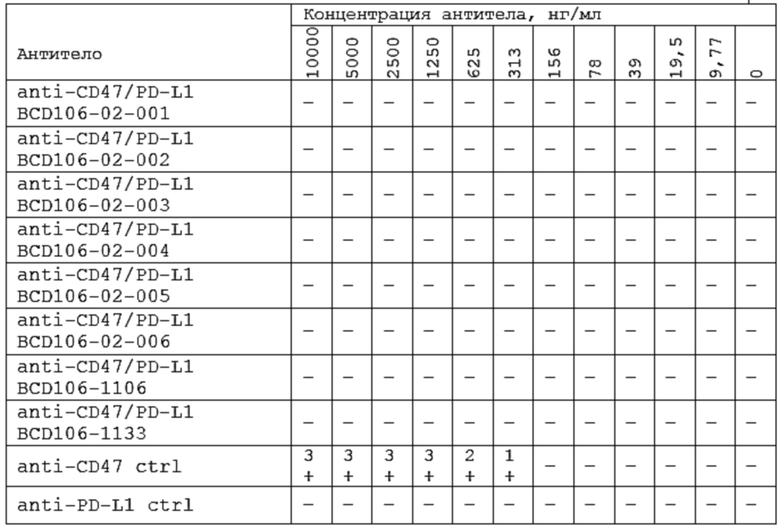
Согласно полученным данным, ни одно из антител против CD47/PD-L1 не вызывают геммаглютинацию, тогда как контрольное воспроизведенное антитела B6H12 моноклонального против CD47 вызывает значительную агглютинацию из-за бивалентного характера антитела, и способности таким образом взаимодействовать с двумя CD47 молекулами, расположенными на разных эритроцитах.
Пример 21.
Анализ комплемент-зависимой цитотоксичности (CDC) биспецифичных анти-CD47/PD-L1 антител.
Для анализа CDC (Complement-Dependent Cytotoxicity – комплемент-зависимая цитотоксичность) в качестве клеток-мишеней использовали линию MDA-MB-231, имеющую на своей поверхности рецепторы PD-L1 и CD47.
Подготовка клеток-мишеней
Культуру MDA-MB-231 культивировали в питательной среде DMEM с добавлением 10% эмбриональной бычьей сыворотки (FBS).
Клетки снимали с поверхности пластика с помощью трипсина и суспендировали в среде DMEM с 0,1% BSA в концентрации 1×106 клеток/мл.
Подготовка разведений исследуемых антител
Все исследуемые анти-CD47/PD-L1 антитела разводили средой DMEM с 0,1% BSA до концентрации 100 мкг/мл. Готовили ряд последовательных разведений с шагом 8. Концентрации исследуемых антител составили (нг/мл): 100000; 12500; 1562,5; 195,3; 24,4; 3,05; 0,38; 0,04; 0,005.
Проведение CDC теста
Разморозили комплемент человека и развели 1:4 в среде DMEM с 0,1% BSA.
В лунки 96-луночного планшета внесли по 50 мкл каждого разведения исследуемых антител, по 50 мкл среды с добавлением 0,1% BSA для каждого образца антитела - контроль клеток, по 150 мкл среды DMEM с 0,1% BSA - контроль среды.
В каждую лунку с исследуемыми антителами и контролем клеток внесли по 50 мкл суспензии клеток MDA-MB-231.
Во все лунки с исследуемыми антителами и контролем клеток внесли по 50 мкл разведенного комплемента. Планшет встряхивали в течение 2-4 мин на орбитальном шейкере при комнатной температуре, поместили в CO2 инкубатор на 2-3 ч с температурой 37ºС.
Добавили по 15 мкл реактива Аламар Синий в лунки анализируемого планшета. Встряхивали планшеты в течение 10-20 минут при комнатной температуре на орбитальном шейкере для перемешивания. Дополнительно инкубировали планшеты в СО2 инкубаторе в течение 18-24 часов.
Встряхивали планшеты в течение 10-20 минут при комнатной температуре на орбитальном шейкере для перемешивания.
Оценили показания флуоресценции в относительных единицах флуоресценции при длине волны возбуждения/испускания 544/590 нм, используя планшетный флуориметр. Полученный сигнал флуоресценции пропорционален количеству жизнеспособных клеток. Результаты представлены на фиг.12-15.
Согласно полученным данным исследуемые антитела не вызывают опосредованный комплементом лизис (CDC) клеточной линии MDA-MB-231.
Пример 22.
Анализ антагонистической активности anti-PD-L1/anti-CD47 биспецифических антител культуре клеток, несущих мембранный PD-L1 рецептор.
Для анализа антагонистической активности анти-PD-L1/CD47 антител против PD-L1 рецептора оценивали способность этих антител реактивировать люциферазный сигнал в репортерной клеточной линии Jurkat-PD1-NFAT-Luc при ко-культивировании с клетками-продуцентами PD-L1.
Подготовка клеток-продуцентов PD-L1
Культуру MDA-MB-231 культивировали в питательной среде DMEM с добавлением 10% эмбриональной бычьей сыворотки (FBS).
Клетки снимали с поверхности пластика с помощью трипсина и суспендировали в концентрации 1*105 клеток/мл в среде DMEM с 10% FBS и 20 нг/мл интерферона гамма. Затем вносили по 200 мкл клеточной суспензии в лунки белого 96-луночного планшета и инкубировали 48ч в CO2 инкубаторе при температуре 37ºС, 5% CO2.
Подготовка разведений исследуемых антител
Все исследуемые анти-CD47/PD-L1 антитела разводили средой RPMI-1640 с 10% FBS до концентрации 5 мкг/мл. Готовили ряд последовательных разведений с шагом 3. Концентрации исследуемых антител составили (нг/мл): 2500; 833,3; 277,7; 92,5; 30,8; 10,2; 3,4; 1,1.
Подготовка клеток Jurkat-PD1-NFAT-Luc
В день постановки эксперимента готовили суспензию клеток Jurkat-PD1-NFAT-Luc с концентрацией 2,5*106 клеток/мл в среде RPMI-1640 с 10% FBS.
Приготовление раствора активирующих антител
В день постановки эксперимента готовили 10-кратную смесь активирующих антител (4 мкг/мл анти-CD3; 4 мкг/мл анти-CD28; 16 мкг/мл анти-mouse в среде RPMI-1640 с 10% FBS).
Проведение теста
Из планшета с клетками MDA-MB-231 удалили среду роста. В лунки с клетками внесли по 40 мкл разведений антител. В контрольные лунки (клетки без исследуемых антител, клетки без исследуемых и активирующих антител) внесли по 40 мкл среды RPMI 1640 10% FBS. Инкубировали при комнатной температуре 30 минут.
Далее во все лунки внесли по 40 мкл суспензии клеток Jurkat-PD1-NFAT-Luc. Затем внесли во все лунки по 10 мкл 10-кратного раствора активирующих антител, кроме контрольных лунок «клетки без исследуемых и активирующих антител». Клетки инкубировали 6 ч в CO2 инкубаторе при температуре 37ºС, 5% CO2.
Внесли во все лунки субстрат к люциферазе One-Glo Luciferase Assay System «Promega» из расчета 1:1 (90 мкл/лунку). Через 5-10 минут измерили уровень люминесценции на планшетном ридере.
Согласно полученным данным Фиг. 16, исследованные anti-PD-L1/anti-CD47 биспецифические антитела, как и контрольное anti-PD-L1 моноспецифическое антитело, являются антагонистами PD-L1-зависимого сигнального пути, и, следовательно, могут стимулировать Т-клеточную зависимую цитотоксичность по отношению к клеткам, несущим PD-L1 рецептор.
Пример 23.
Анализ гомогенности препаратов anti-PD-L1/anti-CD47 биспецифических антител.
Анализ гомогенности препаратов биспецифических антител проводили методом эксклюзионной ВЭЖХ (SEC HPLC) с УФ-детектором. Хроматографию проводили на системе ВЭЖХ Agilent 1100 на колонке Tosoh TSK-Gel G3000SWXL, 7.8 мм x 30 см, кат. № 08541 с предколонкой Tosoh TSKgel Guard SWXL, 6.0 мм x 4.0 см, с диаметром частиц 7 мкм, кат. № 08543. Детектирование проводилось на длинах волн 220 и 280 нм. В качестве примера на Фиг.17 приведен ВЭЖХ профиль препарата BCD106-02-013, на основе VHH47Opt2 (см.пример 12). По результатам данного теста можно заключить, что молекула BCD106-02-013 дает препарат гомогенный 93% по мономеру по агрегационному составу и применим для последующих тестов in vitro и in vivo.
--->
Перечень последовательностей
<110> ЗАКРЫТОЕ АКЦИОНЕРНОЕ ОБЩЕСТВО «БИОКАД»
<120> АНТИТЕЛА СПЕЦИФИЧНЫЕ К CD47 и PD-L1
<140> EA201791961
<141> 2017-10-03
<160> 108
<170> BiSSAP 1.3.6
<210> 1
<211> 5
<212> PRT
<213> Искусственная последовательность
<400> 1
Arg Tyr Trp Met Tyr
1 5
<210> 2
<211> 5
<212> PRT
<213> Искусственная последовательность
<400> 2
Ile Asn Ala Met Asn
1 5
<210> 3
<211> 5
<212> PRT
<213> Искусственная последовательность
<400> 3
Lys Tyr Trp Met Tyr
1 5
<210> 4
<211> 9
<212> PRT
<213> Искусственная последовательность
<400> 4
Ser Ile Phe Ser Ile Asn Ala Met Asn
1 5
<210> 5
<211> 5
<212> PRT
<213> Искусственная последовательность
<400> 5
Asp Tyr Ala Met Ser
1 5
<210> 6
<211> 23
<212> PRT
<213> Искусственная последовательность
<400> 6
Ile Glu Asp Ser Ser Ile Asn Thr Gly Gly Gly Thr Glu Thr Thr Tyr
1 5 10 15
Tyr Thr Asp Ser Val Lys Gly
20
<210> 7
<211> 24
<212> PRT
<213> Искусственная последовательность
<400> 7
Ser Ile Glu Asp Ser Ser Ile Asn Thr Gly Gly Gly Thr Glu Thr Thr
1 5 10 15
Tyr Tyr Thr Asp Ser Val Lys Gly
20
<210> 8
<211> 24
<212> PRT
<213> Искусственная последовательность
<400> 8
Asn Ile Lys Gln Asp Gly Ile Asn Thr Gly Gly Gly Thr Ser Glu Lys
1 5 10 15
Tyr Tyr Val Asp Ser Val Lys Gly
20
<210> 9
<211> 17
<212> PRT
<213> Искусственная последовательность
<400> 9
Ser Ile Glu Asp Ser Ser Glu Thr Thr Tyr Tyr Thr Asp Ser Val Lys
1 5 10 15
Gly
<210> 10
<211> 16
<212> PRT
<213> Искусственная последовательность
<400> 10
Gln Ile Thr Asp Glu Gly Ile Thr Asn Tyr Val Asp Ser Val Lys Gly
1 5 10 15
<210> 11
<211> 18
<212> PRT
<213> Искусственная последовательность
<400> 11
Ser Ile Glu Asp Ser Ser Thr Glu Thr Thr Tyr Tyr Thr Asp Ser Val
1 5 10 15
Lys Gly
<210> 12
<211> 19
<212> PRT
<213> Искусственная последовательность
<400> 12
Ser Ile Glu Asp Ser Ser Ile Thr Glu Thr Thr Tyr Tyr Thr Asp Ser
1 5 10 15
Val Lys Gly
<210> 13
<211> 18
<212> PRT
<213> Искусственная последовательность
<400> 13
Ser Ile Asn Asp Gly Gly Gly Asp Asp Ser Thr Tyr Tyr Ala Asp Ser
1 5 10 15
Val Lys
<210> 14
<211> 16
<212> PRT
<213> Искусственная последовательность
<400> 14
Gly Ile Arg Thr Ser Gly Asp Thr Asp Tyr Ala Asp Ser Val Lys Gly
1 5 10 15
<210> 15
<211> 16
<212> PRT
<213> Искусственная последовательность
<400> 15
Gln Ile Thr Asp Glu Gly Ile Thr Asn Tyr Val Asp Ser Val Lys Gly
1 5 10 15
<210> 16
<211> 17
<212> PRT
<213> Искусственная последовательность
<400> 16
Asp Ile Ser Trp Ser Gly Ser Asn Thr Asn Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 17
<211> 18
<212> PRT
<213> Искусственная последовательность
<400> 17
Gly Asp Tyr Tyr Cys Thr Thr Tyr Glu Cys Gln His Tyr Tyr Gly Met
1 5 10 15
Asp Tyr
<210> 18
<211> 9
<212> PRT
<213> Искусственная последовательность
<400> 18
Val Ile Thr Thr Thr Ser Glu Ile Tyr
1 5
<210> 19
<211> 18
<212> PRT
<213> Искусственная последовательность
<400> 19
Gly Asp Tyr Tyr Cys Thr His Tyr Glu Cys Gln His Tyr Tyr Gly Met
1 5 10 15
Asp Tyr
<210> 20
<211> 12
<212> PRT
<213> Искусственная последовательность
<400> 20
Asn Ala Phe Val Ile Thr Thr Thr Ser Glu Ile Tyr
1 5 10
<210> 21
<211> 13
<212> PRT
<213> Искусственная последовательность
<400> 21
Ala Pro Leu Leu Leu Ala Met Thr Phe Gly Val Gly Ser
1 5 10
<210> 22
<211> 11
<212> PRT
<213> Искусственная последовательность
<400> 22
Arg Ala Ser Gln Ala Ile Ser Ser Tyr Leu Ala
1 5 10
<210> 23
<211> 11
<212> PRT
<213> Искусственная последовательность
<400> 23
Arg Ala Ser Gln Gly Ile Ser Ser Trp Leu Ala
1 5 10
<210> 24
<211> 11
<212> PRT
<213> Искусственная последовательность
<400> 24
Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn
1 5 10
<210> 25
<211> 11
<212> PRT
<213> Искусственная последовательность
<400> 25
Arg Ala Ser Gln Asp Ile Gly Ser Trp Leu Ala
1 5 10
<210> 26
<211> 11
<212> PRT
<213> Искусственная последовательность
<400> 26
Arg Ala Ser Gln Ser Ile Ser Arg Asn Leu Asn
1 5 10
<210> 27
<211> 11
<212> PRT
<213> Искусственная последовательность
<400> 27
Arg Ala Ser Gln His Ile Ser Ser Trp Leu Ala
1 5 10
<210> 28
<211> 11
<212> PRT
<213> Искусственная последовательность
<400> 28
Arg Ala Ser Gln Ser Ile Ser His Tyr Leu Asn
1 5 10
<210> 29
<211> 11
<212> PRT
<213> Искусственная последовательность
<400> 29
Arg Ala Ser Gln Ser Val Ser Ser Tyr Leu Ala
1 5 10
<210> 30
<211> 12
<212> PRT
<213> Искусственная последовательность
<400> 30
Arg Ala Ser Gln Ser Val Ser Ser Asn Tyr Leu Ala
1 5 10
<210> 31
<211> 13
<212> PRT
<213> Искусственная последовательность
<400> 31
Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn Tyr Val Ser
1 5 10
<210> 32
<211> 11
<212> PRT
<213> Искусственная последовательность
<400> 32
Gln Gly Asp Arg Ile Glu Asn Tyr Tyr Thr Ser
1 5 10
<210> 33
<211> 13
<212> PRT
<213> Искусственная последовательность
<400> 33
Thr Gly Ser Ser Ser Asn Ile Gly Asp Asn Tyr Val Asn
1 5 10
<210> 34
<211> 16
<212> PRT
<213> Искусственная последовательность
<400> 34
Thr Ser Ser Gln Ser Leu Val Tyr Arg Asp Gly Asn Thr Tyr Leu Asn
1 5 10 15
<210> 35
<211> 14
<212> PRT
<213> Искусственная последовательность
<400> 35
Gly Leu Ser Ser Gly Thr Val Thr Ala Ile Asn Tyr Pro Gly
1 5 10
<210> 36
<211> 7
<212> PRT
<213> Искусственная последовательность
<400> 36
Ala Ala Ser Asn Leu Gln Ser
1 5
<210> 37
<211> 7
<212> PRT
<213> Искусственная последовательность
<400> 37
Ala Ala Ser Ser Leu Gln Ser
1 5
<210> 38
<211> 7
<212> PRT
<213> Искусственная последовательность
<400> 38
Ala Ala Ser Thr Leu Gln Arg
1 5
<210> 39
<211> 7
<212> PRT
<213> Искусственная последовательность
<400> 39
Thr Ala Ser Thr Leu Gln Ser
1 5
<210> 40
<211> 7
<212> PRT
<213> Искусственная последовательность
<400> 40
Ala Ala Thr Arg Leu Gln Ser
1 5
<210> 41
<211> 7
<212> PRT
<213> Искусственная последовательность
<400> 41
Asp Thr Ser Asn Arg Ala Thr
1 5
<210> 42
<211> 7
<212> PRT
<213> Искусственная последовательность
<400> 42
Gly Thr Ser Ser Arg Ala Thr
1 5
<210> 43
<211> 7
<212> PRT
<213> Искусственная последовательность
<400> 43
Ala Ser Ser Thr Leu Gln Ser
1 5
<210> 44
<211> 7
<212> PRT
<213> Искусственная последовательность
<400> 44
Asp Asn Tyr Arg Arg Pro Ser
1 5
<210> 45
<211> 7
<212> PRT
<213> Искусственная последовательность
<400> 45
Gly Asn Ala Asn Arg Pro Ser
1 5
<210> 46
<211> 7
<212> PRT
<213> Искусственная последовательность
<400> 46
Ser Asn Ser Asn Arg Ala Ser
1 5
<210> 47
<211> 7
<212> PRT
<213> Искусственная последовательность
<400> 47
Lys Val Ser Asp Arg Asp Ser
1 5
<210> 48
<211> 7
<212> PRT
<213> Искусственная последовательность
<400> 48
Gly Ala Ser Ser Arg Ala Thr
1 5
<210> 49
<211> 7
<212> PRT
<213> Искусственная последовательность
<400> 49
Asn Thr Asn Thr Arg His Ser
1 5
<210> 50
<211> 9
<212> PRT
<213> Искусственная последовательность
<400> 50
Gln Gln Ala Ala Ser Val Pro Leu Thr
1 5
<210> 51
<211> 9
<212> PRT
<213> Искусственная последовательность
<400> 51
Gln Gln Ser Tyr Ser Thr Pro Phe Thr
1 5
<210> 52
<211> 9
<212> PRT
<213> Искусственная последовательность
<400> 52
Gln Gln Ser Tyr Ser Thr Pro Trp Thr
1 5
<210> 53
<211> 9
<212> PRT
<213> Искусственная последовательность
<400> 53
Gln Gln Ser His Ser Leu Pro Leu Thr
1 5
<210> 54
<211> 9
<212> PRT
<213> Искусственная последовательность
<400> 54
Gln Gln Ser Tyr Arg Thr Pro Phe Thr
1 5
<210> 55
<211> 9
<212> PRT
<213> Искусственная последовательность
<400> 55
Gln Gln Ala Thr Ser Phe Pro Leu Thr
1 5
<210> 56
<211> 9
<212> PRT
<213> Искусственная последовательность
<400> 56
Gln Gln Ser Tyr Ser Ala Leu Phe Thr
1 5
<210> 57
<211> 9
<212> PRT
<213> Искусственная последовательность
<400> 57
Gln Gln Arg Ser Asn Trp Pro Pro Thr
1 5
<210> 58
<211> 9
<212> PRT
<213> Искусственная последовательность
<400> 58
Gln Gln Ser Asp Thr Ser Pro Arg Val
1 5
<210> 59
<211> 10
<212> PRT
<213> Искусственная последовательность
<400> 59
Gln Gln Ser Leu Ser Ile Pro Gln Val Thr
1 5 10
<210> 60
<211> 11
<212> PRT
<213> Искусственная последовательность
<400> 60
Gly Thr Trp Asp Ser Ser Leu Ser Ala Val Val
1 5 10
<210> 61
<211> 9
<212> PRT
<213> Искусственная последовательность
<400> 61
Gln Ser Gly Ser Ser Thr Glu Asn Ile
1 5
<210> 62
<211> 10
<212> PRT
<213> Искусственная последовательность
<400> 62
Gln Ser Tyr Glu Ile Ser Gly Tyr Pro Val
1 5 10
<210> 63
<211> 9
<212> PRT
<213> Искусственная последовательность
<400> 63
Met Gln Gly Thr His Trp Pro Ser Thr
1 5
<210> 64
<211> 10
<212> PRT
<213> Искусственная последовательность
<400> 64
Gln Gln Tyr Gly Ser Ser Pro Gln Leu Thr
1 5 10
<210> 65
<211> 10
<212> PRT
<213> Искусственная последовательность
<400> 65
Ala Leu Tyr Met Gly Asn Gly Gly His Met
1 5 10
<210> 66
<211> 134
<212> PRT
<213> Искусственная последовательность
<400> 66
Glu Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Thr Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Arg Tyr
20 25 30
Trp Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Glu Asp Ser Ser Ile Asn Thr Gly Gly Gly Thr Glu Thr
50 55 60
Thr Tyr Tyr Thr Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
65 70 75 80
Asn Ala Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Lys Ser Glu
85 90 95
Asp Thr Ala Val Tyr Tyr Cys Ala Lys Gly Asp Tyr Tyr Cys Thr Thr
100 105 110
Tyr Glu Cys Gln His Tyr Tyr Gly Met Asp Tyr Trp Gly Lys Gly Thr
115 120 125
Met Val Thr Val Ser Ser
130
<210> 67
<211> 134
<212> PRT
<213> Искусственная последовательность
<400> 67
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Arg Tyr
20 25 30
Trp Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Glu Asp Ser Ser Ile Asn Thr Gly Gly Gly Thr Glu Thr
50 55 60
Thr Tyr Tyr Thr Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
65 70 75 80
Asn Ala Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu
85 90 95
Asp Thr Ala Val Tyr Tyr Cys Ala Lys Gly Asp Tyr Tyr Cys Thr Thr
100 105 110
Tyr Glu Cys Gln His Tyr Tyr Gly Met Asp Tyr Trp Gly Gln Gly Thr
115 120 125
Thr Val Thr Val Ser Ser
130
<210> 68
<211> 134
<212> PRT
<213> Искусственная последовательность
<400> 68
Glu Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Thr Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Arg Tyr
20 25 30
Trp Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Glu Asp Ser Ser Ile Asn Thr Gly Gly Gly Thr Glu Thr
50 55 60
Thr Tyr Tyr Thr Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
65 70 75 80
Asn Ala Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Lys Ser Glu
85 90 95
Asp Thr Ala Val Tyr Tyr Cys Ala Lys Gly Asp Tyr Tyr Cys Thr Thr
100 105 110
Tyr Glu Cys Gln His Tyr Tyr Gly Met Asp Tyr Trp Gly Lys Gly Thr
115 120 125
Thr Val Thr Val Ser Ser
130
<210> 69
<211> 134
<212> PRT
<213> Искусственная последовательность
<400> 69
Glu Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Thr Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Arg Tyr
20 25 30
Trp Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Glu Asp Ser Ser Ile Asn Thr Gly Gly Gly Thr Glu Thr
50 55 60
Thr Tyr Tyr Thr Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
65 70 75 80
Asn Ala Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Lys Ser Glu
85 90 95
Asp Thr Ala Val Tyr Tyr Cys Ala Lys Gly Asp Tyr Tyr Cys Thr Thr
100 105 110
Tyr Glu Cys Gln His Tyr Tyr Gly Met Asp Tyr Trp Gly Lys Gly Thr
115 120 125
Thr Val Thr Val Ser Ser
130
<210> 70
<211> 134
<212> PRT
<213> Искусственная последовательность
<400> 70
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Thr Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Arg Tyr
20 25 30
Trp Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Glu Asp Ser Ser Ile Asn Thr Gly Gly Gly Thr Glu Thr
50 55 60
Thr Tyr Tyr Thr Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
65 70 75 80
Asn Ala Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Lys Ser Glu
85 90 95
Asp Thr Ala Val Tyr Tyr Cys Ala Lys Gly Asp Tyr Tyr Cys Thr Thr
100 105 110
Tyr Glu Cys Gln His Tyr Tyr Gly Met Asp Tyr Trp Gly Lys Gly Thr
115 120 125
Leu Val Thr Val Ser Ser
130
<210> 71
<211> 134
<212> PRT
<213> Искусственная последовательность
<400> 71
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Thr Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Arg Tyr
20 25 30
Trp Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Glu Asp Ser Ser Ile Asn Thr Gly Gly Gly Thr Glu Thr
50 55 60
Thr Tyr Tyr Thr Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
65 70 75 80
Asn Ala Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Lys Ser Glu
85 90 95
Asp Thr Ala Val Tyr Tyr Cys Ala Lys Gly Asp Tyr Tyr Cys Thr Thr
100 105 110
Tyr Glu Cys Gln His Tyr Tyr Gly Met Asp Tyr Trp Gly Lys Gly Thr
115 120 125
Leu Val Thr Val Ser Ser
130
<210> 72
<211> 134
<212> PRT
<213> Искусственная последовательность
<400> 72
Glu Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Thr Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Arg Tyr
20 25 30
Trp Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Glu Asp Ser Ser Ile Asn Thr Gly Gly Gly Thr Glu Thr
50 55 60
Thr Tyr Tyr Thr Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
65 70 75 80
Asn Ala Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Lys Ser Glu
85 90 95
Asp Thr Ala Val Tyr Tyr Cys Ala Lys Gly Asp Tyr Tyr Cys Thr Thr
100 105 110
Tyr Glu Cys Gln His Tyr Tyr Gly Met Asp Tyr Trp Gly Lys Gly Thr
115 120 125
Leu Val Thr Val Ser Ser
130
<210> 73
<211> 134
<212> PRT
<213> Искусственная последовательность
<400> 73
Glu Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Thr Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Arg Tyr
20 25 30
Trp Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Glu Asp Ser Ser Ile Asn Thr Gly Gly Gly Thr Glu Thr
50 55 60
Thr Tyr Tyr Thr Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
65 70 75 80
Asn Ala Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Lys Ser Glu
85 90 95
Asp Thr Ala Val Tyr Tyr Cys Ala Lys Gly Asp Tyr Tyr Cys Thr Thr
100 105 110
Tyr Glu Cys Gln His Tyr Tyr Gly Met Asp Tyr Trp Gly Lys Gly Thr
115 120 125
Leu Val Thr Val Ser Ser
130
<210> 74
<211> 134
<212> PRT
<213> Искусственная последовательность
<400> 74
Glu Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Thr Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Arg Tyr
20 25 30
Trp Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Glu Asp Ser Ser Ile Asn Thr Gly Gly Gly Thr Glu Thr
50 55 60
Thr Tyr Tyr Thr Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
65 70 75 80
Asn Ala Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Lys Ser Glu
85 90 95
Asp Thr Ala Val Tyr Tyr Cys Ala Lys Gly Asp Tyr Tyr Cys Thr Thr
100 105 110
Tyr Glu Cys Gln His Tyr Tyr Gly Met Asp Tyr Trp Gly Lys Gly Thr
115 120 125
Leu Val Thr Val Ser Ser
130
<210> 75
<211> 134
<212> PRT
<213> Искусственная последовательность
<400> 75
Gln Val Gln Leu Gln Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Thr Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Arg Tyr
20 25 30
Trp Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Glu Asp Ser Ser Ile Asn Thr Gly Gly Gly Thr Glu Thr
50 55 60
Thr Tyr Tyr Thr Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
65 70 75 80
Asn Ala Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Lys Ser Glu
85 90 95
Asp Thr Ala Val Tyr Tyr Cys Ala Lys Gly Asp Tyr Tyr Cys Thr Thr
100 105 110
Tyr Glu Cys Gln His Tyr Tyr Gly Met Asp Tyr Trp Gly Lys Gly Thr
115 120 125
Met Val Thr Val Ser Ser
130
<210> 76
<211> 134
<212> PRT
<213> Искусственная последовательность
<400> 76
Gln Val Gln Leu Gln Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Thr Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Arg Tyr
20 25 30
Trp Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Glu Asp Ser Ser Ile Asn Thr Gly Gly Gly Thr Glu Thr
50 55 60
Thr Tyr Tyr Thr Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
65 70 75 80
Asn Ala Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Lys Ser Glu
85 90 95
Asp Thr Ala Val Tyr Tyr Cys Ala Lys Gly Asp Tyr Tyr Cys Thr Thr
100 105 110
Tyr Glu Cys Gln His Tyr Tyr Gly Met Asp Tyr Trp Gly Lys Gly Thr
115 120 125
Met Val Thr Val Ser Ser
130
<210> 77
<211> 134
<212> PRT
<213> Искусственная последовательность
<400> 77
Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Thr Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Arg Tyr
20 25 30
Trp Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Glu Asp Ser Ser Ile Asn Thr Gly Gly Gly Thr Glu Thr
50 55 60
Thr Tyr Tyr Thr Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
65 70 75 80
Asn Ala Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Lys Ser Glu
85 90 95
Asp Thr Ala Val Tyr Tyr Cys Ala Lys Gly Asp Tyr Tyr Cys Thr Thr
100 105 110
Tyr Glu Cys Gln His Tyr Tyr Gly Met Asp Tyr Trp Gly Lys Gly Thr
115 120 125
Leu Val Thr Val Ser Ser
130
<210> 78
<211> 134
<212> PRT
<213> Искусственная последовательность
<400> 78
Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Thr Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Arg Tyr
20 25 30
Trp Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Glu Asp Ser Ser Ile Asn Thr Gly Gly Gly Thr Glu Thr
50 55 60
Thr Tyr Tyr Thr Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
65 70 75 80
Asn Ala Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Lys Ser Glu
85 90 95
Asp Thr Ala Val Tyr Tyr Cys Ala Lys Gly Asp Tyr Tyr Cys Thr Thr
100 105 110
Tyr Glu Cys Gln His Tyr Tyr Gly Met Asp Tyr Trp Gly Lys Gly Thr
115 120 125
Met Val Thr Val Ser Ser
130
<210> 79
<211> 134
<212> PRT
<213> Искусственная последовательность
<400> 79
Glu Val Gln Leu Gln Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Thr Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Arg Tyr
20 25 30
Trp Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Glu Asp Ser Ser Ile Asn Thr Gly Gly Gly Thr Glu Thr
50 55 60
Thr Tyr Tyr Thr Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
65 70 75 80
Asn Ala Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Lys Ser Glu
85 90 95
Asp Thr Ala Val Tyr Tyr Cys Ala Lys Gly Asp Tyr Tyr Cys Thr Thr
100 105 110
Tyr Glu Cys Gln His Tyr Tyr Gly Met Asp Tyr Trp Gly Lys Gly Thr
115 120 125
Pro Val Thr Val Ser Ser
130
<210> 80
<211> 134
<212> PRT
<213> Искусственная последовательность
<400> 80
Gln Val Thr Leu Arg Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Thr Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Arg Tyr
20 25 30
Trp Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Glu Asp Ser Ser Ile Asn Thr Gly Gly Gly Thr Glu Thr
50 55 60
Thr Tyr Tyr Thr Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
65 70 75 80
Asn Ala Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Lys Ser Glu
85 90 95
Asp Thr Ala Val Tyr Tyr Cys Ala Lys Gly Asp Tyr Tyr Cys Thr Thr
100 105 110
Tyr Glu Cys Gln His Tyr Tyr Gly Met Asp Tyr Trp Gly Lys Gly Thr
115 120 125
Met Val Thr Val Ser Ser
130
<210> 81
<211> 134
<212> PRT
<213> Искусственная последовательность
<400> 81
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Arg Tyr
20 25 30
Trp Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Lys Gln Asp Gly Ile Asn Thr Gly Gly Gly Thr Ser Glu
50 55 60
Lys Tyr Tyr Val Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
65 70 75 80
Asn Ala Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu
85 90 95
Asp Thr Ala Val Tyr Tyr Cys Ala Lys Gly Asp Tyr Tyr Cys Thr Thr
100 105 110
Tyr Glu Cys Gln His Tyr Tyr Gly Met Asp Tyr Trp Gly Gln Gly Thr
115 120 125
Thr Val Thr Val Ser Ser
130
<210> 82
<211> 127
<212> PRT
<213> Искусственная последовательность
<400> 82
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Arg Tyr
20 25 30
Trp Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Glu Asp Ser Ser Glu Thr Thr Tyr Tyr Thr Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Gly Asp Tyr Tyr Cys Thr Thr Tyr Glu Cys Gln His Tyr Tyr
100 105 110
Gly Met Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 83
<211> 118
<212> PRT
<213> Искусственная последовательность
<400> 83
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Arg Ser Ile Phe Ser Ile Asn
20 25 30
Ala Met Asn Trp Tyr Arg Gln Ala Pro Gly Lys Gly Thr Glu Trp Val
35 40 45
Ala Gln Ile Thr Asp Glu Gly Ile Thr Asn Tyr Val Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Ala Phe Val Ile Thr Thr Thr Ser Glu Ile Tyr Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser
115
<210> 84
<211> 128
<212> PRT
<213> Искусственная последовательность
<400> 84
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Arg Tyr
20 25 30
Trp Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Glu Asp Ser Ser Thr Glu Thr Thr Tyr Tyr Thr Asp Ser
50 55 60
Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu
65 70 75 80
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Lys Gly Asp Tyr Tyr Cys Thr Thr Tyr Glu Cys Gln His Tyr
100 105 110
Tyr Gly Met Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 85
<211> 129
<212> PRT
<213> Искусственная последовательность
<400> 85
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Arg Tyr
20 25 30
Trp Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Glu Asp Ser Ser Ile Thr Glu Thr Thr Tyr Tyr Thr Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Ala Lys Gly Asp Tyr Tyr Cys Thr Thr Tyr Glu Cys Gln His
100 105 110
Tyr Tyr Gly Met Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser
115 120 125
Ser
<210> 86
<211> 129
<212> PRT
<213> Искусственная последовательность
<400> 86
Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Gln Ala Ser Gly Phe Thr Phe Arg Arg Tyr
20 25 30
Trp Met Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Asn Asp Gly Gly Gly Asp Asp Ser Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Val Lys Ser Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Ala Lys Gly Asp Tyr Tyr Cys Thr His Tyr Glu Cys Gln His
100 105 110
Tyr Tyr Gly Met Asp Tyr Trp Gly Lys Gly Thr Leu Val Thr Val Ser
115 120 125
Ser
<210> 87
<211> 126
<212> PRT
<213> Искусственная последовательность
<400> 87
Glu Val Gln Leu Val Gln Ser Gly Gly Asp Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Tyr
20 25 30
Trp Met Tyr Trp Val Arg Gln Thr Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Arg Thr Ser Gly Asp Thr Asp Tyr Ala Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Lys Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys Gly Asp Tyr Tyr Cys Thr Thr Tyr Glu Cys Gln His Tyr Tyr Gly
100 105 110
Met Asp Tyr Trp Gly Lys Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 88
<211> 118
<212> PRT
<213> Искусственная последовательность
<400> 88
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Arg Ser Ile Phe Ser Ile Asn
20 25 30
Ala Met Asn Trp Tyr Arg Gln Ala Pro Gly Lys Gly Thr Glu Trp Val
35 40 45
Ala Gln Ile Thr Asp Glu Gly Ile Thr Asn Tyr Val Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Ala Phe Val Ile Thr Thr Thr Ser Glu Ile Tyr Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser
115
<210> 89
<211> 107
<212> PRT
<213> Искусственная последовательность
<400> 89
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ala Ile Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Asn Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Ala Ser Val Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 90
<211> 107
<212> PRT
<213> Искусственная последовательность
<400> 90
Val Ile Trp Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 91
<211> 107
<212> PRT
<213> Искусственная последовательность
<400> 91
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Trp
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 92
<211> 107
<212> PRT
<213> Искусственная последовательность
<400> 92
Asn Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Gly Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly His Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Thr Leu Gln Arg Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Gly Gly Tyr Gly Thr Glu Phe Thr Leu Thr Ile Asp Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Thr Tyr Phe Cys Gln Gln Ser His Ser Leu Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Gln Gly Gly Asn Gln
100 105
<210> 93
<211> 107
<212> PRT
<213> Искусственная последовательность
<400> 93
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Thr Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Arg Asn
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile
35 40 45
Tyr Thr Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Thr Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Ile Tyr His Cys Gln Gln Ser Tyr Arg Thr Pro Phe
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 94
<211> 107
<212> PRT
<213> Искусственная последовательность
<400> 94
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ala Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln His Ile Ser Ser Trp
20 25 30
Leu Ala Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Pro Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Thr Ser Phe Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 95
<211> 107
<212> PRT
<213> Искусственная последовательность
<400> 95
Ala Ile Arg Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser His Tyr
20 25 30
Leu Asn Trp Tyr Gln Trp Lys Pro Gly Lys Val Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Thr Arg Leu Gln Ser Gly Val Pro Pro Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Ile Tyr Phe Cys Gln Gln Ser Tyr Ser Ala Leu Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 96
<211> 107
<212> PRT
<213> Искусственная последовательность
<400> 96
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Arg Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Thr Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 97
<211> 108
<212> PRT
<213> Искусственная последовательность
<400> 97
Glu Thr Thr Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Asn
20 25 30
Tyr Leu Ala Trp Tyr Gln His Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Thr Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asp Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asp Thr Ser Pro
85 90 95
Arg Val Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 98
<211> 108
<212> PRT
<213> Искусственная последовательность
<400> 98
Asn Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ser Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Phe Cys Gln Gln Ser Leu Ser Ile Pro Gln
85 90 95
Val Thr Phe Gly Gly Gly Thr Lys Val Asp Ile Lys
100 105
<210> 99
<211> 110
<212> PRT
<213> Искусственная последовательность
<400> 99
Gln Ser Val Leu Thr Gln Pro Pro Ser Val Ser Ala Ala Pro Ala Gln
1 5 10 15
Lys Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn
20 25 30
Tyr Val Ser Trp Tyr Gln Gln Val Pro Gly Thr Ala Pro Glu Leu Leu
35 40 45
Ile Tyr Asp Asn Tyr Arg Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Thr Leu Ala Ile Thr Gly Leu Gln
65 70 75 80
Thr Gly Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Trp Asp Ser Ser Leu
85 90 95
Ser Ala Val Val Phe Gly Gly Gly Thr Gln Leu Thr Val Leu
100 105 110
<210> 100
<211> 104
<212> PRT
<213> Искусственная последовательность
<400> 100
Glu Leu Thr Gln Pro Ser Ala Val Ser Val Ser Leu Gly Gln Thr Val
1 5 10 15
Arg Ile Thr Cys Gln Gly Asp Arg Ile Glu Asn Tyr Tyr Thr Ser Trp
20 25 30
Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr Gly Asn
35 40 45
Ala Asn Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser Ser Ser
50 55 60
Gly Asn Thr Ala Ser Leu Thr Ile Thr Gly Ala Gln Ala Glu Asp Glu
65 70 75 80
Ala Asp Tyr Tyr Cys Gln Ser Gly Ser Ser Thr Glu Asn Ile Phe Gly
85 90 95
Gly Gly Thr Lys Leu Thr Val Leu
100
<210> 101
<211> 107
<212> PRT
<213> Искусственная последовательность
<400> 101
Leu Pro Val Leu Thr Gln Pro Ser Ala Val Ser Val Ser Leu Gly Gln
1 5 10 15
Thr Ala Arg Ile Thr Cys Gln Gly Asp Arg Ile Glu Asn Tyr Tyr Thr
20 25 30
Ser Trp Phe Arg Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr
35 40 45
Gly Asn Ala Asn Arg Pro Ser Gly Val Pro Glu Arg Phe Ser Gly Ser
50 55 60
Ser Ser Gly Val Thr Ala Thr Leu Thr Ile Ser Gly Ala Gln Ala Glu
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Ser Gly Ser Ser Thr Glu Asn Ile
85 90 95
Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gln
100 105
<210> 102
<211> 107
<212> PRT
<213> Искусственная последовательность
<400> 102
Leu Pro Val Leu Thr Gln Pro Ser Ala Val Ser Val Ser Leu Gly Gln
1 5 10 15
Thr Ala Arg Ile Thr Cys Gln Gly Asp Arg Ile Glu Asn Tyr Tyr Thr
20 25 30
Ser Trp Phe Arg Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr
35 40 45
Gly Asn Ala Asn Arg Pro Ser Gly Val Pro Glu Arg Phe Ser Gly Ser
50 55 60
Ser Ser Gly Val Thr Ala Thr Leu Thr Ile Ser Gly Ala Gln Ala Glu
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Ser Gly Ser Ser Thr Glu Asn Ile
85 90 95
Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gln
100 105
<210> 103
<211> 107
<212> PRT
<213> Искусственная последовательность
<400> 103
Leu Pro Val Leu Thr Gln Pro Ser Ala Val Ser Val Ser Leu Gly Gln
1 5 10 15
Thr Ala Arg Ile Thr Cys Gln Gly Asp Arg Ile Glu Asn Tyr Tyr Thr
20 25 30
Ser Trp Phe Arg Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr
35 40 45
Gly Asn Ala Asn Arg Pro Ser Gly Val Pro Glu Arg Phe Ser Gly Ser
50 55 60
Ser Ser Gly Val Thr Ala Thr Leu Thr Ile Ser Gly Ala Gln Ala Glu
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Ser Gly Ser Ser Thr Glu Asn Ile
85 90 95
Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gln
100 105
<210> 104
<211> 110
<212> PRT
<213> Искусственная последовательность
<400> 104
Asn Phe Met Leu Thr Gln Pro Pro Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Lys Phe Thr Ile Ser Cys Thr Gly Ser Ser Ser Asn Ile Gly Asp Asn
20 25 30
Tyr Val Asn Trp Tyr Gln His Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Asn Ser Asn Arg Ala Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Ser Ser Gly Gly Thr Ala Thr Leu Thr Ile Ser Gly Ala Gln
65 70 75 80
Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gln Ser Tyr Glu Ile Ser Gly
85 90 95
Tyr Pro Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gln
100 105 110
<210> 105
<211> 112
<212> PRT
<213> Искусственная последовательность
<400> 105
Glu Ile Val Leu Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Thr Ser Ser Gln Ser Leu Val Tyr Arg
20 25 30
Asp Gly Asn Thr Tyr Leu Asn Trp Phe Gln Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Arg Leu Ile Tyr Lys Val Ser Asp Arg Asp Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Gly
85 90 95
Thr His Trp Pro Ser Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 106
<211> 108
<212> PRT
<213> Искусственная последовательность
<400> 106
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Pro Gln
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 107
<211> 116
<212> PRT
<213> Искусственная последовательность
<400> 107
Gln Leu Leu Phe Asn Lys Thr Lys Ser Val Glu Phe Thr Phe Cys Asn
1 5 10 15
Asp Thr Val Val Ile Pro Cys Phe Val Thr Asn Met Glu Ala Gln Asn
20 25 30
Thr Thr Glu Val Tyr Val Lys Trp Lys Phe Lys Gly Arg Asp Ile Tyr
35 40 45
Thr Phe Asp Gly Ala Leu Asn Lys Ser Thr Val Pro Thr Asp Phe Ser
50 55 60
Ser Ala Lys Ile Glu Val Ser Gln Leu Leu Lys Gly Asp Ala Ser Leu
65 70 75 80
Lys Met Asp Lys Ser Asp Ala Val Ser His Thr Gly Asn Tyr Thr Cys
85 90 95
Glu Val Thr Glu Leu Thr Arg Glu Gly Glu Thr Ile Ile Glu Leu Lys
100 105 110
Tyr Arg Val Val
115
<210> 108
<211> 220
<212> PRT
<213> Искусственная последовательность
<400> 108
Phe Thr Val Thr Val Pro Lys Asp Leu Tyr Val Val Glu Tyr Gly Ser
1 5 10 15
Asn Met Thr Ile Glu Cys Lys Phe Pro Val Glu Lys Gln Leu Asp Leu
20 25 30
Ala Ala Leu Ile Val Tyr Trp Glu Met Glu Asp Lys Asn Ile Ile Gln
35 40 45
Phe Val His Gly Glu Glu Asp Leu Lys Val Gln His Ser Ser Tyr Arg
50 55 60
Gln Arg Ala Arg Leu Leu Lys Asp Gln Leu Ser Leu Gly Asn Ala Ala
65 70 75 80
Leu Gln Ile Thr Asp Val Lys Leu Gln Asp Ala Gly Val Tyr Arg Cys
85 90 95
Met Ile Ser Tyr Gly Gly Ala Asp Tyr Lys Arg Ile Thr Val Lys Val
100 105 110
Asn Ala Pro Tyr Asn Lys Ile Asn Gln Arg Ile Leu Val Val Asp Pro
115 120 125
Val Thr Ser Glu His Glu Leu Thr Cys Gln Ala Glu Gly Tyr Pro Lys
130 135 140
Ala Glu Val Ile Trp Thr Ser Ser Asp His Gln Val Leu Ser Gly Lys
145 150 155 160
Thr Thr Thr Thr Asn Ser Lys Arg Glu Glu Lys Leu Phe Asn Val Thr
165 170 175
Ser Thr Leu Arg Ile Asn Thr Thr Thr Asn Glu Ile Phe Tyr Cys Thr
180 185 190
Phe Arg Arg Leu Asp Pro Glu Glu Asn His Thr Ala Glu Leu Val Ile
195 200 205
Pro Glu Leu Pro Leu Ala His Pro Pro Asn Glu Arg
210 215 220
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| СЛИТЫЙ БЕЛОК И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2811120C2 |
| Выделенное биспецифическое антитело, которое специфически связывается с CD47 и PD-L1 | 2021 |
|
RU2815823C2 |
| АНТИТЕЛА ПРОТИВ СИГНАЛ-РЕГУЛЯТОРНОГО БЕЛКА АЛЬФА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2017 |
|
RU2771964C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ СОЕДИНЕНИЯ ВНЕКЛЕТОЧНЫХ ДОМЕНОВ ТИПА I И ТИПА II В КАЧЕСТВЕ ГЕТЕРОЛОГИЧНЫХ ХИМЕРНЫХ БЕЛКОВ | 2016 |
|
RU2766200C1 |
| БИСПЕЦИФИЧНЫЙ СЛИТЫЙ БЕЛОК И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2801528C2 |
| АНТИТЕЛО ПРОТИВ SIRPα | 2019 |
|
RU2791002C2 |
| Терапевтические антитела к CD47 | 2016 |
|
RU2748401C2 |
| АНТИ-PD-L1 АНТИТЕЛО ДЛЯ ДЕТЕКЦИИ PD-L1 | 2018 |
|
RU2758723C2 |
| МОНОСПЕЦИФИЧЕСКИЕ И БИСПЕЦИФИЧЕСКИЕ БЕЛКИ С РЕГУЛИРОВАНИЕМ ИММУННОЙ КОНТРОЛЬНОЙ ТОЧКИ ДЛЯ ЛЕЧЕНИЯ РАКА | 2018 |
|
RU2793167C2 |
| КОНСТРУКЦИИ, ИМЕЮЩИЕ SIRP-АЛЬФА ДОМЕН ИЛИ ЕГО ВАРИАНТ | 2016 |
|
RU2740672C2 |
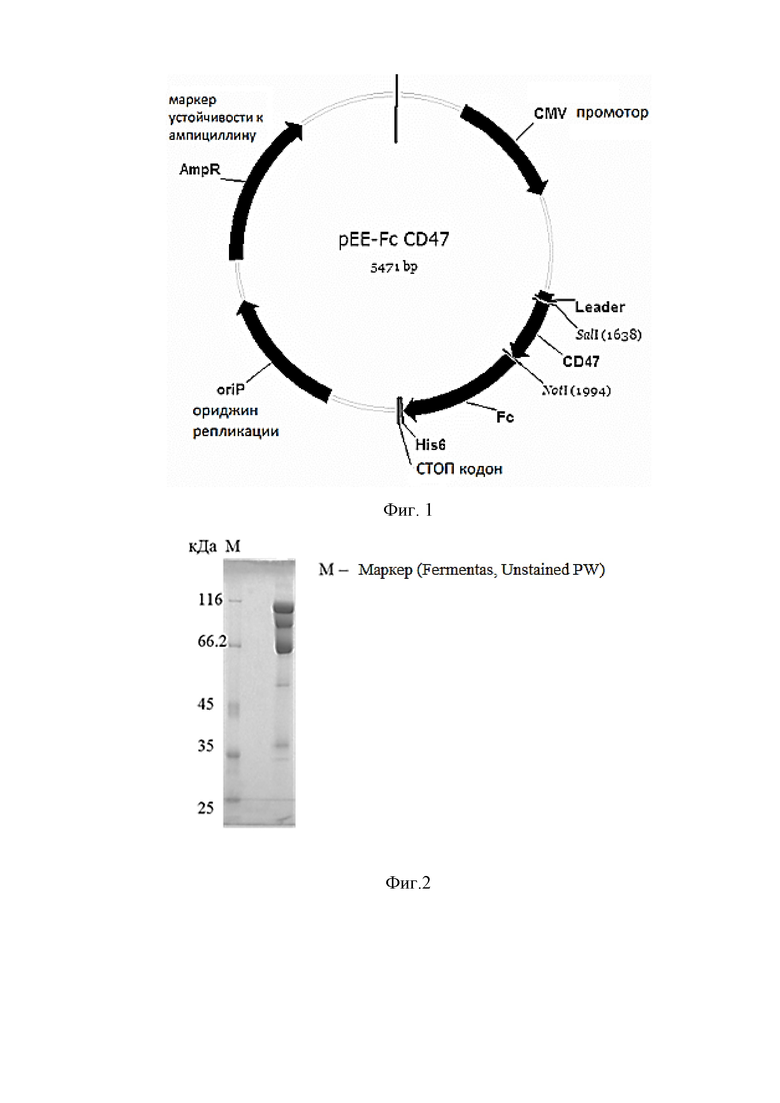
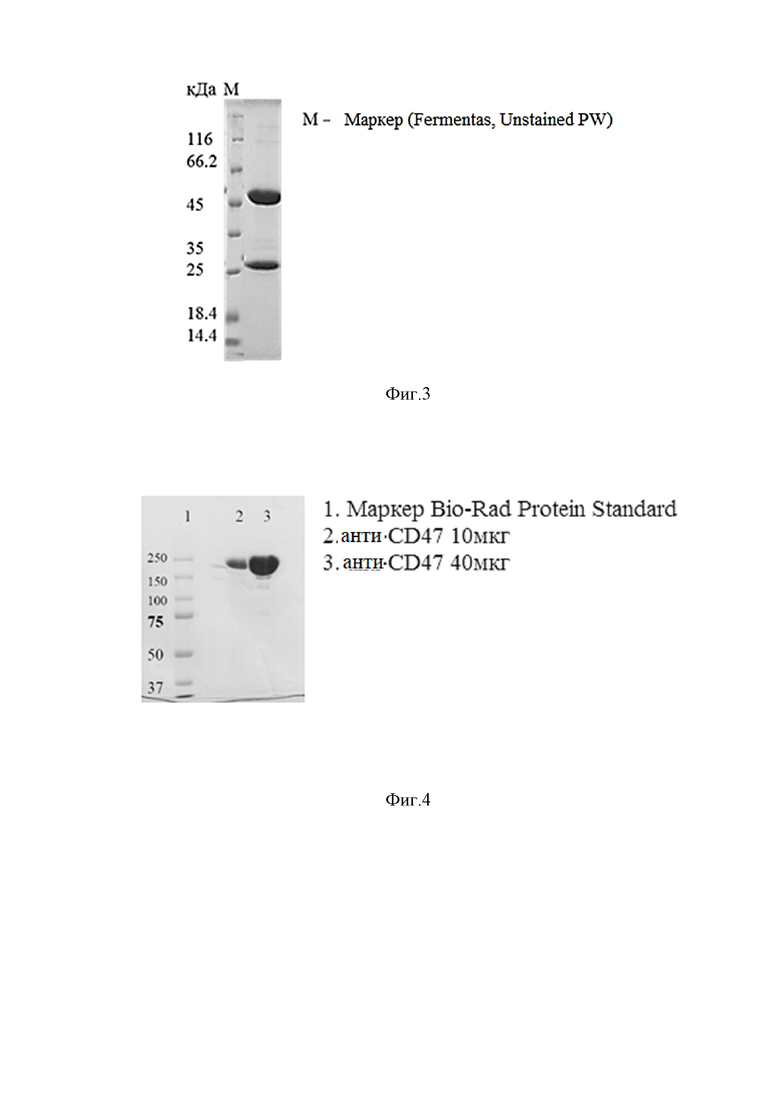
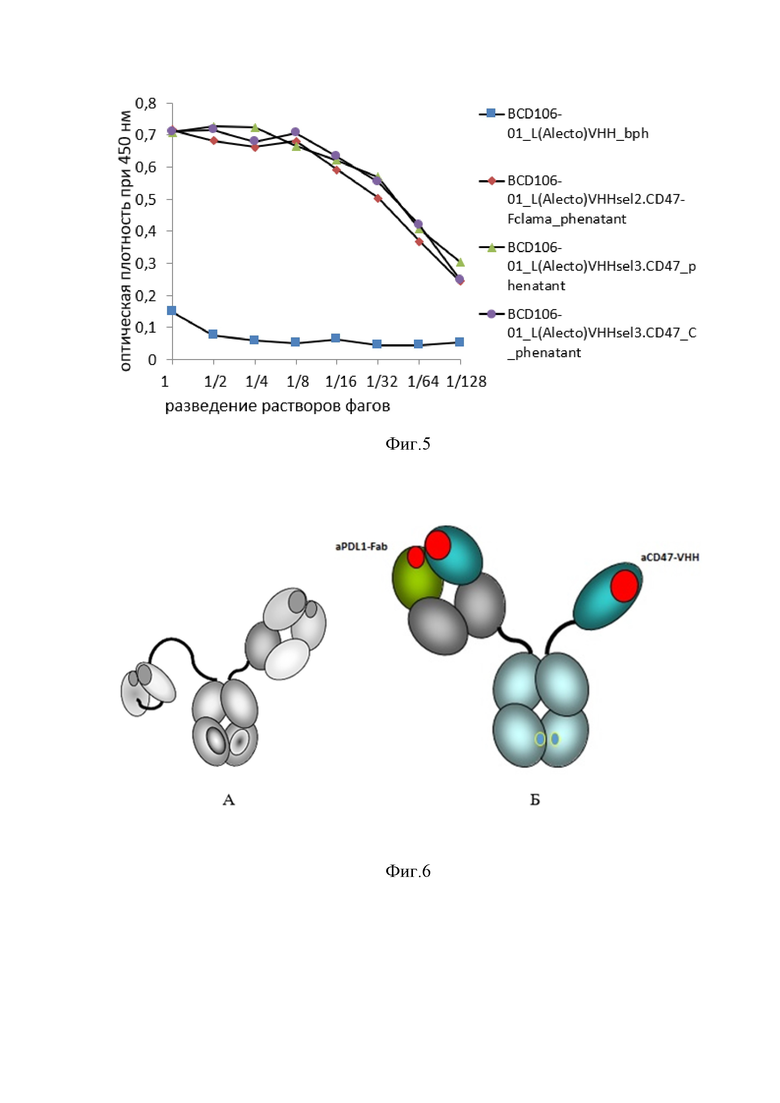

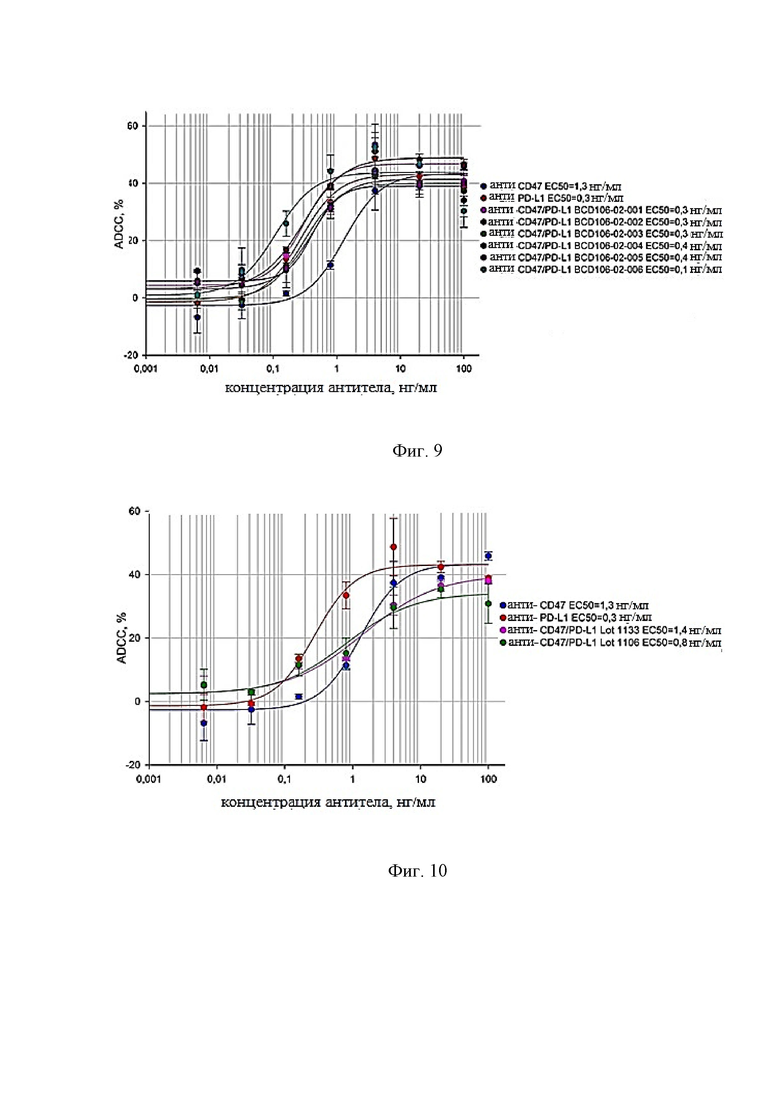

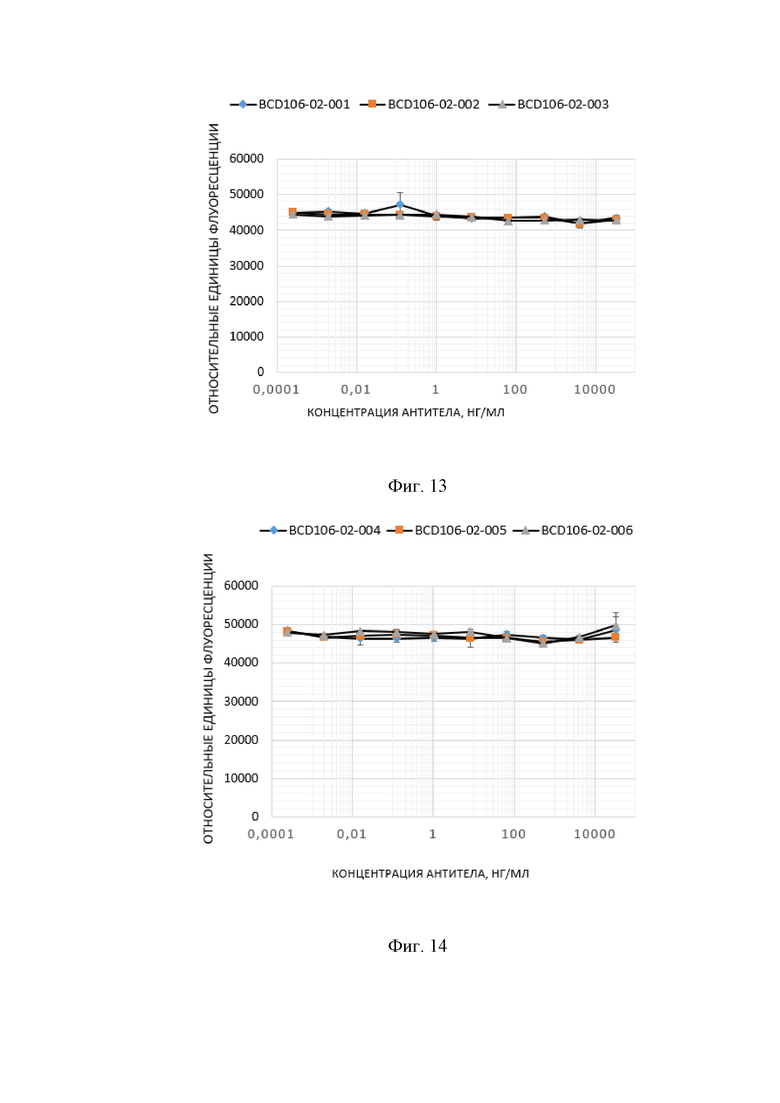
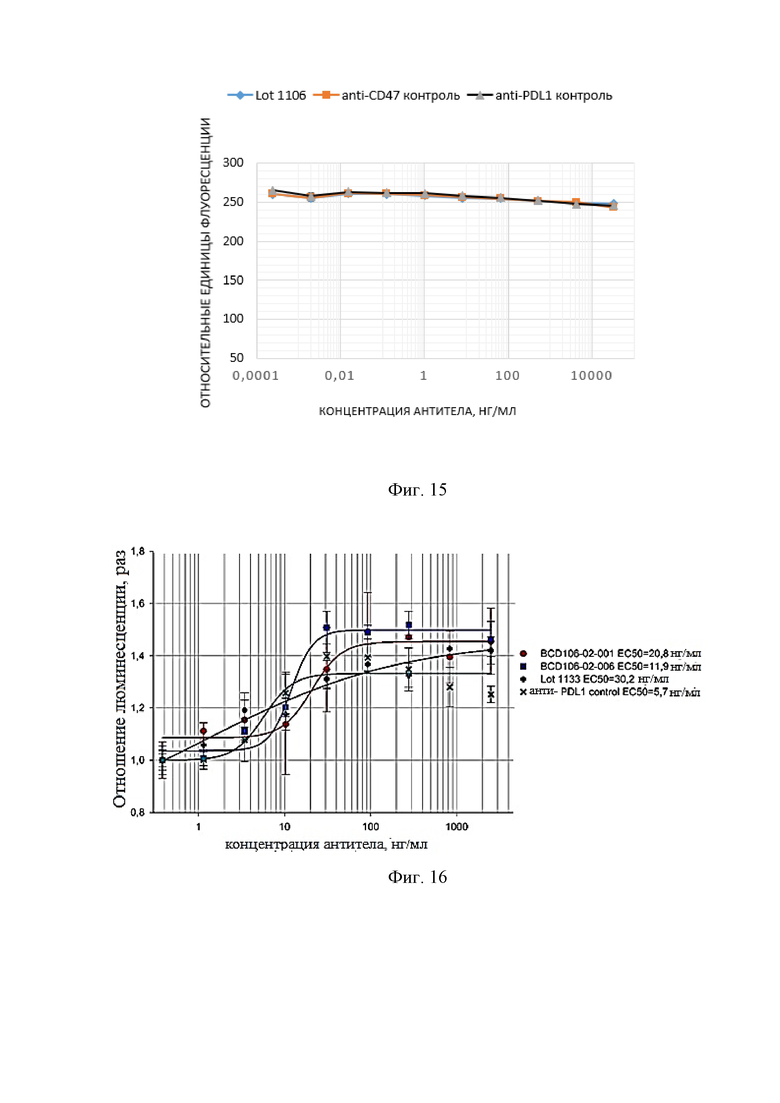
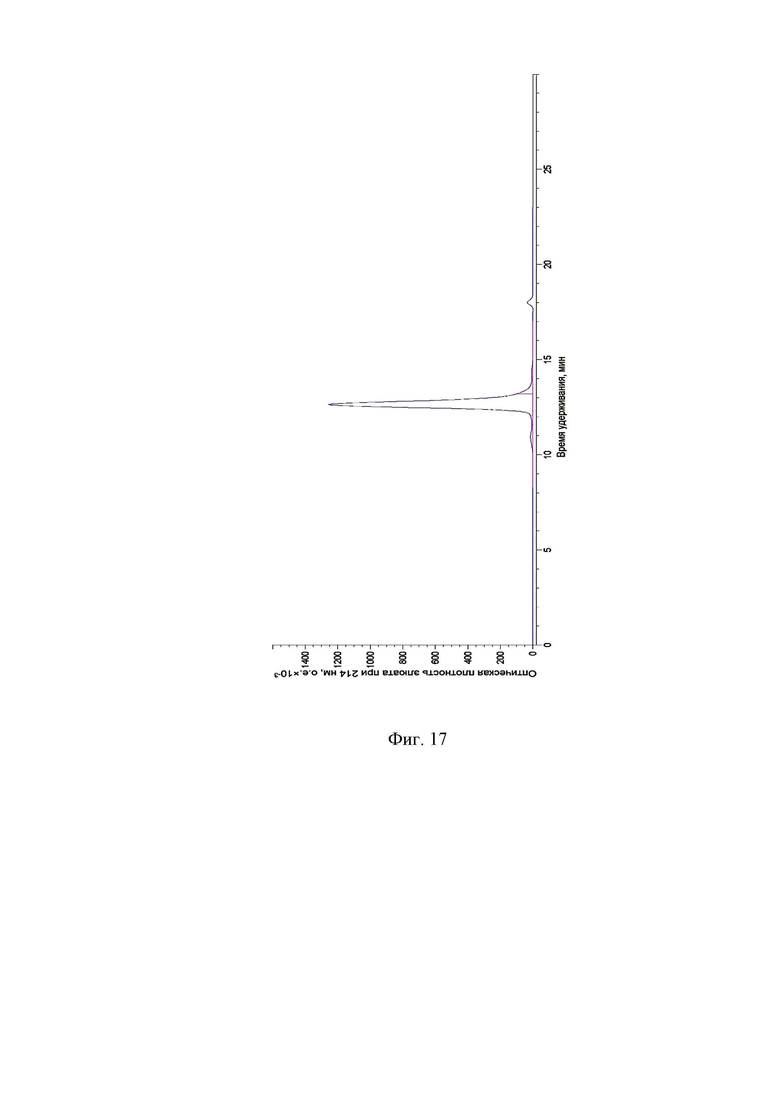
Изобретение относится к области биотехнологии. Предложено биспецифическое антитело, которое специфически связывается с CD47 и PD-L1. Изобретение также относится к нуклеиновой кислоте, кодирующей данное антитело, вектору экспрессии, способу получения антитела и к применению антител и композиций, включающих указанные антитела, в терапии рака. Изобретение обеспечивает специфичное высокоаффинное связывание CD47 и PD-L1 и снижение нежелательных эффектов. 9 н. и 14 з.п. ф-лы, 17 ил., 11 табл., 23 пр.
1. Биспецифическое антитело, которое специфически связывается с CD47 и PD-L1 и включает:
i) первый антигенсвязывающий фрагмент, который специфически связывается c CD47 и включает:
а) вариабельный домен тяжелой цепи, который содержит последовательности CDR1, CDR2, CDR3,
где CDR1 представляет собой последовательность SEQ ID NO: 1,
где CDR2 представляет собой последовательность, выбранную из следующей группы: SEQ ID NO: 6-9, 11, 12,
где CDR3 представляет собой последовательность SEQ ID NO: 17, и
б) вариабельный домен легкой цепи, который содержит последовательности CDR1, CDR2, CDR3,
где CDR1 представляет собой последовательность SEQ ID NO: 32,
CDR2 представляет собой последовательность SEQ ID NO: 45,
CDR3 представляет собой последовательность SEQ ID NO: 61;
ii) второй антигенсвязывающий фрагмент, который специфически связывается c PD-L1 и включает:
а) вариабельный домен тяжелой цепи, который содержит следующие последовательности: SEQ ID NO: 5, SEQ ID NO: 16 и SEQ ID NO: 21, и
б) вариабельный домен легкой цепи, который содержит следующие последовательности: SEQ ID NO: 35, SEQ ID NO: 49 и SEQ ID NO: 65;
и
iii) Fc-фрагмент.
2. Биспецифическое антитело по п.1, где первый антигенсвязывающий фрагмент, который специфически связывается c CD47, включает:
(i) (а) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 1,
CDR2 с аминокислотной последовательностью SEQ ID NO: 6 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 17; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 32,
CDR2 с аминокислотной последовательностью SEQ ID NO: 45 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 61;
(ii) (а) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 1,
CDR2 с аминокислотной последовательностью SEQ ID NO: 7 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 17; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 32,
CDR2 с аминокислотной последовательностью SEQ ID NO: 45 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 61;
(iii) (а) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 1,
CDR2 с аминокислотной последовательностью SEQ ID NO: 8 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 17; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 32,
CDR2 с аминокислотной последовательностью SEQ ID NO: 45 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 61;
(iv) (а) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 1,
CDR2 с аминокислотной последовательностью SEQ ID NO: 9 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 17; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 32,
CDR2 с аминокислотной последовательностью SEQ ID NO: 45 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 61;
(v) (а) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 1,
CDR2 с аминокислотной последовательностью SEQ ID NO: 11 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 17; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 32,
CDR2 с аминокислотной последовательностью SEQ ID NO: 45 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 61;
или
(vi) (а) вариабельный домен тяжелой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 1,
CDR2 с аминокислотной последовательностью SEQ ID NO:12 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 17; и
(b) вариабельный домен легкой цепи, содержащий:
CDR1 с аминокислотной последовательностью SEQ ID NO: 32,
CDR2 с аминокислотной последовательностью SEQ ID NO: 45 и
CDR3 с аминокислотной последовательностью SEQ ID NO: 61.
3. Биспецифическое антитело по п.1, характеризующееся тем, что первый антигенсвязывающий фрагмент, который специфически связывается c CD47, представляет собой Fab, scFv, scFab.
4. Биспецифическое антитело по п.1, характеризующееся тем, что второй антигенсвязывающий фрагмент, который специфически связывается c PD-L1, представляет собой Fab, scFv, scFab.
5. Биспецифическое антитело по п.1, характеризующееся тем, что антитело представляет собой полноразмерное антитело.
6. Биспецифическое антитело по п.1, отличающееся тем, что первый антигенсвязывающий фрагмент, который специфически связывается c CD47, ингибирует взаимодействие CD47 рецептора и SIRP лиганда, и/или второй антигенсвязывающий фрагмент, который специфически связывается c PD-L1, ингибирует взаимодействие PD-L1 с PD-1 рецептором.
7. Биспецифическое антитело по п.1, характеризующееся тем, что первый антигенсвязывающий фрагмент, который специфически связывается c CD47, включает вариабельный домен тяжелой цепи, который содержит последовательность, выбранную из следующей группы: SEQ ID NO: 67, 75, 76, 81, 82, 84, 85.
8. Биспецифическое антитело по п.1, характеризующееся тем, что первый антигенсвязывающий фрагмент, который специфически связывается c CD47, включает вариабельный домен легкой цепи, который содержит последовательность, выбранную из следующей группы: SEQ ID NO: 100-103.
9. Биспецифическое антитело по п.1, характеризующееся тем, что первый антигенсвязывающий фрагмент, который специфически связывается c CD47, включает:
а) вариабельный домен тяжелой цепи, который содержит последовательности, выбранные из следующей группы: SEQ ID NO: 67, 75, 76, 81, 82, 84, 85, и
б) вариабельный домен легкой цепи, который содержит последовательности, выбранные из следующей группы: SEQ ID NO: 100-103.
10. Биспецифическое антитело по п.1, характеризующееся тем, что первый антигенсвязывающий фрагмент, который специфически связывается c CD47, включает:
i) а) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 67 и
б) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 100;
(ii) а) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 85, и
б) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 100;
(iii) а) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 84, и
б) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 100;
(iv) а) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 82, и
б) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 100;
(v) а) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 81, и
б) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 100;
(vi) а) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 75, и
б) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 101;
(vii) а) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 76, и
б) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 101;
(viii) а) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 75, и
б) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 102;
(ix) а) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 76, и
б) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 102;
(x) а) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 75, и
б) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 103;
или
(xi) а) вариабельный домен тяжелой цепи, который содержит аминокислотную последовательность SEQ ID NO: 76, и
б) вариабельный домен легкой цепи, который содержит аминокислотную последовательность SEQ ID NO: 103.
11. Биспецифическое антитело по п.1, характеризующееся тем, что оно вызывает антителозависимую клеточную цитотоксичность, макрофаг-опосредованный фагоцитоз и/или опосредованную T-клетками цитотоксичность в отношении клеток, несущих на поверхности антигены CD47 и/или PD-L1.
12. Биспецифическое антитело по п.1, характеризующееся тем, что оно содержит Fc-фрагмент по меньшей мере с одной мутацией или модификацией, которая повышает антителозависимую клеточно-опосредованную цитотоксичность (ADCC) и/или комплемент-зависимую цитотоксичность (CDC) по сравнению с тем же антителом без мутации или модификации.
13. Нуклеиновая кислота, которая кодирует биспецифическое антитело по любому из пп. 1-12.
14. Нуклеиновая кислота по п. 13, где нуклеиновая кислота представляет собой ДНК.
15. Экспрессионный вектор, содержащий нуклеиновую кислоту по любому из пп. 13, 14.
16. Способ получения клетки-хозяина для получения биспецифического антитела по любому из пп. 1-12, включающий трансформирование клетки вектором по п. 15.
17. Клетка-хозяин для получения биспецифического антитела по любому из пп. 1-12, содержащая нуклеиновую кислоту по любому из пп. 13, 14.
18. Способ получения биспецифического антитела по любому из пп. 1-12, заключающийся в культивировании клетки-хозяина по п. 17 в культуральной среде в условиях, достаточных для получения указанного антитела, при необходимости, с последующим выделением и очисткой полученного антитела.
19. Фармацевтическая композиция для профилактики или лечения заболевания или нарушения, опосредуемого PD-L1 и CD47, содержащая биспецифическое антитело по любому из пп. 1-12, в сочетании с одним или несколькими фармацевтически приемлемыми эксципиентами.
20. Фармацевтическая композиция по п. 19, предназначенная для профилактики или лечения заболевания или нарушения, опосредуемого PD-L1 и CD47, выбранного из группы: ПРГШ (плоскоклеточный рак головы и шеи), рак шейки матки, рак без выявленного первоисточника, глиобластома, рак пищевода, рак мочевого пузыря, ТНРМЖ (трижды негативный рак молочной железы), КРР (колоректальный рак), гепатоцеллюлярная карцинома, меланома, НМРЛ (немелкоклеточный рак легкого), рак почки, рак яичника, MSI КРР (колоректальный рак с высокой микросателлитной нестабильностью), лейкоз (острый или миелобластный), лимфома, множественная миелома, рак молочной железы, рак предстательной железы, саркома, гепатоцеллюлярная карцинома, лимфома Ходжкина, T- и B-клеточный острый лимфобластный лейкоз, мелкоклеточный рак лёгкого, острый миелобластный лейкоз, рефрактерная В-клеточная неходжкинская лимфома, фолликулярная лимфома, В-клеточная лимфома маргинальной зоны, крупноклеточная В-клеточной диффузная лимфома, плоскоклеточный рак головы и шеи, рак поджелудочной железы, рак яичника, острый миелобластный лейкоз и миелодиспластический синдром высокого риска.
21. Способ ингибирования биологической активности PD-L1 и/или CD47 у субъекта, нуждающегося в таком ингибировании, включающий введение субъекту эффективного количества биспецифического антитела по любому из пп. 1-12.
22. Применение биспецифического антитела по любому из пп. 1-12 для лечения у субъекта, нуждающегося в таком лечении заболевания или нарушения, опосредуемого PD-L1 и CD47.
23. Применение антитела по п.22, где заболевание или нарушение выбрано из группы: ПРГШ (плоскоклеточный рак головы и шеи), рак шейки матки, рак без выявленного первоисточника, глиобластома, рак пищевода, рак мочевого пузыря, ТНРМЖ (трижды негативный рак молочной железы), КРР (колоректальный рак), гепатоцеллюлярная карцинома, меланома, НМРЛ (немелкоклеточный рак легкого), рак почки, рак яичника, MSI КРР (колоректальный рак с высокой микросателлитной нестабильностью), лейкоз (острый или миелобластный), лимфома, множественная миелома, рак молочной железы, колоректальный рак, рак предстательной железы, рак мочевого пузыря, саркома, гепатоцеллюлярная карцинома, глиобластома, лимфома Ходжкина, T- и B-клеточный острый лимфобластный лейкоз, мелкоклеточный рак лёгкого, острый миелобластный лейкоз, рефрактерная В-клеточная неходжкинская лимфома, фолликулярная лимфома, В-клеточная лимфома маргинальной зоны, крупноклеточная В-клеточной диффузная лимфома, плоскоклеточный рак головы и шеи, рак поджелудочной железы, рак яичника, острый миелобластный лейкоз и миелодиспластический синдром высокого риска.
| WO 2014087248 А2, 12.06.2014 | |||
| US 2016108123 A1, 21.04.2016 | |||
| BROWN E.J., FRAZIER W.A., integrin-associated protein (CD47) and its ligands, TRENDS in Cell Biology, 2001, Vol.11 No.3, pages 130-135 | |||
| RU 2011128399 A, 20.01.2013. |
Авторы
Даты
2022-09-12—Публикация
2020-04-29—Подача