РОДСТВЕННАЯ ЗАЯВКА
[0001] По настоящей заявке испрашивается приоритет Предварительной заявки США No. 62/580320, поданной 1 ноября 2017 г., полное содержание которой приведено в настоящем описании в качестве ссылки.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
[0002] Настоящее изобретение относится к связанным с CRISPR/Cas9 способам и компонентам для редактирования последовательности-мишени нуклеиновой кислоты, например, гена рецептора II трансформирующего фактора роста β (TGFBR2), или модуляции экспрессии последовательности-мишени нуклеиновой кислоты, например, гена TGFBR2.
УРОВЕНЬ ТЕХНИКИ
[0003] Адоптивный перенос T-клеток с использованием генетически модифицированных T-клеток переведен в клиническое тестирование в качестве терапевтического средства для солидных и гематологических злокачественных опухолей. В исследованиях фазы I и II, включающих гематологические злокачественные опухоли (например, лимфому, хронический лимфоцитарный лейкоз (CLL) и острый лимфоцитарный лейкоз (ALL)), для многих пациентов показан по меньшей мере частичный ответ, при этом для некоторых показаны полные ответы (Kochenderfer, J. N. et al., 2012 Blood 119, 2709-2720). Однако, ответы, наблюдаемые в типах солидной опухоли (включая меланому, почечноклеточный рак и колоректальный рак), на всегда были настолько сильными (Johnson, L. A. et al., 2009 Blood 114, 535-546; Lamers, C. H. et al., 2013 Mol. Ther. 21, 904-912; Warren, R. S. et al., 1998 Cancer Gene Ther. 5, S1-S2).
[0004] Без желания быть связанными с конкретной теорией, на эффективность видов адоптивной T-клеточной терапии у пациентов с солидными опухолями может влиять рад факторов, таких как: (1) пролиферация T-клетки, например, ограниченная пролиферация T-клеток после адоптивного переноса; (2) выживаемость T-клетки, например, индукция апоптоза T-клетки посредством факторов в окружении клетки-мишени, например, клетки злокачественной опухоли; и (3) функция T-клетки, например, ингибирование функции цитотоксической T-клетки посредством ингибирующих факторов, секретированных иммуноцитами хозяина и клетки-мишени, например, клетки злокачественных опухолей. На эти факторы, в свою очередь, может влиять активность трансформирующего фактора роста β (TGF-β), цитокина, продуцируемого широким множеством типов опухолей, который, как показано, напрямую супрессирует инфильтрующие опухоль лимфоциты, так же как индуцирует и стимулирует функцию регуляторных T-клеток (Tрег), способных предотвращать противоопухолевый иммунитет.
[0005] TGFBR2 представляет собой рецептор для TGF-β, который экспрессируется на множестве типов клеток, включая иммуноциты. Показано, что связывание TGF-β посредством TGFBR2 осуществляет понижающую регуляцию активации, пролиферации и дифференцировки T-клетки. Разработка ингибиторов TGFBR2, которые могут уменьшать активность TGFBR2 на реакционноспособных по отношению к опухолям T-клетках, осложнялась отсутствием доклинических моделей на мышах из-за тяжелого аутоиммунного фенотипа, наблюдаемого у мышей, содержащих T-клетки, сконструированные для отсутствия TGFBR2, в определенных условиях. Следовательно, существует необходимость в эффективных способах уменьшения или прекращения ингибирующего T-клетки влияния TGF-β, в контексте опосредованной T-клетками иммунотерапии, включительно.
[0006] CRISPR (короткие палиндромные повторы, расположенные кластерами, равномерно удаленные друг от друга) сформировались в процессе эволюции у бактерий и архей в качестве адаптивной иммунной системы для защиты против вирусной атаки. При воздействии вируса, короткие фрагменты вирусной ДНК интегрируют в локус CRISPR. РНК транскибируется с части локуса CRISPR, включающей вирусную последовательность. Эта РНК, содержащая последовательность, комплементарную вирусному геному, опосредует нацеливание направляемой РНК нуклеазы на последовательность-мишень в вирусном геноме. Направляемая РНК нуклеаза, в свою очередь, расщепляет и таким образом, выключает вирусную мишень.
[0007] Недавно, система CRISPR/Cas9 адаптирована для редактирования генома в эукариотических клетках. Введение сайт-специфических двухцепочечных разрывов (DSB) позволяет изменение последовательности-мишени посредством эндогенных механизмов репарации ДНК, например, соединения негомологичных концов (NHEJ) или направляемой гомологией рекомбинации (HDR). CRISPR/Cas9 представляет собой многообещающий путь для решения проблемы опосредованного TGF-β ингибирования T-клеток в контексте терапии опухолей, но до настоящего времени не идентифицировано осуществимых способов решения этой проблемы в T-клетках для использования в терапии опухолей.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0008] В определенных аспектах, настоящее изобретение относится к системам редактирования генома и родственным композициям и способам для направленного редактирования последовательности нуклеиновой кислоты TGFBR2. В конкретных вариантах осуществления, такое направленное редактирование приводит к изменению (например, понижающей регуляции) экспрессии TGFBR2. В конкретных вариантах осуществления, такое изменение экспрессии происходит в T-клетках. В конкретных вариантах осуществления, изменение экспрессии TGFBR2 в T-клетках включает использование рибонуклеопротеинового (RNP) комплекса в качестве системы редактирования генома, содержащей направляемый РНК белок нуклеазу в комплексе с нРНК, нацеливающей на ген TGFBR2. В конкретных вариантах осуществления, изменение экспрессии TGFBR2 происходит в результате двухцепочечного разрыва, индуцированного посредством RNP, и последующей несовершенной репарации, что приводит к инделам в и/или поблизости от нацеленной последовательности TGFBR2.
[0009] В конкретных вариантах осуществления, настоящее изобретение относится к системам редактирования генома, включающим направляющую РНК с нацеливающим доменом, который является комплементарным последовательности-мишени из гена TGFBR2, и где направляемая РНК нуклеаза представляет собой нуклеазу Cas9. Нацеливающий домен может являться на 70%, 80%, 85%, 90%, 95% или 100% комплементарным.
[0010] В конкретных вариантах осуществления, нацеливающий домен имеет длину 16, 17, 18, 19, 20, 21, 22, 23, 24, 25 или 26 нуклеотидов.
[0011] В конкретных вариантах осуществления, нацеливающий домен имеет по меньшей мере 18 смежных нуклеотидов, которые являются комплементарными гену TGFBR2.
[0012] В конкретных вариантах осуществления, нацеливающий домен содержит нуклеотидную последовательность, которая является идентичной или отличается не более, чем на 3 нуклеотида, от нуклеотидной последовательности, выбранной из SEQ ID NO: 5036-5096. В конкретных вариантах осуществления, нацеливающий домен имеет конфигурацию для образования двухцепочечного разрыва или одноцепочечного разрыва в пределах приблизительно 500 п.о., приблизительно 450 п.о., приблизительно 400 п.о., приблизительно 350 п.о., приблизительно 300 п.о., приблизительно 250 п.о., приблизительно 200 п.о., приблизительно 150 п.о., приблизительно 100 п.о., приблизительно 50 п.о., приблизительно 25 п.о. или приблизительно 10 п.о. от положения мишени в TGFBR2.
[0013] В конкретных вариантах осуществления, описанных в настоящем описании, система редактирования генома является способной изменять ген TGFBR2 посредством нокаута экспрессии гена TGFBR2 или нокдауна экспрессии гена TGFBR2.
[0014] В конкретных вариантах осуществления, системы редактирования генома, описанные в настоящем описании, включают нРНК, содержащую нацеливающий домен, имеющий конфигурацию для нацеливания на кодирующую область или некодирующую область гена TGFBR2, где указанная некодирующая область содержит промоторную область, энхансерную область, интрон, 3’-UTR, 5’-UTR или область сигнала полиаденилирования указанного гена TGFBR2; и кодирующая область включает, например, раннюю кодирующую область указанного гена TGFBR2.
[0015] В конкретных вариантах осуществления, системы редактирования генома, описанные в настоящем описании, имеют последовательность-мишень гена TGFBR2, содержащую последовательность, выбранную из группы, состоящей из SEQ ID NO: 1, 2 и 3.
[0016] В конкретных вариантах осуществления, системы редактирования генома, описанные в настоящем описании, имеют последовательность-мишень гена TGFBR2, содержащую последовательность, выбранную из группы, состоящей из SEQ ID NO: 4-10.
[0017] В конкретных вариантах осуществления, системы редактирования генома, описанные в настоящем описании, включают нацеливающий домен, содержащий нуклеотидную последовательность, которая является идентичной или отличается не более, чем на 3 нуклеотида, от нуклеотидной последовательности, выбранной из SEQ ID NO: 5036-5096. В конкретных вариантах осуществления, нацеливающий домен содержит нуклеотидную последовательность, которая является идентичной или отличается не более, чем на 3 нуклеотида, от нуклеотидной последовательности, выбранной из группы, состоящей из: (a) SEQ ID NO: 5041; (b) SEQ ID NO: 5042; (c) SEQ ID NO: 5047; (d) SEQ ID NO: 5050; (e) SEQ ID NO: 5052; (f) SEQ ID NO: 5092; и (g) SEQ ID NO: 5093. В конкретных вариантах осуществления, система редактирования генома включает пары молекул нРНК, включая, например, пары нРНК, имеющие последовательности-мишени SEQ ID NO: 5042 и 5041 или 5042 и 5092, или SEQ ID NO: 5042 и 5093, или SEQ ID NO: 5093 и 5041.
[0018] В конкретных вариантах осуществления, настоящее изобретение относится к композиции, содержащей молекулу нРНК, содержащую нацеливающий домен, который является комплементарным последовательности-мишени гена TGFBR2. В конкретных вариантах осуществления, композиция содержит одну, две, три или четыре молекулы нРНК. В конкретных вариантах осуществления, композиция дополнительно содержит направляемую РНК нуклеазу, например, молекулу Cas9. В конкретных вариантах осуществления, нацеливающий домен, включенный в такие композиции, содержит нуклеотидную последовательность, которая является идентичной или отличается не более, чем на 3 нуклеотида, от нуклеотидной последовательности, выбранной из SEQ ID NO: 5036-5096. В конкретных вариантах осуществления, нацеливающий домен содержит нуклеотидную последовательность, которая является идентичной или отличается не более, чем на 3 нуклеотида, от нуклеотидной последовательности, выбранной из группы, состоящей из: (a) SEQ ID NO: 5041; (b) SEQ ID NO: 5042; (c) SEQ ID NO: 5047; (d) SEQ ID NO: 5050; (e) SEQ ID NO: 5052; (f) SEQ ID NO: 5092; и (g) SEQ ID NO: 5093. В конкретных вариантах осуществления, композиция содержит пары молекул нРНК, включая, например, пары нРНК, имеющие последовательности-мишени SEQ ID NO: 5042 и 5041 или 5042 и 5092, или SEQ ID NO: 5042 и 5093, или SEQ ID NO: 5093 и 5041.
[0019] В конкретных вариантах осуществления, настоящее изобретение относится к вектору, кодирующему молекулу нРНК, содержащую нацеливающий домен, который является комплементарным последовательности-мишени гена TGFBR2. В конкретных вариантах осуществления, вектор дополнительно кодирует направляемую РНК нуклеазу, например, молекулу Cas9. В конкретных вариантах осуществления, нацеливающий домен нРНК, кодированный вектором, содержит нуклеотидную последовательность, которая является идентичной или отличается не более, чем на 3 нуклеотида, от нуклеотидной последовательности, выбранной из SEQ ID NO: 5036-5096. В конкретных вариантах осуществления, нацеливающий домен содержит нуклеотидную последовательность, которая является идентичной или отличается не более, чем на 3 нуклеотида, от нуклеотидной последовательности, выбранной из группы, состоящей из: (a) SEQ ID NO: 5041; (b) SEQ ID NO: 5042; (c) SEQ ID NO: 5047; (d) SEQ ID NO: 5050; (e) SEQ ID NO: 5052; (f) SEQ ID NO: 5092; и (g) SEQ ID NO: 5093. В конкретных вариантах осуществления, вектор представляет собой вирусный вектор. В конкретных вариантах осуществления, вектор представляет собой аденоассоциированный вирусный (AAV) вектор или лентивирусный (LV) вектор.
[0020] В конкретных вариантах осуществления, настоящее изобретение относится к способу изменения гена TGFBR2 в клетке, включающему введение в указанную клетку одного из: (i) системы редактирования генома, содержащей молекулу нРНК, содержащую нацеливающий домен, который является комплементарным последовательности-мишени указанного гена TGFBR2, и молекулу Cas9; (ii) вектора, содержащего полинуклеотид, кодирующий молекулу нРНК, содержащую нацеливающий домен, который является комплементарным последовательности-мишени указанного гена TGFBR2, и полинуклеотид, кодирующий молекулу Cas9; или (iii) композиции, содержащей молекулу нРНК, содержащую нацеливающий домен, который является комплементарным последовательности-мишени указанного гена TGFBR2, и молекулу Cas9.
[0021] В конкретных вариантах осуществления, настоящее изобретение относится к клетке, содержащей систему редактирования генома, как описано в настоящем описании, композицию нРНК, как описано в настоящем описании, или вектор, как описано в настоящем описании. В конкретных вариантах осуществления, клетка экспрессирует TGFBR2. В конкретных вариантах осуществления, клетка представляет собой T-клетку.
[0022] В конкретных вариантах осуществления, настоящее изобретение относится к нРНК и направляемой РНК нуклеазе, составляющим рибонуклеопротеиновый (RNP) комплекс.
[0023] В конкретных вариантах осуществления, настоящее изобретение относится к введению в клетку двух или более RNP комплексов, содержащих нРНК с различными нацеливающими доменами.
[0024] В конкретных вариантах осуществления, настоящее изобретение относится к RNP комплексам, содержащим ферментативно активные нуклеазы Cas9 (eaCas9).
[0025] В конкретных вариантах осуществления, настоящее изобретение относится к RNP комплексам, содержащим нуклеазы eaCas9, образующие двухцепочечные разрывы в нуклеиновой кислоте-мишени или одноцепочечные разрывы в нуклеиновой кислоте-мишени.
[0026] В конкретных вариантах осуществления, настоящее изобретение относится к двум RNP комплексам, содержащим различные нРНК, используемым для образования одноцепочечных разрывов со смещением в гене TGFBR2 в клетке.
[0027] В конкретных вариантах осуществления, настоящее изобретение относится к клетке, представляющей собой T-клетку или клетку естественного киллера (NK). В конкретных вариантах осуществления, клетка дополнительно содержит сконструированный T-клеточный рецептор (eTCR) или химерный рецептор антигена (CAR).
[0028] В конкретных вариантах осуществления, настоящее изобретение относится к способу опосредованного направляемой РНК нуклеазой изменения экспрессии гена TGFBR2 в клетке, включающему: a) приведение клетки в контакт с достаточным количеством нРНК, нацеленной на TGFBR2, и направляемой РНК нуклеазы; и b) образование первого двухцепочечного разрыва ДНК около положения мишени в TGFBR2 в гене TGFBR2 в клетке, где первый двухцепочечный разрыв ДНК подвергается репарации посредством NHEJ, где указанная репарация изменяет экспрессию гена TGFBR2.
[0029] В конкретных вариантах осуществления, настоящее изобретение относится к образованию второго двухцепочечного разрыва ДНК около положения мишени в TGFBR2. В конкретных вариантах осуществления, первый двухцепочечный разрыв образуется в пределах приблизительно 500 п.о., приблизительно 450 п.о., приблизительно 400 п.о., приблизительно 350 п.о., приблизительно 300 п.о., приблизительно 250 п.о., приблизительно 200 п.о., приблизительно 150 п.о., приблизительно 100 п.о., приблизительно 50 п.о., приблизительно 25 п.о., или приблизительно 10 п.о. от положения мишени в TGFBR2. В конкретных вариантах осуществления, первый и второй двухцепочечные разрывы образуются в пределах приблизительно 500 п.о., приблизительно 450 п.о., приблизительно 400 п.о., приблизительно 350 п.о., приблизительно 300 п.о., приблизительно 250 п.о., приблизительно 200 п.о., приблизительно 150 п.о., приблизительно 100 п.о., приблизительно 50 п.о., приблизительно 25 п.о. или приблизительно 10 п.о. от положения мишени в TGFBR2. В конкретных вариантах осуществления, первый двухцепочечный разрыв образуется в кодирующей области или в некодирующей области указанного гена TGFBR2, где указанная некодирующая область содержит промоторную область, энхансерную область, интрон, 3’-UTR, 5’-UTR или область сигнала полиаденилирования указанного гена TGFBR2. В конкретных вариантах осуществления первый и второй двухцепочечные разрывы образуются в кодирующей области или в некодирующей области указанного гена TGFBR2, где указанная некодирующая область содержит промоторную область, энхансерную область, интрон, 3’-UTR, 5’-UTR или область сигнала полиаденилирования указанного гена TGFBR2.
[0030] В конкретных вариантах осуществления, кодирующая область выбрана из экзона 3, экзона 4 и экзона 5.
[0031] В конкретных вариантах осуществления, нацеливающий домен содержит нуклеотидную последовательность, которая является идентичной или отличается не более, чем на приблизительно 3 нуклеотида, от нуклеотидной последовательности, выбранной из группы, состоящей из SEQ ID NO: 5036-5096.
[0032] В конкретных вариантах осуществления, направляемая РНК нуклеаза представляет собой нуклеазу Cas9 S. pyogenes, и указанный нацеливающий домен содержит нуклеотидную последовательность, которая является идентичной или отличается не более, чем на приблизительно 3 нуклеотида, от нуклеотидной последовательности, выбранной из группы, состоящей из: (a) SEQ ID NO: 5041; (b) SEQ ID NO: 5042; (c) SEQ ID NO: 5047; (d) SEQ ID NO: 5050; (e) SEQ ID NO: 5052; (f) SEQ ID NO: 5092; и (g) SEQ ID NO: 5093.
[0033] В конкретных вариантах осуществления, направляемая РНК нуклеаза представляет собой нуклеазу Cas9 S. aureus.
[0034] В конкретных вариантах осуществления, направляемая РНК нуклеаза представляет собой мутантную нуклеазу Cas9.
[0035] В конкретных вариантах осуществления, репарация посредством NHEJ образует вставку или делецию с частотой, большей или равной 20%.
[0036] В конкретных вариантах осуществления, частота вставки или делеции больше или равна 30%, 40% или 50%.
[0037] В конкретных вариантах осуществления, настоящее изобретение относится к клетке, подвергнутой геномной инженерии, содержащей вставку или делецию поблизости от или внутри положения-мишени гена TGFBR2, где указанное положение-мишень содержит нуклеотидную последовательность, которая является комплементарной или отличается не более, чем на приблизительно 3 нуклеотида, от нуклеотидной последовательности, выбранной из SEQ ID NO: 5036-5096.
[0038] В конкретных вариантах осуществления, вставка или делеция находится в пределах приблизительно 500 п.о., приблизительно 450 п.о., приблизительно 400 п.о., приблизительно 350 п.о., приблизительно 300 п.о., приблизительно 250 п.о., приблизительно 200 п.о., приблизительно 150 п.о., приблизительно 100 п.о., приблизительно 50 п.о., приблизительно 25 п.о. или приблизительно 10 п.о. от положения мишени в TGFBR2.
[0039] В конкретных вариантах осуществления, клетка представляет собой T-клетку или клетку NK. В конкретных вариантах осуществления, клетка дополнительно содержит eTCR или CAR.
[0040] В конкретных вариантах осуществления, настоящее изобретение относится к композиции, содержащей: a) популяцию клеток, подвергнутых геномной инженерии, содержащих вставку или делецию поблизости от или внутри положения-мишени гена TGFBR2, где указанное положение-мишень содержит нуклеотидную последовательность, которая является комплементарной или отличается не более, чем на приблизительно 3 нуклеотида, от нуклеотидной последовательности, выбранной из SEQ ID NO: 5036-5096; и b) фармацевтически приемлемый буфер.
[0041] В конкретных вариантах осуществления, популяция клеток содержит T-клетки или клетки NK. В конкретных вариантах осуществления, клетка дополнительно содержит eTCR или CAR.
[0042] В конкретных вариантах осуществления, настоящее изобретение относится к способу лечения злокачественной опухоли у субъекта, включающему введение субъекту модифицированных иммуноцитов, где модифицированные иммуноциты имеют уменьшенную экспрессию TGFBR2 и, необязательно, экспрессируют сконструированный T-клеточный рецептор (eTCR) или химерный рецептор антигена (CAR), где модифицированные иммуноциты имеют вставку или делецию поблизости от или внутри положения-мишени гена TGFBR2.
[0043] В конкретных вариантах осуществления, модифицированные иммуноциты содержат T-клетки или клетки NK. В конкретных вариантах осуществления, клетка дополнительно содержит eTCR или CAR.
[0044] В конкретных вариантах осуществления, злокачественная опухоль выбрана из группы, состоящей из: лейкоза, лимфомы, например, хронического лимфоцитарного лейкоза (CLL), острого лимфобластного лейкоза (ALL), неходжскинской лимфомы, острого миелоидного лейкоза, множественной миеломы, невосприимчивой фолликулярной лимфомы, лимфомы из клеток мантийной зоны, индолентной B-клеточной лимфомы, злокачественных новообразований B-клеток, злокачественных опухолей ободочной кишки, легкого, печени, молочной железы, предстательной железы, яичников, кожи, меланомы, злокачественных опухолей кости и мозга, рака яичника, эпителиальных злокачественных опухолей, почечноклеточной карциномы, аденокарциномы поджелудочной железы, лимфомы Ходжкина, карциномы шейки матки, колоректального рака, глиобластомы, нейробластомы, саркомы Юинга, медуллобластомы, остеосаркомы, синовиальной саркомы, мезотелиомы и/или любого типа злокачественной опухоли, экспрессирующей TGF-β.
[0045] В конкретных вариантах осуществления, T-клетки представляют собой CD4+ и/или CD8+ T-клетки.
[0046] В конкретных вариантах осуществления, модифицированные иммуноциты сохраняют или имеют увеличенную активность лизиса против клетки-мишени злокачественной опухоли, по сравнению с немодифицированным иммуноцитом.
[0047] В конкретных вариантах осуществления, модифицированные иммуноциты сохраняют или имеют увеличенную экспрессию гранзима B и/или интерферона-гамма в присутствии TGFβ, по сравнению с немодифицированными иммуноцитами.
[0048] В конкретных вариантах осуществления, модифицированные иммуноциты сохраняют или имеют улучшенную персистенцию против повторной стимуляции антигеном, по сравнению с немодифицированными иммуноцитами.
[0049] В конкретных вариантах осуществления, модифицированные иммуноциты сохраняют или имеют увеличенную экспрессию CD25, по сравнению с немодифицированными иммуноцитами.
[0050] В конкретных вариантах осуществления, модифицированные иммуноциты сохраняют или имеют уменьшенную экспрессию PD-1 по сравнению с немодифицированными иммуноцитами.
[0051] В конкретных вариантах осуществления, модифицированные иммуноциты сохраняют или имеют увеличенную пролиферацию, по сравнению с немодифицированными иммуноцитами.
[0052] В конкретных вариантах осуществления, настоящее изобретение относится к композиции, содержащей множество модифицированных T-клеток, где указанные модифицированные T-клетки имеют уменьшенную экспрессию гена TGFBR2, по сравнению с немодифицированными T-клетками.
[0053] В конкретных вариантах осуществления, модифицированные T-клетки имеют уровень экспрессии гена TGFBR2, составляющий приблизительно 50%, приблизительно 40%, приблизительно 30%, приблизительно 20%, приблизительно 10% или приблизительно 5% от уровня экспрессии TGFBR2 в немодифицированных T-клетках.
[0054] В конкретных вариантах осуществления, модифицированные T-клетки дополнительно имеют экспрессию eTCR или CAR.
[0055] В конкретных вариантах осуществления, T-клетки представляют собой CD4+ T-клетки и/или CD8+ T-клетки.
[0056] В конкретных вариантах осуществления, модифицированные T-клетки дополнительно отличаются обладанием: a) увеличенной активностью лизиса против клеток-мишеней злокачественной опухоли, по сравнению с немодифицированными T-клетками; b) сохраненной или увеличенной экспрессией гранзима B и/или интерферона-гамма в присутствии TGFβ, по сравнению с немодифицированными T-клетками; c) сохраненной или увеличенной персистенцией против повторной стимуляции антигеном, по сравнению с немодифицированными T-клетками; d) сохраненной или увеличенной экспрессией CD25, по сравнению с немодифицированными T-клетками; e) сохраненной или уменьшенной экспрессией PD-1, по сравнению с немодифицированными T-клетками; и/или f) сохраненной или увеличенной пролиферацией, по сравнению с немодифицированными T-клетками.
[0057] В конкретных вариантах осуществления, настоящее изобретение относится к композиции, содержащей множество модифицированных T-клеток, где указанные модифицированные T-клетки имеют уменьшенную экспрессию гена TGFBR2, по сравнению с немодифицированными T-клетками, указанные модифицированные T-клетки получены посредством приведения немодифицированных T-клеток в контакт с системой редактирования генома, содержащей: нРНК, содержащую нацеливающий домен, который является комплементарным последовательности-мишени гена TGFBR2; и направляемую РНК нуклеазу.
[0058] В конкретных вариантах осуществления, модифицированные T-клетки дополнительно трансдуцируют вектором, экспрессирующим eTCR или CAR. В конкретных вариантах осуществления, вектор представляет собой вирусный вектор. В конкретных вариантах осуществления, вирусный вектор представляет собой аденоассоциированный вирусный (AAV) вектор или лентивирусный (LV) вектор.
[0059] В конкретных вариантах осуществления, направляемая РНК нуклеаза представляет собой нуклеазу Cas9 S. pyogenes, и указанный нацеливающий домен содержит нуклеотидную последовательность, которая является идентичной или отличается не более, чем на приблизительно 3 нуклеотида, от нуклеотидной последовательности, выбранной из группы, состоящей из: (a) SEQ ID NO: 5041; (b) SEQ ID NO: 5042; (c) SEQ ID NO: 5047; (d) SEQ ID NO: 5050; (e) SEQ ID NO: 5052; (f) SEQ ID NO: 5092; и (g) SEQ ID NO: 5093.
[0060] В конкретных вариантах осуществления, настоящее изобретение относится к композиции, содержащей множество модифицированных T-клеток, где указанные модифицированные T-клетки имеют недостаточность передачи сигналов TGFBR2.
[0061] В конкретных вариантах осуществления, недостаточность передачи сигналов TGFBR2 опосредована экспрессией доминантно-негативной (DN) формы TGFBR2 в указанных модифицированных T-клетках.
[0062] В конкретных вариантах осуществления, модифицированные T-клетки дополнительно трансдуцируют вектором, экспрессирующим eTCR или CAR. В конкретных вариантах осуществления, вектор представляет собой вирусный вектор. В конкретных вариантах осуществления, вирусный вектор представляет собой аденоассоциированный вирусный (AAV) вектор или лентивирусный (LV) вектор.
[0063] В конкретных вариантах осуществления, T-клетки представляют собой CD4+ T-клетки и/или CD8+ T-клетки.
[0064] В конкретных вариантах осуществления, модифицированные T-клетки дополнительно отличаются обладанием: a) увеличенной активностью лизиса против клеток-мишеней злокачественной опухоли, по сравнению с немодифицированными T-клетками; b) сохраненной или увеличенной экспрессией гранзима B и/или интерферона-гамма в присутствии TGFβ, по сравнению с немодифицированными T-клетками; c) сохраненной или увеличенной персистенцией против повторной стимуляции антигеном, по сравнению с немодифицированными T-клетками; d) сохраненной или увеличенной экспрессией CD25, по сравнению с немодифицированными T-клетками; e) сохраненной или уменьшенной экспрессией PD-1, по сравнению с немодифицированными T-клетками; и/или f) сохраненной или увеличенной пролиферацией, по сравнению с немодифицированными T-клетками.
[0065] В конкретных вариантах осуществления, модифицированные иммуноциты дополнительно имеют уменьшенную экспрессию TGFBR2 дикого типа.
[0066] В конкретных вариантах осуществления, экспрессию TGFBR2 дикого типа уменьшают посредством приведения модифицированных иммуноцитов в контакт с системой редактирования генома, содержащей: нРНК, содержащую нацеливающий домен, который является комплементарным последовательности-мишени гена TGFBR2; и направляемую РНК нуклеазу.
[0067] В конкретных вариантах осуществления, настоящее изобретение относится к рибонуклеопротеиновому (RNP) комплексу, содержащему нРНК, содержащую нацеливающий домен, который является комплементарным последовательности-мишени гена TGFBR2, и направляемую РНК нуклеазу.
[0068] В конкретных вариантах осуществления RNP по п.117, направляемая РНК нуклеаза представляет собой нуклеазу Cas9.
[0069] В конкретных вариантах осуществления RNP по п.117, RNP вводят в клетки посредством электропорации.
[0070] Если не определено иное, все технические и научные термины термины, в рамках изобретения, имеют такое же значение, какое является общепринятым для специалиста в области, к которой относится это изобретение. Хотя способы и материалы, сходные или эквивалентные с описанными в настоящем описании, можно использовать в практике или тестировании настоящего изобретения, пригодные способы и материалы описаны ниже. Полное содержание всех публикаций, патентных заявок, патентов и других ссылок, упомянутых в настоящем описании, приведено в качестве ссылки. Кроме того, материалы, способы и примеры являются только иллюстративными, а не ограничивающими.
[0071] Заголовки, включая числовые и буквенные заголовки и подзаголовки, предназначены для организации и представления, и не предназначены для ограничения.
[0072] Другие признаки и преимущества по изобретению станут очевидными из подробного описания, примеров, чертежей и из формулы изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0073] Сопутствующие чертежи предназначены для предоставления иллюстративных и схематических, а не исчерпывающих, примеров конкретных аспектов и вариантов осуществления по настоящему описанию. Чертежи не предназначены для ограничения или связи с какой-либо конкретной теорией или моделью, и не обязательно представлены в масштабе. Без ограничения вышеуказанным, нуклеиновые кислоты и полипептиды можно изображать как линейные последовательности, или как схематические двух- или трехмерные структуры; эти изображения предназначены для иллюстрации, а не для ограничения или связи с какой-либо конкретной моделью или теорией, применительно к их структуре.
[0074] На фиг. 1 показан список иллюстративных нРНК, нацеленных на экзоны 1A-5 рецептора II трансформирующего фактора роста β (TGFBR2), и ассоциированный с ними % активности соединения негомологичных концов (NHEJ).
[0075] На фиг. 2 показана эффективность редактирования генома для конкретных иллюстративных пар нРНК.
[0076] На фиг. 3 показан % образования инделов, как определено посредством miSeq в гене TGFBR2. Семь нРНК тестировали в различных концентрациях RNP для получения кривой зависимости ответа от дозы.
[0077] На фиг. 4A - фиг. 4B показан % редактированных клеток (фиг. 4A) и % частоты инделов (фиг. 4B) для нескольких тестированных нРНК, нацеленных на TGFBR2, и контрольной нРНК, нацеленной на локус AAVS1.
[0078] На фиг. 5 показано сравнение двух нацеленных на TGFBR2 нРНК по их способности образовывать мутации инделы вне рамки.
[0079] На фиг. 6 показана относительная продукция IFN-гамма в первичных T-клетках, трансдуцированных для экспрессии CAR против BCMA, на фоне редактирования гена TGFBR2, в присутствии (10 нг/мл) или в отсутствие TGFβ. Сравнивали одиночные или парные нРНК.
[0080] На фиг. 7 показана относительная пролиферация клеток в первичных T-клетках, трансдуцированных для экспрессии CAR против BCMA, на фоне редактирования гена TGFBR2, в присутствии (10 нг/мл) или в отсутствие TGFβ. Сравнивали одиночные или парные нРНК.
[0081] На фиг. 8A - фиг. 8B показана экспрессия CD25 (фиг. 8A) и PD-1 (фиг. 8B) в первичных T-клетках, трансдуцированных для экспрессии CAR против BCMA на фоне редактирования гена TGFBR2, в присутствии (10 нг/мл) или в отсутствие TGFβ. Сравнивали одиночные или парные нРНК. Клетки также стимулировали с использованием клеток RPMI 8226 в течение 48 часов.
[0082] На фиг. 9 показано фосфорилирование Smad 2/3 в T-клетках, трансдуцированных для экспрессии различных CAR на фоне редактирования гена TGFBR2, в присутствии (10 нг/мл) или в отсутствие TGFβ.
[0083] На фиг. 10 показана относительная экспрессия гранзима B в T-клетках, трансдуцированных для экспрессии различных CAR, на фоне редактирования гена TGFBR2, в присутствии (10 нг/мл) или в отсутствие TGFβ.
[0084] На фиг. 11 показана продукция IFN-гамма в T-клетках, трансдуцированных для экспрессии различных CAR, на фоне редактирования гена TGFBR2, в присутствии (10 нг/мл) или в отсутствие TGFβ.
[0085] На фиг. 12 показана относительная пролиферация T-клетки в T-клетках, трансдуцированных для экспрессии различных CAR, на фоне редактирования гена TGFBR2, в присутствии (10 нг/мл) или в отсутствие TGFβ.
[0086] На фиг. 13A-фиг. 13B показана продукция гранзима B (фиг. 13A) и интерферона-гамма (фиг. 13B) в первичных T-клетках, трансдуцированных для экспрессии CAR против BCMA, на фоне редактирования гена TGFBR2 или DN TGFBR2, в присутствии (10 нг/мл) или в отсутствие TGFβ.
[0087] На фиг. 14 показан относительный % лизиса клеток RPMI 8226 посредством экспрессирующих CAR против BCMA T-клеток, на фоне редактирования гена TGFBR2 или DN TGFBR2, в присутствии (10 нг/мл) или в отсутствие TGFβ.
[0088] На фиг. 15A - фиг. 15F показаны экспрессирующие T-клетки с CAR против BCMA на фоне нередактированного TGFBR2, редактированного гена TGFBR2 или DN TGFBR2 с повторяющейся стимуляцией антигеном TGFβ. На фиг. 15A - фиг. 15C показано расчетное количество клеток после стимуляции тремя различными антигенами. На фиг. 15D - фиг. 15F показан % экспрессирующих CAR против BCMA T-клеток с течением времени, с повторяющейся стимуляцией антигеном TGFβ.
[0089] На фиг. 16A-фиг. 16B показана продукция INF-гамма в первичных T-клетках, трансдуцированных для экспрессии CAR против BCMA на фоне редактирования гена TGFBR2 или DN TGFBR2, в присутствии (10 нг/мл) или в отсутствие TGFβ. T-клетки инкубировали совместно либо с клетками RPMI 8226 (фиг. 16A), либо с клетками OPM2 (фиг. 16B).
[0090] На фиг. 17A - фиг. 17B показана экспрессия CD25 в первичных T-клетках, трансдуцированных для экспрессии CAR против BCMA, на фоне редактирования гена TGFBR2 или DN TGFBR2, в присутствии (10 нг/мл) или в отсутствие TGFβ. T-клетки инкубировали совместно либо с клетками RPMI 8226 (фиг. 17A), либо с клетками OPM2 (фиг. 17B).
[0091] На фиг. 18A - фиг. 18B показана экспрессия PD-1 в первичных T-клетках, трансдуцированных для экспрессии CAR против BCMA, на фоне редактирования гена TGFBR2 или DN TGFBR2, в присутствии (10 нг/мл) или в отсутствие TGFβ. T-клетки инкубировали совместно либо с клетками RPMI 8226 (фиг. 18A), либо с клетками OPM2 (фиг. 18B).
[0092] На фиг. 19A - фиг. 19B показана относительная пролиферация клеток (фиг. 19A) и относительная продукция IFN-гамма (фиг. 19B) для экспрессирующих CAR против BCMA T-клеток, на фоне редактирования гена TGFBR2 или DN TGFBR2, в присутствии (10 нг/мл) или в отсутствие TGFβ. Клетки также стимулировали с использованием клеток RPMI 8226.
[0093] На фиг. 20A - фиг. 20B показан % PD-1+клеток в нескольких CD4+ (фиг. 20A) и CD8+ (фиг. 20B) экспрессирующих CAR против BCMA T-клетках, на фоне редактирования гена TGFBR2 или DN TGFBR2, при увеличивающихся концентрациях TGFβ. Клетки также стимулировали с использованием клеток RPMI 8226 в течение 48 часов.
[0094] На фиг. 21 показан уровень экспрессии генов пути передачи сигнала TGFβ PMEPA1, SKIL, SKI и LDLRAD4 в экспрессирующих CAR против BCMA T-клетках, на фоне редактирования гена TGFBR2 или DN TGFBR2. T-клетки выделяли из селезенки мыши или из опухоли, происходящей из клеток RPMI 8226.
[0095] На фиг. 22 показаны уровни фосфорилирования Smad 2/3, пролиферация, и экспрессия гранзима B в экспрессирующих CAR против CD19 T-клетках, на фоне DN TGFBR2, в присутствии и в отсутствие TGFβ.
[0096] На фиг. 23 показана схема определения того, обеспечивает ли редактирование гена TGFBR2 в T-клетках селективное преимущество над клетками дикого типа.
[0097] На фиг. 24 показаны различные соотношения клеток с CAR против BCMA, TGFBR2-KO и WT-клеток (1, 0,75, 0,5, 0,25). Клетки культивировали совместно с клетками RPMI8226 в соотношении эффектора к мишени 1:1±10 нг/мл TGFβ. Клетки собирали каждые 7 суток для анализа % инделов посредством высокопроизводительного секвенирования. Клетки повторно стимулировали свежими RPMI8226 и повторно доводили до соотношения эффектора к мишени 1:1 еженедельно.
ПОДРОБНОЕ ОПИСАНИЕ
Определения и сокращения
[0098] Если не указано иное, каждый из следующих терминов имеет значение, ассоциированное с ним в этом разделе.
[0099] Неконкретизированные формы единственного числа относятся к по меньшей мере одному из ассоциированных существительных, и использованы взаимозаменяемо с терминами «по меньшей мере один» и «один или несколько». Например, «модуль» обозначает по меньшей мере один модуль, или один или несколько модулей.
[0100] Союзы «или» и «и/или» использованы взаимозаменяемо в качестве неисключительных дизъюнкций.
[0101] Фраза «в основном состоящий из» означает, что перечисленные виды являются преобладающими видами, но что другие виды могут присутствовать в следовых количествах или количествах, не влияющих на структуру, функцию или поведение рассматриваемой композиции. Например, композиция, в основном состоящая из конкретных видов, может, как правило, содержать 90%, 95%, 96% или более этих видов.
[0102] «Домен» используют для описания фрагмента белка или нуклеиновой кислоты. Если не указано иное, домен, не обязательно, должен иметь какое-либо специфическое функциональное свойство.
[0103] «Индел» представляет собой вставку и/или делецию в последовательности нуклеиновой кислоты. Индел может являться продуктом репарации двухцепочечного разрыва ДНК, такого как двухцепочечный разрыв, образованный системой редактирования генома по настоящему описанию. Индел наиболее часто образуется при репарации разрыва посредством пути репарации «пониженной точности», такого как путь NHEJ, описанный ниже. Индел может приводить к вставкам или делециям, образующим мутации в рамке считывания или вне рамки считывания в последовательности-мишени.
[0104] «Конверсия генов» относится к изменению последовательности ДНК посредством включения эндогенной гомологичной последовательности (например, гомологичной последовательности внутри массива генов). «Коррекция генов» относится к изменению последовательности ДНК посредством включения экзогенной гомологичной последовательности, такой как экзогенная одно- или двухцепочечная донорная ДНК-матрица. Конверсия генов и коррекция генов являются продуктами репарации двухцепочечных разрывов ДНК посредством путей HDR, таких как описаны ниже.
[0105] Индел, конверсию генов, коррекцию генов и другие исходы редактирования генома, как правило, оценивают посредством секвенирования (наиболее часто способами «секвенирования нового поколения» или «секвенирования посредством синтеза», хотя секвенирование по Сенджеру все еще можно использовать) и количественно оценивают посредством относительной частоты количественных изменений (например, ±1, ±2 или более оснований) в представляющем интерес участке, среди всех прочтений секвенирования. Образцы ДНК для секвенирования могут быть получены множеством способов, известных в данной области, и они могут включать амплификацию представляющих интерес участков посредством полимеразной цепной реакции (ПЦР), связывание концов ДНК, образованных посредством двухцепочечных разрывов, как в способе GUIDEseq, описанном в Tsai et al. (Nat. Biotechnol. 34(5): 483 (2016), содержание которого приведено в настоящем описании в качестве ссылки) или другие способы, хорошо известные в данной области. Исходы редактирования генома можно также оценивать способами гибридизации in situ, например, посредством системы FiberComb™, коммерциализированной Genomic Vision (Bagneux, France), и посредством любых других пригодных способов, известных в данной области.
[0106] «Alt-HDR», «альтернативная направляемая гомологией рекомбинация» или «альтернативная HDR» использованы взаимозаменяемо для обозначения способа репарации повреждения ДНК с использованием гомологичной нуклеиновой кислоты (например, эндогенной гомологичной последовательности, например, сестринской хроматиды или экзогенной нуклеиновой кислоты, например, нуклеиновой кислоты-матрицы). Alt-HDR отличается от канонической HDR тем, что этот процесс использует пути, отличные от канонической HDR, и может быть ингибирован каноническими медиаторами HDR, RAD51 и BRCA2. Alt-HDR отличается также участием одноцепочечной или имеющей разрывы гомологичной нуклеиновой кислоты-матрицы, в то время как в канонической HDR, как правило, участвует двухцепочечная гомологичная матрица.
[0107] «Каноническая HDR», «каноническая направляемая гомологией рекомбинация» или «cHDR» относятся к способу репарации повреждения ДНК с использованием гомологичной нуклеиновой кислоты (например, эндогенной гомологичной последовательности, например, сестринской хроматиды или экзогенной нуклеиновой кислоты, например, нуклеиновой кислоты-матрицы). Каноническая HDR как правило, действует, когда присутствует значительное разрезание в двухцепочечном разрыве, образующее по меньшей мере одну одноцепочечную часть ДНК. В нормальной клетке, cHDR как правило, включает серии стадий, таких как узнавание разрыва, стабилизация разрыва, разрезание, стабилизация одноцепочечной ДНК, формирование промежуточного продукта кроссинговера ДНК, разрешение промежуточного продукта кроссинговера и лигирование. Этот процесс требует RAD51 и BRCA2, и гомологичная нуклеиновая кислота является, как правило, двухцепочечной.
[0108] Если не указано иное, термин «HDR», в рамках изобретения, включает как каноническую HDR, так и alt-HDR.
[0109] «Соединение негомологичных концов» или «NHEJ» относится к опосредованной лигированием репарации и/или не опосредованной матрицей репарации, включая каноническое NHEJ (cNHEJ) и альтернативное NHEJ (altNHEJ), которое, в свою очередь, включает опосредованное микрогомологией соединение концов (MMEJ), гибридизацию одиночных цепей (SSA), и зависимое от синтеза опосредованное микрогомологией соединение концов (SD-MMEJ).
[0110] «Замещение» или «замещенный», при использовании применительно к модификации молекулы (например, нуклеиновой кислоты или белка), не требует ограничения процесса, но просто указывает на присутствие события замещения.
[0111] «Субъект» обозначает человека или не относящегося к человеку животного. Субъект-человек может находиться в любом возрасте (например, грудной ребенок, ребенок, подросток или взрослый), и может страдать от заболевания, или может нуждаться в изменении гена. Альтернативно, субъект может представлять собой животное, где термин включает, но без ограничения, млекопитающих, птиц, рыб, рептилий, земноводных и более конкретно, нечеловекообразных приматов, грызунов (таких как мыши, крысы, хомяки и т.д.), кроликов, морских свинок, собак, кошек и т.д. В конкретных вариантах осуществления этого изобретения, субъект представляет собой скот, например, корову, лошадь, овцу или козу. В конкретных вариантах осуществления, субъект представляет собой домашнюю птицу.
[0112] «Лечить», «лечение» и «обработка» обозначают лечение заболевания у субъекта (например, субъекта-человека), включая одно или несколько из подавления заболевания, т.е., остановки или предотвращения его развития или прогрессирования; облегчения заболевания, т.е., вызова регрессии состояния заболевания; облегчения одного или нескольких симптомов заболевания; и излечения заболевания.
[0113] «Предотвращать», «предотвращающий» и «предотвращение» относятся к предотвращению заболевания у млекопитающего, например, у человека, включая (a) исключение или пресечение заболевания; (b) влияние на предрасположенность к заболеванию; или (c) предотвращение или задержку начала по меньшей мере одного симптома заболевания.
[0114] «Набор» относится к любой коллекции из двух или более компонентов, которые вместе составляют функциональную единицу, которую можно использовать для конкретной цели. В качестве иллюстрации (а не ограничения), один набор, по настоящему изобретению может включать направляющую РНК, образующую комплекс или способную образовывать комплекс с направляемой РНК нуклеазой, и сопровождаемую (например, суспендированную в или поддающуюся суспендированию в) фармацевтически приемлемым носителем. Набор можно использовать для введения комплекса, например, в клетку или субъекту, с целью вызова желательного геномного изменения в такой клетке или у такого субъекта. Компоненты набора могут быть упакованы вместе, или они могут быть упакованы отдельно. Наборы по настоящему изобретению также, необязательно, включают инструкцию по применению (DFU), описывающую использование набора, например, в соответствии со способом по настоящему изобретению. DFU может быть физически упакована вместе с набором, или может быть сделана доступной для пользователя набора, например, с помощью электронных средств.
[0115] Термины «полинуклеотид», «нуклеотидная последовательность», «нуклеиновая кислота», «молекула нуклеиновой кислоты», «последовательность нуклеиновой кислоты», и «олигонуклеотид» относятся к сериям нуклеотидных оснований (также называемых «нуклеотиды») в ДНК и РНК, и обозначают любую цепь из двух или более нуклеотидов. Полинуклеотиды, нуклеотидные последовательности, нуклеиновые кислоты и т.д. могут представлять собой химерные смеси, или их производные или модифицированные варианты, одноцепочечные или двухцепочечные. Они могут являться модифицированными по группе основания, группе сахара или фосфатному остову, например, для улучшения стабильности молекулы, параметров ее гибридизации и т.д. Нуклеотидная последовательность, как правило, переносит генетическую информацию, включая, но без ограничения, информацию, используемую клеточным аппаратом для получения белков и ферментов. Эти термины включают двух- или одноцепочечную геномную ДНК, РНК, любой синтетический и генетически модифицированный полинуклеотид, и как смысловые, так и антисмысловые полинуклеотиды. Эти термины также включают нуклеиновые кислоты, содержащие модифицированные основания.
[0116] Общепринятую терминологию IUPAC используют в нуклеотидных последовательностях, представленных в настоящем описании, как показано в таблице 1, ниже (см. также Cornish-Bowden A, Nucleic Acids Res. 1985 May 10; 13(9):3021-30, содержание которого приведено в настоящем описании в качестве ссылки). Следует отметить, однако, что «T» обозначает «тимин или урацил» в тех случаях, когда последовательность может быть кодирована посредством либо ДНК, либо РНК, например, в нацеливающих доменах нРНК.
Таблица 1: Терминология IUPAC для нуклеиновой кислоты
[0117] Термины «белок», «пептид» и «полипептид» использованы взаимозаменяемо для обозначения последовательной цепи аминокислот, связанных пептидными связями. Термины включают индивидуальные белки, группы или комплексы белков, ассоциированные вместе, так же как фрагменты или части, варианты, производные и аналоги таких белков. Пептидные последовательности представлены в настоящем описании с использованием общепринятой терминологии, начинающейся с амино- или N-конца слева и продолжающейся до карбоксильного или C-конца справа. Можно использовать стандартные однобуквенные или трехбуквенные сокращенные обозначения.
[0118] Термин «вариант» относится к молекуле, такой как полипептид, полинуклеотид или малая молекула, для которой показана значительная структурная идентичность с эталонной молекулой, но которая структурно отличается от эталонной молекулы по присутствию или уровню одной или нескольких химических групп, по сравнению с эталонной молекулой. Во многих вариантах осуществления, вариант также отличается функционально от своей эталонной молекулы. Как правило, то, можно ли конкретную молекулу корректно считать «вариантом» эталонной молекулы, основано на степени ее структурной идентичности с эталонной молекулой.
Обзор
[0119] Системы редактирования генома, описанные в настоящем описании, как правило, включают одну или несколько нРНК, содержащих нацеливающие домены, комплементарные одной или нескольким последовательностям-мишеням TGFBR2, где последовательности-мишени, в свою очередь, включают последовательности или прилегают к последовательностям смежного с протоспейсером мотива (PAM), узнаваемого одной или несколькими направляемыми РНК нуклеазами, с которыми одна или несколько нРНК могут связываться (например, образовывать комплекс). Соответственно, системы редактирования генома по настоящему изобретению нацелены, сайт-специфическим образом, на одну или несколько последовательностей-мишеней TGFBR2, и действуют для введения изменения внутри или поблизости от этих последовательностей-мишеней TGFBR2.
[0120] Изменения, введенные внутри или поблизости от участков-мишеней TGFBR2 посредством систем редактирования генома по настоящему изобретению, могут, наиболее часто, включать одноцепочечные разрывы ДНК (SSB или «ники») и/или двухцепочечные разрывы ДНК (DSB). Ники и DSB, в свою очередь, подвергаются репарации клетками таким образом, который может приводить к введению небольших инделов или более крупных вставок или делеций в один или несколько участков-мишеней TGFBR2, делеций последовательностей между двумя участками-мишенями TGFBR2, и/или вставок последовательностей (в частности экзогенных последовательностей, введенных в клетки посредством донорных олигонуклеотидов-матриц) в участки TGFBR2, или между двумя участками-мишенями TGFBR2, таким образом, который заменяет эндогенную клеточную последовательность ДНК между этими участками-мишенями. Однако, в некоторых случаях, системы редактирования генома вводят одно или несколько из точечных мутаций (например, посредством дезаминирования цистеина), изменения маркировки ДНК (например, метилирования ДНК, ацетилирования или деацетилирования гистона, или других модификаций хроматина) и/или привлечения транс-действующих факторов, таких как факторы транскрипции. Альтернативно, системы редактирования генома по настоящему изобретению могут вступать в ассоциацию, длительным (например, на протяжении интервала из нескольких недель, месяцев или дольше) или временным (на протяжении интервала из нескольких секунд, минут, часов или суток) образом, с одной или несколькими последовательностями-мишенями TGFBR2, таким образом, предотвращая ассоциацию других факторов (в частности, РНК-полимераз, но также ДНК-полимераз, факторов транскрипции, и/или других цис- или транс-действующих факторов, влияющих на экспрессию гена) с последовательностями-мишенями TGFBR2. Эти и другие способы действия систем редактирования генома и их компонентов подробно описаны ниже под заголовками «направляемые РНК нуклеазы» и «модификации направляемых РНК нуклеаз».
[0121] Последовательности-мишени TGFBR2 и соответствующие последовательности нацеливающего домена нРНК, как правило, но необязательно, локализованы в экзонах, где введение небольшого индела, или более крупной вставки или делеции может приводить к одной или нескольким мутациям (например, мутации со сдвигом рамки считывания, нонсенс-мутации, введению кодона для аминокислоты, нарушающей структуру окружающего белка, и/или удалению кодона для аминокислоты, необходимой для активности белка), уменьшающим или прекращающим функционирование белка TGFBR2. На фиг. 1 показано картирование разрезающей активности различных направляющих РНК S. pyogenes в локализациях, на которые они нацелены, в экзонной структуре гена TGFBR2. Эти мутации обозначены на протяжении этого описания как мутации «нокаута», и их функциональным эффектом является «нокаут» функции белка TGFBR2.
[0122] Определенные последовательности-мишени TGFBR2 можно считать являющимися «горячими точками» участками-мишенями для последовательностей нацеливающего домена нРНК. В рамках изобретения, «горячая точка» относится к участку, предпочтительно подвергаемому нацеливанию, поскольку он приводит к высоким частотам % инделов или эффективному нокдауну или нокауту гена TGFBR2. нРНК, нацеленные на один или несколько из этих предпочтительных участков, могут приводить к частотам % инделов 30% или выше. Например, предпочтительный участок-мишень в гене TGFBR2 может иметь комплементарные нацеливающие домены нРНК, приводящие к частотам % инделов 30%, 40%, 50%, 60%, 70%, 80%, 85%, 90%, 95% или выше. Являющиеся «горячими точками» участки-мишени в гене TGFBR2 описаны в настоящем описании.
[0123] Предпочтительные области горячих точек TGFBR2 показаны в таблице 2:
Таблица 2: Предпочтительные участки-мишени TGFBR2
[0124] Особенно предпочтительные области горячих точек TGFBR2 показаны в таблице 3:
[0125] Последовательность-мишень TGFBR2 может быть, например, локализована в экзоне 3, 4 или 5 гена TGFBR2. Последовательность нацеливающего домена нРНК, соответствующая последовательности-мишени TGFBR2, присутствующей в экзоне 3, 4, или 5 гена TGFBR2, может содержать нуклеотидную последовательность, которая является идентичной или отличается не более, чем на 1, 2 или 3 нуклеотида, от нуклеотидной последовательности, выбранной из SEQ ID NO: 5036-5096. Например, но без ограничения, иллюстративный нацеливающий домен может содержать нуклеотидную последовательность, которая является идентичной или отличается не более, чем на 1, 2 или 3 нуклеотида, от нуклеотидной последовательности, выбранной из группы, состоящей из:
(a) SEQ ID NO: 5041;
(b) SEQ ID NO: 5042;
(c) SEQ ID NO: 5047;
(d) SEQ ID NO: 5050;
(e) SEQ ID NO: 5052;
(f) SEQ ID NO: 5092; и
g) SEQ ID NO: 5093.
Таблица 4 - Нацеливающие последовательности
[0126] В качестве альтернативы нокауту экспрессии TGFBR2, можно осуществлять нацеливание на область регуляции транскрипции, например, промоторную область (например, промоторную область, контролирующую транскрипцию гена TGFBR2) для изменения (например, нокдауна) экспрессии гена. Способ направленного нокдауна может быть опосредован системой CRISPR/Cas, содержащей ферментативно неактивную молекулу Cas9 (eiCas9) или слитого с eiCas9 белка (например, eiCas9, слитого с доменом репрессора транскрипции или модифицирующим хроматин белком), как описано в настоящем описании. Например, одна или несколько молекул нРНК, содержащие нацеливающий домен, могут иметь конфигурацию для нацеливания молекулы eiCas9 или слитого с eiCas9 белка, достаточно близко к области регуляции транскрипции, например, промоторной области (например, промоторной области, контролирующей транскрипцию гена TGFBR2), таким образом, что транскрипцию гена TGFBR2 уменьшают и/или прекращают. В конкретных вариантах осуществления, eiCas9 или слитый с eiCas9 белок можно использовать для нокдауна экспрессии TGFBR2 в T-клетке, например, T-клетке человека.
[0127] Нокаут и/или нокдаун TGFBR2 можно оценивать любым подходящим способом, включая без ограничения, исследование последовательности гена TGFBR2, оценку экспрессии белка TGFBR2 на поверхности клеток (например, посредством иммуноокрашивания и сортировки клеток, в частности посредством активированной флуоресценцией сортировки клеток или FACS, включая проточную цитометрию с непрямым внутриклеточным окрашиванием), детекцию клеточных или молекулярных изменений, опосредованных TGFBR2, оценку эффекта TGF-β на пролиферацию или выживаемость клеток, или посредством Вестерн-блоттинга для детекции уровни белка TGFBR2. Применительно к T-клеткам, в частности, нокаут TGFBR2 можно подтверждать посредством (a) анализа секвенирования локуса TGFBR2 или удлинения праймера T7E1, и/или (b) внутриклеточной оценки FACS фосфорилирования SMAD2/3. Секвенирование и T7E1 более подробно описаны ниже, в то время как анализы фосфорилирования внутриклеточного SMAD2/3 описаны в литературе, например, в Chen, et al., J. Experimental Med. Volume 198, Number 12, December 15, 2003 1875-1886 (полное содержание которого приведено в настоящем описании в качестве ссылки и для всех целей), в частности, в разделе материалы и методы на странице 1877 и дополнительной фигуре S2.
[0128] Нокаут и/или нокдаун TGFBR2 могут соответствовать уменьшению на 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 85%, 90%, 95% или 100% экспрессии TGFBR2, относительно исходного измерения или клетки дикого типа.
[0129] В некоторых аспектах, представленные композиции и способы включают композиции и способы, в которых: по меньшей мере или более чем приблизительно 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90% или 95% клеток в композиции клеток, в которые введено средство (например, нРНК/Cas9) для нокаута или генетического повреждения гена TGFBR2, содержат генетическое повреждение; не экспрессируют эндогенный полипептид TGFBR2; не содержат непрерывный ген TGFBR2, ген TGFBR2 и/или функциональный ген TGFBR2. В некоторых вариантах осуществления, способы, композиции и клетки по настоящему изобретению включают те, в которых по меньшей мере или более чем приблизительно 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90% или 95% клеток в композиции клеток, в которые введено средство (например, нРНК/Cas9) для нокаута или генетического повреждения гена TGFBR2, не экспрессируют полипептид TGFBR2, например, на поверхности клеток. В некоторых вариантах осуществления, по меньшей мере или более чем приблизительно 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90% или 95% клеток в композиции клеток, в которые введено средство (например, нРНК/Cas9) для нокаута или генетического повреждения гена TGFBR2, имеют нокаут по обоим аллелям, т.е. содержат биаллельную делецию, в таком проценте клеток.
[0130] Системы редактирования генома, нацеленные на TGFBR2, можно осуществлять множеством способов, и их осуществление можно адаптировать для условий, в которых клетки редактируют. Конкретные варианты осуществления настоящего изобретения включают доставку направляемых РНК нуклеаз и направляющих РНК, нацеленных на TGFBR2, в клетки ex vivo в форме рибонуклеопротеиновых (RNP) комплексов посредством электропорации, например, с использованием электропораторов и кювет, доступных от коммерческих поставщиков, таких как MaxCyte (Gaithersburg, MD) или Lonza (Basel, Switzerland). Другие варианты осуществления, однако, могут включать in vivo векторы на основе нуклеиновых кислот, такие как вирусные векторы, или липидные наночастицы, для редактирования либо in vivo, либо ex vivo. Детали этих вариантов осуществления более подробно описаны ниже, под заголовком «Осуществление систем редактирования генома».
[0131] Нокаут и/или нокдаун TGFBR2 можно использовать во множестве условий, включая без ограничения, в контексте адаптивной T-клеточной терапии. В соответствии с вариантами осуществления настоящего изобретения, TGFBR2 подвергают нокауту в иммуноците, таком как T-клетка, который подлежит использованию в терапии. В качестве одного примера, T-клетка может экспрессировать сконструированный рецептор, такой как химерный рецептор антигена (CAR) или гетерологичный T-клеточный рецептор (TCR), где рецептор может иметь конфигурацию для узнавания на клетке или ткани антигена, вовлеченного в патологию, такую как опухоль. Независимо от того, экспрессируют они или нет сконструированный рецептор, T-клетки с нокаутом TGFBR2 по настоящему изобретению можно использовать для нацеливания на ткань или орган, в которых TGF-β присутствует в количествах, достаточных для уменьшения пролиферации или активности T-клеток, экспрессирующих TGFBR2.
[0132] Клетки с нокаутом и/или нокдауном TGFBR2 можно использовать в видах «аутологичной» клеточной терапии, в которых клетки собирают от субъекта, изменяют для нокаута или нокдауна экспрессии TGFBR2, и затем возвращают тому же самому субъекту; альтернативно, эти клетки можно вводить другому субъекту при «аллогенной» клеточной терапии. В другом способе, между сбором и введением клеток с TGFBR2 по настоящему изобретению, их можно подвергать манипуляции множеством способов, например, размножению, стимуляции, очистке или сортировке, трансдукции с использованием трансгена, замораживанию и/или размораживанию.
[0133] Нокаут или нокдаун присутствия гена TGFBR2, как описано в настоящем описании, может: (1) улучшать пролиферацию T-клетки; (2) улучшать выживаемость T-клетки; и/или (3) улучшать функцию T-клетки. Нокдаун экспрессии гена TGFBR2 , как описано в настоящем описании может, сходным образом: (1) улучшать пролиферацию T-клетки; (2) улучшать выживаемость T-клетки; и/или (3) улучшать функцию T-клетки.
Системы редактирования генома
[0134] Термин «система редактирования генома» относится к любой системе, имеющей направляемую РНК активность редактирования ДНК. Системы редактирования генома по настоящему описанию включают по меньшей мере два компонента, адаптированных из природных систем CRISPR: направляющую РНК (нРНК) и направляемую РНК нуклеазу. Эти два компонента формируют комплекс, способный к ассоциации со специфической последовательностью нуклеиновой кислоты и редактированию ДНК в или около этой последовательности нуклеиновой кислоты, например, посредством образования одного или нескольких из одноцепочечного разрыва (SSB или ника), двухцепочечного разрыва (DSB) и/или точечной мутации. В конкретных вариантах осуществления, двухцепочечный или одноцепочечный разрыв находится в пределах приблизительно 500 п.о., приблизительно 450 п.о., приблизительно 400 п.о., приблизительно 350 п.о., приблизительно 300 п.о., приблизительно 250 п.о., приблизительно 200 п.о., приблизительно 150 п.о., приблизительно 100 п.о., приблизительно 50 п.о., приблизительно 25 п.о. или приблизительно 10 п.о. от положения мишени в TGFBR2, таким образом, индуцируя изменение экспрессии гена TGFBR2.
[0135] Природные системы CRISPR в ходе эволюции были организованы на два класса и пять типов (Makarova et al. Nat Rev Microbiol. 2011 Jun; 9(6): 467-477 (Makarova), содержание которого приведено в настоящем описании в качестве ссылки), и в то время как в системах редактирования генома по настоящему описанию можно адаптировать компоненты из любого типа или класса природной системы CRISPR, варианты осуществления, представленные в настоящем описании, как правило адаптированы из систем CRISPR класса 2, и типа II или V. Системы класса 2, включающие типы II и V, отличаются относительно крупными, мультидоменными направляемыми РНК белками нуклеазы (например, Cas9 или Cpf1) и одной или несколькими направляющими РНК (например, crРНК и, необязательно, tracrРНК), формирующими рибонуклеопротеиновые (RNP) комплексы, осуществляющие ассоциацию (т.е., нацеливание) и расщепление специфических локусов, комплементарных нацеливающей (или спейсерной) последовательности crРНК. Системы редактирования генома по настоящему изобретению сходным образом осуществляют нацеливание и редактирование клеточных последовательностей ДНК, но значительно отличаются от систем CRISPR, встречающихся в природе. Например, мономолекулярные направляющие РНК, описанные в настоящем описании, не встречаются в природе, и как направляющие РНК, так и направляемые РНК нуклеазы по настоящему изобретению, могут включать любое количество не встречающихся в природе модификаций.
[0136] Системы редактирования генома можно осуществлять (например, вводить или доставлять в клетку или субъекту) множеством способов, и различные варианты осуществления могут являться подходящими для различных применений. Например, систему редактирования генома осуществляют, в конкретных вариантах осуществления, в форме комплекса белок/РНК (рибонуклеопротеинового или RNP), который можно включать в фармацевтическую композицию, которая, необязательно, включает фармацевтически приемлемый носитель и/или инкапсулирующее средство, такое как липидная или полимерная микро- или наночастица, мицелла, липосома и т.д. В конкретных вариантах осуществления, систему редактирования генома осуществляют в форме одной или нескольких нуклеиновых кислот, кодирующих компоненты направляемой РНК нуклеазы и направляющей РНК, описанные выше (необязательно, с одним или несколькими дополнительными компонентами); в конкретных вариантах осуществления, систему редактирования генома осуществляют в форме одного или нескольких векторов, содержащих такие нуклеиновые кислоты, например, вирусного вектора, такого как аденоассоциированный вирус; и в конкретных вариантах осуществления, систему редактирования генома осуществляют в форме комбинации любых из вышеуказанных. Дополнительные или модифицированные варианты осуществления, действующие в соответствии с принципами, указанными в настоящем описании, очевидны специалисту в данной области и входят в объем настоящего изобретения.
[0137] Следует отметить, что системы редактирования генома по настоящему описанию могут являться нацеленными на одиночную специфическую нуклеотидную последовательность, или могут являться нацеленными - и способными к параллельному редактированию - двух или более специфических нуклеотидных последовательностей посредством использования двух или более направляющих РНК. Использование множества нРНК обозначено как «мультиплексирование» на протяжении этого описания, и может быть использовано для нацеливания на множественные, неродственные представляющие интерес последовательности-мишени или для образования множества SSB или DSB внутри одного домена-мишени и, в некоторых случаях, для получения случаев специфического редактирования внутри такого домена-мишени. Например, в Международной публикации патента No. WO 2015/138510 от Maeder et al. (Maeder), приведенной в настоящем описании в качестве ссылки, описана система редактирования генома для коррекции точечной мутации (C.2991+1655A до G) в гене CEP290 человека, что приводит к образованию скрытого участка сплайсинга, который, в свою очередь, уменьшает или прекращает функцию гена. В системе редактирования генома от Maeder используют две направляющие РНК, нацеленные на последовательности на каждой стороне (т.е., фланкирующие) точечной мутации, и образуют DSB, фланкирующие мутацию. Это, в свою очередь, стимулирует делецию лежащей между ними последовательности, включающей мутацию, таким образом, уничтожая скрытый участок сплайсинга и восстанавливая нормальную функцию гена.
[0138] В качестве другого примера, в WO 2016/073990 от Cotta-Ramusino, et al. («Cotta-Ramusino»), содержание которого приведено в настоящем описании в качестве ссылки, описана система редактирования генома, в которой используют две нРНК в комбинации с никазой Cas9 (Cas9, образующей одноцепочечный ник, такой как S. pyogenes D10A), аранжировка, названная «системой двойной никазы». Система двойной никазы от Cotta-Ramusino имеет конфигурацию для образования двух ников на противоположных сторонах представляющей интерес последовательности со смещением на один или несколько нуклеотидов, где ники объединяют для образования двухцепочечного разрыва, имеющего выступающий конец (5’-в случае Cotta-Ramusino, хотя 3’-также являются возможным). Выступающий конец, в свою очередь, может способствовать событиям гомологичной репарации, в некоторых условиях. И, в качестве другого примера, в WO 2015/070083 от Palestrant et al. («Palestrant», содержание которого приведено в настоящем описании в качестве ссылки) описана нРНК, нацеленная на нуклеотидную последовательность, кодирующую Cas9 (обозначенная «ведущая РНК»), которую можно включать в систему редактирования генома, содержащую одну или несколько дополнительных нРНК, чтобы позволять временную экспрессию Cas9, которая может, в ином случае, конститутивно экспрессироваться, например, в некоторых трансдуцированных вирусом клетках. Эти применения мультиплексирования являются иллюстративными, а не ограничивающими, и специалисту в данной области понятно, что другие применения мультиплексирования, как правило, являются совместимыми с системами редактирования генома, описанными в настоящем описании.
[0139] Системы редактирования генома могут, в некоторых случаях, образовывать двухцепочечные разрывы, которые подвергаются репарации посредством клеточных механизмов с использованием двухцепочечного разрыва ДНК, таких как NHEJ или HDR. Эти механизмы описаны в литературе, например, в Davis & Maizels, PNAS, 111(10):E924-932, March 11, 2014 (Davis) (описывающем Alt-HDR); Frit et al. DNA Repair 17(2014) 81-97 (Frit) (описывающем Alt-NHEJ); и Iyama and Wilson III, DNA Repair (Amst.) 2013-Aug; 12(8): 620-636 (Iyama) (описывающем в общем пути канонической HDR и NHEJ).
[0140] Когда системы редактирования генома действуют посредством образования DSB, такие системы, необязательно, включают один или несколько компонентов, способствующих или облегчающих конкретный способ репарации двухцепочечного разрыва или конкретный исход репарации. Например, в Cotta-Ramusino описаны также системы редактирования генома, в которые добавлена одноцепочечная олигонуклеотидная «донорная матрица»; донорная матрица вставляется в область-мишень клеточной ДНК, расщепленную посредством системы редактирования генома, и может приводить к изменению в последовательности-мишени.
[0141] В конкретных вариантах осуществления, системы редактирования генома модифицируют последовательность-мишень, или модифицируют экспрессию гена в или около последовательности-мишени, без образования одно- или двухцепочечных разрывов. Например, система редактирования генома может включать направляемую РНК нуклеазу, слитую с функциональным доменом, которая воздействует на ДНК, таким образом, модифицируя последовательность-мишень или ее экспрессию. В качестве одного примера, направляемая РНК нуклеаза может являться соединенной с (например, слитой с) функциональным доменом цитозиндезаминазы, и может действовать посредством образования направленных замен C-на-A. Иллюстративные слитые белки нуклеазы/дезаминазы описаны в Komor et al. Nature 533, 420-424 (19 May 2016) («Komor»), содержание которого приведено в качестве ссылки. Альтернативно, система редактирования генома может использовать нуклеазу с инактивированным расщеплением (т.е., «неактивную»), такую как неактивная Cas9 (dCas9), и может действовать посредством формирования стабильных комплексов в одной или нескольких областях-мишенях клеточной ДНК, таким образом, создавая помехи для функций, затрагивающих область(области)-мишень, включая, без ограничения, транскрипцию мРНК, ремоделирование хроматина и т.д.
Молекулы направляющей РНК (нРНК)
[0142] Термины «направляющая РНК» и «нРНК» относятся к любой нуклеиновой кислоте, способствующей специфической ассоциации (или «нацеливанию») направляемой РНК нуклеазы, такой как Cas9 или Cpf1, с последовательностью-мишенью, такой как геномная или эписомная последовательность в клетке. нРНК могут являться мономолекулярными (содержащими одиночную молекулу РНК, и альтернативно обозначенными как химерная), или модульными (содержащими более одной, и как правило, две, отдельные молекулы РНК, такие как crРНК и tracrРНК, которые обычно ассоциированы друг с другом, например, посредством образования дуплекса). нРНК и составляющие их компоненты описаны в литературе, например, в Briner et al. (Molecular Cell 56(2), 333-339, October 23, 2014 (Briner), содержание которого приведено в качестве ссылки), и в Cotta-Ramusino.
[0143] У бактерий и архей, системы CRISPR типа II, как правило, включают направляемый РНК белок нуклеазу, такой как Cas9, CRISPR РНК (crРНК), включающую 5’-область, комплементарную чужеродной последовательности, и транс-активирующую crРНК (tracrРНК), включающую 5’-область, комплементарную и формирующую дуплекс с 3’-областью crРНК. Без намерения быть связанными какой-либо теорией, считают, что этот дуплекс облегчает формирование - и является необходимым для активности - комплекса Cas9/нРНК. Поскольку системы CRISPR типа II были адаптированы для использования в редактировании генов, обнаружено, что crРНК и tracrРНК можно соединять в одну мономолекулярную или химерную направляющую РНК, в одном неограничивающем примере, посредством четырех-нуклеотидной (например, GAAA) последовательности «тетрапетли» или «линкера», соединяющей мостиком комплементарные области crРНК (на 3’-конце) и tracrРНК (на 5’-конце). (Mali et al. Science. 2013 Feb 15; 339(6121): 823-826 («Mali»); Jiang et al. Nat Biotechnol. 2013 Mar; 31(3): 233-239 («Jiang»); и Jinek et al., 2012 Science Aug. 17; 337(6096): 816-821 («Jinek»), содержание всех из которых приведено в настоящем описании в качестве ссылки.)
[0144] Направляющие РНК, независимо от того, мономолекулярные они или модульные, включают «нацеливающий домен», полностью или частично комплементарный домену-мишени внутри последовательности-мишени, такой как последовательность ДНК в геноме клетки, где редактирование является желательным. Нацеливающие домены обозначены в литературе различными наименованиями, включая, без ограничения, «направляющие последовательности» (Hsu et al., Nat Biotechnol. 2013 Sep; 31(9): 827-832, («Hsu»), содержание которого приведено в настоящем описании в качестве ссылки), «области комплементарности» (Cotta-Ramusino), «спейсеры» (Briner) и в общей форме как «crРНК» (Jiang). Независимо от данных им наименований, нацеливающие домены, как правило, имеют длину 10-30 нуклеотидов, и в конкретных вариантах осуществления, имеют длину 16-24 нуклеотидов (например, длину 16, 17, 18, 19, 20, 21, 22, 23 или 24 нуклеотидов), и находятся на 5’-конце или около него, в случае нРНК Cas9, и на 3’-конце или около него, в случае нРНК Cpf1.
[0145] В дополнение к нацеливающим доменам, нРНК, как правило (но необязательно, как обсуждают ниже), включают множество доменов, которые могут влиять на формирование или активность комплексов нРНК/Cas9. Например, как упомянуто выше, дуплексная структура, сформированная первым и вторым комплементарными доменами нРНК (также обозначенная как дуплекс повтор:антиповтор), взаимодействует с узнающей (REC) частью Cas9 и может опосредовать формирование комплексов Cas9/нРНК. (Nishimasu et al., Cell 156, 935-949, February 27, 2014 (Nishimasu 2014) и Nishimasu et al., Cell 162, 1113-1126, August 27, 2015 (Nishimasu 2015), содержание обоих из которых приведено в настоящем описании в качестве ссылки). Следует отметить, что первый и/или второй комплементарные домены могут содержать один или несколько поли-A-хвостов, которые могут поддаваться узнаванию РНК-полимеразами в качестве сигнала терминации. Последовательность первого и второго комплементарных доменов, таким образом, необязательно, модифицируют для исключения этих хвостов и стимуляции полной транскрипции нРНК in vitro, например, с использованием замен A-G, как описано в Briner, или замен A-U. Эти и другие сходные модификации первого и второго комплементарных доменов включены в объем настоящего описания.
[0146] Вместе с первым и вторым комплементарными доменами, нРНК Cas9 как правило, включают две или более дополнительных дуплексных областей, участвующих в активности нуклеазы in vivo, но необязательно in vitro. (Nishimasu 2015). Первый домен стебель-петля около 3’-положения второго комплементарного домена обозначают различным образом как «проксимальный домен» (Cotta-Ramusino), «стебель-петля 1» (Nishimasu 2014 и 2015) и «щелевидный контакт» (Briner). Одна или несколько дополнительных структур стебель-петля, как правило, присутствуют около 3’-конца нРНК, где количество меняется в зависимости от вида: нРНК s. pyogenes как правило, включают две 3’-стебель-петли (всего четыре структуры стебель-петля, включая дуплекс повтор:антиповтор), в то время как s. aureus и другие виды имеют только одну (всего три структуры стебель-петля). Описание консервативных структур стебель-петля (и структур нРНК в более общем смысле), организованное по видам, представлено в Briner.
[0147] В то время как предшествующее описание сфокусировано на нРНК для использования с Cas9, следует понимать, что были (или могут быть в будущем) открыты или изобретены другие направляемые РНК нуклеазы, использующие нРНК, которые отличаются некоторым образом от описанных до настоящего времени. Например, Cpf1 («CRISPR из Prevotella и Franciscella 1») представляет собой недавно открытую направляемую РНК нуклеазу, не требующую tracrРНК для функционирования. (Zetsche et al., 2015, Cell 163, 759-771 October 22, 2015 (Zetsche I), содержание которого приведено в настоящем описании в качестве ссылки). нРНК для использования в системе редактирования генома Cpf1, как правило, включает нацеливающий домен и комплементарный домен (альтернативно обозначаемый как «ручка»). Следует отметить также, что в нРНК для использования с Cpf1, нацеливающий домен обычно присутствовать на 3’-конце или около него, а не на 5’-конце, как описано выше применительно к нРНК Cas9 (ручка находится на 5’-конце или около него в нРНК Cpf1).
[0148] Специалисту в данной области понятно, что, хотя могут существовать структурные различия между нРНК из различных прокариотических видов, или между нРНК Cpf1 и Cas9, принципы, по которым действуют нРНК, как правило, согласуются. Из-за этой согласованности действия, нРНК можно определять, в общих чертах, по последовательностям их нацеливающих доменов, и специалисту в данной области понятно, что данную последовательность нацеливающего домена можно включать в любую подходящую нРНК, включая мономолекулярную или химерную нРНК, или нРНК, включающую одну или несколько химических модификаций и/или модификаций последовательности (замен, дополнительных нуклеотидов, укорочений и т.д.). Таким образом, для экономного представления в этом описании, нРНК могут быть описаны единственно применительно к последовательностям их нацеливающих доменов.
[0149] В более общем смысле, специалисту в данной области понятно, что некоторые аспекты настоящего описания относятся к системам, способам и композициям, которые можно осуществлять с использованием множества направляемых РНК нуклеаз. По этой причине, если не указано иное, термин нРНК следует понимать как включающий любую пригодную нРНК, которую можно использовать с любой направляемой РНК нуклеазой, и не только те нРНК, которые являются совместимыми с конкретными видами Cas9 или Cpf1. В качестве иллюстрации, термин нРНК может, в конкретных вариантах осуществления, включать нРНК для использования с любой направляемой РНК нуклеазой, встречающейся в системе CRISPR класса 2, такой как система CRISPR типа II или типа V, или направляемой РНК нуклеазой, происходящей или адаптированной из них.
[0150] В таблице 5 ниже представлены иллюстративные нРНК для нацеливания на TGFBR2 с использованием Cas9 S. pyogenes.
Таблица 5.
Дизайн нРНК
[0151] Способы отбора и подтверждения последовательностей-мишеней, так же как анализов неспецифических взаимодействий, описаны ранее, например, в Mali; Hsu; Fu et al., 2014 Nat Biotechnol 32(3): 279-84, Heigwer et al., 2014 Nat methods 11(2):122-3; Bae et al. (2014) Bioinformatics 30(10): 1473-5; и Xiao A et al. (2014) Bioinformatics 30(8): 1180-1182. Содержание каждой из этих ссылок которого приведено в настоящем описании в качестве ссылки. В качестве неограничивающего примера, дизайн нРНК может включать использование инструмента программного обеспечения для оптимизации выбора потенциальных последовательностей-мишеней, соответствующих пользовательской последовательность-мишени, например, для минимизации общей неспецифической активности на протяжении генома. В то время как неспецифическая активность не является ограниченной расщеплением, эффективность расщепления каждой нецелевой последовательности можно прогнозировать, например, с использованием полученной экспериментально схемы взвешивания. Эти и другие способы отбора направляющей РНК подробно описаны в Maeder и Cotta-Ramusino.
Модификации нРНК
[0152] Активность, стабильность или другие характеристики нРНК можно изменять посредством включения конкретных модификаций. В качестве одного примера, временно экспрессируемые или доставляемые нуклеиновые кислоты могут быть подвержены деградации, например, посредством клеточных нуклеаз. Соответственно, нРНК, описанные в настоящем описании, могут содержать один или несколько модифицированных нуклеозидов или нуклеотидов, придающих устойчивость к нуклеазам. Без намерения быть связанными теорией, считают также, что конкретные модифицированные нРНК, описанные в настоящем описании, могут вызывать уменьшенный врожденный иммунный ответ при введении в клетки. Специалистам в данной области известны конкретные клеточные ответы, обычно наблюдаемые в клетках, например, клетках млекопитающих, в ответ на экзогенные нуклеиновые кислоты, в частности, вирусного или бактериального происхождения. Такие ответы, которые могут включать экспрессию и высвобождение цитокинов и гибель клетки, можно совместно уменьшать или исключать посредством модификаций, представленных в настоящем описании.
[0153] Конкретные иллюстративный модификации, обсуждаемые в этом разделе, можно включать в любом положении в последовательности нРНК, включая, без ограничения, на 5’-конце или около него (например, в пределах 1-10, 1-5 или 1-2 нуклеотидов от 5’-конца) и/или на 3’-конце или около него (например, в пределах 1-10, 1-5 или 1-2 нуклеотидов от 3’-конца). В некоторых случаях, модификации располагают внутри функциональных мотивов, таких как дуплекс повтор-антиповтор нРНК Cas9, структура стебель-петля нРНК Cas9 или Cpf1, и/или нацеливающий домен нРНК.
[0154] В качестве одного примера, 5’-конец нРНК может включать структуру кэпа эукариотической мРНК или аналог кэпа (например, аналог кэпа G(5’)ppp(5’)G, аналог кэпа m7G(5’)ppp(5’)G или аналог кэп-структуры с прямой ориентацией (ARCA) 3’-O-Me-m7G(5’)ppp(5’)G), как показано ниже:

Кэп или аналог кэпа можно включать в ходе либо химического синтеза, либо транскрипции нРНК in vitro.
[0155] Аналогичным образом, 5’-конец нРНК может быть лишен 5’-трифосфатной группы. Например, транскрибированные in vitro нРНК можно обрабатывать фосфатазой (например, с использованием щелочной фосфатазы из кишечника теленка) для удаления 5’-трифосфатной группы.
[0156] Другая распространенная модификация включает добавление, на 3’-конце нРНК, множества (например, 1-10, 10-20, или 25-200) остатков аденина (A), обозначенных как полиA-хвост. ПолиA-хвост можно добавлять к нРНК в ходе химического синтеза, после транскрипции in vitro с использованием полиаденозин-полимеразы (например, поли(A)-полимеразы E. coli) или in vivo посредством последовательности для полиаденилирования, как описано в Maeder.
[0157] Следует отметить, что модификации, описанные в настоящем описании, можно комбинировать любым подходящим образом, например, нРНК, независимо от того, является ли она транскрибированной in vivo с ДНК-вектора или транскрибированной in vitro нРНК, может включать любую или оба из структуры 5’-кэпа или аналога кэпа и 3’-полиA-хвоста.
[0158] Направляющие РНК можно модифицировать по рибозе 3’-концевого U. Например, две концевых гидроксильных группы рибозы U можно окислять до альдегидных групп и сопровождать размыканием рибозного кольца для получения модифицированного нуклеозида, как показано ниже:
 ,
,
где «U» может представлять собой немодифицированный или модифицированный уридин.
[0159] Рибозу 3’-концевого U можно модифицировать с использованием 2’3’-циклического фосфата, как показано ниже:
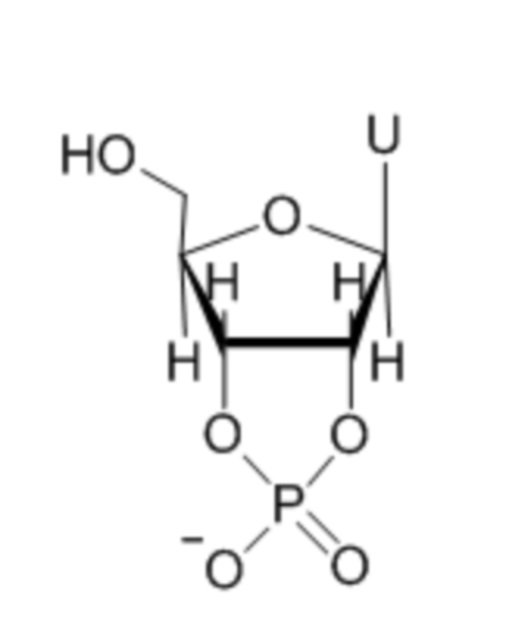 ,
,
где «U» может представлять собой немодифицированный или модифицированный уридин.
[0160] Направляющие РНК могут содержать 3’-нуклеотиды, которые можно стабилизировать против деградации, например, посредством включения одного или нескольких из модифицированных нуклеотидов, описанных в настоящем описании. В конкретных вариантах осуществления, остатки уридина можно заменять на остатки модифицированного уридина, например, 5-(2-амино)пропилуридин и 5-бромуридин, или на любой из остатков модифицированного уридина, описанных в настоящем описании; остатки аденозина и гуанозина можно заменять на остатки модифицированного аденозина и гуанозина, например, с модификациями в 8-положении, например, 8-бромгуанозин, или на любой из остатков модифицированного аденозина или гуанозина, описанных в настоящем описании.
[0161] В конкретных вариантах осуществления, рибонуклеотиды с модифицированным сахаром можно включать в нРНК, например, где 2’-OH-группа заменена группой, выбранной из H, -OR, -R (где R может представлять собой, например, алкил, циклоалкил, арил, аралкил, гетероарил или сахар), гало, -SH, -SR (где R может представлять собой, например, алкил, циклоалкил, арил, аралкил, гетероарил или сахар), амино (где амино может представлять собой, например, NH2; алкиламино, диалкиламино, гетероциклил, ариламино, диариламино, гетероариламино, дигетероариламино или аминокислоту); или циано (-CN). В конкретных вариантах осуществления, фосфатный остов можно модифицировать, как описано в настоящем описании, например, с использованием фосфотиоатной (PhTx) группы. В конкретных вариантах осуществления, каждый из одного или нескольких нуклеотидов из нРНК может независимо представлять собой модифицированный или немодифицированный нуклеотид, включающий, но без ограничения, модифицированный 2’-сахар, например, модифицированный с использованием 2’-O-метила, 2’-O-метоксиэтила или 2’-фтора, включая, например, 2’-F или 2’-O-метил, аденозин (A), 2’-F или 2’-O-метил, цитидин (C), 2’-F или 2’-O-метил, уридин (U), 2’-F или 2’-O-метил, тимидин (T), 2’-F или 2’-O-метил, гуанозин (G), 2’-O-метоксиэтил-5-метилуридин (Teo), 2’-O-метоксиэтиладенозин (Aeo), 2’-O-метоксиэтил-5-метилцитидин (m5Ceo) и любые их комбинации.
[0162] Направляющие РНК могут также включать «запертые» нуклеиновые кислоты (LNA), в которых 2’-OH-группа может быть связана, например, посредством C1-6 алкиленового или C1-6 гетероалкиленового мостика, с 4’-атомом углерода того же сахара рибозы. Любую пригодную группу можно использовать для обеспечения таких мостиков, включая, без ограничения, метиленовые, пропиленовые, эфирные или амино-мостики; O-амино (где амино может представлять собой, например, NH2; алкиламино, диалкиламино, гетероциклил, ариламино, диариламино, гетероариламино или дигетероариламино, этилендиамин или полиамино) и аминоалкокси или O(CH2)n-амино (где амино может представлять собой, например, NH2; алкиламино, диалкиламино, гетероциклил, ариламино, диариламино, гетероариламино, или дигетероариламино, этилендиамин или полиамино).
[0163] В конкретных вариантах осуществления, нРНК может включать модифицированный нуклеотид, который является полициклическим (например, трицикло; и «незапертые» формы, такие как гликоль-нуклеиновая кислота (GNA) (например, R-GNA или S-GNA, где рибоза является замещенной звеньями гликоля, присоединенными к фосфодиэфирным связям), или треозо-нуклеиновая кислота (TNA, где рибоза является замещенной α-L-треофуранoзил-(3’→2’)).
[0164] Как правило, нРНК включают группу сахара рибозы, которая представляет собой 5-членное кольцо, имеющее кислород. Иллюстративные модифицированные нРНК могут включать, без ограничения, замещение кислорода в рибозе (например, серой (S), селеном (Se) или алкиленом, например, таким как метилен или этилен); добавление двойной связи (например, для замены рибозы на циклопентенил или циклогексенил); сужение кольца рибозы (например, для формирования 4-членного кольца циклобутана или оксетан); расширение кольца рибозы (например, для формирования 6- или 7-членного кольца, имеющего дополнительный атом углерода или гетероатом, например, такого как ангидрогексит, альтрит, маннит, циклогексанил, циклогексенил и морфолино, которое также имеет фосфорамидатный остов). Хотя большинство изменений аналогов сахара локализованы в 2’-положении, другие участки поддаются модификации, включая 4’-положение. В конкретных вариантах осуществления, нРНК содержит модификацию 4’-S, 4’-Se или 4’-C-аминометил-2’-O-Me.
[0165] В конкретных вариантах осуществления, деаза-нуклеотиды, например, 7-деаза-аденозин, можно включать в нРНК. В конкретных вариантах осуществления, O- и N-алкилированные нуклеотиды, например, N6-метил аденозин, , можно включать в нРНК. В конкретных вариантах осуществления, один или несколько, или все из нуклеотидов в нРНК представляют собой дезоксинуклеотиды.
Направляемые РНК нуклеазы
[0166] Направляемые РНК нуклеазы по настоящему изобретению включают, но без ограничения, природные нуклеазы CRISPR класса 2, такие как Cas9 и Cpf1, так же как другие нуклеазы, происходящие или полученные из них. В функциональных терминах, направляемые РНК нуклеазы определяют как такие нуклеазы, которые: (a) взаимодействуют с (например, образуют комплекс с) нРНК; и (b) вместе с нРНК, вступают в ассоциацию с, и необязательно, расщепляют или модифицируют, область-мишень ДНК, включающие (i) последовательность, комплементарную нацеливающему домену нРНК и, необязательно, (ii) дополнительную последовательность, обозначенную как «смежный с протоспейсером мотив», или «PAM», более подробно описанный ниже. Как проиллюстрировано в следующих примерах, направляемые РНК нуклеазы можно определять, в общих чертах, по специфичности PAM и активности расщепления, даже несмотря на то, что могут существовать различия между индивидуальными направляемыми РНК нуклеазами, разделяющими одинаковую специфичность PAM или активность расщепления. Специалисту в данной области понятно, что некоторые аспекты по настоящему описанию относятся к системам, способам и композициям, которые можно осуществлять с использованием любой пригодной направляемой РНК нуклеазы, имеющей конкретную специфичность PAM и/или активность расщепления. По этой причине, если не указано иное, термин направляемая РНК нуклеаза следует понимать в качестве общего термина, и он не ограничен каким-либо конкретным типом (например, Cas9 против Cpf1), видом (например, S. pyogenes против S. aureus) или вариантом (например, полноразмерный против усеченного или разделенного; PAM с природной специфичностью против PAM с модифицированной специфичностью и т.д.) направляемой РНК нуклеазы.
[0167] Последовательность PAM названа по родству последовательности с последовательностью «протоспейсера», комплементарной нацеливающим доменам нРНК (или «спейсерам»). Совместно с последовательностями протоспейсера, последовательности PAM определяют области или последовательности-мишени для специфических комбинаций направляемая РНК нуклеаза/нРНК.
[0168] Различные направляемые РНК нуклеазы могут требовать различного родства последовательности между PAM и протоспейсерами.
[0169] В дополнение к узнаванию специфических ориентаций последовательности PAM и протоспейсеров, направляемые РНК нуклеазы также могут узнавать специфические последовательности PAM. Cas9 S. aureus, например, узнает последовательность PAM NNGRRT или NNGRRV, где остатки N находятся непосредственно на 3’-области, узнаваемой нацеливающим доменом нРНК. Cas9 S. pyogenes узнает последовательности NGG PAM. И Cpf1 F. novicida узнает последовательность PAM TTN. Последовательности PAM идентифицированы для множества направляемых РНК нуклеаз, и способ идентификации новых последовательностей PAM описан в Shmakov et al., 2015, Molecular Cell 60, 385-397, November 5, 2015. Следует также отметить, что сконструированные направляемые РНК нуклеазы могут иметь специфичность PAM, отличающуюся от специфичности PAM эталонных молекул (например, в случае сконструированной направляемой РНК нуклеазы, эталонная молекула может представлять собой природный вариант, из которого происходит направляемая РНК нуклеаза, или природный вариант, имеющий наибольшую гомологию аминокислотной последовательности со сконструированной направляемой РНК нуклеазой).
[0170] В дополнение к их специфичности PAM, направляемые РНК нуклеазы можно характеризовать по их активности расщепления ДНК: природные направляемые РНК нуклеазы как правило, образуют DSB в нуклеиновых кислотах-мишенях, но получены сконструированные варианты, образующие только SSB (обсуждаемые выше) Ran & Hsu, et al., Cell 154(6), 1380-1389, September 12, 2013 (Ran), содержание которого приведено в настоящем описании в качестве ссылки), или вообще не осуществляющие разрезания.
Cas9
[0171] Кристаллические структуры определены для Cas9 S. pyogenes (Jinek 2014), и для Cas9 S. aureus в комплексе с мономолекулярной направляющей РНК и ДНК-мишенью (Nishimasu 2014; Anders 2014; и Nishimasu 2015).
[0172] Природный белок Cas9 содержит две части: часть узнавания (REC) и часть нуклеазы (NUC); каждая из которых содержит конкретные структурные и/или функциональные домены. Часть REC содержит богатый аргинином спиральный (BH) домен, и по меньшей мере один домен REC (например, домен REC1 и, необязательно, домен REC2). Часть REC не разделяет структурное сходство с другими известными белками, показывая, что она представляет собой уникальный функциональный домен. Без желания быть связанными с какой-либо теорией, анализы мутаций позволяют предполагать специфические функциональные роли для доменов BH и REC: домен BH, по-видимому, играет роль в узнавании нРНК:ДНК, в то время как домен REC считают взаимодействующим с дуплексом повтор:антиповтор нРНК и опосредующим формирование комплекса Cas9/нРНК.
[0173] Часть NUC содержит домен RuvC, домен HNH и взаимодействующий с PAM (PI) домен. Домен RuvC разделяет структурное сходство с членами суперсемейства ретровирусной интегразы и расщепляет некомплементарную (т.е., нижнюю) цепь нуклеиновой кислоты-мишени. Он может быть сформирован из двух или более разделенных мотивов RuvC (таких как RuvC I, RuvCII и RuvCIII в s. pyogenes и s. aureus). Домен HNH, тем не менее, является структурно сходным с мотивами эндонуклеазы HNN и расщепляет комплементарную (т.е., верхнюю) цепь нуклеиновой кислоты-мишени. Домен PI, как можно предполагать по его названию, вносит вклад в специфичность PAM.
[0174] В то время как определенные функции Cas9 связаны (но не обязательно полностью определены) специфическими доменами, указанными выше, эти и другие функции могут быть опосредованы или подвергаться влиянию других доменов Cas9, или множества доменов в любой части. Например, в Cas9 S. pyogenes, как описано в Nishimasu 2014, дуплекс повтор:антиповтор нРНК попадает в бороздку между частями REC и NUC, и нуклеотиды в дуплексе взаимодействуют с аминокислотами в доменах BH, PI и REC. Некоторые нуклеотиды в первой структуре стебель-петля также взаимодействуют с аминокислотами в множестве доменов (PI, BH и REC1), как и некоторые нуклеотиды во второй и третьей стебель-петлях (доменах RuvC и PI).
Cpf1
[0175] Кристаллическая структура Cpf1 вида Acidaminococcus в комплексе с crРНК и двухцепочечной (ds) ДНК-мишенью, включая последовательность PAM TTTN, разрешена Yamano et al. (Cell. 2016 May 5; 165(4): 949-962 (Yamano), содержание которого приведено в настоящем описании в качестве ссылки). Cpf1, подобно Cas9, имеет две части: часть REC (узнавания) и часть NUC (нуклеазы). Часть REC включает домены REC1 и REC2, лишенные сходства с любыми известными белковыми структурами. Часть NUC, в то же время, включает три домена RuvC (RuvC-I, -II и -III) и домен BH. Однако, в отличие от Cas9, часть REC Cpf1 лишена домена HNH, и включает другие домены, которые также лишены сходства с известными белковыми структурами: структурно уникальный домен PI, три клиновидных домена (WED) (WED-I, -II и -III) и домен нуклеазы (Nuc).
[0176] В то время как Cas9 и Cpf1 разделяют сходство в структуре и функции, следует понимать, что конкретные виды активности Cpf1 опосредованы структурными доменами, которые не являются аналогичными никаким доменам Cas9. Например, расщепление комплементарной цепи ДНК-мишени, по-видимому опосредовано доменом Nuc, который отличается по последовательности и пространственной структуре от домена HNH Cas9. Кроме того, ненацеливающая часть нРНК Cpf1 (ручка) принимает структуру псевдоузла, вместо структуры стебель-петля, сформированной дуплексом повтор:антиповтор в нРНК Cas9.
Модификации направляемых РНК нуклеаз
[0177] Направляемые РНК нуклеазы, описанные выше, имеют виды активности и свойства, которые можно использовать во множестве применений, но специалисту в данной области понятно, что направляемые РНК нуклеазы также можно модифицировать в конкретных случаях, для изменения активности расщепления, специфичности PAM, или других структурных или функциональных признаков.
[0178] Обращаясь сначала к модификациям, изменяющим активность расщепления, мутации, которые уменьшают или прекращают активность доменов внутри части NUC, описаны выше. Иллюстративные мутации, которые можно вводить в домены RuvC, в домен HNH Cas9 или домен Nuc Cpf1, описаны в Ran и Yamano, так же как в Cotta-Ramusino. Как правило, мутации, которые уменьшают или прекращают активность одного из двух доменов нуклеазы, приводят к получению направляемых РНК нуклеаз с активностью никазы, однако, следует отметить, что тип активности никазы меняется в зависимости от того, какой домен является инактивированным. В качестве одного примера, инактивация домена RuvC Cas9 приводит к получению никазы, которая расщепляет комплементарную или верхнюю цепь. С другой стороны, инактивация домена HNH Cas9 приводит к получению никазы, которая расщепляет нижнюю или некомплементарную цепь.
[0179] Модификации специфичности PAM относительно природных эталонных молекул Cas9 описаны в Kleinstiver et al. как для S. pyogenes (Kleinstiver et al., Nature. 2015 Jul 23;523(7561):481-5 (Kleinstiver I), так и для S. aureus (Kleinstiver et al., Nat Biotechnol. 2015 Dec; 33(12): 1293-1298 (Klienstiver II)). В Kleinstiver et al. описаны также модификации, улучшающие точность нацеливания Cas9 (Nature, 2016 January 28; 529, 490-495 (Kleinstiver III)). Содержание каждой из этих ссылок приведено в настоящем описании в качестве ссылки.
[0180] Направляемые РНК нуклеазы были разделены на две или более части, как описано в Zetsche et al. (Nat Biotechnol. 2015 Feb;33(2):139-42 (Zetsche II), содержание которого приведено в качестве ссылки) и в Fine et al. (Sci Rep. 2015 Jul 1;5:10777 (Fine), содержание которого приведено в качестве ссылки).
[0181] Направляемые РНК нуклеазы можно, в конкретных вариантах осуществления, оптимизировать по размеру или укорачивать, например, посредством одной или нескольких делеций, уменьшающих размер нуклеазы, в то же время, все еще сохраняя ассоциацию нРНК, узнавание мишени и PAM, и активность расщепления. В конкретных вариантах осуществления, направляемые РНК нуклеазы являются связанными, ковалентно или нековалентно, с другим полипептидом, нуклеотидом или другой структурой, необязательно, посредством линкера. Иллюстративные связанные нуклеазы и линкеры описаны в Guilinger et al., Nature Biotechnology 32, 577-582 (2014), содержание которого приведено в настоящем описании в качестве ссылки для всех целей.
[0182] Направляемые РНК нуклеазы также, необязательно, включают метку, такую как, но без ограничения, сигнал ядерной локализации для облегчения продвижения белка направляемой РНК нуклеазы в ядро. В конкретных вариантах осуществления, направляемая РНК нуклеаза может включать C- и/или N-концевые сигналы ядерной локализации. Последовательности для ядерной локализации известны в данной области и описаны в Maeder и в других источниках.
[0183] Приведенный выше список модификаций является иллюстративным по характеру, и специалисту в данной области понятно, в свете настоящего описания, что другие модификации могут являться возможными или желательными в конкретных применениях. Для краткости, таким образом, иллюстративные системы, способы и композиции по настоящему описанию представлены со ссылкой на конкретные направляемые РНК нуклеазы, однако, следует понимать, что используемые направляемые РНК нуклеазы можно модифицировать такими способами, которые не изменяют принципов их действия. Такие модификации включены в объем настоящего описанию.
Нуклеиновые кислоты, кодирующие направляемые РНК нуклеазы
[0184] Настоящее изобретение относится к нуклеиновым кислотам, кодирующим направляемые РНК нуклеазы, например, Cas9, Cpf1 или их функциональные фрагменты. Иллюстративные нуклеиновые кислоты, кодирующие направляемые РНК нуклеазы, описаны ранее (см., например, Cong 2013; Wang 2013; Mali 2013; Jinek 2012).
[0185] В некоторых случаях, нуклеиновая кислота, кодирующая направляемую РНК нуклеазу, может представлять собой синтетическую последовательность нуклеиновой кислоты. Например, синтетическая молекула нуклеиновой кислоты может являться химически модифицированной. В конкретных вариантах осуществления, мРНК, кодирующая направляемую РНК нуклеазу, может иметь одно или несколько (например, все) из следующих свойств: она может являться кэпированной; полиаденилированной; и замещенной 5-метилцитидином и/или псевдоуридином.
[0186] Синтетические последовательности нуклеиновой кислоты могут быть также подвергнуты оптимизации кодонного состава, например, по меньшей мере один нераспространенный кодон или менее распространенный кодон заменен на распространенный кодон. Например, синтетическая нуклеиновая кислота может направлять синтез оптимизированной матричной мРНК, например, оптимизированной для экспрессии в системе экспрессии млекопитающего, например, описанной в настоящем описании. Примеры подвергнутых оптимизации кодонного состава кодирующих Cas9 последовательностей представлены в Cotta-Ramusino.
[0187] Дополнительно или альтернативно, нуклеиновая кислота, кодирующая направляемую РНК нуклеазу, может содержать последовательность для ядерной локализации (NLS). Последовательности для ядерной локализации известны в данной области.
Функциональный анализ молекул-кандидатов
[0188] Рассматриваемые в качестве кандидатов направляемые РНК нуклеазы, нРНК и их комплексы, можно оценивать стандартными способами, известными в данной области. См., например, Cotta-Ramusino. Стабильность RNP комплексов можно оценивать посредством дифференциальной сканирующей флуориметрии, как описано ниже.
Дифференциальная сканирующая флуориметрия (DSF)
[0189] Термостабильность рибонуклеопротеиновых (RNP) комплексов, содержащих нРНК и направляемые РНК нуклеазы, можно измерять посредством DSF. Способом DSF измеряют термостабильность белка, которая может увеличиваться в благоприятных условиях, таких как добавление связывающей молекулы РНК, например, нРНК.
[0190] Анализ DSF можно проводить в соответствии с любым подходящим способом, и можно использовать в любом подходящем формате, включая, без ограничения (a) тестирование различных условий (например, различных стехиометрических соотношений нРНК: белок направляемая РНК нуклеаза, различных буферных растворов и т.д.) для идентификации оптимальных условий для формирования RNP; и (b) тестирование модификаций (например, химических модификаций, изменений последовательности и т.д.) направляемой РНК нуклеазы и/или нРНК для идентификации тех модификаций, которые улучшают формирование или стабильность RNP. Одним из результатов считывания в анализе DSF является сдвиг температуры плавления RNP комплекса; относительно высокий сдвиг позволяет предполагать, что RNP комплекс является более стабильным (и может, таким образом иметь более высокую активность или более благоприятную кинетику формирования, кинетику деградации или другую функциональную характеристику), относительно эталонного RNP комплекса, характеризующегося более низким сдвигом. Когда анализ DSF разрабатывают в качестве инструмента скрининга, можно указывать порог сдвига температуры плавления, так что на выходе получают один или несколько RNP, имеющих сдвиг температуры плавления, равный или превышающий порог. Например, порог может составлять 5-10°C (например, 5°, 6°, 7°, 8°, 9°, 10°) или более, и выходом может являться один или несколько RNP, характеризующиеся сдвигом температуры плавления, большим или равным порогу.
[0191] Два неограничивающих примера условий анализа DSF приведены ниже:
[0192] Для определения лучшего раствора для формирования комплексов RNP, фиксированную концентрацию (например, 2 мкМ) Cas9 в воде+10x SYPRO Orange® (Life Technologies кат. #S-6650) распределяют в 384-луночном планшете. Затем добавляют эквимолярное количество нРНК, разведенной в растворах с различными pH и солью. После инкубации при комнатной температуре в течение 10’ и короткого центрифугирования для удаления всех пузырей, термоциклер Bio-Rad CFX384™ Real-Time System C1000 Touch™ с программным обеспечением Bio-Rad CFX Manager используют для осуществления градиента от 20°C до 90°C с увеличением температуры на 1°C каждые 10 секунд.
[0193] Второй анализ состоит из смешивания различных концентраций нРНК с фиксированной концентрацией (например, 2 мкМ) Cas9 в оптимальном буфере из анализа 1 выше и инкубации (например, при RT в течение 10’) в 384-луночном планшете. Добавляют равный объем оптимального буфера+10x SYPRO Orange® (Life Technologies кат. #S-6650), и планшет герметично закрывают с использованием клейкой пленки Microseal® B (MSB-1001). После короткого центрифугирования для удаления всех пузырей, термоциклер Bio-Rad CFX384™ Real-Time System C1000 Touch™ с программным обеспечением Bio-Rad CFX Manager используют для осуществления градиента от 20°C до 90°C с увеличением температуры на 1°C каждые 10 секунд.
Способы редактирования генома
[0194] Системы редактирования генома, описанные выше, используют, в различных вариантах осуществления по настоящему описанию, для осуществления редактирования (т.е., для изменения) в областях-мишенях ДНК (например, ДНК TGFBR2) в клетке или полученной из клетки. Различные способы описаны в настоящем описании для осуществления конкретного редактирования, и эти способы, как правило, описаны применительно к желательному исходу репарации, количеству и расположению индивидуальных точек редактирования (например, SSB или DSB), и участкам-мишеням для таких точек редактирования.
[0195] Способы редактирования генома, включающие образование SSB или DSB, характеризуются исходами репарации, включая: (a) делецию всей или части области-мишени; (b) вставку или замещение во всей или части области-мишени; или (c) прерывание всей или части области-мишени. Эта группировка не предназначена для ограничения или связи с какой-либо конкретной теорией или моделью, и предложена единственно для экономного представления. Специалисту в данной области понятно, что перечисленные исходы не являются взаимоисключающими, и что некоторые случаи репарации могут приводить к другим исходам. Описание конкретных стратегии или способа редактирования не следует понимать как требующее конкретного исхода репарации, если не указано иное.
[0196] Замещение области-мишени, как правило, включает замещение всей или части существующей последовательности внутри области-мишени на гомологичную последовательность, например, посредством коррекции генов или конверсии генов, двух исходов репарации, опосредованных путями HDR. HDR стимулируют с использованием донорной матрицы, которая может являться одноцепочечной или двухцепочечной, как более подробно описано ниже. Одно- или двухцепочечные матрицы могут являться экзогенными, в этом случает они способствуют коррекции генов, или они могут являться эндогенными (например, гомологичная последовательность внутри генома клетки), чтобы способствовать конверсии генов. Экзогенные матрицы могут иметь асимметричные выступающие концы (т.е., часть матрицы, комплементарная участку DSB, может быть сдвинута в направлении 3’- или 5’-, вместо того, чтобы находится в центре донорной матрицы), например, как описано в Richardson et al. (Nature Biotechnology 34, 339-344 (2016), (Richardson), содержание которого приведено в качестве ссылки). В случаях, когда матрица является одноцепочечной, она может соответствовать либо комплементарной (верхней), либо некомплементарной (нижней) цепи области-мишени.
[0197] Конверсию генов и коррекцию генов облегчают, в некоторых случаях, посредством образования одного или нескольких ников в или около области-мишени, как описано в Ran и Cotta-Ramusino. В некоторых случаях, способ двойной никазы используют для образования двух сдвинутых SSB, которые, в свою очередь, образуют один DSB, имеющий выступающий конец (например, 5’-выступающий конец).
[0198] Прерывание и/или делецию всей или части последовательности-мишени можно осуществлять посредством множества исходов репарации. В качестве одного примера, последовательность можно делетировать посредством одновременного образования двух или более DSB, фланкирующих область-мишень, которая затем вырезается при репарации DSB, как описано в Maeder для мутации LCA10. В качестве другого примера, последовательность можно прерывать посредством делеции, полученной посредством образования двухцепочечного разрыва с одноцепочечными выступающими концами, с последующим экзонуклеолитическим процессингом выступающих концов перед репарацией.
[0199] Одна специфическая подгруппа прерываний последовательности-мишени опосредована образованием индела внутри последовательности-мишени, где исход репарации, как правило, опосредован путями NHEJ (включая Alt-NHEJ). NHEJ обозначают как путь репарации «пониженной точности» из-за его ассоциации с мутациями инделами. В некоторых случаях, однако, DSB подвергается репарации посредством NHEJ без изменения окружающей его последовательности (так называемая «совершенная» или «бесшовная» репарация); это, как правило требует совершенного лигирования двух концов DSB. Тем не менее, считают, что возникают инделы из-за ферментного процессинга свободных концов ДНК до их лигирования, что добавляет и/или удаляет нуклеотиды из любой или обеих цепей любого или обоих свободных концов.
[0200] Поскольку ферментный процессинг свободных концов DSB может иметь стохастический характер, мутации инделы имеют тенденцию к изменчивости, возникая согласно некоторому распределению, и могут быть подвержены влиянию множества факторов, включая специфический участок-мишень, использованный тип клетки, использованный способ редактирования генома и т.д. Даже в этом случае, является возможным делать ограниченные обобщения применительно к образованию инделов: делеции, образованные посредством репарации одиночного DSB, наиболее часто лежат в диапазоне 1-50 п.о., но могут достигать более чем 100-200 п.о. Вставки, образованные посредством репарации одиночного DSB, имеют тенденцию являться более короткими и часто включают короткие дупликации последовательности, непосредственно окружающей участок разрыва. Однако, является возможным получать большие вставки, и в этих случаях, вставленную последовательность часто приписывают другим областям генома или плазмидной ДНК, присутствующим в клетках.
[0201] Мутации инделы - и системы редактирования генома, имеющие конфигурацию для образования инделов - можно использовать для прерывания последовательностей-мишеней, например, когда получение конкретной конечной последовательности не требуется и/или когда мутация со сдвигом рамки считывания может являться переносимой. Их также можно использовать в условиях, когда конкретные последовательности являются предпочтительными, в той степени, в которой желательные последовательности имеют тенденцию предпочтительно возникать в результате репарации SSB или DSB в данном участке. Мутации инделы также являются полезным инструментом для оценки или скрининга активности конкретных систем редактирования генома и их компонентов. В этих и других условиях, инделы можно характеризовать по (a) их относительным и абсолютным частотам в геномах клеток, приведенных в контакт с системами редактирования генома и (b) распределению количественных различий относительно нередактированной последовательности, например, ±1, ±2, ±3 и т.д. В качестве одного примера, в условиях поиска лидеров, можно проводить скрининг множества нРНК для идентификации нРНК, наиболее эффективно управляющих разрезанию в участке-мишени, на основании считывания инделов в контролируемых условиях. Направляющие РНК, приводящие к получению инделов с пороговой или более высокой частотой, или приводящие к конкретному распределению инделов, можно отбирать для дальнейшего исследования и разработки. Частоту и распределение инделов также можно использовать в качестве считывания для оценки различных вариантов осуществления системы редактирования генома или составов и способов доставки, например, посредством сохранения нРНК постоянной и изменения других конкретных условий реакции или способов доставки.
Мультиплексные способы
[0202] В то время как иллюстративные способы, обсуждаемые выше, сфокусированы на исходах репарации, опосредованных одиночными DSB, системы редактирования генома по настоящему изобретению можно также использовать для получения двух или более DSB, либо в одном и том же локусе, либо в различных локусах. Способы редактирования, включающие образование множества DSB или SSB, описаны, например, в Cotta-Ramusino.
Дизайн донорной матрицы
[0203] Дизайн донорной матрицы подробно описан в литературе, например, в Cotta-Ramusino. Олигомерные донорные матрицы ДНК (олигодезоксинуклеотиды или ODN), которые могут являться одноцепочечными (ssODN) или двухцепочечными (dsODN), могут быть использованы для облегчения основанной на HDR репарации DSB, и являются особенно полезными для введения изменений в последовательность ДНК-мишень, вставки новой последовательности в последовательность-мишень или замены всей последовательности-мишени.
[0204] Независимо от того, являются ли они одноцепочечными или двухцепочечными, донорные матрицы, как правило, включают области, которые являются гомологичными областям ДНК внутри или поблизости (например, фланкирующими или прилегающими) последовательности-мишени, подлежащей расщеплению. Эти гомологичные области обозначены в настоящем описании как «плечи гомологии» и схематически проиллюстрированы ниже:
[5’-плечо гомологии]-[замещающая последовательность]-[3’-плечо гомологии].
[0205] Плечи гомологии могут иметь любую подходящую длину (включая 0 нуклеотидов, если используют только одно плечо гомологии), и 3’- и 5’-плечи гомологии могут иметь одинаковую длину или могут отличаться по длине. На выбор длины подходящих плеч гомологии может влиять множество факторов, например, намерение избегать гомологии или микрогомологии с конкретными последовательности, такими как повторы Alu или другие очень распространенные элементы. Например, 5’-плечо гомологии можно укорачивать для исключения элемента повтора последовательности. В других вариантах осуществления, 3’-плечо гомологии можно укорачивать, чтобы избегать элемента повтора последовательности. В некоторых вариантах осуществления, как 5’-, так и 3’-плечи гомологии можно укорачивать, чтобы избегать включения конкретных элементов повтора последовательности. Кроме того, некоторые виды дизайна плеч гомологии могут улучшать эффективность редактирования или увеличивать частоту желательного исхода репарации. Например, в Richardson et al. Nature Biotechnology 34, 339-344 (2016) (Richardson), содержание которого приведено в качестве ссылки, обнаружено, что относительная асимметрия 3’- и 5’-плеч гомологии одноцепочечных донорных матриц влияют на скорости и/или исходы репарации.
[0206] Замещающие последовательности в донорных матрицах описаны в других литературных источниках, включая Cotta-Ramusino et al. Замещающая последовательность может иметь любую подходящую длину (включая ноль нуклеотидов, когда желательным исходом репарации является делеция), и как правило, включает одну, две, три или более модификаций последовательности относительно природной последовательности в клетке, в которой редактирование является желательным. Одна из распространенных модификаций последовательности включает изменение природной последовательности для репарации мутации, связанной с заболеванием или состоянием, лечение которого является желательным. Другая распространенная модификация последовательности включает изменение одной или нескольких последовательностей, комплементарных или кодирующих последовательность PAM направляемой РНК нуклеазы или нацеливающего домена нРНК(нескольких нРНК), используемых для получения SSB или DSB, для уменьшения или прекращения повторного расщепления участка-мишени после вставки замещающей последовательности в участок-мишень.
[0207] Когда используют линейный ssODN, он может иметь конфигурацию для (i) гибридизации с цепью с введенными никами нуклеиновой кислоты-мишени, (ii) гибридизации с интактной цепью нуклеиновой кислоты-мишени, (iii) гибридизации с плюс-цепью нуклеиновой кислоты-мишени и/или (iv) гибридизации с минус-цепью нуклеиновой кислоты-мишени. ssODN может иметь любую подходящую длину, например, приблизительно, по меньшей мере, или не более 150-200 нуклеотидов (например, 150, 160, 170, 180, 190 или 200 нуклеотидов).
[0208] Следует отметить, что нуклеиновая кислота-матрица может также представлять собой вектор на основе нуклеиновой кислоты, такой как вирусный геном или кольцевая двухцепочечная ДНК, например, плазмида. Векторы на основе нуклеиновой кислоты, содержащие донорные матрицы, могут включать другие кодирующие или некодирующие элементы. Например, нуклеиновую кислоту-матрицу можно доставлять в качестве части вирусного генома (например, в геноме AAV или лентивируса), который включает определенные элементы геномного остова (например, инвертированные концевые повторы, в случае генома AAV) и необязательно, включает дополнительные последовательности, кодирующие нРНК и/или направляемую РНК нуклеазу. В конкретных вариантах осуществления, донорная матрица может являться соседней с или фланкированной участками-мишенями, узнаваемыми одной или несколькими нРНК, для облегчения образования свободных DSB на одном или обоих концах донорной матрицы, которые могут участвовать в репарации соответствующих SSB или DSB, образованных в клеточной ДНК с использованием тех же самых нРНК. Иллюстративные векторы на основе нуклеиновой кислоты, пригодные для использования в качестве донорных матриц, описаны в Cotta-Ramusino.
[0209] Какой формат не был бы использован, нуклеиновую кислоту-матрицу можно конструировать, чтобы избегать нежелательных последовательностей. В конкретных вариантах осуществления, одно или оба плеча гомологии можно укорачивать, чтобы избегать перекрывания с конкретными элементами повтора последовательности, например, повторы Alu, элементы LINE и т.д.
Клетки-мишени
[0210] Системы редактирования генома по настоящему изобретению можно использовать для манипуляции или изменения клетки, например, для редактирования или изменения нуклеиновой кислоты-мишени. Манипуляцию можно осуществлять, в различных вариантах осуществления, in vivo или ex vivo.
[0211] Множество типов клеток можно подвергать манипуляции или изменению в соответствии с вариантами осуществления настоящего изобретения, и в некоторых случаях, таких как применения in vivo, множество типов клеток подвергают изменению или манипуляции, например, посредством доставки систем редактирования генома по настоящему изобретению в множество типов клеток. В других случаях, однако, может являться желательным ограничение манипуляции или изменения конкретными типом или типами клеток. Например, может являться желательным, в некоторых случаях, редактирование клетки с ограниченным потенциалом дифференцировки или терминально дифференцированной клетки, такой как фоторецепторная клетка, в случае с Maeder, и ожидают, что эта модификация генотипа приводит к изменению фенотипа клетки. В других случаях, однако, может являться желательным редактирование менее дифференцированной, мультипотентой или плюрипотентной, стволовой клетки или клетки-предшественника. В качестве примера, клетка может представлять собой эмбриональную стволовую клетку, индуцированную плюрипотентную стволовую клетку (iPSC), гематопоэтическую стволовую клетку/клетку-предшественника (HSPC), или другой тип стволовой клетки или клетки-предшественника, подвергающуюся дифференцировке до типа клетки, важного для данного применения или показания. В конкретных вариантах осуществления, клетка представляет собой T-клетку.
[0212] Как следствие, клетка, подвергаемая изменению или манипуляции, представляет собой, в различных случаях, делящуюся клетку или неделящуюся клетку, в зависимости от типа(типов) клеток, подвергаемых нацеливанию, и/или желательного исхода редактирования.
[0213] Когда клетки подвергают манипуляции или изменению ex vivo, клетки можно использовать (например, вводить субъекту) немедленно, или их можно поддерживать или сохранять для более позднего использования. Специалистам в данной области понятно, что клетки можно поддерживать в культуре или сохранять (например, замороженными в жидком азоте) с использованием любого пригодного способа, известного в данной области.
Осуществление систем редактирования генома: доставка, составы и способы введения
[0214] Как обсуждают выше, системы редактирования генома по настоящему изобретению можно осуществлять любым подходящим способом, что означает, что компоненты таких систем, включая, без ограничения, направляемую РНК нуклеазу, нРНК и, необязательно, донорную нуклеиновую кислоту-матрицу, можно доставлять, составлять или вводить в любой подходящей форме или комбинации форм, что приводит к трансдукции, экспрессии или введению системы редактирования генома, и/или вызывает желательный исход репарации в клетке, в ткани или у субъекта. В таблицах 3 и 4 указано несколько неограничивающих примеров вариантов осуществления системы редактирования генома. Специалистам в данной области понятно, однако, что эти списки не являются исчерпывающими, и что другие варианты осуществления являются возможными. Применительно к таблице 3, в частности, в таблице перечислено несколько иллюстративных вариантов осуществления системы редактирования генома, содержащей одиночную нРНК и, необязательно, донорную матрицу. Однако, системы редактирования генома по настоящему изобретению могут включать множество нРНК, множество направляемых РНК нуклеаз и другие компоненты, такие как белки, и множество вариантов осуществления станут очевидными специалисту в данной области на основании принципов, проиллюстрированных в таблице. В таблице, [N/A] обозначает, что система редактирования генома не включает указанный компонент.
Таблица 6
[0215] В таблице 7 обобщены различные способы доставки компонентов систем редактирования генома, как описано в настоящем описании. Снова, список предназначен для иллюстрации, а не ограничения.
Таблица 7
Доставка систем редактирования генома на основе нуклеиновых кислот
[0216] Нуклеиновые кислоты, кодирующие различные элементы системы редактирования генома по настоящему изобретению, можно вводить субъектам или доставлять в клетки известными в данной области способами или как описано в настоящем описании. Например, ДНК, кодирующую направляемую РНК нуклеазу и/или кодирующую нРНК, так же как нуклеиновые кислоты донорной матрицы, можно доставлять, например, посредством векторов (например, вирусных или невирусный векторов), не основанных на векторах способов (например, с использованием голой ДНК или комплексов ДНК) или их комбинации
[0217] Нуклеиновые кислоты, кодирующие элементы системы редактирования генома, могут включать последовательности, кодирующие одну, две, три, четыре или более нРНК. Например, нуклеиновые кислоты могут кодировать как первую, так и вторую молекулу нРНК, например, где вторая нРНК имеет второй нацеливающий домен, комплементарный второй последовательности-мишени гена TGFBR2. Нуклеиновые кислоты, описанные в настоящем описании, могут дополнительно содержать нуклеотидную последовательность, кодирующую третью молекулу нРНК, имеющую третий нацеливающий домен, комплементарный третьей последовательности-мишени гена TGFBR2. Композиции нуклеиновых кислот, описанные в настоящем описании, могут дополнительно содержать нуклеотидную последовательность, кодирующую четвертую молекулу нРНК, описанную в настоящем описании, имеющую четвертый нацеливающий домен, комплементарный четвертой последовательности-мишени гена TGFBR2. В конкретных вариантах осуществления, вторая, третья и/или четвертая молекула нРНК содержит нацеливающий домен, содержащий нуклеотидную последовательность, выбранную из SEQ ID NO: 5036-5096.
[0218] Нуклеиновые кислоты, кодирующие системы редактирования генома или их компоненты, можно доставлять непосредственно в клетки в форме голой ДНК или РНК, например, посредством трансфекции или электропорации, или можно конъюгировать с молекулами (например, N-ацетилгалактозамином), стимулирующими поглощение клетками-мишенями (например, эритроцитами, HSC). Векторы на основе нуклеиновой кислоты, такие как векторы, обобщенные в таблице 4, также можно использовать.
[0219] Векторы на основе нуклеиновой кислоты могут содержать одну или несколько последовательностей, кодирующих компоненты системы редактирования генома, такие как направляемая РНК нуклеаза, нРНК и/или донорная матрица. Вектор может также содержать последовательность, кодирующую сигнальный пептид (например, для ядерной локализации, ядрышковой локализации или митохондриальной локализации), ассоциированную (например, вставленную или слитую) с последовательностью, кодирующей белок. В качестве одного примера, векторы на основе нуклеиновой кислоты может включать кодирующую Cas9 последовательность, включающую одну или несколько последовательностей для ядерной локализации (например, последовательность для ядерной локализации из SV40).
[0220] Вектор на основе нуклеиновой кислоты может также включать любое подходящее количество регулярных/контрольных элементов, например, промоторов, энхансеров, интронов, сигналов полиаденилирования, консенсусных последовательностей Козака или внутренних участков связывания рибосомы (IRES). Эти элементы хорошо известны в данной области и описаны в Cotta-Ramusino.
[0221] Векторы на основе нуклеиновой кислоты по настоящему изобретению включают рекомбинантные вирусные векторы. Иллюстративные вирусные векторы указаны в таблице 7, и дополнительные пригодные вирусные векторы и их использование и получение описаны в Cotta-Ramusino. В конкретных вариантах осуществления, вектор представляет собой вирусный вектор, например, аденоассоциированный вирусный (AAV) вектор или лентивирусный (LV) вектор. Другие вирусные векторы, известные в данной области, также можно использовать. Кроме того, вирусные частицы можно использовать для доставки компонентов системы редактирования генома в форме нуклеиновой кислоты и/или пептида. Например, «пустые» вирусные частицы можно собирать для содержания любой подходящей загрузки. Вирусные векторы и вирусные частицы можно также конструировать для включения нацеливающих лигандов для изменения специфичности к ткани-мишени.
[0222] В дополнение к вирусным векторам, невирусные векторы можно использовать для доставки нуклеиновых кислот, кодирующих системы редактирования генома по настоящему изобретению. Одной из важных категорий невирусных векторов на основе нуклеиновой кислоты являются наночастицы, которые могут являться органическими или неорганическими. Наночастицы хорошо известны в данной области и обобщены в Cotta-Ramusino. Любой подходящий дизайн наночастиц можно использовать для доставки компонентов системы редактирования генома или нуклеиновых кислот, кодирующих такие компоненты. Например, органические (например, липидные и/или полимерные) наночастицы могут являться пригодными для использования в качестве носителей для доставки в конкретных вариантах осуществления по настоящему изобретению. Иллюстративные липиды для использования в составах наночастиц, и/или для переноса генов показаны в таблице 8, и в таблице 9 перечислены иллюстративные полимеры для использования для переноса генов и/или составов наночастиц.
Таблица 8: Липиды, используемые для переноса генов
Таблица 9: Полимеры, используемые для переноса генов
[0223] Невирусные векторы, необязательно, включают модификации нацеливания для улучшения поглощения и/или избирательного нацеливания, применительно к конкретным типам клеток. Эти модификации нацеливания могут включать, например, специфические для клетки антигены, моноклональные антитела, одноцепочечные антитела, аптамеры, полимеры, сахара (например, N-ацетилгалактозамин (GalNAc)) и проникающие в клетку пептиды. В таких векторах также, необязательно, используют фузогенные и дестабилизирующие эндосомы пептиды/полимеры, подвергающиеся запускаемым кислотой конформационным изменениям (например, для ускорения высвобождения загрузки эндосом), и/или включают поддающийся расщеплению под воздействием стимулов полимер, например, для высвобождения в клеточном компартменте. Например, можно использовать катионные полимеры на основе дисульфида, расщепляемые в восстанавливающем клеточном окружении.
[0224] В конкретных вариантах осуществления, осуществляют доставку одной или нескольких молекул нуклеиновой кислоты (например, молекул ДНК), отличных от компонентов системы редактирования генома, например, компонента направляемой РНК нуклеазы и/или компонента нРНК, описанных в настоящем описании. В конкретных вариантах осуществления, молекулу нуклеиновой кислоты доставляют в то же самое время, что и один или несколько компонентов системы редактирования генома. В конкретных вариантах осуществления, молекулу нуклеиновой кислоты доставляют до или после доставки (например, через менее чем приблизительно 30 минут, 1 час, 2 часа, 3 часа, 6 часов, 9 часов, 12 часов, 1 сутки, 2 суток, 3 суток, 1 неделю, 2 недели или 4 недели) одного или нескольких из компонентов системы редактирования генома. В конкретных вариантах осуществления, молекулу нуклеиновой кислоты доставляют способами, отличными от способов доставки одного или нескольких компонентов системы редактирования генома, например, компонента направляемой РНК нуклеазы и/или компонента нРНК. Молекулу нуклеиновой кислоты можно доставлять любым из способов доставки, описанных в настоящем описании. Например, молекулу нуклеиновой кислоты можно доставлять посредством вирусного вектора, например, дефектного по интеграции лентивируса, и компонент молекулы направляемой РНК нуклеазы и/или компонент нРНК можно доставлять посредством электропорации, например, таким образом, чтобы можно было уменьшать токсичность, вызванную нуклеиновыми кислотами (например, ДНК). В конкретных вариантах осуществления, молекула нуклеиновой кислоты кодирует терапевтический белок, например, белок, описанный в настоящем описании. В конкретных вариантах осуществления, молекула нуклеиновой кислоты кодирует молекулу РНК, например, молекулу РНК, описанную в настоящем описании.
Доставка RNP и/или РНК, кодирующей компоненты системы редактирования генома
[0225] RNP (комплексы нРНК и направляемых РНК нуклеаз, т.е., рибонуклеопротеиновые комплексы) и/или РНК, кодирующие направляемые РНК нуклеазы и/или нРНК, можно доставлять в клетки или вводить субъектам известными в данной области способами, некоторые из которых описаны в Cotta-Ramusino. In vitro, РНК, кодирующую направляемую РНК нуклеазу и/или кодирующую нРНК, можно доставлять, например, посредством микроинъекции, электропорации, временных компрессии или сжатия клеток (см., например, Lee 2012). Опосредованную липидами трансфекцию, опосредованную пептидами доставку, опосредованную GalNAc или другим конъюгатом доставку, и их комбинации, также можно использовать для доставки in vitro и in vivo.
[0226] In vitro, доставка посредством электропорации включает смешивание клеток с РНК, кодирующей направляемые РНК нуклеазы и/или нРНК, в присутствии или в отсутствие молекул донорной нуклеиновой кислоты-матрицы, в картридже, камере или кювете, и приложение одного или нескольких электрических импульсов определенной длительности и амплитуды. Системы и способы для электропорации известны в данной области, и любой пригодный инструмент и/или способ электропорации можно использовать применительно к различным вариантам осуществления настоящего изобретения
[0227] В конкретных вариантах осуществления, RNP комплексы по настоящему описанию, включая, например, фармацевтические композиции RNP, можно использовать, чтобы: (1) улучшать пролиферацию T-клетки; (2) улучшать выживаемость T-клетки; и/или (3) улучшать функцию T-клетки. Например, но без ограничения, два или более RNP комплекса, содержащие различные нРНК, можно использовать одновременно или последовательно для изменения экспрессии гена TGFBR2 в клетке, например, T-клетке. Такие RNP комплексы могут содержать различные нРНК, нацеленные на различные последовательности в гене TGFBR2. RNP комплексы могут, в конкретных случаях, индуцировать событие расщепления, например, двухцепочечный или одноцепочечный разрыв. Например, RNP комплексы могут содержать ферментативно активные молекулы Cas9 (eaCas9), образующие двухцепочечные разрывы в нуклеиновой кислоте-мишени, или молекулы eaCas9, образующие одноцепочечные разрывы в нуклеиновой кислоте-мишени (например, молекулы никазы). В конкретных вариантах осуществления, способ RNP с двойной никазой можно использовать для образования двух одноцепочечных разрывов со смещением, которые, в свою очередь, образуют одиночный двухцепочечный разрыв, имеющий выступающий конец (например, 5’-выступающий конец).
Способ введения
[0228] Системы редактирования генома, или клетки, подвергнутые изменению или манипуляции с использованием таких систем, можно вводить субъектам посредством любого пригодного способа или пути, местного или системного. Системные способы введения включают пероральные и парентеральные способы. Парентеральные способы включают, в качестве примера, внутривенный способ, способ введения в костный мозг, внутриартериальный, внутримышечный, внутрикожный, подкожный, интраназальный и внутрибрюшинный способы. Компоненты, вводимые системно, можно модифицировать или составлять для нацеливания, например, на HSC, гематопоэтические стволовые клетки/клетки-предшественники, или предшественники эритроидных клеток или клетки-предшественники.
[0229] Местные способы введения включают, в качестве примера, инъекцию в костный мозг в губчатое вещество кости или инъекцию в бедренную кость в полость костного мозга, и инфузию в воротную вену. В конкретных вариантах осуществления, значительно меньшие количества компонентов (по сравнению с системными способами) могут оказывать эффект при местном введении (например, непосредственно в костный мозг), по сравнению с системным введением (например, внутривенно). Местные способы введения могут уменьшать или исключать встречаемость потенциально токсичных побочных эффектов, которые могут возникать, когда терапевтически эффективные количества компонента вводят системно.
[0230] Введение можно осуществлять в форме периодического болюса (например, внутривенно) или в форме непрерывной инфузии из внутреннего резервуара или из внешнего резервуара (например, из пакета для внутривенной инфузии или имплантируемого насоса). Компоненты можно вводить местно, например, посредством непрерывного высвобождения из устройства для доставки лекарственного средства с замедленным высвобождением.
[0231] Кроме того, компоненты можно составлять для обеспечения высвобождения в течение длительного периода времени. Система высвобождения может включать матрицу из биоразлагаемого материала или материала, высвобождающего включенные компоненты посредством диффузии. Компоненты могут быть гомогенно или гетерогенно распределены внутри системы высвобождения. Можно использовать множество систем высвобождения, однако, выбор подходящей системы может зависеть от скорости высвобождения, требуемой при конкретном применении. Можно использовать как неразлагаемые, так и разлагаемые системы высвобождения. Пригодные системы высвобождения включают полимеры и полимерные матрицы, неполимерные матрицы, или неорганические и органические наполнители и разбавители, такие как, но без ограничения, карбонат кальция и сахар (например, трегалозу). Системы высвобождения могут являться природными или синтетическими. Однако, синтетические системы высвобождения являются предпочтительными, поскольку, как правило, они являются более надежными, более воспроизводимыми и обеспечивают более определенные профили высвобождения. Материал для системы высвобождения можно выбирать таким образом, чтобы компоненты, имеющие различные молекулярные массы, высвобождались посредством диффузии через материал или деградации материала.
[0232] Репрезентативные синтетические, биоразлагаемые полимеры включают, например: полиамиды, такие как поли(аминокислоты) и поли(пептиды); полиэфиры, такие как поли(молочная кислота), поли(гликолевая кислота), сополимер(молочной-гликолевой кислоты) и поли(капролактон); поли(ангидриды); полиортоэфиры; поликарбонаты; и их химические производные (замены, добавления химических групп, например, алкила, алкилена, гидроксилирования, окисления и другие модификации, общепринятым образом осуществляемые специалистом в данной области), сополимеры и их смеси. Репрезентативные синтетические, неразлагаемые полимеры включают, например: полиэфиры такие как поли(этиленоксид), поли(этиленгликоль) и поли(тетраметиленоксид); виниловые полимеры-полиакрилаты и полиметакрилаты, такие как метил, этил, другой алкил, гидроксиэтилметакрилат, акриловые и метакриловые кислоты, и другие, такие как поли(виниловый спирт), поли(винилпирролидон) и поли(винилацетат); поли(уретаны); целлюлозу и ее производные, такие как алкил, гидроксиалкил, эфиры, сложные эфиры, нитроцеллюлоза и различные ацетаты целлюлозы; полисилоксаны; и любые их химические производные (замены, добавления химических групп, например, алкила, алкилена, гидроксилирования, окисления и другие модификации, общепринятым образом осуществляемые специалистом в данной области), сополимеры и их смеси.
[0233] Можно использовать также микросферу из сополимера(лактида-гликолида). Как правило, микросферы состоят из полимера молочной кислоты и гликолевой кислоты, структурированного для формирования полых сфер. Сферы могут иметь диаметр приблизительно 15-30 микрон, и могут быть нагружены компонентами, описанными в настоящем описании.
Мультимодальная или дифференциальная доставка компонентов
[0234] Специалисту в данной области понятно, в свете настоящего описания, что различные компоненты систем редактирования генома, описанные в настоящем описании, можно доставлять вместе или отдельно, и одновременно или не одновременно. Отдельная и/или асинхронная доставка компонентов системы редактирования генома может являться, в частности, желательной для обеспечения временного или пространственного контроля над функцией систем редактирования генома и для ограничения конкретных эффектов, вызванных их активностью.
[0235] Различные или дифференциальные способы, в рамках изобретения, относятся к способам доставки, придающим различные фармакодинамические или фармакокинетические свойства молекуле рассматриваемого компонента, например, молекуле направляемой РНК нуклеазы, нРНК, нуклеиновой кислоты-матрицы или нагрузки. Например, способы доставки могут приводить к различному распределению в тканях, различному времени полужизни или различному временному распределению, например, в выбранном компартменте, ткани или органе.
[0236] Некоторые способы доставки, например, доставка посредством вектора на основе нуклеиновой кислоты, персистирующего в клетке или в потомстве клетки, например, посредством автономной репликации или вставки в клеточную нуклеиновую кислоту, приводят к более персистентной экспрессии и присутствию компонента. Примеры включают доставку посредством вируса, например, AAV или лентивируса.
[0237] В качестве примера, компоненты системы редактирования генома, например, направляемую РНК нуклеазу и нРНК, можно доставлять способами, отличающимися, применительно к получаемым в результате времени полужизни или персистенции доставляемого компонента в организме, или в конкретном компартменте, ткани или органе. В конкретных вариантах осуществления, нРНК можно доставлять такими способами. Компонент молекулы направляемой РНК нуклеазы можно доставлять способом, приводящим к меньшей персистенции или меньшему воздействию на организм или конкретный компартмент или ткань, или орган.
[0238] В более общем смысле, в конкретных вариантах осуществления, первый способ доставки используют для доставки первого компонента, и второй способ доставки используют для доставки второго компонента. Первый способ доставки придает первое фармакодинамическое или фармакокинетическое свойство. Первое фармакодинамическое свойство может представлять собой, например, распределение, персистенцию или воздействие компонента, или нуклеиновой кислоты, кодирующей компонент, в организме, компартменте, ткани или органе. Второй способ доставки придает второе фармакодинамическое или фармакокинетическое свойство. Второе фармакодинамическое свойство может представлять собой, например, распределение, персистенцию или воздействие компонента, или нуклеиновой кислоты, кодирующей компонент, в организме, компартменте, ткани или органе.
[0239] В конкретных вариантах осуществления, первое фармакодинамическое или фармакокинетическое свойство, например, распределение, персистенция или воздействие, является более ограниченным, чем второе фармакодинамическое или фармакокинетическое свойство.
[0240] В конкретных вариантах осуществления, первый способ доставки выбирают для оптимизации, например, минимизации, фармакодинамического или фармакокинетического свойства, например, распределения, персистенции или воздействия.
[0241] В конкретных вариантах осуществления, второй способ доставки выбирают для оптимизации, например, максимизации, фармакодинамического или фармакокинетического свойства, например, распределения, персистенции или воздействия.
[0242] В конкретных вариантах осуществления, первый способ доставки включает использование относительно постоянного элемента, например, нуклеиновой кислоты, например, плазмидного или вирусного вектора, например, AAV или лентивируса. Поскольку такие векторы являются относительно постоянными, продукт, транскрибированный с них, может являться относительно постоянным.
[0243] В конкретных вариантах осуществления, второй способ доставки включает относительно временный элемент, например, РНК или белок.
[0244] В конкретных вариантах осуществления, первый компонент содержит нРНК, и способ доставки является относительно постоянным, например, нРНК транскрибируется с плазмидного или вирусного вектора, например, AAV или лентивируса. Транскрипция этих генов может иметь небольшие физиологические последствия, поскольку гены не кодируют белковый продукт, и нРНК являются неспособными действовать в изоляции. Второй компонент, молекулу направляемой РНК нуклеазы, доставляют временным способом, например, в форме мРНК или в форме белка, обеспечивая присутствие и активность полного комплекса молекула направляемой РНК нуклеазы/нРНК только на протяжении короткого периода времени.
[0245] Кроме того, компоненты можно доставлять в различной молекулярной форме или с использованием различных векторов для доставки, комплементирующих друг друга, для увеличения безопасности и тканеспецифичности.
[0246] Использование способов дифференциальной доставки может улучшать активность, безопасность и/или эффективность, например, можно уменьшать вероятность случайной неспецифической модификации. Доставка иммуногенных компонентов, например, молекул Cas9, менее постоянными способами может уменьшать иммуногенность из-за того, что пептиды из фермента Cas бактериального происхождения экспонируются на поверхности клетки посредством молекул MHC. Система доставки из двух частей может уменьшать эти недостатки.
[0247] Способы дифференциальной доставки можно использовать для доставки компонентов к различным, но перекрывающимся областям-мишеням. Формирование активного комплекса минимизируют вне перекрывания областей-мишеней. Таким образом, в конкретных вариантах осуществления, первый компонент, например, нРНК, доставляют первым способом доставки, что приводит к первому пространственному распределению, например, в ткани. Второй компонент, например, молекулу направляемой РНК нуклеазы, доставляют вторым способом доставки, что приводит к второму пространственному распределению, например, в ткани. В конкретных вариантах осуществления, первый способ включает первый элемент, выбранный из липосомы, наночастицы, например, полимерной наночастицы, и нуклеиновой кислоты, например, вирусного вектора. Второй способ включает второй элемент, выбранный из группы. В конкретных вариантах осуществления, первый способ доставки включает первый нацеливающий элемент, например, специфический для клетки рецептор или антитело, и второй способ доставки не включает этот элемент. В конкретных вариантах осуществления, второй способ доставки включает второй нацеливающий элемент, например, второй специфический для клетки рецептор или второе антитело.
[0248] Когда молекулу направляемой РНК нуклеазы доставляют в вирусном векторе для доставки, липосоме или полимерной наночастице, существует потенциал для доставки и терапевтической активности в множестве тканей, когда может являться желательным нацеливание только на единственную ткань. Система для доставки из двух частей может решать эту проблему и увеличивать тканеспецифичность. Если нРНК и молекула направляемой РНК нуклеазы упакованы в разделенные носители для доставки, с различным, но перекрывающимся, тропизмом к тканям, полностью функциональный комплекс может формироваться только в ткани, на которую нацелены оба вектора.
Генетически модифицированные клетки и способы получения клеток, экспрессирующих рекомбинантный рецептор
[0249] Настоящее изобретение относится к клеткам для адоптивной клеточной терапии, например, адоптивной иммунотерапии, и к способам продукции или получения клеток. Клетки включают иммуноциты, такие как T-клетки. Клетки, как правило, модифицируют посредством введения одной или нескольких генетически модифицированных нуклеиновых кислот или их продуктов. Среди таких продуктов присутствуют генетически модифицированные рецепторы антигенов, включая сконструированные T-клеточные рецепторы (TCR) и функциональные не относящиеся к TCR рецепторы антигенов, такие как химерные рецепторы антигенов (CAR), включая активирующие, стимулирующие и костимулирующие CAR, и их комбинации. В некоторых вариантах осуществления, клетки также вводят, либо одновременно, либо последовательно, с нуклеиновой кислотой, кодирующей генетически модифицированный рецептор антигена, со средством (например, RNP Cas9/нРНК), способным повреждать ген, кодирующий TGFBR2.
[0250] В некоторых вариантах осуществления, клетки (например, T-клетки) можно инкубировать или культивировать до, во время и/или после введения молекулы нуклеиновой кислоты, кодирующей рекомбинантный рецептор и/или средство (например, RNP Cas9/нРНК). В некоторых вариантах осуществления, клетки (например, T-клетки) можно инкубировать или культивировать до, во время или после введения молекулы нуклеиновой кислоты, кодирующей рекомбинантный рецептор, например, до, во время или после трансдукции клеток с использованием вирусного вектора (например, лентивирусного вектора), кодирующего рекомбинантный рецептор. В некоторых вариантах осуществления, клетки (например, T-клетки) можно инкубировать или культивировать до, во время или после введения средства (например, RNP Cas9/нРНК), например, до, во время или после приведения клеток в контакт с средством, или до, во время или после доставки средства в клетки, например, посредством электропорации. В некоторых вариантах осуществления, инкубацию можно осуществлять в контексте как введения молекулы нуклеиновой кислоты, кодирующей рекомбинантный рецептор, так и введения средства, например, RNP Cas9/нРНК. В некоторых вариантах осуществления, инкубацию можно осуществлять в присутствии цитокина, такого как IL-2, IL-7 или IL-15, или в присутствии стимулирующих или активирующих средств, индуцирующих пролиферацию или активацию клеток, таких как антитела против CD3/против CD28.
[0251] В некоторых вариантах осуществления, способ включает активацию или стимуляцию клеток с использованием стимулирующего или активирующего средства (например, антител против CD3/против CD28) до введения молекулы нуклеиновой кислоты, кодирующей рекомбинантный рецептор, и средства, например, RNP Cas9/нРНК. В некоторых вариантах осуществления, инкубацию можно также проводить в присутствии цитокина, такого как IL-2 (например, 1 ед./мл - 500 ед./мл, например, 10 ед./мл - 200 ед./мл, например, по меньшей мере или приблизительно 50 ед./мл или 100 ед./мл), IL-7 (например, 0,5 нг/мл - 50 нг/мл, например, 1 нг/мл - 20 нг/мл, например, по меньшей мере или приблизительно 5 нг/мл или 10 нг/мл) или IL-15 (например, 0,1 нг/мл - 50 нг/мл, например, 0,5 нг/мл - 25 нг/мл, например, по меньшей мере или приблизительно 1 нг/мл или 5 нг/мл). В некоторых вариантах осуществления, клетки инкубируют в течение 6 часов - 96 часов, например, 24-48 часов или 24-36 часов, до введения молекулы нуклеиновой кислоты, кодирующей рекомбинантный рецептор (например, посредством трансдукции).
Клетки и подготовка клеток для генетической модификации
[0252] Рекомбинантные рецепторы, связывающиеся со специфическим антигеном, и средства (например, RNP Cas9/нРНК) для генного редактирования гена TGFBR2, кодирующего полипептид TGFBR2, можно вводить в широкое множество клеток. В некоторых вариантах осуществления, рекомбинантный рецептор подвергают модификации, и/или ген-мишень TGFBR2 подвергают манипуляции ex vivo, и полученные генетически модифицированные клетки вводят субъекту. Источники клеток-мишеней для манипуляции ex vivo могут включать, например, кровь субъекта, пуповинную кровь субъекта или костный мозг субъекта. Источники клеток-мишеней для манипуляции ex vivo могут также включать, например, кровь, пуповинную кровь или костный мозг гетерологичного донора.
[0253] В некоторых вариантах осуществления, клетки, например, модифицированные клетки, представляют собой эукариотические клетки, такие как клетки млекопитающих, например, клетки человека. В некоторых вариантах осуществления, клетки происходят из крови, костного мозга, лимфы или лимфоидных органов, представляют собой клетки иммунной системы, такие как клетки врожденного или адаптивного иммунитета, например, миелоидные или лимфоидные клетки, включая лимфоциты, как правило, T-клетки и/или клетки NK. Другие иллюстративные клетки включают стволовые клетки, такие как мультипотентые и плюрипотентные стволовые клетки, включая индуцированные плюрипотентные стволовые клетки (iPSCs). В некоторых аспектах, клетки представляют собой клетки человека. Применительно к субъекту, подлежащему лечению, клетки могут являться аллогенными и/или аутологичными. Клетки, как правило, представляют собой первичные клетки, такие как клетки, выделенные непосредственно от субъекта и/или выделенные от субъекта и замороженные.
[0254] В некоторых вариантах осуществления, клетка-мишень представляет собой T-клетку, например, CD8+ T-клетку (например, наивную CD8+ T-клетку, центральную T-клетку памяти или эффекторную T-клетку памяти), CD4+ T-клетку, T-клетку естественного киллера (NKT-клетки), регуляторную T-клетку (Tрег), стволовую клетку для T-клетки памяти, лимфоидную клетку-предшественника, гематопоэтическую стволовую клетку, клетку естественного киллера (клетку NK) или дендритную клетку. В некоторых вариантах осуществления, клетки представляют собой моноциты или гранулоциты, например, миелоидные клетки, макрофаги, нейтрофилы, дендритные клетки, тучные клетки, эозинофилы и/или базофилы. В одном варианте осуществления, клетка-мишень представляет собой индуцированную плюрипотентную стволовую (iPS) клетку или клетку, происходящую из клетки iPS, например, клетки iPS, полученной от субъекта, подвергнутой манипуляции для изменения (например, индукции мутагенеза) или манипуляции для экспрессии одного или нескольких генов-мишеней, и подвергнутой дифференцировке в, например, T-клетку, например, CD8+ T-клетку (например, наивную CD8+ T-клетку, центральную T-клетку памяти или эффекторную T-клетку памяти), CD4+ T-клетку, стволовую клетку для T-клетки памяти, лимфоидную клетку-предшественника или гематопоэтическую стволовую клетку.
[0255] В некоторых вариантах осуществления, клетки включают одну или несколько подгрупп T-клеток или другие типы клеток, такие как полные популяции T-клеток, CD4+ клеток, CD8+ клеток и их субпопуляции, такие как субпопуляции, определяемые по функции, состоянию активации, зрелости, потенциалу дифференцировки, размножению, рециркуляции, локализации и/или способности к персистенции, антигенной специфичности, типу рецептора антигена, присутствию в конкретном органе или компартменте, маркеру или профилю секреции цитокинов, и/или степени дифференцировки.
[0256] Среди подтипов и субпопуляций T-клеток и/или CD4+ и/или CD8+ T-клеток, присутствуют наивные T-клетки (TN), эффекторные T-клетки (TЭФФ), T-клетки памяти и их подтипы, такие как стволовые T-клетки памяти (TSCM), центральные T-клетки памяти (TCM), эффекторные T-клетки памяти (TEM) или терминально дифференцированные эффекторные T-клетки памяти, инфильтрующие опухоль лимфоциты (TIL), незрелые T-клетки, зрелые T-клетки, T-клетки-помощники, цитотоксические T-клетки, ассоциированные со слизистыми оболочками инвариантные T-клетки (MAIT), природные и адаптивные регуляторные T-клетки (Tрег), T-клетки-помощники, такие как TH1-клетки, TH2-клетки, TH3-клетки, TH17-клетки, TH9-клетки, TH22-клетки, фолликулярные T-клетки-помощники, альфа/бета-T-клетки и дельта/гамма-T-клетки.
[0257] В некоторых вариантах осуществления, способы включают выделение клеток от субъекта, их подготовку, переработку, культивирование и/или модификацию. В некоторых вариантах осуществления, подготовка модифицированных клеток включает одну или несколько стадий культивирования и/или подготовки. Клетки для модификации, как описано, можно выделять из образца, такого как биологический образец, например, полученный или происходящий от субъекта. В некоторых вариантах осуществления, субъект, от которого выделена клетка, представляет собой субъекта, имеющего заболевание или состояние, или необходимость в клеточной терапии, или субъекта, которого планируют подвергать клеточной терапии. Субъект, в некоторых вариантах осуществления представляет собой человека, нуждающегося в конкретном терапевтическом вмешательстве, таком как адоптивная клеточная терапия, для которой клетки выделяют, перерабатывают и/или модифицируют.
[0258] Соответственно, клетки, в некоторых вариантах осуществления, представляют собой первичные клетки, например, первичные клетки человека. Образцы включают ткань, жидкость и другие образцы, отобранные непосредственно у субъекта, так же как образцы, полученные в результате одной или нескольких стадий переработки, таких как разделение, центрифугирование, генетическая модификация (например, трансдукция вирусным вектором), промывка и/или инкубация. Биологический образец может представлять собой образец, полученный непосредственно из биологического источника, или образец, подвергнутый переработке. Биологические образцы включают, но без ограничения, жидкости организма, такие как кровь, плазма, сыворотка, спинномозговая жидкость, синовиальная жидкость, моча и пот, образцы тканей и органов, включая происходящие из них переработанные образцы.
[0259] В некоторых аспектах, образец, из которого получают или выделяют клетки, представляет собой кровь или происходящий из крови образец, или получен из продукта афереза или лейкафереза. Иллюстративные образцы включают цельную кровь, мононуклеарные клетки периферической крови (PBMC), лейкоциты, костный мозг, тимус, биоптат ткани, опухоль, лейкоз, лимфому, лимфатический узел, ассоциированную с кишечником лимфоидную ткань, ассоциированную со слизистой оболочкой лимфоидную ткань, селезенку, другие лимфоидные ткани, печень, легкое, желудок, кишечник, ободочную кишку, почку, поджелудочную железу, молочную железу, кость, предстательную железу, шейку матки, яички, яичники, миндалину или другой орган, и/или происходящие из него клетки. Образцы включают, в контексте клеточной терапии, например, адоптивной клеточной терапии, образцы из аутологичных и аллогенных источников.
[0260] В некоторых вариантах осуществления, клетки происходят из линий клеток, например, линий T-клеток. Клетки, в некоторых вариантах осуществления, получены из ксеногенного источника, например, из мыши, крысы, нечеловекообразного примата или свиньи.
[0261] В некоторых вариантах осуществления, выделение клеток включает одну или несколько стадий получения и/или не основанного на аффинности разделения клеток. В некоторых примерах, клетки промывают, центрифугируют и/или инкубируют в присутствии одного или нескольких реагентов, например, для удаления нежелательных компонентов, обогащения желательных компонентов, лизиса или удаления клеток, чувствительных к конкретным реагентам. В некоторых примерах, клетки разделяют на основании одного или нескольких свойств, таких как плотность, адгерентные свойства, размер, чувствительность и/или устойчивость к конкретным компонентам.
[0262] В некоторых примерах, клетки из циркулирующей крови субъекта получены, например, посредством афереза или лейкафереза. Образцы, в некоторых аспектах, содержат лимфоциты, включая T-клетки, моноциты, гранулоциты, B-клетки, другие ядросодержащие лейкоциты, эритроциты и/или тромбоциты, и, в некоторых аспектах, содержат клетки, отличные от эритроцитов и тромбоцитов.
[0263] В некоторых вариантах осуществления, клетки крови, собранные от субъекта, промывают, например, для удаления фракции плазмы и для помещения клеток в подходящий буфер или среды для последующих стадий переработки. В некоторых вариантах осуществления, клетки промывают фосфатно-солевым буфером (PBS). В некоторых вариантах осуществления, в растворе для промывки отсутствует кальций и/или магний, и/или многие или все двухвалентные катионы. В некоторых аспектах, стадию промывки осуществляют с использованием полуавтоматизированной «проточной» центрифуги (например, устройства для переработки клеток Cobe 2991, Baxter), в соответствии с инструкциями производителя. В некоторых аспектах, стадию промывки осуществляют посредством проточной фильтрации вдоль потока (TFF), в соответствии с инструкциями производителя. В некоторых вариантах осуществления, клетки ресуспендируют во множестве биосовместимых буферов после промывки, например, в таком как не содержащий Ca++/Mg++ PBS. В конкретных вариантах осуществления, компоненты образца клеток крови удаляют, и клетки напрямую ресуспедируют в культуральных средах.
[0264] В некоторых вариантах осуществления, способы включают способы разделения клеток на основании плотности, такие как получение лейкоцитов из периферической крови посредством лизиса эритроцитов и центрифугирования в градиенте перколла или фиколла.
[0265] В некоторых вариантах осуществления, способы выделения включают разделение различных типов клеток на основании экспрессии или присутствия в клетке одной или нескольких специфических молекул, таких как поверхностные маркеры, например, поверхностные белки, внутриклеточные маркеры или нуклеиновая кислота. В некоторых вариантах осуществления, можно использовать любой известный способ разделения на основании таких маркеров. В некоторых вариантах осуществления, разделение представляет собой разделение на основании аффинности или иммуноаффинности. Например, выделение, в некоторых аспектах, включает разделение клеток и популяций клеток на основании экспрессии или уровня экспрессии в клетках одного или нескольких маркеров, как правило, поверхностных маркеров клеток, например, посредством инкубации с антителом или партнером по связыванию, которые специфически связываются с такими маркерами, за которыми, как правило, следуют стадии промывки и отделения клеток, связавшихся с антителом или партнером по связыванию, от клеток, не связавшихся с антителом или партнером по связыванию.
[0266] Такие стадии разделения могут быть основаны на положительном отборе, в котором клетки, связавшиеся с реагентами, сохраняют для дальнейшего использования, и/или на отрицательном отборе, в котором клетки, не связавшиеся с антителом или партнером по связыванию, сохраняют. В некоторых примерах, обе фракции сохраняют для дальнейшего использования. В некоторых аспектах, отрицательный отбор может являться особенно полезным, когда недоступно антитело, которое специфически идентифицирует тип клеток в гетерогенной популяции, так что разделение наилучшим образом проводят на основании маркеров, экспрессированных клетками, отличными от желательной популяции.
[0267] Разделение не обязательно должно приводить к 100% обогащению или удалению конкретной популяции клеток или клеток, экспрессирующих конкретный маркер. Например, положительный отбор или обогащение клеток конкретного типа, таких как клетки, экспрессирующие маркер, относятся к увеличению количества или процента таких клеток, но не должны приводить к полному отсутствию клеток, не экспрессирующих маркер. Подобным образом, отрицательный отбор, удаление или истощение клеток конкретного типа, таких как клетки, экспрессирующие маркер, относятся к уменьшению количества или процента таких клеток, но не должны приводить к полному удалению всех таких клеток.
[0268] В некоторых примерах, проводят множество циклов стадий разделения, где положительно или отрицательно отобранную фракцию с одной стадии подвергают другой стадии разделения, например, последующему положительному или отрицательному отбору. В некоторых примерах, на одной стадии разделения можно истощать клетки, экспрессирующие множество маркеров, одновременно, например, посредством инкубации клеток с множеством антител или партнеров по связыванию, каждое специфическое для маркера, на который нацеливаются для отрицательного отбора. Подобным образом, множество типов клеток можно одновременно положительно отбирать посредством инкубации клеток с множеством антител или партнеров по связыванию, экспрессированных на различных типах клеток.
[0269] В некоторых вариантах осуществления, одну или несколько из популяций T-клеток обогащают или истощают по клеткам, которые являются положительными (маркер+) или экспрессирующими высокие уровни (маркервысокий) одного или нескольких конкретных маркеров, таких как поверхностные маркеры, или которые являются отрицательными (маркер-) или экспрессирующими относительно низкие уровни (маркернизкий) одного или нескольких маркеров. Например, в некоторых аспектах, специфические субпопуляции T-клеток, такие как клетки, положительные для или экспрессирующие высокие уровни одного или нескольких поверхностных маркеров, например, CD28+, CD62L+, CCR7+, CD27+, CD127+, CD4+, CD8+, CD45RA+ и/или CD45RO+ T-клетки, выделяют посредством способов положительного или отрицательного отбора. В некоторых случаях, такие маркеры представляют собой маркеры, которые отсутствуют или экспрессируются на относительно низких уровнях на конкретных популяциях T-клеток (таких как клетки, не относящиеся к клеткам памяти), но присутствуют или экспрессируются на относительно высоких уровнях на других конкретных популяциях T-клеток (таких как клетки памяти). В одном варианте осуществления, клетки (такие как CD8+ клетки или T-клетки, например, CD3+ клетки) обогащают по (т.е., положительно отбирают по) клеткам, которые являются положительными или экспрессирующими высокие уровни на поверхности CD45RO, CCR7, CD28, CD27, CD44, CD127 и/или CD62L, и/или истощают по (например, отрицательно отбирают по) клеткам, которые являются положительными или экспрессирующими высокие уровни на поверхности CD45RA. В некоторых вариантах осуществления, клетки обогащают или истощают по клеткам, положительным или экспрессирующим высокие уровни на поверхности CD122, CD95, CD25, CD27 и/или IL7-Rα (CD127). В некоторых примерах, CD8+ T-клетки обогащают по клеткам, положительным по CD45RO (или отрицательным по CD45RA) и по CD62L.
[0270] Например, CD3+, CD28+ T-клетки можно положительно отбирать с использованием конъюгированных с CD3/CD28 магнитных бусин (например, DYNABEADS® M-450 CD3/CD28 T Cell Expander).
[0271] В некоторых вариантах осуществления, T-клетки отделяют от образца мононуклеарных клеток периферической крови (PBMC) посредством отрицательного отбора по маркерам, экспрессированным на клетках, не относящихся к T-клеткам, таких как B-клетки, моноциты или другие лейкоциты, например, CD14. В некоторых аспектах, стадию отбора CD4+ или CD8+ используют для разделения CD4+ T-клеток-помощников и CD8+ цитотоксических T-клеток. Такие популяции CD4+ и CD8+ можно далее сортировать на субпопуляции посредством положительного или отрицательного отбора по маркерам, экспрессированным или экспрессированным в относительно более высокой степени на одной или нескольких субпопуляциях наивных T-клеток, T-клеток памяти и/или эффекторных T-клеток.
[0272] В некоторых вариантах осуществления, CD8+ клетки дополнительно обогащают или истощают по наивным клеткам, центральным клеткам памяти, эффекторным клеткам памяти и/или центральным стволовым клеткам памяти, например, посредством положительного или отрицательного отбора на основании поверхностных антигенов, ассоциированных с соответствующей субпопуляцией. В некоторых вариантах осуществления, обогащение по центральным T-клеткам памяти (TCM) проводят для увеличения эффективности, например, для улучшения длительной выживаемости, размножения и/или приживления после введения, которые, в некоторых аспектах, являются особенно сильными в таких субпопуляциях. (См. Terakura et al. (2012) Blood.1:72-82; Wang et al. (2012) J Immunother. 35(9):689-701.) В некоторых вариантах осуществления, комбинация обогащенных TCM CD8+ T-клеток и CD4+ T-клеток дополнительно улучшает эффективность.
[0273] В некоторых вариантах осуществления, T-клетки памяти присутствуют в обеих CD62L+ и CD62L- подгруппах CD8+ лимфоцитов периферической крови. PBMC можно обогащать или истощать по CD62L-CD8+ и/или CD62L+CD8+ фракциям, например, с использованием антител против CD8 и против CD62L.
[0274] В некоторых вариантах осуществления, обогащение по центральным T-клеткам памяти (TCM) основано на положительной или высокой поверхностной экспрессии CD45RO, CD62L, CCR7, CD28, CD3, и/или CD 127; в некоторых аспектах, оно основано на отрицательном отборе клеток, экспрессирующих или экспрессирующих на высоком уровне CD45RA и/или гранзим B. В некоторых аспектах, выделение CD8+ популяции, обогащенной по клеткам TCM, проводят посредством истощения клеток, экспрессирующих CD4, CD14, CD45RA, и положительного отбора или обогащения клеток, экспрессирующих CD62L. В одном аспекте, обогащение по центральным T-клеткам памяти (TCM) проводят, начиная с отрицательной фракции клеток, отобранной на основании экспрессии CD4, которую подвергают отрицательному отбору на основании экспрессии CD14 и CD45RA, и положительному отбору на основании CD62L. Такой отбор, в некоторых аспектах, проводят одновременно, и в других аспектах проводят последовательно, в любом порядке. В некоторых аспектах, такую же стадию отбора на основании экспрессии CD4, какую используют для получения популяции или субпопуляции CD8+ клеток, используют также для получения популяции или субпопуляции CD4+ клеток, таким образом, что как положительную, так и отрицательную фракции после разделения на основании CD4 сохраняют и используют в последующих стадиях способов, необязательно, после одной или нескольких дополнительных стадий положительного или отрицательного отбора.
[0275] В конкретном примере, образец PBMC или образец других белых кровяных клеток подвергают отбору CD4+ клеток, при котором как отрицательную, так и положительную фракции сохраняют. Отрицательную фракцию затем подвергают отрицательному отбору на основании экспрессии CD14 и CD45RA или CD19, и положительному отбору на основании маркера, характерного для центральных T-клеток памяти, такого как CD62L или CCR7, где положительный и отрицательный отбор проводят в любом порядке.
[0276] CD4+ T-клетки-помощники сортируют на наивные клетки, центральные клетки памяти и эффекторные клетки посредством идентификации популяций клеток, имеющих антигены клеточной поверхности. CD4+ лимфоциты можно получать посредством стандартных способов. В некоторых вариантах осуществления, наивные CD4+ T-лимфоциты представляют собой CD45RO-, CD45RA+, CD62L+, CD4+ T-клетки. В некоторых вариантах осуществления, центральные CD4+ клетки памяти представляют собой CD62L+ и CD45RO+. В некоторых вариантах осуществления, эффекторные CD4+ клетки представляют собой CD62L- и CD45RO.
[0277] В одном примере, для обогащения CD4+ клеток посредством отрицательного отбора, коктейль моноклональных антител, как правило, включает антитела против CD14, CD20, CD11b, CD16, HLA-DR и CD8. В некоторых вариантах осуществления, антитело или партнер по связыванию связаны с твердой подложкой или матрицей, такой как магнитная бусина или парамагнитная бусина, для обеспечения разделения клеток для положительного и/или отрицательного отбора. Например, в некоторых вариантах осуществления, клетки и популяции клеток отделяют или выделяют с использованием иммуномагнитных (или аффинномагнитных) способов разделения (обзор которых приведен в Methods in Molecular Medicine, vol. 58: Metastasis Research Protocols, Vol. 2: Cell Behavior In vitro and In vivo, p 17-25 Edited by: S. A. Brooks and U. Schumacher © Humana Press Inc., Totowa, NJ).
[0278] В некоторых вариантах осуществления, клетки инкубируют и/или культивируют перед или в сочетании с генетической модификацией. Стадии инкубации могут включать культивирование, культивацию, стимуляцию, активацию и/или размножение. В некоторых вариантах осуществления, композиции или клетки инкубируют в присутствии стимулирующих условий или стимулирующего средства. Такие условия включают условия, разработанные для индукции пролиферации, размножения, активации и/или выживаемости клеток в популяции, для имитации воздействия антигена и/или для примирования клеток для генетической модификации, например, для введения рекомбинантного рецептора антигена.
[0279] Условия могут включать одно или несколько из конкретных сред, температуры, содержания кислорода, содержания диоксида углерода, времени, средств, например, питательных веществ, аминокислот, антибиотиков, ионов и/или стимулирующих факторов, таких как цитокины, хемокины, антигены, партнеры по связыванию, слитые белки, рекомбинантные растворимые рецепторы, и любые другие средства, разработанные для активации клеток.
[0280] В некоторых вариантах осуществления, стимулирующие условия или средства включают одно или несколько средств, например, лиганд, способный активировать внутриклеточный передающий сигналы домен комплекса TCR. В некоторых аспектах, средство запускает или инициирует внутриклеточный каскад передачи сигналов TCR/CD3 в T-клетке. Такие средства могут включать антитела, такие как антитела, специфические для компонента TCR и/или костимулирующего рецептора, например, антитело против CD3, антитело против CD28, например, связанное с твердой подложкой, такой как бусина, и/или один или несколько цитокинов. Необязательно, способ размножения может дополнительно включать стадию добавления антитела против CD3 и/или антитела против CD28 в культуральную среду (например, в концентрации по меньшей мере приблизительно 0,5 нг/мл). В некоторых вариантах осуществления, стимулирующие средства включают IL-2 и/или IL-15, например, концентрацию IL-2 по меньшей мере приблизительно 10 единиц/мл.
[0281] В некоторых аспектах, инкубацию проводят в соответствии с такими способами, как описано в Патенте США No. 6040177 от Riddell et al., Klebanoff et al. (2012) J Immunother. 35(9): 651-660, Terakura et al. (2012) Blood.1:72-82, и/или Wang et al. (2012) J Immunother. 35(9):689-701.
[0282] В некоторых вариантах осуществления, T-клетки размножают посредством добавления в композицию для начала культивирования фидерных клеток, таких как не делящиеся PBMC (например, таким образом, что полученная популяция клеток содержит по меньшей мере приблизительно 5, 10, 20 или 40, или более фидерных клеток PBMC для каждого T-лимфоцита в исходной популяции, подлежащей размножению), и инкубации культуры (например, в течение времени, достаточного для размножения этих количеств T-клеток). В некоторых аспектах, не делящиеся фидерные клетки могут содержать облученные гамма-излучением фидерные клетки PBMC. В некоторых вариантах осуществления, PBMC облучают с использованием гамма-излучения в диапазоне от приблизительно 3000 до 3600 рад для предотвращения деления клеток. В некоторых аспектах, фидерные клетки добавляют в культуральную среду перед добавлением популяций T-клеток.
[0283] В некоторых вариантах осуществления, стимулирующие условия включают температуру, пригодную для роста T-лимфоцитов человека, например, по меньшей мере приблизительно при 25 градусов Цельсия, как правило, по меньшей мере приблизительно при 30 градусов, и, как правило, при или приблизительно при 37 градусов Цельсия. Необязательно, инкубация может дополнительно включать добавление не делящихся трансформированных EBV лимфобластоидных клеток (LCL) в качестве фидерных клеток. LCL можно облучать с использованием гамма-излучения в диапазоне от приблизительно 6000 до 10000 рад. Фидерные клетки LCL, в некоторых аспектах, предоставляют в любом подходящем количестве, например, в соотношении фидерных клеток LCL к исходным T-лимфоцитам по меньшей мере приблизительно 10:1.
[0284] В некоторых вариантах осуществления, способы получения включают стадии замораживания, например, криоконсервации, клеток, либо до, либо после выделения, инкубации и/или модификации. В некоторых вариантах осуществления, на стадии замораживания и последующего размораживания удаляют гранулоциты и, до некоторой степени, моноциты в популяции клеток. В некоторых вариантах осуществления, клетки суспендируют в растворе для замораживания, например, после стадии промывки для удаления плазмы и тромбоцитов. В некоторых аспектах, можно использовать любой из множества известных растворов и параметров для замораживания. Один пример включает использование PBS, содержащего 20% DMSO и 8% человеческого сывороточного альбумина (HSA), или других пригодных сред для замораживания клеток. Затем их разводят средой 1:1, таким образом, чтобы конечная концентрация DMSO и HSA составляли 10% и 4%, соответственно. Затем клетки, как правило, замораживают до -80° C со скоростью 1° в минуту и сохраняют в паровой фазе в сосуде для хранения с жидким азотом.
[0285] В некоторых вариантах осуществления, способы включают повторное введение модифицированных клеток тому же самому пациенту, до или после криоконсервации.
Рекомбинантные рецепторы
[0286] В некоторых вариантах осуществления, клетки содержат одну или несколько нуклеиновых кислот, кодирующих рекомбинантный рецептор, введенные посредством генетической модификации, и генетически модифицированные продукты таких нуклеиновых кислот. В некоторых вариантах осуществления, клетки могут быть продуцированы или получены посредством введения в клетку (например, посредством трансдукции вирусным вектором, таким как ретровирусный или лентивирусный вектор) молекулы нуклеиновой кислоты, кодирующей рекомбинантный рецептор. В некоторых вариантах осуществления, нуклеиновые кислоты являются гетерологичными, т.е., в норме не присутствующими в клетке или образце, полученном из клетки, такими как полученные из другого организма или клетки, которые например, обычно не обнаруживают в клетке, подвергаемой модификации, и/или в организме, из которого происходит такая клетка. В некоторых вариантах осуществления, нуклеиновые кислоты являются неприродными, такими как нуклеиновая кислота, не обнаруженная в природе, включая нуклеиновую кислоту, содержащую химерные комбинации нуклеиновых кислот, кодирующих различные домены из множества различных типов клеток.
[0287] В некоторых вариантах осуществления, клетку-мишень изменяют для связывания с одним или несколькими антигенами-мишенями, такими как один или несколько антигенов опухолей. В некоторых вариантах осуществления, антиген-мишень выбран из ROR1, антигена созревания B-клеток (BCMA), карбоангидразы 9 (CAIX), tEGFR, Her2/neu (рецепторной тирозинкиназы erbB2), L1-CAM, CD19, CD20, CD22, мезотелина, CEA и поверхностного антигена вируса гепатита B, антифолатного рецептора, CD23, CD24, CD30, CD33, CD38, CD44, EGFR, эпителиального гликопротеина 2 (EPG-2), эпителиального гликопротеина 40 (EPG-40), EPHa2, erb-B2, erb-B3, erb-B4, димеров erbB, EGFR vIII, связывающего фолат белка (FBP), FCRL5, FCRH5, фетального рецептора ацетилхолина, GD2, GD3, HMW-MAA, IL-22R-альфа, IL-13R-альфа2, рецептора, содержащего домен вставки киназы (kdr), легкой цепи каппа, Lewis Y, молекулы клеточной адгезии L1, (L1-CAM), ассоциированного с меланомой антигена (MAGE)-A1, MAGE-A3, MAGE-A6, предпочтительно экспрессируемого антигена меланомы (PRAME), сурвивина, TAG72, B7-H6, рецептора альфа 2 IL-13 (IL-13Ra2), CA9, GD3, HMW-MAA, CD171, G250/CAIX, HLA-AI MAGE Al, HLA-A2 NY-ESO-1, PSCA, рецептора-a фолата, CD44v6, CD44v7/8, интегрина avb6, 8H9, NCAM, рецепторов VEGF, 5T4, фетального AchR, лигандов NKG2D, CD44v6, двойного антигена, раково-тестикулярного антигена, мезотелина, мышиного CMV, муцина 1 (MUC1), MUC16, PSCA, NKG2D, NY-ESO-1, MART-1, gp100, онкофетального антигена, ROR1, TAG72, VEGF-R2, карциноэмбрионального антигена (CEA), Her2/neu, рецептора эстрогена, рецептора прогестерона, эфрина B2, CD123, c-Met, GD-2, O-ацетилированного GD2 (OGD2), CE7, антигена опухоли Вильмса 1 (WT-1), циклина, циклина A2, CCL-1, CD138, специфического для патогена антигена и антигена, ассоциированного с универсальной меткой. В некоторых вариантах осуществления, клетку-мишень изменяют для связывания с одним или несколькими из следующих антигенов опухолей, например, посредством TCR или CAR. Антигены опухолей могут включать, но без ограничения, AD034, AKT1, BRAP, CAGE, CDX2, CLP, CT-7, CT8/HOM-TES-85, cTAGE-1, фибулин-1, HAGE, HCA587/MAGE-C2, hCAP-G, HCE661, HER2/neu, HLA-Cw, HOM-HD-21/галектин9, HOM-MEEL-40/SSX2, HOM-RCC-3.1.3/CAXII, HOXA7, HOXB6, Hu, HUB1, KM-HN-3, KM-KN-1, KOC1, KOC2, KOC3, KOC3, LAGE-1, MAGE-1, MAGE-4a, MPP11, MSLN, NNP-1, NY-BR-1, NY-BR-62, NY-BR-85, NY-CO-37, NY-CO-38, NY-ESO-1, NY-ESO-5, NY-LU-12, NY-REN-10, NY-REN-19/LKB/STK11, NY-REN-21, NY-REN-26/BCR, NY-REN-3/NY-CO-38, NY-REN-33/SNC6, NY-REN-43, NY-REN-65, NY-REN-9, NY-SAR-35, OGFr, PLU-1, Rab38, RBPJкаппа, RHAMM, SCP1, SCP-1, SSX3, SSX4, SSX5, TOP2A, TOP2B или тирозиназу.
Рецепторы антигенов:
Химерные рецепторы антигенов (CAR)
[0288] Клетки, как правило, экспрессируют рекомбинантные рецепторы, такие как рецепторы антигенов, включая функциональные не относящиеся к TCR рецепторы антигенов, например, химерные рецепторы антигенов (CAR) и другие антигенсвязывающие рецепторы, такие как трансгенные T-клеточные рецепторы (TCR). Также среди рецепторов присутствуют другие химерные рецепторы.
[0289] Иллюстративные рецепторы антигенов, включая CAR, и способы конструирования и введения таких рецепторов в клетки, включают способы, описанные, например, в публикациях международных патентных заявок номер WO200014257, WO2013126726, WO2012/129514, WO2014031687, WO2013/166321, WO2013/071154, WO2013/123061 в публикациях Патентных заявок США номер US2002131960, US2013287748, US20130149337, в Патентах США No.: 6451995, 7446190, 8252592, 8339645, 8398282, 7446179, 6410319, 7070995, 7265209, 7354762, 7446191, 8324353 и 8479118, и в Европейской патентной заявке номер EP2537416, и/или способы, описанные в Sadelain et al., Cancer Discov. 2013 April; 3(4): 388-398; Davila et al. (2013) PLoS ONE 8(4): e61338; Turtle et al., Curr. Opin. Immunol., 2012 October; 24(5): 633-39; Wu et al., Cancer, 2012 March 18(2): 160-75. В некоторых аспектах, рецепторы антигенов включают CAR, как описано в Патенте США No.: 7446190, и рецепторы, описанные в Публикации международной патентной заявки No.: WO/2014055668 A1. Примеры CAR включают CAR, как описано в любой из вышеупомянутых публикаций, таких как WO2014031687, US 8339645, US 7446179, US 2013/0149337, Патент США No.: 7446190, Патент США No.: 8389282, Kochenderfer et al., 2013, Nature Reviews Clinical Oncology, 10, 267-276 (2013); Wang et al. (2012) J. Immunother. 35(9): 689-701; и Brentjens et al., Sci Transl Med. 2013 5(177). См. также WO2014031687, US 8339645, US 7446179, US 2013/0149337, Патент США No.: 7446190 и Патент США No.: 8389282. Химерные рецепторы, такие как CAR, как правило, включают внеклеточный антигенсвязывающий домен, такой как часть молекулы антитела, как правило, вариабельную область тяжелой (VH) цепи и/или вариабельную область легкой (VL) цепи антитела, например, фрагмент scFv антитела.
[0290] В некоторых вариантах осуществления, антиген, на который нацелен рецептор, представляет собой полипептид. В некоторых вариантах осуществления, он представляет собой углевод или другую молекулу. В некоторых вариантах осуществления, антиген является избирательно экспрессированным или сверхэкспрессированным на клетках, пораженных заболеванием или состоянием, например, клетках опухоли или патогенных клетках, по сравнению с нормальными или не являющимися объектом нацеливания клетками или тканями. В других вариантах осуществления, антиген является экспрессированным на нормальных клетках и/или является экспрессированным на модифицированных клетках.
[0291] Антигены, на которые могут быть нацелены рецепторы, включают, но без ограничения, интегрин αvβ6 (интегрин avb6), антиген созревания B-клеток (BCMA), B7-H6, карбоангидразу 9 (CA9, также известный как CAIX или G250), раково-тестикулярный антиген, раково-тестикулярный антиген 1B (CTAG, также известный как NY-ESO-1 и LAGE-2), карциноэмбриональный антиген (CEA), циклин, циклин A2, лиганд 1 хемокинов с мотивом C-C (CCL-1), CD19, CD20, CD22, CD23, CD24, CD30, CD33, CD38, CD44, CD44v6, CD44v7/8, CD123, CD138, CD171, белок эпидермальный фактор роста (EGFR), укороченный белок эпидермальный фактор роста (tEGFR), рецептор эпидермального фактора роста с мутацией типа III (EGFR vIII), эпителиальный гликопротеин 2 (EPG-2), эпителиальный гликопротеин 40 (EPG-40), эфрин B2, рецептор эфрина A2 (EPHa2), рецептор эстрогена, подобный рецептору Fc белок 5 (FCRL5; также известный как гомолог 5 рецептора Fc или FCRH5), фетальный рецептор ацетилхолина (фетальный AchR), связывающий фолат белок (FBP), рецептор-альфа фолата, фетальный рецептор ацетилхолина, ганглиозид GD2, O-ацетилированный GD2 (OGD2), ганглиозид GD3, гликопротеин 100 (gp100), Her2/neu (рецепторную тирозинкиназу erbB2), Her3 (erb-B3), Her4 (erb-B4), димеры erbB, ассоциированный с меланомой высокомолекулярный антиген человека (HMW-MAA), поверхностный антиген вируса гепатита B, человеческий лейкоцитарный антиген A1 (HLA-AI), человеческий лейкоцитарный антиген A2 (HLA-A2), рецептор альфа IL-22 (IL-22Ra), рецептор альфа 2 IL-13 (IL-13Ra2), рецептор, содержащий домен вставки киназы (kdr), легкую цепь каппа, молекулу клеточной адгезии L1 (L1CAM), эпитоп CE7 из L1-CAM, член A семейства 8, содержащего богатые лейцином повторы (LRRC8A), Lewis Y, ассоциированный с меланомой антиген (MAGE)-A1, MAGE-A3, MAGE-A6, мезотелин, c-Met, мышиный цитомегаловирус (CMV), муцин 1 (MUC1), MUC16, лиганды члена D группы 2 естественных киллеров (NKG2D), мелан A (MART-1), молекулу адгезии нервных клеток (NCAM), онкофетальный антиген, предпочтительно экспрессируемый антиген меланомы (PRAME), рецептор прогестерона, простатспецифический антиген, антиген стволовых клеток предстательной железы (PSCA), простатспецифический мембранный антиген (PSMA), подобный рецепторной тирозинкиназе орфанный рецептор 1 (ROR1), сурвивин, гликопротеин трофобластных клеток (TPBG, также известный как 5T4), опухолеассоциированный гликопротеин 72 (TAG72), рецептор фактора роста эндотелия сосудов (VEGFR), рецептор 2 фактора роста эндотелия сосудов (VEGFR2), антиген опухоли Вильмса 1 (WT-1) и специфический для патогена антиген.
[0292] В некоторых вариантах осуществления, антигены, на которые нацелены рецепторы, в некоторых вариантах осуществления, включают орфанный тирозинкиназный рецептор ROR1, tEGFR, Her2, Ll-CAM, CD19, CD20, CD22, мезотелин, CEA и поверхностный антиген вируса гепатита B, антифолатный рецептор, CD23, CD24, CD30, CD33, CD38, CD44, EGFR, EGP-2, EGP-4, 0EPHa2, ErbB2, 3 или 4, FBP, фетальный рецептор ацетилхолина e, GD2, GD3, HMW-MAA, IL-22R-альфа, IL-13R-альфа2, kdr, легкую цепь каппа, Lewis Y, молекулы клеточной адгезии L1, MAGE-A1, мезотелин, MUC1, MUC16, PSCA, лиганды NKG2D, NY-ESO-1, MART-1, gp100, онкофетальный антиген, ROR1, TAG72, VEGF-R2, карциноэмбриональный антиген (CEA), простатспецифический антиген, PSMA, Her2/neu, рецептор эстрогена, рецептор прогестерона, эфрин B2, CD123, c-Met, GD-2, и MAGE A3, CE7, антиген опухоли Вильмса 1 (WT-1), циклин, такой как циклин A1 (CCNA1) и/или биотинилированные молекулы, и/или молекулы, экспрессированные HIV, HCV, HBV или другими патогенами.
[0293] В некоторых вариантах осуществления, CAR имеет специфичность связывания для опухолеассоциированного антигена, например, CD19, CD20, карбоангидразы IX (CAIX), CD171, CEA, ERBB2, GD2, рецептора-альфа фолата, антигена Lewis Y, простатспецифического мембранного антигена (PSMA) или опухолеассоциированного гликопротеина 72 (TAG72).
[0294] В некоторых вариантах осуществления, CAR связывает специфический для патогена антиген. В некоторых вариантах осуществления, CAR является специфическим для вирусных антигенов (таких как вирусный антиген из HIV, HCV, HBV и т.д.), бактериальных антигенов и/или паразитарных антигенов.
[0295] Среди химерных рецепторов присутствуют химерные рецепторы антигенов (CAR). Химерные рецепторы, такие как CAR, как правило, включают внеклеточный антигенсвязывающий домен, такой как часть молекулы антитела, как правило, вариабельную область тяжелой (VH) цепи и/или вариабельную область легкой (VL) цепи антитела, например, фрагмент scFv антитела.
[0296] В некоторых вариантах осуществления, часть антитела рекомбинантного рецептора, например, CAR, дополнительно включает по меньшей мере часть константной области иммуноглобулина, такую как шарнирная область, например, шарнирная область IgG4 и/или CH1/CL, и/или область Fc. В некоторых вариантах осуществления, константная область или фрагмент происходит из IgG человека, такого как IgG4 или IgG1. В некоторых аспектах, часть константной области служит спейсерной областью между узнающим антиген компонентом, например, scFv, и трансмембранным доменом. Спейсер может иметь длину, обеспечивающую увеличенную способность клетки отвечать после связывания антигена, по сравнению с отсутствием спейсера. Иллюстративные спейсеры, например, шарнирные области, включают спейсеры, описанные в публикации международной патентной заявки номер WO2014031687. В некоторых примерах, спейсер составляет или составляет приблизительно 12 аминокислот в длину, или составляет не более чем 12 аминокислот в длину. Иллюстративные спейсеры включают спейсеры, имеющие по меньшей мере приблизительно 10-229 аминокислот, приблизительно 10-200 аминокислот, приблизительно 10-175 аминокислот, приблизительно 10-150 аминокислот, приблизительно 10-125 аминокислот, приблизительно 10-100 аминокислот, приблизительно 10-75 аминокислот, приблизительно 10-50 аминокислот, приблизительно 10-40 аминокислот, приблизительно 10-30 аминокислот, приблизительно 10-20 аминокислот или приблизительно 10-15 аминокислот, и включая любое целое число между конечными точками любого из перечисленных диапазонов. В некоторых вариантах осуществления, область спейсера имеет приблизительно 12 аминокислоты или менее, приблизительно 119 аминокислот или менее, или приблизительно 229 аминокислот или менее. Иллюстративные спейсеры включают шарнир IgG4 отдельно, шарнир IgG4, связанный с доменами CH2 и CH3, или шарнир IgG4, связанный с доменом CH3.
[0297] Иллюстративные спейсеры включают, но без ограничения, спейсеры, описанные в Hudecek et al. (2013) Clin. Cancer Res., 19:3153 или публикации международной патентной заявки номер WO2014031687.
[0298] Этот узнающий антиген домен, как правило, является связанным с одним или несколькими компонентами для передачи внутриклеточных сигналов, такими как передающие сигналы компоненты, имитирующие активацию через комплекс рецептора антигена, такой как комплекс TCR, в случае CAR, и/или передачу сигнала посредством другого рецептора поверхности клетки. Таким образом, в некоторых вариантах осуществления, антигенсвязывающий компонент (например, антитело) является связанным с одним или несколькими трансмембранными и внутриклеточными доменами передачи сигналов. В некоторых вариантах осуществления, трансмембранный домен слит с внеклеточным доменом. В одном варианте осуществления, используют трансмембранный домен, естественным образом ассоциированный с одним из доменов в рецепторе, например, CAR. В некоторых случаях, трансмембранный домен отбирают или модифицируют посредством замены аминокислот, для исключения связывания таких доменов с трансмембранными доменами одинаковых или различных поверхностных мембранных белков для минимизации взаимодействий с другими членами комплекса рецептора.
[0299] Трансмембранный домен, в некоторых вариантах осуществления, происходит либо из природного, либо из синтетического источника. Когда источник является природным, домен, в некоторых аспектах, происходит из любого связанного с мембраной или трансмембранного белка. Трансмембранные области включают области, происходящие из (т.е., содержащие по меньшей мере трансмембранную область(области) из) цепи альфа, бета или зета T-клеточного рецептора, CD28, CD3-эпсилон, CD45, CD4, CD5, CD8, CD9, CD 16, CD22, CD33, CD37, CD64, CD80, CD86, CD134, CD137, CD154. Альтернативно, трансмембранный домен, в некоторых вариантах осуществления, является синтетическим. В некоторых аспектах, синтетический трансмембранный домен содержит преимущественно гидрофобные остатки, такие как лейцин и валин. В некоторых аспектах, триплет из фенилаланина, триптофана и валина можно обнаружить на каждом конце синтетического трансмембранного домена. В некоторых вариантах осуществления, связывание осуществляют посредством линкеров, спейсеров и/или трансмембранного домена(доменов).
[0300] Среди внутриклеточных доменов передачи сигналов присутствуют домены, имитирующие или приблизительно воспроизводящие сигнал через природный рецептор антигена, сигнал через такой рецептор в комбинации с костимулирующим рецептором, и/или сигнал через костимулирующий рецептор отдельно. В некоторых вариантах осуществления, короткий олиго- или полипептидный линкер, например, линкер между 2 и 10 аминокислот в длину, такой как линкер, содержащий остатки глицина и серина, например, дуплет глицин-серин, присутствует и формирует связь между трансмембранным доменом и цитоплазматическим передающим сигналы доменом CAR.
[0301] Рецептор, например, CAR, как правило, включает по меньшей мере один внутриклеточный передающий сигналы компонент или компоненты. В некоторых вариантах осуществления, рецептор включает внутриклеточный компонент комплекса TCR, такой как цепь CD3 TCR, опосредующая активацию T-клетки и цитотоксичность, например, цепь CD3-зета. Таким образом, в некоторых аспектах, антигенсвязывающий фрагмент является связанным с одним или несколькими модулями передачи сигналов. В некоторых вариантах осуществления, модули передачи сигналов клетки включают трансмембранный домен CD3, внутриклеточные передающие сигналы домены CD3 и/или другие трансмембранные домены CD. В некоторых вариантах осуществления, рецептор, например, CAR, дополнительно включает часть одной или нескольких дополнительных молекул, таких как рецептор Fc γ, CD8, CD4, CD25 или CD16. Например, в некоторых аспектах, CAR или другой химерный рецептор включает химерную молекулу между CD3-зета (CD3-ζ) или рецептором Fc γ и CD8, CD4, CD25 или CD16.
[0302] В некоторых вариантах осуществления, при связывании CAR или другого химерного рецептора, цитоплазматический домен или внутриклеточный передающий сигналы домен рецептора активирует по меньшей мере одно из нормальных эффекторных функций или ответов иммуноцита, например, T-клетки, модифицированной для экспрессии CAR. Например, в некоторых контекстах, CAR индуцирует функцию T-клетки, такую как цитолитическая активность или активность T-клетки-помощника, например, секрецию цитокинов или другие факторы. В некоторых вариантах осуществления, укороченный фрагмент внутриклеточного домена передачи сигналов компонента рецептора антигена или костимулирующей молекулы используют вместо интактной иммуностимулирующей цепи, например, если он передает сигнал эффекторной функции. В некоторых вариантах осуществления, внутриклеточные передающие сигналы домен или домены включают цитоплазматические последовательности T-клеточного рецептора (TCR), и в некоторых аспектах, также цитоплазматические последовательности корецепторов, которые в природном контексте действуют во взаимодействии с такими рецепторами для инициации передачи сигналов после привлечения рецептора антигена, и/или любое производное или вариант таких молекул, и/или любую синтетическую последовательность, имеющую такую же функциональную способность.
[0303] В контексте природного TCR, полная активация, как правило, требует не только передачи сигналов через TCR, но также костимулирующего сигнала. Таким образом, в некоторых вариантах осуществления, для стимуляции полной активации, компонент для образования вторичного или костимулирующего сигнала также включают в CAR. В других вариантах осуществления, CAR не включает компонент для образования костимулирующего сигнала. В некоторых аспектах, дополнительный CAR является экспрессированным на той же клетке и обеспечивает компонент для образования вторичного или костимулирующего сигнала.
[0304] Активацию T-клетки в некоторых аспектах описывают как опосредованную двумя классами цитоплазматических последовательностей для передачи сигналов: последовательностями, инициирующими зависимую от антигена первичную активацию через TCR (передающие первичные сигналы цитоплазматические последовательности), и последовательностями, которые действуют независимым от антигена образом для образования вторичного или костимулирующего сигнала (передающие вторичные сигналы цитоплазматические последовательности). В некоторых аспектах, CAR включает один или оба из таких передающих сигналы компонентов.
[0305] В некоторых аспектах, CAR включает цитоплазматическую передающую первичные сигналы последовательность, которая регулирует первичную активацию комплекса TCR. Передающие первичные сигналы цитоплазматические последовательности, которые действуют стимулирующим образом, могут содержать мотивы передачи сигналов, известные как иммунорецепторные тирозиновые активирующие мотивы или ITAM. Примеры ITAM, содержащих цитоплазматические передающие первичные сигналы последовательности, включают ITAM, происходящие из цепи CD3-зета, FcR-гамма, CD3-гамма, CD3-дельта и CD3-эпсилон. В некоторых вариантах осуществления, цитоплазматические молекула(молекулы) передачи сигналов в CAR содержит(содержат) цитоплазматический передающий сигналы домен, его часть или последовательность, происходящую из CD3-зета.
[0306] В некоторых вариантах осуществления, CAR включает передающий сигналы домен и/или трансмембранный фрагмент костимулирующего рецептора, такого как CD28, 4-1BB, OX40, DAP10, и ICOS. В некоторых аспектах, один и тот же CAR включает как активирующий, так и костимулирующий компоненты.
[0307] В некоторых вариантах осуществления, активирующий домен включен в один CAR, в то время как костимулирующий компонент предоставлен другим CAR, узнающим другой антиген. В некоторых вариантах осуществления, CAR включают активирующие или стимулирующие CAR, костимулирующие CAR, оба экспрессированные на одной и той же клетке (см. WO2014/055668). В некоторых аспектах, клетки включают один или несколько стимулирующих или активирующих CAR и/или костимулирующих CAR. В некоторых вариантах осуществления, клетки дополнительно включают ингибирующие CAR (iCAR, см. Fedorov et al., Sci. Transl. Medicine, 5(215) (December 2013), такие как CAR, узнающие антиген, отличный от антигена, ассоциированного и/или специфического для заболевания или состояния, посредством чего активирующий сигнал, подаваемый через нацеленный на заболевание CAR, уменьшают или ингибируют посредством связывания ингибирующего CAR с его лигандом, например, для уменьшения неспецифических эффектов.
[0308] В конкретных вариантах осуществления, внутриклеточный передающий сигналы домен содержит трансмембранный и передающий сигналы домен CD28, связанный с внутриклеточным доменом CD3 (например, CD3-зета). В некоторых вариантах осуществления, внутриклеточный передающий сигналы домен содержит химерные из CD28 и CD137 (4-1BB, TNFRSF9) костимулирующие домены, связанные с внутриклеточным доменом CD3-зета.
[0309] В некоторых вариантах осуществления, CAR включает один или несколько, например, два или более, костимулирующих домена и активирующий домен, например, первичный активирующий домен, в цитоплазматической части. Иллюстративные CAR включают внутриклеточные компоненты CD3-зета, CD28 и 4-1BB.
[0310] В некоторых вариантах осуществления, CAR или другой рецептор антигена дополнительно включает маркер, такой как поверхностный маркер клетки, который можно использовать для подтверждения трансдукции или модификации клетки для экспрессии рецептора, такой как укороченный вариант рецептора поверхности клетки, такой как укороченный EGFR (tEGFR). В некоторых аспектах, маркер включает весь или часть (например, укороченную форму) CD34, NGFR, или рецептора эпидермального фактора роста (например, tEGFR). В некоторых вариантах осуществления, нуклеиновая кислота, кодирующая маркер, является функционально связанной с полинуклеотидом, кодирующим линкерную последовательность, такую как расщепляемая линкерная последовательность, например, T2A. См. WO2014031687. В некоторых вариантах осуществления, введение конструкции, кодирующей CAR и EGFRt, разделенные посредством переключателя рибосомы T2A, может приводить к экспрессии двух белков с одной и той же конструкции, так что EGFRt можно использовать в качестве маркера для детекции клеток, экспрессирующих такую конструкцию. В некоторых вариантах осуществления, маркер, и необязательно, линкерная последовательность, могут представлять собой любые, как описано в Публикации патентной заявки No. WO 2014/031687. Например, маркер может представлять собой укороченный EGFR (tEGFR), необязательно, связанный с линкерной последовательностью, такой как расщепляемая линкерная последовательность T2A.
[0311] В некоторых вариантах осуществления, маркер представляет собой молекулу, например, поверхностный белок клетки, не обнаруженный в природе на T-клетках или не обнаруженный в природе на поверхности T-клеток, или его фрагмент.
[0312] В некоторых вариантах осуществления, молекула представляет собой не собственную молекулу, например, не собственный белок, т.е., белок, не узнаваемый как «собственный» иммунной системой хозяина, которому будут адоптивно переносить клетки.
[0313] В некоторых вариантах осуществления, маркер не выполняет терапевтической функции и/или не оказывает эффекта, отличного от использования в качестве маркера для генетической модификации, например, для отбора успешно модифицированных клеток. В других вариантах осуществления, маркер может представлять собой терапевтическую молекулу или молекулу, иным образом оказывающую некоторый желательный эффект, такую как лиганд для клетки, которая может быть встречена in vivo, например, костимулирующую молекулу или молекулу иммунной контрольной точки для усиления и/или ослабления ответов клеток после адоптивного переноса и встречи с лигандом.
[0314] В некоторых случаях, CAR обозначают как CAR первого, второго и/или третьего поколения. В некоторых аспектах, CAR первого поколения представляет собой CAR, обеспечивающий единственно индуцированный CD3-цепью сигнал после связывания антигена; в некоторых аспектах, CAR второго поколения представляет собой CAR, обеспечивающий такой сигнал и костимулирующий сигнал, такой как CAR, включающий внутриклеточный передающий сигналы домен из костимулирующего рецептора, такого как CD28 или CD137; в некоторых аспектах, CAR третьего поколения представляет собой CAR, включающий множество костимулирующих доменов из различных костимулирующих рецепторов.
[0315] В некоторых вариантах осуществления, химерный рецептор антигена включает внеклеточный фрагмент, содержащий антитело или фрагмент антитела. В некоторых аспектах, химерный рецептор антигена включает внеклеточный фрагмент, содержащий антитело или фрагмент, и внутриклеточный передающий сигналы домен. В некоторых вариантах осуществления, антитело или фрагмент включает scFv, и внутриклеточный домен содержит ITAM. В некоторых аспектах, внутриклеточный передающий сигналы домен включает передающий сигналы домен зета-цепи из зета-цепи CD3 (CD3ζ). В некоторых вариантах осуществления, химерный рецептор антигена включает трансмембранный домен, связывающий внеклеточный домен и внутриклеточный передающий сигналы домен. В некоторых аспектах, трансмембранный домен содержит трансмембранный фрагмент CD28. Внеклеточный и трансмембранный домен могут быть связаны напрямую или опосредованно. В некоторых вариантах осуществления, внеклеточный и трансмембранный домен связаны посредством спейсера, такого как любой из описанных в настоящем описании. В некоторых вариантах осуществления, химерный рецептор антигена содержит внутриклеточный домен из костимулирующей молекулы T-клетки, например, химерный между трансмембранным доменом и внутриклеточным передающим сигналы доменом. В некоторых аспектах, костимулирующая молекула T-клетки представляет собой CD28 или 41BB.
[0316] В некоторых вариантах осуществления, CAR содержит антитело, например, фрагмент антитела, трансмембранный домен, который представляет собой или содержит трансмембранный фрагмент CD28 или его функциональный вариант, и внутриклеточный передающий сигналы домен, содержащий передающий сигналы фрагмент CD28 или его функциональный вариант и передающий сигналы фрагмент CD3-зета или его функциональный вариант. В некоторых вариантах осуществления, CAR содержит антитело, например, фрагмент антитела, трансмембранный домен, который представляет собой или содержит трансмембранный фрагмент CD28 или его функциональный вариант, и внутриклеточный передающий сигналы домен, содержащий передающий сигналы фрагмент 4-1BB или его функциональный вариант, и передающий сигналы фрагмент CD3-зета или его функциональный вариант. В некоторых таких вариантах осуществления, рецептор дополнительно включает спейсер, содержащий фрагмент молекулы Ig, например, молекулы Ig человека, такой как шарнир Ig, например, шарнир IgG4, например, содержащий только шарнир спейсер.
[0317] В некоторых вариантах осуществления, трансмембранный домен рецептора, например, CAR, представляет собой трансмембранный домен CD28 человека или его вариант, например, 27-аминокислотный трансмембранный домен CD28 человека (No. доступа: P10747.1).
[0318] В некоторых вариантах осуществления, химерный рецептор антигена содержит внутриклеточный домен из костимулирующей молекулы T-клетки. В некоторых аспектах, костимулирующая молекула T-клетки представляет собой CD28 или 41BB.
[0319] В некоторых вариантах осуществления, внутриклеточный передающий сигналы домен содержит внутриклеточный передающий костимулирующие сигналы домен из CD28 человека, или его функциональный вариант или фрагмент, такой как его 41-аминокислотный домен и/или такой домен с заменой LL на GG в положениях 186-187 нативного белка CD28. В некоторых вариантах осуществления, внутриклеточный домен содержит внутриклеточный передающий костимулирующие сигналы домен из 41BB или его функциональный вариант или фрагмент, такой как 42-аминокислотный цитоплазматический домен из 4-1BB человека (No. доступа Q07011.1), или его функциональный вариант или фрагмент.
[0320] В некоторых вариантах осуществления, внутриклеточный передающий сигналы домен содержит передающий стимулирующие сигналы домен CD3-зета человека или его функциональный вариант, такой как 112-ак цитоплазматический домен из изоформы 3 CD3ζ человека (No. доступа: P20963.2) или передающий сигналы домен CD3-зета, как описано в Патенте США No.: 7446190 или Патенте США No. 8911993.
[0321] В некоторых аспектах, спейсер содержит только шарнирную область IgG, например, только шарнир из IgG4 или IgG1. В других вариантах осуществления, спейсер представляет собой шарнир Ig, например, шарнир IgG4, связанный с доменами CH2 и/или CH3. В некоторых вариантах осуществления, спейсер представляет собой шарнир Ig, например, шарнир IgG4, связанный с доменами CH2 и CH3. В некоторых вариантах осуществления, спейсер представляет собой шарнир Ig, например, шарнир IgG4, связанный только с доменом CH3. В некоторых вариантах осуществления, спейсер представляет собой или содержит богатую глицином-серином последовательность или другой гибкий линкер, такой как известные гибкие линкеры.
[0322] Например, в некоторых вариантах осуществления, CAR включает антитело или фрагмент, специфически связывающие антиген, спейсер, такой как любой из содержащих шарнир Ig спейсеров, трансмембранный домен CD28, внутриклеточный передающий сигналы домен CD28 и передающий сигналы домен CD3-зета. В некоторых вариантах осуществления, CAR включает антитело или фрагмент, специфически связывающие антиген, спейсер, такой как любой из содержащих шарнир Ig спейсеров, трансмембранный домен CD28, внутриклеточный передающий сигналы домен CD28 и передающий сигналы домен CD3-зета. В некоторых вариантах осуществления, такие конструкции CAR дополнительно включают элемент проскальзывания рибосомы T2A и/или последовательность tEGFR, например, ниже CAR.
[0323] Термины «полипептид» и «белок» использованы взаимозаменяемо для обозначения полимера из аминокислотных остатков и не ограничены минимальной длиной. Полипептиды, включая представленные рецепторы и другие полипептиды, например, линкеры или пептиды, могут включать аминокислотные остатки, включая природные и/или неприродные аминокислотные остатки. Термины включают также постэкспрессионные модификации полипептида, например, гликозилирование, сиалилирование, ацетилирование и фосфорилирование. В некоторых аспектах, полипептиды могут содержать модификации по отношению к нативной или природной последовательности, при условии, что белок сохраняет желательную активность. Эти модификации могут быть получены намеренно, например, посредством сайт-направленного мутагенеза, или могут быть получены случайно, например, посредством мутаций у хозяев, продуцирующих белки, или ошибок из-за амплификации ПЦР.
T-клеточные рецепторы
[0324] В некоторых вариантах осуществления, генетически модифицированные рецепторы антигенов включают рекомбинантные T-клеточные рецепторы (TCR) и/или TCR, клонированные из природных T-клеток. Таким образом, в некоторых вариантах осуществления, клетку-мишень изменяют для содержания генов специфического T-клеточного рецептора (TCR) (например, гена TRAC и TRBC). TCR или их антигенсвязывающие части включают те, которые узнают пептидный эпитоп или T-клеточный эпитоп полипептида-мишени, такого как антиген опухоли, вирусный или аутоиммунный белок. В некоторых вариантах осуществления, TCR имеет специфичность связывания для опухолеассоциированного антигена, например, карциноэмбрионального антигена (CEA), GP100, антигена 1 меланомы, узнаваемого T-клетками (MART1), антигена A3 меланомы (MAGEA3), NYESO1 или p53.
[0325] В некоторых вариантах осуществления, «T-клеточный рецептор» или «TCR» представляет собой молекулу, которая содержит вариабельные цепи α и β (также известные как TCRα и TCRβ, соответственно) или вариабельные цепи γ и δ (также известные как TCRγ и TCRδ, соответственно), или их антигенсвязывающие фрагменты, и которая является способной специфически связывать пептид, связанный с молекулой MHC. В некоторых вариантах осуществления, TCR находится в форме αβ. Как правило, TCR, существующие в формах αβ и γδ, являются в общем структурно сходными, но экспрессирующие их T-клетки могут иметь отличные анатомические локализации или функции. Как правило, TCR находится или может экспрессироваться на поверхности T-клеток (или T-лимфоцитов), где он, как правило, является ответственным за узнавание антигенов, связанных с молекулами главного комплекса гистосовместимости (MHC).
[0326] В некоторых вариантах осуществления, TCR представляет собой полноразмерный TCR или его антигенсвязывающие части или антигенсвязывающие фрагменты. В некоторых вариантах осуществления, TCR представляет собой интактный или полноразмерный TCR, включая TCR в форме aβ или в форме γδ. В некоторых вариантах осуществления, TCR представляет собой антигенсвязывающий фрагмент, который меньше полноразмерного TCR, но который связывается со специфическим пептидом, вязанным с молекулой MHC, например, связывается с комплексом MHC-пептид. В некоторых случаях, антигенсвязывающие часть или фрагмент TCR могут содержать только часть структурных доменов полноразмерного или интактного TCR, но все еще являются способными связывать пептидный эпитоп, такой как комплекс MHC-пептид, с которым связывается полноразмерный TCR. В некоторых случаях, антигенсвязывающий фрагмент содержит вариабельные домены TCR, такие как вариабельная α-цепь и вариабельная β-цепь TCR, достаточные для формирования участка связывания для связывания со специфическим комплексом MHC-пептид. Как правило, вариабельные цепи TCR содержат определяющие комплементарность области, вовлеченные в узнавание пептида, MHC и/или комплекса MHC-пептид.
[0327] В некоторых вариантах осуществления, вариабельные домены TCR содержат гипервариабельные петли, или CDR, которые, как правило, вносят первичный вклад в способность узнавания и связывания антигена, и в специфичность. В некоторых вариантах осуществления, CDR из TCR или их комбинация формирует весь или по существу весь антигенсвязывающий участок данной молекулы TCR. Различные CDR в вариабельной области TCR, как правило, разделены каркасными областями (FR), которые, как правило, имеют меньшую изменчивость среди молекул TCR, по сравнению с CDR (см., например, Jores et al., Proc. Nat'l Acad. Sci. U.S.A. 87:9138, 1990; Chothia et al., EMBO J. 7:3745, 1988; см. также Lefranc et al., Dev. Comp. Immunol. 27:55, 2003). В некоторых вариантах осуществления, CDR3 является главной CDR, ответственной за связывание с антигеном или специфичность, или является наиболее важной среди трех CDR в данной вариабельной области TCR для узнавания антигена, и/или для взаимодействия с частью процессированного пептида комплекса пептид-MHC. В некоторых контекстах, CDR1 альфа-цепи может взаимодействовать с N-концевой частью определенных антигенных пептидов. В некоторых контекстах, CDR1 бета-цепи может взаимодействовать с C-концевой частью пептида. В некоторых контекстах, CDR2 оказывает наиболее сильное влияние или является первичной CDR, ответственной за взаимодействие с частью MHC или узнавание части MHC из комплекса MHC-пептид. В некоторых вариантах осуществления, вариабельная область β-цепи может содержать дополнительную гипервариабельную область (CDR4 или HVR4), которая, как правило, вовлечена в связывание суперантигена, а не в узнавание антигена (Kotb (1995) Clinical Microbiology Reviews, 8:411-426).
[0328] В некоторых вариантах осуществления, TCR содержит вариабельный домен альфа (Vα) и/или вариабельный домен бета (Vβ), или их антигенсвязывающие фрагменты. В некоторых вариантах осуществления, α-цепь и/или β-цепь TCR может также содержать константный домен, трансмембранный домен и/или короткий цитоплазматический хвост (см., например, Janeway et al., Immunobiology: Immunobiology: The Immune System in Health and Disease, 3rd Ed., Current Biology Publications, p. 4:33, 1997). В некоторых вариантах осуществления, константный домен α-цепи кодирован геном TRAC (номенклатура IMGT) или представляет собой его вариант. В некоторых вариантах осуществления, константная область β-цепи кодирована генами TRBC1 или TRBC2 (номенклатура IMGT) или представляет собой их вариант. В некоторых вариантах осуществления, константный домен является соседним с мембраной клетки. Например, в некоторых случаях, внеклеточная часть TCR, сформированная двумя цепями, содержит два ближних к мембране константных домена, и два отдаленных от мембраны вариабельных домена, где каждый из вариабельных доменов содержит CDR.
[0329] В компетенции специалиста в данной области находится определение или идентификация различных доменов или областей TCR. В некоторых аспектах, остатки TCR являются известными или могут быть идентифицированы в соответствии с системой нумерации Международной иммуногенетической информационной системы (IMGT) (см., например, www.imgt.org; см. также, Lefranc et al. (2003) Developmental and Comparative Immunology, 2&;55-77; и The T Cell Factsbook 2nd Edition, Lefranc and LeFranc Academic Press 2001). С использованием этой системы, последовательности CDR1 внутри цепи Vα и/или цепи Vβ TCR соответствуют аминокислотам, присутствующим между остатками номер 27-38, включительно, последовательности CDR2 внутри цепи Vα и/или цепи Vβ TCR соответствуют аминокислотам, присутствующим между остатками номер 56-65, включительно, и последовательности CDR3 внутри цепи Vα и/или цепи Vβ TCR соответствуют аминокислотам, присутствующим между остатками номер 105-117, включительно.
[0330] В некоторых вариантах осуществления, TCR может представлять собой гетеродимер из двух цепей α и β (или, необязательно, γ и δ), которые являются связанными, например, посредством дисульфидной связи или дисульфидных связей. В некоторых вариантах осуществления, константный домен TCR может содержать короткие связывающие последовательности в которых остаток цистеина формирует дисульфидную связь, таким образом, связывая две цепи TCR. В некоторых вариантах осуществления, TCR может иметь дополнительный остаток цистеина на каждой из цепей α и β, так что TCR содержит две дисульфидные связи в константных доменах. В некоторых вариантах осуществления, каждый из константных и вариабельных доменов содержит дисульфидные связи, сформированные остатками цистеина.
[0331] В некоторых вариантах осуществления, TCR для модификации клеток, как описано, представляет собой TCR, полученный из известной последовательности(последовательностей) TCR, таких как последовательности цепей Vα,β, для которых по существу полноразмерная кодирующая последовательность является легко доступной. Способы получения полноразмерных последовательностей TCR, включая последовательности цепи V, из клеточных источников, хорошо известны. В некоторых вариантах осуществления, нуклеиновые кислоты, кодирующие TCR, можно получать из множества источников, например, посредством полимеразной цепной реакции (ПЦР) амплификации кодирующих TCR нуклеиновых кислот внутри или после выделения из данной клетки или клеток, или синтеза публично доступных последовательностей ДНК TCR. В некоторых вариантах осуществления, TCR получают из биологического источника, например, из клеток, например, из T-клетки (например, цитотоксической T-клетки), T-клеточной гибридомы или другого публично доступного источника. В некоторых вариантах осуществления, T-клетки можно получать из выделенных in vivo клеток. В некоторых вариантах осуществления, T-клетки могут представлять собой культивированные гибридому или клон T-клеток. В некоторых вариантах осуществления, TCR или его антигенсвязывающую часть можно получать синтетически, зная последовательность TCR.
[0332] В некоторых вариантах осуществления, клон T-клеток с высокой аффинностью для антигена-мишени (например, антигена злокачественной опухоли) идентифицируют, выделяют от пациента и вводят в клетки. В некоторых вариантах осуществления, клон TCR для антигена-мишени получают в трансгенных мышах, сконструированных с использованием генов иммунной системы человека (например, системы человеческих лейкоцитарных антигенов, или HLA). См., например, антигены опухолей (см., например, Parkhurst et al. (2009) Clin Cancer Res. 15:169-180 и Cohen et al. (2005) J Immunol. 175:5799-5808. В некоторых вариантах осуществления, фаговый дисплей используют для выделения TCR против антигена-мишени (см., например, Varela-Rohena et al. (2008) Nat Med. 14:1390-1395 и Li (2005) Nat Biotechnol. 23:349-354.
[0333] В некоторых вариантах осуществления, TCR или его антигенсвязывающая часть являются модифицированными или сконструированными. В некоторых вариантах осуществления, способы направленной эволюции используют для получения TCR с измененными свойствами, например, с более высокой аффинностью для специфического комплекса MHC-пептид. В некоторых вариантах осуществления, направленную эволюцию осуществляют способами дисплея, включая, но без ограничения, дрожжевой дисплей (Holler et al. (2003) Nat Immunol, 4, 55-62; Holler et al. (2000) Proc Natl Acad Sci U S A, 97, 5387-92), фаговый дисплей (Li et al. (2005) Nat Biotechnol, 23, 349-54), или T-клеточный дисплей (Chervin et al. (2008) J Immunol Methods, 339, 175-84). В некоторых вариантах осуществления, способы дисплея включают конструирование или модификацию известного, исходного или эталонного TCR. Например, в некоторых случаях, TCR дикого типа можно использовать в качестве матрицы для получения подвергнутых мутагенезу TCR, в которых один или несколько остатков CDR мутированы, и отбирают мутанты с желательным измененным свойством, таким как более высокая аффинность для желательного антигена-мишени.
[0334] В некоторых вариантах осуществления, как описано, TCR может содержать введенную дисульфидную связь или связи. В некоторых вариантах осуществления, природные дисульфидные связи не присутствуют. В некоторых вариантах осуществления, один или несколько природных остатков цистеина (например, в константном домене α-цепи и β-цепи), формирующих природную межцепьевую дисульфидную связь, заменяют на другой остаток, такой как серин или аланин. В некоторых вариантах осуществления, введенную дисульфидную связь можно формировать посредством мутации не относящихся к цистеину остатков в цепях альфа и бета, например, в константном домене цепи α и β, до цистеина. Иллюстративные неприродные дисульфидные связи TCR описаны в опубликованных Международных заявках PCT No. WO 2006/000830 и WO 2006/037960. В некоторых вариантах осуществления, остатки цистеина можно вводить в положении остатка Thr48 α-цепи и Ser57 β-цепи, остатка Thr45 α-цепи и Ser77 β-цепи, остатка Tyr10 α-цепи и Ser17 β-цепи, остатка Thr45 α-цепи и Asp59 β-цепи и/или остатка Ser15 α-цепи и Glu15 β-цепи. В некоторых вариантах осуществления, присутствие неприродных остатков цистеина (например, приводящее к образованию одной или нескольких неприродных дисульфидных связей) в рекомбинантном TCR может обеспечивать преимущество для образования желательного рекомбинантного TCR в клетке, в которую он введен, по сравнению с экспрессией несовпадающей пары TCR, содержащей природную цепь TCR.
[0335] В некоторых вариантах осуществления, цепи TCR содержат трансмембранный домен. В некоторых вариантах осуществления, трансмембранный домен является положительно заряженным. В некоторых случаях, цепь TCR содержит цитоплазматический хвост. В некоторых аспектах, каждая цепь (например, альфа или бета) TCR может иметь один N-концевой вариабельный домен иммуноглобулина, один константный домен иммуноглобулина, трансмембранную область и короткий цитоплазматический хвост на C-конце. В некоторых вариантах осуществления, TCR, например, посредством цитоплазматического хвоста, ассоциирован с инвариантными белками из комплекса CD3, вовлеченными в опосредование передачи сигнала. В некоторых случаях, структура позволяет TCR вступать в ассоциацию с другими молекулами, подобными CD3 и его субъединицам. Например, TCR, содержащий константные домены с трансмембранной областью, может заякоривать белок в мембране клетки и вступать в ассоциацию с инвариантными субъединицами аппарата или комплекса передачи сигналов CD3. Внутриклеточные хвосты передающих сигналы субъединиц CD3 (например, цепей CD3γ, CD3δ, CD3ε и CD3ζ) содержат один или несколько иммунорецепторных тирозиновых активирующих мотивов или ITAM, которые вовлечены в способность комплекса TCR передавать сигналы.
[0336] В некоторых вариантах осуществления, TCR представляет собой полноразмерный TCR. В некоторых вариантах осуществления, TCR представляет собой антигенсвязывающий фрагмент. В некоторых вариантах осуществления, TCR представляет собой димерный TCR (dTCR). В некоторых вариантах осуществления, TCR представляет собой одноцепочечный TCR (sc-TCR). TCR может находится в связанной с клеткой или в растворимой форме. В некоторых вариантах осуществления, для целей представленных способов, TCR находится в связанной с клеткой форме, экспрессированной на поверхности клетки.
[0337] В некоторых вариантах осуществления, dTCR содержит первый полипептид, где последовательность, соответствующая последовательности вариабельной области α-цепи TCR, слита с N-концом последовательности, соответствующей внеклеточной последовательности константной области α-цепи TCR, и второй полипептид, где последовательность, соответствующая последовательности вариабельной области β-цепи TCR, слита с N-концом последовательности, соответствующей внеклеточной последовательности константной области β-цепи TCR, где первый и второй полипептиды связаны посредством дисульфидной связи. В некоторых вариантах осуществления, связь может соответствовать природной межцепьевой дисульфидной связи, присутствующей в природных димерных TCR αβ. В некоторых вариантах осуществления, межцепьевые дисульфидные связи не присутствуют в природном TCR. Например, в некоторых вариантах осуществления, один или несколько остатков цистеина можно включать в внеклеточные последовательности константной области пары полипептидов dTCR. В некоторых случаях, как природная, так и неприродная дисульфидная связь может являться желательной. В некоторых вариантах осуществления, TCR содержит трансмембранную последовательность для заякоривания в мембране.
[0338] В некоторых вариантах осуществления, dTCR содержит α-цепь TCR, содержащую вариабельный домен α, константный домен α и первый мотив для димеризации, присоединенный к C-концу константного домена α, и β-цепь TCR, содержащую вариабельный домен β, константный домен β и первый мотив для димеризации, присоединенный к C-концу константного домена β, где первый и второй мотивы для димеризации легко взаимодействуют с образованием ковалентной связи между аминокислотой в первом мотиве для димеризации и аминокислотой во втором мотиве для димеризации, связывая вместе α-цепь TCR и β-цепь TCR.
[0339] В некоторых вариантах осуществления, TCR представляет собой scTCR, представляющий собой одиночную аминокислотную цепь, содержащую α-цепь и β-цепь, которая является способной связываться с комплексами MHC-пептид. Как правило, scTCR можно получать с использованием способов, известных специалистам в данной области, См., например, Международные публикации PCT No. WO 1996/13593, WO 1996/18105, WO 1999/18129, WO 2004/033685, WO 2006/037960, WO 2011/044186; Патент США No. 7569664; и Schlueter, C. J. et al. J. Mol. Biol. 256, 859 (1996).
[0340] В некоторых вариантах осуществления, scTCR содержит первый фрагмент, состоящий из аминокислотной последовательности, соответствующей вариабельной области α-цепи TCR, второй фрагмент, состоящий из аминокислотной последовательности, соответствующей последовательности вариабельной области β-цепи TCR, слитые с N-концом аминокислотной последовательности, соответствующей внеклеточной последовательности константного домена β-цепи TCR, и линкерную последовательность, связывающую C-конец первого фрагмента с N-концом второго фрагмента.
[0341] В некоторых вариантах осуществления, scTCR содержит первый фрагмент, состоящий из аминокислотной последовательности, соответствующей вариабельной области β-цепи TCR, второй фрагмент, состоящий из аминокислотной последовательности, соответствующей вариабельной области α-цепи TCR, слитый с N-концом аминокислотной последовательности, соответствующей внеклеточной последовательности константного домена α-цепи TCR, и линкерную последовательность, связывающую C-конец первого фрагмента с N-концом второго фрагмента.
[0342] В некоторых вариантах осуществления, scTCR содержит первый фрагмент, состоящий из последовательности вариабельной области α-цепи, слитой с N-концом внеклеточной последовательности константного домена α-цепи, и второй фрагмент, состоящий из последовательности вариабельной области β-цепи, слитой с N-концом последовательности внеклеточной константной и трансмембранной последовательности β-цепи, и, необязательно, линкерную последовательность, связывающую C-конец первого фрагмента с N-концом второго фрагмента.
[0343] В некоторых вариантах осуществления, scTCR содержит первый фрагмент, состоящий из последовательности вариабельной области β-цепи TCR, слитой с N-концом внеклеточной последовательности константного домена β-цепи, и второй фрагмент, состоящий из последовательности вариабельной области α-цепи, слитый с N-концом последовательности внеклеточной константной и трансмембранной последовательности α-цепи, и, необязательно, линкерную последовательность, связывающую C-конец первого фрагмента с N-концом второго фрагмента.
[0344] В некоторых вариантах осуществления, для связывания scTCR с комплексом MHC-пептид, цепи α и β должны образовывать пару таким образом, чтобы последовательности их вариабельных областей были ориентированы для такого связывания. Различные способы стимуляции образования пар α и β в scTCR хорошо известны в данной области. В некоторых вариантах осуществления, включают линкерную последовательность, которая связывает цепи α и β из одной полипептидной цепи. В некоторых вариантах осуществления, линкер должен иметь достаточную длину для перекрывания расстояния между C-концом α-цепи N-концом β-цепи, или наоборот, в то же время необходимо убедиться, что длина линкера не является настолько большой, чтобы блокировать или уменьшать связывание scTCR с комплексом пептид-мишень-MHC.
[0345] В некоторых вариантах осуществления, линкер из scTCR, связывающий первый и второй фрагменты TCR, может представлять собой любой линкер, способный формировать одиночную полипептидную цепь, с сохранением в то же время специфичности связывания TCR. В некоторых вариантах осуществления, линкерная последовательность может, например, иметь формулу -P-ак-P-, где P представляет собой пролин, и ак представляет собой аминокислотную последовательность, где аминокислоты представляют собой глицин и серин. В некоторых вариантах осуществления, первый и второй фрагменты образуют пары таким образом, что последовательности их вариабельных областей ориентированы для такого связывания. Таким образом, в некоторых случаях, линкер имеет достаточную длину для перекрывания расстояния между C-концом первого фрагмента и N-концом второго фрагмента, или наоборот, но не является слишком длинным, чтобы блокировать или уменьшать связывание scTCR с лигандом-мишенью. В некоторых вариантах осуществления, линкер может содержать от или от приблизительно 10 до 45 аминокислоты, например, от 10 до 30 аминокислоты или от 26 до 41 аминокислотных остатков, например, 29, 30, 31 или 32 аминокислот. В некоторых вариантах осуществления, линкер имеет формулу -PGGG-(SGGGG)5-P- или -PGGG-(SGGGG)6-P-, где P представляет собой пролин, G представляет собой глицин, и S представляет собой серин. В некоторых вариантах осуществления, линкер имеет последовательность GSADDAKKDAAKKDGKS).
[0346] В некоторых вариантах осуществления, scTCR содержит дисульфидную связь между остатками одиночной аминокислотной цепи, которые, в некоторых случаях, могут способствовать стабильности образования пары между областями α и β одноцепочечной молекулы (см., например, Патент США No. 7569664). В некоторых вариантах осуществления, scTCR содержит ковалентную дисульфидную связь, связывающую остаток из области иммуноглобулина константного домена α-цепи с остатком из области иммуноглобулина константного домена β-цепи одноцепочечной молекулы. В некоторых вариантах осуществления, дисульфидная связь соответствует природной дисульфидной связи, присутствующей в природном dTCR. В некоторых вариантах осуществления, дисульфидная связь в природном TCR не присутствует. В некоторых вариантах осуществления, дисульфидная связь представляет собой неприродную дисульфидную связь, введенную, например, посредством включения одного или нескольких остатков цистеина в внеклеточные последовательности константной области для областей первой и второй цепи полипептида scTCR. Иллюстративные мутации цистеина включают любые мутации, как описано выше. В некоторых случаях, может присутствовать как природная, так и неприродная дисульфидная связь.
[0347] В некоторых вариантах осуществления, scTCR представляет собой не связанный дисульфидной связью укороченный TCR, в котором гетерологичные лейциновые молнии, слитые с его C-концами, облегчают ассоциацию цепей (см., например, Международную публикацию PCT No. WO 1999/60120). В некоторых вариантах осуществления, scTCR содержит вариабельный домен TCRα, ковалентно связанный с вариабельным доменом TCRβ посредством пептидного линкера (см., например, Международную публикацию PCT No. WO 1999/18129).
[0348] В некоторых вариантах осуществления, любой из TCR, включая dTCR или scTCR, может быть связан с передающими сигналы доменами, что приводит к образованию активного TCR на поверхности T-клетки. В некоторых вариантах осуществления, TCR экспрессируется на поверхности клеток. В некоторых вариантах осуществления, TCR не содержит последовательность, соответствующую трансмембранной последовательности. В некоторых вариантах осуществления, трансмембранный домен может представлять собой трансмембранный домен Cα или Cβ. В некоторых вариантах осуществления, трансмембранный домен может происходить из не относящегося к TCR источника, например, трансмембранной области CD3z, CD28 или B7.1. В некоторых вариантах осуществления, TCR не содержит последовательность, соответствующую цитоплазматическим последовательностям. В некоторых вариантах осуществления, TCR содержит передающий сигналы домен CD3z. В некоторых вариантах осуществления, TCR является способным формировать комплекс TCR с CD3.
[0349] В некоторых вариантах осуществления, TCR или его антигенсвязывающий фрагмент имеет аффинность с равновесной константой связывания для антигена-мишени между или между приблизительно 10-5 и 10-12 M, и всеми ее индивидуальными значениями и диапазонами. В некоторых вариантах осуществления, антиген-мишень представляет собой комплекс MHC-пептид или лиганд.
[0350] В некоторых вариантах осуществления, TCR или его антигенсвязывающий фрагмент может представлять собой полученный рекомбинантным способом природный белок или его мутантную форму, в которой изменены одно или несколько свойств, таких как характеристики связывания. В некоторых вариантах осуществления, TCR может происходить из одного из различных видов животных, таких как человек, мышь, крыса или другое млекопитающее. В некоторых вариантах осуществления, для получения вектора, кодирующего TCR, цепи α и β амплифицируют посредством ПЦР с тотальной кДНК, выделенной из клона T-клеток, экспрессирующего представляющий интерес TCR, и клонируют в экспрессирующий вектор. В некоторых вариантах осуществления, цепи α и β можно получать синтетически.
[0351] В некоторых вариантах осуществления, цепи альфа и бета TCR выделяют и клонируют в экспрессирующий гены вектор. В некоторых вариантах осуществления, транскрипционные единицы могут являться модифицированными в форме бицистронной единицы, содержащей IRES (внутренний участок связывания рибосомы), что позволяет совместную экспрессию продуктов генов (например, кодирующих цепи α и β) посредством матричной РНК с одного промотора. Альтернативно, в некоторых случаях, один промотор может управлять экспрессией РНК, содержащей, в одной открытой рамке считывания (ORF), множество генов (например, кодирующих цепи α и β), отделенные друг от друга последовательностями, кодирующими саморасщепляющийся пептид (например, T2A) или участок узнавания протеазы (например, фурина). ORF, таким образом, кодирует одиночный полибелок, который, либо в ходе (в случае T2A), либо после трансляции, подвергается расщеплению до индивидуальных белков. В некоторых случаях, пептид, такой как T2A, может заставлять рибосому пропускать (проскальзывание рибосомы) синтез пептидной связи на C-конце элемента 2A, что приводит к разделению между концом последовательности 2A и следующим ниже пептидом. Примеры расщепляющихся пептидов 2A, включая те, которые могут индуцировать проскальзывание рибосомы, представляют собой T2A, P2A, E2A и F2A. В некоторых вариантах осуществления, цепи α и β клонируют в различные векторы. В некоторых вариантах осуществления, полученные цепи α и β вставляют в ретровирусный, например, лентивирусный, вектор.
[0352] В некоторых вариантах осуществления, гены TCR альфа и бета связаны посредством пептида проскальзывания рибосомы 2A пикорнавируса, так что обе цепи экспрессируются совместно. В некоторых вариантах осуществления, генетический перенос TCR осуществляют посредством ретровирусных или лентивирусных векторов, или посредством транспозонов (см., например, Baum et al. (2006) Molecular Therapy: The Journal of the American Society of Gene Therapy. 13:1050-1063; Frecha et al. (2010) Molecular Therapy: The Journal of the American Society of Gene Therapy. 18:1748-1757; an Hackett et al. (2010) Molecular Therapy: The Journal of the American Society of Gene Therapy. 18:674-683.
Векторы и способы модификации
[0353] Представленные способы включают экспрессию рекомбинантных рецепторов, включая CAR или TCR, для получения генетически модифицированных клеток, экспрессирующих такие связывающие молекулы. Генетическая модификация, как правило, включает введение нуклеиновой кислоты, кодирующей рекомбинантный или модифицированный компонент, в клетку, например, посредством ретровирусной трансдукции, трансфекции или трансформации.
[0354] В некоторых вариантах осуществления, перенос генов осуществляют посредством сначала стимуляции клетки, например, посредством ее объединения со стимулом, индуцирующим ответ, такой как пролиферация, выживаемость и/или активация, например, как измерено посредством экспрессии цитокина или маркера активации, с последующей трансдукцией активированных клеток, и размножением в культуре до количеств, достаточных для клинических применений.
[0355] Различные способы введения генетически модифицированных компонентов, например, рецепторов антигенов, например, CAR, хорошо известны и могут быть использованы с представленными способами и композициями. Иллюстративные способы включают способы переноса нуклеиновых кислот, кодирующих рецепторы, включая способы посредством вирусных, например, ретровирусных или лентивирусных, трансдукции, транспозонов и электропорации.
[0356] В некоторых вариантах осуществления, нуклеиновую кислоту, кодирующую рекомбинантный рецептор, можно клонировать в подходящий экспрессирующий вектор или векторы. Экспрессирующий вектор может представлять собой любой пригодный рекомбинантный экспрессирующий вектор, и может быть использован для трансформации или трансфекции любого пригодного хозяина. Пригодные векторы включают векторы, разработанные для воспроизведения и размножения или для экспрессии, или для того и другого, таких как плазмиды и вирусы.
[0357] В некоторых вариантах осуществления, вектор может представлять собой вектор из серий pUC (Fermentas Life Sciences), серий pBluescript (Stratagene, La Jolla, Calif.), серий pET (Novagen, Madison, Wis.), серий pGEX (Pharmacia Biotech, Uppsala, Sweden) или серий pEX (Clontech, Palo Alto, Calif.). В некоторых случаях, бактериофаговые векторы, такие как λG10, λGT11, λZapII (Stratagene), λEMBL4 и λNM1149, также можно использовать. В некоторых вариантах осуществления, можно использовать экспрессирующие векторы для растений, и они включают pBI01, pBI101,2, pBI101,3, pBI121 и pBIN19 (Clontech). В некоторых вариантах осуществления, экспрессирующие векторы для животных включают pEUK-Cl, pMAM и pMAMneo (Clontech). В некоторых вариантах осуществления, используют вирусный вектор, такой как ретровирусный вектор.
[0358] В некоторых вариантах осуществления, рекомбинантные экспрессирующие векторы можно получать с использованием стандартных способов рекомбинантной ДНК. В некоторых вариантах осуществления, векторы могут содержать регуляторные последовательности, такие как кодоны инициации и терминации транскрипции и трансляции, которые являются специфическими для типа хозяина (например, бактерии, гриба, растения или животного), для введения которому предназначен вектор, в соответствующих случаях и принимая во внимание, основан ли вектор на ДНК или РНК. В некоторых вариантах осуществления, вектор может содержать неприродный промотор, функционально связанный с нуклеотидной последовательностью, кодирующей рекомбинантный рецептор. В некоторых вариантах осуществления, промотор может представлять собой невирусный промотор или вирусный промотор, такой как промотор цитомегаловируса (CMV), промотор SV40, промотор RSV и промотор, обнаруженный в длинном концевом повторе вируса стволовых клеток мыши. Предусмотрены также другие промоторы, известные специалисту в данной области.
[0359] В некоторых вариантах осуществления, рекомбинантные нуклеиновые кислоты переносят в клетки с использованием рекомбинантных инфекционных вирусных частиц, например, таких как векторы, происходящие из вируса обезьян 40 (SV40), аденовирусов, аденоассоциированного вируса (AAV). В некоторых вариантах осуществления, рекомбинантные нуклеиновые кислоты переносят в T-клетки с использованием рекомбинантных лентивирусных векторов или ретровирусных векторов, таких как гамма-ретровирусные векторы (см., например, Koste et al. (2014) Gene Therapy 2014 Apr 3. doi: 10,1038/gt.2014,25; Carlens et al. (2000) Exp Hematol 28(10): 1137-46; Alonso-Cамино et al. (2013) Mol Ther Nucl Acids 2, e93; Park et al., Trends Biotechnol. 2011 November 29(11): 550-557.
[0360] В некоторых вариантах осуществления, ретровирусный вектор имеет последовательность длинного концевого повтора (LTR), например, из ретровирусного вектора, происходящую из вируса лейкоза мышей Молони (MoMLV), вируса миелопролиферативной саркомы (MPSV), вируса эмбриональных стволовых клеток мыши (MESV), вируса стволовых клеток мыши (MSCV), вируса, образующего очаги в селезенке (SFFV), или аденоассоциированного вируса (AAV). Большинство ретровирусных векторов происходят из ретровирусов мышей. В некоторых вариантах осуществления, ретровирусы включают ретровирусы, происходящие из любого источника среди клеток птиц или млекопитающих. Ретровирусы, как правило, являются амфотропными, что означает, что они являются способными инфицировать клетки-хозяева из нескольких видов, включая человека. В одном варианте осуществления, геном, подлежащим экспрессии, заменяют ретровирусные последовательности gag, pol и/или env. Описан ряд иллюстративных ретровирусных систем (например, Патенты США No. 5219740; 6207453; 5219740; Miller and Rosman (1989) BioTechniques 7:980-990; Miller, A. D. (1990) Human Gene Therapy 1:5-14; Scarpa et al. (1991) Virology 180:849-852; Burns et al. (1993) Proc. Natl. Acad. Sci. USA 90:8033-8037; и Boris-Lawrie and Temin (1993) Cur. Opin. Genet. Develop. 3:102-109.
[0361] Способы лентивирусной трансдукции известны в данной области. Иллюстративные способы описаны, например, в Wang et al. (2012) J. Immunother. 35(9): 689-701; Cooper et al. (2003) Кровь. 101:1637-1644; Verhoeyen et al. (2009) Methods Mol Biol. 506: 97-114; и Cavalieri et al. (2003) Blood. 102(2): 497-505.
[0362] В некоторых вариантах осуществления, рекомбинантные нуклеиновые кислоты переносят в T-клетки посредством электропорации (см., например, Chicaybam et al, (2013) PLoS ONE 8(3): e60298 и Van Tedeloo et al. (2000) Gene Therapy 7(16): 1431-1437). В некоторых вариантах осуществления, рекомбинантные нуклеиновые кислоты переносят в T-клетки посредством транспозиции (см., например, Manuri et al. (2010) Hum Gene Ther 21(4): 427-437; Sharma et al. (2013) Molec Ther Nucl Acids 2, e74; и Huang et al. (2009) Methods Mol Biol 506: 115-126). Другие способы введения и экспрессии генетического материала в иммуноцитах включают трансфекцию с использованием фосфата кальция (например, как описано в Current Protocols in Molecular Biology, John Wiley & Sons, New York. N.Y.), слияние протопластов, опосредованную катионными липосомами трансфекцию; бомбардировку микрочастицами с использованием частиц вольфрама (Johnston, Nature, 346: 776-777 (1990)); и копреципитацию фосфата стронция и ДНК (Brash et al., Mol. Cell Biol., 7: 2031-2034 (1987)).
[0363] Другие способы и векторы для переноса нуклеиновых кислот, кодирующих рекомбинантные продукты, представляют собой способы, описанные, например, в Публикации международной патентной заявки No. WO 2014/055668 и Патенте США No. 7446190.
[0364] В некоторых контекстах, сверхэкспрессия стимулирующего фактора (например, лимфокина или цитокина) может являться токсичной для субъекта. Таким образом, в некоторых контекстах, модифицированные клетки включают фрагменты генов, которые делают клетки чувствительными к отрицательному отбору in vivo, например, при введении в адоптивной иммунотерапии. Например, в некоторых аспектах, клетки модифицируют таким образом, что их можно уничтожать в результате изменения состояния in vivo пациента, которому их вводят. Поддающийся отрицательному отбору фенотип может возникать в результате вставки гена, придающего чувствительность к введенному средству, например, соединению. Поддающиеся отрицательному отбору гены включают ген тимидинкиназы вируса простого герпеса типа I (HSV-I TK) (Wigler et al., Cell II:223, 1977), придающий чувствительность к ганцикловиру; ген клеточной гипоксантин-фосфорибозилтрансферазы (HPRT), ген клеточной аденин-фосфорибозилтрансферазы (APRT), ген бактериальной цитозиндезаминазы (Mullen et al., Proc. Natl. Acad. Sci. USA. 89:33 (1992)).
[0365] В некоторых аспектах, клетки дополнительно модифицируют для стимуляции экспрессии цитокинов или других факторов.
[0366] Среди дополнительных нуклеиновых кислот, например, генов, для введения присутствуют нуклеиновые кислоты для улучшения эффективности терапии, например, посредством стимуляции жизнеспособности и/или функции перенесенных клеток; гены для предоставления генетического маркера для отбора и/или оценки клеток, например, для оценки выживаемости или локализации in vivo; гены для улучшения безопасности, например, посредством придания клетки чувствительности к отрицательному отбору in vivo, как описано в Lupton S. D. et al., Mol. and Cell Biol., 11:6 (1991); и Riddell et al., Human Gene Therapy 3:319-338 (1992); см. также публикации PCT/US91/08442 и PCT/US94/05601 от Lupton et al., описывающие использование бифункциональных поддающихся отбору слитых генов, полученных в результате слияния доминантного положительного селективного маркера с отрицательным селективным маркером. См., например, Riddell et al., Патент США No. 6040177, в столбцах 14-17.
Композиции и составы
[0367] Настоящее изобретение относится также к популяциям таких клеток, к композициям, содержащим такие клетки и/или обогащенным по таким клеткам, например, к таким, в которых клетки, экспрессирующие рекомбинантный рецептор, составляют по меньшей мере 50%, 60%, 70%, 80%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более от общего количества клеток в композиции или от клеток конкретного типа, таких как T-клетки или CD8+ или CD4+ клетки. Среди композиций присутствуют фармацевтические композиции и составы для введения, например, для адоптивной клеточной терапии. Настоящее изобретение относится также к терапевтическим способам введения клеток и композиций субъектам, например, пациентам.
[0368] Настоящее изобретение относится также к композициям, включающим клетки, включая фармацевтические композиции и составы, например, единичную дозированную форму композиций, включающую количество клеток для введения в данной дозе или ее доле. Фармацевтические композиции и составы, как правило, включают один или несколько необязательных фармацевтически приемлемых носителей или наполнителей. В некоторых вариантах осуществления, композиция включает по меньшей мере одно дополнительное лекарственное средство.
[0369] Термин «фармацевтический состав» относится к препарату, который находится в такой форме, чтобы обеспечивать эффективность биологической активности содержащегося в нем активного ингредиента, и который не содержит дополнительных компонентов, неприемлемо токсичных для субъекта, которому будут вводить состав.
[0370] «Фармацевтически приемлемый носитель» относится к ингредиенту в фармацевтическом составе, отличному от активного ингредиента, который является нетоксичным для субъекта. Фармацевтически приемлемый носитель включает, но без ограничения, буфер, наполнитель, стабилизатор или консервант.
[0371] В некоторых аспектах, выбор носителя частично определяется конкретной клеткой и/или способом введения. Соответственно, существует множество пригодных составов. Например, фармацевтическая композиция может содержать консерванты. Пригодные консерванты могут включать, например, метилпарабен, пропилпарабен, бензоат натрия и хлорид бензалкония. В некоторых аспектах, используют смесь из двух или более консервантов. Консерванты или их смеси, как правило, присутствуют в количестве от приблизительно 0,0001% до приблизительно 2% по массе от суммарной композиции. Носители описаны, например, в Remington's Pharmaceutical Sciences 16th edition, Osol, A. Ed. (1980). Фармацевтически приемлемые носители являются, как правило, нетоксичными для реципиентов в используемых дозах и концентрациях, и включают, но без ограничения: буферы, такие как фосфат, цитрат и другие органические кислоты; антиоксиданты, включая аскорбиновую кислоту и метионин; консерванты (такие как хлорид октадецилдиметилбензиламмония; хлорид гексаметэтония; хлорид бензалкония, хлорид бензэтония; фенол, бутил или бензиловый спирт; алкилпарабены, такие как метил- или пропилпарабен; катехол; резорцинол; циклогексанол; 3-пентанол; и м-крезол); полипептиды с низкой молекулярной массой (менее приблизительно 10 остатков); белки, такие как сывороточный альбумин, желатин или иммуноглобулины; гидрофильные полимеры, такие как поливинилпирролидон; аминокислоты, такие как глицин, глутамин, аспарагин, гистидин, аргинин, или лизин; моносахариды, дисахариды и другие углеводы, включая глюкозу, маннозу или декстрины; хелатирующие агенты, такие как ЭДТА; сахара, такие как сахароза, маннит, трегалоза или сорбит; солеобразующие противоионы, такие как натрий; комплексы с металлом (например, комплексы Zn-белок); и/или неионные поверхностно-активные вещества, такие как полиэтиленгликоль (PEG).
[0372] Забуферивающие средства в некоторых аспектах включают в композиции. Пригодные забуферивающие средства включают, например, лимонную кислоту, цитрат натрия, фосфорную кислоту, фосфат калия, и различные другие кислоты и соли. В некоторых аспектах, используют смесь из двух или более забуферивающих средств. Забуферивающие средства или их смеси, как правило, присутствуют в количестве от приблизительно 0,001% до приблизительно 4% по массе от суммарной композиции. Способы получения пригодных для введения фармацевтических композиций известны. Иллюстративные способы описаны более подробно, например, в Remington: The Science and Practice of Pharmacy, Lippincott Williams & Wilkins; 21st ed. (May 1, 2005).
[0373] Составы могут включать водные растворы. Состав или композиция могут также содержать более одного активного ингредиента, которые можно использовать для конкретного признака, заболевания или состояния, подвергаемых лечению с использованием клеток, предпочтительно, ингредиенты с активностью, дополняющей активность клеток, где соответствующие активности не оказывают неблагоприятного влияния друг на друга. Такие активные ингредиенты подходящим образом присутствуют в комбинации в количествах, которые являются эффективными для намеченной цели. Таким образом, в некоторых вариантах осуществления, фармацевтическая композиция дополнительно включает другие фармацевтически активные вещества или лекарственные средства, такие как химиотерапевтические средства, например, аспарагиназа, бусульфан, карбоплатин, цисплатин, даунорубицин, доксорубицин, фторурацил, гемцитабин, гидроксимочевина, метотрексат, паклитаксел, ритуксимаб, винбластин и/или винкристин.
[0374] Фармацевтическая композиция, в некоторых вариантах осуществления, содержит клетки в количествах, эффективных для лечения или предотвращения заболевания или состояния, таких как терапевтически эффективное или профилактически эффективное количество. Терапевтическую или профилактическую эффективность, в некоторых вариантах осуществления, мониторируют посредством периодической оценки подвергаемых лечению субъектов. Желательную дозу можно доставлять посредством однократного болюсного введения клеток, посредством множества болюсных введений клеток, или посредством введения клеток непрерывной инфузией.
[0375] Клетки и композиции можно вводить с использованием стандартных способов, составов и/или устройств для введения. Введение клеток может являться аутологичным или гетерологичным. Например, иммунореактивные клетки или предшественники можно получать от одного субъекта и вводить тому же самому субъекту или другому, совместимому субъекту. Полученные из периферической крови иммунореактивные клетки или их потомство (например, полученное in vivo, ex vivo или in vitro) можно вводить посредством локализованной инъекции, включая введение через катетер, системной инъекции, местной инъекции, внутривенной инъекции или парентерального введения. При введении терапевтической композиции (например, фармацевтической композиции, содержащей генетически модифицированные иммунореактивные клетки), ее, как правило, составляют в единичной дозированной пригодной для инъекции форме (растворе, суспензии, эмульсии).
[0376] Составы включают составы для перорального, внутривенного, внутрибрюшинного, подкожного, внутрилегочного, чрескожного, внутримышечного, интраназального, трансбуккального, подъязычного введения или введения с использованием суппозитория. В некоторых вариантах осуществления, популяции клеток вводят парентерально. Термин «парентеральное», в рамках изобретения, включает внутривенное, внутримышечное, подкожное, ректальное, вагинальное и внутрибрюшинное введение. В некоторых вариантах осуществления, клетки вводят субъекту с использованием периферической системной доставки посредством внутривенной, внутрибрюшинной или подкожной инъекции.
[0377] Композиции, в некоторых вариантах осуществления, представлены в форме стерильных жидких препаратов, например, изотонических водных растворов, суспензий, эмульсий, дисперсий или вязких композиций, которые можно, в некоторых аспектах, забуферивать до выбранного pH. Жидкие препараты обычно проще получать, чем гели, другие вязкие композиции и твердые композиции. Кроме того, жидкие композиции несколько более удобны для введения, особенно посредством инъекции. Вязкие композиции, с другой стороны, можно составлять в пределах соответствующего диапазона вязкости для обеспечения более длительных периодов контакта со специфическими тканями. Жидкие или вязкие композиции могут содержать носители, которые могут представлять собой растворитель или диспергирующую среду, содержащие, например, воду, солевой раствор, фосфатно-солевой буфер, полиол (например, глицерин, пропиленгликоль, жидкий полиэтиленгликоль) и их пригодные смеси.
[0378] Стерильные пригодные для инъекции растворы можно получать посредством включения клеток в растворитель, например, в смеси с пригодным носителем, разбавителем или наполнителем, таким как стерильная вода, физиологический солевой раствор, глюкоза, декстроза или т.п. Композиции могут содержать вспомогательные средства, такие как смачивающие, диспергирующие или эмульгирующие средства (например, метилцеллюлозу), забуферивающие pH средства, гелеобразующие или повышающие вязкость добавки, консерванты, ароматизаторы и/или окрашивающие средства, в зависимости от желательного способа введения и получения. В некоторых аспектах, можно консультироваться со стандартными руководствами для получения пригодных препаратов.
[0379] Различные добавки, увеличивающие стабильность и стерильность композиции, включая противомикробные консерванты, антиоксиданты, хелатирующие агенты и буферы, можно добавлять. Предотвращение действия микроорганизмов можно обеспечивать посредством различных антибактериальных и противогрибковых средств, например, парабенов, хлорбутанола, фенола и сорбиновой кислоты. Длительную абсорбцию пригодной для инъекции фармацевтической формы можно получать с использованием средств, замедляющих абсорбцию, например, моностеарата алюминия и желатина.
[0380] Составы, подлежащие использованию для введения in vivo, как правило, являются стерильными. Стерильность можно легко обеспечивать, например, посредством фильтрации через мембраны для стерилизации фильтрацией.
Способы введения и применения в адоптивной клеточной терапии
[0381] Настоящее изобретение относится к способам введения клеток, популяций и композиций, описанных в настоящем описании, и к применениям таких клеток, популяций и композиций, описанных в настоящем описании, для лечения или предотвращения заболеваний, состояний и нарушений, включая злокачественные опухоли. В некоторых вариантах осуществления, клетки, популяции и композиции вводят субъекту или пациенту, имеющему конкретное заболевание или состояние, подлежащее лечению, например, посредством адоптивной клеточной терапии, такой как адоптивная T клеточная терапия. В некоторых вариантах осуществления, клетки и композиции, полученные представленными способами, такие как модифицированные композиции и композиции на конечном этапе производственного цикла после инкубации и/или других стадий переработки, вводят субъекту, такому как субъект, имеющий заболевание или состояние, или подверженный риску заболевания или состояния. В некоторых аспектах, способы, таким образом, обеспечивают лечение, например, облегчение одного или нескольких симптомов заболевания или состояния, например, посредством уменьшения опухолевой нагрузки при злокачественной опухоли, экспрессирующий антиген, узнаваемый модифицированной T-клеткой.
[0382] Способы введения клеток для адоптивной клеточной терапии известны и могут быть использованы в сочетании с представленными способами и композициями. Например, способы адоптивной T-клеточной терапии описаны, например, в Публикации патентной заявки США No. 2003/0170238 от Gruenberg et al; Патенте США No. 4690915 от Rosenberg; Rosenberg (2011) Nat Rev Clin Oncol. 8(10):577-85). См., например, Themeli et al. (2013) Nat Biotechnol. 31(10): 928-933; Tsukahara et al. (2013) Biochem Biophys Res Commun 438(1): 84-9; Davila et al. (2013) PLoS ONE 8(4): e61338.
[0383] В рамках изобретения, «субъект» представляет собой млекопитающее, такое как человек или другое животное, и как правило, представляет собой человека. В некоторых вариантах осуществления, субъект, например, пациент, которому вводят клетки, популяции клеток или композиции, представляет собой млекопитающее, как правило, примата, такого как человек. В некоторых вариантах осуществления, примат представляет собой обезьяну или высшую обезьяну. Субъект может иметь мужской или женский пол и может находиться в любом подходящем возрасте, включая младенцев, детей, подростков, взрослых и престарелых субъектов. В некоторых вариантах осуществления, субъект представляет собой не относящегося к примату животного, такого как грызун.
[0384] В рамках изобретения, «лечение» (и его грамматические варианты, такие как «лечить» или «проведение лечения») относится к полному или частичному облегчению или уменьшению заболевания или состояния, или нарушения, или симптома, неблагоприятного эффекта или исхода, или ассоциированного с ними фенотипа. Желательные эффекты лечения включают, но без ограничения, предотвращение возникновения или рецидива заболевания, облегчение симптомов, уменьшение любых прямых или опосредованных патологических последствий заболевания, предотвращение метастазирования, уменьшение скорости прогрессирования заболевания, облегчение или смягчение состояния заболевания, и ремиссию или улучшение прогноза. Термины не подразумевают полного излечения заболевания или полного прекращения любого симптома или эффекта(эффектов) всех симптомов или исходов.
[0385] В рамках изобретения, «задержка развития заболевания» означает отсрочку, затруднение, замедление, сдерживание, стабилизацию, супрессию и/или отдаление развития заболевания (такого как злокачественная опухоль). Эта задержка может составлять различные периоды времени, в зависимости от анамнеза заболевания и/или индивидуума, подвергаемого лечению. Как очевидно для специалиста в данной области, достаточная или значительная, задержка может, фактически, включать предотвращение, в том плане, что у индивидуума не развивается заболевание. Например, может быть задержана поздняя стадия злокачественной опухоли, такая как развитие метастазирования.
[0386] «Предотвращение», в рамках изобретения, включает обеспечение профилактики, применительно к возникновению или рецидиву заболевания у субъекта, который может иметь предрасположенность к заболеванию, но у которого еще не диагностировано заболевание. В некоторых вариантах осуществления, представленные клетки и композиции используют для задержки развития заболевания или для замедления прогрессирования заболевания.
[0387] В рамках изобретения, «супрессия» функции или активности представляет собой снижение функции или активности, по сравнению с одинаковыми в ином отношении состояниями, за исключением представляющего интерес условия или параметра, или альтернативно, по сравнению с другим состоянием. Например, клетки, супрессирующие рост опухоли, уменьшают скорость роста опухоли, по сравнению со скоростью роста опухоли в отсутствие клеток.
[0388] «Эффективное количество» средства, например, фармацевтического состава, клеток или композиции, в контексте введения, относится к количеству, эффективному, в дозах/количествах и в течение периодов времени, необходимых для достижения желательного результата, такого как терапевтический или профилактический результат.
[0389] «Терапевтически эффективное количество» средства, например, фармацевтического состава или клеток, относится к количеству, эффективному, в дозах и в течение периодов времени, необходимых для достижения желательного терапевтического результата, например, для лечения заболевания, состояния или нарушения, и/или фармакокинетического или фармакодинамического эффекта лечения. Терапевтически эффективное количество может меняться в соответствии с такими факторами, как состояние заболевания, возраст, пол и масса субъекта, и вводимые популяции клеток. В некоторых вариантах осуществления, представленные способы включают введение клеток и/или композиций в эффективных количествах, например, терапевтически эффективных количествах.
[0390] «Профилактически эффективное количество» относится к количеству, эффективному, в дозах и в течение периодов времени, необходимых для достижения желательного профилактического результата. Как правило, но необязательно, поскольку профилактическую дозу используют у субъектов до или на более ранней стадии заболевания, профилактически эффективное количество может быть менее, чем терапевтически эффективное количество. В контексте более низкой опухолевой нагрузки, профилактически эффективное количество, в некоторых аспектах, может быть выше, чем терапевтически эффективное количество.
[0391] В некоторых вариантах осуществления, субъект имеет персистентное или рецидивирующее заболевание, например, после лечения с использованием другого терапевтического вмешательства, включая химиотерапию, радиоактивное облучение и/или трансплантацию гематопоэтических стволовых клеток (HSCT), например, аллогенную HSCT. В некоторых вариантах осуществления, введение приводит к эффективному лечению субъекта, несмотря на то, что субъект стал устойчивым к другой терапии.
[0392] Способы введения клеток для адоптивной клеточной терапии известны и могут быть использованы в сочетании с представленными способами и композициями. Например, способы адоптивной T-клеточной терапии описаны, например, в Публикации патентной заявки США No. 2003/0170238 от Gruenberg et al; Патенте США No. 4690915 от Rosenberg; Rosenberg (2011) Nat Rev Clin Oncol. 8(10):577-85). См., например, Themeli et al. (2013) Nat Biotechnol. 31(10): 928-933; Tsukahara et al. (2013) Biochem Biophys Res Commun 438(1): 84-9; Davila et al. (2013) PLoS ONE 8(4): e61338.
[0393] В некоторых вариантах осуществления, клеточную терапию, например, адоптивную T-клеточную терапию, осуществляют посредством аутологичного переноса, при котором клетки выделяют и/или иным образом получают от субъекта, подлежащего проведению клеточной терапии, или из образца, полученного от такого субъекта. Таким образом, в некоторых аспектах, клетки получают от субъекта, например, пациента, нуждающегося в лечении, и клетки, после выделения и переработки, вводят тому же самому субъекту.
[0394] В некоторых вариантах осуществления, клеточную терапию, например, адоптивную T-клеточную терапию, осуществляют посредством аллогенного переноса, при котором клетки выделяют и/или иным образом получают от субъекта, отличного от субъекта, подлежащего проведению клеточной терапии или в конечном счете подлежащего проведению клеточной терапии, например, первого субъекта. В таких вариантах осуществления, клетки затем вводят другому субъекту, например, второму субъекту, того же вида. В некоторых вариантах осуществления, первый и второй субъекты являются генетически идентичными. В некоторых вариантах осуществления, первый и второй субъекты являются генетически сходными. В некоторых вариантах осуществления, второй субъект экспрессирует HLA такого же класса или супертипа, что и первый субъект.
[0395] В некоторых вариантах осуществления, субъекта подвергали лечению с использованием лекарственного средства, нацеленного на заболевание или состояние, например, опухоль, до введения клеток или композиции, содержащей клетки. В некоторых аспектах, субъект является невосприимчивым или не отвечающим по отношению к другому лекарственному средству. В некоторых вариантах осуществления, субъект имеет персистентное или рецидивирующее заболевание, например, после лечения с использованием другого терапевтического вмешательства, включая химиотерапию, радиоактивное облучение и/или трансплантацию гематопоэтических стволовых клеток (HSCT), например, аллогенную HSCT. В некоторых вариантах осуществления, введение приводит к эффективному лечению субъекта, несмотря на то, что субъект стал устойчивым к другой терапии.
[0396] В некоторых вариантах осуществления, субъект является способным отвечать на другое лекарственное средство, и лечение с использованием лекарственного средства уменьшает нагрузку заболевания. В некоторых аспектах, субъект первоначально является способным отвечать на лекарственное средство, но имеет проявление рецидива заболевания или состояния с течением времени. В некоторых вариантах осуществления, субъект не имеет рецидива. В некоторых таких вариантах осуществления, определяют, что субъект подвержен риску рецидива, например, высокому риску рецидива, и таким образом, клетки вводят профилактически, например, для уменьшения вероятности или предотвращения рецидива.
[0397] В некоторых аспектах, субъекта не подвергали предшествующему лечению с использованием другого лекарственного средства.
[0398] Среди заболеваний, состояний и нарушений для лечения с использованием представленных композиций, клеток, способов и применений, присутствуют опухоли, включая солидные опухоли, гематологические злокачественные новообразования и меланомы, и инфекционные заболевания, такие как инфекция вирусом или другим патогеном, например, HIV, HCV, HBV, CMV, и паразитарное заболевание. В некоторых вариантах осуществления, заболевание или состояние представляет собой опухоль, злокачественную опухоль, злокачественное новообразование, неоплазию или другое пролиферативное заболевание или нарушение. Такие заболевания включают, но без ограничения, лейкоз, лимфому, например, хронический лимфоцитарный лейкоз (CLL), острый лимфобластный лейкоз (ALL), неходжскинскую лимфому, острый миелоидный лейкоз, множественную миелому, невосприимчивую фолликулярную лимфому, лимфому из клеток мантийной зоны, индолентную B-клеточную лимфому, злокачественные новообразования B-клеток, злокачественные опухоли ободочной кишки, легкого, печени, молочной железы, предстательной железы, яичников, кожи, меланому, злокачественные опухоли кости и мозга, рак яичника, эпителиальные злокачественные опухолей, почечноклеточную карциному, аденокарциному поджелудочной железы, лимфому Ходжкина, карциному шейки матки, колоректальный рак, глиобластому, нейробластому, саркому Юинга, медуллобластому, остеосаркому, синовиальную саркому и/или мезотелиому.
[0399] В некоторых вариантах осуществления, заболевание или состояние представляет собой инфекционное заболевание или состояние, такое как, но без ограничения, вирусные, ретровирусные, бактериальные и протозойные инфекции, иммунодефицит, инфекции цитомегаловируса (CMV), вируса Эпштейна-Барр (EBV), аденовируса, полиомавируса BK. В некоторых вариантах осуществления, заболевание или состояние представляет собой аутоиммунное или воспалительное заболевание или состояние, такое как артрит, например, ревматоидный артрит (RA), диабет типа I, системная красная волчанка (SLE), воспалительное заболевание кишечника, псориаз, склеродермия, аутоимунный тиреоидит, болезнь Грэйва, болезнь Крона, рассеянный склероз, астма и/или заболевание или состояние, ассоциированное с трансплантацией.
[0400] В некоторых вариантах осуществления, антиген, ассоциированный с заболеванием, нарушением или состоянием, выбран из ROR1, антигена созревания B-клеток (BCMA), карбоангидразы 9 (CAIX), tEGFR, Her2/neu (рецепторной тирозинкиназы erbB2), L1-CAM, CD19, CD20, CD22, мезотелина, CEA, и поверхностного антигена вируса гепатита B, антифолатного рецептора, CD23, CD24, CD30, CD33, CD38, CD44, EGFR, эпителиального гликопротеина 2 (EPG-2), эпителиального гликопротеина 40 (EPG-40), EPHa2, erb-B2, erb-B3, erb-B4, димеров erbB, EGFR vIII, связывающего фолат белка (FBP), FCRL5, FCRH5, фетального рецептора ацетилхолина, GD2, GD3, HMW-MAA, IL-22R-альфа, IL-13R-альфа2, рецептора, содержащего домен вставки киназы (kdr), легкой цепи каппа, Lewis Y, молекулы клеточной адгезии L1, (L1-CAM), ассоциированного с меланомой антигена (MAGE)-A1, MAGE-A3, MAGE-A6, предпочтительно экспрессируемого антигена меланомы (PRAME), сурвивина, TAG72, B7-H6, рецептора альфа 2 IL-13 (IL-13Ra2), CA9, GD3, HMW-MAA, CD171, G250/CAIX, HLA-AI MAGE Al, HLA-A2 NY-ESO-1, PSCA, рецептора-a фолата, CD44v6, CD44v7/8, интегрина avb6, 8H9, NCAM, рецепторов VEGF, 5T4, фетального AchR, лигандов NKG2D, CD44v6, двойного антигена, раково-тестикулярного антигена, мезотелина, мышиного CMV, муцина 1 (MUC1), MUC16, PSCA, NKG2D, NY-ESO-1, MART-1, gp100, онкофетального антигена, ROR1, TAG72, VEGF-R2, карциноэмбрионального антигена (CEA), Her2/neu, рецептора эстрогена, рецептора прогестерона, эфрина B2, CD123, c-Met, GD-2, O-ацетилированного GD2 (OGD2), CE7, антигена опухоли Вильмса 1 (WT-1), циклина, циклина A2, CCL-1, CD138, специфического для патогена антигена.
[0401] В некоторых вариантах осуществления, антиген, ассоциированный с заболеванием или нарушением, выбран из группы, состоящей из орфанного тирозинкиназного рецептора ROR1, tEGFR, Her2, Ll-CAM, CD19, CD20, CD22, мезотелина, CEA и поверхностного антигена вируса гепатита B, антифолатного рецептора, CD23, CD24, CD30, CD33, CD38, CD44, EGFR, EGP-2, EGP-4, 0EPHa2, ErbB2, 3 или 4, FBP, фетального рецептора ацетилхолина e, GD2, GD3, HMW-MAA, IL-22R-альфа, IL-13R-альфа2, kdr, легкой цепи каппа, Lewis Y, молекулы клеточной адгезии L1, MAGE-A1, мезотелина, MUC1, MUC16, PSCA, лигандов NKG2D, NY-ESO-1, MART-1, gp100, онкофетального антигена, ROR1, TAG72, VEGF-R2, карциноэмбрионального антигена (CEA), простатспецифического антигена, PSMA, Her2/neu, рецептора эстрогена, рецептора прогестерона, эфрина B2, CD123, CS-1, c-Met, GD-2, и MAGE A3 и/или биотинилированных молекул, и/или молекул, экспрессированных HIV, HCV, HBV или другими патогенами.
[0402] В некоторых вариантах осуществления, клетки вводят в желательной дозе, которая, в некоторых аспектах, включает желательную дозу или количество клеток или типа(типов) клеток и/или желательное соотношение типов клеток. Таким образом, доза клеток в некоторых вариантах осуществления основана на общем количестве клеток (или количестве на кг массы тела) и желательном соотношении индивидуальных популяций или подтипов, таком как соотношение CD4+ и CD8+. В некоторых вариантах осуществления, доза клеток основана на желательном общем количестве (или количестве на кг массы тела) клеток в индивидуальных популяциях или индивидуальных типах клеток. В некоторых вариантах осуществления, доза основана на комбинации таких признаков, например, желательного общего количества клеток, желательного соотношения и желательного общего количества клеток в индивидуальных популяциях.
[0403] В некоторых вариантах осуществления, популяции или подтипы клеток, таких как CD8+ и CD4+ T-клетки, вводят в желательной дозе или в пределах переносимых различий желательной дозы тотальных клеток, например, желательной дозы T-клеток. В некоторых аспектах, желательная доза представляет собой желательное количество клеток или желательное количество клеток на единицу массы тела субъекта, которому вводят клетки, например, клеток/кг. В некоторых аспектах, желательная доза представляет собой или превышает минимальное количество клеток или минимальное количество клеток на единицу массы тела. В некоторых аспектах, среди тотальных клеток, введенных в желательной дозе, индивидуальные популяции или подтипы присутствуют в желательном соотношении или приблизительно в желательном соотношении на выходе (таком как соотношение CD4+ и CD8+), например, в пределах определенных переносимых различий или ошибки такого соотношения.
[0404] В некоторых вариантах осуществления, клетки вводят в желательной дозе или в пределах переносимых различий желательной дозы одного или нескольких из индивидуальных популяций или подтипов клеток, такой как желательная доза CD4+ клеток и/или желательная доза CD8+ клеток. В некоторых аспектах, желательная доза представляет собой желательное количество клеток из подтипа или популяции, или желательное количество таких клеток на единицу массы тела субъекта, которому вводят клетки, например, клеток/кг. В некоторых аспектах, желательная доза представляет собой или превышает минимальное количество клеток из популяции или подтипа, или минимальное количество клеток из популяции или подтипа на единицу массы тела.
[0405] Таким образом, в некоторых вариантах осуществления, дозирование основано на желательной фиксированной дозе тотальных клеток и желательном соотношении, и/или основано на желательной фиксированной дозе одного или нескольких, например, каждого, из индивидуальных подтипов или субпопуляций. Таким образом, в некоторых вариантах осуществления, дозирование основано на желательной фиксированной или минимальной дозе T-клеток и желательном соотношении CD4+ и CD8+ клеток, и/или основано на желательной фиксированной или минимальной дозе CD4+ и/или CD8+ клеток.
[0406] В конкретных вариантах осуществления, клетки или индивидуальные популяции подтипов клеток вводят субъекту в диапазоне от приблизительно одного миллиона до приблизительно 100 миллиардов клеток, например, таком как от 1 миллиона до приблизительно 50 миллиардов клеток (например, приблизительно 5 миллионов клеток, приблизительно 25 миллионов клеток, приблизительно 500 миллионов клеток, приблизительно 1 миллиард клеток, приблизительно 5 миллиардов клеток, приблизительно 20 миллиардов клеток, приблизительно 30 миллиардов клеток, приблизительно 40 миллиардов клеток, или в диапазоне, определяемом любыми двумя из предшествующих значений), например, от приблизительно 10 миллионов до приблизительно 100 миллиардов клеток (например, приблизительно 20 миллионов клеток, приблизительно 30 миллионов клеток, приблизительно 40 миллионов клеток, приблизительно 60 миллионов клеток, приблизительно 70 миллионов клеток, приблизительно 80 миллионов клеток, приблизительно 90 миллионов клеток, приблизительно 10 миллиардов клеток, приблизительно 25 миллиардов клеток, приблизительно 50 миллиардов клеток, приблизительно 75 миллиардов клеток, приблизительно 90 миллиардов клеток, или в диапазоне, определяемом любыми двумя из предшествующих значений), и в некоторых случаях, от приблизительно 100 миллионов клеток до приблизительно 50 миллиардов клеток (например, приблизительно 120 миллионов клеток, приблизительно 250 миллионов клеток, приблизительно 350 миллионов клеток, приблизительно 450 миллионов клеток, приблизительно 650 миллионов клеток, приблизительно 800 миллионов клеток, приблизительно 900 миллионов клеток, приблизительно 3 миллиарда клеток, приблизительно 30 миллиардов клеток, приблизительно 45 миллиардов клеток) или в любом количестве в пределах этих диапазонов.
[0407] В некоторых вариантах осуществления, доза тотальных клеток и/или доза индивидуальных субпопуляций клеток находится в пределах диапазона между точно или приблизительно 104 и точно или приблизительно 109 клеток/килограмм (кг) массы тела, например, между 105 и 106 клеток/кг массы тела, например, точно или приблизительно 1×105 клеток/кг, 1,5×105 клеток/кг, 2×105 клеток/кг или 1×106 клеток/кг массы тела. Например, в некоторых вариантах осуществления, клетки вводят при, или в пределах определенного диапазона ошибки, между точно или приблизительно 104 и точно или приблизительно 109 T-клеток/килограмм (кг) массы тела, например, между 105 и 106 T-клеток/кг массы тела, например, точно или приблизительно 1×105 T-клеток/кг, 1,5×105 T-клеток/кг, 2×105 T-клеток/кг, или 1×106 T-клеток/кг массы тела.
[0408] В некоторых вариантах осуществления, клетки вводят при или в пределах определенного диапазона ошибки между точно или приблизительно 104 и точно или приблизительно 109 CD4+ и/или CD8+ клеток/килограмм (кг) массы тела, например, между 105 и 106 CD4+ и/или CD8+клеток/кг массы тела, например, точно или приблизительно 1×105 CD4+ и/или CD8+ клеток/кг, 1,5×105 CD4+ и/или CD8+ клеток/кг, 2×105 CD4+ и/или CD8+ клеток/кг, или 1×106 CD4+ и/или CD8+ клеток/кг массы тела.
[0409] В некоторых вариантах осуществления, клетки вводят при, или в пределах определенного диапазона ошибки, более чем и/или по меньшей мере приблизительно 1×106, приблизительно 2,5×106, приблизительно 5×106, приблизительно 7,5×106, или приблизительно 9×106 CD4+ клеток, и/или по меньшей мере приблизительно 1×106, приблизительно 2,5×106, приблизительно 5×106, приблизительно 7,5×106, или приблизительно 9×106 CD8+ клетки, и/или по меньшей мере приблизительно 1×106, приблизительно 2,5×106, приблизительно 5×106, приблизительно 7,5×106, или приблизительно 9×106 T-клеток. В некоторых вариантах осуществления, клетки вводят при, или в пределах определенного диапазона ошибки, между приблизительно 108 и 1012 или между приблизительно 1010 и 1011 T-клеток, между приблизительно 108 и 1012 или между приблизительно 1010 и 1011 CD4+ клеток, и/или между приблизительно 108 и 1012 или между приблизительно 1010 и 1011 CD8+ клеток.
[0410] В некоторых вариантах осуществления, клетки вводят в желательном соотношении на выходе или в пределах переносимого диапазона желательного соотношения на выходе множества популяций или подтипов клеток, таких как клетки или подтипы CD4+ и CD8+. В некоторых аспектах, желательное соотношение может представлять собой конкретное соотношение или может представлять собой диапазон соотношений. Например, в некоторых вариантах осуществления, желательное соотношение (например, соотношение CD4+ и CD8+ клеток) составляет между точно или приблизительно 1:5 и точно или приблизительно 5:1 (или более чем приблизительно 1:5 и менее чем приблизительно 5:1), или между точно или приблизительно 1:3 и точно или приблизительно 3:1 (или более чем приблизительно 1:3 и менее чем приблизительно 3:1), например, между точно или приблизительно 2:1 и точно или приблизительно 1:5 (или более чем приблизительно 1:5 и менее чем приблизительно 2:1, например, точно или приблизительно 5:1, 4,5:1, 4:1, 3,5:1, 3:1, 2,5:1, 2:1, 1,9:1, 1,8:1, 1,7:1, 1,6:1, 1,5:1, 1,4:1, 1,3:1, 1,2:1, 1,1:1, 1:1, 1:1,1, 1:1,2, 1:1,3, 1:1,4, 1:1,5, 1:1,6, 1:1,7, 1:1,8, 1:1,9: 1:2, 1:2,5, 1:3, 1:3,5, 1:4, 1:4,5, или 1:5. В некоторых аспектах, переносимое различие находится в пределах приблизительно 1%, приблизительно 2%, приблизительно 3%, приблизительно 4% приблизительно 5%, приблизительно 10%, приблизительно 15%, приблизительно 20%, приблизительно 25%, приблизительно 30%, приблизительно 35%, приблизительно 40%, приблизительно 45%, приблизительно 50% от желательного соотношения, включая любое количество в пределах этих диапазонов.
[0411] Для предотвращения или лечения заболеваний, соответствующая доза может зависеть от типа заболеваний, подлежащих лечению, типа клеток или рекомбинантных рецепторов, тяжести и течения заболевания, того, вводят ли клетки для профилактических или терапевтических целей, предшествующей терапии, анамнеза субъекта и ответа на клетки, и решения лечащего терапевта. Композиции и клетки, в некоторых вариантах осуществления, подходящим образом вводят субъекту за один раз или на протяжении серий обработок.
[0412] Клетки можно вводить любыми пригодными способами, например, посредством болюсной инфузии, посредством инъекции, например, внутривенной или подкожной инъекций, внутриглазной инъекции, периокулярной инъекции, субретинальной инъекции, инъекции в стекловидное тело, инъекции посредством прокола перегородки, субсклеральной инъекции, интрахороидальной инъекции, интракамеральной инъекции, субконъюнктивальной инъекции, инъекции в субтеноново пространство, ретробульбарной инъекции, перибульбарной инъекции или задней околосклеральной доставки. В некоторых вариантах осуществления, их вводят посредством парентерального, внутрилегочного и интраназального, и, если желательно для местного лечения, внутриочагового введения. Парентеральные инфузии включают внутримышечное, внутривенное, внутриартериальное, внутрибрюшинное или подкожное введение. В некоторых вариантах осуществления, данную дозу вводят посредством однократного болюсного введения клеток. В некоторых вариантах осуществления, ее вводят посредством множества болюсных введений клеток, например, в течение периода не более чем 3 суток, или посредством введения клеток непрерывной инфузией.
[0413] В некоторых вариантах осуществления, клетки вводят в качестве части комбинированного лечения, например, одновременно или последовательно, в любом порядке, с другим терапевтическим вмешательством, например, с антителом или модифицированной клеткой или рецептором, или средством, таким как цитотоксическое или лекарственное средство. Клетки, в некоторых вариантах осуществления, вводят совместно с одним или несколькими дополнительными лекарственными средствами или в сочетании с другим терапевтическим вмешательством, либо одновременно, либо последовательно, в любом порядке. В некоторых контекстах, клетки вводят совместно с другой терапией, достаточно близко по времени, таким образом, что популяции клеток усиливают эффект одного или нескольких дополнительных лекарственных средств, или наоборот. В некоторых вариантах осуществления, клетки вводят перед одним или несколькими дополнительными лекарственными средствами. В некоторых вариантах осуществления, клетки вводят после одного или нескольких дополнительных лекарственных средств. В некоторых вариантах осуществления, одно или несколько дополнительных средств включают цитокин, такой как IL-2, например, для улучшения персистенции. В некоторых вариантах осуществления, способы включают введение химиотерапевтического средства.
[0414] После введения клеток, биологическую активность модифицированных популяций клеток в некоторых вариантах осуществления, измеряют, например, посредством любого из ряда известных способов. Параметры для оценки включают специфическое связывание модифицированной или природной T-клетки или другого иммуноцита с антигеном, in vivo, например, посредством визуализации, или ex vivo, например, посредством ELISA или проточной цитометрии. В конкретных вариантах осуществления, способность модифицированных клеток разрушать клетки-мишени можно измерять с использованием любого пригодного способа, известного в данной области, такого как анализы цитотоксичности, описанные, например, в Kochenderfer et al., J. Immunotherapy, 32(7): 689-702 (2009), и Herman et al. J. Immunological Methods, 285(1): 25-40 (2004). В конкретных вариантах осуществления, биологическую активность клеток измеряют посредством анализа экспрессии и/или секреции одного или нескольких цитокинов, таких как CD 107a, IFNγ, IL-2 и TNF. В некоторых аспектах, биологическую активность измеряют посредством оценки клинического исхода, такого как уменьшение опухолевой нагрузки или массы.
[0415] В конкретных вариантах осуществления, модифицированные клетки дополнительно модифицируют любым количеством способов, так что их терапевтическая или профилактическая эффективность увеличивается. Например, сконструированный CAR или TCR, экспрессированный в популяции, можно конъюгировать, либо напрямую, либо опосредованно через линкер, с нацеливающей группой. Практическое осуществление конъюгации соединений, например, CAR или TCR, с нацеливающими группами известны в данной области. См., например, Wadwa et al., J. Drug Targeting 3: 1 1 1 (1995) и Патент США 5087616.
ПРИМЕРЫ
[0416] Следующие примеры являются только иллюстративными и не предназначены для ограничения объема или содержания изобретения никаким образом.
Пример 1 -Начальный скриниг нРНК.
[0417] Направляющие РНК подвергали скринингу посредством образования комплексов коммерчески синтезированных нРНК с Cas9 in vitro и доставки рибонуклеопротеина (RNP) нРНК/Cas9 в клетки посредством электропорации.
[0418] На фиг. 1 показан % частоты инделов для тестированных нРНК. На фиг. 2 показана эффективность редактирования генома для конкретных иллюстративных пар нРНК.
Пример 2 - Анализ нРНК-кандидатов против TGFBR2 в T-клетках.
[0419] Целью редактирования клеток посредством CRISPR-Cas9 является достижение наиболее высокого процента нокаута гена-мишени с использованием наиболее низкой возможной концентрации комплекса нРНК/Cas9 и наиболее низким количеством событий неспецифического связывания. Для определения наилучших возможных нРНК-кандидатов для редактирования гена TGFBR2, тестировали семь потенциальных нРНК. T-клетки трансфицировали с использованием RNP нРНК/Cas9 в различных концентрациях. Заем процент частоты инделов определяли с использованием анализа Illumina miSeq. Результаты показывают частоту % инделов для различных нРНК, лежащую в диапазоне от 20% до 80%, где все нРНК достигали самого высокого % частоты инделов при концентрации RNP 2 мкМ (фиг. 3). Концентрацию RNP 2 мкМ затем использовали для всех экспериментов.
[0420] Отобранные нРНК из анализа miSeq выбирали для дальнейшего анализа в T-клетках с BCMA CAR. нРНК из SEQ ID No: 5050, 5052, 5093 и 5043 использовали в анализе повторного разрезания RNP для определения % редактирования гена TGFBR2. Тестировали также способ двойной нРНК с использованием комбинации из SEQ ID NO5043/5093. В то время как для индивидуальных нРНК из SEQ ID NO: 5043 и 5093 достигали только 20-40% редактирования, обнаружено, что комбинация является более эффективной, с получением значения % редактирования приблизительно 80% (фиг. 4A).
[0421] Высокопроизводительный анализ секвенирования проводили для отобранных нРНК для определения % частоты инделов. Тестировали нРНК из SEQ ID NO: a и b, и двойную комбинацию нРНК c/d. Примечательно, что частот % инделов, настолько высоких, как 95%, достигали для отобранных нРНК (фиг. 4B).
[0422] В то время как % частоты инделов является полезным показателем эффективности нРНК, некоторая часть полученных инделов могут представлять собой вставки или делеции в рамке считывания. Такие инделы в рамке считывания могут приводить к образованию модифицированного гена, белковый продукт которого сохраняет некоторую активность. При попытке получения нокаута гена, инделы вне рамки считывания являются предпочтительными. Чтобы убиться, что тестированные нРНК, фактически, являлись образующими желательные инделы вне рамки считывания, результаты секвенирования анализировали по специфическим типам образованных инделов. Результаты показывают, что в то время как для SEQ ID NO: 5052 получен самый высокий % частоты инделов, для SEQ ID NO: 5050 получен более высокий % частоты инделов вне рамки считывания (фиг. 5).
Пример 3 - Эффективность редактирования генов in vitro в первичных и модифицированных T-клетках.
[0423] Эффекты ингибирования TGFβ анализировали в первичных T-клетках, модифицированных для экспрессии нацеленного на BCMA CAR. T-клетки с CAR против BCMA, кроме того, модифицировали для наличия гена TGFBR2, редактированного посредством системы CRISPR-Cas9 с использованием выбранных нРНК. Контроль AAVS1 для редактирования генов и экспрессирующие T-клетки с CAR против BCMA с нередактированным геном TGFBR2 использовали в качестве контроля. Линии клеток культивировали совместно с линией клеток множественной миеломы RPMI 8226 в присутствии или в отсутствие 10 нг/мл TGFβ. В присутствии избытка TGFβ, для первичных T-клеток и T-клеток с CAR против BCMA показаны ожидаемые ингибирующие эффекты уменьшенной продукции интерферона-гамма (IFNγ). Однако, в подвергнутых редактированию генов T-клетках с CAR против BCMA, эффекты ингибирования TGFβ восстанавливают, восстанавливая уровни продукции IFNγ до уровней, обнаруженных без добавления TGFβ (фиг. 6).
[0424] Ингибирование пролиферации T-клетки является одним из эффектов, вызванных передачей сигналов TGFβ (Tiemessen et al. Int. Immunol. 15:1495-1504. 2003). Для оценки эффектов передачи сигналов TGFβ на пролиферацию клетки, пролиферацию T-клетки с CAR против BCMA мониторировали на фоне редактирования гена TGFBR2- с использованием нескольких нРНК. После редактирования гена TGFBR2, T-клетки с CAR против BCMA являлись способными к пролиферации в присутствии избытка TGFβ (фиг. 7).
[0425] На активность T-клетки влияет экспрессия различных стимулирующих и ингибирующих рецепторов. Экспрессию CD25 оценивали в подвергнутых редактированию гена TGFBR2 T-клетках с CAR против BCMA. Редактирование гена TGFBR2 приводит к более высоким уровням экспрессии CD25, по сравнению с контрольными клетками, при подвергании воздействию TGFβ (фиг. 8A). Экспрессию ингибирующего рецептора, PD-1, также оценивали посредством измерения % PD-1+ клеток в присутствии и в отсутствие избытка TGFβ. Для подвергнутых редактированию гена TGFBR2 T-клеток с CAR против BCMA показано более низкое увеличение уровня PD-1 относительно контрольных клеток. Неожиданно, редактирование генов клеток также приводило к меньшему количеству PD-1+ клеток даже без добавления TGFβ (фиг. 8B).
[0426] Активация пути передачи сигнала TGFβ приводит к фосфорилированию комплекса Smad 2/3, которое, в свою очередь, регулирует множество нижестоящих процессов пути передачи сигнала TGFβ. По этой причине, фосфорилированный Smad 2/3 часто используют в качестве показателя передачи сигнала TGFβ в клетках. Фосфо-Smad2/3 детектировали в T-клетках, трансдуцированных для экспрессии различных CAR, в присутствии или в отсутствие редактирования гена TGFBR2. Экспрессирующие CAR T-клетки, включая контроль редактирования гена AAVS1, в присутствии (10 нг/мл) или в отсутствие TGFβ, использовали в качестве контроля. В то время как избыток TGFβ приводил к ожидаемому увеличению фосфорилирования Smad 2/3 в нередактированных клетках, подвергнутые редактированию гена TGFBR2 клетки сохраняли одинаковый уровень фосфорилирования Smad 2/3 в присутствии и в отсутствие добавления TGFβ (фиг. 9). Результаты показывают, что способ редактирования гена TGFBR2 посредством CRISPR является эффективным для выключения пути передачи сигнала TGFβ.
[0427] Для дополнительного анализа эффектов редактирования гена TGFBR2 на различном фоне T-клеток с CAR, уровни GzmB детектировали в присутствии и в отсутствие TGFβ. Экспрессирующие CAR T-клетки, включая контроль редактирования гена AAVS1, в присутствии (10 нг/мл) или в отсутствие TGFβ, использовали в качестве контроля. Результаты внутриклеточного окрашивания GzmB выявили, что редактирование гена TGFBR2 поддерживает экспрессию GzmB в присутствии TGFβ (фиг. 10).
[0428] Продукцию IFNγ анализировали в эксперименте, подобном описанному на фиг. 10, с использованием анализа детекции цитокинов. В соответствии с предшествующими результатами для экспрессии GzmB, продукция IFNγ сохранялась и даже увеличивалась на фоне редактирования гена TGFBR2, по сравнению с контролем, в условиях избытка TGFβ (фиг. 11).
[0429] Пролиферацию клеток анализировали в эксперименте, подобном описанному на фиг. 10 и фиг. 11, с использованием анализа Edu Click-It от ThermoFisher. Пролиферация клеток сохранялась на фоне редактирования гена TGFBR2, по сравнению с контролем в условиях избытка TGFβ (фиг. 12).
[0430] Совокупные результаты из примера 3 показывают преимущества использования системы редактирования генов CRISPR-Cas9 для редактирования гена TGFBR2. С использованием способа одиночной и двойной нРНК, путь передачи сигнала TGFβ можно эффективно супрессировать на фоне T-клетки с CAR.
Пример 4 - Сравнение способа доминантно-негативного TGFBR2 и способа редактирования генов посредством CRISPR-Cas9.
[0431] Альтернативным способом прекращения передачи сигнала TGFβ является экспрессия доминантно-негативной формы TGFBR2 (DN). Этот вариант TGFBR2 конкурирует с TGFBR2 дикого типа за связывание с TGFβ, таким образом, минимизируя эффективный ответ передачи сигнала.
[0432] Эффекты ингибирования TGFβ анализировали в первичных T-клетках, трансдуцированных для экспрессии CAR против BCMA. Экспрессирующие T-клетки с CAR против BCMA дополнительно модифицировали для экспрессии DN или для редактирования гена TGFBR2 посредством системы CRISPR-Cas9. Редактированные посредством CRISPR-Cas9 клетки редактировали с использованием двойной нРНК из SEQ ID No: 5043 и 5093. Контроль AAVS1 для редактирования генов, экспрессирующие CAR против BCMA T-клетки с нередактированным геном TGFBR2 и экспрессирующие CAR против BCMA T-клетки, включая контроль редактирования гена AAVS1, использовали в качестве контроля. Линии клеток культивировали совместно с линией клеток множественной миеломы RPMI 8226 в присутствии или в отсутствие 10 нг/мл TGFβ. В присутствии избытка TGFβ, для первичных T-клеток и T-клеток с CAR против BCMA показаны ожидаемые ингибирующие эффекты уменьшения продукции GzmB (фиг. 13A) и IFNγ (фиг. 13B). Однако, в редактированных посредством DN или CRISPR T-клетках с CAR против BCMA, эффекты ингибирования TGFβ восстанавливают, восстанавливая продукцию GzmB и IFNγ до уровней, обнаруженных без добавления TGFβ.
[0433] Чтобы дополнительно показать полезность восстановления эффектов ингибирования передачи сигналов TGFβ, T-клетки с CAR против BCMA на фоне редактирования DN или CRISPR анализировали по их активности уничтожения. Экспрессирующие CAR против BCMA T-клетки с нередактированным геном TGFBR2 использовали в качестве контроля. T-клетки с CAR против BCMA культивировали совместно с клетками RPMI 8226 в соотношении 1 T-клетка с CAR против BCMA на 4 клетки RPMI, в присутствии или в отсутствие 10 нг/мл TGFβ. Литическая активность T-клеток с CAR против BCMA сохранялась на фоне как DN, так и редактирования CRISPR, в присутствии TGFβ. Неожиданно, для подвергнутых редактированию посредством CRISPR T-клеток с CAR против BCMA показана превосходная литическая активность, по сравнению с DN клетками (фиг. 14). Литическая активность подвергнутых редактированию посредством CRISPR T-клеток с CAR против BCMA была выше, чем в контрольных клетках, даже без добавления избытка TGFβ.
[0434] Повторяющаяся стимуляция антигеном T-клеток, включая T-клетки с CAR, приводит к уменьшенной персистенции T-клеток и может вызывать индуцированную активацией гибель клеток (AICD) (Gargett et al. Mol. Ther. 24: 1135-1149. 2016). Способы сохранения активности T-клеток против специфического антигена имеют большую важность для улучшения эффективности видов терапии на основе T-клеток. T-клетки с CAR против BCMA на фоне DN или редактирования CRISPR анализировали по их способности к пролиферации в присутствии повторяющейся стимуляции с использованием TGFβ. Экспрессирующие CAR против BCMA T-клетки с нередактированным геном TGFBR2 использовали в качестве контроля. В то время как немодифицированные T-клетки с CAR против BCMA не подвергались пролиферации в течение множества суток стимуляции TGFβ, клетки с TGBR2 DN или редактированием посредством CRISPR-продолжали пролиферацию с течением времени в присутствии TGFβ (фиг. 15A - фиг. 15C). Процент T-клеток с CAR против BCMA также не уменьшался во время повторной стимуляции с использованием TGFβ (фиг. 15D - фиг. 15F).
[0435] Продукцию IFNγ снова анализировали на фоне DN и редактирования генов с использованием способа одиночной, а не двойной, нРНК. Дополнительную линию клеток множественной миеломы, OPM2, использовали для сравнения с использованной ранее линией клеток RPMI 8226, как описано на фиг. 13. В соответствии с предшествующими результатами, ингибирование передачи сигнала TGFβ эффективно сохраняло продукцию IFNγ в присутствии избытка TGFβ. Это было справедливым для обеих линий клеток RPMI (фиг. 16A) и OPM2 (фиг. 16B).
[0436] Экспрессию CD25 анализировали также на фоне DN и редактирования генов с использованием способа одиночной нРНК. Экспрессия CD25 сохранялась в присутствии избытка TGFβ в линиях клеток RPMI (фиг. 17A) и OPM2 (фиг. 17B). Неожиданно, экспрессия CD25 в клетках с DN и редактированием генов являлась увеличенной, по сравнению с немодифицированными T-клетками.
[0437] Экспрессию PD-1 сходным образом детектировали на фоне DN и редактирования генов. Репрессия передачи сигналов TGFβ с использованием любого способа эффективно предотвращала увеличение экспрессии PD-1 в присутствии избытка TGFβ (фиг. 18A и 18B).
[0438] В предшествующих экспериментах использовали TGFβ в установленной дозе 10 нг/мл для стимуляции. Для лучшего понимания того, каким образом редактирование гена TGFBR2 влияет на передачу сигналов TGFβ в физиологических условиях, использовали диапазон 0-100 нг/мл TGFβ. Этот диапазон основан на предшествующей работе, показывающей, что уровни TGFβ в сыворотке лежат в диапазоне приблизительно от 3 до 88 нг/мл (Aref et al. Hematological Oncology. 35: 51-57. 2017) и приблизительно от 3 до 10 нг/мл в костном мозге при множественной миеломе (Bruns et al. Blood. 120: 2620-2630. 2012). Анализ пролиферации клеток использовали для определения относительной кратности размножения клеток на фоне DN и редактирования генов. T-клетки с CAR против BCMA культивировали совместно с клетками RPMI 8226 в соотношении 1:1. Неожиданно, положительные эффекты на пролиферацию клеток можно наблюдать в концентрациях, настолько низких, как 0,1 нг/мл TGFβ, намного ниже физиологических уровней в нормальных условиях или в условиях злокачественной опухоли (фиг. 19A). Эта способность отвечать дополнительно показана по увеличенной продукции IFNγ (фиг. 19B).
[0439] Такой же диапазон концентраций TGFβ использовали для анализа экспрессии PD-1 на CD4+ и CD8+ T-клетках с CAR. И снова, фон DN TGFBR2 и редактирования генов являлись способными поддерживать низкие уровни экспрессии PD-1, настолько низкие, как при 0,1 нг/мл TGFβ (фиг. 20A и 20B).
[0440] Способ DN TGFBR2 использовали для оценки пролиферации клеток, экспрессии гранзима B и фосфорилирования Smad 2/3 в T-клетках, трансдуцированных для экспрессии трех различных CAR. DN TGFBR2 являлся способным к освобождению от антипролиферативных эффектов избытка TGFβ на фоне тестированных T-клеток с CAR. DN являлся способным поддерживать экспрессию гранзима B в присутствии избытка TGFβ на фоне тестированных T-клеток с CAR. Наконец, DN являлся способным эффективно супрессировать передачу сигналов TGFβ в присутствии избытка TGFβ, как измерено посредством уменьшенного фосфорилирования Smad 2/3 на фоне тестированных T-клеток с CAR (фиг. 22). Показаны данные только для одного из трех фонов T-клеток с CAR, однако, сходные результаты наблюдали также на фоне двух других T-клеток с CAR.
Пример 5 - Получение профиля транскрипции T-клеток с CAR против BCMA in vivo .
[0441] Чтобы для способа редактирования гена TGFBR2, описанного в настоящем описании, получить эффективную терапию, иммуносупрессивный путь TGFβ должен присутствовать в условиях in vivo. Если указанный иммуносупрессивный путь TGFβ присутствует, тогда способ редактирования гена TGFBR2 должен эффективно освобождать T-клетки от иммуносупрессивных эффектов TGFβ. Для решения обеих этих проблем, получение профилей транскрипции T-клеток с CAR против BCMA проводили для T-клеток с CAR против BCMA, выделенных из микроокружения опухолей у мышей. Модель ксенотрансплантата опухоли получали посредством имплантации мышам клеток множественной миеломы RPMI 8226 и обеспечения размножения/образования опухоли в течение 21 суток. После 21-суточного инкубационного периода, T-клетки с CAR против BCMA на фоне дикого типа, контроля редактирования гена AAVS, DN TGFBR2, или редактирования гена TGFBR2 инъецировали несущим опухоль мышам. Позволяли регрессию опухоли в течение 14 суток перед выделением инфильтрующих опухоль лейкоцитов (TIL) и T-клеток с CAR из опухоли и селезенки (незлокачественной отрицательной контрольной ткани). После выделения, клетки подвергали анализу RNAseq для определения профилей экспрессии генов членов пути передачи сигнала TGFβ.
[0442] Результаты получение профилей транскрипции выявили, что редактирование гена TGFBR2 в T-клетках с CAR успешно ограничивает экспрессию нескольких членов пути передачи сигнала TGFβ в опухоли, где возникает передача репрессирующих сигналов TGFβ (фиг. 21). Как показано на фиг. 21, члены пути передачи сигнала TGFβ подвержены повышающей регуляции в экспрессирующих CAR против BCMA T-клетках, выделенных из опухоли, но не из селезенки. Данные показывают, что экспрессирующие CAR против BCMA T-клетки подвергаются воздействию обогащенного TGFβ микроокружения опухолей (TME). Кроме того, экспрессирующие CAR против BCMA T-клетки на фоне DN TGFBR2 или редактирования гена TGFBR2, обращают повышающую регуляцию членов пути передачи сигнала TGFβ. Данные показывают, что путь передачи сигнала TGFβ эффективно прекращен.
Пример 6 - Избирательное преимущество способа редактирования гена TGFBR2.
[0443] Для определения того, имеют ли T-клетки с CAR после редактирования гена TGFBR2 преимущество избирательной пролиферации, T-клетки с CAR против BCMA подвергали редактированию генов для получения различного % частоты инделов. Эти отдельные по % инделов популяции T-клеток с CAR культивировали совместно с клетками RPMI 8226 в соотношении 1:1 для стимуляции, в присутствии или в отсутствие 10 нг/мл TGFβ. Клетки оценивали, с использованием высокопроизводительного секвенирования, приблизительно каждые 7 суток для определения того, какая часть клеток подвергнута редактированию генов, и какая часть все еще представляет собой дикий тип (фиг. 23). Клетки повторно стимулировали с использованием свежих клеток RPMI и повторно доводили до соотношения 1:1 еженедельно. Результаты показывают, что редактирование гена TGFBR2 обеспечивает преимущество избирательной пролиферации, по сравнению с клетками дикого типа в иммуностимулирующем окружении (см. фиг. 24).
ВКЛЮЧЕНИЕ В КАЧЕСТВЕ ССЫЛКИ
[0444] Полное содержание всех публикаций, патентов и патентных заявок, упомянутых в настоящем описании, таким образом, приведено в качестве ссылки, как если бы было конкретно и индивидуально указано, что содержание каждой индивидуальной публикации, патента или патентной заявки приведено в качестве ссылки. В случае несоответствия, настоящая заявка, включая любые определения в настоящем описании, имеет преимущество.
ЭКВИВАЛЕНТЫ
[0445] Специалисту в данной области известны, или он способен установить с использованием не более, чем общепринятых экспериментов, множество эквивалентов конкретных вариантов осуществления, описанных в настоящем описании. Такие эквиваленты предназначены для включения в следующую формулу изобретения.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> EDITAS MEDICINE, INC.
JUNO THERAPEUTICS, INC.
<120> СПОСОБЫ, КОМПОЗИЦИИ И КОМПОНЕНТЫ ДЛЯ РЕДАКТИРОВАНИЯ TGFBR2
ПОСРЕДСТВОМ CRISPR-CAS9 В T-КЛЕТКАХ ДЛЯ ИММУНОТЕРАПИИ
<130> 606890: EDT9-002PC
<140> PCT/US2018/058635
<141> 2018-11-01
<150> 62/580320
<151> 2017-11-01
<160> 5102
<170> PatentIn версии 3.5
<210> 1
<211> 169
<212> ДНК
<213> Неизвестно
<220>
<221> источник
<223> /примечание=«Описание неизвестного:
последовательность экзона 3 TGFBR2»
<400> 1
ttaataacga catgatagtc actgacaaca acggtgcagt caagtttcca caactgtgta
60
aattttgtga tgtgagattt tccacctgtg acaaccagaa atcctgcatg agcaactgca
120
gcatcacctc catctgtgag aagccacagg aagtctgtgt ggctgtatg
169
<210> 2
<211> 191
<212> ДНК
<213> Неизвестно
<220>
<221> источник
<223> /примечание=«Описание неизвестного
последовательность экзона 4 TGFBR2»
<400> 2
gagaaagaat gacgagaaca taacactaga gacagtttgc catgacccca agctccccta
60
ccatgacttt attctggaag atgctgcttc tccaaagtgc attatgaagg aaaaaaaaaa
120
gcctggtgag actttcttca tgtgttcctg tagctctgat gagtgcaatg acaacatcat
180
cttctcagaa g
191
<210> 3
<211> 800
<212> ДНК
<213> Неизвестно
<220>
<221> источник
<223> /примечание=«Описание неизвестного
последовательность экзона 5 TGFBR2»
<400> 3
aatataacac cagcaatcct gacttgttgc tagtcatatt tcaagtgaca ggcatcagcc
60
tcctgccacc actgggagtt gccatatctg tcatcatcat cttctactgc taccgcgtta
120
accggcagca gaagctgagt tcaacctggg aaaccggcaa gacgcggaag ctcatggagt
180
tcagcgagca ctgtgccatc atcctggaag atgaccgctc tgacatcagc tccacgtgtg
240
ccaacaacat caaccacaac acagagctgc tgcccattga gctggacacc ctggtgggga
300
aaggtcgctt tgctgaggtc tataaggcca agctgaagca gaacacttca gagcagtttg
360
agacagtggc agtcaagatc tttccctatg aggagtatgc ctcttggaag acagagaagg
420
acatcttctc agacatcaat ctgaagcatg agaacatact ccagttcctg acggctgagg
480
agcggaagac ggagttgggg aaacaatact ggctgatcac cgccttccac gccaagggca
540
acctacagga gtacctgacg cggcatgtca tcagctggga ggacctgcgc aagctgggca
600
gctccctcgc ccgggggatt gctcacctcc acagtgatca cactccatgt gggaggccca
660
agatgcccat cgtgcacagg gacctcaaga gctccaatat cctcgtgaag aacgacctaa
720
cctgctgcct gtgtgacttt gggctttccc tgcgtctgga ccctactctg tctgtggatg
780
acctggctaa cagtgggcag
800
<210> 4
<211> 20
<212> ДНК
<213> Неизвестно
<220>
<221> источник
<223> /примечание=«Описание неизвестного
последовательность-мишень TGFBR2»
<400> 4
gtagctctga tgagtgcaat
20
<210> 5
<211> 20
<212> ДНК
<213> Неизвестно
<220>
<221> источник
<223> /примечание=«Описание неизвестного
последовательность-мишень TGFBR2»
<400> 5
atgaatctct tcactctagg
20
<210> 6
<211> 20
<212> ДНК
<213> Неизвестно
<220>
<221> источник
<223> /примечание=«Описание неизвестного
последовательность-мишень TGFBR2»
<400> 6
acaggagtac ctgacgcggc
20
<210> 7
<211> 20
<212> ДНК
<213> Неизвестно
<220>
<221> источник
<223> /примечание=«Описание неизвестного
последовательность-мишень TGFBR2»
<400> 7
ctgttagcca ggtcatccac
20
<210> 8
<211> 20
<212> ДНК
<213> Неизвестно
<220>
<221> источник
<223> /примечание=«Описание неизвестного
последовательность-мишень TGFBR2»
<400> 8
gggtgtccag ctcaatgggc
20
<210> 9
<211> 20
<212> ДНК
<213> Неизвестно
<220>
<221> источник
<223> /примечание=«Описание неизвестного
последовательность-мишень TGFBR2»
<400> 9
tcataatgca ctttggagaa
20
<210> 10
<211> 20
<212> ДНК
<213> Неизвестно
<220>
<221> источник
<223> /примечание=«Описание неизвестного
последовательность-мишень TGFBR2»
<400> 10
tgactttatt ctggaagatg
20
<210> 11
<400> 11
000
<210> 12
<400> 12
000
<210> 13
<400> 13
000
<210> 14
<400> 14
000
<210> 15
<400> 15
000
<210> 16
<400> 16
000
<210> 17
<400> 17
000
<210> 18
<400> 18
000
<210> 19
<400> 19
000
<210> 20
<400> 20
000
<210> 21
<400> 21
000
<210> 22
<400> 22
000
<210> 23
<400> 23
000
<210> 24
<400> 24
000
<210> 25
<400> 25
000
<210> 26
<400> 26
000
<210> 27
<400> 27
000
<210> 28
<400> 28
000
<210> 29
<400> 29
000
<210> 30
<400> 30
000
<210> 31
<400> 31
000
<210> 32
<400> 32
000
<210> 33
<400> 33
000
<210> 34
<400> 34
000
<210> 35
<400> 35
000
<210> 36
<400> 36
000
<210> 37
<400> 37
000
<210> 38
<400> 38
000
<210> 39
<400> 39
000
<210> 40
<400> 40
000
<210> 41
<400> 41
000
<210> 42
<400> 42
000
<210> 43
<400> 43
000
<210> 44
<400> 44
000
<210> 45
<400> 45
000
<210> 46
<400> 46
000
<210> 47
<400> 47
000
<210> 48
<400> 48
000
<210> 49
<400> 49
000
<210> 50
<400> 50
000
<210> 51
<400> 51
000
<210> 52
<400> 52
000
<210> 53
<400> 53
000
<210> 54
<400> 54
000
<210> 55
<400> 55
000
<210> 56
<400> 56
000
<210> 57
<400> 57
000
<210> 58
<400> 58
000
<210> 59
<400> 59
000
<210> 60
<400> 60
000
<210> 61
<400> 61
000
<210> 62
<400> 62
000
<210> 63
<400> 63
000
<210> 64
<400> 64
000
<210> 65
<400> 65
000
<210> 66
<400> 66
000
<210> 67
<400> 67
000
<210> 68
<400> 68
000
<210> 69
<400> 69
000
<210> 70
<400> 70
000
<210> 71
<400> 71
000
<210> 72
<400> 72
000
<210> 73
<400> 73
000
<210> 74
<400> 74
000
<210> 75
<400> 75
000
<210> 76
<400> 76
000
<210> 77
<400> 77
000
<210> 78
<400> 78
000
<210> 79
<400> 79
000
<210> 80
<400> 80
000
<210> 81
<400> 81
000
<210> 82
<400> 82
000
<210> 83
<400> 83
000
<210> 84
<400> 84
000
<210> 85
<400> 85
000
<210> 86
<400> 86
000
<210> 87
<400> 87
000
<210> 88
<400> 88
000
<210> 89
<400> 89
000
<210> 90
<400> 90
000
<210> 91
<400> 91
000
<210> 92
<400> 92
000
<210> 93
<400> 93
000
<210> 94
<400> 94
000
<210> 95
<400> 95
000
<210> 96
<400> 96
000
<210> 97
<400> 97
000
<210> 98
<400> 98
000
<210> 99
<400> 99
000
<210> 100
<400> 100
000
<210> 101
<400> 101
000
<210> 102
<400> 102
000
<210> 103
<400> 103
000
<210> 104
<400> 104
000
<210> 105
<400> 105
000
<210> 106
<400> 106
000
<210> 107
<400> 107
000
<210> 108
<400> 108
000
<210> 109
<400> 109
000
<210> 110
<400> 110
000
<210> 111
<400> 111
000
<210> 112
<400> 112
000
<210> 113
<400> 113
000
<210> 114
<400> 114
000
<210> 115
<400> 115
000
<210> 116
<400> 116
000
<210> 117
<400> 117
000
<210> 118
<400> 118
000
<210> 119
<400> 119
000
<210> 120
<400> 120
000
<210> 121
<400> 121
000
<210> 122
<400> 122
000
<210> 123
<400> 123
000
<210> 124
<400> 124
000
<210> 125
<400> 125
000
<210> 126
<400> 126
000
<210> 127
<400> 127
000
<210> 128
<400> 128
000
<210> 129
<400> 129
000
<210> 130
<400> 130
000
<210> 131
<400> 131
000
<210> 132
<400> 132
000
<210> 133
<400> 133
000
<210> 134
<400> 134
000
<210> 135
<400> 135
000
<210> 136
<400> 136
000
<210> 137
<400> 137
000
<210> 138
<400> 138
000
<210> 139
<400> 139
000
<210> 140
<400> 140
000
<210> 141
<400> 141
000
<210> 142
<400> 142
000
<210> 143
<400> 143
000
<210> 144
<400> 144
000
<210> 145
<400> 145
000
<210> 146
<400> 146
000
<210> 147
<400> 147
000
<210> 148
<400> 148
000
<210> 149
<400> 149
000
<210> 150
<400> 150
000
<210> 151
<400> 151
000
<210> 152
<400> 152
000
<210> 153
<400> 153
000
<210> 154
<400> 154
000
<210> 155
<400> 155
000
<210> 156
<400> 156
000
<210> 157
<400> 157
000
<210> 158
<400> 158
000
<210> 159
<400> 159
000
<210> 160
<400> 160
000
<210> 161
<400> 161
000
<210> 162
<400> 162
000
<210> 163
<400> 163
000
<210> 164
<400> 164
000
<210> 165
<400> 165
000
<210> 166
<400> 166
000
<210> 167
<400> 167
000
<210> 168
<400> 168
000
<210> 169
<400> 169
000
<210> 170
<400> 170
000
<210> 171
<400> 171
000
<210> 172
<400> 172
000
<210> 173
<400> 173
000
<210> 174
<400> 174
000
<210> 175
<400> 175
000
<210> 176
<400> 176
000
<210> 177
<400> 177
000
<210> 178
<400> 178
000
<210> 179
<400> 179
000
<210> 180
<400> 180
000
<210> 181
<400> 181
000
<210> 182
<400> 182
000
<210> 183
<400> 183
000
<210> 184
<400> 184
000
<210> 185
<400> 185
000
<210> 186
<400> 186
000
<210> 187
<400> 187
000
<210> 188
<400> 188
000
<210> 189
<400> 189
000
<210> 190
<400> 190
000
<210> 191
<400> 191
000
<210> 192
<400> 192
000
<210> 193
<400> 193
000
<210> 194
<400> 194
000
<210> 195
<400> 195
000
<210> 196
<400> 196
000
<210> 197
<400> 197
000
<210> 198
<400> 198
000
<210> 199
<400> 199
000
<210> 200
<400> 200
000
<210> 201
<400> 201
000
<210> 202
<400> 202
000
<210> 203
<400> 203
000
<210> 204
<400> 204
000
<210> 205
<400> 205
000
<210> 206
<400> 206
000
<210> 207
<400> 207
000
<210> 208
<400> 208
000
<210> 209
<400> 209
000
<210> 210
<400> 210
000
<210> 211
<400> 211
000
<210> 212
<400> 212
000
<210> 213
<400> 213
000
<210> 214
<400> 214
000
<210> 215
<400> 215
000
<210> 216
<400> 216
000
<210> 217
<400> 217
000
<210> 218
<400> 218
000
<210> 219
<400> 219
000
<210> 220
<400> 220
000
<210> 221
<400> 221
000
<210> 222
<400> 222
000
<210> 223
<400> 223
000
<210> 224
<400> 224
000
<210> 225
<400> 225
000
<210> 226
<400> 226
000
<210> 227
<400> 227
000
<210> 228
<400> 228
000
<210> 229
<400> 229
000
<210> 230
<400> 230
000
<210> 231
<400> 231
000
<210> 232
<400> 232
000
<210> 233
<400> 233
000
<210> 234
<400> 234
000
<210> 235
<400> 235
000
<210> 236
<400> 236
000
<210> 237
<400> 237
000
<210> 238
<400> 238
000
<210> 239
<400> 239
000
<210> 240
<400> 240
000
<210> 241
<400> 241
000
<210> 242
<400> 242
000
<210> 243
<400> 243
000
<210> 244
<400> 244
000
<210> 245
<400> 245
000
<210> 246
<400> 246
000
<210> 247
<400> 247
000
<210> 248
<400> 248
000
<210> 249
<400> 249
000
<210> 250
<400> 250
000
<210> 251
<400> 251
000
<210> 252
<400> 252
000
<210> 253
<400> 253
000
<210> 254
<400> 254
000
<210> 255
<400> 255
000
<210> 256
<400> 256
000
<210> 257
<400> 257
000
<210> 258
<400> 258
000
<210> 259
<400> 259
000
<210> 260
<400> 260
000
<210> 261
<400> 261
000
<210> 262
<400> 262
000
<210> 263
<400> 263
000
<210> 264
<400> 264
000
<210> 265
<400> 265
000
<210> 266
<400> 266
000
<210> 267
<400> 267
000
<210> 268
<400> 268
000
<210> 269
<400> 269
000
<210> 270
<400> 270
000
<210> 271
<400> 271
000
<210> 272
<400> 272
000
<210> 273
<400> 273
000
<210> 274
<400> 274
000
<210> 275
<400> 275
000
<210> 276
<400> 276
000
<210> 277
<400> 277
000
<210> 278
<400> 278
000
<210> 279
<400> 279
000
<210> 280
<400> 280
000
<210> 281
<400> 281
000
<210> 282
<400> 282
000
<210> 283
<400> 283
000
<210> 284
<400> 284
000
<210> 285
<400> 285
000
<210> 286
<400> 286
000
<210> 287
<400> 287
000
<210> 288
<400> 288
000
<210> 289
<400> 289
000
<210> 290
<400> 290
000
<210> 291
<400> 291
000
<210> 292
<400> 292
000
<210> 293
<400> 293
000
<210> 294
<400> 294
000
<210> 295
<400> 295
000
<210> 296
<400> 296
000
<210> 297
<400> 297
000
<210> 298
<400> 298
000
<210> 299
<400> 299
000
<210> 300
<400> 300
000
<210> 301
<400> 301
000
<210> 302
<400> 302
000
<210> 303
<400> 303
000
<210> 304
<400> 304
000
<210> 305
<400> 305
000
<210> 306
<400> 306
000
<210> 307
<400> 307
000
<210> 308
<400> 308
000
<210> 309
<400> 309
000
<210> 310
<400> 310
000
<210> 311
<400> 311
000
<210> 312
<400> 312
000
<210> 313
<400> 313
000
<210> 314
<400> 314
000
<210> 315
<400> 315
000
<210> 316
<400> 316
000
<210> 317
<400> 317
000
<210> 318
<400> 318
000
<210> 319
<400> 319
000
<210> 320
<400> 320
000
<210> 321
<400> 321
000
<210> 322
<400> 322
000
<210> 323
<400> 323
000
<210> 324
<400> 324
000
<210> 325
<400> 325
000
<210> 326
<400> 326
000
<210> 327
<400> 327
000
<210> 328
<400> 328
000
<210> 329
<400> 329
000
<210> 330
<400> 330
000
<210> 331
<400> 331
000
<210> 332
<400> 332
000
<210> 333
<400> 333
000
<210> 334
<400> 334
000
<210> 335
<400> 335
000
<210> 336
<400> 336
000
<210> 337
<400> 337
000
<210> 338
<400> 338
000
<210> 339
<400> 339
000
<210> 340
<400> 340
000
<210> 341
<400> 341
000
<210> 342
<400> 342
000
<210> 343
<400> 343
000
<210> 344
<400> 344
000
<210> 345
<400> 345
000
<210> 346
<400> 346
000
<210> 347
<400> 347
000
<210> 348
<400> 348
000
<210> 349
<400> 349
000
<210> 350
<400> 350
000
<210> 351
<400> 351
000
<210> 352
<400> 352
000
<210> 353
<400> 353
000
<210> 354
<400> 354
000
<210> 355
<400> 355
000
<210> 356
<400> 356
000
<210> 357
<400> 357
000
<210> 358
<400> 358
000
<210> 359
<400> 359
000
<210> 360
<400> 360
000
<210> 361
<400> 361
000
<210> 362
<400> 362
000
<210> 363
<400> 363
000
<210> 364
<400> 364
000
<210> 365
<400> 365
000
<210> 366
<400> 366
000
<210> 367
<400> 367
000
<210> 368
<400> 368
000
<210> 369
<400> 369
000
<210> 370
<400> 370
000
<210> 371
<400> 371
000
<210> 372
<400> 372
000
<210> 373
<400> 373
000
<210> 374
<400> 374
000
<210> 375
<400> 375
000
<210> 376
<400> 376
000
<210> 377
<400> 377
000
<210> 378
<400> 378
000
<210> 379
<400> 379
000
<210> 380
<400> 380
000
<210> 381
<400> 381
000
<210> 382
<400> 382
000
<210> 383
<400> 383
000
<210> 384
<400> 384
000
<210> 385
<400> 385
000
<210> 386
<400> 386
000
<210> 387
<400> 387
000
<210> 388
<400> 388
000
<210> 389
<400> 389
000
<210> 390
<400> 390
000
<210> 391
<400> 391
000
<210> 392
<400> 392
000
<210> 393
<400> 393
000
<210> 394
<400> 394
000
<210> 395
<400> 395
000
<210> 396
<400> 396
000
<210> 397
<400> 397
000
<210> 398
<400> 398
000
<210> 399
<400> 399
000
<210> 400
<400> 400
000
<210> 401
<400> 401
000
<210> 402
<400> 402
000
<210> 403
<400> 403
000
<210> 404
<400> 404
000
<210> 405
<400> 405
000
<210> 406
<400> 406
000
<210> 407
<400> 407
000
<210> 408
<400> 408
000
<210> 409
<400> 409
000
<210> 410
<400> 410
000
<210> 411
<400> 411
000
<210> 412
<400> 412
000
<210> 413
<400> 413
000
<210> 414
<400> 414
000
<210> 415
<400> 415
000
<210> 416
<400> 416
000
<210> 417
<400> 417
000
<210> 418
<400> 418
000
<210> 419
<400> 419
000
<210> 420
<400> 420
000
<210> 421
<400> 421
000
<210> 422
<400> 422
000
<210> 423
<400> 423
000
<210> 424
<400> 424
000
<210> 425
<400> 425
000
<210> 426
<400> 426
000
<210> 427
<400> 427
000
<210> 428
<400> 428
000
<210> 429
<400> 429
000
<210> 430
<400> 430
000
<210> 431
<400> 431
000
<210> 432
<400> 432
000
<210> 433
<400> 433
000
<210> 434
<400> 434
000
<210> 435
<400> 435
000
<210> 436
<400> 436
000
<210> 437
<400> 437
000
<210> 438
<400> 438
000
<210> 439
<400> 439
000
<210> 440
<400> 440
000
<210> 441
<400> 441
000
<210> 442
<400> 442
000
<210> 443
<400> 443
000
<210> 444
<400> 444
000
<210> 445
<400> 445
000
<210> 446
<400> 446
000
<210> 447
<400> 447
000
<210> 448
<400> 448
000
<210> 449
<400> 449
000
<210> 450
<400> 450
000
<210> 451
<400> 451
000
<210> 452
<400> 452
000
<210> 453
<400> 453
000
<210> 454
<400> 454
000
<210> 455
<400> 455
000
<210> 456
<400> 456
000
<210> 457
<400> 457
000
<210> 458
<400> 458
000
<210> 459
<400> 459
000
<210> 460
<400> 460
000
<210> 461
<400> 461
000
<210> 462
<400> 462
000
<210> 463
<400> 463
000
<210> 464
<400> 464
000
<210> 465
<400> 465
000
<210> 466
<400> 466
000
<210> 467
<400> 467
000
<210> 468
<400> 468
000
<210> 469
<400> 469
000
<210> 470
<400> 470
000
<210> 471
<400> 471
000
<210> 472
<400> 472
000
<210> 473
<400> 473
000
<210> 474
<400> 474
000
<210> 475
<400> 475
000
<210> 476
<400> 476
000
<210> 477
<400> 477
000
<210> 478
<400> 478
000
<210> 479
<400> 479
000
<210> 480
<400> 480
000
<210> 481
<400> 481
000
<210> 482
<400> 482
000
<210> 483
<400> 483
000
<210> 484
<400> 484
000
<210> 485
<400> 485
000
<210> 486
<400> 486
000
<210> 487
<400> 487
000
<210> 488
<400> 488
000
<210> 489
<400> 489
000
<210> 490
<400> 490
000
<210> 491
<400> 491
000
<210> 492
<400> 492
000
<210> 493
<400> 493
000
<210> 494
<400> 494
000
<210> 495
<400> 495
000
<210> 496
<400> 496
000
<210> 497
<400> 497
000
<210> 498
<400> 498
000
<210> 499
<400> 499
000
<210> 500
<400> 500
000
<210> 501
<400> 501
000
<210> 502
<400> 502
000
<210> 503
<400> 503
000
<210> 504
<400> 504
000
<210> 505
<400> 505
000
<210> 506
<400> 506
000
<210> 507
<400> 507
000
<210> 508
<400> 508
000
<210> 509
<400> 509
000
<210> 510
<400> 510
000
<210> 511
<400> 511
000
<210> 512
<400> 512
000
<210> 513
<400> 513
000
<210> 514
<400> 514
000
<210> 515
<400> 515
000
<210> 516
<400> 516
000
<210> 517
<400> 517
000
<210> 518
<400> 518
000
<210> 519
<400> 519
000
<210> 520
<400> 520
000
<210> 521
<400> 521
000
<210> 522
<400> 522
000
<210> 523
<400> 523
000
<210> 524
<400> 524
000
<210> 525
<400> 525
000
<210> 526
<400> 526
000
<210> 527
<400> 527
000
<210> 528
<400> 528
000
<210> 529
<400> 529
000
<210> 530
<400> 530
000
<210> 531
<400> 531
000
<210> 532
<400> 532
000
<210> 533
<400> 533
000
<210> 534
<400> 534
000
<210> 535
<400> 535
000
<210> 536
<400> 536
000
<210> 537
<400> 537
000
<210> 538
<400> 538
000
<210> 539
<400> 539
000
<210> 540
<400> 540
000
<210> 541
<400> 541
000
<210> 542
<400> 542
000
<210> 543
<400> 543
000
<210> 544
<400> 544
000
<210> 545
<400> 545
000
<210> 546
<400> 546
000
<210> 547
<400> 547
000
<210> 548
<400> 548
000
<210> 549
<400> 549
000
<210> 550
<400> 550
000
<210> 551
<400> 551
000
<210> 552
<400> 552
000
<210> 553
<400> 553
000
<210> 554
<400> 554
000
<210> 555
<400> 555
000
<210> 556
<400> 556
000
<210> 557
<400> 557
000
<210> 558
<400> 558
000
<210> 559
<400> 559
000
<210> 560
<400> 560
000
<210> 561
<400> 561
000
<210> 562
<400> 562
000
<210> 563
<400> 563
000
<210> 564
<400> 564
000
<210> 565
<400> 565
000
<210> 566
<400> 566
000
<210> 567
<400> 567
000
<210> 568
<400> 568
000
<210> 569
<400> 569
000
<210> 570
<400> 570
000
<210> 571
<400> 571
000
<210> 572
<400> 572
000
<210> 573
<400> 573
000
<210> 574
<400> 574
000
<210> 575
<400> 575
000
<210> 576
<400> 576
000
<210> 577
<400> 577
000
<210> 578
<400> 578
000
<210> 579
<400> 579
000
<210> 580
<400> 580
000
<210> 581
<400> 581
000
<210> 582
<400> 582
000
<210> 583
<400> 583
000
<210> 584
<400> 584
000
<210> 585
<400> 585
000
<210> 586
<400> 586
000
<210> 587
<400> 587
000
<210> 588
<400> 588
000
<210> 589
<400> 589
000
<210> 590
<400> 590
000
<210> 591
<400> 591
000
<210> 592
<400> 592
000
<210> 593
<400> 593
000
<210> 594
<400> 594
000
<210> 595
<400> 595
000
<210> 596
<400> 596
000
<210> 597
<400> 597
000
<210> 598
<400> 598
000
<210> 599
<400> 599
000
<210> 600
<400> 600
000
<210> 601
<400> 601
000
<210> 602
<400> 602
000
<210> 603
<400> 603
000
<210> 604
<400> 604
000
<210> 605
<400> 605
000
<210> 606
<400> 606
000
<210> 607
<400> 607
000
<210> 608
<400> 608
000
<210> 609
<400> 609
000
<210> 610
<400> 610
000
<210> 611
<400> 611
000
<210> 612
<400> 612
000
<210> 613
<400> 613
000
<210> 614
<400> 614
000
<210> 615
<400> 615
000
<210> 616
<400> 616
000
<210> 617
<400> 617
000
<210> 618
<400> 618
000
<210> 619
<400> 619
000
<210> 620
<400> 620
000
<210> 621
<400> 621
000
<210> 622
<400> 622
000
<210> 623
<400> 623
000
<210> 624
<400> 624
000
<210> 625
<400> 625
000
<210> 626
<400> 626
000
<210> 627
<400> 627
000
<210> 628
<400> 628
000
<210> 629
<400> 629
000
<210> 630
<400> 630
000
<210> 631
<400> 631
000
<210> 632
<400> 632
000
<210> 633
<400> 633
000
<210> 634
<400> 634
000
<210> 635
<400> 635
000
<210> 636
<400> 636
000
<210> 637
<400> 637
000
<210> 638
<400> 638
000
<210> 639
<400> 639
000
<210> 640
<400> 640
000
<210> 641
<400> 641
000
<210> 642
<400> 642
000
<210> 643
<400> 643
000
<210> 644
<400> 644
000
<210> 645
<400> 645
000
<210> 646
<400> 646
000
<210> 647
<400> 647
000
<210> 648
<400> 648
000
<210> 649
<400> 649
000
<210> 650
<400> 650
000
<210> 651
<400> 651
000
<210> 652
<400> 652
000
<210> 653
<400> 653
000
<210> 654
<400> 654
000
<210> 655
<400> 655
000
<210> 656
<400> 656
000
<210> 657
<400> 657
000
<210> 658
<400> 658
000
<210> 659
<400> 659
000
<210> 660
<400> 660
000
<210> 661
<400> 661
000
<210> 662
<400> 662
000
<210> 663
<400> 663
000
<210> 664
<400> 664
000
<210> 665
<400> 665
000
<210> 666
<400> 666
000
<210> 667
<400> 667
000
<210> 668
<400> 668
000
<210> 669
<400> 669
000
<210> 670
<400> 670
000
<210> 671
<400> 671
000
<210> 672
<400> 672
000
<210> 673
<400> 673
000
<210> 674
<400> 674
000
<210> 675
<400> 675
000
<210> 676
<400> 676
000
<210> 677
<400> 677
000
<210> 678
<400> 678
000
<210> 679
<400> 679
000
<210> 680
<400> 680
000
<210> 681
<400> 681
000
<210> 682
<400> 682
000
<210> 683
<400> 683
000
<210> 684
<400> 684
000
<210> 685
<400> 685
000
<210> 686
<400> 686
000
<210> 687
<400> 687
000
<210> 688
<400> 688
000
<210> 689
<400> 689
000
<210> 690
<400> 690
000
<210> 691
<400> 691
000
<210> 692
<400> 692
000
<210> 693
<400> 693
000
<210> 694
<400> 694
000
<210> 695
<400> 695
000
<210> 696
<400> 696
000
<210> 697
<400> 697
000
<210> 698
<400> 698
000
<210> 699
<400> 699
000
<210> 700
<400> 700
000
<210> 701
<400> 701
000
<210> 702
<400> 702
000
<210> 703
<400> 703
000
<210> 704
<400> 704
000
<210> 705
<400> 705
000
<210> 706
<400> 706
000
<210> 707
<400> 707
000
<210> 708
<400> 708
000
<210> 709
<400> 709
000
<210> 710
<400> 710
000
<210> 711
<400> 711
000
<210> 712
<400> 712
000
<210> 713
<400> 713
000
<210> 714
<400> 714
000
<210> 715
<400> 715
000
<210> 716
<400> 716
000
<210> 717
<400> 717
000
<210> 718
<400> 718
000
<210> 719
<400> 719
000
<210> 720
<400> 720
000
<210> 721
<400> 721
000
<210> 722
<400> 722
000
<210> 723
<400> 723
000
<210> 724
<400> 724
000
<210> 725
<400> 725
000
<210> 726
<400> 726
000
<210> 727
<400> 727
000
<210> 728
<400> 728
000
<210> 729
<400> 729
000
<210> 730
<400> 730
000
<210> 731
<400> 731
000
<210> 732
<400> 732
000
<210> 733
<400> 733
000
<210> 734
<400> 734
000
<210> 735
<400> 735
000
<210> 736
<400> 736
000
<210> 737
<400> 737
000
<210> 738
<400> 738
000
<210> 739
<400> 739
000
<210> 740
<400> 740
000
<210> 741
<400> 741
000
<210> 742
<400> 742
000
<210> 743
<400> 743
000
<210> 744
<400> 744
000
<210> 745
<400> 745
000
<210> 746
<400> 746
000
<210> 747
<400> 747
000
<210> 748
<400> 748
000
<210> 749
<400> 749
000
<210> 750
<400> 750
000
<210> 751
<400> 751
000
<210> 752
<400> 752
000
<210> 753
<400> 753
000
<210> 754
<400> 754
000
<210> 755
<400> 755
000
<210> 756
<400> 756
000
<210> 757
<400> 757
000
<210> 758
<400> 758
000
<210> 759
<400> 759
000
<210> 760
<400> 760
000
<210> 761
<400> 761
000
<210> 762
<400> 762
000
<210> 763
<400> 763
000
<210> 764
<400> 764
000
<210> 765
<400> 765
000
<210> 766
<400> 766
000
<210> 767
<400> 767
000
<210> 768
<400> 768
000
<210> 769
<400> 769
000
<210> 770
<400> 770
000
<210> 771
<400> 771
000
<210> 772
<400> 772
000
<210> 773
<400> 773
000
<210> 774
<400> 774
000
<210> 775
<400> 775
000
<210> 776
<400> 776
000
<210> 777
<400> 777
000
<210> 778
<400> 778
000
<210> 779
<400> 779
000
<210> 780
<400> 780
000
<210> 781
<400> 781
000
<210> 782
<400> 782
000
<210> 783
<400> 783
000
<210> 784
<400> 784
000
<210> 785
<400> 785
000
<210> 786
<400> 786
000
<210> 787
<400> 787
000
<210> 788
<400> 788
000
<210> 789
<400> 789
000
<210> 790
<400> 790
000
<210> 791
<400> 791
000
<210> 792
<400> 792
000
<210> 793
<400> 793
000
<210> 794
<400> 794
000
<210> 795
<400> 795
000
<210> 796
<400> 796
000
<210> 797
<400> 797
000
<210> 798
<400> 798
000
<210> 799
<400> 799
000
<210> 800
<400> 800
000
<210> 801
<400> 801
000
<210> 802
<400> 802
000
<210> 803
<400> 803
000
<210> 804
<400> 804
000
<210> 805
<400> 805
000
<210> 806
<400> 806
000
<210> 807
<400> 807
000
<210> 808
<400> 808
000
<210> 809
<400> 809
000
<210> 810
<400> 810
000
<210> 811
<400> 811
000
<210> 812
<400> 812
000
<210> 813
<400> 813
000
<210> 814
<400> 814
000
<210> 815
<400> 815
000
<210> 816
<400> 816
000
<210> 817
<400> 817
000
<210> 818
<400> 818
000
<210> 819
<400> 819
000
<210> 820
<400> 820
000
<210> 821
<400> 821
000
<210> 822
<400> 822
000
<210> 823
<400> 823
000
<210> 824
<400> 824
000
<210> 825
<400> 825
000
<210> 826
<400> 826
000
<210> 827
<400> 827
000
<210> 828
<400> 828
000
<210> 829
<400> 829
000
<210> 830
<400> 830
000
<210> 831
<400> 831
000
<210> 832
<400> 832
000
<210> 833
<400> 833
000
<210> 834
<400> 834
000
<210> 835
<400> 835
000
<210> 836
<400> 836
000
<210> 837
<400> 837
000
<210> 838
<400> 838
000
<210> 839
<400> 839
000
<210> 840
<400> 840
000
<210> 841
<400> 841
000
<210> 842
<400> 842
000
<210> 843
<400> 843
000
<210> 844
<400> 844
000
<210> 845
<400> 845
000
<210> 846
<400> 846
000
<210> 847
<400> 847
000
<210> 848
<400> 848
000
<210> 849
<400> 849
000
<210> 850
<400> 850
000
<210> 851
<400> 851
000
<210> 852
<400> 852
000
<210> 853
<400> 853
000
<210> 854
<400> 854
000
<210> 855
<400> 855
000
<210> 856
<400> 856
000
<210> 857
<400> 857
000
<210> 858
<400> 858
000
<210> 859
<400> 859
000
<210> 860
<400> 860
000
<210> 861
<400> 861
000
<210> 862
<400> 862
000
<210> 863
<400> 863
000
<210> 864
<400> 864
000
<210> 865
<400> 865
000
<210> 866
<400> 866
000
<210> 867
<400> 867
000
<210> 868
<400> 868
000
<210> 869
<400> 869
000
<210> 870
<400> 870
000
<210> 871
<400> 871
000
<210> 872
<400> 872
000
<210> 873
<400> 873
000
<210> 874
<400> 874
000
<210> 875
<400> 875
000
<210> 876
<400> 876
000
<210> 877
<400> 877
000
<210> 878
<400> 878
000
<210> 879
<400> 879
000
<210> 880
<400> 880
000
<210> 881
<400> 881
000
<210> 882
<400> 882
000
<210> 883
<400> 883
000
<210> 884
<400> 884
000
<210> 885
<400> 885
000
<210> 886
<400> 886
000
<210> 887
<400> 887
000
<210> 888
<400> 888
000
<210> 889
<400> 889
000
<210> 890
<400> 890
000
<210> 891
<400> 891
000
<210> 892
<400> 892
000
<210> 893
<400> 893
000
<210> 894
<400> 894
000
<210> 895
<400> 895
000
<210> 896
<400> 896
000
<210> 897
<400> 897
000
<210> 898
<400> 898
000
<210> 899
<400> 899
000
<210> 900
<400> 900
000
<210> 901
<400> 901
000
<210> 902
<400> 902
000
<210> 903
<400> 903
000
<210> 904
<400> 904
000
<210> 905
<400> 905
000
<210> 906
<400> 906
000
<210> 907
<400> 907
000
<210> 908
<400> 908
000
<210> 909
<400> 909
000
<210> 910
<400> 910
000
<210> 911
<400> 911
000
<210> 912
<400> 912
000
<210> 913
<400> 913
000
<210> 914
<400> 914
000
<210> 915
<400> 915
000
<210> 916
<400> 916
000
<210> 917
<400> 917
000
<210> 918
<400> 918
000
<210> 919
<400> 919
000
<210> 920
<400> 920
000
<210> 921
<400> 921
000
<210> 922
<400> 922
000
<210> 923
<400> 923
000
<210> 924
<400> 924
000
<210> 925
<400> 925
000
<210> 926
<400> 926
000
<210> 927
<400> 927
000
<210> 928
<400> 928
000
<210> 929
<400> 929
000
<210> 930
<400> 930
000
<210> 931
<400> 931
000
<210> 932
<400> 932
000
<210> 933
<400> 933
000
<210> 934
<400> 934
000
<210> 935
<400> 935
000
<210> 936
<400> 936
000
<210> 937
<400> 937
000
<210> 938
<400> 938
000
<210> 939
<400> 939
000
<210> 940
<400> 940
000
<210> 941
<400> 941
000
<210> 942
<400> 942
000
<210> 943
<400> 943
000
<210> 944
<400> 944
000
<210> 945
<400> 945
000
<210> 946
<400> 946
000
<210> 947
<400> 947
000
<210> 948
<400> 948
000
<210> 949
<400> 949
000
<210> 950
<400> 950
000
<210> 951
<400> 951
000
<210> 952
<400> 952
000
<210> 953
<400> 953
000
<210> 954
<400> 954
000
<210> 955
<400> 955
000
<210> 956
<400> 956
000
<210> 957
<400> 957
000
<210> 958
<400> 958
000
<210> 959
<400> 959
000
<210> 960
<400> 960
000
<210> 961
<400> 961
000
<210> 962
<400> 962
000
<210> 963
<400> 963
000
<210> 964
<400> 964
000
<210> 965
<400> 965
000
<210> 966
<400> 966
000
<210> 967
<400> 967
000
<210> 968
<400> 968
000
<210> 969
<400> 969
000
<210> 970
<400> 970
000
<210> 971
<400> 971
000
<210> 972
<400> 972
000
<210> 973
<400> 973
000
<210> 974
<400> 974
000
<210> 975
<400> 975
000
<210> 976
<400> 976
000
<210> 977
<400> 977
000
<210> 978
<400> 978
000
<210> 979
<400> 979
000
<210> 980
<400> 980
000
<210> 981
<400> 981
000
<210> 982
<400> 982
000
<210> 983
<400> 983
000
<210> 984
<400> 984
000
<210> 985
<400> 985
000
<210> 986
<400> 986
000
<210> 987
<400> 987
000
<210> 988
<400> 988
000
<210> 989
<400> 989
000
<210> 990
<400> 990
000
<210> 991
<400> 991
000
<210> 992
<400> 992
000
<210> 993
<400> 993
000
<210> 994
<400> 994
000
<210> 995
<400> 995
000
<210> 996
<400> 996
000
<210> 997
<400> 997
000
<210> 998
<400> 998
000
<210> 999
<400> 999
000
<210> 1000
<400> 1000
000
<210> 1001
<400> 1001
000
<210> 1002
<400> 1002
000
<210> 1003
<400> 1003
000
<210> 1004
<400> 1004
000
<210> 1005
<400> 1005
000
<210> 1006
<400> 1006
000
<210> 1007
<400> 1007
000
<210> 1008
<400> 1008
000
<210> 1009
<400> 1009
000
<210> 1010
<400> 1010
000
<210> 1011
<400> 1011
000
<210> 1012
<400> 1012
000
<210> 1013
<400> 1013
000
<210> 1014
<400> 1014
000
<210> 1015
<400> 1015
000
<210> 1016
<400> 1016
000
<210> 1017
<400> 1017
000
<210> 1018
<400> 1018
000
<210> 1019
<400> 1019
000
<210> 1020
<400> 1020
000
<210> 1021
<400> 1021
000
<210> 1022
<400> 1022
000
<210> 1023
<400> 1023
000
<210> 1024
<400> 1024
000
<210> 1025
<400> 1025
000
<210> 1026
<400> 1026
000
<210> 1027
<400> 1027
000
<210> 1028
<400> 1028
000
<210> 1029
<400> 1029
000
<210> 1030
<400> 1030
000
<210> 1031
<400> 1031
000
<210> 1032
<400> 1032
000
<210> 1033
<400> 1033
000
<210> 1034
<400> 1034
000
<210> 1035
<400> 1035
000
<210> 1036
<400> 1036
000
<210> 1037
<400> 1037
000
<210> 1038
<400> 1038
000
<210> 1039
<400> 1039
000
<210> 1040
<400> 1040
000
<210> 1041
<400> 1041
000
<210> 1042
<400> 1042
000
<210> 1043
<400> 1043
000
<210> 1044
<400> 1044
000
<210> 1045
<400> 1045
000
<210> 1046
<400> 1046
000
<210> 1047
<400> 1047
000
<210> 1048
<400> 1048
000
<210> 1049
<400> 1049
000
<210> 1050
<400> 1050
000
<210> 1051
<400> 1051
000
<210> 1052
<400> 1052
000
<210> 1053
<400> 1053
000
<210> 1054
<400> 1054
000
<210> 1055
<400> 1055
000
<210> 1056
<400> 1056
000
<210> 1057
<400> 1057
000
<210> 1058
<400> 1058
000
<210> 1059
<400> 1059
000
<210> 1060
<400> 1060
000
<210> 1061
<400> 1061
000
<210> 1062
<400> 1062
000
<210> 1063
<400> 1063
000
<210> 1064
<400> 1064
000
<210> 1065
<400> 1065
000
<210> 1066
<400> 1066
000
<210> 1067
<400> 1067
000
<210> 1068
<400> 1068
000
<210> 1069
<400> 1069
000
<210> 1070
<400> 1070
000
<210> 1071
<400> 1071
000
<210> 1072
<400> 1072
000
<210> 1073
<400> 1073
000
<210> 1074
<400> 1074
000
<210> 1075
<400> 1075
000
<210> 1076
<400> 1076
000
<210> 1077
<400> 1077
000
<210> 1078
<400> 1078
000
<210> 1079
<400> 1079
000
<210> 1080
<400> 1080
000
<210> 1081
<400> 1081
000
<210> 1082
<400> 1082
000
<210> 1083
<400> 1083
000
<210> 1084
<400> 1084
000
<210> 1085
<400> 1085
000
<210> 1086
<400> 1086
000
<210> 1087
<400> 1087
000
<210> 1088
<400> 1088
000
<210> 1089
<400> 1089
000
<210> 1090
<400> 1090
000
<210> 1091
<400> 1091
000
<210> 1092
<400> 1092
000
<210> 1093
<400> 1093
000
<210> 1094
<400> 1094
000
<210> 1095
<400> 1095
000
<210> 1096
<400> 1096
000
<210> 1097
<400> 1097
000
<210> 1098
<400> 1098
000
<210> 1099
<400> 1099
000
<210> 1100
<400> 1100
000
<210> 1101
<400> 1101
000
<210> 1102
<400> 1102
000
<210> 1103
<400> 1103
000
<210> 1104
<400> 1104
000
<210> 1105
<400> 1105
000
<210> 1106
<400> 1106
000
<210> 1107
<400> 1107
000
<210> 1108
<400> 1108
000
<210> 1109
<400> 1109
000
<210> 1110
<400> 1110
000
<210> 1111
<400> 1111
000
<210> 1112
<400> 1112
000
<210> 1113
<400> 1113
000
<210> 1114
<400> 1114
000
<210> 1115
<400> 1115
000
<210> 1116
<400> 1116
000
<210> 1117
<400> 1117
000
<210> 1118
<400> 1118
000
<210> 1119
<400> 1119
000
<210> 1120
<400> 1120
000
<210> 1121
<400> 1121
000
<210> 1122
<400> 1122
000
<210> 1123
<400> 1123
000
<210> 1124
<400> 1124
000
<210> 1125
<400> 1125
000
<210> 1126
<400> 1126
000
<210> 1127
<400> 1127
000
<210> 1128
<400> 1128
000
<210> 1129
<400> 1129
000
<210> 1130
<400> 1130
000
<210> 1131
<400> 1131
000
<210> 1132
<400> 1132
000
<210> 1133
<400> 1133
000
<210> 1134
<400> 1134
000
<210> 1135
<400> 1135
000
<210> 1136
<400> 1136
000
<210> 1137
<400> 1137
000
<210> 1138
<400> 1138
000
<210> 1139
<400> 1139
000
<210> 1140
<400> 1140
000
<210> 1141
<400> 1141
000
<210> 1142
<400> 1142
000
<210> 1143
<400> 1143
000
<210> 1144
<400> 1144
000
<210> 1145
<400> 1145
000
<210> 1146
<400> 1146
000
<210> 1147
<400> 1147
000
<210> 1148
<400> 1148
000
<210> 1149
<400> 1149
000
<210> 1150
<400> 1150
000
<210> 1151
<400> 1151
000
<210> 1152
<400> 1152
000
<210> 1153
<400> 1153
000
<210> 1154
<400> 1154
000
<210> 1155
<400> 1155
000
<210> 1156
<400> 1156
000
<210> 1157
<400> 1157
000
<210> 1158
<400> 1158
000
<210> 1159
<400> 1159
000
<210> 1160
<400> 1160
000
<210> 1161
<400> 1161
000
<210> 1162
<400> 1162
000
<210> 1163
<400> 1163
000
<210> 1164
<400> 1164
000
<210> 1165
<400> 1165
000
<210> 1166
<400> 1166
000
<210> 1167
<400> 1167
000
<210> 1168
<400> 1168
000
<210> 1169
<400> 1169
000
<210> 1170
<400> 1170
000
<210> 1171
<400> 1171
000
<210> 1172
<400> 1172
000
<210> 1173
<400> 1173
000
<210> 1174
<400> 1174
000
<210> 1175
<400> 1175
000
<210> 1176
<400> 1176
000
<210> 1177
<400> 1177
000
<210> 1178
<400> 1178
000
<210> 1179
<400> 1179
000
<210> 1180
<400> 1180
000
<210> 1181
<400> 1181
000
<210> 1182
<400> 1182
000
<210> 1183
<400> 1183
000
<210> 1184
<400> 1184
000
<210> 1185
<400> 1185
000
<210> 1186
<400> 1186
000
<210> 1187
<400> 1187
000
<210> 1188
<400> 1188
000
<210> 1189
<400> 1189
000
<210> 1190
<400> 1190
000
<210> 1191
<400> 1191
000
<210> 1192
<400> 1192
000
<210> 1193
<400> 1193
000
<210> 1194
<400> 1194
000
<210> 1195
<400> 1195
000
<210> 1196
<400> 1196
000
<210> 1197
<400> 1197
000
<210> 1198
<400> 1198
000
<210> 1199
<400> 1199
000
<210> 1200
<400> 1200
000
<210> 1201
<400> 1201
000
<210> 1202
<400> 1202
000
<210> 1203
<400> 1203
000
<210> 1204
<400> 1204
000
<210> 1205
<400> 1205
000
<210> 1206
<400> 1206
000
<210> 1207
<400> 1207
000
<210> 1208
<400> 1208
000
<210> 1209
<400> 1209
000
<210> 1210
<400> 1210
000
<210> 1211
<400> 1211
000
<210> 1212
<400> 1212
000
<210> 1213
<400> 1213
000
<210> 1214
<400> 1214
000
<210> 1215
<400> 1215
000
<210> 1216
<400> 1216
000
<210> 1217
<400> 1217
000
<210> 1218
<400> 1218
000
<210> 1219
<400> 1219
000
<210> 1220
<400> 1220
000
<210> 1221
<400> 1221
000
<210> 1222
<400> 1222
000
<210> 1223
<400> 1223
000
<210> 1224
<400> 1224
000
<210> 1225
<400> 1225
000
<210> 1226
<400> 1226
000
<210> 1227
<400> 1227
000
<210> 1228
<400> 1228
000
<210> 1229
<400> 1229
000
<210> 1230
<400> 1230
000
<210> 1231
<400> 1231
000
<210> 1232
<400> 1232
000
<210> 1233
<400> 1233
000
<210> 1234
<400> 1234
000
<210> 1235
<400> 1235
000
<210> 1236
<400> 1236
000
<210> 1237
<400> 1237
000
<210> 1238
<400> 1238
000
<210> 1239
<400> 1239
000
<210> 1240
<400> 1240
000
<210> 1241
<400> 1241
000
<210> 1242
<400> 1242
000
<210> 1243
<400> 1243
000
<210> 1244
<400> 1244
000
<210> 1245
<400> 1245
000
<210> 1246
<400> 1246
000
<210> 1247
<400> 1247
000
<210> 1248
<400> 1248
000
<210> 1249
<400> 1249
000
<210> 1250
<400> 1250
000
<210> 1251
<400> 1251
000
<210> 1252
<400> 1252
000
<210> 1253
<400> 1253
000
<210> 1254
<400> 1254
000
<210> 1255
<400> 1255
000
<210> 1256
<400> 1256
000
<210> 1257
<400> 1257
000
<210> 1258
<400> 1258
000
<210> 1259
<400> 1259
000
<210> 1260
<400> 1260
000
<210> 1261
<400> 1261
000
<210> 1262
<400> 1262
000
<210> 1263
<400> 1263
000
<210> 1264
<400> 1264
000
<210> 1265
<400> 1265
000
<210> 1266
<400> 1266
000
<210> 1267
<400> 1267
000
<210> 1268
<400> 1268
000
<210> 1269
<400> 1269
000
<210> 1270
<400> 1270
000
<210> 1271
<400> 1271
000
<210> 1272
<400> 1272
000
<210> 1273
<400> 1273
000
<210> 1274
<400> 1274
000
<210> 1275
<400> 1275
000
<210> 1276
<400> 1276
000
<210> 1277
<400> 1277
000
<210> 1278
<400> 1278
000
<210> 1279
<400> 1279
000
<210> 1280
<400> 1280
000
<210> 1281
<400> 1281
000
<210> 1282
<400> 1282
000
<210> 1283
<400> 1283
000
<210> 1284
<400> 1284
000
<210> 1285
<400> 1285
000
<210> 1286
<400> 1286
000
<210> 1287
<400> 1287
000
<210> 1288
<400> 1288
000
<210> 1289
<400> 1289
000
<210> 1290
<400> 1290
000
<210> 1291
<400> 1291
000
<210> 1292
<400> 1292
000
<210> 1293
<400> 1293
000
<210> 1294
<400> 1294
000
<210> 1295
<400> 1295
000
<210> 1296
<400> 1296
000
<210> 1297
<400> 1297
000
<210> 1298
<400> 1298
000
<210> 1299
<400> 1299
000
<210> 1300
<400> 1300
000
<210> 1301
<400> 1301
000
<210> 1302
<400> 1302
000
<210> 1303
<400> 1303
000
<210> 1304
<400> 1304
000
<210> 1305
<400> 1305
000
<210> 1306
<400> 1306
000
<210> 1307
<400> 1307
000
<210> 1308
<400> 1308
000
<210> 1309
<400> 1309
000
<210> 1310
<400> 1310
000
<210> 1311
<400> 1311
000
<210> 1312
<400> 1312
000
<210> 1313
<400> 1313
000
<210> 1314
<400> 1314
000
<210> 1315
<400> 1315
000
<210> 1316
<400> 1316
000
<210> 1317
<400> 1317
000
<210> 1318
<400> 1318
000
<210> 1319
<400> 1319
000
<210> 1320
<400> 1320
000
<210> 1321
<400> 1321
000
<210> 1322
<400> 1322
000
<210> 1323
<400> 1323
000
<210> 1324
<400> 1324
000
<210> 1325
<400> 1325
000
<210> 1326
<400> 1326
000
<210> 1327
<400> 1327
000
<210> 1328
<400> 1328
000
<210> 1329
<400> 1329
000
<210> 1330
<400> 1330
000
<210> 1331
<400> 1331
000
<210> 1332
<400> 1332
000
<210> 1333
<400> 1333
000
<210> 1334
<400> 1334
000
<210> 1335
<400> 1335
000
<210> 1336
<400> 1336
000
<210> 1337
<400> 1337
000
<210> 1338
<400> 1338
000
<210> 1339
<400> 1339
000
<210> 1340
<400> 1340
000
<210> 1341
<400> 1341
000
<210> 1342
<400> 1342
000
<210> 1343
<400> 1343
000
<210> 1344
<400> 1344
000
<210> 1345
<400> 1345
000
<210> 1346
<400> 1346
000
<210> 1347
<400> 1347
000
<210> 1348
<400> 1348
000
<210> 1349
<400> 1349
000
<210> 1350
<400> 1350
000
<210> 1351
<400> 1351
000
<210> 1352
<400> 1352
000
<210> 1353
<400> 1353
000
<210> 1354
<400> 1354
000
<210> 1355
<400> 1355
000
<210> 1356
<400> 1356
000
<210> 1357
<400> 1357
000
<210> 1358
<400> 1358
000
<210> 1359
<400> 1359
000
<210> 1360
<400> 1360
000
<210> 1361
<400> 1361
000
<210> 1362
<400> 1362
000
<210> 1363
<400> 1363
000
<210> 1364
<400> 1364
000
<210> 1365
<400> 1365
000
<210> 1366
<400> 1366
000
<210> 1367
<400> 1367
000
<210> 1368
<400> 1368
000
<210> 1369
<400> 1369
000
<210> 1370
<400> 1370
000
<210> 1371
<400> 1371
000
<210> 1372
<400> 1372
000
<210> 1373
<400> 1373
000
<210> 1374
<400> 1374
000
<210> 1375
<400> 1375
000
<210> 1376
<400> 1376
000
<210> 1377
<400> 1377
000
<210> 1378
<400> 1378
000
<210> 1379
<400> 1379
000
<210> 1380
<400> 1380
000
<210> 1381
<400> 1381
000
<210> 1382
<400> 1382
000
<210> 1383
<400> 1383
000
<210> 1384
<400> 1384
000
<210> 1385
<400> 1385
000
<210> 1386
<400> 1386
000
<210> 1387
<400> 1387
000
<210> 1388
<400> 1388
000
<210> 1389
<400> 1389
000
<210> 1390
<400> 1390
000
<210> 1391
<400> 1391
000
<210> 1392
<400> 1392
000
<210> 1393
<400> 1393
000
<210> 1394
<400> 1394
000
<210> 1395
<400> 1395
000
<210> 1396
<400> 1396
000
<210> 1397
<400> 1397
000
<210> 1398
<400> 1398
000
<210> 1399
<400> 1399
000
<210> 1400
<400> 1400
000
<210> 1401
<400> 1401
000
<210> 1402
<400> 1402
000
<210> 1403
<400> 1403
000
<210> 1404
<400> 1404
000
<210> 1405
<400> 1405
000
<210> 1406
<400> 1406
000
<210> 1407
<400> 1407
000
<210> 1408
<400> 1408
000
<210> 1409
<400> 1409
000
<210> 1410
<400> 1410
000
<210> 1411
<400> 1411
000
<210> 1412
<400> 1412
000
<210> 1413
<400> 1413
000
<210> 1414
<400> 1414
000
<210> 1415
<400> 1415
000
<210> 1416
<400> 1416
000
<210> 1417
<400> 1417
000
<210> 1418
<400> 1418
000
<210> 1419
<400> 1419
000
<210> 1420
<400> 1420
000
<210> 1421
<400> 1421
000
<210> 1422
<400> 1422
000
<210> 1423
<400> 1423
000
<210> 1424
<400> 1424
000
<210> 1425
<400> 1425
000
<210> 1426
<400> 1426
000
<210> 1427
<400> 1427
000
<210> 1428
<400> 1428
000
<210> 1429
<400> 1429
000
<210> 1430
<400> 1430
000
<210> 1431
<400> 1431
000
<210> 1432
<400> 1432
000
<210> 1433
<400> 1433
000
<210> 1434
<400> 1434
000
<210> 1435
<400> 1435
000
<210> 1436
<400> 1436
000
<210> 1437
<400> 1437
000
<210> 1438
<400> 1438
000
<210> 1439
<400> 1439
000
<210> 1440
<400> 1440
000
<210> 1441
<400> 1441
000
<210> 1442
<400> 1442
000
<210> 1443
<400> 1443
000
<210> 1444
<400> 1444
000
<210> 1445
<400> 1445
000
<210> 1446
<400> 1446
000
<210> 1447
<400> 1447
000
<210> 1448
<400> 1448
000
<210> 1449
<400> 1449
000
<210> 1450
<400> 1450
000
<210> 1451
<400> 1451
000
<210> 1452
<400> 1452
000
<210> 1453
<400> 1453
000
<210> 1454
<400> 1454
000
<210> 1455
<400> 1455
000
<210> 1456
<400> 1456
000
<210> 1457
<400> 1457
000
<210> 1458
<400> 1458
000
<210> 1459
<400> 1459
000
<210> 1460
<400> 1460
000
<210> 1461
<400> 1461
000
<210> 1462
<400> 1462
000
<210> 1463
<400> 1463
000
<210> 1464
<400> 1464
000
<210> 1465
<400> 1465
000
<210> 1466
<400> 1466
000
<210> 1467
<400> 1467
000
<210> 1468
<400> 1468
000
<210> 1469
<400> 1469
000
<210> 1470
<400> 1470
000
<210> 1471
<400> 1471
000
<210> 1472
<400> 1472
000
<210> 1473
<400> 1473
000
<210> 1474
<400> 1474
000
<210> 1475
<400> 1475
000
<210> 1476
<400> 1476
000
<210> 1477
<400> 1477
000
<210> 1478
<400> 1478
000
<210> 1479
<400> 1479
000
<210> 1480
<400> 1480
000
<210> 1481
<400> 1481
000
<210> 1482
<400> 1482
000
<210> 1483
<400> 1483
000
<210> 1484
<400> 1484
000
<210> 1485
<400> 1485
000
<210> 1486
<400> 1486
000
<210> 1487
<400> 1487
000
<210> 1488
<400> 1488
000
<210> 1489
<400> 1489
000
<210> 1490
<400> 1490
000
<210> 1491
<400> 1491
000
<210> 1492
<400> 1492
000
<210> 1493
<400> 1493
000
<210> 1494
<400> 1494
000
<210> 1495
<400> 1495
000
<210> 1496
<400> 1496
000
<210> 1497
<400> 1497
000
<210> 1498
<400> 1498
000
<210> 1499
<400> 1499
000
<210> 1500
<400> 1500
000
<210> 1501
<400> 1501
000
<210> 1502
<400> 1502
000
<210> 1503
<400> 1503
000
<210> 1504
<400> 1504
000
<210> 1505
<400> 1505
000
<210> 1506
<400> 1506
000
<210> 1507
<400> 1507
000
<210> 1508
<400> 1508
000
<210> 1509
<400> 1509
000
<210> 1510
<400> 1510
000
<210> 1511
<400> 1511
000
<210> 1512
<400> 1512
000
<210> 1513
<400> 1513
000
<210> 1514
<400> 1514
000
<210> 1515
<400> 1515
000
<210> 1516
<400> 1516
000
<210> 1517
<400> 1517
000
<210> 1518
<400> 1518
000
<210> 1519
<400> 1519
000
<210> 1520
<400> 1520
000
<210> 1521
<400> 1521
000
<210> 1522
<400> 1522
000
<210> 1523
<400> 1523
000
<210> 1524
<400> 1524
000
<210> 1525
<400> 1525
000
<210> 1526
<400> 1526
000
<210> 1527
<400> 1527
000
<210> 1528
<400> 1528
000
<210> 1529
<400> 1529
000
<210> 1530
<400> 1530
000
<210> 1531
<400> 1531
000
<210> 1532
<400> 1532
000
<210> 1533
<400> 1533
000
<210> 1534
<400> 1534
000
<210> 1535
<400> 1535
000
<210> 1536
<400> 1536
000
<210> 1537
<400> 1537
000
<210> 1538
<400> 1538
000
<210> 1539
<400> 1539
000
<210> 1540
<400> 1540
000
<210> 1541
<400> 1541
000
<210> 1542
<400> 1542
000
<210> 1543
<400> 1543
000
<210> 1544
<400> 1544
000
<210> 1545
<400> 1545
000
<210> 1546
<400> 1546
000
<210> 1547
<400> 1547
000
<210> 1548
<400> 1548
000
<210> 1549
<400> 1549
000
<210> 1550
<400> 1550
000
<210> 1551
<400> 1551
000
<210> 1552
<400> 1552
000
<210> 1553
<400> 1553
000
<210> 1554
<400> 1554
000
<210> 1555
<400> 1555
000
<210> 1556
<400> 1556
000
<210> 1557
<400> 1557
000
<210> 1558
<400> 1558
000
<210> 1559
<400> 1559
000
<210> 1560
<400> 1560
000
<210> 1561
<400> 1561
000
<210> 1562
<400> 1562
000
<210> 1563
<400> 1563
000
<210> 1564
<400> 1564
000
<210> 1565
<400> 1565
000
<210> 1566
<400> 1566
000
<210> 1567
<400> 1567
000
<210> 1568
<400> 1568
000
<210> 1569
<400> 1569
000
<210> 1570
<400> 1570
000
<210> 1571
<400> 1571
000
<210> 1572
<400> 1572
000
<210> 1573
<400> 1573
000
<210> 1574
<400> 1574
000
<210> 1575
<400> 1575
000
<210> 1576
<400> 1576
000
<210> 1577
<400> 1577
000
<210> 1578
<400> 1578
000
<210> 1579
<400> 1579
000
<210> 1580
<400> 1580
000
<210> 1581
<400> 1581
000
<210> 1582
<400> 1582
000
<210> 1583
<400> 1583
000
<210> 1584
<400> 1584
000
<210> 1585
<400> 1585
000
<210> 1586
<400> 1586
000
<210> 1587
<400> 1587
000
<210> 1588
<400> 1588
000
<210> 1589
<400> 1589
000
<210> 1590
<400> 1590
000
<210> 1591
<400> 1591
000
<210> 1592
<400> 1592
000
<210> 1593
<400> 1593
000
<210> 1594
<400> 1594
000
<210> 1595
<400> 1595
000
<210> 1596
<400> 1596
000
<210> 1597
<400> 1597
000
<210> 1598
<400> 1598
000
<210> 1599
<400> 1599
000
<210> 1600
<400> 1600
000
<210> 1601
<400> 1601
000
<210> 1602
<400> 1602
000
<210> 1603
<400> 1603
000
<210> 1604
<400> 1604
000
<210> 1605
<400> 1605
000
<210> 1606
<400> 1606
000
<210> 1607
<400> 1607
000
<210> 1608
<400> 1608
000
<210> 1609
<400> 1609
000
<210> 1610
<400> 1610
000
<210> 1611
<400> 1611
000
<210> 1612
<400> 1612
000
<210> 1613
<400> 1613
000
<210> 1614
<400> 1614
000
<210> 1615
<400> 1615
000
<210> 1616
<400> 1616
000
<210> 1617
<400> 1617
000
<210> 1618
<400> 1618
000
<210> 1619
<400> 1619
000
<210> 1620
<400> 1620
000
<210> 1621
<400> 1621
000
<210> 1622
<400> 1622
000
<210> 1623
<400> 1623
000
<210> 1624
<400> 1624
000
<210> 1625
<400> 1625
000
<210> 1626
<400> 1626
000
<210> 1627
<400> 1627
000
<210> 1628
<400> 1628
000
<210> 1629
<400> 1629
000
<210> 1630
<400> 1630
000
<210> 1631
<400> 1631
000
<210> 1632
<400> 1632
000
<210> 1633
<400> 1633
000
<210> 1634
<400> 1634
000
<210> 1635
<400> 1635
000
<210> 1636
<400> 1636
000
<210> 1637
<400> 1637
000
<210> 1638
<400> 1638
000
<210> 1639
<400> 1639
000
<210> 1640
<400> 1640
000
<210> 1641
<400> 1641
000
<210> 1642
<400> 1642
000
<210> 1643
<400> 1643
000
<210> 1644
<400> 1644
000
<210> 1645
<400> 1645
000
<210> 1646
<400> 1646
000
<210> 1647
<400> 1647
000
<210> 1648
<400> 1648
000
<210> 1649
<400> 1649
000
<210> 1650
<400> 1650
000
<210> 1651
<400> 1651
000
<210> 1652
<400> 1652
000
<210> 1653
<400> 1653
000
<210> 1654
<400> 1654
000
<210> 1655
<400> 1655
000
<210> 1656
<400> 1656
000
<210> 1657
<400> 1657
000
<210> 1658
<400> 1658
000
<210> 1659
<400> 1659
000
<210> 1660
<400> 1660
000
<210> 1661
<400> 1661
000
<210> 1662
<400> 1662
000
<210> 1663
<400> 1663
000
<210> 1664
<400> 1664
000
<210> 1665
<400> 1665
000
<210> 1666
<400> 1666
000
<210> 1667
<400> 1667
000
<210> 1668
<400> 1668
000
<210> 1669
<400> 1669
000
<210> 1670
<400> 1670
000
<210> 1671
<400> 1671
000
<210> 1672
<400> 1672
000
<210> 1673
<400> 1673
000
<210> 1674
<400> 1674
000
<210> 1675
<400> 1675
000
<210> 1676
<400> 1676
000
<210> 1677
<400> 1677
000
<210> 1678
<400> 1678
000
<210> 1679
<400> 1679
000
<210> 1680
<400> 1680
000
<210> 1681
<400> 1681
000
<210> 1682
<400> 1682
000
<210> 1683
<400> 1683
000
<210> 1684
<400> 1684
000
<210> 1685
<400> 1685
000
<210> 1686
<400> 1686
000
<210> 1687
<400> 1687
000
<210> 1688
<400> 1688
000
<210> 1689
<400> 1689
000
<210> 1690
<400> 1690
000
<210> 1691
<400> 1691
000
<210> 1692
<400> 1692
000
<210> 1693
<400> 1693
000
<210> 1694
<400> 1694
000
<210> 1695
<400> 1695
000
<210> 1696
<400> 1696
000
<210> 1697
<400> 1697
000
<210> 1698
<400> 1698
000
<210> 1699
<400> 1699
000
<210> 1700
<400> 1700
000
<210> 1701
<400> 1701
000
<210> 1702
<400> 1702
000
<210> 1703
<400> 1703
000
<210> 1704
<400> 1704
000
<210> 1705
<400> 1705
000
<210> 1706
<400> 1706
000
<210> 1707
<400> 1707
000
<210> 1708
<400> 1708
000
<210> 1709
<400> 1709
000
<210> 1710
<400> 1710
000
<210> 1711
<400> 1711
000
<210> 1712
<400> 1712
000
<210> 1713
<400> 1713
000
<210> 1714
<400> 1714
000
<210> 1715
<400> 1715
000
<210> 1716
<400> 1716
000
<210> 1717
<400> 1717
000
<210> 1718
<400> 1718
000
<210> 1719
<400> 1719
000
<210> 1720
<400> 1720
000
<210> 1721
<400> 1721
000
<210> 1722
<400> 1722
000
<210> 1723
<400> 1723
000
<210> 1724
<400> 1724
000
<210> 1725
<400> 1725
000
<210> 1726
<400> 1726
000
<210> 1727
<400> 1727
000
<210> 1728
<400> 1728
000
<210> 1729
<400> 1729
000
<210> 1730
<400> 1730
000
<210> 1731
<400> 1731
000
<210> 1732
<400> 1732
000
<210> 1733
<400> 1733
000
<210> 1734
<400> 1734
000
<210> 1735
<400> 1735
000
<210> 1736
<400> 1736
000
<210> 1737
<400> 1737
000
<210> 1738
<400> 1738
000
<210> 1739
<400> 1739
000
<210> 1740
<400> 1740
000
<210> 1741
<400> 1741
000
<210> 1742
<400> 1742
000
<210> 1743
<400> 1743
000
<210> 1744
<400> 1744
000
<210> 1745
<400> 1745
000
<210> 1746
<400> 1746
000
<210> 1747
<400> 1747
000
<210> 1748
<400> 1748
000
<210> 1749
<400> 1749
000
<210> 1750
<400> 1750
000
<210> 1751
<400> 1751
000
<210> 1752
<400> 1752
000
<210> 1753
<400> 1753
000
<210> 1754
<400> 1754
000
<210> 1755
<400> 1755
000
<210> 1756
<400> 1756
000
<210> 1757
<400> 1757
000
<210> 1758
<400> 1758
000
<210> 1759
<400> 1759
000
<210> 1760
<400> 1760
000
<210> 1761
<400> 1761
000
<210> 1762
<400> 1762
000
<210> 1763
<400> 1763
000
<210> 1764
<400> 1764
000
<210> 1765
<400> 1765
000
<210> 1766
<400> 1766
000
<210> 1767
<400> 1767
000
<210> 1768
<400> 1768
000
<210> 1769
<400> 1769
000
<210> 1770
<400> 1770
000
<210> 1771
<400> 1771
000
<210> 1772
<400> 1772
000
<210> 1773
<400> 1773
000
<210> 1774
<400> 1774
000
<210> 1775
<400> 1775
000
<210> 1776
<400> 1776
000
<210> 1777
<400> 1777
000
<210> 1778
<400> 1778
000
<210> 1779
<400> 1779
000
<210> 1780
<400> 1780
000
<210> 1781
<400> 1781
000
<210> 1782
<400> 1782
000
<210> 1783
<400> 1783
000
<210> 1784
<400> 1784
000
<210> 1785
<400> 1785
000
<210> 1786
<400> 1786
000
<210> 1787
<400> 1787
000
<210> 1788
<400> 1788
000
<210> 1789
<400> 1789
000
<210> 1790
<400> 1790
000
<210> 1791
<400> 1791
000
<210> 1792
<400> 1792
000
<210> 1793
<400> 1793
000
<210> 1794
<400> 1794
000
<210> 1795
<400> 1795
000
<210> 1796
<400> 1796
000
<210> 1797
<400> 1797
000
<210> 1798
<400> 1798
000
<210> 1799
<400> 1799
000
<210> 1800
<400> 1800
000
<210> 1801
<400> 1801
000
<210> 1802
<400> 1802
000
<210> 1803
<400> 1803
000
<210> 1804
<400> 1804
000
<210> 1805
<400> 1805
000
<210> 1806
<400> 1806
000
<210> 1807
<400> 1807
000
<210> 1808
<400> 1808
000
<210> 1809
<400> 1809
000
<210> 1810
<400> 1810
000
<210> 1811
<400> 1811
000
<210> 1812
<400> 1812
000
<210> 1813
<400> 1813
000
<210> 1814
<400> 1814
000
<210> 1815
<400> 1815
000
<210> 1816
<400> 1816
000
<210> 1817
<400> 1817
000
<210> 1818
<400> 1818
000
<210> 1819
<400> 1819
000
<210> 1820
<400> 1820
000
<210> 1821
<400> 1821
000
<210> 1822
<400> 1822
000
<210> 1823
<400> 1823
000
<210> 1824
<400> 1824
000
<210> 1825
<400> 1825
000
<210> 1826
<400> 1826
000
<210> 1827
<400> 1827
000
<210> 1828
<400> 1828
000
<210> 1829
<400> 1829
000
<210> 1830
<400> 1830
000
<210> 1831
<400> 1831
000
<210> 1832
<400> 1832
000
<210> 1833
<400> 1833
000
<210> 1834
<400> 1834
000
<210> 1835
<400> 1835
000
<210> 1836
<400> 1836
000
<210> 1837
<400> 1837
000
<210> 1838
<400> 1838
000
<210> 1839
<400> 1839
000
<210> 1840
<400> 1840
000
<210> 1841
<400> 1841
000
<210> 1842
<400> 1842
000
<210> 1843
<400> 1843
000
<210> 1844
<400> 1844
000
<210> 1845
<400> 1845
000
<210> 1846
<400> 1846
000
<210> 1847
<400> 1847
000
<210> 1848
<400> 1848
000
<210> 1849
<400> 1849
000
<210> 1850
<400> 1850
000
<210> 1851
<400> 1851
000
<210> 1852
<400> 1852
000
<210> 1853
<400> 1853
000
<210> 1854
<400> 1854
000
<210> 1855
<400> 1855
000
<210> 1856
<400> 1856
000
<210> 1857
<400> 1857
000
<210> 1858
<400> 1858
000
<210> 1859
<400> 1859
000
<210> 1860
<400> 1860
000
<210> 1861
<400> 1861
000
<210> 1862
<400> 1862
000
<210> 1863
<400> 1863
000
<210> 1864
<400> 1864
000
<210> 1865
<400> 1865
000
<210> 1866
<400> 1866
000
<210> 1867
<400> 1867
000
<210> 1868
<400> 1868
000
<210> 1869
<400> 1869
000
<210> 1870
<400> 1870
000
<210> 1871
<400> 1871
000
<210> 1872
<400> 1872
000
<210> 1873
<400> 1873
000
<210> 1874
<400> 1874
000
<210> 1875
<400> 1875
000
<210> 1876
<400> 1876
000
<210> 1877
<400> 1877
000
<210> 1878
<400> 1878
000
<210> 1879
<400> 1879
000
<210> 1880
<400> 1880
000
<210> 1881
<400> 1881
000
<210> 1882
<400> 1882
000
<210> 1883
<400> 1883
000
<210> 1884
<400> 1884
000
<210> 1885
<400> 1885
000
<210> 1886
<400> 1886
000
<210> 1887
<400> 1887
000
<210> 1888
<400> 1888
000
<210> 1889
<400> 1889
000
<210> 1890
<400> 1890
000
<210> 1891
<400> 1891
000
<210> 1892
<400> 1892
000
<210> 1893
<400> 1893
000
<210> 1894
<400> 1894
000
<210> 1895
<400> 1895
000
<210> 1896
<400> 1896
000
<210> 1897
<400> 1897
000
<210> 1898
<400> 1898
000
<210> 1899
<400> 1899
000
<210> 1900
<400> 1900
000
<210> 1901
<400> 1901
000
<210> 1902
<400> 1902
000
<210> 1903
<400> 1903
000
<210> 1904
<400> 1904
000
<210> 1905
<400> 1905
000
<210> 1906
<400> 1906
000
<210> 1907
<400> 1907
000
<210> 1908
<400> 1908
000
<210> 1909
<400> 1909
000
<210> 1910
<400> 1910
000
<210> 1911
<400> 1911
000
<210> 1912
<400> 1912
000
<210> 1913
<400> 1913
000
<210> 1914
<400> 1914
000
<210> 1915
<400> 1915
000
<210> 1916
<400> 1916
000
<210> 1917
<400> 1917
000
<210> 1918
<400> 1918
000
<210> 1919
<400> 1919
000
<210> 1920
<400> 1920
000
<210> 1921
<400> 1921
000
<210> 1922
<400> 1922
000
<210> 1923
<400> 1923
000
<210> 1924
<400> 1924
000
<210> 1925
<400> 1925
000
<210> 1926
<400> 1926
000
<210> 1927
<400> 1927
000
<210> 1928
<400> 1928
000
<210> 1929
<400> 1929
000
<210> 1930
<400> 1930
000
<210> 1931
<400> 1931
000
<210> 1932
<400> 1932
000
<210> 1933
<400> 1933
000
<210> 1934
<400> 1934
000
<210> 1935
<400> 1935
000
<210> 1936
<400> 1936
000
<210> 1937
<400> 1937
000
<210> 1938
<400> 1938
000
<210> 1939
<400> 1939
000
<210> 1940
<400> 1940
000
<210> 1941
<400> 1941
000
<210> 1942
<400> 1942
000
<210> 1943
<400> 1943
000
<210> 1944
<400> 1944
000
<210> 1945
<400> 1945
000
<210> 1946
<400> 1946
000
<210> 1947
<400> 1947
000
<210> 1948
<400> 1948
000
<210> 1949
<400> 1949
000
<210> 1950
<400> 1950
000
<210> 1951
<400> 1951
000
<210> 1952
<400> 1952
000
<210> 1953
<400> 1953
000
<210> 1954
<400> 1954
000
<210> 1955
<400> 1955
000
<210> 1956
<400> 1956
000
<210> 1957
<400> 1957
000
<210> 1958
<400> 1958
000
<210> 1959
<400> 1959
000
<210> 1960
<400> 1960
000
<210> 1961
<400> 1961
000
<210> 1962
<400> 1962
000
<210> 1963
<400> 1963
000
<210> 1964
<400> 1964
000
<210> 1965
<400> 1965
000
<210> 1966
<400> 1966
000
<210> 1967
<400> 1967
000
<210> 1968
<400> 1968
000
<210> 1969
<400> 1969
000
<210> 1970
<400> 1970
000
<210> 1971
<400> 1971
000
<210> 1972
<400> 1972
000
<210> 1973
<400> 1973
000
<210> 1974
<400> 1974
000
<210> 1975
<400> 1975
000
<210> 1976
<400> 1976
000
<210> 1977
<400> 1977
000
<210> 1978
<400> 1978
000
<210> 1979
<400> 1979
000
<210> 1980
<400> 1980
000
<210> 1981
<400> 1981
000
<210> 1982
<400> 1982
000
<210> 1983
<400> 1983
000
<210> 1984
<400> 1984
000
<210> 1985
<400> 1985
000
<210> 1986
<400> 1986
000
<210> 1987
<400> 1987
000
<210> 1988
<400> 1988
000
<210> 1989
<400> 1989
000
<210> 1990
<400> 1990
000
<210> 1991
<400> 1991
000
<210> 1992
<400> 1992
000
<210> 1993
<400> 1993
000
<210> 1994
<400> 1994
000
<210> 1995
<400> 1995
000
<210> 1996
<400> 1996
000
<210> 1997
<400> 1997
000
<210> 1998
<400> 1998
000
<210> 1999
<400> 1999
000
<210> 2000
<400> 2000
000
<210> 2001
<400> 2001
000
<210> 2002
<400> 2002
000
<210> 2003
<400> 2003
000
<210> 2004
<400> 2004
000
<210> 2005
<400> 2005
000
<210> 2006
<400> 2006
000
<210> 2007
<400> 2007
000
<210> 2008
<400> 2008
000
<210> 2009
<400> 2009
000
<210> 2010
<400> 2010
000
<210> 2011
<400> 2011
000
<210> 2012
<400> 2012
000
<210> 2013
<400> 2013
000
<210> 2014
<400> 2014
000
<210> 2015
<400> 2015
000
<210> 2016
<400> 2016
000
<210> 2017
<400> 2017
000
<210> 2018
<400> 2018
000
<210> 2019
<400> 2019
000
<210> 2020
<400> 2020
000
<210> 2021
<400> 2021
000
<210> 2022
<400> 2022
000
<210> 2023
<400> 2023
000
<210> 2024
<400> 2024
000
<210> 2025
<400> 2025
000
<210> 2026
<400> 2026
000
<210> 2027
<400> 2027
000
<210> 2028
<400> 2028
000
<210> 2029
<400> 2029
000
<210> 2030
<400> 2030
000
<210> 2031
<400> 2031
000
<210> 2032
<400> 2032
000
<210> 2033
<400> 2033
000
<210> 2034
<400> 2034
000
<210> 2035
<400> 2035
000
<210> 2036
<400> 2036
000
<210> 2037
<400> 2037
000
<210> 2038
<400> 2038
000
<210> 2039
<400> 2039
000
<210> 2040
<400> 2040
000
<210> 2041
<400> 2041
000
<210> 2042
<400> 2042
000
<210> 2043
<400> 2043
000
<210> 2044
<400> 2044
000
<210> 2045
<400> 2045
000
<210> 2046
<400> 2046
000
<210> 2047
<400> 2047
000
<210> 2048
<400> 2048
000
<210> 2049
<400> 2049
000
<210> 2050
<400> 2050
000
<210> 2051
<400> 2051
000
<210> 2052
<400> 2052
000
<210> 2053
<400> 2053
000
<210> 2054
<400> 2054
000
<210> 2055
<400> 2055
000
<210> 2056
<400> 2056
000
<210> 2057
<400> 2057
000
<210> 2058
<400> 2058
000
<210> 2059
<400> 2059
000
<210> 2060
<400> 2060
000
<210> 2061
<400> 2061
000
<210> 2062
<400> 2062
000
<210> 2063
<400> 2063
000
<210> 2064
<400> 2064
000
<210> 2065
<400> 2065
000
<210> 2066
<400> 2066
000
<210> 2067
<400> 2067
000
<210> 2068
<400> 2068
000
<210> 2069
<400> 2069
000
<210> 2070
<400> 2070
000
<210> 2071
<400> 2071
000
<210> 2072
<400> 2072
000
<210> 2073
<400> 2073
000
<210> 2074
<400> 2074
000
<210> 2075
<400> 2075
000
<210> 2076
<400> 2076
000
<210> 2077
<400> 2077
000
<210> 2078
<400> 2078
000
<210> 2079
<400> 2079
000
<210> 2080
<400> 2080
000
<210> 2081
<400> 2081
000
<210> 2082
<400> 2082
000
<210> 2083
<400> 2083
000
<210> 2084
<400> 2084
000
<210> 2085
<400> 2085
000
<210> 2086
<400> 2086
000
<210> 2087
<400> 2087
000
<210> 2088
<400> 2088
000
<210> 2089
<400> 2089
000
<210> 2090
<400> 2090
000
<210> 2091
<400> 2091
000
<210> 2092
<400> 2092
000
<210> 2093
<400> 2093
000
<210> 2094
<400> 2094
000
<210> 2095
<400> 2095
000
<210> 2096
<400> 2096
000
<210> 2097
<400> 2097
000
<210> 2098
<400> 2098
000
<210> 2099
<400> 2099
000
<210> 2100
<400> 2100
000
<210> 2101
<400> 2101
000
<210> 2102
<400> 2102
000
<210> 2103
<400> 2103
000
<210> 2104
<400> 2104
000
<210> 2105
<400> 2105
000
<210> 2106
<400> 2106
000
<210> 2107
<400> 2107
000
<210> 2108
<400> 2108
000
<210> 2109
<400> 2109
000
<210> 2110
<400> 2110
000
<210> 2111
<400> 2111
000
<210> 2112
<400> 2112
000
<210> 2113
<400> 2113
000
<210> 2114
<400> 2114
000
<210> 2115
<400> 2115
000
<210> 2116
<400> 2116
000
<210> 2117
<400> 2117
000
<210> 2118
<400> 2118
000
<210> 2119
<400> 2119
000
<210> 2120
<400> 2120
000
<210> 2121
<400> 2121
000
<210> 2122
<400> 2122
000
<210> 2123
<400> 2123
000
<210> 2124
<400> 2124
000
<210> 2125
<400> 2125
000
<210> 2126
<400> 2126
000
<210> 2127
<400> 2127
000
<210> 2128
<400> 2128
000
<210> 2129
<400> 2129
000
<210> 2130
<400> 2130
000
<210> 2131
<400> 2131
000
<210> 2132
<400> 2132
000
<210> 2133
<400> 2133
000
<210> 2134
<400> 2134
000
<210> 2135
<400> 2135
000
<210> 2136
<400> 2136
000
<210> 2137
<400> 2137
000
<210> 2138
<400> 2138
000
<210> 2139
<400> 2139
000
<210> 2140
<400> 2140
000
<210> 2141
<400> 2141
000
<210> 2142
<400> 2142
000
<210> 2143
<400> 2143
000
<210> 2144
<400> 2144
000
<210> 2145
<400> 2145
000
<210> 2146
<400> 2146
000
<210> 2147
<400> 2147
000
<210> 2148
<400> 2148
000
<210> 2149
<400> 2149
000
<210> 2150
<400> 2150
000
<210> 2151
<400> 2151
000
<210> 2152
<400> 2152
000
<210> 2153
<400> 2153
000
<210> 2154
<400> 2154
000
<210> 2155
<400> 2155
000
<210> 2156
<400> 2156
000
<210> 2157
<400> 2157
000
<210> 2158
<400> 2158
000
<210> 2159
<400> 2159
000
<210> 2160
<400> 2160
000
<210> 2161
<400> 2161
000
<210> 2162
<400> 2162
000
<210> 2163
<400> 2163
000
<210> 2164
<400> 2164
000
<210> 2165
<400> 2165
000
<210> 2166
<400> 2166
000
<210> 2167
<400> 2167
000
<210> 2168
<400> 2168
000
<210> 2169
<400> 2169
000
<210> 2170
<400> 2170
000
<210> 2171
<400> 2171
000
<210> 2172
<400> 2172
000
<210> 2173
<400> 2173
000
<210> 2174
<400> 2174
000
<210> 2175
<400> 2175
000
<210> 2176
<400> 2176
000
<210> 2177
<400> 2177
000
<210> 2178
<400> 2178
000
<210> 2179
<400> 2179
000
<210> 2180
<400> 2180
000
<210> 2181
<400> 2181
000
<210> 2182
<400> 2182
000
<210> 2183
<400> 2183
000
<210> 2184
<400> 2184
000
<210> 2185
<400> 2185
000
<210> 2186
<400> 2186
000
<210> 2187
<400> 2187
000
<210> 2188
<400> 2188
000
<210> 2189
<400> 2189
000
<210> 2190
<400> 2190
000
<210> 2191
<400> 2191
000
<210> 2192
<400> 2192
000
<210> 2193
<400> 2193
000
<210> 2194
<400> 2194
000
<210> 2195
<400> 2195
000
<210> 2196
<400> 2196
000
<210> 2197
<400> 2197
000
<210> 2198
<400> 2198
000
<210> 2199
<400> 2199
000
<210> 2200
<400> 2200
000
<210> 2201
<400> 2201
000
<210> 2202
<400> 2202
000
<210> 2203
<400> 2203
000
<210> 2204
<400> 2204
000
<210> 2205
<400> 2205
000
<210> 2206
<400> 2206
000
<210> 2207
<400> 2207
000
<210> 2208
<400> 2208
000
<210> 2209
<400> 2209
000
<210> 2210
<400> 2210
000
<210> 2211
<400> 2211
000
<210> 2212
<400> 2212
000
<210> 2213
<400> 2213
000
<210> 2214
<400> 2214
000
<210> 2215
<400> 2215
000
<210> 2216
<400> 2216
000
<210> 2217
<400> 2217
000
<210> 2218
<400> 2218
000
<210> 2219
<400> 2219
000
<210> 2220
<400> 2220
000
<210> 2221
<400> 2221
000
<210> 2222
<400> 2222
000
<210> 2223
<400> 2223
000
<210> 2224
<400> 2224
000
<210> 2225
<400> 2225
000
<210> 2226
<400> 2226
000
<210> 2227
<400> 2227
000
<210> 2228
<400> 2228
000
<210> 2229
<400> 2229
000
<210> 2230
<400> 2230
000
<210> 2231
<400> 2231
000
<210> 2232
<400> 2232
000
<210> 2233
<400> 2233
000
<210> 2234
<400> 2234
000
<210> 2235
<400> 2235
000
<210> 2236
<400> 2236
000
<210> 2237
<400> 2237
000
<210> 2238
<400> 2238
000
<210> 2239
<400> 2239
000
<210> 2240
<400> 2240
000
<210> 2241
<400> 2241
000
<210> 2242
<400> 2242
000
<210> 2243
<400> 2243
000
<210> 2244
<400> 2244
000
<210> 2245
<400> 2245
000
<210> 2246
<400> 2246
000
<210> 2247
<400> 2247
000
<210> 2248
<400> 2248
000
<210> 2249
<400> 2249
000
<210> 2250
<400> 2250
000
<210> 2251
<400> 2251
000
<210> 2252
<400> 2252
000
<210> 2253
<400> 2253
000
<210> 2254
<400> 2254
000
<210> 2255
<400> 2255
000
<210> 2256
<400> 2256
000
<210> 2257
<400> 2257
000
<210> 2258
<400> 2258
000
<210> 2259
<400> 2259
000
<210> 2260
<400> 2260
000
<210> 2261
<400> 2261
000
<210> 2262
<400> 2262
000
<210> 2263
<400> 2263
000
<210> 2264
<400> 2264
000
<210> 2265
<400> 2265
000
<210> 2266
<400> 2266
000
<210> 2267
<400> 2267
000
<210> 2268
<400> 2268
000
<210> 2269
<400> 2269
000
<210> 2270
<400> 2270
000
<210> 2271
<400> 2271
000
<210> 2272
<400> 2272
000
<210> 2273
<400> 2273
000
<210> 2274
<400> 2274
000
<210> 2275
<400> 2275
000
<210> 2276
<400> 2276
000
<210> 2277
<400> 2277
000
<210> 2278
<400> 2278
000
<210> 2279
<400> 2279
000
<210> 2280
<400> 2280
000
<210> 2281
<400> 2281
000
<210> 2282
<400> 2282
000
<210> 2283
<400> 2283
000
<210> 2284
<400> 2284
000
<210> 2285
<400> 2285
000
<210> 2286
<400> 2286
000
<210> 2287
<400> 2287
000
<210> 2288
<400> 2288
000
<210> 2289
<400> 2289
000
<210> 2290
<400> 2290
000
<210> 2291
<400> 2291
000
<210> 2292
<400> 2292
000
<210> 2293
<400> 2293
000
<210> 2294
<400> 2294
000
<210> 2295
<400> 2295
000
<210> 2296
<400> 2296
000
<210> 2297
<400> 2297
000
<210> 2298
<400> 2298
000
<210> 2299
<400> 2299
000
<210> 2300
<400> 2300
000
<210> 2301
<400> 2301
000
<210> 2302
<400> 2302
000
<210> 2303
<400> 2303
000
<210> 2304
<400> 2304
000
<210> 2305
<400> 2305
000
<210> 2306
<400> 2306
000
<210> 2307
<400> 2307
000
<210> 2308
<400> 2308
000
<210> 2309
<400> 2309
000
<210> 2310
<400> 2310
000
<210> 2311
<400> 2311
000
<210> 2312
<400> 2312
000
<210> 2313
<400> 2313
000
<210> 2314
<400> 2314
000
<210> 2315
<400> 2315
000
<210> 2316
<400> 2316
000
<210> 2317
<400> 2317
000
<210> 2318
<400> 2318
000
<210> 2319
<400> 2319
000
<210> 2320
<400> 2320
000
<210> 2321
<400> 2321
000
<210> 2322
<400> 2322
000
<210> 2323
<400> 2323
000
<210> 2324
<400> 2324
000
<210> 2325
<400> 2325
000
<210> 2326
<400> 2326
000
<210> 2327
<400> 2327
000
<210> 2328
<400> 2328
000
<210> 2329
<400> 2329
000
<210> 2330
<400> 2330
000
<210> 2331
<400> 2331
000
<210> 2332
<400> 2332
000
<210> 2333
<400> 2333
000
<210> 2334
<400> 2334
000
<210> 2335
<400> 2335
000
<210> 2336
<400> 2336
000
<210> 2337
<400> 2337
000
<210> 2338
<400> 2338
000
<210> 2339
<400> 2339
000
<210> 2340
<400> 2340
000
<210> 2341
<400> 2341
000
<210> 2342
<400> 2342
000
<210> 2343
<400> 2343
000
<210> 2344
<400> 2344
000
<210> 2345
<400> 2345
000
<210> 2346
<400> 2346
000
<210> 2347
<400> 2347
000
<210> 2348
<400> 2348
000
<210> 2349
<400> 2349
000
<210> 2350
<400> 2350
000
<210> 2351
<400> 2351
000
<210> 2352
<400> 2352
000
<210> 2353
<400> 2353
000
<210> 2354
<400> 2354
000
<210> 2355
<400> 2355
000
<210> 2356
<400> 2356
000
<210> 2357
<400> 2357
000
<210> 2358
<400> 2358
000
<210> 2359
<400> 2359
000
<210> 2360
<400> 2360
000
<210> 2361
<400> 2361
000
<210> 2362
<400> 2362
000
<210> 2363
<400> 2363
000
<210> 2364
<400> 2364
000
<210> 2365
<400> 2365
000
<210> 2366
<400> 2366
000
<210> 2367
<400> 2367
000
<210> 2368
<400> 2368
000
<210> 2369
<400> 2369
000
<210> 2370
<400> 2370
000
<210> 2371
<400> 2371
000
<210> 2372
<400> 2372
000
<210> 2373
<400> 2373
000
<210> 2374
<400> 2374
000
<210> 2375
<400> 2375
000
<210> 2376
<400> 2376
000
<210> 2377
<400> 2377
000
<210> 2378
<400> 2378
000
<210> 2379
<400> 2379
000
<210> 2380
<400> 2380
000
<210> 2381
<400> 2381
000
<210> 2382
<400> 2382
000
<210> 2383
<400> 2383
000
<210> 2384
<400> 2384
000
<210> 2385
<400> 2385
000
<210> 2386
<400> 2386
000
<210> 2387
<400> 2387
000
<210> 2388
<400> 2388
000
<210> 2389
<400> 2389
000
<210> 2390
<400> 2390
000
<210> 2391
<400> 2391
000
<210> 2392
<400> 2392
000
<210> 2393
<400> 2393
000
<210> 2394
<400> 2394
000
<210> 2395
<400> 2395
000
<210> 2396
<400> 2396
000
<210> 2397
<400> 2397
000
<210> 2398
<400> 2398
000
<210> 2399
<400> 2399
000
<210> 2400
<400> 2400
000
<210> 2401
<400> 2401
000
<210> 2402
<400> 2402
000
<210> 2403
<400> 2403
000
<210> 2404
<400> 2404
000
<210> 2405
<400> 2405
000
<210> 2406
<400> 2406
000
<210> 2407
<400> 2407
000
<210> 2408
<400> 2408
000
<210> 2409
<400> 2409
000
<210> 2410
<400> 2410
000
<210> 2411
<400> 2411
000
<210> 2412
<400> 2412
000
<210> 2413
<400> 2413
000
<210> 2414
<400> 2414
000
<210> 2415
<400> 2415
000
<210> 2416
<400> 2416
000
<210> 2417
<400> 2417
000
<210> 2418
<400> 2418
000
<210> 2419
<400> 2419
000
<210> 2420
<400> 2420
000
<210> 2421
<400> 2421
000
<210> 2422
<400> 2422
000
<210> 2423
<400> 2423
000
<210> 2424
<400> 2424
000
<210> 2425
<400> 2425
000
<210> 2426
<400> 2426
000
<210> 2427
<400> 2427
000
<210> 2428
<400> 2428
000
<210> 2429
<400> 2429
000
<210> 2430
<400> 2430
000
<210> 2431
<400> 2431
000
<210> 2432
<400> 2432
000
<210> 2433
<400> 2433
000
<210> 2434
<400> 2434
000
<210> 2435
<400> 2435
000
<210> 2436
<400> 2436
000
<210> 2437
<400> 2437
000
<210> 2438
<400> 2438
000
<210> 2439
<400> 2439
000
<210> 2440
<400> 2440
000
<210> 2441
<400> 2441
000
<210> 2442
<400> 2442
000
<210> 2443
<400> 2443
000
<210> 2444
<400> 2444
000
<210> 2445
<400> 2445
000
<210> 2446
<400> 2446
000
<210> 2447
<400> 2447
000
<210> 2448
<400> 2448
000
<210> 2449
<400> 2449
000
<210> 2450
<400> 2450
000
<210> 2451
<400> 2451
000
<210> 2452
<400> 2452
000
<210> 2453
<400> 2453
000
<210> 2454
<400> 2454
000
<210> 2455
<400> 2455
000
<210> 2456
<400> 2456
000
<210> 2457
<400> 2457
000
<210> 2458
<400> 2458
000
<210> 2459
<400> 2459
000
<210> 2460
<400> 2460
000
<210> 2461
<400> 2461
000
<210> 2462
<400> 2462
000
<210> 2463
<400> 2463
000
<210> 2464
<400> 2464
000
<210> 2465
<400> 2465
000
<210> 2466
<400> 2466
000
<210> 2467
<400> 2467
000
<210> 2468
<400> 2468
000
<210> 2469
<400> 2469
000
<210> 2470
<400> 2470
000
<210> 2471
<400> 2471
000
<210> 2472
<400> 2472
000
<210> 2473
<400> 2473
000
<210> 2474
<400> 2474
000
<210> 2475
<400> 2475
000
<210> 2476
<400> 2476
000
<210> 2477
<400> 2477
000
<210> 2478
<400> 2478
000
<210> 2479
<400> 2479
000
<210> 2480
<400> 2480
000
<210> 2481
<400> 2481
000
<210> 2482
<400> 2482
000
<210> 2483
<400> 2483
000
<210> 2484
<400> 2484
000
<210> 2485
<400> 2485
000
<210> 2486
<400> 2486
000
<210> 2487
<400> 2487
000
<210> 2488
<400> 2488
000
<210> 2489
<400> 2489
000
<210> 2490
<400> 2490
000
<210> 2491
<400> 2491
000
<210> 2492
<400> 2492
000
<210> 2493
<400> 2493
000
<210> 2494
<400> 2494
000
<210> 2495
<400> 2495
000
<210> 2496
<400> 2496
000
<210> 2497
<400> 2497
000
<210> 2498
<400> 2498
000
<210> 2499
<400> 2499
000
<210> 2500
<400> 2500
000
<210> 2501
<400> 2501
000
<210> 2502
<400> 2502
000
<210> 2503
<400> 2503
000
<210> 2504
<400> 2504
000
<210> 2505
<400> 2505
000
<210> 2506
<400> 2506
000
<210> 2507
<400> 2507
000
<210> 2508
<400> 2508
000
<210> 2509
<400> 2509
000
<210> 2510
<400> 2510
000
<210> 2511
<400> 2511
000
<210> 2512
<400> 2512
000
<210> 2513
<400> 2513
000
<210> 2514
<400> 2514
000
<210> 2515
<400> 2515
000
<210> 2516
<400> 2516
000
<210> 2517
<400> 2517
000
<210> 2518
<400> 2518
000
<210> 2519
<400> 2519
000
<210> 2520
<400> 2520
000
<210> 2521
<400> 2521
000
<210> 2522
<400> 2522
000
<210> 2523
<400> 2523
000
<210> 2524
<400> 2524
000
<210> 2525
<400> 2525
000
<210> 2526
<400> 2526
000
<210> 2527
<400> 2527
000
<210> 2528
<400> 2528
000
<210> 2529
<400> 2529
000
<210> 2530
<400> 2530
000
<210> 2531
<400> 2531
000
<210> 2532
<400> 2532
000
<210> 2533
<400> 2533
000
<210> 2534
<400> 2534
000
<210> 2535
<400> 2535
000
<210> 2536
<400> 2536
000
<210> 2537
<400> 2537
000
<210> 2538
<400> 2538
000
<210> 2539
<400> 2539
000
<210> 2540
<400> 2540
000
<210> 2541
<400> 2541
000
<210> 2542
<400> 2542
000
<210> 2543
<400> 2543
000
<210> 2544
<400> 2544
000
<210> 2545
<400> 2545
000
<210> 2546
<400> 2546
000
<210> 2547
<400> 2547
000
<210> 2548
<400> 2548
000
<210> 2549
<400> 2549
000
<210> 2550
<400> 2550
000
<210> 2551
<400> 2551
000
<210> 2552
<400> 2552
000
<210> 2553
<400> 2553
000
<210> 2554
<400> 2554
000
<210> 2555
<400> 2555
000
<210> 2556
<400> 2556
000
<210> 2557
<400> 2557
000
<210> 2558
<400> 2558
000
<210> 2559
<400> 2559
000
<210> 2560
<400> 2560
000
<210> 2561
<400> 2561
000
<210> 2562
<400> 2562
000
<210> 2563
<400> 2563
000
<210> 2564
<400> 2564
000
<210> 2565
<400> 2565
000
<210> 2566
<400> 2566
000
<210> 2567
<400> 2567
000
<210> 2568
<400> 2568
000
<210> 2569
<400> 2569
000
<210> 2570
<400> 2570
000
<210> 2571
<400> 2571
000
<210> 2572
<400> 2572
000
<210> 2573
<400> 2573
000
<210> 2574
<400> 2574
000
<210> 2575
<400> 2575
000
<210> 2576
<400> 2576
000
<210> 2577
<400> 2577
000
<210> 2578
<400> 2578
000
<210> 2579
<400> 2579
000
<210> 2580
<400> 2580
000
<210> 2581
<400> 2581
000
<210> 2582
<400> 2582
000
<210> 2583
<400> 2583
000
<210> 2584
<400> 2584
000
<210> 2585
<400> 2585
000
<210> 2586
<400> 2586
000
<210> 2587
<400> 2587
000
<210> 2588
<400> 2588
000
<210> 2589
<400> 2589
000
<210> 2590
<400> 2590
000
<210> 2591
<400> 2591
000
<210> 2592
<400> 2592
000
<210> 2593
<400> 2593
000
<210> 2594
<400> 2594
000
<210> 2595
<400> 2595
000
<210> 2596
<400> 2596
000
<210> 2597
<400> 2597
000
<210> 2598
<400> 2598
000
<210> 2599
<400> 2599
000
<210> 2600
<400> 2600
000
<210> 2601
<400> 2601
000
<210> 2602
<400> 2602
000
<210> 2603
<400> 2603
000
<210> 2604
<400> 2604
000
<210> 2605
<400> 2605
000
<210> 2606
<400> 2606
000
<210> 2607
<400> 2607
000
<210> 2608
<400> 2608
000
<210> 2609
<400> 2609
000
<210> 2610
<400> 2610
000
<210> 2611
<400> 2611
000
<210> 2612
<400> 2612
000
<210> 2613
<400> 2613
000
<210> 2614
<400> 2614
000
<210> 2615
<400> 2615
000
<210> 2616
<400> 2616
000
<210> 2617
<400> 2617
000
<210> 2618
<400> 2618
000
<210> 2619
<400> 2619
000
<210> 2620
<400> 2620
000
<210> 2621
<400> 2621
000
<210> 2622
<400> 2622
000
<210> 2623
<400> 2623
000
<210> 2624
<400> 2624
000
<210> 2625
<400> 2625
000
<210> 2626
<400> 2626
000
<210> 2627
<400> 2627
000
<210> 2628
<400> 2628
000
<210> 2629
<400> 2629
000
<210> 2630
<400> 2630
000
<210> 2631
<400> 2631
000
<210> 2632
<400> 2632
000
<210> 2633
<400> 2633
000
<210> 2634
<400> 2634
000
<210> 2635
<400> 2635
000
<210> 2636
<400> 2636
000
<210> 2637
<400> 2637
000
<210> 2638
<400> 2638
000
<210> 2639
<400> 2639
000
<210> 2640
<400> 2640
000
<210> 2641
<400> 2641
000
<210> 2642
<400> 2642
000
<210> 2643
<400> 2643
000
<210> 2644
<400> 2644
000
<210> 2645
<400> 2645
000
<210> 2646
<400> 2646
000
<210> 2647
<400> 2647
000
<210> 2648
<400> 2648
000
<210> 2649
<400> 2649
000
<210> 2650
<400> 2650
000
<210> 2651
<400> 2651
000
<210> 2652
<400> 2652
000
<210> 2653
<400> 2653
000
<210> 2654
<400> 2654
000
<210> 2655
<400> 2655
000
<210> 2656
<400> 2656
000
<210> 2657
<400> 2657
000
<210> 2658
<400> 2658
000
<210> 2659
<400> 2659
000
<210> 2660
<400> 2660
000
<210> 2661
<400> 2661
000
<210> 2662
<400> 2662
000
<210> 2663
<400> 2663
000
<210> 2664
<400> 2664
000
<210> 2665
<400> 2665
000
<210> 2666
<400> 2666
000
<210> 2667
<400> 2667
000
<210> 2668
<400> 2668
000
<210> 2669
<400> 2669
000
<210> 2670
<400> 2670
000
<210> 2671
<400> 2671
000
<210> 2672
<400> 2672
000
<210> 2673
<400> 2673
000
<210> 2674
<400> 2674
000
<210> 2675
<400> 2675
000
<210> 2676
<400> 2676
000
<210> 2677
<400> 2677
000
<210> 2678
<400> 2678
000
<210> 2679
<400> 2679
000
<210> 2680
<400> 2680
000
<210> 2681
<400> 2681
000
<210> 2682
<400> 2682
000
<210> 2683
<400> 2683
000
<210> 2684
<400> 2684
000
<210> 2685
<400> 2685
000
<210> 2686
<400> 2686
000
<210> 2687
<400> 2687
000
<210> 2688
<400> 2688
000
<210> 2689
<400> 2689
000
<210> 2690
<400> 2690
000
<210> 2691
<400> 2691
000
<210> 2692
<400> 2692
000
<210> 2693
<400> 2693
000
<210> 2694
<400> 2694
000
<210> 2695
<400> 2695
000
<210> 2696
<400> 2696
000
<210> 2697
<400> 2697
000
<210> 2698
<400> 2698
000
<210> 2699
<400> 2699
000
<210> 2700
<400> 2700
000
<210> 2701
<400> 2701
000
<210> 2702
<400> 2702
000
<210> 2703
<400> 2703
000
<210> 2704
<400> 2704
000
<210> 2705
<400> 2705
000
<210> 2706
<400> 2706
000
<210> 2707
<400> 2707
000
<210> 2708
<400> 2708
000
<210> 2709
<400> 2709
000
<210> 2710
<400> 2710
000
<210> 2711
<400> 2711
000
<210> 2712
<400> 2712
000
<210> 2713
<400> 2713
000
<210> 2714
<400> 2714
000
<210> 2715
<400> 2715
000
<210> 2716
<400> 2716
000
<210> 2717
<400> 2717
000
<210> 2718
<400> 2718
000
<210> 2719
<400> 2719
000
<210> 2720
<400> 2720
000
<210> 2721
<400> 2721
000
<210> 2722
<400> 2722
000
<210> 2723
<400> 2723
000
<210> 2724
<400> 2724
000
<210> 2725
<400> 2725
000
<210> 2726
<400> 2726
000
<210> 2727
<400> 2727
000
<210> 2728
<400> 2728
000
<210> 2729
<400> 2729
000
<210> 2730
<400> 2730
000
<210> 2731
<400> 2731
000
<210> 2732
<400> 2732
000
<210> 2733
<400> 2733
000
<210> 2734
<400> 2734
000
<210> 2735
<400> 2735
000
<210> 2736
<400> 2736
000
<210> 2737
<400> 2737
000
<210> 2738
<400> 2738
000
<210> 2739
<400> 2739
000
<210> 2740
<400> 2740
000
<210> 2741
<400> 2741
000
<210> 2742
<400> 2742
000
<210> 2743
<400> 2743
000
<210> 2744
<400> 2744
000
<210> 2745
<400> 2745
000
<210> 2746
<400> 2746
000
<210> 2747
<400> 2747
000
<210> 2748
<400> 2748
000
<210> 2749
<400> 2749
000
<210> 2750
<400> 2750
000
<210> 2751
<400> 2751
000
<210> 2752
<400> 2752
000
<210> 2753
<400> 2753
000
<210> 2754
<400> 2754
000
<210> 2755
<400> 2755
000
<210> 2756
<400> 2756
000
<210> 2757
<400> 2757
000
<210> 2758
<400> 2758
000
<210> 2759
<400> 2759
000
<210> 2760
<400> 2760
000
<210> 2761
<400> 2761
000
<210> 2762
<400> 2762
000
<210> 2763
<400> 2763
000
<210> 2764
<400> 2764
000
<210> 2765
<400> 2765
000
<210> 2766
<400> 2766
000
<210> 2767
<400> 2767
000
<210> 2768
<400> 2768
000
<210> 2769
<400> 2769
000
<210> 2770
<400> 2770
000
<210> 2771
<400> 2771
000
<210> 2772
<400> 2772
000
<210> 2773
<400> 2773
000
<210> 2774
<400> 2774
000
<210> 2775
<400> 2775
000
<210> 2776
<400> 2776
000
<210> 2777
<400> 2777
000
<210> 2778
<400> 2778
000
<210> 2779
<400> 2779
000
<210> 2780
<400> 2780
000
<210> 2781
<400> 2781
000
<210> 2782
<400> 2782
000
<210> 2783
<400> 2783
000
<210> 2784
<400> 2784
000
<210> 2785
<400> 2785
000
<210> 2786
<400> 2786
000
<210> 2787
<400> 2787
000
<210> 2788
<400> 2788
000
<210> 2789
<400> 2789
000
<210> 2790
<400> 2790
000
<210> 2791
<400> 2791
000
<210> 2792
<400> 2792
000
<210> 2793
<400> 2793
000
<210> 2794
<400> 2794
000
<210> 2795
<400> 2795
000
<210> 2796
<400> 2796
000
<210> 2797
<400> 2797
000
<210> 2798
<400> 2798
000
<210> 2799
<400> 2799
000
<210> 2800
<400> 2800
000
<210> 2801
<400> 2801
000
<210> 2802
<400> 2802
000
<210> 2803
<400> 2803
000
<210> 2804
<400> 2804
000
<210> 2805
<400> 2805
000
<210> 2806
<400> 2806
000
<210> 2807
<400> 2807
000
<210> 2808
<400> 2808
000
<210> 2809
<400> 2809
000
<210> 2810
<400> 2810
000
<210> 2811
<400> 2811
000
<210> 2812
<400> 2812
000
<210> 2813
<400> 2813
000
<210> 2814
<400> 2814
000
<210> 2815
<400> 2815
000
<210> 2816
<400> 2816
000
<210> 2817
<400> 2817
000
<210> 2818
<400> 2818
000
<210> 2819
<400> 2819
000
<210> 2820
<400> 2820
000
<210> 2821
<400> 2821
000
<210> 2822
<400> 2822
000
<210> 2823
<400> 2823
000
<210> 2824
<400> 2824
000
<210> 2825
<400> 2825
000
<210> 2826
<400> 2826
000
<210> 2827
<400> 2827
000
<210> 2828
<400> 2828
000
<210> 2829
<400> 2829
000
<210> 2830
<400> 2830
000
<210> 2831
<400> 2831
000
<210> 2832
<400> 2832
000
<210> 2833
<400> 2833
000
<210> 2834
<400> 2834
000
<210> 2835
<400> 2835
000
<210> 2836
<400> 2836
000
<210> 2837
<400> 2837
000
<210> 2838
<400> 2838
000
<210> 2839
<400> 2839
000
<210> 2840
<400> 2840
000
<210> 2841
<400> 2841
000
<210> 2842
<400> 2842
000
<210> 2843
<400> 2843
000
<210> 2844
<400> 2844
000
<210> 2845
<400> 2845
000
<210> 2846
<400> 2846
000
<210> 2847
<400> 2847
000
<210> 2848
<400> 2848
000
<210> 2849
<400> 2849
000
<210> 2850
<400> 2850
000
<210> 2851
<400> 2851
000
<210> 2852
<400> 2852
000
<210> 2853
<400> 2853
000
<210> 2854
<400> 2854
000
<210> 2855
<400> 2855
000
<210> 2856
<400> 2856
000
<210> 2857
<400> 2857
000
<210> 2858
<400> 2858
000
<210> 2859
<400> 2859
000
<210> 2860
<400> 2860
000
<210> 2861
<400> 2861
000
<210> 2862
<400> 2862
000
<210> 2863
<400> 2863
000
<210> 2864
<400> 2864
000
<210> 2865
<400> 2865
000
<210> 2866
<400> 2866
000
<210> 2867
<400> 2867
000
<210> 2868
<400> 2868
000
<210> 2869
<400> 2869
000
<210> 2870
<400> 2870
000
<210> 2871
<400> 2871
000
<210> 2872
<400> 2872
000
<210> 2873
<400> 2873
000
<210> 2874
<400> 2874
000
<210> 2875
<400> 2875
000
<210> 2876
<400> 2876
000
<210> 2877
<400> 2877
000
<210> 2878
<400> 2878
000
<210> 2879
<400> 2879
000
<210> 2880
<400> 2880
000
<210> 2881
<400> 2881
000
<210> 2882
<400> 2882
000
<210> 2883
<400> 2883
000
<210> 2884
<400> 2884
000
<210> 2885
<400> 2885
000
<210> 2886
<400> 2886
000
<210> 2887
<400> 2887
000
<210> 2888
<400> 2888
000
<210> 2889
<400> 2889
000
<210> 2890
<400> 2890
000
<210> 2891
<400> 2891
000
<210> 2892
<400> 2892
000
<210> 2893
<400> 2893
000
<210> 2894
<400> 2894
000
<210> 2895
<400> 2895
000
<210> 2896
<400> 2896
000
<210> 2897
<400> 2897
000
<210> 2898
<400> 2898
000
<210> 2899
<400> 2899
000
<210> 2900
<400> 2900
000
<210> 2901
<400> 2901
000
<210> 2902
<400> 2902
000
<210> 2903
<400> 2903
000
<210> 2904
<400> 2904
000
<210> 2905
<400> 2905
000
<210> 2906
<400> 2906
000
<210> 2907
<400> 2907
000
<210> 2908
<400> 2908
000
<210> 2909
<400> 2909
000
<210> 2910
<400> 2910
000
<210> 2911
<400> 2911
000
<210> 2912
<400> 2912
000
<210> 2913
<400> 2913
000
<210> 2914
<400> 2914
000
<210> 2915
<400> 2915
000
<210> 2916
<400> 2916
000
<210> 2917
<400> 2917
000
<210> 2918
<400> 2918
000
<210> 2919
<400> 2919
000
<210> 2920
<400> 2920
000
<210> 2921
<400> 2921
000
<210> 2922
<400> 2922
000
<210> 2923
<400> 2923
000
<210> 2924
<400> 2924
000
<210> 2925
<400> 2925
000
<210> 2926
<400> 2926
000
<210> 2927
<400> 2927
000
<210> 2928
<400> 2928
000
<210> 2929
<400> 2929
000
<210> 2930
<400> 2930
000
<210> 2931
<400> 2931
000
<210> 2932
<400> 2932
000
<210> 2933
<400> 2933
000
<210> 2934
<400> 2934
000
<210> 2935
<400> 2935
000
<210> 2936
<400> 2936
000
<210> 2937
<400> 2937
000
<210> 2938
<400> 2938
000
<210> 2939
<400> 2939
000
<210> 2940
<400> 2940
000
<210> 2941
<400> 2941
000
<210> 2942
<400> 2942
000
<210> 2943
<400> 2943
000
<210> 2944
<400> 2944
000
<210> 2945
<400> 2945
000
<210> 2946
<400> 2946
000
<210> 2947
<400> 2947
000
<210> 2948
<400> 2948
000
<210> 2949
<400> 2949
000
<210> 2950
<400> 2950
000
<210> 2951
<400> 2951
000
<210> 2952
<400> 2952
000
<210> 2953
<400> 2953
000
<210> 2954
<400> 2954
000
<210> 2955
<400> 2955
000
<210> 2956
<400> 2956
000
<210> 2957
<400> 2957
000
<210> 2958
<400> 2958
000
<210> 2959
<400> 2959
000
<210> 2960
<400> 2960
000
<210> 2961
<400> 2961
000
<210> 2962
<400> 2962
000
<210> 2963
<400> 2963
000
<210> 2964
<400> 2964
000
<210> 2965
<400> 2965
000
<210> 2966
<400> 2966
000
<210> 2967
<400> 2967
000
<210> 2968
<400> 2968
000
<210> 2969
<400> 2969
000
<210> 2970
<400> 2970
000
<210> 2971
<400> 2971
000
<210> 2972
<400> 2972
000
<210> 2973
<400> 2973
000
<210> 2974
<400> 2974
000
<210> 2975
<400> 2975
000
<210> 2976
<400> 2976
000
<210> 2977
<400> 2977
000
<210> 2978
<400> 2978
000
<210> 2979
<400> 2979
000
<210> 2980
<400> 2980
000
<210> 2981
<400> 2981
000
<210> 2982
<400> 2982
000
<210> 2983
<400> 2983
000
<210> 2984
<400> 2984
000
<210> 2985
<400> 2985
000
<210> 2986
<400> 2986
000
<210> 2987
<400> 2987
000
<210> 2988
<400> 2988
000
<210> 2989
<400> 2989
000
<210> 2990
<400> 2990
000
<210> 2991
<400> 2991
000
<210> 2992
<400> 2992
000
<210> 2993
<400> 2993
000
<210> 2994
<400> 2994
000
<210> 2995
<400> 2995
000
<210> 2996
<400> 2996
000
<210> 2997
<400> 2997
000
<210> 2998
<400> 2998
000
<210> 2999
<400> 2999
000
<210> 3000
<400> 3000
000
<210> 3001
<400> 3001
000
<210> 3002
<400> 3002
000
<210> 3003
<400> 3003
000
<210> 3004
<400> 3004
000
<210> 3005
<400> 3005
000
<210> 3006
<400> 3006
000
<210> 3007
<400> 3007
000
<210> 3008
<400> 3008
000
<210> 3009
<400> 3009
000
<210> 3010
<400> 3010
000
<210> 3011
<400> 3011
000
<210> 3012
<400> 3012
000
<210> 3013
<400> 3013
000
<210> 3014
<400> 3014
000
<210> 3015
<400> 3015
000
<210> 3016
<400> 3016
000
<210> 3017
<400> 3017
000
<210> 3018
<400> 3018
000
<210> 3019
<400> 3019
000
<210> 3020
<400> 3020
000
<210> 3021
<400> 3021
000
<210> 3022
<400> 3022
000
<210> 3023
<400> 3023
000
<210> 3024
<400> 3024
000
<210> 3025
<400> 3025
000
<210> 3026
<400> 3026
000
<210> 3027
<400> 3027
000
<210> 3028
<400> 3028
000
<210> 3029
<400> 3029
000
<210> 3030
<400> 3030
000
<210> 3031
<400> 3031
000
<210> 3032
<400> 3032
000
<210> 3033
<400> 3033
000
<210> 3034
<400> 3034
000
<210> 3035
<400> 3035
000
<210> 3036
<400> 3036
000
<210> 3037
<400> 3037
000
<210> 3038
<400> 3038
000
<210> 3039
<400> 3039
000
<210> 3040
<400> 3040
000
<210> 3041
<400> 3041
000
<210> 3042
<400> 3042
000
<210> 3043
<400> 3043
000
<210> 3044
<400> 3044
000
<210> 3045
<400> 3045
000
<210> 3046
<400> 3046
000
<210> 3047
<400> 3047
000
<210> 3048
<400> 3048
000
<210> 3049
<400> 3049
000
<210> 3050
<400> 3050
000
<210> 3051
<400> 3051
000
<210> 3052
<400> 3052
000
<210> 3053
<400> 3053
000
<210> 3054
<400> 3054
000
<210> 3055
<400> 3055
000
<210> 3056
<400> 3056
000
<210> 3057
<400> 3057
000
<210> 3058
<400> 3058
000
<210> 3059
<400> 3059
000
<210> 3060
<400> 3060
000
<210> 3061
<400> 3061
000
<210> 3062
<400> 3062
000
<210> 3063
<400> 3063
000
<210> 3064
<400> 3064
000
<210> 3065
<400> 3065
000
<210> 3066
<400> 3066
000
<210> 3067
<400> 3067
000
<210> 3068
<400> 3068
000
<210> 3069
<400> 3069
000
<210> 3070
<400> 3070
000
<210> 3071
<400> 3071
000
<210> 3072
<400> 3072
000
<210> 3073
<400> 3073
000
<210> 3074
<400> 3074
000
<210> 3075
<400> 3075
000
<210> 3076
<400> 3076
000
<210> 3077
<400> 3077
000
<210> 3078
<400> 3078
000
<210> 3079
<400> 3079
000
<210> 3080
<400> 3080
000
<210> 3081
<400> 3081
000
<210> 3082
<400> 3082
000
<210> 3083
<400> 3083
000
<210> 3084
<400> 3084
000
<210> 3085
<400> 3085
000
<210> 3086
<400> 3086
000
<210> 3087
<400> 3087
000
<210> 3088
<400> 3088
000
<210> 3089
<400> 3089
000
<210> 3090
<400> 3090
000
<210> 3091
<400> 3091
000
<210> 3092
<400> 3092
000
<210> 3093
<400> 3093
000
<210> 3094
<400> 3094
000
<210> 3095
<400> 3095
000
<210> 3096
<400> 3096
000
<210> 3097
<400> 3097
000
<210> 3098
<400> 3098
000
<210> 3099
<400> 3099
000
<210> 3100
<400> 3100
000
<210> 3101
<400> 3101
000
<210> 3102
<400> 3102
000
<210> 3103
<400> 3103
000
<210> 3104
<400> 3104
000
<210> 3105
<400> 3105
000
<210> 3106
<400> 3106
000
<210> 3107
<400> 3107
000
<210> 3108
<400> 3108
000
<210> 3109
<400> 3109
000
<210> 3110
<400> 3110
000
<210> 3111
<400> 3111
000
<210> 3112
<400> 3112
000
<210> 3113
<400> 3113
000
<210> 3114
<400> 3114
000
<210> 3115
<400> 3115
000
<210> 3116
<400> 3116
000
<210> 3117
<400> 3117
000
<210> 3118
<400> 3118
000
<210> 3119
<400> 3119
000
<210> 3120
<400> 3120
000
<210> 3121
<400> 3121
000
<210> 3122
<400> 3122
000
<210> 3123
<400> 3123
000
<210> 3124
<400> 3124
000
<210> 3125
<400> 3125
000
<210> 3126
<400> 3126
000
<210> 3127
<400> 3127
000
<210> 3128
<400> 3128
000
<210> 3129
<400> 3129
000
<210> 3130
<400> 3130
000
<210> 3131
<400> 3131
000
<210> 3132
<400> 3132
000
<210> 3133
<400> 3133
000
<210> 3134
<400> 3134
000
<210> 3135
<400> 3135
000
<210> 3136
<400> 3136
000
<210> 3137
<400> 3137
000
<210> 3138
<400> 3138
000
<210> 3139
<400> 3139
000
<210> 3140
<400> 3140
000
<210> 3141
<400> 3141
000
<210> 3142
<400> 3142
000
<210> 3143
<400> 3143
000
<210> 3144
<400> 3144
000
<210> 3145
<400> 3145
000
<210> 3146
<400> 3146
000
<210> 3147
<400> 3147
000
<210> 3148
<400> 3148
000
<210> 3149
<400> 3149
000
<210> 3150
<400> 3150
000
<210> 3151
<400> 3151
000
<210> 3152
<400> 3152
000
<210> 3153
<400> 3153
000
<210> 3154
<400> 3154
000
<210> 3155
<400> 3155
000
<210> 3156
<400> 3156
000
<210> 3157
<400> 3157
000
<210> 3158
<400> 3158
000
<210> 3159
<400> 3159
000
<210> 3160
<400> 3160
000
<210> 3161
<400> 3161
000
<210> 3162
<400> 3162
000
<210> 3163
<400> 3163
000
<210> 3164
<400> 3164
000
<210> 3165
<400> 3165
000
<210> 3166
<400> 3166
000
<210> 3167
<400> 3167
000
<210> 3168
<400> 3168
000
<210> 3169
<400> 3169
000
<210> 3170
<400> 3170
000
<210> 3171
<400> 3171
000
<210> 3172
<400> 3172
000
<210> 3173
<400> 3173
000
<210> 3174
<400> 3174
000
<210> 3175
<400> 3175
000
<210> 3176
<400> 3176
000
<210> 3177
<400> 3177
000
<210> 3178
<400> 3178
000
<210> 3179
<400> 3179
000
<210> 3180
<400> 3180
000
<210> 3181
<400> 3181
000
<210> 3182
<400> 3182
000
<210> 3183
<400> 3183
000
<210> 3184
<400> 3184
000
<210> 3185
<400> 3185
000
<210> 3186
<400> 3186
000
<210> 3187
<400> 3187
000
<210> 3188
<400> 3188
000
<210> 3189
<400> 3189
000
<210> 3190
<400> 3190
000
<210> 3191
<400> 3191
000
<210> 3192
<400> 3192
000
<210> 3193
<400> 3193
000
<210> 3194
<400> 3194
000
<210> 3195
<400> 3195
000
<210> 3196
<400> 3196
000
<210> 3197
<400> 3197
000
<210> 3198
<400> 3198
000
<210> 3199
<400> 3199
000
<210> 3200
<400> 3200
000
<210> 3201
<400> 3201
000
<210> 3202
<400> 3202
000
<210> 3203
<400> 3203
000
<210> 3204
<400> 3204
000
<210> 3205
<400> 3205
000
<210> 3206
<400> 3206
000
<210> 3207
<400> 3207
000
<210> 3208
<400> 3208
000
<210> 3209
<400> 3209
000
<210> 3210
<400> 3210
000
<210> 3211
<400> 3211
000
<210> 3212
<400> 3212
000
<210> 3213
<400> 3213
000
<210> 3214
<400> 3214
000
<210> 3215
<400> 3215
000
<210> 3216
<400> 3216
000
<210> 3217
<400> 3217
000
<210> 3218
<400> 3218
000
<210> 3219
<400> 3219
000
<210> 3220
<400> 3220
000
<210> 3221
<400> 3221
000
<210> 3222
<400> 3222
000
<210> 3223
<400> 3223
000
<210> 3224
<400> 3224
000
<210> 3225
<400> 3225
000
<210> 3226
<400> 3226
000
<210> 3227
<400> 3227
000
<210> 3228
<400> 3228
000
<210> 3229
<400> 3229
000
<210> 3230
<400> 3230
000
<210> 3231
<400> 3231
000
<210> 3232
<400> 3232
000
<210> 3233
<400> 3233
000
<210> 3234
<400> 3234
000
<210> 3235
<400> 3235
000
<210> 3236
<400> 3236
000
<210> 3237
<400> 3237
000
<210> 3238
<400> 3238
000
<210> 3239
<400> 3239
000
<210> 3240
<400> 3240
000
<210> 3241
<400> 3241
000
<210> 3242
<400> 3242
000
<210> 3243
<400> 3243
000
<210> 3244
<400> 3244
000
<210> 3245
<400> 3245
000
<210> 3246
<400> 3246
000
<210> 3247
<400> 3247
000
<210> 3248
<400> 3248
000
<210> 3249
<400> 3249
000
<210> 3250
<400> 3250
000
<210> 3251
<400> 3251
000
<210> 3252
<400> 3252
000
<210> 3253
<400> 3253
000
<210> 3254
<400> 3254
000
<210> 3255
<400> 3255
000
<210> 3256
<400> 3256
000
<210> 3257
<400> 3257
000
<210> 3258
<400> 3258
000
<210> 3259
<400> 3259
000
<210> 3260
<400> 3260
000
<210> 3261
<400> 3261
000
<210> 3262
<400> 3262
000
<210> 3263
<400> 3263
000
<210> 3264
<400> 3264
000
<210> 3265
<400> 3265
000
<210> 3266
<400> 3266
000
<210> 3267
<400> 3267
000
<210> 3268
<400> 3268
000
<210> 3269
<400> 3269
000
<210> 3270
<400> 3270
000
<210> 3271
<400> 3271
000
<210> 3272
<400> 3272
000
<210> 3273
<400> 3273
000
<210> 3274
<400> 3274
000
<210> 3275
<400> 3275
000
<210> 3276
<400> 3276
000
<210> 3277
<400> 3277
000
<210> 3278
<400> 3278
000
<210> 3279
<400> 3279
000
<210> 3280
<400> 3280
000
<210> 3281
<400> 3281
000
<210> 3282
<400> 3282
000
<210> 3283
<400> 3283
000
<210> 3284
<400> 3284
000
<210> 3285
<400> 3285
000
<210> 3286
<400> 3286
000
<210> 3287
<400> 3287
000
<210> 3288
<400> 3288
000
<210> 3289
<400> 3289
000
<210> 3290
<400> 3290
000
<210> 3291
<400> 3291
000
<210> 3292
<400> 3292
000
<210> 3293
<400> 3293
000
<210> 3294
<400> 3294
000
<210> 3295
<400> 3295
000
<210> 3296
<400> 3296
000
<210> 3297
<400> 3297
000
<210> 3298
<400> 3298
000
<210> 3299
<400> 3299
000
<210> 3300
<400> 3300
000
<210> 3301
<400> 3301
000
<210> 3302
<400> 3302
000
<210> 3303
<400> 3303
000
<210> 3304
<400> 3304
000
<210> 3305
<400> 3305
000
<210> 3306
<400> 3306
000
<210> 3307
<400> 3307
000
<210> 3308
<400> 3308
000
<210> 3309
<400> 3309
000
<210> 3310
<400> 3310
000
<210> 3311
<400> 3311
000
<210> 3312
<400> 3312
000
<210> 3313
<400> 3313
000
<210> 3314
<400> 3314
000
<210> 3315
<400> 3315
000
<210> 3316
<400> 3316
000
<210> 3317
<400> 3317
000
<210> 3318
<400> 3318
000
<210> 3319
<400> 3319
000
<210> 3320
<400> 3320
000
<210> 3321
<400> 3321
000
<210> 3322
<400> 3322
000
<210> 3323
<400> 3323
000
<210> 3324
<400> 3324
000
<210> 3325
<400> 3325
000
<210> 3326
<400> 3326
000
<210> 3327
<400> 3327
000
<210> 3328
<400> 3328
000
<210> 3329
<400> 3329
000
<210> 3330
<400> 3330
000
<210> 3331
<400> 3331
000
<210> 3332
<400> 3332
000
<210> 3333
<400> 3333
000
<210> 3334
<400> 3334
000
<210> 3335
<400> 3335
000
<210> 3336
<400> 3336
000
<210> 3337
<400> 3337
000
<210> 3338
<400> 3338
000
<210> 3339
<400> 3339
000
<210> 3340
<400> 3340
000
<210> 3341
<400> 3341
000
<210> 3342
<400> 3342
000
<210> 3343
<400> 3343
000
<210> 3344
<400> 3344
000
<210> 3345
<400> 3345
000
<210> 3346
<400> 3346
000
<210> 3347
<400> 3347
000
<210> 3348
<400> 3348
000
<210> 3349
<400> 3349
000
<210> 3350
<400> 3350
000
<210> 3351
<400> 3351
000
<210> 3352
<400> 3352
000
<210> 3353
<400> 3353
000
<210> 3354
<400> 3354
000
<210> 3355
<400> 3355
000
<210> 3356
<400> 3356
000
<210> 3357
<400> 3357
000
<210> 3358
<400> 3358
000
<210> 3359
<400> 3359
000
<210> 3360
<400> 3360
000
<210> 3361
<400> 3361
000
<210> 3362
<400> 3362
000
<210> 3363
<400> 3363
000
<210> 3364
<400> 3364
000
<210> 3365
<400> 3365
000
<210> 3366
<400> 3366
000
<210> 3367
<400> 3367
000
<210> 3368
<400> 3368
000
<210> 3369
<400> 3369
000
<210> 3370
<400> 3370
000
<210> 3371
<400> 3371
000
<210> 3372
<400> 3372
000
<210> 3373
<400> 3373
000
<210> 3374
<400> 3374
000
<210> 3375
<400> 3375
000
<210> 3376
<400> 3376
000
<210> 3377
<400> 3377
000
<210> 3378
<400> 3378
000
<210> 3379
<400> 3379
000
<210> 3380
<400> 3380
000
<210> 3381
<400> 3381
000
<210> 3382
<400> 3382
000
<210> 3383
<400> 3383
000
<210> 3384
<400> 3384
000
<210> 3385
<400> 3385
000
<210> 3386
<400> 3386
000
<210> 3387
<400> 3387
000
<210> 3388
<400> 3388
000
<210> 3389
<400> 3389
000
<210> 3390
<400> 3390
000
<210> 3391
<400> 3391
000
<210> 3392
<400> 3392
000
<210> 3393
<400> 3393
000
<210> 3394
<400> 3394
000
<210> 3395
<400> 3395
000
<210> 3396
<400> 3396
000
<210> 3397
<400> 3397
000
<210> 3398
<400> 3398
000
<210> 3399
<400> 3399
000
<210> 3400
<400> 3400
000
<210> 3401
<400> 3401
000
<210> 3402
<400> 3402
000
<210> 3403
<400> 3403
000
<210> 3404
<400> 3404
000
<210> 3405
<400> 3405
000
<210> 3406
<400> 3406
000
<210> 3407
<400> 3407
000
<210> 3408
<400> 3408
000
<210> 3409
<400> 3409
000
<210> 3410
<400> 3410
000
<210> 3411
<400> 3411
000
<210> 3412
<400> 3412
000
<210> 3413
<400> 3413
000
<210> 3414
<400> 3414
000
<210> 3415
<400> 3415
000
<210> 3416
<400> 3416
000
<210> 3417
<400> 3417
000
<210> 3418
<400> 3418
000
<210> 3419
<400> 3419
000
<210> 3420
<400> 3420
000
<210> 3421
<400> 3421
000
<210> 3422
<400> 3422
000
<210> 3423
<400> 3423
000
<210> 3424
<400> 3424
000
<210> 3425
<400> 3425
000
<210> 3426
<400> 3426
000
<210> 3427
<400> 3427
000
<210> 3428
<400> 3428
000
<210> 3429
<400> 3429
000
<210> 3430
<400> 3430
000
<210> 3431
<400> 3431
000
<210> 3432
<400> 3432
000
<210> 3433
<400> 3433
000
<210> 3434
<400> 3434
000
<210> 3435
<400> 3435
000
<210> 3436
<400> 3436
000
<210> 3437
<400> 3437
000
<210> 3438
<400> 3438
000
<210> 3439
<400> 3439
000
<210> 3440
<400> 3440
000
<210> 3441
<400> 3441
000
<210> 3442
<400> 3442
000
<210> 3443
<400> 3443
000
<210> 3444
<400> 3444
000
<210> 3445
<400> 3445
000
<210> 3446
<400> 3446
000
<210> 3447
<400> 3447
000
<210> 3448
<400> 3448
000
<210> 3449
<400> 3449
000
<210> 3450
<400> 3450
000
<210> 3451
<400> 3451
000
<210> 3452
<400> 3452
000
<210> 3453
<400> 3453
000
<210> 3454
<400> 3454
000
<210> 3455
<400> 3455
000
<210> 3456
<400> 3456
000
<210> 3457
<400> 3457
000
<210> 3458
<400> 3458
000
<210> 3459
<400> 3459
000
<210> 3460
<400> 3460
000
<210> 3461
<400> 3461
000
<210> 3462
<400> 3462
000
<210> 3463
<400> 3463
000
<210> 3464
<400> 3464
000
<210> 3465
<400> 3465
000
<210> 3466
<400> 3466
000
<210> 3467
<400> 3467
000
<210> 3468
<400> 3468
000
<210> 3469
<400> 3469
000
<210> 3470
<400> 3470
000
<210> 3471
<400> 3471
000
<210> 3472
<400> 3472
000
<210> 3473
<400> 3473
000
<210> 3474
<400> 3474
000
<210> 3475
<400> 3475
000
<210> 3476
<400> 3476
000
<210> 3477
<400> 3477
000
<210> 3478
<400> 3478
000
<210> 3479
<400> 3479
000
<210> 3480
<400> 3480
000
<210> 3481
<400> 3481
000
<210> 3482
<400> 3482
000
<210> 3483
<400> 3483
000
<210> 3484
<400> 3484
000
<210> 3485
<400> 3485
000
<210> 3486
<400> 3486
000
<210> 3487
<400> 3487
000
<210> 3488
<400> 3488
000
<210> 3489
<400> 3489
000
<210> 3490
<400> 3490
000
<210> 3491
<400> 3491
000
<210> 3492
<400> 3492
000
<210> 3493
<400> 3493
000
<210> 3494
<400> 3494
000
<210> 3495
<400> 3495
000
<210> 3496
<400> 3496
000
<210> 3497
<400> 3497
000
<210> 3498
<400> 3498
000
<210> 3499
<400> 3499
000
<210> 3500
<400> 3500
000
<210> 3501
<400> 3501
000
<210> 3502
<400> 3502
000
<210> 3503
<400> 3503
000
<210> 3504
<400> 3504
000
<210> 3505
<400> 3505
000
<210> 3506
<400> 3506
000
<210> 3507
<400> 3507
000
<210> 3508
<400> 3508
000
<210> 3509
<400> 3509
000
<210> 3510
<400> 3510
000
<210> 3511
<400> 3511
000
<210> 3512
<400> 3512
000
<210> 3513
<400> 3513
000
<210> 3514
<400> 3514
000
<210> 3515
<400> 3515
000
<210> 3516
<400> 3516
000
<210> 3517
<400> 3517
000
<210> 3518
<400> 3518
000
<210> 3519
<400> 3519
000
<210> 3520
<400> 3520
000
<210> 3521
<400> 3521
000
<210> 3522
<400> 3522
000
<210> 3523
<400> 3523
000
<210> 3524
<400> 3524
000
<210> 3525
<400> 3525
000
<210> 3526
<400> 3526
000
<210> 3527
<400> 3527
000
<210> 3528
<400> 3528
000
<210> 3529
<400> 3529
000
<210> 3530
<400> 3530
000
<210> 3531
<400> 3531
000
<210> 3532
<400> 3532
000
<210> 3533
<400> 3533
000
<210> 3534
<400> 3534
000
<210> 3535
<400> 3535
000
<210> 3536
<400> 3536
000
<210> 3537
<400> 3537
000
<210> 3538
<400> 3538
000
<210> 3539
<400> 3539
000
<210> 3540
<400> 3540
000
<210> 3541
<400> 3541
000
<210> 3542
<400> 3542
000
<210> 3543
<400> 3543
000
<210> 3544
<400> 3544
000
<210> 3545
<400> 3545
000
<210> 3546
<400> 3546
000
<210> 3547
<400> 3547
000
<210> 3548
<400> 3548
000
<210> 3549
<400> 3549
000
<210> 3550
<400> 3550
000
<210> 3551
<400> 3551
000
<210> 3552
<400> 3552
000
<210> 3553
<400> 3553
000
<210> 3554
<400> 3554
000
<210> 3555
<400> 3555
000
<210> 3556
<400> 3556
000
<210> 3557
<400> 3557
000
<210> 3558
<400> 3558
000
<210> 3559
<400> 3559
000
<210> 3560
<400> 3560
000
<210> 3561
<400> 3561
000
<210> 3562
<400> 3562
000
<210> 3563
<400> 3563
000
<210> 3564
<400> 3564
000
<210> 3565
<400> 3565
000
<210> 3566
<400> 3566
000
<210> 3567
<400> 3567
000
<210> 3568
<400> 3568
000
<210> 3569
<400> 3569
000
<210> 3570
<400> 3570
000
<210> 3571
<400> 3571
000
<210> 3572
<400> 3572
000
<210> 3573
<400> 3573
000
<210> 3574
<400> 3574
000
<210> 3575
<400> 3575
000
<210> 3576
<400> 3576
000
<210> 3577
<400> 3577
000
<210> 3578
<400> 3578
000
<210> 3579
<400> 3579
000
<210> 3580
<400> 3580
000
<210> 3581
<400> 3581
000
<210> 3582
<400> 3582
000
<210> 3583
<400> 3583
000
<210> 3584
<400> 3584
000
<210> 3585
<400> 3585
000
<210> 3586
<400> 3586
000
<210> 3587
<400> 3587
000
<210> 3588
<400> 3588
000
<210> 3589
<400> 3589
000
<210> 3590
<400> 3590
000
<210> 3591
<400> 3591
000
<210> 3592
<400> 3592
000
<210> 3593
<400> 3593
000
<210> 3594
<400> 3594
000
<210> 3595
<400> 3595
000
<210> 3596
<400> 3596
000
<210> 3597
<400> 3597
000
<210> 3598
<400> 3598
000
<210> 3599
<400> 3599
000
<210> 3600
<400> 3600
000
<210> 3601
<400> 3601
000
<210> 3602
<400> 3602
000
<210> 3603
<400> 3603
000
<210> 3604
<400> 3604
000
<210> 3605
<400> 3605
000
<210> 3606
<400> 3606
000
<210> 3607
<400> 3607
000
<210> 3608
<400> 3608
000
<210> 3609
<400> 3609
000
<210> 3610
<400> 3610
000
<210> 3611
<400> 3611
000
<210> 3612
<400> 3612
000
<210> 3613
<400> 3613
000
<210> 3614
<400> 3614
000
<210> 3615
<400> 3615
000
<210> 3616
<400> 3616
000
<210> 3617
<400> 3617
000
<210> 3618
<400> 3618
000
<210> 3619
<400> 3619
000
<210> 3620
<400> 3620
000
<210> 3621
<400> 3621
000
<210> 3622
<400> 3622
000
<210> 3623
<400> 3623
000
<210> 3624
<400> 3624
000
<210> 3625
<400> 3625
000
<210> 3626
<400> 3626
000
<210> 3627
<400> 3627
000
<210> 3628
<400> 3628
000
<210> 3629
<400> 3629
000
<210> 3630
<400> 3630
000
<210> 3631
<400> 3631
000
<210> 3632
<400> 3632
000
<210> 3633
<400> 3633
000
<210> 3634
<400> 3634
000
<210> 3635
<400> 3635
000
<210> 3636
<400> 3636
000
<210> 3637
<400> 3637
000
<210> 3638
<400> 3638
000
<210> 3639
<400> 3639
000
<210> 3640
<400> 3640
000
<210> 3641
<400> 3641
000
<210> 3642
<400> 3642
000
<210> 3643
<400> 3643
000
<210> 3644
<400> 3644
000
<210> 3645
<400> 3645
000
<210> 3646
<400> 3646
000
<210> 3647
<400> 3647
000
<210> 3648
<400> 3648
000
<210> 3649
<400> 3649
000
<210> 3650
<400> 3650
000
<210> 3651
<400> 3651
000
<210> 3652
<400> 3652
000
<210> 3653
<400> 3653
000
<210> 3654
<400> 3654
000
<210> 3655
<400> 3655
000
<210> 3656
<400> 3656
000
<210> 3657
<400> 3657
000
<210> 3658
<400> 3658
000
<210> 3659
<400> 3659
000
<210> 3660
<400> 3660
000
<210> 3661
<400> 3661
000
<210> 3662
<400> 3662
000
<210> 3663
<400> 3663
000
<210> 3664
<400> 3664
000
<210> 3665
<400> 3665
000
<210> 3666
<400> 3666
000
<210> 3667
<400> 3667
000
<210> 3668
<400> 3668
000
<210> 3669
<400> 3669
000
<210> 3670
<400> 3670
000
<210> 3671
<400> 3671
000
<210> 3672
<400> 3672
000
<210> 3673
<400> 3673
000
<210> 3674
<400> 3674
000
<210> 3675
<400> 3675
000
<210> 3676
<400> 3676
000
<210> 3677
<400> 3677
000
<210> 3678
<400> 3678
000
<210> 3679
<400> 3679
000
<210> 3680
<400> 3680
000
<210> 3681
<400> 3681
000
<210> 3682
<400> 3682
000
<210> 3683
<400> 3683
000
<210> 3684
<400> 3684
000
<210> 3685
<400> 3685
000
<210> 3686
<400> 3686
000
<210> 3687
<400> 3687
000
<210> 3688
<400> 3688
000
<210> 3689
<400> 3689
000
<210> 3690
<400> 3690
000
<210> 3691
<400> 3691
000
<210> 3692
<400> 3692
000
<210> 3693
<400> 3693
000
<210> 3694
<400> 3694
000
<210> 3695
<400> 3695
000
<210> 3696
<400> 3696
000
<210> 3697
<400> 3697
000
<210> 3698
<400> 3698
000
<210> 3699
<400> 3699
000
<210> 3700
<400> 3700
000
<210> 3701
<400> 3701
000
<210> 3702
<400> 3702
000
<210> 3703
<400> 3703
000
<210> 3704
<400> 3704
000
<210> 3705
<400> 3705
000
<210> 3706
<400> 3706
000
<210> 3707
<400> 3707
000
<210> 3708
<400> 3708
000
<210> 3709
<400> 3709
000
<210> 3710
<400> 3710
000
<210> 3711
<400> 3711
000
<210> 3712
<400> 3712
000
<210> 3713
<400> 3713
000
<210> 3714
<400> 3714
000
<210> 3715
<400> 3715
000
<210> 3716
<400> 3716
000
<210> 3717
<400> 3717
000
<210> 3718
<400> 3718
000
<210> 3719
<400> 3719
000
<210> 3720
<400> 3720
000
<210> 3721
<400> 3721
000
<210> 3722
<400> 3722
000
<210> 3723
<400> 3723
000
<210> 3724
<400> 3724
000
<210> 3725
<400> 3725
000
<210> 3726
<400> 3726
000
<210> 3727
<400> 3727
000
<210> 3728
<400> 3728
000
<210> 3729
<400> 3729
000
<210> 3730
<400> 3730
000
<210> 3731
<400> 3731
000
<210> 3732
<400> 3732
000
<210> 3733
<400> 3733
000
<210> 3734
<400> 3734
000
<210> 3735
<400> 3735
000
<210> 3736
<400> 3736
000
<210> 3737
<400> 3737
000
<210> 3738
<400> 3738
000
<210> 3739
<400> 3739
000
<210> 3740
<400> 3740
000
<210> 3741
<400> 3741
000
<210> 3742
<400> 3742
000
<210> 3743
<400> 3743
000
<210> 3744
<400> 3744
000
<210> 3745
<400> 3745
000
<210> 3746
<400> 3746
000
<210> 3747
<400> 3747
000
<210> 3748
<400> 3748
000
<210> 3749
<400> 3749
000
<210> 3750
<400> 3750
000
<210> 3751
<400> 3751
000
<210> 3752
<400> 3752
000
<210> 3753
<400> 3753
000
<210> 3754
<400> 3754
000
<210> 3755
<400> 3755
000
<210> 3756
<400> 3756
000
<210> 3757
<400> 3757
000
<210> 3758
<400> 3758
000
<210> 3759
<400> 3759
000
<210> 3760
<400> 3760
000
<210> 3761
<400> 3761
000
<210> 3762
<400> 3762
000
<210> 3763
<400> 3763
000
<210> 3764
<400> 3764
000
<210> 3765
<400> 3765
000
<210> 3766
<400> 3766
000
<210> 3767
<400> 3767
000
<210> 3768
<400> 3768
000
<210> 3769
<400> 3769
000
<210> 3770
<400> 3770
000
<210> 3771
<400> 3771
000
<210> 3772
<400> 3772
000
<210> 3773
<400> 3773
000
<210> 3774
<400> 3774
000
<210> 3775
<400> 3775
000
<210> 3776
<400> 3776
000
<210> 3777
<400> 3777
000
<210> 3778
<400> 3778
000
<210> 3779
<400> 3779
000
<210> 3780
<400> 3780
000
<210> 3781
<400> 3781
000
<210> 3782
<400> 3782
000
<210> 3783
<400> 3783
000
<210> 3784
<400> 3784
000
<210> 3785
<400> 3785
000
<210> 3786
<400> 3786
000
<210> 3787
<400> 3787
000
<210> 3788
<400> 3788
000
<210> 3789
<400> 3789
000
<210> 3790
<400> 3790
000
<210> 3791
<400> 3791
000
<210> 3792
<400> 3792
000
<210> 3793
<400> 3793
000
<210> 3794
<400> 3794
000
<210> 3795
<400> 3795
000
<210> 3796
<400> 3796
000
<210> 3797
<400> 3797
000
<210> 3798
<400> 3798
000
<210> 3799
<400> 3799
000
<210> 3800
<400> 3800
000
<210> 3801
<400> 3801
000
<210> 3802
<400> 3802
000
<210> 3803
<400> 3803
000
<210> 3804
<400> 3804
000
<210> 3805
<400> 3805
000
<210> 3806
<400> 3806
000
<210> 3807
<400> 3807
000
<210> 3808
<400> 3808
000
<210> 3809
<400> 3809
000
<210> 3810
<400> 3810
000
<210> 3811
<400> 3811
000
<210> 3812
<400> 3812
000
<210> 3813
<400> 3813
000
<210> 3814
<400> 3814
000
<210> 3815
<400> 3815
000
<210> 3816
<400> 3816
000
<210> 3817
<400> 3817
000
<210> 3818
<400> 3818
000
<210> 3819
<400> 3819
000
<210> 3820
<400> 3820
000
<210> 3821
<400> 3821
000
<210> 3822
<400> 3822
000
<210> 3823
<400> 3823
000
<210> 3824
<400> 3824
000
<210> 3825
<400> 3825
000
<210> 3826
<400> 3826
000
<210> 3827
<400> 3827
000
<210> 3828
<400> 3828
000
<210> 3829
<400> 3829
000
<210> 3830
<400> 3830
000
<210> 3831
<400> 3831
000
<210> 3832
<400> 3832
000
<210> 3833
<400> 3833
000
<210> 3834
<400> 3834
000
<210> 3835
<400> 3835
000
<210> 3836
<400> 3836
000
<210> 3837
<400> 3837
000
<210> 3838
<400> 3838
000
<210> 3839
<400> 3839
000
<210> 3840
<400> 3840
000
<210> 3841
<400> 3841
000
<210> 3842
<400> 3842
000
<210> 3843
<400> 3843
000
<210> 3844
<400> 3844
000
<210> 3845
<400> 3845
000
<210> 3846
<400> 3846
000
<210> 3847
<400> 3847
000
<210> 3848
<400> 3848
000
<210> 3849
<400> 3849
000
<210> 3850
<400> 3850
000
<210> 3851
<400> 3851
000
<210> 3852
<400> 3852
000
<210> 3853
<400> 3853
000
<210> 3854
<400> 3854
000
<210> 3855
<400> 3855
000
<210> 3856
<400> 3856
000
<210> 3857
<400> 3857
000
<210> 3858
<400> 3858
000
<210> 3859
<400> 3859
000
<210> 3860
<400> 3860
000
<210> 3861
<400> 3861
000
<210> 3862
<400> 3862
000
<210> 3863
<400> 3863
000
<210> 3864
<400> 3864
000
<210> 3865
<400> 3865
000
<210> 3866
<400> 3866
000
<210> 3867
<400> 3867
000
<210> 3868
<400> 3868
000
<210> 3869
<400> 3869
000
<210> 3870
<400> 3870
000
<210> 3871
<400> 3871
000
<210> 3872
<400> 3872
000
<210> 3873
<400> 3873
000
<210> 3874
<400> 3874
000
<210> 3875
<400> 3875
000
<210> 3876
<400> 3876
000
<210> 3877
<400> 3877
000
<210> 3878
<400> 3878
000
<210> 3879
<400> 3879
000
<210> 3880
<400> 3880
000
<210> 3881
<400> 3881
000
<210> 3882
<400> 3882
000
<210> 3883
<400> 3883
000
<210> 3884
<400> 3884
000
<210> 3885
<400> 3885
000
<210> 3886
<400> 3886
000
<210> 3887
<400> 3887
000
<210> 3888
<400> 3888
000
<210> 3889
<400> 3889
000
<210> 3890
<400> 3890
000
<210> 3891
<400> 3891
000
<210> 3892
<400> 3892
000
<210> 3893
<400> 3893
000
<210> 3894
<400> 3894
000
<210> 3895
<400> 3895
000
<210> 3896
<400> 3896
000
<210> 3897
<400> 3897
000
<210> 3898
<400> 3898
000
<210> 3899
<400> 3899
000
<210> 3900
<400> 3900
000
<210> 3901
<400> 3901
000
<210> 3902
<400> 3902
000
<210> 3903
<400> 3903
000
<210> 3904
<400> 3904
000
<210> 3905
<400> 3905
000
<210> 3906
<400> 3906
000
<210> 3907
<400> 3907
000
<210> 3908
<400> 3908
000
<210> 3909
<400> 3909
000
<210> 3910
<400> 3910
000
<210> 3911
<400> 3911
000
<210> 3912
<400> 3912
000
<210> 3913
<400> 3913
000
<210> 3914
<400> 3914
000
<210> 3915
<400> 3915
000
<210> 3916
<400> 3916
000
<210> 3917
<400> 3917
000
<210> 3918
<400> 3918
000
<210> 3919
<400> 3919
000
<210> 3920
<400> 3920
000
<210> 3921
<400> 3921
000
<210> 3922
<400> 3922
000
<210> 3923
<400> 3923
000
<210> 3924
<400> 3924
000
<210> 3925
<400> 3925
000
<210> 3926
<400> 3926
000
<210> 3927
<400> 3927
000
<210> 3928
<400> 3928
000
<210> 3929
<400> 3929
000
<210> 3930
<400> 3930
000
<210> 3931
<400> 3931
000
<210> 3932
<400> 3932
000
<210> 3933
<400> 3933
000
<210> 3934
<400> 3934
000
<210> 3935
<400> 3935
000
<210> 3936
<400> 3936
000
<210> 3937
<400> 3937
000
<210> 3938
<400> 3938
000
<210> 3939
<400> 3939
000
<210> 3940
<400> 3940
000
<210> 3941
<400> 3941
000
<210> 3942
<400> 3942
000
<210> 3943
<400> 3943
000
<210> 3944
<400> 3944
000
<210> 3945
<400> 3945
000
<210> 3946
<400> 3946
000
<210> 3947
<400> 3947
000
<210> 3948
<400> 3948
000
<210> 3949
<400> 3949
000
<210> 3950
<400> 3950
000
<210> 3951
<400> 3951
000
<210> 3952
<400> 3952
000
<210> 3953
<400> 3953
000
<210> 3954
<400> 3954
000
<210> 3955
<400> 3955
000
<210> 3956
<400> 3956
000
<210> 3957
<400> 3957
000
<210> 3958
<400> 3958
000
<210> 3959
<400> 3959
000
<210> 3960
<400> 3960
000
<210> 3961
<400> 3961
000
<210> 3962
<400> 3962
000
<210> 3963
<400> 3963
000
<210> 3964
<400> 3964
000
<210> 3965
<400> 3965
000
<210> 3966
<400> 3966
000
<210> 3967
<400> 3967
000
<210> 3968
<400> 3968
000
<210> 3969
<400> 3969
000
<210> 3970
<400> 3970
000
<210> 3971
<400> 3971
000
<210> 3972
<400> 3972
000
<210> 3973
<400> 3973
000
<210> 3974
<400> 3974
000
<210> 3975
<400> 3975
000
<210> 3976
<400> 3976
000
<210> 3977
<400> 3977
000
<210> 3978
<400> 3978
000
<210> 3979
<400> 3979
000
<210> 3980
<400> 3980
000
<210> 3981
<400> 3981
000
<210> 3982
<400> 3982
000
<210> 3983
<400> 3983
000
<210> 3984
<400> 3984
000
<210> 3985
<400> 3985
000
<210> 3986
<400> 3986
000
<210> 3987
<400> 3987
000
<210> 3988
<400> 3988
000
<210> 3989
<400> 3989
000
<210> 3990
<400> 3990
000
<210> 3991
<400> 3991
000
<210> 3992
<400> 3992
000
<210> 3993
<400> 3993
000
<210> 3994
<400> 3994
000
<210> 3995
<400> 3995
000
<210> 3996
<400> 3996
000
<210> 3997
<400> 3997
000
<210> 3998
<400> 3998
000
<210> 3999
<400> 3999
000
<210> 4000
<400> 4000
000
<210> 4001
<400> 4001
000
<210> 4002
<400> 4002
000
<210> 4003
<400> 4003
000
<210> 4004
<400> 4004
000
<210> 4005
<400> 4005
000
<210> 4006
<400> 4006
000
<210> 4007
<400> 4007
000
<210> 4008
<400> 4008
000
<210> 4009
<400> 4009
000
<210> 4010
<400> 4010
000
<210> 4011
<400> 4011
000
<210> 4012
<400> 4012
000
<210> 4013
<400> 4013
000
<210> 4014
<400> 4014
000
<210> 4015
<400> 4015
000
<210> 4016
<400> 4016
000
<210> 4017
<400> 4017
000
<210> 4018
<400> 4018
000
<210> 4019
<400> 4019
000
<210> 4020
<400> 4020
000
<210> 4021
<400> 4021
000
<210> 4022
<400> 4022
000
<210> 4023
<400> 4023
000
<210> 4024
<400> 4024
000
<210> 4025
<400> 4025
000
<210> 4026
<400> 4026
000
<210> 4027
<400> 4027
000
<210> 4028
<400> 4028
000
<210> 4029
<400> 4029
000
<210> 4030
<400> 4030
000
<210> 4031
<400> 4031
000
<210> 4032
<400> 4032
000
<210> 4033
<400> 4033
000
<210> 4034
<400> 4034
000
<210> 4035
<400> 4035
000
<210> 4036
<400> 4036
000
<210> 4037
<400> 4037
000
<210> 4038
<400> 4038
000
<210> 4039
<400> 4039
000
<210> 4040
<400> 4040
000
<210> 4041
<400> 4041
000
<210> 4042
<400> 4042
000
<210> 4043
<400> 4043
000
<210> 4044
<400> 4044
000
<210> 4045
<400> 4045
000
<210> 4046
<400> 4046
000
<210> 4047
<400> 4047
000
<210> 4048
<400> 4048
000
<210> 4049
<400> 4049
000
<210> 4050
<400> 4050
000
<210> 4051
<400> 4051
000
<210> 4052
<400> 4052
000
<210> 4053
<400> 4053
000
<210> 4054
<400> 4054
000
<210> 4055
<400> 4055
000
<210> 4056
<400> 4056
000
<210> 4057
<400> 4057
000
<210> 4058
<400> 4058
000
<210> 4059
<400> 4059
000
<210> 4060
<400> 4060
000
<210> 4061
<400> 4061
000
<210> 4062
<400> 4062
000
<210> 4063
<400> 4063
000
<210> 4064
<400> 4064
000
<210> 4065
<400> 4065
000
<210> 4066
<400> 4066
000
<210> 4067
<400> 4067
000
<210> 4068
<400> 4068
000
<210> 4069
<400> 4069
000
<210> 4070
<400> 4070
000
<210> 4071
<400> 4071
000
<210> 4072
<400> 4072
000
<210> 4073
<400> 4073
000
<210> 4074
<400> 4074
000
<210> 4075
<400> 4075
000
<210> 4076
<400> 4076
000
<210> 4077
<400> 4077
000
<210> 4078
<400> 4078
000
<210> 4079
<400> 4079
000
<210> 4080
<400> 4080
000
<210> 4081
<400> 4081
000
<210> 4082
<400> 4082
000
<210> 4083
<400> 4083
000
<210> 4084
<400> 4084
000
<210> 4085
<400> 4085
000
<210> 4086
<400> 4086
000
<210> 4087
<400> 4087
000
<210> 4088
<400> 4088
000
<210> 4089
<400> 4089
000
<210> 4090
<400> 4090
000
<210> 4091
<400> 4091
000
<210> 4092
<400> 4092
000
<210> 4093
<400> 4093
000
<210> 4094
<400> 4094
000
<210> 4095
<400> 4095
000
<210> 4096
<400> 4096
000
<210> 4097
<400> 4097
000
<210> 4098
<400> 4098
000
<210> 4099
<400> 4099
000
<210> 4100
<400> 4100
000
<210> 4101
<400> 4101
000
<210> 4102
<400> 4102
000
<210> 4103
<400> 4103
000
<210> 4104
<400> 4104
000
<210> 4105
<400> 4105
000
<210> 4106
<400> 4106
000
<210> 4107
<400> 4107
000
<210> 4108
<400> 4108
000
<210> 4109
<400> 4109
000
<210> 4110
<400> 4110
000
<210> 4111
<400> 4111
000
<210> 4112
<400> 4112
000
<210> 4113
<400> 4113
000
<210> 4114
<400> 4114
000
<210> 4115
<400> 4115
000
<210> 4116
<400> 4116
000
<210> 4117
<400> 4117
000
<210> 4118
<400> 4118
000
<210> 4119
<400> 4119
000
<210> 4120
<400> 4120
000
<210> 4121
<400> 4121
000
<210> 4122
<400> 4122
000
<210> 4123
<400> 4123
000
<210> 4124
<400> 4124
000
<210> 4125
<400> 4125
000
<210> 4126
<400> 4126
000
<210> 4127
<400> 4127
000
<210> 4128
<400> 4128
000
<210> 4129
<400> 4129
000
<210> 4130
<400> 4130
000
<210> 4131
<400> 4131
000
<210> 4132
<400> 4132
000
<210> 4133
<400> 4133
000
<210> 4134
<400> 4134
000
<210> 4135
<400> 4135
000
<210> 4136
<400> 4136
000
<210> 4137
<400> 4137
000
<210> 4138
<400> 4138
000
<210> 4139
<400> 4139
000
<210> 4140
<400> 4140
000
<210> 4141
<400> 4141
000
<210> 4142
<400> 4142
000
<210> 4143
<400> 4143
000
<210> 4144
<400> 4144
000
<210> 4145
<400> 4145
000
<210> 4146
<400> 4146
000
<210> 4147
<400> 4147
000
<210> 4148
<400> 4148
000
<210> 4149
<400> 4149
000
<210> 4150
<400> 4150
000
<210> 4151
<400> 4151
000
<210> 4152
<400> 4152
000
<210> 4153
<400> 4153
000
<210> 4154
<400> 4154
000
<210> 4155
<400> 4155
000
<210> 4156
<400> 4156
000
<210> 4157
<400> 4157
000
<210> 4158
<400> 4158
000
<210> 4159
<400> 4159
000
<210> 4160
<400> 4160
000
<210> 4161
<400> 4161
000
<210> 4162
<400> 4162
000
<210> 4163
<400> 4163
000
<210> 4164
<400> 4164
000
<210> 4165
<400> 4165
000
<210> 4166
<400> 4166
000
<210> 4167
<400> 4167
000
<210> 4168
<400> 4168
000
<210> 4169
<400> 4169
000
<210> 4170
<400> 4170
000
<210> 4171
<400> 4171
000
<210> 4172
<400> 4172
000
<210> 4173
<400> 4173
000
<210> 4174
<400> 4174
000
<210> 4175
<400> 4175
000
<210> 4176
<400> 4176
000
<210> 4177
<400> 4177
000
<210> 4178
<400> 4178
000
<210> 4179
<400> 4179
000
<210> 4180
<400> 4180
000
<210> 4181
<400> 4181
000
<210> 4182
<400> 4182
000
<210> 4183
<400> 4183
000
<210> 4184
<400> 4184
000
<210> 4185
<400> 4185
000
<210> 4186
<400> 4186
000
<210> 4187
<400> 4187
000
<210> 4188
<400> 4188
000
<210> 4189
<400> 4189
000
<210> 4190
<400> 4190
000
<210> 4191
<400> 4191
000
<210> 4192
<400> 4192
000
<210> 4193
<400> 4193
000
<210> 4194
<400> 4194
000
<210> 4195
<400> 4195
000
<210> 4196
<400> 4196
000
<210> 4197
<400> 4197
000
<210> 4198
<400> 4198
000
<210> 4199
<400> 4199
000
<210> 4200
<400> 4200
000
<210> 4201
<400> 4201
000
<210> 4202
<400> 4202
000
<210> 4203
<400> 4203
000
<210> 4204
<400> 4204
000
<210> 4205
<400> 4205
000
<210> 4206
<400> 4206
000
<210> 4207
<400> 4207
000
<210> 4208
<400> 4208
000
<210> 4209
<400> 4209
000
<210> 4210
<400> 4210
000
<210> 4211
<400> 4211
000
<210> 4212
<400> 4212
000
<210> 4213
<400> 4213
000
<210> 4214
<400> 4214
000
<210> 4215
<400> 4215
000
<210> 4216
<400> 4216
000
<210> 4217
<400> 4217
000
<210> 4218
<400> 4218
000
<210> 4219
<400> 4219
000
<210> 4220
<400> 4220
000
<210> 4221
<400> 4221
000
<210> 4222
<400> 4222
000
<210> 4223
<400> 4223
000
<210> 4224
<400> 4224
000
<210> 4225
<400> 4225
000
<210> 4226
<400> 4226
000
<210> 4227
<400> 4227
000
<210> 4228
<400> 4228
000
<210> 4229
<400> 4229
000
<210> 4230
<400> 4230
000
<210> 4231
<400> 4231
000
<210> 4232
<400> 4232
000
<210> 4233
<400> 4233
000
<210> 4234
<400> 4234
000
<210> 4235
<400> 4235
000
<210> 4236
<400> 4236
000
<210> 4237
<400> 4237
000
<210> 4238
<400> 4238
000
<210> 4239
<400> 4239
000
<210> 4240
<400> 4240
000
<210> 4241
<400> 4241
000
<210> 4242
<400> 4242
000
<210> 4243
<400> 4243
000
<210> 4244
<400> 4244
000
<210> 4245
<400> 4245
000
<210> 4246
<400> 4246
000
<210> 4247
<400> 4247
000
<210> 4248
<400> 4248
000
<210> 4249
<400> 4249
000
<210> 4250
<400> 4250
000
<210> 4251
<400> 4251
000
<210> 4252
<400> 4252
000
<210> 4253
<400> 4253
000
<210> 4254
<400> 4254
000
<210> 4255
<400> 4255
000
<210> 4256
<400> 4256
000
<210> 4257
<400> 4257
000
<210> 4258
<400> 4258
000
<210> 4259
<400> 4259
000
<210> 4260
<400> 4260
000
<210> 4261
<400> 4261
000
<210> 4262
<400> 4262
000
<210> 4263
<400> 4263
000
<210> 4264
<400> 4264
000
<210> 4265
<400> 4265
000
<210> 4266
<400> 4266
000
<210> 4267
<400> 4267
000
<210> 4268
<400> 4268
000
<210> 4269
<400> 4269
000
<210> 4270
<400> 4270
000
<210> 4271
<400> 4271
000
<210> 4272
<400> 4272
000
<210> 4273
<400> 4273
000
<210> 4274
<400> 4274
000
<210> 4275
<400> 4275
000
<210> 4276
<400> 4276
000
<210> 4277
<400> 4277
000
<210> 4278
<400> 4278
000
<210> 4279
<400> 4279
000
<210> 4280
<400> 4280
000
<210> 4281
<400> 4281
000
<210> 4282
<400> 4282
000
<210> 4283
<400> 4283
000
<210> 4284
<400> 4284
000
<210> 4285
<400> 4285
000
<210> 4286
<400> 4286
000
<210> 4287
<400> 4287
000
<210> 4288
<400> 4288
000
<210> 4289
<400> 4289
000
<210> 4290
<400> 4290
000
<210> 4291
<400> 4291
000
<210> 4292
<400> 4292
000
<210> 4293
<400> 4293
000
<210> 4294
<400> 4294
000
<210> 4295
<400> 4295
000
<210> 4296
<400> 4296
000
<210> 4297
<400> 4297
000
<210> 4298
<400> 4298
000
<210> 4299
<400> 4299
000
<210> 4300
<400> 4300
000
<210> 4301
<400> 4301
000
<210> 4302
<400> 4302
000
<210> 4303
<400> 4303
000
<210> 4304
<400> 4304
000
<210> 4305
<400> 4305
000
<210> 4306
<400> 4306
000
<210> 4307
<400> 4307
000
<210> 4308
<400> 4308
000
<210> 4309
<400> 4309
000
<210> 4310
<400> 4310
000
<210> 4311
<400> 4311
000
<210> 4312
<400> 4312
000
<210> 4313
<400> 4313
000
<210> 4314
<400> 4314
000
<210> 4315
<400> 4315
000
<210> 4316
<400> 4316
000
<210> 4317
<400> 4317
000
<210> 4318
<400> 4318
000
<210> 4319
<400> 4319
000
<210> 4320
<400> 4320
000
<210> 4321
<400> 4321
000
<210> 4322
<400> 4322
000
<210> 4323
<400> 4323
000
<210> 4324
<400> 4324
000
<210> 4325
<400> 4325
000
<210> 4326
<400> 4326
000
<210> 4327
<400> 4327
000
<210> 4328
<400> 4328
000
<210> 4329
<400> 4329
000
<210> 4330
<400> 4330
000
<210> 4331
<400> 4331
000
<210> 4332
<400> 4332
000
<210> 4333
<400> 4333
000
<210> 4334
<400> 4334
000
<210> 4335
<400> 4335
000
<210> 4336
<400> 4336
000
<210> 4337
<400> 4337
000
<210> 4338
<400> 4338
000
<210> 4339
<400> 4339
000
<210> 4340
<400> 4340
000
<210> 4341
<400> 4341
000
<210> 4342
<400> 4342
000
<210> 4343
<400> 4343
000
<210> 4344
<400> 4344
000
<210> 4345
<400> 4345
000
<210> 4346
<400> 4346
000
<210> 4347
<400> 4347
000
<210> 4348
<400> 4348
000
<210> 4349
<400> 4349
000
<210> 4350
<400> 4350
000
<210> 4351
<400> 4351
000
<210> 4352
<400> 4352
000
<210> 4353
<400> 4353
000
<210> 4354
<400> 4354
000
<210> 4355
<400> 4355
000
<210> 4356
<400> 4356
000
<210> 4357
<400> 4357
000
<210> 4358
<400> 4358
000
<210> 4359
<400> 4359
000
<210> 4360
<400> 4360
000
<210> 4361
<400> 4361
000
<210> 4362
<400> 4362
000
<210> 4363
<400> 4363
000
<210> 4364
<400> 4364
000
<210> 4365
<400> 4365
000
<210> 4366
<400> 4366
000
<210> 4367
<400> 4367
000
<210> 4368
<400> 4368
000
<210> 4369
<400> 4369
000
<210> 4370
<400> 4370
000
<210> 4371
<400> 4371
000
<210> 4372
<400> 4372
000
<210> 4373
<400> 4373
000
<210> 4374
<400> 4374
000
<210> 4375
<400> 4375
000
<210> 4376
<400> 4376
000
<210> 4377
<400> 4377
000
<210> 4378
<400> 4378
000
<210> 4379
<400> 4379
000
<210> 4380
<400> 4380
000
<210> 4381
<400> 4381
000
<210> 4382
<400> 4382
000
<210> 4383
<400> 4383
000
<210> 4384
<400> 4384
000
<210> 4385
<400> 4385
000
<210> 4386
<400> 4386
000
<210> 4387
<400> 4387
000
<210> 4388
<400> 4388
000
<210> 4389
<400> 4389
000
<210> 4390
<400> 4390
000
<210> 4391
<400> 4391
000
<210> 4392
<400> 4392
000
<210> 4393
<400> 4393
000
<210> 4394
<400> 4394
000
<210> 4395
<400> 4395
000
<210> 4396
<400> 4396
000
<210> 4397
<400> 4397
000
<210> 4398
<400> 4398
000
<210> 4399
<400> 4399
000
<210> 4400
<400> 4400
000
<210> 4401
<400> 4401
000
<210> 4402
<400> 4402
000
<210> 4403
<400> 4403
000
<210> 4404
<400> 4404
000
<210> 4405
<400> 4405
000
<210> 4406
<400> 4406
000
<210> 4407
<400> 4407
000
<210> 4408
<400> 4408
000
<210> 4409
<400> 4409
000
<210> 4410
<400> 4410
000
<210> 4411
<400> 4411
000
<210> 4412
<400> 4412
000
<210> 4413
<400> 4413
000
<210> 4414
<400> 4414
000
<210> 4415
<400> 4415
000
<210> 4416
<400> 4416
000
<210> 4417
<400> 4417
000
<210> 4418
<400> 4418
000
<210> 4419
<400> 4419
000
<210> 4420
<400> 4420
000
<210> 4421
<400> 4421
000
<210> 4422
<400> 4422
000
<210> 4423
<400> 4423
000
<210> 4424
<400> 4424
000
<210> 4425
<400> 4425
000
<210> 4426
<400> 4426
000
<210> 4427
<400> 4427
000
<210> 4428
<400> 4428
000
<210> 4429
<400> 4429
000
<210> 4430
<400> 4430
000
<210> 4431
<400> 4431
000
<210> 4432
<400> 4432
000
<210> 4433
<400> 4433
000
<210> 4434
<400> 4434
000
<210> 4435
<400> 4435
000
<210> 4436
<400> 4436
000
<210> 4437
<400> 4437
000
<210> 4438
<400> 4438
000
<210> 4439
<400> 4439
000
<210> 4440
<400> 4440
000
<210> 4441
<400> 4441
000
<210> 4442
<400> 4442
000
<210> 4443
<400> 4443
000
<210> 4444
<400> 4444
000
<210> 4445
<400> 4445
000
<210> 4446
<400> 4446
000
<210> 4447
<400> 4447
000
<210> 4448
<400> 4448
000
<210> 4449
<400> 4449
000
<210> 4450
<400> 4450
000
<210> 4451
<400> 4451
000
<210> 4452
<400> 4452
000
<210> 4453
<400> 4453
000
<210> 4454
<400> 4454
000
<210> 4455
<400> 4455
000
<210> 4456
<400> 4456
000
<210> 4457
<400> 4457
000
<210> 4458
<400> 4458
000
<210> 4459
<400> 4459
000
<210> 4460
<400> 4460
000
<210> 4461
<400> 4461
000
<210> 4462
<400> 4462
000
<210> 4463
<400> 4463
000
<210> 4464
<400> 4464
000
<210> 4465
<400> 4465
000
<210> 4466
<400> 4466
000
<210> 4467
<400> 4467
000
<210> 4468
<400> 4468
000
<210> 4469
<400> 4469
000
<210> 4470
<400> 4470
000
<210> 4471
<400> 4471
000
<210> 4472
<400> 4472
000
<210> 4473
<400> 4473
000
<210> 4474
<400> 4474
000
<210> 4475
<400> 4475
000
<210> 4476
<400> 4476
000
<210> 4477
<400> 4477
000
<210> 4478
<400> 4478
000
<210> 4479
<400> 4479
000
<210> 4480
<400> 4480
000
<210> 4481
<400> 4481
000
<210> 4482
<400> 4482
000
<210> 4483
<400> 4483
000
<210> 4484
<400> 4484
000
<210> 4485
<400> 4485
000
<210> 4486
<400> 4486
000
<210> 4487
<400> 4487
000
<210> 4488
<400> 4488
000
<210> 4489
<400> 4489
000
<210> 4490
<400> 4490
000
<210> 4491
<400> 4491
000
<210> 4492
<400> 4492
000
<210> 4493
<400> 4493
000
<210> 4494
<400> 4494
000
<210> 4495
<400> 4495
000
<210> 4496
<400> 4496
000
<210> 4497
<400> 4497
000
<210> 4498
<400> 4498
000
<210> 4499
<400> 4499
000
<210> 4500
<400> 4500
000
<210> 4501
<400> 4501
000
<210> 4502
<400> 4502
000
<210> 4503
<400> 4503
000
<210> 4504
<400> 4504
000
<210> 4505
<400> 4505
000
<210> 4506
<400> 4506
000
<210> 4507
<400> 4507
000
<210> 4508
<400> 4508
000
<210> 4509
<400> 4509
000
<210> 4510
<400> 4510
000
<210> 4511
<400> 4511
000
<210> 4512
<400> 4512
000
<210> 4513
<400> 4513
000
<210> 4514
<400> 4514
000
<210> 4515
<400> 4515
000
<210> 4516
<400> 4516
000
<210> 4517
<400> 4517
000
<210> 4518
<400> 4518
000
<210> 4519
<400> 4519
000
<210> 4520
<400> 4520
000
<210> 4521
<400> 4521
000
<210> 4522
<400> 4522
000
<210> 4523
<400> 4523
000
<210> 4524
<400> 4524
000
<210> 4525
<400> 4525
000
<210> 4526
<400> 4526
000
<210> 4527
<400> 4527
000
<210> 4528
<400> 4528
000
<210> 4529
<400> 4529
000
<210> 4530
<400> 4530
000
<210> 4531
<400> 4531
000
<210> 4532
<400> 4532
000
<210> 4533
<400> 4533
000
<210> 4534
<400> 4534
000
<210> 4535
<400> 4535
000
<210> 4536
<400> 4536
000
<210> 4537
<400> 4537
000
<210> 4538
<400> 4538
000
<210> 4539
<400> 4539
000
<210> 4540
<400> 4540
000
<210> 4541
<400> 4541
000
<210> 4542
<400> 4542
000
<210> 4543
<400> 4543
000
<210> 4544
<400> 4544
000
<210> 4545
<400> 4545
000
<210> 4546
<400> 4546
000
<210> 4547
<400> 4547
000
<210> 4548
<400> 4548
000
<210> 4549
<400> 4549
000
<210> 4550
<400> 4550
000
<210> 4551
<400> 4551
000
<210> 4552
<400> 4552
000
<210> 4553
<400> 4553
000
<210> 4554
<400> 4554
000
<210> 4555
<400> 4555
000
<210> 4556
<400> 4556
000
<210> 4557
<400> 4557
000
<210> 4558
<400> 4558
000
<210> 4559
<400> 4559
000
<210> 4560
<400> 4560
000
<210> 4561
<400> 4561
000
<210> 4562
<400> 4562
000
<210> 4563
<400> 4563
000
<210> 4564
<400> 4564
000
<210> 4565
<400> 4565
000
<210> 4566
<400> 4566
000
<210> 4567
<400> 4567
000
<210> 4568
<400> 4568
000
<210> 4569
<400> 4569
000
<210> 4570
<400> 4570
000
<210> 4571
<400> 4571
000
<210> 4572
<400> 4572
000
<210> 4573
<400> 4573
000
<210> 4574
<400> 4574
000
<210> 4575
<400> 4575
000
<210> 4576
<400> 4576
000
<210> 4577
<400> 4577
000
<210> 4578
<400> 4578
000
<210> 4579
<400> 4579
000
<210> 4580
<400> 4580
000
<210> 4581
<400> 4581
000
<210> 4582
<400> 4582
000
<210> 4583
<400> 4583
000
<210> 4584
<400> 4584
000
<210> 4585
<400> 4585
000
<210> 4586
<400> 4586
000
<210> 4587
<400> 4587
000
<210> 4588
<400> 4588
000
<210> 4589
<400> 4589
000
<210> 4590
<400> 4590
000
<210> 4591
<400> 4591
000
<210> 4592
<400> 4592
000
<210> 4593
<400> 4593
000
<210> 4594
<400> 4594
000
<210> 4595
<400> 4595
000
<210> 4596
<400> 4596
000
<210> 4597
<400> 4597
000
<210> 4598
<400> 4598
000
<210> 4599
<400> 4599
000
<210> 4600
<400> 4600
000
<210> 4601
<400> 4601
000
<210> 4602
<400> 4602
000
<210> 4603
<400> 4603
000
<210> 4604
<400> 4604
000
<210> 4605
<400> 4605
000
<210> 4606
<400> 4606
000
<210> 4607
<400> 4607
000
<210> 4608
<400> 4608
000
<210> 4609
<400> 4609
000
<210> 4610
<400> 4610
000
<210> 4611
<400> 4611
000
<210> 4612
<400> 4612
000
<210> 4613
<400> 4613
000
<210> 4614
<400> 4614
000
<210> 4615
<400> 4615
000
<210> 4616
<400> 4616
000
<210> 4617
<400> 4617
000
<210> 4618
<400> 4618
000
<210> 4619
<400> 4619
000
<210> 4620
<400> 4620
000
<210> 4621
<400> 4621
000
<210> 4622
<400> 4622
000
<210> 4623
<400> 4623
000
<210> 4624
<400> 4624
000
<210> 4625
<400> 4625
000
<210> 4626
<400> 4626
000
<210> 4627
<400> 4627
000
<210> 4628
<400> 4628
000
<210> 4629
<400> 4629
000
<210> 4630
<400> 4630
000
<210> 4631
<400> 4631
000
<210> 4632
<400> 4632
000
<210> 4633
<400> 4633
000
<210> 4634
<400> 4634
000
<210> 4635
<400> 4635
000
<210> 4636
<400> 4636
000
<210> 4637
<400> 4637
000
<210> 4638
<400> 4638
000
<210> 4639
<400> 4639
000
<210> 4640
<400> 4640
000
<210> 4641
<400> 4641
000
<210> 4642
<400> 4642
000
<210> 4643
<400> 4643
000
<210> 4644
<400> 4644
000
<210> 4645
<400> 4645
000
<210> 4646
<400> 4646
000
<210> 4647
<400> 4647
000
<210> 4648
<400> 4648
000
<210> 4649
<400> 4649
000
<210> 4650
<400> 4650
000
<210> 4651
<400> 4651
000
<210> 4652
<400> 4652
000
<210> 4653
<400> 4653
000
<210> 4654
<400> 4654
000
<210> 4655
<400> 4655
000
<210> 4656
<400> 4656
000
<210> 4657
<400> 4657
000
<210> 4658
<400> 4658
000
<210> 4659
<400> 4659
000
<210> 4660
<400> 4660
000
<210> 4661
<400> 4661
000
<210> 4662
<400> 4662
000
<210> 4663
<400> 4663
000
<210> 4664
<400> 4664
000
<210> 4665
<400> 4665
000
<210> 4666
<400> 4666
000
<210> 4667
<400> 4667
000
<210> 4668
<400> 4668
000
<210> 4669
<400> 4669
000
<210> 4670
<400> 4670
000
<210> 4671
<400> 4671
000
<210> 4672
<400> 4672
000
<210> 4673
<400> 4673
000
<210> 4674
<400> 4674
000
<210> 4675
<400> 4675
000
<210> 4676
<400> 4676
000
<210> 4677
<400> 4677
000
<210> 4678
<400> 4678
000
<210> 4679
<400> 4679
000
<210> 4680
<400> 4680
000
<210> 4681
<400> 4681
000
<210> 4682
<400> 4682
000
<210> 4683
<400> 4683
000
<210> 4684
<400> 4684
000
<210> 4685
<400> 4685
000
<210> 4686
<400> 4686
000
<210> 4687
<400> 4687
000
<210> 4688
<400> 4688
000
<210> 4689
<400> 4689
000
<210> 4690
<400> 4690
000
<210> 4691
<400> 4691
000
<210> 4692
<400> 4692
000
<210> 4693
<400> 4693
000
<210> 4694
<400> 4694
000
<210> 4695
<400> 4695
000
<210> 4696
<400> 4696
000
<210> 4697
<400> 4697
000
<210> 4698
<400> 4698
000
<210> 4699
<400> 4699
000
<210> 4700
<400> 4700
000
<210> 4701
<400> 4701
000
<210> 4702
<400> 4702
000
<210> 4703
<400> 4703
000
<210> 4704
<400> 4704
000
<210> 4705
<400> 4705
000
<210> 4706
<400> 4706
000
<210> 4707
<400> 4707
000
<210> 4708
<400> 4708
000
<210> 4709
<400> 4709
000
<210> 4710
<400> 4710
000
<210> 4711
<400> 4711
000
<210> 4712
<400> 4712
000
<210> 4713
<400> 4713
000
<210> 4714
<400> 4714
000
<210> 4715
<400> 4715
000
<210> 4716
<400> 4716
000
<210> 4717
<400> 4717
000
<210> 4718
<400> 4718
000
<210> 4719
<400> 4719
000
<210> 4720
<400> 4720
000
<210> 4721
<400> 4721
000
<210> 4722
<400> 4722
000
<210> 4723
<400> 4723
000
<210> 4724
<400> 4724
000
<210> 4725
<400> 4725
000
<210> 4726
<400> 4726
000
<210> 4727
<400> 4727
000
<210> 4728
<400> 4728
000
<210> 4729
<400> 4729
000
<210> 4730
<400> 4730
000
<210> 4731
<400> 4731
000
<210> 4732
<400> 4732
000
<210> 4733
<400> 4733
000
<210> 4734
<400> 4734
000
<210> 4735
<400> 4735
000
<210> 4736
<400> 4736
000
<210> 4737
<400> 4737
000
<210> 4738
<400> 4738
000
<210> 4739
<400> 4739
000
<210> 4740
<400> 4740
000
<210> 4741
<400> 4741
000
<210> 4742
<400> 4742
000
<210> 4743
<400> 4743
000
<210> 4744
<400> 4744
000
<210> 4745
<400> 4745
000
<210> 4746
<400> 4746
000
<210> 4747
<400> 4747
000
<210> 4748
<400> 4748
000
<210> 4749
<400> 4749
000
<210> 4750
<400> 4750
000
<210> 4751
<400> 4751
000
<210> 4752
<400> 4752
000
<210> 4753
<400> 4753
000
<210> 4754
<400> 4754
000
<210> 4755
<400> 4755
000
<210> 4756
<400> 4756
000
<210> 4757
<400> 4757
000
<210> 4758
<400> 4758
000
<210> 4759
<400> 4759
000
<210> 4760
<400> 4760
000
<210> 4761
<400> 4761
000
<210> 4762
<400> 4762
000
<210> 4763
<400> 4763
000
<210> 4764
<400> 4764
000
<210> 4765
<400> 4765
000
<210> 4766
<400> 4766
000
<210> 4767
<400> 4767
000
<210> 4768
<400> 4768
000
<210> 4769
<400> 4769
000
<210> 4770
<400> 4770
000
<210> 4771
<400> 4771
000
<210> 4772
<400> 4772
000
<210> 4773
<400> 4773
000
<210> 4774
<400> 4774
000
<210> 4775
<400> 4775
000
<210> 4776
<400> 4776
000
<210> 4777
<400> 4777
000
<210> 4778
<400> 4778
000
<210> 4779
<400> 4779
000
<210> 4780
<400> 4780
000
<210> 4781
<400> 4781
000
<210> 4782
<400> 4782
000
<210> 4783
<400> 4783
000
<210> 4784
<400> 4784
000
<210> 4785
<400> 4785
000
<210> 4786
<400> 4786
000
<210> 4787
<400> 4787
000
<210> 4788
<400> 4788
000
<210> 4789
<400> 4789
000
<210> 4790
<400> 4790
000
<210> 4791
<400> 4791
000
<210> 4792
<400> 4792
000
<210> 4793
<400> 4793
000
<210> 4794
<400> 4794
000
<210> 4795
<400> 4795
000
<210> 4796
<400> 4796
000
<210> 4797
<400> 4797
000
<210> 4798
<400> 4798
000
<210> 4799
<400> 4799
000
<210> 4800
<400> 4800
000
<210> 4801
<400> 4801
000
<210> 4802
<400> 4802
000
<210> 4803
<400> 4803
000
<210> 4804
<400> 4804
000
<210> 4805
<400> 4805
000
<210> 4806
<400> 4806
000
<210> 4807
<400> 4807
000
<210> 4808
<400> 4808
000
<210> 4809
<400> 4809
000
<210> 4810
<400> 4810
000
<210> 4811
<400> 4811
000
<210> 4812
<400> 4812
000
<210> 4813
<400> 4813
000
<210> 4814
<400> 4814
000
<210> 4815
<400> 4815
000
<210> 4816
<400> 4816
000
<210> 4817
<400> 4817
000
<210> 4818
<400> 4818
000
<210> 4819
<400> 4819
000
<210> 4820
<400> 4820
000
<210> 4821
<400> 4821
000
<210> 4822
<400> 4822
000
<210> 4823
<400> 4823
000
<210> 4824
<400> 4824
000
<210> 4825
<400> 4825
000
<210> 4826
<400> 4826
000
<210> 4827
<400> 4827
000
<210> 4828
<400> 4828
000
<210> 4829
<400> 4829
000
<210> 4830
<400> 4830
000
<210> 4831
<400> 4831
000
<210> 4832
<400> 4832
000
<210> 4833
<400> 4833
000
<210> 4834
<400> 4834
000
<210> 4835
<400> 4835
000
<210> 4836
<400> 4836
000
<210> 4837
<400> 4837
000
<210> 4838
<400> 4838
000
<210> 4839
<400> 4839
000
<210> 4840
<400> 4840
000
<210> 4841
<400> 4841
000
<210> 4842
<400> 4842
000
<210> 4843
<400> 4843
000
<210> 4844
<400> 4844
000
<210> 4845
<400> 4845
000
<210> 4846
<400> 4846
000
<210> 4847
<400> 4847
000
<210> 4848
<400> 4848
000
<210> 4849
<400> 4849
000
<210> 4850
<400> 4850
000
<210> 4851
<400> 4851
000
<210> 4852
<400> 4852
000
<210> 4853
<400> 4853
000
<210> 4854
<400> 4854
000
<210> 4855
<400> 4855
000
<210> 4856
<400> 4856
000
<210> 4857
<400> 4857
000
<210> 4858
<400> 4858
000
<210> 4859
<400> 4859
000
<210> 4860
<400> 4860
000
<210> 4861
<400> 4861
000
<210> 4862
<400> 4862
000
<210> 4863
<400> 4863
000
<210> 4864
<400> 4864
000
<210> 4865
<400> 4865
000
<210> 4866
<400> 4866
000
<210> 4867
<400> 4867
000
<210> 4868
<400> 4868
000
<210> 4869
<400> 4869
000
<210> 4870
<400> 4870
000
<210> 4871
<400> 4871
000
<210> 4872
<400> 4872
000
<210> 4873
<400> 4873
000
<210> 4874
<400> 4874
000
<210> 4875
<400> 4875
000
<210> 4876
<400> 4876
000
<210> 4877
<400> 4877
000
<210> 4878
<400> 4878
000
<210> 4879
<400> 4879
000
<210> 4880
<400> 4880
000
<210> 4881
<400> 4881
000
<210> 4882
<400> 4882
000
<210> 4883
<400> 4883
000
<210> 4884
<400> 4884
000
<210> 4885
<400> 4885
000
<210> 4886
<400> 4886
000
<210> 4887
<400> 4887
000
<210> 4888
<400> 4888
000
<210> 4889
<400> 4889
000
<210> 4890
<400> 4890
000
<210> 4891
<400> 4891
000
<210> 4892
<400> 4892
000
<210> 4893
<400> 4893
000
<210> 4894
<400> 4894
000
<210> 4895
<400> 4895
000
<210> 4896
<400> 4896
000
<210> 4897
<400> 4897
000
<210> 4898
<400> 4898
000
<210> 4899
<400> 4899
000
<210> 4900
<400> 4900
000
<210> 4901
<400> 4901
000
<210> 4902
<400> 4902
000
<210> 4903
<400> 4903
000
<210> 4904
<400> 4904
000
<210> 4905
<400> 4905
000
<210> 4906
<400> 4906
000
<210> 4907
<400> 4907
000
<210> 4908
<400> 4908
000
<210> 4909
<400> 4909
000
<210> 4910
<400> 4910
000
<210> 4911
<400> 4911
000
<210> 4912
<400> 4912
000
<210> 4913
<400> 4913
000
<210> 4914
<400> 4914
000
<210> 4915
<400> 4915
000
<210> 4916
<400> 4916
000
<210> 4917
<400> 4917
000
<210> 4918
<400> 4918
000
<210> 4919
<400> 4919
000
<210> 4920
<400> 4920
000
<210> 4921
<400> 4921
000
<210> 4922
<400> 4922
000
<210> 4923
<400> 4923
000
<210> 4924
<400> 4924
000
<210> 4925
<400> 4925
000
<210> 4926
<400> 4926
000
<210> 4927
<400> 4927
000
<210> 4928
<400> 4928
000
<210> 4929
<400> 4929
000
<210> 4930
<400> 4930
000
<210> 4931
<400> 4931
000
<210> 4932
<400> 4932
000
<210> 4933
<400> 4933
000
<210> 4934
<400> 4934
000
<210> 4935
<400> 4935
000
<210> 4936
<400> 4936
000
<210> 4937
<400> 4937
000
<210> 4938
<400> 4938
000
<210> 4939
<400> 4939
000
<210> 4940
<400> 4940
000
<210> 4941
<400> 4941
000
<210> 4942
<400> 4942
000
<210> 4943
<400> 4943
000
<210> 4944
<400> 4944
000
<210> 4945
<400> 4945
000
<210> 4946
<400> 4946
000
<210> 4947
<400> 4947
000
<210> 4948
<400> 4948
000
<210> 4949
<400> 4949
000
<210> 4950
<400> 4950
000
<210> 4951
<400> 4951
000
<210> 4952
<400> 4952
000
<210> 4953
<400> 4953
000
<210> 4954
<400> 4954
000
<210> 4955
<400> 4955
000
<210> 4956
<400> 4956
000
<210> 4957
<400> 4957
000
<210> 4958
<400> 4958
000
<210> 4959
<400> 4959
000
<210> 4960
<400> 4960
000
<210> 4961
<400> 4961
000
<210> 4962
<400> 4962
000
<210> 4963
<400> 4963
000
<210> 4964
<400> 4964
000
<210> 4965
<400> 4965
000
<210> 4966
<400> 4966
000
<210> 4967
<400> 4967
000
<210> 4968
<400> 4968
000
<210> 4969
<400> 4969
000
<210> 4970
<400> 4970
000
<210> 4971
<400> 4971
000
<210> 4972
<400> 4972
000
<210> 4973
<400> 4973
000
<210> 4974
<400> 4974
000
<210> 4975
<400> 4975
000
<210> 4976
<400> 4976
000
<210> 4977
<400> 4977
000
<210> 4978
<400> 4978
000
<210> 4979
<400> 4979
000
<210> 4980
<400> 4980
000
<210> 4981
<400> 4981
000
<210> 4982
<400> 4982
000
<210> 4983
<400> 4983
000
<210> 4984
<400> 4984
000
<210> 4985
<400> 4985
000
<210> 4986
<400> 4986
000
<210> 4987
<400> 4987
000
<210> 4988
<400> 4988
000
<210> 4989
<400> 4989
000
<210> 4990
<400> 4990
000
<210> 4991
<400> 4991
000
<210> 4992
<400> 4992
000
<210> 4993
<400> 4993
000
<210> 4994
<400> 4994
000
<210> 4995
<400> 4995
000
<210> 4996
<400> 4996
000
<210> 4997
<400> 4997
000
<210> 4998
<400> 4998
000
<210> 4999
<400> 4999
000
<210> 5000
<400> 5000
000
<210> 5001
<400> 5001
000
<210> 5002
<400> 5002
000
<210> 5003
<400> 5003
000
<210> 5004
<400> 5004
000
<210> 5005
<400> 5005
000
<210> 5006
<400> 5006
000
<210> 5007
<400> 5007
000
<210> 5008
<400> 5008
000
<210> 5009
<400> 5009
000
<210> 5010
<400> 5010
000
<210> 5011
<400> 5011
000
<210> 5012
<400> 5012
000
<210> 5013
<400> 5013
000
<210> 5014
<400> 5014
000
<210> 5015
<400> 5015
000
<210> 5016
<400> 5016
000
<210> 5017
<400> 5017
000
<210> 5018
<400> 5018
000
<210> 5019
<400> 5019
000
<210> 5020
<400> 5020
000
<210> 5021
<400> 5021
000
<210> 5022
<400> 5022
000
<210> 5023
<400> 5023
000
<210> 5024
<400> 5024
000
<210> 5025
<400> 5025
000
<210> 5026
<400> 5026
000
<210> 5027
<400> 5027
000
<210> 5028
<400> 5028
000
<210> 5029
<400> 5029
000
<210> 5030
<400> 5030
000
<210> 5031
<400> 5031
000
<210> 5032
<400> 5032
000
<210> 5033
<400> 5033
000
<210> 5034
<400> 5034
000
<210> 5035
<400> 5035
000
<210> 5036
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5036
ggccgctgca catcgtcctg
20
<210> 5037
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5037
gcggggtctg ccatgggtcg
20
<210> 5038
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5038
agttgctcat gcaggatttc
20
<210> 5039
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5039
aagtcatggt aggggagctt
20
<210> 5040
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5040
agtcatggta ggggagcttg
20
<210> 5041
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5041
attgcactca tcagagctac
20
<210> 5042
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5042
cctagagtga agagattcat
20
<210> 5043
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5043
ccaatgaatc tcttcactct
20
<210> 5044
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5044
aaagtcatgg taggggagct
20
<210> 5045
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5045
gtgagcaatc ccccgggcga
20
<210> 5046
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5046
gtcgttcttc acgaggatat
20
<210> 5047
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5047
gccgcgtcag gtactcctgt
20
<210> 5048
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5048
gacgcggcat gtcatcagct
20
<210> 5049
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5049
gcttctgctg ccggttaacg
20
<210> 5050
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5050
gtggatgacc tggctaacag
20
<210> 5051
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5051
gtgatcacac tccatgtggg
20
<210> 5052
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5052
gcccattgag ctggacaccc
20
<210> 5053
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5053
gcggtcatct tccaggatga
20
<210> 5054
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5054
gggagctgcc cagcttgcgc
20
<210> 5055
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5055
gttgatgttg ttggcacacg
20
<210> 5056
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5056
ggcatcttgg gcctcccaca
20
<210> 5057
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5057
gcggcatgtc atcagctggg
20
<210> 5058
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5058
gctcctcagc cgtcaggaac
20
<210> 5059
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5059
gctggtgtta tattctgatg
20
<210> 5060
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5060
ccgacttctg aacgtgcggt
20
<210> 5061
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5061
tgctggcgat acgcgtccac
20
<210> 5062
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5062
cccgacttct gaacgtgcgg
20
<210> 5063
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5063
ccaccgcacg ttcagaagtc
20
<210> 5064
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5064
tcacccgact tctgaacgtg
20
<210> 5065
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5065
cccaccgcac gttcagaagt
20
<210> 5066
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5066
cgagcagcgg ggtctgccat
20
<210> 5067
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5067
acgagcagcg gggtctgcca
20
<210> 5068
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5068
agcggggtct gccatgggtc
20
<210> 5069
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5069
cctgagcagc ccccgaccca
20
<210> 5070
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5070
aacgtgcggt gggatcgtgc
20
<210> 5071
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5071
ggacgatgtg cagcggccac
20
<210> 5072
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5072
gtccacagga cgatgtgcag
20
<210> 5073
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5073
catgggtcgg gggctgctca
20
<210> 5074
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5074
ccatgggtcg ggggctgctc
20
<210> 5075
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5075
cagcggggtc tgccatgggt
20
<210> 5076
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5076
atgggtcggg ggctgctcag
20
<210> 5077
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5077
cggggtctgc catgggtcgg
20
<210> 5078
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5078
aggaagtctg tgtggctgta
20
<210> 5079
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5079
ctccatctgt gagaagccac
20
<210> 5080
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5080
atgatagtca ctgacaacaa
20
<210> 5081
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5081
gatgctgcag ttgctcatgc
20
<210> 5082
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5082
acagccacac agacttcctg
20
<210> 5083
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5083
gaagccacag gaagtctgtg
20
<210> 5084
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5084
ttcctgtggc ttctcacaga
20
<210> 5085
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5085
ctgtggcttc tcacagatgg
20
<210> 5086
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5086
tcacaaaatt tacacagttg
20
<210> 5087
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5087
cccctaccat gactttattc
20
<210> 5088
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5088
ccagaataaa gtcatggtag
20
<210> 5089
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5089
gacaacatca tcttctcaga
20
<210> 5090
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5090
tccagaataa agtcatggta
20
<210> 5091
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5091
ggtaggggag cttggggtca
20
<210> 5092
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5092
ttctccaaag tgcattatga
20
<210> 5093
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5093
catcttccag aataaagtca
20
<210> 5094
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5094
cacatgaaga aagtctcacc
20
<210> 5095
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5095
ttccagaata aagtcatggt
20
<210> 5096
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<400> 5096
ttttccttca taatgcactt
20
<210> 5097
<211> 10
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<220>
<221> неопределенный признак
<222> (1)..(10)
<223> /примечание=«Эта последовательность может включать 1-10
нуклеотидов»
<400> 5097
aaaaaaaaaa
10
<210> 5098
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
олигонуклеотид»
<220>
<221> неопределенный признак
<222> (1)..(20)
<223> /примечание=«Эта последовательность может включать 10-20
нуклеотидов»
<400> 5098
aaaaaaaaaa aaaaaaaaaa
20
<210> 5099
<211> 200
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
полинуклеотид»
<220>
<221> неопределенный признак
<222> (1)..(200)
<223> /примечание=«Эта последовательность может включать 25-200
нуклеотидов»
<400> 5099
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
60
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
120
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
180
aaaaaaaaaa aaaaaaaaaa
200
<210> 5100
<211> 30
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
полипептид»
<400> 5100
Pro Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Pro
20 25 30
<210> 5101
<211> 35
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
полипептид»
<400> 5101
Pro Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
20 25 30
Gly Gly Pro
35
<210> 5102
<211> 17
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический
пептид»
<400> 5102
Gly Ser Ala Asp Asp Ala Lys Lys Asp Ala Ala Lys Lys Asp Gly Lys
1 5 10 15
Ser
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ ПОЛУЧЕНИЯ КЛЕТОК, ЭКСПРЕССИРУЮЩИХ РЕКОМБИНАНТНЫЙ РЕЦЕПТОР, И РОДСТВЕННЫЕ КОМПОЗИЦИИ | 2019 |
|
RU2835579C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ИММУНООНКОЛОГИИ | 2016 |
|
RU2771624C2 |
| НАЦЕЛИВАНИЕ НА КЛЕТКИ, ОПОСРЕДУЕМОЕ ХИМЕРНЫМ АНТИГЕННЫМ РЕЦЕПТОРОМ | 2018 |
|
RU2783316C2 |
| ДНК-СОДЕРЖАЩИЕ ПОЛИНУКЛЕОТИДЫ И РУКОВОДЯЩИЕ ПОСЛЕДОВАТЕЛЬНОСТИ ДЛЯ СИСТЕМ CRISPR ТИПА V И СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2021 |
|
RU2832314C1 |
| РЕДАКТИРОВАНИЕ ГЕНОВ С ИСПОЛЬЗОВАНИЕМ МОДИФИЦИРОВАННОЙ ДНК С ЗАМКНУТЫМИ КОНЦАМИ (зкДНК) | 2018 |
|
RU2811724C2 |
| МУТАЦИИ ФЕРМЕНТА CRISPR, УМЕНЬШАЮЩИЕ НЕЦЕЛЕВЫЕ ЭФФЕКТЫ | 2016 |
|
RU2752834C2 |
| СПОСОБ СОЗДАНИЯ Т-КЛЕТОК, ПРИГОДНЫХ ДЛЯ АЛЛОГЕННОЙ ТРАНСПЛАНТАЦИИ | 2015 |
|
RU2752933C2 |
| ВАРИАНТЫ, КОМПОЗИЦИИ И МЕТОДЫ ПРИМЕНЕНИЯ ХОМИНГ-ЭНДОНУКЛЕАЗЫ PD-1 | 2017 |
|
RU2781083C2 |
| ВАРИАНТЫ, КОМПОЗИЦИИ И СПОСОБЫ ПРИМЕНЕНИЯ ЭНДОНУКЛЕАЗЫ CBLB | 2018 |
|
RU2779097C2 |
| ИММУННЫЕ КЛЕТКИ, ДЕФЕКТНЫЕ ПО Suv39h1 | 2018 |
|
RU2784531C2 |


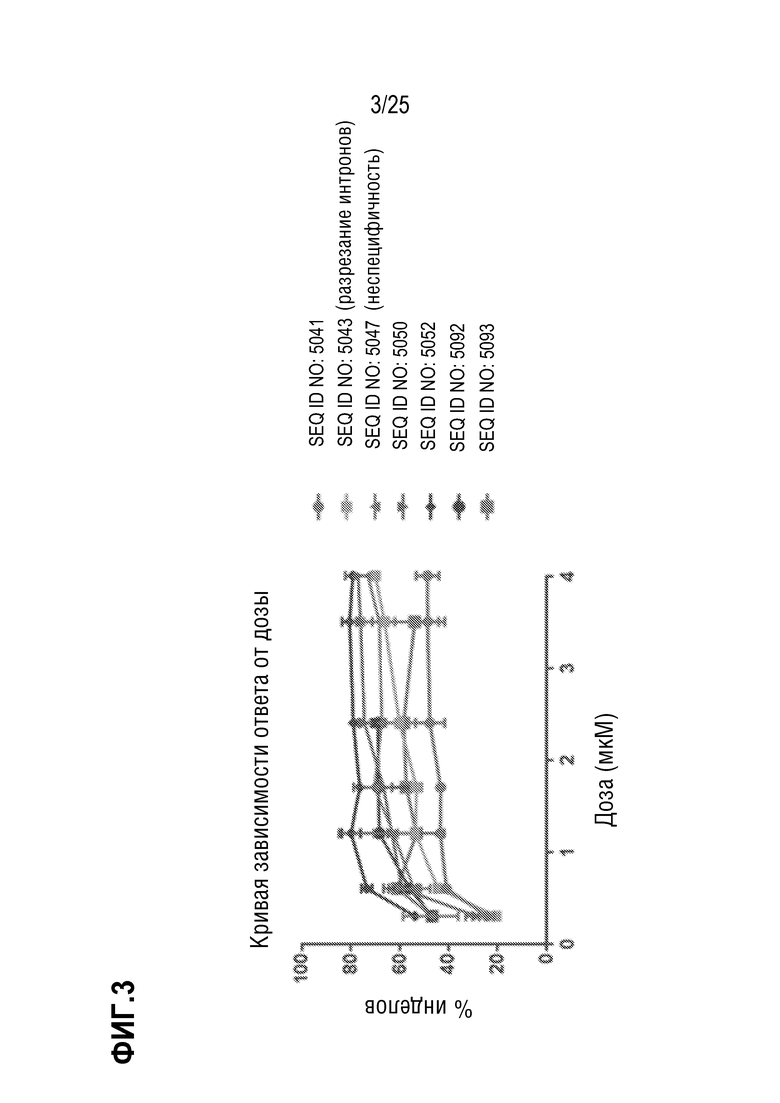
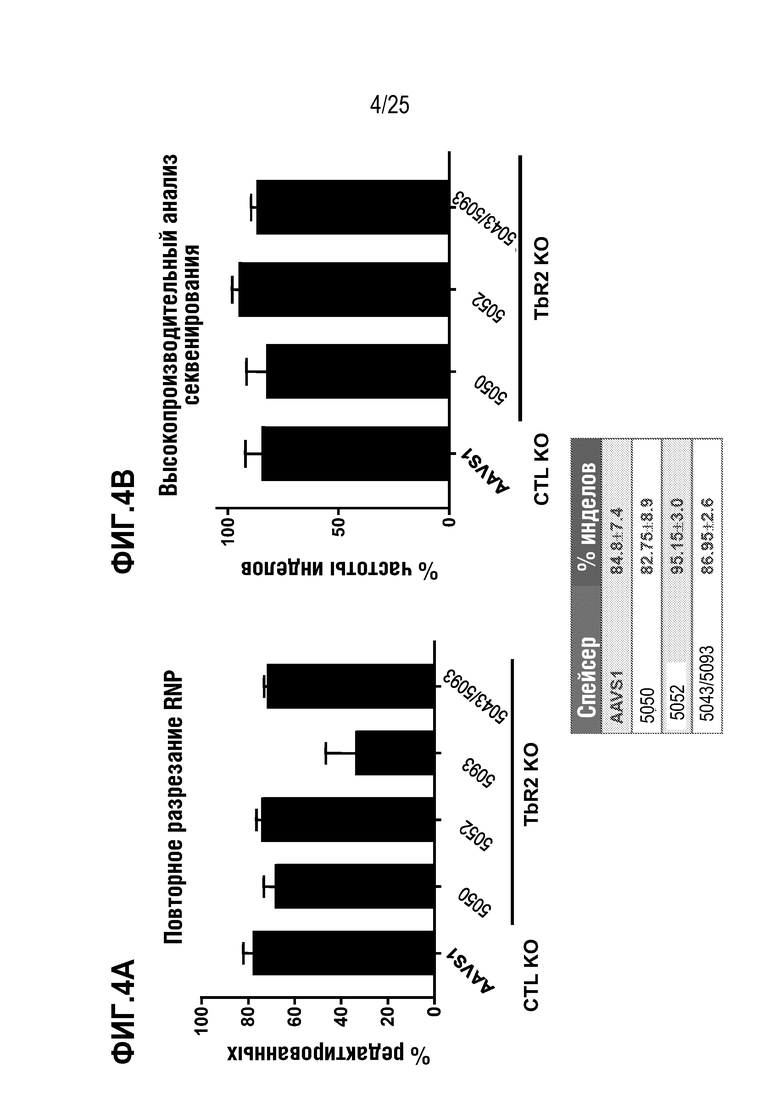

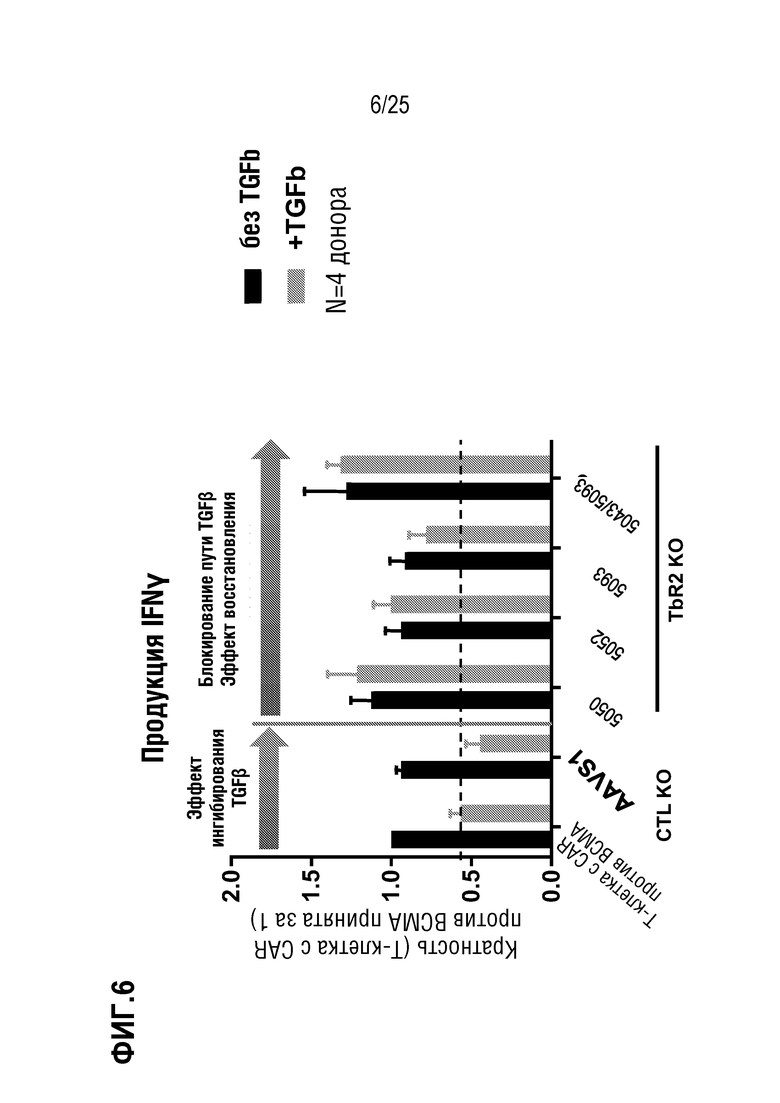
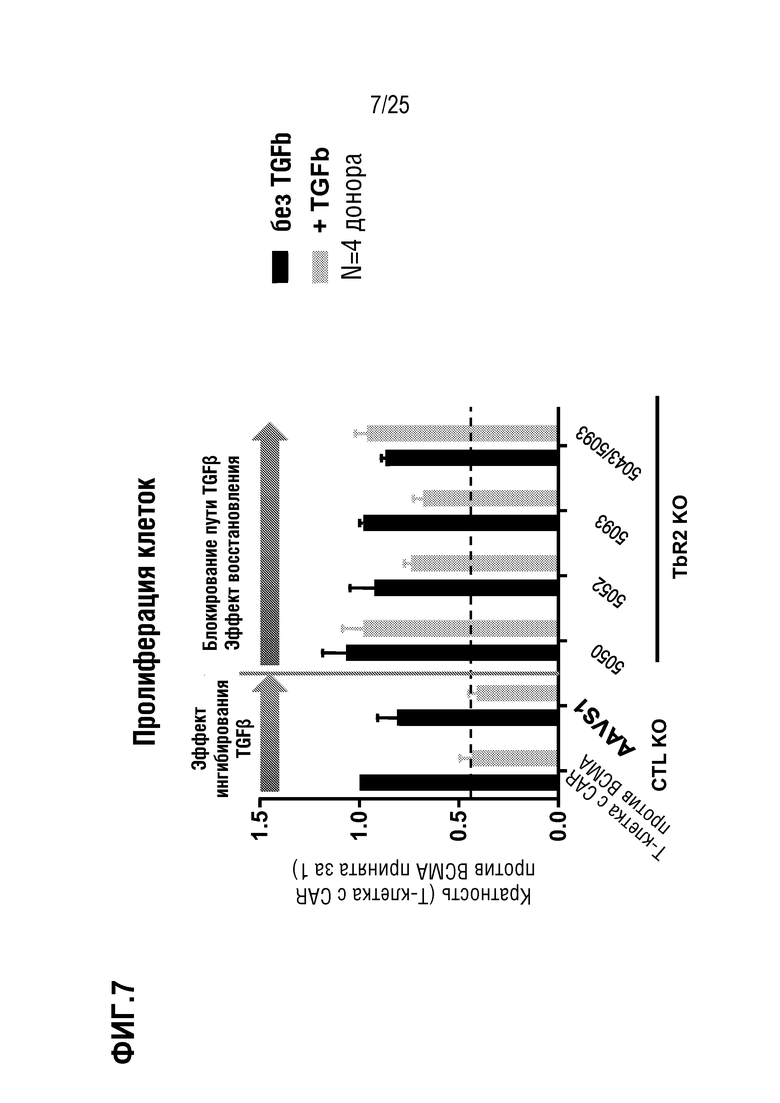
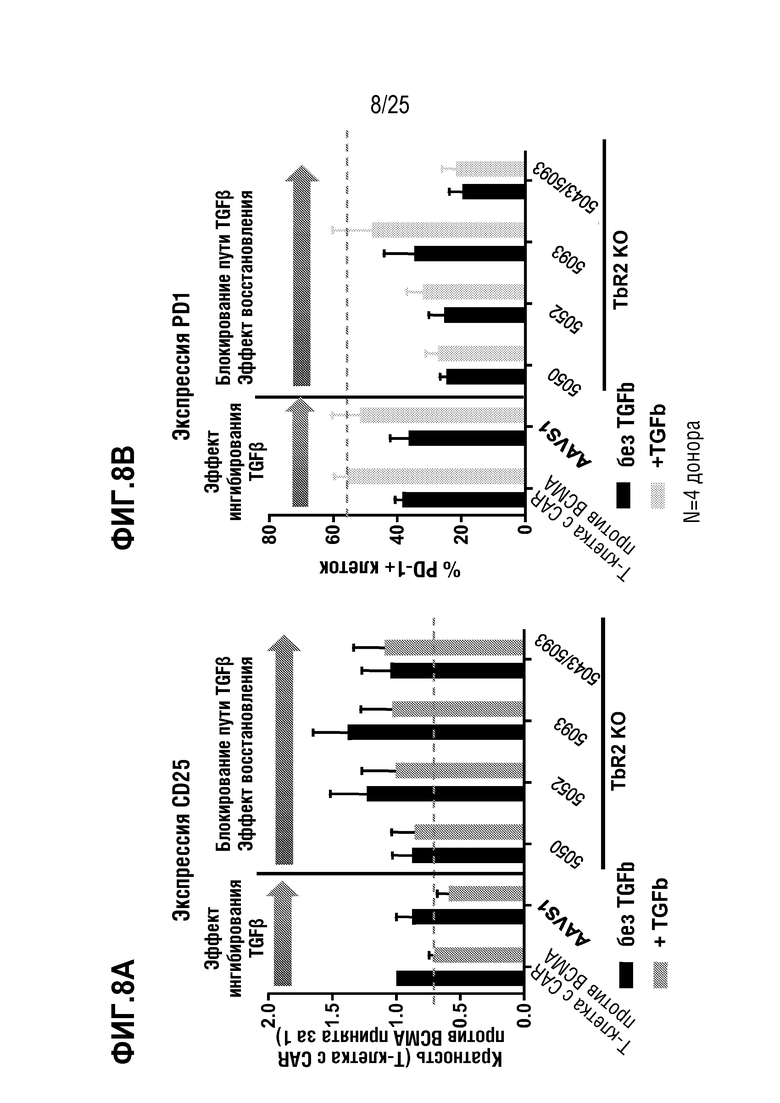
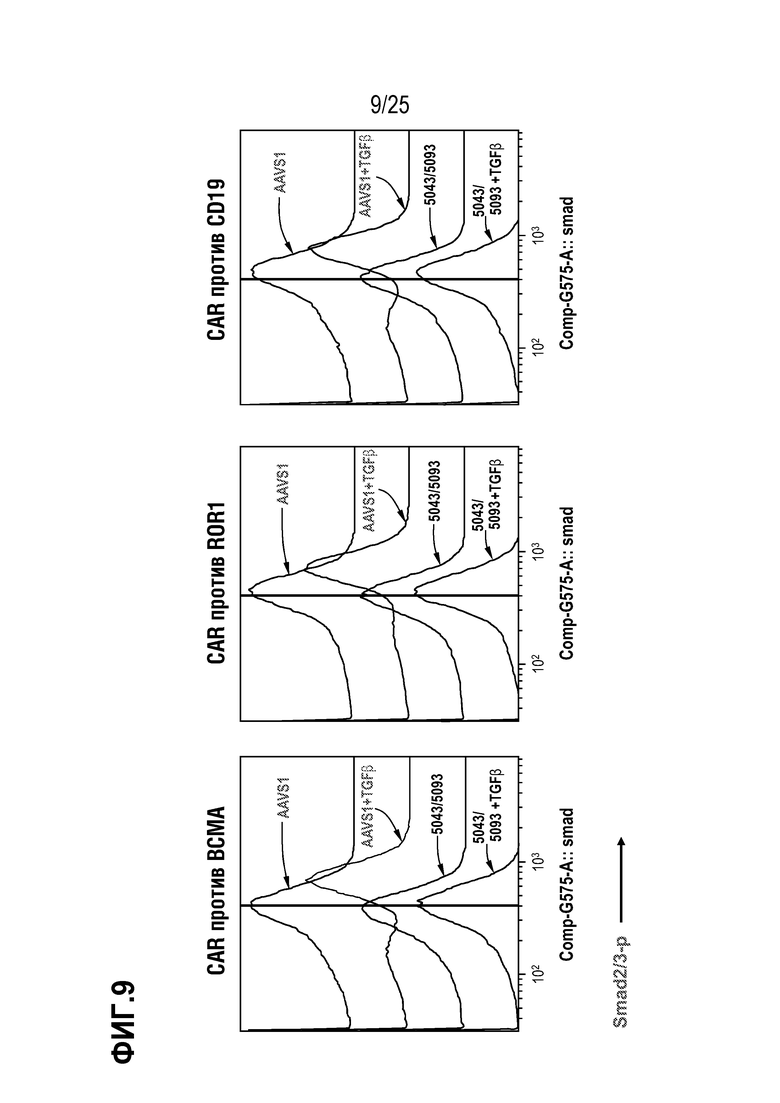
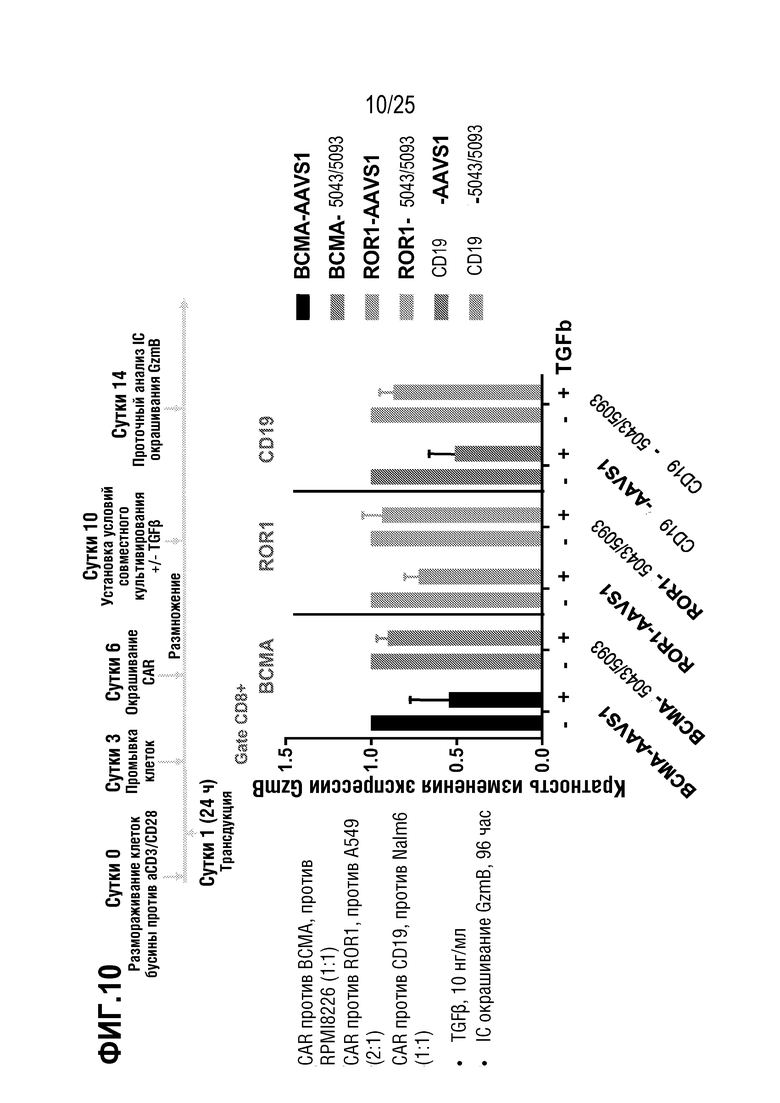

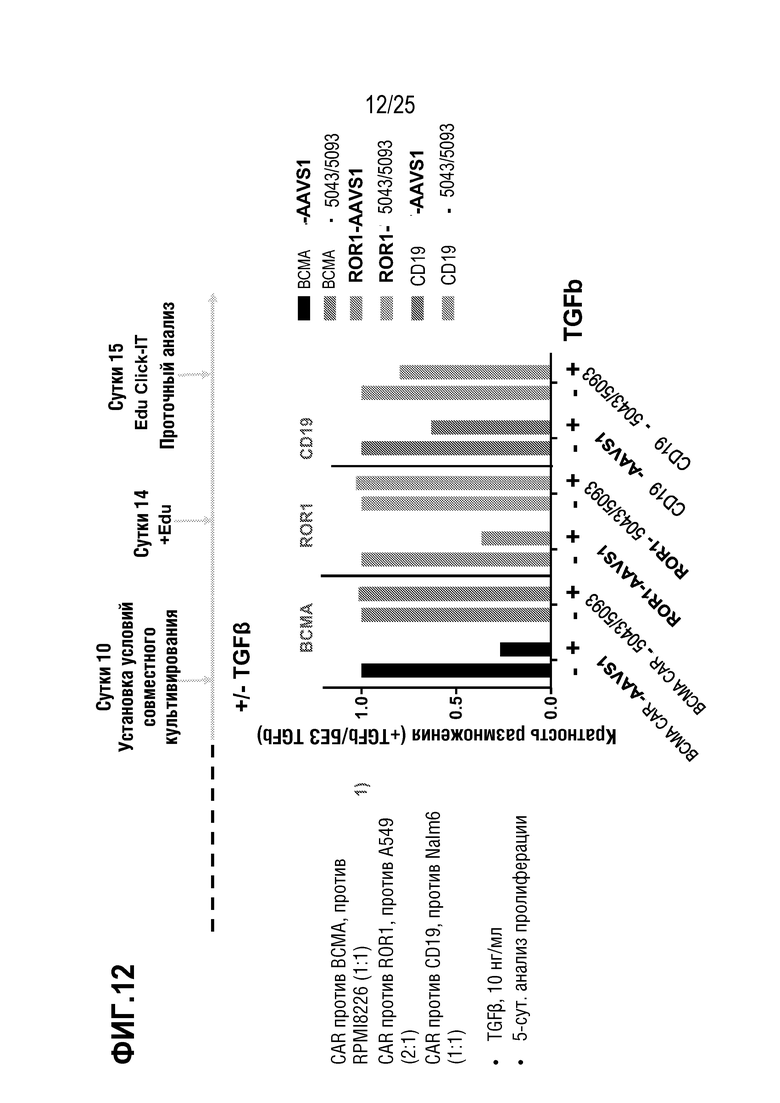
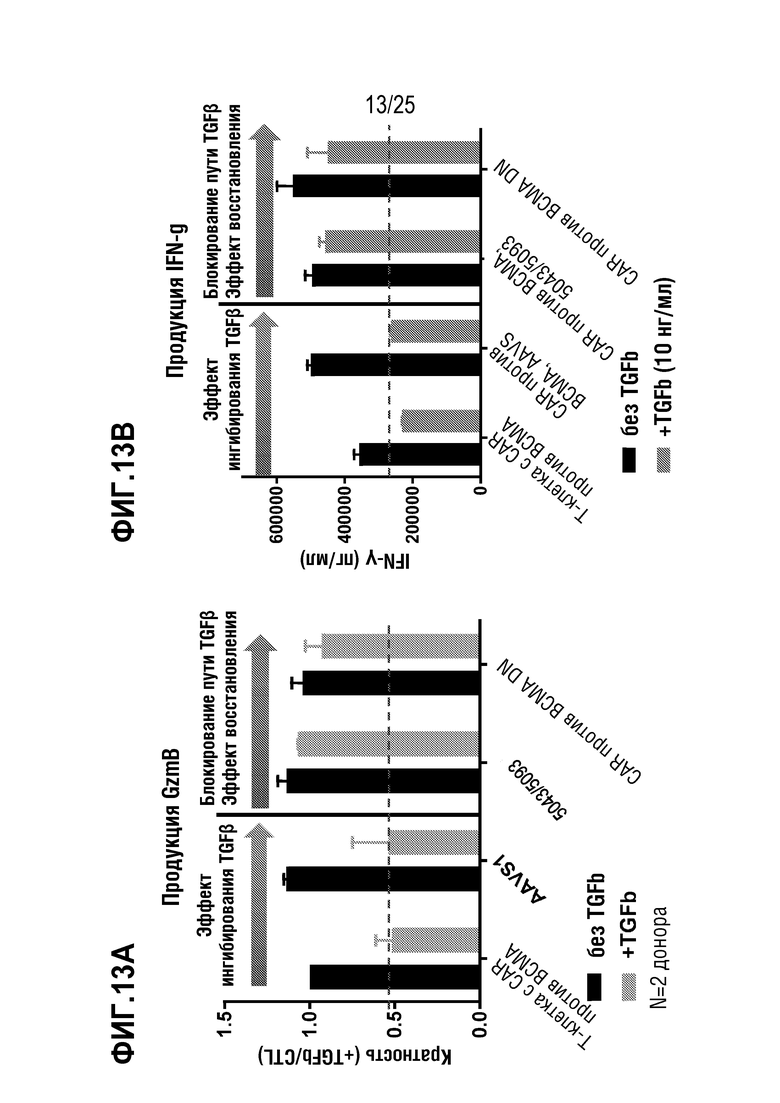
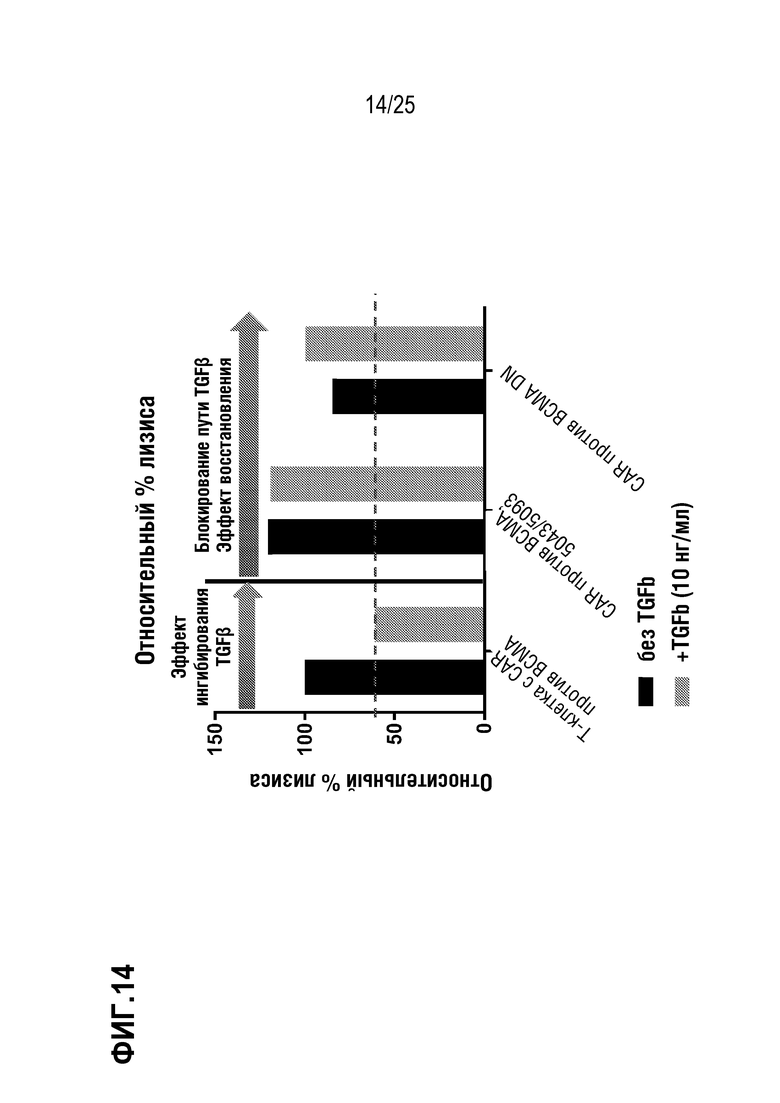

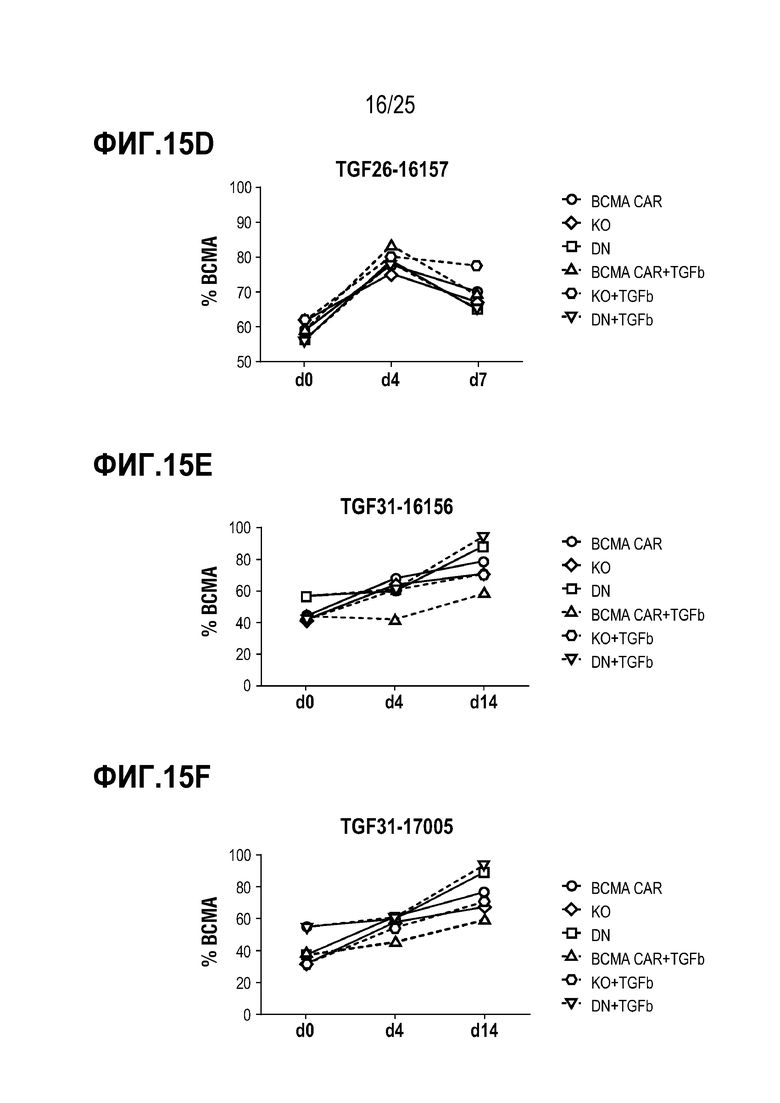
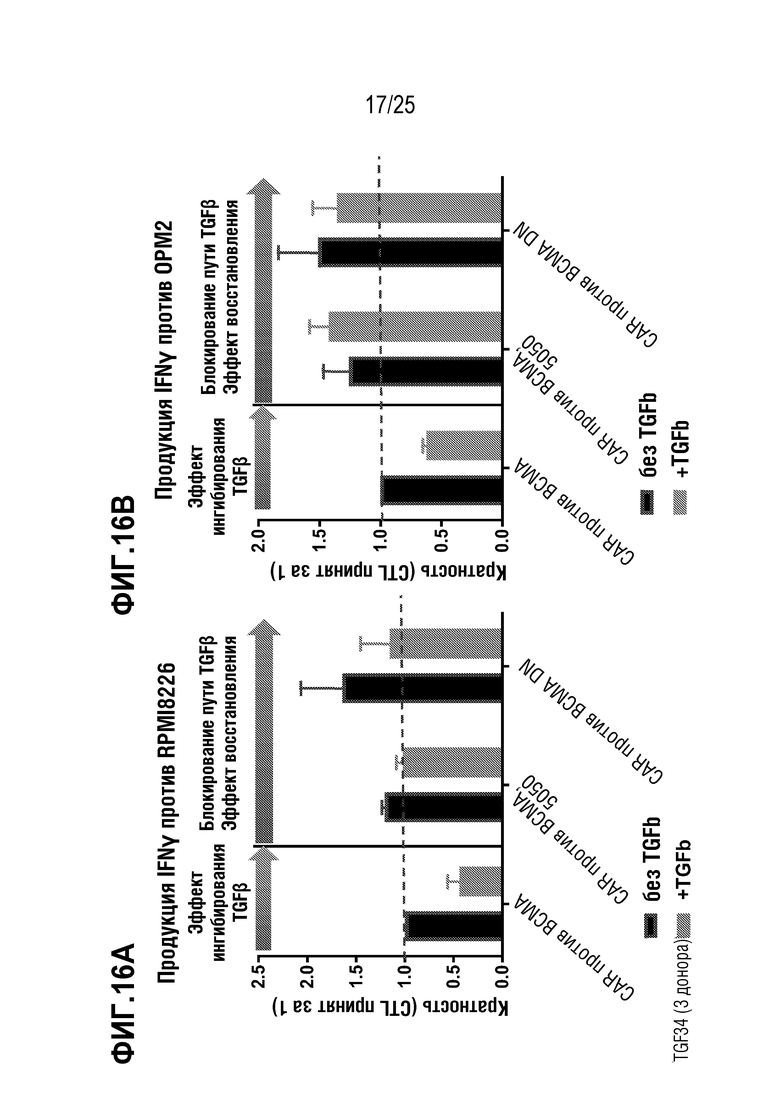
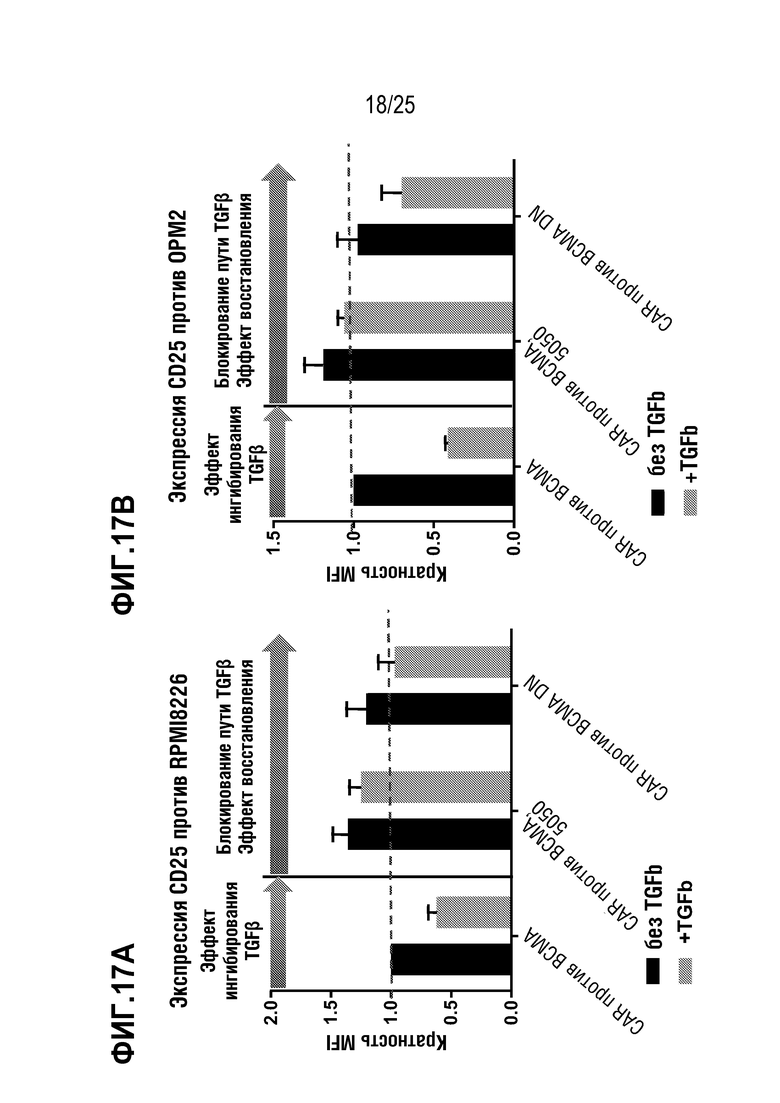
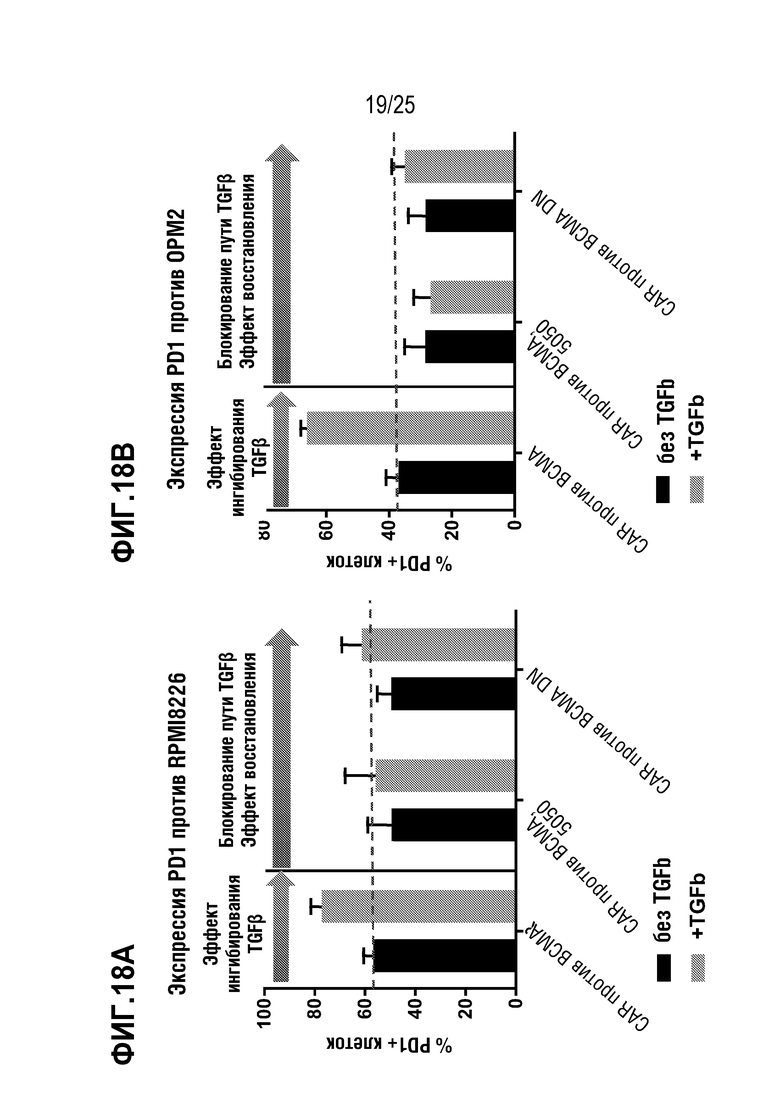



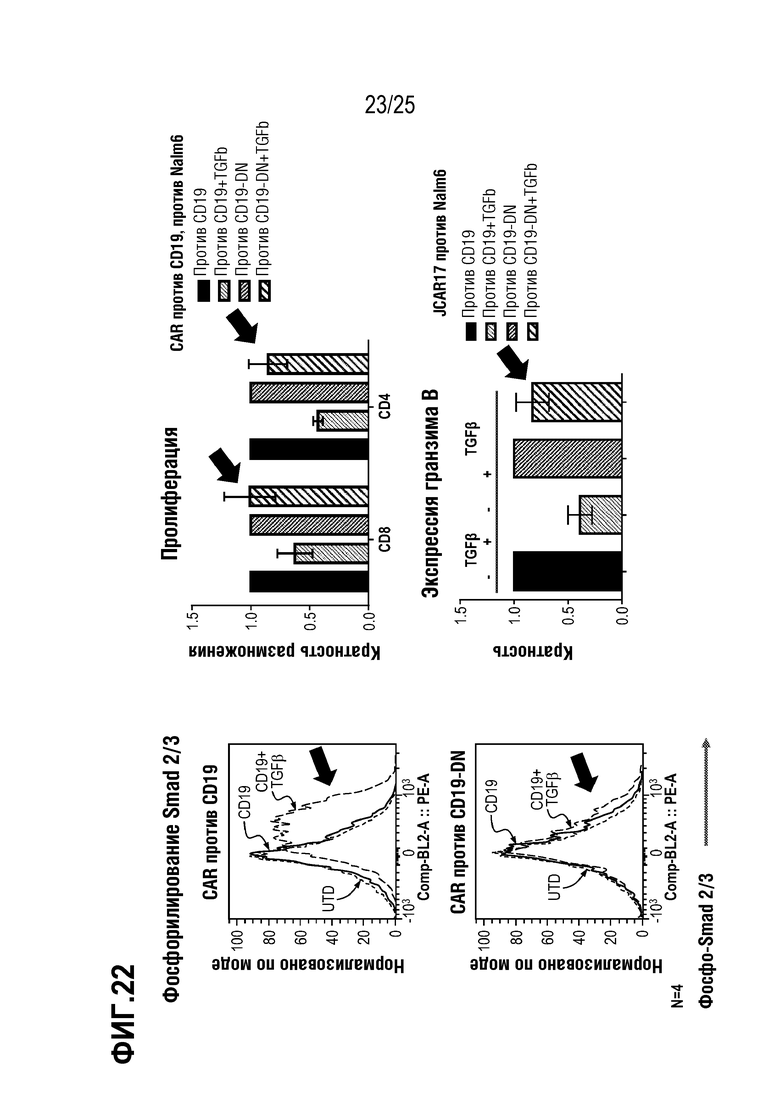

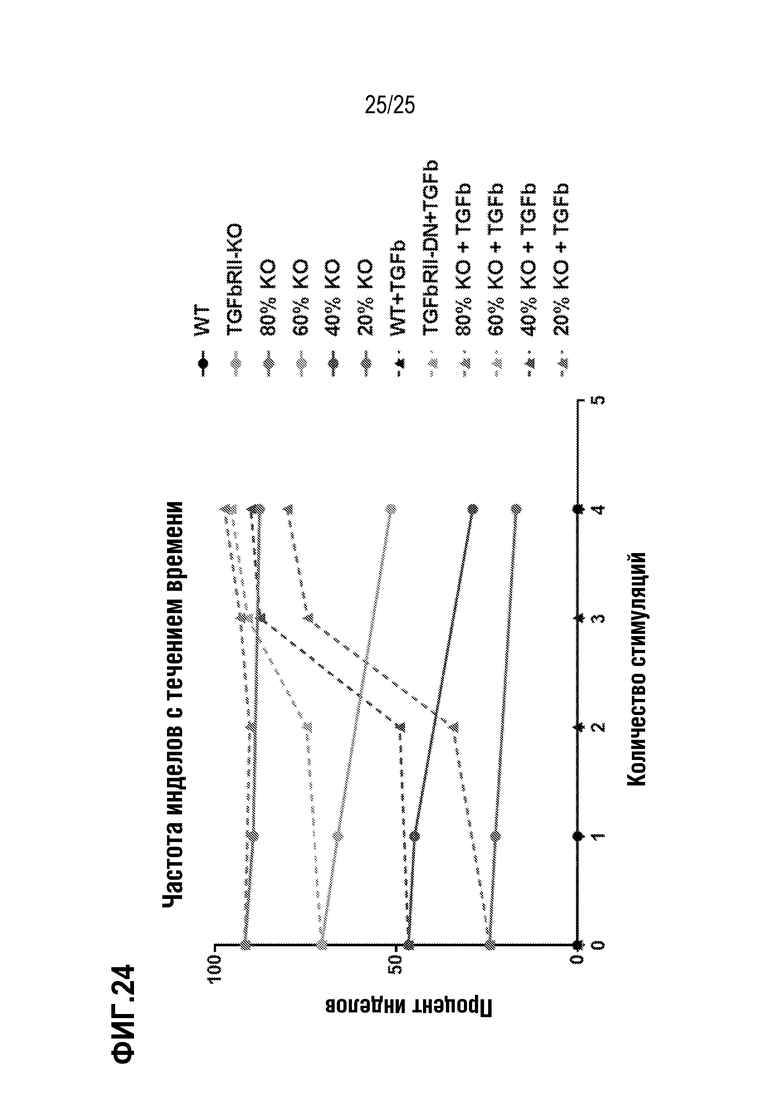
Изобретение относится к области биотехнологии, в частности к системе, содержащей: нРНК, содержащую нацеливающий домен, который является комплементарным последовательности-мишени из гена рецептора II трансформирующего фактора роста β (TGFBR2), и РНК-направляемую нуклеазу, а также к клетке, ее содержащей. Изобретение эффективно для опосредованного TGF-β ингибирования T-клеток в контексте терапии опухолей. 2 н. и 19 з.п. ф-лы, 24 ил., 9 табл., 6 пр.
1. Система редактирования генома, содержащая: нРНК, содержащую нацеливающий домен, который является комплементарным последовательности-мишени из гена рецептора II трансформирующего фактора роста β (TGFBR2); и
РНК-направляемую нуклеазу,
где нацеливающий домен содержит нуклеотидную последовательность, которая идентична или отличается не более чем 3 нуклеотидами от SEQ ID NO: 5050.
2. Система редактирования генома по п. 1, где указанный нацеливающий домен имеет конфигурацию для образования двухцепочечного разрыва или одноцепочечного разрыва в пределах приблизительно 500 п.о., приблизительно 450 п.о., приблизительно 400 п.о., приблизительно 350 п.о., приблизительно 300 п.о., приблизительно 250 п.о., приблизительно 200 п.о., приблизительно 150 п.о., приблизительно 100 п.о., приблизительно 50 п.о., приблизительно 25 п.о. или приблизительно 10 п.о. от положения мишени в TGFBR2, таким образом, изменяя указанный ген TGFBR2.
3. Система редактирования генома по п. 2, где экспрессию гена TGFBR2 подвергают нокауту или нокдауну.
4. Система редактирования генома по любому из пп. 1-3, где указанная РНК-направляемая нуклеаза представляет собой нуклеазу Cas9 S. pyogenes.
5. Система редактирования генома по п. 4, где указанная нуклеаза Cas9 S. pyogenes узнает смежный с протоспейсером мотив (PAM) NGG.
6. Система редактирования генома по любому из пп. 1-3, где указанная РНК-направляемая нуклеаза представляет собой нуклеазу Cas9 S. aureus.
7. Система редактирования генома по п. 6, где указанная нуклеаза Cas9 S. aureus узнает PAM, либо NNNRRT, либо NNNRRV и система редактирования генома нацелена на TGFBR2.
8. Система редактирования генома по любому из пп. 1-7, где указанная РНК-направляемая нуклеаза представляет собой мутантную нуклеазу Cas9.
9. Система редактирования генома по любому из пп. 1-8, где указанная нРНК представляет собой модульную нРНК или химерную нРНК.
10. Система редактирования генома по любому из пп. 1-9, где указанный нацеливающий домен имеет длину приблизительно 17, 18, 19, 20, 21, 22 или 23 нуклеотидов.
11. Система редактирования генома по п. 10, где указанный нацеливающий домен содержит по меньшей мере приблизительно 18 смежных нуклеотидов, которые являются комплементарными гену TGFBR2.
12. Система редактирования генома по любому из пп. 1-11, содержащая две, три или четыре нРНК.
13. Система редактирования генома по любому из пп. 1-12 для применения в изменении указанного гена TGFBR2 в клетке.
14. Система редактирования генома по п. 13, где указанная клетка происходит от субъекта, страдающего злокачественной опухолью.
15. Система редактирования генома по п. 1, где экспрессию TGFBR2 уменьшают на 30% или более относительно исходного измерения.
16. Система редактирования генома по п. 15, где экспрессию белка TGFBR2 определяют посредством Вестерн-блоттинга или непрямого внутриклеточного окрашивания посредством проточной цитометрии.
17. Система редактирования генома по п. 1, где мутацию сдвига рамки считывания вводят в ген TGFBR2.
18. Система редактирования генома по п. 1, где нацеливающий домен идентичен SEQ ID NO: 5050.
19. Сконструированная иммунная клетка, содержащая систему редактирования генома по любому из пп. 1-18, где указанная клетка представляет собой T-клетку или клетку естественного киллера (NK).
20. Клетка по п. 19, где указанная клетка экспрессирует TGFBR2.
21. Клетка по п. 19, дополнительно содержащая сконструированный T-клеточный рецептор (eTCR) или химерный рецептор антигена (CAR).
| JOHN G DOENCH et al., Optimized sgRNA design to maximize activity and minimize off-target effects of CRISPR-Cas9, NATURE BIOTECHNOLOGY, 2016, Vol.34 N | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Переносная печь-плита | 1920 |
|
SU184A1 |
| CHAD M | |||
| TOLEDO, Identification of Cancer-specific Therapeutic Targets and Tumor Suppressor Genes in Glioblastoma Multiforme by Functional Genetics, 2015 | |||
Авторы
Даты
2023-06-22—Публикация
2018-11-01—Подача