Изобретение относится к области биомедицины и касается способа детектирования сшивок ДНК, индуцированных действием генотоксических агентов. Изобретение может быть использовано в генотоксикологических исследованиях для сравнительного скрининга потенциальных ДНК-сшивающих агентов, разработки или индивидуального подбора препаратов для проведения химиотерапии и решения других практических задач биомедицины.
Воздействие неблагоприятных факторов окружающей среды, химиотерапевтических или эндогенных агентов могут спровоцировать разнообразные повреждения ДНК. К наиболее опасным для жизнедеятельности клетки повреждениям относится образование сшивок внутри цепи ДНК, между цепями ДНК и сшивки ДНК с белками. Сшивки представляют серьезную угрозу для целостности генома и жизнеспособности клеток, так как физически блокируют процессы репликации и транскрипции ДНК. Этот цитотоксический эффект лежит в основе механизма действия ряда химиотерапевтических лекарственных препаратов.
Известно несколько методов, используемых для определения ДНК-сшивающего действия генотоксических агентов. Высокочувствительный метод щелочной элюции [Kohn K.W., Erickson L. С. et al. Fractionation of DNA from mammalian cells by alkaline elution // Biochemistry. - 1976. - V. 15, №21. - P. 4629-4637. DOI:10.1021/bi00666a013] позволяет оценить кинетику образования и элиминации сшивок ДНК, однако требует относительно большого количества клеток и включает в анализ объединенный материал из всей популяции клеток, что не позволяет оценить индивидуальные изменения в клетках внутри популяции.
Другой, широко используемый в настоящее время подход, основан на применении метода гель-электрофореза единичных клеток в геле агарозы, известного как «метод ДНК-комет» (Comet assay). Первоначально метод был описан в 1984 году для исследования двунитевых разрывов ДНК в отдельных клетках [Ostling О., Johanson K.J. Microelectrophoretic study of radiation-induced DNA damages in individual mammalian cells // Biochem Biophys Res Commun. - 1984. - V. 123, №1. - P. 291-298. DOI:10.1016/0006-291x(84)90411-х] и позднее был адаптирован для проведения электрофореза в щелочных условиях, что позволило выявлять не только двунитевые разрывы ДНК, но и однонитевые разрывы ДНК и щелочно-лабильные сайты [Singh N.P., Mccoy М.Т. et al. A simple technique for quantitation of low levels of DNA damage in individual cells // Exp Cell Res. - 1988. - V. 175, №1. - P. 184-191. DOI:10.1016/0014-4827(88)90265-0]. Метод ДНК-комет основан на регистрации различий подвижности в постоянном электрическом поле неповрежденной ДНК и фрагментов ДНК лизированных клеток, заключенных в агарозный гель. Образовавшиеся в результате разрывов подвижные фрагменты ДНК мигрируют к аноду, формируя электрофоретический след, напоминающий хвост кометы, а менее подвижная неповрежденная ДНК, преимущественно, находится в голове кометы. Длина и интенсивность окрашивания хвоста зависят от степени поврежденности исследуемой ДНК. О наличии разрывов и степени поврежденности ДНК судят по величине характеристического параметра «%ДНК в хвосте ДНК-кометы», определяемого как процентное отношение количества ДНК в хвосте ДНК-кометы к сумме количества ДНК в хвосте и голове ДНК-кометы. Параметр автоматически рассчитывается программой анализа изображений и отражает изменение электрофоретической подвижности ДНК вследствие воздействия на клетки повреждающего фактора. Метод ДНК-комет имеет высокую чувствительность, для проведения исследований требуется небольшое количество экспериментального материала, а возможность анализа единичных клеток позволяет определить гетерогенность ответа в клеточной популяции.
Однако, использование метода ДНК-комет для анализа сшивок ДНК затруднено тем, что наличие сшивок препятствует расхождению нитей ДНК при щелочной денатурации, что затрудняет миграцию ДНК и разделение сшитых и неповрежденных ДНК в электрическом поле в процессе электрофореза. Как отмечается в работе [Tice R.R., Agurell Е. et. al. Single cell gel/comet assay: guidelines for in vitro and in vivo genetic toxicology testing // Environ Mol Mutagen. - 2000. - V. 35, №3. - P. 206-221. DOI: 10.1002/(sici)1098-2280(2000)35:3<206::aid-em8>3.0.co;2-j], проблема может быть решена увеличением продолжительности электрофореза, чтобы добиться увеличения электрофоретической подвижности контрольных неповрежденных ДНК и их отделения от сшитых ДНК. Однако, в каждом отдельном случае необходимую продолжительность электрофореза определяют экспериментально в зависимости от природы исследуемых клеток и специфики решаемых практических задач. Общепринятым в настоящее время является способ определения сшивок ДНК, согласно которому, на клетки, подвергнутые действию ДНК-сшивающего агента, целенаправленно дополнительно действуют фактором, инициирующим разрывы цепи ДНК, например, ионизирующим излучением [Spanswick V.J., Hartley J.M., Hartley J.А. Measurement of DNA interstrand crosslinking in individual cells using the single cell gel electrophoresis (Comet) assay // Methods in Molecular Biology - 2010 - V. 613, P. 267-282. DOI 10.1007/978-1-60327-418-0_17], пероксидом водорода [Грехова A.K., Горбачева Л.Б. и др. Сравнительные исследования генотоксичности нового ацидокомплекса палладия (II) и цисплатина в лимфоцитах крови человека in vitro // Биомедицинская химия. - 2013. - Т. 59, №1. - С. 107-114. DOI: 10.18097/pbmc20135901107], метиловым метансульфонатом (MMS) [Pfuhler S., Wolf H.U. Detection of DNA-crosslinking agents with the alkaline comet assay // Environ Mol. Mutagen. - 1996. - V. 27, №3. - P. 196-201. DOI:10.1002/(SICI)1098-2280(1996)27:3<196::AID-EM4>3.0.CO;2-D], оксидом стирола [Fikrova P., Stetina R. et al. Detection of DNA crosslinks in peripheral lymphocytes isolated from patients treated with platinum derivates using modified comet assay // Neoplasma. - 2013. - V. 60, №4. - P. 413-418. DOI:10.4149/neo_2013_053], озоно-кислородной смесью [RU 2527345 C1, опубл. 27.08.2014]. Поскольку наличие сшивок замедляет миграцию фрагментированной ДНК, получаемые значения параметра %ДНК в хвосте ДНК-комет в этом случае зависят, как от количества разрывов, так и от количества сшивок ДНК, при этом уменьшение длины и снижение интенсивности флуоресценции хвоста ДНК-кометы определяется количеством сшивок ДНК в клетке.
В качестве прототипа заявляемого способа взят способ определения сшивок ДНК, описанный в работе [Blasiak J., Kowalik J. et al. DNA damage and repair in human lymphocytes exposed to three anticancer platinum drugs // Teratog Carcinog Mutagen. - 2000. - V. 20, №3. - P. 119-131. DOI: 10.1002/(sici) 1520-6866(2000)20:3<119::aid-tcm3>3.0.co;2-z.], в которой для индуцирования разрывов ДНК в клетках лимфоцитов, обработанных ДНК-сшивающими препаратами цисплатин и оксоплатин, использован пероксид водорода. Однако, следует отметить, что перечисленные способы-аналоги, включая прототип, как и большое количество аналогичных, не упомянутых здесь исследований, в которых для определения сшивок ДНК используют дополнительный повреждающий фактор, отличаются между собой, главным образом, объектом исследования и способом искусственного индуцирования разрывов ДНК, увеличивающих подвижность ДНК в электрическом поле. В остальном они характеризуются одной и той же последовательностью операций, осуществляемых в условиях, близких или аналогичных классическому методу ДНК-комет [Singh N.P., 1988], и включают следующие стадии: 1. Обработка суспензии клеток, подвергнутых первоначально действию ДНК-сшивающего агента (в способе-прототипе - цисплаптин или оксоплатин), фактором, индуцирующим разрывы ДНК (в способе-прототипе - пероксидом водорода). 2. Приготовление препаратов (слайдов) с иммобилизованными в агарозу клетками, подвергнутыми действию повреждающих факторов. 3. Лизис клеток (2,5 М NaCl, 100 мМ EDTA, 10 мМ Tris, 1% Triton Х-100 рН 10, 1 час, 4°С). 4. Щелочная денатурация (300 мМ NaOH, 1 мМ Na2EDTA, рН>13, 40 мин, 4°С). 5. Проведение горизонтального электрофореза в том же щелочном буфере (напряженность электрического поля 0,73 В/см, время 30 мин, температура 4°С). 6. Нейтрализация (0,4 М Tris, рН 7,5). 7. Окрашивание ДНК флуоресцентным красителем. 8. Получение микрофотоизображений ДНК-комет, анализ и обработка данных с помощью специализированного программного обеспечения, определяющего, наряду с другими показателями, один из главных характеристических параметров - %ДНК в хвосте ДНК-комет.
Общий недостаток способов-аналогов и прототипа состоит в том, что сшивки ДНК определяют не напрямую, а опосредованно, через уменьшение электрофоретической подвижности фрагментов ДНК, обусловленное предшествующим воздействием на клетку сшивающего агента. Полученные данные представляют собой результат сочетанного последовательного воздействия на клетки двух генотоксических агентов - ДНК-сшивающего агента и агента, индуцирующего разрывы цепи ДНК. Таким образом, действие ДНК-сшивающего агента анализируют на фоне действия повреждающего фактора, вызывающего разрывы цепи ДНК, что может отрицательно сказаться на корректности интерпретации полученных результатов, особенно в случае детектирования небольшого количества сшивок на фоне значительного количества разрывов ДНК [Сорочинская У.Б., Михайленко В.М. Применение метода ДНК-комет для оценки повреждений ДНК, вызванных различными агентами окружающей среды // Онкология. - 2008. - Т. 10, №3. - С. 303-309.]. Также следует отметить, что наличие стадии создания разрывов ДНК (стадия 1) в способе-прототипе и аналогах усложняет анализ, увеличивает время проведения исследования и требует использования специального оборудования и/или дополнительных реагентов.
Проблема, решаемая настоящим изобретением, состоит в том, чтобы упростить известный, основанный на методе ДНК-комет, способ определения сшивок ДНК в клетках, подвергшихся действию ДНК-сшивающих генотоксических агентов, исключив дополнительную стадию обработки клеток факторами, индуцирующими разрывы цепей ДНК.
Проблема решена предлагаемым способом детектирования сшивок ДНК, включающим приготовление препаратов с иммобилизованными в агарозу клетками, лизис клеток, щелочную денатурацию ДНК, проведение горизонтального щелочного электрофореза, нейтрализацию, окрашивание ДНК, получение микрофотографий, анализ и обработку данных, отличающимся тем, что горизонтальный щелочной электрофорез проводят при напряженности электрического поля в диапазоне 1,75-2,8 В/см.
Технический результат изобретения состоит в упрощении анализа за счет сокращения количества стадий реализации способа путем отказа от предусмотренной аналогами дополнительной стадии обработки клеточных образцов повреждающими агентами, индуцирующими разрывы ДНК.
Сущность изобретения поясняется следующими иллюстрациями:
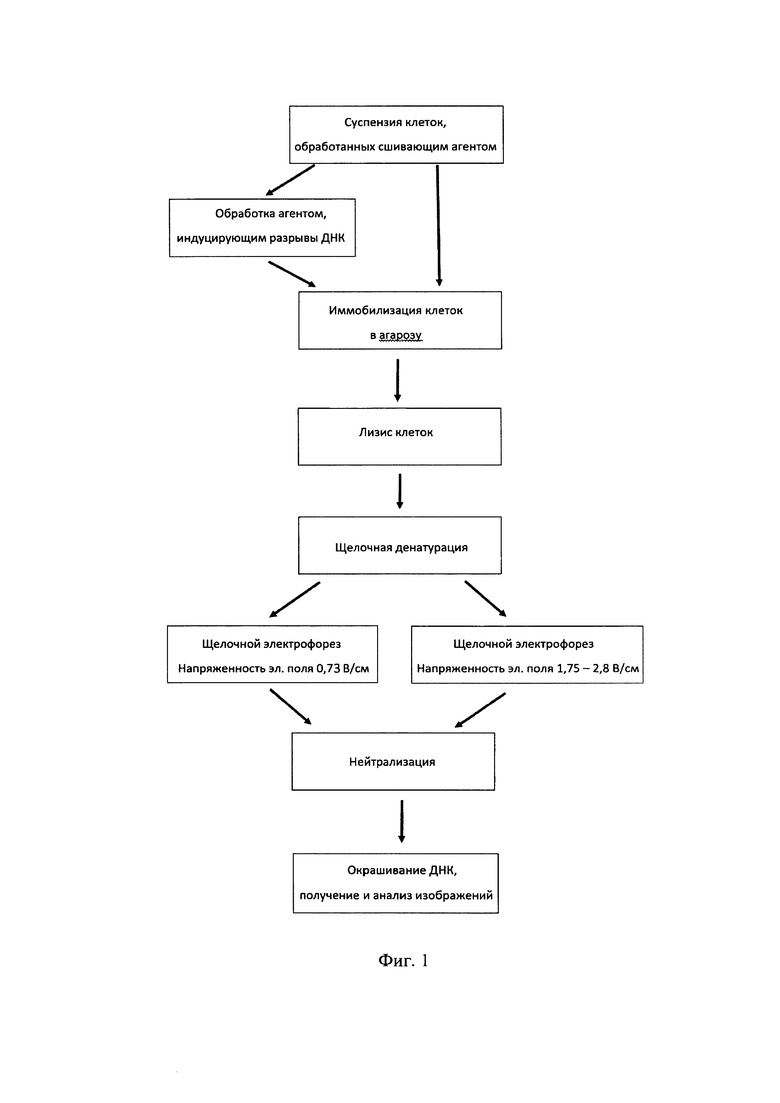
На Фиг. 1 схематически показаны существенные отличия предлагаемого способа от способов-аналогов и прототипа.
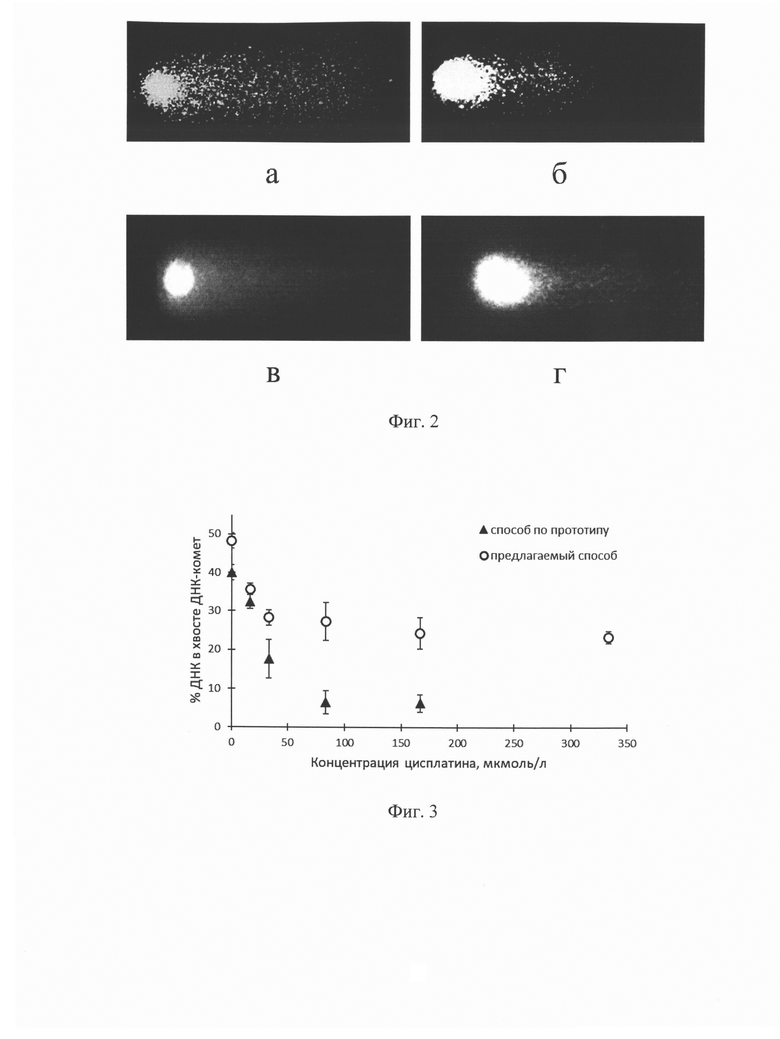
На Фиг. 2 показаны микрофотографии ДНК-комет клеток лимфоцитов здоровых доноров, обработанных различными повреждающими агентами.
а. Клетки обработаны пероксидом водорода (50 мкмоль/л), напряженность электрического поля 0,75 В/см;
б. Клетки обработаны последовательно цисплатином (33 мкмоль/л) и пероксидом водорода (50 мкмоль/л), напряженность электрического поля 0,75 В/см;
в. Клетки не обработаны повреждающими агентами, напряженность электрического поля 2,0 В/см;
г. Клетки, обработаны цисплатином (33 мкмоль/л), напряженность электрического поля 2,0 В/см.
На Фиг. 3 приведены зависимости величины параметра %ДНК в хвосте ДНК-комет лимфоцитов здоровых доноров от концентрации цисплатина. (▲) - по данным работы [Грехова А.К., 2013], (о) - данные получены предлагаемым способом.
На Фиг. 4 показаны микрофотографии ДНК-комет культивируемых клеток аденокарциномы молочной железы (MFC-7), обработанных и не обработанных формальдегидом. Напряженность электрического поля 2,0 В/см.
а. Клетки не обработаны повреждающим агентом (контроль);
б. Клетки обработаны формальдегидом (334 мкмоль/л);
в. Клетки обработаны формальдегидом (1650 мкмоль/л);
г. Клетки обработаны формальдегидом (3300 мкмоль/л).
Существенные отличия предлагаемого способа детектирования сшивок ДНК от способа-прототипа и аналогов показаны на схеме на Фиг. 1. Согласно способу-прототипу, клетки лимфоцитов, обработанные сшивающим агентом - препаратом цисплатин, дополнительно обрабатывают агентом, индуцирующим разрывы ДНК - пероксидом водорода. В предлагаемом способе стадия обработки клеточных образцов агентом, индуцирующим разрывы ДНК, отсутствует. Далее следуют общие для способов-аналогов и предлагаемого способа процедуры - приготовление препаратов (слайдов) с иммобилизованными в агарозу клетками, лизис клеток при рН 10 и температуре 4°С и последующая щелочная денатурация при рН около 13 и выше и температуре 4°С. Условия проведения этих операций, в основном, соответствуют условиям классического метода ДНК-комет, а незначительные вариации, приведенные в разных публикациях, не влияют существенно на результаты анализа. На следующей стадии проводят горизонтальный электрофорез в той же среде, что и щелочную денатурацию, при этом существенно важно, что, в отличие от способа-прототипа, в котором электрофорез проводят при напряженности электрического поля 0,73 В/см, и аналогов, в которых используемый диапазон значений напряженности электрического поля составляет, по литературным данным, от 0,4 до 1,2 В/см, в предлагаемом способе электрофорез проводят при существенно более высоких значениях напряженности электрического поля в диапазоне от 1,75 до 2,8 В/см, предпочтительно, в диапазоне 2,0-2,5 В/см. Условия выполнения последующих стадий - нейтрализация, окрашивание образцов, визуализация (получение микрофотоизображений) и обработка результатов анализа в предлагаемом способе и способах-аналогах совпадают или отличаются несущественно, не влияя на результат анализа.
Таким образом, сущность изобретения состоит в том, что электрофорез проводят при такой напряженности электрического поля, при которой хвост ДНК-комет клеток, содержащих сшивки ДНК, формируют за счет увеличения электрофоретической подвижности неповрежденной ДНК, а не за счет увеличения продолжительности электрофореза или искусственного создания разрывов ДНК, как в аналогах и прототипе.
При выборе оптимального диапазона напряженности электрического поля при проведении электрофореза исходили из литературных данных, согласно которым, для достоверной оценки результатов, полученных методом ДНК-комет, необходимо создать условия, при которых в хвост ДНК-кометы мигрирует не менее 25% содержащихся в клетках ДНК [Tice R., Vasquez М. Protocol for the application of the pH>13 alkaline single cell gel (SCG) assay to the detection of DNA damage in mammalian cells// - 1999. - P. 1-8. http://cometassay.com/Tice%20and%20Vasques.pdf]. Хвост ДНК-комет, содержащий более 50% от общего количества ДНК, может перекрывать соседние клетки, в результате чего анализ ДНК-комет будет невозможен. Таким образом, для целей настоящего изобретения при проведении электрофореза принят диапазон напряженности электрического поля, при котором выход неповрежденной ДНК в хвост составляет от 25 до 50%. На образцах клеток лимфоцитов, полученных от здоровых доноров, и культивируемых клеток аденокарциномы молочной железы (MFC-7) было показано, что в обычных, используемых в методе ДНК-комет условиях проведения электрофореза, выход в хвост ДНК-кометы от 25 до 50% неповрежденной ДНК происходит в диапазоне напряженности электрического поля от 1,75 до 2,8 В/см. Соответствующие экспериментальные данные представлены в Табл. 1.
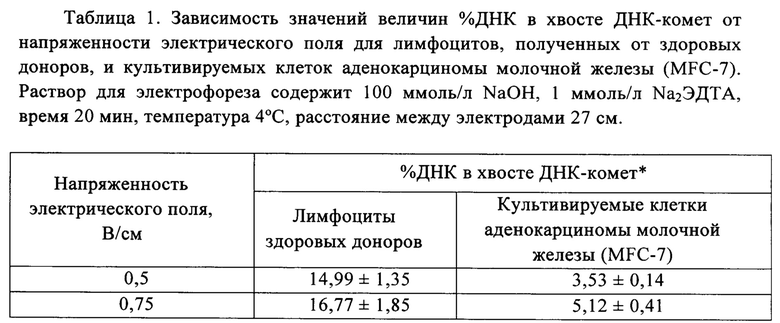

В качестве оптимального интервала напряженности электрического поля для осуществления способа по изобретению для разных видов клеток принят интервал от 2,0 до 2,5 В/см.
Результаты электрофореза в условиях различной напряженности электрического поля показаны на представленных на Фиг. 2 микрофотографиях лимфоцитов здоровых доноров, подвергнутых действию различных повреждающих агентов:
а - клетки обработаны пероксидом водорода, индуцирующим разрывы ДНК, что соответствует классическому методу ДНК-комет [Singh N.P. et. al., (1988)], предложенному первоначально для анализа разрывов ДНК. При напряженности электрического поля 0,75 В/см в хвосте ДНК-кометы находятся относительно подвижные фрагменты ДНК, образовавшиеся под действием повреждающего фактора, а в голове кометы - малоподвижная в этих условиях, неповрежденная ДНК;
б - клетки обработаны сшивающим агентом цисплатином, а затем - пероксидом водорода, вызывающим разрывы ДНК, напряженность электрического поля 0,75 В/см, что соответствует варианту способа, описанному в работе [Грехова А.К. и др., (2013)]. Наличие сшивок замедляет миграцию фрагментированной ДНК в хвост ДНК-кометы, вследствие чего его длина и интенсивность флуоресценции уменьшаются. При относительно низкой напряженности электрического поля в голове кометы находятся как неповрежденная ДНК, малоподвижная в этих условиях, так и еще менее подвижная сшитая в результате действия цисплатина ДНК, что проявляется в увеличении площади головы и ее яркости. Таким образом, фиксируемые параметры хвоста ДНК-комет в данном случае отражают результирующий эффект, зависящий как от количества разрывов ДНК, так и от количества сшивок ДНК.
Микрофотографии «в» и «г» иллюстрируют способ по изобретению:
в - клетки не обработаны повреждающими агентами (контроль), напряженность электрического поля 2,0 В/см. В этих условиях выход неповрежденной ДНК в хвост ДНК-кометы составляет около 50%.
г - клетки обработаны цисплатином, напряженность электрического поля 2,0 В/см. Наблюдается снижение миграции ДНК в электрическом поле, так, что сшитые ДНК остаются, преимущественно, в голове ДНК-кометы, а хвост ДНК-кометы, содержащий неповрежденные ДНК, становится более коротким и менее интенсивно окрашенным, чем в контроле.
Таким образом, получаемые в результате автоматической обработки микрофотоизображений данные, дают, в отличие от прототипа и аналогов, непосредственную информацию о наличии сшивок ДНК, не искаженную дополнительным воздействием агентов, вызывающих разрывы ДНК. При этом отказ от дополнительной стадии создания разрывов ДНК без увеличения длительности электрофореза существенно упрощает, ускоряет и удешевляет анализ.
Следует отметить, что предлагаемый способ, так же, как и аналоги, дает общую информацию обо всех типах сшивок ДНК, образовавшихся под действием генотоксического фактора: внутри- и межцепочечных сшивках ДНК-ДНК и сшивках ДНК-белок. Для получения данных по каждому отдельному виду сшивок требуется проведение дополнительных исследований. Например, для выявления сшивок ДНК-белок лизис клеток проводят в присутствии протеиназы К, действие которой элиминирует сшивки ДНК-белок, не влияя на частоту сшивок ДНК-ДНК, и увеличивает миграционную способность ДНК во время проведения электрофореза [Merk О., Reiser K. et al. Analysis of chromate-induced DNA-protein crosslinks with the comet assay // Mutat Res. - 2000. - V. 471, №1-2. - P. 71-80. DOI:10.1016/sl383-5718(00)00110-8].
Изобретение осуществляют следующим образом.
Готовят препараты (слайды) с иммобилизованными в агарозу клетками, обработанными генотоксическим сшивающим агентом (эксперимент), и клетками, не обработанными сшивающим агентом (контроль) в нескольких повторностях. Затем проводят лизис клеток для диссоциации клеточных структур и удаления большинства белков и последующую щелочную денатурацию для раскручивания двойной спирали ДНК и увеличения миграционной активности ДНК в геле агарозы. В отличие от большинства аналогов, в которых щелочную денатурацию и электрофорез проводят при рН>13, допускается использовать щелочной буфер с рН 12,5-13, поскольку предлагаемый способ детектирования сшивок ДНК не связан, как в аналогах, с анализом разрывов ДНК. Методики проведения этих операций описаны, например, в Методических рекомендациях [Оценка генотоксических свойств методом ДНК-комет in vitro: Методические рекомендации. М.: Федеральный центр гигиены и эпидемиологии Роспотребнадзора, 2011. 16 с.]. Слайды помещают в камеру для горизонтального электрофореза, при этом электрофорез экспериментальных и контрольных образцов проводят одновременно в идентичных условиях. Электрофорез проводят в течение 20 минут в той же среде, что и щелочную денатурацию, при напряженности электрического поля, выбранной внутри интервала значений 1,75-2,8 В/см, в котором величина параметра %ДНК в хвосте ДНК-комет для неповрежденных клеток составляет от 25 до 50%. Оптимальная величина напряженности при проведении электрофореза, отвечающая этому условию, составляет 2,0-2,5 В/см. После завершения электрофореза слайды окрашивают флуоресцентным красителем, получают микрофотографии и проводят анализ и обработку полученных изображений ДНК-комет с помощью специального программного обеспечения, которое определяет, наряду с другими характеристиками, параметр %ДНК в хвосте ДНК-кометы, с помощью которого в сравнении с контролем, проводят оценку сшивающей активности тестируемого генотоксического агента.
ДНК-сшивающее действие генотоксических агентов можно оценивать показателем замедления миграции ДНК (Δ), определяемым как разность значений %ДНК в хвосте ДНК-комет между контрольным, не обработанным сшивающим агентом, и экспериментальным образцом:
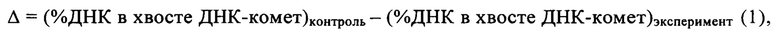
и/или коэффициентом сшивания ДНК (δ), определяемым как отношение значений %ДНК в хвосте ДНК-комет для контрольного и экспериментального образцов:
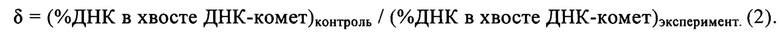
Чем выше значение показателя замедления миграции Δ, тем выше сшивающая активность тестируемого агента и наоборот.
По величине коэффициента сшивания δ сшивающие агенты в концентрации, взятой для исследования, условно делят на три категории:
1. Тестируемый агент обладает в данной концентрации сильным ДНК-сшивающим действием при значении 5, равном или превышающем 2;
2. Тестируемый агент обладает в данной концентрации умеренным ДНК-сшивающим действием при значении 8 от 1 до 2;
3. Тестируемый агент обладает в данной концентрации слабым ДНК-сшивающим действием при значении 5 ниже 1.
Осуществление изобретения продемонстрировано ниже на примерах определения сшивок ДНК под действием таких сшивающих агентов, как коммерческий противоопухолевый препарат «Цисплатин-Тева» ("Teva Pharmaceutical industries LTD", Израиль) в виде 0,5% раствора в 0,9% NaCl, далее цисплатин, и формальдегид, ДНК-сшивающее действие которого описано в работе [Hoffman Е.A., Frey В.L. et al. Formaldehyde crosslinking: a tool for the study of chromatin complexes // J. Biol. Chem. - 2015. - V. 290, №44. - P. 26404-26411. DOI:10.1074/jbc.R115.651679]. Анализ выполнен с использованием двух типов клеток - лимфоциты, полученные от здоровых доноров, и культивируемые клетки аденокарциномы молочной железы (MCF-7).
Приготовление контрольных образцов клеток, не обработанных сшивающим агентом
Готовят клеточную суспензию лимфоцитов, полученных от здоровых доноров (контроль 1), или культивируемых клеток аденокарциномы молочной железы (MCF-7) (контроль 2) с концентрацией клеток 1 млн/мл. Для приготовления образцов для анализа (слайдов) на предметные стекла, предварительно покрытые универсальной 1%-ной агарозой, наносят слой суспензии клеток, смешанной в равных частях с 1%-ной легкоплавкой агарозой, и накрывают покровным стеклом для равномерного распределения суспензии, а затем охлаждают слайд в течение 10 мин при 4°С для застывания геля. Слайды с иммобилизованными в агарозу клетками помещают в лизирующий буфер рН 10 (2,5 моль/л NaCl; 20 ммоль/л Трис-HCl; 100 ммоль/л Na2ЭДТА; 10% ДМСО; 1% Triton Х-100) на 60 мин при температуре 4°С, после чего проводят щелочную денатурацию, выдерживая слайды в течение 20 мин при температуре 4°С в щелочном буфере рН 12,5-13 (100 ммоль/л NaOH, 1 ммоль/л NA2ЭДТА).
Приготовление образцов клеток, обработанных препаратом цисплатин
Клеточную суспензию с концентрацией клеток 1 млн/мл обрабатывают препаратом цисплатин в концентрациях от 16,7 до 501 мкмоль/л при 37°С в течение 60 мин, после чего готовят слайды для анализа, аналогично тому, как описано для контроля. Концентрации сшивающего агента в клеточной суспензии, взятые для исследования, указаны далее в Табл. 2.
Приготовление образцов клеток, обработанных формальдегидом
Клеточную суспензию с концентрацией клеток 1 млн/мл обрабатывают раствором формальдегида в концентрациях от 33 до 3300 мкмоль/л при 37°С в течение 60 мин, после чего готовят слайды для анализа, аналогично тому, как описано для контроля. Концентрации сшивающего агента в клеточной суспензии, взятые для исследования, указаны далее в Табл. 3
Приготовление образцов клеток, обработанных протеиназой К
Препараты (слайды) клеток, контрольные и обработанные формальдегидом, помещают в лизирующий буфер рН 10 (2,5 моль/л NaCl; 20 ммоль/л Трис-HCl; 100 ммоль/л Na2ЭДТА; 2 мг/мл протеиназа К) на 60 мин при 37°С, после чего проводят щелочную денатурацию аналогично тому, как описано для контроля.
Проведение электрофореза, обработка и анализ результатов
Электрофорез проводят в камере для горизонтального электрофореза с расстоянием между электродами 27 см, источник питания Эльф-8 (ДНК-Технология). Электрофорез проводят в щелочном буфере (100 ммоль/л NaOH и 1 ммоль/л Na2ЭДТА), при стабилизации по напряжению 54 В, напряженность электрического поля 2 В/см, время 20 мин, температура 4°С. Одновременно в камеру помещают слайды с препаратами клеток, не обработанных ДНК-сшивающим агентом (контроль), и с экспериментальными образцами. Каждое измерение выполняют в шести повторностях. По завершении электрофореза проводят нейтрализацию (0,4 моль/л Трис-HCl буфере, 4°С, 5 мин), затем окрашивание ДНК флуоресцентным красителем акридиновый оранжевый (2 мкг/мл в фосфатно-солевом буфере, рН 7,4).
Визуализацию и документирование ДНК-комет проводят на люминесцентном микроскопе Axioscop 40 FL, оснащенном цифровой видеокамерой MRc5 (Carl Ziess), с помощью программы AxioVision 4.8. Для анализа и обработки микрофотоизображений ДНК-комет используют программу CASP 1.2.2 (CASPlab).
Результаты определения ДНК-сшивающего действия цисплатина в отношении клеток лимфоцитов здоровых доноров (Пример 1) и культивируемых клеток аденокарциномы молочной железы (MFC-7) (Пример 2) представлены в Табл. 2.
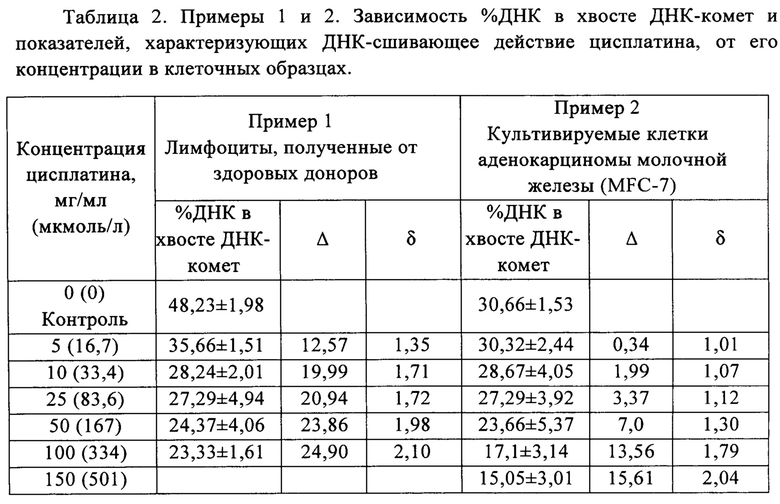
Из данных таблицы видно, что для обоих образцов клеток %ДНК в хвосте ДНК-комет снижается с увеличением концентрации цисплатина, что показывает усиление ДНК-сшивающего действия препарата. При этом генотоксичность препарата по отношению к лимфоцитам здоровых доноров выше, чем по отношению к культивируемым клеткам аденокарциномы молочной железы (MFC-7): для лимфоцитов порог высокой генотоксичности преодолевается при концентрации цисплатина около 100 мг/мл (334 мкмоль/л), а для клеток MFC-7 при концентрации 150 мг/мл (501 мкмоль/л).
На Фиг. 3 сопоставлены результаты оценки ДНК-сшивающего действия цисплатина в отношении клеток лимфоцитов здоровых доноров, полученные по методике описанной в работе [Грехова А.К., 2013], включающей дополнительную стадию индуцирования разрывов ДНК действием пероксида водорода (▲), и предлагаемым способом (о), в котором отсутствие этой стадии компенсируют проведением электрофореза при повышенной напряженности электрического поля, обеспечивающей выход неповрежденной ДНК в хвост ДНК-кометы. Оба способа показывают сходную тенденцию изменения %ДНК в хвосте ДНК-комет от концентрации цисплатина, характеризующуюся двухфазной зависимостью «доза-эффект» - наличием линейного участка до концентрации цисплатина 33 мкмоль/л, который переходит в плато при дальнейшем повышении концентрации сшивающего агента. При этом углы наклона на линейных участках совпадают, что говорит том, что оба способа дают одинаковую информацию о ДНК-сшивающей активности цисплатина в отношении лимфоцитов. Несовпадение полученных абсолютных значениях %ДНК в хвосте ДНК-комет связано с тем, что после образования разрывов ДНК под действием пероксида водорода сразу происходит активация репарационной системы клетки, в то время как в предлагаемом способе хвост ДНК-комет образует неповрежденная ДНК.
Высокую генотоксичность формальдегида подтверждают приведенные в Табл. 3 результаты определения предлагаемым способом ДНК-сшивающего действия формальдегида в отношении культивируемых клеток аденокарциномы молочной железы (MFC-7).
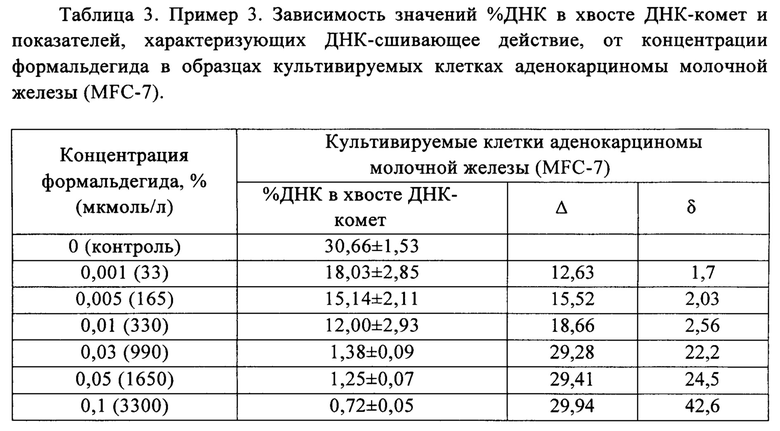
Из данных таблицы следует, что порог высокой генотоксичности в отношении культивируемых клеток аденокарциномы молочной железы (MFC-7) для формальдегида преодолен при концентрации 0,005%.
На микрофотографиях (Фиг. 4), показывающих клетки MFC-7, подвергнутые воздействию формальдегида, отчетливо видны морфологические изменения, происходящие с клетками под действием нарастающих доз генотоксического агента: если в контроле в отсутствие формальдегида выход неповрежденной ДНК в хвост ДНК-кометы составляет более 30% (слайд а), то при концентрации формальдегида 330 мкмоль/л (слайд б) доля ДНК в хвосте ДНК-комет снижена более, чем в два раза. Дальнейшее увеличение концентрации до 1650 мкмоль/л (слайд в) приводит к тому, что все клетки имеют короткие хвосты ДНК-комет, однако, ядра не деформированы. При воздействии формальдегида в концентрации 3300 мкмоль/л (слайд г) хвосты ДНК-комет полностью исчезают и ядра «сжимаются», уменьшаясь в размере.
Как отмечалось выше, предлагаемый способ дает общую информацию обо всех типах сшивок ДНК, образовавшихся под действием генотоксического фактора: внутри- и межцепочечных сшивках ДНК-ДНК и сшивках ДНК-белок. Для того, чтобы получить информацию о доле ДНК сшитой с белком, образующейся под действием генотоксического агента, от общего количества ДНК, лизис клеток проводят в присутствии протеиназы К, вызывающей разрывы сшивок между ДНК и гистоновыми белками, что приводит к увеличению электрофоретической подвижности ДНК в геле агарозы. Сравнивая электрофоретическую подвижность ДНК контрольных и обработанных формальдегидом клеток в зависимости от присутствия в лизирующем буфере протеиназы К, оценивают природу сшивок ДНК. При наличии в клетках сшивок ДНК-белок наблюдают увеличение %ДНК в хвосте ДНК-комет после инкубации слайдов с клетками в лизирующем буфере, содержащем протеиназу К по сравнению с инкубацией слайдов с клетками в лизирующем буфере не содержащем протеиназу К. Разница между %ДНК в хвосте ДНК-комет клеток обработанных и не обработанных протеиназой К отражает %ДНК, сшитой с белком или % сшивок ДНК-белок.
В качестве примера в Табл. 4 показан %ДНК в хвосте ДНК-комет в культивируемых клетках аденокарциномы молочной железы (MCF-7), обработанных и не обработанных протеиназой К, в зависимости от концентрации формальдегида.
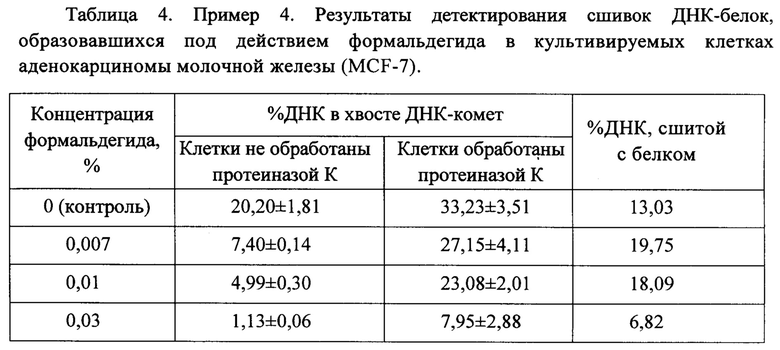
Приведенные результаты показывают, что формальдегид вызывает существенное образование сшивок ДНК-белок, что согласуется с литературными данными о механизме генотоксического действия формальдегида на ДНК [Hoffman Е. et. al. (2015)].
Таким образом, предлагаемый способ детектирования сшивок ДНК, не содержащий, как в аналогах, стадии индуцирования разрывов ДНК, и предполагающий проведение электрофореза в условиях высокой напряженности электрического поля, обеспечивающей выход в хвост ДНК-кометы от 25 до 50% неповрежденной ДНК, позволяет быстро и надежно, с меньшими, чем в аналогах, затратами реактивов, труда и времени, осуществлять непосредственную оценку ДНК-сшивающего действия генотоксических агентов.
| название | год | авторы | номер документа |
|---|---|---|---|
| CПОСОБ ИНДУЦИРОВАННЫХ ПОВРЕЖДЕНИЙ ДНК В ИНДИВИДУАЛЬНЫХ НЕДЕЛИМЫХ ЯДРОСОДЕРЖАЩИХ КЛЕТКАХ | 2013 |
|
RU2527345C1 |
| НАБОР И СПОСОБ ДЛЯ ПРИГОТОВЛЕНИЯ МНОГОСЛОЙНЫХ АГАРОЗНЫХ БЛОКОВ НА ПОВЕРХНОСТИ МИНИ-СТЕКОЛ ДЛЯ МИКРОСКОПИИ | 2013 |
|
RU2558229C2 |
| Средство, снижающее уровень генотоксичности цитостатиков | 2018 |
|
RU2697524C1 |
| СПОСОБ ОЦЕНКИ СТЕПЕНИ ЭКСПОЗИЦИИ ТОКСИЧЕСКИХ ВЕЩЕСТВ НА РАБОТНИКОВ НЕФТЕХИМИЧЕСКИХ ПРОИЗВОДСТВ | 2021 |
|
RU2785267C1 |
| СПОСОБ ОЦЕНКИ СУММАРНОЙ ВЕЛИЧИНЫ ГЕНОТОКСИЧЕСКИХ ЭФФЕКТОВ ЛЕКАРСТВЕННЫХ СРЕДСТВ И ФАКТОРОВ ОКРУЖАЮЩЕЙ СРЕДЫ | 2023 |
|
RU2828488C1 |
| Способ верификации инфицированного панкреонекроза | 2018 |
|
RU2701493C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ФРАГМЕНТАЦИИ ДНК В БАКТЕРИЯХ | 2007 |
|
RU2420596C2 |
| СПОСОБ ДЛЯ ОПРЕДЕЛЕНИЯ ФРАГМЕНТАЦИИ ДНК В СПЕРМАТОЗОИДАХ ЖИВОТНЫХ | 2005 |
|
RU2373288C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ИНФЕКЦИОННЫХ ОСЛОЖНЕНИЙ У ПОСТРАДАВШИХ С ТЯЖЕЛОЙ ТРАВМОЙ, КРОВОПОТЕРЕЙ И ГИПОКСИЕЙ | 2014 |
|
RU2599845C2 |
| Средство, обладающее канцеропревентивным действием в отношении рака яичек и наследственного рака | 2023 |
|
RU2820551C1 |

Изобретение относится к области биотехнологии и раскрывает новый способ детектирования сшивок ДНК, индуцированных действием генотоксических агентов. Изобретение может быть использовано в генотоксикологических исследованиях для сравнительного скрининга потенциальных ДНК-сшивающих агентов, разработки или индивидуального подбора препаратов для проведения химиотерапии и решения других практических задач биомедицины. 2 з.п. ф-лы, 4 табл., 4 ил.
1. Способ детектирования сшивок ДНК, индуцируемых действием генотоксических агентов, включающий последовательное проведение следующих стадий:
1) приготовление препаратов с иммобилизованными в агарозу клетками,
2) лизис клеток,
3) щелочную денатурацию ДНК,
4) проведение горизонтального щелочного электрофореза,
5) нейтрализацию,
6) окрашивание ДНК,
7) получение микрофотографий,
8) анализ и обработку полученных данных;
отличающийся тем, что указанный способ не подразумевает обработки суспензии клеток агентом, индуцирующим разрывы ДНК, и тем, что электрофорез на стадии 4) проводят при напряженности электрического поля в диапазоне 1,75-2,8 В/см.
2. Способ по п. 1, отличающийся тем, что электрофорез проводят при напряженности электрического поля в диапазоне 2,0-2,5 В/см.
3. Способ по пп. 1 и 2, отличающийся тем, что для детектирования сшивок ДНК-белок лизис клеток проводят в присутствии протеиназы К.
| BLASIAK A | |||
| et al.: "DNA damage and repair in human lymphocytes exposed to three anticancer platinum drugs", Teratog | |||
| Carcinog | |||
| Mutagen, 2000, v | |||
| Прибор для промывания газов | 1922 |
|
SU20A1 |
| KOHN K.W | |||
| et al.: "Fractionation of DNA from mammalian cells by alkaline elution", Biochemistry, 1976, v | |||
| Прибор для нагревания перетягиваемых бандажей подвижного состава | 1917 |
|
SU15A1 |
| SINGH N.P | |||
| et al.: "A simple technique for quantitation of | |||
Авторы
Даты
2023-07-03—Публикация
2022-07-05—Подача