Изобретение относится к медицине, а именно к интенсивной терапии и может быть использовано для лечения и профилактики желудочно-кишечных кровотечений у пациентов неврологического и нейрохирургического профиля. Способ может быть использован у пациентов с тяжелой черепно-мозговой травмой, нарушением мозгового кровообращения по ишемическому и геморрагическому типу или перенесших оперативное вмешательство по поводу опухоли головного мозга.
Кровотечение из верхних отделов пищеварительного тракта до сих пор остается одним из наиболее частых и тяжелых осложнений у пациентов в критическом состоянии. По данным литературы частота кровотечений из верхних отделов желудочно-кишечного тракта (ЖКТ) - от 5 до 47%, а смертность от них конкурирует с летальностью от острого инфаркта миокарда и онкологических заболеваний. Около 90% больных хронической язвой желудка и язвой двенадцатиперстной кишки - это люди трудоспособного возраста [Гельфанд Б.Р., Гурьянов В.А., Мартынов А.Н. и др. Профилактика стресс повреждений ЖКТ у больных в критических состояниях // Consilium Medicum. - 2005.- Т. 7.- №6.]. В терапевтической клинике с дестабилизацией хронической соматической патологии имеется риск развития острых повреждений слизистой оболочки желудка и ДПК вне зависимости от других факторов риска. Пациенты в крайне тяжелом и тяжелом состояниях находятся в группе риска стрессовых эрозий слизистой оболочки желудка. Существующие представления о причинах развития кровотечений из верхних отделов ЖКТ базируются на смещении равновесия защитные факторы/агрессивные факторы. При этом независимое влияние на процесс оказывают генетические факторы и нейроэндокринная регуляция. Вероятнее всего при нарушении нормального процесса нейрогуморального регулирования и формирования патологический организации передачи нервного импульса перевес в сторону поражения слизистой оболочки гастродуоденальный зоны увеличивается. Основу механизмов регуляции гастродуоденального комплекса (ГДК) составляют сложные функциональные системы с центральным и периферическим отделами, среди которых особая роль принадлежит «метасимпатической» нервной системе [Метасимпатическая нервная система. Структура. Свойства. Вероятное эволюционное происхождение Всесоюзная конференция по проблемам нейрогуморальной регуляции деятельности висцеральных систем, посвящ. 80-летию со дня рождения акад. В.Н. Черниговского: Тезис доклада и научное сообщение, Ленинград 3-5 марта 1987. - Л., 1987. - С. 98-99.]. На уровне периферического аппарата регуляции желудка и двенадцатиперстной кишки конвергируют нервные и гуморальные влияния из различных источников и формируется постоянная составляющая их многостороннего взаимодействия, которая проявляется в исходном уровне скоррелированности структур гастродуоденального комплекса (Завьялов А.В. Соотношение функций организма: экспериментальный и клинико-физиологический аспекты. М.Медицина 1990]. Острые эрозивно-язвенные поражения желудка и двенадцатиперстной кишки (ДПК) представляют собой гетерогенную группу заболеваний. Наиболее частой причиной их развития является язвенная болезнь. Кроме язвенной болезни острые эрозивно-язвенные поражения желудка и ДПК могут осложнять течение заболеваний различного генеза и неотложных состояний [Будневский А.В. Качество жизни больных хронической сердечной недостаточностью с психосоматическими нарушениями / А.В. Будневский, О.Ю. Ширяев, В.Л. Янковская // Паллиативная медицина и реабилитация. - 2014. - No 4. - С. 5-8.].
В структуре методов лечения гастродуоденальных кровотечений можно выделить консервативные и хирургические. Наиболее часто назначаемые препараты - ингибиторы протонной помпы (ИПП) и антагонисты Н2-гистаминовых рецепторов (АН2Р) [Клинические рекомендации российского общества хирургов 2014 год г. Воронеж].
Недостатком известных способов является воздействие только на местный уровень рН желудка и отсутствие влияния на нейрогуморальное звено регуляции моторной деятельности желудочно-кишечного тракта.
Известен способ консервативного лечения больных с желудочно-кишечными кровотечениями (пат. РФ №2195309, опубл. 27.12.2002 г.), принятый за прототип к заявляемому способу. В известном способе, включающем в себя комплекс консервативных мероприятий, для лечения больных дополнительно применяют аминокислотный гидролизат "аминок" в течение 10-12 дней в дозе 10 г/сут.
Недостатком прототипа является его недостаточная точность, так как представленные группы препаратов не влияют на центральные механизмы регуляции деятельности желудочно-кишечного тракта, которые являются определяющими среди факторов риска. Применение препаратов влияющих на симпатическую регуляцию в комплексе с ИПП повышает эффективность профилактики развития ЖКК из верхних отделов ЖКТ.
Техническим результатом заявляемого способа является повышение эффективности лечения и профилактики желудочно-кишечных кровотечений из верхних отделов ЖКТ у пациентов с тяжелым повреждением головного мозга различной этиологии.
Указанный технический результат достигается за счет того, что в способе профилактики желудочно-кишечных кровотечений из верхних отделов желудочно-кишечного тракта у пациентов с тяжелым повреждением головного мозга различной этиологии, включающим комплексную консервативную терапию с применением ингибиторов протонной помпы (ИПП) омепразол 40 мг 2 раза в сутки, дополнительно вводят внутривенно микроструйно опиоидный анальгетик – фентанил в дозе 1 мкг/кг/ч, альфа-2 адреноагонист – клонидин в дозе 0,8 мкг/кг/ч и гипнотик – тиопентал натрия в дозе 4 мг/кг/ч в течение 24-72 часов, при стабилизации состояния пациента, препараты отменяют в следующей последовательности: гипнотик, опиоидный анальгетик, альфа-2 адреноагонист.
Отличительная особенность заявляемого способа от аналогов и прототипа заключается в том, что - после тяжелой черепно-мозговой травмы, нарушения мозгового кровообращения по геморрагическому типу или оперативного вмешательства по поводу опухоли головного мозга в структуру лечения включают: опиоидный анальгетик, альфа-2 адреноагонист и гипнотик внутривенно микроструйно.
Способ осуществляется следующим образом.
После повреждения головного мозга различной этиологии до появления признаков синдрома пароксизмальной симпатической активности или после развития клинических признаков синдрома в схему лечения помимо ингибиторов протонной помпы - омепразол 40 мг 2 раза в сутки дополнительно вводят: внутривенно микроструйно опиоидный анальгетик – фентанил в дозе 1 мкг/кг/ч, альфа-2 адреноагонист – клонидин в дозе 0,8 мкг/кг/ч и гипнотик – тиопентал натрия в дозе 4 мг/кг/ч в течение 24-72 часов, при стабилизации состояния пациента, препараты отменяют в следующей последовательности: гипнотик, опиоидный анальгетик, альфа-2 адреноагонист. В последующем на фоне стабилизации состояния (клинические данные и данные методов нейровизуализации) применяется ступенчатое последовательное изменение схемы. Последовательное снижение дозировок и отключение препаратов проводится индивидуально в следующей последовательности: гипнотик-опиоидный анальгетик - альфа-2 адреноагонист. Введение препаратов дозировки и длительность зависит от проявлений пароксизмальной симпатической гиперактивности (ПСГА), определяемой по Шкале в таблице 1.
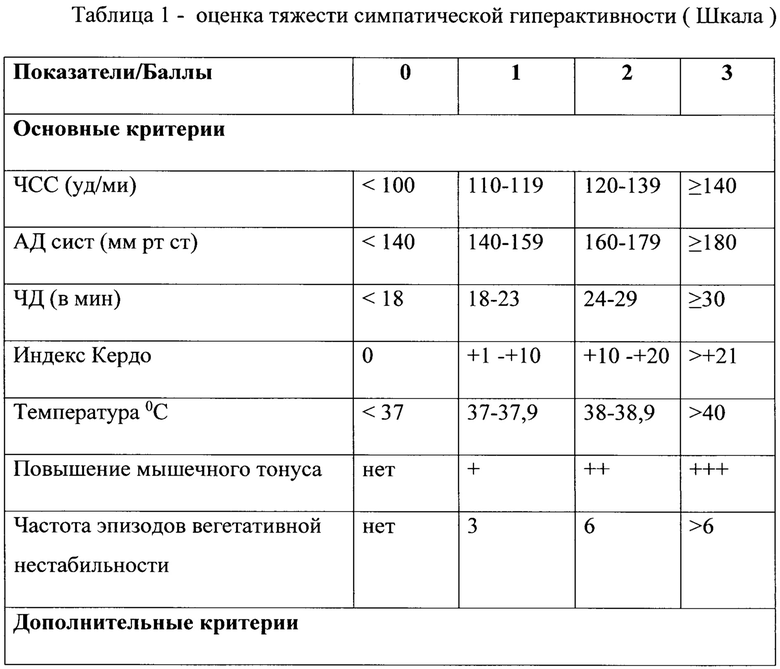
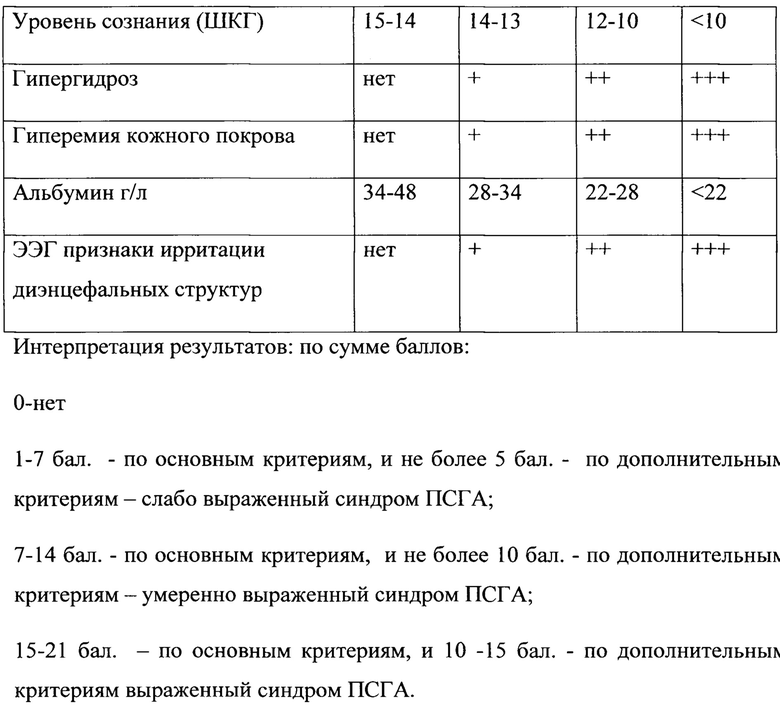
Терапия:
Слабо выраженный синдром ПСГА - бета-блокаторы, фенитоин, нестероидные противовоспалительные препараты (НПВС);
Умеренный синдром ПСГА - бета-блокаторы, фенитоин, альфа-2 адреноагонист, НПВС;
Выраженный синдром ПСГА - лечебный наркоз - опиоидный анальгетик, альфа-2 адреноагонист, гипнотик.
Заявляемый способ разработан и прошел клинические испытания на базе реанимационного отделения РНХИ им. А.Л.Поленова филиала ФГБУ «НМИЦ им В.А. Алмазова» Минздрава России при лечении пациентов с различными видами тяжелого повреждения головного мозга.
Для иллюстрации заявляемого способа приводим выписки из историй болезни пациентов нейрохирургического профиля, у которых, несмотря на риски развития желудочно-кишечных кровотечений из верхних отделов ЖКТ на фоне развития стресс-язв, эпизодов желудочно-кишечных кровотечений (ЖКК) не выявлено.
Клинический примеры:
Пример 1
Пациент Г., 25 лет, находился в РНХИ им. проф. А. Л. Поленова с диагнозом гигантская артериовенозная мальформация (АВМ) левой височной и лобной долей, эпилептический тип течения, состояние после трех этапов эмболизации АВМ неадгезивной композицией. Операция эмболизация АВМ неадгезивной композицией. Осложнение церебросубарахноидально вентрикулярное крововизлияние с тампонадой всех желудочков мозга. Повторное субарахноидально вентрикулярное крововизлияние вследствие разрыва недоэмболизированной части АВМ левого полушария.
В анамнезе эпизоды ночных припадков с потерей сознания и падением с кровати во время припадков с последующими неоднократными переломами костей верхних конечностей и позвоночника. Эпизодов кровоизлияний связанных с АВМ в анамнезе не отмечалось. При поступлении в РНХИ состояние расценивалось как компенсированное, соматически здоров. В плановом порядке выполнена частичная эмболизация АВМ левой лобной и височной долей неадгезивной композицией.
В раннем послеоперационном периоде после выполнения частичной эмболизации АВМ отмечалось резкое угнетение сознания до комы 2 (по GCS 4 балла), по данным инструментальных методов церебросубарахноидально вентрикулярное крововизлияние с тампонадой всех желудочков мозга. В отделении реанимации для профилактики эррозивного повреждения слизистой оболочки верхних отделов ЖКТ и для профилактики развития стресс-индуцированных язв желудка вводились ИПП (омепразол 40 мг 2 раза в сутки), для нейровегетативной стабилизации была начата инфузия опиоидный анальгетик - фентанил 1 мкг/кг/ч, альфа-2 адреноагонист -клонидин 0,8 мкг/кг/ч и гипнотик - тиопентал натрия 4 мг/кг/ч, в течение 24 часов. Выполнена оценка по шкале тяжести проявлений ПСГА. Повторная оценка проводилась через 48 часов. Произведена интубация трахеи, начата искусственная вентилляция легких (ИВЛ). По жизненным показаниям было выполнено оперативное вмешательство: наложение наружного вентрикулярного дренажа в левой точке Денди, а через сутки выполнена декомпрессивная краниотомия в левой лобно-височно теменно-затылочной области, пластика ТМО, наружная декомпрессия, дренирование желудочковой системы по Арендту. Течение наркоза (фентанил, клонидин, пропофол, миоплегия рокурония бромидом) гладкое.
На 30 е сутки повторное кровоизлияние из АВМ, по жизненным показаниям выполнена частичная эмболизация АВМ левой лобной и височной долей.
В послеоперационном периоде в клинической картине доминировали симптомы поражения головного мозга на фоне раздражения смешанной кровью после разрывов АВМ преимущественно на диэнцефальном уровне: тахикардия, тахипноэ, гиперизотермия, гипергидроз, нейродистрофический синдром, электролитные нарушения. Для купирования проявлений симпатической гиперактивности использовалась следующая схема нейровегетативной стабилизации (НВС): опиоидный анальгетик фентанил 1 мкг/кг/ч, альфа-2 адреноагонист клонидин 0,8 мкг/кг/ч и гипнотик - тиопентал натрия 4 мг/кг/ч. При попытке уменьшить дозу фентанила, клонидина и тиопентала натрия, вводимых с целью нейровегетативной стабилизации возобновление признаков симпатической гиперактивности в виде тахикардии, тахипноэ, гипертермии. По данным инструментальных методов обследований в динамике повторных кровоизлияний и выраженных воспалительных изменений не выявлено.
Для оценки степени тяжести симпатической гиперактивности и для подбора схемы нейровегетативной стабилизации использовалась шкала оценки тяжести ПСГА (таблица 1) оценки симпатической гиперактивности и алгоритм принятия решения. По мере стабилизации состояния на 18 е сутки после повторного кровоизлияния выполнено последовательное снижение дозировок и отключение препаратов в следующей последовательности: гипнотик - фентанил- клонидин.
Пример 2.
Пациент Ч., 56 лет. Диагноз: острое нарушение мозгового кровообращения по геморрагическому типу с формированием внутримозговой гематомы в области подкорковых структур правого полушария головного мозга.
Пациент поступил в ФГУ им. проф. А.Л. Поленова в отделение реанимации на 2-е сутки после кровоизлияния. Неврологически - в сознании, левосторонний гемипарез, симптомы раздражения правых височной и затылочной долей. Учитывая значительный объем гематомы (50 мл по данным компьютерной томографии), отек, дислокацию головного мозга, отсутствие положительной динамики на фоне проведения консервативной терапии, на 3-и сутки после поступления больному было выполнено дренирование гематомы через фрезевое отверстие. Течение послеоперационного периода гладкое. Состояние пациента компенсированное, без нарастания неврологической симптоматики. Через двое суток после операции произошло повторное кровоизлияние с прорывом крови в желудочковую систему. Отмечалось угнетение сознания до комы I, симптомы вегетативной нестабильности (проявления ПСГА). Помимо общепринятых лекарственных препаратов с целью воздействия на симпатическую гиперактивность больному проводилась нейро-вегетативная стабилизации (НВС) - опиоидный анальгетик фентанил, 1 мкг/кг/ч, альфа-2 адреноагонист клонидин 0,8 мкг/кг/ч и гипнотик - тиопентал натрия 4 мг/кг/ч. НВС проводилась в течение 72 часов с последующей оценкой неврологического статуса и состояния по шкале оценки ПСГА (таблица 1). Отключен гипнотик, а через 96 часов от момента начала НВС прекращено введение опиоидного анальгетика. Всего НВС в течение 7-ми суток, в дальнейшем использовался адреноагонист клофелин микроструйно 0.8 мк/кг/час.
В течение 10-ти суток после операции проводилась вспомогательная искусственная вентиляция легких. Течение послеоперационного периода осложнилось развитием инфекционных и нейротрофических нарушений. Состояние больного стабилизировалось к 45-м суткам после поступления.
Пациент был выписан на 52-е сутки после поступления. Неврологически при выписке - сознание ясное, контакт затруднен из-за элементов сенсомоторной афазии, левосторонняя гомонимная гемианопсия, глубокий правосторонний гемипарез. Сохраняются симптомы геморрагического цистита.
Таким образом, введение препаратов для НВС обеспечило снижение внутричерепного давления, каудализацию вегетативной регуляции с преобладанием стволового уровня, выключение патологической активности с вышележащих отделов мозга, что позволило стабилизировать состояние пациента в дооперационном периоде и минимизировать выраженность нейрогуморальных нарушений после операций. Несмотря на очевидную заинтересованность слизистой оболочки желудка и верхних отделов ЖКТ, нарушение трофики на фоне потери объема циркулирующих эритроцитов (кровоизлияние на фоне разрыва артериовенозных мальформаций головного мозга (АВМ), эпизодов ЖКК за период госпитализации не выявлено.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ дифференциальной диагностики синдрома пароксизмальной симпатической гиперактивности у пациентов с тяжелым повреждением головного мозга различной этиологии | 2023 |
|
RU2810456C1 |
| Способ профилактики развития инфекционных осложнений и сепсиса у нейрохирургических больных с аневризматической болезнью сосудов головного мозга в остром периоде разрыва аневризмы. Варианты | 2018 |
|
RU2694544C1 |
| Способ лечения устойчивых пароксизмальных состояний и генерализованных миоклоний у пациентов с последствиями тяжелого поражения головного мозга | 2016 |
|
RU2641163C1 |
| ПРИМЕНЕНИЕ АНТАГОНИСТОВ ОПИОИДНЫХ РЕЦЕПТОРОВ ПРИ ЗАБОЛЕВАНИЯХ ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА | 2010 |
|
RU2561873C2 |
| СПОСОБ ПРОВЕДЕНИЯ АНЕСТЕЗИИ ПРИ РЕНТГЕНЭНДОВАСКУЛЯРНЫХ ОПЕРАЦИЯХ У ДЕТЕЙ НА СЕРДЦЕ И КРУПНЫХ СОСУДАХ (ВАРИАНТЫ) | 2011 |
|
RU2485980C2 |
| Способ лечения пациентов в вегетативном состоянии и состоянии малого сознания | 2015 |
|
RU2612264C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ФУНКЦИОНАЛЬНЫХ ЖЕЛУДОЧНО-КИШЕЧНЫХ РАССТРОЙСТВ | 2020 |
|
RU2744125C1 |
| СПОСОБ ВЫЯВЛЕНИЯ ИНТРАОПЕРАЦИОННЫХ ОСЛОЖНЕНИЙ У НЕЙРОХИРУРГИЧЕСКИХ БОЛЬНЫХ | 2017 |
|
RU2686736C1 |
| Способ проведения комбинированной анестезии при шунтирующих операциях у пациентов с портальной гипертензией | 2022 |
|
RU2823512C2 |
| СПОСОБ ОБЕЗБОЛИВАНИЯ ПРИ ОПЕРАТИВНОМ ЛЕЧЕНИИ ЗАБОЛЕВАНИЙ И ПОВРЕЖДЕНИЙ ПОЯСНИЧНО-КРЕСТЦОВОГО ОТДЕЛА ПОЗВОНОЧНИКА | 2003 |
|
RU2259201C2 |
Изобретение относится к медицине, а именно к интенсивной терапии, и может быть использовано для профилактики желудочно-кишечных кровотечений у пациентов неврологического и нейрохирургического профиля с тяжелым повреждением головного мозга различной этиологии. Для этого в комплексе с консервативной терапией, включающей введение ингибиторов протонной помпы (ИПП) – омепразол 40 мг 2 раза в сутки, дополнительно вводят внутривенно микроструйно опиоидный анальгетик – фентанил в дозе 1 мкг/кг/ч, альфа-2 адреноагонист – клонидин в дозе 0,8 мкг/кг/ч и гипнотик – тиопентал натрия в дозе 4 мг/кг/ч в течение 24-72 ч. При стабилизации состояния пациента препараты отменяют в следующей последовательности: гипнотик, опиоидный анальгетик, альфа-2 адреноагонист. Изобретение позволяет повысить эффективность профилактики желудочно-кишечных кровотечений из верхних отделов желудочно-кишечного тракта у пациентов с тяжелым повреждением головного мозга различной этиологии. 1 табл., 2 пр.
Способ профилактики желудочно-кишечных кровотечений из верхних отделов желудочно-кишечного тракта у пациентов с тяжелым повреждением головного мозга различной этиологии, включающий комплексную консервативную терапию с применением ингибиторов протонной помпы (ИПП) – омепразол 40 мг 2 раза в сутки, отличающийся тем, что дополнительно вводят внутривенно микроструйно опиоидный анальгетик – фентанил в дозе 1 мкг/кг/ч, альфа-2 адреноагонист – клонидин в дозе 0,8 мкг/кг/ч и гипнотик – тиопентал натрия в дозе 4 мг/кг/ч в течение 24-72 ч, при стабилизации состояния пациента препараты отменяют в следующей последовательности: гипнотик, опиоидный анальгетик, альфа-2 адреноагонист.
| СПОСОБ КОНСЕРВАТИВНОГО ЛЕЧЕНИЯ БОЛЬНЫХ С ЖЕЛУДОЧНО-КИШЕЧНЫМИ КРОВОТЕЧЕНИЯМИ | 2001 |
|
RU2195309C2 |
| УСТРОЙСТВО ДЛЯ НАРУЖНОЙ КРАНИОЦЕРЕБРАЛЬНОЙ ГИПОТЕРМИИ | 2008 |
|
RU2372060C1 |
| Автоматический пружинный клапан | 1930 |
|
SU25017A1 |
| US 6126680 В1 (MAYO FOUNDATION), 03.10.2000 - реферат | |||
| КОРОЛЕВ М.П | |||
| и др | |||
| Диагностика и лечение кровотечений из верхних отделов желудочно-кишечного тракта у больных острым нарушением мозгового кровообращения, Педиатр | |||
| Станок для придания концам круглых радиаторных трубок шестигранного сечения | 1924 |
|
SU2019A1 |
| Зубчатое колесо со сменным зубчатым ободом | 1922 |
|
SU43A1 |
| ТОРОСЯН Б.Д | |||
| и др | |||
Авторы
Даты
2023-07-03—Публикация
2022-02-04—Подача