Область техники, к которой относится изобретение
Изобретение относится к области медицины, а более конкретно к аналитической медицинской технике, в частности к in vitro диагностике молекулярно-генетическими методами, для проведения реакции изотермической амплификации.
Уровень техники
В качестве ближайшего аналога можно указать US 20210180110 А1 (AUTONOMOUS MEDICAL DEVICES (US)) 17.06.2021, в котором описан аналитический прибор, содержащий корпус со встроенным дисплеем, сканером штрихкода и герметичной крышкой, установленной на направляющих с возможностью продольного перемещения, в корпусе размещены механический дозатор, барабан и системой нагрева, оптический датчик, лазер и аппаратно-программный комплекс для обеспечения управления, барабан установлен с возможностью поворота вокруг своей оси посредством шагового двигателя, а на поверхности барабана выполнены отверстия для установки и фиксации картриджа с ячейками для набора реагентов.
Основным недостатком данного аналога является отсутствие возможности реализации стадии выделения нуклеиновых кислот из патогенов и проведения мультиплексного молекулярно-генетического анализа. Метод ПЦР в реальном времени в данном устройстве реализован как этап иммуно-ПЦР, являющийся более чувствительным по сравнению иммуноферментным анализом способом обнаружения антигенов. Иммуно-ПЦР в предлагаемом решении использования анализатора представляет собой второй этап скринингового исследования и является подтверждающим для предполагаемой инфекции, выявленной в результате мультиплексного исследования с целью обнаружения антител. Отсутствие дополнительных ячеек для амплификации в картридже CD-3 и вращающейся конструкции у анализатора исключает возможность внедрение мультиплексного молекулярно-генетического исследования тестирования в данный анализатор.
Раскрытие сущности изобретения
Достигаемым при использовании предполагаемого изобретения техническим результатом является обеспечение условий для проведения реакции изотермической амплификации во внелабораторных условиях, с возможностью очистки нуклеиновых кислот с помощью магнитных шариков, размещенных в одной из ячеек картриджа, а также распределения реагентов по ячейкам.
Технический результат достигается тем, что аналитический прибор содержит корпус со встроенным дисплеем, сканером штрихкода и герметичной крышкой, установленной на направляющих с возможностью продольного перемещения. В корпусе размещены механический дозатор, барабан со встроенными электромагнитом и системой нагрева, оптический датчик, лазер и аппаратно-программный комплекс для обеспечения управления. Барабан установлен с возможностью поворота вокруг своей оси посредством двигателя, а на поверхности барабана выполнены отверстия для установки и фиксации картриджа с ячейками, в которых содержатся набор реагентов и магнитные шарики. Механический дозатор снабжен направляющей, для обеспечения движения по вертикальной оси и двигателем - по горизонтальной оси.
В частном случае выполнения двигатель является шаговым
Конструкция позволяет обеспечить условия для проведения реакции изотермической амплификации. В корпусе размещены барабан, механический дозатор, оптический датчик и лазер.
Для обеспечения температурного режима под барабаном размещены нагревательные элементы необходимые для регулирования температуры во время проведения реакции. Для сохранения температуры внутри прибора корпус оборудован герметичной крышкой, установленной на направляющих с возможностью продольного перемещения. Конструкция прибора позволяет установить на барабан картридж с ячейками, где проводится идентификация специфических фрагментов нуклеиновых кислот. Шаговый двигатель позволяет барабану вращаться вокруг своей оси.
Механический дозатор снабжен направляющей, позволяющей ему выполнять движения по вертикальной оси и двигателем, выполняющим движения по горизонтальной оси для распределения реагентов по ячейкам. Электромагнит, закрепленный под барабаном, включается, если процесс подразумевает очистку нуклеиновых кислот с помощью магнитных шариков, размещенных в одной из ячеек картриджа.
Лазер, установленный в корпусе анализатора, возбуждает флуоресцентный сигнал, выделяемый по окончании реакции, который считывает оптический датчик. Информация анализируется программным обеспечением прибора и результат отображается на сенсорном дисплее, встроенном в корпус прибора.
Сканер штрихкода используется для идентификации биологических образцов с целью интеграции прибора в лабораторную информационную систему.
Все движения и манипуляции, подвижных составляющих прибора прописаны в программном обеспечении и управляются с помощью аппаратно-программного комплекса. Прибор имеет кнопку включения/выключения, разъем и может работать как от сети, так и от аккумулятора.
Краткое описание чертежей.
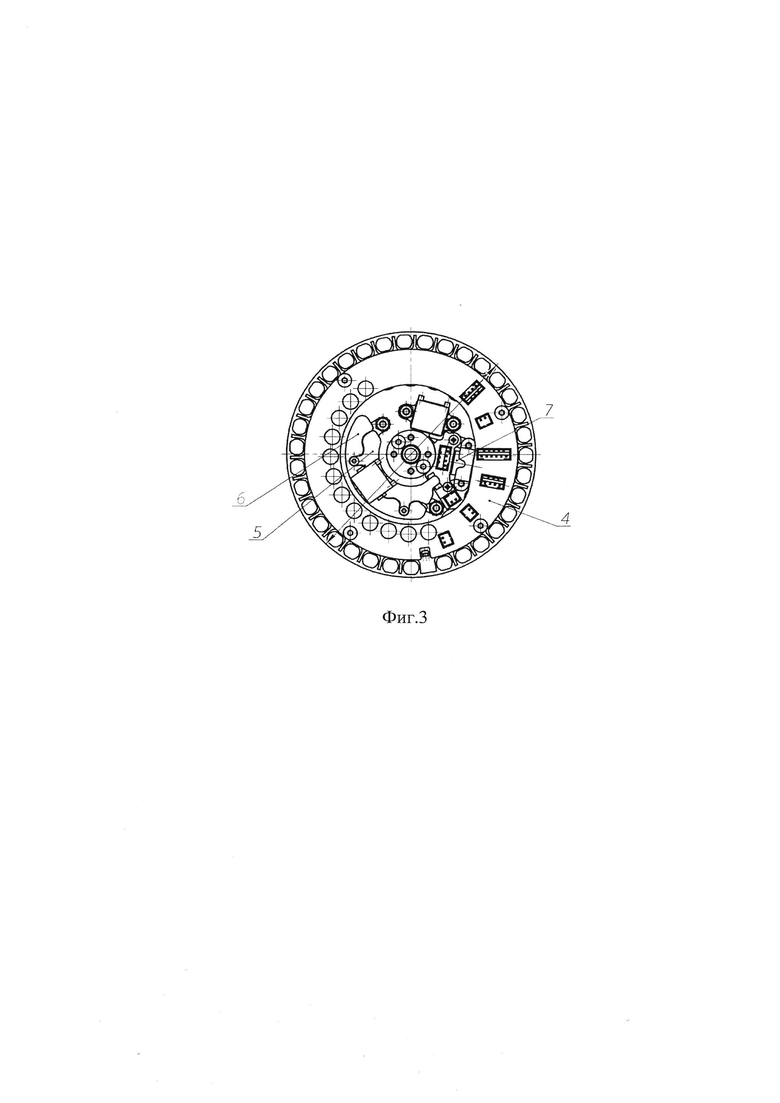
Предлагаемое изобретение поясняется чертежами, где на Фиг. 1 схематично изображен корпус устройства: на Фиг. 2 - схематично представлено устройство в разрезе, Фиг. 3 - схематично изображен барабан устройства.
Аналитический прибор содержит пластиковый корпус 1 с открывающейся крышкой 2, помещенные в корпус механический дозатор 3 и барабан 4 с системой нагрева 5, 6, электромагнит 7, дисплей 8, сканер штрихкода 9, оптический датчик 10, лазер (не указан на чертеже) и аппаратно-программный комплекс 11 для управления анализатором.
Осуществление изобретения.
Предлагаемое устройство функционирует следующим образом.
Крышка 2, установленная на направляющих в корпусе 1, после запуска программы, управляемой аппаратно-программным комплексом 11, открывается автоматически. В корпус 1 прибора, до начала анализа, на барабан 4, помещается картридж (не указан на чертеже) с ячейками в которых содержатся набор реагентов и магнитные шарики.
После закрытия крышки 2 анализатор осуществляет детекцию амплифицированных фрагментов при помощи ДНКзимных наносенсоров внутри картриджа за счет обеспечения прибором необходимого температурного режима и переноса реагентов из одной ячейки в другую.
Необходимый температурный режим достигается с помощью системы нагрева 5, 6, включающей в себя нагревательные элементы, теплообменники, радиаторы, устройства пельтье и конденсаторы.
Перенос реагентов из одной ячейки в другую, осуществляется посредством механического дозатора 3, также сконфигурированного для контроля следующих действий: 1) добавление лизирующего раствора к внесенному образцу, 2) добавление лизированного образца к реагентам для выделения нуклеиновых кислот, 3) промывку выделенных нуклеиновых кислот, 4) добавление нуклеиновых кислот к смесям для амплификации, 5) добавление результатов изотермической ПЦР к смесям для визуализации реакции.
Дозатор закреплен на линейной направляющей, для обеспечения движения по вертикальной оси, установленной на кронштейне, который соединен с двигателем, обеспечивающим перемещение конструкции по горизонтальной оси. После запуска программы, дозатор последовательно выполняет все действия 1-4 так как они все необходимы для проведения реакции.
Дозатор сконструирован и встроен в прибор таким образом, чтоб быстро и четко выполнять все запрограммированные действия, попадая в небольшие лунки картриджа и делая забор реагентов.
Высокоточная работа дозатора позволяет проводить микрофлюидные мультиплексные реакции в открытом и простом по конструкции картридже, что значительно удешевляет стоимость тестирования одного образца.
Электромагнит 7, закрепленный под барабаном, включается, если процесс подразумевает очистку нуклеиновых кислот с помощью магнитных шариков, размещенных в одной из ячеек картриджа.
При обнаружении аналита ДНКзимы собираются в структуру, обладающую ферментативной активностью. При добавлении субстрата и с помощью лазера (не указан на чертеже), установленного в корпусе анализатора, ДНКзимы реализуют реакцию с выделением флуоресцентного продукта, оптический датчик 10, обнаруживает количество флуоресценции, испускаемой образцом и после анализа информации программным обеспечением результат отображается на дисплее 8.
Сканер штрихкода 9 используется для идентификации биологических образцов с целью интеграции прибора в лабораторную информационную систему.
Пример осуществления изобретения
Создание тест-системы
Тест-система состоит из прибора-анализатора и специального картриджа, в котором размещаются реагенты для исследования. Тест-система позволяет проводить диагностическую идентификацию чистой культуры бактерий молекулярно-генетическими методами. Исследование включает в себя 3 последовательные стадии: 1) выделение нуклеиновых кислот, 2) амплификация методом изотермической ПЦР, 3) визуализация накопленного наличия продукта амплификации.
Необходимые реагенты были размещены в картридж, который представляет собой плоскую конструкцию округлой формы с множеством выемок. В картридж также внесли микробиологических изолят для анализа, в приборе установили программу, описывающую алгоритм движения дозатора и температурный режим: 1) дозатор добавил в ячейку с изолятом реагенты для выделения нуклеиновых кислот и перемешал, 2) прибор инкубировал смесь в течение 15 минут, 3) дозатор перенес смесь в ячейку с магнитными шариками, 4) прибор проинкубировал смесь в течение 5 минут, 5) прибор активировал электромагнит, который был поднесен к ячейке с магнитными шариками, 6) дозатор убрал жидкость из ячейки с магнитными шариками и сменил наконечник, 7) дозатор добавил спирт для промывки магнитных шариков, 8) дозатор убрал спирт из ячейки с магнитными шариками, 9) дозатор добавил воду в ячейку с магнитными шариками, 10) прибор активировал электромагнит рядом с ячейкой с магнитными шариками, 11) дозатор отобрал воду с элюированными нуклеиновыми кислотами и разаликвотил в ячейки с реагентами для проведения амплификации и сменил наконечник, 12) прибор повысил температуру во внутреннем пространстве до 65 оС и поддерживал ее в течение 60 минут, 13) после амплификации дозатор разаликвотил амплификационную смесь в 6 ячеек, содержащие по одному набору специфических к патогенам С. albicans, Е. coli, S. agalactiae, L. monocytogenes, S. aureus и N. meningitidis сенсоров для визуализации продукта при помощи производства флуоресцентного продукта, 14) барабан прокручивал картридж, а датчик флуоресцентного сигнала после возбуждения флуоресценции лазером фиксировал уровень флуоресценции в каждой из ячеек, содержащих сенсоры к одному из патогенов, 15) алгоритм путем сравнения уровня сигнала до и после реакции показывает результат исследования на экране.
Пороговое значение для положительного сигнала установили 185 относительных единиц. Все исследования проводили в исследовательской лаборатории, с имитацией полевых условий: приборы работали от аккумулятора, а для внесения клинических и лабораторных образцов использовали дозаторы (Eppendorf).
Образец №1
Вносили чистую культуру С.albicans в количестве около 100 клеток в картридж, содержащий необходимые реагенты для мультиплексной изотермической амплификации и специфические ДНКзимные сенсоры к каждому и патогенов С. albicans, Е. coli, S. agalactiae, L. monocytogenes, S. aureus и N. meningitidis.
Время исследования составило 120 мин.
Результат измерения разницы флуоресценции в конце исследования для каждого из патогенов:
- С.albicans: 215 отн. ед.,
- Е. coli: 113 отн. ед.,
- S. agalactiae: 153 отн. ед.,
- L. monocytogenes: 131 отн. ед.,
- S. aureus: 110 отн. ед.,
- N. meningitidis: 90 отн. ед.
Результат идентификации на экране: С.albicans.
Образец №2
Вносили чистую культуру Е. coli в количестве около 100 клеток в картридж, содержащий необходимые реагенты для мультиплексной изотермической амплификации и специфические ДНКзимные сенсоры к каждому и патогенов С.albicans, Е. coli, S. agalactiae, L. monocytogenes, S. aureus и N. meningitidis.
Время исследования составило 120 мин.
Результат измерения разницы флуоресценции в конце исследования для каждого из патогенов:
- С.albicans: 146 отн. ед.,
- Е. coli: 198 отн. ед.,
- S. agalactiae: 112 отн. ед.,
- L. monocytogenes: 156 отн. ед.,
- S. aureus: 123 отн. ед.,
- N. meningitidis: 110 отн. ед.
Результат идентификации на экране: Е. coli.
Образец №3
Вносили чистую культуру S. aureus в количестве около 100 клеток в картридж, содержащий необходимые реагенты для мультиплексной изотермической амплификации и специфические ДНКзимные сенсоры к каждому и патогенов С. albicans, Е. coli, S. agalactiae, L. monocytogenes, S. aureus и N. meningitidis.
Время исследования составило 120 мин.
Результат измерения разницы флуоресценции в конце исследования для каждого из патогенов:
- С.albicans: 126 отн. ед.,
- Е. coli: 166 отн. ед.,
- S. agalactiae: 125 отн. ед.,
- L. monocytogenes: 162 отн. ед.,
- S. aureus: 233 отн. ед.,
- N. meningitidis: 118 отн. ед.
Результат идентификации на экране: S. aureus.
| название | год | авторы | номер документа |
|---|---|---|---|
| Тест-система и способ обнаружения специфических фрагментов нуклеиновых кислот 16 патогенов с использованием изотермической реакции амплификации | 2023 |
|
RU2810751C1 |
| Диагностическая тест-система для определения этиологии инфекционных заболеваний посредством обнаружения нуклеиновых кислот возбудителей инфекций | 2021 |
|
RU2798567C2 |
| Картридж для стерильного хранения реагентов | 2023 |
|
RU2800875C1 |
| ПРОБИРКА ДЛЯ УДАРНОЙ ОБРАБОТКИ ШАРИКАМИ И СПОСОБ ЭКСТРАКЦИИ ДЕЗОРИБОНУКЛЕИНОВОЙ КИСЛОТЫ И/ИЛИ РИБОНУКЛЕИНОВОЙ КИСЛОТЫ ИЗ МИКРООРГАНИЗМОВ | 2017 |
|
RU2743140C2 |
| Автономная диагностическая микрофлюидная платформа с интегрированными магнитными микрочастицами для активного перемешивания реагентов, оснащенная системой односторонних клапанов, управляемая оператором посредством нажатия на гибкие мембраны | 2021 |
|
RU2778345C2 |
| СИСТЕМА ДЛЯ ВЫДЕЛЕНИЯ НУКЛЕИНОВЫХ КИСЛОТ И ИХ ПОСЛЕДУЮЩЕЙ АМПЛИФИКАЦИИ | 2023 |
|
RU2813921C1 |
| УСТРОЙСТВО ДЛЯ АВТОМАТИЧЕСКОГО ВЫДЕЛЕНИЯ, ОЧИСТКИ И АМПЛИФИКАЦИИ УЧАСТКОВ ДНК Mycobacterium tuberculosis С РЕГИСТРАЦИЕЙ РЕЗУЛЬТАТОВ В РЕЖИМЕ РЕАЛЬНОГО ВРЕМЕНИ | 2024 |
|
RU2837310C1 |
| ПРОБИРКА ДЛЯ УДАРНОЙ ОБРАБОТКИ ШАРИКАМИ И СПОСОБ ЭКСТРАКЦИИ ДЕЗОРИБОНУКЛЕИНОВОЙ КИСЛОТЫ И/ИЛИ РИБОНУКЛЕИНОВОЙ КИСЛОТЫ ИЗ МИКРООРГАНИЗМОВ | 2018 |
|
RU2762314C2 |
| СИСТЕМА (ВАРИАНТЫ) И СПОСОБ ДЕТЕКТИРОВАНИЯ НАЛИЧИЯ АНАЛИТА В ЖИДКОМ ОБРАЗЦЕ | 2011 |
|
RU2653451C2 |
| АВТОМАТИЗИРОВАННОЕ ОБОРУДОВАНИЕ ДЛЯ ПОЛУЧЕНИЯ БИБЛИОТЕК ПЕПТИДОВ Т-КЛЕТОЧНЫХ РЕЦЕПТОРОВ | 2019 |
|
RU2770700C1 |

Изобретение относится к медицинской технике, а именно к аналитическому прибору для проведения реакции изотермической амплификации нуклеиновых кислот во внелабораторных условиях. Устройство содержит корпус со встроенным дисплеем, сканером штрихкода и герметичной крышкой, установленной на направляющих с возможностью продольного перемещения. В корпусе размещены механический дозатор, барабан со встроенной системой нагрева, оптический датчик, лазер и аппаратно-программный комплекс для обеспечения управления. Барабан установлен с возможностью поворота вокруг своей оси посредством двигателя, а на поверхности барабана выполнены отверстия для установки и фиксации картриджа с ячейками для набора реагентов. Барабан выполнен со встроенным электромагнитом, а картридж содержит магнитные шарики. Механический дозатор снабжен направляющей для обеспечения движения по вертикальной оси и двигателем для обеспечения движения по горизонтальной оси. Техническим результатом является обеспечение условий для проведения реакции изотермической амплификации во внелабораторных условиях, с возможностью очистки нуклеиновых кислот с помощью магнитных шариков, размещенных в одной из ячеек картриджа, а также распределения реагентов по ячейкам. 1 з.п. ф-лы, 3 ил.
1. Аналитический прибор для проведения реакции изотермической амплификации нуклеиновых кислот во внелабораторных условиях, содержащий корпус со встроенным дисплеем, сканером штрихкода и герметичной крышкой, установленной на направляющих с возможностью продольного перемещения, в корпусе размещены механический дозатор, барабан со встроенной системой нагрева,. оптический датчик, лазер и аппаратно-программный комплекс для обеспечения управления, барабан установлен с возможностью поворота вокруг своей оси посредством двигателя, а на поверхности барабана выполнены отверстия для установки и фиксации картриджа с ячейками для набора реагентов, отличающийся тем, что барабан выполнен со встроенным электромагнитом, а картридж содержит магнитные шарики, при этом механический дозатор снабжен направляющей для обеспечения движения по вертикальной оси и двигателем для обеспечения движения по горизонтальной оси.
2. Аналитический прибор по п. 1, отличающийся тем, что двигатель является шаговым двигателем.
| US 20210180110 A1, 17.06.2021 | |||
| US 20200080133 A1, 12.03.2020 | |||
| US 20190271647 A1, 05.09.2019 | |||
| US 20210164039 A1, 03.06.2021 | |||
| US 20200224243 A1, 16.07.2020 | |||
| US 20210102242 A1, 08.04.2021 | |||
| WO 2017100442 A1, 15.06.2017 | |||
| US 20220145362 A1, 12.05.2022. |
Авторы
Даты
2023-07-04—Публикация
2023-04-04—Подача