ПЕРЕКРЕСТНЫЕ ССЫЛКИ НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Настоящая заявка испрашивает приоритет согласно разделу 35 Свода законов США §119(е) на основании предварительных заявок на патент США №62/556319; №62/556324; №62/556329; №62/556331; №62/556281 и №62/556335, каждая из которых была подана 8 сентября 2017 г., содержание каждой из которых включено в настоящий документ полностью посредством ссылки.
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
[0002] Настоящая заявка включает перечень последовательностей, поданный в электронном виде в формате ASCII и включенный в настоящий документ полностью посредством ссылки. Указанная копия в формате ASCII, созданная 7 сентября 2018 г., имеет название 080170-090580WOPT SL.txt и размер 205991 байтов.
ОБЛАСТЬ ТЕХНИКИ
[0003] Настоящее изобретение относится к области генной терапии, в том числе к доставке экзогенных последовательностей ДНК в целевую клетку, ткань, орган или организм.
УРОВЕНЬ ТЕХНИКИ
[0004] Целью генной терапии является улучшение клинических исходов для пациентов, страдающих генетическими мутациями или приобретенными заболеваниями, вызываемыми аберрациями в профиле генной экспрессии. Генная терапия включает лечение или предотвращение медицинских состояний, обусловленных дефектными генами или аномальной регуляцией или экспрессией, например, недостаточной экспрессией или избыточной экспрессией, которые могут приводить к нарушению, заболеванию, злокачественному новообразованию и т.п. Например, лечение, предотвращение или облегчение заболевания или нарушения, вызываемого дефектным геном, может быть осуществлено путем доставки корректирующего генетического материала пациенту, приводящей к терапевтической экспрессии указанного генетического материала у указанного пациента. Генная терапия основана на обеспечении транскрипционной кассеты с активным генным продуктом (иногда называемым трансгеном), например, который может приводить к положительному эффекту приобретения функции, отрицательному эффекту утраты функции, или другому исходу, такому как, например, онколитический эффект. Генная терапия может также применяться для лечения заболевания или злокачественного новообразования, вызываемого другими факторами. Лечение моногенных нарушений человека может осуществляться путем доставки и экспрессии нормального гена в целевые клетки. Доставка и экспрессия корректирующего гена в целевых клетках (клетках-мишенях) пациента могут быть осуществлены с применением многочисленных способов, в том числе с применением сконструированных вирусов и вирусных векторов для доставки генов. Среди многочисленных доступных происходящих из вирусов векторов (например, из рекомбинантного ретровируса, рекомбинантного лентивируса, рекомбинантного аденовируса и т.п.) набирает популярность в качестве многоцелевого вектора для генной терапии рекомбинантный аденоассоциированный вирус (rAAV).
[0005] Аденоассоциированные вирусы (AAV) принадлежат к семейству Parvoviridae; более конкретно, они составляют род Dependoparvovirus. Геном AAV состоит из линейной одноцепочечной молекулы ДНК, которая содержит приблизительно 4,7 т.п.о. (кб) и состоит из двух основных открытых рамок считывания (ORF), кодирующих неструктурный белок Rep (репликация) и структурный белок Сар (капсид). В гене cap была идентифицирована вторая ORF, которая кодирует активирующий сборку белок (ΑΑΡ). ДНК, фланкирующие кодирующие области AAV, представляют собой две последовательности цис-действующих инвертированных концевых повтора (ITR) длиной приблизительно 145 нуклеотидов, с прерывистыми палиндромными последовательностями, которые могут укладываться в энергетически стабильные шпилечные структуры, функционирующие в качестве праймеров для репликации ДНК. Наряду с ролью в репликации ДНК указанные последовательности ITR, как было показано, вовлечены в интеграцию вирусной ДНК в клеточный геном, спасение из генома хозяина или плазмиды, и заключение в капсид вирусной нуклеиновой кислоты в зрелых вирионах (Muzyczka, (1992) Curr. Top.Micro. Immunol. 158:97-129).
[0006] Векторы, происходящие из AAV (т.е. рекомбинантные AAV- (rAVV) или AAV-векторы), являются привлекательным способом доставки генетического материала, поскольку (i) они способны инфицировать (трансдуцировать) широкий спектр типов неделящихся и делящихся клеток, в том числе миоциты и нейроны; (ii) они лишены вирусных структурных генов, что обеспечивает уменьшение ответов клетки-хозяина на вирусную инфекцию, например, интерферон-опосредованные ответы; (iii) вирусы дикого типа считаются непатогенными для человека; (iv) в отличие от AAV дикого типа, который способен к интеграции в геном клетки-хозяина, у дефектных по репликации векторов AAV отсутствует ген rep, и обычно они персистируют в виде эписом, что ограничивает риск инсерционного мутагенеза или генотоксичности; и (v) по сравнению с другими векторными системами, AAV-векторы в целом считаются относительно слабыми иммуногенами и, соответственно, не запускают значимого иммунного ответа (см. ii), с увеличением таким образом продолжительности персистенции векторной ДНК и, потенциально, долгосрочной экспрессии терапевтических трансгенов. AAV-векторы могут также быть продуцированы и введены в составы с высокими титрами и доставлены посредством внутриартериальных, внутривенных, или внутрибрюшинных инъекций, обеспечивая распределение вектора и перенос генов в значимые мышечные области путем однократной инъекции у грызунов (Goyenvalle et al., 2004; Fougerousse et al., 2007; Koppanati et al., 2010; Wang et al., 2009) и собак. В клиническом исследовании лечения спинальной мышечной дистрофии типа 1 AAV-векторы доставляли системно для нацеливания на мозг, что приводило к видимым клиническим улучшениям.
[0007] Однако у применения частиц AAV в качестве вектора для доставки генов существует ряд серьезных недостатков. Один существенный недостаток, ассоциированный с rAAV, заключается в ограниченной емкости вирусной упаковки, составляющей приблизительно 4,5 кб гетерологичной ДНК (Dong et al., 1996; Athanasopoulos et al., 2004; Lai et al., 2010). В результате применение AAV-векторов было ограничено кодированием менее чем 15000 Да белка. Второй недостаток заключается в том, что ввиду распространенности инфекции AAV дикого типа в популяции кандидаты для генной терапии rAAV должны проходить скрининг на присутствие нейтрализующих антител, элиминирующих вектор из организма пациента. Третий недостаток связан с иммуногенностью капсида, которая предотвращает повторное введение пациентам, не исключенным из первичного лечения. Иммунная система пациента может отвечать на вектор, который эффективно действует в качестве «бустерного» введения, стимулируя иммунную систему, генерирующую высокие титры антител против AAV, исключая лечение в будущем. В некоторых недавних отчетах описаны проблемы с иммуногенностью в ситуациях с использованием высоких доз. Другой заметный недостаток заключается в относительно медленном начале действия AAV-опосредованной генной экспрессии, учитывая, что одноцепочечная ДНК AAV должна быть преобразована в двунитевую ДНК до гетерологичной генной экспрессии. Хотя были предприняты попытки обойти указанную проблему путем конструирования двунитевых ДНК-векторов, указанная стратегия дополнительно ограничивает размер трансгенной экспрессионной кассеты, которая может быть интегрирована в AAV-вектор (McCarty, 2008; Varenika et al., 2009; Foust et al., 2009).
[0008] Кроме того, стандартные вирионы AAV с капсидами получают путем введения плазмиды или плазмид, содержащих геном AAV, гены rep и гены cap (Grimm et al., 1998). При введении указанных хелперных (вспомогательных) плазмид в транс-положении, происходит «спасение» генома AAV (т.е. высвобождение с последующей амплификацией) из генома хозяина, и дальнейшее заключение в капсид (вирусные капсиды) с получением биологически активных AAV-векторов. Однако, как было обнаружено, такие заключенные в капсиды вирусные AAV-векторы неэффективно трансдуцируют определенные типы клеток и тканей. Указанные капсиды также индуцируют иммунный ответ.
[0009] Соответственно, применение векторов на основе аденоассоциированного вируса (AAV-векторов) для генной терапии ограничено однократным введением пациентам (из-за иммунного ответа у пациентов), ограниченным диапазоном трансгенного генетического материала, подходящего для доставки в AAV-векторах ввиду минимальной емкости вирусной упаковки (приблизительно 4,5 т.п.о.) ассоциированного капсида AAV, а также медленной AAV-опосредованной генной экспрессии. Применение клинической генной терапии с использованием rAAV дополнительно затрудняет межпациентная вариабельность, которую нельзя предсказать на основании дозовой зависимости в моделях на сингенных мышах или другом модельном виде.
[0010] Рекомбинантные бескапсидные AAV-векторы могут быть получены в виде выделенной линейной молекулы нуклеиновой кислоты, содержащей экспрессируемый трансген и промоторные области, фланкированные двумя последовательностями инвертированных концевых повторов (ITR) AAV дикого типа, включая сайт связывания Rep и сайт концевого разрешения. Указанные рекомбинантные AAV-векторы лишены кодирующих последовательностей капсидного белка AAV, и могут быть одно цепочечными, двуцепочечными или дуплексными, с одним или обоими концами, ковалентно связанными посредством двух палиндромных последовательностей ITR дикого типа (например, WO 2012/123430, патент США 9598703). Они позволяют избежать многих проблем AAV-опосредованной генной терапии, в смысле значительно большей трансгенной емкости, быстрого начала трансгенной экспрессии, и действительного распознавания иммунной системой пациента молекул ДНК как вируса, который необходимо вывести. Однако постоянная экспрессия трансгена может быть желательной не во всех случаях, а канонические ITR AAV дикого типа могут не быть оптимизированными для функций зкДНК. Следовательно, сохраняется важная неудовлетворенная потребность в контролируемых рекомбинантных ДНК-векторах с усовершенствованными характеристиками получения и/или экспрессии.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0011] Описанное в настоящем документе изобретение относится к невирусному бескапсидному ДНК-вектору с ковалентно-замкнутыми концами (называемому в настоящем документе «вектором с ДНК с замкнутыми концами», или «зкДНК-вектором»). Описанные в настоящем документе зкДНК-векторы представляют собой бескапсидные линейные дуплексные молекулы ДНК, образованные непрерывной цепью комплементарной ДНК с ковалентно-замкнутыми концами (линейная, непрерывная и бескапсидная структура), которые содержат последовательность инвертированного 5'-концевого повтора (ITR) и последовательность 3'-ITR, отличающиеся друг от друга, или асимметричные относительно друг друга.
[0012] Описанная в настоящем документе технология относится к зкДНК-вектору, содержащему по меньшей мере одну модифицированную последовательность инвертированного концевого повтора (ITR) AAV и экспрессируемый трансген. ЗкДНК-векторы согласно описанию в настоящем документе могут быть продуцированы в эукариотических клетках и, соответственно, свободны от прокариотических модификаций ДНК и загрязнения бактериальными эндотоксинами в клетках насекомых.
[0013] Согласно одному аспекту невирусные бескапсидные ДНК-векторы с ковалентно-замкнутыми концами предпочтительно представляют собой линейные дуплексные молекулы, и могут быть получены из векторного полинуклеотида, который кодирует гетерологичную нуклеиновую кислоту, функционально (т.е. с возможностью осуществления е функции) расположенную между двумя разными последовательностями инвертированных концевых повторов (ITR) (например, ITR AAV), отличающихся тем, что по меньшей мере один из указанных ITR содержит сайт концевого разрешения и сайт связывания белка репликации (RPS) (иногда называемый сайтом связывания репликативного белка), например, сайт связывания Rep; и один из ITR содержит делецию, инсерцию или замену относительно другого ITR, то есть, один из ITR асимметричен относительно другого ITR. Согласно одному варианту реализации по меньшей мере один из ITR представляет собой ITR AAV, например, ITR AAV дикого типа или модифицированный ITR AAV. Согласно одному варианту реализации по меньшей мере один из ITR представляет собой ITR, модифицированную относительно другого ITR - то есть зкДНК содержит ITR, которые являются асимметричными друг относительно друга. Согласно одному варианту реализации по меньшей мере один из ITR представляет собой нефункциональный ITR.
[0014] Согласно некоторым вариантам реализации указанный зкДНК-вектор содержит: (1) экспрессионную кассету, содержащую цис-регуляторный элемент, промотор и по меньшей мере один трансген; или (2) промотор, функционально связанный по меньшей мере с одним трансгеном, и (3) две самокомплементарных последовательности, например, ITR, фланкирующих указанную экспрессионную кассету, причем указанный зкДНК-вектор не ассоциирован с капсидным белком. Согласно некоторым вариантам реализации указанный зкДНК-вектор содержит две самокомплементарных последовательности, обнаруживаемых в геноме AAV, из которых по меньшей мере одна содержит функциональный Rep-связывающий элемент (RBE) (также иногда называемый в настоящем документе «RBS») и сайт концевого разрешения (trs) AAV, или функциональный вариант RBE, и один или более цис-регуляторных элементов, функционально связанных с трансгеном. Согласно некоторым вариантам реализации указанный зкДНК-вектор содержит дополнительные компоненты для регуляции экспрессии трансгена, например, регуляторные переключатели, которые описаны в настоящем документе в разделе «Регуляторные переключатели», для контроля и регуляции экспрессии указанного трансгена, и может включать регуляторный переключатель, например, «аварийный выключатель», обеспечивающий контролируемую клеточную смерть клетки, содержащей зкДНК-вектор.
[0015] Согласно некоторым вариантам реализации указанные две самокомплементарных последовательности могут представлять собой последовательности ITR из любого известного парвовируса, например, депендовируса, такого как AAV (например, AAV1-AAV12). Может применяться любой серотип AAV, в том числе, но не ограничиваясь перечисленным, модифицированная последовательность ITR AAV2, сохраняющая Rep-связывающий сайт (RBS), такой как 5'-GCGCGCTCGCTCGCTC-3' (SEQ ID NO: 531), и сайт концевого разрешения (trs), наряду с вариабельной палиндромной последовательностью, обеспечивающей образование шпилечной вторичной структуры. Согласно некоторым вариантам реализации указанный ITR представляет собой синтетическую последовательность ITR, сохраняющую функциональный Rep-связывающий сайт (RBS), такой как 5'-GCGCGCTCGCTCGCTC-3' (SEQ ID NO: 531), и сайт концевого разрешения (TRS), наряду с вариабельной палиндромной последовательностью, обеспечивающей образование шпилечной вторичной структуры. Согласно некоторым примерам модифицированная последовательность ITR сохраняет последовательность RBS, trs, и структуру и положение Rep-связывающего элемента, образующего концевую петлевую часть шпилечной вторичной структуры одной из ITR из соответствующей последовательности ITR AAV2 дикого типа.
[0016] Примеры последовательностей ITR для применения в зкДНК-векторах раскрыты в любой одной или более таблицах из 2-10А и 10В, или в SEQ ID NO: 2, 52, 101-499 и 545-547, или в частичных последовательностях ITR, представленных на фиг. 26А-26В. Согласно некоторым вариантам реализации указанные зкДНК-векторы не содержат ITR, который содержит любую последовательность, выбранную из SEQ ID NO: 500-529.
[0017] Согласно некоторым вариантам реализации зкДНК-вектор может содержать ITR с модификацией в ITR, соответствующей любым из модификаций в последовательностях ITR или частичных последовательностях ITR, представленных в любой одной или более таблицах из 2, 3, 4, 5, 6, 7, 8, 9, 10А и 10В в настоящем документе.
[0018] В иллюстративном примере согласно настоящему изобретению предложен вектор с ДНК с замкнутыми концами, содержащий промотор, функционально связанный с трансгеном, причем зкДНК не содержит капсидных белков и: (а) получена из зкДНК-плазмиды (например, см. примеры 1-2 и/или фиг. 1А-В), которая кодирует мутированный правый ITR AAV2 с тем же числом внутримолекулярных дуплексных пар оснований, что и SEQ ID NO: 2, или мутированный левый ITR AAV2 с тем же числом внутримолекулярных дуплексных пар оснований, что и SEQ ID NO: 51, в шпилечной вторичной конфигурации (предпочтительно, исключая делецию какой-либо концевой петли AAA или ТТТ в указанной конфигурации относительно указанных референсных последовательностей); и (b) идентифицирована как зкДНК с применением анализа для идентификации зкДНК путем электрофореза в агарозном геле в нативных и денатурирующих условиях согласно примеру 1. Примеры таких модифицированных последовательностей ITR приведены в таблицах 2, 3, 4, 5, 6, 7, 8, 9, 10А и 10В в настоящем документе.
[0019] Описанная в настоящем документе технология также относится к зкДНК-вектору, который может доставлять в целевую клетку и кодировать в целевой клетке один или более трансгенов, например, к зкДНК-вектору, который содержит мультицистронную последовательность, или к зкДНК-вектору, в который встроен трансген вместе с его естественным геномным контекстом (например, трансген, интроны и эндогенные нетранслируемые области). Трансгены могут представлять собой кодирующие белки транскрипты, некодирующие транскрипты, или и то, и другое. Указанный зкДНК-вектор может содержать несколько кодирующих последовательностей и неканонический сайт инициации трансляции или более чем один промотор для экспрессии кодирующих белки транскриптов, некодирующих транскриптов, или и того, и другого. Указанный трансген может содержать последовательность, кодирующую более одного белка, или может представлять собой последовательность некодирующего транскрипта. Экспрессионная кассета может содержать, например, более чем 4000 нуклеотидов, 5000 нуклеотидов, 10000 нуклеотидов или 20000 нуклеотидов, или 30000 нуклеотидов, или 40000 нуклеотидов или 50000 нуклеотидов, или любое количество в диапазоне от приблизительно 4000 до 10000 нуклеотидов, или от 10000 до 50000 нуклеотидов, или более чем 50000 нуклеотидов. Указанные зкДНК-векторы не имеют ограничений по размеру, как заключенные в капсид AAV-векторы, и, соответственно, позволяют обеспечить доставку экспрессионной кассеты большого размера для обеспечения эффективной экспрессии трансгенов. Согласно некоторым вариантам реализации указанный зкДНК-вектор лишен специфического прокариотического метилир ования.
[0020] Указанная экспрессионная кассета может также содержать участок внутренней посадки рибосомы (IRES) и/или 2А-элемент. Цис-регуляторные элементы включают, не ограничиваясь перечисленными, промотор, рибопереключатель, инсулятор, миРНК-регулируемый элемент, посттранскрипционный регуляторный элемент, тканеспецифический и клеточноспецифический промотор и энхансер. Согласно некоторым вариантам реализации указанный ITR может действовать как промотор для трансгена. Согласно некоторым вариантам реализации указанный зкДНК-вектор содержит дополнительные компоненты для регуляции экспрессии трансгена. Например, указанный дополнительный регуляторный компонент может представлять собой регуляторный переключатель согласно описанию в настоящем документе, в том числе, но не ограничиваясь указанным, «аварийный выключатель», который может обеспечивать убийство (киллинг) инфицированной зкДНК клетки при необходимости, и другие индуцируемые и/или репрессируемые элементы.
[0021] Описанная в настоящем документе технология также относится к новым способам доставки и эффективной и селективной экспрессии одного или более трансгенов с применением зкДНК-векторов. ЗкДНК-вектор может поглощаться клетками-хозяевами, а также транспортироваться в ядро в отсутствие капсида AAV. Кроме того, в описанных в настоящем документе зкДНК-векторах отсутствует капсид и, соответственно, они избегают иммунного ответа, который может возникать в ответ на капсид-содержащие векторы.
[0022] Аспекты настоящего изобретения относятся к способам получения зкДНК-векторов, описанных в настоящем документе. Другие варианты реализации относятся к зкДНК-вектору, полученному с применением способа, предложенного согласно настоящему изобретению. Согласно одному варианту реализации указанный бескапсидный невирусный ДНК-вектор (зкДНК-вектор) получают из плазмиды (называемой в настоящем документе «зкДНК-плазмидой»), содержащей полинуклеотидную матрицу экспрессионной конструкции, содержащую в указанном порядке: первый инвертированный 5'-концевой повтор (например, ITR AAV); экспрессионную кассету; и З'-ITR (например, ITR AAV), при этом по меньшей мере один из 5'- и 3'-ITR представляет собой модифицированный ITR, или если модифицированы оба ITR, 5' и 3', они содержат отличающиеся модификации и их последовательности не одинаковы.
[0023] зкДНК-вектор согласно описанию в настоящем документе может быть получен с применением ряда способов, известных специалисту в данной области техники, после прочтения настоящего описания. Например, полинуклеотидная матрица экспрессионной конструкции, используемая для получения зкДНК-векторов согласно настоящему изобретению, может представлять собой зкДНК-плазмиду (например, см. таблицу 12 или фиг. 10В), зкДНК-бакмиду и/или зкДНК-бакуловирус. Согласно одному варианту реализации указанная зкДНК-плазмида содержит сайт рестрикции для клонирования (например, SEQ ID NO: 7), функционально расположенный между ITR, куда может быть инсертирована экспрессионная кассета, содержащая, например, промотор, функционально связанный с трансгеном, например, репортерный ген и/или терапевтический ген). Согласно некоторым вариантам реализации зкДНК-векторы получают с полинуклеотидной матрицы (например, зкДНК-плазмиды, зкДНК-бакмиды, зкДНК-бакуло вируса), содержащей ITR, модифицированный по сравнению с соответствующей последовательностью фланкирующего ITR AAV3 или ITR AAV2 дикого типа, где модификация представлена чем-либо одним или более из делеции, инсерции и/или замены.
[0024] В пермиссивной клетке-хозяине в присутствии, например, Rep, полинуклеотидная матрица, содержащая по меньшей мере один модифицированный ITR, реплицируется с получением зкДНК-векторов. Получение зкДНК-вектора протекает в два этапа: во-первых, эксцизия («спасение») матрицы из остова матрицы (например, зкДНК-плазмиды, зкДНК-бакмиды, генома зкДНК-бакуловируса и т.п.) белками Rep, и во-вторых, опосредованная Rep репликация вырезанного зкДНК-вектора. Белки Rep и сайты связывания Rep различных серотипов AAV хорошо известны специалистам в данной области техники. Специалисту известно, как выбрать белок Rep из серотипа, который связывает и реплицирует последовательность нуклеиновой кислоты, на основании по меньшей мере одного функционального ITR. Например, если репликативно-компетентный ITR взят из серотипа AAV 2, соответствующий Rep должен быть взят из серотипа AAV, который работает с указанным серотипом, например, ITR AAV2 с Rep AAV2 или AAV4, но не с Rep AAV5, который не будет работать. После репликации зкДНК-вектор с ковалентно замкнутыми концами продолжает накапливаться в пермиссивных клетках, и зкДНК-вектор предпочтительно достаточно стабилен во времени в присутствии белка Rep в стандартных условиях для репликации, например, чтобы накапливаться в количестве по меньшей мере 1 пг/клетку, предпочтительно по меньшей мере 2 пг/клетку, предпочтительно по меньшей мере 3 пг/клетку, более предпочтительно по меньшей мере 4 пг/клетку, еще более предпочтительно по меньшей мере 5 пг/клетку.
[0025] Соответственно, согласно одному аспекту настоящее изобретение относится к процессу, включающему следующие этапы: а) инкубация популяции клеток-хозяев (например, клеток насекомых), несущих полинуклеотидную матрицу экспрессионной конструкции (например, зкДНК-плазмиду, зкДНК-бакмиду и/или зкДНК-бакуловирус), которая не содержит кодирующих последовательностей вирусного капсида, в присутствии белка Rep в условиях, эффективных для, и на протяжении времени, достаточного для того чтобы индуцировать продуцирование указанного зкДНК-вектора в клетках-хозяевах, причем указанные клетки-хозяева не содержат кодирующих вирусный капсид последовательностей; и Ь) сбор и выделение зкДНК-вектора из клеток-хозяев. Присутствие белка Rep индуцирует репликацию векторного полинуклеотида с модифицированной ITR, с получением зкДНК-вектора в клетке-хозяине. Однако вирусные частицы (например, вирионы AAV) не экспрессируются. Соответственно, нет обусловленных вирионами ограничений по размеру.
[0026] Наличие зкДНК-вектора, выделенного из клеток-хозяев, может быть подтверждено путем расщепления ДНК, выделенной из клетки-хозяина, рестрикционным ферментом, имеющим один сайт распознавания на указанном зкДНК-векторе, и анализа расщепленного ДНК-материала на денатурирующем и неденатурирующем гелях для подтверждения присутствия характеристических полос линейной и непрерывной ДНК, отличающихся от полос линейной и прерывистой ДНК.
[0027] Согласно некоторым вариантам реализации настоящее изобретение может быть описано любым из следующих пунктов:
1. Невирусный бескапсидный ДНК-вектор с ковалентно-замкнутыми концами (зкДНК-вектор), отличающийся тем, что указанный зкДНК-вектор содержит по меньшей мере одну гетеро логичную нуклеотидную последовательность, функционально расположенную между последовательностями асимметричных инвертированных концевых повторов (асимметричными ITR), причем по меньшей мере один из асимметричных ITR содержит функциональный сайт концевого разрешения и сайт связывания Rep.
2. ЗкДНК-вектор по пункту 1, где указанный зкДНК-вектор при расщеплении рестрикционным ферментом, имеющим один сайт распознавания на указанном зкДНК-векторе, и анализируемый с применением как нативного, так и денатурирующего гель-электрофореза, демонстрирует характеристические полосы линейной и непрерывной ДНК, отличающиеся от полос линейной и прерывистой контрольной ДНК.
3. ЗкДНК-вектор по пунктам 1 или 2, где одна или более из последовательностей асимметричных ITR взяты из вируса, выбранного из парвовируса, депендовируса и аденоассоциированного вируса (AAV).
4. ЗкДНК-вектор по пункту 3, где указанные асимметричные ITR взяты из разных вирусных серотипов.
5. ЗкДНК-вектор по пункту 4, где указанные один или более асимметричных ITR взяты из серотипа AAV, выбранного из AAV1, AAV2, AAV3, AAV4, AAV5, AAV6, AAV7, AAV8, AAV9, AAV10, AAV11 и AAV12.
6. ЗкДНК-вектор по любому из пунктов 1-3, где одна или более из последовательностей асимметричных ITR являются синтетическими.
7. ЗкДНК-вектор по любому из пунктов 1-3 и 6, где один или более из указанных ITR не является ITR дикого типа.
8. ЗкДНК-вектор по любому из пунктов 1-7, где один или оба асимметричных ITR модифицирован(ы) делецией, инсерцией и/или заменой по меньшей мере одна из областей ITR, выбранных из А, А', В, В', С, С', D и D'. Согласно некоторым вариантам реализации один или оба асимметричных ITR могут включать делецию, инсерцию и/или замену в любой комбинации областей В, В', С или С' согласно описанию в таблице 1. Согласно некоторым вариантам реализации один или оба асимметричных ITR могут включать делецию, инсерцию и/или замену в области В, и/или области В', и/или области С, и/или области С'. Согласно некоторым вариантам реализации один или оба асимметричных ITR могут содержать одну или более делеций, инсерций и/или замен в области А, и/или области А', и/или области В, и/или области В', и/или области С, и/или области С', и/или области D, и/или области D'. Например, согласно некоторым вариантам реализации модифицированный ITR может включать удаление или делецию всего конкретного плеча, например, всего плеча А-А' или его части, или всего плеча В-В' или его части, или всего плеча С-С' или его части, или, как вариант, удаление 1, 2, 3, 4, 5, 6, 7, 8, 9 или более пар оснований, образующих стебель петли, при условии, что все еще присутствует последняя петля наверху стебля (например, одно плечо) (например, см. ITR-6). Согласно некоторым вариантам реализации модифицированный ITR может включать удаление 1, 2, 3, 4, 5, 6, 7, 8, 9 или более пар оснований из плеча В-В'. Согласно некоторым вариантам реализации модифицированный ITR может включать удаление 1, 2, 3, 4, 5, 6, 7, 8, 9 или более пар оснований из плеча С-С'. Согласно некоторым вариантам реализации модифицированный ITR может включать удаление 1, 2, 3, 4, 5, 6, 7, 8, 9 или более пар оснований из плеча С-С' и удаление 1, 2, 3, 4, 5, 6, 7, 8, 9 или более пар оснований из плеча В-В'. Предусмотрена любая комбинация удаления пар оснований. Согласно некоторым вариантам реализации в модифицированном ITR отсутствует плечо В-В'. Согласно некоторым вариантам реализации в модифицированном ITR отсутствует плечо С-С'.
9. ЗкДНК-вектор по пункту 8, где указанная делеция, инсерция, и/или замена приводит к делеций всей или части структуры «петля на стебле», в норме образуемой областями А, А', В, В' С или С'. Например, согласно некоторым вариантам реализации 1, 2, 3, 4, 5, 6, 7, 8, 9 или более комплементарных пар оснований удаляют из каждой из частей С и С' плеча С-С' таким образом, что происходит усечение плеча С-С', и/или 1, 2, 3, 4, 5, 6, 7, 8, 9 или более комплементарных пар оснований удаляют из каждой из частей В и В' плеча В-В', таким образом, что происходит усечение плеча С-С' и/или плеча В'-В. Согласно альтернативным вариантам реализации 1, 2, 3, 4, 5, 6, 7, 8, 9 или более пар оснований удаляют из части С плеча С-С' таким образом, что остается только часть С' плеча. Согласно альтернативным вариантам реализации 1, 2, 3, 4, 5, 6, 7, 8, 9 или более пар оснований удаляют из части С' плеча С-С' таким образом, что остается только часть С плеча. Согласно некоторым вариантам реализации 1, 2, 3, 4, 5, 6, 7, 8, 9 или более пар оснований удаляют из части В плеча В-В' таким образом, что остается только часть В' плеча. Согласно альтернативным вариантам реализации 1, 2, 3, 4, 5, 6, 7, 8, 9 или более пар оснований удаляют из части В' плеча В-В' таким образом, что остается только часть В плеча. Согласно некоторым вариантам реализации при любой делеции в области С, области С', области В или области В' все же сохраняется концевая петля «петли на стебле». Согласно некоторым вариантам реализации концевая петля содержит по меньшей мере три аминокислоты. Согласно некоторым вариантам реализации концевая петля плеча С-С' и/или плеча В-В' содержит по меньшей мере три последовательных ТТТ или три последовательных AAA.
10. ЗкДНК-вектор по пункту 8 или пункту 9, где один или оба асимметричных ITR модифицированы делецией, инсерцией и/или заменой, которая приводит к делеции всей или части структуры «петля на стебле», в норме образуемой областями В и В'.
11. ЗкДНК-вектор по любому из пунктов 8-10, где один или оба асимметричных ITR модифицированы делецией, инсерцией и/или заменой, которая приводит к делеции всей или части структуры «петля на стебле», в норме образуемой областями С и С'.
12. ЗкДНК-вектор по пункту 10 или пункту 11, где один или оба асимметричных ITR модифицированы делецией, инсерцией и/или заменой, которая приводит к делеции части структуры «петля на стебле», в норме образуемой областями В и В', и/или частью структуры «петля на стебле», в норме образуемой областями С и С'.
13. ЗкДНК-вектор по любому из пунктов 1-12, где один или оба асимметричных ITR содержат одну структуру «петля на стебле» в области, которая в норме содержит первую структуру «петля на стебле», образованную областями В и В', и вторую структуру «петля на стебле», образованную областями С и С'.
14. ЗкДНК-вектор по пункту 13, где один или оба асимметричных ITR содержат один «стебель» и две «петли» в области, которая в норме содержит первую структуру «петля на стебле», образованную областями В и В', и вторую структуру «петля на стебле», образованную областями С и С'.
15. ЗкДНК-вектор по пункту 13 или пункту 14, где один или оба асимметричных ITR содержат один «стебель» и одну «петлю» в области, которая в норме содержит первую структуру «петля на стебле», образованную областями В и В', и вторую структуру «петля на стебле», образованную областями С и С'.
16. ЗкДНК-вектор по любому из пунктов 1-15, где по меньшей мере один асимметричный ITR представляет собой модифицированный ITR AAV2, содержащий нуклеотидную последовательность, выбранную из: ITR на фиг. 26А или 26В, SEQ ID NO: 101-499 или 545-547, ITR, имеющей последовательность, по меньшей мере на 95% идентичную последовательности ITR на фиг.26А или 26 В, и ITR, имеющей последовательность, по меньшей мере на 95% идентичную SEQ ID NO: 101-499 и 545-547.
17. ЗкДНК-вектор по любому из пунктов 1-16, где по меньшей мере один асимметричный ITR представляет собой модифицированный ITR AAV2, содержащий нуклеотидную последовательность SEQ ID NO. 2, 52, 63 или 64, или нуклеотидную последовательность, по меньшей мере на 95% идентичную SEQ ID NO:. 2, 52, 63 или 64.
18. ЗкДНК-вектор по любому из пунктов 1-16, где 5'-ITR представляет собой ITR AAV дикого типа, а З'-ITR содержит последовательность, выбранную из SEQ ID NO: 2, 64, 102, 104, 106, 108, 110, 112, 114, 116, 118, 120, 122, 124, 126, 128,130, 132, 134, 469-483 и 546, и последовательностей ITR, показанных на фиг. 26А, и последовательностей, по меньшей мере на 95% идентичных любым из указанных выше последовательностей.
19. ЗкДНК-вектор по любому из пунктов 1-16, где 3'-ITR представляет собой ITR AAV дикого типа, a 5'-ITR содержит последовательность, выбранную из SEQ ID NO: 52, 63, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 484^199, 545 и 547, и последовательностей ITR, показанных на фиг. 26В, и последовательностей, по меньшей мере на 95% идентичных любым из указанных выше последовательностей.
20. ЗкДНК-вектор по любому из пунктов 1 16, где 5'-ITR содержит последовательность, выбранную из SEQ ID NO: 52, 63, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 484-499, 545 и 547, и последовательностей ITR, показанных на фиг. 26В, и последовательностей, по меньшей мере на 95% идентичных любым из указанных выше последовательностей; а 3'-ITR содержит последовательность, выбранную из SEQ ID NO: 2, 64, 102, 104, 106, 108, 110, 112, 114, 116, 118, 120, 122, 124, 126, 128,130, 132, 134, 469-483 и 546, и последовательностей ITR, показанных на фиг. 26А, и последовательностей, по меньшей мере на 95% идентичных любым из указанных выше последовательностей.
21. ЗкДНК-вектор по пункту 1, содержащий по меньшей мере два асимметричных ITR, выбранных из: (a) SEQ ID NO: 1 и SEQ ID NO: 52; и (Ъ) SEQ ID NO: 2 и SEQ ID NO: 51.
22. ЗкДНК-вектор по пункту 1, содержащий пару асимметричных ITR, выбранных из: (а) SEQ ID NO: 1 и SEQ ID NO: 52; и (Ъ) SEQ ID NO: 2 и SEQ ID NO: 51.
23. ЗкДНК-вектор по любому из пунктов 1-20, где один или оба асимметричных ITR содержат последовательность, отличную от SEQ ID NO: 2, 52, 63 64, 113, 114 и 557.
24. ЗкДНК-вектор по любому из пунктов 1-24, где вся гетерологичная нуклеотидную последовательность или ее часть находится под контролем по меньшей мере одного регулятор ного переключателя.
25. ЗкДНК-вектор по пункту 24, где по меньшей мере один регуляторный переключатель выбирают из любого регуляторного переключателя или комбинации регуляторных переключателей, перечисленных в таблице 11 или в разделе «Регуляторные переключатели» в настоящем документе. Например, регуляторный переключатель служит для точной настройки экспрессии гетерологичной последовательности нуклеотидов, например, трансгена, и может выполнять, согласно некоторым вариантам реализации, функцию биологического сдерживания зкДНК-вектора. Согласно некоторым вариантам реализации регуляторный переключатель представляет собой переключатель, действующий по принципу «включено/выключено» (двухпозиционный). Без связи с конкретной теорией, двухпозиционный переключатель сконструирован таким образом, чтобы начинать или останавливать (т.е. прекращать) экспрессию гетерологичной последовательности нуклеотидов или трансгена, экспрессируемых с зкДНК-вектора контролируемым и регулируемым образом. Согласно некоторым вариантам реализации указанный регуляторный переключатель представляет собой «аварийный выключатель», который может заставлять клетку, содержащую указанный зкДНК-вектор, переходить к запрограммированной клеточной смерти после активации переключателя. Согласно некоторым вариантам реализации указанный регуляторный переключатель выбирают из чего-либо из перечисленного: бинарный переключатель (например, индуцируемые промоторы, кофакторы или экзогенные агенты дерепрессируют транскрипцию), низкомолекулярный регуляторный переключатель (например, индуцируемая лекарственным средством, или пролекарства активируют или останавливают транскрипцию), регуляторный переключатель с «паролем» (например, комбинацией условий, необходимых для протекания трансгенной экспрессии и/или репрессии), регуляторный переключатель на основе нуклеиновой кислоты (например, механизм на основе нуклеиновой кислоты для контроля экспрессии и/или репрессии), посттрансляционный и/или посттранскрипционный регуляторный переключатель (например, трансгены, экспрессируемые с элементами ответа на сигнал (SRE) или дестабилизирующие домены (DD), предотвращающими функциональность трансгенов до посттрансляционной модификации) или «аварийный выключатель» (например, переключатель для индукции запрограммированной гибели клеток в качестве способа окончательного удаления введенного зкДНК-вектора из системы субъекта).
26. ЗкДНК-вектор по любому из пунктов 1-25, где указанный вектор находится в нано носителе.
27. ЗкДНК-вектор по пункту 26, где указанный наноноситель содержит липидную наночастицу (ЛНЧ).
28. Невирусный бескапсидный ДНК-вектор с ковалентно-замкнутыми концами (зкДНК-вектор) по любому из пунктов 1-25, который получают способом, включающим следующие этапы: (а) инкубация популяции клеток насекомых, несущих экспрессионную конструкцию зкДНК, в присутствии по меньшей мере одного белка Rep, причем указанная экспрессионная конструкция зкДНК кодирует зкДНК-вектор, в условиях, эффективных для, и на протяжении времени, достаточного для того чтобы индуцировать продуцирование указанного зкДНК-вектора в клетках насекомых; и (b) выделение указанного зкДНК-вектора из клеток насекомых.
29. ЗкДНК-вектор по пункту 28, причем указанную экспрессионную конструкцию зкДНК выбирают из зкДНК-плазмиды, зкДНК бакмиды и зкДНК бакуловируса.
30. ЗкДНК-вектор по пункту 28 или пункту 29, где указанная клетка насекомого экспрессирует по меньшей мере один белок Rep.
31. ЗкДНК-вектор по пункту 30, где по меньшей мере один белок Rep взят из вируса, выбранного из парвовируса, депендовируса и аденоассоциированного вируса (AAV).
32. ЗкДНК-вектор по пункту 31, где по меньшей мере один белок Rep взят из серотипа AAV, выбранного из AAV1, AAV2, AAV3, AAV4, AAV5, AAV6, AAV7, AAV8, AAV9, AAV10, AAV11 и AAV12.
33. Экспрессионная конструкция зкДНК, которая кодирует зкДНК-вектор по любому из пунктов 1-25.
34. Экспрессионная конструкция зкДНК по пункту 33, которая представляет собой зкДНК-плазмиду, зкДНК-бакмиду или зкДНК-бакуловирус.
35. Клетка-хозяин, содержащая экспрессионную конструкцию зкДНК по пункту 33 или пункту 34.
36. Клетка-хозяин по пункту 35, которая экспрессирует по меньшей мере один белок Rep.
37. Клетка-хозяин по пункту 36, отличающаяся тем, что по меньшей мере один белок Rep взят из вируса, выбранного из парвовируса, депендовируса и аденоассоциированного вируса (AAV).
38. Клетка-хозяин по пункту 37, отличающаяся тем, что по меньшей мере один белок Rep взят из серотипа AAV, выбранного из AAV1, AAV2, AAV3, AAV4, AAV5, AAV6, AAV7, AAV8, AAV9, AAV10, AAV11 и AAV12.
39. Клетка-хозяин по любому из пунктов 35-38, представляющая собой клетку насекомого.
40. Клетка-хозяин по пункту 39, представляющая собой клетку Sf9.
41. Способ получения зкДНК-вектора, включающий: (а) инкубацию клетки-хозяина по любому из пунктов 35-40 в условиях, эффективных для, и на протяжении времени, достаточного для того чтобы индуцировать продуцирование зкДНК-вектора; и (b) выделение указанной зкДНК из клеток-хозяев.
42. Способ лечения, предотвращения, облегчения, мониторинга или диагностики заболевания или нарушения у субъекта, включающий: введение нуждающемуся в этом субъекту композиции, содержащей зкДНК-вектор по любому из пунктов 1-25, где выбирают по меньшей мере одну гетерологичную нуклеотидную последовательность для лечения, предотвращения, облегчения, диагностики или мониторинга указанного заболевания или нарушения.
43. Способ по пункту 42, где указанная по меньшей мере одна гетерологичная нуклеотидную последовательность при транскрипции или трансляции корректирует аномальное количество эндогенного белка у указанного субъекта.
44. Способ по пункту 42, где указанная по меньшей мере одна гетер ологичная нуклеотидную последовательность при транскрипции или трансляции корректирует аномальную функцию или активность эндогенного белка или пути у указанного субъекта.
45. Способ по любому из пунктов 42-44, где указанная по меньшей мере одна гетерологичная нуклеотидную последовательность кодирует или содержит нуклеотидную молекулу, выбранную из РНК-интерференции (RNAi), миРНК, микроРНК, днкРНК и антисмыслового олиго- или полинуклеотида.
46. Способ по любому из пунктов 42-44, где указанная по меньшей мере одна гетерологичная нуклеотидную последовательность кодирует белок.
47. Способ по пункту 42, где указанная по меньшей мере одна гетерологичная нуклеотидную последовательность кодирует маркерный белок (например, репортерный белок).
48. Способ по любому из пунктов 42-46, где указанная по меньшей мере одна гетерологичная нуклеотидную последовательность кодирует агонист или антагонист эндогенного белка или пути, ассоциированного с указанным заболеванием или нарушением.
49. Способ по любому из пунктов 42-46, где указанная по меньшей мере одна гетерологичная нуклеотидную последовательность кодирует антитело.
50. Способ по любому из пунктов 42-49, где указанное заболевание или нарушение выбрано из: метаболического заболевания или нарушения, заболевания или нарушения ЦНС, глазного заболевания или нарушения, заболевания или нарушения системы крови, заболевания или нарушения печени, иммунного заболевания или нарушения, инфекционного заболевания, мышечного заболевания или нарушения, рака, а также заболевания или нарушения, основанного на аномальный уровень и/или функция генного продукта.
51. Способ по пункту 50, где указанное метаболическое заболевание или нарушение выбрано из диабета, нарушения лизосомального накопления, мукополисахаридозного нарушения, заболевания или нарушения цикла мочевины, и заболевания или нарушения накопления гликогена.
52. Способ по пункту 51, где указанное нарушение лизосомального накопления выбрано из болезни Гоше, болезни Помпе, метахроматической лейкодистрофии (МЛД), фенилкетонурии (ФКУ) и болезни Фабри.
53. Способ по пункту 51, где указанное заболевание или нарушение цикла мочевины представляет собой недостаточность орнитинтранскарбамилазы (ОТС).
54. Способ по пункту 51, где указанное мукополисахаридозное нарушение выбрано из синдрома Слая, синдрома Гурлер, синдрома Шейе, синдрома Гурлер-Шейе, синдрома Гунтера, синдрома Санфилиппо, синдрома Моркио и синдрома Марото-Лами.
55. Способ по пункту 50, где указанное заболевание или нарушение ЦНС выбирают из болезни Альцгеймера, болезни Паркинсона, болезни Гентингтона, болезни Канавана, болезни Лея, болезни Рефсума, синдрома Туретта, первичного бокового склероза, амиотрофического бокового склероза, прогрессирующей мышечной атрофии, болезни Пика, мышечной дистрофии, рассеянного склероза, тяжелой миастении, болезни Бинсвангера, травмы в результате повреждения спинного мозга или головы, болезни Тея-Сакса, болезни Леша-Нихена, эпилепсии, церебральных инфарктов, психиатрических нарушений, шизофрении, лекарственной или наркотической зависимости, неврозов, психоза, деменции, паранойи, связанного с дефицитом внимания нарушения, нарушений сна, связанных с болью нарушений, связанных с питанием или массой тела нарушений, а также раковых заболеваний и опухолей ЦНС.
56. Способ по пункту 50, где указанное глазное заболевание или нарушение выбрано из офтальмологических нарушений, затрагивающих сетчатку, задний путь и/или зрительный нерв.
57. Способ по пункту 55, где указанное офтальмологическое нарушение, затрагивающее сетчатку, задний путь и/или зрительный нерв, выбрано из диабетической ретинопатии, макулярной дегенерации, в том числе возрастной макулярной дегенерации, географической атрофии, сосудистой или «влажной» макулодистрофии, глаукомы, увеита, пигментного ретинита, болезни Штаргардта, врожденного амавроза Лебера (LCA), синдрома Ушера, эластической псевдоксантомы (РХЕ), Х-сцепленного пигментного ретинита (XLRP), Х-сцепленного расслоения сетчатки (XLRS), хороидеремии, врожденной нейропатии зрительного нерва Лебера (LHON), ахроматопсии, палочко-колбочковой дистрофии, эндотелиальной дистрофии роговицы Фукса, диабетического макулярного отека; и раковых заболеваний и опухолей глаз.
58. Способ по пункту 50, где указанное заболевание или нарушение системы крови выбрано из гемофилии А, гемофилии В, талассемии, анемии и рака крови.
59. Способ по пункту 50, где указанное заболевание или нарушение печени выбрано из прогрессирующего семейного внутрипеченочного холестаза (ПСВХ), и раковых заболеваний и опухолей печени.
60. Способ по пункту 42, где указанное заболевание или нарушение представляет собой муковисцедоз.
61. Способ по пунктам 42-60, где указанный зкДНК-вектор вводят в комбинации с фармацевтически приемлемым носителем.
62. Способ доставки терапевтического белка субъекту, включающий введение субъекту композиции, содержащей зкДНК-вектор по любому из пунктов 1-25, где по меньшей мере одна гетерологичная нуклеотидную последовательность кодирует терапевтический белок.
63. Способ по пункту 62, где указанный терапевтический белок представляет собой терапевтическое антитело.
64. Способ по пункту 62, где указанный терапевтический белок выбирают из фермента, эритропоэтина, ангиостатина, эндостатина, супероксиддисмутазы, глобина, лептина, каталазы, тирозингидроксилазы, цитокина, регулятора трансмембранной проводимости при муковисцедозе (CFTR), пептидного фактора роста и гормона.
65. Набор, содержащий зкДНК-вектор по любому из пунктов 1-25 и наноноситель, упакованные в контейнер с вкладышем в упаковку.
66. Набор для получения зкДНК-вектора, содержащий экспрессионную конструкцию, содержащую по меньшей мере один сайт рестрикции для инсерции по меньшей мере одной гетерологичной последовательности нуклеотидов, или регуляторного переключателя, или и первого, и второго, причем указанный по меньшей мере один сайт рестрикции функционально расположен между последовательностями асимметричных инвертированных концевых повторов (асимметричными ITR), и по меньшей мере один из асимметричных ITR содержит функциональный сайт концевого разрешения и сайт связывания Rep.
67. Набор по пункту 66, который подходит для получения зкДНК-вектора по любому из пунктов 1-25.
68. Набор по пункту 66 или пункту 67, дополнительно содержащий популяцию клеток насекомых, которая не содержит кодирующих последовательностей вирусного капсида, где в присутствии белка Rep может быть индуцировано продуцирование зкДНК-вектора.
69. Набор по любому из пунктов 66-68, дополнительно содержащий вектор, содержащий последовательность полинуклеотидов, которая кодирует по меньшей мере один белок Rep, где указанный вектор подходит для экспрессии указанного по меньшей мере одного белка Rep в клетке насекомого.
[0028] Согласно некоторым вариантам реализации один аспект описанной в настоящем документе технологии относится к невирусному бескапсидному ДНК-вектору с ковалентно-замкнутыми концами (зкДНК-вектору), отличающемуся тем, что он содержит по меньшей мере одну гетерологичную нуклеотидную последовательность, функционально расположенную между последовательностями асимметричных инвертированных концевых повторов (асимметричными ITR), причем по меньшей мере один из асимметричных ITR содержит функциональный сайт концевого разрешения и сайт связывания Rep, и, необязательно, указанная гетерологичная последовательность нуклеиновой кислоты кодирует трансген, и указанный вектор не заключен в вирусный капсид.
[0029] Указанные и другие аспекты настоящего изобретения более подробно описаны ниже.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0030] На фиг. 1А изображен пример структуры зкДНК-вектора. Согласно указанному варианту реализации пример зкДНК-вектора включает экспрессионную кассету, содержащую промотор CAG, WPRE и BGHpA. Открытая рамка считывания (ORF), кодирующая трансген люциферазы, встроена в сайт клонирования (R3/R4) между промотором CAG и WPRE. Экспрессионная кассета фланкирована двумя инвертированными концевыми повторами (ITR) - ITR AAV2 дикого типа в начале (на 5'-конце) и модифицированным ITR в конце (на 3'-конце) экспрессионной кассеты, соответственно, указанные два ITR, фланкирующие экспрессионную кассету, являются асимметричными друг относительно друга.
[0031] На фиг. 1В изображен пример структуры зкДНК-вектора с экспрессионной кассетой, содержащей промотор С AG, WPRE и BGHpA. Открытая рамка считывания (ORF), кодирующая трансген люциферазы, встроена в сайт клонирования между промотором CAG и WPRE. Экспрессионная кассета фланкирована двумя инвертированными концевыми повторами (ITR) - модифицированным ITR в начале (на 5'-конце) и ITR дикого типа в конце (на 3'-конце) экспрессионной кассеты.
[0032] На фиг. 1С изображен пример структуры зкДНК-вектора с экспрессионной кассетой, содержащей энхансер/промотор, открытую рамку считывания (ORF) для инсерции трансгена, посттранскрипционный элемент (WPRE) и поли(А)-сигнал. Открытая рамка считывания (ORF) позволяет инсертировать трансген в сайт клонирования между промотором CAG и WPRE. Экспрессионная кассета фланкирована двумя инвертированными концевыми повторами (ITR), которые являются асимметричными друг относительно друга; модифицированный ITR в начале (на 5'-конце) и модифицированный ITR в конце (на 3'-конце) экспрессионной кассеты, при этом и 5'-ITR, и 3TTR модифицированы, но содержат разные модификации (т.е. не содержат одинаковые модификации).
[0033] На фиг. 2А представлена Т-образная структура «петля на стебле» левого ITR дикого типа AAV2 (SEQ ID NO: 538) с идентифицированными плечом А-А', плечом В-В', плечом С-С', двумя сайтами связывания Rep (RBE и RBE'), а также показан сайт концевого разрешения (trs). RBE содержит ряд 4 дуплексных тетрамеров, которые, как полагают, взаимодействуют либо с Rep 78, либо с Rep 68. Кроме того, также RBE' предположительно взаимодействует с комплексом Rep, собранным на ITR дикого типа или мутированном ITR в указанной конструкции. Области D и D' содержат сайты связывания транскрипционных факторов и другие консервативные структуры. На фиг. 2В показана предполагаемая Rep-катализируемая никирующая и лигирующая активность в левом ITR дикого типа (SEQ ID NO: 539), в том числе Т-образная структура типа «петля на стебле» левого ITR дикого типа AAV2 с идентифицированными плечом А-А', плечом В-В', плечом С-С', двумя сайтами связывания Rep (RBE и RBE') а также показан сайт концевого разрешения (trs) и область D и D', содержащие несколько сайтов связывания транскрипционных факторов и другие консервативные структуры.
[0034] На фиг. 3А представлена первичная структура (последовательность полинуклеотидов) (слева) и вторичная структура (справа) RBE-содержащих частей плеча А-А', и плечо С-С' и плечо В-В' левого ITR дикого типа AAV2 (SEQ ID NO: 540). На фиг. 3В показан пример последовательности мутированного ITR (также называемого модифицированным ITR) для левого ITR. Показана первичная структура (слева) и предсказанная вторичная структура (справа) RBE-части плеча А-А', плечо С и плечо В-В' из примера мутированного левого ITR (ITR-1, левый) (SEQ ID NO: 113). На фиг. 3С показана первичная структура (слева) и вторичная структура (справа) RBE-содержащей части петли А-А', и плечи В-В' и С-С' правого ITR AAV2 дикого типа (SEQ ID NO: 541). На фиг. 3D показан пример правого модифицированного ITR. Показана первичная структура (слева) и предсказанная вторичная структура (справа) RBE-содержащей части плеча А-А', В-В' и плечо С из примера мутантного правого ITR (ITR-1, правый) (SEQ ID NO: 114). Может применяться любая комбинация левого и правого ITR (например, ITR AAV2 или другого вирусного серотипа, или синтетические ITR), при условии, что левый ITR асимметричен относительно правого ITR или отличается от него. На каждой из фиг. 3А-3D последовательности полинуклеотидов относятся к последовательности, используемой в плазмиде или бакмиде/ геноме бакуло вируса, использованных для получения зкДНК согласно описанию в настоящем документе. Также на каждой из фиг. 3А-3D приведены соответствующие вторичные структуры зкДНК, полученные на основании конфигураций зкДНК-вектора в плазмиде или бакмиде/ геноме бакуловируса и предсказанных значений свободной энергии Гиббса.
[0035] На фиг. 4А приведено схематическое изображение апстрим (предшествующего) - процесса для получения инфицированных бакуловирусом клеток насекомых (ВИС), которые подходят для получения зкДНК способом, схематически представленным на фиг. 4В. На фиг. 4В схематически представлен пример способа получения зкДНК, а на фиг. 4С показан биохимический способ и процесс подтверждения получения зкДНК-вектора. На фиг. 4D и фиг. 4Е приведены схематические изображения, описывающие процесс идентификации присутствия зкДНК в ДНК, собранной из клеточных осадков, полученных в ходе процессов получения зкДНК на фиг. 4В. На фиг. 4Е показана ДНК с прерывистой структурой. ЗкДНК может быть разрезана рестрикционной эндонуклеазой, имеющей один сайт распознавания на зкДНК-векторе, с получением двух фрагментов ДНК разного размера (1 т.п.о. и 2 т.п.о.) как в нейтральных, так и в денатурирующих условиях. На фиг. 4Е также показана зкДНК, имеющая линейную и непрерывную структуру. Указанный зкДНК-вектор может быть разрезан рестрикционной эндонуклеазой с получением двух фрагментов ДНК, мигрирующих в виде отрезков с 1 т.п.о. и 2 т.п.о. в нейтральных условиях, однако в денатурирующих условиях цепи остаются соединенными и продуцируют одиночные цепи, мигрирующие в виде отрезков с 2 т.п.о. и 4 т.п.о. На фиг. 4D схематически представлены ожидаемые полосы для примера зкДНК, нерасщепленной или расщепленной рестрикционной эндонуклеазой, а затем подвергнутой электрофорезу либо на нативном, либо на денатурирующем геле. На самом левом схематическом изображении показан нативный гель с несколькими полосами, предполагающими, что в дуплексной и неразрезанной форме зкДНК существует по меньшей мере в мономерном и димерном состояниях, которые видны в виде более быстро мигрирующего мономера меньшего размера и медленнее мигрирующего димера, размер которого в 2 раза больше размера мономера. На втором слева схематическом изображении показано, что при разрезании зкДНК рестрикционной эндонуклеазой исходные полосы пропадают и появляются полосы более быстро мигрирующих фрагментов (например, меньшего размера), соответствующие ожидаемым размерам фрагментов, остающихся после расщепления. В денатурирующих условиях исходная дуплексная ДНК является одноцепочечной и мигрирует как соединение в два раза большего размера по сравнению с тем, что наблюдается на нативном геле, поскольку комплементарные цепи ковалентно связаны. Соответственно, на втором схематическом изображении справа расщепленная зкДНК демонстрирует аналогичное распределение полос по сравнению с тем, что наблюдается на нативном геле, однако полосы соответствуют миграции фрагментов, размер которых в два раза больше их эквивалентов в нативном геле. На самом правом схематическом изображении показано, что неразрезанная зкДНК в денатурирующих условиях мигрирует в виде одноцепочечного раскрытого кольца, и, соответственно, размер наблюдаемых полос в два раза больше размера наблюдаемых в нативных условиях при нераскрытом кольце. На указанном чертеже «т.п.о.» относится к относительному размеру нуклеотидных молекул, основанному, в зависимости от контекста, либо на длине нуклеотидной цепи (например, для одно цепочечных молекул, наблюдаемых в денатурирующих условиях), либо на числе пар оснований (например, для двуцепочечных молекул, наблюдаемых в нативных условиях).
[0036] На фиг. 5 приведено иллюстративное изображение прогона через денатурирующий гель примеров зкДНК-векторов с (+) или без (-) расщепления эндонуклеазами (EcoRI для зкДНК-конструкций 1 и 2; BamH1 для зкДНК-конструкций 3 и 4; SpeI для зкДНК-конструкций 5 и 6; и XhoI для зкДНК-конструкций 7 и 8). Размеры для полос, выделенных звездочкой, определены и приведены в нижней части чертежа.
[0037] На фиг. 6А приведены результаты анализа экспрессии белка in vitro, измеряющего активность люциферазы (ось Y, RQ (Luc)) в клетках HEK293 через 48 часов после трансфекции для 400 нг (черный цвет), 200 нг (серый цвет) или 100 нг (белый цвет) конструкций, идентифицированных на оси X (конструкция-1, конструкция-3, конструкция-5, конструкция-7 (таблица 12). На фиг. 6В представлена активность люциферазы (ось Y, RQ (Luc)), измеренная в клетках HEK293 через 48 часов после трансфекции 400 нг (черный цвет), 200 нг (серый цвет), или 100 нг (белый цвет) конструкций, идентифицированных на оси X (конструкция-2, конструкция-4, конструкция-6, конструкция-8) (таблица 12). Также приведена активность люциферазы, измеренная в клетках HEK293, обработанных Fugene без каких-либо плазмид («Fugene»), или в необработанных клетках HEK293 («необработанные»).
[0038] На фиг. 7А показана жизнеспособность клеток HEK293 (ось Y) через 48 часов после трансфекции 400 нг (черный цвет), 200 нг (серый цвет) или 100 нг (белый цвет) конструкций, идентифицированных на оси X (конструкция-1, конструкция-3, конструкция-5, конструкция-7). На фиг. 7В показана жизнеспособность клеток HEK293 (ось Y) через 48 часов после трансфекции 400 нг (черный цвет), 200 нг (серый цвет) или 100 нг (белый цвет) конструкций, идентифицированных на оси X (конструкция-2, конструкция-4, конструкция-6, конструкция-8).
[0039] На фиг. 8А приведен пример Rep-бакмиды в плазмиде pFBDLSR, содержащей последовательности нуклеиновых кислот для белков Rep Rep52 и Rep78. Указанный пример Rep-бакмиды содержит: фрагмент промотора IE1 (SEQ ID NO: 66); нуклеотидную последовательность Rep78, в том числе последовательность Козак (SEQ ID NO: 67), последовательность промотора полиэдрина для Rep52 (SEQ ID NO: 68) и нуклеотидную последовательность Rep58, начиная с последовательности Козак gccgccacc) (SEQ ID NO: 69). На фиг. 8В приведено схематическое изображение примера зкДНК-плазмиды-1, с wt-L ITR, промотором CAG, трансгеном люциферазы, WPRE и последовательностью полиаденилирования; и mod-R (модифицированным правым) ITR.
[0040] На фиг. 9А показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А', и плеча С-С' примера модифицированного левого ITR («ITR-2 (левый)» SEQ OD NO: 101), а на фиг. 9В показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А', и плеча С-С' примера модифицированного правого ITR («ITR-2 (правый)» SEQ ID NO: 102). Предсказано формирование ими структуры с единственным плечом (С-С') и единственной неспаренной петлей. Предсказанные для них значения свободной энергии Гиббса при развертывании: -72,6 ккал/моль.
[0041] На фиг. 10А показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А', и плеча В-В' примера модифицированного левого ITR («ITR-3 (левый)» SEQ ID NO: 103), а на фиг. 10В показана предсказанная структура с наименьшей энергией RBE-co держащей части плеча А-А', и плеча В-В' примера модифицированного правого ITR («ITR-3 (правый)» SEQ ID NO: 104). Предсказано формирование ими структуры с единственным плечом (В-В') и единственной неспаренной петлей. Предсказанные для них значения свободной энергии Гиббса при развертывании: -74,8 ккал/моль.
[0042] На фиг. 11А показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А', и плеча С-С' примера модифицированного левого ITR («ITR-4 (левый)» SEQ ID NO: 105), а на фиг. 11В показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А', и плеча С-С' примера модифицированного правого ITR («ITR-4 (справа)» SEQ ID NO: 106). Предсказано формирование ими структуры с единственным плечом (С-С') и единственной неспаренной петлей. Предсказанные для них значения свободной энергии Гиббса при развертывании: -76,9 ккал/моль.
[0043] На фиг. 12А показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А', и частей С-С' и В-В' примера модифицированного левого ITR, демонстрирующая спаривание комплементарных оснований частей С-В' и С'-В («ITR-10 (левый)» SEQ ID NO: 107), а на фиг. 12В показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А', и частей В-В' и С-С' примера модифицированного правого ITR, демонстрирующая спаривание комплементарных оснований частей В-С и В'-С («ITR-10 (справа)» SEQ ID NO: 108). Предсказано формирование ими структуры с единственным плечом (часть С'-В и С-В', или часть В'-С и В-С') и единственной неспаренной петлей. Предсказанные для них значения свободной энергии Гиббса при развертывании: -83,7 ккал/моль.
[0044] На фиг. 13А показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А' и частей С-С' и В-В' примера модифицированного левого ITR («ITR-17 (левый)» SEQ ID NO: 109), а на фиг. 13В показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А' и частей С-С' и В-В' примера модифицированного правого ITR («ITR-17 (справа)» SEQ ID NO: 110). И для ITR-17 (левый), и для ITR-17 (правый) предсказано формирование структуры с единственным плечом (В-В') и единственной неспаренной петлей. Предсказанные для них значения свободной энергии Гиббса при развертывании: -73,3 ккал/моль.
[0045] На фиг. 14А показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А' примера модифицированного ITR («ITR-6 (левый)» SEQ ID NO: 111), а на фиг. 14В показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А' примера модифицированного ITR («ITR-6 (правый)» SEQ ID NO: 112). И для ITR-6 (левый), и для ITR-6 (правый) предсказано формирование структуры с единственным плечом. Предсказанные для них значения свободной энергии Гиббса при развертывании: -54,4 ккал/моль.
[0046] На фиг. 15А показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А', плеча С и плеча В-В' примера модифицированного левого ITR («ITR-1 (левый)» SEQ ID NO: 113), а на фиг. 15В показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А', плеча С и плеча В-В' примера модифицированного правого ITR («ITR-1 (справа)» SEQ ID NO: 114). И для ITR-1 (левый), и для ITR-1 (правый) предсказано формирование структуры с двумя плечами, одно из которых является усеченным. Предсказанные для них значения свободной энергии Гиббса при развертывании: -74,7 ккал/моль.
[0047] На фиг. 16А показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А'; плеча С' и плеча В-В' примера модифицированного левого ITR («ITR-5 (левый)» SEQ ID NO: 545), а на фиг. 16В показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А', плеча В-В' и плеча С' примера модифицированного правого ITR («ITR-5 (справа)» SEQ ID NO: 116). И для ITR-5 (левый), и для ITR-5 (правый) предсказано формирование структуры с двумя плечами, одно из которых (например, плечо С') является усеченным. Предсказанные для них значения свободной энергии Гиббса при развертывании: -73,4 ккал/моль.
[0048] На фиг. 17А показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А', плеча С-С' и плеча В-В' примера модифицированного левого ITR («ITR-7 (Левый)» SEQ ID NO: 117), а на фиг. 17В показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А', плеча В-В' и плеча С-С' примера модифицированного правого ITR («ITR-7 (справа)» SEQ ID NO: 118). И для ITR-17 (левый), и для ITR-17 (правый) предсказано формирование структуры с двумя плечами, одно из которых (например, плечо В-В') является усеченным. Предсказанные для них значения свободной энергии Гиббса при развертывании: -89,6 ккал/моль.
[0049] На фиг. 18А показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А', плеча С-С' и плеча В-В' примера модифицированного левого ITR («ITR-8 (левый)» SEQ ID NO: 119), а на фиг. 18В показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А', плеча В-В' и плеча С-С' примера модифицированного правого ITR («ITR-8 (справа)» SEQ ID NO: 120). И для ITR-8 (левый), и для ITR-8 (правый) предсказано формирование структуры с двумя плечами, одно из которых является усеченным. Предсказанные для них значения свободной энергии Гиббса при развертывании: -86,9 ккал/моль.
[0050] На фиг. 19А показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А', плеча С-С' и плеча В-В' примера модифицированного левого ITR («ITR-9 (левый)» SEQ ID NO: 121), а на фиг. 19В показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А', плеча В-В' и плеча С-С' примера модифицированного правого ITR («ITR-9 (правый)» SEQ ID NO: 122). И для ITR-9 (левый), и для ITR-9 (правый) предсказано формирование структуры с двумя плечами, одно из которых является усеченным. Предсказанные для них значения свободной энергии Гиббса при развертывании: -85,0 ккал/моль.
[0051] На фиг. 20А показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А', плеча С-С' и плеча В-В' примера модифицированного левого ITR («ITR-11 (левый)» SEQ ID NO: 123), а на фиг. 20В показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А', плеча В-В' и плеча С-С' примера модифицированного правого ITR («ITR-11 (справа)» SEQ ID NO: 124). И для ITR-11 (левый), и для ITR-11 (правый) предсказано формирование структуры с двумя плечами, одно из которых является усеченным. Предсказанные для них значения свободной энергии Гиббса при развертывании: -89,5 ккал/моль.
[0052] На фиг. 21А показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А', плеча С-С' и плеча В-В' примера модифицированного левого ITR («ITR-12 (левый)» SEQ ID NO: 125), а на фиг. 21В показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А', плеча В-В' и плеча С-С' примера модифицированного правого ITR («ITR-12 (правый)» SEQ ID NO: 126). И для ITR-12 (левый), и для ITR-12 (правый) предсказано формирование структуры с двумя плечами, одно из которых является усеченным. Предсказанные для них значения свободной энергии Гиббса при развертывании: -86,2 ккал/моль.
[0053] На фиг. 22А показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А', плеча С-С' и плеча В-В' примера модифицированного левого ITR («ITR-13 (левый)» SEQ ID NO: 127), а на фиг. 22В показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А', плеча В-В' и плеча С-С' примера модифицированного правого ITR («ITR-13 (правый)» SEQ ID NO: 128). И для ITR-13 (левый), и для ITR-13 (правый) предсказано формирование структуры с двумя плечами, одно из которых (например, плечо С-С') является усеченным. Предсказанные для них значения свободной энергии Гиббса при развертывании: -82,9 ккал/моль.
[0054] На фиг. 23А показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А', плеча С-С' и плеча В-В' примера модифицированного левого ITR («ITR-14 (левый)» SEQ ID NO: 129), а на фиг. 23В показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А', плеча В-В' и плеча С-С' примера модифицированного правого ITR («ITR-14 (правый)» SEQ ID NO: 130). И для ITR-14 (левый), и для ITR-14 (правый) предсказано формирование структуры с двумя плечами, одно из которых (например, плечо С-С') является усеченным. Предсказанные для них значения свободной энергии Гиббса при развертывании: -80,5 ккал/моль.
[0055] На фиг. 24А показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А', плеча С-С' и плеча В-С' примера модифицированного левого ITR («ITR-15 (левый)» SEQ ID NO: 131), а на фиг. 24В показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А', плеча В-В' и плеча С-С' примера модифицированного правого ITR («ITR-15 (правый)» SEQ ID NO: 132). И для ITR-15 (левый), и для ITR-15 (правый) предсказано формирование структуры с двумя плечами, одно из которых (например, плечо С-С') является усеченным. Предсказанные для них значения свободной энергии Гиббса при развертывании: -77,2 ккал/моль.
[0056] На фиг. 25А показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А', плеча С-С' и плеча В-С' примера модифицированного левого ITR («ITR-16 (слева) SEQ ID NO: 133), а на фиг. 25В показана предсказанная структура с наименьшей энергией RBE-содержащей части плеча А-А', плеча В-В' и плеча С-С' примера модифицированного правого ITR («ITR-16 (справа)» SEQ ID NO: 134). И для ITR-16 (левый), и для ITR-16 (правый) предсказано формирование структуры с двумя плечами, одно из которых (например, плечо С-С') является усеченным. Предсказанные для них значения свободной энергии Гиббса при развертывании: -73,9 ккал/моль.
[0057] На фиг. 26А показаны предсказанные структуры RBE-содержащей части плеча А-А', и модифицированного плеча В-В' и/или модифицированного плеча С-С' примеров модифицированных правых ITR, приведенных в таблице 10А. На фиг. 26В показаны предсказанные структуры RBE-содержащей части плеча А-А', и модифицированного плеча С-С' и/или модифицированного плеча В-В' примеров модифицированных левых ITR, приведенных в таблице 10В. Показанные структуры являются предсказанными структурами с наименьшей свободной энергией. Обозначение условными цветами: красный = >99% вероятность; оранжевый = 99% - 95% вероятность; бежевый = 95-90% вероятность; темно-зеленый 90% - 80%; ярко-зеленый = 80% - 70%; голубой = 70% - 60%; темно-синий 60% - 50%; и розовый = <50%.
[0058] На фиг. 27 показана активность люциферазы в клетках насекомых Sf9 GlycoBac, трансфицированных выбранными мутантными вариантами асимметричных ITR из таблиц 10А и 10В. ЗкДНК-вектор содержал ген люциферазы, фланкированный ITR дикого типа (wt) и модифицированный асимметричный ITR, выбранный из таблиц 10А или 10В. «ITR-50 R без rep» - известный поддающийся спасению мутант без коинфицирования Rep-содержащим бакуловирусом. «Ложная трансфекция» только реагенты для трансфекции без донорной ДНК.
[0059] На фиг. 28 показан нативный агарозный гель (1% агароза, 1× ТАЕ-буфер) для репрезентативные неочищенных экстрактов зкДНК из культур клеток насекомых Sf9, трансфицированных зкДНК-плазмидами, содержащими левый wt-ITR и другой ITR, выбранный из различных мутантных правых ITR, приведенных в таблице 10А. на каждую дорожку загружали по 2 мкг тотального экстракта. Слева направо: дорожка 1) лэддер 1 Kb Plus Ladder, дорожка 2) ITR-18, правый, дорожка 3) ITR-49, правый, дорожка 4) ITR-19, правый, дорожка 5) ITR-20, правый, дорожка 6) ITR-21, правый, дорожка 7) ITR-22, правый, дорожка 8) ITR-23, правый, дорожка 9) ITR-24, правый, дорожка 10) ITR-25, правый, дорожка 11) ITR-26, правый, дорожка 12) ITR-27, правый, дорожка 13) ITR-28, правый, дорожка 14) ITR-50, правый, дорожка 15) лэддер 1 Kb Plus Ladder.
[0060] На фиг. 29 показан денатурирующий гель (0,8% щелочная агароза) для репрезентативных конструкций из библиотеки мутантных ITR. ЗкДНК-вектор получают с плазмидных конструкций, содержащих левый wt-ITR и другой ITR, выбранный из различных мутантных правых ITR, приведенных в таблице 10А. Слева направо: дорожка 1) ДНК-лэддер 1 Kb Plus Ladder, дорожка 2) ITR-18, правый, неразрезанный, дорожка 3) ITR-18, правый, рестрикционный гидролизат, дорожка 4) ITR-19, правый, неразрезанный, дорожка 5) ITR-19, правый, рестрикционный гидролизат, дорожка 6) ITR-21, правый, неразрезанный, дорожка 7) ITR-21, правый, рестрикционный гидролизат, дорожка 8) ITR-25, правый, неразрезанный, дорожка 9) ITR-25, правый, рестрикционный гидролизат.Экстракты обрабатывали рестрикционной эндонуклеазой EcoRI. Предполагается, что каждый зкДНК-мутант содержит единственный сайт распознавания EcoRI для получения двух характеристических фрагментов, ~2000 п.о. и ~3000 п.о., которые будут двигаться как фрагменты ~4000 и ~6000 п.о., соответственно, в денатурирующих условиях. Необработанные экстракты зкДНК содержат фрагменты ~5000 п.о. и, предположительно, будут мигрировать как фрагменты ~11000 п.о. в денатурирующих условиях.
[0061] На фиг. 30 показана активность люциферазы in vitro в клетках HEK293 с мутантными ITR, правым ITR-18, правым ITR-19, правым ITR-21 и правым ITR-25, и ITR-49, при этом левый ITR в зкДНК-вектор представлен WT ITR. «Ложная трансфекция» только реагенты для трансфекции без донорной ДНК, и «необработанные» - отрицательный контроль.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
I. Определения
[0062] Если в настоящем документе не указано иное, научные и технические термины, используемые применительно к настоящему изобретению, имеют значения, обычно подразумеваемые специалистами в области техники, к которой относится настоящее изобретение. Следует понимать, что настоящее изобретение не ограничено конкретной методикой, протоколами и реагентами, и т.п., описанными в настоящем документе, и поэтому такие методики, протоколы и реагенты могут варьировать. Используемая в настоящем документе терминология служит только для описания конкретных вариантов реализации, и не предназначена для ограничения объема настоящего изобретения, который определен исключительно формулой изобретения. Определения распространенных терминов иммунологии и молекулярной биологии можно найти в следующих источниках: руководство The Merck Manual of Diagnosis and Therapy, 19e изд., издано Merck Sharp & Dohme Corp., 2011 (ISBN 978-0-911910-19-3); Robert S. Porter et al. (ред.), Fields Virology, 6е изд, издание Lippincott Williams & Wilkins, Philadelphia, PA, USA (2013), Knipe, D.M. and Howley, P.M. (ред.), The Encyclopedia of Molecular Cell Biology and Molecular Medicine, издание Blackwell Science Ltd., 1999-2012 (ISBN 9783527600908); и Robert A. Meyers (ред.), Molecular Biology and Biotechnology: a Comprehensive Desk Reference, издание VCH Publishers, Inc., 1995 (ISBN 1-56081-569-8); Immunology by Werner Luttmann, издание Elsevier, 2006; Janeway's Immunobiology, Kenneth Murphy, Allan Mowat, Casey Weaver (ред.), Taylor & Francis Limited, 2014 (ISBN 0815345305, 9780815345305); Lewin's Genes XI, издание Jones & Bartlett Publishers, 2014 (ISBN-1449659055); Michael Richard Green and Joseph Sambrook, Molecular Cloning: A Laboratory Manual, 4е изд.., Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y., USA (2012) (ISBN 1936113414); Davis et al, Basic Methods in Molecular Biology, Elsevier Science Publishing, Inc., New York, USA (2012) (ISBN 044460149X); Laboratory Methods in Enzymology: DNA, Jon Lorsch (ред.) Elsevier, 2013 (ISBN 0124199542); Current Protocols in Molecular Biology (CPMB), Frederick M. Ausubel (ред.), John Wiley and Sons, 2014 (ISBN 047150338X, 9780471503385), Current Protocols in Protein Science (CPPS), John E. Coligan (ред.), John Wiley and Sons, Inc., 2005; и Current Protocols in Immunology (CPI) (John E. Coligan, ADA M Kruisbeek, David H Margulies, Ethan M Shevach, Warren Strobe, (ред.) John Wiley and Sons, Inc., 2003 (ISBN 0471142735, 9780471142737), содержание которых полностью включено посредством ссылок в настоящий документ.
[0063] В настоящем документе термины «гетерологичная нуклеотидная последовательность» и «трансген» используются взаимозаменяемо и относятся к представляющей интерес нуклеиновой кислоте (которая не является нуклеиновой кислотой, кодирующей капсидный полипептид), которая включена в зкДНК-вектор и может быть доставлена и экспрессирована зкДНК-вектором согласно описанию в настоящем документе. Представляющие интерес трансгены включают, не ограничиваясь перечисленными, нуклеиновые кислоты, кодирующие полипептиды, предпочтительно терапевтические (например, для медицинского, диагностического или ветеринарного применения) или иммуногенные полипептиды (например, для вакцин). Согласно некоторым вариантам реализации представляющие интерес нуклеиновые кислоты включают нуклеиновые кислоты, транскрибируемые в терапевтическую РНК. Предусмотренные трансгены для применения в зкДНК-векторах согласно настоящему изобретению включают, не ограничиваясь перечисленными, трансгены, которые экспрессируют или кодируют один или более полипептидов, пептидов, рибозимов, аптамеров, пептидных нуклеиновых кислот, киРНК, RNAi (РНК-интерференция), миРНК, днкРНК, антисмысловые олиго- или полинуклеотиды, антитела, антигенсвязывающие фрагменты или любую комбинацию перечисленного.
[0064] В настоящем документе термины «экспрессионная кассета» и «транскрипционная кассета» используются взаимозаменяемо и относятся к линейному отрезку нуклеиновых кислот, который включает трансген, который функционально связан с одним или более промоторами или другими регуляторными последовательностями, достаточными для направления транскрипции указанного трансгена, однако не включает кодирующие капсид последовательности, другие последовательности вектора или области инвертированных концевых повторов. Экспрессионная кассета может, кроме того, содержать один или более цис-действующих последовательностей (например, промоторов, энхансеров или репрессоров), один или более интронов, и один или более посттранскрипционных регуляторных элементов.
[0065] В настоящем документе термин «концевой повтор» или «TR» включает любой вирусный концевой повтор или синтетическую последовательность, которая содержит по меньшей мере одну минимально требуемую точку начала репликации и область, содержащую палиндромную шпилечную структуру. Rep-связывающая последовательность («RBS») и сайт концевого разрешения («TRS») вместе составляют «минимальную требуемую точку начала репликации» и, соответственно, концевой повтор (TR) содержит по меньшей мере одну RBS и по меньшей мере один TRS. Все TR, обратно комплементарные друг другу, в составе заданного отрезка последовательности полинуклеотидов, как правило, называют «инвертированными концевыми повторами», или «ITR». В контексте вируса ITR опосредуют репликацию, упаковку вируса, интеграцию и спасение провируса. Как было неожиданно обнаружено авторами описанного изобретения, TR, не являющиеся обратно комплементарными по всей длине, могут, тем не менее, выполнять традиционные функции ITR, и, соответственно, термин ITR в настоящем документе относится к TR в зкДНК-геноме или зкДНК-векторе, который способен опосредовать репликацию зкДНК-вектора. Специалисту в данной области техники будет понятно, что в комплексных конфигурациях зкДНК могут присутствовать более двух ITR или пар асимметричных ITR. ITR может представлять собой ITR AAV или ITR не из AAV, или может происходить из ITR AAV или ITR не из AAV. Например, ITR может происходить из вируса семейства Parvoviridae, которое охватывает парвовирусы и депендовирусы (например, парвовирус собак, бычий парвовирус, парвовирус мышей, свиной парвовирус, парвовирус человека В-19), или шпилька SV40, которая служит точкой начала репликации SV40 может применяться в качестве ITR, который может дополнительно быть модифицирован путем усечения, замены, делеции, инсерции и/или добавления. Вирусы семейства Parvoviridae состоят из два подсемейств: Parvovirinae, инфицирующих позвоночных животных, и Densovirinae, инфицирующих беспозвоночных животных. Депендопарвовирусы включают вирусное семейство аденоассоциированных вирусов (AAV), способных к репликации у хозяев - позвоночных животных, в том числе, но не ограничиваясь перечисленными, у человека, видов приматов, бычьих, собачьих, лошадиных и овечьих.
[0066] В настоящем документе термин «асимметричные ITR» относится к паре ITR в составе одного зкДНК-генома или зкДНК-вектора, не обратно комплементарных по всей длине. Различие последовательностей двух ITR может быть обусловлено добавлением нуклеотидов, делецией, усечением или точечной мутацией. Согласно одному варианту реализации один ITR из пары может представлять собой последовательность AAV дикого типа, а другой -последовательность не дикого типа или синтетическую. Согласно другому варианту реализации ни один ITR из пары не представляет собой последовательность AAV дикого типа и последовательности указанных двух ITR различаются. Для удобства в настоящем документе ITR, расположенный в направлении 5' относительно экспрессионной кассеты (выше) в зкДНК-векторе, называется «5'-ITR» или «левым ITR», a ITR, расположенный в направлении 3' относительно экспрессионной кассеты (ниже) в зкДНК-векторе, называется «3'-ITR» или «правым ITR».
[0067] В настоящем документе термин «зкДНК-геном» относится к экспрессионной кассете, которая дополнительно включает по меньшей мере одну область инвертированного концевого повтора. ЗкДНК-геном может дополнительно содержать одну или более спейсерных областей. Согласно некоторым вариантам реализации указанный зкДНК-геном включен в виде полинуклеотида ДНК с межмолекулярными дуплексными структурами в плазмиду или вирусный геном.
[0068] В настоящем документе термин «спейсерная область зкДНК» относится к промежуточной последовательности, которая разделяет функциональные элементы в указанном зкДНК-векторе или зкДНК-геноме. Согласно некоторым вариантам реализации спейсерные области зкДНК удерживают два функциональных элемента на требуемом расстоянии для оптимальной функциональности. Согласно некоторым вариантам реализации спейсерные области зкДНК обеспечивают или увеличивают генетическую стабильность зкДНК-генома в составе, например, плазмиды или бакуловируса. Согласно некоторым вариантам реализации спейсерные области зкДНК облегчают подготовленную генетическую манипуляцию с зкДНК-геномом, обеспечивая удобное расположение сайтов клонирования и т.п. Например, согласно определенным аспектам олигонуклеотидный «полилинкер», содержащий несколько сайтов рестрикции эндонуклеазами или последовательность не из открытой рамки считывания, сконструированный так, чтобы не содержать известных сайтов связывания белка (например, транскрипционный фактор), может быть размещен в зкДНК-геноме для разделения цис-действующих факторов, например, может быть инсертирован 6-мер, 12-мер, 18-мер, 24-мер, 48-мер, 86-мер, 176-мер и т.п., между сайтом концевого разрешения и расположенным в направлении 5' транскрипционным регуляторным элементом. Аналогичным образом, может быть включен спейсер между последовательностью сигнала полиаденилирования и сайтом 3'-концевого разрешения.
[0069] В настоящем документе термины «сайт связывания Rep», «Rep-связывающий элемент», «RBE» и «RBS» используются взаимозаменяемо и относятся к сайту связывания белка Rep (например, Rep 78 AAV или Rep 68 AAV), который при связывании белком Rep позволяет указанному белку Rep проявлять соответствующую сайт-специфическую эндонуклеазную активность на последовательности, включающей RBS. Последовательность RBS и обратно-комплементарная ей последовательность вместе образуют один RBS. Последовательности RBS известны в данной области техники и включают, например, 5'-GCGCGCTCGCTCGCTC-3'(SEQ ID NO: 531), последовательность RBS, идентифицированную в AAV2. Согласно вариантам реализации настоящего изобретения может применяться любая известная последовательность RBS, в том числе другие известные последовательности RBS AAV и другие известные естественные или синтетические последовательности RBS. Без связи с какой-либо теорией считается, что нуклеазный домен белка Rep связывается с дуплексной последовательностью нуклеотидов GCTC, и, соответственно, на дуплексном олигонуклеотиде 5'-(GCGC)(GCTC)(GCTC)(GCTC)-3' (SEQ ID NO: 531) происходит прямое связывание и стабильная сборка двух известных белков Rep AAV. Кроме того, растворимые агрегированные конформеры (т.е. неопределенное число взаимосвязанных белков Rep) диссоциируют и связываются с олигонуклеотидами, которые содержат сайты связывания Rep. Каждый белок Rep взаимодействует и с азотистыми основаниями, и с фосфодиэфирным остовом на каждой цепи. Взаимодействия с азотистыми основаниями обеспечивают специфичность в отношении последовательности, тогда как взаимодействия с фосфодиэфирным остовом являются неспецифическими или менее специфическими в отношении последовательности, и стабилизируют комплекс белка с ДНК.
[0070] В настоящем документе термины «сайт концевого разрешения» и «TRS» используются взаимозаменяемо и относятся к области, в которой Rep образует через тирозин-фосфодиэфирную связь с 5'-тимидином, с получением 3'-ОН, который служит в качестве субстрата для достройки ДНК клеточной ДНК-полимеразой, например, ДНК-полимеразой дельта или ДНК-полимеразой эпсилон. Как вариант, комплекс Rep-тимидин может принимать участие в скоординированной реакции лигирования. Согласно некоторым вариантам реализации TRS охватывает как минимум неспаренный тимидин. Согласно некоторым вариантам реализации эффективность никирования TRS можно контролировать, по меньшей мере отчасти, расстоянием между ним и RBS в пределах одной молекулы. Если акцепторный субстрат представлен комплементарным ITR, итоговый продукт представляет собой внутримолекулярный дуплекс. Последовательности TRS известны в данной области техники и включают, например, 5'-GGTTGA-3' (SEQ ID NO: 45), гексануклеотидную последовательность, идентифицированную в AAV2. Согласно вариантам реализации настоящего изобретения может применяться любая известная последовательность TRS, в том числе другие известные последовательности TRS AAV и другие известные естественные или синтетические последовательности TRS, такие как AGTT (SEQ ID N0: 46), GGTTGG (SEQ ID NO: 47), AGTTGG (SEQ ID NO: 48), AGTTGA (SEQ ID NO: 49); и другие мотивы, такие как RRTTRR (SEQ ID NO: 50).
[0071] В настоящем документе термин «зкДНК-плазмида» относится к плазмиде, которая содержит зкДНК-геном в виде межмолекулярного дуплекса.
[0072] В настоящем документе термин «зкДНК-бакмида» относится к геному инфекционного бакуловируса, включающему зкДНК-геном в виде межмолекулярного дуплекса, способному размножаться в Е. coli в виде плазмиды и, соответственно, функционировать в качестве челночного вектора для бакуловируса.
[0073] В настоящем документе термин «зкДНК-бакуловирус» относится к бакуловирусу, который содержит зкДНК-геном в виде межмолекулярного дуплекса в составе генома бакуловируса.
[0074] В настоящем документе термины «инфицированная зкДНК-бакуловирусом клетка насекомого» и «зкДНК-ВПС» используются взаимозаменяемо, и относятся к клетке-хозяину из беспозвоночного животного (в том числе, но не ограничиваясь указанным, клетке насекомого (например, клетке Sf9)), инфицированной зкДНК-бакуловирусом.
[0075] В настоящем документе термины «вектор с ДНК с замкнутыми концами», «зкДНК-вектор» и «зкДНК» используются взаимозаменяемо и относятся к невирусному бескапсидному ДНК-вектору по меньшей мере с одним ковалентно-замкнутым концом (т.е. содержащему внутримолекулярный дуплекс). Согласно некоторым вариантам реализации зкДНК содержит два ко валентно-замкнутых конца.
[0076] Согласно определению в настоящем документе «репортеры» относятся к белкам, которые могут применяться для обеспечения детектируемых показаний. Репортеры обычно продуцируют измеряемый сигнал, например, флуоресцентный, цветовой или люминесцентный. Кодирующие последовательности репортерных белков кодируют белки, присутствие которых в клетке или организме легко поддается наблюдению. Например, флуоресцентные белки вызывают флуоресценцию клетки при возбуждении светом с конкретной длиной волны, люцифер азы приводят к катализу клеткой реакции, которая генерирует свет, а ферменты, такие как β-галактозидаза, преобразуют субстрат в окрашенный продукт. Примеры репортерных полипептидов, подходящих для экспериментальных или диагностических целей, включают, не ограничиваясь перечисленными, β-лактамазу, β-галактозидазу (LacZ), щелочную фосфатазу (АР), тимидинкиназу (ТК), зеленый флуоресцентный белок (GFP) и другие флуоресцентные белки, хлор амфениколацетил трансфер азу (CAT), люциферазу и другие, хорошо известные в данной области техники.
[0077] В настоящем документе термин «эффекторный белок» относится к полипептиду, который обеспечивает детектируемые показания, либо, например, как репортерный полипептид, либо, более предпочтительно, как полипептид, убивающий клетку, например, токсин, или агент, придающий клетке чувствительность к киллингу определенным агентом или при отсутствии определенного агента. Эффекторные белки включают любой белок или пептид, который прямо нацелен на ДНК и/или РНК клетки-хозяина или повреждает ее. Например, эффекторные белки могут включать, не ограничиваясь перечисленными, рестрикционную эндонуклеазу, которая нацелен на последовательность ДНК клетки-хозяина (геномный или внехромосомный элемент), протеазу, разлагающую полипептидную мишень, необходимую для выживания клетки, ингибитор ДНК-гиразы и токсин рибонуклеазного типа. Согласно некоторым вариантам реализации экспрессия эффекторного белка, контролируемая синтетическим биологическим контуром согласно описанию в настоящем документе, может принимать участие в качестве фактора в другом синтетическом биологическом контуре, с расширением таким образом диапазона и сложности отклика системы биологического контура.
[0078] Термин «транскрипционные регуляторы» относится к транскрипционным активаторам и репрессорам, которые либо активируют, либо подавляют транскрипцию гена, представляющего интерес. Промоторы представляют собой области нуклеиновой кислоты, которые инициируют транскрипцию конкретного гена. Транскрипционные активаторы, как правило, связываются поблизости от транскрипционных промоторов и привлекают РНК-полимеразу, чтобы прямо инициировать транскрипцию. Репрессоры связываются с транскрипционными промоторами и стерически затрудняют инициацию транскрипции РНК-полимеразой. Другие транскрипционные регуляторы могут служить либо активатором, либо репрессором в зависимости от места их связывания и условий в клетке и окружающей среде. Неограничивающие примеры классов транскрипционных регуляторов включают, не ограничиваясь перечисленными, гомеодоменные белки, белки с цинковыми пальцами, белки с мотивом «крылатая спираль» (белки Forkhead) и белки с лейциновой застежкой.
[0079] В настоящем документе «белок-репрессор» или «белок-индуктор» представляет собой белок, который связывается с элементом регулятор ной последовательности и подавляет или активирует, соответственно, транскрипцию последовательностей, функционально связанных с указанным элементом регуляторной последовательности. Предпочтительные белки-репрессоры и беки-индукторы согласно описанию в настоящем документе чувствительны к присутствию или отсутствию по меньшей мере одного входного агента или входного действия окружающей среды. Предпочтительные белки согласно описанию в настоящем документе являются модульными по форме, содержащими, например, отделяемые ДНК-связывающие, и связывающие или реагирующие на входные агенты элементы или домены.
[0080] В настоящем документе «носитель» включает любые растворители, дисперсионные среды, основы, покрытия, разбавители, антибактериальные и антимикотические агенты, изотонические и замедляющие абсорбцию агенты, буферы, растворы-носители, суспензии, коллоиды и т.п. Применение таких сред и агентов для фармацевтически активных веществ хорошо известно в данной области техники. В указанные композиции могут также быть включены дополнительные активные ингредиенты. Выражение «фармацевтически приемлемые» относится к молекулярным объектам и композициям, которые не приводят к токсической, аллергической или аналогичной нежелательной реакции при введении хозяину.
[0081] В настоящем документе «реагирующий на входной агент домен» представляет собой домен транскрипционного фактора, который связывает или иначе отвечает на условия или входной агент таким образом, чтобы обеспечивать реакцию соединенного с ним ДНК-связывающего слитого домена на наличие указанного условия или входного действия. Согласно одному варианту реализации наличие указанного условия или входного действия приводит к конформационному изменению реагирующего на входной агент домена, или белка, с которым он слит, что модифицирует модулирующую транскрипцию активность транскрипционного фактора.
[0082] Термин «in vivo» относится к анализам или процессам, которые происходят в организме или в пределах организма, например, многоклеточного животного. Согласно некоторым аспектам настоящего изобретения может быть указано, что способ или применение осуществляют «in vivo», если используют одноклеточный организм, такой как бактерия. Термин «ех vivo» относится к способам и применениям, которые осуществляют с использованием живой клетки с интактной мембраной, которая находится вне организма многоклеточного животного или растения, например, эксплантатов, культивированных клеток, в том числе первичных клеток и линий клеток, трансформированных линий клеток и экстрагированных тканей или клеток, в том числе клеток крови, и т.п. Термин «in vitro» относится к анализам и способам, не требующим наличия клетки с интактной мембраной, например, на клеточных экстрактах, и может относиться к введению программируемого синтетического биологического контура в неклеточную систему, такую как среда, не содержащая клеток или клеточных систем, таких как клеточные экстракты.
[0083] Термин «промотор» в настоящем документе относится к любой последовательности нуклеиновой кислоты, которая регулирует экспрессию другой последовательности нуклеиновой кислоты путем управления транскрипцией указанной последовательности нуклеиновой кислоты, которая может представлять собой гетерологичный целевой ген, кодирующий белок, или РНК. Промоторы могут быть конститутивными, индуцируемыми, репрессируемыми, тканеспецифическими, или характеризоваться любой комбинацией перечисленного. Промотор представляет собой контрольную область последовательности нуклеиновой кислоты, в которой осуществляется инициация и определяется уровень транскрипции остальной последовательности нуклеиновой кислоты. Промотор может также содержать генетические элементы, в которых может происходить связывание регуляторных белков и молекул, таких как РНК-полимераза, и других транскрипционных факторов. Согласно некоторым вариантам реализации аспектов настоящего документа промотор может управлять экспрессией транскрипционного фактора, который регулирует экспрессию собственно промотора, или транскрипционного фактора другого промотора, используемого в другом модульном компоненте синтетических биологических контуров, описанных в настоящем документе. В последовательности промотора присутствует сайт инициации транскрипции, а также связывающие белки домены, отвечающие за связывание РНК-полимеразы. Эукариотические промоторы часто, однако не всегда содержат «ТАТА»-боксы и «САТ»-боксы. Для управления экспрессией трансгенов в зкДНК-векторах, описанных в настоящем документе могут применяться различные промоторы, в том числе индуцируемые промоторы,.
[0084] Термин «энхансер» в настоящем документе относится к цис-действующей регуляторной последовательности (например, 50-1500 пар оснований), которая связывает один или более белков (например, белков-активаторов или транскрипционного фактора) для повышения транскрипционной активации последовательности нуклеиновой кислоты. Энхансеры могут располагаться на расстоянии до 1 000 000 пар оснований выше сайта начала гена или ниже сайта начала гена, который они регулируют. Энхансер может располагаться в интронной области или в экзонной области не связанного с ним гена.
[0085] Можно сказать, что промотор управляет экспрессией или управляет транскрипцией последовательности нуклеиновой кислоты, которую он регулирует. Выражения «функционально связанный», «функционально расположенный», «под контролем» и «под транскрипционным контролем» показывают, что промотор находится в корректном функциональном положении и/или ориентации относительно последовательности нуклеиновой кислоты, которую он регулирует, для контроля инициации транскрипции и/или экспрессии указанной последовательности. «Инвертированный промотор» в настоящем документе относится к промотору, последовательность нуклеиновой кислоты которого имеет обратную ориентацию, таким образом, что кодирующая цепь становится некодирующей, и наоборот. Последовательности инвертированных промоторов могут применяться согласно различным вариантам реализации для регуляции состояния переключателя. Кроме того, согласно различным вариантам реализации промотор может применяться в сочетании с энхансером.
[0086] Промотор может представлять собой естественным образом ассоциированный с геном или последовательностью промотор, который может быть получен путем выделения некодирующих 5'-последовательностей, расположенных выше кодирующего сегмента и/или экзона определенного гена или последовательности. Такой промотор может называться «эндогенным». Аналогичным образом, согласно некоторым вариантам реализации энхансер может представлять собой естественным образом ассоциированный с последовательностью нуклеиновой кислоты энхансер, расположенный в направлении либо 3', либо 5' относительно указанной последовательности.
[0087] Согласно некоторым вариантам реализации кодирующий сегмент нуклеиновой кислоты помещен под контроль «рекомбинантного промотора» или «гетерологичного промотора», где оба термина относятся к промотору, который обычно не ассоциирован с кодирующей последовательностью нуклеиновой кислоты, с которой он функционально связан, в естественных условиях среды. Рекомбинантный или гетерологичный энхансер относится к энхансеру, обычно не ассоциированному с определенной последовательностью нуклеиновой кислоты в естественных условиях среды. Такие промоторы или энхансеры могут включать промоторы или энхансеры других генов; промоторы или энхансеры, выделенные из любой другой прокариотической, вирусной или эукариотической клетки; и синтетические промоторы или энхансеры, не «встречающиеся в природе» т.е. содержащие разные элементы разных транскрипционных регуляторных областей, и/или мутации, которые изменяют экспрессию, введенные с применением способов генетического конструирования, известных в данной области техники. Наряду с получением последовательностей нуклеиновых кислот промоторов и энхансером синтетическим путем, последовательности промоторов могут быть получены с использованием рекомбинантного клонирования и/или технологии амплификации нуклеиновых кислот, в том числе ПЦР, применительно к синтетическим биологическим контурам и модулям согласно описанию в настоящем документе (см., например, патент США №4683202, патент США №5928906, каждый из которых включен в настоящий документ посредством ссылки). Кроме того, предусмотрена также возможность применения контрольных последовательностей, которые управляют транскрипцией и/или экспрессией последовательностей в неядерных органеллах, таких как митохондрии, хлоропласты и т.п.
[0088] Согласно настоящему раскрытию «индуцируемый промотор» представляет собой промотор, который характеризуется инициацией или усилением транскрипционной активности в присутствии, при влиянии или при контакте с индуктором, или индуцирующим агентом. «Индуктор» или «индуцирующий агент» согласно определению в настоящем документе может быть эндогенным или экзогенным в норме соединением или белком, которое или который вводят таким образом, чтобы обеспечивать его активность в смысле индуцирования транскрипционной активности индуцируемого промотора. Согласно некоторым вариантам реализации указанный индуктор или индуцирующий агент, т.е. химическое вещество, соединение или белок, может сам быть получен в результате транскрипции или экспрессии последовательности нуклеиновой кислоты (т.е. индуктор может представлять собой белок-индуктор, экспрессируемый другим компонентом или модулем), который сам может находиться под контролем индуцируемого промотора. Согласно некоторым вариантам реализации индукция индуцируемого промотора происходит в отсутствие определенных агентов, таких как репрессор. Примеры индуцируемых промоторов включают, не ограничиваясь перечисленными, тетрациклин, металлотионин, экдизон, вирусы млекопитающих (например, поздний аденовирусный промотор; и длинный концевой повтор вируса опухоли молочной железы мышей (MMTV-LTR)) и другие реагирующие на стероиды промоторы, реагирующие на рапамицин промоторы и т.п.
[0089] Термин «субъект» в настоящем документе относится к человеку или животному, лечение которого, в том числе профилактическое лечение, проводят с применением зкДНК-вектора в соответствии с настоящим изобретением. Обычно указанное животное представляет собой позвоночное животное, такое как, не ограничиваясь перечисленными, примат, грызун, домашнее животное или промысловое животное. Приматы включают, не ограничиваясь перечисленными, шимпанзе, яванского макака, коат и макаков, например, макака-резус. Грызуны включают мышей, крыс, сурков, хорьков, кроликов и хомяков. Домашние и промысловые животные включают, не ограничиваясь перечисленными, коров, лошадей, свиней, оленей, бизонов, буйволов, кошачьих, например, домашнюю кошку, виды собачьих, например, собаку, лису, волка, виды птиц, например, курицу, эму, страуса, и рыб, таких как форель, сом и лосось. Согласно определенным вариантам реализации аспектов настоящего изобретения указанный субъект представляет собой млекопитающее, например, примата или человека. Субъект может быть мужского или женского пола. Кроме того, субъект может представлять собой младенца или ребенка. Согласно некоторым вариантам реализации указанный субъект может представлять собой новорожденного или нерожденного субъекта, например, субъекта in utero. Предпочтительно, указанный субъект представляет собой млекопитающее. Указанное млекопитающее может представлять собой, не ограничиваясь приведенными примерами, человека, не являющегося человеком примата, мышь, крысу, собаку, кошку, лошадь или корову. Млекопитающие, не являющиеся человеком, могут быть успешно использованы в качестве субъектов для моделей заболеваний и нарушений на животных. Кроме того, способы и композиции, описанные в настоящем документе, могут применяться для одомашненных животных и/или животных-компаньонов. Субъект-человек может быть любого возраста, пола, принадлежать к любой расе или этнической группе, например, может быть европеоидом (белым), азиатом, африканцем, черным, афроамериканцем, афроевропейцем, испаноамериканцем, представителем ближневосточного этноса и т.п. Согласно некоторым вариантам реализации указанный субъект может представлять собой пациента или другого субъекта в клинических условиях. Согласно некоторым вариантам реализации указанный субъект уже проходит лечение.
[0090] В настоящем документе термин «антитело» применяют в самом широком смысле, и он охватывает различные антительные структуры, в том числе, но не ограничиваясь перечисленными, моноклональные антитела, поликлональные антитела, мультиспецифические антитела (например, биспецифические антитела), и фрагменты антител при условии, что они проявляют требуемую антигенсвязывающую активность. «Фрагмент антитела» относится к молекуле, не являющейся интактным антителом, которая содержит часть интактного антитела, связывающую тот же антиген, с которым связывается указанное интактное антитело. Согласно одному варианту реализации антитело или фрагмент антитела содержит цепь иммуноглобулина или фрагмент антитела, и по меньшей мере одну последовательность вариабельного домена иммуноглобулина. Примеры антител или их фрагментов включают, не ограничиваясь перечисленными, Fv-, scFv-, Fab-фрагмент, Fab'-, F(ab')2, Fab'-SH, од но доменное антитело (dAb), тяжелую цепь, легкую цепь, тяжелую и легкую цепь, полное антитело (например, включающее все из перечисленного: Fc, Fab, тяжелые цепи, легкие цепи, вариабельные области и т.п.), биспецифическое антитело, диатело, линейное антитело, одноцепочечное антитело, интратело, моноклональное антитело, химерное антитело, мультиспецифическое антитело или мультимерное антитело. Антитело или его фрагмент может относиться к любому классу, в том числе, но не ограничиваясь перечисленными, IgA, IgD, IgE, IgG и IgM, и к любому их подклассу, в том числе, но не ограничиваясь перечисленными, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2. Кроме того, антитело может происходить из организма любого млекопитающего, например, приматов, человека, крысы, мыши, лошади, козы и т.п. Согласно одному варианту реализации указанное антитело является антителом человека или гуманизированным антителом. Согласно некоторым вариантам реализации указанное антитело представляет собой модифицированное антитело. Согласно некоторым вариантам реализации компоненты антитела могут экспрессироваться по отдельности, таким образом, что указанное антитело самособирается после экспрессии белковых компонентов. Согласно некоторым вариантам реализации указанное антитело «гуманизировано» для снижения иммуногенных реакций у человека. Согласно некоторым вариантам реализации указанное антитело обладает требуемой функцией, такой как взаимодействие и ингибирование требуемого белка для лечения заболевания или симптома заболевания. Согласно одному варианту реализации указанное антитело или фрагмент антитела содержит каркасную область или Fc-область.
[0091] В настоящем документе термин «антигенсвязывающий домен» молекулы антитела относится к части молекулы антитела, например, молекулы иммуноглобулина (Ig), который принимает участие в связывании антигена. Согласно вариантам реализации сайт связывания антигена образован остатками аминокислот вариабельных (V) областей тяжелых (Н) и легких (L) цепей. Три сильно отличающихся отрезка в составе вариабельных областей тяжелых и легких цепей, называемые гипервариабельными областями, расположены между более консервативными фланкирующими отрезками, называемыми «каркасными областями» (FR). FR представляют собой последовательности аминокислот, которые в естественных условиях обнаруживаются в иммуноглобулинах между гипервариабельными областями и рядом с ними. Согласно вариантам реализации в молекуле антитела три гипервариабельных области легкой цепи и три гипервариабельных области тяжелой цепи расположены друг относительно друга в трехмерном пространстве с образованием антигенсвязывающей поверхности, которая комплементарна трехмерной поверхности связанного антигена. Три гипервариабельных области из каждой из тяжелых и легких цепей называются «определяющими комплементарность областями» или «CDR». Каркасная область и CDR были определены и описаны, например, в источниках: Kabat, Е.A., et al. (1991) Sequences of Proteins of Immunological Interest, Fife изд., U.S. Department of Health and Human Services, NTH Publication No. 91-3242, и Chothia, C. et al. (1987) J. Mol. Biol. 196:901-917. Каждая вариабельная цепь (например, вариабельная тяжелая цепь и вариабельная легкая цепь), как правило, составлена из трех CDR и четырех FR, последовательности аминокислот которых расположены, в направлении от аминоконца к карбоксильному концу, в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3 и FR4.
[0092] В настоящем документе термин «полноразмерное антитело» относится к молекуле иммуноглобулина (Ig) (например, IgG-антитела), например, встречающейся в природе, и образованной фрагментами генов иммуноглобулинов в ходе нормальных рекомбинаторных процессов.
[0093] В настоящем документе термин «функциональный фрагмент антитела» относится к фрагменту, который связывается с тем же антигеном, который распознает интактное (например, полноразмерное) антитело. Термины «фрагмент антитела» или «функциональный фрагмент» также включают выделенные фрагменты, состоящие из вариабельных областей, такие как «Fv»-фрагменты, состоящие из вариабельных областей тяжелых и легких цепей, или рекомбинантные одноцепочечные полипептидные молекулы, в которых вариабельные области тяжелых и легких цепей соединены пептидным линкером («scFv-белки»). Согласно некоторым вариантам реализации фрагмент антитела не содержит частей антител без антигенсвязывающей активности, таких как Fc-фрагменты или одиночные остатки аминокислот.
[0094] В настоящем документе «последовательность вариабельного домена иммуноглобулина» относится к последовательности аминокислот, которая может образовывать структуру вариабельного домена иммуноглобулина. Например, указанная последовательность может включать всю последовательность аминокислот встречающегося в природе вариабельного домена или ее часть. Например, указанная последовательность может включать или не включать одну, две или более N- или С-концевых аминокислот, или может включать другие изменения, которые совместимы с образованием белковой структуры.
[0095] В настоящем документе термин «содержащий» или «содержит» используют в отношении композиций, способов и их соответствующего компонента (или компонентов), имеющего или имеющих существенное значение для указанного способа или указанной композиции, но может включать и не указанные элементы, имеющие существенное значение или нет.
[0096] В настоящем документе термин «состоящий по существу из» относится к элементам, необходимым для определенного варианта реализации. Указанный термин допускает присутствие элементов, которые не оказывают существенного влияния на основную и новую или функциональную характеристику или характеристики указанного варианта реализации.
[0097] Термин «состоящий из» относится к композициям, способам и их соответствующим компонентам согласно описанию в настоящем документе, исключающим какой-либо элемент, не упоминаемый в описании указанного варианта реализации.
[0098] В настоящем описании и прилагаемой формуле изобретения формы единственного числа, в том числе сопровождаемые определением «указанный», включают соответствующие формы множественного числа, если иное явным образом не следует из контекста. Соответственно например, упоминание «указанного способа» включает один или более способов и/или этапов описанного в настоящем документе типа, и/или способов и/или этапов, которые будут очевидными для специалистов в данной области техники после прочтения настоящего описания, и т.д. Аналогичным образом, предполагается, что термин «или» включает «и», если из контекста явным образом не следует иное. Хотя при практической реализации или тестировании настоящего изобретения могут применяться способы и материалы, аналогичные или эквивалентные описанным в настоящем документе, подходящие способы и материалы описаны ниже. Выражение «например» используют в настоящем документе для описания неограничивающего примера.
[0099] За исключением рабочих примеров или иных указанных случаев все числа, отражающие количества ингредиентов или условия реакции согласно настоящему изобретению, во всех случаях должны быть истолкованы как модифицированные термином «приблизительно». Термин «приблизительно» применительно к процентам может означать ±1%. Настоящее изобретение дополнительно более подробно объяснено в приведенных ниже примерах, однако объем настоящего изобретения ими не ограничен.
[00100] Следует понимать, что настоящее изобретение не ограничено конкретной методологией, протоколами и реагентами, и т.п., описанными в настоящем документе, и, таким образом, могут варьировать. Терминология, используемая в настоящем документе, предназначена только для описания конкретных вариантов реализации, и не предназначена для ограничения объема настоящего изобретения, который определен исключительно формулой изобретения.
II. зкДНК-вектор
[00101] Согласно настоящему изобретению предложены новые невирусные бескапсидные молекулы зкДНК с ковалентно-замкнутыми концами (зкДНК). Указанные невирусные бескапсидные молекулы зкДНК могут быть продуцированы в пермиссивных клетках-хозяевах с экспрессионной конструкции (например, зкДНК-плазмиды, зкДНК-бакмиды, зкДНК-бакуловируса, или линией клеток в интегрированном состоянии), содержащей гетерологичный ген (трансген), расположенный между двумя разными последовательностями инвертированных концевых повторов (ITR), при этом ITR отличаются друг от друга. Согласно некоторым вариантам реализации один из ITR модифицирован делецией, инсерцией и/или заменой по сравнению с последовательностью ITR дикого типа (например, ITR AAV); и по меньшей мере один из ITR содержит функциональный сайт концевого разрешения (trs) и сайт связывания Rep. Указанный зкДНК-вектор предпочтительно является дуплексным, например, самокомплементарным, на протяжении по меньшей мере части молекулы, такой как экспрессионная кассета (например, зкДНК не является двуцепочечной кольцевой молекулой). ЗкДНК-вектор имеет ковал ентно замкнутые концы и, соответственно, устойчив к расщеплению экзонуклеазой (например, экзонуклеазой I или экзонуклеазой III), например, на протяжении часа при 37°С.
[00102] ЗкДНК-векторы согласно описанию в настоящем документе не имеют связанных с упаковкой ограничений, налагаемых ограниченным пространством внутри вирусного капсида. ЗкДНК-векторы представляют собой жизнеспособную альтернативу для продуцирования у эукариот вместо продуцирования у прокариот с плазмидных ДНК-векторов, в отличие от инкапсулированных геномов AAV. Это позволяет инсертировать контрольные элементы, например, регуляторные переключатели согласно описанию в настоящем документе, большие трансгены, несколько трансгенов и т.п.
[00103] Согласно одному аспекту зкДНК-вектор содержит, в направлении от 5' к 3': первый инвертированный концевой повтор (ITR) аденоассоциированного вируса (AAV), представляющую интерес нуклеотидную последовательность (например, экспрессионную кассету согласно описанию в настоящем документе) и второй ITR AAV, при этом первый ITR и второй ITR являются асимметричными друг относительно друга, то есть отличаются друг от друга. В примере варианта реализации первый ITR может представлять собой ITR дикого типа и второй ITR может представлять собой мутированный или модифицированный ITR. Согласно некоторым вариантам реализации первый ITR может представлять собой мутированный или модифицированный ITR, а второй ITR - ITR дикого типа. Согласно другому варианту реализации и первый ITR, и второй ITR модифицированы, однако имеют разные последовательности, или содержат разные модификации, или представляют собой модифицированные не идентичным образом ITR. Другими словами, указанные ITR являются асимметричными, в том смысле, что какие-либо изменения в одном ITR не отражаются на другом ITR; или, как вариант, где ITR отличаются друг от друга. Примеры ITR в указанном зкДНК-векторе и для применения при получении зкДНК-плазмиды обсуждаются ниже в разделе, названном «ITR».
[00104] Последовательности ITR дикого типа, или мутированные или иным образом модифицированные последовательности ITR согласно настоящему изобретению представляют собой последовательности ДНК, включенные в экспрессионную конструкцию (например, зкДНК-плазмиду, зкДНК-бакмиду, зкДНК-бакуловирус) для получения зкДНК-вектора. Соответственно, последовательности ITR, фактически содержащиеся в указанном зкДНК векторе, продуцированном с зкДНК-плазмиды или другой экспрессионной конструкции, могут быть или не быть идентичными предложенным последовательностям ITR согласно настоящему изобретению, что обусловлено естественными изменениями, происходящими в процессе получения (например, ошибкой репликации).
[00105] Согласно некоторым вариантам реализации описанный в настоящем документе зкДНК-вектор, содержащий экспрессионную кассету с трансгеном, который может представлять собой, например, регуляторную последовательность, последовательность, кодирующую нуклеиновую кислоту (например, такую как miR или антисмысловая последовательность), или последовательность, кодирующую полипептид (например, такую как трансген). Согласно одному варианту реализации указанный трансген может быть функционально связан с одной или более регуляторными последовательностями, которые допускают или контролируют экспрессию трансгена. Согласно одному варианту реализации указанный полинуклеотид содержит последовательность первого ITR и последовательность второго ITR, причем нуклеотидную последовательность, представляющая интерес, фланкирована указанными последовательностями первого и второго ITR, и указанные последовательности первого и второго ITR являются асимметричными друг относительно друга.
[00106] Согласно одному варианту реализации в каждом из указанных аспектов экспрессионная кассета локализована между двумя ITR, содержащимися вместе с чем-либо одним или более из перечисленного, в следующем порядке: промотор, функционально связанный с трансгеном, посттранскрипционный регуляторный элемент; и сигнал полиаденилирования и терминации. Согласно одному варианту реализации указанный промотор является регулируемым: индуцируемым или репрессируемым. Указанный промотор может представлять собой любую последовательность, которая облегчает транскрипцию трансгена. Согласно одному варианту реализации указанный промотор представляет собой промотор CAG (например, SEQ ID NO: 03) или его вариант. Указанный посттранскрипционный регуляторный элемент представляет собой последовательность который модулирует экспрессию трансгена, в неограничивающем примере - любую последовательность, которая образует третичную структуру, которая усиливает экспрессию трансгена.
[00107] Согласно одному варианту реализации указанный посттранскрипционный регуляторный элемент содержит WPRE (например, SEQ ID NO: 08). Согласно одному варианту реализации указанный сигнал полиаденилирования и терминации содержит поли(А) BGH (например, SEQ ID NO: 09). Дополнительно может быть использован любой цис-регуляторный элемент, известный в данной области техники, или их комбинация, например, энхансерная 5'-последовательность позднего сигнала полиаденилирования SV40 (USE), или другие элементы посттранскрипционного процессинга, в том числе, но не ограничиваясь перечисленными, ген тимидинкиназы вируса простого герпеса, или вируса гепатита В (HBV). Согласно одному варианту реализации длина экспрессионной кассеты в 5'-3' направлении больше известной максимальной длины для заключаемой в капсид вириона AAV последовательности. Согласно одному варианту реализации указанная длина превышает 4,6 т.п.о., или превышает 5 т.п.о., или превышает 6 т.п.о., или превышает 7 т.п.о. Примеры различных экспрессионных кассет приведены в настоящем документе.
[00108] Указанная экспрессионная кассета может содержать более 4000 нуклеотидов, 5000 нуклеотидов, 10 000 нуклеотидов или 20 000 нуклеотидов, или 30 000 нуклеотидов, или 40 000 нуклеотидов или 50 000 нуклеотидов, или любое количество от приблизительно 4000 до 10 000 нуклеотидов, или 10 000-50 000 нуклеотидов, или более чем 50 000 нуклеотидов. Согласно некоторым вариантам реализации указанная экспрессионная кассета может содержать трансген или нуклеиновую кислоту с длиной в диапазоне от 500 до 50 000 нуклеотидов. Согласно некоторым вариантам реализации указанная экспрессионная кассета может содержать трансген или нуклеиновую кислоту с длиной в диапазоне от 500 до 75 000 нуклеотидов. Согласно некоторым вариантам реализации указанная экспрессионная кассета может содержать трансген или нуклеиновую кислоту с длиной в диапазоне от 500 до 10 000 нуклеотидов. Согласно некоторым вариантам реализации указанная экспрессионная кассета может содержать трансген или нуклеиновую кислоту с длиной в диапазоне от 1000 до 10 000 нуклеотидов. Согласно некоторым вариантам реализации указанная экспрессионная кассета может содержать трансген или нуклеиновую кислоту с длиной в диапазоне от 500 до 5 000 нуклеотидов. ЗкДНК-векторы не имеют ограничений по размеру, как заключенные в капсид AAV-векторы, и, соответственно, позволяют обеспечить доставку экспрессионной кассеты большого размера для обеспечения эффективной экспрессии трансгенов. Согласно некоторым вариантам реализации указанный зкДНК-вектор лишен специфического прокариотического метилирования.
[00109] Указанная экспрессионная кассета может также содержать участок внутренней посадки рибосомы (DIES) и/или 2А-элемент.Цис-регуляторные элементы включают, не ограничиваясь перечисленными, промотор, рибопереключатель, инсулятор, миРНК-регулируемый элемент, посттранскрипционный регуляторный элемент, тканеспецифический и клеточноспецифический промотор и энхансер. Согласно некоторым вариантам реализации указанный ITR может действовать как промотор для трансгена. Согласно некоторым вариантам реализации указанный зкДНК-вектор содержит дополнительные компоненты для регуляции экспрессии указанного трансгена, например, регуляторный переключатель, который описан в настоящем документе в разделе «Регуляторные переключатели», для контроля и регуляции экспрессии указанного трансгена, и может содержать, если это требуется, регуляторный переключатель, который представляет собой «аварийный выключатель», позволяющий обеспечивать контролируемую клеточную смерть клетки, содержащей зкДНК-вектор.
[00110] Па фиг.1А-1С приведены схематические изображения неограничивающих примеров зкДНК-векторов, или соответствующая последовательность зкДНК-плазмид. ЗкДНК-векторы являются бескапсидными и могут быть получены с плазмиды, кодирующей, в указанном порядке: первый ITR, экспрессируемую трансгенную кассету и второй ITR, при этом по меньшей мере одна из последовательностей первого и/или второго ITR мутирована относительно соответствующей последовательности ITR AAV2 дикого типа. Указанная экспрессируемая трансгенная кассета предпочтительно включает, в указанном порядке, что-либо одно или более из перечисленного: энхансер/промотор, ORF-репортер (трансген), посттранскрипционный регуляторный элемент (например, WPRE); и сигнал полиаденилирования и терминации (например, поли(А) BGH).
[00111] Указанная экспрессионная кассета может содержать любой представляющий интерес трансген. Представляющие интерес трансгены включают, не ограничиваясь перечисленными, нуклеиновые кислоты, кодирующие полипептиды, или некодирующие нуклеиновые кислоты (например, РНК-интерференция, миРНК и т.п.), предпочтительно терапевтические (например, для медицинского, диагностического или ветеринарного применения) или иммуногенные (например, для вакцин) полипептиды. Согласно некоторым вариантам реализации трансгены в экспрессионной кассете кодирует что-либо одно или более из полипептидов, пептидов, рибозимов, пептидных нуклеиновых кислот, киРНК, РНКи, антисмысловых олигонуклеотидов, антисмысловых полинуклеотидов, антител, антигенсвязывающих фрагментов; или любую комбинацию перечисленного. Согласно некоторым вариантам реализации указанный трансген представляет собой терапевтический ген или маркерный белок. Согласно некоторым вариантам реализации указанный трансген представляет собой агонист или антагонист. Согласно некоторым вариантам реализации указанный антагонист представляет собой миметик или антитело, или фрагмент антитела, или его антигенсвязывающий фрагмент, например, нейтрализующее антитело или фрагмент антитела, и т.п. Согласно некоторым вариантам реализации указанный трансген кодирует антитело, в том числе полноразмерное антитело или фрагмент антитела согласно определению в настоящем документе. Согласно некоторым вариантам реализации указанное антитело представляет собой антигенсвязывающий домен или последовательность вариабельного домена иммуноглобулина согласно определению в настоящем документе.
[00112] В частности, указанный трансген может кодировать один или более терапевтических агентов, в том числе, но не ограничиваясь перечисленными, например, белок (белки), полипептид(ы), пептид(ы), фермент(ы), антитела, антигенсвязывающие фрагменты, а также их варианты и/или активные фрагменты, для применения в лечении, профилактике и/или для облегчения одного или более симптомов заболевания, дисфункции, повреждения и/или нарушения. Примеры трансгенов описаны в настоящем документе в разделе «Способ лечения».
[00113] Многие структурные признаки отличают зкДНК-векторы от экспрессионных векторов на основе плазмид. ЗкДНК-векторы могут характеризоваться одним или более из следующих признаков: отсутствие исходной (т.е. не инсертированной) бактериальной ДНК, отсутствие прокариотической точки начала репликации, автономность, т.е. они не требуют наличия каких-либо последовательностей, кроме двух ITR, включающих Rep-связывающий сайт и сайт концевого разрешения (RBS и TRS), и экзогенной последовательности между указанными ITR, присутствие последовательностей ITR, которые образуют шпильки, эукариотического происхождения (т.е. они продуцируются в эукариотических клетках); и отсутствие метилирования ДНК бактериального типа или же любого другого метилирования, воспринимаемого как аномальное организмом хозяина-млекопитающего. В целом, предпочтительно, чтобы предложенные векторы не содержали какой-либо прокариотической ДНК, однако предусмотрена возможность инсерции какой-либо прокариотической ДНК в виде экзогенной последовательности, согласно неограничивающему примеру, в промоторной или энхансерной области. Другой важный признак, отличающий зкДНК-векторы от плазмидных экспрессионных векторов, заключается в том, что зк ДНК-векторы представлены одноцепочечной линейной ДНК с замкнутыми концами, тогда как плазмиды всегда представлены двуцепочечной ДНК.
[00114] зкДНК-векторы, полученные способами, предложенными согласно настоящему изобретению, предпочтительно имеют линейную и непрерывную структуру, а не прерывистую структуру, по оценке на основании результатов анализа с расщеплением рестрикционными ферментами (фиг.4D). Линейная и непрерывная структура считается более стабильной при атаке клеточных эндонуклеаз, а также с меньшей вероятностью подвергается рекомбинации и вызывает мутагенез. Соответственно, зкДНК-вектор, имеющий линейную и непрерывную структуру, представляет собой предпочтительный вариант реализации. Непрерывный, линейный, одноцепочечный зкДНК-вектор с внутримолекулярными дуплексами может содержать ковалентно связанные концы, без последовательностей, кодирующих белки капсида AAV. Указанные зк ДНК-векторы структурно отличаются от плазмид (в том числе зкДНК-плазмид, описанных в настоящем документе), которые представляют собой кольцевые дуплексные молекулы нуклеиновых кислот бактериального происхождения. Комплементарные цепи плазмид могут быть разделены после денатурации с получением двух молекул нуклеиновой кислоты, тогда как зкДНК-векторы, напротив, хотя и содержат комплементарные цепи, представляют собой одну молекулу ДНК и, соответственно, даже после денатурации остаются в виде одной молекулы. Согласно некоторым вариантам реализации зкДНК-векторы согласно описанию в настоящем документе могут быть получены без метилирования оснований ДНК прокариотического типа, в отличие от плазмид. Соответственно, зкДНК-векторы и зкДНК-плазмиды отличаются как структурой (в частности, линейной или кольцевой), так и способами, которые применяют для получения и очищения указанных отличающихся объектов (см. ниже), а также метилированием ДНК, которое происходит по прокариотическому типу в зкДНК-плазмидах и по эукариотическому типу в зк ДНК-вектор е.
[00115]Некоторые преимущества зкДНК-вектора, описанного в настоящем документе, относительно экспрессионных векторов на основе плазмид, включают, не ограничиваясь перечисленным, следующие: 1) плазмиды содержат последовательности бактериальной ДНК и подвергаются специфическому прокариотическому метилированию, например, метилированию с образованием 6-метиладенозина и 5-метилцитозина, тогда как бескапсидные последовательности AAV-вектора имеют эукариотическое происхождение и не подвергаются специфическому прокариотическому метилированию; в результате бескапсидные AAV-векторы с меньшей вероятностью будут индуцировать воспалительные и иммунные ответы по сравнению с плазмидами; 2) плазмиды требуют наличия гена устойчивости в процессе получения, а зкДНК-векторы - нет; 3) кольцевая плазмида не доставляется в ядро при введении в клетку и требует избыточной нагрузки, чтобы обойти разложение клеточными нуклеазами, а зкДНК-векторы содержат вирусные цис-элементы, т.е. ITR, придающие устойчивость к нуклеазам, и могут быть сконструированы для нацеливания и доставки в ядро. Выдвинуто предположение, что минимальными определяющими элементами, обязательными для функции ITR, являются Rep-связывающий сайт (RBS; 5'-GCGCGCTCGCTCGCTC-3' (SEQ ID NO: 531) для AAV2) и сайт концевого разрешения (TRS; 5'-AGTTGG-3' (SEQ ID NO: 48) для AAV2), плюс вариабельная палиндромная последовательность, обеспечивающая образование шпильки; и 4) зкДНК-векторы не характеризуются часто обнаруживаемой в происходящих из прокариот плазмидах чрезмерной представленностью CpG-динуклеотидов, по имеющимся данными связывающихся с представителем Toll-подобного семейства рецепторов, вызывая опосредованный Т-клетками иммунный ответ. И напротив, трансдукция бескапсидными AAV-векторами согласно описанию в настоящем документе может обеспечивать эффективное нацеливание на типы клеток и тканей, которые трудно трансдуцировать стандартными вирионами AAV, с применением различных реагентов для доставки.
III. ITR
[00116] Согласно настоящему раскрытию зкДНК-векторы содержат гетерологичный ген, расположенный между двумя последовательностями инвертированных концевых повторов (ITR), которые отличаются друг от друга (т.е. представляют собой асимметричные ITR). Согласно некоторым вариантам реализации по меньшей мере один из ITR модифицирован делецией, инсерцией и/или заменой по сравнению с последовательностью ITR дикого типа (например, ITR AAV); и по меньшей мере один из ITR содержит функциональный сайт связывания Rep (RBS; например 5'-GCGCGCTCGCTCGCTC-3' для AAV2, SEQ ID NO: 531) и функциональный сайт концевого разрешения (TRS; например 5'-AGTT-3', SEQ ID NO: 46.) Согласно одному варианту реализации по меньшей мере один из ITR представляет собой нефункциональный ITR. Согласно одному варианту реализации указанные разные ITR не являются ITR дикого типа из разных серотипов.
[00117]Хотя иллюстративные ITR в описании и примерах в настоящем документе представляют собой ITR AAV2, специалисту в данной области техники известно, что, как было указано выше, могут быть использованы ITR любого известного парвовируса, например, депендовируса, такого как AAV (например, из генома AAV1, AAV2, AAV3, AAV4, AAV5, AAV 5, AAV7, AAV8, AAV9, AAV10, AAV11, AAV12, AAVrh8, AAVrh10, AAV-DJ и AAV-DJ8. Например, из NCBI: NC 002077; NC 001401; NC001729; NC001829; NC006152; NC 006260; NC 006261), химерные ITR или ITR из любого синтетического AAV. Согласно некоторым вариантам реализации указанный AAV может инфицировать теплокровных животных, как, например, аденоассоциированные вирусы птиц (AAAV), бычьих (BAAV), собачьих, лошадиных и овечьих. Согласно некоторым вариантам реализации указанный ITR взят из парвовируса В19 (№ доступа GenBank NC 000883), мелкого вируса мышей (MVM) (№ доступа GenBank NC 001510); парвовируса гусей (№ доступа GenBank NC 001701); парвовируса змей 1 (№доступа GenBank NC 006148).
[00118] Согласно некоторым вариантам реализации последовательность ITR может быть взята из вирусов семейства Parvoviridae, которое включает два подсемейства: Parvovirinae, которые инфицируют позвоночных, и Densovirinae, которые инфицируют насекомых, подсемейство Parvovirinae (называемое «парвовирусами») включает род Dependovirus, представителям которого, в большинстве условий, требуется коинфекция хелперным вирусом, таким как аденовирус или герпесвирус, для продуктивной инфекции. Род Dependovirus включает аденоассоциированный вирус (AAV), который обычно инфицирует человека (например, серотипы 2, 3А, 3В, 5 и 6) или приматов (например, серотипы 1 и 4), и родственные вирусы, которые инфицируют других теплокровных животных (например, аденоассоциированные вирусы бычьих, собачьих, лошадиных и овечьих). Парвовирусы и другие представители семейства Parvoviridae в общем описаны в источнике: Kenneth I. Berns, "Parvoviridae: The Viruses and Their Replication," Chapter 69 in FIELDS VIROLOGY (3d Ed. 1996).
[00119] Среднему специалисту в данной области техники известно, что последовательности ITR устроены одинаково и содержат двуцепочечную структуру Холлидея, которая, как правило, представляет собой Т-образную или Y-образную шпилечную структуру (см., например, фиг.2А и фиг.3А), при этом каждый ITR образован двумя палиндромными плечами или петлями (В-В' и С-С'), погруженными в палиндромное плечо большего размера (А-А'), и одноцепочечной последовательностью D (где порядок указанных палиндромных последовательностей определяет поворот ориентации ITR); можно легко определить соответствующие модифицированные последовательности ITR из любого серотипа AAV для применения в зкДНК-векторе или зкДНК-плазмида на основании примеров последовательностей ITR AAV2, предложенных согласно настоящему изобретению. См., например, описание структурного анализа и сравнения последовательностей ITR из разных серотипов AAV (AAV1-AAV6) в источниках: Grimm et al., J. Virology, 2006; 80(1); 426-439; Yan et al, J. Virology, 2005; 364-379; Duan et al., Virology 1999; 261; 8-14.
[00120] В настоящем документе подробно описаны специфические изменения и мутации ITR, но в контексте ITR «измененный» или «мутированный» показывает, что нуклеотиды были инсертированы, делетированы и/или заменены относительно последовательности ITR дикого типа, референсной или исходной последовательности ITR, и могут быть изменены относительно другого фланкирующего ITR в зкДНК-векторе, содержащем два фланкирующих ITR. Измененный или мутированный ITR может представлять собой сконструированный ITR. В настоящем документе «сконструированный» относится к аспекту, подвергнутому манипуляциям, осуществляемыми руками человека. Например, полипептид считают «сконструированным», если по меньшей мере в одном аспекте указанный полипептид, например, его последовательность, был подвергнут манипуляциям, осуществляемым руками человека, таким образом, чтобы он отличался от существующего в природе в указанном аспекте.
[00121] Согласно некоторым вариантам реализации ITR может быть синтетическим. Согласно одному варианту реализации синтетический ITR основан на последовательностях ITR из более чем одного серотипа AAV. Согласно другому варианту реализации синтетический ITR не включает последовательность на основе AAV. Согласно еще одному варианту реализации синтетический ITR сохраняет структуру ITR, описанную выше, хотя содержит только некоторые взятые из AAV последовательности или не содержит таких последовательностей. Согласно некоторым аспектам синтетический ITR может взаимодействовать преимущественно с Rep дикого типа или Rep специфического серотипа, или, в некоторых случаях, его не будет распознавать Rep дикого типа, а будет распознавать только мутированный Rep.
[00122] Последовательности ITR устроены одинаково и содержат двуцепочечную структура Холлидея, которая, как правило представляет собой Т-образную или Y-образную шпилечную структуру (см., например, фиг.2А и фиг.3А), при этом каждый ITR образован двумя палиндромными плечами или петлями (В-В' и С-С'), погруженными в палиндромное плечо большего размера (А-А'), и одноцепочечной последовательностью D (где порядок указанных палиндромных последовательностей определяет поворот ориентации ITR). Специалист в данной области техники может легко определить последовательности ITR или модифицированные последовательности ITR из любого серотипа AAV для применения в зкДНК-векторе или зкДНК-плазмиде, на основании примеров последовательностей ITR AAV2, предложенных согласно настоящему изобретению. См., например, сравнение последовательностей ITR из разных серотипов AAV (AAV1 - AAV6, AAV птиц (AAAV) и бычий AAV (BAAV)), описанное в источнике: Grimm et al., J. Virology, 2006; 80(1); 426-439; где приведен % идентичности левого ITR AAV2 и левого ITR из других серотипов: AAV-1 (84%), AAV-3 (86%), AAV-4 (79%), AAV-5 (58%), AAV-6 (левый ITR) (100%) и AAV-6 (правый ITR) (82%).
[00123] Соответственно, хотя в качестве примеров ITR в зкДНК-векторах согласно настоящему изобретению используют ITR AAV2, зкДНК-вектор согласно описанию в настоящем документе может быть получен с ITR или основан на ITR любого известного серотипа AAV, включая, например, серотип AAV 1 (AAV1), серотип AAV 2 (AAV2), серотип AAV 4 (AAV4), серотип AAV 5 (AAV5), серотип AAV 6 (AAV6), серотип AAV 7 (AAV7), серотип AAV 8 (AAV8), серотип AAV 9 (AAV9), серотип AAV 10 (AAV10), серотип AAV 11 (AAV11) или серотип AAV 12 (AAV12). Специалист может определить соответствующую последовательность в других серотипах с применением известных способов, например, путем определения местоположения изменения: в области А, А', В, В', С, С или D, и определения соответствующей области в другом серотипе. Может быть использован BLAST® (Basic Local Alignment Search Tool) или другая программа для выравнивания гомологичных последовательностей в статусе по умолчанию, чтобы определить соответствующую последовательность. Согласно настоящему изобретению также предложены популяции и совокупности зкДНК-векторов, содержащих ITR из комбинации разных серотипов AAV то есть один ITR может быть взят из одного серотипа AAV, а другой ITR может быть взят из другого серотипа. Без связи с теорией, согласно одному варианту реализации один ITR может быть взят из последовательности ITR AAV2 или основан на ней, а другой ITR указанного зкДНК-вектора может быть взят из любой одной или более последовательностей или основан на любой одной или более последовательностях ITR серотипа AAV 1 (AAV1), серотипа AAV 4 (AAV4), серотипа AAV 5 (AAV5), серотипа AAV 6 (AAV6), серотипа AAV 7 (AAV7), серотипа AAV 8 (AAV8), серотипа AAV 9 (AAV9), серотипа AAV 10 (AAV10), серотипа AAV 11 (AAV11) или серотипа AAV 12 (AAV12).
[00124] Любой парвовирус ITR может применяться в качестве ITR или в качестве основы ITR для модификации. Предпочтительно, указанный парвовирус представляет собой депендовирус. Более предпочтительно, он представляет собой AAV. Выбор серотипа может быть основан на тропизме указанного серотипа к ткани. AAV2 обладает тропизмом к широкому ряду тканей, AAV1 преимущественно нацелен на нервную ткань и скелетные мышцы, a AAV5 преимущественно нацелен на нервную ткань, пигментный эпителий сетчатки, и фоторецепторы. AAV6 преимущественно нацелен на скелетные мышцы и легкие. AAV8 преимущественно нацелен на печень, скелетные мышцы, сердце, и ткани поджелудочной железы. AAV9 преимущественно нацелен на печень, скелетные ткани и ткани легких. Согласно одному варианту реализации модифицированный ITR основан на ITR AAV2. Например, он выбран из группы, состоящей из: SEQ ID NO: 2 и SEQ ID NO: 52. Согласно одному варианту реализации каждого из указанных аспектов векторного полинуклеотида содержит пару ITR, выбранную из группы, состоящей из: SEQ ID NO: 1 и SEQ ID NO: 52; и SEQ ID NO: 2 и SEQ ID NO: 51. Согласно одному варианту реализации каждого из указанных аспектов векторного полинуклеотида или невирусные бескапсидные ДНК-векторы с ковалентно-замкнутыми концами содержат пару разных ITR, выбранных из группы, состоящей из: SEQ ID NO: 101 и SEQ ID NO: 102; SEQ ID NO: 103 и SEQ ID NO: 104, SEQ ID NO: 105 и SEQ ID NO: 106; SEQ ID NO: 107 и SEQ ID NO: 108; SEQ ID NO: 109 и SEQ ID NO: 110; SEQ ID NO: 111 и SEQ ID NO: 112; SEQ ID NO: 113 и SEQ ID NO: 114; и SEQ ID NO: 115 и SEQ ID NO: 116. Согласно некоторым вариантам реализации модифицированный ITR выбирают из любого из ITR или частичных последовательностей ITR из SEQ ID NO: 2, 52, 63, 64, 101-499 или 545-547.
[00125] Согласно некоторым вариантам реализации зкДНК-вектор может содержать ITR с модификацией в ITR, соответствующей любым из модификаций в последовательностях ITR или частичных последовательностях ITR, представленных в любой одной или более таблицах из 2, 3, 4, 5, 6, 7, 8, 9, 10А и 10 В в настоящем документе, или последовательностях, представленных на фиг.26А или 26В.
[00126] Согласно некоторым вариантам реализации зкДНК могут образовывать внутримолекулярную дуплексную вторичную структуру. Примеры вторичной структуры первого ITR и асимметричного второго ITR представлены в контексте структур ITR дикого типа (см., например, фиг.2А, 3А, 3С) и модифицированных ITR (см., например, фиг.2В и фиг. 3В, 3D). Вторичные структуры выводят или предсказывают на основании последовательностей ITR плазмиды, используемых для получения зкДНК-вектора. Примеры вторичных структур модифицированных ITR, где удалена часть структуры «петля на стебле», показаны на фиг.9А 25В и фиг.26А-26В, а также приведены в таблицах 10А и 10В. Примеры вторичных структур модифицированных ITR, содержащих единственный стебель и две петли, показаны на фиг.9А 13В. Пример вторичной структуры модифицированного ITR с единственным стеблем и единственной петлей показан на фиг.14. Согласно некоторым вариантам реализации вторичная структура может быть выведена согласно описанию в настоящем документе с применением термодинамических способов на основании правил ближайшего соседа, предсказывающих стабильность структуры по количественной оценке изменения свободной энергии укладки. Например, структура может быть предсказана путем нахождения структуры с наименьшей свободной энергией. Согласно некоторым вариантам реализации может применяться алгоритм, описанный в источнике: Reuter, J. S., & Mathews, D. H. (2010) RNAstructure: software for RNA secondary structure prediction and analysis. BMC Bioinformatics. 11,129 и реализованный в программном обеспечении RNAstructure (доступно в сети Интернет по адресу: «rna.urmc.rochester.edu/RNAstructureWeb/index.html») для предсказания структуры ITR. Указанный алгоритм может также включать как показатели изменения свободной энергии при 37°С, так и показатели изменения энтальпии из опубликованных экспериментальных данных, для предсказания стабильности конформации при произвольной температуре. С применением программного обеспечения RNAstructure некоторые из структур модифицированных ITR могут быть предсказаны как модифицированные Т-образные структуры типа «петля на стебле» с расчетным изменением свободной энергии Гиббса (AG) для разворачивания в физиологических условиях, приведенным на фиг.3A-13D. При применении программного обеспечения RNAstructure три типа модифицированных ITR характеризуются предсказанной свободной энергией Гиббса для разворачивания, превышающей значения для ITR дикого типа AAV2 (-92,9 ккал/моль), и представлены следующими ITR: (а) Модифицированный ITR, имеющий структуру с единственным плечом/с единственной неспаренной петлей, предложенную согласно настоящему изобретению, с предсказанным значением свободной энергии Гиббса для разворачивания, варьирующим в диапазоне от -85 до -70 ккал/моль. (b) Модифицированный ITR, имеющий структуру с одной шпилькой, предложенную согласно настоящему изобретению, с предсказанным значением свободной энергии для разворачивания, варьирующим в диапазоне от -70 до -40 ккал/моль. (с) Модифицированный ITR, имеющий структуру с двумя плечами, предложенную согласно настоящему изобретению, с предсказанным значением свободной энергии Гиббса для разворачивания, варьирующим в диапазоне от -90 до -70 ккал/моль. Без связи с какой-либо теорией, структуры с большей свободной энергией Гиббса легче разворачиваются для репликации по действием белков репликации Rep 68 или Rep 78. Соответственно, модифицированные ITR, характеризующиеся более высокими значениями свободной энергии Гиббса для разворачивания - например, структура с единственным плечом/с единственной неспаренной петлей, структура с одной шпилькой, усеченная структура отличает тенденция к более эффективной репликации по сравнению с ITR дикого типа.
[00127] Согласно одному варианту реализации левый ITR указанного зкДНК-вектора модифицирован или мутирован относительно структуры ITR AAV дикого типа (wt), а правый ITR представляет собой ITR AAV дикого типа. Согласно одному варианту реализации правый ITR указанного зкДНК-вектора модифицирован относительно структуры ITR AAV дикого типа, а левый ITR представляет собой ITR AAV дикого типа. Согласно такому варианту реализации модификация ITR (например, левого или правого ITR) может быть получена путем делеции, инсерции или замены одного или более нуклеотидов ITR дикого типа, происходящего из генома AAV.
[00128] ITR, применяемые согласно настоящему изобретению, могут быть разрешаемыми и неразрешаемыми, и для применения в зкДНК-векторах предпочтительно выбирают последовательности AAV, при этом предпочтительными являются серотипы 1, 2, 3, 4, 5, 6, 7, 8 и 9. Для разрешаемых ITR AAV не нужна последовательность ITR дикого типа (например, эндогенная последовательность или последовательность ITR AAV дикого типа может быть изменена путем инсерции, делеции, усечения и/или миссенс-мутаций), при условии, что концевой повтор опосредует требуемые функции, например, репликацию вируса, упаковку вируса, интеграцию вируса и/или спасение провируса, и т.п.Как правило, хотя не обязательно, ITR взяты из одного серотипа AAV, например, обе последовательности ITR указанного зкДНК-вектора взяты из AAV2. Указанные ITR могут представлять собой синтетические последовательности, которые функционируют как инвертированные концевые повторы AAV, например, «двойная последовательность D» согласно описанию в патенте США №5478745, выданном Samulski et al. Хотя это и не обязательно, ITR могут быть взяты из одного и того же парвовируса, например, обе последовательности ITR взяты из AAV2.
[00129] Согласно одному варианту реализации зкДНК может включать структуру ITR, мутированную относительно одного из ITR дикого типа согласно описанию в настоящем документе, однако при этом мутантный или модифицированный ITR сохраняет функциональный сайт связывания Rep (RBE или RBE') и сайт концевого разрешения (trs). Согласно одному варианту реализации указанный мутант зкДНК ITR включает функциональный сайт для белка репликации (RPS-1), и при продуцировании используют репликативно-компетентный белок, который связывает указанный сайт RPS-1.
[00130] Согласно одному варианту реализации по меньшей мере один из ITR представляет собой дефектный ITR в отношении связывания Rep и/или никирования Rep.Согласно одному варианту реализации указанный дефект заключается по меньшей мере в 30% снижении относительно ITR дикого типа, согласно другим вариантам реализации он заключается в снижении по меньшей мере на 35%…, 50%…, 65%…, 75%…, 85%…, 90%…, 95%…, 98%…, или полном отсутствии функции, или в любой промежуточной степени снижения. Клетки-хозяева не экспрессируют белки вирусного капсида, и матрица векторного полинуклеотида не содержит каких-либо кодирующих вирусный капсид последовательностей. Согласно одному варианту реализации матрицы векторного полинуклеотида и клетки-хозяева, которые не содержат генов капсида AAV, и итоговый белок также не кодирует и не экспрессирует гены капсидов других вирусов. Кроме того, согласно конкретному варианту реализации молекула нуклеиновой кислоты также не содержит кодирующих последовательностей белка Rep AAV.
[00131] Согласно некоторым вариантам реализации структурный элемент ITR может быть представлен любым структурным элементом, который вовлечен в функциональное взаимодействие ITR с большим белком Rep (например, Rep 78 или Rep 68). Согласно некоторым вариантам реализации указанный структурный элемент обеспечивает селективность взаимодействия ITR с большим белком Rep, т.е. определяет, по меньшей мере отчасти, какой белок Rep функционально взаимодействует с ITR. Согласно другим вариантам реализации указанный структурный элемент физически взаимодействует с большим белком Rep при связывании указанного белка Rep с ITR. Каждый структурный элемент может представлять собой, например, вторичную структуру ITR, нуклеотидную последовательность ITR, промежуток между двумя или более элементами; или комбинацию каких-либо перечисленных элементов. Согласно одному варианту реализации указанные структурные элементы выбраны из группы, состоящей из плеча А и плеча А', плеча В и плеча В', плеча С и плеча С', плеча D, сайта связывания Rep (RBE) и RBE' (т.е. комплементарной RBE последовательности), и сайта концевого разрешения (trs).
[00132] Более конкретно, способность структурного элемента к функциональному взаимодействию с конкретным большим белком Rep может быть изменена путем модификации указанного структурного элемента. Например, нуклеотидную последовательность структурного элемента может быть модифицирована относительно последовательности ITR дикого типа. Согласно одному варианту реализации указанный структурный элемент (например, плечо А, плечо А', плечо В, плечо В', плечо С, плечо С', плечо D, RBE, RBE' и trs) ITR может быть удален и заменен структурным элементом дикого типа из другого парвовируса. Например, структура для замены может быть взята из AAV1, AAV2, AAV3, AAV4, AAV5, AAV6, AAV7, AAV8, AAV9, AAV10, AAV11, AAV12, AAV 13, парвовируса змей (например, парвовируса королевского питона), парвовируса бычьих, парвовируса коз, парвовируса птиц, парвовирус собачьих, парвовируса лошадиных, парвовируса креветок, свиного парвовируса или AAV насекомых. Например, ITR может представлять собой ITR AAV2, а плечо А или А', или RBE могут быть заменены структурным элементом из AAV5. Согласно другому примеру ITR может представлять собой ITR AAV5, а плечи С или С, RBE и trs могут быть заменены структурным элементом из AAV2. Согласно другому примеру ITR AAV может представлять собой ITR AAV5, где плечи В и В' заменены плечами В и В' ITR AAV2.
[00133] Например, в таблице 1 приведены примеры модификаций по меньшей мере одного нуклеотида (например, делеции, инсерции и/или замены) в областях модифицированных ITR, где X указывает на модификацию по меньшей мере одной нуклеиновой кислоты (например, делецию, инсерцию и/или замену) в указанном отделе относительно соответствующего ITR дикого типа. Согласно некоторым вариантам реализации при любой модификации по меньшей мере одного нуклеотида (например, делеции, инсерции и/или замены) в любой из областей С и/или С и/или В и/или В' сохраняются три последовательных нуклеотида Т (т.е. ТТТ) по меньшей мере в одной концевой петле. Например, если модификация приводит к чему-либо из: ITR с единственным плечом (например, с единственным плечом С-С' или единственным плечом В-В'), или с модифицированным плечом С-В' или плечом С'-В, или ITR с двумя плечами, содержащий по меньшей мере одно усеченное плечо (например, усеченное плечо С-С' и/или усеченное плечо В-В'), по меньшей мере в указанном единственном плече, или по меньшей мере в одном из плечей ITR с двумя плечами (где одно плечо может быть усеченным) сохраняются три последовательных нуклеотида Т (т.е. ТТТ) по меньшей мере в одной концевой петле. Согласно некоторым вариантам реализации усеченное плечо С-С и/или усеченное плечо В-В' содержит три последовательных нуклеотида Т (т.е. ТТТ) в концевой петле.
[00134] Таблица 1: Примеры комбинаций модификаций по меньшей мере одного нуклеотида (например, делеции, инсерции и/или замены) в разных областях или плечах В-В' и С-С' ITR (X указывает на модификацию нуклеотида, например, добавление, делецию или замену по меньшей мере одного нуклеотида в области).
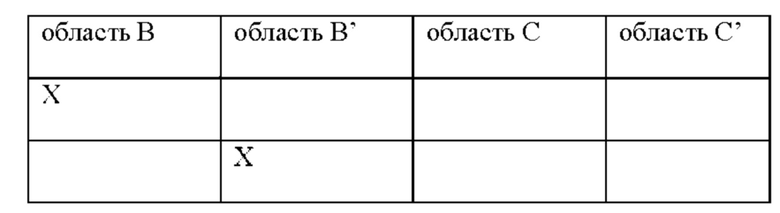
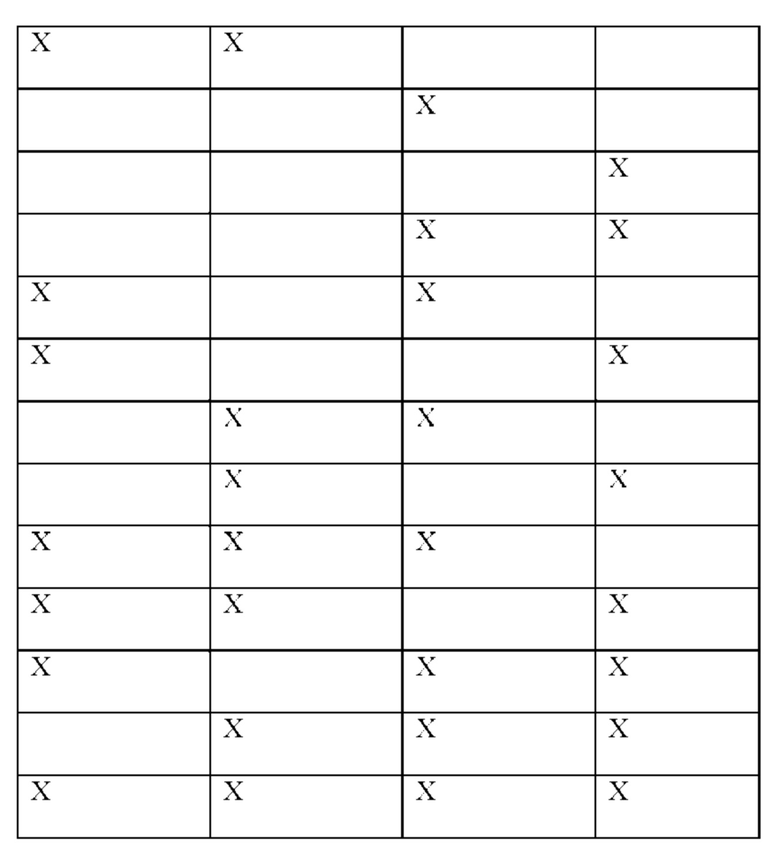
[00135] Согласно некоторым вариантам реализации модифицированный ITR для применения согласно настоящему изобретению может содержать любую из комбинаций модификаций, приведенных в таблице 1, а также модификацию по меньшей мере одного нуклеотида в любой одной или более из областей, выбранных из: области между А' и С, между С и С', между С' и В, между В и В' и между В' и А. Согласно некоторым вариантам реализации при любой модификации по меньшей мере одного нуклеотида (например, делеции, инсерции и/или замене) в областях С, или С', или В, или В', все же сохраняется концевая петля «петли на стебле». Согласно некоторым вариантам реализации при любой модификации по меньшей мере одного нуклеотида (например, делеции, инсерции и/или замене) между С и С' и/или В и В' сохраняются три последовательных нуклеотида Т (т.е. ТТТ) по меньшей мере в одной концевой петле. Согласно альтернативным вариантам реализации при любой модификации по меньшей мере одного нуклеотида (например, делеции, инсерции и/или замене) между С и С' и/или В и В' сохраняются три последовательных нуклеотида А (т.е. AAA) по меньшей мере в одной концевой петле. Согласно некоторым вариантам реализации модифицированный ITR для применения согласно настоящему изобретению может содержать любую из комбинаций модификаций, приведенных в таблице 1, а также модификацию по меньшей мере одного нуклеотида (например, делецию, инсерцию и/или замену) в любой одной или более из областей, выбранных из: А', А и/или D. Например, согласно некоторым вариантам реализации модифицированный ITR для применения согласно настоящему изобретению может содержать любую из комбинаций модификаций, приведенных в таблице 1, а также модификацию по меньшей мере одного нуклеотида (например, делецию, инсерцию и/или замену) в области А. Согласно некоторым вариантам реализации модифицированный ITR для применения согласно настоящему изобретению может содержать любую из комбинаций модификаций, приведенных в таблице 1, а также модификацию по меньшей мере одного нуклеотида (например, делецию, инсерцию и/или замену) в области А'. Согласно некоторым вариантам реализации модифицированный ITR для применения согласно настоящему изобретению может содержать любую из комбинаций модификаций, приведенных в таблице 1, а также модификацию по меньшей мере одного нуклеотида (например, делецию, инсерцию и/или замену) в области А и/или А'. Согласно некоторым вариантам реализации модифицированный ITR для применения согласно настоящему изобретению может содержать любую из комбинаций модификаций, приведенных в таблице 1, а также модификацию по меньшей мере одного нуклеотида (например, делецию, инсерцию и/или замену) в области D.
[00136] Согласно одному варианту реализации нуклеотидную последовательность структурного элемента может быть модифицирована (например, путем модификации 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20 или более нуклеотидов, или любого числа нуклеотидов в имеющемся диапазоне) для получения модифицированного структурного элемента. Примеры специфических модификаций ITR согласно одному варианту реализации приведены в настоящем документе (например, SEQ ID NO: 2, 52, 63, 64, 101-499, или 545 547). Согласно некоторым вариантам реализации ITR может быть модифицирован (например, путем модификации 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, или 20, или более нуклеотидов, или любого числа нуклеотидов в имеющемся диапазоне). Согласно другим вариантам реализации последовательность указанного ITR может быть по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 96%, по меньшей мере на 97%, по меньшей мере на 98%, по меньшей мере на 99% или более идентична последовательности одного из модифицированных ITR из SEQ ID NO: 469 499 или 545-547, или RBE-содержащего отдела плеча А-А' и плеч С-С' и В-В' из SEQ ID NO: 101-134 или 545-547.
[00137] Согласно некоторым вариантам реализации модифицированный ITR может например, включать удаление или делецию всего конкретного плеча, например, всего плеча или части плеча А-А', или всего плеча или части плеча В-В' или всего плеча или части плеча С-С', или, как вариант, удаление 1, 2, 3, 4, 5, 6, 7, 8, 9 или более пар оснований, образующих стебель петли, при условии, что последняя петля наверху стебля (например, одно плечо) все еще присутствует (например, см. ITR-6). Согласно некоторым вариантам реализации модифицированный ITR может включать удаление 1, 2, 3, 4, 5, 6, 7, 8, 9 или более пар оснований из плеча В-В'. Согласно некоторым вариантам реализации модифицированный ITR может включать удаление 1, 2, 3, 4, 5, 6, 7, 8, 9 или более пар оснований из плеча С-С'. Согласно некоторым вариантам реализации модифицированный ITR может включать удаление 1, 2, 3, 4, 5, 6, 7, 8, 9 или более пар оснований из плеча С-С' и удаление 1, 2, 3, 4, 5, 6, 7, 8, 9 или более пар оснований из плеча В-В'. Предусмотрена любая комбинация удаления пар оснований, например, может быть удалено 6 пар оснований в плече С-С' и 2 пары оснований в плече В-В'. В иллюстративном примере на фиг.13А-13 В показан пример модифицированного ITR, где делетировано по меньшей мере 7 пар оснований и из части С, и из части С', заменен нуклеотид в петле между областями С и С', и делетирована по меньшей мере одна пара оснований и из части В, и из части В', таким образом, что указанный модифицированный ITR содержит два плеча, по меньшей мере одно из которых (например, С-С') является усеченным. Отметим, что в указанном примере, поскольку модифицированный ITR содержит делецию по меньшей мере одной пары оснований в каждой из областей В и В', плечо В-В' также усечено относительно WT ITR.
[00138] Согласно некоторым вариантам реализации 1, 2, 3, 4, 5, 6, 7, 8, 9 или более комплементарных пар оснований удаляют и из части С, и из части С' плеча С-С' таким образом, что происходит усечение плеча С-С', то есть если основание удаляют в части С плеча С-С', удаляют и комплементарную пару оснований в части С, с усечением таким образом плеча С-С'. Согласно таким вариантам реализации из плеча С-С' удаляют 2, 4, 6, 8 или более пар оснований таким образом, что происходит усечение плеча С-С'. Согласно альтернативным вариантам реализации 1, 2, 3, 4, 5, 6, 7, 8, 9 или более пар оснований удаляют из части С плеча С-С' таким образом, что остается только часть С' плеча. Согласно альтернативным вариантам реализации 1, 2, 3, 4, 5, 6, 7, 8, 9 или более пар оснований удаляют из части С' плеча С-С' таким образом, что остается только часть С плеча.
[00139] Согласно некоторым вариантам реализации 1, 2, 3, 4, 5, 6, 7, 8, 9 или более комплементарных пар оснований удаляют из каждой из частей В и В' плеча В-В' таким образом, что происходит усечение плеча В-В', то есть если основание удаляют в части В плеча В-В', удаляют и комплементарную пару оснований в части В', с усечением таким образом плеча В-В'. Согласно таким вариантам реализации из плеча В-В' удаляют 2, 4, 6, 8 или более пар оснований таким образом, что происходит усечение плеча В-В'. Согласно альтернативным вариантам реализации из части В плеча В-В' удаляют 1, 2, 3, 4, 5, 6, 7, 8, 9 или более пар оснований таким образом, что остается только часть В' плеча. Согласно альтернативным вариантам реализации из части В' плеча В-В' удаляют 1, 2, 3, 4, 5, 6, 7, 8, 9 или более пар оснований таким образом, что остается только часть В плеча.
[00140] Согласно некоторым вариантам реализации модифицированный ITR может содержать от 1 до 50 (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49 или 50) делеции нуклеотидов относительно полноразмерного ITR дикого типа последовательность. Согласно некоторым вариантам реализации модифицированный ITR может содержать от 1 до 30 делеции нуклеотидов относительно последовательности полноразмерного WT ITR. Согласно некоторым вариантам реализации модифицированный ITR содержит от 2 до 20 делеции нуклеотидов относительно последовательности полноразмерного ITR дикого типа.
[00141]Согласно некоторым вариантам реализации модифицированный ITR образует две противостоящих продольно-асимметричных «петли на стебле», например, длина петли С-С' отличается от длины петли В-В'. Согласно некоторым вариантам реализации длина части С-С' и/или В-В' стебля одной из противостоящих продольно-асимметричных «петель на стебле» модифицированного ITR находится в диапазоне от 8 до 10 пар оснований, а часть с петлей (например, между С-С' или между В-В') содержит 2-5 неспаренных дезоксирибонуклеотидов. Согласно некоторым вариантам реализации одна из продольно-асимметричных «петель на стебле» модифицированного ITR содержит часть С-С' и/или В-В' стебля длиной менее чем 8, или менее чем 7, 6, 5, 4, 3, 2, 1 пар оснований, и часть с петлей (например, между С-С' или между В-В') содержит 0 5 нуклеотидов. Согласно некоторым вариантам реализации модифицированный ITR с продольно-асимметричной «петлей на стебле» содержит часть С-С' и/или В-В' стебля длиной менее чем 3 пар оснований.
[00142] Согласно некоторым вариантам реализации модифицированный ITR не содержит каких-либо делеции нуклеотидов в RBE-содержащей части областей А или А, чтобы не мешать репликации ДНК (например, связыванию с RBE белка Rep, или никированию в сайте концевого разрешения). Согласно некоторым вариантам реализации модифицированный ITR, предложенный для применения согласно настоящему изобретению, содержит одну или более делеции в области В, В', С и/или С согласно описанию в настоящем документе. Некоторые неограничивающие примеры модифицированных ITR приведены на фиг.9А-26В.
[00143] Согласно некоторым вариантам реализации модифицированный ITR может включать делецию плеча В-В', так что остается плечо С-С', например, см. примеры ITR-2 (левого) и ITR-2 (правого) на фиг.9А-9В, и ITR-4 (левого), и для ITR-4 (правого) (фиг.11А-11 В). Согласно некоторым вариантам реализации модифицированный ITR может включать делецию плеча С-С', так что остается плечо В-В', например, см. примеры ITR-3 (левого), и для ITR-3 (правого), приведенные на фиг.10А-10В. Согласно некоторым вариантам реализации модифицированный ITR может включать делецию плеча В-В' и плеча С-С', так что остается единственная «петля на стебле», например, см. примеры ITR-6 (левого), и для ITR-6 (правого), приведенные на фиг. 14А-14В, а также ITR-21 и ITR-37. Согласно некоторым вариантам реализации модифицированный ITR может включать делецию области С', так что остается усеченная С-петля и плечо В-В', например, см. примеры ITR-1 (левого) и ITR-1 (правого), приведенные на фиг. 15А-15В. Аналогичным образом, согласно некоторым вариантам реализации модифицированный ITR может включать делецию области С, так что остается усеченная С'-петля и плечо В-В', например, см. примеры ITR-5 (левого) и ITR-5 (правого), приведенные на фиг. 16А-16В.
[00144] Согласно некоторым вариантам реализации модифицированный ITR может включать делецию пар оснований в любой одной или более из частей: С, С', В или В', таким образом, что между частями С-В' и частями С'-В происходит спаривание комплементарных оснований с получением единственного плеча, например, см. ITR-10 (справа) и ITR-10 (слева) (фиг. 12А-12В).
[00145] Согласно некоторым вариантам реализации наряду с модификацией одного или более нуклеотидов в областях С, С', В и/или В', модифицированный ITR для применения согласно настоящему изобретению может включать модификацию (например, делецию, замену или добавление) по меньшей мере 1, 2, 3, 4, 5, 6 нуклеотидов в любой одной или более областей, выбранных из: области между А' и С, между С и С', между С и В, между В и В' и между В' и А. Например, нуклеотид между В' и С в модифицированном правом ITR может быть заменен с nA на G, С или А, или делетирован, или один или более нуклеотидов может быть добавлен; нуклеотид между С и В в модифицированном левом ITR может быть изменен с Т на G, С или А, или делетирован, или один или более нуклеотидов может быть добавлен.
[00146] Согласно некоторым вариантам реализации настоящего изобретения зкДНК-вектор не содержит модифицированного ITR, состоящего из последовательности нуклеотидов, выбранной из какой-либо из SEQ ID NO: 550-557. Согласно некоторым вариантам реализации настоящего изобретения зкДНК-вектор не содержит модифицированного ITR, содержащего нуклеотидную последовательность, выбранную из какой-либо из SEQ ID NO: 550-557.
[00147] Согласно некоторым вариантам реализации указанный зкДНК-вектор содержит регуляторный переключатель согласно описанию в настоящем документе, и выбранный модифицированный ITR с последовательностью нуклеотидов, выбранной из любой последовательности из группы, состоящей из: SEQ ID NO: 550 557.
[00148] Согласно другому варианту реализации структура структурного элемента может быть модифицирована. Например, в структурном элементе изменяют высоту стебля и/или число нуклеотидов в петле. Например, высота стебля может составлять приблизительно 2, 3, 4, 5, 6, 7, 8 или 9 нуклеотидов, или более, или соответствовать любому числу в имеющемся диапазоне. Согласно одному варианту реализации высота стебля может составлять от приблизительно 5 нуклеотидов до приблизительно 9 нуклеотидов, и он функционально взаимодействует с Rep. Согласно другому варианту реализации высота стебля может составлять приблизительно 7 нуклеотидов, и он функционально взаимодействует с Rep. Согласно другому примеру петля может содержать 3, 4, 5, 6, 7, 8, 9 или 10 нуклеотидов, или более, или любое число нуклеотидов в имеющемся диапазоне.
[00149] Согласно другому варианту реализации число сайтов связывания GAGY или связанных с GAGY сайтов связывания в пределах RBE или расширенного RBE может быть увеличено или уменьшено. Согласно одному примеру RBE или расширенный RBE может содержать 1, 2, 3, 4, 5 или 6, или более сайтов связывания GAGY, или любое число сайтов связывания в имеющемся диапазоне. Каждый сайт связывания GAGY может независимо представлять собой точную последовательность GAGY или последовательность, аналогичную GAGY при условии, что указанная последовательность является достаточной для связывания белков Rep.
[00150] Согласно другому варианту реализации промежуток между двумя элементами (например, не ограничиваясь указанным, RBE и шпилькой) может быть изменен (например, увеличен или уменьшен) для изменения функционального взаимодействия с большим белком Rep. Например, указанный промежуток может составлять приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или 21 нуклеотидов или более, или содержать любое число нуклеотидов в имеющемся диапазоне.
[00151] Описанный в настоящем документе зкДНК-вектор может включать структуру ITR, модифицированную относительно структуры ITR AAV2 дикого типа согласно описанию в настоящем документе, однако все еще содержащую функциональную часть RBE, trs и RBE'. На фиг. 2А и фиг. 2В представлен один возможный механизм действия сайта trs в пределах структуры дикого типа ITR-части зкДНК-вектора. Согласно некоторым вариантам реализации указанный зкДНК-вектор содержит одну или более функциональных последовательностей полинуклеотидов ITR, которые содержат Rep-связывающий сайт (RBS; 5'-GCGCGCTCGCTCGCTC-3' (SEQ ГО NO: 531) для AAV2) и сайт концевого разрешения (TRS; 5'-AGTT (SEQ ID NO: 46)). Согласно некоторым вариантам реализации по меньшей мере один ITR (wt или модифицированный ITR) является функциональным. Согласно альтернативным вариантам реализации в тех случаях, когда зкДНК-вектор содержит два модифицированных ITR, которые отличаются друг от друга или асимметричны друг относительно друга, по меньшей мере один модифицированный ITR является функциональным и по меньшей мере один модифицированный ITR является нефункциональным.
[00152] Согласно некоторым вариантам реализации зкДНК-вектор не содержит модифицированного ITR, выбранного из любой последовательности, состоящей или состоящей по существу из: SEQ ID NO: 500-529 согласно настоящему описанию. Согласно некоторым вариантам реализации зкДНК-вектор не содержит ITR, выбранный из любой последовательности, выбранной из SEQ ID NO: 500-529.
[00153] Согласно некоторым вариантам реализации модифицированный ITR (например, левый или правый ITR) описанного в настоящем документе зкДНК-вектора содержит модификации в плече петли, усеченном плече или спейсере. Примеры последовательностей ITR с модификациями в плече петли, усеченном плече или спейсере приведены в таблице 2.
[00154] Согласно некоторым вариантам реализации модифицированный ITR (например, левый или правый ITR) описанного в настоящем документе зкДНК-вектора содержит модификации в плече петли и усеченном плече. Примеры последовательностей ITR с модификациями в плече петли и усеченном плече приведены в таблице 3.
[00155] Согласно некоторым вариантам реализации модифицированный ITR (например, левый или правый ITR) описанного в настоящем документе зкДНК-вектора содержит модификации в плече петли и спейсере. Примеры последовательностей ITR с модификациями в плече петли и спейсере приведены в таблице 4.
[00156] Согласно некоторым вариантам реализации модифицированный ITR (например, левый или правый ITR) описанного в настоящем документе зкДНК-вектора содержит модификации в усеченном плече и спейсере. Примеры последовательностей ITR с модификациями в усеченном плече и спейсере приведены в таблице 5.
[00157] Согласно некоторым вариантам реализации модифицированный ITR (например, левый или правый ITR) описанного в настоящем документе зкДНК-вектора содержит модификации в плече петли, усеченном плече и спейсере. Примеры последовательностей ITR с модификациями в плече петли, усеченном плече и спейсере приведены в таблице 6.
[00158] Согласно некоторым вариантам реализации ITR (например, левый или правый ITR) модифицирован таким образом, чтобы он характеризовался наименьшей энергией разворачивания («низкоэнергетическая структура»). Низкая энергия соответствует пониженной свободной энергии Гиббса по сравнению с ITR дикого типа. Примеры последовательностей ITR, модифицированных для достижения низкой (т.е. пониженной) энергии разворачивания, представлены в настоящем документе в таблицах 7-9.
[00159] Согласно некоторым вариантам реализации модифицированный ITR выбирают из любого ITR или комбинации ITR, приведенных в таблице 2-9, 10А или 10В.
[00160] Таблица 2: Последовательности ITR с модификациями в плече петли, усеченном плече или спейсере. Они включают последовательность RBS GCGCGCTCGCTCGCTC (SEQ ID NO: 531) на 5'-конце и комплементарную последовательность RBE' GAGCGAGCGAGCGCGC (SEQ ID NO: 536) на самом 3'-конце.
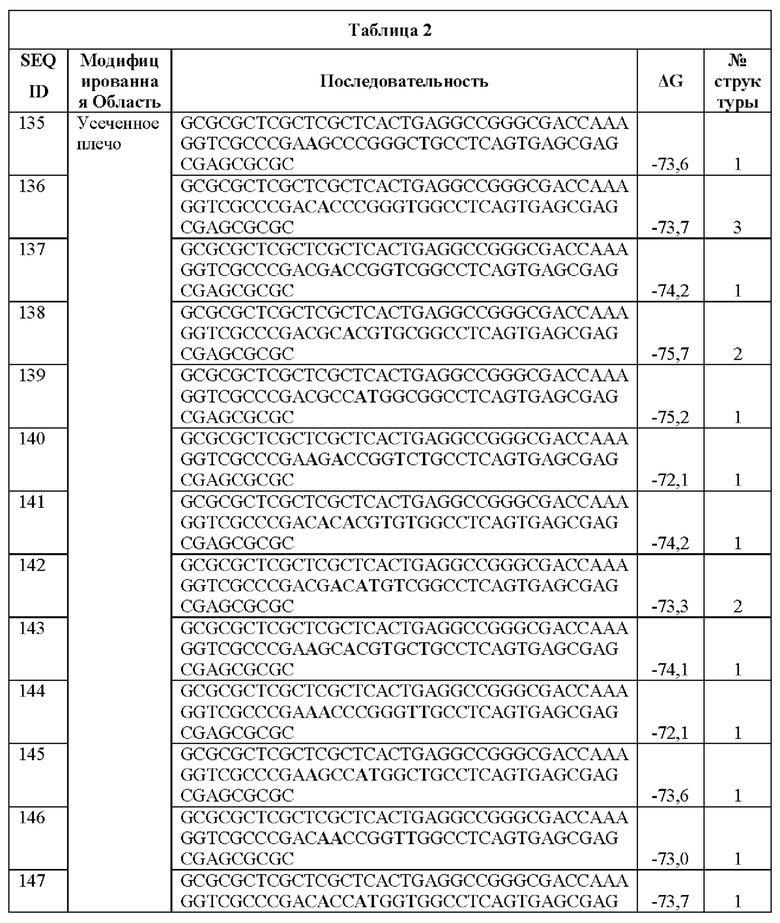
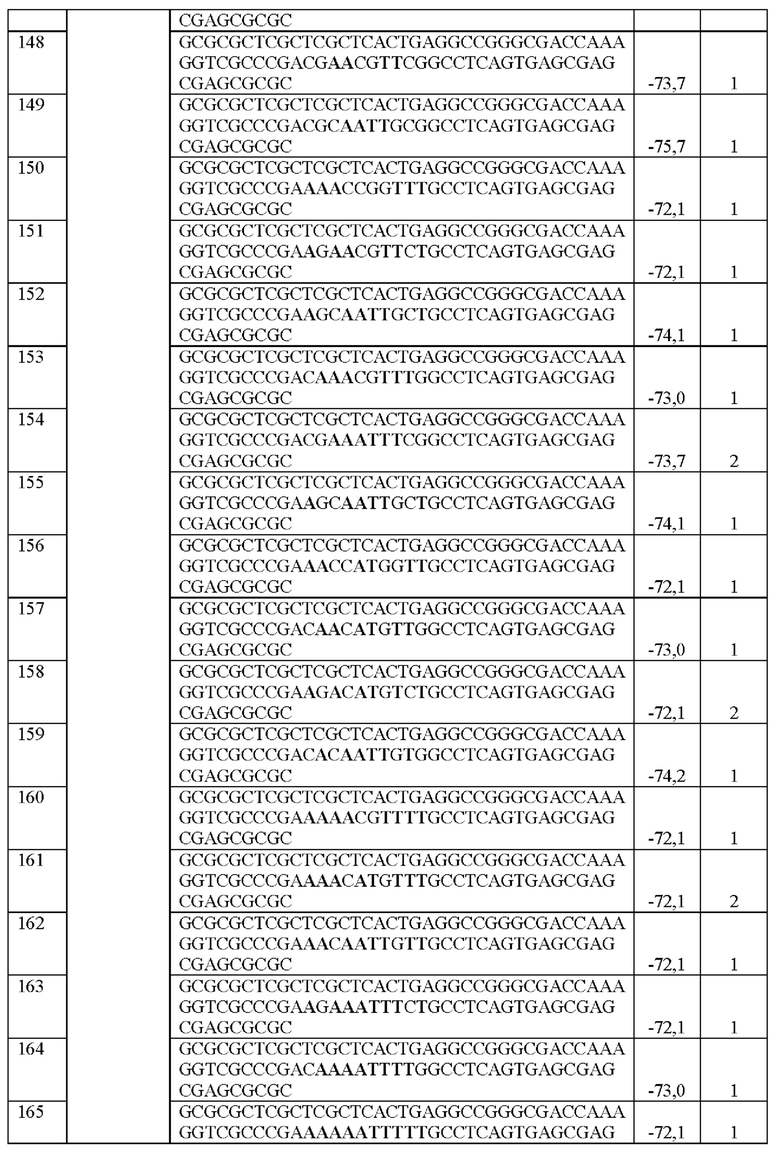

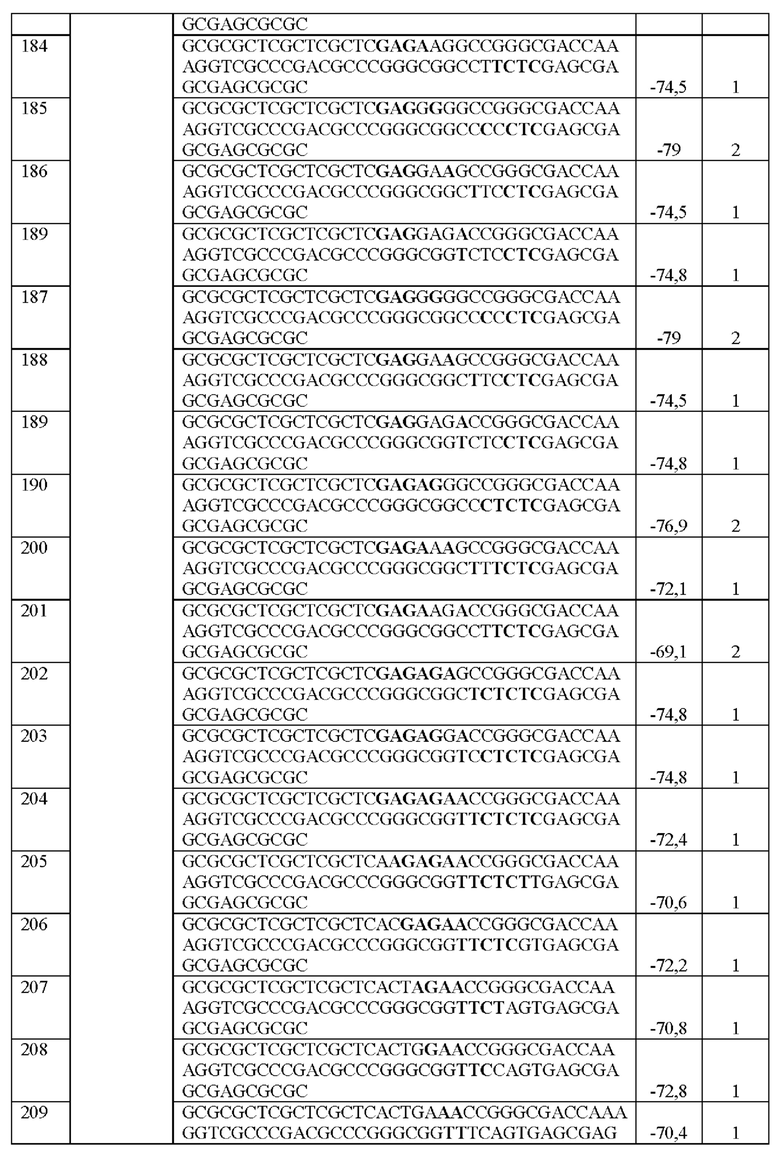
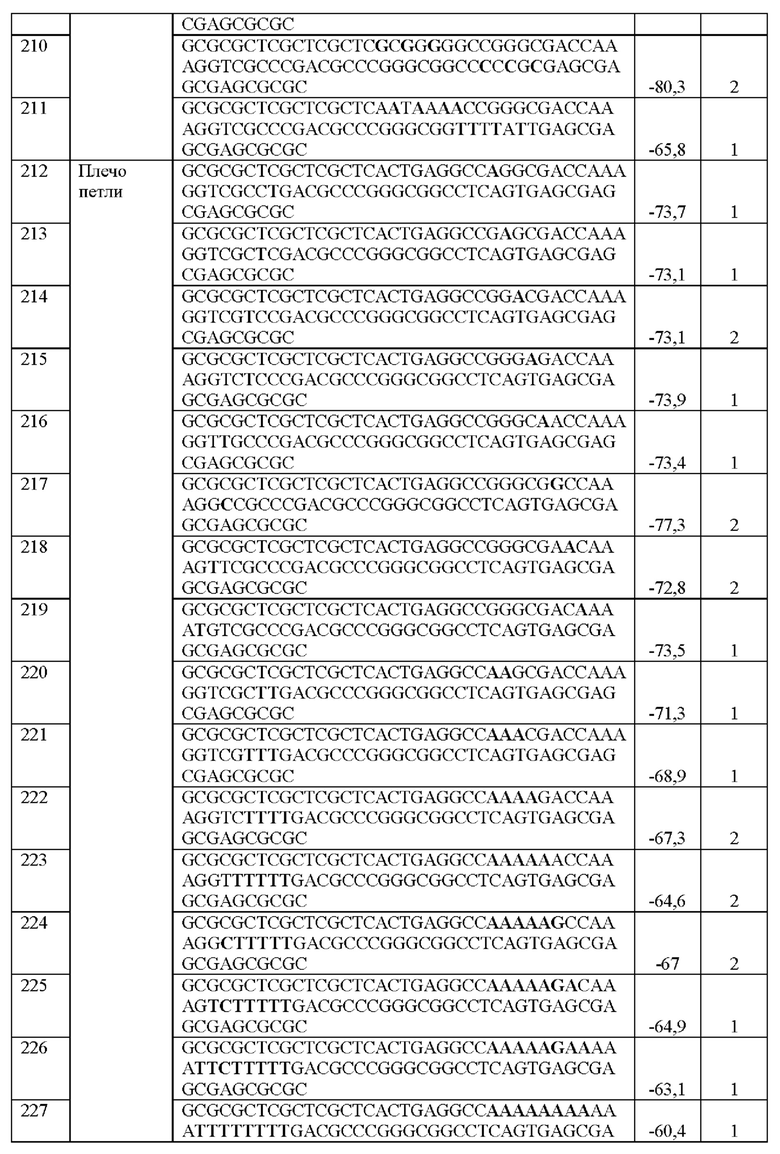

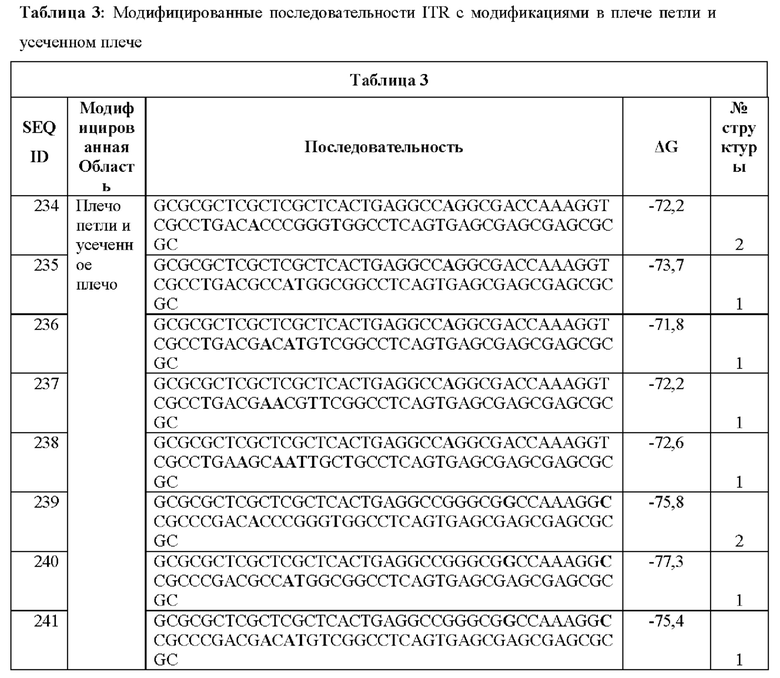
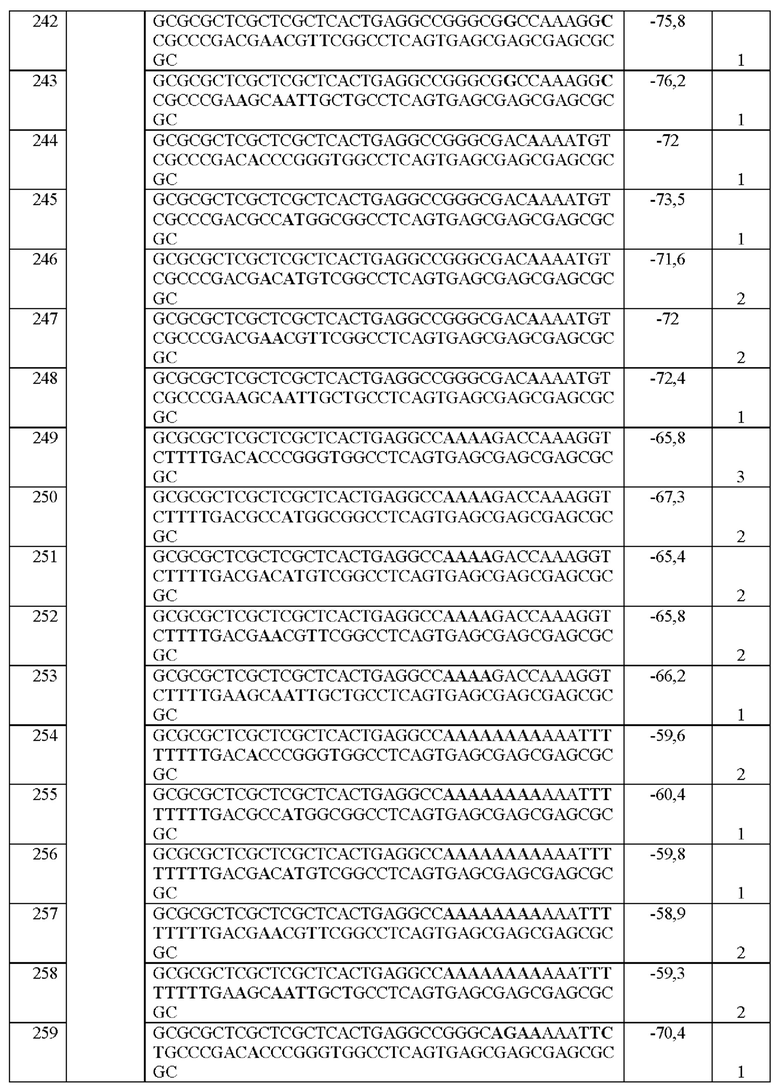


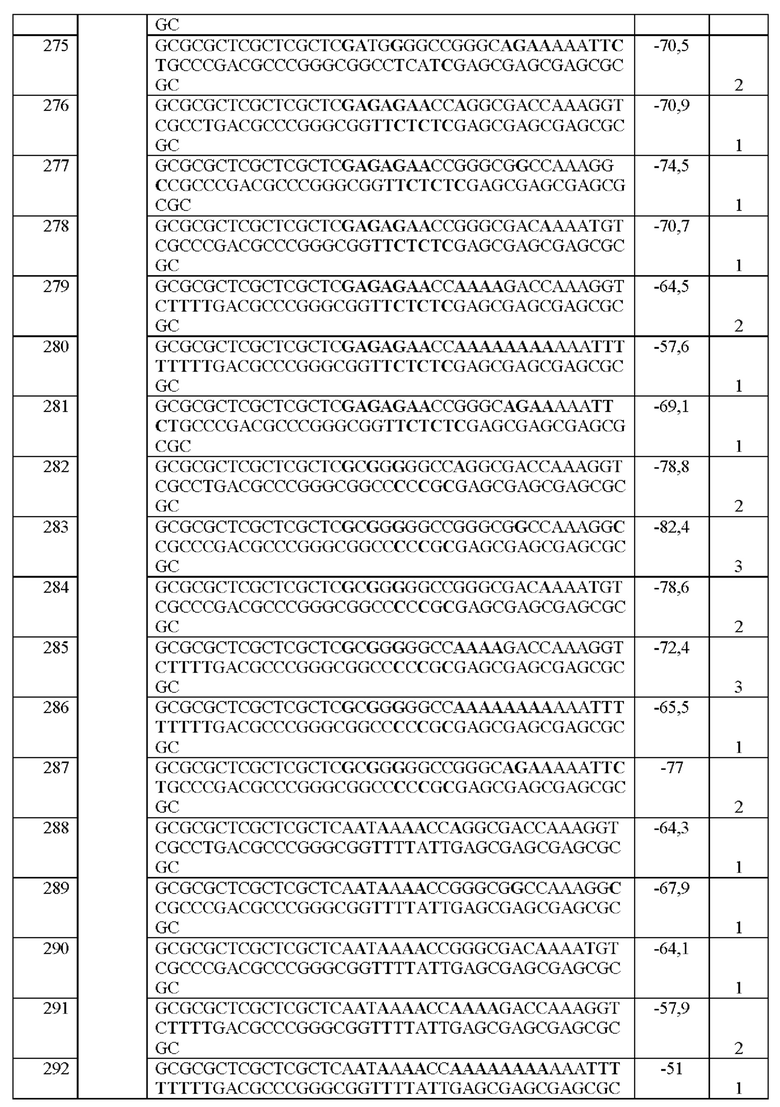

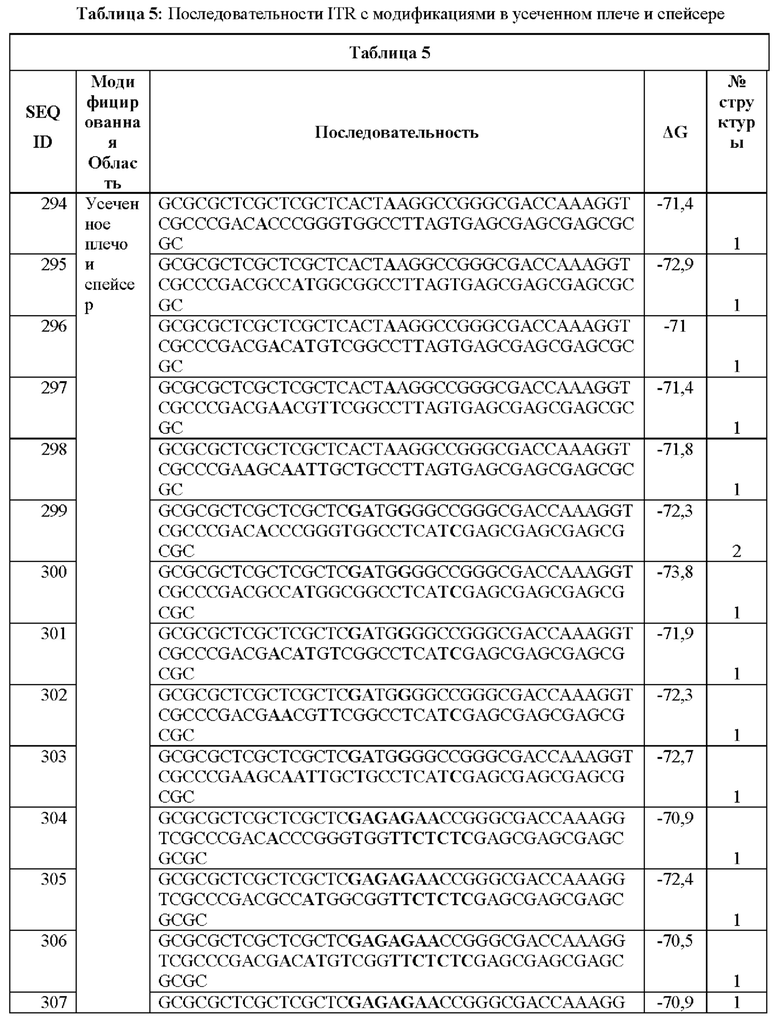
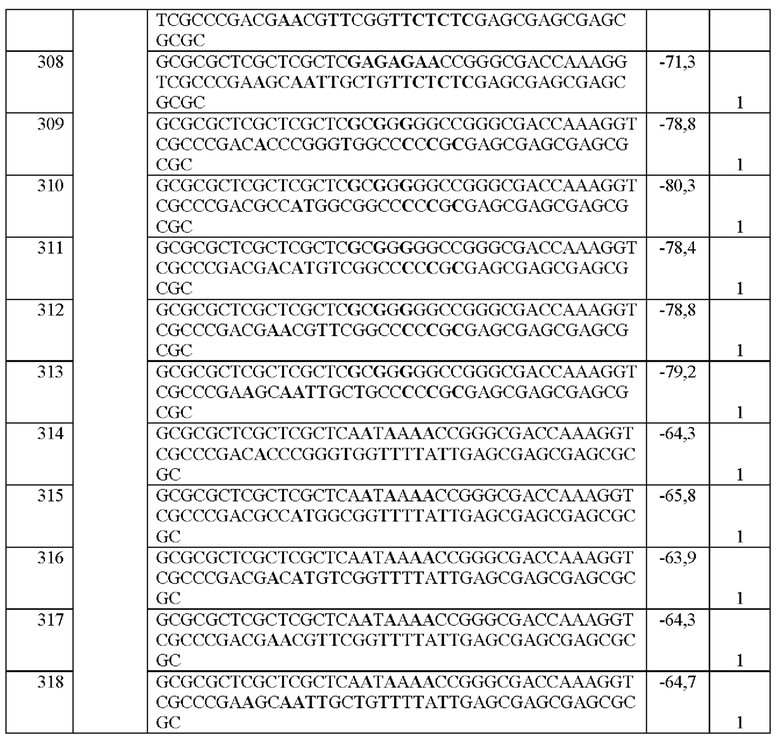

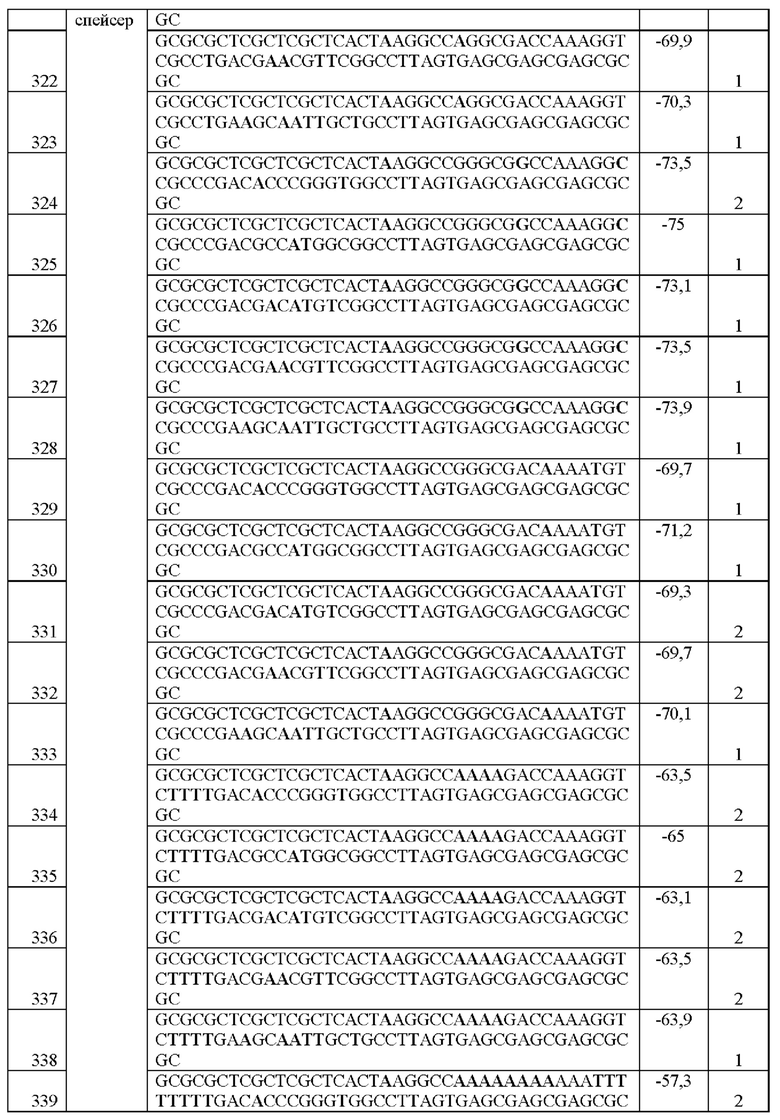
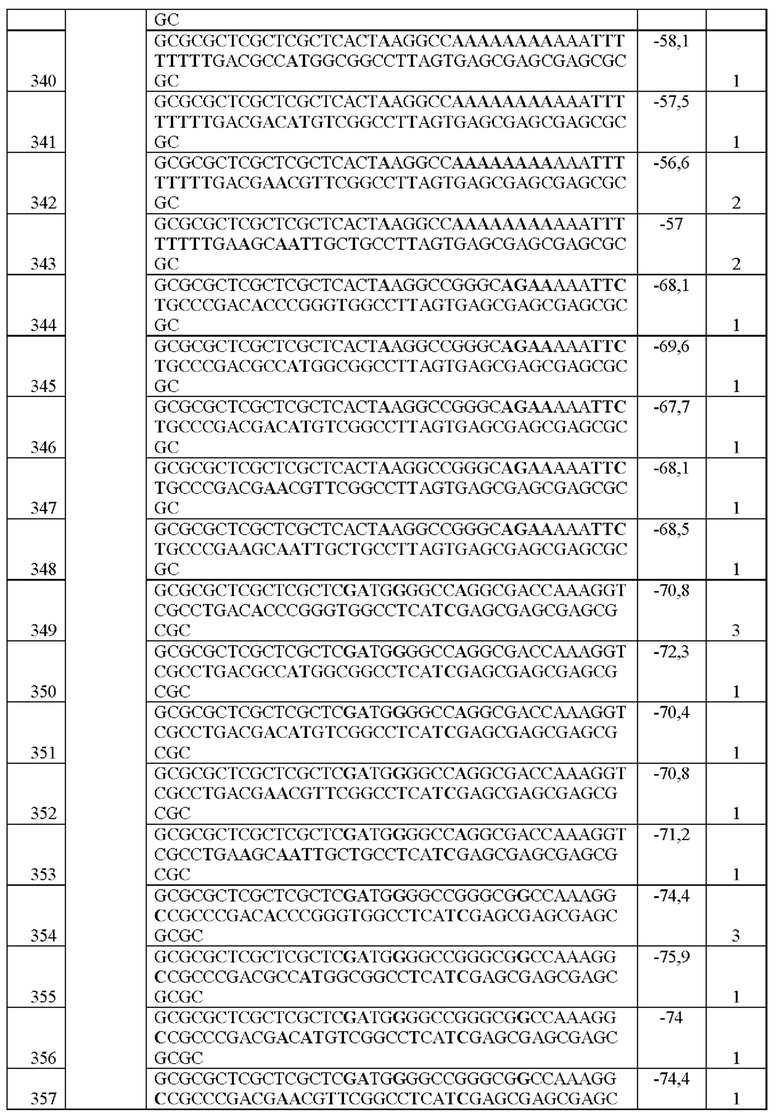
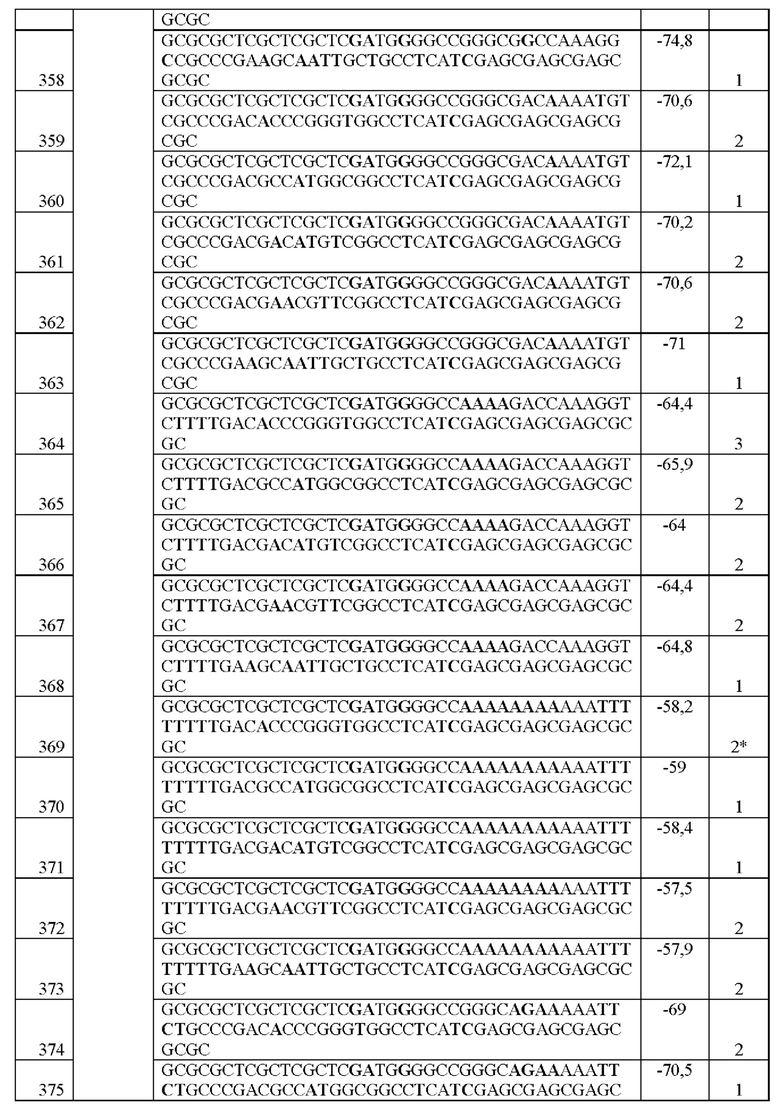
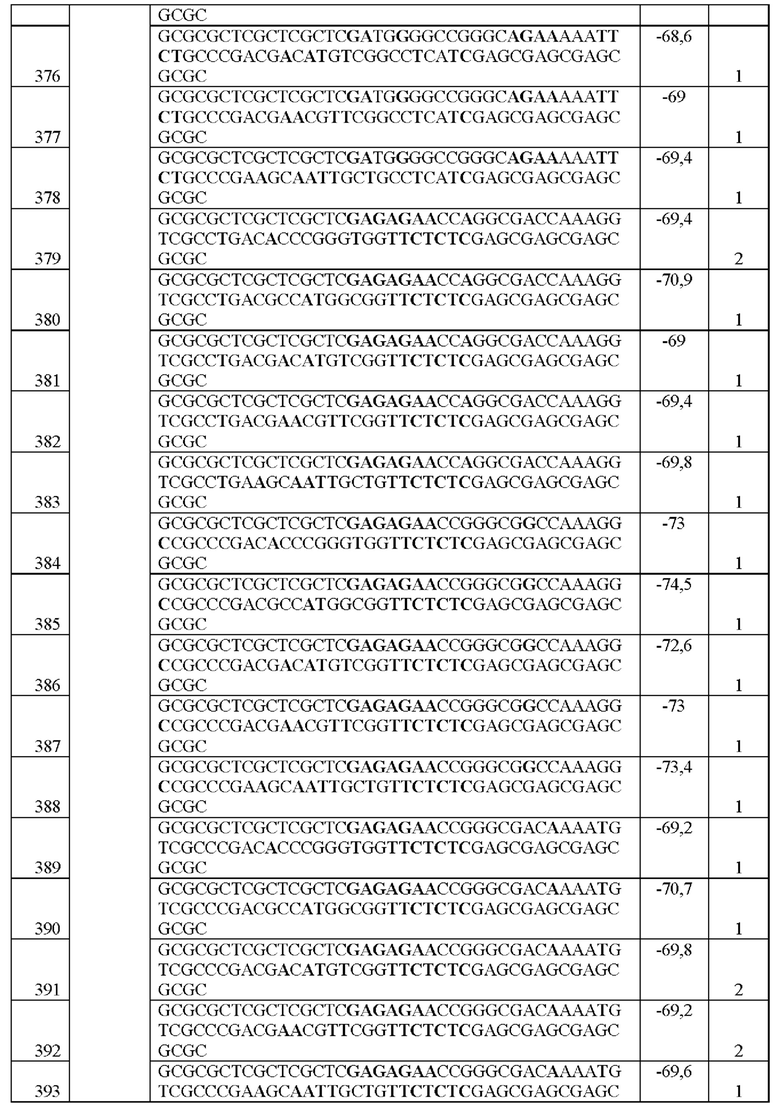
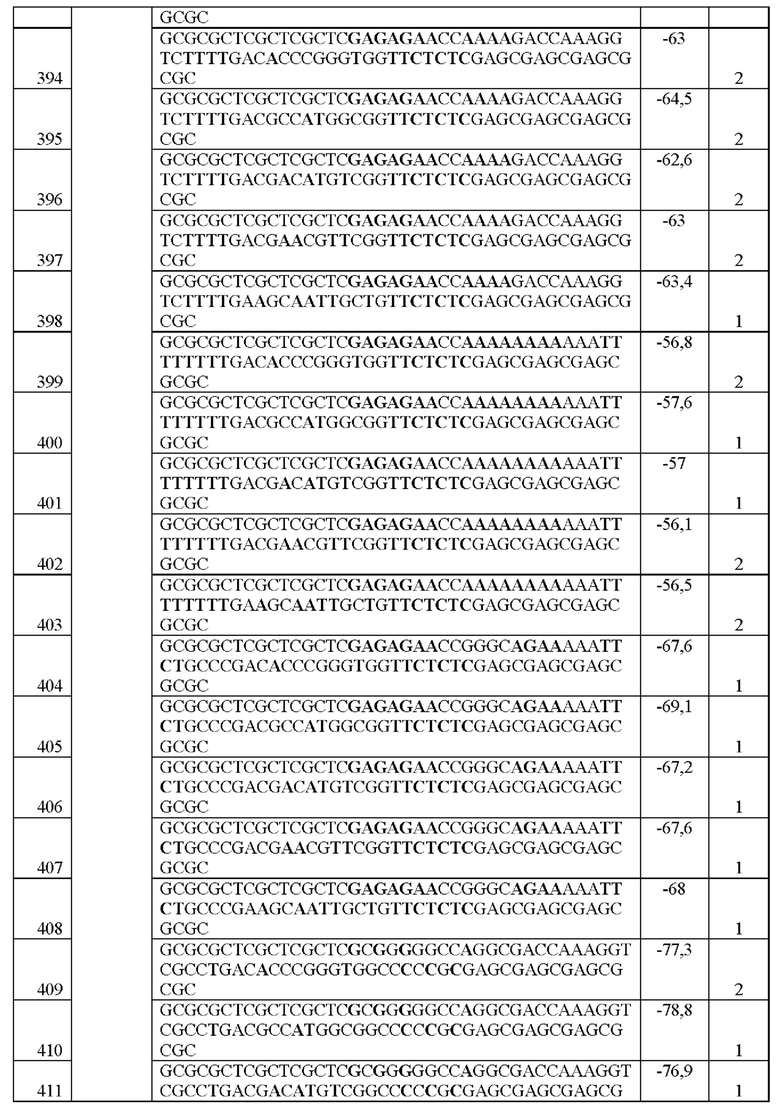
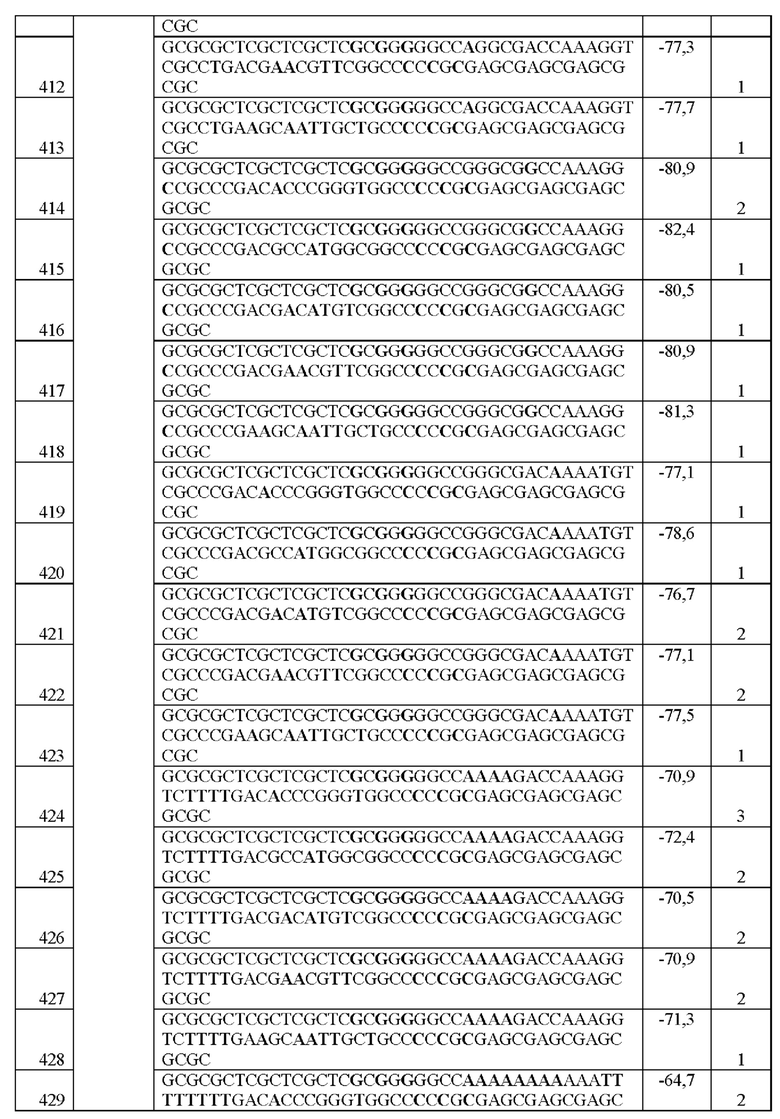
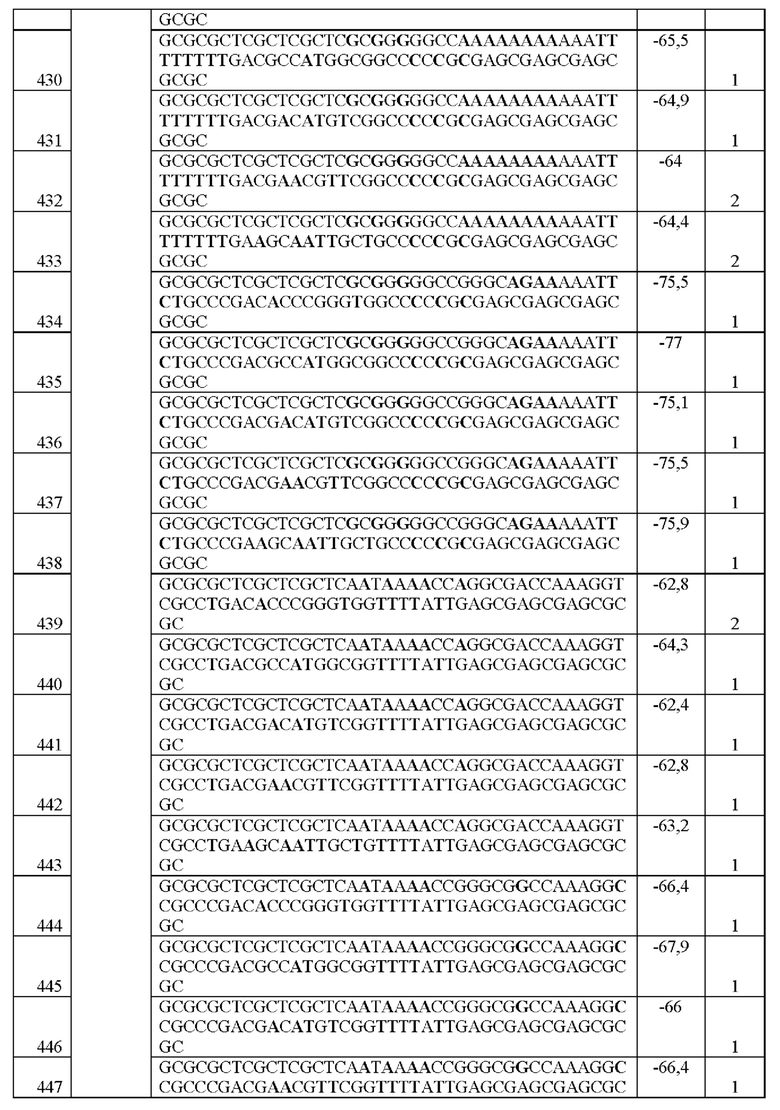
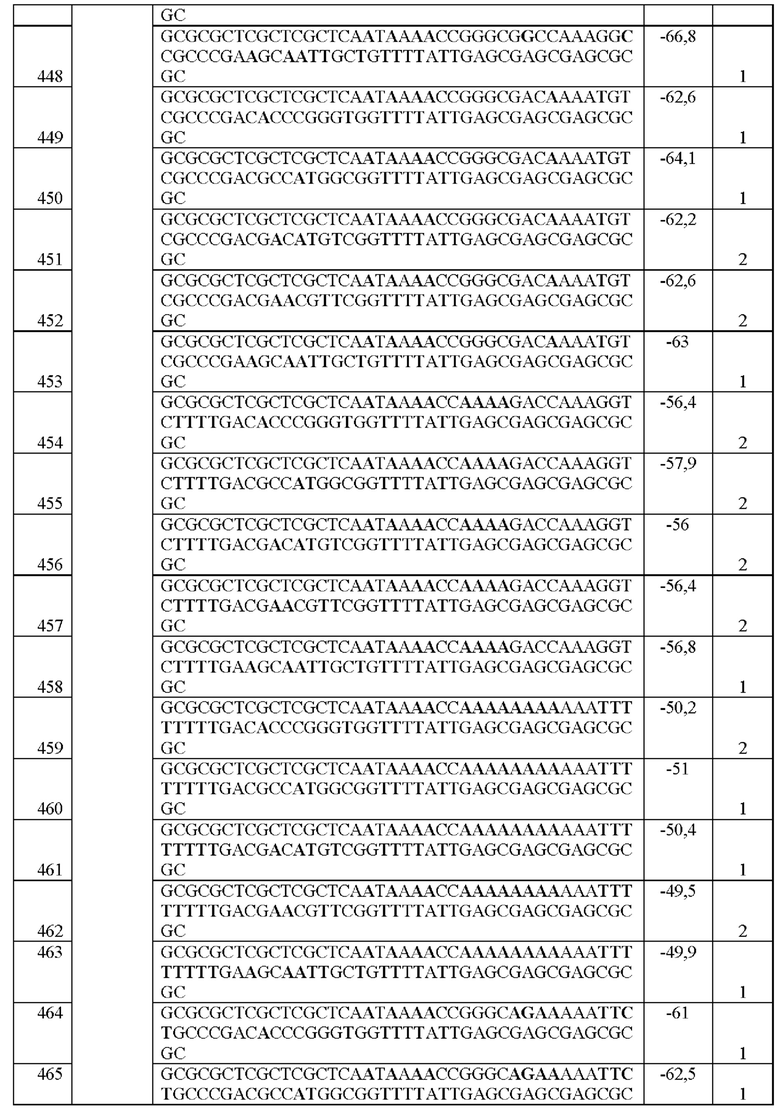
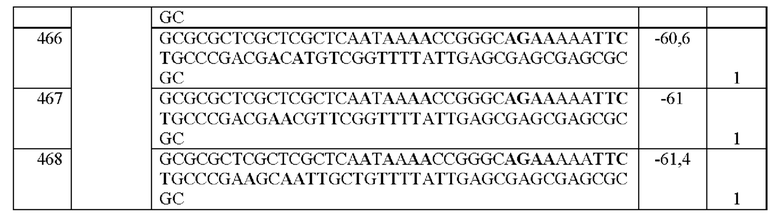
[00161] Согласно настоящему раскрытию может быть получен модифицированный ITR, включающий делецию, инсерцию или замену одного или более нуклеотидов из ITR дикого типа, происходящего из генома AAV. Модифицированный ITR может быть получен путем генетической модификации при размножении в плазмиде в Escherichia coli, или в виде генома бакуловируса в клетках Spodoptera frugiperda, или с применением других биологических способов, например, in vitro с применением полимеразной цепной реакции, или путем химического синтеза.
[00162] Согласно некоторым вариантам реализации модифицированные ITR включают делецию, инсерцию или замену одного или более нуклеотидов из ITR дикого типа AAV2 (левого) (SEQ ID NO: 51) или ITR дикого типа AAV2 (правого) (SEQ ID NO: 1). В частности, делетируют, инсертируют или заменяют один или более нуклеотидов из В-С' или С-С' Т-образной структуры «петля на стебле». Далее, модифицированный ITR не включает модификаций в Rep-связывающих элементах (RBE) и сайте концевого разрешения (trs) ITR дикого типа AAV2, хотя RBE' (ТТТ) может присутствовать или не присутствовать в зависимости от того, подвергалась ли матрица одному раунду репликации, с преобразованием таким образом триплета AAA в комплементарный триплет RBE' - ТТТ.
[00163] Приведены примеры трех типов модифицированных ITR (1) модифицированный ITR, имеющий структуру с наименьшей энергией, содержащий единственное плечо и единственную неспаренную петлю («структура с единственным плечом/с единственной неспаренной петлей»); (2) модифицированный ITR, имеющий структуру с наименьшей энергией с одной шпилькой («структура с одной шпилькой»); и (3) модифицированный ITR, имеющий структуру с наименьшей энергией с двумя плечами, одно из которых является усеченным («усеченная структура»).
[00164] Модифицированный ITR, имеющий структуру с единственным плечом/с единственной неспаренной петлей
[00165] ITR дикого типа может быть модифицирован так, чтобы образовывать вторичную структуру, содержащую единственное плечо и единственную неспаренную петлю (т.е. «структуру с единственным плечом/с единственной неспаренной петлей»). Изменение свободной энергии Гиббса (ΔG) для для разворачивания указанной структуры может варьировать в диапазоне от -85 ккал/моль до -70 ккал/моль. Предложены примеры структур модифицированных ITR.
[00166] Модифицированные ITR, которые, согласно прогнозу, образуют структуру с единственным плечом/с единственной неспаренной петлей, могут включать делецию, инсерцию или замену одного или более нуклеотидов из ITR дикого типа в последовательностях, образующих плечо В и В' и/или плечо С и С'. Модифицированный ITR может быть получен путем генетической модификации или путем биологического и/или химического синтеза.
[00167] Например, ITR-2, левый и правый, приведенные на фиг. 9А-9В (SEQ ID NO: 101 и 102), получены таким образом, чтобы включать делецию двух нуклеотидов из плеча С-С' и делецию 16 нуклеотидов из плеча В-В' в ITR дикого типа AAV2. Три оставшихся нуклеотида в плече В-В' модифицированного ITR не подвергаются комплементарному спариванию. Соответственно, ITR-2, левый и правый, имеют структуру с наименьшей энергией с единственным плечом С-С' и единственной неспаренной петлей. Предсказанное изменение свободной энергии Гиббса для разворачивания указанной структуры составляет приблизительно -72,6 ккал/моль.
[00168] ITR-3, левый и правый, приведенные на фиг. 10А и 10В (SEQ ID NO: 103 и 104), получены таким образом, чтобы включать 19 делеций нуклеотидов в плече С-С из ITR дикого типа AAV2. Три оставшихся нуклеотида в плече В-В' модифицированного ITR не подвергаются комплементарному спариванию. Соответственно, ITR-3, левый и правый, имеют структуру с наименьшей энергией с единственным плечом В-В' и единственной неспаренной петлей. Предсказанное изменение свободной энергии Гиббса для разворачивания указанной структуры составляет приблизительно -74,8 ккал/моль.
[00169] ITR-4, левый и правый, приведенные на фиг. 11А и 11В (SEQ ID NO: 105 и 106), получены таким образом, чтобы включать 19 делеций нуклеотидов в плече В-В' из ITR дикого типа AAV2. Три оставшихся нуклеотида в плече В-В' модифицированного ITR не подвергаются комплементарному спариванию. Соответственно, ITR-4, левый и правый, имеют структуру с наименьшей энергией с единственным плечом С-С' и единственной неспаренной петлей. Предсказанное изменение свободной энергии Гиббса для разворачивания указанной структуры составляет приблизительно -76,9 ккал/моль.
[00170] ITR-10, левый и правый, приведенные на фиг. 12А и 12В (SEQ ID NO: 107 и 108), получены таким образом, чтобы включать 8 делеций нуклеотидов в плече В-В' из ITR дикого типа AAV2. Остальные нуклеотиды в плечах В-В' и С-С' образуют новые комплементарные связи между мотивами В и С' (ITR-10, левый) или между мотивами С и В' (ITR-10, правый). Соответственно, ITR-10, левый и правый, имеют структуру с наименьшей энергией с единственным плечом В-С' или С-В' и единственной неспаренной петлей. Предсказанное изменение свободной энергии Гиббса для разворачивания указанной структуры составляет приблизительно -83,7 ккал/моль.
[00171] ITR-17, левый и правый, приведенные на фиг. 13А и 13В (SEQ ID NO: 109 и 110), получены таким образом, чтобы включать 14 делеций нуклеотидов в плече С-С' из ITR дикого типа AAV2. Остальные восемь нуклеотидов в плече С-С' не образуют комплементарных связей. В результате ITR-17, левый и правый, имеют структуру с наименьшей энергией с единственным плечом В-В' и единственной неспаренной петлей. Предсказанное изменение свободной энергии Гиббса для разворачивания указанной структуры составляет приблизительно -73,3 ккал/моль.
[00172] Последовательности ITR дикого типа, левый или правый (сверху), и различные модифицированные ITR левые или правые (снизу), которые, согласно прогнозу, образуют структуру с единственным плечом/с единственной неспаренной петлей, выравнивают; выравнивание представлено ниже в таблице 7.
[00173] Таблица 7: Выравнивание wt-ITR и модифицированного ITR (ITR-2, ITR-3, ITR-4, ITR-10 и ITR-17), имеющего структуру с единственным плечом/с единственной неспаренной петлей.

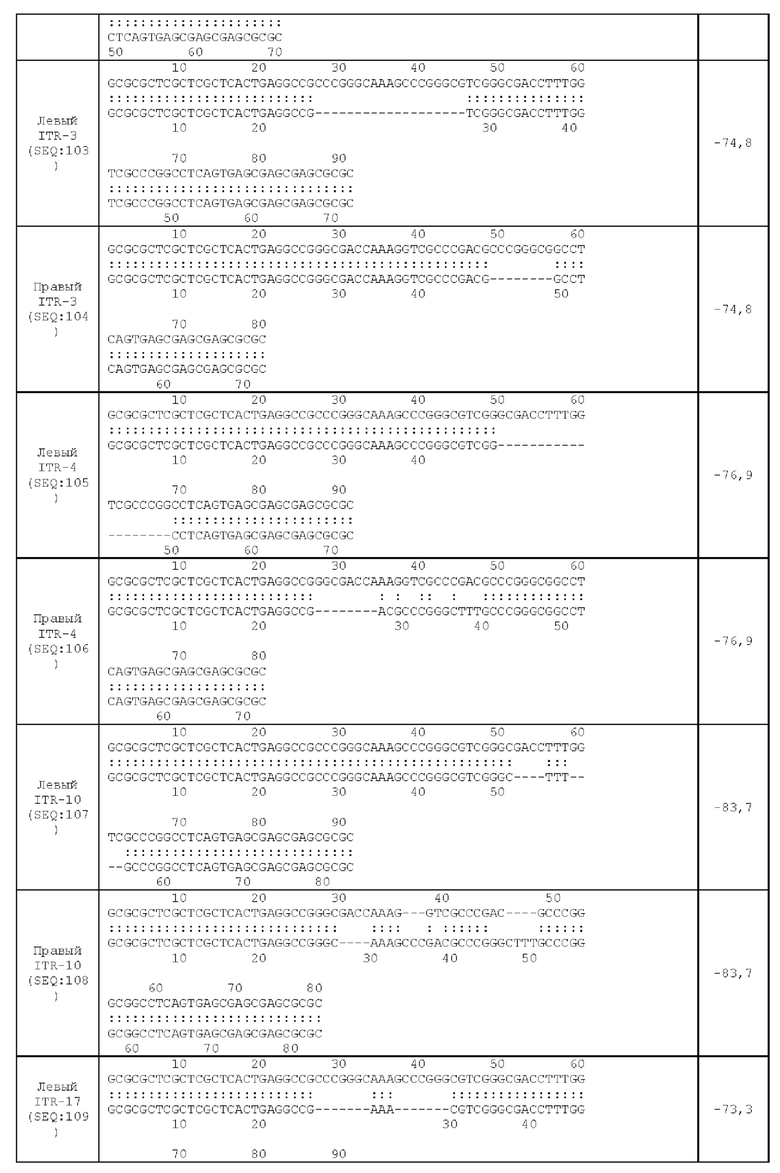

[00174] Модифицированный ITR имеющий структуру с одной шпилькой
[00175] ITR дикого типа может быть модифицирован так, чтобы иметь структуру с наименьшей энергией, содержащую структуру с одной шпилькой. Изменение свободной энергии Гиббса (AG) для разворачивания указанной структуры может варьировать в диапазоне от -70 ккал/моль до -40 ккал/моль. Примеры структур модифицированных ITR предложены на фиг. 14А и 14В.
[00176] Модифицированные ITR, которые, согласно прогнозу, образуют структуру с одной шпилькой, могут включать делецию, инсерцию или замену одного или более нуклеотидов из ITR дикого типа в последовательностях, образующих плечо В и В' и/или плечо С и С'. Модифицированный ITR может быть получен путем генетической модификации или путем биологического и/или химического синтеза.
[00177] Например, ITR-6, левый и правый, приведенные на фиг. 14А и 14В (SEQ ID NO: 111 и 112), включают 40 делеций нуклеотидов в плечах В-В' и С-С' из ITR дикого типа AAV2. Остальные нуклеотиды в модифицированном ITR, согласно прогнозу, образуют структуру с одной шпилькой. Изменение свободной энергии Гиббса для разворачивания указанной структуры составляет приблизительно -54,4 ккал/моль.
[00178] Последовательности ITR дикого типа и ITR-6 (как левого, так и правого) выравнивают; выравнивание приведено ниже в таблице 8.
[00179] Таблица 8: Выравнивание wt-ITR и модифицированного ITR-6, имеющего структуру с одной шпилькой.


[00180] Модифицированный ITR с усеченной структурой
[00181] ITR дикого типа может быть модифицирован так, чтобы иметь структуру с наименьшей энергией, содержащую два плеча, одно из которых является усеченным. Их изменение свободной энергии Гиббса (AG) для разворачивания варьирует в диапазоне от -90 до -70 ккал/моль. Соответственно, их значения свободной энергии Гиббса для разворачивания ниже, чем для ITR дикого типа AAV2.
[00182] Модифицированный ITR может включать делению, инсерцию или замену одного или более нуклеотидов из ITR дикого типа в последовательностях, образующих плечо В и В' и/или плечо С и С'. Согласно некоторым вариантам реализации модифицированный ITR может, например, включать удаление конкретной петли полностью, например, петли А-А', петли В-В' или петли С-С', или, как вариант, удаление 1, 2, 3, 4, 5, 6, 7, 8, 9 или более пар оснований, образующих стебель петли, при условии, что последняя петля на конце стебля все же остается. Модифицированный ITR может быть получен путем генетической модификации или путем биологического и/или химического синтеза.
[00183] Примеры структур модифицированных ITR с усеченной структурой приведены на фиг. 15А-15В.
[00184] Последовательности различных модифицированных ITR которые, согласно прогнозу, образуют усеченную структуру, выравнивают с последовательностью ITR дикого типа; выравнивание приведено ниже в таблице 9.
[00185] Таблица 9: Выравнивание wt-ITR и модифицированного ITR (ITR-5, ITR-7, ITR-8, ITR-9, ITR-11, ITR-12, ITR-13, ITR-14, ITR-1 и ITR-16) с усеченной структурой.

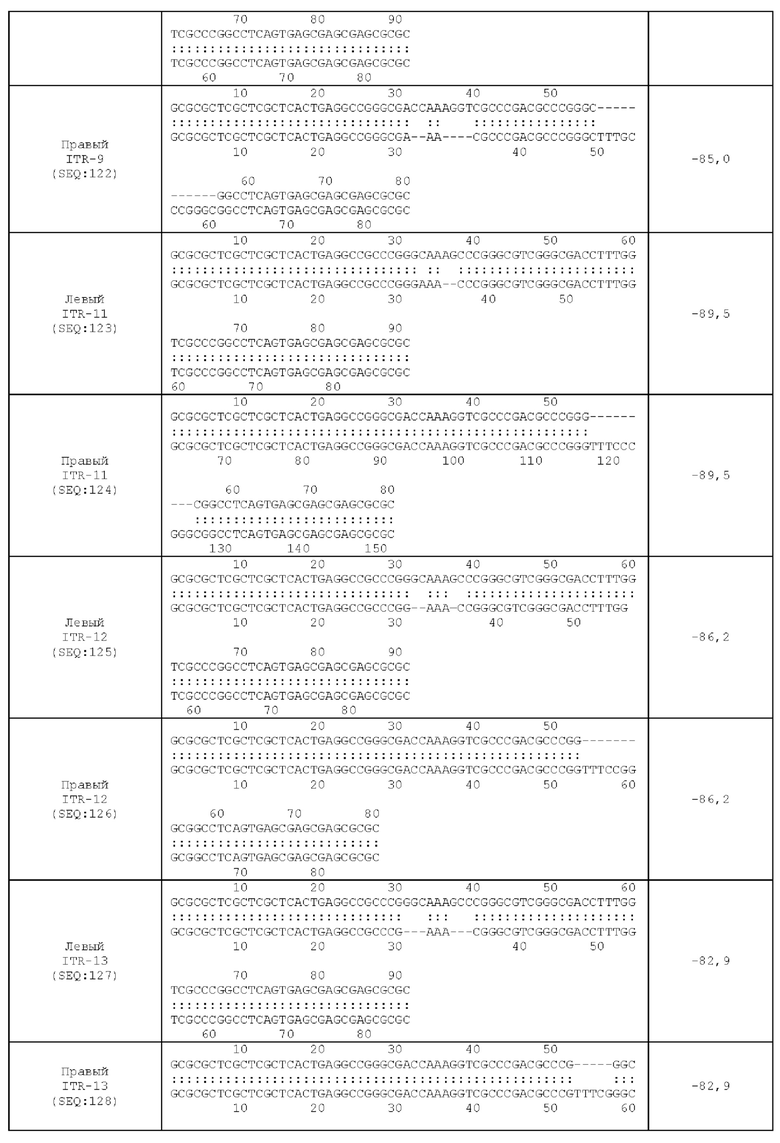
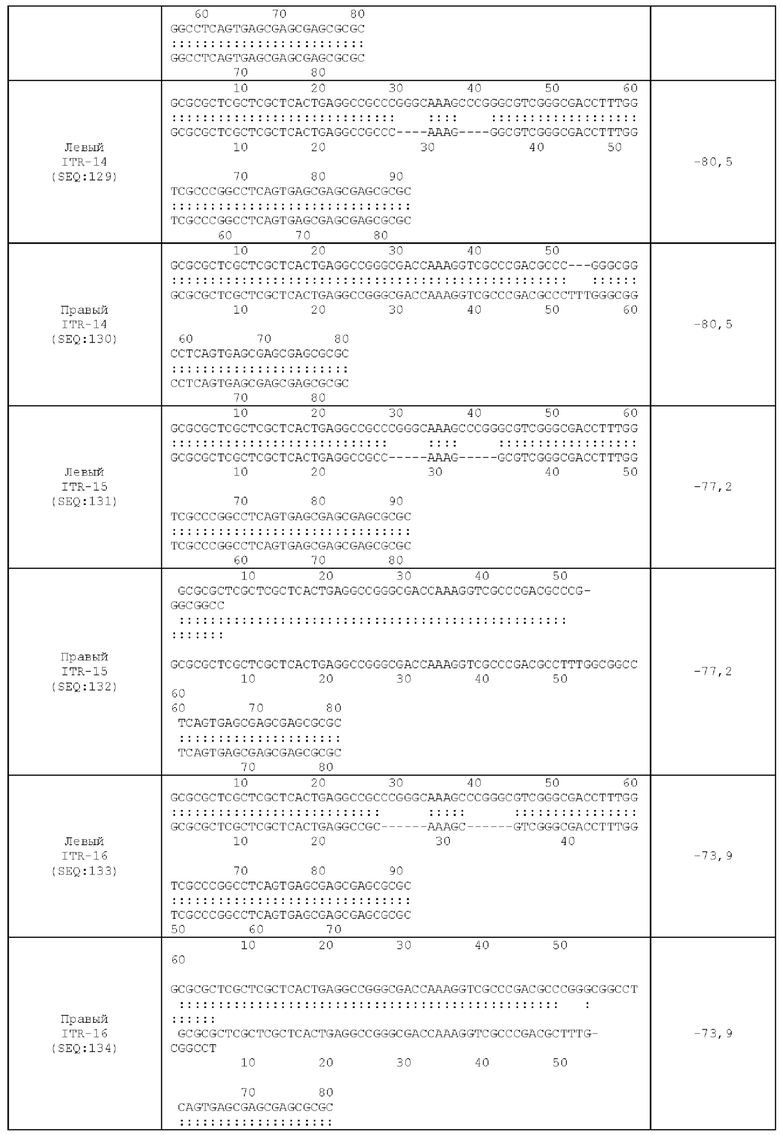

[00186] Дополнительные примеры модифицированных ITR в каждом из представленных выше классов для применения согласно настоящему изобретению приведены в таблицах 10А и 10В. Предсказанная вторичная структура правого модифицированного ITR из таблицы 10А показана на фиг. 26А, а предсказанная вторичная структура левых модифицированных ITR из таблицы 10В показана на фиг. 26В.
[00187] В таблице 10А и таблице 10В приведены примеры правых и левых модифицированных ITR.
[00188] Таблица 10А: Примеры модифицированных правых ITR. Указанные примеры модифицированных правых ITR могут содержать RBE GCGCGCTCGCTCGCTC-3' (SEQ ID NO: 531), спейсер ACTGAGGC (SEQ ID NO: 532), комплемент спейсера GCCTCAGT (SEQ ID NO: 535) и RBE' (т.е. комплемент RBE) GAGCGAGCGAGCGCGC (SEQ ID NO: 536).
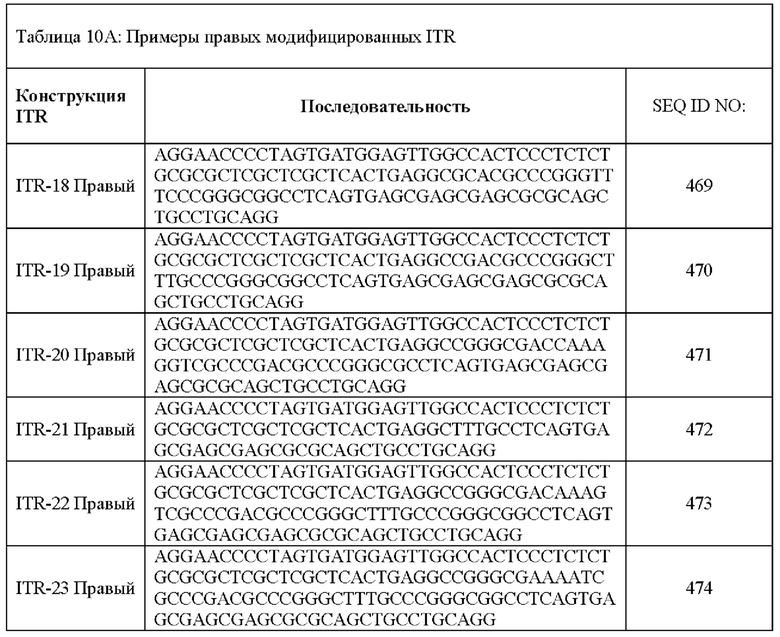
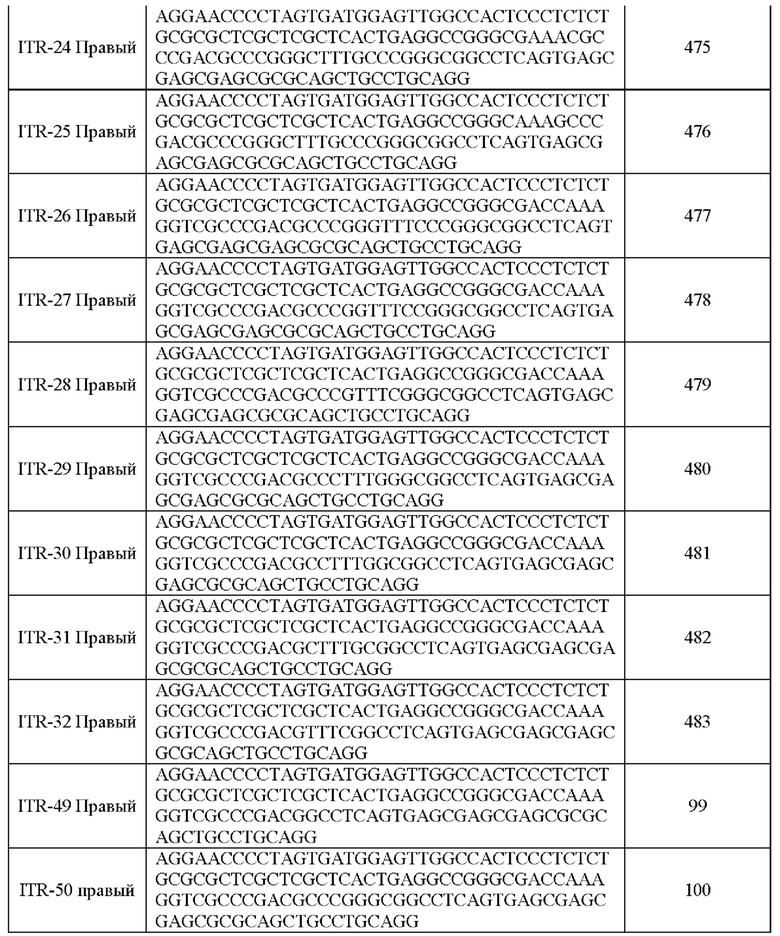
[00189] ТАБЛИЦА 10В: Примеры модифицированных левых ITR. Указанные примеры модифицированных левых ITR могут содержать RBE GCGCGCTCGCTCGCTC-3' (SEQ ID NO: 531), спейсер ACTGAGGC (SEQ ID NO: 532), комплемент спейсера GCCTCAGT (SEQ ID NO: 535) и комплемент RBE (RBE') GAGCGAGCGAGCGCGC (SEQ ID NO: 536).

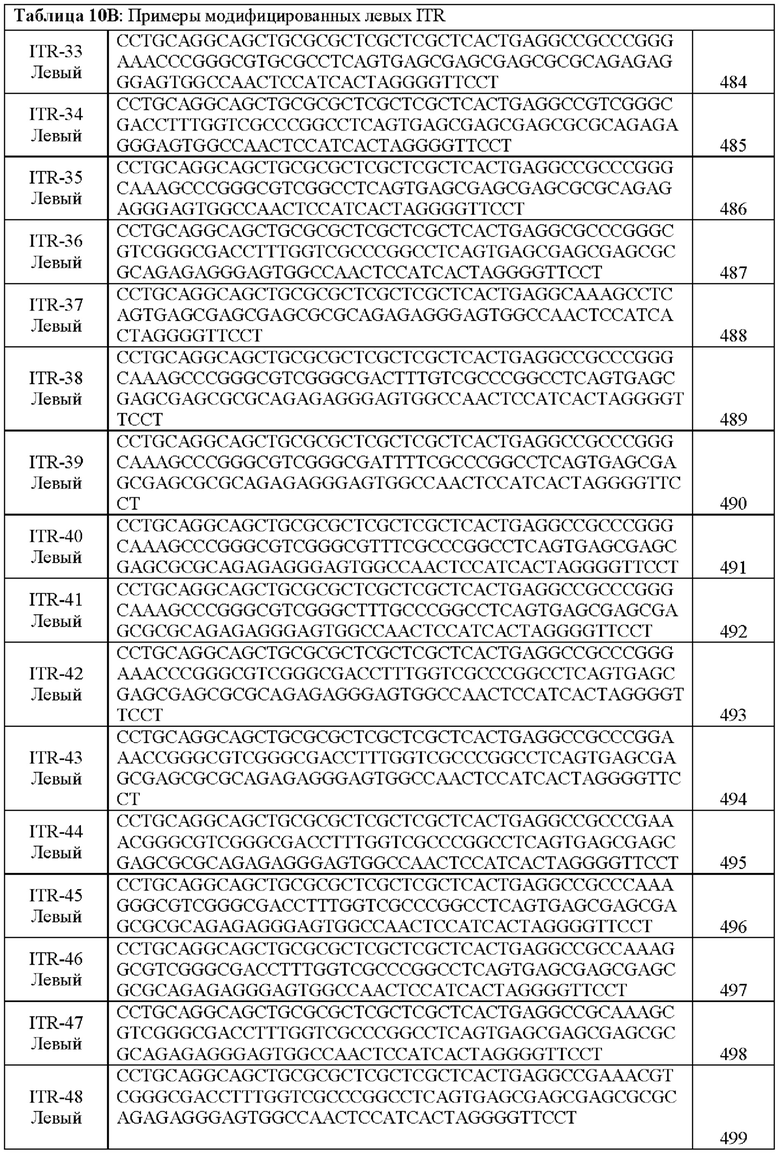
[00190] Согласно вариантам реализации настоящего изобретения зкДНК-вектор согласно описанию в настоящем документе не содержит модифицированной ITR с последовательностью нуклеотидов, выбранной из любой последовательности из группы SEQ ID No: 550, 551, 552, 553, 553, 554, 555, 556, 557.
[00191] При условии, что зкДНК-вектор содержит модифицированный ITR с одной из модификаций в области В, В', С или С' согласно описанию в SEQ ID NO: 550-557, в соответствии с определением в любом одном или более пунктах формулы настоящего изобретения, или любого другого изобретения согласно определению в измененной формуле изобретения, которая может в будущем быть подана с настоящей заявкой, или в любом производном патенте, и в рамках законов любого причастного государства или государств, где заявлена та или иная формула изобретения, авторы настоящего изобретения оговаривают за собой право отказаться от указанного раскрытия в формуле изобретения, прилагаемой к настоящей заявке или любому производному патенту в той мере, в которой это необходимо для предотвращения недействительности настоящей заявки или любого производного патента.
[00192] Например, и без ограничений авторы настоящего изобретения оговаривают за собой право отказаться от любого из указанных ниже объектов изобретения из любого пункта формулы настоящего изобретения, в текущем варианте или с внесенными в будущем изменениями, или из любого производного патента:
[00193] А. Модифицированный ITR, выбранный из любой последовательности из группы, состоящей из: SEQ ID NO: 2, 52, 63 64, 113, 114, 550, 551; 552, 553, 553, 554, 555, 556, 557, используемый в зкДНК-векторе без регуляторного переключателя
[00194] В. Описанный выше модифицированный ITR по А., в зкДНК-векторе без регуляторной последовательности, где гетерологичная нуклеиновая кислота кодирует АВСА4, USA2A var1, VEGFR, СЕР290, BDD-фактор VIII (FVIII), фактор VIII, vWF_His, vWF, лецитинхолестеринацилтрансферазу, РАН, G6PC или CFTR
[00195] Без ограничений, авторы настоящего изобретения утверждают, что оговоренное выше право на отказ применимо по меньшей мере к пунктам формулы 1-57 в настоящей заявке и ко всем пунктам в описании, включая, не ограничиваясь перечисленными, пункты в [0027] и [00397].
IV. Регуляторные элементы.
[00196] Указанные зкДНК-векторы могут быть получены с экспрессионных конструкций, которые дополнительно содержат специфическую комбинацию цис-регуляторных элементов. Указанные цис-регуляторные элементы включают, не ограничиваясь перечисленными, промотор, рибопереключатель, инсулятор, миРНК-регулируемый элемент, посттранскрипционный регуляторный элемент, тканеспецифический и клеточноспецифический промотор и энхансер. Согласно некоторым вариантам реализации указанный ITR может действовать как промотор для трансгена. Согласно некоторым вариантам реализации указанный зкДНК-вектор содержит дополнительные компоненты для регуляции экспрессии указанного трансгена, например, регуляторные переключатели согласно описанию в настоящем документе, для регуляции экспрессии указанного трансгена, или «аварийный выключатель», который может обеспечивать смерть клетки, содержащей зкДНК-вектор.
[00197] ЗкДНК-векторы могут быть получены из экспрессионных конструкций, которые дополнительно содержат специфическую комбинацию цис-регуляторных элементов, таких как посттранскрипционный регуляторный элемент WHP (WPRE) (например, SEQ ID NO: 8) и поли(А) BGH (SEQ ID NO: 9). Подходящие экспрессионные кассеты для применения в экспрессионных конструкциях не ограничены связанным с упаковкой ограничением, налагаемым вирусным капсидом. Экспрессионные кассеты согласно настоящему изобретению включают промотор, который может влиять на общие уровни экспрессии, а также клеточную специфичность. В случае трансгенной экспрессии они могут включать высокоактивный немедленный ранний промотор вирусного происхождения. Экспрессионные кассеты могут содержать тканеспецифические эукариотические промоторы для ограничения трансгенной экспрессии специфическими типами клеток и снижения токсических эффектов и иммунных ответов, вызванных нерегулируемой эктопической экспрессией. Согласно предпочтительным вариантам реализации экспрессионная кассета может содержать синтетический регуляторный элемент, такой как промотор CAG (SEQ ID NO 3). Промотор CAG содержит (i) ранний энхансерный элемент цитомегаловируса (CMV), (ii) промотор, первый экзон и первый интрон гена бета-актина курицы, и (iii) акцептор сплайсинга гена бета-глобина кролика. Как вариант, экспрессионная кассета может содержать промотор альфа-1-антитрипсина (ААТ) (SEQ ID NO: 4 или SEQ ID NO: 74), печень-специфический (LP1) промотор (SEQ ID NO: 5 или SEQ ID NO: 16) или промотор фактора удлинения-l-альфа (EF1a) человека (например, SEQ ID NO: 6 или SEQ ID NO: 15). Согласно некоторым вариантам реализации указанная экспрессионная кассета включает один или более конститутивных промоторов, например, ретровирусный промотор LTR вируса саркомы Рауса (RSV) (необязательно с энхансером RSV), или немедленный ранний промотор цитомегаловируса (CMV) (необязательно с энхансером CMV, например, SEQ ID NO: 22). Как вариант, могут быть использованы индуцируемый промотор, естественный промотор трансгена, тканеспецифический промотор или различные промоторы, известные в данной области техники.
[00198] Подходящие промоторы, в том числе описанные выше, могут происходить из вирусов и могут, соответственно, называться вирусными промоторами, или они могут происходить из любого организма, в том числе прокариотических или эукариотических организмов. Подходящие промоторы могут применяться для управления экспрессией с применением любой РНК-полимеразы (например, pol I, pol II, pol III). Примеры промоторов включают, не ограничиваясь перечисленным, ранний промотор SV40, промотор из длинного концевого повтора вируса опухоли молочной железы мышей (LTR); аденовирусный большой поздний промотор (Ad MLP); промотор вируса простого герпеса (HSV), промотора цитомегаловирус (CMV), такой как область немедленного раннего промотора CMV (CMVIE), промотор вируса саркомы Рауса (RSV), промотор U6 малой ядерной РНК человека (U6, например, SEQ ID NO: 18) (Miyagishi et al., Nature Biotechnology 20, 497-500 (2002)), усиленный промотор U6 (например, Xia et al., Nucleic Acids Res. 2003 Sep. 1; 31(17)), промотор H1 человека (H1) (например, SEQ ID NO: 19), промотор CAG, промотор альфа-1-антитрипсина человека (НААТ) (например, SEQ ID NO: 21), и т.п. Согласно вариантам реализации указанные промоторы изменяют на содержащем 3'-интрон конце таким образом, чтобы они включали один или более сайтов расщепления нуклеазами. Согласно вариантам реализации ДНК, содержащая сайт(ы) расщепления нуклеазой, является чужеродной для промотора ДНК.
[00199] Промотор может содержать одну или более специфических транскрипционных регуляторных последовательностей для дополнительного усиления экспрессии и/или для изменения пространственных и/или временных характеристик их экспрессии. Промотор может также содержать дистальные энхансерные или репрессорные элементы, которые могут быть локализованы на расстоянии до нескольких тысяч пар оснований от сайта старта транскрипции. Промотор может происходить из источников, включающих вирусы, бактерии, грибы, растения, насекомых и животных. Промотор может регулировать экспрессию генного компонента конститутивно или избирательно применительно к клетке, ткани или органу, где происходит экспрессия, или с учетом стадии развития, на которой происходит экспрессия, или в ответ на внешние стимулы, такие как физиологические стрессы, патогены, ионы металлов или индуцирующие агенты. Репрезентативные примеры промоторов включают промотор бактериофага Т7, промотор бактериофага Т3, промотор SP6, лактозный оператор-промотор, tac-промотор, поздний промотор SV40, ранний промотор SV40, RSV-LTR-промотор, CMV IE-промотор, ранний промотор SV40 или поздний промотор SV40 и CMV IE-промотор, а также промоторы, перечисленные ниже. Такие промоторы и/или энхансеры могут применяться для экспрессии любого представляющего интерес гена, например, молекул редактирования генома, донорной последовательности, терапевтических белков и т.п.). Например, вектор может содержать промотор, который функционально связан с последовательностью нуклеиновой кислоты, кодирующей терапевтический белок. Указанный промотор, функционально связанный с кодирующей терапевтический белок последовательностью, может представлять собой промотор вируса обезьян 40 (SV40), промотор вируса опухоли молочной железы мышей (MMTV), промотор вируса иммунодефицита человека (HTV), например, промотор длинного концевого повтора (LTR) вируса иммунодефицита крупного рогатого скота (BIV), промотор вируса Молони, промотор вируса лейкоза птиц (ALV), промотор цитомегаловируса (CMV), такой как немедленный ранний промотор (IE) CMV, промотор вируса Эпштейна-Барр (EBV) или промотор вируса саркомы Рауса (RSV). Указанный промотор может также представлять собой промотор гена человека, например, убиквитина С человека (hUbC), актина человека, миозина человека, гемоглобина человека, креатина мышц человека или металлотионеина человека. Указанный промотор может также представлять собой тканеспецифический промотор, такой как печень-специфический промотор, например, альфа-1-антитрипсина человека (НААТ), естественный или синтетический. Согласно одному варианту реализации доставка в печень может быть достигнута с использованием специфического в отношении эндогенного АроЕ нацеливания композиции, содержащей зкДНК-вектор, в гепатоциты через рецептор липопротеинов низкой плотности (ЛПНП), имеющийся на поверхности гепатоцита.
[00200] Согласно одному варианту реализации используемый промотор представляет собой естественный промотор гена, кодирующего терапевтический белок. Промоторы и другие регуляторный последовательностей соответствующих генов, кодирующих терапевтические белки, известны и были охарактеризованы. Используемая промоторная область может дополнительно включать одну или более дополнительных регуляторных последовательностей (например, естественных), таких как энхансеры (например, SEQ ID NO: 22 и SEQ ID NO: 23).
[00201] Неограничивающие примеры подходящих промоторов для применения в соответствии с настоящим изобретением включают промотор CAG, например (SEQ ID NO: 3), промотор НААТ (SEQ ID NO: 21), промотор EF1-α человека (SEQ ID NO: 6) или фрагмент промотора EF1a (SEQ ID NO: 15), промотор IE2 (например, SEQ ID NO: 20) и промотор EF1-α крысы (SEQ ID NO: 24).
[00202] Последовательности полиаденилирования: последовательность, кодирующая последовательность полиаденилирования, может быть включена в зкДНК-вектор для стабилизации мРНК, экспрессируемой с указанного зкДНК-вектора, и для содействия ядерному экспорту и трансляции. Согласно одному варианту реализации указанный зкДНК-вектор не содержит последовательности полиаденилирования. Согласно другим вариантам реализации указанный вектор включает по меньшей мере 1, по меньшей мере 2, по меньшей мере 3, по меньшей мере 4, по меньшей мере 5, по меньшей мере 10, по меньшей мере 15, по меньшей мере 20, по меньшей мере 25, по меньшей мере 30, по меньшей мере 40, по меньшей мере 45, по меньшей мере 50 или более адениновых динуклеотидов. Согласно некоторым вариантам реализации указанная последовательность полиаденилирования содержит приблизительно 43 нуклеотида, приблизительно 40-50 нуклеотидов, приблизительно 40-55 нуклеотидов, приблизительно 45-50 нуклеотидов, приблизительно 35-50 нуклеотидов или любое количество нуклеотидов в диапазонах между указанными значениями.
[00203] Экспрессионные кассеты могут включать последовательность полиаденилирования, известную в данной области техники, или ее вариант, например, встречающуюся в природе последовательность, выделенную из бычьего гормона роста BGHpA (например, SEQ ID NO: 74) или вируса SV40pA (например, SEQ ID NO: 10), или синтетическую последовательность (например, SEQ ID NO: 27). Некоторые экспрессионные кассеты могут также включать энхансерную 5'-последовательность позднего поли(А)-сигнала SV40 (USE). Согласно некоторым вариантам реализации USE может быть использован в комбинации с SV40pA или гетерологичным поли(А)-сигналом.
[00204] Экспрессионные кассеты могут также включать посттранскрипционный элемент для повышения экспрессии трансгена. Согласно некоторым вариантам реализации для повышения экспрессии трансгена применяют посттранскрипционный регуляторный элемент (WPRE) вируса гепатита сурков (WHP) (например, SEQ ID NO: 8). Могут применяться другие элементы посттранскрипционного процессинга, такие как посттранскрипционный элемент из гена тимидинкиназы вируса простого герпеса или вируса гепатита В (HBV). К трансгенам могут быть присоединены секреторные последовательности, например, последовательности VH-02 и VK-A26, например, SEQ ID NO: 25 и SEQ ID NO: 26.
V. Регуляторные переключатели
[00205] Молекулярный регуляторный переключатель генерирует измеряемое изменение состояния в ответ на сигнал. Такие регуляторные переключатели могут быть успешно скомбинированы с зкДНК-векторами, описанными в настоящем документе, для контроля результатов применения зкДНК-вектора. Согласно некоторым вариантам реализации указанный зкДНК-вектор содержит регуляторный переключатель, который служить для точной настройки экспрессии трансгена. Например, он может служить для обеспечения функции биологического сдерживания зкДНК-вектора. Согласно некоторым вариантам реализации указанный переключатель представляет собой двухпозиционный переключатель, который сконструирован таким образом, чтобы начинать или останавливать (т.е. прекращать) экспрессию представляющего интерес гена в зкДНК контролируемым и регулируемым образом. Согласно некоторым вариантам реализации указанный переключатель может включать ««аварийный выключатель»», который может заставлять клетку, содержащую указанный зкДНК-вектор, переходить к запрограммированной клеточной смерти после активации переключателя.
[00206] А. Бинарные регуляторные переключатели
[00207] Согласно некоторым вариантам реализации указанный зкДНК-вектор содержит регуляторный переключатель, который может служить для контролируемой модуляции экспрессии трансгена. Согласно такому варианту реализации экспрессионная кассета, локализованная между ITR указанного зкДНК-вектора, может дополнительно содержать регуляторную область, например, промотор, цис-элемент, репрессор, энхансер и т.п., функционально связанную с представляющим интерес геном, причем указанную регуляторную область регулируют один или более кофакторов или экзогенных агентов. Соответственно, согласно одному варианту реализации транскрипция и экспрессия представляющего интерес гена с зкДНК-вектора будут происходить только в том случае, если указанные один или более кофакторов или экзогенных агентов присутствуют в клетке. Согласно другому варианту реализации один или более кофакторов или экзогенных агентов могут применяться для дерепрессии транскрипции и экспрессии представляющего интерес гена.
[00208] Любые известные специалисту в данной области техники регуляторные области нуклеиновых кислот могут применяться в зкДНК-векторе, сконструированном так, чтобы включать регуляторный переключатель. Например, регуляторные области могут модулировать низкомолекулярные переключатели, или индуцируемые или репрессируемые промоторы. Неограничивающие примеры индуцируемых промоторов представлены индуцируемыми гормонами или индуцируемыми металлами промоторами. Другие примеры индуцируемых промоторных/энхансерных элементов включают, не ограничиваясь перечисленными, RU486-индуцируемый промотор, экдизон-индуцируемый промотор, рапамицин-индуцируемый промотор и промотор металлотионеина. Предусмотрены для применения классические переключатели на основе тетрациклина или других антибиотиков, в том числе описанные в источнике: Fussenegger et al., Nature Biotechnol. 18: 1203-1208 (2000).
[00209] В. Низкомолекулярные регуляторные переключатели
[00210] Различные регуляторные переключатели на основе малых молекул известны в данной области техники и могут быть скомбинированы с зкДНК-векторами согласно описанию в настоящем документе для получения контролируемого регуляторный переключателем зкДНК-вектора. Согласно некоторым вариантам реализации указанный регуляторный переключатель может быть выбран из чего-либо одного или комбинации перечисленного: ортогональная пара лиганд/ядерный рецептор, например, вариант ретиноидного рецептора/LG335 и GRQCIMFI, наряду с искусственным промотором, контролирующим экспрессию функционально связанного трансгена, например, согласно описанию в источнике: Taylor, et al. ВМС Biotechnology 10 (2010): 15; сконструированные стероидные рецепторы, например, модифицированный рецептор прогестерона, усеченный по С-концу, который не способен связывать прогестерон, но связывает RU486 (мифепристон) (патент США №5364791); рецептор экдизона из Drosophila и его лиганды экдистероиды (Saez, et al., PNAS, 97(26)(2000), 14512-14517; или переключатель, контролируемый антибиотиком триметопримом (ТМР), согласно описанию в Sando R 3rd; Nat Methods. 2013, 10(11): 1085-8.
[00211] Для контроля трансгенной экспрессии зкДНК также предусмотрены для применения другие регуляторные переключатели на основе малых молекул, известные специалисту в данной области техники, которые включают, не ограничиваясь перечисленными, описанные в источнике: Buskirk et al., Cell; Chem and Biol., 2005; 12(2); 151-161; чувствительный к абсцизовой кислоте положительный переключатель; такой как описанные в источнике: Liang, F.-S., et al., (2011) Science Signaling, 4(164); экзогенные чувствительные к L-аргинину положительные переключатели, такие как описанные в источнике: Hartenbach, et al. Nucleic Acids Research, 35 (20), 2007, синтетические чувствительные к желчным кислотам положительные переключатели, такие как описанные в источнике: Rössger et al., Metab Eng. 2014, 21: 81-90; биотин-чувствительные положительные переключатели, такие как описанные в источнике: Weber et al., Metab. Eng. 2009 Mar; 11(2): 117-124; чувствительные к двойной стимуляции пищевыми добавками бензоатом/ванилином регуляторные переключатели, такие как описанные в источнике: Xie et al., Nucleic Acids Research, 2014; 42(14); e116; чувствительные к 4-гидрокситамоксифену переключатели, такие как описанные в источнике: Giuseppe et al., Molecular Therapy, 6(5), 653-663; и чувствительные к флавиноидам (флоретину) регуляторные переключатели, такие как описанные в источнике: Gitzinger et al., Proc. Natl. Acad. Sci. USA. 2009 Jun 30; 106(26): 10638-10643.
[00212] Согласно некоторым вариантам реализации указанный регуляторный переключатель, для контроля трансгена или экспрессируемый зкДНК-вектором, представляет собой переключатель активации пролекарства, такой как описанный в патентах США 8771679 и 6339070.
[00213] Примеры регуляторных переключателей для применения в зкДНК-векторах включают приведенные в таблице 11, однако не ограничены ими.
[00214] С.Регуляторные переключатели с «паролем»
[00215] Согласно некоторым вариантам реализации указанный регуляторный переключатель может представлять собой «переключатель с паролем» или «контур с паролем». Переключатели с паролем позволяют обеспечить точную настройку контроля экспрессии указанного трансгена с зкДНК-вектора при возникновении специфических условий - то есть комбинации условий, наличие которых требуется для протекания трансгенной экспрессии и/или репрессии. Например, для экспрессии трансгена необходимо наличие по меньшей мере условий А и В. Регуляторный переключатель с паролем может быть представлен любым количеством условий, например, по меньшей мере 2, или по меньшей мере 3, или по меньшей мере 4, или по меньшей мере 5, или по меньшей мере 6 или по меньшей мере 7 или более условиями, необходимыми для протекания трансгенной экспрессии. Согласно некоторым вариантам реализации необходимо наличие по меньшей мере 2 условий (например, условий А, В), согласно некоторым вариантам реализации необходимо наличие по меньшей мере 3 условий (например, А, В и С, или А, В и D). Исключительно в качестве примера, для протекания генной экспрессии с зкДНК, содержащей регуляторный переключатель с паролем «АБС», должны присутствовать условия А, В и С. Условия А, В и С могут быть следующими; условие А представлено присутствием состояния или заболевания, условие В представляет собой гормональный ответ, и условие С представляет собой ответ на трансгенную экспрессию. В исключительно иллюстративном примере, когда трансген представляет собой инсулин, условие А выполняется, если у субъекта имеется диабет, условие В выполняется при высоком уровне сахара в крови, а условие С представлено уровнем эндогенного инсулина, не экспрессируемого в требуемых количествах. После падения уровня сахара или достижения требуемого уровня инсулина трансген (например, инсулин) снова выключается до выполнения 3 условий, снова его включающих. В другом иллюстративном примере, когда трансген представляет собой ЕРО, условие А представлено присутствием хронической болезни почек (CKD), условие В выполняется при наличии состояния гипоксии в почках субъекта, условие С представлено нарушением рекрутинга эритропоэтин-продуцирующих клеток (ЭПК) в почках; или, как вариант, нарушением активации HIF-2. После того как уровни кислорода увеличиваются или достигнут требуемый уровень ЕРО, трансген (например, ЕРО) снова выключается до выполнения 3 условий, снова его включающих.
[00216] Регуляторные переключатели с паролем подходят для точной настройки экспрессии трансгена с зкДНК-вектора. Например, регуляторный переключатель с паролем может быть модульным, то есть содержать несколько переключателей, например, тканеспецифический индуцируемый промотор, который включается только в присутствии определенного уровня метаболита. Согласно такому варианту реализации для протекания трансгенной экспрессии с зкДНК-вектора должен присутствовать индуцируемый агент (условие А) в требуемом типе клеток (условие В), и уровень метаболита должен быть равен определенному пороговому значению, или быть выше или ниже определенного порогового значения (условие С). Согласно альтернативным вариантам реализации указанный регуляторный переключатель с паролем может быть разработан таким образом, что трансгенная экспрессия включена при выполнении условий А и В, однако выключается при выполнении условия С. Такой вариант реализации полезен, если условие С является непосредственным результатом для экспрессируемого трансгена - то есть условие С служит в качестве положительной обратной связи в петле для выключения трансгенной экспрессии с зкДНК-вектора после обеспечения трансгеном требуемого терапевтического эффекта достаточной величины.
[00217] Согласно некоторым вариантам реализации регуляторный переключатель с паролем, предусмотренный для применения в указанном зкДНК-векторе, раскрыт в WO 2017/059245, где описан переключатель, называемый «переключателем с паролем», или «сетью с паролем», или «аварийным выключателем с паролем», который представляет собой синтетический биологический контур, задействующий гибридные транскрипционные факторы (ТФ) для конструирования сложных требований к окружающей среде для выживания клеток. Регуляторные переключатели с паролем, описанные в WO 2017/059245, в частности, подходят для применения в зкДНК-векторах, поскольку они являются модульными и и настраиваемыми, в отношении как условий окружающей среды, которые контролируют активацию контура, так и выходных модулей, которые контролируют судьбу клетки. Кроме того, контур с паролем особенно полезен для применения в зкДНК-векторах, поскольку без подходящих молекул-«паролей» он позволяет трансгенную экспрессию только в присутствии требуемых заранее заданных условий. Если с клеткой происходит что-либо непредусмотренное, или по какой-либо причине дополнительная трансгенная экспрессия не требуется, может быть запущен связанный «аварийный выключатель» (т.е. блокиратор).
[00218] Согласно некоторым вариантам реализации регуляторный переключатель с паролем или «контур с паролем», предусмотренный для применения в указанном зкДНК-векторе, содержит гибридные транскрипционные факторы (ТФ) для увеличения диапазона и сложности сигналов окружающей среды, используемых для задания условий биологического сдерживания. В отличие от блокиратора, который запускает клеточную смерть при наличии заранее заданного условия, «контур с паролем» позволяет обеспечить выживание клеток или трансгенную экспрессию при наличии конкретного «пароля», и может быть легко перепрограммирован, чтобы позволять трансгенную экспрессию и/или выживание клеток только при наличии заранее заданного условия окружающей среды или пароля.
[00219] Согласно одному аспекту система с «паролем», которая ограничивает рост клеток условием наличия заранее заданного набора из по меньшей мере двух выбранных агентов, включает одну или более конструкций нуклеиновых кислот, кодирующих экспрессионные модули, содержащие: i) модуль экспрессии токсина, который кодирует токсин, токсичный для клетки-хозяина, где последовательность, кодирующая указанный токсин, функционально связана с промотором Р1, который репрессирован связыванием первого гибридного белка-репрессора hRP1; ii) модуль экспрессии первого гибридного белка-репрессора, который кодирует первый гибридный белок-репрессор hRP1, где экспрессию hRP1 контролирует схема логического сложения, образованная двумя гибридными транскрипционными факторами hTF1 и hTF2, связывание или активность которых реагирует на агенты А1 и А2, соответственно, так что оба агента А1 и А2 необходимы для экспрессии hRP1, при этом в отсутствие любого из А1 и А2 экспрессия hRP1 является недостаточной для репрессии модуля промотора токсина Р1 и продуцирования токсина, таким образом, клетка-хозяин погибает. В указанной системе каждый из гибридных факторов hTF1, hTF2 и hRP1 содержит чувствительный к условиям окружающей среды модуль из одного транскрипционного фактора и модуль распознавания ДНК из другого транскрипционного фактора, что придает связыванию соответствующего регуляторного переключателя с паролем чувствительность к наличию агента окружающей среды, А1 или А2, отличающегося от того, с которым соответствующие субъединицы обычно связываются в природе.
[00220] Соответственно, зкДНК-вектор может содержать «регуляторный контур с паролем» который требует присутствия и/или отсутствия специфических молекул для активации выходного модуля. Согласно некоторым вариантам реализации, если в выходной модуль помещают гены, которые кодируют клеточные токсины, регуляторный контур с паролем может быть использован не только для регуляции трансгенной экспрессии, но и для создания механизма «аварийного выключателя», где указанный контур убивает клетку, если клетка ведет себя нежелательным образом (например, покидает специфическую среду, заданную сенсорными доменами, или дифференцируется в клетку другого типа). Согласно одному неограничивающему примеру модульная структура гибридных транскрипционных факторов, архитектура контура и выходной модуль позволяют изменять конфигурацию контура для восприятия других сигналов окружающей среды, реакции на указанные сигналы окружающей среды иным образом и контроля других функций в клетке наряду с индуцированной клеточной смертью, как известно в данной области техники.
[00221] Все комбинации регуляторных переключателей согласно описанию в настоящем документе, например, низкомолекулярные переключатели, переключатели на основе нуклеиновых кислот, гибридные переключатели на основе малых молекул и нуклеиновых кислот, посттранскрипционные регуляторные переключатели трансгенов, посттрансляционная регуляция, контролируемые излучением переключатели, опосредованные гипоксией переключатели и другие регуляторные переключатели, известные специалистам в данной области техники согласно описанию в настоящем документе могут применяться в регуляторном переключателе с паролем согласно описанию в настоящем документе. Регуляторные переключатели, предусмотренный для применения, также обсуждаются в обзорной статье Kis и соавторов (Kis et al., J R Soc Interface. 12: 20141000 (2015)), и обобщены в таблице 1 статьи Kis. Согласно некоторым вариантам реализации регуляторный переключатель для применения в системе с паролем может быть выбран из любого переключателя или их комбинации из таблицы 11.
[00222] D. Регуляторные переключатели на основе нуклеиновых кислот для контроля трансгенной экспрессии
[00223] Согласно некоторым вариантам реализации регуляторный переключатель для контроля трансгена, экспрессируемого зкДНК, основан на механизме контроля на основе нуклеиновой кислоты. Примеры механизмов контроля на основе нуклеиновых кислот известны в данной области техники и предусмотрены для применения. Например, такие механизмы включают рибопереключатели, такие как описанные, например, в US 2009/0305253, US 2008/0269258, US 2017/0204477, WO 2018026762 А1, в патенте США 9222093 и заявке на европейский патент ЕР 288071, а также в обзоре Villa с соавторами (Villa JK et al., Microbiol Spectr. 2018 May; 6(3)). Также включены реагирующие на метаболиты транскрипционные биосенсоры, такие как описанные в WO 2018/075486 и WO 2017/147585. Другие известные в данной области техники механизмы, предусмотренные для применения, включают сайленсинг указанного трансгена молекулой миРНК или РНК-интерференции (например, miR, мшРНК). Например, указанный зкДНК-вектор может содержать регуляторный переключатель, который кодирует молекулу РНК-интерференции (RNAi), комплементарную трансгену, экспрессируемому указанным зкДНК-вектором. При экспрессии такой RNAi даже при экспрессии трансгена зкДНК-вектором происходит его сайленсинг за счет действия комплементарной молекулы РНК-интерференции, а при отсутствии экспрессии RNAi, если указанный трансген экспрессируется зкДНК-вектором, сайленсинг указанного трансгена за счет РНК-интерференции не происходит. Такой пример контролирующей генную экспрессию молекулы RNAi, или регуляторного переключателя раскрыт в US 2017/0183664. Согласно некоторым вариантам реализации указанный регуляторный переключатель содержит репрессор, который блокирует экспрессию указанного трансгена с зкДНК-вектора. Согласно некоторым вариантам реализации указанный двухпозиционный переключатель представляет собой основанный на малой активирующей транскрипцию РНК (STAR) переключатель, например, такой как описанные в источнике: Chappell J. et al., Nat Chem Biol. 2015 Mar; 11(3): 214-20; и Chappell et al., Microbiol Spectr. 2018 May; 6(3. Согласно некоторым вариантам реализации указанный регуляторный переключатель представляет собой удерживающий переключатель, такой как описанные в источниках: US 2009/0191546, US 2016/0076083, WO 2017/087530, US 2017/0204477, WO 2017/075486; и Green et al, Cell, 2014; 159(4); 925-939.
[00224] Согласно некоторым вариантам реализации указанный регуляторный переключатель представляет собой тканеспецифический самоинактивирующийся регуляторный переключатель, например, согласно описанию в US 2002/0022018, который целенаправленно выключает трансгенную экспрессию в сайте, где трансгенная экспрессия может, напротив, быть неблагоприятной. Согласно некоторым вариантам реализации указанный регуляторный переключатель представляет собой рекомбиназную обратимую систему генной экспрессии, например, согласно описанию в US 2014/0127162 и патенте США 8324436.
[00225] Согласно некоторым вариантам реализации указанный регуляторный переключатель для контроля трансгена или представляющего интерес гена, экспрессируемого зкДНК-вектором, представляет собой гибрид контрольного механизма на основе нуклеиновой кислоты и низко молекулярной регуляторной системой. Такие системы хорошо известны специалистам в данной области техники и предусмотрены для применения согласно настоящему изобретению. Примеры таких регуляторных переключателей включают, не ограничиваясь перечисленными, систему LTRi или систему «Lac-Tet-RNAi», например, согласно описанию в источниках: US 2010/0175141, Deans Т. et al., Cell, 2007, 130(2); 363-372, WO 2008/051854 и патенте США 9388425.
[00226] Согласно некоторым вариантам реализации указанный регуляторный переключатель для контроля трансгена или представляющего интерес гена, экспрессируемого зкДНК-вектором, включает кольцевую пермутацию согласно описанию в патенте США 8338138. Согласно такому варианту реализации указанный молекулярный переключатель мультистабилен, т.е. способен переключаться между по меньшей мере двумя состояниями, или, как вариант, бистабилен, т.е. находится в состоянии либо «включено», либо «выключено», например, в отношении способности или неспособности испускать свет, способности или неспособности к связыванию, способности или неспособности к катализу, способности или неспособности к переносу электронов, и т.д. Согласно другому аспекту указанный молекулярный переключатель задействует слитую молекулу, соответственно, указанный переключатель способен переключаться между более чем двумя состояниями. Например, в ответ на конкретное пороговое состояние, демонстрируемое инсерционной последовательностью или акцепторной последовательностью, соответствующая другая последовательность слитой молекулы может демонстрировать диапазон состояний (например, диапазон связывающей активности, диапазон ферментативного катализа и т.п.). Соответственно, вместо переключения между состояниями «включено» или «выключено» слитая молекула может демонстрировать ступенчатый ответ на стимул.
[00227] Согласно некоторым вариантам реализации регуляторный переключатель на основе нуклеиновой кислоты может быть выбран из любого переключателя или их комбинации из таблицы 11.
[00228] Е. Посттранскрипционные и посттрансляционныерегуляторные переключатели.
[00229] Согласно некоторым вариантам реализации указанный регуляторный переключатель для контроля трансгена или представляющего интерес гена, экспрессируемого зкДНК-вектором, представляет собой систему посттранскрипционной модификации. Например, такой регуляторный переключатель может представлять собой рибопереключатель-аптазим, чувствительный к тетрациклину или теофиллину, согласно описанию в US 2018/0119156, GB 201107768, WO 2001/064956 A3, европейском патенте ЕР 2707487 и Beilstein et al., ACS Synth. Biol, 2015, 4 (5), pp 526-534; Zhong et al, Elife. 2016 Nov 2;5. pii: e18858. Согласно некоторым вариантам реализации предполагается, что специалист в данной области техники может кодировать как трансген, так и ингибиторную миРНК, которая содержит чувствительный к лиганду (отрицательный переключатель) аптамер, с получением в итоге лиганд-чувствительного положительного переключателя.
[00230] Согласно некоторым вариантам реализации указанный регуляторный переключатель для контроля трансгена или представляющего интерес гена, экспрессируемого зкДНК-вектором, представляет собой систему посттрансляционной модификации. Согласно альтернативным вариантам реализации указанный представляющий интерес ген или белок экспрессируется как пробелок или пре-пробелок, или содержит элемент ответа на сигнал (SRE) или дестабилизирующий домен (DD), присоединенный к экспрессируемому белку, что предотвращает корректную укладку и/или активность белка до посттрансляционной модификации. В случае дестабилизирующего домена (DD) или SRE, указанный дестабилизирующий домен посттрансляционно расщепляется в присутствии экзогенного агента или малой молекулы. Специалист в данной области техники может использовать такие способы контроля согласно описанию в патенте США 8173792 и РСТ-заявке WO 2017180587. Другие посттранскрипционные контрольные переключатели, предусмотренные для применения в указанном зкДНК-векторе для контроля активности функционального трансгена, описаны в источниках: Rakhit et al, Chem Biol. 2014;21(9): 1238-52 и Navarro et al, ACS Chem Biol. 2016; 19; 11(8): 2101-2104A.
[00231] Согласно некоторым вариантам реализации регуляторный переключатель для контроля трансгена или представляющего интерес гена, экспрессируемого зкДНК-вектором, представляет собой система посттрансляционной модификации, которая включает лиганд-чувствительные интеины в кодирующей последовательности трансгена, таким образом, что указанный трансген или экспрессируемый белок ингибирован до сплайсинга. Например, это было продемонстрировано с применением как 4-гидрокситамоксифена, так и тиреоидного гормона (см., например, патенты США 7541450, 9200045; 7192739, Buskirk, et al, Proc Natl Acad Sci USA. 2004 Jul 20; 101(29): 10505-10510; ACS Synth Biol. 2016 Dec 16; 5(12): 1475-1484; и 2005 Feb; 14(2): 523-532. Согласно некоторым вариантам реализации посттранскрипционный регуляторный переключатель может быть выбран из любого переключателя или их комбинации из таблицы 11.
[00232] F. Другие примеры регуляторных переключателей
[00233] Для контроля генной экспрессии трансгена, экспрессируемого зкДНК-вектором, в указанном зкДНК-векторе может применяться любой известный регуляторный переключатель, в том числе запускаемый изменениями окружающей среды. Дополнительные примеры включают, не ограничиваясь указанными: ВОС-способ по Suzuki et al., Scientific Reports 8; 10051 (2018); расширение генетического кода и нефизиологическую аминокислоту; контролируемые излучением или ультразвуком положительные/отрицательные переключатели (см., например, Scott S et al, Gene Ther. 2000 Jul;7(13): 1121-5; патенты США 5612318; 5571797; 5770581; 5817636; и WO 1999/0253 85 A1. Согласно некоторым вариантам реализации указанный регуляторный переключатель контролирует имплантируемая система, например, согласно описанию в патентах США 7840263; US 2007/0190028 A1, где генную экспрессию контролирует одна или более форм энергии, в том числе электромагнитная энергия, которая активирует промоторы, функционально связанные с трансгеном в зкДНК-векторе.
[00234] Согласно некоторым вариантам реализации регуляторный переключатель, предусмотренный для применения в указанном зкДНК-векторе, представляет собой опосредованный гипоксией или стресс-активируемый переключатель, например, такой как описанные в источниках: WO 1999060142А2, патенты США 5834306; 6218179; 6709858; US 2015/0322410; Greco et al, (2004) Targeted Cancer Therapies 9, S368, а также элементы FROG, TOAD и NRSE и условно-индуцируемые элементы сайленсинга, в том числе элементы ответа на гипоксию (HRE), элементы воспалительного ответа (IRE) и активируемые сдвиговым напряжением элементы (SSAE), например, согласно описанию в патенте США 9394526. Такой вариант реализации подходит для включения экспрессии указанного трансгена с зкДНК-вектора после ишемии или в ишемических тканях, и/или в опухолях.
[00235] Согласно некоторым вариантам реализации регуляторный переключатель, предусмотренный для применения в указанном зкДЬЖ-векторе, представляет собой оптогенетический (например, контролируемый светом) регуляторный переключатель, например, такой как один из переключателей, описанных в источнике: Polesskaya et al., ВМС Neurosci. 2018; 19(Suppl 1): 12, которые также предусмотрены для применения согласно настоящему изобретению. Согласно таким вариантам реализации зкДНК-вектор может содержать генетические элементы, чувствительные к свету, и может регулировать трансгенную экспрессию в ответ на излучение с видимой длиной волны (например, синий, в ближней ИК-области). зкДНК-векторы, содержащие оптогенетический регуляторные переключатели, подходят для применения при экспрессии трансгена в местоположениях в организме, которых могут достигать источники такого света, например, коже, глазах, мышцах и т.п., и могут также применяться при экспрессии трансгенов с помощью зкДНК-векторов во внутренних органах и тканях, если световой сигнал может быть обеспечен с применением подходящего способа (например, имплантируемого устройства согласно описанию в настоящем документе). Такие оптогенетические регуляторные переключатели включают применение реагирующих на свет элементов или индуцируемого светом транскрипционного эффектора (LITE) (например, описанные в источнике: 2014/0287938), системы Light-On (например, описанной в источнике: Wang et al., Nat Methods. 2012 Feb 12;9(3):266-9; которая, как сообщалось, позволяет обеспечить контроль экспрессии трансгена инсулина in vivo, системы Cry2/CIB1 (например, описанной в источнике: Kennedy et al., Nature Methods; 7, 973 975 (2010); и системы FKF1/GIGANTEA (например, описанной в источнике: Yazawa et al., Nat Biotechnol. 2009 Oct;27(10):941-5).
[00236] G. «Аварийные выключатели»
[00237] Другие варианты реализации настоящего изобретения относятся к зкДНК-вектору, содержащему «аварийный выключатель». «Аварийный выключатель» согласно описанию в настоящем документе позволяет обеспечить киллинг клетки, содержащей зкДНК-вектор, или ее переход к запрограммированной гибели в качестве способа окончательного устранения введенного зкДНК-вектора из системы субъекта. Специалисту в данной области техники будет понятно, что применение «аварийных выключателей» в зкДНК-векторах согласно настоящему изобретению, как правило, сопряжено с нацеливанием указанного зкДНК-вектора на ограниченное число клеток, потеря которого приемлема для субъекта, или на тип клеток, апоптоз которых желателен (например, на раковые клетки). Во всех аспектах ««аварийный выключатель» согласно описанию в настоящем документе разработан так, чтобы обеспечивать быстрый и устойчивый киллинг клетки, содержащей указанный зкДНК-вектор, в отсутствие входного сигнала выживания или другого специфического условия. Другими словами, «аварийный выключатель», кодируемый зкДНК-вектором согласно настоящему изобретению, может ограничивать выживание клетки, содержащей зк ДНК-вектор, окружающей средой, заданной специфическими входными сигналами. Такие «аварийные выключатели» служат для обеспечения функции биологического сдерживания, если требуется либо удалить зкДНК вектор из субъекта, либо обеспечить отсутствие экспрессии кодируемого трансгена. Соответственно, «аварийные выключатели» являются синтетическими биологическими контурами в указанном зкДНК-векторе, сопрягающими сигналы окружающей среды с обусловленным выживанием клетки, содержащей указанный зкДНК-вектор. Согласно некоторым вариантам реализации могут быть разработаны разные зкДНК-векторы, содержащие разные «аварийные выключатели». Это позволяет контролировать, киллинг каких экспрессирующих трансген клеток происходит при использовании коктейлей зкДНК-векторов.
[00238] Согласно некоторым вариантам реализации зкДНК-вектор может содержать «аварийный выключатель», который представляет собой модульный контур биологического сдерживания. Согласно некоторым вариантам реализации «аварийный выключатель» предусмотренный для применения в указанном зкДНК-векторе, раскрыт в WO 2017/059245, где описан переключатель, называемый «аварийным блокиратором», который содержит схему из по меньшей мере двух взаимно ингибирующих, поддающихся репрессии последовательностей, таким образом, что сигнал окружающей среды подавляет активность второй молекулы в указанной конструкции (например, связывающий малую молекулу транскрипционный фактор используют для обеспечения состояния «выживания» за счет репрессии продуцирования токсина). В клетках, содержащих зкДНК-вектор с аварийным блокиратором, после исчезновения сигнала окружающей среды контур необратимо переключается в состояние «смерти» с дерепрессией токсина, что приводящей к его продуцированию, что убивает клетку. Согласно другому варианту реализации предложен синтетический биологический контур, называемый «контуром с паролем» или «аварийным выключателем с паролем», задействующий гибридные транскрипционные факторы (ТФ) для конструирования сложных требований к окружающей среде для выживания клеток. Аварийный блокиратор и аварийный выключатель с паролем, описанные в WO 2017/059245, подходят, в частности, для применения в зкДНК-векторах, поскольку они являются модульными и настраиваемыми, в отношении как условий окружающей среды, которые контролируют активацию контура, так и выходных модулей, которые контролируют судьбу клетки. При правильном выборе токсинов, в том числе, но не ограничиваясь перечисленными, эндонуклеазы, например, EcoRI, контуры с паролем в зкДНК-векторе могут применяться не только для киллинга (убийства, уничтожения) клетки-хозяина, содержащей зкДНК-вектор, но и для разложения ее генома и сопутствующих плазмид.
[00239] Другие «аварийные выключатели», известные специалисту в данной области техники, предусмотрены для применения в зкДНК-векторе согласно описанию в настоящем документе, например, описанные в US 2010/0175141; US 2013/0009799; US 2011/0172826; US 2013/0109568, а также «аварийные выключатели», описанные в источнике: Jusiak et al, Reviews in Cell Biology and molecular Medicine; 2014; 1-56; Kobayashi et al, PNAS, 2004; 101; 8419-9; Marchisio et al. Int. Journal of Biochem and Cell Biol, 2011; 43; 310-319; и Reinshagen et al. Science Translational Medicine, 2018, 11.
[00240] Соответственно, согласно некоторым вариантам реализации указанный зкДНК-вектор может содержать конструкцию нуклеиновой кислоты «аварийного выключателя», которая содержит нуклеиновую кислоту, кодирующую эффекторный токсин или репортерный белок, причем экспрессию указанного эффекторного токсина (например, белка смерти) или репортерного белка контролирует заранее заданное условие. Например, заранее заданное условие может быть представлено присутствием агента окружающей среды, такого как, например, экзогенный агент, без которого клетка будет по умолчанию экспрессировать эффекторный токсин (например, белок смерти) и будет убита. Согласно альтернативным вариантам реализации заранее заданное условие представлено присутствием двух или более агентов окружающей среды, например, клетка будет выживать только при поступлении двух или более необходимых экзогенных агентов, и без любого из них клетка, содержащая указанный зкДНК-вектор, будет убита.
[00241] Согласно некоторым вариантам реализации зкДНК-вектор модифицирован таким образом, чтобы включать аварийный выключатель для уничтожения клеток, содержащих указанный зкДНК-вектор, для эффективной терминации экспрессии in vivo указанного трансгена, экспрессируемого зкДНК-вектором (например, терапевтического гена, белка или пептида, и т.п.). В частности, указанный зкДНК-вектор генетически сконструирован так, чтобы дополнительно экспрессировать переключатель-белок, не функциональный в клетках млекопитающих в нормальных физиологических условиях. Только после введения лекарственного средства или обеспечения условий окружающей среды, специфически нацеленных на указанный переключатель-белок, клетки, экспрессирующие указанный переключатель-белок, будут уничтожены, с прекращением таким образом экспрессии указанного терапевтического белка или пептида. Например, сообщалось, что киллинг клеток, экспрессирующих HSV-тимидинкиназу, может происходить после введения лекарственных средств, таких как ганцикловир и цитозиндезаминаза. См, например, источники: Dey and Evans, Suicide Gene Therapy by Herpes Simplex Virus-1 Thymidine Kinase (HSV-TK), в издании: «Targets in Gene Therapy», ред. You (2011); и Bellinger et al, Proc. Natl. Acad. Sci. USA 96(15):8699-8704 (1999). Согласно некоторым вариантам реализации указанный зкДНК-вектор может содержать «аварийный выключатель» миРНК, называемый DISE («Death Induced by Survival gene Elimination))) (Murmann et al, Oncotarget. 2017; 8:84643-84658. Induction of DISE in ovarian cancer cells in vivo).
[00242] Согласно некоторым аспектам аварийный блокиратор представляет собой биологический контур или систему, обеспечивающий(ую) чувствительность клеточного ответа к заранее заданному условию, такому как отсутствие агента в окружающей клетки среде, например, экзогенного агента. Такой контур или система может содержать конструкцию нуклеиновой кислоты, содержащую экспрессионные модули, которые образуют регуляторный контур с блокиратором, чувствительный к заранее заданному условию, причем указанная конструкция содержит экспрессионные модули, которые образуют регуляторный контур, и включает:
i) первый модуль экспрессии белка-репрессора, где указанный первый белок-репрессор связывает связывающий первый белок-репрессор элемент нуклеиновой кислоты и подавляет транскрипцию кодирующей последовательности, содержащей указанный связывающий первый белок-репрессор элемент, при этом репрессирующая активность первого белка-репрессора чувствительна к ингибированию первым экзогенным агентом, присутствие или отсутствие которого представляет собой заранее заданное условие;
ii) второй модуль экспрессии белка-репрессора, где указанный второй белок-репрессор связывает связывающий второй белок-репрессор элемент нуклеиновой кислоты и подавляет транскрипцию кодирующей последовательности, содержащей указанный связывающий второй белок-репрессор элемент, при этом второй белок-репрессор отличается от первого белка-репрессора; и
iii) модуль экспрессии эффектора, содержащий последовательность нуклеиновой кислоты, кодирующую эффекторный белок, функционально связанный с генетическим элементом, содержащим связывающий элемент для второго белка-репрессора, так что экспрессия второго белка-репрессора вызывает репрессию экспрессии эффектора с модуля экспрессии эффектора, при этом второй модуль экспрессии содержит связывающий первый белок-репрессор элемент нуклеиновой кислоты, который позволяет репрессировать транскрипцию второго белка-репрессора, когда указанный элемент связан первым белком-репрессором, причем соответствующие модули образуют регуляторный контур таким образом, что в отсутствие первого экзогенного агента первый белок-репрессор продуцируется с первого модуля экспрессии белка-репрессора и подавляет транскрипцию со второго модуля экспрессии белка-репрессора, таким образом, что репрессия экспрессии эффектора вторым белком-репрессором отменяется, что приводит к экспрессии эффекторного белка, однако в присутствии первого экзогенного агента активность первого белка-репрессора ингибирована, что позволяет экспрессию второго белка-репрессора, который поддерживает экспрессию эффекторного белка в состоянии «выключено», таким образом, первый экзогенный агент необходим для контура, чтобы поддерживать экспрессию эффекторного белка в состоянии «выключено», а удаление или отсутствие первого экзогенного агента по умолчанию приводит к экспрессии эффекторного белка.
[00243] Согласно некоторым вариантам реализации указанный эффектор представляет собой токсин или белок, который индуцирует программу клеточной смерти. Может быть использован любой белок, токсичный для клетки-хозяина. Согласно некоторым вариантам реализации указанный токсин убивает только те клетки, в которых происходит его экспрессия. Согласно другим вариантам реализации указанный токсин убивает и другие клетки того же организма-хозяина. Любой из многочисленных продуктов, приводящих к клеточной смерти, может быть использован в аварийном блокираторе. В частности, подходят для применения агенты, которые ингибируют репликацию ДНК, трансляцию белка или другие процессы или, например, разрушающие нуклеиновую кислоту клетки-хозяина. Для идентификации эффективного механизма киллинга клеток-хозяев после активации контура тестировали несколько генов токсинов, которые прямо повреждают ДНК или РНК клетки-хозяина. Тестировали эндонуклеазу ecoRI21, ингибитор ДНК-гиразы ccdB22 и токсин рибонуклеазного типа mazF23, поскольку они подробно охарактеризованы, являются естественными для Е. coli и обеспечивают диапазон механизмов киллинга. Для повышения устойчивости контура и обеспечения независимого способа контур-зависимой клеточной смерти указанная система может быть дополнительно адаптирована таким образом, чтобы экспрессировать, например, нацеленную протеазу или нуклеазу, которая дополнительно взаимодействует с репрессором, поддерживающим ген смерти в «выключенном» состоянии. После потери или устранения сигнала выживания репрессия гена смерти еще более эффективно устраняется в результате, например, активного разложения белка-репрессора или его мРНК. В неограничивающих примерах протеазу mƒ-Lon использовали не только для разрушения LacI, но и для нацеливания на важнейшие белки для их разложения. Метка разложения mƒ-Lon pdt#l может быть присоединена к 3'-концу пяти важнейших генов, белковые продукты которых особенно чувствительны к разложению mϕ-Lon 20; жизнеспособность клеток измеряли после удаления АТс. Из протестированных важнейших генов-мишеней ген биосинтеза пептидогликанов murC обеспечивал фенотип, отличавшийся наиболее выраженной и быстрой клеточной смертью (коэффициент выживания <1 × 10-4 в пределах 6 часов).
[00244] В настоящем документе термин «заранее заданный входной сигнал» относится к агенту или условию, влияющему на активность полипептида - транскрипционного фактора известным образом. Обычно такие агенты могут связываться с полипептидом транскрипционным фактором и/или изменять его конформацию, с модификацией таким образом активности полипептида - транскрипционного фактора. Примеры заранее заданных входных действий включают, не ограничиваясь перечисленными, входные агенты окружающей среды, не являющиеся необходимыми для выживания определенного организма хозяина (т.е. в отсутствие синтетического биологического контура согласно описанию в настоящем документе). Условия, которые могут обеспечивать заранее заданный входной сигнал, включают, например, температуру, например, если активность одного или более факторов является температурно-чувствительной, присутствие или отсутствие света, в том числе света определенного спектра длин волн, и концентрацию газа, соли, металла или минерального вещества. Входные агенты окружающей среды включают, например, малые молекулы, биологические агенты, такие как феромоны, гормоны, факторы роста, метаболиты, питательные вещества и т.п., и аналоги перечисленного; концентрации химических веществ, побочные продукты в окружающей среде, ионы металлов; и другие такие молекулы или агенты; уровни освещения; температуру; механический стресс или давление; или электрические сигналы, такие как ток и напряжение.
[00245] Согласно некоторым вариантам реализации репортеры используют для количественного определения силы или активность сигнала, получаемого модулями или программируемыми синтетическими биологическими контурами согласно настоящему изобретению. Согласно некоторым вариантам реализации репортеры могут быть слиты внутри рамки с другими кодирующими белок последовательностями для идентификации локализации указанного белка в клетке или организме. Люциферазы могут применяться в качестве эффекторных белков в различных вариантах реализации, описанных в настоящем документе, например, для измерения низких уровней генной экспрессии, поскольку клетки проявляют тенденцию к незначительной фоновой люминесценции или ее отсутствию в отсутствие люциферазы. Согласно другим вариантам реализации ферменты, которые продуцируют окрашенные субстраты, могут быть количественно определены с применением спектрофотометров или других инструментов, позволяющих измерять поглощение, в том числе планшет-ридеров. Как и люциферазы, такие ферменты, как β-галактозидаза могут применяться для измерения низких уровни генной экспрессии поскольку они имеют свойство амплифицировать слабые сигналы. Согласно некоторым вариантам реализации эффекторный белок может представлять собой фермент, который может разрушать или иным образом уничтожать некоторый токсин. Согласно некоторым вариантам реализации эффекторный белок может представлять собой придающий запах фермент, который преобразует субстрат в пахнущий продукт. Согласно некоторым вариантам реализации эффекторный белок может представлять собой фермент, который фосфорилирует или дефосфорилирует либо малые молекулы, либо другие белки, или фермент, который метилирует или деметилирует другие белки или ДНК.
[00246] Согласно некоторым вариантам реализации эффекторный белок может представлять собой рецептор, лиганд, или литический белок. Рецепторы часто содержат три домена: внеклеточный домен для связывания лигандов, таких как белки, пептиды или малые молекулы, трансмембранный домен и внутриклеточный или цитоплазматический домен, который часто может быть вовлечен в какого-либо рода событие сигнальной трансдукции, например, в фосфорилирование. Согласно некоторым вариантам реализации в качестве эффекторных белков используют последовательности гена транспортера, канала или помпы. Неограничивающие примеры и последовательности эффекторных белков для применения с «аварийными выключателями» согласно описанию в настоящем документе можно найти в Реестре стандартных биологических компонентов («Registry of Standard Biological Parts») в сети Интернет по ссылке parts.igem.org.
[00247] В настоящем документе «модуляторный белок» представляет собой белок, который модулирует экспрессию с целевой последовательности нуклеиновой кислоты. Модуляторные белки включают в том числе, например, транскрипционные факторы, транскрипционные активаторы и репрессоры, и белки которые связывают или модифицируют транскрипционный фактор и влияют на его активность. Согласно некоторым вариантам реализации модуляторный белок включает, например, протеазу, которая разрушает белковый фактор, вовлеченный в регуляцию экспрессии с целевой последовательности нуклеиновой кислоты. Предпочтительные модуляторные белки включают модульные белки, в которых, например, связывающие ДНК элементы или домены и связывающие или реагирующие на входной агент элементы или домены могут быть разделены и перенесены, то есть, например, слияние ДНК-связывающего домена первого модуляторного белка с реагирующим на входной агент доменом второго белка приводит к образованию нового белка, который связывает последовательность ДНК, распознаваемую первым белком, но чувствителен к входному агенту, на который обычно отвечает второй белок. Соответственно, в настоящем документе термин «модуляторный полипептид» и более конкретный термин «репрессорный полипептид» включают, наряду с указанными полипептидами, например, «(репрессорным) полипептидом LacI», варианты или производные таких полипептидов, которые отвечают на другой входной агент или вариант входного агента. Соответственно, в случае полипептида LacI включены мутанты или варианты LacI, которые связываются с агентами, не являющимися лактозой или ИПТГ. В данной области техники известен широкий диапазон таких агентов.
[00248] Таблица 11. Примеры регуляторных переключателей b Положительный переключатель, переключаемый в режим «Включено» эффектором; не удалением эффектора, которое обеспечивает состояние «выключено». с Отрицательный переключатель, переключаемый в режим «выключено» эффектором; не удалением эффектора, которое обеспечивает состояние «включено», dТиганд или другие физические стимулы (например, температура, электромагнитное излучение, электричество), которые стабилизируют переключатель в состоянии «Включено» или «выключено». е Относится к номеру источника, цитируемого в статье: Kis et al, J R Soc Interface. 12:20141000 (2015), причем и указанная статья, и цитируемые в ней источники включены в настоящий документ посредством ссылок.
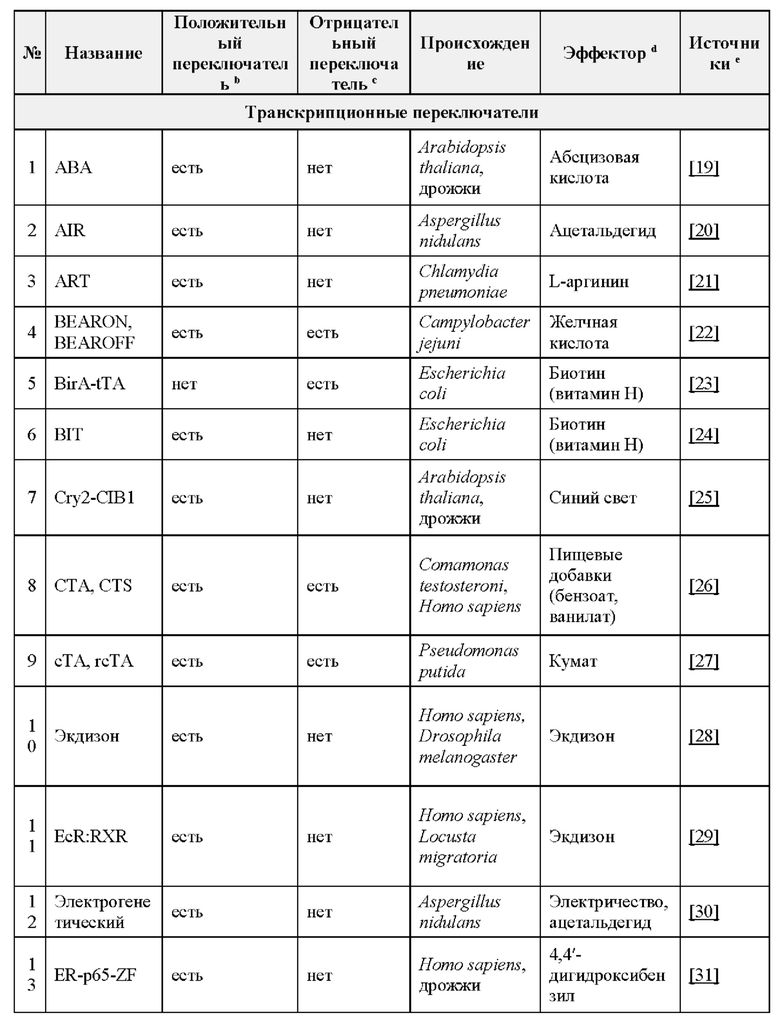
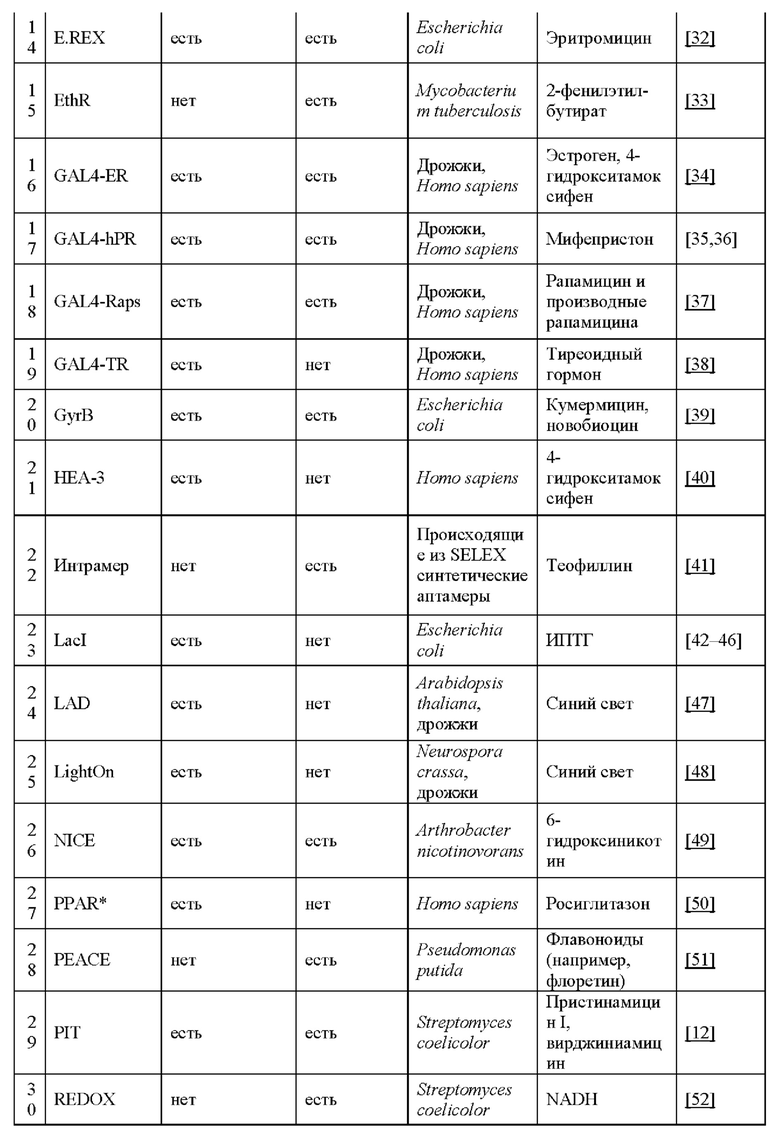
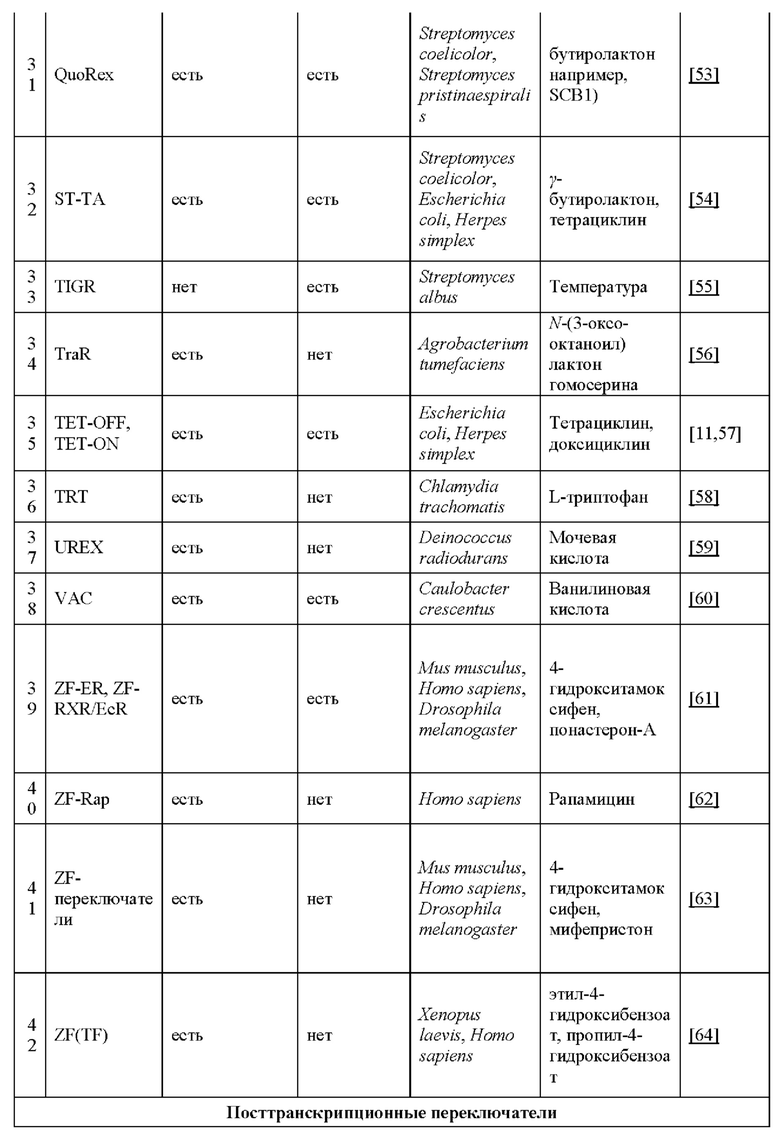
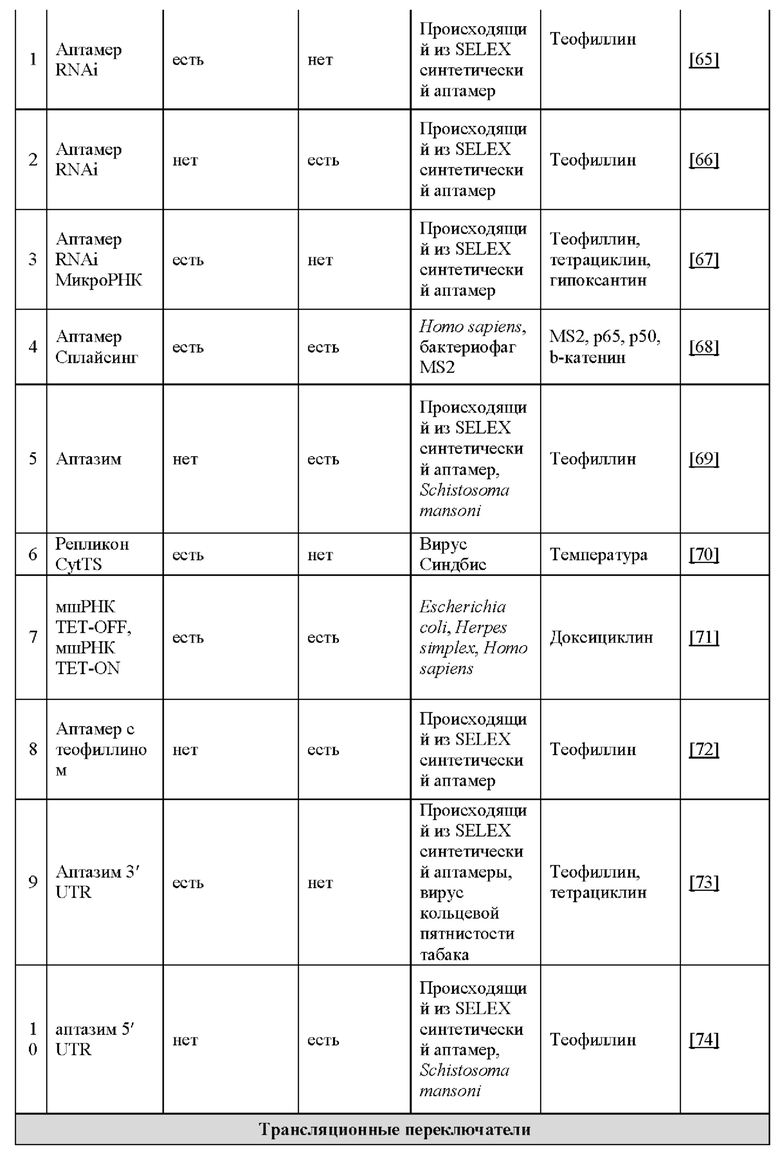
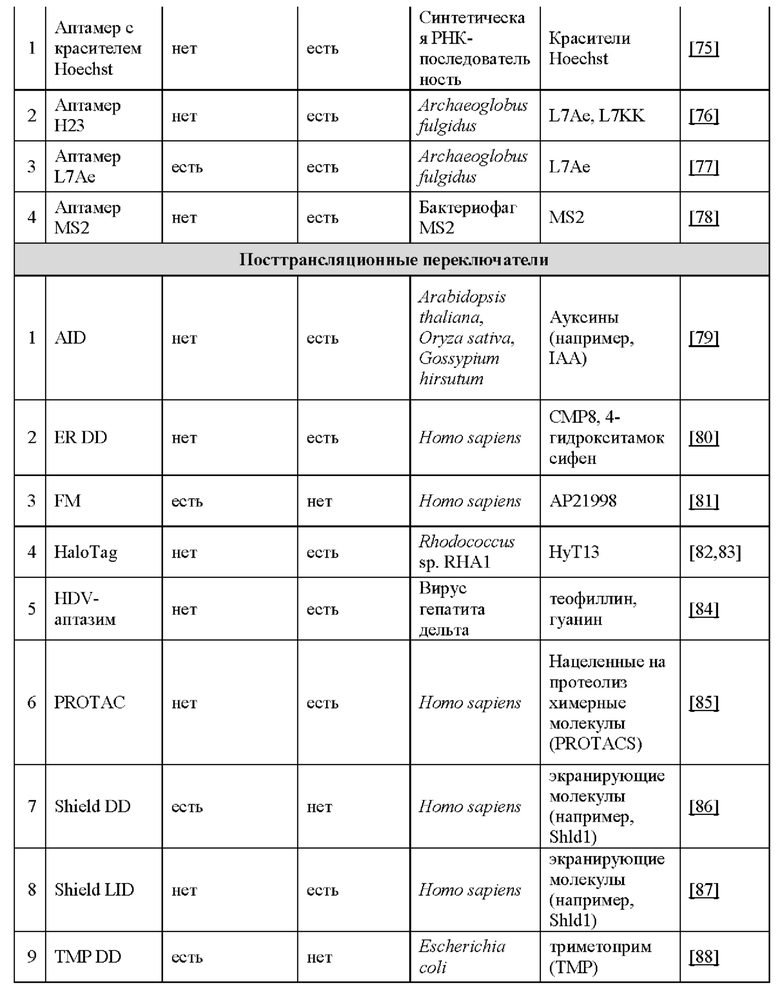
VI. Подробное описание способа получения зкДНК-вектора
А. Получение в целом
[00249] Согласно настоящему раскрытию зкДНК-вектор может быть получен с применением способа, включающего следующие этапы: а) инкубация популяции клеток-хозяев (например, клеток насекомых), несущих полинуклеотидную матрицу экспрессионной конструкции (например, зкДНК-плазмиду, зкДНК-бакмиду и/или зкДНК-бакуловирус), которая не содержит кодирующих последовательностей вирусного капсида, в присутствии белка Rep в условиях, эффективных для, и на протяжении времени, достаточного для того чтобы индуцировать продуцирование указанного зкДНК-вектора в клетках-хозяевах, при этом указанные клетки-хозяева не содержат кодирующих вирусный капсид последовательностей; и b) сбор и выделение зкДНК-вектора из клеток-хозяев. Присутствие белка Rep индуцирует репликацию векторного полинуклеотида с модифицированным ITR для продуцирования зкДНК-вектора в клетке-хозяине. Однако вирусные частицы (например, вирионы AAV) не экспрессируются. Соответственно, отсутствуют ограничения по размеру, такие как естественным образом налагаемые векторами на основе AAV или других вирусов.
[00250] Присутствие зкДНК-вектора, выделенного из клеток-хозяев, может быть подтверждено путем расщепления ДНК, выделенной из клетки-хозяина рестрикционным ферментом, имеющим один сайт распознавания на зкДНК-векторе, и анализа указанного расщепленного ДНК-материала на не денатурирующем геле для подтверждения присутствия характеристических полос линейной и непрерывной ДНК, отличающихся от полос линейной и прерывистой ДНК.
[00251] Согласно еще одному аспекту настоящего изобретения предложено применение линий клеток-хозяев, которые стабильно интегрировали полинуклеотидную матрицу экспрессионного ДНК-вектора (зкДНК-матрицу) в собственный геном, для получения невирусного ДНК-вектора, например, согласно описанию в источнике: Lee, L. et al. (2013) Plos One 8 (8): e69879. Предпочтительно, Rep добавляют в клетки-хозяева с MOI, равной приблизительно 3. Если линия клеток-хозяев представляет собой линию клеток млекопитающего, например, клетки HEK293, указанные линии клеток могут содержать стабильно интегрированную полинуклеотидную векторную матрицу, а второй вектор, например, герпесвирусный, может применяться для введения белка Rep в клетки, обеспечивающего эксцизию и амплификацию зкДНК в присутствии Rep и хелперного вируса.
[00252] Согласно одному варианту реализации клетки-хозяева, используемые для получения зкДНК-векторов, описанных в настоящем документе, представляют собой клетки насекомых, и бакуловирус используют для доставки как полинуклеотида, который кодирует белок Rep, так и полинуклеотидной экспрессионной матричной конструкции невирусного ДНК-вектора для зкДНК, например, согласно описанию в фиг. 4А-4С и примере 1. Согласно некоторым вариантам реализации указанную клетку-хозяина конструируют таким образом, чтобы она экспрессировала белок Rep.
[00253] Затем зкДНК-вектор извлекают и выделяют из клеток-хозяев. Время извлечения и сбора зкДНК-векторов, описанных в настоящем документе, из клеток может быть выбрано и оптимизировано так, чтобы обеспечить высокопродуктивное получение указанных зкДНК-векторов. Например, время извлечения может быть выбрано с учетом жизнеспособности клеток, морфологии клеток, роста клеток и т.п. Согласно одному варианту реализации клетки культивируют в достаточных условиях и собирают через достаточное время после инфекции бакуловирусом для получения зкДНК-векторов, но до начала гибели большинства клеток в результате токсичности бакуловируса. Указанные ДНК-векторы могут быть выделены с применением наборов для очищения плазмид, таких как наборы Endo-Free от Qiagen. Другие способы, разработанные для выделения плазмид, могут быть также адаптированы для ДНК-векторов. Как правило, могут быть использованы любые способы очищения нуклеиновых кислот.
[00254] ДНК-векторы могут быть очищены любым способом очищения ДНК, известным специалистам в данной области техники. Согласно одному варианту реализации зкДНК-векторы очищают как молекулы ДНК. Согласно другому варианту реализации указанный зкДНК-векторы очищают как экзосомы или микрочастицы.
[00255] Присутствие указанного зкДНК-вектора может быть подтверждено путем расщепления векторной ДНК, выделенной из клеток, рестрикционным ферментом, имеющим один сайт распознавания на ДНК-векторе, и анализа и расщепленного, и нерасщепленного ДНК-материала с применением гель-электрофореза для подтверждения присутствия характеристических полос линейной и непрерывной ДНК, отличающихся от полос линейной и прерывистой ДНК. Фиг. 4С и 4Е иллюстрируют один вариант реализации для идентификации присутствия зкДНК-векторов с замкнутыми концами, полученных с применением способов согласно описанию в настоящем документе. Например, на фиг. 5 показан гель, подтверждающий продуцирование зкДНК с нескольких плазмидных конструкций с применением одного варианта реализации для получения векторов согласно описанию в примерах.
В. зкДНК-плазмида
[00256] зкДНК-плазмида представляет собой плазмиду, используемую для последующего получения зкДНК-вектора. Согласно некоторым вариантам реализации зкДНК-плазмида может быть сконструирована с применением известных методик для обеспечения, в виде функционально связанных компонентов, по меньшей мере нижеперечисленного, в направлении транскрипции: (1) 5'-последовательность ITR; (2) экспрессионная кассета, содержащая цис-регуляторный элемент, например, промотор, индуцируемый промотор, регуляторный переключатель, энхансеры и т.п.; и (3) 3'-последовательность ITR, где 3'-последовательность ITR асимметрична относительно 5'-последовательности ITR. Согласно некоторым вариантам реализации указанная экспрессионная кассета, фланкированная ITR, содержит сайт клонирования для введения экзогенной последовательности. Указанная экспрессионная кассета заменяет кодирующие области rep и cap геномов AAV.
[00257] Согласно одному аспекту зкДНК-вектор получают с плазмиды, называемой в настоящем документе «зкДНК-плазмидой», кодирующей в указанном порядке: первый инвертированный концевой повтор (ITR) аденоассоциированного вируса (AAV), экспрессионную кассету, содержащую трансген, и мутированный или модифицированный ITR AAV, причем указанная зкДНК-плазмида не содержит кодирующих последовательностей капсидного белка AAV. Согласно альтернативным вариантам реализации указанная зкДНК-плазмида кодирует в указанном порядке: первый (или 5') модифицированный или мутированный ITR AAV, экспрессионную кассету, содержащую трансген, и второй (или 3') ITR AAV дикого типа, причем указанная зкДНК-плазмида не содержит кодирующих последовательностей капсидного белка AAV, а 5'- и 3'-ITR являются асимметричными друг относительно друга. Согласно альтернативным вариантам реализации указанная зкДНК-плазмида кодирует в указанном порядке: первый (или 5') модифицированный или мутированный ITR AAV, экспрессионную кассету, содержащую трансген, и второй (или 3') мутированный или модифицированный ITR AAV, причем указанная зкДНК-плазмида не содержит кодирующих последовательностей капсидного белка AAV, а модифицированные 5'- и 3'-ITR отличаются и не содержат одинаковых модификаций.
[00258] Согласно дополнительному варианту реализации указанная зкДНК-плазмидная система не содержит кодирующих последовательностей вирусного капсидного белка (т.е. не содержит генов капсида AAV, а также генов капсидов других вирусов). Кроме того, согласно конкретному варианту реализации зкДНК-плазмида также лишена кодирующих последовательностей белка Rep AAV. Соответственно, согласно предпочтительному варианту реализации зкДНК-плазмида не содержит функциональных генов cap AAV и rep AAV, GG-3' для AAV2) помимо вариабельной палиндромной последовательности, обеспечивающей образование шпилек.
[00259] ЗкДНК-плазмида согласно настоящему изобретению может быть получена с применением естественных последовательностей нуклеотидов геномов любых серотипов AAV, хорошо известных в данной области техники. Согласно одному варианту реализации остов зкДНК-плазмиды происходит из генома AAV1, AAV2, AAV3, AAV4, AAV5, AAV5, AAV7, AAV8, AAV9, AAV10, AAV 11, AAV 12, AAVrh8, AAVrh10, AAV-DJ и AAV-DJ8. Например, NCBI: NC 002077; NC 001401; NC001729; NC001829; NC006152; NC 006260; NC 006261; из указателя вирусов Kotin and Smith («The Springer Index of Viruses»), доступного по ссылке, поддерживаемой Springer (веб-адрес: oesys.springer.de/viruses/database/mkchapter.asp?virID=42.04.) (примечание: при указании ссылки или базы данных подразумевается содержание доступного по ссылке ресурса или базы данных на действующую дату подачи настоящей заявки). Согласно конкретному варианту реализации остов зкДНК-плазмиды происходит из генома AAV2. Согласно другому конкретному варианту реализации остов зкДНК-плазмиды представляет собой синтетический остов, генетически сконструированный таким образом, чтобы включать на 5'- и 3'-концах ITR, происходящие из одного из указанных геномов AAV.
[00260] ЗкДНК-плазмида может необязательно включать селектируемый или селективный маркер для применения при получении продуцирующих зкДНК-вектор линии клеток. Согласно одному варианту реализации указанный селективный маркер может быть инсертирован ниже (т.е. в 3'-направлении) 3'-последовательности ITR. Согласно другому варианту реализации указанный селективный маркер может быть инсертирован выше (т.е. в 5'-направлении) 5'-последовательности ITR. Подходящие селективные маркеры включают, например, маркеры, придающие устойчивость к лекарственному средству. Селективные маркеры могут представлять собой, например, ген устойчивости к бластицидину S, канамицину, генетицину и т.п. Согласно предпочтительному варианту реализации указанный селективный лекарственный маркер представляет собой ген устойчивости к бластицидину S.
[00261] Пример зкДНК (например, rAAV0) продуцируют с rAAV-плазмиды. Способ получения rAAV-вектора может включать: (а) доставку в клетку-хозяина rAAV-плазмиды согласно описанию выше, причем и клетка-хозяин, и плазмида лишены кодирующих капсидный белок генов, (b) культивирование указанной клетки-хозяина в условиях, позволяющих получение зкДНК-генома; и (с) извлечение клеток и выделение генома AAV, полученного из указанных клеток.
С. Примеры способа получения зкДНК-векторов из зкДНК-плазмид
[00262] В настоящем документе также предложены способы получения бескапсидных зкДНК-векторов, а именно, способ, обеспечивающий достаточно высокий выход для обеспечения достаточного количества вектора для экспериментов in vivo.
[00263] Согласно некоторым вариантам реализации способ получения зкДНК-вектора включает этапы: (1) введения конструкции нуклеиновой кислоты, содержащей экспрессионную кассету и две асимметричных последовательности ITR в клетку-хозяина (например, клетки Sf9), (2) необязательно, получение клональной линии клеток, например, с применением селективного маркера, присутствующего на плазмиде, (3) введения кодирующего Rep гена (путем либо трансфекции, либо инфекции бакуловирусом, несущим указанный ген) в указанную клетку насекомого; и (4) извлечение указанной клетки и очищение зкДНК-вектора. Конструкция нуклеиновой кислоты, содержащей экспрессионную кассету и две последовательности ITR, описанные выше, для получения бескапсидного AAV-вектора, может быть представлена cfAAV-плазмидой, или бакмидой, или бакуловирусом, полученным с cfAAV-плазмидой согласно приведенному ниже описанию. Указанная конструкция нуклеиновой кислоты может быть введена в клетку-хозяина путем трансфекции, вирусной трансдукции, стабильной интеграции или других способов, известных в данной области техники.
D. Линии клеток:
[00264] Линии клеток-хозяев, используемые для получения зкДНК-вектора, могут включать линии клеток насекомых, происходящие из Spodoptera frugiperda, например, Sf9 Sf21, или клетки Trichoplusia ni или других беспозвоночных, позвоночного животного, или другие линии эукариотических клеток, в том числе клеток млекопитающих. Могут также применяться другие линии клеток, известные специалисту в данной области техники, такие как HEK293, Huh-7, HeLa, HepG2, Hep1A, 911, CHO, COS, MeWo, NIH3T3, A549, HT1 180, моноциты; и зрелые и незрелые дендритные клетки. Линии клеток-хозяев могут быть трансфицированы для стабильной экспрессии ceDBA-плазмиды для высокопродуктивного получения зкДНК-вектора.
[00265] зкДНК-плазмиды могут быть введены в клетки Sf9 путем транзиентной трансфекции с применением реагентов (например, липосомального, фосфата кальция) или физических способов (например, электропорации), известных в данной области техники. Как вариант, могут быть получены стабильные линии клеток Sf9, которые стабильно интегрировали зкДНК-плазмиду в геном. Такие стабильные линии клеток могут быть получены путем включения селективного маркера в зкДНК-плазмиду согласно описанию выше. Если зкДНК-плазмида, используемая для трансфекции линии клеток, включает селективный маркер, например, по антибиотику, клетки, которые были трансфицированы указанной зкДНК-плазмидой и интегрировали зкДНК-плазмиду ДНК в геном, могут быть отобраны путем добавления указанного антибиотика в клеточные ростовые среды. Затем устойчивые клоны указанных клеток могут быть выделены методом разведений с получением отдельных клеток или методик переноса колоний, и размножены.
E. Выделение и очищение зкДНК-векторов:
[00266] Примеры способа получения и выделения зкДНК-векторов описаны на фиг. 4А-4Е и в конкретных примерах ниже. ЗкДНК-векторы согласно описанию в настоящем документе могут быть получены из клетки-продуцента, экспрессирующей белок или белки Rep AAV, дополнительно трансформированных зкДНК-плазмидой, зкДНК-бакмидой или зкДНК-бакуловирусом. Плазмиды, подходящие для получения зкДНК-векторов, включают плазмиды, показанные на фиг. 8А (подходящие для получения Rep BIIC), фиг. 8В (плазмида, используемая для получения зкДНК-вектора).
[00267] Согласно одному аспекту полинуклеотид кодирует белок Rep AAV (Rep 78 или 68), доставляемый в клетку-продуцент в плазмиде (Rep-плазмида), бакмиде (Rep-бакмида) или бакуловирусе (Rep-бакуловирус). Rep-плазмида, Rep-бакмида и Rep-бакуловирус могут быть получены с применением способов, описанных выше.
[00268] Способы получения зкДНК-вектора, который представляет собой пример зкДНК-вектора, описаны в настоящем документе. Экспрессионная конструкция, используемая для получения зкДНК-вектора согласно настоящему изобретению, может представлять собой плазмиду (например, зкДНК-плазмиды), бакмиду (например, зкДНК-бакмиду) и/или бакуловирус (например, зкДНК-бакуловирус). Исключительно в качестве примера, зкДНК-вектор может быть получен из клеток, коинфицированных зкДНК-бакуловирусом и Rep-бакуловирусом. Белки Rep, продуцированные с Rep-бакуловируса, могут реплицировать зкДНК-бакуловирус с получением зкДНК-векторов. Как вариант, зкДНК-векторы могут быть получены из клеток, стабильно трансфицированных конструкцией, содержащей последовательность, кодирующую белок Rep AAV (Rep78/52), доставляемый в Rep-плазмидах, Rep-бакмидах или Rep-бакуловирусе. ЗкДНК-бакуловирусом могут быть транзиентно трансфицированы клетки, он может реплицироваться белком Rep и продуцировать зкДНК-векторы.
[00269] Бакмидой (например, зкДНК-бакмидой) могут быть трансфицированы в пермиссивные клетки насекомых, такие как Sf9, Sf21, Tni (Trichoplusia ni), High Five, и она может генерировать зкДНК-бакуловирус, который представляет собой рекомбинантный бакуловирус, включающий последовательности, содержащие асимметричный ITR и экспрессионную кассету. ЗкДНК-бакуловирусом могут быть снова инфицированы клетки насекомых для получения нового поколения рекомбинантного бакуловируса. Необязательно, указанный этап может быть повторен один раз или несколько раз для получения большего количества рекомбинантного бакуловируса.
[00270] Время извлечения и сбора зкДНК-векторов, описанных в настоящем документе, из клеток может быть выбрано и оптимизировано так, чтобы обеспечить высокопродуктивное получение указанных зкДНК-векторов. Например, время извлечения может быть выбрано с учетом жизнеспособности клеток, морфологии клеток, роста клеток и т.п. Как правило, клетки могут быть извлечены по истечении времени после инфицирования бакуловирусом, достаточного для получения зкДНК-векторов (например, зкДНК-векторы), но до того, как большинство клеток начинает погибать из-за токсичности вируса. ЗкДНК-векторы могут быть выделены из клеток Sf9 с применением наборов для очищения плазмид, таких как наборы от Qiagen ENDO-FREE PLASMID®. Другие способы, разработанные для выделения плазмид, могут также быть адаптированы для зкДНК-векторов. Как правило, могут быть использованы любые известные в данной области техники способы очищения нуклеиновых кислот, а также коммерчески доступные наборы для экстракции ДНК.
[00271] Как вариант, очищение может быть реализовано с использованием процесса щелочного лизиса клеточного осадка, центрифугирования итогового лизата и проведения хроматографического разделения. В одном неограничивающем примере указанный процесс может быть осуществлен путем загрузки супернатанта на ионообменную колонку (например, SARTOBIND Q®), которая сохраняет нуклеиновые кислоты, с последующей элюцией (например, 1,2 М раствором NaCl), и проведения дополнительного хроматографического очищения на гель-фильтрационной колонке (например, 6 Fast Flow GE). Затем бескапсидный AAV-вектор выделяют, например, путем осаждения.
[00272] Согласно некоторым вариантам реализации зкДНК-векторы могут также быть очищены в форме экзосом или микрочастиц. В данной области техники известно, что многие типы клеток высвобождают не только растворимые белки, но и комплексные грузы с белками/нуклеиновыми кислотами путем шеддинга мембранных микровезикул (Cocucci et al, 2009; ЕР 10306226.1) Такие везикулы включают микровезикулы (также называемые микрочастицами) и экзосомы (также называемые нановезикулами); и те, и те содержат белки и РНК в качестве грузов. Микровезикулы образуются путем непосредственного отпочковывания от плазматической мембраны, а экзосомы высвобождаются во внеклеточную среду после слияния мультивезикулярных эндосом с плазматической мембраной. Соответственно, содержащие зкДНК-вектор микровезикулы и/или экзосомы могут быть выделены из клеток, которые были трансдуцированы зкДНК-плазмидой, или бакмидой, или бакуловирусом, продуцированными зкДНК-плазмидой.
[00273] Микровезикулы могут быть выделены путем фильтрации или ультрацентрифугирования культуральной среды при 20000×g, а экзосомы при 100000×g. Оптимальная продолжительность ультрацентрифугирования может быть экспериментально определена и зависит от конкретного типа клеток, из которого выделяют везикулы. Предпочтительно, сначала культуральную среду очищают путем низкоскоростного центрифугирования (например, при 2000×g на протяжении 5-20 минут) и подвергают центрифужной концентрации с использованием, например, центрифужной колонки AMICON® (Millipore, Уотфорд, Великобритания). Микровезикулы и экзосомы могут быть дополнительно очищены посредством FACS или MACS с применением специфических антител, которые распознают специфические поверхностные антигены, присутствующие на микровезикулах и экзосомах. Другие способы очищения микровезикул и экзосом включают, не ограничиваясь перечисленными, иммунопреципитацию, аффинную хроматографию, фильтрацию и магнитные гранулы, покрытые специфическими антителами или аптамерами. После очищения везикулы промывают, например, забуференным фосфатом солевым раствором. Одно из преимуществ применения микровезикул или экзосомы для доставки зкДНК-содержащих везикул заключается в том, что указанные везикулы могут быть нацелены на различные типы клеток путем включения в их мембраны белков, распознаваемых специфическими рецепторами на соответствующих типах клеток, (см. также ЕР 10306226)
[00274] Другой аспект описанного в настоящем документе изобретения относится к способам очищения зкДНК-векторов из линий клеток-хозяев, стабильно интегрировавших зкДНК-конструкцию в собственный геном. Согласно одному варианту реализации зкДНК-векторы очищают в виде молекул ДНК. Согласно другому варианту реализации зкДНК-векторы очищают в виде экзосом или микрочастиц.
[00275] На фиг. 5 показан гель, подтверждающий получение зкДНК с нескольких зкДНК-плазмида конструкций с применением способа, описанного в примерах. Наличие зкДНК подтверждает характеристический паттерн полос на геле, согласно описанию для фиг. 4D в примерах. Другие характеристики процесса получения зкДНК и промежуточные продукты обобщены на фиг. 6А и 6В, и на фиг. 7А и 7В, согласно описанию в примерах.
VII. Фармацевтические композиции
[00276] Согласно другому аспекту предложены фармацевтические композиции. Указанная фармацевтическая композиция содержит зкДНК-вектор согласно описанию в настоящем документе и фармацевтически приемлемый носитель или разбавитель.
[00277] ДНК-векторы согласно описанию в настоящем документе могут быть включены в фармацевтические композиции, подходящие для введения субъекту, для доставки in vivo в клетки, ткани или органы указанного субъекта. Как правило, указанная фармацевтическая композиция содержит зкДНК-вектор согласно описанию в настоящем документе и фармацевтически приемлемый носитель. Например, зкДНК-векторы, описанные в настоящем документе, могут быть включены в фармацевтическую композицию, подходящую для требуемого маршрута терапевтического введения (например, парентерального введения). Также предусмотрены пассивная трансдукция тканей посредством внутривенной или внутриартериальной инфузии под высоким давлением, а также внутриклеточное инъецирование, например, внутриядерная микроинъекция или внутрицитоплазматическая инъекция. Фармацевтические композиции для терапевтического применения могут быть введены в состав раствора, микроэмульсии, дисперсии, липосом или другой упорядоченной структуры, подходящей для зкДНК-вектора в высокой концентрации. Стерильные инъецируемые растворы могут быть получены путем включения зкДНК-векторного соединения в требуемом количестве в подходящий буфер вместе с одним ингредиентом или комбинацией ингредиентов, перечисленных выше, по мере необходимости, с последующей стерилизацией фильтрацией.
[00278] Фармацевтически активные композиции, содержащие зкДНК-вектор, могут быть введены в состав для доставки трансгена в нуклеиновой кислоте в клетки реципиента, что приводит к терапевтической экспрессии в них указанного трансгена. Указанная композиция может также включать фармацевтически приемлемый носитель.
[00279] ЗкДНК-вектор согласно описанию в настоящем документе может быть включен в фармацевтическую композицию, подходящую для местного, системного, внутриамниотического, интратекального, интракраниального, внутриартериального, внутривенного, внутрилимфатического, внутрибрюшинного, подкожного, трахеального, внутритканевого (например, внутримышечного, внутрисердечного, внутрипеченочного, внутрипочечного, интрацеребрального), интратекального, интравезикального, коньюнктивального (например, экстраорбитального, интраорбитального, ретроорбитального, интраретинального, субретинального, хориоидального, субхориоидального, интрастромального, интракамерального и интравитреального), интракохлеарного и мукозального (например, орального, ректального, назального) введения. Также предусмотрены пассивная трансдукция тканей посредством внутривенной или внутриартериальной инфузии под высоким давлением, а также внутриклеточное инъецирование, например, внутриядерная микроинъекция или внутрицитоплазматическая инъекция.
[00280] Фармацевтические композиции в терапевтических целях, как правило, должны быть стерильными и стабильными в условиях получения и хранения. Указанная композиция может быть введена в состав раствора, микроэмульсии, дисперсии, липосом или другой упорядоченной структуры, подходящей для зкДНК-вектора в высокой концентрации. Стерильные инъецируемые растворы могут быть получены путем включения зкДНК-векторного соединения в требуемом количестве в подходящий буфер вместе с одним ингредиентом или комбинацией ингредиентов, перечисленных выше, по мере необходимости, с последующей стерилизацией фильтрацией
[00281] В данной области техники известны различные методики и способы доставки нуклеиновых кислот в клетки. Например, нуклеиновые кислоты, такие как зкДНК, могут быть введены в состав липидных наночастиц (ЛНЧ), липидоидов, липосом, липидных наночастиц, липоплексов или наночастиц типа ядро/оболочка. Как правило, ЛНЧ состоят из молекул нуклеиновой кислоты (например, зкДНК), одного или более ионизируемых или катионных липидов (или их солей), одного или более неионогенных или нейтральных липидов (например, фосфолипида), молекулы, которая предотвращает агрегацию (например, ПЭГ или конъюгата ПЭГ-липид), и, необязательно, стерола (например, холестерина).
[00282] Другой способ доставки нуклеиновых кислот, таких как зкДНК, в клетку состоит в конъюгации нуклеиновой кислоты с лигандом, который интернализует клетка. Например, лиганд может связывать рецептор на поверхности клетки и интернализоваться посредством эндоцитоза. Указанный лиганд может быть ковалентно связан с нуклеотидом в нуклеиновой кислоте. Примеры конъюгатов для доставки нуклеиновых кислот в клетку описаны, например, в WO 2015/006740, WO 2014/025805, WO 2012/037254, WO 2009/082606, WO 2009/073809, WO 2009/018332, WO 2006/112872, WO 2004/090108, WO 2004/091515 и WO 2017/177326.
[00283] Нуклеиновые кислоты, такие как зкДНК, могут также быть доставлены в клетку путем трансфекции. Подходящие способы трансфекции включают, не ограничиваясь перечисленными, опосредованную липидами трансфекцию, опосредованную катионными полимерами трансфекцию или осаждение фосфатом кальция. Реагенты для трансфекции хорошо известны в данной области техники и включают, не ограничиваясь перечисленными, реагент для трансфекции TurboFect (Thermo Fisher Scientific), реагент Pro-Ject (Thermo Fisher Scientific), белковый реагент для трансфекции TRANSPASS™ Р (New England Biolabs), белковый реагент для доставки CHARIOT™ (Active Motif), белковый реагент для трансфекции PROTEOJUICE™ (EMD Millipore), 293-фектин, липофектамин (LIPOFECTAMINE™ 2000), LIPOFECTAMINE™ 3000 (Thermo Fisher Scientific), LIPOFECTAMTNE™ (Thermo Fisher Scientific), липофектин (LIPOFECTIN™, Thermo Fisher Scientific), DMPJE-C, CELLFECTIN™ (Thermo Fisher Scientific), OLIGOFECTAMINE™ (Thermo Fisher Scientific), LIPOFECTACE™, FUGENE™ (Roche, Базель, Швейцария), FUGENE™ HD (Roche), TRANSFECTAM™ (трансфектам, Promega, Мэдисон, Висконсин), TFX-10™ (Promega), TFX-20™ (Promega), TFX-50™ (Promega), трансфектин (TRANSFECTIN™, BioRad, Геркулес, Калифорния), SILENTFECT™ (Bio-Rad), Effectene™ (Qiagen, Валенсия, Калифорния), DC-chol (Avanti Polar Lipids), GENEPORTER™ (Gene Therapy Systems, Сан-Диего, Калифорния), DHARMAFECT 1™ (Dharmacon, Лафайет, Колорадо), DHARMAFECT 2™ (Dharmacon), DHARMAFECT 3™ (Dharmacon), DHARMAFECT 4™ (Dharmacon), ESCORT™ III (Sigma, Сент-Луис, Миссури), и ESCORT™ IV (Sigma Chemical Co.). Нуклеиновые кислоты, такие как зкДНК, могут также быть доставлены в клетку с применением методов микрофлюидики, известных специалистам в данной области техники.
[00284] Способы невирусной доставки нуклеиновых кислот in vivo или ex vivo включают электроперацию, липофекцию (см. патент США №5049386; 4946787; и коммерчески доступные реагенты, такие как трансфектам (Transfectam™) и липофектин (Lipofectin™)), микроинъекция, биолистика, виросомы, липосомы (см., например, Crystal, Science 270: 404-410 (1995); Blaese et al., Cancer Gene Ther. 2: 291-297 (1995); Behr et al., Bioconjugate Chem. 5: 382-389 (1994); Remy et al., Bioconjugate Chem. 5: 647-654 (1994); Gao et al., Gene Therapy 2: 710-722 (1995); Ahmad et al., Cancer Res. 52: 4817-4820 (1992); патенты США №4186183, №4217344, №4235871, №4261975, №4485054, №4501728, №4774085, №4837028 и №4946787), иммунолипосомы, конъюгаты нуклеиновых кислот с поликатионами или липидами, депротеинизированную ДНК и усиленное агентами поглощение ДНК. Сонопорация с применением, например, системы Sonitron 2000 (Rich-Mar), может также применяться для доставки нуклеиновых кислот.
[00285] зкДНК-векторы согласно описанию в настоящем документе могут также быть введены непосредственно в организм для трансдукции клеток in vivo. Введение осуществляют любым из маршрутов, обычно используемых для приведения молекулы в максимально тесный контакт с клетками крови или тканей в том числе, но не ограничиваясь перечисленными, путем инъекции, инфузии, местного нанесения и электроперации. Подходящие способы введения таких нуклеиновых кислот доступны и хорошо известны специалистам в данной области техники, и, хотя для введения конкретной композиции может быть использовано более одного маршрута, конкретный маршрут часто может обеспечить более быструю и более эффективную реакцию, чем другой маршрут.
[00286] Способы введения нуклеиновой кислоты вектор зкДНК-вектор согласно описанию в настоящем документе могут обеспечивать доставку, например, в гематопоэтические стволовые клетки, например, способы согласно описанию в патенте США №5928638.
[00287] ЗкДНК-векторы в соответствии с настоящим изобретением могут быть добавлены в липосомы для доставки в клетку или целевой орган субъекта. Липосомы представляют собой везикулы, имеющие по меньшей мере один липидный бислой. Липосомы обычно используют в качестве носителей для доставки лекарственных/терапевтически средств в контексте фармацевтических разработок. Они работают за счет слияния с клеточной мембраной и перегруппировки ее липидной структуры для доставки лекарственного средства или активного фармацевтического ингредиента (АФИ). Липосомные композиции для такой доставки состоят из фосфолипидов, в частности, соединений, содержащих фосфатидилхолиновую группу, однако указанные композиции могут также включать другие липиды.
[00288] Согласно некоторым аспектам настоящего изобретения предложен липосомный состав, который включает одно или более соединений с функциональной группой полиэтиленгликоля (ПЭГ) (так называемые «пегилированные соединения»), которая может уменьшать иммуногенность/ антигенность, обеспечивать гидрофильность и гидрофобность указанного соединения или соединений, и частоту дозирования. Как вариант, указанный липосомный состав просто включает полимер полиэтиленгликоля (ПЭГ) в качестве дополнительного компонента. Согласно таким аспектам молекулярная масса ПЭГ или функциональной группы ПЭГ может составлять от 62 Да до приблизительно 5000 Да.
[00289] Согласно некоторым аспектам настоящего изобретения предложен липосомный состав, который доставляет АФИ с профилем продленного высвобождения или контролируемого высвобождения на протяжении периода продолжительностью от часов до недель. Согласно некоторым родственным аспектам указанный липосомный состав может содержать водные камеры, связанные липидными бислоями. Согласно другим родственным аспектам указанный липосомный состав инкапсулирует АФИ с компонентами, которые претерпевают физический переход при повышенной температуре, высвобождающий указанный АФИ на протяжении периода продолжительностью от часов до недель.
[00290] Согласно некоторым аспектам указанный липосомный состав содержит сфингомиелин и один или более липидов согласно описанию в настоящем документе. Согласно некоторым аспектам указанный липосомный состав содержит оптисомы.
[00291] Согласно некоторым аспектам настоящего изобретения предложен липосомный состав, который включает один или более липидов, выбранных из: натриевой соли N-(карбонил-метоксиполиэтиленгликоль 2000)-1,2-дистеароил-sn-глицеро-3-фосфоэтаноламина, (дистеароил-sn-глицеро-фосфоэтаноламина), MPEG (метоксиполиэтиленгликоль)-конъюгированного липида, HSPC (гидрогенизированного соевого фосфатидилхолина); ПЭГ (полиэтиленгликоля); DSPE (дистеароил-sn-глицеро-фосфоэтаноламина); DSPC (дистеароилфосфатидилхолина); DOPC (диолеилфосфатидилхолина); DPPG (дипальмитоилфосфатидилглицерина); ЕРС (яичного фосфатидилхолина); DOPS (диолеилфосфатидилсерина); РОРС (пальмитоилолеоилфосфатидилхолина); SM (сфингомиелина); MPEG (метоксиполиэтиленгликоля); DMPC (димиристоилфосфатидилхолина); DMPG (димиристоилфосфатидилглицерина); DSPG (дистеароилфосфатидилглицерина); DEPC (диерукоилфосфатидилхолина); DOPE (диолеоли-sn-глицерофосфоэтаноламина), холестерилсульфата (CS), дипальмитоилфосфатидилглицерина (DPPG), DOPC (диолеоли-sn-глицерофосфатидилхолина) или любой комбинацией перечисленного.
[00292] Согласно некоторым аспектам настоящего изобретения предложен липосомный состав, содержащий фосфолипид, холестерин и пегилированный липид в молярном соотношении 56:38:5. Согласно некоторым аспектам общее содержание липидов в указанном липосомном составе составляет 2-16 мг/мл. Согласно некоторым аспектам настоящего изобретения предложен липосомный состав, содержащий липид, включающий фосфатидилхолиновую функциональную группу, липид, включающий этаноламинную функциональную группу и пегилированный липид. Согласно некоторым аспектам настоящего изобретения предложен липосомный состав, содержащий липид, включающий фосфатидилхолиновую функциональную группу, липид, включающий этаноламинную функциональную группу и пегилированный липид в молярном соотношении 3:0,015:2, соответственно. Согласно некоторым аспектам настоящего изобретения предложен липосомный состав, содержащий липид, включающий фосфатидилхолиновую функциональную группу, холестерин и пегилированный липид. Согласно некоторым аспектам настоящего изобретения предложен липосомный состав, содержащий липид, включающий фосфатидилхолиновую функциональную группу и холестерин. Согласно некоторым аспектам указанный пегилированный липид представляет собой PEG-2000-DSPE. Согласно некоторым аспектам настоящего изобретения предложен липосомный состав, содержащий DPPG, соевый PC, липидный конъюгат MPEG-DSPE и холестерин.
[00293] Согласно некоторым аспектам настоящего изобретения предложен липосомный состав, содержащие один или более липидов, включающих фосфатидилхолиновую функциональную группу, и один или более липидов, включающих этаноламинную функциональную группу. Согласно некоторым аспектам настоящего изобретения предложен липосомный состав, содержащий что-либо одно или более из: липидов, включающих фосфатидилхолиновую функциональную группу, липидов, включающих этаноламинную функциональную группу, и стеролов, например, холестерина. Согласно некоторым аспектам указанный липосомный состав содержит DOPC/ DEPC; и DOPE.
[00294] Согласно некоторым аспектам настоящего изобретения предложен липосомный состав, дополнительно содержащий одно или более фармацевтических вспомогательных веществ, например, сахарозу и/или глицин.
[00295] Согласно некоторым аспектам настоящего изобретения предложен липосомный состав с однослойной или многослойной структурой. Согласно некоторым аспектам настоящего изобретения предложен липосомный состав, который содержит мультивезикулярные частицы и/или частицы на основе пены. Согласно некоторым аспектам настоящего изобретения предложен липосомный состав, относительный размер частиц которого больше обычных наночастиц и составляет приблизительно 150-250 нм. Согласно некоторым аспектам указанный липосомный состав представляет собой лиофилизированный порошок.
[00296] Согласно некоторым аспектам настоящего изобретения предложен липосомный состав, который получают и нагружают зкДНК-векторами, предложенными или описанными в настоящем документе, путем добавления слабого основания к смеси, содержащей выделенные зкДНК вне липосомы. Указанное добавление увеличивает значение рН вне липосом до приблизительно 7,3 и направляет АФИ в липосому. Согласно некоторым аспектам настоящего изобретения предложен липосомный состав с кислотным рН внутри липосомы. В таких случаях рН внутри липосомы может составлять 4-6,9, более предпочтительно, 6,5. Согласно другим аспектам настоящего изобретения предложен липосомный состав, полученный с применением технологии интралипосомальной стабилизации лекарственных средств. В таких случаях используют полимерные или неполимерные высокозаряженные анионы и интралипосомальные захватывающие агенты, например, полифосфат или октасульфат сахарозы.
[00297] Согласно другим аспектам настоящего изобретения предложен липосомный состав, содержащий фосфолипиды, лецитин, фосфатидилхолин и фосфатидилэтаноламин.
[00298] Реагенты для доставки, такие как липосомы, нанокапсулы, микрочастицы, микросферы, липидные частицы, везикулы и т.п., могут применяться для введения композиций согласно настоящему описанию в подходящие клетки-хозяева. В частности, указанные нуклеиновые кислоты могут быть введены в состав для доставки в инкапсулированном виде в липидной частице, липосоме, везикуле, наносфере, наночастице, частице золота, или т.п. Такие составы может быть предпочтительными для введения фармацевтически приемлемых составов нуклеиновых кислот согласно описанию в настоящем документе.
[00299] Различные способы доставки, известные в данной области техники, или их модификации могут применяться для доставки зкДНК-векторов in vitro или in vivo. Например, согласно некоторым вариантам реализации зкДНК-векторы доставляют путем транзиентного проникновения в клеточную мембрану с использованием механической, электрической, ультразвуковой, гидродинамической или лазерной энергии таким образом, чтобы облегчить вход ДНК в целевые клетки. Например, зкДНК-вектор может быть доставлен путем транзиентного нарушения клеточной мембраны путем проталкивания клетки через канал с ограниченным размером, или другими способами, известными в данной области техники. В некоторых случаях зкДНК-вектор по отдельности непосредственно инъецируют в виде депротеинизированной ДНК в кожу, вилочковую железу, сердечную мышцу, скелетные мышцы или клетки печени.
[00300] В некоторых случаях зкДНК-вектор доставляют с помощью генной пушки. Золотые или вольфрамовые сферические частицы (диаметром 1-3 мкм), покрытые бескапсидными AAV-векторами, могут быть разогнаны до высокой скорости газом под давлением для проникновения в клетки целевой ткани.
[00301] Согласно некоторым вариантам реализации для доставки зкДНК-векторов применяют электропорацию. Электропорация вызывает временную дестабилизацию мембран клеток целевой ткани в результате введения в ткань пары электродов, так что молекулы ДНК в среде, окружающей дестабилизированную мембрану, могут проникнуть в цитоплазму и нуклеоплазму клетки. Электропорацию использовали in vivo для многих типов тканей, таких как кожа, легкие и мышцы.
[00302] В некоторых случаях зкДНК-вектор доставляют путем гидродинамической инъекции, которая представляет собой простой и высокоэффективный способ прямой внутриклеточной доставки любых водорастворимых соединений и частиц в внутренние органы и скелетные мышцы всей конечности.
[00303] В некоторых случаях зкДНК-векторы доставляют с применением ультразвука, создавая наноскопические поры в мембране для облегчения внутриклеточной доставки частиц ДНК в клетки внутренних органов или опухолей, так что размер и концентрация плазмидной ДНК имеют огромное значение для эффективности системы. В некоторых случаях зкДНК-векторы доставляют путем магнитофекции с применением магнитных полей для концентрации частиц, содержащих нуклеиновую кислоту, в целевые клетки.
[00304] В некоторых случаях могут применяться химические системы доставки, например, с использованием наномерных комплексов, которые включают компактизацию отрицательно заряженной нуклеиновой кислоты поликатио иными наномерными частицами, принадлежащими к катионным липосомам/мицеллам или катионным полимерам. Катионные липиды, используемые в указанном способе доставки, включают, не ограничиваясь перечисленными, моновалентные катионные липиды, поливалентные катионные липиды, гуанидин-содержащие соединения, соединения - производные холестерина, катионные полимеры, (например, поли(этиленимин), поли-L-лизин, протамин, другие катионные полимеры), и липид-полимерные гибриды.
[00305] А. Экзосомы:
[00306] Согласно некоторым вариантам реализации зкДНК-вектор согласно описанию в настоящем документе доставляют путем упаковки в экзосому. Экзосомы представляют собой небольшие мембранные везикулы эндоцитозного происхождения, которые высвобождаются во внеклеточную среду после слияния мультивезикулярных телец с плазматической мембраны. Их поверхность состоит из липидного бислоя клеточной мембраны донорной клетки, они содержат цитозоль из клетки, которая продуцировала экзосому и экспонируют мембранные белки исходной клетки на поверхности. Экзосомы продуцируют различные типы клеток, в том числе эпителиальные клетки. В- и Т-лимфоциты, тучные клетки (МС), а также дендритные клетки (ДК). Некоторые варианты реализации предусматривают применение экзосом с диаметром от 10 нм до 1 мкм, от 20 нм до 500 нм, от 30 нм до 250 нм, от 50 нм до 100 нм. Экзосомы могут быть выделены для доставки в целевые клетки либо с использованием донорных клеток, либо путем введения в них специфических нуклеиновых кислот.Различные способы, известные в данной области техники, могут применяться для получения экзосом, содержащих бескапсидные AAV-векторы согласно настоящему изобретению.
[00307] В. Микрочастицы/Наночастицы:
[00308] Согласно некоторым вариантам реализации зкДНК-вектор согласно описанию в настоящем документе доставляют с помощью липидной наночастицы. Как правило, липидные наночастицы содержат ионизируемый аминолипид (например, гептатриаконта-6,9,28,31-тетраен-19-ил 4-(диметиламино)бутаноат, DLin-MC3-DMA, фосфатидилхолин (1,2-дистеароил-sn-глицеро-3-фосфохолин, DSPC), холестерин и липид для покрытия (полиэтиленгликоль-димиристолглицерин, ПЭГ-ДМГ), например, согласно описанию в источнике: Tam et al. (2013). Advances in Lipid Nanoparticles for siRNA delivery. Pharmaceuticals 5(3): 498-507.
[00309] Согласно некоторым вариантам реализации липидную наночастицу имеет средний диаметр от приблизительно 10 до приблизительно 1000 нм. Согласно некоторым вариантам реализации липидная наночастица имеет диаметр менее 300 нм. Согласно некоторым вариантам реализации липидная наночастица имеет диаметр от приблизительно 10 до приблизительно 300 нм. Согласно некоторым вариантам реализации липидная наночастица имеет диаметр менее 200 нм. Согласно некоторым вариантам реализации липидная наночастица имеет диаметр от приблизительно 25 до приблизительно 200 нм. Согласно некоторым вариантам реализации состав с липидными наночастицами (например, композиция, содержащая совокупность липидных наночастиц) имеет распределение частиц по размерам, где средний размер (например, диаметр) составляет от приблизительно 70 нм до приблизительно 200 нм, и чаще составляет приблизительно 100 нм или меньше.
[00310] Различные липидные наночастицы, известные в данной области техники, могут применяться для доставки зкДНК-вектора согласно описанию в настоящем документе. Например, различные способы доставки с применением липидных наночастиц описаны в патентах США №9404127, 9006417 и 9518272.
[00311] Со гласно некоторым вариантам реализации зкДНК-вектор согласно описанию в настоящем документе доставляют с применением золотых наночастиц. Как правило, нуклеиновая кислота может быть ковалентно связана с золотой наночастицей или нековалентно связана с золотой наночастицей (например, связана за счет взаимодействия зарядов), например, согласно описанию в источнике: Ding et al. (2014). Gold Nanoparticles for Nucleic Acid Delivery. Mol. Ther. 22(6); 1075-1083. Согласно некоторым вариантам реализации конъюгаты золотых наночастиц и нуклеиновой кислоты получают с применением способов, описанных, например, в патенте США №6812334.
[00312] С. Липосомы
[00313] Образование и применение липосом в целом известно специалистам в данной области техники. Были разработаны липосомы с повышенной стабильностью в сыворотке и увеличенным временем полужизни в кровотоке (патент США №5741516). Кроме того, были описаны различные способы с применением липосом и липосомо подобных составов в качестве потенциальны носителей лекарственных средств (патенты США №5567434; №5552157; №5565213; №5738868 и №5795587).
[00314] Липосомы успешно применяли для нескольких типов клеток, обычно устойчивых к трансфекции при использовании других процедур. Кроме того, липосомы лишены ограничений в отношении длины ДНК, типичных для систем доставки на основе вирусов. Липосомы эффективно применяли для введения генов, лекарственных средств, радиотерапевтических агентов, вирусов, транскрипционных факторов и аллостерических эффекторов в различных культивируемых линиях клеток и у животных. Кроме того, было завершено несколько успешных клинических испытаний, направленных на изучение эффективности опосредованной липосомами доставки лекарственных средств.
[00315] Липосомы образуются из фосфолипидов, диспергированных в водной среде, и спонтанно образующих многослойные везикулы из концентрических бислоев (также называемых многослойными везикулами (MLV). MLV обычно имеют диаметр от 25 нм до 4 мкм. Обработка MLV ультразвуком приводит к образованию небольших однослойных везикул (SUV) с диаметром в диапазоне от 200 до 500 Å, содержащих в сердцевине водный раствор.
[00316] Согласно некоторым вариантам реализации липосома содержит катионные липиды. Термин «катионный липид» включает липиды и синтетические липиды, содержащие и полярные, и неполярные домены, которые способны приобретать положительный заряд при значениях рН, соответствующих или примерно соответствующих физиологическим, связываются с полианионами, такими как нуклеиновые кислоты, и облегчают доставку нуклеиновых кислот в клетки. Согласно некоторым вариантам реализации катионные липиды включают насыщенные и ненасыщенные алкильные и алициклические простые и сложные эфиры аминов, амидов, или их производные. Согласно некоторым вариантам реализации катионные липиды включают прямоцепочечные, разветвленные алкильные, алкенильные группы или любую комбинацию вышеперечисленного. Согласно некоторым вариантам реализации катионные липиды содержат от 1 до приблизительно 25 атомов углерода (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25 атомов углерода. Согласно некоторым вариантам реализации катионные липиды содержат более 25 атомов углерода. Согласно некоторым вариантам реализации прямоцепочечные или разветвленные алкильные или алкеновые группы содержат шесть или более атомов углерода. Катионный липид может также содержать, согласно некоторым вариантам реализации, одну или более алициклических групп. Неограничивающие примеры алициклических групп включают холестерин и другие стероидные группы. Согласно некоторым вариантам реализации катионные липиды получают с одним или более противоионами. Примеры противоионов (анионов) включают, не ограничиваясь перечисленными, Cl-, Br-, I-, F-, ацетат, трифторацетат, сульфат, нитрит и нитрат.
[00317] Неограничивающие примеры катионных липидов включают полиэтиленимин, полиамидоаминные (РАМАМ) сверхразветвленные дендримеры Starburst, липофектин (комбинация DOTMA и DOPE), липофектазу, Липофектамин™ (например, LIPOFECTAMINE™ 2000), DOPE, цитофектин (Gilead Sciences, Фостер Сити, Калифорния) и эуфектины (JBL, Сан-Луис-Обиспо, Калифорния). Примеры катионных липосом могут быть получены из N-[1-(2,3-диолеолокси)-пропил]-N,N,N-триметилхлорида аммония (DOTMA), N-[1-(2,3-диолеолокси)-пропил]-N,N,N-триметиламмония метилсульфата (DOTAP), 3β-[N-(N',N'-диметиламиноэтан)карбамоил]холестерина (DC-Chol), 2,3,-диолеилокси-N-[2(сперминкарбоксамидо)этил]-N,N-диметил-1-пропанаминия трифторацетата (DOSPA), 1,2-димиристилоксипропил-3-диметилгидроксиэтиламмония бромида; и диметилдиоктадециламмония бромида (DDAB). Нуклеиновые кислоты (например, CELiD) могут также быть введены в комплекс, например, с поли(L-лизином), или в указанную смесь могут быть включены или не включены авидин и липиды, например, стерил-поли(L-лизин).
[00318] Согласно некоторым вариантам реализации зкДНК-вектор согласно описанию в настоящем документе доставляют с применением катионного липида, описанного в патенте США №8158601, или полиаминного соединения или липида согласно описанию в патенте США №8034376.
[00319] D. Конъюгаты
[00320] Согласно некоторым вариантам реализации зкДНК-вектор согласно описанию в настоящем документе конъюгирован (например, ковалентно связан) с агентом, который увеличивает поглощение клетками. «Агент, который увеличивает поглощение клетками» представляет собой молекулу, облегчающую транспорт нуклеиновой кислоты через липидную мембрану. Например, нуклеиновая кислота может быть конъюгирована с липофильным соединением (например, холестерином, токоферолом и т.п.), проникающим в клетки пептидом (СРР) (например, пенетратином, TAT, Syn1B и т.п.) и полиаминами (например, спермином). Дополнительные примеры агентов, которые увеличивают поглощение клетками, раскрыты, например, в источнике: Winkler (2013). Oligonucleotide conjugates for therapeutic applications. Ther. Deliv. 4(7); 791-809.
[00321] Согласно некоторым вариантам реализации зкДНК-вектор согласно описанию в настоящем документе конъюгирован с полимером (например, полимерной молекулой) или молекулой фолата (например, молекулой фолиевой кислоты). В целом, в данной области техники известна доставка нуклеиновых кислот, конъюгированных с полимерами, например, согласно описанию в W02000/34343 и W0200 8/0223 09. Согласно некоторым вариантам реализации зкДНК-вектор согласно описанию в настоящем документе конъюгирован с поли(амидным) полимером, например, согласно описанию в патенте США №8987377. Согласно некоторым вариантам реализации нуклеиновая кислота, описанная в настоящем документе, конъюгирована с молекулой фолиевой кислоты согласно описанию в патенте США №8507455.
[00322] Согласно некоторым вариантам реализации зкДНК-вектор согласно описанию в настоящем документе конъюгирован с углеводом, например, согласно описанию в патенте США №8450467.
[00323] Е. Нанокапсула
[00324] Как вариант, могут применяться нанокапсульные составы с зкДНК-вектором согласно описанию в настоящем документе. В общем случае, вещества могут быть заключены в нанокапсулы стабильным и воспроизводимым образом. Чтобы избежать побочных эффектов, обусловленных избыточной внутриклеточной нагрузкой полимерами, такие сверхмелкие частицы (размером около 0,1 мкм) необходимо разрабатывать с использованием полимеров, способных разлагаться in vivo. Предусмотрены для применения биоразлагаемые полиалкилцианоакрилатные наночастицы, отвечающие указанным требованиям.
VIII. Способы доставки зкДНК-векторов
[00325] Согласно некоторым вариантам реализации зкДНК-вектор может быть доставлен в целевую клетку in vitro или in vivo различными подходящими способами. ЗкДНК-векторы могут быть нанесены или инъецированы по отдельности. ЗкДНК-векторы могут быть доставлены в клетку без помощи реагента для трансфекции или другого физического способа. Как вариант, зкДНК-векторы могут быть доставлены с применением любого известного в данной области техники реагента для трансфекции или другого известного в данной области техники физического способа, который облегчает вход ДНК в клетку, например, липосом, спиртов, богатых полилизином соединений, богатых аргинином соединений, фосфата кальция, микровезикул, микроинъекции, электропорации и т.п.
[00326] В то же время, трансдукция бескапсидными AAV-векторами согласно описанию в настоящем документе может обеспечивать эффективное нацеливание на типы клеток и тканей, которые трудно трансдуцировать стандартными AAV вирионами с применением различных реагентов для доставки.
[00327] Согласно другому варианту реализации зкДНК-вектор вводят в ЦНС (например, в головной мозг или в глаз). Указанный зкДНК-вектор может быть введен в спинной мозг, ствол мозга (продолговатый мозг, варолиев мост), средний мозг (гипоталамус, таламус, эпиталамус, питуитарную железу, черную субстанцию, шишковидную железу), мозжечок, конечный мозг (полосатое тело, большой мозг, в том числе затылочные, височные, теменные и лобные доли, кору головного мозга, базальные ганглии, гиппокамп и миндалевидное тело), лимбическую систему, неокортекс, полосатое тело, большой мозг и нижний холмик четверохолмия. Указанный зкДНК-вектор может также быть введен в разные области глаза, такие как сетчатка, роговица и/или зрительный нерв. Указанный зкДНК-вектор может быть доставлен в спинномозговую жидкость (например, посредством люмбарной пункции). Указанный зкДНК-вектор может также быть интраваскулярно введен в ЦНС в ситуациях, когда гематоэнцефалический барьер был нарушен (например, при опухоли головного мозга или церебральном инфаркте).
[00328] Согласно некоторым вариантам реализации указанный зкДНК-вектор может быть введен в требуемую область или области ЦНС любым известным в данной области техники маршрутом, в том числе, но не ограничиваясь перечисленным, путем интратекальной, внутриглазной, интрацеребральной, интравентрикулярной, внутривенной (например, в присутствии сахара, такого как маннит), интраназальной, внутриушной, внутриглазной (например, интравитреально, субретинально, в переднюю камеру) и периокулярной (например, в субтеноново пространство) доставки, а также внутримышечной доставки с ретроградной доставкой в моторные нейроны.
[00329] Согласно некоторым вариантам реализации указанный зкДНК-вектор вводят в виде жидкого состава путем прямой инъекции (например, стереотаксической инъекции) в требуемый область или компартмент в ЦНС. Согласно другим вариантам реализации указанный зкДНК-вектор может быть введен путем местного нанесения на требуемую область, или путем интраназального введения аэрозольного состава. Введение в глаз может быть осуществлено путем местного нанесения жидких капель. В дополнительном альтернативном варианте зкДНК-вектор может быть введен в виде твердого состава для медленного высвобождения (см., например, патент США №7201898). Согласно другим дополнительным вариантам реализации указанный зкДНК-вектор может быть использован для ретроградного транспорта для лечения, облегчения и/или предотвращения заболеваний и нарушений, в которые вовлечены моторные нейроны (например, амиотрофического бокового склероза (ALS); спинальной мышечной атрофии (SMA) и т.п.). Например, указанный зкДНК-вектор может быть доставлен в мышечную ткань, из которой он может мигрировать в нейроны.
VIII. Дополнительные варианты применения зкДНК-векторов
[00330] Композиции и зкДНК-векторы, предложенные согласно настоящему изобретению, могут применяться для доставки трансген в различных целях. Согласно некоторым вариантам реализации указанный трансген кодирует белок или функциональную РНК, предназначенные для применения в целях научных исследований, например, для создания соматической трансгенной модели на животных, несущих указанный трансген, например, для изучения функции продукта указанного трансгена. Согласно другому примеру указанный трансген кодирует белок или функциональную РНК, предназначенные для применения при создании модели заболевания на животных. Согласно некоторым вариантам реализации указанный трансген кодирует один или более пептидов, полипептидов или белков, которые подходят для лечения, предотвращения или облегчения болезненных состояний или нарушений у субъекта-млекопитающего. Указанный трансген может быть перенесен субъекту (например, экспрессироваться у субъекта) в достаточном количестве для лечения заболевания, ассоциированного с пониженной экспрессией, отсутствием экспрессии или дисфункцией гена. Согласно некоторым вариантам реализации указанный трансген может быть перенесен субъекту (например, экспрессироваться у субъекта) в достаточном количестве для лечения заболевания, ассоциированного с повышенной экспрессией, активностью генного продукта, или неадекватной положительной регуляцией гена, которую указанный трансген подавляет или иным образом вызывает необходимое снижение экспрессии.
IX. Способы применения
[00331] ЗкДНК-вектор согласно настоящему изобретению может также применяться в способе доставки представляющей интерес последовательности нуклеотидов в целевую клетку. Указанный способ может, в частности, представлять собой способ доставки представляющего интерес терапевтического гена в клетку нуждающегося в этом субъекта. Настоящее изобретение позволяет обеспечить экспрессию in vivo полипептида, белка или олигонуклеотида, кодируемого терапевтической экзогенной последовательностью ДНК в клетках субъекта, таким образом, чтобы происходила экспрессия терапевтических уровней указанного полипептида, белка или олигонуклеотида. Указанные результаты наблюдаются режимов доставки зкДНК-вектора как in vivo, так и in vitro.
[00332] Способ доставки представляющей интерес нуклеиновой кислоты в клетку субъекта может включать введение указанному субъекту зкДНК-вектора согласно настоящему изобретению, содержащего указанную представляющую интерес нуклеиновую кислоту. Кроме того, согласно настоящему изобретению предложен способ доставки представляющей интерес нуклеиновой кислоты в клетку нуждающегося в этом субъекта, включающий несколько введений зкДНК-вектора согласно настоящему изобретению, содержащего представляющую интерес нуклеиновую кислоту. Поскольку зкДНК-вектор согласно настоящему изобретению не индуцирует иммунный ответ, такой стратегии нескольких введений не будет мешать ответ иммунной системы хозяина против зкДНК-вектора согласно настоящему изобретению, в отличие от того, что часто наблюдается при применении заключенных в капсиды векторов.
[00333] Нуклеиновую кислоту или кислоты зкДНК-вектора вводят в достаточных количествах для трансфекции клеток требуемой ткани и для обеспечения достаточных уровней переноса генов и экспрессии без излишних нежелательных явлений. Стандартные и фармацевтически приемлемые маршруты введения включают, не ограничиваясь перечисленными, внутривенную доставку (например, в липосомном составе), прямую доставку в выбранный орган (например, интрапортальную доставку в печень), внутримышечную доставку и другие парентеральные маршруты введения. Маршруты введения могут быть скомбинированы, если это требуется.
[00334] Доставка зкДНК-вектора не ограничена одним видом зкДНК-вектора. Соответственно, согласно другому аспекту несколько зкДНК-векторов, содержащих разные экзогенные последовательности ДНК, могут быть доставлены одновременно или последовательно в целевые клетку, ткань, орган, или в организм субъекта. Соответственно, указанная стратегия может позволять экспрессию нескольких генов. Доставка может также осуществляться неоднократно и, что важно для генной терапии в клинических условиях, с последующим повышением или понижением доз, учитывая отсутствие направленного против капсида иммунного ответа хозяина ввиду отсутствия вирусного капсида. Ожидается, что направленный против капсида ответ не будет возникать, поскольку капсид отсутствует.
[00335] Согласно настоящему изобретению также предложен способ лечения заболевания у субъекта, включающий введение в нуждающуюся в этом целевую клетку (в частности, мышечную клетку или ткань) субъекта терапевтически эффективного количества зкДНК-вектора, необязательно с фармацевтически приемлемым носителем. Хотя зкДНК-вектор может быть введен в присутствии носителя, такой носитель не является необходимым. Используемый зкДНК-вектор содержит представляющую интерес нуклеотидную последовательность, подходящую для лечения заболевания. В частности, указанный зкДНК-вектор может содержать требуемую экзогенную последовательность ДНК, функционально связанную с контрольными элементами, способными направлять транскрипцию требуемого полипептида, белка или олигонуклеотида, кодируемого указанной экзогенной последовательностью ДНК, при введении субъекту. Указанный зкДНК-вектор может быть введен любым подходящим маршрутом согласно описанию выше и в любых разделах настоящего документа.
X. Способы лечения
[00336] Описанная в настоящем документе технология также демонстрирует способы получения, а также способы применения предложенных зкДНК-векторов различным образом, включая, например, вариантов применения, методик, диагностических процедур и/или режимов генной терапии ex situ, in vitro и in vivo.
[00337] Согласно настоящему изобретению предложен способ лечения заболевания или нарушения у субъекта, включающий введение в нуждающуюся в этом целевую клетку (например, мышечную клетку или ткань, или другой пораженный тип клеток) субъекта терапевтически эффективного количества зкДНК-вектора, необязательно с фармацевтически приемлемым носителем. Хотя указанный зкДНК-вектор может быть введен в присутствии носителя, такой носитель не является необходимым. Используемый зкДНК-вектор содержит представляющую интерес нуклеотидную последовательность, подходящую для лечения заболевания. В частности, указанный зкДНК-вектор может содержать требуемую экзогенную последовательность ДНК, функционально связанную с контрольными элементами, способными направлять транскрипцию требуемого полипептида, белка или олигонуклеотида, кодируемого указанной экзогенной последовательностью ДНК, при введении субъекту. Указанный зкДНК-вектор может быть введен любым подходящим маршрутом согласно описанию выше и в любых разделах настоящего документа.
[00338] Любой трансген может быть доставлен с применением зкДНК-векторов согласно описанию в настоящем документе. Представляющие интерес трансгены включают нуклеиновые кислоты, кодирующие полипептиды, или некодирующие нуклеиновые кислоты (например, РНК-интерференция, миРНК и т.п.), предпочтительно терапевтические (например, для медицинского, диагностического или ветеринарного применения) или иммуногенные (например, для вакцин) полипептиды.
[00339] Согласно некоторым вариантам реализации трансгены для экспрессии с применением зкДНК-векторов, описанных в настоящем документе, экспрессируют или кодируют один или более полипептидов, пептидов, рибозимов, пептидных нуклеиновых кислот, киРНК, RNAi, антисмысловых олигонуклеотидов, антисмысловых полинуклеотидов, антител, антигенсвязывающих фрагментов; или любую комбинацию перечисленного.
[00340] В частности, указанный трансген может кодировать один или более терапевтических агентов, в том числе, но не ограничиваясь перечисленными, например, белков, полипептидов, пептидов, ферментов, антител, антигенсвязывающих фрагментов, а также их вариантов и/или активных фрагментов, агонистов, антагонистов, миметиков для применения при лечении, для профилактики и/или облегчения одного или более симптомов заболевания, дисфункции, повреждения и/или нарушения. Согласно одному аспекту указанные заболевание, дисфункция, травма, повреждение и/или нарушение представляет собой заболевание, дисфункцию, травму, повреждение и/или нарушение у человека.
[00341] Как отмечено в настоящем документе, указанный трансген может кодировать терапевтический белок или пептид, или терапевтическую последовательность нуклеиновой кислоты или терапевтический агент, в том числе, но не ограничиваясь перечисленными, один или более агонистов, антагонистов, антиапоптотических факторов, ингибиторов, рецепторов, цитокинов, цитотоксинов, эритропоэтических агентов, гликопротеинов, факторов роста, рецепторов факторов роста, гормонов, рецепторов гормонов, интерферонов, интерлейкинов, рецепторов интерлейкинов, факторов роста нервов, нейроактивных пептидов, рецепторов нейроактивных пептидов, протеаз, ингибиторов протеаз, протеиндекарбоксилаз, протеинкиназ, ингибиторов протеинкиназ, ферментов, связывающих рецепторы белков, транспортных белков или одного или более их ингибиторов, рецепторов серотонина или одного или более ингибиторов его усвоения, серпинов, рецепторов серпинов, супрессоров опухолей, диагностических молекул, химиотерапевтических агентов, цитотоксинов; или любой комбинации перечисленного.
[00342] Согласно некоторым вариантам реализации трансген в экспрессионной кассете, экспрессионной конструкции или зкДНК-векторе, описанных в настоящем документе, может быть кодон-оптимизирован для клетки-хозяина. В настоящем документе термин «кодон-оптимизированный» или «кодон-оптимизация» относится к способу модификации последовательности нуклеиновой кислоты для улучшения экспрессии в клетках представляющего интерес позвоночного животного, например, мыши или человека (например, гуманизированной), путем замены по меньшей мере одного, более одного или значимого числа кодонов естественной последовательности (например, прокариотической последовательности) кодонами, чаще или чаще всего используемыми в генах указанного позвоночного животного. У различных видов наблюдается конкретное смещение с предпочтением определенных кодонов для конкретной аминокислоты. Как правило, кодон-оптимизация не изменяет последовательность аминокислот исходного транслируемого белка. Оптимизированные кодоны могут быть определены с использованием, например, платформы для кодон-оптимизации и персонализированного синтеза генов от Aptagen Gene Forge® (Aptagen, Inc.) или другой базы данных в открытом доступе.
[00343] Согласно некоторым вариантам реализации указанный зкДНК-вектор экспрессирует трансген у субъекта клетки-хозяина. Согласно некоторым вариантам реализации указанный субъект клетка-хозяин представляет собой клетку-хозяина человека, включая, например, клетки крови, стволовые клетки, гемато поэтические клетки, CD34+ клетки, клетки печени, раковые клетки, клетки сосудов, мышечные клетки, клетки поджелудочной железы, нервные клетки или клетки сетчатки, эпителиальные или эндотелиальные клетки, дендритные клетки, фибробласты или любую другую клетку, происходящую из организма млекопитающих, включая, без ограничений, гепатоциты (т.е. клетки печени), клетки легких, клетки сердца, клетки поджелудочной железы, клетки ЖКТ, диафрагмальные клетки, ренальные (т.е. почечные) клетки, нервные клетки, клетки крови, клетки костного мозга, или клетки любой одной или более выбранных тканей субъекта, для которого предназначена генная терапия. Согласно одному аспекту субъект - клетка-хозяин представляет собой клетку-хозяина человека.
[00344] Согласно настоящему изобретению предложены композиций и составы с зкДНК-векторами, которые включают один или более зкДНК-векторов согласно настоящему изобретению наряду с одним или более фармацевтически приемлемыми буферами, разбавителями или вспомогательными веществами. Такие композиции могут быть включены в один или более диагностических или терапевтических наборов для диагностики, предотвращения, лечения или облегчения одного или более симптомов заболевания, повреждения, нарушения, травмы или дисфункции. Согласно одному аспекту указанное заболевание, повреждение, нарушение, травма или дисфункция представляет собой заболевание, повреждение, нарушение, травму или дисфункцию у человека.
[00345] Согласно другому аспекту описанной в настоящем документе технологии предложен способ предоставления нуждающемуся в этом субъекту диагностически или терапевтически эффективное количество зкДНК-вектора, при этом указанный способ включает доставку в клетку, ткань или орган нуждающегося в этом субъекта некоторого количества зкДНК-вектора согласно описанию в настоящем документе; на протяжении времени, эффективного для обеспечения экспрессии трансгена с указанного зкДНК-вектора, таким образом обеспечивая указанного субъекта диагностически или терапевтически эффективного количества белка, пептида, нуклеиновой кислоты, экспрессируемой указанным зкДНК-вектором. Согласно дополнительному аспекту указанный субъект представляет собой человека.
[00346] Согласно другому аспекту описанной в настоящем документе технологии предложен способ диагностики, предотвращения, лечения или облегчения по меньшей мере одного или более симптомов заболевания, нарушения, дисфункции, повреждения, аномального состояния или травмы у субъекта. В общем и широком смысле указанный способ включает по меньшей мере этап введения нуждающемуся в этом субъекту одного или более из описанных зкДНК-векторов, в количестве и на протяжении времени, достаточных для диагностики, предотвращения, лечения или облегчения одного или более симптомов заболевания, нарушения, дисфункции, повреждения, аномального состояния или травмы у субъекта. Согласно дополнительному аспекту указанный субъект представляет собой человека.
[00347] Согласно другому аспекту предложено применение указанного зкДНК-вектора в качестве инструмента для лечения или уменьшения одного или более симптомов заболевания или болезненных состояний. Существует ряд наследственных заболеваний, для которых известны дефектные гены, которые, как правило, относятся к двум классам: состояния недостаточности, как правило, недостаточности ферментов, которые обычно наследуются рецессивным образом, и разбалансированные состояния, в которые могут быть вовлечены регуляторные или структурные белки, и которые, как правило, но не всегда наследуются доминантным образом. В случае заболеваний с состояниями недостаточности зкДНК-векторы могут применяться для доставки трансгенов, чтобы ввести нормальный ген в пораженные ткани для заместительной терапии, а также, согласно некоторым вариантам реализации для создания моделей заболевания на животных с применением антисмысловых мутаций. В случае разбалансированных болезненных состояний зкДНК-векторы могут применяться для создания модели болезненного состояния в модельной системе, которые затем могут быть использованы в рамках усилий, направленных на противодействие указанному болезненному состоянию. Соответственно, зкДНК-векторы и способы согласно описанию в настоящем документе позволяют лечить генетические заболевания. Согласно настоящему документу лечение болезненного состояния осуществляют путем частичного или полного устранения недостаточности или разбалансированности, которая вызывает заболевание или делает его более тяжелым.
[00348] В общем случае, зкДНК-вектор согласно описанию в настоящем документе могут применяться для доставки любого трансгена для лечения, предотвращения или облегчения симптомов, ассоциированных с любым нарушением, связанным с генной экспрессией. Показательные болезненные состояния включают, не ограничиваясь перечисленными: муковисцедоз (и другие заболевания легких), гемофилию А, гемофилию В, талассемию, анемию и другие нарушения крови, СПИД, болезнь Альцгеймера, болезнь Паркинсона, болезнь Гентингтона, амиотрофический боковой склероз, эпилепсию и другие неврологические нарушения, рак, сахарный диабет, мышечные дистрофии (например, Дюшенна, Беккера), болезнь Гурлера, недостаточность аденозиндезаминазы, метаболические дефекты, дегенеративные заболевания сетчатки глаза (и другие заболевания глаз), митохондриопатии (например, наследственную оптическую нейропатию Лебера (LHON), синдром Лея и подострую склерозирующую энцефалопатию), миопатии (например, плече-лопаточно-лицевую миопатию (FSHD) и кардиомиопатии), заболевания твердых органов (например, головного мозга, печени, почек, сердца); и т.п. Согласно некоторым вариантам реализации зкДНК-векторы согласно описанию в настоящем документе могут быть благоприятным образом использованы в лечении индивидуумов с метаболическими нарушениями (например, недостаточностью орнитинтранскарбамилазы).
[00349] Согласно некоторым вариантам реализации зкДНК-вектор, описанный в настоящем документе, может применяться для лечения, облегчения и/или предотвращения заболевания или нарушения, вызываемое мутацией в гене или генном продукте. Примеры заболеваний или нарушений, лечение которых может проводиться с применением зкДНК-векторов, включают, не ограничиваясь перечисленными, метаболические заболевания или нарушения (например, болезнь Фабри, болезнь Гоше, фенилкетонурию (ФКУ), болезнь накопления гликогена); болезни или нарушения цикла мочевины (например, недостаточность орнитинтранскарбамилазы (ОТС)); лизосомные болезни или нарушения накопления (например, метахроматическую лейкодистрофию (МЛД), мукополисахаридоз типа II (MPSII; синдром Гунтера)); заболевания или нарушения печени (например, прогрессирующий семейный внутрипеченочный холестаз (ПСВХ); заболевания или нарушения крови (например, гемофилию (А и В), талассемию и анемию); рак и опухоли, а также генетические заболевания или нарушения (например, муковисцедоз).
[00350] Согласно еще одному дополнительному аспекту зкДНК-вектор согласно описанию в настоящем документе может применяться для доставки гетерологичной последовательности нуклеотидов в ситуациях, в которых желательна регуляция уровня трансгенной экспрессии (например, трансгенов, кодирующих гормоны или факторы роста, согласно описанию в настоящем документе).
[00351] Соответственно, согласно некоторым вариантам реализации зкДНК-вектор, описанный в настоящем документе, может применяться для коррекции аномального уровня и/или функции генного продукта (например, отсутствия или дефекта белка), который приводит к заболеванию или нарушению. Указанный зкДНК-вектор может продуцировать функциональный белок и/или модифицировать уровни указанного белка для облегчения или снижения симптомов, являющихся результатом конкретного заболевания или нарушения, или обеспечивать преимущества при конкретном заболевании или нарушении, вызываемом отсутствием или дефектом белка. Например, лечение недостаточности ОТС может быть осуществлено путем продуцирования функционального фермента ОТС; лечение гемофилии А и В может быть осуществлено путем модификации уровней фактора VIII, фактора IX и фактора X; лечение ФКУ может быть осуществлено путем модификации уровней фермента фенилаланингидроксилазы; лечение болезни Фабри или болезни Гоше может быть осуществлено путем продуцирования функциональной альфа-галактозидазы или бета-глюкоцереброзидазы, соответственно; лечение МЛД или MPSII может быть осуществлено путем продуцирования функциональной арилсульфатазы А или идуронат-2-сульфатазы, соответственно; лечение муковисцедоза может быть осуществлено путем продуцирования функционального регулятора трансмембранной проводимости при муковисцедозе; лечение болезни накопления гликогена может быть осуществлено путем восстановления функции функционального фермента глюкозо-6-фосфатазы; и лечение ПСВХ может быть осуществлено путем получения функциональных генов АТР8 В1, АВСВ11, АВСВ4 или TJP2.
[00352] Согласно альтернативным вариантам реализации зкДНК-векторы согласно описанию в настоящем документе могут применяться для обеспечения антисмысловой нуклеиновой кислотой клетки in vitro или in vivo. Например, если трансген представляет собой молекулу РНК-интерференции, экспрессия антисмысловой нуклеиновой кислоты или РНК-интерференции в целевой клетке снижает уровень экспрессии конкретного белка указанной клеткой. Соответственно, трансгены, представляющие собой молекулы РНК-интерференции или антисмысловые нуклеиновые кислоты, могут вводиться для снижения экспрессии конкретного белка у нуждающегося в этом субъекта. Антисмысловые нуклеиновые кислоты могут также вводиться в клетки in vitro для регуляции физиологии клеток, например, для оптимизации культуральных систем клеток и тканей.
[00353] Согласно некоторым вариантам реализации примеры трансгенов, кодируемых зкДНК-вектором, включают, не ограничиваясь перечисленными: X, лизосомальные ферменты (например, гексозаминидаза А, ассоциированная с болезнью Тея-Сакса, или идуронатсульфатаза, ассоциированная с синдромом Гунтера/MPS II), эритропоэтин, ангиостатин, эндостатин, супероксиддисмутазу, глобин, лептин, каталазу, тирозингидроксилазу, а также цитокины (например, интерферон, β-интерферон, интерферон-γ, интерлейкин-2, интерлейкин-4, интерлейкин 12, гранулоцитарно-макрофагальный колониестимулирующий фактор, лимфотоксин и т.п.), пептидные факторы роста и гормоны (например, соматотропин, инсулин, инсулиноподобные факторы роста 1 и 2, тромбоцитарный фактор роста (ТРФ), эпидермальный фактор роста (ЭФР), фактор роста фибробластов (ФРФ), фактор роста нервов (ФРН), нейротрофический фактор-3 и 4, нейротрофический фактор головного мозга (BDNF), глиальный фактор роста (GDNF), трансформирующие факторы роста α и β; и т.п.), рецепторы (например, рецептор фактора некроза опухоли). Согласно некоторым примерам вариантов реализации указанный трансген кодирует моноклональное антитело, специфическое в отношении одной или более требуемых мишеней. Согласно некоторым примерам вариантов реализации зкДНК-вектор кодирует более одного трансгена. Согласно некоторым примерам вариантов реализации указанный трансген кодирует слитый белок, содержащий два разных представляющих интерес полипептида. Согласно некоторым вариантам реализации указанный трансген кодирует антитело, в том числе полноразмерное антитело или фрагмент антитела, согласно определению в настоящем документе. Согласно некоторым вариантам реализации указанное антитело представляет собой последовательность антигенсвязывающего домена или вариабельного домена иммуноглобулина согласно определению в настоящем документе. Другие иллюстративные трансгенные последовательности кодируют продукты суицидных генов (тимидинкиназу, цитозиндезаминазу, дифтерийный токсин, цитохром Р450, дезоксицитидинкиназу и фактор некроза опухоли), белки, придающие устойчивость к лекарственному средству, применяемому в противораковой терапии, и продукты генов-супрессоров опухолей.
[00354] Согласно репрезентативному варианту реализации экспрессируемый зкДНК-вектором трансген может применяться для лечения мышечной дистрофии у нуждающегося в этом субъекта, при этом указанный способ включает: введение эффективного для лечения, облегчения или предотвращения количества зкДНК-вектора, описанного в настоящем документе, при этом указанный зкДНК-вектор содержит гетерологичную нуклеиновую кислоту, кодирующую дистрофии, минидистрофин, микродистрофин, пропептид миостатина, фоллистатин, растворимый рецептор активина II типа, ИПФР-1, противовоспалительные полипептиды, такие как доминантный мутант I-κВ, саркоспан, утрофин, микродистрофин, ламинин-α2, α-саркогликан, β-саркогликан, γ-саркогликан, δ-саркогликан, ИПФР-1, антитело или фрагмент антитела к миостатину или пропептиду миостатина, и/или RNAi к миостатину. Согласно конкретным вариантам реализации указанный зкДНК-вектор может быть введен в скелетную, диафрагмальную и/или сердечную мышцу согласно описанию в тексте настоящего документа.
[00355] Согласно некоторым вариантам реализации указанный зкДНК-вектор может применяться для доставки трансгена в скелетную, сердечную или диафрагмальную мышцу, для получения полипептида (например, фермента) или функциональной РНК (например, РНК-интерференции, микро РНК, антисмысловой РНК), которая в норме циркулирует в крови, или для системной доставки в другие ткани для лечения, облегчения и/или предотвращения нарушения (например, метаболического нарушения, такого как диабет (например, доставки инсулина), гемофилии (например, VIII), мукополисахаридозного нарушения (например, синдрома Слая, синдрома Гурлер, синдрома Шейе, синдрома Гурлер-Шейе, синдрома Гунтера, синдрома Санфилиппо А, В, С, D, синдрома Моркио, синдрома Марото-Лами и т.п.) или нарушения лизосомального накопления (такого как болезнь Гоше [глюкоцереброзидаза], болезнь Помпе [лизосомальная кислая альфа-глюкозидаза] или болезни Фабри [альфа-галактозидаза А]) или нарушения накопления гликогена (такого как болезнь Помпе [лизосомальная кислая α-глюкозидаза]). Другие подходящие белки для лечения, облегчения и/или предотвращения метаболических нарушений описаны выше.
[00356] Согласно другим вариантам реализации зкДНК-вектор согласно описанию в настоящем документе может применяться для доставки трансгена в способе лечения, облегчения и/или предотвращения метаболического нарушения у нуждающегося в этом субъекта. Иллюстративные метаболические нарушения и трансгены, кодирующие полипептиды, описаны в настоящем документе. Необязательно, указанный полипептид представляет собой секретируемый полипептид (например, полипептид, который представляет собой секретируемый полипептид в естественном состоянии или сконструированный для секреции, например, за счет образования функциональной связи с секреторной сигнальной последовательностью, как известно в данной области техники).
[00357] Другой аспект настоящего изобретения относится к способу лечения, облегчения и/или предотвращения врожденной сердечной недостаточности или ЗПА у нуждающегося в этом субъекта, при этом указанный способ включает введение зкДНК-вектора согласно описанию в настоящем документе субъекту-млекопитающему, при этом указанный зкДНК-вектор содержит трансген, кодирующий, например, Ca2+-АТФазу саркоплазматического эндоретикулума (SERCA2a), ангиогенный фактор, ингибитор фосфатазы I (I-1), RNAi к фосфоламбану; фосфоламбановую ингибиторную или доминантно-негативную молекулу, такую как фосфоламбан S16E, белок с цинковыми пальцами, который регулирует ген фосфоламбана, β2-адренергический рецептор, бета-2-адренергическую рецепторную киназу (BARK), PI3-киназу, кальсаркан, ингибитор бета-адренергической рецепторной киназы (βARKct), ингибитор 1 протеинфосфатазы 1, S100A1, парвальбумин, аденилилциклазу типа 6, молекулу, которая осуществляет нокдаун сопряженной с G-белком рецепторной киназы типа 2, такую как усеченный конститутивно активный βARKct, Pim-1, PGC-1α, SOD-1, SOD-2, EC-SOD, калликреин, HIF, тимозин-β4, mir-1, mir-133, mir-206 и/или mir-208.
[00358] ЗкДНК-векторы согласно описанию в настоящем документе могут быть введены в легкие субъекта любым подходящим способом, необязательно путем введения аэрозольной суспензии пригодных для вдыхания частиц, содержащих зкДНК-векторы, которую субъект вдыхает. Указанные пригодные для вдыхания частицы могут быть жидкими или твердыми. Аэрозоли из жидких частиц, содержащих зкДНК-векторы, могут быть получены любым подходящим способом, например, с помощью пневматического аэрозольного небулайзера или ультразвукового небулайзера, как известно специалистам в данной области техники. См., например, патент США №4501729. Аэрозоли из твердых частиц, содержащих зкДНК-векторы, могут сходным образом быть получены с помощью любого генератора аэрозолей из твердых частиц, с применением методик, известных в области фармацевтики.
[00359] Согласно некоторым вариантам реализации указанные зкДНК-векторы могут быть введены в ткани ЦНС (например, головной мозг, глаза). Согласно конкретным вариантам реализации зкДНК-векторы согласно описанию в настоящем документе могут вводиться для лечения, облегчения или предотвращения заболеваний ЦНС, в том числе генетических нарушений, нейродегенеративных нарушений, психиатрических нарушений (расстройств) и опухолей. Иллюстративные заболевания ЦНС включают, не ограничиваясь перечисленными, болезнь Альцгеймера, болезнь Паркинсона, болезнь Гентингтона, болезнь Канавана, болезнь Лея, болезнь Рефсума, синдром Туретта, первичный боковой склероз, амиотрофический боковой склероз, прогрессирующую мышечную атрофию, болезнь Пика, мышечную дистрофию, рассеянный склероз, тяжелую миастению, болезнь Бинсвангера, травму в результате повреждения спинного мозга или головы, болезнь Тея-Сакса, болезнь Леша-Нихена, эпилепсию, церебральные инфаркты, психиатрические нарушения, в том числе нарушения настроения (например, депрессию, биполярное аффективное расстройство (нарушение), устойчивое аффективное расстройство, вторичное расстройство настроения), шизофрению, лекарственную или наркотическую зависимость (например, алкоголизм и зависимости от других веществ), неврозы (например, тревожность, обсессивное расстройство, соматоформное расстройство, диссоциативное расстройство, состояние горя, послеродовая депрессия), психоз (например, галлюцинации и бред), деменцию, паранойю, связанные с дефицитом внимания нарушения, психосексуальные нарушения, нарушения сна, связанные с болью нарушения, связанные с питанием или массой тела нарушения (например, ожирение, кахексию, нервную анорексию и булимию), рак и опухоли ЦНС (например, опухоли гипофиза).
[00360] Глазные нарушения, лечение, облегчение или предотвращение которых может быть проведено с применением зкДНК-векторов согласно настоящему изобретению включают офтальмологические нарушения, затрагивающие сетчатку, задний путь и зрительный нерв (например, пигментный ретинит, диабетическую ретинопатию и другие дегенеративные заболевания сетчатки глаза, увеит, возрастную макулярную дегенерацию, глаукому). Многие офтальмологические заболевания и нарушения ассоциированы с одним или более из трех типов признаков: (1) ангиогенез, (2) воспаление и (3) дегенерация. Согласно некоторым вариантам реализации зкДНК-вектор согласно описанию в настоящем документе могут применяться для доставки антиангиогенных факторов; противовоспалительных факторов; факторы, замедляющие дегенерацию клеток, способствующие сохранению клеток или способствующие росту клеток и комбинаций вышеперечисленного. Диабетическая ретинопатия, например, характеризуется ангиогенезом. Лечение диабетической ретинопатии может осуществляться путем доставки одного или более антиангиогенных факторов либо интраокулярно (например, в стекловидное тело), либо периокулярно (например, в субтеноново пространство). Совместно могут быть доставлены один или более нейротрофических факторов, интраокулярно (например, интравитреально) либо периокулярно. Дополнительные заболевания глаз (глазеые заболевание), которые можно лечить или предотвращать с применением зкДНК-векторов согласно настоящему изобретению, включают географическую атрофию, сосудистую или «влажную» макулодистрофию, болезнь Штаргардта, врожденный амавроз Лебера (LCA), синдром Ушера, эластическую псевдоксантому (РХЕ), Х-сцепленный пигментный ретинит (XLRP), Х-сцепленное расслоение сетчатки (XLRS), хороидеремию, врожденную нейропатию зрительного нерва Лебера (LHON), ахроматопсию, палочко-колбочковую дистрофию, эндотелиальную дистрофию роговицы Фукса, диабетический макулярный отек; рак и опухоли глаз.
[00361] Согласно некоторым вариантам реализации лечение, облегчение или предотвращение воспалительных заболеваний или глазных нарушений (например, увеит) может осуществляться с применением зкДНК-векторов согласно настоящему изобретению. Один или более противовоспалительных факторов могут быть экспрессированы за счет интраокулярного введения (например, в камеру стекловидного тела или переднюю камеру) зкДНК-вектора согласно описанию в настоящем документе. Согласно другим вариантам реализации лечение, облегчение или предотвращение заболеваний или глазных нарушений, характеризующиеся дегенерацией сетчатки (например, пигментный ретинит) может осуществляться с применением зкДНК-векторов согласно настоящему изобретению. Интраокулярное введение (например, в стекловидное тело) зкДНК-вектора согласно описанию в настоящем документе, кодирующего один или более нейротрофических факторов, могут применяться для лечения таких заболеваний, связанных с дегенерацией сетчатки. Согласно некоторым вариантам реализации лечение заболевания или нарушения, в которые вовлечены и ангиогенез, и дегенерация сетчатки (например, возрастная макулярная дегенерация), может осуществляться с применением зкДНК-векторов согласно настоящему изобретению. Лечение возрастной макулярной дегенерации может осуществляться путем введения зкДНК-вектора согласно описанию в настоящем документе, кодирующего один или более нейротрофических факторов, интраокулярно (например, в стекловидное тело), и/или кодирующего один или более антиангиогенных факторов, интраокулярно или периокулярно (например, в субтеноново пространство). Глаукома характеризуется повышенным внутриглазным давлением и утратой ганглиозных клеток сетчатки. Варианты лечения глаукомы включают введение одного или более нейропротекторных агентов, которые защищают клетки от эксайтотоксичного повреждения, с применением зкДНК-вектора согласно описанию в настоящем документе. Соответственно, такие агенты включают антагонисты N-метил-D-аспартата (NMDA), цитокины и нейротрофические факторы, которые могут быть доставлены интраокулярно, необязательно интравитреально с применением зкДНК-вектора согласно описанию в настоящем документе.
[00362] Согласно другим вариантам реализации зкДНК-вектор согласно описанию в настоящем документе могут применяться для лечения судорог, например, для снижения возникновения, частоты или тяжести судорог. Эффективность терапевтического лечения судорог может быть оценена на основании поведенческих признаков (например, дрожь, глазные или ротовые тики) и/или электрографическими способами (большинство судорог характеризуются отличительными электрографическими аномалиями). Соответственно, зкДНК-вектор согласно описанию в настоящем документе может также применяться для лечения эпилепсии, для которой характерны множественные припадки в различные моменты времени. Согласно одному репрезентативному варианту реализации соматостатин (или его активный фрагмент) вводят в головной мозг с применением зкДНК-вектор а согласно описанию в настоящем документе для лечения опухоли гипофиза. В соответствии с указанным вариантом реализации зкДНК-вектор согласно описанию в настоящем документе, кодирующий соматостатин (или его активный фрагмент) вводят путем микроинфузии в гипофиз. Сходным образом, такое лечение может применяться для лечения акромегалии (аномальной секреции гормона роста гипофизом). Последовательности нуклеиновых кислот (например, №доступа GenBank J00306) и аминокислот (например, №доступа GenBank Р01166; содержит процессированные активные пептиды соматостатин-28 и соматостатин-14) соматостатинов известны в данной области техники. Согласно конкретным вариантам реализации зкДНК вектор может кодировать трансген, который содержит сигнал секреции согласно описанию в патенте США №7071172.
[00363] Другой аспект настоящего изобретения относится к применению зкДНК-вектора согласно описанию в настоящем документе для получения антисмысловой РНК, РНК-интерференции или другой функциональной РНК (например, рибозима) для системной доставки субъекту in vivo. Соответственно, согласно некоторым вариантам реализации указанный зкДНК-вектор может содержать трансген, который кодирует антисмысловую нуклеиновую кислоту, рибозим (например, согласно описанию в патенте США №5877022), РНК, которые влияют на опосредованный сплайсосомой транс-сплайсинг (см. Puttaraju et al., (1999) Nature Biotech. 17:246; патент США №6013487; патент США №6083702), интерферирующую РНК (РНК-интерференцию), опосредующую сайленсинг генов (см. Sharp et al., (2000) Science 287:2431), или другие нетранслируемые РНК, такие как «направляющие» РНК (Gorman et al., (1998) Proc. Nat. Acad. Sci. USA 95:4929; патент США №5869248, выданный Yuan et al.), и т.п.
[00364] Согласно некоторым вариантам реализации указанный зкДНК-вектор может дополнительно также содержать трансген, который кодирует репортерный полипептид (например, фермент, такой как зеленый флуоресцентный белок или щелочная фосфатаза). Согласно некоторым вариантам реализации трансген, который кодирует репортерный белок, подходящий для применения в экспериментальных или диагностических целях, выбирают из чего-либо из перечисленного: β-лактамаза, β-галактозидаза (LacZ), щелочная фосфатаза, тимидинкиназа, зеленый флуоресцентный белок (GFP), хлорамфениколацетилтрансфераза (CAT), люцифераза, и другие, хорошо известные в данной области техники. Согласно некоторым аспектам зкДНК-векторы, содержащие трансген, кодирующий репортерный полипептид, могут применяться в диагностических целях или в качестве маркеров активности зкДНК-вектора у субъекта, которому его вводят.
[00365] Согласно некоторым вариантам реализации указанный зкДНК-вектор может содержать трансген или гетерологичную нуклеотидную последовательность, которая обладает гомологией в отношении локуса на хромосоме хозяина и рекомбинируется с ним. Указанный подход может быть использован для коррекции генетического дефекта в клетке-хозяине.
[00366] Согласно некоторым вариантам реализации указанный зкДНК-вектор может содержать трансген, который может применяться для экспрессии иммуногенного полипептида у субъекта, например, для вакцинации. Указанный трансген может кодировать любой представляющий интерес иммуноген, известный в данной области техники, в том числе, но не ограничиваясь перечисленными, иммуногены вируса иммунодефицита человека, вируса гриппа, белки gag, опухолевые антигены, раковые антигены, бактериальные антигены, вирусные антигены и т.п.
XI. Введение
[00367] Согласно конкретным вариантам реализации для достижения требуемого уровня генной экспрессии может быть использовано более одного введения (например, два, три, четыре или более введений) с различными интервалами, например, ежедневно, еженедельно, ежемесячно, ежегодно и т.п.
[00368] Примеры способов введения зкДНК-вектора согласно описанию в настоящем документе включают пероральное, ректальное, трансмукозальное, интраназальное, ингаляционное (например, в аэрозоле), буккальное (например, сублингвальное), вагинальное, интратекальное, интраокулярное, чрескожное, интраэндотелиальное введение, введение in utero (или in ovo), парентеральное (например, внутривенное, подкожное, внутрикожное, интракраниальное, внутримышечное [в том числе введение в скелетную, диафрагмальную и/или сердечную мышцу], интраплевральное, интрацеребральное и внутрисуставное), местное (например, на кожу и поверхности слизистых оболочек, в том числе поверхности дыхательных путей, и чрескожное введение), внутрилимфатическое введение и т.п., а также прямую инъекцию в ткань или орган (например, в печень, глаза, скелетные мышцы, сердечную мышцу, диафрагмальную мышцу или головной мозг).
[00369] Может осуществляться введение указанного зкДНК-вектора в любой сайт в организме субъекта, включая, без ограничений, сайт, выбранный из группы, состоящей из головного мозга, скелетных мышц, гладких мышц, сердца, диафрагмы, эпителия дыхательных путей, печени, почек, селезенки, поджелудочной железы, кожи и глаз. Может также осуществляться введение указанного зкДНК-вектора в опухоль (например, в опухоль или возле опухоли, или в лимфатический узел). Наиболее подходящий маршрут в том или ином случае зависит от природы и тяжести состояния, лечение, облегчение и/или предотвращение которого проводят, и от природы конкретного используемого зкДНК-вектора. Кроме того, применение зкДНК позволяет вводить более одного трансгена в единственном векторе или нескольких зкДНК-векторах (например, коктейль зкДНК).
[00370] Введение зкДНК-вектора согласно описанию в настоящем документе в скелетные мышцы в соответствии с настоящим изобретением включает, не ограничиваясь перечисленным, введение в скелетные мышцы в конечностях (например, в плече, предплечье, бедре и/или голени), спине, шее, голове (например, язык), грудной клетки, брюшной полости, таза/промежности и/или пальцев. ЗкДНК-вектор согласно описанию в настоящем документе может быть доставлен в скелетные мышцы путем внутривенного введения, внутриартериального введения, внутрибрюшинного введения, перфузии конечности, (необязательно, перфузии изолированной конечности, ноги и/или руки; см., например, Arruda et al., (2005) Blood 105: 3458-3464), и/или прямой внутримышечной инъекции. Согласно конкретным вариантам реализации зкДНК-вектор согласно описанию в настоящем документе вводят в конечность (руку и/или ногу) субъекта (например, субъекта с мышечной дистрофией, такой как DMD) путем перфузии конечности, необязательно перфузии изолированной конечности (например, путем внутривенного или внутрисуставного введения). Согласно вариантам реализации зкДНК-вектор согласно описанию в настоящем документе может быть введен без использования «гидродинамических» методик.
[00371] Введение зкДНК-вектора согласно описанию в настоящем документе в сердечную мышцу включает введение в левое предсердие, правое предсердие, левый желудочек, правый желудочек и/или перегородку. ЗкДНК-вектор согласно описанию в настоящем документе может быть доставлен в сердечную мышцу путем внутривенного введения, внутриартериального введения, такого как интрааортальное введение, прямой инъекции в сердце (например, в левое предсердие, правое предсердие, левый желудочек, правый желудочек) и/или перфузии коронарной артерии. Введение в диафрагмальную мышцу может быть осуществлено любым подходящим способом, в том числе путем внутривенного введения, внутриартериального введения и/или внутрибрюшинного введения. Введение в гладкие мышцы быть осуществлено любым подходящим способом, в том числе путем внутривенного введения, внутриартериального введения и/или внутрибрюшинного введения. Согласно одному варианту реализации может быть осуществлено введение в эндотелиальные клетки, присутствующие в гладких мышцах, возле и/или на них.
[00372] Согласно некоторым вариантам реализации зкДНК-вектор в соответствии с настоящим изобретением вводят в скелетные мышцы, диафрагмальную мышцу и/или сердечную мышцу (например, для лечения, облегчения и/или предотвращения мышечной дистрофии или заболевания сердца (например, ЗПА или застойной сердечной недостаточности).
[00373] А. Лечение ex vivo
[00374] Согласно некоторым вариантам реализации клетки извлекают из субъекта, вводят в них зкДНК-вектор и возвращают в организм субъекта. Способы извлечения клеток из организма субъекта для лечения ex vivo, с последующим введением обратно в организм субъекта, известны в данной области техники (см., например, патент США №5399346, содержание которого полностью включено в настоящий документ). Как вариант, зкДНК-вектор вводят в клетки от другого субъекта, в культивированные клетки или в клетки из любого другого подходящего источника, и указанные клетки вводят нуждающемуся в этом субъекту.
[00375] Клетки, трансдуцированные зкДНК-вектором, предпочтительно вводят субъекту в «терапевтически эффективном количестве» в комбинации с фармацевтическим носителем. Специалистам в данной области техники будет понятно, что терапевтические эффекты не обязательно должны быть полными или обеспечивать излечение, при условии, что субъект получает некоторое преимущество.
[00376] Согласно некоторым вариантам реализации указанный зкДНК-вектор может кодировать трансген (иногда называемый гетерологичной последовательностью нуклеотидов) представляющий собой любой полипептид, продуцирование которого желательно в клетке in vitro, ex vivo или in vivo. Например, в отличие от применения указанных зкДНК-векторов в способе лечения согласно описанию в настоящем документе, согласно некоторым вариантам реализации указанные зкДНК-векторы могут быть введены в культивированные клетки и экспрессируемый генный продукт выделен из них, например, для получения антигенов или вакцин.
[00377] Указанные зкДНК-векторы могут применяться как в ветеринарии, так и в медицине. Подходящие субъекты для применения способов доставки генов ex vivo согласно описанию выше включают как птиц (например, кур, уток, гусей, перепелок, индейку и фазана), так и млекопитающих (например, человека, крупный рогатый скот, овец, коз, лошадей, кошачьих, собачьих и зайцеобразных), при этом млекопитающие являются предпочтительными. Субъекты-люди являются наиболее предпочтительными. Субъекты-люди включают новорожденных, младенцев, молодых людей и взрослых.
[00378] Один аспект описанной в настоящем документе технологии относится к способу доставки трансгена в клетку. Как правило, в способах in vitro указанный зкДНК-вектор может быть введен в клетку с применением способов согласно описанию в настоящем документе, а также других способов, известных в данной области техники. ЗкДНК-векторы согласно описанию в настоящем документе предпочтительно вводят в клетку в биологически эффективном количестве. Если зкДНК-вектор вводят в клетку in vivo (например, субъекту), биологически-эффективное количество указанного зкДНК-вектора представляет собой количество, достаточное для обеспечения трансдукции и экспрессии указанного трансгена в целевой клетке.
[00379] В. Диапазоны доз
[00380] Для облегчения идентификации оптимальных диапазонов дозировок для применения могут необязательно быть проведены анализы in vivo и/или in vitro. Точная доза для использования в составе также зависит от маршрута введения и серьезности состояния, и должны определяться на основании решения специалиста в данной области техники и с учетом обстоятельств каждого субъекта. Эффективные дозы могут быть экстраполированы на основании кривых зависимости ответа от дозы, полученных in vitro или в тестовых модельных системах на животных.
[00381] ЗкДНК-вектор вводят в достаточных количествах для трансфекции клеток требуемой ткани и для обеспечения достаточных уровней переноса генов и экспрессии без чрезмерных нежелательных явлений. Стандартные и фармацевтически приемлемые маршруты введения включают, не ограничиваясь перечисленными, описанные выше в разделе «Введение», такие как прямая доставка в выбранный орган (например, интрапортальная доставка в печень), пероральная, ингаляционная доставка (в том числе интраназальная и внутритрахеальная), интраокулярная, внутривенная, внутримышечная, подкожная, внутрикожная, внутриопухолевая доставка; и другие маршруты для парентерального введения. Маршруты введения могут быть скомбинированы, если требуется.
[00382] Доза количества зкДНК-вектора, требуемая для достижения конкретного «терапевтического эффекта», варьирует в зависимости от ряда факторов, в том числе, но не ограничиваясь перечисленным: маршрута введения нуклеиновой кислоты, уровня экспрессии гена или РНК, требуемого для достижения терапевтического эффекта, специфического заболевания или нарушения, лечение которого проводят, и стабильности указанного гена или генов, РНК-продукта или продуктов, или итогового экспрессируемого белка или белков. Специалист в данной области техники может легко определить диапазон доз зкДНК-вектора для лечения пациента с конкретным заболеванием или нарушением на основании вышеупомянутых факторов, а также других факторов, хорошо известных в данной области техники.
[00383] Режим дозирования может быть скорректирован для обеспечения оптимального терапевтического ответа. Например, олигонуклеотид может быть введен неоднократно, например, ежедневно может вводиться несколько доз, или доза может быть пропорционально снижена с учетом диктуемой терапевтической ситуацией необходимости. Специалист в данной области техники легко сможет определить подходящие дозы и схемы введения рассматриваемых олигонуклеотидов, как для введения в клетки, так и для введения субъектам.
[00384] «Терапевтически эффективная доза» представлена относительно широким диапазоном, который может быть определен в клинических испытаниях и зависит от конкретного применения (нервные клетки требуют очень незначительных количеств, тогда как системные инъекции требуют значительных количеств). Например, для прямой инъекции in vivo в скелетную или сердечную мышцу субъекта-человека величина терапевтически эффективной дозы будет составлять приблизительно около 1 мкг - 100 г зкДНК-вектора. В тех случаях, когда для доставки зкДНК-вектора используют экзосомы или микрочастицы, терапевтически эффективная доза может быть определена экспериментальным путем, однако предположительно будет доставлено от 1 мкг до приблизительно 100 г вектора.
[00385] Получение составов фармацевтически приемлемых вспомогательных веществ и растворов-носителей хорошо известно специалистам в данной области техники, как и разработка подходящих схем дозирования и лечения для применения конкретных композиций, описанных в настоящем документе, в различных схемах лечения.
[00386] Для трансфекции in vitro эффективное количество зкДНК-вектора для доставки в клетки (1×106 клеток) составляет около 0,1-100 мкг зкДНК-вектор а, предпочтительно от 1 до 20 мкг, более предпочтительно от 1 до 15 мкг, или от 8 до 10 мкг. Для зкДНК-векторов большего размера необходимы более высокие дозы. Если используются экзосомы или микрочастицы, эффективная in vitro доза может быть определена экспериментальным путем, однако должна предположительно обеспечивать доставку в общем такого же количества зкДНК-вектора.
[00387] Лечение может включать введение единственной дозы или нескольких доз. Согласно некоторым вариантам реализации субъекту может быть введено более одной дозы; фактически, при необходимости может быть введено несколько доз, поскольку зкДНК-вектор не вызывает у хозяина иммунного ответа против капсида ввиду отсутствия вирусного капсида. Соответственно, специалист в данной области техники может легко определить подходящее количество доз. Количество введенных доз может, например, составлять порядка 1-100, предпочтительно 2-20 доз.
[00388] Без связи с какой-либо конкретной теорией, отсутствие типичного противовирусного иммунного ответа, вызываемого введением зкДНК-вектора согласно описанию в настоящем документе (т.е. не содержащего компонентов капсида) позволяет неоднократно вводить указанный зкДНК-вектор хозяину. Согласно некоторым вариантам реализации число введений гетерологичной нуклеиновой кислоты субъекту составляет от 2 до 10 раз (например, 2, 3, 4, 5, 6, 7, 8, 9 или 10 раз). Согласно некоторым вариантам реализации зкДНК-вектор доставляют субъекту более 10 раз.
[00389] Согласно некоторым вариантам реализации дозу зкДНК-вектора вводят субъекту не чаще одного раза в календарный день (например, 24-часовой период). Согласно некоторым вариантам реализации дозу зкДНК-вектора вводят субъекту не чаще одного раза в 2, 3, 4, 5, 6, или 7 календарных дней. Согласно некоторым вариантам реализации дозу зкДНК-вектора вводят субъекту не чаще одного раза в календарную неделю (например, 7 календарных дней). Согласно некоторым вариантам реализации дозу зкДНК-вектора вводят субъекту не чаще одного раза в две недели (например, один раз за период продолжительностью две календарных недели). Согласно некоторым вариантам реализации дозу зкДНК-вектора вводят субъекту не чаще одного раза в календарный месяц (например, один раз в 30 календарных дней). Согласно некоторым вариантам реализации дозу зкДНК-вектора вводят субъекту не чаще одного раза за шесть календарных месяцев. Согласно некоторым вариантам реализации дозу зкДНК-вектора вводят субъекту не чаще одного раза в календарный год (например, 365 дней или 366 дней в високосном году).
[00390] С. Единичные лекарственные формы
[00391] Согласно некоторым вариантам реализации указанные фармацевтические композиции могут быть удобным образом представлены в виде единичной лекарственной формы. Единичная лекарственная форма, как правило, адаптирована для одного или более специфических маршрутов введения фармацевтической композиции. Согласно некоторым вариантам реализации указанная единичная лекарственная форма адаптирована для введения путем ингаляции. Согласно некоторым вариантам реализации указанная единичная лекарственная форма адаптирована для введения с помощью испарителя. Согласно некоторым вариантам реализации указанная единичная лекарственная форма адаптирована для введения с помощью небулайзера. Согласно некоторым вариантам реализации указанная единичная лекарственная форма адаптирована для введения с помощью генератора аэрозоля. Согласно некоторым вариантам реализации указанная единичная лекарственная форма адаптирована для перорального введения, для буккального введения или для сублингвального введения. Согласно некоторым вариантам реализации указанная единичная лекарственная форма адаптирована для внутривенного, внутримышечного или подкожного введения. Согласно некоторым вариантам реализации указанная единичная лекарственная форма адаптирована для интратекального или интрацеребровентрикулярного введения. Согласно некоторым вариантам реализации указанный фармацевтическая композиция введена в состав для местного введения. Количество активного ингредиента, которое может быть скомбинировано с материалом носителя для получения единичной лекарственной формы, обычно представлено таким количеством указанного соединения, которое обеспечивает терапевтический эффект.
XII. Различные варианты применения
[00392] Композиции и зкДНК-векторы, предложенные согласно настоящему изобретению могут применяться для доставки трансгена для различных целей согласно описанию выше. Согласно некоторым вариантам реализации указанный трансген кодирует белок или функциональную РНК, предназначенные для применения в научных исследованиях, например, для создания соматической трансгенной модели на животных, несущих указанный трансген, например, для изучения функции указанного трансгенного продукта. Согласно другому примеру указанный трансген кодирует белок или функциональную РНК, предназначенные для применения при создании модели заболевания на животных.
[00393] Согласно некоторым вариантам реализации указанный трансген кодирует один или более пептидов, полипептидов или белков, которые подходят для лечения, облегчения или предотвращения болезненных состояний у субъекта-млекопитающего. Указанный трансген может быть перенесен в организм пациента (например, экспрессируется у пациента) в достаточном количестве для лечения заболеваний, ассоциированных с пониженной экспрессией, отсутствием экспрессии или дисфункцией гена.
[00394] Согласно некоторым вариантам реализации предусмотрены зкДНК-векторы для применения в способах диагностики и скрининга, за счет которого трансген транзиентно или стабильно экспрессируется в клеточной культуральной системе, или, как вариант, в трансгенной модели на животных.
[00395] Согласно другому аспект описанная в настоящем документе технология обеспечивает способ трансдукции популяции клеток млекопитающих. В общем и широком смысле указанный способ включает по меньшей мере этап введения в одну или более клеток в популяции композиции, которая содержит эффективное количество одной или более зкДНК согласно описанию в настоящем документе.
[00396] Кроме того, согласно настоящему изобретению предложены композиции, а также терапевтические и/или диагностические наборы, которые включают один или более описанных зкДНК-векторов или зкДНК-композиций, введенных в состав с одним или более дополнительными ингредиентами, или подготовленных вместе с одной или более инструкциями по их применению.
[00397] Клетки для введения зкДНК-вектора согласно описанию в настоящем документе могут быть любого типа, в том числе, но не ограничиваясь перечисленными, представлять собой нервные клетки (в том числе клетки периферической и центральной нервной системы, в частности, клетки головного мозга), клетки легких, клетки сетчатки, эпителиальные клетки (например, эпителиальные клетки ЖКТ и дыхательного тракта), мышечные клетки, дендритные клетки, клетки поджелудочной железы (в том числе островковые клетки), клетки печени, клетки миокарда, костные клетки (например, стволовые клетки костного мозга), гематопоэтические стволовые клетки, клетки селезенки, кератиноциты, фибробласты, эндотелиальные клетки, клетки предстательной железы, половые зародышевые клетки и т.п. Как вариант, клетка может представлять собой любую клетку-предшественник. Согласно дополнительному варианту клетка может представлять собой стволовую клетку (например, нервную стволовую клетку, стволовую клетку печени). Согласно еще одному дополнительному варианту клетка может представлять собой раковую или опухолевую клетку. Кроме того, указанные клетки могут происходить из любого вида, как указано выше.
[00398] Согласно некоторым вариантам реализации настоящее изобретение может быть описано любым из следующих пунктов:
1А. зкДНК-вектор, содержащий:
экспрессионную кассету, содержащую цис-регуляторный элемент, где указанный цис-регуляторный элемент выбран из группы, состоящей из посттранскрипционного регуляторного элемента и поли(А)-сигнала BGH;
ITR дикого типа в начале (на 5'-конце) экспрессионной кассеты, где указанный ITR дикого типа содержит полинуклеотид из SEQ ID NO: 51; и
модифицированный ITR в конце (на 3'-конце) экспрессионной кассеты, где указанный модифицированный ITR содержит полинуклеотид из SEQ ID NO: 2,
при этом указанный ДНК-вектор лишен специфического прокариотического метилирования и не заключен в капсидный белок AAV.
2А. ДНК-вектор по пункту 1А, где указанный ДНК-вектор имеет линейную и непрерывную структуру.
3А. ДНК-вектор по любому из пунктов 1А-2А, где указанный посттранскрипционный регуляторный элемент содержит посттранскрипционный регуляторный элемент WHP (WPRE).
4А. ДНК-вектор по любому из пунктов 1А-3А, где указанная экспрессионная кассета дополнительно содержит сайт клонирования.
5А. ДНК-вектор по любому из пунктов 1A-4А, где указанная экспрессионная кассета содержит промотор, выбранный из группы, состоящей из промотора CAG, промотора ААТ, промотора LP1 и промотора EF1a.
6А. ДНК-вектор по пункту 1А, где указанная экспрессионная кассета содержит полинуклеотиды из SEQ ID NO: 3, SEQ ID NO: 7, SEQ ID NO: 8 и SEQ ID NO: 9.
7A. ДНК-вектор по любому из пунктов 1A-6A, где указанная экспрессионная кассета дополнительно содержит сайт клонирования и экзогенную последовательность, инсертированную в сайт клонирования.
8А. ДНК-вектор по пункту 7А, где указанная экзогенная последовательность содержит по меньшей мере 2000 нуклеотидов.
9А. ДНК-вектор по пункту 7А, где указанная экзогенная последовательность кодирует белок.
10А. ДНК-вектор по пункту 7А, где указанная экзогенная последовательность кодирует репортерный белок.
11А. Клетка, содержащая ДНК-вектор по любому из пунктов 1А-10А.
12А. Клетка по пункту 11А, дополнительно содержащая белок репликации, выбранный из группы, состоящей из: AAV Rep 78, AAV Rep 68, AAV Rep52 и AAV Rep 40.
13A. Клетка по пункту 12A, отличающаяся тем, что указанный белок репликации кодирует хелперный вирус.
14А. Клетка по любому из пунктов 11А-13А, отличающаяся тем, что указанная клетка не содержит гена, кодирующего капсидный белок AAV.
15А. Фармакологически активный ингредиент, содержащий ДНК-вектор по любому из пунктов 1А-10А и, необязательно, вспомогательное вещество.
16А. Способ доставки экзогенной последовательности в клетку, включающий этап введения ДНК-вектора по любому из пунктов 1А-10А в указанную клетку.
17А. Способ по пункту 16А, где указанный этап введения ДНК-вектора включает гидродинамическую инъекцию.
18А. Способ получения ДНК-вектора, включающий следующие этапы:
введение в клетку конструкции нуклеиновой кислоты или вируса, содержащей (содержащего):
экспрессионную кассету, содержащую цис-регуляторный элемент, где указанный цис-регуляторный элемент выбран из группы, состоящей из посттранскрипционного регуляторного элемента и поли(А)-сигнала BGH;
ITR дикого типа в начале (на 5'-конце) экспрессионной кассеты, где указанный ITR дикого типа содержит полинуклеотид из SEQ ID NO: 51; и
модифицированный ITR в конце (на 3'-конце) экспрессионной кассеты, где указанный модифицированный ITR содержит полинуклеотид из SEQ ID NO: 2,
при этом указанная клетка не содержит капсидного белка AAV; и
сбор указанного ДНК-вектора, полученного из указанной конструкции нуклеиновой кислоты или указанного вируса,
при этом указанный ДНК-вектор лишен специфического прокариотического метилирования.
19А. Способ по пункту 18А, где указанный ДНК-вектор имеет линейную и непрерывную структуру.
20А. Способ по любому из пунктов 18А-19А, где указанный посттранскрипционный регуляторный элемент содержит посттранскрипционный регуляторный элемент WHP (WPRE).
21А. Способ по любому из пунктов 18А-20А, где указанная экспрессионная кассета дополнительно содержит промотор, выбранный из группы, состоящей из промотора CAG, промотора ААТ, промотора LP1 и промотора EF1a.
22А. Способ по пункту 18, где указанная экспрессионная кассета содержит полинуклеотиды из SEQ ID NO: 3, SEQ ID NO: 7, SEQ ID NO: 8 и SEQ ID NO: 9.
23А. Способ по любому из пунктов 18A-22A, где указанная экспрессионная кассета дополнительно содержит экзогенную последовательность.
24А. Способ по пункту 23А, где указанная экзогенная последовательность содержит по меньшей мере 2000 нуклеотидов.
25А. Способ по пункту 23А, где указанная экзогенная последовательность кодирует белок.
26А. Способ по пункту 23А, где указанная экзогенная последовательность кодирует репортерный белок.
27А. Способ по любому из пунктов 18А-26А, где указанная клетка представляет собой клетку насекомого.
28А. ДНК-вектор, полученный способом по любому из пунктов 18-27.
29А. Клетка для получения ДНК-вектора, содержащая:
первый полинуклеотид, содержащий:
экспрессионную кассету, содержащую цис-регуляторный элемент, где указанный цис-регуляторный элемент выбран из группы, состоящей из посттранскрипционного регуляторного элемента и поли(А)-сигнала BGH;
ITR дикого типа в начале (на 5'-конце) экспрессионной кассеты, где указанный ITR дикого типа содержит полинуклеотид из SEQ ID NO: 51; и
модифицированный ITR в конце (на 3'-конце) экспрессионной кассеты, где указанный модифицированный ITR содержит полинуклеотид из SEQ ID NO: 2; и
второй полинуклеотид, кодирующий белок репликации, выбранный из группы, состоящей из AAV78, AAV52, AAV Rep68 и AAV Rep 40,
при этом указанная клетка не содержит гена, кодирующего капсидный белок AAV.
30А. Клетка по пункту 29А, отличающаяся тем, что указанный посттранскрипционный регуляторный элемент содержит посттранскрипционный регуляторный элемент WHP (WPRE).
31А. Клетка по любому из пунктов 29А-30А, отличающаяся тем, что указанная клетка представляет собой клетку насекомого.
32А. ДНК-вектор, полученный из клетки по любому из пунктов 29А-31А путем репликации указанного первого полинуклеотида.
33А. Полинуклеотид для получения ДНК-вектора, содержащий:
экспрессионная кассета, содержащая цис-регуляторный элемент, где указанный цис-регуляторный элемент выбран из группы, состоящей из посттранскрипционного регуляторного элемента и поли(А)-сигнала BGH;
ITR дикого типа в начале (на 5'-конце) экспрессионной кассеты, где указанный ITR дикого типа содержит полинуклеотид из SEQ ID NO: 51; и
модифицированный ITR в конце (на 3'-конце) экспрессионной кассеты, где указанный модифицированный ITR содержит полинуклеотид из SEQ ID NO: 2.
34А. Полинуклеотид по пункту 33А, где указанный посттранскрипционный регуляторный элемент содержит посттранскрипционный регуляторный элемент WHP (WPRE).
35А. Полинуклеотид по любому из пунктов 33А-34А, где указанный полинуклеотид находится в плазмиде, в бакмиде или в бакуловирусе.
36А. Полинуклеотид по любому из пунктов 33А-35А, дополнительно содержащий экзогенную последовательность.
37А. Полинуклеотид по пункту 36А, где указанная экзогенная последовательность содержит по меньшей мере 2000 нуклеотидов.
38А. Полинуклеотид по пункту 36А, где указанная экзогенная последовательность кодирует белок.
39А. Полинуклеотид по пункту 36А, где указанная экзогенная последовательность кодирует репортер
40А. ДНК-вектор, полученный путем репликации полинуклеотида по любому из пунктов 33А-39А белком репликации, выбранным из группы, состоящей из AAV78, AAV52, AAV Rep68 и AAV Rep 40, где указанный ДНК-вектор имеет линейную и непрерывную структуру, лишен специфического прокариотического метилирования и не заключен в капсидный белок AAV.
41 А. ДНК-вектор, содержащий: экспрессионную кассету;
модифицированный ITR в начале (на 5'-конце)
экспрессионной кассеты, где указанный модифицированный
ITR содержит полинуклеотид из SEQ ID NO: 52; и
ITR дикого типа в конце (на 3'-конце) экспрессионной кассеты, где указанный ITR дикого типа содержит полинуклеотид из SEQ ID NO:1,
при этом ДНК-вектор лишен специфического прокариотического метилирования и не заключен в капсидный белок AAV.
42А. ДНК-вектор по пункту 41А, где указанная экспрессионная кассета содержит цис-регуляторный элемент, где указанный цис-регуляторный элемент выбран из группы, состоящей из посттранскрипционного ответного элемента и поли(А)-сигнала.
43А. ДНК-вектор по пункту 42А, где указанный посттранскрипционный ответный элемент содержит посттранскрипционный ответный элемент WHP (WPRE).
44А. ДНК-вектор по любому из пунктов 42А-43А, где указанный поли(А)-сигнал содержит поли(А)-сигнал BGH.
45А. ДНК-вектор по любому из пунктов 41А-44А, где указанная экспрессионная кассета содержит промотор, выбранный из группы, состоящей из промотора CAG, промотора ААТ, промотора LP1 и промотора EF1a.
46А. ДНК-вектор по пункту 41А, где указанная экспрессионная кассета содержит полинуклеотиды из SEQ ID NO: 3, SEQ ID NO: 7, SEQ ID NO: 8 и SEQ ID NO: 9.
47A. ДНК-вектор по любому из пунктов 41A-46A, где указанная экспрессионная кассета содержит экзогенную последовательность.
48А. ДНК-вектор по пункту 47А, где указанная экзогенная последовательность содержит по меньшей мере 2000 нуклеотидов.
49А. ДНК-вектор по пункту 47А, где указанная экзогенная последовательность кодирует белок.
50А. ДНК-вектор по пункту 47А, где указанная экзогенная последовательность кодирует репортерный белок.
51А. Клетка, содержащая ДНК-вектор по любому из пунктов 41А-50A.
52А. Клетка по пункту 52А, дополнительно содержащая белок репликации, выбранный из группы, состоящей из: AAV Rep 78, AAV Rep 68, AAV Rep52 и AAV Rep 40.
53А. Клетка по пункту 51А, отличающаяся тем, что указанный белок репликации кодирует хелперный вирус.
54А. Клетка по любому из пунктов 51-53, отличающаяся тем, что указанная клетка не содержит гена, кодирующего капсидный белок AAV.
55А. Фармакологически активный ингредиент, содержащий: ДНК-вектор по любому из пунктов 1А-10А; и, необязательно, вспомогательное вещество.
56А. Способ доставки экзогенной последовательности в клетку, включающий этап: введения указанный не заключенного в капсид ДНК-вектор по любому из пунктов 1А-10А в указанную клетку.
57А. Способ по пункту 16А, где указанный этап введения ДНК-вектора включает гидродинамическую инъекцию.
58А. Способ получения ДНК-вектора, включающий следующие этапы:
введение в клетку конструкции нуклеиновой кислоты или вируса, содержащей или содержащего:
экспрессионную кассету;
модифицированный ITR в начале (на 5'-конце) экспрессионной кассеты, где указанный модифицированный ITR содержит полинуклеотид из SEQ ID NO: 52; и
ITR дикого типа в конце (на 3'-конце)
экспрессионной кассеты, где указанный
ITR дикого типа содержит полинуклеотид из SEQ ID NO: 1,
при этом указанная клетка не содержит капсидного белка AAV; и
сбор указанного ДНК-вектора, полученного из указанной конструкции нуклеиновой кислоты или указанного вируса,
при этом указанный ДНК-вектор лишен специфического прокариотического метилирования и не заключен в капсидный белок AAV.
59А. Способ по пункту 18А, где указанная экспрессионная кассета содержит цис-регуляторный элемент, причем указанный цис-регуляторный элемент выбран из группы, состоящей из посттранскрипционного ответного элемента и поли(А)-сигнала.
60А. Способ по пункту 59А, где указанный посттранскрипционный ответный элемент включает посттранскрипционный ответный элемент WHP (WPRE).
61А. Способ по любому из пунктов 59А-60А, где указанный поли(А)-сигнал включает поли(А)-сигнал BGH.
62А. Способ по любому из пунктов 18А-61А, где указанная экспрессионная кассета содержит промотор, выбранный из группы, состоящей из промотора CAG, промотора ААТ, промотора LP1 и промотора EF1a.
63А. Способ по пункту 18 А, где указанная экспрессионная кассета содержит полинуклеотиды из SEQ ID NO: 3, SEQ ID NO: 7, SEQ ID NO: 8 и SEQ ID NO: 9.
64А. Способ по любому из пунктов 18A-63A, где указанная экспрессионная кассета дополнительно содержит экзогенную последовательность.
65А. Способ по пункту 23 А, где указанная экзогенная последовательность содержит по меньшей мере 2000 нуклеотидов.
66А. Способ по пункту 23А, где указанная экзогенная последовательность кодирует белок.
67А. Способ по пункту 23А, где указанная экзогенная последовательность кодирует репортерный белок.
68А. Способ по любому из пунктов 18А-26А, где указанная клетка представляет собой клетку насекомого.
69А. ДНК-вектор, полученный способом по любому из пунктов 18А-27А.
70А. ДНК-вектор по пункту 69А, где указанный ДНК-вектор имеет линейную и непрерывную структуру.
71 А. Клетка для получения ДНК-вектора, содержащая: первый полинуклеотид, содержащий: экспрессионную кассету;
модифицированный ITR в начале (на 5'-конце)
экспрессионной кассеты, где указанный модифицированный
ITR содержит полинуклеотид из SEQ ID NO: 52; и
ITR дикого типа в конце (на 3'-конце) экспрессионной кассеты, где указанный ITR дикого типа содержит полинуклеотид из SEQ ID NO: 1; и
второй полинуклеотид, кодирующий белок репликации, выбранный из группы, состоящей из AAV78, AAV52, AAV Rep68 и AAV Rep 40,
при этом указанная клетка не содержит гена, кодирующего капсидный белок AAV.
72А. Клетка по пункту 71А, отличающаяся тем, что указанная клетка представляет собой клетку насекомого.
73А. ДНК-вектор, полученный из клетки по любому из пунктов 29А-50А путем репликации указанного первого полинуклеотида.
74А. Полинуклеотид для получения ДНК-вектора, содержащий:
экспрессионную кассету;
модифицированный ITR в начале (на 5' -конце)
экспрессионной кассеты, где указанный модифицированный
ITR содержит полинуклеотид из SEQ ID NO: 52; и
ITR дикого типа в конце (на 3'-конце) экспрессионной кассеты, где указанный ITR дикого типа содержит полинуклеотид из SEQ ID NO: 1.
75 А. Полинуклеотид по пункту 74А, где указанный полинуклеотид находится в плазмиде, в бакмиде или в бакуловирусе.
76А. Полинуклеотид по любому из пунктов 74А-75А, дополнительно содержащий экзогенную последовательность.
77А. Полинуклеотид по пункту 74А, где указанная экзогенная последовательность содержит по меньшей мере 2000 нуклеотидов.
78А. Полинуклеотид по пункту 74А, где указанная экзогенная последовательность кодирует белок.
79А. Полинуклеотид по пункту 74А, где указанная экзогенная последовательность кодирует репортер
80А. ДНК-вектор, полученный путем репликации полинуклеотида по любому из пунктов 33-39 белком репликации, выбранным из группы, состоящей из AAV78, AAV52, AAV Rep68 и AAV Rep 40, где указанный ДНК-вектор лишен специфического прокариотического метилирования и не заключен в капсидный белок AAV.
81А. ДНК-вектор по пункту 80А, где указанный ДНК-вектор продуцируют в клетке насекомого.
82А. зкДНК-вектор, полученный из плазмиды, содержащей последовательность мутированного ITR AAV из любой из таблиц 2-6 или таблиц 7-10А или 10В.
Согласно некоторым вариантам реализации настоящее изобретение может быть описано любым из следующих пунктов:
1 В. ДНК-вектор, полученный с помощью способа, включающего:
(а) трансфекцию первой популяции клеток насекомых первой рекомбинантной бакмидой, полученной путем транспонирования первой ДНК-плазмидной конструкции в бакуловирусный экспрессионный вектор, причем первая ДНК-плазмидная конструкция содержит последовательно в следующем порядке в едином направлении: первый сайт репликативного белка (RPS-1), промотор, функционально связанный с репортерной последовательностью полинуклеотидов ORF, сигнал посттрансляции и терминации; и второй сайт репликативного белка (RPS-2), где RPS-1 и RPS-2 независимо содержат внутримолекулярные дуплексы и ковалентно соединены, a RPS-1 содержит одну или более делеций, замен или одно или более усечений пар оснований полинуклеотидов относительно RPS-2; а затем извлечение первой популяции клеток насекомых с инъецированным бакуловирусом (BIIC-1);
(b) трансфекцию второй популяции клеток насекомых второй рекомбинантной бакмидой, полученной путем транспонирования второй ДНК-плазмидной конструкции во второй бакуловирусный экспрессионный вектор, причем вторая ДНК-плазмидная конструкция кодирует белок, который связывается по меньшей мере с одним из RPS-1 и RPS-2, а затем извлечение второй популяция клеток насекомых с инъецированным бакуловирусом (BIIC-2);
(c) комбинацию BIIC-1 и BIIC-2 с третьей популяцией клеток насекомых в относительных количествах, обеспечивающих по существу одинаковую множественность заражения (MOI), с последующей инкубацией указанной третьей популяции клеток насекомых, BIIC-1 и BIIC-2 в таких условиях для роста клеток, что белок, кодируемый второй ДНК-плазмидной конструкцией, вступает в реакцию с сайтами RPS-1 и/или RPS-2 для индукции репликации ДНК-вектора, кодируемого первой ДНК-плазмидой, до достижения клеткой насекомого наблюдаемого диаметра приблизительно 15-20 микрометров и жизнеспособности клеток приблизительно 50-80%, с последующим извлечением ДНК из осадков клеток насекомых путем центрифугирования;
(d) экстрагирование ДНК из осадков клеток насекомых с получением продуцированной ДНК из осадков клеток насекомых;
(e) идентификацию ДНК, полученной из осадков клеток насекомых, на нативном геле как в первичной полосе, так и во вторичной полосе на относительном расстоянии друг от друга, указывающем на материал во второй полосе с приблизительно вдвое большей массой относительно материала первичной полосы;
(f) подтверждение присутствия указанного ДНК-вектора в ДНК, полученной из осадков клеток насекомых, на денатурирующем геле, по сдвигу как первичной, и вторичной полос вверх в направлении области меньших масс на геле после расщепления ДНК рестрикционной эндонуклеазой; и
(g) выделение оставшегося ДНК-вектора, полученного из осадков клеток насекомых, с получением высокостабильного ДНК-вектора.
2 В. ДНК-вектор по пункту 1В, где RPS-1 и RPS-2 отличаются и независимо выбраны из последовательности пар полинуклеотидов ДНК из SEQ ID NO: SEQ ID NO: 1 и SEQ ID NO: 52; или SEQ ID NO: 2 и SEQ ID NO: 51; или SEQ ID NO: 101 и SEQ ID NO: 102; или SEQ ID NO: 103 и SEQ ID NO: 104; или SEQ ID NO: 105 и SEQ ID NO: 106; или SEQ ID NO: 107 и SEQ ID NO: 108; или SEQ ID NO: 109 и SEQ ID NO: 110; или SEQ ID NO: 111 и SEQ ID NO: 112; или SEQ ID NO: 113 или SEQ ID NO: 114; и SEQ ID NO: 115 или SEQ ID NO: 116.
Согласно некоторым вариантам реализации настоящее изобретение может быть описано любым из следующих пунктов:
1С. Бескапсидный вектор AAV (cfAAV), содержащий:
экспрессионную кассету, содержащую цис-регуляторный элемент, промотор и экзогенную последовательность; и
две самокомплементарных последовательности, фланкирующие указанную экспрессионную кассету,
причем указанный cfAAV-вектор не ассоциирован с капсидным белком и лишен специфического прокариотического метилирования.
2С. CfAAV-вектор по пункту 1С, где указанные цис-регуляторные элементы выбраны из группы, состоящей из рибо переключателя, инсулятора, миРНК-регулируемого элемента и посттранскрипционного регуляторного элемента.
3С. CfAAV-вектор по любому из пунктов 1С-2С, где указанный ДНК-вектор представляет собой CELiD.
4С. CfAAV-вектор по любому из пунктов 1С-3С, где указанные две самокомплементарных последовательности представляют собой последовательности ITR AAV2.
5С. CfAAV-вектор по любому из пунктов 1С-4С, где указанная экзогенная последовательность содержит участок внутренней посадки рибосомы (IRES) и 2А-элемент.
6С. CfAAV-вектор по пункту 5С, где указанная экспрессионная кассета содержит последовательность, кодирующую более одного белка.
7С. CfAAV-вектор по любому из пунктов 1С-6С, где указанная экспрессионная кассета содержит более чем 4000 нуклеотидов, 5000 нуклеотидов, 10000 нуклеотидов или 20000 нуклеотидов.
8С. Фармакологическая композиция, содержащая cfAAV-вектор по любому из пунктов 1С-7С.
9С. Экспрессионная конструкция, содержащая:
экспрессионную кассету, содержащую цис-регуляторный элемент, промотор и экзогенную последовательность; и две последовательности инвертированных концевых повторов (ITR), фланкирующие указанную экспрессионную кассету,
причем указанная экспрессионная конструкция не содержит открытой рамки считывания, кодирующей капсидный белок.
10С. Экспрессионная конструкция по пункту 9С, отличающаяся тем, что указанные цис-регуляторные элементы выбраны из группы, состоящей из рибопереключателя, инсулятора, миРНК-регулируемого элемента и посттранскрипционного регуляторного элемента.
11С. Экспрессионная кассета по любому из пунктов 9С-10С, отличающаяся тем, что указанная экзогенная последовательность содержит участок внутренней посадки рибосомы (IRES) и 2А-элемент.
12С. Экспрессионная кассета по пункту 11, отличающаяся тем, что указанная экспрессионная кассета содержит последовательность, кодирующую более одного белка.
13С. Экспрессионная конструкция по любому из пунктов 9С-12С, отличающаяся тем, что указанная экспрессионная конструкция находится в плазмиде, в бакмиде или в бакуловирусе.
14С. Способ получения cfAAV-вектора, включающий:
введение экспрессионной конструкции по любому из пунктов 9С-13С в клетку; и
сбор указанного cfAAV-вектора, полученного путем репликации экспрессионной конструкции.
15С. Способ по пункту 14С, дополнительно включающий этап неоднократной репликации экспрессионной конструкции до введения указанной экспрессионной конструкции в клетку.
16С. Способ по пункту 15С, где указанная экспрессионная конструкция находится в плазмиде и этап репликации проводят в Е. coli.
17С. Способ по пункту 16С, дополнительно включающий этап переноса экспрессионной конструкции из плазмиды в бакмиду до введения указанной экспрессионной конструкции в клетку.
18С. Способ по пункту 17С, дополнительно включающий этап переноса экспрессионной конструкции из бакмиды в бакуловирус до введения указанной экспрессионной конструкции в клетку.
19С. Способ по любому из пунктов 14С-18С, дополнительно включающий этап введения белка Rep в клетку.
20С. Способ по любому из пунктов 14С-19С, где указанная клетка представляет собой клетку насекомого.
21С. CfAAV-вектор, полученный с применением способа по любому из пунктов 14С-20C.
22С.CfAAV-вектор по пункту 21С, где указанный ДНК-вектор представляет собой CELiD.
Согласно некоторым вариантам реализации настоящее изобретение может быть описано любым из следующих пунктов:
1D. Бескапсидный невирусный ДНК-вектор, полученный из векторного полинуклеотид а, где указанный векторный полинуклеотид кодирует гетерологичную нуклеиновую кислоту, функционально расположенную между последовательностями ДНК-полинуклеотидов первого и второго инвертированных концевых повторов (ITR) AAV2, при этом по меньшей мере один из ITR содержит по меньшей мере одну полинуклеотидную делению, инсерцию или замену относительно соответствующего ITR AAV2 дикого типа из SEQ ID NO: 1 или SEQ ID NO: 51 для индукции репликации указанного ДНК-вектора в клетке насекомого в присутствии белка Rep, причем указанный ДНК-вектор может быть получен с помощью способа, включающего следующие этапы:
a. инкубация популяции клеток насекомых, несущих указанный векторный полинуклеотид, который не содержит кодирующих последовательностей вирусного капсида, в присутствии белка Rep, в условиях, эффективных для, и на протяжении времени, достаточного для того чтобы индуцировать продуцирование бескапсидной невирусной ДНК в клетках насекомых, причем указанные клетки насекомых не содержат кодирующих вирусный капсид последовательностей; и
b. сбор и выделение бескапсидной невирусной ДНК из клеток насекомых;
причем присутствие бескапсидной невирусной ДНК, выделенной из клеток насекомых, может быть подтверждено путем расщепления ДНК, выделенной из клеток насекомых, рестрикционным ферментом, имеющим один сайт распознавания на ДНК-векторе, и анализа указанного расщепленного ДНК-материала на неденатурирующем геле для подтверждения присутствия характеристических полос линейной и непрерывной ДНК, отличающихся от полос линейной и прерывистой ДНК.
2D. Бескапсидный невирусный ДНК-вектор по пункту 1, где указанный мутированный ITR выбран из группы, состоящей из: SEQ ID NO: 2 и SEQ ID NO: 52.
3D. Бескапсидный невирусный ДНК-вектор по пункту 1, где указанный векторный полинуклеотид содержит пару ITR, выбранную из группы, состоящей из: SEQ ID NO: 1 и SEQ ID NO: 52; и SEQ ID NO: 2 и SEQ ID NO: 51.
4D. Бескапсидный невирусный ДНК-вектор, полученный из векторного полинуклеотида, где указанный векторный полинуклеотид кодирует гетерологичную нуклеиновую кислоту, функционально расположенную между двумя разными последовательностями инвертированных концевых повторов (ITR), причем по меньшей мере один из ITR представляет собой функциональный ITR, содержащий функциональный сайт концевого разрешения и сайт связывания Rep, и один из ITR содержит делецию, инсерцию или замену относительно указанного функционального ITR; присутствие белка Rep индуцирует репликацию указанного векторного полинуклеотида и продуцирование ДНК-вектора в клетке насекомого, причем указанный ДНК-вектор может быть получен с помощью способа, включающего следующие этапы:
a. инкубация популяции клеток насекомых, несущих указанный векторный полинуклеотид, который не содержит кодирующих последовательностей вирусного капсида, в присутствии белка Rep в условиях, эффективных для, и на протяжении времени, достаточного для того чтобы индуцировать продуцирование бескапсидного невирусного ДНК-вектора в клетках насекомых, отличающихся тем, что продуцируемая бескапсидная невирусная ДНК не содержится в указанных клетках насекомых; и
b. сбор и выделение бескапсидной невирусной ДНК из клеток насекомых;
причем присутствие бескапсидной невирусной ДНК, выделенной из клеток насекомых, может быть подтверждено путем расщепления ДНК, выделенной из клеток насекомых, рестрикционным ферментом, имеющим один сайт распознавания на ДНК-векторе, и анализа указанного расщепленного ДНК-материала на неденатурирующем геле для подтверждения присутствия характеристических полос линейной и непрерывной ДНК, отличающихся от полос линейной и прерывистой ДНК.
Согласно некоторым вариантам реализации настоящее изобретение может быть описано любым из следующих пунктов:
1Е. Вектор, содержащий (i) невирусный бескапсидный ДНК-вектор с ковалентно-замкнутыми концами (зкДНК-вектор), где указанный зкДНК-вектор содержит гетерологичную последовательность нуклеиновой кислоты, кодирующую трансген, функционально расположенный между двумя разными последовательностями инвертированных концевых повторов (ITR) AAV, причем один из ITR содержит функциональный сайт концевого разрешения AAV и сайт связывания Rep, и один из ITR содержит делецию, инсерцию или замену относительно другого ITR (модифицированный ITR), причем указанный вектор не заключен в вирусный капсид.
2Е. ЗкДНК-вектор по пункту 1, где указанный зкДНК-вектор при расщеплении рестрикционным ферментом, имеющим один сайт распознавания на указанном зкДНК-векторе, демонстрирует присутствие характеристических полос линейной и непрерывной ДНК, отличающихся от полос линейной и прерывистой контрольной ДНК, при анализе на неденатурирующем геле.
3Е. ЗкДНК-вектор по пункту 1Е, где указанный модифицированный ITR взят из другого серотипа.
4Е. ЗкДНК-вектор по пункту 3Е, где указанный модифицированный ITR не является ITR дикого типа.
5Е. ЗкДНК-вектор по пункту 1Е, где делеция, инсерция или замена происходит по меньшей мере в одной из областей ITR, выбранных из группы, состоящей из А, А', В, В', С, С и D.
6Е. ЗкДНК-вектор по пункту 5Е, где делеция, инсерция или замена приводит к делеции одной из петель, образованных областями А, А', В, В' С или С.
7Е. ЗкДНК-вектор по пункту 1Е, где указанная модификация соответствует изменению в модифицированном ITR AAV2, выбранном из группы, состоящей из SEQ ID NO: 101-498 и 499 или 545-547.
8Е. ЗкДНК-вектор по пункту 1Е, где указанная модификация соответствует изменению в модифицированном ITR AAV2, выбранном из группы, состоящей из SEQ ID NO. 2, 52, 63 и 64.
9Е. ЗкДНК-вектор по пунктам 1Е-8Е, где указанный вектор находится в наноносителе.
10Е. ЗкДНК-вектор по пункту 9Е, где указанный наноноситель содержит липидную наночастицу (ЛНЧ).
11Е. Способ, включающий:
получение невирусной бескапсидной ДНК с ковалентно-замкнутыми концами (зкДНК) с применением векторного полинуклеотид а, где указанный векторный полинуклеотид кодирует гетерологичную нуклеиновую кислоту, функционально расположенную между двумя разными последовательностями инвертированных концевых повторов (ITR), при этом по меньшей мере один из ITR содержит функциональный сайт концевого разрешения и сайт связывания Rep, и один из ITR содержит делецию, инсерцию или замену относительно другого ITR; присутствие белка Rep индуцирует репликацию векторного полинуклеотида и продуцирование ДНК-вектора в клетке насекомого, причем указанный ДНК-вектор может быть получен с помощью способа, включающего следующие этапы:
а. инкубация популяции клеток насекомых, несущих указанный векторный полинуклеотид, который не содержит кодирующих последовательностей вирусного капсида, в присутствии белка Rep в условиях, эффективных для, и на протяжении времени, достаточного для того чтобы индуцировать продуцирование бескапсидного невирусного ДНК-вектора в клетках насекомых, отличающихся тем, что продуцируемая бескапсидная невирусная ДНК не содержится в указанных клетках насекомых; и
b. сбор и выделение бескапсидной невирусной ДНК из клеток насекомых;
причем присутствие бескапсидной невирусной ДНК, выделенной из клеток насекомых, может быть подтверждено путем расщепления ДНК, выделенной из клеток насекомых, рестрикционным ферментом, имеющим один сайт распознавания на ДНК-векторе, и анализа указанного расщепленного ДНК-материала на неденатурирующем геле для подтверждения присутствия характеристических полос линейной и непрерывной ДНК, отличающихся от полос линейной и прерывистой ДНК.
12Е. Бескапсидный невирусный ДНК-вектор, полученный из векторного полинуклеотида, где указанный вектор кодирует гетерологичный ген, функционально расположенный между последовательностями ДНК-полинуклеотидов первого и второго инвертированных концевых повторов (ITR) AAV2, при этом по меньшей мере один из ITR содержит по меньшей мере одну полинуклеотидную делецию, инсерцию или замену относительно соответствующего ITR AAV2 дикого типа из SEQ ID NO: 1 или SEQ ID NO: 51 для индукции репликации указанного ДНК-вектора в клетке насекомого в присутствии белка Rep, причем указанный ДНК-вектор может быть получен с помощью способа, включающего следующие этапы:
(a) инкубация популяции клеток насекомых, несущих указанный векторный полинуклеотид, который не содержит кодирующих последовательностей вирусного капсида, в присутствии белка Rep, в условиях, эффективных для, и на протяжении времени, достаточного для того чтобы индуцировать продуцирование бескапсидной невирусной ДНК в клетках насекомых, причем указанные клетки насекомых не содержат кодирующих вирусный капсид последовательностей; и
(b) сбор и выделение бескапсидной невирусной ДНК из клеток насекомых;
причем присутствие бескапсидной невирусной ДНК, выделенной из клеток насекомых, может быть подтверждено путем расщепления ДНК, выделенной из клеток насекомых, рестрикционным ферментом, имеющим один сайт распознавания на ДНК-векторе, и анализа указанного расщепленного ДНК-материала на неденатурирующем геле для подтверждения присутствия характеристических полос линейной и непрерывной ДНК, отличающихся от полос линейной и прерывистой ДНК.
13Е. Бескапсидный невирусный ДНК-вектор по пункту 12Е, где указанный модифицированный ITR выбран из группы, состоящей из: SEQ ID NO: 2 и SEQ ID NO: 52.
14Е. Бескапсидный невирусный ДНК-вектор по пункту 12Е, где указанный векторный полинуклеотид содержит пару ITR, выбранную из группы, состоящей из: SEQ ID NO: 1 и SEQ ID NO: 52; SEQ ID NO: 2 и SEQ ID NO: 51.
15Е. Бескапсидный невирусный ДНК-вектор, полученный из векторного полинуклеотид а, где указанный векторный полинуклеотид кодирует гетерологичный ген, функционально расположенный между двумя разными последовательностями инвертированных концевых повторов (ITR), причем по меньшей мере один из ITR содержит функциональный сайт концевого разрешения и сайт связывания Rep, и один из ITR содержит делецию, инсерцию или замену, и присутствие белка Rep индуцирует репликацию векторного полинуклеотида и продуцирование ДНК-вектора в клетке насекомого, причем указанный ДНК-вектор может быть получен с помощью способа, включающего следующие этапы:
(a) инкубация популяции клеток насекомых, несущих указанный векторный полинуклеотид, который не содержит кодирующих последовательностей вирусного капсида, в присутствии белка Rep в условиях, эффективных для, и на протяжении времени, достаточного для того чтобы индуцировать продуцирование бескапсидного невирусного ДНК-вектора в клетках насекомых, отличающихся тем, что продуцируемая бескапсидная невирусная ДНК не содержится в указанных клетках насекомых; и
(b) сбор и выделение бескапсидной невирусной ДНК из клеток насекомых;
причем присутствие бескапсидной невирусной ДНК, выделенной из клеток насекомых, может быть подтверждено путем расщепления ДНК, выделенной из клеток насекомых, рестрикционным ферментом, имеющим один сайт распознавания на ДНК-векторе, и анализа указанного расщепленного ДНК-материала на неденатурирующем геле для подтверждения присутствия характеристических полос линейной и непрерывной ДНК, отличающихся от полос линейной и прерывистой ДНК.
17Е. Бескапсидный невирусный ДНК-вектор по пункту 15Е, где один ITR представляет собой дикого типа ITR AAV.
18Е. Способ лечения заболевания у субъекта, при этом указанный способ включает:
совместное введение нуждающемуся в этом субъекту композиции, содержащей (i) невирусный бескапсидный ДНК-вектор с ковалентно-замкнутыми концами (зкДНК-вектор), где указанный зкДНК-вектор содержит гетерологичную последовательность нуклеиновой кислоты, кодирующую трансген, функционально расположенный между двумя разными последовательностями инвертированных концевых повторов (ITR) AAV, причем один из ITR содержит функциональный сайт концевого разрешения AAV и сайт связывания Rep, и один из ITR содержит делению, инсерцию или замену относительно другого ITR.
19Е. Способ по пункту 17Е, где указанный зкДНК-вектор вводят в комбинации с фармацевтически приемлемым носителем.
20Е. Способ доставки терапевтического средства субъекту, при этом указанный способ включает:
введение субъекту композиции, содержащей зкДНК-вектор по пунктам 1Е-10Е и 12Е-16Е.
ПРИМЕРЫ
[00399] Приведенные ниже примеры предназначены для иллюстрации, а не для ограничения.
ПРИМЕР 1: Конструирование зкДНК-векторов
[00400] Описано получение зкДНК-векторов с применением полинуклеотид ной матричной конструкции. Например, полинуклеотидная матричная конструкция, используемая для получения зкДНК-векторов согласно настоящему изобретению, может представлять собой зкДНК-плазмиду, зкДНК-бакмиду и/или зкДНК-бакуловирус. Без ограничения теорией, в пермиссивной клетке-хозяине в присутствии, например, Rep, полинуклеотидная матричная конструкция с двумя ITR и экспрессионной конструкцией, при этом по меньшей мере один из ITR модифицирован, реплицируется с получением зкДНК-векторов. Получение зкДНК-вектора включает два этапа: во-первых, эксцизию («спасение») матрицы из остова матрицы (например, зкДНК-плазмиды, зкДНК-бакмиды, генома зкДНК-бакуловируса и т.п.) посредством белков Rep, и во-вторых, опосредованную Rep репликацию вырезанного зкДНК-вектора.
[00401] Пример способа получения зкДНК-векторов представлен получением из зкДНК-плазмиды согласно описанию в настоящем документе. На фиг.1А и 1В полинуклеотидная матричная конструкция каждой из зкДНК-плазмид включает как левый ITR, так и правый мутированный ITR, между которыми расположены: (i) энхансер/промотор; (ii) сайт клонирования для трансгена; (iii) посттранскрипционный ответный элемент (например, посттранскрипционный регуляторный элемент вируса гепатита сурков (WPRE)); и (iv) сигнал полиаденилирования (например, гена бычьего гормона роста (BGHpA). Также между всеми компонентами вводили уникальные сайты распознавания рестрикционной эндонуклеазой (R1-R6) (представлены на фиг.1А и 1В) для облегчения введения новых генетических компонентов в специфические сайты в указанной конструкции. Сайты для ферментов R3 (PmeI) GTTTAAAC (SEQ ID NO: 7) и R4 (PacI) ТТААТТАА (SEQ ID NO: 542) встраивают в сайт клонирования для введения открытой рамки считывания трансгена. Указанные последовательности клонировали в плазмиду pFastBac НТ В, полученную от ThermoFisher Scientific.
[00402] Вкратце, получали ряд зкДНК-векторов из зкДНК-плазмидных конструкций, приведенных в таблице 12, с применением способа, показанного на фиг. 4А-АС. В таблице 12 указаны номера соответствующих последовательностей полинуклеотидов для каждого компонента, в том числе последовательностей с активностью сайта белка репликации (RPS) (например, сайта связывания Rep) на любом конце промотора, функционально связанного с трансгеном. Номера в таблице 12 относятся к SEQ ID NO в настоящем документе, соответствующим последовательностям каждого компонента.
[00403]
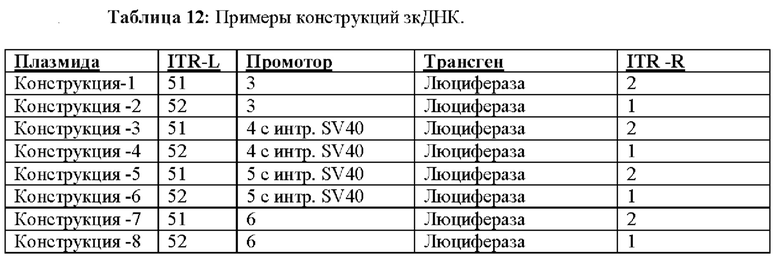
[00404] Согласно некоторым вариантам реализации конструкция для получения зкДНК-векторов содержит промотор, который представляет собой регуляторный переключатель согласно описанию в настоящем документе, например, индуцируемый промотор. Для получения зкДНК-векторов использовали и другие конструкции, например, конструкции 10, 11, 12 и 13 (см., например, таблицу 14А), которые содержат промотор MND или HLCR, функционально связанный с трансгеном люциферазы.
[00405] Получение зкДНК-бакмид:
[00406] Как показано на фиг. 4А, компетентные клетки DH10Bac (MAX EFFICIENCY®
DH10Bac™ Competent Cells, Thermo Fisher) трансформировали либо тестируемыми, либо контрольными плазмидами, следуя протоколу в соответствии с инструкциями производителя. Индуцировали рекомбинацию между плазмидой и бакуловирусным челночным вектором в клетках DH10Bac для получения рекомбинантных зкДНК-бакмид. Рекомбинантные бакмиды отбирали путем скрининга с положительным отбором, основанного на сине-белом скрининге у Е. coli (маркер Ф80dlacZΔM15 обеспечивает α-комплементацию гена β-галактозидазы из бакмидного вектора) на чашке с бактериальным агаром, содержащим X-gal и ИПТГ с антибиотиками для отбора трансформантов, и поддержания бакмиды и плазмид с транспозазой. Белые колонии, появляющиеся в результате транспозиции, которая разрушает β-галактозидный индикаторный ген, собирали и культивировали в 10 мл среды.
[00407] Рекомбинантные зкДНК-бакмиды выделяли из Е. coli и трансфицировали ими клетки насекомых Sf9 или Sf21 с применением FugeneHD для получения инфекционного бакуловируса. Адгезивные клетки насекомых Sf9 или Sf21 культивировали в 50 мл среды в колбах Т25 при 25°С. Через 4 дня культуральную среду (содержащую вирус Р0) отделяли от клеток, фильтровали через фильтр с размером пор 0,45 мкм, отделяя инфекционные бакуловирусные частицы от клеток или клеточного дебриса.
[00408] Необязательно, первую полученную партию бакуловируса (Р0) амплифицировали путем инфицирования интактных клеток насекомых Sf9 или Sf21 в объемах среды от 50 до 500 мл. Клетки поддерживали в суспензионных культурах в инкубаторе с орбитальным шейкером при 130 об/мин при 25°С, проводя мониторинг диаметра и жизнеспособности клеток, до достижения клетками диаметра 18-19 нм (от диаметра интактных клеток 14-15 нм) и плотности ~4,0Е+6 клеток/мл. Через 3-8 дней после инфицирования бакуловирусные частицы Р1 в среде собирали после центрифугирования для удаления клеток и дебриса с последующей фильтрацией через фильтр с размером пор 0,45 мкм.
[00409] Собирали зкДНК-бакуловирус, содержащий тестируемые конструкции, и определяли инфекционную активность, или титр, бакуловируса. В частности, 4×20 мл культур клеток Sf9 с плотностью с плотностью 2.5Е+6 клеток/мл обрабатывали бакуловирусом Р1 в следующих разведениях: 1/1000, 1/10 000, 1/50 000, 1/100000, и инкубировали при 25-27°С. Инфекционность определяли ежедневно на протяжении 45 дней по показателю увеличения диаметра клеток и остановке клеточного цикла, а также изменению жизнеспособности клеток.
[00410] Как показано на фиг. 4А, «Rep-плазмиду» в соответствии с фиг. 8А продуцировали в экспрессионном векторе pFASTBAC™-Dual (ThermoFisher), содержащем как Rep78 (SEQ ID NO: 13) или Rep68 (SEQ ID NO: 12), так и Rep52 (SEQ ID NO: 14) или Rep40 (SEQ ID NO: 11).
[00411] У казанной Rep-плазмидой трансформировали компетентные клетки DH10Bac (MAX EFFICIENCY® DH10Bac™ Competent Cells (Thermo Fisher), следуя предложенному производителем протоколу. Индуцировали рекомбинацию между Rep-плазмидой и бакуловирусным челночным вектором в клетках DH10Bac для получения рекомбинантных бакмид («Rep-бакмид»). Рекомбинантные бакмиды отбирали с применением положительного отбора, который включал сине-белый скрининг на Е. coli (маркер Ф80dlacZΔM15 обеспечивает α-комплементацию гена β-галактозидазы из бакмидного вектора) на чашке с бактериальным агаром, содержащим X-gal и ИПТГ. Выделенные белые колонии извлекали и инокулировали в 10 мл селективной среды (канамицин, гентамицин, тетрациклин в бульоне LB). Рекомбинантные бакмиды (Rep-бакмиды) выделяли из Е. coli и указанными Rep-бакмидами трансфицировали клетки насекомых Sf9 или Sf21 с получением инфекционного бакуловируса.
[00412] Клетки насекомых Sf9 или Sf21 культивировали в 50 мл среды в течение 4 дней, и инфекционный рекомбинантный бакуловирус («Rep-бакуловирус») выделяли из культуры. Необязательно, первое поколение Rep-бакуловируса (Р0) амплифицировали путем инфицирования интактных клеток насекомых Sf9 или Sf21 и культивировали в 50-500 мл среды. Через 3-8 дней после инфицирования бакуловирусные частицы Р1 в среде собирали, отделяя клетки путем центрифугирования или фильтрации, или используя другой способ фракционирования. Собирали Rep-бакуловирус и определяли инфекционную активность бакуловируса. В частности, 4×20 мл культур клеток Sf9 с плотностью 2,5×106 клеток/мл обрабатывали бакуловирусом Р1 в следующих разведениях: 1/1000, 1/10000, 1/50000, 1/100000, и инкубировали. Инфекционность определяли ежедневно на протяжении 4-5 дней по показателю увеличения диаметра клеток и остановке клеточного цикла, а также изменению жизнеспособности клеток.
[00413] Получение и характеризация зкДНК-вектора
[00414] Как показано на фиг. 4В, затем культуральную среду для клеток насекомых Sf9, содержащую либо (1) образец, содержащий зкДНК-бакмиду или зкДНК-бакуловирус, либо (2) Rep-бакуловирус, описанные выше, добавляли в свежую культуру клеток Sf9 (2,5Е+6 клеток/мл, 20 мл) в соотношении 1:1000 и 1:10000, соответственно. Затем клетки культивировали при 130 об/мин при 25°С. Через 4-5 дней после коинфекции детектируют диаметр и жизнеспособность клеток. Когда диаметр клеток достигал 18-20 нм при жизнеспособности ~70-80%, культуры клеток центрифугировали, среду удаляли и собирали клеточные осадки. Клеточные осадки сначала ресуспендировали в подходящем объеме водной среды, либо воды, либо буфера. ЗкДНК-вектор выделяли и очищали от клеток с использованием протокола очищения от Qiagen MIDI PLUS™ (Qiagen, обработка 0,2 мг массы клеточного осадка на колонку).
[00415] Значения выхода для зкДНК-векторов, продуцированных и очищенных из клеток насекомых Sf9, первоначально определяли на основании поглощения УФ при 260 нм. Значения выхода для различных зкДНК-векторов, определенные на основании поглощения УФ, приведены ниже в таблице 13.
[00416]

[00417] Оценка зкДНК-векторов может быть проведена путем идентификации с применением электрофореза на агарозном геле в нативных или денатурирующих условиях, что проиллюстрировано на фиг. 4D, где (а) присутствие характеристических полос, мигрирующих на вдвое большее расстояние на денатурирующих гелях или на нативных гелях после расщепления рестрикционной эндонуклеазой и гель-электрофоретического анализа, и (b) присутствие полос мономера и димера (2×) на денатурирующих гелях для нерасщепленного материала являются характеристическим для присутствия зкДНК-вектора.
[00418] Структуры выделенных зкДНК-векторов дополнительно анализировали путем расщепления ДНК, полученной из ко инфицированных клеток Sf9 (согласно описанию в настоящем документе) рестрикционными эндонуклеазами, выбранными на основании а) присутствия только одного сайта разрезания в зкДНК-векторах, и b) получения итоговых фрагментов, достаточно больших, чтобы быть явно видимыми при фракционировании на 0,8% денатурирующем агарозном геле (>800 п.о.). Как показано на фиг. 4Е, линейные ДНК-векторы с прерывистой структурой и зкДНК-вектор с линейной и непрерывной структурой можно различить по размерам их реакционных продуктов например, ДНК-вектор с прерывистой структурой предположительно дает фрагменты размером 1 т.п.о. и 2 т.п.о., тогда как не заключенный в капсид вектор с непрерывной структурой предположительно дает фрагменты размером 2 т.п.о. и 4 т.п.о.
[00419] Соответственно, чтобы качественным образом продемонстрировать, что выделенные зкДНК-векторы имеют ковалентно замкнутые концы, что требуется по определению, указанные образцы расщепляли рестрикционной эндонуклеазой, идентифицированной в контексте специфической последовательности ДНК-вектора как имеющая единственный сайт рестрикции, предпочтительно, дающей два продукта расщепления неравного размера (например, 1000 п.о. и 2000 п.о.). После расщепления и электрофореза на денатурирующем геле (разделяющем две комплементарные цепи ДНК) линейная ковалентно не замкнутая ДНК будет разделяться на фрагменты размером 1000 п.о. и 2000 п.о., тогда как ковалентно замкнутая ДНК (т.е. ЗкДНК-вектор) будет разделяться на фрагменты вдвое больших размеров (2000 п.о. и 4000 п.о.), поскольку две цепи ДНК соединены, а в данных обстоятельствах развернуты и имеют в два раза большую длину (хотя и являются од но цепочечными). Кроме того, при расщеплении мономерных, димерных и n-мерных форм ДНК-векторов все они будут разделяться на фрагменты одинаковых размеров из-за связывания концов мультимерных ДНК-векторов (см. фиг. 4D).
[00420] На фиг. 5 приведен пример изображения денатурирующего геля со следующими зкДНК-векторами: конструкция-1, конструкция-2, конструкция-3, конструкция-4, конструкция-5, конструкция-6, конструкция-7 и конструкция-8 (все они описаны в таблице 12 выше), с расщеплением (+) или без расщепления (-) эндонуклеазой. Каждый зкДНК-вектор из конструкций 1-8 давал две полосы (*) после реакции с эндонуклеазой. Размеры их фрагментов в двух полосах, определенные по маркеру размера, приведены в нижней части изображения. Размеры полос подтверждают, что каждый из зкДНК-векторов, продуцированных с плазмид, содержащих конструкцию 18, имеет непрерывную структуру.
[00421] В настоящем документе выражение «анализ для идентификации ДНК-векторов путем электрофореза на агарозном геле в условиях нативного и денатурирующего геля» относится к анализу для оценки наличия замкнутых концов зкДНК путем проведения расщепления рестрикционной эндонуклеазой с последующей электрофоретической оценкой продуктов расщепления. Один пример такого анализа приведен ниже, хотя специалисту в данной области техники будет понятно, что возможны многие известные в данной области техники варианты указанного примера. Рестрикционную эндонуклеазу выбирают таким образом, чтобы она представляла собой фермент, разрезающий представляющий интерес зкДНК-вектор в одном месте, что дает продукты с длиной, составляющей приблизительно 1/3 × и 2/3 × длины ДНК-вектора. Это обеспечивает разделение на полосы как на нативном, так и на денатурирующем геле. Перед денатурацией важно удалить из образца буфер. Набор для очищения продуктов ПНР от Qiagen PCR или обессоливающие «центрифужные колонки», например, колонки от GE HEALTHCARE ILUSTRA™ MICROSPIN™ G-25, представляют собой некоторые известные в данной области техники варианты расщепления эндонуклеазами. Указанный анализ включает например, i) расщепление ДНК подходящей рестрикционной эндонуклеазой (или эндонуклеазами), 2) применение, например, набора для очищения продуктов ПНР от Qiagen, элюирование дистиллированной водой, iii) добавление 10× денатурирующего раствора (10×=0,5 М NaOH, 10 мМ ЭДТК), добавление 10Х красителя, не забуференного, и анализ вместе с ДНК-лэддерами, полученными путем добавления 10Х денатурирующего раствора в 4×, на 0,8-1,0% геле, ранее инкубированном с 1 мМ ЭДТК и 200 мМ NaOH, чтобы обеспечить однородность концентрации NaOH в геле и гелевой камере, и осуществляют прогонку геля в присутствии 1× денатурирующего раствора (50 мМ NaOH, 1 мМ ЭДТК). Специалисту в данной области техники будет понятно, какое напряжение использовать для проведения электрофореза в зависимости от размеров и требуемого времени получения результатов. После электрофореза гели осушают и нейтрализуют в 1× ТВЕ или ТАЕ, переносят в дистиллированную воду или 1× ТВЕ/ТАЕ с 1× SYBR Gold. Затем полосы могут быть визуализированы, например, с применением красителя от Thermo Fisher, SYBR® Gold Nucleic Acid Gel Stain (10 000X концентрат в ДМСО) и эпифлуоресцентный свет (синий) или УФ (312 нм).
[00422] Оценка чистоты полученного зкДНК-вектора может быть проведена с применением любого известного в данной области техники способа. Согласно одному неограничивающему примеру способа вклад зкДНК-плазмиды в общее поглощение УФ образцом может быть рассчитан путем сравнения интенсивности флуоресцентности зкДНК-вектора и стандарта. Например, если, на основании поглощения УФ, на гель было загружено 4 мкг зкДНК-вектора, и интенсивность флуоресцентности зкДНК-вектора эквивалентна полосе 2 т.п.о. с известной массой 1 мкг, значит, имеется 1 мкг зкДНК-вектора, и зкДНК-вектор составляет 25% от общего количества поглощающего УФ материала. Затем строят график зависимости интенсивности полосы на геле от вычисленного введенного количества, которому соответствует полоса - например, если длина всего зкДНК-вектора 8 т.п.о., а вырезанная сравнительная полоса соответствует 2 т.п.о., интенсивность полосы на графике будет составлять 25% от общего введенного количества, что в указанном случае составит 0,25 мкг для введенных 1,0 мкг. С использованием разведении несущей зкДНК-вектор плазмиды для построения стандартной кривой получают уравнение линии регрессии, которое затем используют для вычисления количества указанного зкДНК-вектора в соответствующей полосе, которое затем можно использовать для определения процента от общего введенного количества зкДНК-вектора, или процента чистоты.
ПРИМЕР 2: Продуцирование вирусной ДНК в зкДНК-клетках
[00423] Также зкДНК-векторы получали с конструкций 11, 12, 13 и 14, приведенных в таблице 14А. ЗкДНК-плазмиды, содержащие конструкции 11-14, получали с применением способов молекулярного клонирования, хорошо известных в данной области техники. Плазмиды в таблице 14А конструировали с последовательностью WPRE, включающей SEQ ID NO: 8, за которым следовала BGHpA, включающая SEQ ID NO: 9, в нетранслируемой 3'-области между трансгеном и правым ITR.
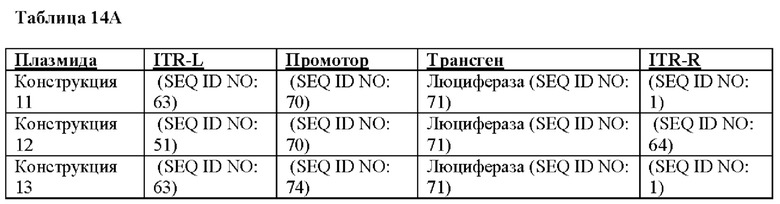

[00424] Остов вектора для конструкций 11-14 содержит: (i) асимметричный ITR-MND-люцифераза-wPPE-ВСН-поли(А)-ITR в pFB-HTb (конструкция 11), (ii) ITR-MND-люцифераза-wPPE-ВСН-поли(А)-асимметричный ITR в pFB-HTb (конструкция 12), (iii) асимметричный ITR-HLCR-AAT-luc-wPRE(O BGH-поли(А-ITR в pFB-HTb (конструкция 13); и ITP-HLCR-ААТ-1uc-wPRE(O-BGH-поли(А)-асимметричный ITR в pFB-HTb (конструкция 14); каждая конструкция содержит по меньшей мере один ITR, асимметричный относительно другого ITR. Указанные конструкции также содержат одну или более из следующих последовательностей: последовательность wPREO (SEQ ID NO: 72) и BGH-поли(А) (SEQ ID NO: 73), или последовательности, по меньшей мере на 85%, или по меньшей мере на 90%, или по меньшей мере на 95% идентичные указанным.
[00425] Далее проводили продуцирование зкДНК-вектора выполняли в соответствии с процедурой на фиг. 4А-4С, например, (а) получение рекомбинантной зкДНК-бакмидной ДНК и трансфекция клетки насекомого рекомбинантной зкДНК-бакмидной ДНК; (b) получение стокового раствора Р1 (низкий титр), стокового раствора Р2 (высокий титр), и определение титра вируса с применением количественной ПЦР для получения 5 мл раствора для доставки, содержащего >1Е+7 бляшкообразующих или инфекционных единиц «БОЕ» на мл стокового раствора BV, BV Stock СОА Выделение зкДНК-вектора проводили путем коинфицирования 50 мл клеток насекомых стоковым раствором BV с получением следующих вариантов парной инфекции: Rep-бакмида согласно описанию в настоящем документе и по меньшей мере одна из следующих конструкций: конструкция 11, конструкция 12, конструкция 13 и конструкция 14. Выделение зкДНК-вектора проводили с применением набора QIAGEN Plasmid Midi Kit с получением очищенного ДНК-материала для дополнительного анализа. В таблице 14В и таблице 14С приведены значения выхода (по результатам детекции OD) зкДНК-вектора, продуцированного с конструкций 11-14.
[00426]

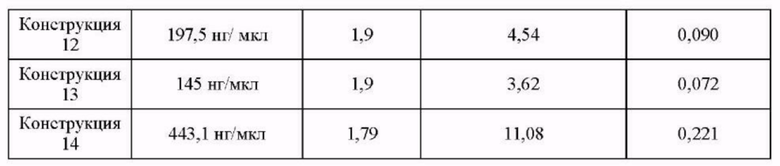
[00427]

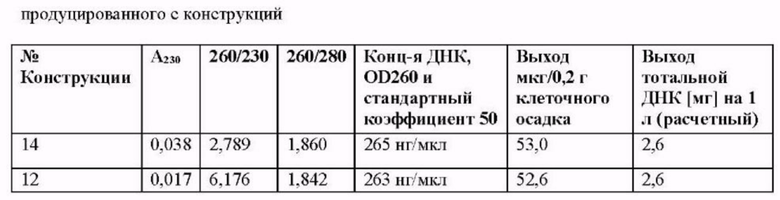
[00428] В таблице 14С приведено количество ДНК-материала, полученного (по результатам детекции OD) с применением конструкций 12 и 14 из таблицы 14С. Выход тотального ДНК-материала был приемлемым по сравнению с типичный выходами, составляющими приблизительно 3 мг/л ДНК-материала в способе из примера 1 (таблица 13) выше.
ПРИМЕР 3: зкДНК-векторы экспрессируют трансген люциферазы in vitro
[00429] Получали конструкции путем введения открытой рамки считывания, кодирующей репортерный ген люциферазы, в сайт клонирования зкДНК-плазмидных конструкций: конструкции-1, конструкции-3, конструкции-5 и конструкции-7. ЗкДНК-плазмиды (см. выше в таблице 12), включающие кодирующую последовательность люциферазы, называют плазмидной конструкцией 1-Luc, плазмидной конструкцией-3-Luc, плазмидной конструкцией-5-Luc и плазмидной конструкцией 7-Luc, соответственно.
[00430] Клетки HEK293 культивировали и трансфицировали 100 нг, 200 нг или 400 нг плазмидных конструкций 1, 3, 5 и 7, с применением FUGENE® (Promega Corp.) в качестве агента для трансфекции. Экспрессию люциферазы с каждой из плазмид определяли на основании активности люциферазы в каждой культуре клеток; результаты приведены на фиг. 6А. Активность люциферазы не детектировалась в необработанных контрольных клетках («необработанных») или клетках, обработанных Fugene по отдельности («Fugene»), что подтверждает, что активность люциферазы является результатом генной экспрессии с плазмид. Как показано на фиг. 6А и фиг. 6В, была детектирована устойчивая экспрессия люциферазы с конструкций 1 и 7. При экспрессии люциферазы с конструкции-? детектировалось дозозависимое увеличение активности люциферазы.
[00431] Рост и жизнеспособность клеток, трансфицированных каждой из плазмид, также были определены и представлены на фиг. 7А и фиг. 7В. Рост и жизнеспособность трансфицированных клеток значимо не отличались в разных группах клеток, обработанных разными конструкциями.
[00432] Соответственно, активность люциферазы, измеренная в каждой группе и нормированная по росту и жизнеспособности клеток, не отличалась от активности люциферазы без нормирования. ЗкДНК-плазмида с конструкцией 1-Luc демонстрировала наиболее устойчивую экспрессию люциферазы, с нормированием или без нормирования.
[00433] Соответственно, данные, представленные на фиг. 6А, 6В, 7А и 7В, демонстрируют, что конструкция 1, содержащая в направлении от 5' к 3'- WT-ITR (SEQ ID NO: 51), промотор CAG (SEQ ID NO: 3), сайт клонирования R3/R4 (SEQ ID NO: 7), WPRE (SEQ ID NO: 8), BGHpA (SEQ ID NO: 9) и модифицированный ITR (SEQ ID NO: 2), эффективно продуцирует зкДНК-вектор, который может экспрессировать белок трансгена, входящего в состав указанного зкДНК-вектора.
ПРИМЕР 4: Экспрессия трансгенного белка люциферазы с зкДНК-векторов in vivo.
[00434] Оценивают экспрессию продуцируемого с описанных выше конструкций 1-8 трансгенного белка с зкДНК-векторов in vivo у мышей. Тестировали зкДНК-вектор, полученный из зкДНК-плазмидной конструкции 1 (согласно описанию в таблице 12), и была продемонстрирована продолжительная и стойкая трансгенная экспрессия люциферазы в модели на мышах после гидродинамической инъекции зкДНК-конструкции без липосом, повторного дозирования (на 28 день) и стойкость (до 42 дня) зкДНК экзогенной люциферазы светлячков. В других экспериментах оценивают экспрессию люциферазы с выбранных зкДНК-векторов in vivo, при этом зкДНК-векторы содержат трансген люциферазы и по меньшей мере один модифицированный ITR, выбранный из любых приведенных в таблицах 10А-10В, или ITR, содержащий по меньшей мере одну из последовательностей, показанных на фиг. 26А-26В.
[00435] Экспрессия люциферазы in vivo: самцам мышей CD-1 IGS возрастом 5-7 недель (Charles River Laboratories) вводят 0,35 мг/кг зкДНК-вектора, экспрессирующего люциферазу, в объеме 1,2 мл посредством в/в гидродинамического введения в хвостовую вену на день 0. Экспрессию люциферазы оценивают с помощью визуализации IVIS на 3, 4, 7, 14, 21, 28, 31, 35 и 42 день. Вкратце, мышам внутрибрюшинно инъецируют 150 мг/кг субстрата люциферина, а затем оценивают люминесценцию всего тела с помощью визуализации IVIS®.
[00436] Визуализацию IVIS осуществляют на 3 день, 4 день, 7 день, 14 день, 21 день, 28 день, 31 день, 35 день и 42 день, и собранные органы визуализируют ex vivo после умерщвления на 42 день.
[00437] На протяжении исследования животных ежедневно взвешивают и проводят мониторинг общего состояния здоровья и самочувствия. При умерщвлении кровь каждого животного собирают путем терминальной пункции сердца, разделяют на два части и обрабатывают для получения 1) плазмы и 2) сыворотки; плазму мгновенно замораживают, а сыворотку используют для панели анализов на ферменты печени, после чего мгновенно замораживают. Кроме того, собирают печень, селезенки, почки и паховые лимфатические узлы (ЛУ) и визуализируют ех vivo с применением IVIS.
[00438] Экспрессию люциферазы в печени оценивают с применением набора для ИФА ELISA на люциферазу MAXDISCOVERY® (BIOO Scientific/PerkmElmer), кПЦР на люциферазу в образцах печени, гистопатологического анализа образцов печени и/или панели анализов на ферменты печени в сыворотке (VetScanVS2; Abaxis Preventative Care Profile Plus).
ПРИМЕР 5: Прогонный скрининг мутантных ITR
[00439] Проводили дополнительные анализы взаимосвязей структуры ITR и образования зкДНК. Конструировали ряд мутантов для оценки влияния специфических структурных изменений на образование зкДНК и способность экспрессировать закодированный в зкДНК трансген. Конструирование мутантов, анализ образования зкДНК и оценка трансгенной экспрессии зкДНК в культуре клеток человека более подробно описаны ниже.
А. Конструирование мутантных ITR
[00440] Библиотеку из 31 плазмиды с кассетами уникальных асимметричных мутантных ITR AAV типа II разрабатывали in silico, a затем проводили оценку в клетках насекомых Sf9 и клетках эмбриональной почки человека (HEK293). Каждая ITR-кассета содержала репортерный ген либо люциферазы (LUC), либо зеленого флуоресцентного белка (GFP), управляемый последовательностью промотора р10 для экспрессии в клетках насекомых, и последовательностью промотора CAG для экспрессии в клетках млекопитающих. Создавали мутации в последовательности ITR в области либо правого, либо левого ITR. Указанная библиотека содержала 15 правосторонних (RS) и 16 левосторонних (LS) мутантов, представленных в таблице 10А и 10В и на фиг. 26А и 26В в настоящем документе.
[00441] Суспензионные культуры Sf9 поддерживали на среде Sf900 III (Gibco) в вентилируемых колбах для тканевых культур 200 мл. Культуры пересевали каждые 48 часов, количество клеток и метрики роста определяли до каждого пересева с применением счетчика ViCell (Beckman Coulter). Культуры поддерживали при встряхивании (окружность 1'', 130 об/мин) при 27°С. Адгезивные культуры клеток HEK293 поддерживали на GlutiMax DMEM (среда Игла, модифицированная по Дульбекко, Gibco) с 1% фетальной бычьей сыворотки и 1% PenStrep в культуральных колбах объемом 250 мл при 37°С и 5% CO2. Культуры трипсинизировали и пересевали каждые 96 часов. Для каждого пересева использовали разведение 1:10 из колбы с 90-100% конфлюентностью.
[00442] ЗкДНК-векторы получали и конструировали согласно описанию в примере 1 выше. Вкратце, как видно на фиг. 4В, клетки Sf9 трансдуцированные плазмидными конструкциями, оставляли для адгезивного роста в течение 24 часов в стационарных условиях при 27°С. Через 24 часа трансфицированные клетки Sf9 инфицировали Rep-вектором из инфицированных бакуловирусом клеток насекомых (BIIC). Ранее была охарактеризована инфекционность BIIC, и их использовали в конечном разведении 1:2000. BIIC, разведенные 1:100 в среде для клеток насекомых Sf900 добавляли в каждую лунку с ранее трансфицированными клетками. BIIC без вектора Rep добавляли в подгруппу лунок в качестве отрицательного контроля. Содержимое планшетов перемешивали путем аккуратного встряхивания на планшетной качалке в течение 2 минут. Затем клетки культивировали в течение дополнительных 48 часов при 27°С в стационарных условиях. Все экспериментальные конструкции и контроли анализировали в трех повторах.
[00443] Через 48 часов 96-луночный планшет извлекали из инкубатора, оставляли на непродолжительное время для уравновешивания до комнатной температуры, и анализировали на экспрессию люциферазы (люциферазный анализ OneGlo (Promega Corporation)). Полную люминесценцию измеряли с помощью микропланшетного ридера SpectraMax M Series. Результаты для репликатов усредняли. Результаты приведены на фиг. 27. Как и ожидалось, три отрицательных контроля (только среда, ложная трансфекция без донорной ДНК; и образец, который обрабатывали в отсутствие клеток с Rep-содержащим бакуловирусом) не демонстрировали значимой экспрессии люциферазы. Устойчивая экспрессия люциферазы наблюдалась в каждом из мутантных образцов, указывая на успешную трансфекцию и экспрессию закодированного в зкДНК трансгена для каждого образца независимо от мутации.
В. Анализ образования зкДНК
[00444] Чтобы подтвердить, что полученная в ходе предшествующего исследования зкДНК имеет ожидаемую структуру с замкнутыми концами, проводили эксперименты для получения достаточных количеств каждой зкДНК, которую затем можно было бы протестировать на наличие надлежащей структуры. Вкратце, суспензионные культуры Sf9 трансфицировали ДНК из одной плазмиды с мутантными ITR из библиотеки. Культуры высевали с плотностью 1,25×106 клеток/мл в культуральные колбы Эрленмейера с ограниченным газообменом. ДНК: липидные комплексы для трансфекции получали с использованием реагента для трансфекции fuGene в соответствии с инструкциями производителя. Получали сложные смеси и инкубировали согласно приведенному ранее описанию для планшетного анализа люциферазы, с увеличением объемов пропорционально числу трансфицированных клеток, как и в анализе с репортерными генами, использовали отношение 4,5:1 (объем реагента/масса ДНК). Параллельно с экспериментальными культурами получали ложнотрансфицированные (только реагенты для трансфекции) и необработанные культуры для контрольного роста. После добавления реагентов для трансфекции культуры оставляли для восстановления на 10-15 минут при комнатной температуре с аккуратным перемешиванием, после чего переносили в инкубатор со встряхиванием с температурой 27°С. Через 24 часа инкубации со встряхиванием во всех колбах (экспериментальных и контрольных) определяли количество клеток и метрики роста с помощью счетчика ViCell (Beckman Coulter). Все колбы (кроме контроля роста) инфицировали содержащими Rep-вектор BIIC в конечном разведении 1:5000. Также получали положительный контроль с применением установленной для получения зкДНК процедуры двойного инфицирования BIIC. Культуру с двойной инфекцией высевали, используя число клеток, равное среднему числу жизнеспособных клеток во всех экспериментальных культурах. Контроль с двойной инфекцией был инфицирован несущими Rep и репортерный ген BIIC в конечном разведении 1:5000 для каждой конструкции, соответственно. После инфицирования культуры возвращали в инкубатор в ранее описанных условиях со встряхиванием. Количество клеток, метрики роста и жизнеспособности определяли ежедневно во всех колбах в течение 3 дней после инфицирования. Измерения в точке времени Т=0 проводили после восстановления только что инфицированных культур в течение ~2 часов в инкубаторе со встряхиванием. Через 3 дня клетки собирали путем центрифугирования в течение 15 минут. Супернатант утилизировали, массу осадка регистрировали и замораживали осадок до -80°С до экстракции ДНК.
[00445] Предполагаемые неочищенные зкДНК экстрагировали из всех колб (экспериментальных и контрольных) с применением набора для очищения Qiagen Plasmid Plus Midi Purification kit (Qiagen) в соответствии с «высокопродуктивным» протоколом производителя. Элюаты количественно определяли на основании оптической плотности, измеренной на NanoDrop OneC (ThermoFisher). Полученные экстракты зкДНК хранили при 4°С.
[00446] Вышеописанные экстракты зкДНК проводили по нативному агарозному (1% агарозы, 1× ТАЕ-буфер) гелю, содержащему 1:10000 разведение красителя SYBR Safe Gel Stain (ThermoFisher Scientific) наряду с лэддером Tracldt 1 Kb Plus DNA Ladder. Затем гель визуализировали с применением Gbox Mini Imager в УФ/синем освещении. Согласно приведенному ранее описанию, ожидаются две первичные полосы для образцов зкДНК, проведенных через нативные гели: полоса ~5,500 п. о., соответствующая мономерной форме, и полоса ~11000 п. о., соответствующая димерной форме. Все мутантные образцы были протестированы, и все демонстрировали ожидаемые полосы мономера и димера на нативных агарозных гелях. Результаты для репрезентативного образца мутантов показаны на фиг. 28. Предполагаемые неочищенные ITR-мутантные зкДНК и контрольные экстракты, полученные в ходе мелкомасштабного производства, дополнительно анализировали с применением сопряженных продуктов расщепления рестриктазой и денатурирующего агарозного геля для подтверждения двуцепочечной структуры ДНК, отличительной для зкДНК. Каждый мутант зкДНК, как ожидается, имеет единственный сайт рестрикции EcoR1, таким образом, если он образован корректно, то будет давать два характеристических фрагмента после расщепления EcoR1. Высокоточную рестрикционную эндонуклеазу EcoR1 (New England Biolabs) использовали для расщепления экстракта предполагаемой зкДНК в соответствии с инструкциями изготовителя. Экстракты ложнотрансфицированных и ростовых контролей не анализировали, поскольку спектрофотометрическое количественное определение с использованием NanoDrop (ThermoFisher), а также анализ на нативном агарозном геле показали отсутствие детектируемого зкДНК/плазмидоподобного продукта в элюатах. Расщепленный материал очищали с применением набора Qiagen PCR Clean-up Kit (Qiagen) в соответствии с инструкциями производителя, за исключением того, что очищенный расщепленный материал элюировали в не содержащей нуклеаз воде вместо элюирующего буфера от Qiagen. Щелочной агарозный гель (0,8% щелочной агарозы) уравновешивали в уравновешивающем буфера (1 мМ ЭДГК, 200 мМ NaOH) в течение ночи при 4°С. 10× денатурирующий раствор (50 мМ NaOH, 1 мМ ЭДГК) добавляли в образцы очищенных расщепленных зкДНК и соответствующей нерасщепленной зкДНК (в общей сложности 1 мкг), и нагревали образцы при 65°С в течение 10 минут. В каждый денатурированный образец добавляли 10× нагрузочный краситель (бромфеноловый синий, 50% глицерин) и перемешивали. Также на гель загружали лэддер Tracldt 1kb Plus DNA Ladder (ThermoFisher Scientific) в качестве референсного образца. Прогонку по гелю проводили в течение ~18 часов при 4°С и постоянном напряжении (25 В) с последующим промыванием деионизиро ванной H2O и нейтрализацией в 1×TAE-буфере (Tris-ацетат, ЭДТК), рН 7,6, в течение 20 минут при аккуратном встряхивании. Затем гель переносили в раствор 1× ТАЕ/ 1× SYBR Gold и оставляли на ~1 час при аккуратном встряхивании. Затем гель визуализировали с применением Gbox Mini Imager (Syngene) в Уф/синем освещении. Ожидалось, что неразрезанные денатурированные образцы будут мигрировать как фрагменты ~11000 п.о., а обработанные EcoR1 образцы будут давать две полосы, одну для ~4000 п.о., а другую для ~6000 п.о.
[00447] Все мутантные образцы давали аналогичные результаты в указанном эксперименте. На каждой дорожке для образцов были видны две значимые полосы в случае обработанных EcoR1 образцов, мигрирующих на денатурирующем геле как фрагменты ожидаемых размеров, резко отличающихся от нерасщепленных мутантных образцов, которые мигрировали как фрагменты ожидаемого размера ~11000 п.о. На фиг. 27 приведены результаты для репрезентативного образца мутантов, где для каждого расщепленного мутантного образца видны две полосы со значениями выше фоновых, в отличие от единственной полосы, видимой в случае нерасщепленных мутантных образцов. Таким образом, мутантные образцы, по-видимому, корректно образуют зкДНК.
С. Функциональная экспрессия в культуре клеток млекопитающих
[00448] Для оценки функциональности зкДНК с мутантными ITR, полученной в результате процесса мелкомасштабного производства, клетки HEK293 трансфицировали несколькими репрезентативными образцами мутантной зкДНК. Активно делящиеся клетки HEK293 высевали в 96-луночные микротитрационные планшеты с плотностью 3×106 клеток на лунку (80% конфлюэнтность) и инкубировали в течение 24 часов в описанных ранее условиях для адгезивных культур HEK293. Через 24 часа проводили трансфекцию 200 нг тотальной неочищенной зкДНК, полученной в ходе мелкомасштабного производства, с применением липофектамина (Invitrogen, TheromoFisher Scientific). Комплексы для трансфекции получали в соответствии с инструкциями производителя; для трансфекции ранее высеянных клеток HEK293 использовали общий объем 10 мкл комплекса для трансфекции. Все экспериментальные конструкции и контроли анализировали в трех повторах. Трансфицированные клетки инкубировали в ранее описанных условиях в течение 72 часов. Через 72 часа 96-луночный планшет извлекали из инкубатора и оставляли на непродолжительное время для уравновешивания до комнатной температуры. Проводили люциферазный анализ OneGlo. После 10 минут обработки на орбитальном шейкере измеряли полную люминесценцию с применением микропланшетного ридера SpectraMax M Series. Результаты для репликатов усредняли. Результаты приведены на фиг. 30. Каждый из протестированных мутантных образцов экспрессировал люциферазу в культуре клеток человека, что указывает на корректное образование и экспрессию зкДНК для каждого образца в контексте клеток человека.
[00449] источники.
[00450] Все источники, перечисленные и раскрытые в настоящем описании и примерах, в том числе патенты, патентные заявки, международные патентные заявки и публикации, включены в настоящий документ полностью посредством ссылок.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> GENERATION BIO INC./ДЖЕНЕРЕЙШЕН БИО ИНК.
<120> MODIFIED CLOSED-ENDED DNA (CEDNA)/
МОДИФИЦИРОВАННАЯ ДНК С ЗАМКНУТЫМИ КОНЦАМИ (ЗКДНК)
<130> 080170-090580WOPT
<140>
<141>
<150> 62/556335
<151> 2017-09-08
<150> 62/556281
<151> 2017-09-08
<150> 62/556319
<151> 2017-09-08
<150> 62/556324
<151> 2017-09-08
<150> 62/556329
<151> 2017-09-08
<150> 62/556331
<151> 2017-09-08
<160> 557
<170> PatentIn, версия 3.5
<210> 1
<211> 141
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 1
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgacc aaaggtcgcc cgacgcccgg gctttgcccg ggcggcctca gtgagcgagc 120
gagcgcgcag ctgcctgcag g 141
<210> 2
<211> 130
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 2
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgacc aaaggtcgcc cgacgcccgg gcggcctcag tgagcgagcg agcgcgcagc 120
tgcctgcagg 130
<210> 3
<211> 1923
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 3
tcaatattgg ccattagcca tattattcat tggttatata gcataaatca atattggcta 60
ttggccattg catacgttgt atctatatca taatatgtac atttatattg gctcatgtcc 120
aatatgaccg ccatgttggc attgattatt gactagttat taatagtaat caattacggg 180
gtcattagtt catagcccat atatggagtt ccgcgttaca taacttacgg taaatggccc 240
gcctggctga ccgcccaacg acccccgccc attgacgtca ataatgacgt atgttcccat 300
agtaacgcca atagggactt tccattgacg tcaatgggtg gagtatttac ggtaaactgc 360
ccacttggca gtacatcaag tgtatcatat gccaagtccg ccccctattg acgtcaatga 420
cggtaaatgg cccgcctggc attatgccca gtacatgacc ttacgggact ttcctacttg 480
gcagtacatc tacgtattag tcatcgctat taccatggtc gaggtgagcc ccacgttctg 540
cttcactctc cccatctccc ccccctcccc acccccaatt ttgtatttat ttatttttta 600
attattttgt gcagcgatgg gggcgggggg gggggggggg cgcgcgccag gcggggcggg 660
gcggggcgag gggcggggcg gggcgaggcg gagaggtgcg gcggcagcca atcagagcgg 720
cgcgctccga aagtttcctt ttatggcgag gcggcggcgg cggcggccct ataaaaagcg 780
aagcgcgcgg cgggcgggag tcgctgcgac gctgccttcg ccccgtgccc cgctccgccg 840
ccgcctcgcg ccgcccgccc cggctctgac tgaccgcgtt actcccacag gtgagcgggc 900
gggacggccc ttctcctccg ggctgtaatt agcgcttggt ttaatgacgg cttgtttctt 960
ttctgtggct gcgtgaaagc cttgaggggc tccgggaggg ccctttgtgc gggggggagc 1020
ggctcggggg gtgcgtgcgt gtgtgtgtgc gtggggagcg ccgcgtgcgg cccgcgctgc 1080
ccggcggctg tgagcgctgc gggcgcggcg cggggctttg tgcgctccgc agtgtgcgcg 1140
aggggagcgc ggccgggggc ggtgccccgc ggtgcggggg gggctgcgag gggaacaaag 1200
gctgcgtgcg gggtgtgtgc gtgggggggt gagcaggggg tgtgggcgcg gcggtcgggc 1260
tgtaaccccc ccctgcaccc ccctccccga gttgctgagc acggcccggc ttcgggtgcg 1320
gggctccgta cggggcgtgg cgcggggctc gccgtgccgg gcggggggtg gcggcaggtg 1380
ggggtgccgg gcggggcggg gccgcctcgg gccggggagg gctcggggga ggggcgcggc 1440
ggcccccgga gcgccggcgg ctgtcgaggc gcggcgagcc gcagccattg ccttttatgg 1500
taatcgtgcg agagggcgca gggacttcct ttgtcccaaa tctgtgcgga gccgaaatct 1560
gggaggcgcc gccgcacccc ctctagcggg cgcggggcga agcggtgcgg cgccggcagg 1620
aaggaaatgg gcggggaggg ccttcgtgcg tcgccgcgcc gccgtcccct tctccctctc 1680
cagcctcggg gctgtccgcg gggggacggc tgccttcggg ggggacgggg cagggcgggg 1740
ttcggcttct ggcgtgtgac cggcggctct agagcctctg ctaaccatgt tttagccttc 1800
ttctttttcc tacagctcct gggcaacgtg ctggttattg tgctgtctca tcatttgtcg 1860
acagaattcc tcgaagatcc gaaggggttc aagcttggca ttccggtact gttggtaaag 1920
cca 1923
<210> 4
<211> 1272
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 4
aggctcagag gcacacagga gtttctgggc tcaccctgcc cccttccaac ccctcagttc 60
ccatcctcca gcagctgttt gtgtgctgcc tctgaagtcc acactgaaca aacttcagcc 120
tactcatgtc cctaaaatgg gcaaacattg caagcagcaa acagcaaaca cacagccctc 180
cctgcctgct gaccttggag ctggggcaga ggtcagagac ctctctgggc ccatgccacc 240
tccaacatcc actcgacccc ttggaatttc ggtggagagg agcagaggtt gtcctggcgt 300
ggtttaggta gtgtgagagg gtccgggttc aaaaccactt gctgggtggg gagtcgtcag 360
taagtggcta tgccccgacc ccgaagcctg tttccccatc tgtacaatgg aaatgataaa 420
gacgcccatc tgatagggtt tttgtggcaa ataaacattt ggtttttttg ttttgttttg 480
ttttgttttt tgagatggag gtttgctctg tcgcccaggc tggagtgcag tgacacaatc 540
tcatctcacc acaaccttcc cctgcctcag cctcccaagt agctgggatt acaagcatgt 600
gccaccacac ctggctaatt ttctattttt agtagagacg ggtttctcca tgttggtcag 660
cctcagcctc ccaagtaact gggattacag gcctgtgcca ccacacccgg ctaatttttt 720
ctatttttga cagggacggg gtttcaccat gttggtcagg ctggtctaga ggtaccggat 780
cttgctacca gtggaacagc cactaaggat tctgcagtga gagcagaggg ccagctaagt 840
ggtactctcc cagagactgt ctgactcacg ccaccccctc caccttggac acaggacgct 900
gtggtttctg agccaggtac aatgactcct ttcggtaagt gcagtggaag ctgtacactg 960
cccaggcaaa gcgtccgggc agcgtaggcg ggcgactcag atcccagcca gtggacttag 1020
cccctgtttg ctcctccgat aactggggtg accttggtta atattcacca gcagcctccc 1080
ccgttgcccc tctggatcca ctgcttaaat acggacgagg acagggccct gtctcctcag 1140
cttcaggcac caccactgac ctgggacagt gaatccggac tctaaggtaa atataaaatt 1200
tttaagtgta taatgtgtta aactactgat tctaattgtt tctctctttt agattccaac 1260
ctttggaact ga 1272
<210> 5
<211> 547
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 5
ccctaaaatg ggcaaacatt gcaagcagca aacagcaaac acacagccct ccctgcctgc 60
tgaccttgga gctggggcag aggtcagaga cctctctggg cccatgccac ctccaacatc 120
cactcgaccc cttggaattt ttcggtggag aggagcagag gttgtcctgg cgtggtttag 180
gtagtgtgag aggggaatga ctcctttcgg taagtgcagt ggaagctgta cactgcccag 240
gcaaagcgtc cgggcagcgt aggcgggcga ctcagatccc agccagtgga cttagcccct 300
gtttgctcct ccgataactg gggtgacctt ggttaatatt caccagcagc ctcccccgtt 360
gcccctctgg atccactgct taaatacgga cgaggacagg gccctgtctc ctcagcttca 420
ggcaccacca ctgacctggg acagtgaatc cggactctaa ggtaaatata aaatttttaa 480
gtgtataatg tgttaaacta ctgattctaa ttgtttctct cttttagatt ccaacctttg 540
gaactga 547
<210> 6
<211> 1179
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 6
ggctccggtg cccgtcagtg ggcagagcgc acatcgccca cagtccccga gaagttgggg 60
ggaggggtcg gcaattgaac cggtgcctag agaaggtggc gcggggtaaa ctgggaaagt 120
gatgtcgtgt actggctccg cctttttccc gagggtgggg gagaaccgta tataagtgca 180
gtagtcgccg tgaacgttct ttttcgcaac gggtttgccg ccagaacaca ggtaagtgcc 240
gtgtgtggtt cccgcgggcc tggcctcttt acgggttatg gcccttgcgt gccttgaatt 300
acttccacct ggctgcagta cgtgattctt gatcccgagc ttcgggttgg aagtgggtgg 360
gagagttcga ggccttgcgc ttaaggagcc ccttcgcctc gtgcttgagt tgaggcctgg 420
cctgggcgct ggggccgccg cgtgcgaatc tggtggcacc ttcgcgcctg tctcgctgct 480
ttcgataagt ctctagccat ttaaaatttt tgatgacctg ctgcgacgct ttttttctgg 540
caagatagtc ttgtaaatgc gggccaagat ctgcacactg gtatttcggt ttttggggcc 600
gcgggcggcg acggggcccg tgcgtcccag cgcacatgtt cggcgaggcg gggcctgcga 660
gcgcggccac cgagaatcgg acgggggtag tctcaagctg gccggcctgc tctggtgcct 720
ggtctcgcgc cgccgtgtat cgccccgccc tgggcggcaa ggctggcccg gtcggcacca 780
gttgcgtgag cggaaagatg gccgcttccc ggccctgctg cagggagctc aaaatggagg 840
acgcggcgct cgggagagcg ggcgggtgag tcacccacac aaaggaaaag ggcctttccg 900
tcctcagccg tcgcttcatg tgactccacg gagtaccggg cgccgtccag gcacctcgat 960
tagttctcga gcttttggag tacgtcgtct ttaggttggg gggaggggtt ttatgcgatg 1020
gagtttcccc acactgagtg ggtggagact gaagttaggc cagcttggca cttgatgtaa 1080
ttctccttgg aatttgccct ttttgagttt ggatcttggt tcattctcaa gcctcagaca 1140
gtggttcaaa gtttttttct tccatttcag gtgtcgtga 1179
<210> 7
<211> 8
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 7
gtttaaac 8
<210> 8
<211> 581
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 8
gagcatctta ccgccattta ttcccatatt tgttctgttt ttcttgattt gggtatacat 60
ttaaatgtta ataaaacaaa atggtggggc aatcatttac atttttaggg atatgtaatt 120
actagttcag gtgtattgcc acaagacaaa catgttaaga aactttcccg ttatttacgc 180
tctgttcctg ttaatcaacc tctggattac aaaatttgtg aaagattgac tgatattctt 240
aactatgttg ctccttttac gctgtgtgga tatgctgctt tatagcctct gtatctagct 300
attgcttccc gtacggcttt cgttttctcc tccttgtata aatcctggtt gctgtctctt 360
ttagaggagt tgtggcccgt tgtccgtcaa cgtggcgtgg tgtgctctgt gtttgctgac 420
gcaaccccca ctggctgggg cattgccacc acctgtcaac tcctttctgg gactttcgct 480
ttccccctcc cgatcgccac ggcagaactc atcgccgcct gccttgcccg ctgctggaca 540
ggggctaggt tgctgggcac tgataattcc gtggtgttgt c 581
<210> 9
<211> 225
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 9
tgtgccttct agttgccagc catctgttgt ttgcccctcc cccgtgcctt ccttgaccct 60
ggaaggtgcc actcccactg tcctttccta ataaaatgag gaaattgcat cgcattgtct 120
gagtaggtgt cattctattc tggggggtgg ggtggggcag gacagcaagg gggaggattg 180
ggaagacaat agcaggcatg ctggggatgc ggtgggctct atggc 225
<210> 10
<211> 213
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 10
taagatacat tgatgagttt ggacaaacca caactagaat gcagtgaaaa aaatgcttta 60
tttgtgaaat ttgtgatgct attgctttat ttgtaaccat tataagctgc aataaacaag 120
ttaacaacaa caattgcatt cattttatgt ttcaggttca gggggaggtg tgggaggttt 180
tttaaagcaa gtaaaacctc tacaaatgtg gta 213
<210> 11
<211> 1260
<212> DNA/ДНК
<213> Аденоассоциированный вирус - 2
<400> 11
atggagctgg tcgggtggct cgtggacaag gggattacct cggagaagca gtggatccag 60
gaggaccagg cctcatacat ctccttcaat gcggcctcca actcgcggtc ccaaatcaag 120
gctgccttgg acaatgcggg aaagattatg agcctgacta aaaccgcccc cgactacctg 180
gtgggccagc agcccgtgga ggacatttcc agcaatcgga tttataaaat tttggaacta 240
aacgggtacg atccccaata tgcggcttcc gtctttctgg gatgggccac gaaaaagttc 300
ggcaagagga acaccatctg gctgtttggg cctgcaacta ccgggaagac caacatcgcg 360
gaggccatag cccacactgt gcccttctac gggtgcgtaa actggaccaa tgagaacttt 420
cccttcaacg actgtgtcga caagatggtg atctggtggg aggaggggaa gatgaccgcc 480
aaggtcgtgg agtcggccaa agccattctc ggaggaagca aggtgcgcgt ggaccagaaa 540
tgcaagtcct cggcccagat agacccgact cccgtgatcg tcacctccaa caccaacatg 600
tgcgccgtga ttgacgggaa ctcaacgacc ttcgaacacc agcagccgtt gcaagaccgg 660
atgttcaaat ttgaactcac ccgccgtctg gatcatgact ttgggaaggt caccaagcag 720
gaagtcaaag actttttccg gtgggcaaag gatcacgtgg ttgaggtgga gcatgaattc 780
tacgtcaaaa agggtggagc caagaaaaga cccgccccca gtgacgcaga tataagtgag 840
cccaaacggg tgcgcgagtc agttgcgcag ccatcgacgt cagacgcgga agcttcgatc 900
aactacgcag acaggtacca aaacaaatgt tctcgtcacg tgggcatgaa tctgatgctg 960
tttccctgca gacaatgcga gagaatgaat cagaattcaa atatctgctt cactcacgga 1020
cagaaagact gtttagagtg ctttcccgtg tcagaatctc aacccgtttc tgtcgtcaaa 1080
aaggcgtatc agaaactgtg ctacattcat catatcatgg gaaaggtgcc agacgcttgc 1140
actgcctgcg atctggtcaa tgtggatttg gatgactgca tctttgaaca ataaatgatt 1200
taaatcaggt atggctgccg atggttatct tccagattgg ctcgaggaca ctctctctga 1260
<210> 12
<211> 1932
<212> DNA/ДНК
<213> Аденоассоциированный вирус - 2
<400> 12
atgccggggt tttacgagat tgtgattaag gtccccagcg accttgacga gcatctgccc 60
ggcatttctg acagctttgt gaactgggtg gccgagaagg aatgggagtt gccgccagat 120
tctgacatgg atctgaatct gattgagcag gcacccctga ccgtggccga gaagctgcag 180
cgcgactttc tgacggaatg gcgccgtgtg agtaaggccc cggaggccct tttctttgtg 240
caatttgaga agggagagag ctacttccac atgcacgtgc tcgtggaaac caccggggtg 300
aaatccatgg ttttgggacg tttcctgagt cagattcgcg aaaaactgat tcagagaatt 360
taccgcggga tcgagccgac tttgccaaac tggttcgcgg tcacaaagac cagaaatggc 420
gccggaggcg ggaacaaggt ggtggatgag tgctacatcc ccaattactt gctccccaaa 480
acccagcctg agctccagtg ggcgtggact aatatggaac agtatttaag cgcctgtttg 540
aatctcacgg agcgtaaacg gttggtggcg cagcatctga cgcacgtgtc gcagacgcag 600
gagcagaaca aagagaatca gaatcccaat tctgatgcgc cggtgatcag atcaaaaact 660
tcagccaggt acatggagct ggtcgggtgg ctcgtggaca aggggattac ctcggagaag 720
cagtggatcc aggaggacca ggcctcatac atctccttca atgcggcctc caactcgcgg 780
tcccaaatca aggctgcctt ggacaatgcg ggaaagatta tgagcctgac taaaaccgcc 840
cccgactacc tggtgggcca gcagcccgtg gaggacattt ccagcaatcg gatttataaa 900
attttggaac taaacgggta cgatccccaa tatgcggctt ccgtctttct gggatgggcc 960
acgaaaaagt tcggcaagag gaacaccatc tggctgtttg ggcctgcaac taccgggaag 1020
accaacatcg cggaggccat agcccacact gtgcccttct acgggtgcgt aaactggacc 1080
aatgagaact ttcccttcaa cgactgtgtc gacaagatgg tgatctggtg ggaggagggg 1140
aagatgaccg ccaaggtcgt ggagtcggcc aaagccattc tcggaggaag caaggtgcgc 1200
gtggaccaga aatgcaagtc ctcggcccag atagacccga ctcccgtgat cgtcacctcc 1260
aacaccaaca tgtgcgccgt gattgacggg aactcaacga ccttcgaaca ccagcagccg 1320
ttgcaagacc ggatgttcaa atttgaactc acccgccgtc tggatcatga ctttgggaag 1380
gtcaccaagc aggaagtcaa agactttttc cggtgggcaa aggatcacgt ggttgaggtg 1440
gagcatgaat tctacgtcaa aaagggtgga gccaagaaaa gacccgcccc cagtgacgca 1500
gatataagtg agcccaaacg ggtgcgcgag tcagttgcgc agccatcgac gtcagacgcg 1560
gaagcttcga tcaactacgc agacaggtac caaaacaaat gttctcgtca cgtgggcatg 1620
aatctgatgc tgtttccctg cagacaatgc gagagaatga atcagaattc aaatatctgc 1680
ttcactcacg gacagaaaga ctgtttagag tgctttcccg tgtcagaatc tcaacccgtt 1740
tctgtcgtca aaaaggcgta tcagaaactg tgctacattc atcatatcat gggaaaggtg 1800
ccagacgctt gcactgcctg cgatctggtc aatgtggatt tggatgactg catctttgaa 1860
caataaatga tttaaatcag gtatggctgc cgatggttat cttccagatt ggctcgagga 1920
cactctctct ga 1932
<210> 13
<211> 1876
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 13
cgcagccacc atggcggggt tttacgagat tgtgattaag gtccccagcg accttgacgg 60
gcatctgccc ggcatttctg acagctttgt gaactgggtg gccgagaagg aatgggagtt 120
gccgccagat tctgacatgg atctgaatct gattgagcag gcacccctga ccgtggccga 180
gaagctgcag cgcgactttc tgacggaatg gcgccgtgtg agtaaggccc cggaggccct 240
tttctttgtg caatttgaga agggagagag ctacttccac atgcacgtgc tcgtggaaac 300
caccggggtg aaatccatgg ttttgggacg tttcctgagt cagattcgcg aaaaactgat 360
tcagagaatt taccgcggga tcgagccgac tttgccaaac tggttcgcgg tcacaaagac 420
cagaaatggc gccggaggcg ggaacaaggt ggtggatgag tgctacatcc ccaattactt 480
gctccccaaa acccagcctg agctccagtg ggcgtggact aatatggaac agtatttaag 540
cgcctgtttg aatctcacgg agcgtaaacg gttggtggcg cagcatctga cgcacgtgtc 600
gcagacgcag gagcagaaca aagagaatca gaatcccaat tctgatgcgc cggtgatcag 660
atcaaaaact tcagccaggt acatggagct ggtcgggtgg ctcgtggaca aggggattac 720
ctcggagaag cagtggatcc aggaggacca ggcctcatac atctccttca atgcggcctc 780
caactcgcgg tcccaaatca aggctgcctt ggacaatgcg ggaaagatta tgagcctgac 840
taaaaccgcc cccgactacc tggtgggcca gcagcccgtg gaggacattt ccagcaatcg 900
gatttataaa attttggaac taaacgggta cgatccccaa tatgcggctt ccgtctttct 960
gggatgggcc acgaaaaagt tcggcaagag gaacaccatc tggctgtttg ggcctgcaac 1020
taccgggaag accaacatcg cggaggccat agcccacact gtgcccttct acgggtgcgt 1080
aaactggacc aatgagaact ttcccttcaa cgactgtgtc gacaagatgg tgatctggtg 1140
ggaggagggg aagatgaccg ccaaggtcgt ggagtcggcc aaagccattc tcggaggaag 1200
caaggtgcgc gtggaccaga aatgcaagtc ctcggcccag atagacccga ctcccgtgat 1260
cgtcacctcc aacaccaaca tgtgcgccgt gattgacggg aactcaacga ccttcgaaca 1320
ccagcagccg ttgcaagacc ggatgttcaa atttgaactc acccgccgtc tggatcatga 1380
ctttgggaag gtcaccaagc aggaagtcaa agactttttc cggtgggcaa aggatcacgt 1440
ggttgaggtg gagcatgaat tctacgtcaa aaagggtgga gccaagaaaa gacccgcccc 1500
cagtgacgca gatataagtg agcccaaacg ggtgcgcgag tcagttgcgc agccatcgac 1560
gtcagacgcg gaagcttcga tcaactacgc agacaggtac caaaacaaat gttctcgtca 1620
cgtgggcatg aatctgatgc tgtttccctg cagacaatgc gagagaatga atcagaattc 1680
aaatatctgc ttcactcacg gacagaaaga ctgtttagag tgctttcccg tgtcagaatc 1740
tcaacccgtt tctgtcgtca aaaaggcgta tcagaaactg tgctacattc atcatatcat 1800
gggaaaggtg ccagacgctt gcactgcctg cgatctggtc aatgtggatt tggatgactg 1860
catctttgaa caataa 1876
<210> 14
<211> 1194
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 14
atggagctgg tcgggtggct cgtggacaag gggattacct cggagaagca gtggatccag 60
gaggaccagg cctcatacat ctccttcaat gcggcctcca actcgcggtc ccaaatcaag 120
gctgccttgg acaatgcggg aaagattatg agcctgacta aaaccgcccc cgactacctg 180
gtgggccagc agcccgtgga ggacatttcc agcaatcgga tttataaaat tttggaacta 240
aacgggtacg atccccaata tgcggcttcc gtctttctgg gatgggccac gaaaaagttc 300
ggcaagagga acaccatctg gctgtttggg cctgcaacta ccgggaagac caacatcgcg 360
gaggccatag cccacactgt gcccttctac gggtgcgtaa actggaccaa tgagaacttt 420
cccttcaacg actgtgtcga caagatggtg atctggtggg aggaggggaa gatgaccgcc 480
aaggtcgtgg agtcggccaa agccattctc ggaggaagca aggtgcgcgt ggaccagaaa 540
tgcaagtcct cggcccagat agacccgact cccgtgatcg tcacctccaa caccaacatg 600
tgcgccgtga ttgacgggaa ctcaacgacc ttcgaacacc agcagccgtt gcaagaccgg 660
atgttcaaat ttgaactcac ccgccgtctg gatcatgact ttgggaaggt caccaagcag 720
gaagtcaaag actttttccg gtgggcaaag gatcacgtgg ttgaggtgga gcatgaattc 780
tacgtcaaaa agggtggagc caagaaaaga cccgccccca gtgacgcaga tataagtgag 840
cccaaacggg tgcgcgagtc agttgcgcag ccatcgacgt cagacgcgga agcttcgatc 900
aactacgcag accgctacca aaacaaatgt tctcgtcacg tgggcatgaa tctgatgctg 960
tttccctgca gacaatgcga gagaatgaat cagaattcaa atatctgctt cactcacgga 1020
cagaaagact gtttagagtg ctttcccgtg tcagaatctc aacccgtttc tgtcgtcaaa 1080
aaggcgtatc agaaactgtg ctacattcat catatcatgg gaaaggtgcc agacgcttgc 1140
actgcctgcg atctggtcaa tgtggatttg gatgactgca tctttgaaca ataa 1194
<210> 15
<211> 141
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 15
aataaacgat aacgccgttg gtggcgtgag gcatgtaaaa ggttacatca ttatcttgtt 60
cgccatccgg ttggtataaa tagacgttca tgttggtttt tgtttcagtt gcaagttggc 120
tgcggcgcgc gcagcacctt t 141
<210> 16
<211> 556
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 16
ccctaaaatg ggcaaacatt gcaagcagca aacagcaaac acacagccct ccctgcctgc 60
tgaccttgga gctggggcag aggtcagaga cctctctggg cccatgccac ctccaacatc 120
cactcgaccc cttggaattt cggtggagag gagcagaggt tgtcctggcg tggtttaggt 180
agtgtgagag gggaatgact cctttcggta agtgcagtgg aagctgtaca ctgcccaggc 240
aaagcgtccg ggcagcgtag gcgggcgact cagatcccag ccagtggact tagcccctgt 300
ttgctcctcc gataactggg gtgaccttgg ttaatattca ccagcagcct cccccgttgc 360
ccctctggat ccactgctta aatacggacg aggacactcg agggccctgt ctcctcagct 420
tcaggcacca ccactgacct gggacagtga atccggacat cgattctaag gtaaatataa 480
aatttttaag tgtataattt gttaaactac tgattctaat tgtttctctc ttttagattc 540
caacctttgg aactga 556
<210> 17
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 17
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgcc cgggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 18
<211> 241
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 18
gagggcctat ttcccatgat tccttcatat ttgcatatac gatacaaggc tgttagagag 60
ataattggaa ttaatttgac tgtaaacaca aagatattag tacaaaatac gtgacgtaga 120
aagtaataat ttcttgggta gtttgcagtt ttaaaattat gttttaaaat ggactatcat 180
atgcttaccg taacttgaaa gtatttcgat ttcttggctt tatatatctt gtggaaagga 240
c 241
<210> 19
<211> 215
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 19
gaacgctgac gtcatcaacc cgctccaagg aatcgcgggc ccagtgtcac taggcgggaa 60
cacccagcgc gcgtgcgccc tggcaggaag atggctgtga gggacagggg agtggcgccc 120
tgcaatattt gcatgtcgct atgtgttctg ggaaatcacc ataaacgtga aatgtctttg 180
gatttgggaa tcgtataaga actgtatgag accac 215
<210> 20
<211> 150
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 20
ataaacgata acgccgttgg tggcgtgagg catgtaaaag gttacatcat tatcttgttc 60
gccatccggt tggtataaat agacgttcat gttggttttt gtttcagttg caagttggct 120
gcggcgcgcg cagcaccttt gcggccatct 150
<210> 21
<211> 546
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 21
ccctaaaatg ggcaaacatt gcaagcagca aacagcaaac acacagccct ccctgcctgc 60
tgaccttgga gctggggcag aggtcagaga cctctctggg cccatgccac ctccaacatc 120
cactcgaccc cttggaattt ttcggtggag aggagcagag gttgtcctgg cgtggtttag 180
gtagtgtgag aggggaatga ctcctttcgg taagtgcagt ggaagctgta cactgcccag 240
gcaaagcgtc cgggcagcgt aggcgggcga ctcagatccc agccagtgga cttagcccct 300
gtttgctcct ccgataactg gggtgacctt ggttaatatt caccagcagc ctcccccgtt 360
gcccctctgg atccactgct taaatacgga cgaggacagg gccctgtctc ctcagcttca 420
ggcaccacca ctgacctggg acagtgaatc cggactctaa ggtaaatata aaatttttaa 480
gtgtataatg tgttaaacta ctgattctaa ttgtttctct cttttagatt ccaacctttg 540
gaactg 546
<210> 22
<211> 317
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 22
ggtgtggaaa gtccccaggc tccccagcag gcagaagtat gcaaagcatg catctcaatt 60
agtcagcaac caggtgtgga aagtccccag gctccccagc aggcagaagt atgcaaagca 120
tgcatctcaa ttagtcagca accatagtcc cgcccctaac tccgcccatc ccgcccctaa 180
ctccgcccag ttccgcccat tctccgcccc atggctgact aatttttttt atttatgcag 240
aggccgaggc cgcctcggcc tctgagctat tccagaagta gtgaggaggc ttttttggag 300
gcctaggctt ttgcaaa 317
<210> 23
<211> 576
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 23
tagtaatcaa ttacggggtc attagttcat agcccatata tggagttccg cgttacataa 60
cttacggtaa atggcccgcc tggctgaccg cccaacgacc cccgcccatt gacgtcaata 120
atgacgtatg ttcccatagt aacgccaata gggactttcc attgacgtca atgggtggag 180
tatttacggt aaactgccca cttggcagta catcaagtgt atcatatgcc aagtacgccc 240
cctattgacg tcaatgacgg taaatggccc gcctggcatt atgcccagta catgacctta 300
tgggactttc ctacttggca gtacatctac gtattagtca tcgctattac catggtgatg 360
cggttttggc agtacatcaa tgggcgtgga tagcggtttg actcacgggg atttccaagt 420
ctccacccca ttgacgtcaa tgggagtttg ttttggcacc aaaatcaacg ggactttcca 480
aaatgtcgta acaactccgc cccattgacg caaatgggcg gtaggcgtgt acggtgggag 540
gtctatataa gcagagctgg tttagtgaac cgtcag 576
<210> 24
<211> 1313
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 24
ggagccgaga gtaattcata caaaaggagg gatcgccttc gcaaggggag agcccaggga 60
ccgtccctaa attctcacag acccaaatcc ctgtagccgc cccacgacag cgcgaggagc 120
atgcgcccag ggctgagcgc gggtagatca gagcacacaa gctcacagtc cccggcggtg 180
gggggagggg cgcgctgagc gggggccagg gagctggcgc ggggcaaact gggaaagtgg 240
tgtcgtgtgc tggctccgcc ctcttcccga gggtggggga gaacggtata taagtgcggt 300
agtcgccttg gacgttcttt ttcgcaacgg gtttgccgtc agaacgcagg tgagtggcgg 360
gtgtggcttc cgcgggcccc ggagctggag ccctgctctg agcgggccgg gctgatatgc 420
gagtgtcgtc cgcagggttt agctgtgagc attcccactt cgagtggcgg gcggtgcggg 480
ggtgagagtg cgaggcctag cggcaacccc gtagcctcgc ctcgtgtccg gcttgaggcc 540
tagcgtggtg tccgccgccg cgtgccactc cggccgcact atgcgttttt tgtccttgct 600
gccctcgatt gccttccagc agcatgggct aacaaaggga gggtgtgggg ctcactctta 660
aggagcccat gaagcttacg ttggatagga atggaagggc aggaggggcg actggggccc 720
gcccgccttc ggagcacatg tccgacgcca cctggatggg gcgaggcctg tggctttccg 780
aagcaatcgg gcgtgagttt agcctacctg ggccatgtgg ccctagcact gggcacggtc 840
tggcctggcg gtgccgcgtt cccttgcctc ccaacaaggg tgaggccgtc ccgcccggca 900
ccagttgctt gcgcggaaag atggccgctc ccggggccct gttgcaagga gctcaaaatg 960
gaggacgcgg cagcccggtg gagcgggcgg gtgagtcacc cacacaaagg aagagggcct 1020
tgcccctcgc cggccgctgc ttcctgtgac cccgtggtct atcggccgca tagtcacctc 1080
gggcttctct tgagcaccgc tcgtcgcggc ggggggaggg gatctaatgg cgttggagtt 1140
tgttcacatt tggtgggtgg agactagtca ggccagcctg gcgctggaag tcattcttgg 1200
aatttgcccc tttgagtttg gagcgaggct aattctcaag cctcttagcg gttcaaaggt 1260
attttctaaa cccgtttcca ggtgttgtga aagccaccgc taattcaaag caa 1313
<210> 25
<211> 19
<212> PRT/Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 25
Met Asp Trp Thr Trp Arg Ile Leu Phe Leu Val Ala Ala Ala Thr Gly
1 5 10 15
Ala His Ser
<210> 26
<211> 19
<212> PRT/Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 26
Met Leu Pro Ser Gln Leu Ile Gly Phe Leu Leu Leu Trp Val Pro Ala
1 5 10 15
Ser Arg Gly
<210> 27
<211> 7
<212> PRT/Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 27
Pro Lys Lys Lys Arg Lys Val
1 5
<210> 28
<400> 28
000
<210> 29
<400> 29
000
<210> 30
<400> 30
000
<210> 31
<400> 31
000
<210> 32
<400> 32
000
<210> 33
<400> 33
000
<210> 34
<400> 34
000
<210> 35
<400> 35
000
<210> 36
<400> 36
000
<210> 37
<400> 37
000
<210> 38
<400> 38
000
<210> 39
<400> 39
000
<210> 40
<400> 40
000
<210> 41
<400> 41
000
<210> 42
<400> 42
000
<210> 43
<400> 43
000
<210> 44
<400> 44
000
<210> 45
<211> 6
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 45
ggttga 6
<210> 46
<211> 4
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 46
agtt 4
<210> 47
<211> 6
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 47
ggttgg 6
<210> 48
<211> 6
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 48
agttgg 6
<210> 49
<211> 6
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 49
agttga 6
<210> 50
<211> 6
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 50
rrttrr 6
<210> 51
<211> 141
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 51
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccgggcaaag cccgggcgtc 60
gggcgacctt tggtcgcccg gcctcagtga gcgagcgagc gcgcagagag ggagtggcca 120
actccatcac taggggttcc t 141
<210> 52
<211> 130
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 52
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccgggcgtcg ggcgaccttt 60
ggtcgcccgg cctcagtgag cgagcgagcg cgcagagagg gagtggccaa ctccatcact 120
aggggttcct 130
<210> 53
<211> 3123
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 53
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccgggaaacc cgggcgtgcc 60
cgggcgcctc agtgagcgag cgagcgcgca gagagggagt ggccaactcc atcactaggg 120
gttcctgaac agagaaacag gagaatatgg gccaaacagg atatctgtgg taagcagttc 180
ctgccccggc tcagggccaa gaacagttgg aacagcagaa tatgggccaa acaggatatc 240
tgtggtaagc agttcctgcc ccggctcagg gccaagaaca gatggtcccc agatgcggtc 300
ccgccctcag cagtttctag agaaccatca gatgtttcca gggtgcccca aggacctgaa 360
atgaccctgt gccttatttg aactaaccaa tcagttcgct tctcgcttct gttcgcgcgc 420
ttctgctccc cgagctctat ataagcagag ctcgtttagt gaaccgtcag atcgcctgga 480
gacgccatcc acgctgtttt gacttccata gaaggccgcc accatggaag acgccaaaaa 540
cataaagaaa ggcccggcgc cattctatcc gctggaagat ggaaccgctg gagagcaact 600
gcataaggct atgaagagat acgccctggt tcctggaaca attgctttta cagatgcaca 660
tatcgaggtg gacatcactt acgctgagta cttcgaaatg tccgttcggt tggcagaagc 720
tatgaaacga tatgggctga atacaaatca cagaatcgtc gtatgcagtg aaaactctct 780
tcaattcttt atgccggtgt tgggcgcgtt atttatcgga gttgcagttg cgcccgcgaa 840
cgacatttat aatgaacgtg aattgctcaa cagtatgggc atttcgcagc ctaccgtggt 900
gttcgtttcc aaaaaggggt tgcaaaaaat tttgaacgtg caaaaaaagc tcccaatcat 960
ccaaaaaatt attatcatgg attctaaaac ggattaccag ggatttcagt cgatgtacac 1020
gttcgtcaca tctcatctac ctcccggttt taatgaatac gattttgtgc cagagtcctt 1080
cgatagggac aagacaattg cactgatcat gaactcctct ggatctactg gtctgcctaa 1140
aggtgtcgct ctgcctcata gaactgcctg cgtgagattc tcgcatgcca gagatcctat 1200
ttttggcaat caaatcattc cggatactgc gattttaagt gttgttccat tccatcacgg 1260
ttttggaatg tttactacac tcggatattt gatatgtgga tttcgagtcg tcttaatgta 1320
tagatttgaa gaagagctgt ttctgaggag ccttcaggat tacaagattc aaagtgcgct 1380
gctggtgcca accctattct ccttcttcgc caaaagcact ctgattgaca aatacgattt 1440
atctaattta cacgaaattg cttctggtgg cgctcccctc tctaaggaag tcggggaagc 1500
ggttgccaag aggttccatc tgccaggtat caggcaagga tatgggctca ctgagactac 1560
atcagctatt ctgattacac ccgaggggga tgataaaccg ggcgcggtcg gtaaagttgt 1620
tccatttttt gaagcgaagg ttgtggatct ggataccggg aaaacgctgg gcgttaatca 1680
aagaggcgaa ctgtgtgtga gaggtcctat gattatgtcc ggttatgtaa acaatccgga 1740
agcgaccaac gccttgattg acaaggatgg atggctacat tctggagaca tagcttactg 1800
ggacgaagac gaacacttct tcatcgttga ccgcctgaag tctctgatta agtacaaagg 1860
ctatcaggtg gctcccgctg aattggaatc catcttgctc caacacccca acatcttcga 1920
cgcaggtgtc gcaggtcttc ccgacgatga cgccggtgaa cttcccgccg ccgttgttgt 1980
tttggagcac ggaaagacga tgacggaaaa agagatcgtg gattacgtcg ccagtcaagt 2040
aacaaccgcg aaaaagttgc gcggaggagt tgtgtttgtg gacgaagtac cgaaaggtct 2100
taccggaaaa ctcgacgcaa gaaaaatcag agagatcctc ataaaggcca agaagggcgg 2160
aaagatcgcc gtgtaagagc atcttaccgc catttattcc catatttgtt ctgtttttct 2220
tgatttgggt atacatttaa atgttaataa aacaaaatgg tggggcaatc atttacattt 2280
ttagggatat gtaattacta gttcaggtgt attgccacaa gacaaacatg ttaagaaact 2340
ttcccgttat ttacgctctg ttcctgttaa tcaacctctg gattacaaaa tttgtgaaag 2400
attgactgat attcttaact atgttgctcc ttttacgctg tgtggatatg ctgctttata 2460
gcctctgtat ctagctattg cttcccgtac ggctttcgtt ttctcctcct tgtataaatc 2520
ctggttgctg tctcttttag aggagttgtg gcccgttgtc cgtcaacgtg gcgtggtgtg 2580
ctctgtgttt gctgacgcaa cccccactgg ctggggcatt gccaccacct gtcaactcct 2640
ttctgggact ttcgctttcc ccctcccgat cgccacggca gaactcatcg ccgcctgcct 2700
tgcccgctgc tggacagggg ctaggttgct gggcactgat aattccgtgg tgttgtctgt 2760
gccttctagt tgccagccat ctgttgtttg cccctccccc gtgccttcct tgaccctgga 2820
aggtgccact cccactgtcc tttcctaata aaatgaggaa attgcatcgc attgtctgag 2880
taggtgtcat tctattctgg ggggtggggt ggggcaggac agcaaggggg aggattggga 2940
agacaatagc aggcatgctg gggatgcggt gggctctatg gcaggaaccc ctagtgatgg 3000
agttggccac tccctctctg cgcgctcgct cgctcactga ggccgggcga ccaaaggtcg 3060
cccgacgccc gggctttgcc cgggcggcct cagtgagcga gcgagcgcgc agctgcctgc 3120
agg 3123
<210> 54
<211> 3117
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 54
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccgggcaaag cccgggcgtc 60
gggcgacctt tggtcgcccg gcctcagtga gcgagcgagc gcgcagagag ggagtggcca 120
actccatcac taggggttcc tgaacagaga aacaggagaa tatgggccaa acaggatatc 180
tgtggtaagc agttcctgcc ccggctcagg gccaagaaca gttggaacag cagaatatgg 240
gccaaacagg atatctgtgg taagcagttc ctgccccggc tcagggccaa gaacagatgg 300
tccccagatg cggtcccgcc ctcagcagtt tctagagaac catcagatgt ttccagggtg 360
ccccaaggac ctgaaatgac cctgtgcctt atttgaacta accaatcagt tcgcttctcg 420
cttctgttcg cgcgcttctg ctccccgagc tctatataag cagagctcgt ttagtgaacc 480
gtcagatcgc ctggagacgc catccacgct gttttgactt ccatagaagg ccgccaccat 540
ggaagacgcc aaaaacataa agaaaggccc ggcgccattc tatccgctgg aagatggaac 600
cgctggagag caactgcata aggctatgaa gagatacgcc ctggttcctg gaacaattgc 660
ttttacagat gcacatatcg aggtggacat cacttacgct gagtacttcg aaatgtccgt 720
tcggttggca gaagctatga aacgatatgg gctgaataca aatcacagaa tcgtcgtatg 780
cagtgaaaac tctcttcaat tctttatgcc ggtgttgggc gcgttattta tcggagttgc 840
agttgcgccc gcgaacgaca tttataatga acgtgaattg ctcaacagta tgggcatttc 900
gcagcctacc gtggtgttcg tttccaaaaa ggggttgcaa aaaattttga acgtgcaaaa 960
aaagctccca atcatccaaa aaattattat catggattct aaaacggatt accagggatt 1020
tcagtcgatg tacacgttcg tcacatctca tctacctccc ggttttaatg aatacgattt 1080
tgtgccagag tccttcgata gggacaagac aattgcactg atcatgaact cctctggatc 1140
tactggtctg cctaaaggtg tcgctctgcc tcatagaact gcctgcgtga gattctcgca 1200
tgccagagat cctatttttg gcaatcaaat cattccggat actgcgattt taagtgttgt 1260
tccattccat cacggttttg gaatgtttac tacactcgga tatttgatat gtggatttcg 1320
agtcgtctta atgtatagat ttgaagaaga gctgtttctg aggagccttc aggattacaa 1380
gattcaaagt gcgctgctgg tgccaaccct attctccttc ttcgccaaaa gcactctgat 1440
tgacaaatac gatttatcta atttacacga aattgcttct ggtggcgctc ccctctctaa 1500
ggaagtcggg gaagcggttg ccaagaggtt ccatctgcca ggtatcaggc aaggatatgg 1560
gctcactgag actacatcag ctattctgat tacacccgag ggggatgata aaccgggcgc 1620
ggtcggtaaa gttgttccat tttttgaagc gaaggttgtg gatctggata ccgggaaaac 1680
gctgggcgtt aatcaaagag gcgaactgtg tgtgagaggt cctatgatta tgtccggtta 1740
tgtaaacaat ccggaagcga ccaacgcctt gattgacaag gatggatggc tacattctgg 1800
agacatagct tactgggacg aagacgaaca cttcttcatc gttgaccgcc tgaagtctct 1860
gattaagtac aaaggctatc aggtggctcc cgctgaattg gaatccatct tgctccaaca 1920
ccccaacatc ttcgacgcag gtgtcgcagg tcttcccgac gatgacgccg gtgaacttcc 1980
cgccgccgtt gttgttttgg agcacggaaa gacgatgacg gaaaaagaga tcgtggatta 2040
cgtcgccagt caagtaacaa ccgcgaaaaa gttgcgcgga ggagttgtgt ttgtggacga 2100
agtaccgaaa ggtcttaccg gaaaactcga cgcaagaaaa atcagagaga tcctcataaa 2160
ggccaagaag ggcggaaaga tcgccgtgta agagcatctt accgccattt attcccatat 2220
ttgttctgtt tttcttgatt tgggtataca tttaaatgtt aataaaacaa aatggtgggg 2280
caatcattta catttttagg gatatgtaat tactagttca ggtgtattgc cacaagacaa 2340
acatgttaag aaactttccc gttatttacg ctctgttcct gttaatcaac ctctggatta 2400
caaaatttgt gaaagattga ctgatattct taactatgtt gctcctttta cgctgtgtgg 2460
atatgctgct ttatagcctc tgtatctagc tattgcttcc cgtacggctt tcgttttctc 2520
ctccttgtat aaatcctggt tgctgtctct tttagaggag ttgtggcccg ttgtccgtca 2580
acgtggcgtg gtgtgctctg tgtttgctga cgcaaccccc actggctggg gcattgccac 2640
cacctgtcaa ctcctttctg ggactttcgc tttccccctc ccgatcgcca cggcagaact 2700
catcgccgcc tgccttgccc gctgctggac aggggctagg ttgctgggca ctgataattc 2760
cgtggtgttg tctgtgcctt ctagttgcca gccatctgtt gtttgcccct cccccgtgcc 2820
ttccttgacc ctggaaggtg ccactcccac tgtcctttcc taataaaatg aggaaattgc 2880
atcgcattgt ctgagtaggt gtcattctat tctggggggt ggggtggggc aggacagcaa 2940
gggggaggat tgggaagaca atagcaggca tgctggggat gcggtgggct ctatggcagg 3000
aacccctagt gatggagttg gccactccct ctctgcgcgc tcgctcgctc actgaggccg 3060
cccgggaaac ccgggcgtgc gcctcagtga gcgagcgagc gcgcagctgc ctgcagg 3117
<210> 55
<400> 55
000
<210> 56
<400> 56
000
<210> 57
<211> 3912
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 57
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccgggaaacc cgggcgtgcc 60
cgggcgcctc agtgagcgag cgagcgcgca gagagggagt ggccaactcc atcactaggg 120
gttcctggct cagaggctca gaggcacaca ggagtttctg ggctcaccct gcccccttcc 180
aacccctcag ttcccatcct ccagcagctg tttgtgtgct gcctctgaag tccacactga 240
acaaacttca gcctactcat gtccctaaaa tgggcaaaca ttgcaagcag caaacagcaa 300
acacacagcc ctccctgcct gctgaccttg gagctggggc agaggtcaga gacctctctg 360
ggcccatgcc acctccaaca tccactcgac cccttggaat ttcggtggag aggagcagag 420
gttgtcctgg cgtggtttag gtagtgtgag agggtccggg ttcaaaacca cttgctgggt 480
ggggagtcgt cagtaagtgg ctatgccccg accccgaagc ctgtttcccc atctgtacaa 540
tggaaatgat aaagacgccc atctgatagg gtttttgtgg caaataaaca tttggttttt 600
ttgttttgtt ttgttttgtt ttttgagatg gaggtttgct ctgtcgccca ggctggagtg 660
cagtgacaca atctcatctc accacaacct tcccctgcct cagcctccca agtagctggg 720
attacaagca tgtgccacca cacctggcta attttctatt tttagtagag acgggtttct 780
ccatgttggt cagcctcagc ctcccaagta actgggatta caggcctgtg ccaccacacc 840
cggctaattt tttctatttt tgacagggac ggggtttcac catgttggtc aggctggtct 900
agaggtaccg gatcttgcta ccagtggaac agccactaag gattctgcag tgagagcaga 960
gggccagcta agtggtactc tcccagagac tgtctgactc acgccacccc ctccaccttg 1020
gacacaggac gctgtggttt ctgagccagg tacaatgact cctttcggta agtgcagtgg 1080
aagctgtaca ctgcccaggc aaagcgtccg ggcagcgtag gcgggcgact cagatcccag 1140
ccagtggact tagcccctgt ttgctcctcc gataactggg gtgaccttgg ttaatattca 1200
ccagcagcct cccccgttgc ccctctggat ccactgctta aatacggacg aggacagggc 1260
cctgtctcct cagcttcagg caccaccact gacctgggac agtgccgcca ccatggaaga 1320
cgccaaaaac ataaagaaag gcccggcgcc attctatccg ctggaagatg gaaccgctgg 1380
agagcaactg cataaggcta tgaagagata cgccctggtt cctggaacaa ttgcttttac 1440
agatgcacat atcgaggtgg acatcactta cgctgagtac ttcgaaatgt ccgttcggtt 1500
ggcagaagct atgaaacgat atgggctgaa tacaaatcac agaatcgtcg tatgcagtga 1560
aaactctctt caattcttta tgccggtgtt gggcgcgtta tttatcggag ttgcagttgc 1620
gcccgcgaac gacatttata atgaacgtga attgctcaac agtatgggca tttcgcagcc 1680
taccgtggtg ttcgtttcca aaaaggggtt gcaaaaaatt ttgaacgtgc aaaaaaagct 1740
cccaatcatc caaaaaatta ttatcatgga ttctaaaacg gattaccagg gatttcagtc 1800
gatgtacacg ttcgtcacat ctcatctacc tcccggtttt aatgaatacg attttgtgcc 1860
agagtccttc gatagggaca agacaattgc actgatcatg aactcctctg gatctactgg 1920
tctgcctaaa ggtgtcgctc tgcctcatag aactgcctgc gtgagattct cgcatgccag 1980
agatcctatt tttggcaatc aaatcattcc ggatactgcg attttaagtg ttgttccatt 2040
ccatcacggt tttggaatgt ttactacact cggatatttg atatgtggat ttcgagtcgt 2100
cttaatgtat agatttgaag aagagctgtt tctgaggagc cttcaggatt acaagattca 2160
aagtgcgctg ctggtgccaa ccctattctc cttcttcgcc aaaagcactc tgattgacaa 2220
atacgattta tctaatttac acgaaattgc ttctggtggc gctcccctct ctaaggaagt 2280
cggggaagcg gttgccaaga ggttccatct gccaggtatc aggcaaggat atgggctcac 2340
tgagactaca tcagctattc tgattacacc cgagggggat gataaaccgg gcgcggtcgg 2400
taaagttgtt ccattttttg aagcgaaggt tgtggatctg gataccggga aaacgctggg 2460
cgttaatcaa agaggcgaac tgtgtgtgag aggtcctatg attatgtccg gttatgtaaa 2520
caatccggaa gcgaccaacg ccttgattga caaggatgga tggctacatt ctggagacat 2580
agcttactgg gacgaagacg aacacttctt catcgttgac cgcctgaagt ctctgattaa 2640
gtacaaaggc tatcaggtgg ctcccgctga attggaatcc atcttgctcc aacaccccaa 2700
catcttcgac gcaggtgtcg caggtcttcc cgacgatgac gccggtgaac ttcccgccgc 2760
cgttgttgtt ttggagcacg gaaagacgat gacggaaaaa gagatcgtgg attacgtcgc 2820
cagtcaagta acaaccgcga aaaagttgcg cggaggagtt gtgtttgtgg acgaagtacc 2880
gaaaggtctt accggaaaac tcgacgcaag aaaaatcaga gagatcctca taaaggccaa 2940
gaagggcgga aagatcgccg tgtaagagca tcttaccgcc atttattccc atatttgttc 3000
tgtttttctt gatttgggta tacatttaaa tgttaataaa acaaaatggt ggggcaatca 3060
tttacatttt tagggatatg taattactag ttcaggtgta ttgccacaag acaaacatgt 3120
taagaaactt tcccgttatt tacgctctgt tcctgttaat caacctctgg attacaaaat 3180
ttgtgaaaga ttgactgata ttcttaacta tgttgctcct tttacgctgt gtggatatgc 3240
tgctttatag cctctgtatc tagctattgc ttcccgtacg gctttcgttt tctcctcctt 3300
gtataaatcc tggttgctgt ctcttttaga ggagttgtgg cccgttgtcc gtcaacgtgg 3360
cgtggtgtgc tctgtgtttg ctgacgcaac ccccactggc tggggcattg ccaccacctg 3420
tcaactcctt tctgggactt tcgctttccc cctcccgatc gccacggcag aactcatcgc 3480
cgcctgcctt gcccgctgct ggacaggggc taggttgctg ggcactgata attccgtggt 3540
gttgtctgtg ccttctagtt gccagccatc tgttgtttgc ccctcccccg tgccttcctt 3600
gaccctggaa ggtgccactc ccactgtcct ttcctaataa aatgaggaaa ttgcatcgca 3660
ttgtctgagt aggtgtcatt ctattctggg gggtggggtg gggcaggaca gcaaggggga 3720
ggattgggaa gacaatagca ggcatgctgg ggatgcggtg ggctctatgg caggaacccc 3780
tagtgatgga gttggccact ccctctctgc gcgctcgctc gctcactgag gccgggcgac 3840
caaaggtcgc ccgacgcccg ggctttgccc gggcggcctc agtgagcgag cgagcgcgca 3900
gctgcctgca gg 3912
<210> 58
<211> 3906
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 58
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccgggcaaag cccgggcgtc 60
gggcgacctt tggtcgcccg gcctcagtga gcgagcgagc gcgcagagag ggagtggcca 120
actccatcac taggggttcc tggctcagag gctcagaggc acacaggagt ttctgggctc 180
accctgcccc cttccaaccc ctcagttccc atcctccagc agctgtttgt gtgctgcctc 240
tgaagtccac actgaacaaa cttcagccta ctcatgtccc taaaatgggc aaacattgca 300
agcagcaaac agcaaacaca cagccctccc tgcctgctga ccttggagct ggggcagagg 360
tcagagacct ctctgggccc atgccacctc caacatccac tcgacccctt ggaatttcgg 420
tggagaggag cagaggttgt cctggcgtgg tttaggtagt gtgagagggt ccgggttcaa 480
aaccacttgc tgggtgggga gtcgtcagta agtggctatg ccccgacccc gaagcctgtt 540
tccccatctg tacaatggaa atgataaaga cgcccatctg atagggtttt tgtggcaaat 600
aaacatttgg tttttttgtt ttgttttgtt ttgttttttg agatggaggt ttgctctgtc 660
gcccaggctg gagtgcagtg acacaatctc atctcaccac aaccttcccc tgcctcagcc 720
tcccaagtag ctgggattac aagcatgtgc caccacacct ggctaatttt ctatttttag 780
tagagacggg tttctccatg ttggtcagcc tcagcctccc aagtaactgg gattacaggc 840
ctgtgccacc acacccggct aattttttct atttttgaca gggacggggt ttcaccatgt 900
tggtcaggct ggtctagagg taccggatct tgctaccagt ggaacagcca ctaaggattc 960
tgcagtgaga gcagagggcc agctaagtgg tactctccca gagactgtct gactcacgcc 1020
accccctcca ccttggacac aggacgctgt ggtttctgag ccaggtacaa tgactccttt 1080
cggtaagtgc agtggaagct gtacactgcc caggcaaagc gtccgggcag cgtaggcggg 1140
cgactcagat cccagccagt ggacttagcc cctgtttgct cctccgataa ctggggtgac 1200
cttggttaat attcaccagc agcctccccc gttgcccctc tggatccact gcttaaatac 1260
ggacgaggac agggccctgt ctcctcagct tcaggcacca ccactgacct gggacagtgc 1320
cgccaccatg gaagacgcca aaaacataaa gaaaggcccg gcgccattct atccgctgga 1380
agatggaacc gctggagagc aactgcataa ggctatgaag agatacgccc tggttcctgg 1440
aacaattgct tttacagatg cacatatcga ggtggacatc acttacgctg agtacttcga 1500
aatgtccgtt cggttggcag aagctatgaa acgatatggg ctgaatacaa atcacagaat 1560
cgtcgtatgc agtgaaaact ctcttcaatt ctttatgccg gtgttgggcg cgttatttat 1620
cggagttgca gttgcgcccg cgaacgacat ttataatgaa cgtgaattgc tcaacagtat 1680
gggcatttcg cagcctaccg tggtgttcgt ttccaaaaag gggttgcaaa aaattttgaa 1740
cgtgcaaaaa aagctcccaa tcatccaaaa aattattatc atggattcta aaacggatta 1800
ccagggattt cagtcgatgt acacgttcgt cacatctcat ctacctcccg gttttaatga 1860
atacgatttt gtgccagagt ccttcgatag ggacaagaca attgcactga tcatgaactc 1920
ctctggatct actggtctgc ctaaaggtgt cgctctgcct catagaactg cctgcgtgag 1980
attctcgcat gccagagatc ctatttttgg caatcaaatc attccggata ctgcgatttt 2040
aagtgttgtt ccattccatc acggttttgg aatgtttact acactcggat atttgatatg 2100
tggatttcga gtcgtcttaa tgtatagatt tgaagaagag ctgtttctga ggagccttca 2160
ggattacaag attcaaagtg cgctgctggt gccaacccta ttctccttct tcgccaaaag 2220
cactctgatt gacaaatacg atttatctaa tttacacgaa attgcttctg gtggcgctcc 2280
cctctctaag gaagtcgggg aagcggttgc caagaggttc catctgccag gtatcaggca 2340
aggatatggg ctcactgaga ctacatcagc tattctgatt acacccgagg gggatgataa 2400
accgggcgcg gtcggtaaag ttgttccatt ttttgaagcg aaggttgtgg atctggatac 2460
cgggaaaacg ctgggcgtta atcaaagagg cgaactgtgt gtgagaggtc ctatgattat 2520
gtccggttat gtaaacaatc cggaagcgac caacgccttg attgacaagg atggatggct 2580
acattctgga gacatagctt actgggacga agacgaacac ttcttcatcg ttgaccgcct 2640
gaagtctctg attaagtaca aaggctatca ggtggctccc gctgaattgg aatccatctt 2700
gctccaacac cccaacatct tcgacgcagg tgtcgcaggt cttcccgacg atgacgccgg 2760
tgaacttccc gccgccgttg ttgttttgga gcacggaaag acgatgacgg aaaaagagat 2820
cgtggattac gtcgccagtc aagtaacaac cgcgaaaaag ttgcgcggag gagttgtgtt 2880
tgtggacgaa gtaccgaaag gtcttaccgg aaaactcgac gcaagaaaaa tcagagagat 2940
cctcataaag gccaagaagg gcggaaagat cgccgtgtaa gagcatctta ccgccattta 3000
ttcccatatt tgttctgttt ttcttgattt gggtatacat ttaaatgtta ataaaacaaa 3060
atggtggggc aatcatttac atttttaggg atatgtaatt actagttcag gtgtattgcc 3120
acaagacaaa catgttaaga aactttcccg ttatttacgc tctgttcctg ttaatcaacc 3180
tctggattac aaaatttgtg aaagattgac tgatattctt aactatgttg ctccttttac 3240
gctgtgtgga tatgctgctt tatagcctct gtatctagct attgcttccc gtacggcttt 3300
cgttttctcc tccttgtata aatcctggtt gctgtctctt ttagaggagt tgtggcccgt 3360
tgtccgtcaa cgtggcgtgg tgtgctctgt gtttgctgac gcaaccccca ctggctgggg 3420
cattgccacc acctgtcaac tcctttctgg gactttcgct ttccccctcc cgatcgccac 3480
ggcagaactc atcgccgcct gccttgcccg ctgctggaca ggggctaggt tgctgggcac 3540
tgataattcc gtggtgttgt ctgtgccttc tagttgccag ccatctgttg tttgcccctc 3600
ccccgtgcct tccttgaccc tggaaggtgc cactcccact gtcctttcct aataaaatga 3660
ggaaattgca tcgcattgtc tgagtaggtg tcattctatt ctggggggtg gggtggggca 3720
ggacagcaag ggggaggatt gggaagacaa tagcaggcat gctggggatg cggtgggctc 3780
tatggcagga acccctagtg atggagttgg ccactccctc tctgcgcgct cgctcgctca 3840
ctgaggccgc ccgggaaacc cgggcgtgcg cctcagtgag cgagcgagcg cgcagctgcc 3900
tgcagg 3906
<210> 59
<400> 59
000
<210> 60
<400> 60
000
<210> 61
<400> 61
000
<210> 62
<400> 62
000
<210> 63
<211> 126
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 63
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccgggaaacc cgggcgtgcc 60
cgggcgcctc agtgagcgag cgagcgcgca gagagggagt ggccaactcc atcactaggg 120
gttcct 126
<210> 64
<211> 120
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 64
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgcccggga aacccgggcg tgcgcctcag tgagcgagcg agcgcgcagc tgcctgcagg 120
<210> 65
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 65
gcgcgctcgc tcgctcactg aggccgcccg ggcgtcgggc gacctttggt cgcccggcct 60
cagtgagcga gcgagcgcgc 80
<210> 66
<211> 141
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 66
aataaacgat aacgccgttg gtggcgtgag gcatgtaaaa ggttacatca ttatcttgtt 60
cgccatccgg ttggtataaa tagacgttca tgttggtttt tgtttcagtt gcaagttggc 120
tgcggcgcgc gcagcacctt t 141
<210> 67
<211> 1876
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 67
cgcagccacc atggcggggt tttacgagat tgtgattaag gtccccagcg accttgacga 60
gcatctgccc ggcatttctg acagctttgt gaactgggtg gccgagaagg aatgggagtt 120
gccgccagat tctgacatgg atctgaatct gattgagcag gcacccctga ccgtggccga 180
gaagctgcag cgcgactttc tgacggaatg gcgccgtgtg agtaaggccc cggaggccct 240
tttctttgtg caatttgaga agggagagag ctacttccac atgcacgtgc tcgtggaaac 300
caccggggtg aaatccatgg ttttgggacg tttcctgagt cagattcgcg aaaaactgat 360
tcagagaatt taccgcggga tcgagccgac tttgccaaac tggttcgcgg tcacaaagac 420
cagaaatggc gccggaggcg ggaacaaggt ggtggatgag tgctacatcc ccaattactt 480
gctccccaaa acccagcctg agctccagtg ggcgtggact aatatggaac agtatttaag 540
cgcctgtttg aatctcacgg agcgtaaacg gttggtggcg cagcatctga cgcacgtgtc 600
gcagacgcag gagcagaaca aagagaatca gaatcccaat tctgatgcgc cggtgatcag 660
atcaaaaact tcagccaggt acatggagct ggtcgggtgg ctcgtggaca aggggattac 720
ctcggagaag cagtggatcc aggaggacca ggcctcatac atctccttca atgcggcctc 780
caactcgcgg tcccaaatca aggctgcctt ggacaatgcg ggaaagatta tgagcctgac 840
taaaaccgcc cccgactacc tggtgggcca gcagcccgtg gaggacattt ccagcaatcg 900
gatttataaa attttggaac taaacgggta cgatccccaa tatgcggctt ccgtctttct 960
gggatgggcc acgaaaaagt tcggcaagag gaacaccatc tggctgtttg ggcctgcaac 1020
taccgggaag accaacatcg cggaggccat agcccacact gtgcccttct acgggtgcgt 1080
aaactggacc aatgagaact ttcccttcaa cgactgtgtc gacaagatgg tgatctggtg 1140
ggaggagggg aagatgaccg ccaaggtcgt ggagtcggcc aaagccattc tcggaggaag 1200
caaggtgcgc gtggaccaga aatgcaagtc ctcggcccag atagacccga ctcccgtgat 1260
cgtcacctcc aacaccaaca tgtgcgccgt gattgacggg aactcaacga ccttcgaaca 1320
ccagcagccg ttgcaagacc ggatgttcaa atttgaactc acccgccgtc tggatcatga 1380
ctttgggaag gtcaccaagc aggaagtcaa agactttttc cggtgggcaa aggatcacgt 1440
ggttgaggtg gagcatgaat tctacgtcaa aaagggtgga gccaagaaaa gacccgcccc 1500
cagtgacgca gatataagtg agcccaaacg ggtgcgcgag tcagttgcgc agccatcgac 1560
gtcagacgcg gaagcttcga tcaactacgc agacaggtac caaaacaaat gttctcgtca 1620
cgtgggcatg aatctgatgc tgtttccctg cagacaatgc gagagaatga atcagaattc 1680
aaatatctgc ttcactcacg gacagaaaga ctgtttagag tgctttcccg tgtcagaatc 1740
tcaacccgtt tctgtcgtca aaaaggcgta tcagaaactg tgctacattc atcatatcat 1800
gggaaaggtg ccagacgctt gcactgcctg cgatctggtc aatgtggatt tggatgactg 1860
catctttgaa caataa 1876
<210> 68
<211> 129
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 68
atcatggaga taattaaaat gataaccatc tcgcaaataa ataagtattt tactgttttc 60
gtaacagttt tgtaataaaa aaacctataa atattccgga ttattcatac cgtcccacca 120
tcgggcgcg 129
<210> 69
<211> 1203
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 69
gccgccacca tggagttggt gggctggctc gtggacaaag gcattacttc ggaaaagcag 60
tggattcagg aggatcaggc atcttacatc tcattcaacg ctgccagtaa ctcgaggtcc 120
cagatcaagg cagcgctgga caacgcggga aagattatga gtctgaccaa aactgctcca 180
gactacctcg ttggtcagca accggtggaa gatatctcca gcaacaggat ctacaagatt 240
ctggagctca acggctacga ccctcaatac gctgcctcag tgttcttggg ttgggccacc 300
aagaaattcg gcaagagaaa cactatctgg ctgttcggcc ccgctaccac tggaaagaca 360
aacatcgcag aagcgattgc tcacacggtg ccattctacg gctgcgtcaa ctggacaaac 420
gagaacttcc cgttcaacga ctgtgtcgat aagatggtta tctggtggga ggaaggaaag 480
atgacggcca aagtggtcga aagcgccaag gcaattctgg gtggctctaa agtgcgcgtc 540
gaccagaagt gcaaatcttc agctcaaatc gatcctaccc ccgttattgt gacatcaaac 600
acgaacatgt gtgccgtgat cgacggaaac agtacaacgt tcgaacacca gcaacctctc 660
caggatcgta tgttcaagtt cgagctcacc cgccgtttgg accatgattt cggcaaggtc 720
actaaacaag aggttaagga cttcttccgc tgggctaaag atcacgttgt ggaggttgaa 780
catgagttct acgtcaagaa aggaggtgct aagaaacgtc cagccccgtc ggacgcagat 840
atctccgaac ctaagagggt gagagagtcg gtcgcacagc caagcacttc tgacgcagaa 900
gcttccatta actacgcaga taggtaccaa aacaagtgca gcagacacgt gggtatgaac 960
ttgatgctgt tcccatgccg ccagtgtgag cgtatgaacc aaaactctaa catctgtttc 1020
acacatggcc agaaggactg cctcgaatgt ttccctgtgt cagagagtca gcccgtctca 1080
gtcgttaaga aagcttacca aaagttgtgc tacatccacc atattatggg taaagtccct 1140
gatgcctgta ccgcttgtga tctggtcaac gtggatttgg acgactgtat tttcgagcaa 1200
taa 1203
<210> 70
<211> 388
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 70
gaacagagaa acaggagaat atgggccaaa caggatatct gtggtaagca gttcctgccc 60
cggctcaggg ccaagaacag ttggaacagc agaatatggg ccaaacagga tatctgtggt 120
aagcagttcc tgccccggct cagggccaag aacagatggt ccccagatgc ggtcccgccc 180
tcagcagttt ctagagaacc atcagatgtt tccagggtgc cccaaggacc tgaaatgacc 240
ctgtgcctta tttgaactaa ccaatcagtt cgcttctcgc ttctgttcgc gcgcttctgc 300
tccccgagct ctatataagc agagctcgtt tagtgaaccg tcagatcgcc tggagacgcc 360
atccacgctg ttttgacttc catagaag 388
<210> 71
<211> 1662
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 71
gccgccacca tggaagacgc caaaaacata aagaaaggcc cggcgccatt ctatccgctg 60
gaagatggaa ccgctggaga gcaactgcat aaggctatga agagatacgc cctggttcct 120
ggaacaattg cttttacaga tgcacatatc gaggtggaca tcacttacgc tgagtacttc 180
gaaatgtccg ttcggttggc agaagctatg aaacgatatg ggctgaatac aaatcacaga 240
atcgtcgtat gcagtgaaaa ctctcttcaa ttctttatgc cggtgttggg cgcgttattt 300
atcggagttg cagttgcgcc cgcgaacgac atttataatg aacgtgaatt gctcaacagt 360
atgggcattt cgcagcctac cgtggtgttc gtttccaaaa aggggttgca aaaaattttg 420
aacgtgcaaa aaaagctccc aatcatccaa aaaattatta tcatggattc taaaacggat 480
taccagggat ttcagtcgat gtacacgttc gtcacatctc atctacctcc cggttttaat 540
gaatacgatt ttgtgccaga gtccttcgat agggacaaga caattgcact gatcatgaac 600
tcctctggat ctactggtct gcctaaaggt gtcgctctgc ctcatagaac tgcctgcgtg 660
agattctcgc atgccagaga tcctattttt ggcaatcaaa tcattccgga tactgcgatt 720
ttaagtgttg ttccattcca tcacggtttt ggaatgttta ctacactcgg atatttgata 780
tgtggatttc gagtcgtctt aatgtataga tttgaagaag agctgtttct gaggagcctt 840
caggattaca agattcaaag tgcgctgctg gtgccaaccc tattctcctt cttcgccaaa 900
agcactctga ttgacaaata cgatttatct aatttacacg aaattgcttc tggtggcgct 960
cccctctcta aggaagtcgg ggaagcggtt gccaagaggt tccatctgcc aggtatcagg 1020
caaggatatg ggctcactga gactacatca gctattctga ttacacccga gggggatgat 1080
aaaccgggcg cggtcggtaa agttgttcca ttttttgaag cgaaggttgt ggatctggat 1140
accgggaaaa cgctgggcgt taatcaaaga ggcgaactgt gtgtgagagg tcctatgatt 1200
atgtccggtt atgtaaacaa tccggaagcg accaacgcct tgattgacaa ggatggatgg 1260
ctacattctg gagacatagc ttactgggac gaagacgaac acttcttcat cgttgaccgc 1320
ctgaagtctc tgattaagta caaaggctat caggtggctc ccgctgaatt ggaatccatc 1380
ttgctccaac accccaacat cttcgacgca ggtgtcgcag gtcttcccga cgatgacgcc 1440
ggtgaacttc ccgccgccgt tgttgttttg gagcacggaa agacgatgac ggaaaaagag 1500
atcgtggatt acgtcgccag tcaagtaaca accgcgaaaa agttgcgcgg aggagttgtg 1560
tttgtggacg aagtaccgaa aggtcttacc ggaaaactcg acgcaagaaa aatcagagag 1620
atcctcataa aggccaagaa gggcggaaag atcgccgtgt aa 1662
<210> 72
<211> 581
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 72
gagcatctta ccgccattta ttcccatatt tgttctgttt ttcttgattt gggtatacat 60
ttaaatgtta ataaaacaaa atggtggggc aatcatttac atttttaggg atatgtaatt 120
actagttcag gtgtattgcc acaagacaaa catgttaaga aactttcccg ttatttacgc 180
tctgttcctg ttaatcaacc tctggattac aaaatttgtg aaagattgac tgatattctt 240
aactatgttg ctccttttac gctgtgtgga tatgctgctt tatagcctct gtatctagct 300
attgcttccc gtacggcttt cgttttctcc tccttgtata aatcctggtt gctgtctctt 360
ttagaggagt tgtggcccgt tgtccgtcaa cgtggcgtgg tgtgctctgt gtttgctgac 420
gcaaccccca ctggctgggg cattgccacc acctgtcaac tcctttctgg gactttcgct 480
ttccccctcc cgatcgccac ggcagaactc atcgccgcct gccttgcccg ctgctggaca 540
ggggctaggt tgctgggcac tgataattcc gtggtgttgt c 581
<210> 73
<211> 225
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 73
tgtgccttct agttgccagc catctgttgt ttgcccctcc cccgtgcctt ccttgaccct 60
ggaaggtgcc actcccactg tcctttccta ataaaatgag gaaattgcat cgcattgtct 120
gagtaggtgt cattctattc tggggggtgg ggtggggcag gacagcaagg gggaggattg 180
ggaagacaat agcaggcatg ctggggatgc ggtgggctct atggc 225
<210> 74
<211> 1177
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 74
ggctcagagg ctcagaggca cacaggagtt tctgggctca ccctgccccc ttccaacccc 60
tcagttccca tcctccagca gctgtttgtg tgctgcctct gaagtccaca ctgaacaaac 120
ttcagcctac tcatgtccct aaaatgggca aacattgcaa gcagcaaaca gcaaacacac 180
agccctccct gcctgctgac cttggagctg gggcagaggt cagagacctc tctgggccca 240
tgccacctcc aacatccact cgaccccttg gaatttcggt ggagaggagc agaggttgtc 300
ctggcgtggt ttaggtagtg tgagagggtc cgggttcaaa accacttgct gggtggggag 360
tcgtcagtaa gtggctatgc cccgaccccg aagcctgttt ccccatctgt acaatggaaa 420
tgataaagac gcccatctga tagggttttt gtggcaaata aacatttggt ttttttgttt 480
tgttttgttt tgttttttga gatggaggtt tgctctgtcg cccaggctgg agtgcagtga 540
cacaatctca tctcaccaca accttcccct gcctcagcct cccaagtagc tgggattaca 600
agcatgtgcc accacacctg gctaattttc tatttttagt agagacgggt ttctccatgt 660
tggtcagcct cagcctccca agtaactggg attacaggcc tgtgccacca cacccggcta 720
attttttcta tttttgacag ggacggggtt tcaccatgtt ggtcaggctg gtctagaggt 780
accggatctt gctaccagtg gaacagccac taaggattct gcagtgagag cagagggcca 840
gctaagtggt actctcccag agactgtctg actcacgcca ccccctccac cttggacaca 900
ggacgctgtg gtttctgagc caggtacaat gactcctttc ggtaagtgca gtggaagctg 960
tacactgccc aggcaaagcg tccgggcagc gtaggcgggc gactcagatc ccagccagtg 1020
gacttagccc ctgtttgctc ctccgataac tggggtgacc ttggttaata ttcaccagca 1080
gcctcccccg ttgcccctct ggatccactg cttaaatacg gacgaggaca gggccctgtc 1140
tcctcagctt caggcaccac cactgacctg ggacagt 1177
<210> 75
<400> 75
000
<210> 76
<400> 76
000
<210> 77
<400> 77
000
<210> 78
<400> 78
000
<210> 79
<400> 79
000
<210> 80
<400> 80
000
<210> 81
<400> 81
000
<210> 82
<400> 82
000
<210> 83
<400> 83
000
<210> 84
<400> 84
000
<210> 85
<400> 85
000
<210> 86
<400> 86
000
<210> 87
<400> 87
000
<210> 88
<400> 88
000
<210> 89
<400> 89
000
<210> 90
<400> 90
000
<210> 91
<400> 91
000
<210> 92
<400> 92
000
<210> 93
<400> 93
000
<210> 94
<400> 94
000
<210> 95
<400> 95
000
<210> 96
<400> 96
000
<210> 97
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 97
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgcc cgggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 98
<211> 72
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 98
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacggc ctcagtgagc 60
gagcgagcgc gc 72
<210> 99
<211> 122
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 99
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgacc aaaggtcgcc cgacggcctc agtgagcgag cgagcgcgca gctgcctgca 120
gg 122
<210> 100
<211> 130
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 100
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgacc aaaggtcgcc cgacgcccgg gcggcctcag tgagcgagcg agcgcgcagc 120
tgcctgcagg 130
<210> 101
<211> 70
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 101
gcgcgctcgc tcgctcactg aggccgcccg ggaaacccgg gcgtgcgcct cagtgagcga 60
gcgagcgcgc 70
<210> 102
<211> 70
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 102
gcgcgctcgc tcgctcactg aggcgcacgc ccgggtttcc cgggcggcct cagtgagcga 60
gcgagcgcgc 70
<210> 103
<211> 72
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 103
gcgcgctcgc tcgctcactg aggccgtcgg gcgacctttg gtcgcccggc ctcagtgagc 60
gagcgagcgc gc 72
<210> 104
<211> 72
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 104
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacggc ctcagtgagc 60
gagcgagcgc gc 72
<210> 105
<211> 72
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 105
gcgcgctcgc tcgctcactg aggccgcccg ggcaaagccc gggcgtcggc ctcagtgagc 60
gagcgagcgc gc 72
<210> 106
<211> 72
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 106
gcgcgctcgc tcgctcactg aggccgacgc ccgggctttg cccgggcggc ctcagtgagc 60
gagcgagcgc gc 72
<210> 107
<211> 83
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 107
gcgcgctcgc tcgctcactg aggccgcccg ggcaaagccc gggcgtcggg ctttgcccgg 60
cctcagtgag cgagcgagcg cgc 83
<210> 108
<211> 83
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 108
gcgcgctcgc tcgctcactg aggccgggca aagcccgacg cccgggcttt gcccgggcgg 60
cctcagtgag cgagcgagcg cgc 83
<210> 109
<211> 77
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 109
gcgcgctcgc tcgctcactg aggccgaaac gtcgggcgac ctttggtcgc ccggcctcag 60
tgagcgagcg agcgcgc 77
<210> 110
<211> 77
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 110
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgtt tcggcctcag 60
tgagcgagcg agcgcgc 77
<210> 111
<211> 51
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 111
gcgcgctcgc tcgctcactg aggcaaagcc tcagtgagcg agcgagcgcg c 51
<210> 112
<211> 51
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 112
gcgcgctcgc tcgctcactg aggctttgcc tcagtgagcg agcgagcgcg c 51
<210> 113
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 113
gcgcgctcgc tcgctcactg aggccgcccg ggcgtcgggc gacctttggt cgcccggcct 60
cagtgagcga gcgagcgcgc 80
<210> 114
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 114
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgcc cgggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 115
<211> 77
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 115
gcgcgctcgc tcgctcactg aggcgcccgg gcgtcgggcg acctttggtc gcccggcctc 60
agtgagcgag cgagcgc 77
<210> 116
<211> 79
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 116
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgcc cgggcgcctc 60
agtgagcgag cgagcgcgc 79
<210> 117
<211> 89
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 117
gcgcgctcgc tcgctcactg aggccgcccg ggcaaagccc gggcgtcggg cgactttgtc 60
gcccggcctc agtgagcgag cgagcgcgc 89
<210> 118
<211> 89
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 118
gcgcgctcgc tcgctcactg aggccgggcg acaaagtcgc ccgacgcccg ggctttgccc 60
gggcggcctc agtgagcgag cgagcgcgc 89
<210> 119
<211> 87
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 119
gcgcgctcgc tcgctcactg aggccgcccg ggcaaagccc gggcgtcggg cgattttcgc 60
ccggcctcag tgagcgagcg agcgcgc 87
<210> 120
<211> 87
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 120
gcgcgctcgc tcgctcactg aggccgggcg aaaatcgccc gacgcccggg ctttgcccgg 60
gcggcctcag tgagcgagcg agcgcgc 87
<210> 121
<211> 85
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 121
gcgcgctcgc tcgctcactg aggccgcccg ggcaaagccc gggcgtcggg cgtttcgccc 60
ggcctcagtg agcgagcgag cgcgc 85
<210> 122
<211> 85
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 122
gcgcgctcgc tcgctcactg aggccgggcg aaacgcccga cgcccgggct ttgcccgggc 60
ggcctcagtg agcgagcgag cgcgc 85
<210> 123
<211> 89
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 123
gcgcgctcgc tcgctcactg aggccgcccg ggaaacccgg gcgtcgggcg acctttggtc 60
gcccggcctc agtgagcgag cgagcgcgc 89
<210> 124
<211> 89
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 124
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgcc cgggtttccc 60
gggcggcctc agtgagcgag cgagcgcgc 89
<210> 125
<211> 87
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 125
gcgcgctcgc tcgctcactg aggccgcccg gaaaccgggc gtcgggcgac ctttggtcgc 60
ccggcctcag tgagcgagcg agcgcgc 87
<210> 126
<211> 87
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 126
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgcc cggtttccgg 60
gcggcctcag tgagcgagcg agcgcgc 87
<210> 127
<211> 85
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 127
gcgcgctcgc tcgctcactg aggccgcccg aaacgggcgt cgggcgacct ttggtcgccc 60
ggcctcagtg agcgagcgag cgcgc 85
<210> 128
<211> 85
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 128
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgcc cgtttcgggc 60
ggcctcagtg agcgagcgag cgcgc 85
<210> 129
<211> 83
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 129
gcgcgctcgc tcgctcactg aggccgccca aagggcgtcg ggcgaccttt ggtcgcccgg 60
cctcagtgag cgagcgagcg cgc 83
<210> 130
<211> 83
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 130
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgcc ctttgggcgg 60
cctcagtgag cgagcgagcg cgc 83
<210> 131
<211> 81
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 131
gcgcgctcgc tcgctcactg aggccgccaa aggcgtcggg cgacctttgg tcgcccggcc 60
tcagtgagcg agcgagcgcg c 81
<210> 132
<211> 81
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 132
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgcc tttggcggcc 60
tcagtgagcg agcgagcgcg c 81
<210> 133
<211> 79
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 133
gcgcgctcgc tcgctcactg aggccgcaaa gcgtcgggcg acctttggtc gcccggcctc 60
agtgagcgag cgagcgcgc 79
<210> 134
<211> 79
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 134
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgct ttgcggcctc 60
agtgagcgag cgagcgcgc 79
<210> 135
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 135
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgaagcc cgggctgcct 60
cagtgagcga gcgagcgcgc 80
<210> 136
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 136
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacacc cgggtggcct 60
cagtgagcga gcgagcgcgc 80
<210> 137
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 137
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgac cggtcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 138
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 138
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgca cgtgcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 139
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 139
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgcc atggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 140
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 140
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgaagac cggtctgcct 60
cagtgagcga gcgagcgcgc 80
<210> 141
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 141
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacaca cgtgtggcct 60
cagtgagcga gcgagcgcgc 80
<210> 142
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 142
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgac atgtcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 143
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 143
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgaagca cgtgctgcct 60
cagtgagcga gcgagcgcgc 80
<210> 144
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 144
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgaaacc cgggttgcct 60
cagtgagcga gcgagcgcgc 80
<210> 145
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 145
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgaagcc atggctgcct 60
cagtgagcga gcgagcgcgc 80
<210> 146
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 146
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacaac cggttggcct 60
cagtgagcga gcgagcgcgc 80
<210> 147
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 147
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacacc atggtggcct 60
cagtgagcga gcgagcgcgc 80
<210> 148
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 148
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgaa cgttcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 149
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 149
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgca attgcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 150
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 150
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgaaaac cggtttgcct 60
cagtgagcga gcgagcgcgc 80
<210> 151
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 151
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgaagaa cgttctgcct 60
cagtgagcga gcgagcgcgc 80
<210> 152
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 152
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgaagca attgctgcct 60
cagtgagcga gcgagcgcgc 80
<210> 153
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 153
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacaaa cgtttggcct 60
cagtgagcga gcgagcgcgc 80
<210> 154
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 154
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgaa atttcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 155
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 155
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgaagca attgctgcct 60
cagtgagcga gcgagcgcgc 80
<210> 156
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 156
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgaaacc atggttgcct 60
cagtgagcga gcgagcgcgc 80
<210> 157
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 157
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacaac atgttggcct 60
cagtgagcga gcgagcgcgc 80
<210> 158
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 158
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgaagac atgtctgcct 60
cagtgagcga gcgagcgcgc 80
<210> 159
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 159
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacaca attgtggcct 60
cagtgagcga gcgagcgcgc 80
<210> 160
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 160
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgaaaaa cgttttgcct 60
cagtgagcga gcgagcgcgc 80
<210> 161
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 161
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgaaaac atgtttgcct 60
cagtgagcga gcgagcgcgc 80
<210> 162
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 162
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgaaaca attgttgcct 60
cagtgagcga gcgagcgcgc 80
<210> 163
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 163
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgaagaa atttctgcct 60
cagtgagcga gcgagcgcgc 80
<210> 164
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 164
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacaaa attttggcct 60
cagtgagcga gcgagcgcgc 80
<210> 165
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 165
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgaaaaa atttttgcct 60
cagtgagcga gcgagcgcgc 80
<210> 166
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 166
gcgcgctcgc tcgctcgctg aggccgggcg accaaaggtc gcccgacgcc cgggcggcct 60
cagcgagcga gcgagcgcgc 80
<210> 167
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 167
gcgcgctcgc tcgctcaatg aggccgggcg accaaaggtc gcccgacgcc cgggcggcct 60
cattgagcga gcgagcgcgc 80
<210> 168
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 168
gcgcgctcgc tcgctcaccg aggccgggcg accaaaggtc gcccgacgcc cgggcggcct 60
cggtgagcga gcgagcgcgc 80
<210> 169
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 169
gcgcgctcgc tcgctcacta aggccgggcg accaaaggtc gcccgacgcc cgggcggcct 60
tagtgagcga gcgagcgcgc 80
<210> 170
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 170
gcgcgctcgc tcgctcactg gggccgggcg accaaaggtc gcccgacgcc cgggcggccc 60
cagtgagcga gcgagcgcgc 80
<210> 171
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 171
gcgcgctcgc tcgctcactg aagccgggcg accaaaggtc gcccgacgcc cgggcggctt 60
cagtgagcga gcgagcgcgc 80
<210> 172
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 172
gcgcgctcgc tcgctcactg agaccgggcg accaaaggtc gcccgacgcc cgggcggtct 60
cagtgagcga gcgagcgcgc 80
<210> 173
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 173
gcgcgctcgc tcgctcgatg aggccgggcg accaaaggtc gcccgacgcc cgggcggcct 60
catcgagcga gcgagcgcgc 80
<210> 174
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 174
gcgcgctcgc tcgctcgcgg aggccgggcg accaaaggtc gcccgacgcc cgggcggcct 60
ccgcgagcga gcgagcgcgc 80
<210> 175
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 175
gcgcgctcgc tcgctcgcta aggccgggcg accaaaggtc gcccgacgcc cgggcggcct 60
tagtgagcga gcgagcgcgc 80
<210> 176
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 176
gcgcgctcgc tcgctcgctg gggccgggcg accaaaggtc gcccgacgcc cgggcggccc 60
cagcgagcga gcgagcgcgc 80
<210> 177
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 177
gcgcgctcgc tcgctcgctg aagccgggcg accaaaggtc gcccgacgcc cgggcggctt 60
cagcgagcga gcgagcgcgc 80
<210> 178
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 178
gcgcgctcgc tcgctcgctg agaccgggcg accaaaggtc gcccgacgcc cgggcggtct 60
cagcgagcga gcgagcgcgc 80
<210> 179
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 179
gcgcgctcgc tcgctcgagg aggccgggcg accaaaggtc gcccgacgcc cgggcggcct 60
cctcgagcga gcgagcgcgc 80
<210> 180
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 180
gcgcgctcgc tcgctcgata aggccgggcg accaaaggtc gcccgacgcc cgggcggcct 60
tatcgagcga gcgagcgcgc 80
<210> 181
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 181
gcgcgctcgc tcgctcgatg gggccgggcg accaaaggtc gcccgacgcc cgggcggcct 60
catcgagcga gcgagcgcgc 80
<210> 182
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 182
gcgcgctcgc tcgctcgatg aagccgggcg accaaaggtc gcccgacgcc cgggcggctt 60
catcgagcga gcgagcgcgc 80
<210> 183
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 183
gcgcgctcgc tcgctcgatg agaccgggcg accaaaggtc gcccgacgcc cgggcggtct 60
catcgagcga gcgagcgcgc 80
<210> 184
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 184
gcgcgctcgc tcgctcgaga aggccgggcg accaaaggtc gcccgacgcc cgggcggcct 60
tctcgagcga gcgagcgcgc 80
<210> 185
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 185
gcgcgctcgc tcgctcgagg gggccgggcg accaaaggtc gcccgacgcc cgggcggccc 60
cctcgagcga gcgagcgcgc 80
<210> 186
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 186
gcgcgctcgc tcgctcgagg aagccgggcg accaaaggtc gcccgacgcc cgggcggctt 60
cctcgagcga gcgagcgcgc 80
<210> 187
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 187
gcgcgctcgc tcgctcgagg gggccgggcg accaaaggtc gcccgacgcc cgggcggccc 60
cctcgagcga gcgagcgcgc 80
<210> 188
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 188
gcgcgctcgc tcgctcgagg aagccgggcg accaaaggtc gcccgacgcc cgggcggctt 60
cctcgagcga gcgagcgcgc 80
<210> 189
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 189
gcgcgctcgc tcgctcgagg agaccgggcg accaaaggtc gcccgacgcc cgggcggtct 60
cctcgagcga gcgagcgcgc 80
<210> 190
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 190
gcgcgctcgc tcgctcgaga gggccgggcg accaaaggtc gcccgacgcc cgggcggccc 60
tctcgagcga gcgagcgcgc 80
<210> 191
<400> 191
000
<210> 192
<400> 192
000
<210> 193
<400> 193
000
<210> 194
<400> 194
000
<210> 195
<400> 195
000
<210> 196
<400> 196
000
<210> 197
<400> 197
000
<210> 198
<400> 198
000
<210> 199
<400> 199
000
<210> 200
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 200
gcgcgctcgc tcgctcgaga aagccgggcg accaaaggtc gcccgacgcc cgggcggctt 60
tctcgagcga gcgagcgcgc 80
<210> 201
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 201
gcgcgctcgc tcgctcgaga agaccgggcg accaaaggtc gcccgacgcc cgggcggcct 60
tctcgagcga gcgagcgcgc 80
<210> 202
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 202
gcgcgctcgc tcgctcgaga gagccgggcg accaaaggtc gcccgacgcc cgggcggctc 60
tctcgagcga gcgagcgcgc 80
<210> 203
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 203
gcgcgctcgc tcgctcgaga ggaccgggcg accaaaggtc gcccgacgcc cgggcggtcc 60
tctcgagcga gcgagcgcgc 80
<210> 204
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 204
gcgcgctcgc tcgctcgaga gaaccgggcg accaaaggtc gcccgacgcc cgggcggttc 60
tctcgagcga gcgagcgcgc 80
<210> 205
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 205
gcgcgctcgc tcgctcaaga gaaccgggcg accaaaggtc gcccgacgcc cgggcggttc 60
tcttgagcga gcgagcgcgc 80
<210> 206
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 206
gcgcgctcgc tcgctcacga gaaccgggcg accaaaggtc gcccgacgcc cgggcggttc 60
tcgtgagcga gcgagcgcgc 80
<210> 207
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 207
gcgcgctcgc tcgctcacta gaaccgggcg accaaaggtc gcccgacgcc cgggcggttc 60
tagtgagcga gcgagcgcgc 80
<210> 208
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 208
gcgcgctcgc tcgctcactg gaaccgggcg accaaaggtc gcccgacgcc cgggcggttc 60
cagtgagcga gcgagcgcgc 80
<210> 209
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 209
gcgcgctcgc tcgctcactg aaaccgggcg accaaaggtc gcccgacgcc cgggcggttt 60
cagtgagcga gcgagcgcgc 80
<210> 210
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 210
gcgcgctcgc tcgctcgcgg gggccgggcg accaaaggtc gcccgacgcc cgggcggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 211
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 211
gcgcgctcgc tcgctcaata aaaccgggcg accaaaggtc gcccgacgcc cgggcggttt 60
tattgagcga gcgagcgcgc 80
<210> 212
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 212
gcgcgctcgc tcgctcactg aggccaggcg accaaaggtc gcctgacgcc cgggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 213
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 213
gcgcgctcgc tcgctcactg aggccgagcg accaaaggtc gctcgacgcc cgggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 214
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 214
gcgcgctcgc tcgctcactg aggccggacg accaaaggtc gtccgacgcc cgggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 215
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 215
gcgcgctcgc tcgctcactg aggccgggag accaaaggtc tcccgacgcc cgggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 216
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 216
gcgcgctcgc tcgctcactg aggccgggca accaaaggtt gcccgacgcc cgggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 217
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 217
gcgcgctcgc tcgctcactg aggccgggcg gccaaaggcc gcccgacgcc cgggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 218
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 218
gcgcgctcgc tcgctcactg aggccgggcg aacaaagttc gcccgacgcc cgggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 219
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 219
gcgcgctcgc tcgctcactg aggccgggcg acaaaatgtc gcccgacgcc cgggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 220
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 220
gcgcgctcgc tcgctcactg aggccaagcg accaaaggtc gcttgacgcc cgggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 221
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 221
gcgcgctcgc tcgctcactg aggccaaacg accaaaggtc gtttgacgcc cgggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 222
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 222
gcgcgctcgc tcgctcactg aggccaaaag accaaaggtc ttttgacgcc cgggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 223
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 223
gcgcgctcgc tcgctcactg aggccaaaaa accaaaggtt ttttgacgcc cgggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 224
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 224
gcgcgctcgc tcgctcactg aggccaaaaa gccaaaggct ttttgacgcc cgggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 225
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 225
gcgcgctcgc tcgctcactg aggccaaaaa gacaaagtct ttttgacgcc cgggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 226
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 226
gcgcgctcgc tcgctcactg aggccaaaaa gaaaaattct ttttgacgcc cgggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 227
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 227
gcgcgctcgc tcgctcactg aggccaaaaa aaaaaatttt ttttgacgcc cgggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 228
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 228
gcgcgctcgc tcgctcactg aggccgaaaa aaaaaatttt tttcgacgcc cgggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 229
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 229
gcgcgctcgc tcgctcactg aggccggaaa gaaaaattct ttccgacgcc cgggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 230
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 230
gcgcgctcgc tcgctcactg aggccgggaa gaaaaattct tcccgacgcc cgggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 231
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 231
gcgcgctcgc tcgctcactg aggccgggca gaaaaattct gcccgacgcc cgggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 232
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 232
gcgcgctcgc tcgctcactg aggccgggcg gaaaaattcc gcccgacgcc cgggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 233
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 233
gcgcgctcgc tcgctcactg aggccgggcg aaaaaatttc gcccgacgcc cgggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 234
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 234
gcgcgctcgc tcgctcactg aggccaggcg accaaaggtc gcctgacacc cgggtggcct 60
cagtgagcga gcgagcgcgc 80
<210> 235
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 235
gcgcgctcgc tcgctcactg aggccaggcg accaaaggtc gcctgacgcc atggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 236
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 236
gcgcgctcgc tcgctcactg aggccaggcg accaaaggtc gcctgacgac atgtcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 237
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 237
gcgcgctcgc tcgctcactg aggccaggcg accaaaggtc gcctgacgaa cgttcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 238
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 238
gcgcgctcgc tcgctcactg aggccaggcg accaaaggtc gcctgaagca attgctgcct 60
cagtgagcga gcgagcgcgc 80
<210> 239
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 239
gcgcgctcgc tcgctcactg aggccgggcg gccaaaggcc gcccgacacc cgggtggcct 60
cagtgagcga gcgagcgcgc 80
<210> 240
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 240
gcgcgctcgc tcgctcactg aggccgggcg gccaaaggcc gcccgacgcc atggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 241
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 241
gcgcgctcgc tcgctcactg aggccgggcg gccaaaggcc gcccgacgac atgtcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 242
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 242
gcgcgctcgc tcgctcactg aggccgggcg gccaaaggcc gcccgacgaa cgttcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 243
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 243
gcgcgctcgc tcgctcactg aggccgggcg gccaaaggcc gcccgaagca attgctgcct 60
cagtgagcga gcgagcgcgc 80
<210> 244
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 244
gcgcgctcgc tcgctcactg aggccgggcg acaaaatgtc gcccgacacc cgggtggcct 60
cagtgagcga gcgagcgcgc 80
<210> 245
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 245
gcgcgctcgc tcgctcactg aggccgggcg acaaaatgtc gcccgacgcc atggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 246
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 246
gcgcgctcgc tcgctcactg aggccgggcg acaaaatgtc gcccgacgac atgtcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 247
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 247
gcgcgctcgc tcgctcactg aggccgggcg acaaaatgtc gcccgacgaa cgttcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 248
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 248
gcgcgctcgc tcgctcactg aggccgggcg acaaaatgtc gcccgaagca attgctgcct 60
cagtgagcga gcgagcgcgc 80
<210> 249
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 249
gcgcgctcgc tcgctcactg aggccaaaag accaaaggtc ttttgacacc cgggtggcct 60
cagtgagcga gcgagcgcgc 80
<210> 250
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 250
gcgcgctcgc tcgctcactg aggccaaaag accaaaggtc ttttgacgcc atggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 251
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 251
gcgcgctcgc tcgctcactg aggccaaaag accaaaggtc ttttgacgac atgtcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 252
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 252
gcgcgctcgc tcgctcactg aggccaaaag accaaaggtc ttttgacgaa cgttcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 253
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 253
gcgcgctcgc tcgctcactg aggccaaaag accaaaggtc ttttgaagca attgctgcct 60
cagtgagcga gcgagcgcgc 80
<210> 254
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 254
gcgcgctcgc tcgctcactg aggccaaaaa aaaaaatttt ttttgacacc cgggtggcct 60
cagtgagcga gcgagcgcgc 80
<210> 255
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 255
gcgcgctcgc tcgctcactg aggccaaaaa aaaaaatttt ttttgacgcc atggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 256
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 256
gcgcgctcgc tcgctcactg aggccaaaaa aaaaaatttt ttttgacgac atgtcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 257
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 257
gcgcgctcgc tcgctcactg aggccaaaaa aaaaaatttt ttttgacgaa cgttcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 258
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 258
gcgcgctcgc tcgctcactg aggccaaaaa aaaaaatttt ttttgaagca attgctgcct 60
cagtgagcga gcgagcgcgc 80
<210> 259
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 259
gcgcgctcgc tcgctcactg aggccgggca gaaaaattct gcccgacacc cgggtggcct 60
cagtgagcga gcgagcgcgc 80
<210> 260
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 260
gcgcgctcgc tcgctcactg aggccgggca gaaaaattct gcccgacgcc atggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 261
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 261
gcgcgctcgc tcgctcactg aggccgggca gaaaaattct gcccgacgac atgtcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 262
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 262
gcgcgctcgc tcgctcactg aggccgggca gaaaaattct gcccgacgaa cgttcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 263
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 263
gcgcgctcgc tcgctcactg aggccgggca gaaaaattct gcccgaagca attgctgcct 60
cagtgagcga gcgagcgcgc 80
<210> 264
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 264
gcgcgctcgc tcgctcacta aggccaggcg accaaaggtc gcctgacgcc cgggcggcct 60
tagtgagcga gcgagcgcgc 80
<210> 265
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 265
gcgcgctcgc tcgctcacta aggccgggcg gccaaaggcc gcccgacgcc cgggcggcct 60
tagtgagcga gcgagcgcgc 80
<210> 266
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 266
gcgcgctcgc tcgctcacta aggccgggcg acaaaatgtc gcccgacgcc cgggcggcct 60
tagtgagcga gcgagcgcgc 80
<210> 267
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 267
gcgcgctcgc tcgctcacta aggccaaaag accaaaggtc ttttgacgcc cgggcggcct 60
tagtgagcga gcgagcgcgc 80
<210> 268
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 268
gcgcgctcgc tcgctcacta aggccaaaaa aaaaaatttt ttttgacgcc cgggcggcct 60
tagtgagcga gcgagcgcgc 80
<210> 269
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 269
gcgcgctcgc tcgctcacta aggccgggca gaaaaattct gcccgacgcc cgggcggcct 60
tagtgagcga gcgagcgcgc 80
<210> 270
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 270
gcgcgctcgc tcgctcgatg gggccaggcg accaaaggtc gcctgacgcc cgggcggcct 60
catcgagcga gcgagcgcgc 80
<210> 271
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 271
gcgcgctcgc tcgctcgatg gggccgggcg gccaaaggcc gcccgacgcc cgggcggcct 60
catcgagcga gcgagcgcgc 80
<210> 272
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 272
gcgcgctcgc tcgctcgatg gggccgggcg acaaaatgtc gcccgacgcc cgggcggcct 60
catcgagcga gcgagcgcgc 80
<210> 273
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 273
gcgcgctcgc tcgctcgatg gggccaaaag accaaaggtc ttttgacgcc cgggcggcct 60
catcgagcga gcgagcgcgc 80
<210> 274
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 274
gcgcgctcgc tcgctcgatg gggccaaaaa aaaaaatttt ttttgacgcc cgggcggcct 60
catcgagcga gcgagcgcgc 80
<210> 275
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 275
gcgcgctcgc tcgctcgatg gggccgggca gaaaaattct gcccgacgcc cgggcggcct 60
catcgagcga gcgagcgcgc 80
<210> 276
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 276
gcgcgctcgc tcgctcgaga gaaccaggcg accaaaggtc gcctgacgcc cgggcggttc 60
tctcgagcga gcgagcgcgc 80
<210> 277
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 277
gcgcgctcgc tcgctcgaga gaaccgggcg gccaaaggcc gcccgacgcc cgggcggttc 60
tctcgagcga gcgagcgcgc 80
<210> 278
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 278
gcgcgctcgc tcgctcgaga gaaccgggcg acaaaatgtc gcccgacgcc cgggcggttc 60
tctcgagcga gcgagcgcgc 80
<210> 279
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 279
gcgcgctcgc tcgctcgaga gaaccaaaag accaaaggtc ttttgacgcc cgggcggttc 60
tctcgagcga gcgagcgcgc 80
<210> 280
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 280
gcgcgctcgc tcgctcgaga gaaccaaaaa aaaaaatttt ttttgacgcc cgggcggttc 60
tctcgagcga gcgagcgcgc 80
<210> 281
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 281
gcgcgctcgc tcgctcgaga gaaccgggca gaaaaattct gcccgacgcc cgggcggttc 60
tctcgagcga gcgagcgcgc 80
<210> 282
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 282
gcgcgctcgc tcgctcgcgg gggccaggcg accaaaggtc gcctgacgcc cgggcggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 283
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 283
gcgcgctcgc tcgctcgcgg gggccgggcg gccaaaggcc gcccgacgcc cgggcggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 284
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 284
gcgcgctcgc tcgctcgcgg gggccgggcg acaaaatgtc gcccgacgcc cgggcggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 285
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 285
gcgcgctcgc tcgctcgcgg gggccaaaag accaaaggtc ttttgacgcc cgggcggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 286
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 286
gcgcgctcgc tcgctcgcgg gggccaaaaa aaaaaatttt ttttgacgcc cgggcggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 287
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 287
gcgcgctcgc tcgctcgcgg gggccgggca gaaaaattct gcccgacgcc cgggcggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 288
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 288
gcgcgctcgc tcgctcaata aaaccaggcg accaaaggtc gcctgacgcc cgggcggttt 60
tattgagcga gcgagcgcgc 80
<210> 289
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 289
gcgcgctcgc tcgctcaata aaaccgggcg gccaaaggcc gcccgacgcc cgggcggttt 60
tattgagcga gcgagcgcgc 80
<210> 290
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 290
gcgcgctcgc tcgctcaata aaaccgggcg acaaaatgtc gcccgacgcc cgggcggttt 60
tattgagcga gcgagcgcgc 80
<210> 291
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 291
gcgcgctcgc tcgctcaata aaaccaaaag accaaaggtc ttttgacgcc cgggcggttt 60
tattgagcga gcgagcgcgc 80
<210> 292
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 292
gcgcgctcgc tcgctcaata aaaccaaaaa aaaaaatttt ttttgacgcc cgggcggttt 60
tattgagcga gcgagcgcgc 80
<210> 293
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 293
gcgcgctcgc tcgctcaata aaaccgggca gaaaaattct gcccgacgcc cgggcggttt 60
tattgagcga gcgagcgcgc 80
<210> 294
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 294
gcgcgctcgc tcgctcacta aggccgggcg accaaaggtc gcccgacacc cgggtggcct 60
tagtgagcga gcgagcgcgc 80
<210> 295
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 295
gcgcgctcgc tcgctcacta aggccgggcg accaaaggtc gcccgacgcc atggcggcct 60
tagtgagcga gcgagcgcgc 80
<210> 296
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 296
gcgcgctcgc tcgctcacta aggccgggcg accaaaggtc gcccgacgac atgtcggcct 60
tagtgagcga gcgagcgcgc 80
<210> 297
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 297
gcgcgctcgc tcgctcacta aggccgggcg accaaaggtc gcccgacgaa cgttcggcct 60
tagtgagcga gcgagcgcgc 80
<210> 298
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 298
gcgcgctcgc tcgctcacta aggccgggcg accaaaggtc gcccgaagca attgctgcct 60
tagtgagcga gcgagcgcgc 80
<210> 299
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 299
gcgcgctcgc tcgctcgatg gggccgggcg accaaaggtc gcccgacacc cgggtggcct 60
catcgagcga gcgagcgcgc 80
<210> 300
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 300
gcgcgctcgc tcgctcgatg gggccgggcg accaaaggtc gcccgacgcc atggcggcct 60
catcgagcga gcgagcgcgc 80
<210> 301
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 301
gcgcgctcgc tcgctcgatg gggccgggcg accaaaggtc gcccgacgac atgtcggcct 60
catcgagcga gcgagcgcgc 80
<210> 302
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 302
gcgcgctcgc tcgctcgatg gggccgggcg accaaaggtc gcccgacgaa cgttcggcct 60
catcgagcga gcgagcgcgc 80
<210> 303
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 303
gcgcgctcgc tcgctcgatg gggccgggcg accaaaggtc gcccgaagca attgctgcct 60
catcgagcga gcgagcgcgc 80
<210> 304
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 304
gcgcgctcgc tcgctcgaga gaaccgggcg accaaaggtc gcccgacacc cgggtggttc 60
tctcgagcga gcgagcgcgc 80
<210> 305
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 305
gcgcgctcgc tcgctcgaga gaaccgggcg accaaaggtc gcccgacgcc atggcggttc 60
tctcgagcga gcgagcgcgc 80
<210> 306
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 306
gcgcgctcgc tcgctcgaga gaaccgggcg accaaaggtc gcccgacgac atgtcggttc 60
tctcgagcga gcgagcgcgc 80
<210> 307
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 307
gcgcgctcgc tcgctcgaga gaaccgggcg accaaaggtc gcccgacgaa cgttcggttc 60
tctcgagcga gcgagcgcgc 80
<210> 308
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 308
gcgcgctcgc tcgctcgaga gaaccgggcg accaaaggtc gcccgaagca attgctgttc 60
tctcgagcga gcgagcgcgc 80
<210> 309
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 309
gcgcgctcgc tcgctcgcgg gggccgggcg accaaaggtc gcccgacacc cgggtggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 310
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 310
gcgcgctcgc tcgctcgcgg gggccgggcg accaaaggtc gcccgacgcc atggcggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 311
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 311
gcgcgctcgc tcgctcgcgg gggccgggcg accaaaggtc gcccgacgac atgtcggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 312
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 312
gcgcgctcgc tcgctcgcgg gggccgggcg accaaaggtc gcccgacgaa cgttcggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 313
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 313
gcgcgctcgc tcgctcgcgg gggccgggcg accaaaggtc gcccgaagca attgctgccc 60
ccgcgagcga gcgagcgcgc 80
<210> 314
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 314
gcgcgctcgc tcgctcaata aaaccgggcg accaaaggtc gcccgacacc cgggtggttt 60
tattgagcga gcgagcgcgc 80
<210> 315
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 315
gcgcgctcgc tcgctcaata aaaccgggcg accaaaggtc gcccgacgcc atggcggttt 60
tattgagcga gcgagcgcgc 80
<210> 316
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 316
gcgcgctcgc tcgctcaata aaaccgggcg accaaaggtc gcccgacgac atgtcggttt 60
tattgagcga gcgagcgcgc 80
<210> 317
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 317
gcgcgctcgc tcgctcaata aaaccgggcg accaaaggtc gcccgacgaa cgttcggttt 60
tattgagcga gcgagcgcgc 80
<210> 318
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 318
gcgcgctcgc tcgctcaata aaaccgggcg accaaaggtc gcccgaagca attgctgttt 60
tattgagcga gcgagcgcgc 80
<210> 319
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 319
gcgcgctcgc tcgctcacta aggccaggcg accaaaggtc gcctgacacc cgggtggcct 60
tagtgagcga gcgagcgcgc 80
<210> 320
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 320
gcgcgctcgc tcgctcacta aggccaggcg accaaaggtc gcctgacgcc atggcggcct 60
tagtgagcga gcgagcgcgc 80
<210> 321
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 321
gcgcgctcgc tcgctcacta aggccaggcg accaaaggtc gcctgacgac atgtcggcct 60
tagtgagcga gcgagcgcgc 80
<210> 322
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 322
gcgcgctcgc tcgctcacta aggccaggcg accaaaggtc gcctgacgaa cgttcggcct 60
tagtgagcga gcgagcgcgc 80
<210> 323
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 323
gcgcgctcgc tcgctcacta aggccaggcg accaaaggtc gcctgaagca attgctgcct 60
tagtgagcga gcgagcgcgc 80
<210> 324
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 324
gcgcgctcgc tcgctcacta aggccgggcg gccaaaggcc gcccgacacc cgggtggcct 60
tagtgagcga gcgagcgcgc 80
<210> 325
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 325
gcgcgctcgc tcgctcacta aggccgggcg gccaaaggcc gcccgacgcc atggcggcct 60
tagtgagcga gcgagcgcgc 80
<210> 326
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 326
gcgcgctcgc tcgctcacta aggccgggcg gccaaaggcc gcccgacgac atgtcggcct 60
tagtgagcga gcgagcgcgc 80
<210> 327
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 327
gcgcgctcgc tcgctcacta aggccgggcg gccaaaggcc gcccgacgaa cgttcggcct 60
tagtgagcga gcgagcgcgc 80
<210> 328
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 328
gcgcgctcgc tcgctcacta aggccgggcg gccaaaggcc gcccgaagca attgctgcct 60
tagtgagcga gcgagcgcgc 80
<210> 329
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 329
gcgcgctcgc tcgctcacta aggccgggcg acaaaatgtc gcccgacacc cgggtggcct 60
tagtgagcga gcgagcgcgc 80
<210> 330
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 330
gcgcgctcgc tcgctcacta aggccgggcg acaaaatgtc gcccgacgcc atggcggcct 60
tagtgagcga gcgagcgcgc 80
<210> 331
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 331
gcgcgctcgc tcgctcacta aggccgggcg acaaaatgtc gcccgacgac atgtcggcct 60
tagtgagcga gcgagcgcgc 80
<210> 332
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 332
gcgcgctcgc tcgctcacta aggccgggcg acaaaatgtc gcccgacgaa cgttcggcct 60
tagtgagcga gcgagcgcgc 80
<210> 333
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 333
gcgcgctcgc tcgctcacta aggccgggcg acaaaatgtc gcccgaagca attgctgcct 60
tagtgagcga gcgagcgcgc 80
<210> 334
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 334
gcgcgctcgc tcgctcacta aggccaaaag accaaaggtc ttttgacacc cgggtggcct 60
tagtgagcga gcgagcgcgc 80
<210> 335
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 335
gcgcgctcgc tcgctcacta aggccaaaag accaaaggtc ttttgacgcc atggcggcct 60
tagtgagcga gcgagcgcgc 80
<210> 336
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 336
gcgcgctcgc tcgctcacta aggccaaaag accaaaggtc ttttgacgac atgtcggcct 60
tagtgagcga gcgagcgcgc 80
<210> 337
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 337
gcgcgctcgc tcgctcacta aggccaaaag accaaaggtc ttttgacgaa cgttcggcct 60
tagtgagcga gcgagcgcgc 80
<210> 338
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 338
gcgcgctcgc tcgctcacta aggccaaaag accaaaggtc ttttgaagca attgctgcct 60
tagtgagcga gcgagcgcgc 80
<210> 339
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 339
gcgcgctcgc tcgctcacta aggccaaaaa aaaaaatttt ttttgacacc cgggtggcct 60
tagtgagcga gcgagcgcgc 80
<210> 340
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 340
gcgcgctcgc tcgctcacta aggccaaaaa aaaaaatttt ttttgacgcc atggcggcct 60
tagtgagcga gcgagcgcgc 80
<210> 341
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 341
gcgcgctcgc tcgctcacta aggccaaaaa aaaaaatttt ttttgacgac atgtcggcct 60
tagtgagcga gcgagcgcgc 80
<210> 342
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 342
gcgcgctcgc tcgctcacta aggccaaaaa aaaaaatttt ttttgacgaa cgttcggcct 60
tagtgagcga gcgagcgcgc 80
<210> 343
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 343
gcgcgctcgc tcgctcacta aggccaaaaa aaaaaatttt ttttgaagca attgctgcct 60
tagtgagcga gcgagcgcgc 80
<210> 344
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 344
gcgcgctcgc tcgctcacta aggccgggca gaaaaattct gcccgacacc cgggtggcct 60
tagtgagcga gcgagcgcgc 80
<210> 345
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 345
gcgcgctcgc tcgctcacta aggccgggca gaaaaattct gcccgacgcc atggcggcct 60
tagtgagcga gcgagcgcgc 80
<210> 346
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 346
gcgcgctcgc tcgctcacta aggccgggca gaaaaattct gcccgacgac atgtcggcct 60
tagtgagcga gcgagcgcgc 80
<210> 347
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 347
gcgcgctcgc tcgctcacta aggccgggca gaaaaattct gcccgacgaa cgttcggcct 60
tagtgagcga gcgagcgcgc 80
<210> 348
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 348
gcgcgctcgc tcgctcacta aggccgggca gaaaaattct gcccgaagca attgctgcct 60
tagtgagcga gcgagcgcgc 80
<210> 349
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 349
gcgcgctcgc tcgctcgatg gggccaggcg accaaaggtc gcctgacacc cgggtggcct 60
catcgagcga gcgagcgcgc 80
<210> 350
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 350
gcgcgctcgc tcgctcgatg gggccaggcg accaaaggtc gcctgacgcc atggcggcct 60
catcgagcga gcgagcgcgc 80
<210> 351
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 351
gcgcgctcgc tcgctcgatg gggccaggcg accaaaggtc gcctgacgac atgtcggcct 60
catcgagcga gcgagcgcgc 80
<210> 352
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 352
gcgcgctcgc tcgctcgatg gggccaggcg accaaaggtc gcctgacgaa cgttcggcct 60
catcgagcga gcgagcgcgc 80
<210> 353
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 353
gcgcgctcgc tcgctcgatg gggccaggcg accaaaggtc gcctgaagca attgctgcct 60
catcgagcga gcgagcgcgc 80
<210> 354
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 354
gcgcgctcgc tcgctcgatg gggccgggcg gccaaaggcc gcccgacacc cgggtggcct 60
catcgagcga gcgagcgcgc 80
<210> 355
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 355
gcgcgctcgc tcgctcgatg gggccgggcg gccaaaggcc gcccgacgcc atggcggcct 60
catcgagcga gcgagcgcgc 80
<210> 356
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 356
gcgcgctcgc tcgctcgatg gggccgggcg gccaaaggcc gcccgacgac atgtcggcct 60
catcgagcga gcgagcgcgc 80
<210> 357
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 357
gcgcgctcgc tcgctcgatg gggccgggcg gccaaaggcc gcccgacgaa cgttcggcct 60
catcgagcga gcgagcgcgc 80
<210> 358
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 358
gcgcgctcgc tcgctcgatg gggccgggcg gccaaaggcc gcccgaagca attgctgcct 60
catcgagcga gcgagcgcgc 80
<210> 359
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 359
gcgcgctcgc tcgctcgatg gggccgggcg acaaaatgtc gcccgacacc cgggtggcct 60
catcgagcga gcgagcgcgc 80
<210> 360
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 360
gcgcgctcgc tcgctcgatg gggccgggcg acaaaatgtc gcccgacgcc atggcggcct 60
catcgagcga gcgagcgcgc 80
<210> 361
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 361
gcgcgctcgc tcgctcgatg gggccgggcg acaaaatgtc gcccgacgac atgtcggcct 60
catcgagcga gcgagcgcgc 80
<210> 362
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 362
gcgcgctcgc tcgctcgatg gggccgggcg acaaaatgtc gcccgacgaa cgttcggcct 60
catcgagcga gcgagcgcgc 80
<210> 363
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 363
gcgcgctcgc tcgctcgatg gggccgggcg acaaaatgtc gcccgaagca attgctgcct 60
catcgagcga gcgagcgcgc 80
<210> 364
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 364
gcgcgctcgc tcgctcgatg gggccaaaag accaaaggtc ttttgacacc cgggtggcct 60
catcgagcga gcgagcgcgc 80
<210> 365
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 365
gcgcgctcgc tcgctcgatg gggccaaaag accaaaggtc ttttgacgcc atggcggcct 60
catcgagcga gcgagcgcgc 80
<210> 366
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 366
gcgcgctcgc tcgctcgatg gggccaaaag accaaaggtc ttttgacgac atgtcggcct 60
catcgagcga gcgagcgcgc 80
<210> 367
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 367
gcgcgctcgc tcgctcgatg gggccaaaag accaaaggtc ttttgacgaa cgttcggcct 60
catcgagcga gcgagcgcgc 80
<210> 368
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 368
gcgcgctcgc tcgctcgatg gggccaaaag accaaaggtc ttttgaagca attgctgcct 60
catcgagcga gcgagcgcgc 80
<210> 369
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 369
gcgcgctcgc tcgctcgatg gggccaaaaa aaaaaatttt ttttgacacc cgggtggcct 60
catcgagcga gcgagcgcgc 80
<210> 370
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 370
gcgcgctcgc tcgctcgatg gggccaaaaa aaaaaatttt ttttgacgcc atggcggcct 60
catcgagcga gcgagcgcgc 80
<210> 371
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 371
gcgcgctcgc tcgctcgatg gggccaaaaa aaaaaatttt ttttgacgac atgtcggcct 60
catcgagcga gcgagcgcgc 80
<210> 372
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 372
gcgcgctcgc tcgctcgatg gggccaaaaa aaaaaatttt ttttgacgaa cgttcggcct 60
catcgagcga gcgagcgcgc 80
<210> 373
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 373
gcgcgctcgc tcgctcgatg gggccaaaaa aaaaaatttt ttttgaagca attgctgcct 60
catcgagcga gcgagcgcgc 80
<210> 374
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 374
gcgcgctcgc tcgctcgatg gggccgggca gaaaaattct gcccgacacc cgggtggcct 60
catcgagcga gcgagcgcgc 80
<210> 375
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 375
gcgcgctcgc tcgctcgatg gggccgggca gaaaaattct gcccgacgcc atggcggcct 60
catcgagcga gcgagcgcgc 80
<210> 376
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 376
gcgcgctcgc tcgctcgatg gggccgggca gaaaaattct gcccgacgac atgtcggcct 60
catcgagcga gcgagcgcgc 80
<210> 377
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 377
gcgcgctcgc tcgctcgatg gggccgggca gaaaaattct gcccgacgaa cgttcggcct 60
catcgagcga gcgagcgcgc 80
<210> 378
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 378
gcgcgctcgc tcgctcgatg gggccgggca gaaaaattct gcccgaagca attgctgcct 60
catcgagcga gcgagcgcgc 80
<210> 379
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 379
gcgcgctcgc tcgctcgaga gaaccaggcg accaaaggtc gcctgacacc cgggtggttc 60
tctcgagcga gcgagcgcgc 80
<210> 380
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 380
gcgcgctcgc tcgctcgaga gaaccaggcg accaaaggtc gcctgacgcc atggcggttc 60
tctcgagcga gcgagcgcgc 80
<210> 381
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 381
gcgcgctcgc tcgctcgaga gaaccaggcg accaaaggtc gcctgacgac atgtcggttc 60
tctcgagcga gcgagcgcgc 80
<210> 382
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 382
gcgcgctcgc tcgctcgaga gaaccaggcg accaaaggtc gcctgacgaa cgttcggttc 60
tctcgagcga gcgagcgcgc 80
<210> 383
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 383
gcgcgctcgc tcgctcgaga gaaccaggcg accaaaggtc gcctgaagca attgctgttc 60
tctcgagcga gcgagcgcgc 80
<210> 384
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 384
gcgcgctcgc tcgctcgaga gaaccgggcg gccaaaggcc gcccgacacc cgggtggttc 60
tctcgagcga gcgagcgcgc 80
<210> 385
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 385
gcgcgctcgc tcgctcgaga gaaccgggcg gccaaaggcc gcccgacgcc atggcggttc 60
tctcgagcga gcgagcgcgc 80
<210> 386
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 386
gcgcgctcgc tcgctcgaga gaaccgggcg gccaaaggcc gcccgacgac atgtcggttc 60
tctcgagcga gcgagcgcgc 80
<210> 387
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 387
gcgcgctcgc tcgctcgaga gaaccgggcg gccaaaggcc gcccgacgaa cgttcggttc 60
tctcgagcga gcgagcgcgc 80
<210> 388
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 388
gcgcgctcgc tcgctcgaga gaaccgggcg gccaaaggcc gcccgaagca attgctgttc 60
tctcgagcga gcgagcgcgc 80
<210> 389
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 389
gcgcgctcgc tcgctcgaga gaaccgggcg acaaaatgtc gcccgacacc cgggtggttc 60
tctcgagcga gcgagcgcgc 80
<210> 390
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 390
gcgcgctcgc tcgctcgaga gaaccgggcg acaaaatgtc gcccgacgcc atggcggttc 60
tctcgagcga gcgagcgcgc 80
<210> 391
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 391
gcgcgctcgc tcgctcgaga gaaccgggcg acaaaatgtc gcccgacgac atgtcggttc 60
tctcgagcga gcgagcgcgc 80
<210> 392
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 392
gcgcgctcgc tcgctcgaga gaaccgggcg acaaaatgtc gcccgacgaa cgttcggttc 60
tctcgagcga gcgagcgcgc 80
<210> 393
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 393
gcgcgctcgc tcgctcgaga gaaccgggcg acaaaatgtc gcccgaagca attgctgttc 60
tctcgagcga gcgagcgcgc 80
<210> 394
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 394
gcgcgctcgc tcgctcgaga gaaccaaaag accaaaggtc ttttgacacc cgggtggttc 60
tctcgagcga gcgagcgcgc 80
<210> 395
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 395
gcgcgctcgc tcgctcgaga gaaccaaaag accaaaggtc ttttgacgcc atggcggttc 60
tctcgagcga gcgagcgcgc 80
<210> 396
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 396
gcgcgctcgc tcgctcgaga gaaccaaaag accaaaggtc ttttgacgac atgtcggttc 60
tctcgagcga gcgagcgcgc 80
<210> 397
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 397
gcgcgctcgc tcgctcgaga gaaccaaaag accaaaggtc ttttgacgaa cgttcggttc 60
tctcgagcga gcgagcgcgc 80
<210> 398
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 398
gcgcgctcgc tcgctcgaga gaaccaaaag accaaaggtc ttttgaagca attgctgttc 60
tctcgagcga gcgagcgcgc 80
<210> 399
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 399
gcgcgctcgc tcgctcgaga gaaccaaaaa aaaaaatttt ttttgacacc cgggtggttc 60
tctcgagcga gcgagcgcgc 80
<210> 400
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 400
gcgcgctcgc tcgctcgaga gaaccaaaaa aaaaaatttt ttttgacgcc atggcggttc 60
tctcgagcga gcgagcgcgc 80
<210> 401
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 401
gcgcgctcgc tcgctcgaga gaaccaaaaa aaaaaatttt ttttgacgac atgtcggttc 60
tctcgagcga gcgagcgcgc 80
<210> 402
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 402
gcgcgctcgc tcgctcgaga gaaccaaaaa aaaaaatttt ttttgacgaa cgttcggttc 60
tctcgagcga gcgagcgcgc 80
<210> 403
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 403
gcgcgctcgc tcgctcgaga gaaccaaaaa aaaaaatttt ttttgaagca attgctgttc 60
tctcgagcga gcgagcgcgc 80
<210> 404
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 404
gcgcgctcgc tcgctcgaga gaaccgggca gaaaaattct gcccgacacc cgggtggttc 60
tctcgagcga gcgagcgcgc 80
<210> 405
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 405
gcgcgctcgc tcgctcgaga gaaccgggca gaaaaattct gcccgacgcc atggcggttc 60
tctcgagcga gcgagcgcgc 80
<210> 406
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 406
gcgcgctcgc tcgctcgaga gaaccgggca gaaaaattct gcccgacgac atgtcggttc 60
tctcgagcga gcgagcgcgc 80
<210> 407
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 407
gcgcgctcgc tcgctcgaga gaaccgggca gaaaaattct gcccgacgaa cgttcggttc 60
tctcgagcga gcgagcgcgc 80
<210> 408
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 408
gcgcgctcgc tcgctcgaga gaaccgggca gaaaaattct gcccgaagca attgctgttc 60
tctcgagcga gcgagcgcgc 80
<210> 409
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 409
gcgcgctcgc tcgctcgcgg gggccaggcg accaaaggtc gcctgacacc cgggtggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 410
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 410
gcgcgctcgc tcgctcgcgg gggccaggcg accaaaggtc gcctgacgcc atggcggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 411
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 411
gcgcgctcgc tcgctcgcgg gggccaggcg accaaaggtc gcctgacgac atgtcggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 412
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 412
gcgcgctcgc tcgctcgcgg gggccaggcg accaaaggtc gcctgacgaa cgttcggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 413
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 413
gcgcgctcgc tcgctcgcgg gggccaggcg accaaaggtc gcctgaagca attgctgccc 60
ccgcgagcga gcgagcgcgc 80
<210> 414
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 414
gcgcgctcgc tcgctcgcgg gggccgggcg gccaaaggcc gcccgacacc cgggtggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 415
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 415
gcgcgctcgc tcgctcgcgg gggccgggcg gccaaaggcc gcccgacgcc atggcggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 416
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 416
gcgcgctcgc tcgctcgcgg gggccgggcg gccaaaggcc gcccgacgac atgtcggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 417
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 417
gcgcgctcgc tcgctcgcgg gggccgggcg gccaaaggcc gcccgacgaa cgttcggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 418
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 418
gcgcgctcgc tcgctcgcgg gggccgggcg gccaaaggcc gcccgaagca attgctgccc 60
ccgcgagcga gcgagcgcgc 80
<210> 419
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 419
gcgcgctcgc tcgctcgcgg gggccgggcg acaaaatgtc gcccgacacc cgggtggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 420
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 420
gcgcgctcgc tcgctcgcgg gggccgggcg acaaaatgtc gcccgacgcc atggcggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 421
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 421
gcgcgctcgc tcgctcgcgg gggccgggcg acaaaatgtc gcccgacgac atgtcggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 422
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 422
gcgcgctcgc tcgctcgcgg gggccgggcg acaaaatgtc gcccgacgaa cgttcggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 423
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 423
gcgcgctcgc tcgctcgcgg gggccgggcg acaaaatgtc gcccgaagca attgctgccc 60
ccgcgagcga gcgagcgcgc 80
<210> 424
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 424
gcgcgctcgc tcgctcgcgg gggccaaaag accaaaggtc ttttgacacc cgggtggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 425
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 425
gcgcgctcgc tcgctcgcgg gggccaaaag accaaaggtc ttttgacgcc atggcggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 426
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 426
gcgcgctcgc tcgctcgcgg gggccaaaag accaaaggtc ttttgacgac atgtcggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 427
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 427
gcgcgctcgc tcgctcgcgg gggccaaaag accaaaggtc ttttgacgaa cgttcggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 428
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 428
gcgcgctcgc tcgctcgcgg gggccaaaag accaaaggtc ttttgaagca attgctgccc 60
ccgcgagcga gcgagcgcgc 80
<210> 429
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 429
gcgcgctcgc tcgctcgcgg gggccaaaaa aaaaaatttt ttttgacacc cgggtggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 430
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 430
gcgcgctcgc tcgctcgcgg gggccaaaaa aaaaaatttt ttttgacgcc atggcggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 431
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 431
gcgcgctcgc tcgctcgcgg gggccaaaaa aaaaaatttt ttttgacgac atgtcggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 432
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 432
gcgcgctcgc tcgctcgcgg gggccaaaaa aaaaaatttt ttttgacgaa cgttcggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 433
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 433
gcgcgctcgc tcgctcgcgg gggccaaaaa aaaaaatttt ttttgaagca attgctgccc 60
ccgcgagcga gcgagcgcgc 80
<210> 434
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 434
gcgcgctcgc tcgctcgcgg gggccgggca gaaaaattct gcccgacacc cgggtggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 435
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 435
gcgcgctcgc tcgctcgcgg gggccgggca gaaaaattct gcccgacgcc atggcggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 436
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 436
gcgcgctcgc tcgctcgcgg gggccgggca gaaaaattct gcccgacgac atgtcggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 437
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 437
gcgcgctcgc tcgctcgcgg gggccgggca gaaaaattct gcccgacgaa cgttcggccc 60
ccgcgagcga gcgagcgcgc 80
<210> 438
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 438
gcgcgctcgc tcgctcgcgg gggccgggca gaaaaattct gcccgaagca attgctgccc 60
ccgcgagcga gcgagcgcgc 80
<210> 439
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 439
gcgcgctcgc tcgctcaata aaaccaggcg accaaaggtc gcctgacacc cgggtggttt 60
tattgagcga gcgagcgcgc 80
<210> 440
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 440
gcgcgctcgc tcgctcaata aaaccaggcg accaaaggtc gcctgacgcc atggcggttt 60
tattgagcga gcgagcgcgc 80
<210> 441
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 441
gcgcgctcgc tcgctcaata aaaccaggcg accaaaggtc gcctgacgac atgtcggttt 60
tattgagcga gcgagcgcgc 80
<210> 442
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 442
gcgcgctcgc tcgctcaata aaaccaggcg accaaaggtc gcctgacgaa cgttcggttt 60
tattgagcga gcgagcgcgc 80
<210> 443
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 443
gcgcgctcgc tcgctcaata aaaccaggcg accaaaggtc gcctgaagca attgctgttt 60
tattgagcga gcgagcgcgc 80
<210> 444
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 444
gcgcgctcgc tcgctcaata aaaccgggcg gccaaaggcc gcccgacacc cgggtggttt 60
tattgagcga gcgagcgcgc 80
<210> 445
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 445
gcgcgctcgc tcgctcaata aaaccgggcg gccaaaggcc gcccgacgcc atggcggttt 60
tattgagcga gcgagcgcgc 80
<210> 446
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 446
gcgcgctcgc tcgctcaata aaaccgggcg gccaaaggcc gcccgacgac atgtcggttt 60
tattgagcga gcgagcgcgc 80
<210> 447
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 447
gcgcgctcgc tcgctcaata aaaccgggcg gccaaaggcc gcccgacgaa cgttcggttt 60
tattgagcga gcgagcgcgc 80
<210> 448
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 448
gcgcgctcgc tcgctcaata aaaccgggcg gccaaaggcc gcccgaagca attgctgttt 60
tattgagcga gcgagcgcgc 80
<210> 449
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 449
gcgcgctcgc tcgctcaata aaaccgggcg acaaaatgtc gcccgacacc cgggtggttt 60
tattgagcga gcgagcgcgc 80
<210> 450
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 450
gcgcgctcgc tcgctcaata aaaccgggcg acaaaatgtc gcccgacgcc atggcggttt 60
tattgagcga gcgagcgcgc 80
<210> 451
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 451
gcgcgctcgc tcgctcaata aaaccgggcg acaaaatgtc gcccgacgac atgtcggttt 60
tattgagcga gcgagcgcgc 80
<210> 452
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 452
gcgcgctcgc tcgctcaata aaaccgggcg acaaaatgtc gcccgacgaa cgttcggttt 60
tattgagcga gcgagcgcgc 80
<210> 453
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 453
gcgcgctcgc tcgctcaata aaaccgggcg acaaaatgtc gcccgaagca attgctgttt 60
tattgagcga gcgagcgcgc 80
<210> 454
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 454
gcgcgctcgc tcgctcaata aaaccaaaag accaaaggtc ttttgacacc cgggtggttt 60
tattgagcga gcgagcgcgc 80
<210> 455
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 455
gcgcgctcgc tcgctcaata aaaccaaaag accaaaggtc ttttgacgcc atggcggttt 60
tattgagcga gcgagcgcgc 80
<210> 456
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 456
gcgcgctcgc tcgctcaata aaaccaaaag accaaaggtc ttttgacgac atgtcggttt 60
tattgagcga gcgagcgcgc 80
<210> 457
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 457
gcgcgctcgc tcgctcaata aaaccaaaag accaaaggtc ttttgacgaa cgttcggttt 60
tattgagcga gcgagcgcgc 80
<210> 458
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 458
gcgcgctcgc tcgctcaata aaaccaaaag accaaaggtc ttttgaagca attgctgttt 60
tattgagcga gcgagcgcgc 80
<210> 459
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 459
gcgcgctcgc tcgctcaata aaaccaaaaa aaaaaatttt ttttgacacc cgggtggttt 60
tattgagcga gcgagcgcgc 80
<210> 460
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 460
gcgcgctcgc tcgctcaata aaaccaaaaa aaaaaatttt ttttgacgcc atggcggttt 60
tattgagcga gcgagcgcgc 80
<210> 461
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 461
gcgcgctcgc tcgctcaata aaaccaaaaa aaaaaatttt ttttgacgac atgtcggttt 60
tattgagcga gcgagcgcgc 80
<210> 462
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 462
gcgcgctcgc tcgctcaata aaaccaaaaa aaaaaatttt ttttgacgaa cgttcggttt 60
tattgagcga gcgagcgcgc 80
<210> 463
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 463
gcgcgctcgc tcgctcaata aaaccaaaaa aaaaaatttt ttttgaagca attgctgttt 60
tattgagcga gcgagcgcgc 80
<210> 464
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 464
gcgcgctcgc tcgctcaata aaaccgggca gaaaaattct gcccgacacc cgggtggttt 60
tattgagcga gcgagcgcgc 80
<210> 465
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 465
gcgcgctcgc tcgctcaata aaaccgggca gaaaaattct gcccgacgcc atggcggttt 60
tattgagcga gcgagcgcgc 80
<210> 466
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 466
gcgcgctcgc tcgctcaata aaaccgggca gaaaaattct gcccgacgac atgtcggttt 60
tattgagcga gcgagcgcgc 80
<210> 467
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 467
gcgcgctcgc tcgctcaata aaaccgggca gaaaaattct gcccgacgaa cgttcggttt 60
tattgagcga gcgagcgcgc 80
<210> 468
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 468
gcgcgctcgc tcgctcaata aaaccgggca gaaaaattct gcccgaagca attgctgttt 60
tattgagcga gcgagcgcgc 80
<210> 469
<211> 120
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 469
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
cgcacgcccg ggtttcccgg gcggcctcag tgagcgagcg agcgcgcagc tgcctgcagg 120
<210> 470
<211> 122
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 470
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgacgcccg ggctttgccc gggcggcctc agtgagcgag cgagcgcgca gctgcctgca 120
gg 122
<210> 471
<211> 129
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 471
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgacc aaaggtcgcc cgacgcccgg gcgcctcagt gagcgagcga gcgcgcagct 120
gcctgcagg 129
<210> 472
<211> 101
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 472
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ctttgcctca gtgagcgagc gagcgcgcag ctgcctgcag g 101
<210> 473
<211> 139
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 473
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgaca aagtcgcccg acgcccgggc tttgcccggg cggcctcagt gagcgagcga 120
gcgcgcagct gcctgcagg 139
<210> 474
<211> 137
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 474
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgaaa atcgcccgac gcccgggctt tgcccgggcg gcctcagtga gcgagcgagc 120
gcgcagctgc ctgcagg 137
<210> 475
<211> 135
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 475
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgaaa cgcccgacgc ccgggctttg cccgggcggc ctcagtgagc gagcgagcgc 120
gcagctgcct gcagg 135
<210> 476
<211> 133
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 476
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcaaag cccgacgccc gggctttgcc cgggcggcct cagtgagcga gcgagcgcgc 120
agctgcctgc agg 133
<210> 477
<211> 139
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 477
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgacc aaaggtcgcc cgacgcccgg gtttcccggg cggcctcagt gagcgagcga 120
gcgcgcagct gcctgcagg 139
<210> 478
<211> 137
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 478
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgacc aaaggtcgcc cgacgcccgg tttccgggcg gcctcagtga gcgagcgagc 120
gcgcagctgc ctgcagg 137
<210> 479
<211> 135
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 479
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgacc aaaggtcgcc cgacgcccgt ttcgggcggc ctcagtgagc gagcgagcgc 120
gcagctgcct gcagg 135
<210> 480
<211> 133
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 480
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgacc aaaggtcgcc cgacgccctt tgggcggcct cagtgagcga gcgagcgcgc 120
agctgcctgc agg 133
<210> 481
<211> 131
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 481
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgacc aaaggtcgcc cgacgccttt ggcggcctca gtgagcgagc gagcgcgcag 120
ctgcctgcag g 131
<210> 482
<211> 129
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 482
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgacc aaaggtcgcc cgacgctttg cggcctcagt gagcgagcga gcgcgcagct 120
gcctgcagg 129
<210> 483
<211> 127
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 483
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgacc aaaggtcgcc cgacgtttcg gcctcagtga gcgagcgagc gcgcagctgc 120
ctgcagg 127
<210> 484
<211> 120
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 484
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccgggaaacc cgggcgtgcg 60
cctcagtgag cgagcgagcg cgcagagagg gagtggccaa ctccatcact aggggttcct 120
<210> 485
<211> 122
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 485
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgt cgggcgacct ttggtcgccc 60
ggcctcagtg agcgagcgag cgcgcagaga gggagtggcc aactccatca ctaggggttc 120
ct 122
<210> 486
<211> 122
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 486
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccgggcaaag cccgggcgtc 60
ggcctcagtg agcgagcgag cgcgcagaga gggagtggcc aactccatca ctaggggttc 120
ct 122
<210> 487
<211> 129
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 487
cctgcaggca gctgcgcgct cgctcgctca ctgaggcgcc cgggcgtcgg gcgacctttg 60
gtcgcccggc ctcagtgagc gagcgagcgc gcagagaggg agtggccaac tccatcacta 120
ggggttcct 129
<210> 488
<211> 101
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 488
cctgcaggca gctgcgcgct cgctcgctca ctgaggcaaa gcctcagtga gcgagcgagc 60
gcgcagagag ggagtggcca actccatcac taggggttcc t 101
<210> 489
<211> 139
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 489
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccgggcaaag cccgggcgtc 60
gggcgacttt gtcgcccggc ctcagtgagc gagcgagcgc gcagagaggg agtggccaac 120
tccatcacta ggggttcct 139
<210> 490
<211> 137
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 490
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccgggcaaag cccgggcgtc 60
gggcgatttt cgcccggcct cagtgagcga gcgagcgcgc agagagggag tggccaactc 120
catcactagg ggttcct 137
<210> 491
<211> 135
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 491
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccgggcaaag cccgggcgtc 60
gggcgtttcg cccggcctca gtgagcgagc gagcgcgcag agagggagtg gccaactcca 120
tcactagggg ttcct 135
<210> 492
<211> 133
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 492
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccgggcaaag cccgggcgtc 60
gggctttgcc cggcctcagt gagcgagcga gcgcgcagag agggagtggc caactccatc 120
actaggggtt cct 133
<210> 493
<211> 139
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 493
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccgggaaacc cgggcgtcgg 60
gcgacctttg gtcgcccggc ctcagtgagc gagcgagcgc gcagagaggg agtggccaac 120
tccatcacta ggggttcct 139
<210> 494
<211> 137
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 494
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccggaaaccg ggcgtcgggc 60
gacctttggt cgcccggcct cagtgagcga gcgagcgcgc agagagggag tggccaactc 120
catcactagg ggttcct 137
<210> 495
<211> 135
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 495
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccgaaacggg cgtcgggcga 60
cctttggtcg cccggcctca gtgagcgagc gagcgcgcag agagggagtg gccaactcca 120
tcactagggg ttcct 135
<210> 496
<211> 133
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 496
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccaaagggcg tcgggcgacc 60
tttggtcgcc cggcctcagt gagcgagcga gcgcgcagag agggagtggc caactccatc 120
actaggggtt cct 133
<210> 497
<211> 131
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 497
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc caaaggcgtc gggcgacctt 60
tggtcgcccg gcctcagtga gcgagcgagc gcgcagagag ggagtggcca actccatcac 120
taggggttcc t 131
<210> 498
<211> 129
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 498
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc aaagcgtcgg gcgacctttg 60
gtcgcccggc ctcagtgagc gagcgagcgc gcagagaggg agtggccaac tccatcacta 120
ggggttcct 129
<210> 499
<211> 127
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 499
cctgcaggca gctgcgcgct cgctcgctca ctgaggccga aacgtcgggc gacctttggt 60
cgcccggcct cagtgagcga gcgagcgcgc agagagggag tggccaactc catcactagg 120
ggttcct 127
<210> 500
<211> 43
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 500
gcccgctggt ttccagcggg ctgcgggccc gaaacgggcc cgc 43
<210> 501
<211> 28
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 501
cgggcccgtg cgggcccaaa gggcccgc 28
<210> 502
<211> 28
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 502
gcccgggcac gcccgggttt cccgggcg 28
<210> 503
<211> 22
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 503
cgtgcgggcc caaagggccc gc 22
<210> 504
<211> 21
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 504
cgggcgacca aaggtcgccc g 21
<210> 505
<211> 20
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 505
cgcccgggct ttgcccgggc 20
<210> 506
<211> 42
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 506
cgggcgacca aaggtcgccc gacgcccggg ctttgcccgg gc 42
<210> 507
<211> 21
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 507
cgggcgacca aaggtcgccc g 21
<210> 508
<211> 20
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 508
cgcccgggct ttgcccgggc 20
<210> 509
<211> 34
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 509
cgggcgacca aaggtcgccc gacgcccggg cggc 34
<210> 510
<211> 21
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 510
cgggcgacca aaggtcgccc g 21
<210> 511
<211> 20
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 511
cgcccgggct ttgcccgggc 20
<210> 512
<211> 30
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 512
cggggcccga cgcccgggct ttgcccgggc 30
<210> 513
<211> 21
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 513
cgggcgacca aaggtcgccc g 21
<210> 514
<211> 20
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 514
cgcccgggct ttgcccgggc 20
<210> 515
<211> 29
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 515
cgggcccgac gcccgggctt tgcccgggc 29
<210> 516
<211> 21
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 516
cgggcgacca aaggtcgccc g 21
<210> 517
<211> 20
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 517
cgcccgggct ttgcccgggc 20
<210> 518
<211> 20
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 518
gcccgggcaa agcccgggcg 20
<210> 519
<211> 21
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 519
cgggcgacct ttggtcgccc g 21
<210> 520
<211> 42
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 520
gcccgggcaa agcccgggcg tcgggcgacc tttggtcgcc cg 42
<210> 521
<211> 20
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 521
gcccgggcaa agcccgggcg 20
<210> 522
<211> 31
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 522
gcccgggcgt cgggcgacct ttggtcgccc g 31
<210> 523
<211> 20
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 523
gcccgggcaa agcccgggcg 20
<210> 524
<211> 21
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 524
cgggcgacct ttggtcgccc g 21
<210> 525
<211> 34
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 525
gccgcccggg cgacgggcga cctttggtcg cccg 34
<210> 526
<211> 20
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 526
gcccgggcaa agcccgggcg 20
<210> 527
<211> 21
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 527
cgggcgacct ttggtcgccc g 21
<210> 528
<211> 31
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 528
gcccgggcgt cgggcgacct ttggtcgccc g 31
<210> 529
<211> 21
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 529
cgggcgacct ttggtcgccc g 21
<210> 530
<211> 1653
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 530
atgccgccac cccggaccgg ccgaggcctt ctctggctgg gtctggttct gagctccgtc 60
tgcgtcgccc tcggatccga aacgcaggcc aactcgacca cagatgctct gaacgttctt 120
ctcatcatcg tggatgacct gcgcccctcc ctgggctgtt atggggataa gctggtgagg 180
tccccaaata ttgaccaact ggcatcccac agcctcctct tccagaatgc ctttgcgcag 240
caagcagtgt gcgccccgag ccgcgtttct ttcctcactg gcaggagacc tgacaccacc 300
cgcctgtacg acttcaactc ctactggagg gtgcacgctg gaaacttctc caccatcccc 360
cagtacttca aggagaatgg ctatgtgacc atgtcggtgg gaaaagtctt tcaccctggg 420
atatcttcta accataccga tgattctccg tatagctggt cttttccacc ttatcatcct 480
tcctctgaga agtatgaaaa cactaagaca tgtcgagggc cagatggaga actccatgcc 540
aacctgcttt gccctgtgga tgtgctggat gttcccgagg gcaccttgcc tgacaaacag 600
agcactgagc aagccataca gttgttggaa aagatgaaaa cgtcagccag tcctttcttc 660
ctggccgttg ggtatcataa gccacacatc cccttcagat accccaagga atttcagaag 720
ttgtatccct tggagaacat caccctggcc cccgatcccg aggtccctga tggcctaccc 780
cctgtggcct acaacccctg gatggacatc aggcaacggg aagacgtcca agccttaaac 840
atcagtgtgc cgtatggtcc aattcctgtg gactttcagc ggaaaatccg ccagagctac 900
tttgcctctg tgtcatattt ggatacacag gtcggccgcc tcttgagtgc tttggacgat 960
cttcagctgg ccaacagcac catcattgca tttacctcgg atcatgggtg ggctctaggt 1020
gaacatggag aatgggccaa atacagcaat tttgatgttg ctacccatgt tcccctgata 1080
ttctatgttc ctggaaggac ggcttcactt ccggaggcag gcgagaagct tttcccttac 1140
ctcgaccctt ttgattccgc ctcacagttg atggagccag gcaggcaatc catggacctt 1200
gtggaacttg tgtctctttt tcccacgctg gctggacttg caggactgca ggttccacct 1260
cgctgccccg ttccttcatt tcacgttgag ctgtgcagag aaggcaagaa ccttctgaag 1320
cattttcgat tccgtgactt ggaagaggat ccgtacctcc ctggtaatcc ccgtgaactg 1380
attgcctata gccagtatcc ccggccttca gacatccctc agtggaattc tgacaagccg 1440
agtttaaaag atataaagat catgggctat tccatacgca ccatagacta taggtatact 1500
gtgtgggttg gcttcaatcc tgatgaattt ctagctaact tttctgacat ccatgcaggg 1560
gaactgtatt ttgtggattc tgacccattg caggatcaca atatgtataa tgattcccaa 1620
ggtggagatc ttttccagtt gttgatgcct tga 1653
<210> 531
<211> 16
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 531
gcgcgctcgc tcgctc 16
<210> 532
<211> 8
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 532
actgaggc 8
<210> 533
<211> 22
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 533
cgggcgacca aaggtcgccc ga 22
<210> 534
<211> 10
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 534
cgcccgggcg 10
<210> 535
<211> 8
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 535
gcctcagt 8
<210> 536
<211> 16
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 536
gagcgagcga gcgcgc 16
<210> 537
<211> 20
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 537
gcccgggcaa agcccgggcg 20
<210> 538
<211> 165
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 538
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgcccgggc aaagcccggg cgtcgggcga cctttggtcg cccggcctca gtgagcgagc 120
gagcgcgcag agagggagtg gccaactcca tcactagggg ttcct 165
<210> 539
<211> 140
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 539
cccctagtga tggagttggc cactccctct ctgcgcgctc gctcgctcac tgaggccgcc 60
cgggcaaagc ccgggcgtcg ggcgaccttt ggtcgcccgg cctcagtgag cgagcgagcg 120
cgcagagaga tcactagggg 140
<210> 540
<211> 91
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 540
gcgcgctcgc tcgctcactg aggccgcccg ggcaaagccc gggcgtcggg cgacctttgg 60
tcgcccggcc tcagtgagcg agcgagcgcg c 91
<210> 541
<211> 91
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 541
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgcc cgggctttgc 60
ccgggcggcc tcagtgagcg agcgagcgcg c 91
<210> 542
<211> 8
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 542
ttaattaa 8
<210> 543
<211> 80
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 543
gcgcgctcgc tcgctcactg aggccgcccg ggcgtcgggc gacctttggt cgcccggcct 60
cagtgagcga gcgagcgcgc 80
<210> 544
<211> 52
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 544
gcgcgctcgc tcgctcactg aggcctttgc ctcagtgagc gagcgagcgc gc 52
<210> 545
<211> 79
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 545
gcgcgctcgc tcgctcactg aggcgcccgg gcgtcgggcg acctttggtc gcccggcctc 60
agtgagcgag cgagcgcgc 79
<210> 546
<211> 81
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 546
ctgcgcgctc gctcgctcac tgaggccggg cgaccaaagg tcgcccgacg tttcggcctc 60
agtgagcgag cgagcgcgca g 81
<210> 547
<211> 81
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 547
ctgcgcgctc gctcgctcac tgaggccgaa acgtcgggcg acctttggtc gcccggcctc 60
agtgagcgag cgagcgcgca g 81
<210> 548
<211> 42
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 548
cgggcgacca aaggtcgccc gacgcccggg ctttgcccgg gc 42
<210> 549
<211> 42
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 549
gcccgggcaa agcccgggcg tcgggcgacc tttggtcgcc cg 42
<210> 550
<211> 144
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 550
aggaacccta gtgatggagt tggccactcc ctctctgcgc gctcgctcgc tcactgaggc 60
cgcccgggca aagcccgggc gtcgggcgac ctttggtcgc ccggcctcag tgagcgagcg 120
agcgcgcaga gagggagtgg ccaa 144
<210> 551
<211> 43
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 551
gcccgctggt ttccagcggg ctgcgggccc gaaacgggcc cgc 43
<210> 552
<211> 28
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 552
cgggcccgtg cgggcccaaa gggcccgc 28
<210> 553
<211> 28
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 553
gcccgggcac gcccgggttt cccgggcg 28
<210> 554
<211> 22
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 554
cgtgcgggcc caaagggccc gc 22
<210> 555
<211> 43
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 555
gcgggccgga aacgggcccg ctgcccgctg gtttccagcg ggc 43
<210> 556
<211> 28
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 556
cgcccgggaa acccgggcgt gcccgggc 28
<210> 557
<211> 28
<212> DNA/ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 557
gggccgcccg ggaaacccgg gcgtgccc 28
<---
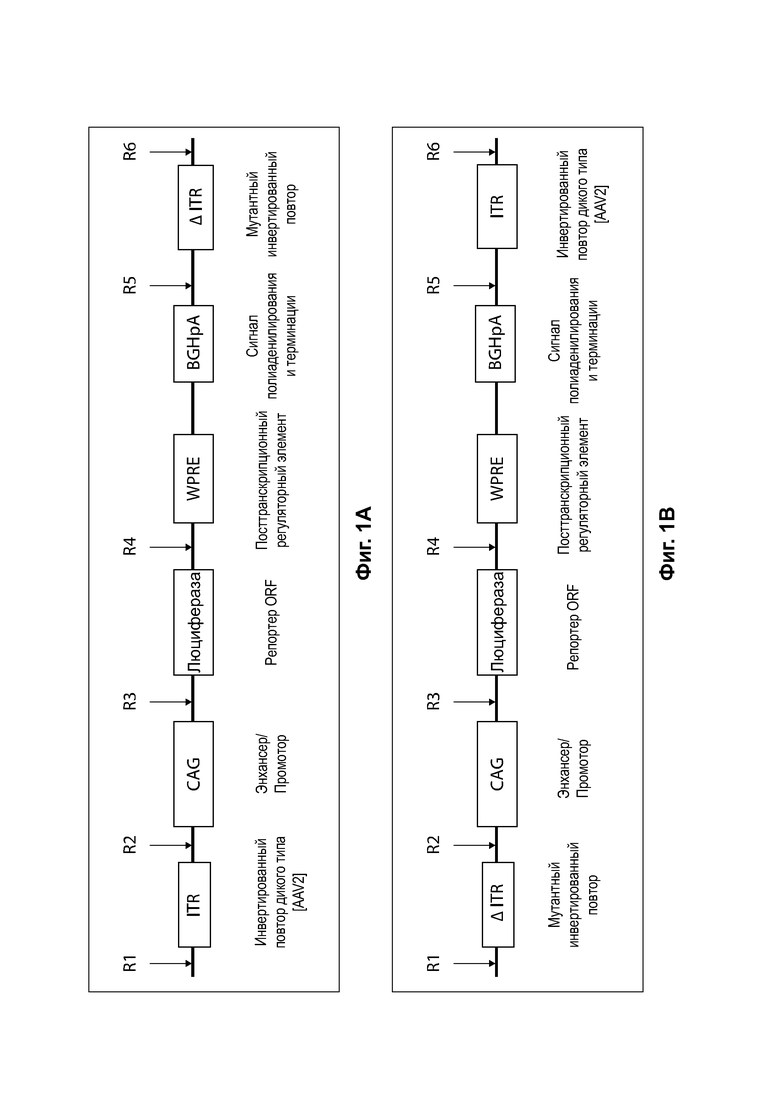
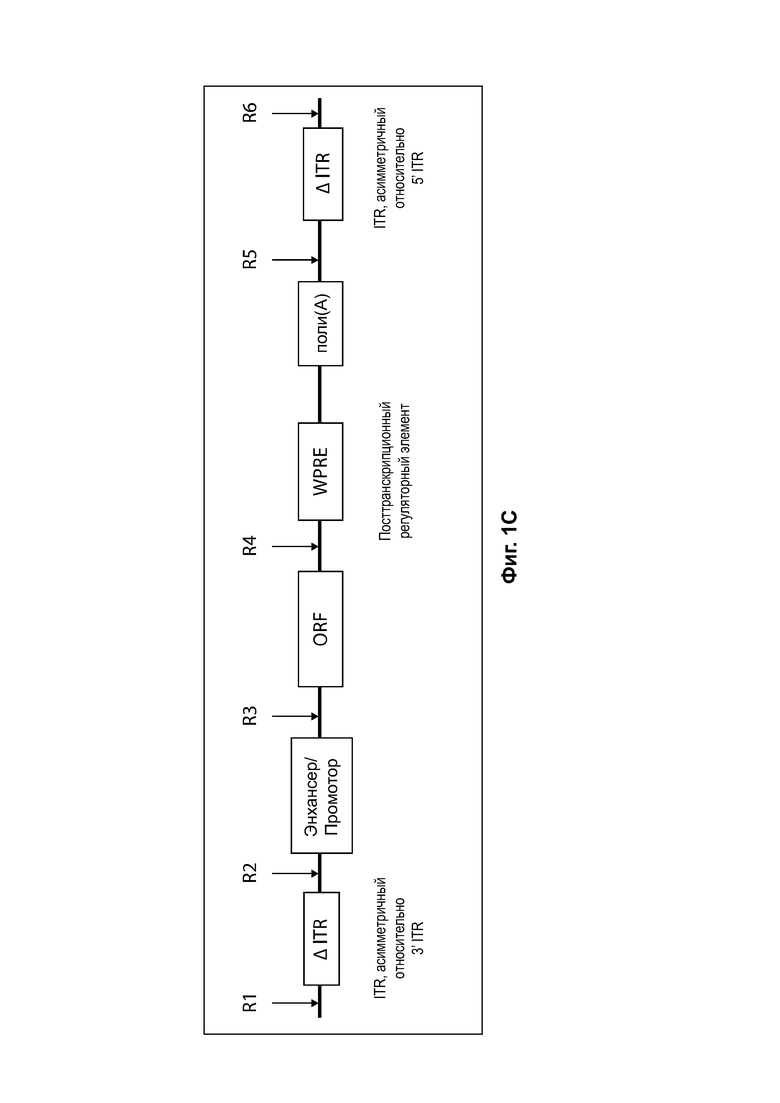
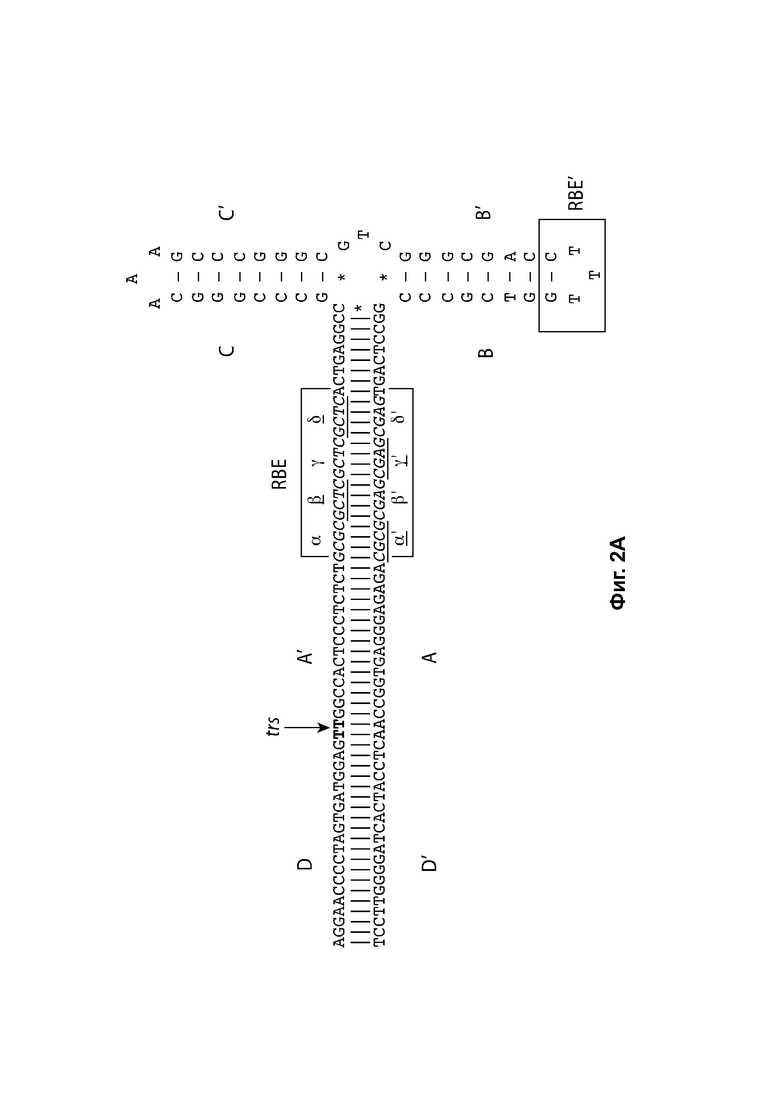
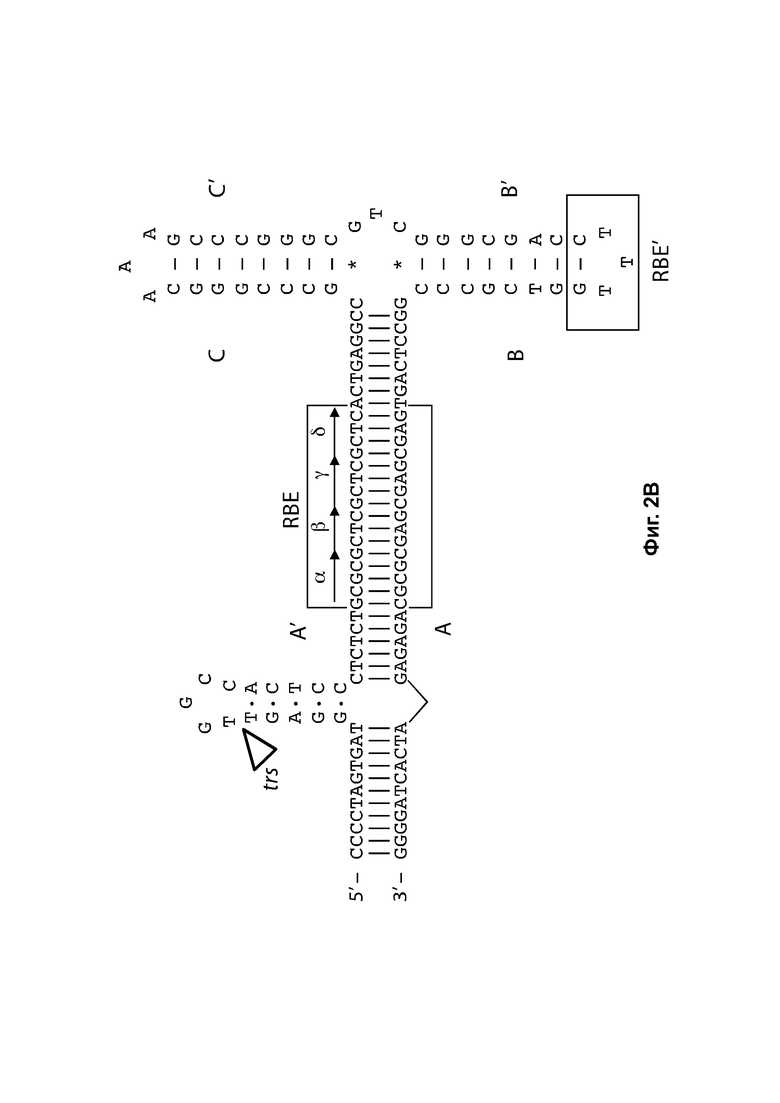
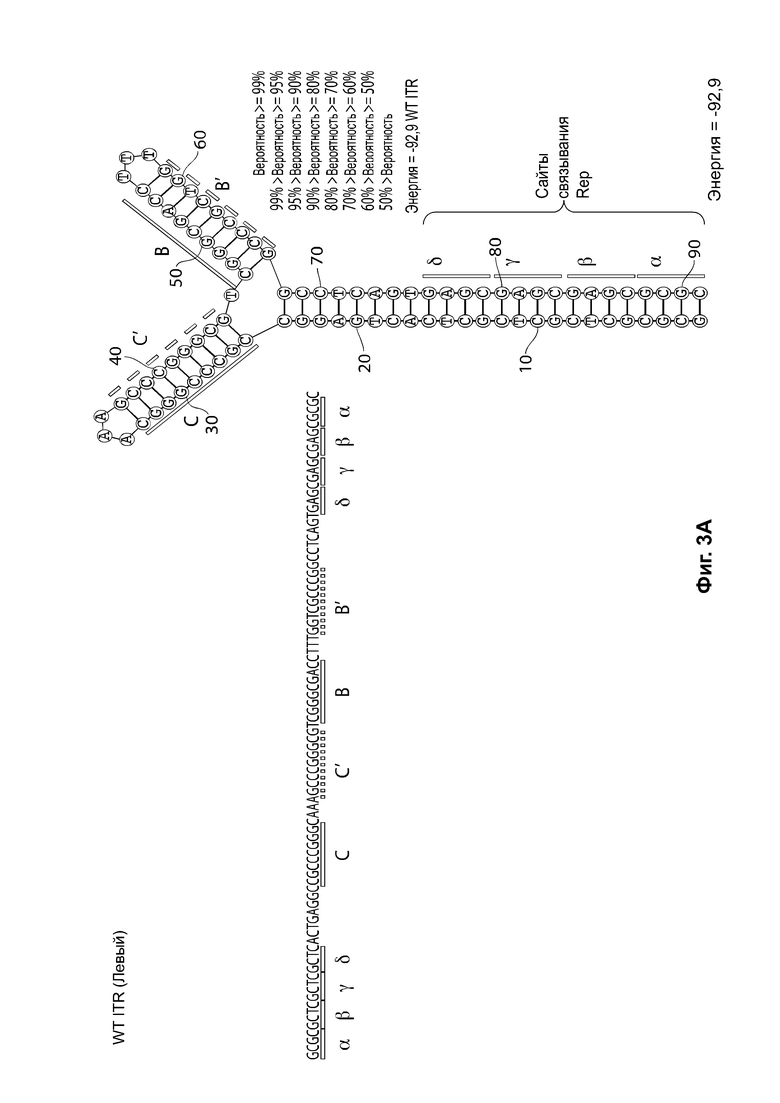
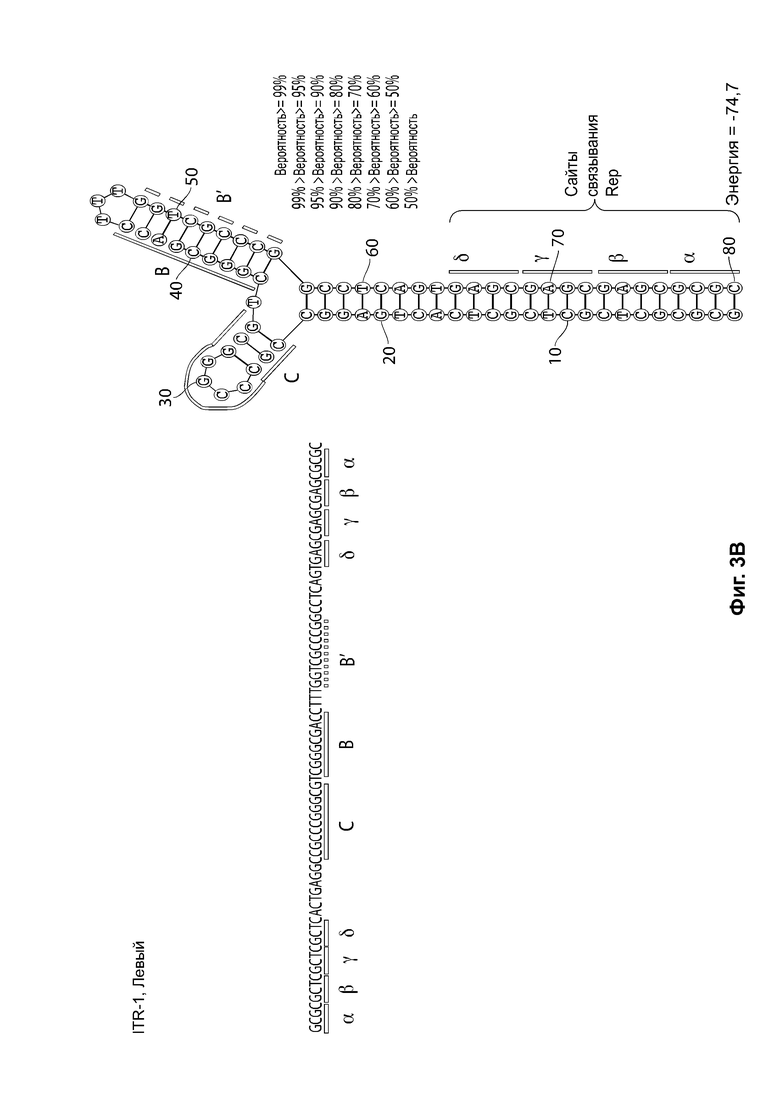
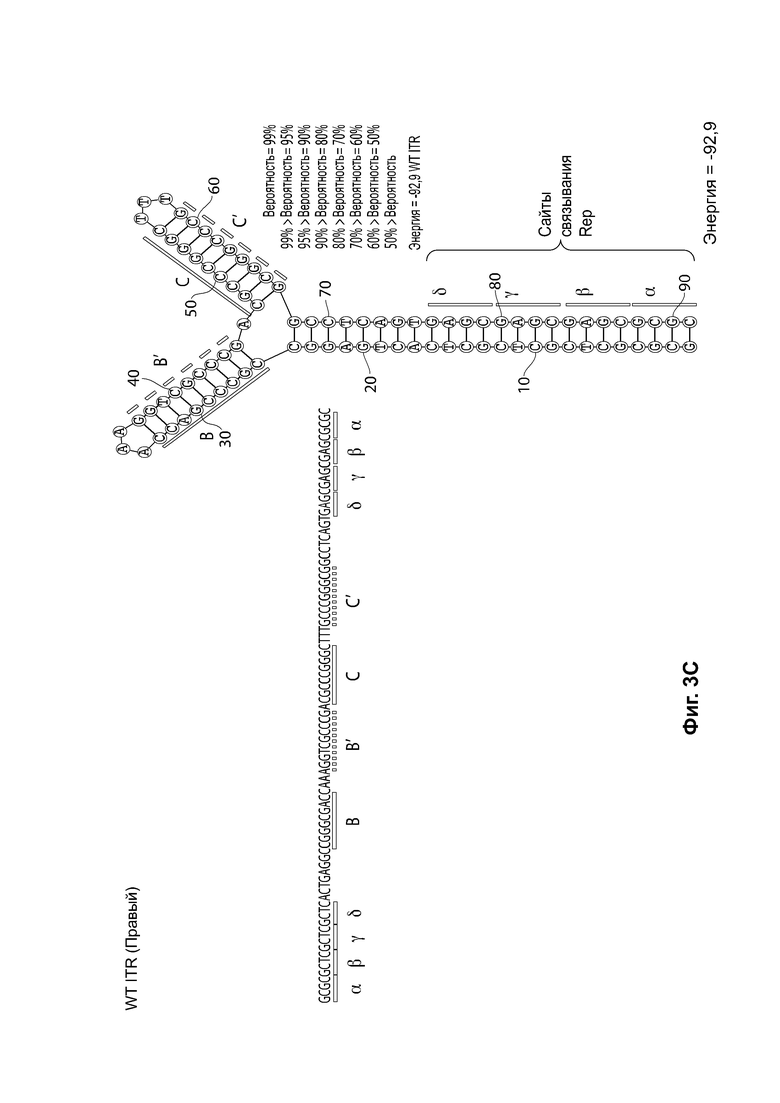
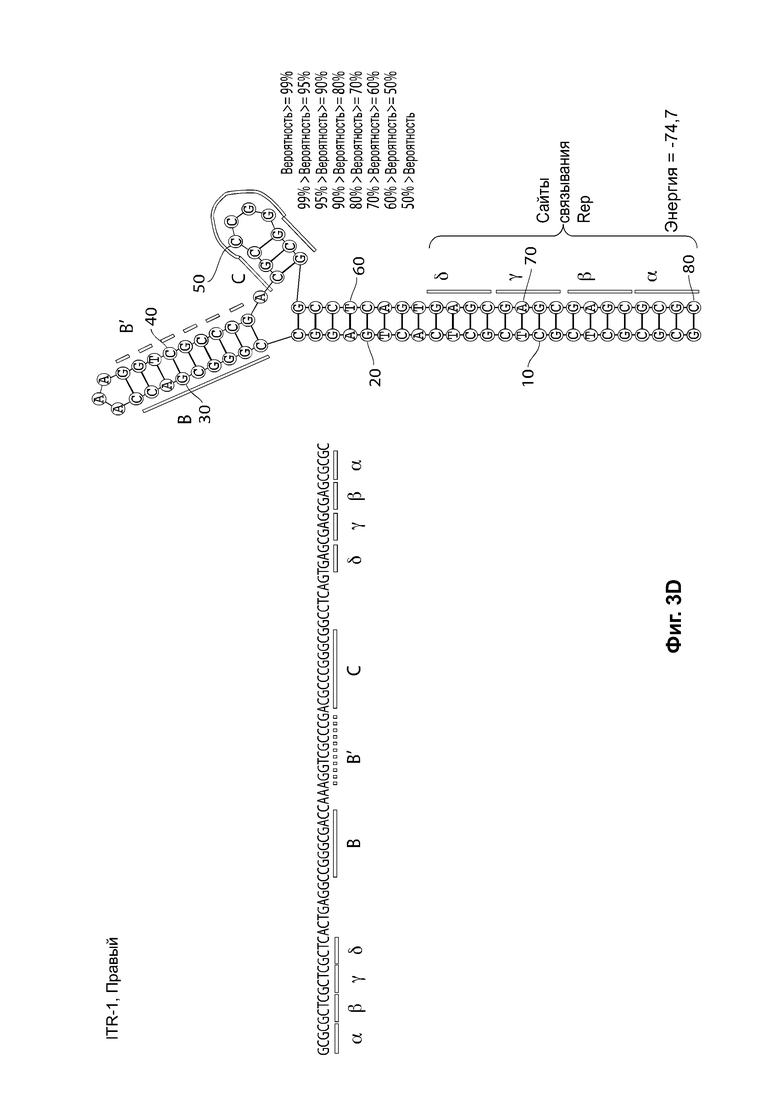
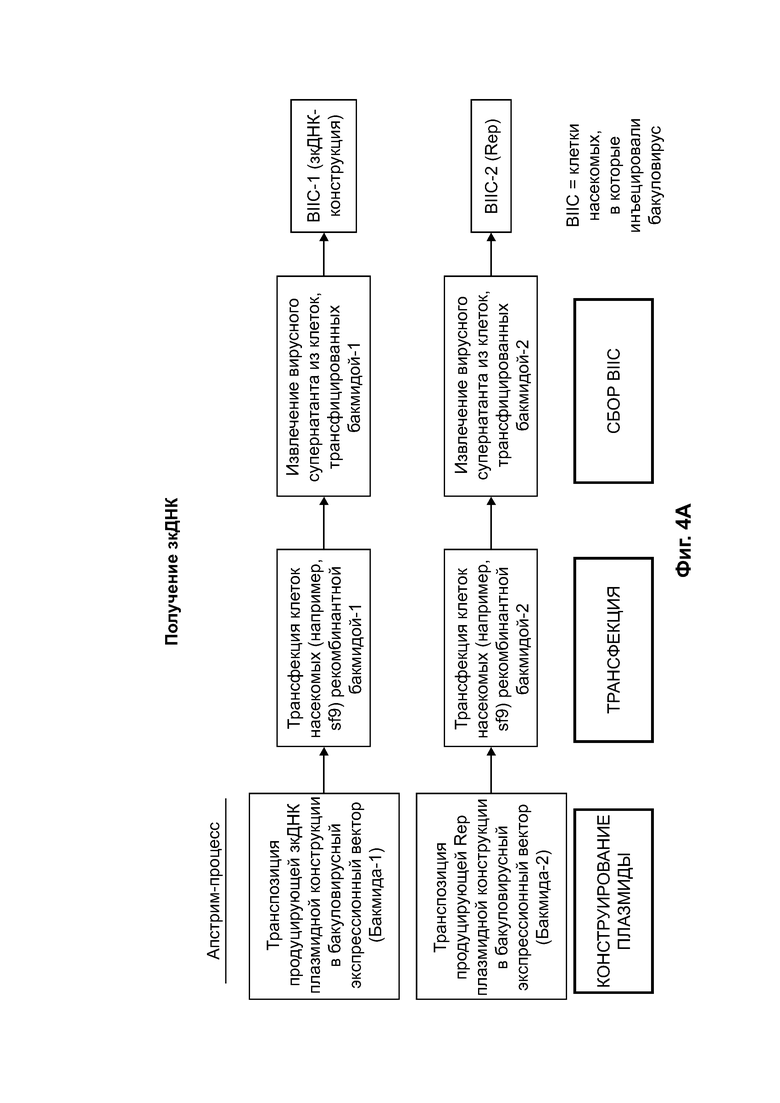
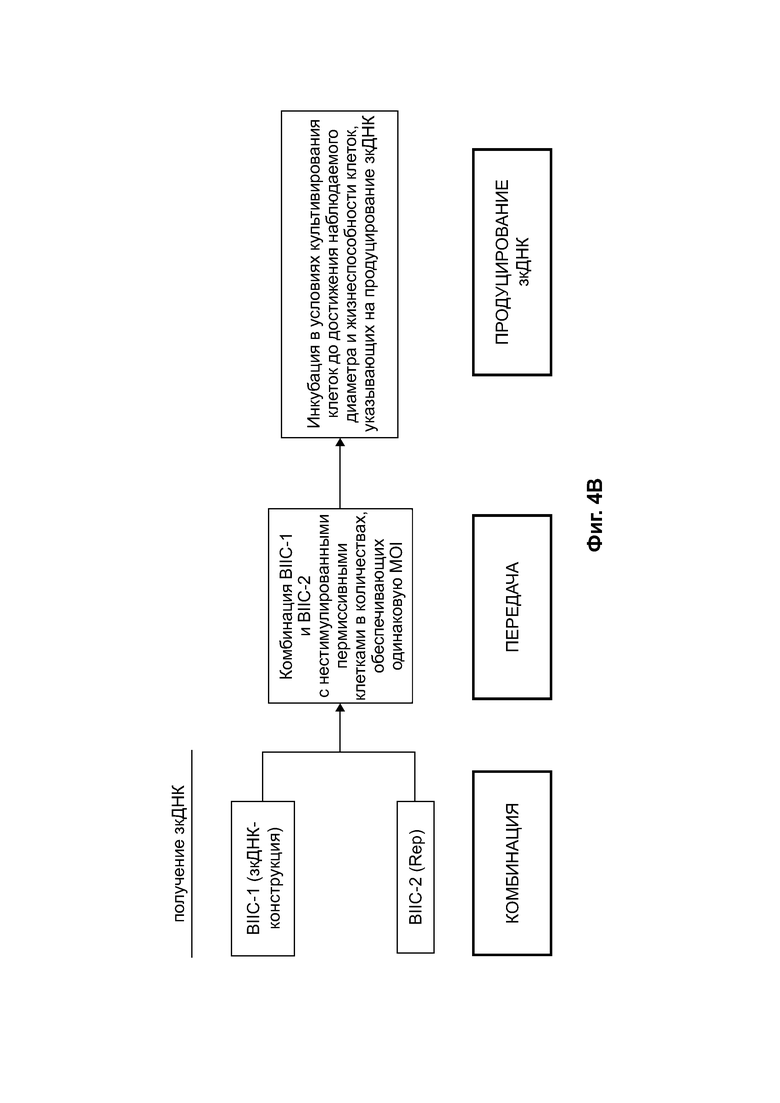
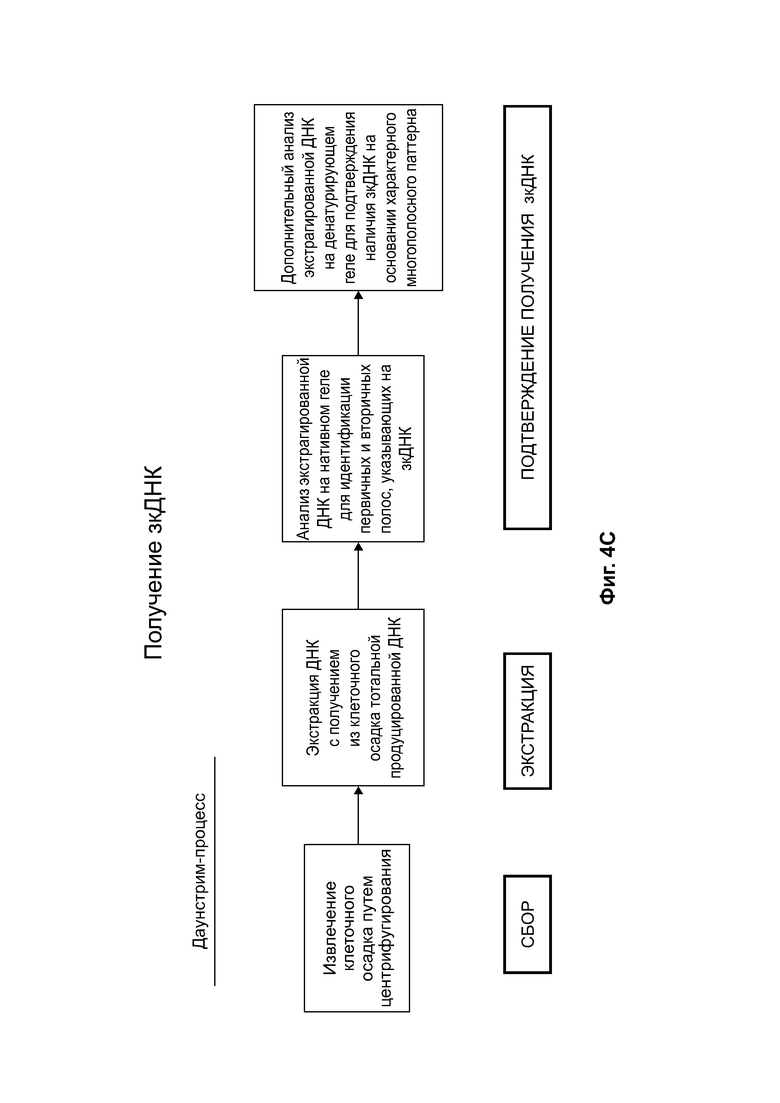
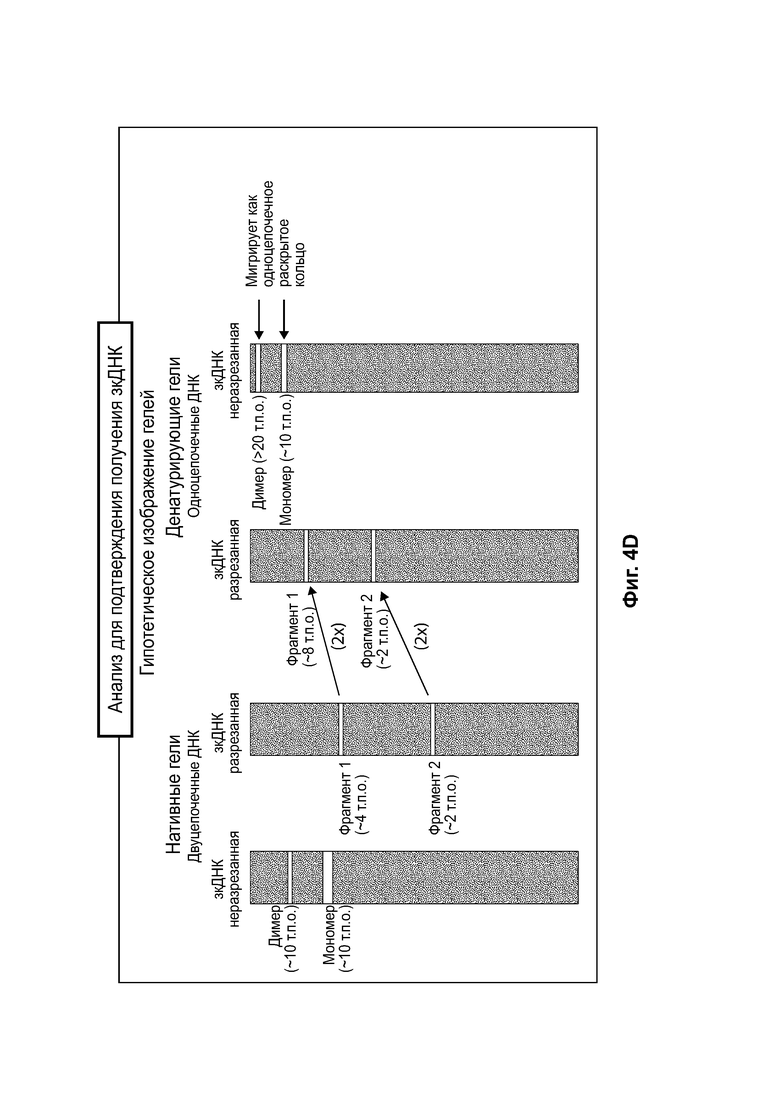
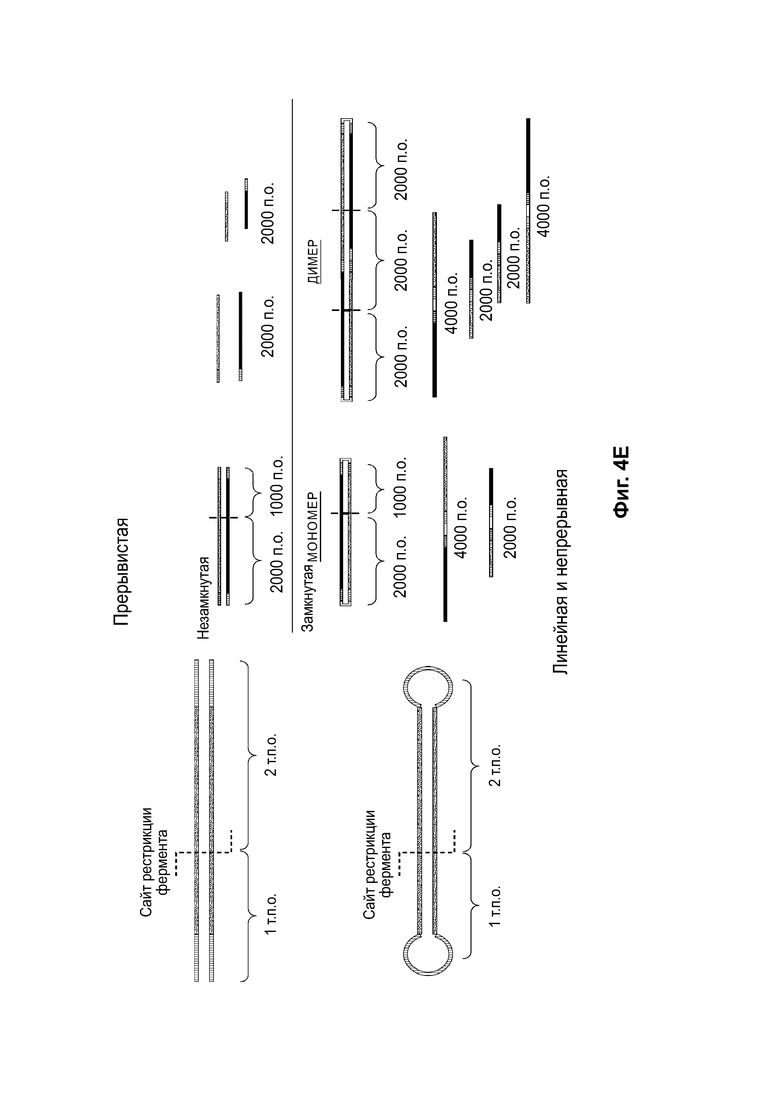
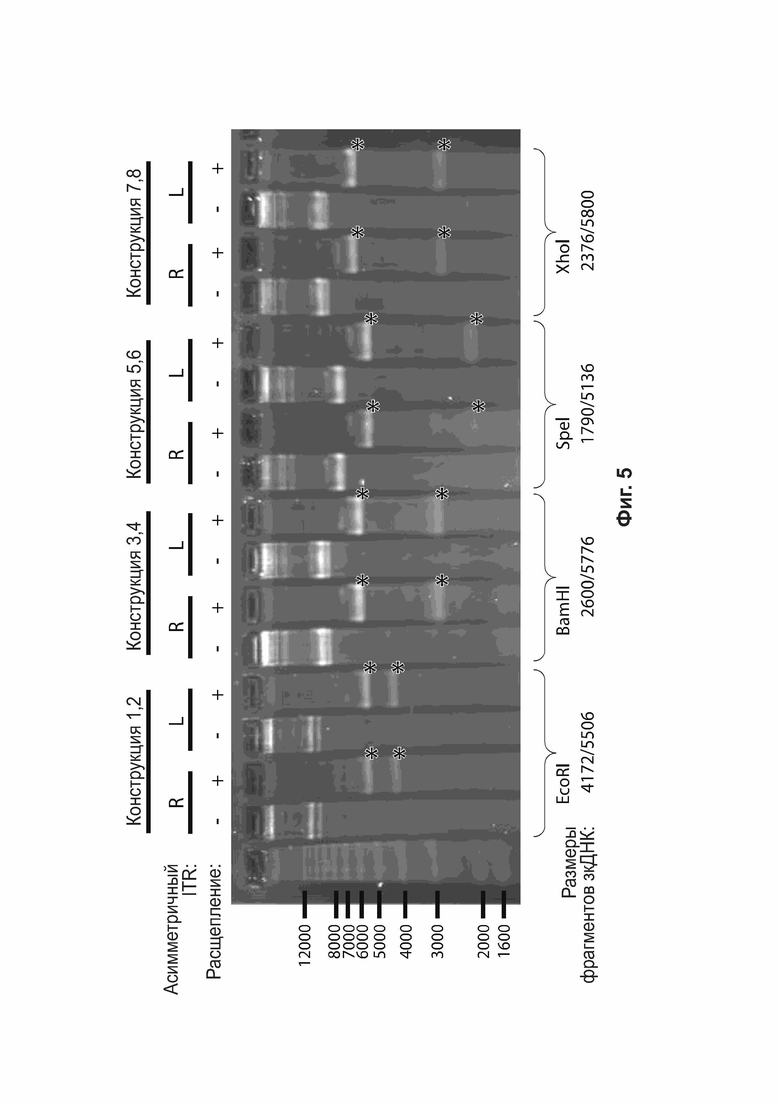
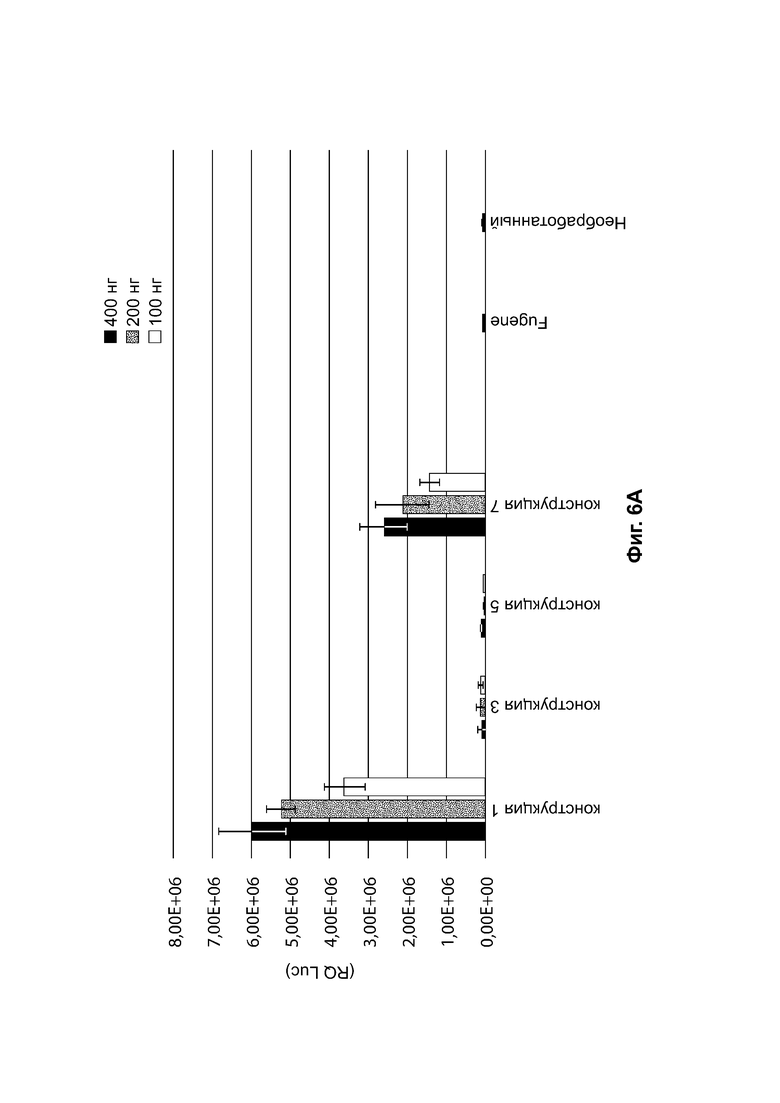
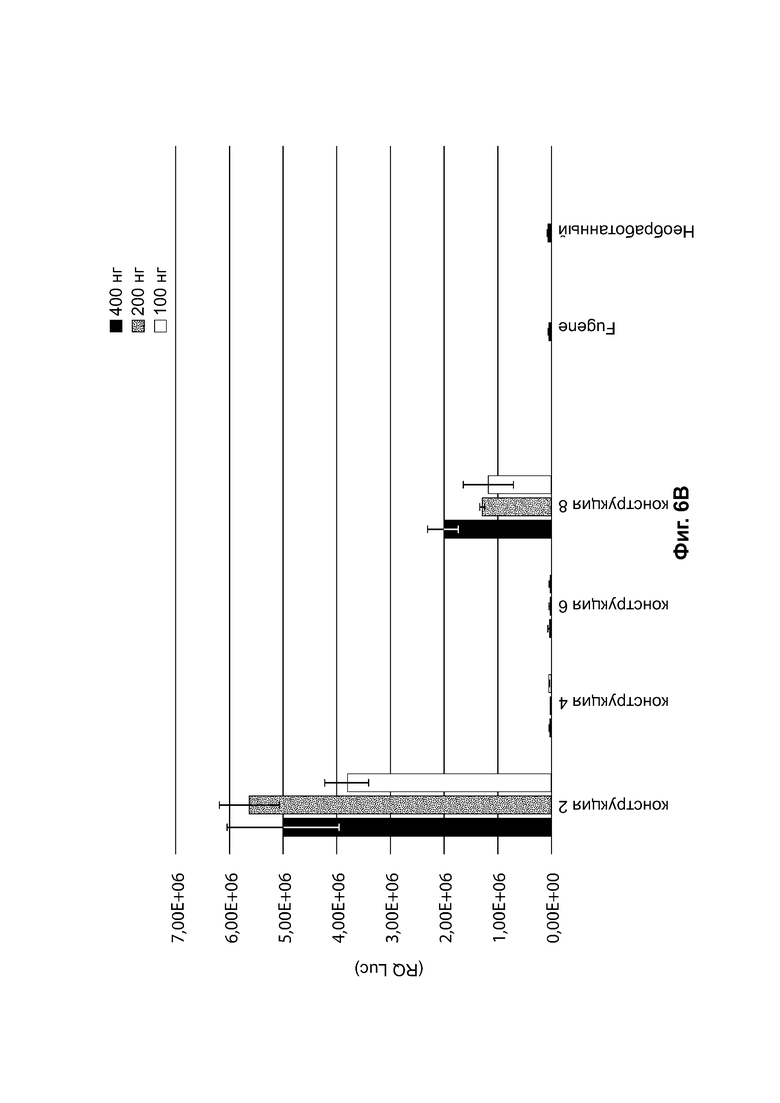
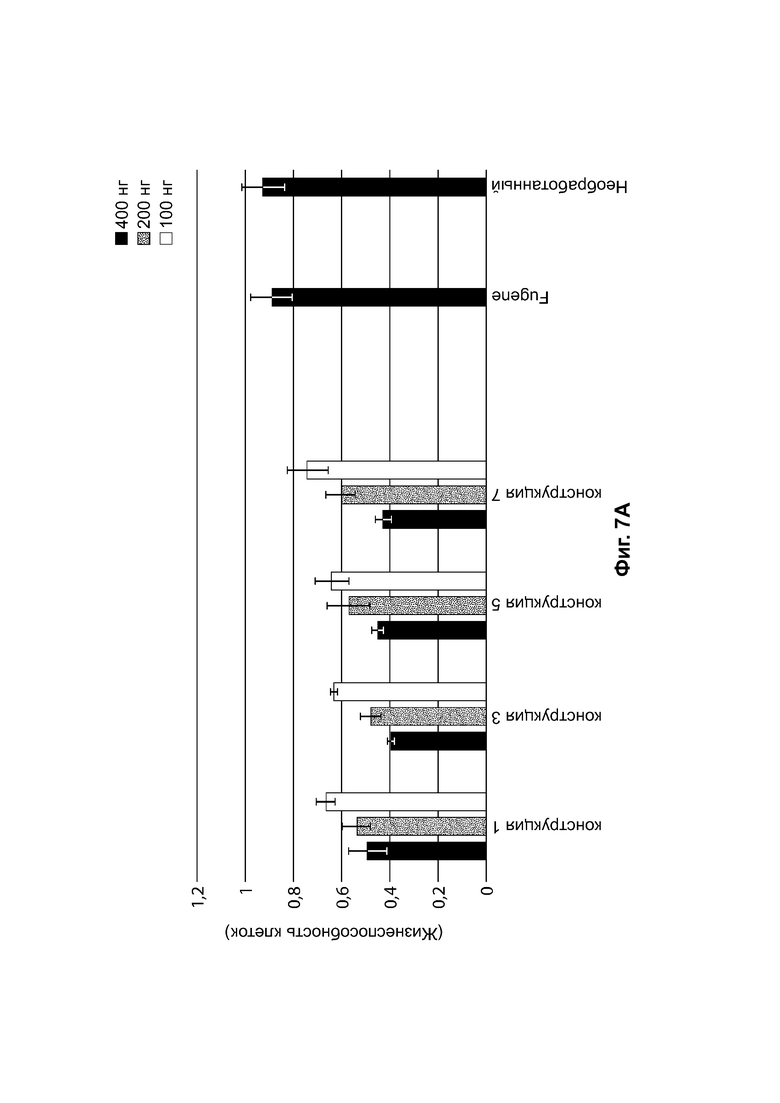
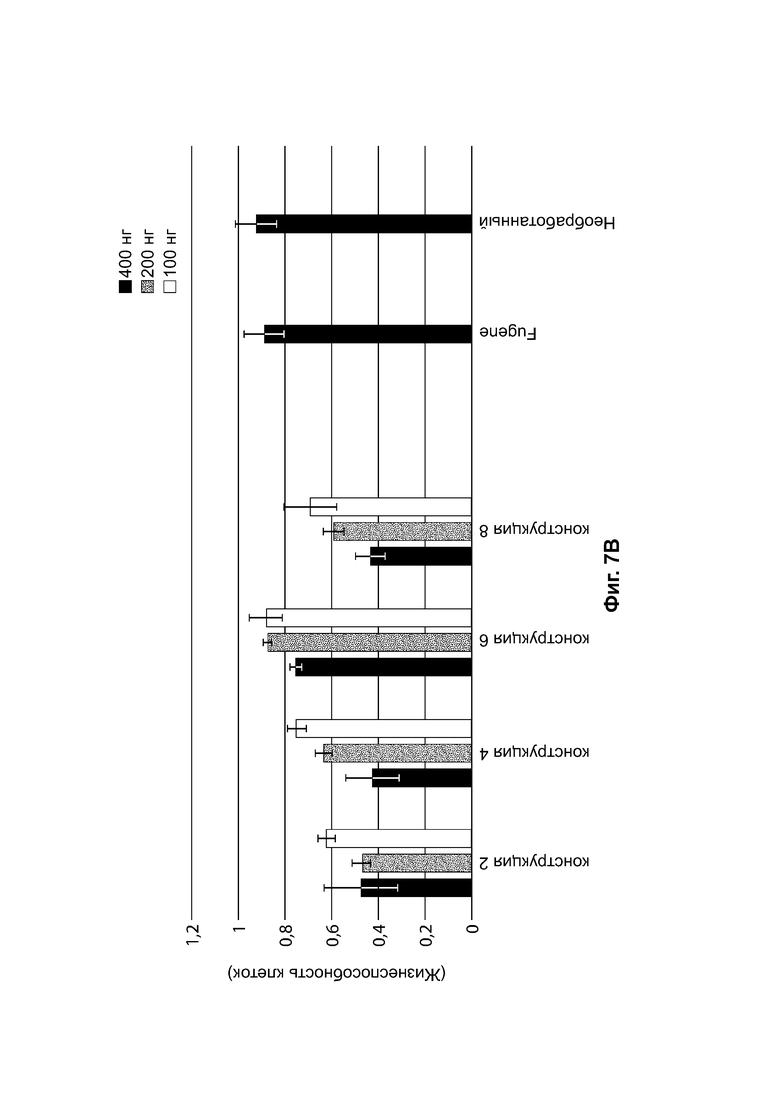
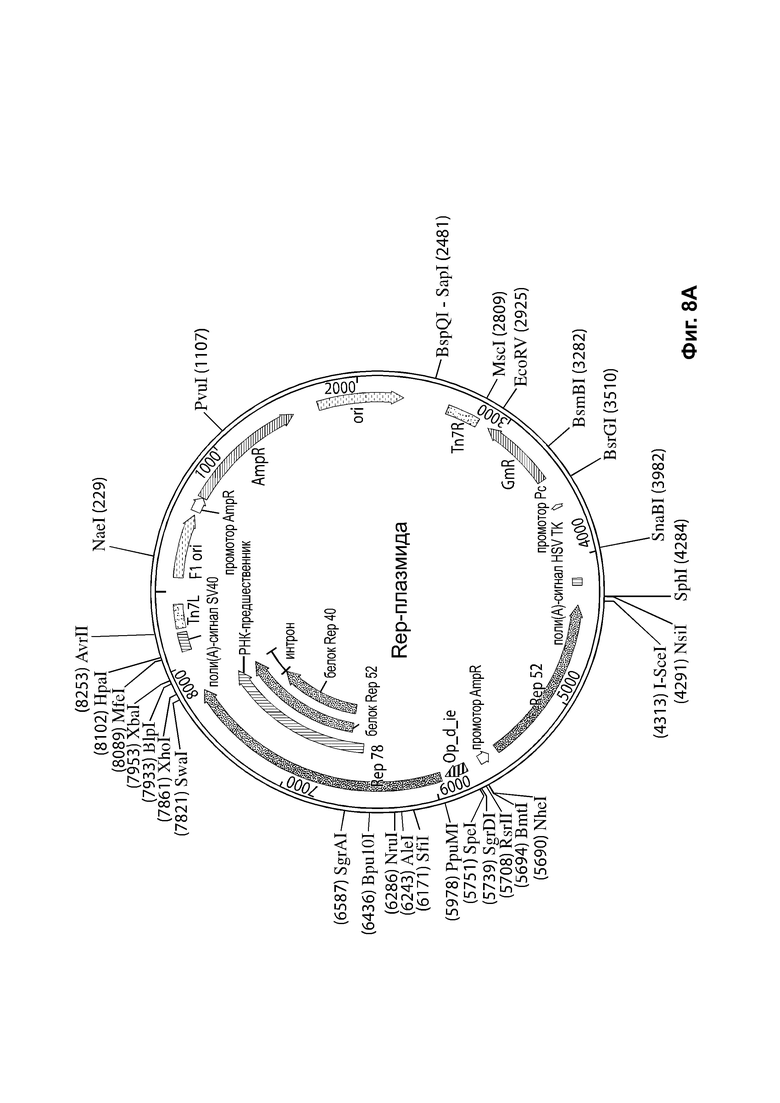
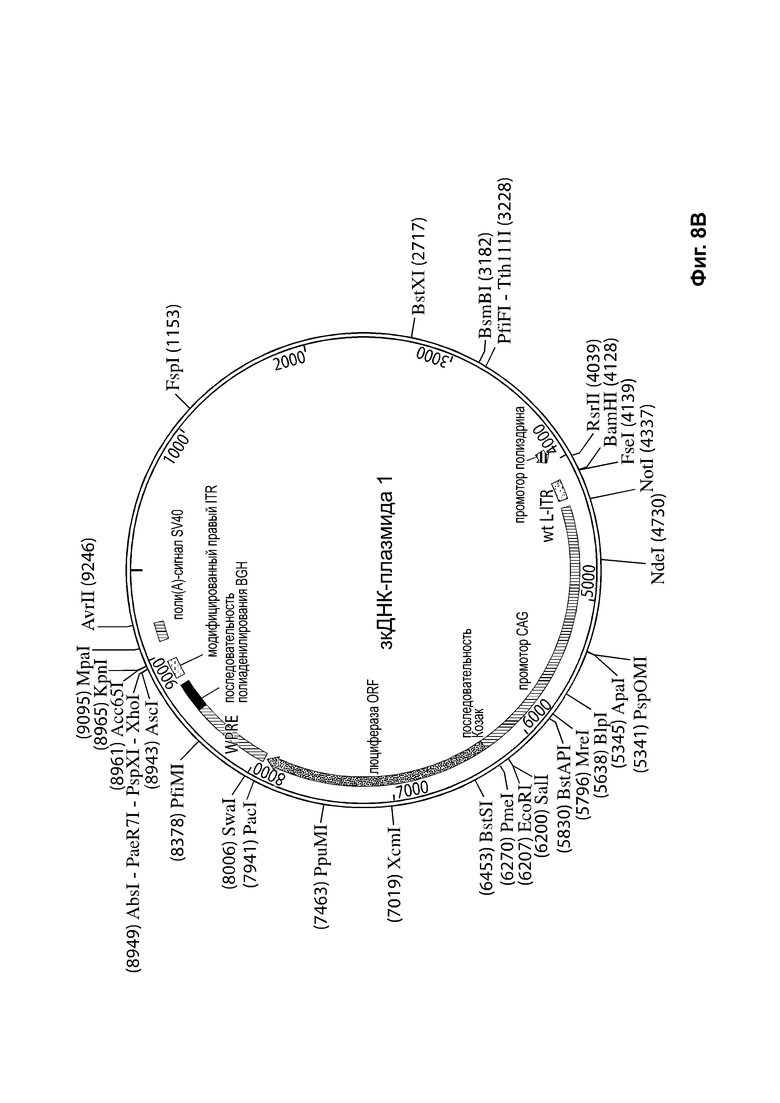
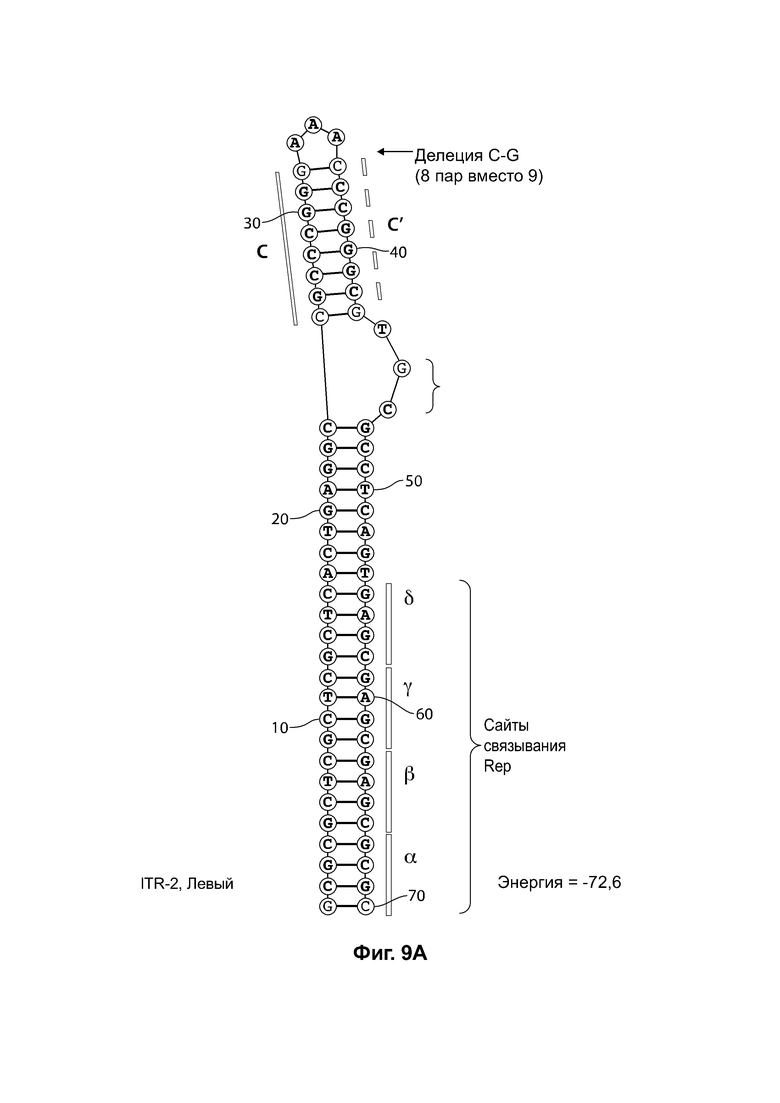
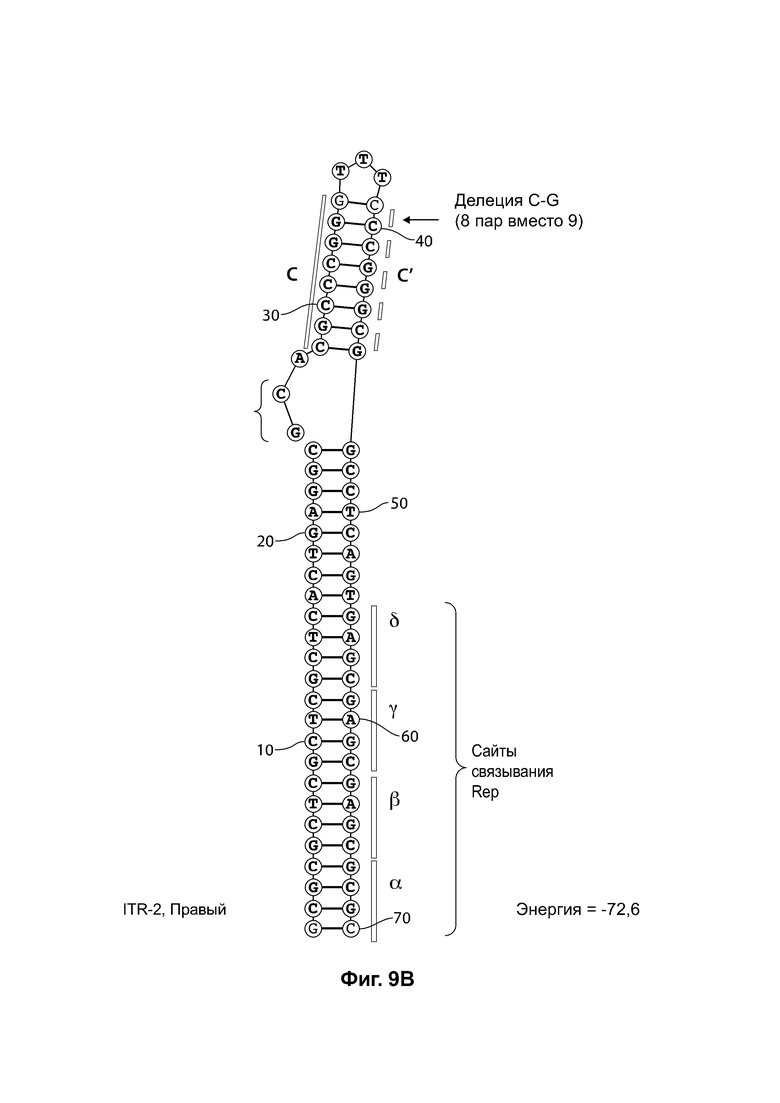
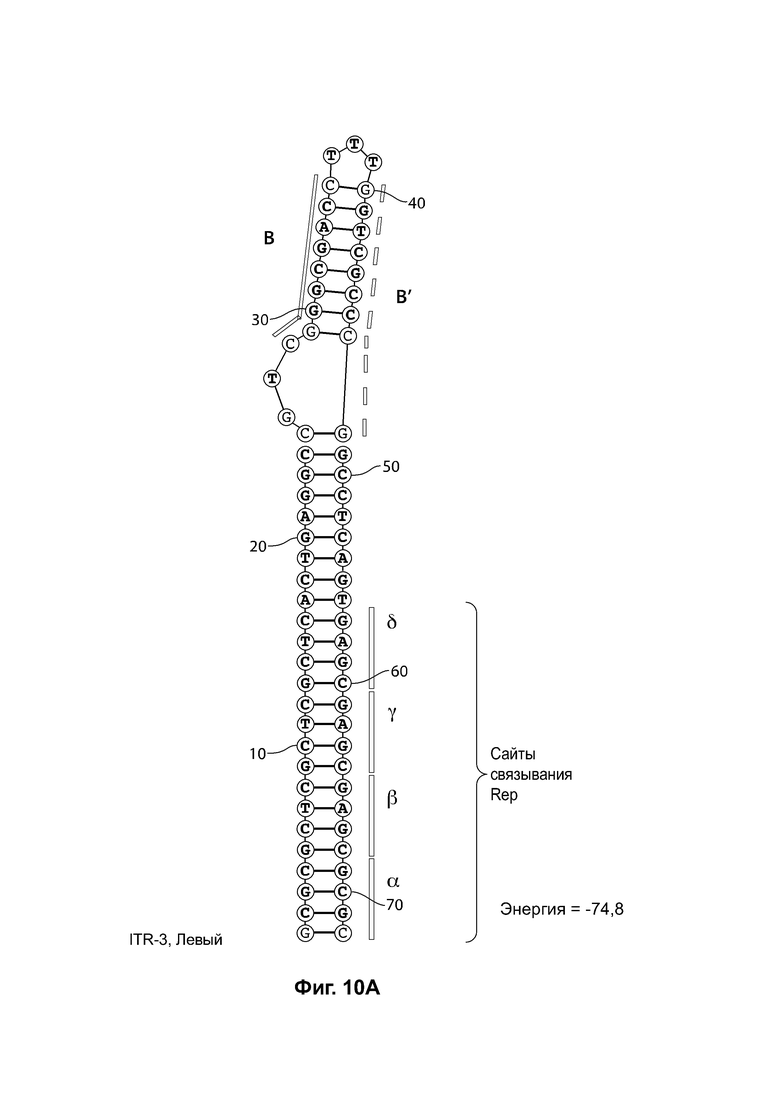
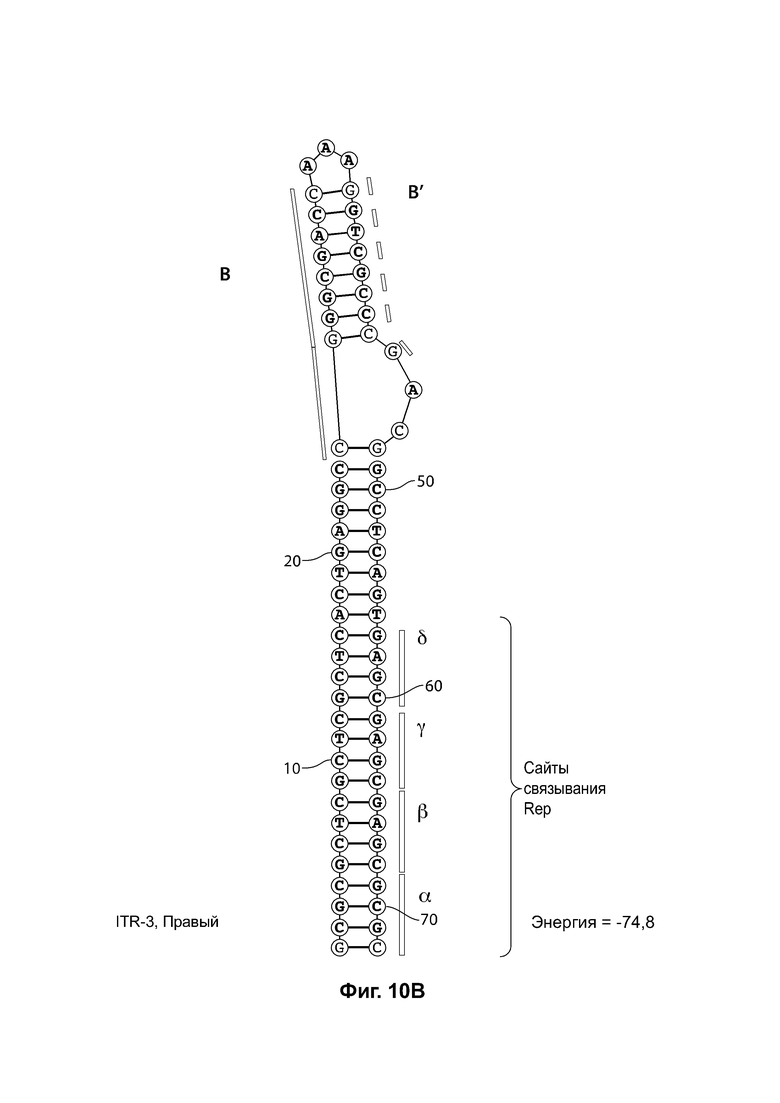
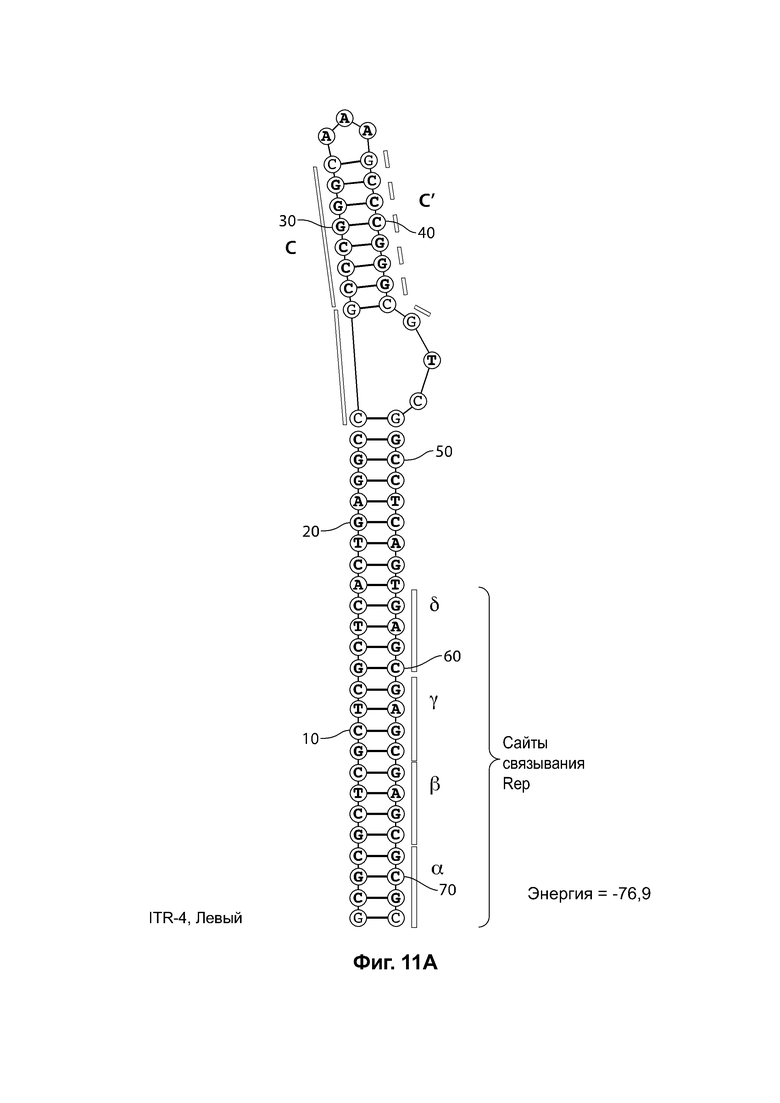
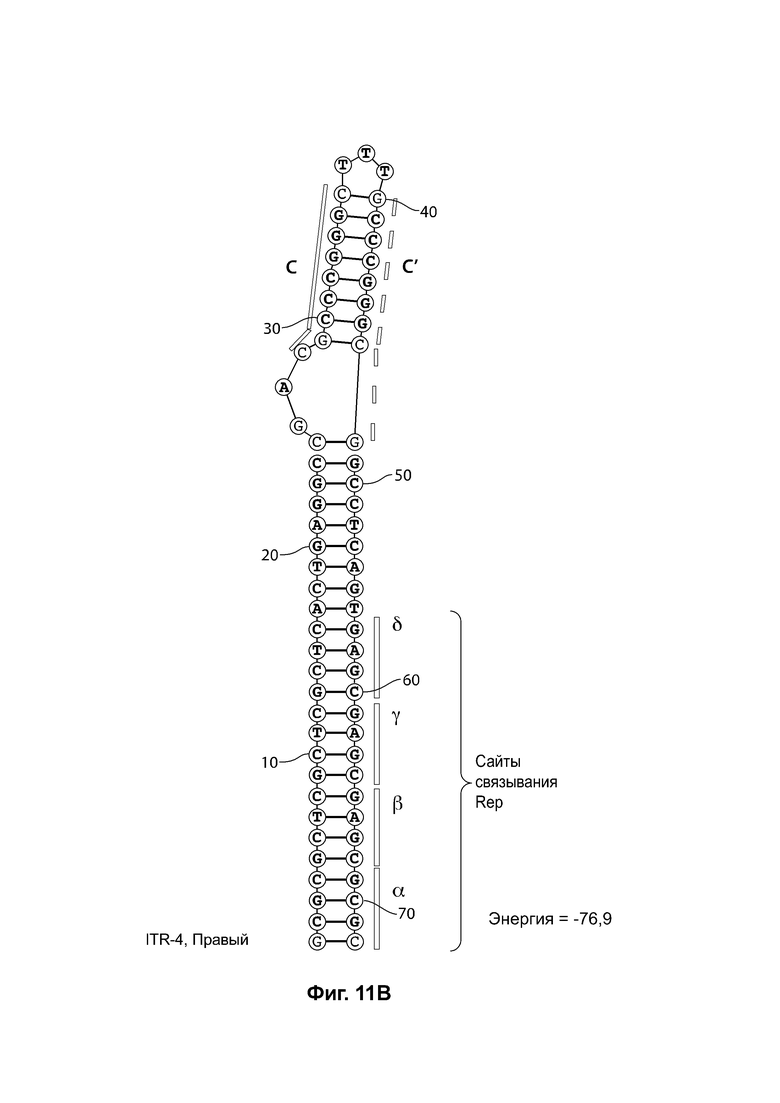
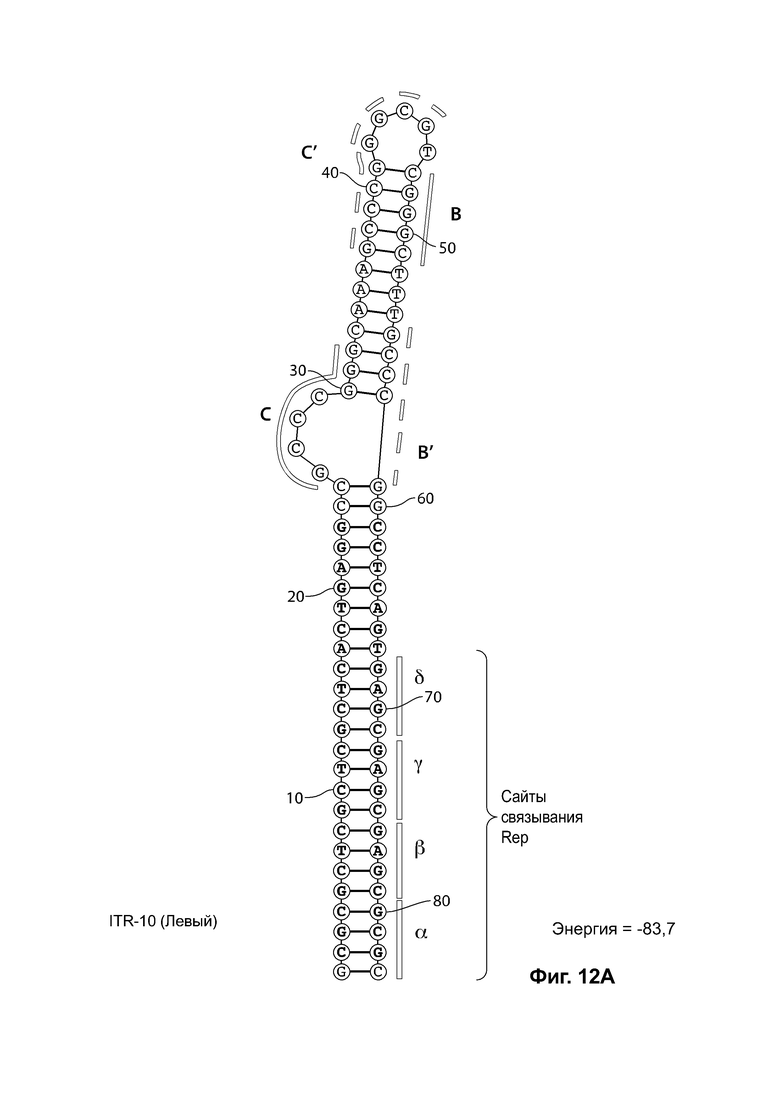
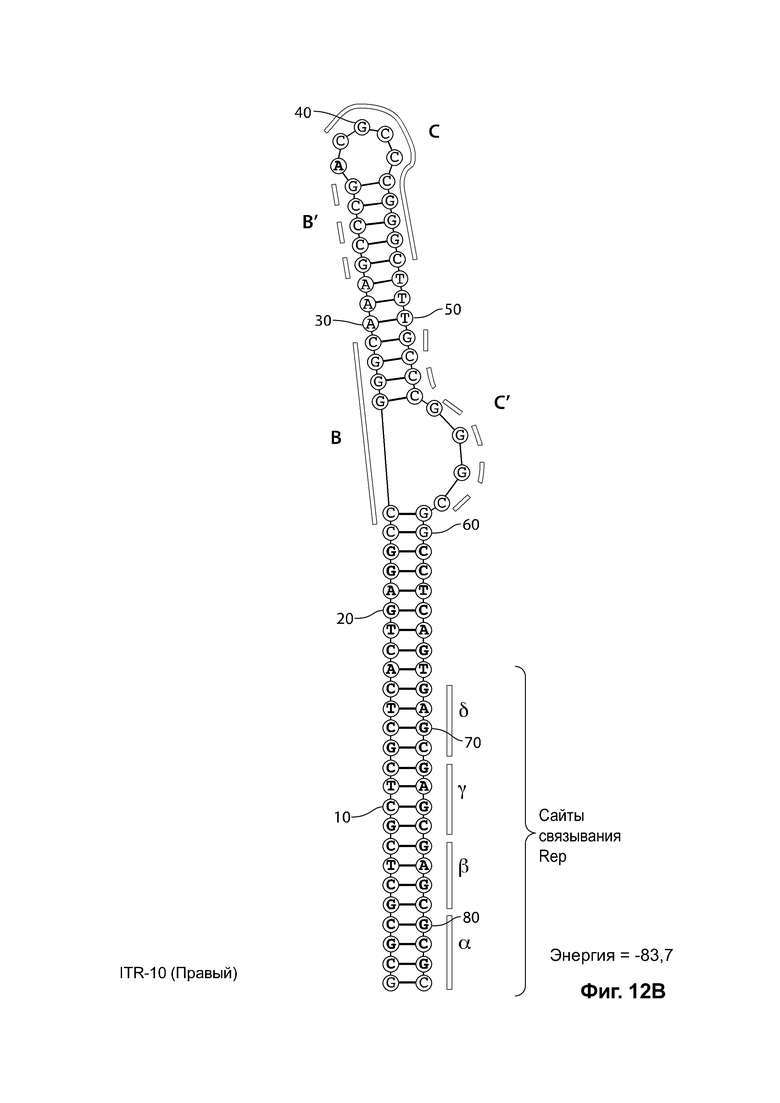
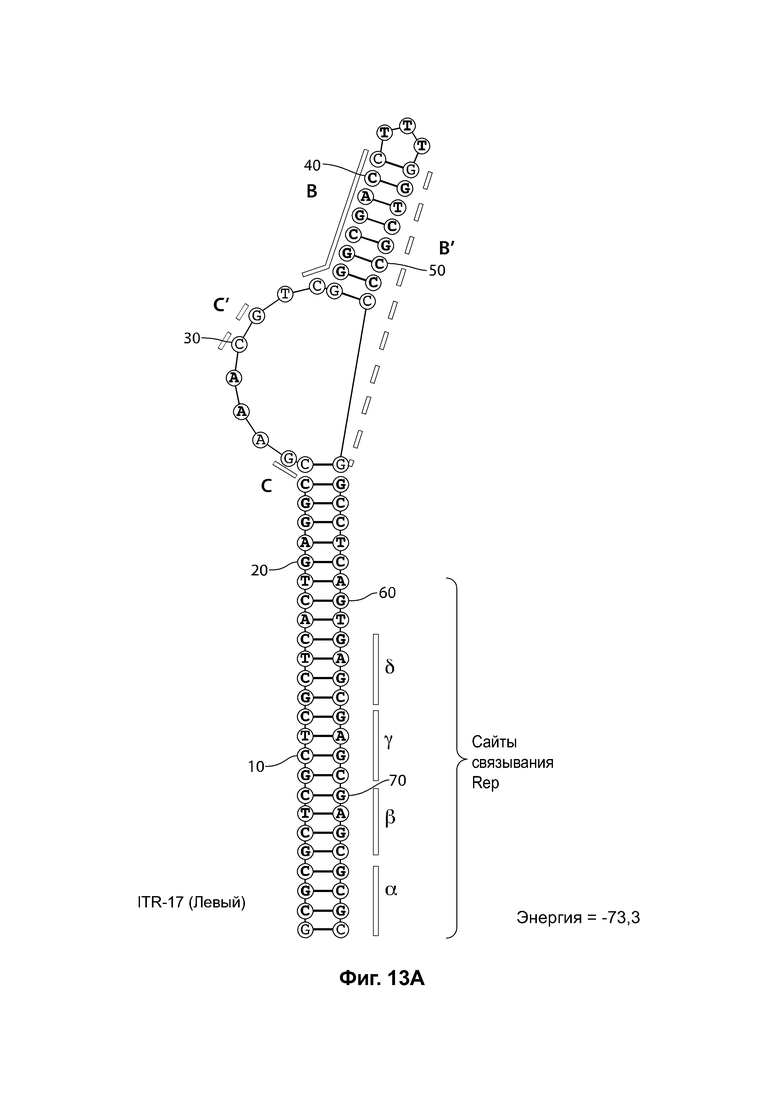
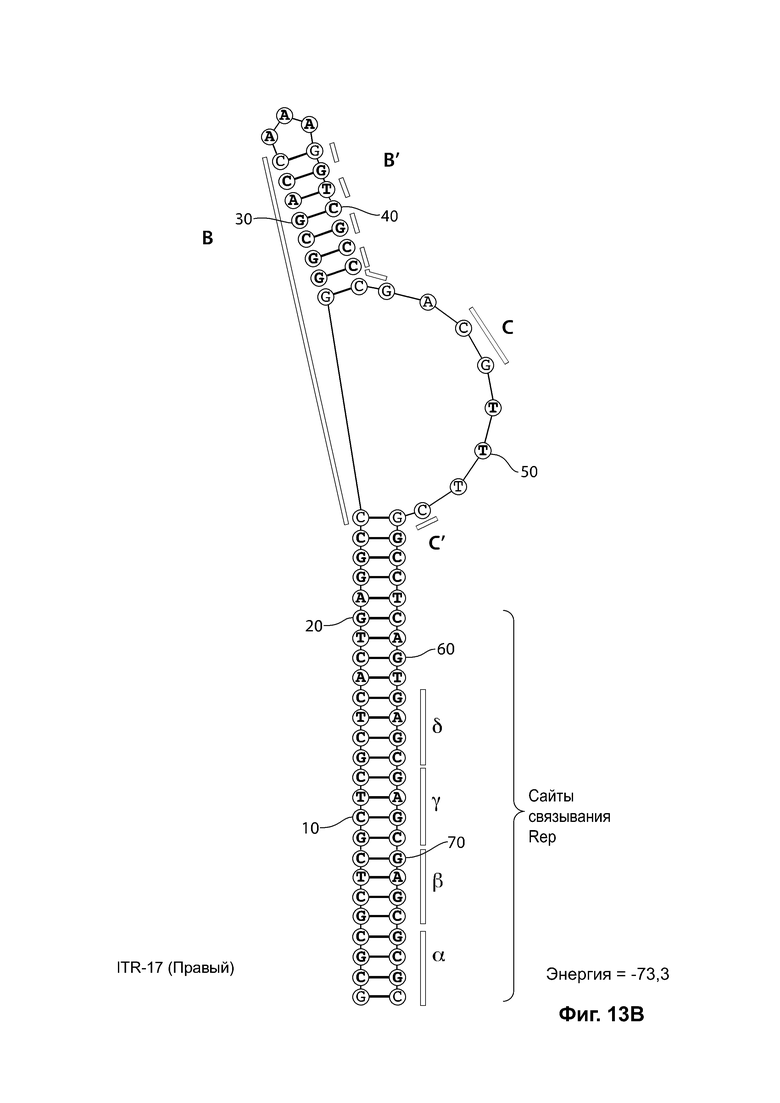
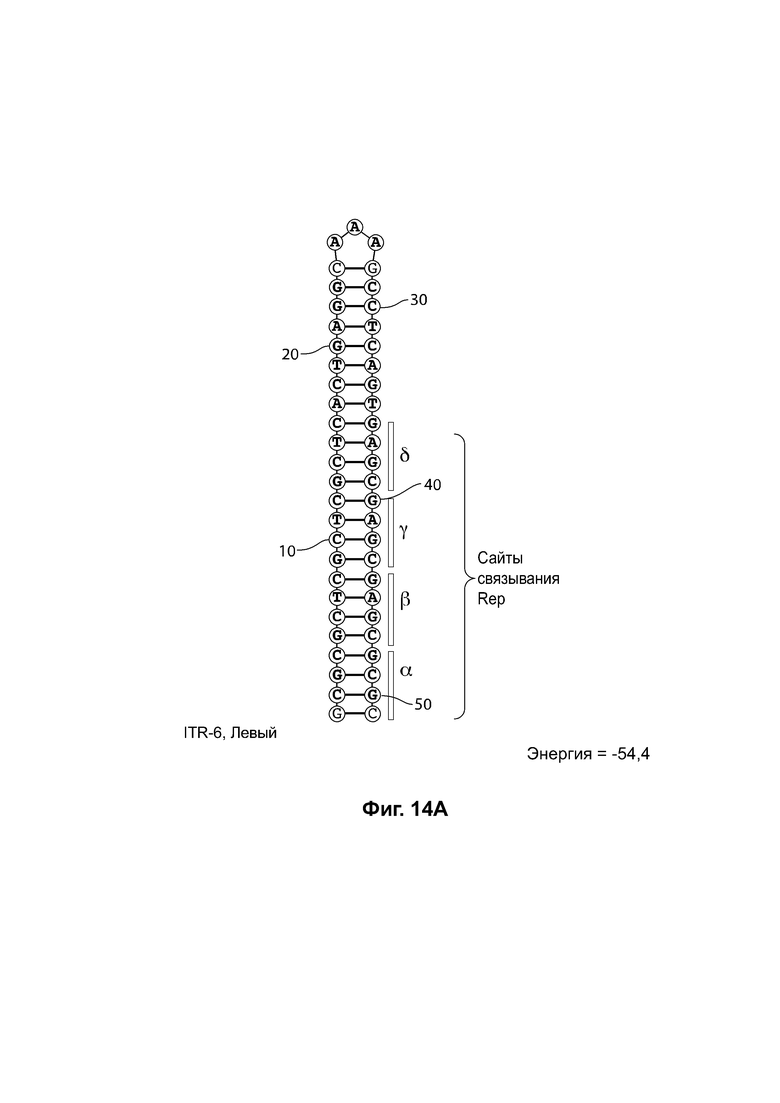
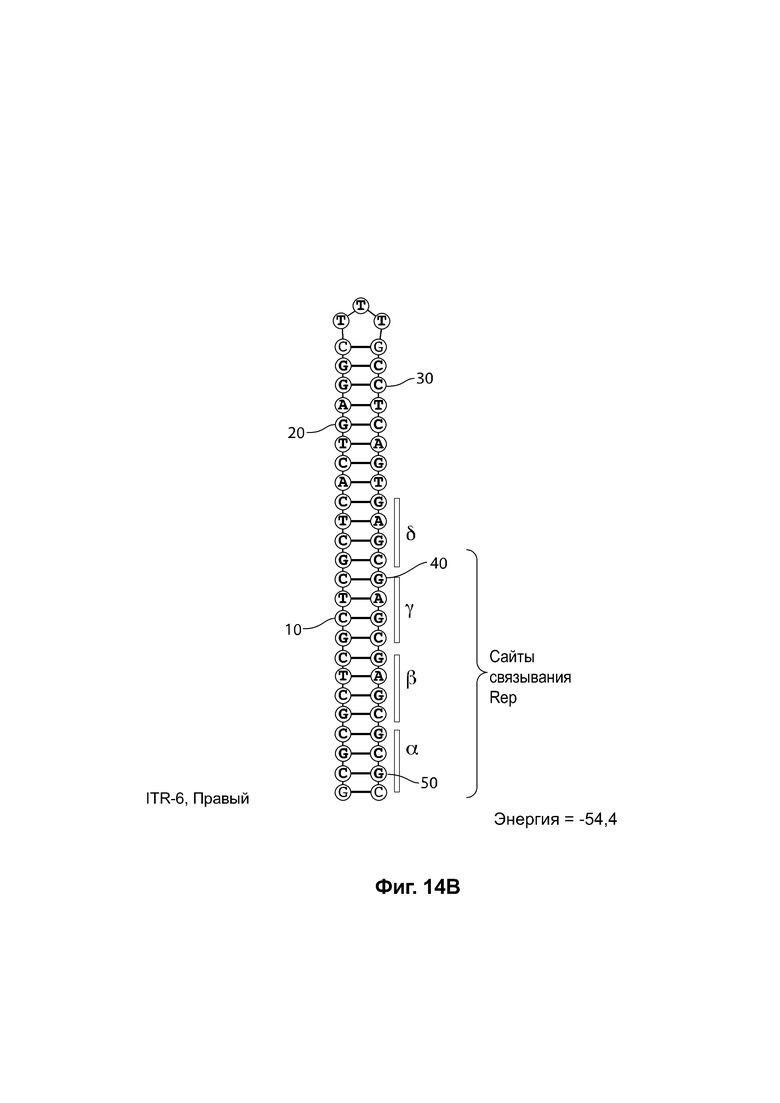
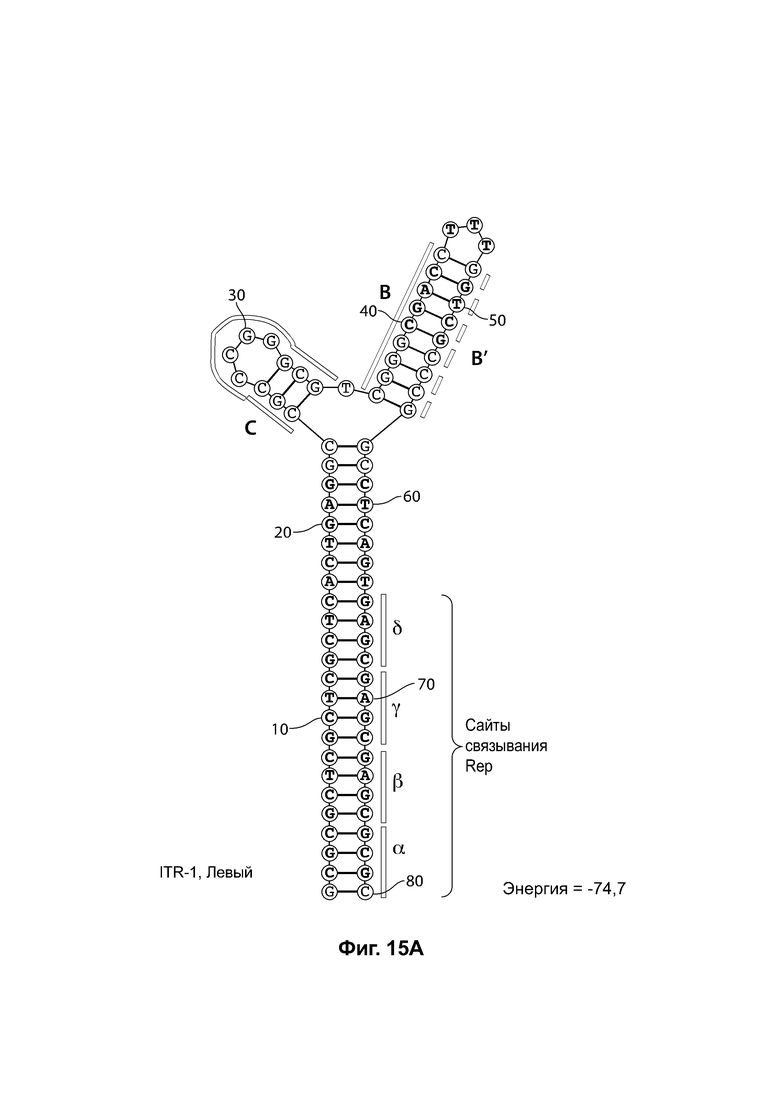
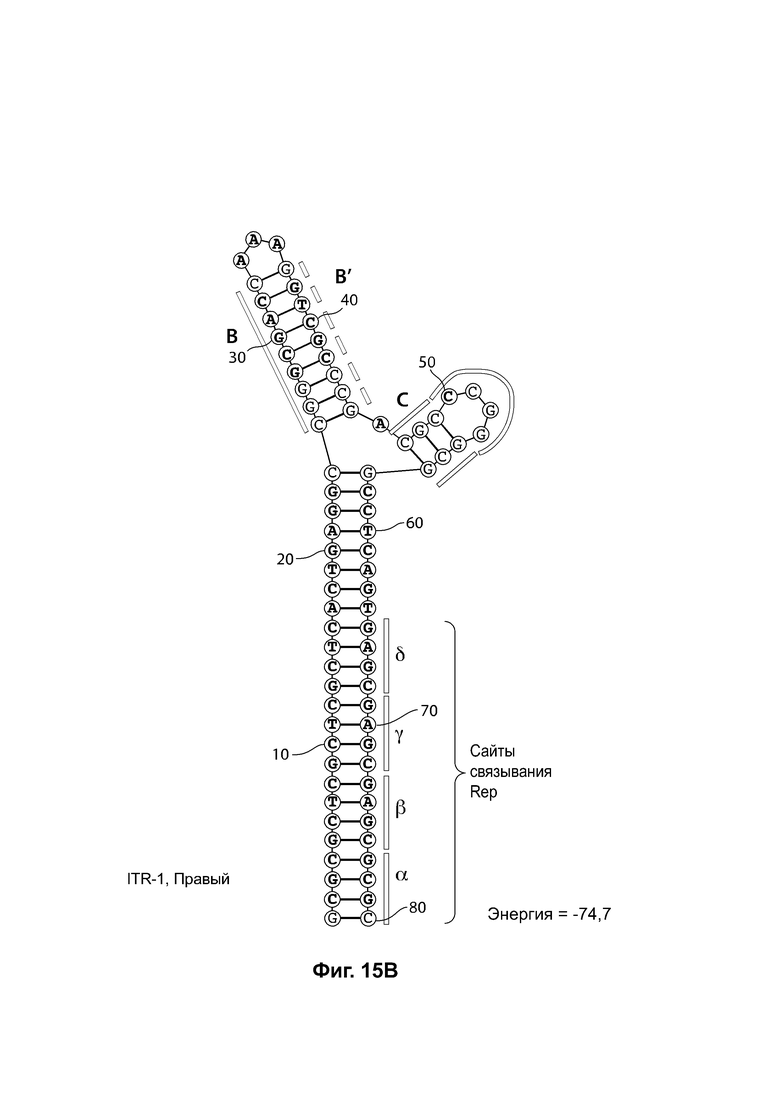
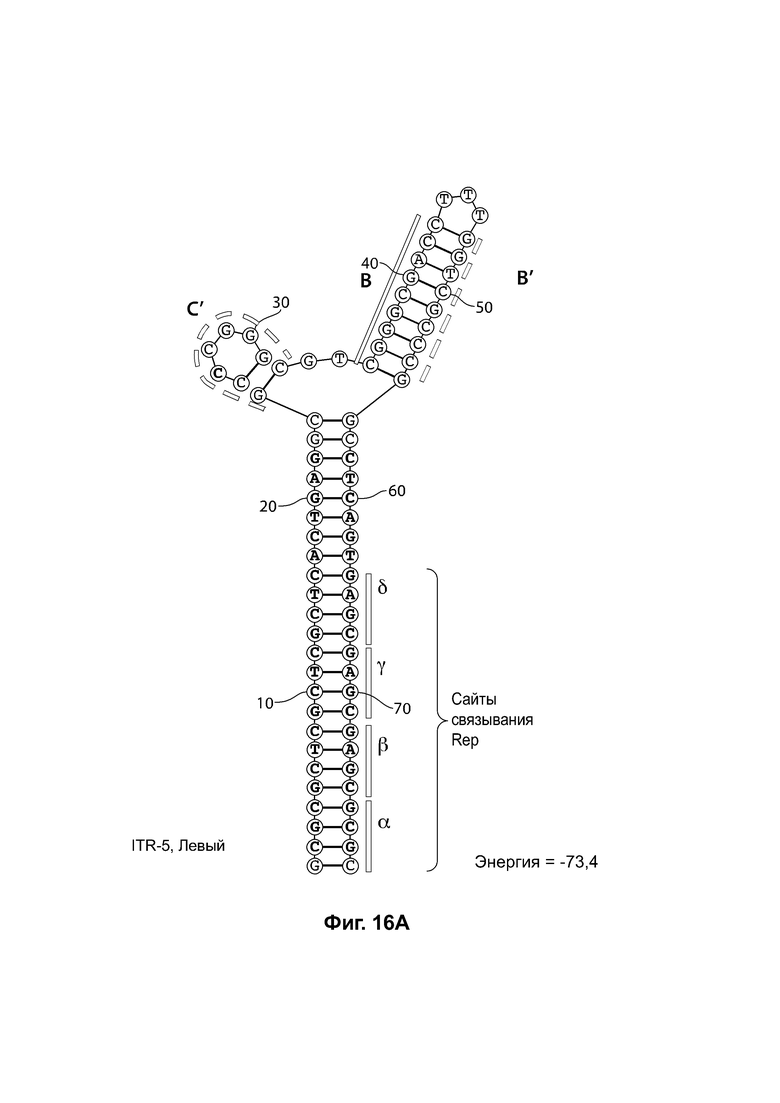
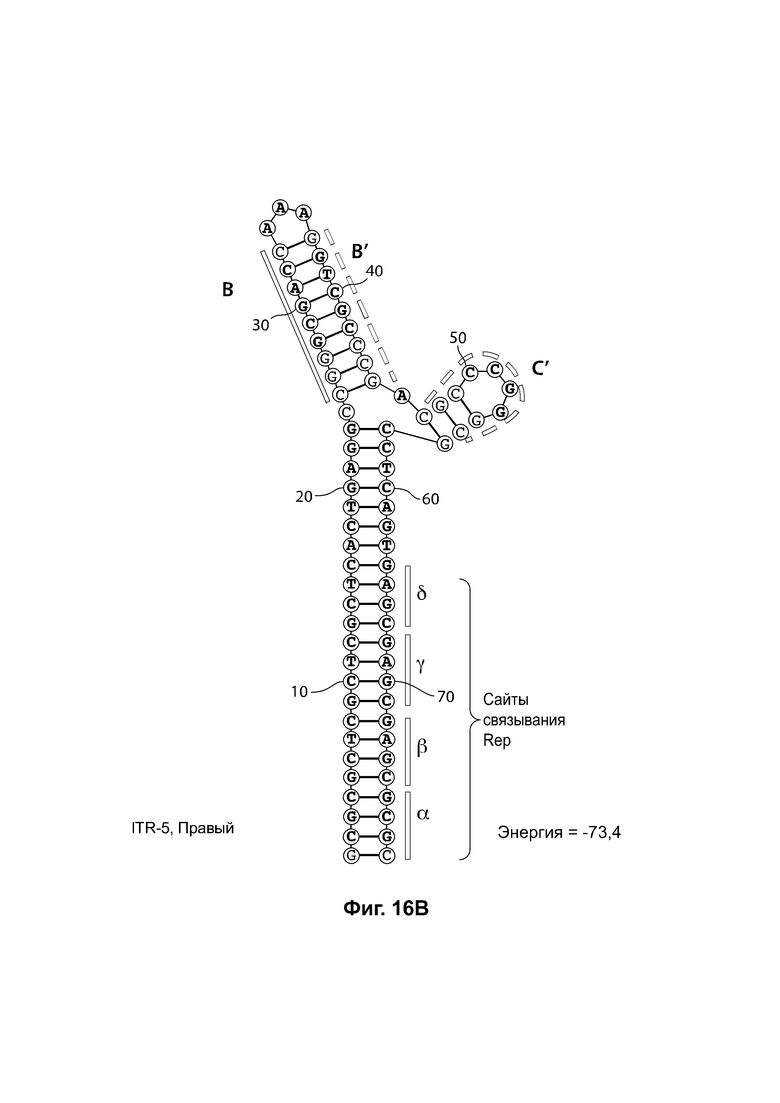
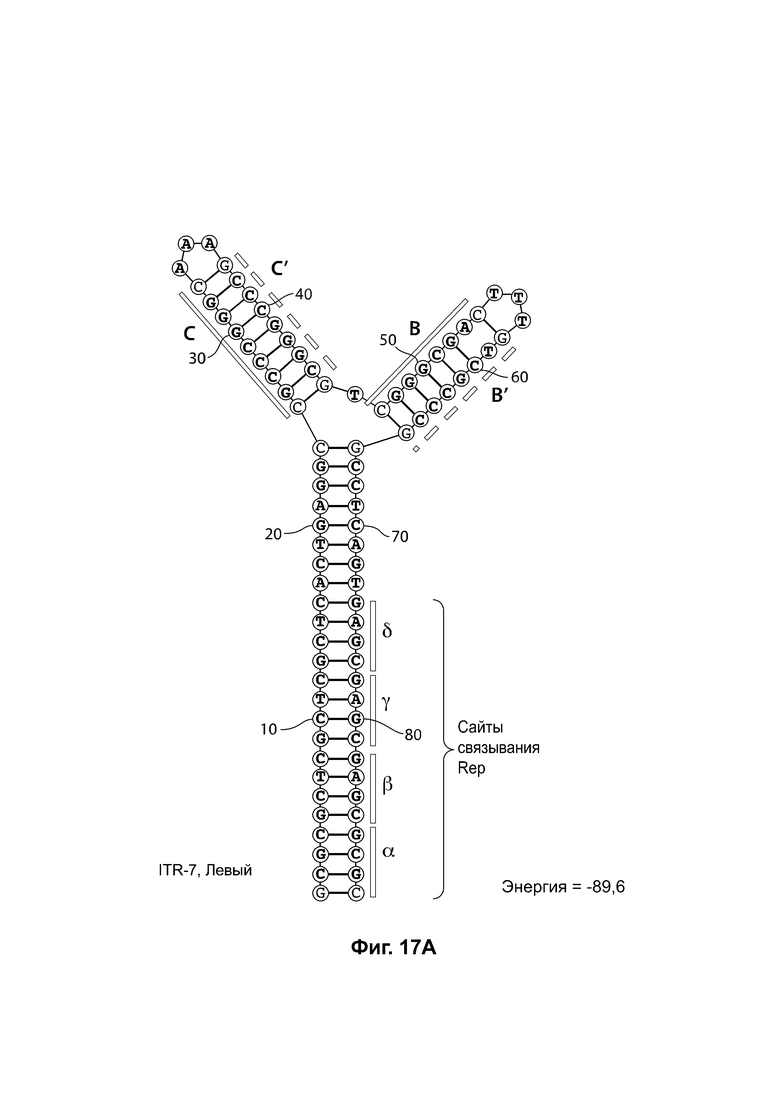
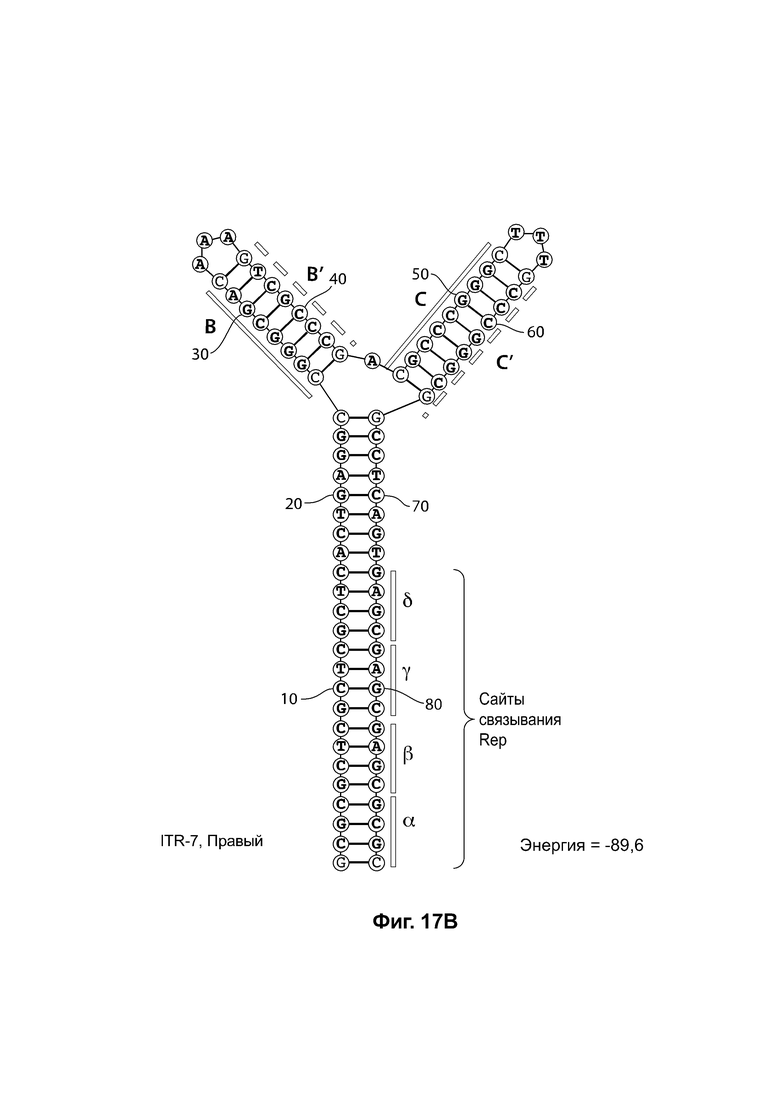


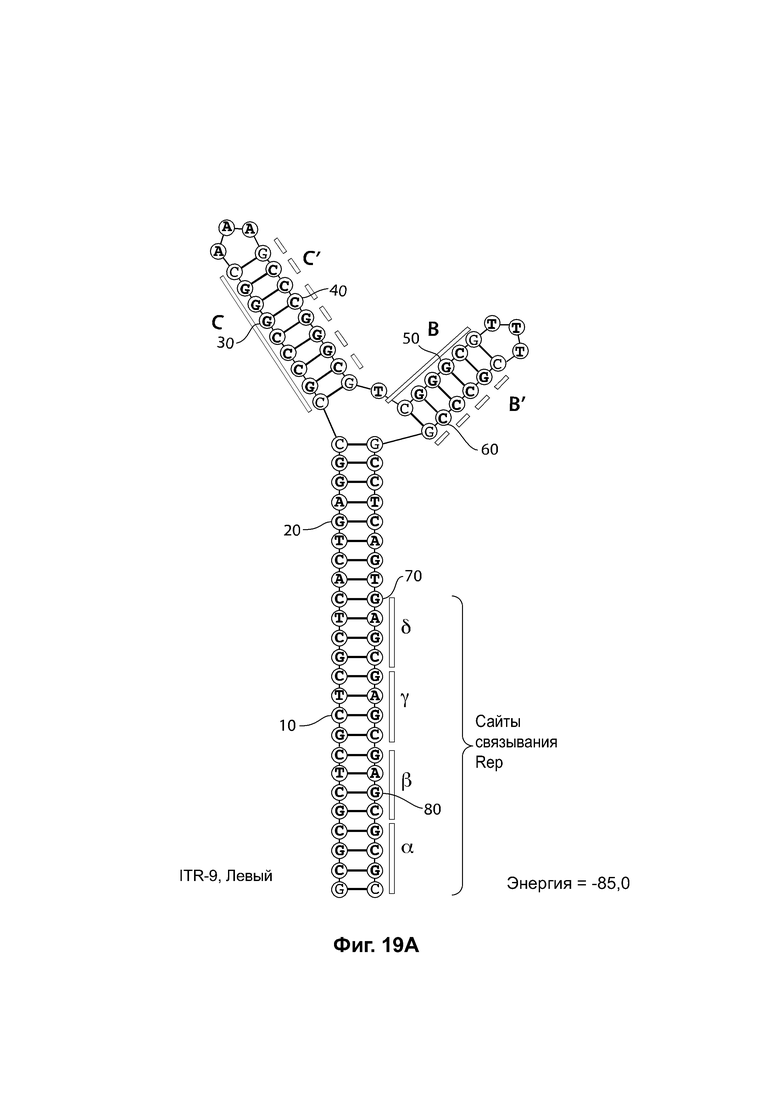
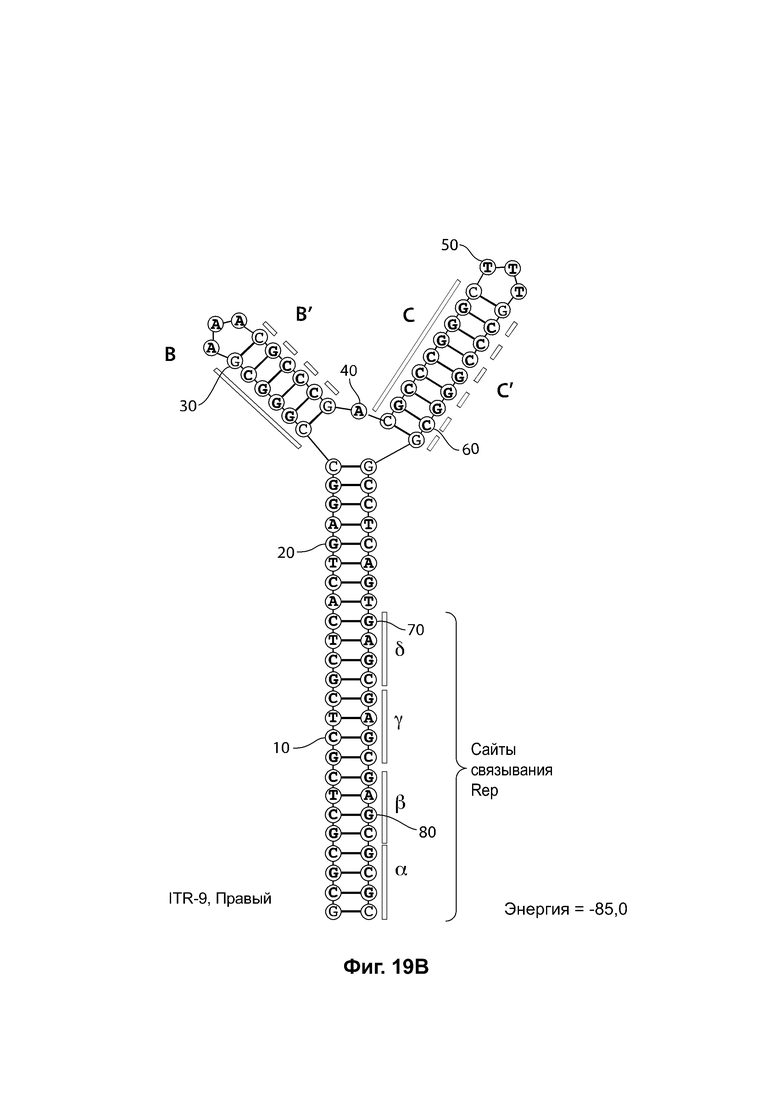
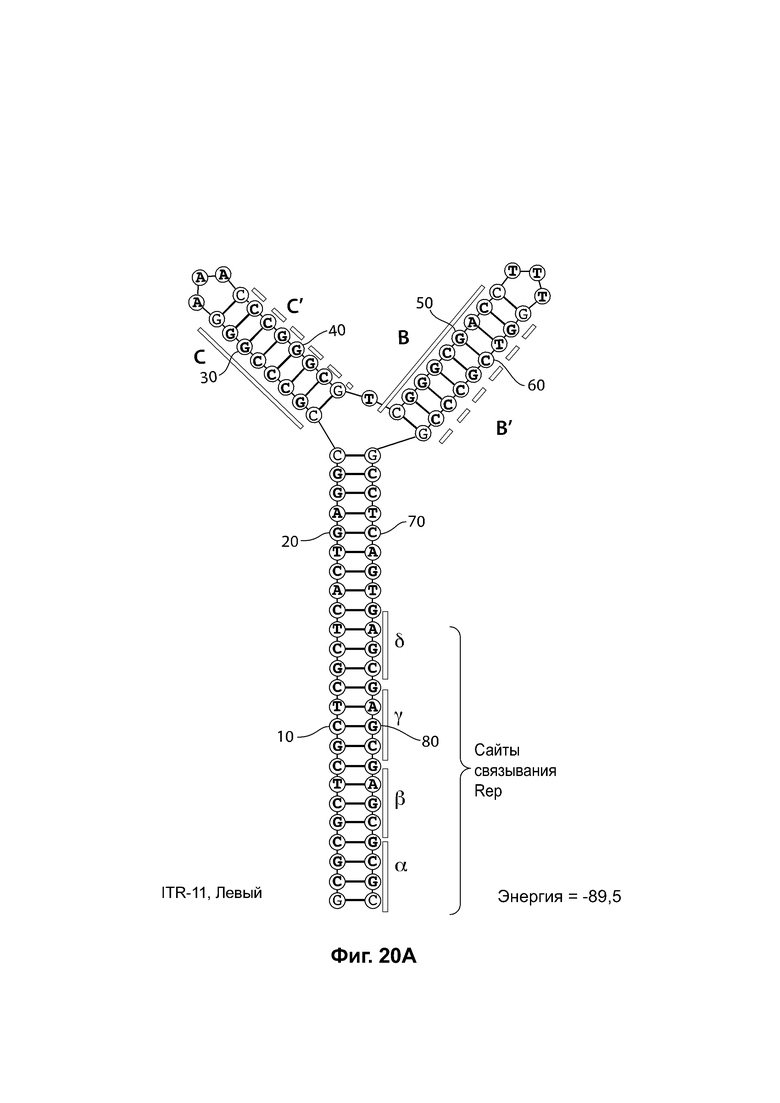
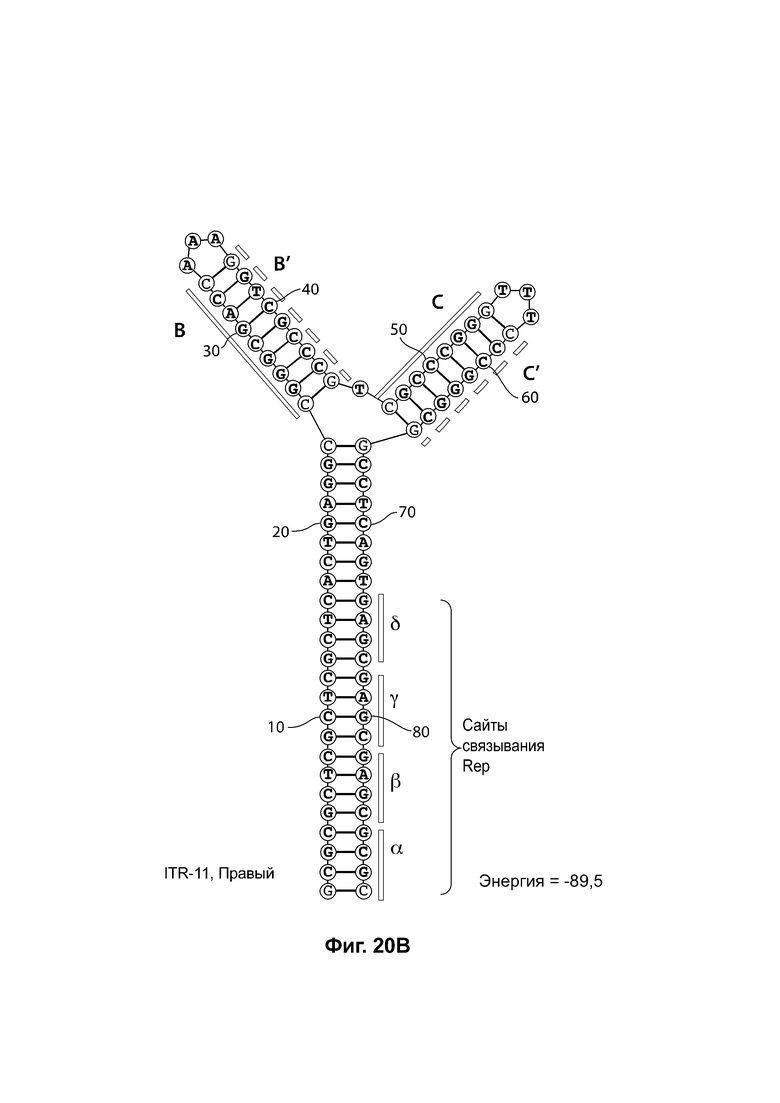
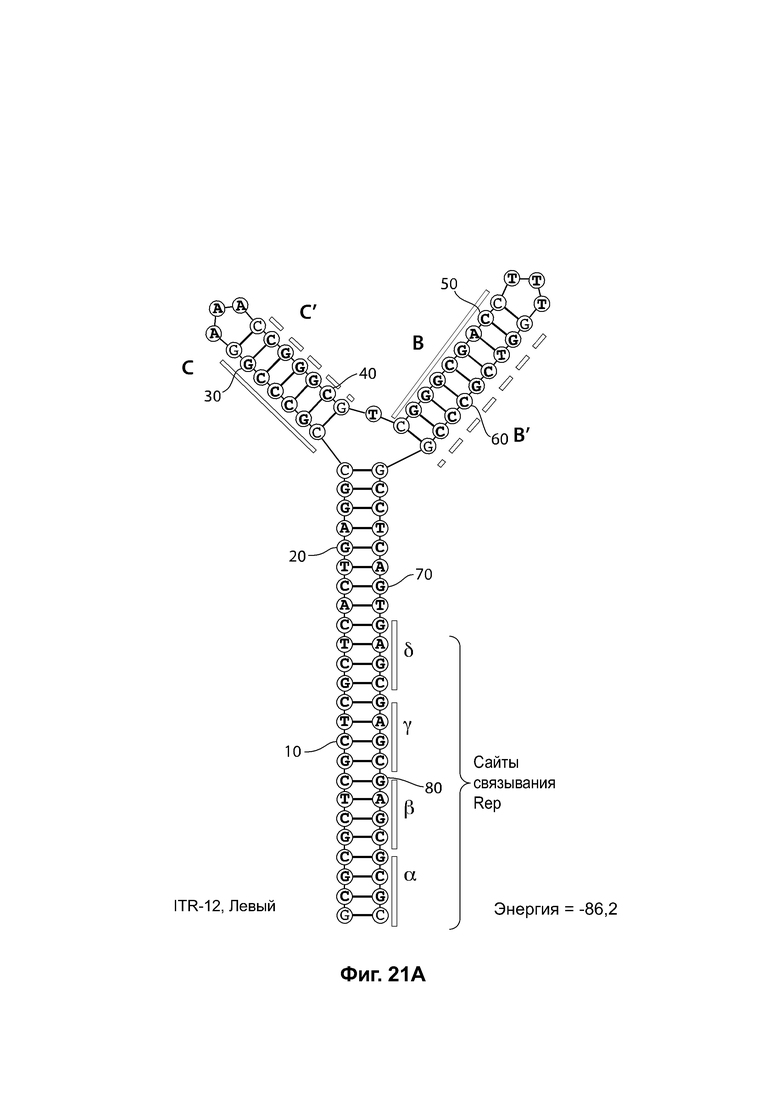
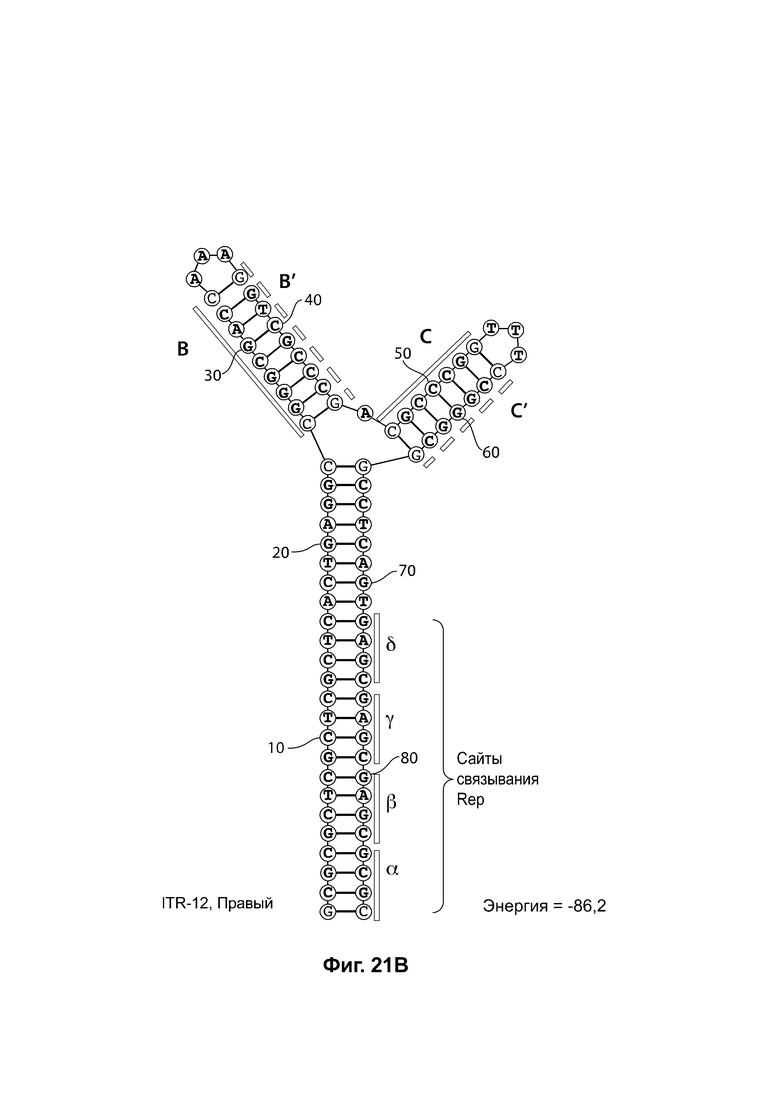
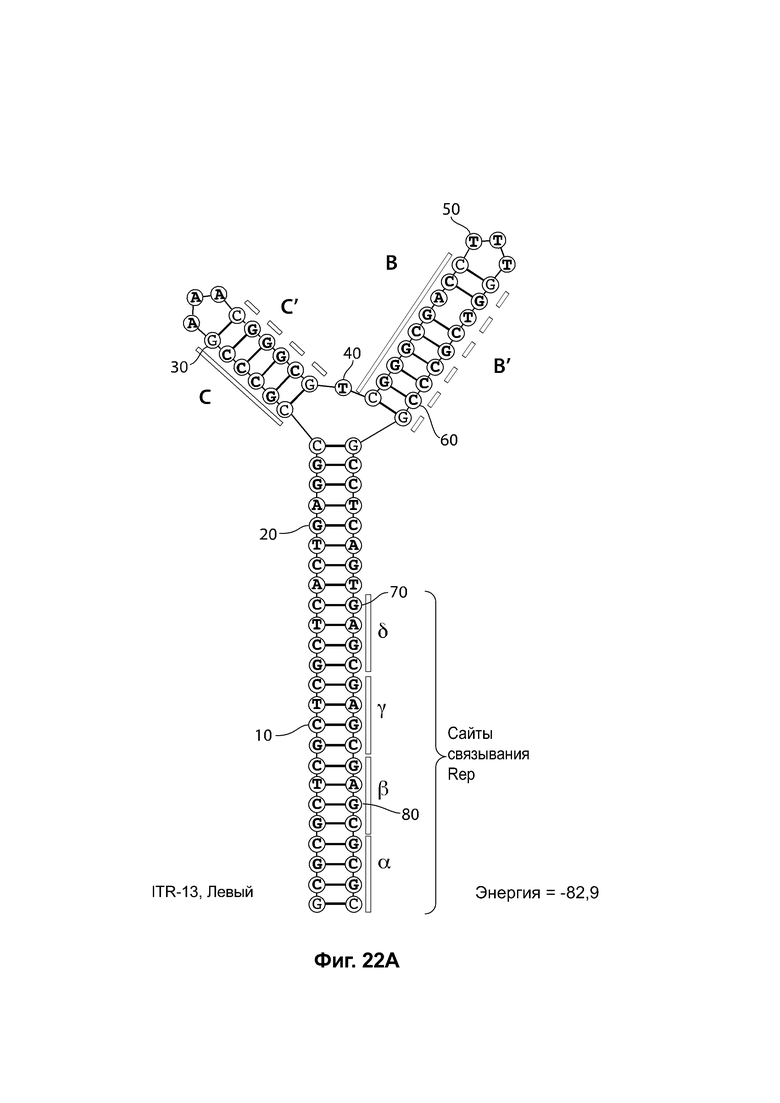
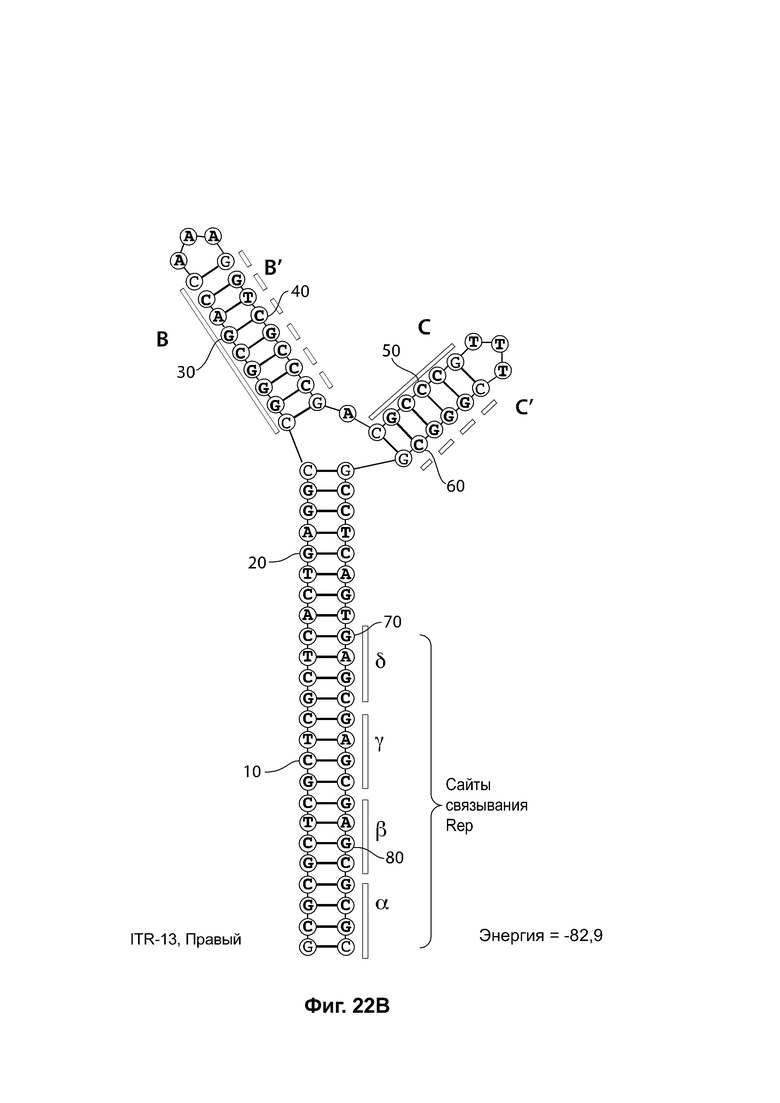
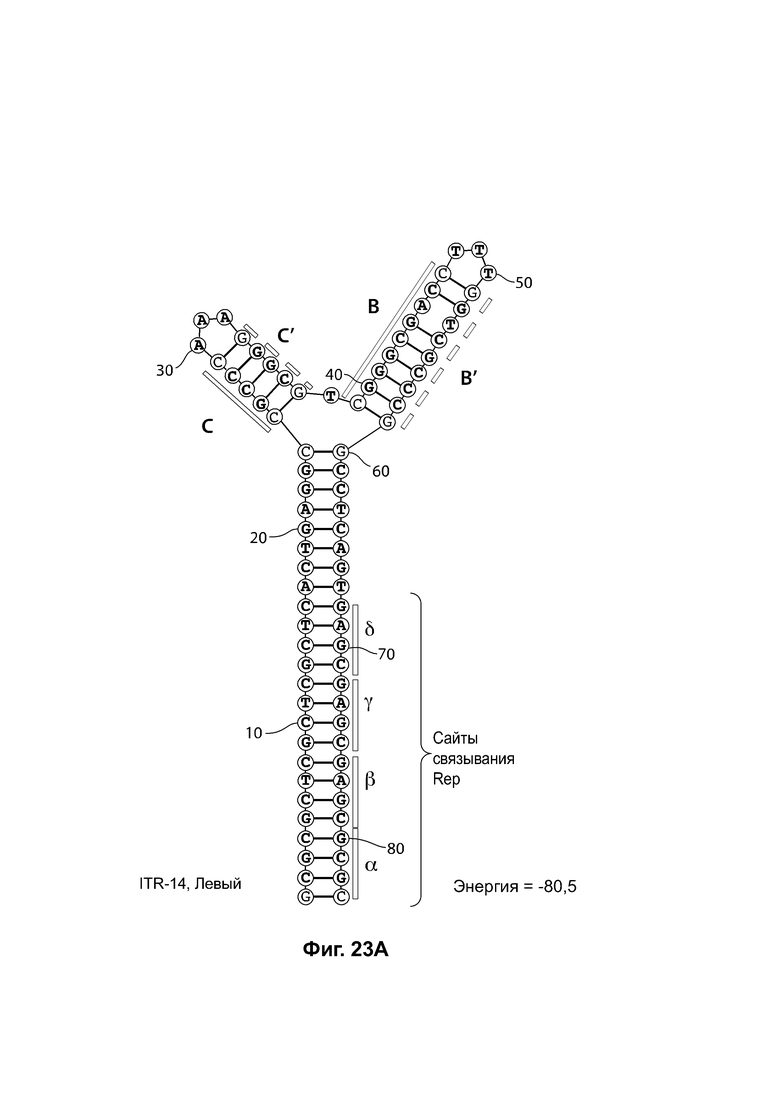
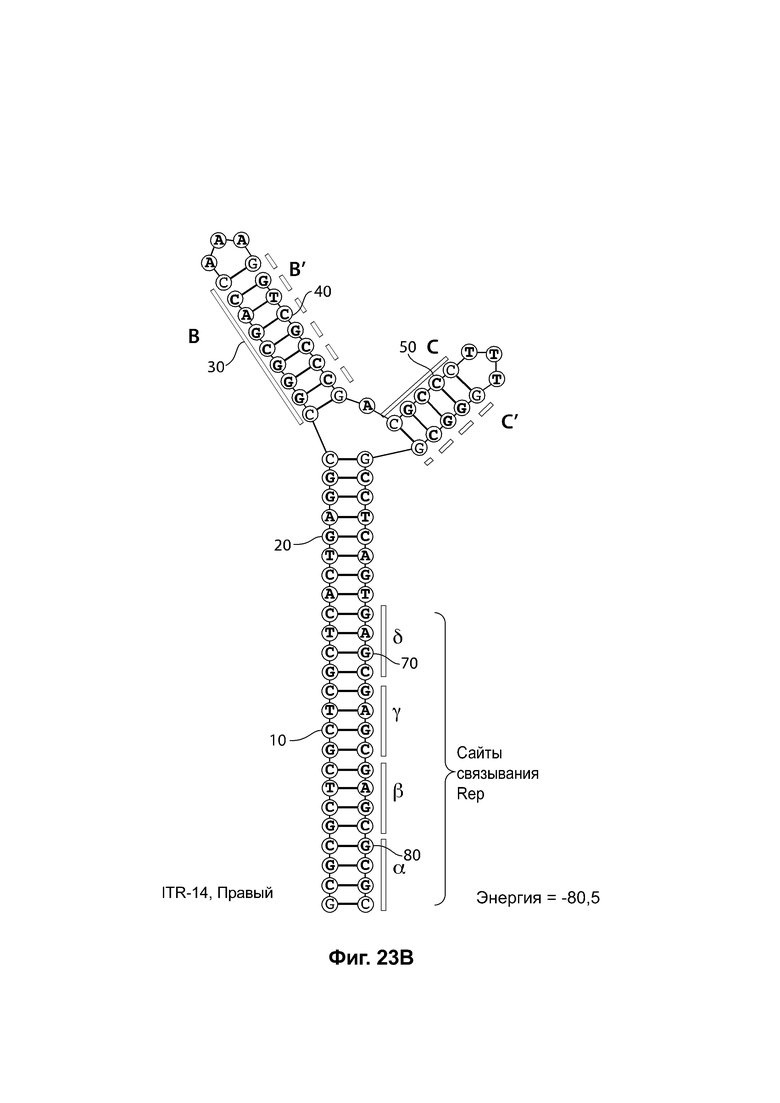
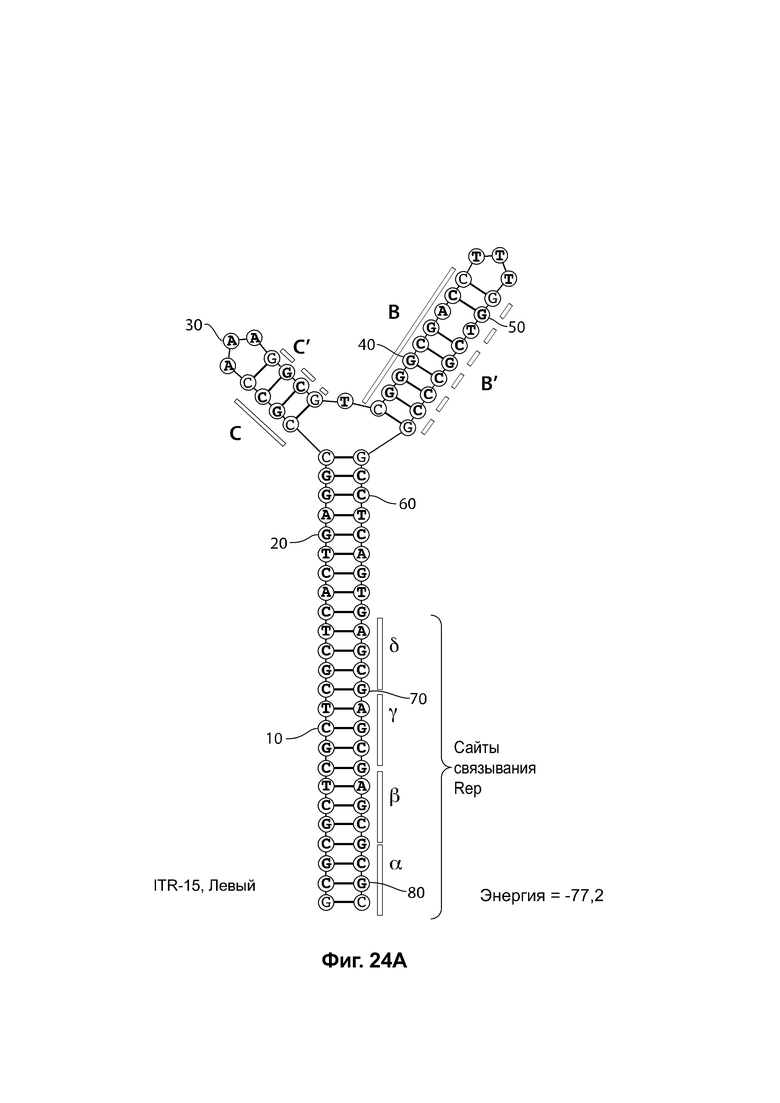
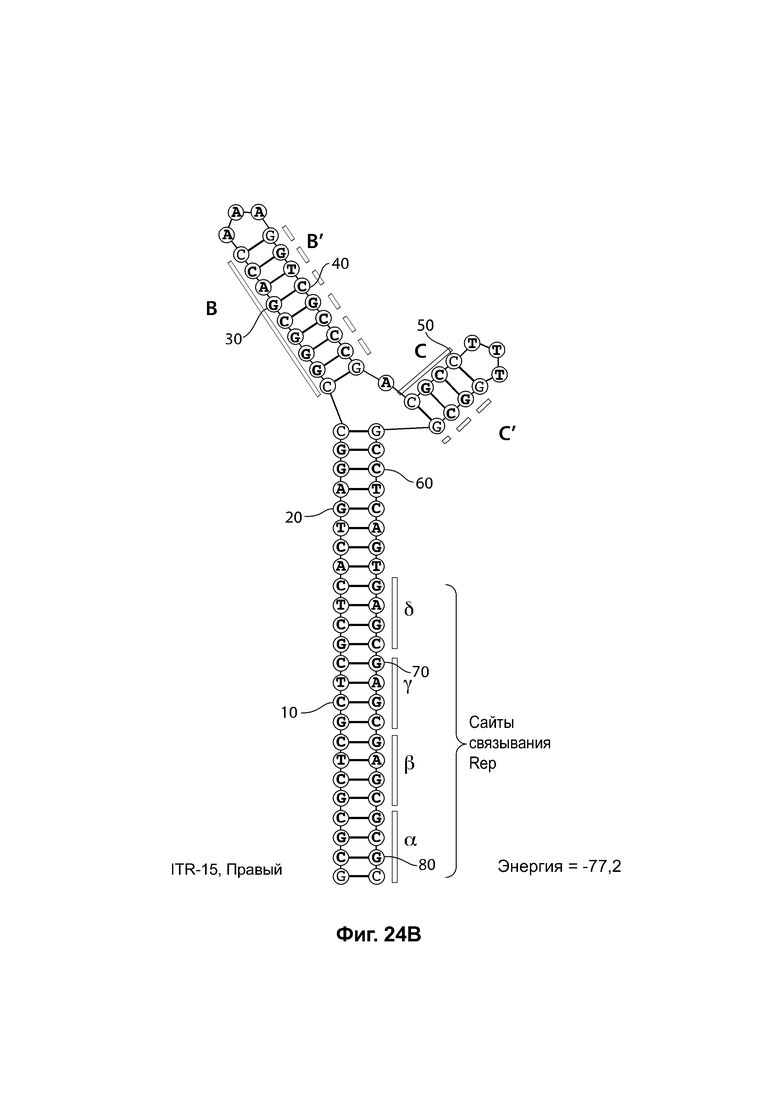
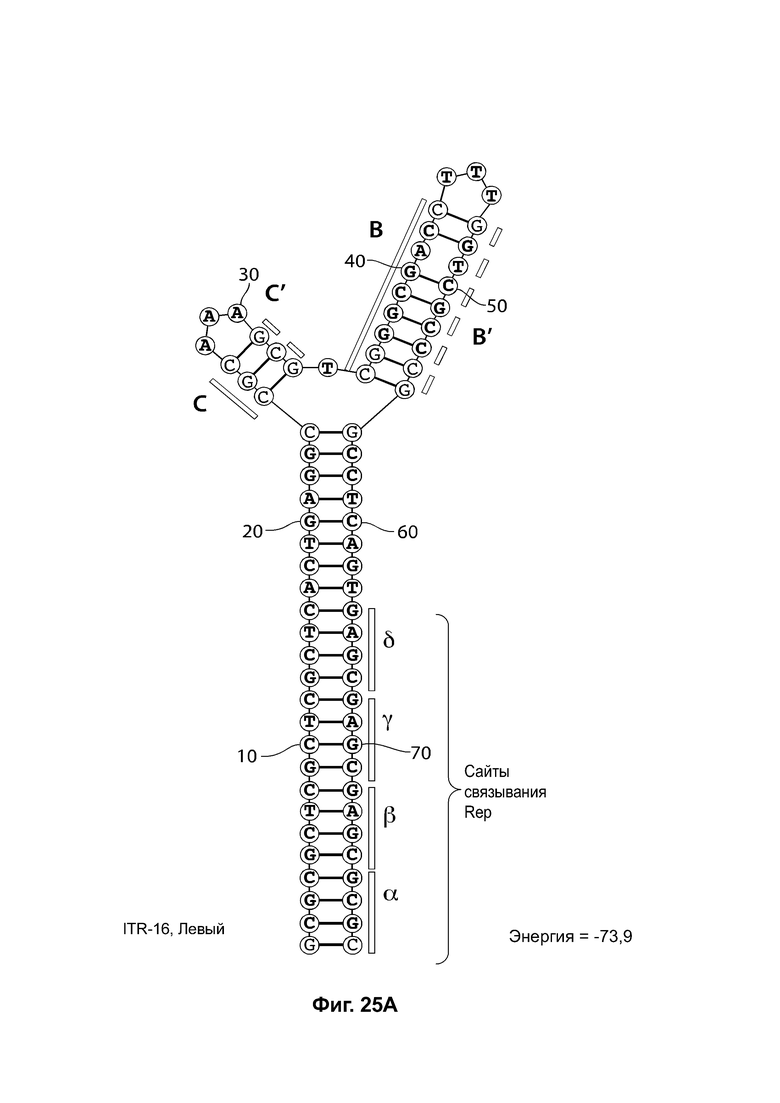
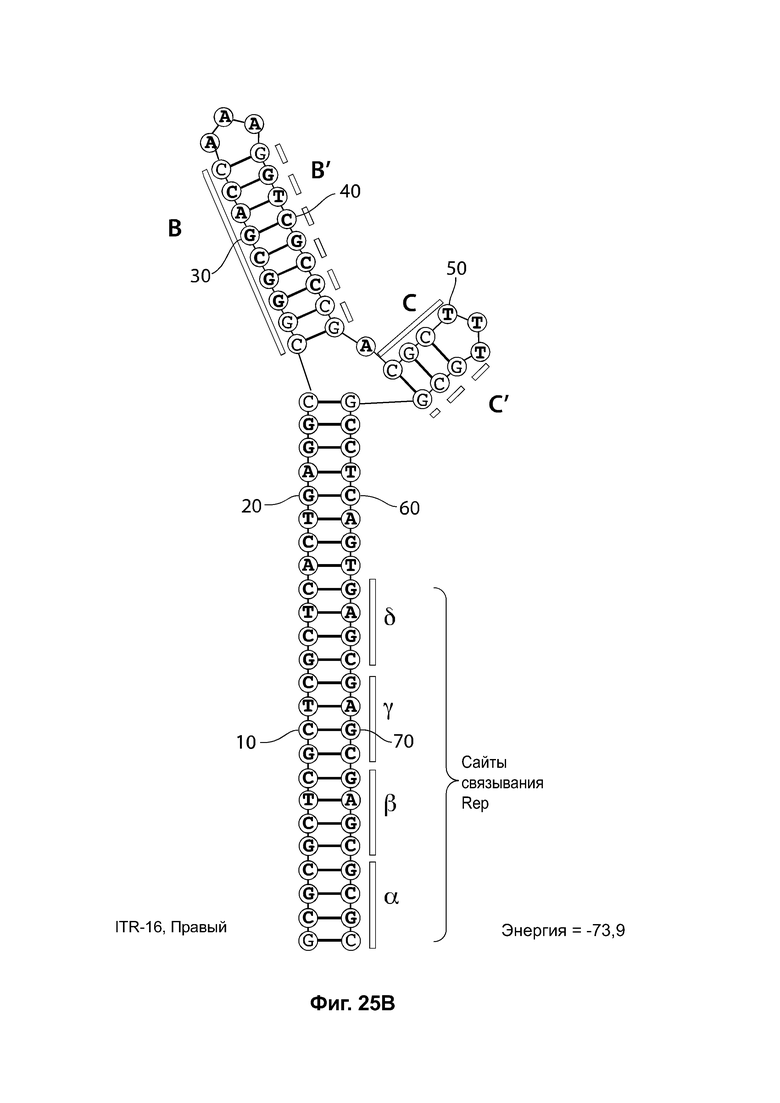
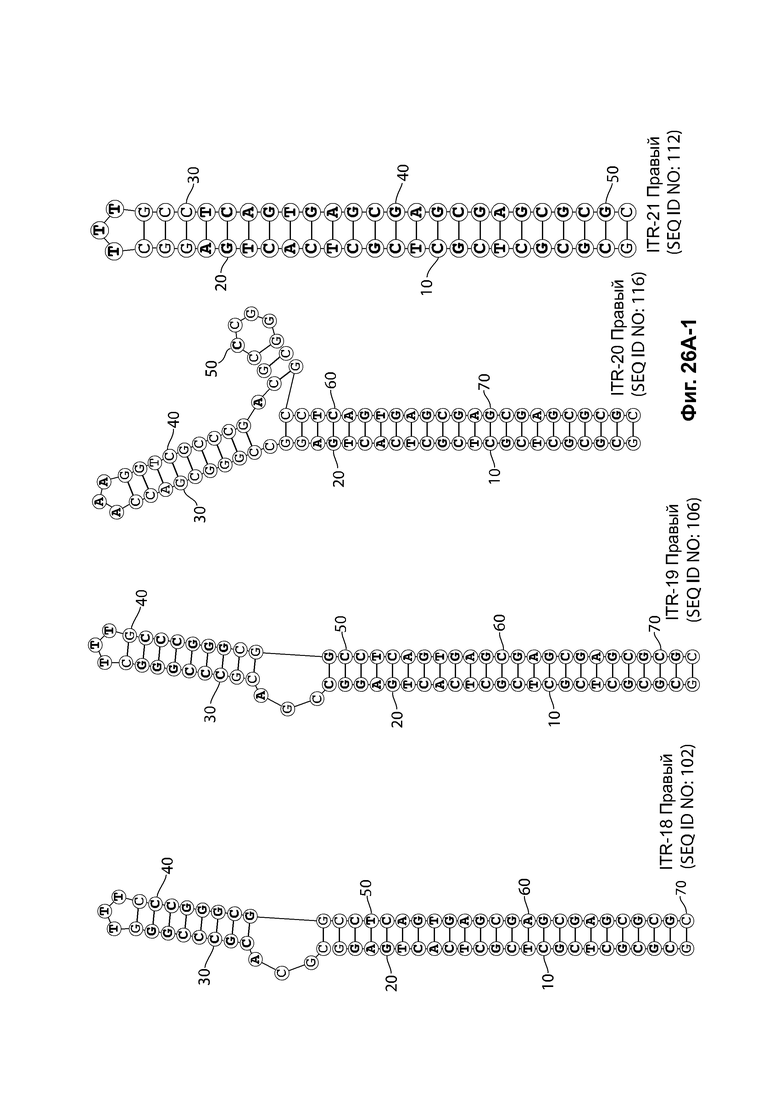
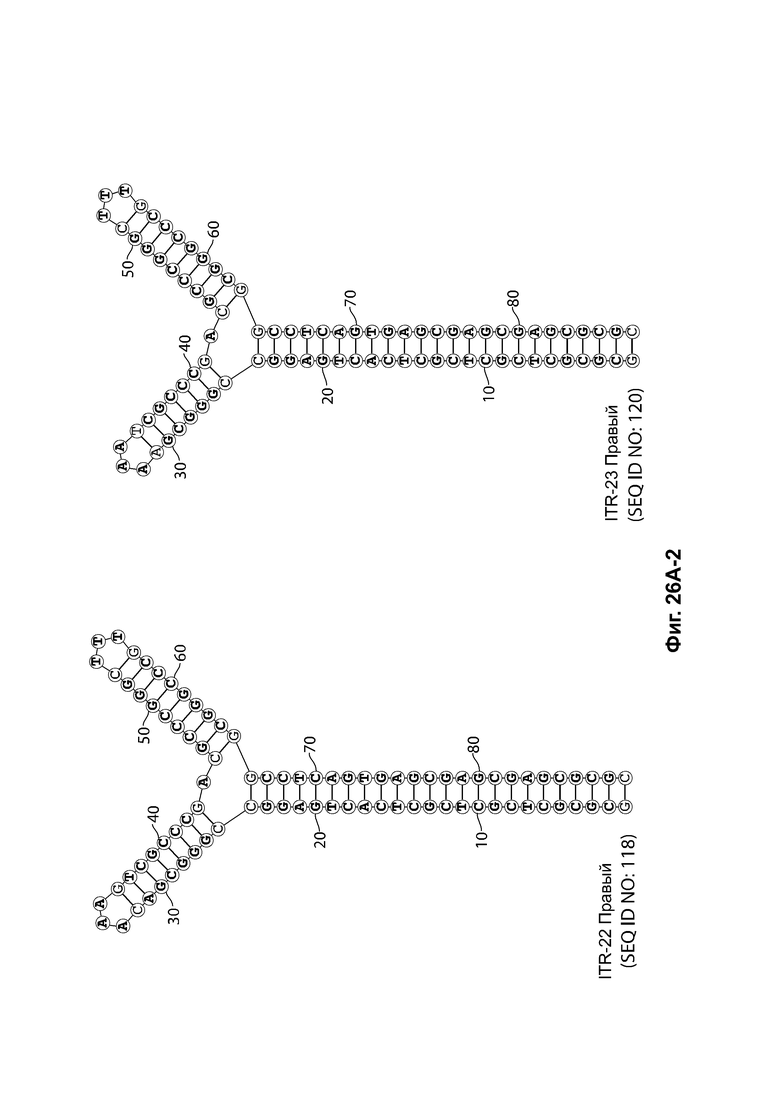
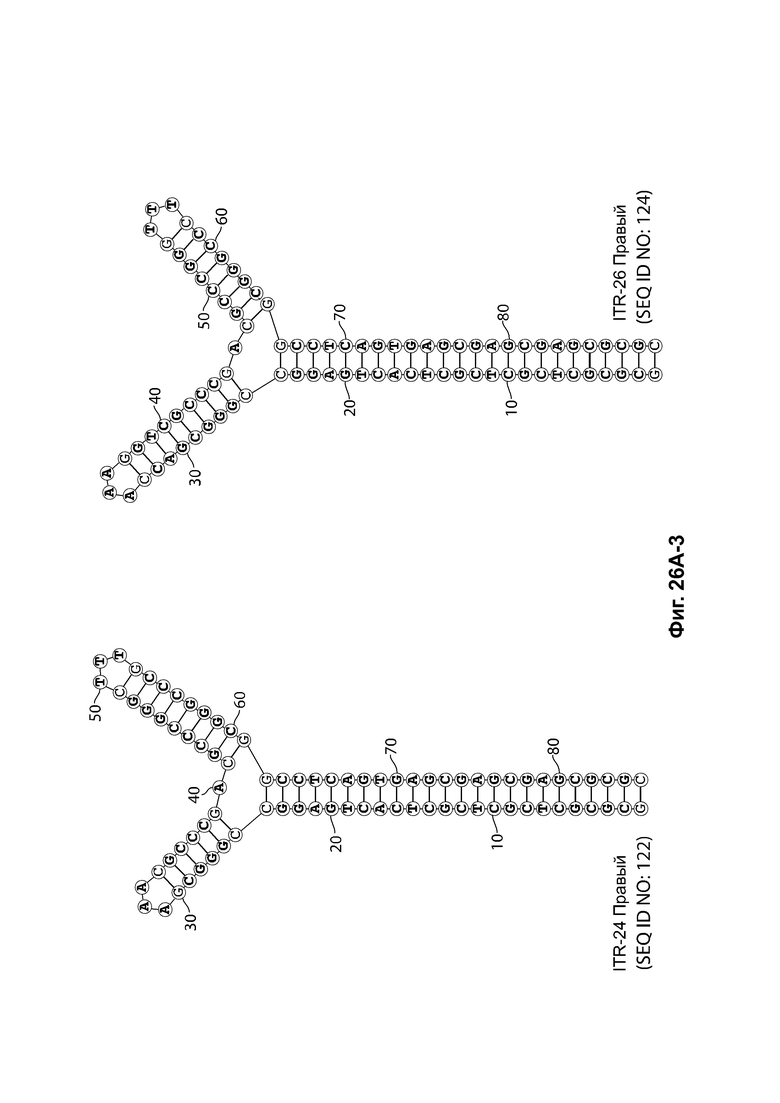
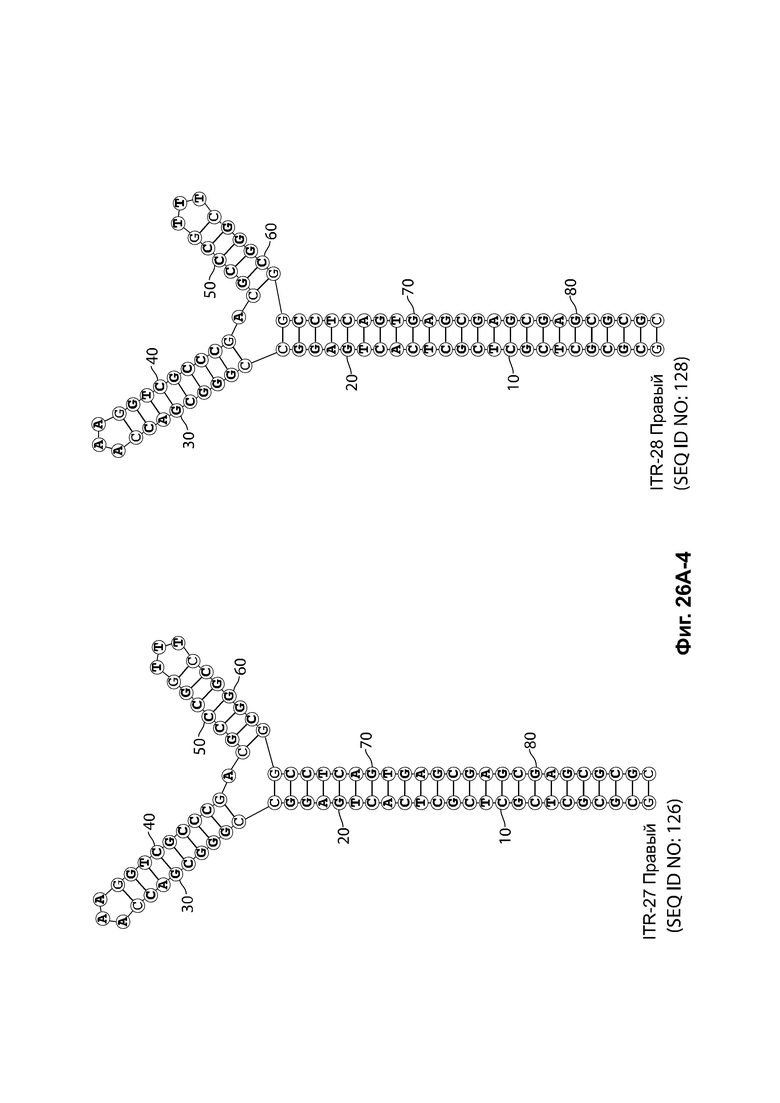
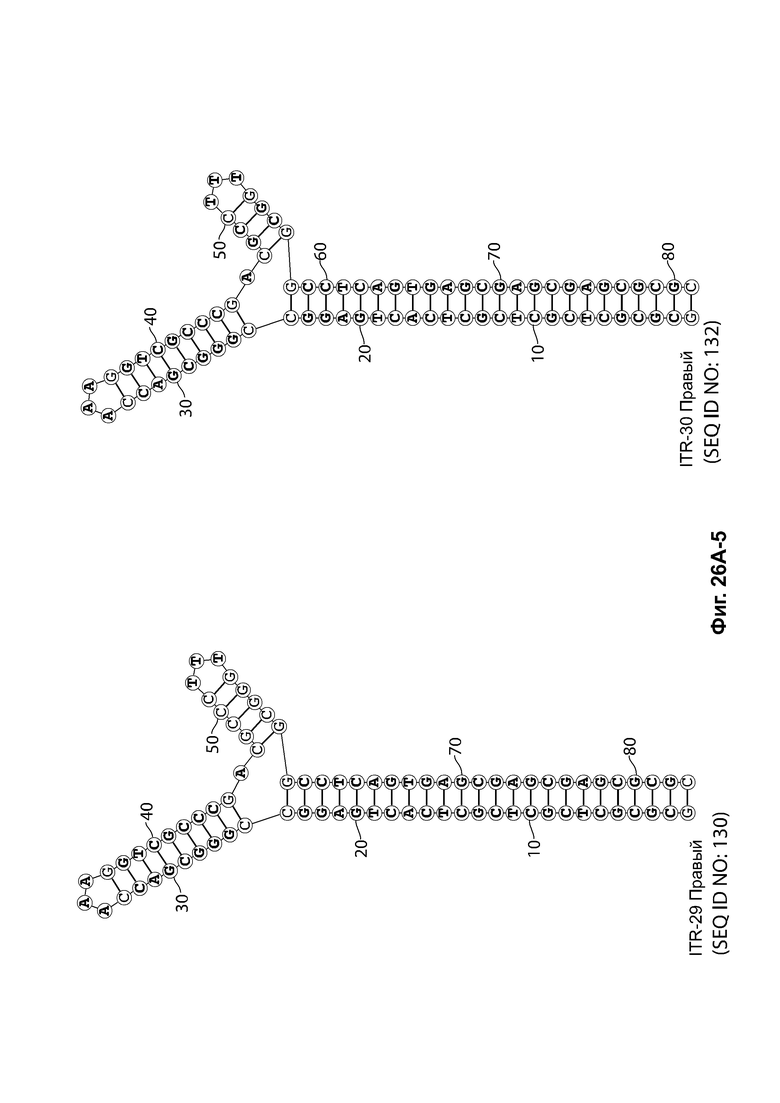
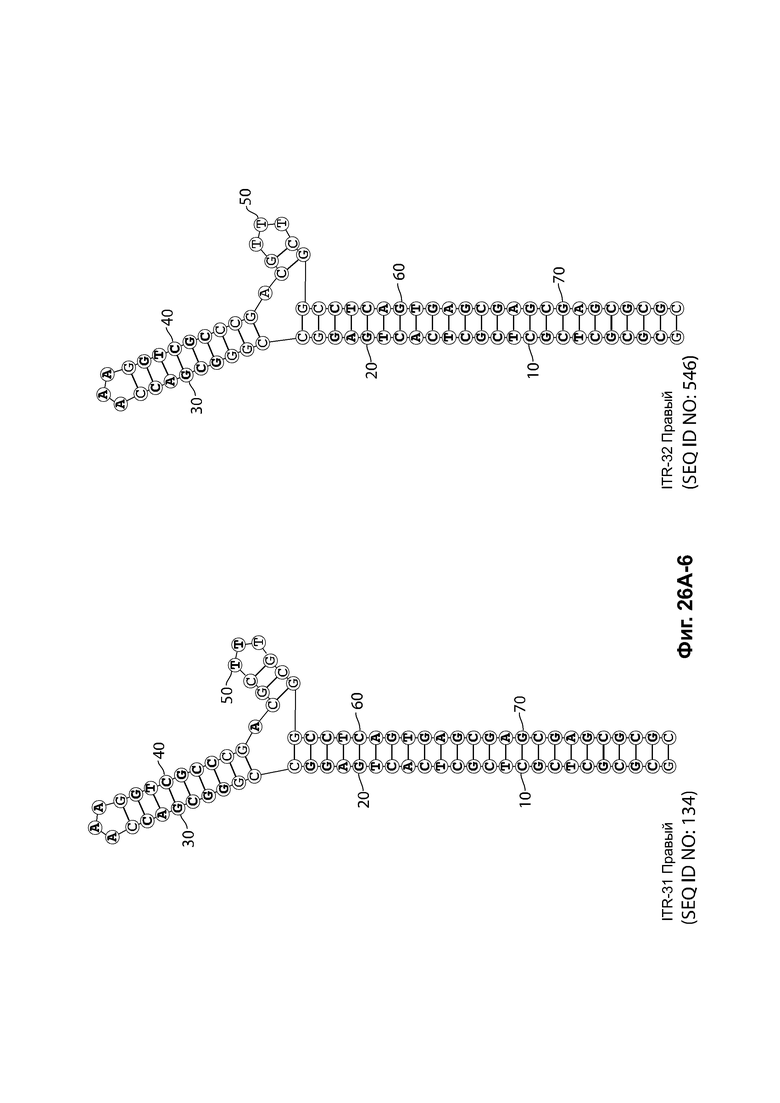
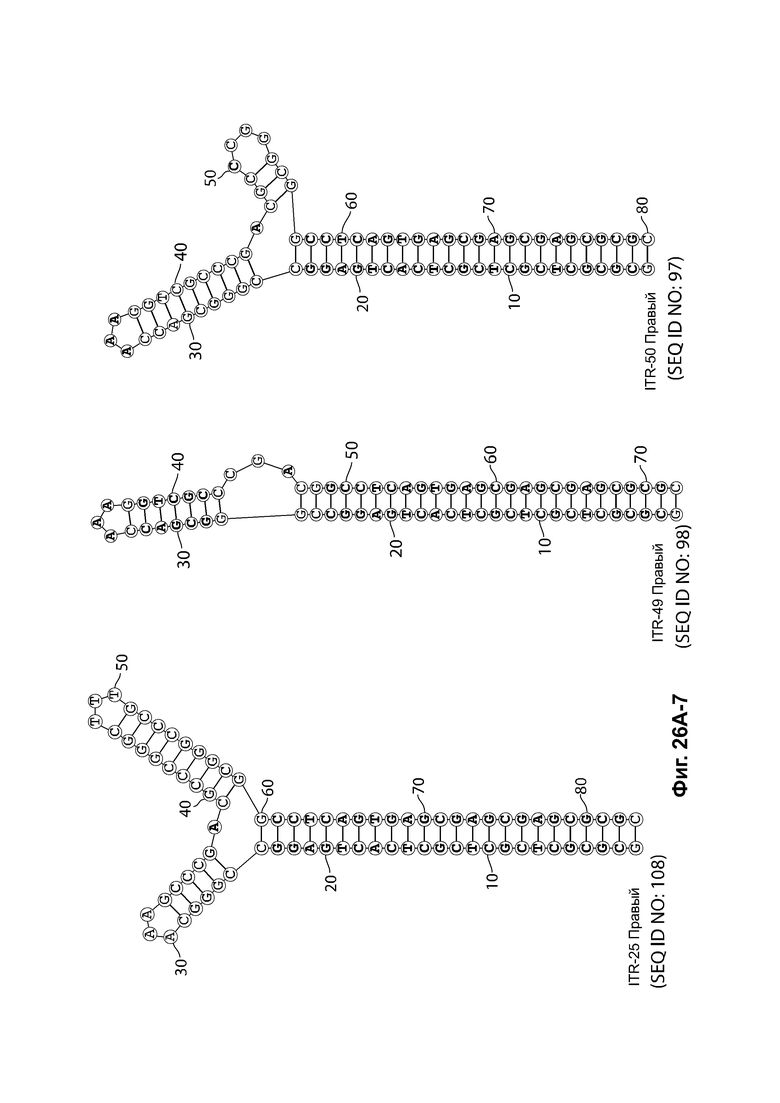
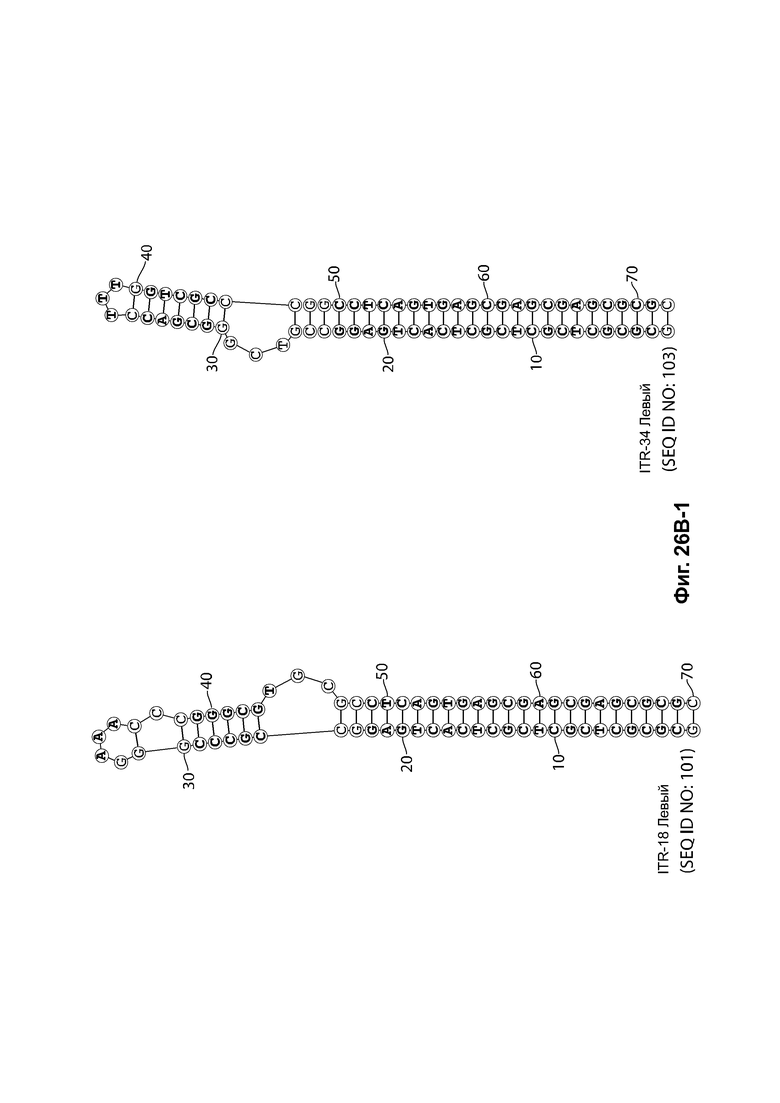
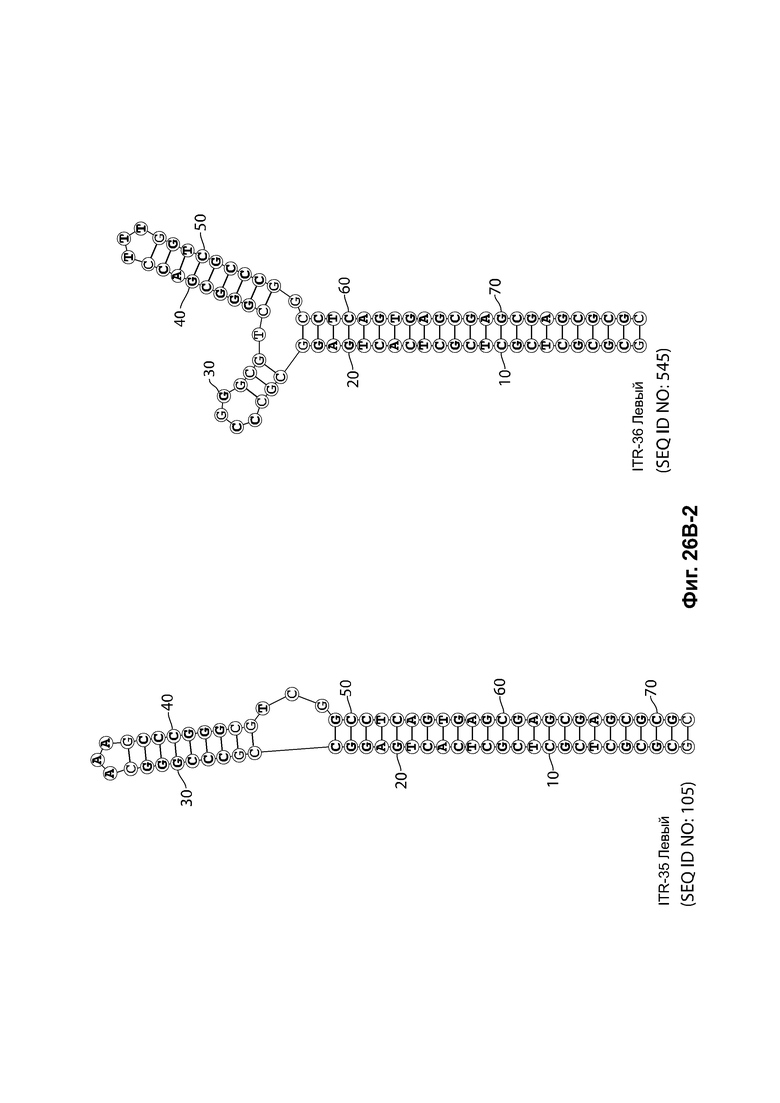
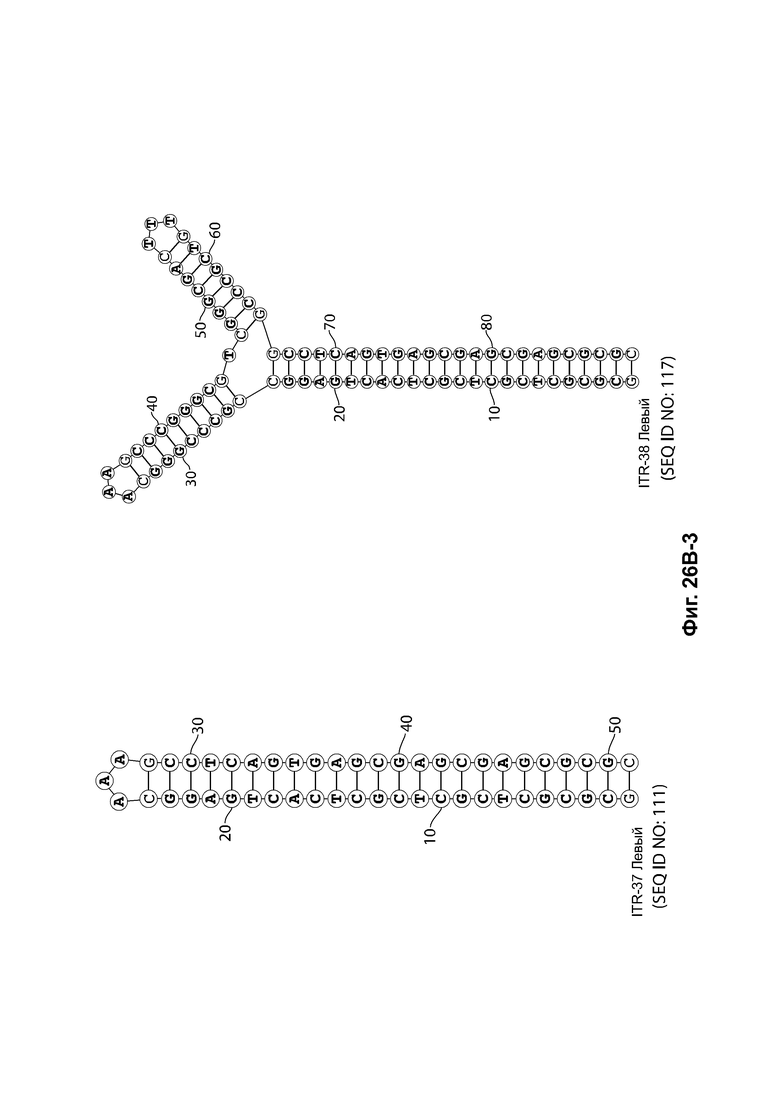
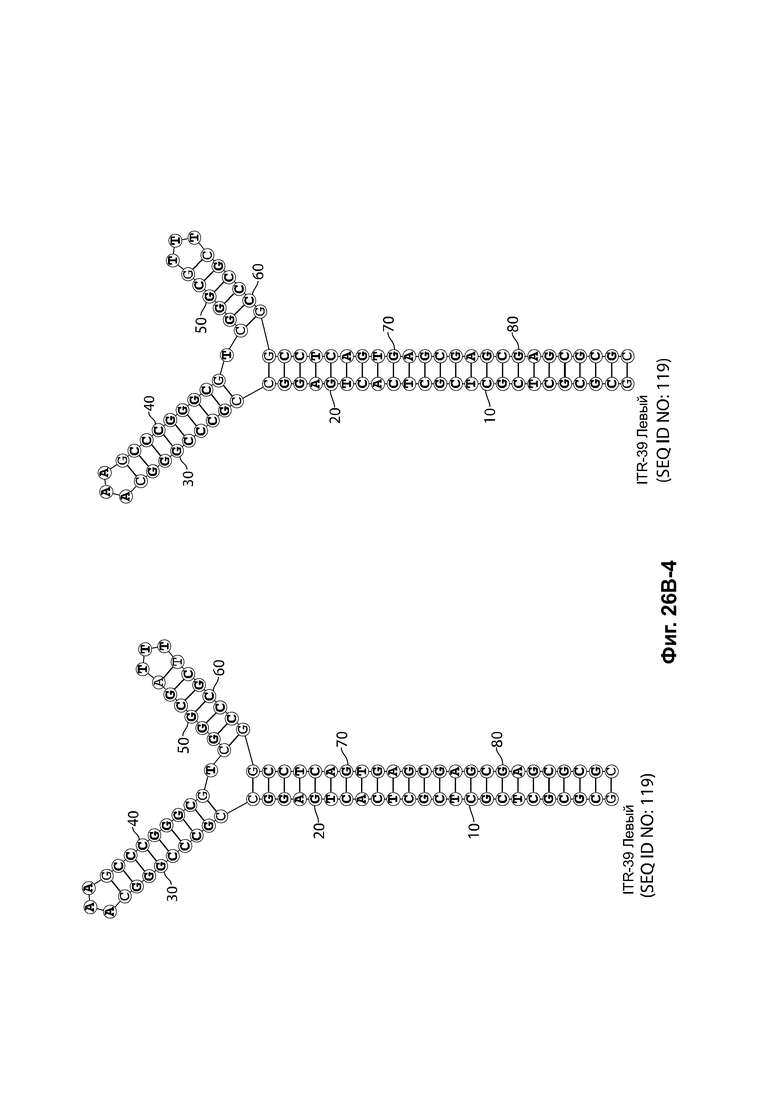
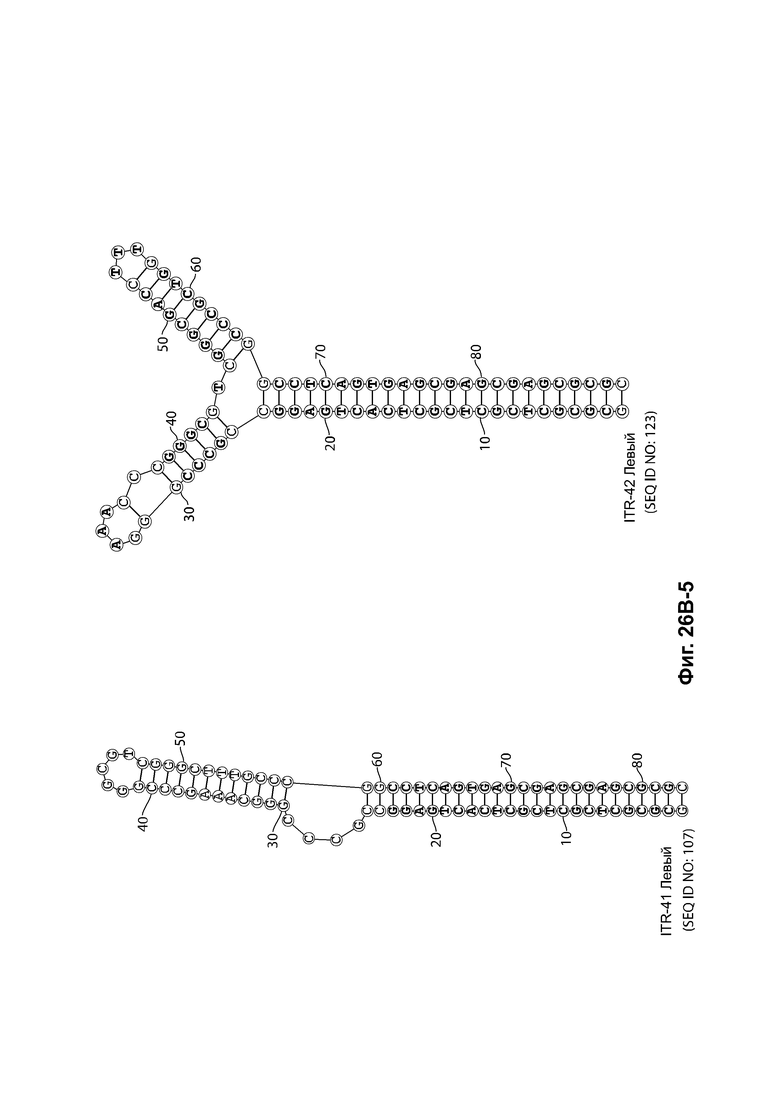
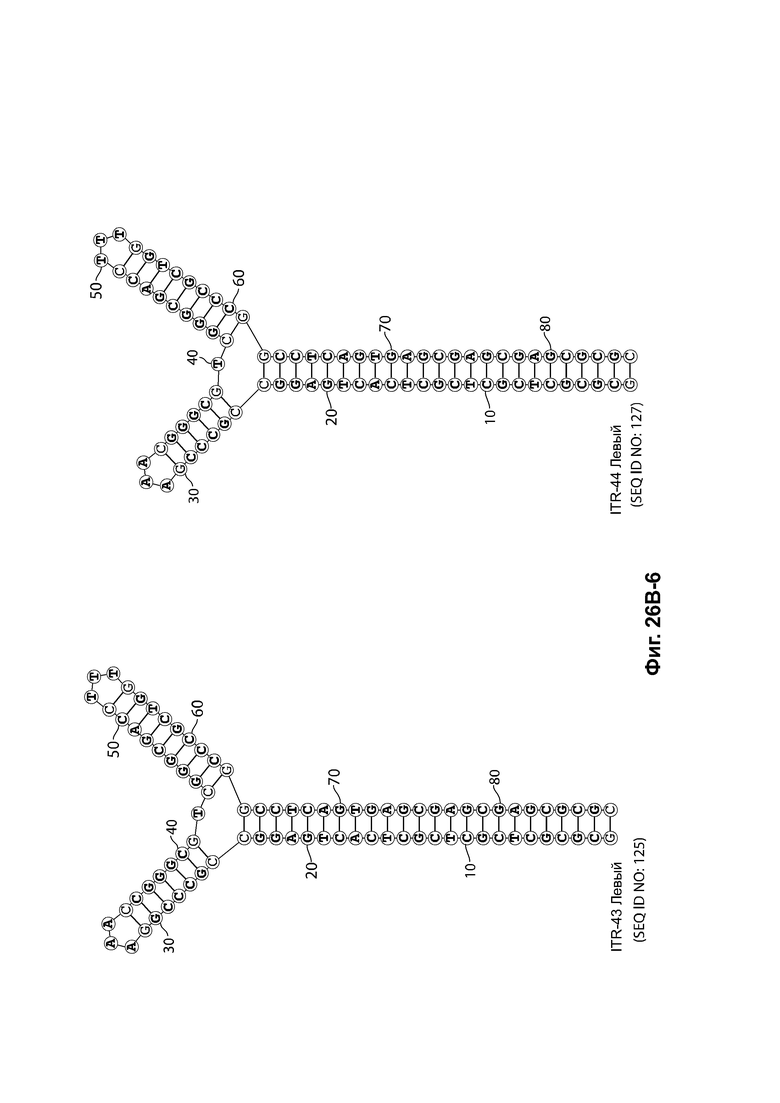
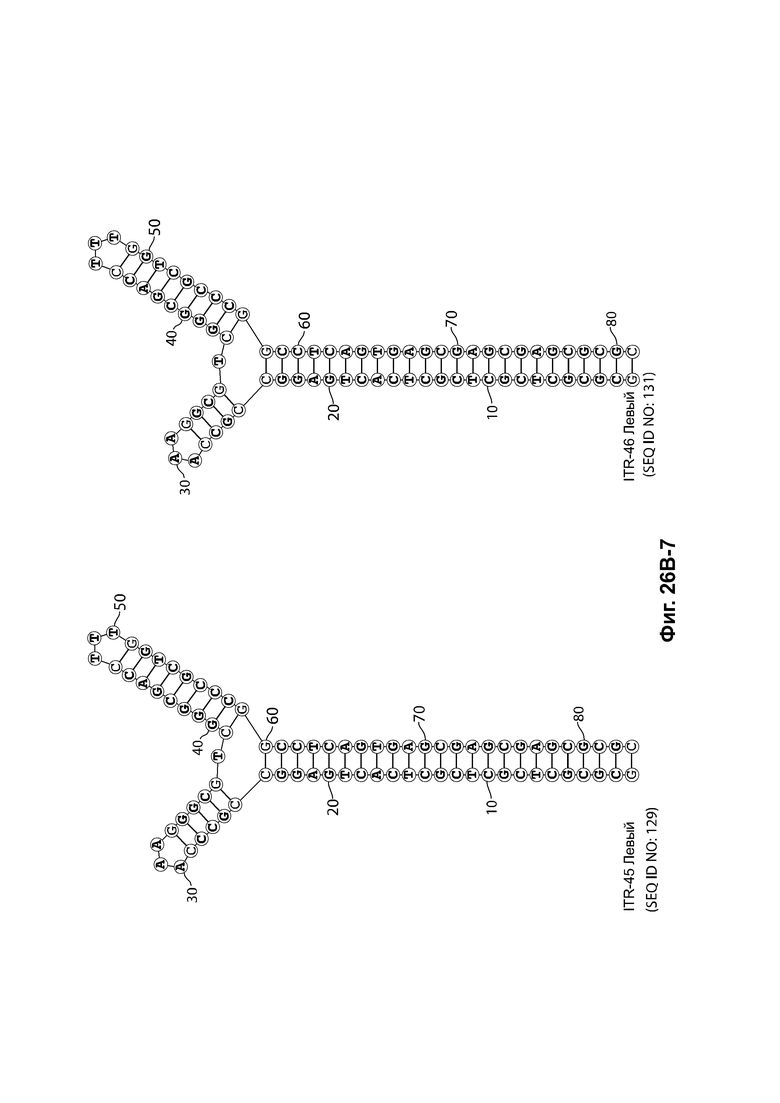
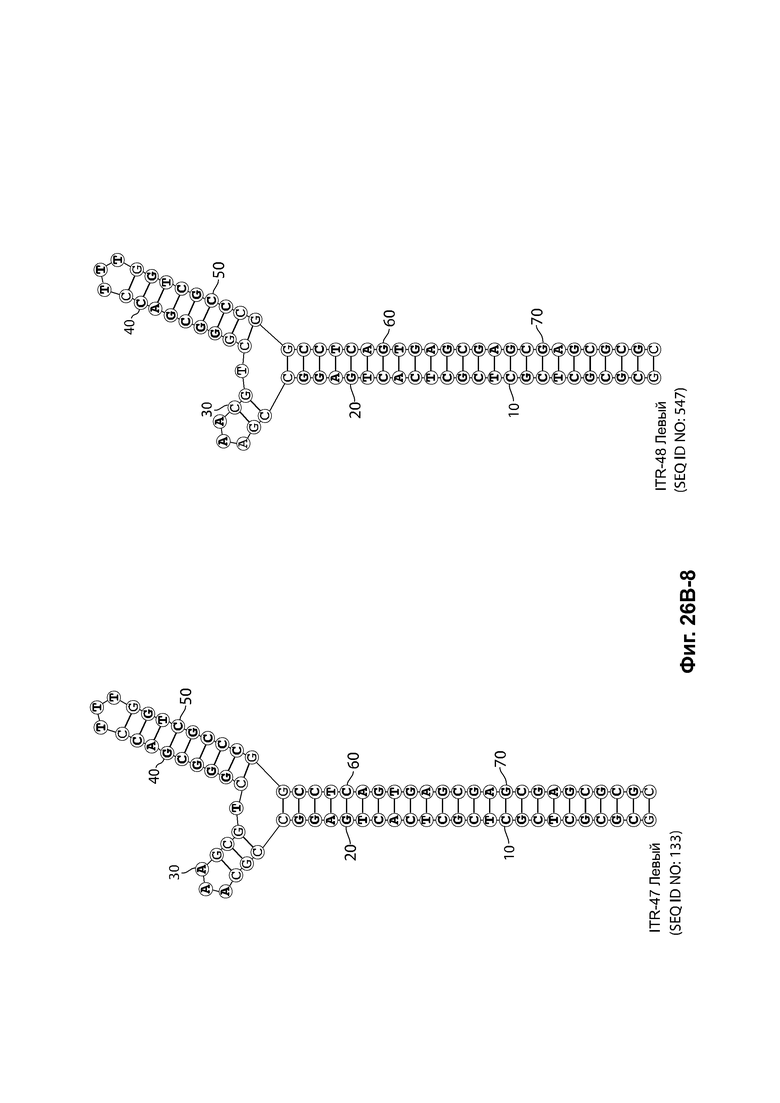
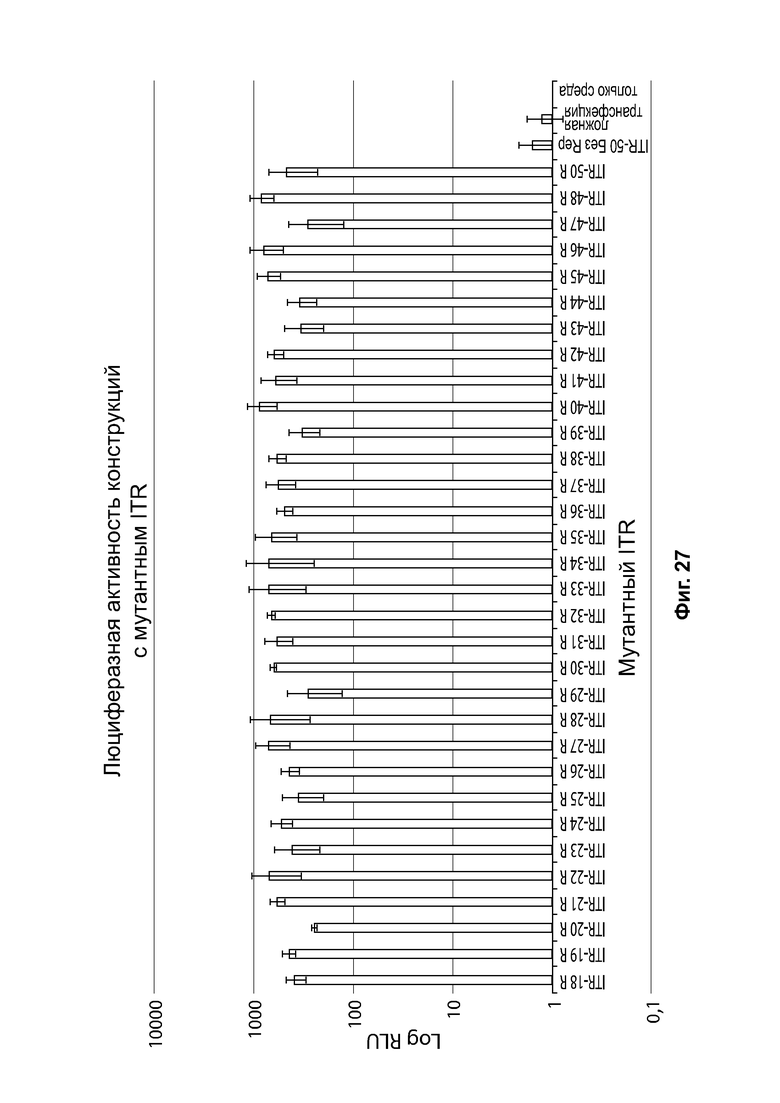


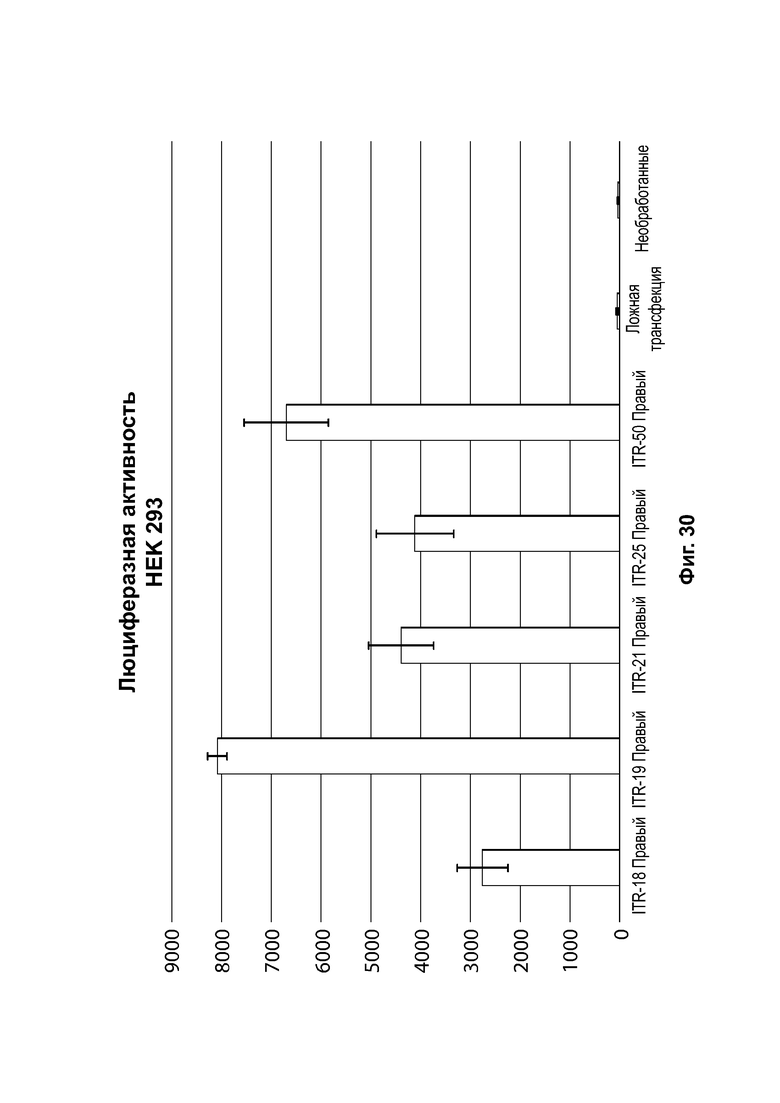
Изобретение относится к области биотехнологии. Описана группа изобретений, включающая невирусный бескапсидный ДНК-вектор с ковалентно-замкнутыми концами для доставки нуклеиновой кислоты, экспрессионную конструкцию зкДНК для продуцирования зкДНК-вектора, клетку-хозяина, продуцирующую экспрессионную конструкцию зкДНК, способ получения зкДНК-вектора, применение композиции, содержащей зкДНК-вектор для получения лекарственного средства для доставки терапевтического белка субъекту для коррекции аномального уровня и/или функции генного продукта, набор для доставки нуклеиновой кислоты и набор для получения зкДНК-вектора. Изобретение расширяет арсенал средств для доставки нуклеиновых кислот. 8 н. и 54 з.п. ф-лы, 62 ил., 17 табл., 5 пр.
1. Невирусный бескапсидный ДНК-вектор с ковалентно-замкнутыми концами (зкДНК-вектор) для доставки нуклеиновой кислоты, характеризующийся тем, что указанный зкДНК-вектор содержит по меньшей мере одну нуклеотидную последовательность, расположенную между асимметричными инвертированными концевыми повторами (асимметричными ITR), где один из ITR содержит делецию по меньшей мере в одной из областей ITR, выбранных из группы, состоящей из А, А', В, В', С, С', D и D' областей ITR, причем по меньшей мере один из асимметричных ITR содержит функциональный сайт концевого разрешения и сайт связывания Rep.
2. ЗкДНК-вектор по п. 1, где один из ITR содержит делецию по меньшей мере в одной структуре, выбранной из группы, состоящей из (i) структуры стебля, которая соответствует областям А и A', (ii) первой структуры «петля на стебле», которая соответствует областям В и В', (iii) второй структуры «петля на стебле», которая соответствует областям С и С', и (iv) структуры, содержащей по меньшей мере сайты связывания транскрипционных факторов, которая соответствует областям D и D'.
3. ЗкДНК-вектор по любому из пп. 1 или 2, где один из ITR содержит делецию всех областей ITR А, А', В, В', С, С', D и D'.
4. ЗкДНК-вектор по любому из пп. 1-3, где указанный зкДНК-вектор демонстрирует характеристические полосы линейной и непрерывной ДНК по сравнению с линейными и прерывистыми ДНК-контролями при расщеплении рестрикционным ферментом, имеющим один сайт распознавания на указанном зкДНК-векторе, анализируемый с применением как нативного, так и денатурирующего гель-электрофореза.
5. ЗкДНК-вектор по пп. 1-3 или 4, где один или более из асимметричных ITR взяты из вируса, выбранного из группы, состоящей из парвовируса, депендовируса и аденоассоциированного вируса (AAV).
6. ЗкДНК-вектор по п. 5, где указанные асимметричные ITR взяты из разных вирусных серотипов.
7. ЗкДНК-вектор по п. 6, где указанные асимметричные ITR взяты из серотипа AAV, выбранного из группы, состоящей из AAV1, AAV2, AAV3, AAV4, AAV5, AAV6, AAV7, AAV8, AAV9, AAV10, AAV11 и AAV12.
8. ЗкДНК-вектор по любому из пп. 1-7, где один или более из асимметричных ITR являются синтетическими.
9. ЗкДНК-вектор по любому из пп. 1-8, где один или оба асимметричных ITR содержат одну структуру «петля на стебле» в области, которая в ITR дикого типа содержала бы первую структуру «петля на стебле», образованную областями В и В', и вторую структуру «петля на стебле», образованную областями С и С'.
10. ЗкДНК-вектор по п. 9, где один или оба асимметричных ITR содержат один «стебель» и две «петли» в области, которая в ITR дикого типа содержала бы первую структуру «петля на стебле», образованную областями В и В', и вторую структуру «петля на стебле», образованную областями С и С'.
11. ЗкДНК-вектор по п. 9 или 10, где один или оба асимметричных ITR содержат один «стебель» и одну «петлю» в области, которая в ITR дикого типа содержала бы первую структуру «петля на стебле», образованную областями В и В', и вторую структуру «петля на стебле», образованную областями С и С'.
12. ЗкДНК-вектор по п. 1, где по меньшей мере один асимметричный ITR представляет собой модифицированный ITR AAV2, содержащий нуклеотидную последовательность, выбранную из группы, состоящей из SEQ ID NO: 101-499 и 545-547, и ITR, имеющий последовательность, по меньшей мере на 95% идентичную SEQ ID NO: 101-499 и 545-547.
13. ЗкДНК-вектор по п. 1, где по меньшей мере один асимметричный ITR представляет собой модифицированный ITR AAV2, содержащий нуклеотидную последовательность, выбранную из группы, состоящей из SEQ ID NO: 2, 52, 63 или 64, или нуклеотидную последовательность, по меньшей мере на 95% идентичную SEQ ID NO: 2, 52, 63 или 64.
14. ЗкДНК-вектор по п. 1, где 5'-ITR представляет собой ITR AAV дикого типа, а 3'-ITR содержит последовательность, выбранную из группы, состоящей из SEQ ID NO: 2, 64, 102, 104, 106, 108, 110, 112, 114, 116, 118, 120, 122, 124, 126, 128, 130, 132, 134, 469-483 и 546 и последовательностей, по меньшей мере на 95% идентичных любым из указанных выше последовательностей.
15. ЗкДНК-вектор по п. 1, где 3'-ITR представляет собой ITR AAV дикого типа, a 5'-ITR содержит последовательность, выбранную из SEQ ID NO: 52, 63, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 484-499, 545 и 547 и последовательностей, по меньшей мере на 95% идентичных любым из указанных выше последовательностей.
16. ЗкДНК-вектор по п. 1, где 5'-ITR содержит последовательность, выбранную из группы, состоящей из SEQ ID NO: 52, 63, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 484-499, 545 и 547 и последовательностей, по меньшей мере на 95% идентичных любым из указанных выше последовательностей; а 3'-ITR содержит последовательность, выбранную из группы, состоящей из SEQ ID NO: 2, 64, 102, 104, 106, 108, 110, 112, 114, 116, 118, 120, 122, 124, 126, 128, 130, 132, 134, 469-483 и 546 и последовательностей, по меньшей мере на 95% идентичных любым из указанных выше последовательностей.
17. ЗкДНК-вектор по п. 1, содержащий по меньшей мере два асимметричных ITR, выбранных из группы, состоящей из:
a. SEQ ID NO: 1 и SEQ ID NO: 52; и
b. SEQ ID NO: 2 и SEQ ID NO: 51.
18. ЗкДНК-вектор по п. 1, содержащий пару асимметричных ITR, выбранных из группы, состоящей из:
a. SEQ ID NO: 1 и SEQ ID NO: 52; и
b. SEQ ID NO: 2 и SEQ ID NO: 51.
19. ЗкДНК-вектор по любому из пп. 1-18, где один или оба асимметричных ITR содержат последовательность, отличную от SEQ ID NO: 2, 52, 63, 64, 113, 114 и 557.
20. ЗкДНК-вектор по любому из пп. 1-19, где зкДНК-вектор содержит по меньшей мере один регуляторный переключатель.
21. ЗкДНК-вектор по п. 20, где по меньшей мере один регуляторный переключатель выбран из группы, состоящей из: ABA; AIR; ART; BEARON, BEAROFF; BirA-tTA; BIT; Cry2-CIB1; СТА, CTS; cTA, rcTA; экдизон; EcR:RXR; электрогенетический переключатель; ER-p65-ZF; E.REX; EthR; GAL4-ER; GAL4-hPR; GAL4-Raps; GAL4-TR; GyrB; HEA-3; интрамер; Lacl; LAD; LightOn; NICE; PPAR*; PEACE; PIT; REDOX; QuoRex; ST-TA; TIGR; TraR; TET-OFF, TET-ON; TRT; UREX; VAC; ZF-ER, ZF-RXR/EcR; ZF-Raps; ZF-переключатели; ZF(TF); аптамер RNAi; аптамер RNAi МикроРНК; аптамер сплайсинг; аптазим; репликон CytTS; мшРНК TET-OFF, мшРНК TET-ON; аптамер с теофиллином; аптазим 3' UTR; аптазим 5' UTR; аптамер с красителем Hoechst; аптамер Н23; аптамер L7Ae; аптамер MS2; AID; ER DD; FM; Halo Tag; HDV-аптазим; PROTAC; Shield DD; Shield LID и TMP DD.
22. ЗкДНК-вектор по любому из пп. 1-21, где указанный вектор находится в наноносителе.
23. ЗкДНК-вектор по п. 22, где указанный наноноситель содержит липидную наночастицу (ЛНЧ).
24. ЗкДНК-вектор по любому из пп. 1-23, где указанный зкДНК-вектор включает аптамер.
25. ЗкДНК-вектор по любому из пп. 1-23, где по меньшей мере один из асимметричных ITR включает аптамер.
26. ЗкДНК-вектор по любому из пп. 24 или 25, где по меньшей мере одна нуклеотидная последовательность содержит последовательность, которая кодирует терапевтический белок.
27. ЗкДНК-вектор по п. 26, где терапевтический белок выбран из группы, состоящей из Фактора VIII, Фактора IX, Фактора X и фенилаланингидроксилаза.
28. Невирусный бескапсидный ДНК-вектор с ковалентно-замкнутыми концами (зкДНК-вектор) по любому из пп. 1-23, который получают способом, включающим следующие этапы:
а. инкубация популяции клеток насекомых, несущих экспрессионную конструкцию зкДНК, в присутствии по меньшей мере одного белка Rep, причем указанная экспрессионная конструкция зкДНК кодирует зкДНК-вектор, в условиях, эффективных для, и на протяжении времени, достаточного для того чтобы индуцировать продуцирование указанного зкДНК-вектора в клетках насекомых; и
b. выделение указанного зкДНК-вектора из клеток насекомых.
29. ЗкДНК-вектор по п. 28, где указанную экспрессионную конструкцию зкДНК выбирают из группы, состоящей из зкДНК-плазмиды, зкДНК-бакмиды и зкДНК-бакуловируса.
30. ЗкДНК-вектор по п. 28 или п. 29, где указанная клетка насекомого экспрессирует по меньшей мере один белок Rep.
31. ЗкДНК-вектор по п. 30, где по меньшей мере один белок Rep взят из вируса, выбранного из группы, состоящей из парвовируса, депендовируса и аденоассоциированного вируса (AAV).
32. ЗкДНК-вектор по п. 31, где по меньшей мере один белок Rep взят из серотипа AAV, выбранного из группы, состоящей из AAV1, AAV2, AAV3, AAV4, AAV5, AAV6, AAV7, AAV8, AAV9, AAV10, AAV11 и AAV12.
33. Экспрессионная конструкция зкДНК для продуцирования зкДНК-вектора по любому из пп. 1-21.
34. Экспрессионная конструкция зкДНК по п. 33, которая выбрана из группы, состоящей из зкДНК-плазмиды, зкДНК-бакмиды и зкДНК-бакуловируса.
35. Клетка-хозяин, продуцирующая экспрессионную конструкцию зкДНК по п. 33 или 34.
36. Клетка-хозяин по п. 35, которая экспрессирует по меньшей мере один белок Rep.
37. Клетка-хозяин по п. 36, отличающаяся тем, что по меньшей мере один белок Rep взят из вируса, выбранного из группы, состоящей из парвовируса, депендовируса и аденоассоциированного вируса (AAV).
38. Клетка-хозяин по п. 37, отличающаяся тем, что по меньшей мере один белок Rep взят из серотипа AAV, выбранного из группы, состоящей из AAV1, AAV2, AAV3, AAV4, AAV5, AAV6, AAV7, AAV8, AAV9, AAV10, AAV11 и AAV12.
39. Клетка-хозяин по любому из пп. 35-38, представляющая собой клетку насекомого.
40. Клетка-хозяин по п. 39, представляющая собой клетку Sf9.
41. Способ получения зкДНК-вектора, включающий:
a. инкубацию клетки-хозяина по любому из пп. 35-40 в условиях, эффективных для, и на протяжении времени, достаточного для того чтобы индуцировать продуцирование зкДНК-вектора; и
b. выделение указанного зкДНК-вектора из клеток-хозяев.
42. Применение зкДНК-вектора по любому из пп. 1-21 для получения лекарственного средства для лечения, предотвращения, облегчения, мониторинга или диагностики заболевания или нарушения, вызываемого мутацией в гене или генном продукте, у субъекта, где по меньшей мере одна нуклеотидная последовательность выбрана для лечения, предотвращения, облегчения, диагностики или мониторинга указанного заболевания или нарушения, вызываемого мутацией в гене или генном продукте, причем заболевание или нарушение, вызываемое мутацией в гене или генном продукте, выбрано из группы, состоящей из: метаболические заболевания или нарушения, болезни или нарушения цикла мочевины, лизосомные болезни или нарушения накопления, заболевания или нарушения печени, заболевания или нарушения крови, рак и опухоли, а также генетические заболевания или нарушения.
43. Применение по п. 42, где:
метаболическое заболевание представляет собой болезнь Фабри, болезнь Гоше, фенилкетонурию (ФКУ) или болезнь накопления гликогена;
болезнь или нарушение цикла мочевины представляет собой недостаточность орнитинтранскарбамилазы (ОТС);
лизосомная болезнь или нарушение накопления представляет собой метахроматическую лейкодистрофию (МЛД) или мукополисахаридоз типа II (MPSII; синдром Гунтера);
заболевание или нарушение печени представляет собой прогрессирующий семейный внутрипеченочный холестаз (ПСВХ);
заболевание или нарушение крови представляет собой гемофилию А, гемофилию В, талассемию или анемию; или
генетическое заболевание или нарушение представляет собой муковисцидоз.
44. Применение по п. 42 или 43, где указанная по меньшей мере одна нуклеотидная последовательность при транскрипции или трансляции модифицирует аномальное количество эндогенного белка у указанного субъекта.
45. Применение по п. 42 или 43, где указанная по меньшей мере одна нуклеотидная последовательность при транскрипции или трансляции модифицирует аномальную функцию или активность эндогенного белка или пути у указанного субъекта.
46. Применение по любому из пп. 42-45, где указанная по меньшей мере одна нуклеотидная последовательность кодирует или содержит нуклеотидную молекулу, выбранную из группы, состоящей из РНКи, миРНК, микроРНК, днкРНК, аптамера, пептидной нуклеиновой кислоты и антисмыслового олиго- или полинуклеотида.
47. Применение по любому из пп. 42-45, где указанная по меньшей мере одна нуклеотидная последовательность кодирует белок.
48. Применение по п. 42, где указанная по меньшей мере одна нуклеотидная последовательность кодирует маркерный белок.
49. Применение по любому из пп. 42-47, где указанная по меньшей мере одна нуклеотидная последовательность кодирует агонист или антагонист эндогенного белка или пути, ассоциированного с указанным заболеванием или нарушением.
50. Применение по любому из пп. 42-47, где указанная по меньшей мере одна нуклеотидная последовательность кодирует антитело.
51. Применение по пп. 42-50, где указанный зкДНК-вектор вводят в комбинации с фармацевтически приемлемым носителем.
52. Применение композиции, содержащей зкДНК-вектор по любому из пп. 1-21 для получения лекарственного средства для доставки терапевтического белка субъекту для коррекции аномального уровня и/или функции генного продукта, где указанная по меньшей мере одна нуклеотидная последовательность кодирует указанный терапевтический белок.
53. Применение по п. 52, где указанный терапевтический белок представляет собой терапевтическое антитело.
54. Применение по п. 52, в котором терапевтический белок выбран из группы, состоящей из Фактора VIII, Фактора IX, Фактора X и фенилаланингидроксилазы.
55. Набор для доставки нуклеиновой кислоты, содержащий зкДНК-вектор по любому из пп. 1-21 и наноноситель, упакованные в контейнер с вкладышем в упаковку.
56. Набор для получения зкДНК-вектора по любому из пп. 1-21, содержащий:
a. экспрессионную конструкцию, содержащую по меньшей мере один сайт рестрикции для инсерции по меньшей мере одной последовательности нуклеотидов, или регуляторного переключателя, или обоих, причем указанный по меньшей мере один сайт рестрикции расположен между асимметричными инвертированными концевыми повторами (асимметричными ITR), и по меньшей мере один из асимметричных ITR содержит функциональный сайт концевого разрешения и сайт связывания Rep, и
b. инструкции по применению для получения зкДНК-вектора.
57. Набор по п. 56, где один из ITR содержит делецию по меньшей мере в одной из областей ITR, выбранных из группы, состоящей из А, А', В, В', С, С', D и D' областей ITR.
58. Набор по п. 57, где один из ITR содержит делецию по меньшей мере в одной структуре, выбранной из группы, состоящей из (i) структуры стебля, которая соответствует областям А и A', (ii) первой структуры «петля на стебле», которая соответствует областям В и В', (iii) второй структуры «петля на стебле», которая соответствует областям С и С', и (iv) структуры, содержащей по меньшей мере сайты связывания транскрипционных факторов, которая соответствует областям D и D'.
59. Набор по любому из пп. 56, 57 или 58, где один из ITR содержит делецию всех областей ITR А, А', В, В', С, C', D и D'.
60. Набор по любому из пп. 56-58 или 59, который подходит для получения зкДНК-вектора по любому из пп. 1-22.
61. Набор по любому из пп. 56-59 или 60, дополнительно содержащий популяцию клеток насекомых, лишенную кодирующих последовательностей вирусного капсида, где в присутствии белка Rep может индуцироваться продуцирование зкДНК-вектора.
62. Набор по любому из пп. 56-61, дополнительно содержащий вектор, содержащий последовательность полинуклеотидов, которая кодирует по меньшей мере один белок Rep, где указанный вектор подходит для экспрессии указанного по меньшей мере одного белка Rep в клетке насекомого.
| US 20140107186 A1, 17.04.2014 | |||
| ГЕННАЯ ТЕРАПИЯ НЕЙРОДЕГЕНЕРАТИВНЫХ НАРУШЕНИЙ | 2010 |
|
RU2603740C2 |
| НОВАЯ ВИРУСНАЯ ВЕКТОРНАЯ КОНСТРУКЦИЯ ДЛЯ НЕЙРОНСПЕЦИФИЧЕСКОГО ОПТИМИЗИРОВАННОГО НЕПРЕРЫВНОГО СИНТЕЗА DOPA IN VIVO | 2010 |
|
RU2606012C2 |
| WO 1997021826 A2, 19.06.1997 | |||
| WO 1997032481 A1, 12.09.1997. | |||
Авторы
Даты
2023-07-14—Публикация
2018-09-07—Подача