[0001] Настоящая заявка испрашивает приоритет согласно предварительной заявке США № 62/817771, поданной 13 марта 2019 г., и предварительной заявке США № 62/857514, поданной 5 июня 2019 г., содержание каждой из которых полностью включено в данный документ посредством ссылки.
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
[0002] Настоящая заявка включает перечень последовательностей, который был подан в электронном виде в формате ASCII, а также последовательности в Таблицах 1-15 в данном документе, каждая из которых полностью включена в данный документ посредством ссылки. Указанная копия в формате ASCII, созданная 10 марта 2020 г., названа 131698-05720_SL.txt и имеет размер 116806 байтов.
ОБЛАСТЬ ТЕХНИКИ
[0003] Настоящее изобретение относится к области генной терапии, включая невирусные векторы для экспрессии трансгена или выделенных полинуклеотидов у субъекта или в клетке. Настоящее раскрытие также относится к конструкциям нуклеиновых кислот, промоторам, векторам и клеткам-хозяевам, включающим полинуклеотиды, а также к способам доставки экзогенных последовательностей ДНК в целевую клетку, ткань, орган или организм. Например, настоящее раскрытие обеспечивает способы применения невирусных зкДНК-векторов для экспрессии фенилаланингидроксилазы (PAH) из клетки, например, экспрессии терапевтического белка PAH для лечения субъекта, страдающего фенилкетонурией (ФКУ). Способы и композиции можно применять, например, для лечения заболевания путем экспрессии PAH в клетке или ткани субъекта, нуждающегося в этом.
УРОВЕНЬ ТЕХНИКИ
[0004] Целью генной терапии является улучшение клинических исходов у пациентов, страдающих либо генетическими мутациями, либо приобретенными заболеваниями, вызванными аберрацией в профиле экспрессии генов. Генная терапия включает лечение или предотвращение медицинских состояний, вызванных дефектными генами или аномальной регуляцией или экспрессией, например, недостаточной экспрессией или избыточной экспрессией, что может привести к нарушению, заболеванию, злокачественному новообразованию и т. д. Например, заболевание или нарушение, вызванное дефектным геном, можно лечить, предотвращать или облегчать путем доставки пациенту корректирующего генетического материала, или можно лечить, предотвращать или облегчать путем изменения или подавления у пациента дефектного гена, например, с помощью корректирующего генетического материала, приводящего к терапевтической экспрессии генетического материала в организме пациента.
[0005] Основой генной терапии является обеспечение транскрипционной кассеты с активным генным продуктом (иногда называемым трансгеном), например, который может приводить к положительному эффекту усиления функции, отрицательному эффекту потери функции или другому исходу. Такие исходы можно отнести к экспрессии терапевтического белка, такого как антитело, функциональный фермент или слитый белок. Генную терапию также можно применять для лечения заболевания или злокачественного новообразования, вызванного другими факторами. Моногенные нарушения у человека можно лечить путем доставки нормального гена в клетки-мишени и его экспрессии в них. Доставку и экспрессию корректирующего гена в клетках-мишенях пациента можно осуществлять с применением многочисленных способов, включая применение сконструированных вирусов и вирусных векторов для доставки генов. Среди многочисленных доступных векторов вирусного происхождения (например, рекомбинантный ретровирус, рекомбинантный лентивирус, рекомбинантный аденовирус и т. п.) рекомбинантный аденоассоциированный вирус (рААВ) приобретает все большую популярность в генной терапии в качестве многоцелевого вектора.
[0006] Аденоассоциированные вирусы (ААВ) принадлежат к семейству Parvoviridae и, более конкретно, составляют род депендопарвовирусов. Векторы, происходящие из ААВ (т. е. рекомбинантные ААВ (рААВ) или ААВ-векторы), являются привлекательным способом доставки генетического материала, поскольку (i) они способны инфицировать (трансдуцировать) широкий спектр типов неделящихся и делящихся клеток, включая миоциты и нейроны; (ii) они лишены вирусных структурных генов, что уменьшает ответы клеток хозяина на вирусную инфекцию, например, опосредуемые интерфероном ответы; (iii) вирусы дикого типа считаются непатологичными у человека; (iv) в отличие от ААВ дикого типа, которые способны интегрироваться в геном клетки хозяина, дефектные по репликации ААВ-векторы лишены гена rep и обычно персистируют в виде эписом, что ограничивает риск инсерционного мутагенеза или генотоксичности; и (v) по сравнению с другими векторными системами ААВ-векторы обычно считаются относительно слабыми иммуногенами и, следовательно, не вызывают значительного иммунного ответа (см. ii), обеспечивая, таким образом, персистенцию векторной ДНК и, потенциально, долговременную экспрессию терапевтических трансгенов.
[0007] Однако применение частиц ААВ в качестве вектора для доставки генов имеет несколько серьезных недостатков. Одним из основных недостатков, ассоциированных с рААВ, является ограниченная емкость вирусной упаковки, составляющая примерно 4,5 тыс. п. о. гетерологичной ДНК (Dong et al., 1996; Athanasopoulos et al., 2004; Lai et al., 2010), вследствие этого применение ААВ-векторов ограничено их способностью кодировать белки размером менее 150000 Да. Вторым недостатком является то, что в результате распространенности инфекции ААВ дикого типа среди населения кандидаты на генную терапию с использованием рААВ должны проходить скрининг на наличие нейтрализующих антител, устраняющих вектор из организма пациента. Третий недостаток связан с иммуногенностью капсида, которая препятствует повторному введению пациентам, которые не были отстранены от начального лечения. Иммунная система пациента может отвечать на вектор, который фактически выступает в роли «бустерной» прививки, стимулирующей выработку высоких титров антител к ААВ иммунной системой, которые исключают возможность лечения в будущем. В некоторых недавних сообщениях выражены опасения, касающиеся иммуногенности в ситуациях, подразумевающих применение высоких доз. Другой заметный недостаток заключается в относительно медленном начале ААВ-опосредуемой экспрессии генов, учитывая, что одноцепочечная ДНК ААВ должна быть преобразована в двухцепочечную ДНК до экспрессии гетерологичного гена.
[0008] Кроме того, обычные вирионы ААВ с капсидами получают путем введения плазмиды или плазмид, содержащих геном ААВ, гены rep и гены cap (Grimm et al., 1998). Однако было обнаружено, что такие вирусные векторы на основе заключенного в капсид ААВ неэффективно трансдуцируют определенные типы клеток и тканей, а капсиды также индуцируют иммунный ответ.
[0009] Соответственно, применение векторов на основе аденоассоциированного вируса (ААВ) для генной терапии ограничено из-за однократного введения пациентам (вследствие иммунного ответа пациента), ограниченного диапазона трансгенного генетического материала, подходящего для доставки в ААВ-векторах ввиду минимальной емкости вирусной упаковки (около 4,5 тыс. п. о.), и медленной ААВ-опосредуемой экспрессии генов.
[0010] Фенилкетонурия (ФКУ) представляет собой редкий наследственный врожденный порок метаболизма, вызванный мутацией в гене PAH. Фенилкетонурия (ФКУ) представляет собой врожденный порок метаболизма, который приводит к снижению метаболизма аминокислоты фенилаланина (Phe). Без лечения ФКУ может привести к умственной отсталости, судорожным припадкам, поведенческим расстройствам и психическим нарушениям. Она также может привести к появлению затхлого запаха и осветлению кожи. Младенцы, рожденные от матерей, у которых лечение фенилкетонурии было неэффективным, могут иметь проблемы с сердцем, маленькую голову и небольшую массу при рождении. ФКУ возникает из-за мутаций в гене PAH, что приводит к низким уровням фермента фенилаланингидроксилазы (PAH), т. е. субъекты, страдающие ФКУ, имеют мутации в PAH, которые приводят к дефициту его ферментативной активности. ФКУ является аутосомно-рецессивной, это означает, что для развития состояния должны быть мутированы обе копии гена. Существует два основных типа, классическая ФКУ и вариант ФКУ, в зависимости от того, сохраняется ли какая-либо ферментативная функция. Те, у кого имеется одна копия мутированного гена PAH, как правило, не имеют симптомов.
[0011] PAH представляет собой фермент, который обычно экспрессируется в печени и необходим для метаболизма поступающего с пищей фенилаланина в тирозин, аминокислоту, отвечающую за продукцию нейротрансмиттеров. PAH катализирует гидроксилирование фенилаланина до тирозина. Дефектный фермент PAH приводит к накоплению поступающего с пищей фенилаланина до потенциально токсичных уровней.
[0012] ФКУ может быть вызвана дефектом одного гена фермента фенилаланингидроксилазы (PAH), что приводит к повышению уровней Phe в сыворотке. У позвоночных PAH превращает Phe в тирозин. В отсутствие PAH единственными другими механизмами удаления Phe являются синтез белка и второстепенный путь разрушения, включающий дезаминирование и окислительное декарбоксилирование боковой цепи аланина с образованием характерного фениллактата и фенилацетата, наблюдаемых в моче пациентов, страдающих ФКУ. К сожалению, типичный рацион содержит больше Phe, чем может быть выведено в отсутствие PAH. В результате накопление Phe у пациентов, страдающих ФКУ, приводит к ряду симптомов, включая аномальное развитие мозга и тяжелую умственную отсталость. (Kaufman, Proc Nat´l Acad Sci USA 96: 3160-3164, 1999).
[0013] Современный стандарт лечения представляет собой строго ограничительную диету (ограничение фенилаланина (Phe)), но она не всегда эффективна, поскольку такое диетическое ограничение трудно поддерживать и оно не корректирует основной дефект. Современная терапия ФКУ заключается в соблюдении диеты с низким количеством пищевых продуктов, содержащих фенилаланин, и приеме специальных добавок. Строгая диета должна начинаться как можно раньше после рождения и должна продолжаться по меньшей мере 10 лет, если не всю жизнь. У некоторых пациентов, страдающих ФКУ, можно применять лекарственное средство дигидрохлорид сапроптерина. Без лечения ФКУ может привести к прогрессирующим и тяжелым неврологическим нарушениям. По оценкам от ФКУ страдают приблизительно 15000 человек в США, и отсутствуют доступные способы лечения генетического дефекта при ФКУ.
[0014] Несмотря на огромные успехи в изучении биохимии, молекулярной биологии и генетики ФКУ, в разработке новых способов лечения этого нарушения был достигнут незначительный прогресс. Существует большая неудовлетворенная потребность в модифицирующих заболевание видах терапии при ФКУ. Во-первых, современные виды терапии не модифицируют заболевание и эффективны только у подгруппы пациентов и по-прежнему требуют строгих диетических ограничений, а их несоблюдение может привести к повреждению нейронов. Во-вторых, отсутствуют одобренные виды генной терапии ФКУ, а виды терапии на основе ААВ не могут применяться у 25%-40% пациентов из-за уже существующих антител. ААВ может быть введен только один раз, и полученные уровни PAH могут быть недостаточно высокими, чтобы быть эффективными, или могут превышать нормальные, уровни доз не поддаются титрованию.
[0015] Соответственно, в данной области существует потребность в технологии, которая обеспечивает экспрессию терапевтического белка PAH в клетке, ткани или в организме субъекта для лечения ФКУ.
КРАТКОЕ ОПИСАНИЕ
[0016] Технология, описанная в данном документе, относится к способам и композициям для лечения фенилкетонурии (ФКУ) путем экспрессии фермента фенилаланингидроксилазы (PAH) с бескапсидного (например, невирусного) ДНК-вектора с ковалентно замкнутыми концами (называемого в данном документе «ДНК-вектор с замкнутыми концами» или «зкДНК-вектор»), причем указанный зкДНК-вектор содержит последовательность нуклеиновой кислоты PAH или ее варианты, оптимизированные по кодонам. Эти зкДНК-векторы можно применять для получения белков PAH для лечения, мониторинга и диагностики. Применение зкДНК-векторов, экспрессирующих PAH, у субъекта для лечения ФКУ можно применять для: (i) обеспечения модифицирующих заболевание уровней фермента PAH, (ii) минимально инвазивной доставки, (iii) повторяемости и дозирования до достижения эффекта, (iv) быстрого начала терапевтического эффекта, (v) устойчивой экспрессии корректирующего фермента PAH в печени, (vi) восстановления функции цикла мочевины, метаболизма фенилаланина, и/или (vii) титрования для достижения соответствующих фармакологических уровней дефектного фермента.
[0017] Соответственно, настоящее изобретение, описанное в данном документе, относится к бескапсидному (например, невирусному) ДНК-вектору с ковалентно замкнутыми концами (называемому в данном документе «ДНК-вектор с замкнутыми концами» или «зкДНК-вектор»), содержащему гетерогенный ген, кодирующий PAH, чтобы обеспечить экспрессию терапевтического белка PAH в клетке.
[0018] Согласно одному аспекту в данном документе раскрыт вектор на основе ДНК с замкнутыми концами (зкДНК), содержащий по меньшей мере одну гетерологичную нуклеотидную последовательность между фланкирующими инвертированными концевыми повторами (ITR), причем по меньшей мере одна гетерологичная нуклеотидная последовательность кодирует по меньшей мере один белок PAH, при этом указанная по меньшей мере одна гетерологичная нуклеотидная последовательность, которая кодирует по меньшей мере один белок PAH, выбрана из последовательности, имеющей по меньшей мере 90% идентичности с любой из последовательностей в Таблице 1. Согласно одному варианту реализации зкДНК-вектор представляет собой бескапсидный вектор. Согласно одному варианту реализации последовательности в Таблице 1 выбраны из группы, состоящей из SEQ ID NO: 380, SEQ ID NO: 381, SEQ ID NO: 382, SEQ ID NO: 383, SEQ ID NO: 384, SEQ ID NO: 385, SEQ ID NO: 386, SEQ ID NO: 387, SEQ ID NO: 388, SEQ ID NO: 389, SEQ ID NO: 390, SEQ ID NO: 391, SEQ ID NO: 392, SEQ ID NO: 393 и SEQ ID NO: 394.
[0019] Согласно одному варианту реализации гетерологичная нуклеотидная последовательность имеет по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичности с SEQ ID NO: 392. Согласно одному варианту реализации гетерологичная нуклеотидная последовательность имеет по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичности с SEQ ID NO: 84. Согласно одному варианту реализации гетерологичная нуклеотидная последовательность имеет по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичности с SEQ ID NO: 394.
[0020] зкДНК-векторы для экспрессии продукции белка PAH, описанные в данном документе, представляют собой бескапсидные линейные дуплексные молекулы ДНК, образованные из непрерывной цепи комплементарной ДНК с ковалентно замкнутыми концами (линейная, непрерывная и неинкапсидированная структура), которые содержат последовательность 5´ инвертированного концевого повтора (ITR) и последовательность 3´-ITR, причем указанные 5´-ITR и 3´-ITR могут иметь одинаковую симметричную трехмерную организацию по отношению друг к другу (т. е. симметричную или по существу симметричную) или, альтернативно, 5´-ITR и 3´-ITR могут иметь различную трехмерную организацию по отношению друг к другу (т. е. асимметричные ITR). Кроме того, ITR могут происходить из одного и того же или разных серотипов. Согласно некоторым вариантам реализации зкДНК-вектор может содержать последовательности ITR, которые имеют симметричную трехмерную пространственную организацию так, что их структура имеет одинаковую форму в геометрическом пространстве, или имеют одинаковые петли A, C-C´ и B-B´ в трехмерном пространстве (т. е. они одинаковы или являются зеркальными отображениями по отношению друг к другу). Согласно некоторым вариантам реализации один ITR может происходить из одного серотипа ААВ, а другой ITR может происходить из другого серотипа ААВ.
[0021] Соответственно, некоторые аспекты технологии, описанной в данном документе, относятся к зкДНК-вектору для улучшенной экспрессии и/или продукции белка описанного выше белка PAH, который содержит последовательности ITR, фланкирующие гетерологичную последовательность нуклеиновой кислоты, содержащую любую последовательность нуклеиновой кислоты PAH, раскрытую в Таблицах 5, при этом указанные последовательности ITR выбраны из любых из: (i) по меньшей мере одного ITR дикого типа (WT) и по меньшей мере одного модифицированного инвертированного концевого повтора (mod-ITR) ААВ (например, асимметричных модифицированных ITR); (ii) двух модифицированных ITR, причем пара mod-ITR имеет различную трехмерную пространственную организацию по отношению друг к другу (например, асимметричные модифицированные ITR), или (iii) пары симметричных или по существу симметричных WT-WT ITR, причем каждый WT-ITR имеет одинаковую трехмерную пространственную организацию, или (iv) пары симметричных или по существу симметричных модифицированных ITR, причем каждый mod-ITR имеет одинаковую трехмерную пространственную организацию. ЗкДНК-векторы, раскрытые в данном документе, могут быть получены в эукариотических клетках и поэтому лишены прокариотических модификаций ДНК и загрязнения бактериальными эндотоксинами в клетках насекомых.
[0022] Способы и композиции, описанные в данном документе, частично относятся к открытию невирусного бескапсидного ДНК-вектора с ковалентно замкнутыми концами (зкДНК-векторы), который можно применять для экспрессии по меньшей мере одного белка PAH или более чем одного белка PAH из клетки, включая, но не ограничиваясь ими, клетки печени.
[00023] Соответственно, в данном документе в одном аспекте предложены ДНК-векторы (например, зкДНК-векторы), содержащие по меньшей мере одну гетерологичную последовательность нуклеиновой кислоты, кодирующую по меньшей мере один трансген, кодирующий белки PAH, функционально связанный с промотором, расположенную между двумя различными последовательностями инвертированных концевых повторов (ITR) ААВ, причем один из ITR содержит функциональный сайт концевого разрешения ААВ и сайт связывания Rep, а один из ITR содержит делецию, вставку или замену относительно другого ITR; при этом указанный трансген кодирует белок PAH; и при этом указанная ДНК при расщеплении рестрикционным ферментом, имеющим один сайт распознавания на ДНК-векторе, отличается наличием характерных полос линейной и непрерывной ДНК по сравнению с контрольными линейными и прерывистыми ДНК при анализе на неденатурирующем геле. Другие аспекты включают доставку белка PAH путем его экспрессии in vivo с зкДНК-вектора, описанного в данном документе, и, кроме того, лечение фенилкетонурии (ФКУ) с применением зкДНК-векторов, кодирующих PAH. В данном документе также предусмотрены клетки, содержащие зкДНК-вектор, кодирующий PAH, описанный в данном документе. В соответствии с некоторыми вариантами реализации зкДНК-вектор содержит последовательность нуклеиновой кислоты, которая на 85% идентична SEQ ID NO: 192. В соответствии с некоторыми вариантами реализации зкДНК-вектор содержит последовательность нуклеиновой кислоты, которая на 90% идентична SEQ ID NO: 192. В соответствии с некоторыми вариантами реализации зкДНК-вектор содержит последовательность нуклеиновой кислоты, которая на 95% идентична SEQ ID NO: 192. В соответствии с некоторыми вариантами реализации зкДНК-вектор содержит последовательность нуклеиновой кислоты, которая на 96% идентична SEQ ID NO: 192. В соответствии с некоторыми вариантами реализации зкДНК-вектор содержит последовательность нуклеиновой кислоты, которая на 97% идентична SEQ ID NO: 192. В соответствии с некоторыми вариантами реализации зкДНК-вектор содержит последовательность нуклеиновой кислоты, которая на 98% идентична SEQ ID NO: 192. В соответствии с некоторыми вариантами реализации зкДНК-вектор содержит последовательность нуклеиновой кислоты, которая на 99% идентична SEQ ID NO: 192. В соответствии с некоторыми вариантами реализации зкДНК-вектор состоит из SEQ ID NO: 192. В соответствии с некоторыми вариантами реализации зкДНК-вектор содержит последовательность нуклеиновой кислоты, которая на 85% идентична SEQ ID NO: 194. В соответствии с некоторыми вариантами реализации зкДНК-вектор содержит последовательность нуклеиновой кислоты, которая на 90% идентична SEQ ID NO: 194. В соответствии с некоторыми вариантами реализации зкДНК-вектор содержит последовательность нуклеиновой кислоты, которая на 95% идентична SEQ ID NO: 194. В соответствии с некоторыми вариантами реализации зкДНК-вектор содержит последовательность нуклеиновой кислоты, которая на 96% идентична SEQ ID NO: 194. В соответствии с некоторыми вариантами реализации зкДНК-вектор содержит последовательность нуклеиновой кислоты, которая на 97% идентична SEQ ID NO: 194. В соответствии с некоторыми вариантами реализации зкДНК-вектор содержит последовательность нуклеиновой кислоты, которая на 98% идентична SEQ ID NO: 194. В соответствии с некоторыми вариантами реализации зкДНК-вектор содержит последовательность нуклеиновой кислоты, которая на 99% идентична SEQ ID NO: 194. В соответствии с некоторыми вариантами реализации зкДНК-вектор состоит из SEQ ID NO: 194.
[0024] Аспекты настоящего изобретения относятся к способам получения зкДНК-векторов, которые можно применять для экспрессии белка PAH в клетке, как описано в данном документе. Другие варианты реализации относятся к зкДНК-вектору, полученному с помощью способа, предложенного в данном документе. Согласно одному варианту реализации бескапсидный (например, невирусный) ДНК-вектор (зкДНК-вектор) для продукции белка PAH получают из плазмиды (называемой в данном документе «зкДНК-плазмидой»), содержащей полинуклеотидную матрицу экспрессионной конструкции, содержащую в указанном порядке: первый 5´-инвертированный концевой повтор (например, ITR ААВ); гетерологичную последовательность нуклеиновой кислоты; и 3´-ITR (например, ITR ААВ), причем указанные 5´-ITR и 3´-ITR могут быть асимметричными по отношению друг к другу или симметричными (например, WT-ITR или модифицированные симметричные ITR), как определено в данном документе.
[0025] зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, может быть получен с помощью ряда средств, которые будут известны обычному квалифицированному специалисту после прочтения этого раскрытия. Например, полинуклеотидная матрица экспрессионной конструкции, используемая для получения зкДНК-векторов согласно настоящему изобретению, может представлять собой зкДНК-плазмиду, зкДНК-бакмиду и/или зкДНК-бакуловирус. Согласно одному варианту реализации зкДНК-плазмида содержит сайт рестрикционного клонирования (например, SEQ ID NO: 123 и/или 124), функционально расположенный между ITR, в который может быть вставлена экспрессионная кассета, содержащая, например, промотор, функционально связанный с трансгеном, например, нуклеиновой кислотой, кодирующей PAH. Согласно некоторым вариантам реализации зкДНК-векторы для экспрессии белка PAH получают из полинуклеотидной матрицы (например, зкДНК-плазмиды, зкДНК-бакмиды, зкДНК-бакуловируса), содержащей симметричные или асимметричные ITR (модифицированные ITR или WT ITR).
[0026] В пермиссивной клетке-хозяине, в присутствии, например, Rep, полинуклеотидная матрица, имеющая по меньшей мере два ITR, реплицируется с получением зкДНК-векторов, экспрессирующих белок PAH. Получение зкДНК-вектора проходит в два этапа: во-первых, вырезание («извлечение») матрицы из остова матрицы (например, генома зкДНК-плазмиды, зкДНК-бакмиды, зкДНК-бакуловируса и т. д.) посредством белков Rep, и, во-вторых, Rep-опосредуемая репликация вырезанного зкДНК-вектора. Белки Rep и сайты связывания Rep различных серотипов ААВ хорошо известны обычным специалистам в данной области техники. Обычный специалист понимает необходимость выбора белка Rep из серотипа, который связывается с последовательностью нуклеиновой кислоты и реплицирует ее, на основе по меньшей мере одного функционального ITR. Например, если компетентный по репликации ITR происходит из серотипа 2 ААВ, соответствующий Rep будет из серотипа ААВ, который работает с этим серотипом, такого как ITR ААВ2 с Rep ААВ2 или ААВ4, но не Rep ААВ5, который не работает. После репликации зкДНК-вектор с ковалентно замкнутыми концами продолжает накапливаться в пермиссивных клетках, и зкДНК-вектор предпочтительно является достаточно стабильным с течением времени в присутствии белка Rep в стандартных условиях репликации, например, для накопления в количестве, составляющем по меньшей мере 1 пг/клетку, предпочтительно по меньшей мере 2 пг/клетку, предпочтительно по меньшей мере 3 пг/клетку, более предпочтительно по меньшей мере 4 пг/клетку, еще более предпочтительно по меньшей мере 5 пг/клетку.
[0027] Соответственно, один аспект настоящего изобретения относится к способу получения зкДНК-вектора для экспрессии таких белков PAH, включающему этапы: а) инкубации популяции клеток-хозяев (например, клеток насекомых), несущих полинуклеотидную матрицу экспрессионной конструкции (например, зкДНК-плазмиду, зкДНК-бакмиду и/или зкДНК-бакуловирус), лишенную последовательностей, кодирующих вирусный капсид, в присутствии белка Rep в условиях, эффективных для индукции продуцирования указанного зкДНК-вектора в клетках-хозяевах и в течение периода времени, достаточного для этого, при этом указанные клетки-хозяева не содержат последовательностей, кодирующих вирусный капсид; и b) сбора и выделения зкДНК-вектора из клеток-хозяев. Присутствие белка Rep индуцирует репликацию векторного полинуклеотида с модифицированным ITR с получением зкДНК-вектора для экспрессии белка PAH в клетке-хозяине. Однако вирусные частицы (например, вирионы ААВ) не экспрессируются. Таким образом, отсутствует ограничение по размеру, налагаемое вирионами.
[0028] Наличие пригодного для экспрессии белка PAH зкДНК-вектора, выделенного из клеток-хозяев, можно подтвердить путем расщепления ДНК, выделенной из клетки-хозяина, рестрикционным ферментом, имеющим один сайт распознавания на зкДНК-векторе, и анализа расщепленного ДНК-материала на денатурирующем и неденатурирующем гелях для подтверждения наличия характерных полос линейной и непрерывной ДНК по сравнению с линейной и прерывистой ДНК.
[0029] В данном документе также предложены способы экспрессии белка PAH, который имеет терапевтическое применение, с применением зкДНК-вектора в клетке или у субъекта. Такие белки PAH можно применять для лечения фенилкетонурии (ФКУ). Соответственно, в данном документе предложены способы лечения фенилкетонурии (ФКУ), включающие введение зкДНК-вектора, кодирующего терапевтический белок PAH, субъекту, нуждающемуся в этом. В соответствии с некоторыми вариантами реализации у субъекта наблюдается по меньшей мере примерно 50% снижение уровня фенилаланина в сыворотке по сравнению с уровнем фенилаланина в сыворотке у субъекта до введения. В соответствии с некоторыми вариантами реализации у субъекта наблюдается по меньшей мере примерно 50%, по меньшей мере примерно 55%, по меньшей мере примерно 60%, по меньшей мере примерно 65%, по меньшей мере примерно 70%, по меньшей мере примерно 75%, по меньшей мере примерно 80%, по меньшей мере примерно 85%, по меньшей мере примерно 90% или по меньшей мере примерно 95% снижение уровня фенилаланина в сыворотке. В соответствии с некоторыми вариантами реализации после введения уровень фенилаланина в сыворотке у субъекта составляет менее примерно 1500 мкМ. В соответствии с некоторыми вариантами реализации после введения уровень фенилаланина в сыворотке у субъекта составляет менее 1500, менее 1250, менее 1000, менее 750, менее 500, менее 400, менее 300, менее 250, менее 200, менее 100, менее 50 мМ. В соответствии с некоторыми вариантами реализации после введения у субъекта наблюдается повышение активности PAH по меньшей мере примерно на 10% по сравнению с уровнем активности PAH до введения. В соответствии с некоторыми вариантами реализации после введения у субъекта наблюдается повышение активности PAH по меньшей мере примерно на 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50% или 55% по сравнению с уровнем активности PAH до введения.
[0030] Согласно некоторым вариантам реализации один аспект технологии, описанной в данном документе, относится к невирусному бескапсидному ДНК-вектору с ковалентно замкнутыми концами (зкДНК-вектору), причем указанный зкДНК-вектор содержит по меньшей мере одну гетерологичную нуклеотидную последовательность, функционально расположенную между двумя последовательностями инвертированных концевых повторов, при этом указанные последовательности ITR могут быть асимметричными или симметричными, или по существу симметричными, в соответствии с определением этих терминов в данном документе, при этом по меньшей мере один из ITR содержит функциональный сайт концевого разрешения и сайт связывания Rep, и необязательно указанная гетерологичная последовательность нуклеиновой кислоты кодирует трансген (например, белок PAH), и при этом указанный вектор не находится в вирусном капсиде.
[0031] Эти и другие аспекты настоящего изобретения более подробно описаны ниже.
ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0032] Варианты реализации настоящего раскрытия, кратко обобщенные выше и более подробно обсуждаемые ниже, будут понятны со ссылкой на иллюстративные варианты реализации раскрытия, представленные на прилагаемых чертежах. Однако прилагаемые чертежи иллюстрируют только типичные варианты реализации настоящего раскрытия и поэтому не должны рассматриваться, как ограничивающие объем, поскольку раскрытие может допускать другие равно эффективные варианты реализации.
[0033] ФИГ. 1А иллюстрирует примерную структуру зкДНК-вектора для экспрессии белка PAH, раскрытого в данном документе, содержащего асимметричные ITR. Согласно этому варианту реализации примерный зкДНК-вектор содержит экспрессионную кассету, содержащую промотор CAG, WPRE и BGHpA. Открытая рамка считывания (ORF), кодирующая трансген PAH, может быть вставлена в сайт клонирования (R3/R4) между промотором CAG и WPRE. Экспрессионная кассета фланкирована двумя инвертированными концевыми повторами (ITR) - ITR дикого типа ААВ2 слева (на 5´-конце) и модифицированным ITR справа (на 3´-конце) от экспрессионной кассеты, поэтому два ITR, фланкирующие экспрессионную кассету, асимметричны по отношению друг к другу.
[0034] ФИГ. 1B иллюстрирует примерную структуру зкДНК-вектора для экспрессии PAH, раскрытого в данном документе, содержащего асимметричные ITR с экспрессионной кассетой, содержащей промотор CAG, WPRE и BGHpA. Открытая рамка считывания (ORF), кодирующая трансген PAH, может быть вставлена в сайт клонирования между промотором CAG и WPRE. Экспрессионная кассета фланкирована двумя инвертированными концевыми повторами (ITR) - модифицированным ITR слева (на 5´-конце) и ITR дикого типа справа (на 3´-конце) от экспрессионной кассеты.
[0035] ФИГ. 1C иллюстрирует примерную структуру зкДНК-вектора для экспрессии PAH, раскрытого в данном документе, содержащего асимметричные ITR, с экспрессионной кассетой, содержащей энхансер/промотор, трансген PAH, посттранскрипционный элемент (WPRE) и сигнал поли(А). Открытая рамка считывания (ORF) позволяет встраивать трансген PAH в сайт клонирования между промотором CAG и WPRE. Экспрессионная кассета фланкирована двумя инвертированными концевыми повторами (ITR), которые асимметричны по отношению друг к другу; модифицированный ITR слева (на 5´-конце) и модифицированный ITR справа (на 3´-конце) от экспрессионной кассеты, причем указанные 5´-ITR и 3´-ITR оба представляют собой модифицированные ITR, но имеют разные модификации (т. е. они не имеют одинаковых модификаций).
[0036] ФИГ. 1D иллюстрирует примерную структуру зкДНК-вектора для экспрессии PAH, раскрытого в данном документе, содержащего симметричные модифицированные ITR или по существу симметричные модифицированные ITR, как определено в данном документе, с экспрессионной кассетой, содержащей промотор CAG, WPRE и BGHpA. Открытая рамка считывания (ORF), кодирующая трансген PAH, вставлена в сайт клонирования между промотором CAG и WPRE. Экспрессионная кассета фланкирована двумя модифицированными инвертированными концевыми повторами (ITR), причем указанные 5´ модифицированный ITR и 3´ модифицированный ITR симметричны или по существу симметричны.
[0037] ФИГ. 1E иллюстрирует примерную структуру зкДНК-вектора для экспрессии PAH, раскрытого в данном документе, содержащего симметричные модифицированные ITR или по существу симметричные модифицированные ITR, как определено в данном документе, с экспрессионной кассетой, содержащей энхансер/промотор, трансген, посттранскрипционный элемент (WPRE) и сигнал поли(A). Открытая рамка считывания (ORF) позволяет вставить трансген (например, PAH) в сайт клонирования между промотором CAG и WPRE. Экспрессионная кассета фланкирована двумя модифицированными инвертированными концевыми повторами (ITR), причем указанные 5´ модифицированный ITR и 3´ модифицированный ITR симметричны или по существу симметричны.
[0038] ФИГ. 1F иллюстрирует примерную структуру зкДНК-вектора для экспрессии PAH, раскрытого в данном документе, содержащего симметричные WT-ITR или по существу симметричные WT-ITR, как определено в данном документе, с экспрессионной кассетой, содержащей промотор CAG, WPRE и BGHpA. Открытая рамка считывания (ORF), кодирующая трансген (например, PAH), вставлена в сайт клонирования между промотором CAG и WPRE. Экспрессионная кассета фланкирована двумя инвертированными концевыми повторами дикого типа (WT-ITR), причем указанные 5´ WT-ITR и 3´ WT-ITR являются симметричными или по существу симметричными.
[0039] ФИГ. 1G иллюстрирует примерную структуру зкДНК-вектора для экспрессии PAH, раскрытого в данном документе, содержащего симметричные модифицированные ITR или по существу симметричные модифицированные ITR, как определено в данном документе, с экспрессионной кассетой, содержащей энхансер/промотор, трансген (например, PAH), посттранскрипционный элемент (WPRE) и сигнал поли(A). Открытая рамка считывания (ORF) позволяет вставить трансген (например, PAH) в сайт клонирования между промотором CAG и WPRE. Экспрессионная кассета фланкирована двумя инвертированными концевыми повторами дикого типа (WT-ITR), причем указанные 5´ WT-ITR и 3´ WT-ITR являются симметричными или по существу симметричными.
[0040] ФИГ. 2A представляет Т-образную структуру стебель-петля левого ITR дикого типа ААВ2 (SEQ ID NO: 52) с идентификацией плеча A-A´, плеча B-B´, плеча C-C´, двух сайтов связывания Rep (RBE и RBE´), а также показывает сайт концевого разрешения (TRS). RBE содержит группу из 4 дуплексных тетрамеров, которые, как полагают, взаимодействуют либо с Rep 78, либо с Rep 68. Кроме того, также полагают, что RBE´ взаимодействует с комплексом Rep, собранным на ITR дикого типа или мутированном ITR в конструкции. Области D и D´ содержат сайты связывания факторов транскрипции и другую консервативную структуру. ФИГ. 2B показывает предполагаемую Rep-катализируемую никирующую и лигирующую активность в левом ITR дикого типа (SEQ ID NO: 53), включая Т-образную структуру стебель-петля левого ITR дикого типа ААВ2 с идентификацией плеча A-A´, плеча B-B´, плеча C-C´, двух сайтов связывания Rep (RBE и RBE´), а также показывает сайт концевого разрешения (TRS) и область D и D´, содержащую несколько сайтов связывания факторов транскрипции и другую консервативную структуру.
[0041] ФИГ. 3A представляет первичную структуру (полинуклеотидную последовательность) (слева) и вторичную структуру (справа) RBE-содержащих частей плеча A-A´, а также плеча C-C´ и B-B´ левого ITR дикого типа ААВ2 (SEQ ID NO: 54). ФИГ. 3B показывает примерную последовательность мутированного ITR (также называемого модифицированным ITR) для левого ITR. Показана первичная структура (слева) и предсказанная вторичная структура (справа) части RBE плеча A-A´, плеча C и плеча B-B´ примерного мутированного левого ITR (ITR-1, слева) (SEQ ID NO: 113). ФИГ. 3C показывает первичную структуру (слева) и вторичную структуру (справа) RBE-содержащей части петли A-A´ и плеч B-B´ и C-C´ правого ITR дикого типа ААВ2 (SEQ ID NO: 55). ФИГ. 3D показывает примерный правый модифицированный ITR. Показана первичная структура (слева) и предсказанная вторичная структура (справа) RBE-содержащей части плеча A-A´, B-B´ и плеча C примерного мутантного правого ITR (ITR-1, справа) (SEQ ID NO: 114). Любая комбинация левого и правого ITR (например, ITR ААВ2 или другого вирусного серотипа или синтетических ITR) может использоваться, как описано в данном документе. Каждая из полинуклеотидных последовательностей на ФИГ. 3A-3D относится к последовательности, используемой в геноме плазмиды или бакмиды/бакуловируса, применяемых для получения зкДНК, как описано в данном документе. Также на каждой из ФИГ. 3A-3D приведены соответствующие вторичные структуры зкДНК, выведенные на основании конфигураций зкДНК-вектора в геноме плазмиды или бакмиды/бакуловируса и предсказанных значений свободной энергии Гиббса.
[0042] ФИГ. 4A представляет собой схему, иллюстрирующую подготовительный способ получения инфицированных бакуловирусом клеток насекомых (BIIC), которые можно применять для получения зкДНК-вектора для экспрессии PAH, раскрытого в данном документе, в способе, описанном на схеме на ФИГ. 4B. ФИГ. 4B представляет собой схему примерного способа получения зкДНК, и ФИГ. 4С иллюстрирует биохимический метод и способ подтверждения получения зкДНК-вектора. ФИГ. 4D и ФИГ. 4E представляют собой схематические иллюстрации, описывающие способ идентификации наличия зкДНК в ДНК, собранной из осадков клеток, полученных во время способов продуцирования зкДНК на ФИГ. 4B. ФИГ. 4D схематически показывает ожидаемые полосы примерной зкДНК, оставленной неразрезанной или расщепленной рестрикционной эндонуклеазой, а затем подвергнутой электрофорезу либо на нативном геле, либо на денатурирующем геле. Самая левая схема представляет собой нативный гель и показывает несколько полос, свидетельствующих о том, что в своей дуплексной и неразрезанной форме зкДНК существует по меньшей мере в мономерном и димерном состояниях, наблюдаемых как быстрее мигрирующий мономер меньшего размера и медленнее мигрирующий димер, размер которого в два раза превышает размер мономера. На второй слева схеме показано, что при разрезании зкДНК рестрикционной эндонуклеазой исходные полосы исчезают и появляются быстрее мигрирующие (например, меньшие по размеру) полосы, соответствующие ожидаемым размерам фрагментов, оставшихся после расщепления. В денатурирующих условиях исходная дуплексная ДНК является одноцепочечной и мигрирует как молекула, размер которой в два раза превышает размер, наблюдаемый на нативном геле, поскольку комплементарные цепи ковалентно связаны. Таким образом, на второй схеме справа расщепленная зкДНК показывает распределение полос, сходное с наблюдаемым на нативном геле, но полосы мигрируют как фрагменты, размер которых в два раза превышает размер их аналогов на нативном геле. На самой правой схеме показано, что неразрезанная зкДНК в денатурирующих условиях мигрирует в виде одноцепочечного раскрытого кольца, поэтому размер наблюдаемых полос в два раза превышает размер полос, наблюдаемых в нативных условиях, в которых кольцо не раскрыто. На этой фигуре «тыс. п. о.» используется для обозначения относительного размера нуклеотидных молекул на основании, в зависимости от контекста, либо длины нуклеотидной цепи (например, для одноцепочечных молекул, наблюдаемых в денатурирующих условиях), либо числа пар оснований (например, для двухцепочечных молекул, наблюдаемых в нативных условиях). ФИГ. 4E показывает ДНК, имеющую прерывистую структуру. ЗкДНК может быть разрезана рестрикционной эндонуклеазой, имеющей один сайт распознавания в зкДНК-векторе, с получением двух фрагментов ДНК с разными размерами (1 тыс. п. о. и 2 тыс. п. о.) как в нейтральных, так и в денатурирующих условиях. ФИГ. 4E также показывает зкДНК, имеющую линейную и непрерывную структуру. ЗкДНК-вектор может быть разрезан рестрикционной эндонуклеазой с получением двух фрагментов ДНК, которые мигрируют как 1 тыс. п. о. и 2 тыс. п. о. в нейтральных условиях, но в денатурирующих условиях цепи остаются соединенными и образуют одиночные цепи, которые мигрируют как 2 тыс. п. о. и 4 тыс. п. о.
[0043] ФИГ. 5 представляет собой примерное изображение анализа в денатурирующем геле примеров зкДНК-векторов с (+) или без (-) расщепления эндонуклеазами (EcoRI для зкДНК-конструкции 1 и 2; BamH1 для зкДНК-конструкции 3 и 4; SpeI для зкДНК-конструкции 5 и 6; и XhoI для зкДНК-конструкции 7 и 8). Конструкции 1-8 описаны в Примере 1 PCT международной заявки PCT/US18/49996, которая полностью включена в данный документ посредством ссылки. Размеры выделенных звездочкой полос были определены и указаны внизу рисунка.
[0044] ФИГ. 6 отображает результаты экспериментов, описанных в Примере 7, и конкретно показывает изображения IVIS, полученные у мышей, получавших контроль ЛНЧ-поли(C) (крайняя слева мышь), и четырех мышей, получавших ЛНЧ-зкДНК-люциферазу (все, кроме крайней слева мыши). У четырех мышей, обработанных зкДНК, наблюдается значительная флуоресценция в области печени мыши.
[0045] ФИГ. 7 отображает результаты эксперимента, описанного в Примере 8. Темные точки (показаны стрелками) указывают на наличие белка, полученного в результате экспрессии трансгена с зкДНК, и демонстрируют ассоциацию введенной ЛНЧ-зкДНК с гепатоцитами.
[0046] ФИГ. 8A и 8B отображают результаты исследований на глазах, изложенных в Примере 9. ФИГ. 8A показывает типичные изображения IVIS из глаз крысы, в которые инъецировали JetPEI®-зкДНК-люциферазу (вверху слева), по сравнению с неинъецированным глазом той же крысы (вверху справа) или глазом крысы, в который инъецировали плазмиду-ДНК люциферазы (внизу слева), и неинъецированным глазом той же крысы (внизу справа). ФИГ. 8B показывает график средней светимости, наблюдаемой в обработанных глазах или соответствующих необработанных глазах в каждой из групп обработки. Крысы, обработанные зкДНК, демонстрировали длительную значительную флуоресценцию (и, следовательно, экспрессию трансгена люциферазы) в течение 99 дней, что существенно разнилось с крысами, получавшими плазмиду-люциферазу, у которых наблюдалась минимальная относительная флуоресценция (и, следовательно, экспрессия трансгена люциферазы).
[0047] ФИГ. 9A и 9B отображают результаты исследования устойчивости зкДНК и повторного введения дозы у мышей Rag2, описанного в Примере 10. ФИГ. 9А показывает график зависимости полного потока от времени, наблюдаемой у получавших ЛНЧ-зкДНК-Luc мышей c57bl/6 дикого типа или мышей Rag2. ФИГ. 9B представляет график, показывающий влияние повторной дозы на уровни экспрессии трансгена люциферазы у мышей Rag2, при этом после введения повторной дозы наблюдали повышенную стабильную экспрессию (стрелка указывает время введения повторной дозы).
[0048] ФИГ. 10 представляет данные исследования экспрессии люциферазы с зкДНК у обработанных мышей, описанного в Примере 11, показывающие полный поток в каждой группе мышей на протяжении исследования. Высокие уровни неметилированного CpG коррелировали с более низким полным потоком, наблюдаемым у мышей с течением времени, в то время как использование специфического для печени промотора коррелировало с продолжительной стабильной экспрессией трансгена с зкДНК-вектора на протяжении по меньшей мере 77 дней.
[0049] ФИГ. 11 представляет собой график, отображающий результаты эксперимента, описанного в Примере 12. Введение каждой из двух конструкций зкДНК PAH (зкДНК № 1, зкДНК № 2) путем гидродинамической доставки мышам PAHenu2 приводило к значительному снижению (уменьшение примерно на 75%) уровней PHE в сыворотке по сравнению с уровнями, обнаруженными у контрольных мышей, обработанных поли(C).
[0050] ФИГ. 12 представляет собой график, отображающий результаты эксперимента, описанного в Примере 13. hPAH Codop2 относится к зкДНК, содержащей оптимизированную по кодонам последовательность варианта 2 PAH человека (codop_v2), связанную с промотором VandenDriessche (VD); hPAH Codop4 относится к зкДНК, содержащей VD_промотор, функционально связанный с вариантом 4 PAH человека, оптимизированным по кодонам и минимизированным по CpG (codop_CpGmin_v4); зкДНК кДНК hPAH относится к немодифицированной кДНК PAH человека, протестированной в отношении влияния на коррекцию PHE у мышей PAHenu2 с дефицитом PAH. ФИГ. 12 показывает динамику уровней PHE в сыворотке (показаны как % PHE, скорректированный относительно контроля PAHenu2). Введение зкДНК, содержащей hPAH Codop2 и Codop4, привело к снижению уровней PHE в сыворотке, это указывает на достаточную активность PAH для коррекции уровней фенилаланина в крови при ФКУ у мышей. Показано, что коррекция стабильна в течение 15 дней эксперимента.
[0051] ФИГ. 13 представляет собой график, отображающий результаты эксперимента, описанного в Примере 14. ЗкДНК, содержащую оптимизированный по кодонам вариант 2 hPAH (Codop2), вводили в низких, средних и высоких дозах. ФИГ. 13 показывает динамику уровней PHE в сыворотке (PHE, мкМ). Введение зкДНК hPAH Codop2 в низких и средних дозах привело к дозозависимому снижению PHE в сыворотке. Примечательно, что введение зкДНК hPAH Codop2 в средней дозировке привело к значительно более сильному эффекту, чем введение в низкой дозе. Было показано, что коррекция стабильна в течение 15 дней эксперимента. У контрольного животного (носитель-КО) концентрация PHE в сыворотке не снижалась.
[0052] ФИГ. 14A представляет собой график, отображающий результаты эксперимента, описанного в Примере 15. Исследовали эффект зкДНК Codop2 на отдельных животных через 3 и 7 дней. Как показано на ФИГ. 14A, ко дню 3 введение Codop2 привело к снижению уровней PHE в сыворотке, это указывает на достаточную активность PAH для коррекции уровней фенилаланина в крови при ФКУ у мышей уже на 3 день.
[0053] ФИГ. 14B представляет собой график, отображающий ферментативную активность PAH человека и полученные в результате уровни фенилаланина в сыворотке, измеренные в ДЕНЬ 3 и ДЕНЬ 7 после инъекции зкДНК, содержащей VD-hPAH Codop2. Овал относится к данным мышей, не имевшим ответа, собранным в ДЕНЬ 7, и соответствует отсутствию коррекции PHE на ФИГ. 14A.
ПОДРОБНОЕ ОПИСАНИЕ
[0054] В данном документе предложен способ лечения фенилкетонурии (ФКУ) с применением зкДНК-вектора, содержащего одну или более нуклеиновых кислот, которые кодируют терапевтический белок PAH или его фрагмент. В данном документе также предложены зкДНК-векторы для экспрессии белка PAH, описанные в данном документе, содержащие одну или более гетерологичных нуклеиновых кислот, которые кодируют белок PAH. Согласно некоторым вариантам реализации экспрессия белка PAH может включать секрецию терапевтического белка из клетки, в которой он экспрессируется, или, альтернативно, в некоторых вариантах реализации экспрессированный белок PAH может действовать или функционировать (например, оказывать свой эффект) внутри клетки, в которой он экспрессируется. Согласно некоторым вариантам реализации зкДНК-вектор экспрессирует белок PAH в печени, мышце (например, скелетной мышце) субъекта или в другой части тела, которая может функционировать как депо для продукции и секреции терапевтического белка PAH во многие системные компартменты.
I. Определения
[0055] Если в данном документе не указано иное, научные и технические термины, используемые применительно к настоящей заявке, должны иметь значения, обычно известные обычным специалистами в области техники, к которой относится данное раскрытие. Следует понимать, что настоящее изобретение не ограничено конкретной методологией, протоколами и реагентами, и т. д., описанными в данном документе, и поэтому допускает варианты. Терминология, используемая в данном документе, предназначена исключительно для описания конкретных вариантов реализации, и не предназначена для ограничения объема настоящего изобретения, который определен исключительно формулой изобретения. Определения обычных терминов в иммунологии и молекулярной биологии можно найти в The Merck Manual of Diagnosis and Therapy, 19 изд., опубликовано Merck Sharp & Dohme Corp., 2011 (ISBN 978-0-911910-19-3); Robert S. Porter et al. (под ред.), Fields Virology, 6 изд., опубликовано Lippincott Williams & Wilkins, Philadelphia, PA, USA (2013), Knipe, D.M. and Howley, P.M. (ed.), The Encyclopedia of Molecular Cell Biology and Molecular Medicine, опубликовано Blackwell Science Ltd., 1999-2012 (ISBN 9783527600908); и Robert A. Meyers (ed.), Molecular Biology and Biotechnology: a Comprehensive Desk Reference, опубликовано VCH Publishers, Inc., 1995 (ISBN 1-56081-569-8); Immunology, Werner Luttmann, опубликовано Elsevier, 2006; Janeway´s Immunobiology, Kenneth Murphy, Allan Mowat, Casey Weaver (под ред.), Taylor & Francis Limited, 2014 (ISBN 0815345305, 9780815345305); Lewin´s Genes XI, опубликовано Jones & Bartlett Publishers, 2014 (ISBN-1449659055); Michael Richard Green and Joseph Sambrook, Molecular Cloning: A Laboratory Manual, 4 изд., Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y., USA (2012) (ISBN 1936113414); Davis et al., Basic Methods in Molecular Biology, Elsevier Science Publishing, Inc., New York, USA (2012) (ISBN 044460149X); Laboratory Methods in Enzymology: DNA, Jon Lorsch (ed.) Elsevier, 2013 (ISBN 0124199542); Current Protocols in Molecular Biology (CPMB), Frederick M. Ausubel (ed.), John Wiley and Sons, 2014 (ISBN047150338X, 9780471503385), Current Protocols in Protein Science (CPPS), John E. Coligan (ed.), John Wiley and Sons, Inc., 2005; и Current Protocols in Immunology (CPI) (John E. Coligan, ADA M Kruisbeek, David H Margulies, Ethan M Shevach, Warren Strobe, (eds.) John Wiley and Sons, Inc., 2003 (ISBN 0471142735, 9780471142737), содержание которых полностью включено в данный документ посредством ссылки).
[0056] В данном документе термины «введение», «введенный» и их варианты относятся к введению субъекту композиции или агента (например, терапевтической нуклеиновой кислоты или иммуносупрессора, описанных в данном документе) и включают одновременное и последовательное введение одной или более композиций или агентов. «Введение» может относиться, например, к терапевтическим, фармакокинетическим, диагностическим, исследовательским методам, к плацебо и к экспериментальным методам. «Введение» также включает способы лечения in vitro и ex vivo. Введение композиции или агента субъекту осуществляют любым подходящим путем, включая перорально, через легкие, интраназально, парентерально (внутривенно, внутримышечно, внутрибрюшинно или подкожно), ректально, введение в лимфатическую систему, внутрь опухоли или местно. Введение субъекту композиции или агента осуществляют с помощью электропорации. Введение включает самостоятельное введение и введение другим лицом. Введение может быть осуществлено любым подходящим путем. Подходящий путь введения позволяет композиции или агенту выполнять их предусмотренную функцию. Например, если подходящим путем является внутривенный, композицию вводят путем введения указанной композиции или агента в вену субъекта.
[0057] В данном документе выражения «терапевтическое средство на основе нуклеиновой кислоты», «терапевтическая нуклеиновая кислота» и «ТНК» используются взаимозаменяемо и относятся к любому варианту терапевтического средства с использованием нуклеиновых кислот в качестве активного компонента терапевтического агента для лечения заболевания или нарушения. В данном документе указанные выражения относятся к терапевтическим средствам на основе РНК и терапевтическим средствам на основе ДНК. Неограничивающие примеры терапевтических средств на основе РНК включают мРНК, антисмысловую РНК и олигонуклеотиды, рибозимы, аптамеры, интерферирующие РНК (РНКи), дцРНК-субстрат Dicer, короткую шпилечную РНК (кшРНК), асимметричную интерферирующую РНК (аиРНК), микроРНК (миРНК). Неограничивающие примеры терапевтических средств на основе ДНК включают миникольцо ДНК, миниген, вирусную ДНК (например, геном лентивируса или ААВ) или невирусные синтетические ДНК-векторы, линейную дуплексную ДНК с замкнутыми концами (зкДНК/CELiD), плазмиды, бакмиды, ДНК-векторы doggybone (dbDNA™), минималистичный вектор для иммунологически определенной экспрессии гена (MIDGE), невирусный ДНК-вектор с минимальной цепью (линейный ковалентно замкнутый ДНК-вектор) или гантелеобразный минимальный ДНК-вектор («гантелеобразную ДНК»).
[0058] В данном документе «эффективное количество» или «терапевтически эффективное количество» терапевтического агента, такого как терапевтический белок PAH или его фрагмент, представляет собой количество, достаточное для получения целевого эффекта, например, обеспечения модифицирующих заболевание уровней фермента PAH, устойчивой экспрессии корректирующего фермента PAH в печени, восстановления функции цикла мочевины, метаболизма фенилаланина и/или достижения соответствующих фармакологических уровней дефектного фермента. Подходящие анализы для измерения экспрессии целевого гена или целевой последовательности включают, например, исследование уровней белка или РНК с применением методик, известных специалистам в данной области техники, таких как дот-блоттинг, Нозерн-блоттинг, гибридизация in situ, ИФА, иммунопреципитация, функциональный ферментный анализ, а также фенотипические анализы, известные специалистам в данной области техники. Однако уровни дозировки основаны на различных факторах, включая тип повреждения, возраст, массу тела, пол, медицинское состояние пациента, тяжесть состояния, путь введения и конкретный применяемый активный агент. Соответственно, схема дозирования может значительно изменяться, однако может быть определена обычным путем лечащим врачом с применением стандартных способов. Кроме того, термины «терапевтическое количество», «терапевтически эффективные количества» и «фармацевтически эффективные количества» включают профилактические или превентивные количества композиций согласно описанному изобретению. В профилактических или превентивных приложениях описанного изобретения фармацевтические композиции или лекарственные средства вводят пациенту, подверженному или по иным причинам имеющему риск развития заболевания, нарушения или состояния, в количестве, достаточном для того чтобы устранить или уменьшить риск, уменьшить степень тяжести или отсрочить начало указанного заболевания, нарушения или состояния, включая биохимические, гистологические и/или поведенческие симптомы указанного заболевания, нарушения или состояния, его осложнения, и промежуточные патологические фенотипы, возникающие в ходе развития указанного заболевания, нарушения или состояния. Обычно предпочтительным является применение максимальной дозы, т. е. самой высокой безопасной дозы в соответствии с некоторым медицинским заключением. В соответствии с некоторыми вариантами реализации заболевание, нарушение или состояние представляет собой ФКУ. Термины «доза» и «дозировка» используются в данном документе взаимозаменяемо.
[0059] В данном документе термин «терапевтический эффект» относится к последствиям лечения, результаты которого оценивают как целевые и благоприятные. Терапевтический эффект может включать, прямо или опосредованно, остановку, уменьшение или устранение проявления заболевания. Терапевтический эффект также может включать, прямо или опосредованно, остановку, уменьшение или устранение прогрессирования проявления заболевания.
[0060] Для любого терапевтического агента, описанного в данном документе, терапевтически эффективное количество может быть изначально определено на основании предварительных исследований in vitro и/или в моделях на животных. Терапевтически эффективная доза также может быть определена на основании данных у человека. Применяемая доза может быть скорректирована на основании относительных биодоступности и эффективности вводимого соединения. Коррекция дозы для достижения максимальной эффективности на основе описанных выше способов и других хорошо известных способов находится в пределах возможностей обычного специалиста в данной области техники. Общие принципы определения терапевтической эффективности, с которыми можно ознакомиться в главе 1 руководства Goodman and Gilman, The Pharmacological Basis of Therapeutics, 10 изд., McGraw-Hill (New York) (2001), включенного в данный документ посредством ссылки, обобщены ниже.
[0061] Фармакокинетические принципы обеспечивают основу для модификации схемы дозирования для получения целевой степени терапевтической эффективности с минимумом неприемлемых нежелательных явлений. Дополнительные рекомендации по модификации дозировки могут быть получены в ситуациях, когда концентрация лекарственного средства в плазме может быть измерена и соотнесена с терапевтическим окном.
[0062] В данном документе термины «гетерологичная нуклеотидная последовательность» и «трансген» используются взаимозаменяемо и относятся к представляющей интерес нуклеиновой кислоте (отличной от нуклеиновой кислоты, кодирующей полипептид капсида), которая встроена в зкДНК-вектор и может быть доставлена и экспрессирована им, как раскрыто в данном документе.
[0063] В данном документе термины «экспрессионная кассета» и «транскрипционная кассета» используются взаимозаменяемо и относятся к линейному участку нуклеиновых кислот, который включает трансген, функционально связанный с одним или более промоторами или другими регуляторными последовательностями, достаточными для направления транскрипции трансгена, но который не содержит кодирующих капсид последовательностей, других векторных последовательностей или областей инвертированных концевых повторов. Экспрессионная кассета может дополнительно содержать одну или более цис-действующих последовательностей (например, промоторов, энхансеров или репрессоров), один или более интронов и один или более посттранскрипционных регуляторных элементов.
[0064] Термины «полинуклеотид» и «нуклеиновая кислота», используемые в данном документе взаимозаменяемо, относятся к полимерной форме нуклеотидов любой длины, будь то рибонуклеотиды или дезоксирибонуклеотиды. Таким образом, этот термин включает одно-, двух- или многоцепочечные ДНК или РНК, геномную ДНК, кДНК, гибриды ДНК-РНК или полимер, включающий пуриновые и пиримидиновые основания или другие природные, химически или биохимически модифицированные, неприродные или дериватизированные нуклеотидные основания. «Олигонуклеотид» обычно относится к полинуклеотидам, содержащим от примерно 5 до примерно 100 нуклеотидов одно- или двухцепочечной ДНК. Однако для целей настоящего раскрытия верхнего предела длины олигонуклеотида не существует. Олигонуклеотиды также известны как «олигомеры» или «олиго» (oligos) и могут быть выделены из генов или химически синтезированы с помощью способов, известных в данной области техники. Термины «полинуклеотид» и «нуклеиновая кислота» следует понимать как включающие, применительно к описываемым вариантам реализации, одноцепочечные (такие как смысловые или антисмысловые) и двухцепочечные полинуклеотиды. ДНК может быть в форме, например, антисмысловых молекул, плазмидной ДНК, дуплексов ДНК-ДНК, предварительно конденсированной ДНК, продуктов ПЦР, векторов (P1, PAC, BAC, YAC, искусственные хромосомы), экспрессионных кассет, химерных последовательностей, хромосомной ДНК или производных и комбинаций указанных групп. ДНК может быть в форме миникольца, плазмиды, бакмиды, минигена, ДНК с минимальной цепью (линейного ковалентно замкнутого ДНК-вектора), линейной дуплексной ДНК с замкнутыми концами (CELiD или зкДНК), ДНК doggybone (dbDNA™), гантелеобразной ДНК, минималистичного вектора для иммунологически определенной экспрессии гена (MIDGE), вирусного вектора или невирусных векторов. РНК может быть в форме короткой интерферирующей РНК (киРНК), дцРНК-субстрата Dicer, короткой шпилечной РНК (кшРНК), асимметричной интерферирующей РНК (аиРНК), микроРНК (миРНК), мРНК, рРНК, тРНК, вирусной РНК (вРНК) и их комбинаций. Нуклеиновые кислоты включают нуклеиновые кислоты, содержащие известные аналоги нуклеотидов или модифицированные остатки или связи остова, которые являются синтетическими, природными и неприродными, и которые имеют связывающие свойства, близкие свойствам референсной нуклеиновой кислоты. Примеры таких аналогов и/или модифицированных остатков включают, без ограничения, фосфотиоаты, фосфодиамидат-морфолиновый олигомер (морфолино), фосфоамидаты, метилфосфонаты, хиральные метилфосфонаты, 2´-O-метилрибонуклеотиды, замкнутую нуклеиновую кислоту (LNA™) и пептидные нуклеиновые кислоты (ПНК). За исключением конкретно указанных ограничений термин включает нуклеиновые кислоты, содержащие известные аналоги природных нуклеотидов, которые имеют связывающие свойства, близкие свойствам референсной нуклеиновой кислоты. Если не указано иное, подразумевается также, что конкретная последовательность нуклеиновой кислоты также включает ее консервативно модифицированные варианты (например, вырожденные замены кодонов), аллели, ортологи, однонуклеотидные полиморфизмы (SNP) и комплементарные последовательности, а также последовательность, указанную явным образом.
[0065] «Нуклеотиды» содержат сахар дезоксирибозу (ДНК) или рибозу (РНК), основание и фосфатную группу. Нуклеотиды соединены между собой посредством фосфатных групп.
[0066] «Основания» включают пурины и пиримидины, которые, в частности, включают природные соединения аденин, тимин, гуанин, цитозин, урацил, инозин и природные аналоги, а также синтетические производные пуринов и пиримидинов, которые включают, но не ограничиваются перечисленными, модификации, которые вводят новые реакционноспособные группы, такие как, но не ограничиваясь перечисленными, амины, спирты, тиолы, карбоксилаты и алкилгалогениды.
[0067] В данном документе термин «интерферирующая РНК» или «РНКи», или «последовательность интерферирующей РНК» включает одноцепочечную РНК (например, зрелую миРНК, олигонуклеотиды оцРНКи, олигонуклеотиды оцДНКи), двухцепочечную РНК (т. е. дуплексную РНК, такую как киРНК, дцРНК-субстрат Dicer, кшРНК, аиРНК или пре-миРНК), гибрид ДНК-РНК (см., например, публикацию РСТ № WO 2004/078941) или гибрид ДНК-ДНК (см., например, публикацию РСТ № WO 2004/104199), который способен уменьшать или ингибировать экспрессию целевого гена или последовательности (например, опосредуя разрушение или ингибируя трансляцию мРНК, которые комплементарны последовательности интерферирующей РНК), когда интерферирующая РНК находится в той же клетке, что и целевой ген или последовательность. Таким образом, интерферирующая РНК относится к одноцепочечной РНК, которая комплементарна последовательности мРНК-мишени, или к двухцепочечной РНК, образованной двумя комплементарными цепями или одной самокомплементарной цепью. Интерферирующая РНК может иметь существенную или полную идентичность с целевым геном или последовательностью или может содержать область несовпадения (т. е. мотив несовпадения). Последовательность интерферирующей РНК может соответствовать полноразмерному целевому гену или его подпоследовательности. Предпочтительно молекулы интерферирующих РНК синтезируют химическим путем. Раскрытия каждого из упомянутых выше патентных документов полностью включены в данный документ посредством ссылки для всех целей.
[0068] Интерферирующая РНК включает «короткую интерферирующую РНК» или «киРНК», например, интерферирующую РНК из примерно 15-60, 15-50 или 15-40 (дуплекс) нуклеотидов в длину, более типично примерно 15-30, 15-25 или 19-25 (дуплекс) нуклеотидов в длину и предпочтительно составляет примерно 20-24, 21-22 или 21-23 (дуплекс) нуклеотида в длину (например, каждая комплементарная последовательность двухцепочечной киРНК составляет 15-60, 15-50, 15-40, 15-30, 15-25 или 19-25 нуклеотидов в длину, предпочтительно примерно 20-24, 21-22 или 21-23 нуклеотида в длину, и двухцепочечная киРНК составляет примерно 15-60, 15-50, 15-40, 15-30, 15-25 или 19-25 пар оснований в длину, предпочтительно примерно 18-22, 19-20 или 19-21 пару оснований в длину). Дуплексы киРНК могут содержать 3´-липкие концы, имеющие от примерно 1 до примерно 4 нуклеотидов или от примерно 2 до примерно 3 нуклеотидов, и 5´-фосфатные концы. Примеры киРНК включают, без ограничения, двухцепочечную полинуклеотидную молекулу, собранную из двух одноцепочечных молекул, причем одна цепь является смысловой цепью, а другая представляет собой комплементарную антисмысловую цепь; двухцепочечную полинуклеотидную молекулу, собранную из одноцепочечной молекулы, в которой смысловая и антисмысловая области соединены линкером на основе нуклеиновой кислоты или на основе, отличной от нуклеиновой кислоты; двухцепочечную полинуклеотидную молекулу со шпилечной вторичной структурой, имеющей самокомплементарные смысловые и антисмысловые области; и кольцевую одноцепочечную полинуклеотидную молекулу с двумя или более петлевыми структурами и стеблем, имеющим самокомплементарные смысловые и антисмысловые области, причем кольцевой полинуклеотид может подвергаться процессингу in vivo или in vitro с получением активной двухцепочечной молекулы киРНК. В данном документе термин «киРНК» включает дуплексы РНК-РНК, а также гибриды ДНК-РНК (см., например, публикацию РСТ № WO 2004/078941, полностью включенную в данный документ посредством ссылки).
[0069] В данном документе термин «конструкция нуклеиновой кислоты» относится к молекуле нуклеиновой кислоты, будь то одноцепочечная или двухцепочечная, которая выделена из природного гена или которая модифицирована так, чтобы она содержала сегменты нуклеиновых кислот, с помощью способа, который в прочих случаях не существовал бы в природе, или является синтетической. Термин «конструкция нуклеиновой кислоты» является синонимом термина «экспрессионная кассета», когда конструкция нуклеиновой кислоты содержит контрольные последовательности, необходимые для экспрессии кодирующей последовательности согласно настоящему раскрытию. «Экспрессионная кассета» включает кодирующую последовательность ДНК, функционально связанную с промотором.
[0070] Под «гибридизуемая» или «комплементарная» или «по существу комплементарная» подразумевается, что нуклеиновая кислота (например, РНК) включает последовательность нуклеотидов, которая позволяет ей нековалентно связываться, т. е. формировать пары оснований по Уотсону-Крику и/или пары оснований G/U, «ренатурировать» или «гибридизироваться» с другой нуклеиновой кислотой специфичным для последовательности, антипараллельным образом (т. е. нуклеиновая кислота специфично связывается с комплементарной нуклеиновой кислотой) в соответствующих условиях температуры и ионной силы раствора in vitro и/или in vivo. Как известно в данной области техники, стандартное спаривание оснований по Уотсону-Крику включает: спаривание аденина (A) с тимидином (T), спаривание аденина (A) с урацилом (U) и спаривание гуанина (G) с цитозином (C). Кроме того, в данной области техники также известно, что при гибридизации двух молекул РНК (например, дцРНК) гуаниновое (G) основание спаривается с урацилом (U). Например, спаривание оснований G/U частично отвечает за вырожденность (т. е. избыточность) генетического кода в случае спаривания оснований анти-кодонов тРНК с кодонами в мРНК. Применительно к настоящему раскрытию гуанин (G) связывающего белок сегмента (дуплекса дцРНК) нацеливающей на ДНК молекулы РНК согласно настоящему изобретению считается комплементарным урацилу (U), и наоборот. Таким образом, когда пара оснований G/U может быть получена в определенном нуклеотидном положении связывающего белок сегмента (дуплекса дцРНК) нацеливающей на ДНК молекулы РНК согласно настоящему изобретению, это положение не рассматривается как некомплементарное, а вместо этого считается комплементарным.
[0071] Термины «пептид», «полипептид» и «белок» используются в данном документе взаимозаменяемо и относятся к полимерной форме аминокислот любой длины, которая может включать кодируемые и некодируемые аминокислоты, химически или биохимически модифицированные или дериватизированные аминокислоты, и полипептиды, имеющие модифицированные пептидные остовы.
[0072] Последовательность ДНК, которая «кодирует» конкретный белок PAH, представляет собой последовательность нуклеиновой кислоты ДНК, которая транскрибируется в конкретную РНК и/или белок. Полинуклеотид ДНК может кодировать РНК (мРНК), которая транслируется в белок, или полинуклеотид ДНК может кодировать РНК, которая не транслируется в белок (например, тРНК, рРНК или нацеливающую на ДНК РНК; также называемые «некодирующими» РНК или «нкРНК»).
В данном документе термин «слитый белок», в используемом в данном документе значении, относится к полипептиду, который содержит белковые домены по меньшей мере из двух разных белков. Например, слитый белок может содержать (i) PAH или его фрагмент и (ii) по меньшей мере один белок, не относящийся к GOI. Слитые белки, охватываемые данным документом, включают, но не ограничиваются перечисленными, антитело или Fc или антигенсвязывающий фрагмент антитела, слитый с белком PAH, например, внеклеточным доменом рецептора, лигандом, ферментом или пептидом. Белок PAH или его фрагмент, который является частью слитого белка, может представлять собой моноспецифичное антитело или биспецифичное или мультиспецифичное антитело.
[0073] В данном документе термин «ген безопасной гавани генома» или «ген безопасной гавани» относится к гену или локусам, в которые последовательность нуклеиновой кислоты может быть вставлена так, чтобы последовательность могла интегрироваться и функционировать предсказуемым образом (например, экспрессировать белок, представляющий интерес) без существенных отрицательных последствий для активности эндогенного гена или стимуляции рака. Согласно некоторым вариантам реализации ген безопасной гавани также представляет собой локусы или ген, в которых вставленная последовательность нуклеиновой кислоты может экспрессироваться эффективнее и на более высоких уровнях, чем в сайте, не являющемся «безопасной гаванью».
[0074] В данном документе термин «доставка гена» означает способ, с помощью которого чужеродную ДНК переносят в клетки-хозяева для приложений генной терапии.
[0075] В данном документе термин «концевой повтор» или «TR» включает любой вирусный концевой повтор или синтетическую последовательность, которая содержит по меньшей мере одну минимальную требуемую точку начала репликации и область, содержащую палиндромную шпилечную структуру. Связывающая Rep последовательность («RBS») (также называемая RBE (связывающий Rep элемент)) и сайт концевого разрешения («TRS») вместе составляют «минимальную требуемую точку начала репликации» и, соответственно, TR содержит по меньшей мере одну RBS и по меньшей мере один TRS. Каждый из TR, обратно комплементарных по отношению друг к другу в пределах определенного участка полинуклеотидной последовательности, как правило, называют «инвертированным концевым повтором» или «ITR». Применительно к вирусу ITR опосредуют репликацию, упаковку вируса, интеграцию и освобождение провируса. Как было неожиданно обнаружено, согласно настоящему изобретению TR, которые не являются обратно комплементарными по всей их длине, все еще могут выполнять обычные функции ITR и, таким образом, в данном документе термин ITR относится к TR в геноме зкДНК или зкДНК-векторе, который способен опосредовать репликацию зкДНК-вектора. Обычный специалист в данной области техники поймет, что в зкДНК-векторах сложной конфигурации может присутствовать более двух пар ITR или асимметричных ITR. ITR может представлять собой ITR ААВ или ITR, не принадлежащий ААВ, или может быть получен из ITR ААВ или ITR, не принадлежащего ААВ. Например, ITR может происходить из вируса семейства Parvoviridae, которое включает парвовирусы и депендовирусы (например, собачий парвовирус, бычий парвовирус, мышиный парвовирус, свиной парвовирус, парвовирус человека B-19), или шпилька SV40, которая служит точкой начала репликации SV40, может применяться в качестве ITR, который может быть дополнительно модифицирован путем усечения, замены, делеции, вставки и/или добавления. Вирусы семейства Parvoviridae состоят из двух подсемейств: Parvovirinae, инфицирующих позвоночных животных, и Densovirinae, инфицирующих беспозвоночных. Депендопарвовирусы включают вирусное семейство аденоассоциированных вирусов (ААВ), которые способны к репликации у позвоночных животных-хозяев, включая, но не ограничиваясь перечисленными, человека, виды приматов, бычьих, собачьих, лошадиных и овечьих. Для удобства в данном документе ITR, расположенный в 5´-направлении (слева) относительно экспрессионной кассеты в зкДНК-векторе, называется «5´-ITR» или «левым ITR», а ITR, расположенный в 3´-направлении (справа) относительно экспрессионной кассеты в зкДНК-векторе, называется «3´-ITR» или «правым ITR».
[0076] «ITR дикого типа» или «WT-ITR» относится к последовательности природной последовательности ITR в ААВ или другом депендовирусе, которая сохраняет, например, активность связывания Rep и никирующую способность Rep. Нуклеотидная последовательность WT-ITR из любого серотипа ААВ может незначительно отличаться от канонической природной последовательности из-за вырожденности генетического кода или дрейфа, и, таким образом, последовательности WT-ITR, предусмотренные для применения в данном документе, включают последовательности WT-ITR, образующиеся в результате природных изменений, происходящих в процессе продуцирования (например, ошибки репликации).
[0077] В данном документе термин «по существу симметричные WT-ITR» или «пара по существу симметричных WT-ITR» относится к паре WT-ITR в одном геноме зкДНК или зкДНК-векторе, которые оба представляют собой ITR дикого типа, которые имеют обратно комплементарные последовательности по всей их длине. Например, ITR может считаться последовательностью дикого типа, даже если он содержит один или более нуклеотидов, отличающихся от канонической природной последовательности, при условии, что указанные изменения не влияют на свойства и общую трехмерную структуру последовательности. Согласно некоторым аспектам отличающиеся нуклеотиды представляют собой консервативные изменения последовательности. В качестве одного неограничивающего примера, последовательность, имеющая по меньшей мере 95%, 96%, 97%, 98% или 99% идентичности последовательности с канонической последовательностью (измеренной, например, с использованием BLAST при настройках по умолчанию), также имеет симметричную трехмерную пространственную организацию с другой последовательностью WT-ITR так, что их трехмерные структуры имеют одинаковую форму в геометрическом пространстве. По существу симметричный WT-ITR содержит одинаковые петли A, C-C´ и B-B´ в трехмерном пространстве. То, что по существу симметричный WT-ITR представляет собой WT может быть функционально подтверждено путем определения наличия в нем функционального сайта связывания Rep (RBE или RBE´) и сайта концевого разрешения (TRS), который спаривается с соответствующим белком Rep. Могут быть протестированы другие функции, включая экспрессию трансгена в пермиссивных условиях, но необязательно.
[0078] В данном документе выражения «модифицированный ITR» или «mod-ITR», или «мутантный ITR» используются в данном документе взаимозаменяемо и относятся к ITR, который содержит мутацию по меньшей мере в одном или более нуклеотидах по сравнению с WT-ITR из того же серотипа. Мутация может приводить к изменению в одной или более из областей A, C, C´, B, B´ в ITR и может приводить к изменению трехмерной пространственной организации (т. е. его трехмерной структуры в геометрическом пространстве) по сравнению с трехмерной пространственной организацией WT-ITR из того же серотипа.
[0079] В данном документе термин «асимметричные ITR», также называемые «парами асимметричных ITR», относится к паре ITR в одном геноме зкДНК или зкДНК-векторе, которые не являются обратно комплементарными по их полной длине. В качестве одного неограничивающего примера, асимметричный ITR в паре не имеет симметричной трехмерной пространственной организации со своим когнатным ITR так, что их трехмерные структуры имеют разные формы в геометрическом пространстве. Другими словами, асимметричные ITR в паре имеют разные общие геометрические структуры, т. е. они имеют разную организацию их петель A, C-C´ и B-B´ в трехмерном пространстве (например, один ITR может иметь короткое плечо C-C´ и/или короткое плечо B-B´ по сравнению с когнатным ITR). Различие по последовательности между двумя ITR может быть обусловлено добавлением, делецией, усечением или точечной мутацией одного или более нуклеотидов. Согласно одному варианту реализации один ITR из пары асимметричных ITR может представлять собой последовательность ITR дикого типа ААВ, а другой ITR представляет собой модифицированный ITR, как определено в данном документе (например, последовательность ITR, не относящуюся к дикому типу, или синтетическую последовательность). Согласно другому варианту реализации ни один ITR из пары асимметричных ITR не является последовательностью ААВ дикого типа, и указанные два ITR представляют собой модифицированные ITR, которые имеют разные формы в геометрическом пространстве (т. е. разную общую геометрическую структуру). Согласно некоторым вариантам реализации один mod-ITR из пары асимметричных ITR может иметь короткое плечо C-C´, а другой ITR может иметь другую модификацию (например, одно плечо или короткое плечо B-B´ и т. д.) так, что они имеют различную трехмерную пространственную организацию по сравнению с когнатным асимметричным mod-ITR.
[0080] В данном документе термин «симметричные ITR» относится к паре ITR в одном зкДНК-геноме или зкДНК-векторе, которые представляют собой последовательности дикого типа или мутированные (например, модифицированные относительно дикого типа) депендовирусные последовательности ITR и обратно комплементарны по всей их длине. В одном неограничивающем примере оба ITR представляют собой последовательности ITR дикого типа из ААВ2. В другом примере ни один из ITR не является последовательностью ITR дикого типа ААВ2 (т. е. они представляют собой модифицированные ITR, также называемые мутантными ITR) и может отличаться по последовательности от ITR дикого типа вследствие добавления, делеции, замены, усечения или точечной мутации нуклеотида. Для удобства в данном документе ITR, расположенный в 5´-направлении (слева) относительно экспрессионной кассеты в зкДНК-векторе, называется «5´-ITR» или «левым ITR», а ITR, расположенный в 3´-направлении (справа) относительно экспрессионной кассеты в зкДНК-векторе, называется «3´-ITR» или «правым ITR».
[0081] В данном документе термин «по существу симметричные модифицированные ITR» или «пара по существу симметричных mod-ITR» относится к паре модифицированных ITR в одном геноме зкДНК или зкДНК-векторе, которые оба имеют обратно комплементарные последовательности по всей их длине. Например, модифицированный ITR может считаться по существу симметричным, даже если он имеет некоторые нуклеотидные последовательности, отличающиеся от обратно комплементарной последовательности, при условии, что указанные изменения не влияют на свойства и общую форму. В качестве одного неограничивающего примера представлена последовательность, которая имеет по меньшей мере 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности последовательности с канонической последовательностью (измеренной с помощью BLAST при настойках по умолчанию), а также имеет симметричную трехмерную пространственную организацию в отношении ее когнатного модифицированного ITR так, что их трехмерные структуры имеют одинаковую форму в геометрическом пространстве. Другими словами, пара по существу симметричных модифицированных ITR имеет одинаково организованные в трехмерном пространстве петли A, C-C´ и B-B´. Согласно некоторым вариантам реализации ITR из пары mod-ITR могут иметь разные обратно комплементарные нуклеотидные последовательности, но все же иметь одинаковую симметричную трехмерную пространственную организацию, т. е. оба ITR содержат мутации, которые приводят к одинаковой общей трехмерной форме. Например, один ITR (например, 5´-ITR) в паре mod-ITR может происходить из одного серотипа, а другой ITR (например, 3´-ITR) может происходить из другого серотипа, однако оба могут иметь одинаковую соответствующую мутацию (например, если 5´-ITR имеет делецию в области C, то когнатный модифицированный 3´-ITR из другого серотипа имеет делецию в соответствующем положении в области C´) так, что пара модифицированных ITR имеет одинаковую симметричную трехмерную пространственную организацию. Согласно таким вариантам реализации каждый ITR в паре модифицированных ITR может происходить из разных серотипов (например, ААВ1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 и 12), таких как комбинация ААВ2 и ААВ6, при этом модификация в одном ITR отображается в соответствующем положении в когнатном ITR из другого серотипа. Согласно одному варианту реализации пара по существу симметричных модифицированных ITR относится к паре модифицированных ITR (mod-ITR) при условии, что различие в нуклеотидных последовательностях между указанными ITR не влияет на свойства или общую форму, и они имеют по существу одинаковую форму в трехмерном пространстве. В качестве неограничивающего примера представлен mod-ITR, который имеет по меньшей мере 95%, 96%, 97%, 98% или 99% идентичности последовательности с каноническим mod-ITR, как определено с помощью стандартных способов, хорошо известных в данной области техники, таких как BLAST (Basic Local Alignment Search Tool) или BLASTN, при настройках по умолчанию, а также имеет симметричную трехмерную пространственную организацию так, что их трехмерная структура имеет одинаковую форму в геометрическом пространстве. Пара по существу симметричных mod-ITR имеет одинаковые петли A, C-C´ и B-B´ в трехмерном пространстве, например, если модифицированный ITR в паре по существу симметричных mod-ITR имеет делецию плеча C-C´, то когнатный mod-ITR имеет соответствующую делецию петли C-C´, а также имеет сходную трехмерную структуру остальных петель A и B-B´ одинаковой формы в геометрическом пространстве со своим когнатным mod-ITR.
[0082] Термин «фланкирование» относится к относительному положению одной последовательности нуклеиновой кислоты по отношению к другой последовательности нуклеиновой кислоты. Обычно в последовательности ABC A и C фланкируют B. То же самое верно для расположения AxBxC. Соответственно, фланкирующая последовательность предшествует фланкируемой последовательности или следует за ней, но не обязательно должна быть смежной с фланкируемой последовательностью или непосредственно прилегать к ней. Согласно одному варианту реализации термин «фланкирование» относится к концевым повторам на каждом конце линейного дуплексного зкДНК-вектора.
[0083] В данном документе термины «лечить», «осуществлять лечение» и/или «лечение» включают подавление, по существу ингибирование, замедление или обращение прогрессирования состояния, по существу облегчение клинических симптомов состояния или по существу предотвращение появления клинических симптомов состояния, получение благоприятных или целевых клинических результатов. В соответствии с некоторыми вариантами реализации состояние представляет собой ФКУ. Лечение также относится к достижению одного или более из следующих: (a) уменьшения степени тяжести нарушения; (b) ограничения развития симптомов, характерных для нарушения (ий), которое лечат; (c) ограничения ухудшения симптомов, характерных для нарушения (ий), которое лечат; (d) ограничения рецидивирования нарушения (ий) у пациентов, ранее имевших указанное нарушение (ия); и (e) ограничения рецидивирования симптомов у пациентов, ранее не имевших симптомов указанного нарушения (ий). Благоприятные или целевые клинические результаты, такие как фармакологические и/или физиологические эффекты, включают, но не ограничиваются перечисленными, предотвращение наступления заболевания, нарушения или состояния у субъекта, который может быть предрасположен к указанному заболеванию, нарушению или состоянию, но еще не испытывает симптомов или у него еще не проявляются симптомы указанного заболевания (профилактическое лечение), облегчение симптомов указанного заболевания, нарушения или состояния, уменьшение интенсивности заболевания, нарушения или состояния, стабилизацию (т. е., отсутствие ухудшения) указанного заболевания, нарушения или состояния, предотвращение распространения указанного заболевания, нарушения или состояния, задержку или замедление прогрессирования указанного заболевания, нарушения или состояния, облегчение или временное облегчение указанного заболевания, нарушения или состояния, и комбинации перечисленных, а также увеличение продолжительности выживания по сравнению с ожидаемым выживанием без лечения.
[0084] В данном документе термин «увеличение», «усиление», «повышение» (и подобные термины) обычно относится к акту увеличения, прямо или опосредовано, концентрации, уровня, функции, активности или поведения относительно природного, ожидаемого или среднего, или относительно контрольного состояния.
[0085] В данном документе термин «минимизировать», «уменьшать», «снижать» и/или «ингибировать» (и подобные термины) обычно относится к акту уменьшения, прямо или опосредовано, концентрации, уровня, функции, активности, поведения относительно природного, ожидаемого, среднего, или относительно контрольного состояния.
[0086] В данном документе термин «зкДНК-геном» относится к экспрессионной кассете, которая дополнительно включает по меньшей мере одну область инвертированного концевого повтора. ЗкДНК-геном может дополнительно содержать одну или более спейсерных областей. Согласно некоторым вариантам реализации зкДНК-геном включен в виде межмолекулярного дуплексного полинуклеотида ДНК в плазмиду или вирусный геном.
[0087] В данном документе термин «спейсерная область зкДНК» относится к промежуточной последовательности, которая разделяет функциональные элементы в зкДНК-векторе или геноме зкДНК. Согласно некоторым вариантам реализации спейсерные области зкДНК удерживают два функциональных элемента на целевом расстоянии для оптимальной функциональности. Согласно некоторым вариантам реализации спейсерные области зкДНК обеспечивают или увеличивают генетическую стабильность зкДНК-генома, например, в плазмиде или бакуловирусе. Согласно некоторым вариантам реализации спейсерные области зкДНК облегчают подготовленные генетические манипуляции с зкДНК-геномом, обеспечивая удобное расположение для сайтов клонирования и т.п. Например, согласно определенным аспектам олигонуклеотидный «полилинкер», содержащий несколько сайтов рестрикционных эндонуклеаз, или последовательность не из открытой рамки считывания, сконструированная так, чтобы в ней отсутствовали известные сайты связывания белка (например, транскрипционного фактора), могут быть размещены в зкДНК-геноме для разделения цис-действующих факторов, например, с помощью 6-членной, 12-членной, 18-членной, 24-членной, 48-членной, 86-членной, 176-членной вставки и т. д. между сайтом концевого разрешения и расположенным в 5´-направлении транскрипционным регуляторным элементом. Аналогичным образом, спейсер может быть встроен между последовательностью сигнала полиаденилирования и 3´-сайтом концевого разрешения.
[0088] В данном документе термины «сайт связывания Rep», «элемент связывания Rep», «RBE» и «RBS» используются взаимозаменяемо и относятся к сайту связывания белка Rep (например, Rep 78 ААВ или Rep 68 ААВ), который после связывания белком Rep позволяет белку Rep выполнять его сайт-специфичную эндонуклеазную активность в отношении последовательности, включающей RBS. Последовательность RBS и ее обратно комплементарная последовательность вместе образуют один RBS. Последовательности RBS известны в данной области техники и включают, например, 5´-GCGCGCTCGCTCGCTC-3´ (SEQ ID NO: 60), представляющую собой последовательность RBS, идентифицированную в ААВ2. В вариантах реализации настоящего изобретения можно применять любую известную последовательность RBS, включая другие известные последовательности RBS ААВ и другие известные природные или синтетические последовательности RBS. Без ограничения какой-либо теорией, считается, что нуклеазный домен белка Rep связывается с дуплексной нуклеотидной последовательностью GCTC и, соответственно, происходит прямое связывание и стабильная сборка двух известных белков Rep ААВ на дуплексном олигонуклеотиде 5´-(GCGC)(GCTC)(GCTC)(GCTC)-3´ (SEQ ID NO: 60). Кроме того, растворимые агрегированные конформеры (т. е. неопределенное число взаимосвязанных белков Rep) диссоциируют и связываются с олигонуклеотидами, которые содержат сайты связывания Rep. Каждый белок Rep взаимодействует как с азотистыми основаниями, так и с фосфодиэфирным остовом на каждой цепи. Взаимодействия с азотистыми основаниями обеспечивают специфичность в отношении последовательности, в то время как взаимодействия с фосфодиэфирным остовом неспецифичны или менее специфичны в отношении последовательности и стабилизируют комплекс белка с ДНК.
[0089] В данном документе термины «сайт концевого разрешения» и «TRS» используются в данном документе взаимозаменяемо и относятся к области, в которой Rep образует тирозин-фосфодиэфирную связь с 5´-тимидином с образованием 3´-ОН, который служит субстратом для удлинения ДНК с помощью клеточной ДНК-полимеразы, например, ДНК-полимеразы дельта или ДНК-полимеразы эпсилон. В качестве альтернативы, комплекс Rep-тимидин может принимать участие в скоординированной реакции лигирования. Согласно некоторым вариантам реализации TRS включает, как минимум, неспаренный тимидин. Согласно некоторым вариантам реализации никирующую эффективность TRS по меньшей мере отчасти можно контролировать за счет расстояния между ним и RBS в пределах одной молекулы. Если акцепторный субстрат представляет собой комплементарный ITR, тогда полученный продукт представляет собой внутримолекулярный дуплекс. Последовательности TRS известны в данной области техники и включают, например, 5´-GGTTGA-3´ (SEQ ID NO: 61), представляющую собой гексануклеотидную последовательность, идентифицированную в ААВ2. В вариантах реализации настоящего изобретения можно применять любую известную последовательность TRS, включая другие известные последовательности TRS ААВ и другие известные природные или синтетические последовательности TRS, такие как AGTT (SEQ ID NO: 62), GGTTGG (SEQ ID NO: 63), AGTTGG (SEQ ID NO: 64), AGTTGA (SEQ ID NO: 65), и другие мотивы, такие как RRTTRR (SEQ ID NO: 66).
[0090] В данном документе термин «зкДНК-плазмида» относится к плазмиде, которая содержит зкДНК-геном в виде межмолекулярного дуплекса.
[0091] В данном документе термин «зкДНК-бакмида» относится к геному инфекционного бакуловируса, содержащему зкДНК-геном в виде межмолекулярного дуплекса, который способен размножаться в E. coli в виде плазмиды и, соответственно, может выполнять роль челночного вектора для бакуловируса.
[0092] В данном документе термин «зкДНК-бакуловирус» относится к бакуловирусу, который содержит зкДНК-геном в виде межмолекулярного дуплекса в геноме бакуловируса.
[0093] В данном документе термины «инфицированная зкДНК-бакуловирусом клетка насекомого» и «зкДНК-BIIC» используются взаимозаменяемо и относятся к клетке беспозвоночного животного-хозяина (включая, но не ограничиваясь этим, клетку насекомого (например, клетку Sf9)), инфицированной зкДНК-бакуловирусом.
[0094] В данном документе термин «зкДНК» относится к бескапсидной линейной двухцепочечной (дц) дуплексной ДНК с замкнутыми концами для невирусного переноса генов, синтетической или другой. Подробное описание зкДНК приведено в международной заявке PCT/US2017/020828, поданной 3 марта 2017 г., содержание которой полностью явным образом включено в данный документ посредством ссылки. Некоторые способы получения зкДНК, содержащей различные последовательности и конфигурации инвертированных концевых повторов (ITR), с использованием клеточных методов описаны в Примере 1 международной заявки PCT/US18/49996, поданной 7 сентября 2018 г., и PCT/US2018/064242, поданной 6 декабря 2018 г., каждая из которых полностью включена в данный документ посредством ссылки. Некоторые способы получения синтетических зкДНК-векторов, содержащих различные последовательности и конфигурации ITR, описаны, например, в международной заявке PCT/US2019/14122, поданной 18 января 2019 г., содержание которой полностью включено в данный документ посредством ссылки.
[0095] В данном документе термин «ДНК-вектор с замкнутыми концами» относится к бескапсидному ДНК-вектору по меньшей мере с одним ковалентно замкнутым концом, причем по меньшей мере часть вектора имеет структуру внутримолекулярного дуплекса.
[0096] В данном документе термины «зкДНК-вектор» и «зкДНК» используются взаимозаменяемо и относятся к ДНК-вектору с замкнутыми концами, содержащему по меньшей мере один концевой палиндром. Согласно некоторым вариантам реализации зкДНК содержит два ковалентно замкнутых конца.
[0097] В данном документе термин «нзДНК» или «никированная зкДНК» относится к ДНК с замкнутыми концами, содержащей одноцепочечный разрыв или пропуск размером 1-100 пар оснований в области «стебля» или спейсерной области, расположенной в 5´-направлении относительно открытой рамки считывания (например, промотора и трансгена, подлежащего экспрессии).
[0098] В данном документе термины «пропуск» и «одноцепочечный разрыв» используются взаимозаменяемо и относятся к прерванной части синтетического ДНК-вектора согласно настоящему изобретению, создавая участок части одноцепочечной ДНК в двухцепочечной в других местах зкДНК. Пропуск может иметь от 1 пары оснований до 100 пар оснований в длину в одной цепи дуплексной ДНК. Типичные пропуски, разработанные и созданные с применением способов, описанных в данном документе, и синтетические векторы, полученные с применением указанных способов, могут иметь, например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59 или 60 пар оснований в длину. Примерные пропуски в настоящем раскрытии могут иметь от 1 пары оснований до 10 пар оснований в длину, от 1 до 20 пар оснований в длину, от 1 до 30 пар оснований в длину.
[0099] Как определено в данном документе «репортеры» относятся к белкам, которые можно применять для обеспечения детектируемых показателей. Репортеры обычно производят измеряемый сигнал, такой как флуоресценция, цвет или люминесценция. Последовательности, кодирующие репортерные белки, кодируют белки, присутствие которых в клетке или в организме легко наблюдать. Например, флуоресцентные белки заставляют клетку флуоресцировать при возбуждении светом с конкретной длиной волны, люциферазы заставляют клетку катализировать реакцию, которая производит свет, а ферменты, такие как β-галактозидаза, преобразуют субстрат в окрашенный продукт. Примерные репортерные полипептиды, которые можно применять для экспериментальных или диагностических целей, включают, но не ограничиваются перечисленными, β-лактамазу, β-галактозидазу (LacZ), щелочную фосфатазу (AP), тимидинкиназу (TK), зеленый флуоресцентный белок (GFP) и другие флуоресцентные белки, хлорамфениколацетилтрансферазу (CAT), люциферазу и другие, хорошо известные в данной области техники.
[00100] В данном документе термины «смысловой» и «антисмысловой» относятся к ориентации структурного элемента на полинуклеотиде. Смысловой и антисмысловой варианты элемента обратно комплементарны друг другу.
[00101] В данном документе термин «синтетический ААВ-вектор» и «получение ААВ-вектора синтетическим путем» относится к ААВ-вектору и синтетическим способам его получения в полностью бесклеточной среде.
[00102] В данном документе «репортеры» относятся к белкам, которые можно применять для обеспечения детектируемых показателей. Репортеры обычно производят измеряемый сигнал, такой как флуоресценция, цвет или люминесценция. Последовательности, кодирующие репортерные белки, кодируют белки, присутствие которых в клетке или в организме легко наблюдать. Например, флуоресцентные белки заставляют клетку флуоресцировать при возбуждении светом с конкретной длиной волны, люциферазы заставляют клетку катализировать реакцию, которая производит свет, а ферменты, такие как β-галактозидаза, преобразуют субстрат в окрашенный продукт. Примерные репортерные полипептиды, которые можно применять для экспериментальных или диагностических целей, включают, но не ограничиваются перечисленными, β-лактамазу, β-галактозидазу (LacZ), щелочную фосфатазу (AP), тимидинкиназу (TK), зеленый флуоресцентный белок (GFP) и другие флуоресцентные белки, хлорамфениколацетилтрансферазу (CAT), люциферазу и другие, хорошо известные в данной области техники.
[00103] В данном документе термин «эффекторный белок» относится к полипептиду, который обеспечивает детектируемый показатель, либо, например, как репортерный полипептид, либо, более предпочтительно, как полипептид, уничтожающий клетку, например, токсин, или агент, придающий клетке чувствительность к уничтожению выбранным агентом или при его отсутствии. Эффекторные белки включают любой белок или пептид, который непосредственно нацелен на ДНК и/или РНК клетки-хозяина или повреждает их. Например, эффекторные белки могут включать, но не ограничиваются перечисленными, рестрикционную эндонуклеазу, которая нацелена на последовательность ДНК клетки-хозяина (будь то геномный или внехромосомный элемент), протеазу, которая расщепляет полипептид-мишень, необходимый для выживания клетки, ингибитор ДНК-гиразы и токсин рибонуклеазного типа. Согласно некоторым вариантам реализации экспрессия эффекторного белка, контролируемая синтетическим биологическим контуром, описанным в данном документе, может принимать участие в качестве фактора в другом синтетическом биологическом контуре, что расширяет диапазон и сложность восприимчивости системы биологического контура.
[00104] Транскрипционные регуляторы относятся к транскрипционным активаторам и репрессорам, которые либо активируют, либо репрессируют транскрипцию представляющего интерес гена, такого как PAH. Промоторы представляют собой области нуклеиновой кислоты, которые инициируют транскрипцию конкретного гена. Транскрипционные активаторы, как правило, связываются поблизости от транскрипционных промоторов и привлекают РНК-полимеразу для непосредственной инициации транскрипции. Репрессоры связываются с транскрипционными промоторами и стерически затрудняют инициацию транскрипции РНК-полимеразой. Другие транскрипционные регуляторы могут служить либо активаторами, либо репрессорами в зависимости от места их связывания и условий в клетке и в окружающей среде. Неограничивающие примеры классов транскрипционных регуляторов включают, но не ограничиваются перечисленными, белки гомеодомена, белки с цинковыми пальцами, белки с мотивом «крылатая спираль» (белки Forkhead) и белки с лейциновой молнией.
[00105] В данном документе «репрессорный белок» или «индукторный белок» представляет собой белок, который связывается с элементом регуляторной последовательности и репрессирует или активирует, соответственно, транскрипцию последовательностей, функционально связанных с указанным элементом регуляторной последовательности. Предпочтительные репрессорные и индукторные белки, описанные в данном документе, чувствительны к присутствию или отсутствию по меньшей мере одного вносимого агента или фактора внешней среды. Предпочтительные белки, описанные в данном документе, являются модульными по форме и содержат, например, отделяемые ДНК-связывающие и связывающие вводимые агенты, или реагирующие на них, элементы или домены.
[00106] В данном документе термин «носитель» включает любые и все возможные растворители, дисперсионные среды, основы, покрытия, разбавители, антибактериальные и противогрибковые агенты, изотонические и замедляющие абсорбцию агенты, буферы, растворы-носители, суспензии, коллоиды и т.п. Применение таких сред и агентов для фармацевтически активных веществ хорошо известно в данной области техники. В композиции также могут быть включены вспомогательные активные ингредиенты. Выражение «фармацевтически приемлемый» относится к молекулярным частицам и композициям, которые не приводят к токсической, аллергической или схожей нежелательной реакции при введении хозяину.
[00107] В данном документе термин «домен, реагирующий на вводимый агент» представляет собой домен транскрипционного фактора, который связывает или иначе отвечает на условие или вводимый агент таким способом, который придает восприимчивость присоединенного к нему ДНК-связывающего слитого домена к наличию указанного условия или вводимого агента. Согласно одному варианту реализации наличие указанного условия или вводимого агента приводит к конформационному изменению в отвечающем на вводимый агент домене, или в белке, с которым он слит, которое модифицирует модулирующую транскрипцию активность транскрипционного фактора.
[00108] Термин «in vivo» относится к анализам или способам, которые реализуют на организме или в организме, таком как многоклеточное животное. Согласно некоторым аспектам, описанным в данном документе, считается, что способ или применение реализуют «in vivo», если используется одноклеточный организм, такой как бактерия. Термин «ex vivo» относится к способам и вариантам применения, которые выполняют с использованием живой клетки с интактной мембраной, находящейся вне организма многоклеточного животного или растения, например, эксплантатов, культивируемых клеток, включая первичные клетки и линии клеток, трансформированных линий клеток, а также экстрагированных тканей или клеток, включая клетки крови, помимо прочего. Термин «in vitro» относится к анализам и способам, которые не требуют присутствия клетки с интактной мембраной, например, клеточных экстрактов, и могут относиться к введению программируемого синтетического биологического контура в бесклеточной системе, такой как среда, не содержащая клеток или клеточных систем, таких как клеточные экстракты.
[00109] В данном документе термин «промотор» относится к любой последовательности нуклеиновой кислоты, которая регулирует экспрессию другой последовательности нуклеиновой кислоты за счет управления транскрипцией указанной последовательности нуклеиновой кислоты, которая может представлять собой гетерологичный целевой ген, кодирующий белок или РНК. Промоторы могут быть конститутивными, индуцируемыми, репрессируемыми, тканеспецифическими или могут представлять собой любую комбинацию перечисленных. Промотор представляет собой контрольную область последовательности нуклеиновой кислоты, в которой осуществляется контроль инициации и скорости транскрипции остальной части последовательности нуклеиновой кислоты. Промотор также может содержать генетические элементы, с которыми могут связываться регуляторные белки и молекулы, такие как РНК-полимераза и другие транскрипционные факторы. Согласно некоторым вариантам реализации аспектов, описанных в данном документе, промотор может управлять экспрессией транскрипционного фактора, который регулирует экспрессию самого промотора. В последовательности промотора может быть расположен сайт инициации транскрипции, а также связывающие белки домены, отвечающие за связывание РНК-полимеразы. Эукариотические промоторы часто, однако не всегда, будут содержать «TATA»-боксы и «CAT»-боксы. Различные промоторы, включая индуцируемые промоторы, могут применяться для управления экспрессией трансгенов в зкДНК-векторах, раскрытых в данном документе. Последовательность промотора может быть ограничена на ее 3´-конце сайтом инициации транскрипции и простирается в восходящем направлении (в 5´-направлении), включая минимальное количество оснований или элементов, необходимых для инициации транскрипции на уровнях, детектируемых выше фона.
[00110] В данном документе термин «энхансер» относится к цис-действующей регуляторной последовательности (например, 50-1500 пар оснований), которая связывает один или более белков (например, белки-активаторы или транскрипционный фактор) для повышения транскрипционной активации последовательности нуклеиновой кислоты. Энхансеры могут быть расположены на расстоянии до 1000000 пар оснований выше сайта начала гена или ниже сайта начала гена, который они регулируют. Энхансер может быть расположен в пределах интронной области или в экзонной области неродственного гена.
[00111] Можно сказать, что промотор управляет экспрессией или управляет транскрипцией последовательности нуклеиновой кислоты, которую он регулирует. Выражения «функционально связанный», «функционально расположенный», «с функциональной связью», «под контролем» и «под транскрипционным контролем» указывают, что промотор находится в корректном функциональном положении и/или ориентации относительно последовательности нуклеиновой кислоты, которую он регулирует, для контроля инициации транскрипции и/или экспрессии указанной последовательности. В данном документе «инвертированный промотор» относится к промотору, в котором последовательность нуклеиновой кислоты располагается в обратной ориентации так, что цепь, которая была смысловой, становится некодирующей цепью, и наоборот. Последовательности инвертированных промоторов могут применяться в различных вариантах реализации для регуляции состояния переключателя. Кроме того, согласно различным вариантам реализации промотор может применяться в сочетании с энхансером.
[00112] Промотор может представлять собой промотор, который в естественных условиях ассоциирован с геном или последовательностью, а также может быть получен путем выделения некодирующих 5´-последовательностей, расположенных в 5´-направлении относительно кодирующего сегмента и/или экзона определенного гена или последовательности. Такой промотор может быть назван «эндогенным». Аналогичным образом, согласно некоторым вариантам реализации, энхансер может представлять собой энхансер, который в естественных условиях ассоциирован с последовательностью нуклеиновой кислоты и расположен либо в 3´, либо в 5´-направлении от указанной последовательности.
[00113] Согласно некоторым вариантам реализации кодирующий сегмент нуклеиновой кислоты расположен под контролем «рекомбинантного промотора» или «гетерологичного промотора», оба указанных термина относятся к промотору, который обычно не ассоциирован с кодируемой последовательностью нуклеиновой кислоты, с которой промотор функционально связан, в ее естественной среде. Рекомбинантный или гетерологичный энхансер относится к энхансеру, обычно не ассоциированному с конкретной последовательностью нуклеиновой кислоты в ее естественной среде. Такие промоторы или энхансеры могут включать промоторы или энхансеры других генов; промоторы или энхансеры, выделенные из любой другой прокариотической, вирусной или эукариотической клетки; и синтетические промоторы или энхансеры, которые не являются «природными», т. е. содержат различные элементы разных транскрипционных регуляторных областей и/или изменяющие экспрессию мутации, введенные с применением способов генетического конструирования, известных в данной области техники. Наряду с получением последовательностей нуклеиновых кислот промоторов и энхансеров синтетическим путем, последовательности промоторов могут быть получены с использованием рекомбинантного клонирования и/или технологии амплификации нуклеиновых кислот, включая ПЦР, применительно к синтетическим биологическим контурам и модулям, раскрытым в данном документе (см., например, патент США № 4683202, патент США № 5928906, каждый из которых включен в данный документ посредством ссылки). Кроме того, также предусмотрена возможность применения контрольных последовательностей, которые управляют транскрипцией и/или экспрессией последовательностей в неядерных органеллах, таких как митохондрии, хлоропласты и т.п.
[00114] Как описано в данном документе, «индуцируемый промотор» представляет собой промотор, который характеризуется инициацией или усилением транскрипционной активности в присутствии, под влиянием или при контакте с индуктором или индуцирующим агентом. «Индуктор» или «индуцирующий агент», как определено в данном документе, может быть эндогенным или обычно является экзогенным соединением или белком, которые вводят таким образом, чтобы обеспечить их активность по индукции транскрипционной активности индуцируемого промотора. Согласно некоторым вариантам реализации индуктор или индуцирующий агент, т. е. химическое вещество, соединение или белок, сам может быть получен в результате транскрипции или экспрессии последовательности нуклеиновой кислоты (т. е. индуктор может представлять собой индукторный белок, экспрессируемый другим компонентом или модулем), который сам может находиться под контролем индуцируемого промотора. Согласно некоторым вариантам реализации индуцируемый промотор индуцируется в отсутствие определенных агентов, таких как репрессор. Примеры индуцируемых промоторов включают, но не ограничиваются перечисленными, чувствительные к тетрациклину, металлотионину, экдизону промоторы, промоторы вирусов млекопитающих (например, поздний промотор аденовируса; и промотор длинного концевого повтора вируса опухоли молочной железы мышей (MMTV-LTR)) и другие чувствительные к стероидам промоторы, чувствительные к рапамицину промоторы и т.п.
[00115] Термины «регуляторные последовательности ДНК», «контрольные элементы» и «регуляторные элементы», используемые в данном документе взаимозаменяемо, относятся к транскрипционным и трансляционным контрольным последовательностям, таким как промоторы, энхансеры, сигналы полиаденилирования, терминаторы, сигналы разрушения белка и т.п., которые обеспечивают и/или регулируют транскрипцию некодирующей последовательности (например, нацеливающей на ДНК РНК) или кодирующей последовательности (например, сайт-направленного модифицирующего полипептида или полипептида Cas9/Csn1) и/или регулируют трансляцию кодируемого полипептида.
[00116] «Функционально связанный» относится к размещению в непосредственной близости, при котором описываемые так компоненты находятся во взаимосвязи, позволяющей им функционировать предусмотренным для них образом. Например, промотор функционально связан с кодирующей последовательностью, если указанный промотор влияет на ее транскрипцию или экспрессию. «Экспрессионная кассета» включает гетерологичную последовательность ДНК, которая функционально связана с промотором или другой регуляторной последовательностью, достаточными для управления транскрипцией трансгена в зкДНК-векторе. Подходящие промоторы включают, например, тканеспецифические промоторы. Промоторы также могут происходить из ААВ.
[00117] В данном документе термин «субъект» относится к человеку или животному, которому предоставляют лечение, включая профилактическое лечение, с применением зкДНК-вектора в соответствии с настоящим изобретением. Обычно животное представляет собой позвоночное животное, такое как, но не ограничиваясь перечисленными, примат, грызун, домашнее животное или промысловое животное. Приматы включают, но не ограничиваются перечисленными, шимпанзе, яванских макак, коат и макак, например, макак-резусов. Грызуны включают мышей, крыс, сурков, хорьков, кроликов и хомяков. Домашние и промысловые животные включают, но не ограничиваются перечисленными, коров, лошадей, свиней, оленей, бизона, буйвола, виды кошачьих, например, домашнюю кошку, виды собачьих, например, собаку, лису, волка, виды птиц, например, курицу, эму, страуса, и рыб, например, форель, сома и лосося. В определенных вариантах реализации аспектов, описанных в данном документе, субъект представляет собой млекопитающее, например, примата или человека. Субъект может быть мужского или женского пола. Кроме того, субъект может быть младенцем или ребенком. Согласно некоторым вариантам реализации субъект может представлять собой новорожденного или нерожденного субъекта, например, субъекта in utero. Предпочтительно субъект представляет собой млекопитающее. Млекопитающее может представлять собой человека, не являющегося человеком примата, мышь, крысу, собаку, кошку, лошадь или корову, однако указанные примеры не являются ограничивающими. Млекопитающие, отличные от человека, могут быть предпочтительно использованы в качестве субъектов в моделях заболеваний и нарушений на животных. Кроме того, способы и композиции, описанные в данном документе, могут быть использованы для одомашненных животных и/или животных-компаньонов. Человек-субъект может быть любого возраста, пола, расы или этнической группы, например, может быть европеоидом (белым), азиатом, африканцем, черным, афроамериканцем, афроевропейцем, испаноамериканцем, представителем ближневосточного этноса и т. д. Согласно некоторым вариантам реализации субъект может представлять собой пациента или другого субъекта в клинических условиях. Согласно некоторым вариантам реализации субъект уже проходит курс лечения. Согласно некоторым вариантам реализации субъект представляет собой эмбрион, плод, новорожденного, младенца, ребенка, подростка или взрослую особь. Согласно некоторым вариантам реализации субъект представляет собой плод человека, новорожденного человека, младенца-человека, ребенка-человека, подростка-человека или взрослого человека. Согласно некоторым вариантам реализации субъект представляет собой эмбрион животного или эмбрион, не принадлежащий человеку, или эмбрион примата, не являющегося человеком. Согласно некоторым вариантам реализации субъект представляет собой эмбрион человека.
[00118] В данном документе термин «клетка-хозяин» включает любой тип клеток, которые являются восприимчивыми к трансформации, трансфекции, трансдукции и т.п. с использованием конструкции нуклеиновой кислоты или зкДНК-вектора для экспрессии согласно настоящему изобретению. В качестве неограничивающих примеров, клетка-хозяин может представлять собой выделенную первичную клетку, плюрипотентные стволовые клетки, CD34+ клетки, индуцированные плюрипотентные стволовые клетки или любую из ряда иммортализованных клеточных линий (например, клетки HepG2). В качестве альтернативы, клетка-хозяин может представлять собой клетку in situ или in vivo в ткани, органе или организме.
[00119] Термин «экзогенный» относится к веществу, присутствующему в клетке, отличной от его природного источника. В данном документе термин «экзогенный» может относиться к нуклеиновой кислоте (например, нуклеиновой кислоте, кодирующей полипептид) или к полипептиду, которые были введены посредством процесса, включающего действия человека, в биологическую систему, такую как клетка или организм, в которой они обычно не обнаруживаются, и введение нуклеиновой кислоты или полипептида в такую клетку или организм является желательным. В качестве альтернативы, «экзогенный» может относиться к нуклеиновой кислоте или полипептиду, которые были введены посредством процесса, включающего действия человека, в биологическую систему, такую как клетка или организм, в которой они обнаруживаются в относительно низких количествах, и увеличение количества нуклеиновой кислоты или полипептида в клетке или организме является желательным, например, для получения эктопической экспрессии или уровней. В отличие от этого термин «эндогенный» относится к веществу, которое является нативным для биологической системы или клетки.
[00120] Термин «идентичность последовательности» относится к сродству между двумя нуклеотидными последовательностями. Для целей настоящего раскрытия степень идентичности последовательностей между двумя дезоксирибонуклеотидными последовательностями определяется с использованием алгоритма Нидлмана-Вунша (Needleman and Wunsch, 1970, выше), реализованного в программе Needle пакета EMBOSS (EMBOSS: The European Molecular Biology Open Software Suite, Rice et al., 2000, выше), предпочтительно, версии 3.0.0 или более поздней. Используемые необязательные параметры представляют собой штраф за открытие пропуска 10, штраф за продление пропуска 0,5 и матрицу замены EDNAFULL (версия EMBOSS NCBI NUC4.4). Выходной показатель Needle, называемый «наибольшей длиной идентичного фрагмента» (полученный с применением опции «-nobrief») используют в качестве процента идентичности и вычисляют следующим образом: (Идентичные дезоксирибонуклеотиды ×100)/(Длина выравнивания - Общее число пропусков в выравнивании). Длина выравнивания составляет предпочтительно по меньшей мере 10 нуклеотидов, предпочтительно по меньшей мере 25 нуклеотидов, более предпочтительно по меньшей мере 50 нуклеотидов и наиболее предпочтительно по меньшей мере 100 нуклеотидов.
[00121] В данном документе термин «гомология» или «гомологичный» определяется как процент нуклеотидных остатков, которые идентичны нуклеотидным остаткам в соответствующей последовательности на хромосоме-мишени после выравнивания последовательностей и введения пробелов, при необходимости, для достижения максимального процента идентичности последовательностей. Выравнивание с целью определения процента гомологии нуклеотидной последовательности может быть достигнуто различными путями, известными в данной области техники, например, с применением общедоступного компьютерного программного обеспечения, такого как программное обеспечение BLAST, BLAST-2, ALIGN, ClustalW2 или Megalign (DNASTAR). Специалисты в данной области техники могут определить соответствующие параметры для выравнивания последовательностей, включая любые алгоритмы, необходимые для достижения максимального выравнивания по всей длине сравниваемых последовательностей. Согласно некоторым вариантам реализации последовательность нуклеиновой кислоты (например, последовательность ДНК), например, гомологичное плечо, считается «гомологичной», когда последовательность по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 91%, по меньшей мере на 92%, по меньшей мере на 93%, по меньшей мере на 94%, по меньшей мере на 95%, по меньшей мере на 96%, по меньшей мере на 97%, по меньшей мере на 98%, по меньшей мере на 99% или более идентична соответствующей нативной или неотредактированной последовательности нуклеиновой кислоты (например, геномной последовательности) клетки-хозяина.
[00122] В данном документе термин «гетерологичный» означает нуклеотидную или полипептидную последовательность, которая не обнаружена в нативной нуклеиновой кислоте или белке, соответственно. Гетерологичная последовательность нуклеиновой кислоты может быть связана с природной последовательностью нуклеиновой кислоты (или ее вариантом) (например, путем генетического конструирования) с получением химерной нуклеотидной последовательности, кодирующей химерный полипептид. Гетерологичная последовательность нуклеиновой кислоты может быть соединена с вариантом полипептида (например, путем генетического конструирования) с получением нуклеотидной последовательности, кодирующей слитый вариант полипептида.
[00123] «Вектор» или «экспрессионный вектор» представляет собой репликон, такой как плазмида, бакмида, фаг, вирус, вирион или космида, к которому может быть присоединен другой сегмент ДНК, т. е. «вставка», чтобы вызвать репликацию присоединенного сегмента в клетке. Вектор может представлять собой конструкцию нуклеиновой кислоты, разработанную для доставки в клетку-хозяина или для переноса между разными клетками-хозяевами. В данном документе вектор может быть вирусным или невирусным по происхождению и/или в конечной форме, однако для цели настоящего раскрытия «вектор» обычно относится к зкДНК-вектору в соответствии с использованием этого термина в данном документе. Термин «вектор» включает любой генетический элемент, который способен к репликации, когда он ассоциирован с надлежащими контрольными элементами, и который может переносить генные последовательности в клетки. Согласно некоторым вариантам реализации вектор может представлять собой экспрессионный вектор или рекомбинантный вектор.
[00124] В данном документе термин «экспрессионный вектор» относится к вектору, который управляет экспрессией РНК или полипептида с последовательностей, связанных с транскрипционными регуляторными последовательностями на векторе. Экспрессируемые последовательности часто, но не обязательно, будут гетерологичными по отношению к клетке. Экспрессионный вектор может содержать дополнительные элементы, например, экспрессионный вектор может иметь две системы репликации, что позволяет поддерживать его в двух организмах, например, в клетках человека для экспрессии и в прокариотическом хозяине для клонирования и амплификации. Термин «экспрессия» относится к клеточным процессам, участвующим в продуцировании РНК и белков и, в соответствующих случаях, в секретировании белков, включая, где это применимо, но не ограничиваясь этим, например, транскрипцию, процессинг транскрипта, трансляцию и укладку, модификацию и процессинг белка. «Продукты экспрессии» включают РНК, транскрибированную с гена, и полипептиды, полученные путем трансляции мРНК, транскрибированной с гена. Термин «ген» означает последовательность нуклеиновой кислоты, которая транскрибируется (ДНК) в РНК in vitro или in vivo, когда она функционально связана с соответствующими регуляторными последовательностями. Ген может включать, но не обязательно, области, предшествующие кодирующей области и следующие за ней, например, 5´-нетранслируемые (5´-UTR) или «лидерные» последовательности и 3´-UTR или «трейлерные» последовательности, а также промежуточные последовательности (интроны) между отдельными кодирующими сегментами (экзонами).
[00125] Под «рекомбинантным вектором» подразумевается вектор, который включает гетерологичную последовательность нуклеиновой кислоты или «трансген», который способен к экспрессии in vivo. Следует понимать, что векторы, описанные в данном документе, в некоторых вариантах реализации, можно комбинировать с другими подходящими композициями и видами терапии. Согласно некоторым вариантам реализации вектор является эписомальным. Применение подходящего эписомального вектора обеспечивает средство поддержания представляющего интерес нуклеотида у субъекта в многокопийной внехромосомной ДНК, что устраняет потенциальные эффекты интеграции в хромосому.
[00126] В данном документе выражение «генетическое заболевание» относится к заболеванию, частично или полностью, прямо или опосредованно, вызванному одной или более аномалиями в геноме, в частности, к состоянию, присутствующему с момента рождения. Аномалия может представлять собой мутацию, вставку или делецию. Аномалия может влиять на кодирующую последовательность гена или его регуляторную последовательность. Генетическое заболевание может представлять собой, но не ограничивается перечисленными, ФКУ, мышечную дистрофию Дюшенна (МДД), гемофилию, муковисцидоз, хорею Хантингтона, семейную гиперхолестеринемию (дефект рецептора ЛПНП), гепатобластому, болезнь Вильсона, врожденную печеночную порфирию, наследственные нарушения метаболизма печени, синдром Леша-Нихана, серповидноклеточную анемию, талассемии, пигментную ксеродерму, анемию Фанкони, пигментный ретинит, атаксию-телеангиэктазию, синдром Блума, ретинобластому и болезнь Тея-Сакса.
[00127] В данном документе термин «ингибирующий полинуклеотид» относится к молекуле ДНК или РНК, которая уменьшает или предотвращает экспрессию (транскрипцию или трансляцию) второго (целевого) полинуклеотида. Ингибирующие полинуклеотиды включают антисмысловые полинуклеотиды, рибозимы и внешние направляющие последовательности. Термин «ингибирующий полинуклеотид» дополнительно включает молекулы ДНК и РНК, например, РНКи, которые кодируют существующие ингибирующие молекулы, такие как молекулы ДНК, которые кодируют рибозимы.
[00128] В данном документе «подавление гена» или «подавленный ген» в отношении активности молекулы РНКи, например, киРНК или миРНК, относится к снижению в клетке уровня мРНК гена-мишени.
[00129] В данном документе термин «РНКи» относится к любому типу интерферирующей РНК, включая, но не ограничиваясь перечисленными, киРНКи, кшРНКи, эндогенную микроРНК и искусственную микроРНК. Например, он включает последовательности, ранее идентифицированные как киРНК, независимо от механизма последующего процессинга РНК (т. е., несмотря на то, что киРНК, как полагают, имеют специфичный способ процессинга in vivo, приводящий к расщеплению мРНК, такие последовательности могут быть включены в векторы между фланкирующими последовательностями, описанными в данном документе). Термин «РНКи» может включать как молекулы РНКи, подавляющие ген, так и эффекторные молекулы РНКи, которые активируют экспрессию гена. Только в качестве примера, согласно некоторым вариантам реализации агенты РНКи, которые служат для ингибирования или подавления гена, можно применять в способах, наборах и композициях, раскрытых в данном документе, например, для ингибирования иммунного ответа (например, врожденного иммунного ответа).
[00130] В данном документе термин «содержащий» или «содержит» используется в отношении композиций, способов и их соответствующего компонента (компонентов), существенных для указанного способа или композиции, но допускающих включение не указанных элементов, будь то существенных или нет.
[00131] В данном документе термин «состоящий по существу из» относится к элементам, необходимым для конкретного варианта реализации. Термин допускает наличие элементов, которые не влияют существенным образом на основную и новую или функциональную характеристику (характеристики) указанного варианта реализации. Использование термина «содержащий» указывает на включение, а не на ограничение.
[00132] Термин «состоящий из» относится к композициям, способам и их соответствующим компонентам, описанным в данном документе, которые не включают никаких элементов, не перечисленных в указанном описании варианта реализации.
[00133] В данном документе термин «состоящий по существу из» относится к элементам, необходимым для конкретного варианта реализации. Термин допускает наличие дополнительных элементов, которые не оказывают существенного влияния на основную и новую или функциональную характеристику (характеристики) указанного варианта реализации настоящего изобретения.
[00134] В настоящем описании и прилагаемой формуле изобретения термины в единственном числе (соотв. «a», «an» и «the» в исходном тексте на английском языке) включают их эквиваленты во множественном числе, если иное явным образом не следует из контекста. Соответственно, например, ссылка на «способ» включает один или более способов и/или этапов типа, описанного в данном документе, и/или таких, которые будут понятны специалистам в данной области техники после прочтения настоящего раскрытия, и т.п. Аналогичным образом, предусмотрено, что термин «или» включает «и», если из контекста явным образом не следует иное. Несмотря на то, что при практической реализации или тестировании настоящего раскрытия могут применяться способы и материалы, сходные или эквивалентные тем, которые описаны в данном документе, ниже описаны подходящие способы и материалы. В данном документе «например» (сокращение «e.g.» в исходном тексте на английском языке, произошедшее от латинского выражения «exempli gratia») указывает на неограничивающий пример. Соответственно, «например» синонимично термину «к примеру».
[00135] Группы альтернативных элементов или вариантов реализации настоящего изобретения, раскрытых в данном документе, не должны рассматриваться как ограничения. На каждый член группы можно ссылаться и заявлять его индивидуально или в любой комбинации с другими членами группы или другими элементами, представленными в данном документе. Один или более членов группы могут быть включены или исключены из группы по соображениям удобства и/или патентоспособности. При любом таком включении или исключении в данном документе считается, что описание изобретения содержит группу, измененную таким образом, чтобы она удовлетворяла условию письменного описания всех групп Маркуша, используемых в прилагаемой формуле изобретения.
[00136] Согласно некоторым вариантам реализации любого из аспектов раскрытие, описанное в данном документе, не касается способа клонирования людей, способов модификации генетической идентичности зародышевой линии человека, вариантов применения эмбрионов человека в промышленных или коммерческих целях, или способов модификации генетической идентичности животных, которые могут причинить им страдания без какой-либо существенной медицинской пользы для человека или животного, а также животных, полученных с помощью таких способов.
[00137] Определения других терминов приведены в данном документе в описании различных аспектов настоящего изобретения.
[00138] Все патенты и другие публикации; включая литературные ссылки, выданные патенты, опубликованные заявки на патент и заявки на патент, находящиеся на рассмотрении одновременно с настоящей заявкой; упомянутые в настоящем описании, явным образом включены в данный документ посредством ссылки с целью описания и раскрытия, например, методологий, описанных в таких публикациях, которые могут быть использованы в связи с технологией, описанной в данном документе. Эти публикации представлены исключительно по причине их раскрытия до даты подачи настоящей заявки. Ничто в этом отношении не должно истолковываться как признание того, что авторы изобретения не обладают правами на более раннее изобретение по отношению к такому раскрытию в силу предшествующего изобретения или по любой другой причине. Все утверждения, касающиеся дат, или представления относительно содержания этих документов основаны на информации, доступной заявителям, и не являются допущением каким-либо образом признания правильности дат или содержания этих документов.
[00139] Описание вариантов реализации настоящего раскрытия не должно рассматриваться как исчерпывающее или ограничивающее настоящее раскрытие точной раскрытой формой. Несмотря на то, что в данном документе в иллюстративных целях описаны конкретные варианты реализации и примеры раскрытия, возможны различные эквивалентные модификации в пределах объема раскрытия, как будет понятно специалистам в соответствующей области техники. Например, хотя этапы или функции способа представлены в указанном порядке, согласно альтернативным вариантам реализации функции могут выполняться в другом порядке, или функции могут выполняться по существу одновременно. Принципиальные положения настоящего раскрытия, предоставленные в данном документе, могут быть применены к другим процедурам или способам в зависимости от ситуации. Различные варианты реализации, описанные в данном документе, могут быть объединены для обеспечения дополнительных вариантов реализации. Аспекты настоящего раскрытия могут быть модифицированы, при необходимости, для применения композиций, функций и концепций вышеупомянутых ссылок и приложения для обеспечения дополнительных вариантов реализации настоящего раскрытия. Кроме того, из соображений биологической функциональной эквивалентности могут быть сделаны некоторые изменения в структуре белка, не влияющие на биологическое или химическое действие в качественном или количественном отношении. Эти и другие изменения могут быть выполнены в раскрытии в свете подробного описания. Все такие модификации предусмотрены, как включенные в объем прилагаемой формулы изобретения.
[00140] Конкретные элементы любого из вышеприведенных вариантов реализации могут быть объединены или заменены элементами других вариантов реализации. Кроме того, хотя преимущества, ассоциированные с некоторыми вариантами реализации настоящего раскрытия, были описаны в контексте этих вариантов реализации, другие варианты реализации также могут демонстрировать такие преимущества, и не все варианты реализации должны обязательно демонстрировать такие преимущества, чтобы попадать в объем раскрытия.
[00141] Описанная в данном документе технология дополнительно иллюстрируется следующими примерами, которые никоим образом не следует истолковывать как дополнительные ограничения. Следует понимать, что настоящее изобретение не ограничено конкретной методологией, протоколами и реагентами, и т. д., описанными в данном документе, и поэтому допускает варианты. Терминология, используемая в данном документе, предназначена исключительно для описания конкретных вариантов реализации и не предназначена для ограничения объема настоящего изобретения, который определен исключительно формулой изобретения.
I. Экспрессия белка PAH с ДНК-вектора с замкнутыми концами (зкДНК)
[00142] Технология, описанная в данном документе, в целом направлена на экспрессию и/или продукцию белка PAH в клетке с невирусного ДНК-вектора, например, зкДНК-вектора, описанного в данном документе. ЗкДНК-векторы для экспрессии белка PAH описаны в данном документе в разделе, озаглавленном «зкДНК-векторы в целом». В частности, зкДНК-векторы для экспрессии белка PAH содержат пару ITR (например, симметричных или асимметричных, как описано в данном документе), а между парой ITR содержат нуклеиновую кислоту, кодирующую белок PAH, как описано в данном документе, функционально связанную с промотором или регуляторной последовательностью. Отличительным преимуществом зкДНК-векторов для экспрессии белка PAH по сравнению с обычными ААВ-векторами и даже лентивирусными векторами является отсутствие ограничения по размеру для гетерологичных последовательностей нуклеиновых кислот, кодирующих целевой белок. Таким образом, даже полноразмерный белок PAH размером 6,8 тыс. п. о. может быть экспрессирован с одного зкДНК-вектора. Таким образом, зкДНК-векторы, описанные в данном документе, можно применять для экспрессии терапевтического белка PAH у субъекта, нуждающегося в этом, например, субъекта, страдающего ФКУ.
[00143] Как будет понятно, технологии зкДНК-векторов, описанные в данном документе, могут быть адаптированы к любому уровню сложности или могут применяться модульно, причем экспрессия различных компонентов белка PAH может контролироваться независимо. Например, конкретно предусмотрено, что технологии зкДНК-векторов, разработанные в данном документе, могут быть простыми, как применение одного зкДНК-вектора для экспрессии одной гетерологичной генной последовательности (например, белка PAH), или могут быть сложными, как применение нескольких зкДНК-векторов, когда каждый вектор экспрессирует несколько белков PAH или ассоциированных кофакторов, или вспомогательных белков, каждый из которых независимо контролируется разными промоторами. Варианты реализации ниже конкретно предусмотрены в данном документе и могут быть адаптированы специалистом в данной области техники при необходимости.
[00144] Согласно одному варианту реализации один зкДНК-вектор можно применять для экспрессии одного компонента белка PAH. В качестве альтернативы, один зкДНК-вектор можно применять для экспрессии нескольких компонентов (например, по меньшей мере 2) белка PAH под контролем одного промотора (например, сильного промотора), необязательно с использованием последовательности (ей) IRES, чтобы обеспечить надлежащую экспрессию каждого из компонентов, например, кофакторов или вспомогательных белков.
[00145] В данном документе также предусмотрен, в другом варианте реализации, один зкДНК-вектор, содержащий по меньшей мере две вставки (например, экспрессирующие тяжелую цепь или легкую цепь), причем экспрессия каждой вставки находится под контролем ее собственного промотора. Промоторы могут включать несколько копий одного и того же промотора, несколько разных промоторов или любую их комбинацию. Специалист в данной области техники поймет, что желательной часто является экспрессия компонентов белка PAH на разных уровнях экспрессии, что позволяет контролировать стехиометрию отдельных экспрессируемых компонентов для обеспечения эффективного укладывания и комбинирования белка PAH в клетке.
[00146] Специалист в данной области техники может предусмотреть дополнительные варианты технологий зкДНК-векторов или адаптировать их из методов получения белка с использованием стандартных векторов.
A. Нуклеиновые кислоты
[00147] В данном документе предложена характеристика и разработка молекул нуклеиновых кислот для потенциального терапевтического применения. В соответствии с некоторыми вариантами реализации нуклеиновые кислоты для терапевтического применения кодируют белок PAH. Согласно некоторым вариантам реализации в соответствующих случаях описана химическая модификация олигонуклеотидов с целью изменения и улучшения свойств in vivo (доставки, стабильности, времени жизни, укладки, специфичности в отношении мишени), а также их биологической функции и механизма, которые напрямую коррелируют с терапевтическим приложением.
[00148] Иллюстративные терапевтические нуклеиновые кислоты согласно настоящему раскрытию, которые могут быть иммуностимулирующими и требуют применения иммуносупрессоров, раскрытых в данном документе, могут включать, но не ограничиваются перечисленными, минигены, плазмиды, миникольца, короткую интерферирующую РНК (киРНК), микроРНК (миРНК), антисмысловые олигонуклеотиды (ASO), рибозимы, двухцепочечную ДНК с замкнутыми концами (например, зкДНК, CELiD, линейную ковалентно замкнутую ДНК («с минимальной цепью»), doggybone (dbDNA™), протеломерную ДНК с замкнутыми концами или гантелеобразную линейную ДНК), дцРНК-субстрат Dicer, короткую шпилечную РНК (кшРНК), асимметричную интерферирующую РНК (аиРНК), микроРНК (миРНК), мРНК, тРНК, рРНК и вирусные ДНК-векторы, вирусный РНК-вектор; и любую их комбинацию.
[00149] киРНК или миРНК, которые могут отрицательно регулировать внутриклеточные уровни конкретных белков посредством процесса, называемого РНК-интерференцией (РНКи), также предусмотрены настоящим изобретением в качестве терапевтических средств на основе нуклеиновых кислот. После введения киРНК или миРНК в цитоплазму клетки-хозяина указанные конструкции двухцепочечной РНК связываются с белком, называемым RISC. Комплекс RISC удаляет смысловую цепь киРНК или миРНК. Комплекс RISC в комбинации с комплементарной мРНК расщепляет мРНК и высвобождает разрезанные цепи. РНКи осуществляется путем индукции специфичного разрушения мРНК, что приводит к отрицательной регуляции соответствующего белка.
[00150] Антисмысловые олигонуклеотиды (ASO) и рибозимы, которые ингибируют трансляцию мРНК в белок, могут представлять собой терапевтические средства на основе нуклеиновых кислот. В случае антисмысловых конструкций указанные одноцепочечные дезоксинуклеиновые кислоты имеют последовательность, комплементарную последовательности мРНК целевого белка, и способны связываться с мРНК посредством спаривания оснований по Уотсону-Крику. Такое связывание предотвращает трансляцию целевой мРНК и/или запускает разрушение транскрипта мРНК РНКазой H. В результате антисмысловой олигонуклеотид имеет повышенную специфичность действия (т. е. отрицательную регуляцию специфического белка, связанного с заболеванием).
[00151] Согласно любому из способов, предложенных в данном документе, терапевтическая нуклеиновая кислота может представлять собой терапевтическую РНК. Терапевтическая РНК может представлять собой ингибитор трансляции мРНК, агент РНК-интерференции (РНКи), каталитически активную молекулу РНК (рибозим), транспортную РНК (тРНК) или РНК, которая связывает транскрипт мРНК (ASO), белок или другой молекулярный лиганд (аптамер). Согласно любому из способов, предложенных в данном документе, агент РНКи может представлять собой двухцепочечную РНК, одноцепочечную РНК, микроРНК, короткую интерферирующую РНК, короткую шпилечную РНК или образующий триплекс олигонуклеотид.
[00152] В соответствии с некоторыми вариантами реализации терапевтическая нуклеиновая кислота представляет собой двухцепочечную ДНК с замкнутыми концами, например, зкДНК. В соответствии с некоторыми вариантами реализации экспрессия и/или продукция терапевтического белка в клетке происходит с невирусного ДНК-вектора, например, зкДНК-вектора. Отличительным преимуществом зкДНК-векторов для экспрессии терапевтического белка по сравнению с обычными ААВ-векторами и даже лентивирусными векторами является отсутствие ограничения по размеру для гетерологичных последовательностей нуклеиновых кислот, кодирующих целевой белок. Таким образом, даже большой терапевтический белок может быть экспрессирован с одного зкДНК-вектора. Таким образом, зкДНК-векторы можно применять для экспрессии терапевтического белка у субъекта, нуждающегося в этом.
[00153] В общем случае зкДНК-вектор для экспрессии терапевтического белка, раскрытый в данном документе, содержит, в направлении от 5´ к 3´: первый инвертированный концевой повтор (ITR) аденоассоциированного вируса (ААВ), нуклеотидную последовательность, представляющую интерес (например, экспрессионную кассету, описанную в данном документе), и второй ITR ААВ. Последовательности ITR выбирают из любых из: (i) по меньшей мере одного WT-ITR и по меньшей мере одного модифицированного инвертированного концевого повтора (mod-ITR) ААВ (например, асимметричных модифицированных ITR); (ii) двух модифицированных ITR, причем пара mod-ITR имеет различную трехмерную пространственную организацию по отношению друг к другу (например, асимметричные модифицированные ITR), или (iii) пары симметричных или по существу симметричных WT-WT-ITR, причем каждый WT-ITR имеет одинаковую трехмерную пространственную организацию, или (iv) пары симметричных или по существу симметричных модифицированных ITR, причем каждый mod-ITR имеет одинаковую трехмерную пространственную организацию.
[00154] Согласно некоторым вариантам реализации трансген, кодирующий белок PAH, также кодирует секреторную последовательность так, что белок PAH направляется в аппарат Гольджи и эндоплазматический ретикулум (ЭР), где будет происходить укладка белка PAH в правильную конформацию молекулами-шаперонами при его прохождении через ЭР и высвобождении из клетки. Примерные секреторные последовательности включают, но не ограничиваются перечисленными, VH-02 (SEQ ID NO: 88) и VK-A26 (SEQ ID NO: 89) и сигнальную последовательность Igκ (SEQ ID NO: 126), а также секреторный сигнал Gluc, обеспечивающий секрецию меченого белка из цитозоля (SEQ ID NO: 188), секреторную последовательность TMD-ST, которая направляет меченый белок в аппарат Гольджи (SEQ ID NO: 189).
[00155] Регуляторные переключатели также можно использовать для точной настройки экспрессии белка PAH так, что белок PAH экспрессируется предусмотренным образом, включая, но не ограничиваясь этим, экспрессию белка PAH на целевом уровне экспрессии или в целевом количестве, или, в качестве альтернативы, в присутствии или в отсутствие конкретного сигнала, включая событие клеточной передачи сигнала. Например, как описано в данном документе, экспрессия белка PAH с зкДНК-вектора может быть включена или выключена при возникновении конкретного состояния, как описано в разделе данного документа, озаглавленном «Регуляторные переключатели».
[00156] Например, и только в целях иллюстрации, белки PAH можно применять для выключения нежелательной реакции, такой как слишком высокий уровень продукции белка PAH. Ген PAH может содержать сигнальный пептидный маркер для доставки белка PAH в целевую клетку. Однако в любой ситуации может быть желательно регулировать экспрессию белка PAH. ЗкДНК-векторы легко приспосабливаются к использованию регуляторных переключателей.
[00157] Отличительным преимуществом зкДНК-векторов по сравнению с обычными ААВ-векторами и даже лентивирусными векторами является отсутствие ограничения по размеру для гетерологичных последовательностей нуклеиновых кислот, кодирующих белок PAH. Таким образом, даже полноразмерный PAH, а также необязательно любые кофакторы или вспомогательные белки могут быть экспрессированы с одного зкДНК-вектора. Кроме того, в зависимости от необходимой стехиометрии можно экспрессировать несколько сегментов одного и того же белка PAH и можно использовать один и тот же или разные промоторы, а также можно использовать регуляторные переключатели для точной настройки экспрессии каждой области. Например, как показано в Примерах, можно применять зкДНК-вектор, который содержит двойную промоторную систему, так, что для каждого домена белка PAH используется разный промотор. Применение зкДНК-плазмиды для получения белка PAH может включать уникальную комбинацию промоторов для экспрессии доменов белка PAH, что приводит к правильному соотношению каждого домена для образования функционального белка PAH. Соответственно, в некоторых вариантах реализации, зкДНК-вектор можно применять для экспрессии различных областей белка PAH по отдельности (например, под контролем другого промотора).
[0015] Согласно другому варианту реализации белок PAH, экспрессируемый с зкДНК-векторов, дополнительно содержит дополнительную функциональную возможность, такую как флуоресценция, ферментативная активность, сигнал секреции или активатор иммунных клеток.
[00159] Согласно некоторым вариантам реализации зкДНК, кодирующая белок PAH, может дополнительно содержать линкерный домен, например. В данном документе «линкерный домен» относится к олиго- или полипептидной области от примерно 2 до 100 аминокислот в длину, которая связывает любые домены/области белка PAH, описанного в данном документе. Согласно некоторым вариантам реализации линкеры могут включать или могут состоять из гибких остатков, таких как глицин и серин, так, что смежные белковые домены могут свободно перемещаться относительно друг друга. Более длинные линкеры могут использоваться, когда желательно гарантировать, что два смежных домена не будут стерически мешать друг другу. Линкеры могут быть расщепляемыми или нерасщепляемыми. Примеры расщепляемых линкеров включают линкеры 2А (например, Т2А), 2А-подобные линкеры или их функциональные эквиваленты и их комбинации. Линкер может представлять собой линкерную область T2A, происходящую из вируса Thosea asigna.
[00160] Специалист в данной области техники может взять известную и/или общедоступную последовательность белка, например, PAH и т. д., и выполнить обратное конструирование последовательности кДНК для кодирования такого белка. Затем кДНК может быть оптимизирована по кодонам, чтобы соответствовать предусмотренной клетке-хозяину, и вставлена в зкДНК-вектор, как описано в данном документе.
B. зкДНК-векторы, экспрессирующие белок PAH
[00161] зкДНК-вектор для экспрессии белка PAH, имеющий одну или более последовательностей, кодирующих целевой PAH, может содержать регуляторные последовательности, такие как промоторы, сигналы секреции, области поли(А) и энхансеры. По меньшей мере, зкДНК-вектор содержит одну или более гетерологичных последовательностей, кодирующих белок PAH.
[00162] Для достижения высокоэффективной и точной сборки белка PAH в некоторых вариантах реализации конкретно предусмотрено, что белок PAH содержит лидерную последовательность для эндоплазматического ретикулума (ЭР) для направления его в ЭР, где происходит укладка белка. Например, последовательность, которая направляет экспрессированный белок (белки) в ЭР для укладки.
[00163] Согласно некоторым вариантам реализации сигнал клеточной или внеклеточной локализации (например, секреторный сигнал, сигнал ядерной локализации, сигнал митохондриальной локализации и т. д.) содержится в зкДНК-векторе, чтобы направлять секрецию или целевую субклеточную локализацию PAH так, что белок PAH может связываться с внутриклеточной мишенью (мишенями) (например, внутри тела) или внеклеточной мишенью (мишенями).
[00164] Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH, описанный в данном документе, обеспечивает сборку и экспрессию любого целевого белка PAH модульным способом. В данном документе термин «модульный» относится к элементам в зкДНК-экспрессирующей плазмиде, которые можно легко удалить из конструкции. Например, модульные элементы в зкДНК-генерирующей плазмиде, содержат уникальные пары сайтов рестрикции, фланкирующие каждый элемент в конструкции, что обеспечивает исключительное манипулирование отдельными элементами (см., например, ФИГ. 1A-1G). Таким образом, платформа зкДНК-вектора может обеспечивать экспрессию и сборку любой целевой конфигурации белка PAH. В данном документе в различных вариантах реализации предложены плазмидные зкДНК-векторы, которые могут уменьшить и/или минимизировать количество манипуляций, необходимых для сборки целевого зкДНК-вектора, кодирующего белок PAH.
C. Примерные белки PAH, экспрессируемые зкДНК-векторами
[00165] В частности, зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, может кодировать, например, но не ограничиваясь перечисленными, белки PAH, а также их варианты и/или активные фрагменты для применения в лечении, профилактике и/или облегчении одного или более симптомов фенилкетонурии (ФКУ). В одном аспекте фенилкетонурия (ФКУ) представляет собой фенилкетонурию человека (ФКУ).
(i) Терапевтические белки PAH и их фрагменты
[00166] По существу любой вариант терапевтического белка PAH или его фрагмента (например, функциональный фрагмент) может кодироваться и экспрессироваться с зкДНК-вектора, как описано в данном документе. Специалист в данной области техники поймет, что терапевтический белок PAH включает все варианты сплайсинга и ортологи белка PAH. Терапевтический белок PAH включает интактные молекулы, а также их фрагменты (например, функциональные).
[00167] Отличительным преимуществом зкДНК-векторов по сравнению с обычными ААВ-векторами и даже лентивирусными векторами является отсутствие ограничения по размеру для гетерологичных последовательностей нуклеиновых кислот, кодирующих целевой белок. Таким образом, несколько полноразмерных терапевтических белков PAH могут быть экспрессированы с одного зкДНК-вектора.
[00168] Белок и ген PAH: ген PAH расположен на хромосоме 12 в полосах 12q22-q24.2. По состоянию на 2000 год в гене PAH было обнаружено примерно 400 мутаций, вызывающих заболевание. Фенилаланингидроксилаза (PAH) также может называться фенилаланин-4-монооксигеназой, фенилаланин-4-гидроксилазой, Phe-4-монооксигеназой, EC 1.14.16.1, EC 1.14.16, PKU1, PKU или PH.
[00169] Белковая последовательность PAH приведена далее: трансляция фермента PAH Homo sapiens (450 аминокислот), номер доступа NM_000277.3
MSTAVLENPGLGRKLSDFGQETSYIEDNCNQNGAISLIFSLKEEVGALAKVLRLFEENDVNLTHIESRPSRLKKDEYEFFTHLDKRSLPALTNIIKILRHDIGATVHELSRDKKKDTVPWFPRTIQELDRFANQILSYGAELDADHPGFKDPVYRARRKQFADIAYNYRHGQPIPRVEYMEEEKKTWGTVFKTLKSLYKTHACYEYNHIFPLLEKYCGFHEDNIPQLEDVSQFLQTCTGFRLRPVAGLLSSRDFLGGLAFRVFHCTQYIRHGSKPMYTPEPDICHELLGHVPLFSDRSFAQFSQEIGLASLGAPDEYIEKLATIYWFTVEFGLCKQGDSIKAYGAGLLSSFGELQYCLSEKPKLLPLELEKTAIQNYTVTEFQPLYYVAESFNDAKEKVRNFAATIPRPFSVRYDPYTQRIEVLDNTQQLKILADSINSEIGILCSALQK (SEQ ID NO: 195)
[00170] PAH преимущественно экспрессируется в печени, с умеренной экспрессией в почках и желчном пузыре. Низкие уровни экспрессии PAH также могут детектироваться в простате, надпочечниках. Во время внутриутробного развития PAH может быть экспрессирован в надпочечниках, сердце, кишечнике, легких и желудке. Соответственно, зкДНК-вектор, экспрессирующий PAH, можно вводить в любую одну или более тканей, выбранных из: печени, почек, желчного пузыря, простаты, надпочечников. Согласно некоторым вариантам реализации, когда зкДНК-вектор, экспрессирующий PAH, вводят младенцу или вводят субъекту in utero, зкДНК-вектор, экспрессирующий PAH, можно вводить в любую одну или более тканей, выбранных из: печени, надпочечников, сердца, кишечника, легкого и желудка.
[00171] Экспрессия терапевтического белка PAH или его фрагмента с зкДНК-вектора может быть достигнута как в пространстве, так и во времени с использованием одного или более индуцируемых или репрессируемых промоторов, известных в данной области техники или описанных в данном документе, включая регуляторные переключатели, описанные в данном документе.
[00172] Согласно одному варианту реализации терапевтический белок PAH представляет собой «вариант терапевтического белка», который относится к терапевтическому белку PAH, имеющему измененную аминокислотную последовательность, композицию или структуру по сравнению с соответствующим нативным терапевтическим белком PAH. Согласно одному варианту реализации PAH представляет собой функциональный вариант (например, дикий тип). Пригодной также может быть экспрессия мутантного варианта белка PAH, такого как точечная мутация или делеционная мутация, которая приводит к фенилкетонурии (ФКУ), например, для создания модели заболевания на животных и/или для оценки лекарственных средств для лечения фенилкетонурии (ФКУ). Доставка мутантных или модифицированных белков PAH в модельную систему на основе клеток или на животных может быть выполнена для создания модели заболевания. Такую модель на основе клеток или на животных можно использовать для исследований и/или скрининга лекарственных средств. Терапевтический белок PAH, экспрессируемый с зкДНК-векторов, может дополнительно содержать последовательность/фрагмент, который придает дополнительную функциональность, такую как флуоресценция, ферментативная активность или сигнал секреции. Согласно одному варианту реализации вариант терапевтического белка PAH содержит ненативную последовательность метки для идентификации (например, иммунную метку), чтобы его можно было отличить от эндогенного терапевтического белка PAH в реципиентной клетке-хозяине.
[00173] Специалист в данной области техники может взять известную и/или общедоступную последовательность белка, например, терапевтического белка PAH, и выполнить обратное конструирование последовательности кДНК для кодирования такого белка. Затем кДНК может быть оптимизирована по кодонам, чтобы соответствовать предусмотренной клетке-хозяину, и вставлена в зкДНК-вектор, как описано в данном документе.
[00174] Согласно одному варианту реализации последовательность, кодирующая терапевтический белок PAH, может быть получена из существующей клетки-хозяина или линии клеток, например, путем обратной транскрипции мРНК, полученной от хозяина, и амплификации последовательности с использованием ПЦР.
(i) зкДНК-векторы, экспрессирующие терапевтический белок PAH
[00175] зкДНК-вектор, имеющий одну или более последовательностей, кодирующих целевой терапевтический белок PAH, может содержать регуляторные последовательности, такие как промоторы (например, см. Таблицу 1), сигналы секреции, области поли(А) и энхансеры. По меньшей мере, зкДНК-вектор содержит одну или более гетерологичных последовательностей, кодирующих терапевтический белок PAH или его функциональный фрагмент. Примерные кассетные вставки для получения зкДНК-векторов, кодирующих терапевтические белки PAH, отображены на Фигурах 1A-1G. Согласно одному варианту реализации зкДНК-вектор содержит последовательность PAH, перечисленную в Таблице 1 в данном документе.
[00176] Таблица 1: Примерные последовательности PAH для лечения ФКУ
[00177] Согласно одному варианту реализации зкДНК-вектор содержит последовательность PAH, перечисленную в Таблице 1 в данном документе. Согласно одному варианту реализации зкДНК-вектор содержит последовательность PAH, имеющую по меньшей мере 90% идентичности с последовательностью PAH, перечисленной в Таблице 1. Согласно одному варианту реализации зкДНК-вектор содержит последовательность PAH, имеющую по меньшей мере 91% идентичности с последовательностью PAH, перечисленной в Таблице 1. Согласно одному варианту реализации зкДНК-вектор содержит последовательность PAH, имеющую по меньшей мере 92% идентичности с последовательностью PAH, перечисленной в Таблице 1. Согласно одному варианту реализации зкДНК-вектор содержит последовательность PAH, имеющую по меньшей мере 93% идентичности с последовательностью PAH, перечисленной в Таблице 1. Согласно одному варианту реализации зкДНК-вектор содержит последовательность PAH, имеющую по меньшей мере 94% идентичности с последовательностью PAH, перечисленной в Таблице 1. Согласно одному варианту реализации зкДНК-вектор содержит последовательность PAH, имеющую по меньшей мере 95% идентичности с последовательностью PAH, перечисленной в Таблице 1. Согласно одному варианту реализации зкДНК-вектор содержит последовательность PAH, имеющую по меньшей мере 96% идентичности с последовательностью PAH, перечисленной в Таблице 1. Согласно одному варианту реализации зкДНК-вектор содержит последовательность PAH, имеющую по меньшей мере 97% идентичности с последовательностью PAH, перечисленной в Таблице 1. Согласно одному варианту реализации зкДНК-вектор содержит последовательность PAH, имеющую по меньшей мере 98% идентичности с последовательностью PAH, перечисленной в Таблице 1. Согласно одному варианту реализации зкДНК-вектор содержит последовательность PAH, имеющую по меньшей мере 99% идентичности с последовательностью PAH, перечисленной в Таблице 1.
[00178] Согласно одному варианту реализации последовательность PAH имеет по меньшей мере 90% идентичности с SEQ ID NO: 380, SEQ ID NO: 381, SEQ ID NO: 382, SEQ ID NO: 383, SEQ ID NO: 384, SEQ ID NO: 385, SEQ ID NO: 386, SEQ ID NO: 387, SEQ ID NO: 388, SEQ ID NO: 389, SEQ ID NO: 390, SEQ ID NO: 391, SEQ ID NO: 392, SEQ ID NO: 393 или SEQ ID NO: 394. Согласно одному варианту реализации последовательность PAH имеет по меньшей мере 91% идентичности с SEQ ID NO: 380, SEQ ID NO: 381, SEQ ID NO: 382, SEQ ID NO: 383, SEQ ID NO: 384, SEQ ID NO: 385, SEQ ID NO: 386, SEQ ID NO: 387, SEQ ID NO: 388, SEQ ID NO: 389, SEQ ID NO: 390, SEQ ID NO: 391, SEQ ID NO: 392, SEQ ID NO: 393 или SEQ ID NO: 394. Согласно одному варианту реализации последовательность PAH имеет по меньшей мере 92% идентичности с SEQ ID NO: 380, SEQ ID NO: 381, SEQ ID NO: 382, SEQ ID NO: 383, SEQ ID NO: 384, SEQ ID NO: 385, SEQ ID NO: 386, SEQ ID NO: 387, SEQ ID NO: 388, SEQ ID NO: 389, SEQ ID NO: 390, SEQ ID NO: 391, SEQ ID NO: 392, SEQ ID NO: 393 или SEQ ID NO: 394. Согласно одному варианту реализации последовательность PAH имеет по меньшей мере 93% идентичности с SEQ ID NO: 380, SEQ ID NO: 381, SEQ ID NO: 382, SEQ ID NO: 383, SEQ ID NO: 384, SEQ ID NO: 385, SEQ ID NO: 386, SEQ ID NO: 387, SEQ ID NO: 388, SEQ ID NO: 389, SEQ ID NO: 390, SEQ ID NO: 391, SEQ ID NO: 392, SEQ ID NO: 393 или SEQ ID NO: 394. Согласно одному варианту реализации последовательность PAH имеет по меньшей мере 94% идентичности с SEQ ID NO: 380, SEQ ID NO: 381, SEQ ID NO: 382, SEQ ID NO: 383, SEQ ID NO: 384, SEQ ID NO: 385, SEQ ID NO: 386, SEQ ID NO: 387, SEQ ID NO: 388, SEQ ID NO: 389, SEQ ID NO: 390, SEQ ID NO: 391, SEQ ID NO: 392, SEQ ID NO: 393 или SEQ ID NO: 394. Согласно одному варианту реализации последовательность PAH имеет по меньшей мере 95% идентичности с SEQ ID NO: 380, SEQ ID NO: 381, SEQ ID NO: 382, SEQ ID NO: 383, SEQ ID NO: 384, SEQ ID NO: 385, SEQ ID NO: 386, SEQ ID NO: 387, SEQ ID NO: 388, SEQ ID NO: 389, SEQ ID NO: 390, SEQ ID NO: 391, SEQ ID NO: 392, SEQ ID NO: 393 или SEQ ID NO: 394. Согласно одному варианту реализации последовательность PAH имеет по меньшей мере 96% идентичности с SEQ ID NO: 380, SEQ ID NO: 381, SEQ ID NO: 382, SEQ ID NO: 383, SEQ ID NO: 384, SEQ ID NO: 385, SEQ ID NO: 386, SEQ ID NO: 387, SEQ ID NO: 388, SEQ ID NO: 389, SEQ ID NO: 390, SEQ ID NO: 391, SEQ ID NO: 392, SEQ ID NO: 393 или SEQ ID NO: 394. Согласно одному варианту реализации последовательность PAH имеет по меньшей мере 97% идентичности с SEQ ID NO: 380, SEQ ID NO: 381, SEQ ID NO: 382, SEQ ID NO: 383, SEQ ID NO: 384, SEQ ID NO: 385, SEQ ID NO: 386, SEQ ID NO: 387, SEQ ID NO: 388, SEQ ID NO: 389, SEQ ID NO: 390, SEQ ID NO: 391, SEQ ID NO: 392, SEQ ID NO: 393 или SEQ ID NO: 394. Согласно одному варианту реализации последовательность PAH имеет по меньшей мере 98% идентичности с SEQ ID NO: 380, SEQ ID NO: 381, SEQ ID NO: 382, SEQ ID NO: 383, SEQ ID NO: 384, SEQ ID NO: 385, SEQ ID NO: 386, SEQ ID NO: 387, SEQ ID NO: 388, SEQ ID NO: 389, SEQ ID NO: 390, SEQ ID NO: 391, SEQ ID NO: 392, SEQ ID NO: 393 или SEQ ID NO: 394. Согласно одному варианту реализации последовательность PAH имеет по меньшей мере 99% идентичности с SEQ ID NO: 380, SEQ ID NO: 381, SEQ ID NO: 382, SEQ ID NO: 383, SEQ ID NO: 384, SEQ ID NO: 385, SEQ ID NO: 386, SEQ ID NO: 387, SEQ ID NO: 388, SEQ ID NO: 389, SEQ ID NO: 390, SEQ ID NO: 391, SEQ ID NO: 392, SEQ ID NO: 393 или SEQ ID NO: 394. Согласно одному варианту реализации последовательность PAH содержит SEQ ID NO: 380, SEQ ID NO: 381, SEQ ID NO: 382, SEQ ID NO: 383, SEQ ID NO: 384, SEQ ID NO: 385, SEQ ID NO: 386, SEQ ID NO: 387, SEQ ID NO: 388, SEQ ID NO: 389, SEQ ID NO: 390, SEQ ID NO: 391, SEQ ID NO: 392, SEQ ID NO: 393 или SEQ ID NO: 394. Согласно одному варианту реализации последовательность PAH состоит из SEQ ID NO: 380, SEQ ID NO: 381, SEQ ID NO: 382, SEQ ID NO: 383, SEQ ID NO: 384, SEQ ID NO: 385, SEQ ID NO: 386, SEQ ID NO: 387, SEQ ID NO: 388, SEQ ID NO: 389, SEQ ID NO: 390, SEQ ID NO: 391, SEQ ID NO: 392, SEQ ID NO: 393 или SEQ ID NO: 394.
[00179] Согласно одному варианту реализации последовательность PAH имеет последовательность, имеющую по меньшей мере 85% идентичности с SEQ ID NO: 382. Согласно одному варианту реализации последовательность PAH имеет последовательность, имеющую по меньшей мере 90% идентичности с SEQ ID NO: 382. Согласно одному варианту реализации последовательность PAH имеет последовательность, имеющую по меньшей мере 95% идентичности с SEQ ID NO: 382. Согласно одному варианту реализации последовательность PAH имеет последовательность, имеющую по меньшей мере 97% идентичности с SEQ ID NO: 382. Согласно одному варианту реализации последовательность PAH имеет последовательность, имеющую по меньшей мере 99% идентичности с SEQ ID NO: 382. Согласно одному варианту реализации последовательность PAH имеет последовательность, имеющую по меньшей мере 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичности с SEQ ID NO: 382. Согласно одному варианту реализации последовательность PAH имеет последовательность, содержащую SEQ ID NO: 382. Согласно одному варианту реализации последовательность PAH имеет последовательность, состоящую из SEQ ID NO: 382.
[00180] Согласно одному варианту реализации последовательность PAH имеет последовательность, имеющую по меньшей мере 85% идентичности с SEQ ID NO: 384. Согласно одному варианту реализации последовательность PAH имеет последовательность, имеющую по меньшей мере 90% идентичности с SEQ ID NO: 384. Согласно одному варианту реализации последовательность PAH имеет последовательность, имеющую по меньшей мере 95% идентичности с SEQ ID NO: 384. Согласно одному варианту реализации последовательность PAH имеет последовательность, имеющую по меньшей мере 97% идентичности с SEQ ID NO: 384. Согласно одному варианту реализации последовательность PAH имеет последовательность, имеющую по меньшей мере 99% идентичности с SEQ ID NO: 384. Согласно одному варианту реализации последовательность PAH имеет последовательность, имеющую по меньшей мере 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичности с SEQ ID NO: 384. Согласно одному варианту реализации последовательность PAH имеет последовательность, содержащую SEQ ID NO: 384. Согласно одному варианту реализации последовательность PAH имеет последовательность, состоящую из SEQ ID NO: 384.
[00181] Согласно одному варианту реализации последовательность PAH имеет последовательность, имеющую по меньшей мере 85% идентичности с SEQ ID NO: 394. Согласно одному варианту реализации последовательность PAH имеет последовательность, имеющую по меньшей мере 90% идентичности с SEQ ID NO: 394. Согласно одному варианту реализации последовательность PAH имеет последовательность, имеющую по меньшей мере 95% идентичности с SEQ ID NO: 394. Согласно одному варианту реализации последовательность PAH имеет последовательность, имеющую по меньшей мере 97% идентичности с SEQ ID NO: 394. Согласно одному варианту реализации последовательность PAH имеет последовательность, имеющую по меньшей мере 99% идентичности с SEQ ID NO: 394. Согласно одному варианту реализации последовательность PAH имеет последовательность, имеющую по меньшей мере 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичности с SEQ ID NO: 394. Согласно одному варианту реализации последовательность PAH имеет последовательность, содержащую SEQ ID NO: 394. Согласно одному варианту реализации последовательность PAH имеет последовательность, состоящую из SEQ ID NO: 394.
(iii) Терапевтические белки PAH и варианты их применения для лечения ФКУ
[00182] ЗкДНК-векторы, описанные в данном документе, можно применять для доставки терапевтических белков PAH для лечения ФКУ, ассоциированной с нефизиологической экспрессией белка PAH и/или мутациями в белках PAH.
[00183] ЗкДНК-векторы, описанные в данном документе, можно применять для экспрессии любого целевого терапевтического белка PAH. Примерные терапевтические белки PAH включают, но не ограничиваются им, любой белок PAH, экспрессируемый последовательностями, изложенными в Таблице 1 в данном документе.
[00184] Согласно одному варианту реализации экспрессированный терапевтический белок PAH является функциональным для лечения фенилкетонурии (ФКУ). Согласно некоторым вариантам реализации терапевтический белок PAH не вызывает реакции иммунной системы.
[00185] Согласно другому варианту реализации зкДНК-векторы, кодирующие терапевтический белок PAH или его фрагмент (например, функциональный фрагмент), можно применять для получения химерного белка. Таким образом, в данном документе конкретно предусмотрено, что зкДНК-вектор, экспрессирующий химерный белок, можно вводить, например, в любую одну или более тканей, выбранных из: печени, почек, желчного пузыря, простаты, надпочечников. Согласно некоторым вариантам реализации, когда зкДНК-вектор, экспрессирующий PAH, вводят младенцу или вводят субъекту in utero, зкДНК-вектор, экспрессирующий PAH, можно вводить в любую одну или более тканей, выбранных из: печени, надпочечников, сердца, кишечника, легкого и желудка, или в стволовую клетку-предшественника клеток печени для лечения фенилкетонурии (ФКУ) in vivo или ex vivo.
[00186] ФКУ: ФКУ представляет собой редкий наследственный врожденный порок метаболизма, вызванный мутацией в гене PAH. PAH представляет собой фермент, который обычно экспрессируется в печени и необходим для метаболизма поступающего с пищей фенилаланина в тирозин, аминокислоту, отвечающую за продукцию нейротрансмиттеров. ФКУ возникает в результате мутаций в PAH, которые приводят к дефициту его ферментативной активности. Соответственно, зкДНК-векторы, экспрессирующие белок PAH, могут экспрессировать PAH в печени или других тканях, включая клетки сетчатки, такие как фоторецепторы и/или клетки RPE. Согласно некоторым вариантам реализации зкДНК-векторы экспрессируют по меньшей мере один белок PAH как в фоторецепторах, так и в клетках RPE.
[00187] PAH обычно эндогенно экспрессируется как в клетках типа PR, так и в клетках типа RPE. Также сообщается, что низкий уровень экспрессии PAH в RPE также может потребоваться для нормальной функции сетчатки. Соответственно, низкий уровень или высокий уровень экспрессии белка PAH зкДНК-вектором в PR, а также необязательно в клетках RPE, иногда может быть необходим для предотвращения дегенерации сетчатки. Этот уровень экспрессии может быть точно настроен с помощью промоторов и/или регуляторных переключателей, описанных в данном документе.
[00188] Соответственно, в некоторых вариантах реализации зкДНК-вектор применяют для экспрессии белка PAH, который представляет собой белок размером 6,8 тыс. п. о., с эндогенного промотора (~1 тыс. п. о.) для восстановления нормального процессинга ретиноидов как в фоторецепторах, так и в RPE. Согласно некоторым вариантам реализации зкДНК-вектор, экспрессирующий белок PAH, вводят супрахориоидальным или интравитреальным путем для лечения большей площади сетчатки. Согласно некоторым вариантам реализации зкДНК-вектор вводят с помощью одного или более из: субретинальной инъекции, супрахориоидальной инъекции или интравитреальной инъекции.
[00189] Способы включают введение субъекту эффективного количества композиции, содержащей зкДНК-вектор, кодирующий терапевтический белок PAH или его фрагмент (например, функциональный фрагмент), как описано в данном документе. Как будет понятно квалифицированному практикующему врачу, термин «эффективное количество» относится к количеству введенной композиции зкДНК, которое приводит к экспрессии белка в «терапевтически эффективном количестве» для лечения заболевания или нарушения.
[00190] Диапазоны дозировок для композиции, содержащей зкДНК-вектор, кодирующий терапевтический белок PAH или его фрагмент (например, функциональный фрагмент), зависят от эффективности (например, эффективности промотора) и включают количества, достаточно большие для получения целевого эффекта, например, экспрессии целевого терапевтического белка PAH для лечения фенилкетонурии (ФКУ). Дозировка не должна быть настолько большой, чтобы вызывать неприемлемые нежелательные побочные эффекты. Обычно дозировка будет варьироваться в зависимости от конкретных характеристик зкДНК-вектора, эффективности экспрессии, а также в зависимости от возраста, состояния и пола пациента. Дозировка может быть определена специалистом в данной области техники и, в отличие от обычных ААВ-векторов, также может быть скорректирована индивидуальным врачом в случае любого осложнения, поскольку зкДНК-векторы не содержат активирующие иммунную систему капсидные белки, которые препятствуют повторному дозированию.
[00191] Введение композиций зкДНК, описанных в данном документе, можно повторять в течение ограниченного периода времени. Согласно некоторым вариантам реализации дозы вводят периодически или с помощью импульсного введения. Согласно предпочтительному варианту реализации указанные выше дозы вводят в течение нескольких месяцев. Продолжительность лечения зависит от клинического прогресса и ответа пациента на терапию. Также предусмотрены «бустерные» обработки с течением времени. Кроме того, уровень экспрессии можно титровать по мере роста субъекта.
[00192] Терапевтический белок PAH может быть экспрессирован у субъекта в течение по меньшей мере 1 недели, по меньшей мере 2 недель, по меньшей мере 1 месяца, по меньшей мере 2 месяцев, по меньшей мере 6 месяцев, по меньшей мере 12 месяцев/одного года, по меньшей мере 2 лет, по меньшей мере 5 лет, по меньшей мере 10 лет, по меньшей мере 15 лет, по меньшей мере 20 лет, по меньшей мере 30 лет, по меньшей мере 40 лет, по меньшей мере 50 лет или более. Долговременная экспрессия может быть достигнута путем повторного введения зкДНК-векторов, описанных в данном документе, через заранее определенные или желательные интервалы.
[00193] В данном документе термин «терапевтически эффективное количество» представляет собой количество экспрессированного терапевтического белка PAH или его функционального фрагмента, которое достаточно для получения статистически значимого, измеримого изменения экспрессии биомаркера заболевания или уменьшения симптомов данного заболевания (см. «Измерение эффективности» ниже). Такие эффективные количества можно откалибровать в клинических исследованиях, а также в исследованиях на животных для конкретной композиции зкДНК.
[00194] Точные количества зкДНК-вектора, необходимые для введения, зависят от суждения практикующего врача и являются индивидуальными для каждого индивидуума. Подходящие схемы введения также являются вариабельными, но типичным является начальное введение с последующими повторными дозами с одним или более интервалами с последующей инъекцией или другим введением. В качестве альтернативы, предусмотрена непрерывная внутривенная инфузия, достаточная для поддержания концентраций в крови в диапазонах, указанных для видов терапии in vivo, в частности, для лечения острых заболеваний/нарушений.
[00195] Агенты, которые можно применять в способах и композициях, описанных в данном документе, можно вводить местно, внутривенно (с помощью болюсной или непрерывной инфузии), с помощью внутриклеточной инъекции, внутритканевой инъекции, перорально, путем ингаляции, внутрибрюшинно, внутримышечно, подкожно, внутрь полости, а также они могут быть доставлены с помощью перистальтических средств, при необходимости, или других средств, известных специалистам в данной области техники. При необходимости, агент может быть введен системно. Он также может быть введен in utero.
[00196] Эффективность конкретного лечения фенилкетонурии (ФКУ) может быть определена квалифицированным врачом. Однако лечение считается «эффективным лечением», в соответствии с использованием этого термина в данном документе, если любой или все признаки или симптомы заболевания или нарушения изменяются благоприятным образом, или если другие клинически принятые симптомы или маркеры заболевания улучшаются или облегчаются, например, по меньшей мере на 10% после лечения зкДНК-вектором, кодирующим PAH или его функциональный фрагмент. Эффективность также может быть измерена по отсутствию у индивидуума ухудшения, которое оценивается по стабилизации заболевания или по потребности в медицинских вмешательствах (т. е. прогрессирование заболевания прекращается или по меньшей мере замедляется). Способы измерения этих показателей известны специалистам в данной области техники и/или описаны в данном документе. Лечение включает любое лечение заболевания у индивидуума или животного (некоторые неограничивающие примеры включают человека или млекопитающее) и включает: (1) ингибирование заболевания, например, прекращение или замедление прогрессирования заболевания или нарушения; или (2) облегчение заболевания, например, вызывающее регресс симптомов; и (3) предотвращение или снижение вероятности развития заболевания, или предотвращение вторичных заболеваний/нарушений, ассоциированных с указанным заболеванием, таких как печеночная или почечная недостаточность. Эффективное количество для лечения заболевания означает такое количество, которое при введении млекопитающему, нуждающемуся в этом, является достаточным, чтобы привести к эффективному лечению этого заболевания, в соответствии с определением этого термина в данном документе.
[00197] Эффективность агента может быть определена путем оценки физических показателей, которые являются специфическими для фенилкетонурии (ФКУ). Стандартные методы анализа показателей ФКУ известны в данной области техники.
[00198] Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, также может кодировать кофакторы или другие полипептиды, смысловые или антисмысловые олигонуклеотиды или РНК (кодирующие или некодирующие; например, киРНК, кшРНК, микро-РНК и их антисмысловые аналоги (например, antagoMiR)), которые можно применять в сочетании с белком PAH, экспрессируемым с зкДНК. Кроме того, экспрессионные кассеты, содержащие последовательность, кодирующую белок PAH, также могут включать экзогенную последовательность, которая кодирует репортерный белок, который будет использоваться в экспериментальных или диагностических целях, такой как β-лактамаза, β-галактозидаза (LacZ), щелочная фосфатаза, тимидинкиназа, зеленый флуоресцентный белок (GFP), хлорамфениколацетилтрансфераза (CAT), люцифераза и другие, хорошо известные в данной области техники.
[00199] Согласно одному варианту реализации зкДНК-вектор содержит последовательность нуклеиновой кислоты для экспрессии белка PAH, который является функциональным для лечения ФКУ. Согласно предпочтительному варианту реализации терапевтический белок PAH не вызывает реакции иммунной системы, если этого не требуется.
I. ЗкДНК-вектор в целом для применения в получении терапевтических белков PAH
[00200] Варианты реализации настоящего изобретения основаны на способах и композициях, содержащих линейные дуплексные векторы с замкнутыми концами (зкДНК), которые могут экспрессировать трансген PAH. Согласно некоторым вариантам реализации трансген представляет собой последовательность, кодирующую белок PAH. ЗкДНК-векторы для экспрессии белка PAH, описанные в данном документе, не ограничены размером, что позволяет, например, обеспечивать экспрессию всех компонентов, необходимых для экспрессии трансгена, с одного вектора. ЗкДНК-вектор для экспрессии белка PAH предпочтительно является дуплексным, например, самокомплементарным, по меньшей мере в части молекулы, такой как экспрессионная кассета (например, зкДНК не является двухцепочечной кольцевой молекулой). ЗкДНК-вектор имеет ковалентно замкнутые концы и, таким образом, устойчив к расщеплению экзонуклеазой (например, экзонуклеазой I или экзонуклеазой III), например, более часа при 37°С.
[00201] В общем случае зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, содержит, в направлении от 5´ к 3´: первый инвертированный концевой повтор (ITR) аденоассоциированного вируса (ААВ), нуклеотидную последовательность, представляющую интерес (например, экспрессионную кассету, описанную в данном документе), и второй ITR ААВ. Последовательности ITR выбирают из любых из: (i) по меньшей мере одного WT-ITR и по меньшей мере одного модифицированного инвертированного концевого повтора ААВ (mod-ITR) (например, асимметричных модифицированных ITR); (ii) двух модифицированных ITR, причем пара mod-ITR имеет различную трехмерную пространственную организацию по отношению друг к другу (например, асимметричные модифицированные ITR), или (iii) пары симметричных или по существу симметричных WT-WT-ITR, причем каждый WT-ITR имеет одинаковую трехмерную пространственную организацию, или (iv) пары симметричных или по существу симметричных модифицированных ITR, причем каждый mod-ITR имеет одинаковую трехмерную пространственную организацию.
[00202] В данный документ включены способы и композиции, содержащие зкДНК-вектор для продукции белка PAH, который может дополнительно включать систему доставки, такую как, но не ограничиваясь этим, систему доставки на основе липосомных наночастиц. В данном документе раскрыты неограничивающие примерные системы на основе липосомных наночастиц, предусмотренные для применения. Согласно некоторым аспектам настоящего раскрытия предложена липидная наночастица, содержащая зкДНК и ионизируемый липид. Например, состав липидных наночастиц, который получают и нагружают зкДНК-вектором, полученным указанным способом, раскрыт в международной заявке PCT/US2018/050042, поданной 7 сентября 2018 г., которая полностью включена в данный документ посредством ссылки.
[00203] ЗкДНК-векторы для экспрессии белка PAH, раскрытые в данном документе, не имеют ограничений по упаковке, налагаемых ограниченным пространством внутри вирусного капсида. ЗкДНК-векторы представляют собой жизнеспособную продуцируемую эукариотами альтернативу плазмидным ДНК-векторам, продуцируемым прокариотами, в отличие от инкапсулированных геномов ААВ. Это позволяет вставлять контрольные элементы, например, регуляторные переключатели, раскрытые в данном документе, большие трансгены, множественные трансгены и т. д.
[00204] ФИГ. 1A-1E схематически показывают неограничивающие примерные зкДНК-векторы для экспрессии белка PAH или соответствующую последовательность зкДНК-плазмид. ЗкДНК-векторы для экспрессии белка PAH являются бескапсидными и могут быть получены из плазмиды, кодирующей в указанном порядке: первый ITR, экспрессионную кассету, содержащую трансген, и второй ITR. Экспрессионная кассета может включать одну или более регуляторных последовательностей, которые обеспечивают и/или контролируют экспрессию трансгена, например, экспрессионная кассета может содержать один или более из следующих элементов, в указанном порядке: энхансер/промотор, ORF репортера (трансгена), посттранскрипционный регуляторный элемент (например, WPRE) и сигнал полиаденилирования и терминации (например, BGH поли(A)).
[00205] Экспрессионная кассета также может содержать участок внутренней посадки рибосомы (IRES) и/или элемент 2A. Цис-регуляторные элементы включают, но не ограничиваются перечисленными, промотор, рибопереключатель, инсулятор, mir-регулируемый элемент, посттранскрипционный регуляторный элемент, промотор, специфический для ткани и типа клеток, и энхансер. Согласно некоторым вариантам реализации ITR может действовать как промотор трансгена, например, белка PAH. Согласно некоторым вариантам реализации зкДНК-вектор содержит дополнительные компоненты для регуляции экспрессии трансгена, например, регуляторный переключатель, которые описаны в данном документе в разделе, озаглавленном «Регуляторные переключатели», для контроля и регуляции экспрессии белка PAH, и могут включать, при необходимости, регуляторный переключатель, который представляет собой «аварийный выключатель» (kill switch) для обеспечения контролируемой гибели клетки, содержащей зкДНК-вектор.
[00206] Экспрессионная кассета может содержать более 4000 нуклеотидов, 5000 нуклеотидов, 10000 нуклеотидов или 20000 нуклеотидов, или 30000 нуклеотидов, или 40000 нуклеотидов, или 50000 нуклеотидов, или любой диапазон примерно от 4000 до 10000 нуклеотидов, или 10000-50000 нуклеотидов, или более 50000 нуклеотидов. Согласно некоторым вариантам реализации экспрессионная кассета может содержать трансген с длиной в диапазоне от 500 до 50000 нуклеотидов. Согласно некоторым вариантам реализации экспрессионная кассета может содержать трансген с длиной в диапазоне от 500 до 75000 нуклеотидов. Согласно некоторым вариантам реализации экспрессионная кассета может содержать трансген с длиной в диапазоне от 500 до 10000 нуклеотидов. Согласно некоторым вариантам реализации экспрессионная кассета может содержать трансген с длиной в диапазоне от 1000 до 10000 нуклеотидов. Согласно некоторым вариантам реализации экспрессионная кассета может содержать трансген с длиной в диапазоне от 500 до 5000 нуклеотидов. Векторы зкДНК не имеют ограничений по размеру ААВ-векторов, заключенных в капсид, что позволяет доставлять экспрессионную кассету большого размера для обеспечения эффективной экспрессии трансгена. Согласно некоторым вариантам реализации зкДНК-вектор лишен специфического для прокариот метилирования.
[00207] ЗкДНК-экспрессионная кассета может включать, например, экспрессируемую экзогенную последовательность (например, открытую рамку считывания) или трансген, который кодирует белок, который либо отсутствует, либо не активен, либо обладает недостаточной активностью у субъекта-реципиента, или ген, который кодирует белок, имеющий целевой биологический или терапевтический эффект. Трансген может кодировать продукт гена, функция которого может заключаться в корректировке экспрессии дефектного гена или транскрипта. В принципе, экспрессионная кассета может включать любой ген, который кодирует белок, полипептид или РНК, который либо снижен, либо отсутствует из-за мутации, или который обеспечивает терапевтическую пользу при сверхэкспрессии, и рассматривается, как включенная в объем настоящего раскрытия.
[00208] кспрессионная кассета может содержать любой трансген (например, кодирующий белок PAH), например, белок PAH, который можно применять для лечения ФКУ у субъекта, то есть терапевтический белок PAH. ЗкДНК-вектор можно применять для доставки и экспрессии любого белка PAH, представляющего интерес, у субъекта, по отдельности или в комбинации с нуклеиновыми кислотами, кодирующими полипептиды, или некодирующими нуклеиновыми кислотами (например, РНКи, miR и т. д.), а также экзогенных генов и нуклеотидных последовательностей, включая вирусные последовательности в геноме субъектов, например, последовательности вируса ВИЧ и тому подобное. Предпочтительно зкДНК-вектор, раскрытый в данном документе, применяют для терапевтических целей (например, для медицинских, диагностических или ветеринарных целей) или для иммуногенных полипептидов. Согласно определенным вариантам реализации зкДНК-вектор можно применять для экспрессии любого гена, представляющего интерес, у субъекта, который включает один или более полипептидов, пептидов, рибозимов, пептидных нуклеиновых кислот, миРНК, РНКи, антисмысловых олигонуклеотидов, антисмысловых полинуклеотидов или РНК (кодирующих или некодирующих; например, киРНК, кшРНК, микро-РНК и их антисмысловых аналогов (например, antagoMiR)), антител, слитых белков или любую их комбинацию.
[00209] Экспрессионная кассета также может кодировать полипептиды, смысловые или антисмысловые олигонуклеотиды или РНК (кодирующие или некодирующие; например, миРНК, кшРНК, микро-РНК и их антисмысловые аналоги (например, antagoMiR)). Экспрессионные кассеты могут включать экзогенную последовательность, которая кодирует репортерный белок, который будет использоваться в экспериментальных или диагностических целях, такой как β-лактамаза, β-галактозидаза (LacZ), щелочная фосфатаза, тимидинкиназа, зеленый флуоресцентный белок (GFP), хлорамфениколацетилтрансфераза (CAT), люцифераза и другие, хорошо известные в данной области техники.
[00210] Последовательности, обеспеченные в экспрессионной кассете, экспрессионная конструкция зкДНК-вектора для экспрессии белка PAH, описанного в данном документе, могут быть оптимизированы по кодонам для целевой клетки-хозяина. В данном документе термин «оптимизированный по кодонам» или «оптимизация кодонов» относится к процессу модификации последовательности нуклеиновой кислоты для усиления экспрессии в клетках позвоночного, представляющего интерес, например, мыши или человека, путем замены по меньшей мере одного или более чем одного или значительного числа кодонов нативной последовательности (например, прокариотической последовательности) кодонами, которые чаще или наиболее часто используются в генах этого позвоночного. Различные виды проявляют определенное предпочтение в отношении некоторых кодонов конкретной аминокислоты. Как правило, оптимизация кодонов не изменяет аминокислотную последовательность исходного транслированного белка. Оптимизированные кодоны могут быть определены с использованием, например, оптимизации кодонов Aptagen´s Gene Forge® и платформы для синтеза генов по заказу (Aptagen, Inc., 2190 Fox Mill Rd. Suite 300, Херндон, Виржиния, 20171) или другой общедоступной базы данных. Согласно некоторым вариантам реализации нуклеиновая кислота, кодирующая белок PAH, оптимизирована для экспрессии у человека и/или представляет собой PAH человека или его функциональный фрагмент, как известно в данной области техники.
[00211] Трансген, экспрессируемый зкДНК-вектором для экспрессии белка PAH, как описано в данном документе, кодирует белок PAH. ЗкДНК-векторы для экспрессии белка PAH отличаются от экспрессионных векторов на основе плазмид по многим структурным признакам. ЗкДНК-векторы могут обладать одним или более из следующих признаков: отсутствие исходной (т. е. не вставленной) бактериальной ДНК, отсутствие прокариотической точки начала репликации, самодостаточность, т. е. им не требуются никакие последовательности, кроме двух ITR, включая сайт связывания Rep и сайт концевого разрешения (RBS и TRS), и экзогенную последовательность между ITR, присутствие последовательностей ITR, которые образуют шпильки, и отсутствие метилирования ДНК бактериального типа или фактически любого другого метилирования, которое считается аномальным у млекопитающего-хозяина. В целом векторы согласно настоящему изобретению предпочтительно не содержат никакой прокариотической ДНК, но предусмотрено, что некоторая прокариотическая ДНК может быть вставлена в виде экзогенной последовательности, в качестве неограничивающего примера, в промоторной или энхансерной области. Еще один важный признак, отличающий зкДНК-векторы от экспрессионных векторов на основе плазмид, заключается в том, что зкДНК-векторы представляют собой одноцепочечные линейные ДНК с замкнутыми концами, в то время как плазмиды всегда представляют собой двухцепочечные ДНК.
[00212] ЗкДНК-векторы для экспрессии белка PAH, продуцируемые с помощью способов, предложенных в данном документе, предпочтительно имеют линейную и непрерывную структуру, а не прерывистую структуру, согласно определению с помощью анализа с использованием расщепления рестрикционными ферментами (ФИГ. 4D). Как полагают, линейная и непрерывная структура более устойчива к атаке клеточными эндонуклеазами, а также с меньшей вероятностью рекомбинируется и вызывает мутагенез. Таким образом, зкДНК-вектор в линейной и непрерывной структуре является предпочтительным вариантом реализации. Непрерывный, линейный, одноцепочечный, с внутримолекулярным дуплексом зкДНК-вектор может иметь ковалентно связанные концевые участки без последовательностей, кодирующих белки капсида ААВ. Эти зкДНК-векторы структурно отличаются от плазмид (включая зкДНК-плазмиды, описанные в данном документе), которые представляют собой кольцевые дуплексные молекулы нуклеиновых кислот бактериального происхождения. Комплементарные цепи плазмид могут быть разделены после денатурации с получением двух молекул нуклеиновых кислот, в то время как зкДНК-векторы, которые имеют комплементарные цепи, представляют собой единую молекулу ДНК и, следовательно, остаются единой молекулой даже после денатурации. Согласно некоторым вариантам реализации зкДНК-векторы, описанные в данном документе, могут быть получены без метилирования оснований ДНК прокариотического типа, в отличие от плазмид. Таким образом, зкДНК-векторы и зкДНК-плазмиды различаются как по структуре (в частности, линейная в сопоставлении с кольцевой), так и с точки зрения методов, используемых для получения и очистки этих различных объектов (см. ниже), а также с точки зрения метилирования ДНК, которое относится к прокариотическому типу для зкДНК-плазмид и эукариотическому типу для зкДНК-вектора.
[00213] Существует несколько преимуществ применения зкДНК-вектора для экспрессии белка PAH, как описано в данном документе, по сравнению с экспрессионными векторами на основе плазмид, такие преимущества включают, но не ограничиваются перечисленными: 1) плазмиды содержат последовательности бактериальной ДНК и подвергаются метилированию, специфическому для прокариотов, например, метилированию 6-метиладенозина и 5-метилцитозина, в то время как последовательности бескапсидного ААВ-вектора имеют эукариотическое происхождение и не подвергаются метилированию, специфическому для прокариотов; в результате бескапсидные ААВ-векторы с меньшей вероятностью индуцируют воспалительные и иммунные ответы по сравнению с плазмидами; 2) в то время как плазмиды требуют присутствия гена устойчивости во время производственного способа, зкДНК-векторы не требуют; 3) в то время как кольцевая плазмида не доставляется в ядро при введении в клетку и требует чрезмерной нагрузки, чтобы преодолеть разрушение клеточными нуклеазами, зкДНК-векторы содержат вирусные цис-элементы, т. е. ITR, которые придают устойчивость к нуклеазам и могут быть сконструированы для нацеливания и доставки в ядро. Предполагается, что минимальными определяющими элементами, необходимыми для функции ITR, являются сайт связывания Rep (RBS; 5´-GCGCGCTCGCTCGCTC-3´ (SEQ ID NO: 60) для ААВ2) и сайт концевого разрешения (TRS; 5´-AGTTGG-3´ (SEQ ID NO: 64) для ААВ2) плюс вариабельная палиндромная последовательность, обеспечивающая образование шпильки; и 4) зкДНК-векторы не имеют избыточной представленности динуклеотидов CpG, часто обнаруживаемых в плазмидах прокариотического происхождения, которые, как сообщается, связывают члена Toll-подобного семейства рецепторов, вызывая опосредуемый Т-клетками иммунный ответ. Напротив, трансдукция бескапсидными ААВ-векторами, описанными в данном документе, может быть эффективно нацелена на типы клеток и тканей, которые трудно трансдуцировать обычными вирионами ААВ с использованием различных реагентов для доставки.
I. Инвертированные концевые повторы (ITR)
[00214] Как раскрыто в данном документе, зкДНК-векторы для экспрессии белка PAH содержат трансген или гетерологичную последовательность нуклеиновой кислоты, расположенные между двумя последовательностями инвертированных концевых повторов (ITR), причем указанные последовательности ITR могут представлять собой пару асимметричных ITR или пару симметричных или по существу симметричных ITR, в соответствии с определением этих терминов в данном документе. ЗкДНК-вектор, раскрытый в данном документе, может содержать последовательности ITR, которые выбраны из любых из: (i) по меньшей мере одного WT ITR и по меньшей мере одного модифицированного инвертированного концевого повтора (mod-ITR) ААВ (например, асимметричных модифицированных ITR); (ii) двух модифицированных ITR, причем пара mod-ITR имеет различную трехмерную пространственную организацию по отношению друг к другу (например, асимметричные модифицированные ITR), или (iii) пары симметричных или по существу симметричных WT-WT ITR, причем каждый WT-ITR имеет одинаковую трехмерную пространственную организацию, или (iv) пары симметричных или по существу симметричных модифицированных ITR, причем каждый mod-ITR имеет одинаковую трехмерную пространственную организацию, при этом указанные способы согласно настоящему раскрытию могут дополнительно включать систему доставки, такую как, но не ограничиваясь этим, система доставки на основе липосомных наночастиц.
[00215] Согласно некоторым вариантам реализации последовательность ITR может происходить из вирусов семейства Parvoviridae, которое включает два подсемейства: Parvovirinae, инфицирующих позвоночных животных, и Densovirinae, инфицирующих насекомых. Подсемейство Parvovirinae (называемое парвовирусами) включает род Dependovirus, члены которого, в большинстве условий, нуждаются в коинфекции вспомогательным вирусом, таким как аденовирус или вирус герпеса, для эффективной инфекции. Род Dependovirus включает аденоассоциированный вирус (ААВ), который обычно инфицирует людей (например, серотипы 2, 3A, 3B, 5 и 6) или приматов (например, серотипы 1 и 4), а также родственные вирусы, которые инфицируют других теплокровных животных (например, аденоассоциированные вирусы бычьих, собачьих, лошадиных и овечьих). Парвовирусы и другие члены семейства Parvoviridae в общих чертах описаны в Kenneth I. Berns, «Parvoviridae: The Viruses and Their Replication», глава 69 в FIELDS VIROLOGY (3 изд. 1996).
[00216] Несмотря на то, что ITR, приведенные в качестве примера в описании и Примерах в данном документе, представляют собой WT-ITR ААВ2, обычный специалист в данной области техники понимает, что, как было указано выше, можно использовать ITR из любого известного парвовируса, например, депендовируса, такого как ААВ (например, из генома ААВ1, ААВ2, ААВ3, ААВ4, ААВ5, ААВ 5, ААВ7, ААВ8, ААВ9, ААВ10, ААВ 11, ААВ12, ААВrh8, ААВrh10, ААВ-DJ и ААВ-DJ8. Например, NCBI: NC 002077; NC 001401; NC001729; NC001829; NC006152; NC 006260; NC 006261), химерные ITR или ITR из любого синтетического ААВ. Согласно некоторым вариантам реализации ААВ может инфицировать теплокровных животных, например, птичьи (ПААВ), бычьи (БААВ), собачьи, лошадиные и овечьи аденоассоциированные вирусы. Согласно некоторым вариантам реализации ITR происходит из парвовируса B19 (номер доступа в GenBank: NC 000883), мелкого мышиного вируса (MVM) (номер доступа в GenBank NC 001510); гусиного парвовируса (номер доступа в GenBank NC 001701); змеиного парвовируса 1 (номер доступа в GenBank NC 006148). Согласно некоторым вариантам реализации 5´ WT-ITR может происходить из одного серотипа, а 3´ WT-ITR может происходить из другого серотипа, как обсуждается в данном документе.
[00217] Обычному специалисту известно, что последовательности ITR имеют общую структуру двухцепочечного соединения Холлидея, которое, как правило, представляет собой Т-образную или Y-образную шпилечную структуру (см., например, ФИГ. 2А и ФИГ. 3A), где каждый WT-ITR образован двумя палиндромными плечами или петлями (B-B´ и C-C´), встроенными в большее палиндромное плечо (A-A´), и одноцепочечной последовательностью D (при этом порядок этих палиндромных последовательностей определяет «флип» или «флоп» ориентацию ITR). См., например, структурный анализ и сравнение последовательностей ITR из различных серотипов ААВ (ААВ1-ААВ6), описанные в Grimm et al., J. Virology, 2006; 80(1); 426-439; Yan et al., J. Virology, 2005; 364-379; Duan et al., Virology 1999; 261; 8-14. Обычный специалист в данной области техники может легко определить последовательности WT-ITR из любого серотипа ААВ для использования в зкДНК-векторе или зкДНК-плазмиде на основе примерных последовательностей ITR ААВ2, предложенных в данном документе. См., например, сравнение последовательностей ITR из разных серотипов ААВ (ААВ1-ААВ6, птичий ААВ (АААВ) и бычий ААВ (ВААВ)), описанное в Grimm et al., J. Virology, 2006; 80(1); 426-439; в котором показан % идентичности левого ITR ААВ2 с левым ITR из других серотипов: ААВ-1 (84%), ААВ-3 (86%), ААВ-4 (79%), ААВ-5 (58%), ААВ-6 (левый ITR) (100%) и ААВ-6 (правый ITR) (82%).
A. Пары симметричных ITR
[00218] Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH, описанный в данном документе, содержит в направлении от 5´ к 3´: первый инвертированный концевой повтор (ITR) аденоассоциированного вируса (ААВ), представляющую интерес нуклеотидную последовательность (например, экспрессионную кассету, описанную в данном документе) и второй ITR ААВ, причем указанный первый ITR (5´-ITR) и второй ITR (3´-ITR) симметричны или по существу симметричны по отношению друг к другу, то есть зкДНК-вектор может содержать последовательности ITR, которые имеют симметричную трехмерную пространственную организацию так, что их структура имеет одинаковую форму в геометрическом пространстве или имеют одинаковые петли A, C-C´ и B-B´ в трехмерном пространстве. В таком варианте реализации пара симметричных ITR или пара по существу симметричных ITR может представлять собой модифицированные ITR (например, mod-ITR), которые не являются ITR дикого типа. Пара mod-ITR может иметь одну и ту же последовательность, которая имеет одну или более модификаций относительно ITR дикого типа, и они обратно комплементарны друг другу (инвертированы). Согласно альтернативным вариантам реализации пара модифицированных ITR по существу симметрична, как определено в данном документе, то есть пара модифицированных ITR может иметь разные последовательности, но соответствующую или одинаковую симметричную трехмерную форму.
(i) ITR дикого типа
[00219] Согласно некоторым вариантам реализации симметричные ITR или по существу симметричные ITR относятся к дикому типу (WT-ITR), как описано в данном документе. Иными словами, оба ITR имеют последовательность дикого типа, но не обязательно должны представлять собой WT-ITR из одного и того же серотипа ААВ. Иными словами, в некоторых вариантах реализации, один WT-ITR может происходить из одного серотипа ААВ, а другой WT-ITR может происходить из другого серотипа ААВ. В таком варианте реализации пара WT-ITR по существу симметрична, как определено в данном документе, то есть они могут иметь одну или более консервативных нуклеотидных модификаций, сохраняя при этом симметричную трехмерную пространственную организацию.
[00220] Соответственно, как раскрыто в данном документе, зкДНК-векторы содержат трансген или гетерологичную последовательность нуклеиновой кислоты, расположенные между двумя фланкирующими последовательностями инвертированных концевых повторов дикого типа (WT-ITR), которые либо обратно комплементарны (инвертированы) по отношению друг к другу, либо, альтернативно, являются по существу симметричными по отношению друг к другу, то есть пара WT-ITR имеет симметричную трехмерную пространственную организацию. Согласно некоторым вариантам реализации последовательность ITR дикого типа (например, WT-ITR ААВ) содержит функциональный сайт связывания Rep (RBS; например, 5′-GCGCGCTCGCTCGCTC-3′ для ААВ2, SEQ ID NO: 60) и функциональный сайт концевого разрешения (TRS; например, 5′-AGTT-3´, SEQ ID NO: 62).
[00221] Согласно одному аспекту зкДНК-векторы для экспрессии белка PAH могут быть получены из векторного полинуклеотида, который кодирует гетерологичную нуклеиновую кислоту, функционально расположенную между двумя последовательностями инвертированных концевых повторов WT (WT-ITR) (например, WT-ITR ААВ). Иными словами, оба ITR имеют последовательность дикого типа, но не обязательно должны представлять собой WT-ITR из одного и того же серотипа ААВ. Иными словами, в некоторых вариантах реализации, один WT-ITR может происходить из одного серотипа ААВ, а другой WT-ITR может происходить из другого серотипа ААВ. В таком варианте реализации пара WT-ITR по существу симметрична, как определено в данном документе, то есть они могут иметь одну или более консервативных нуклеотидных модификаций, сохраняя при этом симметричную трехмерную пространственную организацию. Согласно некоторым вариантам реализации 5´ WT-ITR происходит из одного серотипа ААВ, а 3´ WT-ITR происходит из того же или другого серотипа ААВ. Согласно некоторым вариантам реализации 5´ WT-ITR и 3´ WT-ITR являются зеркальными отображениями друг друга, то есть они симметричны. Согласно некоторым вариантам реализации 5´ WT-ITR и 3´ WT-ITR происходят из одного и того же серотипа ААВ.
[00222] WT-ITR хорошо известны. Согласно одному варианту реализации два ITR происходят из одного и того же серотипа ААВ2. Согласно определенным вариантам реализации можно использовать WT из других серотипов. Существует ряд гомологичных серотипов, например, ААВ2, ААВ4, ААВ6, ААВ8. Согласно одному варианту реализации можно применять высокогомологичные ITR (например, ITR со сходной петлевой структурой). Согласно другому варианту реализации можно применять WT-ITR ААВ, которые различаются в большей степени, например, ААВ2 и ААВ5, и еще в одном варианте реализации можно применять ITR, который по существу представляет собой WT, то есть он имеет основную петлевую структуру WT, но некоторые консервативные нуклеотидные изменения, которые не изменяют и не влияют на свойства. При использовании WT-ITR из одного и того же вирусного серотипа можно дополнительно использовать одну или более регуляторных последовательностей. Согласно определенным вариантам реализации регуляторная последовательность представляет собой регуляторный переключатель, который позволяет модулировать активность зкДНК, например, экспрессию кодируемого белка PAH.
[00223] Согласно некоторым вариантам реализации один аспект технологии, описанной в данном документе, относится к зкДНК-вектору для экспрессии белка PAH, причем указанный зкДНК-вектор содержит по меньшей мере одну гетерологичную нуклеотидную последовательность, кодирующую белок PAH, функционально расположенную между двумя последовательностями инвертированных концевых повторов дикого типа (WT-ITR), при этом указанные WT-ITR могут происходить из одного и того же серотипа, разных серотипов или по существу симметричны по отношению друг к другу (т. е. они имеют симметричную трехмерную пространственную организацию так, что их структура имеет одинаковую форму в геометрическом пространстве, или имеют одинаковые петли A, C-C´ и B-B´ в трехмерном пространстве). Согласно некоторым вариантам реализации симметричные WT-ITR содержат функциональный сайт концевого разрешения и сайт связывания Rep. Согласно некоторым вариантам реализации гетерологичная последовательность нуклеиновой кислоты кодирует трансген, и при этом вектор не находится в вирусном капсиде.
[00224] Согласно некоторым вариантам реализации WT-ITR являются одинаковыми, но обратно комплементарными по отношению друг к другу. Например, последовательность AACG в 5´-ITR может представлять собой CGTT (т. е. обратно комплементарную последовательность) в 3´-ITR в соответствующем сайте. В одном примере смысловая цепь 5´ WT-ITR содержит последовательность ATCGATCG, а соответствующая смысловая цепь 3´ WT-ITR содержит CGATCGAT (т. е. обратно комплементарную последовательность ATCGATCG). Согласно некоторым вариантам реализации WT-ITR зкДНК дополнительно содержит сайт концевого разрешения и сайт связывания репликационного белка (RPS) (иногда называемый сайтом связывания репликативного белка), например, сайт связывания Rep.
[00225] Примерные последовательности WT-ITR для применения в зкДНК-векторах для экспрессии белка PAH, содержащих WT-ITR, показаны в Таблице 3 в данном документе, которая показывает пары WT-ITR (5´ WT-ITR и 3´ WT-ITR).
[00226] В качестве иллюстративного примера, согласно настоящему раскрытию предложен зкДНК-вектор для экспрессии белка PAH, содержащий промотор, функционально связанный с трансгеном (например, гетерологичной последовательностью нуклеиновой кислоты), с регуляторным переключателем или без него, причем указанная зкДНК лишена капсидных белков и: (а) продуцируется с зкДНК-плазмиды (например, см. ФИГ. 1F-1G), которая кодирует WT-ITR, при этом каждый WT-ITR имеет одинаковое количество внутримолекулярных дуплексных пар оснований в его шпилечной вторичной конфигурации (предпочтительно, исключая делецию любой концевой петли AAA или TTT в этой конфигурации по сравнению с этими референсными последовательностями), и (b) идентифицирована как зкДНК с использованием анализа для идентификации зкДНК с помощью электрофореза в агарозном геле на нативном геле и в денатурирующих условиях в Примере 1.
[00227] Согласно некоторым вариантам реализации фланкирующие WT-ITR по существу симметричны друг другу. Согласно этому варианту реализации 5´ WT-ITR может происходить из одного серотипа ААВ, а 3´ WT-ITR может происходить из другого серотипа ААВ так, что WT-ITR не являются идентичными обратно комплементарными последовательностями. Например, 5´ WT-ITR может происходить из ААВ2, а 3´ WT-ITR может происходить из другого серотипа (например, ААВ1, 3, 4, 5, 6, 7, 8, 9, 10, 11 и 12). Согласно некоторым вариантам реализации WT-ITR могут быть выбраны из двух разных парвовирусов, выбранных из любого из: ААВ1, ААВ2, ААВ3, ААВ4, ААВ5, ААВ6, ААВ7, ААВ8, ААВ9, ААВ10, ААВ11, ААВ12, ААВ13, змеиного парвовируса (например, парвовируса королевского питона), бычьего парвовируса, козьего парвовируса, птичьего парвовируса, лошадиного парвовируса, парвовируса креветок, свиного парвовируса или ААВ насекомых. Согласно некоторым вариантам реализации такая комбинация WT ITR представляет собой комбинацию WT ITR из ААВ2 и ААВ6. Согласно одному варианту реализации WT-ITR являются по существу симметричными, когда один ITR инвертирован относительно другого ITR, который идентичен по меньшей мере на 90%, идентичен по меньшей мере на 95%, по меньшей мере на 96%…97%…98%…99%…99,5%, включая все промежуточные значения, и имеет одинаковую симметричную трехмерную пространственную организацию. Согласно некоторым вариантам реализации пара WT-ITR по существу симметрична, поскольку они имеют симметричную трехмерную пространственную организацию, например, имеют одинаковую трехмерную организацию плеч A, C-C´, B-B´ и D. Согласно одному варианту реализации пара по существу симметричных WT-ITR инвертирована по отношению друг к другу и идентична друг другу по меньшей мере на 95%, по меньшей мере на 96%…97%…98%…99%…99,5%, включая все промежуточные значения, и один WT-ITR сохраняет сайт связывания Rep (RBS) 5´-GCGCGCTCGCTCGCTC-3´ (SEQ ID NO: 60) и сайт концевого разрешения (trs). Согласно некоторым вариантам реализации пара по существу симметричных WT-ITR инвертирована по отношению друг к другу и идентична друг другу по меньшей мере на 95%, по меньшей мере на 96%…97%…98%…99%…99,5%, включая все промежуточные значения, и один WT-ITR сохраняет сайт связывания Rep (RBS) 5´-GCGCGCTCGCTCGCTC-3´ (SEQ ID NO: 60) и сайт концевого разрешения (trs) и в дополнение к вариабельной палиндромной последовательности, обеспечивающей образование шпилечной вторичной структуры. Гомология может быть определена с применением стандартных средств, хорошо известных в данной области техники, таких как BLAST («Basic Local Alignment Search Tool»), BLASTN при настройках по умолчанию.
[00228] Согласно некоторым вариантам реализации структурный элемент ITR может представлять собой любой структурный элемент, который участвует в функциональном взаимодействии ITR с большим белком Rep (например, Rep 78 или Rep 68). Согласно определенным вариантам реализации структурный элемент обеспечивает селективность взаимодействия ITR с большим белком Rep, т. е. определяет, по меньшей мере частично, какой белок Rep функционально взаимодействует с ITR. Согласно другим вариантам реализации структурный элемент физически взаимодействует с большим белком Rep, когда белок Rep связан с ITR. Каждый структурный элемент может представлять собой, например, вторичную структуру ITR, нуклеотидную последовательность ITR, промежуток между двумя или более элементами или комбинацию любого из перечисленных выше. Согласно одному варианту реализации структурные элементы выбраны из группы, состоящей из плеча A и A´, плеча B и B´, плеча C и C´, плеча D, сайта связывания Rep (RBE) и RBE´ (т. е. комплементарная последовательность RBE) и сайта концевого разрешения (trs).
[00229] Только в качестве примера, в Таблице 2 указаны примерные комбинации WT-ITR.
[00230] Таблица 2: Примерные комбинации WT-ITR из одного и того же серотипа или разных серотипов, или разных парвовирусов. Показанный порядок не указывает на положение ITR, например, «ААВ1, ААВ2» демонстрирует, что зкДНК может содержать WT-ITR ААВ1 в 5´-положении и WT-ITR ААВ2 в 3´-положении или наоборот WT-ITR ААВ2 в 5´-положении, а WT-ITR ААВ1 в 3´-положении. Сокращения: ААВ серотипа 1 (ААВ1), ААВ серотипа 2 (ААВ2), ААВ серотипа 3 (ААВ3), ААВ серотипа 4 (ААВ4), ААВ серотипа 5 (ААВ5), ААВ серотипа 6 (ААВ6), ААВ серотипа 7 (ААВ7), ААВ серотипа 8 (ААВ8), серотипа ААВ 9 (ААВ9), серотипа ААВ 10 (ААВ10), серотипа ААВ 11 (ААВ11) или серотипа ААВ 12 (ААВ12); геном ААВrh8, ААВrh10, ААВ-DJ и ААВ-DJ8 (например, NCBI: NC 002077; NC 001401; NC001729; NC001829; NC006152; NC 006260; NC 006261), ITR из теплокровных животных (птичий ААВ (ПААВ), бычий ААВ (БААВ), собачий, лошадиный и овечий ААВ), ITR из парвовируса B19 (номер доступа в GenBank: NC 000883), мелкого мышиного вируса (MVM) (номер доступа в GenBank NC 001510); гусь: гусиного парвовируса (номер доступа в GenBank NC 001701); змея: змеиного парвовируса 1 (номер доступа в GenBank NC 006148).
Таблица 2
[00231] Только в качестве примера, в Таблице 3 показаны последовательности примерных WT-ITR из некоторых различных серотипов ААВ.
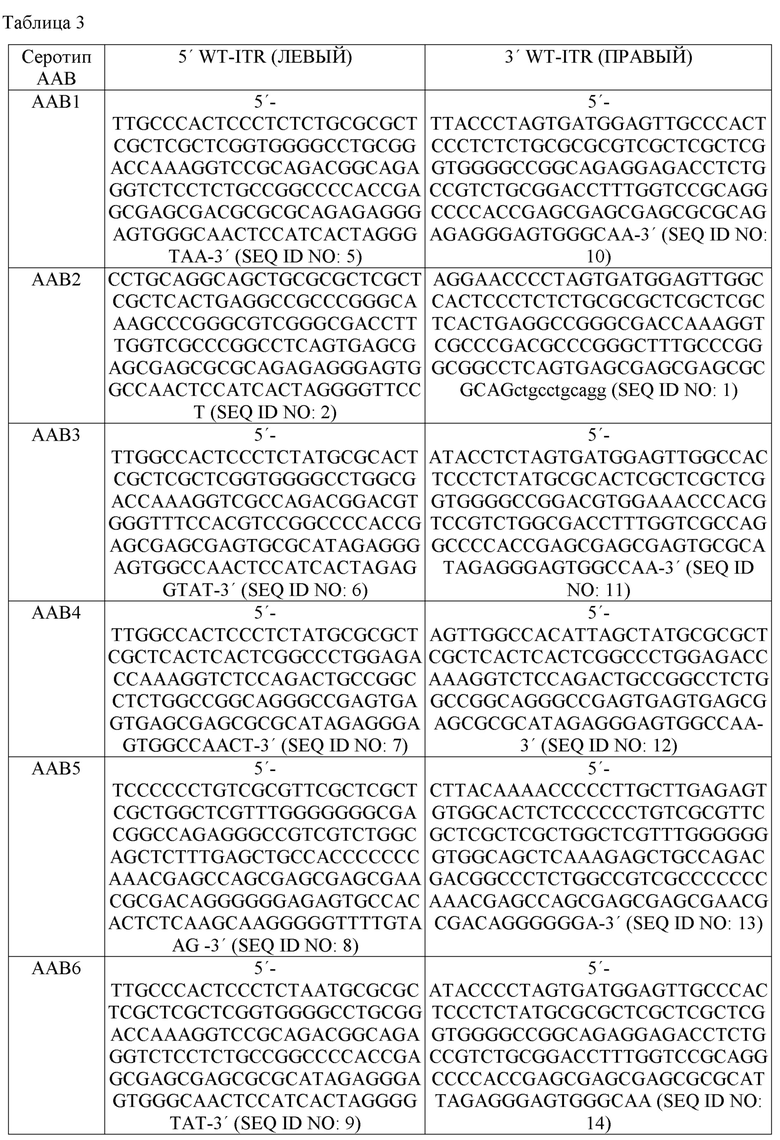
[00232] Согласно некоторым вариантам реализации нуклеотидная последовательность последовательности WT-ITR может быть модифицирована (например, путем модификации 1, 2, 3, 4 или 5 или более нуклеотидов или любого их диапазона), при этом указанная модификация представляет собой замену комплементарным нуклеотидом, например, G для C, и наоборот, и T для A, и наоборот.
[00233] Согласно определенным вариантам реализации настоящего изобретения зкДНК-вектор для экспрессии белка PAH не имеет WT-ITR, состоящего из нуклеотидной последовательности, выбранной из любой из: SEQ ID NO: 1, 2, 5-14. Согласно альтернативным вариантам реализации настоящего изобретения, если зкДНК-вектор имеет WT-ITR, содержащий нуклеотидную последовательность, выбранную из любой из: SEQ ID NO: 1, 2, 5-14, то фланкирующий ITR также представляет собой WT, и зкДНК-вектор содержит регуляторный переключатель, например, как раскрыто в данном документе и в международной заявке PCT/US18/49996 (например, см. Таблицу 11 PCT/US18/49996, которая полностью включена в данный документ посредством ссылки). Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH содержит регуляторный переключатель, как раскрыто в данном документе, и выбранный WT-ITR, имеющий нуклеотидную последовательность, выбранную из любой из группы, состоящей из: SEQ ID NO: 1, 2, 5-14.
[00234] ЗкДНК-вектор, для экспрессии белка PAH, описанный в данном документе, может включать структуры WT-ITR, которые сохраняют функциональные части RBE, trs и RBE´. ФИГ. 2А и ФИГ. 2В, с использованием ITR дикого типа для иллюстративных целей, показывают один возможный механизм функционирования сайта trs внутри части структуры ITR дикого типа зкДНК-вектора. Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH содержит одну или более функциональных полинуклеотидных последовательностей WT-ITR, которые содержат Rep-связывающий сайт (RBS; 5´-GCGCGCTCGCTCGCTC-3´ (SEQ ID NO: 60) для ААВ2) и сайт концевого разрешения (TRS; 5´-AGTT (SEQ ID NO: 62)). Согласно некоторым вариантам реализации по меньшей мере один WT-ITR является функциональным. Согласно альтернативным вариантам реализации, в которых зкДНК-вектор для экспрессии белка PAH содержит два WT-ITR, которые по существу симметричны друг другу, по меньшей мере один WT-ITR является функциональным и по меньшей мере один WT-ITR является нефункциональным.
B. Модифицированные ITR (mod-ITR) в целом для зкДНК-векторов, содержащих пары асимметричных ITR или пары симметричных ITR
[00235] Как обсуждается в данном документе, зкДНК-вектор для экспрессии белка PAH может содержать пару симметричных ITR или пару асимметричных ITR. В обоих случаях один или оба из ITR могут представлять собой модифицированные ITR - различие заключается в том, что в первом случае (то есть симметричные mod-ITR), mod-ITR имеют одинаковую трехмерную пространственную организацию (т. е. имеют одинаковые конфигурации плеча A-A´, C-C´ и B-B´), в то время как во втором случае (т. е. асимметричные mod-ITR), mod-ITR имеют разную трехмерную пространственную организацию (т. е. имеют разную конфигурацию плеч A-A´, C-C´ и B-B´).
[00236] Согласно некоторым вариантам реализации модифицированный ITR представляет собой ITR, который модифицирован путем делеции, вставки и/или замены по сравнению с последовательностью ITR дикого типа (например, ITR ААВ). Согласно некоторым вариантам реализации по меньшей мере один из ITR в зкДНК-векторе содержит функциональный сайт связывания Rep (RBS; например, 5´-GCGCGCTCGCTCGCTC-3´ для ААВ2, SEQ ID NO 60) и функциональный сайт концевого разрешения (TRS; например, 5′-AGTT-3´, SEQ ID NO: 62.) В одном варианте реализации по меньшей мере один из ITR представляет собой нефункциональный ITR. Согласно одному варианту реализации не каждый из разных или модифицированных ITR представляет собой ITR дикого типа из разных серотипов.
[00237] Конкретные изменения и мутации в ITR подробно описаны в данном документе, но в контексте ITR «измененный», «мутированный» или «модифицированный» указывает на то, что нуклеотиды были вставлены, удалены и/или заменены относительно дикого типа, референса или исходной последовательности ITR. Измененный или мутированный ITR может представлять собой сконструированный ITR. В данном документе термин «сконструированный» относится к аспекту манипулирования человеком. Например, полипептид считается «сконструированным», когда по меньшей мере один аспект полипептида, например, его последовательность, подвергся манипуляции человеком, чтобы отличаться от аспекта, который существует в природе.
[00238] Согласно некоторым вариантам реализации mod-ITR может быть синтетическим. Согласно одному варианту реализации синтетический ITR основан на последовательностях ITR более чем из одного серотипа ААВ. Согласно другому варианту реализации синтетический ITR не включает последовательность на основе ААВ. В еще одном варианте реализации синтетический ITR сохраняет структуру ITR, описанную выше, хотя имеет только некоторую часть последовательности, полученной из ААВ, или не имеет ее. Согласно некоторым аспектам синтетический ITR преимущественно может взаимодействовать с Rep дикого типа или Rep конкретного серотипа, или в некоторых случаях не будет распознаваться Rep дикого типа и будет распознаваться только мутированным Rep.
[00239] Квалифицированный специалист может определить соответствующую последовательность в других серотипах с помощью известных средств. Например, определение того, происходит ли изменение в области A, A´, B, B´, C, C´ или D, и определение соответствующей области в другом серотипе. Для определения соответствующей последовательности можно использовать BLAST® (Basic Local Alignment Search Tool) или другие программы гомологического выравнивания с параметрами по умолчанию. Согласно настоящему изобретению также предложены популяции и множество зкДНК-векторов, содержащих mod-ITR из комбинации различных серотипов ААВ, то есть один mod-ITR может происходить из одного серотипа ААВ, а другой mod-ITR может происходить из другого серотипа. Не ограничиваясь какой-либо теорией, согласно одному варианту реализации один ITR может происходить или основываться на последовательности ITR ААВ2, а другой ITR зкДНК-вектора может происходить или основываться на любой одной или более последовательностях ITR ААВ серотипа 1 (ААВ1), ААВ серотипа 4 (ААВ4), ААВ серотипа 5 (ААВ5), ААВ серотипа 6 (ААВ6), ААВ серотипа 7 (ААВ7), ААВ серотипа 8 (ААВ8), ААВ серотипа 9 (ААВ9), ААВ серотипа 10 (ААВ10), ААВ серотипа 11 (ААВ11) или ААВ серотипа 12 (ААВ12).
[00240] Любой ITR парвовируса можно применять в качестве ITR или основного ITR для модификации. Предпочтительно парвовирус представляет собой депендовирус. Более предпочтительно ААВ. Выбранный серотип может быть основан на тканевом тропизме серотипа. ААВ2 обладает широким тканевым тропизмом, ААВ1 преимущественно нацелен на нейроны и скелетные мышцы, а ААВ5 преимущественно нацелен на нейроны, пигментный эпителий сетчатки и фоторецепторы. ААВ6 преимущественно нацелен на скелетные мышцы и легкие. ААВ8 преимущественно нацелен на печень, скелетные мышцы, сердце и ткани поджелудочной железы. ААВ9 преимущественно нацелен на печень, скелетную и легочную ткань. Согласно одному варианту реализации модифицированный ITR основан на ITR ААВ2.
[00241] Более конкретно, способность структурного элемента функционально взаимодействовать с конкретным большим белком Rep может быть изменена путем модификации структурного элемента. Например, нуклеотидная последовательность структурного элемента может быть модифицирована по сравнению с последовательностью ITR дикого типа. Согласно одному варианту реализации структурный элемент (например, плечо A, плечо A´, плечо B, плечо B´, плечо C, плечо C´, плечо D, RBE, RBE´ и trs) ITR можно удалить и заменить структурным элементом дикого типа из другого парвовируса. Например, заменяющая структура может происходить из ААВ1, ААВ2, ААВ3, ААВ4, ААВ5, ААВ6, ААВ7, ААВ8, ААВ9, ААВ10, ААВ11, ААВ12, ААВ13, змеиного парвовируса (например, парвовируса королевского питона), бычьего парвовируса, козьего парвовируса, птичьего парвовируса, собачьего парвовируса, лошадиного парвовируса, парвовируса креветок, свиного парвовируса или ААВ насекомых. Например, ITR может представлять собой ITR ААВ2, а плечо A или A´ или RBE могут быть заменены структурным элементом из ААВ5. В другом примере ITR может представлять собой ITR ААВ5, а плечи C или C´, RBE и trs могут быть заменены структурным элементом из ААВ2. В другом примере ITR ААВ может представлять собой ITR ААВ5, в котором плечи B и B´ заменены B и B´ ITR ААВ2.
[00242] Только в качестве примера, в Таблице 4 указаны примерные модификации по меньшей мере одного нуклеотида (например, делеция, вставка и/или замена) в областях модифицированного ITR, где X указывает на модификацию по меньшей мере одной нуклеиновой кислоты (например, делецию, вставку и/или замену) в этом участке относительно соответствующего ITR дикого типа. Согласно некоторым вариантам реализации любая модификация по меньшей мере одного нуклеотида (например, делеция, вставка и/или замена) в любой из областей C и/или C´, и/или B, и/или B´ сохраняет три последовательных нуклеотида T (т. е. TTT) по меньшей мере в одной концевой петле. Например, если модификация приводит к получению любого из: одноплечевого ITR (например, одно плечо C-C´ или одно плечо B-B´), или модифицированного плеча C-B´ или плеча C´-B, или двухплечевого ITR по меньшей мере с одним усеченным плечом (например, усеченным плечом C-C´ и/или усеченным плечом B-B´), по меньшей мере одно плечо или по меньшей мере одно из двух плеч ITR (где одно плечо может быть усечено) сохраняет три последовательных нуклеотида Т (т. е. ТТТ) по меньшей мере в одной концевой петле. Согласно некоторым вариантам реализации усеченное плечо C-C´ и/или усеченное плечо B-B´ имеет три последовательных Т-нуклеотида (т. е. TTT) в концевой петле.
[00243] Таблица 4: Примерные комбинации модификаций по меньшей мере одного нуклеотида (например, делеция, вставка и/или замена) в различных областях или плечах B-B´ и C-C´ ITR (X указывает модификацию нуклеотида, например, добавление, делецию или замену по меньшей мере одного нуклеотида в области).
[00244] Согласно некоторым вариантам реализации mod-ITR для применения в зкДНК-векторе для экспрессии белка PAH содержит пару асимметричных ITR или пару симметричных mod-ITR, как раскрыто в данном документе, может содержать любую из комбинаций модификаций, показанных в Таблице 4, а также модификацию по меньшей мере одного нуклеотида в любой одной или более областях, выбранных из: между A´ и C, между C и C´, между C´ и B, между B и B´ и между B´ и A. Согласно некоторым вариантам реализации любая модификация по меньшей мере одного нуклеотида (например, делеция, вставка и/или замена) в областях C или C´, B или B´ по-прежнему сохраняет концевую петлю структуры стебель-петля. Согласно некоторым вариантам реализации любая модификация по меньшей мере одного нуклеотида (например, делеция, вставка и/или замена) между C и C´ и/или B и B´ сохраняет три последовательных нуклеотида T (т. е. TTT) по меньшей мере в одной концевой петле. Согласно альтернативным вариантам реализации любая модификация по меньшей мере одного нуклеотида (например, делеция, вставка и/или замена) между C и C´ и/или B и B´ сохраняет три последовательных нуклеотида A (т. е. AAA) по меньшей мере в одной концевой петле. Согласно некоторым вариантам реализации модифицированный ITR для применения в настоящем изобретении может содержать любую из комбинаций модификаций, показанных в Таблице 4, а также модификацию по меньшей мере одного нуклеотида (например, делецию, вставку и/или замену) в любой одной или более из областей, выбранных из: A´, A и/или D. Например, в некоторых вариантах реализации, модифицированный ITR для применения в настоящем изобретении может содержать любую из комбинаций модификаций, показанных в Таблице 4, а также модификацию по меньшей мере одного нуклеотида (например, делецию, вставку и/или замену) в области A. Согласно некоторым вариантам реализации модифицированный ITR для применения в настоящем изобретении может содержать любую из комбинаций модификаций, показанных в Таблице 4, а также модификацию по меньшей мере одного нуклеотида (например, делецию, вставку и/или замену) в области A´. Согласно некоторым вариантам реализации модифицированный ITR для применения в настоящем изобретении может содержать любую из комбинаций модификаций, показанных в Таблице 4, а также модификацию по меньшей мере одного нуклеотида (например, делецию, вставку и/или замену) в области A и/или A´. Согласно некоторым вариантам реализации модифицированный ITR для применения в настоящем изобретении может содержать любую из комбинаций модификаций, показанных в Таблице 4, а также модификацию по меньшей мере одного нуклеотида (например, делецию, вставку и/или замену) в области D.
[00245] Согласно одному варианту реализации нуклеотидная последовательность структурного элемента может быть модифицирована (например, путем модификации 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20 или более нуклеотидов или любого их диапазона) для получения модифицированного структурного элемента. Согласно одному варианту реализации конкретные модификации ITR приведены в данном документе в качестве примеров (например, SEQ ID NO: 3, 4, 15-47, 101-116 или 165-187, или показанные на ФИГ. 7A-7B из PCT/US2018/064242, поданной 6 декабря 2018 г. (например, SEQ ID NO 97-98, 101-103, 105-108, 111-112, 117-134, 545-54 в PCT/US2018/064242). Согласно некоторым вариантам реализации ITR может быть модифицирован (например, путем модификации 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20 или более нуклеотидов или любого их диапазона). Согласно другим вариантам реализации ITR может иметь по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или более идентичности последовательности с одним из модифицированных ITR, имеющих SEQ ID NO: 3, 4, 15-47, 101-116 или 165-187, или с участком, содержащий RBE, плеча A-A´ и плеч C-C´ и B-B´, имеющих SEQ ID NO: 3, 4, 15-47, 101-116 или 165-187, или показанных в Таблицах 2-9 (т. е. SEQ ID NO: 110-112, 115-190, 200-468) международной заявки PCT/US18/49996, которая полностью включена в данный документ посредством ссылки.
[00246] Согласно некоторым вариантам реализации модифицированный ITR может, например, содержать удаление или делецию всего конкретного плеча, например, всего или части плеча A-A´, или всего или части плеча B-B´, или всего или части плеча C-C´, или, альтернативно, удаление 1, 2, 3, 4, 5, 6, 7, 8, 9 или более пар оснований, образующих стебель петли, при условии, что конечная петля, кэпирующая стебель (например, одно плечо), все еще присутствует (например, см. ITR-21 на ФИГ. 7A из PCT/US2018/064242, поданной 6 декабря 2018 г., полностью включенной в данный документ посредством ссылки). Согласно некоторым вариантам реализации модифицированный ITR может содержать удаление 1, 2, 3, 4, 5, 6, 7, 8, 9 или более пар оснований из плеча B-B´. Согласно некоторым вариантам реализации модифицированный ITR может содержать удаление 1, 2, 3, 4, 5, 6, 7, 8, 9 или более пар оснований из плеча C-C´(см., например, ITR-1 на ФИГ. 3B или ITR-45 на ФИГ. 7A из PCT/US2018/064242, поданной 6 декабря 2018 г., полностью включенной в данный документ посредством ссылки). Согласно некоторым вариантам реализации модифицированный ITR может содержать удаление 1, 2, 3, 4, 5, 6, 7, 8, 9 или более пар оснований из плеча C-C´ и удаление 1, 2, 3, 4, 5, 6, 7, 8, 9 или более пар оснований из плеча B-B´. Предусмотрена любая комбинация удаления пар оснований, например, могут быть удалены 6 пар оснований в плече C-C´ и 2 пары оснований в плече B-B´. В качестве иллюстративного примера, ФИГ. 3B показывает примерный модифицированный ITR по меньшей мере с 7 парами оснований, удаленными из каждой из части C и части C´, заменой нуклеотида в петле между областями C и C´ и делецией по меньшей мере одной пары оснований из каждой из области B и областей B´ так, что модифицированный ITR содержит два плеча, из которых по меньшей мере одно плечо (например, C-C´) усечено. Согласно некоторым вариантам реализации модифицированный ITR также содержит делецию по меньшей мере одной пары оснований из каждой из области B и областей B´ так, что плечо B-B´ также усечено относительно WT-ITR.
[00247] Согласно некоторым вариантам реализации модифицированный ITR может иметь от 1 до 50 (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49 или 50) делеций нуклеотидов относительно полноразмерной последовательности ITR дикого типа. Согласно некоторым вариантам реализации модифицированный ITR может иметь от 1 до 30 делеций нуклеотидов относительно полноразмерной последовательности WT-ITR. Согласно некоторым вариантам реализации модифицированный ITR имеет от 2 до 20 делеций нуклеотидов относительно полноразмерной последовательности ITR дикого типа.
[00248] Согласно некоторым вариантам реализации модифицированный ITR не содержит никаких делеций нуклеотидов в RBE-содержащей части областей A или A´, чтобы не препятствовать репликации ДНК (например, связывание RBE белком Rep или образование одноцепочечного разрыва в сайте концевого разрешения). Согласно некоторым вариантам реализации модифицированный ITR, предусмотренный для применения в данном документе, имеет одну или более делеций в области B, B´, C и/или C, как описано в данном документе.
[00249] Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH, содержащий пару симметричных ITR или пару асимметричных ITR, содержит регуляторный переключатель, как раскрыто в данном документе, и по меньшей мере один выбранный модифицированный ITR, имеющий нуклеотидную последовательность, выбранную из любой из группы, состоящей из: SEQ ID NO: 3, 4, 15-47, 101-116 или 165-187.
[00250] Согласно другому варианту реализации структура структурного элемента может быть модифицирована. Например, структурный элемент имеет изменение высоты стебля и/или количества нуклеотидов в петле. Например, высота стебля может составлять примерно 2, 3, 4, 5, 6, 7, 8 или 9 нуклеотидов или более или любое значение в пределах указанного диапазона. Согласно одному варианту реализации высота стебля может составлять от примерно 5 нуклеотидов до примерно 9 нуклеотидов и он функционально взаимодействует с Rep. Согласно другому варианту реализации высота стебля может составлять примерно 7 нуклеотидов и он функционально взаимодействует с Rep. В другом примере петля может иметь 3, 4, 5, 6, 7, 8, 9 или 10 нуклеотидов или более или любое значение в пределах указанного диапазона.
[00251] Согласно другому варианту реализации количество сайтов связывания GAGY или родственных GAGY сайтов связывания в RBE или продленном RBE может быть увеличено или уменьшено. В одном примере RBE или продленный RBE может содержать 1, 2, 3, 4, 5 или 6 или более сайтов связывания GAGY или любое значение в пределах указанного диапазона. Каждый сайт связывания GAGY может независимо представлять собой точную последовательность GAGY или последовательность, сходную с GAGY, при условии, что последовательность достаточна для связывания белка Rep.
[00252] Согласно другому варианту реализации расстояние между двумя элементами (такими как, но не ограничиваясь перечисленными, RBE и шпилька) может быть изменено (например, увеличено или уменьшено) для изменения функционального взаимодействия с большим белком Rep. Например, расстояние может составлять примерно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или 21 нуклеотид или более или любое значение в пределах указанного диапазона.
[00253] зкДНК-вектор для экспрессии белка PAH, описанный в данном документе, может включать структуру ITR, которая модифицирована относительно структуры ITR дикого типа ААВ2, раскрытой в данном документе, но все еще сохраняет функциональную часть RBE, trs и RBE´. ФИГ. 2A и ФИГ. 2В показывают один возможный механизм функционирования сайта trs внутри части структуры ITR дикого типа зкДНК-вектора для экспрессии белка PAH. Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH содержит одну или более функциональных полинуклеотидных последовательностей ITR, которые содержат сайт связывания Rep (RBS; 5´-GCGCGCTCGCTCGCTC-3´ (SEQ ID NO: 60) для ААВ2) и сайт концевого разрешения (TRS; 5´-AGTT (SEQ ID NO: 62)). Согласно некоторым вариантам реализации по меньшей мере один ITR (wt или модифицированный ITR) является функциональным. Согласно альтернативным вариантам реализации, когда зкДНК-вектор для экспрессии белка PAH содержит два модифицированных ITR, которые отличаются или асимметричны по отношению друг к другу, по меньшей мере один модифицированный ITR является функциональным и по меньшей мере один модифицированный ITR является нефункциональным.
[00254] Согласно некоторым вариантам реализации модифицированный ITR (например, левый или правый ITR) зкДНК-вектора для экспрессии белка PAH, как описано в данном документе, имеет модификации в плече петли, усеченном плече или спейсере. Примерные последовательности ITR, имеющие модификации в плече петли, усеченном плече или спейсере, перечислены в Таблице 2 (т. е. SEQ ID NO: 135-190, 200-233); Таблице 3 (например, SEQ ID NO: 234-263); Таблице 4 (например, SEQ ID NO: 264-293); Таблице 5 (например, SEQ ID NO: 294-318 в данном документе); Таблице 6 (например, SEQ ID NO: 319-468); и Таблице 7-9 (например, SEQ ID NO: 101-110, 111-112, 115-134) или в Таблице 10A или 10B (например, SEQ ID NO: 9, 100, 469-483, 484-499) международной заявки PCT/US18/49996, которая полностью включена в данный документ посредством ссылки.
[00255] Согласно некоторым вариантам реализации модифицированный ITR для применения в зкДНК-векторе для экспрессии белка PAH, содержащем пару асимметричных ITR или пару симметричных mod-ITR, выбирают из любых или из комбинации ITR, приведенных в Таблицах 2, 3, 4, 5, 6, 7, 8, 9 и 10A-10B международной заявки PCT/US18/49996, которая полностью включена в данный документ посредством ссылки.
[00256] Дополнительные примерные модифицированные ITR для применения в зкДНК-векторе для экспрессии белка PAH, содержащем пару асимметричных ITR или пару симметричных mod-ITR в каждом из указанных выше классов, представлены в Таблицах 5A и 5B. Прогнозируемая вторичная структура правых модифицированных ITR в Таблице 5A показана на ФИГ. 7A международной заявки PCT/US2018/064242, поданной 6 декабря 2018 г., и прогнозируемая вторичная структура левых модифицированных ITR в Таблице 5B показана на ФИГ. 7B международной заявки PCT/US2018/064242, поданной 6 декабря 2018 г., которая полностью включена в данный документ посредством ссылки.
[00257] В Таблице 5A и Таблице 5B показаны примерные правые и левые модифицированные ITR.
[00258] Таблица 5A: Примерные модифицированные правые ITR. Эти примерные модифицированные правые ITR могут содержать RBE GCGCGCTCGCTCGCTC-3′ (SEQ ID NO: 60), спейсер ACTGAGGC (SEQ ID NO: 69), комплементарную последовательность спейсера GCCTCAGT (SEQ ID NO: 70) и RBE´(т. е. комплементарную последовательность RBE) GAGCGAGCGAGCGCGC (SEQ ID NO: 71).
[00259] Таблица 5B: Примерные модифицированные левые ITR. Эти примерные модифицированные левые ITR могут содержать RBE GCGCGCTCGCTCGCTC-3′ (SEQ ID NO: 60), спейсер ACTGAGGC (SEQ ID NO: 69), комплементарную последовательность спейсера GCCTCAGT (SEQ ID NO: 70) и комплементарную последовательность RBE (т. е. RBE´) GAGCGAGCGAGCGCGC (SEQ ID NO: 71).
[00260] Согласно одному варианту реализации зкДНК-вектор для экспрессии белка PAH содержит, в направлении от 5´ к 3´: первый инвертированный концевой повтор (ITR) аденоассоциированного вируса (ААВ), нуклеотидную последовательность, представляющую интерес (например, экспрессионную кассету, описанную в данном документе), и второй ITR ААВ, причем указанный первый ITR (5´-ITR) и второй ITR (3´-ITR) являются асимметричными по отношению друг к другу, т. е. они имеют разную трехмерную пространственную конфигурацию по отношению друг к другу. В качестве примерного варианта реализации первый ITR может представлять собой ITR дикого типа, а второй ITR может представлять собой мутированный или модифицированный ITR или наоборот первый ITR может представлять собой мутированный или модифицированный ITR, а второй ITR может представлять собой ITR дикого типа. Согласно некоторым вариантам реализации первый ITR и второй ITR оба представляют собой mod-ITR, но имеют разные последовательности или разные модификации и, таким образом, не являются одинаковыми модифицированными ITR и имеют разные трехмерные пространственные конфигурации. Другими словами, зкДНК-вектор с асимметричными ITR содержит ITR, в которых любые изменения в одном ITR относительно WT-ITR не отражаются в другом ITR; или, альтернативно, если асимметричные ITR имеют пару модифицированных асимметричных ITR, они могут иметь различную последовательность и различную трехмерную форму по отношению друг к другу. Примерные асимметричные ITR в зкДНК-векторе для экспрессии белка PAH и для применения в получении зкДНК-плазмиды показаны в Таблицах 5A и 5B.
[00261] Согласно альтернативному варианту реализации зкДНК-вектор для экспрессии белка PAH содержит два симметричных mod-ITR, то есть оба ITR имеют одинаковую последовательность, но обратно комплементарны (инвертированы) друг другу. Согласно некоторым вариантам реализации пара симметричных mod-ITR содержит по меньшей мере одну или любую комбинацию делеции, вставки или замены относительно последовательности ITR дикого типа из того же серотипа ААВ. Добавления, делеции или замены в симметричных ITR одинаковы, но обратно комплементарны друг другу. Например, вставка 3 нуклеотидов в области C 5´-ITR будет отражаться во вставке 3 обратно комплементарных нуклеотидов в соответствующем участке в области C´ 3´-ITR. Исключительно для целей иллюстрации, если добавление представляет собой AACG в 5´-ITR, добавление представляет собой CGTT в 3´-ITR в соответствующем сайте. Например, если смысловая цепь 5´-ITR представляет собой ATCGATCG с добавлением AACG между G и A, это дает последовательность ATCGAACGATCG (SEQ ID NO: 51). Соответствующая смысловая цепь 3´-ITR представляет собой CGATCGAT (обратно комплементарная последовательность ATCGATCG) с добавлением CGTT (т. е. обратно комплементарная последовательность AACG) между T и C, что дает последовательность CGATCGTTCGAT (SEQ ID NO: 49) (обратно комплементарная последовательность ATCGAACGATCG) (SEQ ID NO: 51).
[00262] Согласно альтернативным вариантам реализации пара модифицированных ITR по существу симметрична, как определено в данном документе, то есть пара модифицированных ITR может иметь разную последовательность, но иметь соответствующую или одинаковую симметричную трехмерную форму. Например, один модифицированный ITR может происходить из одного серотипа, а другой модифицированный ITR может происходить из другого серотипа, но они имеют одинаковую мутацию (например, вставку, делецию или замену нуклеотидов) в одной и той же области. Другими словами, только для иллюстративных целей, 5´ mod-ITR может происходить из ААВ2 и иметь делецию в области C, а 3´ mod-ITR может происходить из ААВ5 и иметь соответствующую делецию в области C´, и при условии, что 5´ mod-ITR и 3´ mod-ITR имеют одинаковую или симметричную трехмерную пространственную организацию, они предусмотрены для применения в настоящем изобретении в качестве пары модифицированных ITR.
[00263] Согласно некоторым вариантам реализации пара по существу симметричных mod-ITR имеет одинаковые петли A, C-C´ и B-B´ в трехмерном пространстве, например, если модифицированный ITR в паре по существу симметричных mod-ITR имеет делецию плеча C-C´, то когнатный mod-ITR имеет соответствующую делецию петли C-C´, а также имеет сходную трехмерную структуру остальных петель A и B-B´ одинаковой формы в геометрическом пространстве со своим когнатным mod-ITR. Только в качестве примера, по существу симметричные ITR могут иметь симметричную пространственную организацию так, что их структура имеет одинаковую форму в геометрическом пространстве. Это может происходить, например, когда пара G-C модифицирована, например, в пару C-G или наоборот, или когда пара A-T модифицирована в пару T-A, или наоборот. Следовательно, используя приведенный выше иллюстративный пример модифицированного 5´-ITR как ATCGAACGATCG (SEQ ID NO: 51) и модифицированного 3´-ITR как CGATCGTTCGAT (SEQ ID NO: 49) (т. е. обратно комплементарной последовательности для ATCGAACGATCG (SEQ ID NO: 51)), эти модифицированные ITR все равно были бы симметричными, если бы, например, 5´-ITR имел последовательность ATCGAACCATCG (SEQ ID NO: 50), где G в добавлении модифицирован на C, и по существу симметричный 3´-ITR имеет последовательность CGATCGTTCGAT (SEQ ID NO: 49), без соответствующей модификации T в дополнение к a. Согласно некоторым вариантам реализации такая пара модифицированных ITR является по существу симметричной, поскольку пара модифицированных ITR имеет симметричную стереохимию.
[00264] Таблица 6 показывает примерные пары симметричных модифицированных ITR (т. е. левого модифицированного ITR и симметричного правого модифицированного ITR) для применения в зкДНК-векторе для экспрессии белка PAH. Выделенный жирным шрифтом (красным) участок последовательностей идентифицирует часть последовательностей ITR (т. е. последовательности петель A-A´, C-C´ и B-B´). Эти примерные модифицированные ITR могут содержать RBE GCGCGCTCGCTCGCTC-3′ (SEQ ID NO: 60), спейсер ACTGAGGC (SEQ ID NO: 69), комплементарную последовательность спейсера GCCTCAGT (SEQ ID NO: 70) и RBE´ (т. е. комплементарную последовательность RBE) GAGCGAGCGAGCGCGC (SEQ ID NO: 71).
(модифицированный 5´-ITR)
[00265] Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH, содержащий пару асимметричных ITR, может содержать ITR с модификацией, соответствующей любой из модификаций в последовательностях ITR или неполных последовательностях ITR, показанных в любой одной или более из Таблиц 5A-5B в данном документе, или последовательностях, показанных на ФИГ. 7A-7B международной заявки PCT/US2018/064242, поданной 6 декабря 2018 г., которая полностью включена в данный документ, или раскрытых в Таблицах 2, 3, 4, 5, 6, 7, 8, 9 или 10A-10B международной заявки PCT/US18/49996, поданной 7 сентября 2018 г., полностью включенной в данный документ посредством ссылки.
I. Примерные зкДНК-векторы
[00266] Как описано выше, настоящее раскрытие относится к рекомбинантным экспрессионным зкДНК-векторам и зкДНК-векторам, которые кодируют белок PAH, содержащим любой из: пары асимметричных ITR, пары симметричных ITR или пары по существу симметричных ITR, как описано выше. Согласно определенным вариантам реализации настоящее раскрытие относится к рекомбинантным зкДНК-векторам для экспрессии белка PAH, имеющим фланкирующие последовательности ITR и трансген, причем указанные последовательности ITR являются асимметричными, симметричными или по существу симметричными по отношению друг к другу, как определено в данном документе, и зкДНК дополнительно содержит нуклеотидную последовательность, представляющую интерес (например, экспрессионную кассету, содержащую нуклеиновую кислоту трансгена), расположенную между фланкирующими ITR, при этом указанная молекула нуклеиновой кислоты лишена последовательностей, кодирующих вирусный капсидный белок.
[00267] Экспрессионный зкДНК-вектор для экспрессии белка PAH может представлять собой любой зкДНК-вектор, который можно удобно подвергнуть методикам рекомбинантной ДНК, включая нуклеотидную последовательность (и), описанную в данном документе, при условии, что по меньшей мере один ITR изменен. ЗкДНК-векторы для экспрессии белка PAH согласно настоящему изобретению совместимы с клеткой-хозяином, в которую должен быть введен зкДНК-вектор. Согласно определенным вариантам реализации зкДНК-векторы могут быть линейными. Согласно определенным вариантам реализации зкДНК-векторы могут существовать как внехромосомные объекты. Согласно определенным вариантам реализации зкДНК-векторы согласно настоящему раскрытию могут содержать элемент (ы), который позволяет интегрировать донорную последовательность в геном клетки-хозяина. В данном документе «трансген» и «гетерологичная нуклеотидная последовательность» являются синонимами и кодируют белок PAH, как описано в данном документе.
[00268] На ФИГ. 1A-1G показаны схемы функциональных компонентов двух неограничивающих плазмид, которые можно применять для получения зкДНК-вектора для экспрессии белка PAH. ФИГ. 1A, 1B, 1D, 1F показывают конструкцию зкДНК-векторов или соответствующих последовательностей зкДНК-плазмид для экспрессии белка PAH. ЗкДНК-векторы не имеют капсидов и могут быть получены из плазмиды, кодирующей, в указанном порядке: первый ITR, кассету экспрессируемого трансгена и второй ITR, причем последовательности первого и второго ITR асимметричны, симметричны или по существу симметричны по отношению друг к другу, как определено в данном документе. ЗкДНК-векторы для экспрессии белка PAH не имеют капсидов и могут быть получены из плазмиды, кодирующей, в указанном порядке: первый ITR, экспрессируемый трансген (белок или нуклеиновую кислоту) и второй ITR, причем последовательности первого и второго ITR асимметричны, симметричны или по существу симметричны по отношению друг к другу, как определено в данном документе. Согласно некоторым вариантам реализации кассета экспрессируемого трансгена включает, при необходимости: энхансер/промотор, одно или более плеч гомологии, донорную последовательность, посттранскрипционный регуляторный элемент (например, WPRE, например, SEQ ID NO: 67)), а также сигнал полиаденилирования и терминации (например, BGH поли(A), например, SEQ ID NO: 68).
[00269] ФИГ. 5 изображает гель, подтверждающий продуцирование зкДНК из нескольких плазмидных конструкций с использованием способа, описанного в Примерах. ЗкДНК-вектор подтверждается характерным профилем полос в геле, как обсуждается в отношении ФИГ. 4A выше и в Примерах.
A. Регуляторные элементы.
[00270] зкДНК-векторы для экспрессии белка PAH, описанные в данном документе, содержащие пару асимметричных ITR или пару симметричных ITR, как определено в данном документе, могут дополнительно содержать конкретную комбинацию цис-регуляторных элементов. Цис-регуляторные элементы включают, но не ограничиваются перечисленными, промотор, рибопереключатель, инсулятор, mir-регулируемый элемент, посттранскрипционный регуляторный элемент, промотор, специфический для ткани и типа клеток, и энхансер. Примерные промоторы перечислены в международной заявке № PCT/US2020/021328, например, в Таблице 7, которая полностью включена в данный документ посредством ссылки. Примерные энхансеры перечислены в международной заявке № PCT/US2020/021328, например, в Таблице 8, которая полностью включена в данный документ посредством ссылки. Согласно некоторым вариантам реализации ITR может действовать как промотор трансгена, например, белка PAH. Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH, описанный в данном документе, содержит дополнительные компоненты для регуляции экспрессии трансгена, например, регуляторные переключатели, описанные в данном документе, для регуляции экспрессии трансгена или аварийный выключатель, который может уничтожить клетку, содержащую зкДНК-вектор, кодирующий белок PAH. Регуляторные элементы, включая регуляторные переключатели, которые можно применять в настоящем изобретении, более подробно обсуждаются в международной заявке PCT/US18/49996, которая полностью включена в данный документ посредством ссылки.
[00271] В вариантах реализации вторая нуклеотидная последовательность включает регуляторную последовательность и нуклеотидную последовательность, кодирующую нуклеазу. Согласно определенным вариантам реализации регуляторная последовательность гена функционально связана с нуклеотидной последовательностью, кодирующей нуклеазу. Согласно определенным вариантам реализации регуляторная последовательность пригодна для контроля экспрессии нуклеазы в клетке-хозяине. Согласно определенным вариантам реализации регуляторная последовательность включает подходящую промоторную последовательность, способную направлять транскрипцию гена, функционально связанного с промоторной последовательностью, такого как нуклеотидная последовательность, кодирующая нуклеазу (нуклеазы) согласно настоящему раскрытию. Согласно определенным вариантам реализации вторая нуклеотидная последовательность включает интронную последовательность, связанную с 5´-концом нуклеотидной последовательности, кодирующей нуклеазу. Согласно определенным вариантам реализации последовательность энхансера обеспечена в 5´-направлении относительно промотора для повышения эффективности промотора. Согласно определенным вариантам реализации регуляторная последовательность включает энхансер и промотор, причем вторая нуклеотидная последовательность включает интронную последовательность в 5´-направлении от нуклеотидной последовательности, кодирующей нуклеазу, при этом интрон включает один или более сайтов расщепления нуклеазой, и при этом промотор функционально связан с нуклеотидной последовательностью, кодирующей нуклеазу.
[00272] зкДНК-векторы для экспрессии белка PAH, полученные синтетическим путем или с использованием метода продуцирования на основе клеток, как описано в данном документе в Примерах, могут дополнительно содержать конкретную комбинацию цис-регуляторных элементов, таких как посттранскрипционный регуляторный элемент WHP (WPRE) (например, SEQ ID NO: 67) и BGH поли(A) (SEQ ID NO: 68). Подходящие экспрессионные кассеты для применения в экспрессионных конструкциях не имеют налагаемого вирусным капсидом ограничения по упаковке.
(i) Промоторы:
[00273] Обычный специалист в данной области техники поймет, что промоторы, используемые в зкДНК-векторах для экспрессии белка PAH, как описано в данном документе, должны быть адаптированы в соответствии с конкретными последовательностями, на которые они оказывают промоторное действие.
[00274] Экспрессионные кассеты зкДНК-вектора для экспрессии белка PAH могут включать промотор, который может влиять на общие уровни экспрессии, а также на клеточную специфичность. В случае экспрессии трансгена, например, экспрессии белка PAH, они могут включать высокоактивный немедленный ранний промотор вирусного происхождения. Экспрессионные кассеты могут содержать тканеспецифические эукариотические промоторы для ограничения экспрессии трансгена конкретными типами клеток и снижения токсических эффектов и иммунных ответов, обусловленных нерегулируемой эктопической экспрессией. Согласно некоторым вариантам реализации экспрессионная кассета может содержать промотор или синтетический регуляторный элемент, такой как промотор CAG (SEQ ID NO: 72). Промотор CAG содержит (i) ранний энхансерный элемент цитомегаловируса (CMV), (ii) промотор, первый экзон и первый интрон гена бета-актина курицы, и (iii) акцептор сплайсинга гена бета-глобина кролика. В качестве альтернативы, экспрессионная кассета может содержать промотор альфа-1-антитрипсина (AAT) (SEQ ID NO: 73 или SEQ ID NO: 74), специфический для печени (LP1) промотор (SEQ ID NO: 75 или SEQ ID NO: 76) или промотор фактора удлинения-1-альфа (EF1a) человека (например, SEQ ID NO: 77 или SEQ ID NO: 78). Согласно некоторым вариантам реализации экспрессионная кассета включает один или более конститутивных промоторов, например, ретровирусный LTR-промотор вируса саркомы Рауса (RSV) (необязательно с энхансером RSV) или немедленный ранний промотор цитомегаловируса (CMV) (необязательно с энхансером CMV, например, SEQ ID NO: 79). В качестве альтернативы, можно применять индуцируемый промотор, нативный для трансгена промотор, тканеспецифический промотор или различные промоторы, известные в данной области техники. В соответствии с некоторыми вариантами реализации промотор представляет собой любой промотор или промоторную последовательность, изложенную в международной заявке № PCT/US2020/021328, поданной 6 марта 2020 г., которая полностью включена в данный документ посредством ссылки.
[00275] В соответствии с некоторыми вариантами реализации промотор представляет собой промотор VandenDriessche (VD). В соответствии с некоторыми вариантами реализации промотор VD содержит SEQ ID NO: 191, показанную ниже:
CCGTCTGTCTGCACATTTCGTAGAGCGAGTGTTCCGATACTCTAATCTCCCTAGGCAAGGTTCATATTTGTGTAGGTTACTTATTCTCCTTTTGTTGACTAAGTCAATAATCAGAATCAGCAGGTTTGGAGTCAGCTTGGCAGGGATCAGCAGCCTGGGTTGGAAGGAGGGGGTATAAAAGCCCCTTCACCAGGAGAAGCCGTCACACAGATCCACAAGCTCCTG (SEQ ID NO: 191).
В соответствии с некоторыми вариантами реализации промотор содержит последовательность нуклеиновой кислоты, которая по меньшей мере примерно на 85% идентична SEQ ID NO: 191. В соответствии с некоторыми вариантами реализации промотор содержит последовательность нуклеиновой кислоты, которая по меньшей мере примерно на 90% идентична SEQ ID NO: 191. В соответствии с некоторыми вариантами реализации промотор содержит последовательность нуклеиновой кислоты, которая по меньшей мере примерно на 95% идентична SEQ ID NO: 191. В соответствии с некоторыми вариантами реализации промотор содержит последовательность нуклеиновой кислоты, которая по меньшей мере примерно на 96% идентична SEQ ID NO: 191. В соответствии с некоторыми вариантами реализации промотор содержит последовательность нуклеиновой кислоты, которая по меньшей мере примерно на 97% идентична SEQ ID NO: 191. В соответствии с некоторыми вариантами реализации промотор содержит последовательность нуклеиновой кислоты, которая по меньшей мере примерно на 98% идентична SEQ ID NO: 191. В соответствии с некоторыми вариантами реализации промотор содержит последовательность нуклеиновой кислоты, которая по меньшей мере примерно на 99% идентична SEQ ID NO: 191. В соответствии с некоторыми вариантами реализации промотор состоит из последовательности нуклеиновой кислоты SEQ ID NO: 191.
[00276] Подходящие промоторы могут происходить из вирусов и, соответственно, могут называться вирусными промоторами, или они могут происходить из любого организма, в том числе прокариотических или эукариотических организмов. Для управления экспрессией с помощью любой РНК-полимеразы (например, pol I, pol II, pol III) могут применяться подходящие промоторы. Примерные промоторы включают, но не ограничиваются перечисленными, ранний промотор SV40, промотор длинного концевого повтора (LTR) вируса опухоли молочной железы мыши; большой поздний промотор аденовируса (Ad MLP); промотор вируса простого герпеса (HSV), промотор цитомегаловируса (CMV), такой как область немедленного раннего промотора CMV (CMVIE), промотор вируса саркомы Рауса (RSV), промотор U6 малой ядерной РНК человека (U6, например, SEQ ID NO: 80) (Miyagishi et al., Nature Biotechnology 20, 497-500 (2002)), улучшенный промотор U6 (e.g., Xia et al., Nucleic Acids Res. 2003 Sep. 1; 31(17)), промотор H1 человека (H1) (например, SEQ ID NO: 81 или SEQ ID NO: 155), промотор CAG, промотор альфа-1-антитрипсина человека (HAAT) (например, SEQ ID NO: 82) и т.п. Согласно определенным вариантам реализации указанные промоторы изменяют на их содержащем интрон 3′-конце так, чтобы они включали один или более сайтов расщепления нуклеазами. Согласно определенным вариантам реализации ДНК, содержащая сайт(ы) расщепления нуклеазой, является чужеродной для ДНК промотора.
[00277] Согласно одному варианту реализации используемый промотор представляет собой нативный промотор гена, кодирующего терапевтический белок. Промоторы и другие регуляторные последовательности соответствующих генов, кодирующих терапевтические белки, известны и были охарактеризованы. Используемая промоторная область может дополнительно включать одну или более дополнительных регуляторных последовательностей (например, нативных), например, энхансеров (например, SEQ ID NO: 79 и SEQ ID NO: 83), включая энхансер SV40 (SEQ ID NO: 126).
[00278] Согласно некоторым вариантам реализации промотор также может представлять собой промотор из гена человека, такого как убиквитин С человека (hUbC), актин человека, миозин человека, гемоглобин человека, мышечный креатин человека или металлотионеин человека. Промотор также может представлять собой тканеспецифический промотор, такой как специфический для печени промотор, например, альфа-1-антитрипсина человека (HAAT), природный или синтетический. Согласно одному варианту реализации доставку в печень можно обеспечить с использованием специфичного нацеливания на эндогенный ApoE композиции, содержащей зкДНК-вектор, которую направляют в гепатоциты за счет рецептора липопротеина низкой плотности (ЛНП), присутствующего на поверхности гепатоцита.
[00279] еограничивающие примеры промоторов, подходящих для применения в соответствии с настоящим изобретением, включают любой из следующих: промотор CAG, например, (SEQ ID NO: 72), промотор HAAT (SEQ ID NO: 82), промотор EF1-α человека (SEQ ID NO: 77) или фрагмент промотора EF1a (SEQ ID NO: 78), промотор IE2 (например, SEQ ID NO: 84) и промотор EF1-α крысы (SEQ ID NO: 85), промотор mEF1 (SEQ ID NO: 59) или фрагмент промотора 1E1 (SEQ ID NO: 125).
(ii) Энхансеры
[00280] Согласно некоторым вариантам реализации зкДНК, экспрессирующая PAH, содержит один или более энхансеров. Согласно некоторым вариантам реализации последовательность энхансера расположена в 5´-направлении от последовательности промотора. Согласно некоторым вариантам реализации последовательность энхансера расположена в 3´-направлении от последовательности промотора. В соответствии с некоторыми вариантами реализации энхансер представляет собой любой энхансер или энхансерную последовательность, изложенную в международной заявке № PCT/US2020/021328, поданной 6 марта 2020 г., которая полностью включена в данный документ посредством ссылки.
(iii) Последовательности 5´-UTR и интронные последовательности
[00281] Согласно некоторым вариантам реализации зкДНК-вектор содержит последовательность 5´-UTR и/или интронную последовательность, которая расположена в 3´-направлении от последовательности 5´-ITR. Согласно некоторым вариантам реализации 5´-UTR расположена в 5´-направлении от трансгена, например, последовательности, кодирующей белок PAH. Примерные последовательности 5´-UTR перечислены в международной заявке № PCT/US2020/021328, например, в Таблице 9А, которая полностью включена в данный документ посредством ссылки.
(iv) Последовательности 3´-UTR
[00282] Согласно некоторым вариантам реализации зкДНК-вектор содержит последовательность 3´-UTR, которая расположена в 5´-направлении от последовательности 3´-ITR. Согласно некоторым вариантам реализации 3´-UTR расположена в 3´-направлении от трансгена, например, последовательности, кодирующей белок PAH. Примерные последовательности 3´-UTR перечислены в международной заявке № PCT/US2020/021328, например, в Таблице 9В, которая полностью включена в данный документ посредством ссылки.
(v) Последовательности полиаденилирования
[00283] Последовательность, кодирующая последовательность полиаденилирования, может быть включена в зкДНК-вектор для экспрессии белка PAH для стабилизации мРНК, экспрессируемой с указанного зкДНК-вектора, и для содействия ядерному экспорту и трансляции. Согласно одному варианту реализации зкДНК-вектор не включает последовательность полиаденилирования. Согласно другим вариантам реализации зкДНК-вектор для экспрессии белка PAH включает по меньшей мере 1, по меньшей мере 2, по меньшей мере 3, по меньшей мере 4, по меньшей мере 5, по меньшей мере 10, по меньшей мере 15, по меньшей мере 20, по меньшей мере 25, по меньшей мере 30, по меньшей мере 40, по меньшей мере 45, по меньшей мере 50 или более адениновых динуклеотидов. Согласно некоторым вариантам реализации последовательность полиаденилирования содержит примерно 43 нуклеотида, примерно 40-50 нуклеотидов, примерно 40-55 нуклеотидов, примерно 45-50 нуклеотидов, примерно 35-50 нуклеотидов или любой диапазон между указанными значениями.
[00284] Экспрессионные кассеты могут включать любую последовательность полиаденилирования, известную в данной области техники, или ее вариант. Согласно некоторым вариантам реализации последовательность полиаденилирования (поли(A)) выбрана из любой из последовательностей, перечисленных в международной заявке № PCT/US2020/021328, например, в Таблице 10, которая полностью включена в данный документ посредством ссылки. Также можно использовать другие последовательности поли(A), широко известные в данной области техники, например, включая, но не ограничиваясь перечисленными, природную последовательность, выделенную из бычьего BGHpA (например, SEQ ID NO: 68) или SV40pA вируса (например, SEQ ID NO: 86) или синтетическую последовательность (SEQ ID NO: 87). Некоторые экспрессионные кассеты также могут включать последовательность 5´-энхансера позднего поли(А)-сигнала (USE) SV40. Согласно некоторым вариантам реализации последовательность USE можно применять в комбинации с SV40pA или гетерологичным сигналом поли(A). Последовательности поли(A) расположены в 3´-направлении от трансгена, кодирующего белок PAH.
[00285] Экспрессионные кассеты также могут включать посттранскрипционный элемент для повышения экспрессии трансгена. Согласно некоторым вариантам реализации для повышения экспрессии трансгена применяют посттранскрипционный регуляторный элемент вируса гепатита североамериканского сурка (WPRE) (например, SEQ ID NO: 67). Можно применять другие элементы посттранскрипционного процессинга, такие как посттранскрипционный элемент из гена тимидинкиназы вируса простого герпеса или вируса гепатита B (HBV). С трансгенами могут быть связаны секреторные последовательности, например, последовательности VH-02 и VK-A26, например, SEQ ID NO: 88 и SEQ ID NO: 89.
(vi) Последовательности ядерной локализации
[00286] Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH содержит одну или более последовательностей ядерной локализации (NLS), например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более NLS. Согласно некоторым вариантам реализации одна или более NLS расположены на амино-конце или рядом с ним, на карбокси-конце или рядом с ним, или в их комбинации (например, одна или более NLS на амино-конце и/или одна или более NLS на карбокси-конце). В случае присутствия более чем одной NLS, каждая из них может быть выбрана независимо от других так, что одна NLS будет присутствовать более чем в одной копии и/или в комбинации с одной или более другими NLS, присутствующими в одной или более копиях. Неограничивающие примеры NLS приведены в Таблице 7.
Таблица 7: Сигналы ядерной локализации
B. Дополнительные компоненты зкДНК-векторов
[00287] зкДНК-векторы для экспрессии белка PAH согласно настоящему раскрытию могут содержать нуклеотиды, которые кодируют другие компоненты для экспрессии гена. Например, для выбора событий нацеливания на конкретные гены защитная кшРНК может быть встроена в микроРНК и вставлена в рекомбинантный зкДНК-вектор, предназначенный для сайт-специфической интеграции в высокоактивный локус, такой как локус альбумина. Такие варианты реализации могут обеспечивать систему для отбора и размножения генетически модифицированных гепатоцитов in vivo в любом генетическом окружении, например, как описано в Nygaard et al., A universal system to select gene-modified hepatocytes in vivo, Gene Therapy, June 8, 2016. ЗкДНК-векторы согласно настоящему раскрытию могут содержать один или более селективных маркеров, которые позволяют проводить селекцию трансформированных, трансфицированных, трансдуцированных или подобных клеток. Селективный маркер представляет собой ген, продукт которого обеспечивает биоцидную или вирусную устойчивость, устойчивость к тяжелым металлам, прототрофию ауксотрофам, NeoR и т.п. Согласно определенным вариантам реализации в донорные последовательности включены маркеры для положительной селекции, такие как NeoR. Маркеры для отрицательной селекции могут быть включены после донорных последовательностей, например, последовательность нуклеиновой кислоты HSV-tk, кодирующая маркер для отрицательной селекции, может быть включена в конструкцию нуклеиновой кислоты после донорной последовательности.
C. Регуляторные переключатели
[00288] Молекулярный регуляторный переключатель представляет собой переключатель, который генерирует измеряемое изменение состояния в ответ на сигнал. Такие регуляторные переключатели можно подходящим образом комбинировать с зкДНК-векторами для экспрессии белка PAH, описанными в данном документе, чтобы контролировать выход экспрессии белка PAH с зкДНК-вектора. Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH содержит регуляторный переключатель, который служит для тонкой настройки экспрессии белка PAH. Например, он может выполнять функцию биосдерживания зкДНК-вектора. Согласно некоторым вариантам реализации переключатель представляет собой двухпозиционный («ON/OFF») переключатель, который предназначен для запуска или остановки (т. е. прекращения) экспрессии белка PAH в зкДНК-векторе контролируемым и регулируемым образом. Согласно некоторым вариантам реализации указанный переключатель может включать «аварийный выключатель», который может давать клетке, содержащей указанный зкДНК-вектор, команду для запуска механизма запрограммированной клеточной смерти после активации переключателя. Примерные регуляторные переключатели, предусмотренные для применения в зкДНК-векторе для экспрессии белка PAH, могут применяться для регуляции экспрессии трансгена и более подробно обсуждаются в международной заявке PCT/US18/49996, которая полностью включена в данный документ посредством ссылки
(i) Бинарные регуляторные переключатели
[00289] Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH содержит регуляторный переключатель, который может служить для контролируемой модуляции экспрессии белка PAH. Например, экспрессионная кассета, расположенная между ITR зкДНК-вектора, может дополнительно содержать регуляторную область, например, промотор, цис-элемент, репрессор, энхансер и т. д., которая функционально связана с последовательностью нуклеиновой кислоты, кодирующей белок PAH, причем указанная регуляторная область регулируется одним или более кофакторами или экзогенными агентами. В качестве неограничивающего примера, регуляторные области могут модулироваться низкомолекулярными переключателями или индуцируемыми или репрессируемыми промоторами. Неограничивающие примеры индуцируемых промоторов представляют собой индуцируемые гормонами или индуцируемые металлами промоторы. Другие примерные индуцируемые промоторные/энхансерные элементы включают, но не ограничиваются перечисленными, индуцируемый RU486 промотор, индуцируемый экдизоном промотор, индуцируемый рапамицином промотор и промотор металлотионеина.
(ii) Низкомолекулярные регуляторные переключатели
[00290] Различные известные из уровня техники регуляторные переключатели на основе малых молекул известны в данной области техники и могут быть скомбинированы с зкДНК-векторами для экспрессии белка PAH, раскрытыми в данном документе, с получением контролируемого регуляторным переключателем зкДНК-вектора. Согласно некоторым вариантам реализации регуляторный переключатель может быть выбран из чего-либо одного или комбинации следующего: пара ортогональный лиганд/ядерный рецептор, например, вариант ретиноидного рецептора/LG335 и GRQCIMFI, вместе с искусственным промотором, контролирующим экспрессию функционально связанного трансгена, как раскрыто в Taylor et al. BMC Biotechnology 10 (2010): 15; сконструированные рецепторы стероидов, например, модифицированный рецептор прогестерона с усеченным С-концом, который не может связывать прогестерон, но связывает RU486 (мифепристон) (патент США № 5364791); рецептор экдизона дрозофилы (Drosophila) и его экдистероидные лиганды (Saez, et al., PNAS, 97(26)(2000), 14512-14517); или переключатель, контролируемый антибиотиком триметопримом (TMP), как раскрыто в Sando R 3rd; Nat Methods. 2013, 10(11):1085-8. Согласно некоторым вариантам реализации регуляторный переключатель для контроля трансгена или экспрессируемый зкДНК-вектором представляет собой переключатель для активации пролекарств, такой как раскрытые в патентах США 8771679 и 6339070, которые полностью включены в данный документ посредством ссылки.
(iii) Регуляторные переключатели «с кодом доступа»
[00291] Согласно некоторым вариантам реализации регуляторный переключатель может представлять собой «переключатель с кодом доступа» или «контур с кодом доступа». Переключатели с кодом доступа позволяют точно настроить контроль экспрессии трансгена с зкДНК-вектора при возникновении конкретных условий, т. е. для осуществления экспрессии и/или репрессии трансгена должна иметься комбинация условий. Например, для осуществления экспрессии трансгена должны возникнуть по меньшей мере условия A и B. Регуляторный переключатель с кодом доступа может представлять собой любое число условий, например, по меньшей мере 2 или по меньшей мере 3, или по меньшей мере 4, или по меньшей мере 5, или по меньшей мере 6, или по меньшей мере 7 или более условий, наличие которых необходимо для осуществления экспрессии трансгена. Согласно некоторым вариантам реализации должны возникнуть по меньшей мере 2 условия (например, условия A, B), а в некоторых вариантах реализации должны возникнуть по меньшей мере 3 условия (например, A, B и C или A, B и D). Только в качестве примера, для осуществления экспрессии гена с зкДНК, содержащей регуляторный переключатель с кодом доступа «ABC», требуется наличие условий A, B и C. Условия A, B и C могут быть следующими; условие A представляет собой наличие состояния или заболевания, условие B представляет собой гормональный ответ, и условие C представляет собой ответ на экспрессию трансгена. Например, если трансген редактирует дефектный ген EPO, то условием A является наличие хронической болезни почек (ХБП), условие B осуществляется при наличии гипоксических условий в почках субъекта, условие C заключается в нарушении привлечения эритропоэтин-продуцирующих клеток (ЭПК) в почках; или, альтернативно, в нарушении активации HIF-2. При повышении уровней кислорода или достижении целевого уровня EPO трансген снова отключается до момента возникновения 3 условий, которые его опять включат.
[00292] Согласно некоторым вариантам реализации регуляторный переключатель с кодом доступа или «контур с кодом доступа», предусмотренный для применения в зкДНК-векторе, содержит гибридные транскрипционные факторы (TF) для расширения диапазона и уровня сложности сигналов окружающей среды, используемых для определения условий биосдерживания. В отличие от блокирующего (deadman) выключателя, который запускает гибель клетки при наличии заранее определенного условия, «контур с кодом доступа» позволяет обеспечить выживание клеток или экспрессию трансгена при наличии конкретного «кода доступа», и может быть легко перепрограммирован, что позволяет обеспечить экспрессию трансгена и/или выживание клеток только при наличии заранее заданного условия окружающей среды или кода доступа.
[00293] Любые и все комбинации регуляторных переключателей, раскрытых в данном документе, например, низкомолекулярные переключатели, переключатели на основе нуклеиновых кислот, гибридные переключатели на основе малых молекул и нуклеиновых кислот, посттранскрипционные регуляторные переключатели трансгенов, посттрансляционная регуляция, контролируемые излучением переключатели, опосредуемые гипоксией переключатели и другие регуляторные переключатели, известные специалистам в данной области техники, раскрытые в данном документе, могут применяться в регуляторном переключателе с кодом доступа, как раскрыто в данном документе. Регуляторные переключатели, предусмотренные для применения, также обсуждаются в обзорной статье Kis et al., JR Soc Interface. 12: 20141000 (2015) и обобщены в Таблице 1 статьи Kis. Согласно некоторым вариантам реализации регуляторный переключатель для применения в системе с кодом доступа может быть выбран из любых переключателей или их комбинаций, раскрытых в Таблице 11 международной заявки на патент PCT/US18/49996, которая полностью включена в данный документ посредством ссылки.
(iv) Регуляторные переключатели на основе нуклеиновых кислот для контроля экспрессии трансгена
[00294] Согласно некоторым вариантам реализации регуляторный переключатель для контроля белка PAH, экспрессируемого зкДНК, основан на механизме контроля на основе нуклеиновых кислот. Примерные механизмы контроля на основе нуклеиновых кислот известны в данной области техники и предусмотрены для применения. Например, такие механизмы включают рибопереключатели, такие как раскрытые, например, в US2009/0305253, US2008/0269258, US2017/0204477, WO2018026762A1, патенте США 9222093 и заявке на европейский патент EP288071, а также раскрытые в обзорной статье Villa JK et al. Microbiol Spectr. 2018 May;6(3). Также включены чувствительные к метаболитам транскрипционные биосенсоры, такие как раскрытые в WO2018/075486 и WO2017/147585. Другие известные в данной области техники механизмы, предусмотренные для применения, включают подавление трансгена с применением киРНК или молекулы РНКи (например, miR, кшРНК). Например, зкДНК-вектор может содержать регуляторный переключатель, кодирующий молекулу РНКи, которая комплементарна части трансгена, экспрессируемого зкДНК-вектором. При экспрессии такой РНКи, даже если трансген (например, белок PAH) экспрессируется зкДНК-вектором, будет происходить его подавление под действием комплементарной молекулы РНКи, а если РНКи не экспрессируется, при экспрессии трансгена (например, белка PAH) зкДНК-вектором, подавление трансгена под действием РНКи не происходит.
[00295] Согласно некоторым вариантам реализации регуляторный переключатель представляет собой тканеспецифический самоинактивирующийся регуляторный переключатель, например, раскрытый в US2002/0022018, благодаря чему регуляторный переключатель преднамеренно выключает трансген (например, белок PAH) в сайте, где в противном случае экспрессия трансгена могла бы быть неблагоприятной. Согласно некоторым вариантам реализации регуляторный переключатель представляет собой обратимую с помощью рекомбиназы систему экспрессии гена, например, раскрытую в US2014/0127162 и патенте США 8324436.
(v) Посттранскрипционные и посттрансляционные регуляторные переключатели.
[00296] Согласно некоторым вариантам реализации регуляторный переключатель для контроля экспрессии белка PAH зкДНК-вектором представляет собой систему посттранскрипционной модификации. Например, такой регуляторный переключатель может представлять собой рибопереключатель-аптазим, чувствительный к тетрациклину или теофиллину, раскрытый в US2018/0119156, GB201107768, WO2001/064956A3, патенте EP 2707487 и Beilstein et al., ACS Synth. Biol., 2015, 4 (5), pp 526-534; Zhong et al., Elife. 2016 Nov 2;5. pii: e18858. Согласно некоторым вариантам реализации предусмотрено, что обычный специалист в данной области техники может закодировать как трансген, так и ингибиторную киРНК, которая содержит чувствительный к лиганду аптамер (отрицательный переключатель), в результате чего будет получен положительный переключатель, чувствительный к лиганду.
(vi) Другие примерные регуляторные переключатели
[00297] Любой известный регуляторный переключатель может быть использован в зкДНК-векторе для контроля экспрессии белка PAH зкДНК-вектором, включая переключатели, запускаемые изменениями окружающей среды. Дополнительные примеры включают, но не ограничиваются перечисленными; метод BOC согласно Suzuki et al., Scientific Reports 8; 10051 (2018); расширение генетического кода и нефизиологическую аминокислоту; контролируемые излучением или контролируемые ультразвуком положительные/отрицательные (on/off) переключатели (см., например, Scott S. et al., Gene Ther. 2000 Jul;7(13):1121-5; патенты США 5612318; 5571797; 5770581; 5817636; и WO1999/025385A1. Согласно некоторым вариантам реализации регуляторный переключатель контролируется имплантируемой системой, например, раскрытой в патенте США 7840263; US2007/0190028A1, в которой экспрессия гена контролируется одной или более формами энергии, включая электромагнитную энергию, что активирует промоторы, функционально связанные с трансгеном в зкДНК-векторе.
[00298] Согласно некоторым вариантам реализации регуляторный переключатель, предусмотренный для применения в зкДНК-векторе, представляет собой опосредуемый гипоксией или активируемый стрессом переключатель, например, такой как те, которые раскрыты в WO1999060142A2, патентах США 5834306; 6218179; 6709858; US2015/0322410; Greco et al., (2004) Targeted Cancer Therapies 9, S368, полностью включенных в данный документ посредством ссылки, а также элементы FROG, TOAD и NRSE и условно индуцируемые подавляющие элементы, включая элементы ответа на гипоксию (HRE), элементы ответа на воспаление (IRE) и активируемые сдвиговым напряжением элементы (SSAE), например, как раскрыто в патенте США 9394526, полностью включенном в данный документ посредством ссылки. Такой вариант реализации можно применять для «включения» экспрессии трансгена с зкДНК-вектора после ишемии или в ишемических тканях и/или в опухолях.
(vii) «Аварийные выключатели»
[00299] Другие варианты реализации, описанные в данном документе, относятся к зкДНК-вектору для экспрессии белка PAH, описанному в данном документе, содержащему аварийный выключатель. «Аварийный выключатель», раскрытый в данном документе, позволяет уничтожить клетку, содержащую указанный зкДНК-вектор, или подвергнуть ее программируемой клеточной гибели в качестве способа окончательного удаления введенного зкДНК-вектора из системы субъекта. Обычный специалист в данной области техники поймет, что применение «аварийных выключателей» в зкДНК-векторах для экспрессии белка PAH, как правило, будет сопряжено с нацеливанием зкДНК-вектора на ограниченное число клеток, потеря которого является приемлемой для субъекта, или на тип клеток, апоптоз которых желателен (например, на раковые клетки). Во всех аспектах «аварийный выключатель», раскрытый в данном документе, разработан таким образом, чтобы обеспечить быстрое и надежное уничтожение клетки, содержащей зкДНК-вектор, в отсутствие входного сигнала выживания или другого заданного условия. Другими словами, «аварийный выключатель», кодируемый зкДНК-вектором для экспрессии белка PAH, описанным в данном документе, может ограничивать выживание клетки, содержащей зкДНК-вектор, окружающей средой, задаваемой специфическими входными сигналами. Такие «аварийные выключатели» служат для обеспечения функции биологического сдерживания, если потребуется удалить зкДНК-вектор для экспрессии белка PAH у субъекта или обеспечить отсутствие экспрессии с него кодируемого белка PAH.
[00300] Другие «аварийные выключатели», известные обычному специалисту в данной области техники, предусмотрены для применения в зкДНК-векторе для экспрессии белка PAH, раскрытом в данном документе, например, как раскрыто в US2010/0175141; US2013/0009799; US2011/0172826; US2013/0109568, а также «аварийные выключатели», раскрытые в Jusiak et al, Reviews in Cell Biology and Molecular Medicine; 2014; 1-56; Kobayashi et al., PNAS, 2004; 101; 8419-9; Marchisio et al., Int. Journal of Biochem and Cell Biol., 2011; 43; 310-319; и в Reinshagen et al., Science Translational Medicine, 2018, 11, содержание которых полностью включено в данный документ посредством ссылки.
[00301] Соответственно, согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH может содержать конструкцию нуклеиновой кислоты «аварийного выключателя», которая содержит нуклеиновую кислоту, кодирующую эффекторный токсин или репортерный белок, причем экспрессия эффекторного токсина (например, белка смерти) или репортерного белка контролируется с помощью заранее заданного условия. Например, предварительно заданным условием может быть наличие агента окружающей среды, такого как, например, экзогенный агент, без которого клетка по умолчанию будет экспрессировать эффекторный токсин (например, белок смерти) и будет уничтожена. Согласно альтернативным вариантам реализации предварительно заданным условием является наличие двух или более агентов окружающей среды, например, клетка будет выживать только при подаче двух или более необходимых экзогенных агентов, и без какого-либо из них клетка, содержащая зкДНК-вектор, уничтожается.
[00302] Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH модифицируют для включения «аварийного выключателя» для разрушения клеток, содержащих указанный зкДНК-вектор, для эффективной остановки экспрессии трансгена, экспрессируемого указанным зкДНК-вектором (например, экспрессии белка PAH) in vivo. В частности, зкДНК-вектор дополнительно генетически сконструирован для экспрессии белка-переключателя, который не функционирует в клетках млекопитающих в нормальных физиологических условиях. Клетки, экспрессирующие белок-переключатель, будут разрушены только после введения лекарственного средства или воздействия условия окружающей среды, специфически нацеленных на указанный белок-переключатель, что остановит экспрессию терапевтического белка или пептида. Например, сообщалось, что клетки, экспрессирующие тимидинкиназу HSV, могут быть уничтожены при введении таких лекарственных средств как ганцикловир и цитозиндезаминаза. См., например, Dey and Evans, Suicide Gene Therapy by Herpes Simplex Virus-1 Thymidine Kinase (HSV-TK), в Targets in Gene Therapy, под редакцией You (2011); и Beltinger et al., Proc. Natl. Acad. Sci. USA 96(15):8699-8704 (1999). Согласно некоторым вариантам реализации зкДНК-вектор может содержать «аварийный выключатель» на основе киРНК, называемый DISE (гибель, индуцируемая устранением гена выживания, «Death Induced by Survival gene Elimination») (Murmann et al., Oncotarget. 2017; 8:84643-84658. Induction of DISE in ovarian cancer cells in vivo).
VI. Подробное описание способа получения зкДНК-вектора
А. Получение в целом
[00303] Определенные способы получения зкДНК-вектора для экспрессии белка PAH, содержащего пару асимметричных ITR или пару симметричных ITR, как определено в данном документе, описаны в разделе IV международной заявки PCT/US18/49996, поданной 7 сентября 2018 г., которая полностью включена в данный документ посредством ссылки. Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, может быть получен с использованием клеток насекомых, как описано в данном документе. Согласно альтернативным вариантам реализации зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, может быть получен синтетическим способом и, в некоторых вариантах реализации, бесклеточным способом, как раскрыто в международной заявке PCT/US19/14122, поданной 18 января 2019 г., которая полностью включена в данный документ посредством ссылки.
[00304] Как описано в данном документе, согласно одному варианту реализации, зкДНК-вектор для экспрессии белка PAH может быть получен, например, с помощью способа, включающего этапы: a) инкубации популяции клеток-хозяев (например, клеток насекомых), несущих полинуклеотидную матрицу экспрессионной конструкции (например, зкДНК-плазмиду, зкДНК-бакмиду и/или зкДНК-бакуловирус), лишенную последовательностей, кодирующих вирусный капсид, в присутствии белка Rep в условиях, эффективных для индукции продуцирования указанного зкДНК-вектора в клетках-хозяевах и в течение периода времени, достаточного для этого, при этом указанные клетки-хозяева не содержат последовательностей, кодирующих вирусный капсид; и b) сбора и выделения зкДНК-вектора из клеток-хозяев. Присутствие белка Rep индуцирует репликацию векторного полинуклеотида с модифицированным ITR для продуцирования зкДНК-вектора в клетке-хозяине. Однако вирусные частицы (например, вирионы ААВ) не экспрессируются. Таким образом, отсутствует ограничение по размеру, такое как присутствующее в естественных условиях в ААВ-векторах или других вирусных векторах.
[00305] Присутствие зкДНК-вектора, выделенного из клеток-хозяев, может быть подтверждено путем расщепления ДНК, выделенной из клетки-хозяина, рестрикционным ферментом, имеющим один сайт распознавания на зкДНК-векторе, и анализа расщепленного ДНК-материала на неденатурирующем геле для подтверждения присутствия характерных полос линейной и непрерывной ДНК по сравнению с линейной и прерывистой ДНК.
[00306] Согласно еще одному аспекту настоящего изобретения предложено применение линий клеток-хозяев, имеющих стабильно интегрированную в собственный геном полинуклеотидную матрицу для экспрессии ДНК-вектора (зкДНК-матрицу), в получении невирусного ДНК-вектора, например, как описано в Lee, L. et al. (2013) Plos One 8(8): e69879. Предпочтительно Rep добавляют к клеткам-хозяевам при MOI равной примерно 3. Когда линия клеток-хозяев представляет собой линию клеток млекопитающего, например, клетки HEK293, линии клеток могут иметь стабильно интегрированную полинуклеотидную матрицу вектора, и второй вектор, такой как вирус герпеса, может использоваться для введения в клетки белка Rep, что позволяет вырезать и амплифицировать зкДНК в присутствии Rep и вспомогательного вируса.
[00307] Согласно одному варианту реализации клетки-хозяева, используемые для получения зкДНК-векторов для экспрессии белка PAH, описанных в данном документе, представляют собой клетки насекомых, и для доставки как полинуклеотида, который кодирует белок Rep, так и полинуклеотидной матрицы экспрессионной конструкции невирусного ДНК-вектора для зкДНК используют бакуловирус, например, согласно описанию на ФИГ. 4A-4C и в Примере 1. Согласно некоторым вариантам реализации клетку-хозяина конструируют так, чтобы она экспрессировала белок Rep.
[00308] Затем зкДНК-вектор собирают и выделяют из клеток-хозяев. Время сбора и извлечения зкДНК-векторов, описанных в данном документе, из клеток может быть выбрано и оптимизировано так, чтобы достичь продуцирования указанных зкДНК-векторов с высоким выходом. Например, время сбора может быть выбрано с учетом жизнеспособности клеток, морфологии клеток, размножения клеток и т. д. Согласно одному варианту реализации клетки культивируют в достаточных условиях и собирают через достаточное время после инфекции бакуловирусом, чтобы получить зкДНК-векторы, но до начала гибели большинства клеток из-за токсичности бакуловируса. ДНК-векторы могут быть выделены с применением наборов для очистки плазмид, таких как не содержащие эндотоксинов наборы для выделения плазмид (Endo-Free Plasmid Kits) от Qiagen. Другие способы, разработанные для выделения плазмид, также могут быть адаптированы для ДНК-векторов. Обычно могут быть использованы любые способы очистки нуклеиновых кислот.
[00309] ДНК-векторы могут быть очищены с помощью любых способов очистки ДНК, известных специалистам в данной области техники. Согласно одному варианту реализации зкДНК-векторы очищают в виде молекул ДНК. Согласно другому варианту реализации зкДНК-векторы очищают в виде экзосом или микрочастиц.
[00310] Наличие зкДНК-вектора для экспрессии белка PAH может быть подтверждено путем расщепления векторной ДНК, выделенной из клеток, рестрикционным ферментом, имеющим один сайт распознавания на ДНК-векторе, и анализа как расщепленного, так и нерасщепленного ДНК-материала с использованием гель-электрофореза, чтобы подтвердить наличие характерных полос линейной и непрерывной ДНК по сравнению с линейной и прерывистой ДНК. ФИГ. 4C и ФИГ. 4D иллюстрируют один вариант реализации для идентификации наличия зкДНК-векторов с замкнутыми концами, продуцируемых с помощью способов, описанных в данном документе.
B. зкДНК-плазмида
[00311] зкДНК-плазмида представляет собой плазмиду, используемую для последующего получения зкДНК-вектора для экспрессии белка PAH. Согласно некоторым вариантам реализации зкДНК-плазмида может быть сконструирована с использованием известных методик, чтобы обеспечить по меньшей мере элементы, перечисленные далее, в виде функционально связанных компонентов в направлении транскрипции: (1) модифицированную последовательность 5´-ITR; (2) экспрессионную кассету, содержащую цис-регуляторный элемент, например, промотор, индуцируемый промотор, регуляторный переключатель, энхансеры и т.п.; и (3) модифицированную последовательность 3´-ITR, причем указанная последовательность 3´-ITR симметрична относительно последовательности 5´-ITR. Согласно некоторым вариантам реализации экспрессионная кассета, фланкированная ITR, содержит сайт клонирования для введения экзогенной последовательности. Экспрессионная кассета заменяет области, кодирующие rep и cap, геномов ААВ.
[00312] Согласно одному аспекту зкДНК-вектор для экспрессии белка PAH получают из плазмиды, называемой в данном документе «зкДНК-плазмидой», кодирующей, в указанном порядке: первый инвертированный концевой повтор (ITR) аденоассоциированного вируса (ААВ), экспрессионную кассету, содержащую трансген, и мутированный или модифицированный ITR ААВ, причем указанная зкДНК-плазмида лишена последовательностей, кодирующих капсидный белок ААВ. Согласно альтернативным вариантам реализации зкДНК-плазмида кодирует, в указанном порядке: первый (или 5´) модифицированный или мутированный ITR ААВ, экспрессионную кассету, содержащую трансген, и второй (или 3´) модифицированный ITR ААВ, причем указанная зкДНК-плазмида лишена последовательностей, кодирующих капсидный белок ААВ, и при этом указанные 5´- и 3´-ITR являются симметричными по отношению друг к другу. Согласно альтернативным вариантам реализации зкДНК-плазмида кодирует, в указанном порядке: первый (или 5´) модифицированный или мутированный ITR ААВ, экспрессионную кассету, содержащую трансген, и второй (или 3´) мутированный или модифицированный ITR ААВ, причем указанная зкДНК-плазмида лишена последовательностей, кодирующих капсидный белок ААВ, и при этом указанные модифицированные 5´- и 3´-ITR имеют одинаковые модификации (т. е. они являются обратно комплементарными или симметричными по отношению друг к другу).
[00313] Согласно дополнительному варианту реализации система зкДНК-плазмиды лишена последовательностей, кодирующих вирусный капсидный белок (т. е. лишена генов капсида ААВ, а также генов капсидов других вирусов). Кроме того, согласно конкретному варианту реализации зкДНК-плазмида также лишена последовательностей, кодирующих белок Rep ААВ. Соответственно, в предпочтительном варианте реализации зкДНК-плазмида лишена функциональных генов cap ААВ и rep ААВ, GG-3' для ААВ2, а также вариабельной палиндромной последовательности, обеспечивающей образование шпильки.
[00314] ЗкДНК-плазмида согласно настоящему изобретению может быть получена с использованием природных нуклеотидных последовательностей из геномов любых серотипов ААВ, хорошо известных в данной области техники. Согласно одному варианту реализации остов зкДНК-плазмиды происходит из генома ААВ1, ААВ2, ААВ3, ААВ4, ААВ5, ААВ5, ААВ7, ААВ8, ААВ9, ААВ10, ААВ11, ААВ12, ААВrh8, ААВrh10, ААВ-DJ и ААВ-DJ8. Например, NCBI: NC 002077; NC 001401; NC001729; NC001829; NC006152; NC 006260; NC 006261; из указателя вирусов Kotin and Smith («The Springer Index of Viruses»), доступного по ссылке, поддерживаемой Springer (веб-адрес: oesys.springer.de/viruses/database/mkchapter.asp?virID=42.04.) (примечание: ссылки на указатель URL или базу данных подразумевают содержание доступного по ссылке ресурса URL или базы данных на фактическую дату подачи данной заявки). В конкретном варианте реализации остов зкДНК-плазмиды происходит из генома ААВ2. В другом конкретном варианте реализации остов зкДНК-плазмиды представляет собой синтетический остов, генетически сконструированный для включения на его 5´- и 3´-концах ITR, происходящих из одного из указанных геномов ААВ.
[00315] ЗкДНК-плазмида необязательно может включать селектируемый или селективный маркер для использования при создании линии клеток, продуцирующей зкДНК-вектор. Согласно одному варианту реализации селективный маркер может быть вставлен после (т. е. в 3´-направлении) последовательности 3´-ITR. Согласно другому варианту реализации селективный маркер может быть вставлен перед (т. е. в 5´-направлении) последовательностью 5´-ITR. Подходящие селективные маркеры включают, например, маркеры, придающие устойчивость к лекарственному средству. Селективные маркеры могут представлять собой, например, гены устойчивости к бластицидину S, канамицину, генетицину и т.п. Согласно предпочтительному варианту реализации селективный маркер для отбора по чувствительности к лекарственному средству представляет собой ген устойчивости к бластицидину S.
[00316] Примерный зкДНК-вектор (например, рААВ0) для экспрессии белка PAH получают из плазмиды рААВ. Способ получения рААВ-вектора может включать: (а) доставку в клетку-хозяина плазмиды рААВ, как описано выше, при этом как клетка-хозяин, так и плазмида лишены генов, кодирующих капсидный белок, (b) культивирование клетки-хозяина в условиях, обеспечивающих продуцирование генома зкДНК; и (c) сбор клеток и выделение генома ААВ, продуцированного из указанных клеток.
C. Примерный способ получения зкДНК-векторов из зкДНК-плазмид
[00317] В данном документе также предложены способы получения бескапсидных зкДНК-векторов для экспрессии белка PAH, в частности, способ с достаточно высоким выходом для обеспечения достаточного количества вектора для экспериментов in vivo.
[00318] Согласно некоторым вариантам реализации способ получения зкДНК-вектора для экспрессии белка PAH включает следующие этапы: (1) введение конструкции нуклеиновой кислоты, содержащей экспрессионную кассету и последовательности двух симметричных ITR, в клетку-хозяина (например, клетки Sf9), (2) необязательно создание клональной линии клеток, например, с применением селективного маркера, присутствующего на плазмиде, (3) введение кодирующего Rep гена (либо путем трансфекции, либо инфекции бакуловирусом, несущим указанный ген) в указанную клетку насекомого; и (4) сбор клеток и очистку зкДНК-вектора. Конструкция нуклеиновой кислоты, содержащая экспрессионную кассету и последовательности двух ITR, описанная выше для получения зкДНК-вектора, может иметь форму зкДНК-плазмиды или бакмиды, или бакуловируса, полученных с использованием зкДНК-плазмиды, как описано ниже. Конструкция нуклеиновой кислоты может быть введена в клетку-хозяина путем трансфекции, вирусной трансдукции, стабильной интеграции или других способов, известных в данной области техники.
D. Линии клеток
[00319] Линии клеток-хозяев, используемые в получении зкДНК-вектора для экспрессии белка PAH, могут включать линии клеток насекомых, происходящие из Spodoptera frugiperda, такие как клетки Sf9, Sf21, или клетки Trichoplusia ni, или линии клеток других беспозвоночных животных, позвоночных животных или других эукариотов, включая клетки млекопитающих. Также могут быть использованы другие линии клеток, известные обычному специалисту в данной области техники, такие как HEK293, Huh-7, HeLa, HepG2, HeplA, 911, CHO, COS, MeWo, NIH3T3, A549, HT1 180, моноциты, а также зрелые и незрелые дендритные клетки. Линии клеток-хозяев могут быть трансфицированы для стабильной экспрессии зкДНК-плазмиды для получения зкДНК-вектора с высоким выходом.
[00320] ЗкДНК-плазмиды могут быть введены в клетки Sf9 путем кратковременной трансфекции с использованием реагентов (например, липосомальных, фосфата кальция) или физических средств (например, электропорации), известных в данной области техники. В качестве альтернативы, могут быть созданы стабильные линии клеток Sf9 с зкДНК-плазмидой, стабильно интегрированной в их геномы. Такие стабильные линии клеток могут быть созданы путем включения селективного маркера в зкДНК-плазмиду, как описано выше. Если зкДНК-плазмида, используемая для трансфекции линии клеток, включает селективный маркер, например, для антибиотика, клетки, которые были трансфицированы зкДНК-плазмидой и интегрировали ДНК зкДНК-плазмиды в их геном, могут быть отобраны путем добавления антибиотика в среды для культивирования клеток. Затем устойчивые клоны клеток могут быть выделены с помощью методик разведения до получения отдельных клеток или переноса колоний и размножены.
E. Выделение и очистка зкДНК-векторов:
[00321] Примеры способа получения и выделения зкДНК-векторов описаны на ФИГ. 4A-4E и в конкретных примерах ниже. ЗкДНК-векторы для экспрессии белка PAH, раскрытые в данном документе, могут быть получены из клеток-продуцентов, экспрессирующих белок (белки) Rep ААВ, дополнительно трансформированных зкДНК-плазмидой, зкДНК-бакмидой или зкДНК-бакуловирусом. Плазмиды, которые можно применять для получения зкДНК-векторов, включают плазмиды, которые кодируют белок PAH, или плазмиды, кодирующие один или более белков REP.
[00322] Согласно одному аспекту полинуклеотид кодирует белок Rep ААВ (Rep 78 или 68), доставляемый в клетку-продуцент в плазмиде (Rep-плазмиде), бакмиде (Rep-бакмиде) или бакуловирусе (Rep-бакуловирусе). Rep-плазмида, Rep-бакмида и Rep-бакуловирус могут быть получены с помощью способов, описанных выше.
[00323] В данном документе описаны способы получения зкДНК-вектора для экспрессии белка PAH. Экспрессионные конструкции, используемые для получения зкДНК-вектора для экспрессии белка PAH, описанного в данном документе, могут представлять собой плазмиду (например, зкДНК-плазмиды), бакмиду (например, зкДНК-бакмиду) и/или бакуловирус (например, зкДНК-бакуловирус). В качестве неограничивающего примера, зкДНК-вектор может быть получен из клеток, коинфицированных зкДНК-бакуловирусом и Rep-бакуловирусом. Белки Rep продуцированные с Rep-бакуловируса, могут реплицировать зкДНК-бакуловирус с получением зкДНК-векторов. В качестве варианта, зкДНК-векторы для экспрессии белка PAH могут быть получены из клеток, стабильно трансфицированных конструкцией, содержащей последовательность, кодирующую белок Rep AAV (Rep78/52), доставленной в Rep-плазмидах, Rep-бакмидах или Rep-бакуловирусе. ЗкДНК-бакуловирус может быть кратковременно трансфицирован в клетки, реплицирован с помощью белка Rep и может продуцировать зкДНК-векторы.
[00324] Бакмида (например, зкДНК-бакмида) может быть трансфицирована в пермиссивные клетки насекомых, такие как клетка Sf9, Sf21, Tni (Trichoplusia ni), клетка High Five, и генерировать зкДНК-бакуловирус, который представляет собой рекомбинантный бакуловирус, включающий последовательности, содержащие симметричные ITR и экспрессионную кассету. Клетки насекомых могут быть снова инфицированы зкДНК-бакуловирусом для получения следующего поколения рекомбинантного бакуловируса. Необязательно этап может быть повторен один или более раз для получения большего количества рекомбинантного бакуловируса.
[00325] Время сбора и извлечения зкДНК-векторов для экспрессии белка PAH, описанных в данном документе, из клеток может быть выбрано и оптимизировано так, чтобы достичь продуцирования указанных зкДНК-векторов с высоким выходом. Например, время сбора может быть выбрано с учетом жизнеспособности клеток, морфологии клеток, размножения клеток и т. д. Обычно клетки могут быть собраны через период времени после инфекции бакуловирусом, достаточный для получения зкДНК-векторов (например, зкДНК-векторов), но до начала гибели большинства клеток из-за вирусной токсичности. ЗкДНК-векторы могут быть выделены из клеток Sf9 с использованием наборов для очистки плазмид, таких как наборы Qiagen ENDO-FREE PLASMID®. Другие способы, разработанные для выделения плазмид, также могут быть адаптированы для зкДНК-векторов. Обычно можно использовать любые известные в данной области техники способы очистки нуклеиновых кислот, а также коммерчески доступные наборы для экстракции ДНК.
[00326] В качестве альтернативы, очистку можно осуществлять путем щелочного лизиса клеточного осадка, центрифугирования полученного лизата и выполнения хроматографического разделения. В качестве одного неограничивающего примера, указанный способ можно выполнять путем загрузки супернатанта на ионообменную колонку (например, SARTOBIND Q®), которая удерживает нуклеиновые кислоты, с последующим элюированием (например, 1,2 М раствором NaCl) и выполнением дальнейшей хроматографической очистки на колонке для гель-фильтрации (например, на 6 Fast Flow GE). Бескапсидный ААВ-вектор затем выделяют, например, путем осаждения.
[00327] Согласно некоторым вариантам реализации зкДНК-векторы для экспрессии белка PAH также могут быть очищены в форме экзосом или микрочастиц. В данной области техники известно, что многие типы клеток высвобождают не только растворимые белки, но и сложные грузы белок/нуклеиновая кислота путем отделения мембранных микровезикул (Cocucci et al, 2009; EP 10306226.1, полностью включенные в данный документ посредством ссылки). Такие везикулы включают микровезикулы (также называемые микрочастицами) и экзосомы (также называемые нановезикулами), и первые, и вторые содержат в качестве груза белки и РНК. Микровезикулы образуются в результате прямого отпочковывания плазматической мембраны, а экзосомы высвобождаются во внеклеточную среду при слиянии мультивезикулярных эндосом с плазматической мембраной. Соответственно, содержащие зкДНК-вектор микровезикулы и/или экзосомы могут быть выделены из клеток, трансдуцированных зкДНК-плазмидой или бакмидой, или бакуловирусом, полученным с использованием зкДНК-плазмиды.
[00328] Микровезикулы могут быть выделены путем фильтрации или ультрацентрифугирования культуральной среды при 20000×g, а экзосомы - при 100000×g. Оптимальная продолжительность ультрацентрифугирования может быть определена экспериментально и зависит от конкретного типа клеток, из которых выделяют везикулы. Предпочтительно культуральную среду сначала очищают с помощью низкоскоростного центрифугирования (например, при 2000×g в течение 5-20 минут) и подвергают центробежному концентрированию с использованием, например, центрифужной колонки AMICON® (Millipore, Уотфорд, Великобритания). Микровезикулы и экзосомы могут быть дополнительно очищены с помощью FACS или MACS с использованием специфичных антител, распознающих конкретные поверхностные антигены, присутствующие на микровезикулах и экзосомах. Другие способы очистки микровезикул и экзосом включают, но не ограничиваются перечисленными, иммунопреципитацию, аффинную хроматографию, фильтрацию и магнитные гранулы, покрытые специфичными антителами или аптамерами. После очистки везикулы промывают, например, фосфатно-солевым буфером (ФСБ). Одним из преимуществ использования микровезикул или экзосом для доставки содержащих зкДНК везикул является то, что такие везикулы могут быть нацелены на клетки различных типов путем включения в их мембраны белков, распознаваемых специфическими рецепторами на соответствующих типах клеток. (см. также EP 10306226)
[00329] Другой аспект настоящего изобретения относится к способам очистки зкДНК-векторов из линий клеток-хозяев, которые стабильно интегрировали конструкцию зкДНК в их собственный геном. Согласно одному варианту реализации зкДНК-векторы очищают в виде молекул ДНК. Согласно другому варианту реализации зкДНК-векторы очищают в виде экзосом или микрочастиц.
[00330] ФИГ. 5 международной заявки PCT/US18/49996 показывает гель, подтверждающий продуцирование зкДНК из нескольких конструкций зкДНК-плазмид с использованием способа, описанного в Примерах. ЗкДНК-вектор подтверждается характерным профилем полос в геле, как обсуждается в отношении ФИГ. 4D в Примерах.
VII. Фармацевтические композиции
[00331] Согласно другому аспекту предложены фармацевтические композиции. Фармацевтическая композиция содержит зкДНК-вектор для экспрессии белка PAH, описанный в данном документе, и фармацевтически приемлемый носитель или разбавитель.
[00332] зкДНК-векторы для экспрессии белка PAH, описанные в данном документе, могут быть включены в фармацевтические композиции, пригодные для введения субъекту для in vivo доставки в клетки, ткани или органы субъекта. Как правило, фармацевтическая композиция содержит зкДНК-вектор, раскрытый в данном документе, и фармацевтически приемлемый носитель. Например, зкДНК-векторы для экспрессии белка PAH, описанные в данном документе, могут быть включены в фармацевтическую композицию, подходящую для целевого пути терапевтического введения (например, парентерального введения). Также предусмотрена пассивная трансдукция ткани путем внутривенной или внутриартериальной инфузии под высоким давлением, а также внутриклеточной инъекции, такой как внутриядерная микроинъекция или внутрицитоплазматическая инъекция. Фармацевтические композиции для терапевтических целей могут быть изготовлены в виде раствора, микроэмульсии, дисперсии, липосом или другой упорядоченной структуры, подходящей для высокой концентрации зкДНК-вектора. Стерильные растворы для инъекций могут быть приготовлены путем включения соединения зкДНК-вектора в необходимом количестве в соответствующем буфере с одним или комбинацией ингредиентов, перечисленных выше, при необходимости, с последующей стерилизацией путем фильтрации, включая зкДНК-вектор, который может быть изготовлен для доставки трансгена в нуклеиновой кислоте в клетки реципиента, что приводит к терапевтической экспрессии в них трансгена или донорной последовательности. Композиция также может включать фармацевтически приемлемый носитель.
[00333] Фармацевтически активные композиции, содержащие зкДНК-вектор для экспрессии белка PAH, могут быть изготовлены для доставки трансгена для различных целей в клетку, например, в клетки субъекта.
[00334] Фармацевтические композиции для терапевтических целей, как правило, должны быть стерильными и стабильными в условиях изготовления и хранения. Композиция может быть изготовлена в виде раствора, микроэмульсии, дисперсии, липосом или другой упорядоченной структуры, подходящей для высокой концентрации зкДНК-вектора. Стерильные растворы для инъекций могут быть приготовлены путем включения соединения зкДНК-вектора в необходимом количестве в соответствующем буфере с одним или комбинацией ингредиентов, перечисленных выше, при необходимости, с последующей стерилизацией путем фильтрации.
[00335] зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, может быть включен в фармацевтическую композицию, пригодную для местного, системного, внутриамниотического, интратекального, внутричерепного, внутриартериального, внутривенного, внутрилимфатического, внутрибрюшинного, подкожного, трахеального, внутритканевого (например, внутримышечного, внутрисердечного, внутрипеченочного, внутрипочечного, интрацеребрального), интратекального, интравезикального, конъюнктивального (например, экстраорбитального, интраорбитального, ретроорбитального, интраретинального, субретинального, хориоидального, субхориоидального, интрастромального, интракамерального и интравитреального), интракохлеарного и мукозального (например, перорального, ректального, назального) введения. Также предусмотрена пассивная трансдукция ткани путем внутривенной или внутриартериальной инфузии под высоким давлением, а также внутриклеточной инъекции, такой как внутриядерная микроинъекция или внутрицитоплазматическая инъекция.
[00336] В некоторых аспектах способы, предложенные в данном документе, включают доставку одного или более зкДНК-векторов для экспрессии белка PAH, раскрытых в данном документе, в клетку-хозяина. В данном документе также предложены клетки, полученные с помощью таких способов, и организмы (такие как животные, растения или грибы), содержащие или полученные из таких клеток. Способы доставки нуклеиновых кислот могут включать липофекцию, нуклеофекцию, микроинъекцию, биолистику, липосомы, иммунолипосомы, конъюгаты поликатион или липид:нуклеиновая кислота, «незащищенную» ДНК и усиленное агентом поглощение ДНК. Липофекция описана, например, в патентах США №№ 5049386, 4946787 и 4897355), полностью включенных в данный документ посредством ссылки, и реагенты для липофекции продаются коммерчески (например, трансфектам (Transfectam™) и липофектин (Lipofectin™)). Доставка может осуществляться в клетки (например, введение in vitro или ex vivo) или в ткани-мишени (например, введение in vivo).
[00337] В данной области техники известны различные методики и способы доставки нуклеиновых кислот в клетки. Например, нуклеиновые кислоты, такие как зкДНК для экспрессии белка PAH, могут быть изготовлены в виде состава липидных наночастиц (ЛНЧ), липидоидов, липосом, липидных наночастиц, липоплексов или наночастиц типа ядро-оболочка. Как правило, ЛНЧ состоят из молекул нуклеиновой кислоты (например, зкДНК), одного или более ионизируемых или катионных липидов (или их солей), одного или более неионных или нейтральных липидов (например, фосфолипида), молекулы, которая предотвращает агрегацию (например, ПЭГ или конъюгата ПЭГ-липид), и необязательно стерина (например, холестерина).
[00338] Другой способ доставки нуклеиновых кислот, таких как зкДНК для экспрессии белка PAH, в клетку, заключается в конъюгации нуклеиновой кислоты с лигандом, который интернализуется клеткой. Например, лиганд может связывать рецептор на поверхности клетки и интернализоваться за счет эндоцитоза. Лиганд может быть ковалентно связан с нуклеотидом в нуклеиновой кислоте. Примерные конъюгаты для доставки нуклеиновых кислот в клетку описаны, например, в WO2015/006740, WO2014/025805, WO2012/037254, WO2009/082606, WO2009/073809, WO2009/018332, WO2006/112872, WO2004/090108, WO2004/091515 и WO2017/177326, содержание которых полностью включено в данный документ посредством ссылки.
[00339] Нуклеиновые кислоты, такие как зкДНК-векторы для экспрессии белка PAH, также могут быть доставлены в клетку путем трансфекции. Подходящие способы трансфекции включают, но не ограничиваются перечисленными, опосредуемую липидами трансфекцию, опосредуемую катионным полимером трансфекцию или осаждение фосфатом кальция. Реагенты для трансфекции хорошо известны в данной области техники и включают, но не ограничиваются перечисленными, реагент для трансфекции TurboFect (Thermo Fisher Scientific), реагент Pro-Ject (Thermo Fisher Scientific), реагент для трансфекции белков TRANSPASS™ P (New England Biolabs), реагент для доставки белков CHARIOT™ (Active Motif), реагент для трансфекции белков PROTEOJUICE™ (EMD Millipore), 293fectin, LIPOFECTAMINE™ 2000, LIPOFECTAMINE™ 3000 (Thermo Fisher Scientific), LIPOFECTAMINE™ (Thermo Fisher Scientific), LIPOFECTIN™ (Thermo Fisher Scientific), DMRIE-C, CELLFECTIN™ (Thermo Fisher Scientific), OLIGOFECTAMINE™ (Thermo Fisher Scientific), LIPOFECTACE™, FUGENE™ (Roche, Базель, Швейцария), FUGENE™ HD (Roche), TRANSFECTAM™ (трансфектам, Promega, Мэдисон, Висконсин), TFX-10™ (Promega), TFX-20™ (Promega), TFX-50™ (Promega), TRANSFECTIN™ (BioRad, Геркулес, Калифорния), SILENTFECT™ (Bio-Rad), Effectene™ (Qiagen®, Валенсия, Калифорния), DC-chol (Avanti Polar Lipids), GENEPORTER™ (Gene Therapy Systems, Сан-Диего, Калифорния), DHARMAFECT 1™ (Dharmacon, Лафайет, Колорадо), DHARMAFECT 2™ (Dharmacon), DHARMAFECT 3™ (Dharmacon), DHARMAFECT 4™ (Dharmacon), ESCORT™ III (Sigma, Сент-Луис, Миссури) и ESCORT™ IV (Sigma Chemical Co.). Нуклеиновые кислоты, такие как зкДНК, также могут быть доставлены в клетку с помощью микроструйных способов, известных специалистам в данной области техники.
[00340] зкДНК-векторы для экспрессии белка PAH, описанные в данном документе, также можно вводить непосредственно в организм для трансдукции клеток in vivo. Введение осуществляют любым из путей, обычно используемых для приведения молекулы в максимальный контакт с клетками крови или тканей, включая, но не ограничиваясь перечисленными, инъекцию, инфузию, местное нанесение и электропорацию. Подходящие способы введения таких нуклеиновых кислот доступны и хорошо известны специалистам в данной области техники, и хотя для введения конкретной композиции можно использовать более одного пути, конкретный путь часто может обеспечить более быструю и более эффективную реакцию по сравнению с другим путем введения.
[00341] Способы введения векторной нуклеиновой кислоты, такой как зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, могут включать доставку в гемопоэтические стволовые клетки, например, с помощью способов, описанных, например, в патенте США № 5928638, который полностью включен в данный документ посредством ссылки.
[00342] зкДНК-векторы для экспрессии белка PAH в соответствии с настоящим изобретением могут быть добавлены к липосомам для доставки в клетку или орган-мишень у субъекта. Липосомы представляют собой везикулы, которые имеют по меньшей мере один липидный бислой. Липосомы, как правило, используются в качестве носителей для доставки лекарственных/терапевтических средств в контексте фармацевтической разработки. Они функционируют путем слияния с клеточной мембраной и перегруппировки ее липидной структуры для доставки лекарственного средства или активного фармацевтического ингредиента (АФИ). Липосомальные композиции для такой доставки состоят из фосфолипидов, в частности, соединений, содержащих фосфатидилхолиновую группу, однако указанные композиции также могут включать другие липиды. Примерные липосомы и липосомные составы, включая, но не ограничиваясь перечисленными, соединения, содержащие функциональные группы полиэтиленгликоля (ПЭГ), раскрыты в международной заявке PCT/US2018/050042, поданной 7 сентября 2018 г., и в международной заявке PCT/US2018/064242, поданной 6 декабря 2018 г., например, см. раздел, озаглавленный «Фармацевтические композиции», содержание каждой из которых полностью включено в данный документ посредством ссылки.
[00343] Различные способы доставки, известные в данной области техники, или их модификации, могут быть использованы для доставки зкДНК-векторов in vitro или in vivo. Например, согласно некоторым вариантам реализации зкДНК-векторы для экспрессии белка PAH доставляют, образуя кратковременное отверстие в клеточной мембране с использованием механической, электрической, ультразвуковой, гидродинамической или лазерной энергии так, чтобы облегчить вход ДНК в целевые клетки. Например, зкДНК-вектор может быть доставлен путем кратковременного разрыва клеточной мембраны путем продавливания клетки через канал ограниченного размера или другими способами, известными в данной области техники. В некоторых случаях зкДНК-вектор по отдельности напрямую вводят в виде незащищенной ДНК путем инъекции в любую из: любую одну или более тканей, выбранных из: печени, почек, желчного пузыря, простаты, надпочечников, сердца, кишечника, легкого и желудка, кожи, тимуса, сердечной мышцы или скелетной мышцы. В некоторых случаях зкДНК-вектор доставляют с помощью генной пушки. Сферические частицы золота или вольфрама (диаметром 1-3 мкм), покрытые бескапсидными ААВ-векторами, могут быть разогнаны до высокой скорости с помощью сжатого газа для проникновения в клетки целевой ткани.
[00344] Композиции, содержащие зкДНК-вектор для экспрессии белка PAH и фармацевтически приемлемый носитель, конкретно предусмотрены в данном документе. Согласно некоторым вариантам реализации зкДНК-вектор изготовлен с липидной системой доставки, например, липосомами, как описано в данном документе. Согласно некоторым вариантам реализации такие композиции вводят любым путем, желательным для квалифицированного специалиста. Композиции могут быть введены субъекту различными путями, включая пероральный, парентеральный, сублингвальный, трансдермальный, ректальный, трансмукозальный, местный, путем ингаляции, путем буккального введения, внутриплевральный, внутривенный, внутриартериальный, внутрибрюшинный, подкожный, внутримышечный, интраназальный, интратекальный и внутрисуставной или их комбинации. Для ветеринарного применения композиция может быть введена в виде достаточно приемлемого состава в соответствии с обычной ветеринарной практикой. Ветеринарный врач может легко определить схему дозирования и путь введения, которые наиболее подходят для конкретного животного. Композиции могут быть ведены с помощью обычных шприцев, безыгольных инъекционных устройств, «генных пушек с бомбардировкой микрочастицами» или других физических методов, таких как электропорация («ЭП»), гидродинамические методы или применение ультразвука.
[00345] В некоторых случаях зкДНК-вектор для экспрессии белка PAH доставляют путем гидродинамической инъекции, которая представляет собой простой и высокоэффективный способ прямой внутриклеточной доставки любых водорастворимых соединений и частиц во внутренние органы и скелетные мышцы во всей конечности.
[00346] В некоторых случаях зкДНК-векторы для экспрессии белка PAH доставляют с помощью ультразвука, создавая наноскопические поры в мембране для облегчения внутриклеточной доставки частиц ДНК в клетки внутренних органов или опухолей, поэтому размер и концентрация плазмидной ДНК имеют большое значение для эффективности системы. В некоторых случаях зкДНК-векторы доставляют путем магнитофекции с использованием магнитных полей для концентрирования частиц, содержащих нуклеиновую кислоту, в клетках-мишенях.
[00347] В некоторых случаях могут быть использованы химические системы доставки, например, с использованием наномерных комплексов, которые включают уплотнение отрицательно заряженной нуклеиновой кислоты поликатионными наномерными частицами, в составе катионной липосомы/мицеллы или катионных полимеров. Катионные липиды, используемые в указанном способе доставки, включают, но не ограничиваются перечисленными, моновалентные катионные липиды, поливалентные катионные липиды, гуанидин-содержащие соединения, соединения производных холестерина, катионные полимеры (например, полиэтиленимин, поли-L-лизин, протамин, другие катионные полимеры) и гибриды липид-полимер.
А. Экзосомы:
[00348] Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, доставляют упакованным в экзосоме. Экзосомы представляют собой небольшие мембранные везикулы эндоцитарного происхождения, которые высвобождаются во внеклеточную среду после слияния мультивезикулярных телец с плазматической мембраной. Их поверхность состоит из липидного бислоя клеточной мембраны донорной клетки, они содержат цитозоль из клетки, которая продуцировала экзосому, и экспонируют на поверхности мембранные белки родительской клетки. Экзосомы продуцируются различными типами клеток, в том числе эпителиальными клетками, В- и Т-лимфоцитами, тучными клетками (MC), а также дендритными клетками (DC). Согласно некоторым вариантам реализации для применения предусмотрены экзосомы с диаметром от 10 нм до 1 мкм, от 20 нм до 500 нм, от 30 нм до 250 нм, от 50 до 100 нм. Экзосомы могут быть выделены для доставки в целевые клетки либо с использованием их донорных клеток, либо путем введения в них конкретных нуклеиновых кислот. Для получения экзосом, содержащих бескапсидные ААВ-векторы согласно настоящему изобретению, могут быть использованы различные подходы, известные в данной области техники.
А. Микрочастица/наночастицы
[00349] Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, доставляют с помощью липидной наночастицы. Обычно липидные наночастицы содержат ионизируемый аминолипид (например, гептатриаконта-6,9,28,31-тетраен-19-ил-4-(диметиламино)бутаноат, DLin-MC3-DMA, фосфатидилхолин(1,2-дистеароил-sn-глицеро-3-фосфохолин, DSPC), холестерин и липид оболочки (полиэтиленгликоль-димиристоилглицерин, ПЭГ-ДМГ), например, как раскрыто Tam et al. (2013). Advances in Lipid Nanoparticles for siRNA delivery. Pharmaceuticals 5(3): 498-507.
[00350] Согласно некоторым вариантам реализации липидная наночастица имеет средний диаметр от примерно 10 до примерно 1000 нм. Согласно некоторым вариантам реализации липидная наночастица имеет диаметр менее 300 нм. Согласно некоторым вариантам реализации липидная наночастица имеет диаметр от примерно 10 до примерно 300 нм. Согласно некоторым вариантам реализации липидная наночастица имеет диаметр менее 200 нм. Согласно некоторым вариантам реализации липидная наночастица имеет диаметр от примерно 25 до примерно 200 нм. Согласно некоторым вариантам реализации препарат липидных наночастиц (например, композиция, содержащая множество липидных наночастиц) имеет распределение по размерам, при котором средний размер (например, диаметр) составляет от примерно 70 нм до примерно 200 нм, и более типично средний размер составляет примерно 100 нм или менее.
[00351] Для доставки ДНК-вектора для экспрессии белка PAH, раскрытого в данном документе, могут быть использованы различные липидные наночастицы, известные в данной области техники. Например, различные способы доставки с применением липидных наночастиц описаны в патентах США №№ 9404127, 9006417 и 9518272.
[00352] Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, доставляют с помощью наночастицы золота. Обычно нуклеиновая кислота может быть ковалентно связана с наночастицей золота или нековалентно связана с наночастицей золота (например, связана заряд-зарядным взаимодействием), например, согласно описанию Ding et al. (2014). Gold Nanoparticles for Nucleic Acid Delivery. Mol. Ther. 22(6); 1075-1083. Согласно некоторым вариантам реализации конъюгаты наночастицы золота с нуклеиновой кислотой получают с использованием способов, описанных, например, в патенте США № 6812334.
B. Конъюгаты
[00353] Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, конъюгирован (например, ковалентно связан) с агентом, который увеличивает клеточное поглощение. «Агент, который увеличивает клеточное поглощение» представляет собой молекулу, которая облегчает транспорт нуклеиновой кислоты через липидную мембрану. Например, нуклеиновая кислота может быть конъюгирована с липофильным соединением (например, холестерином, токоферолом и т. д.), проникающим в клетки пептидом (СРР) (например, пенетратином, ТАТ, Syn1B и т. д.) и полиаминами (например, спермином). Дополнительные примеры агентов, которые увеличивают поглощение клетками, раскрыты, например, в Winkler (2013). Oligonucleotide conjugates for therapeutic applications. Ther. Deliv. 4(7); 791-809.
[00354] Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, конъюгирован с полимером (например, полимерной молекулой) или молекулой фолата (например, молекулой фолиевой кислоты). В целом, доставка нуклеиновых кислот, конъюгированных с полимерами, известна в данной области техники, например, описана в WO2000/34343 и WO2008/022309. Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, конъюгирован с полиамидным полимером, например, согласно описанию в патенте США № 8987377. Согласно некоторым вариантам реализации нуклеиновая кислота, описанная в настоящем раскрытии, конъюгирована с молекулой фолиевой кислоты согласно описанию в патенте США № 8507455.
[00355] Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, конъюгирован с углеводом, например, как описано в патенте США № 8450467.
С. Нанокапсула
[00356] В качестве альтернативы, могут применяться нанокапсульные составы зкДНК-вектора для экспрессии белка PAH, раскрытого в данном документе. Обычно нанокапсулы могут захватывать вещества стабильным и воспроизводимым образом. Чтобы избежать побочных эффектов, обусловленных внутриклеточной перегрузкой полимерами, такие ультрадисперсные частицы (размером около 0,1 мкм) необходимо конструировать с использованием полимеров, способных разлагаться in vivo. Предусмотрено применение биоразлагаемых полиалкил-цианоакрилатных наночастиц, которые удовлетворяют таким требованиям.
D. Липосомы
[00357] ЗкДНК-векторы для экспрессии белка PAH в соответствии с настоящим изобретением могут быть добавлены к липосомам для доставки в клетку или орган-мишень у субъекта. Липосомы представляют собой везикулы, которые имеют по меньшей мере один липидный бислой. Липосомы, как правило, используются в качестве носителей для доставки лекарственных/терапевтических средств в контексте фармацевтической разработки. Они функционируют путем слияния с клеточной мембраной и перегруппировки ее липидной структуры для доставки лекарственного средства или активного фармацевтического ингредиента (АФИ). Липосомальные композиции для такой доставки состоят из фосфолипидов, в частности, соединений, содержащих фосфатидилхолиновую группу, однако указанные композиции также могут включать другие липиды.
[00358] Изготовление и применение липосом в целом известно специалистам в данной области техники. Были разработаны липосомы с улучшенной стабильностью в сыворотке и временем полужизни в кровотоке (патент США № 5741516). Кроме того, были описаны различные способы получения липосом и липосомоподобных препаратов в качестве потенциальных носителей лекарственных средств (патенты США №№ 5567434; 5552157; 5565213; 5738868 и 5795587, полностью включенные в данный документ посредством ссылки).
E. Примерные композиции липосом и липидных наночастиц (ЛНЧ)
[00359] ЗкДНК-векторы для экспрессии белка PAH в соответствии с настоящим изобретением могут быть добавлены к липосомам для доставки в клетку, например, в клетку, нуждающуюся в экспрессии трансгена. Липосомы представляют собой везикулы, которые имеют по меньшей мере один липидный бислой. Липосомы, как правило, используются в качестве носителей для доставки лекарственных/терапевтических средств в контексте фармацевтической разработки. Они работают за счет слияния с клеточной мембраной и перегруппировки ее липидной структуры для доставки лекарственного средства или активного фармацевтического ингредиента (АФИ). Липосомальные композиции для такой доставки состоят из фосфолипидов, в частности, соединений, содержащих фосфатидилхолиновую группу, однако указанные композиции также могут включать другие липиды.
[00360] Липидные наночастицы (ЛНЧ), содержащие зкДНК-векторы, раскрыты в международной заявке PCT/US2018/050042, поданной 7 сентября 2018 г., и международной заявке PCT/US2018/064242, поданной 6 декабря 2018 г., которые полностью включены в данный документ, и предусмотрены для применения в способах и композициях зкДНК-векторов для экспрессии белка PAH, раскрытых в данном документе.
[00361] Согласно некоторым аспектам настоящего раскрытия предложен липосомальный состав, который включает одно или более соединений с функциональной группой полиэтиленгликоля (ПЭГ) (так называемых «пегилированных соединений»), которые могут снижать иммуногенность/антигенность, обеспечивать гидрофильность и гидрофобность, а также уменьшать частоту дозирования соединения (соединений). В других случаях, липосомальный состав просто включает полимер полиэтиленгликоль (ПЭГ) в качестве дополнительного компонента. В таких аспектах молекулярная масса ПЭГ или функциональной группы ПЭГ может составлять от 62 Да до примерно 5000 Да.
[00362] Согласно некоторым аспектам настоящего раскрытия предложен липосомальный состав, который доставит АФИ с профилем пролонгированного или контролируемого высвобождения на протяжении периода времени от нескольких часов до недель. Согласно некоторым родственным аспектам липосомальный состав может содержать водные камеры, которые ограничены липидными бислоями. Согласно другим родственным аспектам липосомальный состав инкапсулирует АФИ с компонентами, которые претерпевают физический переход при повышенной температуре, который высвобождает АФИ в течение периода от нескольких часов до недель.
[00363] Согласно некоторым аспектам липосомальный состав содержит сфингомиелин и один или более липидов, раскрытых в данном документе. Согласно некоторым аспектам липосомальный состав содержит оптисомы.
[00364] Согласно некоторым аспектам настоящего раскрытия предложен липосомальный состав, который содержит один или более липидов, выбранных из: натриевой соли N-(карбонилметоксиполиэтиленгликоль 2000)-1,2-дистеароил-sn-глицеро-3-фосфоэтаноламина, (дистеароил-sn-глицерофосфоэтаноламина), MPEG (метоксиполиэтиленгликоль)-конъюгированного липида, HSPC (гидрогенизированного соевого фосфатидилхолина); ПЭГ (полиэтиленгликоля); DSPE (дистеароил-sn-глицерофосфоэтаноламина); DSPC (дистеароилфосфатидилхолина); DOPC (диолеоилфосфатидилхолина); DPPG (дипальмитоилфосфатидилглицерина); EPC (яичного фосфатидилхолина); DOPS (диолеоилфосфатидилсерина); POPC (пальмитоилолеоилфосфатидилхолина); SM (сфингомиелина); MPEG (метоксиполиэтиленгликоля); DMPC (димиристоилфосфатидилхолина); DMPG (димиристоилфосфатидилглицерина); DSPG (дистеароилфосфатидилглицерина); DEPC (диэрукоилфосфатидилхолина); DOPE (диолеоил-sn-глицерофосфоэтаноламина), сульфата холестерина (CS), дипальмитоилфосфатидилглицерина (DPPG), DOPC (диолеоил-sn-глицерофосфатидилхолина) или любой их комбинации.
[00365] Согласно некоторым аспектам настоящего раскрытия предложен липосомальный состав, содержащий фосфолипид, холестерин и пегилированный липид в молярном соотношении 56:38:5. Согласно некоторым аспектам общее содержание липидов в липосомальном составе составляет 2-16 мг/мл. Согласно некоторым аспектам настоящего раскрытия предложен липосомальный состав, содержащий липид, содержащий фосфатидилхолиновую функциональную группу, липид, содержащий этаноламиновую функциональную группу, и пегилированный липид. Согласно некоторым аспектам настоящего изобретения предложен липосомальный состав, содержащий липид, содержащий фосфатидилхолиновую функциональную группу, липид, содержащий этаноламиновую функциональную группу, и пегилированный липид, в молярном соотношении 3:0,015:2, соответственно. Согласно некоторым аспектам настоящего изобретения предложен липосомальный состав, содержащий липид, содержащий фосфатидилхолиновую функциональную группу, холестерин и пегилированный липид. Согласно некоторым аспектам настоящего изобретения предложен липосомальный состав, содержащий липид, содержащий фосфатидилхолиновую функциональную группу, и холестерин. Согласно некоторым аспектам пегилированный липид представляет собой ПЭГ-2000-DSPE. Согласно некоторым аспектам настоящего раскрытия предложен липосомальный состав, содержащий DPPG, соевый ФХ, липидный конъюгат MPEG-DSPE и холестерин.
[00366] Согласно некоторым аспектам настоящего раскрытия предложен липосомальный состав, содержащий один или более липидов, содержащих фосфатидилхолиновую функциональную группу, и один или более липидов, содержащих этаноламиновую функциональную группу. Согласно некоторым аспектам настоящего раскрытия предложен липосомальный состав, содержащий одно или более из: липидов, содержащих фосфатидилхолиновую функциональную группу, липидов, содержащих этаноламиновую функциональную группу, и стеринов, например, холестерина. Согласно некоторым аспектам липосомальный состав содержит DOPC/DEPC; и DOPE.
[00367] Согласно некоторым аспектам настоящего раскрытия предложен липосомальный состав, дополнительно содержащий одно или более фармацевтических вспомогательных веществ, например, сахарозу и/или глицин.
[00368] Согласно некоторым аспектам настоящего раскрытия предложен липосомальный состав с униламеллярной или мультиламеллярной структурой. Согласно некоторым аспектам настоящего раскрытия предложен липосомальный состав, который содержит мультивезикулярные частицы и/или частицы на основе пены. Согласно некоторым аспектам настоящего раскрытия предложен липосомальный состав, относительный размер которого больше, чем у обычных наночастиц, и составляет примерно от 150 до 250 нм. Согласно некоторым аспектам липосомальный состав представляет собой лиофилизированный порошок.
[00369] Согласно некоторым аспектам настоящего раскрытия предложен липосомальный состав, который получают и нагружают зкДНК-векторами, раскрытыми или описанными в данном документе, путем добавления слабого основания к смеси, содержащей выделенную зкДНК вне липосомы. Такое добавление повышает значение pH вне липосом до приблизительно 7,3 и стимулирует вход АФИ в липосому. Согласно некоторым аспектам настоящего раскрытия предложен липосомальный состав, имеющий кислый pH внутри липосомы. В таких случаях значение pH внутри липосом может составлять 4-6,9 и более предпочтительно pH 6,5. Согласно другим аспектам настоящего раскрытия предложен липосомальный состав, полученный с применением технологии внутрилипосомальной стабилизации лекарственных средств. В таких случаях используют полимерные или неполимерные высокозаряженные анионы и внутрилипосомальные захватывающие агенты, например, полифосфат или октасульфат сахарозы.
[00370] Согласно некоторым аспектам настоящего раскрытия предложена липидная наночастица, содержащая зкДНК и ионизируемый липид. Например, состав липидных наночастиц, который получают и нагружают зкДНК, полученной с помощью способа, раскрытого в международной заявке PCT/US2018/050042, поданной 7 сентября 2018 г., которая включена в данный документ. Это можно осуществлять путем интенсивного смешивания этанольных растворов липидов с водным раствором зкДНК при низком pH, при котором происходит протонирование ионизируемого липида и обеспечиваются благоприятные энергетические характеристики для ассоциации зкДНК/липида и нуклеации частиц. Частицы могут быть дополнительно стабилизированы путем разбавления водой и удаления органического растворителя. Частицы могут быть сконцентрированы до целевого уровня.
[00371] Обычно липидные частицы получают при соотношении общего количества липида и зкДНК (массовом или весовом) от примерно 10:1 до 30:1. Согласно некоторым вариантам реализации соотношение липида и зкДНК (массовое соотношение; отношение масс./масс.) может находиться в диапазоне значений от примерно 1:1 до примерно 25:1, от примерно 10:1 до примерно 14:1, от примерно 3:1 до примерно 15:1, от примерно 4:1 до примерно 10:1, от примерно 5:1 до примерно 9:1 или от примерно 6:1 до примерно 9:1. Количества липидов и зкДНК могут быть скорректированы, чтобы обеспечить целевое соотношение N/P, например, соотношение N/P, равное 3, 4, 5, 6, 7, 8, 9, 10 или выше. Обычно общее содержание липидов в составе липидных частиц может быть в диапазоне от примерно 5 мг/мл до примерно 30 мг/мл.
[00372] Ионизируемый липид, как правило, применяется для конденсации груза нуклеиновой кислоты, например, зкДНК, при низком pH, и для стимуляции ассоциации мембран и их фузогенности. Обычно ионизируемые липиды представляют собой липиды, содержащие по меньшей мере одну аминогруппу, которая положительно заряжена или становится протонированной в кислых условиях, например, при рН 6,5 или ниже. В данном документе ионизируемые липиды также называют катионными липидами.
[00373] Примерные ионизируемые липиды описаны в международных РСТ публикациях патентов WO2015/095340, WO2015/199952, WO2018/011633, WO2017/049245, WO2015/061467, WO2012/040184, WO2012/000104, WO2015/074085, WO2016/081029, WO2017/004143, WO2017/075531, WO2017/117528, WO2011/022460, WO2013/148541, WO2013/116126, WO2011/153120, WO2012/044638, WO2012/054365, WO2011/090965, WO2013/016058, WO2012/162210, WO2008/042973, WO2010/129709, WO2010/144740, WO2012/099755, WO2013/049328, WO2013/086322, WO2013/086373, WO2011/071860, WO2009/132131, WO2010/048536, WO2010/088537, WO2010/054401, WO2010/054406, WO2010/054405, WO2010/054384, WO2012/016184, WO2009/086558, WO2010/042877, WO2011/000106, WO2011/000107, WO2005/120152, WO2011/141705, WO2013/126803, WO2006/007712, WO2011/038160, WO2005/121348, WO2011/066651, WO2009/127060, WO2011/141704, WO2006/069782, WO2012/031043, WO2013/006825, WO2013/033563, WO2013/089151, WO2017/099823, WO2015/095346 и WO2013/086354, и публикациях патентов США US2016/0311759, US2015/0376115, US2016/0151284, US2017/0210697, US2015/0140070, US2013/0178541, US2013/0303587, US2015/0141678, US2015/0239926, US2016/0376224, US2017/0119904, US2012/0149894, US2015/0057373, US2013/0090372, US2013/0274523, US2013/0274504, US2013/0274504, US2009/0023673, US2012/0128760, US2010/0324120, US2014/0200257, US2015/0203446, US2018/0005363, US2014/0308304, US2013/0338210, US2012/0101148, US2012/0027796, US2012/0058144, US2013/0323269, US2011/0117125, US2011/0256175, US2012/0202871, US2011/0076335, US2006/0083780, US2013/0123338, US2015/0064242, US2006/0051405, US2013/0065939, US2006/0008910, US2003/0022649, US2010/0130588, US2013/0116307, US2010/0062967, US2013/0202684, US2014/0141070, US2014/0255472, US2014/0039032, US2018/0028664, US2016/0317458 и US2013/0195920, содержание которых полностью включено в данный документ посредством ссылки.
[00374] Согласно некоторым вариантам реализации ионизируемый липид представляет собой MC3 (6Z,9Z,28Z,31Z)-гептатриаконта-6,9,28,31-тетраен-19-ил-4-(диметиламино)бутаноат (DLin-MC3-DMA или MC3), имеющий следующую структуру:
 .
.
[00375] ипид DLin-MC3-DMA описан в Jayaraman et al., Angew. Chem. Int. Ed Engl. (2012), 51(34): 8529-8533, содержание которой полностью включено в данный документ посредством ссылки.
[00376] Согласно некоторым вариантам реализации ионизируемый липид представляет собой липид ATX-002, описанный в WO 2015/074085, содержание которого полностью включено в данный документ посредством ссылки.
[00377] Согласно некоторым вариантам реализации ионизируемый липид представляет собой (13Z,16Z)-N,N-диметил-3-нонилдокоза-13,16-диен-1-амин (Соединение 32), описанный в WO2012/040184, содержание которого полностью включено в данный документ посредством ссылки.
[00378] Согласно некоторым вариантам реализации ионизируемый липид представляет собой Соединение 6 или Соединение 22, описанные в WO2015/199952, содержание которого полностью включено в данный документ посредством ссылки.
[00379] Без ограничений, ионизируемый липид может составлять 20-90% (мол.) от общего количества липидов, присутствующих в липидной наночастице. Например, молярное содержание ионизируемого липида может составлять 20-70% (мол.), 30-60% (мол.) или 40-50% (мол.) от общего количества липидов, присутствующих в липидной наночастице. Согласно некоторым вариантам реализации ионизируемый липид составляет от примерно 50 мол.% до примерно 90 мол.%, от общего количества липидов, присутствующих в липидной наночастице.
[00380] Согласно некоторым аспектам липидная наночастица может дополнительно содержать некатионный липид. Неионогенные липиды включают амфипатические липиды, нейтральные липиды и анионные липиды. Соответственно, некатионный липид может представлять собой нейтральный незаряженный, цвиттерионный или анионный липид. Некатионные липиды, как правило, применяют для усиления фузогенности.
[00381] Примерные некатионные липиды, предусмотренные для применения в способах и композициях, раскрытых в данном документе, описаны в международной заявке PCT/US2018/050042, поданной 7 сентября 2018 г., и PCT/US2018/064242, поданной 6 декабря 2018 г., которые полностью включены в данный документ. Примерные некатионные липиды описаны в публикации международной заявки WO2017/099823 и публикации патента США US2018/0028664, содержание которых полностью включено в данный документ посредством ссылки.
[00382] Некатионный липид может составлять 0-30% (мол.) от общего количества липидов, присутствующих в липидной наночастице. Например, содержание некатионного липида составляет 5-20% (мол.) или 10-15% (мол.) от общего количества липидов, присутствующих в липидной наночастице. Согласно различным вариантам реализации молярное соотношение ионизируемого липида и нейтрального липида колеблется от примерно 2:1 до примерно 8:1.
[00383] Согласно некоторым вариантам реализации липидные наночастицы не содержат каких-либо фосфолипидов. Согласно некоторым аспектам липидная наночастица может дополнительно содержать компонент, такой как стерин, для обеспечения целостности мембраны.
[00384] Один примерный стерин, который подходит для применения в липидной наночастице, представляет собой холестерин и его производные. Примерные производные холестерина описаны в международной заявке WO2009/127060 и публикации патента США US2010/0130588, содержание которых полностью включено в данный документ посредством ссылки.
[00385] Компонент, обеспечивающий целостность мембраны, такой как стерин, может составлять 0-50% (мол.) от общего количества липидов, присутствующих в липидной наночастице. Согласно некоторым вариантам реализации такой компонент составляет 20-50% (мол.) 30-40% (мол.) от общего содержания липидов липидной наночастицы.
[00386] Согласно некоторым аспектам липидная наночастица может дополнительно содержать полиэтиленгликоль (ПЭГ) или молекулу конъюгированного липида. Обычно их используют для ингибирования агрегации липидных наночастиц и/или для обеспечения стерической стабилизации. Примерные конъюгированные липиды включают, но не ограничиваются перечисленными, конъюгаты ПЭГ-липид, конъюгаты полиоксазолин (POZ)-липид, конъюгаты полиамид-липид (такие как конъюгаты ATTA-липид), конъюгаты катионная группа-полимер-липид (CPL) и их смеси. Согласно некоторым вариантам реализации молекула конъюгированного липида представляет собой конъюгат ПЭГ-липид, например, метоксиполиэтиленгликоль-конъюгированный липид. Примерные конъюгаты ПЭГ-липид включают, но не ограничиваются перечисленными, ПЭГ-диацилглицерин (ДАГ) (такой как 1-(монометоксиполиэтиленгликоль)-2,3-димиристоилглицерин (ПЭГ-ДМГ)), ПЭГ-диалкилоксипропил (ДАА), ПЭГ-фосфолипид, ПЭГ-церамид (Cer), пегилированный фосфатидилэтаноламин (ПЭГ-ФЭ), ПЭГ-сукцинатдиацилглицерин (PEGS-DAG) (такой как 4-O-(2´,3´-ди(тетрадеканоилокси)пропил-1-O)-(w-метокси(полиэтокси)этил)бутандиоат (PEG-S-DMG)), ПЭГ-диалкоксипропилкарбам, натриевая соль N-(карбонилметоксиполиэтиленгликоль 2000)-1,2-дистеароил-sn-глицеро-3-фосфоэтаноламина или их смесь. Дополнительные примерные конъюгаты ПЭГ-липид описаны, например, в US5885613, US6287591, US2003/0077829, US2003/0077829, US2005/0175682, US2008/0020058, US2011/0117125, US2010/0130588, US2016/0376224 и US2017/0119904, содержание которых полностью включено в данный документ посредством ссылки.
[00387] Согласно некоторым вариантам реализации ПЭГ-липид представляет собой соединение, раскрытое в US2018/0028664, содержание которого полностью включено в данный документ посредством ссылки. Согласно некоторым вариантам реализации ПЭГ-липид раскрыт в US20150376115 или в US2016/0376224, содержание которых полностью включено в данный документ посредством ссылки.
[00388] Конъюгат ПЭГ-ДАА может представлять собой, например, ПЭГ-дилаурилоксипропил, ПЭГ-димиристилоксипропил, ПЭГ-дипальмитилоксипропил или ПЭГ-дистеарилоксипропил. ПЭГ-липид может представлять собой одно или более из ПЭГ-ДМГ, ПЭГ-дилаурилглицерина, ПЭГ-дипальмитоилглицерина, ПЭГ-дистерилглицерина, ПЭГ-дилаурилгликамида, ПЭГ-димиристилгликамида, ПЭГ-дипальмитоилгликамида, ПЭГ-дистерилгликамида, ПЭГ-холестерина (1-[8´-(холест-5-ен-3β-окси)карбоксамидо-3´,6´-диоксаоктанил]карбамоил-[омега]-метилполиэтиленгликоль, ПЭГ-DMB (простой эфир 3,4-дитетрадекоксилбензил-[омега]-метилполиэтиленгликоля) и 1,2-димиристоил-sn-глицеро-3-фосфоэтаноламин-N-[метоксиполиэтиленгликоль-2000]. В некоторых примерах ПЭГ-липид может быть выбран из группы, состоящей из ПЭГ-ДМГ, 1,2-димиристоил-sn-глицеро-3-фосфоэтаноламин-N-[метоксиполиэтиленгликоля-2000].
[00389] Липиды, конъюгированные с молекулой, отличной от ПЭГ, также могут быть использованы вместо ПЭГ-липида. Например, конъюгаты полиоксазолин (POZ)-липид, конъюгаты полиамид-липид (такие как конъюгаты ATTA-липид) и конъюгаты катионная группа-полимер-липид (CPL) могут применяться вместо или вместе с ПЭГ-липидом. Примерные конъюгированные липиды, т. е. ПЭГ-липиды, конъюгаты (POZ)-липид, конъюгаты АТТА-липид и катионный полимер-липиды, описаны в публикациях международных заявок на патент WO1996/010392, WO1998/051278, WO2002/087541, WO2005/026372, WO2008/147438, WO2009/086558, WO2012/000104, WO2017/117528, WO2017/099823, WO2015/199952, WO2017/004143, WO2015/095346, WO2012/000104, WO2012/000104 и WO2010/006282, публикациях заявок на патент США US2003/0077829, US2005/0175682, US2008/0020058, US2011/0117125, US2013/0303587, US2018/0028664, US2015/0376115, US2016/0376224, US2016/0317458, US2013/0303587, US2013/0303587 и US20110123453, и патентах США US5885613, US6287591, US6320017 и US6586559, содержание которых полностью включено в данный документ посредством ссылки.
[00390] Согласно некоторым вариантам реализации одно или более дополнительных соединений могут представлять собой терапевтический агент. Терапевтический агент может быть выбран из любого класса, подходящего для применения в терапевтических целях. Другими словами, терапевтический агент может быть выбран из любого класса, подходящего для применения в терапевтических целях. Другими словами, терапевтический агент может быть выбран в соответствии с терапевтической целью и целевым биологическим действием. Например, если зкДНК в ЛНЧ можно применять для лечения ФКУ, дополнительное соединение может представлять собой агент, направленный против ФКУ (например, химиотерапевтический агент или другую терапию ФКУ (включая, но не ограничиваясь перечисленными, малую молекулу или антитело). Согласно другому примеру, если ЛНЧ, содержащую зкДНК, можно применять для лечения инфекции, дополнительное соединение может представлять собой антимикробный агент (например, антибиотик или противовирусное соединение). Согласно еще одному примеру, если ЛНЧ, содержащую зкДНК, можно применять для лечения иммунного заболевания или нарушения, дополнительное соединение может представлять собой соединение, которое модулирует иммунный ответ (например, иммуносупрессор, иммуностимулирующее соединение или соединение, модулирующее один или более конкретных иммунных путей). Согласно некоторым вариантам реализации в композициях и способах согласно настоящему изобретению могут применяться другие смеси различных липидных наночастиц, содержащих другие соединения, такие как зкДНК, кодирующая другой белок или другое соединение, такое как терапевтическое средство.
[00391] Согласно некоторым вариантам реализации дополнительное соединение представляет собой иммуномодулирующий агент. Например, дополнительное соединение представляет собой иммуносупрессор. Согласно некоторым вариантам реализации дополнительное соединение представляет собой иммуностимулирующий агент. В данном документе также предложена фармацевтическая композиция, содержащая инкапсулированный в липидную наночастицу продуцируемый клеткой насекомого или синтетически продуцируемый зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, и фармацевтически приемлемый носитель или вспомогательное вещество.
[00392] Согласно некоторым аспектам настоящего раскрытия предложен состав липидных наночастиц, дополнительно содержащий одно или более фармацевтических вспомогательных веществ. Согласно некоторым вариантам реализации состав липидных наночастиц дополнительно содержит сахарозу, tris, трегалозу и/или глицин.
[00393] зкДНК-вектор может образовывать комплексы с липидной частью (portion) частицы или может быть инкапсулирован в липидной части (position) липидной наночастицы. Согласно некоторым вариантам реализации зкДНК может быть полностью инкапсулирована в липидной части липидной наночастицы, что защищает ее от разрушения нуклеазой, например, в водном растворе. Согласно некоторым вариантам реализации зкДНК в липидной наночастице не разрушается в значительной степени после воздействия на липидную наночастицу нуклеазы при 37°С в течение по меньшей мере примерно 20, 30, 45 или 60 минут. Согласно некоторым вариантам реализации зкДНК в липидной наночастице не разрушается в значительной степени после инкубации частицы в сыворотке при 37°С в течение по меньшей мере примерно 30, 45 или 60 минут, или по меньшей мере примерно 2, 3, 4, 5, 6, 7, 8, 9, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28, 30, 32, 34 или 36 часов.
[00394] Согласно определенным вариантам реализации липидные наночастицы по существу нетоксичны для субъекта, например, млекопитающего, такого как человек. Согласно некоторым аспектам состав липидных наночастиц представляет собой лиофилизированный порошок.
[00395] Согласно некоторым вариантам реализации липидные наночастицы представляют собой частицы с твердой сердцевиной, которые имеют по меньшей мере один липидный бислой. Согласно другим вариантам реализации липидные наночастицы имеют небислойную структуру, т. е., имеют неламеллярную (т. е., небислойную) морфологию. Без ограничений, небислойная морфология может включать, например, трехмерные трубки, стержни, частицы кубической симметрии и т. д. Например, морфологию липидных наночастиц (ламеллярных в сравнении с неламеллярными) можно легко оценить и охарактеризовать с использованием, например, анализа методом «крио-ТЭМ» (криотрансмиссионная электронная микроскопия), как описано в US2010/0130588, содержание которого полностью включено в данный документ посредством ссылки.
[00396] Согласно некоторым другим вариантам реализации липидные наночастицы, имеющие неламеллярную морфологию, являются электронно-плотными. Согласно некоторым аспектам настоящего раскрытия предложена липидная наночастица, которая является либо однослойной, либо многослойной по структуре. Согласно некоторым аспектам настоящего раскрытия предложен состав липидных наночастиц, который содержит мультивезикулярные частицы и/или частицы на основе пены.
[00397] Контролируя композицию и содержание липидных компонентов, можно контролировать скорость, с которой липидный конъюгат высвобождается из липидной частицы, и, в свою очередь, скорость, с которой липидная наночастица становится фузогенной. Кроме того, другие переменные, включая, например, pH, температуру или ионную силу, могут применяться для изменения и/или контроля скорости, с которой липидная наночастица становится фузогенной. Другие способы, которые могут применяться для контроля скорости, с которой указанная липидная наночастица становится фузогенной, будут понятны обычным специалистам в данной области техники после ознакомления с указанным описанием. Также будет понятно, что размер липидных частиц можно контролировать путем контроля композиции и концентрации липидного конъюгата.
[00398] pKa катионных липидов в составах может быть сопоставлена с эффективностью ЛНЧ для доставки нуклеиновых кислот (см. Jayaraman et al, Angewandte Chemie, International Edition (2012), 51(34), 8529-8533; Semple et al, Nature Biotechnology 28, 172-176 (2010), обе работы полностью включены в данный документ посредством ссылки). Предпочтительный диапазон pKa составляет от ~5 до ~7. pKa катионного липида в липидных наночастицах может быть определена с использованием анализа, основанного на флуоресценции 2-(п-толуидино)-6-нафталинсульфоновой кислоты (TNS).
VIII. Способы применения
[00399] ЗкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, также можно применять в способе доставки представляющей интерес нуклеотидной последовательности (например, кодирующей белок PAH) в клетку-мишень (например, клетку-хозяина). Способ, в частности, может представлять собой способ доставки белка PAH в клетку субъекта, нуждающегося в этом, и лечения ФКУ. Настоящее изобретение обеспечивает экспрессию in vivo белка PAH, закодированного в зкДНК-векторе, в клетке у субъекта так, чтобы возник терапевтический эффект экспрессии белка PAH. Указанные результаты наблюдаются как в in vivo, так и в in vitro режимах доставки зкДНК-вектора.
[00400] Кроме того, согласно настоящему изобретению предложен способ доставки белка PAH в клетку субъекта, нуждающегося в этом, включающий многократные введения зкДНК-вектора согласно настоящему изобретению, кодирующего указанный белок PAH. Поскольку зкДНК-вектор согласно настоящему изобретению не индуцирует иммунный ответ, подобный тому, который, как правило, наблюдается против инкапсидированных вирусных векторов, такая стратегия многократного введения, вероятно, будет иметь больший успех в системе на основе зкДНК. ЗкДНК-вектор вводят в количествах, достаточных для трансфекции клеток целевой ткани и обеспечения достаточных уровней переноса генов и экспрессии белка PAH без неоправданных нежелательных эффектов. Обычные и фармацевтически приемлемые пути введения включают, но не ограничиваются перечисленными, введение в сетчатку (например, субретинальную инъекцию, супрахориоидальную инъекцию или интравитреальную инъекцию), внутривенное введение (например, в липосомальном составе), прямую доставку в выбранный орган (например, в любую одну или более тканей, выбранных из: печени, почек, желчного пузыря, простаты, надпочечников, сердца, кишечника, легкого и желудка), внутримышечный и другие парентеральные пути введения. Пути введения могут быть скомбинированы, при необходимости.
[00401] Доставка зкДНК-вектора для экспрессии белка PAH, описанного в данном документе, не ограничивается доставкой экспрессируемого белка PAH. Например, зкДНК-векторы, полученные с помощью обычного способа (например, с использованием способа продуцирования на основе клеток (например, способов продуцирования в клетках насекомых)) или синтетического способа, как описано в данном документе, можно применять вместе с другими предложенными системами доставки, чтобы обеспечить часть генной терапии. Один неограничивающий пример системы, которую можно комбинировать с зкДНК-векторами в соответствии с настоящим раскрытием, включает системы, которые доставляют по отдельности один или более кофакторов или иммунных супрессоров для эффективной генной экспрессии зкДНК-вектора, экспрессирующего белок PAH.
[00402] Согласно настоящему изобретению также предложен способ лечения ФКУ у субъекта, включающий введение в нуждающуюся в этом целевую клетку (в частности, в мышечную клетку или ткань) указанного субъекта терапевтически эффективного количества зкДНК-вектора, необязательно с фармацевтически приемлемым носителем. Несмотря на то, что зкДНК-вектор может быть введен в присутствии носителя, такой носитель не является необходимым. Выбранный зкДНК-вектор содержит нуклеотидную последовательность, кодирующую белок PAH, который можно применять для лечения ФКУ. В частности, зкДНК-вектор может содержать целевую последовательность белка PAH, функционально связанную с контрольными элементами, способными управлять транскрипцией целевого белка PAH, кодируемого экзогенной последовательностью ДНК, при введении субъекту. ЗкДНК-вектор может быть введен любым подходящим путем, предложенным выше и в других разделах данного документа.
[00403] Композиции и векторы, предложенные в данном документе, можно применять для доставки белка PAH с различными целями. Согласно некоторым вариантам реализации трансген кодирует белок PAH, который предназначен для применения в исследовательских целях, например, для создания соматической трансгенной модели на животных, несущей трансген, например, для исследования функции продукта белка PAH. В другом примере трансген кодирует белок PAH, который предназначен для применения с целью создания модели ФКУ на животных. Согласно некоторым вариантам реализации кодируемый белок PAH можно применять для лечения или предотвращения ФКУ у млекопитающего-субъекта. Белок PAH может быть перенесен в организм пациента (например, экспрессирован у пациента) в количестве, достаточном для лечения ФКУ, ассоциированной с пониженной экспрессией, отсутствием экспрессии или дисфункцией указанного гена.
[00404] В принципе, экспрессионная кассета может включать нуклеиновую кислоту или любой трансген, который кодирует белок PAH, который либо снижен, либо отсутствует из-за мутации, либо который обеспечивает терапевтическую пользу при сверхэкспрессии, и рассматривается, как включенная в объем настоящего изобретения. Предпочтительно не вставленная бактериальная ДНК не присутствует и предпочтительно бактериальная ДНК не присутствует в композициях зкДНК, предложенных в данном документе.
[00405] ЗкДНК-вектор не ограничивается одной молекулой зкДНК-вектора. Таким образом, в другом аспекте несколько зкДНК-векторов, экспрессирующих разные белки или один и тот же белок PAH, но функционально связанный с различными промоторами или цис-регуляторными элементами, могут быть доставлены одновременно или последовательно в целевую клетку, ткань, орган или в организм субъекта. Таким образом, эта стратегия может обеспечить одновременную генную терапию несколькими белками или доставку их генов. Также можно разместить разные части белка PAH в отдельных зкДНК-векторах (например, разные домены и/или кофакторы, необходимые для функциональности белка PAH), например, которые могут быть введены одновременно или в разные моменты времени, и которые можно регулировать по отдельности, добавляя посредством этого дополнительный уровень контроля экспрессии белка PAH. Доставку также можно выполнять несколько раз и, что важно для генной терапии в клинических условиях, с последующим увеличением или снижением доз, учитывая отсутствие иммунного ответа хозяина против капсида вследствие отсутствия вирусного капсида. Ожидается, что ответ против капсида не возникнет из-за отсутствия капсида.
[00406] Согласно настоящему изобретению также предложен способ лечения у субъекта ФКУ, включающий введение в нуждающуюся в этом целевую клетку (в частности, в мышечную клетку или ткань) указанного субъекта терапевтически эффективного количества зкДНК-вектора, раскрытого в данном документе, необязательно с фармацевтически приемлемым носителем. Несмотря на то, что зкДНК-вектор может быть введен в присутствии носителя, такой носитель не является необходимым. Реализованный зкДНК-вектор содержит представляющую интерес нуклеотидную последовательность, подходящую для лечения ФКУ. В частности, зкДНК-вектор может содержать целевую экзогенную последовательность ДНК, функционально связанную с контрольными элементами, способными управлять транскрипцией целевого полипептида, белка или олигонуклеотида, кодируемого указанной экзогенной последовательностью ДНК, при введении субъекту. ЗкДНК-вектор может быть введен любым подходящим путем, предложенным выше и в других разделах данного документа.
IX. Способы доставки зкДНК-векторов для продукции белка PAH
[00407] Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH может быть доставлен в клетку-мишень in vitro или in vivo различными подходящими способами. ЗкДНК-векторы могут быть применены или инъецированы по отдельности. ДНК-векторы могут быть доставлены в клетку без помощи реагента для трансфекции или других физических средств. В качестве альтернативы, зкДНК-векторы для экспрессии белка PAH могут быть доставлены с использованием любого известного в данной области техники реагента для трансфекции или других известных в данной области техники физических средств, которые облегчают проникновение ДНК в клетку, например, липосом, спиртов, соединений, богатых полилизином, соединений, богатых аргинином, фосфата кальция, микровезикул, микроинъекции, электропорации и т.п.
[00408] зкДНК-векторы для экспрессии белка PAH, раскрытые в данном документе, могут быть эффективно нацелены на типы клеток и тканей, которые обычно трудно трансдуцировать обычными вирионами ААВ с использованием различных реагентов для доставки.
[00409] Один аспект технологии, описанной в данном документе, относится к способу доставки белка PAH в клетку. Как правило, для способов in vivo и in vitro зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, может быть введен в клетку с использованием способов, раскрытых в данном документе, а также других способов, известных в данной области техники. ЗкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, предпочтительно вводят в клетку в биологически эффективном количестве. Если зкДНК-вектор вводят в клетку in vivo (например, субъекту), биологически эффективное количество зкДНК-вектора представляет собой количество, достаточное для трансдукции и экспрессии белка PAH в клетке-мишени.
[00410] Примерные способы введения зкДНК-вектора для экспрессии белка PAH, раскрытого в данном документе, включают пероральный, ректальный, трансмукозальный, интраназальный, ингаляционный (например, с помощью аэрозоля), буккальный (например, сублингвальный), вагинальный, интратекальный, внутриглазной, трансдермальный, внутриэндотелиальный, in utero (или in ovo), парентеральный (например, внутривенный, подкожный, внутрикожный, внутричерепной, внутримышечный [включая введение в скелетную, диафрагмальную и/или сердечную мышцу], внутриплевральный, внутримозговой и внутрисуставной). Введение может представлять собой системную или прямую доставку в печень или куда-либо еще (например, в любые почки, желчный пузырь, простату, надпочечники, сердце, кишечник, легкое и желудок).
[00411] Введение может быть местным (например, на поверхность кожи и слизистых оболочек, включая поверхности дыхательных путей и трансдермальное введение), внутрилимфатическим и т.п., а также путем прямой инъекции в ткань или орган (например, но не ограничиваясь этим, в печень, а также в глаз, мышцы, включая скелетную мышцу, сердечную мышцу, диафрагмальную мышцу, или головной мозг).
[00412] ЗкДНК-вектор может быть введен в любое место у субъекта, включая, без ограничения, место, выбранное из группы, состоящей из печени и/или также глаз, головного мозга, скелетной мышцы, гладкой мышцы, сердца, диафрагмы, эпителия дыхательных путей, почки, селезенки, поджелудочной железы, кожи.
[00413] Наиболее подходящий путь в любом конкретном случае будет зависеть от характера и тяжести состояния, подлежащего лечению, облегчению и/или предотвращению, а также от характера конкретного используемого зкДНК-вектора. Кроме того, зкДНК позволяет вводить более одного белка PAH в одном векторе или в нескольких зкДНК-векторах (например, смесь зкДНК).
А. Внутримышечное введение зкДНК-вектора
[00414] Согласно некоторым вариантам реализации способ лечения заболевания у субъекта включает введение в нуждающуюся в этом целевую клетку (в частности, в мышечную клетку или ткань) указанного субъекта терапевтически эффективного количества зкДНК-вектора, кодирующего белок PAH, необязательно с фармацевтически приемлемым носителем. Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH вводят в мышечную ткань субъекта.
[00415] Согласно некоторым вариантам реализации зкДНК-вектор может быть введен в любое место у субъекта, включая, без ограничения, место, выбранное из группы, состоящей из скелетной мышцы, гладкой мышцы, сердца, диафрагмы или мышц глаза.
[00416] Введение зкДНК-вектора для экспрессии белка PAH, раскрытого в данном документе, в скелетную мышцу в соответствии с настоящим изобретением включает, но не ограничивается этим, введение в скелетную мышцу в конечностях (например, верхнюю часть плеча, нижнюю часть плеча, верхнюю части ноги и/или нижнюю часть ноги), спину, шею, голову (например, язык), грудную клетку, живот, таз/промежность и/или пальцы. ЗкДНК-вектор, раскрытый в данном документе, может быть доставлен в скелетную мышцу путем внутривенного введения, внутриартериального введения, внутрибрюшинного введения, перфузии конечности (необязательно изолированной перфузии конечности для ноги и/или руки; см., например, Arruda et al., (2005) Blood 105: 3458-3464), и/или путем прямой внутримышечной инъекции. Согласно конкретным вариантам реализации зкДНК-вектор, раскрытый в данном документе, вводят в печень, глаз, конечность (руку и/или ногу) субъекта (например, субъекта с мышечной дистрофией, такой как МДД) путем перфузии конечности, необязательно изолированной перфузии конечности (например, путем внутривенного или внутрисуставного введения). В вариантах реализации зкДНК-вектор, раскрытый в данном документе, можно вводить без применения «гидродинамических» методик.
[00417] Например, доставка в ткань (например, сетчатку) обычных вирусных векторов часто усиливается гидродинамическими методиками (например, внутривенным/внутривенным введением в большом объеме), которые увеличивают давление в сосудистой сети и облегчают способность вирусного вектора пересекать барьер из эндотелиальных клеток. Согласно конкретным вариантам реализации зкДНК-векторы, описанные в данном документе, можно вводить без гидродинамических методик, таких как инфузии большого объема и/или повышенное внутрисосудистое давление (например, выше нормального систолического давления, например, повышение внутрисосудистого давления на величину менее или равную 5%, 10%, 15%, 20%, 25% от нормального систолического давления). Такие методы могут уменьшить или позволяют избежать побочных эффектов, ассоциированных с гидродинамическими методиками, таких как отек, повреждение нервов и/или синдром сдавливания.
[00418] Кроме того, композиция, содержащая зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, которую вводят в скелетную мышцу, может быть введена в скелетную мышцу в конечностях (например, в верхнюю часть плеча, нижнюю часть плеча, верхнюю части ноги и/или нижнюю часть ноги), спину, шею, голову (например, язык), грудную клетку, живот, таз/промежность и/или пальцы. Подходящие скелетные мышцы включают, но не ограничиваются перечисленными, abductor digiti minimi (в кисти), abductor digiti minimi (в стопе), abductor hallucis, abductor ossis metatarsi quinti, abductor pollicis brevis, abductor pollicis longus, adductor brevis, adductor hallucis, adductor longus, adductor magnus, adductor pollicis, anconeus, anterior scalene, articularis genus, biceps brachii, biceps femoris, brachialis, brachioradialis, buccinator, coracobrachialis, corrugator supercilii, deltoid, depressor anguli oris, depressor labii inferioris, digastric, dorsal interossei (в кисти), dorsal interossei (в стопе), extensor carpi radialis brevis, extensor carpi radialis longus, extensor carpi ulnaris, extensor digiti minimi, extensor digitorum, extensor digitorum brevis, extensor digitorum longus, extensor hallucis brevis, extensor hallucis longus, extensor indicis, extensor pollicis brevis, extensor pollicis longus, flexor carpi radialis, flexor carpi ulnaris, flexor digiti minimi brevis (в кисти), flexor digiti minimi brevis (в стопе), flexor digitorum brevis, flexor digitorum longus, flexor digitorum profundus, flexor digitorum superficialis, flexor hallucis brevis, flexor hallucis longus, flexor pollicis brevis, flexor pollicis longus, frontalis, gastrocnemius, geniohyoid, gluteus maximus, gluteus medius, gluteus minimus, gracilis, iliocostalis cervicis, iliocostalis lumborum, iliocostalis thoracis, illiacus, inferior gemellus, inferior oblique, inferior rectus, infraspinatus, interspinalis, intertransversi, lateral pterygoid, lateral rectus, latissimus dorsi, levator anguli oris, levator labii superioris, levator labii superioris alaeque nasi, levator palpebrae superioris, levator scapulae, long rotators, longissimus capitis, longissimus cervicis, longissimus thoracis, longus capitis, longus colli, lumbricals (в кисти), lumbricals (в стопе), masseter, medial pterygoid, medial rectus, middle scalene, multifidus, mylohyoid, obliquus capitis inferior, obliquus capitis superior, obturator externus, obturator internus, occipitalis, omohyoid, opponens digiti minimi, opponens pollicis, orbicularis oculi, orbicularis oris, palmar interossei, palmaris brevis, palmaris longus, pectineus, pectoralis major, pectoralis minor, peroneus brevis, peroneus longus, peroneus tertius, piriformis, plantar interossei, plantaris, platysma, popliteus, posterior scalene, pronator quadratus, pronator teres, psoas major, quadratus femoris, quadratus plantae, rectus capitis anterior, rectus capitis lateralis, rectus capitis posterior major, rectus capitis posterior minor, rectus femoris, rhomboid major, rhomboid minor, risorius, sartorius, scalenus minimus, semimembranosus, semispinalis capitis, semispinalis cervicis, semispinalis thoracis, semitendinosus, serratus anterior, short rotators, soleus, spinalis capitis, spinalis cervicis, spinalis thoracis, splenius capitis, splenius cervicis, sternocleidomastoid, sternohyoid, sternothyroid, stylohyoid, subclavius, subscapularis, superior gemellus, superior oblique, superior rectus, supinator, supraspinatus, temporalis, tensor fascia lata, teres major, teres minor, thoracis, thyrohyoid, tibialis anterior, tibialis posterior, trapezius, triceps brachii, vastus intermedius, vastus lateralis, vastus medialis, zygomaticus major и zygomaticus minor, а также любую другую подходящую скелетную мышцу, известную в данной области техники.
[00419] Введение зкДНК-вектора для экспрессии белка PAH, раскрытого в данном документе, в диафрагмальную мышцу можно осуществлять любым подходящим способом, включая внутривенное введение, внутриартериальное введение и/или внутрибрюшинное введение. Согласно некоторым вариантам реализации доставка экспрессированного с зкДНК-вектора трансгена в ткань-мишень также может быть достигнута путем доставки синтетического депо, содержащего зкДНК-вектор, причем депо, содержащее зкДНК-вектор, имплантируют в скелетную, гладкомышечную, сердечную и/или диафрагмальную мышечную ткань или мышечная ткань может быть приведена в контакт с пленкой или другим матриксом, содержащим зкДНК-вектор, как описано в данном документе. Такие имплантируемые матриксы или субстраты описаны в патенте США № 7201898, полностью включенном в данный документ посредством ссылки.
[00420] Введение зкДНК-вектора для экспрессии белка PAH, раскрытого в данном документе, в сердечную мышцу включает введение в левое предсердие, правое предсердие, левый желудочек, правый желудочек и/или перегородку. ЗкДНК-вектор, описанный в данном документе, может быть доставлен в сердечную мышцу путем внутривенного введения, внутриартериального введения, такого как внутриаортальное введение, прямой сердечной инъекции (например, в левое предсердие, правое предсердие, левый желудочек, правый желудочек), и/или перфузии коронарной артерии.
[00421] Введение зкДНК-вектора для экспрессии белка PAH, раскрытого в данном документе, в гладкую мышцу можно осуществлять любым подходящим способом, включая внутривенное введение, внутриартериальное введение и/или внутрибрюшинное введение. Согласно одному варианту реализации введение можно осуществлять в эндотелиальные клетки, присутствующие в гладких мышцах, рядом с ними и/или на них. Неограничивающие примеры гладких мышц включают радужную оболочку глаза, бронхиолы легкого, мышцы гортани (голосовые связки), мышечные слои желудка, пищевода, тонкого и толстого кишечника желудочно-кишечного тракта, мочеточника, детрузора мочевого пузыря, миометрия матки, полового члена или простаты.
[00422] Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, вводят в скелетную мышцу, диафрагмальную мышцу и/или сердечную мышцу. В типичных вариантах реализации зкДНК-вектор в соответствии с настоящим изобретением применяют для лечения и/или предотвращения нарушений скелетной, сердечной и/или диафрагмальной мышцы.
[00423] В частности, предусмотрено, что композиция, содержащая зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, может быть доставлена в одну или более мышц глаза (например, Lateral rectus, Medial rectus, Superior rectus, Inferior rectus, Superior oblique, Inferior oblique), мимические мышцы (такие мышцы как Occipitofrontalis, Temporoparietalis, Procerus, Nasalis, Depressor septi nasi, Orbicularis oculi, Corrugator supercilii, Depressor supercilii, Auriculars, Orbicularis oris, Depressor anguli oris, Risorius, Zygomaticus major, Zygomaticus minor, Levator labii superioris, Levator labii superioris alaeque nasi, Depressor labii inferioris, Levator anguli oris, Buccinator, Mentalis) или мышцы языка (например, подбородочно-язычную мышцу, подъязычно-язычную мышцу, хрящеязычную мышцу, шилоязычную мышцу, небно-язычную мышцу, верхнюю продольную мышцу, нижнюю продольную мышцу, вертикальную мышцу и поперечную мышцу).
(i) Внутримышечная инъекция:
[00424] Согласно некоторым вариантам реализации композиция, содержащая зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, может быть введена путем инъекции в одно или более мест конкретной мышцы, например, скелетной мышцы (например, дельтовидной, латеральной широкой мышцы бедра, вентро-ягодичной мышцы тыльной ягодичной мышцы или переднебоковой мышцы бедра для младенцев), субъекта с помощью иглы. Композиция, содержащая зкДНК, может быть введена в другие подтипы мышечных клеток. Неограничивающие примеры подтипов мышечных клеток включают клетки скелетных мышц, клетки сердечной мышцы, клетки гладких мышц и/или клетки диафрагмальной мышцы.
[00425] Способы внутримышечной инъекции известны специалистам в данной области техники и поэтому в данном документе подробно не описываются. Однако при выполнении внутримышечной инъекции соответствующий размер иглы следует определять на основании возраста и комплекции пациента, вязкости композиции, а также места инъекции. В Таблице 8 приведены рекомендации по примерным местам инъекции и соответствующему размеру иглы:
Таблица 8: Рекомендации по внутримышечной инъекции пациентам-людям
Вязкий раствор или раствор на масляной основе: 18-21 калибр
Обычный взрослый: 25 мм
Крупный взрослый (более 150 фунтов): 25-38 мм
Дети и младенцы: потребуется игла меньшего размера
Вязкий раствор или раствор на масляной основе: 18-21 калибр
Дети/младенцы: 22-25 калибр
130-260 фунтов: 25 мм
Женщины:
<130 фунтов: 16 мм
130-200 фунтов: 25 мм
>200 фунтов: 38 мм
[00426] Согласно определенным вариантам реализации зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, изготавливают в небольшом объеме, например, примерном объеме, изложенном в Таблице 8, для конкретного субъекта. Согласно некоторым вариантам реализации перед инъекцией субъекту может быть введен общий или местный анестетик, при необходимости. Это особенно желательно, если требуется несколько инъекций или если инъекцию вводят в более глубокую мышцу, а не в обычные места инъекций, указанные выше.
[00427] Согласно некоторым вариантам реализации внутримышечную инъекцию можно комбинировать с электропорацией, давлением доставки или использованием реагентов для трансфекции для усиления клеточного поглощения зкДНК-вектора.
(ii) Реагенты для трансфекции
[00428] Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, изготавливают в виде композиций, содержащих один или более реагентов для трансфекции, чтобы облегчить поглощение векторов в мышечные трубочки или мышечную ткань. Таким образом, в одном варианте реализации, нуклеиновые кислоты, описанные в данном документе, вводят в мышечную клетку, мышечную трубочку или мышечную ткань путем трансфекции с использованием способов, описанных в другом месте в данном документе.
(iii) Электропорация
[00429] Согласно определенным вариантам реализации зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, вводят без носителя для облегчения проникновения зкДНК в клетки или в физиологически инертном фармацевтически приемлемом носителе (т. е. в любом носителе, который не улучшает или не усиливает поглощение бескапсидных невирусных векторов в мышечные трубочки). Согласно таким вариантам реализации поглощение бескапсидного невирусного вектора может быть облегчено путем электропорации клетки или ткани.
[00430] Клеточные мембраны естественным образом устойчивы к проникновению внеклеточных объектов в цитоплазму клетки. Одним из методов временного уменьшения этой устойчивости является «электропорация», когда электрические поля используют для создания пор в клетках, не вызывая необратимого повреждения клеток. Эти поры достаточно велики, чтобы позволить ДНК-векторам, фармацевтическим препаратам, ДНК и другим полярным соединениям проникать внутрь клетки. Со временем поры в клеточной мембране закрываются, и клетка снова становится непроницаемой.
[00431] Электропорацию можно использовать в приложениях как in vitro, так и in vivo для введения, например, экзогенной ДНК в живые клетки. Для приложений in vitro, как правило, смешивают образец живых клеток с композицией, содержащей, например, ДНК. Затем клетки помещают между электродами, такими как параллельные пластины, и к смеси клетка/композиция прикладывают электрическое поле.
[00432] Существует ряд методов электропорации in vivo; электроды могут быть обеспечены в различных конфигурациях, таких как, например, штангенциркуль, который захватывает эпидермис, лежащий над областью клеток, подлежащих обработке. В качестве альтернативы, в ткань могут быть введены игольчатые электроды для доступа к клеткам, расположенным глубже. В любом случае, после инъекционного введения композиции, содержащей, например, нуклеиновые кислоты, в область обработки, электроды прикладывают к области электрическое поле. В некоторых приложениях электропорации электрическое поле представляет собой одиночный прямоугольный импульс порядка 100-500 В/см с длительностью от 10 до 60 мс. Такой импульс может генерироваться, например, в известных приложениях Electro Square Porator T820, производимых BTX Division Genetronics, Inc.
[00433] Как правило, успешное поглощение, например, нуклеиновых кислот, происходит только в том случае, если мышцу электрически стимулировать сразу или вскоре после введения композиции, например, путем инъекции в мышцу.
[00434] Согласно определенным вариантам реализации электропорация достигается с использованием импульсов электрических полей или с использованием схем обработки с низким напряжением/длинными импульсами (например, с использованием системы электропорации с прямоугольными импульсами). Примерные генераторы импульсов, способные генерировать импульсное электрическое поле, включают, например, ECM600, который может генерировать экспоненциальную форму волны, и ElectroSquarePorator (T820), который может генерировать прямоугольную форму волны, оба из которых доступны от BTX, подразделения Genetronics, Inc. (Сан-Диего, Калифорния). Системы электропорации с прямоугольной волной доставляют контролируемые электрические импульсы, которые быстро повышаются до заданного напряжения, остаются на этом уровне в течение заданного периода времени (длительность импульса), а затем быстро падают до нуля.
[00435] Согласно некоторым вариантам реализации местный анестетик вводят, например, путем инъекции в место обработки, чтобы уменьшить боль, которая может быть ассоциирована с электропорацией ткани в присутствии композиции, содержащей бескапсидный невирусный вектор, как описано в данном документе. Кроме того, специалист в данной области техники поймет, что следует выбирать дозу композиции, которая сводит к минимуму и/или предотвращает чрезмерное повреждение ткани, приводящее к фиброзу, некрозу или воспалению мышцы.
(iv) Давление доставки
[00436] Согласно некоторым вариантам реализации доставку зкДНК-вектора для экспрессии белка PAH, раскрытого в данном документе, в мышечную ткань облегчают с помощью давления доставки, при котором используется комбинация больших объемов и быстрой инъекции в артерию, снабжающую конечность (например, подвздошную артерию). Этот способ введения может быть достигнут с помощью множества способов, которые включают вливание в сосудистую сеть конечности композиции, содержащей зкДНК-вектор, как правило, при изоляции мышцы от большого круга кровообращения с помощью жгута сосудистого зажима. В одном методе композиция циркулирует через сосудистую сеть конечности, чтобы обеспечить возможность экстравазации в клетки. В другом методе внутрисосудистое гидродинамическое давление увеличивается для расширения сосудистых лож и увеличения поглощения зкДНК-вектора в мышечные клетки или ткань. Согласно одному варианту реализации композицию зкДНК вводят в артерию.
(v) Композиции липидных наночастиц
[00437] Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, для внутримышечной доставки изготавливают в виде композиции, содержащей липосому, как описано в другом месте в данном документе.
(vi) Системное введение зкДНК-вектора, нацеленного на мышечную ткань
[00438] Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, изготавливают для нацеливания на мышцу за счет введения путем непрямой доставки, при котором зкДНК транспортируется в мышцу, а не в печень. Соответственно, технология, описанная в данном документе, включает непрямое введение композиций, содержащих зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, в мышечную ткань, например, путем системного введения. Такие композиции можно вводить местно, внутривенно (с помощью болюсной или непрерывной инфузии), с помощью внутриклеточной инъекции, внутритканевой инъекции, перорально, путем ингаляции, внутрибрюшинно, подкожно, внутрь полости, а также их можно доставлять с помощью перистальтических средств, при необходимости, или с помощью других средств, известных специалистам в данной области техники. При необходимости, агент может быть введен системно, например, путем внутривенной инфузии.
[00439] Согласно некоторым вариантам реализации поглощение зкДНК-вектора для экспрессии белка PAH, раскрытого в данном документе, в мышечные клетки/ткань увеличивается за счет использования нацеливающего агента или фрагмента, который преимущественно направляет вектор в мышечную ткань. Таким образом, в некоторых вариантах реализации бескапсидный зкДНК-вектор может быть сконцентрирован в мышечной ткани по сравнению с количеством бескапсидных зкДНК-векторов, присутствующих в других клетках или тканях организма.
[00440] Согласно некоторым вариантам реализации композиция, содержащая зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, дополнительно содержит фрагмент, нацеливающий на мышечные клетки. Согласно другим вариантам реализации экспрессированный генный продукт содержит нацеливающий фрагмент, специфический для ткани, в котором его действие является желательным. Нацеливающий фрагмент может включать любую молекулу или комплекс молекул, которые способны нацеливаться, взаимодействовать, соединяться и/или связываться с внутриклеточным, поверхностным или внеклеточным биомаркером клетки или ткани. Биомаркер может включать, например, клеточную протеазу, киназу, белок, рецептор клеточной поверхности, липид и/или алифатическую кислоту. Другие примеры биомаркеров, на которые могут быть нацелены, с которыми могут взаимодействовать, соединяться и/или связываться нацеливающие фрагменты, включают молекулы, ассоциированные с конкретным заболеванием. Например, биомаркеры могут включать рецепторы клеточной поверхности, участвующие в развитии рака, такие как рецептор эпидермального фактора роста и рецептор трансферрина. Нацеливающие фрагменты могут включать, но не ограничиваются перечисленными, синтетические соединения, природные соединения или продукты, макромолекулярные объекты, биосконструированные молекулы (например, полипептиды, липиды, полинуклеотиды, антитела, фрагменты антител) и малые объекты (например, малые молекулы, нейротрансмиттеры, субстраты, лиганды, гормоны и соединения элементов), которые связываются с молекулами, экспрессируемыми в целевой мышечной ткани.
[00441] Согласно определенным вариантам реализации нацеливающий фрагмент может дополнительно содержать рецепторную молекулу, включая, например, рецепторы, которые естественным образом распознают конкретную целевую молекулу клетки-мишени. Такие рецепторные молекулы включают рецепторы, которые были модифицированы для повышения их специфичности взаимодействия с молекулой-мишенью, рецепторы, которые были модифицированы для взаимодействия с целевой молекулой-мишенью, не распознаваемой рецептором в естественных условиях, и фрагменты таких рецепторов (см., например, Skerra, 2000, J. Molecular Recognition, 13:167-187). Предпочтительный рецептор представляет собой рецептор хемокина. Примерные рецепторы хемокинов описаны, например, в Lapidot et al, 2002, Exp Hematol, 30:973-81 и Onuffer et al, 2002, Trends Pharmacol Sci, 23:459-67.
[00442] Согласно другим вариантам реализации дополнительный нацеливающий фрагмент может содержать молекулу лиганда, включая, например, лиганды, которые естественным образом распознают конкретный целевой рецептор клетки-мишени, такой как лиганд трансферрина (Tf). Такие молекулы лигандов включают лиганды, которые были модифицированы для повышения их специфичности взаимодействия с рецептором-мишенью, лиганды, которые были модифицированы для взаимодействия с целевым рецептором, который не распознается лигандом в естественных условиях, и фрагменты таких лигандов.
[00443] Согласно другим вариантам реализации нацеливающий фрагмент может содержать аптамер. Аптамеры представляют собой олигонуклеотиды, выбранные для специфичного связывания с целевой молекулярной структурой клетки-мишени. Аптамеры, как правило, представляют собой продукты способа селекции по аффинности, сходного с селекцией по аффинности при фаговом дисплее (также известной как молекулярная эволюция in vitro). Способ включает выполнение нескольких тандемных итераций разделения по аффинности, например, с использованием твердой подложки, с которой связан патологический иммуноген, с последующей полимеразной цепной реакцией (ПЦР) для амплификации нуклеиновых кислот, которые связались с иммуногенами. Таким образом, каждый раунд аффинного разделения обогащает популяцию нуклеиновых кислот молекулами, которые успешно связывают целевой иммуноген. Таким путем случайный пул нуклеиновых кислот может быть «обучен» с получением аптамеров, которые специфично связывают молекулы-мишени. Аптамеры, как правило, представляют собой РНК, но могут представлять собой ДНК или ее аналоги или производные, такие как, без ограничения, пептидные нуклеиновые кислоты (ПНК) и фосфотиоатные нуклеиновые кислоты.
[00444] Согласно некоторым вариантам реализации нацеливающий фрагмент может содержать фоторазлагаемый лиганд (т. е. «запертый» лиганд), который высвобождается, например, под действием сфокусированного луча света так, что бескапсидные невирусные векторы или генный продукт нацеливаются на конкретную ткань.
[00445] В данном документе также предусмотрено, что композиции доставляют в несколько мест в одной или более мышцах субъекта. Таким образом, инъекции могут быть сделаны в по меньшей мере 2, по меньшей мере 3, по меньшей мере 4, по меньшей мере 5, по меньшей мере 6, по меньшей мере 7, по меньшей мере 8, по меньшей мере 9, по меньшей мере 10, по меньшей мере 15, по меньшей мере 20, по меньшей мере 25, по меньшей мере 30, по меньшей мере 35, по меньшей мере 40, по меньшей мере 45, по меньшей мере 50, по меньшей мере 55, по меньшей мере 60, по меньшей мере 65, по меньшей мере 70, по меньшей мере 75, по меньшей мере 80, по меньшей мере 85, по меньшей мере 90, по меньшей мере 95, по меньшей мере 100 местах инъекций. Такие места могут быть распределены по площади одной мышцы или могут быть распределены между несколькими мышцами.
B. Введение зкДНК-вектора для экспрессии белка PAH в немышечные места
[00446] Согласно другому варианту реализации зкДНК-вектор для экспрессии белка PAH вводят в печень. ЗкДНК-вектор также можно вводить в различные области глаза, такие как роговица и/или зрительный нерв. ЗкДНК-вектор также можно вводить в спинной мозг, ствол мозга (продолговатый мозг, мост), средний мозг (гипоталамус, таламус, эпиталамус, гипофиз, черную субстанцию, эпифиз), мозжечок, конечный мозг (полосатое тело, полушария головного мозга, включая затылочную, височную, теменную и лобную доли, кору, базальные ганглии, гиппокамп и амигдалу), лимбическую систему, неокортекс, полосатое тело, полушария головного мозга и нижний холмик четверохолмия. ЗкДНК-вектор может быть доставлен в спинномозговую жидкость (например, с помощью люмбальной пункции). ЗкДНК-вектор для экспрессии белка PAH можно дополнительно вводить внутрисосудисто в ЦНС в ситуациях, когда нарушен гематоэнцефалический барьер (например, опухоль головного мозга или церебральный инфаркт).
[00447] Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH можно вводить в целевую область (области) глаза любым путем, известным в данной области техники, включая, но не ограничиваясь перечисленными, интратекальную, внутриглазную, интрацеребральную, внутрижелудочковую, внутривенную (например, в присутствии сахара, такого как маннит), интраназальную, внутриушную, внутриглазную (например, интравитреальную, субретинальную, в переднюю камеру) и периокулярную (например, в субтенонову область) доставку, а также внутримышечную доставку с ретроградной доставкой к двигательным нейронам.
[00448] Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH вводят в жидком составе путем прямой инъекции (например, стереотаксической инъекции) в целевую область или компартмент в ЦНС. Согласно другим вариантам реализации зкДНК-вектор может быть обеспечен путем местного нанесения на целевую область или путем интраназального введения аэрозольного состава. Введение в глаз можно осуществлять путем местного нанесения жидких капель. В качестве дополнительной альтернативы зкДНК-вектор можно вводить в виде твердого состава с медленным высвобождением (см., например, патент США № 7201898). Согласно другим дополнительным вариантам реализации зкДНК-вектор можно применять для ретроградного транспорта для лечения, облегчения и/или предотвращения заболеваний и нарушений, затрагивающих двигательные нейроны (например, бокового амиотрофического склероза (БАС); спинальной мышечной атрофии (СМА) и т. д.). Например, зкДНК-вектор может быть доставлен в мышечную ткань, из которой он может мигрировать в нейроны.
C. Лечение ex vivo
[00449] Согласно некоторым вариантам реализации клетки извлекают из организма субъекта, вводят в них зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, и затем клетки возвращают в организм субъекта. Способы извлечения клеток из организма субъекта для лечения ex vivo с последующим введением обратно в организм субъекта известны в данной области техники (см., например, патент США № 5399346; содержание которого полностью включено в данный документ). В качестве альтернативы, зкДНК-вектор вводят в клетки, полученные от другого субъекта, в культивируемые клетки или в клетки из любого другого подходящего источника, и указанные клетки вводят нуждающемуся в этом субъекту.
[00450] Клетки, трансдуцированные зкДНК-вектором для экспрессии белка PAH, раскрытым в данном документе, предпочтительно вводят субъекту в «терапевтически эффективном количестве» в комбинации с фармацевтическим носителем. Специалисты в данной области техники поймут, что терапевтические эффекты не обязательно должны быть полными или обеспечивать исцеление, при условии, что для субъекта они в какой-то мере благоприятны.
[00451] Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, может кодировать белок PAH, описанный в данном документе (иногда называемый трансгеном или гетерологичной нуклеотидной последовательностью), который должен продуцироваться в клетке in vitro, ex vivo или in vivo. Например, в отличие от применения зкДНК-векторов, описанных в данном документе, в способе лечения, который обсуждается в данном документе, в некоторых вариантах реализации зкДНК-вектор для экспрессии белка PAH может быть введен в культивируемые клетки, и экспрессированный белок PAH может быть выделен из клеток, например, для получения антител и слитых белков. Согласно некоторым вариантам реализации культивируемые клетки, содержащие зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, можно применять для коммерческого получения антител или слитых белков, например, в качестве источника клеток для мелкомасштабного или крупномасштабного биоизготовления антител или слитых белков. В альтернативных вариантах реализации зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, вводят в клетки у субъекта-хозяина, не являющегося человеком, для продуцирования антител или слитых белков in vivo, включая мелкомасштабное получение, а также коммерческое крупномасштабное получение белка PAH.
[00452] ЗкДНК-векторы для экспрессии белка PAH, раскрытые в данном документе, можно применять как в ветеринарных, так и в медицинских приложениях. Подходящие субъекты для способов доставки генов ex vivo, описанных выше, включают как птиц (например, кур, уток, гусей, перепелов, индеек и фазанов), так и млекопитающих (например, человека, бычьих, овечьих, козьих, лошадиных, кошачьих, собачьих и зайцеобразных), при этом предпочтительными являются млекопитающие. Субъекты-люди являются наиболее предпочтительными. Субъекты-люди включают новорожденных, младенцев, детей и подростков, и взрослых людей.
D. Диапазоны доз
[00453] В данном документе предложены способы лечения, включающие введение субъекту эффективного количества композиции, содержащей зкДНК-вектор, кодирующий белок PAH, как описано в данном документе. Как будет понятно квалифицированному практикующему врачу, термин «эффективное количество» относится к количеству введенной композиции зкДНК, которое приводит к экспрессии белка PAH в «терапевтически эффективном количестве» для лечения ФКУ.
[00454] Анализы in vivo и/или in vitro необязательно можно использовать, чтобы облегчить определение оптимальных диапазонов дозировок для применения. Точная доза, которая должна быть использована в составе, также будет зависеть от пути введения и серьезности состояния и должна определяться в соответствии с суждением обычного специалиста в данной области техники и обстоятельствами каждого субъекта. Эффективные дозы можно экстраполировать из кривых доза-ответ, полученных из тест-систем in vitro или в моделях на животных, например.
[00455] ЗкДНК-векторы для экспрессии белка PAH, раскрытые в данном документе, вводят в количествах, достаточных для трансфекции клеток целевой ткани и обеспечения достаточных уровней переноса и экспрессии генов без неоправданных нежелательных эффектов. Обычные и фармацевтически приемлемые пути введения включают, но не ограничиваются ими, те, которые описаны выше в разделе «Введение», такие как прямая доставка в выбранный орган (например, внутрипортальная доставка в печень), пероральный, ингаляционный (включая интраназальную и внутритрахеальную доставку), внутриглазной, внутривенный, внутримышечный, подкожный, внутрикожный, внутриопухолевый и другие исходные пути введения. Пути введения могут быть скомбинированы, если требуется.
[00456] Доза количества зкДНК-векторов для экспрессии белка PAH, раскрытых в данном документе, необходимая для достижения определенного «терапевтического эффекта», будет варьироваться в зависимости от нескольких факторов, включая, но не ограничиваясь перечисленными: путь введения нуклеиновой кислоты, уровень экспрессии гена или РНК, необходимый для достижения терапевтического эффекта, конкретное заболевание или нарушение, подлежащее лечению, и стабильность гена (ов), продукта (ов) РНК или полученного экспрессированного белка (ов). Специалист в данной области техники может легко определить диапазон доз зкДНК-вектора для лечения пациента, страдающего конкретным заболеванием или нарушением, на основании вышеупомянутых факторов, а также других факторов, которые хорошо известны в данной области техники.
[00457] Схему дозирования можно корректировать для обеспечения оптимального терапевтического ответа. Например, олигонуклеотид может быть введен повторно, например, несколько доз могут быть введены ежедневно или дозу можно пропорционально уменьшать в соответствии с требованиями терапевтической ситуации. Обычный специалист в данной области техники легко сможет определить подходящие дозы и схемы введения рассматриваемых олигонуклеотидов, независимо от того, должны быть введены олигонуклеотиды в клетки или субъектам.
[00458] «Терапевтически эффективная доза» будет находиться в относительно широком диапазоне, который может быть определен посредством клинических исследований, и будет зависеть от конкретного применения (нервным клеткам потребуются очень небольшие количества, в то время как системная инъекция потребует больших количеств). Например, для прямой инъекции in vivo в скелетную или сердечную мышцу субъекта-человека терапевтически эффективная доза будет порядка от примерно 1 мкг до 100 г зкДНК-вектора. Если для доставки зкДНК-вектора используются экзосомы или микрочастицы, то терапевтически эффективная доза может быть определена экспериментально, но ожидается, что она доставит от 1 мкг до примерно 100 г вектора. Более того, терапевтически эффективная доза представляет собой количество зкДНК-вектора, которое экспрессирует достаточное количество трансгена, чтобы оказывать влияние на субъекта, которое приводит к уменьшению одного или более симптомов заболевания, но не приводит к значительным нецелевым эффектам или значительным нежелательным побочным эффектам. Согласно одному варианту реализации «терапевтически эффективное количество» представляет собой количество экспрессированного белка PAH, которое достаточно для получения статистически значимого, измеримого изменения экспрессии биомаркера ФКУ или уменьшения симптома конкретного заболевания. Такие эффективные количества можно откалибровать в клинических исследованиях, а также в исследованиях на животных для конкретной композиции зкДНК-вектора.
[00459] Изготовление фармацевтически приемлемых вспомогательных веществ и растворов носителей хорошо известно специалистам в данной области техники, как и разработка подходящих схем дозирования и лечения для использования конкретных композиций, описанных в данном документе, в различных схемах лечения.
[00460] Для трансфекции in vitro эффективное количество зкДНК-векторов для экспрессии белка PAH, раскрытых в данном документе, для доставки в клетки (1×106 клеток) будет порядка от 0,1 до 100 мкг зкДНК-вектора, предпочтительно от 1 до 20 мкг и более предпочтительно от 1 до 15 мкг или от 8 до 10 мкг. Для более крупных зкДНК-векторов потребуются более высокие дозы. При использовании экзосом или микрочастиц, эффективная доза in vitro может быть определена экспериментально, но она будет предназначена для доставки в целом того же количества зкДНК-вектора.
[00461] Для лечения ФКУ подходящая дозировка зкДНК-вектора, который экспрессирует белок PAH, раскрытого в данном документе, будет зависеть от конкретного типа заболевания, подлежащего лечению, типа белка PAH, степени тяжести и течения заболевания ФКУ, предыдущей терапии, истории болезни пациента и реакции на антитело, а также от решения лечащего врача. ЗкДНК-вектор, кодирующий белок PAH, подходящим образом вводят пациенту за один раз или в течение ряда обработок. В данном документе предусмотрены различные схемы дозирования, включая, но не ограничиваясь перечисленными, однократное или многократное введение в различные моменты времени, болюсное введение и импульсную инфузию.
[00462] В зависимости от типа и степени тяжести заболевания зкДНК-вектор вводят в количестве, при котором кодируемый белок PAH экспрессируется в диапазоне от примерно 0, 3 мг/кг до 100 мг/кг (например, от 15 мг/кг до 100 мг/кг или любой дозировке в пределах этого диапазона), с помощью одного или более отдельных введений или непрерывной инфузии. Одной типичной суточной дозы зкДНК-вектора достаточно, чтобы привести к экспрессии кодируемого белка PAH в диапазоне от примерно 15 мг/кг до 100 мг/кг или более, в зависимости от факторов, упомянутых выше. Одна примерная доза зкДНК-вектора представляет собой количество, достаточное для того чтобы привести к экспрессии кодируемого белка PAH, как раскрыто в данном документе, в диапазоне от примерно 10 мг/кг до примерно 50 мг/кг. Таким образом, пациенту может быть введена одна или более доз зкДНК-вектора в количестве, достаточном для того чтобы привести к экспрессии кодируемого белка PAH при примерно 0,5 мг/кг, 1 мг/кг, 1,5 мг/кг, 2,0 мг/кг, 3 мг/кг, 4,0 мг/кг, 5 мг/кг, 10 мг/кг, 15 мг/кг, 20 мг/кг, 25 мг/кг, 30 мг/кг, 35 мг/кг, 40 мг/кг, 50 мг/кг, 60 мг/кг, 70 мг/кг, 80 мг/кг, 90 мг/кг или 100 мг/кг (или любой их комбинации). Согласно некоторым вариантам реализации зкДНК-вектор представляет собой количество, достаточное для того чтобы привести к экспрессии кодируемого белка PAH для общей дозы в диапазоне от 50 мг до 2500 мг. Примерная доза зкДНК-вектора представляет собой количество, достаточное для того чтобы привести к общей экспрессии кодируемого белка PAH примерно 50 мг, примерно 100 мг, 200 мг, 300 мг, 400 мг, примерно 500 мг, примерно 600 мг, примерно 700 мг, примерно 720 мг, примерно 1000 мг, примерно 1050 мг, примерно 1100 мг, примерно 1200 мг, примерно 1300 мг, примерно 1400 мг, примерно 1500 мг, примерно 1600 мг, примерно 1700 мг, примерно 1800 мг, примерно 1900 мг, примерно 2000 мг, примерно 2050 мг, примерно 2100 мг, примерно 2200 мг, примерно 2300 мг, примерно 2400 мг или примерно 2500 мг (или любой их комбинации). Поскольку экспрессию белка PAH с зкДНК-вектора можно тщательно контролировать с помощью регуляторных переключателей в данном документе или, альтернативно, многократной дозы зкДНК-вектора, вводимой субъекту, экспрессию белка PAH с зкДНК-вектора можно контролировать так, что дозы экспрессированного белка PAH можно вводить с перерывами, например, каждую неделю, каждые две недели, каждые три недели, каждые четыре недели, каждый месяц, каждые два месяца, каждые три месяца или каждые шесть месяцев с зкДНК-вектора. Ход этой терапии можно контролировать с помощью обычных методик и анализов.
[00463] Согласно определенным вариантам реализации зкДНК-вектор вводят в количестве, достаточном для того чтобы привести к экспрессии кодируемого белка PAH в дозе 15 мг/кг, 30 мг/кг, 40 мг/кг, 45 мг/кг, 50 мг/кг, 60 мг/кг или в фиксированной дозе, например, 300 мг, 500 мг, 700 мг, 800 мг или выше. Согласно некоторым вариантам реализации экспрессию белка PAH с зкДНК-вектора контролируют так, что белок PAH экспрессируется каждый день, через день, каждую неделю, каждые 2 недели или каждые 4 недели в течение некоторого периода времени. Согласно некоторым вариантам реализации экспрессию белка PAH с зкДНК-вектора контролируют так, что белок PAH экспрессируется каждые 2 недели или каждые 4 недели в течение некоторого периода времени. Согласно определенным вариантам реализации период времени составляет 6 месяцев, один год, восемнадцать месяцев, два года, пять лет, десять лет, 15 лет, 20 лет или продолжительность жизни пациента.
[00464] Лечение может включать введение однократной дозы или многократных доз. Согласно некоторым вариантам реализации субъекту можно вводить более одной дозы; фактически, при необходимости можно вводить многократные дозы, поскольку зкДНК-вектор не вызывает иммунного ответа хозяина против капсида ввиду отсутствия вирусного капсида. Таким образом, специалист в данной области техники может легко определить подходящее количество доз. Количество вводимых доз может составлять, например, порядка 1-100, предпочтительно 2-20 доз.
[00465] Не ограничиваясь какой-либо конкретной теорией, отсутствие типичного противовирусного иммунного ответа, вызванного введением зкДНК-вектора, как описано в настоящем раскрытии (т. е. отсутствие компонентов капсида), позволяет вводить хозяину зкДНК-вектор для экспрессии белка PAH несколько раз. Согласно некоторым вариантам реализации количество раз доставки гетерологичной нуклеиновой кислоты субъекту находится в диапазоне от 2 до 10 раз (например, 2, 3, 4, 5, 6, 7, 8, 9 или 10 раз). Согласно некоторым вариантам реализации зкДНК-вектор доставляют субъекту более 10 раз.
[00466] Согласно некоторым вариантам реализации дозу зкДНК-вектора для экспрессии белка PAH, раскрытого в данном документе, вводят субъекту не чаще одного раза в календарный день (например, в течение 24-часового периода). Согласно некоторым вариантам реализации дозу зкДНК-вектора вводят субъекту не чаще одного раза в 2, 3, 4, 5, 6 или 7 календарных дней. Согласно некоторым вариантам реализации дозу зкДНК-вектора для экспрессии белка PAH, раскрытого в данном документе, вводят субъекту не чаще одного раза в календарную неделю (например, 7 календарных дней). Согласно некоторым вариантам реализации дозу зкДНК-вектора вводят субъекту не чаще, чем один раз в две недели (например, один раз в период в две календарные недели). Согласно некоторым вариантам реализации дозу зкДНК-вектора вводят субъекту не чаще одного раза в календарный месяц (например, один раз в 30 календарных дней). Согласно некоторым вариантам реализации дозу зкДНК-вектора вводят субъекту не чаще одного раза в шесть календарных месяцев. Согласно некоторым вариантам реализации дозу зкДНК-вектора вводят субъекту не чаще одного раза в календарный год (например, 365 дней или 366 дней в високосный год).
[00467] В конкретных вариантах реализации для достижения целевого уровня экспрессии гена на протяжении различных периодов времени, например, ежедневно, еженедельно, ежемесячно, ежегодно и т. д., можно использовать более одного введения (например, два, три, четыре или более введений) зкДНК-вектора для экспрессии белка PAH, раскрытого в данном документе.
[00468] Согласно некоторым вариантам реализации терапевтический белок PAH, кодируемый зкДНК-вектором, раскрытым в данном документе, можно регулировать с помощью регуляторного переключателя, индуцируемого или репрессируемого промотора так, что он экспрессируется у субъекта в течение по меньшей мере 1 часа, по меньшей мере 2 часов, по меньшей мере 5 часов, по меньшей мере 10 часов, по меньшей мере 12 часов, по меньшей мере 18 часов, по меньшей мере 24 часов, по меньшей мере 36 часов, по меньшей мере 48 часов, по меньшей мере 72 часов, по меньшей мере 1 недели, по меньшей мере 2 недель, по меньшей мере 1 месяца, по меньшей мере 2 месяцев, по меньшей мере 6 месяцев, по меньшей мере 12 месяцев/одного года, по меньшей мере 2 лет, по меньшей мере 5 лет, по меньшей мере 10 лет, по меньшей мере 15 лет, по меньшей мере 20 лет, по меньшей мере 30 лет, по меньшей мере 40 лет, по меньшей мере 50 лет или более. Согласно одному варианту реализации экспрессия может быть достигнута путем повторного введения зкДНК-векторов, описанных в данном документе, через заранее определенные или желательные интервалы. В качестве альтернативы, зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, может дополнительно содержать компоненты системы редактирования генов (например, CRISPR/Cas, TALEN, эндонуклеазы цинковых пальцев и т. д.), что позволяет вставлять одну или более последовательностей нуклеиновых кислот, кодирующих белок PAH, для по существу постоянного лечения или «излечения» заболевания. Такие зкДНК-векторы, содержащие компоненты редактирования генов, раскрыты в международной заявке PCT/US18/64242 и могут включать 5´ и 3´ плечи гомологии (например, SEQ ID NO: 151-154, или последовательности, имеющие по меньшей мере 40%, 50%, 60%, 70% или 80% гомологии с ними) для вставки нуклеиновой кислоты, кодирующей белок PAH, в области «безопасной гавани», такие как, но не включая их, ген альбумина или ген CCR5. В качестве примера, зкДНК-вектор, экспрессирующий белок PAH, может содержать по меньшей мере одно плечо гомологии, специфичное в отношении геномной «безопасной гавани» (GSH), для встраивания трансгена PAH в геномную «безопасную гавань», как раскрыто в международной заявке на патент PCT/US2019/020225, поданной 1 марта 2019 г., которая полностью включена в данный документ посредством ссылки.
[00469] Продолжительность лечения зависит от клинического прогресса и ответа пациента на терапию. Предусмотрено непрерывное введение относительно низких поддерживающих доз после начальной более высокой терапевтической дозы.
E. Единичные лекарственные формы
[00470] Согласно некоторым вариантам реализации фармацевтические композиции, содержащие зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, могут быть удобно представлены в виде единичной лекарственной формы. Единичная лекарственная форма, как правило, адаптирована для одного или более конкретных путей введения фармацевтической композиции. Согласно некоторым вариантам реализации единичная лекарственная форма адаптирована для капель, которые будут введены непосредственно в глаз. Согласно некоторым вариантам реализации единичная лекарственная форма адаптирована для введения путем ингаляции. Согласно некоторым вариантам реализации единичная лекарственная форма адаптирована для введения с помощью испарителя. Согласно некоторым вариантам реализации единичная лекарственная форма адаптирована для введения с помощью небулайзера. Согласно некоторым вариантам реализации единичная лекарственная форма адаптирована для введения с помощью генератора аэрозоля. Согласно некоторым вариантам реализации единичная лекарственная форма адаптирована для перорального введения, для буккального введения или для сублингвального введения. Согласно некоторым вариантам реализации единичная лекарственная форма адаптирована для внутривенного, внутримышечного или подкожного введения. Согласно некоторым вариантам реализации единичная лекарственная форма адаптирована для субретинальной инъекции, супрахориоидальной инъекции или интравитреальной инъекции.
[00471] Согласно некоторым вариантам реализации единичная лекарственная форма адаптирована для интратекального или интрацеребровентрикулярного введения. Согласно некоторым вариантам реализации фармацевтическая композиция изготовлена для местного введения. Количество активного ингредиента, которое можно комбинировать с материалом носителя для получения единичной лекарственной формы, обычно будет представлять собой количество соединения, которое вызывает терапевтический эффект.
X. Способы лечения
[00472] Технология, описанная в данном документе, также демонстрирует способы получения, а также способы применения раскрытых зкДНК-векторов для экспрессии белка PAH различными путями, включая, например, ex vivo, ex situ, in vitro и in vivo приложения, методологии, диагностические процедуры и/или схемы генной терапии.
[00473] Согласно одному варианту реализации экспрессированный терапевтический белок PAH, экспрессируемый с зкДНК-вектора, раскрытого в данном документе, является функциональным для лечения заболевания. Согласно предпочтительному варианту реализации терапевтический белок PAH не вызывает реакции иммунной системы, если этого не требуется.
[00474] В данном документе предложен способ лечения ФКУ у субъекта, включающий введение в клетку-мишень, которая нуждается в этом (например, мышечную клетку или ткань, или другой тип пораженных клеток), указанного субъекта терапевтически эффективного количества зкДНК-вектора для экспрессии белка PAH, раскрытого в данном документе, необязательно с фармацевтически приемлемым носителем. Несмотря на то, что указанный зкДНК-вектор может быть введен в присутствии носителя, такой носитель не является необходимым. Реализованный зкДНК-вектор содержит нуклеотидную последовательность, кодирующую белок PAH, как описано в данном документе, которую можно применять для лечения заболевания. В частности, зкДНК-вектор для экспрессии белка PAH может содержать целевую последовательность ДНК белка PAH, функционально связанную с контрольными элементами, способными управлять транскрипцией целевого белка PAH, кодируемого экзогенной последовательностью ДНК, при введении в организм субъекта. ЗкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, может быть введен любым подходящим путем, предложенным выше и в других разделах данного документа.
[00475] В данном документе раскрыты композиции и составы зкДНК-векторов для экспрессии белка PAH, как раскрыто в данном документе, которые включают один или более зкДНК-векторов согласно настоящему изобретению вместе с одним или более фармацевтически приемлемыми буферами, разбавителями или вспомогательными веществами. Такие композиции могут быть включены в один или более диагностических или терапевтических наборов для диагностики, предотвращения, лечения или облегчения одного или более симптомов ФКУ. В одном аспекте заболевание, поражение, нарушение, травма или дисфункция представляет собой заболевание, поражение, нарушение, травму или дисфункцию человека.
[00476] Другой аспект технологии, описанной в данном документе, обеспечивает способ обеспечения субъекту, нуждающемуся в этом, диагностически или терапевтически эффективного количества зкДНК-вектора для экспрессии белка PAH, раскрытого в данном документе, причем указанный способ включает обеспечение в клетке, ткани или органе субъекта, нуждающегося в этом, количества зкДНК-вектора, раскрытого в данном документе; и в течение времени, эффективного для обеспечения экспрессии белка PAH с зкДНК-вектора, что обеспечивает субъекту диагностически или терапевтически эффективное количество белка PAH, экспрессируемого зкДНК-вектором. Согласно дополнительному аспекту субъект представляет собой человека.
[00477] Другой аспект технологии, описанной в данном документе, обеспечивает способ диагностики, предотвращения, лечения или облегчения по меньшей мере одного или более симптомов ФКУ, нарушения, дисфункции, поражения, аномального состояния или травмы у субъекта. В целом и в общем смысле, способ включает по меньшей мере этап введения субъекту, нуждающемуся в этом, одного или более из раскрытых зкДНК-векторов для продукции белка PAH в количестве и в течение времени, достаточных для диагностики, предотвращения, лечения или облегчения одного или более симптомов заболевания, нарушения, дисфункции, поражения, аномального состояния или травмы у субъекта. В таком варианте реализации у субъекта может быть оценена эффективность белка PAH или, альтернативно, проведено детектирование белка PAH или тканевого расположения белка PAH (включая клеточное и субклеточное расположение) у субъекта. Таким образом, зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, можно применять в качестве диагностического инструмента in vivo, например, для детектирования рака или других показаний. Согласно дополнительному аспекту субъект представляет собой человека.
[00478] Другим аспектом является применение зкДНК-вектора для экспрессии белка PAH, раскрытого в данном документе, в качестве инструмента для лечения или уменьшения одного или более симптомов ФКУ или патологических состояний. Существует ряд наследственных заболеваний, при которых известны дефектные гены, и, как правило, они делятся на два класса: дефицитные состояния, обычно ферментов, которые обычно наследуются рецессивным образом, и несбалансированные состояния, которые могут включать регуляторные или структурные белки и которые, как правило, но не всегда, наследуются доминантным образом. Для несбалансированных патологических состояний зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, можно применять для создания состояния ФКУ в модельной системе, которую затем можно использовать в мероприятиях по противодействию патологическому состоянию. Таким образом, зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, позволяет лечить генетические заболевания. В данном документе состояние ФКУ лечат путем частичного или полного излечения дефицита или дисбаланса, который вызывает заболевание или делает его более тяжелым.
А. Клетки-хозяева
[00479] Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, доставляет трансген белка PAH в рассматриваемую клетку-хозяина. Согласно некоторым вариантам реализации клетки представляют собой фоторецепторные клетки. Согласно некоторым вариантам реализации клетки представляют собой клетки RPE. Согласно некоторым вариантам реализации рассматриваемая клетка-хозяин представляет собой клетку-хозяина человека, включая, например, клетки крови, стволовые клетки, гемопоэтические клетки, CD34+ клетки, клетки печени, раковые клетки, сосудистые клетки, мышечные клетки, клетки поджелудочной железы, нервные клетки, клетки глаза или клетки сетчатки, эпителиальные или эндотелиальные клетки, дендритные клетки, фибробласты или любые другие клетки, происходящие от млекопитающего, включая, без ограничения, клетки печени (т. е. печеночные), клетки легких, сердечные клетки, клетки поджелудочной железы, клетки кишечника, диафрагмальные клетки, почечные клетки (т. е. почки), нервные клетки, клетки крови, клетки костного мозга или любой одной или более выбранных тканей субъекта, для которых предусмотрена генная терапия. В одном аспекте рассматриваемая клетка-хозяин представляет собой клетку-хозяина человека.
[00480] Настоящее раскрытие также относится к рекомбинантным клеткам-хозяевам, как упомянуто выше, включая зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе. Таким образом, можно использовать несколько клеток-хозяев в зависимости от цели, что очевидно для квалифицированного специалиста. Конструкцию или зкДНК-вектор для экспрессии белка PAH, раскрытые в данном документе, включая донорную последовательность, вводят в клетку-хозяина так, что донорная последовательность поддерживается в интегрированном в хромосому виде, как описано ранее. Термин «клетка-хозяин» включает любое потомство родительской клетки, которое не идентично родительской клетке из-за мутаций, происходящих во время репликации. Выбор клетки-хозяина будет в значительной степени зависеть от донорной последовательности и ее источника.
[00481] Клетка-хозяин также может представлять собой эукариота, например, клетку млекопитающего, насекомого, растения или гриба. Согласно одному варианту реализации клетка-хозяин представляет собой клетку человека (например, первичную клетку, стволовую клетку или иммортализованную линию клеток). Согласно некоторым вариантам реализации в клетку-хозяина можно вводить зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, ex vivo, а затем доставлять субъекту после события генной терапии. Клетка-хозяин может представлять собой любой тип клеток, например, соматическую клетку или стволовую клетку, индуцированную плюрипотентную стволовую клетку или клетку крови, например, Т-клетку или В-клетку, или клетку костного мозга. Согласно определенным вариантам реализации клетка-хозяин представляет собой аллогенную клетку. Например, конструирование Т-клеточного генома можно применять для разных видов иммунотерапии рака, модуляции заболевания, такой как терапия ВИЧ (например, нокаут рецептора, такого как CXCR4 и CCR5), и разных видов терапии иммунодефицита. Мишенями для иммунотерапии могут быть рецепторы ГКГС на B-клетках. Согласно некоторым вариантам реализации клетки-хозяева с модифицированным геномом, например, стволовые клетки костного мозга, например, CD34+ клетки, или индуцированные плюрипотентные стволовые клетки могут быть трансплантированы обратно пациенту для экспрессии терапевтического белка.
B. Дополнительные заболевания для генной терапии
[00482] В целом зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, можно применять для доставки любого белка PAH в соответствии с приведенным выше описанием для лечения, предотвращения или облегчения симптомов, ассоциированных с ФКУ, связанной с нарушенной экспрессией белка или экспрессией гена у субъекта.
[00483] Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, можно применять для доставки белка PAH в скелетную, сердечную или диафрагмальную мышцу, для продукции белка PAH для секреции и циркуляции в крови или для системной доставки в другие ткани для лечения, облегчения и/или предотвращения ФКУ.
[00484] ЗкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, можно вводить в легкие субъекта с помощью любых подходящих средств, необязательно путем введения аэрозольной суспензии пригодных для вдыхания частиц, содержащих зкДНК-векторы, которые субъект вдыхает. Пригодные для вдыхания частицы могут быть жидкими или твердыми. Аэрозоли жидких частиц, содержащих зкДНК-векторы, могут быть получены с помощью любых подходящих средств, таких как аэрозольный небулайзер под давлением или ультразвуковой небулайзер, как известно специалистам в данной области техники. См., например, патент США № 4501729. Аэрозоли твердых частиц, содержащих зкДНК-векторы, могут быть получены сходным образом с помощью любого генератора аэрозолей лекарственного средства в виде твердых частиц с помощью методик, известных в фармацевтике.
[00485] Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, можно вводить в ткани ЦНС (например, головной мозг, глаз).
[00486] Глазные нарушения, которые можно лечить, облегчать или предотвращать с помощью зкДНК-вектора для экспрессии белка PAH, раскрытого в данном документе, включают офтальмологические расстройства, затрагивающие сетчатку, задний тракт и зрительный нерв (например, пигментный ретинит, диабетическую ретинопатию и другие дегенеративные заболевания сетчатки, увеит, возрастную дегенерацию макулы, глаукому). Многие офтальмологические заболевания и нарушения ассоциированы с одним или более из трех типов показаний: (1) ангиогенезом, (2) воспалением и (3) дегенерацией. Согласно некоторым вариантам реализации зкДНК-вектор, раскрытый в данном документе, можно применять для доставки антиангиогенных факторов; противовоспалительных факторов; факторов, которые замедляют дегенерацию клеток, способствуют сохранению клеток или способствуют росту клеток, и комбинаций перечисленных выше. Диабетическая ретинопатия, например, характеризуется ангиогенезом. Диабетическую ретинопатию можно лечить путем доставки одного или более антиангиогенных антител или слитых белков интраокулярно (например, в стекловидное тело) или периокулярно (например, в субтеноновую область). Дополнительные глазные заболевания, которые можно лечить, облегчать или предотвращать с помощью зкДНК-векторов согласно настоящему изобретению, включают географическую атрофию, сосудистую или «влажную» дегенерацию макулы, ФКУ, врожденный амавроз Лебера (LCA), синдром Ушера, эластическую псевдоксантому (PXE), x-связанный пигментный ретинит (XLRP), x-связанное расслоение сетчатки (XLRS), хороидеремию, наследственную оптическую нейропатию Лебера (LHON), архоматопсию, палочко-колбочковую дистрофию, эндотелиальную дистрофию роговицы Фукса, диабетический макулярный отек и глазной рак или опухоли.
[00487] Согласно некоторым вариантам реализации воспалительные глазные заболевания или нарушения (например, увеит) можно лечить, облегчать или предупреждать с помощью зкДНК-вектора для экспрессии белка PAH, раскрытого в данном документе. Одно или более противовоспалительных антител или слитых белков могут быть экспрессированы путем внутриглазного (например, стекловидное тело или передняя камера) введения зкДНК-вектора, раскрытого в данном документе.
[00488] Согласно некоторым вариантам реализации зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, может кодировать белок PAH, который ассоциирован с трансгеном, кодирующим репортерный полипептид (например, фермент, такой как зеленый флуоресцентный белок или щелочная фосфатаза). Согласно некоторым вариантам реализации трансген, который кодирует репортерный белок, подходящий для экспериментальных или диагностических целей, выбирают из любого из: β-лактамазы, β-галактозидазы (LacZ), щелочной фосфатазы, тимидинкиназы, зеленого флуоресцентного белка (GFP), хлорамфениколацетилтрансферазы (CAT), люциферазы и других, хорошо известных в данной области техники. В некоторых аспектах зкДНК-векторы, экспрессирующие белок PAH, связанный с репортерным полипептидом, можно применять для диагностических целей, а также для определения эффективности или в качестве маркеров активности зкДНК-вектора у субъекта, которому их вводят.
C. Тестирование успешной экспрессии гена с использованием зкДНК-вектора
[00489] Для тестирования эффективности доставки гена белка PAH с помощью зкДНК-вектора можно использовать анализы, хорошо известные в данной области техники, которые можно выполнять как на моделях in vitro, так и на моделях in vivo. Уровни экспрессии белка PAH с помощью зкДНК могут быть оценены специалистом в данной области техники путем измерения уровней мРНК и белка PAH (например, ПЦР с обратной транскрипцией, анализ методом Вестерн-блоттинга и иммуноферментный анализ (ИФА)). Согласно одному варианту реализации зкДНК содержит репортерный белок, который можно использовать для оценки экспрессии белка PAH, например, путем исследования экспрессии репортерного белка с помощью флуоресцентной микроскопии или устройства для считывания люминесценции планшетов. В случае приложений in vivo для тестирования функциональности данного белка PAH можно использовать анализы функции белков, чтобы определить успешность экспрессии гена. Специалист сможет определить лучший тест для измерения функциональности белка PAH, экспрессируемого вектором зкДНК, in vitro или in vivo.
[00490] В данном документе предусмотрено, что эффекты экспрессии гена белка PAH с зкДНК-вектора в клетке или у субъекта могут длиться по меньшей мере 1 месяц, по меньшей мере 2 месяца, по меньшей мере 3 месяца, по меньшей мере четыре месяца, по меньшей мере 5 месяцев, по меньшей мере шесть месяцев, по меньшей мере 10 месяцев, по меньшей мере 12 месяцев, по меньшей мере 18 месяцев, по меньшей мере 2 года, по меньшей мере 5 лет, по меньшей мере 10 лет, по меньшей мере 20 лет или они могут быть постоянными.
[00491] Согласно некоторым вариантам реализации белок PAH в экспрессионной кассете, экспрессионной конструкции или зкДНК-векторе, описанных в данном документе, может быть оптимизирован по кодонам для клетки-хозяина. В данном документе термин «оптимизированный по кодонам» или «оптимизация кодонов» относится к процессу модификации последовательности нуклеиновой кислоты для усиления экспрессии в клетках позвоночного, представляющего интерес, например, мыши или человека (например, гуманизация), путем замены по меньшей мере одного или более чем одного или значительного числа кодонов нативной последовательности (например, прокариотической последовательности) кодонами, которые чаще или наиболее часто используются в генах этого позвоночного. Различные виды проявляют определенное предпочтение в отношении некоторых кодонов конкретной аминокислоты. Как правило, оптимизация кодонов не изменяет аминокислотную последовательность исходного транслированного белка. Оптимизированные кодоны могут быть определены с использованием, например, оптимизации кодонов Aptagen´s Gene Forge® и платформы для синтеза генов по заказу (Aptagen, Inc.) или другой общедоступной базы данных.
D. Определение эффективности путем оценки экспрессии белка PAH с зкДНК-вектора
[00492] По существу любой метод, известный в данной области техники для определения экспрессии белка, может быть использован для анализа экспрессии белка PAH с зкДНК-вектора. Неограничивающие примеры таких методов/анализов включают иммуноферментный анализ (ИФА), аффинный ИФА, ELISPOT, последовательное разведение, проточную цитометрию, анализ методом поверхностного плазмонного резонанса, анализ кинетического исключения, масс-спектрометрию, Вестерн-блоттинг, иммунопреципитацию и ПЦР.
[00493] Для оценки экспрессии белка PAH in vivo биологический образец может быть получен от субъекта для анализа. Примеры биологических образцов включают образец биожидкости, образец физиологической жидкости, кровь (включая цельную кровь), сыворотку, плазму, мочу, слюну, биопсию и/или образец ткани и т. д. Биологический образец или образец ткани также может относиться к образцу ткани или жидкости, выделенному у индивидуума, включая, но не ограничиваясь перечисленными, биопсию опухоли, стул, спинномозговую жидкость, плевральную жидкость, аспираты сосков, лимфатическую жидкость, внешние срезы кожи, дыхательного, кишечного и мочеполового путей, слезы, слюну, грудное молоко, клетки (включая, но не ограничиваясь перечисленными, клетки крови), опухоли, органы, а также образцы компонентов культуры клеток in vitro. Термин также включает смесь упомянутых выше образцов. Термин «образец» также включает необработанные или предварительно обработанные (или подвергнутые предварительному процессингу) биологические образцы. Согласно некоторым вариантам реализации образец, используемый для анализов и способов, описанных в данном документе, включает образец сыворотки, собранный у субъекта, подлежащего тестированию.
E. Определение эффективности экспрессированного белка PAH по клиническим параметрам
[00494] Эффективность конкретного белка PAH, экспрессированного зкДНК-вектором, для лечения ФКУ (т. е. функциональная экспрессия), может быть определена квалифицированным клиницистом. Однако лечение считается «эффективным лечением», в соответствии с использованием этого термина в данном документе, если любой или все признаки или симптомы ФКУ изменяются благоприятным образом, или если другие клинически принятые симптомы или маркеры заболевания улучшаются или облегчаются, например, по меньшей мере на 10% после лечения зкДНК-вектором, кодирующим терапевтический белок PAH, как описано в данном документе. Эффективность также может быть измерена по отсутствию у индивидуума ухудшения, которое оценивается по стабилизации ФКУ или по потребности в медицинских вмешательствах (т. е. прогрессирование заболевания прекращается или по меньшей мере замедляется). Способы измерения этих показателей известны специалистам в данной области техники и/или описаны в данном документе. Лечение включает любое лечение заболевания у индивидуума или животного (некоторые неограничивающие примеры включают человека или млекопитающее) и включает: (1) ингибирование ФКУ, например, прекращение или замедление прогрессирования ФКУ; или (2) облегчение ФКУ, например, вызывающее регресс симптомов ФКУ; и (3) предотвращение или снижение вероятности развития заболевания ФКУ, или предотвращение вторичных заболеваний/нарушений, ассоциированных с ФКУ. Эффективное количество для лечения заболевания означает такое количество, которое, при введении нуждающемуся в этом млекопитающему, является достаточным для обеспечения эффективного лечения, в соответствии с определением этого термина в данном документе, этого заболевания. Эффективность агента может быть определена путем оценки физических показателей, которые являются специфическими для заболевания ФКУ. Врач может оценить любой один или более из клинических симптомов ФКУ, которые включают: ** (i) снижение уровня фенилаланина (Phe) в сыворотке при соблюдении обычной диеты. Снижение уровня Phe является ключевым биомаркером при разработке способов лечения ФКУ; (ii) восстановление метаболического соотношения Phe и тирозина при соблюдении нормальной диеты. Этот путь отвечает за продуцирование нейротрансмиттеров; и/или (iii) оценку сниженных уровней Phe в сыворотке.
XI. Различные приложения зкДНК-векторов, экспрессирующих антитела или слитые белки
[00495] Как раскрыто в данном документе, композиции и зкДНК-векторы для экспрессии белка PAH, описанные в данном документе, можно применять для экспрессии белка PAH для ряда целей. Согласно одному варианту реализации зкДНК-вектор, экспрессирующий белок PAH, можно применять для создания соматической трансгенной модели на животных, несущей трансген, например, для исследования функции или прогрессирования заболевания ФКУ. Согласно некоторым вариантам реализации зкДНК-вектор, экспрессирующий белок PAH, можно применять для лечения, предотвращения или облегчения состояний или нарушений ФКУ у субъекта-млекопитающего.
[00496] Согласно некоторым вариантам реализации белок PAH может быть экспрессирован с зкДНК-вектора у субъекта в количестве, достаточном для лечения заболевания, ассоциированного с повышенной экспрессией, повышенной активностью продукта гена или нефизиологической положительной регуляцией гена.
[00497] Согласно некоторым вариантам реализации белок PAH может быть экспрессирован с зкДНК-вектора у субъекта в количестве, достаточном для лечения ФКУ со сниженной экспрессией, отсутствием экспрессии или дисфункцией белка.
[00498] Обычный специалист в данной области техники поймет, что трансген может не представлять собой открытую рамку считывания гена, который сам транскрибируется; вместо этого он может представлять собой промоторную область или репрессорную область гена-мишени, и зкДНК-вектор может модифицировать такую область, что в результате модулирует экспрессию гена PAH.
[00499] Композиции и зкДНК-векторы для экспрессии белка PAH, раскрытые в данном документе, можно применять для доставки белка PAH для различных целей, как описано выше.
[00500] Согласно некоторым вариантам реализации трансген кодирует один или более белков PAH, которые можно применять для лечения, облегчения или предотвращения состояний ФКУ у субъекта-млекопитающего. Белок PAH, экспрессируемый зкДНК-вектором, вводят пациенту в количестве, достаточном для лечения ФКУ, ассоциированной с аномальной последовательностью гена, что может привести к любому одному или более из следующего: повышенной экспрессии белка, сверхактивности белка, сниженной экспрессии, отсутствию экспрессии или дисфункции целевого гена или белка.
[00501] Согласно некоторым вариантам реализации зкДНК-векторы для экспрессии белка PAH, раскрытые в данном документе, предназначены для применения в методах диагностики и скрининга, посредством которых белок PAH временно или стабильно экспрессируется в системе на основе культуры клеток или, альтернативно, в модели на трансгенном животном.
[00502] Другой аспект технологии, описанной в данном документе, обеспечивает способ трансдукции популяции клеток млекопитающего зкДНК-вектором для экспрессии белка PAH, раскрытым в данном документе. В целом и в общем смысле, способ включает по меньшей мере этап введения в одну или более клеток популяции композиции, которая содержит эффективное количество одного или более из зкДНК-векторов для экспрессии белка PAH, раскрытых в данном документе.
[00503] Кроме того, согласно настоящему изобретению предложены композиции, а также терапевтические и/или диагностические наборы, которые включают один или более из раскрытых зкДНК-векторов для экспрессии белка PAH, как раскрыто в данном документе, или композиций зкДНК, изготовленных с одним или более дополнительными ингредиентами или приготовленных в соответствии с одной или более инструкциями по их применению.
[00504] Клетка, в которую должен быть введен зкДНК-вектор для экспрессии белка PAH, раскрытый в данном документе, может быть любого типа, включая, но не ограничиваясь перечисленными, нервные клетки (включая клетки периферической и центральной нервной системы, в частности, клетки головного мозга), клетки легких, клетки сетчатки, эпителиальные клетки (например, кишечные и респираторные эпителиальные клетки), мышечные клетки, дендритные клетки, клетки поджелудочной железы (включая островковые клетки), печеночные клетки, клетки миокарда, костные клетки (например, стволовые клетки костного мозга), гемопоэтические стволовые клетки, клетки селезенки, кератиноциты, фибробласты, эндотелиальные клетки, клетки простаты, половые клетки и т.п. В качестве альтернативы, клетка может представлять собой любую клетку-предшественника. В качестве дополнительной альтернативы, клетка может представлять собой стволовую клетку (например, нервную стволовую клетку, стволовую клетку печени). В качестве еще одной альтернативы, клетка может представлять собой раковую или опухолевую клетку. Более того, клетки могут быть любого видового происхождения, как указано выше.
А. Получение и очистка зкДНК-векторов, экспрессирующих PAH
[00505] ЗкДНК-векторы, раскрытые в данном документе, должны применяться для получения белка PAH как in vitro, так и in vivo. Белки PAH, полученные таким образом, могут быть выделены, протестированы в отношении целевой функции и очищены для дальнейшего использования в исследованиях или в качестве терапевтического лечения. Каждая система получения белка имеет свои преимущества/недостатки. В то время как белки, полученные in vitro, можно легко очистить и получить белки за короткое время, белки, полученные in vivo, могут иметь посттрансляционные модификации, такие как гликозилирование.
[00506] Терапевтический белок PAH, полученный с использованием зкДНК-векторов, может быть очищен с помощью любого метода, известного специалистам в данной области техники, например, ионообменной хроматографии, аффинной хроматографии, осаждения или электрофореза.
[00507] Терапевтический белок PAH, полученный с помощью способов и композиций, описанных в данном документе, может быть протестирован для оценки связывания с целевым белком-мишенью.
ПРИМЕРЫ
[00508] Примеры ниже представлены в качестве иллюстрации, а не ограничения. Обычные специалисты в данной области техники поймут, что зкДНК-векторы могут быть сконструированы из любых ITR дикого типа или модифицированных ITR, описанных в данном документе, и что примерные методы ниже могут быть использованы для конструирования и оценки активности таких зкДНК-векторов. Несмотря на то, что способы приведены в качестве примера для определенных зкДНК-векторов, они применимы к любому зкДНК-вектору в соответствии с описанием.
ПРИМЕР 1: Конструирование зкДНК-векторов с использованием метода на основе клеток насекомых
[00509] Получение зкДНК-векторов с использованием полинуклеотидной матрицы конструкции описано в Примере 1 заявки PCT/US18/49996, которая полностью включена в данный документ посредством ссылки. Например, полинуклеотидная матрица конструкции, используемая для получения зкДНК-векторов согласно настоящему изобретению, может представлять собой зкДНК-плазмиду, зкДНК-бакмиду и/или зкДНК-бакуловирус. Не ограничиваясь какой-либо теорией, в пермиссивной клетке-хозяине в присутствии, например, Rep, полинуклеотидная матрица конструкции, содержащая два симметричных ITR и экспрессионную конструкцию, где по меньшей мере один из ITR модифицирован относительно последовательности ITR дикого типа, реплицируется с получением зкДНК-векторов. Получение зкДНК-вектора проходит в два этапа: во-первых, вырезание («извлечение») матрицы из остова матрицы (например, генома зкДНК-плазмиды, зкДНК-бакмиды, зкДНК-бакуловируса и т.д.) с помощью белков Rep, и, во-вторых, Rep-опосредуемая репликация вырезанного зкДНК-вектора.
[00510] Примерный способ получения зкДНК-векторов представляет собой получение из зкДНК-плазмиды, как описано в данном документе. На ФИГ. 1А и 1В полинуклеотидная матрица конструкции каждой из зкДНК-плазмид включает как левый модифицированный ITR, так и правый модифицированный ITR, с расположенными между указанными ITR следующими элементами: (i) энхансер/промотор; (ii) сайт клонирования для трансгена; (iii) посттранскрипционный элемент ответа (например, посттранскрипционный регуляторный элемент вируса гепатита североамериканского сурка (WPRE)); и (iv) сигнал полиаденилирования (например, из гена бычьего гормона роста (BGHpA)). Уникальные сайты распознавания рестрикционной эндонуклеазой (R1-R6) (показанные на ФИГ. 1A и ФИГ. 1B) также были введены между каждым компонентом для облегчения введения новых генетических компонентов в конкретные сайты в конструкции. Сайты ферментов R3 (PmeI) GTTTAAAC (SEQ ID NO: 123) и R4 (PacI) TTAATTAA (SEQ ID NO: 124) конструировали в сайте клонирования для введения открытой рамки считывания трансгена. Эти последовательности клонировали в плазмиду pFastBac HT B, полученную от ThermoFisher Scientific.
[00511] Получение зкДНК-бакмид:
[00512] Компетентные клетки DH10Bac (MAX EFFICIENCY® DH10Bac™ Competent Cells, Thermo Fisher) трансформировали либо тестируемой, либо контрольной плазмидами, следуя протоколу в соответствии с инструкциями производителя. Чтобы получить рекомбинантные зкДНК-бакмиды, в клетках DH10Bac индуцировали рекомбинацию между плазмидой и бакуловирусным челночным вектором. Рекомбинантные бакмиды отбирали путем положительного скринингового отбора на основании скрининга по сине-белому окрашиванию E. coli (маркер Φ80dlacZΔM15 обеспечивает α-комплементацию гена β-галактозидазы из бакмидного вектора) на чашке с бактериальным агаром, содержащим X-gal и IPTG с антибиотиками для отбора трансформантов и поддержания бакмиды и плазмид на основе транспозаз. Белые колонии, образующиеся в результате транспозиции, которая разрушает индикаторный ген β-галактозиды, собирали и культивировали в 10 мл сред.
[00513] Рекомбинантные зкДНК-бакмиды выделяли из E.coli и трансфицировали ими клетки насекомых Sf9 или Sf21 с использованием FugeneHD для получения инфекционного бакуловируса. Адгезивные клетки насекомых Sf9 или Sf21 культивировали в 50 мл сред в колбах T25 при 25°С. Через 4 дня культуральную среду (содержащую вирус P0) отделяли от клеток, фильтровали через фильтр с размером пор 0,45 мкм, отделяя инфекционные бакуловирусные частицы от клеток или клеточного дебриса.
[00514] Необязательно первое поколение бакуловируса (P0) амплифицировали путем инфицирования наивных клеток насекомых Sf9 или Sf21 в 50-500 мл сред. Клетки поддерживали в суспензионных культурах в инкубаторе с орбитальным шейкером при 130 об./мин при 25°С, отслеживая диаметр и жизнеспособность клеток до тех пор, пока клетки не достигнут диаметра 18-19 нм (от диаметра наивных клеток, равного 14-15 нм) и плотности ~4,0×106 клеток/мл. Через 3-8 дней после инфицирования бакуловирусные частицы P1 в среде собирали после центрифугирования для удаления клеток и дебриса с последующей фильтрацией через фильтр с размером пор 0,45 мкм.
[00515] ЗкДНК-бакуловирус, содержащий тестируемые конструкции, собирали и определяли инфекционную активность или титр бакуловируса. В частности, четыре ×20 мл культур клеток Sf9 при 2,5×106 клеток/мл обрабатывали бакуловирусом P1 в следующих разведениях: 1/1000, 1/10000, 1/50000, 1/100000 и инкубировали при 25-27°C. Инфективность определяли ежедневно на протяжении 4-5 дней по показателю увеличения диаметра клеток и остановке клеточного цикла, а также изменению жизнеспособности клеток.
[00516] «Rep-плазмиду», раскрытую на ФИГ. 8A из PCT/US18/49996, которая полностью включена в данный документ посредством ссылки, получали в экспрессионном векторе pFASTBAC™-Dual (ThermoFisher), содержащем как Rep78 (SEQ ID NO: 131 или 133), так и Rep52 (SEQ ID NO: 132) или Rep68 (SEQ ID NO: 130) и Rep40 (SEQ ID NO: 129). Rep-плазмиду трансформировали в компетентные клетки DH10Bac (компетентные клетки MAX EFFICIENCY® DH10Bac™ (Thermo Fisher)), следуя предоставленному производителем протоколу. Для получения рекомбинантных бакмид («Rep-бакмид») в клетках DH10Bac индуцировали рекомбинацию между Rep-плазмидой и бакуловирусным челночным вектором. Рекомбинантные бакмиды отбирали путем положительного отбора, который включал скрининг по сине-белому окрашиванию E. coli (маркер Φ80dlacZΔM15 обеспечивает α-комплементацию гена β-галактозидазы из бакмидного вектора) на чашке с бактериальным агаром, содержащим X-gal и IPTG. Одиночные белые колонии собирали и инокулировали в 10 мл селективных сред (канамицин, гентамицин, тетрациклин в бульоне LB). Рекомбинантные бакмиды (Rep-бакмиды) выделяли из E.coli, и трансфицировали клетки насекомых Sf9 или Sf21 указанными Rep-бакмидами, чтобы получить инфекционный бакуловирус.
[00517] Клетки насекомых Sf9 или Sf21 культивировали в 50 мл сред в течение 4 дней и выделяли из культуры инфекционный рекомбинантный бакуловирус («Rep-бакуловирус»). Необязательно Rep-бакуловирус первого поколения (P0) амплифицировали путем инфицирования наивных клеток насекомых Sf9 или Sf21 и культивировали в 50-500 мл сред. Через 3-8 дней после инфицирования бакуловирусные частицы P1 в среде собирали, отделяя клетки путем центрифугирования или фильтрации, или используя другой способ фракционирования. Собирали Rep-бакуловирус и определяли инфекционную активность бакуловируса. В частности, четыре ×20 мл культур клеток Sf9 при 2,5×106 клеток/мл обрабатывали бакуловирусом P1 в следующих разведениях, 1/1000, 1/10000, 1/50000, 1/100000, и инкубировали. Инфективность определяли ежедневно на протяжении 4-5 дней по показателю увеличения диаметра клеток и остановке клеточного цикла, а также изменению жизнеспособности клеток.
[00518] Получение и характеристика зкДНК-вектора
[00519] На ФИГ. 4B среду для культивирования клеток насекомых Sf9, содержащую (1) образец, содержащий зкДНК-бакмиду или зкДНК-бакуловирус, и (2) Rep-бакуловирус, описанный выше, затем добавляли к свежей культуре клеток Sf9 (2,5×106 клеток/мл, 20 мл) при соотношении 1:1000 и 1:10000, соответственно. Затем клетки культивировали при 130 об./мин при 25°С. Через 4-5 дней после коинфицирования детектировали диаметр и жизнеспособность клеток. Когда диаметр клеток достигал 18-20 нм при жизнеспособности ~70-80%, клеточные культуры центрифугировали, среду удаляли и собирали клеточные осадки. Клеточные осадки сначала ресуспендировали в достаточном объеме водной среды, либо воды, либо буфера. ЗкДНК-вектор выделяли и очищали из клеток с использованием протокола очистки Qiagen MIDI PLUS™ (Qiagen, 0,2 мг массы осадка клеток, обработанной на колонку).
[00520] Значения выхода зкДНК-векторов, полученных и очищенных из клеток насекомых Sf9, первоначально определяли на основании поглощения в УФ-диапазоне при 260 нм.
[00521] ДНК-векторы можно идентифицировать с помощью электрофореза в агарозном геле в нативных или денатурирующих условиях, как проиллюстрировано на ФИГ. 4D, где (а) наличие характерных полос, мигрирующих при двукратно большем размере на денатурирующих гелях, по сравнению с нативными гелями, после расщепления рестрикционной эндонуклеазой и анализа методом гель-электрофореза, и (b) наличие полос мономера и димера (2x) на денатурирующих гелях для нерасщепленного материала характеризует наличие зкДНК-вектора.
[00522] Структуры выделенных зкДНК-векторов анализировали далее путем расщепления ДНК, полученной из коинфицированных клеток Sf9 (как описано в данном документе), рестрикционными эндонуклеазами, выбранными на основании a) присутствия только одного сайта разрезания в зкДНК-векторах, и b) получения фрагментов достаточно большого размера, чтобы они были отчетливо видны при фракционировании на 0,8% денатурирующем агарозном геле (>800 п.о.). Как проиллюстрировано на ФИГ. 4D и 4E, линейные ДНК-векторы с прерывистой структурой и зкДНК-вектор с линейной и непрерывной структурой можно различить по размеру их продуктов реакции - например, ожидается, что ДНК-вектор с прерывистой структурой даст фрагменты размером 1 тыс. п. о. и 2 тыс. п. о., в то время как бескапсидный вектор с непрерывной структурой, как ожидается, даст фрагменты размером 2 тыс. п. о. и 4 тыс. п. о.
[00523] Таким образом, чтобы качественно продемонстрировать, что выделенные зкДНК-векторы имеют ковалентно замкнутые концы, как требует их определение, образцы расщепляли рестрикционной эндонуклеазой, идентифицированной на основании конкретной последовательности ДНК-вектора как эндонуклеаза с одним сайтом рестрикции, что предпочтительно приводит к получению двух продуктов расщепления неравного размера (например, 1000 п. о. и 2000 п. о.). После расщепления и электрофореза на денатурирующем геле (который разделяет две комплементарные цепи ДНК), линейная, не замкнутая ковалентно ДНК будет разделяться на фрагменты размером 1000 п.о. и 2000 п.о., в то время как ковалентно замкнутая ДНК (т. е. зкДНК-вектор) будет разделяться на фрагменты в 2 раза большего размера (2000 п.о. и 4000 п.о.), так как две цепи ДНК связаны, уже развернуты и имеют вдвое большую длину (но одноцепочечные). Кроме того, при расщеплении мономерных, димерных и n-мерных форм ДНК-векторов все они будут разделяться на фрагменты одинаковых размеров из-за связанных между собой концов мультимерных ДНК-векторов (см. ФИГ. 4D).
[00524] В данном документе выражение «анализ для идентификации ДНК-векторов с помощью электрофореза на агарозном геле на нативном геле и в денатурирующих условиях» относится к анализу для оценки наличия замкнутых концов зкДНК путем выполнения расщепления рестрикционной эндонуклеазой с последующей электрофоретической оценкой продуктов расщепления. Ниже приведен один такой примерный анализ, хотя обычный специалист в данной области техники поймет, что возможны многие известные в данной области техники вариации этого примера. Рестрикционную эндонуклеазу выбирают таким образом, чтобы это был фермент, выполняющий один разрез представляющего интерес зкДНК-вектора с образованием продуктов, длина которых составляет приблизительно 1/3× и 2/3× от длины ДНК-вектора. Это обеспечивает разделение полос как на нативном, так и на денатурирующем гелях. Перед денатурацией важно удалить буфер из образца. Набор для очистки продуктов ПЦР от Qiagen или «центрифужные колонки» для обессоливания, например, колонки GE HEALTHCARE ILUSTRA™ MICROSPIN™ G-25, представляют собой некоторые из известных в данной области техники средств для расщепления эндонуклеазами. Анализ включает, например, i) расщепление ДНК соответствующей рестрикционной эндонуклеазой (ами), 2) внесение, например, в набор для очистки продуктов ПЦР от Qiagen, элюирование дистиллированной водой, iii) добавление 10-кратного денатурирующего раствора (10x = 0,5 M NaOH, 10 мМ ЭДТА), добавление 10-кратного красителя, не забуференного, и проведение анализа с использованием маркеров молекулярной массы ДНК, приготовленных путем добавления 10-кратного денатурирующего раствора к 4-кратному, на 0,8-1,0% геле, предварительно инкубированном с 1 мМ ЭДТА и 200 мМ NaOH, чтобы обеспечить одинаковую концентрацию NaOH в геле и в боксе для геля, и анализ геля в присутствии 1x денатурирующего раствора (50 мМ NaOH, 1 мМ ЭДТА). Обычный специалист в данной области техники поймет, какое напряжение использовать для проведения электрофореза на основании размера и желаемого времени получения результатов. После электрофореза гели дренируют, нейтрализуют в 1x TBE или TAE и переносят в дистиллированную воду или 1x TBE/TAE с 1x SYBR Gold. Затем полосы могут быть визуализированы, например, с использованием красителя SYBR® Gold Nucleic Acid Gel Stain от Thermo Fisher (10000-кратный концентрат в ДМСО) и эпифлуоресцентного света (синего) или УФ (312 нм).
[00525] Чистоту полученного зкДНК-вектора можно оценить с помощью любого метода, известного в данной области техники. В качестве одного примерного и неограничивающего метода, вклад зкДНК-плазмиды в общее поглощение в УФ-диапазоне образца можно оценить путем сравнения интенсивности флуоресценции зкДНК-вектора со стандартом. Например, если на основании поглощения в УФ-диапазоне определено, что на гель загружено 4 мкг зкДНК-вектора, а интенсивность флуоресценции зкДНК-вектора эквивалентна полосе 2 тыс. п. о. при известной массе 1 мкг, значит, масса зкДНК-вектора равна 1 мкг, и зкДНК-вектор составляет 25% от общего количества поглощающего УФ материала. Затем строят график зависимости интенсивности полосы на геле от вычисленного введенного количества, которому соответствует полоса - например, если общее количество зкДНК-вектора соответствует 8 тыс. п. о., а вырезанная сравнительная полоса соответствует 2 тыс. п. о., то интенсивность указанной полосы на графике будет соответствовать 25% от общего введенного количества, что в данном случае составит 0,25 мкг при введении 1,0 мкг. Используя титрование плазмиды зкДНК-вектора для построения стандартной кривой, затем рассчитывают количество для полосы зкДНК-вектора, используя уравнение линии регрессии, которое затем можно использовать для определения процента от общего введенного количества, представленного зкДНК-вектором, или процента чистоты.
[00526] Для сравнительных целей в Примере 1 описано получение зкДНК-векторов с использованием метода на основе клеток насекомых и полинуклеотидной матрицы конструкции, а также описано в Примере 1 из PCT/US18/49996, которая полностью включена в данный документ посредством ссылки. Например, полинуклеотидная матрица конструкции, используемая для получения зкДНК-векторов согласно настоящему изобретению в соответствии с Примером 1, может представлять собой зкДНК-плазмиду, зкДНК-бакмиду и/или зкДНК-бакуловирус. Не ограничиваясь какой-либо теорией, в пермиссивной клетке-хозяине в присутствии, например, Rep, полинуклеотидная матрица конструкции, содержащая два симметричных ITR и экспрессионную конструкцию, где по меньшей мере один из ITR модифицирован относительно последовательности ITR дикого типа, реплицируется с получением зкДНК-векторов. Получение зкДНК-вектора проходит в два этапа: во-первых, вырезание («извлечение») матрицы из остова матрицы (например, генома зкДНК-плазмиды, зкДНК-бакмиды, зкДНК-бакуловируса и т.д.) с помощью белков Rep, и, во-вторых, Rep-опосредуемая репликация вырезанного зкДНК-вектора.
[00527] Примерный способ получения зкДНК-векторов в способе с использованием клетки насекомого представляет собой получение из зкДНК-плазмиды, как описано в данном документе. На ФИГ. 1А и 1В полинуклеотидная матрица конструкции каждой из зкДНК-плазмид включает как левый модифицированный ITR, так и правый модифицированный ITR, с расположенными между указанными ITR следующими элементами: (i) энхансер/промотор; (ii) сайт клонирования для трансгена; (iii) посттранскрипционный элемент ответа (например, посттранскрипционный регуляторный элемент вируса гепатита североамериканского сурка (WPRE)); и (iv) сигнал полиаденилирования (например, из гена бычьего гормона роста (BGHpA)). Уникальные сайты распознавания рестрикционной эндонуклеазой (R1-R6) (показанные на ФИГ. 1A и ФИГ. 1B) также были введены между каждым компонентом для облегчения введения новых генетических компонентов в конкретные сайты в конструкции. Сайты ферментов R3 (PmeI) GTTTAAAC (SEQ ID NO: 123) и R4 (PacI) TTAATTAA (SEQ ID NO: 124) конструировали в сайте клонирования для введения открытой рамки считывания трансгена. Эти последовательности клонировали в плазмиду pFastBac HT B, полученную от ThermoFisher Scientific.
ПРИМЕР 2: Синтетическое получение зкДНК путем вырезания из двухцепочечной молекулы ДНК
[00528] Синтетическое получение зкДНК-векторов описано в Примерах 2-6 международной заявки PCT/US19/14122, поданной 18 января 2019 г., которая полностью включена в данный документ посредством ссылки. Один примерный способ получения зкДНК-вектора с применением синтетического способа включает вырезание двухцепочечной молекулы ДНК. В общих чертах, зкДНК-вектор может быть получен с применением конструкции двухцепочечной ДНК, например, см. ФИГ. 7A-8E из PCT/US19/14122. Согласно некоторым вариантам реализации конструкция двухцепочечной ДНК представляет собой зкДНК-плазмиду, например, см. ФИГ. 6 в международной заявке на патент PCT/US2018/064242, поданной 6 декабря 2018 г.
[00529] Согласно некоторым вариантам реализации конструкция для получения зкДНК-вектора содержит регуляторный переключатель, описанный в данном документе.
[00530] В иллюстративных целях в Примере 2 описано получение зкДНК-векторов в качестве примерных ДНК-векторов с замкнутыми концами, полученных с использованием этого метода. Однако, хотя в этом Примере зкДНК-векторы приведены в качестве примеров для иллюстрации синтетических способов получения in vitro для получения ДНК-вектора с замкнутыми концами путем вырезания двухцепочечного полинуклеотида, содержащего ITR и экспрессионную кассету (например, гетерологичную последовательность нуклеиновой кислоты), с последующим лигированием свободных 3´ и 5´ концов, как описано в данном документе, обычному специалисту в данной области техники известно, что, как проиллюстрировано выше, полинуклеотидную молекулу двухцепочечной ДНК можно модифицировать так, чтобы получить любой целевой ДНК-вектор с замкнутыми концами, включая, но не ограничиваясь этим, doggybone ДНК, гантелеобразную ДНК и т.п. Примерные зкДНК-векторы для получения антител или слитых белков, которые могут быть получены с помощью синтетического метода получения, описанного в Примере 2, обсуждаются в разделах, озаглавленных «III зкДНК-векторы в целом». Примерные антитела и слитые белки, экспрессируемые зкДНК-векторами, описаны в разделе, озаглавленном «IIC Примерные антитела и слитые белки, экспрессируемые зкДНК-векторами».
[00531] Способ включает (i) вырезание последовательности, кодирующей экспрессионную кассету, из конструкции двухцепочечной ДНК, и (ii) образование шпилечных структур на одном или более ITR, и (iii) соединение свободных 5'- и 3'-концов путем лигирования, например, с помощью ДНК-лигазы Т4.
[00532] Конструкция двухцепочечной ДНК содержит, в порядке от 5' к 3': первый сайт рестрикционной эндонуклеазы; левый ITR; экспрессионную кассету; правый ITR; и второй сайт рестрикционной эндонуклеазы. Конструкцию двухцепочечной ДНК затем приводят в контакт с одной или более рестрикционными эндонуклеазами для образования двухцепочечных разрывов в обоих сайтах рестрикционных эндонуклеаз. Одна эндонуклеаза может нацелено действовать на оба сайта, или каждый сайт может быть мишенью разной эндонуклеазы, при условии, что сайты рестрикции не присутствуют в матрице зкДНК-вектора. Это позволяет вырезать последовательность между сайтами рестрикционной эндонуклеазы из остальной части конструкции двухцепочечной ДНК (см. Фиг. 9 PCT/US19/14122). После лигирования образуется ДНК-вектор с замкнутыми концами.
[00533] Один или оба ITR, используемые в способе, могут представлять собой ITR дикого типа. Также могут быть использованы модифицированные ITR, причем указанная модификация может включать делецию, вставку или замену одного или более нуклеотидов из ITR дикого типа в последовательностях, образующих плечо B и B' и/или плечо C и C' (см., например, Фиг. 6-8 и 10 ФИГ. 11B из PCT/US19/14122), и может иметь две или более шпилечных петель (см., например, ФИГ. 6-8, ФИГ. 11B из PCT/US19/14122) или одну шпилечную петлю (см., например, ФИГ. 10A-10B, ФИГ. 11B из PCT/US19/14122). ITR, модифицированный шпилечной петлей, может быть получен путем генетической модификации существующего олиго или путем биологического и/или химического синтеза de novo.
[00534] В неограничивающем примере ITR-6 слева и справа (SEQ ID NO: 111 и 112) включают 40 делеций нуклеотидов в плечах B-B' и C-C' из ITR дикого типа ААВ2. Прогнозируется, что нуклеотиды, оставшиеся в модифицированном ITR, образуют одну шпилечную структуру. Свободная энергия Гиббса разворачивания структуры составляет примерно -54,4 ккал/моль. В ITR также могут быть внесены другие модификации, включая необязательную делецию функционального сайта связывания Rep или сайта Trs.
ПРИМЕР 3: получение зкДНК за счет конструирования олигонуклеотидов
[00535] Другой примерный способ получения зкДНК-вектора с использованием синтетического способа, который включает сборку различных олигонуклеотидов, представлен в Примере 3 из PCT/US19/14122, полностью включенной в данный документ посредством ссылки, в котором зкДНК-вектор получают путем синтеза 5'-олигонуклеотида и 3'-олигонуклеотида ITR и лигирования указанных олигонуклеотидов ITR в двухцепочечный полинуклеотид, содержащий экспрессионную кассету. На ФИГ. 11B из PCT/US19/14122 представлен примерный способ лигирования 5'-олигонуклеотида ITR и 3'-олигонуклеотида ITR в двухцепочечный полинуклеотид, содержащий экспрессионную кассету.
[00536] Как раскрыто в данном документе, олигонуклеотиды ITR могут содержать WT-ITR (например, см. ФИГ. 3A, ФИГ. 3C) или модифицированные ITR (например, см. ФИГ. 3B и ФИГ. 3D). (См. также, например, ФИГ. 6A, 6B, 7A и 7B из PCT/US19/14122, которая полностью включена в данный документ). Примерные олигонуклеотиды ITR включают, но не ограничиваются перечисленными, SEQ ID NO: 134-145 (например, см. Таблицу 7 в PCT/US19/14122). Модифицированные ITR могут включать делецию, вставку или замену одного или более нуклеотидов из ITR дикого типа в последовательностях, образующих плечо B и B' и/или плечо C и C'. Олигонуклеотиды ITR, содержащие WT-ITR или mod-ITR, описанные в данном документе, для использования в бесклеточном синтезе могут быть получены путем генетической модификации или биологического и/или химического синтеза. Как обсуждается в данном документе, олигонуклеотиды ITR в Примерах 2 и 3 могут содержать WT-ITR или модифицированные ITR (mod-ITR) в симметричных или асимметричных конфигурациях, как обсуждается в данном документе.
ПРИМЕР 4: получение зкДНК за счет одноцепочечной молекулы ДНК
[00537] В другом примерном способе получения зкДНК-вектора с использованием синтетического способа, представленном в Примере 4 из PCT/US19/14122, полностью включенной в данный документ посредством ссылки, используют одноцепочечную линейную ДНК, содержащую два смысловых ITR, которые фланкируют смысловую последовательность экспрессионной кассеты и ковалентно присоединены к двум антисмысловым ITR, которые фланкируют антисмысловую последовательность экспрессионной кассеты, а концы указанной одноцепочечной линейной ДНК затем лигируют с образованием одноцепочечной молекулы с замкнутыми концами. Один неограничивающий пример включает синтез и/или продуцирование молекулы одноцепочечной ДНК, ренатурацию частей указанной молекулы с образованием одной линейной молекулы ДНК, которая содержит одну или более областей вторичной структуры со спаренными основаниями, с последующим лигированием свободных 5'- и 3'-концов между собой с образованием замкнутой одноцепочечной молекулы.
[00538] Примерная одноцепочечная молекула ДНК для получения зкДНК-вектора содержит, от 5' к 3': смысловой первый ITR; смысловую последовательность экспрессионной кассеты; смысловой второй ITR; антисмысловой второй ITR; антисмысловую последовательность экспрессионной кассеты; и антисмысловой первый ITR.
[00539] Молекула одноцепочечной ДНК для использования в примерном способе Примера 4 может быть образована с помощью любой методологии синтеза ДНК, описанной в данном документе, например, путем синтеза ДНК in vitro, или обеспечена путем расщепления конструкции ДНК (например, плазмиды) нуклеазами и плавления полученных фрагментов дцДНК для получения фрагментов оцДНК.
[00540] Ренатурацию можно осуществлять путем понижения температуры ниже расчетных температур плавления пар смысловой и антисмысловой последовательностей. Температура плавления зависит от содержания конкретных нуклеотидных оснований и характеристик используемого раствора, например, от концентрации соли. Температуры плавления для любой конкретной последовательности и комбинации растворов легко рассчитываются обычным специалистом в данной области техники.
[00541] Свободные 5' и 3' концы ренатурированной молекулы могут быть лигированы друг с другом или лигированы со шпилечной молекулой с образованием зкДНК-вектора. Подходящие примерные методологии лигирования и шпилечные молекулы описаны в Примерах 2 и 3.
ПРИМЕР 5: Очистка и/или подтверждение получения зкДНК
[00542] Любой из продуктов ДНК-вектора, полученных с помощью способов, описанных в данном документе, например, включая способы получения на основе клеток насекомых, описанные в Примере 1, или синтетические способы получения, описанные в Примерах 2-4, может быть очищен, например, для удаления примесей, неиспользованных компонентов или побочных продуктов с использованием методов, обычно известных квалифицированному специалисту; и/или может быть проанализирован для подтверждения того, что полученный ДНК-вектор (в данном случае зкДНК-вектор) представляет собой целевую молекулу. Примерным методом очистки ДНК-вектора, например, зкДНК, является использование протокола очистки Qiagen Midi Plus (Qiagen) и/или очистки на геле.
[00543] Ниже приведен примерный метод подтверждения идентичности зкДНК-векторов.
[00544] ДНК-векторы можно идентифицировать с помощью электрофореза в агарозном геле в нативных или денатурирующих условиях, как проиллюстрировано на ФИГ. 4D, где (а) наличие характерных полос, мигрирующих при двукратно большем размере на денатурирующих гелях, по сравнению с нативными гелями, после расщепления рестрикционной эндонуклеазой и анализа методом гель-электрофореза, и (b) наличие полос мономера и димера (2x) на денатурирующих гелях для нерасщепленного материала характеризует наличие зкДНК-вектора.
[00545] Структуры выделенных зкДНК-векторов были дополнительно проанализированы путем расщепления очищенной ДНК рестрикционными эндонуклеазами, выбранными на основании a) присутствия только одного сайта разрезания в зкДНК-векторах, и b) получения фрагментов достаточно большого размера, чтобы они были отчетливо видны при фракционировании на 0,8% денатурирующем агарозном геле (>800 п.о.). Как проиллюстрировано на ФИГ. 4C и 4D, линейные ДНК-векторы с прерывистой структурой и зкДНК-вектор с линейной и непрерывной структурой можно различить по размеру их продуктов реакции - например, ожидается, что ДНК-вектор с прерывистой структурой даст фрагменты размером 1 тыс. п. о. и 2 тыс. п. о., в то время как зкДНК-вектор с непрерывной структурой, как ожидается, даст фрагменты размером 2 тыс. п. о. и 4 тыс. п. о.
[00546] Таким образом, чтобы качественно продемонстрировать, что выделенные зкДНК-векторы имеют ковалентно замкнутые концы, как требует их определение, образцы расщепляли рестрикционной эндонуклеазой, идентифицированной на основании конкретной последовательности ДНК-вектора как эндонуклеаза с одним сайтом рестрикции, что предпочтительно приводит к получению двух продуктов расщепления неравного размера (например, 1000 п. о. и 2000 п. о.). После расщепления и электрофореза на денатурирующем геле (который разделяет две комплементарные цепи ДНК), линейная, не замкнутая ковалентно ДНК будет разделяться на фрагменты размером 1000 п.о. и 2000 п.о., в то время как ковалентно замкнутая ДНК (т. е. зкДНК-вектор) будет разделяться на фрагменты в 2 раза большего размера (2000 п.о. и 4000 п.о.), так как две цепи ДНК связаны, уже развернуты и имеют вдвое большую длину (но одноцепочечные). Кроме того, при расщеплении мономерных, димерных и n-мерных форм ДНК-векторов все они будут разделяться на фрагменты одинаковых размеров из-за связанных между собой концов мультимерных ДНК-векторов (см. ФИГ. 4E).
[00547] В данном документе выражение «анализ для идентификации ДНК-векторов с помощью электрофореза на агарозном геле на нативном геле и в денатурирующих условиях» относится к анализу для оценки наличия замкнутых концов зкДНК путем выполнения расщепления рестрикционной эндонуклеазой с последующей электрофоретической оценкой продуктов расщепления. Ниже приведен один такой примерный анализ, хотя обычный специалист в данной области техники поймет, что возможны многие известные в данной области техники вариации этого примера. Рестрикционную эндонуклеазу выбирают таким образом, чтобы это был фермент, выполняющий один разрез представляющего интерес зкДНК-вектора с образованием продуктов, длина которых составляет приблизительно 1/3× и 2/3× от длины ДНК-вектора. Это обеспечивает разделение полос как на нативном, так и на денатурирующем гелях. Перед денатурацией важно удалить буфер из образца. Набор для очистки продуктов ПЦР от Qiagen или «центрифужные колонки» для обессоливания, например, колонки GE HEALTHCARE ILUSTRA™ MICROSPIN™ G-25, представляют собой некоторые из известных в данной области техники средств для расщепления эндонуклеазами. Анализ включает, например, i) расщепление ДНК соответствующей рестрикционной эндонуклеазой (ами), 2) внесение, например, в набор для очистки продуктов ПЦР от Qiagen, элюирование дистиллированной водой, iii) добавление 10-кратного денатурирующего раствора (10x = 0,5 M NaOH, 10 мМ ЭДТА), добавление 10-кратного красителя, не забуференного, и проведение анализа с использованием маркеров молекулярной массы ДНК, приготовленных путем добавления 10-кратного денатурирующего раствора к 4-кратному, на 0,8-1,0% геле, предварительно инкубированном с 1 мМ ЭДТА и 200 мМ NaOH, чтобы обеспечить одинаковую концентрацию NaOH в геле и в боксе для геля, и анализ геля в присутствии 1x денатурирующего раствора (50 мМ NaOH, 1 мМ ЭДТА). Обычный специалист в данной области техники поймет, какое напряжение использовать для проведения электрофореза на основании размера и желаемого времени получения результатов. После электрофореза гели дренируют, нейтрализуют в 1x TBE или TAE и переносят в дистиллированную воду или 1x TBE/TAE с 1x SYBR Gold. Затем полосы могут быть визуализированы, например, с использованием красителя SYBR® Gold Nucleic Acid Gel Stain от Thermo Fisher (10000-кратный концентрат в ДМСО) и эпифлуоресцентного света (синего) или УФ (312 нм). Вышеупомянутый метод на основе геля может быть адаптирован для целей очистки путем выделения зкДНК-вектора из полосы геля и обеспечения его ренатурации.
[00548] Чистоту полученного зкДНК-вектора можно оценить с помощью любого метода, известного в данной области техники. В качестве одного примерного и неограничивающего метода, вклад зкДНК-плазмиды в общее поглощение в УФ-диапазоне образца можно оценить путем сравнения интенсивности флуоресценции зкДНК-вектора со стандартом. Например, если на основании поглощения в УФ-диапазоне определено, что на гель загружено 4 мкг зкДНК-вектора, а интенсивность флуоресценции зкДНК-вектора эквивалентна полосе 2 тыс. п. о. при известной массе 1 мкг, значит, масса зкДНК-вектора равна 1 мкг, и зкДНК-вектор составляет 25% от общего количества поглощающего УФ материала. Затем строят график зависимости интенсивности полосы на геле от вычисленного введенного количества, которому соответствует полоса - например, если общее количество зкДНК-вектора соответствует 8 тыс. п. о., а вырезанная сравнительная полоса соответствует 2 тыс. п. о., то интенсивность указанной полосы на графике будет соответствовать 25% от общего введенного количества, что в данном случае составит 0,25 мкг при введении 1,0 мкг. Используя титрование плазмиды зкДНК-вектора для построения стандартной кривой, затем рассчитывают количество для полосы зкДНК-вектора, используя уравнение линии регрессии, которое затем можно использовать для определения процента от общего введенного количества, представленного зкДНК-вектором, или процента чистоты.
ПРИМЕР 6: Контролируемая экспрессия трансгена с зкДНК: экспрессия трансгена с зкДНК-вектора in vivo может поддерживаться и/или повышаться путем повторного введения дозы.
[00549] ЗкДНК-вектор получали в соответствии со способами, описанными в Примере 1 выше, с использованием зкДНК-плазмиды, содержащей промотор CAG (SEQ ID NO: 72) и трансген люциферазы (SEQ ID NO: 56), в качестве примерного PAH, фланкированный асимметричными ITR (например, 5'-WT-ITR (SEQ ID NO: 2) и 3' mod-ITR (SEQ ID NO: 3)), и оценивали в различных программах лечения in vivo. Этот зкДНК-вектор использовали во всех последующих экспериментах, описанных в Примерах 6-10. В Примере 6 зкДНК-вектор очищали, изготавливали в виде состава с липидной наночастицей (ЛНЧ-зкДНК) и вводили путем инъекции в хвостовую вену каждой мыши CD-1® IGS. Липосомы изготавливали с использованием подходящей смеси липидов, содержащей четыре компонента для образования липосом на основе липидных наночастиц (ЛНЧ), включая катионные липиды, вспомогательные липиды, холестерин и ПЭГ-липиды.
[00550] Для оценки устойчивой экспрессии трансгена in vivo с зкДНК-вектора на протяжении длительного периода времени ЛНЧ-зкДНК вводили в стерильном ФСБ путем внутривенной инъекции в хвостовую вену мышам CD-1® IGS в возрасте приблизительно 5-7 недель. Была проведена оценка трех групп с разными дозировками: 0,1 мг/кг, 0,5 мг/кг и 1,0 мг/кг, по десять мышей на группу (за исключением группы 1,0 мг/кг, в которой было 15 мышей на группу). Инъекции вводили в день 0. Пять мышей из каждой группы получали инъекцию дополнительной идентичной дозы в день 28. Экспрессию люциферазы измеряли путем визуализации IVIS после внутривенного введения мышам CD-1® IGS (Charles River Laboratories; мыши дикого типа (WT)). Экспрессию люциферазы оценивали с помощью визуализации IVIS после введения путем внутрибрюшинной инъекции 150 мг/кг субстрата люциферина в дни 3, 4, 7, 14, 21, 28, 31, 35 и 42 и регулярно (например, еженедельно, два раза в неделю или через каждые 10 суток, или через каждые 2 недели) в период между днями 42-110. Экспрессия трансгена люциферазы, в качестве примерного PAH, измеренная с помощью визуализации IVIS в течение по меньшей мере 132 дней после 3 разных протоколов введения (данные не показаны).
[00551] Расширенное исследование выполняли для изучения эффекта повторной дозы, например, повторного введения ЛНЧ-зкДНК, экспрессирующей люциферазу, субъектам, получавшим ЛНЧ-зкДНК. В частности, оценивали возможность повышения уровней экспрессии путем одного или более дополнительных введений зкДНК-вектора.
[00552] В этом исследовании биораспределение экспрессии люциферазы с зкДНК-вектора оценивали с помощью IVIS у мышей CD-1® IGS после первоначального внутривенного введения 1,0 мг/кг (т. е. праймирующей дозы) в дни 0 и 28 (Группа A). Второе введение зкДНК-вектора осуществляли путем инъекции в хвостовую вену 3 мг/кг (Группа B) или 10 мг/кг (Группа C) в 1,2 мл в хвостовую вену в день 84. В этом исследовании использовали по пять (5) мышей CD-1® в каждой из Групп A, B и C. Визуализацию IVIS экспрессии люциферазы у мышей выполняли перед введением дополнительных доз в дни 49, 56, 63 и 70, как описано выше, а также после введения повторных доз в день 84 и в дни 91, 98, 105, 112 и 132. Экспрессию люциферазы оценивали и детектировали во всех трех Группах A, B и C по меньшей мере до дня 110 (самый продолжительный оцененный период).
[00553] Было показано, что уровень экспрессии люциферазы повышается с помощью повторной дозы (т. е. повторного введения композиции зкДНК) ЛНЧ-зкДНК-Luc, согласно определению путем оценки активности люциферазы в присутствии люциферина. Экспрессия трансгена люциферазы, в качестве примерного PAH, измеренная с помощью визуализации IVIS в течение по меньшей мере 110 дней после 3 разных протоколов введения (Группы A, B и C). У мышей, не получавших никакой дополнительной повторной дозы (праймирующая доза 1 мг/кг (т. е. Группа А)), наблюдали стабильную экспрессию люциферазы на протяжении всего исследования. Мыши в группе B, которым вводили повторную дозу 3 мг/кг зкДНК-вектора, демонстрировали приблизительно семикратное увеличение наблюдаемой светимости по сравнению с мышами в Группе C. Неожиданно, мыши, получившие повторную дозу 10 мг/кг зкДНК-вектора, продемонстрировали 17-кратное увеличение наблюдаемой светимости люциферазы по сравнению с мышами, не получавшими какой-либо повторной дозы (Группа А).
[00554] Группа A мышей CD-1® IGS демонстрирует экспрессию люциферазы после внутривенного введения 1 мг/кг зкДНК-вектора в хвостовую вену в дни 0 и 28. Группы B и C мышей CD-1® IGS демонстрируют экспрессию люциферазы после введения 1 мг/кг зкДНК-вектора в первый момент времени (день 0) и введения повторной дозы зкДНК-вектора во второй момент времени в день 84. Второе введение (т. е. повторная доза) зкДНК-вектора повысило экспрессию по меньшей мере в 7 раз, и даже до 17 раз.
[00555] 3-кратное увеличение дозы (т. е. количества) зкДНК-вектора при повторном введении дозы в Группе В (т. е. при повторном введении дозы 3 мг/кг) привело к 7-кратному увеличению экспрессии люциферазы. Также неожиданно 10-кратное увеличение количества зкДНК-вектора при повторном введении дозы (т. е. при повторном введении дозы 10 мг/кг) в Группе С привело к 17-кратному увеличению экспрессии люциферазы. Таким образом, второе введение (т. е. повторная доза) зкДНК повысило экспрессию по меньшей мере в 7 раз, и даже до 17 раз. Это показывает, что повышение экспрессии трансгена в результате повторной дозы больше, чем ожидалось, и зависит от дозы или количества зкДНК-вектора при введении повторной дозы и, по-видимому, является синергическим по отношению к начальной экспрессии трансгена после первоначального праймирующего введения в день 0. Таким образом, дозозависимое повышение экспрессии трансгена не является аддитивным, скорее, уровень экспрессии трансгена является дозозависимым и сверхпропорционален суммарному количеству зкДНК-вектора, введенному в каждый момент времени.
[00556] Обе группы B и C показали значительное дозозависимое повышение экспрессии люциферазы по сравнению с контрольными мышами (Группа A), которые не получали повторной дозы зкДНК-вектора во второй момент времени. В совокупности эти данные показывают, что экспрессия трансгена с зкДНК-вектора может быть повышена дозозависимым образом с помощью повторной дозы (т. е. повторного введения) зкДНК-вектора по меньшей мере во второй момент времени.
[00557] В совокупности эти данные демонстрируют, что уровень экспрессии трансгена, например, PAH, с зкДНК-векторов может поддерживаться на устойчивом уровне на протяжении по меньшей мере 84 дней и может быть повышен in vivo после повторной дозы зкДНК-вектора, введенной по меньшей мере во второй момент времени.
ПРИМЕР 7: Устойчивая экспрессия трансгена in vivo зкДНК-векторами, изготовленными в виде составов с ЛНЧ
[00558] Воспроизводимость результатов, полученных в Примере 6, с другой липидной наночастицей оценивали in vivo на мышах. В день 0 мышам вводили дозу либо зкДНК-вектора, содержащего трансген люциферазы, управляемый промотором CAG, который был инкапсулирован в ЛНЧ, отличную от использованной в Примере 6, либо тех же ЛНЧ, содержащих поли(C), но без зкДНК или гена люциферазы. В частности, самцам мышей CD-1® в возрасте приблизительно 4 недель вводили однократную инъекцию 0,5 мг/кг ЛНЧ-TTX-люциферазы или контрольных ЛНЧ-поли(C), вводимых внутривенно через латеральную хвостовую вену в день 0. В день 14 животным вводили системно люциферин в дозе 150 мг/кг путем внутрибрюшинной инъекции при 2,5 мл/кг. Приблизительно через 15 минут после введения люциферина каждое животное визуализировали с использованием системы визуализации in vivo («IVIS»).
[00559] Как показано на ФИГ. 7, значительная флуоресценция в печени наблюдалась у всех четырех мышей, получивших зкДНК, при этом за исключением места инъекции у животных наблюдалась очень незначительная флуоресценция, это указывает на то, что ЛНЧ опосредовали специфичную для печени доставку конструкции зкДНК, и что доставленный зкДНК-вектор был способен к контролируемой устойчивой экспрессии своего трансгена в течение по меньшей мере двух недель после введения.
ПРИМЕР 8: Устойчивая экспрессия трансгена в печени in vivo после введения зкДНК-вектора
[00560] В отдельном эксперименте оценивали локализацию зкДНК, доставленной с помощью ЛНЧ, в печени экспериментальных животных. ЗкДНК-вектор, содержащий представляющий интерес функциональный трансген, инкапсулировали в те же ЛНЧ, что и использованные в Примере 7, и вводили мышам in vivo при уровне дозы 0,5 мг/кг путем внутривенной инъекции. Через 6 часов мышей умерщвляли и отбирали образцы печени, фиксировали формалином и заливали парафином с использованием стандартных протоколов. Анализы методом гибридизации in situ RNAscope® выполняли для визуализации зкДНК-векторов в ткани с использованием зонда, специфичного для трансгена зкДНК, и детектирования с использованием хромогенной реакции и окрашивания гематоксилином (Advanced Cell Diagnostics). ФИГ. 8 показывает результаты, которые указывают на наличие зкДНК в гепатоцитах.
ПРИМЕР 9: Устойчивая экспрессия трансгена зкДНК в глазах in vivo
[00561] Устойчивость экспрессии трансгена зкДНК-вектора в тканях, отличных от печени, оценивали для определения переносимости и экспрессии зкДНК-вектора после введения в глаза in vivo. Несмотря на то, что люциферазу использовали в качестве примерного трансгена в Примере 9, обычный специалист может легко заменить трансген люциферазы последовательностью PAH из любой из последовательностей, перечисленных в Таблице 5.
[00562] В день 0 самцам крыс Sprague Dawley в возрасте приблизительно 9 недель вводили путем субретинальной инъекции 5 мкл либо зкДНК-вектора, содержащего трансген люциферазы, в виде состава с реагентом для трансфекции jetPEI® (Polyplus), либо плазмидной ДНК, кодирующей люциферазу, в виде состава с jetPEI®, в обоих случаях в концентрации 0,25 мкг/мкл. В каждой группе тестировали по четыре крысы. Животным давали седативное средство и вводили исследуемый препарат в правый глаз путем субретинальной инъекции с помощью иглы калибра 33. Левый глаз каждого животного оставляли интактным. Сразу после инъекции глаза проверяли методом оптической когерентной томографии или визуализации глазного дна, чтобы подтвердить наличие субретинального пузырька. Крысы получали бупренорфин и местную мазь с антибиотиком в соответствии со стандартными процедурами.
[00563] В дни 7, 14, 21, 28 и 35 животным в обеих группах вводили системно свежеприготовленный люциферин в дозе 150 мг/кг путем внутрибрюшинной инъекции при 2,5 мл/кг. Через 5-15 минут после введения люциферина всех животных визуализировали с использованием IVIS под анестезией изофлураном. Полный поток [фотон/с] и средний поток (фотон/с/ср/см2) в представляющей интерес области, включающей глаз, получали при экспозиции 5 минут. Результаты представлены графически в виде средней светимости в обработанном глазу («инъецированный») для каждой группы лечения относительно средней светимости в необработанном глазу («неинъецированный») для каждой группы лечения (ФИГ. 9B). Значительная флуоресценция легко детектировалась в глазах, в которые был введен зкДНК-вектор, но была намного слабее в глазах, в которые была введена плазмида (ФИГ. 9A). Через 35 дней крыс, которым инъецировали плазмиду, умерщвляли, продолжая исследование для крыс, получивших зкДНК, с инъекцией люциферина и визуализацией IVIS в дни 42, 49, 56, 63, 70 и 99. Результаты демонстрируют, что зкДНК-вектор, введенный в глаз крысы путем однократной инъекции, опосредует экспрессию трансгена in vivo и что такая экспрессия поддерживалась на высоком уровне на протяжении по меньшей мере 99 дней после инъекции.
ПРИМЕР 10: Длительное введение доз и введение повторных доз зкДНК-вектора у мышей Rag2.
[00564] В ситуациях, когда один или более трансгенов, кодируемых в экспрессионной генной кассете зкДНК-вектора, экспрессируются в среде хозяина (например, в клетке или в организме субъекта), где экспрессированный белок распознается как чужеродный, существует вероятность того, что у хозяина выработается адаптивный иммунный ответ, который может привести к нежелательному истощению продукта экспрессии, которое может быть ошибочно принято за отсутствие экспрессии. В некоторых случаях это может происходить с репортерной молекулой, которая является гетерологичной для нормальной среды хозяина. Соответственно, экспрессию трансгена зкДНК-вектора оценивали in vivo в модели на мышах Rag2, в которой отсутствуют B- и T-клетки и, следовательно, не вырабатывается адаптивный иммунный ответ на ненативные для мышей белки, такие как люцифераза. В общих чертах, в день 0 мышам линий c57bl/6 и Rag2 с подавленными генами вводили путем внутривенной инъекции в хвостовую вену 0,5 мг/кг инкапсулированного в ЛНЧ зкДНК-вектора, экспрессирующего люциферазу, или контроля поли(C), а в день 21 некоторым мышам вводили повторную дозу того же самого ЛНЧ-инкапсулированного зкДНК-вектора при том же уровне дозы. Все тестируемые группы состояли из 4 мышей в каждой. Визуализацию IVIS выполняли после инъекции люциферина, как описано в Примере 9, с недельными интервалами.
[00565] При сравнении полного потока, наблюдаемого в анализах IVIS, флуоресценция, наблюдаемая у мышей дикого типа (косвенная мера присутствия экспрессированной люциферазы), которым вводили ЛНЧ-зкДНК-вектор-Luc, постепенно снижалась после дня 21, в то время как мыши Rag2, которым вводили тот же самый препарат, проявили относительно постоянную устойчивую экспрессию люциферазы на протяжении 42 дней эксперимента (ФИГ. 9A). Снижение у мышей дикого типа, наблюдаемое приблизительно в день 21, соответствует временному интервалу, в котором можно ожидать появления адаптивного иммунного ответа. Повторное введение ЛНЧ с зкДНК-вектором мышам Rag2 приводило к заметному увеличению экспрессии, которая была устойчивой в течение по меньшей мере 21 дня, на протяжении которых проводили наблюдения в этом исследовании (ФИГ. 9B). Результаты позволяют предположить, что адаптивный иммунитет может играть определенную роль при экспрессии ненативного белка с зкДНК-вектора у хозяина, и что наблюдаемое снижение экспрессии в период времени 20+ дней с момента первоначального введения может указывать на мешающий адаптивный иммунный ответ на экспрессируемую молекулу, а не на снижение экспрессии (или в дополнение к ней). Следует отметить, что этот ответ, как ожидается, будет низким в случае экспрессии у хозяина нативных белков, когда, предположительно, хозяин будет правильно распознавать экспрессированные молекулы как собственные и не будет вырабатывать такой иммунный ответ.
ПРИМЕР 11: Влияние специфической для печени экспрессии и модуляции CpG на устойчивую экспрессию
[00566] Как описано в Примере 10, нежелательный иммунный ответ хозяина в некоторых случаях может искусственно ослаблять то, что иначе могло бы быть устойчивой экспрессией одного или более целевых трансгенов с введенного зкДНК-вектора. Использовали два подхода, чтобы оценить влияние избегания и/или ослабления потенциального иммунного ответа хозяина на устойчивую экспрессию с зкДНК-вектора. Во-первых, поскольку вектор зкДНК-Luc, использованный в предшествующих примерах, находился под контролем конститутивного промотора CAG, была получена сходная конструкция с использованием специфического для печени промотора (hAAT) или другого конститутивного промотора (hEF-1), чтобы определить, будет ли избегание длительного воздействия миелоидных клеток или тканей, не относящихся к печени, снижать любые наблюдаемые иммунные эффекты. Во-вторых, некоторые конструкции зкДНК-люцифераза конструировали так, чтобы иметь пониженное содержание CpG, известного триггера иммунной реакции хозяина. Измеряли экспрессию гена люциферазы, кодируемой зкДНК, при введении мышам таких модифицированных зкДНК-векторов с замененным промотором.
[00567] Использовали три разных зкДНК-вектора, каждый из которых кодировал люциферазу в качестве трансгена. Первый зкДНК-вектор имел большое количество неметилированного CpG (~350) и содержал конститутивный промотор CAG («зкДНК CAG»); второй имел умеренное количество неметилированного CpG (~60) и содержал специфический для печени промотор hAAT («зкДНК hAAT с низким содержанием CpG»); и третий представлял собой метилированную форму второго, не содержащую неметилированного CpG, и также содержал промотор hAAT («зкДНК hAAT без CpG»). В остальном зкДНК-векторы были идентичны. Векторы готовили, как описано выше.
[00568] Четыре группы по четыре самца мышей CD-1®, в возрасте приблизительно 4 недель, получали один из зкДНК-векторов, инкапсулированных в ЛНЧ, или контроль поли(C). В день 0 каждой мыши вводили путем однократной внутривенной инъекции в хвостовую вену 0,5 мг/кг зкДНК-вектора в объеме 5 мл/кг. Значения массы тела регистрировали в дни -1, -, 1, 2, 3, 7 и еженедельно после этого, до умерщвления мышей. Образцы цельной крови и сыворотки брали в дни 0, 1 и 35. Прижизненную визуализацию проводили в дни 7, 14, 21, 28 и 35, и затем еженедельно с использованием системы визуализации in vivo (IVIS). Для визуализации каждой мыши вводили люциферин при 150 мг/кг путем внутрибрюшинной инъекции при 2,5 мл/кг. Через 15 минут каждую мышь анестезировали и визуализировали. Мышей умерщвляли в день 93 и собирали терминальные ткани, включая печень и селезенку. Измерения цитокинов проводили через 6 часов после введения дозы в день 0.
[00569] Несмотря на то, что у всех получивших зкДНК мышей наблюдали значительную флуоресценцию в дни 7 и 14, у мышей, получивших зкДНК CAG, флуоресценция быстро снижалась после дня 14 и более постепенно уменьшалась на протяжении оставшейся части исследования. Напротив, у мышей, получивших зкДНК hAAT с низким содержанием CpG и без CpG, полный поток оставался на стабильно высоком уровне (Фиг. 10). Это позволяет предположить, что направление доставки зкДНК-вектора специфически в печень приводило к устойчивой и длительной экспрессии трансгена с вектора в течение по меньшей мере 77 дней после однократной инъекции. Конструкции с минимизированным содержанием CpG или с полным отсутствием CpG имели сходные профили длительной устойчивой экспрессии, в то время как конструкция с конститутивным промотором и высоким содержанием CpG проявила снижение экспрессии с течением времени, это позволяет предположить, что иммунная активация хозяина при введении зкДНК-вектора может играть определенную роль в любом снижении экспрессии, наблюдаемом при введении такого вектора субъекту. Эти результаты обеспечивают альтернативные методы адаптации продолжительности ответа к желаемому уровню путем выбора ограниченного конкретной тканью промотора и/или изменения содержания CpG в зкДНК-векторе в том случае, если наблюдается иммунный ответ хозяина - потенциально, специфичный в отношении трансгена ответ.
ПРИМЕР 12: Гидродинамическая доставка зкДНК, экспрессирующей PAH
[00570] Гидродинамическая инъекция в хвостовую вену является хорошо известным методом введения нуклеиновой кислоты в печень у грызунов. В этой системе инъекция под давлением большого объема неинкапсулированной нуклеиновой кислоты приводит к кратковременному увеличению проницаемости клеток и доставке непосредственно в ткани и клетки. Это обеспечивает экспериментальный механизм обхода многих иммунных систем хозяина, таких как привлечение макрофагов, что обеспечивает возможность наблюдать доставку и экспрессию в отсутствие такой активности.
[00571] Два разных зкДНК-вектора, каждый с левым ITR дикого типа и усеченным мутантным правым ITR и имеющие трансгенную область, кодирующую PAH человека, получали и очищали, как описано выше в Примерах 1 и 5. Каждый зкДНК-вектор PAH находился под контролем разного специфического для печени промотора. В анализ также был включен контрольный ЛНЧ-инкапсулированный поли(C). Каждый из зкДНК-векторов PAH (по отдельности, без какой-либо инкапсуляции ЛНЧ) и контроль вводили подобранным по возрасту мышам обоего пола PAHenu2 в возрасте приблизительно 4-6 недель. Незащищенные зкДНК-векторы вводили при 5 мкг на животное (6 животных на группу) с помощью гидродинамической внутривенной инъекции через латеральную хвостовую вену в объеме <100 мг/мл. Массу тела измеряли в дни -1, 0, 1, 2, 3, 7 и 14. Образцы крови собирали у каждого обработанного животного в дни -1, 3, 7 и 14. Количество фенилаланина в образцах сыворотки обработанных животных измеряли с помощью высокопроизводительной масс-спектрометрии и выражали как процент от уровней, наблюдаемых у обработанных контролем животных.
[00572] Как показано на ФИГ. 11, уровни фенилаланина в этой модели на мутантных мышах оставались стабильно высокими в течение эксперимента у обработанных контролем животных. Введение любого из зкДНК-векторов снижало уровни фенилаланина у мышей приблизительно на 75% на протяжении эксперимента (ФИГ. 11). Этот эксперимент продемонстрировал, что зкДНК-векторы, введенные с помощью гидродинамической инъекции, экспрессировали активный PAH, который был способен системно снижать уровни фенилаланина в модели ФКУ на мышах.
ПРИМЕР 13: Фармакологическое исследование для оценки биохимической коррекции уровней фенилаланина путем экспрессии фермента PAH человека у мышей PAHenu2 с помощью гидродинамической инъекции
[00573] Доступная модель дефицита PAH на мышах, мышь PAHenu2, позволяет исследовать эффект экспрессии фермента PAH человека на уровень фенилаланина у мышей PAHenu2. Дефицит PAH ассоциирован с нарушением клиренса фенилаланина и, как следствие, с гиперфенилаланинемией.
[00574] ЗкДНК-векторы получали, как описано в Примере 12. Каждый из зкДНК-векторов PAH (по отдельности, без какой-либо инкапсуляции ЛНЧ) и контроль вводили подобранным по возрасту мышам обоего пола PAHenu2 в возрасте приблизительно 4-6 недель. Незащищенные зкДНК-векторы вводили при 5 мкг на животное (6 животных на группу) с помощью гидродинамической внутривенной инъекции через латеральную хвостовую вену в объеме <100 мг/мл. Массу тела измеряли в дни -1, 0, 1, 2, 3, 7 и 14. Образцы крови собирали у каждого обработанного животного в дни -1, 3, 7 и 14. Количество фенилаланина в образцах сыворотки обработанных животных измеряли с помощью высокопроизводительной масс-спектрометрии и выражали как процент от уровней, наблюдаемых у контрольных обработанных животных (PAHenu2).
[00575] Дизайн исследования показан ниже в Таблице 9 и Таблице 10.
Таблица 9
Таблица 10
№ = номер; в/в = внутривенно; ROA = путь введения; WT = дикий тип; KO = нокаут.
[00576] Исследуемые препараты поставлялись в виде концентрированного исходного раствора и хранились при номинальной температуре 4°C. Составы не перемешивали на вортексе и не центрифугировали. Группы размещали в прозрачных поликарбонатных клетках с контактной подстилкой на вентилируемой стойке в процедурной комнате. Корм и фильтрованную водопроводную воду, подкисленную 1 н. HCl до заданного pH 2,5-3,0, предоставляли животным ad libitum.
[00577] Кровь собирали в промежуточных и конечных временных точках, как показано в Таблицах 11A и 11B, соответственно.
Таблица 11A
День -3(~), 3, 7, 14, 21
День 28
День -3(~), 3, 7, 14, 21
День 28
[00578] аЦельную кровь собирали в пробирки для отделения сыворотки с активатором свертывания; MOV = максимальный доступный объем
[00579] Таблица 11B
Левая доля печени, хранившаяся в 10% NBF (EPL)
3х куска по ~25-50 мг
взвешенные и мгновенно замороженные по отдельности
(Lake Pharma)
Замороженные образцы, хранящиеся при номинальной температуре -70°C
(n = 2 для Pure Honey / n = 3 для Lake Pharma)
[00580] № = номер, NBF = нейтральный забуференный формалин
[00581] Сбор образцов крови выполняли, как описано ниже в Таблице 12.
Таблица 12
Цельная кровь
Назначение
(терминальный)
[00582] Детали исследования описаны далее:
[00583] Вид (количество, пол, возраст): Для групп 1-8: 36 + 2 запасные мыши PAHenu2 (обоего пола, возраст ~4-6 недель, подобранные по возрасту); 10 + 1 запасная мышь WT (однопометники; подобранные по возрасту). Для групп 1-7: 30 мышей PAHenu2 (обоего пола, возраст ~7-10 недель, подобранные по возрасту); 10 WT (однопометники; подобранные по возрасту).
[00584] Класс соединения: ДНК в липидных наночастицах.
[00585] Наблюдения за клеткой: Наблюдения за клеткой выполняли ежедневно.
[00586] Клинические наблюдения: Клинические наблюдения выполняли через ~1, ~6 и ~24 часа после введения дозы в День.
[00587] Масса тела: Массу тела всех животных регистрировали в Дни -4, 0, 1, 2, 3, 7, 14, 21, 28, в том числе до умерщвления.
[00588] Лекарственная форма: Исследуемые препараты поставляются в виде концентрированного исходного раствора. Исходный раствор разбавляют ФСБ непосредственно перед использованием. Полученные материалы хранят при температуре ~4°C (или на влажном льду), если дозирование не выполняется немедленно.
[00589] Введение дозы: Исследуемые материалы для Групп 1-8 и Групп 1-7 вводили в День 0 путем гидродинамического внутривенного (в/в) введения в установленном объеме на животное, 90-100 мл/кг (в зависимости от самого легкого животного в группе) через латеральную хвостовую вену (введение дозы в течение 5 секунд).
[00590] Голодание перед сбором крови и вскрытием: Все животные (все группы) голодали в течение минимум 4 часов до сбора крови в исходных условиях перед введением дозы в День 3 (~), а также в День 3, 7, 14, 21 и 28 (перед терминальным сбором крови).
[00591] Сбор крови: После каждого сбора животным подкожно вводили 0,5-1,0 мл раствора Рингера с лактатом. У животных собирали кровь в соответствии с приведенными выше таблицами сбора крови.
[00592] После 4-часового голодания в Дни -3 (~), 3, 7, 14 и 21 у животных брали цельную кровь для выделения сыворотки, которую собирали путем надрезания хвостовой вены, из подкожной вены или из глазничного синуса (при вдыхании изофлурана в соответствии с СОП учреждения). Будут сделаны две (2) аликвоты. Все образцы хранили при номинальной температуре -70°C до отправки.
[00593] Восстановление после анестезии: За животными непрерывно наблюдали, пока они находились под анестезией, во время восстановления и до восстановления подвижности.
[00594] Умерщвление и терминальный сбор крови: В День 28 после 4-часового голодания животных умерщвляли путем асфиксии в CO2 с последующей торакотомией и обескровливанием. Максимальный доступный объем крови собирали с помощью сердечной пункции и обрабатывали для получения сыворотки в соответствии с СОП учреждения и хранили в двух (2) аликвотах.
[00595] Перфузия: После обескровливания всех животных подвергали перфузии сердца физиологическим раствором. В общих чертах, внутрисердечную перфузию всего тела выполняли путем введения иглы калибра 23/21, прикрепленной к 10 мл шприцу, содержащему физиологический раствор, в просвет левого желудочка для перфузии. Правое предсердие было рассечено, чтобы обеспечить дренажный выход для перфузата. После того, как игла была помещена в сердце, к поршню прикладывали легкое и постоянное давление для перфузии животного. Адекватный поток промывочного раствора обеспечивали до тех пор, пока выходящий перфузат не станет прозрачным (без видимой крови), это указывает на то, что промывочный раствор насытил тело и процедура завершена.
[00596] Сбор ткани: Терминальные ткани собирали у агонирующих животных, которых умерщвляли до запланированной временной точки. При наличии возможности, собирали и сохраняли ткани животных, которые были найдены мертвыми.
[00597] После умерщвления и перфузии забирали печень. Из печени собирали два (2) среза по ~50 мг, но не взвешивали и мгновенно замораживали как можно скорее. Затем собирали и взвешивали три (3) среза по ~25-50 мг (≤50 мг). Срезы мгновенно замораживали по отдельности и хранили при номинальной температуре -70°C до отправки. Левую долю печени помещали в кассеты для гистологии, фиксировали в 10% NBF и охлаждали (~4°C). Ткань в 10% NBF хранили охлажденной (~4°C) до отправки в герметичном контейнере на пакетах со льдом.
[00598] Уровни фенилаланина (PHE): Образцы сыворотки анализировали с помощью Pure Honey для определения уровней PHE.
[00599] Уровни активности: Два (2) замороженных образца печени анализировали с помощью Pure Honey для определения уровней активности.
[00600] Результаты: Как показано на ФИГ. 12, уровни фенилаланина (% PHE относительно контроля) в этой модели на мутантных мышах оставались стабильно высокими в ходе эксперимента у обработанных контролем животных. Введение любого из зкДНК-векторов (Codop2 или Codop4) снижало уровни фенилаланина у мышей на протяжении эксперимента (ФИГ. 12). Эти результаты продемонстрировали, что зкДНК-векторы, вводимые с помощью гидродинамической инъекции, экспрессировали активный PAH, который был способен системно снижать уровни фенилаланина в модели ФКУ на мышах. ЗкДНК, содержащая промотор VD, связанный с оптимизированным по кодонам вариантом 2 PAH человека (Codop2), функционировала лучше всего из трех протестированных экспериментальных зкДНК-векторов. Этот результат, показывающий, что оптимизированный по кодонам вариант 2 PAH человека (Codop2) функционировал незначительно лучше, чем оптимизированный по кодонам вариант 4 PAH человека (Codop4), был неожиданным, по меньшей мере частично, поскольку вариант 4 был сконструирован с минимизацией CpG, что, как ожидается, обычно приводит к повышенной экспрессии трансгена, которая будет коррелировать со снижением уровней PHE в экспериментальной системе, описанной в данном документе. Однако было обнаружено, что Codop2 (без минимизации CpG) снижал уровни PHE больше, чем Codop4 (с минимизацией CpG).
[00601] ПРИМЕР 14: Фармакологическое исследование для оценки биохимической коррекции уровней фенилаланина путем экспрессии фермента PAH человека у мышей PAHenu2 на основании ответа на дозу, введенную путем в/в гидродинамической инъекции
[00602] ЗкДНК-векторы получали, как описано в Примере 12. Каждый из зкДНК-векторов PAH (по отдельности, без какой-либо инкапсуляции ЛНЧ) и контроль вводили подобранным по возрасту мышам обоего пола PAHenu2 в возрасте приблизительно 4-6 недель. Незащищенные зкДНК-векторы вводили при 0,5 мкг на животное, 5 мкг на животное или 50 мкг на животное (5 животных на группу) путем гидродинамической внутривенной инъекции через латеральную хвостовую вену в объеме <100 мг/мл. Массу тела измеряли в дни -1, 0, 1, 2, 3, 7 и 14. Образцы крови собирали у каждого обработанного животного в дни -1, 3, 7 и 14. Количество фенилаланина в образцах сыворотки обработанных животных измеряли с помощью высокопроизводительной масс-спектрометрии.
[00603] Дизайн исследования показан ниже в Таблице 13.
Таблица 13
[00604] Сбор крови проводили, как описано в Примере 13.
[00605] Детали исследования описаны далее:
[00606] Вид (количество, пол, возраст): 35 + 1 запасная мышь PAH´ (обоего пола, =возраст 6-9 недель, подобранные по возрасту); 10 + 2 запасные мыши WT (однопометники; подобранные по возрасту).
[00607] Класс соединения: ДНК в липидных наночастицах
[00608] Наблюдения за клеткой: Наблюдения за клеткой выполняли ежедневно.
[00609] Клинические наблюдения: Клинические наблюдения выполняли через -1, =6 и =24 часа после введения дозы исследуемого материала (День 0). Дополнительные наблюдения выполняли в виде исключения.
[00610] Масса тела: Массу тела всех животных регистрировали в Дни -4, 0, 1, 2, 3, 7, 14, 21, 28, в том числе до умерщвления.
[00611] Лекарственная форма: Исследуемые препараты поставлялись в виде концентрированного исходного раствора. Исходный раствор разбавляли тФСБ непосредственно перед использованием.
[00612] Введение дозы: Исследуемые материалы для групп 1-9 вводили в День 0 путем гидродинамического в/в введения в установленном объеме на животное, 90-100 мл/кг (в зависимости от самого легкого животного в группе) через латеральную хвостовую вену (введение дозы в течение 5 секунд).
[00613] Голодание перед сбором крови и вскрытием: Все животные (все группы) голодали в течение минимум 4 часов до сбора крови в исходных условиях перед введением дозы в День -4 (=), а также в День 3, 7, 14 и 21.
[00614] Сбор крови: После каждого сбора животным подкожно вводили 0,5-1,0 мл раствора Рингера с лактатом. У животных брали кровь в соответствии с таблицами сбора крови. В Дни -4 (--), 3, 7, 14 и 21 у животных собирали цельную кровь для получения сыворотки натощак (см. таблицу выше). Цельную кровь для получения сыворотки собирали путем надрезания хвостовой вены, из подкожной вены или из глазничного синуса (при вдыхании изофлурана в соответствии с СОП учреждения). Цельную кровь собирали в пробирки для отделения сыворотки с активатором свертывания. Была сделана одна (1) аликвота. До отправки все образцы хранили при номинальной температуре -70°C.
[00615] Восстановление после анестезии: За животными непрерывно наблюдали, пока они находились под анестезией, во время восстановления и до восстановления подвижности.
[00616] Умерщвление и терминальный сбор крови: В День 28 после 4-часового голодания животных умерщвляли путем асфиксии в CO2 с последующей торакотомией и обескровливанием. Максимальный доступный объем крови собирали с помощью сердечной пункции и обрабатывали для получения сыворотки в соответствии с СОП учреждения и хранили в двух (2) аликвотах.
[00617] Перфузия: После обескровливания всех животных подвергали перфузии сердца физиологическим раствором. В общих чертах, внутрисердечную перфузию всего тела выполняли путем введения иглы калибра 23/21, прикрепленной к 10 мл шприцу, содержащему физиологический раствор, в просвет левого желудочка для перфузии. Правое предсердие было рассечено, чтобы обеспечить дренажный выход для перфузата. После того, как игла была помещена в сердце, к поршню прикладывали легкое и постоянное давление для перфузии животного. Адекватный поток промывочного раствора обеспечивали до тех пор, пока выходящий перфузат не станет прозрачным (без видимой крови), это указывает на то, что промывочный раствор насытил тело и процедура завершена.
[00618] Сбор ткани: Терминальные ткани собирали у агонирующих животных, которых умерщвляли до запланированной временной точки. При наличии возможности, собирали и сохраняли ткани животных, которые были найдены мертвыми.
[00619] После умерщвления и перфузии забирали печень. Из печени собирали два (2) среза по ~50 мг, но не взвешивали и мгновенно замораживали как можно скорее. Затем собирали и взвешивали три (3) среза по ~25-50 мг (<50 мг). Срезы мгновенно замораживали по отдельности и хранили при номинальной температуре -70°C до отправки. Всю оставшуюся печень выбрасывали.
[00620] Уровни фенилаланина (PHE): Образцы сыворотки анализировали с помощью Pure Honey для определения уровней PHE.
[00621] Уровни активности: Два (2) замороженных образца печени анализировали с помощью Pure Honey для определения уровней активности.
[00622] Результаты: Как показано на ФИГ. 13, уровни фенилаланина в этой модели на мутантных мышах оставались стабильно высокими в ходе эксперимента у обработанных контролем животных. Введение зкДНК-вектора, содержащего VD-hPAH codop2, снижало уровни фенилаланина у мышей на протяжении эксперимента дозозависимым образом (ФИГ. 13). Этот эксперимент продемонстрировал, что зкДНК-векторы, введенные путем гидродинамической инъекции, экспрессировали активный PAH, который был способен системно дозозависимо снижать уровни фенилаланина в модели ФКУ на мышах.
ПРИМЕР 15: Фармакологическое исследование для оценки биохимической коррекции уровней фенилаланина путем экспрессии фермента PAH человека у мышей PAHenu2 с помощью гидродинамической инъекции - корреляция PHE с конструкции hPAH-codop2 с активностью фермента PAH
[00623] Следующее исследование проводили для определения эффекта экспрессии фермента PAH человека на уровень фенилаланина у мышей PAHenu2 и для корреляции экспрессии PAH человека с активностью фермента.
[00624] зкДНК-векторы получали, как описано в Примере 12. Каждый из зкДНК-векторов PAH (по отдельности, без какой-либо инкапсуляции ЛНЧ) и контроль вводили подобранным по возрасту мышам обоего пола PAHenu2 в возрасте приблизительно 4-6 недель. Незащищенные зкДНК-векторы вводили при 5 мкг на животное (6 животных на группу) с помощью гидродинамической внутривенной инъекции через латеральную хвостовую вену в объеме <100 мг/мл. Массу тела измеряли в дни -1, 0, 1, 2, 3, 7 и 14. Образцы крови собирали у каждого обработанного животного в дни -1, 3, 7 и 14. Количество фенилаланина в образцах сыворотки обработанных животных измеряли с помощью высокопроизводительной масс-спектрометрии и выражали как процент от уровней, наблюдаемых у обработанных контролем животных (PAHenu2).
[00625] Дизайн исследования показан ниже в Таблице 14.
Таблица 14
№ = номер; в/в = внутривенно; ROA = путь введения; WT = дикий тип; KO = нокаут.
[00626] Кровь собирали в промежуточных и конечных временных точках, как показано в Таблицах 15A и 15B, соответственно.
Таблица 15A
День -2, 3, 7, 14 и 21
Если применимо до умерщвления
[00627] Цельную кровь собирали в пробирки для отделения сыворотки с активатором свертывания; MOV = максимальный доступный объем
Таблица 15B
(Pure Honey)
2х куска по ~50 мг, не взвешенные и мгновенно замороженные по отдельности (Pure Honey)
4х куска по ~25-50 мг, взвешенные и мгновенно замороженные по отдельности (Lake Pharma)
Замороженные образцы, хранящиеся при номинальной температуре -70°C.
[00628] № = номер, NBF = нейтральный забуференный формалин
[00629] Детали исследования описаны далее:
[00630] Вид (количество, пол, возраст): 55 + 2 запасные мыши PAHenu2 (обоего пола, возраст ~5-8 недель, подобранные по возрасту); 5 + 1 запасная мышь WT (обоего пола, однопометники; подобранные по возрасту).
[00631] Класс соединения: ДНК в липидных наночастицах
[00632] Наблюдения за клеткой: Наблюдения за клеткой выполняли ежедневно.
[00633] Клинические наблюдения: Клинические наблюдения выполняли через ~1, ~6 и ~24 часа после введения дозы в День. Дополнительные наблюдения будут сделаны в качестве исключения.
[00634] Масса тела: Массу тела всех животных, если применимо, регистрировали в Дни -2, 0, 1, 2, 3, 7, 14, 21 и 28 (до умерщвления).
[00635] Лекарственная форма: Исследуемые препараты поставлялись в виде концентрированного исходного раствора. Исходный раствор разбавляли ФСБ, предоставленным Спонсором, непосредственно перед использованием.
[00636] Введение дозы: Исследуемые материалы для Групп 1-12 вводили в День 0 путем гидродинамического в/в введения в установленном объеме на животное, 90-100 мл/кг (в зависимости от самого легкого животного в группе) через латеральную хвостовую вену (введение дозы в течение 5 секунд).
[00637] Голодание перед сбором крови и вскрытием: Все животные (все группы) голодали в течение минимум 4 часов перед всеми сборами крови и вскрытием: Дни -2, 3, 7, 14, 21 и 28.
[00638] Сбор крови: После каждого сбора животным подкожно вводили 0,5-1,0 мл раствора Рингера с лактатом. В Дни -2, 3, 7, 14 и 21 у животных будет собрана цельная кровь для получения сыворотки натощак. Были сделаны две (2) аликвоты. До отправки все образцы хранили при номинальной температуре -70°C.
[00639] Восстановление после анестезии: За животными непрерывно наблюдали, пока они находились под анестезией, во время восстановления и до восстановления подвижности.
[00640] Умерщвление и терминальный сбор крови: В День 28 после 4-часового голодания животных умерщвляли путем асфиксии в CO2 с последующей торакотомией и обескровливанием. Максимальный доступный объем крови собирали с помощью сердечной пункции и обрабатывали для получения сыворотки в соответствии с СОП учреждения и хранили в двух (2) аликвотах.
[00641] Перфузия: После обескровливания всех животных подвергали перфузии сердца физиологическим раствором. В общих чертах, внутрисердечную перфузию всего тела выполняли путем введения иглы калибра 23/21, прикрепленной к 10 мл шприцу, содержащему физиологический раствор, в просвет левого желудочка для перфузии. Правое предсердие было рассечено, чтобы обеспечить дренажный выход для перфузата. После того, как игла была помещена в сердце, к поршню прикладывали легкое и постоянное давление для перфузии животного. Адекватный поток промывочного раствора обеспечивали до тех пор, пока выходящий перфузат не станет прозрачным (без видимой крови), это указывает на то, что промывочный раствор насытил тело и процедура завершена.
[00642] Сбор ткани: Терминальные ткани собирали у агонирующих животных, которых умерщвляли до запланированной временной точки. При наличии возможности, собирали и сохраняли ткани животных, которые были найдены мертвыми.
[00643] После умерщвления и перфузии печень собирали. Из печени собирали два (2) среза по ~50 мг, но не взвешивали и мгновенно замораживали как можно скорее. Затем собирали и взвешивали четыре (4) среза по ~25-50 мг (≤50 мг). Срезы мгновенно замораживали по отдельности и хранили при номинальной температуре -70°C до отправки.
[00644] Левую долю печени помещали в кассеты для гистологии, фиксировали в 10% NBF и охлаждали (~4°C). Ткань в 10% NBF хранили охлажденной (~4°C) до отправки в герметичном контейнере на пакетах со льдом.
[00645] Вся оставшаяся печень будет выброшена.
[00646] Уровни фенилаланина (PHE): Образцы сыворотки анализировали с помощью Pure Honey для определения уровней PHE.
[00647] Уровни активности: Два (2) замороженных образца печени анализировали с помощью Pure Honey для определения уровней активности.
[00648] Результаты: Как показано на ФИГ. 14A-14B, ко дню 3 введение зкДНК, содержащей оптимизированный по кодонам вариант 2 PAH человека («Codop2»), привело к снижению уровней PHE в сыворотке, это указывает на достаточную активность PAH для коррекции уровней фенилаланина в крови при ФКУ мышей уже на день 3.
Последовательности нуклеиновых кислот:
[00649] Последовательность нуклеиновой кислоты зкДНК, содержащей оптимизированный по кодонам вариант 2 PAH человека (зкДНК «hPAH Codop2»), показана ниже. Промотор подчеркнут (SEQ ID NO: 191), а открытая рамка считывания (ORF) оптимизированного по кодонам варианта 2 PAH показана двойным подчеркиванием (SEQ ID NO: 382).
[00650] AAAGTAGCCGAAGATGACGGTTTGTCACATGGAGTTGGCAGGATGTTTGATTAAAAACATAACAGGAAGAAAAATGCCCCGCTGTGGGCGGACAAAATAGTTGGGAACTGGGAGGGGTGGAAATGGAGTTTTTAAGGATTATTTAGGGAAGAGTGACAAAATAGATGGGAACTGGGTGTAGCGTCGTAAGCTAATACGAAAATTAAAAATGACAAAATAGTTTGGAACTAGATTTCACTTATCTGGTTCGGATCTCCTAGGCCTGCAGGCAGCTGCGCGCTCGCTCGCTCACTGAGGCCGCCCGGGCAAAGCCCGGGCGTCGGGCGACCTTTGGTCGCCCGGCCTCAGTGAGCGAGCGAGCGCGCAGAGAGGGAGTGGCCAACTCCATCACTAGGGGTTCCTTGTAGTTAATGATTAACCCGCCATGCTACTTATCGCGGCCGCCGGGGGAGGCTGCTGGTGAATATTAACCAAGGTCACCCCAGTTATCGGAGGAGCAAACAGGGGCTAAGTCCACACGCGTGGTACCGTCTGTCTGCACATTTCGTAGAGCGAGTGTTCCGATACTCTAATCTCCCTAGGCAAGGTTCATATTTGTGTAGGTTACTTATTCTCCTTTTGTTGACTAAGTCAATAATCAGAATCAGCAGGTTTGGAGTCAGCTTGGCAGGGATCAGCAGCCTGGGTTGGAAGGAGGGGGTATAAAAGCCCCTTCACCAGGAGAAGCCGTCACACAGATCCACAAGCTCCTGAAGAGGTAAGGGTTTAAGGGATGGTTGGTTGGTGGGGTATTAATGTTTAATTACCTGGAGCACCTGCCTGAAATCACTTTTTTTCAGGTTGGTTTAAACCGCAGCCACCATGAGCACCGCCGTGCTGGAAAATCCTGGCCTGGGCAGAAAGCTGAGCGACTTCGGCCAAGAGACAAGCTACATCGAGGACAACTGCAACCAGAACGGCGCCATCAGCCTGATCTTCAGCCTGAAAGAAGAAGTGGGCGCCCTGGCCAAGGTGCTGAGACTGTTCGAAGAGAACGACGTGAACCTGACACACATCGAGAGCAGACCCAGCAGACTGAAGAAGGACGAGTACGAGTTCTTCACCCACCTGGACAAGCGGAGCCTGCCTGCTCTGACCAACATCATCAAGATCCTGCGGCACGACATCGGCGCCACAGTGCACGAACTGAGCCGGGACAAGAAAAAGGACACCGTGCCATGGTTCCCCAGAACCATCCAAGAGCTGGACAGATTCGCCAACCAGATCCTGAGCTATGGCGCCGAGCTGGACGCTGATCACCCTGGCTTTAAGGACCCCGTGTACCGGGCCAGAAGAAAGCAGTTTGCCGATATCGCCTACAACTACCGGCACGGCCAGCCTATTCCTCGGGTCGAGTACATGGAAGAGGAAAAGAAAACCTGGGGCACCGTGTTCAAGACCCTGAAGTCCCTGTACAAGACCCACGCCTGCTACGAGTACAACCACATCTTCCCACTGCTCGAAAAGTACTGCGGCTTCCACGAGGACAATATCCCTCAGCTTGAGGACGTGTCCCAGTTCCTGCAGACCTGCACCGGCTTTAGACTGAGGCCAGTTGCCGGACTGCTGAGCAGCAGAGATTTTCTCGGCGGCCTGGCCTTCAGAGTGTTCCACTGTACCCAGTACATCAGACACGGCAGCAAGCCCATGTACACCCCTGAGCCTGATATCTGCCACGAGCTGCTGGGACATGTGCCCCTGTTCAGCGATAGAAGCTTCGCCCAGTTCAGCCAAGAGATCGGACTGGCTTCTCTGGGAGCCCCTGACGAGTACATTGAGAAGCTGGCCACCATCTACTGGTTCACCGTGGAATTCGGCCTGTGCAAGCAGGGCGACAGCATCAAAGCTTATGGCGCTGGCCTGCTGTCTAGCTTCGGCGAGCTGCAGTACTGTCTGAGCGAGAAGCCTAAGCTGCTGCCCCTGGAACTGGAAAAGACCGCCATCCAGAACTACACCGTGACCGAGTTCCAGCCTCTGTACTACGTGGCCGAGAGCTTCAACGACGCCAAAGAAAAAGTGCGGAACTTCGCCGCCACCATTCCTCGGCCTTTCAGCGTCAGATACGACCCCTACACACAGCGGATCGAGGTGCTGGACAACACACAGCAGCTGAAAATTCTGGCCGACTCCATCAACAGCGAGATCGGCATCCTGTGCAGCGCCCTGCAGAAAATCAAGTGATAGTTAATTAAGAGCATCTTACCGCCATTTATTCCCATATTTGTTCTGTTTTTCTTGATTTGGGTATACATTTAAATGTTAATAAAACAAAATGGTGGGGCAATCATTTACATTTTTAGGGATATGTAATTACTAGTTCAGGTGTATTGCCACAAGACAAACATGTTAAGAAACTTTCCCGTTATTTACGCTCTGTTCCTGTTAATCAACCTCTGGATTACAAAATTTGTGAAAGATTGACTGATATTCTTAACTATGTTGCTCCTTTTACGCTGTGTGGATATGCTGCTTTATAGCCTCTGTATCTAGCTATTGCTTCCCGTACGGCTTTCGTTTTCTCCTCCTTGTATAAATCCTGGTTGCTGTCTCTTTTAGAGGAGTTGTGGCCCGTTGTCCGTCAACGTGGCGTGGTGTGCTCTGTGTTTGCTGACGCAACCCCCACTGGCTGGGGCATTGCCACCACCTGTCAACTCCTTTCTGGGACTTTCGCTTTCCCCCTCCCGATCGCCACGGCAGAACTCATCGCCGCCTGCCTTGCCCGCTGCTGGACAGGGGCTAGGTTGCTGGGCACTGATAATTCCGTGGTGTTGTCTGTGCCTTCTAGTTGCCAGCCATCTGTTGTTTGCCCCTCCCCCGTGCCTTCCTTGACCCTGGAAGGTGCCACTCCCACTGTCCTTTCCTAATAAAATGAGGAAATTGCATCGCATTGTCTGAGTAGGTGTCATTCTATTCTGGGGGGTGGGGTGGGGCAGGACAGCAAGGGGGAGGATTGGGAAGACAATAGCAGGCATGCTGGGGATGCGGTGGGCTCTATGGCTCTAGAGCATGGCTACGTAGATAAGTAGCATGGCGGGTTAATCATTAACTACACCTGCAGGAGGAACCCCTAGTGATGGAGTTGGCCACTCCCTCTCTGCGCGCTCGCTCGCTCACTGAGGCCGGGCGACCAAAGGTCGCCCGACGCCCGGGCGGCCTCAGTGAGCGAGCGAGCGCGCAGCTGCCTGCAGGGGCGCGCCTCGAGCCATGGTGCTAGCAGCTGATGCATAGCATGCGGTACCGGGAGATGGGGGAGGCTAACTGAAACACGGAAGGAGACAATACCGGAAGGAACCCGCGCTATGACGGCAATAAAAAGACAGAATAAAACGCACGGGTGTTGGGTCGTTTGTTCATAAACGCGGGGTTCGGTCCCAGGGCTGGCACTCTGTCGATACCCCACCGAGACCCCATTGGGACCAATACGCCCGCGTTTCTTCCTTTTCCCCACCCCAACCCCCAAGTTCGGGTGAAGGCCCAGGGCTCGCAGCCAACGTCGGGGCGGCAAGCCCTGCCATAGCCACTACGGGTACGTAGGCCAACCACTAGAACTATAGCTAGAGTCCTGGGCGAACAAACGATGCTCGCCTTCCAGAAAACCGAGGATGCGAACCACTTCATCCGGGGTCAGCACCACCGGCAAGCGCCGCGACGGCCGAGGTCTACCGATCTCCTGAAGCCAGGGCAGATCCGTGCACAGCACCTTGCCGTAGAAGAACAGCAAGGCCGCCAATGCCTGACGATGCGTGGAGACCGAAACCTTGCGCTCGTTCGCCAGCCAGGACAGAAATGCCTCGACTTCGCTGCTGCCCAAGGTTGCCGGGTGACGCACACCGTGGAAACGGATGAAGGCACGAACCCAGTTGACATAAGCCTGTTCGGTTCGTAAACTGTAATGCAAGTAGCGTATGCGCTCACGCAACTGGTCCAGAACCTTGACCGAACGCAGCGGTGGTAACGGCGCAGTGGCGGTTTTCATGGCTTGTTATGACTGTTTTTTTGTACAGTCTATGCCTCGGGCATCCAAGCAGCAAGCGCGTTACGCCGTGGGTCGATGTTTGATGTTATGGAGCAGCAACGATGTTACGCAGCAGCAACGATGTTACGCAGCAGGGCAGTCGCCCTAAAACAAAGTTAGGTGGCTCAAGTATGGGCATCATTCGCACATGTAGGCTCGGCCCTGACCAAGTCAAATCCATGCGGGCTGCTCTTGATCTTTTCGGTCGTGAGTTCGGAGACGTAGCCACCTACTCCCAACATCAGCCGGACTCCGATTACCTCGGGAACTTGCTCCGTAGTAAGACATTCATCGCGCTTGCTGCCTTCGACCAAGAAGCGGTTGTTGGCGCTCTCGCGGCTTACGTTCTGCCCAGGTTTGAGCAGCCGCGTAGTGAGATCTATATCTATGATCTCGCAGTCTCCGGCGAGCACCGGAGGCAGGGCATTGCCACCGCGCTCATCAATCTCCTCAAGCATGAGGCCAACGCGCTTGGTGCTTATGTGATCTACGTGCAAGCAGATTACGGTGACGATCCCGCAGTGGCTCTCTATACAAAGTTGGGCATACGGGAAGAAGTGATGCACTTTGATATCGACCCAAGTACCGCCACCTAACAATTCGTTCAAGCCGAGATCGGCTTCCCGGCCGCGGAGTTGTTCGGTAAATTGTCACAACGCCGCGAATATAGTCTTTACCATGCCCTTGGCCACGCCCCTCTTTAATACGACGGGCAATTTGCACTTCAGAAAATGAAGAGTTTGCTTTAGCCATAACAAAAGTCCAGTATGCTTTTTCACAGCATAACTGGACTGATTTCAGTTTACAACTATTCTGTCTAGTTTAAGACTTTATTGTCATAGTTTAGATCTATTTTGTTCAGTTTAAGACTTTATTGTCCGCCCACACCCGCTTACGCAGGGCATCCATTTATTACTCAACCGTAACCGATTTTGCCAGGTTACGCGGCTGGTCTGCGGTGTGAAATACCGCACAGATGCGTAAGGAGAAAATACCGCATCAGGCGCTCTTCCGCTTCCTCGCTCACTGACTCGCTGCGCTCGGTCGTTCGGCTGCGGCGAGCGGTATCAGCTCACTCAAAGGCGGTAATACGGTTATCCACAGAATCAGGGGATAACGCAGGAAAGAACATGTGAGCAAAAGGCCAGCAAAAGGCCAGGAACCGTAAAAAGGCCGCGTTGCTGGCGTTTTTCCATAGGCTCCGCCCCCCTGACGAGCATCACAAAAATCGACGCTCAAGTCAGAGGTGGCGAAACCCGACAGGACTATAAAGATACCAGGCGTTTCCCCCTGGAAGCTCCCTCGTGCGCTCTCCTGTTCCGACCCTGCCGCTTACCGGATACCTGTCCGCCTTTCTCCCTTCGGGAAGCGTGGCGCTTTCTCAATGCTCACGCTGTAGGTATCTCAGTTCGGTGTAGGTCGTTCGCTCCAAGCTGGGCTGTGTGCACGAACCCCCCGTTCAGCCCGACCGCTGCGCCTTATCCGGTAACTATCGTCTTGAGTCCAACCCGGTAAGACACGACTTATCGCCACTGGCAGCAGCCACTGGTAACAGGATTAGCAGAGCGAGGTATGTAGGCGGTGCTACAGAGTTCTTGAAGTGGTGGCCTAACTACGGCTACACTAGAAGGACAGTATTTGGTATCTGCGCTCTGCTGAAGCCAGTTACCTTCGGAAAAAGAGTTGGTAGCTCTTGATCCGGCAAACAAACCACCGCTGGTAGCGGTGGTTTTTTTGTTTGCAAGCAGCAGATTACGCGCAGAAAAAAAGGATCTCAAGAAGATCCTTTGATCTTTTCTACGGGGTCTGACGCTCAGTGGAACGAAAACTCACGTTAAGGGATTTTGGTCATGAGATTATCAAAAAGGATCTTCACCTAGATCCTTTTAAATTAAAAATGAAGTTTTAAATCAATCTAAAGTATATATGAGTAAACTTGGTCTGACAGTTACCAATGCTTAATCAGTGAGGCACCTATCTCAGCGATCTGTCTATTTCGTTCATCCATAGTTGCCTGACTCCCCGTCGTGTAGATAACTACGATACGGGAGGGCTTACCATCTGGCCCCAGTGCTGCAATGATACCGCGAGACCCACGCTCACCGGCTCCAGATTTATCAGCAATAAACCAGCCAGCCGGAAGGGCCGAGCGCAGAAGTGGTCCTGCAACTTTATCCGCCTCCATCCAGTCTATTAATTGTTGCCGGGAAGCTAGAGTAAGTAGTTCGCCAGTTAATAGTTTGCGCAACGTTGTTGCCATTGCTACAGGCATCGTGGTGTCACGCTCGTCGTTTGGTATGGCTTCATTCAGCTCCGGTTCCCAACGATCAAGGCGAGTTACATGATCCCCCATGTTGTGCAAAAAAGCGGTTAGCTCCTTCGGTCCTCCGATCGTTGTCAGAAGTAAGTTGGCCGCAGTGTTATCACTCATGGTTATGGCAGCACTGCATAATTCTCTTACTGTCATGCCATCCGTAAGATGCTTTTCTGTGACTGGTGAGTACTCAACCAAGTCATTCTGAGAATAGTGTATGCGGCGACCGAGTTGCTCTTGCCCGGCGTCAATACGGGATAATACCGCGCCACATAGCAGAACTTTAAAAGTGCTCATCATTGGAAAACGTTCTTCGGGGCGAAAACTCTCAAGGATCTTACCGCTGTTGAGATCCAGTTCGATGTAACCCACTCGTGCACCCAACTGATCTTCAGCATCTTTTACTTTCACCAGCGTTTCTGGGTGAGCAAAAACAGGAAGGCAAAATGCCGCAAAAAAGGGAATAAGGGCGACACGGAAATGTTGAATACTCATACTCTTCCTTTTTCAATATTATTGAAGCATTTATCAGGGTTATTGTCTCATGAGCGGATACATATTTGAATGTATTTAGAAAAATAAACAAATAGGGGTTCCGCGCACATTTCCCCGAAAAGTGCCACCTGAAATTGTAAACGTTAATATTTTGTTAAAATTCGCGTTAAATTTTTGTTAAATCAGCTCATTTTTTAACCAATAGGCCGAAATCGGCAAAATCCCTTATAAATCAAAAGAATAGACCGAGATAGGGTTGAGTGTTGTTCCAGTTTGGAACAAGAGTCCACTATTAAAGAACGTGGACTCCAACGTCAAAGGGCGAAAAACCGTCTATCAGGGCGATGGCCCACTACGTGAACCATCACCCTAATCAAGTTTTTTGGGGTCGAGGTGCCGTAAAGCACTAAATCGGAACCCTAAAGGGAGCCCCCGATTTAGAGCTTGACGGGGAAAGCCGGCGAACGTGGCGAGAAAGGAAGGGAAGAAAGCGAAAGGAGCGGGCGCTAGGGCGCTGGCAAGTGTAGCGGTCACGCTGCGCGTAACCACCACACCCGCCGCGCTTAATGCGCCGCTACAGGGCGCGTCCCATTCGCCATTCAGGCTGCAAATAAGCGTTGATATTCAGTCAATTACAAACATTAATAACGAAGAGATGACAGAAAAATTTTCATTCTGTGACAGAGAA (SEQ ID NO: 192)
[00651] Конструкция зкДНК выше включает левый-ITR_v1:спейсер_левый-ITR_v2.1: VandenDriessche_Набор промоторов: Сайт_PmeI: Модифицированный_минимальный_консенсус_Козак: hPAH_codop_ORF_v2: Сайт_PacI: WPRE_3pUTR: bGH/спейсер:спейсер_правый-ITR_v1:правый-ITR_v1
[00652] В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей оптимизированный по кодонам вариант 2 PAH человека (зкДНК «hPAH Codop2»), содержит SEQ ID NO: 192. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей оптимизированный по кодонам вариант 2 PAH человека (зкДНК «hPAH Codop2»), по меньшей мере на 85% идентична SEQ ID NO: 192. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей оптимизированный по кодонам вариант 2 PAH человека (зкДНК «hPAH Codop2»), по меньшей мере на 90% идентична SEQ ID NO: 192. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей оптимизированный по кодонам вариант 2 PAH человека (зкДНК «hPAH Codop2»), по меньшей мере на 91% идентична SEQ ID NO: 192. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей оптимизированный по кодонам вариант 2 PAH человека (зкДНК «hPAH Codop2»), по меньшей мере на 92% идентична SEQ ID NO: 192. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей оптимизированный по кодонам вариант 2 PAH человека (зкДНК «hPAH Codop2»), по меньшей мере на 93% идентична SEQ ID NO: 192. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей оптимизированный по кодонам вариант 2 PAH человека (зкДНК «hPAH Codop2»), по меньшей мере на 94% идентична SEQ ID NO: 192. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей оптимизированный по кодонам вариант 2 PAH человека (зкДНК «hPAH Codop2»), по меньшей мере на 95% идентична SEQ ID NO: 192. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей оптимизированный по кодонам вариант 2 PAH человека (зкДНК «hPAH Codop2»), по меньшей мере на 96% идентична SEQ ID NO: 192. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей оптимизированный по кодонам вариант 2 PAH человека (зкДНК «hPAH Codop2»), по меньшей мере на 97% идентична SEQ ID NO: 192. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей оптимизированный по кодонам вариант 2 PAH человека (зкДНК «hPAH Codop2»), по меньшей мере на 98% идентична SEQ ID NO: 192. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей оптимизированный по кодонам вариант 2 PAH человека (зкДНК «hPAH Codop2»), по меньшей мере на 99% идентична SEQ ID NO: 192. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей оптимизированный по кодонам вариант 2 PAH человека (зкДНК «hPAH Codop2»), состоит из SEQ ID NO: 192.
[00653] Последовательность нуклеиновой кислоты зкДНК, содержащей кДНК PAH человека (промотор VD зкДНК, связанный с кДНК hPAH без оптимизации кодонов), показана ниже. Промотор подчеркнут (SEQ ID NO: 191), а открытая рамка считывания (ORF) PAH показана двойным подчеркиванием (SEQ ID NO: 394).
[00654] GGCCGGCCCCTGCAGGCAGCTGCGCGCTCGCTCGCTCACTGAGGCCGCCCGGGCAAAGCCCGGGCGTCGGGCGACCTTTGGTCGCCCGGCCTCAGTGAGCGAGCGAGCGCGCAGAGAGGGAGTGGCCAACTCCATCACTAGGGGTTCCTTGTAGTTAATGATTAACCCGCCATGCTACTTATCTACGTAGCCATGCTCTAGACGGGGGAGGCTGCTGGTGAATATTAACCAAGGTCACCCCAGTTATCGGAGGAGCAAACAGGGGCTAAGTCCACACGCGTGGTACCGTCTGTCTGCACATTTCGTAGAGCGAGTGTTCCGATACTCTAATCTCCCTAGGCAAGGTTCATATTTGTGTAGGTTACTTATTCTCCTTTTGTTGACTAAGTCAATAATCAGAATCAGCAGGTTTGGAGTCAGCTTGGCAGGGATCAGCAGCCTGGGTTGGAAGGAGGGGGTATAAAAGCCCCTTCACCAGGAGAAGCCGTCACACAGATCCACAAGCTCCTGAAGAGGTAAGGGTTTAAGGGATGGTTGGTTGGTGGGGTATTAATGTTTAATTACCTGGAGCACCTGCCTGAAATCACTTTTTTTCAGGTTGGTTTAAACGCCGCCACCATGTCCACTGCGGTCCTGGAAAACCCAGGCTTGGGCAGGAAACTCTCTGACTTTGGACAGGAAACAAGCTATATTGAAGACAACTGCAATCAAAATGGTGCCATATCACTGATCTTCTCACTCAAAGAAGAAGTTGGTGCATTGGCCAAAGTATTGCGCTTATTTGAGGAGAATGATGTAAACCTGACCCACATTGAATCTAGACCTTCTCGTTTAAAGAAAGATGAGTATGAATTTTTCACCCATTTGGATAAACGTAGCCTGCCTGCTCTGACAAACATCATCAAGATCTTGAGGCATGACATTGGTGCCACTGTCCATGAGCTTTCACGAGATAAGAAGAAAGACACAGTGCCCTGGTTCCCAAGAACCATTCAAGAGCTGGACAGATTTGCCAATCAGATTCTCAGCTATGGAGCGGAACTGGATGCTGACCACCCTGGTTTTAAAGATCCTGTGTACCGTGCAAGACGGAAGCAGTTTGCTGACATTGCCTACAACTACCGCCATGGGCAGCCCATCCCTCGAGTGGAATACATGGAGGAAGAAAAGAAAACATGGGGCACAGTGTTCAAGACTCTGAAGTCCTTGTATAAAACCCATGCTTGCTATGAGTACAATCACATTTTTCCACTTCTTGAAAAGTACTGTGGCTTCCATGAAGATAACATTCCCCAGCTGGAAGACGTTTCTCAGTTCCTGCAGACTTGCACTGGTTTCCGCCTCCGACCTGTGGCTGGCCTGCTTTCCTCTCGGGATTTCTTGGGTGGCCTGGCCTTCCGAGTCTTCCACTGCACACAGTACATCAGACATGGATCCAAGCCCATGTATACCCCCGAACCTGACATCTGCCATGAGCTGTTGGGACATGTGCCCTTGTTTTCAGATCGCAGCTTTGCCCAGTTTTCCCAGGAAATTGGCCTTGCCTCTCTGGGTGCACCTGATGAATACATTGAAAAGCTCGCCACAATTTACTGGTTTACTGTGGAGTTTGGGCTCTGCAAACAAGGAGACTCCATAAAGGCATATGGTGCTGGGCTCCTGTCATCCTTTGGTGAATTACAGTACTGCTTATCAGAGAAGCCAAAGCTTCTCCCCCTGGAGCTGGAGAAGACAGCCATCCAAAATTACACTGTCACGGAGTTCCAGCCCCTCTATTACGTGGCAGAGAGTTTTAATGATGCCAAGGAGAAAGTAAGGAACTTTGCTGCCACAATACCTCGGCCCTTCTCAGTTCGCTACGACCCATACACCCAAAGGATTGAGGTCTTGGACAATACCCAGCAGCTTAAGATTTTGGCTGATTCCATTAACAGTGAAATTGGAATCCTTTGCAGTGCCCTCCAGAAAATAAAGTAATTAATTAAGAGCATCTTACCGCCATTTATTCCCATATTTGTTCTGTTTTTCTTGATTTGGGTATACATTTAAATGTTAATAAAACAAAATGGTGGGGCAATCATTTACATTTTTAGGGATATGTAATTACTAGTTCAGGTGTATTGCCACAAGACAAACATGTTAAGAAACTTTCCCGTTATTTACGCTCTGTTCCTGTTAATCAACCTCTGGATTACAAAATTTGTGAAAGATTGACTGATATTCTTAACTATGTTGCTCCTTTTACGCTGTGTGGATATGCTGCTTTATAGCCTCTGTATCTAGCTATTGCTTCCCGTACGGCTTTCGTTTTCTCCTCCTTGTATAAATCCTGGTTGCTGTCTCTTTTAGAGGAGTTGTGGCCCGTTGTCCGTCAACGTGGCGTGGTGTGCTCTGTGTTTGCTGACGCAACCCCCACTGGCTGGGGCATTGCCACCACCTGTCAACTCCTTTCTGGGACTTTCGCTTTCCCCCTCCCGATCGCCACGGCAGAACTCATCGCCGCCTGCCTTGCCCGCTGCTGGACAGGGGCTAGGTTGCTGGGCACTGATAATTCCGTGGTGTTGTCTGTGCCTTCTAGTTGCCAGCCATCTGTTGTTTGCCCCTCCCCCGTGCCTTCCTTGACCCTGGAAGGTGCCACTCCCACTGTCCTTTCCTAATAAAATGAGGAAATTGCATCGCATTGTCTGAGTAGGTGTCATTCTATTCTGGGGGGTGGGGTGGGGCAGGACAGCAAGGGGGAGGATTGGGAAGACAATAGCAGGCATGCTGGGGATGCGGTGGGCTCTATGGCTCTAGAGCATGGCTACGTAGATAAGTAGCATGGCGGGTTAATCATTAACTACACCTGCAGGAGGAACCCCTAGTGATGGAGTTGGCCACTCCCTCTCTGCGCGCTCGCTCGCTCACTGAGGCCGGGCGACCAAAGGTCGCCCGACGCCCGGGCGGCCTCAGTGAGCGAGCGAGCGCGCAGCTGCCTGCAGGGGCGCGCCTCGAGGCATGCGGTACCAAGCTTGTCGAGAAGTACTAGAGGATCATAATCAGCCATACCACATTTGTAGAGGTTTTACTTGCTTTAAAAAACCTCCCACACCTCCCCCTGAACCTGAAACATAAAATGAATGCAATTGTTGTTGTTAACTTGTTTATTGCAGCTTATAATGGTTACAAATAAAGCAATAGCATCACAAATTTCACAAATAAAGCATTTTTTTCACTGCATTCTAGTTGTGGTTTGTCCAAACTCATCAATGTATCTTATCATGTCTGGATCTGATCACTGATATCGCCTAGGAGATCCGAACCAGATAAGTGAAATCTAGTTCCAAACTATTTTGTCATTTTTAATTTTCGTATTAGCTTACGACGCTACACCCAGTTCCCATCTATTTTGTCACTCTTCCCTAAATAATCCTTAAAAACTCCATTTCCACCCCTCCCAGTTCCCAACTATTTTGTCCGCCCACAGCGGGGCATTTTTCTTCCTGTTATGTTTTTAATCAAACATCCTGCCAACTCCATGTGACAAACCGTCATCTTCGGCTACTTTTTCTCTGTCACAGAATGAAAATTTTTCTGTCATCTCTTCGTTATTAATGTTTGTAATTGACTGAATATCAACGCTTATTTGCAGCCTGAATGGCGAATGGGACGCGCCCTGTAGCGGCGCATTAAGCGCGGCGGGTGTGGTGGTTACGCGCAGCGTGACCGCTACACTTGCCAGCGCCCTAGCGCCCGCTCCTTTCGCTTTCTTCCCTTCCTTTCTCGCCACGTTCGCCGGCTTTCCCCGTCAAGCTCTAAATCGGGGGCTCCCTTTAGGGTTCCGATTTAGTGCTTTACGGCACCTCGACCCCAAAAAACTTGATTAGGGTGATGGTTCACGTAGTGGGCCATCGCCCTGATAGACGGTTTTTCGCCCTTTGACGTTGGAGTCCACGTTCTTTAATAGTGGACTCTTGTTCCAAACTGGAACAACACTCAACCCTATCTCGGTCTATTCTTTTGATTTATAAGGGATTTTGCCGATTTCGGCCTATTGGTTAAAAAATGAGCTGATTTAACAAAAATTTAACGCGAATTTTAACAAAATATTAACGTTTACAATTTCAGGTGGCACTTTTCGGGGAAATGTGCGCGGAACCCCTATTTGTTTATTTTTCTAAATACATTCAAATATGTATCCGCTCATGAGACAATAACCCTGATAAATGCTTCAATAATATTGAAAAAGGAAGAGTATGAGTATTCAACATTTCCGTGTCGCCCTTATTCCCTTTTTTGCGGCATTTTGCCTTCCTGTTTTTGCTCACCCAGAAACGCTGGTGAAAGTAAAAGATGCTGAAGATCAGTTGGGTGCACGAGTGGGTTACATCGAACTGGATCTCAACAGCGGTAAGATCCTTGAGAGTTTTCGCCCCGAAGAACGTTTTCCAATGATGAGCACTTTTAAAGTTCTGCTATGTGGCGCGGTATTATCCCGTATTGACGCCGGGCAAGAGCAACTCGGTCGCCGCATACACTATTCTCAGAATGACTTGGTTGAGTACTCACCAGTCACAGAAAAGCATCTTACGGATGGCATGACAGTAAGAGAATTATGCAGTGCTGCCATAACCATGAGTGATAACACTGCGGCCAACTTACTTCTGACAACGATCGGAGGACCGAAGGAGCTAACCGCTTTTTTGCACAACATGGGGGATCATGTAACTCGCCTTGATCGTTGGGAACCGGAGCTGAATGAAGCCATACCAAACGACGAGCGTGACACCACGATGCCTGTAGCAATGGCAACAACGTTGCGCAAACTATTAACTGGCGAACTACTTACTCTAGCTTCCCGGCAACAATTAATAGACTGGATGGAGGCGGATAAAGTTGCAGGACCACTTCTGCGCTCGGCCCTTCCGGCTGGCTGGTTTATTGCTGATAAATCTGGAGCCGGTGAGCGTGGGTCTCGCGGTATCATTGCAGCACTGGGGCCAGATGGTAAGCCCTCCCGTATCGTAGTTATCTACACGACGGGGAGTCAGGCAACTATGGATGAACGAAATAGACAGATCGCTGAGATAGGTGCCTCACTGATTAAGCATTGGTAACTGTCAGACCAAGTTTACTCATATATACTTTAGATTGATTTAAAACTTCATTTTTAATTTAAAAGGATCTAGGTGAAGATCCTTTTTGATAATCTCATGACCAAAATCCCTTAACGTGAGTTTTCGTTCCACTGAGCGTCAGACCCCGTAGAAAAGATCAAAGGATCTTCTTGAGATCCTTTTTTTCTGCGCGTAATCTGCTGCTTGCAAACAAAAAAACCACCGCTACCAGCGGTGGTTTGTTTGCCGGATCAAGAGCTACCAACTCTTTTTCCGAAGGTAACTGGCTTCAGCAGAGCGCAGATACCAAATACTGTCCTTCTAGTGTAGCCGTAGTTAGGCCACCACTTCAAGAACTCTGTAGCACCGCCTACATACCTCGCTCTGCTAATCCTGTTACCAGTGGCTGCTGCCAGTGGCGATAAGTCGTGTCTTACCGGGTTGGACTCAAGACGATAGTTACCGGATAAGGCGCAGCGGTCGGGCTGAACGGGGGGTTCGTGCACACAGCCCAGCTTGGAGCGAACGACCTACACCGAACTGAGATACCTACAGCGTGAGCATTGAGAAAGCGCCACGCTTCCCGAAGGGAGAAAGGCGGACAGGTATCCGGTAAGCGGCAGGGTCGGAACAGGAGAGCGCACGAGGGAGCTTCCAGGGGGAAACGCCTGGTATCTTTATAGTCCTGTCGGGTTTCGCCACCTCTGACTTGAGCGTCGATTTTTGTGATGCTCGTCAGGGGGGCGGAGCCTATGGAAAAACGCCAGCAACGCGGCCTTTTTACGGTTCCTGGCCTTTTGCTGGCCTTTTGCTCACATGTTCTTTCCTGCGTTATCCCCTGATTCTGTGGATAACCGTATTACCGCCTTTGAGTGAGCTGATACCGCTCGCCGCAGCCGAACGACCGAGCGCAGCGAGTCAGTGAGCGAGGAAGCGGAAGAGCGCCTGATGCGGTATTTTCTCCTTACGCATCTGTGCGGTATTTCACACCGCAGACCAGCCGCGTAACCTGGCAAAATCGGTTACGGTTGAGTAATAAATGGATGCCCTGCGTAAGCGGGTGTGGGCGGACAATAAAGTCTTAAACTGAACAAAATAGATCTAAACTATGACAATAAAGTCTTAAACTAGACAGAATAGTTGTAAACTGAAATCAGTCCAGTTATGCTGTGAAAAAGCATACTGGACTTTTGTTATGGCTAAAGCAAACTCTTCATTTTCTGAAGTGCAAATTGCCCGTCGTATTAAAGAGGGGCGTGGCCAAGGGCATGGTAAAGACTATATTCGCGGCGTTGTGACAATTTACCGAACAACTCCGCGGCCGGGAAGCCGATCTCGGCTTGAACGAATTGTTAGGTGGCGGTACTTGGGTCGATATCAAAGTGCATCACTTCTTCCCGTATGCCCAACTTTGTATAGAGAGCCACTGCGGGATCGTCACCGTAATCTGCTTGCACGTAGATCACATAAGCACCAAGCGCGTTGGCCTCATGCTTGAGGAGATTGATGAGCGCGGTGGCAATGCCCTGCCTCCGGTGCTCGCCGGAGACTGCGAGATCATAGATATAGATCTCACTACGCGGCTGCTCAAACCTGGGCAGAACGTAAGCCGCGAGAGCGCCAACAACCGCTTCTTGGTCGAAGGCAGCAAGCGCGATGAATGTCTTACTACGGAGCAAGTTCCCGAGGTAATCGGAGTCCGGCTGATGTTGGGAGTAGGTGGCTACGTCTCCGAACTCACGACCGAAAAGATCAAGAGCAGCCCGCATGGATTTGACTTGGTCAGGGCCGAGCCTACATGTGCGAATGATGCCCATACTTGAGCCACCTAACTTTGTTTTAGGGCGACTGCCCTGCTGCGTAACATCGTTGCTGCTGCGTAACATCGTTGCTGCTCCATAACATCAAACATCGACCCACGGCGTAACGCGCTTGCTGCTTGGATGCCCGAGGCATAGACTGTACAAAAAAACAGTCATAACAAGCCATGAAAACCGCCACTGCGCCGTTACCACCGCTGCGTTCGGTCAAGGTTCTGGACCAGTTGCGTGAGCGCATACGCTACTTGCATTACAGTTTACGAACCGAACAGGCTTATGTCAACTGGGTTCGTGCCTTCATCCGTTTCCACGGTGTGCGTCACCCGGCAACCTTGGGCAGCAGCGAAGTCGAGGCATTTCTGTCCTGGCTGGCGAACGAGCGCAAGGTTTCGGTCTCCACGCATCGTCAGGCATTGGCGGCCTTGCTGTTCTTCTACGGCAAGGTGCTGTGCACGGATCTGCCCTGGCTTCAGGAGATCGGAAGACCTCGGCCGTCGCGGCGCTTGCCGGTGGTGCTGACCCCGGATGAAGTGGTTCGCATCCTCGGTTTTCTGGAAGGCGAGCATCGTTTGTTCGCCCAGGACTCTAGCTATAGTTCTAGTGGTTGGCTACGTATACTCCGGAATATTAATAGATCATGGAGATAATTAAAATGATAACCATCTCGCAAATAAATAAGTATTTTACTGTTTTCGTAACAGTTTTGTAATAAAAAAACCTATAAATATTCCGGATTATTCATACCGTCCCACCATCGGGCGCGGATCTCGGTCCGAAACCATGTCGTACTACCATCACCATCACCATCACGATTACGATATCCCAACGACCGAAAACCTGTATTTTCAGGGCGCCATGGGATCC (SEQ ID NO: 193)
[00655] Конструкция выше включает следующие элементы. Левый-ITR_v1:спейсер_левый-ITR_v1: VandenDriessche_Набор промоторов: Сайт_PmeI: Консенсус_Козак:hPAH_кДНК_ORF_v3: Сайт_PacI: WPRE_3pUTR:bGH:спейсер_правый-ITR_v1:правый-ITR_v1.
[00656] В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей кДНК PAH человека (промотор VD зкДНК, связанный с кДНК hPAH без оптимизации кодонов), содержит SEQ ID NO: 193. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей кДНК PAH человека (промотор VD зкДНК, связанный с кДНК hPAH без оптимизации кодонов), по меньшей мере на 85% идентична SEQ ID NO: 193. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей кДНК PAH человека (промотор VD зкДНК, связанный с кДНК hPAH без оптимизации кодонов), по меньшей мере на 90% идентична SEQ ID NO: 193. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей кДНК PAH человека (промотор VD зкДНК, связанный с кДНК hPAH без оптимизации кодонов), по меньшей мере на 91% идентична SEQ ID NO: 193. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей кДНК PAH человека (промотор VD зкДНК, связанный с кДНК hPAH без оптимизации кодонов), по меньшей мере на 92% идентична SEQ ID NO: 193. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей кДНК PAH человека (промотор VD зкДНК, связанный с кДНК hPAH без оптимизации кодонов), по меньшей мере на 93% идентична SEQ ID NO: 193. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей кДНК PAH человека (промотор VD зкДНК, связанный с кДНК hPAH без оптимизации кодонов), по меньшей мере на 94% идентична SEQ ID NO: 193. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей кДНК PAH человека (промотор VD зкДНК, связанный с кДНК hPAH без оптимизации кодонов), по меньшей мере на 95% идентична SEQ ID NO: 193. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей кДНК PAH человека (промотор VD зкДНК, связанный с кДНК hPAH без оптимизации кодонов), по меньшей мере на 96% идентична SEQ ID NO: 193. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей кДНК PAH человека (промотор VD зкДНК, связанный с кДНК hPAH без оптимизации кодонов), по меньшей мере на 97% идентична SEQ ID NO: 193. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей кДНК PAH человека (промотор VD зкДНК, связанный с кДНК hPAH без оптимизации кодонов), по меньшей мере на 98% идентична SEQ ID NO: 193. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей кДНК PAH человека (промотор VD зкДНК, связанный с кДНК hPAH без оптимизации кодонов), по меньшей мере на 99% идентична SEQ ID NO: 193. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей кДНК PAH человека (промотор VD зкДНК, связанный с кДНК hPAH без оптимизации кодонов), состоит из SEQ ID NO: 193.
[00657] Последовательность нуклеиновой кислоты зкДНК, содержащей оптимизированный по кодонам вариант 4 hPAH (PAH человека с минимизацией CpG и оптимизацией кодонов), показана ниже. Промотор подчеркнут (SEQ ID NO: 191), а открытая рамка считывания (ORF) оптимизированного по кодонам варианта 4 hPAH показана двойным подчеркиванием (SEQ ID NO: 384).
[00658] GGCCGGCCCCTGCAGGCAGCTGCGCGCTCGCTCGCTCACTGAGGCCGCCCGGGCAAAGCCCGGGCGTCGGGCGACCTTTGGTCGCCCGGCCTCAGTGAGCGAGCGAGCGCGCAGAGAGGGAGTGGCCAACTCCATCACTAGGGGTTCCTTGTAGTTAATGATTAACCCGCCATGCTACTTATCTACGTAGCCATGCTCTAGACGGGGGAGGCTGCTGGTGAATATTAACCAAGGTCACCCCAGTTATCGGAGGAGCAAACAGGGGCTAAGTCCACACGCGTGGTACCGTCTGTCTGCACATTTCGTAGAGCGAGTGTTCCGATACTCTAATCTCCCTAGGCAAGGTTCATATTTGTGTAGGTTACTTATTCTCCTTTTGTTGACTAAGTCAATAATCAGAATCAGCAGGTTTGGAGTCAGCTTGGCAGGGATCAGCAGCCTGGGTTGGAAGGAGGGGGTATAAAAGCCCCTTCACCAGGAGAAGCCGTCACACAGATCCACAAGCTCCTGAAGAGGTAAGGGTTTAAGGGATGGTTGGTTGGTGGGGTATTAATGTTTAATTACCTGGAGCACCTGCCTGAAATCACTTTTTTTCAGGTTGGTTTAAACGCCGCCACCATGAGTACAGCTGTGCTTGAAAATCCTGGCCTGGGCAGGAAGCTTAGTGACTTTGGCCAGGAAACATCTTATATTGAAGACAACTGCAACCAGAATGGTGCCATTTCTCTTATCTTCTCCCTGAAAGAAGAGGTGGGAGCCCTGGCAAAGGTTTTAAGGCTCTTTGAGGAGAATGATGTGAATTTGACACACATTGAGTCCAGGCCTTCTAGACTCAAGAAAGATGAATATGAGTTCTTCACCCACCTGGACAAGAGGAGTCTCCCTGCTCTGACCAACATTATCAAGATCTTGAGACATGATATAGGAGCTACAGTGCATGAACTTTCAAGGGATAAAAAGAAGGACACTGTCCCCTGGTTTCCCAGAACTATCCAAGAATTAGACAGGTTTGCCAATCAGATCCTGAGCTATGGTGCAGAATTAGATGCAGACCACCCTGGGTTTAAAGACCCTGTGTATAGAGCCAGAAGAAAGCAGTTTGCTGACATTGCATACAACTACAGGCATGGGCAGCCCATTCCTAGGGTGGAGTACATGGAGGAAGAAAAAAAGACCTGGGGCACAGTTTTCAAGACCCTGAAGAGCCTTTACAAGACACATGCCTGCTATGAATATAACCATATATTTCCATTGTTGGAGAAATACTGTGGATTTCATGAAGATAACATCCCCCAGCTGGAGGATGTTAGTCAGTTTCTGCAGACCTGCACAGGCTTTAGACTGAGGCCAGTTGCAGGACTGCTAAGTTCTAGGGACTTCCTGGGTGGGCTAGCCTTCAGAGTGTTCCACTGTACCCAATATATAAGGCATGGATCCAAGCCCATGTACACCCCTGAGCCTGATATCTGCCATGAGCTATTGGGCCATGTCCCCCTATTTTCTGACAGAAGCTTTGCCCAGTTCTCCCAGGAGATTGGATTAGCCTCTCTGGGAGCTCCTGATGAGTACATTGAGAAGTTAGCAACCATCTACTGGTTCACTGTGGAATTTGGCCTTTGCAAACAAGGGGATAGTATAAAGGCTTATGGAGCAGGTCTGCTTAGCAGTTTTGGAGAGCTGCAGTACTGCCTGTCAGAAAAGCCAAAGCTCCTACCATTAGAACTAGAAAAGACTGCCATCCAGAACTATACAGTCACTGAATTCCAGCCTCTCTACTATGTGGCTGAGTCTTTCAATGATGCCAAGGAGAAGGTGAGAAATTTTGCAGCCACCATTCCCAGGCCCTTCTCTGTTAGATATGACCCCTACACTCAGAGGATTGAGGTCCTGGACAATACCCAGCAACTAAAAATTCTGGCTGATTCCATTAATTCTGAAATTGGCATCCTCTGCTCTGCTCTCCAGAAGATTAAATGATTAATTAAGAGCATCTTACCGCCATTTATTCCCATATTTGTTCTGTTTTTCTTGATTTGGGTATACATTTAAATGTTAATAAAACAAAATGGTGGGGCAATCATTTACATTTTTAGGGATATGTAATTACTAGTTCAGGTGTATTGCCACAAGACAAACATGTTAAGAAACTTTCCCGTTATTTACGCTCTGTTCCTGTTAATCAACCTCTGGATTACAAAATTTGTGAAAGATTGACTGATATTCTTAACTATGTTGCTCCTTTTACGCTGTGTGGATATGCTGCTTTATAGCCTCTGTATCTAGCTATTGCTTCCCGTACGGCTTTCGTTTTCTCCTCCTTGTATAAATCCTGGTTGCTGTCTCTTTTAGAGGAGTTGTGGCCCGTTGTCCGTCAACGTGGCGTGGTGTGCTCTGTGTTTGCTGACGCAACCCCCACTGGCTGGGGCATTGCCACCACCTGTCAACTCCTTTCTGGGACTTTCGCTTTCCCCCTCCCGATCGCCACGGCAGAACTCATCGCCGCCTGCCTTGCCCGCTGCTGGACAGGGGCTAGGTTGCTGGGCACTGATAATTCCGTGGTGTTGTCTGTGCCTTCTAGTTGCCAGCCATCTGTTGTTTGCCCCTCCCCCGTGCCTTCCTTGACCCTGGAAGGTGCCACTCCCACTGTCCTTTCCTAATAAAATGAGGAAATTGCATCGCATTGTCTGAGTAGGTGTCATTCTATTCTGGGGGGTGGGGTGGGGCAGGACAGCAAGGGGGAGGATTGGGAAGACAATAGCAGGCATGCTGGGGATGCGGTGGGCTCTATGGCTCTAGAGCATGGCTACGTAGATAAGTAGCATGGCGGGTTAATCATTAACTACACCTGCAGGAGGAACCCCTAGTGATGGAGTTGGCCACTCCCTCTCTGCGCGCTCGCTCGCTCACTGAGGCCGGGCGACCAAAGGTCGCCCGACGCCCGGGCGGCCTCAGTGAGCGAGCGAGCGCGCAGCTGCCTGCAGGGGCGCGCCTCGAGGCATGCGGTACCAAGCTTGTCGAGAAGTACTAGAGGATCATAATCAGCCATACCACATTTGTAGAGGTTTTACTTGCTTTAAAAAACCTCCCACACCTCCCCCTGAACCTGAAACATAAAATGAATGCAATTGTTGTTGTTAACTTGTTTATTGCAGCTTATAATGGTTACAAATAAAGCAATAGCATCACAAATTTCACAAATAAAGCATTTTTTTCACTGCATTCTAGTTGTGGTTTGTCCAAACTCATCAATGTATCTTATCATGTCTGGATCTGATCACTGATATCGCCTAGGAGATCCGAACCAGATAAGTGAAATCTAGTTCCAAACTATTTTGTCATTTTTAATTTTCGTATTAGCTTACGACGCTACACCCAGTTCCCATCTATTTTGTCACTCTTCCCTAAATAATCCTTAAAAACTCCATTTCCACCCCTCCCAGTTCCCAACTATTTTGTCCGCCCACAGCGGGGCATTTTTCTTCCTGTTATGTTTTTAATCAAACATCCTGCCAACTCCATGTGACAAACCGTCATCTTCGGCTACTTTTTCTCTGTCACAGAATGAAAATTTTTCTGTCATCTCTTCGTTATTAATGTTTGTAATTGACTGAATATCAACGCTTATTTGCAGCCTGAATGGCGAATGGGACGCGCCCTGTAGCGGCGCATTAAGCGCGGCGGGTGTGGTGGTTACGCGCAGCGTGACCGCTACACTTGCCAGCGCCCTAGCGCCCGCTCCTTTCGCTTTCTTCCCTTCCTTTCTCGCCACGTTCGCCGGCTTTCCCCGTCAAGCTCTAAATCGGGGGCTCCCTTTAGGGTTCCGATTTAGTGCTTTACGGCACCTCGACCCCAAAAAACTTGATTAGGGTGATGGTTCACGTAGTGGGCCATCGCCCTGATAGACGGTTTTTCGCCCTTTGACGTTGGAGTCCACGTTCTTTAATAGTGGACTCTTGTTCCAAACTGGAACAACACTCAACCCTATCTCGGTCTATTCTTTTGATTTATAAGGGATTTTGCCGATTTCGGCCTATTGGTTAAAAAATGAGCTGATTTAACAAAAATTTAACGCGAATTTTAACAAAATATTAACGTTTACAATTTCAGGTGGCACTTTTCGGGGAAATGTGCGCGGAACCCCTATTTGTTTATTTTTCTAAATACATTCAAATATGTATCCGCTCATGAGACAATAACCCTGATAAATGCTTCAATAATATTGAAAAAGGAAGAGTATGAGTATTCAACATTTCCGTGTCGCCCTTATTCCCTTTTTTGCGGCATTTTGCCTTCCTGTTTTTGCTCACCCAGAAACGCTGGTGAAAGTAAAAGATGCTGAAGATCAGTTGGGTGCACGAGTGGGTTACATCGAACTGGATCTCAACAGCGGTAAGATCCTTGAGAGTTTTCGCCCCGAAGAACGTTTTCCAATGATGAGCACTTTTAAAGTTCTGCTATGTGGCGCGGTATTATCCCGTATTGACGCCGGGCAAGAGCAACTCGGTCGCCGCATACACTATTCTCAGAATGACTTGGTTGAGTACTCACCAGTCACAGAAAAGCATCTTACGGATGGCATGACAGTAAGAGAATTATGCAGTGCTGCCATAACCATGAGTGATAACACTGCGGCCAACTTACTTCTGACAACGATCGGAGGACCGAAGGAGCTAACCGCTTTTTTGCACAACATGGGGGATCATGTAACTCGCCTTGATCGTTGGGAACCGGAGCTGAATGAAGCCATACCAAACGACGAGCGTGACACCACGATGCCTGTAGCAATGGCAACAACGTTGCGCAAACTATTAACTGGCGAACTACTTACTCTAGCTTCCCGGCAACAATTAATAGACTGGATGGAGGCGGATAAAGTTGCAGGACCACTTCTGCGCTCGGCCCTTCCGGCTGGCTGGTTTATTGCTGATAAATCTGGAGCCGGTGAGCGTGGGTCTCGCGGTATCATTGCAGCACTGGGGCCAGATGGTAAGCCCTCCCGTATCGTAGTTATCTACACGACGGGGAGTCAGGCAACTATGGATGAACGAAATAGACAGATCGCTGAGATAGGTGCCTCACTGATTAAGCATTGGTAACTGTCAGACCAAGTTTACTCATATATACTTTAGATTGATTTAAAACTTCATTTTTAATTTAAAAGGATCTAGGTGAAGATCCTTTTTGATAATCTCATGACCAAAATCCCTTAACGTGAGTTTTCGTTCCACTGAGCGTCAGACCCCGTAGAAAAGATCAAAGGATCTTCTTGAGATCCTTTTTTTCTGCGCGTAATCTGCTGCTTGCAAACAAAAAAACCACCGCTACCAGCGGTGGTTTGTTTGCCGGATCAAGAGCTACCAACTCTTTTTCCGAAGGTAACTGGCTTCAGCAGAGCGCAGATACCAAATACTGTCCTTCTAGTGTAGCCGTAGTTAGGCCACCACTTCAAGAACTCTGTAGCACCGCCTACATACCTCGCTCTGCTAATCCTGTTACCAGTGGCTGCTGCCAGTGGCGATAAGTCGTGTCTTACCGGGTTGGACTCAAGACGATAGTTACCGGATAAGGCGCAGCGGTCGGGCTGAACGGGGGGTTCGTGCACACAGCCCAGCTTGGAGCGAACGACCTACACCGAACTGAGATACCTACAGCGTGAGCATTGAGAAAGCGCCACGCTTCCCGAAGGGAGAAAGGCGGACAGGTATCCGGTAAGCGGCAGGGTCGGAACAGGAGAGCGCACGAGGGAGCTTCCAGGGGGAAACGCCTGGTATCTTTATAGTCCTGTCGGGTTTCGCCACCTCTGACTTGAGCGTCGATTTTTGTGATGCTCGTCAGGGGGGCGGAGCCTATGGAAAAACGCCAGCAACGCGGCCTTTTTACGGTTCCTGGCCTTTTGCTGGCCTTTTGCTCACATGTTCTTTCCTGCGTTATCCCCTGATTCTGTGGATAACCGTATTACCGCCTTTGAGTGAGCTGATACCGCTCGCCGCAGCCGAACGACCGAGCGCAGCGAGTCAGTGAGCGAGGAAGCGGAAGAGCGCCTGATGCGGTATTTTCTCCTTACGCATCTGTGCGGTATTTCACACCGCAGACCAGCCGCGTAACCTGGCAAAATCGGTTACGGTTGAGTAATAAATGGATGCCCTGCGTAAGCGGGTGTGGGCGGACAATAAAGTCTTAAACTGAACAAAATAGATCTAAACTATGACAATAAAGTCTTAAACTAGACAGAATAGTTGTAAACTGAAATCAGTCCAGTTATGCTGTGAAAAAGCATACTGGACTTTTGTTATGGCTAAAGCAAACTCTTCATTTTCTGAAGTGCAAATTGCCCGTCGTATTAAAGAGGGGCGTGGCCAAGGGCATGGTAAAGACTATATTCGCGGCGTTGTGACAATTTACCGAACAACTCCGCGGCCGGGAAGCCGATCTCGGCTTGAACGAATTGTTAGGTGGCGGTACTTGGGTCGATATCAAAGTGCATCACTTCTTCCCGTATGCCCAACTTTGTATAGAGAGCCACTGCGGGATCGTCACCGTAATCTGCTTGCACGTAGATCACATAAGCACCAAGCGCGTTGGCCTCATGCTTGAGGAGATTGATGAGCGCGGTGGCAATGCCCTGCCTCCGGTGCTCGCCGGAGACTGCGAGATCATAGATATAGATCTCACTACGCGGCTGCTCAAACCTGGGCAGAACGTAAGCCGCGAGAGCGCCAACAACCGCTTCTTGGTCGAAGGCAGCAAGCGCGATGAATGTCTTACTACGGAGCAAGTTCCCGAGGTAATCGGAGTCCGGCTGATGTTGGGAGTAGGTGGCTACGTCTCCGAACTCACGACCGAAAAGATCAAGAGCAGCCCGCATGGATTTGACTTGGTCAGGGCCGAGCCTACATGTGCGAATGATGCCCATACTTGAGCCACCTAACTTTGTTTTAGGGCGACTGCCCTGCTGCGTAACATCGTTGCTGCTGCGTAACATCGTTGCTGCTCCATAACATCAAACATCGACCCACGGCGTAACGCGCTTGCTGCTTGGATGCCCGAGGCATAGACTGTACAAAAAAACAGTCATAACAAGCCATGAAAACCGCCACTGCGCCGTTACCACCGCTGCGTTCGGTCAAGGTTCTGGACCAGTTGCGTGAGCGCATACGCTACTTGCATTACAGTTTACGAACCGAACAGGCTTATGTCAACTGGGTTCGTGCCTTCATCCGTTTCCACGGTGTGCGTCACCCGGCAACCTTGGGCAGCAGCGAAGTCGAGGCATTTCTGTCCTGGCTGGCGAACGAGCGCAAGGTTTCGGTCTCCACGCATCGTCAGGCATTGGCGGCCTTGCTGTTCTTCTACGGCAAGGTGCTGTGCACGGATCTGCCCTGGCTTCAGGAGATCGGAAGACCTCGGCCGTCGCGGCGCTTGCCGGTGGTGCTGACCCCGGATGAAGTGGTTCGCATCCTCGGTTTTCTGGAAGGCGAGCATCGTTTGTTCGCCCAGGACTCTAGCTATAGTTCTAGTGGTTGGCTACGTATACTCCGGAATATTAATAGATCATGGAGATAATTAAAATGATAACCATCTCGCAAATAAATAAGTATTTTACTGTTTTCGTAACAGTTTTGTAATAAAAAAACCTATAAATATTCCGGATTATTCATACCGTCCCACCATCGGGCGCGGATCTCGGTCCGAAACCATGTCGTACTACCATCACCATCACCATCACGATTACGATATCCCAACGACCGAAAACCTGTATTTTCAGGGCGCCATGGGATCC (SEQ ID NO: 194)
[00659] Конструкция выше включает левый-ITR_v1:спейсер_левый-ITR_v1: VandenDriessche_Набор промоторов: Сайт_PmeI: Консенсус_Козак: hPAH_CpGmin-codop_ORF_v4: Сайт_PacI: WPRE_3pUTR:bGH:спейсер_правый-ITR_v1:правый-ITR_v1.
[00660] В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей вариант 4 hPAH (PAH человека с минимизацией CpG и оптимизацией кодонов), содержит SEQ ID NO: 194. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей вариант 4 hPAH (PAH человека с минимизацией CpG и оптимизацией кодонов), по меньшей мере на 85% идентична SEQ ID NO: 194. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей вариант 4 hPAH (PAH человека с минимизацией CpG и оптимизацией кодонов), по меньшей мере на 90% идентична SEQ ID NO: 194. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей вариант 4 hPAH (PAH человека с минимизацией CpG и оптимизацией кодонов), по меньшей мере на 91% идентична SEQ ID NO: 194. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей вариант 4 hPAH (PAH человека с минимизацией CpG и оптимизацией кодонов), по меньшей мере на 92% идентична SEQ ID NO: 194. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей вариант 4 hPAH (PAH человека с минимизацией CpG и оптимизацией кодонов), по меньшей мере на 93% идентична SEQ ID NO: 194. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей вариант 4 hPAH (PAH человека с минимизацией CpG и оптимизацией кодонов), по меньшей мере на 94% идентична SEQ ID NO: 194. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей вариант 4 hPAH (PAH человека с минимизацией CpG и оптимизацией кодонов), по меньшей мере на 95% идентична SEQ ID NO: 194. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей вариант 4 hPAH (PAH человека с минимизацией CpG и оптимизацией кодонов), по меньшей мере на 96% идентична SEQ ID NO: 194. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей вариант 4 hPAH (PAH человека с минимизацией CpG и оптимизацией кодонов), по меньшей мере на 97% идентична SEQ ID NO: 194. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей вариант 4 hPAH (PAH человека с минимизацией CpG и оптимизацией кодонов), по меньшей мере на 98% идентична SEQ ID NO: 194. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей вариант 4 hPAH (PAH человека с минимизацией CpG и оптимизацией кодонов), по меньшей мере на 99% идентична SEQ ID NO: 194. В соответствии с некоторыми вариантами реализации последовательность нуклеиновой кислоты зкДНК, содержащей вариант 4 hPAH (PAH человека с минимизацией CpG и оптимизацией кодонов), состоит из SEQ ID NO: 194.
ССЫЛКИ
[00661] Все публикации и ссылки, включая, но не ограничиваясь перечисленными, патенты и заявки на патенты, указанные в данном описании и в Примерах в данном документе, полностью включены посредством ссылки, как если бы каждая отдельная публикация или ссылка была конкретно и по отдельности указана для включения в данный документ посредством ссылки во всей полноте. Любая заявка на патент, согласно которой настоящая заявка испрашивает приоритет, также включена в данный документ посредством ссылки способом, описанным выше для публикаций и ссылок.
--->
Перечень последовательностей
<110> ДЖЕНЕРЕЙШЕН БИО КО.
<120> Невирусные ДНК-векторы и варианты их применения для экспрессии
терапевтического средства на основе фенилаланингидроксилазы (PAH)
<130> 131698-05720
<140> PCT/US2020/022595
<141> 2020-03-13
<150> 62/857,514
<151> 2019-06-05
<150> 62/817,771
<151> 2019-03-13
<160> 396
<170> PatentIn version 3.5
<210> 1
<211> 141
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 1
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgacc aaaggtcgcc cgacgcccgg gctttgcccg ggcggcctca gtgagcgagc 120
gagcgcgcag ctgcctgcag g 141
<210> 2
<211> 141
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 2
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccgggcaaag cccgggcgtc 60
gggcgacctt tggtcgcccg gcctcagtga gcgagcgagc gcgcagagag ggagtggcca 120
actccatcac taggggttcc t 141
<210> 3
<211> 130
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 3
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgacc aaaggtcgcc cgacgcccgg gcggcctcag tgagcgagcg agcgcgcagc 120
tgcctgcagg 130
<210> 4
<211> 130
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 4
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccgggcgtcg ggcgaccttt 60
ggtcgcccgg cctcagtgag cgagcgagcg cgcagagagg gagtggccaa ctccatcact 120
aggggttcct 130
<210> 5
<211> 143
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 5
ttgcccactc cctctctgcg cgctcgctcg ctcggtgggg cctgcggacc aaaggtccgc 60
agacggcaga ggtctcctct gccggcccca ccgagcgagc gacgcgcgca gagagggagt 120
gggcaactcc atcactaggg taa 143
<210> 6
<211> 144
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 6
ttggccactc cctctatgcg cactcgctcg ctcggtgggg cctggcgacc aaaggtcgcc 60
agacggacgt gggtttccac gtccggcccc accgagcgag cgagtgcgca tagagggagt 120
ggccaactcc atcactagag gtat 144
<210> 7
<211> 127
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 7
ttggccactc cctctatgcg cgctcgctca ctcactcggc cctggagacc aaaggtctcc 60
agactgccgg cctctggccg gcagggccga gtgagtgagc gagcgcgcat agagggagtg 120
gccaact 127
<210> 8
<211> 166
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 8
tcccccctgt cgcgttcgct cgctcgctgg ctcgtttggg ggggcgacgg ccagagggcc 60
gtcgtctggc agctctttga gctgccaccc ccccaaacga gccagcgagc gagcgaacgc 120
gacagggggg agagtgccac actctcaagc aagggggttt tgtaag 166
<210> 9
<211> 144
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 9
ttgcccactc cctctaatgc gcgctcgctc gctcggtggg gcctgcggac caaaggtccg 60
cagacggcag aggtctcctc tgccggcccc accgagcgag cgagcgcgca tagagggagt 120
gggcaactcc atcactaggg gtat 144
<210> 10
<211> 143
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 10
ttaccctagt gatggagttg cccactccct ctctgcgcgc gtcgctcgct cggtggggcc 60
ggcagaggag acctctgccg tctgcggacc tttggtccgc aggccccacc gagcgagcga 120
gcgcgcagag agggagtggg caa 143
<210> 11
<211> 144
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 11
atacctctag tgatggagtt ggccactccc tctatgcgca ctcgctcgct cggtggggcc 60
ggacgtggaa acccacgtcc gtctggcgac ctttggtcgc caggccccac cgagcgagcg 120
agtgcgcata gagggagtgg ccaa 144
<210> 12
<211> 127
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 12
agttggccac attagctatg cgcgctcgct cactcactcg gccctggaga ccaaaggtct 60
ccagactgcc ggcctctggc cggcagggcc gagtgagtga gcgagcgcgc atagagggag 120
tggccaa 127
<210> 13
<211> 166
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 13
cttacaaaac ccccttgctt gagagtgtgg cactctcccc cctgtcgcgt tcgctcgctc 60
gctggctcgt ttgggggggt ggcagctcaa agagctgcca gacgacggcc ctctggccgt 120
cgccccccca aacgagccag cgagcgagcg aacgcgacag ggggga 166
<210> 14
<211> 144
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 14
atacccctag tgatggagtt gcccactccc tctatgcgcg ctcgctcgct cggtggggcc 60
ggcagaggag acctctgccg tctgcggacc tttggtccgc aggccccacc gagcgagcga 120
gcgcgcatta gagggagtgg gcaa 144
<210> 15
<211> 120
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 15
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
cgcacgcccg ggtttcccgg gcggcctcag tgagcgagcg agcgcgcagc tgcctgcagg 120
<210> 16
<211> 122
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 16
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgacgcccg ggctttgccc gggcggcctc agtgagcgag cgagcgcgca gctgcctgca 120
gg 122
<210> 17
<211> 129
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 17
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgacc aaaggtcgcc cgacgcccgg gcgcctcagt gagcgagcga gcgcgcagct 120
gcctgcagg 129
<210> 18
<211> 101
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 18
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ctttgcctca gtgagcgagc gagcgcgcag ctgcctgcag g 101
<210> 19
<211> 139
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 19
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgaca aagtcgcccg acgcccgggc tttgcccggg cggcctcagt gagcgagcga 120
gcgcgcagct gcctgcagg 139
<210> 20
<211> 137
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 20
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgaaa atcgcccgac gcccgggctt tgcccgggcg gcctcagtga gcgagcgagc 120
gcgcagctgc ctgcagg 137
<210> 21
<211> 135
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 21
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgaaa cgcccgacgc ccgggctttg cccgggcggc ctcagtgagc gagcgagcgc 120
gcagctgcct gcagg 135
<210> 22
<211> 133
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 22
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcaaag cccgacgccc gggctttgcc cgggcggcct cagtgagcga gcgagcgcgc 120
agctgcctgc agg 133
<210> 23
<211> 139
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 23
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgacc aaaggtcgcc cgacgcccgg gtttcccggg cggcctcagt gagcgagcga 120
gcgcgcagct gcctgcagg 139
<210> 24
<211> 137
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 24
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgacc aaaggtcgcc cgacgcccgg tttccgggcg gcctcagtga gcgagcgagc 120
gcgcagctgc ctgcagg 137
<210> 25
<211> 135
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 25
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgacc aaaggtcgcc cgacgcccgt ttcgggcggc ctcagtgagc gagcgagcgc 120
gcagctgcct gcagg 135
<210> 26
<211> 133
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 26
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgacc aaaggtcgcc cgacgccctt tgggcggcct cagtgagcga gcgagcgcgc 120
agctgcctgc agg 133
<210> 27
<211> 131
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 27
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgacc aaaggtcgcc cgacgccttt ggcggcctca gtgagcgagc gagcgcgcag 120
ctgcctgcag g 131
<210> 28
<211> 129
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 28
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgacc aaaggtcgcc cgacgctttg cggcctcagt gagcgagcga gcgcgcagct 120
gcctgcagg 129
<210> 29
<211> 127
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 29
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgacc aaaggtcgcc cgacgtttcg gcctcagtga gcgagcgagc gcgcagctgc 120
ctgcagg 127
<210> 30
<211> 122
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 30
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgacc aaaggtcgcc cgacggcctc agtgagcgag cgagcgcgca gctgcctgca 120
gg 122
<210> 31
<211> 130
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 31
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgacc aaaggtcgcc cgacgcccgg gcggcctcag tgagcgagcg agcgcgcagc 120
tgcctgcagg 130
<210> 32
<211> 120
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 32
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccgggaaacc cgggcgtgcg 60
cctcagtgag cgagcgagcg cgcagagagg gagtggccaa ctccatcact aggggttcct 120
<210> 33
<211> 122
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 33
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgt cgggcgacct ttggtcgccc 60
ggcctcagtg agcgagcgag cgcgcagaga gggagtggcc aactccatca ctaggggttc 120
ct 122
<210> 34
<211> 122
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 34
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccgggcaaag cccgggcgtc 60
ggcctcagtg agcgagcgag cgcgcagaga gggagtggcc aactccatca ctaggggttc 120
ct 122
<210> 35
<211> 129
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 35
cctgcaggca gctgcgcgct cgctcgctca ctgaggcgcc cgggcgtcgg gcgacctttg 60
gtcgcccggc ctcagtgagc gagcgagcgc gcagagaggg agtggccaac tccatcacta 120
ggggttcct 129
<210> 36
<211> 101
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 36
cctgcaggca gctgcgcgct cgctcgctca ctgaggcaaa gcctcagtga gcgagcgagc 60
gcgcagagag ggagtggcca actccatcac taggggttcc t 101
<210> 37
<211> 139
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 37
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccgggcaaag cccgggcgtc 60
gggcgacttt gtcgcccggc ctcagtgagc gagcgagcgc gcagagaggg agtggccaac 120
tccatcacta ggggttcct 139
<210> 38
<211> 137
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 38
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccgggcaaag cccgggcgtc 60
gggcgatttt cgcccggcct cagtgagcga gcgagcgcgc agagagggag tggccaactc 120
catcactagg ggttcct 137
<210> 39
<211> 135
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 39
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccgggcaaag cccgggcgtc 60
gggcgtttcg cccggcctca gtgagcgagc gagcgcgcag agagggagtg gccaactcca 120
tcactagggg ttcct 135
<210> 40
<211> 133
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 40
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccgggcaaag cccgggcgtc 60
gggctttgcc cggcctcagt gagcgagcga gcgcgcagag agggagtggc caactccatc 120
actaggggtt cct 133
<210> 41
<211> 139
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 41
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccgggaaacc cgggcgtcgg 60
gcgacctttg gtcgcccggc ctcagtgagc gagcgagcgc gcagagaggg agtggccaac 120
tccatcacta ggggttcct 139
<210> 42
<211> 137
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 42
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccggaaaccg ggcgtcgggc 60
gacctttggt cgcccggcct cagtgagcga gcgagcgcgc agagagggag tggccaactc 120
catcactagg ggttcct 137
<210> 43
<211> 135
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 43
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccgaaacggg cgtcgggcga 60
cctttggtcg cccggcctca gtgagcgagc gagcgcgcag agagggagtg gccaactcca 120
tcactagggg ttcct 135
<210> 44
<211> 133
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 44
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccaaagggcg tcgggcgacc 60
tttggtcgcc cggcctcagt gagcgagcga gcgcgcagag agggagtggc caactccatc 120
actaggggtt cct 133
<210> 45
<211> 131
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 45
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc caaaggcgtc gggcgacctt 60
tggtcgcccg gcctcagtga gcgagcgagc gcgcagagag ggagtggcca actccatcac 120
taggggttcc t 131
<210> 46
<211> 129
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 46
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc aaagcgtcgg gcgacctttg 60
gtcgcccggc ctcagtgagc gagcgagcgc gcagagaggg agtggccaac tccatcacta 120
ggggttcct 129
<210> 47
<211> 127
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 47
cctgcaggca gctgcgcgct cgctcgctca ctgaggccga aacgtcgggc gacctttggt 60
cgcccggcct cagtgagcga gcgagcgcgc agagagggag tggccaactc catcactagg 120
ggttcct 127
<210> 48
<211> 122
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 48
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgggcgacc aaaggtcgcc cgacggcctc agtgagcgag cgagcgcgca gctgcctgca 120
gg 122
<210> 49
<211> 12
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 49
cgatcgttcg at 12
<210> 50
<211> 12
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 50
atcgaaccat cg 12
<210> 51
<211> 12
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 51
atcgaacgat cg 12
<210> 52
<211> 165
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 52
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg 60
ccgcccgggc aaagcccggg cgtcgggcga cctttggtcg cccggcctca gtgagcgagc 120
gagcgcgcag agagggagtg gccaactcca tcactagggg ttcct 165
<210> 53
<211> 140
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 53
cccctagtga tggagttggc cactccctct ctgcgcgctc gctcgctcac tgaggccgcc 60
cgggcaaagc ccgggcgtcg ggcgaccttt ggtcgcccgg cctcagtgag cgagcgagcg 120
cgcagagaga tcactagggg 140
<210> 54
<211> 91
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 54
gcgcgctcgc tcgctcactg aggccgcccg ggcaaagccc gggcgtcggg cgacctttgg 60
tcgcccggcc tcagtgagcg agcgagcgcg c 91
<210> 55
<211> 91
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 55
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgcc cgggctttgc 60
ccgggcggcc tcagtgagcg agcgagcgcg c 91
<210> 56
<211> 1662
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 56
gccgccacca tggaagacgc caaaaacata aagaaaggcc cggcgccatt ctatccgctg 60
gaagatggaa ccgctggaga gcaactgcat aaggctatga agagatacgc cctggttcct 120
ggaacaattg cttttacaga tgcacatatc gaggtggaca tcacttacgc tgagtacttc 180
gaaatgtccg ttcggttggc agaagctatg aaacgatatg ggctgaatac aaatcacaga 240
atcgtcgtat gcagtgaaaa ctctcttcaa ttctttatgc cggtgttggg cgcgttattt 300
atcggagttg cagttgcgcc cgcgaacgac atttataatg aacgtgaatt gctcaacagt 360
atgggcattt cgcagcctac cgtggtgttc gtttccaaaa aggggttgca aaaaattttg 420
aacgtgcaaa aaaagctccc aatcatccaa aaaattatta tcatggattc taaaacggat 480
taccagggat ttcagtcgat gtacacgttc gtcacatctc atctacctcc cggttttaat 540
gaatacgatt ttgtgccaga gtccttcgat agggacaaga caattgcact gatcatgaac 600
tcctctggat ctactggtct gcctaaaggt gtcgctctgc ctcatagaac tgcctgcgtg 660
agattctcgc atgccagaga tcctattttt ggcaatcaaa tcattccgga tactgcgatt 720
ttaagtgttg ttccattcca tcacggtttt ggaatgttta ctacactcgg atatttgata 780
tgtggatttc gagtcgtctt aatgtataga tttgaagaag agctgtttct gaggagcctt 840
caggattaca agattcaaag tgcgctgctg gtgccaaccc tattctcctt cttcgccaaa 900
agcactctga ttgacaaata cgatttatct aatttacacg aaattgcttc tggtggcgct 960
cccctctcta aggaagtcgg ggaagcggtt gccaagaggt tccatctgcc aggtatcagg 1020
caaggatatg ggctcactga gactacatca gctattctga ttacacccga gggggatgat 1080
aaaccgggcg cggtcggtaa agttgttcca ttttttgaag cgaaggttgt ggatctggat 1140
accgggaaaa cgctgggcgt taatcaaaga ggcgaactgt gtgtgagagg tcctatgatt 1200
atgtccggtt atgtaaacaa tccggaagcg accaacgcct tgattgacaa ggatggatgg 1260
ctacattctg gagacatagc ttactgggac gaagacgaac acttcttcat cgttgaccgc 1320
ctgaagtctc tgattaagta caaaggctat caggtggctc ccgctgaatt ggaatccatc 1380
ttgctccaac accccaacat cttcgacgca ggtgtcgcag gtcttcccga cgatgacgcc 1440
ggtgaacttc ccgccgccgt tgttgttttg gagcacggaa agacgatgac ggaaaaagag 1500
atcgtggatt acgtcgccag tcaagtaaca accgcgaaaa agttgcgcgg aggagttgtg 1560
tttgtggacg aagtaccgaa aggtcttacc ggaaaactcg acgcaagaaa aatcagagag 1620
atcctcataa aggccaagaa gggcggaaag atcgccgtgt aa 1662
<210> 57
<211> 453
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полипептид
<220>
<221> MOD_RES
<222> (1)..(1)
<223> Любая аминокислота
<400> 57
Xaa Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ala Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Phe Asp Gly Thr Lys Lys Tyr Tyr Thr Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Thr Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Arg Gly Ile Gly Ala Arg Arg Gly Pro Tyr Tyr Met Asp
100 105 110
Val Trp Gly Lys Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys
115 120 125
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
130 135 140
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
145 150 155 160
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
165 170 175
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
180 185 190
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
195 200 205
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro
210 215 220
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
225 230 235 240
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
245 250 255
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
260 265 270
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
275 280 285
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
290 295 300
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
305 310 315 320
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
325 330 335
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
340 345 350
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly
450
<210> 58
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полипептид
<400> 58
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 59
<211> 1310
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 59
ggagccgaga gtaattcata caaaaggagg gatcgccttc gcaaggggag agcccaggga 60
ccgtccctaa attctcacag acccaaatcc ctgtagccgc cccacgacag cgcgaggagc 120
atgcgctcag ggctgagcgc ggggagagca gagcacacaa gctcatagac cctggtcgtg 180
ggggggagga ccggggagct ggcgcggggc aaactgggaa agcggtgtcg tgtgctggct 240
ccgccctctt cccgagggtg ggggagaacg gtatataagt gcggcagtcg ccttggacgt 300
tctttttcgc aacgggtttg ccgtcagaac gcaggtgagg ggcgggtgtg gcttccgcgg 360
gccgccgagc tggaggtcct gctccgagcg ggccgggccc cgctgtcgtc ggcggggatt 420
agctgcgagc attcccgctt cgagttgcgg gcggcgcggg aggcagagtg cgaggcctag 480
cggcaacccc gtagcctcgc ctcgtgtccg gcttgaggcc tagcgtggtg tccgcgccgc 540
cgccgcgtgc tactccggcc gcactctggt cttttttttt tttgttgttg ttgccctgct 600
gccttcgatt gccgttcagc aataggggct aacaaaggga gggtgcgggg cttgctcgcc 660
cggagcccgg agaggtcatg gttggggagg aatggaggga caggagtggc ggctggggcc 720
cgcccgcctt cggagcacat gtccgacgcc acctggatgg ggcgaggcct ggggtttttc 780
ccgaagcaac caggctgggg ttagcgtgcc gaggccatgt ggccccagca cccggcacga 840
tctggcttgg cggcgccgcg ttgccctgcc tccctaacta gggtgaggcc atcccgtccg 900
gcaccagttg cgtgcgtgga aagatggccg ctcccgggcc ctgttgcaag gagctcaaaa 960
tggaggacgc ggcagcccgg tggagcgggc gggtgagtca cccacacaaa ggaagagggc 1020
ctggtccctc accggctgct gcttcctgtg accccgtggt cctatcggcc gcaatagtca 1080
cctcgggctt ttgagcacgg ctagtcgcgg cggggggagg ggatgtaatg gcgttggagt 1140
ttgttcacat ttggtgggtg gagactagtc aggccagcct ggcgctggaa gtcatttttg 1200
gaatttgtcc ccttgagttt tgagcggagc taattctcgg gcttcttagc ggttcaaagg 1260
tatcttttaa accctttttt aggtgttgtg aaaaccaccg ctaattcaaa 1310
<210> 60
<211> 16
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 60
gcgcgctcgc tcgctc 16
<210> 61
<211> 6
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 61
ggttga 6
<210> 62
<211> 4
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 62
agtt 4
<210> 63
<211> 6
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 63
ggttgg 6
<210> 64
<211> 6
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 64
agttgg 6
<210> 65
<211> 6
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 65
agttga 6
<210> 66
<211> 6
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 66
rrttrr 6
<210> 67
<211> 581
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 67
gagcatctta ccgccattta ttcccatatt tgttctgttt ttcttgattt gggtatacat 60
ttaaatgtta ataaaacaaa atggtggggc aatcatttac atttttaggg atatgtaatt 120
actagttcag gtgtattgcc acaagacaaa catgttaaga aactttcccg ttatttacgc 180
tctgttcctg ttaatcaacc tctggattac aaaatttgtg aaagattgac tgatattctt 240
aactatgttg ctccttttac gctgtgtgga tatgctgctt tatagcctct gtatctagct 300
attgcttccc gtacggcttt cgttttctcc tccttgtata aatcctggtt gctgtctctt 360
ttagaggagt tgtggcccgt tgtccgtcaa cgtggcgtgg tgtgctctgt gtttgctgac 420
gcaaccccca ctggctgggg cattgccacc acctgtcaac tcctttctgg gactttcgct 480
ttccccctcc cgatcgccac ggcagaactc atcgccgcct gccttgcccg ctgctggaca 540
ggggctaggt tgctgggcac tgataattcc gtggtgttgt c 581
<210> 68
<211> 225
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 68
tgtgccttct agttgccagc catctgttgt ttgcccctcc cccgtgcctt ccttgaccct 60
ggaaggtgcc actcccactg tcctttccta ataaaatgag gaaattgcat cgcattgtct 120
gagtaggtgt cattctattc tggggggtgg ggtggggcag gacagcaagg gggaggattg 180
ggaagacaat agcaggcatg ctggggatgc ggtgggctct atggc 225
<210> 69
<211> 8
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 69
actgaggc 8
<210> 70
<211> 8
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 70
gcctcagt 8
<210> 71
<211> 16
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 71
gagcgagcga gcgcgc 16
<210> 72
<211> 1923
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 72
tcaatattgg ccattagcca tattattcat tggttatata gcataaatca atattggcta 60
ttggccattg catacgttgt atctatatca taatatgtac atttatattg gctcatgtcc 120
aatatgaccg ccatgttggc attgattatt gactagttat taatagtaat caattacggg 180
gtcattagtt catagcccat atatggagtt ccgcgttaca taacttacgg taaatggccc 240
gcctggctga ccgcccaacg acccccgccc attgacgtca ataatgacgt atgttcccat 300
agtaacgcca atagggactt tccattgacg tcaatgggtg gagtatttac ggtaaactgc 360
ccacttggca gtacatcaag tgtatcatat gccaagtccg ccccctattg acgtcaatga 420
cggtaaatgg cccgcctggc attatgccca gtacatgacc ttacgggact ttcctacttg 480
gcagtacatc tacgtattag tcatcgctat taccatggtc gaggtgagcc ccacgttctg 540
cttcactctc cccatctccc ccccctcccc acccccaatt ttgtatttat ttatttttta 600
attattttgt gcagcgatgg gggcgggggg gggggggggg cgcgcgccag gcggggcggg 660
gcggggcgag gggcggggcg gggcgaggcg gagaggtgcg gcggcagcca atcagagcgg 720
cgcgctccga aagtttcctt ttatggcgag gcggcggcgg cggcggccct ataaaaagcg 780
aagcgcgcgg cgggcgggag tcgctgcgac gctgccttcg ccccgtgccc cgctccgccg 840
ccgcctcgcg ccgcccgccc cggctctgac tgaccgcgtt actcccacag gtgagcgggc 900
gggacggccc ttctcctccg ggctgtaatt agcgcttggt ttaatgacgg cttgtttctt 960
ttctgtggct gcgtgaaagc cttgaggggc tccgggaggg ccctttgtgc gggggggagc 1020
ggctcggggg gtgcgtgcgt gtgtgtgtgc gtggggagcg ccgcgtgcgg cccgcgctgc 1080
ccggcggctg tgagcgctgc gggcgcggcg cggggctttg tgcgctccgc agtgtgcgcg 1140
aggggagcgc ggccgggggc ggtgccccgc ggtgcggggg gggctgcgag gggaacaaag 1200
gctgcgtgcg gggtgtgtgc gtgggggggt gagcaggggg tgtgggcgcg gcggtcgggc 1260
tgtaaccccc ccctgcaccc ccctccccga gttgctgagc acggcccggc ttcgggtgcg 1320
gggctccgta cggggcgtgg cgcggggctc gccgtgccgg gcggggggtg gcggcaggtg 1380
ggggtgccgg gcggggcggg gccgcctcgg gccggggagg gctcggggga ggggcgcggc 1440
ggcccccgga gcgccggcgg ctgtcgaggc gcggcgagcc gcagccattg ccttttatgg 1500
taatcgtgcg agagggcgca gggacttcct ttgtcccaaa tctgtgcgga gccgaaatct 1560
gggaggcgcc gccgcacccc ctctagcggg cgcggggcga agcggtgcgg cgccggcagg 1620
aaggaaatgg gcggggaggg ccttcgtgcg tcgccgcgcc gccgtcccct tctccctctc 1680
cagcctcggg gctgtccgcg gggggacggc tgccttcggg ggggacgggg cagggcgggg 1740
ttcggcttct ggcgtgtgac cggcggctct agagcctctg ctaaccatgt tttagccttc 1800
ttctttttcc tacagctcct gggcaacgtg ctggttattg tgctgtctca tcatttgtcg 1860
acagaattcc tcgaagatcc gaaggggttc aagcttggca ttccggtact gttggtaaag 1920
cca 1923
<210> 73
<211> 1272
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 73
aggctcagag gcacacagga gtttctgggc tcaccctgcc cccttccaac ccctcagttc 60
ccatcctcca gcagctgttt gtgtgctgcc tctgaagtcc acactgaaca aacttcagcc 120
tactcatgtc cctaaaatgg gcaaacattg caagcagcaa acagcaaaca cacagccctc 180
cctgcctgct gaccttggag ctggggcaga ggtcagagac ctctctgggc ccatgccacc 240
tccaacatcc actcgacccc ttggaatttc ggtggagagg agcagaggtt gtcctggcgt 300
ggtttaggta gtgtgagagg gtccgggttc aaaaccactt gctgggtggg gagtcgtcag 360
taagtggcta tgccccgacc ccgaagcctg tttccccatc tgtacaatgg aaatgataaa 420
gacgcccatc tgatagggtt tttgtggcaa ataaacattt ggtttttttg ttttgttttg 480
ttttgttttt tgagatggag gtttgctctg tcgcccaggc tggagtgcag tgacacaatc 540
tcatctcacc acaaccttcc cctgcctcag cctcccaagt agctgggatt acaagcatgt 600
gccaccacac ctggctaatt ttctattttt agtagagacg ggtttctcca tgttggtcag 660
cctcagcctc ccaagtaact gggattacag gcctgtgcca ccacacccgg ctaatttttt 720
ctatttttga cagggacggg gtttcaccat gttggtcagg ctggtctaga ggtaccggat 780
cttgctacca gtggaacagc cactaaggat tctgcagtga gagcagaggg ccagctaagt 840
ggtactctcc cagagactgt ctgactcacg ccaccccctc caccttggac acaggacgct 900
gtggtttctg agccaggtac aatgactcct ttcggtaagt gcagtggaag ctgtacactg 960
cccaggcaaa gcgtccgggc agcgtaggcg ggcgactcag atcccagcca gtggacttag 1020
cccctgtttg ctcctccgat aactggggtg accttggtta atattcacca gcagcctccc 1080
ccgttgcccc tctggatcca ctgcttaaat acggacgagg acagggccct gtctcctcag 1140
cttcaggcac caccactgac ctgggacagt gaatccggac tctaaggtaa atataaaatt 1200
tttaagtgta taatgtgtta aactactgat tctaattgtt tctctctttt agattccaac 1260
ctttggaact ga 1272
<210> 74
<211> 1177
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 74
ggctcagagg ctcagaggca cacaggagtt tctgggctca ccctgccccc ttccaacccc 60
tcagttccca tcctccagca gctgtttgtg tgctgcctct gaagtccaca ctgaacaaac 120
ttcagcctac tcatgtccct aaaatgggca aacattgcaa gcagcaaaca gcaaacacac 180
agccctccct gcctgctgac cttggagctg gggcagaggt cagagacctc tctgggccca 240
tgccacctcc aacatccact cgaccccttg gaatttcggt ggagaggagc agaggttgtc 300
ctggcgtggt ttaggtagtg tgagagggtc cgggttcaaa accacttgct gggtggggag 360
tcgtcagtaa gtggctatgc cccgaccccg aagcctgttt ccccatctgt acaatggaaa 420
tgataaagac gcccatctga tagggttttt gtggcaaata aacatttggt ttttttgttt 480
tgttttgttt tgttttttga gatggaggtt tgctctgtcg cccaggctgg agtgcagtga 540
cacaatctca tctcaccaca accttcccct gcctcagcct cccaagtagc tgggattaca 600
agcatgtgcc accacacctg gctaattttc tatttttagt agagacgggt ttctccatgt 660
tggtcagcct cagcctccca agtaactggg attacaggcc tgtgccacca cacccggcta 720
attttttcta tttttgacag ggacggggtt tcaccatgtt ggtcaggctg gtctagaggt 780
accggatctt gctaccagtg gaacagccac taaggattct gcagtgagag cagagggcca 840
gctaagtggt actctcccag agactgtctg actcacgcca ccccctccac cttggacaca 900
ggacgctgtg gtttctgagc caggtacaat gactcctttc ggtaagtgca gtggaagctg 960
tacactgccc aggcaaagcg tccgggcagc gtaggcgggc gactcagatc ccagccagtg 1020
gacttagccc ctgtttgctc ctccgataac tggggtgacc ttggttaata ttcaccagca 1080
gcctcccccg ttgcccctct ggatccactg cttaaatacg gacgaggaca gggccctgtc 1140
tcctcagctt caggcaccac cactgacctg ggacagt 1177
<210> 75
<211> 547
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 75
ccctaaaatg ggcaaacatt gcaagcagca aacagcaaac acacagccct ccctgcctgc 60
tgaccttgga gctggggcag aggtcagaga cctctctggg cccatgccac ctccaacatc 120
cactcgaccc cttggaattt ttcggtggag aggagcagag gttgtcctgg cgtggtttag 180
gtagtgtgag aggggaatga ctcctttcgg taagtgcagt ggaagctgta cactgcccag 240
gcaaagcgtc cgggcagcgt aggcgggcga ctcagatccc agccagtgga cttagcccct 300
gtttgctcct ccgataactg gggtgacctt ggttaatatt caccagcagc ctcccccgtt 360
gcccctctgg atccactgct taaatacgga cgaggacagg gccctgtctc ctcagcttca 420
ggcaccacca ctgacctggg acagtgaatc cggactctaa ggtaaatata aaatttttaa 480
gtgtataatg tgttaaacta ctgattctaa ttgtttctct cttttagatt ccaacctttg 540
gaactga 547
<210> 76
<211> 556
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 76
ccctaaaatg ggcaaacatt gcaagcagca aacagcaaac acacagccct ccctgcctgc 60
tgaccttgga gctggggcag aggtcagaga cctctctggg cccatgccac ctccaacatc 120
cactcgaccc cttggaattt cggtggagag gagcagaggt tgtcctggcg tggtttaggt 180
agtgtgagag gggaatgact cctttcggta agtgcagtgg aagctgtaca ctgcccaggc 240
aaagcgtccg ggcagcgtag gcgggcgact cagatcccag ccagtggact tagcccctgt 300
ttgctcctcc gataactggg gtgaccttgg ttaatattca ccagcagcct cccccgttgc 360
ccctctggat ccactgctta aatacggacg aggacactcg agggccctgt ctcctcagct 420
tcaggcacca ccactgacct gggacagtga atccggacat cgattctaag gtaaatataa 480
aatttttaag tgtataattt gttaaactac tgattctaat tgtttctctc ttttagattc 540
caacctttgg aactga 556
<210> 77
<211> 1179
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 77
ggctccggtg cccgtcagtg ggcagagcgc acatcgccca cagtccccga gaagttgggg 60
ggaggggtcg gcaattgaac cggtgcctag agaaggtggc gcggggtaaa ctgggaaagt 120
gatgtcgtgt actggctccg cctttttccc gagggtgggg gagaaccgta tataagtgca 180
gtagtcgccg tgaacgttct ttttcgcaac gggtttgccg ccagaacaca ggtaagtgcc 240
gtgtgtggtt cccgcgggcc tggcctcttt acgggttatg gcccttgcgt gccttgaatt 300
acttccacct ggctgcagta cgtgattctt gatcccgagc ttcgggttgg aagtgggtgg 360
gagagttcga ggccttgcgc ttaaggagcc ccttcgcctc gtgcttgagt tgaggcctgg 420
cctgggcgct ggggccgccg cgtgcgaatc tggtggcacc ttcgcgcctg tctcgctgct 480
ttcgataagt ctctagccat ttaaaatttt tgatgacctg ctgcgacgct ttttttctgg 540
caagatagtc ttgtaaatgc gggccaagat ctgcacactg gtatttcggt ttttggggcc 600
gcgggcggcg acggggcccg tgcgtcccag cgcacatgtt cggcgaggcg gggcctgcga 660
gcgcggccac cgagaatcgg acgggggtag tctcaagctg gccggcctgc tctggtgcct 720
ggtctcgcgc cgccgtgtat cgccccgccc tgggcggcaa ggctggcccg gtcggcacca 780
gttgcgtgag cggaaagatg gccgcttccc ggccctgctg cagggagctc aaaatggagg 840
acgcggcgct cgggagagcg ggcgggtgag tcacccacac aaaggaaaag ggcctttccg 900
tcctcagccg tcgcttcatg tgactccacg gagtaccggg cgccgtccag gcacctcgat 960
tagttctcga gcttttggag tacgtcgtct ttaggttggg gggaggggtt ttatgcgatg 1020
gagtttcccc acactgagtg ggtggagact gaagttaggc cagcttggca cttgatgtaa 1080
ttctccttgg aatttgccct ttttgagttt ggatcttggt tcattctcaa gcctcagaca 1140
gtggttcaaa gtttttttct tccatttcag gtgtcgtga 1179
<210> 78
<211> 141
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 78
aataaacgat aacgccgttg gtggcgtgag gcatgtaaaa ggttacatca ttatcttgtt 60
cgccatccgg ttggtataaa tagacgttca tgttggtttt tgtttcagtt gcaagttggc 120
tgcggcgcgc gcagcacctt t 141
<210> 79
<211> 317
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 79
ggtgtggaaa gtccccaggc tccccagcag gcagaagtat gcaaagcatg catctcaatt 60
agtcagcaac caggtgtgga aagtccccag gctccccagc aggcagaagt atgcaaagca 120
tgcatctcaa ttagtcagca accatagtcc cgcccctaac tccgcccatc ccgcccctaa 180
ctccgcccag ttccgcccat tctccgcccc atggctgact aatttttttt atttatgcag 240
aggccgaggc cgcctcggcc tctgagctat tccagaagta gtgaggaggc ttttttggag 300
gcctaggctt ttgcaaa 317
<210> 80
<211> 241
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 80
gagggcctat ttcccatgat tccttcatat ttgcatatac gatacaaggc tgttagagag 60
ataattggaa ttaatttgac tgtaaacaca aagatattag tacaaaatac gtgacgtaga 120
aagtaataat ttcttgggta gtttgcagtt ttaaaattat gttttaaaat ggactatcat 180
atgcttaccg taacttgaaa gtatttcgat ttcttggctt tatatatctt gtggaaagga 240
c 241
<210> 81
<211> 215
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 81
gaacgctgac gtcatcaacc cgctccaagg aatcgcgggc ccagtgtcac taggcgggaa 60
cacccagcgc gcgtgcgccc tggcaggaag atggctgtga gggacagggg agtggcgccc 120
tgcaatattt gcatgtcgct atgtgttctg ggaaatcacc ataaacgtga aatgtctttg 180
gatttgggaa tcgtataaga actgtatgag accac 215
<210> 82
<211> 546
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 82
ccctaaaatg ggcaaacatt gcaagcagca aacagcaaac acacagccct ccctgcctgc 60
tgaccttgga gctggggcag aggtcagaga cctctctggg cccatgccac ctccaacatc 120
cactcgaccc cttggaattt ttcggtggag aggagcagag gttgtcctgg cgtggtttag 180
gtagtgtgag aggggaatga ctcctttcgg taagtgcagt ggaagctgta cactgcccag 240
gcaaagcgtc cgggcagcgt aggcgggcga ctcagatccc agccagtgga cttagcccct 300
gtttgctcct ccgataactg gggtgacctt ggttaatatt caccagcagc ctcccccgtt 360
gcccctctgg atccactgct taaatacgga cgaggacagg gccctgtctc ctcagcttca 420
ggcaccacca ctgacctggg acagtgaatc cggactctaa ggtaaatata aaatttttaa 480
gtgtataatg tgttaaacta ctgattctaa ttgtttctct cttttagatt ccaacctttg 540
gaactg 546
<210> 83
<211> 576
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 83
tagtaatcaa ttacggggtc attagttcat agcccatata tggagttccg cgttacataa 60
cttacggtaa atggcccgcc tggctgaccg cccaacgacc cccgcccatt gacgtcaata 120
atgacgtatg ttcccatagt aacgccaata gggactttcc attgacgtca atgggtggag 180
tatttacggt aaactgccca cttggcagta catcaagtgt atcatatgcc aagtacgccc 240
cctattgacg tcaatgacgg taaatggccc gcctggcatt atgcccagta catgacctta 300
tgggactttc ctacttggca gtacatctac gtattagtca tcgctattac catggtgatg 360
cggttttggc agtacatcaa tgggcgtgga tagcggtttg actcacgggg atttccaagt 420
ctccacccca ttgacgtcaa tgggagtttg ttttggcacc aaaatcaacg ggactttcca 480
aaatgtcgta acaactccgc cccattgacg caaatgggcg gtaggcgtgt acggtgggag 540
gtctatataa gcagagctgg tttagtgaac cgtcag 576
<210> 84
<211> 150
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 84
ataaacgata acgccgttgg tggcgtgagg catgtaaaag gttacatcat tatcttgttc 60
gccatccggt tggtataaat agacgttcat gttggttttt gtttcagttg caagttggct 120
gcggcgcgcg cagcaccttt gcggccatct 150
<210> 85
<211> 1313
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 85
ggagccgaga gtaattcata caaaaggagg gatcgccttc gcaaggggag agcccaggga 60
ccgtccctaa attctcacag acccaaatcc ctgtagccgc cccacgacag cgcgaggagc 120
atgcgcccag ggctgagcgc gggtagatca gagcacacaa gctcacagtc cccggcggtg 180
gggggagggg cgcgctgagc gggggccagg gagctggcgc ggggcaaact gggaaagtgg 240
tgtcgtgtgc tggctccgcc ctcttcccga gggtggggga gaacggtata taagtgcggt 300
agtcgccttg gacgttcttt ttcgcaacgg gtttgccgtc agaacgcagg tgagtggcgg 360
gtgtggcttc cgcgggcccc ggagctggag ccctgctctg agcgggccgg gctgatatgc 420
gagtgtcgtc cgcagggttt agctgtgagc attcccactt cgagtggcgg gcggtgcggg 480
ggtgagagtg cgaggcctag cggcaacccc gtagcctcgc ctcgtgtccg gcttgaggcc 540
tagcgtggtg tccgccgccg cgtgccactc cggccgcact atgcgttttt tgtccttgct 600
gccctcgatt gccttccagc agcatgggct aacaaaggga gggtgtgggg ctcactctta 660
aggagcccat gaagcttacg ttggatagga atggaagggc aggaggggcg actggggccc 720
gcccgccttc ggagcacatg tccgacgcca cctggatggg gcgaggcctg tggctttccg 780
aagcaatcgg gcgtgagttt agcctacctg ggccatgtgg ccctagcact gggcacggtc 840
tggcctggcg gtgccgcgtt cccttgcctc ccaacaaggg tgaggccgtc ccgcccggca 900
ccagttgctt gcgcggaaag atggccgctc ccggggccct gttgcaagga gctcaaaatg 960
gaggacgcgg cagcccggtg gagcgggcgg gtgagtcacc cacacaaagg aagagggcct 1020
tgcccctcgc cggccgctgc ttcctgtgac cccgtggtct atcggccgca tagtcacctc 1080
gggcttctct tgagcaccgc tcgtcgcggc ggggggaggg gatctaatgg cgttggagtt 1140
tgttcacatt tggtgggtgg agactagtca ggccagcctg gcgctggaag tcattcttgg 1200
aatttgcccc tttgagtttg gagcgaggct aattctcaag cctcttagcg gttcaaaggt 1260
attttctaaa cccgtttcca ggtgttgtga aagccaccgc taattcaaag caa 1313
<210> 86
<211> 213
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 86
taagatacat tgatgagttt ggacaaacca caactagaat gcagtgaaaa aaatgcttta 60
tttgtgaaat ttgtgatgct attgctttat ttgtaaccat tataagctgc aataaacaag 120
ttaacaacaa caattgcatt cattttatgt ttcaggttca gggggaggtg tgggaggttt 180
tttaaagcaa gtaaaacctc tacaaatgtg gta 213
<210> 87
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический пептид
<400> 87
Pro Lys Lys Lys Arg Lys Val
1 5
<210> 88
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический пептид
<400> 88
Met Asp Trp Thr Trp Arg Ile Leu Phe Leu Val Ala Ala Ala Thr Gly
1 5 10 15
Ala His Ser
<210> 89
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический пептид
<400> 89
Met Leu Pro Ser Gln Leu Ile Gly Phe Leu Leu Leu Trp Val Pro Ala
1 5 10 15
Ser Arg Gly
<210> 90
<211> 7
<212> БЕЛОК
<213> Обезьяний вирус 40
<400> 90
Pro Lys Lys Lys Arg Lys Val
1 5
<210> 91
<211> 21
<212> ДНК
<213> Обезьяний вирус 40
<400> 91
cccaagaaga agaggaaggt g 21
<210> 92
<211> 16
<212> БЕЛОК
<213> Неизвестный
<220>
<223> Описание неизвестного: двусоставная последовательность
NLS нуклеоплазмина
<400> 92
Lys Arg Pro Ala Ala Thr Lys Lys Ala Gly Gln Ala Lys Lys Lys Lys
1 5 10 15
<210> 93
<211> 9
<212> БЕЛОК
<213> Неизвестный
<220>
<223> Описание неизвестного: последовательность NLS C-myc
<400> 93
Pro Ala Ala Lys Arg Val Lys Leu Asp
1 5
<210> 94
<211> 11
<212> БЕЛОК
<213> Неизвестный
<220>
<223> Описание неизвестного: последовательность NLS C-myc
<400> 94
Arg Gln Arg Arg Asn Glu Leu Lys Arg Ser Pro
1 5 10
<210> 95
<211> 38
<212> БЕЛОК
<213> Homo sapiens
<400> 95
Asn Gln Ser Ser Asn Phe Gly Pro Met Lys Gly Gly Asn Phe Gly Gly
1 5 10 15
Arg Ser Ser Gly Pro Tyr Gly Gly Gly Gly Gln Tyr Phe Ala Lys Pro
20 25 30
Arg Asn Gln Gly Gly Tyr
35
<210> 96
<211> 42
<212> БЕЛОК
<213> Неизвестный
<220>
<223> Описание неизвестного: домен IBB из последовательности импортина-альфа
<400> 96
Arg Met Arg Ile Glx Phe Lys Asn Lys Gly Lys Asp Thr Ala Glu Leu
1 5 10 15
Arg Arg Arg Arg Val Glu Val Ser Val Glu Leu Arg Lys Ala Lys Lys
20 25 30
Asp Glu Gln Ile Leu Lys Arg Arg Asn Val
35 40
<210> 97
<211> 8
<212> БЕЛОК
<213> Неизвестный
<220>
<223> Описание неизвестного: последовательность Т-белка миомы
<400> 97
Val Ser Arg Lys Arg Pro Arg Pro
1 5
<210> 98
<211> 8
<212> БЕЛОК
<213> Неизвестный
<220>
<223> Описание неизвестного: последовательность Т-белка миомы
<400> 98
Pro Pro Lys Lys Ala Arg Glu Asp
1 5
<210> 99
<211> 8
<212> БЕЛОК
<213> Homo sapiens
<400> 99
Pro Gln Pro Lys Lys Lys Pro Leu
1 5
<210> 100
<211> 12
<212> БЕЛОК
<213> Mus musculus
<400> 100
Ser Ala Leu Ile Lys Lys Lys Lys Lys Met Ala Pro
1 5 10
<210> 101
<211> 70
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 101
gcgcgctcgc tcgctcactg aggccgcccg ggaaacccgg gcgtgcgcct cagtgagcga 60
gcgagcgcgc 70
<210> 102
<211> 70
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 102
gcgcgctcgc tcgctcactg aggcgcacgc ccgggtttcc cgggcggcct cagtgagcga 60
gcgagcgcgc 70
<210> 103
<211> 72
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 103
gcgcgctcgc tcgctcactg aggccgtcgg gcgacctttg gtcgcccggc ctcagtgagc 60
gagcgagcgc gc 72
<210> 104
<211> 72
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 104
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacggc ctcagtgagc 60
gagcgagcgc gc 72
<210> 105
<211> 72
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 105
gcgcgctcgc tcgctcactg aggccgcccg ggcaaagccc gggcgtcggc ctcagtgagc 60
gagcgagcgc gc 72
<210> 106
<211> 72
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 106
gcgcgctcgc tcgctcactg aggccgacgc ccgggctttg cccgggcggc ctcagtgagc 60
gagcgagcgc gc 72
<210> 107
<211> 83
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 107
gcgcgctcgc tcgctcactg aggccgcccg ggcaaagccc gggcgtcggg ctttgcccgg 60
cctcagtgag cgagcgagcg cgc 83
<210> 108
<211> 83
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 108
gcgcgctcgc tcgctcactg aggccgggca aagcccgacg cccgggcttt gcccgggcgg 60
cctcagtgag cgagcgagcg cgc 83
<210> 109
<211> 77
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 109
gcgcgctcgc tcgctcactg aggccgaaac gtcgggcgac ctttggtcgc ccggcctcag 60
tgagcgagcg agcgcgc 77
<210> 110
<211> 77
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 110
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgtt tcggcctcag 60
tgagcgagcg agcgcgc 77
<210> 111
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 111
gcgcgctcgc tcgctcactg aggcaaagcc tcagtgagcg agcgagcgcg c 51
<210> 112
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 112
gcgcgctcgc tcgctcactg aggctttgcc tcagtgagcg agcgagcgcg c 51
<210> 113
<211> 80
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 113
gcgcgctcgc tcgctcactg aggccgcccg ggcgtcgggc gacctttggt cgcccggcct 60
cagtgagcga gcgagcgcgc 80
<210> 114
<211> 80
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 114
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgcc cgggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 115
<211> 79
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 115
gcgcgctcgc tcgctcactg aggcgcccgg gcgtcgggcg acctttggtc gcccggcctc 60
agtgagcgag cgagcgcgc 79
<210> 116
<211> 79
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 116
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgcc cgggcgcctc 60
agtgagcgag cgagcgcgc 79
<210> 117
<211> 5
<212> БЕЛОК
<213> Вирус гриппа
<400> 117
Asp Arg Leu Arg Arg
1 5
<210> 118
<211> 7
<212> БЕЛОК
<213> Вирус гриппа
<400> 118
Pro Lys Gln Lys Lys Arg Lys
1 5
<210> 119
<211> 10
<212> БЕЛОК
<213> Вирус гепатита дельта
<400> 119
Arg Lys Leu Lys Lys Lys Ile Lys Lys Leu
1 5 10
<210> 120
<211> 10
<212> БЕЛОК
<213> Mus musculus
<400> 120
Arg Glu Lys Lys Lys Phe Leu Lys Arg Arg
1 5 10
<210> 121
<211> 20
<212> БЕЛОК
<213> Homo sapiens
<400> 121
Lys Arg Lys Gly Asp Glu Val Asp Gly Val Asp Glu Val Ala Lys Lys
1 5 10 15
Lys Ser Lys Lys
20
<210> 122
<211> 17
<212> БЕЛОК
<213> Homo sapiens
<400> 122
Arg Lys Cys Leu Gln Ala Gly Met Asn Leu Glu Ala Arg Lys Thr Lys
1 5 10 15
Lys
<210> 123
<211> 8
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 123
gtttaaac 8
<210> 124
<211> 8
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 124
ttaattaa 8
<210> 125
<211> 141
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 125
aataaacgat aacgccgttg gtggcgtgag gcatgtaaaa ggttacatca ttatcttgtt 60
cgccatccgg ttggtataaa tagacgttca tgttggtttt tgtttcagtt gcaagttggc 120
tgcggcgcgc gcagcacctt t 141
<210> 126
<211> 317
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 126
ggtgtggaaa gtccccaggc tccccagcag gcagaagtat gcaaagcatg catctcaatt 60
agtcagcaac caggtgtgga aagtccccag gctccccagc aggcagaagt atgcaaagca 120
tgcatctcaa ttagtcagca accatagtcc cgcccctaac tccgcccatc ccgcccctaa 180
ctccgcccag ttccgcccat tctccgcccc atggctgact aatttttttt atttatgcag 240
aggccgaggc cgcctcggcc tctgagctat tccagaagta gtgaggaggc ttttttggag 300
gcctaggctt ttgcaaa 317
<210> 127
<211> 72
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 127
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacggc ctcagtgagc 60
gagcgagcgc gc 72
<210> 128
<211> 60
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 128
gagacagaca cactcctgct atgggtactg ctgctctggg ttccaggttc cactggtgac 60
<210> 129
<211> 1260
<212> ДНК
<213> Аденоассоциированный вирус - 2
<400> 129
atggagctgg tcgggtggct cgtggacaag gggattacct cggagaagca gtggatccag 60
gaggaccagg cctcatacat ctccttcaat gcggcctcca actcgcggtc ccaaatcaag 120
gctgccttgg acaatgcggg aaagattatg agcctgacta aaaccgcccc cgactacctg 180
gtgggccagc agcccgtgga ggacatttcc agcaatcgga tttataaaat tttggaacta 240
aacgggtacg atccccaata tgcggcttcc gtctttctgg gatgggccac gaaaaagttc 300
ggcaagagga acaccatctg gctgtttggg cctgcaacta ccgggaagac caacatcgcg 360
gaggccatag cccacactgt gcccttctac gggtgcgtaa actggaccaa tgagaacttt 420
cccttcaacg actgtgtcga caagatggtg atctggtggg aggaggggaa gatgaccgcc 480
aaggtcgtgg agtcggccaa agccattctc ggaggaagca aggtgcgcgt ggaccagaaa 540
tgcaagtcct cggcccagat agacccgact cccgtgatcg tcacctccaa caccaacatg 600
tgcgccgtga ttgacgggaa ctcaacgacc ttcgaacacc agcagccgtt gcaagaccgg 660
atgttcaaat ttgaactcac ccgccgtctg gatcatgact ttgggaaggt caccaagcag 720
gaagtcaaag actttttccg gtgggcaaag gatcacgtgg ttgaggtgga gcatgaattc 780
tacgtcaaaa agggtggagc caagaaaaga cccgccccca gtgacgcaga tataagtgag 840
cccaaacggg tgcgcgagtc agttgcgcag ccatcgacgt cagacgcgga agcttcgatc 900
aactacgcag acaggtacca aaacaaatgt tctcgtcacg tgggcatgaa tctgatgctg 960
tttccctgca gacaatgcga gagaatgaat cagaattcaa atatctgctt cactcacgga 1020
cagaaagact gtttagagtg ctttcccgtg tcagaatctc aacccgtttc tgtcgtcaaa 1080
aaggcgtatc agaaactgtg ctacattcat catatcatgg gaaaggtgcc agacgcttgc 1140
actgcctgcg atctggtcaa tgtggatttg gatgactgca tctttgaaca ataaatgatt 1200
taaatcaggt atggctgccg atggttatct tccagattgg ctcgaggaca ctctctctga 1260
<210> 130
<211> 1932
<212> ДНК
<213> Аденоассоциированный вирус - 2
<400> 130
atgccggggt tttacgagat tgtgattaag gtccccagcg accttgacga gcatctgccc 60
ggcatttctg acagctttgt gaactgggtg gccgagaagg aatgggagtt gccgccagat 120
tctgacatgg atctgaatct gattgagcag gcacccctga ccgtggccga gaagctgcag 180
cgcgactttc tgacggaatg gcgccgtgtg agtaaggccc cggaggccct tttctttgtg 240
caatttgaga agggagagag ctacttccac atgcacgtgc tcgtggaaac caccggggtg 300
aaatccatgg ttttgggacg tttcctgagt cagattcgcg aaaaactgat tcagagaatt 360
taccgcggga tcgagccgac tttgccaaac tggttcgcgg tcacaaagac cagaaatggc 420
gccggaggcg ggaacaaggt ggtggatgag tgctacatcc ccaattactt gctccccaaa 480
acccagcctg agctccagtg ggcgtggact aatatggaac agtatttaag cgcctgtttg 540
aatctcacgg agcgtaaacg gttggtggcg cagcatctga cgcacgtgtc gcagacgcag 600
gagcagaaca aagagaatca gaatcccaat tctgatgcgc cggtgatcag atcaaaaact 660
tcagccaggt acatggagct ggtcgggtgg ctcgtggaca aggggattac ctcggagaag 720
cagtggatcc aggaggacca ggcctcatac atctccttca atgcggcctc caactcgcgg 780
tcccaaatca aggctgcctt ggacaatgcg ggaaagatta tgagcctgac taaaaccgcc 840
cccgactacc tggtgggcca gcagcccgtg gaggacattt ccagcaatcg gatttataaa 900
attttggaac taaacgggta cgatccccaa tatgcggctt ccgtctttct gggatgggcc 960
acgaaaaagt tcggcaagag gaacaccatc tggctgtttg ggcctgcaac taccgggaag 1020
accaacatcg cggaggccat agcccacact gtgcccttct acgggtgcgt aaactggacc 1080
aatgagaact ttcccttcaa cgactgtgtc gacaagatgg tgatctggtg ggaggagggg 1140
aagatgaccg ccaaggtcgt ggagtcggcc aaagccattc tcggaggaag caaggtgcgc 1200
gtggaccaga aatgcaagtc ctcggcccag atagacccga ctcccgtgat cgtcacctcc 1260
aacaccaaca tgtgcgccgt gattgacggg aactcaacga ccttcgaaca ccagcagccg 1320
ttgcaagacc ggatgttcaa atttgaactc acccgccgtc tggatcatga ctttgggaag 1380
gtcaccaagc aggaagtcaa agactttttc cggtgggcaa aggatcacgt ggttgaggtg 1440
gagcatgaat tctacgtcaa aaagggtgga gccaagaaaa gacccgcccc cagtgacgca 1500
gatataagtg agcccaaacg ggtgcgcgag tcagttgcgc agccatcgac gtcagacgcg 1560
gaagcttcga tcaactacgc agacaggtac caaaacaaat gttctcgtca cgtgggcatg 1620
aatctgatgc tgtttccctg cagacaatgc gagagaatga atcagaattc aaatatctgc 1680
ttcactcacg gacagaaaga ctgtttagag tgctttcccg tgtcagaatc tcaacccgtt 1740
tctgtcgtca aaaaggcgta tcagaaactg tgctacattc atcatatcat gggaaaggtg 1800
ccagacgctt gcactgcctg cgatctggtc aatgtggatt tggatgactg catctttgaa 1860
caataaatga tttaaatcag gtatggctgc cgatggttat cttccagatt ggctcgagga 1920
cactctctct ga 1932
<210> 131
<211> 1876
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 131
cgcagccacc atggcggggt tttacgagat tgtgattaag gtccccagcg accttgacgg 60
gcatctgccc ggcatttctg acagctttgt gaactgggtg gccgagaagg aatgggagtt 120
gccgccagat tctgacatgg atctgaatct gattgagcag gcacccctga ccgtggccga 180
gaagctgcag cgcgactttc tgacggaatg gcgccgtgtg agtaaggccc cggaggccct 240
tttctttgtg caatttgaga agggagagag ctacttccac atgcacgtgc tcgtggaaac 300
caccggggtg aaatccatgg ttttgggacg tttcctgagt cagattcgcg aaaaactgat 360
tcagagaatt taccgcggga tcgagccgac tttgccaaac tggttcgcgg tcacaaagac 420
cagaaatggc gccggaggcg ggaacaaggt ggtggatgag tgctacatcc ccaattactt 480
gctccccaaa acccagcctg agctccagtg ggcgtggact aatatggaac agtatttaag 540
cgcctgtttg aatctcacgg agcgtaaacg gttggtggcg cagcatctga cgcacgtgtc 600
gcagacgcag gagcagaaca aagagaatca gaatcccaat tctgatgcgc cggtgatcag 660
atcaaaaact tcagccaggt acatggagct ggtcgggtgg ctcgtggaca aggggattac 720
ctcggagaag cagtggatcc aggaggacca ggcctcatac atctccttca atgcggcctc 780
caactcgcgg tcccaaatca aggctgcctt ggacaatgcg ggaaagatta tgagcctgac 840
taaaaccgcc cccgactacc tggtgggcca gcagcccgtg gaggacattt ccagcaatcg 900
gatttataaa attttggaac taaacgggta cgatccccaa tatgcggctt ccgtctttct 960
gggatgggcc acgaaaaagt tcggcaagag gaacaccatc tggctgtttg ggcctgcaac 1020
taccgggaag accaacatcg cggaggccat agcccacact gtgcccttct acgggtgcgt 1080
aaactggacc aatgagaact ttcccttcaa cgactgtgtc gacaagatgg tgatctggtg 1140
ggaggagggg aagatgaccg ccaaggtcgt ggagtcggcc aaagccattc tcggaggaag 1200
caaggtgcgc gtggaccaga aatgcaagtc ctcggcccag atagacccga ctcccgtgat 1260
cgtcacctcc aacaccaaca tgtgcgccgt gattgacggg aactcaacga ccttcgaaca 1320
ccagcagccg ttgcaagacc ggatgttcaa atttgaactc acccgccgtc tggatcatga 1380
ctttgggaag gtcaccaagc aggaagtcaa agactttttc cggtgggcaa aggatcacgt 1440
ggttgaggtg gagcatgaat tctacgtcaa aaagggtgga gccaagaaaa gacccgcccc 1500
cagtgacgca gatataagtg agcccaaacg ggtgcgcgag tcagttgcgc agccatcgac 1560
gtcagacgcg gaagcttcga tcaactacgc agacaggtac caaaacaaat gttctcgtca 1620
cgtgggcatg aatctgatgc tgtttccctg cagacaatgc gagagaatga atcagaattc 1680
aaatatctgc ttcactcacg gacagaaaga ctgtttagag tgctttcccg tgtcagaatc 1740
tcaacccgtt tctgtcgtca aaaaggcgta tcagaaactg tgctacattc atcatatcat 1800
gggaaaggtg ccagacgctt gcactgcctg cgatctggtc aatgtggatt tggatgactg 1860
catctttgaa caataa 1876
<210> 132
<211> 1194
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 132
atggagctgg tcgggtggct cgtggacaag gggattacct cggagaagca gtggatccag 60
gaggaccagg cctcatacat ctccttcaat gcggcctcca actcgcggtc ccaaatcaag 120
gctgccttgg acaatgcggg aaagattatg agcctgacta aaaccgcccc cgactacctg 180
gtgggccagc agcccgtgga ggacatttcc agcaatcgga tttataaaat tttggaacta 240
aacgggtacg atccccaata tgcggcttcc gtctttctgg gatgggccac gaaaaagttc 300
ggcaagagga acaccatctg gctgtttggg cctgcaacta ccgggaagac caacatcgcg 360
gaggccatag cccacactgt gcccttctac gggtgcgtaa actggaccaa tgagaacttt 420
cccttcaacg actgtgtcga caagatggtg atctggtggg aggaggggaa gatgaccgcc 480
aaggtcgtgg agtcggccaa agccattctc ggaggaagca aggtgcgcgt ggaccagaaa 540
tgcaagtcct cggcccagat agacccgact cccgtgatcg tcacctccaa caccaacatg 600
tgcgccgtga ttgacgggaa ctcaacgacc ttcgaacacc agcagccgtt gcaagaccgg 660
atgttcaaat ttgaactcac ccgccgtctg gatcatgact ttgggaaggt caccaagcag 720
gaagtcaaag actttttccg gtgggcaaag gatcacgtgg ttgaggtgga gcatgaattc 780
tacgtcaaaa agggtggagc caagaaaaga cccgccccca gtgacgcaga tataagtgag 840
cccaaacggg tgcgcgagtc agttgcgcag ccatcgacgt cagacgcgga agcttcgatc 900
aactacgcag accgctacca aaacaaatgt tctcgtcacg tgggcatgaa tctgatgctg 960
tttccctgca gacaatgcga gagaatgaat cagaattcaa atatctgctt cactcacgga 1020
cagaaagact gtttagagtg ctttcccgtg tcagaatctc aacccgtttc tgtcgtcaaa 1080
aaggcgtatc agaaactgtg ctacattcat catatcatgg gaaaggtgcc agacgcttgc 1140
actgcctgcg atctggtcaa tgtggatttg gatgactgca tctttgaaca ataa 1194
<210> 133
<211> 1876
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 133
cgcagccacc atggcggggt tttacgagat tgtgattaag gtccccagcg accttgacgg 60
gcatctgccc ggcatttctg acagctttgt gaactgggtg gccgagaagg aatgggagtt 120
gccgccagat tctgacatgg atctgaatct gattgagcag gcacccctga ccgtggccga 180
gaagctgcag cgcgactttc tgacggaatg gcgccgtgtg agtaaggccc cggaggccct 240
tttctttgtg caatttgaga agggagagag ctacttccac atgcacgtgc tcgtggaaac 300
caccggggtg aaatccatgg ttttgggacg tttcctgagt cagattcgcg aaaaactgat 360
tcagagaatt taccgcggga tcgagccgac tttgccaaac tggttcgcgg tcacaaagac 420
cagaaatggc gccggaggcg ggaacaaggt ggtggatgag tgctacatcc ccaattactt 480
gctccccaaa acccagcctg agctccagtg ggcgtggact aatatggaac agtatttaag 540
cgcctgtttg aatctcacgg agcgtaaacg gttggtggcg cagcatctga cgcacgtgtc 600
gcagacgcag gagcagaaca aagagaatca gaatcccaat tctgatgcgc cggtgatcag 660
atcaaaaact tcagccaggt acatggagct ggtcgggtgg ctcgtggaca aggggattac 720
ctcggagaag cagtggatcc aggaggacca ggcctcatac atctccttca atgcggcctc 780
caactcgcgg tcccaaatca aggctgcctt ggacaatgcg ggaaagatta tgagcctgac 840
taaaaccgcc cccgactacc tggtgggcca gcagcccgtg gaggacattt ccagcaatcg 900
gatttataaa attttggaac taaacgggta cgatccccaa tatgcggctt ccgtctttct 960
gggatgggcc acgaaaaagt tcggcaagag gaacaccatc tggctgtttg ggcctgcaac 1020
taccgggaag accaacatcg cggaggccat agcccacact gtgcccttct acgggtgcgt 1080
aaactggacc aatgagaact ttcccttcaa cgactgtgtc gacaagatgg tgatctggtg 1140
ggaggagggg aagatgaccg ccaaggtcgt ggagtcggcc aaagccattc tcggaggaag 1200
caaggtgcgc gtggaccaga aatgcaagtc ctcggcccag atagacccga ctcccgtgat 1260
cgtcacctcc aacaccaaca tgtgcgccgt gattgacggg aactcaacga ccttcgaaca 1320
ccagcagccg ttgcaagacc ggatgttcaa atttgaactc acccgccgtc tggatcatga 1380
ctttgggaag gtcaccaagc aggaagtcaa agactttttc cggtgggcaa aggatcacgt 1440
ggttgaggtg gagcatgaat tctacgtcaa aaagggtgga gccaagaaaa gacccgcccc 1500
cagtgacgca gatataagtg agcccaaacg ggtgcgcgag tcagttgcgc agccatcgac 1560
gtcagacgcg gaagcttcga tcaactacgc agacaggtac caaaacaaat gttctcgtca 1620
cgtgggcatg aatctgatgc tgtttccctg cagacaatgc gagagaatga atcagaattc 1680
aaatatctgc ttcactcacg gacagaaaga ctgtttagag tgctttcccg tgtcagaatc 1740
tcaacccgtt tctgtcgtca aaaaggcgta tcagaaactg tgctacattc atcatatcat 1800
gggaaaggtg ccagacgctt gcactgcctg cgatctggtc aatgtggatt tggatgactg 1860
catctttgaa caataa 1876
<210> 134
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 134
ctaggccgcc cgggcaaagc ccgggcgtcg ggcgaccttt ggtcgcccgg c 51
<210> 135
<211> 65
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 135
ctaggactga ggccgcccgg gcaaagcccg ggcgtcgggc gacctttggt cgcccggcct 60
cagtc 65
<210> 136
<211> 67
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 136
ggactgaggc cgcccgggca aagcccgggc gtcgggcgac ctttggtcgc ccggcctcag 60
tcctgca 67
<210> 137
<211> 41
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 137
gtgcgggcga ccaaaggtcg cccgacgccc gggcgcactc a 41
<210> 138
<211> 56
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 138
ggactgaggc cgggcgacca aaggtcgccc gacgcccggg cggcctcagt cctgca 56
<210> 139
<211> 54
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 139
ctaggactga ggccgcccgg gcgtcgggcg acctttggtc gcccggcctc agtc 54
<210> 140
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 140
ggactgaggc cgggcgacca aaggtcgccc gacggcctca gtcctgca 48
<210> 141
<211> 46
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 141
ctaggactga ggccgtcggg cgacctttgg tcgcccggcc tcagtc 46
<210> 142
<211> 67
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 142
ggactgaggc ccgggcgacc aaaggtcgcc cgacgcccgg gctttgcccg ggcgcctcag 60
tcctgca 67
<210> 143
<211> 47
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 143
atacctaggc acgcgtgtta ctagttatta atagtaatca attacgg 47
<210> 144
<211> 29
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 144
atacctaggg gccgcacgcg tgttactag 29
<210> 145
<211> 42
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 145
atacactcag tgcctgcagg cacgtggtcc ggagatccag ac 42
<210> 146
<211> 3754
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 146
cctaggtgag cgagcgagcg cgcagagagg gagtggccaa ctccatcact aggggttcct 60
tgtagttaat gattaacccg ccatgctact tatcgcggcc gctcaatatt ggccattagc 120
catattattc attggttata tagcataaat caatattggc tattggccat tgcatacgtt 180
gtatctatat cataatatgt acatttatat tggctcatgt ccaatatgac cgccatgttg 240
gcattgatta ttgactagtt attaatagta atcaattacg gggtcattag ttcatagccc 300
atatatggag ttccgcgtta cataacttac ggtaaatggc ccgcctggct gaccgcccaa 360
cgacccccgc ccattgacgt caataatgac gtatgttccc atagtaacgc caatagggac 420
tttccattga cgtcaatggg tggagtattt acggtaaact gcccacttgg cagtacatca 480
agtgtatcat atgccaagtc cgccccctat tgacgtcaat gacggtaaat ggcccgcctg 540
gcattatgcc cagtacatga ccttacggga ctttcctact tggcagtaca tctacgtatt 600
agtcatcgct attaccatgg tcgaggtgag ccccacgttc tgcttcactc tccccatctc 660
ccccccctcc ccacccccaa ttttgtattt atttattttt taattatttt gtgcagcgat 720
gggggcgggg gggggggggg ggcgcgcgcc aggcggggcg gggcggggcg aggggcgggg 780
cggggcgagg cggagaggtg cggcggcagc caatcagagc ggcgcgctcc gaaagtttcc 840
ttttatggcg aggcggcggc ggcggcggcc ctataaaaag cgaagcgcgc ggcgggcggg 900
agtcgctgcg acgctgcctt cgccccgtgc cccgctccgc cgccgcctcg cgccgcccgc 960
cccggctctg actgaccgcg ttactcccac aggtgagcgg gcgggacggc ccttctcctc 1020
cgggctgtaa ttagcgcttg gtttaatgac ggcttgtttc ttttctgtgg ctgcgtgaaa 1080
gccttgaggg gctccgggag ggccctttgt gcggggggga gcggctcggg gggtgcgtgc 1140
gtgtgtgtgt gcgtggggag cgccgcgtgc ggcccgcgct gcccggcggc tgtgagcgct 1200
gcgggcgcgg cgcggggctt tgtgcgctcc gcagtgtgcg cgaggggagc gcggccgggg 1260
gcggtgcccc gcggtgcggg gggggctgcg aggggaacaa aggctgcgtg cggggtgtgt 1320
gcgtgggggg gtgagcaggg ggtgtgggcg cggcggtcgg gctgtaaccc ccccctgcac 1380
ccccctcccc gagttgctga gcacggcccg gcttcgggtg cggggctccg tacggggcgt 1440
ggcgcggggc tcgccgtgcc gggcgggggg tggcggcagg tgggggtgcc gggcggggcg 1500
gggccgcctc gggccgggga gggctcgggg gaggggcgcg gcggcccccg gagcgccggc 1560
ggctgtcgag gcgcggcgag ccgcagccat tgccttttat ggtaatcgtg cgagagggcg 1620
cagggacttc ctttgtccca aatctgtgcg gagccgaaat ctgggaggcg ccgccgcacc 1680
ccctctagcg ggcgcggggc gaagcggtgc ggcgccggca ggaaggaaat gggcggggag 1740
ggccttcgtg cgtcgccgcg ccgccgtccc cttctccctc tccagcctcg gggctgtccg 1800
cggggggacg gctgccttcg ggggggacgg ggcagggcgg ggttcggctt ctggcgtgtg 1860
accggcggct ctagagcctc tgctaaccat gttttagcct tcttcttttt cctacagctc 1920
ctgggcaacg tgctggttat tgtgctgtct catcatttgt cgacagaatt cctcgaagat 1980
ccgaaggggt tcaagcttgg cattccggta ctgttggtaa agccagttta aacgccgcca 2040
ccatggtgag caagggcgag gagctgttca ccggggtggt gcccatcctg gtcgagctgg 2100
acggcgacgt aaacggccac aagttcagcg tgtccggcga gggcgagggc gatgccacct 2160
acggcaagct gaccctgaag ttcatctgca ccaccggcaa gctgcccgtg ccctggccca 2220
ccctcgtgac caccctgacc tacggcgtgc agtgcttcag ccgctacccc gaccacatga 2280
agcagcacga cttcttcaag tccgccatgc ccgaaggcta cgtccaggag cgcaccatct 2340
tcttcaagga cgacggcaac tacaagaccc gcgccgaggt gaagttcgag ggcgacaccc 2400
tggtgaaccg catcgagctg aagggcatcg acttcaagga ggacggcaac atcctggggc 2460
acaagctgga gtacaactac aacagccaca acgtctatat catggccgac aagcagaaga 2520
acggcatcaa ggtgaacttc aagatccgcc acaacatcga ggacggcagc gtgcagctcg 2580
ccgaccacta ccagcagaac acccccatcg gcgacggccc cgtgctgctg cccgacaacc 2640
actacctgag cacccagtcc gccctgagca aagaccccaa cgagaagcgc gatcacatgg 2700
tcctgctgga gttcgtgacc gccgccggga tcactctcgg catggacgag ctgtacaagt 2760
aattaattaa gagcatctta ccgccattta ttcccatatt tgttctgttt ttcttgattt 2820
gggtatacat ttaaatgtta ataaaacaaa atggtggggc aatcatttac atttttaggg 2880
atatgtaatt actagttcag gtgtattgcc acaagacaaa catgttaaga aactttcccg 2940
ttatttacgc tctgttcctg ttaatcaacc tctggattac aaaatttgtg aaagattgac 3000
tgatattctt aactatgttg ctccttttac gctgtgtgga tatgctgctt tatagcctct 3060
gtatctagct attgcttccc gtacggcttt cgttttctcc tccttgtata aatcctggtt 3120
gctgtctctt ttagaggagt tgtggcccgt tgtccgtcaa cgtggcgtgg tgtgctctgt 3180
gtttgctgac gcaaccccca ctggctgggg cattgccacc acctgtcaac tcctttctgg 3240
gactttcgct ttccccctcc cgatcgccac ggcagaactc atcgccgcct gccttgcccg 3300
ctgctggaca ggggctaggt tgctgggcac tgataattcc gtggtgttgt ctgtgccttc 3360
tagttgccag ccatctgttg tttgcccctc ccccgtgcct tccttgaccc tggaaggtgc 3420
cactcccact gtcctttcct aataaaatga ggaaattgca tcgcattgtc tgagtaggtg 3480
tcattctatt ctggggggtg gggtggggca ggacagcaag ggggaggatt gggaagacaa 3540
tagcaggcat gctggggatg cggtgggctc tatggctcta gagcatggct acgtagataa 3600
gtagcatggc gggttaatca ttaactacac ctgcagcagg aacccctagt gatggagttg 3660
gccactccct ctctgcgcgc tcgctcgctc cctgcaggac tgaggccggg cgaccaaagg 3720
tcgcccgacg cccgggcggc ctcagtcctg cagg 3754
<210> 147
<211> 8418
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 147
ggcagctgcg cgctcgctcg ctcacctagg ccgcccgggc aaagcccggg cgtcgggcga 60
cctttggtcg cccggcctag gtgagcgagc gagcgcgcag agagggagtg gccaactcca 120
tcactagggg ttccttgtag ttaatgatta acccgccatg ctacttatcg cggccgctca 180
atattggcca ttagccatat tattcattgg ttatatagca taaatcaata ttggctattg 240
gccattgcat acgttgtatc tatatcataa tatgtacatt tatattggct catgtccaat 300
atgaccgcca tgttggcatt gattattgac tagttattaa tagtaatcaa ttacggggtc 360
attagttcat agcccatata tggagttccg cgttacataa cttacggtaa atggcccgcc 420
tggctgaccg cccaacgacc cccgcccatt gacgtcaata atgacgtatg ttcccatagt 480
aacgccaata gggactttcc attgacgtca atgggtggag tatttacggt aaactgccca 540
cttggcagta catcaagtgt atcatatgcc aagtccgccc cctattgacg tcaatgacgg 600
taaatggccc gcctggcatt atgcccagta catgacctta cgggactttc ctacttggca 660
gtacatctac gtattagtca tcgctattac catggtcgag gtgagcccca cgttctgctt 720
cactctcccc atctcccccc cctccccacc cccaattttg tatttattta ttttttaatt 780
attttgtgca gcgatggggg cggggggggg gggggggcgc gcgccaggcg gggcggggcg 840
gggcgagggg cggggcgggg cgaggcggag aggtgcggcg gcagccaatc agagcggcgc 900
gctccgaaag tttcctttta tggcgaggcg gcggcggcgg cggccctata aaaagcgaag 960
cgcgcggcgg gcgggagtcg ctgcgacgct gccttcgccc cgtgccccgc tccgccgccg 1020
cctcgcgccg cccgccccgg ctctgactga ccgcgttact cccacaggtg agcgggcggg 1080
acggcccttc tcctccgggc tgtaattagc gcttggttta atgacggctt gtttcttttc 1140
tgtggctgcg tgaaagcctt gaggggctcc gggagggccc tttgtgcggg ggggagcggc 1200
tcggggggtg cgtgcgtgtg tgtgtgcgtg gggagcgccg cgtgcggccc gcgctgcccg 1260
gcggctgtga gcgctgcggg cgcggcgcgg ggctttgtgc gctccgcagt gtgcgcgagg 1320
ggagcgcggc cgggggcggt gccccgcggt gcgggggggg ctgcgagggg aacaaaggct 1380
gcgtgcgggg tgtgtgcgtg ggggggtgag cagggggtgt gggcgcggcg gtcgggctgt 1440
aacccccccc tgcacccccc tccccgagtt gctgagcacg gcccggcttc gggtgcgggg 1500
ctccgtacgg ggcgtggcgc ggggctcgcc gtgccgggcg gggggtggcg gcaggtgggg 1560
gtgccgggcg gggcggggcc gcctcgggcc ggggagggct cgggggaggg gcgcggcggc 1620
ccccggagcg ccggcggctg tcgaggcgcg gcgagccgca gccattgcct tttatggtaa 1680
tcgtgcgaga gggcgcaggg acttcctttg tcccaaatct gtgcggagcc gaaatctggg 1740
aggcgccgcc gcaccccctc tagcgggcgc ggggcgaagc ggtgcggcgc cggcaggaag 1800
gaaatgggcg gggagggcct tcgtgcgtcg ccgcgccgcc gtccccttct ccctctccag 1860
cctcggggct gtccgcgggg ggacggctgc cttcgggggg gacggggcag ggcggggttc 1920
ggcttctggc gtgtgaccgg cggctctaga gcctctgcta accatgtttt agccttcttc 1980
tttttcctac agctcctggg caacgtgctg gttattgtgc tgtctcatca tttgtcgaca 2040
gaattcctcg aagatccgaa ggggttcaag cttggcattc cggtactgtt ggtaaagcca 2100
gtttaaacgc cgccaccatg gtgagcaagg gcgaggagct gttcaccggg gtggtgccca 2160
tcctggtcga gctggacggc gacgtaaacg gccacaagtt cagcgtgtcc ggcgagggcg 2220
agggcgatgc cacctacggc aagctgaccc tgaagttcat ctgcaccacc ggcaagctgc 2280
ccgtgccctg gcccaccctc gtgaccaccc tgacctacgg cgtgcagtgc ttcagccgct 2340
accccgacca catgaagcag cacgacttct tcaagtccgc catgcccgaa ggctacgtcc 2400
aggagcgcac catcttcttc aaggacgacg gcaactacaa gacccgcgcc gaggtgaagt 2460
tcgagggcga caccctggtg aaccgcatcg agctgaaggg catcgacttc aaggaggacg 2520
gcaacatcct ggggcacaag ctggagtaca actacaacag ccacaacgtc tatatcatgg 2580
ccgacaagca gaagaacggc atcaaggtga acttcaagat ccgccacaac atcgaggacg 2640
gcagcgtgca gctcgccgac cactaccagc agaacacccc catcggcgac ggccccgtgc 2700
tgctgcccga caaccactac ctgagcaccc agtccgccct gagcaaagac cccaacgaga 2760
agcgcgatca catggtcctg ctggagttcg tgaccgccgc cgggatcact ctcggcatgg 2820
acgagctgta caagtaatta attaagagca tcttaccgcc atttattccc atatttgttc 2880
tgtttttctt gatttgggta tacatttaaa tgttaataaa acaaaatggt ggggcaatca 2940
tttacatttt tagggatatg taattactag ttcaggtgta ttgccacaag acaaacatgt 3000
taagaaactt tcccgttatt tacgctctgt tcctgttaat caacctctgg attacaaaat 3060
ttgtgaaaga ttgactgata ttcttaacta tgttgctcct tttacgctgt gtggatatgc 3120
tgctttatag cctctgtatc tagctattgc ttcccgtacg gctttcgttt tctcctcctt 3180
gtataaatcc tggttgctgt ctcttttaga ggagttgtgg cccgttgtcc gtcaacgtgg 3240
cgtggtgtgc tctgtgtttg ctgacgcaac ccccactggc tggggcattg ccaccacctg 3300
tcaactcctt tctgggactt tcgctttccc cctcccgatc gccacggcag aactcatcgc 3360
cgcctgcctt gcccgctgct ggacaggggc taggttgctg ggcactgata attccgtggt 3420
gttgtctgtg ccttctagtt gccagccatc tgttgtttgc ccctcccccg tgccttcctt 3480
gaccctggaa ggtgccactc ccactgtcct ttcctaataa aatgaggaaa ttgcatcgca 3540
ttgtctgagt aggtgtcatt ctattctggg gggtggggtg gggcaggaca gcaaggggga 3600
ggattgggaa gacaatagca ggcatgctgg ggatgcggtg ggctctatgg ctctagagca 3660
tggctacgta gataagtagc atggcgggtt aatcattaac tacacctgca gcaggaaccc 3720
ctagtgatgg agttggccac tccctctctg cgcgctcgct cgctccctgc aggactgagg 3780
ccgggcgacc aaaggtcgcc cgacgcccgg gcggcctcag tcctgcaggg agcgagcgag 3840
cgcgcagctg cctgcacggg cgcgccggta ccgggagatg ggggaggcta actgaaacac 3900
ggaaggagac aataccggaa ggaacccgcg ctatgacggc aataaaaaga cagaataaaa 3960
cgcacgggtg ttgggtcgtt tgttcataaa cgcggggttc ggtcccaggg ctggcactct 4020
gtcgataccc caccgagacc ccattgggac caatacgccc gcgtttcttc cttttcccca 4080
ccccaacccc caagttcggg tgaaggccca gggctcgcag ccaacgtcgg ggcggcaagc 4140
cctgccatag ccactacggg tacgtaggcc aaccactaga actatagcta gagtcctggg 4200
cgaacaaacg atgctcgcct tccagaaaac cgaggatgcg aaccacttca tccggggtca 4260
gcaccaccgg caagcgccgc gacggccgag gtctaccgat ctcctgaagc cagggcagat 4320
ccgtgcacag caccttgccg tagaagaaca gcaaggccgc caatgcctga cgatgcgtgg 4380
agaccgaaac cttgcgctcg ttcgccagcc aggacagaaa tgcctcgact tcgctgctgc 4440
ccaaggttgc cgggtgacgc acaccgtgga aacggatgaa ggcacgaacc cagttgacat 4500
aagcctgttc ggttcgtaaa ctgtaatgca agtagcgtat gcgctcacgc aactggtcca 4560
gaaccttgac cgaacgcagc ggtggtaacg gcgcagtggc ggttttcatg gcttgttatg 4620
actgtttttt tgtacagtct atgcctcggg catccaagca gcaagcgcgt tacgccgtgg 4680
gtcgatgttt gatgttatgg agcagcaacg atgttacgca gcagcaacga tgttacgcag 4740
cagggcagtc gccctaaaac aaagttaggt ggctcaagta tgggcatcat tcgcacatgt 4800
aggctcggcc ctgaccaagt caaatccatg cgggctgctc ttgatctttt cggtcgtgag 4860
ttcggagacg tagccaccta ctcccaacat cagccggact ccgattacct cgggaacttg 4920
ctccgtagta agacattcat cgcgcttgct gccttcgacc aagaagcggt tgttggcgct 4980
ctcgcggctt acgttctgcc caggtttgag cagccgcgta gtgagatcta tatctatgat 5040
ctcgcagtct ccggcgagca ccggaggcag ggcattgcca ccgcgctcat caatctcctc 5100
aagcatgagg ccaacgcgct tggtgcttat gtgatctacg tgcaagcaga ttacggtgac 5160
gatcccgcag tggctctcta tacaaagttg ggcatacggg aagaagtgat gcactttgat 5220
atcgacccaa gtaccgccac ctaacaattc gttcaagccg agatcggctt cccggccgcg 5280
gagttgttcg gtaaattgtc acaacgccgc gaatatagtc tttaccatgc ccttggccac 5340
gcccctcttt aatacgacgg gcaatttgca cttcagaaaa tgaagagttt gctttagcca 5400
taacaaaagt ccagtatgct ttttcacagc ataactggac tgatttcagt ttacaactat 5460
tctgtctagt ttaagacttt attgtcatag tttagatcta ttttgttcag tttaagactt 5520
tattgtccgc ccacacccgc ttacgcaggg catccattta ttactcaacc gtaaccgatt 5580
ttgccaggtt acgcggctgg tctgcggtgt gaaataccgc acagatgcgt aaggagaaaa 5640
taccgcatca ggcgctcttc cgcttcctcg ctcactgact cgctgcgctc ggtcgttcgg 5700
ctgcggcgag cggtatcagc tcactcaaag gcggtaatac ggttatccac agaatcaggg 5760
gataacgcag gaaagaacat gtgagcaaaa ggccagcaaa aggccaggaa ccgtaaaaag 5820
gccgcgttgc tggcgttttt ccataggctc cgcccccctg acgagcatca caaaaatcga 5880
cgctcaagtc agaggtggcg aaacccgaca ggactataaa gataccaggc gtttccccct 5940
ggaagctccc tcgtgcgctc tcctgttccg accctgccgc ttaccggata cctgtccgcc 6000
tttctccctt cgggaagcgt ggcgctttct caatgctcac gctgtaggta tctcagttcg 6060
gtgtaggtcg ttcgctccaa gctgggctgt gtgcacgaac cccccgttca gcccgaccgc 6120
tgcgccttat ccggtaacta tcgtcttgag tccaacccgg taagacacga cttatcgcca 6180
ctggcagcag ccactggtaa caggattagc agagcgaggt atgtaggcgg tgctacagag 6240
ttcttgaagt ggtggcctaa ctacggctac actagaagga cagtatttgg tatctgcgct 6300
ctgctgaagc cagttacctt cggaaaaaga gttggtagct cttgatccgg caaacaaacc 6360
accgctggta gcggtggttt ttttgtttgc aagcagcaga ttacgcgcag aaaaaaagga 6420
tctcaagaag atcctttgat cttttctacg gggtctgacg ctcagtggaa cgaaaactca 6480
cgttaaggga ttttggtcat gagattatca aaaaggatct tcacctagat ccttttaaat 6540
taaaaatgaa gttttaaatc aatctaaagt atatatgagt aaacttggtc tgacagttac 6600
caatgcttaa tcagtgaggc acctatctca gcgatctgtc tatttcgttc atccatagtt 6660
gcctgactcc ccgtcgtgta gataactacg atacgggagg gcttaccatc tggccccagt 6720
gctgcaatga taccgcgaga cccacgctca ccggctccag atttatcagc aataaaccag 6780
ccagccggaa gggccgagcg cagaagtggt cctgcaactt tatccgcctc catccagtct 6840
attaattgtt gccgggaagc tagagtaagt agttcgccag ttaatagttt gcgcaacgtt 6900
gttgccattg ctacaggcat cgtggtgtca cgctcgtcgt ttggtatggc ttcattcagc 6960
tccggttccc aacgatcaag gcgagttaca tgatccccca tgttgtgcaa aaaagcggtt 7020
agctccttcg gtcctccgat cgttgtcaga agtaagttgg ccgcagtgtt atcactcatg 7080
gttatggcag cactgcataa ttctcttact gtcatgccat ccgtaagatg cttttctgtg 7140
actggtgagt actcaaccaa gtcattctga gaatagtgta tgcggcgacc gagttgctct 7200
tgcccggcgt caatacggga taataccgcg ccacatagca gaactttaaa agtgctcatc 7260
attggaaaac gttcttcggg gcgaaaactc tcaaggatct taccgctgtt gagatccagt 7320
tcgatgtaac ccactcgtgc acccaactga tcttcagcat cttttacttt caccagcgtt 7380
tctgggtgag caaaaacagg aaggcaaaat gccgcaaaaa agggaataag ggcgacacgg 7440
aaatgttgaa tactcatact cttccttttt caatattatt gaagcattta tcagggttat 7500
tgtctcatga gcggatacat atttgaatgt atttagaaaa ataaacaaat aggggttccg 7560
cgcacatttc cccgaaaagt gccacctgaa attgtaaacg ttaatatttt gttaaaattc 7620
gcgttaaatt tttgttaaat cagctcattt tttaaccaat aggccgaaat cggcaaaatc 7680
ccttataaat caaaagaata gaccgagata gggttgagtg ttgttccagt ttggaacaag 7740
agtccactat taaagaacgt ggactccaac gtcaaagggc gaaaaaccgt ctatcagggc 7800
gatggcccac tacgtgaacc atcaccctaa tcaagttttt tggggtcgag gtgccgtaaa 7860
gcactaaatc ggaaccctaa agggagcccc cgatttagag cttgacgggg aaagccggcg 7920
aacgtggcga gaaaggaagg gaagaaagcg aaaggagcgg gcgctagggc gctggcaagt 7980
gtagcggtca cgctgcgcgt aaccaccaca cccgccgcgc ttaatgcgcc gctacagggc 8040
gcgtcccatt cgccattcag gctgcaaata agcgttgata ttcagtcaat tacaaacatt 8100
aataacgaag agatgacaga aaaattttca ttctgtgaca gagaaaaagt agccgaagat 8160
gacggtttgt cacatggagt tggcaggatg tttgattaaa aacataacag gaagaaaaat 8220
gccccgctgt gggcggacaa aatagttggg aactgggagg ggtggaaatg gagtttttaa 8280
ggattattta gggaagagtg acaaaataga tgggaactgg gtgtagcgtc gtaagctaat 8340
acgaaaatta aaaatgacaa aatagtttgg aactagattt cacttatctg gttcggatct 8400
cctagtgagc tccctgca 8418
<210> 148
<211> 225
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 148
tgtgccttct agttgccagc catctgttgt ttgcccctcc cccgtgcctt ccttgaccct 60
ggaaggtgcc actcccactg tcctttccta ataaaatgag gaaattgcat cgcattgtct 120
gagtaggtgt cattctattc tggggggtgg ggtggggcag gacagcaagg gggaggattg 180
ggaagacaat agcaggcatg ctggggatgc ggtgggctct atggc 225
<210> 149
<211> 1177
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 149
ggctcagagg ctcagaggca cacaggagtt tctgggctca ccctgccccc ttccaacccc 60
tcagttccca tcctccagca gctgtttgtg tgctgcctct gaagtccaca ctgaacaaac 120
ttcagcctac tcatgtccct aaaatgggca aacattgcaa gcagcaaaca gcaaacacac 180
agccctccct gcctgctgac cttggagctg gggcagaggt cagagacctc tctgggccca 240
tgccacctcc aacatccact cgaccccttg gaatttcggt ggagaggagc agaggttgtc 300
ctggcgtggt ttaggtagtg tgagagggtc cgggttcaaa accacttgct gggtggggag 360
tcgtcagtaa gtggctatgc cccgaccccg aagcctgttt ccccatctgt acaatggaaa 420
tgataaagac gcccatctga tagggttttt gtggcaaata aacatttggt ttttttgttt 480
tgttttgttt tgttttttga gatggaggtt tgctctgtcg cccaggctgg agtgcagtga 540
cacaatctca tctcaccaca accttcccct gcctcagcct cccaagtagc tgggattaca 600
agcatgtgcc accacacctg gctaattttc tatttttagt agagacgggt ttctccatgt 660
tggtcagcct cagcctccca agtaactggg attacaggcc tgtgccacca cacccggcta 720
attttttcta tttttgacag ggacggggtt tcaccatgtt ggtcaggctg gtctagaggt 780
accggatctt gctaccagtg gaacagccac taaggattct gcagtgagag cagagggcca 840
gctaagtggt actctcccag agactgtctg actcacgcca ccccctccac cttggacaca 900
ggacgctgtg gtttctgagc caggtacaat gactcctttc ggtaagtgca gtggaagctg 960
tacactgccc aggcaaagcg tccgggcagc gtaggcgggc gactcagatc ccagccagtg 1020
gacttagccc ctgtttgctc ctccgataac tggggtgacc ttggttaata ttcaccagca 1080
gcctcccccg ttgcccctct ggatccactg cttaaatacg gacgaggaca gggccctgtc 1140
tcctcagctt caggcaccac cactgacctg ggacagt 1177
<210> 150
<211> 1326
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 150
ctgcagggcc cactagtgga gccgagagta attcatacaa aaggagggat cgccttcgca 60
aggggagagc ccagggaccg tccctaaatt ctcacagacc caaatccctg tagccgcccc 120
acgacagcgc gaggagcatg cgcccagggc tgagcgcggg tagatcagag cacacaagct 180
cacagtcccc ggcggtgggg ggaggggcgc gctgagcggg ggccagggag ctggcgcggg 240
gcaaactggg aaagtggtgt cgtgtgctgg ctccgccctc ttcccgaggg tgggggagaa 300
cggtatataa gtgcggtagt cgccttggac gttctttttc gcaacgggtt tgccgtcaga 360
acgcaggtga gtggcgggtg tggcttccgc gggccccgga gctggagccc tgctctgagc 420
gggccgggct gatatgcgag tgtcgtccgc agggtttagc tgtgagcatt cccacttcga 480
gtggcgggcg gtgcgggggt gagagtgcga ggcctagcgg caaccccgta gcctcgcctc 540
gtgtccggct tgaggcctag cgtggtgtcc gccgccgcgt gccactccgg ccgcactatg 600
cgttttttgt ccttgctgcc ctcgattgcc ttccagcagc atgggctaac aaagggaggg 660
tgtggggctc actcttaagg agcccatgaa gcttacgttg gataggaatg gaagggcagg 720
aggggcgact ggggcccgcc cgccttcgga gcacatgtcc gacgccacct ggatggggcg 780
aggcctgtgg ctttccgaag caatcgggcg tgagtttagc ctacctgggc catgtggccc 840
tagcactggg cacggtctgg cctggcggtg ccgcgttccc ttgcctccca acaagggtga 900
ggccgtcccg cccggcacca gttgcttgcg cggaaagatg gccgctcccg gggccctgtt 960
gcaaggagct caaaatggag gacgcggcag cccggtggag cgggcgggtg agtcacccac 1020
acaaaggaag agggccttgc ccctcgccgg ccgctgcttc ctgtgacccc gtggtctatc 1080
ggccgcatag tcacctcggg cttctcttga gcaccgctcg tcgcggcggg gggaggggat 1140
ctaatggcgt tggagtttgt tcacatttgg tgggtggaga ctagtcaggc cagcctggcg 1200
ctggaagtca ttcttggaat ttgccccttt gagtttggag cgaggctaat tctcaagcct 1260
cttagcggtt caaaggtatt ttctaaaccc gtttccaggt gttgtgaaag ccaccgctaa 1320
ttcaaa 1326
<210> 151
<211> 573
<212> ДНК
<213> Mus musculus
<400> 151
gtaagagttt tatgtttttt catctctgct tgtatttttc tagtaatgga agcctggtat 60
tttaaaatag ttaaattttc ctttagtgct gatttctaga ttattattac tgttgttgtt 120
gttattattg tcattatttg catctgagaa cccttaggtg gttatattat tgatatattt 180
ttggtatctt tgatgacaat aatgggggat tttgaaagct tagctttaaa tttcttttaa 240
ttaaaaaaaa atgctaggca gaatgactca aattacgttg gatacagttg aatttattac 300
ggtctcatag ggcctgcctg ctcgaccatg ctatactaaa aattaaaagt gtgtgttact 360
aattttataa atggagtttc catttatatt tacctttatt tcttatttac cattgtctta 420
gtagatattt acaaacatga cagaaacact aaatcttgag tttgaatgca cagatataaa 480
cacttaacgg gttttaaaaa taataatgtt ggtgaaaaaa tataactttg agtgtagcag 540
agaggaacca ttgccacctt cagattttcc tgt 573
<210> 152
<211> 1993
<212> ДНК
<213> Mus musculus
<400> 152
acgatcggga actggcatct tcagggagta gcttaggtca gtgaagagaa gaacaaaaag 60
cagcatatta cagttagttg tcttcatcaa tctttaaata tgttgtgtgg tttttctctc 120
cctgtttcca cagacaagag tgagatcgcc catcggtata atgatttggg agaacaacat 180
ttcaaaggcc tgtaagttat aatgctgaaa gcccacttaa tatttctggt agtattagtt 240
aaagttttaa aacacctttt tccaccttga gtgtgagaat tgtagagcag tgctgtccag 300
tagaaatgtg tgcattgaca gaaagactgt ggatctgtgc tgagcaatgt ggcagccaga 360
gatcacaagg ctatcaagca ctttgcacat ggcaagtgta actgagaagc acacattcaa 420
ataatagtta attttaattg aatgtatcta gccatgtgtg gctagtagct cctttcctgg 480
agagagaatc tggagcccac atctaacttg ttaagtctgg aatcttattt tttatttctg 540
gaaaggtcta tgaactatag ttttgggggc agctcactta ctaactttta atgcaataag 600
atctcatggt atcttgagaa cattattttg tctctttgta gtactgaaac cttatacatg 660
tgaagtaagg ggtctatact taagtcacat ctccaacctt agtaatgttt taatgtagta 720
aaaaaatgag taattaattt atttttagaa ggtcaatagt atcatgtatt ccaaataaca 780
gaggtatatg gttagaaaag aaacaattca aaggacttat ataatatcta gccttgacaa 840
tgaataaatt tagagagtag tttgcctgtt tgcctcatgt tcataaatct attgacacat 900
atgtgcatct gcacttcagc atggtagaag tccatattcc tttgcttgga aaggcaggtg 960
ttcccattac gcctcagaga atagctgacg ggaagaggct ttctagatag ttgtatgaaa 1020
gatatacaaa atctcgcagg tatacacagg catgatttgc tggttgggag agccacttgc 1080
ctcatactga ggtttttgtg tctgcttttc agagtcctga ttgccttttc ccagtatctc 1140
cagaaatgct catacgatga gcatgccaaa ttagtgcagg aagtaacaga ctttgcaaag 1200
acgtgtgttg ccgatgagtc tgccgccaac tgtgacaaat cccttgtgag taccttctga 1260
ttttgtggat ctactttcct gctttctgga actctgtttc aaagccaatc atgactccat 1320
cacttaaggc cccgggaaca ctgtggcaga gggcagcaga gagattgata aagccagggt 1380
gatgggaatt ttctgtggga ctccatttca tagtaattgc agaagctaca atacactcaa 1440
aaagtctcac cacatgactg cccaaatggg agcttgacag tgacagtgac agtagatatg 1500
ccaaagtgga tgagggaaag accacaagag ctaaaccctg taaaaagaac tgtaggcaac 1560
taaggaatgc agagagaaga agttgccttg gaagagcata ccaactgcct ctccaatacc 1620
aatggtcatc cctaaaacat acgtatgaat aacatgcaga ctaagcaggc tacatttagg 1680
aatatacatg tatttacata aatgtatatg catgtaacaa caatgaatga aaactgaggt 1740
catggatctg aaagagagca agggggctta catgagaggg tttggaggga ggggttggag 1800
ggagggaggt attattcttt agttttacag ggaacgtagt aaaaacatag gcttctccca 1860
aaggagcaga gcccatgagg agctgtgcaa ggttccccag cttgatttta cctgctcctc 1920
aaattccctt gatttgtttt tattataatg actttactcc tagcttttag tgtcagatag 1980
aaaacatgga agg 1993
<210> 153
<211> 1350
<212> ДНК
<213> Homo sapiens
<400> 153
taggaggctg aggcaggagg atcgcttgag cccaggagtt cgagaccagc ctgggcaaca 60
tagtgtgatc ttgtatctat aaaaataaac aaaattagct tggtgtggtg gcgcctgtag 120
tccccagcca cttggagggg tgaggtgaga ggattgcttg agcccgggat ggtccaggct 180
gcagtgagcc atgatcgtgc cactgcactc cagcctgggc gacagagtga gaccctgtct 240
cacaacaaca acaacaacaa caaaaaggct gagctgcacc atgcttgacc cagtttctta 300
aaattgttgt caaagcttca ttcactccat ggtgctatag agcacaagat tttatttggt 360
gagatggtgc tttcatgaat tcccccaaca gagccaagct ctccatctag tggacaggga 420
agctagcagc aaaccttccc ttcactacaa aacttcattg cttggccaaa aagagagtta 480
attcaatgta gacatctatg taggcaatta aaaacctatt gatgtataaa acagtttgca 540
ttcatggagg gcaactaaat acattctagg actttataaa agatcacttt ttatttatgc 600
acagggtgga acaagatgga ttatcaagtg tcaagtccaa tctatgacat caattattat 660
acatcggagc cctgccaaaa aatcaatgtg aagcaaatcg cagcccgcct cctgcctccg 720
ctctactcac tggtgttcat ctttggtttt gtgggcaaca tgctggtcat cctcatcctg 780
ataaactgca aaaggctgaa gagcatgact gacatctacc tgctcaacct ggccatctct 840
gacctgtttt tccttcttac tgtccccttc tgggctcact atgctgccgc ccagtgggac 900
tttggaaata caatgtgtca actcttgaca gggctctatt ttataggctt cttctctgga 960
atcttcttca tcatcctcct gacaatcgat aggtacctgg ctgtcgtcca tgctgtgttt 1020
gctttaaaag ccaggacggt cacctttggg gtggtgacaa gtgtgatcac ttgggtggtg 1080
gctgtgtttg cgtctctccc aggaatcatc tttaccagat ctcaaaaaga aggtcttcat 1140
tacacctgca gctctcattt tccatacagt cagtatcaat tctggaagaa tttccagaca 1200
ttaaagatag tcatcttggg gctggtcctg ccgctgcttg tcatggtcat ctgctactcg 1260
ggaatcctaa aaactctgct tcggtgtcga aatgagaaga agaggcacag ggctgtgagg 1320
cttatcttca ccatcatgat tgtttatttt 1350
<210> 154
<211> 1223
<212> ДНК
<213> Homo sapiens
<400> 154
tgacagagac tcttgggatg acgcactgct gcatcaaccc catcatctat gcctttgtcg 60
gggagaagtt cagaaactac ctcttagtct tcttccaaaa gcacattgcc aaacgcttct 120
gcaaatgctg ttctattttc cagcaagagg ctcccgagcg agcaagctca gtttacaccc 180
gatccactgg ggagcaggaa atatctgtgg gcttgtgaca cggactcaag tgggctggtg 240
acccagtcag agttgtgcac atggcttagt tttcatacac agcctgggct gggggtgggg 300
tgggagaggt cttttttaaa aggaagttac tgttatagag ggtctaagat tcatccattt 360
atttggcatc tgtttaaagt agattagatc ttttaagccc atcaattata gaaagccaaa 420
tcaaaatatg ttgatgaaaa atagcaacct ttttatctcc ccttcacatg catcaagtta 480
ttgacaaact ctcccttcac tccgaaagtt ccttatgtat atttaaaaga aagcctcaga 540
gaattgctga ttcttgagtt tagtgatctg aacagaaata ccaaaattat ttcagaaatg 600
tacaactttt tacctagtac aaggcaacat ataggttgta aatgtgttta aaacaggtct 660
ttgtcttgct atggggagaa aagacatgaa tatgattagt aaagaaatga cacttttcat 720
gtgtgatttc ccctccaagg tatggttaat aagtttcact gacttagaac caggcgagag 780
acttgtggcc tgggagagct ggggaagctt cttaaatgag aaggaatttg agttggatca 840
tctattgctg gcaaagacag aagcctcact gcaagcactg catgggcaag cttggctgta 900
gaaggagaca gagctggttg ggaagacatg gggaggaagg acaaggctag atcatgaaga 960
accttgacgg cattgctccg tctaagtcat gagctgagca gggagatcct ggttggtgtt 1020
gcagaaggtt tactctgtgg ccaaaggagg gtcaggaagg atgagcattt agggcaagga 1080
gaccaccaac agccctcagg tcagggtgag gatggcctct gctaagctca aggcgtgagg 1140
atgggaagga gggaggtatt cgtaaggatg ggaaggaggg aggtattcgt gcagcatatg 1200
aggatgcaga gtcagcagaa ctg 1223
<210> 155
<211> 215
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 155
gaacgctgac gtcatcaacc cgctccaagg aatcgcgggc ccagtgtcac taggcgggaa 60
cacccagcgc gcgtgcgccc tggcaggaag atggctgtga gggacagggg agtggcgccc 120
tgcaatattt gcatgtcgct atgtgttctg ggaaatcacc ataaacgtga aatgtctttg 180
gatttgggaa tcttataagt tctgtatgag accac 215
<210> 156
<211> 141
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 156
cctgcaggca gctgcgcgct cgctcgctca cctaggccgc ccgggcaaag cccgggcgtc 60
gggcgacctt tggtcgcccg gcctaggtga gcgagcgagc gcgcagagag ggagtggcca 120
actccatcac taggggttcc t 141
<210> 157
<211> 19
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 157
gcgcgctcgc tcgctcacc 19
<210> 158
<211> 22
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 158
ctaggtgagc gagcgagcgc gc 22
<210> 159
<211> 75
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 159
cctgcaggac tgaggccgcc cgggcaaagc ccgggcgtcg ggcgaccttt ggtcgcccgg 60
cctcagtcct gcagg 75
<210> 160
<211> 130
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 160
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagt 60
gcgggcgacc aaaggtcgcc cgacgcccgg gcgcactcag tgagcgagcg agcgcgcagc 120
tgcctgcagg 130
<210> 161
<211> 142
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 161
cctgcaggca gctgcgcgct cgctcgctcc ctaggactga ggccgcccgg gcgtcgggcg 60
acctttggtc gcccggcctc agtcctaggg agcgagcgag cgcgcagaga gggagtggcc 120
aactccatca ctaggggttc ct 142
<210> 162
<211> 80
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 162
gcgcgctcgc tcgctcactg agtgcgggcg accaaaggtc gcccgacgcc cgggcgcact 60
cagtgagcga gcgagcgcgc 80
<210> 163
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 163
gcgcgctcgc tcgctcactg a 21
<210> 164
<211> 18
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 164
gtgagcgagc gagcgcgc 18
<210> 165
<211> 89
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 165
gcgcgctcgc tcgctcactg aggccgcccg ggcaaagccc gggcgtcggg cgactttgtc 60
gcccggcctc agtgagcgag cgagcgcgc 89
<210> 166
<211> 89
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 166
gcgcgctcgc tcgctcactg aggccgggcg acaaagtcgc ccgacgcccg ggctttgccc 60
gggcggcctc agtgagcgag cgagcgcgc 89
<210> 167
<211> 87
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 167
gcgcgctcgc tcgctcactg aggccgcccg ggcaaagccc gggcgtcggg cgattttcgc 60
ccggcctcag tgagcgagcg agcgcgc 87
<210> 168
<211> 87
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 168
gcgcgctcgc tcgctcactg aggccgggcg aaaatcgccc gacgcccggg ctttgcccgg 60
gcggcctcag tgagcgagcg agcgcgc 87
<210> 169
<211> 85
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 169
gcgcgctcgc tcgctcactg aggccgcccg ggcaaagccc gggcgtcggg cgtttcgccc 60
ggcctcagtg agcgagcgag cgcgc 85
<210> 170
<211> 85
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 170
gcgcgctcgc tcgctcactg aggccgggcg aaacgcccga cgcccgggct ttgcccgggc 60
ggcctcagtg agcgagcgag cgcgc 85
<210> 171
<211> 89
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 171
gcgcgctcgc tcgctcactg aggccgcccg ggaaacccgg gcgtcgggcg acctttggtc 60
gcccggcctc agtgagcgag cgagcgcgc 89
<210> 172
<211> 89
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 172
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgcc cgggtttccc 60
gggcggcctc agtgagcgag cgagcgcgc 89
<210> 173
<211> 87
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 173
gcgcgctcgc tcgctcactg aggccgcccg gaaaccgggc gtcgggcgac ctttggtcgc 60
ccggcctcag tgagcgagcg agcgcgc 87
<210> 174
<211> 87
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 174
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgcc cggtttccgg 60
gcggcctcag tgagcgagcg agcgcgc 87
<210> 175
<211> 85
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 175
gcgcgctcgc tcgctcactg aggccgcccg aaacgggcgt cgggcgacct ttggtcgccc 60
ggcctcagtg agcgagcgag cgcgc 85
<210> 176
<211> 85
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 176
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgcc cgtttcgggc 60
ggcctcagtg agcgagcgag cgcgc 85
<210> 177
<211> 83
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 177
gcgcgctcgc tcgctcactg aggccgccca aagggcgtcg ggcgaccttt ggtcgcccgg 60
cctcagtgag cgagcgagcg cgc 83
<210> 178
<211> 83
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 178
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgcc ctttgggcgg 60
cctcagtgag cgagcgagcg cgc 83
<210> 179
<211> 81
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 179
gcgcgctcgc tcgctcactg aggccgccaa aggcgtcggg cgacctttgg tcgcccggcc 60
tcagtgagcg agcgagcgcg c 81
<210> 180
<211> 81
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 180
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgcc tttggcggcc 60
tcagtgagcg agcgagcgcg c 81
<210> 181
<211> 79
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 181
gcgcgctcgc tcgctcactg aggccgcaaa gcgtcgggcg acctttggtc gcccggcctc 60
agtgagcgag cgagcgcgc 79
<210> 182
<211> 79
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 182
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgct ttgcggcctc 60
agtgagcgag cgagcgcgc 79
<210> 183
<211> 81
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 183
ctgcgcgctc gctcgctcac tgaggccgaa acgtcgggcg acctttggtc gcccggcctc 60
agtgagcgag cgagcgcgca g 81
<210> 184
<211> 81
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 184
ctgcgcgctc gctcgctcac tgaggccggg cgaccaaagg tcgcccgacg tttcggcctc 60
agtgagcgag cgagcgcgca g 81
<210> 185
<211> 72
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 185
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacggc ctcagtgagc 60
gagcgagcgc gc 72
<210> 186
<211> 80
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 186
gcgcgctcgc tcgctcactg aggccgggcg accaaaggtc gcccgacgcc cgggcggcct 60
cagtgagcga gcgagcgcgc 80
<210> 187
<211> 79
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 187
gcgcgctcgc tcgctcactg aggcgcccgg gcgtcgggcg acctttggtc gcccggcctc 60
agtgagcgag cgagcgcgc 79
<210> 188
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 188
ggagtcaaag ttctgtttgc cctgatctgc atcgctgtgg ccgaggcc 48
<210> 189
<211> 99
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 189
attcatacca acttgaagaa aaagttcagc ctcttcatcc tggtctttct cctgttcgca 60
gtcatctgtg tttggaagaa agggagcgac tatgaggcc 99
<210> 190
<211> 588
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 190
gcccctctcc ctcccccccc cctaacgtta ctggccgaag ccgcttggaa taaggccggt 60
gtgcgtttgt ctatatgtta ttttccacca tattgccgtc ttttggcaat gtgagggccc 120
ggaaacctgg ccctgtcttc ttgacgagca ttcctagggg tctttcccct ctcgccaaag 180
gaatgcaagg tctgttgaat gtcgtgaagg aagcagttcc tctggaagct tcttgaagac 240
aaacaacgtc tgtagcgacc ctttgcaggc agcggaaccc cccacctggc gacaggtgcc 300
tctgcggcca aaagccacgt gtataagata cacctgcaaa ggcggcacaa ccccagtgcc 360
acgttgtgag ttggatagtt gtggaaagag tcaaatggct ctcctcaagc gtattcaaca 420
aggggctgaa ggatgcccag aaggtacccc attgtatggg atctgatctg gggcctcggt 480
gcacatgctt tacatgtgtt tagtcgaggt taaaaaaacg tctaggcccc ccgaaccacg 540
gggacgtggt tttcctttga aaaacacgat gataatatgg ccacaacc 588
<210> 191
<211> 225
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 191
ccgtctgtct gcacatttcg tagagcgagt gttccgatac tctaatctcc ctaggcaagg 60
ttcatatttg tgtaggttac ttattctcct tttgttgact aagtcaataa tcagaatcag 120
caggtttgga gtcagcttgg cagggatcag cagcctgggt tggaaggagg gggtataaaa 180
gccccttcac caggagaagc cgtcacacag atccacaagc tcctg 225
<210> 192
<211> 7551
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 192
aaagtagccg aagatgacgg tttgtcacat ggagttggca ggatgtttga ttaaaaacat 60
aacaggaaga aaaatgcccc gctgtgggcg gacaaaatag ttgggaactg ggaggggtgg 120
aaatggagtt tttaaggatt atttagggaa gagtgacaaa atagatggga actgggtgta 180
gcgtcgtaag ctaatacgaa aattaaaaat gacaaaatag tttggaacta gatttcactt 240
atctggttcg gatctcctag gcctgcaggc agctgcgcgc tcgctcgctc actgaggccg 300
cccgggcaaa gcccgggcgt cgggcgacct ttggtcgccc ggcctcagtg agcgagcgag 360
cgcgcagaga gggagtggcc aactccatca ctaggggttc cttgtagtta atgattaacc 420
cgccatgcta cttatcgcgg ccgccggggg aggctgctgg tgaatattaa ccaaggtcac 480
cccagttatc ggaggagcaa acaggggcta agtccacacg cgtggtaccg tctgtctgca 540
catttcgtag agcgagtgtt ccgatactct aatctcccta ggcaaggttc atatttgtgt 600
aggttactta ttctcctttt gttgactaag tcaataatca gaatcagcag gtttggagtc 660
agcttggcag ggatcagcag cctgggttgg aaggaggggg tataaaagcc ccttcaccag 720
gagaagccgt cacacagatc cacaagctcc tgaagaggta agggtttaag ggatggttgg 780
ttggtggggt attaatgttt aattacctgg agcacctgcc tgaaatcact ttttttcagg 840
ttggtttaaa ccgcagccac catgagcacc gccgtgctgg aaaatcctgg cctgggcaga 900
aagctgagcg acttcggcca agagacaagc tacatcgagg acaactgcaa ccagaacggc 960
gccatcagcc tgatcttcag cctgaaagaa gaagtgggcg ccctggccaa ggtgctgaga 1020
ctgttcgaag agaacgacgt gaacctgaca cacatcgaga gcagacccag cagactgaag 1080
aaggacgagt acgagttctt cacccacctg gacaagcgga gcctgcctgc tctgaccaac 1140
atcatcaaga tcctgcggca cgacatcggc gccacagtgc acgaactgag ccgggacaag 1200
aaaaaggaca ccgtgccatg gttccccaga accatccaag agctggacag attcgccaac 1260
cagatcctga gctatggcgc cgagctggac gctgatcacc ctggctttaa ggaccccgtg 1320
taccgggcca gaagaaagca gtttgccgat atcgcctaca actaccggca cggccagcct 1380
attcctcggg tcgagtacat ggaagaggaa aagaaaacct ggggcaccgt gttcaagacc 1440
ctgaagtccc tgtacaagac ccacgcctgc tacgagtaca accacatctt cccactgctc 1500
gaaaagtact gcggcttcca cgaggacaat atccctcagc ttgaggacgt gtcccagttc 1560
ctgcagacct gcaccggctt tagactgagg ccagttgccg gactgctgag cagcagagat 1620
tttctcggcg gcctggcctt cagagtgttc cactgtaccc agtacatcag acacggcagc 1680
aagcccatgt acacccctga gcctgatatc tgccacgagc tgctgggaca tgtgcccctg 1740
ttcagcgata gaagcttcgc ccagttcagc caagagatcg gactggcttc tctgggagcc 1800
cctgacgagt acattgagaa gctggccacc atctactggt tcaccgtgga attcggcctg 1860
tgcaagcagg gcgacagcat caaagcttat ggcgctggcc tgctgtctag cttcggcgag 1920
ctgcagtact gtctgagcga gaagcctaag ctgctgcccc tggaactgga aaagaccgcc 1980
atccagaact acaccgtgac cgagttccag cctctgtact acgtggccga gagcttcaac 2040
gacgccaaag aaaaagtgcg gaacttcgcc gccaccattc ctcggccttt cagcgtcaga 2100
tacgacccct acacacagcg gatcgaggtg ctggacaaca cacagcagct gaaaattctg 2160
gccgactcca tcaacagcga gatcggcatc ctgtgcagcg ccctgcagaa aatcaagtga 2220
tagttaatta agagcatctt accgccattt attcccatat ttgttctgtt tttcttgatt 2280
tgggtataca tttaaatgtt aataaaacaa aatggtgggg caatcattta catttttagg 2340
gatatgtaat tactagttca ggtgtattgc cacaagacaa acatgttaag aaactttccc 2400
gttatttacg ctctgttcct gttaatcaac ctctggatta caaaatttgt gaaagattga 2460
ctgatattct taactatgtt gctcctttta cgctgtgtgg atatgctgct ttatagcctc 2520
tgtatctagc tattgcttcc cgtacggctt tcgttttctc ctccttgtat aaatcctggt 2580
tgctgtctct tttagaggag ttgtggcccg ttgtccgtca acgtggcgtg gtgtgctctg 2640
tgtttgctga cgcaaccccc actggctggg gcattgccac cacctgtcaa ctcctttctg 2700
ggactttcgc tttccccctc ccgatcgcca cggcagaact catcgccgcc tgccttgccc 2760
gctgctggac aggggctagg ttgctgggca ctgataattc cgtggtgttg tctgtgcctt 2820
ctagttgcca gccatctgtt gtttgcccct cccccgtgcc ttccttgacc ctggaaggtg 2880
ccactcccac tgtcctttcc taataaaatg aggaaattgc atcgcattgt ctgagtaggt 2940
gtcattctat tctggggggt ggggtggggc aggacagcaa gggggaggat tgggaagaca 3000
atagcaggca tgctggggat gcggtgggct ctatggctct agagcatggc tacgtagata 3060
agtagcatgg cgggttaatc attaactaca cctgcaggag gaacccctag tgatggagtt 3120
ggccactccc tctctgcgcg ctcgctcgct cactgaggcc gggcgaccaa aggtcgcccg 3180
acgcccgggc ggcctcagtg agcgagcgag cgcgcagctg cctgcagggg cgcgcctcga 3240
gccatggtgc tagcagctga tgcatagcat gcggtaccgg gagatggggg aggctaactg 3300
aaacacggaa ggagacaata ccggaaggaa cccgcgctat gacggcaata aaaagacaga 3360
ataaaacgca cgggtgttgg gtcgtttgtt cataaacgcg gggttcggtc ccagggctgg 3420
cactctgtcg ataccccacc gagaccccat tgggaccaat acgcccgcgt ttcttccttt 3480
tccccacccc aacccccaag ttcgggtgaa ggcccagggc tcgcagccaa cgtcggggcg 3540
gcaagccctg ccatagccac tacgggtacg taggccaacc actagaacta tagctagagt 3600
cctgggcgaa caaacgatgc tcgccttcca gaaaaccgag gatgcgaacc acttcatccg 3660
gggtcagcac caccggcaag cgccgcgacg gccgaggtct accgatctcc tgaagccagg 3720
gcagatccgt gcacagcacc ttgccgtaga agaacagcaa ggccgccaat gcctgacgat 3780
gcgtggagac cgaaaccttg cgctcgttcg ccagccagga cagaaatgcc tcgacttcgc 3840
tgctgcccaa ggttgccggg tgacgcacac cgtggaaacg gatgaaggca cgaacccagt 3900
tgacataagc ctgttcggtt cgtaaactgt aatgcaagta gcgtatgcgc tcacgcaact 3960
ggtccagaac cttgaccgaa cgcagcggtg gtaacggcgc agtggcggtt ttcatggctt 4020
gttatgactg tttttttgta cagtctatgc ctcgggcatc caagcagcaa gcgcgttacg 4080
ccgtgggtcg atgtttgatg ttatggagca gcaacgatgt tacgcagcag caacgatgtt 4140
acgcagcagg gcagtcgccc taaaacaaag ttaggtggct caagtatggg catcattcgc 4200
acatgtaggc tcggccctga ccaagtcaaa tccatgcggg ctgctcttga tcttttcggt 4260
cgtgagttcg gagacgtagc cacctactcc caacatcagc cggactccga ttacctcggg 4320
aacttgctcc gtagtaagac attcatcgcg cttgctgcct tcgaccaaga agcggttgtt 4380
ggcgctctcg cggcttacgt tctgcccagg tttgagcagc cgcgtagtga gatctatatc 4440
tatgatctcg cagtctccgg cgagcaccgg aggcagggca ttgccaccgc gctcatcaat 4500
ctcctcaagc atgaggccaa cgcgcttggt gcttatgtga tctacgtgca agcagattac 4560
ggtgacgatc ccgcagtggc tctctataca aagttgggca tacgggaaga agtgatgcac 4620
tttgatatcg acccaagtac cgccacctaa caattcgttc aagccgagat cggcttcccg 4680
gccgcggagt tgttcggtaa attgtcacaa cgccgcgaat atagtcttta ccatgccctt 4740
ggccacgccc ctctttaata cgacgggcaa tttgcacttc agaaaatgaa gagtttgctt 4800
tagccataac aaaagtccag tatgcttttt cacagcataa ctggactgat ttcagtttac 4860
aactattctg tctagtttaa gactttattg tcatagttta gatctatttt gttcagttta 4920
agactttatt gtccgcccac acccgcttac gcagggcatc catttattac tcaaccgtaa 4980
ccgattttgc caggttacgc ggctggtctg cggtgtgaaa taccgcacag atgcgtaagg 5040
agaaaatacc gcatcaggcg ctcttccgct tcctcgctca ctgactcgct gcgctcggtc 5100
gttcggctgc ggcgagcggt atcagctcac tcaaaggcgg taatacggtt atccacagaa 5160
tcaggggata acgcaggaaa gaacatgtga gcaaaaggcc agcaaaaggc caggaaccgt 5220
aaaaaggccg cgttgctggc gtttttccat aggctccgcc cccctgacga gcatcacaaa 5280
aatcgacgct caagtcagag gtggcgaaac ccgacaggac tataaagata ccaggcgttt 5340
ccccctggaa gctccctcgt gcgctctcct gttccgaccc tgccgcttac cggatacctg 5400
tccgcctttc tcccttcggg aagcgtggcg ctttctcaat gctcacgctg taggtatctc 5460
agttcggtgt aggtcgttcg ctccaagctg ggctgtgtgc acgaaccccc cgttcagccc 5520
gaccgctgcg ccttatccgg taactatcgt cttgagtcca acccggtaag acacgactta 5580
tcgccactgg cagcagccac tggtaacagg attagcagag cgaggtatgt aggcggtgct 5640
acagagttct tgaagtggtg gcctaactac ggctacacta gaaggacagt atttggtatc 5700
tgcgctctgc tgaagccagt taccttcgga aaaagagttg gtagctcttg atccggcaaa 5760
caaaccaccg ctggtagcgg tggttttttt gtttgcaagc agcagattac gcgcagaaaa 5820
aaaggatctc aagaagatcc tttgatcttt tctacggggt ctgacgctca gtggaacgaa 5880
aactcacgtt aagggatttt ggtcatgaga ttatcaaaaa ggatcttcac ctagatcctt 5940
ttaaattaaa aatgaagttt taaatcaatc taaagtatat atgagtaaac ttggtctgac 6000
agttaccaat gcttaatcag tgaggcacct atctcagcga tctgtctatt tcgttcatcc 6060
atagttgcct gactccccgt cgtgtagata actacgatac gggagggctt accatctggc 6120
cccagtgctg caatgatacc gcgagaccca cgctcaccgg ctccagattt atcagcaata 6180
aaccagccag ccggaagggc cgagcgcaga agtggtcctg caactttatc cgcctccatc 6240
cagtctatta attgttgccg ggaagctaga gtaagtagtt cgccagttaa tagtttgcgc 6300
aacgttgttg ccattgctac aggcatcgtg gtgtcacgct cgtcgtttgg tatggcttca 6360
ttcagctccg gttcccaacg atcaaggcga gttacatgat cccccatgtt gtgcaaaaaa 6420
gcggttagct ccttcggtcc tccgatcgtt gtcagaagta agttggccgc agtgttatca 6480
ctcatggtta tggcagcact gcataattct cttactgtca tgccatccgt aagatgcttt 6540
tctgtgactg gtgagtactc aaccaagtca ttctgagaat agtgtatgcg gcgaccgagt 6600
tgctcttgcc cggcgtcaat acgggataat accgcgccac atagcagaac tttaaaagtg 6660
ctcatcattg gaaaacgttc ttcggggcga aaactctcaa ggatcttacc gctgttgaga 6720
tccagttcga tgtaacccac tcgtgcaccc aactgatctt cagcatcttt tactttcacc 6780
agcgtttctg ggtgagcaaa aacaggaagg caaaatgccg caaaaaaggg aataagggcg 6840
acacggaaat gttgaatact catactcttc ctttttcaat attattgaag catttatcag 6900
ggttattgtc tcatgagcgg atacatattt gaatgtattt agaaaaataa acaaataggg 6960
gttccgcgca catttccccg aaaagtgcca cctgaaattg taaacgttaa tattttgtta 7020
aaattcgcgt taaatttttg ttaaatcagc tcatttttta accaataggc cgaaatcggc 7080
aaaatccctt ataaatcaaa agaatagacc gagatagggt tgagtgttgt tccagtttgg 7140
aacaagagtc cactattaaa gaacgtggac tccaacgtca aagggcgaaa aaccgtctat 7200
cagggcgatg gcccactacg tgaaccatca ccctaatcaa gttttttggg gtcgaggtgc 7260
cgtaaagcac taaatcggaa ccctaaaggg agcccccgat ttagagcttg acggggaaag 7320
ccggcgaacg tggcgagaaa ggaagggaag aaagcgaaag gagcgggcgc tagggcgctg 7380
gcaagtgtag cggtcacgct gcgcgtaacc accacacccg ccgcgcttaa tgcgccgcta 7440
cagggcgcgt cccattcgcc attcaggctg caaataagcg ttgatattca gtcaattaca 7500
aacattaata acgaagagat gacagaaaaa ttttcattct gtgacagaga a 7551
<210> 193
<211> 7780
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 193
ggccggcccc tgcaggcagc tgcgcgctcg ctcgctcact gaggccgccc gggcaaagcc 60
cgggcgtcgg gcgacctttg gtcgcccggc ctcagtgagc gagcgagcgc gcagagaggg 120
agtggccaac tccatcacta ggggttcctt gtagttaatg attaacccgc catgctactt 180
atctacgtag ccatgctcta gacgggggag gctgctggtg aatattaacc aaggtcaccc 240
cagttatcgg aggagcaaac aggggctaag tccacacgcg tggtaccgtc tgtctgcaca 300
tttcgtagag cgagtgttcc gatactctaa tctccctagg caaggttcat atttgtgtag 360
gttacttatt ctccttttgt tgactaagtc aataatcaga atcagcaggt ttggagtcag 420
cttggcaggg atcagcagcc tgggttggaa ggagggggta taaaagcccc ttcaccagga 480
gaagccgtca cacagatcca caagctcctg aagaggtaag ggtttaaggg atggttggtt 540
ggtggggtat taatgtttaa ttacctggag cacctgcctg aaatcacttt ttttcaggtt 600
ggtttaaacg ccgccaccat gtccactgcg gtcctggaaa acccaggctt gggcaggaaa 660
ctctctgact ttggacagga aacaagctat attgaagaca actgcaatca aaatggtgcc 720
atatcactga tcttctcact caaagaagaa gttggtgcat tggccaaagt attgcgctta 780
tttgaggaga atgatgtaaa cctgacccac attgaatcta gaccttctcg tttaaagaaa 840
gatgagtatg aatttttcac ccatttggat aaacgtagcc tgcctgctct gacaaacatc 900
atcaagatct tgaggcatga cattggtgcc actgtccatg agctttcacg agataagaag 960
aaagacacag tgccctggtt cccaagaacc attcaagagc tggacagatt tgccaatcag 1020
attctcagct atggagcgga actggatgct gaccaccctg gttttaaaga tcctgtgtac 1080
cgtgcaagac ggaagcagtt tgctgacatt gcctacaact accgccatgg gcagcccatc 1140
cctcgagtgg aatacatgga ggaagaaaag aaaacatggg gcacagtgtt caagactctg 1200
aagtccttgt ataaaaccca tgcttgctat gagtacaatc acatttttcc acttcttgaa 1260
aagtactgtg gcttccatga agataacatt ccccagctgg aagacgtttc tcagttcctg 1320
cagacttgca ctggtttccg cctccgacct gtggctggcc tgctttcctc tcgggatttc 1380
ttgggtggcc tggccttccg agtcttccac tgcacacagt acatcagaca tggatccaag 1440
cccatgtata cccccgaacc tgacatctgc catgagctgt tgggacatgt gcccttgttt 1500
tcagatcgca gctttgccca gttttcccag gaaattggcc ttgcctctct gggtgcacct 1560
gatgaataca ttgaaaagct cgccacaatt tactggttta ctgtggagtt tgggctctgc 1620
aaacaaggag actccataaa ggcatatggt gctgggctcc tgtcatcctt tggtgaatta 1680
cagtactgct tatcagagaa gccaaagctt ctccccctgg agctggagaa gacagccatc 1740
caaaattaca ctgtcacgga gttccagccc ctctattacg tggcagagag ttttaatgat 1800
gccaaggaga aagtaaggaa ctttgctgcc acaatacctc ggcccttctc agttcgctac 1860
gacccataca cccaaaggat tgaggtcttg gacaataccc agcagcttaa gattttggct 1920
gattccatta acagtgaaat tggaatcctt tgcagtgccc tccagaaaat aaagtaatta 1980
attaagagca tcttaccgcc atttattccc atatttgttc tgtttttctt gatttgggta 2040
tacatttaaa tgttaataaa acaaaatggt ggggcaatca tttacatttt tagggatatg 2100
taattactag ttcaggtgta ttgccacaag acaaacatgt taagaaactt tcccgttatt 2160
tacgctctgt tcctgttaat caacctctgg attacaaaat ttgtgaaaga ttgactgata 2220
ttcttaacta tgttgctcct tttacgctgt gtggatatgc tgctttatag cctctgtatc 2280
tagctattgc ttcccgtacg gctttcgttt tctcctcctt gtataaatcc tggttgctgt 2340
ctcttttaga ggagttgtgg cccgttgtcc gtcaacgtgg cgtggtgtgc tctgtgtttg 2400
ctgacgcaac ccccactggc tggggcattg ccaccacctg tcaactcctt tctgggactt 2460
tcgctttccc cctcccgatc gccacggcag aactcatcgc cgcctgcctt gcccgctgct 2520
ggacaggggc taggttgctg ggcactgata attccgtggt gttgtctgtg ccttctagtt 2580
gccagccatc tgttgtttgc ccctcccccg tgccttcctt gaccctggaa ggtgccactc 2640
ccactgtcct ttcctaataa aatgaggaaa ttgcatcgca ttgtctgagt aggtgtcatt 2700
ctattctggg gggtggggtg gggcaggaca gcaaggggga ggattgggaa gacaatagca 2760
ggcatgctgg ggatgcggtg ggctctatgg ctctagagca tggctacgta gataagtagc 2820
atggcgggtt aatcattaac tacacctgca ggaggaaccc ctagtgatgg agttggccac 2880
tccctctctg cgcgctcgct cgctcactga ggccgggcga ccaaaggtcg cccgacgccc 2940
gggcggcctc agtgagcgag cgagcgcgca gctgcctgca ggggcgcgcc tcgaggcatg 3000
cggtaccaag cttgtcgaga agtactagag gatcataatc agccatacca catttgtaga 3060
ggttttactt gctttaaaaa acctcccaca cctccccctg aacctgaaac ataaaatgaa 3120
tgcaattgtt gttgttaact tgtttattgc agcttataat ggttacaaat aaagcaatag 3180
catcacaaat ttcacaaata aagcattttt ttcactgcat tctagttgtg gtttgtccaa 3240
actcatcaat gtatcttatc atgtctggat ctgatcactg atatcgccta ggagatccga 3300
accagataag tgaaatctag ttccaaacta ttttgtcatt tttaattttc gtattagctt 3360
acgacgctac acccagttcc catctatttt gtcactcttc cctaaataat ccttaaaaac 3420
tccatttcca cccctcccag ttcccaacta ttttgtccgc ccacagcggg gcatttttct 3480
tcctgttatg tttttaatca aacatcctgc caactccatg tgacaaaccg tcatcttcgg 3540
ctactttttc tctgtcacag aatgaaaatt tttctgtcat ctcttcgtta ttaatgtttg 3600
taattgactg aatatcaacg cttatttgca gcctgaatgg cgaatgggac gcgccctgta 3660
gcggcgcatt aagcgcggcg ggtgtggtgg ttacgcgcag cgtgaccgct acacttgcca 3720
gcgccctagc gcccgctcct ttcgctttct tcccttcctt tctcgccacg ttcgccggct 3780
ttccccgtca agctctaaat cgggggctcc ctttagggtt ccgatttagt gctttacggc 3840
acctcgaccc caaaaaactt gattagggtg atggttcacg tagtgggcca tcgccctgat 3900
agacggtttt tcgccctttg acgttggagt ccacgttctt taatagtgga ctcttgttcc 3960
aaactggaac aacactcaac cctatctcgg tctattcttt tgatttataa gggattttgc 4020
cgatttcggc ctattggtta aaaaatgagc tgatttaaca aaaatttaac gcgaatttta 4080
acaaaatatt aacgtttaca atttcaggtg gcacttttcg gggaaatgtg cgcggaaccc 4140
ctatttgttt atttttctaa atacattcaa atatgtatcc gctcatgaga caataaccct 4200
gataaatgct tcaataatat tgaaaaagga agagtatgag tattcaacat ttccgtgtcg 4260
cccttattcc cttttttgcg gcattttgcc ttcctgtttt tgctcaccca gaaacgctgg 4320
tgaaagtaaa agatgctgaa gatcagttgg gtgcacgagt gggttacatc gaactggatc 4380
tcaacagcgg taagatcctt gagagttttc gccccgaaga acgttttcca atgatgagca 4440
cttttaaagt tctgctatgt ggcgcggtat tatcccgtat tgacgccggg caagagcaac 4500
tcggtcgccg catacactat tctcagaatg acttggttga gtactcacca gtcacagaaa 4560
agcatcttac ggatggcatg acagtaagag aattatgcag tgctgccata accatgagtg 4620
ataacactgc ggccaactta cttctgacaa cgatcggagg accgaaggag ctaaccgctt 4680
ttttgcacaa catgggggat catgtaactc gccttgatcg ttgggaaccg gagctgaatg 4740
aagccatacc aaacgacgag cgtgacacca cgatgcctgt agcaatggca acaacgttgc 4800
gcaaactatt aactggcgaa ctacttactc tagcttcccg gcaacaatta atagactgga 4860
tggaggcgga taaagttgca ggaccacttc tgcgctcggc ccttccggct ggctggttta 4920
ttgctgataa atctggagcc ggtgagcgtg ggtctcgcgg tatcattgca gcactggggc 4980
cagatggtaa gccctcccgt atcgtagtta tctacacgac ggggagtcag gcaactatgg 5040
atgaacgaaa tagacagatc gctgagatag gtgcctcact gattaagcat tggtaactgt 5100
cagaccaagt ttactcatat atactttaga ttgatttaaa acttcatttt taatttaaaa 5160
ggatctaggt gaagatcctt tttgataatc tcatgaccaa aatcccttaa cgtgagtttt 5220
cgttccactg agcgtcagac cccgtagaaa agatcaaagg atcttcttga gatccttttt 5280
ttctgcgcgt aatctgctgc ttgcaaacaa aaaaaccacc gctaccagcg gtggtttgtt 5340
tgccggatca agagctacca actctttttc cgaaggtaac tggcttcagc agagcgcaga 5400
taccaaatac tgtccttcta gtgtagccgt agttaggcca ccacttcaag aactctgtag 5460
caccgcctac atacctcgct ctgctaatcc tgttaccagt ggctgctgcc agtggcgata 5520
agtcgtgtct taccgggttg gactcaagac gatagttacc ggataaggcg cagcggtcgg 5580
gctgaacggg gggttcgtgc acacagccca gcttggagcg aacgacctac accgaactga 5640
gatacctaca gcgtgagcat tgagaaagcg ccacgcttcc cgaagggaga aaggcggaca 5700
ggtatccggt aagcggcagg gtcggaacag gagagcgcac gagggagctt ccagggggaa 5760
acgcctggta tctttatagt cctgtcgggt ttcgccacct ctgacttgag cgtcgatttt 5820
tgtgatgctc gtcagggggg cggagcctat ggaaaaacgc cagcaacgcg gcctttttac 5880
ggttcctggc cttttgctgg ccttttgctc acatgttctt tcctgcgtta tcccctgatt 5940
ctgtggataa ccgtattacc gcctttgagt gagctgatac cgctcgccgc agccgaacga 6000
ccgagcgcag cgagtcagtg agcgaggaag cggaagagcg cctgatgcgg tattttctcc 6060
ttacgcatct gtgcggtatt tcacaccgca gaccagccgc gtaacctggc aaaatcggtt 6120
acggttgagt aataaatgga tgccctgcgt aagcgggtgt gggcggacaa taaagtctta 6180
aactgaacaa aatagatcta aactatgaca ataaagtctt aaactagaca gaatagttgt 6240
aaactgaaat cagtccagtt atgctgtgaa aaagcatact ggacttttgt tatggctaaa 6300
gcaaactctt cattttctga agtgcaaatt gcccgtcgta ttaaagaggg gcgtggccaa 6360
gggcatggta aagactatat tcgcggcgtt gtgacaattt accgaacaac tccgcggccg 6420
ggaagccgat ctcggcttga acgaattgtt aggtggcggt acttgggtcg atatcaaagt 6480
gcatcacttc ttcccgtatg cccaactttg tatagagagc cactgcggga tcgtcaccgt 6540
aatctgcttg cacgtagatc acataagcac caagcgcgtt ggcctcatgc ttgaggagat 6600
tgatgagcgc ggtggcaatg ccctgcctcc ggtgctcgcc ggagactgcg agatcataga 6660
tatagatctc actacgcggc tgctcaaacc tgggcagaac gtaagccgcg agagcgccaa 6720
caaccgcttc ttggtcgaag gcagcaagcg cgatgaatgt cttactacgg agcaagttcc 6780
cgaggtaatc ggagtccggc tgatgttggg agtaggtggc tacgtctccg aactcacgac 6840
cgaaaagatc aagagcagcc cgcatggatt tgacttggtc agggccgagc ctacatgtgc 6900
gaatgatgcc catacttgag ccacctaact ttgttttagg gcgactgccc tgctgcgtaa 6960
catcgttgct gctgcgtaac atcgttgctg ctccataaca tcaaacatcg acccacggcg 7020
taacgcgctt gctgcttgga tgcccgaggc atagactgta caaaaaaaca gtcataacaa 7080
gccatgaaaa ccgccactgc gccgttacca ccgctgcgtt cggtcaaggt tctggaccag 7140
ttgcgtgagc gcatacgcta cttgcattac agtttacgaa ccgaacaggc ttatgtcaac 7200
tgggttcgtg ccttcatccg tttccacggt gtgcgtcacc cggcaacctt gggcagcagc 7260
gaagtcgagg catttctgtc ctggctggcg aacgagcgca aggtttcggt ctccacgcat 7320
cgtcaggcat tggcggcctt gctgttcttc tacggcaagg tgctgtgcac ggatctgccc 7380
tggcttcagg agatcggaag acctcggccg tcgcggcgct tgccggtggt gctgaccccg 7440
gatgaagtgg ttcgcatcct cggttttctg gaaggcgagc atcgtttgtt cgcccaggac 7500
tctagctata gttctagtgg ttggctacgt atactccgga atattaatag atcatggaga 7560
taattaaaat gataaccatc tcgcaaataa ataagtattt tactgttttc gtaacagttt 7620
tgtaataaaa aaacctataa atattccgga ttattcatac cgtcccacca tcgggcgcgg 7680
atctcggtcc gaaaccatgt cgtactacca tcaccatcac catcacgatt acgatatccc 7740
aacgaccgaa aacctgtatt ttcagggcgc catgggatcc 7780
<210> 194
<211> 7780
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 194
ggccggcccc tgcaggcagc tgcgcgctcg ctcgctcact gaggccgccc gggcaaagcc 60
cgggcgtcgg gcgacctttg gtcgcccggc ctcagtgagc gagcgagcgc gcagagaggg 120
agtggccaac tccatcacta ggggttcctt gtagttaatg attaacccgc catgctactt 180
atctacgtag ccatgctcta gacgggggag gctgctggtg aatattaacc aaggtcaccc 240
cagttatcgg aggagcaaac aggggctaag tccacacgcg tggtaccgtc tgtctgcaca 300
tttcgtagag cgagtgttcc gatactctaa tctccctagg caaggttcat atttgtgtag 360
gttacttatt ctccttttgt tgactaagtc aataatcaga atcagcaggt ttggagtcag 420
cttggcaggg atcagcagcc tgggttggaa ggagggggta taaaagcccc ttcaccagga 480
gaagccgtca cacagatcca caagctcctg aagaggtaag ggtttaaggg atggttggtt 540
ggtggggtat taatgtttaa ttacctggag cacctgcctg aaatcacttt ttttcaggtt 600
ggtttaaacg ccgccaccat gagtacagct gtgcttgaaa atcctggcct gggcaggaag 660
cttagtgact ttggccagga aacatcttat attgaagaca actgcaacca gaatggtgcc 720
atttctctta tcttctccct gaaagaagag gtgggagccc tggcaaaggt tttaaggctc 780
tttgaggaga atgatgtgaa tttgacacac attgagtcca ggccttctag actcaagaaa 840
gatgaatatg agttcttcac ccacctggac aagaggagtc tccctgctct gaccaacatt 900
atcaagatct tgagacatga tataggagct acagtgcatg aactttcaag ggataaaaag 960
aaggacactg tcccctggtt tcccagaact atccaagaat tagacaggtt tgccaatcag 1020
atcctgagct atggtgcaga attagatgca gaccaccctg ggtttaaaga ccctgtgtat 1080
agagccagaa gaaagcagtt tgctgacatt gcatacaact acaggcatgg gcagcccatt 1140
cctagggtgg agtacatgga ggaagaaaaa aagacctggg gcacagtttt caagaccctg 1200
aagagccttt acaagacaca tgcctgctat gaatataacc atatatttcc attgttggag 1260
aaatactgtg gatttcatga agataacatc ccccagctgg aggatgttag tcagtttctg 1320
cagacctgca caggctttag actgaggcca gttgcaggac tgctaagttc tagggacttc 1380
ctgggtgggc tagccttcag agtgttccac tgtacccaat atataaggca tggatccaag 1440
cccatgtaca cccctgagcc tgatatctgc catgagctat tgggccatgt ccccctattt 1500
tctgacagaa gctttgccca gttctcccag gagattggat tagcctctct gggagctcct 1560
gatgagtaca ttgagaagtt agcaaccatc tactggttca ctgtggaatt tggcctttgc 1620
aaacaagggg atagtataaa ggcttatgga gcaggtctgc ttagcagttt tggagagctg 1680
cagtactgcc tgtcagaaaa gccaaagctc ctaccattag aactagaaaa gactgccatc 1740
cagaactata cagtcactga attccagcct ctctactatg tggctgagtc tttcaatgat 1800
gccaaggaga aggtgagaaa ttttgcagcc accattccca ggcccttctc tgttagatat 1860
gacccctaca ctcagaggat tgaggtcctg gacaataccc agcaactaaa aattctggct 1920
gattccatta attctgaaat tggcatcctc tgctctgctc tccagaagat taaatgatta 1980
attaagagca tcttaccgcc atttattccc atatttgttc tgtttttctt gatttgggta 2040
tacatttaaa tgttaataaa acaaaatggt ggggcaatca tttacatttt tagggatatg 2100
taattactag ttcaggtgta ttgccacaag acaaacatgt taagaaactt tcccgttatt 2160
tacgctctgt tcctgttaat caacctctgg attacaaaat ttgtgaaaga ttgactgata 2220
ttcttaacta tgttgctcct tttacgctgt gtggatatgc tgctttatag cctctgtatc 2280
tagctattgc ttcccgtacg gctttcgttt tctcctcctt gtataaatcc tggttgctgt 2340
ctcttttaga ggagttgtgg cccgttgtcc gtcaacgtgg cgtggtgtgc tctgtgtttg 2400
ctgacgcaac ccccactggc tggggcattg ccaccacctg tcaactcctt tctgggactt 2460
tcgctttccc cctcccgatc gccacggcag aactcatcgc cgcctgcctt gcccgctgct 2520
ggacaggggc taggttgctg ggcactgata attccgtggt gttgtctgtg ccttctagtt 2580
gccagccatc tgttgtttgc ccctcccccg tgccttcctt gaccctggaa ggtgccactc 2640
ccactgtcct ttcctaataa aatgaggaaa ttgcatcgca ttgtctgagt aggtgtcatt 2700
ctattctggg gggtggggtg gggcaggaca gcaaggggga ggattgggaa gacaatagca 2760
ggcatgctgg ggatgcggtg ggctctatgg ctctagagca tggctacgta gataagtagc 2820
atggcgggtt aatcattaac tacacctgca ggaggaaccc ctagtgatgg agttggccac 2880
tccctctctg cgcgctcgct cgctcactga ggccgggcga ccaaaggtcg cccgacgccc 2940
gggcggcctc agtgagcgag cgagcgcgca gctgcctgca ggggcgcgcc tcgaggcatg 3000
cggtaccaag cttgtcgaga agtactagag gatcataatc agccatacca catttgtaga 3060
ggttttactt gctttaaaaa acctcccaca cctccccctg aacctgaaac ataaaatgaa 3120
tgcaattgtt gttgttaact tgtttattgc agcttataat ggttacaaat aaagcaatag 3180
catcacaaat ttcacaaata aagcattttt ttcactgcat tctagttgtg gtttgtccaa 3240
actcatcaat gtatcttatc atgtctggat ctgatcactg atatcgccta ggagatccga 3300
accagataag tgaaatctag ttccaaacta ttttgtcatt tttaattttc gtattagctt 3360
acgacgctac acccagttcc catctatttt gtcactcttc cctaaataat ccttaaaaac 3420
tccatttcca cccctcccag ttcccaacta ttttgtccgc ccacagcggg gcatttttct 3480
tcctgttatg tttttaatca aacatcctgc caactccatg tgacaaaccg tcatcttcgg 3540
ctactttttc tctgtcacag aatgaaaatt tttctgtcat ctcttcgtta ttaatgtttg 3600
taattgactg aatatcaacg cttatttgca gcctgaatgg cgaatgggac gcgccctgta 3660
gcggcgcatt aagcgcggcg ggtgtggtgg ttacgcgcag cgtgaccgct acacttgcca 3720
gcgccctagc gcccgctcct ttcgctttct tcccttcctt tctcgccacg ttcgccggct 3780
ttccccgtca agctctaaat cgggggctcc ctttagggtt ccgatttagt gctttacggc 3840
acctcgaccc caaaaaactt gattagggtg atggttcacg tagtgggcca tcgccctgat 3900
agacggtttt tcgccctttg acgttggagt ccacgttctt taatagtgga ctcttgttcc 3960
aaactggaac aacactcaac cctatctcgg tctattcttt tgatttataa gggattttgc 4020
cgatttcggc ctattggtta aaaaatgagc tgatttaaca aaaatttaac gcgaatttta 4080
acaaaatatt aacgtttaca atttcaggtg gcacttttcg gggaaatgtg cgcggaaccc 4140
ctatttgttt atttttctaa atacattcaa atatgtatcc gctcatgaga caataaccct 4200
gataaatgct tcaataatat tgaaaaagga agagtatgag tattcaacat ttccgtgtcg 4260
cccttattcc cttttttgcg gcattttgcc ttcctgtttt tgctcaccca gaaacgctgg 4320
tgaaagtaaa agatgctgaa gatcagttgg gtgcacgagt gggttacatc gaactggatc 4380
tcaacagcgg taagatcctt gagagttttc gccccgaaga acgttttcca atgatgagca 4440
cttttaaagt tctgctatgt ggcgcggtat tatcccgtat tgacgccggg caagagcaac 4500
tcggtcgccg catacactat tctcagaatg acttggttga gtactcacca gtcacagaaa 4560
agcatcttac ggatggcatg acagtaagag aattatgcag tgctgccata accatgagtg 4620
ataacactgc ggccaactta cttctgacaa cgatcggagg accgaaggag ctaaccgctt 4680
ttttgcacaa catgggggat catgtaactc gccttgatcg ttgggaaccg gagctgaatg 4740
aagccatacc aaacgacgag cgtgacacca cgatgcctgt agcaatggca acaacgttgc 4800
gcaaactatt aactggcgaa ctacttactc tagcttcccg gcaacaatta atagactgga 4860
tggaggcgga taaagttgca ggaccacttc tgcgctcggc ccttccggct ggctggttta 4920
ttgctgataa atctggagcc ggtgagcgtg ggtctcgcgg tatcattgca gcactggggc 4980
cagatggtaa gccctcccgt atcgtagtta tctacacgac ggggagtcag gcaactatgg 5040
atgaacgaaa tagacagatc gctgagatag gtgcctcact gattaagcat tggtaactgt 5100
cagaccaagt ttactcatat atactttaga ttgatttaaa acttcatttt taatttaaaa 5160
ggatctaggt gaagatcctt tttgataatc tcatgaccaa aatcccttaa cgtgagtttt 5220
cgttccactg agcgtcagac cccgtagaaa agatcaaagg atcttcttga gatccttttt 5280
ttctgcgcgt aatctgctgc ttgcaaacaa aaaaaccacc gctaccagcg gtggtttgtt 5340
tgccggatca agagctacca actctttttc cgaaggtaac tggcttcagc agagcgcaga 5400
taccaaatac tgtccttcta gtgtagccgt agttaggcca ccacttcaag aactctgtag 5460
caccgcctac atacctcgct ctgctaatcc tgttaccagt ggctgctgcc agtggcgata 5520
agtcgtgtct taccgggttg gactcaagac gatagttacc ggataaggcg cagcggtcgg 5580
gctgaacggg gggttcgtgc acacagccca gcttggagcg aacgacctac accgaactga 5640
gatacctaca gcgtgagcat tgagaaagcg ccacgcttcc cgaagggaga aaggcggaca 5700
ggtatccggt aagcggcagg gtcggaacag gagagcgcac gagggagctt ccagggggaa 5760
acgcctggta tctttatagt cctgtcgggt ttcgccacct ctgacttgag cgtcgatttt 5820
tgtgatgctc gtcagggggg cggagcctat ggaaaaacgc cagcaacgcg gcctttttac 5880
ggttcctggc cttttgctgg ccttttgctc acatgttctt tcctgcgtta tcccctgatt 5940
ctgtggataa ccgtattacc gcctttgagt gagctgatac cgctcgccgc agccgaacga 6000
ccgagcgcag cgagtcagtg agcgaggaag cggaagagcg cctgatgcgg tattttctcc 6060
ttacgcatct gtgcggtatt tcacaccgca gaccagccgc gtaacctggc aaaatcggtt 6120
acggttgagt aataaatgga tgccctgcgt aagcgggtgt gggcggacaa taaagtctta 6180
aactgaacaa aatagatcta aactatgaca ataaagtctt aaactagaca gaatagttgt 6240
aaactgaaat cagtccagtt atgctgtgaa aaagcatact ggacttttgt tatggctaaa 6300
gcaaactctt cattttctga agtgcaaatt gcccgtcgta ttaaagaggg gcgtggccaa 6360
gggcatggta aagactatat tcgcggcgtt gtgacaattt accgaacaac tccgcggccg 6420
ggaagccgat ctcggcttga acgaattgtt aggtggcggt acttgggtcg atatcaaagt 6480
gcatcacttc ttcccgtatg cccaactttg tatagagagc cactgcggga tcgtcaccgt 6540
aatctgcttg cacgtagatc acataagcac caagcgcgtt ggcctcatgc ttgaggagat 6600
tgatgagcgc ggtggcaatg ccctgcctcc ggtgctcgcc ggagactgcg agatcataga 6660
tatagatctc actacgcggc tgctcaaacc tgggcagaac gtaagccgcg agagcgccaa 6720
caaccgcttc ttggtcgaag gcagcaagcg cgatgaatgt cttactacgg agcaagttcc 6780
cgaggtaatc ggagtccggc tgatgttggg agtaggtggc tacgtctccg aactcacgac 6840
cgaaaagatc aagagcagcc cgcatggatt tgacttggtc agggccgagc ctacatgtgc 6900
gaatgatgcc catacttgag ccacctaact ttgttttagg gcgactgccc tgctgcgtaa 6960
catcgttgct gctgcgtaac atcgttgctg ctccataaca tcaaacatcg acccacggcg 7020
taacgcgctt gctgcttgga tgcccgaggc atagactgta caaaaaaaca gtcataacaa 7080
gccatgaaaa ccgccactgc gccgttacca ccgctgcgtt cggtcaaggt tctggaccag 7140
ttgcgtgagc gcatacgcta cttgcattac agtttacgaa ccgaacaggc ttatgtcaac 7200
tgggttcgtg ccttcatccg tttccacggt gtgcgtcacc cggcaacctt gggcagcagc 7260
gaagtcgagg catttctgtc ctggctggcg aacgagcgca aggtttcggt ctccacgcat 7320
cgtcaggcat tggcggcctt gctgttcttc tacggcaagg tgctgtgcac ggatctgccc 7380
tggcttcagg agatcggaag acctcggccg tcgcggcgct tgccggtggt gctgaccccg 7440
gatgaagtgg ttcgcatcct cggttttctg gaaggcgagc atcgtttgtt cgcccaggac 7500
tctagctata gttctagtgg ttggctacgt atactccgga atattaatag atcatggaga 7560
taattaaaat gataaccatc tcgcaaataa ataagtattt tactgttttc gtaacagttt 7620
tgtaataaaa aaacctataa atattccgga ttattcatac cgtcccacca tcgggcgcgg 7680
atctcggtcc gaaaccatgt cgtactacca tcaccatcac catcacgatt acgatatccc 7740
aacgaccgaa aacctgtatt ttcagggcgc catgggatcc 7780
<210> 195
<211> 450
<212> БЕЛОК
<213> Homo sapiens
<400> 195
Met Ser Thr Ala Val Leu Glu Asn Pro Gly Leu Gly Arg Lys Leu Ser
1 5 10 15
Asp Phe Gly Gln Glu Thr Ser Tyr Ile Glu Asp Asn Cys Asn Gln Asn
20 25 30
Gly Ala Ile Ser Leu Ile Phe Ser Leu Lys Glu Glu Val Gly Ala Leu
35 40 45
Ala Lys Val Leu Arg Leu Phe Glu Glu Asn Asp Val Asn Leu Thr His
50 55 60
Ile Glu Ser Arg Pro Ser Arg Leu Lys Lys Asp Glu Tyr Glu Phe Phe
65 70 75 80
Thr His Leu Asp Lys Arg Ser Leu Pro Ala Leu Thr Asn Ile Ile Lys
85 90 95
Ile Leu Arg His Asp Ile Gly Ala Thr Val His Glu Leu Ser Arg Asp
100 105 110
Lys Lys Lys Asp Thr Val Pro Trp Phe Pro Arg Thr Ile Gln Glu Leu
115 120 125
Asp Arg Phe Ala Asn Gln Ile Leu Ser Tyr Gly Ala Glu Leu Asp Ala
130 135 140
Asp His Pro Gly Phe Lys Asp Pro Val Tyr Arg Ala Arg Arg Lys Gln
145 150 155 160
Phe Ala Asp Ile Ala Tyr Asn Tyr Arg His Gly Gln Pro Ile Pro Arg
165 170 175
Val Glu Tyr Met Glu Glu Glu Lys Lys Thr Trp Gly Thr Val Phe Lys
180 185 190
Thr Leu Lys Ser Leu Tyr Lys Thr His Ala Cys Tyr Glu Tyr Asn His
195 200 205
Ile Phe Pro Leu Leu Glu Lys Tyr Cys Gly Phe His Glu Asp Asn Ile
210 215 220
Pro Gln Leu Glu Asp Val Ser Gln Phe Leu Gln Thr Cys Thr Gly Phe
225 230 235 240
Arg Leu Arg Pro Val Ala Gly Leu Leu Ser Ser Arg Asp Phe Leu Gly
245 250 255
Gly Leu Ala Phe Arg Val Phe His Cys Thr Gln Tyr Ile Arg His Gly
260 265 270
Ser Lys Pro Met Tyr Thr Pro Glu Pro Asp Ile Cys His Glu Leu Leu
275 280 285
Gly His Val Pro Leu Phe Ser Asp Arg Ser Phe Ala Gln Phe Ser Gln
290 295 300
Glu Ile Gly Leu Ala Ser Leu Gly Ala Pro Asp Glu Tyr Ile Glu Lys
305 310 315 320
Leu Ala Thr Ile Tyr Trp Phe Thr Val Glu Phe Gly Leu Cys Lys Gln
325 330 335
Gly Asp Ser Ile Lys Ala Tyr Gly Ala Gly Leu Leu Ser Ser Phe Gly
340 345 350
Glu Leu Gln Tyr Cys Leu Ser Glu Lys Pro Lys Leu Leu Pro Leu Glu
355 360 365
Leu Glu Lys Thr Ala Ile Gln Asn Tyr Thr Val Thr Glu Phe Gln Pro
370 375 380
Leu Tyr Tyr Val Ala Glu Ser Phe Asn Asp Ala Lys Glu Lys Val Arg
385 390 395 400
Asn Phe Ala Ala Thr Ile Pro Arg Pro Phe Ser Val Arg Tyr Asp Pro
405 410 415
Tyr Thr Gln Arg Ile Glu Val Leu Asp Asn Thr Gln Gln Leu Lys Ile
420 425 430
Leu Ala Asp Ser Ile Asn Ser Glu Ile Gly Ile Leu Cys Ser Ala Leu
435 440 445
Gln Lys
450
<210> 196
<400> 196
000
<210> 197
<400> 197
000
<210> 198
<400> 198
000
<210> 199
<400> 199
000
<210> 200
<400> 200
000
<210> 201
<400> 201
000
<210> 202
<400> 202
000
<210> 203
<400> 203
000
<210> 204
<400> 204
000
<210> 205
<400> 205
000
<210> 206
<400> 206
000
<210> 207
<400> 207
000
<210> 208
<400> 208
000
<210> 209
<400> 209
000
<210> 210
<400> 210
000
<210> 211
<400> 211
000
<210> 212
<400> 212
000
<210> 213
<400> 213
000
<210> 214
<400> 214
000
<210> 215
<400> 215
000
<210> 216
<400> 216
000
<210> 217
<400> 217
000
<210> 218
<400> 218
000
<210> 219
<400> 219
000
<210> 220
<400> 220
000
<210> 221
<400> 221
000
<210> 222
<400> 222
000
<210> 223
<400> 223
000
<210> 224
<400> 224
000
<210> 225
<400> 225
000
<210> 226
<400> 226
000
<210> 227
<400> 227
000
<210> 228
<400> 228
000
<210> 229
<400> 229
000
<210> 230
<400> 230
000
<210> 231
<400> 231
000
<210> 232
<400> 232
000
<210> 233
<400> 233
000
<210> 234
<400> 234
000
<210> 235
<400> 235
000
<210> 236
<400> 236
000
<210> 237
<400> 237
000
<210> 238
<400> 238
000
<210> 239
<400> 239
000
<210> 240
<400> 240
000
<210> 241
<400> 241
000
<210> 242
<400> 242
000
<210> 243
<400> 243
000
<210> 244
<400> 244
000
<210> 245
<400> 245
000
<210> 246
<400> 246
000
<210> 247
<400> 247
000
<210> 248
<400> 248
000
<210> 249
<400> 249
000
<210> 250
<400> 250
000
<210> 251
<400> 251
000
<210> 252
<400> 252
000
<210> 253
<400> 253
000
<210> 254
<400> 254
000
<210> 255
<400> 255
000
<210> 256
<400> 256
000
<210> 257
<400> 257
000
<210> 258
<400> 258
000
<210> 259
<400> 259
000
<210> 260
<400> 260
000
<210> 261
<400> 261
000
<210> 262
<400> 262
000
<210> 263
<400> 263
000
<210> 264
<400> 264
000
<210> 265
<400> 265
000
<210> 266
<400> 266
000
<210> 267
<400> 267
000
<210> 268
<400> 268
000
<210> 269
<400> 269
000
<210> 270
<400> 270
000
<210> 271
<400> 271
000
<210> 272
<400> 272
000
<210> 273
<400> 273
000
<210> 274
<400> 274
000
<210> 275
<400> 275
000
<210> 276
<400> 276
000
<210> 277
<400> 277
000
<210> 278
<400> 278
000
<210> 279
<400> 279
000
<210> 280
<400> 280
000
<210> 281
<400> 281
000
<210> 282
<400> 282
000
<210> 283
<400> 283
000
<210> 284
<400> 284
000
<210> 285
<400> 285
000
<210> 286
<400> 286
000
<210> 287
<400> 287
000
<210> 288
<400> 288
000
<210> 289
<400> 289
000
<210> 290
<400> 290
000
<210> 291
<400> 291
000
<210> 292
<400> 292
000
<210> 293
<400> 293
000
<210> 294
<400> 294
000
<210> 295
<400> 295
000
<210> 296
<400> 296
000
<210> 297
<400> 297
000
<210> 298
<400> 298
000
<210> 299
<400> 299
000
<210> 300
<400> 300
000
<210> 301
<400> 301
000
<210> 302
<400> 302
000
<210> 303
<400> 303
000
<210> 304
<400> 304
000
<210> 305
<400> 305
000
<210> 306
<400> 306
000
<210> 307
<400> 307
000
<210> 308
<400> 308
000
<210> 309
<400> 309
000
<210> 310
<400> 310
000
<210> 311
<400> 311
000
<210> 312
<400> 312
000
<210> 313
<400> 313
000
<210> 314
<400> 314
000
<210> 315
<400> 315
000
<210> 316
<400> 316
000
<210> 317
<400> 317
000
<210> 318
<400> 318
000
<210> 319
<400> 319
000
<210> 320
<400> 320
000
<210> 321
<400> 321
000
<210> 322
<400> 322
000
<210> 323
<400> 323
000
<210> 324
<400> 324
000
<210> 325
<400> 325
000
<210> 326
<400> 326
000
<210> 327
<400> 327
000
<210> 328
<400> 328
000
<210> 329
<400> 329
000
<210> 330
<400> 330
000
<210> 331
<400> 331
000
<210> 332
<400> 332
000
<210> 333
<400> 333
000
<210> 334
<400> 334
000
<210> 335
<400> 335
000
<210> 336
<400> 336
000
<210> 337
<400> 337
000
<210> 338
<400> 338
000
<210> 339
<400> 339
000
<210> 340
<400> 340
000
<210> 341
<400> 341
000
<210> 342
<400> 342
000
<210> 343
<400> 343
000
<210> 344
<400> 344
000
<210> 345
<400> 345
000
<210> 346
<400> 346
000
<210> 347
<400> 347
000
<210> 348
<400> 348
000
<210> 349
<400> 349
000
<210> 350
<400> 350
000
<210> 351
<400> 351
000
<210> 352
<400> 352
000
<210> 353
<400> 353
000
<210> 354
<400> 354
000
<210> 355
<400> 355
000
<210> 356
<400> 356
000
<210> 357
<400> 357
000
<210> 358
<400> 358
000
<210> 359
<400> 359
000
<210> 360
<400> 360
000
<210> 361
<400> 361
000
<210> 362
<400> 362
000
<210> 363
<400> 363
000
<210> 364
<400> 364
000
<210> 365
<400> 365
000
<210> 366
<400> 366
000
<210> 367
<400> 367
000
<210> 368
<400> 368
000
<210> 369
<400> 369
000
<210> 370
<400> 370
000
<210> 371
<400> 371
000
<210> 372
<400> 372
000
<210> 373
<400> 373
000
<210> 374
<400> 374
000
<210> 375
<400> 375
000
<210> 376
<400> 376
000
<210> 377
<400> 377
000
<210> 378
<400> 378
000
<210> 379
<400> 379
000
<210> 380
<211> 1365
<212> ДНК
<213> Mus musculus
<400> 380
atggcagctg ttgtcctgga gaacggagtc ctgagcagaa aactctcaga ctttgggcag 60
gaaacaagtt acatcgaaga caactccaat caaaatggtg ctgtatctct gatattctca 120
ctcaaagagg aagttggtgc cctggccaag gtcctgcgct tatttgagga gaatgagatc 180
aacctgacac acattgaatc cagaccttcc cgtttaaaca aagatgagta tgagtttttc 240
acctatctgg ataagcgtag caagcccgtc ctgggcagca tcatcaagag cctgaggaac 300
gacattggtg ccactgtcca tgagctttcc cgagacaagg aaaagaacac agtgccctgg 360
ttcccaagga ccattcagga gctggacaga ttcgccaatc agattctcag ctatggagcc 420
gaactggatg cagaccaccc aggctttaaa gatcctgtgt accgggcgag acgaaagcag 480
tttgctgaca ttgcctacaa ctaccgccat gggcagccca ttcctcgggt ggaatacaca 540
gaggaggaga ggaagacctg gggaacggtg ttcaggactc tgaaggcctt gtataaaaca 600
catgcctgct acgagcacaa ccacatcttc cctcttctgg aaaagtactg cggtttccgt 660
gaagacaaca tcccgcagct ggaagatgtt tctcagtttc tgcagacttg tactggtttc 720
cgcctccgtc ctgttgctgg cttactgtcg tctcgagatt tcttgggtgg cctggccttc 780
cgagtcttcc actgcacaca gtacattagg catggatcta agcccatgta cacacctgaa 840
cctgatatct gtcatgaact cttgggacat gtgcccttgt tttcagatag aagctttgcc 900
cagttttctc aggaaattgg gcttgcatcg ctgggggcac ctgatgagta cattgagaaa 960
ctggccacaa tttactggtt tactgtggag tttgggcttt gcaaggaagg agattctata 1020
aaggcatatg gtgctgggct cttgtcatcc tttggagaat tacagtactg tttatcagac 1080
aagccaaagc tcctgcccct ggagctagag aagacagcct gccaggagta tactgtcaca 1140
gagttccagc ctctgtacta tgtggccgag agtttcaatg atgccaagga gaaagtgagg 1200
acttttgctg ccacaatccc ccggcccttc tccgttcgct atgaccccta cactcaaagg 1260
gttgaggtcc tggacaatac tcagcagttg aagattttag ctgactccat taatagtgag 1320
gttggaatcc tttgccatgc cctgcagaaa ataaagtcat gataa 1365
<210> 381
<211> 1362
<212> ДНК
<213> Homo sapiens
<400> 381
atgtccactg cggtcctgga aaacccaggc ttgggcagga aactctctga ctttggacag 60
gaaacaagct atattgaaga caactgcaat caaaatggtg ccatatcact gatcttctca 120
ctcaaagaag aagttggtgc attggccaaa gtattgcgct tatttgagga gaatgatgta 180
aacctgaccc acattgaatc tagaccttct cgtttaaaga aagatgagta tgaatttttc 240
acccatttgg ataaacgtag cctgcctgct ctgacaaaca tcatcaagat cttgaggcat 300
gacattggtg ccactgtcca tgagctttca cgagataaga agaaagacac agtgccctgg 360
ttcccaagaa ccattcaaga gctggacaga tttgccaatc agattctcag ctatggagcg 420
gaactggatg ctgaccaccc tggttttaaa gatcctgtgt accgtgcaag acggaagcag 480
tttgctgaca ttgcctacaa ctaccgccat gggcagccca tccctcgagt ggaatacatg 540
gaggaagaaa agaaaacatg gggcacagtg ttcaagactc tgaagtcctt gtataaaacc 600
catgcttgct atgagtacaa tcacattttt ccacttcttg aaaagtactg tggcttccat 660
gaagataaca ttccccagct ggaagacgtt tctcaattcc tgcagacttg cactggtttc 720
cgcctccgac ctgtggctgg cctgctttcc tctcgggatt tcttgggtgg cctggccttc 780
cgagtcttcc actgcacaca gtacatcaga catggatcca agcccatgta tacccccgaa 840
cctgacatct gccatgagct gttgggacat gtgcccttgt tttcagatcg cagctttgcc 900
cagttttccc aggaaattgg ccttgcctct ctgggtgcac ctgatgaata cattgaaaag 960
ctcgccacaa tttactggtt tactgtggag tttgggctct gcaaacaagg agactccata 1020
aaggcatatg gtgctgggct cctgtcatcc tttggtgaat tacagtactg cttatcagag 1080
aagccaaagc ttctccccct ggagctggag aagacagcca tccaaaatta cactgtcacg 1140
gagttccagc ccctgtatta cgtggcagag agttttaatg atgccaagga gaaagtaagg 1200
aactttgctg ccacaatacc tcggcccttc tcagttcgct acgacccata cacccaaagg 1260
attgaggtct tggacaatac ccagcagctt aagattttgg ctgattccat taacagtgaa 1320
attggaatcc tttgcagtgc cctccagaaa ataaagtaat aa 1362
<210> 382
<211> 1359
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 382
atgagcaccg ccgtgctgga aaatcctggc ctgggcagaa agctgagcga cttcggccaa 60
gagacaagct acatcgagga caactgcaac cagaacggcg ccatcagcct gatcttcagc 120
ctgaaagaag aagtgggcgc cctggccaag gtgctgagac tgttcgaaga gaacgacgtg 180
aacctgacac acatcgagag cagacccagc agactgaaga aggacgagta cgagttcttc 240
acccacctgg acaagcggag cctgcctgct ctgaccaaca tcatcaagat cctgcggcac 300
gacatcggcg ccacagtgca cgaactgagc cgggacaaga aaaaggacac cgtgccatgg 360
ttccccagaa ccatccaaga gctggacaga ttcgccaacc agatcctgag ctatggcgcc 420
gagctggacg ctgatcaccc tggctttaag gaccccgtgt accgggccag aagaaagcag 480
tttgccgata tcgcctacaa ctaccggcac ggccagccta ttcctcgggt cgagtacatg 540
gaagaggaaa agaaaacctg gggcaccgtg ttcaagaccc tgaagtccct gtacaagacc 600
cacgcctgct acgagtacaa ccacatcttc ccactgctcg aaaagtactg cggcttccac 660
gaggacaata tccctcagct tgaggacgtg tcccagttcc tgcagacctg caccggcttt 720
agactgaggc cagttgccgg actgctgagc agcagagatt ttctcggcgg cctggccttc 780
agagtgttcc actgtaccca gtacatcaga cacggcagca agcccatgta cacccctgag 840
cctgatatct gccacgagct gctgggacat gtgcccctgt tcagcgatag aagcttcgcc 900
cagttcagcc aagagatcgg actggcttct ctgggagccc ctgacgagta cattgagaag 960
ctggccacca tctactggtt caccgtggaa ttcggcctgt gcaagcaggg cgacagcatc 1020
aaagcttatg gcgctggcct gctgtctagc ttcggcgagc tgcagtactg tctgagcgag 1080
aagcctaagc tgctgcccct ggaactggaa aagaccgcca tccagaacta caccgtgacc 1140
gagttccagc ctctgtacta cgtggccgag agcttcaacg acgccaaaga aaaagtgcgg 1200
aacttcgccg ccaccattcc tcggcctttc agcgtcagat acgaccccta cacacagcgg 1260
atcgaggtgc tggacaacac acagcagctg aaaattctgg ccgactccat caacagcgag 1320
atcggcatcc tgtgcagcgc cctgcagaaa atcaagtga 1359
<210> 383
<211> 1359
<212> ДНК
<213> Homo sapiens
<400> 383
atgtccactg cggtcctgga aaacccaggc ttgggcagga aactctctga ctttggacag 60
gaaacaagct atattgaaga caactgcaat caaaatggtg ccatatcact gatcttctca 120
ctcaaagaag aagttggtgc attggccaaa gtattgcgct tatttgagga gaatgatgta 180
aacctgaccc acattgaatc tagaccttct cgtttaaaga aagatgagta tgaatttttc 240
acccatttgg ataaacgtag cctgcctgct ctgacaaaca tcatcaagat cttgaggcat 300
gacattggtg ccactgtcca tgagctttca cgagataaga agaaagacac agtgccctgg 360
ttcccaagaa ccattcaaga gctggacaga tttgccaatc agattctcag ctatggagcg 420
gaactggatg ctgaccaccc tggttttaaa gatcctgtgt accgtgcaag acggaagcag 480
tttgctgaca ttgcctacaa ctaccgccat gggcagccca tccctcgagt ggaatacatg 540
gaggaagaaa agaaaacatg gggcacagtg ttcaagactc tgaagtcctt gtataaaacc 600
catgcttgct atgagtacaa tcacattttt ccacttcttg aaaagtactg tggcttccat 660
gaagataaca ttccccagct ggaagacgtt tctcagttcc tgcagacttg cactggtttc 720
cgcctccgac ctgtggctgg cctgctttcc tctcgggatt tcttgggtgg cctggccttc 780
cgagtcttcc actgcacaca gtacatcaga catggatcca agcccatgta tacccccgaa 840
cctgacatct gccatgagct gttgggacat gtgcccttgt tttcagatcg cagctttgcc 900
cagttttccc aggaaattgg ccttgcctct ctgggtgcac ctgatgaata cattgaaaag 960
ctcgccacaa tttactggtt tactgtggag tttgggctct gcaaacaagg agactccata 1020
aaggcatatg gtgctgggct cctgtcatcc tttggtgaat tacagtactg cttatcagag 1080
aagccaaagc ttctccccct ggagctggag aagacagcca tccaaaatta cactgtcacg 1140
gagttccagc ccctctatta cgtggcagag agttttaatg atgccaagga gaaagtaagg 1200
aactttgctg ccacaatacc tcggcccttc tcagttcgct acgacccata cacccaaagg 1260
attgaggtct tggacaatac ccagcagctt aagattttgg ctgattccat taacagtgaa 1320
attggaatcc tttgcagtgc cctccagaaa ataaagtaa 1359
<210> 384
<211> 1359
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 384
atgagtacag ctgtgcttga aaatcctggc ctgggcagga agcttagtga ctttggccag 60
gaaacatctt atattgaaga caactgcaac cagaatggtg ccatttctct tatcttctcc 120
ctgaaagaag aggtgggagc cctggcaaag gttttaaggc tctttgagga gaatgatgtg 180
aatttgacac acattgagtc caggccttct agactcaaga aagatgaata tgagttcttc 240
acccacctgg acaagaggag tctccctgct ctgaccaaca ttatcaagat cttgagacat 300
gatataggag ctacagtgca tgaactttca agggataaaa agaaggacac tgtcccctgg 360
tttcccagaa ctatccaaga attagacagg tttgccaatc agatcctgag ctatggtgca 420
gaattagatg cagaccaccc tgggtttaaa gaccctgtgt atagagccag aagaaagcag 480
tttgctgaca ttgcatacaa ctacaggcat gggcagccca ttcctagggt ggagtacatg 540
gaggaagaaa aaaagacctg gggcacagtt ttcaagaccc tgaagagcct ttacaagaca 600
catgcctgct atgaatataa ccatatattt ccattgttgg agaaatactg tggatttcat 660
gaagataaca tcccccagct ggaggatgtt agtcagtttc tgcagacctg cacaggcttt 720
agactgaggc cagttgcagg actgctaagt tctagggact tcctgggtgg gctagccttc 780
agagtgttcc actgtaccca atatataagg catggatcca agcccatgta cacccctgag 840
cctgatatct gccatgagct attgggccat gtccccctat tttctgacag aagctttgcc 900
cagttctccc aggagattgg attagcctct ctgggagctc ctgatgagta cattgagaag 960
ttagcaacca tctactggtt cactgtggaa tttggccttt gcaaacaagg ggatagtata 1020
aaggcttatg gagcaggtct gcttagcagt tttggagagc tgcagtactg cctgtcagaa 1080
aagccaaagc tcctaccatt agaactagaa aagactgcca tccagaacta tacagtcact 1140
gaattccagc ctctctacta tgtggctgag tctttcaatg atgccaagga gaaggtgaga 1200
aattttgcag ccaccattcc caggcccttc tctgttagat atgaccccta cactcagagg 1260
attgaggtcc tggacaatac ccagcaacta aaaattctgg ctgattccat taattctgaa 1320
attggcatcc tctgctctgc tctccagaag attaaatga 1359
<210> 385
<211> 1451
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 385
atgagtacag ctgtgcttga aaatcctggc ctgggcagga agcttagtga ctttggccag 60
aagaggtaag ggtttaaggg atggttggtt ggtggggtat taatgtttaa ttacctggag 120
cacctgcctg aaatcacttt ttttcaggtt gggaaacatc ttatattgaa gacaactgca 180
accagaatgg tgccatttct cttatcttct ccctgaaaga agaggtggga gccctggcaa 240
aggttttaag gctctttgag gagaatgatg tgaatttgac acacattgag tccaggcctt 300
ctagactcaa gaaagatgaa tatgagttct tcacccacct ggacaagagg agtctccctg 360
ctctgaccaa cattatcaag atcttgagac atgatatagg agctacagtg catgaacttt 420
caagggataa aaagaaggac actgtcccct ggtttcccag aactatccaa gaattagaca 480
ggtttgccaa tcagatcctg agctatggtg cagaattaga tgcagaccac cctgggttta 540
aagaccctgt gtatagagcc agaagaaagc agtttgctga cattgcatac aactacaggc 600
atgggcagcc cattcctagg gtggagtaca tggaggaaga aaaaaagacc tggggcacag 660
ttttcaagac cctgaagagc ctttacaaga cacatgcctg ctatgaatat aaccatatat 720
ttccattgtt ggagaaatac tgtggatttc atgaagataa catcccccag ctggaggatg 780
ttagtcagtt tctgcagacc tgcacaggct ttagactgag gccagttgca ggactgctaa 840
gttctaggga cttcctgggt gggctagcct tcagagtgtt ccactgtacc caatatataa 900
ggcatggatc caagcccatg tacacccctg agcctgatat ctgccatgag ctattgggcc 960
atgtccccct attttctgac agaagctttg cccagttctc ccaggagatt ggattagcct 1020
ctctgggagc tcctgatgag tacattgaga agttagcaac catctactgg ttcactgtgg 1080
aatttggcct ttgcaaacaa ggggatagta taaaggctta tggagcaggt ctgcttagca 1140
gttttggaga gctgcagtac tgcctgtcag aaaagccaaa gctcctacca ttagaactag 1200
aaaagactgc catccagaac tatacagtca ctgaattcca gcctctctac tatgtggctg 1260
agtctttcaa tgatgccaag gagaaggtga gaaattttgc agccaccatt cccaggccct 1320
tctctgttag atatgacccc tacactcaga ggattgaggt cctggacaat acccagcaac 1380
taaaaattct ggctgattcc attaattctg aaattggcat cctctgctct gctctccaga 1440
agattaaatg a 1451
<210> 386
<211> 3359
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 386
atgagtacag ctgtgcttga aaatcctggc ctgggcagga agcttagtga ctttggccag 60
gtgagccagg gcagcctgag ctgctcagtt aggggaattt gggcctccag agaaagagat 120
cccaagactg ctggtgcttc ctggtttcat aagctcagta agaagtctga attggttgga 180
agctgatgag aatatccagg aagtcaacag acaaatgtcc tcaacaattg tttctaagta 240
ggagaacatc tgtcctgggt ggctttcaca ggaatgaatg accattgctt tagggggttg 300
gggatctggc ctccagaact gccaccaatt agctgtgtgt ctttggacaa gttactgtcc 360
ctctctgttg tctgtttact cttctgtaca ctgaaggggc tggtccctaa tgatctggga 420
tgggatgtgg aatccttcta gatttctttt gtaatattta taaagtgctc tcagcaaggt 480
atcaaaatgg caaaattgtg agtaactatc ctcctttcat tttgggaaga agatgaggca 540
tgaagagaat tcagacagaa acttactcag accaggggag gcagaaacta agcagagagg 600
aaaatgacca agagttagcc ctgggcatgg aatgtgaaag aaccctaaag gtgacttgga 660
aataatgccc aaggtatatt ccattctcct ggatttgttg gcattttctt gaggtgaaga 720
attgcagaat acattcttta atgtgaccta catatttacc catgtgagga agtctgctcc 780
tggactcttg agattcagtc ataaagccca ggccagggaa ataatgtaag tctgcaggcc 840
cctgtcatca gtaggattag ggagaagagt tctcagtaga aaacagggag gctggagaga 900
aaagaatggt taatgttaag gttaatataa ctagaaagac tgcagaactt aggactgatt 960
tttatttgaa tccttaaaaa aaaaaatttc ttatgaaaat agtacatggc tcttaggaga 1020
cagaacttat tgtacagagg aacagtgtga gagtcagagt gaattttatg tattattttt 1080
ggacttaggc taatgattta gcaaactctg gaatgtcagc cctaacccca accttggttt 1140
tctgtcacat gcatgtagta agtgctagat cctggacatt ctttgagatt tagtttaaga 1200
ctaagtttat tttctgatag gttatttgtg tactttcatg gattttgtaa ctctttttca 1260
acaattggat gtctcagatc tcagcatatg ggagcaagtt aatgcttcct gagatctttg 1320
ccaaaggtca agaggtcatt tttgtgtatt tataattttc catcattttt atatacttct 1380
caatattctt tttaaactat tcttttcctt ttttcatcct ctgaatactg ttttgacaga 1440
tcttgttatt agcatgcttt cagggatgag aaaactaaga aagctgaatg atttgcccaa 1500
agtagtccac ctggaaaatg aaagagagag gattccaatc caggtcttag gattcaaaag 1560
cctgtgcatg ttccattttt agtactttcc acactgtatt tctcaatgtc tttctgggac 1620
attttataaa tcatattata tcacctctaa ggatctttca gtttgttata tatgtgtcta 1680
ttaagttaga ttgtgagctc ctaaaagata aagcattgtc ttattcatct ttaaatttct 1740
cagagcccaa atagtgcctg gaacctagta gttgctcaat aaaaggtatt gaatttacag 1800
gattgaatgg tgacatcaat gaataattga agattcctta agctgataac tgacccagta 1860
gcatcattga tcatttaatt gccctggact tacttatttt ccaccacact acatatttct 1920
gtatagaata tatatagctc attgtattgc aagatttaac tagaagaaag agttcatgct 1980
tgctttgtcc atgtaggttt aacaggaatg aattgctaaa ctgtggaaaa tgttttaaac 2040
aaatgcatct tatcctgtag gaaacatctt atattgaaga caactgcaac cagaatggtg 2100
ccatttctct tatcttctcc ctgaaagaag aggtgggagc cctggcaaag gttttaaggc 2160
tctttgagga gaatgatgtg aatttgacac acattgagtc caggccttct agactcaaga 2220
aagatgaata tgagttcttc acccacctgg acaagaggag tctccctgct ctgaccaaca 2280
ttatcaagat cttgagacat gatataggag ctacagtgca tgaactttca agggataaaa 2340
agaaggacac tgtcccctgg tttcccagaa ctatccaaga attagacagg tttgccaatc 2400
agatcctgag ctatggtgca gaattagatg cagaccaccc tgggtttaaa gaccctgtgt 2460
atagagccag aagaaagcag tttgctgaca ttgcatacaa ctacaggcat gggcagccca 2520
ttcctagggt ggagtacatg gaggaagaaa aaaagacctg gggcacagtt ttcaagaccc 2580
tgaagagcct ttacaagaca catgcctgct atgaatataa ccatatattt ccattgttgg 2640
agaaatactg tggatttcat gaagataaca tcccccagct ggaggatgtt agtcagtttc 2700
tgcagacctg cacaggcttt agactgaggc cagttgcagg actgctaagt tctagggact 2760
tcctgggtgg gctagccttc agagtgttcc actgtaccca atatataagg catggatcca 2820
agcccatgta cacccctgag cctgatatct gccatgagct attgggccat gtccccctat 2880
tttctgacag aagctttgcc cagttctccc aggagattgg attagcctct ctgggagctc 2940
ctgatgagta cattgagaag ttagcaacca tctactggtt cactgtggaa tttggccttt 3000
gcaaacaagg ggatagtata aaggcttatg gagcaggtct gcttagcagt tttggagagc 3060
tgcagtactg cctgtcagaa aagccaaagc tcctaccatt agaactagaa aagactgcca 3120
tccagaacta tacagtcact gaattccagc ctctctacta tgtggctgag tctttcaatg 3180
atgccaagga gaaggtgaga aattttgcag ccaccattcc caggcccttc tctgttagat 3240
atgaccccta cactcagagg attgaggtcc tggacaatac ccagcaacta aaaattctgg 3300
ctgattccat taattctgaa attggcatcc tctgctctgc tctccagaag attaaatga 3359
<210> 387
<211> 1362
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 387
atggccgctg tggtgctgga aaatggcgtg ctgagcagaa agctgagcga cttcggccaa 60
gagacaagct acatcgagga caacagcaac cagaacggcg ctgtgtccct gatcttcagc 120
ctgaaagaag aagtgggcgc cctggccaag gtgctgagac tgtttgagga aaacgagatc 180
aacctgacgc acatcgagag cagacccagc agactgaaca aggacgagta cgagttcttc 240
acctacctgg acaagagaag caagcccgtg ctgggcagca tcatcaagag cctgagaaac 300
gacatcggcg ccaccgtgca cgagctgagc agggacaaag aaaagaacac cgtgccatgg 360
ttccccagga ccatccaaga gctggacaga ttcgccaacc agatcctgtc ttacggcgcc 420
gagctggacg ctgatcaccc tggctttaag gaccccgtgt acagagccag aagaaagcag 480
ttcgccgata tcgcctacaa ctacagacac ggccagccta ttcctagagt cgagtacacc 540
gaggaagaga gaaagacctg gggcaccgtg ttcagaaccc tgaaggccct gtacaagacc 600
cacgcctgct acgagcacaa ccacatcttc ccactgctcg aaaagtactg cggcttccgc 660
gaggataaca tccctcagct tgaggacgtg tcccagttcc tgcagacctg cacaggcttc 720
agactgaggc cagttgctgg cctgctgtcc agcagagatt ttctcggcgg cctggccttc 780
agagtgttcc actgtaccca gtacatcagg cacggcagca agcccatgta cacccctgag 840
cctgacatct gccacgagct gctgggacat gtgcctctgt tcagcgacag aagcttcgcc 900
cagttcagcc aagagatcgg cctggctagt ctgggcgctc ctgatgagta catcgagaag 960
ctggccacca tctactggtt caccgtggaa ttcggcctgt gcaaagaggg cgacagcatc 1020
aaggcttatg gcgccggact gctgtctagc tttggcgagc tgcagtactg tctgagcgac 1080
aagcctaagc tgctgcccct ggaactggaa aagaccgcct gccaagagta cacagtgacc 1140
gagttccagc ctctgtacta cgtggccgag agcttcaacg acgccaaaga aaaagtgcgg 1200
accttcgccg ctacaatccc cagacctttc agcgtcagat acgaccccta cacacagcgc 1260
gtggaagtgc tggacaacac acagcagctg aagattctgg ccgactccat caacagcgaa 1320
gtgggcatcc tgtgtcacgc cctgcagaaa atcaagagct ga 1362
<210> 388
<211> 5531
<212> ДНК
<213> Homo sapiens
<400> 388
atgtccactg cggtcctgga aaacccaggc ttgggcagga aactctctga ctttggacag 60
gtgagccacg gcagcctgag ctgctcagtt aggggaattt gggcctccag agaaagagat 120
ccgaagactg ctggtgcttc ctggtttcat aagctcagta agaagtctga attcgttgga 180
agctgatgag aatatccagg aagtcaacag acaaatgtcc tcaacaattg tttctaagta 240
ggagaacatc tgtcctcggt ggctttcaca ggaatgaatg accattgctt tagggggttg 300
gggatctggc ctccagaact gccaccaatt agctgtgtgt ctttggacaa gttactgtcc 360
ctctctgttg tctgtttact cttctgtaca ctgaaggggc tggtccctaa tgatctggga 420
tgggatgtgg aatccttcta gatttctttt gtaatattta taaagtgctc tcagcaaggt 480
atcaaaatgg caaaattgtg agtaactatc ctcctttcat tttgggaaga agatgaggca 540
tgaagagaat tcagacagaa acttactcag accaggggag gcagaaacta agcagagagg 600
aaaatgacca agagttagcc ctgggcatgg aatgtgaaag aaccctaaac gtgacttgga 660
aataatgccc aaggtatatt ccattctccg ggatttgttg gcattttctt gaggtgaaga 720
attgcagaat acattcttta atgtgaccta catatttacc catgggagga agtctgctcc 780
tggactcttg agattcagtc ataaagccca ggccagggaa ataatgtaag tctgcaggcc 840
cctgtcatca gtaggattag ggagaagagt tctcagtaga aaacagggag gctggagaga 900
aaagaatggt taatgttaac gttaatataa ctagaaagac tgcagaactt aggactgatt 960
tttatttgaa tccttaaaaa aaaaaatttc ttatgaaaat agtacatggc tcttaggaga 1020
cagaacttat tgtacagagg aacagcgtga gagtcagagt gatcccagaa caggtcctgg 1080
ctccatcctg cacatagttt tggtgctgct ggcaatacgg tccccacaac tgtgggaagg 1140
ggttaggggc agggatctca tcaggaaagc ataggggttt aaagttcttt atagagcact 1200
tagaagattg agaatccaca aattatatta ataacaaaca aagtagtgtc gtgttatata 1260
gtaaatgtga atttgcagac acatttaggg aaaagttata attaaaaaaa taggctgtat 1320
atatatcaat ggttccaaaa ttttctatgg ttaagaatca cctgggatgg ttttgaaatg 1380
gcagattcta agacaacttg attcaacagg tttaggtaaa gcccagggaa ctgcattata 1440
agaaggaatc acctgtaatt ttggagtcaa gatccaagga acactcattg agaaacactg 1500
atttacaaag tgcatggaga gaaatggagc aagtgaaggg ggatcagcat ggtgaaatat 1560
aggctgttag gagtgctatt gactaactgt ctggtgactg gaccagagta aatcttttac 1620
tttgcaagaa acaggactaa attcccatat tatgtccata gcaaagggaa ttatgtagaa 1680
aaattgataa ttaggagcct gagttcttga ccagcctcca ctacctatgt ggcctcaggt 1740
gagttatttt ctccctttgg ctctaagttt tccccatctg taatgtaagg gagtttaact 1800
agatgagcac taaggacaaa tcaatttctg tgagtcaatt attatgaaat accatgtggg 1860
catcaaatgc caagtggaaa gcatagataa agaagtgatt gtgcacctgg gctgagggga 1920
acaaacattt cctaagagaa ttgagaccca aaagagcctt taaggaaggt gagatcttgg 1980
aaagggaaat ttggtgaata ctctaatgag gagctaaaaa ggcaagaaag aaagcagctt 2040
ggctggaaag gaggttcctg taggtgggcc tccagagatt cggtaccaca gaaactgcca 2100
aacatcagca agaagccatg gggatggagc gtttgaggga ttctaaatag aaggacaaga 2160
gtaaaaatgt caggctggat cgatgcaggc cactaagaaa tggattcagg tgatggcagt 2220
gggaagaaag gacctgatgc ccagaggcat ttctggagaa gatgagatca gacttgtgat 2280
tggctgaaca cacactgtag tggggtgggg tttagggggt gactcaactt caagcccagg 2340
tacattcaag tctgaattgc cctagtcaaa agtggcatct gtggatgtgt atcagaaata 2400
tcttactttt cttggaagcc aacaggagaa aagagtgcta ccaagtgaac tagagacagg 2460
aatatctttt gtcatttcaa ggaaactgga aagaagaagg ctcagtattc tttagtagga 2520
agaagactta agtcagagac tcatctgtac ctctctggca gggtttaaaa gggggaagag 2580
gaatagaggc tgcaagagat tgtgattcat ggacagtatg cagagatcaa atgacctggg 2640
ttcagatcct ggctccactg ctaactgtgt aactataggc aagttcctta acctctctaa 2700
gccttaatct tgtcatcaat aaaagggggc acttggtgcc taataaaacc tacctcttag 2760
gttgttgcca aattacatga gataatccaa atcaagtgct tattataata cccagaaatt 2820
ataggctcta aataaatgtt tatataggct ctaaataaat gaagtttttt agaaagataa 2880
catcatgatc aaaatgggat atttaacagt ttagtcttcc atttcatttg aagctcccta 2940
aaatcactct tgctgataaa tttgtttttt ccttcacacc tcagtttcat gggatgtttt 3000
ggcaaaaatc tgaattttct gaattgaaag aattttttgc taagggtcat cagtattcat 3060
gcagggcttg ttattctgag tcactaagag tttcctaaca cagccttctc tcattgagat 3120
gatgtaacat ctattccatt aatttcatta acttgcttac aagagagtaa ttgttctgca 3180
aatttttttc ttcccagttt taggtacctg ctgcttattg tggacacaca tagaatttta 3240
tgtattattt ttcgacttag gctaatgatt tagcaaactc tggaatgtca gccctaaccc 3300
caaccttggt tttctgtcac atgcatgtag taagtgctag atcctggaca ttctttgaga 3360
tttagtttaa gactaagttt attttctgat aggttatttg tgtactttca tggattttgt 3420
aactcttttt caacaattgg atgtctcaga tctcagcata tgggagcaag ttaatgcttc 3480
ctgagatctt tgccaaaggt caagaggtca tttttgtgta tttataattt tccatcattt 3540
ttatatactt ctcaatattc tttttaaact attcttttcc ttttttcatc ctctgaatac 3600
tgttttgaca gatcttgtta ttagcatgct ttcacggatg agaaaactaa gaaagctgaa 3660
tgatttgccc aaagtagtcc acctggaaaa tgaaagagag aggattccaa tccaggtctt 3720
acgattcaaa agcctgtgca tgttccattt ttagtacttt ccacactgta tttctcaatg 3780
tctttctggg acattttata aatcatatta tatcacctct aaggatcttt cagtttgtta 3840
tatatgtgtc tattaagtta gattgtgagc tcctaaaaga taaagcattg tcttattcat 3900
ctttaaattt ctcagagccc aaatagtgcc tggaacctag tagttgctca ataaaaggta 3960
ttgaatttac aggattgaat ggtgacatca atgaataatt gaagattcct taagctgata 4020
actgacccag tagcatcatt gatcatttaa ttgccctgga cttacttatt ttccaccaca 4080
ctacatattt ctgtatagaa tatatatagc tcattgtatt gcaagattta actagaagaa 4140
agagttcatg cttgctttgt ccatggaggt ttaacaggaa tgaattgcta aactgtggaa 4200
aatgttttaa acaaatgcat cttatcctgt aggaaacaag ctatattgaa gacaactgca 4260
atcaaaatgg tgccatatca ctgatcttct cactcaaaga agaagttggt gcattggcca 4320
aagtattgcg cttatttgag gagaatgatg taaacctgac ccacattgaa tctagacctt 4380
ctcgtttaaa gaaagatgag tatgaatttt tcacccattt ggataaacgt agcctgcctg 4440
ctctgacaaa catcatcaag atcttgaggc atgacattgg tgccactgtc catgagcttt 4500
cacgagataa gaagaaagac acagtgccct ggttcccaag aaccattcaa gagctggaca 4560
gatttgccaa tcagattctc agctatggag cggaactgga tgctgaccac cctggtttta 4620
aagatcctgt gtaccgtgca agacggaagc agtttgctga cattgcctac aactaccgcc 4680
atgggcagcc catccctcga gtggaataca tggaggaaga aaagaaaaca tggggcacag 4740
tgttcaagac tctgaagtcc ttgtataaaa cccatgcttg ctatgagtac aatcacattt 4800
ttccacttct tgaaaagtac tgtggcttcc atgaagataa cattccccag ctggaagacg 4860
tttctcaatt cctgcagact tgcactggtt tccgcctccg acctgtggct ggcctgcttt 4920
cctctcggga tttcttgggt ggcctggcct tccgagtctt ccactgcaca cagtacatca 4980
gacatggatc caagcccatg tatacccccg aacctgacat ctgccatgag ctgttgggac 5040
atgtgccctt gttttcagat cgcagctttg cccagttttc ccaggaaatt ggccttgcct 5100
ctctgggtgc acctgatgaa tacattgaaa agctcgccac aatttactgg tttactgtgg 5160
agtttgggct ctgcaaacaa ggagactcca taaaggcata tggtgctggg ctcctgtcat 5220
cctttggtga attacagtac tgcttatcag agaagccaaa gcttctcccc ctggagctgg 5280
agaagacagc catccaaaat tacactgtca cggagttcca gcccctgtat tacgtggcag 5340
agagttttaa tgatgccaag gagaaagtaa ggaactttgc tgccacaata cctcggccct 5400
tctcagttcg ctacgaccca tacacccaaa ggattgaggt cttggacaat acccagcagc 5460
ttaagatttt ggctgattcc attaacagtg aaattggaat cctttgcagt gccctccaga 5520
aaataaagta a 5531
<210> 389
<211> 1359
<212> ДНК
<213> Homo sapiens
<400> 389
atgtccactg cggtcctgga aaacccaggc ttgggcagga aactctctga ctttggacag 60
gaaacaagct atattgaaga caactgcaat caaaatggtg ccatatcact gatcttctca 120
ctcaaagaag aagttggtgc attggccaaa gtattgcgct tatttgagga gaatgatgta 180
aacctgaccc acattgaatc tagaccttct cgtttaaaga aagatgagta tgaatttttc 240
acccatttgg ataaacgtag cctgcctgct ctgacaaaca tcatcaagat cttgaggcat 300
gacattggtg ccactgtcca tgagctttca cgagataaga agaaagacac agtgccctgg 360
ttcccaagaa ccattcaaga gctggacaga tttgccaatc agattctcag ctatggagcg 420
gaactggatg ctgaccaccc tggttttaaa gatcctgtgt accgtgcaag acggaagcag 480
tttgctgaca ttgcctacaa ctaccgccat gggcagccca tccctcgagt ggaatacatg 540
gaggaagaaa agaaaacatg gggcacagtg ttcaagactc tgaagtcctt gtataaaacc 600
catgcttgct atgagtacaa tcacattttt ccacttcttg aaaagtactg tggcttccat 660
gaagataaca ttccccagct ggaagacgtt tctcaattcc tgcagacttg cactggtttc 720
cgcctccgac ctgtggctgg cctgctttcc tctcgggatt tcttgggtgg cctggccttc 780
cgagtcttcc actgcacaca gtacatcaga catggatcca agcccatgta tacccccgaa 840
cctgacatct gccatgagct gttgggacat gtgcccttgt tttcagatcg cagctttgcc 900
cagttttccc aggaaattgg ccttgcctct ctgggtgcac ctgatgaata cattgaaaag 960
ctcgccacaa tttactggtt tactgtggag tttgggctct gcaaacaagg agactccata 1020
aaggcatatg gtgctgggct cctgtcatcc tttggtgaat tacagtactg cttatcagag 1080
aagccaaagc ttctccccct ggagctggag aagacagcca tccaaaatta cactgtcacg 1140
gagttccagc ccctgtatta cgtggcagag agttttaatg atgccaagga gaaagtaagg 1200
aactttgctg ccacaatacc tcggcccttc tcagttcgct acgacccata cacccaaagg 1260
attgaggtct tggacaatac ccagcagctt aagattttgg ctgattccat taacagtgaa 1320
attggaatcc tttgcagtgc cctccagaaa ataaagtaa 1359
<210> 390
<211> 1451
<212> ДНК
<213> Homo sapiens
<400> 390
atgtccactg cggtcctgga aaacccaggc ttgggcagga aactctctga ctttggacag 60
aagaggtaag ggtttaaggg atggttggtt ggtggggtat taatgtttaa ttacctggag 120
cacctgcctg aaatcacttt ttttcaggtt gggaaacaag ctatattgaa gacaactgca 180
atcaaaatgg tgccatatca ctgatcttct cactcaaaga agaagttggt gcattggcca 240
aagtattgcg cttatttgag gagaatgatg taaacctgac ccacattgaa tctagacctt 300
ctcgtttaaa gaaagatgag tatgaatttt tcacccattt ggataaacgt agcctgcctg 360
ctctgacaaa catcatcaag atcttgaggc atgacattgg tgccactgtc catgagcttt 420
cacgagataa gaagaaagac acagtgccct ggttcccaag aaccattcaa gagctggaca 480
gatttgccaa tcagattctc agctatggag cggaactgga tgctgaccac cctggtttta 540
aagatcctgt gtaccgtgca agacggaagc agtttgctga cattgcctac aactaccgcc 600
atgggcagcc catccctcga gtggaataca tggaggaaga aaagaaaaca tggggcacag 660
tgttcaagac tctgaagtcc ttgtataaaa cccatgcttg ctatgagtac aatcacattt 720
ttccacttct tgaaaagtac tgtggcttcc atgaagataa cattccccag ctggaagacg 780
tttctcaatt cctgcagact tgcactggtt tccgcctccg acctgtggct ggcctgcttt 840
cctctcggga tttcttgggt ggcctggcct tccgagtctt ccactgcaca cagtacatca 900
gacatggatc caagcccatg tatacccccg aacctgacat ctgccatgag ctgttgggac 960
atgtgccctt gttttcagat cgcagctttg cccagttttc ccaggaaatt ggccttgcct 1020
ctctgggtgc acctgatgaa tacattgaaa agctcgccac aatttactgg tttactgtgg 1080
agtttgggct ctgcaaacaa ggagactcca taaaggcata tggtgctggg ctcctgtcat 1140
cctttggtga attacagtac tgcttatcag agaagccaaa gcttctcccc ctggagctgg 1200
agaagacagc catccaaaat tacactgtca cggagttcca gcccctgtat tacgtggcag 1260
agagttttaa tgatgccaag gagaaagtaa ggaactttgc tgccacaata cctcggccct 1320
tctcagttcg ctacgaccca tacacccaaa ggattgaggt cttggacaat acccagcagc 1380
ttaagatttt ggctgattcc attaacagtg aaattggaat cctttgcagt gccctccaga 1440
aaataaagta a 1451
<210> 391
<211> 1588
<212> ДНК
<213> Homo sapiens
<400> 391
atgtccactg cggtcctgga aaacccaggc ttgggcagga aactctctga ctttggacag 60
gtgagccacg gcagcctgag ctgctcagtt aggggaattt gggcctccag agaaagagat 120
ccgaagactg ctggtgcttc ctggtttcat aagctcagta agaagtctga attcgttgga 180
agctgatgat agaagaaaga gttcatgctt gctttgtcca tggaggttta acaggaatga 240
attgctaaac tgtggaaaat gttttaaaca aatgcatctt atcctgtagg aaacaagcta 300
tattgaagac aactgcaatc aaaatggtgc catatcactg atcttctcac tcaaagaaga 360
agttggtgca ttggccaaag tattgcgctt atttgaggag aatgatgtaa acctgaccca 420
cattgaatct agaccttctc gtttaaagaa agatgagtat gaatttttca cccatttgga 480
taaacgtagc ctgcctgctc tgacaaacat catcaagatc ttgaggcatg acattggtgc 540
cactgtccat gagctttcac gagataagaa gaaagacaca gtgccctggt tcccaagaac 600
cattcaagag ctggacagat ttgccaatca gattctcagc tatggagcgg aactggatgc 660
tgaccaccct ggttttaaag atcctgtgta ccgtgcaaga cggaagcagt ttgctgacat 720
tgcctacaac taccgccatg ggcagcccat ccctcgagtg gaatacatgg aggaagaaaa 780
gaaaacatgg ggcacagtgt tcaagactct gaagtccttg tataaaaccc atgcttgcta 840
tgagtacaat cacatttttc cacttcttga aaagtactgt ggcttccatg aagataacat 900
tccccagctg gaagacgttt ctcaattcct gcagacttgc actggtttcc gcctccgacc 960
tgtggctggc ctgctttcct ctcgggattt cttgggtggc ctggccttcc gagtcttcca 1020
ctgcacacag tacatcagac atggatccaa gcccatgtat acccccgaac ctgacatctg 1080
ccatgagctg ttgggacatg tgcccttgtt ttcagatcgc agctttgccc agttttccca 1140
ggaaattggc cttgcctctc tgggtgcacc tgatgaatac attgaaaagc tcgccacaat 1200
ttactggttt actgtggagt ttgggctctg caaacaagga gactccataa aggcatatgg 1260
tgctgggctc ctgtcatcct ttggtgaatt acagtactgc ttatcagaga agccaaagct 1320
tctccccctg gagctggaga agacagccat ccaaaattac actgtcacgg agttccagcc 1380
cctgtattac gtggcagaga gttttaatga tgccaaggag aaagtaagga actttgctgc 1440
cacaatacct cggcccttct cagttcgcta cgacccatac acccaaagga ttgaggtctt 1500
ggacaatacc cagcagctta agattttggc tgattccatt aacagtgaaa ttggaatcct 1560
ttgcagtgcc ctccagaaaa taaagtaa 1588
<210> 392
<211> 1398
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 392
atggcagctg ttgtcctgga gaacggagtc ctgagcagaa aactctcaga ctttgggcag 60
gaaacaagtt acatcgaaga caactccaat caaaatggtg ctgtatctct gatattctca 120
ctcaaagagg aagttggtgc cctggccaag gtcctgcgct tatttgagga gaatgagatc 180
aacctgacac acattgaatc cagaccttcc cgtttaaaca aagatgagta tgagtttttc 240
acctatctgg ataagcgtag caagcccgtc ctgggcagca tcatcaagag cctgaggaac 300
gacattggtg ccactgtcca tgagctttcc cgagacaagg aaaagaacac agtgccctgg 360
ttcccaagga ccattcagga gctggacaga ttcgccaatc agattctcag ctatggagcc 420
gaactggatg cagaccaccc aggctttaaa gatcctgtgt accgggcgag acgaaagcag 480
tttgctgaca ttgcctacaa ctaccgccat gggcagccca ttcctcgggt ggaatacaca 540
gaggaggaga ggaagacctg gggaacggtg ttcaggactc tgaaggcctt gtataaaaca 600
catgcctgct acgagcacaa ccacatcttc cctcttctgg aaaagtactg cggtttccgt 660
gaagacaaca tcccgcagct ggaagatgtt tctcagtttc tgcagacttg tactggtttc 720
cgcctccgtc ctgttgctgg cttactgtcg tctcgagatt tcttgggtgg cctggccttc 780
cgagtcttcc actgcacaca gtacattagg catggatcta agcccatgta cacacctgaa 840
cctgatatct gtcatgaact cttgggacat gtgcccttgt tttcagatag aagctttgcc 900
cagttttctc aggaaattgg gcttgcatcg ctgggggcac ctgatgagta cattgagaaa 960
ctggccacaa tttactggtt tactgtggag tttgggcttt gcaaggaagg agattctata 1020
aaggcatatg gtgctgggct cttgtcatcc tttggagaat tacagtactg tttatcagac 1080
aagccaaagc tcctgcccct ggagctagag aagacagcct gccaggagta tactgtcaca 1140
gagttccagc ctctgtacta tgtggccgag agtttcaatg atgccaagga gaaagtgagg 1200
acttttgctg ccacaatccc ccggcccttc tccgttcgct atgaccccta cactcaaagg 1260
gttgaggtcc tggacaatac tcagcagttg aagattttag ctgactccat taatagtgag 1320
gttggaatcc tttgccatgc cctgcagaaa ataaagtcag ggggtggagg ctctcatcac 1380
catcaccatc actaatga 1398
<210> 393
<211> 1395
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 393
atggccgctg tggtgctgga gaacggcgtg ctgtccagaa agctgtctga cttcggacag 60
gagaccagct acatcgagga taactccaac cagaacggcg ccgtgagcct gatcttctcc 120
ctgaaggagg aagtgggagc cctggctaag gtgctgagac tgtttgagga gaacgagatc 180
aacctgaccc acatcgagtc caggccttct agactgaaca aggacgagta cgagttcttt 240
acatacctgg ataagcggtc taagccagtg ctgggctcta tcatcaagag cctgagaaac 300
gatatcggag ctaccgtgca cgagctgagc cgggacaagg agaagaacac cgtgccctgg 360
ttccccagga caatccagga gctggataga tttgccaacc agatcctgag ctacggagct 420
gagctggacg ctgatcaccc tggattcaag gaccccgtgt accgcgctag gagaaagcag 480
tttgccgaca tcgcttacaa ctacaggcac ggacagccaa tccctcgcgt ggagtacaca 540
gaggaggaga ggaagacctg gggaacagtg ttcagaaccc tgaaggccct gtacaagaca 600
cacgcttgct acgagcacaa ccacatcttc cccctgctgg agaagtactg tggctttagg 660
gaggacaaca tccctcagct ggaggacgtg agccagttcc tgcagacctg cacaggattt 720
aggctgaggc cagtggccgg actgctgagc tcccgggatt tcctgggcgg actggctttc 780
cgcgtgtttc actgcaccca gtacatcagg cacggctcta agccaatgta cacaccagag 840
cccgatatct gtcacgagct gctgggacac gtgcccctgt ttagcgaccg gtccttcgcc 900
cagttttctc aggagatcgg cctggccagc ctgggagctc ctgacgagta catcgagaag 960
ctggctacca tctactggtt cacagtggag tttggcctgt gcaaggaggg agattccatc 1020
aaggcctacg gcgctggact gctgtctagc ttcggcgagc tgcagtactg cctgtctgac 1080
aagccaaagc tgctgcccct ggagctggag aagaccgcct gtcaggagta caccgtgaca 1140
gagttccagc ccctgtacta cgtggccgag agctttaacg acgctaagga gaaggtgcgc 1200
accttcgccg ctacaatccc tcggccattt tccgtgcgct acgaccctta cacccagagg 1260
gtggaggtgc tggataacac acagcagctg aagatcctgg ccgactctat caacagcgaa 1320
gtgggcatcc tgtgccacgc tctgcagaag atcaagtccg gaggaggagg atctcatcac 1380
caccaccacc actga 1395
<210> 394
<211> 1363
<212> ДНК
<213> Homo sapiens
<400> 394
atgtccactg cggtcctgga aaacccaggc ttgggcagga aactctctga ctttggacag 60
gaaacaagct atattgaaga caactgcaat caaaatggtg ccatatcact gatcttctca 120
ctcaaagaag aagttggtgc attggccaaa gtattgcgct tatttgagga gaatgatgta 180
aacctgaccc acattgaatc tagaccttct cgtttaaaga aagatgagta tgaatttttc 240
acccatttgg ataaacgtag cctgcctgct ctgacaaaca tcatcaagat cttgaggcat 300
gacattggtg ccactgtcca tgagctttca cgagataaga agaaagacac agtgccctgg 360
ttcccaagaa ccattcaaga gctggacaga tttgccaatc agattctcag ctatggagcg 420
gaactggatg ctgaccaccc tggttttaaa gatcctgtgt accgtgcaag acggaagcag 480
tttgctgaca ttgcctacaa ctaccgccat gggcagccca tccctcgagt ggaatacatg 540
gaggaagaaa agaaaacatg gggcacagtg ttcaagactc tgaagtcctt gtataaaacc 600
catgcttgct atgagtacaa tcacattttt ccacttcttg aaaagtactg tggcttccat 660
gaagataaca ttccccagct ggaagacgtt tctcagttcc tgcagacttg cactggtttc 720
cgcctccgac ctgtggctgg cctgctttcc tctcgggatt tcttgggtgg cctggccttc 780
cgagtcttcc actgcacaca gtacatcaga catggatcca agcccatgta tacccccgaa 840
cctgacatct gccatgagct gttgggacat gtgcccttgt tttcagatcg cagctttgcc 900
cagttttccc aggaaattgg ccttgcctct ctgggtgcac ctgatgaata cattgaaaag 960
ctcgccacaa tttactggtt tactgtggag tttgggctct gcaaacaagg agactccata 1020
aaggcatatg gtgctgggct cctgtcatcc tttggtgaat tacagtactg cttatcagag 1080
aagccaaagc ttctccccct ggagctggag aagacagcca tccaaaatta cactgtcacg 1140
gagttccagc ccctctatta cgtggcagag agttttaatg atgccaagga gaaagtaagg 1200
aactttgctg ccacaatacc tcggcccttc tcagttcgct acgacccata cacccaaagg 1260
attgaggtct tggacaatac ccagcagctt aagattttgg ctgattccat taacagtgaa 1320
attggaatcc tttgcagtgc cctccagaaa ataaagtaat taa 1363
<210> 395
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический пептид
<400> 395
Gly Gly Gly Gly Ser
1 5
<210> 396
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая метка 6xHis
<400> 396
His His His His His His
1 5
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| НЕВИРУСНЫЕ ДНК-ВЕКТОРЫ И ИХ ПРИМЕНЕНИЕ ДЛЯ ПРОДУЦИРОВАНИЯ АНТИТЕЛ И СЛИТЫХ БЕЛКОВ | 2019 |
|
RU2800914C2 |
| ДНК С ЗАМКНУТЫМИ КОНЦАМИ (зкДНК) И ПРИМЕНЕНИЕ В СПОСОБАХ УМЕНЬШЕНИЯ ИММУННОГО ОТВЕТА, СВЯЗАННОГО С ГЕННОЙ ТЕРАПИЕЙ ИЛИ ТЕРАПИЕЙ НУКЛЕИНОВОЙ КИСЛОТОЙ | 2020 |
|
RU2829367C2 |
| ДНК-ВЕКТОРЫ С ЗАМКНУТЫМИ КОНЦАМИ, ПОЛУЧАЕМЫЕ ПУТЕМ БЕСКЛЕТОЧНОГО СИНТЕЗА, И СПОСОБ ПОЛУЧЕНИЯ зкДНК-ВЕКТОРОВ | 2019 |
|
RU2820586C2 |
| НЕВИРУСНЫЕ ДНК-ВЕКТОРЫ И ВАРИАНТЫ ИХ ПРИМЕНЕНИЯ ДЛЯ ЭКСПРЕССИИ ТЕРАПЕВТИЧЕСКОГО СРЕДСТВА НА ОСНОВЕ ФАКТОРА VIII (FVIII) | 2020 |
|
RU2812852C2 |
| МОДИФИЦИРОВАННАЯ ДНК С ЗАМКНУТЫМИ КОНЦАМИ (зкДНК), СОДЕРЖАЩАЯ СИММЕТРИЧНЫЕ МОДИФИЦИРОВАННЫЕ ИНВЕРТИРОВАННЫЕ КОНЦЕВЫЕ ПОВТОРЫ | 2019 |
|
RU2816963C2 |
| МОДИФИЦИРОВАННАЯ ДНК С ЗАМКНУТЫМИ КОНЦАМИ (зкДНК) | 2018 |
|
RU2800026C2 |
| РЕДАКТИРОВАНИЕ ГЕНОВ С ИСПОЛЬЗОВАНИЕМ МОДИФИЦИРОВАННОЙ ДНК С ЗАМКНУТЫМИ КОНЦАМИ (зкДНК) | 2018 |
|
RU2811724C2 |
| МОДУЛЯЦИЯ АКТИВНОСТИ REP БЕЛКА ПРИ ПОЛУЧЕНИИ ДНК С ЗАМКНУТЫМИ КОНЦАМИ (ЗКДНК) | 2020 |
|
RU2812850C2 |
| КОНТРОЛИРУЕМАЯ ЭКСПРЕССИЯ ТРАНСГЕНОВ С ИСПОЛЬЗОВАНИЕМ ДНК-ВЕКТОРОВ С ЗАМКНУТЫМИ КОНЦАМИ (зкДНК) | 2019 |
|
RU2816871C2 |
| СОСТАВЫ НЕВИРУСНЫХ БЕСКАПСИДНЫХ ДНК-ВЕКТОРОВ НА ОСНОВЕ ЛИПИДНЫХ НАНОЧАСТИЦ | 2018 |
|
RU2778407C2 |
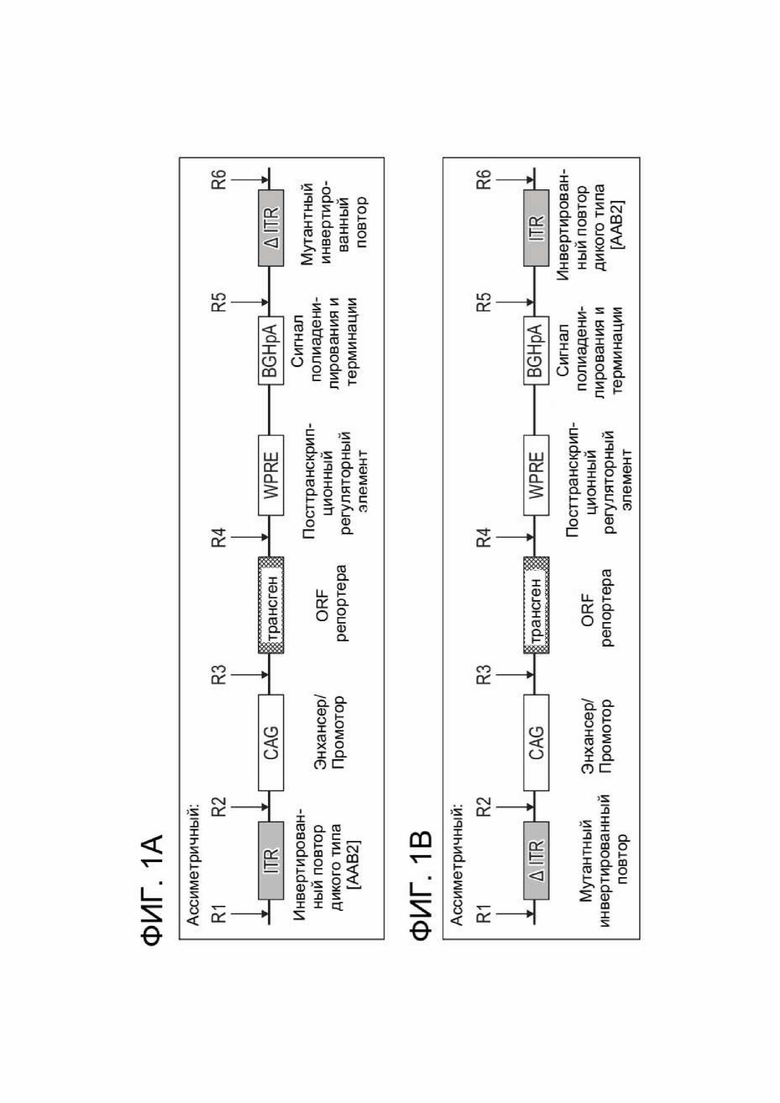
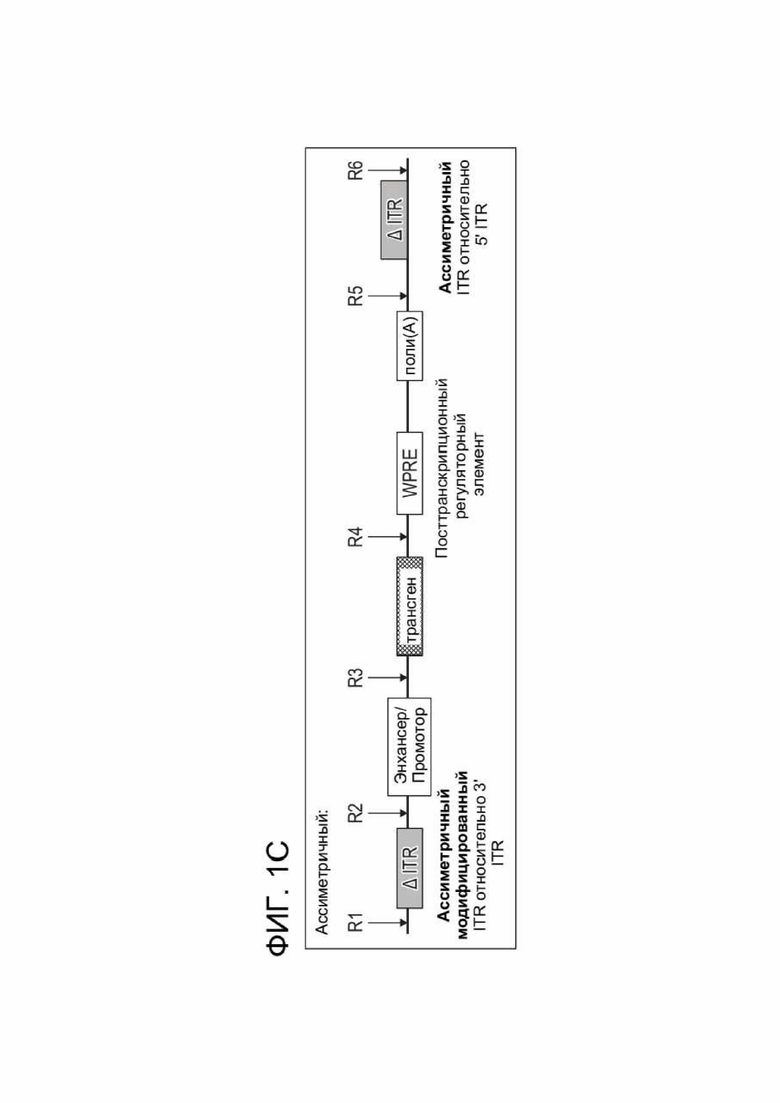
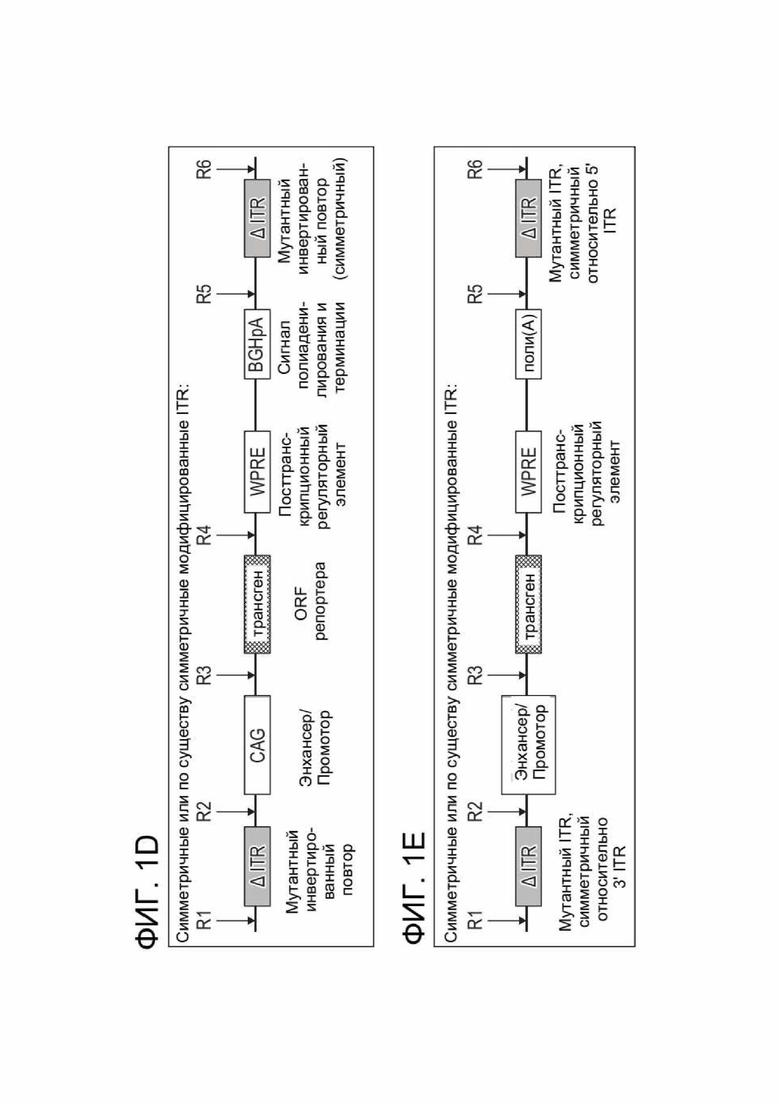
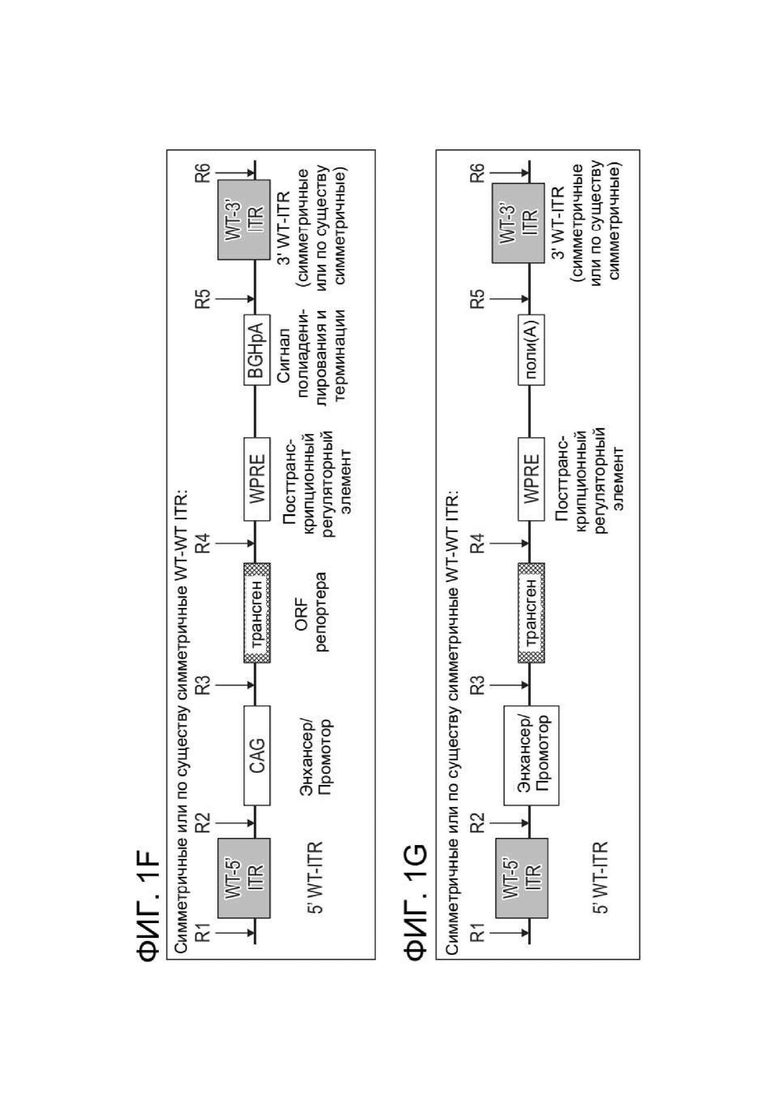
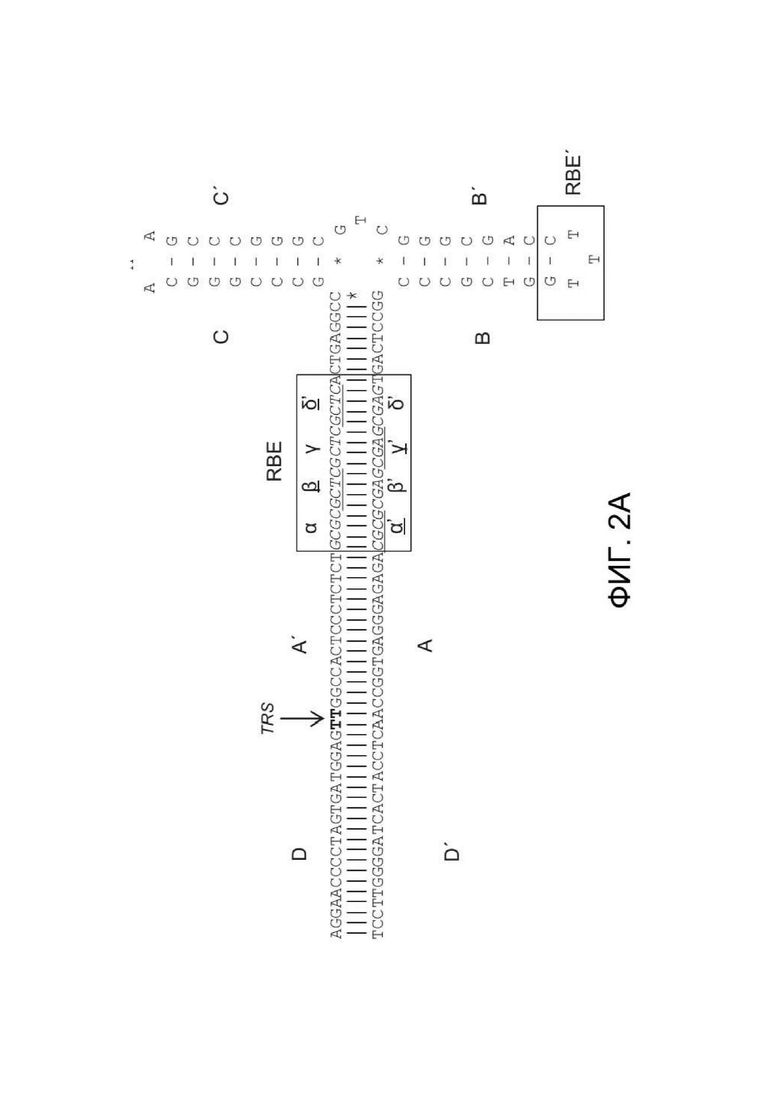
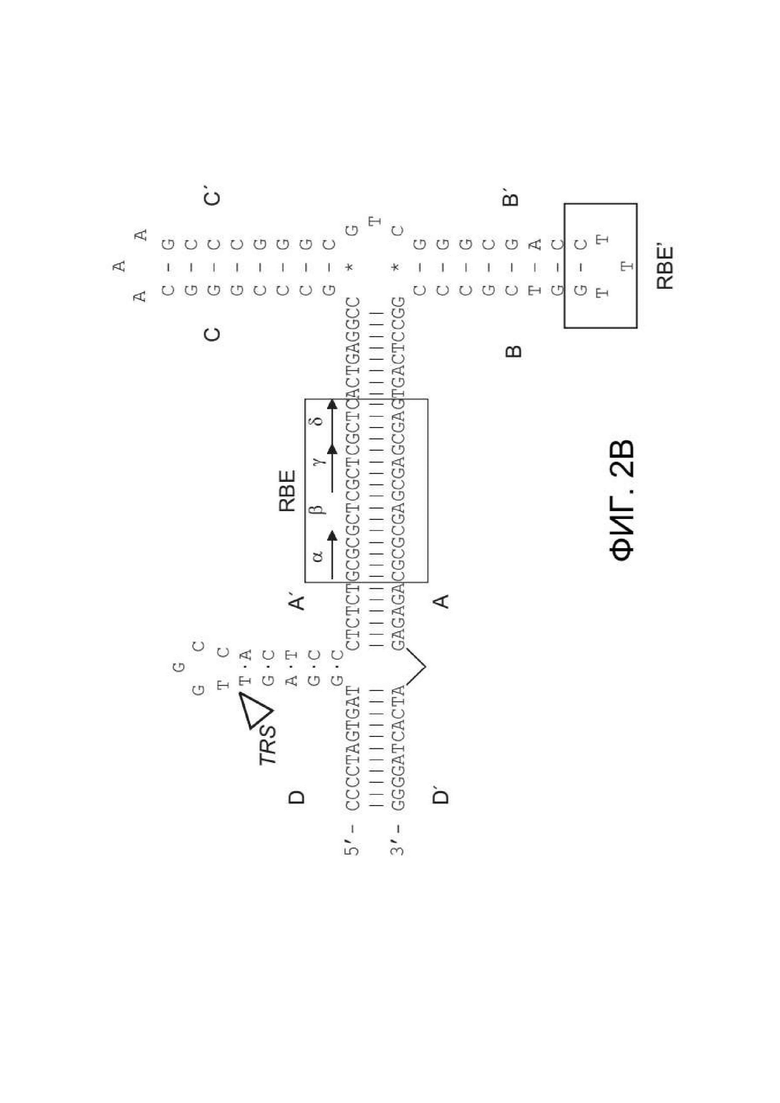
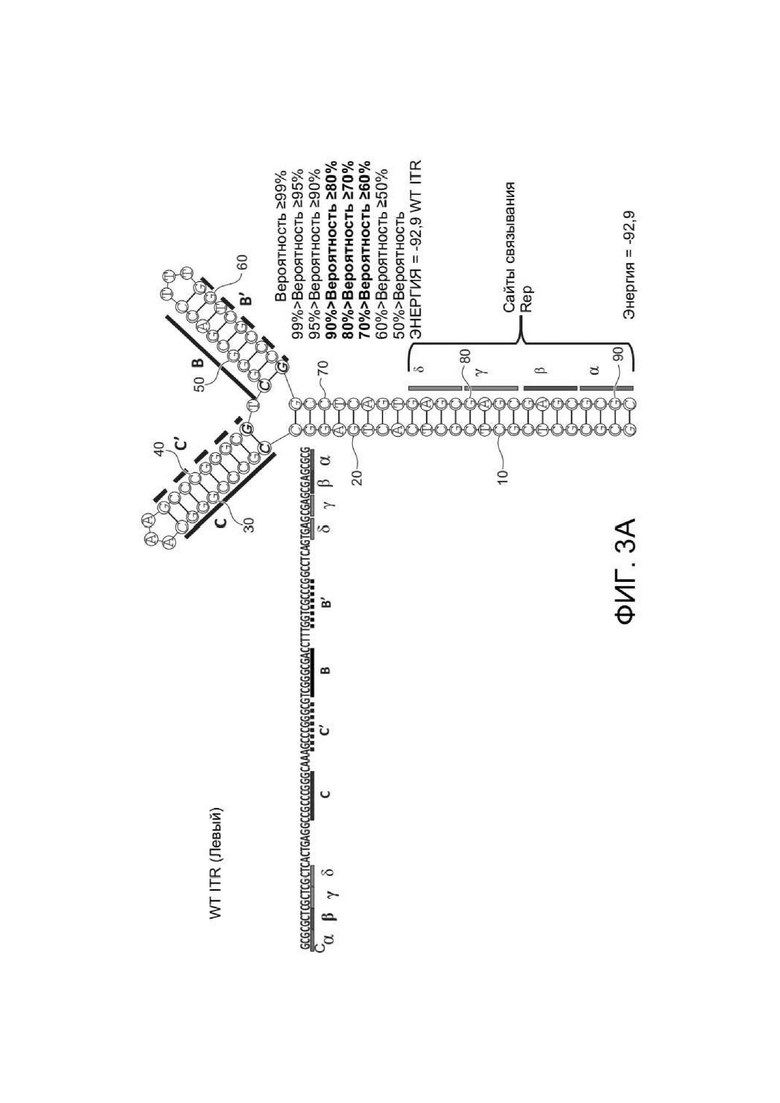
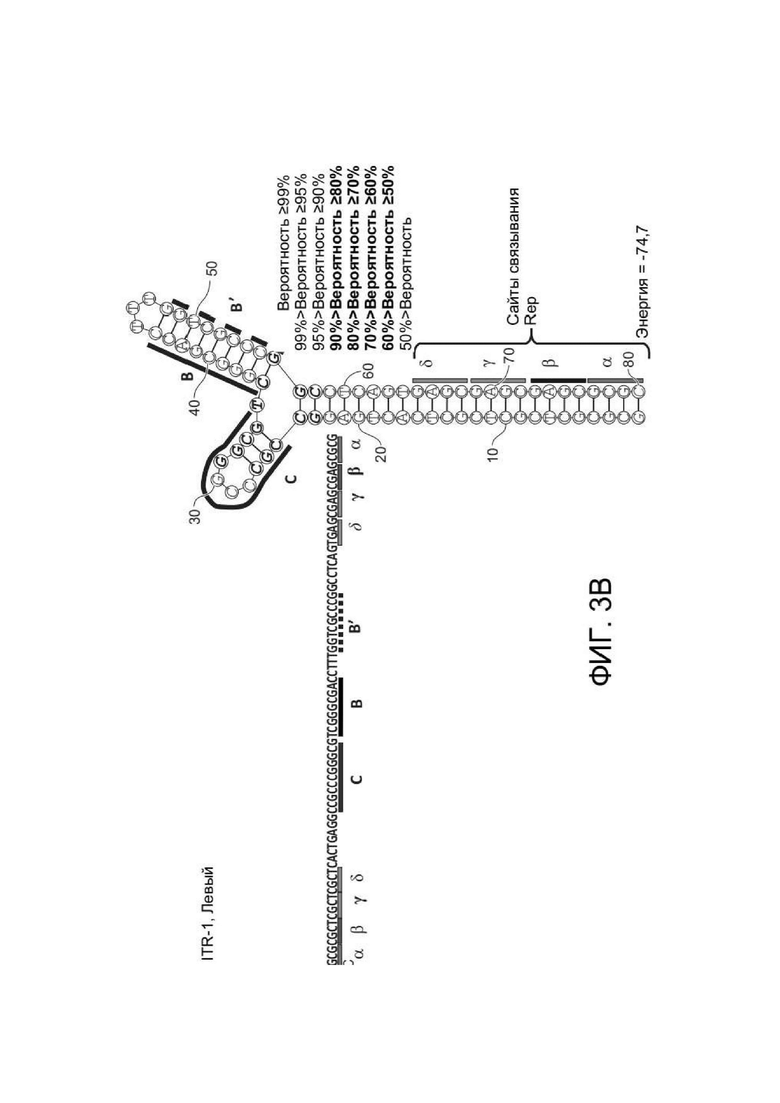
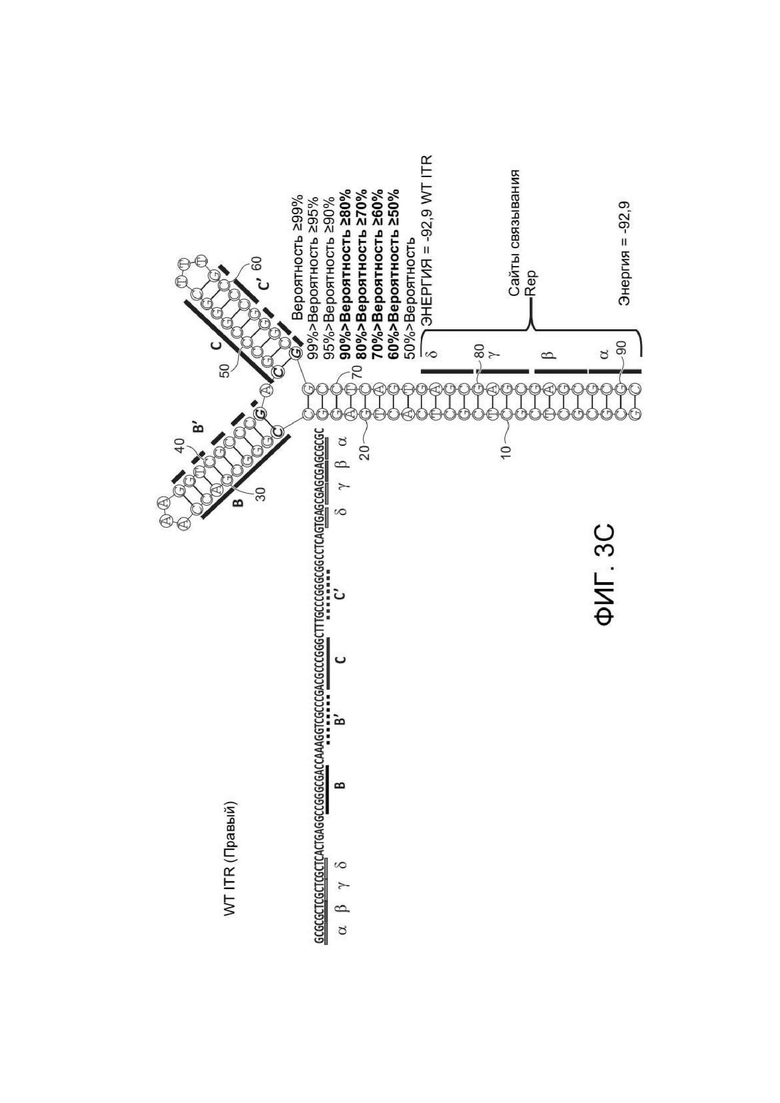
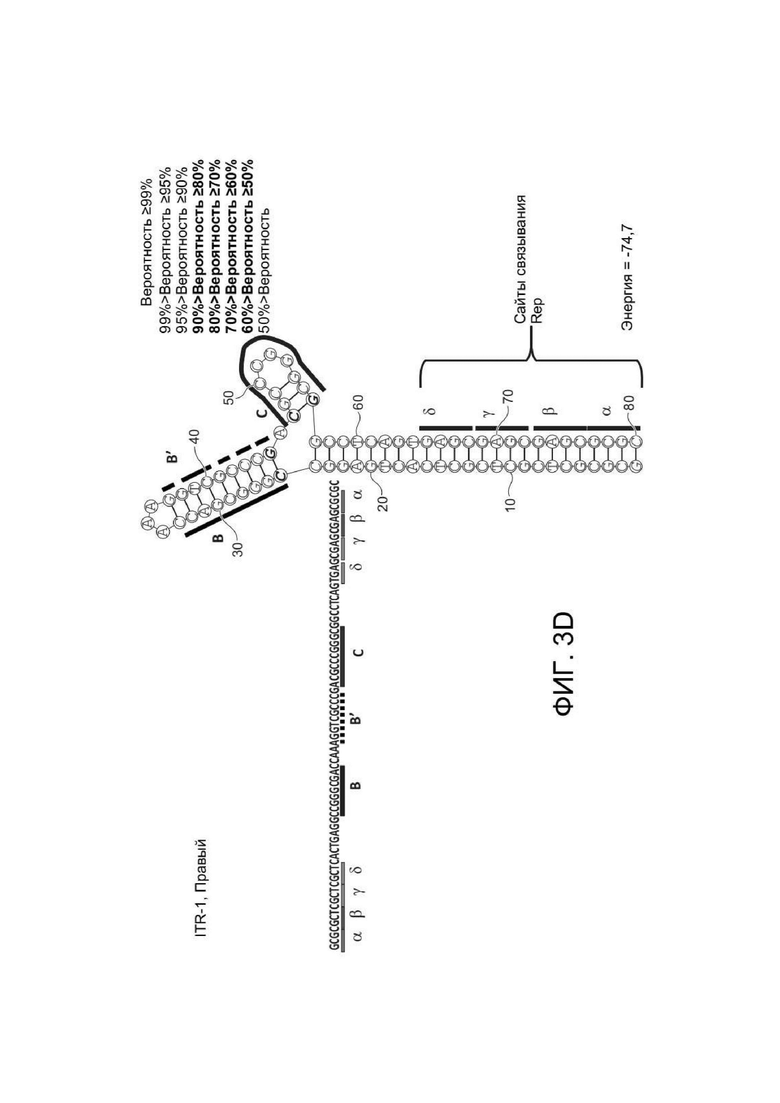
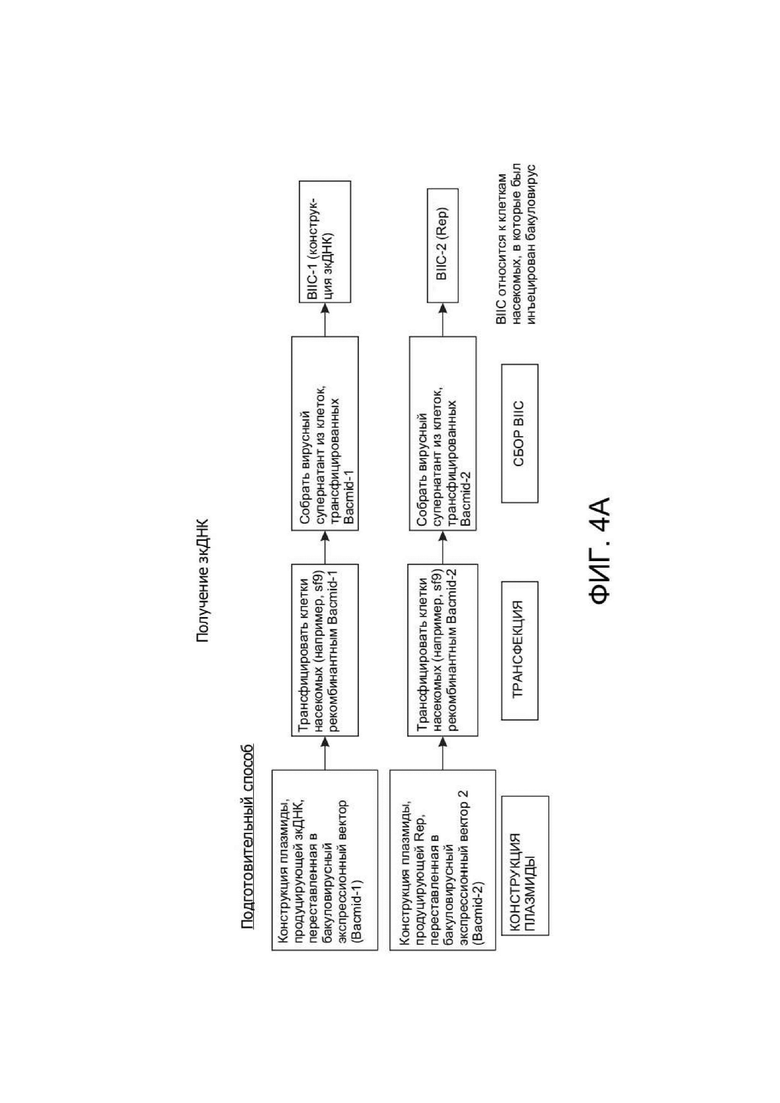
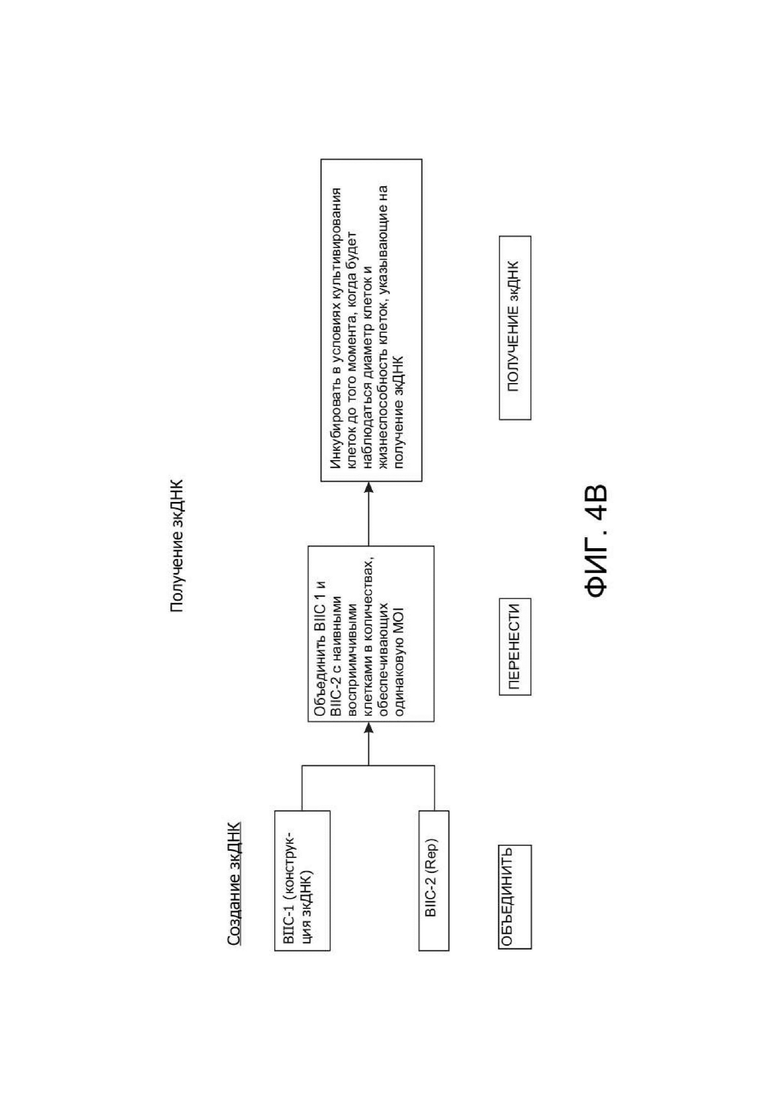
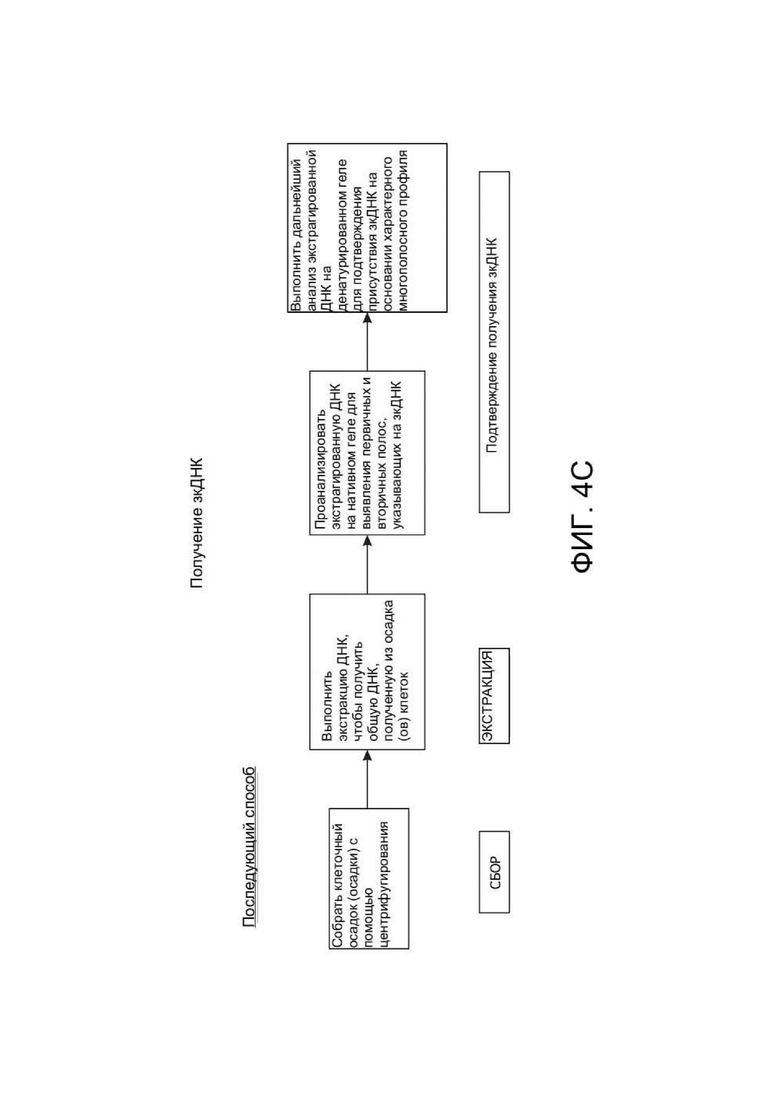
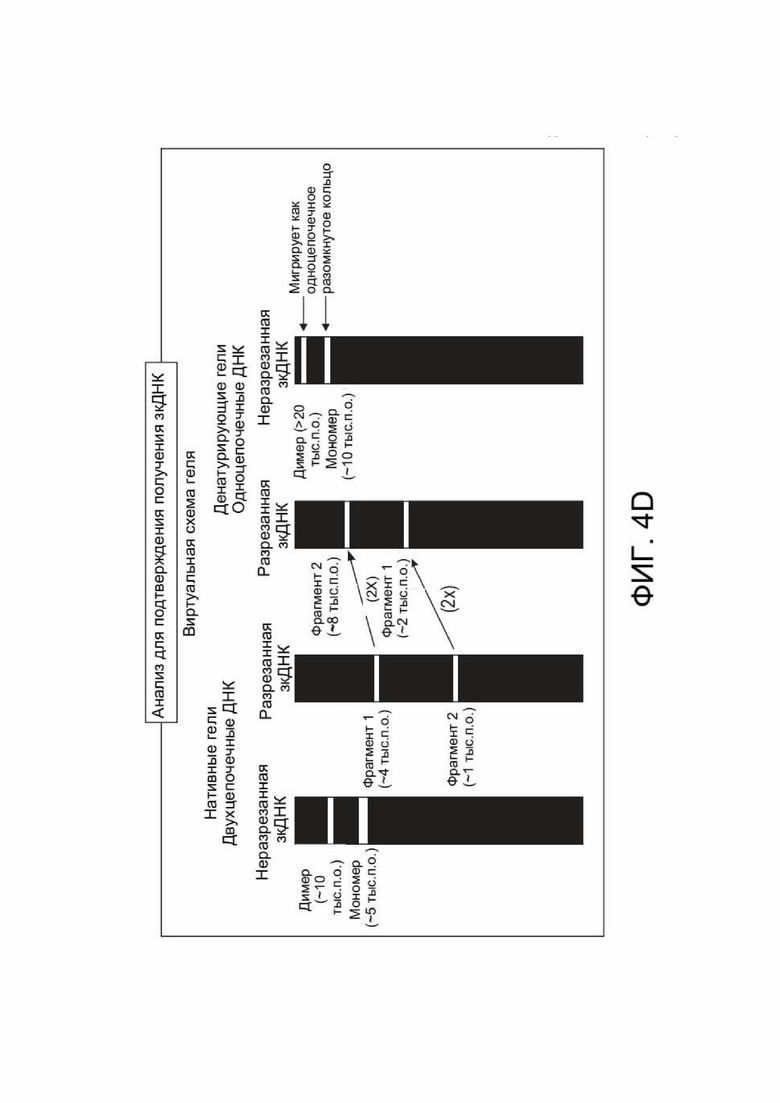
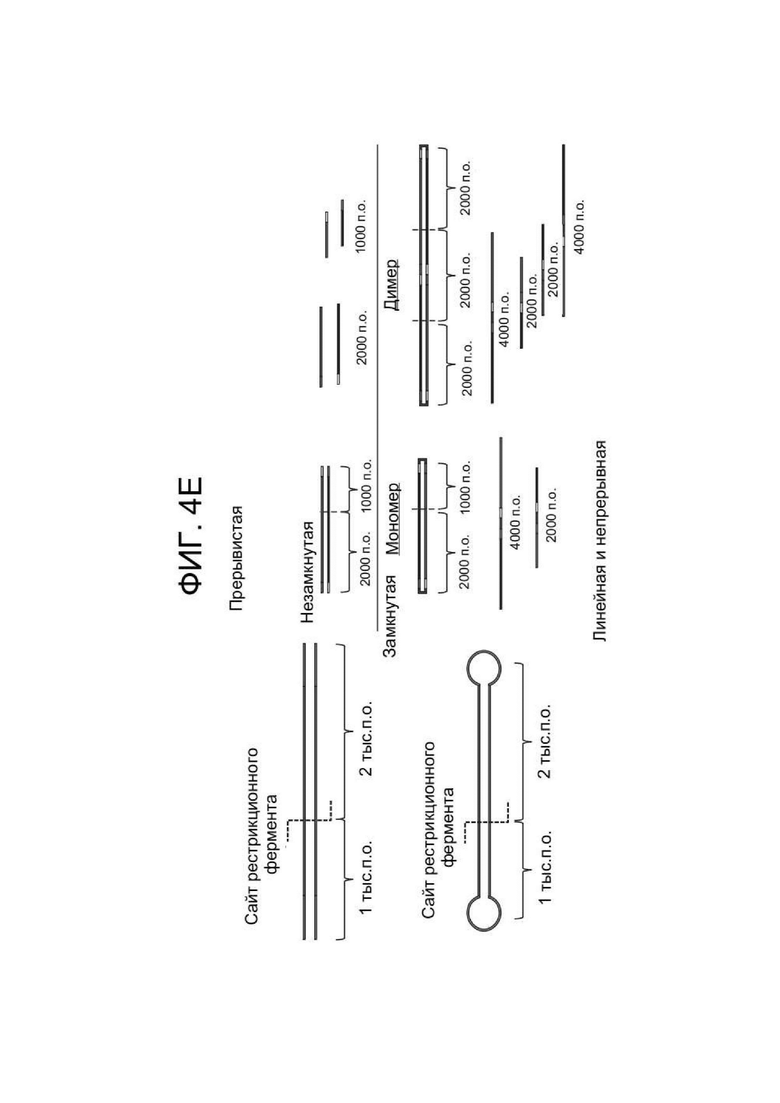
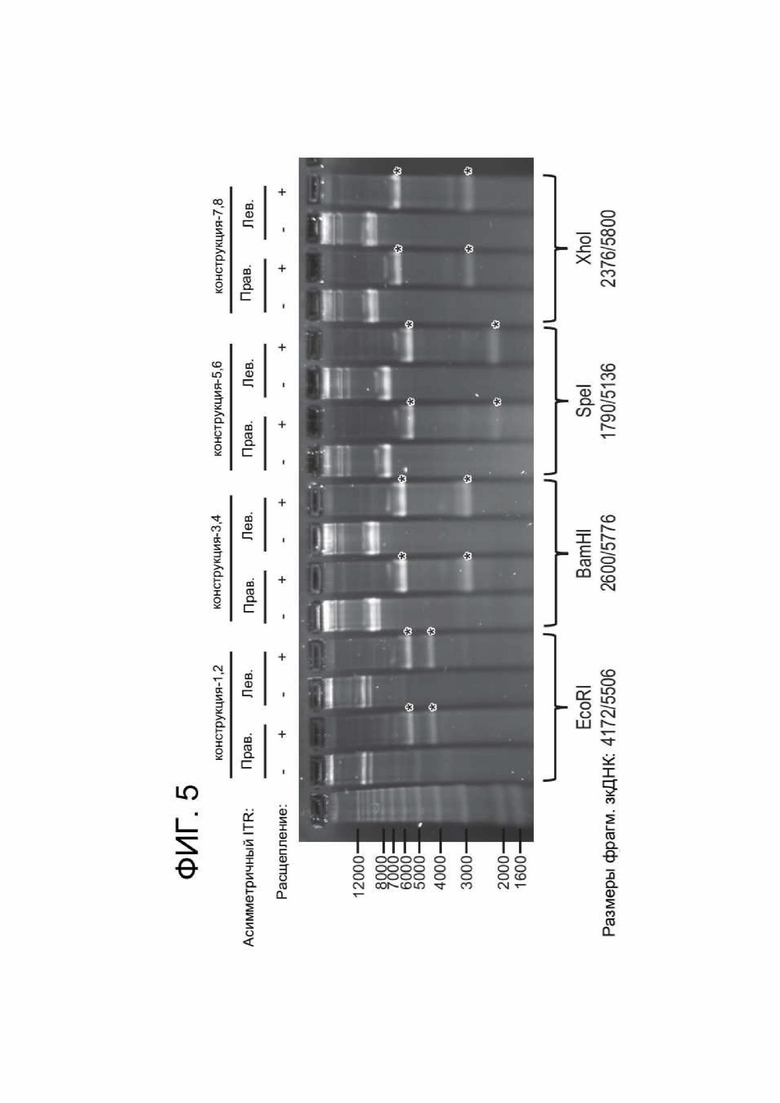
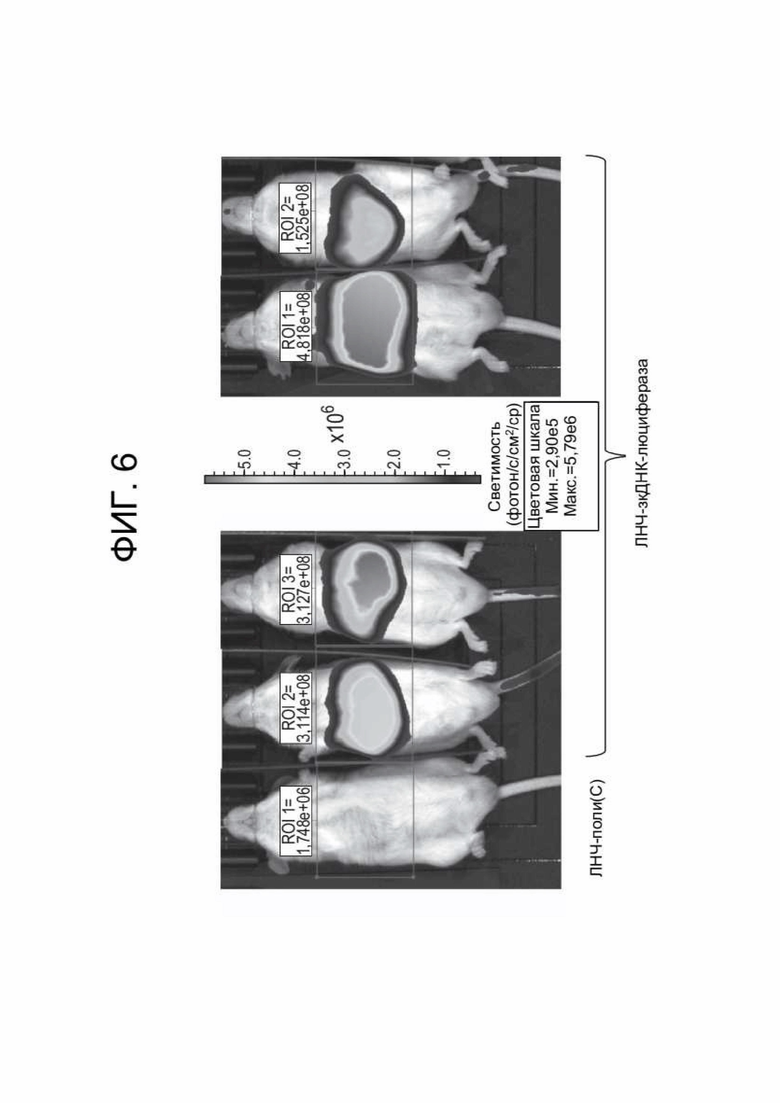

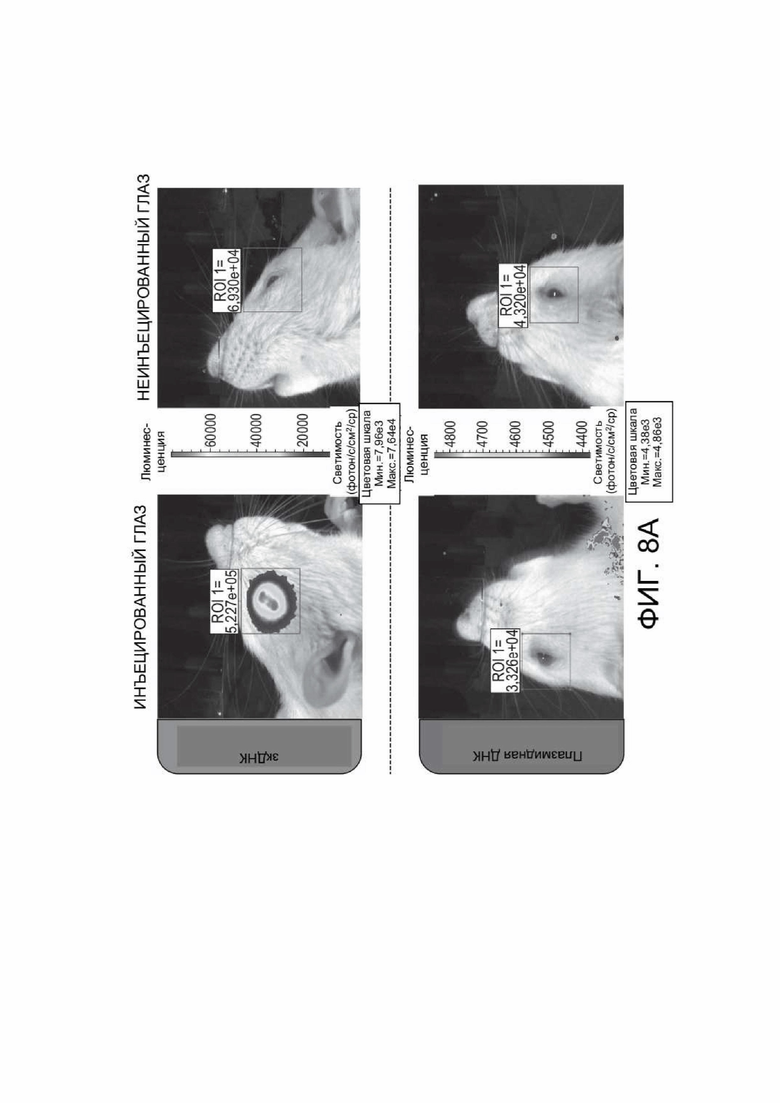
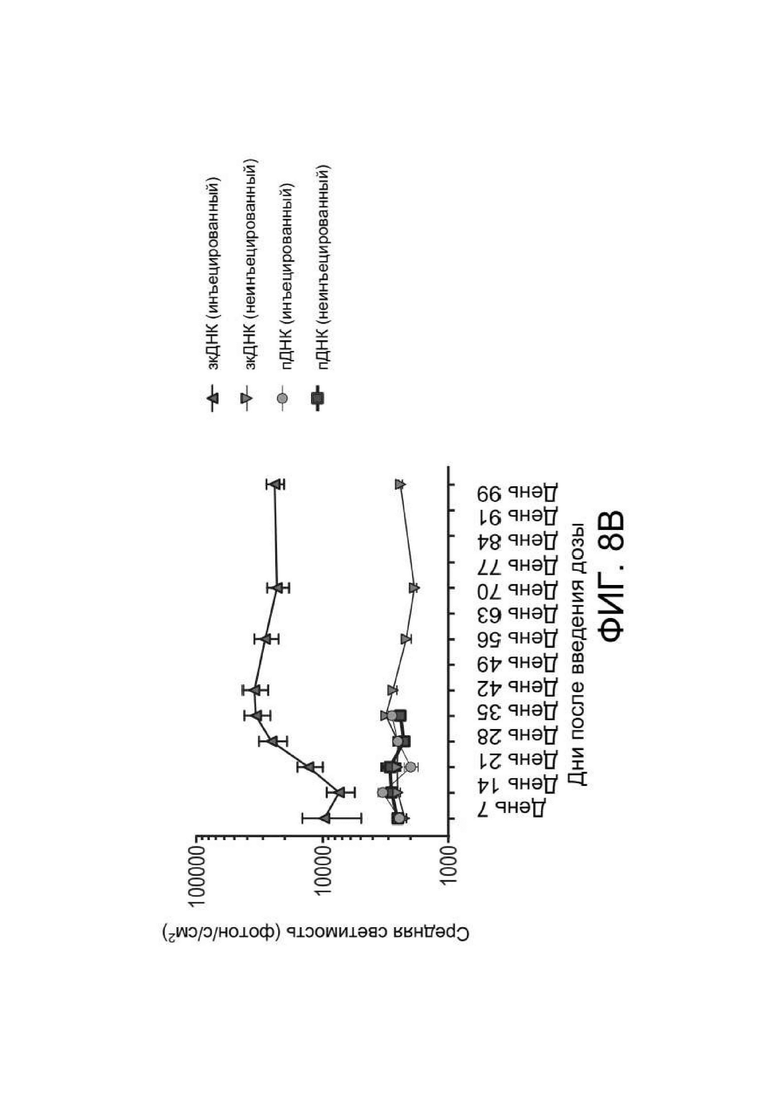
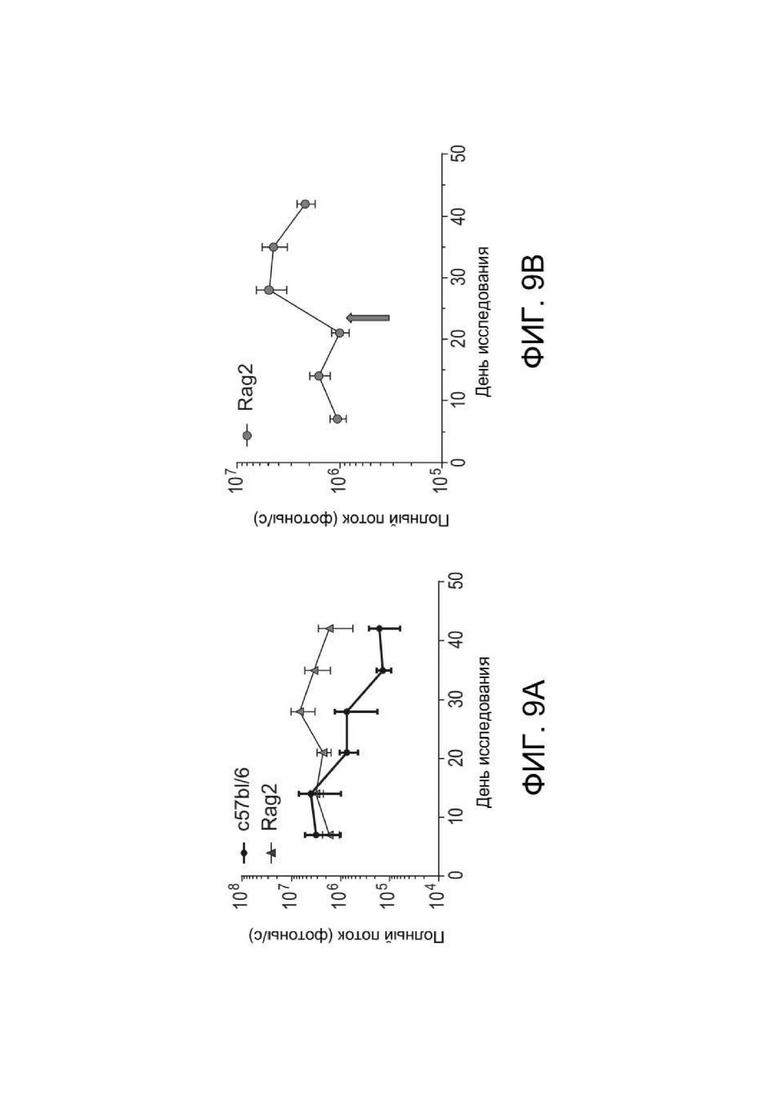
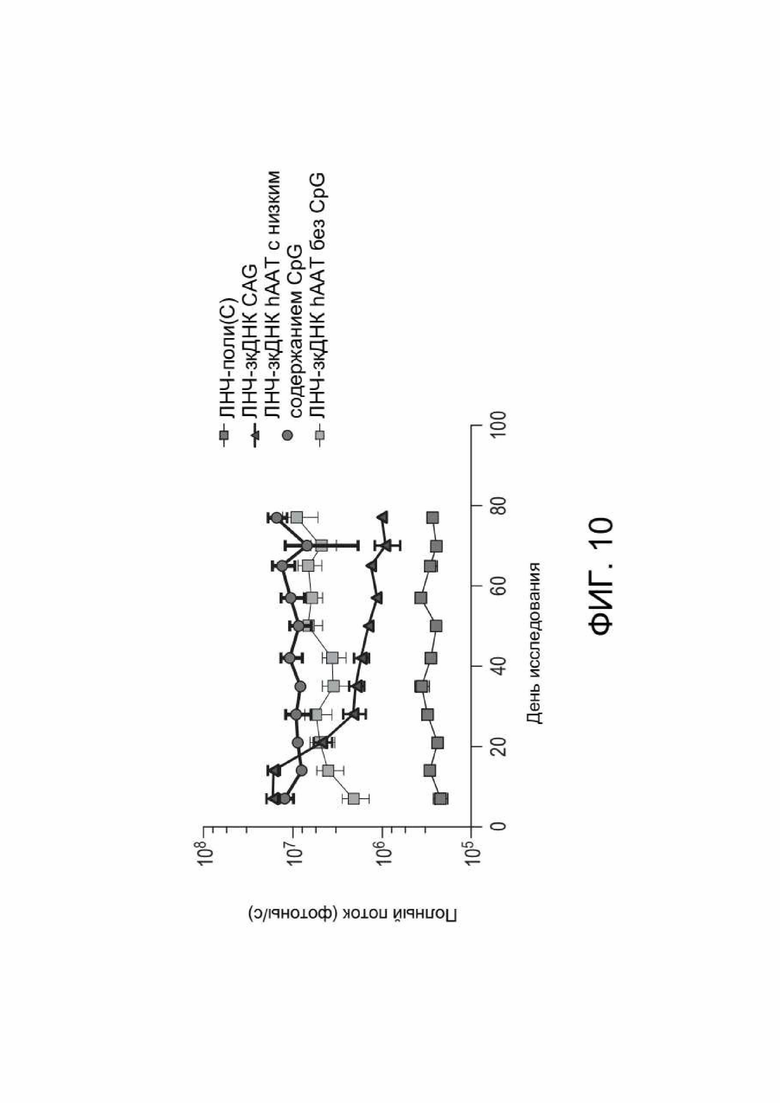
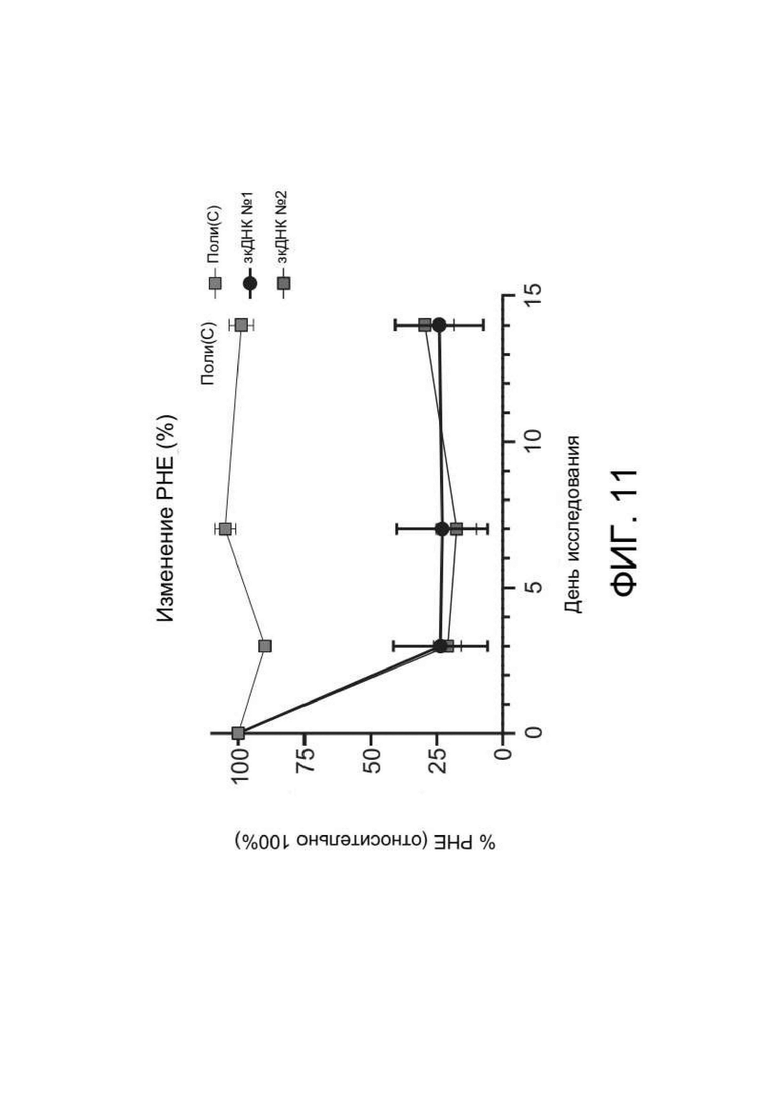
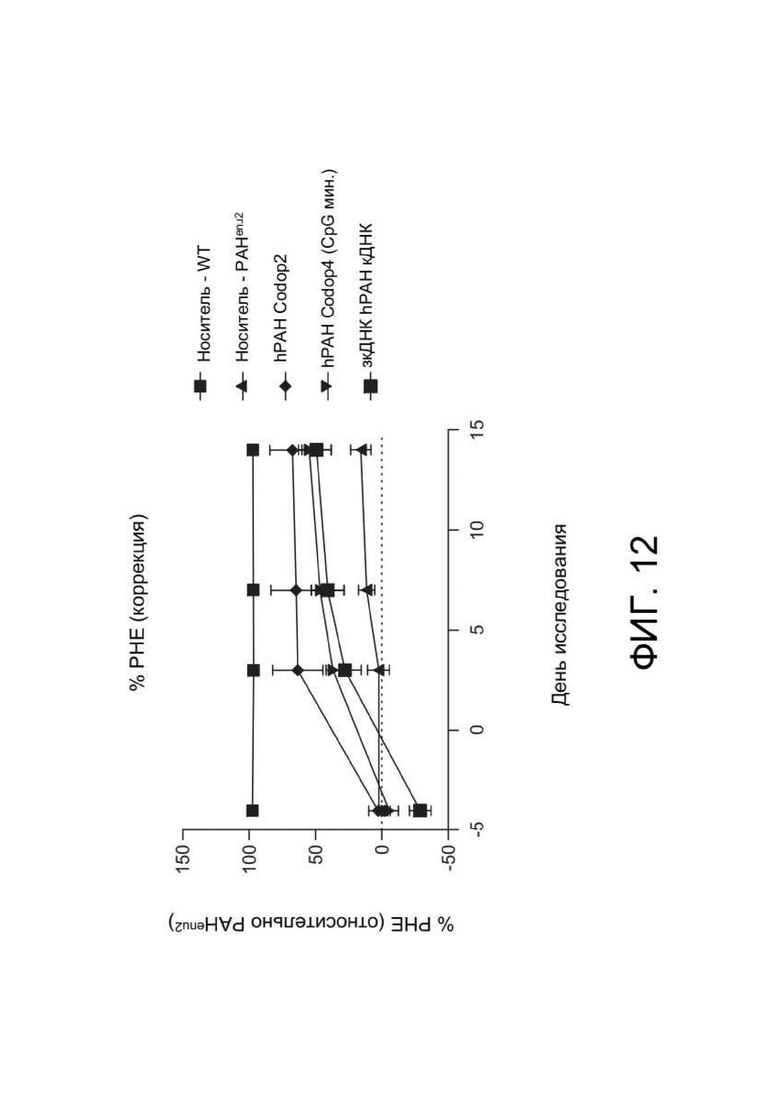
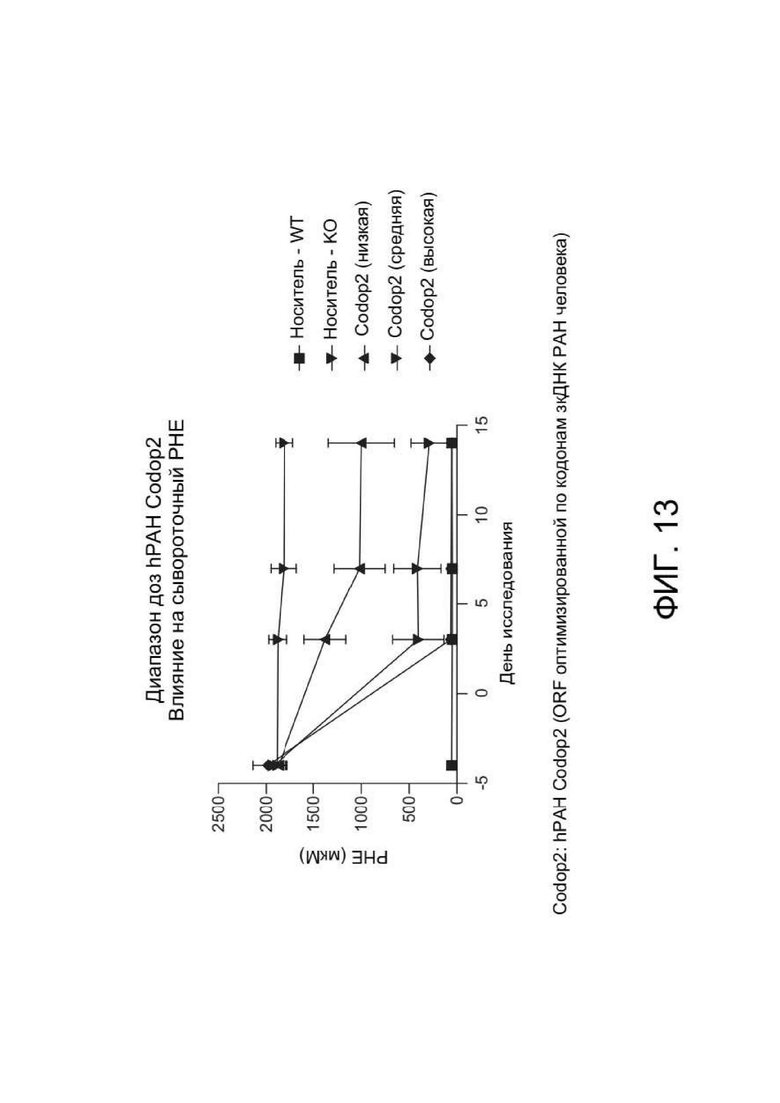
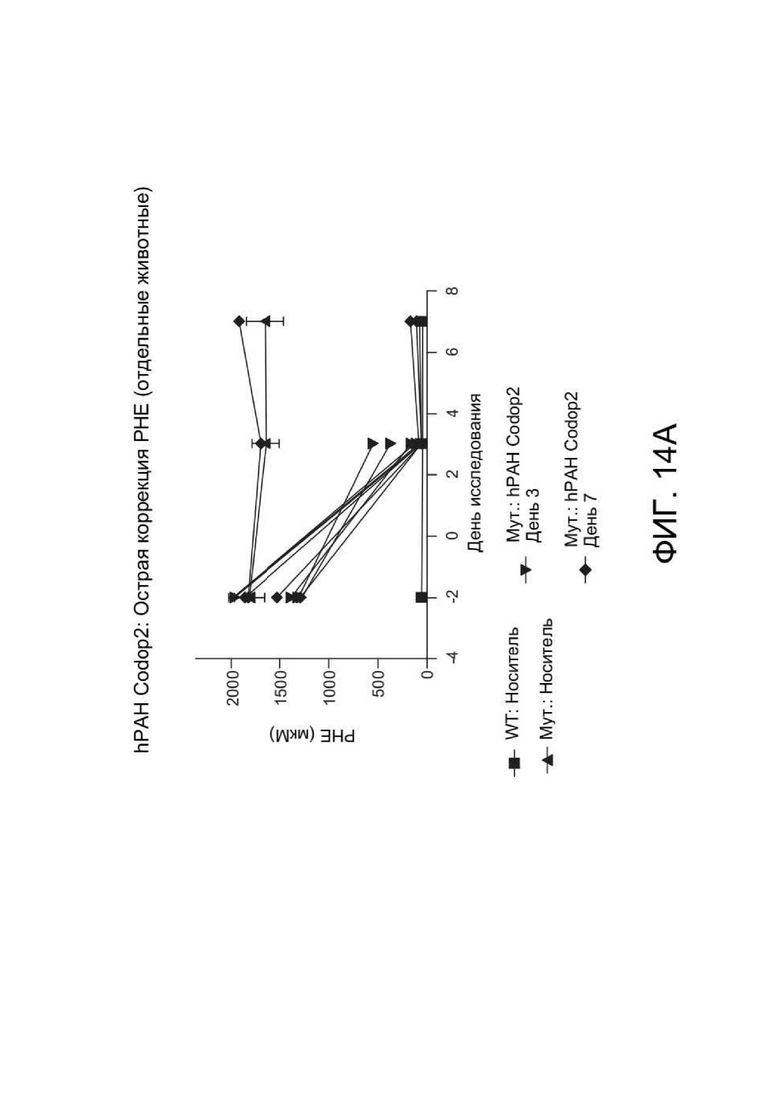
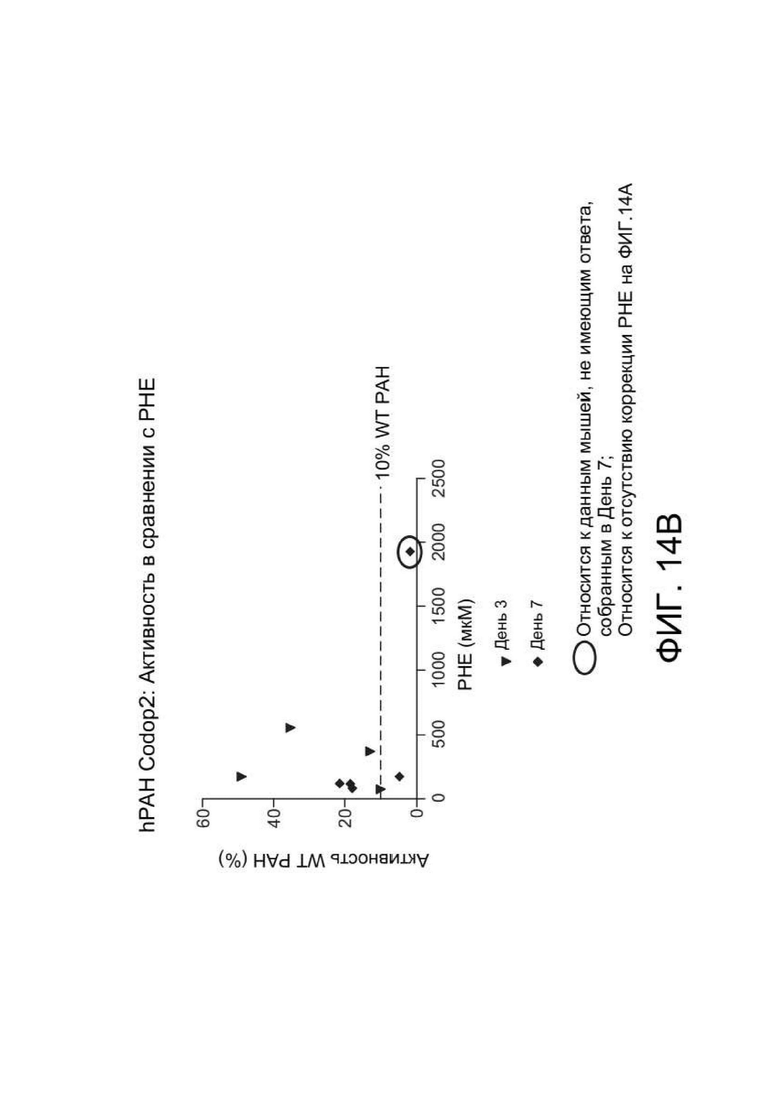
Изобретение относится к области биотехнологии. Описана группа изобретений, включающая бескапсидный вирусный вектор на основе ДНК с замкнутыми концами (зкДНК) для экспрессии белка фенилаланингидроксилазы (РАН), способ экспрессии белка РАН в клетке, включающий приведение клетки в контакт с вышеуказанным вектором, способ лечения субъекта, страдающего фенилкетонурией (ФКУ), фармацевтическую композицию для генной терапии, клетку для продуцирования белка РАН, композицию для доставки зкДНК-вектора, набор для доставки зкДНК-вектора. Изобретение расширяет арсенал средств для экспрессии белка РАН. 7 н. и 52 з.п. ф-лы, 14 ил., 15 табл., 15 пр.
1. Бескапсидный вектор на основе ДНК с замкнутыми концами (зкДНК) для экспрессии белка фенилаланингидроксилазы (РАН), содержащий:
по меньшей мере одну последовательность нуклеиновой кислоты, расположенную между фланкирующими инвертированными концевыми повторами (ITR), причем указанная по меньшей мере одна последовательность нуклеиновой кислоты кодирует по меньшей мере один белок фенилаланингидроксилазы (РАН), и оптимизирована по кодонам для экспрессии в клетке, при этом указанная по меньшей мере одна последовательность нуклеиновой кислоты содержит последовательность, имеющую по меньшей мере 90% идентичности с последовательностью, выбранной из группы, состоящей из последовательностей SEQ ID NO:382, SEQ ID NO:380, SEQ ID NO:381 и SEQ ID NO:383-394.
2. ЗкДНК-вектор по п. 1, отличающийся тем, что указанная по меньшей мере одна последовательность нуклеиновой кислоты содержит последовательность, имеющую по меньшей мере 95% идентичности с SEQ ID NO:382.
3. ЗкДНК-вектор по п. 1, отличающийся тем, что указанная по меньшей мере одна последовательность нуклеиновой кислоты содержит SEQ ID NO:382.
4. ЗкДНК-вектор по п. 1 или 2, отличающийся тем, что указанный зкДНК-вектор содержит промотор, функционально связанный с указанной по меньшей мере одной последовательностью нуклеиновой кислоты, которая кодирует указанный по меньшей мере один белок РАН.
5. ЗкДНК-вектор по п. 4, отличающийся тем, что указанный промотор содержит последовательность нуклеиновой кислоты, имеющую по меньшей мере 85% идентичности с SEQ ID NO: 191.
6. ЗкДНК-вектор по любому из пп. 1-5, отличающийся тем, что указанный зкДНК-вектор содержит энхансер.
7. ЗкДНК-вектор по любому из пп. 1-6, отличающийся тем, что указанный зкДНК-вектор содержит 5'-UTR и/или последовательность интрона.
8. ЗкДНК-вектор по любому из пп. 1-7, отличающийся тем, что указанный зкДНК-вектор содержит 3'-UTR.
9. ЗкДНК-вектор по любому из пп. 1-8, отличающийся тем, что указанный зкДНК-вектор содержит по меньшей мере одну последовательность поли(А).
10. ЗкДНК-вектор по любому из пп. 1-9, отличающийся тем, что указанная по меньшей мере одна последовательность нуклеиновой кислоты представляет собой кДНК.
11. ЗкДНК-вектор по любому из пп. 1-10, отличающийся тем, что по меньшей мере один из фланкирующих ITR содержит функциональный сайт концевого разрешения (TRS) и сайт связывания репликационного белка (Rep).
12. ЗкДНК-вектор по любому из пп. 1-11, отличающийся тем, что один или оба указанных фланкирующих ITR происходят из вируса, выбранного из группы, состоящей из парвовируса, депендовируса и аденоассоциированного вируса (ААВ).
13. ЗкДНК-вектор по любому из пп. 1-12, отличающийся тем, что указанные фланкирующие ITR являются симметричными или асимметричными.
14. ЗкДНК-вектор по п. 13, отличающийся тем, что указанные фланкирующие ITR являются симметричными или по существу симметричными.
15. ЗкДНК-вектор по п. 13, отличающийся тем, что указанные фланкирующие ITR являются асимметричными.
16. ЗкДНК-вектор по любому из пп. 1-15, отличающийся тем, что один из указанных фланкирующих ITR представляет собой ITR дикого типа, или оба указанных фланкирующих ITR представляют собой ITR дикого типа.
17. ЗкДНК-вектор по любому из пп. 1-16, отличающийся тем, что указанные фланкирующие ITR происходят из различных вирусных серотипов.
18. ЗкДНК-вектор по любому из пп. 1-17, отличающийся тем, что указанные фланкирующие ITR происходят из пары вирусных серотипов, выбранных из группы, состоящей из пар вирусных серотипов AAV1,AAV1; AAV2,AAV2; AAV3,AAV3; AAV4,AAV4; AAV5,AAV5; AAV1,AAV2; AAV2,AAV3; AAV3,AAV4; AAV4,AAV5; AAV5,AAV6; AAV1,AAV3; AAV2,AAV4; AAV3,AAV5; AAV4,AAV6; AAV5,AAV7; AAV1,AAV4; AAV2,AAV5; AAV3,AAV6; AAV4,AAV7; AAV5,AAV8; AAV1,AAV5; AAV2,AAV6; AAV3,AAV7; AAV4,AAV8; AAV5,AAV9; AAV1,AAV6; AAV2,AAV7; AAV3,AAV8; AAV4,AAV9; AAV5,AAV10; AAV1,AAV7; AAV2,AAV8; AAV3,AAV9; AAV4,AAV10; AAV5,AAV11; AAV1,AAV8; AAV2,AAV9; AAV3,AAV10; AAV4,AAV11; AAV5,AAV12; AAV1,AAV9; AAV2,AAV10; AAV3,AAV11; AAV4,AAV12; AAV5,AAVRH8; AAV1,AAV10; AAV2,AAV11; AAV3,AAV12; AAV4,AAVRH8; AAV5,AAVRH10; AAV1,AAV11; AAV2,AAV12; AAV3,AAVRH8; AAV4,AAVRH10; AAV5,AAV13; AAV1,AAV12; AAV2,AAVRH8; AAV3,AAVRH10; AAV4,AAV13; AAV5,AAVDJ; AAV1,AAVRH8; AAV2,AAVRH10; AAV3,AAV13; AAV4,AAVDJ; AAV5,AAVDJ8; AAV1,AAVRH10; AAV2,AAV13; AAV3,AAVDJ; AAV4,AAVDJ8; AAB5, птичий; AAB1, AAB13; AAB2, AABDJ; AAB3, AABDJ8; AAB4, птичий; AAB5, бычий; AAB1, AABDJ; AAB2, AABDJ8; ААВ3, птичий; AAB4, бычий; ААВ5, собачий; ААВ1, AABDJ8; ААВ2, птичий; ААВ3, бычий; ААВ4, собачий; ААВ5, лошадиный; ААВ1, птичий; ААВ2, бычий; ААВ3, собачий; ААВ4, лошадиный; ААВ5, козий; ААВ1, бычий; ААВ2, собачий; ААВ3, лошадиный; ААВ4, козий; ААВ5, креветки; ААВ1, собачий; ААВ2, лошадиный; ААВ3, козий; ААВ4, креветки; ААВ5, свиной; ААВ1, лошадиный; ААВ2, козий; ААВ3, креветки; ААВ4, свиной; ААВ5, насекомых; ААВ1, козий; ААВ2, креветки; ААВ3, свиной; ААВ4, насекомых; ААВ5, овечий; ААВ1, креветки; ААВ2, свиной; ААВ3, насекомых; ААВ4, овечий; ААВ5, В19; ААВ1, свиной; ААВ2, насекомых; ААВ3, овечий; ААВ4, В19; ААВ5, MVM; ААВ1, насекомых; ААВ2, овечий; ААВ3, В19; ААВ4, MVM; ААВ5, гусиный; ААВ1, овечий; ААВ2, В19; ААВ3, MVM; ААВ4, гусиный; ААВ5, змеиный; ААВ1, В19; ААВ2, MVM; ААВ3, гусиный; ААВ4, змеиный; ААВ1, MVM; ААВ2, гусиный; ААВ3, змеиный; ААВ1, гусиный; ААВ2, змеиный; ААВ1, змеиный; ААВ6, ААВ6; ААВ7, ААВ7; ААВ8, ААВ8; ААВ9, ААВ9; ААВ10, ААВ10; ААВ6, ААВ7; ААВ7, ААВ8; ААВ8, ААВ9; ААВ9, ААВ10; ААВ10, ААВ11; ААВ6, ААВ8; ААВ7, ААВ9; ААВ8, ААВ10; ААВ9, ААВ11; ААВ10, ААВ12; ААВ6, ААВ9; ААВ7, ААВ10; ААВ8, ААВ11; ААВ9, ААВ12; ААВ10, AABRH8; ААВ6, ААВ10; ААВ7, ААВ11; ААВ8, ААВ12; ААВ9, AABRH8; ААВ10, AABRH10; ААВ6, ААВ11; ААВ7, ААВ12; ААВ8, AABRH8; ААВ9, AABRH10; ААВ10, ААВ13; ААВ6, ААВ12; ААВ7, AABRH8; ААВ8, AABRH10; ААВ9, ААВ13; ААВ10, AABDJ; ААВ6, AABRH8; ААВ7, AABRH10; ААВ8, ААВ13; ААВ9, AABDJ; ААВ10, AABDJ8; ААВ6, AABRH10; ААВ7, ААВ13; ААВ8, AABDJ; ААВ9, AABDJ8; ААВ10, птичий; ААВ6, ААВ13; ААВ7, AABDJ; ААВ8, AABDJ8; ААВ9, птичий; ААВ10, бычий; ААВ6, AABDJ; ААВ7, AABDJ8; ААВ8, птичий; ААВ9, бычий; ААВ10, собачий; ААВ6, AABDJ8; ААВ7, птичий; ААВ8, бычий; ААВ9, собачий; ААВ10, лошадиный; ААВ6, птичий; ААВ7, бычий; ААВ8, собачий; ААВ9, лошадиный; ААВ10, козий; ААВ6, бычий; ААВ7, собачий; ААВ8, лошадиный; ААВ9, козий; ААВ10, креветки; ААВ6, собачий; ААВ7, лошадиный; ААВ8, козий; ААВ9, креветки; ААВ10, свиной; ААВ6, лошадиный; ААВ7, козий; ААВ8, креветки; ААВ9, свиной; ААВ10, насекомых; ААВ6, козий; ААВ7, креветки; ААВ8, свиной; ААВ9, насекомых; ААВ10, овечий; ААВ6, креветки; ААВ7, свиной; ААВ8, насекомых; ААВ9, овечий; АВ10, В19; ААВ6, свиной; ААВ7, насекомых; ААВ8, овечий; ААВ9, В19; ААВ10, MVM; ААВ6, насекомых; ААВ7, овечий; ААВ8, В19; ААВ9, MVM; ААВ10, гусиный; ААВ6, овечий; ААВ7, В19; ААВ8, MVM; АВ9, гусиный; ААВ10, змеиный; ААВ6, В19; ААВ7, MVM; ААВ8, гусиный; ААВ9, змеиный; ААВ6, MVM; ААВ7, гусиный; ААВ8, змеиный; ААВ6, гусиный; ААВ7, змеиный; ААВ6, змеиный; ААВ11, ААВ11; ААВ12, ААВ12; AABRH8, AABRH8; AABRH10, AABRH10; ААВ13, ААВ13; ААВ11, ААВ12; ААВ12, AABRH8; AABRH8, AABRH10; AABRH10, ААВ13; ААВ13, AABDJ; ААВ11, AABRH8; ААВ12, AABRH10; AABRH8, ААВ13; AABRH10, AABDJ; ААВ13, AABDJ8; ААВ11, AABRH10; ААВ12, ААВ13; AABRH8, AABDJ; AABRH10, AABDJ8; ААВ13, птичий; ААВ11, ААВ 13; ААВ 12, AABDJ; AABRH8, AABDJ8; AABRH10, птичий; ААВ13, бычий; ААВ11, AABDJ; ААВ12, AABDJ8; AABRH8, птичий; AABRH10, бычий; ААВ13, собачий; ААВ11, AABDJ8; ААВ12, птичий; AABRH8, бычий; AABRH10, собачий; ААВ13, лошадиный; ААВ11, птичий; ААВ12, бычий; AABRH8, собачий; AABRH10, лошадиный; ААВ13, козий; ААВ11, бычий; ААВ12, собачий; AABRH8, лошадиный; AABRH10, козий; ААВ13, креветки; ААВ11, собачий; ААВ12, лошадиный; AABRH8, козий; AABRH10, креветки; ААВ13, свиной; ААВ11, лошадиный; ААВ12, козий; AABRH8, креветки; AABRH10, свиной; ААВ13, насекомых; ААВ11, козий; ААВ12, креветки; AABRH8, свиной; AABRH10, насекомых; ААВ13, овечий; AABU, креветки; ААВ12, свиной; AABRH8, насекомых; AABRH10, овечий; ААВ13, В19; ААВ11, свиной; ААВ12, насекомых; AABRH8, овечий; ABRH10, В19; ААВ13, MVM; ААВ11, насекомых; ААВ12, овечий; AABRH8, В19; AABRH10, MVM; ААВ13, гусиный; ААВ11, овечий; ААВ12, В19; AABRH8, MVM; AABRH10, гусиный; ААВ13, змеиный; ААВ11, В19; ААВ12, MVM; AABRH8, гусиный; AABRH10, змеиный; ААВ11, MVM; ААВ12, гусиный; AABRH8, змеиный; ААВ11, гусиный; ААВ12, змеиный; ААВ11, змеиный; AABDJ, AABDJ; AABDJ8, AVVDJ8; птичий, птичий; бычий, бычий; собачий, собачий; AABDJ, AABDJ8; AABDJ8, птичий; птичий, бычий; бычий, собачий; собачий, лошадиный; AABDJ, птичий; AABDJ8, бычий; птичий, собачий; бычий, лошадиный; собачий, козий; AABDJ, бычий; AABDJ8, собачий; птичий, лошадиный; бычий, козий; собачий, креветки; AABDJ, собачий; AABDJ8, лошадиный; птичий, козий; бычий, креветки; собачий, свиной; AABDJ, лошадиный; AABDJ8, козий; птичий, креветки; бычий, свиной; собачий, насекомых; AABDJ, козий; AABDJ8, креветки; птичий, свиной; бычий, насекомых; собачий, овечий; AABDJ, креветки; AABDJ8, свиной; птичий, насекомых; бычий, овечий; собачий, В19; AABDJ, свиной; AABDJ8, насекомых; птичий, овечий; бычий, В19; собачий, MVM; AABDJ, насекомых; AABDJ8, овечий; птичий, В19; бычий, MVM; собачий, гусиный; AABDJ, овечий; AABDJ8, В19; птичий, MVM; бычий, гусиный; собачий, змеиный; AABDJ, В19; AABDJ8, MVM; птичий, гусиный; бычий, змеиный; AABDJ, MVM; AABDJ8, гусиный; птичий, змеиный; AABDJ, гусиный; AABDJ8, змеиный; AABDJ, змеиный; лошадиный, лошадиный; козий, козий; креветки, креветки; свиной, свиной; насекомых, насекомых; лошадиный, козий; козий, креветки; креветки, свиной; свиной, насекомых; насекомых, овечий; лошадиный, креветки; козий, свиной; креветки, насекомых; свиной, овечий; насекомых, В19; лошадиный, свиной; козий, насекомых; креветки, овечий; свиной, В19; насекомых, MVM; лошадиный, насекомых; козий, овечий; креветки, В19; свиной, MVM; насекомых, гусиный; лошадиный, овечий; козий, В19; креветки, MVM; свиной, гусиный; насекомых, змеиный; лошадиный, В19; козий, MVM; креветки, гусиный; свиной, змеиный; лошадиный, MVM; козий, гусиный; креветки, змеиный; лошадиный, гусиный; козий, змеиный; лошадиный, змеиный; овечий, овечий; В19, В19; MVM, MVM; гусиный, гусиный; змеиный, змеиный; овечий, В19; В19, MVM; MVM, гусиный; гусиный, змеиный; овечий, MVM; В19, гусиный; MVM, змеиный; овечий, гусиный; В19, змеиный; овечий, змеиный.
19. ЗкДНК-вектор по любому из пп. 1-18, отличающийся тем, что один или оба указанных фланкирующих ITR содержат последовательность, выбранную из группы, состоящей из последовательностей SEQ ID NO:1, 2, 5-48.
20. ЗкДНК-вектор по любому из пп. 1-19, отличающийся тем, что по меньшей мере один из указанных фланкирующих ITR изменен относительно последовательности ITR дикого типа ААВ путем делеции, добавления или замены, которые влияют на общую трехмерную конформацию указанного ITR.
21. ЗкДНК-вектор по любому из пп. 1-20, отличающийся тем, что один или оба указанных фланкирующих ITR происходят из серотипа ААВ, выбранного из группы, состоящей из ААВ1, ААВ2, ААВ3, ААВ4, ААВ5, ААВ6, ААВ7, ААВ8, ААВ9, ААВ10, ААВ11 и ААВ12.
22. ЗкДНК-вектор по любому из пп. 1-21, отличающийся тем, что один или оба указанных фланкирующих ITR являются синтетическими.
23. ЗкДНК-вектор по любому из пп. 1-22, отличающийся тем, что один из указанных фланкирующих ITR не является ITR дикого типа, или оба указанных фланкирующих ITR не являются ITR дикого типа.
24. ЗкДНК-вектор по любому из пп. 1-23, отличающийся тем, что один или оба указанных фланкирующих ITR модифицированы путем делеции, вставки и/или замены по меньшей мере в одной из областей указанных ITR, выбранных из группы, состоящей из А, А', В, В', С, C', D и D'.
25. ЗкДНК-вектор по п. 24, отличающийся тем, что указанная делеция, вставка и/или замена приводит к делеции всей или части структуры стебель-петля, образуемой указанными областями А, А', В, В', С или С'.
26. ЗкДНК-вектор по любому из пп. 1-25, отличающийся тем, что один или оба указанных фланкирующих ITR модифицированы путем делеции, вставки и/или замены, которая приводит к делеции всей или части структуры стебель-петля, образуемой указанными областями В и В'.
27. ЗкДНК-вектор по любому из пп. 1-25, отличающийся тем, что один или оба указанных фланкирующих ITR модифицированы путем делеции, вставки и/или замены, которая приводит к делеции всей или части структуры стебель-петля, образуемой указанными областями С и С'.
28. ЗкДНК-вектор по любому из пп. 1-25, отличающийся тем, что один или оба указанных фланкирующих ITR модифицированы путем делеции, вставки и/или замены, которая приводит к делеции всей или части структуры стебель-петля, образуемой указанными областями В и В', и/или всей или части структуры стебель-петля, образуемой указанными областями С и С'.
29. ЗкДНК-вектор по любому из пп. 1-28, отличающийся тем, что один или оба указанных фланкирующих ITR содержат единственную структуру стебель-петля в области, которая, в ITR дикого типа, содержит первую структуру стебель-петля, образуемую указанными областями В и В', и вторую структуру стебель-петля, образуемую указанными областями С и С'.
30. ЗкДНК-вектор по любому из пп. 1-29, отличающийся тем, что один или оба указанных фланкирующих ITR содержат один стебель и две петли в области, которая, в ITR дикого типа, содержит первую структуру стебель-петля, образуемую указанными областями В и В', и вторую структуру стебель-петля, образуемую указанными областями С и С'.
31. ЗкДНК-вектор по любому из пп. 1-30, отличающийся тем, что один или оба указанных фланкирующих ITR содержат один стебель и одну петлю в области, которая, в ITR дикого типа, содержит первую структуру стебель-петля, образуемую указанными областями В и В', и вторую структуру стебель-петля, образуемую указанными областями С и С'.
32. ЗкДНК-вектор по любому из пп. 1-31, отличающийся тем, что оба фланкирующих ITR изменяют таким образом, что это приводит к общей трехмерной симметрии, при которой указанные ITR инвертированы по отношению друг к другу.
33. ЗкДНК-вектор по любому из пп. 1-32, отличающийся тем, что указанная по меньшей мере одна последовательность нуклеиновой кислоты содержит последовательность, имеющую по меньшей мере 90% идентичности с последовательностью, выбранной из группы, состоящей из SEQ ID NO:382, SEQ ID NO:381, SEQ ID NO:383, SEQ ID NO:384, SEQ ID NO:385, SEQ ID NO:386, SEQ ID NO:387, SEQ ID NO:388, SEQ ID NO:389, SEQ ID NO:390, SEQ ID NO:391, SEQ ID NO:392, SEQ ID NO:393 и SEQ ID NO:394.
34. ЗкДНК-вектор по любому из пп. 1-33, отличающийся тем, что указанная по меньшей мере одна последовательность нуклеиновой кислоты содержит последовательность, имеющую по меньшей мере 90% идентичности с последовательностью, выбранной из группы, состоящей из SEQ ID NO:382, SEQ ID NO:384, SEQ ID NO:394, SEQ ID NO:385, и SEQ ID NO:386.
35. ЗкДНК-вектор по любому из пп. 1-34, отличающийся тем, что указанный зкДНК-вектор содержит последовательность нуклеиновой кислоты, которая по меньшей мере на 90% идентична последовательности, выбранной из группы, состоящей из SEQ ID NO:192, SEQ ID NO:193 и SEQ ID NO:194.
36. ЗкДНК-вектор по любому из пп. 1-35, отличающийся тем, что по указанный зкДНК-вектор содержит по меньшей мере один регуляторный переключатель.
37. ЗкДНК-вектор по п. 36, отличающийся тем, что указанный по меньшей мере один регуляторный переключатель выбран из группы, состоящей из бинарного регуляторного переключателя, низкомолекулярного регуляторного переключателя, регуляторного переключателя «с кодом доступа», регуляторного переключателя на основе нуклеиновой кислоты, посттранскрипционного регуляторного переключателя, контролируемого излучением или контролируемого ультразвуком регуляторного переключателя, опосредуемого гипоксией регуляторного переключателя, регуляторного переключателя воспалительного ответа, активируемого сдвигом регуляторного переключателя и аварийного выключателя («kill switch»).
38. Способ экспрессии белка РАН в клетке, причем указанный способ включает приведение указанной клетки в контакт с зкДНК-вектором по любому из пп. 1-37.
39. Способ по п. 38, отличающийся тем, что указанная клетка представляет собой клетку печени.
40. Способ по п. 38 или 39, отличающийся тем, что указанная клетка находится в условиях in vitro или in vivo.
41. Способ по любому из пп. 38-40, отличающийся тем, что указанная по меньшей мере одна последовательность нуклеиновой кислоты выбрана из группы, состоящей из SEQ ID NO:382, SEQ ID NO:380, SEQ ID NO:381 и SEQ ID NO:383 - SEQ ID NO:394.
42. Способ по п. 41, отличающийся тем, что указанная по меньшей мере одна последовательность нуклеиновой кислоты содержит последовательность, имеющую по меньшей мере 95% идентичности с SEQ ID NO:382.
43. Способ по п. 41, отличающийся тем, что указанная по меньшей мере одна последовательность нуклеиновой кислоты содержит SEQ ID NO:382.
44. Способ лечения субъекта, страдающего фенилкетонурией (ФКУ), причем указанный способ включает введение указанному субъекту зкДНК-вектора по любому из пп. 1-37.
45. Способ по п. 44, отличающийся тем, что указанная по меньшей мере одна последовательность нуклеиновой кислоты, которая кодирует указанный по меньшей мере один белок РАН, содержит последовательность, имеющую по меньшей мере 90% идентичности с последовательностью, выбранной из группы, состоящей из: SEQ ID NO:382, SEQ ID NO:380, SEQ ID NO:381 и SEQ ID NO:383-394.
46. Способ по п. 44 или 45, отличающийся тем, что указанная по меньшей мере одна последовательность нуклеиновой кислоты, которая кодирует указанный по меньшей мере один белок РАН, содержит последовательность, имеющую по меньшей мере 95% идентичности с SEQ ID NO:382.
47. Способ по п. 44 или 45, отличающийся тем, что указанная по меньшей мере одна последовательность нуклеиновой кислоты, которая кодирует указанный по меньшей мере один белок РАН, содержит SEQ ID NO:382.
48. Способ по п. 44 или 45, отличающийся тем, что указанный зкДНК-вектор подлежит введению в клетку печени.
49. Способ по любому из пп. 38-48, отличающийся тем, что указанный зкДНК-вектор экспрессирует белок РАН в клетке печени.
50. Способ по любому из пп. 44-49, отличающийся тем, что указанный зкДНК-вектор вводят с помощью любого одного или более из путей, выбранных из группы, состоящей из: внутривенная инъекция, внутримышечная инъекция, и инфузия.
51. Способ по любому из пп. 44-50, отличающийся тем, что у указанного субъекта наблюдается по меньшей мере примерно 50% снижение уровня фенилаланина в сыворотке по сравнению с уровнем фенилаланина в сыворотке у указанного субъекта до введения.
52. Способ по любому из пп. 44-51, отличающийся тем, что у указанного субъекта уровень фенилаланина в сыворотке после введения составляет менее примерно 1500 мкМ.
53. Способ по любому из пп. 44-52, отличающийся тем, что у указанного субъекта после введения наблюдается повышение активности РАН по меньшей мере примерно на 10% по сравнению с уровнем активности РАН до введения.
54. Фармацевтическая композиция для генной терапии, содержащая зкДНК-вектор по любому из пп. 1-37.
55. Клетка для продуцирования белка РАН, содержащая зкДНК-вектор по любому из пп. 1-37.
56. Клетка по п. 55, отличающаяся тем, что указанная клетка представляет собой клетку печени.
57. Композиция для доставки зкДНК-вектора, содержащая зкДНК-вектор по любому из пп. 1-37 и липид.
58. Композиция по п. 57, отличающаяся тем, что указанный липид представляет собой липидную наночастицу (ЛНЧ).
59. Набор для доставки зкДНК-вектора, содержащий зкДНК-вектор по любому из пп. 1-37, фармацевтическую композицию по п. 54, клетку по п. 55 или 56 или композицию по п. 57 или 58 и инструкции по применению.
| WO 2018126112 A1, 05.07.2018 | |||
| WO 2001068822 A2, 20.09.2001 | |||
| WO 2019032898 A1, 14.02.2019 | |||
| КОМПОЗИЦИИ ВЕКТОРА AAV И СПОСОБЫ ПЕРЕНОСА ГЕНОВ В КЛЕТКИ, ОРГАНЫ И ТКАНИ | 2013 |
|
RU2653444C2 |
| Eisensmith R | |||
| C., Woo S | |||
| L | |||
| C | |||
| Gene therapy for phenylketonuria //European journal of pediatrics, 1996, 155, p | |||
| Устройство для электрической сигнализации | 1918 |
|
SU16A1 |
| Strisciuglio P., Concolino D | |||
| New strategies for the treatment of phenylketonuria (PKU) //Metabolites, 2014, | |||
Авторы
Даты
2024-02-22—Публикация
2020-03-13—Подача