Область техники
Настоящее изобретение относится к новым конъюгатам антитело-лекарственное средство (ADC), нацеленным на DLK1, активным метаболитам таких ADC, способам получения таких ADC, применению таких ADC в лечении и/или профилактике заболеваний и применению таких ADC в производстве лекарственных срдств для лечения и/или профилактики заболеваний, более конкретно, к применению таких ADC при производстве лекарствнных средств для лечения и/или предотвращения пролиферативных и/или ангиогенетических заболеваний, например рака. Более конкретно, настоящее изобретение относится к конъюгату антитело-лекарственное средство, содержащему антитело, связывающееся с DLK1, или его антигенсвязывающий фрагмент, и фармацевтической композиции, содержащей их.
Уровень техники
Рак представляет собой заболевание, вызванное аномальными образованиями неконтролируемого роста клеток в тканях организма и результатом неконтролируемого роста клеток в различных тканях. Опухоли на ранних стадиях рака могут быть удалены с помощью хирургических и радиотерапевтических мер, а метастазирующие опухоли обычно лечат паллиативно с помощью химиотерапии.
Большинство химиотерапевтических средств, вводимых не перорально, могут вызывать нежелательные побочные эффекты или серьезную токсичность в результате системного введения. Соответственно, основное внимание при разработке уделялось разработке новых химиотерапевтических средств для достижения повышенной эффективности и минимальной токсичности/побочных эффектов за счет улучшенного и селективного действия химиотерапевтических средств на опухолевые клетки или непосредственно прилегающие ткани.
Конъюгат антитело-лекарственное средство (ADC) представляет собой новую таргетную технологию, при которой токсин или лекарственное средство связывается с антителом, которое, в свою очередь, связывается с антигеном, токсином или лекарственным средством, высвобождаемым в опухолевую клетку, и т.п., вызывая гибель клетки. Эта технология имеет превосходную эффективность по сравнению с лекарственными средствами на основе антител и способна существенно снизить риск побочных эффектов по сравнению с обычными противораковыми средствами, поскольку она специально доставляет лекарственные средства к раковым клеткам-мишеням с минимальным воздействием на здоровые клетки и высвобождает лекарственные средства только при определенных условиях.
Основная структура конъюгата антитело-лекарственное средство представляет собой «антитело-линкер-низкомолекулярное лекарственное средство (токсин)». В данной работе линкер должен играть не только функциональную роль в связывании антитела и лекарственного средства, но также обеспечивать надлежащее высвобождение лекарственного средства посредством диссоциации антитело-лекарственное средство (например, в результате гидролиза ферментом) после его циркуляции в организме и достигает целевых клеток и проявляет эффективность в отношении раковых клеток-мишеней. То есть стабильность линкера играет очень важную роль в эффективности и системной токсичности конъюгата антитело-лекарственное средство (Discovery Medicine 2010, 10(53): 329-39).
Авторы настоящего изобретения разработали и получили патент на линкер, содержащий эффективную саморасщепляющуюся группу, которая более стабильна в плазме и в кровотоке и позволяет лекарственному средству легко высвобождаться и проявлять эффективность в раковой клетке (зарегистрированный патент Кореи No. 1628872, и тому подобное). Между тем, использование моноклональных антител для лечения рака имеет значительный успех. Моноклональные антитела подходят для целенаправленного воздействия на опухолевые ткани и опухолевые клетки. Конъюгаты антитело-лекарственное средство стали новым и мощным вариантом лечения лимфом и солидных опухолей, и в последнее время иммунорегуляторные антитела получают значительный успех в клинических испытаниях. Разработка терапевтических антител основана на глубоком понимании серологии рака, технологии белковой инженерии, механизмов действия и устойчивости, а также взаимодействия между иммунной системой и раковыми клетками.
Антигены, которые экспрессируются на поверхности раковых клеток человека, определяются как широкий спектр мишеней, которые чрезмерно экспрессируются по сравнению с нормальными тканями, мутируют или избирательно экспрессируются. Ключевой проблемой является определение подходящих антигенов для терапии на основе антител. Эти терапевтические средства опосредуют изменения функции антигена или рецептора (т.е. в качестве стимулятора или антагониста), регулируют иммунную систему посредством активации Fc и Т-клеток и проявляют эффективность за счет доставки специфических лекарств, которые связываются с антителами, нацеленными на специфические антигены. Молекулярные методы, которые могут изменять фармакокинетику, функциональную функцию, размер и иммунную стимуляцию антител, становятся ключевыми элементами в разработке новых методов лечения на основе антител. Данные клинических испытаний терапевтических антител у онкологических больных подчеркивают важность подходов к выбору оптимизированных антител, включая аффинность и связывание целевого антигена и антител, выбор структуры антител и терапевтические подходы (блокирование передачи сигналов или иммунной функции).
В настоящее время ведутся соответствующие исследования антител, антигеном которых является DLK1. DLK1 человеческого происхождения (дельта-подобный 1 гомолог (Drosophila)) представляет собой однопроходной трансмембранный белок, вся цепь которого состоит из 383 аминокислот. Белок имеет 6 доменов EGF (повтор, подобный эпидермальному фактору роста) во внеклеточном домене.
DLK1 обычно называют геном DLK1 из-за его гомологии в аминокислотной последовательности с Delta, лигандом рецептора Notch, который является регулирующим фактором дифференцировки клеток, и другими названиями, под которыми он упоминается, являются, Pref-1, pG2, SCP-1 и ZOG. Хотя DLK1 является трансмембранным белком, он хорошо известен как белок, в котором внеклеточный домен отделяется от клеточной мембраны с помощью TACE (фермента, преобразующего фактор некроза опухоли альфа) и функционирует отдельно.
DLK1 проявляет высокую экспрессию в недифференцированных фетальных клетках с высоким индексом пролиферации. В частности, в то время как высокая экспрессия проявляется в печени, почках, скелетных мышцах и головном мозге и т.п. плода, экспрессия не наблюдается в большинстве тканей после рождения, причем экспрессия ограничена только определенными клетками, такими как преадипоциты, клетки панкреатического островка, стромальные клетки тимуса и клетки надпочечников.
Что касается исследования функций DLK1, DLK1 наиболее изучен как Pref-1 (фактор преадипоцитов-1), который является фактором, подавляющим дифференцировку жировых клеток. Сообщается, что помимо своей способности супрессировать дифференцировку жировых клеток, DLK1 способен супрессировать дифференцировку гемопоэтических стволовых клеток, играть роль в регуляции дифференцировки лимфоидных клеток-предшественников и быть связанным с заживлением ран.
Кроме того, сообщается, что DLK1 экспрессируется с высокой частотой при различных раковых заболеваниях или опухолях. Раковые заболвания, в которых экспрессия DLK1 была подтверждена на сегодняшний день, содержат солидные виды рака нейроэндокринных опухолей, нейробластому, глиому, нейрофиброматоз 1 типа, мелкоклеточный рак легких, рак печени, рак почек, рак яичников, колоректальный рак, рак груди и рак поджелудочной железы, и рак крови, миелодиспластический синдром и острый миелоидный лейкоз. Что касается исследования связи между nDLK1 и раком, были сообщения о том, что DLK1 сверхэкспрессируется в раковых клетках головного мозга (глиомах) и что сверхэкспрессия кДНК DLK1 в раковых клетках головного мозга увеличивает пролиферацию и миграцию раковых клеток мозга. Также сообщалось, что экспрессия DLK1 при раке печени повышена по сравнению с нормальными клетками печени, и что, когда экспрессия DLK1 снижается с помощью тестов миРНК, размер опухоли уменьшается.
Исходя из этого технического уровня, авторы настоящего изобретения работали над разработкой антител, которые специфически связываются с DLK1, в результате чего разработали антитело против DLK1, демонстрирующее превосходное связывание с DLK1. Авторы изобретения подтвердили, что, применяя линкер, содержащий эффективную саморасщепляющуюся группу, которая более стабильна в плазме и в кровотоке и позволяет лекарственному средству легко высвобождаться и проявлять эффективность в раковой клетке, к антителу против DLK1 для дополнительного усиления действия антитела, можно обеспечить новый конъюгат антитело-лекарственное средство (ADC), который нацелен на DLK1 и эффективен при лечении и/или профилактике раковых заболеваний, и, таким образом, завершили настоящее изобретение.
Подробное описание изобретения
Техническая задача
Целью настоящего изобретения является предоставление нового конъюгата антитело-лекарственное средство, нацеленного на DLK1, или его соль или сольват.
Другой целью настоящего изобретения является предоставление конъюгата лекарственное средство-антитело, содержащего антитело, которое специфически связывается с DLK1, и лекарственное средство, связывающееся с ним, и фармацевтической композиции, содержащей вышеуказанное.
Другой целью настоящего изобретения является предоставление способа профилактики или лечения пролиферативного, рака или ангиогенетического заболевания, при этом способ содержит стадию введения индивидууму конъюгата антитело-лекарственное средство, содержащего фармацевтически эффективное количество антитела, которое специфически связывается с DLK1 и лекарственного средства, которое связывается с ним.
Другой целью настоящего изобретения является предоставление применения конъюгата антитело-лекарственное средство, содержащего фармацевтически эффективное количество антитела, которое специфически связывается с DLK1, и лекарственного средства, которое связывается с ним, в виде фармацевтической композиции, для профилактики или лечения пролиферативного, рака или ангиогенетического заболевания.
Еще одной целью настоящего изобретения является предоставление системы антитело-линкер-лекарственное средство (токсин), которая позволяет лекарственному средству и/или токсину безопасно достигать клетки-мишени и эффективно проявлять эффективность при значительном снижении токсичности, посредством технологии слияния линкера, содержащего саморасщепляющуюся группу, которая более стабильна в плазме и в кровотоке и позволяет лекарственному средству легко высвобождаться в раковой клетке для максимального повышения эффективности.
Техническое решение
Один аспект настоящего изобретения предоставляет конъюгат антитела общей формулы I или его фармацевтически приемлемую соль или сольват.
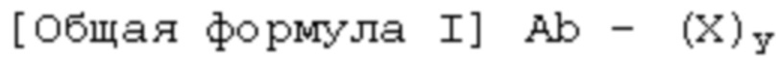
где:
Ab представляет собой антитело против DLK1 или его антигенсвязывающий фрагмент,
X независимо представляет собой химический остаток, содержащий по меньшей мере одно активное средство и линкер, и;
линкер связывает антитело и активное средство, и;
y представляет собой целое число от 1 до 20.
Антитело против DLK1 или его антигенсвязывающий фрагмент, то есть антитело, которое связывается с DLK1, или его антигенсвязывающий фрагмент, содержит: вариабельную область тяжелой цепи, содержащую по меньшей мере одну CDR1 тяжелой цепи, выбранную из группы, содержащей SEQ ID NO: 2, 16, 30, 44, 58, 72 и 86, по меньшей мере, одну CDR2 тяжелой цепи, выбранную из группы, содержащей SEQ ID NO: 4, 18, 32, 46, 60, 74 и 88, и по меньшей мере, одну CDR3 тяжелой цепи, выбранную из группы, содержащей SEQ ID NO: 6, 20, 34, 48, 62, 76 и 90, и;
вариабельную область легкой цепи, содержащую по меньшей мере одну CDR1 легкой цепи, выбранную из группы, содержащей SEQ ID NO: 9, 23, 37, 51, 65, 79, 93, 115 и 121, по меньшей мере, одну CDR2 легкой цепи, выбранную из группы, содержащей SEQ ID NO: 11, 25, 39, 53, 67, 81 и 95, и по меньшей мере, одну CDR3 легкой цепи, выбранную из группы, содержащей SEQ ID NO: 13, 27, 41, 55, 69, 83, 97, 116 и 125.
Антитело по настоящему изобретению может, например, специфически связываться с внеклеточным доменом человеческого DLK1.
Термин «антитело», используемый в настоящем описании, относится к DLK1, в частности антителу против DLK1, которое специфически связывается с внеклеточным доменом человеческого белка DLK1. В объем настоящего изобретения входит не только полная форма антитела, которое специфически связывается с DLK1, но также антигенсвязывающие фрагменты молекулы антитела.
Полное антитело имеет структуру, состоящую из 2 полноразмерных тяжелых цепей и 2 полноразмерных легких цепей, соответствующие легкие цепи связаны с тяжелой цепью дисульфидной связью. Константные области тяжелой цепи имеют типы гамма (γ), мю (μ), альфа (α), дельта (δ) и эпсилон (ε) с подклассами гамма1 (γ1), гамма2 (γ2), гамма3 (γ3), гамма4 (γ1), альфа1 (α1) и альфа2 (α2). Константная область легкой цепи имеет типы каппа (κ) и лямбда (λ).
Антигенсвязывающий фрагмент антитела или фрагмент антитела относится к фрагменту с функциональностью связывания с антигеном и содержит Fab, F(ab'), F(ab')2 и Fv и т.п. Среди фрагментов антител Fab имеет структуру вариабельных областей легкой цепи и тяжелой цепи, константную область легкой цепи и первую константную область тяжелой цепи (CH1) и 1 антигенсвязывающий участок. Fab' отличается от Fab тем, что он имеет шарнирную область, содержащую по меньшей мере один остаток цистеина на C-конце домена CH1 тяжелой цепи. Антитело F(ab)'2 образуется, когда остаток цистеина шарнирной области Fab' образует дисульфидную связь. Fv представляет собой минимальный фрагмент антитела, который имеет только вариабельную область тяжелой цепи и вариабельную область легкой цепи, и рекомбинантные технологии получения фрагментов Fv раскрыты в опубликованных международных заявках на патент PCT WO 88/10649, WO 88/106630, WO 88/07085, WO 88/07086 и WO 88/09344. Двухцепочечный Fv имеет вариабельную область тяжелой цепи и вариабельную область легкой цепи, связанные нековалентной связью, и одноцепочечный Fv (scFv) обычно имеет вариабельную область тяжелой цепи и вариабельную область легкой цепи, связанные ковалентной связью через пептидный линкер, или связанные непосредственно по С-концу, образуя структуры, такие как димер, а также двухцепочечный Fv. Такие фрагменты антител могут быть получены с использованием белок-гидролизирующего фермента (например, рестрикционное разрезание всего антитела папаином дает Fab, и разрезание пепсином может дать фрагмент F(ab)'2), а также могут быть получены с использованием технологии рекомбинантных генов.
В вариантах осуществления антитело согласно настоящему изобретению имеет форму Fv (например, scFv) или полную форму антитела. Кроме того, константная область тяжелой цепи может быть любым изотипом, выбранным из гамма (γ), мю (μ), альфа (α), дельта (δ) и эпсилон (ε). Например, константная область представляет собой гамма1 (IgG1), гамма3 (IgG3) или гамма4 (IgG4). Константная область легкой цепи может быть каппа- или лямбда-типа.
Термин «тяжелая цепь», используемый в настоящем описании, относится к полноразмерной тяжелой цепи, содержащей вариабельный домен VH, который содержит аминокислотные последовательности, имеющие достаточное количество последовательностей вариабельной области для придания специфичности к антигену, и три константных домена CH1, CH2 и CH3, и все ее фрагменты. Кроме того, термин «легкая цепь», используемый в настоящем описании, относится к полноразмерной легкой цепи, содержащей вариабельный домен VL, который содержит аминокислотные последовательности, имеющие соответствующие последовательности вариабельной области для придания специфичности к антигену, и константный домен CL, и все ее фрагменты.
Антитело по изобретению содержит, но не ограничивается ими, моноклональное антитело, мультиспецифическое антитело, человеческое антитело, гуманизированное антитело, химерное антитело, одноцепочечные Fv (scFV), одноцепочечное антитело, Fab-фрагмент, F(ab')-фрагмент, связанные дисульфидными мостиками Fv-фрагменты (sdFV) и антиидиотипическое (анти-Id) антитело или эпитоп-связывающие фрагменты вышеуказанных антител и т.п.
Моноклональные антитела относятся к антителам, полученным из группы по существу гомогенных антител, то есть отдельные антитела, составляющие совокупность, идентичны, за исключением возможных естественных мутаций, которые могут присутствовать в небольших количествах. Моноклональные антитела являются высокоспецифичными и направлены против одного антигенного сайта. В отличие от препарата обычного (поликлонального) антитела, который содержит различные антитела, направленные против различных определяющих факторов, соответствующие моноклональные антитела направлены против одного определяющего фактора на антигене. Например, моноклональные антитела для использования в настоящем изобретении могут быть получены с использованием гибридомного способа или с использованием способов рекомбинантных ДНК на бактериях или эукариотических клетках животных или растительных клетках (см. патент США 4816567). Кроме того, моноклональное антитело может быть выделено из фаговой библиотеки антител.
В одном варианте осуществления настоящего изобретения метод фагового дисплея использовали для сортировки библиотеки природных одноцепочечных Fv человека (библиотека нативных одноцепочечных Fv человека) для получения семи типов моноклональных антител человека, которые специфически связываются с DLK1.
«Фаговый дисплей» представляет собой метод отображения мутантного полипептида в виде слитого белка с фагом, например, по меньшей мере, части белка оболочки на поверхности фаговой частицы. Полезность фагового дисплея заключается в быстрой и эффективной классификации последовательностей, которые связываются с антигенами-мишенями с высокой аффинностью, в больших библиотеках рандомизированных вариантов белков. Отображение пептидов и библиотек белков на фагах используют для скрининга миллионов полипептидов с целью идентификации полипептидов со специфическими свойствами связывания.
Технология фагового дисплея предоставила мощный инструмент для создания и скрининга новых белков, которые связываются со специфическими лигандами (например, антигенами). Применяя технологию фагового дисплея, можно создавать большие библиотеки вариантов белков и быстро классифицировать последовательности, которые связываются с высоким сродством с антигенами-мишенями. Нуклеиновую кислоту, кодирующую мутантный полипептид, сливают с последовательностью нуклеиновой кислоты, кодирующей белок вирусной оболочки, например белок гена III или белок гена VIII. Была разработана монофазная система фагового дисплея, в которой последовательность нуклеиновой кислоты, кодирующую белок или полипептид, сливают с последовательностью нуклеиновой кислоты, кодирующей часть белка гена III. В системе 1-фагового дисплея слитый ген экспрессируется на низком уровне и белок гена III дикого типа также экспрессируется, и, таким образом, сохраняется инфекционность частиц.
Демонстрация экспрессии пептидов на поверхности фиброзного фага и экспрессии функциональных фрагментов антител в периферической цитоплазме E. coli важна для разработки библиотек фагового дисплея антител. Библиотеки антител или антигенсвязывающих полипептидов были получены разными способами, например, путем изменения одного гена путем вставки случайной последовательности ДНК или путем клонирования связанной последовательности гена. Скрининг может быть выполнен в библиотеках в отношении экспрессии антител или антигенсвязывающих белков, имеющих желаемые характеристики.
Технология фагового дисплея имеет несколько преимуществ по сравнению с обычными гибридомными и рекомбинантными способами получения антител с желаемыми характеристиками. Этот способ обеспечивает создание больших библиотек антител с различными последовательностями в течение короткого времени без использования животных. Производство гибридом и производство гуманизированных антител может занять нескольких месяцев. Кроме того, поскольку иммунитет не требуется, то библиотеки фаговых антител могут генерировать антитела против антигенов, которые токсичны или имеют низкую антигенность. Библиотеки фаговых антител также можно применять для получения и идентификации новых терапевтических антител.
Могут быть использованы способы получения человеческих антител из неиммунизированных людей, последовательностей зародышевой линии или репертуаров субсенсибилизированного Ig B-клеток, которые иммунизируют с использованием библиотеки фагового дисплея. Для получения недетектируемой или неиммуногенной антигенсвязывающей библиотеки можно использовать различные лимфатические ткани.
Методы идентификации и отделения высокоаффинных антител из библиотек фагового дисплея важны для разделения новых антител для терапии. Выдление высокоаффинных антител из библиотеки может зависеть от размера библиотеки, эффективности продукции в бактериальных клетках и разнообразия библиотек. Размер библиотек уменьшается из-за неправильного сворачивания белка антитела или антигенсвязывающего белка и неэффективной продукции из-за присутствия стоп-кодона. Экспрессия в бактериальных клетках может подавляться, при неправильном сворачивании антитела или антигенсвязывающего домена. Экспрессия может быть улучшена путем попеременного мутирования остатков на поверхности границ вариабельных/константных или выбранных остатков CDR. Последовательность каркасной области является одним из элементов, обеспечивающих соответствующую укладку в случае создания фаговых библиотек антител в бактериальных клетках.
Важно создавать различные библиотеки антител или антигенсвязывающих белков для отделения высокоаффинных антител. Было обнаружено, что области CDR3 часто участвуют в связывании антигена. Поскольку область CDR3 тяжелой цепи значительно различается по размеру, последовательности и структурной конформации, то можно получить различные библиотеки с использованием области CDR3.
Кроме того, разнообразие может быть получено путем рандомизации участков CDR вариабельных тяжелых и легких цепей с использованием всех 20 аминокислот в каждом положении. Использование всех 20 аминокислот приводит к увеличению вариабельности последовательностей антител и увеличению вероятности идентификации новых антител.
«Эпитоп» относится к белковой детерминанте, способную к специфическому связыванию с антителом. Эпитопы обычно состоят из группы химически активных поверхностных молекул, таких как аминокислоты или боковые цепи сахаров, и, как правило, имеют специфические трехмерные структурные характеристики, а также специфические характеристики заряда. Трехмерные эпитопы и непространственные эпитопы различаются тем, что связывание с первыми, но не с последними, утрачивается, в присутствии денатурирующего растворителя.
Антитело нечеловеческого происхождения (например, мышиное) в «гуманизированной» форме представляет собой химерное антитело, содержащее минимальную последовательность, полученную из нечеловеческого иммуноглобулина. В большинстве случаев гуманизированное антитело представляет собой вид нечеловеческого происхождения (донорское антитело), такой как мышиное, крысиное, кроличье или нечеловеческое, имеющий желаемую специфичность, аффинность и способность удерживать остаток из гипервариабельной области реципиента, и представляет собой человеческий иммуноглобулин (акцепторное антитело), в котором остаток гипервариабельной области реципиента заменен остатком гипервариабельной области приматов.
Вышеупомянутое «человеческое антитело» означает молекулу, полученную из иммуноглобулина человека, где все аминокислотные последовательности, составляющие антитело, включая определяющую комплементарность область и структурную область, состоят из человеческого иммуноглобулина.
Другая цепь(и) может быть получена из другого вида или может быть получена из другого класса или подгруппы антител, например, часть тяжелой цепи и/или легкой цепи, полученная из определенного вида или идентичная или гомологичная соответствующей последовательности в антителе, принадлежащем к определенному классу или подклассу антител, «химерные» антитела (иммуноглобулины), идентичные или гомологичные соответствующим последовательностям в антителах, принадлежащих к подклассу, а также фрагментам указанных антител, проявляющим желаемую биологическую активность.
Используемый в настоящем документе термин «вариабельный домен антитела» относится к областям легкой и тяжелой цепи молекулы антитела, содержащим определяющие комплементарность области (CDR; т.е. CDR1, CDR2 и CDR3), и аминокислотную последовательность каркасной области (FR). VH относится к вариабельному домену тяжелой цепи. VL относится к вариабельному домену легкой цепи.
Термин «определяющие комплементарность области» (CDR; то есть CDR1, CDR2 и CDR3) относятся к аминокислотному остатку вариабельного домена антитела, который необходим для связывания антигена. Каждый вариабельный домен обычно имеет три области CDR, идентифицированные как CDR1, CDR2 и CDR3.
В настоящем изобретении антитело, связывающееся с DLK1, или его антигенсвязывающий фрагмент, может, в частности, содержать последовательности CDR, указанные в таблице 1 ниже. Из них, корейская заявка на патент No. 10-2018-0107639 подтвердила, что антитела против DLK1 двух типов (18A5 и 27F7) и два других мутантных антитела 18A5 (18A5_LS_1A10 и 18A5_AM_1A12) способны связываться с клетками, где DLK1 сверхэкспрессируется, и могут быть превращены в конъюгаты анти-DLK1-антитело-лекарственное средство, которые могут нацеливаться на DLK1, экспрессируемый на поверхности раковых клеток, чтобы вызывать апоптоз раковых клеток.
[Таблица 1]

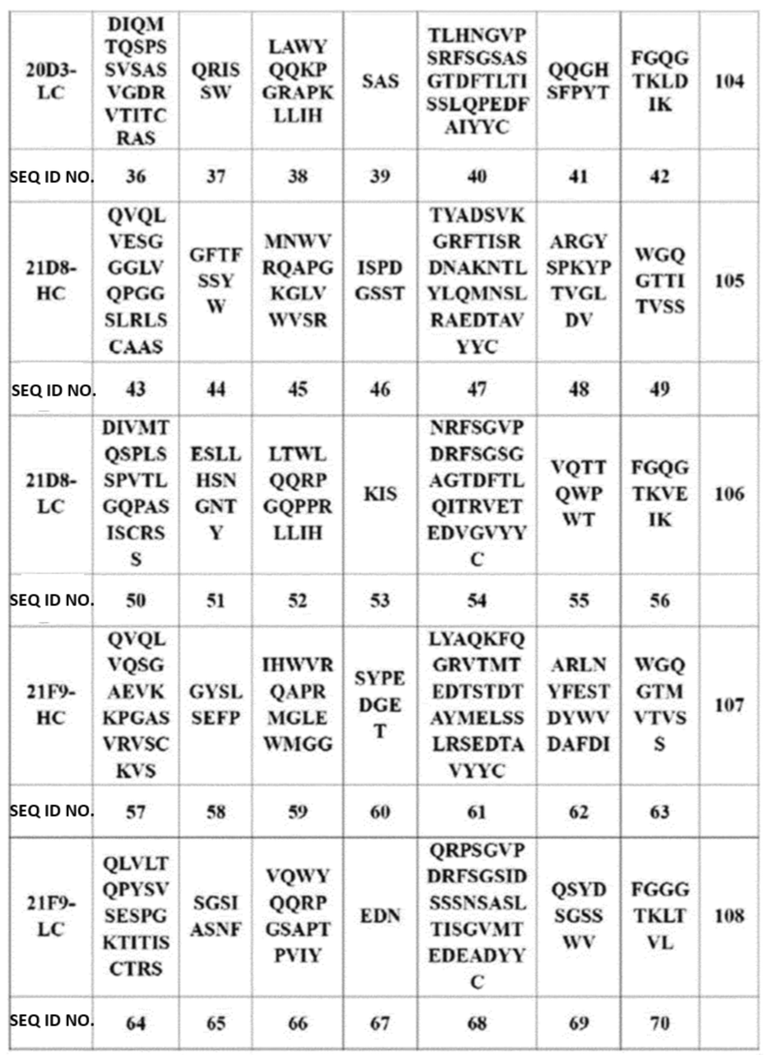
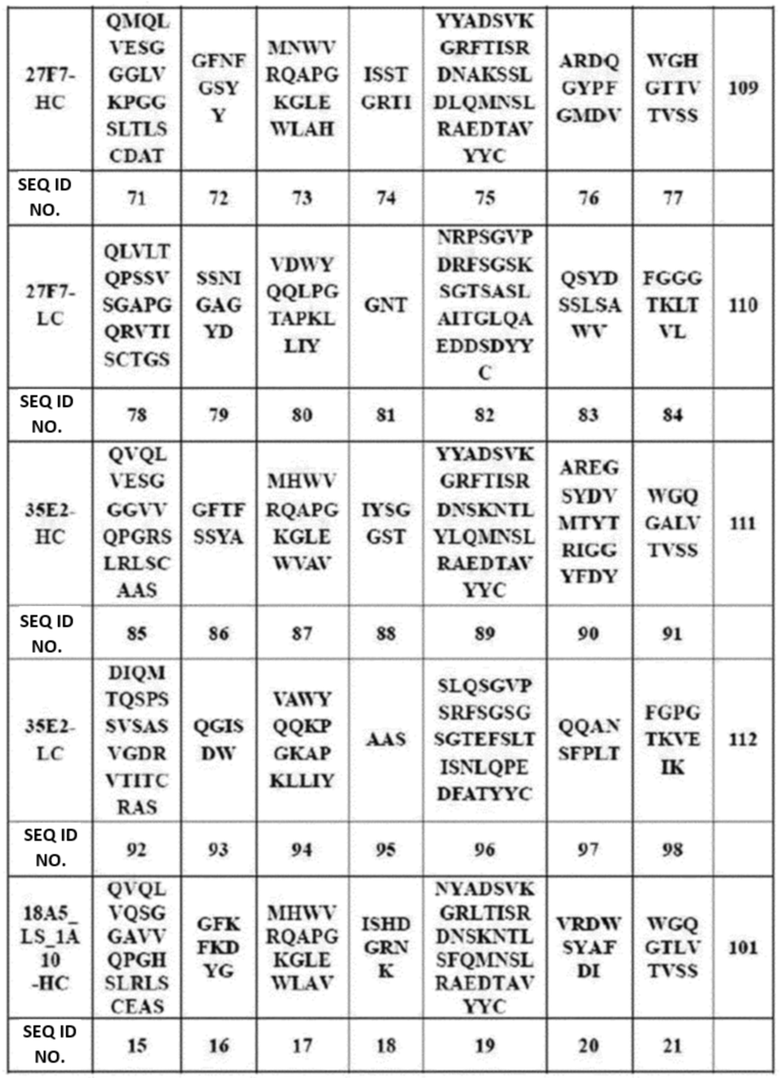
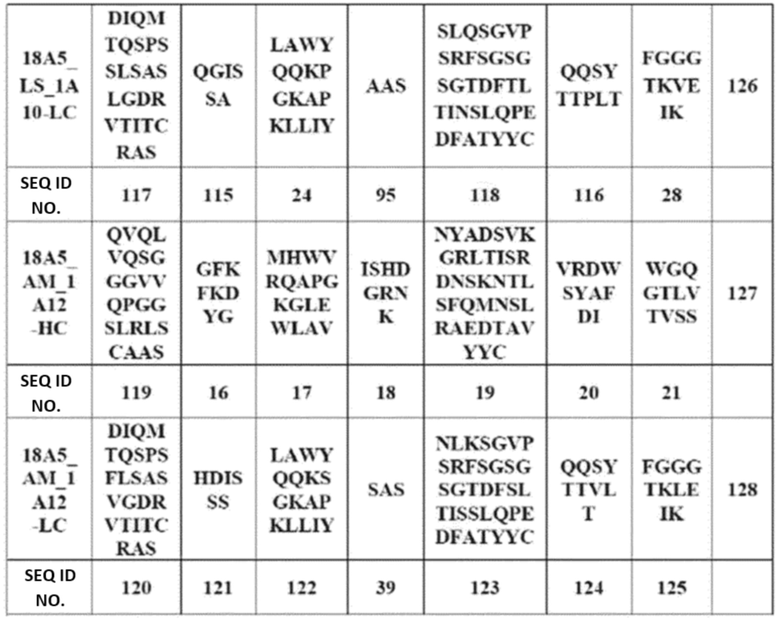
«Каркасная область» (FR) представляет собой остаток вариабельного домена, отличный от остатка CDR. Каждый вариабельный домен обычно имеет четыре FR, обозначаемые как FR1, FR2, FR3 и FR4.
Варианты осуществления настоящего изобретения могут содержать: по меньшей мере одну FR1 тяжелой цепи, выбранную из группы, содержащей SEQ ID NO: 1, 15, 29, 43, 57, 71, 85 и 119; по меньшей мере одну FR2 тяжелой цепи, выбранную из группы, содержащей SEQ ID NO: 3, 17, 31, 45, 59, 73 и 87; по меньшей мере одну FR3 тяжелой цепи, выбранную из группы, содержащей SEQ ID NO: 5, 19, 33, 47, 61, 75 и 89; по меньшей мере одну FR4 тяжелой цепи, выбранную из группы, содержащей SEQ ID NO: 7, 21, 35, 49, 63, 77 и 91; по меньшей мере одну FR1 легкой цепи, выбранную из группы, содержащей SEQ ID NO: 8, 22, 36, 50, 64, 78, 92, 117 и 120; по меньшей мере одну FR2 легкой цепи, выбранную из группы, содержащей SEQ ID NO: 10, 24, 38, 52, 66, 80, 94 и 122; по меньшей мере одну F3 легкой цепи, выбранную из группы, содержащей SEQ ID NO: 12, 26, 40, 54, 68, 82, 96, 118 и 123, и; по меньшей мере одну FR4 легкой цепи, выбранную из группы, содержащей SEQ ID NO: 14, 28, 42, 56, 70, 84, 98 и 125.
Фрагмент «Fv» представляет собой фрагмент антитела, который содержит полные сайты распознавания и связывания антитела. Эта область состоит из одного вариабельного домена тяжелой цепи и одного вариабельного домена легкой цепи, например, димеры, по существу, прочно ковалентно связанные с scFv.
Фрагмент «Fab» содержит вариабельный и константный домены легкой цепи, а также вариабельный и первый константный домен (CH1) тяжелой цепи. Фрагменты антитела F(ab')2 обычно содержат пару фрагментов Fab, ковалентно связанных через их цистеин шарнира вблизи их карбоксильных концов.
«Одноцепочечный Fv» или «scFv» фрагмент антитела содержит домены антитела VH и VL, в котором эти домены присутствуют в одной полипептидной цепи. Полипептид Fv может дополнительно содержать полипептидный линкер между доменом VH и доменом VL для того, чтобы scFv образовывал желаемую структуру для связывания антигена.
Антитело по настоящему изобретению может быть одновалентным или двухвалентным и содержать одинарную цепь или двойную цепь.
Функционально аффинность связывания антитела с внеклеточным доменом DLK1 находится в диапазоне от 10-5 M до 10-12 M. Например, аффинность связывания составляет от 10-6 M до 10-12 M, 10-7 M-10-12 M, 10-8 M-10-12 M, 10-9 M-10-12 M, 10-5 M-10-11 M, 10-6 M-10-11 M, 10-7 M-10-11 M, 10-8 M-10-11 M, 10-9 M-10-11 M, 10-10 M-10-11 M, 10-5 M-10-10 M, 10-6 M-10-10 M, 10-7 M-10-10 M, 10-8 M-10-10 M, 10-9 M-10-10 M, 10-5 M-10-9 M, 10-6 M-10-9 M, 10-7 M-10-9 M, 10-8 M-10-9 M, 10-5 M-10-8 M, 10-6 M-10-8 M, 10-7 M-10-8 M, 10-5 M-10-7 M, 10-6 M-10-7 M или 10-5 M-10-6 M.
Кроме того, антитела по настоящему изобретению представляют собой антитела с повышенной аффинностью к антигену. Термин «аффинность» относится к способности специфически распознавать и связываться с конкретными сайтами антигена. Высокая специфичность вместе со специфичностью этих антител является важным фактором иммунного ответа. Любой из различных анализов, известных в данной области, например радиоиммуноанализы (RIA) и ELISA, может быть использован для определения аффинности, которая может быть выражена в виде различных количественных значений. Аффинность антитела к антигену обычно может быть представлена константой диссоциации (Kd) специфического взаимодействия антитело-антиген. Более низкое значение Kd указывает на более высокую аффинность антитела к антигену. Например, значение Kd для антитела 18A5 по настоящему изобретению составляет 0,52, а для антитела 27F7 составляет 0,22. Это указывает на то, что это антитела с высокой аффинностью, которые специфично связываются с человеческим DLK1.
Связывание антитела с внеклеточным доменом DLK1 или его антигенсвязывающим фрагментом может содержать вариабельную область тяжелой цепи, включая последовательность, которая имеет по меньшей мере 90% гомологии последовательности с последовательностью, выбранной из группы, содержащей SEQ ID NO: 99, 101, 103, 105, 107, 109, 111 и 127. Связывание антитела с внеклеточным доменом DLK1, или его антигенсвязывающего фрагмента, может содержать вариабельную область тяжелой цепи, выбранную из группы, содержащей SEQ ID NO: 99, 101, 103, 105, 107, 109, 111 и 127.
Кроме того, связывание антитела с внеклеточным доменом DLK1, или его антигенсвязывающего фрагмента, может содержать вариабельную область легкой цепи, включая последовательность, которая имеет по меньшей мере 90% гомологии последовательности с последовательностью, выбранной из группы, содержащей SEQ ID NO: 100, 102, 104, 106, 108, 110, 112, 126 и 128. Связывание антитела с внеклеточным доменом DLK1, или его антигенсвязывающего фрагмента, может содержать вариабельную область легкой цепи, выбранную из группы, содержащей SEQ ID NO: 100, 102, 104, 106, 108, 110, 112, 126 и 128.
Антитело или фрагмент антитела по настоящему изобретению может содержать, в рамках специфического распознавания DLK1, последовательность антитела против DLK1 по настоящему изобретению, описанную в настоящем документе, а также ее биологические эквиваленты. Например, в аминокислотную последовательность антитела могут быть внесены дополнительные изменения для дополнительного улучшения аффинности связывания и/или других биологических свойств антитела. Такие модификации содержат, например, делецию, вставку и/или замену остатков аминокислотной последовательности антитела. Такие вариации аминокислот получают на основе относительного сходства заместителей боковой цепи аминокислот, такого как гидрофобность, гидрофильность, заряд, размер и тому подобное. При анализе размера, формы и типа заместителей боковой цепи аминокислоты, аргинин, лизин и гистидин оба являются положительно заряженными остатками; аланин, глицин и серин имеют одинаковые размеры; фенилаланин, триптофан и тирозин имеют похожие формы. Таким образом, исходя из этих соображений, аргинин, лизин и гистидин; аланин, глицин и серин; и фенилаланин, триптофан и тирозин являются биологически функциональными эквивалентами.
Принимая во внимание мутацию, обладающую вышеупомянутой биологической эквивалентной активностью, антитело по настоящему изобретению или молекула нуклеиновой кислоты, кодирующая его, интерпретируется как содержащая последовательность, демонстрирующую существенную идентичность с последовательностями SEQ ID NO. Вышеупомянутая существенная идентичность определяется путем выравнивания вышеописанной последовательности настоящего изобретения с любой другой последовательностью, насколько это возможно, и анализа выровненной последовательности с использованием алгоритма, обычно используемого в данной области, с гомологией не менее 90%, и наиболее предпочтительно по меньшей мере 95% гомологии, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99%.
Способы выравнивания для сравнения последовательностей хорошо известны в данной области. NCBI Basic Local Alignment Search Tool (BLAST) (средство поиска основного локального выравнивания) доступен из NBCI и может использоваться в сочетании с программами анализа последовательностей, такими как blastp, blasm, blastx, tblastn и tblastx в интернете. BLSAT доступен на www.ncbi.nlm.nih.gov/BLAST/. Сравнение гомологии последовательностей с использованием этой программы можно найти на сайте www.ncbi.nlm.nih.gov/BLAST/blast_help.html.
Исходя из этого, антитело или его антигенсвязывающий фрагмент по настоящему изобретению составляет 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% по сравнению с указанной последовательностью или всеми, описанными в описании.
Исходя из этого, антитело или его антигенсвязывающий фрагмент настоящего изобретения составляет 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% по сравнению с заданной последовательностью или всеми описанными в описании. Такая гомология может быть определена путем сравнения последовательностей и/или выравнивания способами, известными в данной области. Например, алгоритмы сравнения последовательностей (например, BLAST или BLAST 2.0), ручное выравнивание, визуальный осмотр могут использоваться для определения процента гомологии последовательностей нуклеиновых кислот или белков по изобретению.
В другом аспекте настоящее изобретение относится к нуклеиновой кислоте, кодирующей антитело или его антигенсвязывающий фрагмент.
Нуклеиновая кислота, кодирующая антитело или его антигенсвязывающий фрагмент по настоящему изобретению, может быть выделена для рекомбинантного получения антитела или его антигенсвязывающего фрагмента. Нуклеиновую кислоту выделяют и вставляют в реплицируемый вектор для дальнейшего клонирования (амплификации ДНК) или для дальнейшей экспрессии. Исходя из этого, настоящее изобретение относится к вектору, содержащему нуклеиновую кислоту в другом аспекте.
«Нуклеиновая кислота» предназначен для охвата молекул ДНК (гДНК и кДНК) и РНК, а нуклеотиды, которые являются основными строительными блоками нуклеиновых кислот, содержат природные нуклеотиды, а также аналоги с модифицированными фрагментами сахара или основания. Последовательности нуклеиновых кислот, кодирующие вариабельные области тяжелой и легкой цепи изобретения, могут быть модифицированы. Такие модификации включают добавление, делецию или неконсервативные или консервативные замены нуклеотидов.
ДНК, кодирующая антитело, может быть легко выделена или синтезирована с использованием обычных процедур (например, с использованием олигонуклеотидных зондов, способных специфически связываться с ДНК, кодирующей тяжелую и легкую цепи антитела). Доступно множество векторов. Компоненты вектора, как правило, содержат, но не ограничиваются ими, один или несколько из следующих компонентов: сигнальную последовательность, точку начала репликации, один или несколько маркерных генов, энхансерные элементы, промоторы и последовательности терминации транскрипции.
Используемый в настоящем описании термин «вектор» относится к плазмидному вектору как средству для экспрессии представляющего интерес гена в клетке-хозяине; космидному вектору; вирусным векторам, таким как бактериофаговые векторы, аденовирусные векторы, ретровирусные векторы и векторы на основе аденоассоциированного вируса, и т.п. Нуклеиновая кислота, кодирующая антитело в векторе, функционально связана с промотором.
«Функционально связанный» означает функциональное связывание между последовательностью контроля экспрессии нуклеиновой кислоты (например, массивом сайта связывания промоторов, сигнальных последовательностей или регулятором транскрипции) и другой последовательностью нуклеиновой кислоты, при этом регуляторной последовательностью является другая нуклеиновая кислота. Для контроля транскрипции и/или трансляции последовательности.
В случае прокариотической клетки в качестве хозяина, мощные промоторы, способные стимулировать транскрипцию (например, tac-промотор, lac-промотор, lacUV5-промотор, lpp-промотор, pLλ-промотор, pRλ-промотор, rac5-промотор, amp-промотор, recA-промотор, SP6-промотор, trp-промотор и T7-промотор и т.п.), сайты связывания рибосомы для инициации трансляции и последовательности терминации транскрипции/трансляции. Кроме того, например, если в качестве хозяина применяют эукариотическую клетку, может использоваться промотор, полученный из генома клеток млекопитающих (например, промотор металлотионеина, промотор β-актина, промотор гемоглобина человека или промотор креатина мышц человека) или промоторы, полученные из вирусов животного (например, поздний промотор аденовируса, промотор вируса коровьей оспы 7,5K, промотор SV40, цитомегаловирусный (CMV) промотор, промотор HSV tk, промотор вируса опухоли молочной железы мыши (MMTV), промотор LTR HIV), промотор вируса Морони, промотор вируса Эпштейна-Барра (EBV) и промотор вируса саркомы Рауса (RSV)), и обычно имеет последовательность полиаденилирования в качестве последовательности терминации транскрипции.
В некоторых случаях вектор может быть слит с другими последовательностями для облегчения очистки экспрессируемого из него антитела. Последовательности для слияния, содержат, например, глутатион-S-трансферазу (Pharmacia, США), мальтоза-связывающий белок (NEB, США), FLAG (IBI, США) и 6x His (гексагистидин; Quiagen, США).
Такие векторы содержат гены устойчивости к антибиотикам, обычно используемые в данной области в качестве селективных маркеров, и содержат, например, гены устойчивости к ампициллину, гентамицину, карбенициллину, хлорамфениколу, стрептомицину, канамицину, генетицину, неомицину и тетрациклину.
В другом аспекте настоящее изобретение относится к клетке, трансформированной вышеуказанным вектором. Клетки, используемые для продуцирования антител по изобретению, могут быть прокариотическими, дрожжевыми или высшими эукариотическими клетками, но не ограничиваются ими.
Можно использовать бактериальные штаммы, такие как Escherichia coli, Bacillus subtilis и Bacillus thuringiensis, Streptomyces и Pseudomonas (например, Pseudomonas putida), и прокариотические клетки-хозяева, такие как Proteus mirabilis и Staphylococcus (например, Staphylococcus carnosus).
Однако наибольший интерес представляют клетки животных, и примеры полезных линий клеток-хозяев представляют собой, но не ограничиваются ими, COS-7, BHK, CHO, CHOK1, DXB-11, DG-44, CHO / -DHFR, CV1, COS-7, HEK293, BHK, TM4, VERO, HELA, MDCK, BRL 3A, W138, Hep G2, SK-Hep, MMT, TRI, MRC 5, FS4, 3T3, RIN, A549, PC12, K562, PER.C6, SP2/0, NS-0, U20S или HT1080.
В другом аспекте настоящее изобретение относится к способу получения вышеуказанных антител или их антигенсвязывающих фрагментов, включающему: (а) стадию культивирования клеток; и (b) стадию выделения антитела или его антигенсвязывающего фрагмента из культивируемых клеток.
Клетки можно культивировать в различных средах. В качестве культуральной среды можно без ограничений использовать коммерчески доступные среды. Все другие необходимые добавки, известные специалистам в данной области, могут быть включены в соответствующих концентрациях. Условия культивирования, такие как температура, pH и т.п., обычно используются с клетками-хозяевами, выбранными для экспрессии, что будет очевидно специалистам в данной области.
При выделении антитела или его антигенсвязывающего фрагмента примеси могут быть удалены, например, центрифугированием или ультрафильтрацией, и полученный продукт может быть очищен с использованием, например, аффинной хроматографии или тому подобное. Могут быть использованы другие способы очистки, такие как анионообменная или катионообменная хроматография, хроматография гидрофобного взаимодействия, хроматография на гидроксиапатита и т.п.
В одном аспекте настоящего изобретения линкер между антителом и активным средством может быть расщепляемым.
В одном аспекте настоящего изобретения линкер имеет структуру химической формулы IIa, приведенной ниже:
[Химическая формула IIa]
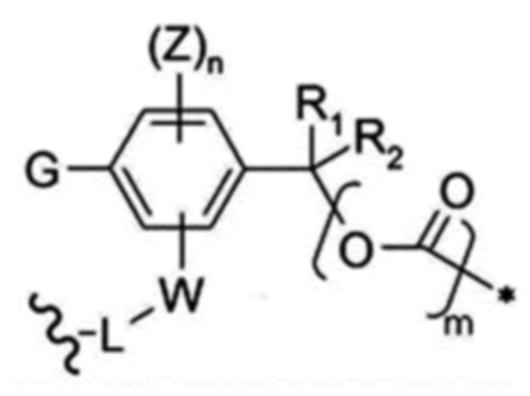
где:
G представляет собой сахар, сахарную кислоту или производное сахара;
W представляет собой -C(O)-, -C(O)NR'-, -C(O)O-, -S(O)2NR'-, -P(O)R''NR'-, -S(O)NR'- или -PO2NR'-; В случае, когда C(O), S или P непосредственно связаны с фенильным кольцом, R' и R'' представляют собой, соответственно и независимо, водород, (C1-C8) алкил, (C3-C8) циклоалкил, (C1-C8) алкокси, (C1-C8) алкилтио, моно- или ди-(C1-C8) алкиламино, (C3-C20) гетероарил, или (C6-C20) арил;
Каждый Z представляет собой, соответственно и независимо, (C1-C8) алкил, галоген, циано или нитро;
n представляет собой целое число от 0 до 3;
m имеет значение 0 или 1;
L отсутствует, или;
содержит по меньшей мере одно ответвляющееся звено (BR) и по меньшей мере одно соединительное звено;
R1 и R2 представляют собой, соответственно и независимо, водород, (C1-C8) алкил или (C3-C8) циклоалкил, или R1 и R2, вместе с атомами углерода, с которыми они связаны, образуют (C3-C8) циклоалкильное кольцо, и;
В приведенной выше формуле, ‘~’ обозначает область, которая связывается с антителом, и * обозначает область, которая связывается с лекарственным средством или токсином.
В одном аспекте настоящего изобретения, сахар или сахарная кислота представляет собой моносахарид.
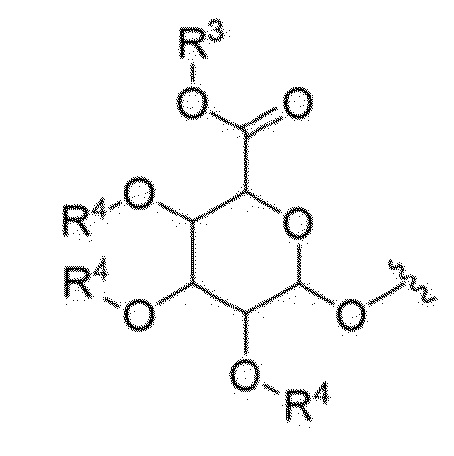
В одном аспекте настоящего изобретения, G представляет собой фрагмент глюкуроновой кислоты или соединение, имеющее структуру химической формулы (IIIa), приведенной ниже:
[Химическая формула (IIIa)]
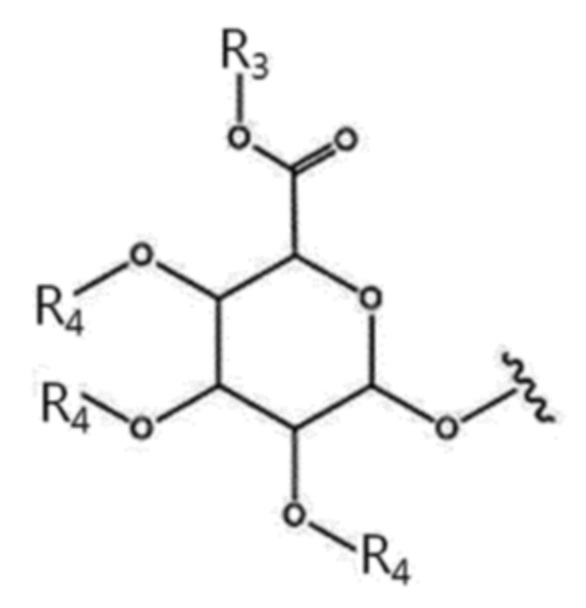
где:
R3 представляет собой водород или карбоксилзащитную группу, и;
каждый R4 представляет собой, соответственно и независимо, водород или гидроксилзащитную группу.
В одном аспекте настоящего изобретения, R3 представляет собой водород, и каждый R4 представляет собой водород.
Кроме того, R1 и R2 являются соответственно водородом.
Кроме того, каждый Z представляет собой, соответственно и независимо, (C1-C8) алкил, галоген, циано или нитро.
Кроме того, W представляет собой -C(O)-, -C(O)NR'- или -C(O)O-. Более конкретно, W представляет собой -C(O)NR'-, где C(O) связана с фенильным кольцом, и NR' связана с L.
Кроме того, n имеет значение 0, 1, 2 или 3, в частности, 0, 1 или 2, и более конкретно, 0.
Более конкретно, G представляет собой соединение химической формулы (IIIa) ниже:
[Химическая формула (IIIa)]
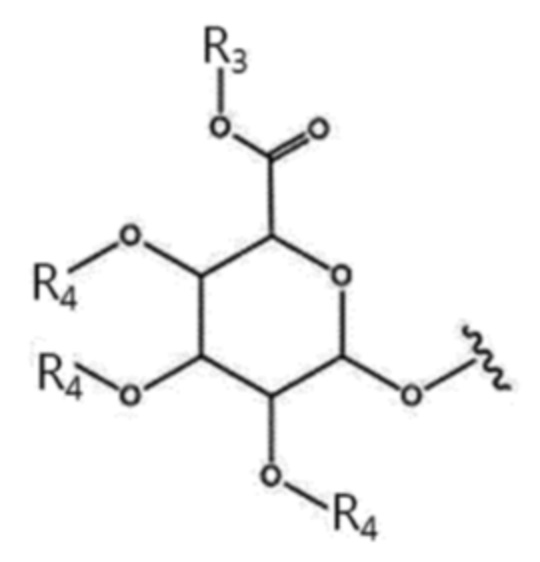
где:
R3 представляет собой водород или карбоксилзащитную группу;
Каждый R4 представляет собой, соответственно и независимо, водород или гидроксилзащитную группу, и;
W представляет собой -C(O)NR'-, где C(O) связана с фенильным кольцом, и NR' связана с L, каждый Z представляет собой (C1-C8) алкил, галоген, циано или нитро, n имеет значение 0, m имеет значение 1, и R1 и R2 являются соответственно водородом.
В одном аспекте настоящего изобретения по меньшей мере одно ответвляющееся звено представляет собой алкилен, имеющий от 1 до 100 атомов углерода, где атомы углерода алкилена могут быть замещены одним или несколькими гетероатомами, выбранными из группы, состоящей из N, O и S, и алкилен может быть дополнительно замещен одним или несколькими алкилами, имеющими от 1 до 20 атомов углерода.
В частности, по меньшей мере одно ответвляющееся звено представляет собой C1-C50 алкилен или гетероалкилен с 1-50 атомами и может удовлетворять по меньшей мере одному из следующего:
(i) ответвляющееся звено содержит по меньшей мере одну ненасыщенную связь;
(ii) 2 атома в ответвляющемся звене такие же, как и в заместителе, что завершает гетероарилен;
(iii) ответвляющееся звено представляет собой гетероалкилен с 1-50 атомами, и;
(iv) алкилен замещен по меньшей мере одним C1-20 алкилом.
Кроме того, по меньшей мере одно ответвляющееся звено представляет собой азотсодержащий гетероалкилен с 1-50 атомами, линкер содержит по меньшей мере 2 атома гидрофильной аминокислоты, и азот может образовывать пептидную связь с карбонилом гидрофильной аминокислоты.
В одном аспекте настоящего изобретения, по меньшей мере одно ответвляющееся звено представляет собой гидрофильную аминокислоту.
В одном аспекте настоящего изобретения, гидрофильная аминокислота может представлять собой аргинин, аспартат, аспарагин, глутамат, глутамин, гистидин, лизин, орнитин, пролин, серин или треонин.
Кроме того, гидрофильная аминокислота может ковалентно связывать оксим линкера с полиэтиленгликолевым звеном линкера.
В одном аспекте настоящего изобретения, гидрофильная аминокислота может быть аминокислотой, содержащей боковую цепь, имеющую фрагмент, который имеет электрический заряд в водном растворе при нейтральном pH.
В одном аспекте настоящего изобретения, гидрофильная аминокислота представляет собой аспартат или глутамат.
В одном аспекте настоящего изобретения, гидрофильная аминокислота представляет собой орнитин или лизин.
В одном аспекте настоящего изобретения, по меньшей мере одно ответвляющееся звено представляет собой -C(O)-, -C(O)NR'-, -C(O)O-, -S(O)2NR'-, -P(O)R''NR'-, -S(O)NR'- или -PO2NR'-, и R' и R'' представляют собой, соответственно и независимо, водород, (C1-C8) алкил, (C3-C8) циклоалкил, (C1-C8) алкокси, (C1-C8) алкилтио, моно- или ди-(C1-C8) алкиламино, (C3-C20) гетероарил, или (C6-C20) арил.
В одном аспекте настоящего изобретения, по меньшей мере одно ответвляющееся звено представляет собой -C(O)NR'-, и R' представляет собой водород.
В одном аспекте настоящего изобретения, по меньшей мере, одно соединительное звено представлено общей формулой VIII или общей формулой IX:
[Общая формула VIII]
-(CH2)r(V(CH2)p)q-
[Общая формула IX]
-(CH2CH2X)w-
где: V представляет собой одинарную связь, -O-, -S-, -NR21-, -C(O)NR22-, NR23C(O)-, NR24SO2- или -SO2NR25-;
X представляет собой -O-, C1-C8 алкилен или -NR21-;
R21-R25, независимо и соответственно, представляют собой водород, (C1-C6) алкил, (C1-C6) алкил (C6-C20) арил или (C1-C6) алкил (C3-C20) гетероарил;
r представляет собой целое число от 0 до 10;
p представляет собой целое число от 0 до 10;
q представляет собой целое число от 1 до 20, и;
w представляет собой целое число от 1 до 20.
В одном аспекте настоящего изобретения, q может иметь значение от 4 до 20, более конкретно, от 6 до 20. Кроме того, q может иметь значение от 2 до 12, более конкретно, 2, 5 или 11. Кроме того, может иметь значение 2. Кроме того, p может иметь значение 2. Кроме того, V может быть -O-.
Более конкретно, r может иметь значение 2, p может иметь значение 2, q может иметь значение 2, 5 или 11, и V может быть -O-.
Кроме того, в одном аспекте настоящего изобретения, X может быть -O-. Кроме того, w может быть целым числом от 6 до 20.
Более конкретно, X может быть -O-, и w может иметь значение от 6 до 20.
В одном аспекте настоящего изобретения, по меньшей мере одно соединительное звено содержит по меньшей мере одно полиэтиленгликолевое звено, представленное 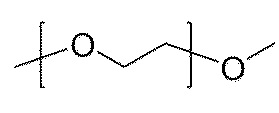 или
или  , где n имеет значение от 1 до 12.
, где n имеет значение от 1 до 12.
В одном аспекте настоящего изобретения, по меньшей мере одно соединительное звено может содержать от 1 до 12 групп -OCH2CH2-, от 3 до 12 групп -OCH2CH2-, от 5 до 12 групп -OCH2CH2-, от 6 до 12 групп -OCH2CH2- или 3 группы -OCH2CH2-.
В одном аспекте настоящего изобретения, по меньшей мере одно соединительное звено представляет собой -(CH2CH2X)w-,
где X представляет собой одинарную связь, -O-, (C1-C8) алкилен или -NR21-;
R21 представляет собой водород, (C1-C6) алкил, (C1-C6) алкил (C6-C20) арил или (C1-C6) алкил (C3-C20) гетероарил, и;
w представляет собой целое число от 1 до 20, в частности, 1, 3, 6 или 12.
В одном аспекте настоящего изобретения X представляет собой -O-, и w представляет собой целое число от 6 до 20.
В одном аспекте настоящего изобретения, линкер дополнительно содержит связывающие звенья, образованные реакциями 1,3-диполярного циклоприсоединения, реакциями гетеро-дилса, реакциями нуклеофильного замещения, реакциями карбонила неальдольного типа, присоединениями к кратным углерод-углеродным связям, реакциями окисления или клик-реакциями.
В одном аспекте настоящего изобретения, связывающее звено образовано взаимодействием между ацетиленом и азидом или взаимодействием между альдегидом или кетонной группой и гидразином или алкоксиамином.
В одном аспекте настоящего изобретения, связывающее звено представляет собой:
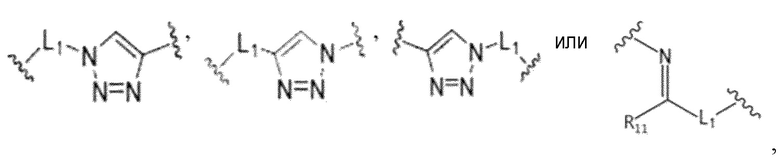
где
L1 представляет собой одинарную связь или алкилен, имеющий от 1 до 30 атомов углерода;
R11 представляет собой водород или алкил, имеющий от 1 до 10 атомов углерода, в частности, метил.
В одном аспекте настоящего изобретения, L1 представляет собой одинарную связь, алкилен с 11 атомами углерода или алкилен с 12 атомами углерода.
Кроме того, в одном аспекте изобретения связывающее звено содержит
 или
или
 ,
,
V представляет собой одинарную связь, -O-, -S-, -NR21-, -C(O)NR22-, NR23C(O)-, NR24SO2- или -SO2NR25-;
R21-R25, независимо и соответственно, представляют собой водород, C1-C6 алкил, C1-C6 алкил C6-C20 арил или C1-C6 алкил C3-C20 гетероарил;
r представляет собой целое число от 1 до 10;
p представляет собой целое число от 0 до 10;
q представляет собой целое число от 1 до 20, и;
L1 представляет собой одинарную связь.
В одном аспекте настоящего изобретения, r может иметь значение 2 или 3. Кроме того, p может иметь значение 1 или 2. Кроме того, q может иметь значение от 1 до 6.
Более конкретно, в связывающем звене, r может иметь значение 2 или 3; p может иметь значение 1 или 2, и; q может иметь значение от 1 до 6.
Кроме того, в одном аспекте настоящего изобретения, связывающее звено может представлять собой
 или;
или;
 , где:
, где:
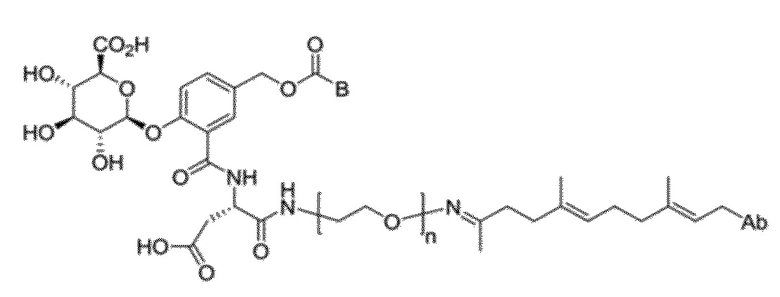
где Ab представляет собой антитело против DLK1; B представляет собой активное средство, и; n представляет собой целое число от 0 до 20.
В одном аспекте настоящего изобретения, ответвляющееся звено представляет собой  или
или 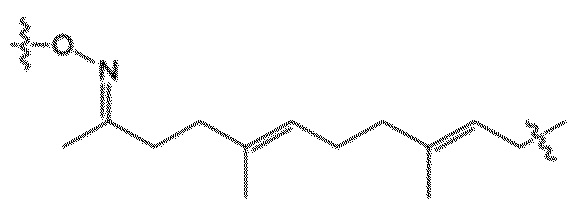 .
.
В одном аспекте настоящего изобретения, линкер может содержать от 3 до 50 гетероалкиленов, включая оксим,
атом кислорода оксима находится на стороне L, связанной с W, и атом углерода оксима находится на стороне L, связанной с Ab, или;
атом углерода оксима находится на стороне L, связанной с W, и атом кислорода оксима находится на стороне L, связанной с Ab.
В одном аспекте настоящего изобретения, линкер может дополнительно содержать по меньшей мере одно изопренильное звено, имеющее структуру 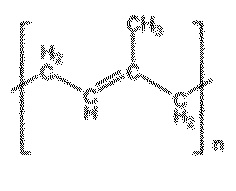 , где n равно по меньшей мере 2.
, где n равно по меньшей мере 2.
В одном аспекте настоящего изобретения по меньшей мере одно изопренильное звено представляет собой субстрат изопреноидтрансферазы или продукт изопреноидтрансферазы.
В одном аспекте настоящего изобретения, изопренильное звено линкера ковалентно связывается с антителом через тиоэфирную связь, и тиоэфирная связь содержит атом серы цистеина.
Кроме того, изопренильное звено может ковалентно связывать оксим, включенный в линкер, с антителом.
В одном аспекте настоящего изобретения, антитело содержит аминокислотный мотив, распознаваемый изопреноидтрансферазой, и тиоэфирная связь содержит атом серы цистеина аминокислотного мотива.
В одном аспекте настоящего изобретения, антитело, связывающееся с DLK1, или его антигенсвязывающий фрагмент, содержит аминокислотный мотив, распознаваемый изопреноидтрансферазой, и тиоэфирная связь содержит атом серы цистеина аминокислотного мотива.
В одном аспекте настоящего изобретения, аминокислотный мотив представляет собой последовательность, выбранную из группы, состоящей из CXX, CXC, XCXC, XXCC и CYYX, где C означает цистеин; Y в каждом случае независимо обозначает алифатическую аминокислоту; X в каждом случае независимо обозначает глутамин, глутамат, серин, цистеин, метионин, аланин или лейцин, и; тиоэфирная связь содержит атом серы цистеина аминокислотного мотива.
В одном аспекте настоящего изобретения, аминокислотный мотив представляет собой последовательность CYYX, и Y в каждом случае независимо представляет собой аланин, изолейцин, лейцин, метионин или валин.
В одном аспекте настоящего изобретения, аминокислотный мотив представляет собой последовательность CVIM или CVLL.
В одном аспекте настоящего изобретения, по меньшей мере, одна из 1-10 аминокислот, предшествующих аминокислотному мотиву, может быть, соответственно и независимо, выбрана из глицина, аргинина, аспарагиновой кислоты и серина. Например, в одном аспекте настоящего изобретения, по меньшей мере, одна из 7 аминокислот, предшествующих аминокислотному мотиву, представляет собой глицин. Альтернативно, по меньшей мере, 3 из 7 аминокислот, предшествующих аминокислотному мотиву, соответственно и независимо, выбраны из глицина, аргинина, аспарагиновой кислоты и серина. Альтернативно, 1-10 аминокислот, предшествующих аминокислотному мотиву, представляют собой глицин. В частности, по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 аминокислот, предшествующих аминокислотному мотиву, представляют собой глицин.
В одном аспекте настоящего изобретения, антитело может содержать аминокислотную последовательность GGGGGGGCVIM.
В одном аспекте настоящего изобретения, L содержит по меньшей мере один линкер-ответвления, ковалентно связанный с Ab,
i) соответствующие линкеры-ответвления содержат ответвляющееся звено, ковалентно связанное с Ab первичным линкером (PL);
ii) соответствующие линкеры-ответвления связывают первое активное средство с ответвляющимся звеном и содержат первое ответвление (B1), содержащее второй линкер (SL) и расщепляющуюся группу (CG), и;
iii) соответствующие линкеры-ответвления содержат а) второе ответвление (В2), где второе активное средство ковалентно связано с ответвляющимся звеном вторым линкером (SL) и расщепляющейся группой (CG), или b) второе ответвление, где полиэтиленгликолевый фрагмент ковалентно связан с ответвляющимся звеном,
и соответствующие расщепляющиеся группы гидролизуются для высвобождения активного средства из конъюгата антитела.
В одном аспекте настоящего изобретения, линкер-ответвление представляет собой  ,
, 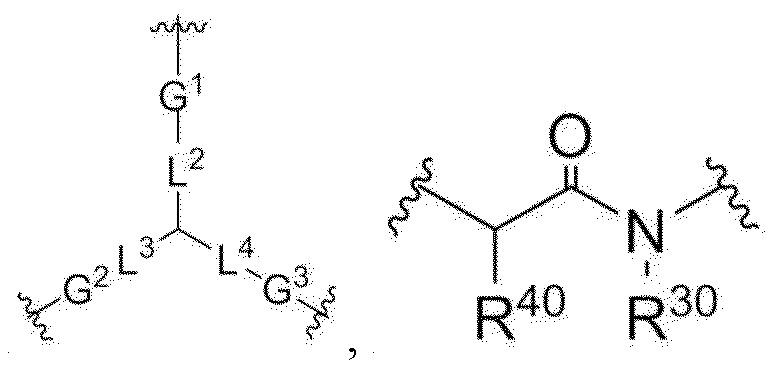 или
или  ;
;
L2, L3 и L4 представляют собой, соответственно и независимо, прямые связи или -CnH2n-, n представляет собой целое число от 1 до 30,
G1, G2 и G3 представляют собой, соответственно и независимо, прямую связь, 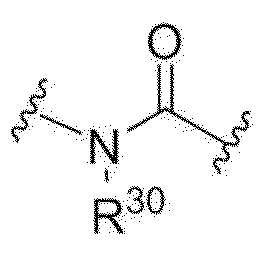 ,
, 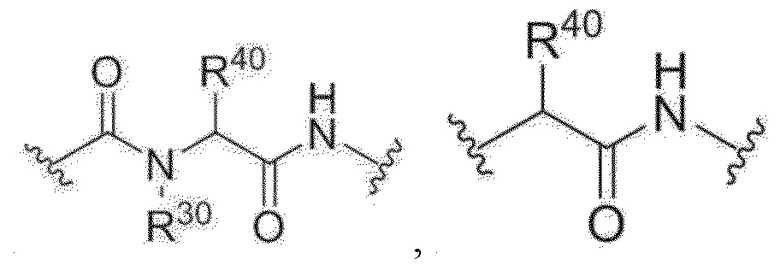 или
или  , и;
, и;
R30 представляет собой водород или C1-30 алки.
Более конкретно, линкер-ответвление содержит
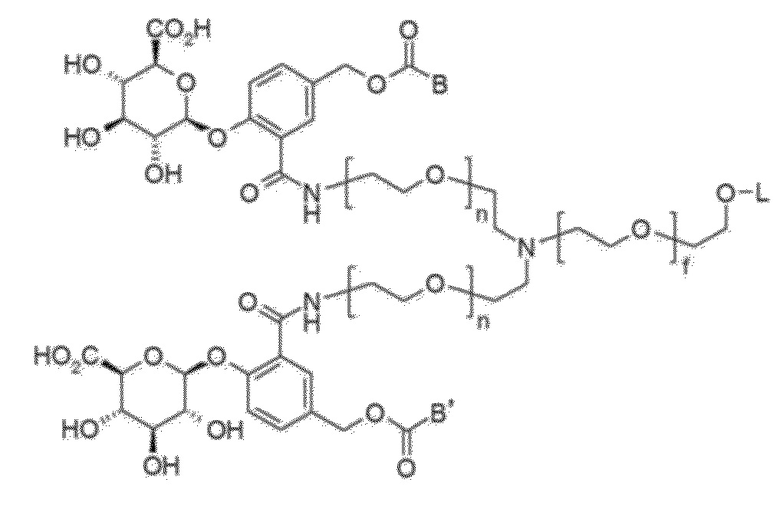 ,
,
B и B' обозначают активные средства, которые могут быть различными или идентичными;
n обозначает, соответственно и независимо, целое число от 0 до 30;
f обозначает, соответственно и независимо, целое число от 0 до 30, и;
L обозначает связь с Ab.
В одном аспекте настоящего изобретения, n представляет собой целое число от 1 до 20, более конкретно, целое число от 1 до 10, или от 4 до 20.
В одном аспекте настоящего изобретения, L содержит оксим, и по меньшей мере одно полиэтиленгликолевое звено ковалентно связывает оксим с активным средством.
В одном аспекте настоящего изобретения, расщепляющаяся группа может быть расщеплена внутри внутри клетки-мишени, и расщепляющаяся группа может высвободить одно или несколько активных средств.
В одном аспекте настоящего изобретения, линкер содержит по меньшей мере один линкер-ответвление, ковалентно связанный с Ab, и содержит по меньшей мере два активных средства, ковалентно связанных с линкер-ответвлением.
В частности, 1 линкер-ответвление может связываться с Ab.
Кроме того, два или более линкера-ответвлений могут связываться с Ab, и соответствующие линкеры-ответвления могут связываться по крайней мере с двумя активными средствами. Более конкретно, 3 линкера-ответвления могут связываться с Ab. Альтернативно 4 линкер-ответвление может связываться с Ab.
В одном аспекте настоящего изобретения, соответствующие линкеры-ответвления связываются по меньшей мере с двумя идентичными или различными активными средствами. В одном аспекте настоящего изобретения, соответствующие активные средства связаны с линкером-ответвлением расщепляемой связью.
В одном аспекте настоящего изобретения, соответствующие линкеры-ответвления содержат ответвляющееся звено, соответствующие активные средства связаны с ответвляющимся звеном через второй линкер, и ответвляющиеся звенья связаны с антителом посредством первого линкера.
В одном аспекте настоящего изобретения, ответвляющееся звено может быть атомом азота. Кроме того, ответвляющееся звено может быть амидом, и первый линкер или второй линкер может содержать карбонил амида. Альтернативно, ответвляющееся звено может быть лизиновым звеном.
В еще одном аспекте настоящего изобретения линкер может содержать:
(a) по меньшей мере одно ответвляющееся звено; (b) по меньшей мере одно соединительное звено; (c) по меньшей мере одно связывающее звено (BU), и; по меньшей мере одно триггерное звено (TU).
В данном случае, соединительное звено соединяет триггерное звено и связывающее звено, триггерное звено и ответвляющееся звено, или ответвляющееся звено и связывающее звено;
по меньшей мере одно триггерное звено может высвобождать по меньшей мере одно лекарственное средство или токсин, и ответвляющееся звено связывает соединительное звено и триггерное звено, или соединительное звено и другое соединительное звено.
В одном аспекте настоящего изобретения, триггерное звено имеет структуру химической формулы (IIb), ниже:
[Химическая формула (IIb)]
 ,
,
где:
G представляет собой сахар, сахарную кислоту или производное сахара;
W представляет собой -C(O)-, -C(O)NR'-, -C(O)O-, -S(O)2NR'-, -P(O)R''NR'-, -S(O)NR'- или -PO2NR'-; В случае, когда C(O), S или P непосредственно связаны с фенильным кольцом, R' и R'' представляют собой, соответственно и независимо, водород, (C1-C8) алкил, (C3-C8) циклоалкил, (C1-C8) алкокси, (C1-C8) алкилтио, моно- или ди-(C1-C8) алкиламино, (C3-C20) гетероарил, или (C6-C20) арил, и W связан с соединительным звеном или ответвляющимся звеном;
Каждый Z представляет собой, соответственно и независимо, (C1-C8) алкил, галоген, циано или нитро;
n представляет собой целое число от 1 до 3;
m имеет значение 0 или 1;
R1 и R2 представляют собой, соответственно и независимо, водород, (C1-C8) алкил или (C3-C8) циклоалкил, или R1 и R2, вместе с атомами углерода, с которыми они связаны, образуют (C3-C8) циклоалкильное кольцо.
В одном аспекте настоящего изобретения, сахар или сахарная кислота представляет собой моносахарид.
В одном аспекте настоящего изобретения, G представляет собой соединение, имеющее структуру химической формулы (IIIa) ниже:
[Химическая формула (IIIa)]
 ,
,
где:
R3 представляет собой водород или карбоксилзащитную группу, и;
Каждый R4 представляет собой, соответственно и независимо, водород или гидроксилзащитную группу.
В одном аспекте настоящего изобретения, R3 представляет собой водород, и каждый R4 представляет собой водород.
В одном аспекте настоящего изобретения, W представляет собой -C(O)NR'-, где C(O) связана с фенильным кольцом, и NR' связана с L.
В одном аспекте настоящего изобретения, Z представляет собой водород.
В одном аспекте настоящего изобретения, R1 и R2 являются соответственно водородом.
В одном аспекте настоящего изобретения, соединительное звено представлено как -(CH2)r(V(CH2)p)q-, -((CH2)pV)q-, -(CH2)r(V(CH2)p)qY-, -((CH2)pV)q(CH2)r-, -Y((CH2)pV)q- или -(CH2)r(V(CH2)p)qYCH2-,
где:
r представляет собой целое число от 0 до 10;
p представляет собой целое число от 1 до 10;
q представляет собой целое число от 1 до 20;
V и Y, независимо и соответственно, представляют собой одинарную связь, -O-, -S-, -NR21-, -C(O)NR22-, NR23C(O)-, NR24SO2- или -SO2NR25- и;
R21-R25, независимо и соответственно, представляют собой водород, (C1-C6) алкил, (C1-C6) алкил (C6-C20) арил или (C1-C6) алкил (C3-C20) гетероарил.
В одном аспекте настоящего изобретения, r имеет значение 2.
В одном аспекте настоящего изобретения, p имеет значение 2.
В одном аспекте настоящего изобретения, q представляет собой целое число от 6 до 20.
В одном аспекте настоящего изобретения, q имеет значение 2, 5 или 11.
В одном аспекте настоящего изобретения, V и Y представляют собой, соответственно и независимо, -O-.
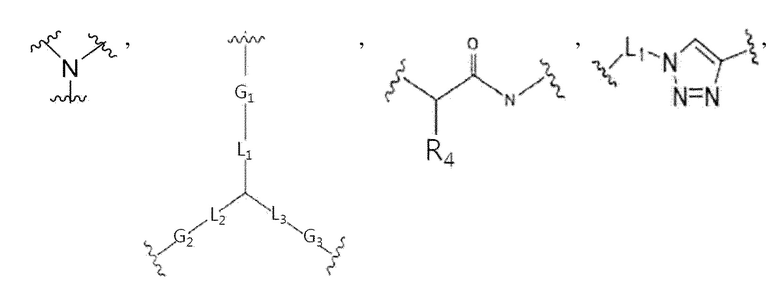
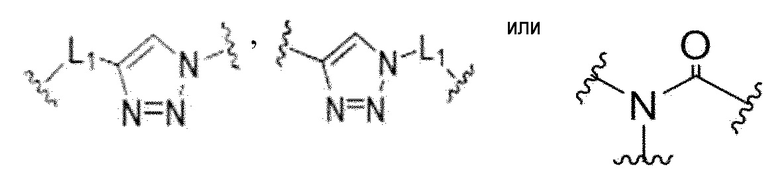 ,
,
где:
L1, L2 и L3 представляют собой, соответственно и независимо, прямую связь или -CnH2n-;
n представляет собой целое число от 1 до 30;
где:
G1, G2 и G3 представляют собой, соответственно и независимо, прямую связь,  ,
, 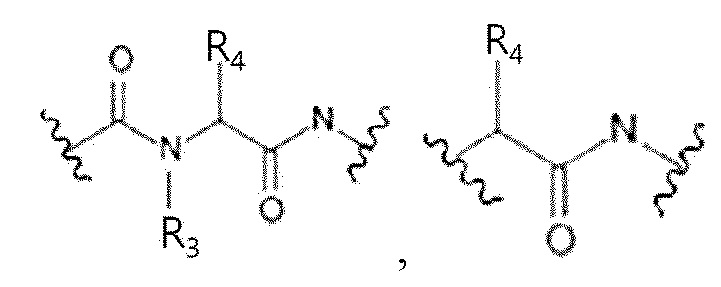 или
или 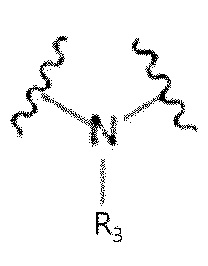 ,
,
R3 представляет собой водород или C1-C30 алкил;
R4 представляет собой водород или L4-COOR5; L4 представляет собой прямую связь или -CnH2n-; n представляет собой целое число от 1 до 10, и R5 представляет собой водород или C1-C30 алкил.
В одном аспекте настоящего изобретения, ответвляющееся звено представляет собой
 ,
,
где L1 представляет собой прямую связь или алкилен, имеющий от 1 до 30 атомов углерода;
R11 представляет собой водород или алкил, имеющий от 1 до 10 атомов углерода, в частности, метил;
L2 представляет собой алкилен, имеющий от 1 до 30 атомов углерода, и;
ответвляющееся звено связывает соединительное звено и антитело.
В одном аспекте настоящего изобретения, L1 представляет собой алкилен, имеющий 12 атомов углерода.
В одном аспекте настоящего изобретения, R11 представляет собой метил.
В одном аспекте настоящего изобретения, L2 представляет собой алкилен, имеющий 11 атомав углерода.
В одном аспекте настоящего изобретения, ответвляющееся звено представляет собой
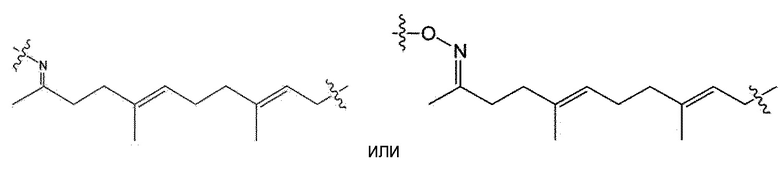 .
.
В одном аспекте настоящего изобретения, изопренильное звено линкера ковалентно связывается с антителом через тиоэфирную связь, и тиоэфирная связь содержит атом серы цистеина.
В одном аспекте настоящего изобретения, антитело содержит аминокислотный мотив, распознаваемый изопреноидтрансферазой, и тиоэфирная связь содержит атом серы цистеина аминокислотного мотива.
В одном аспекте настоящего изобретения, аминокислотный мотив представляет собой последовательность, выбранную из группы, состоящей из CXX, CXC, XCXC, XXCC и CYYX, где C означает цистеин; Y в каждом случае независимо обозначает алифатическую аминокислоту; X в каждом случае независимо обозначает глутамин, глутамат, серин, цистеин, метионин, аланин или лейцин, и; тиоэфирная связь содержит атом серы цистеина аминокислотного мотива.
В одном аспекте настоящего изобретения, аминокислотный мотив представляет собой последовательность CYYX, и Y в каждом случае независимо представляет собой аланин, изолейцин, лейцин, метионин или валин.
В одном аспекте настоящего изобретения, аминокислотный мотив представляет собой последовательность CVIM или CVLL.
В одном аспекте настоящего изобретения, по меньшей мере, одна из 7 аминокислот, предшествующих аминокислотному мотиву, может быть, соответственно и независимо, выбрана из глицина, аргинина, аспарагиновой кислоты и серина.
В одном аспекте настоящего изобретения, по меньшей мере 3 из 7 аминокислот, предшествующих аминокислотному мотиву, соответственно и независимо выбраны из глицина, аргинина, аспарагиновой кислоты и серина.
Альтернативно, 1-10 аминокислот, предшествующих аминокислотному мотиву, представляют собой глицин. В частности, по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 аминокислот, предшествующих аминокислотному мотиву, представляют собой глицин.
В одном аспекте настоящего изобретения, антитело может содержать аминокислотную последовательность GGGGGGGCVIM.
Кроме того, в одном аспекте настоящего изобретения, активное средство может быть химиотерапевтическим средством или токсином.
Кроме того, активное средство может быть иммунорегуляторным соединением, противораковым средством, противовирусным средством, антибактериальным средством, противогрибковым, противопаразитарным средством или их комбинацией, и активные средства, перечисленные ниже, могут использоваться выборочно:
(a) эрлотиниб, бортезомиб, фулвестрант, сутент, летрозол, иматиниба мезилат, PTK787/ZK 222584, оксалиплатин, 5-фторурацил, лейковорин, рапамицин, лапатиниб, лонафарниб, сорафениб, гефитиниб, AG1478, AG1571, тиотепа, циклофосфамид, бусульфан, импросульфан, пипосульфан, бензодопа, карбоквон, метуредопа, уредопа, этиленимин, алтретамин, триэтиленмеламин, триэтиленфосфорамид, триэтилентиофосфорамид, тейметилолмеламин, буллатацин, буллатациионон, камптотецин, топотекан, бриостатин, каллистатин, CC-1065, адозелезин, карзелезин, бизелезин, криптофицин 1, криптофицин 8, доластатин, дуокармицин, KW-2189, CB1-TM1, элеутеробин, панкратистатин, саркодиктиин, спонгистатин, хлорамбуцил, хлорнафазин, холофосфамид, эстрамустин, ифосфамид, мехлорэтамин, мелфалан, новэмбихин, фенестерин, преднимустин, трофосфамид, урамустин, кармустин, хлорозотоксин, фотемустин, ломустин, нимустин, ранимустин, калихеамицин, калихеамицин гамма 1, калихеамицин омега 1, динемицин, динемицин А, клодронат, эсперамицин, неокарциностатин хромофор, аклациномизины, актиномицин, антримицин, азасерин, блеомицины, катциномицин, карабицин, карниномицин, карзинофилин, хромомицины, дактиномицин, даунорубицин, деторубуцин, 6-диазо-5-оксо-L-норлейцин, доксорубицин, морфолинодоксорубицин, цианоморфолинодоксорубицин, 2-пирролинодоксорубицин, липосомальный доксорубицин, дезоксидоксорубицин, эпирубицин, эзорубицин, марцелломицин, митомицин C, микофеноловая кислота, ногаламицин, оливомицины, пепломицин, потфиромицин, пуромицин, квеламицин, родорубицин, стрептомигрин, стрептозоцин, тудерцидин, убенимекс, зиностатин, зорубицин, 5-fluoDLKacil, деноптерин, метотрексат, птероптерин, триметрексат, флударабин, 6-меркаптопурин, тиамиприн, тиогуанин, анцитабин, азацитидин, 6-азауридин, кармофур, цитарабин, дидезоксиуридин, доксифлуридин, эноцитабин, флоксуридин, калустерон, дромостанолон, пропионат, эпитиостанол, мепитиостан, тестолактон, аминоглутетимид, митотан, трилостан, фолиновая кислота, ацеглатон, альдофосфамид гликозид, аминолевулиновая кислота, энилурацил, амсакрин, бестрабуцил, бисантрен, эдатрексат, дефофамин, демоколцин, диазиквон, элфорнитин, эллиптиния ацетат, этоглюцид, нитрат галлия, гидроксимочевина, лентинан, лонидаинин, майтанзин, ансамитоцины, митогуазон, митоксантрон, мопиданмол, нитраерин, пентостатин, фенамет, пирарубицин, лозоксантрон, 2-этилгидразид, прокарбазин, полисахарид-k, разоксан, ризоксин, сизофиран, спирогерманий, тенуазоновая кислота, триакизуон, 2,2',2''-трихлортриэтиламин, токсин Т-2, верракурин A, роридин A, ангуидин, уретан, виндезин, дакарбазин, манномустин, митобронитол, митолактол, пипоброман, гацитозин, арабинозид, циклофосфамид, тиотепа, паклитаксел, альбумин-сконструированная композиция наночастиц паклитаксела, доцетаксел, хлорамбуцил, гемцитабин, 6-тиогуанин, меркаптопурин, цисплатин, карбоплатин, винбластин, платина, этопозид, ифосфамид, митоксантрон, винкристин, винорелбин, новантрон, тенипозид, эдатрексат, дауномицин, аминоптерин, кселода, ибандронат, CPT-11, ингибитор топоизомеразы RFS 2000, дифторметилорнитин, ретиноевая кислота, капецитабин или их фармацевтически приемлемые соли, сольваты или кислоты;
(b) монокин, лимфокин, традиционный полипептидный гормон, паратиреоидный гормон, тироксин, релаксин, pDLKelaxin, гликопротеиновый гормон, фолликулостимулирующий гормон, тиреостимулирующий гормон, лютеинизирующий гормон, фактор роста печени фактор роста фибробластов, пролактин, плацентарный лактоген, фактор некроза опухоли, фактор некроза опухоли α, фактор некроза опухоли β, мюллерова ингибирующая субстанция, мышиный гонадотропин-ассоциированный пептид, ингибин, активин, фактор роста эндотелия сосудов, тромбопоэтин, эритропоэтин, остеоиндуктивный фактор, интерферон, интерферон-α, интерферон-β, интерферон-γ, колониестимулирующий фактор (CSF), макрофагальный-CSF, гранулоцитарно-макрофагальный-CSF), гранулоцитарно-макрофагальный-CSF, гранулоцитарный CSF, интерлейкин (IL), IL-1, IL-1α, IL-2, IL-3, IL-4, IL-5, IL-6, IL-7, IL-8, IL-9, IL-10, IL-11, I L-12, фактор некроза опухоли, TNF-α, TNF-β, полипептидный фактор, LIF, kit-лиганд или их смеси;
(c) дифтерийный токсин, ботулинический токсин, столбнячный токсин, дизентерийный токсин, холерный токсин, аманитин, α-аматинин, пирролобензодиазепин, производное пирролобензодиазепина, индолинобензодиазепин, пиридобензодиазепин, тетродотоксин, бреветоксин, цигуатоксин, рицин, AM токсин, ауристатин, тубулизин, гелданамицин, майтансиноид, калихеамицин, дауномицин, доксорубицин, метотрексат, виндезин, SG2285, доластатин, аналог доластатина, ауристатин, криптофицин, камптотецин, ризоксин, производные ризоксина, CC-1065, аналоги или производные CC-1065, дуокармицин, эндииновый антибиотик, эсперамицин, эпотилон, токсоид или их смеси;
(d) аффинный лиганд, где аффинный лиганд представляет собой субстрат, ингибитор, активное средство, нейромедиатор, радиоактивный изотоп или их смеси;
(e) радиоактивная метка, 32P, 35S, флуоресцентный краситель, электронноплотный реагент, фермент, биотин, стрептавидин, диоксигенин, гаптен, иммуногенный белок, молекула нуклеиновой кислоты с последовательностью, комплементарной мишени, или их смеси;
(f) иммуномодулирующее соединение, противораковое средство, противовирусное средство, антибактериальное средство, противогрибковое средство, противопаразитарное средство или их смеси;
(g) тамоксифен, ралоксифен, дролоксифен, 4-гидрокситамоксифен, триоксифен, кеоксифен, LY117018, онапристон или торемифен;
(h) 4(5)-имидазол, аминоглутетимид, мегестрола ацетат, эксеместан, летрозол или анастрозол
(i) флутамид, нилутамид, бикалутамид, лейпролид, гозерелин или троксацитабин;
(j) ингибитор ароматазы;
(k) ингибитор протеинкиназы;
(l) ингибитор липидкиназы;
(m) антисмысловой олигонуклеотид;
(n) рибозим;
(o) вакцина, и;
(p) антиангиогенное средство.
Еще один аспект настоящего изобретения в отношении получения лекарственного средства для профилактики или лечения пролиферативного, рака или ангиогенетического заболевания предусматривает применение конъюгата антитело-лекарственное средство или его фармацевтически приемлемой соли или сольвата.
Еще один аспект настоящего изобретения предоставляет способ для лекарственного средства для профилактики или лечения пролиферативного, рака или ангиогенетического заболевания путем введения индивидууму фармацевтической композиции для профилактики или лечения пролиферативного, рака или ангиогенетического заболевания, фармацевтическую композицию, содержащую конъюгат антитело-лекарственное средство или его фармацевтически приемлемую соль или сольват, в качестве активного ингредиента, где фармацевтическая композиция смешана и вводится по меньшей мере с одним антипролиферативным, цитостатическим или цитотоксическим веществом.
Еще один аспект настоящего изобретения предоставляет конъюгат антитело-лекарственное средство общей формулы Ia, приведенной ниже:
[Общая формула Ia]
Ab-(Линкер-D)n,
где:
Ab представляет собой антитело против DLK1;
Линкер представляет собой линкер;
D представляет собой пирролобензодиазепиновый димер в качестве активного средства, и;
линкер и антитело связаны через положение N10 или N10' пирролобензодиазепинового димера.
В данном случае пролекарство пирролобензодиазепинового димера, его фармацевтически приемлемая соль или сольват, где: в положениях N10 и N10' пирролобензодиазепинового димера, соответственно и независимо, присоединен любой из выбранных из группы, состоящей из -C(O)O*, -S(O)O*, -C(O)*, -C(O)NR*, -S(O)2NR*, -(P(O)R')NR*, -S(O)NR* и -PO2NR* групп;
где * представляет собой область, к которой присоединен линкер;
где R и R' представляют собой, соответственно и независимо, H, OH, N3, CN, NO2, SH, NH2, ONH2, NHNH2, галоген, замещенный или незамещенный C1-8 алкил, замещенный или незамещенный C3-8 циклоалкил, замещенный или незамещенный C1-8 алкокси, замещенный или незамещенный C1-8 алкилтио, замещенный или незамещенный C3-20 гетероарил, замещенный или незамещенный C5-20 арил или моно- или ди-C1-8 алкиламино, и;
где, в случае, когда C1-8 алкил, C3-8 циклоалкил, C1-8 алкокси, C1-8 алкилтио, C3-20 гетероарил или C5-20 арил замещены, замещение осуществляется группой замещения, выбранной из группы, содержащей H, OH, N3, CN, NO2, SH, NH2, ONH2, NNH2, галоген, C1-6 алкил, C1-6 алкокси и C6-12 арил.
Пролекарство пирролобензодиазепинового димера, его фармацевтически приемлемая соль или сольват можно использовать в качестве активного средства.
В одном аспекте настоящего изобретения, предоставляется предшественник пирролобензодиазепинового димера. В случае введения в форме предшественника в соответствии с настоящим изобретением, существуют преимущества перед обычными лекарственными средствами PBD в том, что: необходимы дополнительные реакции для превращения в эффективное лекарство при контакте с кровью, предотвращая возможность побочных реакций, которые могут возникнуть при неожиданном растворении линкера; в том, что токсичность для нормальных клеток снижается, и в том, что лекарственное средство более стабильно.
Кроме того, при получении конъюгатов антитело-лекарственное средство, поскольку конъюгат антитело-лекарственное средство, полученный с использованием обычных методов, имеет высокое содержание примесей, а экспонированная иминная группа подвергается атаке нуклеофилов, создается риск образования лекарственного средства с нежелательной структурой. С другой стороны, конъюгат антитело-лекарственное средство, полученный с использованием способа по настоящему изобретению, имеет преимущество простоты выделения благодаря высокой чистоте и дополнительно улучшенным физическим свойствам по сравнению с обычным PBD или димером PBD.
В одном аспекте настоящего изобретения, предшественник пирролобензодиазепинового димера представляет собой предшественник пирролобензодиазепинового димера, отличающийся тем, что он имеет структуру общей формулы X или общей формулы XI, приведенной ниже, или его фармацевтически приемлемой соли или сольвата:
[Общая формула X]
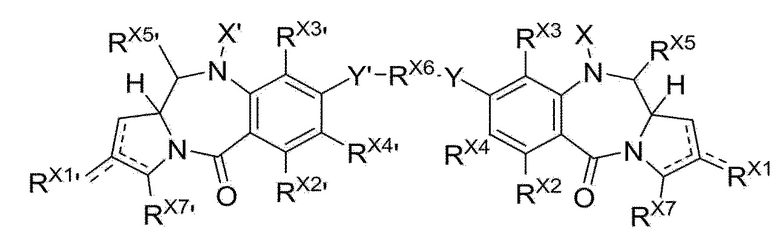
[Общая формула XI]
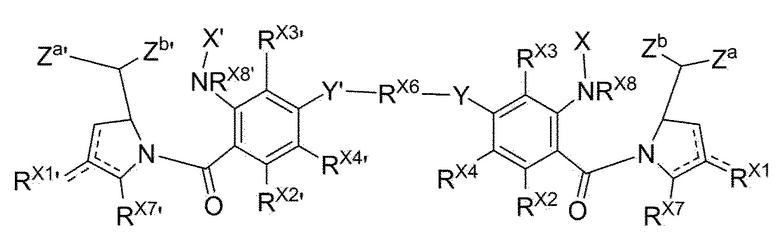
В приведенных выше формулах:
Пунктирные линии обозначают возможное наличие двойных связей между C1 и C2, между C2 и C3, между C'1 и C'2 или между C'2 и C'3;
RX1 и RX1' независимо выбраны из H, OH, =O, =CH2 CN, Rm ORm, =CH-Rm', =C(Rm')2, O-SO2-Rm, CO2Rm, CORm, галогена и дигалогена;
Rm' выбран из Rm, CO2Rm, CORm, CHO, CO2H и галогена;
каждый Rm независимо выбран из группы, состоящей из C1-12 алкила, C2-12 алкенила, C2-12 алкинила, C5-20 арила, C5-20 гетероарила, C3-6 циклоалкила, 3-7-членного гетероциклила, 3-7-членного гетероциклоалкила и 5-7-членного гетероарила;
RX2, RX2', RX3, RX3', RX5 и RX5' независимо выбраны из H, Rm, OH, ORm, SH, SRm, NH2, NHRm, NRm2, NO2, Me3SN и галогена;
RX4 и RX4' независимо выбраны из H, Rm, OH, ORm, SH, SRm, NH2, NHRm, NRm2, NO2, Me3SN, галогена, C1-6 алкила, C1-6 алкокси, C2-6 алкенила, C2-6 алкинила, C3-6 циклоалкила, 3-7-членного гетероциклоалкила, C5-12 арил, 5-7-членного гетероарила, -CN, -NCO, -ORn, -OC(O)Rn, -OC(O)NRnRn', -OS(O)Rn, -OS(O)2Rn, -SRn, -S(O)Rn, -S(O)2Rn, -S(O)NRnRn', -S(O)2NRnRn', -OS(O)NRnRn', -OS(O)2NRnRn', -NRnRn', -NRnC(O)Ro, -NRnC(O)ORo, -NRnC(O)NRoRo', -NRnS(O)Ro, -NRnS(O)2Ro, -NRnS(O)NRoRo', -NRnS(O)2NRoRo', -C(O)Rn, -C(O)ORn и -C(O)NRnRn';
RX и RX' независимо выбраны из H, OH, N3, CN, NO2, SH, NH2, ONH2, NHNH2, галогена, C1-8 алкила, C3-8 циклоалкила, C1-8 алкокси, C1-8 алкилтио, C3-20 гетероарила, C5-20 арила или моно- или ди-C1-8 алкиламино;
Y и Y' независимо выбраны из O, S и N(H);
Rx6 независимо выбран из C3-12 алкилена, C3-12 алкенилена, или C3-12 гетероалкилена;
RX7 и RX7' независимо выбраны из H, C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C3-6 циклоалкила, 3-7-членного гетероциклоалкила, C6-10 арила, 5-7-членного гетероарила, -ORr, -OC(O)Rr, -OC(O)NRrRr', -OS(O)Rr, -OS(O)2Rr, -SRr, -S(O)Rr, -S(O)2Rr, -S(O)NRrRr', -S(O)2NRrRr', -OS(O)NRrRr', -OS(O)2NRrRr', -NRrRr', -NRrC(O)Rs, -NRrC(O)ORs, -NRrC(O)NRsRs', -NRrS(O)Rs, -NRrS(O)2Rs, -NRrS(O)NRsRs', -NRrS(O)2NRsRs, -C(O)Rr, -C(O)ORs или -C(O)NRrRr';
каждый Rr, Rr', Rs и Rs' независимо выбран из H, C1-7 алкила, C2-7 алкенила, C2-7 алкинила, C3-13 циклоалкила, 3-7-членного гетероциклоалкила, C5-10 арила и 5-7-членного гетероарила;
каждый RX8 и RX8' независимо выбран из H, C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C3-6 гетероалкила, 3-7-членного гетероциклоалкила, C5-10 арила, 5-7-членного гетероарила, -S(O)Rm, -S(O)2Rm, -S(O)NRmRm', -S(O)2NRmRm', -NRmRm', -NRmC(O)Rm, -NRmC(O)ORn, -NRmC(O)NRnRn', -NRmS(O)Rn, -NRmS(O)2Rn, -NRmS(O)NRnRn', -NRmS(O)2NRnRn', -C(O)Rm, -C(O)ORm и -C(O)NRmRm';
Za выбран из ORX12a, NRX12aRX12a или SRX12a;
Zb выбран из ORX13a, NRX13aRX13a или SRX13a;
Za' выбран из ORX12a, NRX12aRX12a или SRX12a;
Zb' выбран из ORX13a', NRX13a'RX13a' или SRX13a';
каждый RX12a, RX12a', RX13a' и Rx13a' независимо выбран из H, C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C3-6 циклоалкила, 3-7-членного гетероциклоалкила, C5-10 арила, 5-7-членного гетероарила, -C(O)RX15a, -C(O)ORX15a и -C(O)NRX15aRX15a';, и;
каждый RX15a и Rx15a' независимо выбран из C1-12 алкила, C2-12 алкенила, C2-12 алкинила, C5-20 арила, C5-20 гетероарила, C3-6 циклоалкила, 3-7-членного гетероциклила, 3-7-членного гетероциклоалкила, и 5-7-членного гетероарила, и:
RX13a и RX14a необязательно соединяют атомы, к которым они присоединены, с образованием 3-7-членного гетероциклила, 3-7-членного гетероциклоалкила, или 3-7-членного гетероарила, и RX13a' и RX14a' необязательно соединяют атомы, к которым они присоединены, с образованием 3-7-членного гетероциклила, 3-7-членного гетероциклоалкила или 3-7-членного гетероарила, и;
каждый из Rn, Rn', Ro, Ro', Rp и Rp' независимо выбран из H, C1-7 алкила, C2-7 алкенила, C2-7 алкинила, C3-13 циклоалкила, 3-7-членного гетероциклоалкила, C5-10 арила и 5-7-членного гетероарила.
Кроме того, Rm независимо выбран из группы, состоящей из C1-12 алкила, C2-12 алкенила, C2-12 алкинила, C5-20 арила, C5-20 гетероарила, C3-6 циклоалкила, 3-7-членного гетероциклила, 3-7-членного гетероциклоалкила и 5-7-членного гетероарила, и;
Rm дополнительно замещен C1-12 алкилом, C2-12 алкенилом, C2-12 алкинилом, C5-20 арилом, C5-20 гетероарилом, C3-6 циклоалкилом, 3-7-членным гетероциклилом, 3-7-членным гетероциклоалкилом или 5-7-членным гетероарилом.
Кроме того, Rx4 и Rx4' независимо выбраны из H, Rm, OH, ORm, SH, SRm, NH2, NHRm, NRmRm', NO2, Me3Sn, галогена, C1-6 алкил C1-6 алкокси, C2-6 алкенила, C2-6 алкинила, C3-6 циклоалкила, 3-7-членного гетероциклоалкила, C5-12 арила, 5-7-членного гетероарила, -CN, -NCO, -ORn, -OC(O)Rn, -OC(O)NRnRn', -OS(O)Rn, -OS(O)2Rn, -SRn, -S(O)Rn, -S(O)2Rn, -S(O)NRnRn', -S(O)2NRnRn', -OS(O)NRnRn', -OS(O)2NRnRn', -NRnRn', -NRnC(O)Ro, -NRnC(O)ORo, -NRnC(O)NRoRo', -NRnS(O)Ro, -NRnS(O)2Ro, -NRnS(O)NRoRo',-NRnS(O)2NRoRo', -C(O)Rn, -C(O)ORn и -C(O)NRnRn', и;
RX4 или RX4' представляет собой C1-6 алкил, C1-6 алкокси, C2-6 алкенил, C2-6 алкинил, C3-6 циклоалкил, 3-7-членный гетероциклоалкил, C5-12 арил или 5-7-членный гетероарил, и дополнительно замещен по меньшей мере одним C1-6 алкилом, C1-6 алкокси, C2-6 алкенилом, C2-6 алкинилом, C3-6 циклоалкилом, 3-7-членным гетероциклоалкилом, C5-10 арилом, 5-7-членным гетероарилом, -ORp, -OC(O)Rp, -OC(O)NRpRp', -OS(O)Rp, -OS(O)2Rp, -SRp, -S(O)Rp, -S(O)2Rp, -S(O)NRpRp', -S(O)2NRpRp', -OS(O)NRpRp', -OS(O)2NRpRp', -NRpRp', -NRpC(O)Rq, -NRpC(O)ORq, -NRpC(O)NRqRq', -NRpS(O)Rq, -NRpS(O)2Rq, -NRpS(O)NRqRq', -NRpS(O)2NRqRq', -C(O)Rp, -C(O)ORp или -C(O)NRpRp.
Кроме того, RX7 и RX7' независимо выбраны из H, C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C3-6 циклоалкила, 3-7-членного гетероциклоалкила, C6-10 арила, 5-7-членного гетероарила, -ORr, -OC(O)Rr, -OC(O)NRrRr', -OS(O)Rr, -OS(O)2Rr, -SRr, -S(O)Rr, -S(O)2Rr, -S(O)NRrRr', -S(O)2NRrRr', -OS(O)NRrRr', -OS(O)2NRrRr', -NRrRr', -NRrC(O)Rs, -NRrC(O)ORs, -NRrC(O)NRsRs', -NRrS(O)Rs, -NRrS(O)2Rs, -NRrS(O)NRsRs', -NRrS(O)2NRsRs, -C(O)Rr, -C(O)ORs или -C(O)NRrRr';
RX7 и RX7' независимо выбраны из C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C3-6 циклоалкила, 3-7-членного гетероциклоалкила, C6-10 арила, или 5-7-членного гетероарила, и дополнительно замещены C1-6 алкилом, C2-6 алкенилом, C2-6 алкинилом, C3-6 циклоалкилом, 3-7-членным гетероциклоалкилом, C6-10 арилом, 5-7-членным гетероарилом, -ORt, -OC(O)Rt, -OC(O)NRtRt', -OS(O)Rt, -OS(O)2Rt, -SRt, -S(O)Rt, -S(O)2Rt, -S(O)NRtRt', -S(O)2NRtRt', -OS(O)NRtRt', -OS(O)2NRtRt', -NRtRt', -NRtC(O)Ru, -NRtC(O)ORu, -NRtC(O)NRuRu', -NRtS(O)Ru, -NRtS(O)2Ru, -NRtS(O)NRuRu', -NRtS(O)2NRuRu', -C(O)Rt, -C(O)ORt или -C(O)NRtRt', и;
Rr, Rr', Rs, Rs', Rt, Rt', Ru и Ru' независимо выбраны из H, C1-7 алкила, C2-7 алкенила, C2-7 алкинила, C3-13 циклоалкила, 3-7-членного гетероциклоалкила, C5-10 арила, и 5-7-членного гетероарила.
Кроме того, RX1 и RX1' независимо выбраны из Rm, и;
Rm выбран из C1-6 алкила, C2-6 алкенила, C5-7 арила и C3-6 гетероарила.
Кроме того, RX2, RX2', RX3, RX3', RX5 и RX5' независимо выбраны из H или OH.
Кроме того, RX4 и RX4' независимо выбраны из Rm, и;
Rm представляет собой C1-6 алкокси.
Кроме того, RX4 и RX4' независимо представляют собой любые группы, выбранные из группы, состоящей из метокси, этокси и бутокси.
Кроме того, Y и Y' представляют собой O.
Кроме того, Rx6 представляет собой C3-12 алкилен, C3-12 алкенилен или C3-12 гетероалкилен, с Rx6, замещенным -NH2, -NHRm, -NHC(O)Rm, -NHC(O)Rm, -NHC(O)CH2-[OCH2CH2]n-RXX или -[CH2CH2O]n-RXX;
RXX представляет собой H, OH, N3, CN, NO2, SH, NH2, ONH2, NHNH2, галоген, C1-8 алкил, C3-8 циклоалкил, C1-8 алкокси, C1-8 алкилтио, C3-20 гетероарил, C5-20 арил или моно- или ди-C1-8 алкиламино, и;
n представляет собой целое число от 1 до 6.
Кроме того, в одном аспекте настоящего изобретения активное средство представляет собой пирролобензодиазепиновый димер, обозначенный общей формулой XII или общей формулой XIII;
[Общая формула XII]
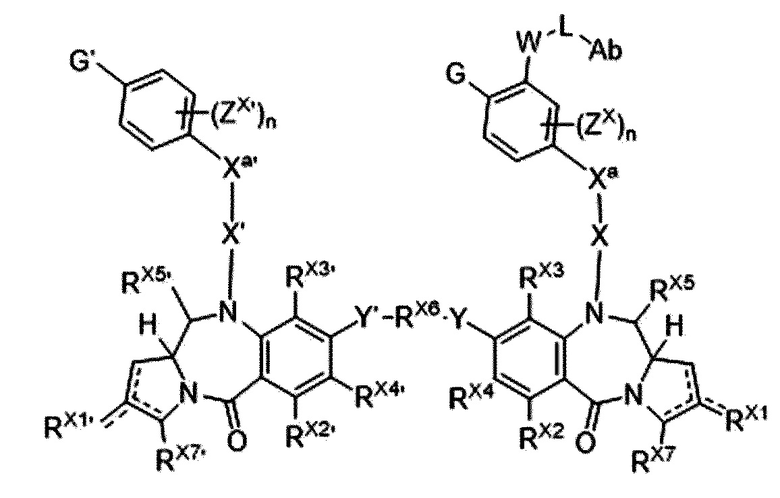
[Общая формула XIII]
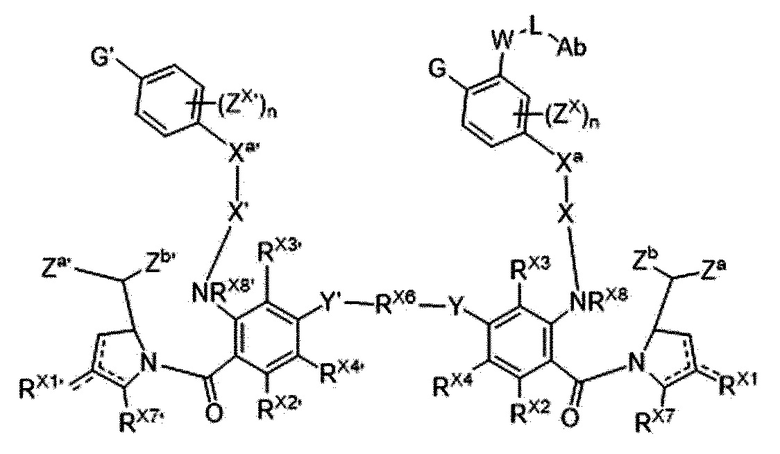
Xa и Xa' независимо выбраны из группы, содержащей связь или C1-6 алкилен;
ZX' и ZX независимо выбраны из водорода, C1-8 алкила, галогена, циано, нитро,  или -(CH2)m-OCH3;
или -(CH2)m-OCH3;
Соответствующие R80, R90 и R100 выбраны из водорода, C1-8 алкила, C2-6 алкенила и C1-6 алкокси, и;
m представляет собой целое число от 0 до 12.
ZX' и ZX независимо представляют собой любое, выбранное из группы, состоящей из водорода, 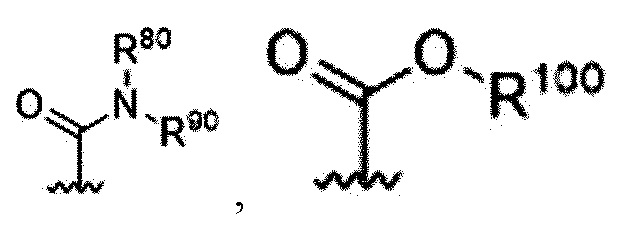 и -(CH2)m-OCH3;
и -(CH2)m-OCH3;
Соответствующие R80, R90 и R100 выбраны из водорода, C1-3 алкила и C1-3 алкокси;
m представляет собой целое число от 1 до 6 и;
активное средство представляет собой любое средство, выбранное из группы, состоящей из:

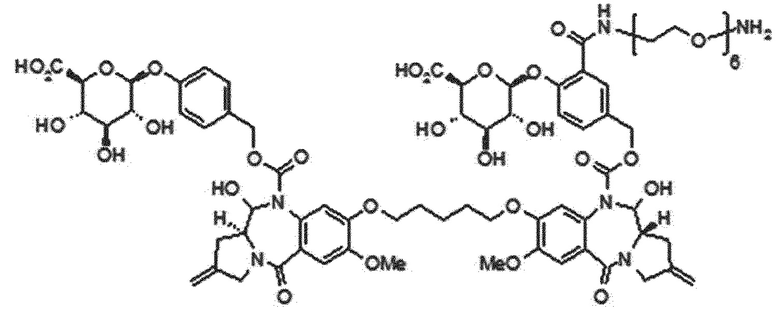
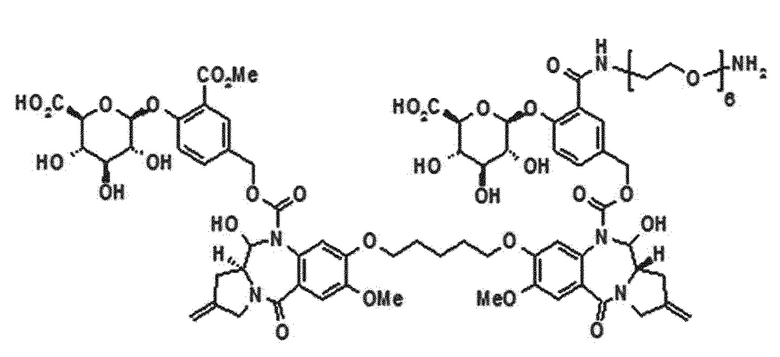

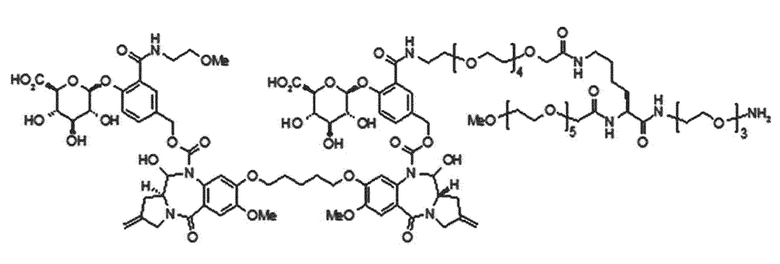
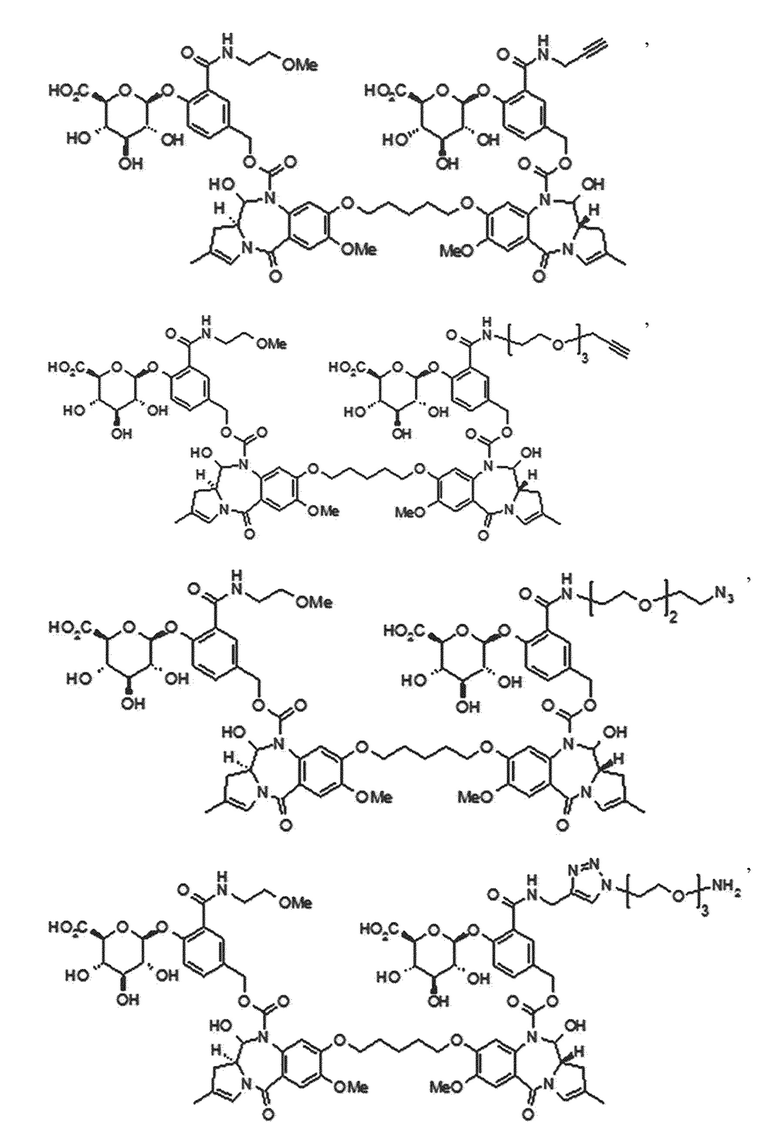
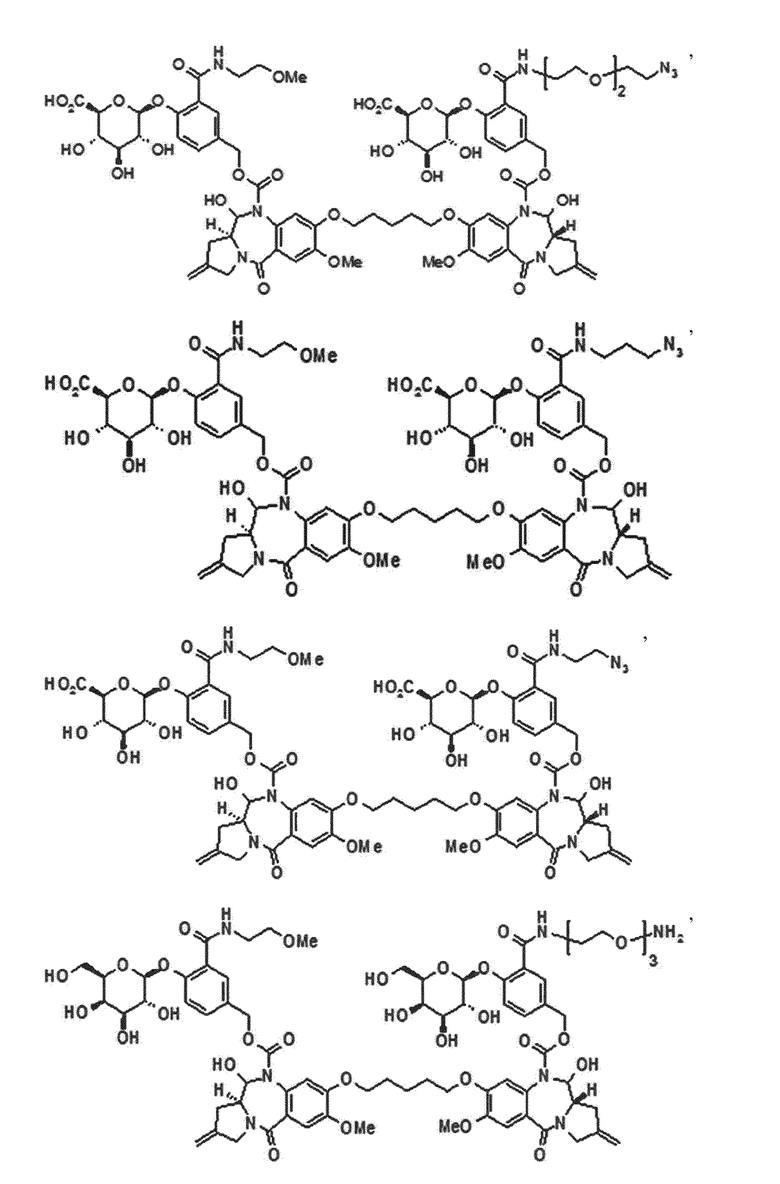
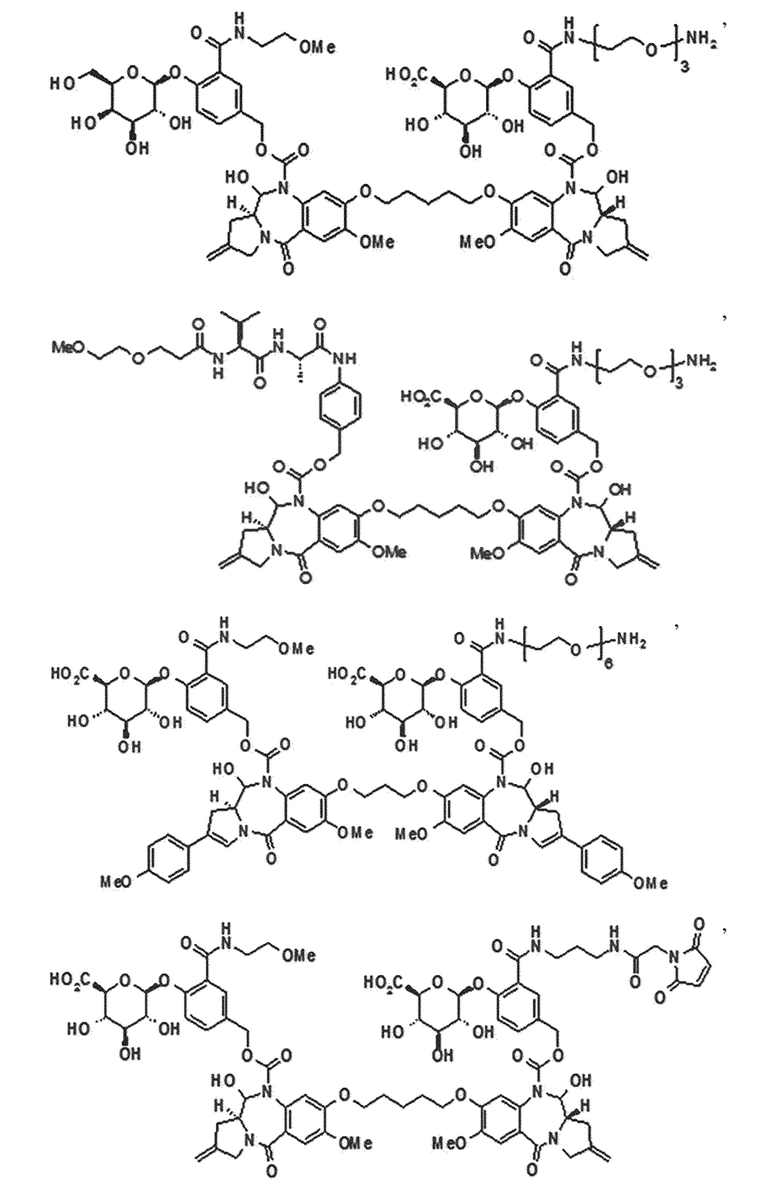
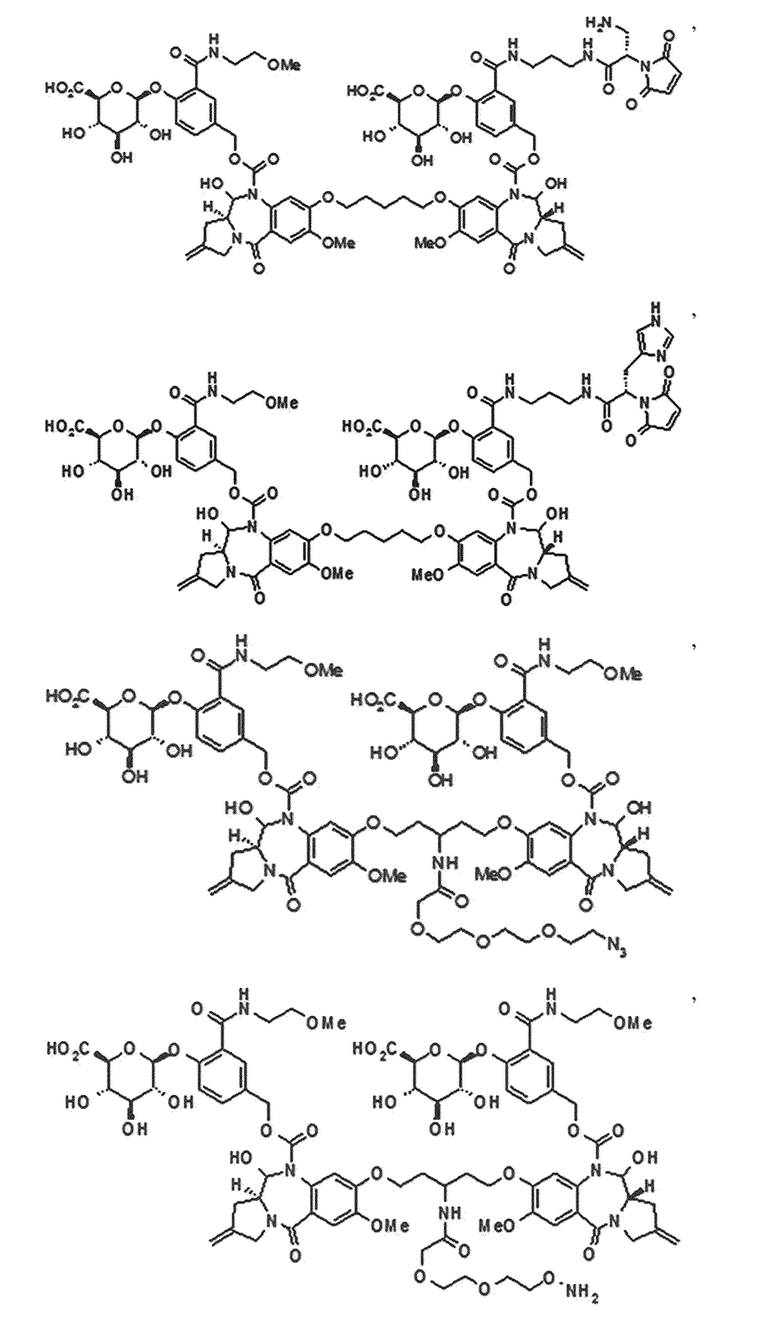
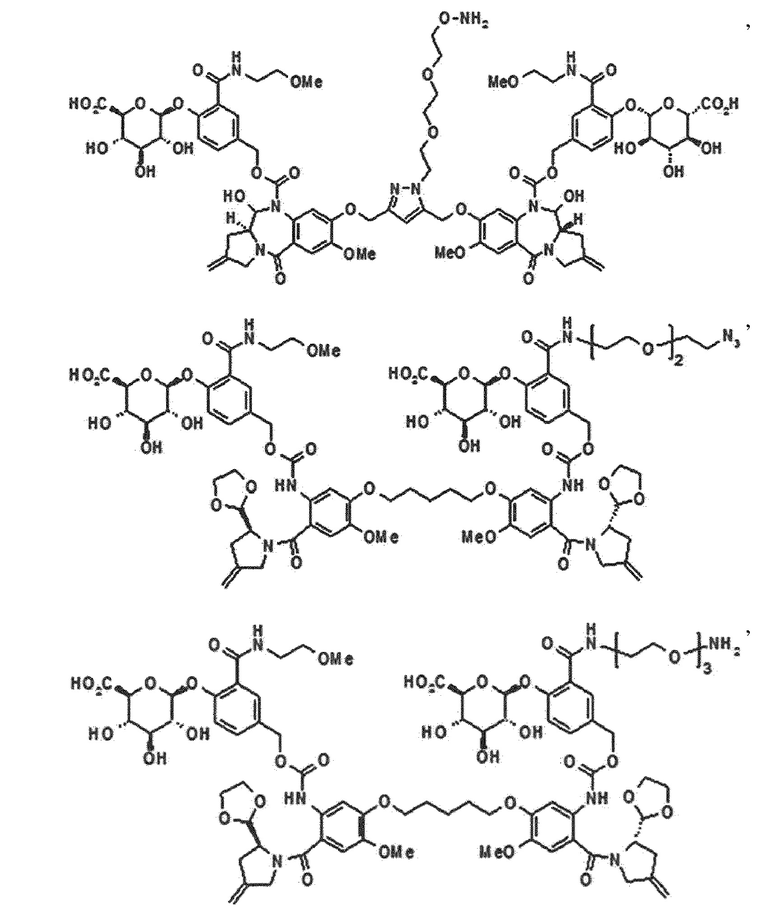
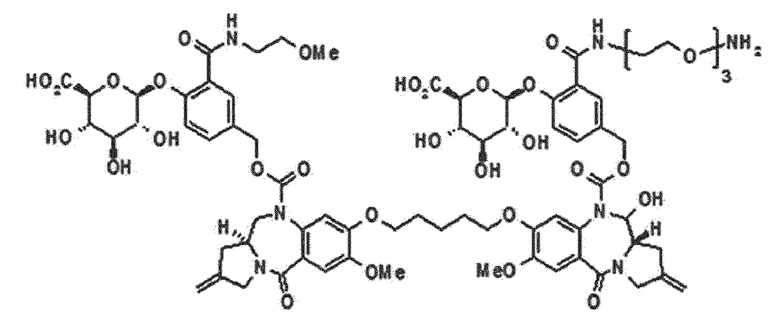 и
и
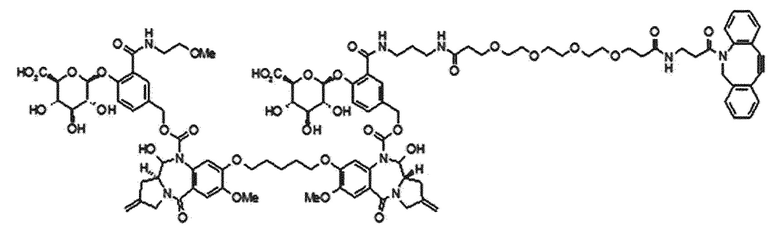
В настоящем описании «конъюгаты» относятся к агентам, связывающим клетки, которые ковалентно связаны с одной или несколькими молекулами цитотоксического соединения. В настоящем описании «связывающий клетку агент» представляет собой молекулу, имеющую сродство к биологической мишени, например, к лиганду, белку, антителу, в частности, моноклональному антителу, белку или фрагменту антитела, и связывающий агент служит для направления биологически активного соединения к биологической мишени. В одном аспекте настоящего изобретения, конъюгат может быть разработан для нацеливания на опухолевые клетки через антигены клеточной поверхности. Антиген может быть антигеном клеточной поверхности, который сверхэкспрессируется или экспрессируется в клетках аномального типа. В частности, антиген-мишень может экспрессироваться только на пролиферативных клетках (например, опухолевых клетках). Антигены-мишени могут быть выбраны на основе различной экспрессии, обычно между пролиферативными и нормальными тканями. В настоящем изобретении лиганд связан с линкером.
В настоящем описании «антитело» относится к молекуле иммуноглобулина, которая через по меньшей мере 1 сайт распознавания антигена, расположенный в вариабельной области молекулы иммуноглобулина, может специфично связываться с мишенью, например углеводом, полинуклеотидом, липидом или полипептидом и тому подобное. Термин «антитело», используемый в настоящем описании, охватывает не только полное моноклональное или поликлональное антитело, но также и заданную антигенсвязывающую область (например, «антигенсвязывающий фрагмент») полного антитела, обладающего способностью связываться со специфичностью к определенному антигену) или его одну цепь, слитый белок, содержащий антитело, или любую другую модифицированную структуру молекулы иммуноглобулина, содержащую сайт распознавания антигена, неограничивающими примерами которых являются: Fab; Fab'; F(ab')2Fd фрагмент; фрагмент Fv; фрагмент однодоменного антитела (dAb); выделенная определяющая комплементарность область (CDR); одноцепочечное (scFv) и однодоменное антитело (например, акулье и верблюжье антитело), максиантитело, миниантитело, интраантитело, диантитело, триантитело, тетраантитело, v-NAR, или бис-scFv (см., например, литература [Hollinger and Hudson, 2005, Nature Biotechnology 23(9): 1126-1136]”.
Антитела содержат любую категорию антител, например IgG, IgA или IgM (или их подкатегории), и антитело не обязательно должно быть определенного типа. В зависимости от аминокислотной последовательности константного домена тяжелой цепи антитела иммуноглобулин может быть отнесен к разным категориям. Существует пять основных типов иммуноглобулинов: IgA, IgD, IgE, IgG и IgM, некоторые из которых могут быть дополнительно разделены на подкатегории (изотипы), например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2. Константные домены тяжелой цепи (HC), соответствующие различным категориям, соответственно обозначаются как альфа, дельта, эпсилон, гамма и мю. Структуры субъединиц и трехмерная конфигурация различных категорий иммуноглобулинов хорошо известны в данной области. Антитело по настоящему изобретению может быть получено с использованием методик, широко известных в смежных областях, например рекомбинантных методик, методов фагового дисплея, методов синтеза, комбинаций вышеупомянутых методов или других методов, хорошо известных в смежных областях.
В настоящем описании «выделенное антитело» относится к антителу, которое по существу не содержит другое антитело, обладающее специфичностью к другому антигену, которое может по существу не содержать другой клеточный материал и/или химические вещества.
В настоящем описании «биологическая мишень» относится к антигену, расположенному на поверхности опухоли, раковой клетки или внеклеточного матрикса.
В настоящем описании «линкер» относится к соединению, которое ковалентно связывает цитотоксическое соединение с лигандом. В одном из аспектов настоящего изобретения линкер, описанный в PCT/US2016/063564 и PCT/US2016/063595, может использоваться в качестве линкера.
В настоящем описании «терапевтическое средство» относится к средству, которое проявляет цитотоксичность, ингибирование пролиферации клеток и/или иммуномодулирующее действие на раковые клетки или активированные иммунные клетки. Примеры терапевтических средств содержат цитотоксические средства, химиотерапевтические средства, ингибиторы пролиферации клеток и иммуномодуляторы.
В настоящем описании «химиотерапевтическое средство» представляет собой химическое соединение, используемое при лечении рака.
В настоящем описании термин «субъект» содержит человека и животных, не относящихся к человеку, в частности, млекопитающих. Примеры субъектов содержат человека, например, с расстройствами, такими как описанные в настоящем документе, например, пациента-человека, страдающего раком, или здоровых субъектов. «Не относящееся к человеку животное» используется для всех позвоночных животных, таких как немлекопитающие (например, куры, амфибии, рептилии) и млекопитающих, таких как приматы, не относящиеся к человеку, домашний скот и/или животные (например, овцы, собаки, кошки, коровы, свиньи и т.п.) и грызуны (например, мыши, крысы, хомяки, морские свинки и т.п.). В некоторых вариантах осуществления субъектом является пациент-человек. В некоторых примерах субъект представляет собой пациента-человека.
В настоящем описании «лечение» относится как к терапевтическому лечению, так и к профилактическим или превентивным мерам. Субъект, нуждающийся в лечении, содержит субъекта, уже имеющего заболевание, и субъекта, восприимчивого к заболеванию, или субъекта, у которого необходимо предотвратить расстройство. Таким образом, при использовании в отношении субъекта, нуждающегося в лечении заболевания или лечении, термин охватывает торможение или замедление прогрессирования заболевания, ремиссию заболевания, предотвращение симптомов, уменьшение тяжести заболевания и/или симптомов, но не ограничивается ими.
В настоящем описании «вводить» или «введение» относится к предоставлению и/или контактированию и/или доставке соединения или соединений любым подходящим путем для достижения желаемого эффекта. Введение может быть пероральным, сублингвальным, парентеральным (например, внутривенным, подкожным, внутрикожным, внутримышечным, внутрисуставным, внутриартериальным, интратекальным, интрастернальным, интраспинальным, ректальным, назальным, буккальным, ректальным, вагинальным, назальным, офтальмологическим, путем ингаляции и имплантации.
В настоящем описании «незамещенная или замещенная» относится к исходной группе, которая может быть незамещенной или замещенной, «замещенная» относится к исходной группе, имеющей по меньшей мере 1 группу заместителя, и группа заместителя относится к химической части, которая ковалентно связана с исходной группой или слита с исходной группой.
В настоящем описании «галоген» относится к фтору, хлору, брому или йоду и т.п.
В настоящем описании «алкил» представляет собой одновалентный фрагмент, полученный удалением атома водорода от атома углерода алифатического или алициклического, насыщенного или ненасыщенного (ненасыщенного, полностью ненасыщенного) углеводородного соединения. Примеры насыщенных алкилов содержат метил, этил, бутил, н-пентил (амил), н-гексил, н-гептил и тому подобное, насыщенные циклические алкильные группы, такие как метил, этил, изопропил, изобутил, втор-бутил, трет-бутил, изопентил и неопентил и тому подобное.
В настоящем изобретении «алкокси» относится к -OR, где R представляет собой алкильную группу, и примеры содержат метокси, этокси, н-пропокси, изопропокси, н-бутокси, втор-бутокси, изобутокси и трет-бутокси и т.п.
В настоящем изобретении «арил» относится к одновалентному фрагменту, полученному удалением атома водорода от атома ароматического кольца ароматического соединения, имеющего кольцевой атом.
В настоящем изобретении «алкенил» представляет собой алкил, имеющий по меньшей мере одну двойную связь углерод-углерод. Примерами ненасыщенных алкенильных групп являются этенил (винил, -CH=CH2), 1-пропенил (-CH=CH-CH3), 2-пропенил, изопропенил, бутенил, пентенил и гексенил и т.п.
В настоящем изобретении «алкинил» представляет собой алкильную группу, имеющую по меньшей мере одну тройную связь углерод-углерод, и примеры ненасыщенной алкинильной группы содержат этинил и 2-пропинил и т.п.
В настоящем изобретении «карбокси» относится к -C(=O)OH.
В настоящем изобретении «формил» относится к -C(=O)H.
В настоящем изобретении «арил» относится к одновалентному фрагменту, полученному удалением атома водорода от атома ароматического кольца ароматического соединения. Например, "C5-7 арил" представляет собой фрагмент, имеющий от 5 до 7 кольцевых атомов, который представляет собой одновалентный фрагмент, полученный удалением атома водорода от атомов ароматического кольца ароматического соединения, а «C5-10 арил» представляет собой фрагмент, имеющий от 5 до 10 кольцевых атомов, который представляет собой одновалентный фрагмент, полученный удалением атома водорода от атомов ароматического кольца ароматического соединения. В настоящем описании префиксы (C5-7, C5-10, и т.п.) относятся к числу атомов в кольце или диапазону числа атомов в кольце, независимо от того, являются ли они атомами углерода или гетероатомами. Например, «C5-6 арил» относится к арильной группе, имеющей 5 или 6 кольцевых атомов. В данном случае атомы кольца могут быть все атомами углерода, как в «карбоарильной группе». Примеры карбоарильной группы содержат, но не ограничиваются ими, группы, полученные из бензола, нафталина, азулена, антрацена, фенантрена, нафтацена и пирена. Примеры арильных групп, которые содержат конденсированное кольцо, в котором по крайней мере одно из них представляет собой ароматическое кольцо, содержат, но не ограничиваются ими, группы, производные от индана, индена, изоиндена, тетралина, аценафтена, флуорена, феналена, ацесфенантрена и азеантрена. Альтернативно, кольцевые атомы могут содержать один или несколько гетероатомов, как в «гетероарильной группе».
В настоящем изобретении «гетероарил» относится к арилу, содержащему один или несколько гетероатомов, таких как пиридин, пиримидин, бензотиофен, фурил, диоксоланил, пирролил, оксазолил, пиридил, пиридазинил, в частности, бензофуран, изобензофуран, индол, изоиндол, индолизин, индолин, изоиндолин, пурин (аденин или гуанин), бензимидазол, индазол, бензоксазол, бензизоксазол, бензодиоксол, бензофуран, бензотриазол, бензотиофуран, бензотиазол, C9, имеющий два конденсированных кольца, полученных из бензотиазола, хромена, изохромена, хромана, ис-хромана, бензодиоксана, хинолина, изохинолина, хинолизина, бензоксазина, бензодиазина, пиридопиридина, хиноксалина, хиназолина, циннолина, фталазина, нафтиридина, C10, имеющий два конденсированных кольца, полученных из птеридина, C11, имеющий два конденсированных кольца, полученных из бензодиазепина, карбазола, дибензофурана, дибензотиофена, карболина, пиримидина, C13, имеющий три конденсированных кольца, полученных из пиридоиндола, акридина, ксантена, тиоксантена, феноксатиина, феназина, феноксазина, фенотиазина, тиантрена, фенантридина, фенантролина, и C14, имеющий три конденсированных кольца, полученных из феназина.
В настоящем изобретении, “циклоалкил” относится к алкильной группе, которая представляет собой циклоалкильную группу, и относится к одновалентному фрагменту, полученному удалением атома водорода от алициклического кольцевого атома циклического углеводородного соединения. Примеры циклоалкильных групп содержат, но не ограничиваются ими, группы, полученные из:
насыщенных углеводородных соединений с одним кольцом: циклопропан, циклобутан, циклопентан, циклогексан, циклогептан, метилциклопропан, диметилциклопропан, метилциклобутан, диметилциклобутан, метилциклопентан, диметилциклопентан и метилциклогексан;
ненасыщенных углеводородных соединений с одним кольцом: циклопропен, циклобутен, циклопентен, циклогексен, метилциклопропен, диметилциклопропен, метилциклобутен, диметилциклобутен, метилциклопентен, диметилциклопентен и метилциклогексен;
и насыщенных гетероциклических углеводородных соединений: норкаран, норфенен и норборнен.
В настоящем изобретении «гетероциклил» относится к одновалентному фрагменту, полученному удалением атома водорода от кольцевого атома гетероциклического соединения.
В настоящем изобретении префиксы (например, C1-12, C3-8, и т.п.) относятся к числу атомов в кольце или диапазону числа атомов в кольце, независимо от того, являются ли они атомами углерода или гетероатомами. Например, термин “C3-6 гетероциклил” используемый в настоящем описании, относится к гетероциклильной группе, имеющей от 3 до 6 кольцевых атомов.
Примеры однокольцевых гетероциклильных групп содержат, но не ограничиваются ими, группы, полученные из:
N1: азиридин, азетидин, пирролидин, пирролин, 2H- или 3H-пиррол, пиперидин, дигидропиридин, тетрагидропиридин, азепин;
N2: имидазолидин, пиразолидин, имидазолин, пиразолин, пиперазин;
O1: оксиран, оксетан, оксолан, оксол, оксан, дигидропиран, пиран, оксепин;
O2: диоксолан, диоксан и диоксепан;
O3: триоксан;
N1O1: тетрагидрооксазол, дигидрооксазол, тетрагидроизоксазол, дигидроизоксазол, морфолин, тетрагидрооксазин, дигидрооксазин,
S1: тииран, тиетан, тиолан, тиан, тайпан;
N1S1: тиазолин, тиазолидин, тиоморфолин;
N2O1: оксадиазин;
O1S1: оксатиол, оксатиан и;
N1O1S1: оксатиазин.
В настоящем изобретении «пролекарство» относится к соединениям, которые в физиологических условиях in vivo (например, ферментативное окисление, восстановление и/или гидролиз) могут под действием фермента или желудочной кислоты прямо или косвенно превращаться в пирролобензодиазепиновое лекарственное средство.
В настоящем изобретении «фармацевтически приемлемая соль» может быть кислотно-аддитивной солью, образованной фармацевтически приемлемой свободной кислотой, где свободная кислота представляет собой органическую кислоту или неорганическую кислоту.
Органические кислоты содержат, но не ограничиваются ими, лимонную кислоту, уксусную кислоту, молочную кислоту, винную кислоту, малеиновую кислоту, фумаровую кислоту, муравьиную кислоту, пропионовую кислоту, щавелевую кислоту, трифторуксусную кислоту, бензойную кислоту, глюконовую кислоту, метансульфоновую кислоту, гликолевую кислоту, янтарную кислоту, 4-толуолсульфоновую кислоту, глутаминовую кислоту и аспарагиновую кислоту. Также неорганические кислоты содержат, но не ограничиваются ими, хлористоводродную кислоту, бромноватую кислоту, серную кислоту и фосфорную кислоту.
Например, если соединение имеет функциональную группу, которая является анионом или может быть анионом (например, -COOH может быть -COO-), подходящий катион может быть использован для образования соли. Примеры подходящих неорганических катионов содержат, но не ограничиваются ими, Na+ и K+, щелочноземельные катионы, такие как Ca2+ и Mg2+, и другие катионы, такие как Al3+, Примеры подходящих органических катионов содержат, но не ограничиваются ими, ион аммония (т.е., NH4+) и замещенные ионы аммония (например, NH3R+, NH2R2+, NHR3+, NR4+).
Некоторые примеры подходящих замещенных ионов аммония являются производными из следующих: этиламин, диэтиламин, дициклогексиламин, триэтиламин, бутиламин, этилендиамин, этаноламин, диэтаноламин, пиперазин, бензиламин, фенилбензиламин, холин, меглумин и трометамин, а также аминокислоты, такие как лизин и аргинин. Примером типичного иона четвертичного аммония является N(CH3)4+.
Если соединение имеет функциональную группу, которая может быть катионом или катионом (например, -NH2 может быть -NH3+), соль может быть образована с подходящим анионом. Примеры подходящих неорганических анионов содержат, но не ограничиваются ими, анионы, полученные из следующих неорганических кислот: хлористоводродная кислота, бромистоводородная кислота, йодистоводородная кислота, серная кислота, серная кислота, азотная кислота, азотистая кислота, фосфорная кислота и фосфористая кислота.
Примеры подходящих органических анионов содержат, но не ограничиваются ими, анионы, полученные из органических кислот, таких как: 2-ацетоксибензойная кислота, уксусная кислота, аскорбиновая кислота, аспарагиновая кислота, бензойная кислота, камфорсульфоновая кислота, коричная кислота, лимонная кислота, но не ограничиваются ими, дисульфоновая кислота, этансульфоновая кислота, фумаровая кислота, глутароновая кислота, глюконовая кислота, глутаминовая кислота, гликолевая кислота, гидроксималеиновая кислота, гидроксинафталинкарбоновой кислотой, изетионовая кислота, молочная кислота, но не ограничиваются ими, яблочная кислота, метансульфоновая кислота, слизистая кислота, олеиновая кислота, щавелевая кислота, пальмитиновая кислота, паминовая кислота, пантотеновая кислота, фенилуксусная кислота, фенилсульфоновая кислота, пропионовая кислота, пировиноградная кислота, салициловая кислота, стеариновая кислота, янтарная кислота, сульфаниловая кислота и винная кислота и т.п. Примеры подходящих мультимерных органических анионов содержат, но не ограничиваются ими, анионы, полученные из следующих мультимерных кислот: дубильная кислота, карбоксиметилцеллюлоза и т.п.
В настоящем изобретении «сольват» относится к молекулярному комплексу между соединением согласно настоящему изобретению и молекулами растворителя, примеры которого содержат, но не ограничиваются ими, воду, изопропанол, этанол, метанол, диметилсульфоксид, этилацетат, уксусную кислоту, этаноламин или соединение согласно настоящему изобретению, связанное с их смешанным растворителем.
Может быть удобно или желательно получать, очищать и/или обрабатывать сольваты, соответствующие активным соединениям. В настоящем описании термин «сольват» используется в его обычном смысле для обозначения растворенных веществ (например, активных соединений и солей активных соединений) и комплексов растворителей. Когда растворителем является вода, сольват можно отнести к гидрату, такому как моногидрат, дигидрат или тригидрат и т.п.
Фармацевтическая композиция по настоящему изобретению может содержать фармацевтически приемлемый носитель. Примеры фармацевтически приемлемого носителя содержат большие макромолекулы, которые медленно метаболизируются, такие как белки, полисахариды, полимолочная кислота, полигликолевая кислота, полимерные аминокислоты, сополимеры аминокислот, липидные агрегаты и т.п. Такие фармацевтически приемлемые носители могут быть надлежащим образом выбраны и использованы специалистом в данной области.
Композиция, содержащая фармацевтически приемлемый носитель, может иметь различные пероральные или парентеральные лекарственные формы. В случае лекарственной формы обычно используется разбавитель или эксципиент, такой как наполнитель, экстендер, связующее, смачивающий агент, разрыхлитель или поверхностно-активное вещество.
Твердые лекарственной формы для перорального введения содержат таблетки, пилюли, порошки, гранулы, капсулы и т.п., которые могут содержать по меньшей мере один эксципиент, такой как крахмал, карбонат кальция, сахароза или лактоза, желатин. В дополнение к простым эксципиентам также могут использоваться смазывающие вещества, такие как стеарат магния, тальк и т.п.
Жидкие препараты для перорального введения содержат суспензии, растворы, эмульсии, сиропы и тому подобное. В дополнение к воде и жидкому парафину, которые обычно используются в качестве простых разбавителей, могут быть включены различные эксципиенты, такие как смачивающие агенты, подсластители, ароматизаторы, консерванты и тому подобное.
Лекарственные формы для парентерального введения содержат стерилизованные водные растворы, неводные растворы, суспензии, эмульсии, лиофилизированные препараты и суппозитории. Примеры неводного растворителя и суспендирующего агента содержат пропиленгликоль, полиэтиленгликоль, растительное масло, такое как оливковое масло, и сложный эфир для инъекций, такой как этилолеат. Примеры основы суппозитория содержат витепсол, макрогол, твин 61, какао бумагу, лаурин, глицерожелатин и тому подобное.
Фармацевтическая композиция может быть в форме таблеток, пилюль, порошков, гранул, капсул, суспензий, растворов, эмульсий, сиропов, стерилизованных водных растворов, неводных растворителей, суспензий, эмульсий, замораженной, она может иметь одну лекарственную форму.
Для внутривенной, внутрикожной или подкожной инъекции активный ингредиент может быть в форме приемлемого водного раствора для парентерального введения, не содержать пирогенов и иметь соответствующий pH, изотоничность и стабильность. Специалист в данной области может получить соответствующий раствор с использованием изотонического носителя, такого как раствор хлорида натрия, раствор Рингера или раствор лактата Рингера, и при необходимости могут быть включены консерванты, стабилизаторы, буферы, антиоксиданты и другие добавки. Твердые лекарственные формы, подходящие для инъекций, также могут быть приготовлены в виде эмульсий или в форме полипептида, инкапсулированного в липосомы.
Используемая в настоящем описании фраза «эффективное количество» или «терапевтически эффективное количество» относится к количеству, необходимому для достижения желаемого терапевтического результата (для дозы, продолжительности и способов введения). Эффективное количество представляет собой, по меньшей мере, минимальное количество активного средства, необходимое для предоставления терапевтического эффекта субъекту, и составляет меньше токсического количества. Например, вводимое количество может находиться в диапазоне от приблизительно 100 нг до приблизительно 100 мг/кг на пациента, более типично от приблизительно 1 мкг/кг до приблизительно 10 мг/кг. В случае, когда активное соединение представляет собой соль, сложный эфир, амид или пролекарство, доза рассчитывается на основе исходного соединения, и, соответственно, фактическая используемая масса также пропорционально увеличивается. Соединение пирролобензодиазепина согласно настоящему изобретению может быть составлено таким образом, чтобы оно содержало от 0,1 до 3000 мг, от 1 мг до 2000 мг или от 10 мг до 1000 мг активного ингредиента на стандартную лекарственную форму, но не ограничивается этим. Активный ингредиент можно вводить так, чтобы пиковая концентрация активного соединения в плазме составляла приблизительно от 0,05 мкМ до 100 мкМ, от 1 мкМ до 50 мкМ или от 5 мкМ до 30 мкМ. Например, необязательно его можно вводить путем внутривенной инъекции раствора от 0,1% масс./об. до 5% масс./об. активного ингредиента в физиологическом растворе.
В фармацевтической композиции концентрация активного соединения определяется скоростью абсорбции, инактивации и выведения лекарственного средства, а также другими факторами, известными не специалистам в данной области. Вводимая доза может варьироваться в зависимости от тяжести симптомов или заболевания. Кроме того, доза и применяемая терапия для конкретного пациента могут быть скорректированы в соответствии с профессиональным суждением старшего врача, с учетом степени симптомов и болезни пациента, потребности в лекарственном средстве, возраста и реактивности на лекарственное средство и тому подобное. Диапазон концентраций, указанный в настоящем изобретении, предназначен только в качестве примера, и способ осуществления заявленной композиции этим не ограничивается. Кроме того, активный ингредиент можно вводить однократно или меньшие дозы можно вводить многократно.
Соединение-пролекарство или соединение пролекарство-линкер, или соединение-конъюгат пролекарство-линкер-лиганд можно использовать для лечения пролиферативных заболеваний, в частности рака. Термин «пролиферативное заболевание» относится к чрезмерному, аномальному, нежелательному или нерегулируемому росту клеток in vitro или in vivo, например, гиперплазия или цитогенез. Неограничивающие примеры пролиферативного заболевания включают новообразование, опухоль, рак, лейкоз, псориаз, заболевание костей, фиброзную дисплазию и фарингеальный артериосклероз. Неограничивающими примерами рака являются рак легких, мелкоклеточная карцинома легких, рак желудочно-кишечного тракта, рак толстой кишки, рак кишечника, рак молочной железы, рак яичников, рак простаты, рак яичек, рак печени, рак почки, рак мочевого пузыря, рак поджелудочной железы, рак головного мозга, саркома, остеосаркома, саркома Капоши и меланома.
Преимущества изобретения
Конъюгат антитело-лекарственное средство согласно настоящему изобретению, содержащий антитело против DLK1, которое специфично связывается с DLK1-экспрессирующими клетками и интернализуется в клетку, обладает преимуществами способности эффективно, селективно и специфично доставлять лекарственное средство, и позволяет лекарственному средству стабильно связываться с антителом, чтобы проявлять предполагаемую цитотоксичность при сохранении стабильности in vivo. В частности, с помощью технологии слияния линкера, содержащего саморасщепляющуюся группу, настоящее изобретение обеспечивает систему лекарственное средство-линкер-лиганд, которая позволяет лекарственному средству и/или токсину стабильно достигать клетки-мишени и эффективно проявлять лекарственный эффект при существенно сниженной токсичности.
Краткое описание фигур
Фиг. 1 представляет собой диаграмму, подтверждающую эффективность ADC согласно настоящему изобретению на животной модели опухоли, полученной от пациента.
Лучший способ(ы) для реализации изобретения
Далее настоящее изобретение описывается более подробно с помощью вариантов осуществления и экспериментальных примеров.
Следующие ниже варианты осуществления и экспериментальные примеры предназначены для помощи в понимании настоящего изобретения и не предназначены для ограничения объема настоящего изобретения.
<Пример 1> Получение соединений 1, 2, 3 и 4
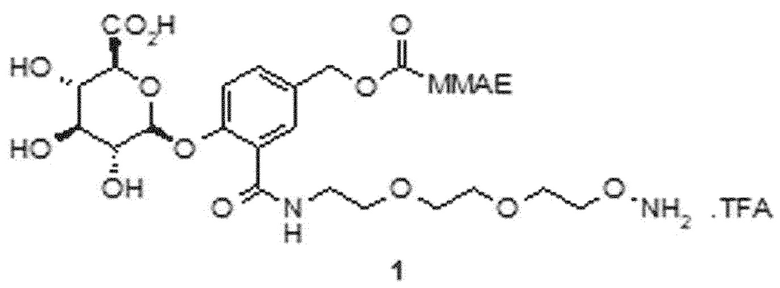

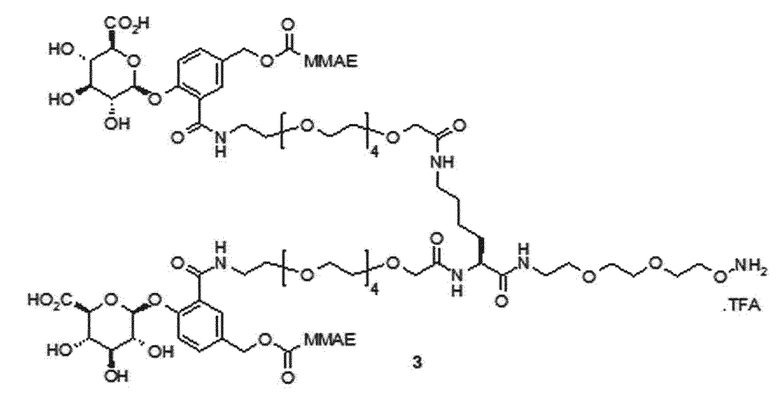

Соединения 1, 2, 3 и 4 получали с использованием способа, описанного в международной патентной публикации WO 2017-089895.
В соединениях 1, 2, 3 и 4 структура MMAE представляет собой следующую.

<Пример 2> Получение соединений 5, 6, 7 и 8


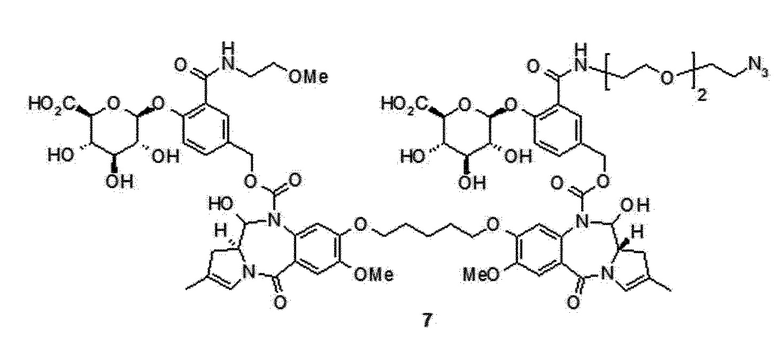
Соединения 5, 6 и 7 получали с использованием способа, описанного в Корейском выложенном патенте No. 10-2018-0110645.

Соединение 8 получали с использованием способа, описанного в Корейской патентной заявке No. 10-2019-0000514.
<Пример 3> Получение ADC
ADC получали с помощью следующих двух стадий, и обычно используемые LCB14-0511 и LCB14-0606 получали с использованием способа, описанного в Корейском выложенном патенте No. 10-2014-0035393. Структурные формулы LCB14-0511 и LCB14-0606 представляют собой следующие:

Стадия 1: Получение пренилированного антитела
Смесь для реакции пренилирования антитела (18A5) получали с использованием способа, описанного в Корейской патентной заявке No. 10-2018-0107639, и подвергали взаимодействию в течение 16 часов при 30°С. Реакционная смесь состояла из 24 мкM антитела (18A5), 200 нM FTase (Calbiochem #344145) и буферного раствора (50 мM Tris-HCl (pH 7,4), 5 мM MgCl2, 10 мкM ZnCl2, 0,144 мM DTT), содержащего 0,144 мM LCB14-0511 или LCB14-0606. После завершения реакции пренилированное антитело обессоливали, используя колонку с сефарозой G25 (система очистки AKTA, GE healthcare), уравновешенную буферным раствором PBS.
Стадия 2: Метод конъюгации лекарств
<Конъюгация путем образования оксимной связи>
Смесь для реакции образования оксимной связи между пренилированным антителом и линкером-лекарственным средством получали путем смешивания 100 мМ Na-ацетатного буферного раствора с pH 5,2, 10% DMSO, 20 мкМ антитела и 200 мкМ линкер-лекарственного средства (собственного получения, соединения 1, 2, 3, 4, 5, 7 и 8 из вариантов осуществления 1 и 2), и слегка перемешивали при 30°C. После взаимодействия в течение 6 или 24 часов проводили процесс FLPC (система очистки AKTA, GE healthcare) для удаления небольших излишков использованных соединений. Белковую фракцию собирали и концентрировали.
<Конъюгация путем клик-реакции>
Смесь для реакции образования оксимной связи между пренилированным антителом и линкером-лекарственным средством представляла собой 10% DMSO, 20 мкМ антитела и 200 мкМ линкер-лекарственное средство (собственного получения, соединение 6 из варианта осуществления 2), 1 мМ пентагидрат сульфата меди(II), 2 мМ (BimC4A)3 (Sigma-Aldrich 696854), 10 мМ аскорбата натрия и 10 мМ аминогуанидин гидрохлорида, подвергали взаимодействию в течение 3 часов при 25°C, затем обрабатывали 2,0 мМ EDTA и подвергали взаимодействию в течение 30 минут. После реакции взаимодействия проводили процесс FLPC (система очистки AKTA, GE healthcare) для удаления небольших излишков использованных соединений. Белковую фракцию собирали и концентрировали.
[Таблица 2] Список полученных ADC
Экспериментальный пример 1: Оценка цитотоксичности in vitro
Измеряли активность ингибирования пролиферации клеток линии раковых клеток лекарственных средств, указанных в таблице 3 ниже, и ADC, полученных в <варианте осуществления 3> выше. Для этой цели использовали коммерчески доступную линию раковых клеток поджелудочной железы человека MIA-PaCa2 (DLK1-отрицательную или нормальную) и клеточную линию со сверхэкспрессией MIA-PaCa-2-DLK1. В качестве лекарственного средства использовали MMAF-OMe в качестве ADC, и использовали ADC из таблицы 2. В 96-луночном планшете в каждую лунку засевали от 4000 до 5000 клеток соответствующих линий раковых клеток для группы 72-часовой обработки, от 2000 до 3000 клеток для группы 96-часовой обработки и от 800 до 1000 клеток для группы 168-часовой обработки. После культивирования в течение 24 часов их обрабатывали лекарственным средством и ADC в концентрации от 0,0015 до 10,0 нМ (серийно разводили в три раза). Спустя 72, 96 и 168 часов, соответственно, количество живых клеток измеряли с использованием красителя SRB (сульфородамин B).
[Таблица 3]

*NT: не проверенный.
Было подтверждено, что большинство комплексов антитело-лекарственное средство обладают существенно улучшенной цитотоксичностью в линиях раковых клеток поджелудочной железы со сверхэкспрессией DLK1, чем в линиях раковых клеток поджелудочной железы без экспрессии DLK1. Было подтверждено, что в линиях раковых клеток поджелудочной железы, сверхэкспрессирующих DLK1, комплексы антитело-лекарство на основе пирролобензодиазепина (ADC 5, 7 и 8) проявляют более сильную цитотоксичность, чем комплексы антитело-лекарство на основе ауристатина (ADC 1, 2, 3 и 4). Кроме того, было подтверждено, что комплексы антитело-лекарственное средство на основе пирролобензодиазепина проявляют более сильную цитотоксичность по сравнению с комплексами антитело-лекарственное средство на основе ауристатина с более длительным временем реакции.
Экспериментальный пример 2: Оценка эффективности in vivo
На животной модели опухоли, полученной от пациента, оценивали эффективность ADC, полученных в <Варианте осуществления 3>. В частности, модель мышей мелкоклеточного рака легкого, полученного от пациентов (модель PDX), была предоставлена компанией Champions Oncology. Контрольной группе модели PDX внутривенно вводили PBS в хвост, в то время как экспериментальным группам вводили ADC4 при 6 мг/кг /Q4D(один раз в 4 дня)*4, 6 мг/кг /QW(раз в неделю)*4 и 9 мг/кг /QW*4 с последующим измерением размера опухоли.
По результатам, как показано на фиг. 1, опухоли исчезли у всех 8 индивидуальных экспериментальных животных в каждой из группы 6 мг/кг /Q4D*4 и группы 9 мг/кг /QW*4 (CR, полная ремиссия), при этом опухоли исчезли у 6 из 8 экспериментальных животных в группе 6 мг/кг /QW*4.
Промышленная применимость
Новые конъюгаты антитело-лекарственное средство (ADC), нацеленные на DLK1, и фармацевтические композиции, содержащие их, могут быть использованы в получении лекарственных средств для лечения и/или профилактики пролиферативных заболеваний и/или ангиогенетических заболеваний, например рака.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> legochembioscience
ybiologics
<120> КОНЬЮГАТЫ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО, ВКЛЮЧАЮЩИЕ АНТИТЕЛО
ПРОТИВ ЧЕЛОВЕЧЕСКОГО DLK1, И ИХ ПРИМЕНЕНИЕ
<130> PCT2020-005
<150> KR 10-2019-0025987
<151> 2019-03-06
<150> KR 10-2020-0027373
<151> 2020-03-04
<160> 128
<170> KoPatentIn 3.0
<210> 1
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 1
Gln Val Gln Leu Val Glu Ser Gly Gly Thr Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser
20 25
<210> 2
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 2
Gly Phe Thr Phe Ser Ser His Ala
1 5
<210> 3
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 3
Met Ser Trp Val Arg Gln Thr Pro Gly Lys Gly Leu Glu Trp Val Ser
1 5 10 15
Ser
<210> 4
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 4
Ile Thr Lys Ser Gly Ser Gly Thr
1 5
<210> 5
<211> 38
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 5
Tyr Ser Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn
1 5 10 15
Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp
20 25 30
Thr Ala Val Tyr Tyr Cys
35
<210> 6
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 6
Thr Arg Glu Gly Leu Gly Tyr Tyr Tyr Gly Met Asp Val
1 5 10
<210> 7
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 7
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
1 5 10
<210> 8
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 8
Gln Leu Val Leu Thr Gln Pro Pro Ser Val Ser Gly Ala Pro Gly Gln
1 5 10 15
Arg Val Ile Ile Ser Cys Thr Gly Ser
20 25
<210> 9
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 9
Ser Ser Asn Ile Gly Ala Gly Tyr Asp
1 5
<210> 10
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 10
Val His Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Arg Leu Leu Ile
1 5 10 15
Tyr
<210> 11
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 11
Gly Ser Thr
1
<210> 12
<211> 36
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 12
Asn Arg Pro Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly
1 5 10 15
Thr Ser Ala Ser Leu Ala Ile Thr Gly Leu Gln Ala Glu Asp Glu Ala
20 25 30
Asp Tyr Tyr Cys
35
<210> 13
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 13
Gln Ser Tyr Asp Asn Ser Leu Ser Ala His Tyr Val
1 5 10
<210> 14
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 14
Phe Gly Thr Gly Thr Lys Val Thr Val Leu
1 5 10
<210> 15
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 15
Gln Val Gln Leu Val Gln Ser Gly Gly Ala Val Val Gln Pro Gly His
1 5 10 15
Ser Leu Arg Leu Ser Cys Glu Ala Ser
20 25
<210> 16
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 16
Gly Phe Lys Phe Lys Asp Tyr Gly
1 5
<210> 17
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 17
Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Leu Ala
1 5 10 15
Val
<210> 18
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 18
Ile Ser His Asp Gly Arg Asn Lys
1 5
<210> 19
<211> 38
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 19
Asn Tyr Ala Asp Ser Val Lys Gly Arg Leu Thr Ile Ser Arg Asp Asn
1 5 10 15
Ser Lys Asn Thr Leu Ser Phe Gln Met Asn Ser Leu Arg Ala Glu Asp
20 25 30
Thr Ala Val Tyr Tyr Cys
35
<210> 20
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 20
Val Arg Asp Trp Ser Tyr Ala Phe Asp Ile
1 5 10
<210> 21
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 21
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
1 5 10
<210> 22
<211> 26
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 22
Asp Ile Gln Met Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Asn Ile Thr Cys Arg Ala Ser
20 25
<210> 23
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 23
Gln Asp Ile Ser Arg Arg
1 5
<210> 24
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 24
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
1 5 10 15
Tyr
<210> 25
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 25
Gly Ala Ala
1
<210> 26
<211> 36
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 26
Ser Leu Gln Ser Ala Val Ala Ser Arg Phe Ser Gly Ser Gly Ser Gly
1 5 10 15
Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
20 25 30
Asn Tyr Tyr Cys
35
<210> 27
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 27
Gln Gln Ile Tyr Thr Thr Pro Leu Thr
1 5
<210> 28
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 28
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
1 5 10
<210> 29
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 29
Gln Met Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser
20 25
<210> 30
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 30
Gly Phe Thr Phe Asp Asp Tyr Ala
1 5
<210> 31
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 31
Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser
1 5 10 15
Gly
<210> 32
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 32
Ile Ser Trp Asn Ser Gly Ser Ile
1 5
<210> 33
<211> 38
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 33
Gly Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn
1 5 10 15
Ala Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp
20 25 30
Thr Ala Val Tyr Tyr Cys
35
<210> 34
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 34
Thr Lys Gly Pro Gly Leu Ala Thr Gly Lys Val Tyr Phe Asn Ser
1 5 10 15
<210> 35
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 35
Trp Gly Gln Gly Thr Gln Val Thr Val Ser Ser
1 5 10
<210> 36
<211> 26
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 36
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser
20 25
<210> 37
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 37
Gln Arg Ile Ser Ser Trp
1 5
<210> 38
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 38
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Arg Ala Pro Lys Leu Leu Ile
1 5 10 15
His
<210> 39
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 39
Ser Ala Ser
1
<210> 40
<211> 36
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 40
Thr Leu His Asn Gly Val Pro Ser Arg Phe Ser Gly Ser Ala Ser Gly
1 5 10 15
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
20 25 30
Ile Tyr Tyr Cys
35
<210> 41
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 41
Gln Gln Gly His Ser Phe Pro Tyr Thr
1 5
<210> 42
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 42
Phe Gly Gln Gly Thr Lys Leu Asp Ile Lys
1 5 10
<210> 43
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 43
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser
20 25
<210> 44
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 44
Gly Phe Thr Phe Ser Ser Tyr Trp
1 5
<210> 45
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 45
Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Val Trp Val Ser
1 5 10 15
Arg
<210> 46
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 46
Ile Ser Pro Asp Gly Ser Ser Thr
1 5
<210> 47
<211> 38
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 47
Thr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn
1 5 10 15
Ala Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp
20 25 30
Thr Ala Val Tyr Tyr Cys
35
<210> 48
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 48
Ala Arg Gly Tyr Ser Pro Lys Tyr Pro Thr Val Gly Leu Asp Val
1 5 10 15
<210> 49
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 49
Trp Gly Gln Gly Thr Thr Ile Thr Val Ser Ser
1 5 10
<210> 50
<211> 26
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 50
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Ser Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser
20 25
<210> 51
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 51
Glu Ser Leu Leu His Ser Asn Gly Asn Thr Tyr
1 5 10
<210> 52
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 52
Leu Thr Trp Leu Gln Gln Arg Pro Gly Gln Pro Pro Arg Leu Leu Ile
1 5 10 15
His
<210> 53
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 53
Lys Ile Ser
1
<210> 54
<211> 36
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 54
Asn Arg Phe Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ala Gly
1 5 10 15
Thr Asp Phe Thr Leu Gln Ile Thr Arg Val Glu Thr Glu Asp Val Gly
20 25 30
Val Tyr Tyr Cys
35
<210> 55
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 55
Val Gln Thr Thr Gln Trp Pro Trp Thr
1 5
<210> 56
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 56
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
1 5 10
<210> 57
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 57
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Arg Val Ser Cys Lys Val Ser
20 25
<210> 58
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 58
Gly Tyr Ser Leu Ser Glu Phe Pro
1 5
<210> 59
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 59
Ile His Trp Val Arg Gln Ala Pro Arg Met Gly Leu Glu Trp Met Gly
1 5 10 15
Gly
<210> 60
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 60
Ser Tyr Pro Glu Asp Gly Glu Thr
1 5
<210> 61
<211> 38
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 61
Leu Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Glu Asp Thr
1 5 10 15
Ser Thr Asp Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp
20 25 30
Thr Ala Val Tyr Tyr Cys
35
<210> 62
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 62
Ala Arg Leu Asn Tyr Phe Glu Ser Thr Asp Tyr Trp Val Asp Ala Phe
1 5 10 15
Asp Ile
<210> 63
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 63
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
1 5 10
<210> 64
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 64
Gln Leu Val Leu Thr Gln Pro Tyr Ser Val Ser Glu Ser Pro Gly Lys
1 5 10 15
Thr Ile Thr Ile Ser Cys Thr Arg Ser
20 25
<210> 65
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 65
Ser Gly Ser Ile Ala Ser Asn Phe
1 5
<210> 66
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 66
Val Gln Trp Tyr Gln Gln Arg Pro Gly Ser Ala Pro Thr Pro Val Ile
1 5 10 15
Tyr
<210> 67
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 67
Glu Asp Asn
1
<210> 68
<211> 38
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 68
Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Ile Asp Ser
1 5 10 15
Ser Ser Asn Ser Ala Ser Leu Thr Ile Ser Gly Val Met Thr Glu Asp
20 25 30
Glu Ala Asp Tyr Tyr Cys
35
<210> 69
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 69
Gln Ser Tyr Asp Ser Gly Ser Ser Trp Val
1 5 10
<210> 70
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 70
Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
1 5 10
<210> 71
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 71
Gln Met Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Thr Leu Ser Cys Asp Ala Thr
20 25
<210> 72
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 72
Gly Phe Asn Phe Gly Ser Tyr Tyr
1 5
<210> 73
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 73
Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Leu Ala
1 5 10 15
His
<210> 74
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 74
Ile Ser Ser Thr Gly Arg Thr Ile
1 5
<210> 75
<211> 38
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 75
Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn
1 5 10 15
Ala Lys Ser Ser Leu Asp Leu Gln Met Asn Ser Leu Arg Ala Glu Asp
20 25 30
Thr Ala Val Tyr Tyr Cys
35
<210> 76
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 76
Ala Arg Asp Gln Gly Tyr Pro Phe Gly Met Asp Val
1 5 10
<210> 77
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 77
Trp Gly His Gly Thr Thr Val Thr Val Ser Ser
1 5 10
<210> 78
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 78
Gln Leu Val Leu Thr Gln Pro Ser Ser Val Ser Gly Ala Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Thr Gly Ser
20 25
<210> 79
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 79
Ser Ser Asn Ile Gly Ala Gly Tyr Asp
1 5
<210> 80
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 80
Val Asp Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu Ile
1 5 10 15
Tyr
<210> 81
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 81
Gly Asn Thr
1
<210> 82
<211> 36
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 82
Asn Arg Pro Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly
1 5 10 15
Thr Ser Ala Ser Leu Ala Ile Thr Gly Leu Gln Ala Glu Asp Asp Ser
20 25 30
Asp Tyr Tyr Cys
35
<210> 83
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 83
Gln Ser Tyr Asp Ser Ser Leu Ser Ala Trp Val
1 5 10
<210> 84
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 84
Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
1 5 10
<210> 85
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 85
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser
20 25
<210> 86
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 86
Gly Phe Thr Phe Ser Ser Tyr Ala
1 5
<210> 87
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 87
Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala
1 5 10 15
Val
<210> 88
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 88
Ile Tyr Ser Gly Gly Ser Thr
1 5
<210> 89
<211> 38
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 89
Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn
1 5 10 15
Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp
20 25 30
Thr Ala Val Tyr Tyr Cys
35
<210> 90
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 90
Ala Arg Glu Gly Ser Tyr Asp Val Met Thr Tyr Thr Arg Ile Gly Gly
1 5 10 15
Tyr Phe Asp Tyr
20
<210> 91
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 91
Trp Gly Gln Gly Ala Leu Val Thr Val Ser Ser
1 5 10
<210> 92
<211> 26
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 92
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser
20 25
<210> 93
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 93
Gln Gly Ile Ser Asp Trp
1 5
<210> 94
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 94
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
1 5 10 15
Tyr
<210> 95
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 95
Ala Ala Ser
1
<210> 96
<211> 36
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 96
Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
1 5 10 15
Thr Glu Phe Ser Leu Thr Ile Ser Asn Leu Gln Pro Glu Asp Phe Ala
20 25 30
Thr Tyr Tyr Cys
35
<210> 97
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 97
Gln Gln Ala Asn Ser Phe Pro Leu Thr
1 5
<210> 98
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 98
Phe Gly Pro Gly Thr Lys Val Glu Ile Lys
1 5 10
<210> 99
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 99
Gln Val Gln Leu Val Glu Ser Gly Gly Thr Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser His
20 25 30
Ala Met Ser Trp Val Arg Gln Thr Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Thr Lys Ser Gly Ser Gly Thr Tyr Ser Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Glu Gly Leu Gly Tyr Tyr Tyr Gly Met Asp Val Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 100
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 100
Gln Leu Val Leu Thr Gln Pro Pro Ser Val Ser Gly Ala Pro Gly Gln
1 5 10 15
Arg Val Ile Ile Ser Cys Thr Gly Ser Ser Ser Asn Ile Gly Ala Gly
20 25 30
Tyr Asp Val His Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Arg Leu
35 40 45
Leu Ile Tyr Gly Ser Thr Asn Arg Pro Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Thr Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gln Ser Tyr Asp Asn Ser
85 90 95
Leu Ser Ala His Tyr Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 101
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 101
Gln Val Gln Leu Val Gln Ser Gly Gly Ala Val Val Gln Pro Gly His
1 5 10 15
Ser Leu Arg Leu Ser Cys Glu Ala Ser Gly Phe Lys Phe Lys Asp Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Ala Val Ile Ser His Asp Gly Arg Asn Lys Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Leu Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Ser
65 70 75 80
Phe Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Arg Asp Trp Ser Tyr Ala Phe Asp Ile Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 102
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 102
Asp Ile Gln Met Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Asn Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser Arg Arg
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Gly Ala Ala Ser Leu Gln Ser Ala Val Ala Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Asn Tyr Tyr Cys Gln Gln Ile Tyr Thr Thr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 103
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 103
Gln Met Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Asn Ser Gly Ser Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Lys Gly Pro Gly Leu Ala Thr Gly Lys Val Tyr Phe Asn Ser Trp
100 105 110
Gly Gln Gly Thr Gln Val Thr Val Ser Ser
115 120
<210> 104
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 104
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Arg Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Arg Ala Pro Lys Leu Leu Ile
35 40 45
His Ser Ala Ser Thr Leu His Asn Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Ala Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Ile Tyr Tyr Cys Gln Gln Gly His Ser Phe Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Asp Ile Lys
100 105
<210> 105
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 105
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Val Trp Val
35 40 45
Ser Arg Ile Ser Pro Asp Gly Ser Ser Thr Thr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Tyr Ser Pro Lys Tyr Pro Thr Val Gly Leu Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Ile Thr Val Ser Ser
115 120
<210> 106
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 106
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Ser Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Glu Ser Leu Leu His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu Thr Trp Leu Gln Gln Arg Pro Gly Gln Pro
35 40 45
Pro Arg Leu Leu Ile His Lys Ile Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ala Gly Thr Asp Phe Thr Leu Gln Ile
65 70 75 80
Thr Arg Val Glu Thr Glu Asp Val Gly Val Tyr Tyr Cys Val Gln Thr
85 90 95
Thr Gln Trp Pro Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 107
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 107
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Arg Val Ser Cys Lys Val Ser Gly Tyr Ser Leu Ser Glu Phe
20 25 30
Pro Ile His Trp Val Arg Gln Ala Pro Arg Met Gly Leu Glu Trp Met
35 40 45
Gly Gly Ser Tyr Pro Glu Asp Gly Glu Thr Leu Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Glu Asp Thr Ser Thr Asp Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Leu Asn Tyr Phe Glu Ser Thr Asp Tyr Trp Val Asp Ala Phe
100 105 110
Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 108
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 108
Gln Leu Val Leu Thr Gln Pro Tyr Ser Val Ser Glu Ser Pro Gly Lys
1 5 10 15
Thr Ile Thr Ile Ser Cys Thr Arg Ser Ser Gly Ser Ile Ala Ser Asn
20 25 30
Phe Val Gln Trp Tyr Gln Gln Arg Pro Gly Ser Ala Pro Thr Pro Val
35 40 45
Ile Tyr Glu Asp Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Ile Asp Ser Ser Ser Asn Ser Ala Ser Leu Thr Ile Ser Gly
65 70 75 80
Val Met Thr Glu Asp Glu Ala Asp Tyr Tyr Cys Gln Ser Tyr Asp Ser
85 90 95
Ser Ser Ser Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 109
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 109
Gln Met Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Thr Leu Ser Cys Asp Ala Thr Gly Phe Asn Phe Gly Ser Tyr
20 25 30
Tyr Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Ala His Ile Ser Ser Thr Gly Arg Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Ser Ser Leu Asp
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gln Gly Tyr Pro Phe Gly Met Asp Val Trp Gly His Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 110
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 110
Gln Leu Val Leu Thr Gln Pro Ser Ser Val Ser Gly Ala Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Thr Gly Ser Ser Ser Asn Ile Gly Ala Gly
20 25 30
Tyr Asp Val Asp Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu
35 40 45
Leu Ile Tyr Gly Asn Thr Asn Arg Pro Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Thr Gly Leu
65 70 75 80
Gln Ala Glu Asp Asp Ser Asp Tyr Tyr Cys Gln Ser Tyr Asp Ser Ser
85 90 95
Leu Ser Ala Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 111
<211> 126
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 111
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Tyr Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Glu Gly Ser Tyr Asp Val Met Thr Tyr Thr Arg Ile Gly Gly Tyr
100 105 110
Phe Asp Tyr Trp Gly Gln Gly Ala Leu Val Thr Val Ser Ser
115 120 125
<210> 112
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 112
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Asp Trp
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ser Leu Thr Ile Ser Asn Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn Ser Phe Pro Leu
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Glu Ile Lys
100 105
<210> 113
<211> 38
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 113
agggggccgt gggggccgct gaatgcttcc cggcctgc 38
<210> 114
<211> 40
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 114
tagcggccga cgcggccaac tggccctcgg tgaggagagg 40
<210> 115
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 115
Gln Gly Ile Ser Ser Ala
1 5
<210> 116
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 116
Gln Gln Ser Tyr Thr Thr Pro Leu Thr
1 5
<210> 117
<211> 26
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 117
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser
20 25
<210> 118
<211> 36
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 118
Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
1 5 10 15
Thr Asp Phe Thr Leu Thr Ile Asn Ser Leu Gln Pro Glu Asp Phe Ala
20 25 30
Thr Tyr Tyr Cys
35
<210> 119
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 119
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Val Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser
20 25
<210> 120
<211> 26
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 120
Asp Ile Gln Met Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser
20 25
<210> 121
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 121
His Asp Ile Ser Ser Ser
1 5
<210> 122
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 122
Leu Ala Trp Tyr Gln Gln Lys Ser Gly Lys Ala Pro Lys Leu Leu Ile
1 5 10 15
Tyr
<210> 123
<211> 36
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 123
Asn Leu Lys Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
1 5 10 15
Thr Asp Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
20 25 30
Thr Tyr Tyr Cys
35
<210> 124
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 124
Gln Gln Ser Tyr Thr Thr Val Leu Thr
1 5
<210> 125
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 125
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
1 5 10
<210> 126
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 126
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Ala
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Thr Thr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 127
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 127
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Val Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Lys Phe Lys Asp Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Ala Val Ile Ser His Asp Gly Arg Asn Lys Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Leu Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Ser
65 70 75 80
Phe Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Arg Asp Trp Ser Tyr Ala Phe Asp Ile Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 128
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусственная последовательность
<400> 128
Asp Ile Gln Met Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser His Asp Ile Ser Ser Ser
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Ser Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Leu Lys Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Ser Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Thr Thr Val Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| СЛИТЫЙ БЕЛОК, ВКЛЮЧАЮЩИЙ IL-12 И АНТИТЕЛО ПРОТИВ FAP, И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2831612C1 |
| АНТИ-LILRB1 АНТИТЕЛО И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2801535C1 |
| АНТИТЕЛА ПРОТИВ БЕЛКА-1 ЗАПРОГРАММИРОВАННОЙ КЛЕТОЧНОЙ СМЕРТИ (PD-1) И ИХ ПРИМЕНЕНИЕ | 2017 |
|
RU2725950C1 |
| ПОЛИПЕПТИД, СПЕЦИФИЧНЫЙ К МУЦИНУ-1, И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2805840C1 |
| БИСПЕЦИФИЧЕСКОЕ АНТИТЕЛО АНТИ-EGFR/АНТИ-4-1ВВ И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2831836C2 |
| НОВОЕ АНТИ-С-МЕТ АНТИТЕЛО И ЕГО ПРИМЕНЕНИЕ | 2018 |
|
RU2751720C2 |
| Антитела против TIGIT и их применение | 2019 |
|
RU2750705C1 |
| СЛИТЫЙ БЕЛОК GDF15 ДЛИТЕЛЬНОГО ДЕЙСТВИЯ И СОДЕРЖАЩАЯ ЕГО ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2020 |
|
RU2836280C1 |
| СЛИТЫЕ С FGF21 БЕЛКИ ДЛИТЕЛЬНОГО ДЕЙСТВИЯ И СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2016 |
|
RU2741087C2 |
| АНТИ-CEACAM1 АНТИТЕЛО И ЕГО ПРИМЕНЕНИЕ | 2018 |
|
RU2754876C2 |

Изобретение относится к новым конъюгатам антитело-лекарственное средство (ADC), содержащим антитело, связывающееся с DLK1, или его антигенсвязывающий фрагмент, и фармацевтической композиции, содержащей указанные конъюгаты, для профилактики или лечения рака, ассоциированного с экспрессией DLK1. 2 н. и 57 з.п. ф-лы, 1 ил., 3 табл., 3 пр.
1. Конъюгат антитела, представленный общей формулой I
[Общая формула I] Ab - (X)y,
где Ab представляет собой антитело или антигенсвязывающий фрагмент, которые специфически связываются с DLK1, где Ab содержит определяющую комплементарность область 1 вариабельной области тяжелой цепи (CDRH1), определяющую комплементарность область 2 вариабельной области тяжелой цепи (CDRH2), определяющую комплементарность область 3 вариабельной области тяжелой цепи (CDRH3), определяющую комплементарность область 1 вариабельной области легкой цепи (CDRL1), определяющую комплементарность область 2 вариабельной области легкой цепи (CDRL2) и определяющую комплементарность область 3 вариабельной области легкой цепи (CDRL3); где
(a) (i) CDRH1 содержит аминокислотную последовательность SEQ ID NO: 16;
(ii) CDRH2 содержит аминокислотную последовательность SEQ ID NO: 18;
(iii) CDRH3 содержит аминокислотную последовательность SEQ ID NO: 20;
(iv) CDRL1 содержит аминокислотную последовательность SEQ ID NO: 23;
(v) CDRL2 содержит аминокислотную последовательность SEQ ID NO: 25; и
(vi) CDRL3 содержит аминокислотную последовательность SEQ ID NO: 27;
(b) (i) CDRH1 содержит аминокислотную последовательность SEQ ID NO: 2;
(ii) CDRH2 содержит аминокислотную последовательность SEQ ID NO: 4;
(iii) CDRH3 содержит аминокислотную последовательность SEQ ID NO: 6;
(iv) CDRL1 содержит аминокислотную последовательность SEQ ID NO: 9;
(v) CDRL2 содержит аминокислотную последовательность SEQ ID NO: 11; и
(vi) CDRL3 содержит аминокислотную последовательность SEQ ID NO: 13;
(c) (i) CDRH1 содержит аминокислотную последовательность SEQ ID NO: 30;
(ii) CDRH2 содержит аминокислотную последовательность SEQ ID NO: 32;
(iii) CDRH3 содержит аминокислотную последовательность SEQ ID NO: 34;
(iv) CDRL1 содержит аминокислотную последовательность SEQ ID NO: 37;
(v) CDRL2 содержит аминокислотную последовательность SEQ ID NO: 39; и
(vi) CDRL3 содержит аминокислотную последовательность SEQ ID NO: 41;
(d) (i) CDRH1 содержит аминокислотную последовательность SEQ ID NO: 44;
(ii) CDRH2 содержит аминокислотную последовательность SEQ ID NO: 46;
(iii) CDRH3 содержит аминокислотную последовательность SEQ ID NO: 48;
(iv) CDRL1 содержит аминокислотную последовательность SEQ ID NO: 51;
(v) CDRL2 содержит аминокислотную последовательность SEQ ID NO: 53; и
(vi) CDRL3 содержит аминокислотную последовательность SEQ ID NO: 55;
(e) (i) CDRH1 содержит аминокислотную последовательность SEQ ID NO: 58;
(ii) CDRH2 содержит аминокислотную последовательность SEQ ID NO: 60;
(iii) CDRH3 содержит аминокислотную последовательность SEQ ID NO: 62;
(iv) CDRL1 содержит аминокислотную последовательность SEQ ID NO: 65;
(v) CDRL2 содержит аминокислотную последовательность SEQ ID NO: 67; и
(vi) CDRL3 содержит аминокислотную последовательность SEQ ID NO: 69;
(f) (i) CDRH1 содержит аминокислотную последовательность SEQ ID NO: 72;
(ii) CDRH2 содержит аминокислотную последовательность SEQ ID NO: 74;
(iii) CDRH3 содержит аминокислотную последовательность SEQ ID NO: 76;
(iv) CDRL1 содержит аминокислотную последовательность SEQ ID NO: 79;
(v) CDRL2 содержит аминокислотную последовательность SEQ ID NO: 81; и
(vi) CDRL3 содержит аминокислотную последовательность SEQ ID NO: 83;
(g) (i) CDRH1 содержит аминокислотную последовательность SEQ ID NO: 86;
(ii) CDRH2 содержит аминокислотную последовательность SEQ ID NO: 88;
(iii) CDRH3 содержит аминокислотную последовательность SEQ ID NO: 90;
(iv) CDRL1 содержит аминокислотную последовательность SEQ ID NO: 93;
(v) CDRL2 содержит аминокислотную последовательность SEQ ID NO: 95; и
(vi) CDRL3 содержит аминокислотную последовательность SEQ ID NO: 97;
(h) (i) CDRH1 содержит аминокислотную последовательность SEQ ID NO: 16;
(ii) CDRH2 содержит аминокислотную последовательность SEQ ID NO: 18;
(iii) CDRH3 содержит аминокислотную последовательность SEQ ID NO: 20;
(iv) CDRL1 содержит аминокислотную последовательность SEQ ID NO: 115;
(v) CDRL2 содержит аминокислотную последовательность SEQ ID NO: 95; и
(vi) CDRL3 содержит аминокислотную последовательность SEQ ID NO: 116; или
(i) (i) CDRH1 содержит аминокислотную последовательность SEQ ID NO: 16;
(ii) CDRH2 содержит аминокислотную последовательность SEQ ID NO: 18;
(iii) CDRH3 содержит аминокислотную последовательность SEQ ID NO: 20;
(iv) CDRL1 содержит аминокислотную последовательность SEQ ID NO: 121;
(v) CDRL2 содержит аминокислотную последовательность SEQ ID NO: 39; и
(vi) CDRL3 содержит аминокислотную последовательность SEQ ID NO: 124;
каждый X независимо представляет собой химический фрагмент, содержащий по меньшей мере одно активное средство и линкер, где линкер связывает антитело с по меньшей мере одним активным средством, и
y представляет собой от 1 до 20, где активное средство представляет собой химиотерапевтическое средство, токсин, иммунорегуляторное соединение, противораковое средство, противовирусное средство, антибактериальное средство, противогрибковое средство или противопаразитарное средство.
2. Конъюгат антитела по п. 1, где антитело или его антигенсвязывающий фрагмент содержат:
по меньшей мере одну FR1 тяжелой цепи, содержащую последовательность, выбранную из SEQ ID NO: 1, 15, 29, 43, 57, 71, 85 и 119;
по меньшей мере одну FR2 тяжелой цепи, содержащую последовательность, выбранную из SEQ ID NO: 3, 17, 31, 45, 59, 73 и 87;
по меньшей мере одну FR3 тяжелой цепи, содержащую последовательность, выбранную из SEQ ID NO: 5, 19, 33, 47, 61, 75 и 89;
по меньшей мере одну FR4 тяжелой цепи, содержащую последовательность, выбранную из SEQ ID NO: 7, 21, 35, 49, 63, 77 и 91;
по меньшей мере одну FR1 легкой цепи, содержащую последовательность, выбранную из SEQ ID NO: 8, 22, 36, 50, 64, 78, 92, 117 и 120;
по меньшей мере одну FR2 легкой цепи, содержащую последовательность, выбранную из SEQ ID NO: 10, 24, 38, 52, 66, 80, 94 и 122;
по меньшей мере одну FR3 легкой цепи, содержащую последовательность, выбранную из SEQ ID NO: 12, 26, 40, 54, 68, 82, 96, 118 и 123; и
по меньшей мере одну FR4 легкой цепи, содержащую последовательность, выбранную из SEQ ID NO: 14, 28, 42, 56, 70, 84, 98 и 125.
3. Конъюгат антитела по п. 1, отличающийся тем, что антитело или антигенсвязывающий фрагмент содержат вариабельную область тяжелой цепи, содержащую последовательность, которая имеет по меньшей мере 90% идентичности последовательности с последовательностью, выбранной из SEQ ID NO: 99, 101, 103, 105, 107, 109, 111 и 127.
4. Конъюгат антитела по п. 1, отличающийся тем, что антитело или его антигенсвязывающий фрагмент содержат вариабельную область легкой цепи, содержащую последовательность, которая имеет по меньшей мере 90% идентичности последовательности с последовательностью, выбранной из группы, содержащей SEQ ID NO: 100, 102, 104, 106, 108, 110, 112, 126 и 128.
5. Конъюгат антитела по п. 1, отличающийся тем, что по меньшей мере X имеет структуру, представленную общей формулой II
[Общая формула II]

где G представляет собой фрагмент глюкуроновой кислоты или 
R3 представляет собой водород или карбоксилзащитную группу;
каждый R4 независимо представляют собой водород или гидроксилзащитную группу;
B представляет собой активное средство;
R1 и R2 каждый независимо представляют собой водород, (C1-C8) алкил или (C3-C8) циклоалкил;
W представляет собой -C(O)-, -C(O)NR'-, -C(O)O-, -SO2NR'-, -P(O)R''NR'-, -SONR'- или -PO2NR’-, где C, S или P непосредственно связаны с фенильным кольцом; R’ и R’’ каждый независимо представляют собой водород, (C1-C8) алкил, (C3-C8) циклоалкил, (C1-C8) алкокси, (C1-C8) алкилтио, моно- или ди-(C1-C8) алкиламино, (C3-C20) гетероарил или (C6-C20) арил;
каждый Z представляет собой, независимо, (C1-C8) алкил, галоген, циано или нитро;
n представляет собой от 1 до 3;
L содержит:
A) C1-C50 алкилен или гетероалкилен с 1-50 атомами и удовлетворяет по меньшей мере одному из следующих условий:
(i) L содержит по меньшей мере одну ненасыщенную связь;
(ii) 2 атома в L замещены двухвалентным заместителем так же, как и в заместителе, который завершает гетероарилен;
(iii) L представляет собой гетероалкилен с 1-50 атомами; и
(iv) алкилен замещен по меньшей мере одним C1-20 алкилом;
B) по меньшей мере одну изопренильную группу, представленную общей формулой III
[Общая формула III]

6. Конъюгат антитела по п. 5, отличающийся тем, что L представляет собой азотсодержащий гетероалкилен с 1-50 атомами,
линкер, содержащий по меньшей мере 2 атома гидрофильной аминокислоты; и азот образует пептидную связь с карбонилом гидрофильной аминокислоты, выбранной из аргинина, аспартата, аспарагина, глутамата, глутамина, гистидина, лизина, орнитина, пролина, серина или треонина.
7. Конъюгат антитела по п. 5, отличающийся тем, что W представляет собой -C(O)NR’- и азот в W представляет собой атом азота гидрофильной аминокислоты, выбранной из аргинина, аспартата, аспарагина, глутамата, глутамина, гистидина, лизина, орнитина, пролина, серина или треонина.
8. Конъюгат антитела по п. 6 или 7, отличающийся тем, что аминокислота ковалентно связывает оксим линкера с полиэтиленгликолевым звеном линкера.
9. Конъюгат антитела по п. 6 или 7, отличающийся тем, что гидрофильная аминокислота представляет собой аминокислоту, выбранную из аспартата, глутамата, орнитина, лизина и аргинина, содержащую боковую цепь, имеющую фрагмент, представляющий заряд при нейтральном pH в водном растворе.
10. Конъюгат антитела по п. 5, отличающийся тем, что линкер содержит пептид, содержащий от 2 до 20 аминокислот, выбранных из аланина, аспартата, аспарагина, глутамата, глутамина, глицина, лизина, орнитина, пролина, серина и треонина, и содержащий по меньшей мере одну гидрофильную аминокислоту, выбранную из аспартата, глутамата, орнитина, лизина и аргинина, содержащую боковую цепь, имеющую фрагмент, который проявляет заряд при нейтральном pH в водном растворе.
11. Конъюгат антитела по п. 10, отличающийся тем, что W представляет собой -C(O)NR’- и азот в W представляет собой атом азота N-концевой аминокислоты пептида.
12. Конъюгат антитела по п. 5, отличающийся тем, что пептид ковалентно связывает оксим линкера с полиэтиленгликолевым звеном линкера.
13. Конъюгат антитела по п. 5, отличающийся тем, что L ковалентно связан с антителом тиоэфирной связью, которая содержит атом серы цистеина антитела.
14. Конъюгат антитела по п. 13, отличающийся тем, что антитело содержит аминокислоту, которая может распознаваться изопреноидтрансферазой на С-конце антитела, и тиоэфирная связь содержит атом серы цистеина антитела.
15. Конъюгат антитела п. 14, отличающийся тем, что аминокислотный мотив представляет собой последовательность CYYX;
C представляет собой цистеин;
Y представляет собой алифатическую аминокислоту, выбранную из аланина, изолейцина, лейцина, метионина и валина;
X представляет собой любой, выбранный из глутамина, глутамата, серина, цистеина, метионина, аланина и лейцина; и
тиоэфирная связь содержит атом серы цистеина аминокислотного мотива.
16. Конъюгат антитела по п. 15, отличающийся тем, что аминокислотный мотив представляет собой последовательность CVIM или CVLL.
17. Конъюгат антитела по любому из пп. 14-16, отличающийся тем, что по меньшей мере одна из 1-10 аминокислот, предшествующих аминокислотному мотиву, выбрана из глицина, пролина, аспарагиновой кислоты, аргинина и серина.
18. Конъюгат антитела по п. 17, отличающийся тем, что от 1 до 10 аминокислот, предшествующих аминокислотному мотиву, представляют собой соответственно глицин.
19. Конъюгат антитела по п. 5, отличающийся тем, что L содержит аминопоследовательность GGGGGGGCVIM на С-конце.
20. Конъюгат антитела по п. 5, отличающийся тем, что L содержит по меньшей мере одно звено производного изопренила общей формулы III, которое может распознаваться изопреноидтрансферазой:
[Общая формула III]

21. Конъюгат антитела по п. 5, отличающийся тем, что L представляет собой 3-50 гетероалкилен, содержащий оксим, атом кислорода оксима находится на стороне L, связанной с W, и атом углерода оксима находится на стороне L, связанной с Ab, или атом углерода оксима находится на стороне L, связанной с W, и атом кислорода оксима находится на стороне L, связанной с Ab.
22. Конъюгат антитела по п. 20 или 21, отличающийся тем, что L содержит оксим и по меньшей мере одно изопренильное звено ковалентно связывает оксим с Ab.
23. Конъюгат антитела по п. 5, отличающийся тем, что L содержит  или
или 
24. Конъюгат антитела по п. 5, отличающийся тем, что L дополнительно содержит связывающее звено, представленное общей формулой VIII или общей формулой IX:
[Общая формула VIII]
-(CH2)r(V(CH2)p)q-,
[Общая формула IX]
-(CH2CH2X)w-,
где V представляет собой одинарную связь, -O-, -S-, -NR21-, -C(O)NR22-, NR23C(O)-, NR24SO2- или -SO2NR25-;
X представляет собой -O-, C1-C8 алкилен или -NR21-;
R21 - R25 каждый независимо представляют собой водород, (C1-C6) алкил, (C1-C6) алкил (C6-C20) арил или (C1-C6) алкил (C3-C20) гетероарил;
r представляет собой от 0 до 10;
p представляет собой от 0 до 10;
q представляет собой от 1 до 20; и
w представляет собой от 1 до 20.
25. Конъюгат антитела по п. 24, отличающийся тем, что L содержит от 1 до 20 полиэтиленгликолевых звеньев, представленных 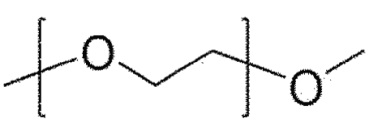 или
или 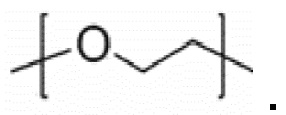
26. Конъюгат антитела по п. 25, отличающийся тем, что L содержит от 1 до 12 групп -OCH2CH2-.
27. Конъюгат антитела по п. 25, отличающийся тем, что L содержит оксим и 1-20 полиэтиленгликолевых звеньев ковалентно связывают оксим с активным средством.
28. Конъюгат антитела п. 5, отличающийся тем, что L дополнительно содержит связывающее звено, образованное реакцией 1,3-диполярного циклоприсоединения, реакцией гетеро-дилса, реакцией нуклеофильного замещения, реакцией карбонила неальдольного типа, присоединением к кратным углерод-углеродным связям, реакцией окисления или клик-реакцией.
29. Конъюгат антитела по п.28, отличающийся тем, что связывающее звено образовано взаимодействием между ацетиленом и азидом или взаимодействием между альдегидом или кетонной группой и гидразином или алкоксиамином.
30. Конъюгат антитела по п. 5, отличающийся тем, что L дополнительно содержит связывающие звенья, представленные общими формулами IV, V, VI или VII:
[Общая формула IV]
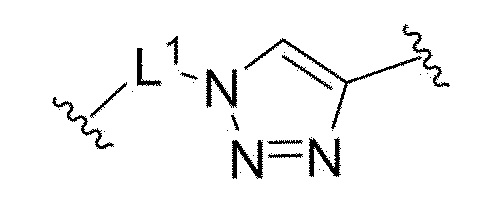 ,
,
[Общая формула V]
 ,
,
[Общая формула VI]
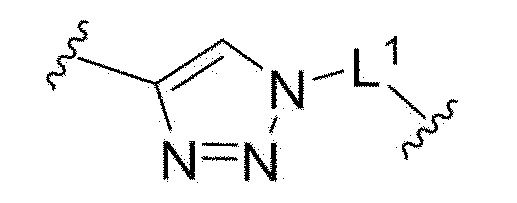 ,
,
[Общая формула VII]
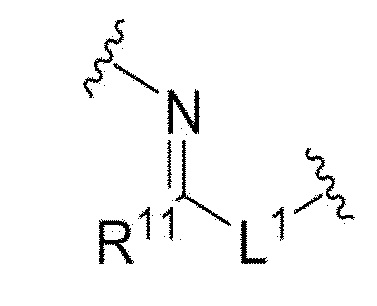 ,
,
где L1 представляет собой одинарную связь или C1-C30 алкилен; и
R11 представляет собой водород или C1-C10 алкил.
31. Конъюгат антитела по п. 30, где L1 представляет собой одинарную связь или C11 или C12 алкилен.
32. Конъюгат антитела по п. 30, отличающийся тем, что L содержит 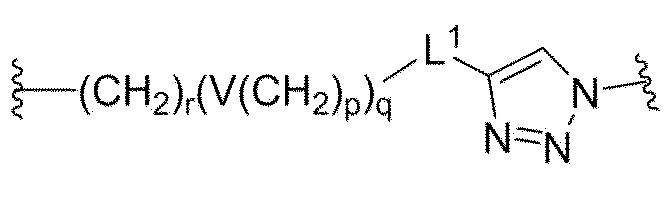 или
или  где
где
V представляет собой одинарную связь, -O-, -S-, -NR21-, -C(O)NR22-, NR23C(O)-, NR24SO2- или -SO2NR25-;
R21 - R25 каждый независимо представляют собой водород, (C1-6) алкил, (C1-6) алкил (C6-20) арил, или (C1-6) алкил (C3-20) гетероарил;
r представляет собой от 0 до 10;
p представляет собой от 0 до 10;
q представляет собой от 1 до 20; и
L1 представляет собой одинарную связь.
33. Конъюгат антитела по п. 32, отличающийся тем, что по меньшей мере один X представлен
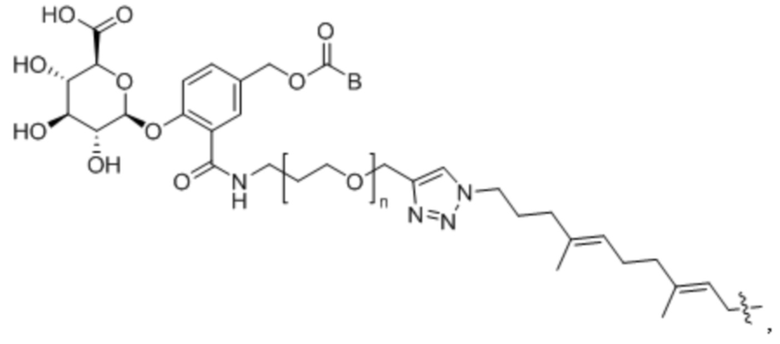
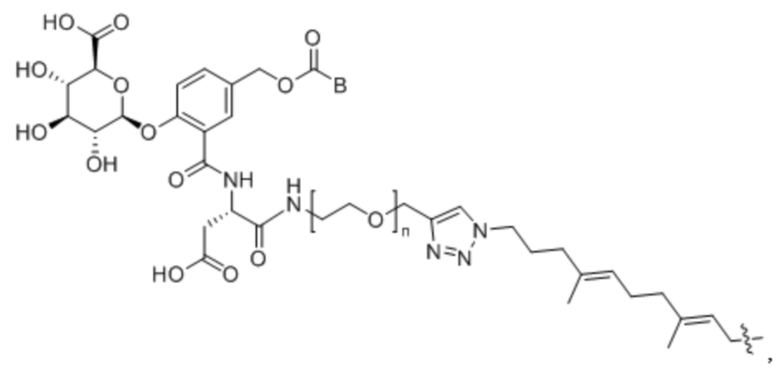
 и
и
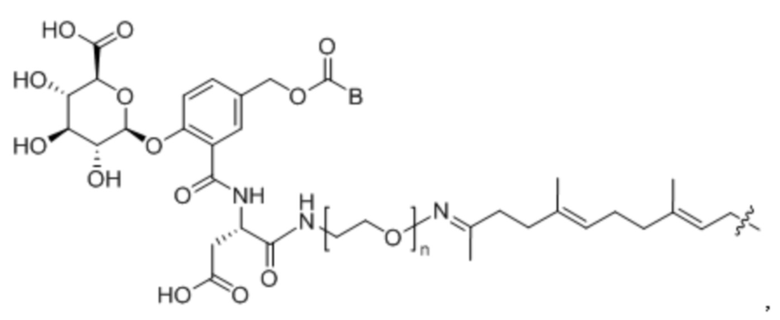
B представляет собой активное средство;
n представляет собой от 0 до 20; и
связь, перекрытая волнистой линией, представляет собой связь с антителом.
34. Конъюгат антитела по п. 5, отличающийся тем, что изопреноидтрансфераза представляет собой фарнезилпротеинтрансферазу (FTase) или геранилгеранилтрансферазу (GGTase).
35. Конъюгат антитела по п. 5, отличающийся тем, что L содержит по меньшей мере один линкер-ответвление, ковалентно связанный с Ab,
i) соответствующие линкеры-ответвления содержат ответвляющееся звено (BR), ковалентно связанное с Ab первичным линкером (PL);
ii) соответствующие линкеры-ответвления связывают первое активное средство с ответвляющимся звеном и содержат первое ответвление (B1), содержащее второй линкер (SL) и расщепляющуюся группу (CG); и
iii) соответствующие линкеры-ответвления содержат а) второе ответвление (В2), где второе активное средство ковалентно связано с ответвляющимся звеном вторым линкером (SL) и расщепляющейся группой (CG), или b) второе ответвление, где полиэтиленгликолевый фрагмент ковалентно связан с ответвляющимся звеном; и
iv) соответствующие расщепляющиеся группы гидролизуются для высвобождения активного средства из конъюгата антитела.
36. Конъюгат антитела по п. 35, отличающийся тем, что линкер-ответвление представляет собой 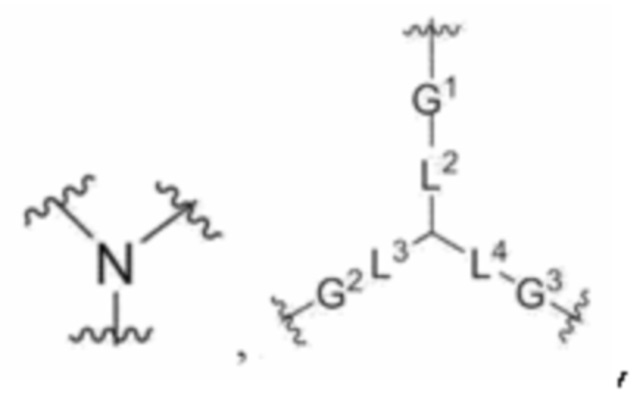
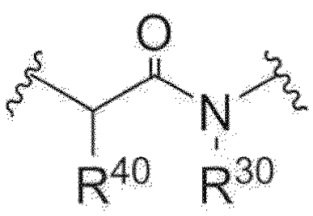 или
или 
L2, L3 и L4 представляют собой, соответственно и независимо, прямые связи или -CnH2n-; n представляет собой целое число от 1 до 30;
G1, G2 и G3 представляют собой, независимо, прямую связь 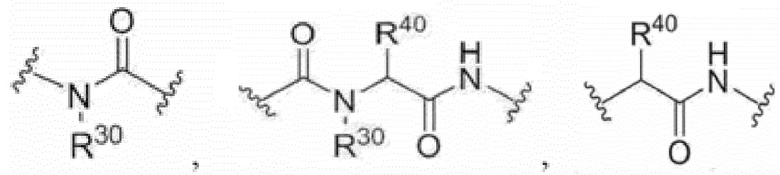 или
или 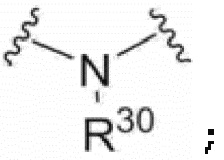 и R30 представляет собой водород или C1-30 алкил.
и R30 представляет собой водород или C1-30 алкил.
37. Конъюгат антитела по п. 36, отличающийся тем, что содержит

где B и B’ обозначают активные средства, которые могут быть различными или идентичными;
n обозначает, соответственно и независимо, целое число от 0 до 30;
f обозначает, соответственно и независимо, целое число от 0 до 30; и
L обозначает связь с Ab.
38. Конъюгат антитела по п. 37, отличающийся тем, что L содержит оксим и 1-20 полиэтиленгликолевых звеньев, которые ковалентно связывают оксим с активным средством.
39. Конъюгат антитела по п. 35, отличающийся тем, что расщепляющаяся группа может быть расщеплена внутри клетки-мишени и расщепляющаяся группа может высвободить одно или несколько активных средств.
40. Конъюгат антитела по п. 5, отличающийся тем, что L содержит от 1 до 6 ответвленных линкеров, ковалентно связанных с Ab, и от 2 до 6 одинаковых или различных активных средств, ковалентно связанных с ответвленными линкерами.
41. Конъюгат антитела по п. 40, отличающийся тем, что соответствующие активные средства связаны с ответвленными линкерами расщепляемой связью.
42. Конъюгат антитела по п. 40, отличающийся тем, что соответствующие ответвленные линкеры содержат ответвляющееся звено, соответствующие активные средства связаны с ответвляющимся звеном через второй линкер и ответвляющиеся звенья связаны с Ab первым линкером.
43. Конъюгат антитела по п. 42, отличающийся тем, что ответвляющееся звено представляет собой азотное звено или лизиновое звено.
44. Конъюгат антитела по п. 42, отличающийся тем, что ответвляющееся звено представляет собой амид и первый линкер или второй линкер содержит карбонил амида.
45. Конъюгат антитела по п. 5, отличающийся тем, что активное средство представляет собой химиотерапевтическое средство или токсин.
46. Конъюгат антитела по п. 5, отличающийся тем, что активное средство представляет собой иммунорегуляторное соединение, противораковое средство, противовирусное средство, антибактериальное средство, противогрибковое средство, противопаразитарное средство или их комбинацию.
47. Конъюгат антитела по п. 5, отличающийся тем, что активное средство выбрано из следующих:
(a) эрлотиниб, бортезомиб, фулвестрант, сутент, летрозол, иматиниба мезилат, PTK787/ZK 222584, оксалиплатин, 5-фторурацил, лейковорин, рапамицин, лапатиниб, лонафарниб, сорафениб, гефитиниб, AG1478, AG1571, тиотепа, циклофосфамид, бусульфан, импросульфан, пипосульфан, бензодопа, карбоквон, метуредопа, уредопа, этиленимин, алтретамин, триэтиленмеламин, триэтиленфосфорамид, триэтилентиофосфорамид, триметилолмеламин, буллатацин, буллатацинон, камптотецин, топотекан, бриостатин, каллистатин, CC-1065, адозелезин, карзелезин, бизелезин, криптофицин 1, криптофицин 8, доластатин, дуокармицин, KW-2189, CB1-TM1, элеутеробин, панкратистатин, саркодиктиин, спонгистатин, хлорамбуцил, хлорнафазин, холофосфамид, эстрамустин, ифосфамид, мехлорэтамин, мелфалан, новэмбихин, фенестерин, преднимустин, трофосфамид, урамустин, кармустин, хлорозотоксин, фотемустин, ломустин, нимустин, ранимустин, калихеамицин, калихеамицин гамма 1, калихеамицин омега 1, динемицин, динемицин А, клодронат, эсперамицин, неокарциностатин хромофор, аклациномизины, актиномицин, антримицин, азасерин, блеомицины, катциномицин, карабицин, карниномицин, карзинофилин, хромомицины, дактиномицин, даунорубицин, деторубуцин, 6-диазо-5-оксо-L-норлейцин, доксорубицин, морфолинодоксорубицин, цианоморфолинодоксорубицин, 2-пирролинодоксорубицин, липосомальный доксорубицин, дезоксидоксорубицин, эпирубицин, эзорубицин, марцелломицин, митомицин C, микофеноловая кислота, ногаламицин, оливомицины, пепломицин, потфиромицин, пуромицин, квеламицин, родорубицин, стрептомигрин, стрептозоцин, тудерцидин, убенимекс, зиностатин, зорубицин, 5-фторурацил, деноптерин, метотрексат, птероптерин, триметрексат, флударабин, 6-меркаптопурин, тиамиприн, тиогуанин, анцитабин, азацитидин, 6-азауридин, кармофур, цитарабин, дидезоксиуридин, доксифлуридин, эноцитабин, флоксуридин, калустерон, дромостанолон, пропионат, эпитиостанол, мепитиостан, тестолактон, аминоглутетимид, митотан, трилостан, фолиновая кислота, ацеглатон, альдофосфамид гликозид, аминолевулиновая кислота, энилурацил, амсакрин, бестрабуцил, бисантрен, эдатрексат, дефофамин, демеколцин, диазиквон, элфорнитин, эллиптиния ацетат, этоглюцид, нитрат галлия, гидроксимочевина, лентинан, лонидаинин, майтанзин, ансамитоцины, митогуазон, митоксантрон, мопиданмол, нитраерин, пентостатин, фенамет, пирарубицин, лозоксантрон, 2-этилгидразид, прокарбазин, полисахарид-k, разоксан, ризоксин, сизофиран, спирогерманий, тенуазоновая кислота, 2,2’,2’’-трихлортриэтиламин, токсин Т-2, верракурин A, роридин A, ангуидин, уретан, виндезин, дакарбазин, манномустин, митобронитол, митолактол, пипоброман, гацитозин, арабинозид, циклофосфамид, тиотепа, паклитаксел, альбумин-сконструированная композиция наночастиц паклитаксела, доцетаксел, хлорамбуцил, гемцитабин, 6-тиогуанин, меркаптопурин, цисплатин, карбоплатин, винбластин, платина, этопозид, ифосфамид, митоксантрон, винкристин, винорелбин, новантрон, тенипозид, эдатрексат, дауномицин, аминоптерин, кселода, ибандронат, CPT-11, ингибитор топоизомеразы RFS 2000, дифторметилорнитин, ретиноевая кислота или капецитабин;
(b) монокин, лимфокин, традиционный полипептидный гормон, паратиреоидный гормон, тироксин, релаксин, прорелаксин, гликопротеиновый гормон, фолликулостимулирующий гормон, тиреостимулирующий гормон, лютеинизирующий гормон, фактор роста печени, фактор роста фибробластов, пролактин, плацентарный лактоген, фактор некроза опухоли, фактор некроза опухоли α, фактор некроза опухоли β, мюллерова ингибирующая субстанция, мышиный гонадотропин-ассоциированный пептид, ингибин, активин, фактор роста эндотелия сосудов, тромбопоэтин, эритропоэтин, остеоиндуктивный фактор, интерферон, интерферон-α, интерферон-β, интерферон-γ, колониестимулирующий фактор (CSF), макрофагальный-CSF, гранулоцитарно-макрофагальный-CSF, гранулоцитарно-макрофагальный-CSF, гранулоцитарный CSF, интерлейкин (IL), IL-1, IL-1α, IL-2, IL-3, IL-4, IL-5, IL-6, IL-7, IL-8, IL-9, IL-10, IL-11, I L-12, фактор некроза опухоли, TNF-α, TNF-β, полипептидный фактор, LIF, kit или лиганд;
(c) дифтерийный токсин, ботулинический токсин, столбнячный токсин, дизентерийный токсин, холерный токсин, аманитин, α-аматинин, пирролобензодиазепин, производное пирролобензодиазепина, индолинобензодиазепин, пиридобензодиазепин, тетродотоксин, бреветоксин, цигуатоксин, рицин, AM токсин, ауристатин, тубулизин, гелданамицин, майтансиноид, калихеамицин, дауномицин, доксорубицин, метотрексат, виндезин, SG2285, доластатин, аналог доластатина, ауристатин, криптофицин, камптотецин, ризоксин, производные ризоксина, CC-1065, аналоги или производные CC-1065, дуокармицин, эндииновый антибиотик, эсперамицин, эпотилон или токсоид;
(d) аффинный лиганд, где аффинный лиганд представляет собой субстрат, ингибитор, активное средство, нейромедиатор или радиоактивный изотоп;
(e) радиоактивная метка, 32P, 35S, флуоресцентный краситель, электронноплотный реагент, фермент, биотин, стрептавидин, диоксигенин, гаптен, иммуногенный белок или молекула нуклеиновой кислоты с последовательностью, комплементарной мишени;
(f) тамоксифен, ралоксифен, дролоксифен, 4-гидрокситамоксифен, триоксифен, кеоксифен, LY117018, онапристон или торемифен;
(g) 4(5)-имидазол, аминоглутетимид, мегестрола ацетат, эксеместан, летрозол или анастрозол;
(h) флутамид, нилутамид, бикалутамид, лейпролид, гозерелин или троксацитабин;
(i) ингибитор ароматазы;
(j) ингибитор протеинкиназы;
(k) ингибитор липидкиназы;
(l) антисмысловой олигонуклеотид;
(m) рибозим;
(n) вакцина; и
(o) антиангиогенное средство.
48. Конъюгат антитела по п. 1, отличающийся тем, что активное средство представляет собой пирролобензодиазепиновый димер.
49. Конъюгат антитела по п. 48, отличающийся тем, что активатор представляет собой пирролобензодиазепиновый димер;
пирролобензодиазепиновый димер замещен X в положении N10 или X’ в положении N’10, где X или X’ связывает пирролобензодиазепиновый димер с линкером;
X и X’ представляют собой, соответственно и независимо, -C(O)O*, -S(O)O-*, -C(O)-*, -C(O)NRX-*, -S(O)2NRX-*, -P(O)R’NRX-*, -S(O)NRX-* или -PO2NRX-*;
RX представляет собой C1-8 алкил, C3-8 циклоалкил, C3-20 гетероарил или C5-20 арил;
RX’ представляет собой OH, N3, CN, SH, C1-8 алкил, C3-8 циклоалкил, C1-8 алкокси, C1-8 алкилтио, C3-20 гетероарил, C5-20 арил или амино; и
* представляет собой участок связывания между пирролобензодиазепиновым димером и линкером.
50. Конъюгат антитела по п. 49, отличающийся тем, что пирролобензодиазепиновый димер имеет структуру, представленную общей формулой X или общей формулой XI ниже:
[Общая формула X]
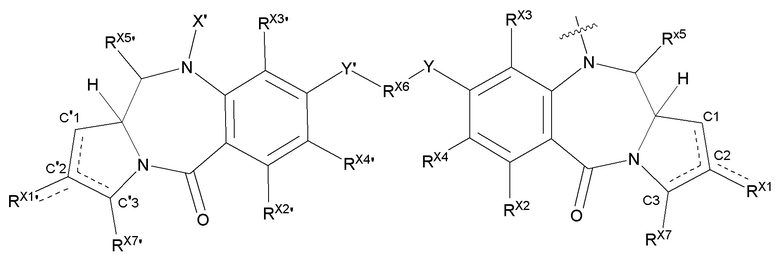 ,
,
[Общая формула XI]
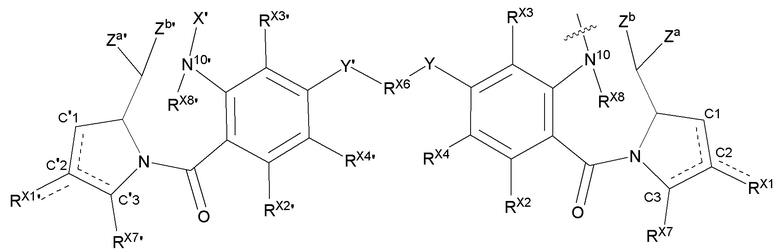 ,
,
где пунктирная линия представляет собой необязательную двойную связь, разрешенную валентностью;
связь, перекрытая волнистой линией, представляет собой связь с L;
RX1 и RX1’ независимо выбраны из H, OH, =O, =CH2 CN, Rm ORm, =CH-Rm’, =C(Rm’)2, O-SO2-Rm, CO2Rm, CORm, галогена и дигалогена;
Rm’ выбран из Rm, CO2Rm, CORm, CHO, CO2H и галогена;
каждый Rm независимо выбран из C1-12 алкила, C2-12 алкенила, C2-12 алкинила, C5-20 арила, C5-20 гетероарила, C3-6 циклоалкила, 3-7-членного гетероциклила, 3-7-членного гетероциклоалкила и 5-7-членного гетероарила;
RX2, RX2’, RX3, RX3’, RX5 и RX5’ каждый независимо выбраны из H, Rm, OH, ORm, SH, SRm, NH2, NHRm, NRm2, NO2, Me3Sn и галогена;
RX4 и RX4’ независимо выбраны из H, Rm, OH, ORm, SH, SRm, NH2, NHRm, NRm2, NO2, Me3Sn, галогена, C1-6 алкила, C1-6 алкенила, C2-6 алкинила, C2-6 арила, C3-6 гетероарила, C3-6 циклоалкила, 3-7-членного гетероциклоалкила, C5-12 арила, 5-7-членного гетероарила, -CN, -NCO, -ORn, -OC(O)Rn, -OC(O)NRnRn’, -OS(O)Rn, -OS(O)2Rn, -SRn, -S(O)Rn, -S(O)2Rn, -S(O)NRnRn’, -S(O)2NRnRn’, -OS(O)NRnRn’, -OS(O)2NRnRn’, -NRnRn’, -NRnC(O)Ro, -NRnC(O)ORo, -NRnC(O)NRoRo’, -NRnS(O)Ro, -NRnS(O)2Ro, -NRnS(O)NRoRo', -NRnS(O)2NRoRo', -C(O)Rn, -C(O)ORn и -C(O)NRnRn';
RX и RX’ каждый независимо выбраны из H, OH, N3, CN, NO2, SH, NH2, ONH2, NHNH2, галогена, C1-8 алкил, C3-8 циклоалкила, C1-8 алкокси, C1-8 алкилтио, C3-20 гетероарила, C5-20 арила или моно- или ди-C1-8 алкиламино;
Y и Y’ каждый независимо выбраны из O, S и N(H);
Rx6 представляет собой C3-12 алкилена, C3-12 алкенилена, или C3-12 гетероалкилена;
RX7 и RX7’ каждый независимо выбраны из H, C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C3-6 циклоалкила, 3-7-членного гетероциклоалкила, C6-10 арила, 5-7-членного гетероарила, -ORr, -OC(O)Rr, -OC(O)NRrRr’, -OS(O)Rr, -OS(O)2Rr, -SRr, -S(O)Rr, -S(O)2Rr, -S(O)NRrRr’, -S(O)2NRrRr', -OS(O)NRrRr', -OS(O)2NRrRr', -NRrRr', -NRrC(O)Rs, -NRrC(O)ORs, -NRrC(O)NRsRs’, -NRrS(O)Rs, -NRrS(O)2Rs, -NRrS(O)NRsRs’, -NRrS(O)2NRsRs, -C(O)Rr, -C(O)ORs и -C(O)NRrRr';
каждый Rr, Rr’, Rs и Rs’ независимо выбран из H, C1-7 алкила, C2-7 алкенила, C2-7 алкинила, C3-13 циклоалкила, 3-7-членного гетероциклоалкила, C5-10 арила и 5-7-членного гетероарила;
каждый RX8 и RX8’ независимо выбран из H, C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C3-6 гетероалкила, 3-7-членного гетероциклоалкила, C5-10 арила, 5-7-членного гетероарила, -S(O)Rm, -S(O)2Rm, -S(O)NRmRm', -S(O)2NRmRm', -NRmRm', -NRmC(O)Rm, -NRmC(O)ORn, -NRmC(O)NRnRn', -NRmS(O)Rn, -NRmS(O)2Rn, -NRmS(O)NRnRn', -NRmS(O)2NRnRn', -C(O)Rm, -C(O)ORm и -C(O)NRmRm';
Za представляет собой ORX12a, NRX12aRX12a или SRX12a;
Zb представляет собой ORX13a, NRX13aRX13a или SRX13a;
Za’ представляет собой ORX12a’, NRX12a’RX12a’ или SRX12a’;
Zb’ представляет собой ORX13a’, NRX13a’RX13a’ или SRX13a’;
каждый RX12a, RX12a’, RX13a и Rx13a’ независимо выбран из H, C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C3-6 циклоалкила, 3-7-членного гетероциклоалкила, C5-10 арила, 5-7-членного гетероарила, -C(O)RX15a, -C(O)ORX15a и -C(O)NRX15aRX15a’; и
каждый RX15a и Rx15a’ независимо выбран из C1-12 алкила, C2-12 алкенила, C2-12 алкинила, C5-20 арила, C5-20 гетероарила, C3-6 циклоалкила, 3-7-членного гетероциклила, 3-7-членного гетероциклоалкила и 5-7-членного гетероарила; и
RX13a и RX14a необязательно соединяют атомы, к которым они присоединены, с образованием 3-7-членного гетероциклила, 3-7-членного гетероциклоалкила или 3-7-членного гетероарила, и RX13a’ и RX14a’ необязательно соединяют атомы, к которым они присоединены, с образованием 3-7-членного гетероциклила, 3-7-членного гетероциклоалкила или 3-7-членного гетероарила; и
каждый из Rn, Rn’, Ro, Ro’, Rp и Rp’ независимо выбран из H, C1-7 алкила, C2-7 алкенила, C2-7 алкинила, C3-13 циклоалкила, 3-7-членного гетероциклоалкила, C5-10 арила и 5-7-членного гетероарила.
51. Конъюгат антитела по п. 50, отличающийся тем, что Rm представляет собой C1-12 алкила, C2-12 алкенила, C2-12 алкинила, C5-20 арила, C5-20 гетероарила, C3-6 циклоалкила, 3-7-членного гетероциклила, 3-7-членного гетероциклоалкила и 5-7-членного гетероарила; и Rm дополнительно замещен C1-12 алкилом, C2-12 алкенилом, C2-12 алкинилом, C5-20 арилом, C5-20 гетероарилом, C3-6 циклоалкилом, 3-7-членным гетероциклилом, 3-7-членным гетероциклоалкилом или 5-7-членным гетероарилом.
52. Конъюгат антитела по п. 50, отличающийся тем, что Rx4 и Rx4’ каждый выбраны из H, Rm, OH, ORm, SH, SRm, NH2, NHRm, NRmRm’, NO2, Me3Sn, галогена, C1-6 алкил C1-6 алкокси, C2-6 алкенила, C2-6 алкинила, C3-6 циклоалкила, 3-7-членного гетероциклоалкила, C5-12 арила, 5-7-членного гетероарила, -CN, -NCO, -ORn, -OC(O)Rn, -OC(O)NRnRn', -OS(O)Rn, -OS(O)2Rn, -SRn, -S(O)Rn, -S(O)2Rn, -S(O)NRnRn', -S(O)2NRnRn', -OS(O)NRnRn', -OS(O)2NRnRn', -NRnRn', -NRnC(O)Ro, -NRnC(O)ORo, -NRnC(O)NRoRo', -NRnS(O)Ro, -NRnS(O)2Ro, -NRnS(O)NRoRo',-NRnS(O)2NRoRo', -C(O)Rn, -C(O)ORn и -C(O)NRnRn'; и RX4 или RX4’ представляет собой C1-6 алкил, C1-6 алкокси, C2-6 алкенил, C2-6 алкинил, C3-6 циклоалкил, 3-7-членный гетероциклоалкил, C5-12 арил или 5-7-членный гетероарил и дополнительно замещен по меньшей мере одним C1-6 алкилом, C1-6 алкокси, C2-6 алкенилом, C2-6 алкинилом, C3-6 циклоалкилом, 3-7-членным гетероциклоалкилом, C5-10 арилом, 5-7-членным гетероарилом, -ORp, -OC(O)Rp, -C(O)NRpRp', -OS(O)Rp, -OS(O)2Rp, -SRp,-S(O)Rp, -S(O)2Rp, -S(O)NRpRp', -S(O)2NRpRp', -OS(O)NRpRp', -OS(O)2NRpRp', -NRpRp',-NRpC(O)Rq, -NRpC(O)ORq, -NRpC(O)NRqRq', -NRpS(O)Rq, -NRpS(O)2Rq, -NRpS(O)NRqRq', -NRpS(O)2NRqRq', -C(O)Rp, -C(O)ORp или -C(O)NRpRp.
53. Конъюгат антитела по п. 50, отличающийся тем, что RX7 и RX7’ представляют собой каждый H, C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C3-6 циклоалкила, 3-7-членного гетероциклоалкила, C6-10 арила, 5-7-членного гетероарила, -ORr, -OC(O)Rr, -OC(O)NRrRr', -OS(O)Rr, -OS(O)2Rr, -SRr, -S(O)Rr, -S(O)2Rr, -S(O)NRrRr', -S(O)2NRrRr', -OS(O)NRrRr', -OS(O)2NRrRr', -NRrRr', -NRrC(O)Rs, -NRrC(O)ORs, -NRrC(O)NRsRs', -NRrS(O)Rs, -NRrS(O)2Rs, -NRrS(O)NRsRs', -NRrS(O)2NRsRs, -C(O)Rr, -C(O)ORs или -C(O)NRrRr'; RX7 и RX7’ представляют собой каждый H, C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C3-6 циклоалкила, 3-7-членного гетероциклоалкила, C6-10 арила или 5-7-членного гетероарила, и дополнительно замещены C1-6 алкилом, C2-6 алкенилом, C2-6 алкинилом, C3-6 циклоалкилом, 3-7-членным гетероциклоалкилом, C6-10 арилом, 5-7-членным гетероарилом, -ORt, -OC(O)Rt, -OC(O)NRtRt', -OS(O)Rt, -OS(O)2Rt, -SRt, -S(O)Rt, -S(O)2Rt, -S(O)NRtRt', -S(O)2NRtRt', -OS(O)NRtRt', -OS(O)2NRtRt', -NRtRt', -NRtC(O)Ru, -NRtC(O)ORu,-NRtC(O)NRuRu', -NRtS(O)Ru, -NRtS(O)2Ru, -NRtS(O)NRuRu', -NRtS(O)2NRuRu', -C(O)Rt, -C(O)ORt или -C(O)NRtRt'; и Rr, Rr’, Rs, Rs’, Rt, Rt’, Ru и Ru’ каждый выбран из H, C1-7 алкила, C2-7 алкенила, C2-7 алкинила, C3-13 циклоалкила, 3-7-членного гетероциклоалкила, C5-10 арила и 5-7-членного гетероарила.
54. Конъюгат антитела по п. 50, отличающийся тем, что Rx6 представляет собой C3-12 алкилен, C3-12 алкенилен или C3-12 гетероалкилен, с Rx6, замещенным -NH2, -NHRm, -NHC(O)Rm, -NHC(O)CH2, [OCH2CH2]n-RXX или -[CH2CH2O]n-RXX; RXX представляет собой H, OH, N3, CN, NO2, SH, NH2, ONH2, NHNH2, галоген, C1-8 алкил, C3-8 циклоалкил, C1-8 алкокси, C1-8 алкилтио, C3-20 гетероарил, C5-20 арил или моно- или ди-C1-8 алкиламино; и n представляет собой от 1 до 6.
55. Конъюгат антитела по п. 50, отличающийся тем, что активное средство представляет собой пирролобензодиазепиновый димер, представленный общей формулой XII или общей формулой XIII:
[Общая формула XII]
 ,
,
[Общая формула XIII]
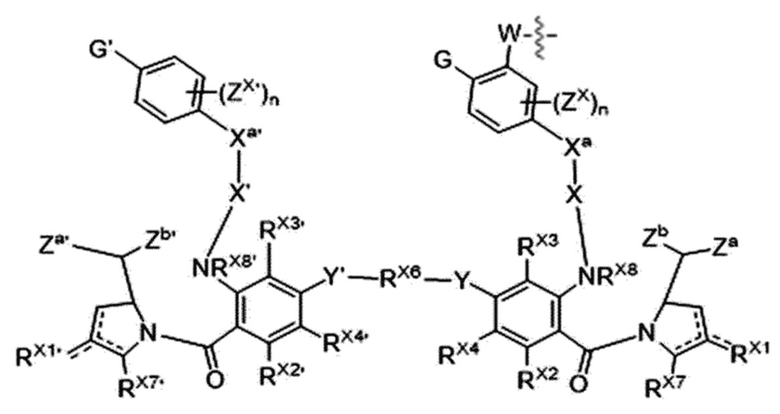 ,
,
Xa и Xa’ независимо выбраны из связи или C1-6 алкилена;
ZX’ и ZX независимо выбраны из водорода, C1-8 алкила, галогена, циано, нитро,  и -(CH2)m-OCH3;
и -(CH2)m-OCH3;
каждый R80, R90 и R100 выбран из водорода, C1-8 алкила, C2-6 алкенила, C1-6 алкокси, алкоксиалкила и -(CH2CH2O)m-(CH2)m2CH3; и
m представляет собой от 0 до 12, и m2 представляет собой от 1 до 12.
56. Конъюгат антитела по п. 1, отличающийся тем, что активное средство представляет собой

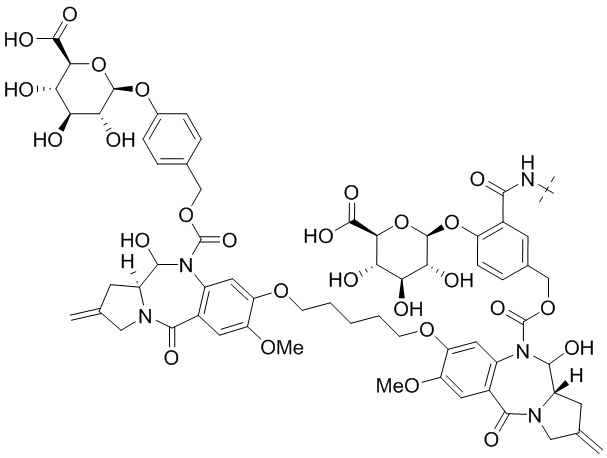
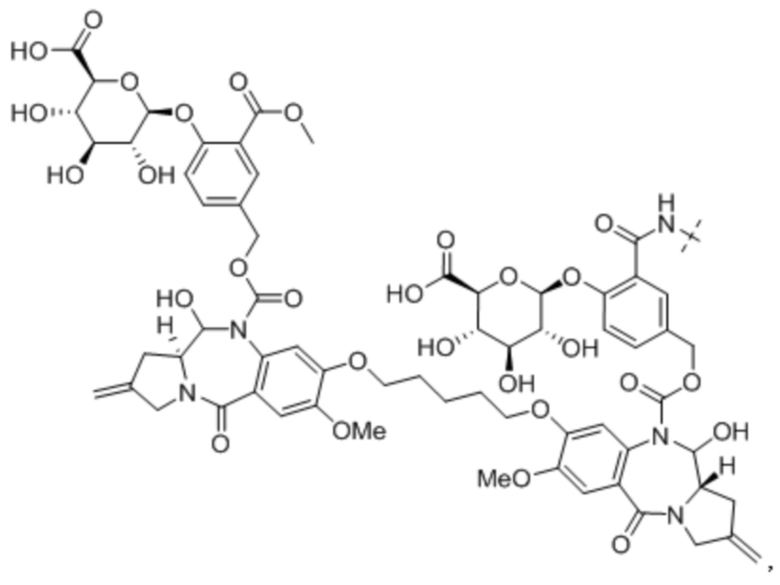

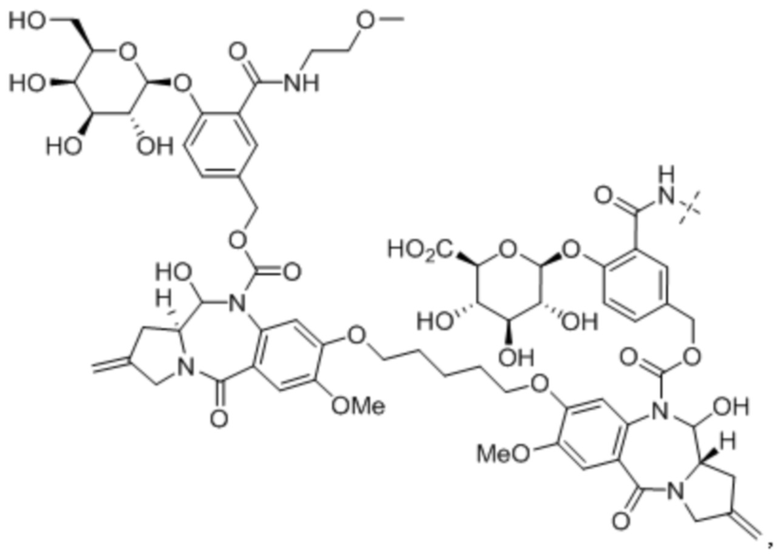
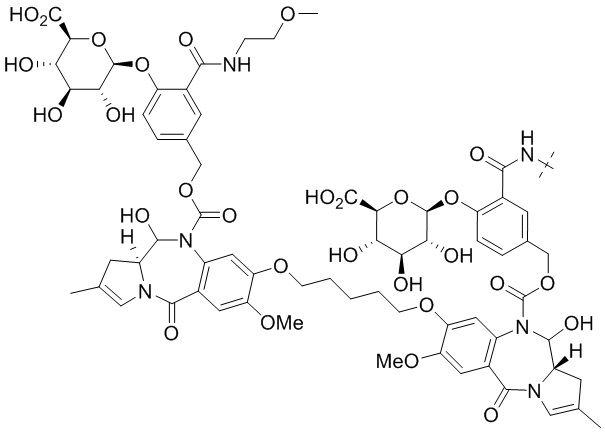
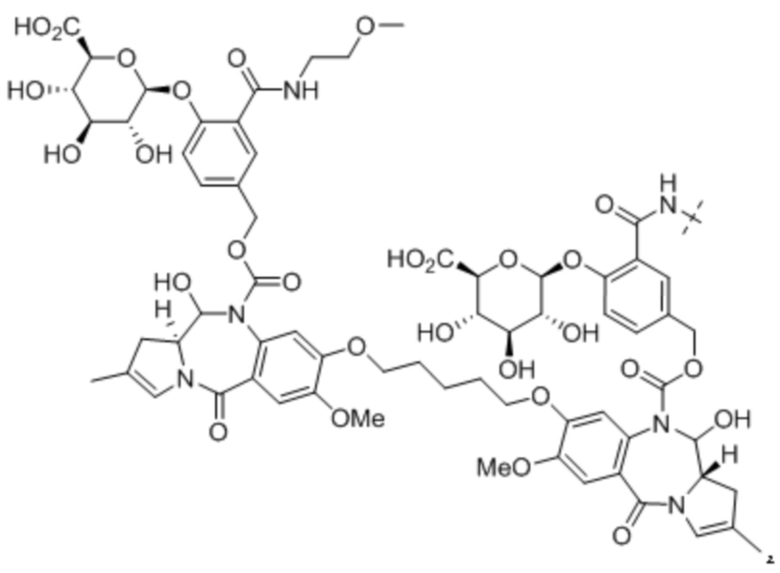
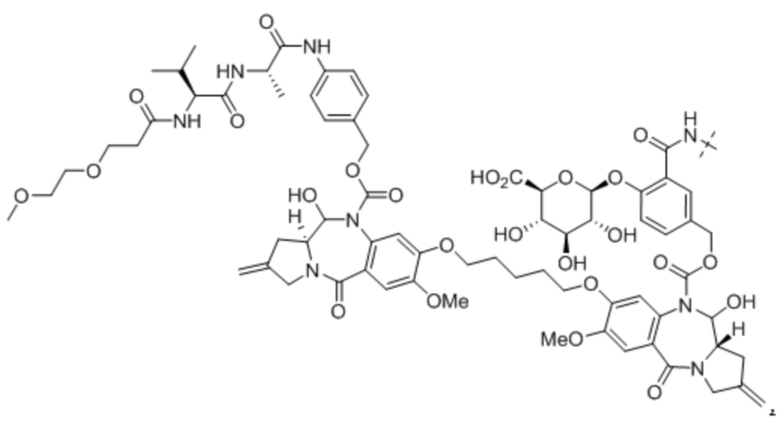

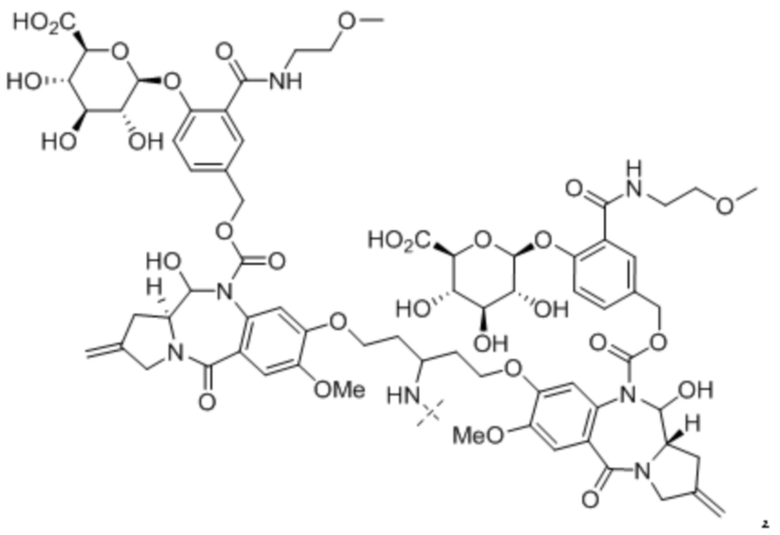
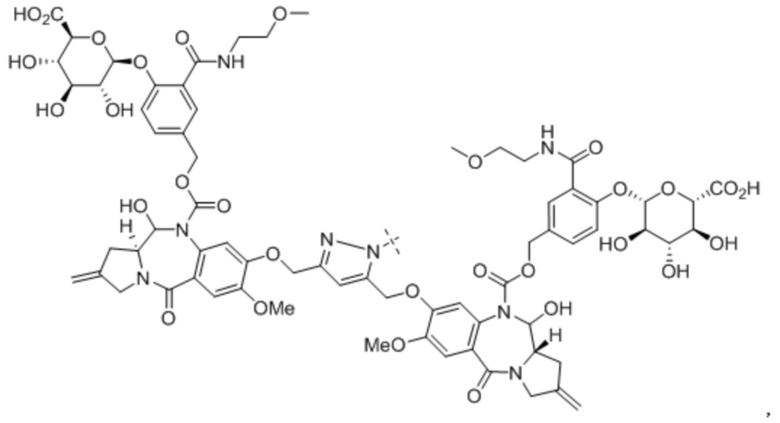 или
или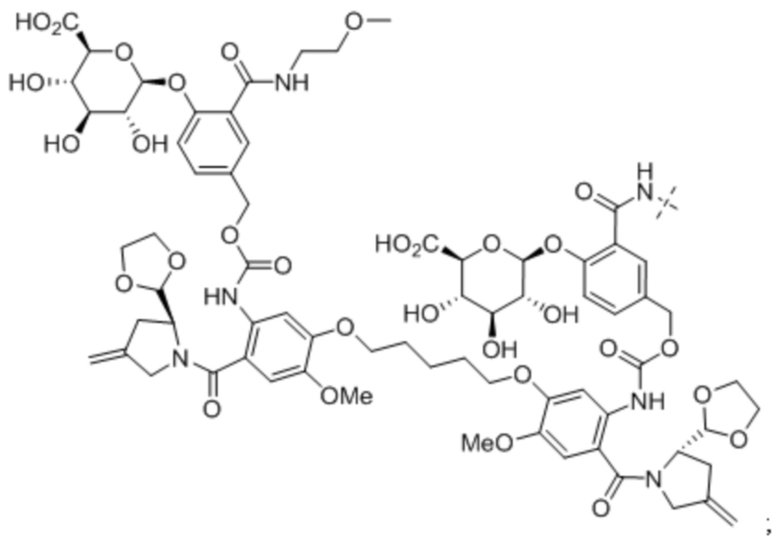
и связь, перекрытая пунктирной линией, представляет собой точку соединения с L.
57. Фармацевтическая композиция для профилактики или лечения рака, ассоциированного с экспрессией DLK1, содержащая эффективное количество конъюгата антитела по п.1.
58. Фармацевтическая композиция по п. 57, дополнительно содержащая фармацевтически эффективное количество химиотерапевтического средства.
59. Фармацевтическая композиция по п. 57, отличающаяся тем, что рак выбран из рака легкого, мелкоклеточной карциномы легких, рака желудочно-кишечного тракта, рака толстой кишки, рака кишечника, рака молочной железы, рака яичников, рака простаты, рака яичек, рака печени, рака почки, рака мочевого пузыря, рака поджелудочной железы, рака головного мозга, саркомы, остеосаркомы, саркомы Капоши и меланомы.
| KR 1020190018400 A, 22.02.2019 | |||
| КОНЪЮГАТЫ БЕЛОК-АКТИВНОЕ ВЕЩЕСТВО И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2012 |
|
RU2613906C2 |
| KR 1020120113175 A, 12.10.2012 | |||
| WO 2018069490 A1, 19.04.2018 | |||
| KR 1020180110645 A, 10.10.2018. | |||
Авторы
Даты
2023-08-11—Публикация
2020-03-05—Подача