ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка испрашивает преимущество и приоритет заявки на патент Китая № 201810872672.X, поданной в Национальное управление интеллектуальной собственности КНР 2 августа 2018 г., и заявки на патент Китая № 201810989128.3, поданной в Национальное управление интеллектуальной собственности КНР 28 августа 2018 г., содержание каждого из которых включено в данный документ посредством ссылки во всей своей полноте.
ОБЛАСТЬ ТЕХНИКИ
Настоящая заявка относится к боратному соединению производного азетидина, способу его получения, фармацевтическим композициям, содержащим его и к его применению в лечении заболеваний, ассоциированных с множественной миеломой.
ПРЕДПОСЫЛКИ К СОЗДАНИЮ ИЗОБРЕТЕНИЯ
Множественная миелома (MM) представляет собой злокачественное пролиферативное заболевание плазматических клеток, характеризующееся атипичной пролиферацией клональных плазматических клеток в костном мозге, и обуславливает нарушение кроветворной функции, возникновение остеолитических очагов поражения в костном мозге и обнаружение моноклональных иммуноглобулинов или их фрагментов (M-белок) в сыворотке и/или моче, и при этом ее клинические проявления представляют собой боль в костях, анемию, гиперкальцемию, поражение функции почек, инфекцию и кровоизлияние и т.д. Бортезомиб представляет собой обратимый ингибитор протеасом, который обеспечивает лечение множественной миеломы путем способствования апоптозу клеток миеломы. Однако при длительном лечении у многих пациентов с множественной миеломой частично развивается устойчивость к бортезомибу. Следовательно, для лечения множественной миеломы существует необходимость в создании новых, безопасных и высокоустойчивых лекарственных средств.
КРАТКОЕ ОПИСАНИЕ
Настоящая заявка предусматривает боратное производное азетидина, которое представляет собой пролекарство на основе соединения бороновой кислоты и производного азетидина и превосходит соединение бороновой кислоты с точки зрения стабильности.
В одном аспекте в настоящей заявке предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер,
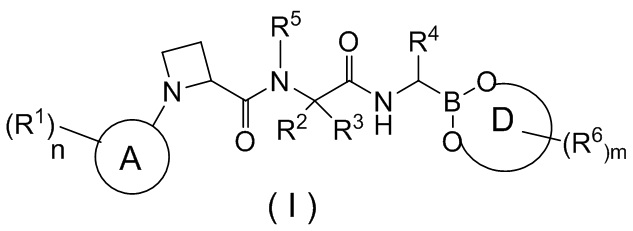 ,
,
где
кольцо A выбрано из группы, состоящей из фенила и 5-10-членного гетероарила;
каждый из R1 независимо выбран из группы, состоящей из галогена, CN, OH, NH2, C1-6алкила и C1-6гетероалкила, где C1-6алкил или C1-6гетероалкил необязательно замещены одной или более группами, выбранными из группы, состоящей из галогена, OH и NH2;
n выбран из группы, состоящей из 0, 1, 2, 3, 4 и 5;
каждый из R2 и R3 независимо выбран из группы, состоящей из H и C1-6алкила;
R4 выбран из C1-6алкила;
R5 выбран из группы, состоящей из H и C1-3алкила;
кольцо D выбрано из 5-10-членного гетероциклила, где 5-10-членный гетероциклил замещен по меньшей мере одним =O;
каждый R6 независимо выбран из группы, состоящей из галогена, OH, NH2, COOH, C1-6алкила, C3-6циклоалкила, C1-6гетероалкила, C6-10арила и 5-10-членного гетероарила, где C1-6алкил, C3-6циклоалкил, C1-6гетероалкил, C6-10арил или 5-10-членный гетероарил необязательно замещены одной или более группами, выбранными из группы, состоящей из COOH, галогена, OH, NH2 и SH; и
m выбран из группы, состоящей из 0, 1, 2, 3, 4 и 5.
В некоторых вариантах осуществления кольцо A выбрано из группы, состоящей из фенила и 5-6-членного гетероарила, где 5-6-членный гетероарил содержит по меньшей мере один атом кольца, выбранный из группы, состоящей из азота и серы. В некоторых вариантах осуществления кольцо A выбрано из группы, состоящей из фенила, пиридинила и тиазолила. В некоторых вариантах осуществления кольцо A представляет собой фенил.
В некоторых вариантах осуществления каждый из R1 независимо выбран из группы, состоящей из галогена, CN, OH, NH2, C1-3алкила и C1-3алкокси, где C1-3алкил или C1-3алкокси необязательно замещены одной или более группами, выбранными из группы, состоящей из галогена, OH и NH2. В некоторых вариантах осуществления каждый из R1 независимо выбран из группы, состоящей из галогена, CN, C1-3алкила или C1-3алкила, замещенного одним или более галогенами. В некоторых вариантах осуществления каждый из R1 независимо выбран из группы, состоящей из фтора, хлора, брома, йода, CN, C1-3алкила или C1-3алкила, замещенного 1, 2 и 3 атомами фтора. В некоторых вариантах осуществления каждый из R1 независимо выбран из группы, состоящей из фтора, CN и трифторметила. В некоторых вариантах осуществления каждый из R1 независимо выбран из фтора.
В некоторых вариантах осуществления n выбран из группы, состоящей из 0, 1 и 2. В некоторых вариантах осуществления n выбран из группы, состоящей из 1 и 2. В некоторых вариантах осуществления n равняется 2.
В некоторых вариантах осуществления структурное звено 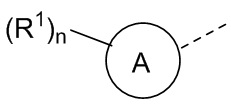 соединения формулы (I) выбрано из группы, состоящей из
соединения формулы (I) выбрано из группы, состоящей из  ,
,  и
и  .
.
В некоторых вариантах осуществления структурное звено  соединения формулы (I) выбрано из группы, состоящей из
соединения формулы (I) выбрано из группы, состоящей из  ,
,  ,
,  и
и  .
.
В некоторых вариантах осуществления структурное звено  соединения формулы (I) выбрано из группы, состоящей из
соединения формулы (I) выбрано из группы, состоящей из 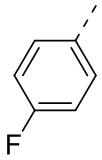 ,
, 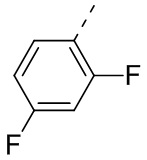 ,
,  ,
,  и
и 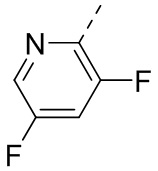 . В некоторых вариантах осуществления структурное звено
. В некоторых вариантах осуществления структурное звено  соединения формулы (I) представляет собой
соединения формулы (I) представляет собой  .
.
В некоторых вариантах осуществления каждый из R2 и R3 независимо выбран из группы, состоящей из H и C1-3алкила. В некоторых вариантах осуществления каждый из R2 и R3 независимо выбран из H.
В некоторых вариантах осуществления R4 выбран из C3-5алкила. В некоторых вариантах осуществления R4 выбран из C4алкила. В некоторых вариантах осуществления R4 представляет собой изобутил.
В некоторых вариантах осуществления R5 выбран из группы, состоящей из H и метила. В некоторых вариантах осуществления R5 представляет собой H.
В некоторых вариантах осуществления кольцо D выбрано из 5-10-членного гетероциклила, где 5-10-членный гетероциклил замещен одним =O. В некоторых вариантах осуществления кольцо D выбрано из 5-10-членного гетероциклила, где кольцо D представляет собой 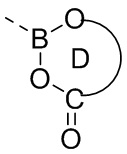 . В некоторых вариантах осуществления кольцо D выбрано из 5-10-членного гетероциклила, где кольцо D представляет собой
. В некоторых вариантах осуществления кольцо D выбрано из 5-10-членного гетероциклила, где кольцо D представляет собой  , и гетероатомы в атомах кольца 5-10-членного гетероциклила включают только бор и кислород.
, и гетероатомы в атомах кольца 5-10-членного гетероциклила включают только бор и кислород.
В некоторых вариантах осуществления кольцо D выбрано из группы, состоящей из 5-членного гетероциклила, 6-членного гетероциклила и 10-членного гетероциклила, где 5-членный гетероциклил, 6-членный гетероциклил или 10-членный гетероциклил замещены по меньшей мере одним =O. В некоторых вариантах осуществления кольцо D выбрано из группы, состоящей из 5-членного гетероциклила, 6-членного гетероциклила и 10-членного гетероциклила, где 5-членный гетероциклил, 6-членный гетероциклил или 10-членный гетероциклил замещены одним =O. В некоторых вариантах осуществления кольцо D выбрано из группы, состоящей из 5-членного гетероциклила, 6-членного гетероциклила и 10-членного гетероциклила, где кольцо D представляет собой  . В некоторых вариантах осуществления кольцо D выбрано из группы, состоящей из 5-членного гетероциклила, 6-членного гетероциклила и 10-членного гетероциклила, где кольцо D представляет собой
. В некоторых вариантах осуществления кольцо D выбрано из группы, состоящей из 5-членного гетероциклила, 6-членного гетероциклила и 10-членного гетероциклила, где кольцо D представляет собой  , и гетероатомы в атомах кольца 5-членного гетероциклила, 6-членного гетероциклила или 10-членного гетероциклила включают только бор и кислород.
, и гетероатомы в атомах кольца 5-членного гетероциклила, 6-членного гетероциклила или 10-членного гетероциклила включают только бор и кислород.
В некоторых вариантах осуществления кольцо D выбрано из группы, состоящей из 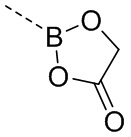 ,
, 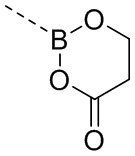 и
и  . В некоторых вариантах осуществления кольцо D представляет собой
. В некоторых вариантах осуществления кольцо D представляет собой  .
.
В некоторых вариантах осуществления m выбран из группы, состоящей из 0, 1, 2 и 3. В некоторых вариантах осуществления m выбран из группы, состоящей из 0, 1 и 2. В некоторых вариантах осуществления m выбран из группы, состоящей из 0 и 1.
В некоторых вариантах осуществления каждый из R6 независимо выбран из OH, NH2, COOH и C1-6алкила, где C1-6алкил необязательно замещен одной или более группами, выбранными из группы, состоящей из COOH, OH и NH2. В некоторых вариантах осуществления каждый из R6 независимо выбран из C1-4алкила, необязательно замещенного одним или более COOH. В некоторых вариантах осуществления каждый из R6 независимо выбран из группы, состоящей из метила, трет-бутила и карбоксиметила. В некоторых вариантах осуществления R6 представляет собой карбоксиметил.
В некоторых вариантах осуществления структурное звено 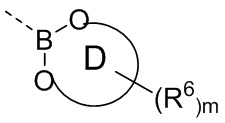 соединения формулы (I) представляет собой
соединения формулы (I) представляет собой  .
.
В некоторых вариантах осуществления структурное звено  соединения формулы (I) выбрано из группы, состоящей из
соединения формулы (I) выбрано из группы, состоящей из 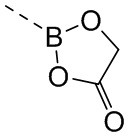 ,
, 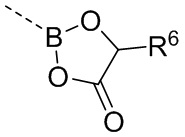 ,
, 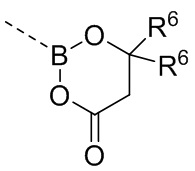 и
и  .
.
В некоторых вариантах осуществления структурное звено  соединения формулы (I) выбрано из группы, состоящей из
соединения формулы (I) выбрано из группы, состоящей из  ,
, 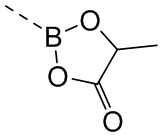 ,
,  ,
, 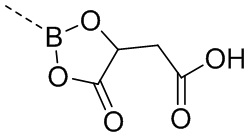 ,
, 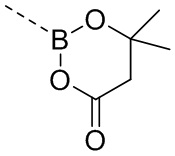 и
и  . В некоторых вариантах осуществления структурное звено
. В некоторых вариантах осуществления структурное звено  соединения формулы (I) представляет собой
соединения формулы (I) представляет собой  .
.
В некоторых вариантах осуществления структурное звено  соединения формулы (I) выбрано из группы, состоящей из
соединения формулы (I) выбрано из группы, состоящей из  ,
,  ,
,  ,
,  ,
,  и
и  . В некоторых вариантах осуществления структурное звено
. В некоторых вариантах осуществления структурное звено  соединения формулы (I) представляет собой
соединения формулы (I) представляет собой  .
.
В некоторых вариантах осуществления соединение формулы (I), раскрытое в данном документе, представляет собой пролекарство на основе соединения формулы (I-0),
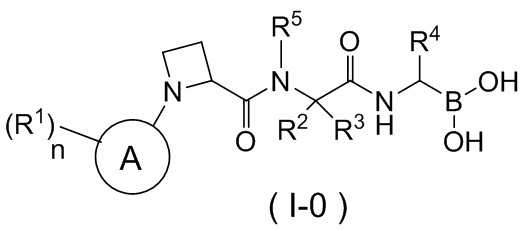 ,
,
где кольцо A, n, R1, R2, R3, R4 и R5 являются такими, как определено выше для соединения формулы (I).
В некоторых вариантах осуществления структурное звено  соединения формулы (I-0) является таким, как определено выше для соединения формулы (I).
соединения формулы (I-0) является таким, как определено выше для соединения формулы (I).
В другом аспекте в настоящей заявке также предусмотрено соединение формулы (I-a) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер,
 ,
,
где кольцо A, кольцо D, n, R1, R2, R3, R4, R5, R6 и m являются такими, как определено выше для соединения формулы (I).
В некоторых вариантах осуществления структурное звено  или
или  соединения формулы (I-a), является таким, как определено выше для соединения формулы (I).
соединения формулы (I-a), является таким, как определено выше для соединения формулы (I).
В некоторых вариантах осуществления соединение формулы (I-a), раскрытое в данном документе, представляет собой пролекарство на основе соединения формулы (I-a-0),
 ,
,
где кольцо A, n, R1, R2, R3, R4 и R5 являются такими, как определено выше для соединения формулы (I).
В некоторых вариантах осуществления структурные звенья  соединения формулы (I-a-0) являются такими, как определено выше для соединения формулы (I).
соединения формулы (I-a-0) являются такими, как определено выше для соединения формулы (I).
В другом аспекте в настоящей заявке также предусмотрено соединение формулы (II) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер,
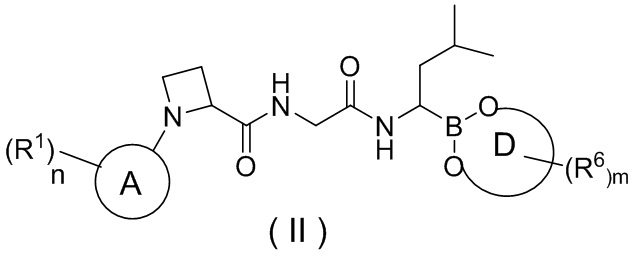 ,
,
где кольцо A, кольцо D, n, R1, R6 и m являются такими, как определено выше для соединения формулы (I).
В некоторых вариантах осуществления структурное звено  или
или  соединения формулы (II) является таким, как определено выше для соединения формулы (I).
соединения формулы (II) является таким, как определено выше для соединения формулы (I).
В другом аспекте в настоящей заявке также предусмотрено соединение формулы (II) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер,
 ,
,
где кольцо A, кольцо D, n, R1, R6 и m являются такими, как определено выше для соединения формулы (II).
В некоторых вариантах осуществления структурное звено  или
или  соединения формулы (II-a) является таким, как определено выше для соединения формулы (II).
соединения формулы (II-a) является таким, как определено выше для соединения формулы (II).
В другом аспекте в настоящей заявке также предусмотрено соединение формулы (III) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер,
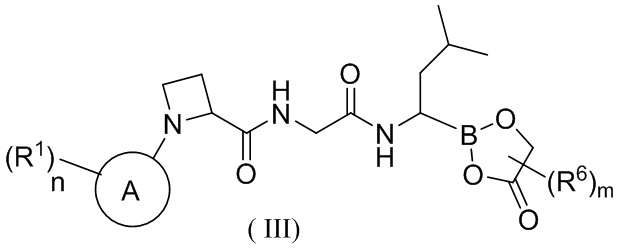 ,
,
где кольцо A, n, R6, m и R1 являются такими, как определено выше для соединения формулы (I).
В некоторых вариантах осуществления структурное звено  соединения формулы (II) является таким, как определено выше для соединения формулы (I).
соединения формулы (II) является таким, как определено выше для соединения формулы (I).
В некоторых вариантах осуществления структурное звено  соединения формулы (III) выбрано из группы, состоящей из
соединения формулы (III) выбрано из группы, состоящей из  ,
,  ,
,  и
и  . В некоторых вариантах осуществления структурное звено
. В некоторых вариантах осуществления структурное звено  соединения формулы (III) представляет собой
соединения формулы (III) представляет собой  .
.
В некоторых вариантах осуществления структурное звено  соединения формулы (III) выбрано из группы, состоящей из
соединения формулы (III) выбрано из группы, состоящей из  ,
,  ,
,  и
и  . В некоторых вариантах осуществления структурное звено
. В некоторых вариантах осуществления структурное звено  соединения формулы (III) представляет собой
соединения формулы (III) представляет собой  .
.
В другом аспекте в настоящей заявке также предусмотрено соединение формулы (III-a) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер,
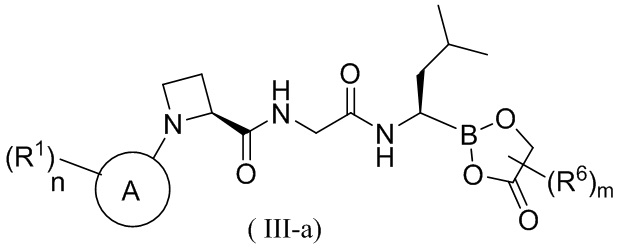 ,
,
где кольцо A, n, R1, R6 и m, а также структурные звенья  и
и 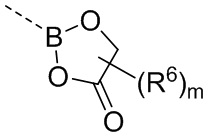 соединения формулы (III-a) являются такими, как определено выше для соединения формулы (III).
соединения формулы (III-a) являются такими, как определено выше для соединения формулы (III).
В другом аспекте в настоящей заявке также предусмотрено соединение формулы (IV) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер,
 ,
,
где кольцо A, n и R1 являются такими, как определено выше для соединения формулы (I);
X выбран из -C(Ra)2-, и Y выбран из -C(Rb)2-; или X выбран из =C(Rc)-, и Y выбран из =C(Rd)-; где каждый из Ra, Rb, Rc и Rd независимо выбран из группы, состоящей из водорода и C1-6алкила, где C1-6алкил необязательно замещен одним или более -COOH; или Ra и Rb соединены с образованием 3-6-членного кольца; или Rc и Rd соединены с образованием 3-6-членного кольца.
В некоторых вариантах осуществления структурное звено  соединения формулы (IV) является таким, как определено выше для соединения формулы (I).
соединения формулы (IV) является таким, как определено выше для соединения формулы (I).
В некоторых вариантах осуществления соединения формулы (IV) каждый из Ra, Rb, Rc и Rd независимо выбран из группы, состоящей из водорода и C1-6алкила, где C1-6алкил необязательно замещен одним или более -COOH; или Rc и Rd соединены с образованием 3-6-членного кольца.
В некоторых вариантах осуществления соединения формулы (IV) каждый из Ra, Rb, Rc и Rd независимо выбран из группы, состоящей из водорода и C1-6алкила; или Ra и Rb соединены с образованием 3-6-членного кольца; или Rc и Rd соединены с образованием 3-6-членного кольца.
В некоторых вариантах осуществления соединения формулы (IV) каждый из Ra и Rb независимо выбран из группы, состоящей из водорода и C1-6алкила; или Rc и Rd соединены с образованием 5-6-членного кольца.
В некоторых вариантах осуществления в соединении формулы (IV) каждый из Ra и Rb независимо выбран из группы, состоящей из водорода и C1-3алкила; или Rc и Rd соединены с образованием фенила.
В некоторых вариантах осуществления в соединении формулы (IV) Ra представляет собой метил, и Rb представляет собой водород; или Rc и Rd соединены с образованием фенила.
В некоторых вариантах осуществления структурное звено  в соединении формулы (IV) выбрано из группы, состоящей из
в соединении формулы (IV) выбрано из группы, состоящей из  и
и  .
.
В другом аспекте в настоящей заявке также предусмотрено соединение формулы (IV-a) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер,
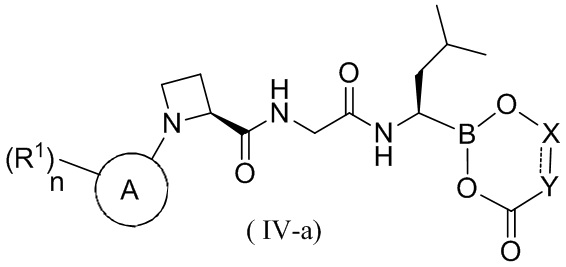 ,
,
где кольцо A, n, R1, X и Y являются такими, как определено выше для соединения формулы (IV).
В некоторых вариантах осуществления структурное звено  соединения формулы (IV-a) является таким, как определено выше для соединения формулы (I).
соединения формулы (IV-a) является таким, как определено выше для соединения формулы (I).
В некоторых вариантах осуществления соединение формулы (II), соединение формулы (III) или соединение формулы (IV), раскрытые в данном документе, представляют собой пролекарство на основе соединения формулы (II-0),
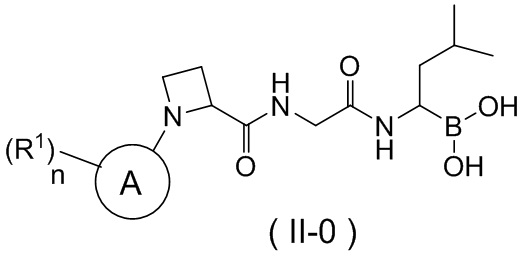 ,
,
где кольцо A, n и R1 являются такими, как определено выше для соединения формулы (I).
В некоторых вариантах осуществления структурное звено  соединения формулы (II-0) является таким, как определено выше для соединения формулы (I).
соединения формулы (II-0) является таким, как определено выше для соединения формулы (I).
В некоторых вариантах осуществления соединение формулы (II-a), соединение формулы (III-a) или соединение формулы (IV-a) согласно настоящей заявке представляют собой пролекарство на основе соединения формулы (II-a-0),
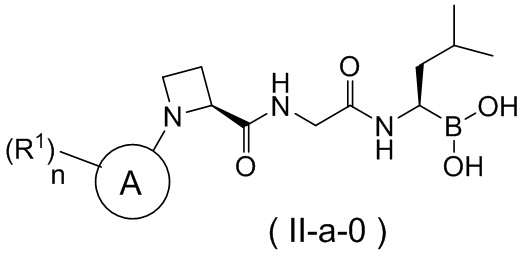 ,
,
где кольцо A, n и R1 являются такими, как определено выше для соединения формулы (I).
В некоторых вариантах осуществления структурное звено  соединения формулы (II-a-0) является таким, как определено выше для соединения формулы (I).
соединения формулы (II-a-0) является таким, как определено выше для соединения формулы (I).
В другом аспекте настоящая заявка также предусматривает соединение, выбранное из группы, состоящей из следующих структурных формул:
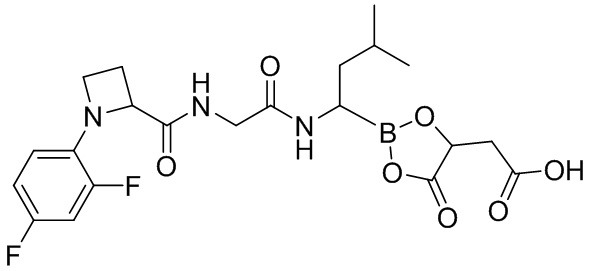

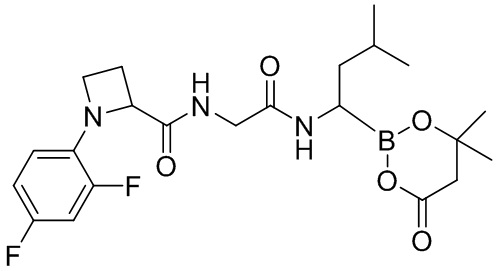
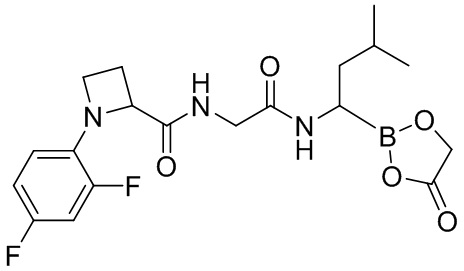




 и
и  ,
,
или его фармацевтически приемлемую соль, его таутомер, его стереоизомер или его геометрический изомер.
В некоторых вариантах осуществления каждое из вышеописанных соединений, раскрытых в данном документе, представляет собой пролекарство на основе следующих соединений:



 или
или 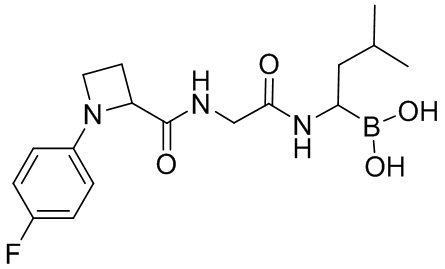 .
.
В другом аспекте настоящая заявка также предусматривает соединение, выбранное из группы, состоящей из следующих структурных формул:
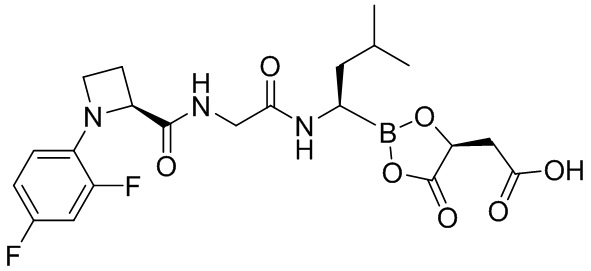
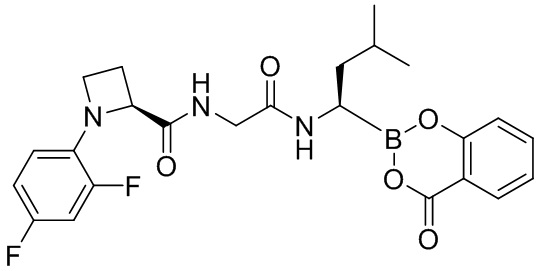
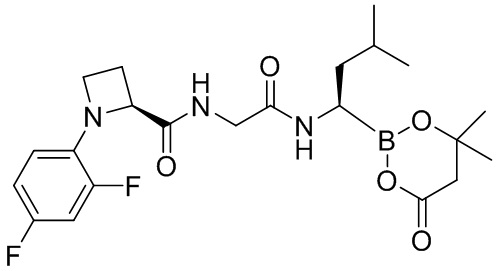
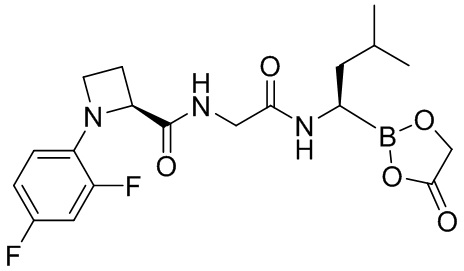
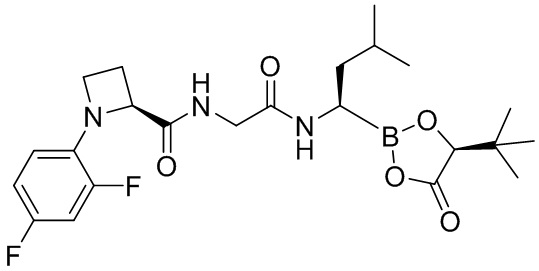

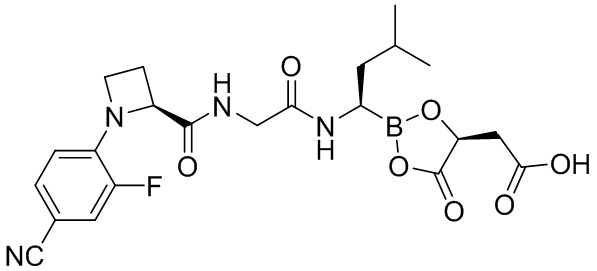

 и
и 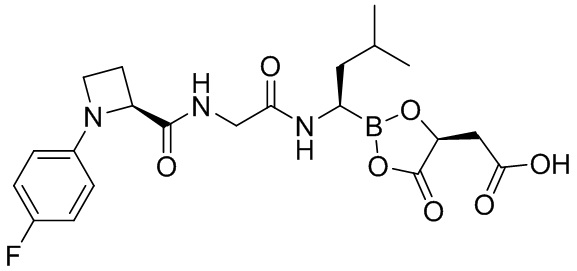 ,
,
или его фармацевтически приемлемую соль, его таутомер или его геометрический изомер.
В некоторых вариантах осуществления каждое из вышеописанных соединений, раскрытых в данном документе, представляет собой пролекарство на основе следующих соединений:
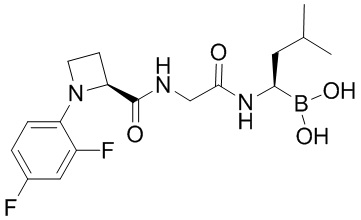
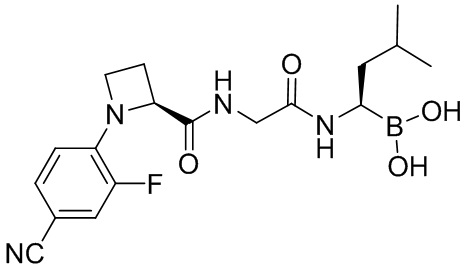
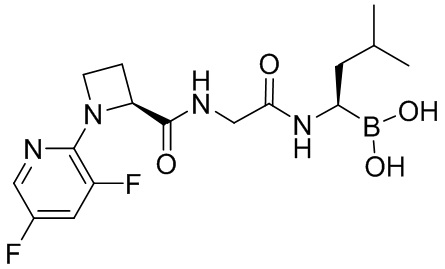
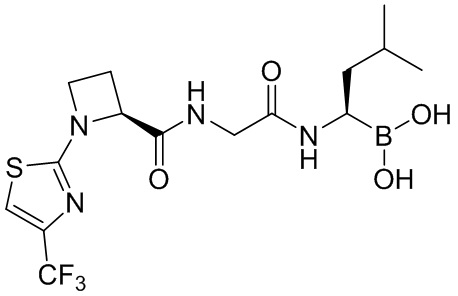 или
или 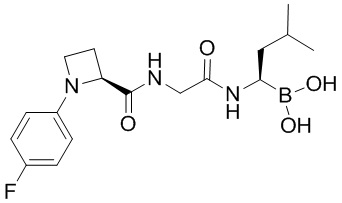 .
.
В другом аспекте настоящая заявка также предусматривает соединение I-1:
 ,
,
или его фармацевтически приемлемую соль, его таутомер или его геометрический изомер.
В другом аспекте в настоящей заявке также предусмотрена фармацевтическая композиция, содержащая соединение формулы (I), или его фармацевтически приемлемую соль, его таутомер, его стереоизомер или его геометрический изомер, В некоторых вариантах осуществления фармацевтическая композиция, раскрытая в данном документе, дополнительно содержит одно или более из фармацевтически приемлемых вспомогательных средств, носителей и разбавителей.
В другом аспекте в настоящей заявке также представлен способ лечения множественной миеломы у млекопитающего, предусматривающий введение млекопитающему, предпочтительно человеку, нуждающемуся в лечении, терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли, его таутомера, его стереоизомера или его геометрического изомера или фармацевтической композиции на его основе.
В другом аспекте настоящая заявка также предусматривает применение соединения формулы (I) или его фармацевтически приемлемой соли, его таутомера, его стереоизомера, или его геометрического изомера, или фармацевтической композиции на его основе, в получении лекарственного препарата для предупреждения или лечения множественной миеломы.
В другом аспекте настоящая заявка также предусматривает применение соединения формулы (I), или его фармацевтически приемлемой соли, его таутомера, его стереоизомера, или его геометрического изомера, или фармацевтической композиции на его основе, для предупреждения или лечения множественной миеломы.
В другом аспекте настоящая заявка также предусматривает соединение формулы (I) или его фармацевтически приемлемую соль, его таутомер, его стереоизомер, или его геометрический изомер, или фармацевтическую композицию на его основе для предупреждения или лечения множественной миеломы.
В другом аспекте настоящая заявка предусматривает кристалл соединения I-1, который имеет превосходные свойства в по меньшей мере одной из следующих характеристик: фармакокинетика, биологическая доступность, гигроскопичность, стабильность, растворимость, чистота, простота получения и т.п.,
 .
.
Настоящая заявка предусматривает кристалл формы I соединения I-1, характеризующийся тем, что на порошковой рентгеновской дифрактограмме (XRPD) с применением Cu-Kα-излучения кристалл формы I соединения I-1 характеризуется дифракционными пиками при следующих значениях 2θ: приблизительно 6,00, 11,98, 17,88, 20,88 и 21,48. В некоторых вариантах осуществления кристалл формы I соединения I-1 характеризуется дифракционными пиками при следующих значениях 2θ: приблизительно 6,00, 8,90, 11,98, 17,88, 20,88, 21,48, 24,60 и 25,44. В некоторых вариантах осуществления кристалл формы I соединения I-1 характеризуется дифракционными пиками при следующих значениях 2θ: приблизительно 6,00, 8,90, 11,98, 13,70, 16,50, 17,88, 20,88, 21,48, 24,60 и 25,44. В некоторых вариантах осуществления кристалл формы I соединения I-1 характеризуется дифракционными пиками при следующих значениях 2θ: приблизительно 6,00, 8,90, 11,98, 12,80, 13,70, 16,50, 17,88, 20,88, 21,48, 24,60, 25,44, 27,66, 28,94 и 30,25.
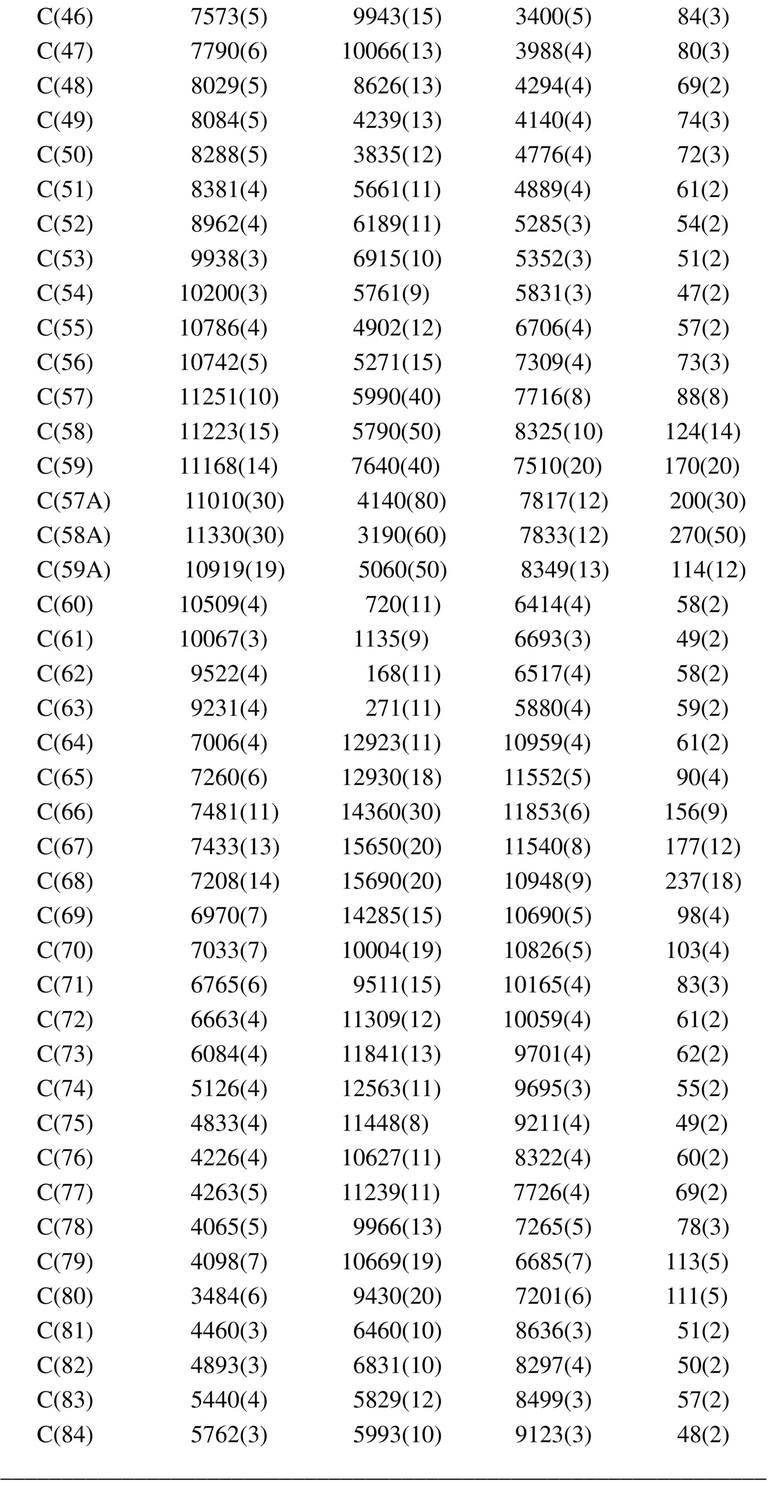
Кроме того, на порошковой рентгеновской дифрактограмме кристалла формы I соединения I-1, раскрытой в данном документе, полученной с применением Cu-Kα-излучения, положения пика и значения относительной интенсивности дифракционных пиков являются такими, как показано ниже в таблице 1.
Таблица 1. Положения пиков и относительные интенсивности дифракционного пика на порошковой рентгеновской дифрактограмме кристалла формы I соединения I-1.
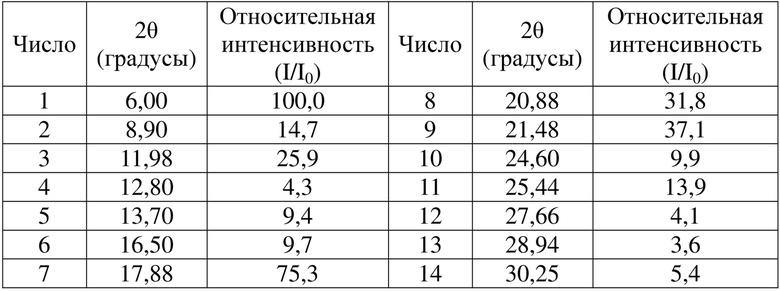
В конкретном варианте осуществления дифрактограмма XRPD кристалла формы II соединения I-1, представленного в данном документе, показана на фиг. 1.
В конкретном варианте осуществления настоящая заявка предусматривает кристалл формы I соединения I-1, где кристалл характеризуется следующим: кристаллическая система: моноклинная система; пространственная группа: P 21; параметры ячеек: a = 24,4220(5) Å, b = 8,4507(2) Å, c = 24,4590(5) Å, α = 90 градусов, β = 107,683(1) градусы, γ = 90 градусов; Z = 8.
В настоящей заявке измерительный прибор для порошковой рентгеновской дифракционной спектрометрии представляет собой рентгеновский дифрактометр Bruker D8 Advance, и условиями и способами являются: рентгеновская трубка: Cu, Kα, (λ = 1,54056 Ǻ), 40 кВ, 40 мА; щель: 0,60 мм/10,50 мм/7,10 мм; диапазон сканирования: 3-40° или 4-40°, время [с]: 0,12; длина шага: 0,02°.
Для любой конкретной кристаллической формы относительные интенсивности дифракционных пиков могут изменяться из-за предпочтительной ориентации, вызванной такими факторами, как, например, строение кристалла, что также хорошо известно в области кристаллографии. В случае влияния предпочтительной ориентации интенсивность пика может изменяться, но положение дифракционного пика кристаллической формы изменяться не может. Кроме того, для любой конкретной кристаллической формы могут иметь место небольшие погрешности в расположении пиков, что также хорошо известно в области кристаллографии. Например, положение пика может смещаться вследствие изменения температуры, изменения положения образца или калибровки измерительного прибора во время анализа образца, при этом погрешность измерения значения угла 2θ в некоторых случаях составляет приблизительно ±0,2 градуса и, следовательно, специалистам в данной области техники хорошо известно, что данную погрешность следует учитывать при определении каждой кристаллической структуры.
В другом аспекте в настоящей заявке представлен способ получения кристалла формы I соединения I-1, предусматривающий стадию осаждения соединения I-1 из растворителя, где растворитель выбран из одной или более групп, состоящих из изопропилацетата, метанола, этанола, изопропанола, н-бутанола, ацетонитрила, ацетона, этилацетата, метил-трет-бутилового эфира, н-гептана и 2-метилтетрагидрофурана.
В некоторых вариантах осуществления растворитель представляет собой изопропилацетат.
В некоторых вариантах осуществления в настоящей заявке представлен способ получения кристалла формы I соединения I-1, предусматривающий следующие стадии:
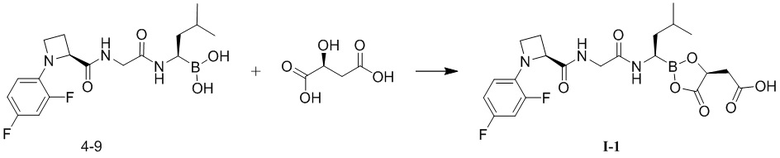 ,
,
1) обеспечение реакции L-яблочной кислоты с соединением 4-9 в изопропилацетате с получением соединения I-1; и
2) осаждение твердого вещества.
В некоторых вариантах осуществления стадия 1) представляет собой: растворение L-яблочной кислоты в изопропилацетате, растворение соединения 4-9 в изопропилацетате, и смешивание двух растворов.
В некоторых вариантах осуществления за стадией 2) следует отделение твердого вещества, осажденного на стадии 2). В некоторых конкретных вариантах осуществления после того, как твердое осажденное вещество на стадии 2) отделяют, отделенное твердое вещество высушивают.
В еще одном аспекте настоящая заявка предусматривает кристаллическую композицию, содержащую кристалл соединения I-1, где кристалл соединения I-1 составляет более 50%, предпочтительно более 80%, более предпочтительно более 90% и наиболее предпочтительно более 95% веса кристаллической композиции, и где кристалл соединения I-1 представляет собой кристалл формы I соединения I-1.
В еще одном аспекте настоящая заявка предусматривает фармацевтическую композицию, содержащую терапевтически эффективное количество кристалла соединения I-1, описанного в данном документе, или его кристаллической композиции, где кристалл соединения I-1 представляет собой кристалл формы I соединения I-1. Фармацевтическая композиция, раскрытая в данном документе, может содержать фармацевтически приемлемое вспомогательное вещество или не содержит его. Кроме того, фармацевтическая композиция, раскрытая в данном документе, может дополнительно содержать одно или более других терапевтических средств.
В другом аспекте в настоящей заявке также представлен способ лечения множественной миеломы у млекопитающего, предусматривающий введение млекопитающему, предпочтительно человеку, нуждающемуся в лечении, терапевтически эффективного количества кристалла соединения I-1, или его кристаллической композиции, или фармацевтической композиции на его основе, где кристалл соединения I-1 представляет собой кристалл формы I соединения I-1.
В другом аспекте настоящая заявка дополнительно предусматривает применение кристалла соединения I-1, или его кристаллической композиции, или фармацевтической композиции на его основе в получении лекарственного препарата для предупреждения или лечения множественной миеломы, где кристалл соединения I-1 представляет собой кристалл формы I соединения I-1.
В другом аспекте настоящая заявка также предусматривает применение кристалла соединения I-1, или его кристаллической композиции, или фармацевтический композиции на его основе в предупреждении или лечении множественной миеломы, где кристалл соединения I-1 представляет собой кристалл формы I соединения I-1.
В другом аспекте в настоящей заявке также представлен кристалл соединения I-1, или его кристаллическая композиция, или фармацевтическая композиция на его основе для предупреждения или лечения множественной миеломы, где кристалл соединения I-1 представляет собой кристалл формы I соединения I-1.
ОПРЕДЕЛЕНИЯ
Если не указано иное, следующие термины, применяемые в настоящей заявке, имеют следующие значения. Конкретный термин, если конкретно не указано другое, не следует считать неопределенным или неясным, а следует понимать в соответствии с его общепринятым значением в данной области. При ссылке на торговое наименование, оно относится к его соответствующему коммерческому продукту или его активному ингредиенту.
Пунктирная линия ( ) в структурном звене или группе в настоящей заявке обозначает ковалентную связь.
) в структурном звене или группе в настоящей заявке обозначает ковалентную связь.
Термин «замещенный» означает, что любой один или более атомов водорода при конкретном атоме замещены заместителями при условии, что валентность конкретного атома является нормальной, и полученное соединение является стабильным. Если заместитель представляет собой оксогруппу (т.е. =O), то это означает, что два атома водорода замещены, и оксогруппа не присутствует в ароматической группе.
Термины «необязательный» или «необязательно» означают, что описанное далее событие или обстоятельство может происходить или может не происходить. Описание включает случаи, при которых событие или обстоятельство возникает, и случаи, при которых не возникает. Например, фраза «этил представляет собой необязательно замещенный галоген» означает, что этил может быть незамещенным (-CH2CH3), монозамещенным (например, -CH2CH2F), полизамещенным (например, -CHFCH2F, -CH2CHF2 и т.п.) или полностью замещенным (-CF2CF3). Специалистам в данной области будет понятно, что для любых групп, содержащих один или более заместителей, не будут осуществляться какие-либо замещения или схемы замещения, которые являются пространственно нецелесообразными и/или невозможными с точки зрения синтеза.
Если какая-либо переменная (например, R1) встречается более одного раза в составе или структуре соединения, то определение переменной в каждом случае является независимым. Например, если группа замещена 0-2 R1, то группа может быть необязательно замещена не более чем двумя R1, и определение R1 в каждом случае является независимым. В другом примере каждый из R1 в структурном звене  является независимым, и они могут быть одинаковыми или разными. Кроме того, комбинация заместителей и/или их вариантов допускается, только если комбинация приводит к получению стабильного соединения.
является независимым, и они могут быть одинаковыми или разными. Кроме того, комбинация заместителей и/или их вариантов допускается, только если комбинация приводит к получению стабильного соединения.
«Cm-n» в настоящей заявке означает, что фрагмент содержит целое число атомов углерода в указанном диапазоне m-n. Например, «C1-6» означает, что группа может иметь 1 атом углерода, 2 атома углерода, 3 атома углерода, 4 атома углерода, 5 атомов углерода или 6 атомов углерода.
Термин «галогено» или «галоген» относится к фтору, хлору, брому и йоду.
Термин «амино» относится к группе -NH2.
Термин «алкил» относится к нециклическому углеводородному радикалу с общей формулой CnH2n+1. Алкил может быть линейным или разветвленным. Например, термин «C1-6алкил» относится к алкилу, содержащему 1-6 атомов углерода (например, метилу, этилу, н-пропилу, изопропилу, н-бутилу, изобутилу, втор-бутилу, трет-бутилу, н-пентилу, 1-метилбутилу, 2-метилбутилу, 3-метилбутилу, неопентилу, гексилу, 2-метилпентилу и т. д.).
Термины «гетероциклическое кольцо», «гетероциклил» и «гетероциклическая группа» могут использоваться взаимозаменяемо и относятся к стабильному 3-7-членному моноциклическому или конденсированному 7-10-членному или мостиковому 6-10-членному бициклическому гетероциклическому фрагменту, который является насыщенным или частично ненасыщенным и имеет один или более гетероатомов в дополнение к атому углеродов. Гетероатом может быть выбран из одной или более групп, состоящих из N, S и O. Гетероциклическое кольцо может быть присоединено к боковым группам любого гетероатома или атома углерода с образованием стабильной структуры, и любой из атомов кольца может быть необязательно замещен. Примеры насыщенных или частично ненасыщенных гетероциклилов включают без ограничения тетрагидрофуранил, тетрагидротиенил, пирролидинил, пирролидинoнил, пиперидинил, пирролинил, тетрагидрохинолил, тетрагидроизохинолил, декагидрохинолил, оксазолидинил, пиперазинил, диоксанил, диоксоланил, диазепинил, оксоазепинил, тиазепинил, морфолинил и хинуклидинил.
Термин «циклоалкил» относится к полностью насыщенному углеродному кольцу, находящемуся в форме моноциклической, мостиковой циклической структуры или спироструктуры. Если не указано иное, то углеродное кольцо, как правило, представляет собой 3-10-членное кольцо. Неограничивающие примеры циклоалкила включают без ограничения циклопропил, циклобутил, циклопентил, циклогексил, норборнил(бицикло[2.2.1]гептил), бицикло[2.2.2]октил, адамантил и т.д.
Термин «арил» относится к ароматической моноциклической или конденсированной полициклической группе атомов углерода с сопряженной пи-электронной системой. Например, арил может содержать 6-20 атомов углерода, 6-14 атомов углерода или 6-12 атомов углерода. Неограничивающие примеры арила включают без ограничения фенил, нафтил, антрил, 1,2,3,4-тетрагидронафталин и т.д.
Термин «гетероарил» относится к моноциклической или конденсированной полициклической системе, которая содержит по меньшей мере один атом кольца, выбранный из группы, состоящей из N, O и S, при этом оставшиеся атомы в кольце представляют собой C, и которая содержит по меньшей мере одно ароматическое кольцо. Предпочтительно гетероарил содержит одно 4-8-членное кольцо, в частности, 5-8-членное кольцо, или множество конденсированных колец, содержащих 6-14 атомов кольца, в частности, 6-10 атомов кольца. Неограничивающие примеры гетероарила включают без ограничения пирролил, фуранил, тиенил, имидазолил, оксазолил, пиразолил, пиридинил, пиримидинил, пиразинил, хинолил, изохинолил, тетразолил, триазолил, триазинил, бензофуранил, бензотиенил, индолил, изоиндолил и т.д.
Термин «гетероалкил» представляет собой линейный или разветвленный алкил, который содержит предпочтительно 1-14 атомов углерода, более предпочтительно 1-10 атомов углерода, еще более предпочтительно 1-6 атомов углерода и наиболее предпочтительно 1-3 атома углерода в цепи, где один или более атомов углерода замещены гетероатомом, выбранным из группы, состоящей из S, O и N. Иллюстративный гетероалкил включает алкиловый эфир, вторичный алкиламин и третичный алкиламин, алкиламид, алкилсульфид и т.д., такие как алкокси, алкилтио и алкиламино; если не указано иное, C1-6гетероалкил включает C1-, C2-, C3-, C4-, C5- и C6гетероалкил, например, C1-6алкокси, C1-6алкилтио, C1-6алкиламино.
Термин «алкоксильный» относится к -O-алкилу.
Термин «лечение» означает введение соединения или состава, описанного в данном документе, с целью предотвращения, облегчения или устранения симптомов заболевания или одного или более симптомов, связанных с заболеванием, и включает:
(i) предотвращение возникновения заболевания или болезненного состояния к млекопитающего, в частности, когда такое млекопитающее предрасположено к болезненному состоянию, но еще не диагностировано его наличие;
(ii) подавление заболевания или болезненного состояния, т.е. остановка его развития; и
(iii) облегчение заболевания или болезненного состояния, т.е. вызывание ремиссии.
Термин «терапевтически эффективное количество» относится к количеству соединения, раскрытого в данном документе, для (i) лечения или предупреждения конкретного заболевания, состояния или нарушения; (ii) облегчения, улучшения или устранения одного или более симптомов конкретного заболевания, состояния или нарушения или (iii) предупреждения или замедления начала одного или более симптомов конкретного заболевания, состояния или нарушения, описанных в данном документе. Количество соединения, раскрытого в данном документе, содержащего «терапевтически эффективное количество», изменяется в зависимости от соединения, болезненного состояния и его тяжести, пути введения и возраста млекопитающего, подлежащего лечению, но его обычно могут определить специалисты в данной области, исходя из их собственных знаний и раскрытия настоящей заявки.
Термин «фармацевтически приемлемый» применяется в данном документе для тех соединений, материалов, композиций и/или лекарственных форм, которые, в пределах объема тщательной медицинской оценки, являются подходящими для применения в контакте с тканями человека и животных без чрезмерной токсичности, раздражения, аллергической реакции или других проблем или осложнений, и соизмеримы с приемлемым соотношением польза/риск.
Фармацевтически приемлемая соль, например, может представлять собой соль металла, соль аммония, соль, образованную с органическим основанием, соль, образованную с неорганической кислотой, соль, образованную с органической кислотой, соль, образованную с основной или кислотной аминокислотой и т.д.
Термин «фармацевтическая композиция» относится к смеси, состоящей из одного или более соединений или их фармацевтически приемлемых солей, раскрытых в данном документе, и фармацевтически приемлемого вспомогательного вещества. Фармацевтическая композиция предназначена для облегчения введения соединения в организм.
Термин «фармацевтически приемлемые вспомогательные вещества» относится к тем вспомогательным веществам, которые не вызывают значительного раздражающего воздействия в организме и не ухудшают биологическую активность и свойства активного соединения. Подходящие вспомогательные вещества широко известны специалистам в данной области, например углевод, воск, водорастворимые и/или набухающие в воде полимеры, гидрофильные или гидрофобные материалы, желатин, масло, растворитель, вода.
В настоящей заявке слово «содержат» и его варианты, такие как «содержит» или «содержащий», будут пониматься в открытом, неисключительном смысле, т.е. «включающие без ограничения».
Соединения и промежуточные соединения, раскрытые в данном документе, могут также существовать в различных таутомерных формах, и все такие формы включены в объем настоящей заявки. Термин «таутомер» или «таутомерная форма» относится к структурным изомерам разных энергий, которые являются взаимопревращаемыми при переходе через низкоэнергетический барьер. Например, протонный таутомер (также известный как прототропный таутомер) предусматривает взаимопревращение с помощью переноса протона, такое как изомеризация кето-енола и изомеризация имин-енамина. Конкретный пример протонного таутомера представляет собой имидазольный фрагмент, где протон может переноситься между двумя азотами в кольце. Таутомер включает взаимопревращение с помощью рекомбинации некоторых связывающих электронов.
Если не указано иное, абсолютная конфигурация стереогенного центра представлена посредством сплошной клиновидной связи ( ). Если не указано иное, соединения, раскрытые в данном документе, включают геометрические изомеры как E, так и Z, если они содержат олефиновые двойные связи или другие центры геометрической асимметрии. Подобным образом, все таутомерные формы включены в объем настоящей заявки.
). Если не указано иное, соединения, раскрытые в данном документе, включают геометрические изомеры как E, так и Z, если они содержат олефиновые двойные связи или другие центры геометрической асимметрии. Подобным образом, все таутомерные формы включены в объем настоящей заявки.
Соединения, раскрытые в данном документе, могут существовать в конкретных геометрических изомерных или стереоизомерных формах. Все такие соединения предусмотрены в данном документе, в том числе таутомеры, цис-изомеры и транс-изомеры, (−)- и (+)-энантиомеры, (R)- и (S)-энантиомеры, диастереомеры, (D)-изомеры, (L)-изомеры и их рацемические смеси и другие смеси, такие как обогащенные энантиомерами или диастереомерами смеси, все из которых включены в объем настоящей заявки. Заместители, такие как алкил, могут иметь дополнительный асимметричный атом углерода. Все такие изомеры и их смеси включены в объем настоящей заявки.
Настоящая заявка также содержит меченные изотопом соединения, которые идентичны тем, что перечислены в данном документе, но один или более атомов которых заменены атомом, имеющим атомную массу или массовое число, отличные от атомной массы или массового числа, которые обычно встречаются в природе. Примеры изотопов, которые могут быть включены в соединения, раскрытые в данном документе, включают изотопы водорода, углерода, азота, кислорода, фосфора, серы, фтора, йода и хлора, такие как 2H, 3H, 11C, 13C, 14C, 13N, 15N, 15O, 17O, 18O, 31P, 32P, 35S, 18F, 123I, 125I и 36Cl.
Определенные меченные изотопом соединения, раскрытые в данном документе (например, соединения, меченные с помощью 3H и 14C), могут использоваться в анализе распределения соединений и/или субстрата в тканях. Тритированные изотопы (т.е. 3H) и изотопы углерода-14 (т.е. 14C) особенно предпочтительны из-за простоты их получения и обнаружения. Позитронно-активные изотопы, такие как 15O, 13N, 11C и 18F, могут использоваться в исследованиях позитронно-эмиссионной томографии (PET) с целью определения заполненности субстрата. Меченные изотопом соединения, раскрытые в данном документе, как правило, могут быть получены с помощью следующих процедур, аналогичных тем, которые раскрытые на схемах и/или в нижеприведенных примерах одновременно с замещением неизотопно меченного реагента на меченный изотопом реагент.
Кроме того, замещение с помощью более тяжелых изотопов, таких как дейтерий (т.е. 2H), может обеспечить определенные терапевтические преимущества (например, увеличенный период полувыведения in vivo или снижение требований к дозировке), связанные с более высокой метаболической стабильностью, и, следовательно, может быть предпочтительно при некоторых обстоятельствах, в которых замещение дейтерием может быть частичным или полным, при этом частичное замещение дейтерием относится к замещению по меньшей мере одного водорода по меньшей мере одним дейтерием.
Соединение, раскрытое в данном документе, может быть асимметричным, например, иметь один или более стереоизомеров. Если не указано иное, в настоящую заявку включены все стереоизомеры, такие как энантиомеры и диастереомеры. Соединение с асимметрическими атомами углерода, раскрытые в данном документе, может быть выделено в оптически чистой форме или рацемической форме. Оптически чистая форма может быть выделена из рацемической смеси или может быть синтезирована с применением хирального исходного материала или хирального реагента.
Фармацевтическую композицию, раскрытую в данном документе, можно получать путем объединения соединения, раскрытого в данном документе, с подходящим фармацевтически приемлемым вспомогательным веществом, и ее можно составлять, например, в виде твердого вещества, полутвердого вещества, жидкости или газового состава, например, в виде таблетки, пилюли, капсулы, порошка, гранулы, мази, эмульсии, суспензии, суппозитория, инъекции, средства для ингаляции, геля, микросферы, аерозоля и т.д.
Типичные пути введения соединения или его фармацевтически приемлемой соли или фармацевтической композиции на его основе, раскрытых в данном документе, включают без ограничения пероральный, ректальный, местный, ингаляционный, парентеральный, сублингвальный, интравагинальный, интраназальный, интраокулярный, интраперитонеальный, внутримышечный, подкожный, внутривенный пути введение и т.д.
Фармацевтическая композиция, раскрытая в данном документе, может быть изготовлена с помощью способов, широко известных в уровне техники, таких как традиционное смешивание, растворение, гранулирование, дражирование, измельчение, эмульгирование, лиофилизирование и т.д.
В некоторых вариантах осуществления фармацевтическая композиция находится в пероральной форме. В случае перорального введения фармацевтическую композицию можно составлять путем смешивания активных соединений с фармацевтически приемлемым вспомогательным веществом, широко известным в уровне техники. Такие вспомогательные вещества могут обеспечивать возможность составления соединений в соответствии с настоящей заявкой в виде таблеток, пилюль, пастилок, драже, капсул, жидкостей, гелей, взвесей, суспензий и т.п. для перорального введения пациентам.
Твердая пероральная фармацевтическая композиция может быть получена с помощью традиционного смешивания, наполнения или таблетирования. Например, ее можно получать с помощью следующего способа: смешивание активного соединения с твердыми вспомогательными веществами, необязательное размалывание полученной смеси, добавление при необходимости дополнительных пригодных вспомогательных веществ, а затем формирование смеси в гранулы с получением ядер таблеток или ядер драже. Подходящие вспомогательные вещества включают без ограничения связующие, разбавители, разрыхлители, смазочные средства, вещества, способствующие скольжению, подсластители или ароматизирующие средства и т.д.
Фармацевтическая композиция может также быть пригодной для парентерального введения, например, в виде стерильных растворов, суспензий или лиофилизированных продуктов в подходящей единичной лекарственной форме.
Во всех способах введения соединения общей формулы (I), описанного в данном документе, суточная доза введения составляет от 0,01 мг/кг до 200 мг/кг веса тела, вводимых в форме однократных или разделенных доз.
Соединения, раскрытые в данном документе, могут быть получены с помощью разнообразных способов синтеза, хорошо известных специалистам в данной области, в том числе конкретных вариантов осуществления, перечисленных ниже, вариантов осуществления, полученных путем их комбинирования с другими способами химического синтеза, и их эквивалентов, известных специалистам в данной области техники. Предпочтительные варианты осуществления включают без ограничения примеры, раскрытые в данном документе.
Химические реакции согласно вариантам осуществления, раскрытым в данном документе, проводятся в подходящем растворителе, который должен быть пригодным для химических реакций в настоящей заявке, а также с реагентами и материалами, необходимыми для химических реакций. Иногда для того, чтобы получить соединения по настоящему изобретению, специалисту в данной области необходимо модифицировать или выбрать стадии синтеза или схему реакций на основе представленных вариантов осуществления.
Ключевым аспектом при планировании пути синтеза в данной области является выбор соответствующих защитных групп для реакционноспособных функциональных групп (например, аминогрупп в настоящем изобретении). Например, можно ссылаться на Greene's Protective Groups in Organic Synthesis (4th Ed.) Hoboken, New Jersey: John Wiley & Sons, Inc. Все ссылочные материалы, цитируемые в данном документе, включены посредством ссылки во всей своей полноте.
В некоторых вариантах осуществления соединение формулы (I), раскрытое в данном документе, может быть получено специалистом в данной области с помощью следующего общего пути и с применением способов, известных в уровне техники:
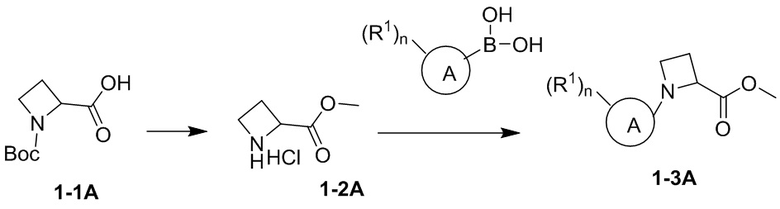


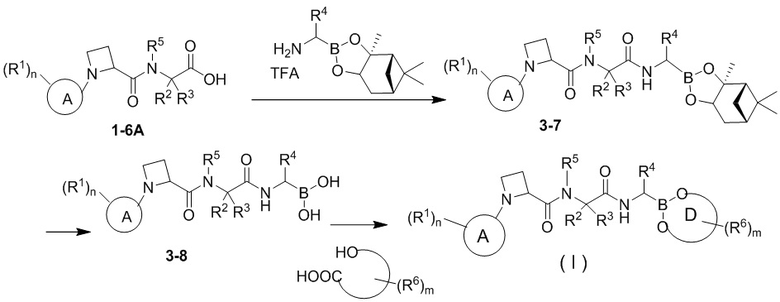 .
.
В данной заявке применяют следующие сокращения:
TBTU представляет собой тетрафторборат O-бензoтриазол-N,N,N',N'-тетраметилурония; TMSCl представляет собой триметилхлорсилан; Cu(OAc)2 представляет собой ацетат меди; TEA представляет собой триэтиламин; DMF представляет собой N,N-диметилформамид; DIEA/DIPEA представляет собой N,N-диизопропилэтиламин; HPLC представляет собой высокоэффективную жидкостную хроматографию; SFC представляет собой сверхкритическую флюидную хроматографию; DMSO представляет собой диметилсульфоксид; MeOH представляет собой метанол; THF представляет собой тетрагидрофуран; DCM представляет собой дихлорметан; Cy представляет собой циклогексил; и TFA представляет собой трифторуксусную кислоту.
Для лучшего понимания в настоящей заявке дополнительно описаны следующие примеры, которые, однако, не предназначены для ограничения объема настоящей заявки. Все реагенты, применяемые в настоящей заявке, являются коммерчески доступными и их можно применять без дополнительной очистки.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
На фиг. 1 представлена дифрактограмма XRPD кристалла формы I соединения I-1, полученная в примере 4 согласно настоящей заявке; и
на фиг. 2 представлена дифрактограмма XRPD кристалла формы I соединение I-1, полученная методом расчета.
ПОДРОБНОЕ ОПИСАНИЕ
Пример 1. Синтез соединения 1-9

Стадия 1. Синтез соединения 1-2
В смешанный раствор соединения 1-1 (10,00 г) и метанола (100,00 мл) добавляли TMSCl (27 г) при 0°C и реакционную смесь перемешивали при комнатной температуре в течение 12 часов в атмосфере азота. Реакционную смесь концентрировали при пониженном давлении с получением соединения 1-2. Соединение 1-2: 1H ЯМР: (400 МГц, метанол-d4) δ 5,04-5,17 (m, 1H), 4,11 (q, J=9,12 Гц, 1H), 3,91 (dt, J=5,90, 9,98 Гц, 1H), 3,84 (s, 3H), 2,59-2,86 (m, 2H).
Стадия 2. Синтез соединения 1-3
В раствор 4-фторбензолбороновой кислоты (7 г) в ацетонитриле (80,00 мл) добавляли соединение 1-2 (2,53 г), молекулярное сито 4Å (2,00 г), Cu(OAc)2 (3,33 г) и TEA (6,75 г) при комнатной температуре. Реакционную смесь нагревали до 80°C и затем перемешивали в течение 12 часов. Реакционную смесь фильтровали и фильтрат концентрировали. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле (подвижная фаза: петролейный эфир:этилацетат = 3:1) с получением соединения 1-3. Соединение 1-3: 1H ЯМР: (400 МГц, хлороформ-d) δ 6,87-7,02 (m, 2H), 6,41-6,54 (m, 2H), 4,45 (dd, J=7,65, 8,66 Гц, 1H), 4,00 (ddd, J=3,89, 6,71, 8,47 Гц, 1H), 3,82 (s, 3H), 3,58-3,75 (m, 1H), 2,46-2,75 (m, 2H). MS (ESI) масса/заряд: 209,9 [M+1].
Стадия 3. Синтез соединения 1-4
В смешанный раствор соединения 1-3 (700,00 мг) в метаноле (3,00 мл), тетрагидрофуране (3,00 мл) и воде (1,50 мл) добавляли LiOH·H2O (702,83 мг) на ледяной бане. Реакционную смесь перемешивали при температуре от 0°C до комнатной температуры в течение 3 часов и затем доводили до pH = 6 с помощью 1 моль/л хлористоводородной кислоты. Смешанный раствор концентрировали и экстрагировали этилацетатом и органические фазы объединяли и концентрировали для удаления растворителя с получением соединения 1-4, которое применяли непосредственно на следующей стадии. Соединение 1-4: MS (ESI) масса/заряд: 195,9 [M+1].
Стадия 4. Синтез соединения 1-5
В раствор соединения 1-4 (150,00 мг) в DMF (3,00 мл) добавляли гидрохлорид метилового сложного эфира глицина (115,78 мг), TBTU (296,09 мг) и DIEA (397,27 мг, 0,53 мл) при −10°C. Реакционную смесь перемешивали при −10°C – 0°C в течение 3 часов и затем добавляли насыщенный водный раствор хлорида аммония (10 мл). Водную фазу экстрагировали этилацетатом. Органические фазы объединяли и промывали насыщенным солевым раствором, высушивали над безводным сульфатом натрия, фильтровали и концентрировали с удалением растворителя и полученный продукт очищали с помощью колоночной хроматографии на силикагеле (подвижная фаза: петролейный эфир:этилацетат = 1:1) с получением соединения 1-5. Соединение 1-5: 1H ЯМР: (400 МГц, хлороформ-d) δ 7,41 (br s, 1H), 6,90-7,04 (m, 2H), 6,44-6,57 (m, 2H), 4,28-4,37 (m, 1H), 4,11 (dd, J=5,90, 8,66 Гц, 2H), 3,98 (ddd, J=3,39, 6,90, 8,53 Гц, 1H), 3,66-3,80 (m, 4H), 2,45-2,69 (m, 2H). MS (ESI) масса/заряд: 266,9 [M+1].
Стадия 5. Синтез соединения 1-6
В смешанный раствор соединения 1-5 (160,00 мг) в THF (2,00 мл), MeOH (2,00 мл) и H2O (1,00 мл) добавляли LiOH⋅H2O (126,07 мг). Реакционную смесь перемешивали при температуре от 0°C до комнатной температуры в течение 12 часов и затем доводили до pH = 3 с помощью 1 моль/л хлористоводородной кислоты. Смешанный раствор концентрировали и экстрагировали этилацетатом. Органические фазы объединяли и концентрировали для удаления растворителя с получением соединения 1-6, которое применяли непосредственно на следующей стадии. Соединение 1-6: MS (ESI) масса/заряд: 252,9 [M+1].
Стадия 6. Синтез соединения 1-8
В раствор соединения 1-6 (150,0 мг) в DMF (5,00 мл) добавляли соединение 1-7 (178,10 мг), TBTU (229,12 мг) и DIEA (307,42 мг, 415,43 мкл) при −10°C. Реакционную смесь перемешивали при −10°C – 0°C в течение 2 часов и затем добавляли воду (5 мл). Водную фазу экстрагировали этилацетатом и органические фазы объединяли и промывали насыщенным солевым раствором, высушивали над безводным сульфатом натрия, фильтровали и концентрировали для удаления растворителя с получением соединения 1-8. Соединение 1-8: MS (ESI) масса/заряд: 448,1 [M+1].
Стадия 7. Синтез соединения 1-9
В раствор соединения 1-8 (260,00 мг) в метаноле (5,00 мл) добавляли изобутилбороновую кислоту (414,73 мг) и водный раствор HCl (1 моль/л, 41,55 мкл) на ледяной бане. Реакционную смесь нагревали до комнатной температуры и затем перемешивали в течение 3 часов. Реакционную смесь концентрировали при пониженном давлении с получением неочищенного продукта, который очищали с помощью препаративной HPLC и затем разделяли с помощью SFC с получением соединения 1-9. Соединение 1-9: 1H ЯМР (400 МГц, метанол-d4) δ 6,76-6,93 (m, 2H), 6,63 (br d, J=4,52 Гц, 2H), 4,59 (br s, 5H), 4,08 (br d, J=10,29 Гц, 1H), 2,73 (br s, 1H), 2,07-2,40 (m, 2H), 1,52-1,75 (m, 1H), 1,31 (br d, J=16,81 Гц, 2H), 0,80-0,97 (m, 6H). MS (ESI) масса/заряд: (M-17) 347,9.
Условия разделения с помощью препаративной HPLC были следующими:
колонка для хроматографии: Phenomenex Synergi C18 150 × 30 мм × 4 мкм;
подвижная фаза: A: вода (0,225% муравьиной кислоты), B: метанол;
градиент элюирования: B%: от 55% до 85%;
время выхода пика: 10 мин.
Условия разделения с помощью SFC были следующими:
колонка для хроматографии: AD (250 мм × 30 мм, 5 мм);
подвижная фаза: A: диоксид углерода, B: метанол;
градиент элюирования: B%: от 20% до 20%;
расход: 50 мл/мин;
Последовательность выхода пиков – второй пик, появляющийся при высокоэффективной хиральной жидкостной колоночной хроматографии.
Пример 2. Синтез соединения 2-8
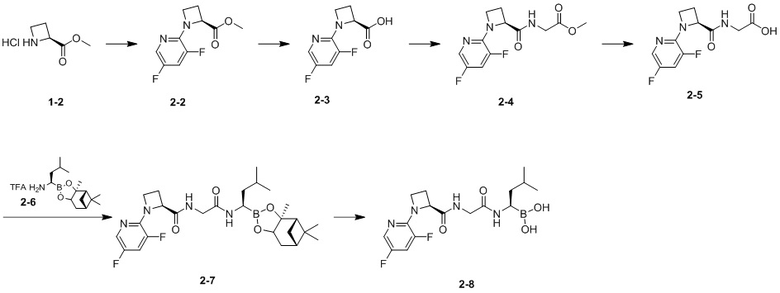
Стадия 1. Синтез соединения 2-2
В раствор соединения 1-2 (173,15 мг) и 2,3,5-трифторпиридина (0,1 г) в DMSO (10 мл) добавляли K3PO4 (319,03 мг) при комнатной температуре. Реакционную смесь нагревали до 120°C и перемешивали в течение 48 часов. Затем реакционный раствор переносили, разбавляли водой (10 мл) и экстрагировали этилацетатом и органические фазы объединяли и промывали насыщенным солевым раствором, высушивали над безводным сульфатом натрия, фильтровали и концентрировали с удалением растворителя. Остаток очищали с помощью колоночной хроматографии на силикагеле (подвижная фаза: петролейный эфир:этилацетат = 5:1) с получением соединения 2-2. Соединение 2-2: 1H ЯМР (400 МГц, хлороформ-d) δ 7,87 (d, J=2,26 Гц, 1H), 7,06 (ddd, J=2,38, 8,09, 10,85 Гц, 1H), 4,83-4,93 (m, 1H), 4,20-4,31 (m, 1H), 3,98-4,09 (m, 1H), 3,74-3,84 (m, 3H), 2,67 (dtd, J=5,14, 8,94, 11,11 Гц, 1H), 2,49 (tdd, J=6,68, 8,78, 11,23 Гц, 1H). MS (ESI) масса/заряд: 228,9 [M+1].
Стадия 2. Синтез соединения 2-3
В смешанный раствор соединения 2-2 (280,00 мг) в MeOH (1,00 мл), THF (1,00 мл) и H2O (0,50 мл) добавляли LiOH⋅H2O (257,43 мг) при 0°C. Реакционную смесь перемешивали при комнатной температуре в течение 1 часа и затем доводили pH до 6-7 с помощью 1 моль/л хлористоводородной кислоты и смесь концентрировали с получением соединения 2-3, которое применяли непосредственно на следующей стадии. Соединение 2-3: MS (ESI) масса/заряд: 214,9 [M+1].
Стадия 3. Синтез соединения 2-4
В раствор соединения 2-3 (0,3 г) в DCM (10 мл) добавляли гидрохлорид метилового сложного эфира глицина (211,05 мг), TBTU (539,71 мг) и DIPEA (724,14 мг) при −10°C. Реакционную смесь перемешивали при −10°C – 0°C в течение 3 часов и затем добавляли воду (10 мл). Водную фазу экстрагировали дихлорметаном и органические фазы объединяли и промывали насыщенным солевым раствором, высушивали над безводным сульфатом натрия, фильтровали и концентрировали с удалением растворителя и полученный продукт очищали с помощью колоночной хроматографии на силикагеле (подвижная фаза: петролейный эфир:этилацетат = 1:1) с получением соединения 2-4. Соединение 2-4: 1H ЯМР (400 МГц, хлороформ-d) δ 8,03 (s, 1H), 7,92 (d, J=2,26 Гц, 1H), 7,13 (ddd, J=2,38, 7,91, 10,79 Гц, 1H), 4,85 (t, J=8,66 Гц, 1H), 4,18 (br d, J=5,77 Гц, 1H), 4,00-4,06 (m, 1H), 3,76 (s, 3H), 2,66-2,78 (m, 1H), 2,49-2,63 (m, 1H). MS (ESI) масса/заряд: 285,9 [M+1].
Стадия 4. Синтез соединения 2-5
В смешанный раствор соединения 2-4 (0,45 г) в THF (2,00 мл), воде (1,00 мл) и MeOH (2,00 мл) добавляли LiOH⋅H2O (330,98 мл) при 0°C и реакционную смесь перемешивали при комнатной температуре в течение 2 часов и затем доводили до pH = 6 или близко к нему с помощью 1 моль/л разбавленной хлористоводородной кислоты. Смешанный раствор концентрировали и экстрагировали этилацетатом. Органические фазы объединяли и концентрировали для удаления растворителя с получением соединения 2-5, которое применяли непосредственно на следующей стадии. Соединение 2-5: MS (ESI) масса/заряд: 271,9 [M+1].
Стадия 5. Синтез соединения 2-7
В раствор соединения 2-5 (0,3 г) в DCM (4,00 мл) добавляли соединение 2-6 (503,35 мг), TBTU (426,18 мг) и DIPEA (314,50 мг, 423,85 мг) при −10°C. Реакционную смесь перемешивали при −10°C – 20°C в течение 2 часов и затем добавляли воду (10 мл). Водную фазу экстрагировали этилацетатом и органические фазы объединяли и промывали насыщенным солевым раствором, высушивали над безводным сульфатом натрия, фильтровали и концентрировали для удаления растворителя с получением соединения 2-7. Соединение 2-7: MS (ESI) масса/заряд: 519,1 [M+1].
Стадия 6. Синтез соединения 2-8
В раствор соединения 2-7 (0,45 г) в MeOH (3,00 мл) добавляли н-гексан (4,00 мл), изобутилбороновую кислоту (619,42 мг) и водный раствор HCl (1 моль/л, 1,74 мл) при 0°C. Реакционную смесь перемешивали при 0°C – 25°C в течение 12 часов и затем реакционный раствор подвергали разделению жидкостей и слой метанола доводили до pH = 5-6 с помощью 1 моль/л раствора NaHCO3. Затем проводили разделение с помощью препаративной HPLC с получением соединения 2-8. Соединение 2-8: 1H ЯМР (400 МГц, метанол-d4) δ 7,89 (br s, 1H), 7,43 (br t, J=9,54 Гц, 1H), 4,78-4,83 (m, 1H), 3,96-4,24 (m, 4H), 2,74 (br s, 1H), 2,63 (br d, J=7,03 Гц, 1H), 2,46-2,58 (m, 1H), 1,65 (br d, J=6,02 Гц, 1H), 1,35 (br t, J=6,90 Гц, 2H), 0,92 (br d, J=5,77 Гц, 6H). MS (ESI) масса/заряд: 367,1 [M-17].
Условия разделения с помощью HPLC для соединения 2-8:
колонка для хроматографии: Xtimate C18 150 × 25 мм × 5 мкм;
подвижная фаза: A: вода (содержащая 0,225% FA), B: метанол;
градиент элюирования: B%: от 55% до 85%;
при высокоэффективной жидкостной колоночной хроматографии время удерживания составляет 9,5 мин.
Соединение 2-9 синтезировали с помощью такого же способа, как в примере 2, за исключением того, что применяли соединение a вместо 2,3,5-трифторпиридина на стадии 1 примера 2; данные ядерного магнитного резонанса (ЯМР), масс-спектрометрии (MS) и условия разделения с помощью HPLC для соединения 2-9 показаны в таблице 2 ниже.
Таблица 2

Пример 3. Синтез соединения 3-7
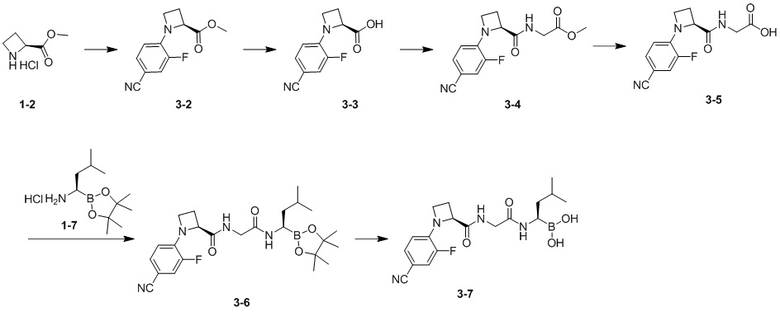
В соответствии с процедурой получения на стадии 1 – стадии 4 примера 2 получали соединение 3-5.
Стадия 1. Синтез соединения 3-6
В раствор соединения 3-5 (300,0 мг) в DMF (5,00 мл) добавляли соединение 1-7 (324,08 мг), TBTU (416,91 мг) и DIEA (559,39 мг, 753,90 мкл) при −10°C. Реакционную смесь перемешивали при −10°C – 0°C в течение 0,5 часа и затем добавляли воду (5 мл). Водную фазу экстрагировали этилацетатом и органические фазы объединяли и промывали насыщенным солевым раствором, высушивали над безводным сульфатом натрия, фильтровали и концентрировали для удаления растворителя с получением соединения 3-6. Соединение 3-6: MS (ESI) масса/заряд: 473,0 [M+1].
Стадия 2. Синтез соединения 3-7
В раствор соединения 3-6 (500,00 мг) в метаноле (5,00 мл) добавляли изобутилбороновую кислоту (755,34 мг) и водный раствор HCl (1 моль/л, 2,12 мл) на ледяной бане. Реакционную смесь нагревали до комнатной температуры и затем перемешивали в течение 3 часов. Реакционную смесь концентрировали при пониженном давлении и затем очищали с помощью препаративной HPLC с последующим разделением с помощью SFC с получением соединения 3-7. Соединение 3-7: 1H ЯМР (400 МГц, метанол-d4) δ 7,28-7,44 (m, 2H), 6,64 (t, J=8,78 Гц, 1H), 4,73-4,80 (m, 2H), 3,96-4,32 (m, 4H), 2,62-2,81 (m, 2H), 2,38-2,57 (m, 1H), 1,64 (qd, J=6,86, 13,55 Гц, 1H), 1,23-1,43 (m, 2H), 0,93 (d, J=6,53 Гц, 6H). MS (ESI) масса/заряд: (M-17) 373,0.
Условия разделения с помощью препаративной HPLC были следующими:
колонка для хроматографии: Xtimate C18 150 × 25 мм × 5 мкм;
подвижная фаза: A: вода (0,225% муравьиной кислоты), B: ацетонитрил;
градиент элюирования: B%: от 46% до 76%;
время выхода пика: 13 мин.
Условия разделения с помощью SFC были следующими:
колонка для хроматографии: AD (250 мм × 30 мм, 5 мм);
подвижная фаза: A: диоксид углерода, B: этанол;
градиент элюирования: B%: от 15% до 15%;
расход: 50 мл/мин;
Последовательность выхода пиков – второй пик, появляющийся при высокоэффективной хиральной жидкостной колоночной хроматографии.
Пример 4. Синтез соединения I-1

Стадия 1. Синтез соединения 4-3
Добавляли N,N-диизопропилэтиламин (22,02 г) в раствор на основе ацетонитрила (200 мл), содержащий соединение 4-1 (10 г) и соединение 4-2 (20,13 г) при комнатной температуре. Реакционную смесь перемешивали при 100°C в течение 16 часов, затем охлаждали до комнатной температуры и затем добавляли в этилацетат. Органическую фазу промывали водой и насыщенным солевым раствором и затем органическую фазу высушивали над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали с удалением растворителя и остаток очищали с помощью колоночной хроматографии на силикагеле (подвижная фаза: петролейный эфир:этилацетат = 10:1) с получением соединения 4-3. Соединение 4-3: MS (ESI) масса/заряд: 227,9 [M+1].
Стадия 2. Синтез соединения 4-4
В смешанный раствор соединения 4-3 (7,2 г) в метаноле (20 мл), тетрагидрофуране (20 мл) и воде (10 мл) добавляли LiOH·H2O (6,65 г) при 0°C. Реакционную смесь перемешивали при комнатной температуре в течение 1 часа, затем концентрировали при пониженном давлении, разбавляли водой и этилацетатом и затем подвергали разделению жидкостей. Водную фазу доводили до pH = 6 с помощью 1 моль/л хлористоводородной кислоты и затем экстрагировали этилацетатом. Органические фазы объединяли и промывали насыщенным солевым раствором, высушивали над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали для удаления растворителя с получением соединения 4-4, которое применяли непосредственно на следующей стадии. Соединение 4-4: MS (ESI) масса/заряд: 213,9 [M+1].
Стадия 3. Синтез соединения 4-5
В раствор соединения 4-4 (1,5 г) в дихлорметане (50 мл) добавляли гидрохлорид метилового сложного эфира глицина (1,06 г), TBTU (2,71 г) и N,N-диизопропилэтиламин (3,64 г) при −10°C. Реакционную смесь перемешивали при −10°C – 0°C в течение 3 часов, затем разбавляли водой (40 мл) и экстрагировали дихлорметаном. Органические фазы объединяли, промывали насыщенным солевым раствором, высушивали над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали с удалением растворителя и остаток очищали с помощью колоночной хроматографии на силикагеле (подвижная фаза: петролейный эфир:этилацетат = 5:1) с получением соединения 4-5. Соединение 4-5: MS (ESI) масса/заряд: 284,9 [M+1].
Стадия 4. Синтез соединения 4-6
В смешанный раствор соединения 4-5 (0,5 г) в тетрагидрофуране (2 мл), метаноле (2 мл) и воде (1 мл) добавляли LiOH⋅H2O (369,03 мг) при 0°C. Реакционную смесь перемешивали при 0°C – 20°C в течение 2 часов, затем концентрировали и разбавляли водой (3 мл) и затем подвергали разделению жидкостей. Водную фазу доводили до pH = 6 с помощью 1 моль/л хлористоводородной кислоты и экстрагировали этилацетатом. Органические фазы объединяли, промывали насыщенным солевым раствором, высушивали над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали для удаления растворителя с получением соединения 4-6, которое применяли непосредственно в следующей реакции. Соединение 4-6: MS (ESI) масса/заряд: 270,9 [M+1].
Стадия 5. Синтез соединения 4-8
В раствор соединения 4-6 (0,26 г), соединения 2-6 (437,84 мг) и TBTU (370,71 мг) в дихлорметане (10 мл) добавляли N,N-диизопропилэтиламин (273,56 мг) при −10°C. Реакционную смесь медленно нагревали до комнатной температуры и перемешивали дополнительно в течение 2 часов и затем реакционную смесь разбавляли водой (10 мл) и экстрагировали дихлорметаном. Органические фазы объединяли, промывали насыщенным солевым раствором, высушивали над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали с удалением растворителя и остаток очищали с помощью колоночной хроматографии на силикагеле (подвижная фаза: петролейный эфир:этилацетат = 1:1) с получением соединения 4-8. Соединение 4-8: MS (ESI) масса/заряд: 518,2 [M+1].
Стадия 6. Синтез соединения 4-9
В смешанный раствор соединения 4-8 (0,17 г) в метаноле (4 мл) и н-гексане (6 мл) добавляли изобутилбороновую кислоту (234,45 мг) и 1 моль/л HCl (1,31 мл) при 0°C. Реакционную смесь медленно нагревали до комнатной температуры и перемешивали дополнительно в течение 12 часов и затем концентрировали при пониженном давлении для удаления растворителя с получением остатка. Остаток очищали с помощью препаративной HPLC и затем разделяли с помощью SFC с получением соединения 4-9. Соединение 4-9: 1H ЯМР (400 МГц, метанол-d4) δ 6,83 (br s, 2H), 6,61 (br s, 1H), 4,49 (br s, 1H), 4,10 (br s, 3H), 3,84 (br s, 1H), 2,75 (br s, 1H), 2,59 (br s, 1H), 2,48 (br s, 1H), 1,62 (br s, 1H), 1,30 (br s, 2H), 0,92 (br s, 6H). MS (ESI) масса/заряд: 366,1 [M-17].
Способ разделения с помощью препаративной HPLC для соединения 4-9:
колонка для хроматографии: Xtimate C18 150 × 25 мм, 5 мкм;
подвижная фаза: вода (0,225% FA)-MeOH;
градиент элюирования: от 61% до 85%;
время удерживания: 9,5 мин.
Способ разделения с помощью препаративной SFC для соединения 4-9:
колонка для хроматографии: C2 250 мм × 30 мм, 10 мкм;
подвижная фаза: A: диоксид углерода, B: метанол;
градиент элюирования B%: от 30% до 30%;
расход: 60 мл/мин.
Последовательность выхода пиков соединения 4-9 – второй пик, появляющийся при высокоэффективной хиральной жидкостной колоночной хроматографии.
Стадия 7. Синтез соединения I-1
Способ 1. Добавляли L-яблочную кислоту (332 мг) в изопропилацетат (2,5 мл) и смесь нагревали до 70°C при перемешивании и затем добавляли раствор соединения 4-9 (1,0 г) в 2,5 мл изопропилацетата через 10 минут. Затем нагревание останавливали и смесь охлаждали до 25°C и перемешивали дополнительно в течение 5 дней при данной температуре. Смешанный раствор фильтровали с собиранием осадка на фильтре, который высушивали в вакууме с получением соединения I-1, которое представляло собой кристалл формы I соединения I-1.
Способ 2. Добавляли соединение I-1 (68,9 г) в реакционную колбу и затем добавляли 440 мл изопропилацетата и смешанный раствор перемешивали при комнатной температуре в атмосфере азота в течение 24 часов. Смешанный раствор фильтровали и высушивали с получением кристалла формы I соединения I-1 (64,4 г), и порошковая рентгеновская дифрактограмма полученного кристалла с применением излучения Cu-Kα показана на фиг. 1.
Соединение I-1: 1H ЯМР (400 МГц, DMSO-d6) δ 12,30 (br s, 1H), 10,65 (br s, 1H), 8,57 (br t, J=5,77 Гц, 1H), 7,11 (ddd, J=2,64, 9,16, 12,30 Гц, 1H), 6,91 (br t, J=8,16 Гц, 1H), 6,53 (dt, J=5,65, 9,60 Гц, 1H), 4,44 (br t, J=7,91 Гц, 1H), 4,37 (dd, J=3,89, 7,65 Гц, 1H), 4,10 (br s, 2H), 3,91-4,01 (m, 1H), 3,76 (q, J=7,36 Гц, 1H), 2,61 (br d, J=10,79 Гц, 2H), 2,19-2,44 (m, 3H), 1,61 (td, J=6,71, 13,68 Гц, 1H), 1,20-1,36 (m, 2H), 0,86 (t, J=6,02 Гц, 6H).
Способ получения монокристалла формы I соединения I-1. Добавляли 50 мг соединения I-1 в пробирку для микроволновой обработки, добавляли 1 мл этанола для растворения и затем пробирку для микроволновой обработки помещали в химический стакан, заполненный н-гексаном, для отстаивания, и монокристаллы медленно осаждались из этанола.
Параметры ячейки, кристаллографические данные и положения атомов и т.д. монокристаллического кристалла соединения I-1 формы I показаны в таблице 3 и таблице 4 ниже, и полученная порошковая рентгеновская дифрактограмма кристалла формы I соединения I-1, полученная в результате расчетов, показана на фиг. 2.
Таблица 3. Кристаллографические данные и уточнение структуры


Таблица 4. Координаты атомов (×104) и эквивалентные изотропные параметры смещения (Å2×103) 
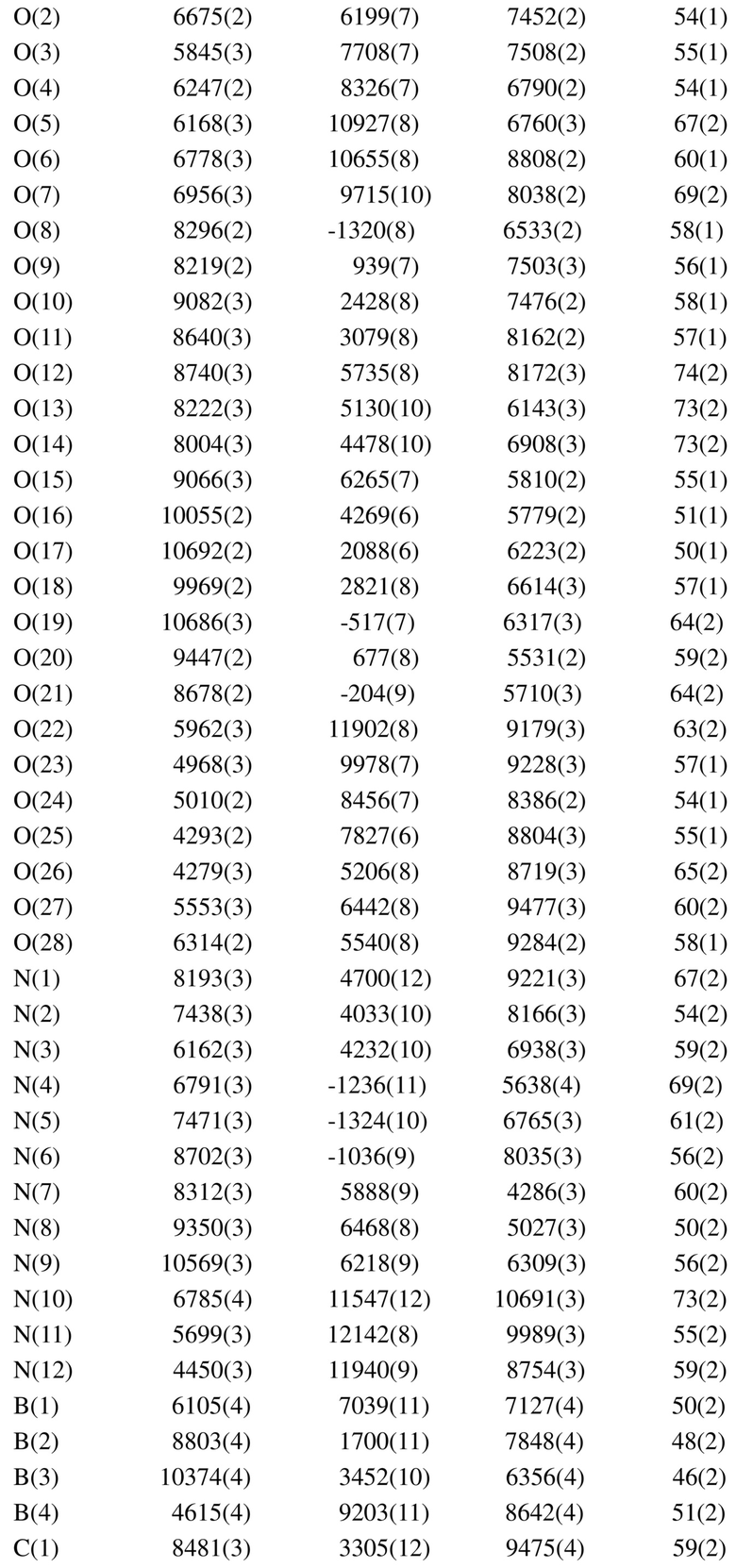

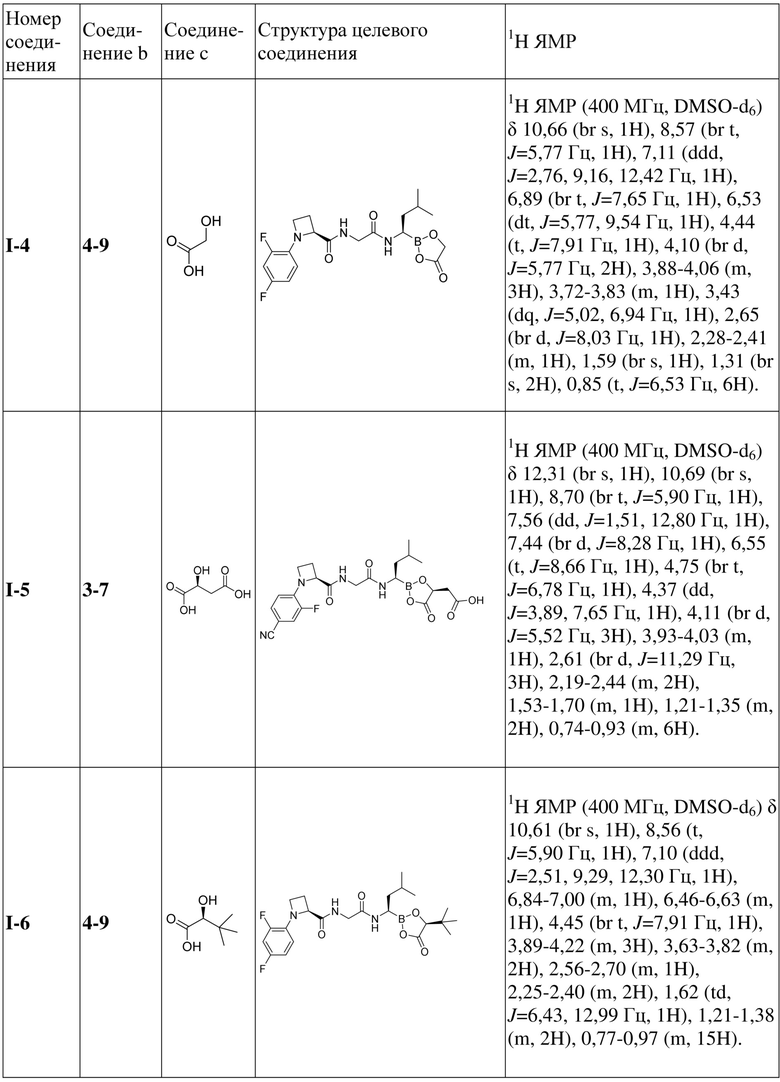
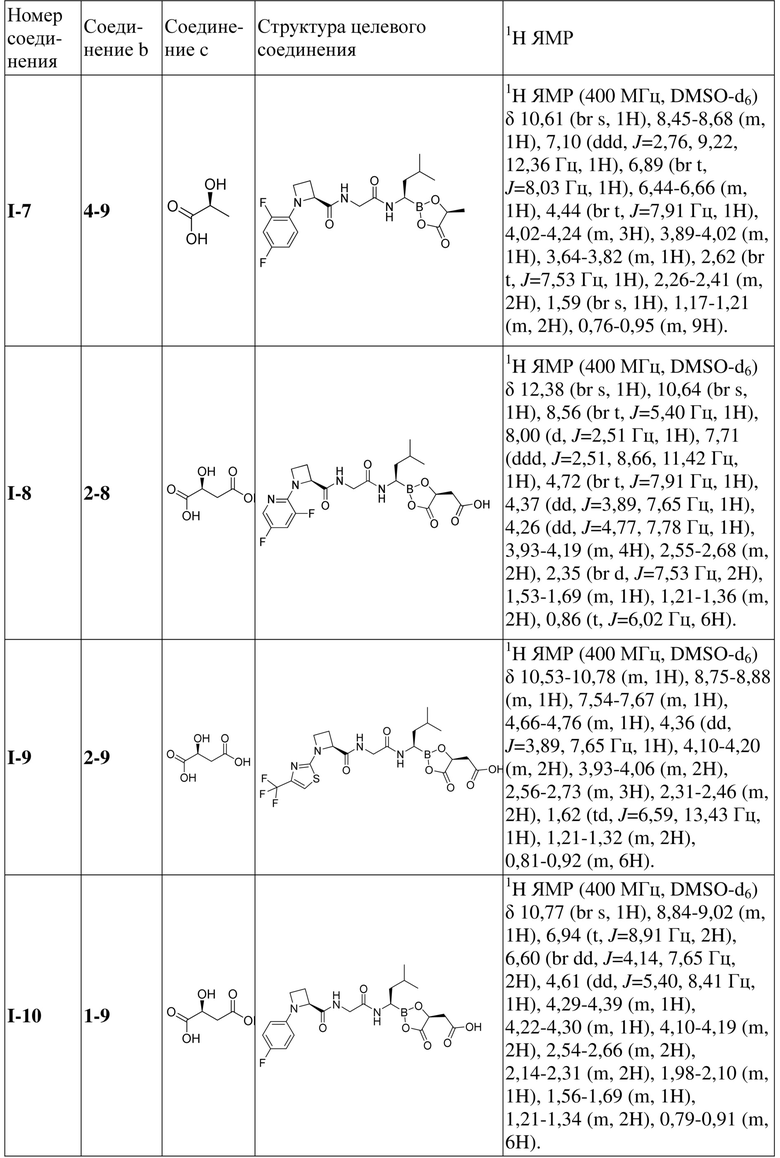
Следующие целевые соединения (соединение I-2 – соединение I-10) получали в соответствии с процедурой из способа 1 на стадии 7 примера 4, где соединение 4-9 из способа 1 на стадии 7 примера 4 соответствует соединению b в таблице 5 ниже, и L-яблочная кислота из способа 1 на стадии 7 примера 4 соответствует соединению c в таблице 5 ниже.
Таблица 5

Экспериментальный пример 1.
Эксперимент антипролиферативного эффекта in vitro в отношении клеток MM1.S
В данном эксперименте исследовали эффект соединений в отношении ингибирования пролиферации клеток путем определения их эффекта в отношении клеточной активности in vitro в линии опухолевых клеток MM1.S.
Клетки MM1.S высевали в 96-луночный культуральный планшет при плотности 7,000 клеток на лунку и затем планшеты инкубировали в течение ночи в инкубаторе при 37°C, 5% CO2 и 100% относительной влажности. Тестируемые соединения добавляли в лунки, содержащие культуру клеток, при концентрации 0,3 нМ – 2000 нМ и затем планшет возвращали обратно в инкубатор с контролем среды-носителя (добавляли DMSO, без тестируемого соединения) и холостым контролем. Планшеты инкубировали в течение 2 дней в инкубаторе при 37°C, 5% CO2 и 100% относительной влажности. Образцы обрабатывали с помощью стандартного способа с применением набора для люминесцентного анализа клеточной активности CellTiter-Glo от Promega (Promega-G7571), и сигналы люминесценции считывали на планшет-ридере SpectraMax i3x от Molecular Devices. Степень ингибирования для тестируемого соединения рассчитывали с применением следующей формулы:
 .
.
Результаты показаны в таблице 6.
Таблица 6


Экспериментальный пример 2. Тестирование соединений в отношении стабильности микросом печени
Каждое из тестируемых соединений совместно инкубировали с микросомами печени мышей CD-1, крыс SD и человека, чтобы оценить стабильность тестируемых соединений.
Получение образцов растворов тестируемых соединений. Добавляли 10 мМ раствор иллюстративного соединения в DMSO (5 мкл) к смеси растворителей, состоящей из DMSO (45 мкл), метанола и воды (450 мкл, объемное соотношение метанола и воды равно 1:1), с получением 100 мкМ раствора тестируемого соединения; добавляли 50 мкл 100 мкМ раствора тестируемого соединения к 450 мкл 100 мМ буфера на основе фосфата калия с получением 10 мкМ раствора тестируемого соединения.
Предварительно инкубировали 10 мкМ раствор тестируемого соединения с микросомами трех видов (человека, крысы и мыши соответственно) в течение 10 минут, и затем рабочий раствор никотинамид-аденин-динуклеотидфосфата (NADPH) для регенерации системы добавляли в планшет для инкубации в соответствии с каждым контрольным моментом времени для инициирования реакции, и наконец, через 0, 5, 10, 20, 30 и 60 минут в реакционный планшет добавляли останавливающий раствор (100% ACN) для остановки реакции. Тестируемые соединения определяли с применением способа LC-MS/MS. Результаты тестирования в отношении стабильности микросом печени для тестируемых соединений показаны в таблице 7.
Таблица 7

Примечание: H означает человека, R означает крысу, и M означает мышь.
Экспериментальный пример 3. Тестирование соединений в отношении проницаемости клеточной мембраны
Тестируемые соединения оценивали в отношении проницаемости клеточной мембраны с применением клеток MDR1-MDCK II.
Каждое из тестируемых соединений (10 мМ раствор соединения в DMSO) разбавляли буфером для переноса (HBSS с 10 мМ Hepes, pH = 7,4) и составляли в образцы при конечной концентрации 2 мкМ, а затем проводили введение в обоих направлениях (A-B и B-A). После введения планшет с клетками инкубировали в течение 150 минут в инкубаторе при 37°C, 5% CO2 и насыщенной влажности. После 150 минут инкубации образцы собирали и полуколичественно определяли значения концентрации тестируемых соединений в переносимых образцах с применением способа LC-MS/MS. Результаты тестирования в отношении проницаемости клеточной мембраны для тестируемых соединений показаны в таблице 8.
Таблица 8

Примечание: Papp от A до B означает скорость, с которой соединение входит в клетку; Papp от B до A означает скорость, с которой клетка секретирует соединение; коэффициент эффлюкса = Papp от B до A/Papp от A до B.
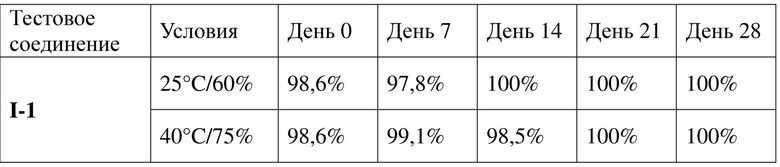
Экспериментальный пример 4. Испытание стабильности
Приблизительно 50 мг образца помещали в чистую одноразовую чашку Петри и распределяли тонким слоем. Чашку Петри покрывали алюминиевой фольгой, в которой делали несколько небольших отверстий. Образец, в двух повторностях, помещали в боксы для изучения стабильности при 25°C ± 2°C/60% RH ± 5% RH и 40°C ± 2°C/75% RH ± 5% RH соответственно, и отбирали пробы в запланированные моменты времени, и состав соединения определяли с применением способа HPLC, и результаты показаны в таблице 9.
Таблица 9
| название | год | авторы | номер документа |
|---|---|---|---|
| КОНДЕНСИРОВАННОЕ ТРИЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ В КАЧЕСТВЕ ДВОЙНОГО ИНГИБИТОРА PDE3/PDE4 | 2019 |
|
RU2827863C2 |
| СОДЕРЖАЩЕЕ ЗАМЕСТИТЕЛЬ, ПРЕДСТАВЛЯЮЩИЙ СОБОЙ БУТАН, В ГЕТЕРОЦИКЛИЧЕСКОМ КОЛЬЦЕ ПРОИЗВОДНОЕ ПИРИДОНА ДЛЯ ЛЕЧЕНИЯ ФИБРОЗА И ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ | 2017 |
|
RU2738844C2 |
| СОЕДИНЕНИЯ НА ОСНОВЕ ИЗОТИАЗОЛО[5,4-d]ПИРИМИДИНА В КАЧЕСТВЕ ИНГИБИТОРА IRAK4 | 2019 |
|
RU2801942C2 |
| СОЕДИНЕНИЕ, ПРЕДСТАВЛЯЮЩЕЕ СОБОЙ ПРОЛЕКАРСТВО ЛАНОСТЕРИНА, А ТАКЖЕ СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ПРИМЕНЕНИЕ | 2018 |
|
RU2720677C1 |
| АНТАГОНИСТ ЭСТРОГЕНОВОГО РЕЦЕПТОРА | 2019 |
|
RU2832735C2 |
| КОНДЕНСИРОВАННОЕ АЗА-ГЕТЕРОЦИКЛИЧЕСКОЕ АМИДНОЕ СОЕДИНЕНИЕ И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2811975C1 |
| СОЕДИНЕНИЕ 3,4-ДИГИДРОИЗОХИНОЛИНА И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2825312C1 |
| Фторвинилбензамидное соединение в качестве иммуномодулятора PD-L1 | 2020 |
|
RU2789450C1 |
| КЛАСС КОНДЕНСИРОВАННЫХ КОЛЬЦЕВЫХ СОЕДИНЕНИЙ И ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ | 2021 |
|
RU2831125C1 |
| ТИОФЕНОВОЕ СОЕДИНЕНИЕ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2017 |
|
RU2709473C1 |

Изобретение относится к боратному соединению производного азетидина, в частности к соединению формулы (I), его фармацевтически приемлемой соли, его таутомеру, его стереоизомеру или его геометрическому изомеру. В формуле (I): кольцо A выбрано из группы, состоящей из фенила и 5-10-членного гетероарила, где гетероарил содержит по меньшей мере один атом кольца, выбранный из группы, состоящей из N, O и S; каждый R1 независимо выбран из группы, состоящей из галогена, CN, OH, NH2 и C1-6алкила, где C1-6алкил необязательно замещен одной или более группами, выбранными из группы, состоящей из галогена, OH и NH2; n выбран из группы, состоящей из 0, 1, 2, 3, 4 и 5; каждый из R2 и R3 независимо выбран из группы, состоящей из H; R4 выбран из C1-6алкила; R5 выбран из группы, состоящей из H; кольцо D выбрано из 5-10-членного гетероциклила, где 5-10-членный гетероциклил замещен по меньшей мере одним =O, и где гетероатомы в атомах кольца 5-10-членного гетероциклила включают только атомы бора и кислорода; каждый R6 независимо выбран из группы, состоящей из C1-6алкила, где C1-6алкил необязательно замещен одной или более группами COOH; и m выбран из группы, состоящей из 0, 1, 2, 3, 4 и 5. Также предложены кристалл соединения I-1, фармацевтическая композиция, содержащая вышеуказанное соединение или кристалл, способ лечения множественной миеломы и применение вышеуказанного соединения, кристалла или фармацевтической композиции. Предложенное соединение может быть использовано для предупреждения или лечения множественной миеломы. 6 н. и 31 з.п. ф-лы, 2 ил., 9 табл., 8 пр.


1. Соединение формулы (I), его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер,
 ,
,
где
кольцо A выбрано из группы, состоящей из фенила и 5-10-членного гетероарила, где гетероарил содержит по меньшей мере один атом кольца, выбранный из группы, состоящей из N, O и S;
каждый R1 независимо выбран из группы, состоящей из галогена, CN, OH, NH2 и C1-6алкила, где C1-6алкил необязательно замещен одной или более группами, выбранными из группы, состоящей из галогена, OH и NH2;
n выбран из группы, состоящей из 0, 1, 2, 3, 4 и 5;
каждый из R2 и R3 независимо выбран из группы, состоящей из H;
R4 выбран из C1-6алкила;
R5 выбран из группы, состоящей из H;
кольцо D выбрано из 5-10-членного гетероциклила, где 5-10-членный гетероциклил замещен по меньшей мере одним =O, и где гетероатомы в атомах кольца 5-10-членного гетероциклила включают только атомы бора и кислорода;
каждый R6 независимо выбран из группы, состоящей из C1-6алкила, где C1-6алкил необязательно замещен одной или более группами COOH; и
m выбран из группы, состоящей из 0, 1, 2, 3, 4 и 5.
2. Соединение формулы (I) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер по п. 1, где кольцо A выбрано из группы, состоящей из фенила и 5-6-членного гетероарила, где 5-6-членный гетероарил содержит по меньшей мере один атом кольца, выбранный из группы, состоящей из азота и серы.
3. Соединение формулы (I) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер по п. 2, где кольцо A выбрано из группы, состоящей из фенила, пиридинила и тиазолила.
4. Соединение формулы (I) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер по п. 3, где кольцо A представляет собой фенил.
5. Соединение формулы (I) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер по любому из пп. 1-4, где каждый R1 независимо выбран из группы, состоящей из фтора, хлора, брома, йода, CN, C1-3алкила и C1-3алкила, замещенного 1, 2 или 3 атомами фтора.
6. Соединение формулы (I) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер по п. 5, где каждый R1 независимо выбран из группы, состоящей из фтора, CN и трифторметила.
7. Соединение формулы (I) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер по любому из пп. 1-6, где n выбран из группы, состоящей из 0, 1 и 2.
8. Соединение формулы (I) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер по п. 7, где n выбран из группы, состоящей из 1 и 2.
9. Соединение формулы (I) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер по любому из пп. 1-8, где структурное звено 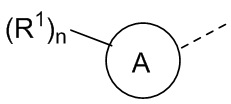 выбрано из группы, состоящей из
выбрано из группы, состоящей из 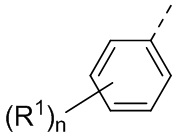 ,
,  и
и 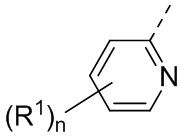 .
.
10. Соединение формулы (I) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер по п. 9, где структурное звено  выбрано из группы, состоящей из
выбрано из группы, состоящей из 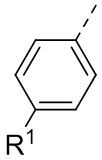 ,
,  ,
, 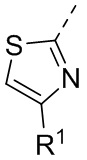 и
и 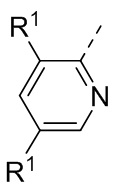 .
.
11. Соединение формулы (I) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер по п. 10, где структурное звено  выбрано из группы, состоящей из
выбрано из группы, состоящей из  ,
, 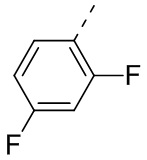 ,
,  ,
,  и
и  .
.
12. Соединение формулы (I) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер по любому из пп. 1-11, где R4 выбран из C3-5алкила.
13. Соединение формулы (I) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер по п. 12, где R4 представляет собой изобутил.
14. Соединение формулы (I), его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер по любому из пп. 1-13, где кольцо D выбрано из 5-10-членного гетероциклила, где кольцо D представляет собой  .
.
15. Соединение формулы (I) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер по п. 14, где кольцо D выбрано из группы, состоящей из 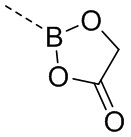 ,
,  и
и 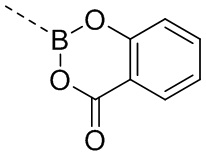 .
.
16. Соединение формулы (I) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер по любому из пп. 1-15, где m выбран из группы, состоящей из 0, 1, 2 и 3.
17. Соединение формулы (I) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер по п. 16, где m выбран из группы, состоящей из 0 и 1.
18. Соединение формулы (I) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер по любому из пп. 1-17, где каждый R6 независимо выбран из C1-4алкила, необязательно замещенного одним или более COOH.
19. Соединение формулы (I) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер по п. 18, где каждый R6 независимо выбран из группы, состоящей из метила, трет-бутила и карбоксиметила.
20. Соединение формулы (I) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер по любому из пп. 1-19, где структурное звено 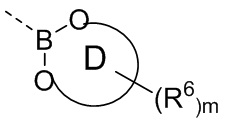 представляет собой
представляет собой 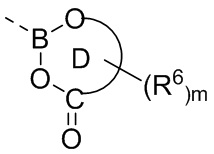 .
.
21. Соединение формулы (I) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер по п. 20, где структурное звено 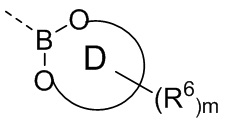 выбрано из группы, состоящей из
выбрано из группы, состоящей из 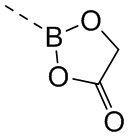 ,
, 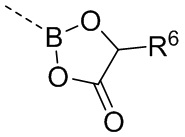 ,
,  и
и 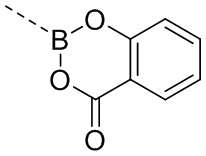 .
.
22. Соединение формулы (I) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер по п. 21, где структурное звено  выбрано из группы, состоящей из
выбрано из группы, состоящей из  ,
,  ,
,  ,
,  ,
,  и
и  .
.
23. Соединение формулы (I) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер по п. 22, где структурное звено  выбрано из группы, состоящей из
выбрано из группы, состоящей из  ,
, 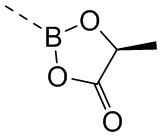 ,
,  ,
,  ,
,  и
и  .
.
24. Соединение формулы (I) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер по любому из пп. 1-23, где соединение формулы (I) выбрано из группы, состоящей из соединения формулы (I-a), соединения формулы (II), соединения формулы (II-a), соединения формулы (III), соединения формулы (III-a), соединения формулы (IV) и соединения формулы (IV-a):
 ,
, 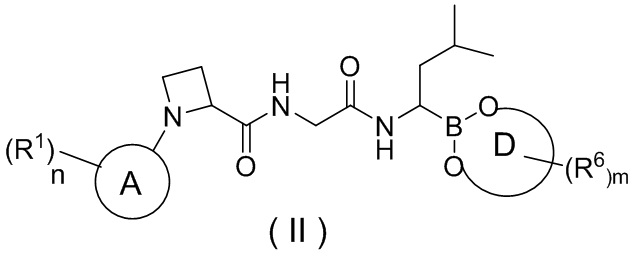 ,
,  ,
,  ,
, 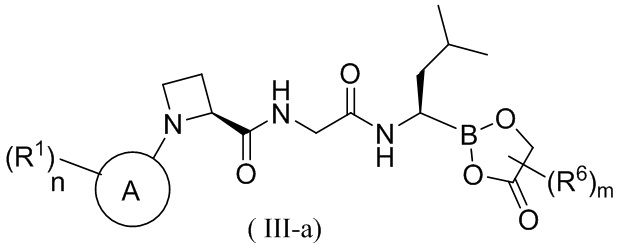 ,
,  ,
, 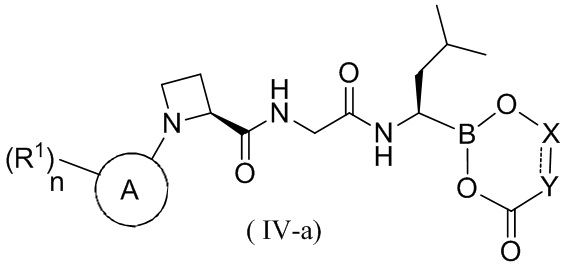 ,
,
где X выбран из -C(Ra)2-, и Y выбран из -C(Rb)2-; или X выбран из =C(Rc)-, и Y выбран из =C(Rd)-, где каждый из Ra, Rb, Rc и Rd независимо выбран из группы, состоящей из водорода и C1-6алкила, где C1-6алкил необязательно замещен одним или более -COOH, или Ra и Rb соединены с образованием 3-6-членного кольца, или Rc и Rd соединены с образованием 3-6-членного кольца.
25. Соединение формулы (I) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер по п. 24, где каждый из Ra и Rb независимо выбран из группы, состоящей из водорода и C1-6алкила, или Rc и Rd соединены с образованием 5-6-членного кольца.
26. Соединение формулы (I) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер по п. 25, где каждый из Ra и Rb независимо выбран из группы, состоящей из водорода и C1-3алкила, или Rc и Rd соединены с образованием фенила.
27. Соединение формулы (I) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер по п. 24, где структурное звено  выбрано из группы, состоящей из
выбрано из группы, состоящей из  ,
,  ,
,  и
и  .
.
28. Соединение формулы (I) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер по п. 1, представляющие собой соединение, выбранное из группы, состоящей из:
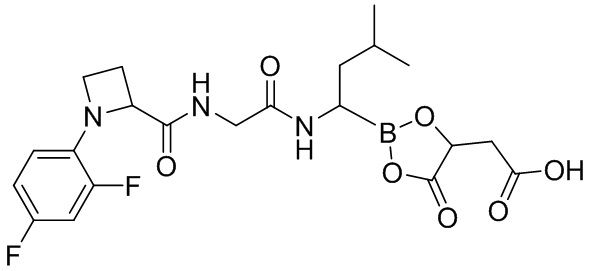

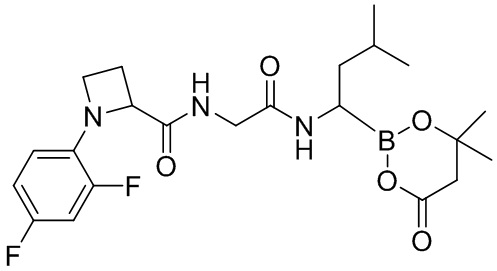
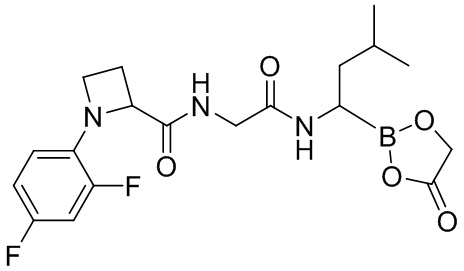

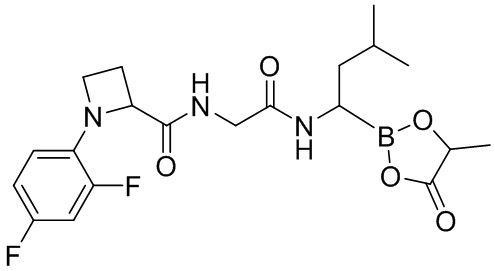
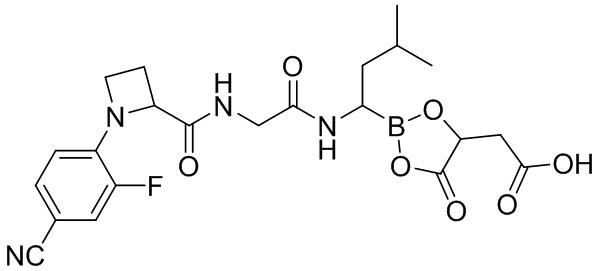

 и
и 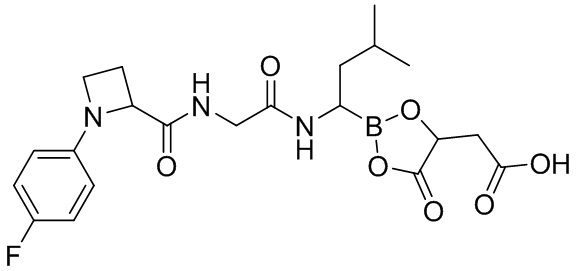 , или его фармацевтически приемлемую соль, таутомер, его стереоизомер или его геометрический изомер.
, или его фармацевтически приемлемую соль, таутомер, его стереоизомер или его геометрический изомер.
29. Соединение формулы (I) или его фармацевтически приемлемая соль, его таутомер, его стереоизомер или его геометрический изомер по п. 1, представляющие собой соединение, выбранное из группы, состоящей из:


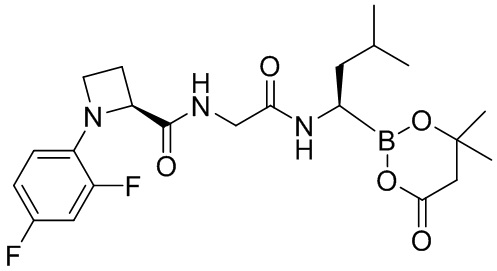




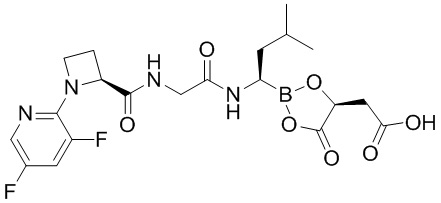
 и
и 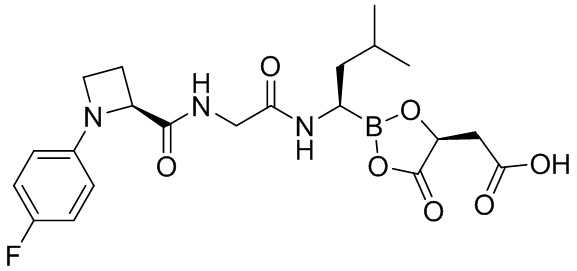 , или его фармацевтически приемлемую соль, его таутомер или его геометрический изомер.
, или его фармацевтически приемлемую соль, его таутомер или его геометрический изомер.
30. Кристалл соединения I-1, где на дифракционной рентгенограмме (XRD) с применением Cu-Kα-излучения кристалл характеризуется дифракционными пиками при следующих значениях 2θ: 6,00, 11,98, 17,88, 20,88 и 21,48,
 .
.
31. Кристалл соединения I-1 по п. 30, где кристалл характеризуется дифракционными пиками при следующих значениях 2θ: 6,00, 8,90, 11,98, 17,88, 20,88, 21,48, 24,60 и 25,44.
32. Кристалл соединения I-1 по п. 31, где кристалл характеризуется дифракционными пиками при следующих значениях 2θ: 6,00, 8,90, 11,98, 13,70, 16,50, 17,88, 20,88, 21,48, 24,60 и 25,44.
33. Кристалл соединения I-1 по п. 32, где кристалл характеризуется дифракционными пиками при следующих значениях 2θ: 6,00, 8,90, 11,98, 12,80, 13,70, 16,50, 17,88, 20,88, 21,48, 24,60, 25,44, 27,66, 28,94 и 30,25.
34. Кристалл соединения I-1, где кристалл характеризуется следующим: кристаллическая система: моноклинная система; пространственная группа: P 21; параметры ячейки: a = 24,4220(5) Å, b = 8,4507(2) Å, c = 24,4590(5) Å, α = 90 градусов, β = 107,683(1) градуса, γ = 90 градусов; Z = 8,
 .
.
35. Фармацевтическая композиция для предупреждения или лечения множественной миеломы, содержащая соединение формулы (I) или его фармацевтически приемлемую соль, его таутомер, его стереоизомер или его геометрический изомер по любому из пп. 1-29 и/или кристалл соединения I-1 по любому из пп. 30-34.
36. Способ лечения множественной миеломы у млекопитающего, предусматривающий введение млекопитающему, нуждающемуся в лечении, терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли, его таутомера, его стереоизомера или его геометрического изомера по любому из пп. 1-29, кристалла соединения I-1 по любому из пп. 30-34 или фармацевтической композиции по п. 35.
37. Применение соединения формулы (I) или его фармацевтически приемлемой соли, его таутомера, его стереоизомера или его геометрического изомера по любому из пп. 1-29, кристалла соединения I-1 по любому из пп. 30-34 или фармацевтической композиции по п. 35 для предупреждения или лечения множественной миеломы.
| WO 2012177835 A1, 27.12.2012 | |||
| CN 105732683 A, 06.07.2016 | |||
| Плавучий улавливатель жиров с поверхности воды | 1929 |
|
SU27346A1 |
| Воронка для прядения искусственного шелка по вытяжному способу | 1929 |
|
SU28622A1 |
| WO 2010012222 A1, 04.02.2010 | |||
| ZHU Y | |||
| et al., Design, synthesis, biological evaluation, and structure-activity relationship (SAR) discussion of dipeptidyl boronate proteasome inhibitors, Part I: comprehensive understanding of the SAR of | |||
Авторы
Даты
2023-08-24—Публикация
2019-08-02—Подача