Изобретение относится к способу синтеза алифатических трийодпроизводных, а именно трийодид- N,N-диметилгидразения формулы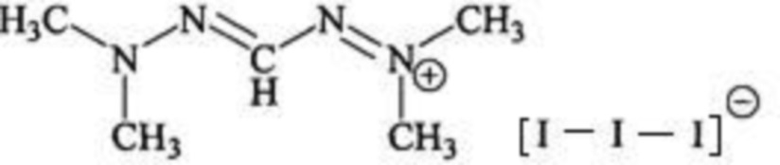 .
.
Йодированные производные достаточно востребованы в органической химии. Так, например, на их основе возможен синтез йодосодержащих лекарственных препаратов, активно использующихся в лечении зоба и рака щитовидной железы [1]. В их числе препараты тиреоидных гормонов: монокомпонентные: лиотиронин, левотироксин натрия; комбинированные: тиреотом; антитиреоидные средства (снижают уровень гормона щитовидной железы): тиоамиды: пропилтиоурацил, тиамазол; анионные ингибиторы: калия перхлорат; рентгенконтрастные средства (применяются для улучшения визуализации щитовидной железы при рентгеновской диагностике): йопаноевая кислота; радиоактивный йод (131) выпускается в форме Йодотопа; препараты иодидов: иодид калия, раствор Люголя.
Основными методами получения ароматических и жирноароматических полийодпроизводных являются:
- введение йода в ароматические кольца мезитилена, пара-ксилола, трет-бутилбензола в присутствии йодноватистой и уксусной кислот в водном растворе при нагревании реакционной смеси в течение 15 минут. В случае бензола реакция проводится при 200оС в запаянной трубке [2].
- прямое йодирование бензола с надсернокислым натрием в среде уксусной кислоты, при нагревании в течение 15 ч [2].
- йодирование 5-йодо-2-хлор-параксилола через прибавление при температуре 135°С в течение 2 минут смесь серной и азотной кислоты (1:1) к раствору четырёххлористого углерода и уксусной кислоты (1:1), состоящей из 2-хлорпараксилола и йода, с последующем нагреванием раствора до 250°С в течение 45 минут и экстракцией целевого продукта [2].
- диазотирование по Гриссу и реакцию Зондмейера [3]. Диазотирование по Гриссу проводится в водном растворе соляной кислоты и ариламина. При 0-5°С по каплям прибавляется раствор нитрита натрия. Затем для осуществления реакции Зондмейера соль диазония в воде приливают к предварительно охлажденному водному раствору йодида калия, после чего реакционную смесь оставляют на 2 часа, азот выделяют непродолжительным нагреванием в присутствии обратного холодильника, целевой продукт – перегонкой с водяным паром.
Недостатками этих способов являются проведение реакции при высоких или низких температурах, взрывоопасность реакционной смеси, сложности осуществления синтеза.
Известен способа получения метилйода [4]. Взаимодействием йода и метанола в присутствии смеси красного и жёлтого фосфора и температуре до 70-75°С. Недостатком этого способа является использование труднодоступных и токсичных реактивов (смесь красного и белого фосфора, метанола), сбор сложной химической установки, обеспечение полного протекания спиртового раствора йода через делительную воронку (во избежание засорения запорной трубы крана кристаллами йода), регулируя краны холодильника и делительной воронки, контроль температуры реакционной смеси (70-75°С в процессе добавления йода в растворе, снижение температуры до 55°С при выделении целевого продукта).
Наиболее близким к заявляемому изобретению является способ, основанный на взаимодействии диметилсульфата, йодида калия в водном растворе в присутствии карбоната кальция [4]. Недостатками данного способа являются токсичность диметилсульфата и длительность его добавления, что создаёт необходимость работы в нитриловых перчатках в вытяжном шкафу и максимального ограничения контакта с данным веществом, сбор сложной реакционной установки, что обусловлено быстрым выделением из реакционной смеси йодистого метила и сложностью его фиксации; необходимостью контроля температуры и необходимость её увеличения в ходе синтеза (с 60 до 70°С).
Задачей является разработка простой и эффективной методики синтеза трийодида N,N-диметилгидразения.
Техническим результатом является получение ранее неописанного в литературе йодпроизводного, относительно низкая себестоимость реактивов, простота синтеза, уменьшение времени и температуры проведения реакции, расширение средств аналогичного назначения, переработка некондиционного ракетного топлива «Гептил» (несимметричного диметилгидразина (НДМГ)).
Технический результат достигается тем, что способ получения трийодида N,N-диметилгидразения формулы  , согласно изобретению, включает взаимодействие диметилгидразона глиоксаля, броммалоннитрила, йодида калия в водно-диоксановом растворе. Способ отличается тем, что реакцию проводят при комнатной температуре в течение 72 часов, или при нагревании до 40°С в течение 5 минут, или при действии ультразвука частотой 90-100 Гц в течение 5 минут, или при действии микроволнового излучения 150W в течение 8 минут.
, согласно изобретению, включает взаимодействие диметилгидразона глиоксаля, броммалоннитрила, йодида калия в водно-диоксановом растворе. Способ отличается тем, что реакцию проводят при комнатной температуре в течение 72 часов, или при нагревании до 40°С в течение 5 минут, или при действии ультразвука частотой 90-100 Гц в течение 5 минут, или при действии микроволнового излучения 150W в течение 8 минут.
Сущность изобретения состоит во взаимодействии двух эквивалентов броммалоннитрила, одного эквивалента N,N-диметилгидразона глиоксаля и трёх эквивалентов йодида калия в водно-диоксановой среде. Реакция проводится при стандартных условиях (20°С, 1 атм.) в течение 72 часов, температуре 35-40°С 5 минут, под действием ультразвука при частоте 90-100 Гц в течение 5 минут, при микроволновом излучении 150W 8 минут. Целевой продукт, выпавший в осадок, отфильтровывают на фильтре Шота, промывают холодным этилацетатом.
Схема модифицированной реакции Видеквиста с N,N-диметилгидразоном глиоксаля:
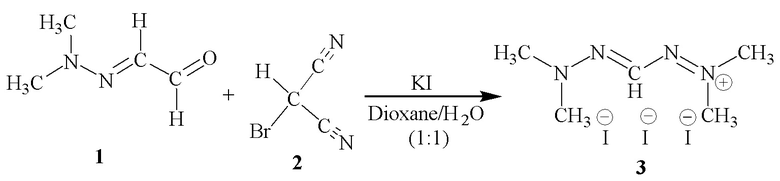
Для получения используют следующие соединения: некондиционное, подлежащее утилизации ракетное топливо на основе НДМГ («Газпром Нефтехим» г. Салават), глиоксаль 40% (ГОСТ 4517-87), дистиллированная вода (ГОСТ 58144-2018), дихлорметан (ГОСТ 9968-86), сульфат натрия (ГОСТ 4166-76), малононитрил (СКТБ Технолог, CAS № 109-77-3), бром (ГОСТ 4109-79), йодид калия (ГОСТ 4232-74), диоксан (ГОСТ 10455-80), этилацетат (ГОСТ 8981-78).
Глиоксаль 40%, дихлорметан, малононитрил, бром были приобретены у коммерческих поставщиков и использовались без дальнейшей очистки. НДМГ был перегнан при температуре 64оС. Протекание реакции и чистоту продуктов контролируют методом ТСХ на пластинах Sorbfil (пятна визуализировались в УФ-свете, при обработке парами йода или при нагревании). Температура плавления и разложения определена на приборе Optimelt MPA100. Спектры ЯМР 1Н и 13С записаны в ДМСО-d6 с внутренним стандартом ТМС на спектрометре Bruker AVANCE400 WB при рабочей частоте 400,13 МГц для 1H и 100,61 МГц для 13C.
Данные рентгеновской дифракции монокристаллов были собраны на дифрактометре Bruker Smart Apex II CCD. Структуры расшифрованы прямым методом с использованием программы SHELXT-2014/5 и уточнены полноматричным методом наименьших квадратов по F2 с использованием программы SHELXL-2017/1. Расчеты проводились с использованием пакета программ WinGX-2014.1. Неводородные атомы уточнены анизотропно.
Синтез диметилгидразона глиоксаля осуществляют следующим образом: для этого к 4 г 40% раствора глиоксаля (0,07 моль) в 50 мл воды по каплям прибавляют 4,14 г (0,07 моль) НДМГ. Водный раствор перемешивают в течение 1 часа, затем экстрагируют продукт реакции дихлорметаном (25 мл 3 раза). Органический слой сушат над сульфатом натрия в течение 1,5 часа. Дихлорметан отогняют на роторе при температуре 35оС, 150 об./мин. Диметилгидразон глиоксаля перегоняют под вакуумом. Получают жидкий продукт светло-жёлтого цвета, выход 70% (4,8 г).
Синтез броммалоннитрила осуществляют следующим образом: для этого к 1,32 г (0,02 моль) малоннитрила в 10 мл воды добавляют 3,2 г (0,02 моль). Раствор перемешивают на магнитной мешалке. Через несколько минут после обесцвечивания реакционной смеси в осадок выпадает жёлтая эвтетика (продукты диспропорционирования броммалоннитрила – малоннитрил и диброммалоннитрил), которую используют в дальнейшем синтезе в количестве 5,97 г (0,04 моль).
Примеры осуществления способа приведены ниже.
Пример 1. Способ получения трийодида N,N-диметилгидразения
К 5,97 г (0,04 моль) двум эквивалентам броммалононитрила и 10,25 г (0,06 моль) йодида калия в водном диоксане прикапывают 2,06 г (0,02 моль) диметилгидразона глиоксаля. Реакционную смесь выдерживают при комнатной температуре 72 ч. После выпадения игл осадка трийодида N,N-диметилгидразения  реакционную смесь фильтруют, осадок промывают этилацетатом. Выход 78% (8,19 г). т. пл. 168°С с разложением. ЯМР 1Н δ, м. д., J, Гц (ДМСО-d6): 3.59 (d, J = 14.5 Hz, 6H, N(CH35,4)2), 3.31 (d, J = 23.8 Hz, 6H, N(CH36,2)2), 2.53 (s, 1H, CH7). ЯМР 13С м. д., (ДМСО-d6): 69.56 (CH17), 47.72 (N(CH35,4)2, 44.88 (N(CH35,4)2). Найдено, C, 11.58; H, 2.77; I, 74.42; N, 11.01. C5H13N4I3. Вычислено,%: C, 11.78; H, 2.57; I, 74.66; N, 10.99.
реакционную смесь фильтруют, осадок промывают этилацетатом. Выход 78% (8,19 г). т. пл. 168°С с разложением. ЯМР 1Н δ, м. д., J, Гц (ДМСО-d6): 3.59 (d, J = 14.5 Hz, 6H, N(CH35,4)2), 3.31 (d, J = 23.8 Hz, 6H, N(CH36,2)2), 2.53 (s, 1H, CH7). ЯМР 13С м. д., (ДМСО-d6): 69.56 (CH17), 47.72 (N(CH35,4)2, 44.88 (N(CH35,4)2). Найдено, C, 11.58; H, 2.77; I, 74.42; N, 11.01. C5H13N4I3. Вычислено,%: C, 11.78; H, 2.57; I, 74.66; N, 10.99.
Пример 2. Способ получения трийодида N,N-диметилгидразения
Способ осуществляют аналогично способу 1, отличающийся тем, что реакционную смесь выдерживают при температуре 35-40оС 5 минут. Выход 78% (8,19 г). т. пл. 168°С с разложением. ЯМР 1Н δ, м. д., J, Гц (ДМСО-d6): 3.59 (d, J = 14.5 Hz, 6H, N(CH35,4)2), 3.31 (d, J = 23.8 Hz, 6H, N(CH36,2)2), 2.53 (s, 1H, CH7). ЯМР 13С м. д., (ДМСО-d6): 69.56 (CH17), 47.72 (N(CH35,4)2, 44.88 (N(CH35,4)2). Найдено, C, 11.58; H, 2.77; I, 74.42; N, 11.01. C5H13N4I3. Вычислено,%: C, 11.78; H, 2.57; I, 74.66; N, 10.99.
Пример 3. Способ получения трийодида N,N-диметилгидразения
Способ осуществляют аналогично способу 1, отличающийся тем, что реакционную смесь помещают в ультразвуковой реактор с частотой 90-100 Гц на 5 минут. Выпавший аморфный осадок трийодида N,N-диметилгидразения  фильтруют, промывают этилацетатом. Выход 81% (8,51 г). т. пл. 168°С с разложением. ЯМР 1Н δ, м. д., J, Гц (ДМСО-d6): 3.59 (d, J = 14.5 Hz, 6H, N(CH35,4)2), 3.31 (d, J = 23.8 Hz, 6H, N(CH36,2)2), 2.53 (s, 1H, CH7). ЯМР 13С м. д., (ДМСО-d6): 69.56 (CH17), 47.72 (N(CH35,4)2, 44.88 (N(CH35,4)2). Найдено, C, 11.58; H, 2.77; I, 74.42; N, 11.01. C5H13N4I3. Вычислено,%: C, 11.78; H, 2.57; I, 74.66; N, 10.99.
фильтруют, промывают этилацетатом. Выход 81% (8,51 г). т. пл. 168°С с разложением. ЯМР 1Н δ, м. д., J, Гц (ДМСО-d6): 3.59 (d, J = 14.5 Hz, 6H, N(CH35,4)2), 3.31 (d, J = 23.8 Hz, 6H, N(CH36,2)2), 2.53 (s, 1H, CH7). ЯМР 13С м. д., (ДМСО-d6): 69.56 (CH17), 47.72 (N(CH35,4)2, 44.88 (N(CH35,4)2). Найдено, C, 11.58; H, 2.77; I, 74.42; N, 11.01. C5H13N4I3. Вычислено,%: C, 11.78; H, 2.57; I, 74.66; N, 10.99.
Пример 4. Способ получения трийодида N,N-диметилгидразения
Способ осуществляют аналогично способу 1, отличающийся тем, что реакционную смесь помещают в микроволновую печь при излучении 150W в течение 8 минут. Мелкокристаллический осадок трийодида N,N-диметилгидразения  фильтруют, промывают этилацетатом. Выход 77% (8,13 г). т. пл. 168°С с разложением. ЯМР 1Н δ, м. д., J, Гц (ДМСО-d6): 3.59 (d, J = 14.5 Hz, 6H, N(CH35,4)2), 3.31 (d, J = 23.8 Hz, 6H, N(CH36,2)2), 2.53 (s, 1H, CH7). ЯМР 13С м. д., (ДМСО-d6): 69.56 (CH17), 47.72 (N(CH35,4)2, 44.88 (N(CH35,4)2). Найдено, C, 11.58; H, 2.77; I, 74.42; N, 11.01. C5H13N4I3. Вычислено,%: C, 11.78; H, 2.57; I, 74.66; N, 10.99.
фильтруют, промывают этилацетатом. Выход 77% (8,13 г). т. пл. 168°С с разложением. ЯМР 1Н δ, м. д., J, Гц (ДМСО-d6): 3.59 (d, J = 14.5 Hz, 6H, N(CH35,4)2), 3.31 (d, J = 23.8 Hz, 6H, N(CH36,2)2), 2.53 (s, 1H, CH7). ЯМР 13С м. д., (ДМСО-d6): 69.56 (CH17), 47.72 (N(CH35,4)2, 44.88 (N(CH35,4)2). Найдено, C, 11.58; H, 2.77; I, 74.42; N, 11.01. C5H13N4I3. Вычислено,%: C, 11.78; H, 2.57; I, 74.66; N, 10.99.
Таким образом, разработана эффективная методика получения потенциального лекарственного препарата в отношении щитовидной железы с одновременной переработкой некондиционного ракетного топлива.
Список литературы
[1] Рождественский, Д. А. Препараты гормонов щитовидной железы и антитиреоидные средства / Д. А. Рождественский // Вестник фармации. - 2003. - № 3. - С. 61-79.
[2] Хиккинботтом В. Реакции органических соединений. – Рипол Классик, 1939.
[3] О. А. Голубчиков Органический практикум Санкт-Петербург Нии химии СПбГу – 2012
[4] Гарольд С. К., Луис Ф. Ф. Органические синтезы, Сборник, том 2, стр.399 (1943); Том 13, стр.60 (1933).
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения N,N-диметил-4-бифениламина и его производных | 2022 |
|
RU2794095C1 |
| БЕНЗАМИДНЫЕ ПРОИЗВОДНЫЕ, ОБЛАДАЮЩИЕ ПРОТИВОРАКОВОЙ АКТИВНОСТЬЮ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ | 2011 |
|
RU2565079C2 |
| СПОСОБ ПОЛУЧЕНИЯ ТИОФЕНГЛИКОЗИДНЫХ ПРОИЗВОДНЫХ | 2005 |
|
RU2394835C2 |
| ТРИЙОДИДЫ 1,2,3-ЗАМЕЩЕННЫХ БЕНЗИМИДАЗОЛИЯ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2000 |
|
RU2198880C2 |
| Способ получения 5,8-(бис(метилен(N,N-диметил-N-додециламмоний))-2-этил-4H-[1,3]диоксино[4,5-c]пиридиний дихлорида | 2019 |
|
RU2697848C1 |
| ПРОИЗВОДНЫЕ И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ N-АДАМАНТИЛМЕТИЛА В КАЧЕСТВЕ ФАРМАЦЕВТИЧЕСКИХ КОМПОЗИЦИЙ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2002 |
|
RU2300525C2 |
| Способ получения пирроло[3,4-с]хинолинов | 2022 |
|
RU2802332C1 |
| СПОСОБ ДЕТОКСИКАЦИИ НЕСИММЕТРИЧНОГО ДИМЕТИЛГИДРАЗИНА В ПОЧВЕ И ГРУНТЕ | 2009 |
|
RU2424020C1 |
| Способ получения N-((гидроксиамино)-оксоалкил)-2-(хиназолин-4-иламино)-бензамидов | 2019 |
|
RU2722694C1 |
| 2,4-Диарил-6-алкил-1,3,5-триазины и способ их получения | 2023 |
|
RU2812149C1 |
Изобретение относится к способу получения нового соединения, а именно трийодида N,N-диметилгидразения формулы 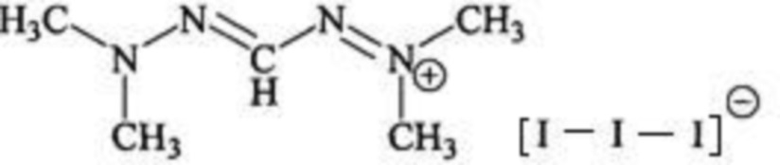 , который может найти применение для синтеза йодсодержащих лекарственных препаратов. Способ заключается во взамодействии диметилгидразона глиоксаля с броммалоннитрилом и йодидом калия в водно-диоксановом растворе. Предпочтительно реакцию осуществляют при комнатной температуре в течение 72 ч, или при нагревании до 40°С в течение 5 мин, или при действии ультразвука частотой 90-100 Гц или микроволнового излучения 150 W. 1 з.п. ф-лы, 4 пр.
, который может найти применение для синтеза йодсодержащих лекарственных препаратов. Способ заключается во взамодействии диметилгидразона глиоксаля с броммалоннитрилом и йодидом калия в водно-диоксановом растворе. Предпочтительно реакцию осуществляют при комнатной температуре в течение 72 ч, или при нагревании до 40°С в течение 5 мин, или при действии ультразвука частотой 90-100 Гц или микроволнового излучения 150 W. 1 з.п. ф-лы, 4 пр.
1 Способ получения трийодида N,N-диметилгидразения формулы 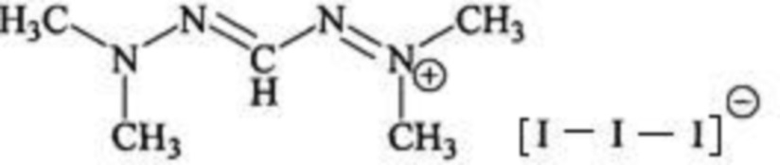 , включающий взамодействие диметилгидразона глиоксаля, броммалоннитрила и йодида калия в водно-диоксановом растворе.
, включающий взамодействие диметилгидразона глиоксаля, броммалоннитрила и йодида калия в водно-диоксановом растворе.
2. Способ получения трийодида N,N-диметилгидразения формулы  по п. 1, отличающийся тем, что реакцию проводят при комнатной температуре в течение 72 ч, или при нагревании до 40°С в течение 5 мин, или при действии ультразвука частотой 90-100 Гц в течение 5 мин, или при действии микроволнового излучения 150 W в течение 8 мин.
по п. 1, отличающийся тем, что реакцию проводят при комнатной температуре в течение 72 ч, или при нагревании до 40°С в течение 5 мин, или при действии ультразвука частотой 90-100 Гц в течение 5 мин, или при действии микроволнового излучения 150 W в течение 8 мин.
| ТРИЙОДИДЫ ЧЕТВЕРТИЧНЫХ АЗОТИСТЫХ ОСНОВАНИЙ И ИХ ВОДОРАСТВОРИМАЯ КОМПОЗИЦИЯ | 1998 |
|
RU2154053C2 |
| US 5023332 A, 11.06.1991 | |||
| Этил-3-(2,2-диметил-2-этилгидразиний)пропионат иодистый, проявляющий антиаритмическую активность | 1987 |
|
SU1680693A1 |
| BARTON D | |||
| H | |||
| R | |||
| ET AL., A new reaction of hydrazones, JOURNAL OF THE CHEMICAL SOCIETY (Resumed), 1962, 470 | |||
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
Авторы
Даты
2023-08-24—Публикация
2023-02-09—Подача