ОБЛАСТЬ ТЕХНИКИ
[0001] Настоящая технология относится к пирролидиновым и пиперидиновым соединениям, их стереоизомерам и фармацевтически приемлемым солям, обладающим ингибирующей активностью в отношении белка активации фибробластов (FAP). Также предусмотрены способы получения, фармацевтические композиции и способы применения.
УРОВЕНЬ ТЕХНИКИ
[0002] Белок активации фибробластов (FAP) представляет собой гомодимерную интегральную мембранную сериновую протеазу типа II, принадлежащую к группе дипептидилпептидазы-4 (дипептидилпептидаза IV, DPP4). Эта группа белков включает белки других подтипов, такие как DPP7, 8, 9 и т.д. FAP и DPP4 имеют около 50% сходства аминокислотной последовательности. Однако, в отличие от DPP4, который экспрессируется в большинстве биологических тканей, FAP экспрессируется в участках ремоделирования тканей, включая, но не ограничиваясь ими, злокачественную опухоль, фиброз, атеросклероз и артрит.
[0003] FAP, как и DPP4, обладает дипептидилпептидазной активностью, способной расщеплять постпролиновую связь по двум или более остаткам с N-конца, но, в отличие от DPP4, FAP также обладает специфической ферментативной активностью эндопептидазы, способной расщеплять глицин-пролиновую связь, присутствующую в субстрате (Aertgeerts et al., J. Biol. Chem., 2005, 280, 19441). Кроме того, FAP обладает коллагеназной активностью, способной расщеплять желатин и коллаген типа 1 (CN-1) (Fuming Zi et al., Molecular Medicine Reports, November 2015, 3203).
[0004] FAP экспрессируется там, где происходит ремоделирование ткани, например, при фиброзе печени (Levy et al., Hepatol, 1999, 29:1768). Было обнаружено, что у пациентов с фиброзом печени в результате злоупотребления алкоголем или вирусной инфекции, в клетках экспрессируется большое количество FAP, связанного с чрезмерным рубцеванием и заболеваниями печени. В качестве примера сообщалось, что экспрессия FAP увеличивается в активированных звездчатых клетках печени (далее «aHSC») и миофибробластах, которые играют важную роль в фиброзе печени (Levy et al., Hepatol., 1999, 29, 1768; Lay AJ et al., Front. Biosci. [Landmark Ed] 2019, 24, 1-17).
[0005] Субстраты, расщепляемые FAP, включают α2-антиплазмин, белок Sprouty-2, а также желатин и коллаген 1 типа (CN-1). Недавно сообщалось, что фактор роста фибробластов-21 (FGF21), который является одним из немитогенных гепатокинов, также является субстратом, расщепляемым FAP (D.R. Dunshee et al., J. Biol. Chem., 2016, 291, 5986).
[0006] Соответственно, существует потребность в ингибиторах FAP, которые можно успешно применять для профилактики и лечения заболеваний.
РАСКРЫТИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
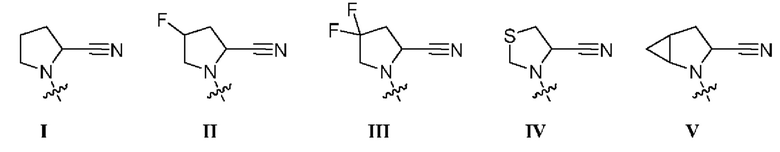
[0007] В данном документе в одном аспекте представлено соединение формулы 1:
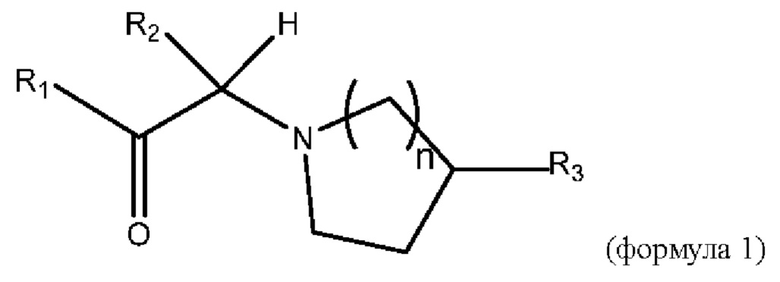
где
n представляет собой 1 или 2;
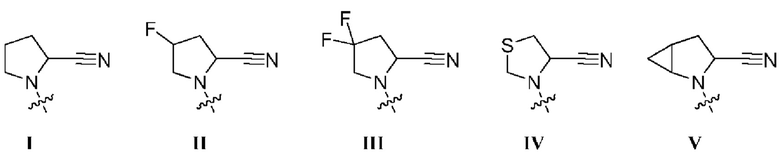
R1 выбран из группы, состоящей из формул I, II, III, IV, и IV;
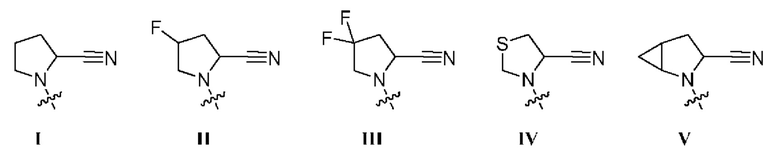
R2 представляет собой водород или C1-3алкил;
R3 представляет собой 5-12-членный гетероарил, причем указанный гетероарил содержит от 1 до 3 гетероатомов, выбранных из О, N и S, и необязательно замещен 1-3 Z,
3-12-членный неароматический гетероцикл, причем указанный гетероцикл содержит от 1 до 3 гетероатомов, выбранных из О, N и S, и необязательно замещен 1-3 Z,
-NR4R5, -OR4, -C(O)NHR4, -NHC(O)(CH2)mR4, -NHS(O)2R4, -(CH2)mCH2R4, или -(CH2)mNHR4,
где m представляет собой 0 или 1;
R4 представляет собой фенил, замещенный 1-3 Z,
гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила,
дигидробензо[1,4]диоксинила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинила, где указанный гетероцикл необязательно замещен 1-3 Z,
нафтил, необязательно замещенный 1-3 Z или
гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила, пиразинила, имидазолила, пиразолила, триазолила, оксазолила, тиазолила, фуранила, пирролила, тиофенила, хинолинила, изохинолинила, хроменонила, хиназолинила, бензоксазолила, бензофуранила, бензотиофенила, индолила, индолинила, бензимидазолила, бензоксазолила, бензотиазолила, индазолила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила, акридинила и нафтиридинила, где указанный гетероарил необязательно замещен 1-3 Z;
R5 представляет собой водород или C1-3алкил; и
каждый Z независимо выбран из группы, состоящей из гидрокси, амино, галогена, циано, нитро, карбоновой кислоты, С1-5алкила, необязательно замещенного 1-3 Z1, С2-6алкенила, необязательно замещенного Z1, С2-6алкинила, необязательно замещенного Z1, С1-5алкокси, необязательно замещенного 1-3 Z1, С1-5алкилтио, необязательно замещенного Z1, моно- или ди-С1-5алкиламино, необязательно замещенного Z1, пиперазинила, необязательно замещенного Z1, С1-5алкилсульфониламино, необязательно замещенного Z1, С1-5алкилкарбониламино, необязательно замещенного Z1, аминосульфонила, необязательно замещенного Z1, аминокарбонила, необязательно замещенного Z1, С1-5алкиламинокарбонила, необязательно замещенного Z1, фенила, необязательно замещенного Z1, фенокси, необязательно замещенного Z1, бензила, необязательно замещенного Z1, бензоила, необязательно замещенного Z1, фениламинокарбонила, необязательно замещенного Z1, пиразолила, необязательно замещенного Z1, бензоксазолила, необязательно замещенного Z1, C1-5алкоксикарбонила, необязательно замещенного Z1, бензилокси, необязательно замещенного Z1, C1-5алкилсульфонила, необязательно замещенного Z1 ацетила, морфолинила, необязательно замещенного Z1, -NR6C(O)R7 и -C(O)NR6R7;
где каждый Z1 независимо выбран из галогена, гидроксила, амино, C1-5алкиламино, циано, ацетила, C1-5алкила, С1-5галогеналкила, С3-6карбоцикла, С3-6гетероцикла, при этом указанный С3-6карбоцикл и указанный С3-6гетероцикл необязательно замещен галогеном, гидроксилом, С1-5алкилом или C1-5галогеналкилом;
R6 представляет собой водород или C1-3алкильную группу;
R7 представляет собой C1-3алкильную группу, необязательно замещенную фенилом,
фенил, необязательно замещенный 1-3 Z2 или
гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила, пиразинила, имидазолила, пиразолила, триазолила, оксазолила, тиазолила, фуранила, пирролила, тиофенила, хинолинила, изохинолинила, хроменонила, хиназолинила, бензоксазолила, бензофуранила, бензотиофенила, индолила, индолинила, бензимидазолила, бензоксазолила, бензотиазолила, индазолила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила, акридинила и нафтиридинила, где указанный гетероарил необязательно замещен 1-3 Z2; и
каждый Z2 независимо выбран из группы, состоящей из гидрокси, амино, галогена, циано, нитро, гидроксикарбонила, С1-5алкила, необязательно замещенного 1-3 Z3, С2-6алкенила, С2-6алкинила, C1-5алкокси, необязательно замещенного 1-3 Z3, С1-5алкилтио, моно- или ди-С1-5алкиламино, пиперазинила, необязательно замещенного Z3, С1-5алкилсульфониламино, С1-5алкилкарбониламино, аминосульфонила, аминокарбонила, С1-5алкиламинокарбонила, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила;
где каждый Z3 независимо выбран из галогена, амино или ацетила;
или стереоизомер, или смесь стереоизомеров, или его фармацевтически приемлемая соль.
[0008] В некоторых вариантах осуществления изобретения R1 выбран из группы, состоящей из соединений формул I, II, III и V:
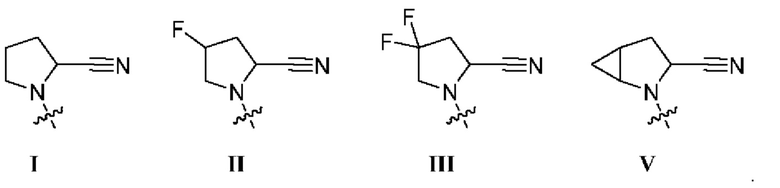
[0009] В некоторых вариантах осуществления изобретения R1 представляет собой соединение формулы I. 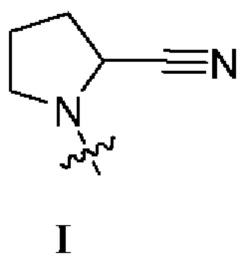 . В некоторых вариантах осуществления изобретения R1 представляет собой соединение формулы II.
. В некоторых вариантах осуществления изобретения R1 представляет собой соединение формулы II. 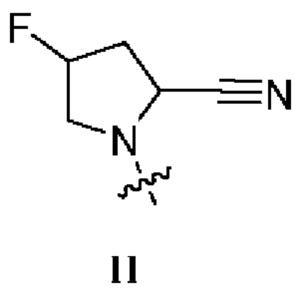 . В некоторых вариантах осуществления изобретения R1 представляет собой соединение Формулы III.
. В некоторых вариантах осуществления изобретения R1 представляет собой соединение Формулы III. 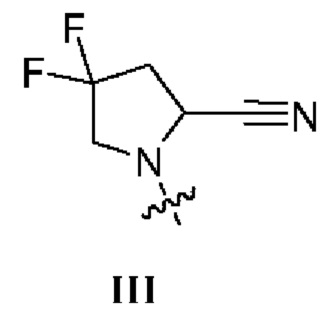 . В некоторых вариантах осуществления изобретения R1 представляет собой соединение формулы IV.
. В некоторых вариантах осуществления изобретения R1 представляет собой соединение формулы IV. 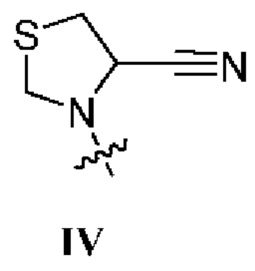 . В некоторых вариантах осуществления изобретения R1 представляет собой соединение формулы V
. В некоторых вариантах осуществления изобретения R1 представляет собой соединение формулы V 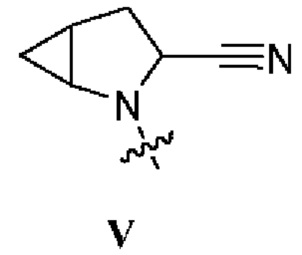 .
.
[0010] В некоторых вариантах осуществления R1 представляет собой заместитель, выбранный из группы, состоящей из соединений формул Ia-Va,

[0011] В некоторых вариантах осуществления R1 представляет собой заместитель, выбранный из группы, состоящей из соединений формул Ia, IIa, IIIa, и Va:
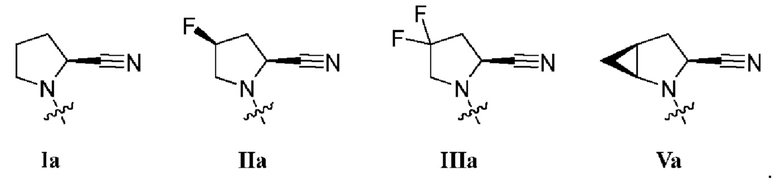
[0012] В некоторых вариантах осуществления изобретения R1 представляет собой соединение формулы Ia: 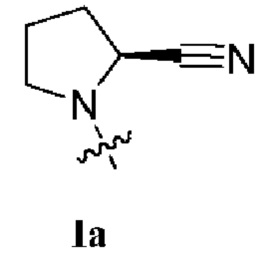 . В некоторых вариантах осуществления изобретения R1 представляет собой соединение формулы IIa:
. В некоторых вариантах осуществления изобретения R1 представляет собой соединение формулы IIa: 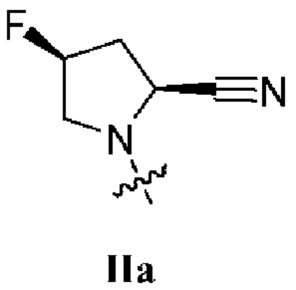 . В некоторых вариантах осуществления изобретения R1 представляет собой соединение формулы IIIa:
. В некоторых вариантах осуществления изобретения R1 представляет собой соединение формулы IIIa:  . В некоторых вариантах осуществления изобретения R1 представляет собой соединение формулы IVa:
. В некоторых вариантах осуществления изобретения R1 представляет собой соединение формулы IVa: 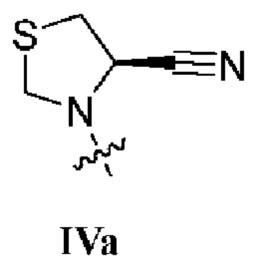 . В некоторых вариантах осуществления изобретения R1 представляет собой соединение формулы Va:
. В некоторых вариантах осуществления изобретения R1 представляет собой соединение формулы Va: 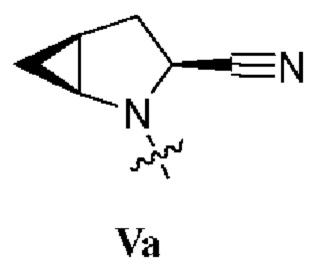 .
.
[0013] В некоторых вариантах осуществления R2 представляет собой водород. В некоторых вариантах осуществления R2 представляет собой С1-3алкил.
[0014] В некоторых вариантах осуществления соединение или его стереоизомер или смесь стереоизомеров или его фармацевтически приемлемая соль имеет структуру формулы 1а:
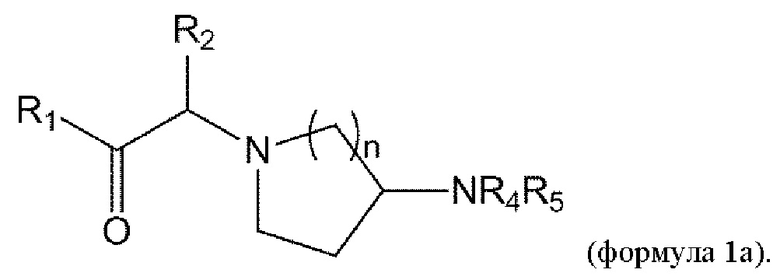
В дополнительных вариантах осуществления R5 представляет собой водород. В других вариантах осуществления R5 представляет собой C1-3алкил.
[0015] В некоторых вариантах осуществления соединение или его стереоизомер или смесь стереоизомеров или его фармацевтически приемлемая соль имеет структуру формулы 1b:
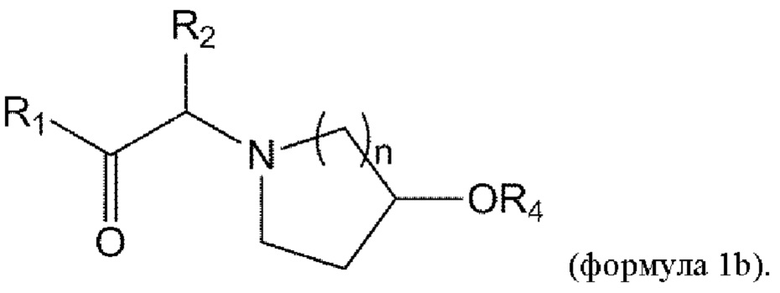
[0016] В некоторых вариантах осуществления соединение или его стереоизомер или смесь стереоизомеров или его фармацевтически приемлемая соль имеет структуру формулы 1с:
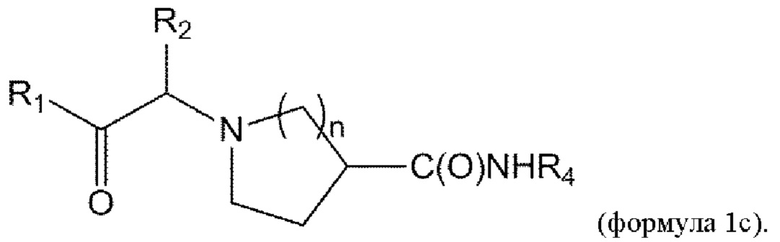
[0017] В некоторых вариантах осуществления соединение или его стереоизомер или смесь стереоизомеров или его фармацевтически приемлемая соль имеет структуру формулы 1d:
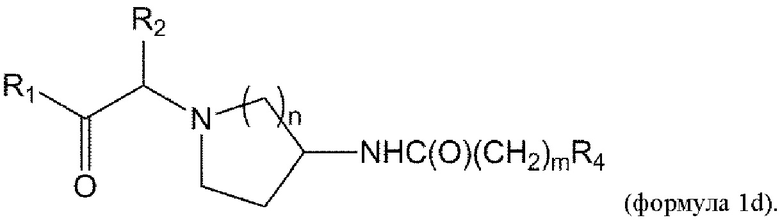 В дополнительных вариантах осуществления m равно 0. В других вариантах осуществления m равно 1.
В дополнительных вариантах осуществления m равно 0. В других вариантах осуществления m равно 1.
[0018] В некоторых вариантах осуществления соединение или его стереоизомер или смесь стереоизомеров или его фармацевтически приемлемая соль имеет структуру формулы 1е:
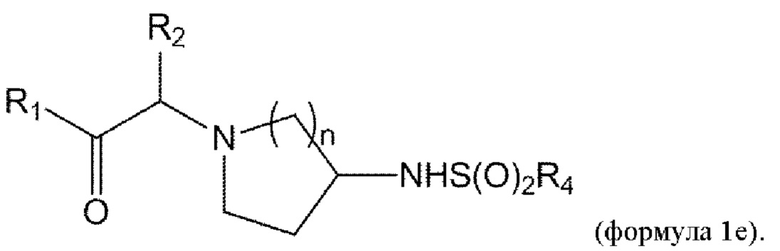
[0019] В некоторых вариантах осуществления изобретения R3 представляет собой заместитель, выбранный из группы, состоящей из -NR4R5, -OR4, -C(O)NHR4, -NHC(O)(CH2)mR4, и -NHS(O)2R4. В некоторых вариантах осуществления изобретения R3 представляет собой заместитель, выбранный из группы, состоящей из -NR4R5, -OR4, и -NHC(O)(CH2)mR4. В некоторых вариантах осуществления изобретения R3 представляет собой заместитель, выбранный из группы, состоящей из -NR4R5 и -OR4.
[0020] В некоторых вариантах осуществления изобретения R4 представляет собой фенил, замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, галогена, циано, нитро, карбоновой кислоты, С1-5алкила, необязательно замещенного 1-3 галогенами или аминогруппой, С2-6алкенила, С2-6алкинила, С1-5алкокси, С1-5алкилтио, моно- или ди-С1-5алкиламино, пиперазинила, необязательно замещенного ацетилом, С1-5алкилсульфониламино, С1-5алкилкарбониламино, аминосульфонила, аминокарбонила, С1-5алкиламинокарбонила, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила. В дополнительных вариантах осуществления R4 представляет собой фенил, замещенный заместителем, выбранным из группы, состоящей из пиперазинила, необязательно замещенного ацетилом, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила.
[0021] В некоторых вариантах осуществления изобретения R4 представляет собой гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, дигидробензо[1,4]диоксинила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинила, причем указанный гетероцикл необязательно замещен 1-3 Z. В дополнительных вариантах осуществления R4 представляет собой гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинила.
[0022] В некоторых вариантах осуществления изобретения R4 представляет собой нафтил, необязательно замещенный галогеном.
[0023] В некоторых вариантах осуществления изобретения R4 представляет собой гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила, пиразинила, имидазолила, пиразолила, триазолила, оксазолила, тиазолила, фуранила, пирролила, тиофенила, хинолинила, изохинолинила, хроменонила, хиназолинила, бензоксазолила, бензофуранила, бензотиофенила, индолила, индолинила, бензимидазолила, бензоксазолила, бензотиазолила, индазолила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила, акридинила и нафтиридинила, где указанный гетероарил необязательно замещен 1-3 Z, где каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-С1-5алкиламино, циано, нитро, галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, C1-5алкокси, необязательно замещенного от 1 до 3 галогенов, C1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила, С1-5алкилсульфонила, морфолинила, -NR6C(O)R7 и -C(O)NR6R7. В дополнительных вариантах осуществления R4 представляет собой гетероарил, выбранный из группы, состоящей из пиридинила, хинолинила, изохинолинила, хроменонила, хиназолинила, бензофуранила, индолинила, бензимидазолила, бензотиофенила, бензотиазолила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила, акридинила и нафтиридинила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, необязательно замещенного 1-3 галогенами, C1-5алкоксикарбонила, бензилокси, ацетила, морфолинила, -NR6C(O)R7, -C(O)NR6R7 и фенила, необязательно замещенного галогеном; где R6 представляет собой водород или C1-3алкильную группу; и R7 представляет собой C1-3алкильную группу, необязательно замещенную фенилом, фенил или гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила и изоксазолила.
[0024] В других вариантах осуществления R4 представляет собой фенил, замещенный заместителем, выбранным из группы, состоящей из пиперазинила, необязательно замещенного ацетилом, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила;
гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинила;
нафтил, необязательно замещенный галогеном; или
гетероарил, выбранный из группы, состоящей из пиридинила, хинолинила, изохинолинила, хрома, хиназолинила, бензофуранила, индолинила, бензимидазолила, бензотиофенила, бензотиазолила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила, акридинила и нафтиридинила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, необязательно замещенного 1-3 галогенами, С1-5алкоксикарбонила, бензилокси, ацетила, морфолинила, -NR6C(O)R7, -C(O)NR6R7 и фенила, необязательно замещенного галогеном; где R6 представляет собой водород или C1-3алкильную группу; и R7 представляет собой C1-3алкильную группу, необязательно замещенную фенилом, фенил или гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила и изоксазолила.
[0025] В некоторых вариантах осуществления изобретения R4 представляет собой фенил, замещенный фенилом; нафтил; гетероарил, выбранный из группы, состоящей из пиридинила, хинолинила, изохинолинила, хроменонила, хиназолинила, бензофуранила, индолинила, бензимидазолила, бензотиофенила, бензотиазолила, фуро[3,2-с]пиридинила и нафтиридинила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, циано, нитро, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, необязательно замещенного 1-3 галогенами, бензилокси, ацетила, морфолинила, -NR6C(O)R7, -C(O)NR6R7. В дополнительных вариантах осуществления R4 представляет собой фенил, замещенный фенилом. В других вариантах осуществления изобретения R4 представляет собой нафтил. В других вариантах осуществления изобретения R4 представляет собой гетероарил, выбранный из группы, состоящей из пиридинила, хинолинила, изохинолинила, хрома, хиназолинила, бензофуранила, индолинила, бензимидазолила, бензотиофенила, бензотиазолила, фуро[3,2-с]пиридинила и нафтиридинила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, циано, нитро, галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, необязательно замещенного 1-3 галогенами, бензилокси, ацетила, морфолинила, -NR6C(O)R7, -C(O)NR6R7. R6 представляет собой водород или C1-3алкильную группу; и R7 представляет собой C1-3алкильную группу, необязательно замещенную фенилом, фенил или гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила и изоксазолила. В дополнительных вариантах осуществления R4 представляет собой хинолинил или изохинолинил, каждый из которых необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, циано, нитро, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, необязательно замещенного 1-3 галогенами, бензилокси, ацетила, морфолинила, -NR6C(O)R7 и -C(O)NR6R7. В дополнительных вариантах осуществления R4 представляет собой хинолинил, необязательно замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, циано, нитро, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, необязательно замещенного 1-3 галогенами, бензилокси, ацетила, морфолинила, -NR6C(O)R7 и -C(O)NR6R7. В других вариантах осуществления изобретения R4 представляет собой бензофуранил, бензотиофенил или фуро[3,2-с]пиридинил, каждый из которых необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из галогена, С1-5алкила и С1-5алкокси. В дополнительных вариантах осуществления R4 представляет собой бензофуранил или бензотиофенил, каждый из которых необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из галогена, С1-5алкила и С1-5алкокси.
[0026] В других вариантах осуществления R4 представляет собой фенил, замещенный заместителем, выбранным из группы, состоящей из пиперазинила, необязательно замещенного ацетилом, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила;
гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинила;
нафтил, необязательно замещенный галогеном; или
гетероарил, выбранный из группы, состоящей из пиридинила, хинолинила, изохинолинила, хиназолинила, тиено[2,3-d]пиримидинила, изоксазолила и акридинила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из циано, галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, C1-5алкокси, необязательно замещенного 1-3 галогенами, бензилокси и фенила, необязательно замещенного галогеном. В дополнительных вариантах осуществления R4 представляет собой фенил, замещенный заместителем, выбранным из группы, состоящей из пиперазинила, необязательно замещенного ацетилом, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила. В других вариантах осуществления изобретения R4 представляет собой гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-. В других вариантах осуществления изобретения R4 представляет собой нафтил, необязательно замещенный галогеном. В других вариантах осуществления изобретения R4 представляет собой гетероарил, выбранный из группы, состоящей из пиридинила, хинолинила, изохинолинила, хиназолинила, тиено[2,3-d]пиримидинила, изоксазолила и акридинила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из циано, галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, необязательно замещенного 1-3 галогенами, бензилокси и фенила, необязательно замещенного галогеном. В дополнительных вариантах осуществления R4 представляет собой хинолинил, изохинолинил или хиназолинил, каждый из которых необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из циано, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, и С1-5алкокси, необязательно замещенного 1-3 галогенами.
[0027] В некоторых вариантах осуществления R4 представляет собой хинолинил.
[0028] В некоторых вариантах осуществления изобретения R4 представляет собой фенил, замещенный фенилом; нафтил; или гетероарил, выбранный из группы, состоящей из хинолинила, изохинолинила, бензофуранила и бензотиофенила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, галогена, С1-5алкила и С1-5алкокси. В дополнительных вариантах осуществления R4 представляет собой фенил, замещенный фенилом. В других вариантах осуществления изобретения R4 представляет собой нафтил. В других вариантах осуществления изобретения R4 представляет собой гетероарил, выбранный из группы, состоящей из хинолинила, изохинолинила, бензофуранила и бензотиофенила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, галогена, С1-5алкила и С1-5алкокси. В дополнительных вариантах осуществления R4 представляет собой бензофуранил, необязательно замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, галогена, C1-5алкила и С1-5алкокси. В других вариантах осуществления изобретения R4 представляет собой хинолинил или изохинолинил, каждый из которых необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, галогена, C1-5алкила и C1-5алкокси.
[0029] В некоторых вариантах осуществления R4 представляет собой бензофуранил или бензотиофенил.
[0030] В некоторых вариантах осуществления изобретения R3 представляет собой 3-12-членный неароматический гетероцикл, содержащий азот, причем указанный гетероцикл необязательно замещен 1-3 Z. В некоторых вариантах осуществления R3 представляет собой 5-12-членный гетероарил, необязательно замещенный 1-5 Z. В некоторых вариантах осуществления R3 представляет собой 2-оксо-2,3-дигидро-1Н-бензо[d]имидазол-1-ил.
[0031] В некоторых вариантах осуществления изобретения n представляет собой 1 или 2; R1 представляет собой заместитель, выбранный из группы, состоящей из соединений формул I, II, III, и V; R2 представляет собой водород; R3 представляет собой заместитель, выбранный из группы, состоящей из -NR4R5, -OR4, -C(O)NHR4, -NHC(O)(CH2)mR4, и -NHS(O)2R4; где m представляет собой 0 или 1; где R1 представляет собой фенил, замещенный заместителем, выбранным из группы, состоящей из пиперазинила, необязательно замещенного ацетилом, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила; гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинила; нафтил, необязательно замещенный галогеном; или гетероарил, выбранный из группы, состоящей из пиридинила, хинолинила, изохинолинила, хиназолинила, бензофуранила, бензотиофенила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила и акридинила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, необязательно замещенного 1-3 галогенами, С1-5алкоксикарбонила, бензилокси и фенила, необязательно замещенного галогеном; и R5 представляет собой водород.
[0032] В некоторых вариантах осуществления n представляет собой 1. В некоторых вариантах осуществления n представляет собой 2.
[0033] В некоторых вариантах осуществления соединение или его стереоизомер или смесь стереоизомеров или его фармацевтически приемлемую соль выбирают из таблицы 1 или стереоизомеров или смеси стереоизомеров или их фармацевтически приемлемой соли.
[0034] В данном документе в другом аспекте представлена фармацевтическая композиция, содержащая соединение, описанное в настоящем документе, или стереоизомер или смесь стереоизомеров, или его фармацевтически приемлемую соль, и по меньшей мере один фармацевтически приемлемый эксципиент.
[0035] В данном документе в другом аспекте представлен способ ингибирования белка активации фибробластов у млекопитающего, включающий введение млекопитающему терапевтически эффективного количества соединения или его стереоизомеров или смеси стереоизомеров или его фармацевтически приемлемой соли, описанной в настоящем документе.
[0036] В настоящем документе в другом аспекте предложен способ лечения не алкогольного стеатогепатита (НАСГ) у субъекта, нуждающегося в этом, включающий введение субъекту терапевтически эффективного количества соединения, описанного в данном документе, или его стереоизомеров или смеси стереоизомеров или его фармацевтически приемлемой соли или терапевтически эффективного количества фармацевтической композиции, описанной в настоящем документе.
[0037] В данном документе в другом аспекте представлено применение соединения, описанного в настоящем документе, или его стереоизомера или смеси стереоизомеров или его фармацевтически приемлемой соли для производства лекарственного средства для лечения НАСГ.
[0038] В настоящем документе в другом аспекте предложено соединение, описанное в настоящем документе, или его стереоизомер или смесь стереоизомеров, или его фармацевтически приемлемая соль для применения в лечении НАСГ.
[0039] В настоящем документе в другом аспекте предложена композиция, описанная в настоящем документе для применения в лечении НАСГ.
[0040] В настоящем документе в другом аспекте представлено соединение, описанное в настоящем документе, или его стереоизомер или смесь стереоизомеров, или его фармацевтически приемлемая соль для применения при ингибировании белка активации фибробластов.
[0041] В настоящем документе в другом аспекте предложена композиция, описанная в настоящем документе для применения при ингибировании белка активации фибробластов.
[0042] В настоящем документе в другом аспекте предложен способ лечения заболевания, опосредованного белком активации фибробластов у субъекта, нуждающегося в этом, включающий введение субъекту терапевтически эффективного количества соединения, описанного в данном документе, или его стереоизомеров или смеси стереоизомеров или его фармацевтически приемлемой соли или терапевтически эффективного количества фармацевтической композиции, описанной в настоящем документе. В некоторых вариантах осуществления заболевание, опосредованное белком активации фибробластов, выбрано из группы, состоящей из липидных и липопротеиновых нарушений, состояний и заболеваний, которые возникают в результате хронической жировой и фиброзной дистрофии органов вследствие накопления липидов и, в частности, триглицеридов, и последующей активации профибротических путей, сахарного диабета I или II типа и клинических осложнений сахарного диабета I и II типа, хронических внутрипеченочных или некоторых форм внепеченочных холестатических состояний, фиброза печени, острых внутрипеченочных холестатических состояний, обструктивных или хронических воспалительных заболеваний, возникающих из-за неправильного состава желчи, желудочно-кишечных заболеваний со сниженным усвоением пищевых жиров и жирорастворимых пищевых витаминов, воспалительных заболеваний кишечника, ожирения и метаболического синдрома (сочетания дислипидемии, диабета и аномально высокого индекса массы тела), персистирующих инфекций внутриклеточными бактериями или паразитарными простейшими, незлокачественных гиперпролиферативных заболеваний, злокачественных гиперпролиферативных заболеваний, аденокарциномы толстой кишки и гепатоцеллюлярной карциномы, в частности, стеатоза печени и связанных с ним синдромов, инфекции гепатита В, инфекции гепатита С и/или холестатических и фиброзных эффектов, которые связаны с алкогольным циррозом печени или с вирусными формами гепатита, печеночной недостаточности или нарушении функции печени в результате хронических заболеваний печени или хирургической резекции печени, острого инфаркта миокарда, острого инсульта, тромбоза, возникающего как конечная точка хронического обструктивного атеросклероза, остеоартрита, ревматоидного артрита, псориаза и ишемического инсульта, по отдельности или любой их комбинации.
[0043] В настоящем документе в другом аспекте представлено соединение, описанное в настоящем документе, или его стереоизомер или смесь стереоизомеров, или его фармацевтически приемлемая соль для применения при лечении заболевания, опосредованного белком активации фибробластов. В некоторых вариантах осуществления заболевание, опосредованное белком активации фибробластов, выбрано из группы, состоящей из липидных и липопротеиновых нарушений, состояний и заболеваний, которые возникают в результате хронической жировой и фиброзной дистрофии органов вследствие накопления липидов и, в частности, триглицеридов, и последующей активации профибротических путей, сахарного диабета I или II типа и клинических осложнений сахарного диабета I и II типа, хронических внутрипеченочных или некоторых форм внепеченочных холестатических состояний, фиброза печени, острых внутрипеченочных холестатических состояний, обструктивных или хронических воспалительных заболеваний, возникающих из-за неправильного состава желчи, желудочно-кишечных заболеваний со сниженным усвоением пищевых жиров и жирорастворимых пищевых витаминов, воспалительных заболеваний кишечника, ожирения и метаболического синдрома (сочетания дислипидемии, диабета и аномально высокого индекса массы тела), персистирующих инфекций внутриклеточными бактериями или паразитарными простейшими, незлокачественных гиперпролиферативных заболеваний, злокачественных гиперпролиферативных заболеваний, аденокарциномы толстой кишки и гепатоцеллюлярной карциномы, в частности, стеатоза печени и связанных с ним синдромов, инфекции гепатита В, инфекции гепатита С и/или холестатических и фиброзных эффектов, которые связаны с алкогольным циррозом печени или с вирусными формами гепатита, печеночной недостаточности или нарушении функции печени в результате хронических заболеваний печени или хирургической резекции печени, острого инфаркта миокарда, острого инсульта, тромбоза, возникающего как конечная точка хронического обструктивного атеросклероза, остеоартрита, ревматоидного артрита, псориаза и ишемического инсульта, по отдельности или любой их комбинации.
[0044] В настоящем документе в другом аспекте предложен способ лечения рака у субъекта, нуждающегося в этом, включающий введение субъекту терапевтически эффективного количества соединения, описанного в данном документе, или его стереоизомеров или смеси стереоизомеров или его фармацевтически приемлемой соли или терапевтически эффективного количества фармацевтической композиции, описанной в настоящем документе.
[0045] В данном документе в другом аспекте представлено соединение, описанное в настоящем документе, или его стереоизомер или смесь стереоизомеров, или его фармацевтически приемлемая соль для применения в лечении рака.
[0046] В другом аспекте настоящего документа предложен способ ингибирования деградации фактора роста фибробластов-21 у субъекта, включающий введение субъекту терапевтически эффективного количества соединения, или его стереоизомера, или смеси стереоизомеров, или его фармацевтически приемлемой соли, описанной в настоящем документе.
[0047] В настоящем документе в другом аспекте представлено соединение, описанное в настоящем документе, или его стереоизомер или смесь стереоизомеров, или его фармацевтически приемлемая соль ля применения при ингибировании деградации фактора роста фибробластов-21.
[0048] В данном документе в другом аспекте представлен способ получения соединения формулы 1а,
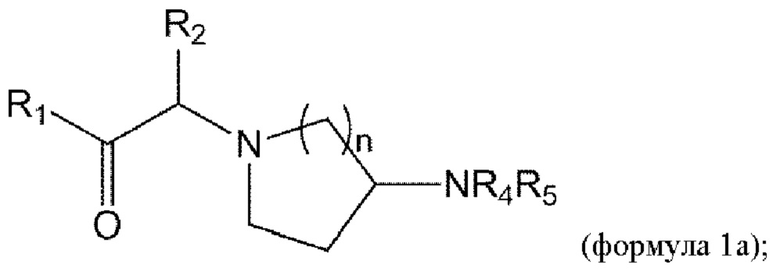
или его стереоизомера или смеси стереоизомеров или его фармацевтически приемлемой соли, причем указанный способ включает
взаимодействие соединения формулы 2а с соединением формулы 2аа в условиях, опосредованных металлами, с получением соединения формулы 3а:
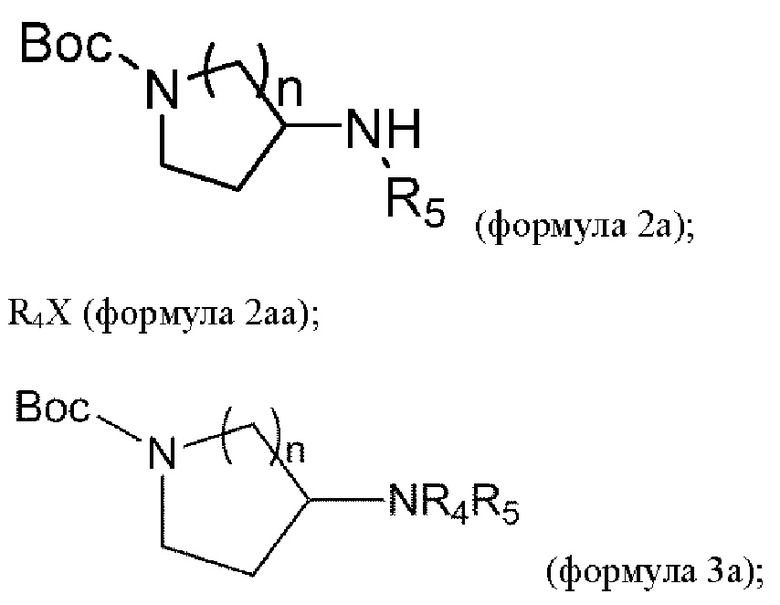
удаление Вос из соединения формулы 3а в условиях реакции с получением соединения формулы 4а:
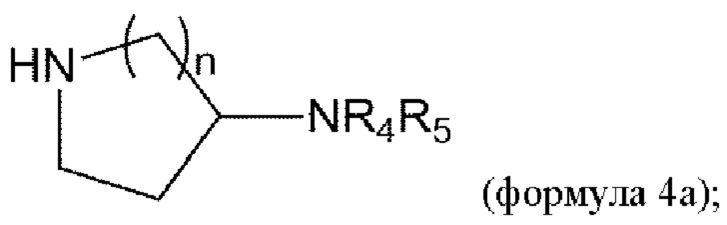 и
и
взаимодействие соединения формулы 4а с соединением формулы 5 с получением соединения формулы 1а или его изомера или его фармацевтически приемлемой соли:
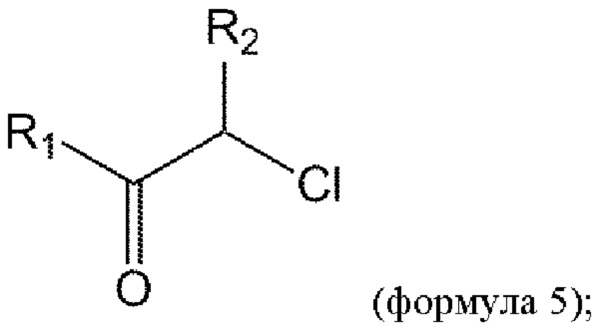
где n представляет собой 1 или 2.
где X представляет собой галоген,
где R1 представляет собой заместитель, выбранный из группы, состоящей из соединений формул I-V,
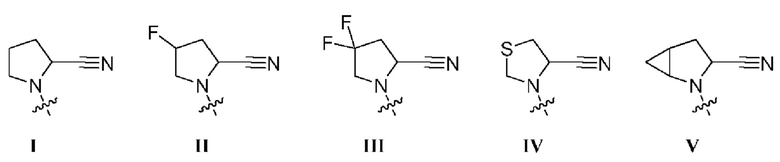
где R2 представляет собой водород или C1-3алкил,
где R4 представляет собой фенил, замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, галогена, циано, нитро, карбоновой кислоты, С1-5алкила, необязательно замещенного 1-3 галогенами или аминогруппой, С2-6алкенила, С2-6алкинила, С1-5алкокси, C1-5алкилтио, моно- или ди-С1-5алкиламино, пиперазинила, необязательно замещенного ацетилом, C1-5алкилсульфониламино, С1-5алкилкарбониламино, аминосульфонила, аминокарбонила, C1-5алкиламинокарбонила, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила;
гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, дигидробензо[1,4]диоксинила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинил;
нафтил, необязательно замещенный галогеном; или
гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила, пиразинила, имидазолила, пиразолила, триазолила, оксазолила, тиазолила, фуранила, пирролила, тиофенила, хинолинила, изохинолинила, хроменонила, хиназолинила, бензоксазолила, бензофуранила, бензотиофенила, индолила, индолинила, бензимидазолила, бензоксазолила, бензотиазолила, индазолила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила, акридинила и нафтиридинила, где указанный гетероарил необязательно замещен 1-3 Z, где каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-С1-5алкиламино, циано, нитро, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, С1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила, С1-5алкилсульфонила, морфолинила, -NR6C(O)R7, и -C(O)NR6R7;
где R5 представляет собой водород или C1-3алкил;
где R6 представляет собой водород или С1-3алкильную группу; и
где R7 представляет собой C1-3алкильную группу, необязательно замещенную фенилом; фенил; или гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила и изоксазолила.
[0049] В данном документе в другом аспекте представлен способ получения соединения формулы 1а,

или его стереоизомера или смеси стереоизомеров или его фармацевтически приемлемой соли, причем указанный способ включает
взаимодействие соединения формулы 2а с соединением формулы 2аа в условиях, опосредованных металлами, с получением соединения формулы 3а:
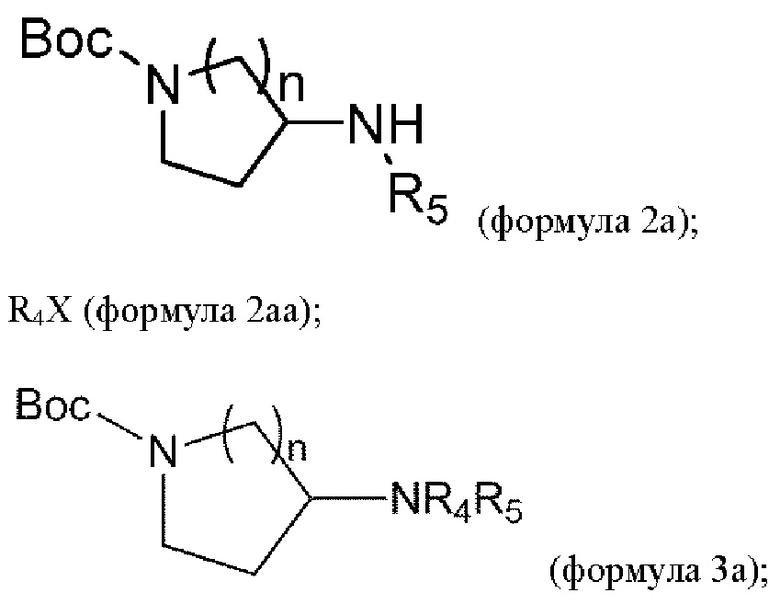
удаление Вос из соединения формулы 3а в условиях реакции с получением соединения формулы 4а:
 и
и
взаимодействие соединения формулы 4а с соединением формулы 5 с получением соединения формулы 1а или его изомера или его фармацевтически приемлемой соли:
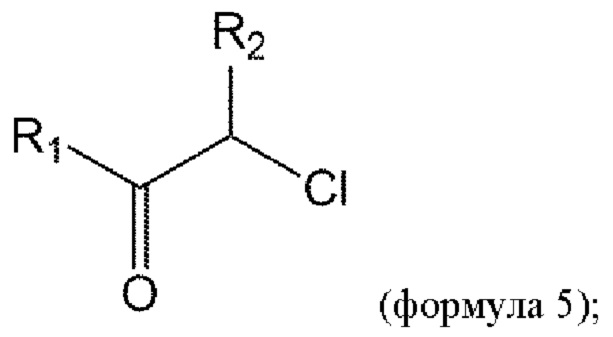
где n представляет собой 1 или 2.
где X представляет собой галоген,
где R1 представляет собой заместитель, выбранный из группы, состоящей из соединений формул I-V,
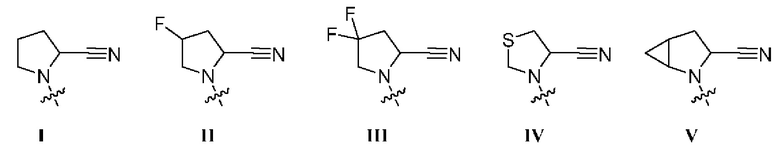
где R2 представляет собой водород или С1-3алкил,
где R4 представляет собой фенил, замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, галогена, циано, нитро, карбоновой кислоты, С1-5алкила, необязательно замещенного 1-3 галогенами или аминогруппой, С2-6алкенила, С2-6алкинила, С1-5алкокси, С1-5алкилтио, моно- или ди-С1-5алкиламино, пиперазинила, необязательно замещенного ацетилом, C1-5алкилсульфониламино, С1-5алкилкарбониламино, аминосульфонила, аминокарбонила, C1-5алкиламинокарбонила, фенила, фенокси, бензила, бензоина, фениламинокарбонила, пиразолила и бензоксазолила;
гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, дигидробензо[1,4]диоксинила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинил;
нафтил, необязательно замещенный галогеном; или
гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила, пиразинила, имидазолила, пиразолила, триазолила, оксазолила, тиазолила, фуранила, пирролила, тиофенила, хинолинила, изохинолинила, хроменонила, хиназолинила, бензоксазолила, бензофуранила, бензотиофенила, индолила, индолинила, бензимидазолила, бензоксазолила, бензотиазолила, индазолила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила и акридинила, где указанный гетероарил необязательно замещен 1-3 Z, где каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-С1-5алкиламино, циано, нитро, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, С1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила и C1-5алкилсульфонила, и
где R5 представляет собой водород или C1-3алкил.
[0050] В некоторых вариантах осуществления изобретения опосредованные металлами условия содержат палладиевый катализатор, лиганд и основание при температуре реакции в диапазоне от 50°С до 150°С.
[0051] В данном документе в другом аспекте представлен способ получения соединения формулы 1b,
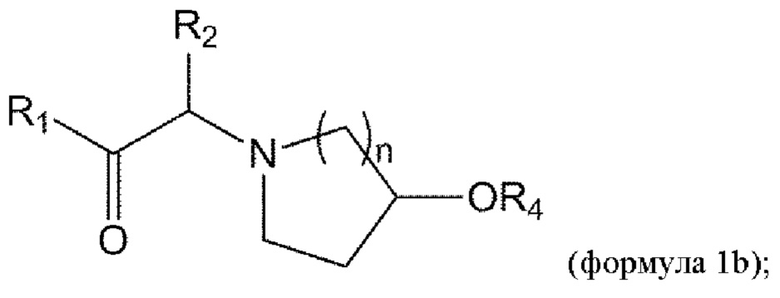
или его стереоизомера или смеси стереоизомеров или его фармацевтически приемлемой соли, причем указанный способ включает
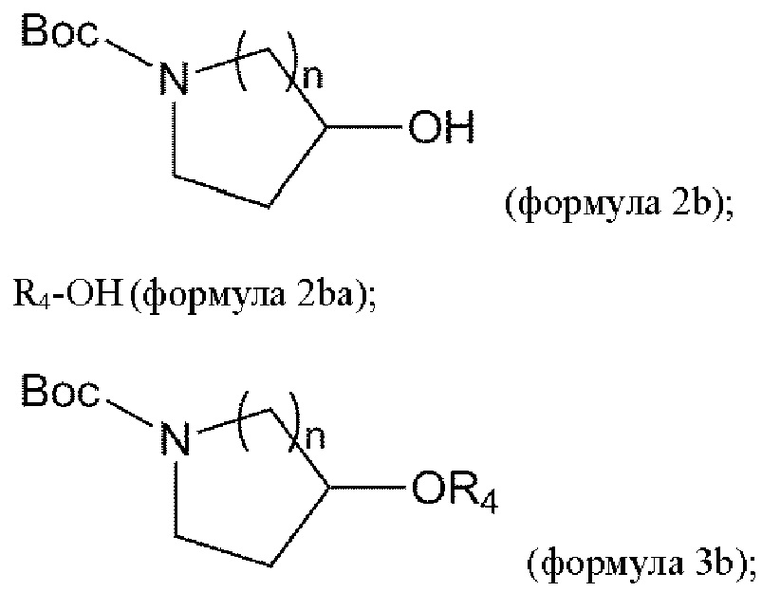
взаимодействие соединения формулы 2b с соединением формулы 2ba в условиях реакции Мицунобу с получением соединения формулы 3b:
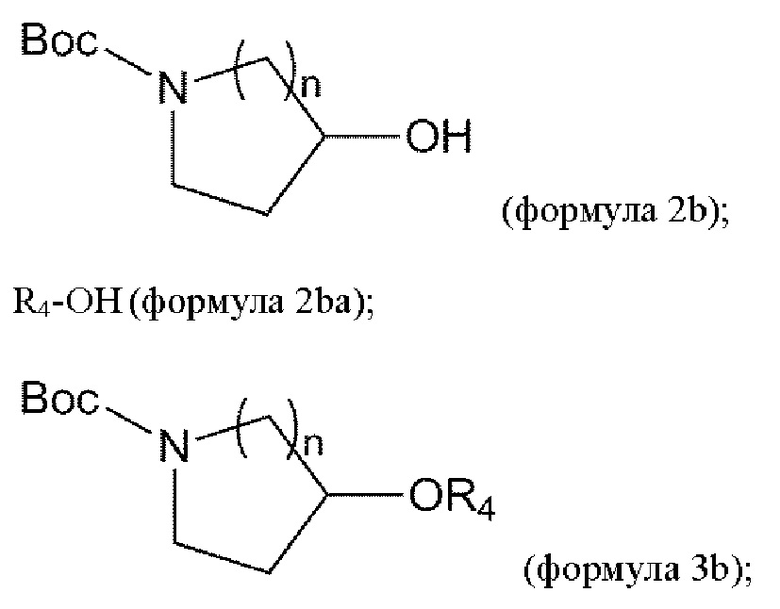
удаление Вос из соединения формулы 3b в условиях реакции с получением соединения формулы 4b:
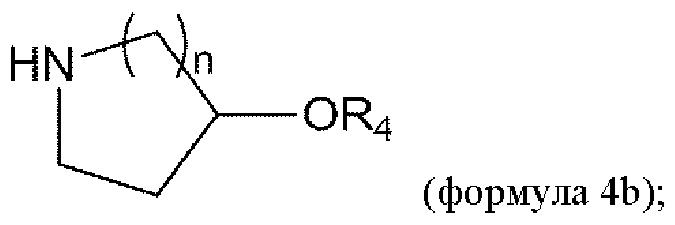 и
и
взаимодействие соединения формулы 4b с соединением формулы 5 с получением соединения формулы 1b или его изомеров или его фармацевтически приемлемой соли:
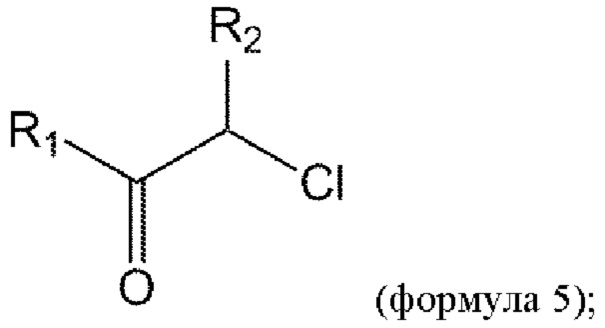
где n представляет собой 1 или 2.
где R1 представляет собой заместитель, выбранный из группы, состоящей из соединений формул I-V,
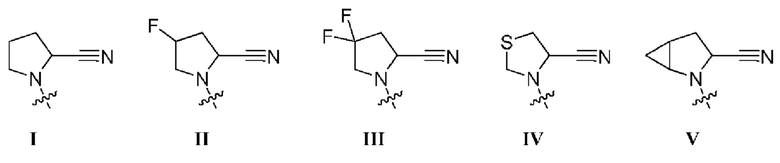
где R2 представляет собой водород или C1-3алкил и
где R4 представляет собой фенил, замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, галогена, циано, нитро, карбоновой кислоты, C1-5алкила, необязательно замещенного 1-3 галогенами или аминогруппой, С2-6алкенила, С2-6алкинила, С1-5алкокси, C1-5алкилтио, моно- или ди-С1-5алкиламино, пиперазинила, необязательно замещенного ацетилом, C1-5алкилсульфониламино, С1-5алкилкарбониламино, аминосульфонила, аминокарбонила, C1-5алкиламинокарбонила, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила;
гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, дигидробензо[1,4]диоксинила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинил;
нафтил, необязательно замещенный галогеном; или
гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила, пиразинила, имидазолила, пиразолила, триазолила, оксазолила, тиазолила, фуранила, пирролила, тиофенила, хинолинила, изохинолинила, хроменонила, хиназолинила, бензоксазолила, бензофуранила, бензотиофенила, индолила, индолинила, бензимидазолила, бензоксазолила, бензотиазолила, индазолила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила, акридинила и нафтиридинила, где указанный гетероарил необязательно замещен 1-3 Z, где каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-С1-5алкиламино, циано, нитро, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, C1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила, C1-5алкилсульфонила, морфолинила, -NR6C(O)R7, и -C(O)NR6R7;
где R6 представляет собой водород или C1-3алкильную группу; и
где R7 представляет собой C1-3алкильную группу, необязательно замещенную фенилом; фенил; или гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила и изоксазолила.
[0052] В данном документе в другом аспекте представлен способ получения соединения формулы 1b,
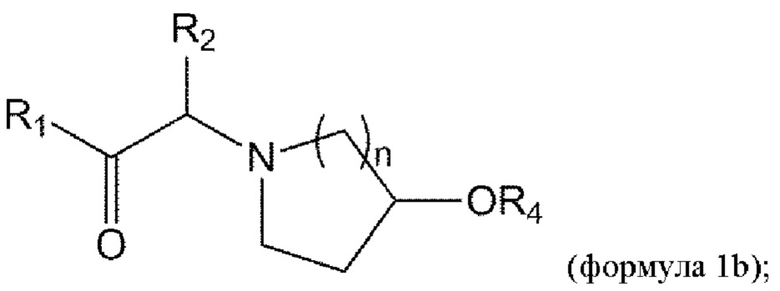
или его стереоизомера или смеси стереоизомеров или его фармацевтически приемлемой соли, причем указанный способ включает
взаимодействие соединения формулы 2b с соединением формулы 2ba в условиях реакции Мицунобу с получением соединения формулы 3b:
удаление Вос из соединения формулы 3b в условиях реакции с получением соединения формулы 4b:
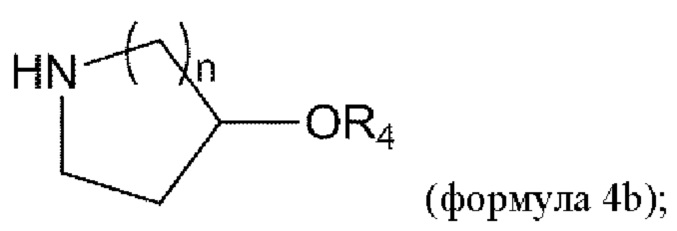 и
и
взаимодействие соединения формулы 4b с соединением формулы 5 с получением соединения формулы 1b или его изомеров или его фармацевтически приемлемой соли:
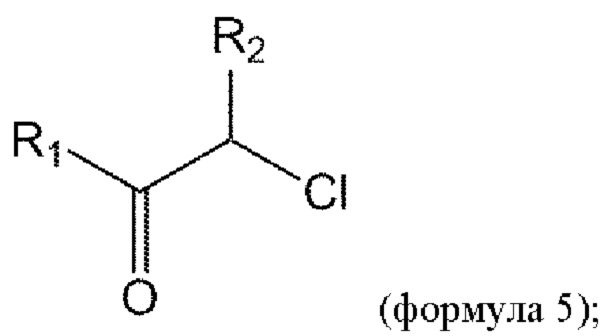
где n представляет собой 1 или 2.
где R1 представляет собой заместитель, выбранный из группы, состоящей из соединений формул I-V,

где R2 представляет собой водород или C1-3алкил и
где R4 представляет собой фенил, замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, галогена, циано, нитро, карбоновой кислоты, С1-5алкила, необязательно замещенного 1-3 галогенами или аминогруппой, С2-6алкенила, С2-6алкинила, С1-5алкокси, C1-5алкилтио, моно- или ди-С1-5алкиламино, пиперазинила, необязательно замещенного ацетилом, C1-5алкилсульфониламино, С1-5алкилкарбониламино, аминосульфонила, аминокарбонила, C1-5алкиламинокарбонила, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила;
гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, дигидробензо[1,4]диоксинила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинил;
нафтил, необязательно замещенный галогеном; или
гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила, пиразинила, имидазолила, пиразолила, триазолила, оксазолила, тиазолила, фуранила, пирролила, тиофенила, хинолинила, изохинолинила, хроменонила, хиназолинила, бензоксазолила, бензофуранила, бензотиофенила, индолила, индолинила, бензимидазолила, бензоксазолила, бензотиазолила, индазолила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила и акридинила, где указанный гетероарил необязательно замещен 1-3 Z, где каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-С1-5алкиламино, циано, нитро, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, С1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила и С1-5алкилсульфонила.
[0053] В данном документе в другом аспекте представлен способ получения соединения формулы 1с,
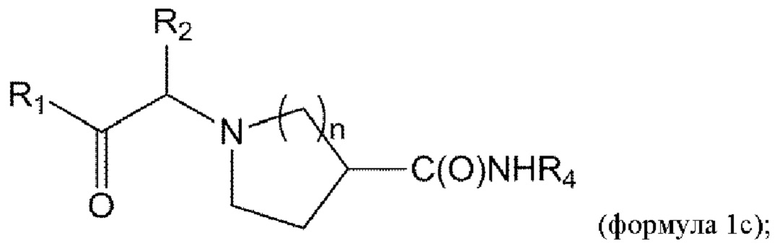
или его стереоизомера или смеси стереоизомеров или его фармацевтически приемлемой соли, причем указанный способ включает
взаимодействие соединения формулы 2с с соединением формулы 2са в условиях амидного связывания с получением соединения формулы 3с:
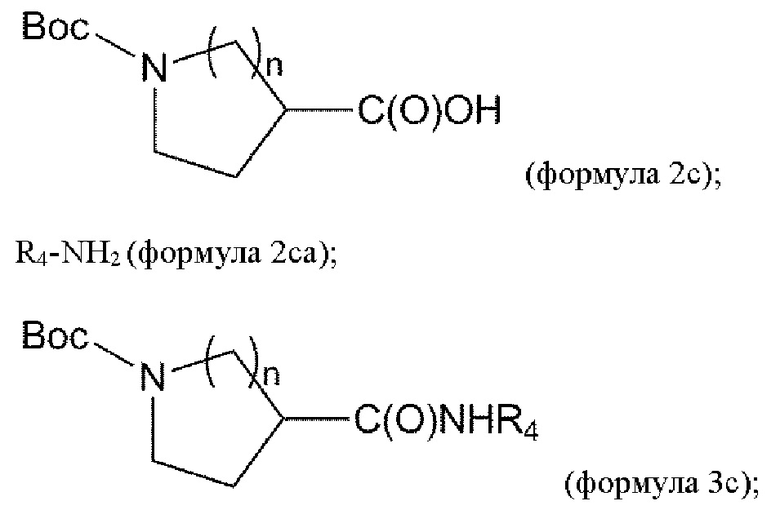
удаление Вос из соединения формулы 3с в условиях реакции с получением соединения формулы 4с:
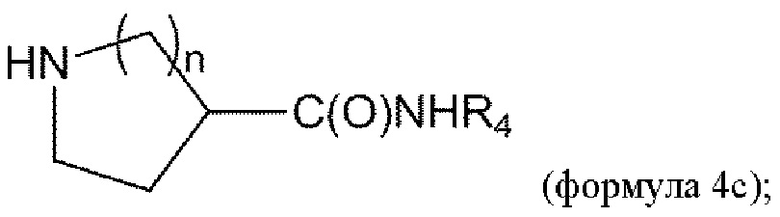 и
и
взаимодействие соединения формулы 4с с соединением формулы 5 с получением соединения формулы 1с или его изомеров или его фармацевтически приемлемой соли:
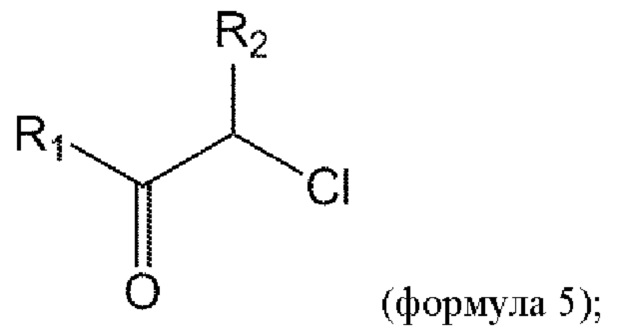
где n представляет собой 1 или 2.
где R1 представляет собой заместитель, выбранный из группы, состоящей из соединений формул I-V,
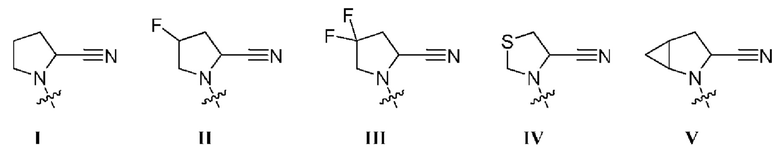
где R2 представляет собой водород или C1-3алкил и
где R4 представляет собой фенил, замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, галогена, циано, нитро, карбоновой кислоты, С1-5алкила, необязательно замещенного 1-3 галогенами или аминогруппой, С2-6алкенила, С2-6алкинила, С1-5алкокси, C1-5алкилтио, моно- или ди-С1-5алкиламино, пиперазинила, необязательно замещенного ацетилом, C1-5алкилсульфониламино, С1-5алкилкарбониламино, аминосульфонила, аминокарбонила, C1-5алкиламинокарбонила, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила;
гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, дигидробензо[1,4]диоксинила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинил;
нафтил, необязательно замещенный галогеном; или
гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила, пиразинила, имидазолила, пиразолила, триазолила, оксазолила, тиазолила, фуранила, пирролила, тиофенила, хинолинила, изохинолинила, хроменонила, хиназолинила, бензоксазолила, бензофуранила, бензотиофенила, индолила, индолинила, бензимидазолила, бензоксазолила, бензотиазолила, индазолила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила, акридинила и нафтиридинила, где указанный гетероарил необязательно замещен 1-3 Z, где каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-С1-5алкиламино, циано, нитро, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, С1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила, С1-5алкилсульфонила, морфолинила, -NR6C(O)R7, и -C(O)NR6R7;
где R6 представляет собой водород или C1-3алкильную группу; и
где R7 представляет собой C1-3алкильную группу, необязательно замещенную фенилом; фенил; или гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила и изоксазолила.
[0054] В данном документе в другом аспекте представлен способ получения соединения формулы 1с,
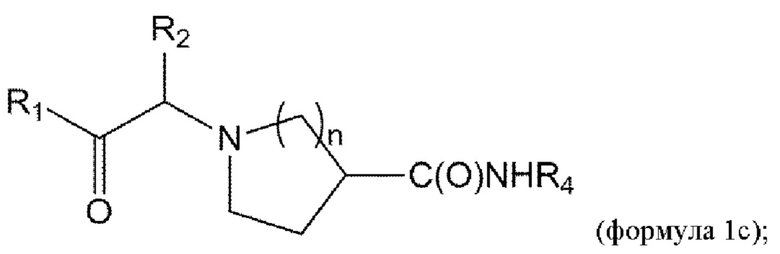
или его стереоизомера или смеси стереоизомеров или его фармацевтически приемлемой соли, причем указанный способ включает
взаимодействие соединения формулы 2с с соединением формулы 2са в условиях амидного связывания с получением соединения формулы 3с:

удаление Вос из соединения формулы 3с в условиях реакции с получением соединения формулы 4с:
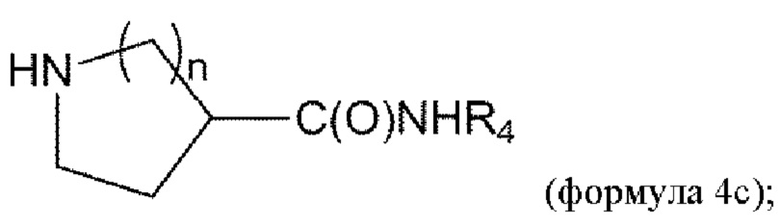 и
и
взаимодействие соединения формулы 4с с соединением формулы 5 с получением соединения формулы 1с или его изомеров или его фармацевтически приемлемой соли:

где n представляет собой 1 или 2.
где R1 представляет собой заместитель, выбранный из группы, состоящей из соединений формул I-V,
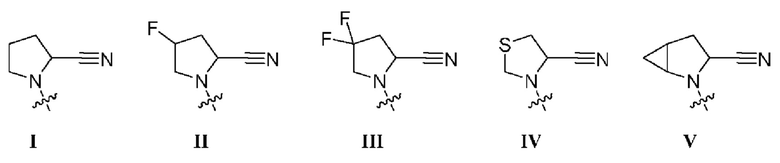
где R2 представляет собой водород или C1-3алкил и
где R4 представляет собой фенил, замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, галогена, циано, нитро, карбоновой кислоты, С1-5алкила, необязательно замещенного 1-3 галогенами или аминогруппой, С2-6алкенила, С2-6алкинила, С1-5алкокси, C1-5алкилтио, моно- или ди-С1-5алкиламино, пиперазинила, необязательно замещенного ацетилом, C1-5алкилсульфониламино, С1-5алкилкарбониламино, аминосульфонила, аминокарбонила, C1-5алкиламинокарбонила, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила;
гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, дигидробензо[1,4]диоксинила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинил;
нафтил, необязательно замещенный галогеном; или
гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила, пиразинила, имидазолила, пиразолила, триазолила, оксазолила, тиазолила, фуранила, пирролила, тиофенила, хинолинила, изохинолинила, хроменонила, хиназолинила, бензоксазолила, бензофуранила, бензотиофенила, индолила, индолинила, бензимидазолила, бензоксазолила, бензотиазолила, индазолила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила и акридинила, где указанный гетероарил необязательно замещен 1-3 Z, где каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-С1-5алкиламино, циано, нитро, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, С1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила и С1-5алкилсульфонила.
[0055] В данном документе в другом аспекте представлен способ получения соединения формулы 1d,
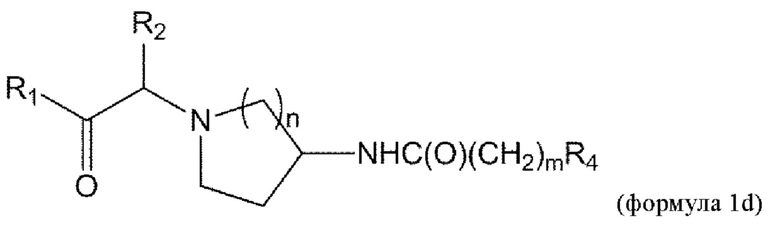
или его стереоизомера или смеси стереоизомеров или его фармацевтически приемлемой соли, причем указанный способ включает
взаимодействие соединения формулы 5 с соединением формулы 9 с получением соединения формулы 10:
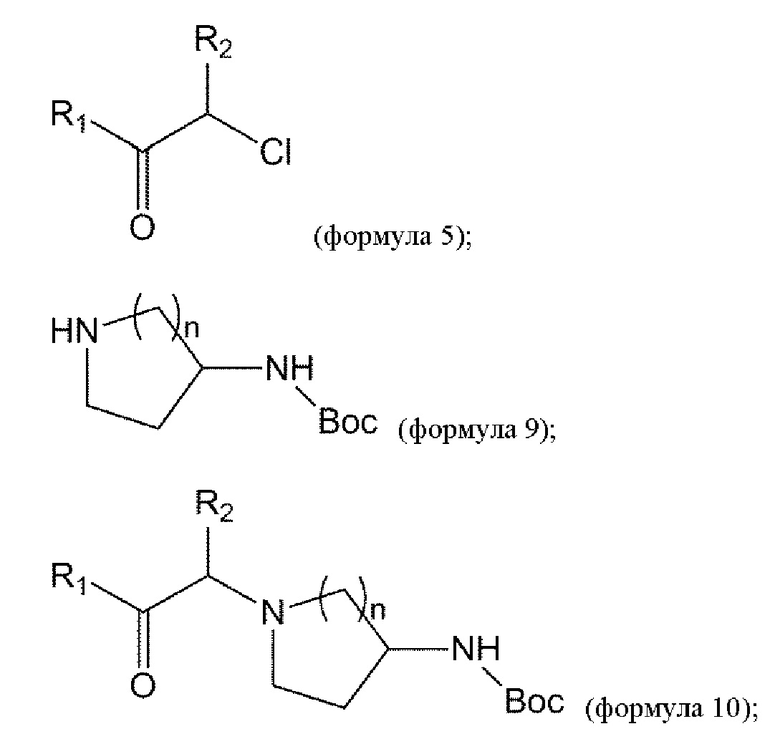
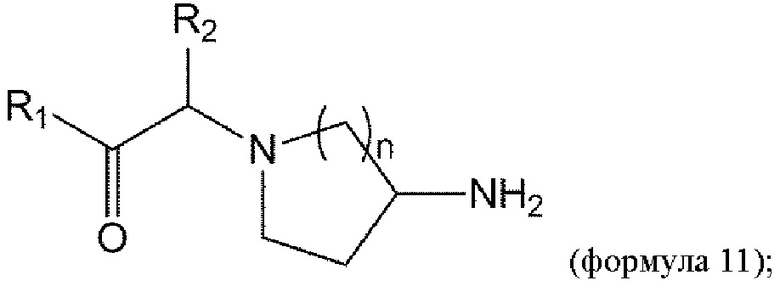
удаление Вос из соединения формулы 10 в условиях реакции с получением соединения формулы 11:
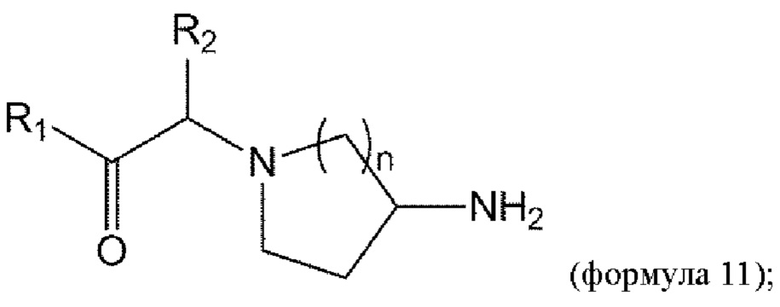 и
и
взаимодействие соединения формулы 11 с соединением формулы 11а с получением соединения формулы 1d или его изомера или его фармацевтически приемлемой соли:
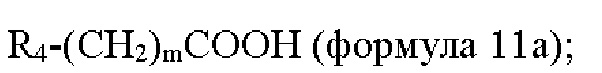
где n представляет собой 1 или 2.
где R1 представляет собой заместитель, выбранный из группы, состоящей из соединений формул I-V,
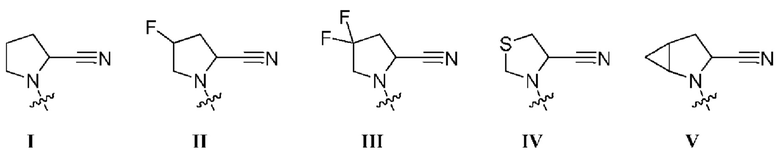
где R2 представляет собой водород или C1-3алкил,
где m представляет собой 0 или 1, и
где R4 представляет собой фенил, замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, галогена, циано, нитро, карбоновой кислоты, С1-5алкила, необязательно замещенного 1-3 галогенами или аминогруппой, С2-6алкенила, С2-6алкинила, С1-5алкокси, C1-5алкилтио, моно- или ди-С1-5алкиламино, пиперазинила, необязательно замещенного ацетилом, C1-5алкилсульфониламино, С1-5алкилкарбониламино, аминосульфонила, аминокарбонила, C1-5алкиламинокарбонила, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила;
гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, дигидробензо[1,4]диоксинила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинил;
нафтил, необязательно замещенный галогеном; или
гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила, пиразинила, имидазолила, пиразолила, триазолила, оксазолила, тиазолила, фуранила, пирролила, тиофенила, хинолинила, изохинолинила, хроменонила, хиназолинила, бензоксазолила, бензофуранила, бензотиофенила, индолила, индолинила, бензимидазолила, бензоксазолила, бензотиазолила, индазолила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила, акридинила и нафтиридинила, где указанный гетероарил необязательно замещен 1-3 Z, где каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-С1-5алкиламино, циано, нитро, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, C1-5алкокси, С1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила, C1-5алкилсульфонила, морфолинила, -NR6C(O)R7, и -C(O)NR6R7;
где R6 представляет собой водород или С1-3алкильную группу; и
где R7 представляет собой С1-3алкильную группу, необязательно замещенную фенилом; фенил; или гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила и изоксазолила.
[0056] В данном документе в другом аспекте представлен способ получения соединения формулы 1d,
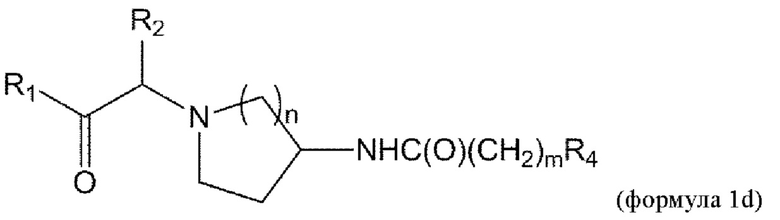
или его стереоизомера или смеси стереоизомеров или его фармацевтически приемлемой соли, причем указанный способ включает
взаимодействие соединения формулы 5 с соединением формулы 9 с получением соединения формулы 10:
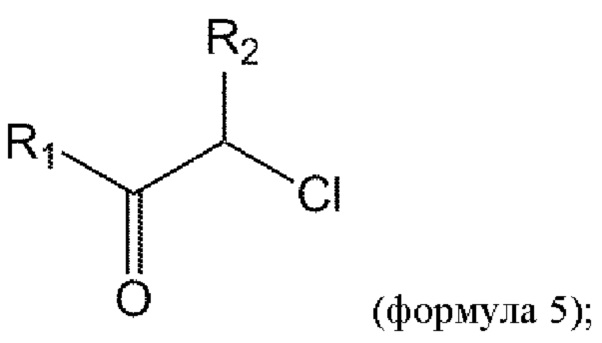
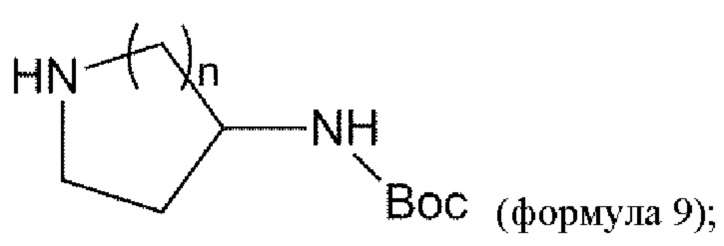
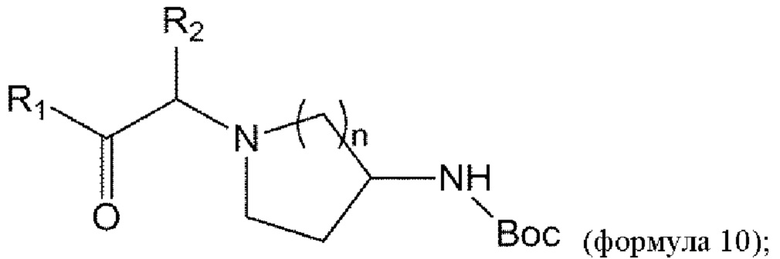
удаление Вос из соединения формулы 10 в условиях реакции с получением соединения формулы 11:
 и
и
взаимодействие соединения формулы 11 с соединением формулы 11а с получением соединения формулы 1d или его изомера или его фармацевтически приемлемой соли:
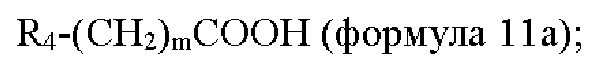
где n представляет собой 1 или 2.
где R1 представляет собой заместитель, выбранный из группы, состоящей из соединений формул I-V,
где R2 представляет собой водород или C1-3алкил,
где m представляет собой 0 или 1, и
где R4 представляет собой фенил, замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, галогена, циано, нитро, карбоновой кислоты, C1-5алкила, необязательно замещенного 1-3 галогенами или аминогруппой, С2-6алкенила, С2-6алкинила, С1-5алкокси, C1-5алкилтио, моно- или ди-С1-5алкиламино, пиперазинила, необязательно замещенного ацетилом, C1-5алкилсульфониламино, С1-5алкилкарбониламино, амино сульфонила, аминокарбонила, C1-5алкиламинокарбонила, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила;
гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, дигидробензо[1,4]диоксинила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинил;
нафтил, необязательно замещенный галогеном; или
гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила, пиразинила, имидазолила, пиразолила, триазолила, оксазолила, тиазолила, фуранила, пирролила, тиофенила, хинолинила, изохинолинила, хроменонила, хиназолинила, бензоксазолила, бензофуранила, бензотиофенила, индолила, индолинила, бензимидазолила, бензоксазолила, бензотиазолила, индазолила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила и акридинила, где указанный гетероарил необязательно замещен 1-3 Z, где каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-С1-5алкиламино, циано, нитро, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, С1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила и С1-5алкилсульфонила.
[0057] В данном документе в другом аспекте представлен способ получения соединения формулы 1е,

или его стереоизомера или смеси стереоизомеров или его фармацевтически приемлемой соли, причем указанный способ включает
взаимодействие соединения формулы 5 с соединением формулы 9 с получением соединения формулы 10:
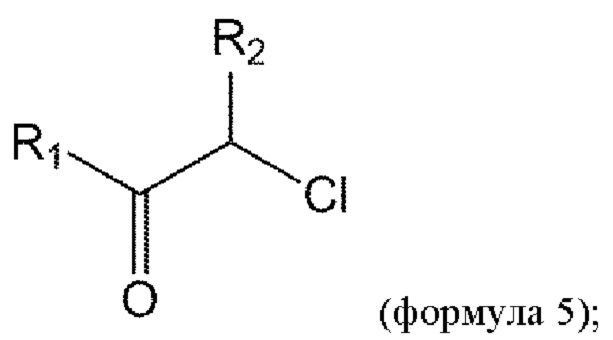
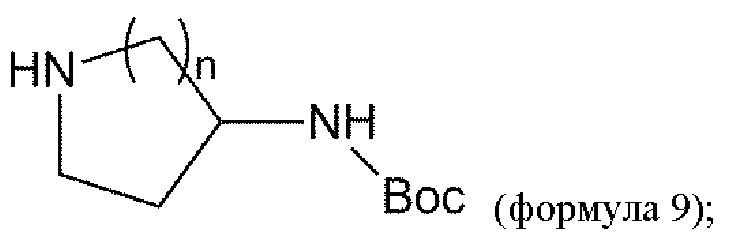
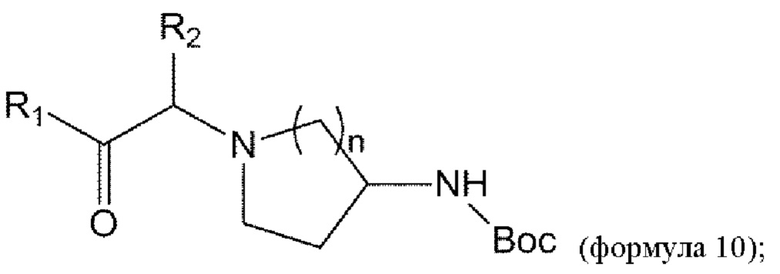
удаление Вос из соединения формулы 10 в условиях реакции с получением соединения формулы 11:
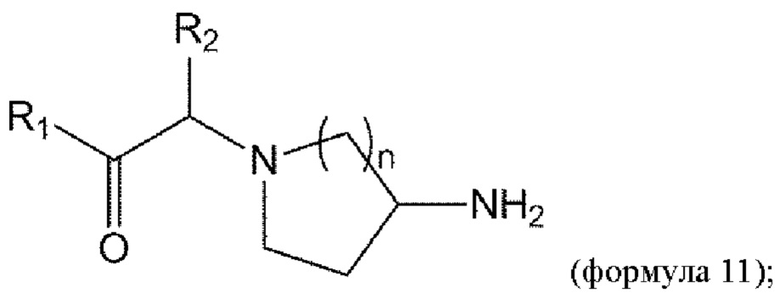 и
и
взаимодействие соединения формулы 11 с соединением формулы 11b с получением соединения формулы 1d или его изомеров или его фармацевтически приемлемой соли:
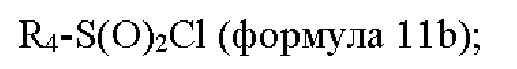
где n представляет собой 1 или 2.
где R1 представляет собой заместитель, выбранный из группы, состоящей из соединений формул I-V,

где R2 представляет собой водород или C1-3алкил и
где R4 представляет собой фенил, замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, галогена, циано, нитро, карбоновой кислоты, С1-5алкила, необязательно замещенного 1-3 галогенами или аминогруппой, С2-6алкенила, С2-6алкинила, С1-5алкокси, C1-5алкилтио, моно- или ди-С1-5алкиламино, пиперазинила, необязательно замещенного ацетилом, C1-5алкилсульфониламино, C1-5алкилкарбониламино, аминосульфонила, аминокарбонила, C1-5алкиламинокарбонила, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила;
гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, дигидробензо[1,4]диоксинила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинил;
нафтил, необязательно замещенный галогеном; или
гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила, пиразинила, имидазолила, пиразолила, триазолила, оксазолила, тиазолила, фуранила, пирролила, тиофенила, хинолинила, изохинолинила, хроменонила, хиназолинила, бензоксазолила, бензофуранила, бензотиофенила, индолила, индолинила, бензимидазолила, бензоксазолила, бензотиазолила, индазолила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила, акридинила и нафтиридинила, где указанный гетероарил необязательно замещен 1-3 Z, где каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-С1-5алкиламино, циано, нитро, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, С1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила, С1-5алкилсульфонила, морфолинила, -NR6C(O)R7, и -C(O)NR6R7;
где R6 представляет собой водород или С1-3алкильную группу; и
где R7 представляет собой C1-3алкильную группу, необязательно замещенную фенилом; фенил; или гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила и изоксазолила.
[0058] В данном документе в другом аспекте представлен способ получения соединения формулы 1е,
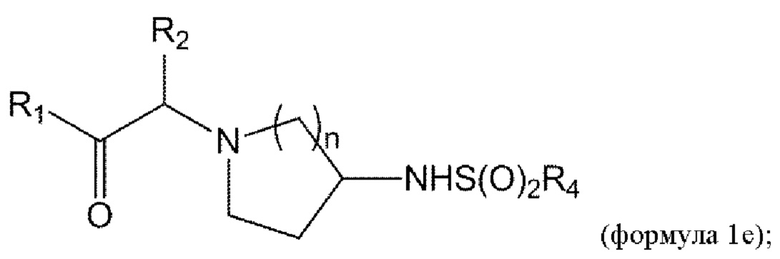
или его стереоизомера или смеси стереоизомеров или его фармацевтически приемлемой соли, причем указанный способ включает
взаимодействие соединения формулы 5 с соединением формулы 9 с получением соединения формулы 10:
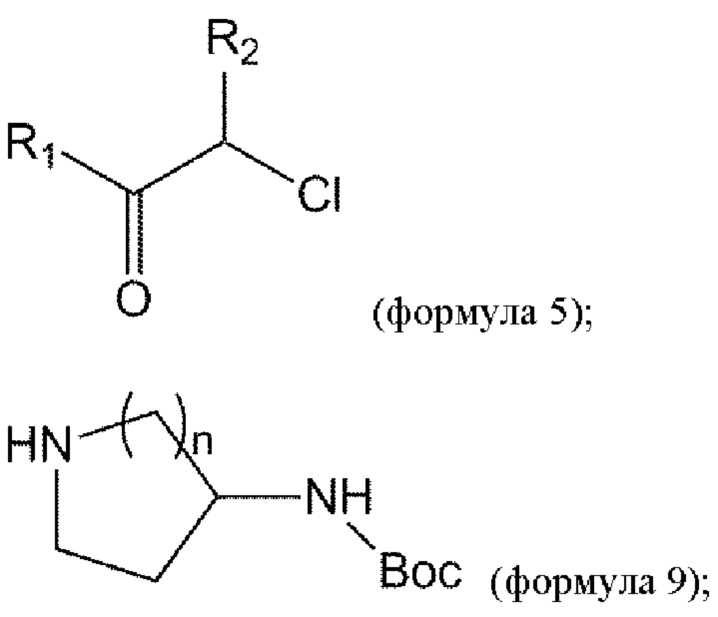
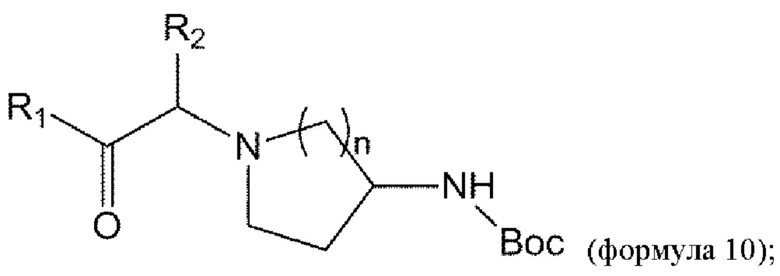
удаление Вос из соединения формулы 10 в условиях реакции с получением соединения формулы 11:
 и
и
взаимодействие соединения формулы 11 с соединением формулы 11b с получением соединения формулы 1d или его изомеров или его фармацевтически приемлемой соли:
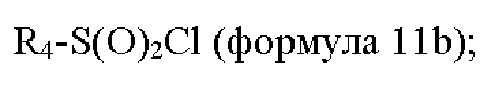
где n представляет собой 1 или 2.
где R1 представляет собой заместитель, выбранный из группы, состоящей из соединений формул I-V,
где R2 представляет собой водород или С1-3алкил и
где R4 представляет собой фенил, замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, галогена, циано, нитро, карбоновой кислоты, С1-5алкила, необязательно замещенного 1-3 галогенами или аминогруппой, С2-6алкенила, С2-6алкинила, С1-5алкокси, C1-5алкилтио, моно- или ди-С1-5алкиламино, пиперазинила, необязательно замещенного ацетилом, C1-5алкилсульфониламино, С1-5алкилкарбониламино, аминосульфонила, аминокарбонила, C1-5алкиламинокарбонила, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила;
гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, дигидробензо[1,4]диоксинила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинил;
нафтил, необязательно замещенный галогеном; или
гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила, пиразинила, имидазолила, пиразолила, триазолила, оксазолила, тиазолила, фуранила, пирролила, тиофенила, хинолинила, изохинолинила, хроменонила, хиназолинила, бензоксазолила, бензофуранила, бензотиофенила, индолила, индолинила, бензимидазолила, бензоксазолила, бензотиазолила, индазолила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила и акридинила, где указанный гетероарил необязательно замещен 1-3 Z, где каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-С1-5алкиламино, циано, нитро, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, С1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила и С1-5алкилсульфонила.
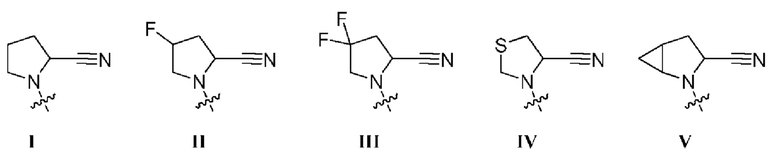
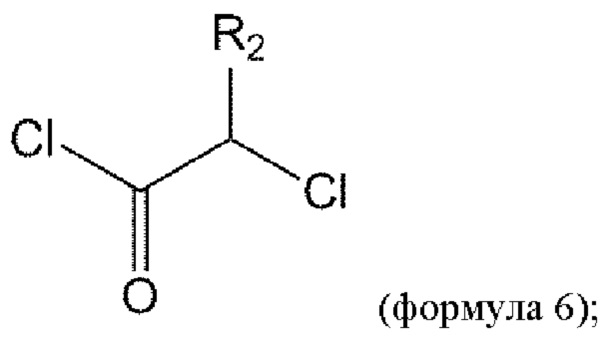
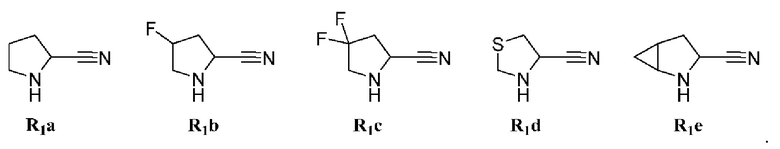
[0059] В некоторых вариантах осуществления соединение формулы 5 получают путем взаимодействия соединения формулы 6 с соединением любой из формул R1a-R1e для получения соединения формулы 5:
[0060] В данном документе в другом аспекте представлен способ получения соединения формулы 1b,
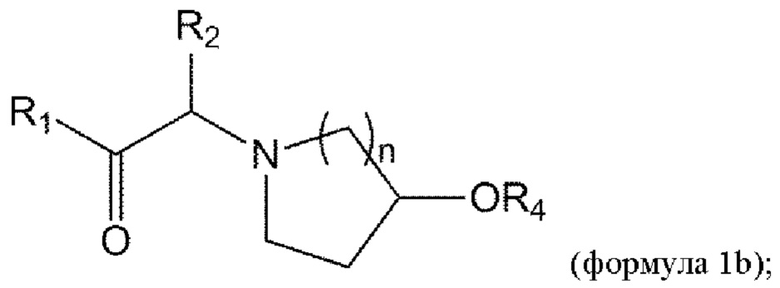
или его стереоизомера или смеси стереоизомеров или его фармацевтически приемлемой соли, причем указанный способ включает
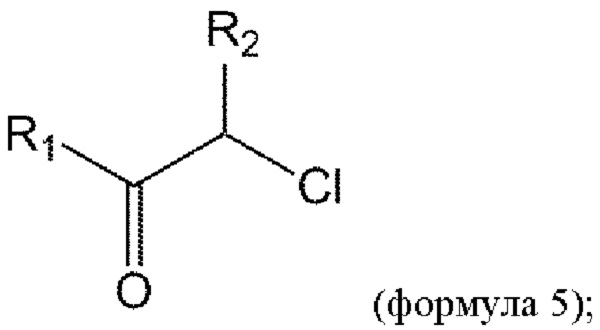
взаимодействие соединения формулы 5 с соединением формулы 7 с получением соединения формулы 8:
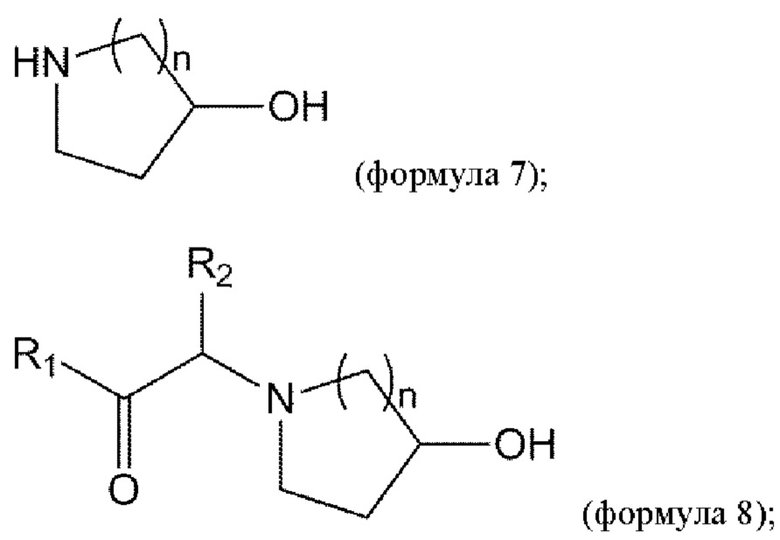 и
и
взаимодействие соединения формулы 8 с соединением формулы 2ba в условиях реакции Мицунобу с получением соединения формулы 1b или его изомера или его фармацевтически приемлемой соли:
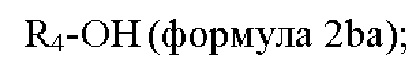
где n представляет собой 1 или 2.
где R1 представляет собой заместитель, выбранный из группы, состоящей из соединений формул I-V,

где R2 представляет собой водород или C1-3алкил,
где R4 представляет собой фенил, замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, галогена, циано, нитро, карбоновой кислоты, С1-5алкила, необязательно замещенного 1-3 галогенами или аминогруппой, С2-6алкенила, С2-6алкинила, С1-5алкокси, C1-5алкилтио, моно- или ди-С1-5алкиламино, пиперазинила, необязательно замещенного ацетилом, C1-5алкилсульфониламино, С1-5алкилкарбониламино, амино сульфонила, аминокарбонила, C1-5алкиламинокарбонила, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила;
гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, дигидробензо[1,4]диоксинила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинил;
нафтил, необязательно замещенный галогеном; или
гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила, пиразинила, имидазолила, пиразолила, триазолила, оксазолила, тиазолила, фуранила, пирролила, тиофенила, хинолинила, изохинолинила, хроменонила, хиназолинила, бензоксазолила, бензофуранила, бензотиофенила, индолила, индолинила, бензимидазолила, бензоксазолила, бензотиазолила, индазолила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила, акридинила и нафтиридинила, где указанный гетероарил необязательно замещен 1-3 Z, где каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-С1-5алкиламино, циано, нитро, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, С1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила, С1-5алкилсульфонила, морфолинила, -NR6C(O)R7, и -C(O)NR6R7;
где R6 представляет собой водород или C1-3алкильную группу; и
где R7 представляет собой C1-3алкильную группу, необязательно замещенную фенилом; фенил; или гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила и изоксазолила.
[0061] В данном документе в другом аспекте представлен способ получения соединения формулы 1b,
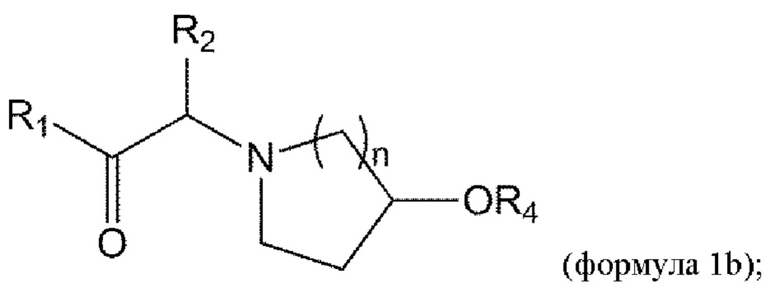
или его стереоизомера или смеси стереоизомеров или его фармацевтически приемлемой соли, причем указанный способ включает
взаимодействие соединения формулы 5 с соединением формулы 7 с получением соединения формулы 8:
 и
и
взаимодействие соединения формулы 8 с соединением формулы 2ba в условиях реакции Мицунобу с получением соединения формулы lb или его изомера или его фармацевтически приемлемой соли:
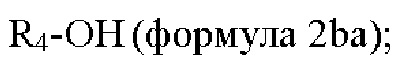
где n представляет собой 1 или 2.
где R1 представляет собой заместитель, выбранный из группы, состоящей из соединений формул I-V,
где R2 представляет собой водород или C1-3алкил,
где R4 представляет собой фенил, замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, галогена, циано, нитро, карбоновой кислоты, C1-5алкила, необязательно замещенного 1-3 галогенами или аминогруппой, С2-6алкенила, С2-6алкинила, С1-5алкокси, C1-5алкилтио, моно- или ди-С1-5алкиламино, пиперазинила, необязательно замещенного ацетилом, С1-5алкилсульфониламино, С1-5алкилкарбониламино, аминосульфонила, аминокарбонила, С1-5алкиламинокарбонила, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила;
гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, дигидробензо[1,4]диоксинила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинил;
нафтил, необязательно замещенный галогеном; или
гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила, пиразинила, имидазолила, пиразолила, триазолила, оксазолила, тиазолила, фуранила, пирролила, тиофенила, хинолинила, изохинолинила, хроменонила, хиназолинила, бензоксазолила, бензофуранила, бензотиофенила, индолила, индолинила, бензимидазолила, бензоксазолила, бензотиазолила, индазолила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила и акридинила, где указанный гетероарил необязательно замещен 1-3 Z, где каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-С1-5алкиламино, циано, нитро, галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, C1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила и С1-5алкилсульфонила.
ПОДРОБНОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
[0062] Следует отметить, что применяемые в настоящем документе и в прилагаемой формуле изобретения формы единственного числа включают ссылки на множественное число, если из контекста явно не следует иное. Кроме того, следует отметить, что формула изобретения может быть составлена таким образом, чтобы исключить любой необязательный элемент. Как таковое, данное утверждение предназначено для того, чтобы служить в качестве предшествующей основы для использования такой исключительной терминологии, как «исключительно», «только» и т.п., в связи с перечислением элементов формулы изобретения или использованием «отрицательного» ограничения.
[0063] Используемый в настоящем документе термин «содержащий» или «содержит» предназначен для обозначения того, что композиции и способы включают перечисленные элементы, но не исключают других. Композиция или способ «состоящий по существу из» элементов, как определено в настоящем документе, не исключают других материалов или этапов, которые не оказывают существенного влияния на основные и новые характеристики заявленной технологии. Термин «состоящий из» означает исключение больше микроэлементов из других ингредиентов и существенных этапов способа. Варианты осуществления, определенные каждым из этих переходных терминов, входят в объем данной технологии. Если вариант осуществления определяется одним из этих терминов (например, «содержащий»), следует понимать, что данное раскрытие также включает альтернативные варианты осуществления, такие как «состоящий по существу из» и «состоящий из» для указанного варианта осуществления.
[0064] Термин «по существу» означает почти полностью или полностью, например, 95%, 96%, 97%, 98%, 99% или более от некоторого заданного количества.
[0065] Используемый в настоящем документе термин «около» будет понятен специалистам в данной области техники и будет варьироваться в некоторой степени в зависимости от контекста, в котором он используется. Если используются термины, которые не очевидны для специалистов в данной области техники, учитывая контекст, в котором он используется, «около» будет означать до плюс или минус 10% конкретного значения.
[0066] В настоящем документе представлены определенные диапазоны с числовыми значениями, которым предшествует термин «около». Термин «около» используется в настоящем документе для обеспечения буквальной поддержки точного числа, которому оно предшествует, а также числа, которое близко или приблизительно соответствует числу, которому предшествует термин. При определении того, является ли число близким или приблизительным к специально названному числу, близкое или приблизительное неназванное число может быть числом, которое в представленном контексте, обеспечивает существенный эквивалент специально названного числа.
[0067] Если указан диапазон значений, подразумевается, что каждое промежуточное значение с точностью до десятой доли единицы нижнего предела, если контекст явно не указывает иное, между верхним и нижним пределом этого диапазона и любым другим установленным или промежуточным значением в указанном диапазоне охватывается настоящей технологией. Верхний и нижний пределы этих меньших диапазонов могут независимо включаться в меньшие диапазоны, а также охватываются настоящей технологией, с учетом любого специально исключенного предела в указанном диапазоне. Если указанный диапазон включает один или оба предела, диапазоны, исключающие один или оба из этих включенных пределов, также включены в настоящую технологию.
[0068] Как правило, термин «замещенный» относится к органической группе (например, алкильной группе), в которой одна или более связей с содержащимся в ней атомом водорода заменены связью с атомами, отличными от водорода или углерода. Замещенные группы также включают группы, в которых одна или более связей с атомом углерода(ов) или водорода(ов) заменены одной или более связями, включая двойные или тройные связи, с гетероатомом. Следует понимать, что настоящее изобретение включает варианты осуществления, в которых, например, «замещенный алкил» необязательно содержит один или более алкенов и/или алкина. Замещенная группа будет замещена одним или более заместителями, если не указано иное. В некоторых вариантах осуществления замещенная группа замещена 1, 2, 3, 4, 5 или 6 заместителями. Примеры замещающих групп включают: алкилы, галоген алкилы, галогены (т.е. F, Cl, Br и I); гидроксилы; алкокси, алкенокси, алкинокси, арилокси, аралкилокси, гетероциклилокси и гетероциклилалкоксигруппы; арильные группы; гетероарильные группы; циклоалкильные группы; гетероциклильные группы; карбонилы (оксо); карбоксилы; эфиры; карбаматы; уретаны; мочевины; оксимы; гидроксиламины; алкоксиамины; аралкоксиамины; тиолы; сульфиды; сульфоксиды; сульфоны; сульфонилы; сульфонамиды; амины; N-оксиды; гидразины; гидразиды; гидразоны; азиды; амиды; мочевины; амидины; гуанидины; енамины; имиды; изоцианаты; изотиоцианаты; цианаты; тиоцианаты; имины; нитрогруппы; нитрилы (т.е. CN); и т.п. В настоящем документе «необязательно замещенная группа» относится к группе, которая является замещенной или незамещенной. Таким образом, «необязательно замещенный» и «замещенный или незамещенный» могут использоваться взаимозаменяемо.
[0069] Замещенные кольцевые группы, такие как замещенные карбоциклические, замещенные циклоалкильные, замещенные арильные, замещенные гетероциклические и замещенные гетероарильные группы, также включают кольца и системы с сочлененными кольцами, в которых связь с атомом водорода заменена связью с атомом углерода. Следовательно, замещенные карбоциклические, замещенные циклоалкильные, замещенные арильные, замещенные гетероциклические и замещенные гетероарильные группы также могут быть замещены замещенными или незамещенными алкильными, алкенильными и алкинильными группами, как определено ниже.
[0070] Используемый в настоящем документе термин «карбоциклическая группа» или «карбоцикл» включает ароматические (также называемые арильными) и неароматические кольцевые соединения (такие как циклоалкил), содержащие 3 или более членов кольца и не содержащие каких-либо гетероатомных членов кольца. В некоторых вариантах осуществления карбоцикл включает от 3 до 20 циклов, тогда как другие такие группы имеют от 3 до 6, от 3 до 10, от 3 до 12, от 3 до 15 или от 5 до 12 циклов.
[0071] В настоящем документе «арильная группа» относится к циклическому ароматическому углеводороду, который не содержит гетероатомов. Арильные группы включают моноциклические, бициклические и полициклические кольцевые системы. Таким образом, арильные группы включают, без ограничений, фенил, азуленил, гепталенил, бифениленил, индацил, фторенил, фенантрин, трифениленил, пиренил, нафтазенил, хриозил, бифенил, антраценил, инденил, инданил, пенталенил и нафтильные группы. В некоторых вариантах осуществления арильные группы содержат 6-14 атомов углерода, а в других - от 6 до 12 или даже 6-10 атомов углерода в кольцевых участках групп. Хотя фраза «арильные группы» включает группы, содержащие сочлененные кольца, такие как конденсированные ароматические-алифатические кольцевые системы (например, инданил, тетрагидронафтил и т.п.), она не включает арильные группы, которые имеют другие группы, такие как алкильные или галогеновые группы, связанные с одним из кольцевых элементов. Скорее такие группы, как толил, называются замещенными арильными группами. Репрезентативные замещенные арильные группы могут быть монозамещены или замещены более одного раза. Например, монозамещенные арильные группы включают, но не ограничиваются ими, 2-, 3-, 4-, 5- или 6-замещенные фенильные или нафтильные группы, которые могут быть замещены заместителями, такими как перечисленные выше.
[0072] Используемый в настоящем документе термин «циклоалкильная группа» относится к циклической алкильной группе, такой как, но не ограничиваясь ими, циклопропильная, циклобутильная, циклопентильная, циклогексильная, циклогептильная и циклооктильная группы. В некоторых вариантах осуществления циклоалкильная группа имеет от 3 до 8 атомов углерода в кольце, тогда как в других вариантах осуществления количество атомов углерода в кольце находится в диапазоне от 3 до 5, от 3 до 6 или от 3 до 7. Циклоалкильные группы дополнительно включают моно-, бициклические и полициклические кольцевые системы, такие как, например, мостиковые циклоалкильные группы, как описано ниже, и сочлененные кольца, такие как, без ограничений, декалинил и т.п. В некоторых вариантах осуществления полициклические циклоалкильные группы имеют три кольца. Замененные циклоалкильные группы могут быть замещены одним или более раз неводородными и неуглеродными группами, как определено выше. Однако замещенные циклоалкильные группы также включают кольца, которые замещены прямыми или разветвленными алкильными группами, как определено выше. Типичные замещенные циклоалкильные группы могут быть монозамещеиными или замещенными более чем один раз, такими как, без ограничений, 2,2-, 2,3-, 2,4-, 2,5- или 2,6-ди-замещенными циклогексильными группами, которые могут быть замещены заместителями, такими как перечисленные выше. В некоторых вариантах осуществления циклоалкильная группа имеет одну или более алкеновых связей, но не является ароматической.
[0073] Используемый в данном документе термин «гетероциклическая группа» или «гетероцикл» включает ароматические (также называемые гетероарильными) и неароматические кольцевые соединения, содержащие 3 или более кольцевых элементов, из которых один или более представляет собой гетероатом, такой как, без ограничений, N, О, S или В. В некоторых вариантах осуществления гетероциклические группы включают от 3 до 20 членов кольца, тогда как другие такие группы имеют от 3 до 6, от 3 до 10, от 3 до 12, от 3 до 15 или от 5 до 12 членов кольца. Гетероциклические группы охватывают ненасыщенные, частично насыщенные и насыщенные кольцевые системы, такие как, например, имидазолильная, имидазолинильная и имидазолидинильная группы. Фраза «гетероциклическая группа» включает соединения с сочлененными кольцами, включая те, которые содержат конденсированные ароматические и неароматические группы, такие как, например, бензотриазолил, 2,3-дигидробензо[1,4]диоксинил и бензо[1,3]диоксолил. Фраза также включает мостиковые полициклические кольцевые системы, содержащие гетероатом, такой как, но не ограничиваясь этим, хинуклидил. Однако эта фраза не включает гетероциклические группы, которые содержат другие группы, такие как алкильные, оксо- или галогеногруппы, связанные с одним из членов кольца. Скорее их называют «замещенными гетероциклическими группами». Гетероциклические группы включают, но не ограничиваются ими, акридинил, азиридинил, азетидинил, пирролидинил, имидазолидинил, пиразолидинил, тиазолидинил, тетрагидротиофенил, тетрагидрофуранил, диоксолил, фуранил, тиофенил, пирролил, пирролинил, имидазолил, имидазолинил, пиразолил, пиразолинил, триазолил, тетразолил, оксазолил, изоксазолил, тиазолил, тиазолинил, изотиазолил, тиадиазолил, оксадиазолил, хроменонил, пиперидил, пиперазинил, морфолинил, тиоморфолинил, тетрагидропиранил, тетрагидротиопиранил, оксатиан, диоксил, дитианил, пиранил, пиридил, пиримидинил, пиридазинил, пиразинил, триазинил, дигидропиридил, дигидродитиинил, дигидродитионил, гомопиперазинил, хинуклидил, индолил, индолинил, изоиндолил, азаиндолил (пирролопиридил), индазолил, индолизинил, бензотриазолил, бензимидазолил, бензофуранил, бензотиофенил, бензтиазолил, бензоксадиазолил, бензоксазинил, бензодитиинил, бензоксатиинил, бензотиазинил, бензоксазолил, бензотиазолил, бензотиадиазолил, бензо[1,3]диоксолил, дигидробензо[1,4]диоксинил, 2,3-дигидробензофуранил, 2-оксо-1,2-дигидрохинолинил, 2-оксо-1,2,3,4-тетрагидрохинолинил, пиразолопиридил, имидазопиридил (азабензимидазолил), триазолопиридил, изоксазолопиридил, фуро[3,2-с]пиридинил, тиено[2,3-d]пиримидинил, тиено[3,2-с]пиридинил, пуринил, ксантинил, аденинил, гуанинил, хинолинил, изохинолинил, хинолизинил, хиноксалинил, хиназолинил, циннолинил, фталазинил, нафтиридинил, птеридинил, тианафталинил, дигидробензотиазинил, дигидробензофуранил, дигидроиндолил, дигидробензодиоксинил, тетрагидроиндолил, тетрагидроиндазолил, тетрагидробензимидазолил, тетрагидробензотриазолил, тетрагидропирролопиридил, тетрагидропиразолопиридил, тетрагидроимидазопиридил, тетрагидротриазолопиридил и тетрагидрохинолинильные группы. Репрезентативные замещенные гетероциклические группы могут быть монозамещенными или замещенными более одного раза, например, пиридильные или пиперазинильные группы, которые являются 2-, 3-, 4-, 5- или 6-замещенными или дизамещенными с различными заместителями, такими как перечисленные выше. В некоторых вариантах осуществления термин «нафтиридинил» относится к 1,8-нафтиридинилу; 2,6-нафтиридинилу; или 1,5-нафтиридинилу или любой комбинации двух или более из них.
[0074] Используемый в настоящем документе термин «гетероарильная группа» относится к ароматическому кольцевому соединению, содержащему 5 или более членов кольца, из которых один или несколько являются гетероатомами, такими как, но не ограничиваясь ими, N, О, S или В. В некоторых вариантах осуществления один или более гетероатомов независимо выбирают из N, О или S. В некоторых вариантах осуществления от 1 до 4 гетероатомов независимо выбирают из N, О или S. В некоторых вариантах осуществления от 1 до 5 гетероатомов независимо выбирают из N, О или S. В некоторых вариантах осуществления гетероарильные группы включают от 5 до 14 членов кольца, тогда как другие такие группы содержат от 5 до 6, от 5 до 9, от 5 до 10, от 6 до 9, от 6 до 10 или от 6 до 14 членов кольца. Например, 5-членная гетероарильная группа имеет 5 членов кольца; 6-членная гетероарильная группа имеет 6 членов кольца; и 9-членная гетероарильная группа имеет 9 членов кольца (например, бензотиофен, но не ограничиваясь этим). Гетероарильные группы включают, но не ограничиваются ими, такие группы, как пирролил, пиразолил, триазолил, тетразолил, оксазолил, изоксазолил, тиазолил, пиридил, пиридазинил, пиримидинил, пиразинил, тиофенил, бензотиофенил, фуранил, бензофуранил, индолил, азаиндолил (пирролопиридил), индазолил, бензимидазолил, имидазопиридил (азабензимидазолил), пиразолопиридил, триазолопиридил, бензотриазолил, бензоксазолил, бензотиазолил, бензотиадиазолил, имидазопиридил, изоксазолопиридил, тианафталинил, пуринил, ксантинил, аденинил, гуанинил, нафтиридинил, хинолинил, изохинолинил, тетрагидрохинолинил, хиноксалинил и хиназолинил. Хотя фраза «гетероарильные группы» включает соединения с сочлененными кольцами, такие как индолил и 2,3-дигидроиндолил, эта фраза не включает гетероарильные группы, которые имеют другие группы, связанные с одним из членов кольца, такие как алкильные группы. Скорее гетероарильные группы с таким замещением называются «замещенными гетероарильными группами». Типичные замещенные гетероарильные группы могут быть замещены одним или более раз различными заместителями, такими как перечисленные выше. Азолильная группа представляет собой 5-членную гетероарильную группу, содержащую атом азота и по меньшей мере один другой атом, выбранный из азота, серы и кислорода в составе кольца. Азолильные группы включают имидазол, пиразол, 1,2,3-триазол, 1,2,4-триазол, тетразол, пентазол, оксазол, изоксазол, 1,2,4-оксадиазол, 1,2,5-оксадиазол, 1,3,4-оксадиазол, тиазол, изотиазол, 1,2,3-тиадиазол, 1,2,4-тиадиазол, 1,2,5-тиадиазол и 1,3,4-тиадиазол.
[0075] В настоящем документе термин «алкил» относится к алифатическому углеводородному радикалу, который охватывает как прямые, так и разветвленные углеводородные радикалы. В некоторых вариантах осуществления алкил имеет от 1 до приблизительно 20 атомов углерода, от 1 до 12 атомов углерода, от 1 до 8 атомов углерода, от 1 до 6 атомов углерода или от 1 до 4 атомов углерода. Например, С1-6алкил относится к алифатическому углеводороду, имеющему от 1 до 6 атомов углерода, который включает метил, этил, пропил, н-бутил, н-пентил, н-гексил, изопропил, изобутил, втор-бутил, трет-бутил, неопентил, изопентил и т.п.
[0076] Кроме того, в настоящем документе термин «гидрокси» определяется как -ОН.
[0077] Используемый в настоящем документе термин «алкокси», если не указано иное, относится к радикалу, образованному замещением атома водорода гидроксильной группы алкилом, как определено выше. Например, С1-6алкокси включает метокси, этокси, пропокси, н-бутокси, н-пенталокси, изопропокси, втор-бутокси, трет-бутокси, неопентилокси, изопентилокси и т.п.
[0078] Кроме того, в настоящем документе термин «галоген» относится к фтору, брому, хлору и йоду.
[0079] Кроме того, в настоящем документе термин «амино» определяется как -NH2 и термин «алкиламино» относится к моно- или диалкильному замещенному амину. Например, C1-6алкиламино включает моно- или ди-С1-6алкилзамещенный амино.
[0080] Кроме того, в настоящем документе термин «алкилтио» определяется как -SR* (где R* представляет собой алкил), и термин «циано» определяется как -CN.
[0081] Специалистам в данной области будет понятно, что соединения настоящей технологии могут проявлять явления таутомерии, конформационной изомерии, геометрической изомерии и/или оптической изомерии. Поскольку графические материалы формулы и формулы изобретения могут представлять собой только одну из возможных таутомерных, конформационных изомерных, оптических изомерных или геометрических изомерных форм, следует понимать, что настоящая технология охватывает любые таутомерные, конформационные изомерные, оптические изомерные и/или геометрические изомерные формы соединений, имеющих одно или более из описанных в настоящем документе средств, а также смеси этих различных форм. Используемый в настоящем документе термин «изомер» относится к таутомеру конформационному изомеру, оптическому изомеру, геометрическому изомеру соединения или любой их комбинации.
[0082] Как вполне будет понятно специалисту в данной области, широкий спектр функциональных групп и других структур может проявлять таутомерию, и все таутомеры соединений, как описано в настоящем документе, входят в объем настоящей технологии.
[0083] Стереоизомеры соединений, также известные как «оптические изомеры», включают все хиральные, диастереомерные и рацемические формы структуры, если явно не указано иное. Таким образом, соединения, используемые в настоящей технологии, включают обогащенные или разделенные оптические изомеры по любому или всем стереогенным атомам, как видно из изображений. Как рацемические, так и диастереомерные смеси, а также отдельные оптические изомеры могут быть выделены или синтезированы таким образом, чтобы они были практически свободны от их энантиомерных или диастереомерных партнеров, и все они входят в объем настоящей технологии.
[0084] Под термином «фармацевтически приемлемый» подразумевается материал, который не является биологически или иным образом нежелательным, например, материал может быть включен в фармацевтическую композицию, вводимую пациенту, без возникновения нежелательных биологических эффектов или вредного взаимодействия с любым из других компонентов композиции, в которой он содержится. Когда термин «фармацевтически приемлемый» используется для обозначения фармацевтического носителя или эксципиента, подразумевается, что носитель или наполнитель соответствует требуемым стандартам токсикологических и производственных испытаний или что он включен в Справочник по неактивным компонентам, подготовленный Управлением по надзору за качеством продуктов питания и медикаментов США.
[0085] Как правило, ссылка на определенный фрагмент, который может быть защищен (такой как гидрокси, амин, карбонил и т.д.), включает защищенные группы в некоторых вариантах осуществления изобретения. Например, в некоторых вариантах осуществления фрагмент -ОН, включенный в настоящий документ, также включает -ОР, где Р представляет собой защитную группу. Защитные группы, упомянутые в настоящем документе, могут быть выбраны специалистом в данной области и включают группы и стратегии, изложенные в данной области, например такие, как описаны в R. Larock, Comprehensive Organic Transformations, VCH Publishers (1989); T.W. Greene and P.G.M. Wuts, Greene's protective groups in organic synthesis, John Wiley & Sons (2006); L. Fieser and M. Fieser, Fieser and Fieser's Reagents for Organic Synthesis, John Wiley and Sons (1994); and L. Paquette, ed., Encyclopedia of Reagents for Organic Synthesis, John Wiley and Sons (1995), и последующие их издания.
[0086] Термин «субъект» относится к животному, такому как млекопитающее (включая человека), которое было или будет объектом лечения, наблюдения или эксперимента. «Субъект» и «пациент» могут использоваться взаимозаменяемо, если не указано иное. Способы, описанные в настоящем документе, могут быть использованы в терапии человека и/или ветеринарии. В некоторых вариантах осуществления субъект представляет собой млекопитающее. В некоторых вариантах осуществления субъект представляет собой человека.
[0087] Термины «терапевтически эффективное количество» и «эффективное количество» используются взаимозаменяемо и относятся к количеству соединения, которое является достаточным для лечения, как определено ниже, при введении пациенту (например, человеку), нуждающемуся в таком лечении, в одной или более дозах. Терапевтически эффективное количество будет варьироваться в зависимости от пациента, заболевания, которое лечат, массы и/или возраста пациента, тяжести заболевания или способа введения, определяемого квалифицированным врачом или лицом, осуществляющим уход.
[0088] Термин «лечение» означает введение соединения, описанного в данном документе, с целью (i) отсрочить начало заболевания, то есть предотвратить развитие клинических симптомов заболевания или отсрочить его развитие; (ii) ингибирования заболевания, то есть купирования развития клинических симптомов; и/или (iii) облегчения заболевания, то есть вызывания регрессии клинических симптомов или их тяжести.
[0089] Если не указано иное, все технические и научные термины, применяемые в настоящем документе, имеют то же значение, которое обычно понимается специалистом в области техники, к которой относится настоящая технология. Хотя любые способы и материалы, подобные или эквивалентные тем, что описаны в настоящем документе, также могут быть использованы при практическом применении или тестировании настоящей технологии, здесь описаны репрезентативные иллюстративные способы и материалы.
[0090] Авторы настоящего изобретения обнаружили, что конкретные пирролидиновые или пиперидиновые соединения, хотя и проявляют низкую ингибирующую активность в отношении других ферментов семейства DPP (DPP4, DPP7, DPP8, DPP9, PREP), проявляют селективную ингибирующую активность в отношении FAP. Таким образом, пирролидиновые или пиперидиновые соединения или их соли можно эффективно использовать для лечения и профилактики различных FAP-опосредованных заболеваний, например рака, заживления ран, ожирения, диабета, стеатоза, неалкогольного стеатогепатита (НАСГ) и цирроза печени.
[0091] Таким образом, настоящая технология предлагает соединения пирролидина и пиперидина, их стереоизомеры или их фармацевтически приемлемые соли, способы их получения, содержащие их фармацевтические композиции и их применение.
[0092] В соответствии с одним аспектом настоящей технологии предлагается соединение пирролидина или пиперидина, его стереоизомер или смесь стереоизомеров или его фармацевтически приемлемая соль.
[0093] В соответствии с другим аспектом настоящей технологии предложен способ приготовления пирролидина или пиперидина.
[0094] В соответствии с другим аспектом настоящей технологии предложена фармацевтическая композиция, содержащая пирролидин или пиперидин в качестве активного ингредиента.
[0095] В соответствии с другим аспектом настоящей технологии предложен способ лечения, включающий введение пирролидина или раствора пиперидина, описанного в данном документе.
[0096] В соответствии с другим аспектом настоящей технологии предложено применение пирролидина или соединения пиперидина или его стереоизомера или смеси стереоизомеров или его фармацевтически приемлемой соли при производстве лекарственного средства для ингибирования белков активации фибробластов.
[0097] В настоящей технологии было обнаружено, что соединения согласно настоящей технологии, т.е. пирролидин или пиперидин, или их стереоизомеры, или их фармацевтически приемлемые соли проявляют ингибирующую активность на FAP. Таким образом, соединения в соответствии с настоящей технологией или их стереоизомеры или их фармацевтически приемлемые соли можно эффективно применять для лечения и профилактики различных FAP-опосредованных заболеваний, например, при раке, ранозаживлении, ожирении, диабете, стеатозе, неалкогольном стеатогепатите (НАСГ) и циррозе печени.
[0098] В одном аспекте в настоящем документе предложено соединение формулы X или его стереоизомер или смесь стереоизомеров или его фармацевтически приемлемой соли:
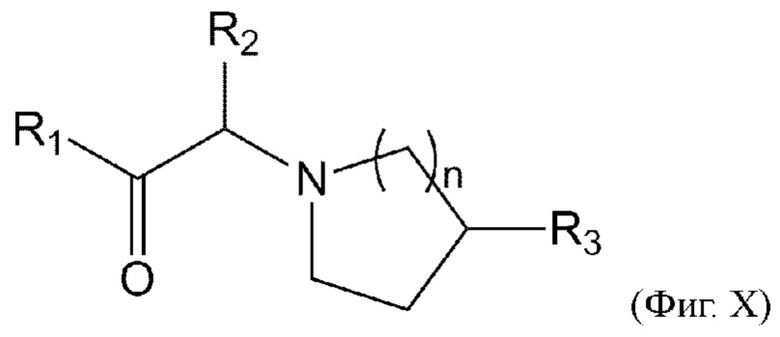
где
n представляет собой 1 или 2;
R1 представляет собой заместитель, выбранный из группы, состоящей из соединений формул I-V,
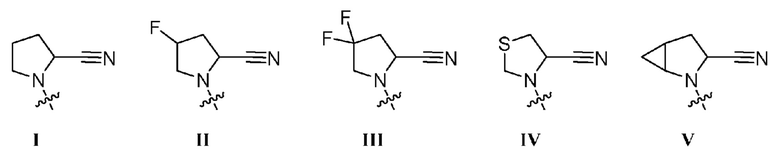
R2 представляет собой водород или C1-3алкил;
R3 представляет собой 5-12-членный замещенный или незамещенный гетероарил, где указанный гетероарил содержит от 1 до 3 гетероатомов, независимо выбранных из О, N и S,
3-12-членный замещенный или незамещенный неароматический гетероцикл, причем указанный гетероцикл содержит от 1 до 3 гетероатомов, независимо выбранных из О, N и S,
-NR4R5, -OR4, -C(O)NHR4, -NHC(O)(CH2)mR4, или -NHS(O)2R4,
где m представляет собой 0 или 1;
R4 представляет собой замещенный фенил; замещенный или незамещенный нафтил; замещенный или незамещенный неароматический гетероцикл; или замещенный или незамещенный гетероарил; и
R5 представляет собой водород или C1 3.
[0099] В другом аспекте в настоящем документе предложено соединение формулы Ха или стереоизомер или смесь стереоизомеров или его фармацевтически приемлемая соль:
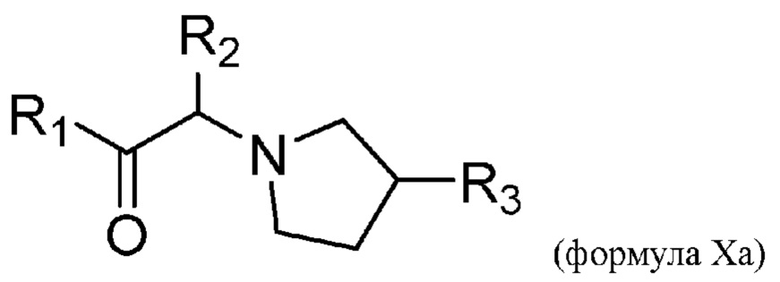
где
n представляет собой 1 или 2,
R1 представляет собой заместитель, выбранный из группы, состоящей из соединений формул I-V,

R1 представляет собой водород или C1-3алкил;
R3 представляет собой 5-12-членный замещенный или незамещенный гетероарил, где указанный гетероарил содержит от 1 до 3 гетероатомов, независимо выбранных из О, N и S,
3-12-членный замещенный или незамещенный неароматический гетероцикл, причем указанный гетероцикл содержит от 1 до 3 гетероатомов, независимо выбранных из О, N и S,
-NR4R3, -OR4, -C(O)NHR4, -NHC(O)(CH2)mR4, или -NHS(O)2R4,
где m представляет собой 0 или 1;
R4 представляет собой замещенный фенил; замещенный или незамещенный нафтил; замещенный или незамещенный неароматический гетероцикл; или замещенный или незамещенный гетероарил; и
R5 представляет собой водород или C1-3.
[0100] В другом аспекте в настоящем документе предложено соединение формулы Xb или стереоизомер или смесь стереоизомеров или его фармацевтически приемлемая соль:
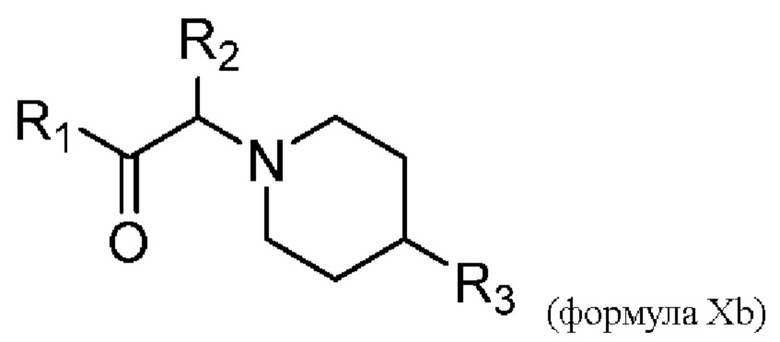
где
n представляет собой 1 или 2;
R1 представляет собой заместитель, выбранный из группы, состоящей из соединений формул I-V,
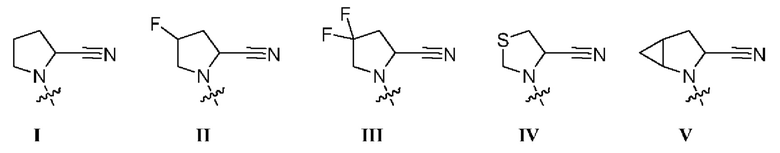
R2 представляет собой водород или C1-3алкил;
R3 представляет собой 5-12-членный замещенный или незамещенный гетероарил, где указанный гетероарил содержит от 1 до 3 гетероатомов, независимо выбранных из О, N и S,
3-12-членный замещенный или незамещенный неароматический гетероцикл, причем указанный гетероцикл содержит от 1 до 3 гетероатомов, независимо выбранных из О, N и S,
-NR4R5, -OR4, -C(O)NHR4, -NHC(O)(CH2)mR4, или -NHS(O)2R4,
где m представляет собой 0 или 1;
R4 представляет собой замещенный фенил; замещенный или незамещенный нафтил; замещенный или незамещенный неароматический гетероцикл; или замещенный или незамещенный гетероарил; и
R5 представляет собой водород или C1-3.
[0101] В другом аспекте в настоящем документе предложено соединение формулы 1а или его стереоизомер или смесь стереоизомеров или его фармацевтически приемлемая соль:

где R1, R2, R4, R5 и n являются такими, как определено в вариантах осуществления выше или ниже.
[0102] В другом аспекте в данном документе предложено соединение формулы 1b или стереоизомер или смесь стереоизомеров или его фармацевтически приемлемая соль:
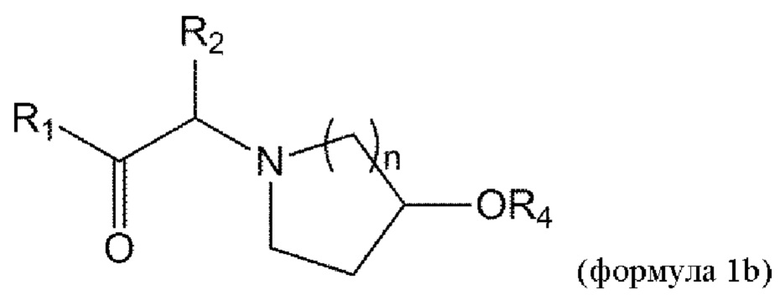
где R1, R2, R4 и n являются такими, как определено в вариантах осуществления выше или ниже.
[0103] В другом аспекте в данном документе предложено соединение формулы 1с или стереоизомер или смесь стереоизомеров или его фармацевтически приемлемая соль:
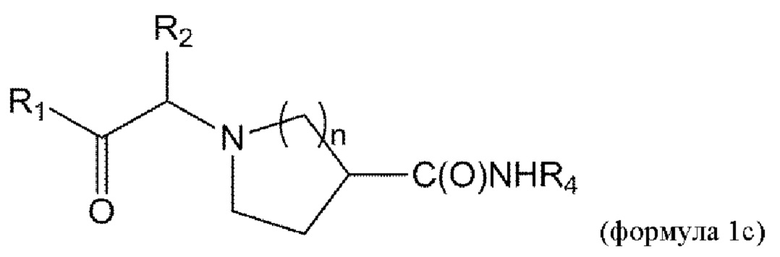
где R1, R2, R4 и n являются такими, как определено в вариантах осуществления выше или ниже.
[0104] В другом аспекте в данном документе предложено соединение формулы 1d или стереоизомер или смесь стереоизомеров или его фармацевтически приемлемая соль:

где R1, R2, R4, m и n являются такими, как определено в вариантах осуществления выше или ниже.
[0105] В другом аспекте в данном документе предложено соединение формулы 1е или стереоизомер или смесь стереоизомеров или его фармацевтически приемлемая соль:
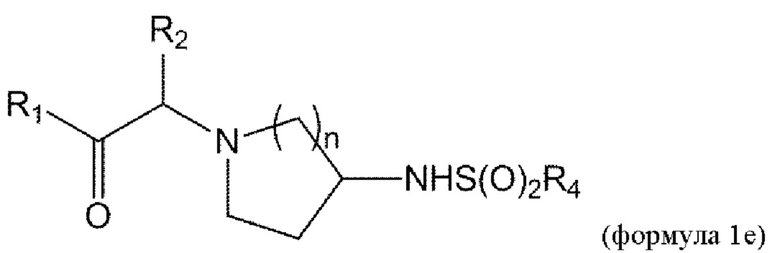
где R1, R2, R4 и n являются такими, как определено в вариантах осуществления выше или ниже.
[0106] В некоторых вариантах осуществления формул X, Ха, Xb, 1a, 1b, 1c, 1d и 1e, R4 представляет собой
фенил, замещенный 1-3 Z; гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, дигидробензо[1,4]диоксинила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинила, где указанный гетероцикл необязательно замещен 1-3 Z,
нафтил, необязательно замещенный 1-3 Z или
гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила, пиразинила, имидазолила, пиразолила, триазолила, оксазолила, тиазолила, фуранила, пирролила, тиофенила, хинолинила, изохинолинила, хроменонила, хиназолинила, бензоксазолила, бензофуранила, бензотиофенила, индолила, индолинила, бензимидазолила бензоксазолила, бензотиазолила, индазолила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила и акридинила, где указанный гетероарил необязательно замещен 1-3 Z; и
каждый Z независимо выбран из группы, состоящей из гидрокси, амино, галогена, циано, нитро, карбоновой кислоты, С1-5алкила, необязательно замещенного 1-3 Z1, С2-6алкенила, необязательно замещенного Z1, С2-6алкинила, необязательно замещенного Z1, С1-5алкокси, необязательно замещенного 1-3 Z1, С1-5алкилтио, необязательно замещенного Z1, моно- или ди-С1-5алкиламино, необязательно замещенного Z1, пиперазинила, необязательно замещенного Z1, С1-5алкилсульфониламино, необязательно замещенного Z1, C1-5алкилкарбониламино, необязательно замещенного Z1, аминосульфонила, необязательно замещенного Z1, аминокарбонила, необязательно замещенного Z1, C1-5алкиламинокарбонила, необязательно замещенного Z1, фенила, необязательно замещенного Z1, фенокси, необязательно замещенного Z1, бензила, необязательно замещенного Z1, бензоила, необязательно замещенного Z1, фениламинокарбонила, необязательно замещенного Z1, пиразолила, необязательно замещенного Z1, бензоксазолила, необязательно замещенного Z1, C1-5алкоксикарбонила, необязательно замещенного Z1, бензилокси, необязательно замещенного Z1, C1-5алкилсульфонила, необязательно замещенного Z1;
где каждый Z1 независимо выбран из галогена, гидроксила, амино, С1-5алкиламино, циано, ацетила, C1-5алкила, C1-5галогеналкила, С3-6карбоцикла, С3-6гетероцикла, при этом указанный С3-6карбоцикл и указанный С3-6гетероцикл необязательно замещен галогеном, гидроксилом, С1-5галкилом или C1-5галоалкилом.
[0107] В некоторых вариантах осуществления изобретения формулы X, Ха, Xb, 1a, 1b, 1c, 1d, и 1e, R4 представляют собой фенил, замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, галогена, циано, нитро, карбоновой кислоты, C1-5алкила, необязательно замещенного 1-3 галогенами или аминогруппой, С2-6алкенила, С2-6алкинила, C1-5алкокси, C1-5алкилтио, моно- или ди-C1-5алкиламино, пиперазинила, необязательно замещенного ацетилом, С1-5алкилсульфониламино, C1-5алкилкарбониламино, аминосульфонила, аминокарбонила, C1-5алкиламинокарбонила, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила; или
R4 представляет собой гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, дигидробензо[1,4]диоксинила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинил; или
R4 представляет собой нафтил, необязательно замещенный галогеном; или
R4 представляет собой гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила, пиразинила, имидазолила, пиразолила, триазолила, оксазолила, тиазолила, фуранила, пирролила, тиофенила, хинолинила, изохинолинила, хроменонила, хиназолинила, бензоксазолила, бензофуранила, бензотиофенила, индолила, индолинила, бензимидазолила, бензоксазолила, бензотиазолила, индазолила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила и акридинила, где гетероарил необязательно замещен 1-3 Z, где каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-С1-5алкиламино, циано, нитро, галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, необязательно замещенного 1-3 галогенами, C1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила и C1-5алкилсульфонила.
[0108] В другом аспекте настоящая технология обеспечивает соединение, обладающее ингибирующей активностью в отношении FAP, или его соли, то есть соединение формулы 1, или его стереоизомер, или смесь стереоизомеров, или его фармацевтически приемлемая соль:
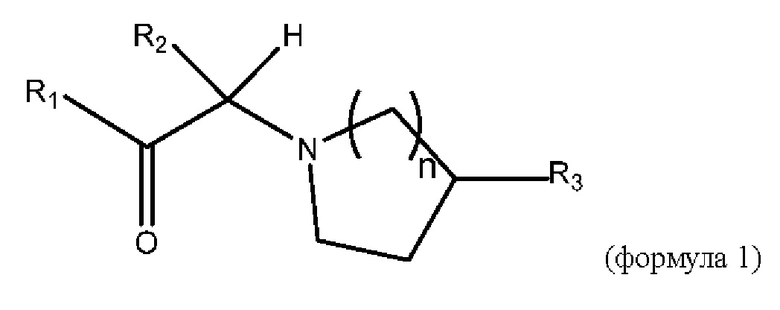
где
n представляет собой 1 или 2;
R1 выбран из группы, состоящей из формул I, II, III, IV, и IV;
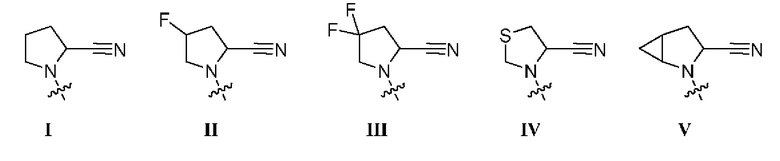
R2 представляет собой водород или C1-3алкил;
R3 представляет собой 5-12-членный гетероарил, причем указанный гетероарил содержит от 1 до 3 гетероатомов, независимо выбранных из О, N и S, и необязательно замещен 1-3 Z, 3-12-членный неароматический гетероцикл, причем указанный гетероцикл содержит от 1 до 3 гетероатомов, независимо выбранных из О, N и S, и необязательно замещен 1-3 Z, -NR4R3, -OR4, -C(O)NHR4, -NHC(O)(CH2)mR4, -NHS(O)2R4, -(CH2)mCH2R4, или -(CH2)mNHR4,
где m представляет собой 0 или 1;
R4 представляет собой фенил, замещенный 1-3 Z,
гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, дигидробензо[1,4]диоксинила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и2-оксо-1,2,3,4-тетрагидрохинолинила, где указанный гетероцикл необязательно замещен 1-3 Z, нафтил, необязательно замещенный 1-3 Z или
гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила, пиразинила, имидазолила, пиразолила, триазолила, оксазолила, тиазолила, фуранила, пирролила, тиофенила, хинолинила, изохинолинила, хроменонила, хиназолинила, бензоксазолила, бензофуранила, бензотиофенила, индолила, индолинила, бензимидазолила бензоксазолила, бензотиазолила, индазолила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила, акридинила и нафтиридинила, где указанный гетероарил необязательно замещен 1-3 Z;
R5 представляет собой водород или C1-3алкил; и
каждый Z независимо выбран из группы, состоящей из гидрокси, амино, галогена, циано, нитро, карбоновой кислоты, C1-5алкила, необязательно замещенного 1-3 Z1, С2-6алкенила, необязательно замещенного Z1, С2-6алкинила, необязательно замещенного Z1, С1-5алкокси, необязательно замещенного 1-3 Z1, C1-5алкилтио, необязательно замещенного Z1, моно- или ди-С1-5алкиламино, необязательно замещенного Z1, пиперазинила, необязательно замещенного Z1, С1-5алкилсульфониламино, необязательно замещенного Z1, С1-5алкилкарбониламино, необязательно замещенного Z1, аминосульфонила, необязательно замещенного Z1, аминокарбонила, необязательно замещенного Z1, C1-5алкиламинокарбонила, необязательно замещенного Z1, фенила, необязательно замещенного Z1, фенокси, необязательно замещенного Z1, бензила, необязательно замещенного Z1, бензоина, необязательно замещенного Z1, фениламинокарбонила, необязательно замещенного Z1, пиразолила, необязательно замещенного Z1, бензоксазолила, необязательно замещенного Z1, C1-5алкоксикарбонила, необязательно замещенного Z1, бензилокси, необязательно замещенного Z1, C1-5алкилсульфонила, необязательно замещенного Z1, ацетила, морфолинил, необязательно замещенного Z1, -NR6C(O)R7, и -C(O)NR6R7;
где каждый Z1 независимо выбран из галогена, гидроксила, амино, С1-5алкиламино, циано, ацетила, C1-5алкила, С1-5галогеналкила, С3-6карбоцикла, С3-6гетероцикла, при этом указанный С3-6карбоцикл и указанный С3-6гетероцикл необязательно замещен галогеном, гидроксилом, С1-5алкилом или C1-5;
R6 представляет собой водород или C1-3алкильную группу;
R7 представляет собой C1-3алкильную группу, необязательно замещенную фенилом, фенил, необязательно замещенный 1-3 Z2 или
гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила, пиразинила, имидазолила, пиразолила, триазолила, оксазолила, тиазолила, фуранила, пирролила, тиофенила, хинолинила, изохинолинила, хроменонила, хиназолинила, бензоксазолила, бензофуранила, бензотиофенила, индолила, индолинила, бензимидазолила бензоксазолила, бензотиазолила, индазолила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила, акридинила и нафтиридинила, где указанный гетероарил необязательно замещен 1-3 Z2; и
каждый Z2 независимо выбран из группы, состоящей из гидрокси, амино, галогена, циано, нитро, гидроксикарбонила, С1-5алкила, необязательно замещенного 1-3 Z3, С2-6алкенила, С2-6алкинила, C1-5алкокси, необязательно замещенного 1-3 Z3, С1-5алкилтио, моно- или ди-С1-5алкиламино, пиперазинила, необязательно замещенного Z3, С1-5алкилсульфониламино, С1-5алкилкарбониламино, аминосульфонила, аминокарбонила, С1-5алкиламинокарбонила, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила;
где каждый Z3 независимо выбран из галогена, амино или ацетила.
[0109] В некоторых вариантах осуществления соединение формулы 1 или его стереоизомер или смесь стереоизомеров или его фармацевтически приемлемая соль:
n представляет собой 1 или 2;
R1 выбран из группы, состоящей из формул I, II, III, IV и V:
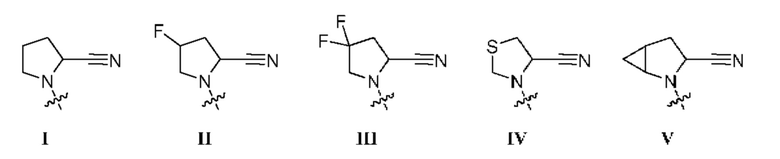
R2 представляет собой водород или C1-3алкил;
R3 представляет собой 5-12-членный гетероарил, причем указанный гетероарил содержит от 1 до 3 гетероатомов, независимо выбранных из О, N и S, и необязательно замещен 1-3 Z, 3-12-членный неароматический гетероцикл, причем указанный гетероцикл содержит от 1 до 3 гетероатомов, независимо выбранных из О, N и S, и необязательно замещен 1-3 Z, -NR4R5, -OR4, -C(O)NHR4, -NHC(O)(CH2)mR4, или -NHS(O)2R4,
где m представляет собой 0 или 1;
R4 представляет собой фенил, замещенный 1-3 Z,
гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, дигидробензо[1,4]диоксинила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинила, где указанный гетероцикл необязательно замещен 1-3 Z, нафтил, необязательно замещенный 1-3 Z или
гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила, пиразинила, имидазолила, пиразолила, триазолила, оксазолила, тиазолила, фуранила, пирролила, тиофенила, хинолинила, изохинолинила, хроменонила, хиназолинила, бензоксазолила, бензофуранила, бензотиофенила, индолила, индолинила, бензимидазолила, бензоксазолила, бензотиазолила, индазолила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила и акридинила, где указанный гетероарил необязательно замещен 1-3 Z;
R5 представляет собой водород или C1-3алкил; и
каждый Z независимо выбран из группы, состоящей из гидрокси, амино, галогена, циано, нитро, карбоновой кислоты, С1-5алкила, необязательно замещенного 1-3 Z1, С2-6алкенила, необязательно замещенного Z1, С2-6алкинила, необязательно замещенного Z1, С1-5алкокси, необязательно замещенного 1-3 Z1, С1-5алкилтио, необязательно замещенного Z1, моно- или ди-С1-5алкиламино, необязательно замещенного Z1, пиперазинила, необязательно замещенного Z1, C1-5алкилсульфониламино, необязательно замещенного Z1, C1-5алкилкарбониламино, необязательно замещенного Z1, аминосульфонила, необязательно замещенного Z1, аминокарбонила, необязательно замещенного Z1, С1-5алкиламинокарбонила, необязательно замещенного Z1, фенила, необязательно замещенного Z1, фенокси, необязательно замещенного Z1, бензила, необязательно замещенного Z1, бензоина, необязательно замещенного Z1, фениламинокарбонила, необязательно замещенного Z1, пиразолила, необязательно замещенного Z1, бензоксазолила, необязательно замещенного Z1, C1-5алкоксикарбонила, необязательно замещенного Z1, бензилокси, необязательно замещенного Z1, C1-5алкилсульфонила, необязательно замещенного Z1;
где каждый Z1 независимо выбран из галогена, гидроксила, амино, С1-5алкиламино, циано, ацетила, С1-5алкила, C1-5галогеналкила, С3-6карбоцикла, С3-6гетероцикла, при этом указанный С3-6карбоцикл и указанный С3-6гетероцикл необязательно замещен галогеном, гидроксилом, С1-5алкилом или C1-5галоалкилом.
[0110] В некоторых вариантах осуществления изобретения R1 выбран из группы, состоящей из соединений формул I, II, III и V:
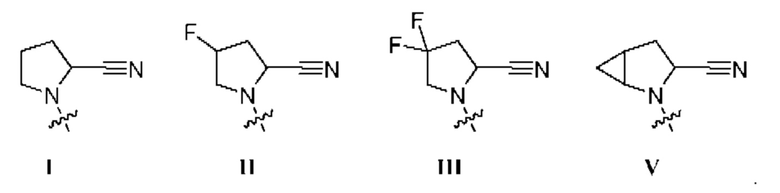
В некоторых вариантах осуществления изобретения R1 представляет собой заместитель формулы I. В некоторых вариантах осуществления изобретения R1 представляет собой заместитель формулы П. В некоторых вариантах осуществления изобретения R1 представляет собой заместитель формулы III. В некоторых вариантах осуществления изобретения R1 представляет собой заместитель формулы IV В некоторых вариантах осуществления изобретения R1 представляет собой заместитель формулы V.
[0111] В некоторых вариантах осуществления R1 представляет собой заместитель, выбранный из группы, состоящей из соединений формул Ia-Va,
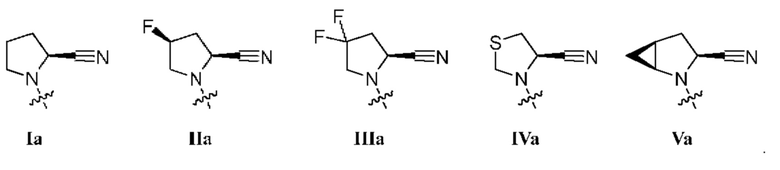
[0112] В некоторых вариантах осуществления R1 представляет собой заместитель, выбранный из группы, состоящей из соединений формул Ia, IIa, IIIa, и Va:
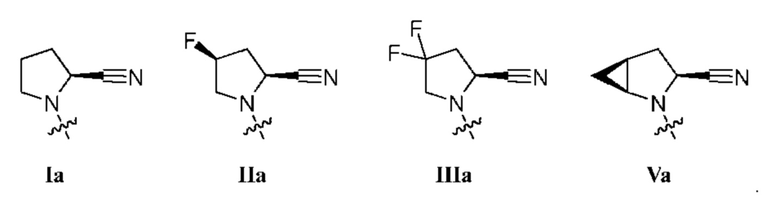
[0113] В некоторых вариантах осуществления изобретения R1 представляет собой соединение формулы Ia:
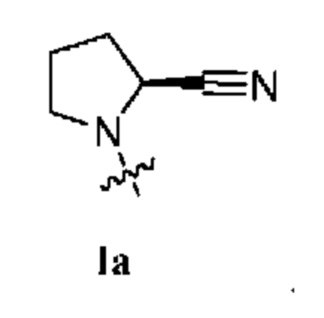
[0114] В некоторых вариантах осуществления изобретения R1 представляет собой соединение формулы IIa:
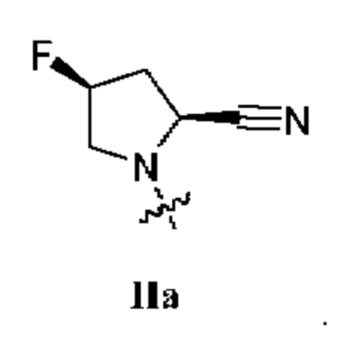
[0115] В некоторых вариантах осуществления изобретения R1 представляет собой соединение формулы IIIa:
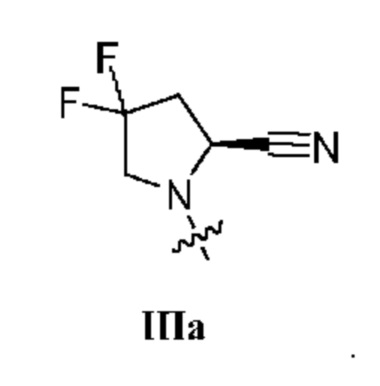
[0116] В некоторых вариантах осуществления изобретения R1 представляет собой соединение формулы IVa:
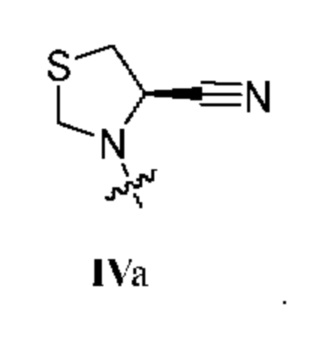
[0117] В некоторых вариантах осуществления изобретения R1 представляет собой соединение формулы Va:
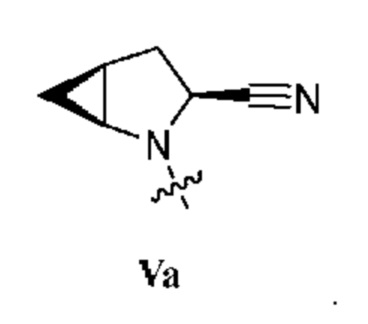
[0118] В некоторых вариантах осуществления R2 представляет собой водород. В некоторых вариантах осуществления R2 представляет собой C1-3алкил.
[0119] В некоторых вариантах осуществления m представляет собой 0. В некоторых вариантах осуществления m представляет собой 1.
[0120] В некоторых вариантах осуществления n представляет собой 1. В некоторых вариантах осуществления n представляет собой 2.
[0121] В некоторых вариантах осуществления изобретения R3 представляет собой заместитель, выбранный из группы, состоящей из -NR4R3, -OR4, -C(O)NHR4, -NHC(O)(CH2)mR4, и -NHS(O)2R4. В некоторых вариантах осуществления изобретения R3 представляет собой заместитель, выбранный из группы, состоящей из -NR4R3, -OR4, и -NHC(O)(CH2)mR4. В некоторых вариантах осуществления изобретения R3 представляет собой заместитель, выбранный из группы, состоящей из -NR4R5 и -OR4. В некоторых вариантах осуществления R3 представляет собой -NR4R3. В некоторых вариантах осуществления R3 представляет собой -OR4. В некоторых вариантах осуществления R3 представляет собой -C(O)NHR4. В некоторых вариантах осуществления R3 представляет собой -NHC(O)(CH2)mR4. В некоторых вариантах осуществления R3 представляет собой -NHS(O)2R4.
[0122] В некоторых вариантах осуществления изобретения R3 представляет собой 3-12-членный неароматический гетероцикл, 1-3 атома азота, причем указанный гетероцикл необязательно замещен 1-3 Z. В некоторых вариантах осуществления R3 представляет собой 5-12-членный гетероарил, необязательно замещенный 1-5 Z. В некоторых вариантах осуществления R3 представляет собой 2-оксо-2,3-дигидро-1H-бензо[d]имидазол-1-ил.
[0123] В других вариантах осуществления R4 представляет собой фенил, замещенный заместителем, выбранным из группы, состоящей из пиперазинила, необязательно замещенного ацетилом, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила; или R4 представляет собой гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинила; или R4 представляет собой нафтил, необязательно замещенный галогеном; или R4 представляет собой гетероарил, выбранный из группы, состоящей из пиридинила, хинолинила, изохинолинила, хиназолинила, бензофуранила, бензотиофенила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила и акридинила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, C1-5алкокси, необязательно замещенного 1-3 галогенами, C1-5алкоксикарбонила, бензилокси и фенила, необязательно замещенного галогеном.
[0124] В некоторых вариантах осуществления изобретения R4 представляет собой фенил, замещенный фенилом; или R4 представляет собой нафтил; или R4 представляет собой гетероарил, выбранный из группы, состоящей из хинолинила, изохинолинила, бензофуранила, бензотиофенила и фуро[3,2-с]пиридинила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, и С1-5алкокси, необязательно замещенного 1-3 галогенами.
[0125] В некоторых вариантах осуществления изобретения R4 представляет собой фенил, замещенный фенилом; или R4 представляет собой нафтил; или R4 представляет собой гетероарил, выбранный из группы, состоящей из хинолинила, изохинолинила, бензофуранила и бензотиофенила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, галогена, С1-5алкила и С1-5алкокси.
[0126] В других вариантах осуществления R4 представляет собой фенил, замещенный заместителем, выбранным из группы, состоящей из пиперазинила, необязательно замещенного ацетилом, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила; или R4 представляет собой гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинила; или R4 представляет собой нафтил, необязательно замещенный галогеном; или R4 представляет собой гетероарил, выбранный из группы, состоящей из пиридинила, хинолинила, изохинолинила, хиназолинила, тиено[2,3-d]пиримидинила, изоксазолила и акридинила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, необязательно замещенного 1-3 галогенами, бензилокси и фенила, необязательно замещенного галогеном.
[0127] В некоторых вариантах осуществления изобретения R4 представляет собой фенил, замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, галогена, циано, нитро, карбоновой кислоты, С1-5алкила, необязательно замещенного 1-3 галогенами или аминогруппой, С2-6алкенила, С2-6алкинила, С1-5алкокси, С1-5алкилтио, моно- или ди-С1-5алкиламино, пиперазинила, необязательно замещенного ацетилом, С1-5алкилсульфониламино, С1-5алкилкарбониламино, аминосульфонила, аминокарбонила, С1-5алкиламинокарбонила, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила.
[0128] В других вариантах осуществления R4 представляет собой фенил, замещенный заместителем, выбранным из группы, состоящей из пиперазинила, необязательно замещенного ацетилом, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила. В некоторых вариантах осуществления изобретения R4 представляет собой фенил, замещенный фенилом.
[0129] В некоторых вариантах осуществления изобретения, R4 представляет собой гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, дигидробензо[1,4]диоксинила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинил. В других вариантах осуществления изобретения R4 представляет собой гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-.
[0130] В некоторых вариантах осуществления изобретения R4 представляет собой нафтил, необязательно замещенный галогеном. В других вариантах осуществления R4 представляет собой нафтил.
[0131] В некоторых вариантах осуществления изобретения R4 представляет собой гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила, пиразинипа, имидазолила, пиразолила, триазолипа, оксазолила, тиазолипа, фуранипа, пирролила, тиофенипа, хинолинила, изохинолинипа, хроменонила, хиназолинипа, бензоксазолила, бензофуранила, бензотиофенила, индолила, индолинила, бензимидазолила, бензоксазолила, бензотиазолила, индазолила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила, акридинипа и нафтиридинила, где указанный гетероарил необязательно замещен 1-3 Z, где каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-С1-5алкиламино, циано, нитро, галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, C1-5алкокси, необязательно замещенного от 1 до 3 галогенов, C1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила, C1-5алкилсульфонила, морфолинипа, -NR6C(O)R7, и -C(O)NR6R7. В некоторых вариантах осуществления R4 представляет собой гетероарил, выбранный из группы, состоящей из пиридинила, хинолинила, изохинолинипа, хрома, хиназолинипа, бензофуранила, индолинила, бензимидазолила, бензотиофенила, бензотиазолила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила, акридинипа и нафтиридинила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, циано, нитро, галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, C1-5алкокси, необязательно замещенного 1-3 галогенами, С1-5алкоксикарбонила, бензилокси, ацетила, морфолинипа, -NR6C(O)R7, -C(O)NR6R7 и фенила, необязательно замещенного галогеном; R6 представляет собой водород или C1-5алкильную группу; и R7 представляет собой C1-5алкильную группу, необязательно замещенную фенилом, фенил или гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила и изоксазолила. В некоторых вариантах осуществления изобретения R4 представляет собой гетероарил, выбранный из группы, состоящей из пиридинила, хинолинила, изохинолинила, хрома, хиназолинила, бензофуранила, индолинила, бензимидазолила, бензотиофенила, бензотиазолила, фуро[3,2-с]пиридинила и нафтиридинила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, циано, нитро, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, C1-5алкокси, необязательно замещенного 1-3 галогенами, бензилокси, ацетила, морфолинила, -NR6C(O)R7, -C(O)NR6R7 В некоторых вариантах осуществления изобретения R4 представляет собой гетероарил, выбранный из группы, состоящей из пиридинила, хинолинила, изохинолинила, хрома, хиназолинила, бензофуранила, индолинила, бензимидазолила, бензотиофенила, бензотиазолила, фуро[3,2-с]пиридинила и нафтиридинила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, циано, нитро, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, необязательно замещенного 1-3 галогенами, бензилокси, ацетила, морфолинила, -NR6C(O)R7, -C(O)NR6R7; R6 представляет собой водород или C1-3алкильную группу; и R7 представляет собой C1-3алкильную группу, необязательно замещенную фенилом, фенил или гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила и изоксазолила.
[0132] В некоторых вариантах осуществления R4 представляет собой хинолинил или изохинолинил, каждый из которых необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, циано, нитро, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, C1-5алкокси, необязательно замещенного 1-3 галогенами, бензилокси, ацетила, морфолинила, -NR6C(O)R7, -C(O)NR6R7; R6 представляет собой водород или C1-3алкильную группу; и R7 представляет собой C1-3алкильную группу, необязательно замещенную фенилом, фенил или гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила и изоксазолила. В некоторых вариантах осуществления изобретения R4 представляет собой хинолинил, необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, циано, нитро, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, необязательно замещенного 1-3 галогенами, бензилокси, ацетила, морфолинила, -NR6C(O)R7, -C(O)NR6R7; R6 представляет собой водород или C1-3алкильную группу; и R7 представляет собой C1-3алкильную группу, необязательно замещенную фенилом, фенил или гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила и изоксазолила.
[0133] В некоторых вариантах осуществления изобретения R4 представляет собой гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила, пиразинила, имидазолила, пиразолила, триазолила, оксазолила, тиазолила, фуранила, пирролила, тиофенила, хинолинила, изохинолинила, хроменонила, хиназолинила, бензоксазолила, бензофуранила, бензотиофенила, индолила, индолинила, бензимидазолила, бензоксазолила, бензотиазолила, индазолила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила и акридинила, где гетероарил необязательно замещен 1-3 Z, где каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-C1-5алкиламино, циано, нитро, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, необязательно замещенного 1-3 галогенами, С1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила и С1-5алкилсульфонила. В некоторых вариантах осуществления изобретения R4 представляет собой гетероарил, выбранный из группы, состоящей из пиридинила, хинолинила, изохинолинила, хиназолинила, бензофуранила, бензотиофенила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила и акридинила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, необязательно замещенного 1-3 галогенами, С1-5алкоксикарбонила, бензилокси и фенила, необязательно замещенного галогеном. В некоторых вариантах осуществления изобретения R4 представляет собой гетероарил, выбранный из группы, состоящей из хинолинила, изохинолинила, бензофуранила, бензотиофенила и фуро[3,2-с]пиридинила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, и C1-5алкокси, необязательно замещенного 1-3 галогенами.
[0134] В некоторых вариантах осуществления изобретения R4 представляет собой гетероарил, выбранный из группы, состоящей из хинолинила, изохинолинила, бензофуранила и бензотиофенила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, галогена, C1-5алкила и С1-5алкокси.
[0135] В некоторых вариантах осуществления изобретения R4 представляет собой гетероарил, выбранный из группы, состоящей из пиридинила, хинолинила, изохинолинила, хиназолинила, тиено[2,3-d]пиримидинила, изоксазолила и акридинила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из циано, галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, необязательно замещенного 1-3 галогенами, бензилокси и фенила, необязательно замещенного галогеном. В некоторых вариантах осуществления изобретения R4 представляет собой гетероарил, выбранный из группы, состоящей из пиридинила, хинолинила, изохинолинила, хиназолинила, тиено[2,3-d]пиримидинила, изоксазолила и акридинила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, необязательно замещенного 1-3 галогенами, бензилокси и фенила, необязательно замещенного галогеном.
[0136] В некоторых вариантах осуществления R4 представляет собой хинолинил, изохинолинил или хиназолинил, каждый из которых необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из циано, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, и C1-5алкокси, необязательно замещенного 1-3 галогенами. В некоторых вариантах осуществления R4 представляет собой хинолинил, изохинолинил или хиназолинил, каждый из которых необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, и С1-5алкокси, необязательно замещенного 1-3 галогенами.
[0137] В некоторых вариантах осуществления R4 представляет собой хинолинил или изохинолинил, каждый из которых необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, и С1-5алкокси, необязательно замещенного 1-3 галогенами.
[0138] В некоторых вариантах осуществления изобретения R4 представляет собой хинолинил или изохинолинил, каждый из которых необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, галогена, С1-5алкила и С1-5алкокси. В некоторых вариантах осуществления R4 представляет собой хинолинил, необязательно замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, и С1-5алкокси, необязательно замещенного 1-3 галогенами.
[0139] В некоторых вариантах осуществления изобретения R4 представляет собой бензофуранил, бензотиофенил или фуро[3,2-с]пиридинил, каждый из которых необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из галогена, C1-5алкила и С1-5алкокси. В некоторых вариантах осуществления R4 представляет собой бензофуранил или бензотиофенил, каждый из которых необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из галогена, C1-5алкил и C1-5алкокси. В некоторых вариантах осуществления R4 представляет собой бензофуранил, необязательно замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, галогена, C1-5алкила и C1-5алкокси. В некоторых вариантах осуществления R4 представляет собой бензофуранил или бензотиофенил.
[0140] В некоторых вариантах осуществления изобретения R4 представляет собой пиридинил, причем указанный R4 представляет собой необязательно замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-С1-5алкиламино, циано, нигро, галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, C1-5алкокси, необязательно замещенного 1-3 галогенами, C1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила, C1-5алкилсульфонила, морфолинила, -NR6C(O)R7 и -C(O)NR6R7. В некоторых вариантах осуществления изобретения R4 представляет собой пиридинил, причем указанный R4 представляет собой необязательно замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-C1-5алкиламино, циано, нитро, галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, C1-5алкокси, необязательно замещенного 1-3 галогенами, C1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила, C1-5алкилсульфонила, морфолинила, -NR6C(O)R7 и -C(O)NR6R7; R6 представляет собой водород или C1-3алкильную группу; и R7 представляет собой C1-3алкильную группу, необязательно замещенную фенилом, фенил или гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила и изоксазолила.
[0141] В некоторых вариантах осуществления изобретения R4 представляет собой хроменонил, причем указанный R4 представляет собой необязательно замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-С1-5алкиламино, циано, нигро, галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, C1-5алкокси, необязательно замещенного 1-3 галогенами, C1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила, C1-5алкилсульфонила, морфолинила, -NR6C(O)R7 и -C(O)NR6R7. В некоторых вариантах осуществления изобретения R4 представляет собой хроменонил, причем указанный R4 представляет собой необязательно замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-C1-5алкиламино, циано, нитро, галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, C1-5алкокси, необязательно замещенного 1-3 галогенами, C1-3алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила, C1-3алкилсульфонила, морфолинила, -NR6C(O)R7, и -С(O)NR6R7. R6 представляет собой водород или C1-3алкильную группу; и R7 представляет собой C1-3алкильную группу, необязательно замещенную фенилом, фенил или гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила и изоксазолила.
[0142] В некоторых вариантах осуществления изобретения R4 представляет собой хиназолинил, причем указанный R4 представляет собой необязательно замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-С1-5алкиламино, циано, нитро, галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, C1-5алкокси, необязательно замещенного 1-3 галогенами, C1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила, C1-5алкилсульфонила, морфолинила, -NR6C(O)R7, и -C(O)NR6R7. В некоторых вариантах осуществления изобретения R4 представляет собой хиназолинил, причем указанный R4 представляет собой необязательно замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-C1-5алкиламино, циано, нитро, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, необязательно замещенного 1-3 галогенами, С1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила, С1-5алкилсульфонила, морфолинила, -NR6C(O)R7, и -C(O)NR6R7; R6 представляет собой водород или С1-3алкильггую группу; и R7 представляет собой С1-3алкильггую группу, необязательно замещенную фенилом, фенил или гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила и изоксазолила.
[0143] В некоторых вариантах осуществления изобретения R4 представляет собой бензотиофенил, причем указанный R4 представляет собой необязательно замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-С1-5алкиламино, циано, нитро, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, необязательно замещенного 1-3 галогенами, C1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила, C1-5алкилсульфонила, морфолинила, -NR6C(O)R7, и -C(O)NR6R7. В некоторых вариантах осуществления изобретения R4 представляет собой бензотиофенил, причем указанный R4 представляет собой необязательно замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-C1-5алкиламино, циано, нитро, галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, необязательно замещенного 1-3 галогенами, С1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила, С1-5алкилсульфонила, морфолинила, -NR6C(O)R7, и -C(O)NR6R7; R6 представляет собой водород или C1-3алкильную группу; и R7 представляет собой C1-3алкильную группу, необязательно замещенную фенилом, фенил или гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила и изоксазолила.
[0144] В некоторых вариантах осуществления изобретения R4 представляет собой индолинил, причем указанный R4 представляет собой необязательно замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-С1-5алкиламино, циано, нитро, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, C1-5алкокси, необязательно замещенного 1-3 галогенами, C1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила, C1-5алкилсульфонила, морфолинила, -NR6C(O)R7, и -C(O)NR6R7. В некоторых вариантах осуществления изобретения R4 представляет собой индолинил, причем указанный R4 представляет собой необязательно замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-C1-5алкиламино, циано, нитро, галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, необязательно замещенного 1-3 галогенами, С1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила, С1-5алкилсульфонила, морфолинила, -NR6C(O)R7, и -C(O)NR6R7; R6 представляет собой водород или C1-3алкильную группу; и R7 представляет собой C1-3алкильную группу, необязательно замещенную фенилом, фенил или гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила и изоксазолила.
[0145] В некоторых вариантах осуществления изобретения R4 представляет собой бензотиазолил, причем указанный R4 представляет собой необязательно замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-С1-5алкиламино, циано, нитро, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, необязательно замещенного 1-3 галогенами, C1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила, C1-5алкилсульфонила, морфолинила, -NR6C(O)R7, и -C(O)NR6R7. В некоторых вариантах осуществления изобретения R4 представляет собой бензотиазолил, причем указанный R4 представляет собой необязательно замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-C1-5алкиламино, циано, нитро, галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, C1-5алкокси, необязательно замещенного 1-3 галогенами, C1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила, C1-5алкилсульфонила, морфолинила, -NR6C(O)R7, и -С(O)NR6R7; R6 представляет собой водород или C1-3алкильную группу; и R7 представляет собой C1-3алкильную группу, необязательно замещенную фенилом, фенил или гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила и изоксазолила.
[0146] В некоторых вариантах осуществления изобретения R4 представляет собой фуро[3,2-с]пиридинил, причем указанный R4 представляет собой необязательно замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-С1-3алкиламино, циано, нитро, галогена, C1-3алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, необязательно замещенного 1-3 галогенами, С1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила, C1-5алкилсульфонила, морфолинила, -NR6C(O)R7, и -C(O)NR6R7. В некоторых вариантах осуществления изобретения R4 представляет собой фуро[3,2-с]пиридинил, причем указанный R4 представляет собой необязательно замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-С1-5алкиламино, циано, нитро, галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, C1-5алкокси, необязательно замещенного 1-3 галогенами, C1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила, C1-5алкилсульфонила, морфолинила, -NR6C(O)R7, и -C(O)NR6R7; R6 представляет собой водород или С1-3алкильную группу; и R7 представляет собой C1-3алкильную группу, необязательно замещенную фенилом, фенил или гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила и изоксазолила.
[0147] В некоторых вариантах осуществления изобретения R4 представляет собой нафтиридинил, причем указанный R4 представляет собой необязательно замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-С1-5алкиламино, циано, нитро, галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, C1-5алкокси, необязательно замещенного 1-3 галогенами, C1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила, C1-5алкилсульфонила, морфолинила, -NR6C(O)R7, и -C(O)NR6R7. В некоторых вариантах осуществления изобретения R4 представляет собой нафтиридинил, причем указанный R4 представляет собой необязательно замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-C1-5алкиламино, циано, нитро, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, C1-5алкокси, необязательно замещенного 1-3 галогенами, C1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила, С1-5алкилсульфонила, морфолинила, -NR6C(O)R7, и -C(O)NR6R7; R6 представляет собой водород или C1-3алкильную группу; и R7 представляет собой C1-3алкильную группу, необязательно замещенную фенилом, фенил или гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила и изоксазолила.
[0148] В некоторых вариантах осуществления R4 представляет собой замещенный или незамещенный пиридинил. В некоторых вариантах осуществления R4 представляет собой замещенный или незамещенный пиримидинил. В некоторых вариантах осуществления R4 представляет собой замещенный или незамещенный пиразинил. В некоторых вариантах осуществления R4 представляет собой замещенный или незамещенный имидазолил. В некоторых вариантах осуществления R4 представляет собой замещенный или незамещенный пиразолил. В некоторых вариантах осуществления R4 представляет собой замещенный или незамещенный триазолил. В некоторых вариантах осуществления R4 представляет собой замещенный или незамещенный оксазолил. В некоторых вариантах осуществления R4 представляет собой замещенный или незамещенный оксазолил. В некоторых вариантах осуществления R4 представляет собой замещенный или незамещенный фуранил. В некоторых вариантах осуществления R4 представляет собой замещенный или незамещенный пирролил. В некоторых вариантах осуществления R4 представляет собой замещенный или незамещенный тиофенил. В некоторых вариантах осуществления R4 представляет собой замещенный или незамещенный хинолинил. В некоторых вариантах осуществления R4 представляет собой замещенный или незамещенный изохинолинил. В некоторых вариантах осуществления R4 представляет собой замещенный или незамещенный хроменонил. В некоторых вариантах осуществления R4 представляет собой замещенный или незамещенный хиназолинил. В некоторых вариантах осуществления R4 представляет собой замещенный или незамещенный бензоксазолил. В некоторых вариантах осуществления R4 представляет собой замещенный или незамещенный бензофуранил. В некоторых вариантах осуществления R4 представляет собой замещенный или незамещенный бензотиофенил. В некоторых вариантах осуществления R4 представляет собой замещенный или незамещенный индолил. В некоторых вариантах осуществления R4 представляет собой замещенный или незамещенный индолинил. В некоторых вариантах осуществления R4 представляет собой замещенный или незамещенный бензимидазолил. В некоторых вариантах осуществления R4 представляет собой замещенный или незамещенный бензоксазолил. В некоторых вариантах осуществления R4 представляет собой замещенный или незамещенный бензотиазолил. В некоторых вариантах осуществления R4 представляет собой замещенный или незамещенный индазолил. В некоторых вариантах осуществления изобретения R4 представляет собой замещенный или незамещенный фуро[3,2-с]пиридинил. В некоторых вариантах осуществления R4 представляет собой замещенный или незамещенный тиено[2,3-d]пиримидинил. В некоторых вариантах осуществления R4 представляет собой замещенный или незамещенный тиено[3,2-с]пиридинил. В некоторых вариантах осуществления R4 представляет собой замещенный или незамещенный изоксазолил. В некоторых вариантах осуществления R4 представляет собой замещенный или незамещенный акридинил. В некоторых вариантах осуществления R4 представляет собой замещенный или незамещенный нафтиридинил.
[0149] В других вариантах осуществления R4 представляет собой фенил, замещенный заместителем, выбранным из группы, состоящей из пиперазинила, необязательно замещенного ацетилом, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила;
гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинила;
нафтил, необязательно замещенный галогеном; или
гетероарил, выбранный из группы, состоящей из пиридинила, хинолинила, изохинолинила, хрома, хиназолинила, бензофуранила, индолинила, бензимидазолила, бензотиофенила, бензотиазолила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила, акридинила и нафтиридинила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, циано, нитро, галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, необязательно замещенного 1-3 галогенами, С1-5алкоксикарбонила, бензилокси, ацетила, морфолинила, -NR6C(O)R7, -C(O)NR6R7 и фенила, необязательно замещенного галогеном;
где R6 представляет собой водород или C1-3алкильную группу; и R7 представляет собой C1-3алкильную группу, необязательно замещенную фенилом, фенил или
гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила и изоксазолила.
[0150] В других вариантах осуществления R4 представляет собой фенил, замещенный заместителем, выбранным из группы, состоящей из пиперазинила, необязательно замещенного ацетилом, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила;
гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинила;
нафтил, необязательно замещенный галогеном; или
или гетероарил, выбранный из группы, состоящей из пиридинила, хинолинила, изохинолинила, хиназолинила, бензофуранила, бензотиофенила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила и акридинила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, C1-5алкокси, необязательно замещенного 1-3 галогенами, C1-3алкоксикарбонила, бензилокси и фенила, необязательно замещенного галогеном.
[0151] В некоторых вариантах осуществления изобретения R4 представляет собой фенил, замещенный фенилом;
нафтил; или
гетероарил, выбранный из группы, состоящей из пиридинила, хинолинила, изохинолинила, хрома, хиназолинила, бензофуранила, индолинила, бензимидазолила, бензотиофенила, бензотиазолила, фуро[3,2-с]пиридинила и нафтиридинила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, циано, нитро, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, С1-5алкокси, необязательно замещенного 1-3 галогенами, бензилокси, ацетила, морфолинила, -NR6C(O)R7, -C(O)NR6R7.
[0152] В некоторых вариантах осуществления изобретения R4 представляет собой фенил, замещенный фенилом;
нафтил; или
гетероарил, выбранный из группы, состоящей из хинолинила, изохинолинила, бензофуранила, бензотиофенила и фуро[3,2-с]пиридинила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из галогена, C1-5-залкила, необязательно замещенного 1-3 галогенами, и С1-5алкокси, необязательно замещенного 1-3 галогенами.
[0153] В некоторых вариантах осуществления R5 представляет собой водород. В некоторых вариантах осуществления R5 представляет собой C1-3алкил.
[0154] В некоторых вариантах осуществления R6 представляет собой водород. В некоторых вариантах осуществления R6 представляет собой C1-3алкильную группу.
[0155] В некоторых вариантах осуществления изобретения R7 представляет собой C1-3алкильную группу, необязательно замещенную фенилом.
[0156] В некоторых вариантах осуществления изобретения R7 представляет собой фенил, необязательно замещенный 1-3 Z2;
причем каждый Z2 независимо выбран из группы, состоящей из гидрокси, амино, галогена, циано, нитро, гидроксикарбонила, С1-5алкила, необязательно замещенного 1-3 Z3, C2-6алкенила, C2-6алкинила, C1-5алкокси, необязательно замещенного 1-3 Z3, C1-5алкилтио, моно- или ди-С1-5алкиламино, пиперазинила, необязательно замещенного Z3, C1-5алкилсульфониламино, C1-5алкилкарбониламино, аминосульфонила, аминокарбонила, С1-5алкиламинокарбонила, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила; где каждый Z3 независимо выбран из галогена, амино или ацетила
[0157] В некоторых вариантах осуществления изобретения R7 представляет собой гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила, пиразинила, имидазолила, пиразолила, триазолила, оксазолила, тиазолила, фуранила, пирролила, тиофенила, хинолинила, изохинолинила, хроменонила, хиназолинила, бензоксазолила, бензофуранила, бензотиофенила, индолила, индолинила, бензимидазолила бензоксазолила, бензотиазолила, индазолила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила, акридинила и нафтиридинила, где указанный гетероарил необязательно замещен 1-3 Z2;
причем каждый Z2 независимо выбран из группы, состоящей из гидрокси, амино, галогена, циано, нитро, гидроксикарбонила, C1-5алкила, необязательно замещенного 1-3 Z3, C2-6алкенила, С2-6алкинила, C1-5алкокси, необязательно замещенного 1-3 Z3, C1-5алкилтио, моно- или ди-С1-5алкиламино, пиперазинила, необязательно замещенного Z3, C1-5алкилсульфониламино, C1-5алкилкарбониламино, амино сульфонила, аминокарбонила, С1-5алкиламинокарбонила, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила; где каждый Z3 независимо выбран из галогена, амино или ацетила.
[0158] В некоторых вариантах осуществления R6 представляет собой водород или C1-3алкильную группу, и R7 представляет собой C1-3алкильную группу, необязательно замещенную фенилом, фенил или гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила и изоксазолила.
[0159] В одном варианте осуществления настоящей технологии предложено соединение формул X, Ха, Xb, 1, 1а, 1b, 1c, 1d, или 1е или его стереоизомер или смесь стереоизомеров или его фармацевтически приемлемую соль, причем
n представляет собой 1 или 2;
R1 представляет собой заместитель, выбранный из группы, состоящей из формул I, II, III, и V;
R2 представляет собой водород;
R3 представляет собой заместитель, выбранный из группы, состоящей из -NR4R5, -OR4, -C(O)NHR4, -NHC(O)(CH2)mR4, и -NHS(O)2R4,
где m представляет собой 0 или 1;
R4 представляет собой фенил, замещенный заместителем, выбранным из группы, состоящей из пиперазинила, необязательно замещенного ацетилом, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила;
нафтил, необязательно замещенный галогеном; или
или гетероарил, выбранный из группы, состоящей из пиридинила, хинолинила, изохинолинила, 2-оксо-1,2-дигидрохинолинила, 2-оксо-1,2,3,4-тетрагидрохинолинила, хиназолинила, бензофуранила, 2,3-дигидробензофуранила, бензотиофенила, бензо[d][1,3]диоксолила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила и акридинила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, галогена, С1-5алкила, необязательно замещенного 1-3 галогенами, C1-5алкокси, необязательно замещенного 1-3 галогенами, C1-5алкоксикарбонила, бензилокси и фенила, необязательно замещенного галогеном, и
R5 представляет собой водород.
[0160] В другом аспекте соединение формул X, Ха, Xb, 1, 1, 1a, 1b, 1c, 1d, или 1е или его стереоизомер или смесь стереоизомеров или его фармацевтически приемлемую соль выбирают из следующих соединений или их стереоизомеров или их фармацевтически приемлемой соли:
(R)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)-N-(хинолин-3-ил)пирролидин-3-карбоксамида;
(R)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)-N-(хинолин-4-ил)пирролидин-3-карбоксамида;
(S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)-N-(хинолин-3-ил)пирролидин-3-карбоксамида;
(S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)-N-(хинолин-4-ил)пирролидин-3-карбоксамида;
(S)-1-(2-((S)-3-(хинолин-4-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-4,4-дифтор-1-(2-((S)-3-(хинолин-3-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-4,4-дифтор-1-(2-((S)-3-(хинолин-4-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-4,4-дифтор-1-(2-((S)-3-(изохинолин-4-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(бензо[b]тиофен-4-иламино)пирролидин-1-ил)ацетил)-4,4-дифторпирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(бензо[b]тиофен-7-иламино)пирролидин-1-ил)ацетил)-4,4-дифторпирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(бензофуран-7-иламино)пирролидин-1-ил)ацетил)-4,4-дифторпирролидин-2-карбонитрил;
(S)-4,4-дифтор-1-(2-(SS)-3-(фуро[3,2-с]пиридин-7-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-([1,1'-бифенил]-2-иламино)пирролидин-1-ил)ацетил)-4,4-дифторпирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-([1,1'-бифенил]-4-иламино)пирролидин-1-ил)ацетил)-4,4-дифторпирролидин-2-карбонитрил;
(S)-4,4-дифтор-1-(2-((S)-3-(нафталин-2-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-([1,1'-бифенил]-3-иламино)пирролидин-1-ил)ацетил)-4,4-дифторпирролидин-2-карбонитрил;
(S)-1-(2-((R)-3-(хинолин-3-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((R)-3-([1,1'-бифенил]-3-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(изохинолин-4-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(бензо[b]тиофен-4-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(бензо[b]тиофен-7-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(бензофуран-7-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(фуро[3,2-с]пиридин-7-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((R)-3-(изохинолин-4-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((R)-3-(бензо[b]тиофен-7-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(1S,3S,5S)-2-(2-((S)-3-(фуро[3,2-с]пиридин-7-иламино)пирролидин-1-ил)ацетил)-2-азабицикло[3.1.0]гексан-3-карбонитрил;
(S)-1-(2-((S)-3-(хинолин-5-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(2S,4S)-4-фтор-1-(2-((S)-3-(фуро[3,2-с]пиридин-7-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
N-((S)-1-(2-(2S,4S)-2-циано-4-фторпирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-6-фторбензофуран-3-карбоксамида;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)хинолин-4-карбоксамида;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)хинолин-3-карбоксамида;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)хинолин-5-карбоксамида;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)хинолин-2-карбоксамида;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)хинолин-8-карбоксамида;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)изохинолин-1-карбоксамида;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)бензо[b]тиофен-2-карбоксамида;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)бензофуран-3-карбоксамида;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-2-(нафталин-1-ил)ацетамид;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-[1,1'-бифенил]-2-карбоксамида;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)бензофуран-2-карбоксамида;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)бензо[b]тиофен-3-карбоксамида;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-2-метилбензофуран-3-карбоксамида;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-5-фторбензофуран-3-карбоксамида;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-6-фторбензофуран-3-карбоксамида;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-7-метилбензофуран-3-карбоксамида;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-5-метоксибензофуран-3-карбоксамида;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-7-метоксибензофуран-3-карбоксамида;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-4-гидроксибензофуран-3-карбоксамида;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-6-гидроксибензофуран-3-карбоксамида;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-7-фторбензофуран-3-карбоксамида;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-5,7-дифторбензофуран-3-карбоксамида;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-5-метилбензофуран-3-карбоксамида;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-6-метилбензофуран-3-карбоксамида;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-6-метоксибензофуран-3-карбоксамида;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)бензофуран-4-карбоксамида;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)бензофуран-5-карбоксамида;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)бензофуран-6-карбоксамида;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)бензофуран-7-карбоксамида;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)бензофуран-2-сульфонамид;
N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)бензо[b]тиофен-2-сульфонамид;
(S)-1-(2-((S)-3-(хинолин-4-илокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-(((S))-3-(нафталин-1-илокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-(((S))-3-(хинолин-6-илокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
((S))-1-(2-((S)-3-(хинолин-8-илокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
((S))-1-(2-(((S))-(S)-(изохинолин-5-илокси)пирролидин-1-ил)ацетил)пирролидин-2карбонитрил;
(S)-1-(2-((S)-3-(хинолин-5-илокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(бензо[d][1,3]диоксол-5-илокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(тиено[2,3-d]пиримидин-4-илокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(изохинолин-3-илокси)пирролвдин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(3-бромтиено[3,2-с]пирролидин-4-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(4-хлорнафталин-1-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(2-(1Н-пиразол-3-ил)фенокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(4-хлорхиназолин-8-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(4-хлорхиназолин-6-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(2-оксо-1,2-дигидрохинолин-5-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(2-оксо-1,2,3,4-тетрагидрохинолин-5-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(2-оксо-1,2,3,4-тетрагидрохинолин-6-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(2-метилхинолин-8-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-((7-хлорхинолин-4-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(7-бромхинолин-4-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(5-хлорхинолин-8-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-([1,1'-бифенил]-3-илокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-([1,1'-бифенил]-4-илокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(6-метоксихинолин-4-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(7,8-дифторхинолин-4-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
метил-6-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)окси)-2,3-дигидробензофуран-2-карбоксилат;
(S)-1-(2-((S)-3-(4-феноксифенокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(3-феноксифенокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(4-бензилфенокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(2-бензилфенокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(3-бензоилфенокси)пирролвдин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(4-бензоилфенокси)пирролвдин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(4-(бензолокси)пиридин-2-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(7-(трифторметил)хинолин-4-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(8-(трифторметил)хинолин-4-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(акридин-4-илокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(2-(бензо[d]оксазол-2-ил)фенокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(4-(4-ацетилпиперазин-1-ил)фенокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
2-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)окси)-N-фенилбензамида;
(S)-1-(2-((S)-3-(7-метоксихинолин-4-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(6,7-диметоксихинолин-4-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(3-(4-бромфенил)изоксазол-5-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-4,4-дифтор-1-(2-((S)-3-(6-метоксихинолин-4-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-4,4-дифтор-1-(2-((S)-3-(8-(трифторметил)хинолин-4-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-4,4-дифтор-1-(2-((S)-3-(хинолин-5-илокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-4,4-дифтор-1-(2-((S)-3-(изохинолин-5-илокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(7-хлорхинолин-4-ил)окси)пирролидин-1-ил)ацетил)-4,4-дифторпирролидин-2-карбонитрил;
(S)-4,4-дифтор-1-(2-((S)-3-(2-оксо-1,2-дигидрохинолин-5-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-((S)-3-(5-хлорхинолин-8-ил)окси)пирролидин-1-ил)ацетил)-4,4-дифторпирролидин-2-карбонитрил;
(S)-1-(2-(4-(хинолин-5-иламино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-(4-(хинолин-4-иламино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(1S,3S,5S)-2-(2-(4-(хинолин-4-иламино)пиперидин-1-ил)ацетил)-2-азабицикло[3.1.0]гексан-3-карбонитрил;
(2S,4S)-4-фтор-1-(2-(4-(хинолин-5-иламино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-4,4-дифтор-1-(2-(4-(хинолин-5-иламино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(1S,3S,5S)-2-(2-(4-(хинолин-5-иламино)пиперидин-1-ил)ацетил)-2-азабицикло[3.1.0]гексан-3-карбонитрил;
(S)-1-(2-(4-(фуро[3,2-с]пиридин-7-иламино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-(4-(хинолин-3-илокси)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-(4-(хинолин-4-илокси)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-(4-(хинолин-5-илокси)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-(4-(хинолин-6-илокси)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-(4-(3-метилхинолин-5-ил)амино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-(4-(б-метилхинолин-5-ил)амино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-(4-(7-фторхинолин-5-ил)амино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-(4-(7-метоксихинолин-5-ил)амино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(S)-1-(2-(4-(8-метоксихинолин-5-ил)амино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(2S,4S)-4-фтор-1-(2-(4-((б-фторхинолин-4-ил)окси)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(2S,4S)-1-(2-(4-((6-хлорхинолин-4-ил)окси)пиперидин-1-ил)ацетил)-4-фторпирролидин-2-карбонитрил;
(2S,4S)-4-фтор-1-(2-(4-((б-метоксихинолин-4-ил)окси)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(2S,4S)-4-фтор-1-(2-(4-((7-метоксихинолин-4-ил)окси)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(2S,4S)-1-(2-(4-((6,7-диметоксихинолин-4-ил)окси)пиперидин-1-ил)ацетил)-4-фторпирролидин-2-карбонитрил;
(2S,4S)-4-фтор-1-(2-(4-((3-метилхинолин-5-ил)амино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(2S,4S)-4-фтор-1-(2-(4-((7-фторхинолин-5-ил)амино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(2S,4S)-4-фтор-1-(2-(4-((7-метоксихинолин-5-ил)амино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил;
(2S,4S)-4-фтор-1-(2-(4-((6-метилхинолин-5-ил)амино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил;и
(2S,4S)-4-фтор-1-(2-(4-((8-метоксихинолин-5-ил)амино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил.
[0161] В другом аспекте соединение формул X, Ха, Xb, 1, 1, 1a, 1b, 1c, 1d или 1е или его стереоизомер или смесь стереоизомеров или его фармацевтически приемлемая соль выбраны из соединений или стереоизомеров или смеси стереоизомеров, или их фармацевтически приемлемой соли, перечисленных в таблице 1.
[0162] Соединение формул X, Ха, Xb, 1, 1а, 1b, 1c, 1d или 1е или его фармацевтически приемлемая соль могут иметь заместитель, содержащий асимметричный атом углерода (например, заместитель R2). В этом случае соединение формулы 1 или его соль могут существовать в виде оптического изомера, такого как (R) или (S), или рацемат (RS). Таким образом, если не указано иное, соединение формулы 1 или его соль содержит оптический изомер, такой как (R) или (S), и рацемат (RS). Кроме того, в некоторых вариантах осуществления соединение Формулы 1 или его соль могут существовать в виде геометрического изомера цис- или транс-структуры с двойной связью в зависимости от заместителя. Таким образом, в некоторых вариантах осуществления, если не указано иное, соединение формулы 1 или его соль содержит как геометрические изомеры цис- и транс-структур. Кроме того, соединение формулы 1 или его соль могут существовать в виде диастереомера и, если не указано иное, содержит как диастереомеры, так и их смеси.
[0163] Соединения, представленные в описании, представляют собой ингибиторы FAP. Ингибирование FAP может быть измерено, например, путем определения концентрации полумаксимального ингибирования (IC50). Один способ определения IC50 для FAP в экспериментальной секции.
[0164] В некоторых вариантах осуществления соединения представляют собой селективные ингибиторы FAP. Селективность может быть определена, например, путем сравнения ингибирования FAP с ингибированием других семейств DPP, таких как DPP7 (дипептидилпептидаза 7), DPP8 (дипептидилпептидаза 8), DPP9 (дипептидилпептидаза 9) или PREP (пролилиолигопепаза). В одном варианте осуществления «селективная ингибирующая активность» означает, что IC50 для FAP, полученная в результате анализа фермента in vitro (анализ фермента in vitro), по меньшей мере в 100 раз ниже, чем IC50 для DPP7, по меньшей мере в 100 раз ниже, чем ICjo для DPP8, по меньшей мере в 100 раз ниже, чем IC50 DPP9, или по меньшей мере в 100 раз ниже, чем IC50 PREP. В альтернативном варианте осуществления «селективная ингибирующая активность» означает, что IC50 для FAP, полученная в результате анализа фермента in vitro (анализ фермента in vitro), по меньшей мере в 100 раз ниже, чем IC50 для DPP7, по меньшей мере в 100 раз ниже, чем IC50 для DPP8, по меньшей мере в 100 раз ниже, чем IC50 DPP9, и по меньшей мере в 100 раз ниже, чем IC50 PREP.
[0165] Соединение формулы 1 настоящей технологии может быть в форме фармацевтически приемлемой соли. Используемый здесь термин «фармацевтически приемлемая соль» представляет собой соли или цвиттер-ионные формы соединений по настоящей технологии, которые являются растворимыми или диспергируемыми в воде или масле; которые подходят для лечения заболеваний без нежелательной токсичности, раздражения и аллергического ответа; которые соизмеримы с разумным соотношением польза/риск, и которые эффективны для их предполагаемого применения. Соли могут быть получены во время окончательного выделения и очистки соединений или отдельно, например, посредством взаимодействия соответствующего соединения в форме свободного основания с подходящей кислотой. Такие соли включают обычные кислотно-аддитивные соли, например, соль, полученную из неорганической кислоты, такой как соляная кислота, бромная кислота, серная кислота, сульфаминовая кислота, фосфорная кислота или азотная кислота, и соль, полученную из органической кислоты, такой как уксусная кислота, пропионовая кислота, янтарная кислота, гликолевая кислота, стеариновая кислота, лимонная кислота, малеиновая кислота, малоновая кислота, метансульфоновая кислота, винная кислота, яблочная кислота, фенилуксусная кислота, глутаминовая кислота, бензойная кислота, салициловая кислота, 2-ацетоксибензойная кислота, фумаровая кислота, п-толуолсульфокислота, щавелевая кислота или трифторуксусная кислота. Кроме того, указанные соли включают в себя стандартные типы соли металлов, например соль, полученную из металла, такого как литий, натрий, калий, магний или кальций. Указанная кислотно-аддитивная соль или соль металла могут быть получены в соответствии с обычными способами.
[0166] Соединение формулы 1 или его соль в соответствии с данной технологией можно получить различными способами. Например, соединение формулы 1а, в котором R3 формулы 1 представляет собой -NR4R5 или его соль можно получить способом, включающим этап реагирования соединения формулы 2а с R4X с получением соединения формулы 3а; этап проведения реакции снятия защиты соединения формулы 3а выше для получения соединения формулы 4а или его соли; и этап взаимодействия соединения формулы 4а или его соли с соединением формулы 5 с образованием соединения формулы 1а.

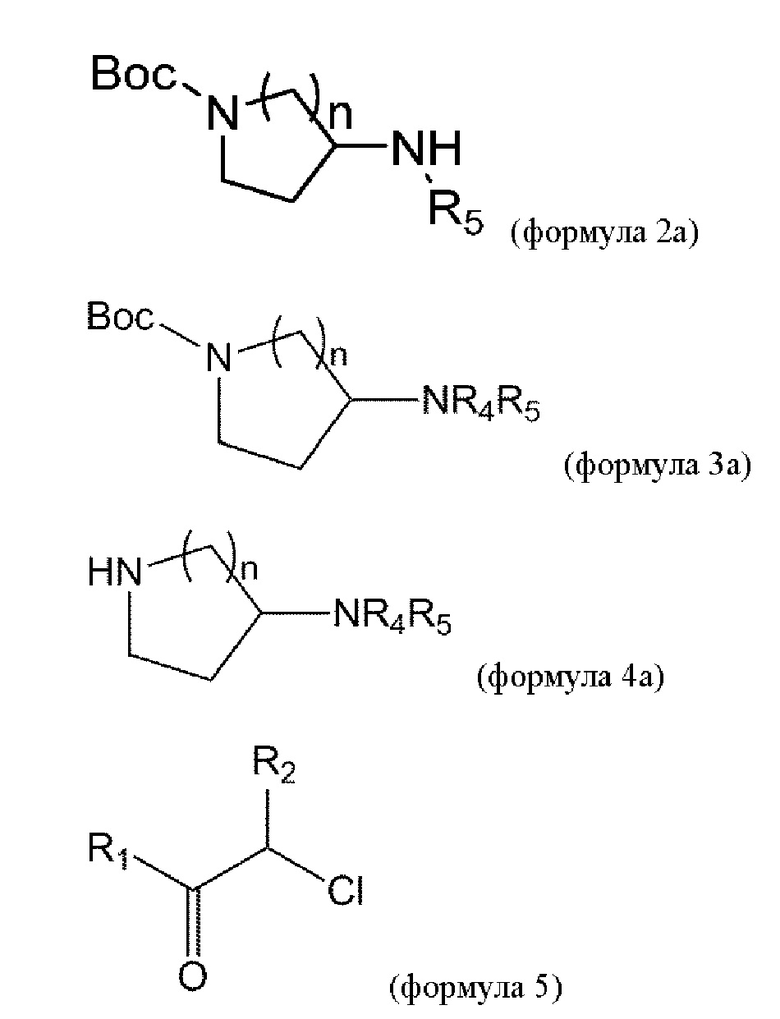
В указанных формулах 1а, 2а, 3а, 4а и 5 X представляет собой галоген (например, Br, F, Cl, Br, или I), Вое представляет собой защитную группу для амина (например, трет-бутоксикарбонил, 9-фторилметилоксикарбонил (FMOC), бензилоксикарбонил (CBZ), трифенилметил (тритил) и т.д.), a R1, Р2, Р4, P5 и n являются такими же, как определено выше.
[0167] Соединение формулы 2а является коммерчески доступным. Реакция соединения указанной выше формулы 2а с R4X можно проводить с использованием палладиевого катализатора по реакции Бухвальда-Хартвига. Палладиевый катализатор включает диацетат палладия (Pd(OAc)2), трис(дибензилиденацетон)дипалладий (Pd2(dba)3), тетракис(трифенилфосфин)палладий (Pd(PPh3)4) или палладийди[1,1'-бис(дифенилфосфино)ферроцен]дихлорид (PdCl2(dppf)2) и т.д. Кроме того, в дополнение к палладиевому катализатору могут быть добавлены лиганд и основание. Указанный лиганд включает (S)-2,2-бис(дифенилфосфино)-1,1-бинафтил (BINAP), 1,1'-бис(дифенилфосфино)ферроцен(dppf) или (три-О-толил)фосфин(Р(O-Tol)3) и т.д., и указанное основание включает в себя неорганическое основание, такое как карбонат цезия (Cs2CO3), карбонат натрия (Na2CO3), карбонат калия (K2CO3), фторид калия (KF), фторид цезия (CsF), гидроксид натрия (NaOH), фосфонат калия (K3PO4), трет-бутоксид натрия (трет-BuONa), трет-бутоксид калия (трет-BuOK) или т.п. Реакцию можно проводить в неполярном органическом растворителе, таком как бензол или толуол, или полярный органический растворитель, такой как диоксан, тетрагидрофуран, ацетонитрил, 1,2-диметоксиэтан, N,N-диметилформамид или т.п., при температуре в диапазоне от 50°С до 150°С, предпочтительно от 80°С до 110°С. Другие условия реакции, включая, например, время реакции, могут быть определены в соответствии с известными способами реакции Бухвальда-Хартвига (Barbara Czako et al, STRATEGIC APPLICATIONS of NAMED REACTIONS in ORGANIC SYNTHESIS, 2005).
[0168] В некоторых вариантах осуществления реакцию соединения формулы 2а с R4X проводят посредством нуклеофильного замещения. Реакция нуклеофильного замещения может проводиться при комнатной температуре или в условиях кипения (от 20°С до 120°С) с использованием основания, такого как карбонат цезия, карбонат калия и т.д., в растворителе, таком как ацетонитрил, дихлорметан или т.п.
[0169] Снятие защиты соединения формулы 3а можно осуществлять обычными способами удаления защитной группы амина. Например, указанная защитная группа амина в органическом растворителе, таком как дихлорметан и т.д., может быть удалена с использованием кислоты, такой как трифторуксусная кислота, или может быть удалена в форме гидрохлоридной соли с использованием хлорида водорода, растворенного в органических растворителях, таких как диэтиловый эфир, 1,4-диоксан и т.д.
[0170] Реакция соединения указанной выше формулы 4а или его соли с соединением формулы 5 может быть осуществлена посредством нуклеофильного замещения. Реакцию нуклеофильного замещения можно проводить при комнатной температуре или умеренно теплой температуре (от 20°С до 60°С) с использованием основания, такого как карбонат цезия, карбонат калия и т.д., в растворителе, таком как ацетонитрил, дихлорметан или т.п.
[0171] Соединение формулы 5 выше может быть получено путем взаимодействия соединения формулы 6 с соединениями формул R1a-R1e, соответственно.
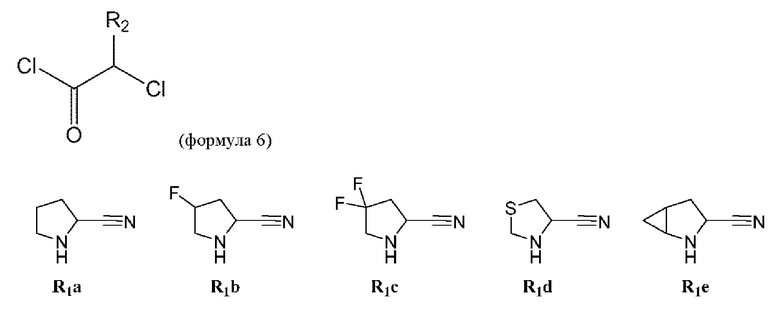
В указанной формуле 6 R2 является таким же, как определено выше.
[0172] Соединение формулы 6 и соединения формул R1a-R1e являются коммерчески доступными. Реакция соединения формулы 6 с соединениями формул R1a-R1e может быть превращена в соединение формулы 5 посредством нуклеофильного ацилзамещения. Реакцию нуклеофильного ацилзамещения можно проводить с использованием карбоната цезия, карбоната калия и т.д. в растворителе, таком как ацетонитрил, дихлорметан и т.п., и ее можно проводить при температуре от 0°С до комнатной температуры.
[0173] Кроме того, настоящая технология включает в себя процесс приготовления соединения формулы 1b, в котором R3 представляет собой -OR4 или его стереоизомер или смесь стереоизомеров или его фармацевтически приемлемую соль. Таким образом, настоящая технология включает в себя процесс приготовления соединения формулы 1b или стереоизомера или смеси стереоизомеров или его фармацевтически приемлемой соли, включающий этап реагирования соединения формулы 2b с R4-OH для получения соединения формулы 3b; этап осуществления реакции снятия защиты соединения формулы 3b выше для получения соединения формулы 4b или его соли; и этап взаимодействия соединения формулы 4b или его соли с соединением формулы 5 с получением соединения формулы 1b.
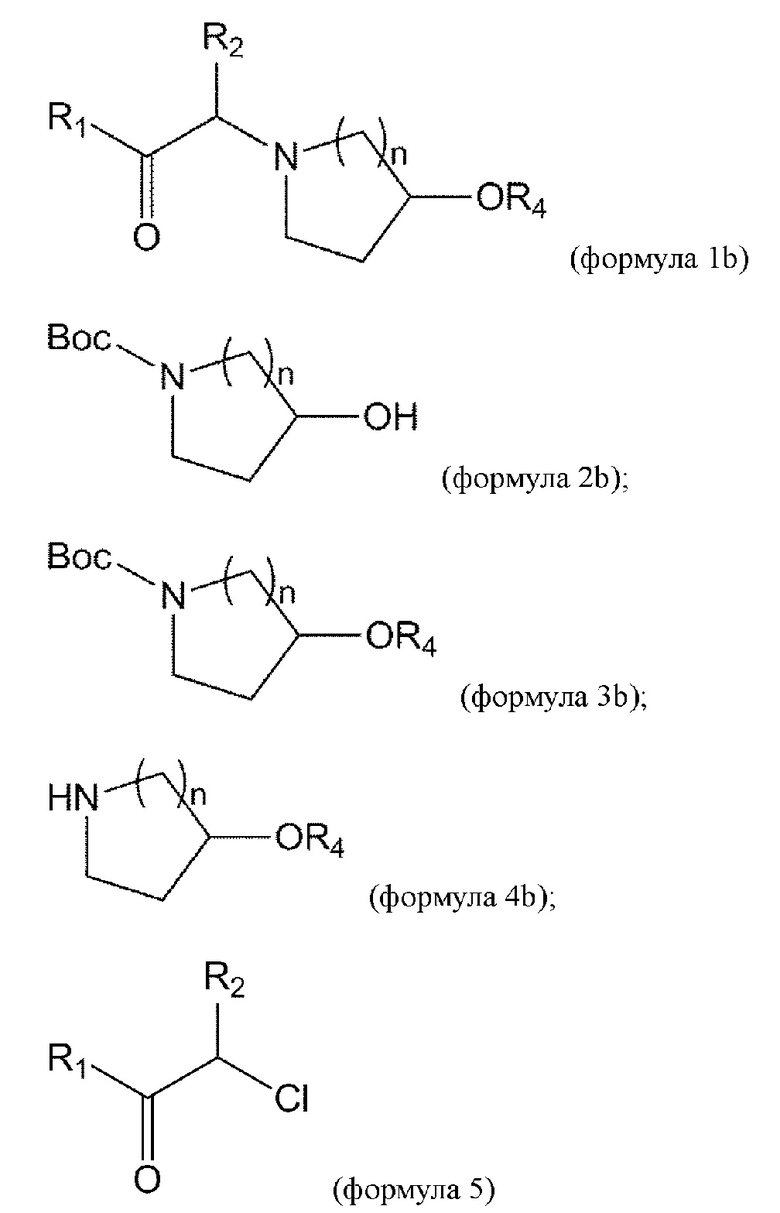
В указанных формулах 1b, 2b, 3b, 4b и 5 Boc представляет собой защитную группу амина (например, трет-бутоксикарбонил, 9-флуоренилметилоксикарбонил (FMOC), бензилоксикарбонил (CBZ), трифенилметил (тритил) и т.д.), a R1, R2, R4 и n такие же, как определено выше.
[0174] Соединение формулы 2b является коммерчески доступным. Реакция соединения указанной выше формулы 2b с R4-OH может быть проведена по реакции Мицунобу. Реакцию Мицунобу можно проводить при комнатной температуре или в условиях умеренно теплой температуры (от 20°С до 60°С) с использованием диалкилазодикарбоксилата, такого как диэтилазодикарбоксилат (DEAD), диизопропилазодикарбоксилат (DTAD), ди-2-метоксиэтилазодикарбоксилат (DMEAD), 1,1'-(азодикарбонил)дипиперидин и т.д. и триалкилфосфин или триарилфосфин, такой как трифенилфосфин (PPh3), трибутилфосфин (PBu3) и т.д. Другие условия реакции, включая, например, время реакции, можно определить в соответствии с известными методами для реакции Мицунобу (Barbara Czako and Laszlo Kurti, STRATEGIC APPLICATIONS of NAMED REACTIONS in ORGANIC SYNTHESIS, 2005).
[0175] Снятие защиты соединения формулы 3b можно осуществлять обычными способами удаления защитной группы амина. Например, указанная защитная группа амина в органическом растворителе, таком как дихлорметан и т.д., может быть удалена с использованием кислоты, такой как трифторуксусная кислота, или может быть удалена в форме гидрохлоридной соли с использованием хлорида водорода, растворенного в органических растворителях, таких как диэтиловый эфир, 1,4-диоксан и т.д.
[0176] Реакция соединения указанной выше формулы 4b или его соли с соединением формулы 5 может быть осуществлена посредством нуклеофильного замещения. Реакцию нуклеофильного замещения можно проводить при комнатной температуре или умеренно теплой температуре (от 20°С до 60°С) с использованием основания, такого как карбонат цезия, карбонат калия и т.д., в растворителе, таком как ацетонитрил, дихлорметан или т.п.
[0177] Настоящая технология включает в себя процесс приготовления соединения формулы 1b или стереоизомера или смеси стереоизомеров или его фармацевтически приемлемой соли, включающий этап реагирования соединения формулы 5 с соединением формулы 7 для получения соединения формулы 8; этап взаимодействия соединения формулы 8 с R4-OH для получения соединения формулы 1b.
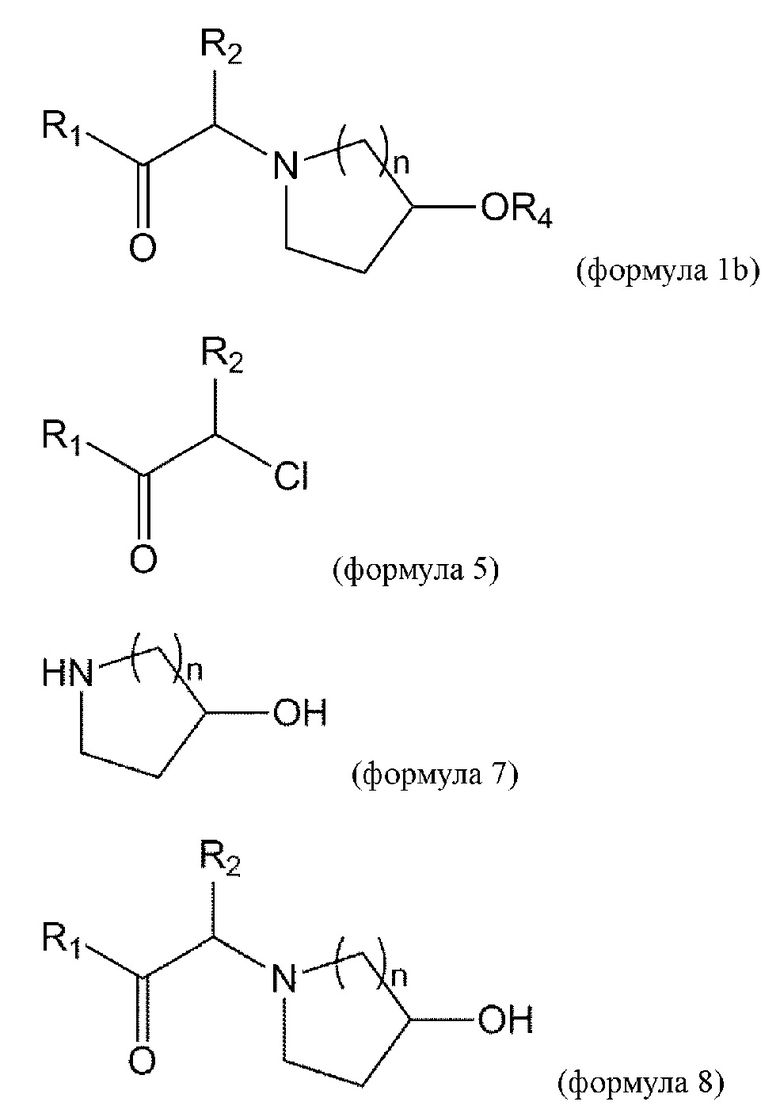
В указанных формулах 1b, 5, 7 и 8 R1, R2, R4 и n являются такими же, как определено выше.
[0178] Соединение формулы 7 является коммерчески доступным. Реакция соединения указанной выше формулы 5 или его соли с соединением формулы 7 может быть осуществлена посредством нуклеофильного замещения. Реакцию нуклеофильного замещения можно проводить при комнатной температуре или умеренно теплой температуре (от 20°С до 60°С) с использованием основания, такого как карбонат цезия, карбонат калия и т.д., в растворителе, таком как ацетонитрил, дихлорметан или т.п.
[0179] Реакция соединения указанной выше формулы 8 с R4-OH может быть проведена по реакции Мицунобу.
[0180] Кроме того, настоящая технология включает в себя процесс приготовления соединения формулы 1с, в котором R3 формулы 1 представляет собой -C(ONHR4 или его стереоизомер или смесь стереоизомеров или его фармацевтически приемлемую соль. Таким образом, настоящая технология включает в себя процесс приготовления соединения формулы 1с или стереоизомера или смеси стереоизомеров или его фармацевтически приемлемой соли, включающий этап реагирования соединения формулы 2с с R4-NH2 для получения соединения формулы 3c; этап осуществления реакции снятия защиты соединения формулы 3с выше для получения соединения формулы 4с или его соли; и этап взаимодействия соединения формулы 4с или его соли с соединением формулы 5 с получением соединения формулы 1с.
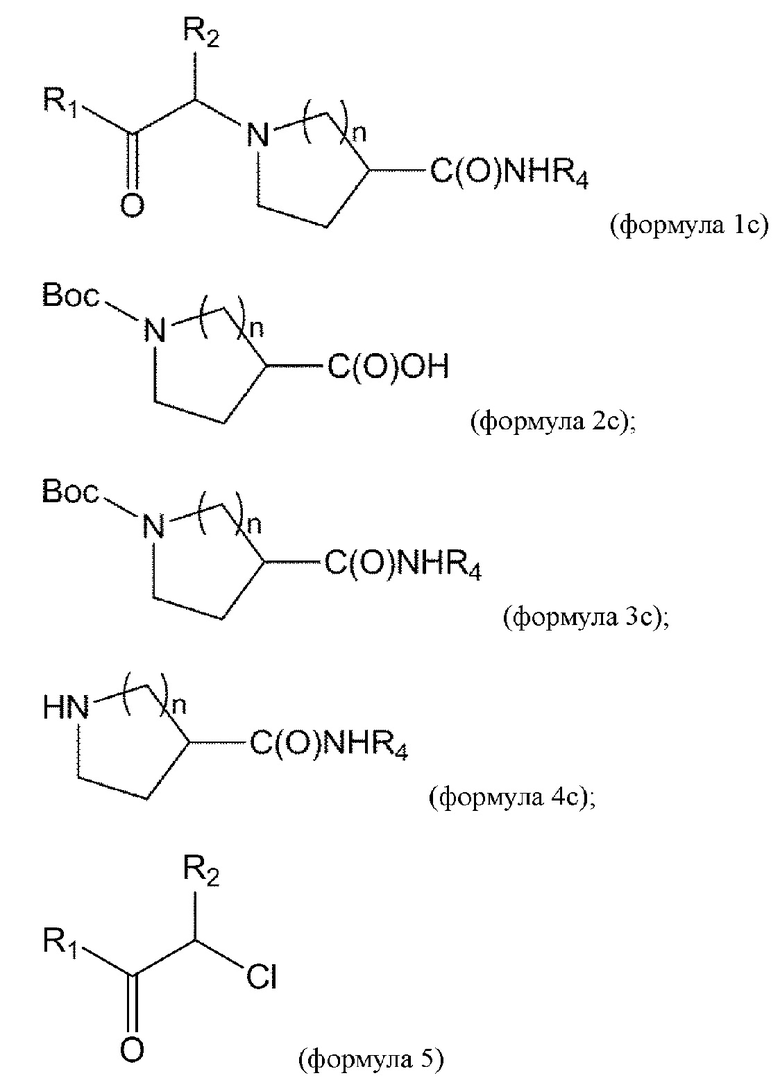
В указанных формулах 1с, 2с, 3с, 4с и 5 Boc представляет собой защитную группу амина (например, трет-бутоксикарбонил, 9-флуоренилметилоксикарбонил (FMOC), бензилоксикарбонил (CBZ), трифенилметил (тритил) и т.д.), a R1, R2, R4 и 11 такие же, как определено выше.
[0181] Соединение формулы 2с является коммерчески доступным. Реакцию соединения указанной выше формулы 2с с R4-NH2 можно осуществлять посредством реакции сочетания амида. Указанная реакция сочетания амида может быть проведена с использованием основания, такого как диизопропиламин, диизопропилэтиламин, триэтиламин и т.д., и реагента сочетания, такого как O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилуриний гексафторфосфат (HATU), О-(бензотриазол-1-ил)-N,N,N',N'-тетраметилуроний гексафторфосфат (HBTU) и т.д. Упомянутую реакцию сочетания можно проводить в органических растворителях, таких как дихлорметан, N,N-диметилформамид и т.д., и ее можно проводить при комнатной температуре или в условиях умеренно теплой температуры (от 20°С до 60°С).
[0182] Снятие защиты соединения формулы 3с можно осуществлять обычными способами удаления защитной группы амина. Например, указанная защитная группа амина в органическом растворителе, таком как дихлорметан и т.д., может быть удалена с использованием кислоты, такой как трифторуксусная кислота, или может быть удалена в форме гидрохлоридной соли с использованием хлорида водорода, растворенного в органических растворителях, таких как диэтиловый эфир, 1,4-диоксан и т.д.
[0183] Реакция соединения указанной выше формулы 4с или его соли с соединением формулы 5 можно осуществлять посредством нуклеофильного замещения. Реакцию нуклеофильного замещения можно проводить при комнатной температуре или умеренно теплой температуре (от 20°С до 60°С) с использованием основания, такого как карбонат цезия, карбонат калия и т.д., в растворителе, таком как ацетонитрил, дихлорметан или т.п.
[0184] Кроме того, настоящая технология включает в себя процесс приготовления соединения формулы 1d, в котором формулы 1 представляет собой -NHC(O)(CH2)mR4 или его стереоизомер или смесь стереоизомеров или его фармацевтически приемлемую соль. Таким образом, настоящая технология включает в себя процесс приготовления соединения формулы 1d или стереоизомер или смеси стереоизомеров или его фармацевтически приемлемой соли, включающий этап реагирования соединения формулы 5 с соединением формулы 9 для получения соединения формулы 10; этап осуществления реакции снятия защиты соединения указанной выше формулы 10 для получения соединения формулы 11 или его соли; и этап взаимодействия соединения формулы 11 с R4-(CH2)mCOOH для получения соединения формулы 1d.
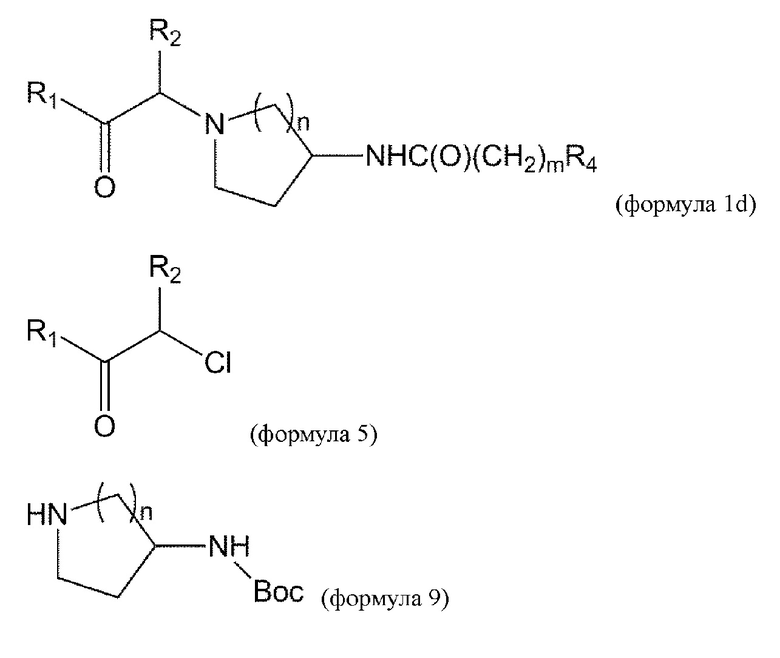
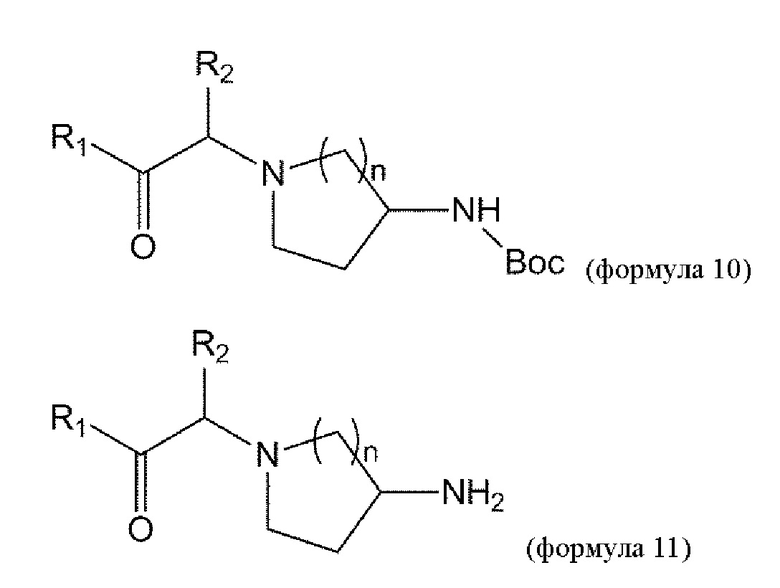
В указанных формулах 1d, 5, 9, 10 и 11 Boc представляет собой защитную группу амина (например, трет-бутоксикарбонил, 9-флуоренилметилоксикарбонил (FMOC), бензилоксикарбонил (CBZ), трифенилметил (тритил) и т.д.), a R1, R2, R4, пит такие же, как определено выше.
[0185] Соединение формулы 9 является коммерчески доступным. Реакцию соединения указанной выше формулы 5 с соединением формулы 9 можно осуществлять посредством нуклеофильного замещения. Реакцию нуклеофильного замещения можно проводить при комнатной температуре или умеренно теплой температуре (от 20°С до 60°С) с использованием основания, такого как карбонат цезия, карбонат калия и т.д., в растворителе, таком как ацетонитрил, дихлорметан или т.п.
[0186] Снятие защиты соединения формулы 10 можно осуществлять обычными способами удаления защитной группы амина. Например, указанная защитная группа амина в органическом растворителе, таком как дихлорметан и т.д., может быть удалена с использованием кислоты, такой как трифторуксусная кислота, или может быть удалена в форме гидрохлоридной соли с использованием хлорида водорода, растворенного в органических растворителях, таких как диэтиловый эфир, 1,4-диоксан и т.д.
[0187] Реакция соединения указанной выше формулы 11 с R4-(CH2)mCOOH может быть осуществлена посредством реакции сочетания амида. Указанная реакция сочетания амида может быть проведена с использованием основания, такого как диизопропиламин, диизопропилэтиламин, триэтиламин и т.д., и реагента сочетания, такого как O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилуриний гексафторфосфат (HATU), O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилуроний гексафторфосфат (HBTU) и т.д. Упомянутую реакцию сочетания можно проводить в органических растворителях, таких как дихлорметан, N,N-диметилформамид и т.д., и ее можно проводить при комнатной температуре или в условиях умеренно теплой температуры (от 20°С до 60°С).
[0188] Кроме того, настоящая технология включает в себя процесс приготовления соединения формулы 1е, в котором R3 формулы 1 представляет собой -NHS(O)2R4 или его стереоизомер или смесь стереоизомеров или его фармацевтически приемлемую соль. Таким образом, настоящая технология включает в себя процесс приготовления соединения формулы 1е или стереоизомера или смеси стереоизомеров или его фармацевтически приемлемой соли, включающий этап реагирования соединения формулы 11 представленный в настоящем документе с R4-S(O)2Cl для получения соединения формулы 1е.
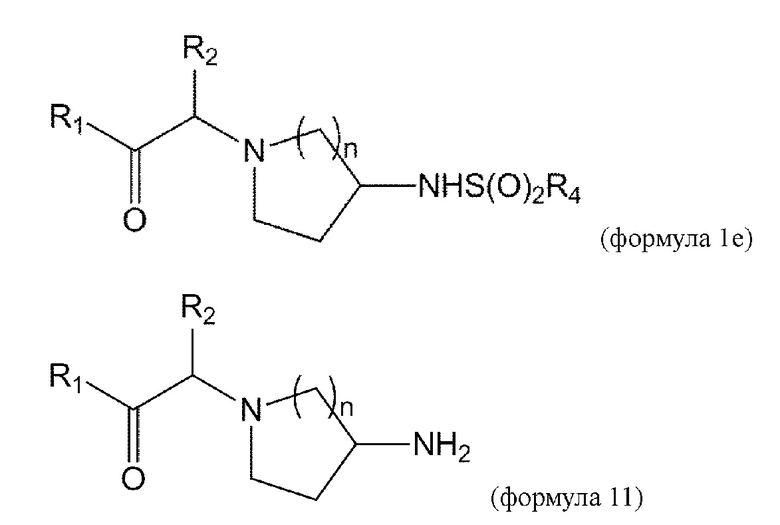
В указанных формулах 1е и 11 R1, R2, R4 и n являются такими же, как определено выше.
[0189] Реакция соединения указанной выше формулы 11 или его соли с R4-S(O)2Cl можно проводить посредством нуклеофильного замещения. Реакцию нуклеофильного замещения можно проводить при комнатной температуре или умеренно теплой температуре (от 20°С до 60°С) с использованием основания, такого как карбонат цезия, карбонат калия и т.д., в растворителе, таком как ацетонитрил, дихлорметан или т.п.
[0190] Как правило, FAP не экспрессируется в нормальных тканях, но его экспрессия увеличивается в стромальных фибробластах злокачественных опухолей, таких как рак молочной железы, колоректальный рак, рак яичников и т.п. (Garin-Chesa et al., Proc. Natl. Acad. Sci., 1990, 87: 7235). Соответственно, ингибирование FAP может быть целью лечения злокачественной опухоли. Фактически сообщалось, что ValboroPro (РТ-100, Talobostat), известный как ингибитор FAP, при пероральном введении проявляет противораковую активность у мышей, задерживая пролиферацию и вызывая дегенерацию опухолей (Adams et al., Cancer Res., 2004, 64: 5471). Однако Val-boroPro (РТ-100, талабостат), известный как ингибитор FAP, также обладает ингибирующей активностью в отношении DPP4, PREP и т.д. Таким образом, необходимо улучшить низкую селективность в отношении FAP. (О. Ryabtsova et al. Bioorg. Med. Chem. Lett., 2012, 3412-3417).
[0191] Кроме того, поскольку FAP регулирует метаболические функции и экспрессируется в активированных звездчатых клетках печени (aHSC) и участках ремоделирования тканей, связанных с фиброзом печени, ингибирование FAP может быть полезным для лечения неалкогольной жировой болезни печени (НАЖБП). Неалкогольная жировая болезнь печени (НАЖБП) гистологически включает простой стеатоз, неалкогольный стеатогепатит (НАСГ) и цирроз печени. Среди них, в отличие от простого стеатоза (неалкогольная жировая дистрофия печени, НАЖБП), НАСГ потенциально может прогрессировать до цирроза печени и гепатоцеллюлярной карциномы. Известно, что помимо резистентности к инсулину важную роль в прогрессировании НАСГ играют окислительный стресс, воспалительный каскад и фиброз. Таким образом, ингибирование FAP может улучшить резистентность к инсулину, которая является одним из ключевых факторов НАСГ, и может регулировать гепатопротекторный эффект и функцию активированных звездчатых клеток печени (aHSC) посредством регуляции FGF21 и, таким образом, может иметь потенциал для лечения НАСГ (Lay AJ et al., Front. Biosci. (Landmark Ed), 2019, 24, 1-17).
[0192] Пирролидин и пиперидин в соответствии с настоящей технологией, т.е. соединение формул X, Ха, Xb, 1, 1a, 1b, 1c, 1d или 1e, или его стереоизомер или смесь стереоизомеров, или его фармацевтически приемлемая соль, обладают ингибирующей активностью в отношении FAP и, таким образом, могут быть с пользой применены для профилактики или лечения заболевания, опосредованного белком активации фибробластов (FAP). Предпочтительно, соединение формулы 1 в соответствии с настоящей технологией или его стереоизомер или смесь стереоизомеров или его фармацевтически приемлемую соль можно эффективно применять для профилактики или лечения ожирения, диабета, стеатоза и неалкогольного стеатогепатита (НАСТ).
[0193] В некоторых вариантах осуществления настоящего изобретения предложено применение пирролидин и пиперидиновых соединений в соответствии с настоящей технологией, т.е. соединение формул X, Ха, Xb, 1, 1а, 1b, 1c, 1d или 1e, или стереоизомер или смесь их стереоизомеров, или его фармацевтически приемлемая соль, при получении лекарственного средства для профилактики и/или лечения липидных и липопротеиновых нарушений (таких как, без ограничений, гиперхолестеролемия, гипертриглицеридемия и атеросклероз), состояний и заболеваний, которые возникают из-за накопления липидов и, в частности, триглицеридов, и последующей активации профиброзных путей (таких как, но не ограничиваясь ими, гиперхоле стеринемия, гипертриглицеридемия и атеросклероз), состояний и заболеваний, возникающих в результате хронической жировой и фиброзной дегенерации органов из-за накопления липидов и, в частности, триглицеридов и последующей активации профибротических путей (таких как, но не ограничиваясь ими, НАСГ и хронические холестатические состояния в печени, гломерулосклероз и диабетическая нефропатия в почках, дегенерация желтого пятна и диабетическая ретинопатия в глазах и нейродегенеративные заболевания, такие как болезнь Альцгеймера в головном мозге или диабетическая невропатии периферической нервной системы), диабета типа I или типа II и клинических осложнений диабета типа I и типа II (таких, как, но не ограничиваясь ими, диабетическая нефропатия, диабетическая ретинопатия, диабетическая нейропатия или окклюзионное заболевание периферических артерий (PAOD)), хронических внутрипеченочных или некоторых форм внепеченочных холестатических состояний, фиброза печени, острых внутрипеченочных холестатических состояний, обструктивных или хронических воспалительных заболеваний, возникающих из-за неправильного состава желчи (таких как, но не ограничиваясь, желчнокаменная болезнь, также известная как холестериновые камни в желчном пузыре), желудочно-кишечных заболеваний при сниженном потреблении пищевых жиров и жирорастворимых пищевых витаминов, воспалительных заболеваниях кишечника, ожирении и метаболическом синдроме (сочетании дислипидемии, диабета и аномально высокого индекса массы тела), персистирующих инфекций внутриклеточными бактериями или паразитарными простейшими, незлокачественных гиперпролиферативных заболеваний, злокачественных гиперпролиферативггьгх заболеваний (такие как, но не ограничиваясь ими, различные формы рака, особенно определенные формы рака молочной железы, печени или толстой кишки, или заболевания, выбранные из группы, состоящей из гепатоцеллюлярной карциномы, аденомы толстой кишки и полипоза), аденокарциномы толстой кишки и гепатоцеллюлярной карциномы, в частности, стеатоза печени и ассоциированных синдромов, инфекции гепатита В, инфекции гепатита С и/или холестатических и фиброзных эффектов, связанных с алкогольным циррозом или вирусными формами гепатита, печеночной недостаточностью или нарушением функции печени в результате хронических заболеваний печени или хирургической резекции печени, острого инфаркта миокарда, острого инсульта, тромбоза, являющегося конечной точкой хронического обструктивного атеросклероза, остеоартрита, ревматоидного артрита, псориаза или ишемического инсульта, по отдельности или в любой их комбинации.
[0194] В некоторых вариантах осуществления изобретения соединения и/или фармацевтические композиции, описанные в настоящем документе, используются для профилактики и/или лечения хронических внутрипеченочных состояний, таких как первичный цирроз печени (РВС), первичный склерозирующий холангит (PSC), прогрессирующий наследственный внутрипеченочный холестаз (PFIC), алкогольный цирроз и связанный с ним холестаз, а также некоторые формы внепеченочных холестатических состояний или фиброз печени.
[0195] В некоторых вариантах осуществления настоящего изобретения предложен способ лечения хронических внутрипече ночных состояний и/или некоторых форм внепеченочных холестатических состояний у пациента, нуждающегося в этом, причем способ включает в себя, по существу состоит, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе. В некоторых вариантах осуществления хронические внутрипеченочные условия выбраны из РВС, PSC, PFIC и алкогольного цирроза и связанного с нимхолестаза.
[0196] В некоторых вариантах осуществления настоящего изобретения предложен способ лечения фиброза печени у пациента, нуждающегося в этом, причем способ включает в себя, по существу состоит, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе.
[0197] В некоторых вариантах осуществления настоящего изобретения предложен способ лечения расстройства липидного или липопротеинового обмена у пациента, нуждающегося в этом, причем способ включает в себя, по существу состоит, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе. В некоторых вариантах осуществления расстройство липидного или липопротеинового обмена выбрано из гиперхолестеролемии, гипертриглицеридемии и атеросклероза.
[0198] В некоторых вариантах осуществления в настоящем документе предложен способ лечения состояния или заболевания, возникающего в результате хронической жировой и фиброзной дегенерации органов из-за накопления липидов и, в частности, накопления триглицеридов и последующей активации профибротических путей у пациента, нуждающегося в этом, причем способ включает в себя, по существу состоит, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе. В некоторых вариантах осуществления состояние или заболевание, возникающее в результате хронической жировой и фиброзной дегенерации органов вследствие накопления липидов и, в частности, накопления триглицеридов и последующей активации профибротических путей, выбирают из НАСГ и хронических холестатических состояний печени, гломерулосклероза и диабетической нефропатии почек, дегенерации желтого пятна и диабетической ретинопатии глаз, а также нейродегенеративных заболеваний. В некоторых дополнительных вариантах осуществления нейродегенеративные заболевания выбраны из болезни Альцгеймера в головном мозге и диабетических нейропатиях в периферической нервной системе.
[0199] В некоторых вариантах осуществления настоящего изобретения предложен способ лечения диабета I или II типа и клинических осложнений диабета I и II типа у пациента, нуждающегося в этом, при этом способ включает в себя, по существу состоит, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе. В некоторых вариантах осуществления настоящего изобретения предложен способ лечения диабета I типа у пациента, нуждающегося в этом, причем способ включает в себя, по существу состоит, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе. В некоторых вариантах осуществления настоящего изобретения предложен способ лечения диабета I типа у пациента, нуждающегося в этом, причем способ включает в себя, по существу состоит, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе. В некоторых вариантах осуществления настоящего изобретения предложен способ лечения одного или более клинических осложнений диабета I или II типа у пациента, нуждающегося в этом, при этом способ включает в себя, по существу состоит из, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе. В некоторых вариантах осуществления клинические осложнения диабета I и II типа выбраны из диабетической нефропатии, диабетической ретинопатии, диабетической нейропатии и периферической артериальной болезни (PAOD) или любой их комбинации.
[0200] В некоторых вариантах осуществления настоящего изобретения предложен способ лечения острых внутрипеченочных холестатических состояний у пациента, нуждающегося в этом, причем способ включает в себя, по существу состоит, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе.
[0201] В некоторых вариантах осуществления в настоящем документе предложен способ лечения обструктивных или хронических воспалительных заболеваний, возникающих из-за неправильного состава желчи у пациента, нуждающегося в этом, причем способ включает в себя, по существу состоит, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе. В некоторых вариантах осуществления обструктивные или хронические воспалительные заболевания, возникающие из-за неправильного состава желчи, представляют собой желчнокаменную болезнь, также известную как холестериновые камни в желчном пузыре.
[0202] В некоторых вариантах осуществления настоящего изобретения предложен способ лечения желудочно-кишечных заболеваний, связанных с пониженным потреблением пищевого жира и жирорастворимых пищевых витаминов у пациента, нуждающегося в этом, причем способ включает в себя, по существу состоит, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе.
[0203] В некоторых вариантах осуществления настоящего изобретения предложен способ лечения воспалительных заболеваний кишечника у пациента, нуждающегося в этом, при этом способ включает в себя, по существу состоит из, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе.
[0204] В некоторых вариантах осуществления настоящего изобретения предложен способ лечения ожирения и метаболического синдрома у пациента, нуждающегося в этом, при этом способ включает в себя, по существу состоит из, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе.
[0205] В некоторых вариантах осуществления в настоящем документе предложен способ лечения персистирующих инфекций, вызываемых внутриклеточными бактериями или паразитарными простейшими, у пациента, нуждающегося в этом, причем способ включает в себя, по существу состоит, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе.
[0206] В некоторых вариантах осуществления настоящего изобретения предложен способ лечения незлокачественных гиперпролиферативных расстройств у пациента, нуждающегося в этом, при этом способ включает в себя, по существу состоит из, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе.
[0207] В некоторых вариантах осуществления настоящего изобретения предложен способ лечения злокачественных гиперпролиферативных расстройств у пациента, нуждающегося в этом, при этом способ включает в себя, по существу состоит из, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе. В некоторых вариантах осуществления злокачественные гиперпролиферативные расстройства выбраны из различных форм рака, в частности, определенных форм рака молочной железы, печени или толстой кишки, или расстройства, выбранного из группы, состоящей из гепатоцеллюлярной карциномы, аденомы толстой кишки и полипоза.
[0208] В некоторых вариантах осуществления настоящего изобретения предложен способ лечения аденокарциномы толстой кишки у пациента, нуждающегося в этом, причем способ включает в себя, по существу состоит, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе.
[0209] В некоторых вариантах осуществления настоящего изобретения предложен способ лечения гепатоцеллюлярной карциномы у пациента, нуждающегося в этом, причем способ включает в себя, по существу состоит, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе.
[0210] В некоторых вариантах осуществления настоящего изобретения предложен способ лечения стеатоза печени и связанных с ним синдромов у пациента, нуждающегося в этом, при этом способ включает в себя, по существу состоит из, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе.
[0211] В некоторых вариантах осуществления настоящего изобретения предложен способ лечения инфекции гепатита В у пациента, нуждающегося в этом, при этом способ включает в себя, по существу состоит из, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе.
[0212] В некоторых вариантах осуществления настоящего изобретения предложен способ лечения инфекции гепатита С у пациента, нуждающегося в этом, при этом способ включает в себя, по существу состоит из, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе.
[0213] В некоторых вариантах осуществления в настоящем документе предложен способ лечения холестатических и фиброзных эффектов, связанных с вызванным алкоголем циррозом печени или вирусными формами гепатита у пациента, нуждающегося в этом, причем способ включает в себя, по существу состоит, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе.
[0214] В некоторых вариантах осуществления в настоящем документе предложен способ лечения печеночной недостаточности или нарушения функции печени в результате хронических заболеваний печени или хирургической резекции печени у пациента, нуждающегося в этом, причем способ включает в себя, по существу состоит, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе.
[0215] В некоторых вариантах осуществления настоящего изобретения предложен способ лечения острого инфаркта миокарда у пациента, нуждающегося в этом, причем способ включает в себя, по существу состоит, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе.
[0216] В некоторых вариантах осуществления настоящего изобретения предложен способ лечения острого инсульта у пациента, нуждающегося в этом, причем способ включает в себя, по существу состоит, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе.
[0217] В некоторых вариантах осуществления в настоящем документе предложен способ лечения тромбоза, который возникает как конечная точка хронического обструктивного атеросклероза у пациента, нуждающегося в этом, причем способ включает в себя, по существу состоит, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе.
[0218] В некоторых вариантах осуществления настоящего изобретения предложен способ лечения остеоартрита у пациента, нуждающегося в этом, при этом способ включает в себя, по существу состоит из, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе.
[0219] В некоторых вариантах осуществления настоящего изобретения предложен способ лечения ревматоидного артрита у пациента, нуждающегося в этом, причем способ включает в себя, по существу состоит, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе.
[0220] В некоторых вариантах осуществления настоящего изобретения предложен способ лечения псориаза у пациента, нуждающегося в этом, при этом способ включает в себя, по существу состоит из, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе.
[0221] В некоторых вариантах осуществления в настоящем документе предложен способ лечения ишемического инсульта у пациента, нуждающегося в этом, причем способ включает в себя, по существу состоит, или состоит из введения пациенту терапевтически эффективного количества соединения или композиции, описанной в настоящем документе.
[0222] FAP экспрессируется не только в форме, прикрепленной к клеточной мембране, но также в форме, секретируемой из клетки и циркулирующей в крови (циркулирующий FAP, далее «с-FAP»), и обе формы имеют одинаковую ферментативную активность. c-FAP можно количественно определить на уровне антигена с помощью твердофазного иммуноферментного анализа (ИФА) или можно количественно определить на уровне ферментативной активности с использованием специфичного для FAP субстрата, и этот количественный анализ FAP показал, что указанные уровни коррелируют со степенью индукции указанных заболеваний (Ultte de Willige S et al, PLoS One, June 5, 2017, 12). To есть c-FAP можно использовать в качестве индикатора для диагностики заболевания, такого как хроническое заболевание печени, злокачественная опухоль и т.д. Соответственно, в другом аспекте в настоящем документе предусмотрены способы применения соединений, описанных в настоящем документе, с обнаружением с-FAP. В некоторых вариантах осуществления в настоящем документе представлены способы диагностики заболевания, описанного в настоящем документе, у субъекта, причем способ включает контакт крови субъекта с соединением, описанным в настоящем документе, и определение концентрации c-FAP в крови.
[0223] Известно, что FGF-21 обладает эффектами против ожирения и диабета (М.J. Potthoff et al., Nature Reviews Endocrinology, 2017, 13, and 74), эффектом регуляции метаболизма липидов (Murata Y et al. J Nutr Metab. 2011; 2011: 981315), и, как известно, обладает мощным гепатопротекторным эффектом (Y. Yu et al, molecular & Cellular Biochemistry, 2015, 403, 287). Таким образом, ингибирование активности FAP может регулировать разложение FGF-21 с помощью FAP и может быть полезно для лечения метаболических синдромов, таких как ожирение, диабет и т.д.
[0224] Соответственно, в другом аспекте в данном документе предложены способы регуляции деградации FGF-21 путем ингибирования FAP с использованием соединения, описанного в данном документе.
[0225] Таким образом, настоящая технология включает фармацевтическую композицию для ингибирования FAP, содержащую терапевтически эффективное количество соединения формул X, Ха, Xb, 1, 1a, 1b, 1c, 1d или 1e, или его стереоизомера или смеси стереоизомеров, или его фармацевтически приемлемой соли в качестве активного ингредиента. В одном варианте осуществления настоящая технология обеспечивает фармацевтическую композицию для профилактики или лечения ожирения, диабета, стеатоза и не алкогольного стеатогепатита (НАСГ), содержащего терапевтически эффективное количество соединения формул X, Ха, Xb, 1, 1a, 1b, 1с, 1d или 1e, или его стереоизомера или смеси стереоизомеров, или его фармацевтически приемлемой соли в качестве активного ингредиента.
[0226] В некоторых вариантах осуществления соединения по данному изобретению могут быть объединены с одним или более дополнительными средствами для профилактики или лечения заболевания или состояния, подходящими для лечения путем ингибирования FAP.
[0227] В некоторых вариантах осуществления композиции, описанные в настоящем документе, содержат по меньшей мере один дополнительный активный агент.
[0228] Примеры дополнительных активных агентов включают, но не ограничиваются ими, один или более из ингибитора АПФ, ингибитора ацетил-КоА-карбоксилазы (например, фирсокостат), агониста рецептора аденозина A3, агониста рецептора адипонектина, ингибитора протеинкиназы AKT, АМР-активированного протеинкиназы (AMPK), агониста рецептора амилина, антагониста рецептора ангиотензина II АТ-1, ингибитора сигнальной киназы апоптоза 1, ингибиторов аутотаксина, биоактивных липидов, агонистов кальцитонина, ингибитора каспазы, стимулятора каспазы-3, ингибитора катепсина, ингибитора кавеолина 1, антагониста хемокинов CCR2, антагониста хемокинов CCR3, антагониста хемокинов CCR5, двойного антагониста CCR2/CCR5 (например, ценикривирок), стимулятора хлоридных каналов, ингибжора CNR1, ингибитора циклина D1, ингибитора цитохрома Р450 7А1, ингибитора DGAT1/2, ингибжора дипептидилпептидазы IV, модулятора эндосиалина, ингибитора лиганда эотаксина, модулятора белка внеклеточного матрикса, агониста фарнезоидного рецептора X (например, обетахоловая кислота, тропофексор или цилофексор), ингибитора синтазы жирных кислот, агонистов рецептора FGF1, пегилированных лигандов FGF21, фактора роста фибробластов (FGF-15, FGF-19, FGF-21), ингибитора галектина-3, агониста рецептора глюкагона, агониста глюкагоноподобного пептида 1, агонистов рецептора 1 желчных кислот, связанных с G-белком, модулятора Hedgehog (Hh), ингибитора протеазы NS3 вируса гепатита С, модулятора ядерного фактора 4 альфа гепатоцитов (TTNF4A), модулятора фактора роста гепатоцитов, ингибитора редуктазы HMG СоА, агониста IL-10, антагониста IL-17, ингибиторов котранспортера натрия желчных кислот в подвздошной кишке, сенсибилизатора инсулина, модулятора интегрина, ингибитора интерлейкина-1 рецептора-ассоциированной киназы 4 (IRAK4), ингибитора тирозинкиназы Jak2, ингибиторов кетогексокиназы, стимулятора Клото бета, ингибитора 5-липоксигеназы, ингибитора липопротеина липазы, рецептора X печени, стимулятора гена LPL, антагониста рецептора лизофосфатидата-1, ингибитора гомолога 2 лизилоксидазы, ингибитора матриксных металлопротеиназ (MMPs), ингибитора протеинкиназы MEKK-5, ингибиторов мембранной медь-аминоксидазы (VAP-1), ингибитора метионинаминопептидазы-2, модулятора метилового CpG-связывающего белка 2, ингибитора микроРНК-21 (miR-21), митохондриального разобщителя, стимуляторов основного белка миелина, ингибитор белка 3 домена PYD NACHT LRR PYD (NLRP3), стимуляторов сиртуина НАД-зависимой деацетилазы, ингибитора НАДФН-оксидазы (NOX), агониста рецептора никотиновой кислоты 1, стимулятора пуринорецепторов P2Y13, ингибитора ФДЭ-3, ингибитора ФДЭ-4, ингибитора ФДЭ-5, бета-модулятора рецептора PDGF, ингибитора фосфолипазы С, агониста PPAR-альфа, агониста PPAR-дельта, агониста PPAR-гамма, гамма-модулятора PPAR (например, элафибринор), антагониста активируемого протеазой рецептора-2, модулятора протеинкиназы, ингибитора Rho-ассоциированной протеинкиназы, ингибитора натрий-глюкозного транспортера-2, ингибитора фактора транскрипции SREBP, ингибитора STAT-1, ингибитора стеароил-КоА-десатуразы-1, супрессора стимулятора передачи сигналов цитокинов-1, супрессора стимуляторов передачи сигналов цитокинов-3, β-селективных агонистов рецепторов гормонов щитовидной железы, таких как М GL-3196, трансформирующего фактора роста β (TGF-β), активируемой трансформирующим фактором роста β киназы 1 (TAK1), бета-агониста рецептора гормона щитовидной железы, антагониста TLR-4, ингибитора трансглутаминазы, модулятора рецептора тирозинкиназы, модулятора GPCR, ядерного модулятора гормональных рецепторов, модулятора WNT и модулятора YAP/TAZ. Примеры ингибиторов JAK включают, но не ограничиваются ими, филготониб и тофацитиниб. Неограничивающим примером ингибитора сигнальной киназы апоптоза является селонсертиб.
[0229] Соединение формул X, Ха, Xb, 1, 1а, 1b, 1c, 1d или 1е или его стереоизомер или смесь стереоизомеров или его фармацевтически приемлемая соль и по меньшей мере один дополнительный активный агент можно вводить в любом порядке или даже одновременно. Множественные активные агенты могут быть предо ставлены в одной унифицированной форме или в нескольких формах (только в качестве примера, либо в виде одной таблетки, либо в виде двух отдельных таблеток). Один из активных агентов может быть введен в виде нескольких доз или оба могут быть введены в виде нескольких доз. Если применяется не одновременное введение, время между несколькими дозами может варьироваться от более чем нуля недель до менее чем четырех недель. Кроме того, комбинированные способы, композиции и составы не должны ограничиваться использованием только двух агентов.
[0230] Фармацевтическая композиция по настоящей технологии может содержать фармацевтически приемлемый носитель, такой как разбавители, вещества для улучшения распадаемости таблеток, подсластители, глиданты или ароматизаторы, и может быть приготовлена в виде лекарственной формы для перорального введения, такой как таблетки, капсулы, порошки, гранулы, суспензии, эмульсии или сиропы; или парентерального введения, такой как жидкости для наружного применения, суспензии для наружного применения, эмульсии для наружного применения, гели (мази и т.п.), средства для ингаляций, средства для распыления, инъекции и т.д. Указанные лекарственные формы могут быть приготовлены в различных формах, например, в виде лекарственной формы для однократного введения или для многократного введения.
[0231] Фармацевтическая композиция настоящей технологии может содержать эксципиентъг, такие как лактоза, кукурузный крахмал или т.п., глиданты, такие как стеарат магния и т.д., эмульгирующие агенты, суспендирующие агенты, стабилизаторы и изотонические агенты и т.д. При необходимости можно добавлять подсластитель и/или ароматизатор. Примеры эксципиентов включают, без ограничения, полиэтиленгликоль (ПЭГ), гидрогенизированное касторовое масло (НСО), хромофоры, углеводы, крахмалы (например, кукурузный крахмал), неорганические соли, противомикробные агенты, антиоксиданты, связующие/наполнители, поверхностно-активные вещества, смазывающие вещества (например, стеарат кальция или магния), вещества, способствующие скольжению, такие как тальк, вещества для улучшения распадаемости таблеток, разбавители, буферы, кислоты, основания, пленочные покрытия, их комбинации и т.п.
[0232] Конкретные углеводные эксципиенты включают, например: моносахариды, такие как фруктоза, мальтоза, галактоза, глюкоза, d-манноза, сорбоза и т.п.; дисахариды, такие как лактоза, сахароза, трегалоза, целлобиоза и т.п.; полисахариды, такие как рафиноза, мелезитоза, мальтодекстрины, декстран, крахмалы и т.п.; и альдитолы, такие как маннит, ксилит, мальтит, лактит, ксилит, сорбит (глюцил), пираннозилсорбит, миоинозитол и т.п.;
[0233] Неорганические соли или буферы включают, но не ограничиваются ими, лимонную кислоту, хлорид натрия, хлорид калия, сульфат натрия, нитрат калия, монофосфат натрия, двухосновный фосфат натрия и их комбинации.
[0234] Подходящие антиоксиданты для применения в настоящем описании включают, например, аскорбилпальмитат, бутилированный гидроксианизол, бутилированный гидрокситолуол, гипофосфоровую кислоту, монотиогаицерин, пропилгаллат, бисульфит натрия, сульфоксилат натрия, метабисульфит натрия и их комбинации.
[0235] Дополнительные иллюстративные эксципиенты включают поверхностно-активные вещества, такие как полисорбаты, например, «Tween 20» и «Tween 80», и плюроники, такие как F68 и F88 (оба доступны от BASF, Mount Olive, NJ), сложные эфиры сорбитана, липиды (например, фосфолипиды, такие как лецитин и другие фосфатидилхолины и фосфатидилэтаноламины), жирные кислоты и сложные эфиры жирных кислот, стероиды, такие как холестерин, и хелатирующие агенты, такие как ЭДТД цинк и другие подобные подходящие катионы.
[0236] Кроме того, композиция, описанная в настоящем документе, может необязательно содержать одну или более кислот или оснований. Не имеющие ограничительного характера примеры кислот, которые можно использовать, включают кислоты, выбранные из группы, состоящей из соляной кислоты, уксусной кислоты, фосфорной кислоты, лимонной кислоты, яблочной кислоты, молочной кислоты, муравьиной кислоты, трихлоруксусной кислоты, азотной кислоты, перхлоровой кислоты, фосфорной кислоты, серной кислоты, фумаровой кислоты и их комбинаций. Не имеющие ограничительного характера примеры подходящих оснований включают основания, выбранные из группы, состоящей из гидроксида натрия, ацетата натрия, гидроксида аммония, гидроксида калия, ацетата аммония, ацетата калия, фосфата натрия, фосфата калия, цитрата натрия, формиата натрия, сульфата натрия, сульфата калия, фумарата калия и их комбинаций.
[0237] Количество любого отдельного эксципиента в композиции будет варьироваться в зависимости от роли вспомогательного вещества, требований к дозированию компонентов активного агента и конкретных потребностей композиции.
[0238] Однако, как правило, эксципиент будет присутствовать в композиции в количестве от около 1% до около 99% по массе, предпочтительно от около 5% до около 98% по массе, более предпочтительно от около 15 до около 95% по массе эксципиента. Как правило, количество эксципиента, присутствующего в композиции согласно настоящему изобретению, выбрано из следующего: по меньшей мере около 2%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90% или даже 95% по массе.
[0239] Композицию настоящей технологии можно вводить перорально или парентерально, включая ингаляцию, внутривенное, внутрибрюшинное, подкожное, ректальное и местное введение. Следовательно, композиция по настоящей технологии может быть приготовлена в различных формах, таких как таблетки, капсулы, водные растворы, суспензии и т.п. В случае таблеток для перорального введения в них можно добавлять носители, такие как лактоза, кукурузный крахмал и смазывающие агенты, например стеарат магния. В случае капсул для перорального введения лактоза и/или высушенный кукурузный крахмал можно использовать в качестве разбавителя. Когда для перорального введения требуется водная суспензия, активный ингредиент можно комбинировать с эмульгирующими и/или суспендирующими агентами. При необходимости могут быть добавлены некоторые подсластители и/или ароматизаторы. Для внутримышечного, внутрибрюшинного, подкожного и внутривенного введения, как правило, готовят стерильные растворы активного ингредиента, рН растворов следует соответствующим образом отрегулировать изабуферить. При внутривенном введении следует контролировать обитую концентрацию растворенных веществ, чтобы сделать препарат изотоническим. Композиция по настоящей технологии может быть в форме водного раствора, содержащего фармацевтически приемлемые носители, например физиологический раствор, имеющий уровень рН 7,4. Растворы можно вводить во внутримышечный кровоток пациента путем местной болюсной инъекции.
[0240] Указанное соединение пирролидина или пиперидина, то есть соединение формул X, Ха, Xb, 1, 1a, 1b, 1c, 1d или 1e, или его стереоизомер, или смесь стереоизомеров, или его фармацевтически приемлемую соль можно вводить пациенту в эффективном количестве от примерно 0,001 мг/кг до примерно 100 мг/кг в день. Конечно, дозировка может быть изменена в соответствии с возрастом, весом, восприимчивостью пациента, симптомами или клинической эффективностью соединения. Это включает 0,001, 0,0025, 0,005, 0,0075, 0,01, 0,025, 0,05, 0,075, 0,1, 0,25, 0,5, 0,75, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95 или 100 мг/кг.
[0241] Как правило, терапевтически эффективное количество соединения формул X, Ха, Xb, 1, 1а, 1b, 1c, 1d или 1e или его стереоизомер или смеси стереоизомеров или его фармацевтически приемлемая соль будут варьироваться от общей суточной дозы от около 0,1 мг/день до 1000 мг/сутки, около 30-720 мг/день, около 60-600 мг/день или около 100-480 мг/день или более. В некоторых вариантах осуществления терапевтически эффективное количество соединения формул X, Ха, Xb, 1, 1a, 1b, 1c, 1d или 1e или его фармацевтически приемлемой соли будет находиться в диапазоне около 1-240 мг/день, около 30-240 мг/день, около 30-200 мг/день, около 30-120 мг/день, около 1-120 мг/день, около 50-150 мг/день, около 60-150 мг/день, около 60-120 мг/день или около 60-100 мг/день при введении либо в виде однократной дозы, либо в виде нескольких доз. В некоторых вариантах осуществления несколько доз включают две, три или четыре дозы в день.
[0242] В некоторых вариантах осуществления терапевтически эффективное количество соединения формул X, Ха, Xb, 1, 1а, 1b, 1c, 1d или 1e, или его стереоизомера, или смеси стереоизомеров, или его фармацевтически приемлемой соли составляет по меньшей мере 0,1 мг/сут, по меньшей мере 0,5 мг/сут, по меньшей мере 1 мг/сут, по меньшей мере 5 мг/сут, по меньшей мере 10 мг/сут, по меньшей мере 20 мг/сут, по меньшей мере 30 мг/сут, по меньшей мере 40 мг/сут, по меньшей мере 50 мг/сут, по меньшей мере 60 мг/сут, по меньшей мере 70 мг/сут, по меньшей мере 80 мг/сут, по меньшей мере 90 мг/сут, по меньшей мере 100 мг/сут, по меньшей мере 110 мг/сут, по меньшей мере 120 мг/сут, по меньшей мере 130 мг/сут, по меньшей мере 140 мг/сут, по меньшей мере 150 мг/сут, по меньшей мере 160 мг/сут, по меньшей мере 170 мг/сут, по меньшей мере 180 мг/сут, по меньшей мере 190 мг/сут, по меньшей мере 200 мг/сут, по меньшей мере 225 мг/сут, по меньшей мере 250 мг/сут, по меньшей мере 275 мг/сут, по меньшей мере 300 мг/сут, по меньшей мере 325 мг/ сут, по меньшей мере 350 мг/сут, по меньшей мере 375 мг/сут, по меньшей мере 400 мг/сут, по меньшей мере 425 мг/сут, по меньшей мере 450 мг/сут, по меньшей мере 475 мг/сут, по меньшей мере 500 мг/сут, по меньшей мере 525 мг/сут, по меньшей мере 550 мг/сут, по меньшей мере 575 мг/сут, по меньшей мере 600 мг/сут, по меньшей мере 625 мг/сут, по меньшей мере 650 мг/сут, по меньшей мере 675 мг/сут, по меньшей мере 700 мг/сут, по меньшей мере 725 мг/сут, по меньшей мере 750 мг/сут, по меньшей мере 775 мг/сут, по меньшей мере 800 мг/сут, по меньшей мере 825 мг/сут, по меньшей мере 850 мг/сут, по меньшей мере 875 мг/сут, по меньшей мере 900 мг в сутки, по меньшей мере 925 мг/сут, по меньшей мере 950 мг/сут, по меньшей мере 975 мг/сут или по меньшей мере 1000 мг/сут.
[0243] Настоящая технология также включает способ ингибирования белка активации фибробластов (FAP) у млекопитающего, включающий введение млекопитающему терапевтически эффективного количества соединения формул X, Ха, Xb, 1, 1a, 1b, 1c, 1d или 1е или стереоизомер или смеси стереоизомеров или его фармацевтически приемлемой соли. В одном варианте осуществления настоящего изобретения предложен способ лечения ожирения, диабета, стеатоза и неалкогольного стеатогепатита (НАСГ), включающий введение млекопитающему терапевтически эффективного количества соединения формул X, Ха, Xb, 1, 1а, 1b, 1c, 1d или 1е или стереоизомеров или смеси стереоизомеров или его фармацевтически приемлемой соли. В некоторых вариантах осуществления настоящего изобретения предложен способ лечения НАСГ у субъекта, нуждающегося в этом, при этом способ включает в себя, по существу состоит из, или состоит из введения субъекту терапевтически эффективного количества соединения формул X, Ха, Xb, 1, 1a, 1b, 1c, 1d или 1e или его стереоизомера или смеси стереоизомеров или его фармацевтически приемлемой соли. Млекопитающие включают, но не ограничиваются ими, мышей, грызунов, крыс, обезьян, человека, сельскохозяйственных животных, собак, кошек, спортивных животных и домашних животных.
[0244] В настоящей технологии предложено применение соединения формул X, Ха, Xb, 1, 1а, 1b, 1c, 1d или 1e или стереоизомеров или смеси стереоизомеров или его фармацевтически приемлемой соли в производстве лекарственного средства для ингибирования активации фибробластов (FAP) у млекопитающих. В одном варианте осуществления в настоящей технологии предложено применение соединения формул X, Ха, Xb, 1, 1a, 1b, 1c, 1d или 1e или стереоизомеров или смеси стереоизомеров или его фармацевтически приемлемой солив производстве лекарственного средства для лечения или профилактики ожирения, диабета, стеатоза и не алкогольного стеатогепатита (НАСГ).
[0245] Далее настоящая технология дополнена примерами и экспериментальных примерами. Однако приведенные ниже примеры и экспериментальные примеры приведены только в целях иллюстрации и не предназначены для ограничения объема изобретения.
[0246] Как будет очевидно специалистам в данной области техники после прочтения настоящего описания, каждый из отдельных вариантов осуществления, описанных и проиллюстрированных в настоящем документе, имеет отдельные компоненты и признаки, которые можно легко отделить или объединить с признаками любого из других нескольких вариантов осуществления без отступления от объема или сущности настоящей технологии. Любой указанный способ может быть осуществлен в указанном порядке или в любом другом порядке, который является логически возможным.
ПРИМЕРЫ
[0247] Анализы соединений, полученных в следующих примерах, проводили следующим образом: Анализ спектра ядерного магнитного резонанса (ЯМР) проводили с использованием спектрометра Bruker 400 МГц и спектрометра Agilent 600 МГц и их химических сдвигов в м.д. Кроме того, указанные молекулярные массы измеряли с помощью жидкостной хроматографии/масс-селективного детектора (MSD) Agilent 1260 Infinity, оснащенного интерфейсом электростатического распыления (с помощью одноквадрупольного анализа, это указывает на значение m/z в ESI (ESI-MS (катион), который представлен пиком [М+Н]+). Колоночную хроматографию проводили на силикагеле (Merck, 70-230 меш). (W.C. Still, J. Org. Chem., 43, 2923, 1978). Кроме того, сокращения, используемые в следующих примерах, являются следующими: Me - метил, Et - этил, Ph - фенил, а Boc - трет-бутилоксикарбонил. Кроме того, исходные вещества в каждом примере [0248] [0249] представляют собой известные соединения, которые были синтезированы в соответствии с литературой или приобретены, например, у Sigma-Aldrich.
[0250] Эталонный пример 1. (S)-1-(2-хлорацетил)пирролидин-2-карбонитрил
[0251] (S)-пирролидин-2-карбонитрил гидрохлорид (7 г, 52,8 ммоль) растворяли в дихлорметане (264 мл). Полученный раствор добавляли с помощью триэтиламина (22,1 мл, 158,3 ммоль) и затем охлаждали до 0°С. К реакционной смеси медленно по каплям добавляли раствор, в котором 2-хлорацетилхлорид (4,63 мл, 58,1 ммоль) растворяли в дихлорметане (10 мл). Реакционную смесь перемешивали в течение 2 часов при 0°С и затем добавляли воду для экстракции водного слоя дихлорметаном. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (этилацетат / н-гексан = 2/1, об./об.), получая указанное в заголовке соединение (7,6 г). 1Н-ЯМР (CDCl3, 400 МГц) δ 4,81 (д, 1 Н), 4,24-4,11 (м, 2 Н), 3,73 (с, 2 Н), 3,61 (с, 1 Н), 3,61 (с, 1 Н) 2,42-2,05 (м, 4 Н)
[0252] Эталонный пример 2. (2S,4S)-1-(2-хлорацетил)-4-фторпирролидин-2-карбонитрил
[0253] Указанное в заголовке соединение в виде твердого вещества (6,31 г) получали таким же образом, как в примере 1, за исключением того, что вместо (S)-пирролидин-2-карбонитрил гидрохлорида использовали (2S,4S)-4-фторпирролидин-2-карбонитрил гидрохлорид (7,95 г, 52,8 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 5,52-5,31 (м, 1 Н), 5,06-4,94 (м, 1 Н), 4,26-3,84 (м, 3 Н) 2,80-2,68 (м, 1 Н), 2,42-2,32 (м, 1 Н)
[0254] Эталонный пример 3. (2S)-1-(2-хлорацетил)-4,4-дифторпирролидин-2-карбонитрил
[0255] Указанное в заголовке соединение в виде твердого вещества (8,57 г) получали таким же образом, как в примере 1, за исключением того, что вместо (S)-пирролидин-2-карбонитрил гидрохлорида использовали (2S)-4,4-дифторпирролидин-2-карбонитрил 4-метилбензолсульфонат (16,1 г, 52,8 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 4,97 (с, 1 Н), 4,04 (с, 3 Н), 2,79 (с, 2 Н), 1,55 (с, 1 Н)
[0256] Эталонный пример 4. (1S,3S,5S)-2-(2-хлорацетил)-2-азабицикло[3.1.0]гексан-3-карбонитрил
[0257] Указанное в заголовке соединение в виде жидкости (8 г) получали таким же образом, как в примере 1, за исключением того, что вместо (S)-пирролидин-2-карбонитрил гидрохлорида использовали (1S,3S,5S)-2-азабицикло[3.1.0]гексан-3-карбонитрил 4-метилбензолсульфонат (14,8 г, 52,8 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 4,96 (д, 1 Н), 4,25-1,14 (м, 2 Н), 3,62-3,58 (м, 1 Н), 2,65-2,58 (м, 1 Н), 2,42 (д, 1 Н), 1,94-1,90 (м, 1 Н), 1,16-1,05 (м, 2 Н)
[0258] Эталонный пример 5. (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид
[0259] Стадия 1: трет-бутил (S)-3-(хинолин-4-иламино)пирролидин-1-карбоксилат
[0260] Трет-бутил (S)-3-аминопирролидин-1-карбоксилат (500 мг, 2,68 ммоль) растворяли в безводном толуоле. К полученному раствору добавляли 4-бромхинолин (670,2 мг, 3,22 ммоль), карбонат цезия (1,31 г, 4,02 ммоль), трис(дибензилиденацетон)дииалладий(0) (245,8 мг, 0,27 ммоль), и (+/-)-2,2'-бис(дифенилфосфино)-1,1'-бинафталин (167,1 мг, 0,27 ммоль). Реакционную смесь нагревали в колбе с обратным холодильником и перемешивали при 100°С в течение ночи. После завершения реакции реакционную смесь охлаждали до комнатной температуры и затем добавляли воду для экстракции водного слоя этилацетатом. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали колоночной хроматографией на силикагеле (этилацетат/н-гексан = 1/1, об./об.), получая указанное в заголовке соединение (633,5 мг). 1H-ЯМР (CDCl3, 400 МГц) δ 8,53 (д, 1Н), 8,14 (д, 1Н), 7,99 (д, 1Н), 7,60 (т, 1Н), 7,36 (т, 1Н), 6,47 (д, 1Н), 4,80 (м, 1Н), 4,39 (м, 1Н), 3,89-3,98 (м, 1Н), 3,79-3,89 (м, 1Н), 3,63-3,74 (м, 1Н), 3,51-3,63 (м, 1Н), 2,21-2,30 (м, 1Н), 1,96-2,08 (м, 1Н), 1,46 (с, 9Н)
[0261] Стадия 2: (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид
[0262] Трет-бутил (S)-3-(хинолин-4-иламино)пирролидин-1-карбоксилат (472 мг, 1,51 ммоль), полученный на стадии 1, растворяли в дихлорметане (8,4 мл), а затем туда же добавляли (по каплям) в избытке 4,0 М соляную кислоту, растворенную в 1,4-диоксане. Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции полученное твердое соединение фильтровали, промывали и сушили в вакууме, получая указанное в заголовке соединение (394,5 мг). 1Н-ЯМР ((CD3)2SO, 400 МГц) δ 14,6 (с, 1Н), 9,75 (с, 1Н), 9,46 (д, 1Н), 8,98 (д, 1Н), 8,66 (д, 1Н), 8,08 (д, 1Н), 8,00 (дд, 1Н), 7,74 (дд, 1Н), 6,98 (д, 1Н), 4,74-4,82 (м, 1Н), 3,35-3,59 (м, 2Н), 2,23-2,32 (м, 1Н), 2,18-2,28 (м, 1Н)
[0263] Эталонный пример 6. (S)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид
[0264] Стадия 1: трет-бутил-((S)-3-(хинолин-3-иламино)пирролидин-1-карбоксилат
[0265] Указанное в заголовке соединение (576,3 мг) получали так же, как на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 3-бромхинолин (670,2 мг, 3,22 ммоль). 1Н-ЯМР (CDCl3, 400 МГц) δ 8,40-8,53 (м, 1Н), 7,88-8,02 (м, 1Н), 7,60-7,74 (м, 1Н), 7,34-7,55 (м, 2Н), 6,95-7,09 (м, 1Н), 4,17-4,33 (м, 1Н), 3,80 (м, 1Н), 3,42-3,64 (м, 2Н), 3,21-3,41 (м, 1Н), 2,13-2,42 (м, 2Н), 1,87-2,02 (м, 1Н), 1,34-1,60 (м, 9Н)
[0266] Стадия 2: (S)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид
[0267] Указанное в заголовке соединение (473,5 мг) получали так же, как на стадии 2 эталонного примера 5, и использовали на следующей стадии без какой-либо дополнительной очистки.
[0268] Эталонный пример 7. (S)-N-(пирролидин-3-ил)изохинолин-4-амина гидрохлорид
[0269] Стадия 1: трет-бутил-(S)-3-(изохинолин-4-иламино)пирролидин-1-карбоксилат
[0270] Указанное в заголовке соединение (457,9 мг) получали таким же образом, как на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 4-бромизохинолин (670,2 мг, 3,22 ммоль). 1Н-ЯМР (CDCl3, 400 МГц) δ 8,85 (с, 1Н), 8,11 (д, 1Н), 8,01-8,15 (м, 1Н), 7,93 (д, 1Н), 7,54-7,68 (м, 2Н), 4,91-4,94 (м, 1Н), 4,39-4,48 (м, 1Н), 3,62-3,86 (м, 2Н), 3,29-3,43 (м, 2Н), 2,31-2,41 (м, 1Н), 1,90-1,99 (м, 1Н), 1,47 (с, 9Н)
[0271] Стадия 2: (S)-N-(пирролидин-3-ил)изохинолин-4-амина гидрохлорид
[0272] Указанное в заголовке соединение (343,2 мг) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0273] Эталонный пример 8. (S)-N-(бензо[b]тиофен-4-ил)пирролидин-3-амина гидрохлорид
[0274] Стадия 1: трет-бутил-(S)-3-(бензо[b]тиофен-4-иламино)пирролидин-1-карбоксилат
[0275] Указанное в заголовке соединение (351,6 мг) получали таким же образом, как на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 4-бромбензо[b]тиофен (686,2 мг, 3,22 ммоль). 1Н-ЯМР (CDCl3, 400 МГц) δ 7,26-7,37 (м, 2Н), 7,15-7,24 (м, 2Н), 6,53 (д, 1Н), 4,07-4,25 (м, 2Н), 3,77-3,82 (м, 1Н), 3,43-3,63 (м, 2Н), 3,26-3,42 (м, 1Н), 2,25-2,35 (м, 1Н), 1,93-2,07 (м, 1Н), 1,42-1,52 (м, 9Н)
[0276] Стадия 2: (S)-N-(бензо[b]тиофен-4-ил)пирролидин-3-амина гидрохлорид
[0277] Указанное в заголовке соединение (200,3 мг) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0278] Эталонный пример 9. (S)-N-(бензо[b]тиофен-7-ил)пирролидин-3-амина гидрохлорид
[0279] Стадия 1: трет-бутил-(S)-3-(бензо[b]тиофен-7-иламино)пирролидин-1-карбоксилат
[0280] Указанное в заголовке соединение (264,5 мг) получали таким же образом, как на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 7-бромбензо[b]тиофен (686,2 мг, 3,22 ммоль). 1Н-ЯМР (CDCl3, 400 МГц) δ 7,34-7,40 (м, 1Н), 7,26-7,33 (м, 3Н), 6,59 (д, 1Н), 4,23-4,32 (м, 1Н), 3,79-3,88 (м, 1Н), 3,70-3,82 (м, 1Н), 3,46-3,61 (м, 2Н), 3,24-3,42 (м, 1Н), 2,24-2,32 (м, 1Н), 1,90-2,04 (м, 1Н), 1,47 (с, 9Н)
[0281] Стадия 2: (S)-N-(бензо[b]тиофен-7-ил)пирролидин-3-амина гидрохлорид
[0282] Указанное в заголовке соединение (172 мг) получали таким же образом, как и на стадии 2
эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0283] Эталонный пример 10. (S)-N-(бензофуран-7-ил)пирролидин-3-амина гидрохлорид
[0284] Стадия 1: трет-бутил-(S)-3-(бензофуран-7-иламино)пирролидин-1-карбоксилат
[0285] Указанное в заголовке соединение (555,9 мг) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 7-бромбензофуран (641,2 мг, 3,22 ммоль). 1Н-ЯМР (CDCl3, 400 МГц) δ 7,55-7,67 (м, 1Н), 7,10-7,35 (м, 1Н), 6,99-7,05 (м, 1Н), 6,72-6,85 (м, 1Н), 6,54 (д, 1Н), 4,19-4,31 (м, 2Н), 3,69-3,82 (м, 1Н), 3,48-3,62 (м, 2Н), 3,27-3,43 (м, 1Н), 2,18-2,27 (м, 1Н), 1,97-2,03 (м, 1Н), 1,46 (с, 9Н)
[0286] Стадия 2: (S)-N-(бензофуран-7-ил)пирролидин-3-амина гидрохлорид
[0287] Указанное в заголовке соединение (342,8 мг) получали таким же образом, как и на стадии 2 эталонного примера 5 [0288] и использовали на следующей стадии без дополнительной очистки.
[0289] Эталонный пример 11. (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорид
[0290] Стадия 1: трет-бутил-(S)-3-(фуро[3,2-с]пиридин-7-иламино)пирролидин-1-карбоксилат
[0291] Указанное в заголовке соединение (171,5 мг) получали таким же образом, как на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 7-бромфуро[3,2-с]пиридин (640,2 мг, 3,22 ммоль). 1Н-ЯМР (CDCl3, 400 МГц) δ 8,40 (с, 1Н), 7,91 (с, 1Н), 7,60 (д, 1Н), 6,81 (д, 1Н), 4,30-4,45 (м, 1Н), 4,07-4,29 (м, 1Н), 3,76-3,89 (м, 1Н), 3,47-3,60 (м, 2Н), 3,28-3,44 (м, 1Н), 2,43-2,65 (м, 1Н), 2,19-2,34 (м, 11Н), 1,94-2,03 (м, 1Н), 1,46 (с, 9Н)
[0292] Стадия 2: (S)-N-(пирролидин-3-ил)фуро[3,2-c]пиридин-7-амин гидрохлорид
[0293] Указанное в заголовке соединение (100,9 мг) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0294] Эталонный пример 12. (S)-N-([1,1'-бифенил]-2-ил)тфролидин-3-амина гидрохлорид
[0295] Стадия 1: трет-бутил (S)-3-([1,1'-бифенил]-2-иламино)пирролидин-1 -карбоксилат
[0296] Указанное в заголовке соединение (836,3 мг) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 2-бромбифенил (750,0 мг, 3,22 ммоль). 1Н-ЯМР (CDCl3, 400 МГц) δ 7,40-7,58 (м, 2Н), 7,32-7,40 (м, 3Н), 7,18-7,24 (м, 1Н), 7,04-7,13 (м, 1Н), 6,75-6,86 (м, 1Н), 6,66-6,72 (м, 1Н), 4,03-4,10 (м, 1Н), 3,93-4,01 (м, 1Н), 3,67-3,75 (м, 1Н), 3,27-3,47 (м, 2Н), 3,11-3,25 (м, 1Н), 2,09-2,19 (м, 1Н), 1,48-1,58 (м, 1Н), 1,38-1,47 (с, 9Н)
[0297] Стадия 2: (S)-N-([1,1'-бифенил]-2-ил)пирролидин-3-амина гидрохлорид
[0298] Указанное в заголовке соединение (562 мг) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0299] Эталонный пример 13. (S)-N-([1,1'-бифенил]-4-ил)тфролидин-3-амина гидрохлорид
[0300] Стадия 1: трет-бутил (S)-3-([1,1'-бифенил]-4-иламино)пирролидин-1 -карбоксилат
[0301] Указанное в заголовке соединение (756,5 мг) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 4-бромбифенил (750,0 мг, 3,22 ммоль). 1Н-ЯМР (CDCl3, 400 МГц) δ 7,47-7,56 (м, 2Н), 7,40-7,46 (м, 2Н), 7,35-7,40 (м, 2Н), 7,22-7,29 (м, 2Н), 6,66-6,68 (м, 1Н), 3,99-4,08 (м, 1Н), 3,87-3,91 (м, 1Н), 3,70-3,85 (м, 1Н), 3,42-3,54 (м, 2Н), 3,18-3,32 (м, 1Н), 2,13-2,21 (м, 1Н), 1,42-1,51 (м, 9Н)
[0302] Стадия 2: (S)-N-([1,1'-бифенил]-4-ил)пирролидин-3-амина гидрохлорид
[0303] Указанное в заголовке соединение (414 мг) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0304] Эталонный пример 14. (S)-N-(нафталин-2-ил)пирролидин-3-амин
[0305] Стадия 1: трет-бутил (S)-3-(нафталин-2-иламино)пирролидин-1-карбоксилат
[0306] Трет-бутил (S)-3-аминопирролидин-1-карбоксилат (500 мг, 2,68 ммоль) растворяли в безводном толуоле. К полученному раствору добавляют 2-бромнафтален (665,2 мг, 3,22 ммоль), карбонат цезия (1,31 г, 4,02 ммоль), трис(дибензилиденацетон)дипалладпй(0) (245,8 мг, 0,27 ммоль), и (+/-)-2,2'-бис(дифенилфосфино)-1,1'-бинафталин (167,1 мг, 0,27 ммоль). Реакционную смесь нагревали в колбе с обратным холодильником и перемешивали при 100°С в течение ночи. После завершения реакции реакционную смесь охлаждали до комнатной температуры и затем добавляли воду для экстракции водного слоя этилацетатом. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали колоночной хроматографией на силикагеле (этилацетат/н-гексан = 1/1, об./об.), получая указанное в заголовке соединение (633,5 мг). МС (ИЭР) m/z - 312,4 (М+Н)+
[0307] Стадия 2: (S)-N-(нафталин-2-ил)пирролидин-3-амин
[0308] Трет-бутил (S)-3-(нафталин-2-иламино)пирролидин-1-карбоксилат (633,5 мг, 2,02 ммоль), полученный на стадии 1, растворяли в дихпорметане (11,2 мл), а затем туда же добавляли (по каплям) в избытке 4,0 М соляную кислоту, растворенную в 1,4-диоксане. Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции остаток, полученный концентрированием при пониженном давлении, растворяли в дихлорметане, раствор промывали 1Н водным раствором гидроксида натрия и соляным раствором, сушили над безводным сульфатом магния и затем концентрировали при пониженном давлении с получением указанного в заголовке соединения (318,6 мг). 1Н-ЯМР (CDCl3, 400 МГц) δ 7,58-7,71 (м, 3Н), 7,36 (дд, 1Н), 7,19 (дд, 1Н), 6,84 (дд, 1Н), 6,74-6,82 (м, 1Н), 4,01-4,12 (м, 1Н), 3,88-3,98 (м, 0,9Н), 3,73-3,79 (м, 0,2Н), 3,57-3,65 (м, 0,3Н), 3,04-3,30 (м, 2Н), 2,81-3,00 (м, 2Н), 2,16-2,28 (м, 1Н), 1,64-1,78 (м, 1Н)
[0309] Эталонный пример 15. (S)-N-([1,1'-бифенил]-3-ил)пирролидин-3-амина гидрохлорид
[0310] Стадия 1: трет-бутил (S)-3-([1,1'-бифенил]-3-иламино)пирролидин-1 -карбоксилат
[0311] Указанное в заголовке соединение (562,4 мг) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 3-бромбифенил (750,0 мг, 3,22 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 7,52-7,60 (м, 2Н), 7,36-7,47 (м, 3Н), 7,31-7,35 (м, 1Н), 6,96-7,05 (м, 1Н), 6,80-6,93 (м, 1Н), 6,60-6,75 (м, 1Н), 4,03-4,15 (м, 1Н), 3,84-3,95 (м, 1Н), 3,65-3,77 (м, 1Н), 3,47-3,52 (м, 1Н), 3,18-3,35 (м, 1Н), 2,15-2,25 (м, 1Н), 1,86-1,98 (м, 1Н), 1,40-1,52 (м, 9Н)
[0312] Стадия 2: (S)-N-([1,1'-бифенил]-3-ил)пирролидин-3-амина гидрохлорид
[0313] Указанное в заголовке соединение (342,2 мг) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0314] Эталонный пример 16. (S)-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0315] Стадия 1: трет-бутил (S)-3-(хинолин-5-иламино)пирролидин-1-карбоксилат
[0316] Указанное в заголовке соединение (297,4 мг) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 5-бромхинолин (670,2 мг, 3,22 ммоль). 1H-ЯМР (CD3OD, 400 МГц) δ 9,67-9,72 (м, 1Н), 9,06-9,21 (м, 1Н), 7,90-8,00 (м, 2Н), 7,46-7,52 (м, 1Н), 7,01-7,11 (м, 1Н), 4,58 (м, 1Н), 3,60-3,75 (м, 2Н), 3,53-3,59 (м, 2Н), 2,45-2,52 (м, 1Н), 2,37-2,42 (м, 1Н)
[0317] Стадия 2: (S)-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0318] Указанное в заголовке соединение (342,2 мг) получали таким же образом, как и на стадии 2 эталонного примера 5, использовали на следующей стадии без дополнительной очистки.
[0319] Эталонный пример 17. (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид
[0320] Стадия 1: трет-бутил-(R)-3-(хинолин-3-иламино)пирролидин-1-карбоксилат
[0321] Трет-бутил (R)-3-аминопирролидин-1 -карбоксилат (500 мг, 2,68 ммоль) растворяли в безводном толуоле. К полученному раствору добавляют 3-бромхинолин (670,2 мг, 3,22 ммоль), карбонат цезия (1,31 г, 4,02 ммоль), трис(дибензилпденацетон)дипалладпй(0) (245,8 мг, 0,27 ммоль), и (+/-)-2,2'-бис(дифенилфосфино)-1,1'-бинафталин (167,1 мг, 0,27 ммоль). Реакционную смесь нагревали в колбе с обратным холодильником и перемешивали при 100°С в течение ночи. После завершения реакции реакционную смесь охлаждали до комнатной температуры и затем добавляли воду для экстракции водного слоя этилацетатом. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали колоночной хроматографией на силикагеле (этилацетат/н-гексан = 1/1, об./об.), получая указанное в заголовке соединение (472 мг). 1Н-ЯМР (CDCl3, 400 МГц) δ 8,41-8,52 (м, 1Н), 7,94-8,11 (м, 1Н), 7,57-7,68 (м, 1Н), 7,38-7,51 (м, 2Н), 7,02-7,13 (м, 1Н), 4,27 (м, 1Н), 3,89-3,92 (м, 1Н), 3,51-3,75 (м, 2Н), 3,32-3,42 (м, 1Н), 2,26-2,31 (м, 1Н), 1,90-2,13 (м, 2Н), 1,40-1,60 (м, 9Н)
[0322] Стадия 2: (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид
[0323] Указанное в заголовке соединение (344,7 мг) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0324] Эталонный пример 18. (R)-N-([1,1'-бифенил]-3-ил)пирролидин-3-амина гидрохлорид
[0325] Стадия 1: трет-бутил (R)-3-([1,1'-бифенил]-3-ил)пирролидин-1-карбоксилат
[0326] Указанное в заголовке соединение (621.3 мг) получали таким же образом, как на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 3-бромбифенил (750,0 мг, 3,22 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 7,55-7,68 (м, 2Н), 7,38-7,53 (м, 2Н), 7,30-7,35 (м, 1Н), 7,23-7,28 (м, 1Н), 6,94-7,08 (м, 1Н), 6,79-6,84 (м, 1Н), 6,58-6,63 (м, 1Н), 4,04-4,12 (м, 1Н), 3,90-4,03 (м, 1Н), 3,71-3,85 (м, 1Н), 3,46-3,52 (м, 2Н), 3,15-3,35 (м, 1Н), 2,16-2,20 (м, 1Н), 1,82-1,98 (м, 1Н), 1,46-1,58 (м, 9Н)
[0327] Стадия 2: (R)-N-([1,1'-бифенил]-3-ил)пирролидин-3-амина гидрохлорид
[0328] Указанное в заголовке соединение (383,7 мг) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0329] Эталонный пример 19. (R)-N-(пирролидин-3-ил)изохинолин-4-амина гидрохлорид
[0330] Стадия 1: трет-бутил-(R)-3-(изохинолин-4-иламино)пирролидин-1-карбоксилат
[0331] Указанное в заголовке соединение (447,7 мг) получали таким же образом, как на стадии 1 эталонного примера 17, за исключением того, что вместо 4-бромхинолина использовали 3-бромизохинолин (670,2 мг, 3,22 ммоль). МС (ИЭР) m/z - 314,2 (М+Н)+
[0332] Стадия 2: (R)-N-(пирролидин-3-ил)изохинолин-4-амина гидрохлорид
[0333] Указанное в заголовке соединение (299,7 мг) получали таким же образом, как и на стадии 2 эталонного примера 5. МС (ИЭР) m/z - 214,2 (М+Н)+
[0334] Эталонный пример 20. (R)-N-(бензо[b]тиофен-7-ил)пирролидин-3-амина гидрохлорид
[0335] Стадия 1: трет-бутил-(R)-3-(бензо[b]тиофен-7-иламино)пирролидин-1-карбоксилат
[0336] Указанное в заголовке соединение (128 мг) получали таким же образом, как на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 7-бромбензо[b]тиофен (685,0 мг, 3,22 ммоль). 1Н-ЯМР (CDCl3, 400 МГц) δ 7,21-7,45 (м, 4 Н), 6,57-6,62 (м, 1Н), 4,21-4,31 (м, 1Н), 3,73-3,82 (м, 2Н), 3,44-3,60 (м, 2Н), 3,26-3,40 (м, 1Н), 2,23-2,25 (м, 1Н), 1,97-2,21 (м, 1Н), 1,40-1,56 (м, 9Н)
[0337] Стадия 2: (R)-N-(бензо[b]тиофен-7-ил)пирролидин-3-амина гидрохлорид
[0338] Указанное в заголовке соединение (79,0 мг) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0339] Эталонный пример 21. (S)-N-(хинолин-4-ил)пирролидин-3-карбокс амида гидрохлорид
[0340] Стадия 1: трет-бутил (S)-3-(хинолин-4-илкамамоил)пирролидин-1-карбоксилат
[0341] (S)-1-(трет-бутоксикарбонил)пирролидин-3-карбоновая кислота (300 мг, 1,39 ммоль) растворяли в дихлорметане. К полученному раствору добавляли 4-аминохинолин (200,9 мг, 1,39 ммоль), HATU (O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилуран гексафторфосфат) (794,9 мг, 2,09 ммоль) и диизопропилэтиламин (0,49 мл, 2,79 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции к реакционной смеси добавляли воду. Водный слой реакционной смеси экстрагировали дихлорметаном. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (дихлорметан / метанол = 20/1, об./об.) с получением указанного в заголовке соединения (250 мг). 1Н-ЯМР (CDCl3, 400 МГц) δ 9,05 (с, 1Н), 8,80 (с, 1Н), 8,63 (с, 1Н), 8,38 (с, 1Н), 7,95 (д, 2Н), 7,71 (с, 1Н), 3,71-3,46 (м, 5 Н), 2,83 (с, 10 Н), 2,32-2,18 (м, 2Н), 1,50-1,43 (д, 9Н)
[0342] Стадия 2: (S)-N-(хинолин-4-ил)пирролидин-3-карбоксамида гидрохлорид
[0343] Трет-бутил (S)-3-(хинолин-4-илкамамоил)пирролидин-1-карбоксилат (450 мг, 1,32 ммоль), приготовленный на стадии 1, растворяли в дихлорметане (7,3 мл), а затем туда же добавляли (по каплям) в избытке 4,0 М соляную кислоту, растворенную в 1,4-диоксане. Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции полученное твердое вещество фильтровали и высушивали с получением указанного в заголовке соединения (220 мг). Указанное в заголовке соединение использовали на следующей стадии без дополнительной очистки.
[0344] Эталонный пример 22. (S)-N-(хинолин-3-ил)пирролидин-3-карбоксамида гидрохлорид
[0345] Стадия 1: трет-бутил (S)-3-(хинолин-3-илкамамоил)пирролидин-1-карбоксилат
[0346] Указанное в заголовке соединение (100 мг) получали таким же образом, как на стадии 1 эталонного примера 21, за исключением того, что вместо 4-аминохинолина использовали 3-аминохинолин (200,9 мг, 1,39 ммоль). МС (ИЭР) m/z - 342,4 (М + Н)+
[0347] Стадия 2: (S)-N-(хинолин-3-ил)пирролидин-3-карбоксамида гидрохлорид
[0348] Указанное в заголовке соединение (190,7 мг) получали таким же образом, как и на стадии 2 эталонного примера 21, и использовали на следующей стадии без дополнительной очистки.
[0349] Эталонный пример 23. (R)-N-(хинолин-4-ил)пирролидин-3-карбоксамида гидрохлорид
[0350] Стадия 1: трет-бутил (R)-3-(хинолин-4-илкамамоил)пирролидин-1-карбоксилат
[0351] Указанное в заголовке соединение (340 м г) получали таким же образом, как на стадии 1 эталонного примера 21, за исключением того, что вместо (S)-1-(трет-бутоксикарбонил)пирролидин-3-карбоновой кислоты использовали (R)-1-(трет-бутоксикарбонил)пирролидин-3-карбоновую кислоту (300 мг, 1,39 ммоль). 1Н-ЯМР (CDCl3, 400 МГц) δ 9,05 (с, 1Н), 8,80 (с, 1Н), 8,63 (с, 1Н), 8,38 (с, 1Н), 7,95 (д, 2Н), 7,71 (с, 1Н), 3,71-3,46 (м, 5 Н), 2,83 (с, 10Н), 2,32-2,18 (м, 2Н), 1,50-1,43 (д, 9Н)
[0352] Стадия 2: (R)-N-(хинолин-4-ил)пирролидин-3-карбоксамида гидрохлорид
[0353] Указанное в заголовке соединение (260 мг) получали таким же образом, как и на стадии 2 эталонного примера 21, и использовали на следующей стадии без дополнительной очистки.
[0354] Эталонный пример 24. (R)-N-(хинолин-3-ил)пирролидин-3-карбоксамида гидрохлорид
[0355] Стадия 1: трет-бутил (R)-3-(хинолин-3-илкамамоил)пирролидин-1-карбоксилат
[0356] Указанное в заголовке соединение (450 мг) получали таким же образом, как на стадии 1
эталонного примера 21, за исключением того, что вместо 4-аминохинолина использовали 3-аминохинолин (200,9 мг, 1,39 ммоль). МС (ИЭР) m/z - 342,4 (М+Н)+
[0357] Стадия 2: (R)-N-(хинолин-3-ил)пирролидин-3-карбоксамида гидрохлорид
[0358] Указанное в заголовке соединение (310,7 мг) получали таким же образом, как и на стадии 2 эталонного примера 21, и использовали на следующей стадии без дополнительной очистки.
[0359] Эталонный пример 25. (S)-1-(2-((S)-3-аминопирролидин-1-ил)ацетил)пирролидин-2-карбонитрил трифторацетат
[0360] Стадия 1: трет-бутил (S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)карбамат
[0361] (S)-1-(2-хлорацетил)пирролидин-2-карбонитрил (3 г, 17,4 ммоль), полученный в эталонном примере 1, растворяли в безводном дихлорметане (34,8 мл). К полученному раствору добавляли (3S)-(-)-3-(трет-бутоксикарбониламино)пирролидин (3,56 г, 19,1 ммоль) и карбонат калия (4,8 г, 34,8 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции к реакционной смеси добавляли воду. Водный слой реакционной смеси экстрагировали дихлорметаном. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (этилацетат/н-гексан = 4/1, об./об.) с получением указанного в заголовке соединения (2,33 г.) 1Н-ЯМР (CDCl3, 400 МГц) δ 4,77-4,82 (м, 1Н), 3,60-3,74 (м, 1Н), 3,30-3,55 (м, 6Н), 3,05-3,28 (м, 1Н), 2,10-2,44 (м, 4Н), 1,68-1,86 (м, 4Н), 1,41-1,54 (м, 9Н)
[0362] Стадия 2: (S)-1-(2-((S)-3-аминогшрролидин-1-ил)ацетил)пирролидин-2-карбонитрил трифторацетат
[0363] Трет-бутил (S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтип)пирролидин-3-ил)карбамат (2,6 г, 8,06 ммоль), приготовленный на стадии 1, растворяли в дихлорметане (44,8 мл) и добавляли к ней трифторуксусную кислоту (по каплям) в избытке. Реакционную смесь перемешивали в течение ночи при комнатной температуре и концентрировали с получением указанного в заголовке соединения (1,3 г). 1Н-ЯМР (CD3OD, 400 МГц) δ 4,79-4,91 (м, 1Н), 4,41 (кв, 2Н), 4,09-4,21 (м, 1Н), 3,96-4,05 (м, 1Н), 3,54-3,81 (м, 5 Н), 2,55-2,67 (м, 1Н), 2,10-2,31 (м, 5Н)
[0364] Эталонный пример 26. (S)-1-(2-((R)-3-гидроксипирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[0365] (S)-1-(2-хлорацетил)пирролидин-2-карбонитрил (2 г, 11,6 ммоль), полученный в эталонном примере 1, растворяли в безводном ацетонитриле (23,2 мл). К полученному раствору добавляли (R)-3-пирролидинол (1,12 мл, 13,9 ммоль) и карбонат калия (4 г, 28,9 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции реакционную смесь фильтровали. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (этилацетат/н-гексан = 1/1, об./об.) с получением указанного в заголовке соединения (2,42 г). 1Н-ЯМР (CDCl3, 400 МГц) δ 4,74(д, 1Н), 4,35(с, 1Н), 3,65-3,63(м, 1Н), 3,51-3,33(м, 3Н), 3,11-2,96(м, 2Н), 2,88-2,80(м, 2Н), 2,55-2,47(м, 1Н), 2,35-2,16(м, 5 Н), 1,90-1,75(м, 1Н)
[0366] Эталонный пример 27. (S)-4,4-дифтор-1-(2-((R)-3-гидроксипирролидин-1-ил)-2-оксоэтил)пирролидин-2-карбонитрил
[0367] Указанное в заголовке соединение (2,52 г) получали таким же образом, как в эталонном примере 26, за исключением того, что вместо (S)-1-(2-хлорацетил)пирролидин-2-карбонитрила использовали (2S)-1-(2-хлорацетил)-4,4-дифторпирролидин-2-карбонитрил (1,4 г, 11,6 ммоль), полученный в эталонном примере 3. МС (ИЭР) m/z - 260,2 (М+Н)+
[0368] Эталонный пример 28. N-(пиперидин-4-ил)хинолин-4-амина гидрохлорид
[0369] Стадия 1: трет-бутил-4-(хинолин-4-иламино)пиперидин-1-карбоксилат
[0370] Трет-бутил-4-аминопиперидин-1-карбоксилат (500 мг, 2,68 ммоль) растворяли в безводном толуоле. К полученному раствору добавляют 4-бромхинолин (670,2 мг, 3,22 ммоль), карбонат цезия (1,31 г, 4,02 ммоль), трис(дибензилиденацетон)дииалладий(0) (245,8 мг, 0,27 ммоль), и (+/-)-2,2'-бис(дифенилфосфино)-1,1'-бинафталин (167,1 мг, 0,27 ммоль). Реакционную смесь нагревали в колбе с обратным холодильником и перемешивали при 100°С в течение ночи. После завершения реакции реакционную смесь охлаждали до комнатной температуры и затем добавляли воду для экстракции водного слоя этилацетатом. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (этилацетат/н-гексан=1/1, об./об.) с получением указанного в заголовке соединения (720 мг). 1Н-ЯМР (CDCl3, 400 МГц) δ 8,56 (д, 1Н), 7,99 (д, 1Н), 7,72 (д, 1Н), 7,63 (т, 1Н), 7,43 (т, 1Н), 6,47 (д, 1Н), 4,93 (д, 1Н), 4,12 (д, 2Н), 3,68 (с, 1Н), 3,00 (т, 1Н), 2,17-2,14 (м, 2Н), 1,53-1,44 (м, 12Н)
[0371] Стадия 2: Т^-(пиперидин-4-ил)хинолин-4-амина гидрохлорид
[0372] Трет-бутил 4-(хинолин-4-иламино)пиперидин-1 -карбоксилат (720 мг, 2,20 ммоль), полученный
на стадии 1, растворяли в дихлорметане (12,2 мл). К полученному раствору добавляли по каплям избыток 4,0 М соляной кислоты, растворенной в 1,4-диоксане. Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции полученное из нее твердое вещество фильтровали и высушивали с получением указанного в заголовке соединения (320 мг). Указанное в заголовке соединение использовали на следующей стадии без дополнительной очистки.
[0373] Эталонный пример 29.1М-(пиперидин-4-ил)хинолин-5-амина гидрохлорид
[0374] Стадия 1: трет-бутил-4-(хинолин-5-иламино)пиперидин-1 -карбоксилат
[0375] Указанное в заголовке соединение (500 мг) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 5-бромхинолин (500 мг, 2,50 ммоль). 1Н-ЯМР (CDCl3, 400 МГц) δ 8,87 (с, 1Н), 8,15 (д, 1Н), 7,58-7,49 (м, 2Н), 7,34-7,32 (м, 1Н), 6,69 (д, 1Н), 4,17 (д, 3Н), 3,64 (с, 1Н), 3,02 (т, 2Н), 2,18-2,15 (м, 2Н), 1,49-1,45 (м, 11Н)
[0376] Стадия 2: N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид
[0377] Указанное в заголовке соединение (390 мг) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[0378] Эталонный пример 30. N-(пиперидин-4-ил)фуро[3,2-с]пиридин-7-амина гидрохлорид
[0379] Указанное в заголовке соединение (324 мг) получали так же, как в эталонном примере 28, за исключением того, что на стадии 1 вместо 4-бромхинолина использовали 7-бромфуро[3,2-с]пиридин (495,1 мг, 2,50 ммоль). 1Н-ЯМР (CD3OD, 400 МГц) δ 8,6 (с, 1Н), 8,26 (с, 1Н), 8,17 (с, 1Н), 7,29 (с, 1Н), 4,00 (с, 1Н), 3,52 (д, 2Н), 3,24 (т, 2Н), 2,32 (д, 2Н), 1,91 (кв, 2Н)
[0380] Эталонный пример 31. 3-(пиперидин-4-илокси)хинолина гидрохлорид
[0381] Стадия 1: трет-бутил 4-(хинолин-3-илокси)пиперидин-1-карбоксилат
[0382] Трет-бутил-4-гидроксипиперидин-1-карбоксилат (200 мг, 1,0 ммоль) растворяли в
тетрагидрофуране (4,97 мл). К полученному раствору добавляли 3-хинолинол (144,25 мг, 1,0 ммоль) и трифенилфосфин (391 мг, 1,5 ммоль). Смесь охлаждали до 0°С, а затем по каплям медленно добавляли DIAD (диизопропилазодикарбоксилат) (0,29 мл, 1,5 ммоль) в течение 15 минут. Реакционную смесь перемешивали в течение 12 ч при комнатной температуре. После завершения реакции в реакционную смесь добавляли насыщенный раствор хлорида аммония и насыщенный раствор гидрокарбоната натрия. Водный слой реакционной смеси экстрагировали этилацетатом. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (дихлорметан/метанол = 10/1, об./об.) с получением указанного в заголовке соединения (280 мг.) МС (ИЭР) m/z - 330,2 (М + Н)+
[0383] Стадия 2: 3-(пиперидин-4-илокси) хинолин гидрохлорид
[0384] Трет-бутил 4-(хинолин-3-илокси)пиперидин-1-карбоксилат (280 мг, 0,85 ммоль) растворяли в дихлорметане (4,7 мл). К полученному раствору добавляли по каплям избыток 4,0 М соляной кислоты, растворенной в 1,4-диоксане. Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции полученное из нее твердое вещество фильтровали и высушивали с получением указанного в заголовке соединения (47 мг). Указанное в заголовке соединение использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 230,1 (М+Н)+
[0385] Эталонный пример 32. 4-(пиперидин-4-илокси)хинолина гидрохлорид
[0386] Указанное в заголовке соединение (100 мг) получали таким же образом, как в примере 31, за исключением того, что на стадии 1 вместо 3-хинолинола использовали 4-хинолинол (144,25 мг, 1,0 ммоль). МС (ИЭР) m/z - 230,1 (М+Н)+
[0387] Эталонный пример 33. 5-(пиперидин-4-илокси)хинолина гидрохлорид
[0388] Указанное в заголовке соединение (60 мг) получали таким же образом, как в примере 31, за исключением того, что на стадии 1 вместо 3-хинолинола использовали 5-хинолинол (144,25 мг, 1,0 ммоль). Указанное в заголовке соединение использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 230,1 (М+Н)+
[0389] Эталонный пример 34. 6-(пиперидин-4-илокси)хинолина гидрохлорид
[0390] Указанное в заголовке соединение (40 мг) получали таким же образом, как в примере 31, за исключением того, что на стадии 1 вместо 3-хинолинола использовали 6-хинолинол (144,25 мг, 1,0 ммоль). Указанное в заголовке соединение использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 230,1 (М+Н)+
[0391] Эталонный пример 35. 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид
[0392] Указанное в заголовке соединение (81,8 мг) получали таким же образом, как в примере 28, за исключением того, что вместо 4-бромхинолина на стадии 1 использовали 5-бром-3-метилхинолин (554,4 мг, 2,50 ммоль). Указанное в заголовке соединение использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 242,3 (М+Н)+
[0393] Эталонный пример 36. 6-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид
[0394] Указанное в заголовке соединение (40,2 мг) получали таким же образом, как в примере 28, за исключением того, что вместо 4-бромхинолина на стадии 1 использовали 5-бром-6-метилхинолин (554,4 мг, 2,50 ммоль). Указанное в заголовке соединение использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 242,3 (М+Н)+
[0395] Эталонный пример 37. 7-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид
[0396] Указанное в заголовке соединение (251 мг) получали таким же образом, как в примере 28, за исключением того, что вместо 4-бромхинолина на стадии 1 использовали 5-бром-7-фторхинолин (564 мг, 2,50 ммоль). Указанное в заголовке соединение использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 246,3 (М+Н)+
[0397] Эталонный пример 38. 7-метокси-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид
[0398] Указанное в заголовке соединение (106 мг) получали таким же образом, как в примере 28, за исключением того, что вместо 4-бромхинолина на стадии 1 использовали 5-бром-7-метоксихинолин (594 мг, 2,50 ммоль). Указанное в заголовке соединение использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 258,3 (М+Н)+
[0399] Эталонный пример 39. 8-метокси-г-Т-(пиперидин-4-ил)хинолин-5-амина гидрохлорид
[0400] Указанное в заголовке соединение (27 мг) получали таким же образом, как в примере 28, за исключением того, что вместо 4-бромхинолина на стадии 1 использовали 5-бром-8-метоксихинолин (594 мг, 2,50 ммоль). Указанное в заголовке соединение использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 258,3 (М+Н)+
[0401] Эталонный пример 40. 6-фтор-4-(пиперидин-4-илокси)хинолина гидрохлорид
[0402] Указанное в заголовке соединение (214 мг) получали таким же образом, как в примере 31, за исключением того, что вместо 3-хинолинола на стадии 1 использовали 6-фторхинолин-4-ол (202,6 мг, 1,2 ммоль). Указанное в заголовке соединение использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 246,3 (М+Н)+
[0403] Эталонный пример 41. 6-хлор-4-(пиперидин-4-илокси)хинолина гидрохлорид
[0404] Указанное в заголовке соединение (197 мг) получали таким же образом, как в примере 31, за исключением того, что вместо 3-хинолинола на стадии 1 использовали 6-хлорхинолин-4-ол (223,1 мг, 1,2 ммоль). Указанное в заголовке соединение использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 262,8 (М+Н)+
[0405] Эталонный пример 42. 6-метокси-4-(пиперидин-4-илокси)хинолина гидрохлорид
[0406] Указанное в заголовке соединение (108,6 мг) получали таким же образом, как в примере 31, за исключением того, что на стадии 1 вместо 3-хинолинола использовали 6-метоксихинолин-4-ол (217,6 мг, 1,2 ммоль). Указанное в заголовке соединение использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 258,3 (М+Н)+
[0407] Эталонный пример 43. 7-метокси-4-(пиперидин-4-илокси)хинолина гидрохлорид
[0408] Указанное в заголовке соединение (39,2 мг) получали таким же образом, как в примере 31, за исключением того, что на стадии 1 вместо 3-хинолинола использовали 7-метоксихинолин-4-ол (217,6 мг, 1,2 ммоль). Указанное в заголовке соединение использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 258,3 (М+Н)+
[0409] Эталонный пример 44. 6,7-диметокси-4-(пиперидин-4-илокси)хинолина гидрохлорид
[0410] Указанное в заголовке соединение (24,7 мг) получали таким же образом, как в примере 31, за исключением того, что вместо 3-хинолинола на стадии 1 использовали 6,7-диметоксихинолин-4-ол (254,9 мг, 1,2 ммоль). Указанное в заголовке соединение использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 288,3 (М+Н)+
[0411] Эталонный пример 45. (S)-6-фтор-N-(пирролидин-3-ил)бензофуран-3-карбоксамида гидрохлорида
[0412] Стадия 1: трет-бутил (S)-3-(6-фторбензофуран-3-карбоксамидо)пирролидин-1-карбоксилат
[0413] Трет-бутил (S)-3-аминопирролидин-1-карбоксилат (500 мг, 2,68 ммоль) растворяли в диметилформамиде (5,4 мл). К полученному раствору добавляли 6-фторбензофуран-3-карбоновую кислоту (725,4 мг, 4,02 ммоль), HATU (O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилурониягексафторфосфат) (1541,4 мг, 4,05 ммоль) идиизопропилэтиламин(4,67 мл, 26,8 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции к реакционной смеси добавляли воду. Водный слой реакционной смеси экстрагировали этилацетатом. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (гексан / этилацетат = 1/4, об./об.) с получением указанного в заголовке соединения (766 мг). 1Н-ЯМР (CDCl3, 400 МГц) δ 8,17 (с, 1Н), 7,95 (с, 1Н), 7,22 (д, 1Н), 7,10 (т, 1Н), 6,73-6,52 (м, 1Н), 4,67 (с, 1Н), 3,70 (д, 1Н), 3,47 (д, 2Н), 3,32 (с, 1Н), 2,23 (с, 1Н), 2,00 (д, 1Н), 1,46 (с, 9Н)
[0414] Стадия 2: (S)-6-фтор-N-(пирролидин-3-ил)бензофуран-3-карбоксамида гидрохлорид
[0415] Трет-бутил (S)-3-(6-фторбензофуран-3-карбоксамидо)пирролидин-1-карбоксилат (280 мг, 0,85 ммоль) растворяли в дихлорметане (4,7 мл), а затем туда же добавляли (по каплям) в избытке 4,0 М соляную кислоту, растворенную в 1,4-диоксане. Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции полученное из нее твердое вещество фильтровали и высушивали с получением указанного в заголовке соединения (47 мг). Указанное в заголовке соединение использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 249,2 (М+Н)+
[0416] Эталонный пример 46. (S)-6-метокси-N-(пирролидин-3-ил)бензофуран-3-карбоксамида гидрохлорида
[0417] Стадия 1: трет-бутил (S)-3-(6-метоксибензофуран-3-карбоксамидо)пирролидин-1-карбоксилат
[0418] Указанное в заголовке соединение (399,3 мг, 41,3%) получали таким же образом, как и на стадии 1 эталонного примера 45, за исключением того, что вместо 6-фторбензофуран-3-карбоновой кислоты использовали 6-метоксибензофуран-3-карбоновую кислоту (772,5 мг, 4,02 ммоль). 1Н ЯМР (CDCl3, 400 МГц) δ 8,06 (с, 1Н), 7,78 (д, 1Н), 7,03 (с, 1Н), 6,97 (д, 1Н), 4,68 (с, 1Н), 3,86 (с, 3Н), 3,72 (с, 1Н), 3,51-3,32 (м, 3Н), 2,26-2,25 (м, 1Н), 1,98-1,83 (м, 2Н), 1,47 (с, 9Н).
[0419] Стадия 2: (S)-6-метокси-N-(пирролидин-3-ил)бензофуран-3-карбоксамида гидрохлорид
[0420] Указанное в заголовке соединение (295,9 мг, 90,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки. 1Н ЯМР (MeOD4, 400 МГц) δ 8,35 (с, 1Н), 7,90 (с, 1Н), 7,14 (с, 1Н), 697, (д, 1Н), 4,63-4,62 (м, 1Н), 3,85 (с, 3Н), 3,61-3,58 (м, 2Н), 3,43-3,41 (м, 2Н), 2,45-2,40 (м, 1Н), 2,23-2,22 (м, 1Н).
[0421] Эталонный пример 47. (R)-N-метил-N-(пирролидин-3-ил)хинолин-2-амина гидрохлорид
[0422] Стадия 1: трет-бутил-(R)-3-(метил(хинолин-2-ил)амино)пирролидин-1-карбоксилат
[0423] (R)-трет-бутил 3-(метиламино)пирролидин-1-карбоксилат (250,0 мг, 1,25 ммоль) растворяли в безводном толуоле. К полученному раствору добавляли 2-бромхинолин (259,7 мг, 1,25 ммоль), карбонат цезия (488,1 мг, 1,50 ммоль), трис(дибензилиденацетон)дипалладий (0) (114,3 мг, 0,13 ммоль) и (+/-)-2,2'-бис(дифенилфоспино)-1,1'-бинафталин (93,3 мг, 0,15 ммоль). Реакционную смесь нагревали в колбе с обратным холодильником и перемешивали при 100°С в течение ночи. После завершения реакции реакционную смесь охлаждали до комнатной температуры и затем добавляли воду для экстракции водного слоя этилацетатом. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (этилацетат / н-гексан = 1/1, об./об.) с получением указанного в заголовке соединения (56,4 мг, 13,8%). МС (ИЭР) m/z - 328,2 (М+Н)+
[0424] Стадия 2: (R)-N-метил-N-(пирролидин-3-ил)хинолин-2-амина гидрохлорид
[0425] Указанное в заголовке соединение (25,5 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0426] Эталонный пример 48. (R)-N-метил-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид
[0427] Стадия 1: трет-бутил-(R)-3-(метил (хинолин-3-ил)амино)пирролидин-1-карбоксилат
[0428] Указанное в заголовке соединение (220,4 мг, 53,9%) получали таким же образом, как и на стадии 1 эталонного примера 47, за исключением того, что вместо 2-бромхинолина использовали 3-бромхинолин (259,7 мг, 1,25 ммоль). МС (ИЭР) m/z - 328,2 (М+Н)+
[0429] Стадия 2: (R)-N-метил-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид
[0430] Указанное в заголовке соединение (168,8 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0431] Эталонный пример 49. (R)-N-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0432] Стадия 1: трет-бутил-(R)-3-(метил(хинолин-5-ил)амино)пирролидин-1-карбоксилат
[0433] Указанное в заголовке соединение (109,4 мг, 26,8%) получали таким же образом, как на стадии 1 эталонного примера 47, за исключением того, что вместо 2-бромхинолина использовали 5-бромхинолин (259,7 мг, 1,25 ммоль). МС (ИЭР) m/z - 328,1 (М+Н)+
[0434] Стадия 2: (R)-N-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0435] Указанное в заголовке соединение (88,1 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0436] Эталонный пример 50. (R)-N-метил-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид
[0437] Стадия 1: трет-бутил (R)-3-(метил(хинолин-6-ил)амино)пирролидин-1-карбоксилат
[0438] Указанное в заголовке соединение (73,9 мг, 18,1%) получали таким же образом, как и на стадии 1 эталонного примера 47, за исключением того, что вместо 2-бромхинолина использовали 6-бромхинолин (259,7 мг, 1,25 ммоль). МС (ИЭР) m/z - 328,3 (М+Н)+
[0439] Стадия 2: (R)-N-метил-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид
[0440] Указанное в заголовке соединение (59,5 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0441] Эталонный пример 51. (R)-N-метил-N-(пирролидин-3-ил)хинолин-7-амина гидрохлорид
[0442] Стадия 1: трет-бутил-(R)-3-(метил(хинолин-7-ил)амино)пирролидин-1-карбоксилат
[0443] Указанное в заголовке соединение (131,9 мг, 32,3%) получали таким же образом, как на стадии 1 эталонного примера 47, за исключением того, что вместо 2-бромхинолина использовали 7-бромхинолин (259,7 мг, 1,25 ммоль). МС (ИЭР) m/z - 358,2 (М+Н)+
[0444] Стадия 2: (R)-N-метил-N-(пирролидин-3-ил)хинолин-7-амина гидрохлорид
[0445] Указанное в заголовке соединение (106,3 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0446] Эталонный пример 52. (S)-N-метил-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид
[0447] Стадия 1: трет-бутил (S)-3-((метил(хинолин-3-ил)амино)пирролидин-1-карбоксилат
[0448] (S)-трет-бутил 3-(метиламино)пирролидин-1-карбоксилат (250,0 мг, 1,25 ммоль) растворяли в безводном толуоле. К полученному раствору добавляли 3-бромхинолин (259,7 мг, 1,25 ммоль), карбонат цезия (488,1 мг, 1,50 ммоль), трис(дибензилиденацетон)дипалладий (0) (114,3 мг, 0,13 ммоль) и (+/-)-2,2'-бис(дифенилфоспино)-1,1'-бинафталин (93,3 мг, 0,15 ммоль). Реакционную смесь нагревали в колбе с обратным холодильником и перемешивали при 100°С в течение ночи. После завершения реакции реакционную смесь охлаждали до комнатной температуры и затем добавляли воду для экстракции водного слоя этилацетатом. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (этилацетат / н-гексан = 1/1, об./об.) с получением указанного в заголовке соединения (252,5 мг, 61,8%). МС (ИЭР) m/z - 328,3 (М+Н)+
[0449] Стадия 2: (S)-N-метил-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид
[0450] Указанное в заголовке соединение (203,4 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0451] Эталонный пример 53. (S)-N-метил-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид
[0452] Стадия 1: трет-бутил (S)-3-((метил (хинолин-4-ил)амино)пирролидин-1-карбоксилат
[0453] Указанное в заголовке соединение (74,2 мг, 18,2%) получали таким же образом, как и на стадии 1 эталонного примера 52, за исключением того, что вместо 3-бромхинолина использовали 4-бромхинолин (259,7 мг, 1,25 ммоль). МС (ИЭР) m/z - 328,3 (М+Н)+
[0454] Стадия 2: (S)-N-метил-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид
[0455] Указанное в заголовке соединение (59,8 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0456] Эталонный пример 54. (S)-N-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0457] Стадия 1: трет-бутил (S)-3-((метил(хинолин-5-ил)амино)пирролидин-1-карбоксилат
[0458] Указанное в заголовке соединение (124,2 мг, 30,4%) получали таким же образом, как и на стадии 1 эталонного примера 52, за исключением того, что вместо 3-бромхинолина использовали 5-бромхинолин (259,7 мг, 1,25 ммоль). МС (ИЭР) m/z - 328,2 (М + H)+
[0459] Стадия 2: (S)-N-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0460] Указанное в заголовке соединение (100,1 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0461] Эталонный пример 55. (S)-N-метил-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид
[0462] Стадия 1: трет-бутил (S)-3-((метил (хинолин-6-ил)амино)пирролидин-1 -карбоксилат
[0463] Указанное в заголовке соединение (120,5 мг, 29,5%) получали таким же образом, как и на стадии 1 эталонного примера 52, за исключением того, что вместо 3-бромхинолина использовали 6-бромхинолин (259,7 мг, 1,25 ммоль). МС (ИЭР) m/z - 328,3 (М+H)+
[0464] Стадия 2: (S)-N-метил-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид
[0465] Указанное в заголовке соединение (97,1 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0466] Эталонный пример 56. (S)-N-метил-N-(пирролидин-3-ил)хинолин-7-амина гидрохлорид
[0467] Стадия 1: трет-бутил (S)-3-((метил(хинолин-7-ил)амино)пирролидин-1-карбоксилат
[0468] Указанное в заголовке соединение (260,0 мг, 63,6%) получали таким же образом, как и на стадии 1 эталонного примера 52, за исключением того, что вместо 3-бромхинолина использовали 7-бромхинолин (259,7 мг, 1,25 ммоль). МС (ИЭР) m/z - 328,2 (М+Н)+
[0469] Стадия 2: (S)-N-метил-N-(пирролидин-3-ил)хинолин-7-амина гидрохлорид
[0470] Указанное в заголовке соединение (209,5 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0471] Эталонный пример 57. (S)-N-метил-N-(пирролидин-3-ил)изохинолин-4-амина гидрохлорид
[0472] Стадия 1: трет-бутил (S)-3-((изохинолин-4-ил(метил)амино)пирролидин-1-карбоксилат
[0473] Указанное в заголовке соединение (69,0 мг, 16,9%) получали таким же образом, как и на стадии 1 эталонного примера 52, за исключением того, что вместо 3-бромхинолина использовали 4-бромизохинолин (259,7 мг, 1,25 ммоль). МС (ИЭР) m/z - 328,3 (М+Н)+
[0474] Стадия 2: (S)-N-метил-N-(пирролидин-3-ил)изохинолин-4-амина гидрохлорид
[0475] Указанное в заголовке соединение (55,6 мг, 100,0%) получали таким же образом, как на стадии 2 эталонного примера 21, и использовали на следующей стадии без дополнительной очистки.
[0476] Эталонный пример 58. (S)-N-метил-N-(пирролидин-3-ил)изохинолин-5-амина гидрохлорид
[0477] Стадия 1: трет-бутил (S)-3-((изохинолин-5-ил (метил)амино)пирролидин-1-карбоксилат
[0478] Указанное в заголовке соединение (87,8 мг, 21,5%) получали таким же образом, как и на стадии 1 эталонного примера 52, за исключением того, что вместо 3-бромхинолина использовали 5-бромизохинолин (259,7 мг, 1,25 ммоль). МС (ИЭР) m/z - 328,3 (М+Н)+
[0479] Стадия 2: (S)-N-метил-N-(пирролвдин-3-ил)изохинолин-5-амина гидрохлорид
[0480] Указанное в заголовке соединение (70,7 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0481] Эталонный пример 59. (S)-N,4-диметил-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид
[0482] Стадия 1: трет-бутил (S)-3-(метил(4-метилхинолин-3-ил)амино)пирролидин-1-карбоксилат
[0483] Указанное в заголовке соединение (60,4 мг, 14,2%) получали таким же образом, как и на стадии 1 эталонного примера 52, за исключением того, что вместо 3-бромхинолина использовали 3-бром-4-метилхинолин (277,2 мг, 1,25 ммоль). МС (ИЭР) m/z - 342,2 (М+Н)+
[0484] Стадия 2: (S)-N,4-диметил-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид
[0485] Указанное в заголовке соединение (49,1 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0486] Эталонный пример 60. (S)-N,6-диметил-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид
[0487] Стадия 1: трет-бутил (S)-3-(метил(6-метилхинолин-3-ил)амино)пирролидин-1-карбоксилат
[0488] Указанное в заголовке соединение (244,0 мг, 57,3%) получали таким же образом, как и на стадии 1 эталонного примера 52, за исключением того, что вместо 3-бромхинолина использовали 3-бром-6-метилхинолин (277,2 мг, 1,25 ммоль). МС (ИЭР) m/z - 342,2 (М+Н)+
[0489] Стадия 2: (S)-N,6-диметил-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид
[0490] Указанное в заголовке соединение (198,5 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0491] Эталонный пример 61. (S)-6-фтор-N-метил-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид
[0492] Стадия 1: трет-бутил (S)-3-((6-фторхинолин-3-ил)(метил)амино)пирролидин-1-карбоксилат
[0493] Указанное в заголовке соединение (314,7 мг, 73,0%) получали таким же образом, как и на стадии 1 эталонного примера 52, за исключением того, что вместо 3-бромхинолина использовали 3-бром-6-фторхинолин (282,2 мг, 1,25 ммоль). МС (ИЭР) m/z - 346,3 (М+Н)+
[0494] Стадия 2: (S)-6-фтор-N-метил-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид
[0495] Указанное в заголовке соединение (256,7 мг, 100,0%) получали таким же образом, как на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0496] Эталонный пример 62. (S)-6-метокси-N-метил-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид
[0497] Стадия 1: трет-бутил (S)-3-((6-метоксихинолин-3-ил)(метил)амино)пирролидин-1-карбоксилат
[0498] Указанное в заголовке соединение (264,3 мг, 59,2%) получали таким же образом, как и на стадии 1 эталонного примера 52, за исключением того, что вместо 3-бромхинолина использовали 3-бром-6-метоксихинолин (297,2 мг, 1,25 ммоль). МС (ИЭР) m/z - 358,2 (М+Н)+
[0499] Стадия 2: (S)-6-метокси-N-метил-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид
[0500] Указанное в заголовке соединение (217,2 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0501] Эталонный пример 63. (S)-7-метокси-N-метил-N-(пирролвдин-3-ил)хинолин-3-амина гидрохлорид
[0502] Стадия 1: трет-бутил (S)-3-((7-метоксихинолин-3-ил)(метил)амино)пирролидин-1-карбоксилат
[0503] Указанное в заголовке соединение (177,0 мг, 39,7%) получали таким же образом, как и на стадии 1 эталонного примера 52, за исключением того, что вместо 3-бромхинолина использовали 3-бром-7-метоксихинолин (297,2 мг, 1,25 ммоль). МС (ИЭР) m/z - 358,2 (М+Н)+
[0504] Стадия 2: (S)-7-метокси-N-метил-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид
[0505] Указанное в заголовке соединение (145,5 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0506] Эталонный пример 64. (S)-8-метокси-N-метил-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид
[0507] Стадия 1: трет-бутил (S)-3-((8-метоксихинолин-3-ил)(метил)амино)пирролидин-1-карбоксилат
[0508] Указанное в заголовке соединение (359,9 мг, 80,7%) получали таким же образом, как и на стадии 1 эталонного примера 52, за исключением того, что вместо 3-бромхинолина использовали 3-бром-8-метоксихинолин (297,2 мг, 1,25 ммоль). МС (ИЭР) m/z - 358,2 (М+Н)+
[0509] Стадия 2: (S)-8-метокси-N-метил-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид
[0510] Указанное в заголовке соединение (295,8 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0511] Эталонный пример 65. (S)-N,3-диметил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0512] Стадия 1: трет-бутил (S)-3-((метил (3-метилхинолин-5-ил)амино)пирролидин-1-карбоксилат
[0513] Указанное в заголовке соединение (115,1 мг, 27,0%) получали таким же образом, как и на стадии 1 эталонного примера 52, за исключением того, что вместо 3-бромхинолина использовали 5-бром-3-метилхинолин (277,2 мг, 1,25 ммоль). МС (ИЭР) m/z - 342,2 (М+Н)+
[0514] Стадия 2: (S)-N,3-диметил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0515] Указанное в заголовке соединение (93,6 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0516] Эталонный пример 66. (S)-3-фтор-N-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0517] Стадия 1: трет-бутил (S)-3-((3-фторхинолин-5-ил)(метил)амино)пирролидин-1-карбоксилат
[0518] Указанное в заголовке соединение (286,6 мг, 66,5%) получали таким же образом, как и на стадии 1 эталонного примера 52, за исключением того, что вместо 3-бромхинолина использовали 5-бром-3-фторхинолин (282,2 мг, 1,25 ммоль). МС (ИЭР) m/z - 346,2 (М+Н)+
[0519] Стадия 2: (S)-3-фтор-N-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0520] Указанное в заголовке соединение (233,8 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0521] Эталонный пример 67. (S)-7-фтор-N-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0522] Стадия 1: трет-бутил (S)-3-((7-фторхинолин-5-ил)(метил)амино)пирролидин-1-карбоксилат
[0523] Указанное в заголовке соединение (223,7 мг, 51,9%) получали таким же образом, как и на стадии 1 эталонного примера 52, за исключением того, что вместо 3-бромхинолина использовали 5-бром-7-фторхинолин (282,2 мг, 1,25 ммоль). МС (ИЭР) m/z - 346,2 (М+Н)+
[0524] Стадия 2: (S)-7-фтор-N-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0525] Указанное в заголовке соединение (182,5 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0526] Эталонный пример 68. (S)-8-фтор-N-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0527] Стадия 1: трет-бутил (S)-3-((8-фторхинолин-5-ил)(метил)амино)пирролидин-1-карбоксилат
[0528] Указанное в заголовке соединение (209,9 мг, 48,7%) получали таким же образом, как и на стадии 1 эталонного примера 52, за исключением того, что вместо 3-бромхинолина использовали 5-бром-8-фторхинолин (282,2 мг, 1,25 ммоль). МС (ИЭР) m/z - 346,2 (М+Н)+
[0529] Стадия 2: (S)-8-фтор-N-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0530] Указанное в заголовке соединение (171,2 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0531] Эталонный пример 69. (S)-N-метил-N-(пирролидин-3-ил)-8-(трифторметил)хинолин-5-амина гидрохлорид
[0532] Стадия 1: трет-бутил (S)-3-((метил(8-(трифторметил)хинолин-5-ил)амино) пирролидин-1-карбоксилат
[0533] Указанное в заголовке соединение (416,4 мг, 84,4%) получали таким же образом, как и на стадии 1 эталонного примера 52, за исключением того, что вместо 3-бромхинолина использовали 5-бром-8-(трифторметил)хинолин (344,6 мг, 1,25 ммоль). МС (ИЭР) m/z - 396,2 (М + Н)+
[0534] Стадия 2: (S)-N-метил-N-(пирролидин-3-ил)-8-(трифторметил)хинолин-5-амина гидрохлорид
[0535] Указанное в заголовке соединение (349,4 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0536] Эталонный пример 70. (S)-N-метил-N-(пирролвдин-3-ил)-8-(трифторметокси)хинолин-5-амина гидрохлорид
[0537] Стадия 1: трет-бутил (S)-3-((метил(8-(трифторметокси)хинолин-5-ил)амино)пирролидин-1-карбоксилат
[0538] Указанное в заголовке соединение (432,5 мг, 84,2%) получали таким же образом, как и на стадии 1 эталонного примера 52, за исключением того, что вместо 3-бромхинолина использовали 5-бром-8-трифторметоксихинолин (364,6 мг, 1,25 ммоль). МС (ИЭР) m/z - 412,2 (М+Н)+
[0539] Стадия 2: (S)-N-метил-N-(пирролидин-3-ил)-8-(трифторметокси)хинолин-5-амина гидрохлорид
[0540] Указанное в заголовке соединение (365,6 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0541] Эталонный пример 71. (R)-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0542] Стадия 1: трет-бутил-(R)-3-(хинолин-5-иламино)пирролидин-1-карбоксилат
[0543] Указанное в заголовке соединение (589,6 мг, 70,0%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 5-бромхинолин (558,5 мг, 2,68 ммоль). МС (ИЭР) m/z - 314,2 (М+Н)+
[0544] Стадия 2: (R)-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0545] Указанное в заголовке соединение (466,5 мг, 86,6%) получали таким же образом, как и на стадии 2 эталонного примера 5. МС (ИЭР) m/z - 214,2 (М+Н)+
[0546] Эталонный пример 72. (R)-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид
[0547] Стадия 1: трет-бутил-(R)-3-(хинолин-6-иламино)пирролидин-1-карбоксилат
[0548] Указанное в заголовке соединение (389,3 мг, 46,3%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 6-бромхинолин (558,5 мг, 2,68 ммоль). МС (ИЭР) m/z - 314,2 (М+Н)+
[0549] Стадия 2: (R)-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид
[0550] Указанное в заголовке соединение (298,1 мг, 94,1%) получали таким же образом, как и на стадии 2 эталонного примера 5. МС (ИЭР) m/z - 214,2 (М+Н)+
[0551] Эталонный пример 73. (R)-N-(пирролидин-3-ил)хинолин-7-амина гидрохлорид
[0552] Стадия 1: трет-бутил-(R)-3-(хинолин-7-иламино)пирролидин-1-карбоксилат
[0553] Указанное в заголовке соединение (356,5 мг, 42,4%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 7-бромхинолин (558,5 мг, 2,68 ммоль). МС (ИЭР) m/z - 314,2 (М + Н)+
[0554] Стадия 2: (R)-N-(пирролидин-3-ил)хинолин-7-амина гидрохлорид
[0555] Указанное в заголовке соединение (261,9 мг, 82,6%) получали таким же образом, как и на стадии 2 эталонного примера 5. МС (ИЭР) m/z - 214,2 (М+Н)+
[0556] Эталонный пример 74. (R)-N-(пирролидин-3-ил)хинолин-8-амина гидрохлорид
[0557] Стадия 1: трет-бутил-(R)-3-(хинолин-8-иламино)пирролидин-1-карбоксилат
[0558] Указанное в заголовке соединение (692,6 мг, 82,3%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 8-бромхинолин (558,5 мг, 2,68 ммоль). МС (ИЭР) m/z - 314,2 (М+Н)+
[0559] Стадия 2: (R)-N-(пирролидин-3-ил)хинолин-8-амина гидрохлорид
[0560] Указанное в заголовке соединение (589,4 мг, 93,1%) получали таким же образом, как и на стадии 2 эталонного примера 5. МС (ИЭР) m/z - 214,2 (М+Н)+
[0561] Эталонный пример 75. (R)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид
[0562] Стадия 1: трет-бутил-(R)-3-(хинолин-4-иламино)пирролидин-1-карбоксилат
[0563] Указанное в заголовке соединение (490,9 мг, 58,4%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 4-бромхинолин (558,5 мг, 2,68 ммоль). МС (ИЭР) m/z - 314,2 (М+Н)+
[0564] Стадия 2: (R)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид
[0565] Указанное в заголовке соединение (195,4 мг, 43,6%) получали таким же образом, как и на стадии 2 эталонного примера 5. МС (ИЭР) m/z - 214,2 (М+Н)+
[0566] Эталонный пример 76. (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорид
[0567] Стадия 1: трет-бутил (R)-3-((1,8-нафтиридин-3-ил)амино)пирролидин-1-карбоксилат
[0568] Указанное в заголовке соединение (278,2 мг, 65,9%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 3-бром-1,8-нафтиридин (280,6 мг, 1,34 ммоль). МС (ИЭР) m/z - 315,1 (М+Н)+
[0569] Стадия 2: (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорид
[0570] Указанное в заголовке соединение (254,2 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0571] Эталонный пример 77. (R)-7-хлор-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорид
[0572] Стадия 1: трет-бутил (R)-3-((7-хлор-1,8-нафтиридин-3-ил)амино)пирролидин-1-карбоксилат
[0573] Указанное в заголовке соединение (174,8 мг, 37,3%) получали таким же образом, как на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 6-бром-2-хлор-1,8-нафтиридин (326,8 мг, 1,34 ммоль). МС (ИЭР) m/z - 349,1 (М + Н)+
[0574] Стадия 2: (R)-7-хлор-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорид
[0575] Указанное в заголовке соединение (161,2 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0576] Эталонный пример 78. (R)-6-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0577] Стадия 1: трет-бутил (R)-3-((6-фторхинолин-5-ил)амино)пирролидин-1-карбоксилат
[0578] Указанное в заголовке соединение (187,1 мг, 42,1%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 5-бром-6-фторхинолин (303,4 мг, 1,34 ммоль). МС (ИЭР) m/z - 332,2 (М+Н)+
[0579] Стадия 2: (R)-6-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0580] Указанное в заголовке соединение (171,9 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0581] Эталонный пример 79. (R)-7-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0582] Стадия 1: трет-бутил (R)-3-((7-фторхинолин-5-ил)амино)пирролидин-1-карбоксилат
[0583] Указанное в заголовке соединение (129,4 мг, 29,1%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 5-бром-7-фторхинолин (303,4 мг, 1,34 ммоль). МС (ИЭР) m/z - 332,2 (М+Н)+
[0584] Стадия 2: (R)-7-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0585] Указанное в заголовке соединение (118,6 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0586] Эталонный пример 80. (R)-8-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0587] Стадия 1: трет-бутил (R)-3-((8-фторхинолин-5-ил)амино)пирролидин-1-карбоксилат
[0588] Указанное в заголовке соединение (330,4 мг, 74,3%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 5-бром-8-фторхинолин (303,4 мг, 1,34 ммоль). МС (ИЭР) m/z - 332,2 (М+Н)+
[0589] Стадия 2: (R)-8-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0590] Указанное в заголовке соединение (303,3 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0591] Эталонный пример 81. (R)-6-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0592] Стадия 1: трет-бутил (R)-3-((6-метоксихинолин-5-ил)амино)пирролидин-1-карбоксилат
[0593] Указанное в заголовке соединение (427,4 мг, 92,7%) получали таким же образом, как на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 5-бром-6-метоксихинолин (319,6 мг, 1,34 ммоль). МС (ИЭР) m/z - 344,2 (М + Н)+
[0594] Стадия 2: (R)-6-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0595] Указанное в заголовке соединение (393,7 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0596] Эталонный пример 82. (R)-7-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0597] Стадия 1: трет-бутил (R)-3-((7-метоксихинолин-5-ил)амино)пирролидин-1-карбоксилат
[0598] Указанное в заголовке соединение (460,9 мг, 100,0%) получали таким же образом, как на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 5-бром-7 метоксихинолин (319,6 мг, 1,34 ммоль). МС (ИЭР) m/z - 344,2 (М+Н)+
[0599] Стадия 2: (R)-7-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0600] Указанное в заголовке соединение (424,4 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0601] Эталонный пример 83. (R)-8-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0602] Стадия 1: трет-бутил (R)-3-((8-метоксихинолин-5-ил)амино)пирролидин-1-карбоксилат
[0603] Указанное в заголовке соединение (180,0 мг, 39,1%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 5-бром-8 метоксихинолин (319,6 мг, 1,34 ммоль). МС (ИЭР) m/z - 344,2 (М+Н)+
[0604] Стадия 2: (R)-8-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0605] Указанное в заголовке соединение (165,7 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0606] Эталонный пример 84. (R)-3-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0607] Стадия 1: трет-бутил (R)-3-((3-метилхинолин-5-ил)амино)пирролидин-1 -карбоксилат
[0608] Указанное в заголовке соединение (314,2 мг, 71,5%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 5-бром-3 метилхинолин (298,1 мг, 1,34 ммоль). МС (ИЭР) m/z - 328,2 (М+Н)+
[0609] Стадия 2: (R)-3-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0610] Указанное в заголовке соединение (288,2 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0611] Эталонный пример 85. (R)-6-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0612] Стадия 1: трет-бутил (R)-3-((6-метоксихинолин-5-ил)амино)пирролидин-1-карбоксилат
[0613] Указанное в заголовке соединение (419,0 мг, 95,3%) получали таким же образом, как на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 5-бром-6-метоксихинолин (298,1 мг, 1,34 ммоль). МС (ИЭР) m/z - 328,2 (М + Н)+
[0614] Стадия 2: (R)-6-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0615] Указанное в заголовке соединение (384,3 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0616] Эталонный пример 86. (R)-8-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0617] Стадия 1: трет-бутил (R)-3-((8-метилхинолин-5-ил)амино)пирролидин-1-карбоксилат
[0618] Указанное в заголовке соединение (290,5 мг, 66,1%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 5-бром-8-метилхинолин (298,1 мг, 1,34 ммоль). МС (ИЭР) m/z - 328,2 (М+Н)+
[0619] Стадия 2: (R)-8-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0620] Указанное в заголовке соединение (266,3 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0621] Эталонный пример 87. (R)-N-(пирролидин-3-ил)-7-(трифторметил)хинолин-5-амина гидрохлорид
[0622] Стадия 1: трет-бутил (R)-3-((7-(трифторметил)хинолин-5-ил)амино)пирролидин-1-карбоксилат
[0623] Указанное в заголовке соединение (424,1 мг, 82,8%) получали таким же образом, как на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 5-бром-7-(трифторметил)хинолин (370,5 мг, 1,34 ммоль). МС (ИЭР) m/z - 382,2 (М+Н)+
[0624] Стадия 2: (R)-N-(пирролидин-3-ил)-7-(трифторметил)хинолин-5-амина гидрохлорид
[0625] Указанное в заголовке соединение (393,9 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0626] Эталонный пример 88. (R)-N-(пирролидин-3-ил)-8-(трифторметил)хинолин-5-амина гидрохлорид
[0627] Стадия 1: трет-бутил (R)-3-((8-(трифторметил)хинолин-5-ил)амино)пирролидин-1-карбоксилат
[0628] Указанное в заголовке соединение (186,5 мг, 36,4%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 5-бром-8-(трифторметил)хинолин (370,5 мг, 1,34 ммоль). МС (ИЭР) m/z - 382,2 (М+Н)+
[0629] Стадия 2: (R)-N-(пирролидин-3-ил)-8-(трифторметил)хинолин-5-амина гидрохлорид
[0630] Указанное в заголовке соединение (173,2 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0631] Эталонный пример 89. (R)-3-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0632] Стадия 1: трет-бутил (R)-3-((3-фторхинолин-5-ил)амино)пирролидин-1-карбоксилат
[0633] Указанное в заголовке соединение (251,6 мг, 56,6%) получали таким же образом, как на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 5-бром-3-фторхинолин (303,4 мг, 1,34 ммоль). МС (ИЭР) m/z - 332,2 (М + Н)+
[0634] Стадия 2: (R)-3-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0635] Указанное в заголовке соединение (230,9 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0636] Эталонный пример 90. (R)-3-хлор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0637] Стадия 1: трет-бутил (R)-3-((3-хлорхинолин-5-ил)амино)пирролидин-1-карбоксилат
[0638] Указанное в заголовке соединение (320,1 мг, 68,6%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 5-бром-3-хлорхинолин (325,5 мг, 1,34 ммоль). МС (ИЭР) m/z - 348,2 (М+Н)+
[0639] Стадия 2: (R)-3-хлор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0640] Указанное в заголовке соединение (295,0 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0641] Эталонный пример 91. (R)-N-(пирролидин-3-ил)-8-(трифторметокси)хинолин-5-амина гидрохлорид
[0642] Стадия 1: трет-бутил (R)-3-((8-(трифторметокси)хинолин-5-ил)амино)пирролидин-1-карбоксилат
[0643] Указанное в заголовке соединение (470,2 мг, 88,2%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 5-бром-8-трифторметоксихинолин (392,0 мг, 1,34 ммоль). МС (ИЭР) m/z - 398,2 (М+Н)+
[0644] Стадия 2: (R)-N-(пирролидин-3-ил)-8-(трифторметокси)хинолин-5-амина гидрохлорид
[0645] Указанное в заголовке соединение (438,0 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0646] Эталонный пример 92. (R)-6-метил-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид
[0647] Стадия 1: трет-бутил (R)-3-((6-метилхинолин-4-ил)амино)пирролидин-1-карбоксилат
[0648] Указанное в заголовке соединение (47,1 мг, 10,7%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 4-бром-6-метилхинолин (298,1 мг, 1,34 ммоль). МС (ИЭР) m/z - 328,2 (М+Н)+
[0649] Стадия 2: (R)-6-метил-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид
[0650] Указанное в заголовке соединение (43,2 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0651] Эталонный пример 93. (R)-6-метокси-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид
[0652] Стадия 1: трет-бутил (R)-3-((6-метоксихинолин-4-ил)амино)пирролидин-1-карбоксилат
[0653] Указанное в заголовке соединение (326,8 мг, 70,9%) получали таким же образом, как на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 4-бром-6-метоксихинолин (319,6 мг, 1,34 ммоль). МС (ИЭР) m/z - 344,1 (М + Н)+
[0654] Стадия 2: (R)-6-метокси-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид
[0655] Указанное в заголовке соединение (301,1 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0656] Эталонный пример 94. (R)-8-хлор-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид
[0657] Стадия 1: трет-бутил (R)-3-((8-хлорхинолин-4-ил)амино)пирролидин-1-карбоксилат
[0658] Указанное в заголовке соединение (126,9 мг, 27,2%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 4-бром-8-хлорхинолин (325,5 мг, 1,34 ммоль). МС (ИЭР) m/z - 348,2 (М+Н)+
[0659] Стадия 2: (R)-8-хлор-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид
[0660] Указанное в заголовке соединение (117,0 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0661] Эталонный пример 95. (R)-8-метил-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид
[0662] Стадия 1: трет-бутил (R)-3-((8-метилхинолин-4-ил)амино)пирролидин-1-карбоксилат
[0663] Указанное в заголовке соединение (425,0 мг, 96,7%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 4-бром-8-метилхинолин (298,1 мг, 1,34 ммоль). МС (ИЭР) m/z - 328,2 (М+Н)+
[0664] Стадия 2: (R)-8-метил-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид
[0665] Указанное в заголовке соединение (406,2 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0666] Эталонный пример 96. (R)-6-фтор-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид
[0667] Стадия 1: трет-бутил (R)-3-((6-фторхинолин-4-ил)амино)пирролидин-1-карбоксилат
[0668] Указанное в заголовке соединение (367,0 мг, 82,7%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 4-бром-6-фторхинолин (303,4 мг, 1,34 ммоль). МС (ИЭР) m/z - 332,2 (М+Н)+
[0669] Стадия 2: (R)-6-фтор-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид
[0670] Указанное в заголовке соединение (337,7 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0671] Эталонный пример 97. (R)-6-хлор-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид
[0672] Стадия 1: трет-бутил (R)-3-((6-хлорхинолин-4-ил)амино)пирролидин-1-карбоксилат
[0673] Указанное в заголовке соединение (298,1 мг, 63,9%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 4-бром-6-хлорхинолин (325,5 мг, 1,34 ммоль). МС (ИЭР) m/z - 348,1 (М+Н)+
[0674] Стадия 2: (R)-6-хлор-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид
[0675] Указанное в заголовке соединение (274,8 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0676] Эталонный пример 98. (R)-7-метокси-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид
[0677] Стадия 1: трет-бутил (R)-3-((7-метоксихинолин-4-ил)амино)пирролидин-1-карбоксилат
[0678] Указанное в заголовке соединение (423,5 мг, 91,9%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 4-бром-7-метокси-хинолин (319,6 мг, 1,34 ммоль). МС (ИЭР) m/z - 344,2 (М+Н)+
[0679] Стадия 2: (R)-7-метокси-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид
[0680] Указанное в заголовке соединение (358,2 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0681] Эталонный пример 99. (R)-8-фтор-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид
[0682] Стадия 1: трет-бутил (R)-3-((8-фторхинолин-4-ил)амино)пирролидин-1-карбоксилат
[0683] Указанное в заголовке соединение (444,7 мг, 100,0%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 4-бром-8-фторхинолин (303,4 мг, 1,34 ммоль). МС (ИЭР) m/z - 332,2 (М+Н)+
[0684] Стадия 2: (R)-8-фтор-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид
[0685] Указанное в заголовке соединение (418,0 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0686] Эталонный пример 100. (R)-8-метокси-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид
[0687] Стадия 1: трет-бутил (R)-3-((8-метоксихинолин-4-ил)амино)пирролидин-1-карбоксилат
[0688] Указанное в заголовке соединение (348,5 мг, 75,6%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 4-бром-8-метоксихинолин (319,6 мг, 1,34 ммоль). МС (ИЭР) m/z - 344,2 (М+Н)+
[0689] Стадия 2: (R)-8-метокси-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид
[0690] Указанное в заголовке соединение (316,4 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0691] Эталонный пример 101. (R)-N-(пирролидин-3-ил)-8-(трифторметил)хинолин-4-амина гидрохлорид
[0692] Стадия 1: трет-бутил (R)-3-((8-(трифторметил)хинолин-4-ил)амино)пирролидин-1-карбоксилат
[0693] Указанное в заголовке соединение (511,8 мг, 100,0%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 4-бром-8(трифторметил)хинолин (370,5 мг, 1,34 ммоль). МС (ИЭР) m/z - 382,2 (М+Н)+
[0694] Стадия 2: (R)-N-(пирролидин-3-ил)-8-(трифторметил)хинолин-4-амина гидрохлорид
[0695] Указанное в заголовке соединение (499,4 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0696] Эталонный пример 102. (R)-3-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0697] Стадия 1: трет-бутил (R)-3-((3-метоксихинолин-5-ил)амино)пирролидин-1-карбоксилат
[0698] Указанное в заголовке соединение (662,7 мг, 71,9%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 5-бром-3-метоксихинолин (639,1 мг, 2,69 ммоль). МС (ИЭР) m/z - 344,2 (М+Н)+
[0699] Стадия 2: (R)-3-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0700] Указанное в заголовке соединение (610,3 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0701] Эталонный пример 103. (R)-2-хлор-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид
[0702] Стадия 1: трет-бутил (R)-3-((2-хлорхинолин-6-ил)амино)пирролидин-1-карбоксилат
[0703] Указанное в заголовке соединение (720,5 мг, 77,2%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 2-хлор-6-бромхинолин (651,0 мг, 2,69 ммоль). МС (ИЭР) m/z - 348,2 (М+Н)+
[0704] Стадия 2: (R)-2-хлор-N-(пирролидин-3-ип)хинолин-6-амина гидрохлорид
[0705] Указанное в заголовке соединение (618,5 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0706] Эталонный пример 104. (R)-N-(пирролидин-3-ил)-2-(трифторметил)хинолин-6-амина гидрохлорид
[0707] Стадия 1: трет-бутил (R)-3-((2-(трифторметил)хинолин-6-ил)амино)пирролидин-1-карбоксилат
[0708] Указанное в заголовке соединение (408,1 мг, 79,7%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 6-бром-2-(трифторметил)хинолин (370,5 мг, 1,34 ммоль). МС (ИЭР) m/z - 382,2 (М+Н)+
[0709] Стадия 2: (R)-N-(1 гирролидин-3-ил)-2-(трифторметил)хинолин-6-амина гидрохлорид
[0710] Указанное в заголовке соединение (379,0 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0711] Эталонный пример 105. (R)-3-метил-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид
[0712] Стадия 1: трет-бутил (R)-3-((3-метилхинолин-6-ил)амино)пирролидин-1-карбоксилат
[0713] Указанное в заголовке соединение (328,0 мг, 74,6%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 6-бром-3-метилхинолин (298,1 мг, 1,34 ммоль). МС (ИЭР) m/z - 328,2 (М+Н)+
[0714] Стадия 2: (R)-3-метил-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид
[0715] Указанное в заголовке соединение (300,8 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0716] Эталонный пример 106. (R)-4-метокси-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид
[0717] Стадия 1: трет-бутил (R)-3-((4-метоксихинолин-7-ил)амино)пирролидин-1-карбоксилат
[0718] Указанное в заголовке соединение (239,7 мг, 52,0%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 6-бром-4-метокси-хинолин (319,6 мг, 1,34 ммоль). МС (ИЭР) m/z - 344,2 (М+Н)+
[0719] Стадия 2: (R)-4-метокси-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид
[0720] Указанное в заголовке соединение (220,7 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0721] Эталонный пример 107. (R)-8-метил-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид
[0722] Стадия 1: трет-бутил (R)-3-((8-метилхинолин-6-ил)амино)пирролидин-1-карбоксилат
[0723] Указанное в заголовке соединение (258,6 мг, 58,8%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 6-бром-8-метилхинолин (298,1 мг, 1,34 ммоль). МС (ИЭР) m/z - 328,2 (М+Н)+
[0724] Стадия 2: (R)-8-метил-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид
[0725] Указанное в заголовке соединение (238,2 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0726] Эталонный пример 108. (R)-8-хлор-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид
[0727] Стадия 1: трет-бутил (R)-3-((8-хлорхинолин-6-ил)амино)пирролидин-1-карбоксилат
[0728] Указанное в заголовке соединение (311,9 мг, 66,8%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 6-бром-8-хлорхинолин (325,5 мг, 1,34 ммоль). МС (ИЭР) m/z - 348,1 (М+Н)+
[0729] Стадия 2: (R)-8-хлор-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид
[0730] Указанное в заголовке соединение (287,6 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0731] Эталонный пример 109. (R)-N-(пирролидин-3-ил)-8-(трифторметил)хинолин-6-амина гидрохлорид
[0732] Стадия 1: трет-бутил (R)-3-((8-(трифторметил)хинолин-6-ил)амино)пирролидин-1-карбоксилат
[0733] Указанное в заголовке соединение (424,5 мг, 82,9%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 6-бром-8-(трифторметил)хинолин (370,5 мг, 1,34 ммоль). МС (ИЭР) m/z - 382,1 (М+Н)+
[0734] Стадия 2: (R)-N-(пирролидин-3-ил)-8-(трифторметил)хинолин-6-амина гидрохлорид
[0735] Указанное в заголовке соединение (394,2 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0736] Эталонный пример 110. (R)-8-фтор-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид
[0737] Стадия 1: трет-бутил (R)-3-((8-фторхинолин-6-ил)амино)пирролидин-1-карбоксилат
[0738] Указанное в заголовке соединение (167,0 мг, 37,5%) получали таким же образом, как и на стадии 1 эталонного примера 17, за исключением того, что вместо 3-бромхинолина использовали 6-бром-8-фторхинолин (303,4 мг, 1,34 ммоль). МС (ИЭР) m/z - 332,2 (М+Н)+
[0739] Стадия 2: (R)-8-фтор-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид
[0740] Указанное в заголовке соединение (153,3 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0741] Эталонный пример 111. (S)-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид
[0742] Стадия 1: трет-бутил (S)-3-(хинолин-6-иламино)пирролидин-1-карбоксилат
[0743] Указанное в заголовке соединение (610,0 мг, 72,5%) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 6-бромхинолин (558,5 мг, 2,68 ммоль). МС (ИЭР) m/z - 314,2 (М+Н)+
[0744] Стадия 2: (S)-Т^-(пирролидин-3-ил)хинолин-6-амина гидрохлорид
[0745] Указанное в заголовке соединение (102,0 мг, 61,3%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 214,2 (М+Н)+
[0746] Эталонный пример 112. (S)-5-(пирролидин-3-иламино)хинолин-2-карбонитрил гидрохлорид
[0747] Стадия 1: трет-бутил (S)-3-((2-цианохинолин-5-ил)амино)пирролидин-1 -карбоксилат
[0748] Указанное в заголовке соединение (818 мг, 90,0%) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 5-бромхинолин-2-карбонитрил (625,6 мг, 2,68 ммоль). МС (ИЭР) m/z - 339,2 (М+Н)+
[0749] Стадия 2: (S)-5-(пирролидин-3-иламино)хинолин-2-карбонитрил гидрохлорид
[0750] Указанное в заголовке соединение (200,2 мг, 66,5%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0751] Эталонный пример 113. (S)-5-(пирролидин-3-иламино)хинолин-3-карбонитрил гидрохлорид
[0752] Стадия 1: трет-бутил (S)-3-((3-цианохинолин-5-ил)амино)пирролидин-1-карбоксилат
[0753] Указанное в заголовке соединение (698,0 мг, 76,8%) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 5-бромхинолин-3-карбонитрил (625,6 мг, 2,68 ммоль). МС (ИЭР) m/z - 339,2 (М+Н)+
[0754] Стадия 2: (S)-5-(пирролидин-3-иламино)хинолин-3-карбонитрил гидрохлорид
[0755] Указанное в заголовке соединение (143,2 мг, 47,9%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки
[0756] Эталонный пример 114. (S)-3-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0757] Стадия 1: трет-бутил (S)-3-((3-метоксихинолин-5-ил)амино)пирролидин-1-карбоксилат
[0758] Указанное в заголовке соединение (446,2 мг, 48,4%) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 5-бром-3-метоксихинолин (639,2 мг, 2,68 ммоль). МС (ИЭР) m/z - 344,2 (М+Н)+
[0759] Стадия 2: (S)-3-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0760] Указанное в заголовке соединение (187,5 мг, 59,3%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки
[0761] Эталонный пример 115. (S)-3-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0762] Стадия 1: трет-бутил (S)-3-((3-фторхинолин-5-ил)амино)пирролидин-1-карбоксилат
[0763] Указанное в заголовке соединение (668,7 мг, 75,1%) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 5-бром-3-фторхинолин (606,8 мг, 2,68 ммоль). МС (ИЭР) m/z - 333,1 (М+Н)+
[0764] Стадия 2:. (S)-3-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0765] Указанное в заголовке соединение (392,5 мг, 63,9%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки
[0766] Эталонный пример 116. (S)-3-хлор-1М-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0767] Стадия 1: трет-бутил (S)-3-((3-хлорхинолин-5-ил)амино)пирролидин-1-карбоксилат
[0768] Указанное в заголовке соединение (613,0 мг, 65,6%) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 5-бром-3-хлорхинолин (651,0 мг, 2,68 ммоль). МС (ИЭР) m/z - 348,2 (М+Н)+
[0769] Стадия 2: (S)-3-хлор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0770] Указанное в заголовке соединение (163,7 мг, 28,9%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки
[0771] Эталонный пример 117. (S)-7-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0772] Стадия 1: трет-бутил (S)-3-((7-фторхинолин-5-ил)амино)пирролидин-1-карбоксилат
[0773] Указанное в заголовке соединение (875,0 мг, 98,3%) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 5-бром-7-фторхинолин (606,8 мг, 2,68 ммоль). МС (ИЭР) m/z - 333,1 (М+Н)+
[0774] Стадия 2: (S)-7-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0775] Указанное в заголовке соединение (250,0 мг, 38,3%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки
[0776] Эталонный пример 118. (S)-7-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0777] Стадия 1: трет-бутил (S)-3-((7-метоксихинолин-5-ил)амино)пирролидин-1-карбоксилат
[0778] Указанное в заголовке соединение (848,2 мг, 92,0%) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 5-бром-7-метоксихинолин (639,2 мг, 2,68 ммоль). 1Н-ЯМР (CDCl3, 400 МГц) δ 8,78 (д, 1Н), 8,02 (д, 1Н), 7,19 (дд, 1Н), 6,89 (с, 1Н), 6,28 (с, 1Н), 4,43 (д, 1Н), 4,15 (с, 1Н), 3,93 (с, 3Н), 3,79 (с, 1Н), 3,56-3,36 (м, 3Н), 2,27 (с, 1Н), 2,05-1,93 (м, 1Н), 1,47 (с, 9Н).
[0779] Стадия 2: (S)-7-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0780] Указанное в заголовке соединение (485,0 мг, 62,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки
[0781] Эталонный пример 119. (S)-N-(пирролидин-3-ил)-7-(трифторметил)хинолин-5-амина гидрохлорид
[0782] Стадия 1: трет-бутил (S)-3-((7-(трифторметил)хинолин-5-ил)амино)пирролидин-1-карбоксилат
[0783] Указанное в заголовке соединение (888,5 мг, 86,7%) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 5-бром-7-(трифторметил)хинолин (741,1 мг, 2,68 ммоль). 1Н-ЯМР (CDCl3, 400 МГц) δ 8,97 (д, 1Н), 8,19 (д, 1Н), 7,80 (с, 1Н), 7,47- 7,44 (м, 1Н), 6,73 (с, 1Н), 4,63 (с, 1Н), 4,26 (с, 1Н), 3,83 (с, 1Н), 3,59-3,39 (м, 3Н), 2,37-2,29 (м, 1Н) 2,07-2,05 (м, 1Н), 1,49 (с, 9Н).
[0784] Стадия 2: (S)-N-(пирролидин-3-ил)-7-(трифторметил)хинолин-5-амина гидрохлорид
[0785] Указанное в заголовке соединение (325,0 мг, 39,3%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки
[0786] Эталонный пример 120. (S)-6-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0787] Стадия 1: трет-бутил (S)-3-((6-метилхинолин-5-ил)амино)пирролидин-1-карбоксилат
[0788] Указанное в заголовке соединение (683,2 мг, 77,7%) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 5-бром-6-метилхинолин (596,2 мг, 2,68 ммоль). 1Н-ЯМР (CDCl3, 400 МГц) δ 8,84 (д, 1Н), 8,39 (д, 1Н), 7,75 (д, 1Н), 7,52 (д, 1Н), 7,37 (д, 1Н), 3,97 (с, 1Н), 3,64-3,29 (м, 5 Н), 2,43 (с, 3Н), 2,15-1,97 (м, 2Н), 1,48-1,45 (с, 9Н)
[0789] Стадия 2: (S)-6-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0790] Указанное в заголовке соединение (495,0 мг, 79,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки
[0791] Эталонный пример 121. (S)-6-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0792] Стадия 1: трет-бутил (S)-3-((6-метоксихинолин-5-ил)амино)пирролидин-1-карбоксилат
[0793] Указанное в заголовке соединение (378,5 мг, 41,0%) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 5-бром-6-метоксихинолин (639,2 мг, 2,68 ммоль). 1Н-ЯМР (CDCl3, 400 МГц) δ 8,78 (с, 1Н), 8,39 (д, 1Н), 7,83 (д, 1Н), 7,48 (д, 1Н), 7,35-7,33 (м, 1Н), 4,00-3,97 (м, 4 Н), 3,61-3,31 (м, 5 Н), 2,05-1,90 (м, 2Н), 1,48-1,46 (с, 9Н).
[0794] Стадия 2: (S)-6-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0795] Указанное в заголовке соединение (248,5 мг, 71,2%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки
[0796] Эталонный пример 122. (S)-6-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0797] Стадия 1: трет-бутил (S)-3-((6-фторхинолин-5-ил)амино)пирролидин-1-карбоксилат
[0798] Указанное в заголовке соединение (344,7 мг, 38,7%) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 5-бром-6-фторхинолин (606,8 мг, 2,68 ммоль). 1Н-ЯМР (CDCl3, 400 МГц) δ 8,88 (с, 1Н), 8,37 (д, 1Н), 7,75 (с, 1Н), 7,49 (т, 1Н), 7,41 (дд, 1Н), 4,14 (д, 1Н), 3,69-3,36 (м, 5 Н), 2,16-2,08 (м, 1Н), 1,93 (с, 1Н), 1,48-1,46 (м, 9Н).
[0799] Стадия 2: (S)-6-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0800] Указанное в заголовке соединение (251,7 мг, 79,5%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки
[0801] Эталонный пример 123. (S)-8-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0802] Стадия 1: трет-бутил (S)-3-((8-метилхинолин-5-ил)амино)пирролидин-1-карбоксилат
[0803] Указанное в заголовке соединение (631,0 мг, 71,7%) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 5-бром-8-метилхинолин (596,2 мг, 2,68 ммоль). 1Н-ЯМР (CDCl3, 400 МГц) δ 8,94 (д, 1Н), 8,17 (д, 1Н), 7,41 (с, 1Н), 7,36 (дд, 1Н), 6,60 (д, 1Н), 4,19 (с, 2Н), 3,83-3,78 (м, 1Н), 3,56-3,48 (м, 2Н), 3,40-3,32 (м, 1Н), 2,69 (с, 3Н), 2,27 (м, 1Н), 2,04 (с, 1Н), 1,47 (с, 9Н).
[0804] Стадия 2: (S)-8-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0805] Указанное в заголовке соединение (489,3 мг, 84,5%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки
[0806] Эталонный пример 124. (S)-8-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0807] Стадия 1: трет-бутил (S)-3-((8-метоксихинолин-5-ил)амино)пирролидин-1-карбоксилат
[0808] Указанное в заголовке соединение (712,0 мг, 77,2%) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 5-бром-8-метоксихинолин (639,2 мг, 2,68 ммоль). 1Н-ЯМР (CDCl3, 400 МГц) δ 8,94 (д, 1Н), 8,20 (д, 1Н), 7,42 (дд, 1Н), 6,96 (с, 1Н), 6,64 (д, 1Н), 4,15-4,13 (м, 1Н), 4,04 (с, 3Н), 3,88-3,76 (м, 2Н), 3,49-3,33 (м, 3Н), 2,29-2,24 (м, 1Н), 2,05-2,02 (м, 1Н), 1,47 (с, 9Н).
[0809] Стадия 2: (S)-8-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0810] Указанное в заголовке соединение (505,5 мг, 77,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки
[0811] Эталонный пример 125. (S)-8-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0812] Стадия 1: трет-бутил (S)-3-((8-фторхинолин-5-ил)амино)пирролидин-1-карбоксилат
[0813] Указанное в заголовке соединение (852,0 мг, 95,7%) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 5-бром-8-фторхинолин (606,8 мг, 2,68 ммоль). 1Н-ЯМР (CDCl3, 400 МГц) δ 8,95 (д, 1Н), 8,20 (д, 1Н), 7,43 (дд, 1Н), 7,29 (т, 1Н), 6,55 (дд, 1Н), 4,17 (с, 2Н), 3,81 (с, 1Н), 3,56-3,35 (м, 3Н), 2,28 (с, 1Н), 2,04 (с, 1Н), 1,47 (с, 9Н).
[0814] Стадия 2: (S)-8-фтор-1М-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0815] Указанное в заголовке соединение (556,6 мг, 71,2%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки
[0816] Эталонный пример 126. (S)-N-(пирролидин-3-ил)-8-(трифторметил)хинолин-5-амина гидрохлорид
[0817] Стадия 1: трет-бутил (S)-3-((8-(трифторметил)хинолин-5-ил)амино)пирролидин-1-карбоксилат
[0818] Указанное в заголовке соединение (318,0 мг, 31,0%) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 5-бром-8-(трифторметил)хинолин (741,1 мг, 2,68 ммоль). 1Н-ЯМР (CDCl3, 400 МГц) δ 9,04 (д, 1Н), 8,16 (д, 1Н), 7,92 (д, 1Н), 7,43 (дд, 1Н), 6,59 (д, 1Н), 4,78 (с, 1Н), 4,26 (с, 1Н), 3,84 (с, 1Н), 3,59-3,37 (м, 3Н), 2,37-2,32 (м, 1Н), 2,07-2,05 (м, 1Н), 1,48 (с, 9Н).
[0819] Стадия 2: (S)-N-(пирролидин-3-ил)-8-(трифторметил)хинолин-5-амина гидрохлорид
[0820] Указанное в заголовке соединение (175,0 мг, 59,3%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки
[0821] Эталонный пример 127. (S)-N-(пирролидин-3-ил)-8-(трифторметокси)хинолин-5-амина гидрохлорид
[0822] Стадия 1: трет-бутил (S)-3-((8-(трифторметокси)хинолин-5-ил)амино)пирролидин-1-карбоксилат
[0823] Указанное в заголовке соединение (844,5 мг, 79,1%) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 5-бром-8-(трифторметокси)хинолин (784,0 мг, 2,68 ммоль). 1Н-ЯМР (CDCl3, 400 МГц) δ 8,99 (д, 1Н), 8,19 (д, 1Н), 7,51 (д, 1Н), 7,42 (дд, 1Н), 6,56 (д, 1Н), 4,50 (с, 1Н), 4,19 (с, 1Н), 3,81 (с, 1Н), 3,56-3,36 (м, 2Н), 2,35-2,25 (м, 1Н), 2,05 (с, 1Н), 1,48 (с, 9Н).
[0824] Стадия 2: (S)-N-(пирролидин-3-ил)-8-(трифторметокси)хинолин-5-амина гидрохлорид
[0825] Указанное в заголовке соединение (505,3 мг, 64,2%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки
[0826] Эталонный пример 128. (S)-5-(пирролидин-3-иламино)хинолин-8-карбонитрил гидрохлорид
[0827] Стадия 1: трет-бутил (S)-3-((8-цианохинолин-5-ил)амино)пирролидин-1-карбоксилат
[0828] Указанное в заголовке соединение (800,0 мг, 88,0%) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 5-бромхинолин-8-карбонитрил (625,6 мг, 2,68 ммоль). 1Н-ЯМР (CDCl3, 400 МГц) δ 9,01 (д, 1Н), 8,26 (д, 1Н), 7,94 (д, 1Н), 7,42 (дд, 1Н), 6,60 (д, 1Н), 5,30-5,25 (м, 1Н), 4,27 (с, 1Н), 3,83 (с, 1Н), 3,57-3,40 (м, 3Н), 2,38-2,31 (м, 1Н), 2,11 (с, 1Н), 1,48 (с, 9Н).
[0829] Стадия 2: (S)-5-(пирролидин-3-иламино)хинолин-8-карбонитрил гидрохлорид
[0830] Указанное в заголовке соединение (525,0 мг, 71,3%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки
[0831] Эталонный пример 129. (S)-8-(бензилокси)-N-(пирролвдин-3-ил)хинолин-5-амина гидрохлорид
[0832] Стадия 1: трет-бутил (S)-3-((8-(бензилокси)хинолин-5-ил)амино)пирролидин-1-карбоксилат
[0833] Указанное в заголовке соединение (1120,0 мг, 99,6%) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 8-(бензилокси)-5-бромхинолин (843,4 мг, 2,68 ммоль). 1Н-ЯМР (CDCl3, 400 МГц) δ 8,97 (д, 1Н), 8,19 (д, 1Н), 7,50 (д, 2Н), 7,41 (дд, 1Н), 7,35 (т, 2Н), 7,29 (д, 1Н), 6,93 (д, 1Н), 6,51 (д, 1Н), 5,38 (с, 2Н), 4,13-4,08 (м, 1Н), 3,93 (с, 1Н), 3,76-3,72 (м, 1Н), 3,53-3,47 (м, 2Н), 3,39-3,28 (м, 1Н), 2,25-2,20 (м, 1Н), 1,99 (с, 1Н), 1,46 (с, 9Н).
[0834] Стадия 2: (S)-8-(бензилокси)-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0835] Указанное в заголовке соединение (1000,0 мг, 79,7%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки
[0836] Эталонный пример 130. (S)-N-(пирролидин-3-ил)хинолин-7-амина гидрохлорид
[0837] Стадия 1: трет-бутил (S)-3-(хинолин-7-иламино)пирролидин-1-карбоксилат
[0838] Указанное в заголовке соединение (631,5 мг, 75,0%) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 7-бромхинолин (558,5 мг, 2,68 ммоль). МС (ИЭР) m/z - 314,2 (М+Н)+
[0839] Стадия 2: (S)-N-(пирролидин-3-ил)хинолин-7-амина гидрохлорид
[0840] Указанное в заголовке соединение (110,0 мг, 64,1%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 214,2 (М+Н)+
[0841] Эталонный пример 131. (S)-N-(пирролидин-3-ил)-8-(трифторметил)хинолин-4-амина гидрохлорид
[0842] Стадия 1: трет-бутил (S)-3-((8-(трифторметил)хинолин-4-ил)амино)пирролидин-1-карбоксилат
[0843] Указанное в заголовке соединение (384,0 мг, 37,5%) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 4-бром-8-(трифторметил)хинолин (741,0 мг, 2,68 ммоль). МС (ИЭР) m/z - 382,2 (М+Н)+
[0844] Стадия 2: (S)-N-(пирролидин-3-ил)-8-(трифторметил)хинолин-4-амина гидрохлорид
[0845] Указанное в заголовке соединение (254,0 мг, 71,2%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 282,2 (М+Н)+
[0846] Эталонный пример 132. (S)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорид
[0847] Стадия 1: трет-бутил (S)-3-((1,8-нафтиридин-3-ил)амино)пирролидин-1-карбоксилат
[0848] Указанное в заголовке соединение (215,3 мг, 51,0%) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 3-бром-1,8-нафтиридин (280,6 мг, 1,34 ммоль). МС (ИЭР) m/z - 315,1 (М+Н)+
[0849] Стадия 2: (S)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорид
[0850] Указанное в заголовке соединение (196,7 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0851] Эталонный пример 133. (S)-7-хлор-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорид
[0852] Стадия 1: трет-бутил (S)-3-((7-хлор-1,8-нафтиридин-3-ил)амино)пирролидин-1-карбоксилат
[0853] Указанное в заголовке соединение (168,8 мг, 36,1%) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 6-бром-2-хлор-1,8-нафтиридин (326,8 мг, 1,34 ммоль). МС (ИЭР) m/z - 349,2 (М+Н)+
[0854] Стадия 2: (S)-7-хлор-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорид
[0855] Указанное в заголовке соединение (155,6 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0856] Эталонный пример 134. (S)-8-этокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0857] Стадия 1: трет-бутил (S)-3-((8-этоксихинолин-5-ил)амино)пирролидин-1-карбоксилат
[0858] Указанное в заголовке соединение (561,0 мг, 58,4%) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 5-бром-8-этоксихинолин (676,8 мг, 2,68 ммоль). МС (ИЭР) m/z - 358,2 (М+Н)+
[0859] Стадия 2: (S)-8-этокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид
[0860] Указанное в заголовке соединение (321,0 мг, 61,9%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 258,2 (М+Н)+
[0861] Эталонный пример 135. (S)-5-(пирролидин-3-иламино)хинолин-8-ола гидрохлорид
[0862] Стадия 1: 5-бром-8-(трет-бутилдиметилсилил)окси)хинолин
[0863] 5-Бромхинолин-8-ол (1 г, 4,46 ммоль) растворяли в безводном дихлорметане. К полученному раствору добавляли трет-бутилдиметилсилилхлорид (0,74 г, 4,91 ммоль) и имидазол (0,67 г, 9,819 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции реакционную смесь разбавляли дихлорметаном и затем добавляли воду для экстракции водного слоя. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (только н-гексаном) с получением указанного в заголовке соединения (1,16 г, 76,8%). 1Н-ЯМР (CDCl3, 400 МГц) δ 8,88 (дд, 1Н), 8,47 (дд, 1Н), 7,68 (д, 1Н), 7,49 (кв, 1Н), 7,07 (д, 1Н), 1,07 (с, 9Н), 0,27 (с, 6 Н)
[0864] Стадия 2: трет-бутил (S)-3-((8-(трет-бутилдиметилсилил)окси)хинолин-5-ил)амино)пирролидин-1-карбоксилат
[0865] 5-бром-8-(трет-бутилдиметилсилил)окси)хинолин (500 мг, 1,47 ммоль), полученный на стадии 1, растворяли в безводном толуоле. К полученному раствору добавляли трет-бутил (S)-3-аминопирролидин-1-карбоксилат (275,3 мг, 1,47 ммоль), карбонат цезия (578 мг, 1,77 ммоль), трис (дибензилиденацетон)дипалладий (0)(162,4 мг, 0,17 ммоль) nRuphos (82,7 мг, 0,17 ммоль). Реакционную смесь нагревали в колбе с обратным холодильником и перемешивали при 100°С в течение ночи. После завершения реакции реакционную смесь охлаждали до комнатной температуры и затем добавляли воду для экстракции водного слоя этилацетатом. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (этилацетат / н-гексан = 1/1, об./об.) с получением указанного в заголовке соединения (655,3 мг, 99,9%). МС (ИЭР) m/z - 444,3 (М+Н)+
[0866] Стадия 3. (S)-5-(пирролидин-3-иламино)хинолин-8-ола гидрохлорид
[0867] трет-бутил (S)-3-((8-(трет-бутилдиметилсилил)окси)хинолин-5-ил)амино)пирролидин-1-карбоксилат (655,3 мг, 1,47 ммоль), полученный на стадии 2, растворяли в дихлорметане (8,4 мл), а затем туда же добавляли (по каплям) в избытке 4,0 М соляную кислоту, растворенную в 1,4-диоксане. Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции, полученное твердое соединение фильтровали, промывали и высушивали вакуумом с получением указанного в заголовке соединения (405,2 мг, 91,2%). 1Н-ЯМР ((CD3)2SO, 400 МГц) δ 9,55 (д, 1Н), 8,99 (д, 1Н), 7,98 (кв, 1Н), 7,43 (д, 1Н), 6,96 (д, 1Н), 4,48-4,46 (м, 1Н), 3,67-3,61 (м, 2Н), 3,53-3,47 (м, 2Н), 2,53-2,44 (м, 1Н), 2,36-2,29 (м, 1Н).
[0868] Эталонный пример 136. (S)-8-метил-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид
[0869] Стадия 1: трет-бутил (S)-3-((8-метилхинолин-6-ил)амино)пирролидин-1-карбоксилат
[0870] Указанное в заголовке соединение (261,6 мг, 59,5%) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 6-бром-8-метилхинолин (298,1 мг, 1,34 ммоль). МС (ИЭР) m/z - 328,2 (М+Н)+
[0871] Стадия 2: (S)-8-метил-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид
[0872] Указанное в заголовке соединение (238,2 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0873] Эталонный пример 137. (S)-8-фтор-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид
[0874] Стадия 1: трет-бутил (S)-3-((8-фторхинолин-6-ил)амино)пирролидин-1-карбоксилат
[0875] Указанное в заголовке соединение (391,1 мг, 87,9%) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 6-бром-8-фторхинолин (303,4 мг, 1,34 ммоль). МС (ИЭР) m/z - 332,2 (М+Н)+
[0876] Стадия 2: (S)-8-фтор-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид
[0877] Указанное в заголовке соединение (294,2 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0878] Эталонный пример 138. (S)-8-хлор-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид
[0879] Стадия 1: трет-бутил (S)-3-((8-хлорхинолин-6-ил)амино)пирролидин-1 -карбоксилат
[0880] Указанное в заголовке соединение (316,5 мг, 67,8%) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 6-бром-8-хлорхинолин (325,5 мг, 1,34 ммоль). МС (ИЭР) m/z - 348,1 (М+Н)+
[0881] Стадия 2: (S)-8-хлор-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид
[0882] Указанное в заголовке соединение (287,6 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки.
[0883] Эталонный пример 139. (S)-N-(пирролидин-3-ил)-8-(трифторметил)хинолин-6-амина гидрохлорид
[0884] Стадия 1: трет-бутил (S)-3-((8-(трифторметил)хинолин-6-ил)амино)пирролидин-1-карбоксилат
[0885] Указанное в заголовке соединение (232,4 мг, 45,4%) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали 6-бром-8-(трифторметил)хинолин (370,5 мг, 1,34 ммоль). МС (ИЭР) m/z - 382,1 (М+Н)+
[0886] Стадия 2: (S)-N-(пирролидин-3-ил)-8-(трифторметил)хинолин-6-амина гидрохлорид
[0887] Указанное в заголовке соединение (394,2 мг, 100,0%) получали таким же образом, как на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки
[0888] Эталонный пример 140. (S)-N-метил-5-(пирролидин-3-иламино)хинолин-8-карбоксамида гидрохлорид
[0889] Стадия 1: 5-Бром-N-метилхинолин-8-карбоксамид
[0890] 5-Бромхинолин-8-карбоновую кислоту (300 мг, 1,19 ммоль) растворяли в диметилформамиде.
К полученному раствору добавляли метанамин (0,06 мл, 1,42 ммоль), HATU (O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилуран гексафторфосфат) (633,6 мг, 1,67 ммоль) и диизопропилэтиламин (769,16 мг, 5,95 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции к реакционной смеси добавляли воду. Водный слой реакционной смеси экстрагировали дихлорметаном. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (этилацетат / н-гексан = 1/1, об./об.) с получением указанного в заголовке соединения (229,8 мг, 72,8%). 1Н-ЯМР (CDCl3, 400 МГц) δ 8,96 (дд, 1Н), 8,74 (д, 1Н), 8,72 (дд, 1Н), 7,99 (д, 1Н), 7,60 (кв, 1Н), 3,16 (д, 3Н).
[0891] Стадия 2: трет-бутил (S)-3-((8-(метилкарбамоил)хинолин-5-ил)амино)пирролидин-1-карбоксилат
[0892] 5-Бром-N-метилхинолин-8-карбоксамид (192 мг, 0,72 ммоль), полученный на стадии 1, растворяли в безводном толуоле. К полученному раствору добавляли трет-бутил (S)-3-аминопирролидин-1-карбоксилат (135,0 мг, 0,72 ммоль), карбонат цезия (192,4 мг, 0,591 ммоль), трис(дибензилиденацетон)дипалладий (0) (49,2 мг, 0,05 ммоль) и (+/-)-2,2'-бис(дифенилфоспино)-1,1'-бинафталин (40,1 мг, 0,06 ммоль). Реакционную смесь нагревали в колбе с обратным холодильником и перемешивали при 100°С в течение ночи. После завершения реакции реакционную смесь охлаждали до комнатной температуры и затем добавляли воду для экстракции водного слоя этилацетатом. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (этилацетат / н-гексан = 1/1, об./об.) с получением указанного в заголовке соединения (106,3 мг, 39,6%). МС (ИЭР) m/z - 371,2 (М+Н)+
[0893] Стадия 3. (S)-N-метил-5-(пирролидин-3-иламино)хинолин-8-карбоксамида гидрохлорид
[0894] трет-бутил (S)-3-((8-(метилкарбамоил)хинолин-5-ил)амино)пирролидин-1-карбоксилат (106,3 мг, 0,287 ммоль), полученный на стадии 2, растворяли в дихлорметане (8,4 мл), а затем туда же добавляли (по каплям) в избытке 4,0 М соляную кислоту, растворенную в 1,4-диоксане. Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции, полученное твердое соединение фильтровали, промывали и высушивали вакуумом с получением указанного в заголовке соединения (12,5 мг, 16,1%). МС (ИЭР) m/z - 271,1 (М+Н)+
[0895] Эталонный пример 141. (S)-N,N-диметил-5-(пирролидин-3-иламино)хинолин-8-карбоксамида
[0896] Стадия 1: 5-Бром-N,N-диметилхинолин-8-карбоксамид
[0897] Указанное в заголовке соединение (179,1 мг, 53,9%) получали таким же образом, как и на стадии 1 эталонного примера 140, за исключением того, что вместо метанамина использовали диметиламин (64,1 мг, 1,42 ммоль). 1Н-ЯМР (CDCl3, 400 МГц) δ 8,95 (дд, 1Н), 8,55 (дд, 1Н), 7,86 (д, 1Н), 7,56-7,52 (м, 2Н), 3,24 (с, 3Н), 2,77 (с, 3Н).
[0898] Стадия 2: трет-бутил (S)-3-((8-(диметилкарбамоил)хинолин-5-ил)амино)пирролидин-1-карбоксилат
[0899] Указанное в заголовке соединение (86,2 мг, 23,2%) получали таким же образом, как и на стадии 2 эталонного примера 140. МС (ИЭР) m/z - 385,2 (М+Н)+
[0900] Стадия 3. (S)-N,N-диметил-5-(пирролидин-3-иламино)хинолин-8-карбоксамида гидрохлорид
[0901] Указанное в заголовке соединение (57,0 мг, 71,4%) получали таким же образом, как и на стадии 3 эталонного примера 140, и использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 285,1 (М+Н)+
[0902] Эталонный пример 142. (S)-N-фенил-5-(пирролидин-3-иламино)хинолин-8-карбоксамида гидрохлорид
[0903] Стадия 1: 5-Бром-N-фенилхинолин-8-карбоксамид
[0904] Указанное в заголовке соединение (348,12 мг, 89,4%) получали таким же образом, как и на стадии 1 эталонного примера 140, за исключением того, что вместо метанамина использовали анилин (132,2 мг, 1,42 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 13,41 (с, 1Н), 9,03 (д, 1Н), 8,80 (д, 1Н), 8,75 (д, 1Н), 8,02 (д, 1Н), 7,87 (д, 2Н), 7,64 (кв, 1Н), 7,42 (т, 2Н), 7,16 (т, 1Н).
[0905] Стадия 2: трет-бутил (S)-3-((8-(фенилкарбамоил)хинолин-5-ил)амино)пирролидин-1-карбоксилат
[0906] Указанное в заголовке соединение (54,0 мг, 38,3%) получали таким же образом, как и на стадии 2 эталонного примера 140. МС (ИЭР) m/z - 433,2 (М+Н)+
[0907] Стадия 3. (S)-N-фенил-5-(пирролидин-3-иламино)хинолин-8-карбоксамида гидрохлорид
[0908] Указанное в заголовке соединение (47,4 мг, 93,6%) получали таким же образом, как и на стадии 3 эталонного примера 140, и использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 333,2 (М+Н)+
[0909] Эталонный пример 143. (S)-N-метил-N-фенил-5-(пирролидин-3-иламино)хинолин-8-карбоксамида гидрохлорид
[0910] Стадия 1: 5-Бром-N-метил-N-фенилхинолин-8-карбоксамид
[0911] Указанное в заголовке соединение (365,2 мг, 89,9%) получали таким же образом, как и на стадии 1 эталонного примера 140, за исключением того, что вместо метанамина использовали N-метиланилин (152,2 мг, 1,42 ммоль). 1Н-ЯМР (CDCl3, 400 МГц) δ 8,95 (дд, 1Н), 8,35 (дд, 1Н), 7,56 (д, 1Н), 7,41 (кв, 1Н), 7,30 (д, 1Н), 7,05 (д, 2Н), 6,97-6,91 (м, 3Н), 3,59 (с, 3Н)
[0912] Стадия 2: трет-бутил (S)-3-((8-(метил(фенил)карбамоил)хинолин-5-ил)амино)пирролидин-1-карбоксилат
[0913] Указанное в заголовке соединение (92,2 мг, 36,4%) получали таким же образом, как и на стадии 2 эталонного примера 140. МС (ИЭР) m/z - 447,2 (М+Н)+
[0914] Стадия 3. (S)-N-метил-N-фенил-5-(пирролидин-3-иламино)хинолин-8-карбоксамида гидрохлорид
[0915] Указанное в заголовке соединение (85 мг, 98,5%) получали таким же образом, как и на стадии 3 эталонного примера 140, и использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 347,2 (М+Н)+
[0916] Эталонный пример 144. (S)-N-бензил-N-метил-5-(пирролидин-3-иламино)хинолин-8-карбоксамида гидрохлорид
[0917] Стадия 1: N-бензил-5-бром-N-метилхинолин-8-карбоксамид
[0918] Указанное в заголовке соединение (382,5 мг, 90,4%) получали таким же образом, как и на стадии 1 эталонного примера 140, за исключением того, что вместо метанамина использовали N-метил-1-фенилметанамин (172,0 мг, 1,42 ммоль). 1Н-ЯМР (CDCl3, 400 МГц) δ 8,99-8,98 (м, 1H), 8,54-8,49 (м, 1Н), 7,86-7,78 (м, 1Н), 7,59-7,50 (м, 3H), 7,41-7,37 (м, 1H), 7,31-7,19 (м, 3Н), 4,93 (с, 1H), 4,29 (с, 1Н), 3,15 (с, 1,5Н), 2,65 (с, 1,5Н)
[0919] Стадия 2: трет-бутил (S)-3-((8-(бензил(метил)карбамоил)хинолин-5-ил)амино)пирролидин-1-карбоксилат
[0920] Указанное в заголовке соединение (90,1 мг, 31,2%) получали таким же образом, как и на стадии 2 эталонного примера 140. МС (ИЭР) m/z - 461,2 (М+Н)+
[0921] Стадия 3. (S)-N-бензил-N-метил-5-(пирролидин-3-иламино)хинолин-8-карбоксамида гидрохлорид
[0922] Указанное в заголовке соединение (76,0 мг, 89,2%) получали таким же образом, как и на стадии 3 эталонного примера 140, и использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 361,2 (М+Н)+
[0923] Эталонный пример 145. (S)-N-(пиридин-3-ил)-5-(пирролидин-3-иламино)хинолин-8-карбоксамида гидрохлорид
[0924] Стадия 1: 5-Бром-N-(пирид-3-ил)хинолин-8-карбоксамид
[0925] Указанное в заголовке соединение (259,5 мг, 66,4%) получали таким же образом, как и на стадии 1 эталонного примера 140, за исключением того, что вместо метанамина использовали 3-аминопиридин (123,2 мг, 1,42 ммоль). 1Н-ЯМР (CDCl3, 400 МГц) δ 9,09 (дд, 1Н), 8,88 (д, 1Н), 8,83-8,79 (м, 2Н), 8,51 (дт, 1Н), 8,41 (дд, 1Н), 8,07 (д, 1Н), 7,70 (дд, 1Н), 7,36 (дд, 1Н).
[0926] Стадия 2: трет-бутил (S)-3-((8-(пиридин-3-илкарбамоип)хинолин-5-ил)амино)пирролидин-1-карбоксилат
[0927] Указанное в заголовке соединение (273,9 мг, 79,9%) получали таким же образом, как и на стадии 2 эталонного примера 140. МС (ИЭР) m/z - 434,2 (М + Н)+
[0928] Стадия 3. (S)-N-(пиридин-3-ил)-5-(пирролидин-3-иламино)хинолин-8-карбоксамида гидрохлорид
[0929] Указанное в заголовке соединение (221,4 мг, 86,2%) получали таким же образом, как и на стадии 3 эталонного примера 140, и использовали на следующей стадии без дополнительной очистки.
[0930] Эталонный пример 146. (S)-N-(пирвдин-4-ил)-5-(пирролидин-3-иламино)хинолин-8-карбоксамида гидрохлорид
[0931] Стадия 1: 5-Бром-N-(пирид-4-ил)хинолин-8-карбоксамид
[0932] Указанное в заголовке соединение (325,5 мг, 83,3%) получали таким же образом, как и на стадии 1 эталонного примера 140, за исключением того, что вместо метанамина использовали 4-аминопиридин (123,2 мг, 1,42 ммоль). 1Н-ЯМР (CDCl3, 400 МГц) δ 9,07 (дд, 1Н), 8,81 (д, 2 И), 8,59 (д, 2Н), 8,07 (д, 1Н), 7,79 (д, 2 И), 7,71 (дд, 1Н).
[0933] Стадия 2: трет-бутил (S)-3-((8-(пиридин-4-илкарбамоил)хинолин-5-ил)амино)пирролидин-1-карбоксилат
[0934] Указанное в заголовке соединение (363,6 мг, 84,5%) получали таким же образом, как и на стадии 2 эталонного примера 140. МС (ИЭР) m/z - 434,2 (М+Н)+
[0935] Стадия 3. (S)-N-(пирвдин-4-ил)-5-(пирролидин-3-иламино)хинолин-8-карбоксамида гидрохлорид
[0936] Указанное в заголовке соединение (330,0 мг, 96,7%) получали таким же образом, как и на стадии 3 эталонного примера 140, и использовали на следующей стадии без дополнительной очистки.
[0937] Эталонный пример 147. (S)-N-(пирвдин-2-ил)-5-(пирролидин-3-иламино)хинолин-8-карбоксамида гидрохлорид
[0938] Стадия 1: 5-Бром-N-(пирид-2-ил)хинолин-8-карбоксамид
[0939] Указанное в заголовке соединение (262,5 мг, 67,2%) получали таким же образом, как и на стадии 1 эталонного примера 140, за исключением того, что вместо метанамина использовали 2-аминопиридин (123,2 мг, 1,42 ммоль). 1Н-ЯМР (CDCl3, 400 МГц) δ 9,19 (дд, 1Н), 8,82 (д, 1H), 8,77 (дд,1Н), 8,52 (д, 1Н), 8,44 (дд, 1H), 8,05 (д, 1Н), 7,78 (тд, 1Н), 7,68 (дд, 1H), 7,10 (дд, 1Н).
[0940] Стадия 2: трет-бутил (S)-3-((8-(пиридин-2-илкарбамоил)хинолин-5-ил)амино)пирролидин-1-карбоксилат
[0941] Указанное в заголовке соединение (318,9 мг, 91,9%) получали таким же образом, как и на стадии 2 эталонного примера 140. МС (ИЭР) m/z - 434,2 (М+Н)+
[0942] Стадия 3. (S)-N-(пирвдин-2-ил)-5-(пирролидин-3-иламино)хинолин-8-карбоксамида
[0943] Указанное в заголовке соединение (287,1 мг, 96,0%) получали таким же образом, как на стадии 3 эталонного примера 140, и использовали на следующей стадии без дополнительной очистки.
[0944] Эталонный пример 148. (S)-N-(5-(пирролидин-3-иламино)хинолин-8-ил)ацетамида гидрохлорид
[0945] Стадия 1: трет-бутил (S)-3-((8-ацетамидохинолин-5-ил)амино)пирролидин-1-карбоксилат
[0946] Указанное в заголовке соединение (434,0 мг, 43,6%) получали таким же образом, как и на стадии 1 эталонного примера 5, за исключением того, что вместо 4-бромхинолина использовали N-(5-бромхинолин-8-ил) ацетамид (711,7 мг, 2,68 ммоль). МС (ИЭР) m/z - 371,2 (М+Н)+
[0947] Стадия 2: (S)-N-(5-(пирролидин-3-иламино)хинолин-8-ил)ацетамида гидрохлорид
[0948] Указанное в заголовке соединение (300,5 мг, 74,6%) получали таким же образом, как и на стадии 2 эталонного примера 5, и использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 271,2 (М+Н)+
[0949] Эталонный пример 149. (S)-N-(5-(пирролидин-3-иламино)хинолин-8-ил)бензамида гидрохлорид
[0950] Стадия 1: N-(5-бромхинолин-8-ил) бензамид
[0951] 5-Бромхинолин-8-амин (500 мг, 2,24 ммоль) растворяли в диметилформамиде. К полученному раствору добавляли бензойную кислоту (355,8 мг, 2,91 ммоль), HATU (O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилуран гексафторфосфат) (1278,4 мг, 8,96 ммоль) и диизопропилэтиламин (11158,83 мг, 8,96 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции к реакционной смеси добавляли воду. Водный слой реакционной смеси экстрагировали дихлорметаном. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (этилацетат / н-гексан = 1/1, об./об.) с получением указанного в заголовке соединения (88,3 мг, 12,0%). МС (ИЭР) m/z - 327,0 (М+Н)+
[0952] Стадия 2: трет-бутил (S)-3-((8-(фенилкарбамоил)хинолин-5-ил)амино)пирролидин-1-карбоксилат
[0953] Указанное в заголовке соединение (72,4 мг, 31,1%) получали таким же образом, как и на стадии 2 эталонного примера 140, за исключением того, что вместо 5-бром-N-метилхинолин-8-карбоксамида использовали N-(5-бромхинолин-8-ил) бензамид (192 мг, 0,58 ммоль). МС (ИЭР) m/z - 433,2 (М+Н)+
[0954] Стадия 3. (S)-N-(5-(пирролидин-3-иламино)хинолин-8-ил)бензамида гидрохлорид
[0955] Указанное в заголовке соединение (60,1 мг, 88,6%) получали таким же образом, как и на стадии 3 эталонного примера 140, и использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 333,1 (М+Н)+
[0956] Эталонный пример 150. (S)-6-метокси-4-(пирролидин-3-илокси)хинолина гидрохлорид
[0957] Стадия 1: трет-бутил (S)-3-((6-метоксихинолин-4-ил)окси)пирролидин-1-карбоксилат
[0958] Трет-бутил (R)-3-гидроксипирролидин-1-карбоксилат (187 мг, 1,0 ммоль) растворяли в тетрагидрофуране (5,0 мл). К полученному раствору добавляли 4-гидрокси-6-метоксихинолин (175 мг, 1,0 ммоль) и трифенилфосфин (393 мг, 1,5 ммоль). Смесь охлаждали до 0°С. Затем по каплям медленно добавляли DIAD (диизопропилазодикарбоксилат) (0,29 мл, 1,5 ммоль) в течение 15 минут. Реакционную смесь перемешивали в течение 12 ч при комнатной температуре. После завершения реакции реакционную смесь выпаривали в вакууме и затем очищали с помощью колоночной хроматографии на силикагеле (этилацетат / метанол = 10/1, об./об.) с получением указанного в заголовке соединения (275 мг, 80%). МС (ИЭР) m/z - 345,2 (М+Н)+
[0959] Стадия 2: (S)-6-метокси-4-(пирролидин-3-илокси)хинолина гидрохлорид
[0960] трет-бутил (S)-3-((6-метоксихинолин-4-ил)окси)пирролидин-1-карбоксилат (275 мг, 0,80 ммоль), приготовленный на стадии 1, растворяли в дихлорметане (2,4 мл) и метаноле (0,2 мл). К полученному раствору добавляли по каплям избыток 4,0 М соляной кислоты, растворенной в 1,4-диоксане. Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции полученное твердое вещество фильтровали и высушивали с получением указанного в заголовке соединения (224 мг, 100%). Указанное в заголовке соединение использовали на следующей стадии без дополнительной очистки.
[0961] Эталонный пример 151. (S)-6,7-диметокси-4-(пирролидин-3-илокси)хинолина гидрохлорид
[0962] Стадия 1: трет-бутил-(S)-3-((6,7-диметоксихинолин-4-ил)окси)пирролидин-1-карбоксилат
[0963] Трет-бутил (R)-3-гидроксипирролидин-1-карбоксилат (187 мг, 1,0 ммоль) растворяли в тетрагидрофуране (5,0 мл). К полученному раствору добавляли 4-гидрокси-6,7-диметоксихинолин (205 мг, 1,0 ммоль) и трифенилфосфин (393 мг, 1,5 ммоль). Смесь охлаждали до 0°С. Затем по каплям медленно добавляли DIAD (диизопропилазодикарбоксилат) (0,29 мл, 1,5 ммоль) в течение 15 минут. Реакционную смесь перемешивали в течение 12 ч при комнатной температуре. После завершения реакции реакционную смесь выпаривали в вакууме и затем очищали с помощью колоночной хроматографии на силикагеле (этилацетат / метанол = 10/1, об./об.) с получением указанного в заголовке соединения (138 мг, 37%). МС (ИЭР) m/z - 375,2 (М+Н)+
[0964] Стадия 2: (S)-6,7-диметокси-4-(пирролидин-3-илокси)хинолина гидрохлорид
[0965] трет-бутил-(S)-3-((б,7-диметоксихинолин-4-ил)окси)пирролидин-1-карбоксилат (138 мг, 0,37 ммоль), полученный на стадии 1, растворяли в дихлорметане (1,0 мл) и метаноле (0,1 мл). К полученному раствору добавляли по каплям избыток 4,0 М соляной кислоты, растворенной в 1,4-диоксане. Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции полученное твердое вещество фильтровали и высушивали с получением указанного в заголовке соединения (114 мг, 100%)). Указанное в заголовке соединение использовали на следующей стадии без дополнительной очистки.
[0966] Эталонный пример 152. N-(пиперидин-4-ил)хинолин-8-карбоксамида гидрохлорид
[0967] Стадия 1: трет-бутил 4-(хинолин-8-карбоксамидо) пиперидин-1-карбоксилат
[0968] 4-Амино-1-трет-бутоксикарбонилпиперидин (250,0 мг, 1,25 ммоль) растворяли в дихлорметане.
К полученному раствору добавляли 8-хинолинкарбоновую кислоту (216,2 мг, 1,25 ммоль), гидрат 1-гидроксибензотриазола (337,3 мг, 2,50 ммоль), EDAC (N-(3-диметиламинопропил) гидрохлорид-N'-этилкарбодиимида) (478,6 мг, 2,50 ммоль) и триэтиламин (0,35 мл, 2,50 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции к реакционной смеси добавляли воду. Водный слой реакционной смеси экстрагировали дихлорметаном. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (этилацетат / н-гексан = 1/1, об./об.) с получением указанного в заголовке соединения (443,6 мг, 99,9%). МС (ИЭР) m/z - 356,2 (М+Н)+
[0969] Стадия 2: N-(пиперидин-4-ил)хинолин-8-карбоксамида гидрохлорид
[0970] Трет-бутил 4-(хинолин-8-карбоксамидо) пиперидин-1-карбоксилат (443,6 мг, 1,25 ммоль), приготовленный на стадии 1, растворяли в дихлорметане (5,0 мл), а затем туда же добавляли (по каплям) в избытке 4,0 М соляную кислоту, растворенную в 1,4-диоксане. Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции полученное твердое вещество фильтровали и высушивали с получением указанного в заголовке соединения (409,7 мг, 100,0%). Указанное в заголовке соединение использовали на следующей стадии без дополнительной очистки.
[0971] Эталонный пример 153. N-этил-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид
[0972] Стадия 1: трет-бутил 4-(этил(хинолин-3-ил)амино)пиперидин-1-карбоксилат
[0973] Трет-бутил 4-(этиламино)пиперидин-1 -карбоксилат (109,7 мг, 0,48 ммоль) растворяли в безводном толуоле. К полученному раствору добавляли 3-бромхинолин (100,0 мг, 0,48 ммоль), карбонат цезия (187,9 мг, 0,58 ммоль), трис(дибензилиденацетон)дипалладий (0) (44,0 мг, 0,04 ммоль) и (+/-)-2,2'-бис(дифенилфоспино)-1,1'-бинафталин (29,9 мг, 0,27 ммоль). Реакционную смесь нагревали в колбе с обратным холодильником и перемешивали при 100°С в течение ночи. После завершения реакции реакционную смесь охлаждали до комнатной температуры и затем добавляли воду для экстракции водного слоя этилацетатом. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (этилацетат / н-гексан = 1/1, об./об.) с получением указанного в заголовке соединения (120,0 мг, 70,2%). МС (ИЭР) m/z - 356,2 (М+Н)+
[0974] Стадия 2: N-этил-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид
[0975] трет-бутил 4-(этил(хинолин-3-ил)амино)пиперидин-1-карбоксилат (120 мг, 0,34 ммоль), полученный на стадии 1, растворяли в дихлорметане (2,2 мл), а затем туда же добавляли (по каплям) в избытке 4,0 М соляную кислоту, растворенную в 1,4-диоксане. Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции, полученное твердое соединение фильтровали, промывали и высушивали вакуумом с получением указанного в заголовке соединения (72,7 мг, 65,6%) и использовали на следующей стадии без дополнительной очистки.
[0976] Эталонный пример 154. N-этил-N-(пиперидин-4-и)хинолин-6-амина гидрохлорид
[0977] Стадия 1: трет-бутил 4-(этил(хинолин-6-ил)амино)пирролидин-1-карбоксилат
[0978] Указанное в заголовке соединение (97,3 мг, 56,9%) получали таким же образом, как и на стадии 1 эталонного примера 153, за исключением того, что вместо 3-бромхинолина использовали 6-бромхинолин (100,0 мг, 0,48 ммоль). МС (ИЭР) m/z - 356,2 (М+Н)+
[0979] Стадия 2: N-этил-N-(пиперидин-4-ил)хинолин-6-амина гидрохлорид
[0980] Указанное в заголовке соединение (67,0 мг, 77,8%) получали таким же образом, как и на стадии 2 эталонного примера 153, и использовали на следующей стадии без дополнительной очистки.
[0981] Эталонный пример 155. N-этил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид
[0982] Стадия 1: трет-бутил 4-(этил(хинолин-5-ил)амино)пиперидин-1-карбоксилат
[0983] Указанное в заголовке соединение (93,1 мг, 54,4%) получали таким же образом, как и на стадии 1 эталонного примера 153, за исключением того, что вместо 3-бромхинолина использовали 5-бромхинолин (100,0 мг, 0,48 ммоль). МС (ИЭР) m/z - 356,2 (М+Н)+
[0984] Стадия 2: К-этил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид
[0985] Указанное в заголовке соединение (68,6 мг, 76,5%) получали таким же образом, как и на стадии 2 эталонного примера 153, и использовали на следующей стадии без дополнительной очистки.
[0986] Эталонный пример 156. N-метил-N-(пиперидин-4-ил)хинолин-2-амина гидрохлорид
[0987] Стадия 1: трет-бутил 4-(метил(хинолин-2-ил)амино)пиперидин-1-карбоксилат
[0988] Трет-бутил 4-(метиламино)пиперидин-1-карбоксилат (500,0 мг, 2,33 ммоль) растворяли в безводном толуоле. К полученному раствору добавляли 2-бромхинолин (485,4 мг, 2,33 ммоль), карбонат цезия (910 мг, 2,80 ммоль), трис(дибензилиденацетон)дипалладий (0) (210,0 мг, 0,23 ммоль) и (+/-)-2,2'-бис(дифенилфоспино)-1,1'-бинафталин (170,0 мг, 0,28 ммоль). Реакционную смесь нагревали в колбе с обратным холодильником и перемешивали при 100°С в течение ночи. После завершения реакции реакционную смесь охлаждали до комнатной температуры и затем добавляли воду для экстракции водного слоя этилацетатом. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (этилацетат / н-гексан = 1/1, об./об.) с получением указанного в заголовке соединения (203,8 мг, 25,5%). МС (ИЭР) m/z - 342,3 (М+Н)+
[0989] Стадия 2: N-метил-N-(пиперидин-4-ил)хинолин-2-амина гидрохлорид
[0990] Трет-бутил 4-(метил(хинолин-2-ил)амино)пиперидин-1-карбоксилат (203,8 мг, 0,34 ммоль), полученный на стадии 1, растворяли в дихлорметане (3,1 мл), а затем туда же добавляли (по каплям) в избытке 4,0 М соляную кислоту, растворенную в 1,4-диоксане. Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции, полученное твердое соединение фильтровали, промывали и высушивали вакуумом с получением указанного в заголовке соединения (128,8 мг, 68,6%) и использовали на следующей стадии без дополнительной очистки.
[0992] Стадия 1: трет-бутил 4-(метил(хинолин-4-ил)амино)пиперидин-1-карбоксилат
[0993] Указанное в заголовке соединение (85,2 мг, 15,5%) получали таким же образом, как на стадии 1 эталонного примера 156, за исключением того, что вместо 2-бромхинолина использовали 4-бромхинолин (485,4 мг, 2,33 ммоль). МС (ИЭР) m/z - 342,3 (М+Н)+
[0994] Стадия 2: N-метил-N-(пиперидин-4-ил)хинолин-4-амина гидрохлорид
[0995] Указанное в заголовке соединение (85,2 мг, 74,6%) получали таким же образом, как и на стадии 2 эталонного примера 156, и использовали на следующей стадии без дополнительной очистки.
[0996] Эталонный пример 158. N-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид
[0997] Стадия 1: трет-бутил 4-(метил(хинолин-5-ил)амино)пиперидин-1-карбоксилат
[0998] Указанное в заголовке соединение (154,7 мг, 19,4%) получали таким же образом, как на стадии 1 эталонного примера 156, за исключением того, что вместо 2-бромхинолина использовали 5-бромхинолин (485,4 мг, 2,33 ммоль). МС (ИЭР) m/z - 342,3 (М+Н)+
[0999] Стадия 2: N-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид
[1000] Указанное в заголовке соединение (141,0 мг, 99,1%) получали таким же образом, как и на стадии 2 эталонного примера 156, и использовали на следующей стадии без дополнительной очистки.
[1001] Эталонный пример 159. N-метил-N-(пиперидин-4-ил)хинолин-6-амина гидрохлорид
[1002] Стадия 1: трет-бутил 4-(метил(хинолин-6-ил)амино)пиперидин-1-карбоксилат
[1003] Указанное в заголовке соединение (184,2 мг, 23,1%) получали таким же образом, как на стадии 1 эталонного примера 156, за исключением того, что вместо 2-бромхинолина использовали 6-бромхинолин (485,4 мг, 2,33 ммоль). МС (ИЭР) m/z - 342,3 (М+Н)+
[1004] Стадия 2: N-метил-N-(пиперидин-4-ил)хинолин-6-амина гидрохлорид
[1005] Указанное в заголовке соединение (155,4 мг, 91,6%) получали таким же образом, как и на стадии 2 эталонного примера 156, и использовали на следующей стадии без дополнительной очистки.
[1006] Эталонный пример 160. N-метил-N-(пиперидин-4-ил)хинолин-7-амина гидрохлорид
[1007] Стадия 1: трет-бутил 4-(метил(хинолин-7-ил)амино)пиперидин-1-карбоксилат
[1008] Указанное в заголовке соединение (220,4 мг, 27,6%) получали таким же образом, как и на стадии 1 эталонного примера 156, за исключением того, что вместо 2-бромхинолина использовали 7-бромхинолин (485,4 мг, 2,33 ммоль). МС (ИЭР) m/z - 342,3 (М+Н)+
[1009] Стадия 2: N-метил-N-(пиперидин-4-ил)хинолин-7-амина гидрохлорид
[1010] Указанное в заголовке соединение (198,0 мг, 97,6%) получали таким же образом, как и на стадии 2 эталонного примера 156, и использовали на следующей стадии без дополнительной очистки.
[1011] Эталонный пример 161. N-метил-N-(пиперидин-4-ил)фуро[3,2-с]пиридин-7-амина гидрохлорид
[1012] Стадия 1: трет-бутил 4-(фуро[3,2-с]пиридин-7-ил (метил)амино)пиперидин-1-карбоксилат
[1013] Указанное в заголовке соединение (230,8 мг, 29,8%) получали таким же образом, как на стадии 1 эталонного примера 156, за исключением того, что вместо 2-бромхинолина использовали 7-бромфуро[3,2-с]пиридин (462,0 мг, 2,33 ммоль). МС (ИЭР) m/z - 332,3 (М+Н)+
[1014] Стадия 2: N-метил-N-(пиперидин-4-ил)фуро[3,2-с]пиридин-7-амина гидрохлорид
[1015] Указанное в заголовке соединение (153,7 мг, 72,5%) получали таким же образом, как и на стадии 2 эталонного примера 156, и использовали на следующей стадии без дополнительной очистки.
[1016] Эталонный пример 162. N-метил-N-(пиперидин-4-ил)изохинолин-5-амина гидрохлорид
[1017] Стадия 1: трет-бутил 4-(метил(изохинолин-5-ил)амино)пиперидин-1-карбоксилат
[1018] Указанное в заголовке соединение (228,0 мг, 28,6%) получали таким же образом, как на стадии 1 эталонного примера 156, за исключением того, что вместо 2-бромхинолина использовали 5-бромизохинолин (485,4 мг, 2,33 ммоль). МС (ИЭР) m/z - 342,3 (М+Н)+
[1019] Стадия 2: N-метил-N-(пиперидин-4-ил)изохинолин-5-амина гидрохлорид
[1020] Указанное в заголовке соединение (126,6 мг, 60,4%) получали таким же образом, как и на стадии 2 эталонного примера 156, и использовали на следующей стадии без дополнительной очистки.
[1021] Эталонный пример 163. N-метил-N-(пиперидин-4-ил)изохинолин-6-амина гидрохлорид
[1022] Стадия 1: трет-бутил 4-(метил(изохинолин-6-ил)амино)пиперидин-1-карбоксилат
[1023] Указанное в заголовке соединение (165,0 мг, 20,7%) получали таким же образом, как на стадии 1 эталонного примера 156, за исключением того, что вместо 2-бромхинолина использовали 6-бромизохинолин (485,4 мг, 2,33 ммоль). МС (ИЭР) m/z - 342,3 (М+Н)+
[1024] Стадия 2: N-метил-N-(пиперидин-4-ил)изохинолин-6-амина гидрохлорид
[1025] Указанное в заголовке соединение (119,0 мг, 47,6%) получали таким же образом, как и на стадии 2 эталонного примера 156, и использовали на следующей стадии без дополнительной очистки.
[1026] Эталонный пример 164. N-метил-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид
[1027] Стадия 1: трет-бутил 4-(метил(хинолин-3-ил)амино)пиперидин-1-карбоксилат
[1028] Указанное в заголовке соединение (124,0 мг, 15,5%) получали таким же образом, как на стадии 1 эталонного примера 156, за исключением того, что вместо 2-бромхинолина использовали 3-бромхинолин (485,4 мг, 2,33 ммоль). МС (ИЭР) m/z - 342,3 (М+Н)+
[1029] Стадия 2: N-метил-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид
[1030] Указанное в заголовке соединение (69,5 мг, 60,9%) получали таким же образом, как и на стадии 2 эталонного примера 156, и использовали на следующей стадии без дополнительной очистки.
[1031] Эталонный пример 165. N-метил-N-(пиперидин-4-ил)изохинолин-3-амина гидрохлорид
[1032] Стадия 1: трет-бутил 4-(метил(изохинолин-3-ил)амино)пиперидин-1-карбоксилат
[1033] Указанное в заголовке соединение (406,5 мг, 51,0%) получали таким же образом, как на стадии 1 эталонного примера 156, за исключением того, что вместо 2-бромхинолина использовали 3-бромизохинолин (485,4 мг, 2,33 ммоль). МС (ИЭР) m/z - 342,3 (М+Н)+
[1034] Стадия 2: N-метил-N-(пиперидин-4-ил)изохинолин-3-амина гидрохлорид
[1035] Указанное в заголовке соединение (238,6 мг, 63,8%) получали таким же образом, как и на стадии 2 эталонного примера 156, и использовали на следующей стадии без дополнительной очистки.
[1036] Эталонный пример 166. N-метил-N-(пиперидин-4-ил)изохинолин-7-амина гидрохлорид
[1037] Стадия 1: трет-бутил 4-(метил(изохинолин-7-ил)амино)пиперидин-1-карбоксилат
[1038] Указанное в заголовке соединение (245,0 мг, 30,7%) получали таким же образом, как и на стадии 1 эталонного примера 156, за исключением того, что вместо 2-бромхинолина использовали 7-бромизохинолин (485,4 мг, 2,33 ммоль). МС (ИЭР) m/z - 342,3 (М+Н)+
[1039] Стадия 2: N-метил-N-(пиперидин-4-ил)изохинолин-7-амина гидрохлорид
[1040] Указанное в заголовке соединение (132,7 мг, 58,3%) получали таким же образом, как и на стадии 2 эталонного примера 156, и использовали на следующей стадии без дополнительной очистки.
[1041] Эталонный пример 167. N-метил-N-(пиперидин-4-ил)изохинолин-8-амина гидрохлорид
[1042] Стадия 1: трет-бутил 4-(метил(изохинолин-8-ил)амино)пиперидин-1-карбоксилат
[1043] Указанное в заголовке соединение (514,5 мг, 64,6%) получали таким же образом, как на стадии 1 эталонного примера 156, за исключением того, что вместо 2-бромхинолина использовали 8-бромизохинолин (485,4 мг, 2,33 ммоль). МС (ИЭР) m/z - 342,3 (М+Н)+
[1044] Стадия 2: N-метил-N-(пиперидин-4-ил)изохинолин-8-амина гидрохлорид
[1045] Указанное в заголовке соединение (303,3 мг, 64,1%) получали таким же образом, как и на стадии 2 эталонного примера 156, и использовали на следующей стадии без дополнительной очистки.
[1046] Эталонный пример 168. N,6-диметил-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид
[1047] Стадия 1: трет-бутил 4-(метил(6-метилхинолин-3-ил)амино)пиперидин-1-карбоксилат
[1048] Указанное в заголовке соединение (750,3 мг, 45,2%) получали таким же образом, как и на стадии 1 эталонного примера 156, за исключением того, что вместо 2-бромхинолина использовали 3-бром-6-метилхинолин(518,1 мг, 2,33 ммоль). МС (ИЭР) m/z - 356,2 (М+Н)+
[1049] Стадия 2: N,6-диметил-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид
[1050] Указанное в заголовке соединение (525,6 мг, 75,8%) получали таким же образом, как и на стадии 2 эталонного примера 156, и использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 256,2 (М+Н)+
[1051] Эталонный пример 169. 6-метокси-N-метил-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид
[1052] Стадия 1: трет-бутил 4-(метил(6-метоксихинолин-3-ил)амино)пиперидин-1-карбоксилат
[1053] Указанное в заголовке соединение (781,3 мг, 45,2%) получали таким же образом, как на стадии 1 эталонного примера 156, за исключением того, что вместо 2-бромхинолина использовали 3-бром-6-метоксихинолин (555,5 мг, 2,33 ммоль). МС (ИЭР) m/z - 372,2 (М+Н)+
[1054] Стадия 2: 6-метокси-N-метил-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид
[1055] Указанное в заголовке соединение (420,3 мг, 57,8%) получали таким же образом, как и на стадии 2 эталонного примера 156, и использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 272,1 (М+Н)+
[1056] Эталонный пример 170. 7-метокси-N-метил-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид
[1057] Стадия 1: трет-бутил 4-(метил(7-метоксихинолин-3-ил)амино)пиперидин-1-карбоксилат
[1058] Указанное в заголовке соединение (778,3 мг, 44,9%) получали таким же образом, как на стадии 1 эталонного примера 156, за исключением того, что вместо 2-бромхинолина использовали 3-бром-7-метоксихинолин (555,5 мг, 2,33 ммоль). МС (ИЭР) m/z - 372,2 (М+Н)+
[1059] Стадия 2: 7-метокси-N-метил-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид
[1060] Указанное в заголовке соединение (303,3 мг, 41,7%) получали таким же образом, как и на стадии 2 эталонного примера 156, и использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 272,2 (М+Н)+
[1061] Эталонный пример 171. 8-метокси-N-метил-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид
[1062] Стадия 1: трет-бутил 4-(метил(8-метоксихинолин-3-ил)амино)пиперидин-1-карбоксилат
[1063] Указанное в заголовке соединение (780,0 мг, 45,0%) получали таким же образом, как на стадии 1 эталонного примера 156, за исключением того, что вместо 2-бромхинолина использовали 3-бром-8-метоксихинолин (555,5 мг, 2,33 ммоль). МС (ИЭР) m/z - 372,2 (М+Н)+
[1064] Стадия 2: 8-метокси-N-метил-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид
[1065] Указанное в заголовке соединение (645,5 мг, 88,8%) получали таким же образом, как и на стадии 2 эталонного примера 156, и использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 272,2 (М+Н)+
[1066] Эталонный пример 172. 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид
[1067] Стадия 1: трет-бутил 4-((8-фторхинолин-5-ил)амино)пиперидин-1-карбоксилат
[1068] Указанное в заголовке соединение (163,9 мг, 38,0%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 5-бром-8-фторхинолин (282,2 мг, 1,25 ммоль). МС (ИЭР) m/z - 293,1 (М+Н)+
[1069] Стадия 2: 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид
[1070] Указанное в заголовке соединение (151,0 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1071] Эталонный пример 173. 8-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид
[1072] Стадия 1: трет-бутил 4-((8-метилхинолин-5-ил)амино)пиперидин-1-карбоксилат
[1073] Указанное в заголовке соединение (66,5 мг, 15,6%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 5-бром-8-метилхинолин (277,2 мг, 1,25 ммоль). МС (ИЭР) m/z - 342,3 (М+Н)+
[1074] Стадия 2: 8-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид
[1075] Указанное в заголовке соединение (61,2 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1076] Эталонный пример 174. 8-(бензилокси)-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид
[1077] Стадия 1: трет-бутил 4-((8-(бензилокси)хинолин-5-ил)амино)пиперидин-1-карбоксилат
[1078] Указанное в заголовке соединение (143,2 мг, 26,5%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 8-(бензилокси)-5-бромхинолин (392,2 мг, 1,25 ммоль). МС (ИЭР) m/z - 434,3 (М+Н)+
[1079] Стадия 2: 8-(бензилокси)-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид
[1080] Указанное в заголовке соединение (134,2 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1081] Эталонный пример 175. 3-хлор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид
[1082] Стадия 1: трет-бутил 4-((3-хлорхинолин-5-ил)амино) пиперидин-1-карбоксилат
[1083] Указанное в заголовке соединение (261,0 мг, 57,8%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 5-бром-3-хлорхинолин (302,7 мг, 1,25 ммоль). МС (ИЭР) m/z - 262,1 (М+Н)+
[1084] Стадия 2: 3-хлор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид
[1085] Указанное в заголовке соединение (241,4 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1086] Эталонный пример 176. N-(пиперидин-4-ил)-8-(трифторметил)хинолин-5-амина гидрохлорид
[1087] Стадия 1: трет-бутил 4-((8-(трифторметил)хинолин-5-ил)амино)пиперидин-1-карбоксилат
[1088] Указанное в заголовке соединение (147,6 мг, 29,9%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 5-бром-8-(трифторметил)хинолин (344,6 мг, 1,25 ммоль). МС (ИЭР) m/z - 396,2 (М+Н)+
[1089] Стадия 2: N-(пиперидин-4-ил)-8-(трифторметил)хинолин-5-амина гидрохлорид
[1090] Указанное в заголовке соединение (137,5 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1091] Эталонный пример 177. 5-(пиперидин-4-иламино) хинолин-2-карбонитрил гидрохлорид
[1092] Стадия 1: трет-бутил 4-((8-(трифторметил)хинолин-5-ил)амино)пиперидин-1-карбоксилат
[1093] Указанное в заголовке соединение (324,8 мг, 73,8%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 5-бромхинолин-2-карбонитрил (290,9 мг, 1,25 ммоль). МС (ИЭР) m/z -353,2 (М+Н)+
[1094] Стадия 2: 5-(пиперидин-4-иламино) хинолин-2-карбонитрил гидрохлорид
[1095] Указанное в заголовке соединение (299,7 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1096] Эталонный пример 178. N-(бензо[b]тиофен-4-ил)пиперидин-4-амина гидрохлорид
[1097] Стадия 1: трет-бутил 4-(бензо[b]тиофен-4-иламино)пиперидин-1-карбоксилат
[1098] Указанное в заголовке соединение (220,4 мг, 53,1%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 4-бромбензо[b]тиофен (266,0 мг, 1,25 ммоль). МС (ИЭР) m/z - 333,1 (М+Н)+
[1099] Стадия 2: N-(бензо[b]тиофен-4-ил)пиперидин-4-амина гидрохлорид
[1100] Указанное в заголовке соединение (220,4 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1101] Эталонный пример 179. 6-фтор-N-(пиперидин-4-ил)хинолин-4-амина гидрохлорид
[1102] Стадия 1: трет-бутил 4-((6-фторхинолин-4-ил)амино)пиперидин-1-карбоксилат
[1103] Указанное в заголовке соединение (167,7 мг, 38,9%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 4-бром-6-фторхинолин (282,2 мг, 1,25 ммоль). МС (ИЭР) m/z - 346,2 (М+Н)+
[1104] Стадия 2: 6-фтор-N-(пиперидин-4-ил)хинолин-4-амина гидрохлорид
[1105] Указанное в заголовке соединение (154,5 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1106] Эталонный пример 180. 6-хлор-N-(пиперидин-4-ил)хинолин-4-амина гидрохлорид
[1107] Стадия 1: трет-бутил 4-((6-хлорхинолин-4-ил)амино) пиперидин-1-карбоксилат
[1108] Указанное в заголовке соединение (210,0 мг, 46,5%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 4-бром-6-хлорхинолин (302,7 мг, 1,25 ммоль). МС (ИЭР) m/z - 362,2 (М+Н)+
[1109] Стадия 2: 6-хлор-N-(пиперидин-4-ил)хинолин-4-амина гидрохлорид
[1110] Указанное в заголовке соединение (194,2 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1111] Эталонный пример 181. N-(пиперидин-4-ил)изохинолин-4-амина гидрохлорид
[1112] Стадия 1: трет-бутил-4-(изохинолин-4-иламино)пиперидин-1-карбоксилат
[1113] Указанное в заголовке соединение (381,7 мг, 93,4%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 4-бромизохинолин (259,7 мг, 1,25 ммоль). МС (ИЭР) m/z - 328,2 (М+Н)+
[1114] Стадия 2: N-(пиперидин-4-ил)изохинолин-4-амина гидрохлорид
[1115] Указанное в заголовке соединение (350,0 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1116] Эталонный пример 182. N-(пиперидин-4-ил)изохинолин-5-амина гидрохлорид
[1117] Стадия 1: трет-бутил-4-(изохинолин-5-иламино)пиперидин-1-карбоксилат
[1118] Указанное в заголовке соединение (333,6 мг, 81,6%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 5-бромизохинолин (259,7 мг, 1,25 ммоль). МС (ИЭР) m/z - 328,2 (М+Н)+
[1119] Стадия 2: N-(пиперидин-4-ил)изохинолин-5-амина гидрохлорид
[1120] Указанное в заголовке соединение (305,9 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1121] Эталонный пример 183. N-(пиперидин-4-ил)изохинолин-6-амина гидрохлорид
[1122] Стадия 1: трет-бутил-4-(изохинолин-6-иламино)пиперидин-1-карбоксилат
[1123] Указанное в заголовке соединение (150,1 мг, 36,7%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 6-бромизохинолин (259,7 мг, 1,25 ммоль). МС (ИЭР) m/z - 328,2 (М+Н)+
[1124] Стадия 2: N-(пиперидин-4-ил)изохинолин-6-амина гидрохлорид
[1125] Указанное в заголовке соединение (137,6 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1126] Эталонный пример 184. N-(пиперидин-4-ил)изохинолин-8-амина гидрохлорид
[1127] Стадия 1: трет-бутил-4-(изохинолин-8-иламино)пиперидин-1-карбоксилат
[1128] Указанное в заголовке соединение (408,7 мг, 99,9%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 8-бромизохинолин (259,7 мг, 1,25 ммоль). МС (ИЭР) m/z - 328,2 (М+Н)+
[1129] Стадия 2: N-(пиперидин-4-ил)изохинолин-8-амина гидрохлорид
[1130] Указанное в заголовке соединение (374,8 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1131] Эталонный пример 185. 8-метил-N-(пиперидин-4-ил)хинолин-4-амина гидрохлорид
[1132] Стадия 1: трет-бутил 4-((8-метилхинолин-4-ил)амино)пиперидин-1-карбоксилат
[1133] Указанное в заголовке соединение (336,4 мг, 78,9%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 4-бром-8-метилхинолин (277,2 мг, 1,25 ммоль). МС (ИЭР) m/z - 342,2 (М+Н)+
[1134] Стадия 2: 8-метил-N-(пиперидин-4-ил)хинолин-4-амина гидрохлорид
[1135] Указанное в заголовке соединение (309,6 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1136] Эталонный пример 186. 8-хлор-N-(пиперидин-4-ил)хинолин-4-амина гидрохлорид
[1137] Стадия 1: трет-бутил 4-((8-хлорхинолин-4-ил)амино) пиперидин-1-карбоксилат
[1138] Указанное в заголовке соединение (75,8 мг, 16,8%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 4-бром-8-хлорхинолин (302,7 мг, 1,25 ммоль). МС (ИЭР) m/z - 362,2 (М+Н)+
[1139] Стадия 2: 8-хлор-N-(пиперидин-4-ил)хинолин-4-амина гидрохлорид
[1140] Указанное в заголовке соединение (70,1 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1141] Эталонный пример 187. 8-фтор-N-(пиперидин-4-ил)хинолин-4-амина гидрохлорид
[1142] Стадия 1: трет-бутил 4-((8-фторхинолин-4-ил)амино)пиперидин-1-карбоксилат
[1143] Указанное в заголовке соединение (209,4 мг, 48,6%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 4-бром-8-фторхинолин (282,2 мг, 1,25 ммоль). МС (ИЭР) m/z - 346,2 (М+Н)+
[1144] Стадия 2: 8-фтор-N-(пиперидин-4-ил)хинолин-4-амина гидрохлорид
[1145] Указанное в заголовке соединение (192,9 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1146] Эталонный пример 188. N-(пиперидин-4-ил)-8-(трифторметил)хинолин-4-амина гидрохлорид
[1147] Стадия 1: трет-бутил 4-((8-(трифторметил)хинолин-4-ил)амино)пиперидин-1-карбоксилат
[1148] Указанное в заголовке соединение (366,5 мг, 74,3%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 4-бром-8-(трифторметил)хинолин (344,6 мг, 1,25 ммоль). МС (ИЭР) m/z -396,2 (М+Н)+
[1149] Стадия 2: N-(пиперидин-4-ил)-8-(трифторметил)хинолин-4-амина гидрохлорид
[1150] Указанное в заголовке соединение (341,3 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1151] Эталонный пример 189. N-(пиперидин-4-ил)-8-(трифторметокси)хинолин-5-амина гидрохлорид
[1152] Стадия 1: трет-бутил 4-((8-(трифторметокси)хинолин-5-ил)амино)пиперидин-1-карбоксилат
[1153] Указанное в заголовке соединение (437,1 мг, 85,1%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 5-бром-8-трифторметоксихинолин (364,6 мг, 1,25 ммоль). МС (ИЭР) m/z - 412,2 (М+Н)+
[1154] Стадия 2: N-(пиперидин-4-ил)-8-(трифторметокси)хинолин-5-амина гидрохлорид
[1155] Указанное в заголовке соединение (408,2 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1156] Эталонный пример 190. 3-метокси-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид
[1157] Стадия 1: трет-бутил 4-((3-метоксихинолин-5-ил)амино)пиперидин-1-карбоксилат
[1158] Указанное в заголовке соединение (327,6 мг, 73,4%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 5-бром-3-метоксихинолин (297,2 мг, 1,25 ммоль). МС (ИЭР) m/z - 358,2 (М+Н)+
[1159] Стадия 2: 3-метокси-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид
[1160] Указанное в заголовке соединение (302,7 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1161] Эталонный пример 191. 3-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид
[1162] Стадия 1: трет-бутил 4-((3-фторхинолин-5-ил)амино)пиперидин-1-карбоксилат
[1163] Указанное в заголовке соединение (343,7 мг, 79,7%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 5-бром-3-фторхинолин (282,2 мг, 1,25 ммоль). МС (ИЭР) m/z - 346,2 (М+Н)+
[1164] Стадия 2: 3-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид
[1165] Указанное в заголовке соединение (316,6 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1166] Эталонный пример 192. 1-хлор-N-(пиперидин-4-ил)изохинолин-5-амина гидрохлорид
[1167] Стадия 1: трет-бутил 4-((1-хлоризохинолин-5-ил)амино)пиперидин-1-карбоксилат
[1168] Указанное в заголовке соединение (49,5 мг, 11,0%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 5-бром-1-хлоризохинолин (302,7 мг, 1,25 ммоль). МС (ИЭР) m/z - 362,2 (М+Н)+
[1169] Стадия 2: 1-хлор-N-(пиперидин-4-ил)изохинолин-5-амина гидрохлорид
[1170] Указанное в заголовке соединение (45,8 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1171] Эталонный пример 193. 3-хлор-N-(пиперидин-4-ил)изохинолин-5-амина гидрохлорид
[1172] Стадия 1: трет-бутил 4-((3-хлоризохинолин-5-ил)амино)пиперидин-1-карбоксилат
[1173] Указанное в заголовке соединение (332,2 мг, 73,5%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 5-бром-3-хлоризохинолин (302,7 мг, 1,25 ммоль). МС (ИЭР) m/z - 362,2 (М+Н)+
[1174] Стадия 2: 3-хлор-N-(пиперидин-4-ил)изохинолин-5-амина гидрохлорид
[1175] Указанное в заголовке соединение (307,2 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1176] Эталонный пример 194. 8-хлор-N-(пиперидин-4-ил)изохинолин-5-амина гидрохлорид
[1177] Стадия 1: трет-бутил 4-((8-хлоризохинолин-5-ил)амино)пиперидин-1-карбоксилат
[1178] Указанное в заголовке соединение (265,1 мг, 58,7%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 5-бром-8-хлоризохинолин (302,7 мг, 1,25 ммоль). МС (ИЭР) m/z - 362,2 (М+Н)+
[1179] Стадия 2: 8-хлор-N-(пиперидин-4-ил)изохинолин-5-амина гидрохлорид
[1180] Указанное в заголовке соединение (245,2 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1181] Эталонный пример 195. 4-метил-N-(пиперидин-4-ил)изохинолин-5-амина гидрохлорид
[1182] Стадия 1: трет-бутил 4-((4-метилизохинолин-5-ил)амино)пиперидин-1-карбоксилат
[1183] Указанное в заголовке соединение (284,3 мг, 66,7%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 5-бром-4-метилизохинолин (277,2 мг, 1,25 ммоль). МС (ИЭР) m/z - 342,2 (М+Н)+
[1184] Стадия 2: 4-метил-N-(пиперидин-4-ил)изохинолин-5-амина гидрохлорид
[1185] Указанное в заголовке соединение (261,6 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1186] Эталонный пример 196. 3-метокси-N-(пиперидин-4-ил)изохинолин-5-амина гидрохлорид
[1187] Стадия 1: трет-бутил 4-((3-метоксиизохинолин-5-ил)амино)пиперидин-1-карбоксилат
[1188] Указанное в заголовке соединение (407,0 мг, 91,2%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 5-бром-3-метоксиизохинолин (297,2 мг, 1,25 ммоль). МС (ИЭР) m/z - 358,2 (М+Н)+
[1189] Стадия 2: 3-метокси-N-(пиперидин-4-ил)изохинолин-5-амина гидрохлорид
[1190] Указанное в заголовке соединение (376,0 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1191] Эталонный пример 197. 8-нитро-N-(пиперидин-4-ил)изохинолин-5-амина гидрохлорид
[1192] Стадия 1: трет-бутил 4-((8-нитроизохинолин-5-ил)амино)пиперидин-1-карбоксилат
[1193] Указанное в заголовке соединение (178,1 мг, 38,2%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 5-бром-8-нитроизохинолин (315,9 мг, 1,25 ммоль). МС (ИЭР) m/z - 373,2 (М+Н)+
[1194] Стадия 2: 8-нитро-N-(пиперидин-4-ил)изохинолин-5-амина гидрохлорид
[1195] Указанное в заголовке соединение (165,1 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1196] Эталонный пример 198. 8-фтор-N-(пиперидин-4-ил)изохинолин-5-амина гидрохлорид
[1197] Стадия 1: трет-бутил 4-((8-фторизохинолин-5-ил)амино)пиперидин-1-карбоксилат
[1198] Указанное в заголовке соединение (377,9 мг, 87,7%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 5-бром-8-фторизохинолин (282,2 мг, 1,25 ммоль). МС (ИЭР) m/z - 346,2 (М+Н)+
[1199] Стадия 2: 8-фтор-N-(пиперидин-4-ил)изохинолин-5-амина гидрохлорид
[1200] Указанное в заголовке соединение (348,2 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1201] Эталонный пример 199. 2-хлор-6,7-диметокси-N-(пиперидин-4-ил)хиназолин-4-амина гидрохлорид
[1202] Стадия 1: трет-бутил 4-((2-хлор-6,7-диметоксихиназолин-4-ил)амино)пиперидин-1-карбоксилат
[1203] Трет-бутил 4-аминопиперидин-1-карбоксилат (250,0 мг, 1,25 ммоль) растворялив безводном дихлорметане. К полученному раствору добавляли 2,4-дихлор-6,7-диметоксихиназолин (291,1 мг, 1,12 ммоль) и триэтиламин (0,35 мл, 2,50 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции к реакционной смеси добавляли насыщенный водный раствор NH4Cl. Водный слой реакционной смеси экстрагировали дихлорметаном. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (этилацетат / н-гексан = 1/1, об./об.) с получением указанного в заголовке соединения (204,0 мг, 38,6%). МС (ИЭР) m/z - 423,2 (М+Н)+
[1204] Стадия 2: 2-хлор-6,7-диметокси-N-(пиперидин-4-ил)хиназолин-4-амина гидрохлорид
[1205] трет-бутил 4-((2-хлор-6,7-диметоксихиназолин-4-ил)амино)пиперидин-1-карбоксилат (204,0 мг, 0,48 ммоль), приготовленный на стадии 1, растворяли в дихлорметане (5,0 мл). К полученному раствору добавляли по каплям избыток 4,0 М соляной кислоты, растворенной в 1,4-диоксане. Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции полученное твердое вещество фильтровали и высушивали с получением указанного в заголовке соединения (190,9 мг, 100,0%). Указанное в заголовке соединение использовали на следующей стадии без дополнительной очистки.
[1206] Эталонный пример 200. 2-хлор-8-метил-N-(пиперидин-4-ил)хиназолин-4-амина гидрохлорид
[1207] Стадия 1: трет-бутил 4-((2-хлор-8-метилхиназолин-4-ил)амино)пиперидин-1-карбоксилат
[1208] Указанное в заголовке соединение (138,7 мг, 29,5%) получали таким же образом, как и на стадии 1 эталонного примера 199, за исключением того, что вместо 2,4-дихлор-6,7-диметоксихиназолина использовали 2,4-дихлор-8-метилхиназолин (239,4 мг, 1,25 ммоль). МС (ИЭР) m/z - 377,2 (М+Н)+
[1209] Стадия 2: 2-хлор-8-метил-N-(пиперидин-4-ил)хиназолин-4-амина гидрохлорид
[1210] Указанное в заголовке соединение (128,7 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 199, и использовали на следующей стадии без дополнительной очистки.
[1211] Эталонный пример 201. N-(пиперидин-4-ил)-2,6-нафтиридин-4-амина гидрохлорид
[1212] Стадия 1: трет-бутил 4-((2,6-нафтиридин-4-ил)амино)пиперидин-1-карбоксилат
[1213] Указанное в заголовке соединение (113,5 мг, 27,7%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 4-бром-2,6-нафтиридин (260,9 мг, 1,25 ммоль). МС (ИЭР) m/z - 329,2 (М+Н)+
[1214] Стадия 2: N-(пиперидин-4-ил)-2,6-нафтиридин-4-амина гидрохлорид
[1215] Указанное в заголовке соединение (104,1 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1216] Эталонный пример 202. 8-хлор-N-(пиперидин-4-ил)изохинолин-4-амина гидрохлорид
[1217] Стадия 1: трет-бутил 4-((8-хлоризохинолин-4-ил)амино)пиперидин-1-карбоксилат
[1218] Указанное в заголовке соединение (102,8 мг, 22,8%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 4-бром-8-хлоризохинолин (302,7 мг, 1,25 ммоль). МС (ИЭР) m/z - 362,2 (М+Н)+
[1219] Стадия 2: 8-хлор-N-(пиперидин-4-ил)изохинолин-4-амина гидрохлорид
[1220] Указанное в заголовке соединение (95,1 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1221] Эталонный пример 203. N-(пиперидин-4-ил)хинолин-3- амина гидрохлорид [1222] Стадия 1: трет-бутил 4-(хинолин-3-иламино)пиперидин-1-карбоксилат
[1223] Указанное в заголовке соединение (212,5 мг, 99,9%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 3-бромхинолин (135,0 мг, 0,65 ммоль). МС (ИЭР) m/z - 328,2 (М+Н)+
[1224] Стадия 2: N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид
[1225] Указанное в заголовке соединение (202,9 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1226] Эталонный пример 204. 6-метил-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид
[1227] Стадия 1: трет-бутил 4-((6-метилхинолин-3-ил)амино)пиперидин-1-карбоксилат
[1228] Указанное в заголовке соединение (143,3 мг, 64,7%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 3-бром-6-метилхинолин (144,2 мг, 0,65 ммоль). МС (ИЭР) m/z - 342,3 (М+Н)+
[1229] Стадия 2: 6-метил-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид
[1230] Указанное в заголовке соединение (131,9 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1231] Эталонный пример 205. 6-фтор-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид
[1232] Стадия 1: трет-бутил 4-((6-фторхинолин-3-ил)амино)пиперидин-1-карбоксилат
[1233] Указанное в заголовке соединение (218,3 мг, 64,7%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 3-бром-6-фторхинолин (146,7 мг, 0,65 ммоль). МС (ИЭР) m/z - 346,2 (М+Н)+
[1234] Стадия 2: 6-фтор-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид
[1235] Указанное в заголовке соединение (201,1 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1236] Эталонный пример 206. 6-метокси-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид
[1237] Стадия 1: трет-бутил 4-((6-метоксихинолин-3-ил)амино)пиперидин-1-карбоксилат
[1238] Указанное в заголовке соединение (194,2 мг, 83,7%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 3-бром-6-метоксихинолин (154,5 мг, 0,65 ммоль). МС (ИЭР) m/z - 358,2 (М+Н)+
[1239] Стадия 2: 6-метокси-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид
[1240] Указанное в заголовке соединение (179,4 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1241] Эталонный пример 207. 7-метокси-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид
[1242] Стадия 1: трет-бутил 4-((7-метоксихинолин-3-ил)амино)пиперидин-1-карбоксилат
[1243] Указанное в заголовке соединение (66,0 мг, 28,5%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 3-бром-7-метоксихинолин (154,5 мг, 0,65 ммоль). МС (ИЭР) m/z - 358,2 (М+Н)+
[1244] Стадия 2: 7-метокси-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид
[1245] Указанное в заголовке соединение (61,0 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1246] Эталонный пример 208. 8-метокси-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид
[1247] Стадия 1: трет-бутил 4-((8-метоксихинолин-3-ил)амино)пиперидин-1-карбоксилат
[1248] Указанное в заголовке соединение (78,5 мг, 33,8%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 3-бром-8-метоксихинолин (154,5 мг, 0,65 ммоль). МС (ИЭР) m/z - 358,1 (М+Н)+
[1249] Стадия 2: 8-метокси-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид
[1250] Указанное в заголовке соединение (72,5 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1251] Эталонный пример 209. N-(пиперидин-4-ил)-1,8-нафтиридин-3-амина гидрохлорид
[1252] Стадия 1: трет-бутил 4-((1,8-нафтиридин-3-ил)амино)пиперидин-1-карбоксилат
[1253] Указанное в заголовке соединение (189,1 мг, 46,1%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 3-бром-1,8-нафтиридин (260,9 мг, 1,25 ммоль). МС (ИЭР) m/z - 329,2 (М+Н)+
[1254] Стадия 2: N-(пиперидин-4-ил)-1,8-нафтиридин-3-амина гидрохлорид
[1255] Указанное в заголовке соединение (173,4 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1256] Эталонный пример 210. 7-хлор-N-(пиперидин-4-ил)-1,8-нафтиридин-3-амина гидрохлорид
[1257] Стадия 1: трет-бутил 4-((7-хлор-1,8-нафтиридин-3-ил)амино)пиперидин-1-карбоксилат
[1258] Указанное в заголовке соединение (57,9 мг, 12,8%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 6-бром-2-хлор-1,8-нафтиридин (303,9 мг, 1,25 ммоль). МС (ИЭР) m/z - 363,2 (М+Н)+
[1259] Стадия 2: 7-хлор-N-(пиперидин-4-ил)-1,8-нафтиридин-3-амина гидрохлорид
[1260] Указанное в заголовке соединение (53,6 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1261] Эталонный пример 211. 8-этокси-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид
[1262] Стадия 1: трет-бутил 4-((8-этоксихинолин-5-ил)амино)пиперидин-1-карбоксилат
[1263] Указанное в заголовке соединение (776,4 мг, 83,7%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 5-бром-8-этоксихинолин (629,4 мг, 2,49 ммоль). МС (ИЭР) m/z - 372,2 (М+Н)+
[1264] Стадия 2: 8-этокси-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид
[1265] Указанное в заголовке соединение (432,6 мг, 60,1%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 272,2 (М+Н)+
[1266] Эталонный пример 212. N-(пиперидин-4-ил)бензо[d]тиазол-7-амина гидрохлорид
[1267] Стадия 1: трет-бутил 4-(1,3-бензотиазол-7-иламино)пиперидин-1-карбоксилат
[1268] 1-Boc-4-пиперидон (250,0 мг, 1,26 ммоль) растворяли в безводном дихлорметане. К полученному раствору добавляли бензо[d]тиазол-7-амин (188,5 мг, 1,26 ммоль), уксусную кислоту (0,15 мл) и триацетоксиборгидрид натрия (265,9 мг, 1,26 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции в реакционную смесь добавляли насыщенный водный раствор карбоната натрия. Водный слой реакционной смеси экстрагировали дихлорметаном. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (этилацетат / н-гексан = 1/1, об./об.) с получением указанного в заголовке соединения (375,3 мг, 89,7%). МС (ИЭР) m/z - 334,2 (М+Н)+
[1269] Стадия 2: N-(пиперидин-4-ил)бензо[d]тиазол-7-амина гидрохлорид
[1270] Трет-бутил 4-(1,3-бензотиазол-7-иламино)пиперидин-1-карбоксилат (375,3 мг, 1,13 ммоль), полученный на стадии 1, растворяли в дихлорметане (5,0 мл). К полученному раствору добавляли по каплям избыток 4,0 М соляной кислоты, растворенной в 1,4-диоксане. Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции полученное твердое вещество фильтровали и высушивали с получением указанного в заголовке соединения (344,8 мг, 100,0%). Указанное в заголовке соединение использовали на следующей стадии без дополнительной очистки.
[1271] Эталонный пример 213. 1-(4-(пиперидин-4-иламино) индолин-1-ил) этан-1-он гидрохлорид
[1272] Стадия 1: трет-бутил 4-[(1-ацетилиндолин-4-ил)амино]пиперидин-1-карбоксилат
[1273] Указанное в заголовке соединение (310,2 мг, 68,8%) получали таким же образом, как на стадии 1 эталонного примера 212, за исключением того, что вместо бензо[d]тиазол-7-амин использовали 1-(4-аминоиндолин-1-ил)этанон (221,1 мг, 1,26 ммоль). МС (ИЭР) m/z - 360,2 (М+Н)+
[1274] Стадия 2: 1-(4-(пиперидин-4-иламино) индолин-1-ил) этан-1-он гидрохлорид
[1275] Указанное в заголовке соединение (286,8 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 212, и использовали на следующей стадии без дополнительной очистки.
[1276] Эталонный пример 214. 8-метил-N-(пиперидин-4-ил)хинолин-6-амина гидрохлорид
[1277] Стадия 1: трет-бутил 4-((8-метилхинолин-6-ил)амино)пиперидин-1-карбоксилат
[1278] Указанное в заголовке соединение (196,4 мг, 50,1%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 6-бром-8-метилхинолин (255,0 мг, 1,15 ммоль). МС (ИЭР) m/z - 342,2 (М+Н)+
[1279] Стадия 2: 8-метил-N-(пиперидин-4-ил)хинолин-6-амина гидрохлорид
[1280] Указанное в заголовке соединение (180,7 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1281] Эталонный пример 215. 8-фтор-N-(пиперидин-4-ил)хинолин-6-амина гидрохлорид
[1282] Стадия 1: трет-бутил 4-((8-фторхинолин-6-ил)амино)пиперидин-1-карбоксилат
[1283] Указанное в заголовке соединение (317,3 мг, 80,0%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 6-бром-8-фторхинолин (259,6 мг, 1,15 ммоль). МС (ИЭР) m/z - 346,2 (М+Н)+
[1284] Стадия 2: 8-фтор-N-(пиперидин-4-ил)хинолин-6-амина гидрохлорид
[1285] Указанное в заголовке соединение (292,4 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1286] Эталонный пример 216. 8-хлор-N-(пиперидин-4-ил)хинолин-6-амина гидрохлорид
[1287] Стадия 1: трет-бутил 4-((8-хлорхинолин-6-ил)амино) пиперидин-1-карбоксилат
[1288] Указанное в заголовке соединение (369,5 мг, 88,9%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 6-бром-8-хлорхинолин (278,5 мг, 1,15 ммоль). МС (ИЭР) m/z - 362,2 (М+Н)+
[1289] Стадия 2: 8-хлор-N-(пиперидин-4-ил)хинолин-6-амина гидрохлорид
[1290] Указанное в заголовке соединение (341,7 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1291] Эталонный пример 217. N-(пиперидин-4-ил)-8-(трифторметил)хинолин-6-амина гидрохлорид
[1292] Стадия 1: трет-бутил 4-((8-(трифторметил)хинолин-6-ил)амино)пиперидин-1-карбоксилат
[1293] Указанное в заголовке соединение (284,3 мг, 62,6%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 6-бром-8-(трифторметил)хинолин (317,0 мг, 1,15 ммоль). МС (ИЭР) m/z - 396,2 (М+Н)+
[1294] Стадия 2: N-(пиперидин-4-ил)-8-(трифторметил)хинолин-6-амина гидрохлорид
[1295] Указанное в заголовке соединение (264,8 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1296] Эталонный пример 218. 4-(пиперидин-4-иламино)-2Н-хромен-2-она гидрохлорид
[1297] Стадия 1: трет-бутил 4-((2-оксо-2Н-хромен-4-ил)амино) пиперидин-1-карбоксилат
[1298] Трет-бутил 4-аминопиперидин-1-карбоксилат (300 мг, 1,4 ммоль) растворяли в безводном DMF. К полученному раствору добавляли 4-бром-2Н-хромен-2-он (337,1 мг, 1,49 ммоль) и карбонат калия (414,0 мг, 2,996 ммоль). Реакционную смесь перемешивали при 100°С в течение ночи. После завершения реакции реакционную смесь охлаждали до комнатной температуры и затем добавляли воду для экстракции водного слоя этилацетатом. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (этилацетат / н-гексан = 1/1, об./об.) с получением указанного в заголовке соединения (300 мг, 58,1%). 1H-ЯМР (MeOD4, 400 МГц) δ 8,01 (дд, 1Н), 7,61 (тд, 1Н), 7,36-7,32 (м, 2Н), 5,41 (с, 1Н), 4,16 (д, 2Н), 3,77-3,75 (м, 1Н), 2,97 (с, 2Н), 2,07-2,02 (м, 2Н), 1,60-1,53 (м, 2Н), 1,49 (с, 9Н).
[1299] Стадия 2: 4-(пиперидин-4-иламино)-2Н-хромен-2-она гидрохлорид
[1300] Указанное в заголовке соединение (210,0 мг, 76,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки. 1H-ЯМР (MeOD4, 400 МГц) δ 8,05 (дд, 1Н), 7,63 (тд, 1Н), 7,38-7,33 (м, 2Н), 5,45 (с, 1Н), 3,95-3,89 (м, 1Н), 3,53 (д, 2Н), 3,22 (тд, 2Н), 2,33 (д, 2Н), 2,00-1,89 (м, 2Н).
[1301] Эталонный пример 219. N-(пиперидин-4-ил)-1,5-нафтиридин-4-амингидрохлорид
[1302] Стадия 1: трет-бутил 4-((1,5-нафтиридин-4-ил)амино)пиперидин-1-карбоксилат
[1303] Указанное в заголовке соединение (700,0 мг, 85,4%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 4-бром-1,5-нафтиридин (521,8 мг, 2,49 ммоль). МС (ИЭР) m/z - 329,2 (М+Н)+
[1304] Стадия 2: N-(пиперидин-4-ил)-1,5-нафтиридин-4-амингидрохлорид
[1305] Указанное в заголовке соединение (321,0 мг, 80,6%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки. МС (ИЭР) m/z - 229,2 (М+Н)+
[1306] Эталонный пример 220. N-(пиперидин-4-ил)-2-(трифторметил)хинолин-6-амина гидрохлорид
[1307] Стадия 1: трет-бутил 4-((2-(трифторметил)хинолин-6-ил)амино)пиперидин-1-карбоксилат
[1308] Указанное в заголовке соединение (462,5 мг, 93,7%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 6-бром- 2-(трифторметил)хинолин (344,6 мг, 1,25 ммоль). МС (ИЭР) m/z - 396,2 (М+Н)+
[1309] Стадия 2: N-(пиперидин-4-ил)-2-(трифторметил)хинолин-6-амина гидрохлорид
[1310] Указанное в заголовке соединение (430,8 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1311] Эталонный пример 221. 4-метокси-N-(пиперидин-4-ил)хинолин-6-амина гидрохлорид
[1312] Стадия 1: трет-бутил 4-((4-метоксихинолин-6-ил)амино)пиперидин-1-карбоксилат
[1313] Указанное в заголовке соединение (110,2 мг, 24,7%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 6-бром-4-метокси-хинолин (297,2 мг, 1,25 ммоль). МС (ИЭР) m/z - 358,2 (М+Н)+
[1314] Стадия 2: 4-метокси-N-(пиперидин-4-ил)хинолин-6-амина гидрохлорид
[1315] Указанное в заголовке соединение (101,7 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1316] Эталонный пример 222. 2-бром-N-(пиперидин-4-ил)пиридин-4-амина гидрохлорид
[1317] Стадия 1: трет-бутил 4-[(2-бром-4-пиридил)амино]пиперидин-1-карбоксилат
[1318] Указанное в заголовке соединение (257,0 мг, 57,5%) получали таким же образом, как на стадии 1 эталонного примера 212, за исключением того, что вместо бензо[d]тиазол-7-амин использовали 4-амино-2-бромпиридин (217,1 мг, 1,26 ммоль). МС (ИЭР) m/z - 358,1 (М+Н)+
[1319] Стадия 2: 2-бром-N-(пиперидин-4-ил)пиридин-4-амина гидрохлорид
[1320] Указанное в заголовке соединение (237,3 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 212, и использовали на следующей стадии без дополнительной очистки.
[1321] Эталонный пример 223. N-(пиперидин-4-ил)-1H-бензо[d]имидазол-7-амина гидрохлорид
[1322] Стадия 1: трет-бутил 4-((1Н-бензо[d]имидазол-7-ил)амино)пиперидин-1-карбоксилат
[1323] Указанное в заголовке соединение (319,6 мг, 80,5%) получали таким же образом, как и на стадии 1 эталонного примера 212, за исключением того, что вместо бензо[d]тиазол-7-амина использовали 3Н-бензо[d]имидазол-4-амин (167,1 мг, 1,26 ммоль). МС (ИЭР) m/z - 317,2 (М+Н)+
[1324] Стадия 2: N-(пиперидин-4-ил)-1Н-бензо[d]имидазол-7-амина гидрохлорид
[1325] Указанное в заголовке соединение (292,1 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 212, и использовали на следующей стадии без дополнительной очистки.
[1326] Эталонный пример 224. 2-хлор-6-морфолино-N-(пиперидин-4-ил)пиридин-4-амина гидрохлорид
[1327] Стадия 1: трет-бутил 4-((2-хлор-6-морфолинопиридин-4-ил)амино)пиперидин-1-карбоксилат
[1328] Указанное в заголовке соединение (463,1 мг, 93,0%) получали таким же образом, как на стадии 1 эталонного примера 212, за исключением того, что вместо бензо[d]тиазол-7-амина использовали 4-амино-2-хлор-6-морфолинопиридин (268,1 мг, 1,26 ммоль). МС (ИЭР) m/z - 397,2 (М+Н)+
[1329] Стадия 2: 2-хлор-6-морфолино-N-(пиперидин-4-ил) пиридин-4-амина гидрохлорид
[1330] Указанное в заголовке соединение (431,5 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 212, и использовали на следующей стадии без дополнительной очистки.
[1331] Эталонный пример 225. N-(пиперидин-4-ил)-3-(трифторметил)хинолин-5-амина гидрохлорид
[1332] Стадия 1: трет-бутил 4-((3-(трифторметил)хинолин-5-ил)амино)пиперидин-1-карбоксилат
[1333] Указанное в заголовке соединение (853,9 мг, 86,5%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали 5-бром- 3-(трифторметил)хинолин (689,2 мг, 2,50 ммоль). МС (ИЭР) m/z - 396,1 (М+Н)+
[1334] Стадия 2: N-(пиперидин-4-ил)-3-(трифторметил)хинолин-5-амина гидрохлорид
[1335] Указанное в заголовке соединение (795,0 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки.
[1336] Эталонный пример 226. N-фенил-5-(пиперидин-4-иламино)хинолин-3-карбоксамида гидрохлорид
[1337] Стадия 1: 5-бром-N-фенилхинолин-3-карбоксамид
[1338] 5-Бромхинолин-3-карбоновую кислоту (300 мг, 1,19 ммоль) растворяли в диметилформамиде. К полученному раствору добавляли анилин (133,0 мг, 1,42 ммоль), HATU (O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилуран гексафторфосфат) (633,6 мг, 1,67 ммоль) и диизопропилэтиламин (769,16 мг, 5,95 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции к реакционной смеси добавляли воду. Водный слой реакционной смеси экстрагировали дихлорметаном. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (этилацетат / н-гексан = 1/1, об./об.) с получением указанного в заголовке соединения (144,0 мг, 36,9%). 1H-ЯМР (CDCl3, 400 МГц) δ 9,40 (дд, 1Н), 8,97 (д, 1Н), 8,16 (д, 1Н), 7,99 (с, 1Н), 7,94 (д, 1Н), 7,73-7,68 (м, 3H)m 7,44 (т, 2Н), 7,23 (т, 1Н).
[1339] Стадия 2: трет-бутил-4-(3-(фенилкарбамоил)хинолин-5-ил)амино)пиперидин-1-карбоксилат
[1340] 5-Бром-N-фенилхинолин-3-карбоксамид (144,0 мг, 0,44 ммоль), полученный на стадии 1, растворяли в безводном толуоле. К полученному раствору добавляли трет-бутил-4-аминопиперидин-1-карбоксилат (88,2 мг, 0,44 ммоль), карбонат цезия (103,1 мг, 0,53 ммоль), трис(дибензилиденацетон)дипалладий(0) (36,6 мг, 0,04 ммоль) и(+/-)-2,2'-бис(дифенилфоспино)-1,1'-бинафталин (32,9 мг, 0,05 ммоль). Реакционную смесь нагревали в колбе с обратным холодильником и перемешивали при 100°С в течение ночи. После завершения реакции реакционную смесь охлаждали до комнатной температуры и затем добавляли воду для экстракции водного слоя этилацетатом.
Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (этилацетат / н-гексан = 1/1, об./об.) с получением указанного в заголовке соединения (81,4 мг, 41,4%). МС (ИЭР) m/z - 447,2 (М+Н)+
[1341] Стадия 3: N-фенил-5-(пиперидин-4-иламино)хинолин-3-карбоксамида гидрохлорид
[1342] трет-бутил 4-((3-(фенилкарбамоил)хинолин-5-ил)амино)пиперидин-1-карбоксилат (81,4 мг, 0,18 ммоль), полученный на стадии 2, растворяли в дихлорметане (8,4 мл), а затем туда же добавляли (по каплям) в избытке 4,0 М соляную кислоту, растворенную в 1,4-диоксане. Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции, полученное твердое соединение фильтровали, промывали и высушивали вакуумом с получением указанного в заголовке соединения (5,4 мг, 7,2%).
[1343] Эталонный пример 227. N-бензил-N-метил-5-(пиперидин-4-иламино) хинолин-3-карбоксамида гидрохлорид
[1344] Стадия 1: N-бензил-5-бром-N-метилхинолин-3-карбоксамид
[1345] Указанное в заголовке соединение (172,2 мг, 40,7%) получали таким же образом, как и на стадии 1 эталонного примера 226, за исключением того, что вместо анилина использовали N-метил-1-фенилметанамин (173,0 мг, 1,42 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 9,04 (с, 1Н), 8,64 (с, 1Н), 8,11 (с, 1Н), 7,89,7,86 (м, 1Н), 7,64-7,62 (м, 1Н), 7,43-7,35 (м, 4Н), 7,24-7,23 (м, 1Н), 4,73 (д, 2Н), 3,08 (д, 3Н).
[1346] Стадия 2: трет-бутил-4-(3-(бензил (метил) карбамоил)хинолин-5-ил)амино)пиперидин-1-карбоксилат
[1347] Указанное в заголовке соединение (120,8 мг, 52,4%) получали таким же образом, как и на стадии 2 эталонного примера 226. МС (ИЭР) m/z - 475,3 (М+Н)+
[1348] Стадия 3: N-бензил-N-метил-5-(пиперидин-4-иламино)хинолин-3-карбоксамида гидрохлорид
[1349] Указанное в заголовке соединение (105,3 мг, 92,4%) получали таким же образом, как и на стадии 3 эталонного примера 226, и использовали на следующей стадии без дополнительной очистки.
[1350] Эталонный пример 228. N-метил-5-(пиперидин-4-иламино)хинолин-8-карбоксамида гидрохлорид
[1351] Стадия 1: трет-бутил 4-((8-(метилкарбамоил)хинолин-5-ил)амино)пиперидин-1-карбоксилат
[1352] Указанное в заголовке соединение (116,9 мг, 42,0%) получали таким же образом, как и на стадии 2 примера 140, за исключением того, что вместо трет-бутил (S)-3-аминопирролидин-1-карбоксилата использовали трет-бутил-4-аминопиперидин-1-карбоксилат (144,2 мг, 0,72 ммоль). МС (ИЭР) m/z - 385,2 (М+Н)+
[1353] Стадия 2: N-метил-5-(пиперидин-4-иламино)хинолин-8-карбоксамида гидрохлорид
[1354] Указанное в заголовке соединение (71,3 мг, 85,6%) получали таким же образом, как и на стадии 3 эталонного примера 140, и использовали на следующей стадии без дополнительной очистки.
[1355] Эталонный пример 229. N,N-диметил-5-(пиперидин-4-иламино)хинолин-8-карбоксамида гидрохлорид
[1356] Стадия 1: трет-бутил 4-((8-(диметилкарбамоил)хинолин-5-ил)амино)пиперидин-1-карбоксилат
[1357] Указанное в заголовке соединение (84,9 мг, 32,9%) получали таким же образом, как на стадии 2 примера 141, за исключением того, что вместо трет-бутил (S)-3-аминопирролидин-1-карбоксилата использовали трет-бутил-4-аминопиперидин-1-карбоксилат (128,0 мг, 0,64 ммоль). МС (ИЭР) m/z - 399,2 (М+Н)+
[1358] Стадия 2: N,N-диметил-5-(пиперидин-4-иламино)хинолин-8-карбоксамида гидрохлорид
[1359] Указанное в заголовке соединение (60,1 мг, 23,4%) получали таким же образом, как и на стадии 3 эталонного примера 141, и использовали на следующей стадии без дополнительной очистки
[1360] Эталонный пример 230. N-метил-N-фенил-5-(пиперидин-4-иламино)хинолин-8-карбоксамида гидрохлорид
[1361] Стадия 1: трет-бутил 4-((8-(метил (фенил)карбамоил)хинолин-5-ил)амино)пиперидин-1-карбоксилат
[1362] Указанное в заголовке соединение (196,6 мг, 39,9%) получали таким же образом, как на стадии 2 примера 143, за исключением того, что вместо трет-бутил (5)-3-аминопирролидин-1-карбоксилата использовали трет-бутил-4-аминопиперидин-1-карбоксилат (128,0 мг, 0,64 ммоль). МС (ИЭР) m/z - 461,3 (М+Н)+
[1363] Стадия 2: N-метил-N-фенил-5-(пиперидин-4-иламино)хинолин-8-карбоксамида гидрохлорид
[1364] Указанное в заголовке соединение (134,2 мг, 72,6%) получали таким же образом, как и на стадии 3 эталонного примера 143, и использовали на следующей стадии без дополнительной очистки
[1365] Эталонный пример 231. N-бензил-N-метил-5-(пиперидин-4-иламино)хинолин-8-карбоксамида гидрохлорид
[1366] Стадия 1: трет-бутил 4-((8-(бензил(метил)карбамоил)хинолин-5-ил)амино)пиперидин-1-карбоксилат
[1367] Указанное в заголовке соединение (218,1 мг, 32,4%) получали таким же образом, как и на стадии 2 примера 144, за исключением того, что вместо трет-бутил (5)-3-аминопирролидин-1-карбоксилата использовали трет-бутил-4-аминопиперидин-1-карбоксилат (215,0 мг, 1,07 ммоль). МС (ИЭР) m/z - 475,3 (М+Н)+
[1368] Стадия 2: N-метил-N-фенил-5-(пиперидин-4-иламино)хинолин-8-карбоксамида гидрохлорид
[1369] Указанное в заголовке соединение (179,2 мг, 87,1%) получали таким же образом, как и на стадии 3 эталонного примера 144, и использовали на следующей стадии без дополнительной очистки
[1370] Эталонный пример 232. N-фенил-5-(пиперидин-4-иламино)хинолин-8-карбоксамида гидрохлорид
[1371] Стадия 1: трет-бутил 4-((8-(фенилкарбамоил)хинолин-5-ил)амино)пиперидин-1-карбоксилат
[1372] Указанное в заголовке соединение (196,9 мг, 41,6%) получали таким же образом, как на стадии 2 примера 142, за исключением того, что вместо трет-бутил (S)-3-аминопирролидин-1-карбоксилата использовали трет-бутил-4-аминопиперидин-1-карбоксилат (213,0 мг, 1,06 ммоль). МС (ИЭР) m/z - 447,2 (М+Н)+
[1373] Стадия 2: N-фенил-5-(пиперидин-4-иламино)хинолин-8-карбоксамида гидрохлорид
[1374] Указанное в заголовке соединение (100,8 мг, 54,4%) получали таким же образом, как и на стадии 3 эталонного примера 142, и использовали на следующей стадии без дополнительной очистки
[1375] Эталонный пример 233. 5-(пиперидин-4-иламино)-К-(пиридин-2-ил)хинолин-8-карбоксамида гидрохлорид
[1376] Стадия 1: трет-бутил 4-((8-(пиридин-2-илкарбамоил)хинолин-5-ил)амино)пиперидин-1-карбоксилат
[1377] Указанное в заголовке соединение (100,6 мг, 45,0%) получали таким же образом, как на стадии 2 примера 147, за исключением того, что вместо трет-бутил (S)-3-аминопирролидин-1-карбоксилата использовали трет-бутил-4-аминопиперидин-1-карбоксилат (100,0 мг, 0,50 ммоль). МС (ИЭР) m/z - 448,2 (М+Н)+
[1378] Стадия 2: 5-(пиперидин-4-иламино)-N-(пиридин-2-ил)хинолин-8-карбоксамида гидрохлорид
[1379] Указанное в заголовке соединение (63,5 мг, 67,6%) получали таким же образом, как и на стадии 3 эталонного примера 147, и использовали на следующей стадии без дополнительной очистки. 1H-ЯМР (MeOD4, 400 МГц) δ 9,40 (с, 1Н), 9,18 (дд, 1Н), 8,84 (д, 1Н), 8,53-8,49 (м, 2Н), 8,02 (д, 1Н), 7,89 (дд, 1Н), 7,67 (т, 1Н), 7,17 (д, 1Н), 4,22-4,17 (м, 1Н), 3,58 (д, 2Н), 3,30-3,26 (м, 2Н), 2,39 (д, 2Н), 2,12-2,02 (м, 2Н).
[1380] Эталонный пример 234. 5-(пиперидин-4-иламино)-N-(пиридин-3-ил)хинолин-8-карбоксамида гидрохлорид
[1381] Стадия 1: трет-бутил 4-((8-(пиридин-3-илкарбамоил)хинолин-5-ил)амино)пиперидин-1-карбоксилат
[1382] Указанное в заголовке соединение (210,3 мг, 94,1%) получали таким же образом, как и на стадии 2 примера 145, за исключением того, что вместо трет-бутил (S)-3-аминопирролидин-1-карбоксилата использовали трет-бутил-4-аминопиперидин-1-карбоксилат (100,0 мг, 0,50 ммоль). МС (ИЭР) m/z - 448,2 (М+Н)+
[1383] Стадия 2: 5-(пиперидин-4-иламино)-N-(пиридин-3-ил)хинолин-8-карбоксамида гидрохлорид
[1384] Указанное в заголовке соединение (195,3 мг, 98,9%) получали таким же образом, как и на стадии 3 эталонного примера 145, и использовали на следующей стадии без дополнительной очистки. 1H-ЯМР (MeOD4, 400 МГц) δ 9,66 (д, 1Н), 9,16 (дд, 1Н), 8,88 (д, 1Н), 8,80 (д, 1Н), 8,73-8,71 (м, 1Н), 8,63 (д, 1Н), 8,14-8,11 (м, 1Н), 7,94-7,88 (м, 1Н), 7,17 (д, 1Н), 4,22-4,17 (м, 1Н), 3,58 (д, 2Н), 3,27 (д, 2Н), 2,40 (д, 2Н), 2,03 (д, 2Н).
[1385] Эталонный пример 235. 5-(пиперидин-4-иламино)-N-(пиридин-4-ил)хинолин-8-карбоксамида гидрохлорид
[1386] Стадия 1: трет-бутил 4-((8-(пиридин-4-илкарбамоил)хинолин-5-ил)амино)пиперидин-1-карбоксилат
[1387] Указанное в заголовке соединение (130,1 мг, 58,2%) получали таким же образом, как на стадии 2 примера 146, за исключением того, что вместо трет-бутил (5)-3-аминопирролидин-1-карбоксилата использовали трет-бутил-4-аминопиперидин-1-карбоксилат (100,0 мг, 0,50 ммоль). МС (ИЭР) m/z - 448,2 (М+Н)+
[1388] Стадия 2: 5-(пиперидин-4-иламино)-N-(пиридин-4-ил)хинолин-8-карбоксамида гидрохлорид
[1389] Указанное в заголовке соединение (68,6 мг, 56,0%) получали таким же образом, как и на стадии 3 эталонного примера 146, и использовали на следующей стадии без дополнительной очистки. 1H-ЯМР (MeOD4, 400 МГц) δ 9,34-9,24 (м, 1Н), 9,15 (д, 1Н), 8,79 (д, 1Н), 8,67 (д, 2Н), 8,47 (д, 2Н), 7,84 (с, 1Н), 7,12 (д, 1Н), 4,18-4,12 (м, 1Н), 3,57 (д, 2Н), 3,26 (д, 2Н), 2,40 (д, 2Н), 2,07-1,96 (м, 2Н).
[1390] Эталонный пример 236. 5-(пиперидин-4-иламино)-N-(пиримидин-2-ил)хинолин-8-карбоксамида гидрохлорид
[1391] Стадия 1: 5-Бром-N-(пиримидин-2-ил)хинолин-8-карбоксамид
[1392] Указанное в заголовке соединение (140,1 мг, 21,4%) получали таким же образом, как и на стадии 1 эталонного примера 140, за исключением того, что вместо метанамина использовали пиримидин-2-амин (188,6 мг, 1,98 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 9,16 (дд, 1Н), 8,87 (д, 1Н), 8,79 (дд, 1Н), 8,76 (д, 2Н), 8,07 (д, 1Н), 7,69 (дд, 1Н), 7,08 (т, 1Н).
[1393] Стадия 2: трет-бутил-4-(8-(пиримидин-2-илкарбамоил)хинолин-5-ил)амино)пиперидин-1-карбоксилат
[1394] Указанное в заголовке соединение (144,4 мг, 75,8%) получали таким же образом, как и на стадии 1 эталонного примера 233, за исключением того, что вместо 5-бром-N-(пиридин-2-ил)хинолин-8-карбоксамида (140,3 мг, 0,43 ммоль), полученного на стадии 1, использовали 5-бром-N-(пиримидин-2-ил)хинолин-8-карбоксамид. МС (ИЭР) m/z - 449,2 (М+Н)+
[1395] Стадия 3: (S)-N-(пиридин-4-ил)-5-(пирролидин-3-иламино)хинолин-8-карбоксамида гидрохлорид
[1396] Указанное в заголовке соединение (63,6 мг, 46,9%) получали таким же образом, как и на стадии 2 эталонного примера 233, и использовали на следующей стадии без дополнительной очистки. 1H-ЯМР (MeOD4, 400 МГц) δ 9,32 (д, 1Н), 9,13 (д, 1Н), 9,01 (д, 2Н), 8,78 (д, 1Н), 7,85 (дд, 1Н), 7,61 (т, 1Н), 7,14 (д, 1Н), 4,20-4,14 (м, 1Н), 3,58 (д, 2Н), 3,27 (д, 2Н), 2,40 (д, 2Н), 2,10-2,00 (м, 2Н).
[1397] Эталонный пример 237. N-(изоксазол-3-ил)-5-(пиперидин-4-иламино)хинолин-8-карбоксамида гидрохлорид
[1398] Стадия 1: 5-Бром-N-(изоксазол-3-ил)хинолин-8-карбоксамид
[1399] Указанное в заголовке соединение (158,8 мг, 41,9%) получали таким же образом, как и на стадии 1 эталонного примера 140, за исключением того, что вместо метанамина использовали изоксазол-3-амин (118,0 мг, 1,42 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 9,09 (дд, 1Н), 8,78 (дд, 2Н), 8,38 (дд, 1Н), 8,05 (дд, 1Н), 7,69 (дд, 1Н), 7,29 (д, 1Н).
[1400] Стадия 2: трет-бутил-4-(8-(изоксазол-3-илкарбамоил)хинолин-5-ил)амино)пиперидин-1-карбоксилат
[1401] Указанное в заголовке соединение (84,9 мг, 38,8%) получали таким же образом, как на стадии 1 эталонного примера 233, за исключением того, что вместо 5-бром-N-(пиридин-2-ил)хинолин-8-карбоксамида использовали 5-бром-N-(изоксазол-3-ил)хинолин-8-карбоксамида (158,8 мг, 0,5 ммоль). МС (ИЭР) m/z - 438,2 (М+Н)+
[1402] Стадия 3: N-(изоксазол-3-ил)-5-(пиперидин-4-иламино)хинолин-8-карбоксамид гидрохлорид
[1403] Указанное в заголовке соединение (21,6 мг, 27,3%) получали таким же образом, как и на стадии 2 эталонного примера 233, и использовали на следующей стадии без дополнительной очистки.
[1404] Эталонный пример 238. N-(5-(пиперидин-4-иламино) хинолин-8-ил) ацетамид гидрохлорид
[1405] Стадия 1: трет-бутил 4-((8-ацетамидохинолин-5-ил)амино)пиперидин-1-карбоксилат
[1406] Указанное в заголовке соединение (264,2 мг, 27,5%) получали таким же образом, как и на стадии 1 эталонного примера 28, за исключением того, что вместо 4-бромхинолина использовали N-(5-бромхинолин-8-ил) ацетамид (661,8 мг, 2,49 ммоль). МС (ИЭР) m/z - 385,2 (М+Н)+
[1407] Стадия 2: N-(5-(пиперидин-4-иламино)хинолин-8-ил)ацетамид гидрохлорид
[1408] Указанное в заголовке соединение (204,2 мг, 83,1%) получали таким же образом, как и на стадии 2 эталонного примера 28, и использовали на следующей стадии без дополнительной очистки. 1H-ЯМР (MeOD4, 400 МГц) δ 9,54 (дд, 1Н), 9,00 (дд, 1Н), 7,95 (дд, 1Н), 7,79 (д, 1Н), 7,08 (д, 1Н), 4,02-3,05 (м, 1Н), 3,55 (м, 2Н), 3,25 (тд, 2Н), 2,39 (д, 2Н), 2,30 (с, 3Н), 2,00-1,89 (м, 2Н).
[1409] Эталонный пример 239. 6-метил-4-(пиперидин-4-илокси)хинолина гидрохлорид
[1410] Стадия 1: трет-бутил 4-((6-метилхинолин-4-ил)окси)пиперидин-1-карбоксилат
[1411] Указанное в заголовке соединение (425,3 мг, 100,0%) получали таким же образом, как и на стадии 1 эталонного примера 31, за исключением того, что вместо 3-хинолинола использовали 4-гидрокси-6-метилхинолин (197,7 мг, 1,24 ммоль). МС (ИЭР) m/z - 343,2 (М+Н)+
[1412] Стадия 2: 6-метил-4-(пиперидин-4-илокси)хинолина гидрохлорид
[1413] Указанное в заголовке соединение (346,3 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 31, и использовали на следующей стадии без дополнительной очистки.
[1414] Эталонный пример 240. 4-(пиперидин-4-илокси)-6-(трифторметил)хинолина гидрохлорид
[1415] Стадия 1: трет-бутил 4-((6-(трифторметил)хинолин-4-ил)окси)пиперидин-1-карбоксилат
[1416] Указанное в заголовке соединение (492,3 мг, 100,0%) получали таким же образом, как и на стадии 1 эталонного примера 31, за исключением того, что вместо 3-хинолинола использовали 6-(трифторметил)хинолин-4-ол (264,8 мг, 1,24 ммоль). МС (ИЭР) m/z -397,1 (М+Н)+
[1417] Стадия 2: 4-(пиперидин-4-илокси)-6-(трифторметил)хинолина гидрохлорид
[1418] Указанное в заголовке соединение (413,3 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 31, и использовали на следующей стадии без дополнительной очистки.
[1419] Эталонный пример 241. 4-(пиперидин-4-илокси)-2-(трифторметил)хинолина гидрохлорид
[1420] Стадия 1: трет-бутил 4-((2-(трифторметил)хинолин-4-ил)окси)пиперидин-1-карбоксилат
[1421] Указанное в заголовке соединение (347,0 мг, 70,5%) получали таким же образом, как и на стадии 1 эталонного примера 31, за исключением того, что вместо 3-хинолинола использовали 4-гидрокси-2-трифторметилхинолин (264,8 мг, 1,24 ммоль). МС (ИЭР) m/z - 397,1 (М+Н)+
[1422] Стадия 2: 4-(пиперидин-4-илокси)-2-(трифторметил)хинолина гидрохлорид
[1423] Указанное в заголовке соединение (291,3 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 31, и использовали на следующей стадии без дополнительной очистки.
[1424] Эталонный пример 242. 6-фтор-4-(пиперидин-4-илокси)-2-(трифторметил)хинолина гидрохлорид
[1425] Стадия 1: трет-бутил 4-((6-фтор-2-(трифторметил)хинолин-4-ил)окси)пиперидин-1-карбоксилат
[1426] Указанное в заголовке соединение (302,0 мг, 58,7%) получали таким же образом, как на стадии 1 эталонного примера 31, за исключением того, что вместо 3-хинолинола использовали 6-фтор-2-(трифторметил)хинолин-4-ол (287,1 мг, 1,24 ммоль). МС (ИЭР) m/z - 415,2 (М+Н)+
[1427] Стадия 2: 6-фтор-4-(пиперидин-4-илокси)-2-(трифторметил)хинолина гидрохлорид
[1428] Указанное в заголовке соединение (255,6 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 31, и использовали на следующей стадии без дополнительной очистки.
[1429] Эталонный пример 243. 6-метокси-4-(пиперидин-4-илокси)-2-(трифторметил)хинолина гидрохлорид
[1430] Стадия 1: трет-бутил 4-((6-метокси-2-(трифторметил)хинолин-4-ил)окси)пиперидин-1-карбоксилат
[1431] Указанное в заголовке соединение (357,1 мг, 67,4%) получали таким же образом, как и на стадии 1 эталонного примера 31, за исключением того, что вместо 3-хинолинола использовали 6-метокси-2-(трифторметил)хинолин-4-ол (302,1 мг, 1,24 ммоль). МС (ИЭР) m/z - 427,2 (М+Н)+
[1432] Стадия 2: 6-метокси-4-(пиперидин-4-илокси)-2-(трифторметил)хинолина гидрохлорид
[1433] Указанное в заголовке соединение (303,8 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 31, и использовали на следующей стадии без дополнительной очистки.
[1434] Эталонный пример 244. 8-метокси-4-(пиперидин-4-илокси)-2-(трифторметил)хинолина гидрохлорид
[1435] Стадия 1: трет-бутил 4-((8-метокси-2-(трифторметил)хинолин-4-ил)окси)пиперидин-1-карбоксилат
[1436] Указанное в заголовке соединение (487,7 мг, 92,1%) получали таким же образом, как на стадии 1 эталонного примера 31, за исключением того, что вместо 3-хинолинола использовали 8-метокси- 2-(трифторметил)хинолин-4-ол (302,1 мг, 1,24 ммоль). МС (ИЭР) m/z - 427,2 (М+Н)+
[1437] Стадия 2: 8-метокси-4-(пиперидин-4-илокси)-2-(трифторметил)хинолина гидрохлорид
[1438] Указанное в заголовке соединение (414,9 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 31, и использовали на следующей стадии без дополнительной очистки.
[1439] Эталонный пример 245. 3-фтор-5-(пиперидин-4-илокси)хинолина гидрохлорид
[1440] Стадия 1: трет-бутил 4-((3-фторхинолин-5-ил)окси)пиперидин-1-карбоксилат
[1441] Указанное в заголовке соединение (430,2 мг, 100,0%) получали таким же образом, как и на стадии 1 эталонного примера 31, за исключением того, что вместо 3-хинолинола использовали 3-фторхинолин-5-ол (202,7 мг, 1,24 ммоль). МС (ИЭР) m/z - 347,2 (М+Н)+
[1442] Стадия 2: 3-фтор-5-(пиперидин-4-илокси)хинолина гидрохлорид
[1443] Указанное в заголовке соединение (442,2 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 31, и использовали на следующей стадии без дополнительной очистки.
[1444] Эталонный пример 246. 5-(пиперидин-4-илокси)хинолин-2-карбонитрил гидрохлорид
[1445] Стадия 1: трет-бутил 4-((2-цианохинолин-5-ил)окси)пиперидин-1-карбоксилат
[1446] Указанное в заголовке соединение (438,9 мг, 100,0%) получали таким же образом, как и на стадии 1 эталонного примера 31, за исключением того, что вместо 3-хинолинола использовали 5-гидроксихинолин-2-карбонитрил (211,4 мг, 1,24 ммоль). МС (ИЭР) m/z - 354,2 (М+Н)+
[1447] Стадия 2: 5-(пиперидин-4-илокси)хинолин-2-карбонитрил гидрохлорид
[1448] Указанное в заголовке соединение (381,6 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 31, и использовали на следующей стадии без дополнительной очистки.
[1449] Эталонный пример 247. 8-хлор-5-(пиперидин-4-илокси)хинолина гидрохлорид
[1450] Стадия 1: трет-бутил 4-((8-хлорхинолин-5-ил)окси)пиперидин-1-карбоксилат
[1451] Указанное в заголовке соединение (450,7 мг, 100,0%) получали таким же образом, как и на стадии 1 эталонного примера 31, за исключением того, что вместо 3-хинолинола использовали 8-хлорхинолин-5-ол (223,1 мг, 1,24 ммоль). МС (ИЭР) m/z - 363,2 (М+Н)+
[1452] Стадия 2: 8-хлор-5-(пиперидин-4-илокси)хинолина гидрохлорид
[1453] Указанное в заголовке соединение (660,6 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 31, и использовали на следующей стадии без дополнительной очистки.
[1454] Эталонный пример 248. 1-(пиперидин-4-илокси) изохинолина гидрохлорид
[1455] Стадия 1: трет-бутил 4-(изохинолин-1-илокси)пиперидин-1-карбоксилат
[1456] Указанное в заголовке соединение (155,8 мг, 38,2%) получали таким же образом, как и на стадии 1 эталонного примера 31, за исключением того, что вместо 3-хинолинола использовали 1-гидроксиизохинолин (180,3 мг, 1,24 ммоль). МС (ИЭР) m/z - 329,2 (М+Н)+
[1457] Стадия 2: 1-(пиперидин-4-илокси) изохинолина гидрохлорид
[1458] Указанное в заголовке соединение (125,6 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 31, и использовали на следующей стадии без дополнительной очистки.
[1459] Эталонный пример 249. 4-(пиперидин-4-илокси) изохинолина гидрохлорид
[1460] Стадия 1: трет-бутил 4-(изохинолин-4-илокси)пиперидин-1-карбоксилат
[1461] Указанное в заголовке соединение (407,9 мг, 100,0%) получали таким же образом, как и на стадии 1 эталонного примера 31, за исключением того, что вместо 3-хинолинола использовали 4-гидроксиизохинолин (180,3 мг, 1,24 ммоль). МС (ИЭР) m/z - 329,1 (М+Н)+
[1462] Стадия 2: 4-(пиперидин-4-илокси) изохинолина гидрохлорид
[1463] Указанное в заголовке соединение (328,8 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 31, и использовали на следующей стадии без дополнительной очистки.
[1464] Эталонный пример 250. 5-(пиперидин-4-илокси) изохинолина гидрохлорид
[1465] Стадия 1: трет-бутил 4-(изохинолин-5-илокси)пиперидин-1-карбоксилат
[1466] Указанное в заголовке соединение (194,1 мг, 47,6%) получали таким же образом, как и на стадии 1 эталонного примера 31, за исключением того, что вместо 3-хинолинола использовали 5-гидроксиизохинолин (180,3 мг, 1,24 ммоль). МС (ИЭР) m/z - 329,1 (М+Н)+
[1467] Стадия 2: 5-(пиперидин-4-илокси) изохинолина гидрохлорид
[1468] Указанное в заголовке соединение (156,5 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 31, и использовали на следующей стадии без дополнительной очистки.
[1469] Эталонный пример 251. 6-(пиперидин-4-илокси) изохинолина гидрохлорид
[1470] Стадия 1: трет-бутил 4-(изохинолин-6-илокси)пиперидин-1-карбоксилат
[1471] Указанное в заголовке соединение (407,9 мг, 100,0%) получали таким же образом, как и на стадии 1 эталонного примера 31, за исключением того, что вместо 3-хинолинола использовали 6-гидроксиизохинолин (180,3 мг, 1,24 ммоль). МС (ИЭР) m/z - 329,2 (М+Н)+
[1472] Стадия 2: 6-(пиперидин-4-илокси) изохинолина гидрохлорид
[1473] Указанное в заголовке соединение (328,9 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 31, и использовали на следующей стадии без дополнительной очистки.
[1474] Эталонный пример 252. 7-(пиперидин-4-илокси) изохинолина гидрохлорид
[1475] Стадия 1: трет-бутил 4-(изохинолин-7-илокси)пиперидин-1-карбоксилат
[1476] Указанное в заголовке соединение (407,9 мг, 100,0%) получали таким же образом, как и на стадии 1 эталонного примера 31, за исключением того, что вместо 3-хинолинола использовали 7-гидроксиизохинолин (180,3 мг, 1,24 ммоль). МС (ИЭР) m/z - 329,2 (М+Н)+
[1477] Стадия 2: 7-(пиперидин-4-илокси) изохинолина гидрохлорид
[1478] Указанное в заголовке соединение (328,9 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 31, и использовали на следующей стадии без дополнительной очистки.
[1479] Эталонный пример 253. 6-метокси-2-метил-4-(пиперидин-4-илокси)хинолина гидрохлорид
[1480] Стадия 1: трет-бутил 4-((6-метокси-2-метилхинолин-4-ил)окси)пиперидин-1-карбоксилат
[1481] Указанное в заголовке соединение (462,6 мг, 100,0%) получали таким же образом, как и на стадии 1 эталонного примера 31, за исключением того, что вместо 3-хинолинола использовали 6-метокси-2-метилхинолин-4-ол (235,0 мг, 1,24 ммоль). МС (ИЭР) m/z - 373,2 (М+Н)+
[1482] Стадия 2: 6-метокси-2-метил-4-(пиперидин-4-илокси)хинолина гидрохлорид
[1483] Указанное в заголовке соединение (383,6 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 31, и использовали на следующей стадии без дополнительной очистки.
[1484] Эталонный пример 254. 7-хлор-4-(пиперидин-4-илокси)хинолина гидрохлорид
[1485] Стадия 1: трет-бутил 4-((7-хлорхинолин-4-ил)окси)пиперидин-1-карбоксилат
[1486] Указанное в заголовке соединение (450,7 мг, 99,9%) получали таким же образом, как и на стадии 1 эталонного примера 31, за исключением того, что вместо 3-хинолинола использовали 7-хлорхинолин-4-ол (223,1 мг, 1,24 ммоль). МС (ИЭР) m/z - 363,2 (М+Н)+
[1487] Стадия 2: 7-хлор-4-(пиперидин-4-илокси)хинолина гидрохлорид
[1488] Указанное в заголовке соединение (371,6 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 31, и использовали на следующей стадии без дополнительной очистки.
[1489] Эталонный пример 255. 7-метил-4-(пиперидин-4-илокси)хинолина гидрохлорид
[1490] Стадия 1: трет-бутил 4-((7-метилхинолин-4-ил)окси)пиперидин-1-карбоксилат
[1491] Указанное в заголовке соединение (500,0 мг, 98,0%) получали таким же образом, как и на стадии 1 эталонного примера 31, за исключением того, что вместо 3-хинолинола использовали 7-метилхинолин-4-ол (237,3 мг, 1,49 ммоль). МС (ИЭР) m/z - 343,3 (М+Н)+
[1492] Стадия 2: 7-метил-4-(пиперидин-4-илокси)хинолина гидрохлорид
[1493] Указанное в заголовке соединение (407,0 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 31, и использовали на следующей стадии без дополнительной очистки.
[1494] Эталонный пример 256. 7-фтор-4-(пиперидин-4-илокси)хинолина гидрохлорид
[1495] Стадия 1: трет-бутил 4-((7-фторхинолин-4-ил)окси)пиперидин-1-карбоксилат
[1496] Указанное в заголовке соединение (516,0 мг, 99,9%) получали таким же образом, как и на стадии 1 эталонного примера 31, за исключением того, что вместо 3-хинолинола использовали 7-фторхинолин-4-ол (243,2 мг, 1,49 ммоль). МС (ИЭР) m/z - 347,2 (М+Н)+
[1497] Стадия 2: 7-фтор-4-(пиперидин-4-илокси)хинолина гидрохлорид
[1498] Указанное в заголовке соединение (421,3 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 31, и использовали на следующей стадии без дополнительной очистки.
[1499] Эталонный пример 257. 4-(пиперидин-4-илокси)хинолин-8-карбонитрил гидрохлорид
[1500] Стадия 1: трет-бутил 4-((8-цианохинолин-4-ил)окси)пиперидин-1-карбоксилат
[1501] Указанное в заголовке соединение (505,4 мг, 95,9%) получали таким же образом, как и на стадии 1 эталонного примера 31, за исключением того, что вместо 3-хинолинола использовали 4-гидроксихинолин-8-карбонитрил (253,7 мг, 1,49 ммоль). МС (ИЭР) m/z - 354,2 (М+Н)+
[1502] Стадия 2: 4-(пиперидин-4-илокси)хинолин-8-карбонитрил гидрохлорид
[1503] Указанное в заголовке соединение (414,4 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 31, и использовали на следующей стадии без дополнительной очистки.
[1504] Эталонный пример 258. 8-фтор-4-(пиперидин-4-илокси)хинолина гидрохлорид
[1505] Стадия 1: трет-бутил 4-((8-фторхинолин-4-ил)окси)пиперидин-1-карбоксилат
[1506] Указанное в заголовке соединение (516,0 мг, 99,9%) получали таким же образом, как и на стадии 1 эталонного примера 31, за исключением того, что вместо 3-хинолинола использовали 8-фтор-4-гидроксихинолин (243,2 мг, 1,49 ммоль). МС (ИЭР) m/z - 347,1 (М+Н)+
[1507] Стадия 2: 8-фтор-4-(пиперидин-4-илокси)хинолина гидрохлорид
[1508] Указанное в заголовке соединение (421,3 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 31, и использовали на следующей стадии без дополнительной очистки.
[1509] Эталонный пример 259. 2-метил-4-(пиперидин-4-илокси)хинолина гидрохлорид
[1510] Стадия 1: трет-бутил 4-((2-метилхинолин-4-ил)окси)пиперидин-1-карбоксилат
[1511] Указанное в заголовке соединение (510,0 мг, 99,9%) получали таким же образом, как и на стадии 1 эталонного примера 31, за исключением того, что вместо 3-хинолинола использовали 4-гидрокси-2-метилхинолин (237,3 мг, 1,49 ммоль). МС (ИЭР) m/z - 343,2 (М+Н)+
[1512] Стадия 2: 2-метил-4-(пиперидин-4-илокси)хинолина гидрохлорид
[1513] Указанное в заголовке соединение (415,4 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 31, и использовали на следующей стадии без дополнительной очистки.
[1514] Эталонный пример 260. 6-фтор-2-метил-4-(пиперидин-4-илокси)хинолина гидрохлорид
[1515] Стадия 1: трет-бутил 4-((6-фтор-2-метилхинолин-4-ил)окси)пиперидин-1-карбоксилат
[1516] Указанное в заголовке соединение (537,0 мг, 99,9%) получали таким же образом, как и на стадии 1 эталонного примера 31, за исключением того, что вместо 3-хинолинола использовали 6-фтор-2-метилхинолин-4 (264,1 мг, 1,49 ммоль). МС (ИЭР) m/z - 361,2 (М+Н)+
[1517] Стадия 2: 6-фтор-2-метил-4-(пиперидин-4-илокси)хинолина гидрохлорид
[1518] Указанное в заголовке соединение (442,2 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 31, и использовали на следующей стадии без дополнительной очистки.
[1519] Эталонный пример 261. 8-метокси-4-(пиперидин-4-илокси)хинолина гидрохлорид
[1520] Стадия 1: трет-бутил 4-((8-метоксихинолин-4-ил)окси)пиперидин-1-карбоксилат
[1521] Указанное в заголовке соединение (118,7 мг, 22,2%) получали таким же образом, как и на стадии 1 эталонного примера 31, за исключением того, что вместо 3-хинолинола использовали 4-гидрокси-8-метоксихинолин (261,1 мг, 1,49 ммоль). МС (ИЭР) m/z - 359,2 (М+Н)+
[1522] Стадия 2: 8-метокси-4-(пиперидин-4-илокси)хинолина гидрохлорид
[1523] Указанное в заголовке соединение (97,6 мг, 100,0%) получали таким же образом, как и на стадии 2 эталонного примера 31, и использовали на следующей стадии без дополнительной очистки.
[1524] Эталонный пример 262. 8-метил-4-(пиперидин-4-илокси)хинолина гидрохлорид
[1525] Стадия 1: трет-бутил 4-((8-метилхинолин-4-ил)окси)пиперидин-1-карбоксилат
[1526] Указанное в заголовке соединение (510,0 мг, 99,9%) получали таким же образом, как и на стадии 1 эталонного примера 31, за исключением того, что вместо 3-хинолинола использовали 8-метилхинолин-4-ол (237,3 мг, 1,49 ммоль). МС (ИЭР) m/z - 343,2 (М+Н)+
[1527] Стадия 2: 8-метил-4-(пиперидин-4-илокси)хинолина гидрохлорид
[1528] Указанное в заголовке соединение (415,4 мг, 100,0%) получали таким же образом, как и на стадии 2 Эталонного примера 31, и использовали на следующей стадии без дополнительной очистки.
[1529] Пример 1. (R)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)-N-(хинолин-3-ил)пирролидин-3-карбоксамид
[1530] (S)-1-(2-хлорацетил)пирролидин-2-карбонитрил (30 мг, 0,17 ммоль), полученный в эталонном примере 1, растворяли в безводном дихлорметане (1,2 мл). К полученному раствору добавляли (R)-N-(хинолин-3-ил)пирролидин-3-карбоксамида гидрохлорид (54,6 мг, 0,19 ммоль), полученный в эталонном примере 24, и карбонат калия (96,0 мг, 0,69 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции к реакционной смеси добавляли воду. Водный слой реакционной смеси экстрагировали дихлорметаном. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (этилацетат / метанол = 10/1, об./об.) с получением указанного в заголовке соединения (31,6 мг). 1H-ЯМР (CDCl3, 400 МГц) δ 10,45 (с, 1Н), 9,12 (с, 1Н), 8,75 (с, 1Н), 7,97 (д, 1Н), 7,73 (д, 1Н), 7,55-7,46 (м, 2Н), 4,78 (с, 1Н), 3,74-3,18 (м, 7Н), 2,82 (с, 1Н), 2,59-2,18 (м, 8Н)
[1531] Пример 2. (R)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)-N-(хинолин-4-ил)пирролидин-3-карбоксамид
[1532] Указанное в заголовке соединение (33,3 мг) получали таким же образом, как и в примере 1, за исключением того, что вместо (R)-N-(хинолин-3-ил)пирролидин-3-карбоксамида гидрохлорида использовали (R)-N-(хинолин-4-ил)пирролидин-3-карбоксамида гидрохлорид (54,6 мг, 0,19 ммоль), полученного в эталонном примере 23. 1H-ЯМР (CDCl3, 400 МГц) δ 10,62 (с, 1Н), 8,78 (с, 1Н), 8,31-8,26 (м, 2Н), 8,05 (д, 1Н), 7,71-7,62 (м, 2Н), 4,78 (д, 1Н), 3,71-3,19 (м, 8Н), 2,82 (с, 1Н), 2,62-2,05 (м, 8Н)
[1533] Пример 3. (S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)-N-(хинолин-3-ил)пирролидин-3-карбоксамид
[1534] Указанное в заголовке соединение (6,3 мг) получали таким же образом, как и в примере 1, за исключением того, что вместо (R)-N-(хинолин-3-ил)пирролидин-3-карбоксамида гидрохлорида использовали (S)-N-(хинолин-3-ил)пирролидин-3-карбоксамида гидрохлорида (54,6 мг, 0,19 ммоль), полученного в эталонном примере 22. 1H-ЯМР (CDCl3, 400 МГц) δ 10,36 (д, 1Н), 9,11 (д, 1Н), 8,84 (д, 1Н), 8,02 (т, 1Н), 7,81 (д, 1Н), 7,60-7,47 (м, 2Н), 4,83 (д, 1Н), 3,69-3,04 (м, 7 Н), 2,56-2,05 (м, 10Н)
[1535] Пример 4. (S)-1-(2-((3)-2-цианопирролидин-1-ил)-2-оксоэтил)-N-(хинолин-4-ил)пирролидин-3-карбоксамид
[1536] Указанное в заголовке соединение (14,3 мг) получали таким же образом, как ив примере 1, за исключением того, что вместо (R)-N-(хинолин-3-ил)пирролидин-3-карбоксамида гидрохлорида использовали (S)-N-(хинолин-4-ил)пирролидин-3-карбоксамида гидрохлорида (54,6 мг, 0,19 ммоль), полученного в эталонном примере 21. 1H-ЯМР (CDCl3, 400 МГц) δ 10,42 (с, 1Н), 8,77 (д, 1Н), 8,35-8,03 (м, 3Н), 7,71-7,58 (м, 2Н), 4,79 (д, 1Н), 3,70-3,35 (м, 6Н), 3,22 (с, 1Н), 2,48-2,05 (м, 9Н)
[1537] Пример 5. (S)-1-(2-((S)-3-(хинолин-4-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1538] (S)-1-(2-хлорацетил)пирролидин-2-карбонитрил (20 мг, 0,12 ммоль), полученный в эталонном примере 1, растворяли в безводном дихлорметане (4 мл). К полученному раствору добавляли (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид (39,8 мг, 0,14 ммоль), полученный в эталонном примере 5, и карбонат калия (48,0 мг, 0,35 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции к реакционной смеси добавляли воду. Водный слой реакционной смеси экстрагировали дихлорметаном. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (дихлорметан / метанол = 10/1, об./об.) с получением указанного в заголовке соединения (11,4 мг). 1H-ЯМР (CDCl3, 400 МГц) δ 8,65-8,72 (м, 1Н), 8,00 (д, 1Н), 7,87-7,93 (м, 1Н), 7,77-7,82 (м, 1Н), 7,67-7,75 (м, 1Н), 7,58-7,62 (м, 1Н), 4,75-4,82 (м, 1Н), 4,25-4,31 (м, 1Н), 3,63-3,70 (м, 1Н), 3,44-3,52 (м, 2Н), 3,12-3,22 (м, 1Н), 3,08 (д, 1Н), 2,80 (дд, 0,3 Н), 2,64-2,71 (м, 0,5 Н), 2,26-2,36 (м, 2Н), 2,13-2,25 (м, 2Н)
[1539] Пример 6. (S)-4,4-дифтор-1-(2-((S)-3-(хинолин-3-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1540] (2S)-1-(2-хлорацетил)-4,4-дифторпирролидин-2-карбонитрил (25,0 мг 0,12 ммоль), полученный в эталонном примере 3, растворяли в безводном дихлорметане (4 мл). К полученному раствору добавляли (S)-N-(пирролидин-3-ил)хинолин-3 -амина гидрохлорид (34,3 мг 0,12 ммоль), полученный в эталонном примере 6 и карбонат калия (48,0 мг, 0,35 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции к реакционной смеси добавляли воду. Водный слой реакционной смеси экстрагировали дихлорметаном. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (дихлорметан/ метанол = 10/1, об./об.) с получением указанного в заголовке соединения (6,1 мг). 1H-ЯМР (CDCl3, 400 МГц) δ 8,42 (с, 1Н), 7,85-7,96 (м, 1Н), 7,50-7,64 (м, 1Н), 7,36-7,46 (м, 2Н), 6,96 (с, 1Н), 5,17-5,28 (м, 0,4Н), 4,89-5,01 (м, 0,6Н), 4,32-4,56 (м, 1Н), 4,05-4,19 (м, 2Н), 3,37-3,55 (м, 1Н), 3,30-3,36 (м, 1Н), 2,91-3,11 (м, 2Н), 2,68-2,86 (м, 3Н), 2,33-2,53 (м, 2Н), 1,78-1,99 (м, 2Н)
[1541] Пример 7. (S)-4,4-дифтор-1-(2-((S)-3-(хинолин-4-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1542] Указанное в заголовке соединение (5,3 мг) получали таким же образом, как и в примере 6, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид (34,3 мг 0,12 ммоль), полученный в эталонном примере 5. 1H-ЯМР (CDCl3, 400 МГц) δ 8,68 (с, 1Н), 7,90 (д, 1Н), 7,85 (д, 1Н), 7,76-7,83 (м, 1Н), 7,62-7,72 (м, 1Н), 7,54-7,62 (м, 1Н), 5,13-5,21 (м, 0,4Н), 4,91-5,02 (м, 0,6Н), 4,65-4,80 (м, 1Н), 4,26 (м, 1Н), 3,98-4,15 (м, 2Н), 3,78-3,91 (м, 0,5Н), 3,47-3,59 (м, 0,5Н), 3,34-3,43 (м, 1,5Н), 2,87-3,14 (м, 3Н), 2,59-2,81 (м, 3Н), 2,35-2,59 (м, 1,5Н)
[1543] Пример 8. (S)-4,4-дифтор-1-(2-((S)-3-(изохинолин-4-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1544] Указанное в заголовке соединение (16,3 мг) получали таким же образом, как и в примере 6, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (S)-N-(пирролидин-3-ил)изохинолин-4-амина гидрохлорид (34,3 мг, 0,12 ммоль), полученный в эталонном примере 7. 1H-ЯМР (CDCl3, 400 МГц) δ 8,51 (д, 1Н), 7,96 (д, 1Н), 7,83-7,91 (м, 1Н), 7,59-7,65 (м, 1Н), 7,42 (т, 1Н), 5,92 (д, 0,6Н), 5,69 (д, 0,4Н), 5,11 (дд, 0,4Н), 4,91 (т, 0,6Н), 4,16-4,28 (м, 1Н), 3,72-4,12 (м, 2Н), 3,59 (д, 0,5Н), 3,37 (с, 1Н), 3,31 (д, 0,5Н), 3,07-3,18 (м, 0,5Н), 2,99-3,07 (м, 1Н), 2,89-2,95 (м, 1Н), 2,55-2,76 (м, 5Н), 2,44-2,55 (м, 0,5Н), 2,30-2,41 (м, 1Н), 1,92 (м, 1Н)
[1545] Пример 9. (S)-1-(2-((S)-3-(бензо[b]тиофен-4-иламино)пирролидин-1-ил)ацетил)-4,4-дифторпирролидин-2-карбонитрил
[1546] Указанное в заголовке соединение (5,62 мг) получали таким же образом, как и в примере 6, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (S)-N-(бензо[b]тиофен-4-ил)пирролидин-3-амина гидрохлорид (26,2 мг, 0,12 ммоль), полученный в эталонном примере 8. 1H-ЯМР (CDCl3, 400 МГц) δ 7,23-7,36 (м, 3Н), 7,16-7,23 (м, 1Н), 6,35 (с, 1Н), 5,15 (д, 0,4Н), 4,88 (т, 0,6Н), 4,18 (с, 1Н), 3,94-4,05 (м, 1,6Н), 3,81-3,91 (м, 0,5Н), 3,44-3,53 (м, 0,5Н), 3,31-3,40 (м, 0,5Н), 3,25-3,31 (м, 1Н), 3,03-3,11 (м, 0,4Н), 2,86-2,99 (м, 1,6Н), 2,76-2,82 (м, 0,5Н), 2,29-2,72 (м, 5Н), 1,79-1,98 (м, 1Н)
[1547] Пример 10. (S)-1-(2-((S)-3-(бензо[b]тиофен-7-иламино)пирролидин-1-ил)ацетил)-4,4-дифторпирролид ин-2-карбонитрил
[1548] Указанное в заголовке соединение (10,9 мг) получали таким же образом, как и в примере 6, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (S)-N-(бензо[b]тиофен-7-ил)пирролидин-3-амина гидрохлорид (26,2 мг, 0,12 ммоль), полученный в эталонном примере 9. 1H-ЯМР (CDCl3, 400 МГц) δ 7,34-7,41 (м, 1Н), 7,20-7,34 (м, 4 Н), 6,47-6,57 (м, 1Н), 5,37 (д, 0,5Н), 4,89 (т, 0,7Н), 4,17-4,28 (м, 1Н), 3,75-4,08 (м, 3Н), 3,35-3,55 (м, 1Н), 3,21-3,35 (м, 1Н), 2,78-3,13 (м, 2Н), 2,55-2,73 (м, 4Н), 2,31-2,53 (м, 2Н), 1,78-1,97 (м, 1Н)
[1549] Пример 11. (S)-1-(2-((S)-3-(бензофуран-7-иламино)пирролидин-1-ил)ацетил)-4,4-дифторпирролид ин-2-карбонитрил
[1550] Указанное в заголовке соединение (6,91 мг) получали таким же образом, как и в примере 6, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали гидрохлорид (S)-N-(бензофуран-7-ил)пирролидин-3-амина (24,27 мг, 0,12 ммоль), полученный в эталонном примере 10. 1H-ЯМР (CDCl3, 400 МГц) δ 7,55 (с, 1Н), 7,08 (т, 1Н), 6,97 (д, 1Н), 6,72 (с, 1Н), 6,45-6,50 (м, 1Н), 5,44 (д, 0,3Н), 4,90 (дд, 0,6Н), 4,13-4,29 (м, 1Н), 3,75-4,08 (м, 2Н), 3,32-3,59 (м, 1Н), 3,23-3,32 (м, 1Н), 2,85-3,08 (м, 2Н), 2,55-2,78 (м, 4Н), 2,32-2,53 (м, 1Н), 1,72-1,93 (м, 1Н)
[1551] Пример 12. (S)-4,4-дифтор-1-(2-((S)-3-(фуро[3,2-с]пиридин-7-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1552] Указанное в заголовке соединение (4,59 мг) получали таким же образом, как и в примере 6, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорид (24,4 мг, 0,12 ммоль), полученный в эталонном примере 11. 1H-ЯМР (CDCl3, 400 МГц) δ 8,39 (с, 1Н), 7,87 (с, 1Н), 7,61-7,72 (м, 1Н), 6,82-6,98 (м, 1Н), 5,31-5,41 (м, 0,4Н), 4,92-5,03 (м, 0,7Н), 4,21-4,45 (м, 2Н), 3,49-3,62 (м, 1Н), 3,33-3,40 (м, 1Н), 2,94-3,12 (м, 2Н), 2,58-2,87 (м, 6 Н), 2,37-2,54 (м, 2Н), 1,77-2,00 (м, 1Н)
[1553] Пример 13. (S)-1-(2-((S)-3-([1,1'-бифенил]-2-иламино)пирролидин-1-ил)ацетил)-4,4-дифторпирролидин-2-карбонитрил
[1554] Указанное в заголовке соединение (14,9 мг) получали таким же образом, как и в примере 6, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (S)-N-([1,1'-бифенил]-2-ил)пирролидин-3-амина гидрохлорид (28,6 мг, 0,12 ммоль), полученныйв эталонном примере 12. 1H-ЯМР (CDCl3, 400 МГц) δ 7,32-7,48 (м, 5Н), 7,19-7,26 (м, 1Н), 7,09 (д, 1Н), 6,78 (уш т, 1Н), 6,64 (д, 1Н), 5,36 (уш т, 0,3Н), 4,87-4,92 (м, 0,6Н), 3,75-4,22 (м, 4Н), 3,57 (уш д, 0,5Н), 3,20-3,30 (м, 1,6Н), 2,79-2,93 (м, 1Н), 2,62-2,76 (м, 2Н), 2,43-2,61 (м, 2Н), 2,24-2,35 (м, 1Н), 1,56-1,70 (м, 1 Н)
[1555] Пример 14. (S)-1-(2-((S)-3-([1,1'-бифенил]-4-иламино)пирролидин-1-ил)ацетил)-4,4-дифторпирролидин-2-карбонитрил
[1556] Указанное в заголовке соединение (13,3 мг) получали таким же образом, как и в примере 6, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (S)-N-([1,1'-бифенил]-4-ил)пирролидин-3-амина гидрохлорид (28,6 мг, 0,12 ммоль), полученныйв эталонном примере 13. 1H-ЯМР (CDCl3, 400 МГц) δ 7,53 (д, 2Н), 7,41-7,51 (м, 2Н), 7,39 (т, 2Н), 7,22-7,30 (м, 1Н), 6,65 (д, 2Н), 5,31-5,48 (с, 0,4Н), 4,95-5,12 (м, 0,6Н), 3,96-4,17 (м, 3Н), 3,33-3,52 (м, 1Н), 2,84-3,08 (м, 2Н), 2,56-2,81 (м, 4Н), 2,27-2,53 (м, 2Н), 1,78-1,85 (м, 1Н)
[1557] Пример 15. (S)-4,4-дифтор-1-(2-((S)-3-(нафталин-2-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1558] Указанное в заголовке соединение (13,8 мг) получали таким же образом, как и в примере 6, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (S)-N-(нафталин-2-ил)пирролидин-3-амин (25,5 мг, 0,12 ммоль), полученныйв эталонном примере 14. 1H-ЯМР (CDCl3, 400 МГц) δ 7,58-7,68 (м, 3Н), 7,36 (т, 1Н), 7,16-7,26 (м, 1Н), 6,85 (д, 1Н), 6,73-6,81 (м, 1Н), 5,26 (д, 0,3Н), 4,89 (т, 0,6Н), 4,08-4,19 (м, 1Н), 3,82-3,92 (м, 0,5Н), 3,37-3,57 (м, 1Н), 3,23-3,33 (м, 1Н), 2,87-3,04 (м, 1,5Н), 2,55-2,83 (м, 4Н), 2,30-2,47 (м, 1Н), 1,81-1,93 (м, 1Н)
[1559] Пример 16. (S)-1-(2-((S)-3-([1,1'-бифенил]-3-иламино)пирролидин-1-ил)ацетил)-4,4-дифторпирролидин-2-карбонитрил
[1560] Указанное в заголовке соединение (8,3 мг) получали таким же образом, как и в примере 6, за исключением того, что (S)-N-([1,1'-бифенил]-3-ил)пирролидин-3-амина гидрохлорид (28,6 мг, 0,12 ммоль), полученный в эталонном примере 15, использовали вместо (S)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида. 1H-ЯМР (CDCl3, 400 МГц) δ 7,55 (д, 2Н), 7,41 (т, 2Н), 7,30-7,35 (м, 1Н), 7,20-7,25 (м, 1Н), 6,93 (д, 1Н), 6,77 (с, 1Н), 6,54-6,62 (м, 1Н), 5,28 (м, 0,3Н), 4,90 (м, 0,6Н), 3,95-4,14 (м, 3Н), 3,77-3,87 (м, 0,4Н), 3,42-3,52 (м, 0,6Н), 3,23-3,29 (м, 1Н), 2,84-3,01 (м, 1Н), 2,54-2,78 (м, 4Н), 2,29-2,44 (м, 1Н), 1,68-1,84(м, 1Н)
[1561] Пример 17. (S)-1-(2-((R)-3-(хинолин-3-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1562] (S)-1-(2-хлорацетил)пирролидин-2-карбонитрил (25,0 мг 0,12 ммоль), полученный в эталонном примере 1, растворяли в безводном дихлорметане (4 мл). К полученному раствору добавляли (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид (34,3 мг 0,12 ммоль), полученный в эталонном примере 17, и карбонат калия (48,0 мг, 0,35 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции к реакционной смеси добавляли воду. Водный слой реакционной смеси экстрагировали дихлорметаном. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (дихлорметан / метанол = 10/1, об./об.) с получением указанного в заголовке соединения (6,1 мг). 1H-ЯМР (CDCl1, 400 МГц) δ 8,39-8,54 (м, 1Н), 7,93 (д, 1Н), 7,60-7,72 (м, 1Н), 7,37-7,44 (м, 2,0Н), 6,96 (с, 1Н), 4,83-4,91 (м, 0,4Н), 4,76-4,81 (м, 1Н), 4,50 (м, 0,6Н), 3,67-3,81 (м, 1Н), 3,46-3,56 (м, 1Н), 3,28-3,43 (м, 2Н), 3,02-3,12 (м, 2Н), 2,80-2,90 (м, 1Н), 2,52-2,73 (м, 1Н), 2,10-2,48 (м, 5Н), 1,81 (м, 2Н)
[1563] Пример 18. (S)-1-(2-((R)-3-([1,1'-бифенил]-3-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1564] Указанное в заголовке соединение (6,92 мг) получали таким же образом, как и в примере 17, за исключением того, что вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (R)-N-([1,1'-бифенил]-3-ил)пирролидин-3-амина гидрохлорид (28,6 мг, 0,12 ммоль), полученныйв эталонном примере 18. 1H-ЯМР (CDCl3, 400 МГц) δ 7,56 (д, 2Н), 7,41 (т, 2Н), 7,33 (д, 1Н), 7,20-7,32 (м, 1Н), 6,92 (д, 1Н), 6,79 (с, 1Н), 6,58 (д, 1Н), 4,89-4,96 (м, 0,3Н), 4,74 (м, 0,7Н), 4,11-4,24 (м, 1Н), 3,65-3,72 (м, 1Н), 3,29-3,56 (м, 4Н), 2,88-3,02 (м, 2Н), 2,79-2,85 (м, 1Н), 2,63-2,71 (м, 1Н), 2,04-2,45 (м, 5Н), 1,78-1,85 (м, 1Н)
[1565] Пример 19. (S)-1-(2-((S)-3-(изохинолин-4-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1566] Указанное в заголовке соединение (4,78 мг) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид использовали (S)-N-(пирролидин-3-ил)изохинолин-4-амина гидрохлорид (25,6 мг, 0,12 ммоль), полученный в эталонном примере 7. 1H-ЯМР (CDCl2, 400 МГц) δ 8,41-8,54 (м, 1Н), 7,93-8,22 (м, 2Н), 7,65-7,75 (м, 1Н), 7,39-7,53 (м, 1Н), 7,36-7,41 (м, 0,5Н), 6,34-6,44 (м, 1Н), 6,22-6,32 (м, 0,4Н), 4,72-4,86 (м, 1Н), 4,24-4,34 (м, 1Н), 3,43-3,72 (м, 4Н), 3,24-3,36 (м, 1Н), 2,98-3,17 (м, 2Н), 2,83-2,94 (м, 1Н), 1,93-2,54 (м, 7Н)
[1567] Пример 20. (S)-1-(2-((S)-3-(бензо[b]тиофен-4-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1568] Указанное в заголовке соединение (8,46 мг) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид использовали (S)-N-(бензо[b]тиофен-4-ил)пирролидин-3-амина гидрохлорид (26,2 мг, 0,12 ммоль), полученный в эталонном примере 8. 1H-ЯМР (CDCl3, 400 МГц) δ 7,33-7,42 (м, 1Н), 7,28-7,32 (м, 1Н), 7,20-7,25 (м, 1Н), 7,17-7,20 (м, 1Н), 6,44 (дд, 1Н), 4,63-4,88 (м, 1Н), 4,19-4,24 (м, 1Н), 3,26-3,69 (м, 4Н), 2,98-3,18 (м, 1Н), 2,82-2,95 (м, 1Н), 2,62-2,76 (м, 1Н), 1,83-2,52 (м, 7Н)
[1569] Пример 21. (S)-1-(2-((S)-3-(бензо[b]тиофен-7-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1570] Указанное в заголовке соединение (6,55 мг) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-N-(бензо[b]тиофен-7-ил)пирролидин-3-амина гидрохлорид (26,2 мг, 0,12 ммоль), полученный в эталонном примере 9. 1H-ЯМР (CDCl3, 400 МГц) δ 7,24-7,37 (м, 4Н), 6,50-6,72 (м, 1Н), 4,99-5,02 (м, 0,4Н), 4,74-4,82 (м, 0,6Н), 4,24-4,32 (м, 1Н), 3,97-4,13 (м, 1Н), 3,57-3,68 (м, 1Н), 3,24-3,52 (м, 3Н), 3,03-3,10 (м, 1Н), 2,95-3,01 (м, 0,6Н), 2,75-2,84 (м, 1Н), 2,62-2,71 (м, 0,6Н), 2,34-2,46 (м, 1Н), 1,75-2,28 (м, 5Н)
[1571] Пример 22. (S)-1-(2-((3)-3-(бензофуран-7-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1572] Указанное в заголовке соединение (22,5 мг) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-N-(бензофуран-7-ил)пирролидин-3-амина гидрохлорид (24,27 мг, 0,12 ммоль), полученный в эталонном примере 10. 1H-ЯМР (CDCl3, 400 МГц) δ 7,54-7,65 (м, 1Н), 7,08 (т, 1Н), 6,96 (д, 1Н), 6,72 (с, 1Н), 6,47-6,52 (м, 1Н), 5,06-5,12 (м, 0,3 Н), 4,74-4,85 (м, 0,6 Н), 4,18-4,30 (м, 1Н), 3,58-3,68 (м, 1Н), 3,44-3,56 (м, 1Н), 3,24-3,42 (м, 2Н), 2,89-3,14 (м, 2Н), 2,65-2,87 (м, 2Н), 2,33-2,51 (м, 1Н), 1,94-2,29 (м, 4 Н), 1,78-1,91 (м, 1Н)
[1573] Пример 23. (S)-1-(2-((S)-3-(фуро[3,2-с]пиридин-7-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1574] Указанное в заголовке соединение (14,0 мг) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-4-ил)хинолин-3-амина гидрохлорида использовали (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорид (24,4 мг, 0,12 ммоль), полученный в эталонном примере 11. 1H-ЯМР (CDCl3, 400 МГц) δ 8,37 (с, 1Н), 7,87 (с, 1Н), 7,60-7,71 (м, 1Н), 6,80-6,95 (м, 1Н), 4,96-5,02 (м, 0,3 Н), 4,77-4,88 (м, 0,7 Н), 4,37-4,51 (м, 1Н), 4,30-4,35 (м, 1Н), 3,59-3,72 (м, 1Н), 3,40-3,55 (м, 1Н), 2,97-3,11 (м, 2Н), 2,80-2,89 (м, 1,4Н), 2,60-2,68 (м, 0,6Н), 2,04-2,55 (м, 6Н), 1,81-1,95 (м, 1Н)
[1575] Пример 24. (S)-1-(2-((R)-3-(изохинолин-4-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1576] Указанное в заголовке соединение (12,4 мг) получали таким же образом, как ив примере 17, за исключением того, что вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (R)-N-(пирролидин-3-ил)изохинолин-4-амина гидрохлорид, полученный в эталонном примере 19. 1H-ЯМР (CDCl3, 400 МГц) δ 8,52-8,62 (м, 1Н), 7,94-8,01 (м, 2Н), 7,59-7,65 (м, 1Н), 7,39-7,47 (м, 1Н), 6,38-6,54 (м, 1Н), 4,76-4,84 (м, 1Н), 4,14-4,35 (м, 1Н), 3,60-3,68 (м, 1Н), 3,33-3,58 (м, 3Н), 3,13-3,23 (м, 1Н), 2,90-3,10 (м, 2Н), 2,58-2,78 (м, 1Н), 2,08-2,50 (м, 5Н), 1,87-2,00 (м, 1Н)
[1577] Пример 25. (S)-1-(2-((R)-3-(бензо[b]тиофен-7-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1578] Указанное в заголовке соединение (4,5 мг) получали таким же образом, как и в примере 17, за исключением того, что вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид использовали (R)-N-(бензо[b]тиофен-7-ил)пирролидин-3-амина гидрохлорид (26,2 мг, 0,12 ммоль), полученный в эталонном примере 20. 1H-ЯМР (CDCl3, 400 МГц) δ 7,24-7,38 (м, 4Н), 6,54-6,72 (м, 1Н), 5,02-5,12 (м, 0,4Н), 4,75-4,82 (м, 0,7Н), 4,25-4,32 (м, 1Н), 3,61-3,88 (м, 1Н), 3,47-3,58 (м, 1Н), 3,28-3,46 (м, 2Н), 2,87-3,10 (м, 2Н), 2,79-2,87 (м, 1Н), 2,59-2,73 (м, 1Н), 2,32-2,50 (м, 1Н), 2,04-2,30 (м, 4Н), 1,79-1,93 (м, 1Н)
[1579] Пример 26. (1S,3S,5S)-2-(2-((S)-3-(фуро[3,2-с]пиридин-7-иламино)пирролидин-1-ил)ацетил)-2-азабицикло[3.1.0]гексан-3-карбонитрил
[1580] (1S,3S,5S)-2-(2-хлорацетил)-2-азабицикло[3.1.0]гексан-3-карбонитрил (22,2 мг, 0,12 ммоль), полученный в эталонном примере 4, растворяли в безводном ацетонитриле (4 мл). К полученному раствору добавляли (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорид (33,1 мг, 0,12 ммоль), полученный в эталонном примере 11 и карбонат калия (48,0 мг, 0,35 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции к реакционной смеси добавляли воду. Водный слой реакционной смеси экстрагировали дихлорметаном. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (дихлорметан / метанол = 10/1, об./об.) с получением указанного в заголовке соединения (1,8 мг). 1H-ЯМР (CDCl3, 400 МГц) δ 8,84 (м, 1Н), 8,37 (д, 0,6Н), 8,28 (д, 0,4Н), 7,54-7,72 (м, 1Н), 7,46-7,52 (м, 1Н), 7,33-7,42 (м, 1Н), 6,56-6,72 (м, 1Н), 5,42-5,51 (м, 0,6Н), 5,09-5,24 (м, 0,4Н), 4,75-4,92 (м, 1Н), 4,20-4,31 (м, 1Н), 3,62-3,78 (м, 1Н), 3,24-3,57 (м, 3Н), 2,92-3,20 (м, 3Н), 2,59-2,76 (м, 1Н), 1,86-2,49 (м, 6Н)
[1581] Пример 27. (S)-1-(2-((3)-3-(хинолин-5-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1582] Указанное в заголовке соединение (18,1 мг) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид использовали (S)-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (34,3 мг 0,12 ммоль), полученный в эталонном примере 16. 1H-ЯМР (CDCl3, 400 МГц) δ 8,84 (м, 1Н), 8,37 (д, 0,6Н), 8,28 (д, 0,4Н), 7,54-7,72 (м, 1Н), 7,46-7,52 (м, 1Н), 7,33-7,42 (м, 1Н), 6,56-6,72 (м, 1Н), 5,42-5,51 (м, 0,6Н), 5,09-5,24 (м, 0,4Н), 4,75-4,92 (м, 1Н), 4,20-4,31 (м, 1Н), 3,62-3,78 (м, 1Н), 3,24-3,57 (м, 3Н), 2,92-3,20 (м, 3Н), 2,59-2,76 (м, 1Н), 1,86-2,49 (м, 6Н)
[1583] Пример 28. (2S,4S)-4-фтор-1-(2-((S)-3-(фуро[3,2-с]пиридин-7-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил;
[1584] (2S,4S)-1-(2-хлорацетил)-4-фторпирролидин-2-карбонитрил (20,0 мг, 0,10 ммоль), полученный в эталонном примере 2, растворяли в безводном дихлорметане (4 мл). К полученному раствору добавляли (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорид (31,8 мг 0,12 ммоль), полученный в эталонном примере 11 и карбонат калия (29,0 мг, 0,21 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции к реакционной смеси добавляли воду Водный слой реакционной смеси экстрагировали дихлорметаном. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (дихлорметан / метанол = 10/1, об./об.) с получением у казанного в заголовке соединения (27,7 мг). 1H-ЯМР (CD3OD, 400 МГц) δ 8,36 (с, 1Н), 7,89 (д, 1Н), 7,13 (с, 1Н), 6,98 (д, 1Н), 5,51-5,38 (м, 1Н), 5,00 (с, 1Н), 4,03 (с, 1Н), 3,85-3,73 (м, 1Н), 3,58-3,39 (м, 2Н), 3,07-3,04 (м, 1Н) 2,92-2,84 (м, 2Н), 2,69-2,31 (м, 4Н), 1,88-1,86 (м, 1Н)
[1585] Пример 29. N-((S)-1-(2-(2S,4S)-2-циано-4-фторпирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-6-фторбензофуран-3-карбоксамида;
[1586] (2S,4S)-1-(2-хлорацетил)-4-фторпирролидин-2-карбонитрил (20,0 мг, 0,10 ммоль), полученный в эталонном примере 2, растворяли в безводном ацетонитриле (1 мл). К полученному раствору добавляли (S)-6-фтор-N-(пирролидин-3-ил)бензофуран-3-карбоксамид гидрохлорид (32,8 мг 0,12 ммоль), полученный в эталонном примере 45 и карбонат калия (29,0 мг, 0,21 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции к реакционной смеси добавляли воду. Водный слой реакционной смеси экстрагировали дихлорметаном. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (дихлорметан / метанол = 10/1, об./об.) с получением у казанного в заголовке соединения (4,3 мг). 1H ЯМР (CD3OD, 400 МГц) δ 8,36 (с, 1Н), 8,03 (с, 1Н), 7,35 (д, 1Н), 7,15 (т, 1Н), 5,51-5,38 (м, 1Н), 5,00 (дд, 1Н), 4,60 (с, 1Н), 4,03 (дд, 1Н), 3,85-3,73 (м, 1Н), 3,64-3,36 (м, 2Н), 3,07-3,04 (м, 1Н) 2,92-2,86 (м, 2Н), 2,69-2,32 (м, 4Н), 1,88-1,86 (м, 1Н)
[1587] Пример 30. N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)хинолин-4-карбоксамид
[1588] (S)-1-(2-((S)-3-Аминопирролидин-1-ил)ацетил)пирролидин-2-карбонитрил трифторацетат (20 мг, 0,09 ммоль), полученный в эталонном примере 25, растворяли в диметилформамиде (2 мл). К полученному раствору добавляли хинолин-4-карбоновую кислоту (31,2 мг, 0,18 ммоль), HATU (O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилуран гексафторфосфат) (24,9 мг, 0,18 ммоль) и диизопропилэтиламин (47 мкл, 0,27 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции к реакционной смеси добавляли воду. Водный слой реакционной смеси экстрагировали этилацетатом. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (дихлорметан / метанол = 20/1, об./об.) с получением указанного в заголовке соединения (7 мг). 1H-ЯМР (CDCl3, 400 МГц) δ 8,92-9,01 (м, 1Н), 8,33 (д, 1Н), 8,14 (д, 1Н), 7,76 (т, 1Н), 7,49-7,69 (м, 2Н), 4,77-7,89 (м, 1Н), 4,68-4,75 (м, 1Н), 3,55-3,67 (м, 1Н), 3,43 (кв, 2Н), 3,18 (м, 1Н), 2,99 (м, 2Н), 2,58-2,83 (м, 1Н), 2,07-2,51 (м, 5Н), 1,78-2,02 (м, 3Н)
[1589] Пример 31. N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)хинолин-3-карбоксамид
[1590] Указанное в заголовке соединение (7,23 мг) получали таким же образом, как и в примере 30, за исключением того, что вместо хинолин-4-карбоновой кислоты использовали хинолин-3-карбоновую кислоту (31,2 мг, 0,18 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 9,41-9,50 (м, 1Н), 8,73-8,85 (м, 1Н), 8,12-8,21 (м, 1Н), 7,97-8,11 (м, 1Н), 7,78-7,95 (м, 1Н), 7,60-7,72 (м, 1Н), 4,74-4,88 (м, 2Н), 3,36-3,78 (м, 4Н), 3,26-3,32 (м, 2Н), 3,02-3,12 (м, 1Н), 2,73-2,82 (м, 1Н), 2,13-2,45 (м, 5Н), 2,05-2,12 (м, 2Н)
[1591] Пример 32. N-((S)-1-(2-((S)-2-цшнопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)хинолин-5-карбоксамид
[1592] Указанное в заголовке соединение (11,7 мг) получали таким же образом, как и в примере 30, за исключением того, что вместо хинолин-4-карбоновой кислоты использовали хинолин-5-карбоновую кислоту (31,2 мг, 0,18 ммоль). 1H-ЯМР (CD3OD, 400 МГц): Сдвиг = 9,23 (д, 0,3Н), 8,83-8,94 (м, 1Н), 8,76 (д, 0,7Н), 8,12 (д, 1Н), 7,81-7,92 (м, 2Н), 7,67-7,80 (м, 1Н), 5,78-4,87 (м, 0,5Н), 4,6-4,77 (м, 0,7Н), 3,66-3,75 (м, 1Н), 3,66-3,65 (м, 2Н), 3,43-3,42 (м, 1Н), 2,72-3,23 (м, 4Н), 1,89-2,26 (м, 4Н), 1,24-1,26 (м, 4Н), 1,24-1,40 (м, 2Н)
[1593] Пример 33. N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)хинолин-2-карбоксамид
[1594] Указанное в заголовке соединение (14,4 мг) получали таким же образом, как и в примере 30, за исключением того, что вместо хинолин-4-карбоновой кислоты использовали хинолин-2-карбоновую кислоту (31,2 мг, 0,18 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,67-8,81 (м, 1Н), 8,29-8,42 (м, 2Н), 8,12-8,24 (м, 1Н), 7,87-8,10 (м, 1Н), 7,77-7,86 (м, 1Н), 7,62-7,72 (м, 1Н), 5,11-5,19 (м, 0,3Н), 4,78-7,85 (м, 1,7Н), 3,60-3,77 (м, 1Н), 3,54-3,59 (м, 1Н), 3,42-3,51 (м, 2Н), 3,27-3,42 (м, 1Н), 3,01-3,11 (м, 1Н), 2,82-2,92 (м, 1Н), 2,62-2,72 (м, 1Н), 2,54-2,60 (м, 1Н), 2,17-2,42 (м, 4Н), 1,94-2,02 (м, 1Н), 1,44-1,59 (м, 1Н)
[1595] Пример 34. N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)хинолин-8-карбоксамид
[1596] Указанное в заголовке соединение (4,82 мг) получали таким же образом, как и в примере 30, за исключением того, что вместо хинолин-4-карбоновой кислоты использовали хинолин-8-карбоновую кислоту (31,2 мг, 0,18 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,92-9,02 (м, 1Н), 8,75-8,88 (м, 1Н), 8,21-8,34 (м, 1Н), 7,92-8,03 (м, 1Н), 7,61-7,73 (м, 1Н), 7,45-7,59 (м, 1Н), 4,61-4,91 (м, 1,7Н), 3,33-3,82 (м, 4Н), 2,73-3,24 (м, 3Н), 2,41-2,63 (м, 1Н), 1,87-2,34 (м, 6Н)
[1597] Пример 35. N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил) изохинолин-1-карбоксамид
[1598] Указанное в заголовке соединение (4,9 мг) получали таким же образом, как и в примере 30, за исключением того, что вместо хинолин-4-карбоновой кислоты использовали изохинолин-1-карбоновую кислоту (31,2 мг, 0,18 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 9,55-9,68 (м, 1Н), 8,45-8,58 (м, 2Н), 7,83-7,98 (м, 1Н), 7,75-7,81 (м, 1Н), 7,61-7,74 (м, 2Н), 5,18-5,26 (м, 0,3Н), 4,77-4,87 (м, 0,7Н), 4,64-4,74 (м, 1Н), 3,57-3,71 (м, 2Н), 3,40-3,55 (м, 1Н), 3,10-3,28 (м, 1Н), 2,85-2,96 (м, 2Н), 2,39-2,72 (м, 2Н), 2,17-2,35 (м, 3Н), 1,84-2,10 (м, 2Н)
[1599] Пример 36. N-((S)-1 -(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)бензо[b]тиофен-2-карбоксамид
[1600] Указанное в заголовке соединение (8,0 мг) получали таким же образом, как и в примере 30, за исключением того, что вместо хинолин-4-карбоновой кислоты использовали бензо[b]тиофен-2-карбоновую кислоту (32,6 мг, 0,18 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,20-8,29 (м, 0,5Н), 7,97-8,12 (м, 0,6Н), 7,80-7,89 (м, 2Н), 7,39-7,52 (м, 2Н), 4,77-4,89 (м, 1Н), 4,67-4,72 (м, 1Н), 3,39-3,73 (м, 3Н), 3,06-3,25 (м, 2Н), 2,93-3,00 (м, 1Н), 2,71-2,82 (м, 1Н), 2,13-2,47 (м, 5Н), 1,95 (м, 1Н)
[1601] Пример 37. N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)бензофуран-3-карбоксамид
[1602] Указанное в заголовке соединение (6,4 мг) получали таким же образом, как и в примере 30, за исключением того, что вместо хинолин-4-карбоновой кислоты использовали бензофуран-3-карбоновую кислоту (29,2 мг, 0,18 ммоль). 1H-ЯМР (CDCl2, 400 МГц) δ 8,26-8,36 (м, 0,7Н), 8,14-8,21 (м, 1,4Н), 7,81-7,92 (м, 0,6Н), 7,52-7,68 (м, 1Н), 7,35-7,51 (м, 2Н), 7,05-7,13 (м, 0,3Н), 4,75-4,82 (м, 2Н), 3,64-3,82 (м, 2Н), 3,39-3,52 (м, 3Н), 3,00-3,26 (м, 2Н), 2,94-3,00 (м, 1Н), 2,69-2,85 (м, 1Н), 2,11-2,46 (м, 6Н), 1,87-2,02 (м, 1Н)
[1603] Пример 38. N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-2-(нафталин-1-ил)ацетамид
[1604] Указанное в заголовке соединение (6,6 мг) получали таким же образом, как и в примере 30, за исключением того, что вместо хинолин-4-карбоновой кислоты использовали 2-(нафталин-1-ил)уксусную кислоту (31,2 мг, 0,18 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 7,95-8,03 (м, 1Н), 7,79-7,90 (м, 2Н), 7,41-7,57 (м, 4Н), 6,06-6,33 (м, 1Н), 4,62 (м, 0,6Н), 4,45 (м, 1Н), 3,92-4,07 (м, 2Н), 3,36-3,52 (м, 1Н), 3,18-3,30 (м, 2Н), 2,64-3,08 (м, 2Н), 2,32-2,55 (м, 2Н), 2,07-2,30 (м, 4Н), 1,48-1,58 (м, 1Н)
[1605] Пример 39. N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-[1,1'-бифенил]-2-карбоксамид
[1606] Указанное в заголовке соединение (7,6 мг) получали таким же образом, как и в примере 30, за исключением того, что вместо хинолин-4-карбоновой кислоты использовали[1,1'-бифенил]-2-карбоновую кислоту (35,7 мг, 0,18 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 7,66-7,76 (м, 1Н), 7,34-7,50 (м, 8Н), 5,87-6,07 (м, 1Н), 4,40-4,78 (м, 2Н), 3,56-3,72 (м, 2Н), 3,06-3,30 (м, 2Н), 2,65-2,81 (м, 1Н), 2,58-2,64 (м, 1Н), 2,19-2,39 (м, 3Н), 2,03-2,18 (м, 4Н), 1,25-1,35 (м, 2Н)
[1607] Пример 40. N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил) бе нзофуран-2-карб оксамид
[1608] Указанное в заголовке соединение (8,4 мг) получали таким же образом, как и в примере 30, за исключением того, что вместо хинолин-4-карбоновой кислоты использовали бензофуран-2-карбоновую кислоту (29,2 мг, 0,18 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 7,66-7,75 (м, 1Н), 7,49-7,59 (м, 1Н), 7,37-7,49 (м, 2Н), 7,27-7,33 (м, 1Н), 4,91 (м, 0,3Н), 4,79 (м, 0,7Н), 4,71-4,78 (м, 1Н), 3,62-3,71 (м, 1Н), 3,41-3,60 (м, 2Н), 3,08-3,28 (м, 1Н), 2,88-2,98 (м, 2Н), 2,52-2,83 (м, 1Н), 2,03-2,42 (м, 5Н), 1,79-1,98 (м, 1Н)
[1609] Пример 41. N-((S)-1-(2-((3)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)бензо[b]тиофен-3-карбоксамид
[1610] Указанное в заголовке соединение (10,4 мг) получали таким же образом, как и в примере 30, за исключением того, что вместо хинолин-4-карбоновой кислоты использовали бензо[b]тиофен-3-карбоновую кислоту (32,1 мг, 0,18 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,49-8,58 (м, 1Н), 8,08 (с, 0,6Н), 7,96 (с, 0,4Н), 7,85-7,95 (м, 1Н), 7,68-7,82 (м, 0,6Н), 7,34-7,48 (м, 2Н), 7,10 (м, 0,4Н), 4,72-4,82 (м, 2Н), 3,39-3,75 (м, 4Н), 3,10-3,26 (м, 1Н), 2,88-3,07 (м, 2Н), 2,56-2,77 (м, 1Н), 2,09-2,50 (м, 5Н), 1,86-2,02 (м, 1Н)
[1611] Пример 42. N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-2-метилбензофуран-3-карбоксамид
[1612] Указанное в заголовке соединение (14,4 мг) получали таким же образом, как и в примере 30, за исключением того, что вместо хинолин-4-карбоновой кислоты использовали 2-метилбензофуран-3-карбоновую кислоту (31,7 мг, 0,18 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 7,68-7,82 (м, 1Н), 7,43-7,52 (м, 1Н), 7,27-7,33 (м, 1Н), 6,97-7,12 (м, 0,7Н), 6,58-6,71 (м, 0,3Н), 4,69-4,91 (м, 2Н), 3,60-3,73 (м, 1Н), 3,32-3,59 (м, 3Н), 3,08-3,24 (м, 1Н), 2,92-3,05 (м, 2Н), 2,78-2,90 (м, 1Н), 2,71-2,75 (м, 3Н), 2,65-2,71 (м, 1Н), 2,08-2,49 (м, 5Н), 1,86-2,00 (м, 1Н)
[1613] Пример 43. N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-5-фторбензофуран-3-карбоксамид
[1614] Указанное в заголовке соединение (6,5 мг) получали таким же образом, как и в примере 30, за исключением того, что вместо хинолин-4-карбоновой кислоты использовали 5-фторбензофуран-3-карбоновую кислоту (32,4 мг, 0,18 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,33 (с, 0,6Н), 8,16-8,22 (м, 0,3Н), 8,12-8,14 (м, 0,7Н), 7,74-7,92 (м, 1Н), 7,43-7,52 (м, 1Н), 6,95-7,17 (м, 1Н), 4,64-4,86 (м, 2Н), 3,49-3,72 (м, 3Н), 3,43 (м, 1Н), 3,21-3,35 (м, 1Н), 3,16 (м, 1Н), 2,91-3,10 (м, 1Н), 2,69-2,86 (м, 1Н), 2,13-2,40 (м, 5Н)
[1615] Пример 44. N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-6-фторбензофуран-3-карбоксамид
[1616] Указанное в заголовке соединение (9,8 мг) получали таким же образом, как и в примере 30, за исключением того, что вместо хинолин-4-карбоновой кислоты использовали 6-фторбензофуран-3-карбоновую кислоту (32,4 мг, 0,18 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,29 (с, 1Н), 8,01-8,18 (м, 2Н), 7,21-7,40 (м, 1Н), 7,05-7,17 (м, 1Н), 4,73-4,85 (м, 2Н), 3,48-3,71 (м, 3Н), 3,36-3,47 (м, 1Н), 3,06-3,29 (м, 2Н), 2,94-3,05 (м, 1Н), 2,66-2,80 (м, 1Н), 2,11-2,39 (м, 5Н), 1,84-2,03 (м, 1Н)
[1617] Пример 45. N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-7-метилбензофуран-3-карбоксамид
[1618] Указанное в заголовке соединение (8,5 мг) получали таким же образом, как и в примере 30, за исключением того, что вместо хинолин-4-карбоновой кислоты использовали 7-метилбензофуран-3-карбоновую кислоту (31,7 мг, 0,18 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,29 (с, 0,7Н), 8,17 (с, 0,4Н), 7,80-8,00 (м, 2Н), 7,20-7,25 (м, 1Н), 7,14-7,18 (м, 1Н), 4,69-4,84 (м, 2Н), 3,53-3,69 (м, 3Н), 3,27-3,49 (м, 2Н), 3,11-3,25 (м, 1Н), 2,77-2,97 (м, 1Н), 2,52-2,62 (с, 3Н), 2,10-2,42 (м, 5Н), 1,99-2,04 (м, 1Н)
[1619] Пример 46. N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-5-метоксибензофуран-3-карбоксамид
[1620] Указанное в заголовке соединение (5,9 мг) получали таким же образом, как и в примере 30, за исключением того, что вместо хинолин-4-карбоновой кислоты использовали 5-метоксибензофуран-3-карбоновую кислоту (34,6 мг, 0,18 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,27 (с, 0,7Н), 8,12 (с, 0,4Н), 8,00 (д, 0,7Н), 7,60-7,69 (м, 1Н), 7,38 (д, 1Н), 7,09-7,24 (м, 0,4Н), 6,93 (д, J-9,1, 1Н), 4,68-4,81 (м, 2Н), 3,88 (с, 3Н), 3,50-3,70 (м, 3Н), 3,25-3,49 (м, 2Н), 2,98-3,23 (м, 2Н), 2,68-2,79 (м, 1Н), 2,11-2,41 (м, 5Н), 1,97-2,03 (м, 1Н)
[1621] Пример 47. N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-7-метоксибензофуран-3-карбоксамид
[1622] Указанное в заголовке соединение (1,1 мг) получали таким же образом, как и в примере 30, за исключением того, что вместо хинолин-4-карбоновой кислоты использовали 7-метоксибензофуран-3-карбоновую кислоту (34,6 мг, 0,18 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,28 (с, 0,6Н), 8,16 (с, 0,5Н), 7,79-8,15 (м, 0,5Н), 7,61-7,74 (м, 1Н), 7,28-7,33 (м, 0,6Н), 6,86 (д, 1.), 4,76-4,87 (м, 2Н), 4,01-4,21 (с, 3Н), 3,52-3,72 (м, 3Н), 3,44-3,51 (м, 1Н), 3,33-3,42 (м, 1Н), 3,16-3,32 (м, 1Н), 3,08-3,15 (м, 1Н), 2,73-2,86 (м, 1Н), 2,11-2,45 (м, 5Н), 1,90-2,04 (м, 1Н)
[1623] Пример 48. N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-4-гидроксибензофуран-3-карбоксамид
[1624] Указанное в заголовке соединение (1,8 мг) получали таким же образом, как и в примере 30, за исключением того, что вместо хинолин-4-карбоновой кислоты использовали 4-гидроксибензофуран-3-карбоновую кислоту (32,1 мг, 0,18 ммоль). 1H-ЯМР (CDCl2, 400 МГц) δ 9,15-9,21 (м, 0,8Н), 8,36 (с, 0,7Н), 8,13 (с, 0,3Н), 7,88 (м, 0,2Н), 7,19-7,25 (м, 1Н), 6,98-7,12 (м, 1Н), 6,76 (д, 1Н), 4,77-4,88 (м, 1Н), 4,67-4,76 (м, 1Н), 3,54-3,75 (м, 3Н), 3,35-3,51 (м, 1Н), 3,15-3,28 (м, 2Н), 3,02 (м, 1Н), 2,67-2,90 (м, 1Н), 2,14-2,42 (м, 5Н), 2,05 (с, 1Н)
[1625] Пример 49. N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-6-гидроксибензофуран-3-карбоксамид
[1626] Указанное в заголовке соединение (7,6 мг) получали таким же образом, как и в примере 30, за исключением того, что вместо хинолин-4-карбоновой кислоты использовали 6-гидроксибензофуран-3-карбоновую кислоту (32,1 мг, 0,18 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,05-8,12 (м, 1Н), 7,80-7,98 (м, 1Н), 7,64-7,78 (м, 1Н), 6,99-7,12 (м, 1Н), 6,82-6,98 (м, 1Н), 4,76-4,82 (м, 2Н), 3,48-3,84 (м, 3Н), 3,41-3,47 (м, 1Н), 3,31-3,40 (м, 1Н), 2,91-3,23 (м, 2Н), 2,62-2,81 (м, 1Н), 2,11-2,40 (м, 5Н), 1,86-2,01 (м, 1Н)
[1627] Пример 50. N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-7-фторбензофуран-3-карбоксамид
[1628] Указанное в заголовке соединение (9,6 мг) получали таким же образом, как и в примере 30, за исключением того, что вместо хинолин-4-карбоновой кислоты использовали 7-фторбензофуран-3-карбоновую кислоту (32,4 мг, 0,18 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,32 (с, 0,6Н), 8,18 (с, 0,3Н), 8,04-8,12 (м, 0,6Н), 7,88-7,98 (м, 1,0Н), 7,18-7,34 (м, 1,4Н), 7,03-7,14 (м, 1Н), 4,67-4,85 (м, 2Н), 3,35-3,78 (м, 4Н), 3,05-3,27 (м, 2Н), 2,98-3,03 (м, 1Н), 2,66-2,79 (м, 1Н), 2,12-2,48 (м, 5Н), 1,87-2,03 (м, 1Н)
[1629] Пример 51. N-((S)-1-(2-((5)-2-цшнопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-5,7-дифторбензофуран-3-карбоксамид
[1630] Указанное в заголовке соединение (12 мг) получали таким же образом, как и в примере 30, за исключением того, что вместо хинолин-4-карбоновой кислоты использовали 5,7-дифторбензофуран-3-карбоновую кислоту (35,6 мг, 0,18 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,38 (с, 0,7Н), 8,31 (д, 0,6Н), 8,21 (с, 0,3Н), 7,67-7,77 (м, 1Н), 7,36 (д, 0,3Н), 6,88 (т, 1Н), 4,77-4,89 (м, 1Н), 4,65-4,73 (м, 1Н), 3,36-3,74 (м, 4Н), 3,08-3,28 (м, 2Н), 3,00-3,07 (м, 1Н), 2,69-2,82 (м, 1Н), 2,13-2,41 (м, 5Н), 1,86-2,05 (м, 1Н)
[1631] Пример 52. N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-5-метилбензофуран-3-карбоксамид
[1632] Указанное в заголовке соединение (6,2 мг) получали таким же образом, как и в примере 30, за исключением того, что вместо хинолин-4-карбоновой кислоты использовали 5-метилбензофуран-3-карбоновую кислоту (31,7 мг, 0,18 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,22 (с, 0,6Н), 8,10 (с, 0,4Н), 7,91 (с, 1Н), 7,69 (м, 0,7Н), 7,38 (д, 1Н), 7,15 (д, 1Н), 7,03 (м, 0,3Н), 4,67-4,82 (м, 2Н), 3,37-3,77 (м, 4Н), 2,89-3,32 (м, 3Н), 2,63-2,85 (м, 1Н), 2,45-2,50 (м, 3Н), 2,12-2,39 (м, 5Н), 1,97-2,11 (м, 1Н)
[1633] Пример 53. N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-6-метилбензофуран-3-карбоксамид
[1634] Указанное в заголовке соединение (3,3 мг) получали таким же образом, как и в примере 30, за исключением того, что вместо хинолин-4-карбоновой кислоты использовали 6-метилбензофуран-3-карбоновую кислоту (31,7 мг, 0,18 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,20 (с, 0,7Н), 8,08 (с, 0,3Н), 7,88-8,04 (м, 1Н), 7,75 (м, 0,7Н), 7,28-7,36 (м, 1Н), 7,10-7,21 (м, 1Н), 7,04 (м, 0,3Н), 4,67-4,81 (м, 2Н), 3,52-3,74 (м, 3Н), 3,38-3,52 (м, 1Н), 3,22-3,36 (м, 1Н), 2,96-3,21 (м, 2Н), 2,72-2,83 (м, 1Н), 2,48 (с, 3Н), 2,12-2,39 (м, 5Н), 2,00-2,11 (м, 1Н)
[1635] Пример 54. N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)-6-метоксибензофуран-3-карбоксамид
[1636] Указанное в заголовке соединение (1,8 мг) получали таким же образом, как и в примере 30, за исключением того, что вместо хинолин-4-карбоновой кислоты использовали 6-метоксибензофуран-3-карбоновую кислоту (34,6 мг, 0,18 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,16 (с, 0,7Н), 7,93-8,08 (м, 1,4Н), 7,75 (м, 0,7Н), 6,94-7,08 (м, 2,4Н), 4,67-4,83 (м, 2Н), 3,86 (с, 3Н), 3,50-3,71 (м, 3Н), 3,44-3,49 (м, 1Н), 2,94-3,32 (м, 3Н), 2,73-2,91 (м, 1Н), 2,12-2,40 (м, 5Н), 1,99-2,11 (м, 1Н)
[1637] Пример 55. N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)бензофуран-4-карбоксамид
[1638] Указанное в заголовке соединение (7,0 мг) получали таким же образом, как и в примере 30, за исключением того, что вместо хинолин-4-карбоновой кислоты примера 28 использовали бензофуран-4-карбоновую кислоту (29,2 мг, 0,18 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 7,50-7,74 (м, 3Н), 7,29-7,44 (м, 2Н), 4,75-4,86 (м, 2Н), 3,35-3,71 (м, 4Н), 2,93-3,34 (м, 3Н), 2,62-2,80 (м, 1Н), 2,32-2,52 (м, 3Н), 2,17-2,31 (м, 3Н), 1,95-2,13 (м, 2Н)
[1639] Пример 56. N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)бензофуран-5-карбоксамид
[1640] Указанное в заголовке соединение (10,6 мг) получали таким же образом, как и в примере 30, за исключением того, что вместо хинолин-4-карбоновой кислоты использовали бензофуран-5-карбоновую кислоту (29,2 мг, 0,18 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,11-8,24 (м, 1Н), 7,76-7,99 (м, 1,7Н), 7,66-7,75 (м, 1Н), 7,53-7,62 (м, 1Н), 7,06-7,24 (м, 0,4Н), 6,80-6,90 (м, 1Н), 4,75 (м, 2Н), 3,39-3,73 (м, 4Н), 2,84-3,31 (м, 4Н), 2,70-2,82 (м, 1Н), 2,09-2,47 (м, 5Н), 1,94-2,08 (м, 1Н)
[1641] Пример 57. N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)бензофуран-6-карбоксамид
[1642] Указанное в заголовке соединение (15,0 мг) получали таким же образом, как и в примере 30, за исключением того, что вместо хинолин-4-карбоновой кислоты использовали бензофуран-6-карбоновую кислоту (29,2 мг, 0,18 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,00-8,15 (м, 1Н), 7,57-7,87 (м, 3,7Н), 7,15-7,24 (м, 0,4Н), 6,80-6,92 (м, 1Н), 4,76-4,86 (м, 2Н), 3,38-3,75 (м, 4Н), 3,10-3,27 (м, 1Н), 2,80-3,05 (м, 2Н), 2,56-2,78 (м, 1Н), 2,07-2,47 (м, 6Н), 1,93-2,05 (м, 1Н)
[1643] Пример 58. N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)бензофуран-7-карбоксамид
[1644] Указанное в заголовке соединение (11,2 мг) получали таким же образом, как и в примере 30, за исключением того, что вместо хинолин-4-карбоновой кислоты использовали бензофуран-7-карбоновую кислоту (29,2 мг, 0,18 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,08 (м, 1Н), 7,68-7,95 (м, 3Н), 7,30-7,41 (м, 1Н), 6,87 (с, 1Н), 5,06 (м, 0,4Н), 4,78-4,89 (м, 1,6Н), 3,59-3,78 (м, 1Н), 3,30-3,55 (м, 3Н), 3,14-3,28 (м, 1Н), 2,77-3,03 (м, 2Н), 2,38-2,69 (м, 2Н), 2,01-2,35 (м, 5Н), 1,93-2,00 (м, 1Н)
[1645] Пример 59. N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)бензофуран-2-сульфонамид
[1646] (S)-1-(2-((S)-3-Аминопирролидин-1-ил)ацетил)пирролидин-2-карбонитрил трифторацетат (30 мг, 0,13 ммоль), полученный в эталонном примере 25, растворяли в безводном дихлорметане (2 мл). К полученному раствору добавляли триэтиламин (60 мкл, 0,40 ммоль) и бензофуран 2-сульфонилхлорид (32,2 мг, 0,15 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции к реакционной смеси добавляли воду. Водный слой реакционной смеси экстрагировали дихлорметаном. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (этилацетат / метанол = 20/1, об./об.) с получением указанного в заголовке соединения (7,3 мг). 1H-ЯМР (CDCl3, 400 МГц) δ 7,68-7,79 (м, 1Н), 7,56-7,62 (м, 1Н), 7,46-7,55 (м, 1Н), 7,31-7,40 (м, 2Н), 4,68-4,80 (м, 1Н), 4,09-4,12 (м, 1Н), 3,55-3,77 (м, 1Н), 3,21-3,53 (м, 3Н), 2,74-3,16 (м, 3Н), 2,42-2,69 (м, 1Н), 2,02-2,40 (м, 7Н), 1,76-1,86 (м, 1Н)
[1647] Пример 60. N-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)бензо[b]тиофен-2-сульфонамид
[1648] Указанное в заголовке соединение (8,7 мг) получали таким же образом, как и в примере 59, за исключением того, что вместо бензофуран 2-сульфонилхлорида использовали бензо[b]тиофен-2-сульфонилхлорид (34,6 мг, 0,15 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 7,87-7,99 (м, 3Н), 7,46-7,58 (м, 2Н), 4,73-4,82 (м, 1Н), 4,03-4,12 (м, 1Н), 3,57-3,62 (м, 1Н), 3,24-3,42 (м, 2Н), 3,09-3,21 (м, 1Н), 2,53-2,88 (м, 2Н), 2,41-2,51 (м, 1Н), 2,09-2,31 (м, 6Н), 1,67-1,85 (м, 1Н)
[1649] Пример 61. (S)-1-(2-((S)-3-(хинолин-4-илокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1650] (S)-1-(2-((R)-3-гидроксипирролидин-1-ил)ацетил)пирролидин-2-карбонитрил (242 мг, 1,08 ммоль), полученный в эталонном примере 26, растворяли в тетрагидрофуране (9,03 мл). К полученному раствору добавляли 4-хинолинол (15,7,34 мг, 1,08 ммоль) и трифенилфосфин (568,6 мг, 2,17 ммоль). Раствор смеси охлаждали до 0°С. Затем по каплям медленно добавляли DIAD (диизопропилазодикарбоксилат) (0,43 мл, 2,17 ммоль) в течение 15 минут.Реакционную смесь перемешивали в течение 12 ч при комнатной температуре. После завершения реакции в реакционную смесь добавляли насыщенный раствор хлорида аммония и насыщенный раствор гидро карбоната натрия. Водный слой реакционной смеси экстрагировали этилацетатом. Экстрагированный органический ело и высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (дихлорметан / метанол = 10/1, об./об.) с получением указанного в заголовке соединения (18,5 мг). 1H-ЯМР (CDCl3, 400 МГц) δ 8,73 (д, 1Н), 8,19 (т, 1Н), 8,04 (д, 1Н), 7,70 (т, 1Н), 7,51 (м, 1Н), 6,64 (д, 1Н), 5,16-5,09 (м, 1,3Н), 4,76 (д, 0,7Н), 3,71-3,63 (м, 2Н), 3,53-3,51 (м, 1Н), 3,41-3,37 (м, 1Н), 3,15-2,72 (м, 3Н), 2,46-2,29 (м, 1Н), 2,27-1,98 (м, 6Н)
[1651] Пример 62. (S)-1-(2-((S)-3-(нафталин-1-илокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1652] Указанное в заголовке соединение (68 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали нафталин-1-ол (160 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,23 (т, 1Н), 7,80 (д, 1Н), 7,46-7,40 (м, 3Н), 7,32 (т, 1Н), 6,72 (д, 1Н), 5,27 (д, 0,3Н), 5,05 (м, 1Н), 4,76 (м, 0,7Н), 3,72-3,31 (м, 5Н), 3,05-3,03 (м, 1Н), 2,95-2,91 (м, 2Н), 2,41-2,38 (м, 1Н), 2,25-2,14 (м, 4Н), 2,02-1,98 (м, 1Н), 1,89 (м, 1Н)
[1653] Пример 63. (S)-1-(2-((S)-3-(хинолин-6-илокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1654] Указанное в заголовке соединение (87 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 6-хинолинол (160 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,76 (с, 1Н), 8,04-7,98 (м, 2Н), 7,35-7,27 (м, 2Н), 6,97 (с, 1Н), 5,24-4,76 (м, 2Н), 3,68-3,34 (м, 5Н), 3,01-2,89 (м, 3Н), 2,44-2,10 (м, 7Н)
[1655] Пример 64. (S)-1-(2-((S)-3-(хинолин-8-илокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1656] Указанное в заголовке соединение (57 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 8-хинолинол (160 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,93 (с, 1Н), 8,14 (д, 1Н), 7,44-7,38 (м, 3Н), 7,00-6,96 (м, 1Н), 5,47 (д, 0,4Н), 5,14 (с, 1Н), 4,75 (д, 0,6Н), 3,79-3,66 (м, 2Н), 3,64-3,30 (м, 3Н), 3,09-2,84 (м, 3Н), 2,47-2,43 (м, 1Н), 2,28-2,03 (м, 6Н)
[1657] Пример 65. (S)-1-(2-((S)-3-(изохинолин-5-илокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1658] Указанное в заголовке соединение (62 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 5-изохинолинол (160 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 9,20 (с, 1Н), 8,51 (с, 1Н), 8,00-7,99 (м, 1Н), 7,54-7,46 (м, 2Н), 6,91 (д, 1Н), 5,19 (д, 0,3Н), 5,05 (с, 1Н), 4,76 (д, 0,7Н), 3,71-3,63 (м, 2Н), 3,53-3,51 (м, 1Н), 3,42-3,38 (м, 2Н), 3,13-2,91 (м, 3Н), 2,48-2,41 (м, 1Н), 2,34-1,99 (м, 6Н)
[1659] Пример 66. (S)-1-(2-((S)-3-(хинолин-5-илокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1660] Указанное в заголовке соединение (89 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 5-хинолинол (160 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,90 (с, 1Н), 8,59 (т, 1Н), 7,69 (д, 1Н), 7,58 (т, 1Н), 7,37 (с, 1Н), 6,76 (д, 1Н), 5,15 (м, 0,3Н), 5,05 (м, 1Н), 4,76 (м, 0,7Н), 3,71-3,61 (м, 2Н), 3,50 (м, 1Н), 3,41-3,37 (м, 1Н), 3,00-2,86 (м, 3Н), 2,45-2,40 (м, 1Н), 2,28-2,07 (м, 6Н)
[1661] Пример 67. (S)-1-(2-((S)-3-(бензо[d][1,3]диоксол-5-илокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1662] Указанное в заголовке соединение (76 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали бензо[d][1,3]диоксол-5-ол (150 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 6,69 (д, 1Н), 6,44 (д, 1Н), 6,24 (т, 1Н), 5,90 (с, 2Н), 5,28 (д, 0,3Н), 4,94-4,92 (м, 1Н), 4,75 (м, 0,7Н), 3,72-3,63 (м, 2Н), 3,52-3,50 (м, 1Н), 3,37-3,21 (м, 1Н), 2,94-2,74 (м, 3Н), 2,33-2,00 (м, 7Н)
[1663] Пример 68. (S)-1-(2-((S)-3-(тиено[2,3-d]пиримидин-4-илокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1664] Указанное в заголовке соединение (63 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали тиено[2,3-d]пиримидин-4-ол (160 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,62 (с, 1Н), 7,38 (с, 2Н), 5,72 (м, 1Н), 5,20 (д, 0,3Н), 4,76 (м, 0,7Н), 3,71-3,62 (м, 2Н), 3,53-3,52 (м, 1Н), 3,45-3,35 (м, 1Н), 3,27-3,22 (м, 1Н), 3,04 (д, 2Н), 2,49-2,44 (м, 1Н), 2,42-2,04 (м, 6Н)
[1665] Пример 69. (S)-1-(2-((S)-3-(изохинолин-3-илокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1666] Указанное в заголовке соединение (123 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 3-изохинолинол (151 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,89 (с, 1Н), 7,84 (д, 1Н), 7,65 (д, 1Н), 7,54 (м, 1Н), 7,34 (м, 1Н), 6,96 (м, 1Н), 5,47 (м, 1Н), 4,71 (м, 1Н), 3,68-3,37 (м, 4Н), 3,07-2,89 (м, 3Н), 2,41-2,01 (м, 7Н)
[1667] Пример 70. (S)-1-(2-((S)-3-(3-бромтиено[3,2-с]пиридин-4-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1668] Указанное в заголовке соединение (70,2 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 3-бромтиено[3,2-с]пиридин-4-ол (151 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 7,92 (с, 1Н), 7,34 (м, 2Н), 5,62 (м, 1Н), 4,75 (м, 1Н), 3,72-3,39 (м, 4Н), 3,04-2,91 (м, 3Н), 2,42 (м, 1Н), 2,27-2,19 (м, 6Н)
[1669] Пример 71. (S)-1-(2-((S)-3-(4-хлорнафталин-1-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1670] Указанное в заголовке соединение (94,0 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 4-хлорнафталин-1-ол (194 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,27 (д, 1Н), 8,16 (д, 1Н), 7,58 (м, 1Н), 7,52 (м, 1Н), 7,40 (д, 1Н), 6,60 (д, 1Н), 4,90 (м, 1Н), 4,70 (м, 1Н), 3,61-3,27 (м, 4Н), 2,97-2,69 (м, 3Н), 2,39-1,93 (м, 7Н)
[1671] Пример 72. (S)-1-(2-((S)-3-(2-(1Н-пиразол-3-ил)фенокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1672] Указанное в заголовке соединение (81 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 2-(1Н-пиразол-3-ил)фенол (173 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 7,63 (д, 1Н), 7,56 (с, 1Н), 7,25 (м, 1Н), 7,04 (м, 1Н), 6,97 (д, 1Н), 6,58 (с, 1Н), 5,03 (с, 1Н), 4,72 (с, 1Н), 3,59 (д, 2Н), 3,44-3,40 (м, 2Н), 3,22-3,02 (м, 3Н), 2,31-2,30 (м, 1Н), 2,20-1,98 (м, 6Н)
[1673] Пример 73. (S)-1-(2-((S)-3-(4-хлорхиназолин-8-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1674] Указанное в заголовке соединение (72 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола в примере 59 использовали 4-хлорхиназолин-8-ол (194 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 7,85-7,47 (м, 3Н), 7,20 (м, 1Н), 5,03 (с, 1Н), 4,76 (с, 1Н), 3,66-3,54 (м, 4Н), 3,18-2,96 (м, 4Н), 2,49-2,05 (м, 6Н)
[1675] Пример 74. (S)-1-(2-((S)-3-(4-хлорхиназолин-6-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1676] Указанное в заголовке соединение (90,7 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 4-хлорхиназолин-6-ол (194 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 7,97 (м, 1Н), 7,62-7,54 (м, 2Н), 7,37 (д, 1Н), 5,06 (с, 1Н), 4,75 (с, 1Н), 3,69-3,36 (м, 4Н), 3,10-2,92 (м, 4Н), 2,49-2,18 (м, 6Н)
[1677] Пример 75. (S)-1-(2-((S)-3-(2-оксо-1,2-дигидрохинолин-5-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1678] Указанное в заголовке соединение (93,9 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 5-гидроксихинолин-2(1Н)-он (176 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 11,68 (м, 1Н), 8,17 (м, 1Н), 7,37-7,26 (м, 1Н), 6,61 (м, 1Н), 6,49 (м, 1Н), 5,10 (с, 2Н), 3,70-3,30 (м, 4Н), 2,96-2,85 (м, 3Н), 2,38-1,92 (м, 7Н)
[1679] Пример 76. (S)-1-(2-((S)-3-(2-оксо-1,2,3,4-тетрагидрохинолин-5-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1680] Указанное в заголовке соединение (112,3 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 5-гидрокси-3,4-дигидрохинолин-2(1H)-он (176 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 9,71 (с, 0,5Н), 8,49 (с, 0,5Н), 7,07 (т, 1Н), 6,44 (м, 2Н), 4,87 (с, 1Н), 4,76 (с, 1Н), 3,69-3,30 (м, 4Н), 2,92-2,79 (м, 5Н), 2,70-2,57 (м, 2Н), 2,33-2,06 (м, 7Н)
[1681] Пример 77. (S)-1-(2-((S)-3-(2-оксо-1,2,3,4-тетрагидрохинолин-6-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1682] Указанное в заголовке соединение (94,0 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 6-гидрокси-3,4-дигидрохинолин-2(1H)-он (176 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 9,02 (с, 1Н), 6,76 (д, 1Н), 6,64 (м, 2Н), 4,79-4,75 (м, 2Н), 3,68-3,24 (м, 5Н), 2,90-2,59 (м, 7Н), 2,27-2,02 (м, 6Н)
[1683] Пример 78. (S)-1-(2-((S)-3-(2-метилхинолин-8-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1684] Указанное в заголовке соединение (74,5 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 2-метилхинолин-8-ол (171,7 мг, 1,08 ммоль). 1H ЯМР (CDCl3, 400 МГц) δ 8,28 (с, 1Н), 7,52 (с, 1Н), 7,34 (д, 2Н), 6,89 (д, 1Н), 5,09 (с, 1Н), 4,98 (с, 1Н), 3,78-3,53 (м, 4Н), 3,42-3,16 (м, 3Н), 2,80-2,75 (м, 4Н), 2,43-2,04 (м, 6Н)
[1685] Пример 79. (S)-1-(2-((S)-3-((7-хлорхинолин-4-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1686] Указанное в заголовке соединение (50,7 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 7-хлорхинолин-4-ол (194 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,69 (с, 1Н), 8,13 (д, 1Н), 8,00 (с, 1Н), 7,43 (д, 1Н), 6,62 (с, 1Н), 5,07 (с, 1,3Н), 4,75 (с, 0,7Н), 3,69-3,27 (м, 4Н), 3,09-2,86 (м, 3Н), 2,46-2,45 (м, 1Н), 2,28-2,00 (м, 6Н)
[1687] Пример 80. (S)-1-(2-((S)-3-(7-бромхинолин-4-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1688] Указанное в заголовке соединение (48,6 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 7-бромхинолин-4-ол (237 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,67 (с, 1Н), 8,17 (с, 1Н), 8,05 (д, 1Н), 7,55 (д, 1Н), 6,63 (с, 1Н), 5,06 (с, 1,3Н), 4,75 (с, 0,7Н), 3,71-3,26 (м, 4Н), 3,03-2,85 (м, 3Н), 2,45-2,44 (м, 1Н), 2,31-1,99 (м, 6Н)
[1689] Пример 81. (S)-1-(2-((S)-3-(5-хлорхинолин-8-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1690] Указанное в заголовке соединение (41 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 5-хлорхинолин-8-ол (194 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,95 (с, 1Н), 8,53 (д, 1Н), 7,53-7,49 (м, 2Н), 6,92 (д, 1Н), 5,11 (с, 1Н), 4,75 (с, 1Н), 3,79-3,35 (м, 5Н), 3,16-2,93 (м, 2Н), 2,45 (м, 1Н), 2,22-2,04 (м, 6Н)
[1691] Пример 82. (S)-1-(2-((S)-3-([1,1'-бифенил]-3-илокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1692] Указанное в заголовке соединение (81 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали [1,1'-бифенил]-3-ол (184 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 7,56-7,48 (м, 2Н), 7,42-7,27 (м, 4Н), 7,17-7,06 (м, 2Н), 6,90-6,67 (м, 1Н), 4,91 (с, 1Н), 4,72 (с, 1Н), 3,74-3,27 (м, 5Н), 2,88-2,83 (м, 2Н), 2,31 (м, 1Н), 2,30-2,11 (м, 6Н)
[1693] Пример 83. (S)-1-(2-((S)-3-([1,1'-бифенил]-4-илокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1694] Указанное в заголовке соединение (63,7 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали [1,1'-бифенил]-4-ол (184 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 7,53-7,48 (м, 4Н), 7,39 (т, 2Н), 7,28 (т, 1Н), 6,90 (д, 2Н), 4,88 (с, 1Н), 4,72 (с, 1Н), 3,74-3,28 (м, 5Н), 2,87-2,80 (м, 2Н), 2,31 (м, 1Н), 2,12-1,97 (м, 6Н)
[1695] Пример 84. (S)-1-(2-((S)-3-(6-метоксихинолин-4-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1696] Указанное в заголовке соединение (70,2 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 6-метоксихинолин-4-ол (183 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,57 (с, 1Н), 7,94 (д, 1Н), 7,43 (с, 1Н), 7,34 (д, 1Н), 6,60 (с, 1Н), 5,06 (с, 1,4Н), 4,75 (с, 0,6Н), 3,93 (с, 3Н), 3,71-3,69 (м, 2Н), 3,63-3,25 (м, 3Н), 3,04-2,84 (м, 2Н), 2,45 (м, 1Н), 2,27-1,98 (м, 6Н)
[1697] Пример 85. (S)-1-(2-((S)-3-(7,8-дифторхинолин-4-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1698] Указанное в заголовке соединение (62,6 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 7,8-дифторхинолин-4-ол (194 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,75 (с, 1Н), 7,94 (с, 1Н), 7,33 (д, 1Н), 6,67 (с, 1Н), 5,09 (с, 1,4Н), 4,76 (с, 0,6Н), 3,93 (с, 3Н), 3,71-3,66 (м, 2Н), 3,56-3,27 (м, 3Н), 3,06-2,86 (м, 2Н), 2,48-2,45 (м, 1Н), 2,29-2,00 (м, 6Н)
[1699] Пример 86. Метил-6-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)окси)-2,3-дигидробензофуран-2-карбоксилат
[1700] Указанное в заголовке соединение (85,3 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали метил-6-гидрокси-2,3-дигидробензофуран-2-карбоксилат (205 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 7,02 (д, 1Н), 6,41-6,36 (м, 2Н), 5,23 (т, 1Н), 4,80 (с, 1Н), 4,72 (с, 1Н), 4,08 (м, 1Н), 3,80 (с, 3Н), 3,74-3,65 (м, 2Н), 3,51-3,39 (м, 3Н), 3,33-3,25 (м, 2Н), 2,91-2,86 (м, 2Н), 2,25-2,04 (м, 6Н)
[1701] Пример 87. (S)-1-(2-((S)-3-(4-феноксифенокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1702] Указанное в заголовке соединение (50,7 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 4-феноксифенол (205 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 7,29-2,27 (м, 2Н), 7,03 (с, 1Н), 6,94 (с, 4Н), 6,82 (д, 2Н), 4,81-4,69 (м, 2Н), 3,74-3,62 (м, 2Н), 3,51-3,43 (м, 1Н), 3,39-3,35 (м, 1Н), 3,32-3,24 (м, 1Н), 2,87-2,82 (т, 2Н), 2,29-2,04 (м, 7Н)
[1703] Пример 88. (S)-1-(2-((S)-3-(3-феноксифенокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1704] Указанное в заголовке соединение (95 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 3-феноксифенол (205 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 7,34 (т, 2Н), 7,19 (т, 1Н), 7,13 (т, 1Н), 7,02 (д, 2Н), 6,57 (д, 2Н), 6,49 (с, 1Н), 4,81 (с, 1Н), 4,74 (с, 1Н), 3,71-3,63 (м, 1Н), 3,51-3,49 (м, 1Н), 3,38-3,23 (м, 2Н), 2,86-2,62 (м, 3Н), 2,27-2,02 (м, 7Н)
[1705] Пример 89. (S)-1-(2-((S)-3-(4-бензилфенокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1706] Указанное в заголовке соединение (96,1 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 4-бензилфенол (194 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 7,26 (с, 2Н), 7,17 (т, 3Н), 7,08 (д, 2Н), 6,76 (д, 2Н), 4,81 (с, 1Н), 4,74 (с, 1Н), 3,90 (с, 2Н), 3,73-3,67 (м, 2Н), 3,51-3,27 (м, 2Н), 2,85-2,76 (м, 3Н), 2,26-2,02 (м, 7Н)
[1707] Пример 90. (S)-1-(2-((S)-3-(2-бензилфенокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1708] Указанное в заголовке соединение (69,1 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 2-бензилфенол (194 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 7,26-7,09 (м, 7Н), 6,87 (т, 1Н), 6,74 (д, 1Н), 4,93 (с, 1Н), 4,73 (с, 1Н), 3,94 (с, 2Н), 3,71-3,64 (м, 1Н), 3,57-3,48 (м, 1Н), 3,32-3,24 (м, 2Н), 2,84-2,64 (м, 3Н), 2,23-1,97 (м, 7Н)
[1709] Пример 91. (S)-1-(2-((S)-3-(3-бензоилфенокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1710] Указанное в заголовке соединение (93,9 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 3-гидроксибензофенон (216 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 7,79 (д, 2Н), 7,59 (д, 1Н), 7,50 (т, 2Н), 7,37-7,27 (м, 3Н), 7,09 (д, 1Н), 4,93 (с, 1Н), 4,47 (с, 1Н), 3,73-3,65 (м, 2Н), 3,56-3,30 (м, 2Н), 2,97-2,86 (м, 3Н), 2,34-1,98 (м, 7Н)
[1711] Пример 92. (S)-1-(2-((S)-3-(4-бензоилфенокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1712] Указанное в заголовке соединение (49,7 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 4-гидроксибензофенон (216 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 7,80 (д, 2Н), 7,74 (д, 2Н), 7,56 (д, 1Н), 7,48 (д, 2Н), 6,91 (д, 2Н), 4,97 (c, 1H), 4,73 (с, 1H), 3,75-3,65 (м, 2H), 3,57-3,40 (м, 2H), 3,00-2,88 (м, 3H), 2,38-2,36 (м, 1H), 2,18-1,99 (м, 6Н)
[1713] Пример 93. (S)-1-(2-((S)-3-(4-(бензилокси)пиридин-2-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1714] Указанное в заголовке соединение (95,0 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 4-(бензилокси)пиридин-2-ол (216 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 7,92 (д, 1Н), 7,38-7,34 (м, 6Н), 6,51 (с, 1Н), 5,43 (с, 1Н), 5,03 (с, 2Н), 4,72 (с, 1Н), 3,72-3,44 (м, 2Н), 3,38-3,28 (м, 2Н), 3,17-3,13 (м, 1Н), 2,96-2,87 (м, 1Н), 2,80-2,71 (м, 1Н), 2,35-2,30 (м, 1Н), 2,19-1,97 (м, 6Н)
[1715] Пример 94. (S)-1-(2-((S)-3-(7-(трифторметил)хинолин-4-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1716] Указанное в заголовке соединение (97,2 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 7-(трифторметил)хинолин-4-ол (227 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,78 (с, 1Н), 8,30 (с, 2Н), 7,64 (д, 1Н), 6,74 (д, 1Н), 5,10 (с, 1Н), 4,76 (с, 1Н), 3,72-3,24 (м, 4Н), 3,13-2,96 (м, 2Н), 2,86 (м, 1Н), 2,50-2,45 (м, 1Н), 2,18-1,99 (м, 6Н)
[1717] Пример 95. (S)-1-(2-((S)-3-(8-(трифторметил)хинолин-4-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1718] Указанное в заголовке соединение (57,2 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 8-(трифторметил)хинолин-4-ол (227 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,84 (д, 1Н), 8,43 (д, 1Н), 8,03 (д, 1Н), 7,53 (т, 1Н), 6,74 (с, 1Н), 5,08 (с, 1Н), 4,75 (с, 1Н), 3,72-3,38 (м, 4Н), 3,29-2,82 (м, 3Н), 2,47-2,45 (м, 1Н), 2,26-1,98 (м, 6Н)
[1719] Пример 96. (S)-1-(2-((S)-3-(акридин-4-илокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1720] Указанное в заголовке соединение (51,8 мг) получали таким же образом, как ив примере 61, за исключением того, что вместо 4-хинолинола использовали акридин-4-ол (205 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,67 (с, 1Н), 8,31 (д, 1Н), 7,92 (д, 1Н), 7,69 (м, 1Н), 7,52-7,48 (т, 2Н), 7,36 (т, 1Н), 6,92 (д, 1Н), 5,01 (с, 1Н), 4,76 (с, 1Н), 3,76-3,27 (м, 6Н), 2,85 (м, 1Н), 2,45 (м, 1Н), 2,21-1,96 (м, 6Н)
[1721] Пример 97. (S)-1-(2-((S)-3-(2-(бензо[d]оксазол-2-ил)фенокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1722] Указанное в заголовке соединение (71,3 мг) получали таким же образом, как ив примере 61, за исключением того, что вместо 4-хинолинола примера 61 использовали 2-(бензо[d]оксазол-2-ил)-фенол (227 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,09 (д, 1Н), 7,77 (с, 1Н), 7,58 (с, 1Н), 7,44 (т, 1Н), 7,34 (м, 2Н), 7,06 (т, 1Н), 6,96 (д, 1Н), 4,99 (с, 1Н), 4,69 (с, 1Н), 3,69-3,54 (м, 1Н), 3,48-3,27 (м, 3Н), 3,03-2,84 (м, 3Н), 2,37-2,32 (м, 1Н), 2,17-1,88 (м, 6Н)
[1723] Пример 98. (S)-1-(2-((S)-3-(4-(4-ацетилпиперазин-1-ил)фенокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1724] Указанное в заголовке соединение (85,3 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 4-(4-ацетилпиперазин-1-ил)фенол (238 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 6,88 (д, 2Н), 6,79 (д, 2Н), 4,78 (с, 1,4Н), 4,47 (с, 0,6Н), 3,74-3,68 (м, 3Н), 3,60-3,50 (м, 3Н), 3,36-3,34 (м, 1Н), 3,17-3,15 (м, 1Н), 3,04-3,01 (м, 5Н), 2,84-2,77 (м, 2Н), 2,28-1,99 (м, 10Н)
[1725] Пример 99. 2-((S)-1-(2-((S)-2-цианопирролидин-1-ил)-2-оксоэтил)пирролидин-3-ил)окси)-N-фенилбензамид
[1726] Указанное в заголовке соединение (40,0 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 2-гидрокси-N-фенилбензамид (227 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 10,06-9,94 (м, 1Н), 8,21 (д, 1Н), 7,73 (д, 2Н), 7,41 (т, 1Н), 7,33 (м, 2Н), 7,09 (д, 2Н), 6,91 (д, 1Н), 5,06 (с, 1Н), 4,58 (с, 1Н), 3,61-3,26 (м, 4Н), 3,07-2,99 (м, 2Н), 2,69-2,67 (м, 1Н), 2,40-2,38 (м, 1Н), 2,10-1,80 (м, 6Н)
[1727] Пример 100. (S)-1-(2-((S)-3-(7-метоксихинолин-4-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1728] Указанное в заголовке соединение (58,3 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 7-метоксихинолин-4-ол (183 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,60 (с, 1Н), 8,07 (д, 1Н), 7,34 (с, 1Н), 7,12 (д, 1Н), 6,51 (с, 1Н), 5,02 (м, 1,2Н), 4,72 (с, 0,8 Н), 3,91 (с, 4Н), 3,64-3,57 (м, 1Н), 3,46-3,28 (м, 3Н), 2,99-2,80 (м, 2Н), 2,40 (м, 1Н), 2,12-2,10 (м, 6Н)
[1729] Пример 101. (S)-1-(2-((S)-3-(6,7-диметоксихинолин-4-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1730] Указанное в заголовке соединение (73,4 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали 6,7-диметоксихинолин-4-ол (216 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,52 (д, 1Н), 7,40 (с, 1Н), 7,35 (с, 1Н), 6,54 (с, 1Н), 5,04-5,03 (м, 1Н), 4,73 (с, 1Н), 4,02 (д, 6Н), 3,80-3,51 (м, 1Н), 3,48-3,26 (м, 3Н), 3,05-2,93 (м, 2Н), 2,80-2,79 (м, 1Н), 2,47-2,42 (м, 1Н), 2,24-1,99 (м, 6Н)
[1731] Пример 102. (S)-1-(2-((S)-3-(3-(4-бромфенил)изоксазол-5-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1732] Указанное в заголовке соединение (79,9 мг) получали таким же образом, как и в примере 61, за исключением того, что вместо 4-хинолинола использовали (3-(4-бромфенил)изоксазол-5-ол (258 мг, 1,08 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 7,61-7,50 (м, 5Н), 5,04 (с, 1Н), 4,74 (с, 1Н), 3,65-3,61 (м, 1Н), 3,50-3,41 (м, 2Н), 3,17-2,86 (м, 4Н), 2,38 (м, 1Н), 2,26-2,08 (м, 6Н)
[1733] Пример 103. (S)-4,4-дифтор-1-(2-((S)-3-(6-метоксихинолин-4-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1734] (S)-4,4-Дифтор-1-(2-(R)-3-гидроксипирролидин-1-ил)-2-оксоэтил)пирролидин-2-карбонитрил (260 мг, 1,00 ммоль), полученный в эталонном примере 27, растворяли в тетрагидрофуране (10 мл). К полученному раствору добавляли 6-метоксихинолин-4-ол (180 мг, 1,0 ммоль) и трифенилфосфин (520 мг, 2,0 ммоль). Раствор смеси охлаждали до 0°С. Затем по каплям медленно добавляли DIAD (диизопропилазодикарбоксилат) (0,39 мл, 2,0 ммоль) в течение 15 минут. Реакционную смесь перемешивали в течение 12 ч при комнатной температуре. После завершения реакции в реакционную смесь добавляли насыщенный раствор хлорида аммония и насыщенный раствор гидрокарбоната натрия. Водный слой реакционной смеси экстрагировали этилацетатом. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (дихлорметан / метанол = 10/1, об./об.) с получением указанного в заголовке соединения (45 мг). 1H-ЯМР (CDCl3, 400 МГц) δ 8,54 (д, 1Н), 7,92 (д, 1Н), 7,43-7,38 (м, 1Н), 7,33-7,26 (м, 1Н), 6,55 (с, 1Н), 4,99-4,95 (м, 2Н), 4,13-,98 (м, 1Н), 3,91-3,85 (м, 4Н), 3,70-3,58 (м, 1Н), 3,50-3,35 (м, 1Н), 3,11-2,96 (м, 3Н), 2,70-2,66 (м, 3Н), 2,44-,40 (м, 1Н), 2,12-2,09 (м 1Н)
[1735] Пример 104. (S)-4,4-дифтор-1-(2-((S)-3-(8-(трифторметил)хинолин-4-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1736] Указанное в заголовке соединение (87 мг) получали таким же образом, как и в примере 103, за исключением того, что вместо 6-метоксихинолин-4-ола использовали 8-(трифторметил)хинолин-4-ол (210 мг, 1,0 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,82 (с, 1Н), 8,41 (д, 1Н), 8,02 (д, 1Н), 6,71 (с, 1Н), 5,11-4,98 (м, 2Н), 4,16-4,06 (м, 2Н), 3,65-3,42 (м, 2Н), 3,16-2,99 (м, 3Н), 2,73-2,72 (м, 3Н), 2,43 (м, 1Н), 2,12-2,01 (м, 1Н)
[1737] Пример 105. (S)-4,4-дифтор-1-(2-((S)-3-(хинолин-5-илокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1738] Указанное в заголовке соединение (68 мг) получали таким же образом, как и в примере 103, за исключением того, что вместо 6-метоксихинолин-4-ола использовали хинолин-5-ол (150 мг, 1,0 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,87 (с, 1Н), 8,55 (д, 1Н), 7,68 (д, 1Н), 7,56 (т, 1Н), 7,36 (с, 1Н), 6,73 (д, 1Н), 4,97 (м, 2Н), 4,13-3,97 (м, 2Н), 3,68-3,36 (м, 2Н), 3,09 (м, 1Н), 2,99-2,91 (м, 2Н), 2,68 (м, 3Н), 2,39-2,36 (м, 1Н), 2,21-2,03 (м, 1Н)
[1739] Пример 106. (S)-4,4-дифтор-1-(2-((S)-3-(изохинолин-5-илокси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1740] Указанное в заголовке соединение (59 мг) получали таким же образом, как и в примере 103, за исключением того, что вместо 6-метоксихинолин-4-ола использовали изохинолин-5-ол (150 мг, 1,0 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 9,17 (с, 1Н), 8,49 (д, 1Н), 7,98 (д, 1Н), 7,50-7,44 (м, 2Н), 6,89 (д, 1Н), 4,99 (м, 2Н), 4,12-3,69 (м, 2Н), 3,44-3,39 (м, 2Н), 3,16-2,93 (м, 3Н), 2,72-2,70 (м, 3Н), 2,41-2,38 (м, 1Н), 2,24-2,13 (м, 1Н)
[1741] Пример 107. (S)-1-(2-((S)-3-(7-хлорхинолин-4-ил)окси)пирролидин-1-ил)ацетил)-4,4-дифторпирролидин-2-карбонитрил
[1742] Указанное в заголовке соединение (37 мг) получали таким же образом, как и в примере 103, за исключением того, что вместо 6-метоксихинолин-4-ола использовали 7-хлорхинолин-4-ол (180 мг, 1,0 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,65 (с, 1Н), 8,06 (д, 1Н), 7,96 (с, 1Н), 7,47-7,31 (м, 1Н), 6,58 (д, 1Н), 5,01-4,97 (м, 2Н), 4,17-3,99 (м, 2Н), 3,86-3,35 (м, 2Н), 3,12-3,11 (м, 1Н), 3,02-2,97 (м, 2Н), 2,77-2,71 (м, 3Н), 2,42-2,41 (м, 1Н), 2,12-2,10 (м, 1Н)
[1743] Пример 108. (S)-4,4-дифтор-1-(2-((S)-3-(2-оксо-1,2-дигидрохинолин-5-ил)окси)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1744] Указанное в заголовке соединение (64 мг) получали таким же образом, как и в примере 103, за исключением того, что вместо 6-метоксихинолин-4-ола использовали 5-гидроксихинолин-2(1H)-он (160 мг, 1,0 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 12,24 (с, 1Н), 8,18 (д, 1Н), 7,37 (м, 1Н), 7,01 (с, 1Н), 6,62 (д, 1Н), 6,50 (д, 1Н), 4,97 (с, 2Н), 4,15-4,00 (м, 2Н), 3,39 (м, 2Н), 3,12-3,03 (м, 3Н), 2,92-2,72 (м, 3Н), 2,53-2,36 (м, 1Н), 2,09 (м, 1Н)
[1745] Пример 109. (S)-1-(2-((S)-3-(5-хлорхинолин-8-ил)окси)пирролидин-1-ил)ацетил)-4,4-дифторпирролидин-2-карбонитрил
[1746] Указанное в заголовке соединение (81 мг) получали таким же образом, как ив примере 103, за исключением того, что вместо 6-метоксихинолин-4-ола использовали 5-хлорхинолин-8-ол (180 мг, 1,0 ммоль). 1H-ЯМР (CDCl3, 400 МГц) δ 8,91 (с, 1Н), 8,50 (д, 1Н), 7,52-7,46 (м, 2Н), 6,86 (д, 1Н), 5,06-4,99 (м, 2Н), 4,10-3,84 (м, 3Н), 3,51-3,32 (м, 1Н), 3,09-3,07 (м, 3Н), 2,87-2,57 (м, 3Н), 2,39 (м, 1Н), 2,21 (м, 1Н)
[1747] Пример 110. (S)-1-(2-(4-(хинолин-5-иламино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1748] (S)-1-(2-хлорацетил)пирролидин-2-карбонитрил (28,75 мг, 0,16 ммоль), полученный в эталонном примере 1, растворяли в безводном дихлорметане (4 мл). К полученному раствору добавляли N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид (50,0 мг, 0,16 ммоль), полученный в эталонном примере 29 и карбонат калия (115,0 мг, 0,83 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции к реакционной смеси добавляли воду. Водный слой реакционной смеси экстрагировали дихлорметаном. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (дихлорметан / метанол = 10/1, об./об.) с получением указанного в заголовке соединения (12 мг). 1H-ЯМР (CDCl3, 400 МГц) δ 8,83 (д, 1Н), 8,25 (д, 1Н), 7,54-7,42 (м, 2Н), 7,28 (с, 1Н), 6,52 (д, 1Н), 5,15 (д, 0,3Н), 4,80 (с, 0,7Н), 4,12 (д, 1Н), 3,69-2,90 (м, 8Н), 2,37-2,04 (м, 8Н), 1,79-1,64 (м, 2Н)
[1749] Пример 111. (S)-1-(2-(4-(хинолин-4-иламино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1750] Указанное в заголовке соединение (19,8 мг) получали таким же образом, как в примере 110, за исключением того, что вместо N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-(пиперидин-4-ил)хинолин-4-амина гидрохлорид (50,0 мг, 0,16 ммоль), полученный в эталонном примере 28. 1H-ЯМР (CD3OD, 400 МГц) δ 8,35-8,32 (м, 2Н), 7,81 (с, 2Н), 7,59 (с, 1Н), 6,79 (д, 1Н), 4,80 (с, 1Н), 3,78 (с, 2Н), 3,60-3,35 (м, 2Н), 3,08 (д, 2Н), 2,42-1,82 (м, 11Н), 1,28 (с, 1Н)
[1751] Пример 112. (1S,3S,5S)-2-(2-(4-(хинолин-4-иламино)пиперидин-1-ил)ацетил)-2-азабицикло[3.1.0]гексан-3-карбонитрил
[1752] (1S,3S,5S)-2-(2-хлорацетил)-2-азабицикло[3.1.0]гексан-3-карбонитрил (25 мг, 0,14 ммоль), полученный в эталонном примере 4, растворяли в безводном ацетонитриле (3,5 мл). К полученному раствору добавляли N-(пиперидин-4-ил)хинолин-4-амина гидрохлорид (50,0 мг, 0,16 ммоль), полученный в эталонном примере 28, и карбонат калия (115,0 мг, 0,83 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции к реакционной смеси добавляли воду Водный слой реакционной смеси экстрагировали дихлорметаном. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (дихлорметан / метанол = 10/1, об./об.) с получением у казанного в заголовке соединения (11,9 мг). 1H-ЯМР (CD3OD, 400 МГц) δ 8,39 (д, 2Н), 7,84 (с, 2Н), 7,64 (с, 1Н), 6,88 (с, 1Н), 5,04 (с, 1Н), 3,84 (с, 2Н), 3,57-3,46 (м, 2Н), 3,10 (с, 2Н), 2,63 (с, 1Н), 2,43 (д, 2Н), 2,30 (д, 1Н), 2,03-2,18 (м, 1Н), 2,10-1,75 (м, 4Н), 1,25-0,92 (с, 3Н)
[1753] Пример 113. (2S,4S)-4-фтор-1-(2-(4-(хинолин-5-иламино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1754] Указанное в заголовке соединение (29,9 мг) получали таким же образом, как и в примере 110, за исключением того, что (2S,4S)-1-(2-хлорацетил)-4-фторпирролидин-2-карбонитрил (25,4 мг, 0,14 ммоль), полученный в эталонном примере 2, использовали вместо (S)-1-(2-хлорацетил)пирролидин-2-карбонитрила. 1H-ЯМР (CD3OD, 400 МГц) δ 8,72 (с, 1Н), 8,63 (д, 1Н), 7,56 (т, 1Н), 7,42 (с, 1Н), 7,28 (д, 1Н), 6,73 (д, 1Н), 5,45 (д, 1Н), 4,99 (д, 1Н), 3,91-3,78 (м, 1Н), 3,61-3,43 (м, 3Н), 3,16-3,08 (м, 2Н), 2,61-2,45 (м, 4Н), 2,18 (кв, 2Н), 2,01-1,78 (м, 4Н)
[1755] Пример 114. (S)-4,4-дифтор-1-(2-(4-(хинолин-5-иламино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1756] Указанное в заголовке соединение (12,6 мг) получали таким же образом, как и в примере 110, за исключением того, что (2S)-1-(2-хлорацетил)-4,4-дифторпирролидин-2-карбонитрил (27,8 мг, 0,14 ммоль), полученный в эталонном примере 3, использовали вместо (S)-1-(2-хлорацетил)пирролидин-2-карбонитрила. 1H-ЯМР (CD3OD, 400 МГц) δ 8,72 (д, 1Н), 8,62 (д, 1Н), 7,54 (т, 1Н), 7,40 (д, 1Н), 7,27 (д, 1Н), 6,71 (д, 1Н), 5,58-5,05 (м, 1Н), 4,25-4,09 (м, 2Н), 3,53-3,24 (м, 3Н), 3,00 (д, 2Н), 2,90-2,74 (м, 2Н), 2,39 (т, 2Н), 2,13 (д, 2Н), 1,72 (д, 2Н), 1,28 (с, 1Н)
[1757] Пример 115. (1S,3S,5S)-2-(2-(4-(хинолин-5-иламино)пиперидин-1-ил)ацетил)-2-азабицикло[3.1.0]гексан-3-карбонитрил
[1758] Указанное в заголовке соединение (33,6 мг) получали таким же образом, как и в примере 112, за исключением того, что вместо N-(пиперидин-4-ил)хинолин-4-амина гидрохлорида использовали N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид (50,0 мг, 0,16 ммоль), полученный в эталонном примере 29. 1H-ЯМР (CD3OD, 400 МГц) δ 8,72 (с, 1Н), 8,66 (д, 1Н), 7,56 (т, 1Н), 7,41 (д, 1Н), 7,29 (д, 1Н), 6,73 (д, 1Н), 5,56-5,05 (м, 1Н), 3,81 (с, 1Н), 3,77 (с, 1Н), 3,65 (д, 2Н), 3,22-3,06 (м, 2Н), 2,64 (т, 3Н), 2,47-1,81 (м, 7Н), 1,28-1,07 (м, 2Н)
[1759] Пример 116. (S)-1-(2-(4-(фуро[3,2-с]пиридин-7-иламино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1760] Указанное в заголовке соединение (21,6 мг) получали таким же образом, как и в примере 110, за исключением того, что вместо N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-(пиперидин-4-ил)фуро[3,2-с]пиридин-7-амина гидрохлорид (40,6 г, 0,16 ммоль), полученный в эталонном примере 30. 1H-ЯМР (CDCl3, 400 МГц) δ 8,35 (с, 1Н), 7,91 (с, 1Н), 7,61 (с, 1Н), 6,81 (с, 1Н), 4,76 (с, 1Н), 3,94 (с, 1Н), 3,74 (с, 1Н), 3,57 (д, 2Н), 3,43-3,36 (м, 1Н), 3,24 (с, 1Н), 2,84-3,03 (м, 2Н), 2,44-2,14 (м, 7Н), 1,87-1,52 (м, 2Н)
[1761] Пример 117. (S)-1-(2-(4-(хинолин-3-илокси)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1762] (S)-1-(2-хлорацетил)пирролидин-2-карбонитрил (60 мг, 0,35 ммоль), полученный в эталонном примере 1, растворяли в безводном дихлорметане (2,4 мл). К полученному раствору добавляли 3-(пиперидин-4-илокси)хинолина гидрохлорид (104,7 мг, 0,35 ммоль), полученный в эталонном примере 31, и карбонат калия (192,2 мг, 1,39 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции к реакционной смеси добавляли воду. Водный слой реакционной смеси экстрагировали дихлорметаном. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (дихлорметан / метанол = 10/1, об./об.) с получением указанного в заголовке соединения (22,1 мг). 1H-ЯМР (CDCl3, 400 МГц) δ 8,66 (д, 1Н), 8,04 (д, 1Н), 7,71 (д, 1Н), 7,57-7,49 (м, 2Н) 7,40 (с, 1Н), 5,20 (д, 0,3Н), 4,76 (д, 0,6Н), 4,52 (с, 1Н), 3,75-3,54 (м, 2Н), 3,44-3,24 (м, 2Н) 2,82-2,51 (м, 5Н) 2,28-1,94 (м, 8Н)
[1763] Пример 118. (S)-1-(2-(4-(хинолин-4-илокси)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1764] Указанное в заголовке соединение (23,6 мг) получали таким же образом, как и в примере 117, за исключением того, что вместо 3-(пиперидин-4-илокси)хинолина гидрохлорида использовали 4-(пиперидин-4-илокси)хинолина гидрохлорид (104,7 мг, 0,35 ммоль), полученный в эталонном примере 32. 1H-ЯМР (CDCl3, 400 МГц) δ 8,72 (д, 1Н), 8,23 (д, 1Н), 8,03 (д, 1Н), 7,70 (т, 1Н), 7,52 (т, 1Н), 6,72 (д, 1Н) 5,17 (д, 0,3Н), 4,76 (д, 0,6Н), 4,69 (с, 1Н), 3,75-3,55 (м, 2Н), 3,43-3,24 (м, 2Н) 2,93-2,36 (м, 5Н) 2,28-2,05 (м, 8Н)
[1765] Пример 119. (S)-1-(2-(4-(хинолин-5-илокси)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1766] Указанное в заголовке соединение (20,2 мг) получали таким же образом, как и в примере 117, за исключением того, что вместо 3-(пиперидин-4-илокси)хинолина гидрохлорида использовали 5-(пиперидин-4-илокси)хинолина гидрохлорид (104,7 мг, 0,35 ммоль), полученный в эталонном примере 33. 1H-ЯМР (CDCl3, 400 МГц) δ 8,90 (с, 1Н), 8,61 (д, 1Н), 7,68 (д, 1Н), 7,60 (т, 1Н), 7,39 (кв, 1Н), 6,88 (д, 1Н) 5,21 (д, 0,3Н), 4,76 (с, 0,6Н), 4,61 (с, 1Н), 3,76-3,54 (м, 2Н), 3,44-3,23 (м, 2Н) 2,83-2,58 (м, 5Н) 2,28-2,01 (м, 8Н)
[1767] Пример 120. (S)-1-(2-(4-(хинолин-6-илокси)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1768] Указанное в заголовке соединение (24,4 мг) получали таким же образом, как и в примере 117, за исключением того, что вместо 3-(пиперидин-4-илокси)хинолина гидрохлорида использовали 6-(пиперидин-4-илокси)хинолина гидрохлорид (104,7 мг, 0,35 ммоль), полученный в эталонном примере 34. 1H-ЯМР (CDCl3, 400 МГц) δ 8,76 (д, 1Н), 8,05-8,00 (м, 2Н), 7,38-7,34 (м, 2Н), 7,10 (с, 1Н), 5,24 (д, 0,3 Н), 4,76 (с, 0,6 Н), 4,53 (с, 1Н), 3,75-3,54 (м, 2Н), 3,46-3,23 (м, 2Н) 2,86 (с, 2Н) 2,62-2,50 (м, 3Н), 2,35-1,96 (м, 8Н)
[1769] Пример 121. (S)-1-(2-(4-(3-метилхинолин-5-ил)амино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1770] (S)-1-(2-хлорацетил)пирролидин-2-карбонитрил (152,05 мг, 0,88 ммоль), полученный в эталонном примере 1, растворяли в безводном ацетонитриле (4,4 мл). К полученному раствору добавляли 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид (308,94 мг, 0,88 ммоль), полученный в эталонном примере 35, карбонат калия (487,0 мг, 3,52 ммоль) и йодид калия (1,46 мг, 0,01 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции к реакционной смеси добавляли воду. Водный слой реакционной смеси экстрагировали дихлорметаном. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (дихлорметан / метанол = 10/1, об./об.) с получением указанного в заголовке соединения (72 мг). 1H-ЯМР (CDCl3, 400 МГц) δ 8,70 (с, 1Н), 7,93 (с, 1Н), 7,47-7,41 (м, 2Н), 6,62 (д, 1Н), 5,15 (д, 1Н), 4,74 (с, 1Н), 3,72-3,18 (м, 4Н), 2,98-2,89 (м, 2Н), 2,65 (с, 1Н), 2,50 (с, 3Н), 2,39-2,04 (м, 8Н), 1,68-1,66 (м, 2Н)
[1771] Пример 122. (S)-1-(2-(4-(6-метилхинолин-5-ил)амино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1772] Указанное в заголовке соединение (21,8 мг) получали аналогично тому, как описано в Примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 6-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид (268,4 мг, 0,96 ммоль), полученный в эталонном примере 36. 1H-ЯМР (CDCl3, 400 МГц) δ 8,82 (с, 1Н), 8,38 (д, 1Н), 7,70 (д, 1Н), 7,49 (д, 1Н), 7,35 (с, 1Н), 4,74 (с, 1Н), 3,72-3,52 (м, 2Н), 3,34-2,93 (м, 5Н), 2,44 (с, 3Н), 2,27-1,63 (м, 9Н), 1,26 (м, 2Н)
[1773] Пример 123. (S)-1-(2-(4-(7-фторхинолин-5-ил)амино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1774] Указанное в заголовке соединение (36,4 мг) получали аналогично тому, как описано в примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 7-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид (329,36 мг, 0,93 ммоль), полученный в эталонном примере 37. 1H-ЯМР (CDCl3, 400 МГц) δ 8,82 (с, 1Н), 8,10 (д, 1Н), 7,26 (с, 1Н), 7,05 (д, 1Н), 6,37 (д, 1Н), 4,75 (с, 1Н), 4,59 (с, 1Н), 3,74-3,22 (м, 5Н), 3,00-2,90 (м, 2Н), 2,39-1,67 (м, 8Н), 1,26 (м, 2Н)
[1775] Пример 124. (S)-1-(2-(4-(7-метоксихинолин-5-ил)амино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1776] Указанное в заголовке соединение (4,6 мг) получали аналогично тому, как описано в Примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 7-метокси-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид (291,0 мг, 0,88 ммоль), полученный в эталонном примере 38. 1H-ЯМР (CDCl3, 400 МГц) δ 8,76 (с, 1Н), 8,04 (с, 1Н), 7,19 (с, 1Н), 6,87 (с, 1Н), 6,28 (с, 1Н), 4,77 (с, 1Н), 3,75 (с, 3Н), 3,65-3,15 (м, 5Н), 2,99-2,90 (м, 2Н), 2,40-1,46 (м, 9 Н), 1,26 (м, 2Н)
[1777] Пример 125. (S)-1-(2-(4-(8-метоксихинолин-5-ил)амино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1778] Указанное в заголовке соединение (6,1 мг) получали аналогично тому, как описано в примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 8-метокси-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид (291,0 мг, 0,88 ммоль), полученный в эталонном примере 39. 1H-ЯМР (CDCl3, 400 МГц) δ 8,93 (с, 1Н), 8,24 (с, 1Н), 7,41 (с, 1Н), 6,94 (с, 1Н), 6,65 (с, 1Н), 4,76 (с, 1Н), 4,03 (с, 3Н), 3,73-3,14 (м, 7Н), 3,02-2,05 (м, 9Н), 1,63 (м, 2Н)
[1779] Пример 126. (2S,4S)-4-фтор-1-(2-(4-((6-фторхинолин-4-ил)окси)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1780] (2S,4S)-1-(2-хлорацетил)-4-фторпирролидин-2-карбонитрил (214 мг, 1,12 ммоль), полученный в эталонном примере 2, растворяли в безводном ацетонитриле (4 мл). К полученному раствору добавляли 6-фтор-4-(пиперидин-4-илокси)хинолина гидрохлорид (400 мг, 1,12 ммоль), полученный в эталонном примере 40, карбонат калия (621,8 мг, 5,00 ммоль) и йодид калия (1,87 мг, 0,011 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции к реакционной смеси добавляли воду. Водный слой реакционной смеси экстрагировали дихлорметаном. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (дихлорметан / метанол = 10/1, об./об.) с получением указанного в заголовке соединения (20 мг). 1H-ЯМР (CDCl3, 400 МГц) δ 8,69 (с, 1Н), 8,02 (д, 1Н), 7,80 (д, 1Н), 7,47 (т, 1Н), 6,73 (с, 1Н), 5,50-5,30 (м, 1Н), 4,95 (д, 1Н), 4,69 (с, 1Н), 4,24-3,77 (м, 2Н), 3,51-3,22 (м, 2Н), 2,80-2,15 (м, 10Н)
[1781] Пример 127. (2S,4S)-1-(2-(4-((6-хлорхинолин-4-ил)окси)пиперидин-1-ил)ацетил)-4-фторпирролидин-2-карбонитрил
[1782] Указанное в заголовке соединение (17,0 мг) получали таким же образом, как ив примере 126, за исключением того, что вместо 6-фтор-4-(пиперидин-4-илокси)хинолина гидрохлорида использовали 6-хлор-4-(пиперидин-4-илокси)хинолина гидрохлорид (336,7 мг, 1,12 ммоль), полученный в эталонном примере 41. 1H-ЯМР (CDCl3, 400 МГц) δ 8,71 (с, 1Н), 8,17 (с, 1Н), 7,96 (с, 1Н), 7,62 (с, 1Н), 6,74 (с, 1Н), 5,43 (т, 1Н), 4,95 (с, 1Н), 4,68 (с, 1Н), 4,24-3,70 (м, 2Н), 3,53-3,27 (м, 2Н), 2,82-1,84 (м, 10Н)
[1783] Пример 128. (2S,4S)-4-фтор-1-(2-(4-((6-метоксихинолин-4-ил)окси)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1784] Указанное в заголовке соединение (24,1 мг) получали таким же образом, как описано в примере 126, за исключением того, что вместо 6-фтор-4-(пиперидин-4-илокси)хинолина гидрохлорида использовали 6-метокси-4-(пиперидин-4-илокси)хинолина гидрохлорид (410,0 мг, 1,12 ммоль), полученный в эталонном примере 42. 1H-ЯМР (CDCl3, 400 МГц) δ 8,95 (д, 1Н), 7,94 (д, 1Н), 7,47 (с, 1Н), 7,35 (д, 1Н), 6,70 (д, 1Н), 5,49-5,30 (м, 1Н), 4,94 (д, 1Н), 4,68 (с, 1Н), 4,25-4,10 (м, 1Н), 3,95 (с, 3Н), 3,92-3,21 (м, 3Н), 2,86-2,13 (м, 10Н)
[1785] Пример 129. (2S,4S)-4-фтор-1-(2-(4-((7-метоксихинолин-4-ил)окси)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1786] Указанное в заголовке соединение (4,5 мг) получали таким же образом, как описано в примере 126, за исключением того, что вместо 6-фтор-4-(пиперидин-4-илокси)хинолина гидрохлорида использовали 7-метокси-4-(пиперидин-4-илокси)хинолина гидрохлорид (331,7 мг, 1,12 ммоль), полученный в эталонном примере 43. 1H-ЯМР (CDCl3, 400 МГц) δ 8,64 (с, 1Н), 8,10 (д, 1Н), 7,37 (с, 1Н), 7,15 (д, 1Н), 6,62 (с, 1Н), 5,49-5,30 (м, 1Н), 4,95 (д, 1Н), 4,68 (с, 1Н), 4,25-4,11 (м, 1Н), 3,95 (с, 3Н), 3,89-3,71 (м, 1Н), 3,52-3,25 (м, 2Н), 2,80-2,05 (м, 10Н)
[1787] Пример 130. (2S,4S)-1-(2-(4-((6,7-диметоксихинолин-4-ил)окси)пиперидин-1-ил)ацетил)-4-фторпирролидин-2-карбонитрил
[1788] Указанное в заголовке соединение (4,7 мг) получали таким же образом, как и в примере 126, за исключением того, что вместо 6-фтор-4-(пиперидин-4-илокси)хинолина гидрохлорида использовали 6,7-диметокси-4-(пиперидин-4-илокси)хинолина гидрохлорид (407,1 мг, 1,12 ммоль), полученный в эталонном примере 44. 1H-ЯМР (CDCl3, 400 МГц) δ 8,55 (с, 1Н), 7,43 (д, 1Н), 7,39 (с, 1Н), 6,65 (с, 1Н), 5,49-5,37 (м, 1Н), 4,95 (д, 1Н), 4,68 (с, 1Н), 4,28-4,11 (м, 1Н), 4,00 (с, 6Н), 3,87-3,78 (м, 1Н), 3,52-3,22 (м, 2Н), 2,88-2,01 (м, 10Н)
[1789] Пример 131. (2S,4S)-4-фтор-1-(2-(4-((3-метилхинолин-5-ил)амино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1790] (2S,4S)-1-(2-хлорацетил)-4-фторпирролидин-2-карбонитрил (20,5 мг, 0,11 ммоль), полученный в эталонном примере 2, растворяли в безводном ацетонитриле (4 мл). К полученному раствору добавляли 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид (37,7 мг, 0,11 ммоль), полученный в эталонном примере 35, карбонат калия (59,38 мг, 0,43 ммоль) и йодид калия (0,18 мг, 0,001 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции к реакционной смеси добавляли воду Водный слой реакционной смеси экстрагировали дихлорметаном. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (дихлорметан / метанол = 10/1, об./об.) с получением указанного в заголовке соединения (3 мг). 1H-ЯМР (CDCl3, 400 МГц) δ 8,73 (с, 1Н), 7,89 (с, 1Н), 7,48-7,45 (м, 2Н), 6,63 (д, 1Н), 5,49-5,29 (м, 1Н), 4,96 (д, 1Н), 4,28-3,25 (м, 5Н), 2,98-2,65 (м, 3Н), 2,54 (с, 3Н), 2,41-2,05 (м, 5Н), 1,88-1,26 (м, 3Н)
[1791] Пример 132. (2S,4S)-4-фтор-1-(2-(4-((7-фторхинолин-5-ил)амино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1792] Указанное в заголовке соединение (14 мг) получали аналогично тому, как описано в Примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 7-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид (30,12 мг, 0,11 ммоль), полученный в эталонном примере 37. 1H-ЯМР (CDCl3, 400 МГц) δ 8,85 (с, 1Н), 8,08 (д, 1Н), 7,07 (д, 1Н), 6,39 (д, 1Н), 5,49-5,37 (м, 1Н), 4,95 (д, 1Н), 4,50-3,74 (м, 3Н), 3,47-3,20 (м, 3Н), 3,00-2,64 (м, 3Н), 2,44-2,05 (м, 6Н), 1,85-1,64 (м, 2Н)
[1793] Пример 133. (2S,4S)-4-фтор-1-(2-(4-((7-метоксихинолин-5-ил)амино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1794] Указанное в заголовке соединение (4 мг) получали аналогично тому, как описано в Примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 7-метокси-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид (35,3 мг, 0,11 ммоль), приготовленный в эталонном примере 38. 1H-ЯМР (CDCl3, 400 МГц) δ 8,78 (с, 1Н), 8,01 (д, 1Н), 7,20-7,18 (м, 1Н), 6,86 (с, 1Н), 6,27 (с, 1Н), 5,49-5,36 (м, 1Н), 4,95 (д, 1Н), 4,26-3,98 (м, 1Н), 3,93 (с, 3Н), 3,87-3,70 (м, 1Н), 3,38-3,16 (м, 3Н), 2,94-2,64 (м, 3Н), 2,39-2,05 (м, 6Н), 1,82-1,64 (м, 2Н)
[1795] Пример 134. (2S,4S)-4-фтор-1-(2-(4-((6-метилхинолин-5-ил)амино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1796] Указанное в заголовке соединение (14,1 мг) получали аналогично тому, как описано в Примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 6-метил-N-(пиперидин-4-ил)хинолин-5-амин (34,6 мг, 0,11 ммоль), полученный в эталонном примере 36. 1H-ЯМР (CDCl3, 400 МГц) δ 8,83 (с, 1Н), 8,38 (д, 1Н), 7,71 (д, 1Н), 7,50 (д, 1Н), 7,37-7,35 (м, 1Н), 5,48-5,35 (м, 1Н), 4,93 (д, 1Н), 4,22-3,72 (м, 2Н), 3,42-3,15 (м, 3Н), 2,96-2,63 (м, 3Н), 2,44 (с, 3Н), 2,36-1,26 (м, 8Н)
[1797] Пример 135. (2S,4S)-4-фтор-1-(2-(4-((8-метоксихинолин-5-ил)амино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1798] Указанное в заголовке соединение (1,67 мг) получали аналогично тому, как описано в примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид использовали 8-метокси-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид (35,3 мг, 0,11 ммоль), приготовленный в эталонном примере 39. 1H-ЯМР (CDCl3, 400 МГц) δ 8,94 (с, 1Н), 8,20 (д, 1Н), 7,42 (д, 1Н), 6,96 (д, 1Н), 6,65 (д, 1Н), 5,48-5,36 (м, 1Н), 4,95 (д, 1Н), 4,27-4,13 (м, 1Н), 4,03 (с, 3Н), 3,99-3,77 (м, 1Н), 3,49-2,64 (м, 7Н), 2,38-1,26 (м, 7Н).
[1799] Пример 136. 6-метокси-N-[(3S)-1-[2-оксо-2-[(2S,4S)-2-циано-4-фторпирролидин-1-ил]этил]пирролидин-3-ил]бензофуран-3-карбоксамид
[1800] Указанное в заголовке соединение (10,0 мг, 23,1%) получали таким же образом, как и в примере 29, за исключением того, что вместо (S)-6-фтор-N-(пирролидин-3-ил)бензофуран-3-карбоксамида гидрохлорида использовали (S)-6-метокси-N-(пирролидин-3-ил)бензофуран-3-карбоксамида гидрохлорид (37,9 мг, 0,12 ммоль) в эталонном примере 46. 1H-ЯМР (CDCl3, 400 МГц) δ 8,24 (с, 1Н), 7,89 (д, 1Н), 7,13 (с, 1Н), 6,97 (д, 1Н), 5,51-4,98 (м, 2Н), 4,60 (с, 1Н), 4,07-3,99 (м, 1Н), 3,85 (с, 3Н), 3,82-3,39 (м, 3Н), 3,07 (с, 1Н), 2,87 (с, 2Н), 2,61-2,36 (м, 3Н), 1,87 (с, 1Н)
[1801] Пример 137. (2S)-1-[2-[(3R)-3-[метил(2-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1802] Указанное в заголовке соединение (24,0 мг, 38,3%) получали таким же образом, как и в примере 17, за исключением того, что вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (R)-N-метил-N-(пирролидин-3-ил)хинолин-2-амина гидрохлорид (45,5 мг, 0,17 ммоль), полученный в эталонном примере 47. 1H-ЯМР (CDCl3, 400 МГц) δ 7,88 (д, 1Н), 7,68 (д, 1Н), 7,60 (д, 1Н), 7,53 (т, 1Н), 7,19 (т, 1Н), 6,91 (д, 1Н), 5,70-5,50 (м, 1Н), 5,25-4,79 (м, 1Н), 3,76-3,56 (м, 2Н), 3,44-3,28 (м, 2Н), 3,16 (с, 3Н), 3,13-2,97 (м, 2Н), 2,88-2,58 (м, 2Н), 2,40-2,20 (м, 3Н), 2,20-2,13 (м, 2Н), 1,94-1,89 (м, 1Н)
[1803] Пример 138. (2S)-1-[2-[(3R)-3-[метил(3-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1804] Указанное в заголовке соединение (109,3 мг, 47,0%) получали таким же образом, как и в примере 17, за исключением того, что вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (R)-N-метил-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид (168,8 мг, 0,64 ммоль), полученный в эталонном примере 48. 1H-ЯМР (CDCl3, 400 МГц) δ 8,77 (с, 1Н), 7,96 (д, 1Н), 7,64 (д, 1Н), 7,45-7,28 (м, 2Н), 7,23 (с, 1Н), 5,15-4,77 (м, 1Н), 4,70-4,50 (м, 1Н), 3,73-3,70 (м, 1Н), 3,60-3,52 (м, 1Н), 3,48-3,26 (м, 2Н), 3,04 (с, 3Н), 3,03-2,88 (м, 1Н), 2,86-2,77 (м, 2Н), 2,64 (дд, 1Н), 2,40-2,20 (м, 3Н), 2,20-2,05 (м, 2Н), 1,97-1,91 (м, 1Н)
[1805] Пример 139. (2S)-1-[2-[(3R)-3-[метил(5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1806] Указанное в заголовке соединение (1,5 мг, 12,0%) получали таким же образом, как ив примере 17, за исключением того, что (R)-N-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (88,1 мг, 0,33 ммоль), полученный в эталонном примере 49, использовали вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида. 1H-ЯМР (CDCl3, 400 МГц) δ 8,91 (д, 1Н), 8,63 (д, 1Н), 7,84 (д, 1Н), 7,64 (т, 1Н), 7,41 (т, 1Н), 7,21 (д, 1Н), 5,20-4,70 (м, 1Н), 4,10-3,90 (м, 1Н), 3,80-3,66 (м, 1Н), 3,60-3,40 (м, 2Н), 3,38-3,20 (м, 2Н), 3,00-2,88 (м, 1Н), 2,81 (с, 3Н), 2,81-2,70 (м, 2Н), 2,40-2,20 (м, 2Н), 2,20-2,00 (м, 3Н), 2,00-1,80 (м, 1Н)
[1807] Пример 140. (2S)-1-[2-[(3R)-3-[метил(6-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1808] Указанное в заголовке соединение (16,5 мг, 19,9%) получали таким же образом, как и в примере 17, за исключением того, что (R)-N-метил-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид (59,5 мг, 0,23 ммоль), полученный в эталонном примере 50, использовали вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида. 1H-ЯМР (CDCl3, 400 МГц) δ 8,64 (д, 1Н), 8,00-7,94 (м, 2Н), 7,44 (д, 1Н), 7,30-7,20 (м, 1Н), 6,88 (д, 1Н), 5,15-4,73 (м, 1Н), 4,73-4,58 (м, 1Н), 3,80-3,62 (м, 1Н), 3,62-3,45 (м, 2Н), 3,46-3,20 (м, 2Н), 3,04 (с, 3Н), 3,03-2,78 (м, 2Н), 2,78-2,58 (м, 1Н), 2,48-2,22 (м, 3Н), 2,22-2,10 (м, 2Н), 2,01-1,82 (м, 1Н)
[1809] Пример 141. (2S)-1-[2-[(3R)-3-[метил(7-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1810] Указанное в заголовке соединение (74,9 мг, 51,1%) получали таким же образом, как и в примере 17, за исключением того, что (R)-N-метил-N-(пирролидин-3-ил)хинолин-7-амина гидрохлорид (106,3 мг, 0,40 ммоль), полученный в эталонном примере 51, использовали вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида. 1H-ЯМР (CDCl3, 400 МГц) δ 8,75 (с, 1Н), 7,97 (д, 1Н), 7,65 (д, 1Н), 7,28-7,23 (м, 2Н), 7,12 (т, 1Н), 5,20-4,74 (м, 1Н), 4,74-4,61 (м, 1Н), 3,82-3,64 (м, 1Н), 3,64-3,50 (м, 1Н), 3,46-3,24 (м, 2Н), 3,07 (с, 3Н), 3,07-2,83 (м, 2Н), 2,83-2,66 (м, 1Н), 2,60 (кв, 1Н), 2,46-2,22 (м, 3Н), 2,22-2,10 (м, 2Н), 2,00-1,92 (м, 1Н)
[1811] Пример 142. (2S)-1-[2-[(3S)-3-[метил(3-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1812] Указанное в заголовке соединение (165,8 мг, 59,1%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-N-метил-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид (203,4 мг, 0,77 ммоль), полученный в эталонном примере 52. 1H-ЯМР (CDCl3, 400 МГц) δ 8,75 (с, 1Н), 7,94 (д 1Н), 7,63 (т, 1Н), 7,44-7,41 (м, 2Н), 7,22 (с, 1Н), 5,16-4,70 (м, 1Н), 4,70-4,52 (м, 1Н), 3,80-3,60 (м, 1Н), 3,60-3,48 (м, 1Н), 3,48-3,18 (м, 2Н), 3,02 (с, 3Н), 3,02-2,70 (м, 2Н), 2,60 (дд, 1Н), 2,50-2,34 (м, 1Н), 2,34-2,20 (м, 3Н), 2,20-2,04 (м, 2Н), 2,04-1,88 (м, 1Н)
[1813] Пример 143. (2S)-1-[2-[(3S)-3-[метил(4-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1814] Указанное в заголовке соединение (60,3 мг, 73,1%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-N-метил-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид (59,8 мг, 0,23 ммоль), полученный в эталонном примере 53. 1H-ЯМР (CDCl3, 400 МГц) δ 8,69 (д, 1Н), 8,06-8,04 (м, 2Н), 7,66 (т, 1Н), 7,48 (т, 1Н), 6,84 (д, 1Н), 5,18-4,76 (м, 1Н), 4,48-4,30 (м, 1Н), 3,82-3,60 (м, 1Н), 3,60-3,44 (м, 1Н), 3,44-3,20 (м, 2Н), 3,01 (с, 3Н), 3,01-2,90 (м, 2Н), 2,90-2,80 (м, 1Н), 2,70-2,58 (м, 1Н), 2,40-2,30 (м, 1Н), 2,30-2,20 (м, 3Н), 2,20-1,94 (м, 2Н)
[1815] Пример 144. (2S)-1-[2-[(3S)-3-[метил(5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1816] Указанное в заголовке соединение (22,9 мг, 16,6%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-N-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (100,1 мг, 0,38 ммоль), полученный в эталонном примере 54, использовали. 1H-ЯМР (CDCl3, 400 МГц) δ 8,90 (д, 1Н), 8,62 (д, 1Н), 7,83 (д, 1Н), 7,63 (т, 1Н), 7,41 (т, 1Н), 7,21 (д, 1Н), 5,20-4,70 (м, 1Н), 4,12-3,98 (м, 1Н), 3,80-3,60 (м, 1Н), 3,60-3,40 (м, 1Н), 3,40-3,20 (м, 2Н), 3,02-2,90 (м, 1Н), 2,79 (с, 3Н), 2,78-2,60 (м, 3Н), 2,40-2,20 (м, 2Н), 2,20-2,00 (м, 3Н), 2,00-1,84 (м, 1Н)
[1817] Пример 145. (2S)-1-[2-[(3S)-3-[метил(6-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1818] Указанное в заголовке соединение (85,9 мг, 64,1%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-N-метил-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид (97,1 мг, 0,37 ммоль), полученный в эталонном примере 55. 1H-ЯМР (CDCl3, 400 МГц) δ 8,62 (д, 1Н), 8,08-7,90 (м, 2Н), 7,42 (д, 1Н), 7,28-7,25 (м, 1Н), 6,87 (д, 1Н), 5,20-4,74 (м, 1Н), 4,74-4,50 (м, 1Н), 3,80-3,60 (м, 1Н), 3,60-3,48 (м, 1Н), 3,48-3,20 (м, 2Н), 3,10 (с, 3Н), 3,10-2,90 (м, 2Н), 2,90-2,72 (м, 1Н), 2,70-2,50 (м, 1Н), 2,50-2,23 (м, 2Н), 2,23-2,05 (м, 3Н), 2,05-1,80 (м, 1Н)
[1819] Пример 146. (2S)-1-[2-[(3S)-3-[метил(7-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1820] Указанное в заголовке соединение (142,4 мг, 49,4%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-N-метил-N-(пирролидин-3-ил)хинолин-7-амина гидрохлорид (209,5 мг, 0,79 ммоль), полученный в эталонном примере 56. 1H-ЯМР (CDCl3, 400 МГц) δ 8,73 (с, 1Н), 7,98 (д, 1Н), 7,65 (д, 1Н), 7,28-7,23 (м, 2Н), 7,14-7,10 (м, 1Н), 5,20-4,74 (м, 1Н), 4,74-4,60 (м, 1Н), 3,80-3,60 (м, 1Н), 3,60-3,48 (м, 1Н), 3,48-3,20 (м, 2Н), 3,07 (с, 3Н), 3,07-2,90 (м, 1Н), 2,90-2,72 (м, 1Н), 2,70-2,50 (м, 1Н), 2,50-2,20 (м, 3Н), 2,20-2,00 (м, 3Н), 2,00-1,85 (м, 1Н)
[1821] Пример 147. (2S)-1-[2-[(3S)-3-[4-изохинолил(метил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1822] Указанное в заголовке соединение (2,4 мг, 3,3%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид использовали (S)-N-метил-N-(пирролидин-3-ил)изохинолин-4-амина гидрохлорид (55,6 мг, 0,21 ммоль), полученный в эталонном примере 57. 1H-ЯМР (CDCl3, 400 МГц) δ 8,98 (с, 1Н), 8,24 (с, 1Н), 8,19 (д, 1Н), 7,97 (д, 1Н), 7,70 (т, 1Н), 7,61 (т, 1Н), 5,25-4,74 (м, 1Н), 4,23-4,10 (м, 1Н), 3,80-3,60 (м, 1Н), 3,60-3,40 (м, 1Н), 3,40-3,20 (м, 2Н), 3,05-2,90 (м, 1Н), 2,86 (с, 3Н), 2,86-2,78 (м, 2Н), 2,78-2,66 (м, 1Н), 2,40-2,24 (м, 2Н), 2,24-2,10 (м, 3Н), 2,05-1,90 (м, 1Н)
[1823] Пример 148. (2S)-1-[2-[(3S)-3-[5-изохинолил(метил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1824] Указанное в заголовке соединение (10,9 мг, 11,2%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-N-метил-N-(пирролидин-3-ил)изохинолин-5-амина гидрохлорид (70,7 мг, 0,27 ммоль), полученный в эталонном примере 58. 1H-ЯМР (CDCl3, 400 МГц) δ 9,22 (с, 1Н), 8,53 (д, 1Н), 8,00 (д, 1Н), 7,68 (д, 1Н), 7,52 (т, 1Н), 7,33 (д, 1Н), 5,20-4,70 (м, 1Н), 4,18-4,00 (м, 1Н), 3,80-3,60 (м, 1Н), 3,60-3,42 (м, 1Н), 3,42-3,20 (м, 2Н), 3,00-2,88 (м, 1Н), 2,80 (с, 3Н), 2,80-2,70 (м, 2Н), 2,70-2,60 (м, 1Н), 2,40-2,20 (м, 2Н), 2,20-2,05 (м, 3Н), 2,00-1,85 (м, 1Н)
[1825] Пример 149. (2S)-1-[2-[(3S)-3-[метил-(4-метил-3-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1826] Указанное в заголовке соединение (37,4 мг, 55,9%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-N, 4-диметил-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид (49,1 мг, 0,18 ммоль), полученный в эталонном примере 59. 1H-ЯМР (CDCl3, 400 МГц) δ 8,79 (с, 1Н), 8,05 (д, 1Н), 7,99 (д, 1Н), 7,64 (т, 1Н), 7,55 (т, 1Н), 5,20-4,70 (м, 1Н), 4,10-3,96 (м, 1Н), 3,78-3,60 (м, 1Н), 3,60-3,44 (м, 1Н), 3,40-3,20 (м, 2Н), 3,04-2,90 (м, 1Н), 2,90-2,78 (м, 1Н), 2,74 (с, 3Н), 2,74-2,70 (м, 1Н), 2,68 (с, 3Н), 2,68-2,50 (м, 1Н), 2,34-2,20 (м, 2Н), 2,20-2,00 (м, 3Н), 2,00-1,74 (м, 1Н)
[1827] Пример 150. (2S)-1-[2-[(3S)-3-[метил-(6-метил-3-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1828] Указанное в заголовке соединение (224,5 мг, 83,2%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-N, 6-диметил-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид (198,5 мг, 0,72 ммоль), полученный в эталонном примере 60. 1H-ЯМР (CDCl3, 400 МГц) δ 8,67 (с, 1Н), 7,83 (д, 1Н), 7,40 (с, 1Н), 7,28 (д, 1Н), 7,15 (с, 1Н), 5,18-4,74 (м, 1Н), 4,70-4,50 (м, 1Н), 3,80-3,60 (м, 1Н), 3,60-3,48 (м, 1Н), 3,48-3,20 (м, 2Н), 3,01 (с, 3Н), 3,01-2,90 (м, 2Н), 2,90-2,72 (м, 1Н), 2,68-2,52 (м, 1Н), 2,50 (с, 3Н), 2,45-2,24 (м, 2Н), 2,24-2,08 (м, 3Н), 2,08-1,88 (м, 1Н)
[1829] Пример 151. (S)-1-(2-((S)-3-((6-фторхинолин-3-ил)(метил)амино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1830] Указанное в заголовке соединение (273,7 мг, 78,8%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-6-фтор-N-метил-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид (256,7 мг, 0,91 ммоль), полученный в эталонном примере 61. 1H-ЯМР (CDCl3, 400 МГц) δ 8,69 (с, 1Н), 7,91 (д, 1Н), 7,22-7,13 (м, 2Н), 7,10 (с, 1Н), 5,12-4,72 (м, 1Н), 4,72-4,58 (м, 1Н), 3,82-3,60 (м, 1Н), 3,60-3,48 (м, 1Н), 3,48-3,20 (м, 2Н), 3,04 (с, 3Н), 3,04-2,90 (м, 2Н), 2,90-2,70 (м, 1Н), 2,68-2,52 (м, 1Н), 2,45-2,24 (м, 2Н), 2,24-2,06 (м, 3Н), 2,06-1,85 (м, 1Н)
[1831] Пример 152. (S)-1-(2-((S)-3-((6-метоксихинолин-3-ил)(метил)амино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1832] Указанное в заголовке соединение (196,9 мг, 67,7%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-6-метокси-N-метил-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид (217,2 мг, 0,74 ммоль), полученный в эталонном примере 62. 1H-ЯМР (CDCl3, 400 МГц) δ 8,59 (с, 1Н), 7,83 (д, 1Н), 7,14 (с, 1Н), 7,08 (д, 1Н), 6,93 (с, 1Н), 5,16-4,74 (м, 1Н), 4,70-4,55 (м, 1Н), 3,91 (с, 3Н), 3,88-3,62 (м, 1Н), 3,62-3,48 (м, 1Н), 3,48-3,20 (м, 2Н), 3,02 (с, 3Н), 3,02-2,90 (м, 2Н), 2,90-2,73 (м, 1Н), 2,68-2,55 (м, 1Н), 2,42-2,24 (м, 2Н), 2,24-2,08 (м, 3Н), 2,08-1,86 (м, 1Н)
[1833] Пример 153. (S)-1-(2-((S)-3-((7-метоксихинолин-3-ил)(метил)амино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1834] Указанное в заголовке соединение (61,5 мг, 31,5%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-7-метокси-N-метил-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид (145,5 мг, 0,50 ммоль), полученный в эталонном примере 63. 1H-ЯМР (CDCl3, 400 МГц) δ 8,70 (с, 1Н), 7,55 (д, 1Н), 7,33 (с, 1Н), 7,28 (с, 1Н), 7,14 (д, 1Н), 5,20-4,72 (м, 1Н), 4,62-4,49 (м, 1Н), 3,93 (с, 3Н), 3,88-3,62 (м, 1Н), 3,62-3,50 (м, 1Н), 3,50-3,20 (м, 2Н), 2,99 (с, 3Н), 2,99-2,90 (м, 2Н), 2,90-2,73 (м, 1Н), 2,73-2,56 (м, 1Н), 2,46-2,05 (м, 5Н), 2,05-1,82 (м, 1Н)
[1835] Пример 154. (S)-1-(2-((S)-3-((8-метоксихинолин-3-ил)(метил)амино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1836] Указанное в заголовке соединение (180,2 мг, 45,5%) получали таким же образом, как и в примере 5, за исключением того, что (S)-8-метокси-N-метил-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид (295,8 мг, 1,01 ммоль), полученный в эталонном примере 64, использовали вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида. 1H-ЯМР (CDCl3, 400 МГц) δ 8,73 (с, 1Н), 7,35 (т, 1Н), 7,22-7,19 (м, 2Н), 6,79 (д, 1Н), 5,18-4,72 (м, 1Н), 4,70-4,50 (м, 1Н), 4,06 (с, 3Н), 3,82-3,60 (м, 1Н), 3,60-3,49 (м, 1Н), 3,49-3,18 (м, 2Н), 3,03 (с, 3Н), 3,03-2,90 (м, 2Н), 2,90-2,70 (м, 1Н), 2,66-2,52 (м, 1Н), 2,40-2,22 (м, 2Н), 2,22-2,08 (м, 3Н), 2,05-1,82 (м, 1Н)
[1837] Пример 155. (2S,4S)-4-фтор-1-[2-[(3S)-3-[метил-(3-метил-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1838] Указанное в заголовке соединение (38,9 мг, 29,1%) получали таким же образом, как и в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-N,3-диметил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (93,6 мг, 0,34 ммоль), полученный в эталонном примере 65. 1H-ЯМР (CDCl3, 600 МГц) δ 8,72 (с, 1Н), 8,34 (с, 1Н), 7,77 (д, 1Н), 7,53 (т, 1Н), 7,15 (д, 1Н), 5,46-4,90 (м, 2Н), 4,20-3,98 (м, 2Н), 3,80-3,60 (м, 1Н), 3,40-3,25 (м, 2Н), 3,02-2,90 (м, 1Н), 2,90-2,75 (м, 1Н), 2,75 (с, 3Н), 2,75-2,60 (м, 3Н), 2,53 (с, 3Н), 2,40-2,20 (м, 1Н), 2,15-2,05 (м, 1Н), 1,98-1,80 (м, 1Н)
[1839] Пример 156. (2S,4S)-4-фтор-1-(2-((S)-3-((3-фторхинолин-5-ил)(метил)амино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1840] Указанное в заголовке соединение (264,4 мг, 79,8%) получали таким же образом, как и в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорид использовали (S)-3-фтор-N-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (233,8 мг, 0,83 ммоль), приготовленный в эталонном примере 66. 1H-ЯМР (CDCl3, 600 МГц) δ 8,77 (с, 1Н), 8,20 (д, 1Н), 7,82 (д, 1Н), 7,58 (т, 1Н), 7,24 (д, 1Н), 5,50-4,90 (м, 2Н), 4,20-3,98 (м, 2Н), 3,80-3,68 (м, 1Н), 3,60-3,18 (м, 2Н), 2,98-2,76 (м, 2Н), 2,76 (с, 3Н), 2,76-2,50 (м, 3Н), 2,40-2,20 (м, 1Н), 2,18-2,05 (м, 1Н), 1,94-1,78 (м, 1Н)
[1841] Пример 157. (2S,4S)-4-фтор-1-(2-((S)-3-((7-фторхинолин-5-ил)(метил)амино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1842] Указанное в заголовке соединение (238,2 мг, 92,0%)получали таким же образом, как и в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-7-фтор-N-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (182,5 мг, 0,65 ммоль), приготовленный в эталонном примере 67. 1H-ЯМР (CDCl3, 600 МГц) δ 8,85 (д, 1Н), 8,47 (д, 1Н), 7,39 (т, 1Н), 7,33 (с, 1Н), 6,92 (с, 1Н), 5,48-4,90 (м, 2Н), 4,20-3,88 (м, 2Н), 3,80-3,68 (м, 1Н), 3,60-3,18 (м, 2Н), 2,98-2,80 (м, 2Н), 2,76 (с, 3Н), 2,76-2,60 (м, 3Н), 2,40-2,20 (м, 1Н), 2,18-2,08 (м, 1Н), 2,00-1,88 (м, 1Н)
[1843] Пример 158. (2S,4S)-4-фтор-1-(2-((S)-3-((8-фторхинолин-5-ил)(метил)амино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1844] Указанное в заголовке соединение (196,6 мг, 80,9%)получали таким же образом, как и в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-8-фтор-N-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (171,2 мг, 0,61 ммоль), полученный в эталонном примере 68. 1H-ЯМР (CDCl3, 600 МГц) δ 8,92 (с, 1Н), 8,61 (д, 1Н), 7,45 (д, 1Н), 7,29 (т, 1Н), 7,12 (д, 1Н), 5,48-4,90 (м, 2Н), 4,20-3,84 (м, 2Н), 3,78-3,64 (м, 1Н), 3,60-3,14 (м, 2Н), 3,00-2,72 (м, 2Н), 2,72 (с, 3Н), 2,72-2,50 (м, 3Н), 2,38-2,20 (м, 1Н), 2,12-2,00 (м, 1Н), 1,90-1,80 (м, 1Н)
[1845] Пример 159. (2S,4S)-4-фтор-1-[2-[(3S)-3-[метил-[8-(трифторметил)-5-хинолил]амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1846] Указанное в заголовке соединение (324,1 мг, 68,5%) получали таким же образом, как и в примере 28, за исключением того, что вместо S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-N-метил-N-(пирролидин-3-ил)-8-(трифторметил)хинолин-5-амина гидрохлорид (349,4 мг, 1,05 ммоль), полученный в эталонном примере 69. 1H-ЯМР (CDCl3, 600 МГц) δ 9,02 (д, 1Н), 8,54 (д, 1Н), 7,95 (д, 1Н), 7,46 (т, 1Н), 7,10 (д, 1Н), 5,50-4,90 (м, 2Н), 4,26-3,90 (м, 2Н), 3,82-3,68 (м, 1Н), 3,70-3,16 (м, 2Н), 3,00-2,85 (м, 1Н), 2,85 (с, 3Н), 2,85-2,78 (м, 2Н), 2,78-2,60 (м, 2Н), 2,40-2,24 (м, 1Н), 2,20-2,10 (м, 1Н), 2,00-1,90 (м, 1Н)
[1847] Пример 160. (2S,4S)-4-фтор-1-[2-[(3S)-3-[метил-[8-(трифторметокси)-5-хинолил]амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1848] Указанное в заголовке соединение (271,0 мг, 55,4%) получали таким же образом, как и в примере 28, за исключением того, что вместо S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-N-метил-N-(пирролидин-3-ил)-8-(трифторметокси)хинолин-5-амина гидрохлорид (365,6 мг, 1,05 ммоль), полученный в эталонном примере 70. 1H-ЯМР (CDCl3, 600 МГц) δ 9,00 (д, 1Н), 8,59 (д, 1Н), 7,52 (д, 1Н), 7,47 (т, 1Н), 7,13 (д, 1Н), 5,48-4,90 (м, 2Н), 4,24-3,88 (м, 2Н), 3,80-3,68 (м, 1Н), 3,60-3,16 (м, 2Н), 3,05-2,78 (м, 2Н), 2,78 (с, 3Н), 2,78-2,60 (м, 3Н), 2,40-2,22 (м, 1Н), 2,20-2,10 (м, 1Н), 1,98-1,85 (м, 1Н)
[1849] Пример 161. (S)-1-(2-((R)-3-(хинолин-5-иламино)пирролидин-1-ил)ацетил)пирролидин-2-карбонитрил
[1850] Указанное в заголовке соединение (2,5 мг, 5,19%) получали таким же образом, как ив примере 17, за исключением того, что вместо гидрохлорида (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид использовали (R)-N-(пирролидин-3-ил)хинолин-5-амина (25,6 мг, 0,12 ммоль), приготовленный в эталонном примере 71. 1H-ЯМР (CDCl3, 400 МГц) δ 8,87 (с, 1Н), 8,31 (дд, 1Н), 7,55 (т, 1Н), 7,47 (д, 1Н), 7,36-7,30 (м, 1Н), 6,57 (д, 1Н), 4,82 (дд, 1Н), 4,21 (с, 1Н), 3,69-3,35 (м, 4Н), 3,14-2,47 (м, 4Н), 2,41-1,90 (м, 7Н)
[1851] Пример 162. (2S)-1-[2-[(3R)-3-(6-хинолиламино)пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1852] Указанное в заголовке соединение (11,4 мг, 22,5%) получали таким же образом, как и в примере 17, за исключением того, что вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид использовали (R)-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид (25,6 мг, 0,12 ммоль), приготовленный в эталонном примере 72. 1H-ЯМР (CDCl3, 400 МГц) δ 8,57 (д, 1Н), 7,86 (дд, 2Н), 7,25-7,22 (м, 1Н), 7,07 (дд, 1Н), 6,62 (с, 1Н), 4,87-4,62 (м, 2Н), 4,11 (с, 1Н), 3,66-3,28 (м, 4Н), 3,01-2,82 (м, 3Н), 2,64-2,09 (м, 6Н), 1,83-1,79 (м, 1Н)
[1853] Пример 163. (2S)-1-[2-[(3R)-3-(7-хинолиламино)пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1854] Указанное в заголовке соединение (3,4 мг, 6,72%) получали таким же образом, как и в примере 17, за исключением того, что вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (R)-N-(пирролидин-3-ил)хинолин-7-амина гидрохлорид (25,6 мг, 0,12 ммоль), полученный в эталонном примере 73. 1H-ЯМР (CDCl3, 400 МГц) δ 8,71 (д, 1Н), 7,94 (д, 1Н), 7,57-7,54 (м, 1Н), 7,10 (кв, 1Н), 6,99 (д, 1Н), 6,93-6,90 (м, 1Н), 4,93-4,73 (м, 2Н), 4,18 (с, 1Н), 3,69-3,31 (м, 4Н), 3,09-2,85 (м, 3Н), 2,60-2,16 (м, 6Н), 1,86 (м, 1Н)
[1855] Пример 164. (2S)-1-[2-[(3R)-3-(8-хинолиламино)пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1856] Указанное в заголовке соединение (9,5 мг, 18,7%) получали таким же образом, как и в примере 17, за исключением того, что вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (R)-N-(пирролидин-3-ил)хинолин-8-амина (25,6 мг, 0,12 ммоль), полученный в эталонном примере 74. 1H-ЯМР (CDCl3, 400 МГц) δ 8,70-8,69 (м, 1Н), 8,05 (д, 1Н), 7,39-7,35 (м, 2Н), 7,08-7,05 (м, 1Н), 6,64 (д, 1Н), 6,29 (д, 1Н), 5,24-4,71 (м, 1Н), 4,23 (с, 1Н), 3,75-3,52 (м, 2,3Н), 3,36-3,28 (м, 1,7Н), 3,15-3,11 (м, 1Н), 2,91-2,74 (м, 3Н), 2,49-2,07 (м, 5Н), 1,93-1,190 (м, 1Н)
[1857] Пример 165. (2S,4S)-4-фтор-1-[2-[(3R)-3-(3-хинолиламино)пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1858] Указанное в заголовке соединение (15,3 мг, 39,7%) получали таким же образом, как в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид (25,6 мг, 0,12 ммоль), полученный в эталонном примере 17. 1H-ЯМР (CDCl3, 400 МГц) δ 8,42-8,39 (м, 1Н), 7,88 (д, 1Н), 7,57 (д, 1Н), 7,40-7,34 (м, 2Н), 6,90-6,89 (м, 1Н), 5,36-5,20 (м, 1Н), 5,06-4,83 (м, 2Н), 4,07-3,54 (м, 3Н),3,40-3,23 (м, 1Н), 2,96-2,95 (м, 2Н), 2,88-2,80 (м, 2Н), 2,67-2,51 (м, 2Н), 2,40-2,10 (м, 2Н), 1,77-1,76 (м, 1Н)
[1859] Пример 166. (2S,4S)-4-фтор-1-[2-[(3R)-3-(5-хинолиламино)пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1860] Указанное в заголовке соединение (16,9 мг, 44,0%) получали таким же образом, как описано в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (R)-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (25,6 мг, 0,12 ммоль), полученный в эталонном примере 71. 1H-ЯМР (CDCl3, 400 МГц) δ 8,53 (д, 1Н), 7,85 (д, 1Н), 7,79 (д, 1Н), 7,21-7,18 (м, 1Н), 7,05-7,03 (м, 1Н), 6,58-6,56 (м, 1Н), 5,34-5,18 (м, 1Н), 5,07-4,72 (м, 2Н), 4,09-3,20 (м, 5Н), 2,90-2,73 (м, 3Н), 2,64-2,47 (м, 2Н), 2,37-2,09 (м, 2Н), 1,73-1,70 (м, 1Н)
[1861] Пример 167. (2S,4S)-4-фтор-1-[2-[(3R)-3-(6-хинолиламино)пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1862] Указанное в заголовке соединение (1,2 мг, 3,1%) получали таким же образом, как в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (R)-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид (25,6 мг, 0,12 ммоль), полученный в эталонном примере 72. 1H ЯМР (CD3OD, 400 МГц) δ 8,75 (дд, 1Н), 8,67-8,60 (м, 1Н), 7,60-7,56 (м, 1Н), 7,46-7,43 (м, 1Н), 7,33-7,31 (д, 1Н), 6,69-6,66 (м, 1Н), 5,51 (с, 1Н), 5,39-5,31 (м, 1Н), 5,00 (д, 1Н), 4,25-4,24 (м, 1Н), 4,09-4,00 (м, 1Н), 3,87-3,74 (м, 1Н), 3,59-3,42 (м, 1Н), 3,09-3,04 (м, 2Н), 2,95-2,88 (м, 1Н), 2,71-2,39 (м, 4Н), 1,97-1,91 (м, 1Н).
[1863] Пример 168. (2S,4S)-4-фтор-1-[2-[(3R)-3-(7-хинолиламино)пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1864] Указанное в заголовке соединение (1,5 мг, 3,9%) получали таким же образом, как описано в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (R)-N-(пирролидин-3-ил)хинолин-7-амина гидрохлорид (25,6 мг, 0,12 ммоль), приготовленный в эталонном примере 73. 1H-ЯМР (CDCl3, 400 МГц) δ 8,72-8,71 (м, 1Н), 7,96 (д, 1Н), 7,58-7,55 (м, 1Н), 7,13-7,10 (м, 1Н), 6,99 (с, 1Н), 6,92-6,90 (м, 1Н), 5,48-5,29 (м, 1Н), 5,18-4,93 (м, 1Н), 4,77-4,61 (м, 1Н), 4,23-4,18 (м, 1Н), 4,11-3,79 (м, 2Н), 3,48-3,32 (м, 2Н), 3,04-2,22 (м, 7Н), 1,90-1,85 (м, 1Н)
[1865] Пример 169. (2S,4S)-4-фтор-1-[2-[(3R)-3-(8-хинолиламино)пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1866] Указанное в заголовке соединение (16,7 мг, 43,2%) получали таким же образом, как описано в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорид использовали (R)-N-(пирролидин-3-ил)хинолин-8-амина гидрохлорид (25,6 мг, 0,12 ммоль), приготовленный в эталонном примере 74. 1H-ЯМР (CDCl3, 400 МГц) δ 8,69-8,67 (м, 1Н), 8,05-8,03 (м, 1Н), 7,39-7,34 (м, 2Н), 7,08-7,04 (м, 1Н), 6,64-6,61 (м, 1Н), 6,25 (д, 1Н), 5,44-5,19 (м, 1,3Н), 4,83 (д, 0,7Н), 4,19-4,17 (м, 1Н), 4,05-3,65 (м, 2Н), 3,39-3,07 (м, 2Н), 3,00-2,02 (м, 7Н), 1,92-1,85 (м, 1Н)
[1867] Пример 170. (2S,4S)-4-фтор-1-[2-[(3R)-3-(4-хинолиламино)пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1868] Указанное в заголовке соединение (1,1 мг, 2,91%) получали таким же образом, как в примере 28, за исключением того, что (R)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид (25,6 мг, 0,12 ммоль), приготовленный в эталонном примере 75, использовали вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида. 1H ЯМР (CDOD3, 400 МГц) δ 8,38 (дд, 1Н), 8,22-8,15 (м, 1Н), 7,83 (д, 1Н), 7,66 (т, 1Н), 7,49-7,45 (м, 1Н), 6,53 (д, 1Н), 5,51-5,00 (м, 2Н), 4,35-4,31 (м, 1Н), 4,08-4,00 (м, 1Н), 3,86-3,74 (м, 1Н), 3,62-3,57 (м, 1Н), 3,45 (д, 1Н), 3,13-2,92 (м, 3Н), 2,67-2,36 (м, 4Н), 1,97-1,90 (м, 1Н)
[1869] Пример 171. (2S,4S)-4-фтор-1-[2-[(3R)-3-(1,8-нафтиридин-3-иламино)пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1870] (2S)-1-(2-хлорацетил)-4-фторпирролидин-2-карбонитрил (168,7 мг, 0,89 ммоль), полученный в эталонном примере 2, растворяли в безводном дихлорметане (4 мл). К полученному раствору добавляли (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорид (254,1 мг 0,89 ммоль), полученный в эталонном примере 76 и карбонат калия (492,0 мг, 3,56 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции к реакционной смеси добавляли воду Водный слой реакционной смеси экстрагировали дихлорметаном. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (дихлорметан / метанол = 10/1, об./об.) с получением указанного в заголовке соединения (50,1 мг, 15,4%). 1H-ЯМР (CDCl3, 600 МГц) δ 8,79 (с, 1Н), 8,61 (д, 1Н), 7,96 (д, 1Н), 7,35 (т, 1Н), 6,90 (д, 1Н), 5,50-5,28 (м, 1Н), 5,10-4,70 (м, 1Н), 4,20-4,00 (м, 2Н), 3,98-3,70 (м, 1Н), 3,60-3,30 (м, 2Н), 3,10-2,98 (м, 2Н), 2,95-2,82 (м, 2Н), 2,80-2,55 (м, 2Н), 2,50-2,20 (м, 2Н), 1,90-1,80 (м, 1Н)
[1871] Пример 172. (2S,4S)-4-фтор-1-[2-[(3R)-3-[(7-хлор-1,8-нафтиридин-3-ил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1872] Указанное в заголовке соединение (8,5 мг, 4,2%) получали таким же образом, как и в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида использовали (R)-7-хлор-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорид (161,2 мг, 0,50 ммоль), полученный в эталонном примере 77. 1H-ЯМР (CDCl3, 600 МГц) δ 8,58 (с, 1Н), 7,91 (д, 1Н), 7,35 (д, 1Н), 6,91 (с, 1Н), 5,50-5,30 (м, 1Н), 5,08-4,75 (м, 1Н), 4,20-4,00 (м, 2Н), 3,96-3,68 (м, 1Н), 3,65-3,30 (м, 2Н), 3,14-3,00 (м, 2Н), 2,98-2,72 (м, 2Н), 2,72-2,50 (м, 2Н), 2,50-2,25 (м, 2Н), 1,90-1,80 (м, 1Н)
[1873] Пример 173. (2S,4S)-4-фтор-1-[2-[(3R)-3-[(6-фтор-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1874] Указанное в заголовке соединение (138,8 мг, 63,7%) получали таким же образом, как и в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида использовали (R)-6-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (171,9 мг, 0,57 ммоль), полученный в эталонном примере 78. 1H-ЯМР (CDCl3, 400 МГц) δ 8,86 (д, 1Н), 8,43 (д, 1Н), 7,68 (д, 1Н), 7,47-7,39 (м, 2Н), 5,52-5,35 (м, 1Н), 5,35-4,94 (м, 1Н), 4,30-4,06 (м, 2Н), 4,04-3,70 (м, 1Н), 3,70-3,38 (м, 2Н), 3,18-3,00 (м, 1Н), 2,98-2,85 (м, 1Н), 2,82-2,60 (м, 2Н), 2,60-2,40 (м, 2Н), 2,40-2,20 (м, 2Н), 2,00-1,85 (м, 1Н)
[1875] Пример 174. (2S,4S)-4-фтор-1-[2-[(3R)-3-[(7-фтор-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1876] Указанное в заголовке соединение (54,9 мг, 36,4%) получали таким же образом, как и в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида использовали (R)-7-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (118,6 мг, 0,39 ммоль), полученный в эталонном примере 79. 1H-ЯМР (CDCl3, 400 МГц) δ 8,84 (д, 1Н), 8,29 (д, 1Н), 7,31-7,25 (м, 1Н), 7,08 (с, 1Н), 6,33 (с, 1Н), 5,70-5,34 (м, 1Н), 5,10-4,93 (м, 1Н), 4,30-3,70 (м, 3Н), 3,70-3,40 (м, 2Н), 3,20-3,00 (м, 2Н), 2,98-2,42 (м, 4Н), 2,42-2,22 (м, 2Н), 2,00-1,85 (м, 1Н)
[1877] Пример 175. (2S,4S)-4-фтор-1-[2-[(3R)-3-[(8-фтор-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1878] Указанное в заголовке соединение (45,6 мг, 11,8%) получали таким же образом, как и в примере 171, за исключением того, что (R)-8-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (303,3 мг, 1,00 ммоль), приготовленный в эталонном примере 80, использовали вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида. 1H-ЯМР (CDCl3, 400 МГц) δ 8,95 (д, 1Н), 8,32 (д, 1Н), 7,42 (т, 1Н), 7,32-7,22 (м, 1Н), 6,46 (д, 1Н), 5,50-5,30 (м, 1Н), 5,10-4,90 (м, 1Н), 4,30-3,74 (м, 3Н), 3,74-3,35 (м, 2Н), 3,15-2,85 (м, 2Н), 2,80-2,58 (м, 4Н), 2,58-2,20 (м, 2Н), 2,00-1,85 (м, 1Н)
[1879] Пример 176. (2S,4S)-4-фтор-1-[2-[(3R)-3-[(6-метокси-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1880] Указанное в заголовке соединение (132,2 мг, 26,7%) получали таким же образом, как и в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида использовали (R)-6-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (393,7 мг, 1,25 ммоль), полученный в эталонном примере 81. 1H-ЯМР (CDCl3, 400 МГц) δ 8,76 (д, 1Н), 8,39 (д, 1Н), 7,79 (д, 1Н), 7,46 (д, 1Н), 7,33 (т, 1Н), 5,50-5,24 (м, 1Н), 5,24-4,90 (м, 1Н), 4,25-4,00 (м, 2Н), 3,96 (с, 3Н), 3,96-3,70 (м, 1Н), 3,70-3,30 (м, 2Н), 3,10-3,00 (м, 1Н), 3,00-2,82 (м, 1Н), 2,80-2,32 (м, 4Н), 2,32-1,95 (м, 2Н), 1,90-1,78 (м, 1Н)
[1881] Пример 177. (2S,4S)-4-фтор-1-[2-[(3R)-3-[(7-метокси-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1882] Указанное в заголовке соединение (107,8 мг, 20,2%) получали таким же образом, как в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида использовали (R)-7-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (424,4 мг, 1,34 ммоль), полученный в эталонном примере 82. 1H-ЯМР (CDCl3, 400 МГц) δ 8,78 (д, 1Н), 8,14 (д, 1Н), 7,19 (т, 1Н), 6,86 (с, 1Н), 6,21 (с, 1Н), 5,50-5,28 (м, 1Н), 5,12-4,92 (м, 1Н), 4,28-3,95 (м, 2Н), 3,93 (с, 3Н), 3,90-3,62 (м, 1Н), 3,50-3,33 (м, 2Н), 3,10-2,90 (м, 2Н), 2,80-2,42 (м, 4Н), 2,42-2,20 (м, 2Н), 2,00-1,85 (м, 1Н)
[1883] Пример 178. (2S,4S)-4-фтор-1-[2-[(3R)-3-[(8-метокси-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1884] Указанное в заголовке соединение (11,1 мг, 5,3%) получали таким же образом, как ив примере 171, за исключением того, что (R)-8-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (165,7 мг, 0,52 ммоль), приготовленный в эталонном примере 83, использовали вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида. 1H-ЯМР (CDCl3, 400 МГц) δ 8,94 (д, 1Н), 8,27 (д, 1Н), 7,43 (т, 1Н), 6,96 (д, 1Н), 6,54 (д, 1Н), 5,49-5,28 (м, 1Н), 5,19-4,92 (м, 1Н), 4,28-4,10 (м, 2Н), 4,06 (с, 3Н), 4,00-3,80 (м, 1Н), 3,78-3,33 (м, 2Н), 3,10-3,00 (м, 2Н), 3,00-2,96 (м, 1Н), 2,96-2,60 (м, 3Н), 2,60-2,30 (м, 2Н), 1,95-1,85 (м, 1Н)
[1885] Пример 179. (2S,4S)-4-фтор-1-[2-[(3R)-3-[(3-метил-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1886] Указанное в заголовке соединение (258,9 мг, 70,7%) получали таким же образом, как и в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида использовали (R)-3-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (288,2 мг, 0,96 ммоль), полученный в эталонном примере 84. 1H-ЯМР (CDCl3, 400 МГц) δ 8,72 (д, 1Н), 8,06 (с, 1Н), 7,50-7,42 (м, 2Н), 6,54 (д, 1Н), 5,48-5,28 (м, 1Н), 5,15-4,98 (м, 1Н), 4,30-3,62 (м, 3Н), 3,60-3,32 (м, 2Н), 3,12-3,00 (м, 2Н), 3,00-2,90 (м, 1Н), 2,80-2,60 (м, 2Н), 2,53 (с, 3Н), 2,53-2,40 (м, 1Н), 2,40-2,18 (м, 2Н), 2,00-1,85 (м, 1Н)
[1887] Пример 180. (2S,4S)-4-фтор-1-[2-[(3R)-3-[(6-метил-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1888] Указанное в заголовке соединение (206,3 мг, 42,3%) получали таким же образом, как и в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорид использовали (R)-6-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (384,3 мг, 1,28 ммоль), полученный в эталонном примере 85. 1H-ЯМР (CDCl3, 400 МГц) δ 8,82 (д, 1Н), 8,43 (д, 1Н), 7,70 (д, 1Н), 7,50 (д, 1Н), 7,37 (т, 1Н), 5,50-5,28 (м, 1Н), 5,20-4,90 (м, 1Н), 4,20-4,00 (м, 2Н), 4,00-3,70 (м, 2Н), 3,54-3,28 (м, 2Н), 3,20-3,00 (м, 1Н), 2,90-2,64 (м, 2Н), 2,64-2,50 (м, 2Н), 2,46 (с, 3Н), 2,46-2,15 (м, 2Н), 1,98-1,80 (м, 1Н)
[1889] Пример 181. (2S,4S)-4-фтор-1-[2-[(3R)-3-[(8-метил-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1890] Указанное в заголовке соединение (106,3 мг, 31,5%) получали таким же образом, как и в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорид использовали (R)-8-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (266,3 мг, 0,89 ммоль), полученный в эталонном примере 86. 1H-ЯМР (CDCl3, 400 МГц) δ 8,93 (д, 1Н), 8,25 (д, 1Н), 7,42-7,33 (м, 2Н), 6,51 (д, 1Н), 5,49-5,28 (м, 1Н), 5,18-4,90 (м, 1Н), 4,30-4,00 (м, 2Н), 4,00-3,64 (м, 2Н), 3,60-3,34 (м, 2Н), 3,10-3,00 (м, 2Н), 3,00-2,90 (м, 1Н), 2,80-2,69 (м, 1Н), 2,69 (с, 3Н), 2,69-2,18 (м, 3Н), 1,98-1,85 (м, 1Н)
[1891] Пример 182. (2S,4S)-4-фтор-1-[2-[(3R)-3-[[7-(трифторметил)-5-хинолил]амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1892] Указанное в заголовке соединение (184,3 мг, 38,0%) получали таким же образом, как и в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида использовали (R)-N-(пирролидин-3-ил)-7-(трифторметил)хинолин-5-амина гидрохлорид (393,9 мг, 1,11 ммоль), полученный в эталонном примере 87. 1H-ЯМР (CDCl3, 400 МГц) δ 8,95 (д, 1Н), 8,40 (д, 1Н), 7,74 (с, 1Н), 7,44 (т, 1Н), 6,64 (с, 1Н), 5,78-5,40 (м, 1Н), 5,03-4,97 (м, 1Н), 4,38-4,20 (м, 1Н), 4,10-3,74 (м, 2Н), 3,70-3,35 (м, 2Н), 3,22-2,85 (м, 3Н), 2,82-2,42 (м, 3Н), 2,42-2,22 (м, 2Н), 2,05-1,88 (м, 1Н)
[1893] Пример 183. (2S,4S)-4-фтор-1-[2-[(3R)-3-[[8-(трифторметил)-5-хинолил]амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1894] Указанное в заголовке соединение (116,0 мг, 54,4%) получали таким же образом, как и в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида использовали (R)-N-(пирролидин-3-ил)-8-(трифторметил)хинолин-5-амина гидрохлорид (173,2 мг, 0,49 ммоль), полученный в эталонном примере 88. 1H-ЯМР (CDCl3, 400 МГц) δ 9,01 (д, 1Н), 8,41 (д, 1Н), 7,90 (д, 1Н), 7,41 (т, 1Н), 6,49 (д, 1Н), 5,52-5,28 (м, 1Н), 5,05-4,93 (м, 1Н), 4,38-4,20 (м, 1Н), 4,10-3,94 (м, 1Н), 3,94-3,70 (м, 1Н), 3,70-3,35 (м, 2Н), 3,25-2,95 (м, 3Н), 2,95-2,55 (м, 3Н), 2,55-2,22 (м, 2Н), 2,05-1,85 (м, 1Н)
[1895] Пример 184. (2S,4S)-4-фтор-1-[2-[(3R)-3-[(3-фтор-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1896] Указанное в заголовке соединение (255,8 мг, 87,5%) получали таким же образом, как и в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида использовали (R)-3-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (230,9 мг, 0,76 ммоль), полученный в эталонном примере 89. 1H-ЯМР (CDCl3, 400 МГц) δ 8,77 (с, 1Н), 7,99 (д, 1Н), 7,52-7,49 (м, 2Н), 6,61 (д, 1Н), 5,54-5,28 (м, 1Н), 5,10-4,95 (м, 1Н), 4,30-4,14 (м, 1Н), 4,10-3,94 (м, 1Н), 3,94-3,65 (м, 1Н), 3,65-3,37 (м, 2Н), 3,18-2,88 (м, 3Н), 2,85-2,58 (м, 2Н), 2,55-2,20 (м, 3Н), 2,00-1,95 (м, 1Н)
[1897] Пример 185. (2S,4S)-4-фтор-1-[2-[(3R)-3-[(3-хлор-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1898] Указанное в заголовке соединение (27,4 мг, 7,4%) получали таким же образом, как и в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида использовали (R)-3-хлор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (295,0 мг, 0,92 ммоль), полученный в эталонном примере 90. 1H-ЯМР (CDCl3, 400 МГц) δ 8,78 (с, 1Н), 8,36 (с, 1Н), 7,54 (т, 1Н), 7,45 (д, 1Н), 6,61 (д, 1Н), 5,54-5,25 (м, 1Н), 5,10-4,95 (м, 1Н), 4,30-4,15 (м, 1Н), 4,10-3,84 (м, 1Н), 3,84-3,65 (м, 1Н), 3,65-3,40 (м, 2Н), 3,20-2,90 (м, 3Н), 2,84-2,40 (м, 3Н), 2,40-2,20 (м, 2Н), 2,00-1,86 (м, 1Н)
[1899] Пример 186. (2S,4S)-4-фтор-1-[2-[(3R)-3-[[8-(трифторметокси)-5-хинолил]амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1900] Указанное в заголовке соединение (200,3 мг, 37,5%) получали таким же образом, как и в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида использовали (R)-N-(пирролидин-3-ил)-8-(трифторметокси)хинолин-5-амина гидрохлорид (438,0 мг, 1,18 ммоль), полученный в эталонном примере 91. 1H-ЯМР (CDCl3, 400 МГц) δ 9,00 (д, 1Н), 8,35 (д, 1Н), 7,50-7,41 (м, 2Н), 6,48 (д, 1Н), 5,52-5,24 (м, 1Н), 5,10-4,92 (м, 1Н), 4,30-4,15 (м, 1Н), 4,15-3,98 (м, 1Н), 3,98-3,70 (м, 1Н), 3,70-3,38 (м, 2Н), 3,20-2,88 (м, 3Н), 2,84-2,40 (м, 3Н), 2,40-2,20 (м, 2Н), 2,00-1,85 (м, 1Н)
[1901] Пример 187. (2S,4S)-4-фтор-1-[2-[(3R)-3-[(6-метил-4-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1902] Указанное в заголовке соединение (3,7 мг, 6,7%) получали таким же образом, как и в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида использовали (R)-6-метил-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид (43,2 мг, 0,14 ммоль), полученный в эталонном примере 92. 1H-ЯМР (CDCl3, 400 МГц) δ 8,27-8,23 (м, 3Н), 7,57 (д, 1Н), 6,43 (д, 1Н), 5,60-5,40 (м, 1Н), 5,14-5,06 (м, 1Н), 4,30-4,20 (м, 1Н), 4,05-3,90 (м, 1Н), 3,90-3,80 (м, 1Н), 3,80-3,60 (м, 2Н), 3,54-3,45 (м, 1Н), 3,32-3,05 (м, 3Н), 3,05-2,70 (м, 2Н), 2,59 (с, 3Н), 2,59-2,38 (м, 1Н), 2,28-2,16 (м, 1Н), 2,08-1,98 (м, 1Н)
[1903] Пример 188. (2S,4S)-4-фтор-1-[2-[(3R)-3-[(6-метокси-4-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1904] Указанное в заголовке соединение (37,8 мг, 10,0%) получали аналогично тому, как описано в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида использовали (R)-6-метокси-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид (301,1 мг, 0,95 ммоль), полученный в эталонном примере 93. 1H-ЯМР (CDCl3, 400 МГц) δ 8,19 (д, 1Н), 8,13 (д, 1Н), 7,48 (с, 1Н), 7,30-7,20 (м, 1Н), 6,39 (д, 1Н), 5,58-5,40 (м, 1Н), 5,20-5,10 (м, 1Н), 4,34-4,20 (м, 1Н), 4,06 (с, 3Н), 4,00-3,88 (м, 1Н), 3,88-3,70 (м, 1Н), 3,70-3,60 (м, 2Н), 3,49-3,40 (м, 1Н), 3,38-3,00 (м, 3Н), 3,00-2,84 (м, 1Н), 2,84-2,72 (м, 1Н), 2,72-2,30 (м, 1Н), 2,30-2,10 (м, 1Н), 2,10-1,95 (м, 1Н)
[1905] Пример 189. (2S,4S)-4-фтор-1-[2-[(3R)-3-[(8-хлор-4-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1906] Указанное в заголовке соединение (60,4 мг, 41,1%) получали таким же образом, как и в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида использовали (R)-8-хлор-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид (117,0 мг, 0,37 ммоль), полученный в эталонном примере 94. 1H-ЯМР (CDCl3, 400 МГц) δ 8,55 (д, 1Н), 7,48-7,41 (м, 3Н), 6,67 (д, 1Н), 5,54-5,38 (м, 1Н), 5,30-4,88 (м, 1Н), 4,30-4,18 (м, 1Н), 4,18-3,90 (м, 1Н), 3,90-3,70 (м, 1Н), 3,50-3,30 (м, 2Н), 3,20-3,00 (м, 1Н), 3,00-2,85 (м, 1Н), 2,85-2,58 (м, 3Н), 2,58-2,30 (м, 2Н), 2,30-2,10 (м, 1Н), 2,00-1,86 (м, 1Н)
[1907] Пример 190. (2S,4S)-4-фтор-1-[2-[(3R)-3-[(8-метил-4-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1908] Указанное в заголовке соединение (140,6 мг, 27,3%) получали таким же образом, как и в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида использовали (R)-8-метил-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид (406,2 мг, 1,35 ммоль), полученный в эталонном примере 95. 1H-ЯМР (CDCl3, 400 МГц) δ 8,61 (д, 1Н), 7,74 (д, 1Н), 7,50 (д, 1Н), 7,35 (т, 1Н), 6,41 (д, 1Н), 5,50-5,30 (м, 1Н), 5,10-4,90 (м, 1Н), 4,34-4,18 (м, 1Н), 4,18-3,82 (м, 1Н), 3,82-3,60 (м, 1Н), 3,60-3,40 (м, 2Н), 3,18-2,94 (м, 3Н), 2,77 (с, 3Н), 2,77-2,42 (м, 3Н), 2,42-2,18 (м, 2Н), 2,00-1,8 8 (м, 1Н)
[1909] Пример 191. (2S,4S)-4-фтор-1-[2-[(3R)-3-[(6-фтор-4-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1910] Указанное в заголовке соединение (65,2 мг, 15,2%) получали таким же образом, как и в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида использовали (R)-6-фтор-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид (337,7 мг, 1,11 ммоль), полученный в эталонном примере 96. 1H-ЯМР (CDCl3, 400 МГц) δ 8,51 (с, 1Н), 7,96 (д, 1Н), 7,66 (д, 1Н), 7,40 (д, 1Н), 6,40 (д, 1Н), 5,52-5,30 (м, 1Н), 5,05-4,95 (м, 1Н), 4,34-4,18 (м, 1Н), 4,10-3,94 (м, 1Н), 3,94-3,74 (м, 1Н), 3,70-3,40 (м, 2Н), 3,25-3,10 (м, 1Н), 3,10-2,95 (м, 2Н), 2,85-2,60 (м, 2Н), 2,52-2,24 (м, 3Н), 2,00-1,90 (м, 1Н)
[1911] Пример 192. (2S,4S)-4-фтор-1-[2-[(3R)-3-[(6-хлор-4-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1912] Указанное в заголовке соединение (109,4 мг, 31,7%) получали таким же образом, как и в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида использовали (R)-6-хлор-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид (274,8 мг, 0,86 ммоль), полученный в эталонном примере 97. 1H-ЯМР (CDCl3, 400 МГц) δ 8,51 (д, 1Н), 8,07 (с, 1Н), 7,90 (д, 1Н), 7,55 (д, 1Н), 6,38 (д, 1Н), 5,55-5,30 (м, 1Н), 5,08-4,95 (м, 1Н), 4,30-4,15 (м, 1Н), 4,08-3,70 (м, 1Н), 3,70-3,40 (м, 2Н), 3,30-3,20 (м, 1Н), 3,15-3,00 (м, 2Н), 2,85-2,65 (м, 2Н), 2,52-2,20 (м, 3Н), 2,00-1,90 (м, 1Н)
[1913] Пример 193. (2S,4S)-4-фтор-1-[2-[(3R)-3-[(7-метокси-4-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1914] Указанное в заголовке соединение (159,2 мг, 35,4%) получали таким же образом, как описано в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида использовали (R)-7-метокси-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид (358,2 мг, 1,13 ммоль), полученный в эталонном примере 98. 1H-ЯМР (CDCl3, 400 МГц) δ 8,47 (д, 1Н), 7,81 (д, 1Н), 7,33 (с, 1Н), 7,11 (д, 1Н), 6,31 (д, 1Н), 5,50-5,30 (м, 1Н), 5,10-4,94 (м, 1Н), 4,35-4,20 (м, 1Н), 4,10-3,94 (м, 1Н), 3,94 (с, 3Н), 3,94-3,66 (м, 2Н), 3,66-3,40 (м, 2Н), 3,15-2,90 (м, 2Н), 2,80-2,40 (м, 2Н), 2,40-2,20 (м, 3Н), 2,00-1,85 (м, 1Н)
[1915] Пример 194. (2S,4S)-4-фтор-1-[2-[(3R)-3-[(8-фтор-4-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1916] Указанное в заголовке соединение (29,9 мг, 5,7%) получали таким же образом, как и в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида использовали (R)-8-фтор-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид (418,0 мг, 1,37 ммоль), полученный в эталонном примере 99. 1H-ЯМР (MeOD, 400 МГц) δ 8,41 (д, 1Н), 8,03 (д, 1Н), 7,44-7,39 (м, 2Н), 6,62 (д, 1Н), 5,55-5,30 (м, 1Н), 5,05-4,96 (м, 1Н), 4,40-4,30 (м, 1Н), 4,10-4,00 (м, 1Н), 3,90-3,70 (м, 1Н), 3,65-3,40 (м, 2Н), 3,16-3,00 (м, 3Н), 2,75-2,60 (м, 2Н), 2,60-2,35 (м, 3Н), 2,05-1,90 (м, 1Н)
[1917] Пример 195. (2S,4S)-4-фтор-1-[2-[(3R)-3-[(8-метокси-4-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1918] Указанное в заголовке соединение (13,2 мг, 3,3%) получали таким же образом, как ив примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида использовали (R)-8-метокси-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид (316,4 мг, 1,00 ммоль), полученный в эталонном примере 100. 1H-ЯМР (CDCl3, 400 МГц) δ 8,57 (д, 1Н), 7,67 (д, 1Н), 7,41 (т, 1Н), 7,05 (д, 1Н), 6,44 (д, 1Н), 5,55-5,30 (м, 1Н), 5,20-5,00 (м, 1Н), 4,35-4,20 (м, 1Н), 4,07 (с, 3Н), 4,07-3,90 (м, 1Н), 3,90-3,70 (м, 1Н), 3,70-3,45 (м, 2Н), 3,25-3,15 (м, 1Н), 3,15-2,90 (м, 3Н), 2,84-2,50 (м, 2Н), 2,50-2,25 (м, 2Н), 2,06-1,90 (м, 1Н)
[1919] Пример 196. (2S,4S)-4-фтор-1-[2-[(3R)-3-[[8-(трифторметил)-4-хинолил]амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
Указанное в заголовке соединение (30,8 мг, 5,0%) получали таким же образом, как и в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида использовали (R)-N-(пирролидин-3-ил)-8-(трифторметил)хинолин-4-амина гидрохлорид (499,4 мг, 1,41 ммоль), полученный в эталонном примере 101. 1H-ЯМР (CDCl3, 400 МГц) δ 8,64 (д, 1Н), 8,22 (д, 1Н), 7,97 (д, 1Н), 7,44 (т, 1Н), 6,43 (д, 1Н), 5,52-5,28 (м, 1Н), 5,00-4,90 (м, 1Н), 4,30-4,15 (м, 1Н), 4,04-3,84 (м, 1Н), 3,80-3,60 (м, 1Н), 3,60-3,35 (м, 2Н), 3,20-2,85 (м, 3Н), 2,80-2,40 (м, 3Н), 2,40-2,30 (м, 1Н), 2,30-2,20 (м, 1Н), 2,00-1,85 (м, 1Н)
[1920] Пример 197. (2S)-1-[2-[(3R)-3-[(7-фтор-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1921] Указанное в заголовке соединение (207,1 мг, 90,3%) получали таким же образом, как и в примере 17, за исключением того, что вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (R)-7-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (189,8 мг, 0,62 ммоль), полученный в эталонном примере 79. 1H-ЯМР (CDCl3, 400 МГц) δ 8,81 (д, 1Н), 8,33 (д, 1Н), 7,27 (т, 1Н), 7,04 (с, 1Н), 6,31 (с, 1Н), 5,95-5,50 (м, 1Н), 4,85-4,75 (м, 1Н), 4,24-4,08 (м, 1Н), 3,70-3,55 (м, 2Н), 3,55-3,30 (м, 2Н), 3,20-2,80 (м, 3Н), 2,75-2,50 (м, 1Н), 2,50-2,20 (м, 4Н), 2,20-2,00 (м, 2Н), 2,00-1,85 (м, 1Н)
[1922] Пример 198. (2S)-1-[2-[(3R)-3-[(7-метокси-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1923] Указанное в заголовке соединение (287,5 мг, 59,0%) получали таким же образом, как и в примере 17, за исключением того, что вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (R)-7-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (406,4 мг, 1,29 ммоль), полученный в эталонном примере 82. 1H-ЯМР (CDCl3, 400 МГц) δ 8,76 (д, 1Н), 8,20 (д, 1Н), 7,18 (т, 1Н), 6,84 (с, 1Н), 6,20 (с, 1Н), 5,35-5,10 (м, 1Н), 4,90-4,70 (м, 1Н), 4,25-4,10 (м, 1Н), 3,92 (с, 3Н), 3,70-3,60 (м, 1Н), 3,60-3,30 (м, 3Н), 3,15-2,85 (м, 3Н), 2,70-2,40 (м, 1Н), 2,40-2,20 (м, 2Н), 2,20-2,00 (м, 2Н), 2,00-1,85 (м, 1Н)
[1924] Пример 199. (2S)-1-[2-[(3R)-3-[(8-фтор-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1925] Указанное в заголовке соединение (91,5 мг, 23,6%) получали таким же образом, как и в примере 17, за исключением того, что вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (R)-8-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (320,6 мг, 1,05 ммоль), полученный в эталонном примере 80. 1H-ЯМР (CDCl3, 400 МГц) δ 8,93 (д, 1Н), 8,36 (д, 1Н), 7,42 (д, 1Н), 7,29-7,24 (м, 1Н), 6,44 (с, 1Н), 5,18-4,90 (м, 1Н), 4,90-4,70 (м, 1Н), 4,30-4,10 (м, 1Н), 3,70-3,60 (м, 1Н), 3,60-3,30 (м, 3Н), 3,20-2,80 (м, 3Н), 2,75-2,50 (м, 1Н), 2,50-2,10 (м, 4Н), 2,00-1,80 (м, 1Н)
[1926] Пример 200. (2S)-1-[2-[(3R)-3-[(8-метил-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1927] Указанное в заголовке соединение (172,5 мг, 51,9%) получали таким же образом, как и в примере 17, за исключением того, что вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (R)-8-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (275,0 мг, 0,92 ммоль), полученный в эталонном примере 86. 1H-ЯМР (CDCl3, 400 МГц) δ 8,92 (д, 1Н), 8,31 (д, 1Н), 7,40 (д, 1Н), 7,35 (т, 1Н), 6,51 (д, 1Н), 4,95-4,74 (м, 1Н), 4,30-4,15 (м, 1Н), 3,70-3,60 (м, 1Н), 3,60-3,35 (м, 3Н), 3,15-2,85 (м, 3Н), 2,68 (с, 3Н), 2,68-2,40 (м, 2Н), 2,40-2,30 (м, 1Н), 2,30-2,20 (м, 1Н), 2,20-2,00 (м, 2Н), 2,00-1,80 (м, 1Н)
[1928] Пример 201. (2S)-1-[2-[(3R)-3-[[8-(трифторметил)-5-хинолил]амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1929] Указанное в заголовке соединение (118,4 мг, 62,7%) получали таким же образом, как и в примере 17, за исключением того, что вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (R)-N-(пирролидин-3-ил)-8-(трифторметил)хинолин-5-амина гидрохлорид (160,5 мг, 0,45 ммоль), полученный в эталонном примере 88. 1H-ЯМР (CDCl3, 400 МГц) δ 9,00 (д, 1Н), 8,48 (д, 1Н), 7,88 (д, 1Н), 7,42 (т, 1Н), 6,47 (д, 1Н), 6,30-5,70 (м, 1Н), 4,85-4,75 (м, 1Н), 4,30-4,15 (м, 1Н), 3,70-3,60 (м, 1Н), 3,60-3,30 (м, 3Н), 3,28-3,15 (м, 1Н), 3,15-2,80 (м, 2Н), 2,80-2,50 (м, 1Н), 2,50-2,10 (м, 4Н), 2,10-1,85 (м, 1Н)
[1930] Пример 202. (2S)-1-[2-[(3R)-3-[[8-(трифторметокси)-5-хинолил]амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1931] Указанное в заголовке соединение (97,5 мг, 17,9%) получали таким же образом, как и в примере 17, за исключением того, что вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (R)-N-(пирролидин-3-ил)-8-(трифторметокси)хинолин-5-амина гидрохлорид (464,2 мг, 1,25 ммоль), полученный в эталонном примере 91. 1H-ЯМР (CDCl3, 400 МГц) δ 8,98 (д, 1Н), 8,42 (д, 1Н), 7,49 (д, 1Н), 7,43 (т, 1Н), 6,45 (д, 1Н), 5,70-5,30 (м, 1Н), 4,85-4,75 (м, 1Н), 4,30-4,15 (м, 1Н), 3,70-3,56 (м, 1Н), 3,56-3,30 (м, 3Н), 3,20-3,00 (м, 3Н), 2,90-2,70 (м, 1Н), 2,60-2,40 (м, 1Н), 2,40-2,08 (м, 3Н), 2,05-1,88 (м, 1Н)
[1932] Пример 203. (2S)-1-[2-[(3R)-3-[(3-хлор-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1933] Указанное в заголовке соединение (265,9 мг, 76,4%) получали таким же образом, как и в примере 17, за исключением того, что вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (R)-3-хлор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (290,8 мг, 0,91 ммоль), полученный в эталонном примере 90. 1H-ЯМР (CDCl3, 400 МГц) δ 8,75 (д, 1Н), 8,43 (с, 1Н), 7,53 (д, 1Н), 7,43 (т, 1Н), 6,59 (с, 1Н), 5,60-5,20 (м, 1Н), 4,85-4,75 (м, 1Н), 4,30-4,15 (м, 1Н), 3,70-3,60 (м, 1Н), 3,60-3,30 (м, 3Н), 3,20-3,10 (м, 1Н), 3,10-2,95 (м, 2Н), 2,80-2,50 (м, 1Н), 2,50-2,20 (м, 3Н), 2,20-2,00 (м, 1Н), 2,00-1,85 (м, 1Н)
[1934] Пример 204. (2S)-1-[2-[(3R)-3-[(3-метокси-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1935] Указанное в заголовке соединение (338,5 мг, 92,4%) получали таким же образом, как и в примере 17, за исключением того, что вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (R)-3-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (305,2 мг, 0,97 ммоль), полученный в эталонном примере 102. 1H-ЯМР (CDCl3, 400 МГц) δ 8,62 (д, 1Н), 7,65 (с, 1Н), 7,42-7,38 (м, 2Н), 6,57 (д, 1Н), 5,55-5,10 (м, 1Н), 4,85-4,70 (м, 1Н), 4,30-4,15 (м, 1Н), 4,01 (с, 3Н), 3,65-3,55 (м, 1Н), 3,55-3,40 (м, 3Н), 3,35-3,15 (м, 1Н), 3,10-2,95 (м, 2Н), 2,85-2,60 (м, 1Н), 2,40-2,20 (м, 2Н), 2,20-2,05 (м, 2Н), 2,05-1,85 (м, 1Н)
[1936] Пример 205. (2S,4S)-4-фтор-1-[2-[(3R)-3-[(3-метокси-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1937] Указанное в заголовке соединение (349,0 мг, 91,0%) получали таким же образом, как и в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида использовали (R)-3-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (305,2 мг, 0,97 ммоль), полученный в эталонном примере 102. 1H-ЯМР (CDCl3, 400 МГц) δ 8,65 (д, 1Н), 7,59 (с, 1Н), 7,46-7,38 (м, 2Н), 6,59 (д, 1Н), 5,55-5,25 (м, 1Н), 5,10-4,90 (м, 1Н), 4,35-4,20 (м, 1Н), 4,02 (с, 3Н), 4,00-3,80 (м, 3Н), 3,80-3,60 (м, 1Н), 3,60-3,35 (м, 2Н), 3,25-3,00 (м, 2Н), 2,90-2,60 (м, 2Н), 2,60-2,20 (м, 2Н), 2,05-1,90 (м, 1Н)
[1938] Пример 206. (2S)-1-[2-[(3R)-3-[(2-хлор-6-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1939] Указанное в заголовке соединение (61,1 мг, 20,3%) получали таким же образом, как в примере 17, за исключением того, что вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (R)-2-хлор-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид (251,8 мг, 0,79 ммоль), полученный в эталонном примере 103. 1H-ЯМР (CDCl3, 400 МГц) δ 7,86 (д, 1Н), 7,78 (д, 1Н), 7,27-7,23 (м, 1Н), 7,09 (д, 1Н), 6,64 (с, 1Н), 4,90-4,75 (м, 1Н), 4,20-4,10 (м, 1Н), 3,75-3,60 (м, 1Н), 3,60-3,30 (м, 3Н), 3,10-3,00 (м, 2Н), 2,90-2,65 (м, 2Н), 2,60-2,20 (м, 3Н), 2,20-2,10 (м, 2Н), 1,88-1,78 (м, 1Н)
[1940] Пример 207. (2S,4S)-4-фтор-1-[2-[(3R)-3-[(2-хлор-6-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1941] Указанное в заголовке соединение (54,3 мг, 17,2%) получали таким же образом, как описано в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида использовали (R)-2-хлор-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид (251,8 мг, 0,79 ммоль), полученный в эталонном примере 103. 1H-ЯМР (CDCl3, 400 МГц) δ 7,86 (д, 1Н), 7,79 (д, 1Н), 7,27-7,23 (м, 1Н), 7,09 (д, 1Н), 6,64 (с, 1Н), 5,54-5,30 (м, 1Н), 5,10-4,90 (м, 1Н), 4,22-4,04 (м, 1Н), 4,00-3,70(м, 1Н), 3,60-3,30 (м, 3Н), 3,10-2,90 (м, 2Н), 2,90-2,58 (м, 3Н), 2,55-2,20 (м, 3Н), 1,90-1,75 (м, 1Н)
[1942] Пример 208. (2S)-1-[2-[(3R)-3-[(3-метил-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1943] Указанное в заголовке соединение (4,3 мг, 4,0%) получали таким же образом, как и в примере 17, за исключением того, что вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (R)-3-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (89,8 мг, 0,30 ммоль), полученный в эталонном примере 84. 1H-ЯМР (CDCl3, 400 МГц) δ 8,73 (с, 1Н), 8,10 (с, 1Н), 7,50-7,42 (м, 2Н), 6,56 (д, 1Н), 5,25-4,90 (м, 1Н), 4,90-4,75 (м, 1Н), 4,30-4,15 (м, 1Н), 3,74-3,60(м, 1Н), 3,60-3,38 (м, 3Н), 3,20-2,90 (м, 3Н), 2,75-2,60 (м, 1Н), 2,72 (с, 3Н), 2,40-2,26 (м, 2Н), 2,26-2,00 (м, 2Н), 2,00-1,85 (м, 1Н)
[1944] Пример 209. (2S)-1-[2-[(3R)-3-[(3-фтор-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1945] Указанное в заголовке соединение (73,0 мг, 66,5%) получали таким же образом, как и в примере 17, за исключением того, что вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (R)-3-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (120,5 мг, 0,40 ммоль), полученный в эталонном примере 89. 1H-ЯМР (CDCl3, 400 МГц) δ 8,77 (с, 1Н), 8,04 (д, 1Н), 7,52-7,46 (м, 2Н), 6,62 (д, 1Н), 5,30-5,05 (м, 1Н), 4,88-4,78 (м, 1Н), 4,30-4,15 (м, 1Н), 3,74-3,60(м, 1Н), 3,60-3,30 (м, 3Н), 3,20-2,85 (м, 3Н), 2,80-2,50 (м, 1Н), 2,40-2,24 (м, 2Н), 2,24-2,10 (м, 2Н), 2,00-1,85 (м, 1Н)
[1946] Пример 210. (2S,4S)-4-фтор-1-[2-[(3R)-3-[[2-(трифторметил)-6-хинолил]амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1947] Указанное в заголовке соединение (84,0 мг, 18,0%) получали таким же образом, как и в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида использовали (R)-N-(пирролидин-3-ил)-2-(трифторметил)хинолин-6-амина гидрохлорид (379,0 мг, 1,07 ммоль), полученный в эталонном примере 104. 1H-ЯМР (CDCl3, 400 МГц) δ 8,03 (д, 1Н), 7,96 (д, 1Н), 7,58 (д, 1Н), 7,16 (д, 1Н), 6,66 (с, 1Н), 5,52-5,30 (м, 1Н), 5,10-4,90 (м, 1Н), 4,30-4,10 (м, 1Н), 4,10-3,65(м, 3Н), 3,65-3,34 (м, 2Н), 3,12-3,00 (м, 2Н), 3,00-2,80 (м, 1Н), 2,80-2,58 (м, 2Н), 2,54-2,20 (м, 2Н), 1,98-1,80 (м, 1Н)
[1948] Пример 211. (25,45)-4-фтор-1-[2-[(3R)-3-[(3-метил-6-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1949] Указанное в заголовке соединение (98,8 мг, 25,9%) получали таким же образом, как описано в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида использовали (R)-3-метил-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид (300,8 мг, 1,00 ммоль), полученный в эталонном примере 105. 1H-ЯМР (CDCl3, 400 МГц) δ 8,47 (с, 1Н), 7,82 (д, 1Н), 7,68 (с, 1Н), 7,00 (д, 1Н), 6,59 (с, 1Н), 5,50-5,25 (м, 1Н), 5,15-4,90 (м, 1Н), 4,40-4,15 (м, 1Н), 4,15-3,70(м, 3Н), 3,54-3,30 (м, 2Н), 3,05-2,94 (м, 2Н), 2,94-2,60 (м, 3Н), 2,45 (с, 3Н), 2,45-2,20 (м, 2Н), 1,90-1,75 (м, 1Н)
[1950] Пример 212. (2S,4S)-4-фтор-1-[2-[(3R)-3-[(4-метокси-6-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1951] Указанное в заголовке соединение (44,8 мг, 16,2%) получали таким же образом, как и в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида использовали (R)-4-метокси-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид (220,7 мг, 0,70 ммоль), полученный в эталонном примере 106. 1H-ямр (CDCl3, 400 МГц) δ 8,50 (д, 1Н), 7,82 (д, 1Н), 7,08-7,03 (м, 2Н), 6,66 (д, 1Н), 5,50-5,30 (м, 1Н), 5,20-4,90 (м, 1Н), 4,30-4,18 (м, 1Н), 4,18-4,05(м, 1Н), 4,03 (с, 3Н), 4,03-3,70 (м, 2Н), 3,05-2,95 (м, 2Н), 2,95-2,80 (м, 2Н), 2,80-2,58 (м, 2Н), 2,55-2,20 (м, 3Н), 1,90-1,75 (м, 1Н)
[1952] Пример 213. (2S,4S)-4-фтор-1-[2-[(3R)-3-[(8-метил-6-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1953] Указанное в заголовке соединение (95,3 мг, 31,6%) получали таким же образом, как и в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида использовали (R)-8-метил-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид (237,2 мг, 0,79 ммоль), полученный в эталонном примере 107. 1H-ЯМР (CDCl3, 400 МГц) δ 8,65 (д, 1Н), 7,88 (д, 1Н), 7,29-7,24 (м, 1Н), 6,96 (с, 1Н), 6,52 (с, 1Н), 5,50-5,28 (м, 1Н), 5,20-4,90 (м, 1Н), 4,25-4,15 (м, 1Н), 4,15-3,70 (м, 3Н), 3,55-3,30 (м, 2Н), 3,05-2,95 (м, 2Н), 2,95-2,75 (м, 2Н), 2,72 (с, 3Н), 2,72-2,55 (м, 1Н), 2,50-2,20 (м, 2Н), 1,90-1,75 (м, 1Н)
[1954] Пример 214. (2S,4S)-4-фтор-1-[2-[(3R)-3-[(8-фтор-6-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1955] Указанное в заголовке соединение (220,7 мг, 59,3%) получали таким же образом, как и в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида использовали (R)-8-фтор-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид (294,2 мг, 0,97 ммоль), полученный в эталонном примере 110. 1H-ЯМР (CDCl3, 400 МГц) δ 8,63 (с, 1Н), 7,90 (д, 1Н), 7,32-7,27 (м, 1Н), 6,82 (д, 1Н), 6,45 (с, 1Н), 5,50-5,30 (м, 1Н), 5,14-4,90 (м, 1Н), 4,20-4,00 (м, 2Н), 4,00-3,65 (м, 2Н), 3,60-3,30 (м, 2Н), 3,10-2,90 (м, 2Н), 2,90-2,70 (м, 2Н), 2,70-2,50 (м, 1Н), 2,50-2,20 (м, 2Н), 1,90-1,70 (м, 1Н)
[1956] Пример 215. (2S,4S)-4-фтор-1-[2-[(3R)-3-[(8-хлор-6-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1957] Указанное в заголовке соединение (59,4 мг, 16,5%) получали таким же образом, как и в примере 171, за исключением того, что (R)-8-хлор-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид (287,6 мг, 0,90 ммоль), полученный в эталонном примере 108, использовали вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида. 1H-ЯМР (CDCl3, 400 МГц) δ 8,73 (с, 1Н), 7,92 (д, 1Н), 7,32 (т, 1Н), 7,27-7,25 (м, 1Н), 6,59 (с, 1Н), 5,52-5,28 (м, 1Н), 5,10-4,90 (м, 1Н), 4,25-4,00 (м, 2Н), 4,00-3,68 (м, 2Н), 3,60-3,30 (м, 2Н), 3,10-3,00 (м, 2Н), 2,95-2,55 (м, 3Н), 2,50-2,20 (м, 2Н), 1,90-1,70 (м, 1Н)
[1958] Пример 216. (2S,4S)-4-фтор-1-[2-[(3R)-3-[[8-(трифторметил)-6-хинолил]амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1959] Указанное в заголовке соединение (18,0 мг, 3,7%) получали таким же образом, как и в примере 171, за исключением того, что вместо (R)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорида использовали (R)-N-(пирролидин-3-ил)-8-(трифторметил)хинолин-6-амина гидрохлорид (394,2 мг, 1,11 ммоль), полученный в эталонном примере 109. 1H-ЯМР (CDCl3, 400 МГц) δ 8,77 (д, 1Н), 7,95 (д, 1Н), 7,46 (с, 1Н), 7,35 (т, 1Н), 6,79 (с, 1Н), 5,55-5,30 (м, 1Н), 5,10-4,90 (м, 1Н), 4,30-4,02 (м, 2Н), 4,02-3,65 (м, 2Н), 3,60-3,30 (м, 2Н), 3,12-2,98 (м, 2Н), 2,95-2,60 (м, 3Н), 2,55-2,20 (м, 2Н), 1,90-1,80 (м, 1Н)
[1960] Пример 217. (2S)-1-[2-[(3R)-3-[2-(трифторметил)-6-хинолил]амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1961] Указанное в заголовке соединение (17,6 мг, 4,6%) получали таким же образом, как и в примере 17, за исключением того, что вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (R)-N-(пирролидин-3-ил)-2-(трифторметил)хинолин-6-амина гидрохлорид (324,5 мг, 0,92 ммоль), полученный в эталонном примере 104. 1H-ЯМР (CDCl3, 400 МГц) δ 8,04 (д, 1Н), 7,96 (д, 1Н), 7,58 (д, 1Н), 7,17 (д, 1Н), 6,67 (с, 1Н), 4,90-4,75 (м, 1Н), 4,25-4,15 (м, 1Н), 3,75-3,60 (м, 1Н), 3,60-3,45 (м, 2Н), 3,45-3,30 (м, 2Н), 3,10-3,00 (м, 2Н), 2,95-2,55 (м, 2Н), 2,50-2,10 (м, 4Н), 1,95-1,80 (м, 1Н)
[1962] Пример 218. (2S)-1-[2-[(3R)-3-[(3-метил-6-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1963] Указанное в заголовке соединение (224,2 мг, 55,4%) получали аналогично тому, как описано в примере 17, за исключением того, что вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (R)-3-метил-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид (334,2 мг, 1,11 ммоль), полученный в эталонном примере 105. 1H-ЯМР (CDCl3, 400 МГц) δ 8,45 (с, 1Н), 7,82 (д, 1Н), 7,67 (с, 1Н), 7,01 (д, 1Н), 6,58 (с, 1Н), 4,95-4,70 (м, 1Н), 4,25-4,10 (м, 1Н), 3,75-3,40 (м, 3Н), 3,40-3,30 (м, 2Н), 3,10-2,95 (м, 2Н), 2,90-2,55 (м, 2Н), 2,44 (с, 3Н), 2,44-2,20 (м, 2Н), 2,20-1,90 (м, 2Н), 1,90-1,75 (м, 1Н)
[1964] Пример 219. (2S)-1-[2-[(3R)-3-[(4-метокси-6-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1965] Указанное в заголовке соединение (143,4 мг, 44,5%) получали таким же образом, как и в примере 17, за исключением того, что вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (R)-4-метокси-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид (268,8 мг, 0,85 ммоль), полученный в эталонном примере 106. 1H-ЯМР (CDCl3, 400 МГц) δ 8,48 (д, 1Н), 7,81 (д, 1Н), 7,07-7,02 (м, 2Н), 6,65 (д, 1Н), 4,95-4,75 (м, 1Н), 4,30-4,15 (м, 1Н), 4,02 (с, 3Н), 3,75-3,45 (м, 3Н), 3,45-3,30 (м, 2Н), 3,10-2,95 (м, 2Н), 2,90-2,50 (м, 2Н), 2,50-2,30 (м, 2Н), 2,30-2,00 (м, 2Н), 1,90-1,75 (м, 1Н)
[1966] Пример 220. (2S)-1-[2-[(3R)-3-[(8-метил-6-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1967] Указанное в заголовке соединение (200,6 мг, 97,0%) получали таким же образом, как и в примере 17, за исключением того, что вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (R)-8-метил-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид (170,8 мг, 0,57 ммоль), полученный в эталонном примере 107. 1H-ЯМР (CDCl3, 400 МГц) δ 8,64 (д, 1Н), 7,88 (д, 1Н), 7,26-7,24 (м, 1Н), 6,95 (с, 1Н), 6,52 (с, 1Н), 4,95-4,75 (м, 1Н), 4,25-4,10 (м, 1Н), 3,75-3,45 (м, 3Н), 3,45-3,30 (м, 2Н), 3,10-2,95 (м, 2Н), 2,90-2,80 (м, 1Н), 2,72 (с, 3Н), 2,70-2,50 (м, 1Н), 2,50-2,30 (м, 1Н), 2,30-2,10 (м, 3Н), 1,90-1,75 (м, 1Н)
[1968] Пример 221. (2S)-1-[2-[(3R)-3-[(8-фтор-6-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1969] Указанное в заголовке соединение (121,2 мг, 65,5%) получали таким же образом, как и в примере 17, за исключением того, что вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (R)-8-фтор-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид (153,3 мг, 0,50 ммоль), полученный в эталонном примере 110. 1H-ЯМР (CDCl3, 400 МГц) δ 8,62 (с, 1Н), 7,89 (д, 1Н), 7,29 (т, 1Н), 6,82 (д, 1Н), 6,45 (с, 1Н), 4,90-4,75 (м, 1Н), 4,25-4,05 (м, 1Н), 3,75-3,60 (м, 1Н), 3,60-3,44 (м, 2Н), 3,44-3,30 (м, 2Н), 3,10-2,95 (м, 2Н), 2,95-2,50 (м, 2Н), 2,50-2,10 (м, 4Н), 1,90-1,75 (м, 1Н)
[1970] Пример 222. (2S)-1-[2-[(3R)-3-[(8-хлор-6-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1971] Указанное в заголовке соединение (77,7 мг, 57,4%) получали таким же образом, как и в примере 17, за исключением того, что (R)-8-хлор-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид (112,9 мг, 0,35 ммоль), полученный в эталонном примере 108, использовали вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида. 1H-ЯМР (CDCl3, 400 МГц) δ 8,72 (д, 1Н), 7,91 (д, 1Н), 7,33-7,25 (м, 2Н), 6,58 (с, 1Н), 4,90-4,75 (м, 1Н), 4,20-4,10 (м, 1Н), 3,74-3,60 (м, 1Н), 3,60-3,42 (м, 2Н), 3,42-3,30 (м, 2Н), 3,10-2,95 (м, 2Н), 2,90-2,50 (м, 2Н), 2,50-2,20 (м, 2Н), 2,20-2,05 (м, 2Н), 1,90-1,75 (м, 1Н)
[1972] Пример 223. (2S)-1-[2-[(3R)-3-[(6-метил-4-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1973] Указанное в заголовке соединение (233,0 мг, 64,8%) получали таким же образом, как в примере 17, за исключением того, что вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (R)-6-метил-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид (297,2 мг, 0,99 ммоль), полученный в эталонном примере 92. 1H-ЯМР (CDCl3, 400 МГц) δ 8,43 (д, 1Н), 7,99 (д, 1Н), 7,91 (с, 1Н), 7,50 (д, 1Н), 6,38 (д, 1Н), 4,90-4,75 (м, 1Н), 4,35-4,20 (м, 1Н), 3,72-3,60 (м, 2Н), 3,60-3,40 (м, 3Н), 3,35-3,25 (м, 1Н), 3,20-2,98 (м, 2Н), 2,85-2,75 (м, 1Н), 2,57 (с, 3Н), 2,50-2,10 (м, 4Н), 2,10-1,90 (м, 1Н)
[1974] Пример 224. (2S)-1-[2-[(3R)-3-[(6-метокси-4-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1975] Указанное в заголовке соединение (340,7 мг, 73,1%) получали таким же образом, как и в примере 17, за исключением того, что вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (R)-6-метокси-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид (388,7 мг, 1,23 ммоль), полученный в эталонном примере 93. 1H-ЯМР (CDCl3, 400 МГц) δ 8,39 (д, 1Н), 7,99 (д, 1Н), 7,42 (с, 1Н), 7,32 (д, 1Н), 6,39 (д, 1Н), 4,85-4,75 (м, 1Н), 4,35-4,20 (м, 1Н), 4,04 (с, 3Н), 3,75-3,50 (м, 3Н), 3,50-3,30 (м, 2Н), 3,25-2,85 (м, 3Н), 2,85-2,60 (м, 1Н), 2,50-2,10 (м, 4Н), 2,10-1,90 (м, 1Н)
[1976] Пример 225. (2S)-1-[2-[(3R)-3-[(6-фтор-4-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1977] Указанное в заголовке соединение (267,8 мг, 64,0%) получали таким же образом, как и в примере 17, за исключением того, что вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (R)-6-фтор-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид (346,5 мг, 1,14 ммоль), полученный в эталонном примере 96. 1H-ЯМР (CDCl3, 400 МГц) δ 8,50 (д, 1Н), 7,95 (д, 1Н), 7,72 (д, 1Н), 7,38 (с, 1Н), 6,39 (д, 1Н), 4,90-4,75 (м, 1Н), 4,35-4,15 (м, 1Н), 3,75-3,60 (м, 1Н), 3,60-3,35 (м, 3Н), 3,25-3,15 (м, 1Н), 3,15-2,90 (м, 2Н), 2,80-2,60 (м, 1Н), 2,50-2,35 (м, 1Н), 2,35-2,10 (м, 4Н), 2,00-1,85 (м, 1Н)
[1978] Пример 226. (2S)-1-[2-[(3R)-3-[(6-хлор-4-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1979] Указанное в заголовке соединение (335,8 мг, 70,7%) получали таким же образом, как в примере 17, за исключением того, что вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (R)-6-хлор-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид (397,0 мг, 1,24 ммоль), полученный в эталонном примере 97. 1H-ЯМР (CDCl3, 400 МГц) δ 8,50 (д, 1Н), 8,14 (с, 1Н), 7,88 (д, 1Н), 7,54 (д, 1Н), 6,38 (д, 1Н), 4,90-4,75 (м, 1Н), 4,30-4,15 (м, 1Н), 3,75-3,55 (м, 2Н), 3,55-3,35 (м, 3Н), 3,30-3,20 (м, 1Н), 3,18-2,90 (м, 2Н), 2,85-2,60 (м, 1Н), 2,50-2,10 (м, 4Н), 2,00-1,85 (м, 1Н)
[1980] Пример 227. (2S)-1-[2-[(3R)-3-[(8-фтор-4-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1981] Указанное в заголовке соединение (59,4 мг, 12,1%) получали таким же образом, как и в примере 17, за исключением того, что вместо (R)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорида использовали (R)-8-фтор-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид (407,6 мг, 1,34 ммоль), полученный в эталонном примере 99. 1H-ЯМР (CDCl3, 400 МГц) δ 8,59 (д, 1Н), 7,81 (д, 1Н), 7,38-7,31 (м, 2Н), 6,44 (д, 1Н), 4,85-4,75 (м, 1Н), 4,40-4,20 (м, 1Н), 3,75-3,60 (м, 2Н), 3,60-3,35 (м, 3Н), 3,30-3,20 (м, 1Н), 3,18-2,90 (м, 2Н), 2,85-2,60 (м, 1Н), 2,55-2,15 (м, 4Н), 2,00-1,85 (м, 1Н)
[1982] Пример 228. (2S,4S)-4-фтор-1-[2-[(3S)-3-(5-хинолиламино)пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1983] (2S,4S)-1-(2-хлорацетил)-4-фторпирролидин-2-карбонитрил (20,0 мг, 0,10 ммоль), полученный в эталонном примере 2, растворяли в безводном дихлорметане (4 мл). К полученному раствору добавляли (S)-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (36,0 мг 0,12 ммоль), полученный в эталонном примере 16 и карбонат калия (29,0 мг, 0,21 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции к реакционной смеси добавляли воду. Водный слой реакционной смеси экстрагировали дихлорметаном. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (дихлорметан / метанол = 10/1, об./об.) с получением указанного в заголовке соединения (5,3 мг, 13,7%). 1H-ЯМР (CDCl3, 400 МГц) δ 8,86 (м, 1Н), 8,30 (м, 1Н), 7,48-7,54 (м, 2Н), 7,33 (м, 1Н), 6,55 (м, 1Н), 5,25-5,49 (м, 1Н), 4,97 (м, 1Н), 4,31 (м, 1Н), 3,82-3,92 (м, 1Н), 3,62-3,80 (м, 1Н), 3,32-3,60 (м, 2Н), 3,01-3,25 (м, 2Н), 2,62-2,82 (м, 2Н), 2,21-2,42 (м, 2Н), 1,96-2,19 (м, 3Н)
[1984] Пример 229. (2S)-1-[2-[(3S)-3-(3-хинолиламино)пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1985] Указанное в заголовке соединение (7,7 мг, 38,3%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-N-(пирролидин-3-ил)хинолин-3-амина гидрохлорид (25,6 мг, 0,12 ммоль), полученный в эталонном примере 6. 1H-ЯМР (CDCl3, 400 МГц) δ 8,44 (д, 1Н), 7,93 (д, 1Н), 7,60 (д, 1Н), 7,41-7,39 (м, 2Н), 6,96 (д, 1Н), 4,87-4,67 (м, 2Н), 4,12-4,11 (м, 1Н), 3,65-3,62 (м, 1Н), 3,55-3,41 (м, 2Н), 3,09-3,00 (м, 2Н), 2,86-2,79 (м, 1Н), 2,67-2,05 (м, 7Н), 1,88-1,79 (м, 1Н).
[1986] Пример 230. (2S)-1-[2-[(3S)-3-(6-хинолиламино)пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1987] Указанное в заголовке соединение (11,4 мг, 56,5%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид (25,6 мг, 0,12 ммоль), полученный в эталонном примере 111. 1H-ЯМР (CDCl3, 400 МГц) δ 8,58 (д, 1Н), 7,90 (д, 1Н), 7,84 (д, 1Н), 7,26-1,23 (м, 1Н), 7,10-7,08 (м, 1Н), 6,63 (с, 1Н), 4,90-4,65 (м, 2Н), 4,12-4,11 (м, 1Н), 3,62-3,32 (м, 3Н), 3,02-3,01 (м, 2Н), 2,82-2,79 (м, 2Н), 2,66-2,04 (м, 6Н), 1,85-1,80 (м, 1Н).
[1988] Пример 231. 5-[(3S)-1-[2-оксо-2-[(2S)-2-цианопирролидин-1-ил]этил]пирролидин-3-ил]амино]хинолин-2-карбонитрил
[1989] Указанное в заголовке соединение (3,0 мг, 13,8%) получали таким же образом, как ив примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-5-(пирролидин-3-иламино)хинолин-2-карбонитрила гидрохлорид (37,3 мг, 0,12 ммоль), полученный в эталонном примере 112. 1H-ЯМР (CDCl3, 400 МГц) δ 8,62-8,42 (м, 1Н), 7,66-7,58 (м, 2Н), 7,49-7,43 (м, 1Н), 6,67-6,63 (м, 1Н), 6,06 (д, 0,6Н), 5,34 (д, 0,4Н), 4,79-4,71 (м, 1Н), 4,25-4,20 (м, 1Н), 3,70-3,43 (м, 3Н), 3,28-2,99 (м, 3Н), 2,79-2,73 (м, 1Н), 2,48-2,13 (м, 5Н), 2,05-1,95 (м, 2Н).
[1990] Пример 232. 5-[(3S)-1-[2-оксо-2-[(2S)-2-цианопирролидин-1-ил]этил]пирролидин-3-ил]амино]хинолин-3-карбонитрил
[1991] Указанное в заголовке соединение (1,9 мг, 13,8%) получали таким же образом, как ив примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-5-(пирролидин-3-иламино)хинолин-3-карбонитрил гидрохлорид (37,3 мг, 0,12 ммоль), полученный в эталонном примере 113. 1H-ЯМР (CDCl3, 400 МГц) δ 8,95-8,93 (м, 1,6Н), 8,79 (с, 0,4Н), 7,71-7,65 (м, 1Н), 7,45-7,39 (м, 1Н), 6,64-6,61 (м, 1Н), 6,45 (д, 0,7Н), 5,79 (д, 0,3Н), 4,87-4,70 (м, 1Н), 4,25-4,16 (м, 1Н), 3,72-3,64 (м, 1Н), 3,58-3,54 (м, 1,3Н), 3,49-3,43 (м, 0,7Н), 3,35-3,28 (м, 1Н), 3,15-3,09 (м, 1Н), 3,05-3,00 (м, 1Н), 2,93-2,77 (м, 1Н), 2,42-2,11 (м, 5Н), 2,03-1,96 (м, 1Н), 1,85-1,82 (м, 1Н).
[1992] Пример 233. (2S)-1-[2-[(3S)-3-[(3-метокси-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1993] Указанное в заголовке соединение (10,6 мг, 24,2%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-3-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (37,9 мг, 0,12 ммоль), полученный в эталонном примере 114. 1H-ЯМР (CDCl3, 400 МГц) δ 8,63 (д, 1Н), 7,64-7,53 (м, 1Н), 7,45-7,37 (м, 2Н), 6,57 (кв, 1Н), 5,39-5,38 (м, 0,5Н), 5,02-5,00 (м, 0,5Н), 4,72 (т, 1Н), 4,21 (с, 1Н), 4,01 (с, 1,7Н), 3,94 (с, 1,3Н), 3,64-3,39 (м, 3Н), 3,23-3,14 (м, 2Н), 3,03-2,98 (м, 1Н), 2,73-2,68 (м, 1Н), 2,48-2,00 (м, 7Н).
[1994] Пример 234. (2S)-1-[2-[(3S)-3-[(3-фтор-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1995] Указанное в заголовке соединение (5,7 мг, 13,3%) получали таким же образом, как ив примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-3-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (36,5 мг, 0,12 ммоль), полученный в эталонном примере 115. 1H-ЯМР (CDCl3, 400 МГц) δ 8,76 (с, 1Н), 7,99 (дд, 1Н), 7,52-7,46 (м, 2Н), 6,60 (т, 1Н), 4,97-4,79 (м, 1Н), 4,21-4,19 (м, 1Н), 3,67-3,43 (м, 4Н), 3,31-3,07 (м, 2Н), 2,96 (д, 1Н), 2,81-2,71 (м, 1Н), 2,48-1,94 (м, 7Н).
[1996] Пример 235. (2S)-1-[2-[(3S)-3-[(3-хлор-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1997] Указанное в заголовке соединение (13,7 мг, 34,4%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-3-хлор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (38,4 мг, 0,12 ммоль), полученный в эталонном примере 116. 1H-ЯМР (CDCl3, 400 МГц) δ 8,75 (с, 1Н), 8,41-8,30 (м, 1Н), 7,55-7,50 (м, 1Н), 7,44-7,40 (м, 1Н), 6,57 (д, 1Н), 5,53 (д, 0,7Н), 5,12 (д, 0,3Н), 4,79 (д, 1Н), 4,21-4,16 (м, 1Н), 3,67-3,41 (м, 3Н), 3,34-3,08 (м, 2Н), 2,94 (д, 1Н), 2,84-2,68 (м, 1Н), 2,45-1,92 (м, 7Н).
[1998] Пример 236. (2S)-1-[2-[(3S)-3-[(7-фтор-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[1999] Указанное в заголовке соединение (6,8 мг, 16,1%) получали таким же образом, как ив примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-7-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (36,5 мг, 0,12 ммоль), полученный в эталонном примере 117. 1H-ЯМР (CDCl3, 400 МГц) δ 8,82 (с, 1Н), 8,37-8,21 (м, 1Н), 7,30-7,24 (м, 1Н), 7,06-7,02 (м, 1Н), 6,32-6,27 (м, 1Н), 5,94 (д, 0,7Н), 5,40 (д, 0,3Н), 4,75 (дд, 1Н), 4,18-4,13 (м, 1Н), 3,67-3,43 (м, 3Н), 3,28-2,98 (м, 3Н), 2,77-2,67 (м, 1Н), 2,52-1,92 (м, 7Н).
[2000] Пример 237. (2S)-1-[2-[(3S)-3-[(7-метокси-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2001] Указанное в заголовке соединение (10,1 мг, 16,1%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-7-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (37,9 мг, 0,12 ммоль), полученный в эталонном примере 118. 1H-ЯМР (CDCl3, 400 МГц) δ 8,75 (с, 1Н), 8,25-8,14 (м, 1Н), 7,20-7,16 (м, 1Н), 6,83 (с, 1Н), 6,18 (д, 1Н), 5,45 (д, 0,6Н), 5,11 (д, 0,3Н), 4,78-4,75 (м, 1Н), 4,14-4,13 (м, 1Н), 3,92 (с, 3Н), 3,65-3,27 (м, 4Н), 3,13-2,95 (м, 2Н), 2,74-2,60 (м, 1Н), 2,37-1,94 (м, 7Н).
[2002] Пример 238. (2S)-1-[2-[(3S)-3-[[7-(трифторметил)-5-хинолил]амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2003] Указанное в заголовке соединение (15,0 мг, 31,0%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-N-(пирролидин-3-ил)-7-(трифторметил)хинолин-5-амина гидрохлорид (42,5 мг, 0,12 ммоль), полученный в эталонном примере 119. 1H-ЯМР (CDCl3, 400 МГц) δ 8,93-8,90 (м, 1Н), 8,51-8,33 (м, 1Н), 7,70 (д, 1Н), 7,45-7,40 (м, 1Н), 6,61 (д, 1Н), 6,15 (д, 0,7Н), 5,51 (д, 0,3Н), 4,77-4,72 (м, 1Н), 4,25-4,20 (м, 1Н), 3,69-3,24 (м, 4Н), 3,18-3,01 (м, 2Н), 2,79-2,65 (м, 1Н), 2,57-1,95 (м, 7Н).
[2004] Пример 239. (2S)-1-[2-[(3S)-3-[(6-метил-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2005] Указанное в заголовке соединение (3,3 мг, 7,9%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-6-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (36,0 мг, 0,12 ммоль), полученный в эталонном примере 120. 1H-ЯМР (CDCl3, 400 МГц) δ 8,82 (с, 1Н), 8,47-8,41 (м, 1Н), 7,69 (д, 1Н), 7,50 (д, 1Н), 7,36 (кв, 1Н), 4,98-4,77 (м, 1Н), 4,02 (с, 1Н), 3,73-3,66 (м, 1Н), 3,57-3,29 (м, 3Н), 3,19-3,11 (м, 1Н), 2,87-2,79 (м, 1Н), 2,60-2,39 (м, 5Н), 2,29-2,15 (м, 5Н), 1,93-1,84 (м, 2Н).
[2006] Пример 240. (2S)-1-[2-[(3S)-3-[(6-метокси-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2007] Указанное в заголовке соединение (5,1 мг, 11,6%) получали таким же образом, как ив примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-6-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (37,9 мг, 0,12 ммоль), полученный в эталонном примере 121. 1H-ЯМР (CDCl3, 400 МГц) δ 8,77 (с, 1Н), 8,43-8,38 (м, 1Н), 7,77 (д, 1Н), 7,47 (д, 1Н), 7,34 (кв, 1Н), 5,13-4,76 (м, 1Н), 4,11-4,05 (м, 1Н), 3,98 (с, 3Н), 3,75-3,65 (м, 1Н), 3,58-3,35 (м, 3Н), 3,04-2,98 (м, 1Н), 2,81-2,78 (м, 1Н), 2,70-2,36 (м, 2Н), 2,32-2,05 (м, 5Н), 1,97-1,82 (м, 2Н).
[2008] Пример 241. (2S)-1-[2-[(3S)-3-[(6-фтор-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2009] Указанное в заголовке соединение (12,8 мг, 30,1%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-6-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (36,5 мг, 0,12 ммоль), полученный в эталонном примере 122. 1H-ЯМР (CDCl3, 400 МГц) δ 8,86-8,83 (м, 1Н), 8,55-8,42 (м, 1Н), 7,70-7,63 (м, 1Н), 7,48-7,38 (м, 2Н), 5,03-4,76 (м, 1Н), 4,65-4,17 (м, 2Н), 3,73-3,64 (м, 1Н), 3,58-3,37 (м, 3Н), 3,16-3,09 (м, 1Н), 2,94-2,81 (м, 1Н), 2,59-2,47 (м, 1Н), 2,38-2,11 (м, 6Н), 2,02-1,83 (м, 1Н).
[2010] Пример 242. (2S)-1-[2-[(3S)-3-[(8-метил-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2011] Указанное в заголовке соединение (15,6 мг, 37,2%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-8-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (36,0 мг, 0,12 ммоль), полученный в эталонном примере 123. 1H-ЯМР (CDCl3, 400 МГц) δ 8,91 (с, 1Н), 8,34-8,26 (м, 1Н), 7,40-7,33 (м, 2Н), 6,51-6,47 (м, 1Н), 5,03-4,74 (м, 2Н), 4,22-4,14 (м, 1Н), 3,69-3,28 (м, 4Н), 3,10-3,05 (м, 1Н), 2,94-2,92 (м, 1Н), 2,76-2,63 (м, 4Н), 2,47-1,91 (м, 7Н)
[2012] Пример 243. (2S)-1-[2-[(3S)-3-[(8-метокси-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2013] Указанное в заголовке соединение (3,7 мг, 8,5%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-8-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (37,9 мг, 0,12 ммоль), полученный в эталонном примере 124. 1H-ЯМР (CDCl3, 400 МГц) δ 8,93 (с, 1Н), 8,34-8,27 (м, 1Н), 7,43-7,40 (м, 1Н), 6,95 (д, 1Н), 6,55-6,50 (м, 1Н), 4,86-4,77 (м, 1Н), 4,20-4,13 (м, 1Н), 4,02 (с, 3Н), 3,69-3,32 (м, 4Н), 3,14-3,11 (м, 1Н), 2,95-2,92 (м, 1Н), 2,79-2,68 (м, 1Н), 2,43-1,83 (м, 8Н)
[2014] Пример 244. (2S)-1-[2-[(3S)-3-[(8-фтор-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2015] Указанное в заголовке соединение (1,9 мг, 4,3%) получали таким же образом, как ив примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-8-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (36,5 мг, 0,12 ммоль), полученный в эталонном примере 125. 1H-ЯМР (CDCl3, 400 МГц) δ 8,93 (с, 1Н), 8,42-8,29 (м, 1Н), 7,44-7,41 (м, 1Н), 7,29-7,24 (м, 1Н), 6,46-6,41 (м, 1Н), 4,79-4,77 (м, 1Н), 4,17 (с, 1Н), 3,74-3,31 (м, 4Н), 3,31-3,11 (м, 2Н), 3,03-2,95 (м, 1Н), 2,78-2,73 (м, 1Н), 2,49-1,92 (м, 7Н)
[2016] Пример 245. (2S)-1-[2-[(3S)-3-[[8-(трифторметил)-5-хинолил]амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2017] Указанное в заголовке соединение (9,9 мг, 20,4%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-N-(пирролидин-3-ил)-8-(трифторметил)хинолин-5-амина гидрохлорид (42,5 мг, 0,12 ммоль), полученный в эталонном примере 126. 1H-ЯМР (CDCl3, 400 МГц) δ 8,99 (д, 1Н), 8,51-8,31 (м, 1Н), 7,89-7,86 (м, 1Н), 7,44-7,38 (м, 1Н), 6,49-6,45 (м, 1Н), 6,37 (д, 0,6Н), 6,65 (д, 0,4Н), 4,78-4,69 (м, 1Н), 4,25-4,19 (м, 1Н), 3,68-3,41 (м, 3Н), 3,28-2,98 (м, 3Н), 2,79-2,71 (м, 1Н), 2,49-1,92 (м, 7Н)
[2018] Пример 246. (2S)-1-[2-[(3S)-3-[[8-(трифторметокси)-5-хинолил]амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2019] Указанное в заголовке соединение (23,6 мг, 46,9%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-N-(пирролидин-3-ил)-8-(трифторметокси)хинолин-5-амина гидрохлорид (44,4 мг, 0,12 ммоль), полученный в эталонном примере 127. 1H-ямр (CDCl3, 400 МГц) δ 8,97-8,95 (м, 1Н), 8,45-8,30 (м, 1Н), 7,46 (д, 1Н), 7,42-7,38 (м, 1Н), 6,43 (т, 1Н), 5,76 (д, 0,6Н), 5,25 (д, 0,4Н), 4,76 (с, 1Н), 4,17 (с, 1Н), 3,63-3,24 (м, 3Н), 3,13-2,95 (м, 3Н), 2,77-2,66 (м, 1Н), 2,47-1,92 (м, 7Н)
[2020] Пример 247. 5-[(3S)-1-[2-оксо-2-[(2S)-2-цианопирролидин-1-ил]этил]пирролидин-3-ил]амино]хинолин-8-карбонитрил
[2021] Указанное в заголовке соединение (1,2 мг, 2,8%) получали таким же образом, как ив примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-5-(пирролидин-3-иламино)хинолин-8-карбонитрил гидрохлорид (37,3 мг, 0,12 ммоль), полученный в эталонном примере 128. 1H-ЯМР (CDCl3, 400 МГц) δ 9,02-9,00 (м, 1Н), 8,62-8,34 (м, 1Н), 7,92 (т, 1Н), 7,14 (д, 1Н), 6,51-6,48 (м, 1Н), 4,80-4,67 (м, 1Н), 4,26-4,22 (м, 1Н), 3,75-3,43 (м, 4Н), 3,31-3,14 (м, 3Н), 2,85-2,80 (м, 1Н), 2,44-2,01 (м, 7Н)
[2022] Пример 248. (2S)-1-[2-[(3S)-3-[(8-бензилокси-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2023] Указанное в заголовке соединение (19,5 мг, 29,3%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-8-(бензилокси)-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (47,1 мг, 0,12 ммоль), полученный в эталонном примере 129. 1H-ЯМР (CDCl3, 400 МГц) δ 8,95 (с, 1Н), 8,33-8,26 (м, 1Н), 7,50 (д, 2Н), 7,41-7,33 (м, 3Н), 7,29-7,26 (м, 1Н), 6,91 (д, 1Н), 6,42-6,37 (м, 1Н), 5,35 (с, 2Н), 4,82-4,73 (м, 1Н), 4,08 (с, 1Н), 3,61-3,60 (м, 1Н), 3,50-3,27 (м, 3Н), 3,05-3,01 (м, 1,6 Н), 2,89-2,86 (м, 1Н), 2,72-2,61 (м, 1Н), 2,42-1,86 (м, 7,4 Н)
[2024] Пример 249. (2S,4S)-4-фтор-1-[2-[(3S)-3-(3-хинолиламино)пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2025] Указанное в заголовке соединение (10,2 мг, 26,6%) получали таким же образом, как в примере 28, за исключением того, что (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорид (25,6 мг, 0,12 ммоль), полученный в эталонном примере 5, использовали вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида. 1H ЯМР (MeOD4, 400 МГц) δ 8,40 (д, 1Н), 7,80 (д, 1Н), 7,67 (д, 1Н), 7,43-7,38 (м, 2Н), 7,12 (с, 1Н), 5,49-4,96 (м, 2Н), 4,17-3,73 (м, 3Н), 3,61-3,37 (м, 2Н), 3,10-2,91 (м, 2Н), 2,74-2,35 (м, 5Н), 1,84-1,76 (м, 1Н).
[2026] Пример 250. (2S,4S)-4-фтор-1-[2-[(3S)-3-(6-хинолиламино)пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2027] Указанное в заголовке соединение (4,9 мг, 12,8%) получали таким же образом, как в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид (25,6 мг, 0,12 ммоль), полученный в эталонном примере 111. 1H-ЯМР (CDCl3, 400 МГц) δ 8,60 (д, 1Н), 7,91-7,84 (м, 2Н), 7,27-7,25 (м, 1Н), 7,09 (т, 1Н), 6,63 (с, 1Н), 5,46-5,13 (м, 1Н), 5,15-4,90 (м, 1Н), 4,59-4,47 (м, 1Н), 4,17-3,66 (м, 3Н), 3,52-3,32 (м, 2Н), 3,10-2,99 (м, 1Н), 2,88-2,61 (м, 3Н), 2,48-2,21 (м, 3Н), 1,88-1,81 (м, 1Н).
[2028] Пример 251. (2S,4S)-4-фтор-1-[2-[(3S)-3-(7-хинолиламино)пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2029] Указанное в заголовке соединение (12,2 мг, 31,6%) получали таким же образом, как описано в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-N-(пирролидин-3-ил)хинолин-7-амина гидрохлорид (25,6 мг, 0,12 ммоль), полученный в эталонном примере 130. 1H ЯМР (MeOD4, 400 МГц) δ 8,56 (с, 1Н), 8,07 (д, 1Н), 7,62 (д, 1Н), 7,16-7,13 (м, 1Н), 7,05 (д, 1Н), 6,84 (с, 1Н), 5,49-4,95 (м, 2Н), 4,19-3,71 (м, 3Н), 3,59-3,37 (м, 2Н), 3,05-2,95 (м, 2Н), 2,81-2,35 (м, 5Н), 1,87-1,78 (м, 1Н).
[2030] Пример 252. 5-[(3S)-1-[2-оксо-2-[(2S,4S)-2-циано-4-фторпирролидин-1-ил]этил]пирролидин-3-ил]амино]хинолин-2-карбонитрил
[2031] Указанное в заголовке соединение (3,8 мг, 9,2%) получали таким же образом, как описано в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-5-(пирролидин-3-иламино)хинолин-2-карбонитрил (37,3 мг, 0,12 ммоль), полученный в эталонном примере 112. 1H ЯМР (MeOD4, 400 МГц) δ 8,77-8,71 (м, 1Н), 7,72-7,64 (м, 2Н), 7,34 (д, 1Н), 6,73 (д, 1Н), 5,49-4,99 (м, 2Н), 4,20-3,73 (м, 3Н), 3,66-3,40 (м, 2Н), 3,05-2,87 (м, 3Н), 2,70-2,39 (м, 4Н), 1,94-1,86 (м, 1Н).
[2032] Пример 253. 5-[(3S)-1-[2-оксо-2-[(2S,4S)-2-циано-4-фторпирролидин-1-ил]этил]пирролидин-3-ил]амино]хинолин-3-карбонитрил
[2033] Указанное в заголовке соединение (4,4 мг, 10,7%) получали таким же образом, как ив примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-5-(пирролидин-3-иламино)хинолин-3-карбонитрил гидрохлорид (37,3 мг, 0,12 ммоль), полученный в эталонном примере 113. 1H ЯМР (MeOD4, 400 МГц) δ 9,12 (д, 1Н), 8,92 (с, 1Н), 7,73 (t, 1Н), 7,33 (д, 1Н), 6,74 (д, 1Н), 5,52-4,99 (м, 2Н), 4,30-3,74 (м, 3Н), 3,66-3,42 (м, 2Н), 3,11-2,89 (м, 3Н), 2,70-2,37 (м, 4Н), 1,97-1,89 (м, 1Н).
[2034] Пример 254. (2S,4S)-4-фтор-1-[2-[(3S)-3-[(3-метокси-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2035] Указанное в заголовке соединение (2,3 мг, 5,4%) получали таким же образом, как и в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-3-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (37,9 мг, 0,12 ммоль), полученный в эталонном примере 114. 1H ЯМР (MeOD4, 400 МГц) δ 8,51 (с, 1Н), 7,97 (т, 1Н), 7,43-7,28 (м, 2Н), 6,76-6,68 (м, 1Н), 5,50-4,99 (м, 2Н), 4,30-3,92 (м, 5Н), 3,82-3,42 (м, 4Н), 3,14-2,91 (м, 2Н), 2,70-2,31 (м, 4Н), 2,23-1,92 (м, 1Н).
[2036] Пример 255. (2S,4S)-4-фтор-1-[2-[(3S)-3-[(3-фтор-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2037] Указанное в заголовке соединение (4,7 мг, 11,7%) получали таким же образом, как и в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-3-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (36,5 мг, 0,12 ммоль), полученный в эталонном примере 115. 1H ЯМР (MeOD4, 400 МГц) δ 8,70 (д, 1Н), 8,39-8,32 (м, 1Н), 7,51 (т, 1Н), 7,34 (д, 1Н), 6,64 (д, 1Н), 5,49-4,97 (м, 2Н), 4,23-4,15 (м, 1Н), 4,05-3,38 (м, 4Н), 3,07-2,85 (м, 3Н), 2,67-2,35 (м, 4Н), 1,92-1,85 (м, 1Н).
[2038] Пример 256. (2S,4S)-4-фтор-1-[2-[(3S)-3-[(3-хлор-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2039] Указанное в заголовке соединение (4,9 мг, 11,8%) получали таким же образом, как и в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-3-хлор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (38,4 мг, 0,12 ммоль), полученный в эталонном примере 116. 1H ЯМР (MeOD4, 400 МГц) δ 8,69-8,67 (м, 2Н), 7,55 (т, 1Н), 7,29 (д, 1Н), 6,64 (д, 1Н), 5,49-4,97 (м, 2Н), 4,23-4,15 (м, 1Н), 4,05-3,71 (м, 2Н), 3,63-3,38 (м, 2Н), 3,08-2,89 (м, 3Н), 2,66-2,36 (м, 4Н), 1,90-1,87 (м, 1Н).
[2040] Пример 257. (2S,4S)-4-фтор-1-[2-[(3S)-3-[(7-метокси-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2041] Указанное в заголовке соединение (3,0 мг, 7,2%) получали таким же образом, как и в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-7-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (37,9 мг, 0,12 ммоль), полученный в эталонном примере 118. 1H ЯМР (MeOD4, 400 МГц) δ 8,60 (д, 1Н), 8,48-8,42 (м, 1Н), 7,24 (кв, 1Н), 6,70 (с, 1Н), 6,19 (с, 1Н), 5,49-4,95 (м, 2Н), 4,13-4,09 (м, 1Н), 4,00-3,91 (дд, 1Н), 3,89 (с, 3Н), 3,81-3,66 (м, 1Н), 3,61-3,36 (м, 2Н), 3,04-2,88 (м, 3Н), 2,60-2,32 (м, 4Н), 1,88-1,85 (м, 1Н).
[2042] Пример 258. (2S,4S)-4-фтор-1-[2-[(3S)-3-[[7-(трифторметил)-5-хинолил]амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2043] Указанное в заголовке соединение (3,5 мг, 7,7%) получали таким же образом, как и в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-N-(пирролидин-3-ил)-7-(трифторметил)хинолин-5-амина гидрохлорид (42,5 мг, 0,12 ммоль), полученный в эталонном примере 119. 1H ЯМР (MeOD4, 400 МГц) δ 8,87 (д, 1Н), 8,74-8,67 (м, 1Н), 7,58-7,55 (м, 2Н), 6,68 (с, 1Н), 5,51-4,99 (м, 2Н), 4,29-4,24 (м, 1Н), 4,07-3,98 (дд, 1Н), 3,85-3,73(м, 1Н), 3,68-3,42 (м, 2Н), 3,12-2,92 (м, 3Н), 2,71-2,37 (м, 4Н), 1,97-1,90 (м, 1Н).
[2044] Пример 259. (2S,4S)-4-фтор-1-[2-[(3S)-3-[(6-метил-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2045] Указанное в заголовке соединение (5,3 мг, 13,3%) получали таким же образом, как ив примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-6-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (36,0 мг, 0,12 ммоль), полученный в эталонном примере 120. 1H ЯМР (MeOD4, 400 МГц) δ 8,71 (д, 1Н), 8,67-8,61 (м, 1Н), 7,57 (кв, 2Н), 7,48 (кв, 1Н), 5,49-4,96 (м, 2Н), 4,08-3,99 (м, 2Н), 3,83-3,71 (м, 1Н), 3,59-3,42(м, 1Н), 3,32-3,28 (м, 1Н), 3,12-3,05 (м, 1Н), 2,86-2,80 (м, 1Н), 2,70-2,32 (м, 7Н), 2,25-2,16 (м, 1Н), 1,92-1,81 (м, 1Н).
[2046] Пример 260. (2S,4S)-4-фтор-1-[2-[(3S)-3-[(6-метокси-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2047] Указанное в заголовке соединение (2,5 мг, 5,9%) получали таким же образом, как и в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-6-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (37,9 мг, 0,12 ммоль), полученный в эталонном примере 121. 1H ЯМР (MeOD4, 400 МГц) δ 8,67 (д, 1Н), 8,58-8,53 (м, 1Н), 7,70 (д, 1Н), 7,65-7,62 (м, 1Н), 7,45 (дд, 1Н), 5,49-4,96 (м, 2Н), 4,12-4,00 (м, 5Н), 3,87-3,75 (м, 1Н), 3,62-3,32 (м, 2Н), 3,04-2,99 (м, 1Н), 2,85-2,36 (м, 5Н), 2,23-2,09 (м, 1Н), 1,95-1,76 (м, 1Н).
[2048] Пример 261. (2S,4S)-4-фтор-1-[2-[(3S)-3-[(6-фтор-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2049] Указанное в заголовке соединение (4,6 мг, 11,3%) получали таким же образом, как и в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-6-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (36,5 мг, 0,12 ммоль), полученный в эталонном примере 122. 1H ЯМР (MeOD4, 400 МГц) δ 8,75-8,64 (м, 2Н), 7,54-7,50 (м, 3Н), 5,49-4,98 (м, 2Н), 4,35 (уш. с, 1Н), 4,06-3,72 (м, 2Н), 3,61-3,32 (м, 2Н), 3,12-3,06 (м, 1Н), 2,95-2,68 (м, 2Н), 2,64-2,19 (м, 4Н), 1,94-1,82 (м, 1Н).
[2050] Пример 262. (2S,4S)-4-фтор-1-[2-[(3S)-3-[(8-метил-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2051] Указанное в заголовке соединение (8,6 мг, 21,6%) получали таким же образом, как и в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-8-метил-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (36,0 мг, 0,12 ммоль), полученный в эталонном примере 123. 1H ЯМР (MeOD4, 400 МГц) δ 8,78 (с, 1 Н), 8,60-8,58 (м, 1 Н), 7,41 (уш. с, 2 Н), 6,56 (д, 1 Н), 5,49-4,96 (м, 2 Н), 4,17 (уш. с, 1 Н), 4,06-3,71 (м, 2 Н), 3,58-3,38 (м, 2 Н), 3,00-2,88 (м, 3 Н), 2,64-2,39 (м, 7 Н), 1,94-1,84 (м, 1 Н).
[2052] Пример 263. (2S,4S)-4-фтор-1-[2-[(3S)-3-[(8-метокси-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2053] Указанное в заголовке соединение (11,5 мг, 27,6%) получали таким же образом, как и в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-8-метокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (37,9 мг, 0,12 ммоль), полученный в эталонном примере 124. 1H-ЯМР (CDCl3, 400 МГц) δ 8,93 (с, 1 Н), 8,29 (д, 1 Н), 7,43-7,40 (м, 1 Н), 6,95 (д, 1 Н), 6,52 (дд, 1 Н), 5,49-4,95 (м, 2 Н), 4,19-3,67 (м, 6 Н), 3,55-3,36 (м, 2 Н), 3,17-2,89 (м, 2 Н), 2,77-2,61 (м, 2 Н), 2,52-2,13 (м, 3 Н), 2,05-1,86 (м, 2 Н).
[2054] Пример 264. (2S,4S)-4-фтор-1-[2-[(3S)-3-[(8-фтор-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2055] Указанное в заголовке соединение (1,8 мг, 4,5%) получали таким же образом, как ив
примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-8-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (36,5 мг, 0,12 ммоль), полученный в эталонном примере 125. 1H ЯМР (MeOD4, 400 МГц) δ 8,82 (д, 1 Н), 8,69-8,63 (м, 1 Н), 7,54 (дд, 1 Н), 7,33 (т, 1 Н), 6,57 (дд, 1 Н), 5,50-5,38 (м, 1 Н), 5,32-4,98 (м, 1 Н), 4,24-4,17 (м, 1 Н), 4,14-3,99 (м, 1 Н), 3,86-3,73 (м, 1 Н), 3,67-3,44 (м, 2 Н), 3,09-2,88 (м, 3 Н), 2,75-2,33 (м, 4 Н), 1,93-1,88 (м, 1 Н).
[2056] Пример 265. (2S,4S)-4-фтор-1-[2-[(3S)-3-[[8-(трифторметил)-5-хинолил]амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2057] Указанное в заголовке соединение (3,9 мг, 8,6%) получали таким же образом, как и в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-N-(пирролидин-3-ил)-8-(трифторметил)хинолин-5-амина гидрохлорид (42,5 мг, 0,12 ммоль), полученный в примере 126. 1H ЯМР (MeOD4, 400 МГц) δ 8,85 (д, 1 Н), 8,69-8,62 (м, 1 Н), 7,88 (д, 1 Н), 7,49 (дд, 1 Н), 6,58 (д, 1 Н), 5,49-4,98 (м, 2 Н), 4,24 (уш. с, 1 Н), 4,06-3,97 (м, 1 Н), 3,83-3,40 (м, 3 Н), 3,09-2,90 (м, 3 Н), 2,68-2,36 (м, 4 Н), 1,98-1,88 (м, 1 Н).
[2058] Пример 266. (2S,4S)-4-фтор-1-[2-[(3S)-3-[[8-(трифторметокси)-5-хинолил]амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2059] Указанное в заголовке соединение (5,5 мг, 11,7%) получали таким же образом, как и в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-N-(пирролвдин-3-ил)-8-(трифторметокси)хинолин-5-амина гидрохлорид (44,4 мг, 0,12 ммоль), полученный в примере 127. 1H ЯМР (MeOD4, 400 МГц) δ 8,84 (д, 1 Н), 8,69-8,63 (м, 1 Н), 7,53-7,50 (м, 2 Н), 6,56 (д, 1 Н), 5,49-5,37 (м, 1 Н), 5,30-4,98 (м, 1 Н), 4,19 (уш. с, 1 Н), 4,06-3,97 (м, 1 Н), 3,83-3,72 (м, 1 Н), 3,66-3,40 (м, 2 Н), 3,08-2,88 (м, 3 Н), 2,69-2,36 (м, 4 Н), 1,91-1,88 (м, 1 Н).
[2060] Пример 267. 5-[(3S)-1-[2-оксо-2-[(2S,4S)-2-циано-4-фторпирролидин-1-ил]этил]пирролидин-3-ил]амино]хинолин-8-карбонитрил
[2061] Указанное в заголовке соединение (2,6 мг, 6,3%) получали таким же образом, как и в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-5-(пирролидин-3-иламино)хинолин-8-карбонитрил гидрохлорид (37,3 мг, 0,12 ммоль), полученный в эталонном примере 128. 1H ЯМР (MeOD4, 400 МГц) δ 8,89 (д, 1 Н), 8,77-8,69 (м, 1 Н), 7,98 (д, 1 Н), 7,53 (дд, 1 Н), 6,68 (д, 1 Н), 5,50-5,38 (м, 1 Н), 5,31-5,00 (м, 1 Н), 4,38-4,30 (м, 1 Н), 4,09-4,00 (м, 1 Н), 3,86-3,43 (м, 3 Н), 3,13-2,92 (м, 3 Н), 2,72-2,41 (м, 4 Н), 2,02-1,96 (м, 1 Н).
[2062] Пример 268. (2S,4S)-4-фтор-1-[2-[(3S)-3-[(8-бензилокси-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2063] Указанное в заголовке соединение (3,2 мг, 6,4%) получали таким же образом, как и в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-8-(бензилокси)-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (47,1 мг, 0,12 ммоль), полученный в эталонном примере 129. 1H ЯМР (MeOD4, 400 МГц) δ 8,78 (д, 1 Н), 8,58-8,53 (м, 1 Н),7,51-7,45 (м, 3 Н), 7,35-7,25 (м, 3 Н), 7,03 (д, 1 Н), 6,47 (д, 1 Н), 5,49-5,25 (м, 3,2 Н), 4,95-4,93 (м, 0,8 Н), 4,04-3,64 (м, 3 Н), 3,58-3,29 (м, 2 Н), 2,97-2,80 (м, 3 Н), 2,58-2,28 (м, 4 Н), 1,87-1,80 (м, 1 Н).
[2064] Пример 269. (2S,4S)-4-фтор-1-[2-[(3S)-3-[(7-фтор-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2065] Указанное в заголовке соединение (7,2 мг, 15,9%) получали таким же образом, как и в примере 28, за исключением того, что вместо (S)-N-(пирролвдин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-7-фтор-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (36,5 мг, 0,12 ммоль), полученный в эталонном примере 117. 1H ЯМР (CDCl3, 400 МГц) δ 8,79 (т, 1 Η), 8,30-8,22 (м, 1 Η), 7,26-7,23 (м, 1 Η), 7,04-7,00 (м, 1 Η), 6,28 (м, 1 Η), 5,71-5,46 (м, 1 Η), 5,38-5,25 (м, 1 Η), 4,89 (т, 1 Η), 4,15-3,44 (м, 3 Η), 3,34-3,26 (м, 1 Η), 3,17-2,94 (м, 2 Η), 2,73-2,22 (м, 6 Η), 2,03-1,91 (м, 1 Η).
[2066] Пример 270. (2S)-1-[2-[(3S)-3-[[8-(трифторметил)-4-хинолил]амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2067] Указанное в заголовке соединение (12,2 мг, 24,3%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-N-(пирролидин-3-ил)-8-(трифторметил)хинолин-4-амина гидрохлорид (42,5 мг, 0,12 ммоль), полученный в эталонном примере 131. 1H ЯМР (CDCl3, 400 МГц) δ 8,68 (т, 1 Н), 8,18 (дд, 1 Н), 8,00 (т, 1 Н), 7,47 (т, 1 Н), 6,45 (т, 1 Н), 6,21 (дд, 1 Н), 5,52-5,30 (м, 1 Н), 4,93 (дд, 1 Н), 4,26-3,54 (м, 4 Н), 3,45-3,02 (м, 3,5 Н), 2,78-2,26 (м, 4,5 Н), 2,10-1,88 (м, 1 Н).
[2068] Пример 271. (2S,4S)-4-фтор-1-[2-[(3S)-3-[[8-(трифторметил)-4-хинолил]амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2069] Указанное в заголовке соединение (8,0 мг, 15,4%) получали таким же образом, как и в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-N-(пирролвдин-3-ил)-8-(трифторметил)хинолин-4-амина гидрохлорид (42,5 мг, 0,12 ммоль), полученный в эталонном примере 131. 1H ЯМР (CDCl3, 400 МГц) δ 8,68 (т, 1 Η), 8,22 (дд, 1 Η), 8,00 (т, 1 Η), 7,47 (дд, 1 Η), 6,47 (т, 1 Η), 6,42 (дд, 1 Η), 4,82-4,69 (м, 1 Η), 4,24 (д, 1 Η), 3,66-3,45 (м, 3 Η), 3,30-3,01 (м, 3 Η), 2,82-2,76 (м, 1 Η), 2,50-2,13 (м, 5 Η), 2,06-1,99 (м, 1 Η).
[2070] Пример 272. (2S,4S)-4-фтор-1-[2-[(3S)-3-(1,8-нафтиридин-3-иламино)пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2071] Указанное в заголовке соединение (67,7 мг, 26,6%) получали таким же образом, как и в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорид (196,7 мг, 0,69 ммоль), полученный в эталонном примере 132. 1H-ЯМР (CDCl3, 600 МГц) δ 8,79 (д, 1 Н), 8,62 (с, 1 Н), 7,96 (д, 1 Н), 7,35 (т, 1 Н), 6,90 (с, 1 Н), 5,50-5,30 (м, 1 Н), 5,10-4,70 (м, 1 Н), 4,20-4,05 (м, 1 Н), 3,95-3,70 (м, 2 Н), 3,60-3,35 (м, 2 Н), 3,15-3,00 (м, 2 Н), 2,90-2,65 (м, 3 Н), 2,50-2,25 (м, 3 Н), 1,95-1,80 (м, 1 Н)
[2072] Пример 273. (2S,4S)-4-фтор-1-[2-[(3S)-3-[(7-хлор-1,8-нафтиридин-3-ил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2073] Указанное в заголовке соединение (10,1 мг, 5,2%) получали таким же образом, как и в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-7-хлор-N-(пирролидин-3-ил)-1,8-нафтиридин-3-амина гидрохлорид (155,6 мг, 0,48 ммоль), полученный в эталонном примере 13S. 1H-ЯМР (CDCl3, 600 МГц) δ 8,58 (с, 1 Н), 7,90 (д, 1 Н), 7,34 (д, 1 Н), 6,90 (с, 1 Н), 5,50-5,30 (м, 1 Н), 5,10-4,90 (м, 1 Н), 4,20-4,00 (м, 2 Н), 4,00-3,65 (м, 1 Н), 3,60-3,30 (м, 2 Н), 3,20-3,00 (м, 2 Н), 2,90-2,60 (м, 3 Н), 2,50-2,25 (м, 3 Н), 1,95-1,80 (м, 1 Н)
[2074] Пример 274. (2S)-1-[2-[(3S)-3-[(8-этокси-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2075] Указанное в заголовке соединение (3,4 мг, 7,5%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-8-этокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (39,6 мг, 0,12 ммоль), полученный в эталонном примере 134. 1H ЯМР (CDCl3, 400 МГц) δ 8,93-8,91 (м, 1 Н), 8,31-8,24 (м, 1 Н), 7,39-7,35 (м, 1 Н), 6,94 (д, 1 Н), 6,49 (дд, 1 Н), 4,85-4,72 (м, 1 Н), 4,66^1,45 (м, 1 Н), 4,23 (кв, 2 Н), 4,13-4,09 (м, 1 Н), 3,65-3,28 (м, 4 Н), 3,09-2,99 (м, 1 Н), 2,89-2,86 (м, 1 Н), 2,75-2,63 (м, 1 Н), 2,45-1,83 (м, 7 Н), 1,56 (т, 3 Н).
[2076] Пример 275. (2S,4S)-4-фтор-1-[2-[(3S)-3-[(8-этокси-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2077] Указанное в заголовке соединение (3,5 мг, 8,0%) получали таким же образом, как в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-8-этокси-N-(пирролидин-3-ил)хинолин-5-амина гидрохлорид (39,6 мг, 0,12 ммоль), полученный в эталонном примере 134. 1H ЯМР (CDCl3, 400 МГц) δ 8,90 (т, 1 Η), 8,26 (д, 1 Η), 7,37-7,33 (м, 1 Η), 6,93 (д, 1 Η), 6,46 (дд, 1 Η), 5,41-5,17 (м, 1 Η), 5,07-4,84 (м, 1 Η), 4,54-4,39 (м, 1 Η), 4,20 (кв, 2 Η), 4,13-3,99 (м, 1,5 Η), 3,89-3,58 (м, 1,5 Η), 3,50-3,25 (м, 2 Η), 3,09-2,81 (м, 2 Η), 2,72-2,08 (м, 5 Η), 1,98-1,80 (м, 1 Η), 1,54 (тд, 3 Н).
[2078] Пример 276. (2S,4S)-4-фтор-1-[2-[(3S)-3-[(8-гидрокси-5-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2079] Указанное в заголовке соединение (2,5 мг, 5,4%) получали таким же образом, как и в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-5-(пирролидин-3-иламино)хинолин-8-ола гидрохлорид (36,2 мг, 0,12 ммоль), полученный в эталонном примере 135. 1H ЯМР (CDCl3, 400 МГц) δ 8,78 (с, 1 Н), 8,31 (д, 1 Н), 7,69 (уш. с, 1 Н), 7,42 (дд, 1 Н), 7,06 (д, 1 Н), 6,53 (дд, 1 Н), 5,50-5,24 (м, 1 Н), 5,07-4,95 (м, 1 Н), 4,19-4,11 (м, 2 Н), 3,96-3.69 (м, 2 Н), 3,56-3,34 (м, 2 Н), 3,50-3,25 (м, 2 Н), 3,16-2,89 (м, 2 Н), 2,76-2,16 (м, 5 Н), 2,05-1,87 (м, 1 Н).
[2080] Пример 277. (2S,4S)-4-фтор-1-[2-[(3S)-3-[(8-метил-6-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2081] Указанное в заголовке соединение (122,9 мг, 40,3%) получали таким же образом, как и в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-8-метил-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид (239,9 мг, 0,80 ммоль), полученный в эталонном примере 136. 1H-ЯМР (CDCl3, 600 МГц) δ 8,63 (с, 1 Н), 7,88 (д, 1 Н), 7,27-7,24 (м, 1 Н), 6,95 (д, 1 Н), 6,50 (с, 1 Н), 5,50-5,25 (м, 1 Н), 5,20-4,90 (м, 1 Н), 4,20-4,05 (м, 2 Н), 4,00-3.70 (м, 1 Н), 3,55-3,30 (м, 2 Н), 3,15-3,00 (м, 2 Н), 2,95-2,75 (м, 2 Н), 2,71 (с, 3 Н), 2,71-2,60 (м, 1 Н), 2,50-2,20 (м, 3 Н), 1,95-1,80 (м, 1 Н)
[2082] Пример 278. (2S,4S)-4-фтор-1-[2-[(3S)-3-[(8-фтор-6-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2083] Указанное в заголовке соединение (222,3 мг, 48,9%) получали таким же образом, как и в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-8-фтор-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид (358,9 мг, 1,18 ммоль), полученный в эталонном примере 137. 1H-ЯМР (CDCl3, 600 МГц) δ 8,62 (с, 1 Н), 7,89 (д, 1 Н), 7,29 (д, 1 Н), 6,80 (т, 1 Н), 6,44 (с, 1 Н), 5,50-5,35 (м, 1 Н), 5,10-4,90 (м, 1 Н), 4,20-4,05 (м, 2 Н), 3,95-3,70 (м, 1 Н), 3,60-3,30 (м, 2 Н), 3,15-2,95 (м, 2 Н), 2,90-2,60 (м, 3 Н), 2,50-2,20 (м, 3 Н), 1,90-1,75 (м, 1 Н)
[2084] Пример 279. (2S,4S)-4-фтор-1-[2-[(3S)-3-[(8-хлор-6-хинолил)амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2085] Указанное в заголовке соединение (314,5 мг, 86,0%) получали таким же образом, как и в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-8-хлор-N-(пирролидин-3-ил)хинолин-6-амина гидрохлорид (291,8 мг, 0,91 ммоль), полученный в эталонном примере 138. 1H-ЯМР (CDCl3, 600 МГц) δ 8,68 (с, 1 Н), 7,88 (д, 1 Н), 7,29-7,22 (м, 2 Н), 6,54 (с, 1 Н), 5,50-5,25 (м, 1 Н), 5,10-4,85 (м, 1 Н), 4,20-4,00 (м, 2 Н), 3,95-3,65 (м, 1 Н), 3,55-3,25 (м, 2 Н), 3,10-2,90 (м, 2 Н), 2,90-2,55 (м, 3 Н), 2,45-2,20 (м, 3 Н), 1,90-1,75 (м, 1 Н)
[2086] Пример 280. (2S,4S)-4-фтор-1-[2-[(3S)-3-[[8-(трифторметил)-6-хинолил]амино]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2087] Указанное в заголовке соединение (72,1 мг, 27,3%) получали таким же образом, как и в примере 28, за исключением того, что вместо (S)-N-(пирролвдин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-N-(пирролвдин-3-ил)-8-(трифторметил)хинолин-6-амина гидрохлорид (215,7 мг, 0,61 ммоль), полученный в эталонном примере 139. 1H-ЯМР (CDCl3, 600 МГц) δ 8,75 (с, 1 Н), 7,94 (д, 1 Н), 7,45 (д, 1 Н), 7,34 (т, 1 Н), 6,77 (с, 1 Н), 5,50-5,35 (м, 1 Н), 5,10-4,90 (м, 1 Н), 4,20-4,05 (м, 2 Н), 3,95-3,65 (м, 1 Н), 3,60-3,30 (м, 2 Н), 3,15-3,00 (м, 2 Н), 2,90-2,60 (м, 3 Н), 2,50-2,20 (м, 3 Н), 1,95-1,80 (м, 1Н)
[2088] Пример 281. N-метил-5-[[(3S)-1-[2-оксо-2-[(2S,4S)-2-циано-4-фторпирролидин-1-ил]этил]пирролидин-3-ил]амино]хинолин-8-карбоксамид
[2089] Указанное в заголовке соединение (8,6 мг, 16,9%) получали таким же образом, как описано в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-N-метил-5-(пирролидин-3-иламино)хинолин-8-карбоксамид (41,0 мг, 0,12 ммоль), полученного в эталонном примере 140. 1H ЯМР (CDCl3, 400 МГц) δ 10,95 (т, 1 Η), 8,87-8,85 (м, 1 Η), 8,72 (дд, 1 Η), 8,42 (дд, 1 Η), 7,41-7,36 (м, 1 Η), 6,61 (дд, 1 Η), 5,93-5,62 (м, 1 Η), 5,53-5,27 (м, 1 Η), 4,94 (дд, 1 Η), 4,30-4,22 (м, 1 Η), 4,16-4,07 (м, 1 Η), 3,92-3,69 (м, 2 Η), 3,67-3,38 (м, 2 Η), 3,29-3,03 (м, 6 Η), 2,75-2,63 (м, 2 Η), 2,54-2,20 (м, 1 Η), 2,10-1,95 (м, 1 Η).
[2090] Пример 282. N,N-диметил-5-[[(3S)-1-[2-оксо-2-[(2S,4S)-2-циано-4-фторпирролидин-1-ил]этил]пирролидин-3-ил]амино]хинолин-8-карбоксамид
[2091] Указанное в заголовке соединение (10,0 мг, 19,0%) получали таким же образом, как описано в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-N,N-диметил-5-(пирролидин-3-иламино)хинолин-8-карбоксамида гидрохлорид (42,7 мг, 0,12 ммоль), полученного в эталонном примере 141. 1H ЯМР (CDCl3, 400 МГц) δ 8,86-8,84 (м, 1 Н), 8,31-8,26 (м, 1 Н), 7,46 (д, 1 Н), 7,30-7,28 (м, 1 Н), 6,49-6,44 (м, 1 Н), 5,62-4,80 (м, 3 Н), 4,16-4,14 (м, 1 Н), 3,96-3,63 (м, 2 Н), 3,60-3,25 (м, 2 Н), 3,22 (д, 3 Н), 3,17-2,87 (м, 2 Н), 2,80 (д, 3 Н), 2,62-2,20 (м, 5Н), 2,03-1,95 (м, 1 Н).
[2092] Пример 283. N-фенил-5-[[(3S)-1-[2-оксо-2-[(2S,4S)-2-циано-4-фторпирролидин-1-ил]этил]пирролидин-3-ил]амино]хинолин-8-карбоксамид
[2093] Указанное в заголовке соединение (12,0 мг, 21,2%) получали таким же образом, как описано в примере 28, за исключением того, что вместо (S)-N-(пирролцдин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-N-фенил-5-(пирролидин-3-иламино)хинолин-8-карбоксамида гидрохлорид (48,5 мг, 0,12 ммоль), полученный в эталонном примере 142. 1H ЯМР (CDCl3, 400 МГц) δ 8,88 (т, 1 Η), 8,74-8,71 (м, 1 Η), 7,43 (д, 1 Η), 7,85 (д, 2 Η), 7,39-7,35 (м, 3 Η), 7,11-7,07 (м, 1 Η), 6,57 (дд, 1 Η), 6,28-5,81 (м, 1 Η), 5,43-5,24 (м, 1 Η), 4,91 (дд, 1 Η), 4,23-4,15 (м, 1 Η), 4,03-3,15 (м, 5 Η), 3,08-2,99 (м, 2 Η), 2,75-2,18 (м, 5 Η), 2,03-1,95 (м, 1 Η).
[2094] Пример 284. N-метил-N-фенил-5-[[(3S)-1-[2-оксо-2-[(2S,4S)-2-циано-4-фторпирролидин-1-ил]этил]пирролидин-3-ил]амино]хинолин-8-карбоксамид
[2095] Указанное в заголовке соединение (17,6 мг, 28,6%) получали аналогично тому, как описано в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-N-метил-N-фенил-5-(пирролвдин-3-иламино)хинолин-8-карбоксамида гидрохлорид (50,21 мг, 0,12 ммоль), полученный в эталонном примере 143. 1H ЯМР (CDCl3, 400 МГц) δ 8,85-8,81 (м, 1 Н), 8,21-8,15 (м, 1 Н), 7,29-7,00 (м, 7 Н), 6,27-6,22 (м, 1 Н), 5,38-5,15 (м, 1 Н), 4,89 (дд, 1 Н), 4,02-3,66 (м, 2 Н), 3,59-3,50 (м, 2 Н), 3,42 (с, 3 Н), 3,35-3,22 (м, 2 Н), 3,06-2,79 (м, 2 Н), 2,61-1,98 (м, 5 Н), 1,89-1,78 (м, 1 Н).
[2096] Пример 285. N-бензил-N-метил-5-[[(3S)-1-[2-оксо-2-[(2S,4S)-2-циано-4-фторпирролидин-1-ил]этил]пирролидин-3-ил]амино]хинолин-8-карбоксамид
[2097] Указанное в заголовке соединение (11,0 мг, 17,8%) получали таким же образом, как описано в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-N-бензил-N-метил-5-(пирролидин-3-иламино)хинолин-8-карбоксамида гидрохлорид (51,89 мг, 0,12 ммоль), полученный в эталонном примере 144. 1Н ЯМР (CDCl3, 400 МГц) δ 8,88-8,85 (м, 1 Н), 8,35-8,27 (м, 1 Н), 7,51 (т, 2 Н), 7,37 (т, 1 Н), 7,29-7,17 (м, 4 Н), 6,48-6,40 (м, 1 Н), 5,79-5,13 (м, 3 Н), 5,05-4,76 (м, 1 Н), 4,40-4,11 (м, 2Н), 3,84-3,58 (м, 2 Н), 3,42 (с, 3 Н), 3,35-3,20 (м, 2 Н), 3,08 (с, 2 Н), 3,02-2,16 (м, 5 Н), 1,98-1,86 (м, 1 Н).
[2098] Пример 286. N-метил-5-[[(3S)-1-[2-оксо-2-[(23)-2-цианопирролидин-1-ил]этил]пирролидин-3-ил] амино]хинолин-8-карбоксамид
[2099] Указанное в заголовке соединение (10,1 мг, 29,7%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-N-метил-5-(пирролидин-3-иламино)хинолин-8-карбоксамид (29,0 мг, 0,084 ммоль), полученный в эталонном примере 140. 1H ЯМР (CDCl3, 400 МГц) δ 10,98-10,94 (м, 1 Н), 8,85-8,83 (м, 1 Н), 8,70 (дд, 1 Н), 8,48 (дд, 1 Н), 7,40-7,34 (м, 1 Н), 6,60 (дд, 1 Н), 6,39-5,65 (м, 1 Н), 4,78-4,73 (м, 1 Н), 4,27-4,24 (м, 1 Н), 3,66-3,42 (м, 3 Н), 3,29-3,01 (м, 5 Н), 2,79-2,70 (м, 1 Н), 2,49-2,36 (м, 1 Н), 2,33-1,96 (м, 7 Н)
[2100] Пример 287. N-фенил-5-[[(3S)-1-[2-оксо-2-[(2S)-2-цианопирролидин-1-ил]этил]пирролидин-3-ил] амино]хинолин-8-карбоксамид
[2101] Указанное в заголовке соединение (4,4 мг, 12,1%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-N-фенил-5-(пирролидин-3-иламино)хинолин-8-карбоксамида гидрохлорид (30,0 мг, 0,074 ммоль), полученный в эталонном примере 142. 1H ЯМР (CDCl3, 400 МГц) δ 8,88 (т, 1 Η), 8,72 (дд, 1 Η), 8,43 (дд, 1 Η), 7,85 (д, 2 Η), 7,39-7,35 (м, 3 Η), 7,09 (т, 1 Η), 6,57 (дд, 1 Η), 6,28-5,81 (м, 1 Η), 5,44-5,24 (м, 1 Η), 4,91 (дд, 1 Η),4,23-4,15 (м, 1 Η), 4,04-3,17 (м, 5 Η), 3,08-2,99 (м, 2 Η), 2,75-2,60 (м, 2 Η), 2,39-2,18 (м, 2 Η), 2,05-1,93 (м, 1 H)
[2102] Пример 288. N-бензил-N-метил-5-[[(3S)-1-[2-оксо-2-[(2S)-2-цианопирролидин-1-ил]этил]пирролидин-3-ил]амино]хинолин-8-карбоксамид
[2103] Указанное в заголовке соединение (6,89 мг, 11,5%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-N-бензил-N-метил-5-(пирролидин-3-иламино)хинолин-8-карбоксамид гидрохлорид (52,0 мг, 0,12 ммоль), полученный в эталонном примере 144. 1H ЯМР (CDCl3, 400 МГц) δ 8,91-8,88 (м, 1 Н), 8,33 (дт, 1 Н), 7,53 (дд, 2 Н), 7,40 (т, 1 Н), 7,33-7,25 (м, 2 Н), 7,23-7,19 (м, 2 Н), 6,52-6,43(м, 1 Н), 5,80-5,32(м, 1 Η), 4,99-4,74 (м, 1 Η), 4,38-4,32 (м, 1 Η), 4,22-4,13 (м, 1 Η), 3,63-3,43 (м, 4 Η), 3,10 (с, 3 Η), 2,99-2,94 (м, 1 Η), 2,70-2,66 (м, 3 Η), 2,45-1,92 (м, 7 Η).
[2104] Пример 289. N-метил-N-фенил-5-[[(3S)-1-[2-оксо-2-[(2S)-2-цианопирролидин-1-ил]этил]пирролидин-3-ил]амино]хинолин-8-карбоксамид
[2105] Указанное в заголовке соединение (5,9 мг, 10,2%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-N-метил-М-фенил-5-(пирролидин-3-иламино)хинолин-8-карбоксамида гидрохлорид (50,3 мг, 0,12 ммоль), полученный в эталонном примере 143. 1H ЯМР (CDCl3, 400 МГц) δ 8,86-8,82 (дд, 1 Н),8,38-8,28 (м, 2 Н), 7,29-7,25 (м, 2 Н), 7,05-7,00 (м, 4 Н), 6,18 (д, 1 Н), 4,76 (д, 1 Н), 4,09 (уш. с, 1 Н), 3,98-3,70 (м, 2 Н), 3,66- 3,15 (м, 7 Н), 3,03 (уш. с, 1 Н), 2,32-2,07 (м, 4 Н), 2,02-1,96 (м, 1 Н).
[2106] Пример 290. N-(3-пиридил)-5-[[(3S)-1-[2-оксо-2-[(2S)-2-цианопирролидин-1-ил]этил]пирролидин-3-ил]амино]хинолин-8-карбоксамид
[2107] Указанное в заголовке соединение (21,8 мг, 50,5%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-N-(пиридин-3-ил)-5-(пирролидин-3-иламино)хинолин-8-карбоксамид гидрохлорида (36,9 мг, 0,09 ммоль), полученный в эталонном примере 145. 1H ЯМР (CDCl3, 400 МГц) δ 8,91-8,88 (м, 1 Н), 8,86-8,84 (м, 1 Н), 8,75-8,71 (м, 1 Н), 8,67 (д, 0,7 Н), 8,46-8,44 (м, 1,3 Н), 8,31 (д, 1 Н), 7,44-7,39 (м, 1 Н), 7,31-7,28 (м, 1 Н), 6,87 (д, 0,7 Н), 6,62 (д, 1 Н), 5,95 (д, 0,3 Н), 4,78-4,70 (м, 1 Н), 4,24 (с, 1 Н), 3,67-3,40 (м, 3 Н), 3,17-3,11 (м, 2 Н), 2,81-2,69 (м, 1 Н), 2,49-2,12 (м, 8 Н), 2,04-1,97 (м, 1 Н).
[2108] Пример 291. N-(4-пиридил)-5-[[(3S)-1-[2-оксо-2-[(2S)-2-цианопирролидин-1-ил]этил]пирролидин-3-ил]амино]хинолин-8-карбоксамид
[2109] Указанное в заголовке соединение (11,2 мг, 19,8%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-N-(пиридин-4-ил)-5-(пирролидин-3-иламино)хинолин-8-карбоксамида гидрохлорид (48,7 мг, 0,12 ммоль), полученный в эталонном примере 146. 1H ЯМР (CDCl3, 400 МГц) δ 8,91-8,87 (м, 1 Н), 8,74-8,67 (м, 1,7 Н), 8,49-8,44 (дд, 2,3 Н), 7,76 (д, 2 Н), 7,45-7,39 (м, 1 Н), 7,00 (д, 0,7 Н), 6,62 (д, 1 Н), 6,01 (д, 0,3 Н), 4,78-4,70 (м, 1 Н), 4,25 (с, 1 Н), 3,67-3,40 (м, 3 Н), 3,19-3,12 (м, 2 Н), 2,82-2,70 (м, 1 Н), 2,49-2,08 (м, 8Н), 2,04-1,97 (м, 1 Н).
[2110] Пример 292. N-(4-пиридил)-5-[[(3S)-1-[2-оксо-2-[(2S,4S)-2-циано-4-фторпирролидин-1-ил]этил]пирролидин-3-ил]амино]хинолин-8-карбоксамид
[2111] Указанное в заголовке соединение (8,4 мг, 14,3%) получали таким же образом, как описано в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-N-(пиридин-4-ил)-5-(пирролидин-3-иламино)хинолин-8-карбоксамида гидрохлорид (48,7 мг, 0,12 ммоль), полученный в эталонном примере 146. 1Н ЯМР (CDCl3, 400 МГц) δ 8,92-8,89 (м, 1 Н), 8,72 (т, 1 Н), 8,59-8,43 (м, 3 Н), 7,76-7,74 (м, 2 Н), 7,45-7,41 (м, 1 Н), 6,63 (д, 1 Н), 6,54 (д, 0,6 Н), 5,97 (д, 0,4 Н), 5,52-5,28 (м, 1 Н), 4,93 (дд, 1 Н), 4,30-4,25 (м, 1 Н), 4,01-3,39 (м, 4 Н), 3,29-3,06 (м, 3 Н), 2,79-2,65 (м, 2 Н), 2,53-2,24 (м, 2 Н), 2,11-1,99 (м, 1 Н).
[2112] Пример 293. N-(2-пиридил)-5-[[(35)-1-[2-оксо-2-[(25)-2-цианопирролидин-1-ил]этил]пирролидин-3-ил]амино]хинолин-8-карбоксамид
[2113] Указанное в заголовке соединение (4,3 мг, 7,6%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-N-(пиридин-2-ил)-5-(пирролидин-3-иламино)хинолин-8-карбоксамида гидрохлорид (48,7 мг, 0,12 ммоль), полученный в эталонном примере 147. 1H ЯМР (CDCl3, 400 МГц) δ 9,06 (тд, 1 Н), 8,80 (дд, 1 Н), 8,64 (дд, 0,6 Н), 8,54 (д, 1 Н), 8,44-8,40 (м, 1,4 Н), 7,76-7,71 (м, 1 Н), 7,48-7,41 (м, 1 Н), 7,04-7,00 (м, 1 Н), 6,74-6,65 (м, 1,6 Н), 5,85 (д, 0,4 Н), 4,81-4,70 (м, 1 Н), 4,30-4,28 (м, 1 Н), 3,68-3,43 (м, 4 Н), 3,28-3,04 (м, 3 Н), 2,82-2,76 (м, 1 Н), 2,51-2,11 (м, 6Н), 2,03-2,00 (м, 1 Н).
[2114] Пример 294. N-(2-пиридил)-5-[[(3S)-1-[2-оксо-2-[(2S,4S)-2-циано-4-фторпирролидин-1-ил]этил]пирролидин-3-ил]амино]хинолин-8-карбоксамид
[2115] Указанное в заголовке соединение (1,7 мг, 2,9%) получали таким же образом, как описано в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-N-(пирвдин-2-ил)-5-(пирролидин-3-иламино)хинолин-8-карбоксамида гидрохлорид (48,7 мг, 0,12 ммоль), полученный в эталонном примере 147. 1H ЯМР (CDCl3, 400 МГц) δ 9,06 (тд, 1 Н), 8,79 (дд, 1 Н), 8,54-8,40 (м, 3 Н), 7,76-7,71 (м, 1 Н), 7,45-7,41 (м, 1 Н), 7,04-7,00 (м, 1 Н), 6,65 (т, 1 Н), 6,28 (д, 0,5 Н), 5,85 (д, 0,5 Н), 5,51-5,28 (м, 1 Н), 4,93 (дд, 1 Н), 4,32-4,26 (м, 1 Н), 4,13-3,39 (м, 4 Н), 3,29-3,05 (м, 3 Н), 2,78-2,64 (м, 2 Н), 2,57-2,21 (м, 3 Н), 2,12-1,97 (м, 1 Н).
[2116] Пример 295. N-(3-пиридил)-5-[[(3S)-1-[2-оксо-2-[(2S,4S)-2-циано-4-фторпирролидин-1-ил]этил]пирролидин-3-ил]амино]хинолин-8-карбоксамид
[2117] Указанное в заголовке соединение (2,6 мг, 5,5%) получали таким же образом, как описано в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-N-(пиридин-3-ил)-5-(пирролидин-3-иламино)хинолин-8-карбоксамида гидрохлорид (36,9 мг, 0,09 ммоль), полученный в эталонном примере 145. 1Н ЯМР (CDCl3, 400 МГц) δ 8,96-8,95 (м, 1 Н), 8,86 (т, 1 Н), 8,80-8,77 (м, 1 Н), 8,59-8,45 (м, 2 Н), 8,33-8,32 (м, 1 Н), 7,49-7,44 (м, 1 Н), 7,34-7,30 (м, 1 Н), 6,67 (т, 1 Н), 6,38 (д, 0,5 Н), 5,89 (д, 0,5 Н), 5,54-5,30 (м, 1 Н), 4,94 (дд, 1 Н), 4,34-4,28 (м, 1 Н), 4,15-3,39 (м, 4 Н), 3,29-3,07 (м, 3 Н), 2,80-2,67 (м, 2 Н), 2,58-2,23 (м, 3 Н), 2,13-1,99 (м, 1 Н).
[2118] Пример 296. N-[5-[[(3S)-1-[2-оксо-2-[(2S)-2-цианопирролидин-1-ил]этил]пирролидин-3-ил] амино]-8-хинолил] ацетамид
[2119] Указанное в заголовке соединение (5,9 мг, 12,2%) получали таким же образом, как и в примере 5, за исключением того, что вместо (S)-N-(пирролидин-3-ил)хинолин-4-амина гидрохлорида использовали (S)-N-(5-(пирролидин-3-иламино)хинолин-8-ил)ацетамид гидрохлорид (41,2 мг, 0,12 ммоль), полученный в эталонном примере 148. 1H ЯМР (CDCl3, 400 МГц) δ 9,47 (с, 1 Н), 8,76-8,74 (м, 1 Н), 8,59-8.57 (м, 1 Н), 8,39-8,28 (м, 1 Н), 7,40-7,36 (м, 1 Н), 6,52 (т, 1 Н), 4,79-4,72 (м, 1 Н), 4,17-4,09 (м, 1 Н), 3,64-3.58 (м, 1 Н), 3,54-3,23 (м, 3 Н), 3,09-2,91 (м, 3 Н), 2,74-2,59 (м, 1 Н), 2,47-2,02 (м, 9 Н), 1,96-1,86 (м, 1 Н).
[2120] Пример 297. N-[5-[[(3S)-1-[2-оксо-2-[(2S,4S)-2-циано-4-фторпирролидин-1-ил]этил]пирролидин-3-ил]амино]-8-хинолил]ацетамид
[2121] Указанное в заголовке соединение (3,9 мг, 7,6%) получали таким же образом, как и в примере 28, за исключением того, что вместо (S)-N-(пирролвдин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-N-(5-(пирролидин-3-иламино)хинолин-8-ил) ацетамид гидрохлорид (41,2 мг, 0,12 ммоль), полученный в эталонном примере 148. 1H ЯМР (CDCl3, 400 МГц) δ 9,47-9,46 (м, 1 Н), 8,77-8,74 (м, 1 Н), 8,56 (д, 1 Н), 8,3S-8,29 (м, 1 Н), 7,39-7,36 (м, 1 Н), 6,52-6,48 (м, 1 Н), 5,45-5,21 (м, 1 Н), 5,01-4,88 (м, 2 Н), 4,17-4,12 (м, 1 Н), 4,08-3,38 (м, 3 Н), 3,31-3,26 (м, 1 Н), 3,14-3,01 (м, 1 Н), 2,96-2,89 (м, 1 Н), 2,71-2,54 (м, 2 Н), 2,47-2,18 (м, 5 Н), 2,00-1,83 (м, 1 Н).
[2122] Пример 298. N-[5-[[(3S)-1-[2-оксо-2-[(2S,4S)-2-циано-4-фторпирролидин-1-ил]этил] пирролидин-3-ил] амино]-8-хинолил]бензамид
[2123] Указанное в заголовке соединение (9,8 мг, 16,8%) получали таким же образом, как и в примере 28, за исключением того, что вместо (S)-N-(пирролидин-3-ил)фуро[3,2-с]пиридин-7-амина гидрохлорида использовали (S)-N-(5-(пирролидин-3-иламино)хинолин-8-ил) бензамид гидрохлорид (48,5 мг, 0,12 ммоль), полученный в эталонном примере 149. 1H ЯМР (CDCl3, 400 МГц) δ 10,46 (с, 1 Н), 8,83-8,78 (м, 2 Н), 8,36-8,3S (м, 1 Н), 8,06-8,02 (м, 2 Н), 7,60-7,48 (м, 3 Н), 7,43-7,40 (м, 1 Н), 6,59 (т, 1 Н), 5,47-5,23 (м, 1 Н), 5,02-4,91 (м, 2 Н), 4,22-4,18 (м, 1 Н), 4,15-3,55 (м, 3 Н), 3,48-3,13 (м, 1 Н), 3,10-2,93 (м, 2 Н), 2,75-2,59 (м, 2 Н), 2,53-2,16 (м, 2,5 Н), 2,05-1,88 (м, 1,5 Н).
[2124] Пример 299. (2S,4S)-4-фтор-1-[2-[(3S)-3-[(6-метокси-4-хинолил)окси]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2125] (2S,4S)-1-(2-хлорацетил)-4-фторпирролидин-2-карбонитрил (152 мг, 0,80 ммоль), полученный в эталонном примере 2, растворяли в безводном ацетонитриле (4,0 мл). К полученному раствору добавляли (S)-6-метокси-4-(пирролидин-3-илокси)хинолина гидрохлорид (224 мг, 0,80 ммоль), полученный в эталонном примере 150, карбонат калия (441 мг, 3,2 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции к реакционной смеси добавляли воду. Водный слой реакционной смеси экстрагировали дихлорметаном. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (дихлорметан / метанол = 10/1, об./об.) с получением указанного в заголовке соединения (76 мг, 24%). 1H ЯМР (CDCl3, 600 МГц) δ 8,54 (д, 1 Н), 7,89 (д, 1 Н), 7,41 (с, 1 Н), 7,32 (д, 1 Н), 6,56 (д, 1 Н), 5,41-5,17 (м, 1,3 Н), 5,12-5,00 (м, 1 Н), 4,91 (д, 0,7 Н), 4,17-4,04 (м, 1 Н), 3,91 (с, 3 Н), 3,79-3,29 (м, 3 Н), 3,23-3,09 (м, 1 Н), 3,07-2,89 (м, 2 Н), 2,75-2,54 (м, 2 Н), 2,48-2,40 (м, 1 Н), 2,32-2,09 (м, 2 Н)
[2126] Пример 300. (2S,4S)-4-фтор-1-[2-[(3S)-3-[(6,7-диметокси-4-хинолил)окси]пирролидин-1-ил]ацетил]пирролидин-2-карбонитрил
[2127] (2S,4S)-1-(2-хлорацетил)-4-фторпирролидин-2-карбонитрил (71 мг, 0,37 ммоль), полученный в эталонном примере 2, растворяли в безводном ацетонитриле (2,0 мл). К полученному раствору добавляли (S)-6,7-диметокси-4-(пирролидин-3-илокси)хинолина гидрохлорид (114 мг, 0,37 ммоль), полученный в эталонном примере 151, карбонат калия (204 мг, 1,5 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции к реакционной смеси добавляли воду. Водный слой реакционной смеси экстрагировали дихлорметаном. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищали с помощью колоночной хроматографии на силикагеле (дихлорметан / метанол = 10/1, об./об.) с получением указанного в заголовке соединения (40 мг, 25%). 1H ЯМР (CDCl3, 600 МГц) δ 8,52 (д, 1 Н), 7,39 (с, 1 Н), 7,35 (с, 1 Н), 6,53 (д, 1 Н), 5,46-5,20 (м, 1,4 Н), 5,14-5,01 (м, 1 Н), 4,94 (д, 0,6 Н), 4,23-4,12 (м, 1 Н), 4,01 (д, 6 Н), 3,96-3,60 (м, 2 Н), 3,47-2,91 (м, 4 Н), 2,80-2,57 (м, 2 Н), 2,50-2,40 (м, 1 Н), 2,37-2,10 (м, 2 Н)
[2128] Пример 301. N-[1-[2-оксо-2-[(25)-2-цианопирролидин-1-ил]этил]-4-пиперидил]хинолин-8-карбоксамид
[2129] Указанное в заголовке соединение (424,3 мг, 86,9%) получали таким же образом, как в примере 110, за исключением того, что вместо N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-(пиперидин-4-ил)хинолин-8-карбоксамида гидрохлорид (409,7 мг, 1,25 ммоль), полученный в эталонном примере 152. 1H-ЯМР (CDCl3, 400 МГц) δ 11,47 (с, 1 Н), 8,92 (д, 1 Н), 8,83 (д, 1 Н), 8,28 (д, 1 Н), 7,96 (д, 1 Н), 7,66 (т, 1 Н), 7,49 (т, 1 Н), 5,40-4,70 (м, 1 Н), 4,30-4,10 (м, 1 Н), 3,85-3,50 (м, 2 Н), 3,50-3,10 (м, 2 Н), 3,00-2,75 (м, 2 Н), 2,55-2,20 (м, 4 Н), 2,20-2,00 (м, 4 Н), 2,00-1,70 (м, 2 Н)
[2130] Пример 302. (2S)-1-[2-[4-[этил(3-хинолил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2131] Указанное в заголовке соединение (132,5 мг, 38,4%) получали аналогично тому, как описано в примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-этил-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид (230,4 мг, 0,88 ммоль), полученный в эталонном примере 153. 1H ЯМР (CDCl3, 400 МГц) δ 8,67 (д, 1 Н), 7,92-7,90 (м, 1 Н), 7,61-7,59 (м, 1 Н), 7,41-7,36 (м, 2 Н), 7,14 (д, 1 Н), 5,07-4,73 (м, 1 Н), 3,74-3,61 (м, 2 Н), 3,56-3,47 (м, 1 Н), 3,44-3,38 (м, 2 Н), 3,36-3,19 (м, 2 Н), 3,08-2,96 (м, 2 Н), 2,33-2,03 (м, 7 Н), 1,90-1,85 (м, 3 Н), 1,21 (т, 3 Н).
[2132] Пример 303. (2S)-1-[2-[4-[этил(6-хинолил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2133] Указанное в заголовке соединение (274,8 мг, 79,7%) получали аналогично тому, как описано в примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-этил-N-(пиперидин-4-ил)хинолин-6-амина гидрохлорид (230,4 мг, 0,88 ммоль), полученный в эталонном примере 154. 1H ЯМР (CDCl3, 400 МГц) δ 8,54 (дд, 1 Н), 7,90-7,86 (м, 2 Н), 7,30 (дд, 1 Н), 7,19 (кв, 1 Н), 6,77 (д, 1 Н), 5,06-4,79 (м, 1 Н), 3,71-3,58 (м, 2 Н), 3,53-3,43 (м, 1 Н), 3,39-3,3S (м, 2 Н), 3,29-3,12 (м, 2 Н), 3,04-2,93 (м, 2 Н), 2,31-1,96 (м, 6 Н), 1,86-1,78 (м, 4 Н), 1,18 (т, 3 Н).
[2134] Пример 304. (2S,4S)-1-[2-[4-[этил(3-хинолил)амино]-1-пиперидил]ацетил]-4-фторпирролидин-2-карбонитрил
[2135] Указанное в заголовке соединение (12,4 мг, 27,5%) получали таким же образом, как и в примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-этил-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид (36,1 мг, 0,11 ммоль), полученный в эталонном примере 153. 1H ЯМР (CDCl3, 400 МГц) δ 8,69 (д, 1 Н), 7,95-7,92 (м, 1 Н), 7,63-7,61 (м, 1 Н), 7,44-7,40 (м, 2 Н), 7,17 (с, 1 Н), 5,51-4,94 (м, 2 Н), 4,21-4,12 (м, 1 Н), 4,02-3,71 (м, 2 Н), 3,47-3,40 (м, 3 Н), 3,30-3,19 (м, 2 Н), 3,12-2,99 (м, 2 Н), 2,80-2,64 (м, 1 Н), 2,50-2,24 (м, 3 Н), 1,89-1,88 (м, 3 Н), 1,23 (т, 3 Н).
[2136] Пример 305. (2S,4S)-1-[2-[4-[этил(5-хинолил)амино]-1-пиперидил]ацетил]-4-фторпирролидин-2-карбонитрил
[2137] Указанное в заголовке соединение (39,8 мг, 88,5%) получали таким же образом, как и в примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-этил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид (36,1 мг, 0,11 ммоль), полученный в эталонном примере 155. 1H ЯМР (CDCl3, 400 МГц) δ 8,84 (д, 1 Н), 8,63 (м, 1 Н), 7,83 (д, 1 Н), 7,61 (т, 1 Н), 7,35 (кв, 1 Н), 7,26 (d 1 Η), 5,44-4,83 (м, 2 Η), 4,10-3,83 (м, 1 Η), 3,79-3,66 (м, 1 Η), 3,37-3,06 (м, 4 Η), 2,99-2,94 (м, 1 Η), 2,90-2,76 (м, 2 Η), 2,69-2,20 (м, 2 Η), 2,07-2,00 (м, 2 Η), 1,81-1,59 (м, 4 Η), 0,86 (т, 3 Η).
[2138] Пример 306. (2S,4S)-1-[2-[4-[этил(6-хинолил)амино]-1-пиперидил]ацетил]-4-фторпирролидин-2-карбонитрил
[2139] Указанное в заголовке соединение (35,4 мг, 78,6%) получали таким же образом, как и в примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-этил-N-(пиперидин-4-ил)хинолин-6-амина гидрохлорид (36,1 мг, 0,11 ммоль), полученный в эталонном примере 154. 1H ЯМР (CDCl3, 400 МГц) δ 8,54 (дд, 1 Н), 7,90 (с, 1 Н), 7,87 (с, 1 Н), 7,32-7,29 (м, 1 Н), 7,20 (кв, 1 Н), 6,78-6,77 (м, 1 Н), 5,44-4,87 (м, 2 Н), 4,13-4,04 (м, 1 Н), 3,95-3,64 (м, 2 Н), 3,39-3,34 (м, 2 Н), 3,26-3,13 (м, 2 Н), 3,06-2,94 (м, 2 Н), 2,36-2,22 (м, 3 Н), 1,86-1,82 (м, 4 Н), 1,18 (т, 3 Н).
[2140] Пример 307. (2S)-1-[2-[4-[метил(2-хинолил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2141] Указанное в заголовке соединение (45,7 мг, 13,7%) получали аналогично тому, как описано в примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-метил-N-(пиперидин-4-ил)хинолин-2-амина гидрохлорид (276,5 мг, 0,88 ммоль), полученный в эталонном примере 156. 1H ЯМР (CDCl3, 400 МГц) δ 7,86 (д, 1 Н), 7,67 (д, 1 Н), 7,58 (д, 1 Н), 7,51 (т, 1 Н), 7,17 (т, 1 Н), 6,88 (д, 1 Н), 5,19-4,71 (м, 2 Н), 3,81-3,73 (м, 2 Н), 3,59-3,55 (м, 1 Н), 3,42-3,22 (м, 2 Н), 3,08-3,04 (м, 4 Н), 2,39 (т, 2 Н), 2,29-2,11 (м, 4 Н), 1,96-1,90 (м, 2 Н), 1,76 (д, 2 Н).
[2142] Пример 308. (2S)-1-[2-[4-[метил(4-хинолил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2143] Указанное в заголовке соединение (79,5 мг, 23,9%) получали таким же образом, как в примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-метил-N-(пиперидин-4-ил)хинолин-4-амина гидрохлорид (276,5 мг, 0,88 ммоль), полученный в эталонном примере 157. 1H ЯМР (CDCl3, 400 МГц) δ 8,67 (д, 1 Н), 8,04 (д, 1 Н), 7,94 (д, 1 Н), 7,65 (т, 1 Н), 7,46 (т, 1 Н), 6,85 (д, 1 Н), 5,09-4,75 (м, 1 Н), 3,70-3,48 (м, 3 Н), 3,31-3,12 (м, 4 Н), 2,89 (с, 3 Н), 2,29-2,01 (м, 8 Н), 1,80 (д, 2 Н).
[2144] Пример 309. (2S)-1-[2-[4-[метил(5-хинолил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2145] Указанное в заголовке соединение (220,8 мг, 66,4%) получали аналогично тому, как описано в примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид (276,5 мг, 0,88 ммоль), полученный в эталонном примере 158. 1H ЯМР (CDCl3, 400 МГц) δ 8,88 (д, 1 Н), 8,51 (д, 1 Н), 7,80 (д, 1 Н), 7,62 (т, 1 Н), 7,38 (кв, 1 Н), 7,20 (д, 1 Н), 5,18-4,72 (м, 1 Н), 3,72-3,48 (м, 2 Н), 3,33-3,02 (м, 3 Н), 2,95-2,81 (м, 5 Н), 2,34-2,06 (м, 6 Н), 2,01-1,80 (м, 4 Н).
[2146] Пример 310. (2S)-1-[2-[4-[метил(6-хинолил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2147] Указанное в заголовке соединение (171,0 мг, 51,4%) получали аналогично тому, как описано в Примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-метил-N-(пиперидин-4-ил)хинолин-6-амина гидрохлорид (276,5 мг, 0,88 ммоль), приготовленный в эталонном примере 159. 1H ЯМР (CDCl3, 400 МГц) δ 8,62 (д, 1 Н), 7,93 (д, 2 Н), 7,42 (д, 1 Н), 7,26 (кв, 1 Н), 6,85 (д, 1 Н), 5,11-4,75 (м, 1 Н), 3,79-3,63 (м, 2 Н), 3,58-3,49 (м, 1 Н), 3,38-3,20 (м, 2 Н), 3,16-2,97 (м, 2 Н), 3,29 (с, 3 Н), 2,35-2,08 (м, 7 Н), 1,99-1,88 (м, 1 Н), 1,78-1,75 (м, 2 Н).
[2148] Пример 311. (2S)-1-[2-[4-[метил(7-хинолил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2149] Указанное в заголовке соединение (35,8 мг, 10,7%) получали аналогично тому, как описано в Примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-метил-N-(пиперидин-4-ил)хинолин-7-амина гидрохлорид (276,5 мг, 0,88 ммоль), полученный в эталонном примере 160. 1H ЯМР (CDCl3, 400 МГц) δ 8,73 (д, 1 Н), 7,96 (д, 1 Н), 7,64 (д, 1 Н), 7,22 (д, 2 Н), 7,10 (кв, 1 Н), 5,14-4,77 (м, 1 Н), 3,86-3,55 (м, 3 Н), 3,39-3,00 (м, 4 Н), 2,94 (с, 3 Н), 2,45-2,09 (м, 6 Н), 2,03-1,89 (м, 2 Н), 1,81-1,78 (м, 2 Н).
[2150] Пример 312. (2S)-1-[2-[4-[фуро[3,2-с]пиридин-7-ил(метил)амино]-1-пиперидил]ацетил]пирролид ин-2-карбонитрил
[2151] Указанное в заголовке соединение (139,4 мг, 43,1%) получали таким же образом, как и в примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-метил-N-(пиперидин-4-ил)фуро[3,2-с]пиридин-7-амина гидрохлорид (267,7 мг, 0,88 ммоль), полученный в эталонном примере 161. 1H ЯМР (CDCl3, 400 МГц) δ 8,46 (с, 1 Н), 7,98 (с, 1 Н), 7,63 (с, 1 Н), 6,81 (с, 1 Н), 5,17-4,75 (м, 1 Н), 3,96-3,90 (м, 1 Н), 3,76-3,64 (м, 1 Н), 3,57-3,51 (м, 1 Н), 3,39-3,19 (м, 2 Н), 3,04-2,95 (м, 5 Н), 2,36-1,92 (м, 8 Н), 1,81-1,78 (м, 2 Н).
[2152] Пример 313. (2S)-1-[2-[4-[5-изохинолил(метил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2153] Указанное в заголовке соединение (28,4 мг, 8,5%) получали таким же образом, как и в примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-метил-N-(пиперидин-4-ил)изохинолин-5-амина гидрохлорид (267,7 мг, 0,88 ммоль), полученный в эталонном примере 162. 1H ЯМР (MeOD4, 400 МГц) δ 9,18 (с, 1 Н), 8,42 (д, 1 Н), 8,06 (д, 1 Н), 7,75 (д, 1 Н), 7,64-7,51 (м, 2 Н), 4,74-4,64 (м, 1 Н), 3,73-3,50 (м, 2 Н), 3,26-2,85 (м, 8 Н), 2,22-2,09 (м, 6 Н), 1,95-1,80 (м, 4 Н).
[2154] Пример 314. (2S)-1-(2-(4-(изохинолин-6-ил(метил)амино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил
[2155] Указанное в заголовке соединение (146,1 мг, 44,0%) получали таким же образом, как и в примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-метил-N-(пиперидин-4-ил)изохинолин-6-амина гидрохлорид (267,7 мг, 0,88 ммоль), полученный в эталонном примере 163. 1H ЯМР (MeOD4, 400 МГц) δ 8,84 (с, 1 Н), 8,13 (д, 1 Н), 7,86 (д, 1 Н), 7,51 (д, 1 Н), 7,41-7,38 (м, 1 Н), 6,92 (с, 1 Н), 5,17-4,76 (м, 1 Н), 3,96-3,90 (м, 1 Н), 3,78-3,73 (м, 1 Н), 3,61-3,53 (м, 1 Н), 3,45-3,22 (м, 3 Н), 3,10-3,08 (м, 2 Н), 2,96 (с, 3 Н), 2,39-2,33 (м, 2 Н), 2,28-2,12 (м, 4 Н), 2,05-1,96 (м, 1 Н), 1,74-1,71 (м, 2 Н).
[2156] Пример 315. (2S,4S)-4-фтор-1-[2-[4-[метил(б-хинолил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2157] Указанное в заголовке соединение (4,4 мг, 10,2%) получали таким же образом, как и в примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-метил-N-(пиперидин-4-ил)хинолин-6-амина гидрохлорид(34,5 мг, 0,11 ммоль), полученный в эталонном примере 159. 1H ЯМР (CDCl3, 400 МГц) δ 8,62 (д, 1 Н), 7,94 (д, 2 Н), 7,41 (д, 1 Н), 7,27 (т, 1 Н), 6,85 (с, 1 Н), 5,49-4,93 (м, 2 Н), 4,21-3,91 (м, 1 Н), 3,87-3,75 (м, 2 Н), 3,46-3,18 (м, 2 Н), 3,11-2,98 (м, 2 Н), 2,91 (с, 3 Н), 2,80-2,63 (м, 1 Н), 2,40-2,24 (м, 3 Н), 2,15-1,90 (м, 2 Н), 1,79-1,76 (м, 2 Н).
[2158] Пример 316. (2S,4S)-4-фтор-1-[2-[4-[метил(3-хинолил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2159] Указанное в заголовке соединение (12,0 мг, 27,5%) получали таким же образом, как и в примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-метил-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид (34,5 мг, 0,11 ммоль), полученный в эталонном примере 164. 1H ЯМР (CDCl3, 400 МГц) δ 8,76 (д, 1 Н), 7,97-7,95 (м, 1 Н), 7,66-7,64 (м, 1 Н), 7,46-7,43 (м, 2 Н), 7,22 (д, 1 Н), 5,51-4,95 (м, 2 Н), 4,22-3,92 (м, 1 Н), 3,88-3,75 (м, 2 Н), 3,46-3,19 (м, 2 Н), 3,12-3,00 (м, 2 Н), 2,92 (с, 3 Н), 2,81-2,65 (м, 1 Н), 2,41-2,24 (м, 3 Н), 2,18-1,79 (м, 4 Н).
[2160] Пример 317. (2S,4S)-4-фтор-1-[2-[4-[3-изохинолил(метил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2161] Указанное в заголовке соединение (18,7 мг, 43,1%) получали таким же образом, как и в примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-метил-N-(пиперидин-4-ил)изохинолин-3-амина гидрохлорид (34,5 мг, 0,11 ммоль), полученный в эталонном примере 165. 1H ЯМР (CDCl3, 400 МГц) δ 8,75 (д, 1 Н), 7,95 (кв, 1 Н), 7,65-7,63 (м, 1 Н), 7,43 (кв, 2 Н), 7,21 (д, 1 Н), 5,49-4,93 (м, 2 Н), 4,20-3,91 (м, 1 Н), 3,87-3,73 (м, 2 Н), 3,45-3,17 (м, 2 Н), 3,11-2,99 (м, 2 Н), 2,91 (с, 3 Н), 2,76-2,63 (м, 1 Н), 2,40-2,24 (м, 3 Н), 2,13-1,77 (м, 4 Н).
[2162] Пример 318. (2S,4S)-4-фтор-1-[2-[4-[5-изохинолил(метил)амино]-1-пиперид ил]ацетил]пирролидин-2-карбонитрил
[2163] Указанное в заголовке соединение (28,4 мг, 65,4%) получали таким же образом, как и в примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-метил-N-(пиперидин-4-ил)юохинолин-5-амина гидрохлорид (34,5 мг, 0,11 ммоль), полученный в эталонном примере 162. 1H ЯМР (CDCl3, 400 МГц) δ 9,21 (с, 1 Н), 8,51 (дд, 1 Н), 7,91 (д, 1 Н), 7,65 (д, 1 Η), 7,52 (т, 1 Η), 7,33 (д, 1 Η), 5,47-4,91 (м, 2 Η), 4,18-3,90 (м, 1 Η), 3,85-3,72 (м, 1 Η), 3,42-3,13 (м, 3 Η), 2,99-2,86 (м, 2 Η), 2,82 (с, 3 Η), 2,78-2,61 (м, 1 Η), 2,38-1,82 (м, 7 Η).
[2164] Пример 319. (2S,4S)-4-фтор-1-[2-[4-[7-изохинолил(метил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2165] Указанное в заголовке соединение (14,0 мг, 32,1%) получали таким же образом, как и в примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-метил-N-(пиперидин-4-ил)юохинолин-7-амина гидрохлорид (34,5 мг, 0,11 ммоль), полученный в эталонном примере 166. 1H ЯМР (CDCl3, 400 МГц) δ 9,06 (с, 1 Н), 8,27 (дд, 1 Н), 7,69 (д, 1 Н), 7,49 (д, 1 Н), 7,40 (д, 1 Н), 7,02 (с, 1 Н), 5,51-4,95 (м, 2 Н), 4,23-3,92 (м, 1 Н), 3,88-3,75 (м, 2 Н), 3,47-3,23 (м, 2 Н), 3,12-3,00 (м, 2 Н), 2,92 (с, 3 Н), 2,77-2,65 (м, 1 Н), 2,41-2,29 (м, 3 Н), 2,05-1,89 (м, 2 Н), 1,80-1,77 (м, 2 H).
[2166] Пример 320. (2S,4S)-4-фтор-1-[2-[4-[8-изохинолил(метил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2167] Указанное в заголовке соединение (20,4 мг, 46,9%) получали таким же образом, как и в примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-метил-N-(пиперидин-4-ил)юохинолин-8-амина гидрохлорид (34,5 мг, 0,11 ммоль), полученный в эталонном примере 166. 1H ЯМР (CDCl3, 400 МГц) δ 9,51 (с, 1 Н), 8,45 (дд, 1 Н), 7,59-7,43 (м, 3 Н), 7,17 (д, 1 Н), 5,45-4,87 (м, 2 Н), 4,11-3,70 (м, 2 Н), 3,47-3,09 (м, 3 Н), 2,92-2,89 (м, 2 Н), 2,82 (с, 3 Н), 2,74-2,57 (м, 2 Н), 2,37-2,22 (м, 2 Н), 2,09-2,03 (м, 2 Н), 1,88-1,81 (м, 2 Н).
[2168] Пример 321. (2S)-1-[2-[4-[3-изохинолил(метил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2169] Указанное в заголовке соединение (97,5 мг, 28,0%) получали таким же образом, как и в примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-метил-N-(пиперидин-4-ил)изохинолин-3-амина гидрохлорид (27б,5 мг, 0,88 ммоль), полученный в эталонном примере 165. 1H ЯМР (CDCl3, 400 МГц) δ 8,75 (д, 1 Н), 7,96-7,93 (м, 1 Н), 7,65-7,63 (м, 1 Н), 7,44-7,42 (м, 2 Н), 7,20 (д, 1 Н), 5,10-4,76 (м, 1 Н), 3,79-3,65 (м, 2 Н), 3,57-3,51 (м, 1 Н), 3,38-3,17 (м, 2 Н), 3,12-3,07 (м, 2 Н), 2,91 (с, 3 Н), 2,37-1,79 (м, 10 Н).
[2170] Пример 322. (2S)-1-[2-[4-[метил-(6-метил-3-хинолил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2171] Указанное в заголовке соединение (75,9 мг, 22,0%) получали аналогично тому, как описано в примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали Ν, 6-диметил-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид (344,5 мг, 0,88 ммоль), полученный в эталонном примере 168. 1H ЯМР (CDCl3, 400 МГц) δ 8,65 (д, 1 Н), 7,82 (д, 1 Н), 7,39 (с, 1 Н), 7,24 (д, 1 Н), 7,11 (д, 1 Н), 5,09-4,75 (м, 1 Н), 4,21-3,96 (м, 2 Н), 3,67-3,50 (м, 3 Н), 3,3S-3,18 (м, 2Н), 3,06-2,96 (м, 2 Н), 2,88 (с, 3 Н), 2,47 (с, 3 Н), 2,30-2,06 (м, 5 Н), 1,98-1,87 (м, 3 Н).
[2172] Пример 323. (S)-1-(2-(4-((б-метоксихинолин-3-ил)(метил)амино)пиперидин-1-ил)ацетил)пирролид ин-2-карбонитрил
[2173] Указанное в заголовке соединение (55,8 мг, 15,5%) получали таким же образом, как и в примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 6-метокси-N-метил-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид (344,5 мг, 0,88 ммоль), полученный в эталонном примере 169. 1H ЯМР (CDCl3, 400 МГц) δ 8,54 (д, 1 Н), 7,80 (д, 1 Н), 7,09 (д, 1 Н), 7,04 (дд, 1 Н), 6,69 (д, 1 Н), 5,06-4,72 (м, 1 Н), 3,87 (с, 3 Н), 3,75-3,60 (м, 2 Н), 3,55-3,46 (м, 1 Н), 3,34-3,13 (м, 2 Н), 3,05-2,94 (м, 2 Н), 2,87 (с, 3 Н), 2,36-1,86 (м, 8 Н), 1,74 (д, 2 Н).
[2174] Пример 324. (2S)-1-[2-[4-[(7-метокси-3-хинолил)-метил-амино]-1-пиперидил]ацетил]пирролид ин-2-карбонитрил
[2175] Указанное в заголовке соединение (59,0 мг, 16,4%) получали аналогично тому, как описано в примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 7-метокси-N-метил-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид (344,5 мг, 0,88 ммоль), полученный в эталонном примере 170. 1H ЯМР (CDCl3, 400 МГц) δ 8,68 (д, 1 Н), 7,55 (д, 1 Н), 7,32 (д, 1 Н), 7,24 (д, 1 Н), 7,13 (д, 1 Н), 5,13-4,78 (м, 1 Н), 4,15-3,96 (м, 1 Н), 3,92 (с, 3 Н), 3,71-3,49 (м, 3 Н), 3,35-3,17 (м, 2 Н), 3,07-2,97 (м, 2 Н), 2,88 (с, 3 Н), 2,47 (с, 3 Н), 2,33-1,87 (м, 10 Н).
[2176] Пример 325. (2S)-1-[2-[4-[метил-(8-метокси-3-хинолил)амино]-1-пиперидил]ацетил]пирролид ин-2-карбонитрил
[2177] Указанное в заголовке соединение (53,3 мг, 14,8%) получали аналогично тому, как описано в Примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 8-метокси-N-метил-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид (344,5 мг, 0,88 ммоль), приготовленный в эталонном примере 171. 1H ЯМР (CDCl3, 400 МГц) δ 8,65 (д, 1 Н), 7,27 (т, 1 Н), 7,14 (д, 1 Н), 7,10 (д, 1 Н), 6,71 (д, 1 Н), 5,02-4,67 (м, 1 Н), 3,97 (с, 3 Н), 3,71-3,40 (м, 3 Н), 3,29-3,08 (м, 2 Н), 3,00-2,90 (м, 2Н), 2,83 (с, 3 Н), 2,31-1,97 (м, 6Н), 1,92-1,82 (м, 2Н), 1,71-1,68 (м, 2Н).
[2178] Пример 326. (2S,4S)-4-фтор-1-[2-[4-[метил-(6-метил-3-хинолил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2179] Указанное в заголовке соединение (13,0 мг, 28,9%) получали аналогично тому, как описано в примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-гидрохлорид N,6-диметил-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид (36,1 мг, 0,11 ммоль), полученный в эталонном примере 168. 1H ЯМР (CDCl3, 400 МГц) δ 8,66 (д, 1 Н), 7,83 (д, 1 Н), 7,40 (с, 1 Н), 7,27-7,24 (м, 1 Н), 7,12 (д, 1 Н), 5,49-4,93 (м, 2 Н), 4,19-4,01 (м, 1 Н), 3,81-3,70 (м, 2 Н), 3,29-3,15 (м, 2 Н), 3,09-2,93 (м,2 Н), 2,88 (с, 3 Н), 2,47 (с, 3 Н), 2,24-1,89 (м, 6 Н), 1,79-1,76 (м, 2 Н).
[2180] Пример 327. (2S,4S)-4-фтор-1-(2-(4-((6-метоксихинолин-3-ил)(метил)амино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил
[2181] Указанное в заголовке соединение (7,3 мг, 15,5%) получали таким же образом, как и в примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 6-метокси-N-метил-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид (37,8 мг, 0,11 ммоль), полученный в эталонном примере 169. 1H ЯМР (CDCl3, 400 МГц) δ 8,54 (д, 1 Н), 7,80 (д, 1 Н), 7,09 (д, 1 Н), 7,04 (дд, 1 Н), 6,90 (д, 1 Н), 5,46-5,24 (м, 2 Н), 4,14-3,90 (м, 1 Н), 3,87 (с, 3 Н), 3,84-3,68 (м, 2 Н), 3,40-3,13 (м, 2 Η), 3,07-2,92 (м, 2 Η), 2,86 (с, 3 Η), 2,75-2,57 (м, 1 Η), 2,37-2,20 (м, 3 Η), 2,10-1,84 (м, 2 Η), 1,76-1,63 (м, 2 Η).
[2182] Пример 328. (2S,4S)-4-фтор-1-(2-(4-((7-метоксихинолин-3-ил)(метил)амино)пиперидин-1-ил)ацетил)пирролидин-2-карбонитрил
[2183] Указанное в заголовке соединение (11,6 мг, 24,7%) получали таким же образом, как и в примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 7-метокси-N-метил-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид (37,8 мг, 0,11 ммоль), полученный в эталонном примере 170. 1H ЯМР (CDCl3, 400 МГц) δ 8,68 (с, 1 Н), 7,55 (д, 1 Н), 7,32 (д, 1 Н), 7,24 (д, 1 Н), 7,13 (дд, 1 Н), 5,50-4,94 (м, 2 Н), 4,21-4,12 (м, 1 Н), 3,87 (с, 3 Н), 3,78-3,64 (м, 2 Н), 3,46-3,17 (м, 2 Н), 3,10-2,97 (м, 2 Н), 2,88 (с, 3 Н), 2,80-2,64 (м, 1 Н), 2,49-2,24 (м, 3 Н), 2,12-2,02 (м, 1 Н), 1,97-1,84 (м, 3 Н).
[2184] Пример 329. (2S,4S)-4-фтор-1-[2-[4-[(8-метокси-3-хинолил)-метил-амино]-1-пиперидил]ацетил]пирролид ин-2-карбонитрил
[2185] Указанное в заголовке соединение (3,8 мг, 8,0%) получали аналогично тому, как описано в Примере 131, за исключением того, что вместо 3-метил-М-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 8-метокси-N-метил-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид (37,8 мг, 0,11 ммоль), приготовленный в эталонном примере 171. 1H ЯМР (CDCl3, 400 МГц) δ 8,72 (д, 1 Н), 7,35 (т, 1 Н), 7,22 (д, 1 Н), 7,18 (д, 1 Н), 6,80 (д, 1 Н), 5,50-4,94 (м, 2 Н), 4,21-4,12 (м, 1 Н), 4,06 (с, 3 Н), 3,88-3,73 (м, 2 Н), 3,46-3,21 (м, 2 Н), 3,11-2,96 (м, 2 Н), 2,91 (с, 3 Н), 2,80-2,65 (м, 1 Н), 2,50-2,22 (м, 3 Н), 2,15-1,86 (м, 2 Н), 1,81-1,78 (м, 3 Н).
[2186] Пример 330. (2S,4S)-4-фтор-1-[2-[4-[(8-фтор-5-хинолил)амино]-1-пиперидил]ацетил]пирролид ин-2-карбонитрил
[2187] (2S,4S)-1-(2-хлорацетил)-4-фторпирролидин-2-карбонитрил (90,4 мг, 0,47 ммоль), полученный в эталонном примере 2, растворяли в безводном ацетонитриле (4 мл). К полученному раствору добавляли 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид (151,0 мг, 0,47 ммоль), полученный в эталонном примере 172, и карбонат калия (262,3 мг, 1,90 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции к реакционной смеси добавляли воду. Водный слой реакционной смеси экстрагировали этилацетатом. Экстрагированный органический слой высушивали и фильтровали над безводным сульфатом магния. Отфильтрованный раствор концентрировали и затем очищалис помощью колоночной хроматографии на силикагеле (дихлорметан / метанол = 10/1, об./об.) с получением указанного в заголовке соединения (76,2 мг, 40,2%). 1H-ЯМР (CD3OD, 400 МГц) δ 8,94 (д, 1 Н), 8,18 (д, 1 Н), 7,42 (д, 1 Н), 7,30-7,26 (м, 1 Н), 6,55 (д, 1 Н), 5,50-5,30 (м, 1 Н), 5,10-4,80 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,05-3,85 (м, 1 Н), 3,85-3,70 (м, 2 Н), 3,55-3,15 (м, 2 Н), 3,05-2,85 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,50-2,30 (м, 2 Н), 2,20-2,05 (м, 2 Н), 1,90-1,55 (м, 3 Н)
[2188] Пример 331. (2S,4S)-4-фтор-1-[2-[4-[(8-метил-5-хинолил)амино]-1-пиперидил]ацетил]пирролид ин-2-карбонитрил
[2189] Указанное в заголовке соединение (46,7 мг, 24,9%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 8-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид (61,2 мг, 0,20 ммоль), полученный в эталонном примере 173. 1H-ЯМР (CDCl3, 400 МГц) δ 8,93 (д, 1 Н), 8,17 (д, 1 Н), 7,42-7,33 (м, 2 Н), 6,60 (д, 1 Н), 5,55-5,30 (м, 1 Н), 5,05-4,90 (м, 1 Н), 4,30-4,10 (м, 1 Н), 4,05-3,65 (м, 2 Н), 3,55-3,16 (м, 3 Н), 3,05-2,85 (м, 2 Н), 2,80-2,68 (м, 1 Н), 2,68 (с, 3 Н), 2,50-2,25 (м, 2 Н), 2,25-2,05 (м, 2 Н), 1,95-1,50 (м, 3 Н)
[2190] Пример 332. (2S,4S)-1-[2-[4-[(8-бензилокси-5-хинолил)амино]-1-пиперидил]ацетил]-4-фторпирролидин-2-карбонитрил
[2191] Указанное в заголовке соединение (109,7 мг, 47,4%) получали таким же образом, как и в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 8-(бензилокси)-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид (134,2 мг, 0,3S ммоль), полученный в эталонном примере 174. 1H-ЯМР (CDCl3, 400 МГц) δ 8,97 (д, 1 Н), 8,19 (д, 1 Н), 7,51-7,49 (м, 2 Н), 7,41-7,26 (м, 4 Н), 6,92 (д, 1 Н), 6,53 (д, 1 Н), 5,55-5,30 (м, 1 Н), 5,48 (с, 2 Н), 5,00-4,85 (м, 1 Н), 4,30-4,10 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,55-3,20 (м, 3 Н), 3,05-2,80 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,50-2,25 (м, 2 Н), 2,25-2,05 (м, 2 Н), 1,80-1,50 (м, 3 Н)
[2192] Пример 333. (2S,4S)-1-[2-[4-[(3-хлор-5-хинолил)амино]-1-пиперидил]ацетил]-4-фторпирролидин-2-карбонитрил
[2193] Указанное в заголовке соединение (191,7 мг, 97,1%) получали таким же образом, как и в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 3-хлор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид (241,4 мг, 0,72 ммоль), полученный в эталонном примере 175. 1H-ЯМР (CDCl3, 400 МГц) δ 8,80 (с, 1 Н), 8,13 (с, 1 Н), 7,55 (т, 1 Н), 7,45 (д, 1 Н), 6,68 (д, 1 Н), 5,50-5,30 (м, 1 Н), 5,00-4,85 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,10-3,70 (м, 2Н), 3,60-3,10 (м, 3 Н), 3,10-2,85 (м, 2 Н), 2,85-2,60 (м, 1 Н), 2,50-2,30 (м, 2 Н), 2,30-2,10 (м, 2 Н), 1,90-1,50 (м, 3 Н)
[2194] Пример 334. (2S,4S)-4-фтор-1-[2-[4-[[8-(трифторметил)-5-хинолил]амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2195] Указанное в заголовке соединение (116,6 мг, 54,7%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-(пиперидин-4-ил)-8-(трифторметил)хинолин-5-амина гидрохлорид (137,5 мг, 0,37 ммоль), полученный в эталонном примере 176. 1H-ЯМР (CDCl3, 400 МГц) δ 9,01 (д, 1 Н), 8,16 (д, 1 Н), 7,89 (д, 1 Н), 7,41 (т, 1 Н), 6,56 (д, 1 Н), 5,55-5,30 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,30-4,10 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,70-3,15 (м, 3 Н), 3,10-2,85 (м, 2 Н), 2,80-2,55 (м, 1 Н), 2,50-2,35 (м, 2 Н), 2,35-2,10 (м, 2 Н), 1,95-1,55 (м, 3 Н)
[2196] Пример 335. 5-[[1-[2-оксо-2-[(2S,4S)-2-циано-4-фторпирролидин-1-ил]этил]-4-пиперидил]амино]хинолин-2-карбонитрил
[2197] Указанное в заголовке соединение (42,1 мг, 21,8%) получали таким же образом, как и в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 5-(пиперидин-4-иламино)хинолин-2-карбонитрил гидрохлорид (299,7 мг, 0,92 ммоль), полученный в эталонном примере 177. 1H-ЯМР (CDCl3, 400 МГц) δ 8,29 (д, 1 Н), 7,68-7,59 (м, 2 Н), 7,50 (д, 1 Н), 6,76 (д, 1 Н), 5,60-5,30 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,30-4,10 (м, 1 Н), 4,10-3,70 (м, 2 Н), 3,60-3,20 (м, 3 Н), 3,10-2,90 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,50-2,30 (м, 2 Н), 2,30-2,10 (м, 2 Н), 1,90-1,55 (м, 3 Н)
[2198] Пример 336. (2S,4S)-1-(2-(4-(бензо[b]тиофен-4-иламино)пиперидин-1-ил)ацетил)-4-фторпирролидин-2-карбонитрил
[2199] Указанное в заголовке соединение (239,9 мг, 93,6%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-(бензо[b]тиофен-4-ил)пиперидин-4-амина гидрохлорид (202,4 мг, 0,66 ммоль), полученный в эталонном примере 178. 1H-ЯМР (CDCl3, 400 МГц) δ 7,31 (с, 1 Н), 7,31-7,17 (м, 3 Н), 6,52 (д, 1 Н), 5,50-5,25 (м, 1 Н), 4,95-4,85 (м, 1 Н), 4,25-4,15 (м, 1 Н), 4,15-3,70 (м, 2 Н), 3,55-3,10 (м, 3 Н), 3,00-2,80 (м, 2 Н), 2,75-2,60 (м, 1 Н), 2,40-2,25 (м, 2 Н), 2,20-2,05 (м, 2 Н), 1,85-1,50 (м, 3 Н)
[2200] Пример 337. (2S,4S)-4-фтор-1-[2-[4-[(6-фтор-4-хинолил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2201] Указанное в заголовке соединение (22,9 мг, 23,2%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 6-фтор-N-(пиперидин-4-ил)хинолин-4-амина гидрохлорид (154,5 мг, 0,49 ммоль), полученный в эталонном примере 179. 1H-ЯМР (CDCl3, 400 МГц) δ 8,53 (д, 1 Н), 7,97 (д, 1 Н), 7,40 (с, 1 Н), 7,33 (д, 1 Н), 6,46 (д, 1 Н), 5,55-5,35 (м, 1 Н), 5,05-4,95 (м, 1 Н), 4,30-4,10 (м, 1 Н), 3,90-3,50 (м, 3 Н), 3,50-3,10 (м, 2 Н), 3,05-2,90 (м, 2 Н), 2,85-2,70 (м, 1 Н), 2,50-2,35 (м, 2 Н), 2,25-2,10 (м, 2 Н), 1,80-1,60 (м, 3 Н)
[2202] Пример 3S8. (2S,4S)-1-[2-[4-[(6-хлор-4-хинолил)амино]-1-пиперидил]ацетил]-4-фторпирролидин-2-карбонитрил
[2203] Указанное в заголовке соединение (35,0 мг, 34,0%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 6-хлор-N-(пиперидин-4-ил)хинолин-4-амина гидрохлорид (194,2 мг, 0,58 ммоль), полученный в эталонном примере 180. 1H-ЯМР (CDCl3, 400 МГц) δ 8,54 (д, 1 Н), 7,92 (д, 1 Н), 7,69 (с, 1 Н), 7,57 (д, 1 Н), 6,46 (д, 1 Н), 5,55-5,30 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,35-4,20 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,65-3,20 (м, 3 Н), 3,05-2,90 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,50-2,30 (м, 2 Н), 2,20-2,10 (м, 2 Н), 1,90-1,60 (м, 3 Н)
[2204] Пример 339. (2S,4S)-4-фтор-1-[2-[4-(4-изохиноламино)-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2205] Указанное в заголовке соединение (180,2 мг, 40,5%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-(пиперидин-4-ил)изохинолин-4-амина гидрохлорид (350,0 мг, 1,17 ммоль), полученный в эталонном примере 181. 1H-ЯМР (CDCl3, 400 МГц) δ 8,68 (с, 1 Н), 7,92-7,88 (м, 2 Н), 7,78 (д, 1 Н), 7,66 (т, 1 Н), 7,58 (т, 1 Н), 5,55-5,25 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,15-3,70 (м, 2 Н), 3,65-3,20 (м, 3 Н), 3,10-2,85 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,50-2,30 (м, 2 Н), 2,30-2,15 (м, 2 Н), 1,90-1,65 (м, 3 Н)
[2206] Пример 340. (2S,4S)-4-фтор-1-[2-[4-(5-изохиноламино)-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2207] Указанное в заголовке соединение (153,2 мг, 34,5%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-(пиперидин-4-ил)изохинолин-5-амина гидрохлорид (305,9 мг, 1,02 ммоль), полученный в эталонном примере 182. 1H-ЯМР (CDCl3, 400 МГц) δ 9,15 (с, 1 Η), 8,47 (д, 1 Η), 7,54 (д, 1 Η), 7,45 (т, 1 Η), 7.31 (д, 1 Η), 6,78 (д, 1 Η), 5,55-5,25 (м, 1 Η), 5,00-4,85 (м, 1 Η), 4,30-4,15 (м, 1 Η), 4,10-3,70 (м, 2 Η), 3,60-3,15 (м, 3 Η), 3,05-2,85 (м, 2 Η), 2,80-2,60 (м, 1 Η), 2,50-2,30 (м, 2 Η), 2,30-2,10 (м, 2 Η), 1,90-1,55 (м, 3 Η)
[2208] Пример 341. (2S,4S)-4-фтор-1-[2-[4-(6-изохиноламино)-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2209] Указанное в заголовке соединение (28,4 мг, 6,4%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-(пиперидин-4-ил)изохинолин-6-амина гидрохлорид (137,6 мг, 0,46 ммоль), полученный в эталонном примере 183. 1H-ЯМР (CDCl3, 400 МГц) δ 8,93 (с, 1 Н), 8,31 (д, 1 Н), 7,71 (д, 1 Н), 7,37 (д, 1 Н), 6,89 (д, 1 Н), 6,65 (с, 1 Н), 5,55-5,25 (м, 1 Н), 5,00-4,85 (м, 1 Н), 4,35-4,15 (м, 1 Н), 4,15-3,70 (м, 2 Н), 3,55-3,15 (м, 3 Н), 3,05-2,85 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,50-2,30 (м, 2 Н), 2,25-2,05 (м, 2 Н), 1,75-1,50 (м, 3 Н)
[2210] Пример 342. (2S,4S)-4-фтор-1-[2-[4-(8-изохиноламино)-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2211] Указанное в заголовке соединение (40,8 мг, 9,2%) получали таким же образом, как и в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-(пиперидин-4-ил)изохинолин-8-амина гидрохлорид (374,8 мг, 1,25 ммоль), полученный в эталонном примере 184. 1H-ЯМР (CDCl3, 400 МГц) δ 9,32 (с, 1 Н), 8,45 (д, 1 Н), 7,57-7,50 (м, 2 Н), 7,12 (д, 1 Н), 6,68 (д, 1 Н), 5,60-5,25 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,60-3,20 (м, 3 Н), 3,05-2,85 (м, 2 Н), 2,85-2,60 (м, 1 Н), 2,55-2,30 (м, 2 Н), 2,30-2,10 (м, 2 Н), 1,90-1,60 (м, 3 Н)
[2212] Пример 343. (2S,4S)-4-фтор-1-[2-[4-[(8-метил-4-хинолил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2213] Указанное в заголовке соединение (205,7 мг, 52,8%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 8-метил-N-(пиперидин-4-ил)хинолин-4-амина гидрохлорид (309,6 мг, 0,99 ммоль), полученный в эталонном примере 185. 1H-ЯМР (CDCl3, 400 МГц) δ 8,58 (д, 1 Н), 7,58 (д, 1 Н), 7,50 (д, 1 Н), 7.32 (т, 1 Н), 6,46 (д, 1 Н), 5,50-5,25 (м, 1 Н), 5,00-4,80 (м, 1 Н), 4,30-4,10 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,65-3,15 (м, 3 Н), 3,05-2,85 (м, 2 Н), 2,76 (с, 3 Н), 2,76-2,55 (м, 1 Н), 2,45-2,30 (м, 2Н), 2,20-2,05 (м, 2 Н), 1,85-1,55 (м, 3 Н)
[2214] Пример 344. (2S,4S)-1-[2-[4-[(8-хлор-4-хинолил)амино]-1-пиперидил]ацетил]-4-фторпирролидин-2-карбонитрил
[2215] Указанное в заголовке соединение (16,6 мг, 4,1%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 8-хлор-N-(пиперидин-4-ил)хинолин-4-амина гидрохлорид (70,1 мг, 0,21 ммоль), полученный в эталонном примере 186. 1H-ЯМР (CDCl3, 400 МГц) δ 8,54 (д, 1 Н), 7,46-7,37 (м, 3 Н), 6,71 (д, 1 Н), 5,70-5,20 (м, 1 Н), 5,05-4,85 (м, 1 Н), 4,30-4,10 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,60-3,15 (м, 3 Н), 3,00-2,80 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,50-2,30 (м, 2 Н), 2,20-2,05 (м, 2 Н), 1,90-1,50 (м, 3 Н)
[2216] Пример 345. (2S,4S)-4-фтор-1-[2-[4-[(8-фтор-4-хинолил)амино]-1-пиперидил]ацетил]пирролид ин-2-карбонитрил
[2217] Указанное в заголовке соединение (18,7 мг, 4,8%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 8-фтор-N-(пиперидин-4-ил)хинолин-4-амина гидрохлорид (192,9 мг, 0,61 ммоль), полученный в эталонном примере 187. 1H-ЯМР (CDCl3, 400 МГц) δ 8,59 (д, 1 Н), 7,49 (д, 1 Н), 7,36-7,33 (м, 2 Н), 6,50 (д, 1 Н), 5,55-5,25 (м, 1 Н), 5,05-4,90 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,65-3,20 (м, 3 Н), 3,10-2,85 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,50-2,30 (м, 2 Н), 2,20-2,05 (м, 2 Н), 1,90-1,50 (м, 3 Н)
[2218] Пример 346. (2S,4S)-4-фтор-1-[2-[4-[[8-(трифторметил)-4-хинолил]амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2219] Указанное в заголовке соединение (347,4 мг, 78,5%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-(пиперидин-4-ил)-8-(трифторметил)хинолин-4-амина гидрохлорид (341,3 мг, 0,93 ммоль), полученный в эталонном примере 188. 1H-ЯМР (CDCl3, 400 МГц) δ 8,65 (д, 1 Н), 7,99-7,95 (м, 2 Н), 7,44 (т, 1 Н), 6,51 (д, 1 Н), 5,50-5,20 (м, 1 Н), 5,10-4,85 (м, 1 Н), 4,30-4,10 (м, 1 Н), 4,00-3,65 (м, 2 Н), 3,60-3,10 (м, 3 Н), 3,05-2,80 (м, 2 Н), 2,75-2,55 (м, 1 Н), 2,50-2,25 (м, 2 Н), 2,25-2,05 (м, 2 Н), 1,90-1,55 (м, 3 Н)
[2220] Пример 347. (2S,4S)-4-фтор-1-[2-[4-[[8-(трифторметокси)-5-хинолил]амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2221] Указанное в заголовке соединение (125,5 мг, 82,2%) получали таким же образом, как и в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-(пиперидин-4-ил)-8-(трифторметокси)хинолин-5-амина гидрохлорид (408,2 мг, 1,06 ммоль), полученный в эталонном примере 189. 1H-ЯМР (CDCl3, 400 МГц) δ 9,00 (д, 1 Н), 8,18 (д, 1 Н), 7,50 (д, 1 Н), 7,43 (т, 1 Н), 6,56 (д, 1 Н), 5,55-5,25 (м, 1 Н), 5,05-4,90 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,60-3,20 (м, 3 Н), 3,10-2,90 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,50-2,35 (м, 2 Н), 2,35-2,10 (м, 2 Н), 1,90-1,60 (м, 3 Н)
[2222] Пример 348. (2S,4S)-4-фтор-1-[2-[4-[(3-метокси-5-хинолил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2223] Указанное в заголовке соединение (284,9 мг, 75,5%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 3-метокси-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид (302,7 мг, 0,92 ммоль), полученный в эталонном примере 190. 1H-ЯМР (CDCl3, 400 МГц) δ 8,65 (с, 1 Н), 7,47-7,38 (м, 2 Н), 7,34 (с, 1 Н), 6,68 (д, 1 Н), 5,50-5,20 (м, 1 Н), 5,00-4,85 (м, 1 Н), 4,30-4,15 (м, 1 Н), 3,90 (с, 3 Н), 4,10-3,70 (м, 2 Н), 3,55-3,10 (м, 3 Н), 3,05-2,85 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,45-2,30 (м, 2 Н), 2,30-2,10 (м, 2 Н), 1,95-1,55 (м, 3 Н)
[2224] Пример 349. (2S,4S)-4-фтор-1-[2-[4-[(3-фтор-5-хинолил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2225] Указанное в заголовке соединение (147,1 мг, 37,0%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 3-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид (316,6 мг, 1,00 ммоль), полученный в эталонном примере 191. 1H-ЯМР (CDCl3, 400 МГц) δ 8,75 (с, 1 Н), 7,81 (д, 1 Н), 7,54-7,47 (м, 2 Н), 6,69 (д, 1 Н), 5,50-5,20 (м, 1 Н), 5,00-4,80 (м, 1 Н), 4,30-4,10 (м, 1 Н), 4,10-3,70 (м, 2 Н), 3,60-3,10 (м, 3 Н), 3,00-2,80 (м, 2 Н), 2,80-2,55 (м, 1 Н), 2,50-2,30 (м, 2 Н), 2,30-2,10 (м, 2 Н), 1,85-1,50 (м, 3 Н)
[2226] Пример 350. (2S,4S)-4-фтор-1-[2-[4-[фуро[3,2-с]пиридин-7-ил(метил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2227] Указанное в заголовке соединение (8,9 мг, 21,0%) получали таким же образом, как и в примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-метил-N-(пиперидин-4-ил)фуро[3,2-с]пиридин-7-амина гидрохлорид (3S,4 мг, 0,11 ммоль), полученный в эталонном примере 161. 1H ЯМР (MeOD4, 400 МГц) δ 8,35 (с, 1 Н), 7,87 (д, 2 Н), 6,96 (д, 1 Н), 5,51-4,96 (м, 2 Н), 4,15-3,75 (м, 3 Н), 3,42-3,20 (м, 2 Н), 3,06-3,01 (м, 2 Н), 2,95 (с, 3 Н), 2,66-2,40 (м, 2 Н), 2,29-2,23 (м, 2 Н), 2,04-1,95 (м, 2 Н), 1,75-1,73 (м, 2 Н).
[2228] Пример 351. (2S,4S)-1-[2-[4-[(1-хлор-5-изохинолил)амино]-1-пиперидил]ацетил]-4-фторпирролидин-2-карбонитрил
[2229] Указанное в заголовке соединение (34,6 мг, 60,8%) получали таким же образом, как и в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 1-хлор-N-(пиперидин-4-ил)изохинолин-5-амина гидрохлорид (45,8 мг, 0,14 ммоль), полученный в эталонном примере 192. 1H-ЯМР (CDCl3, 400 МГц) δ 8,21 (д, 1 Н), 8,06 (д, 1 Н), 7,88-7,49 (м, 2 Н), 6,83 (д, 1 Н), 5,55-5,25 (м, 1 Н), 5,00-4,85 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,15-3,70 (м, 2 Н), 3,60-3,20 (м, 3 Н), 3,05-2,85 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,50-2,30 (м, 2 Н), 2,30-2,10 (м, 2 Н), 1,85-1,55 (м, 3 Н)
[2230] Пример 352. (2S,4S)-1-[2-[4-[(3-хлор-5-изохинолил)амино]-1-пиперидил]ацетил]-4-фторпирролидин-2-карбонитрил
[2231] Указанное в заголовке соединение (194,4 мг, 50,9%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 3-хлор-N-(пиперидин-4-ил)изохинолин-5-амина гидрохлорид (307,2 мг, 0,92 ммоль), полученный в эталонном примере 193. 1H-ЯМР (CDCl3, 400 МГц) δ 8,95 (с, 1 Н), 7,66 (с, 1 Н), 7,43 (т, 1 Н), 7,28 (д, 1 Н), 6,76 (д, 1 Н), 5,55-5,35 (м, 1 Н), 5,00-4,85 (м, 1 Н), 4,30-4,10 (м, 1 Н), 4,00-3,70 (м, 2 Н), 3,55-3,15 (м, 3 Н), 3,05-2,85 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,50-2,25 (м, 2 Н), 2,25-2,10 (м, 2 Н), 1,90-1,50 (м, 3 Н)
[2232] Пример 353. (2S,4S)-1-[2-[4-[(8-хлор-5-изохинолил)амино]-1-пиперидил]ацетил]-4-фторпирролидин-2-карбонитрил
[2233] Указанное в заголовке соединение (193,7 мг, 63,6%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 8-хлор-N-(пиперидин-4-ил)изохинолин-5-амина гидрохлорид (245,2 мг, 0,73 ммоль), полученный в эталонном примере 194. 1H-ЯМР (CDCl3, 400 МГц) δ 9,58 (с, 1 Н), 8,57 (д, 1 Н), 7,54 (д, 1 Н), 7,45 (д, 1 Н), 6,67 (д, 1 Н), 5,55-5,25 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,30-4,10 (м, 1 Н), 4,00-3,65 (м, 2 Н), 3,60-3,20 (м, 3 Н), 3,10-2,85 (м, 2 Н), 2,85-2,60 (м, 1 Н), 2,50-2,30 (м, 2 Н), 2,30-2,10 (м, 2 Н), 1,90-1,55 (м, 3 Н)
[2234] Пример 354. (2S,4S)-4-фтор-1-[2-[4-[(4-метил-5-изохинолил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2235] Указанное в заголовке соединение (307,2 мг, 93,3%) получали таким же образом, как и в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 4-метил-N-(пиперидин-4-ил)изохинолин-5-амина гидрохлорид (261,6 мг, 0,83 ммоль), полученный в эталонном примере 195. 1H-ЯМР (CDCl3, 400 МГц) δ 8,93 (с, 1 Н), 8,11 (с, 1 Н), 7,39 (т, 1 Н), 7,27-7,23 (м, 1 Н), 6,73 (д, 1 Н), 5,50-5,20 (м, 1 Н), 5,00-4,80 (м, 1 Н), 4,30-4,10 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,55-3,15 (м, 3 Н), 2,91 (с, 3 Н), 2,91-2,80 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,55-2,30 (м, 2 Н), 2,30-2,10 (м, 2 Н), 1,85-1,50(м, 3 Н)
[2236] Пример 355. (2S,4S)-4-фтор-1-[2-[4-[(3-метокси-5-изохинолил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2237] Указанное в заголовке соединение (76,0 мг, 16,2%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 3-метокси-N-(пиперидин-4-ил)изохинолин-5-амина гидрохлорид (376,0 мг, 1,14 ммоль), полученный в эталонном примере 196. 1H-ЯМР (CDCl3, 400 МГц) δ 8,86 (с, 1 Н), 7,48-7,21 (м, 2 Н), 6,91 (с, 1 Н), 6,66 (д, 1 Н), 5,60-5,30 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,30-4,10 (м, 1 Н), 4,05 (с, 3 Н), 4,05-3,70 (м, 2 Н), 3,60-3,20 (м, 3 Н), 3,10-2,90 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,60-2,30 (м, 2 Н), 2,30-2,10 (м, 2 Н), 1,85-1,50 (м, 3 Н)
[2238] Пример 356. (2S,4S)-4-фтор-1-[2-[4-[(8-нитро-5-изохинолил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2239] Указанное в заголовке соединение (95,6 мг, 19,7%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 8-нитро-N-(пиперидин-4-ил)изохинолин-5-амина гидрохлорид (165,1 мг, 0,48 ммоль), полученный в эталонном примере 197. 1H-ЯМР (CDCl3, 400 МГц) δ 8,66 (д, 1 Н), 8,50 (д, 1 Н), 7,58 (д, 1 Н), 7,26 (с, 1 Н), 6,66 (д, 1 Н), 5,60-5,20 (м, 1 Н), 5,00-4,85 (м, 1 Н), 4,30-4,10 (м, 1 Н), 4,00-3,70 (м, 2 Н), 3,70-3,15 (м, 3 Н), 3,10-2,90 (м, 2 Н), 2,85-2,60 (м, 1 Н), 2,55-2,30 (м, 2 Н), 2,30-2,10 (м, 2 Н), 1,85-1,50 (м, 3 Н)
[2240] Пример 357. (2S,4S)-4-фтор-1-[2-[4-[(8-фтор-5-изохинолил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2241] Указанное в заголовке соединение (225,9 мг, 49,7%) получали таким же образом, как и в примере 3S0, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 8-фтор-N-(пиперидин-4-ил)изохинолин-5-амина гидрохлорид (348,2 мг, 1,09 ммоль), полученный в эталонном примере 198. 1H-ЯМР (CDCl3, 400 МГц) δ 9,45 (с, 1 Н), 8,56 (д, 1 Н), 7,57 (д, 1 Н), 7,10 (д, 1 Н), 6,66 (д, 1 Н), 5,55-5,25 (м, 1 Н), 5,00-4,85 (м, 1 Н), 4,30-4,10 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,55-3,15 (м, 3 Н), 3,05-2,85 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,55-2,30 (м, 2 Н), 2,25-2,05 (м, 2 Н), 1,85-1,55 (м, 3 Н)
[2242] Пример 358. (2S)-1-[2-[4-[(2-хлор-6,7-диметокси-хиназолин-4-ил)амино]-1-пиперидил] ацетил]пирролидин-2-карбонитрил
[2243] Указанное в заголовке соединение (210,7 мг, 95,2%) получали таким же образом, как описано в примере 110, за исключением того, что вместо N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 2-хлор-6,7-диметокси-N-(пиперидин-4-ил)хиназолин-4-амина гидрохлор ид (190,9 мг, 0,48 ммоль), полученный в эталонном примере 199. 1H-ЯМР (CDCl3, 400 МГц) δ 7,07-7,02 (м, 2 Н), 6,20-6,10 (м, 1 Н), 5,00-4,70 (м, 1 Н), 4,40-4,20 (м, 1 Н), 3,95 (с, 3 Н), 3,93 (с, 3 Н), 3,75-3,40 (м, 2 Н), 3,35-3,10 (м, 2 Н), 3,05-2,85 (м, 2 Н), 2,45-2,25 (м, 3 Н), 2,25-2,00 (м, 4 Н), 1,90-1,60 (м, 3 Н)
[2244] Пример 359. (2S)-1-[2-[4-[(2-хлор-8-метилхиназолин-4-ил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2245] Указанное в заголовке соединение (148,0 мг, 74,3%) получали таким же образом, как и в примере 110, за исключением того, что вместо N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 2-хлор-8-метил-N-(пиперидин-4-ил)хиназолин-4-амина гидрохлорид (128,7 мг, 0,37 ммоль), полученный в эталонном примере 200. 1H-ЯМР (CDCl3, 400 МГц) δ 7,59-7,54 (м, 2 Н), 7,34 (т, 1 Н), 5,90-5,75 (м, 1 Н), 5,10-4,70 (м, 1 Н), 4,40-4,20 (м, 1 Н), 3,80-3,50 (м, 2 Н), 3,40-3,10 (м, 2 Н), 3,10-2,85 (м, 2 Н), 2,64 (с, 3 Н), 2,50-2,20 (м, 3 Н), 2,20-2,00 (м, 4 Н), 1,90-1,60 (м, 3 Н)
[2246] Пример 360. (2S,4S)-4-фтор-1-[2-[4-(2,б-нафтиридин-4-иламино)-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2247] Указанное в заголовке соединение (55,6 мг, 42,1%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-(пиперидин-4-ил)-2,6-нафтиридин-4-амина гидрохлорид (104,1 мг, 0,35 ммоль), полученный в эталонном примере 201. 1H-ЯМР (CDCl3, 400 МГц) δ 9,10 (с, 1 Н), 8,58 (д, 1 Н), 8,11 (д, 1 Н), 7,54 (с, 1 Н), 7,00 (с, 1 Н), 5,55-5,25 (м, 1 Н), 5,05-4,90 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,50-3,15 (м, 3 Н), 3,05-2,85 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,50-2,30 (м, 2 Н), 2,30-2,10 (м, 2 Н), 1,95-1,60 (м, 3 Н)
[2248] Пример 361. (2S,4S)-1-[2-[4-[(8-хлор-4-изохинолил)амино]-1-пиперидил]ацетил]-4-фторпирролидин-2-карбонитрил
[2249] Указанное в заголовке соединение (91,6 мг, 63,7%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 8-хлор-N-(пиперидин-4-ил)изохинолин-4-амина гидрохлорид (95,1 мг, 0,28 ммоль), полученный в эталонном примере 202. 1H-ЯМР (CDCl3, 400 МГц) δ 8,29 (д, 1 Н), 7,81-7,66 (м, 3 Н), 7,61 (с, 1 Н), 5,55-5,30 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,15-3,70 (м, 2 Н), 3,60-3,20 (м, 3 Н), 3,10-2,90 (м, 2 Н), 2,85-2,65 (м, 1 Н), 2,50-2,35 (м, 2 Н), 2,35-2,15 (м, 2 Н), 1,90-1,60 (м, 3 Н)
[2250] Пример 362. (2S,4S)-4-фтор-1-[2-[4-(3-хинолламино)-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2251] Указанное в заголовке соединение (154,9 мг, 60,1%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид (202,9 мг, 0,68 ммоль), полученный в эталонном примере 203. 1H-ЯМР (CDCl3, 400 МГц) δ 8,44 (с, 1 Н), 7,95 (д, 1 Н), 7,62 (д, 1 Н), 7,44-7,43 (м, 2 Н), 7,03 (с, 1 Н), 5,50-5,30 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,15-3,70 (м, 2 Н), 3,55-3,20 (м, 3 Н), 3,10-2,90 (м, 2 Н), 2,85-2,60 (м, 1 Н), 2,55-2,35 (м, 3 Н), 2,35-2,10 (м, 2 Н), 1,80-1,50 (м, 2 Н)
[2252] Пример 363. (2S,4S)-4-фтор-1-[2-[4-[(6-метил-3-хинолил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2253] Указанное в заголовке соединение (102,5 мг, 38,4%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 6-метил-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид (131,9 мг, 0,42 ммоль), полученный в эталонном примере 204. 1H-ЯМР (CDCl3, 400 МГц) δ 8,35 (с, 1 Н), 7,82 (д, 1 Н), 7,38 (с, 1 Н), 7,24 (д, 1 Н), 6,95 (с, 1 Н), 5,55-5,25 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,30-4,10 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,55-3,20 (м, 3 Н), 3,05-2,80 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,45 (с, 3 Н), 2,45-2,20 (м, 3 Н), 2,20-2,10 (м, 2 Н), 1,80-1,50 (м, 2 Н)
[2254] Пример 364. (2S,4S)-4-фтор-1-[2-[4-[(6-фтор-3-хинолил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2255] Указанное в заголовке соединение (167,9 мг, 62,2%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 6-фтор-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид (201,1 мг, 0,63 ммоль), полученный в эталонном примере 205. 1H-ЯМР (CDCl3, 400 МГц) δ 8,35 (с, 1 Н), 7,90 (д, 1 Н), 7,23-7,13 (м, 2 Н), 6,93 (с, 1 Н), 5,55-5,30 (м, 1 Н), 5,05-4,95 (м, 1 Н), 4,30-4,10 (м, 1 Н), 4,05-3,75 (м, 2 Н), 3,55-3,20 (м, 3 Н), 3,10-2,90 (м, 2 Н), 2,85-2,60 (м, 1 Н), 2,50-2,25 (м, 3 Н), 2,25-2,10 (м, 2 Н), 1,85-1,50 (м, 2 Н)
[2256] Пример 365. (2S,4S)-4-фтор-1-[2-[4-[(6-метокси-3-хинолил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2257] Указанное в заголовке соединение (85,7 мг, 30,8%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 6-метокси-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид (179,4 мг, 0,54 ммоль), полученный в эталонном примере 206. 1H-ЯМР (CDCl3, 400 МГц) δ 8,26 (с, 1 Н), 7,82 (д, 1 Н), 7,06 (д, 1 Н), 6,93 (с, 1 Н), 6,91 (с, 1 Н), 5,50-5,25 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,30-4,10 (м, 1 Н), 3,90 (с, 3 Н), 4,05-3,70 (м, 2 Н), 3,55-3,20 (м, 3 Н), 3,05-2,85 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,50-2,30 (м, 3 Н), 2,30-2,10 (м, 2 Н), 1,85-1,50 (м, 2 Н)
[2258] Пример 366. (2S,4S)-4-фтор-1-[2-[4-[(7-метокси-3-хинолил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2259] Указанное в заголовке соединение (39,6 мг, 14,2%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 7-метокси-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид (61,0 мг, 0,19 ммоль), полученный в эталонном примере 207. 1H-ЯМР (CDCl3, 400 МГц) δ 8,38 (с, 1 Н), 7,52 (д, 1 Н), 7,31 (с, 1 Н), 7,13 (д, 1 Н), 7,05 (с, 1 Н), 5,55-5,30 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,25-4,10 (м, 1 Н), 3,90 (с, 3 Н), 4,05-3,70 (м, 2 Н), 3,55-3,20 (м, 3 Н), 3,05-2,85 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,50-2,25 (м, 3 Н), 2,25-2,05 (м, 2 Н), 1,80-1,50 (м, 2 Н)
[2260] Пример 367. (2S,4S)-4-фтор-1-[2-[4-[(8-метокси-3-хинолил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2261] Указанное в заголовке соединение (29,5 мг, 10,6%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 8-метокси-N-(пиперидин-4-ил)хинолин-3-амина гидрохлорид (72,5 мг, 0,22 ммоль), полученный в эталонном примере 208. 1H-ЯМР (CDCl3, 400 МГц) δ 8,42 (с, 1 Н), 7,36 (т, 1 Н), 7,19 (д, 1 Н), 7,00 (с, 1 Н), 6,79 (д, 1 Н), 5,55-5,30 (м, 1 Н), 5,05-4,90 (м, 1 Н), 4,30-4,10 (м, 1 Н), 4,06 (с, 3 Н), 4,06-3,70 (м, 2 Н), 3,60-3,25 (м, 3 Н), 3,10-2,90 (м, 2 Н), 2,85-2,60 (м, 1 Н), 2,60-2,35 (м, 3 Н), 2,35-2,10 (м, 2 Н), 1,80-1,55 (м, 2 Н)
[2262] Пример 368. (2S,4S)-4-фтор-1-[2-[4-(1,8-нафтиридин-3-иламино)-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2263] Указанное в заголовке соединение (109,4 мг, 49,7%) получали таким же образом, как и в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-(пиперидин-4-ил)-1,8-нафтиридин-3-амина гидрохлорид (173,4 мг, 0,58 ммоль), полученный в эталонном примере 209. 1H-ЯМР (CDCl3, 600 МГц) δ 8,79 (д, 1 Н), 8,59 (с, 1 Н), 7,96 (д, 1 Н), 7,35 (т, 1 Н), 6,95 (с, 1 Н), 5,50-5,30 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,25-4,15 (м, 1 Н), 4,00-3,70 (м, 2 Н), 3,50-3,20 (м, 3 Н), 3,05-2,85 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,50-2,30 (м, 3 Н), 2,20-2,10 (м, 2 Н), 1,80-1,55 (м, 2 Н)
[2264] Пример 369. (2S,4S)-1-[2-[4-[(7-хлор-1,8-нафтиридин-3-ил)амино]-1-пиперидил]ацетил]-4-фторпирролидин-2-карбонитрил
[2265] Указанное в заголовке соединение (13,8 мг, 20,6%) получали таким же образом, как и в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 7-хлор-N-(пиперидин-4-ил)-1,8-нафтиридин-3-амина гидрохлорид (53,6 мг, 0,16 ммоль), полученный в эталонном примере 210. 1H-ЯМР (CDCl3, 600 МГц) δ 8,55 (с, 1 Н), 7,90 (д, 1 Н), 7,35 (д, 1 Н), 6,95 (с, 1 Н), 5,50-5,30 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,30-4,10 (м, 1 Н), 4,00-3,70 (м, 2 Н), 3,50-3,20 (м, 3 Н), 3,05-2,90 (м, 2 Н), 2,80-2,65 (м, 1 Н), 2,50-2,30 (м, 3 Н), 2,20-2,10 (м, 2 Н), 1,80-1,55 (м, 2 Н)
[2266] Пример 370. (2S)-1-[2-[4-[(8-этокси-5-хинолил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2267] Указанное в заголовке соединение (35,4 мг, 9,8%) получали аналогично тому, как описано в примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 8-этокси-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид (302,9 мг, 0,88 ммоль), полученный в эталонном примере 211. 1H ЯМР (CDCl3, 400 МГц) δ 8,90 (дд, 1 Н), 8,18 (дд, 1 Н), 7,34 (кв, 1 Н), 6,93 (д, 1 Н), 6,59 (д, 1 Н), 5,17-4,69 (м, 1 Н), 4,21 (кв, 2 Н), 3,73-3,58 (м, 2 Н), 3,53-3,46 (м, 1 Н), 3,37-3,13 (м, 3 Н), 2,93-2,83 (м, 2 Н), 2,35-2,00 (м, 8 Н), 1,73-1,56 (м, 2 Н), 1,53 (т, 3 Н).
[2268] Пример 371. (2S,4S)-1-[2-[4-[(8-этокси-5-хинолил)амино]-1-пиперидил]ацетил]-4-фторпирролидин-2-карбонитрил
[2269] Указанное в заголовке соединение (2,4 мг, 5,0%) получали аналогично тому, как описано в примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 8-этокси-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорид (37,8 мг, 0,11 ммоль), полученный в эталонном примере 211. 1H ЯМР (CDCl3, 400 МГц) δ 8,90 (дд, 1 Н), 8,18 (дд, 1 Н), 7,36 (кв, 1 Н), 6,94 (д, 1 Η), 6,60 (д, 1 Η), 5,46-4,87 (м, 2 Η), 4,22 (кв, 2 Η), 4,17-3,67 (м, 1 Η), 3,83-3,68 (м, 2 Η), 3,44-3,21 (м, 2 Η), 3,18 (с, 1 Η), 2,96-2,84 (м, 2 Η), 2,73-2,56 (м, 1 Η), 2,35-2,10 (м, 5 Η), 1,75-1,53 (м, 5 Η).
[2270] Пример 372. (2S,4S)-1-[2-[4-(1,3-бензотиазол-7-иламино)-1-пиперидил]ацетил]-4-фторпирролидин-2-карбонитрил
[2271] Указанное в заголовке соединение (266,8 мг, 61,2%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-(пиперидин-4-ил)бензо[d]тиазол-7-амина гидрохлорид (344,8 мг, 1,13 ммоль), полученный в эталонном примере 212. 1H-ЯМР (CDCl3, 600 МГц) δ 8,92 (с, 1 Н), 7,56 (д, 1 Н), 7,38 (т, 1 Н), 6,66 (д, 1 Н), 5,50-5,30 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,25-4,15 (м, 1 Н), 4,00-3,70 (м, 2 Н), 3,60-3,15 (м, 3 Н), 3,00-2,80 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,50-2,20 (м, 3 Н), 2,20-2,10 (м, 2 Н), 1,85-1,50 (м, 2 Н)
[2272] Пример 373. (2S,4S)-1-[2-[4-[(1-ацетилиндолин-4-ил)амино]-1-гшперидил]ацетил]-4-фторпирролидин-2-карбонитрил
[2273] Указанное в заголовке соединение (45,8 мг, 12,8%) получали таким же образом, как и в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 1-(4-(пиперидин-4-иламино)индолин-1-ил)этан-1-он гидрохлорид (286,8 мг, 0,86 ммоль), полученный в эталонном примере 213. 1H-ЯМР (CDCl3, 400 МГц) δ 7,63 (д, 1 Н), 7,10 (т, 1 Н), 6,36 (д, 1 Н), 5,50-5,25 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,30-4,10 (м, 1 Н), 4,09 (т, 2 Н), 4,00-3,70 (м, 2Н), 3,50-3,15 (м, 3 Н), 3,00-2,80 (м, 4 Н), 2,80-2,60 (м, 1 Н), 2,45-2,25 (м, 3 Н), 2,21 (с, 3 Н), 2,20-2,00 (м, 2 Н), 1,75-1,45 (м, 2 Н)
[2274] Пример 374. (2S,4S)-4-фтор-1-[2-[4-[(8-метил-6-хинолил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2275] Указанное в заголовке соединение (149,1 мг, 65,6%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 8-метил-N-(пиперидин-4-ил)хинолин-6-амина гидрохлорид (180,7 мг, 0,58 ммоль), полученный в эталонном примере 214. 1H-ЯМР (CDCl3, 400 МГц) δ 8,64 (д, 1 Н), 7,88 (д, 1 Н), 7,28-7,24 (м, 1 Н), 6,94 (с, 1 Н), 6,57 (с, 1 Н), 5,50-5,25 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,50-3,20 (м, 3 Н), 3,00-2,85 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,72 (с, 3 Н), 2,50-2,20 (м, 3 Н), 2,20-2,10 (м, 2 Н), 1,80-1,50 (м, 2 Н)
[2276] Пример 375. (2S,4S)-4-фтор-1-[2-[4-[(8-фтор-6-хинолил)амино]-1-пиперидил]ацетил]пирролид ин-2-карбонитрил
[2277] Указанное в заголовке соединение (305,3 мг, 83,1%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 8-фтор-N-(пиперидин-4-ил)хинолин-6-амина гидрохлорид (292,4 мг, 0,92 ммоль), полученный в эталонном примере 215. 1H-ЯМР (CDCl3, 400 МГц) δ 8,63 (с, 1 Н), 7,89 (д, 1 Н), 7,32-7,28 (м, 1 Н), 6,80 (д, 1 Н), 6,50 (с, 1 Н), 5,50-5,25 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,50-3,20 (м, 3 Н), 3,05-2,85 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,50-2,20 (м, 3 Н), 2,20-2,05 (м, 2 Н), 1,80-1,50 (м, 2 Н)
[2278] Пример 376. (2S,4S)-1-[2-[4-[(8-хлор-6-хинолил)амино]-1-пиперидил]ацетил]-4-фторпирролидин-2-карбонитрил
[2279] Указанное в заголовке соединение (265,9 мг, 62,6%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 8-хлор-N-(пиперидин-4-ил)хинолин-6-амина гидрохлорид (341,7 мг, 1,02 ммоль), полученный в эталонном примере 216. 1H-ЯМР (CDCl3, 400 МГц) δ 8,80 (д, 1 Н), 8,71 (д, 1 Н), 7,32 (т, 1 Н), 7,24 (с, 1 Н), 6,62 (с, 1 Н), 5,50-5,25 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,30-4,10 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,50-3,20 (м, 3 Н), 3,00-2,85 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,50-2,20 (м, 3 Н), 2,20-2,05 (м, 2 Н), 1,80-1,50 (м, 2 Н)
[2280] Пример 377. (2S,4S)-4-фтор-1-[2-[4-[[8-(трифторметил)-6-хинолил]амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2281] Указанное в заголовке соединение (270,6 мг, 83,7%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-(пиперидин-4-ил)-8-(трифторметил)хинолин-6-амина гидрохлорид (264,8 мг, 0,72 ммоль), полученный в эталонном примере 217. 1H-ЯМР (CDCl3, 400 МГц) δ 8,75 (д, 1 Н), 7,95 (д, 1 Н), 7,44 (с, 1 Н), 7,35 (т, 1 Н), 6,83 (с, 1 Н), 5,50-5,30 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,30-4,10 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,55-3,20 (м, 3 Н), 3,05-2,85 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,50-2,20 (м, 3 Н), 2,20-2,05 (м, 2 Н), 1,80-1,50 (м, 2 Н)
[2282] Пример 378. (2S)-1-[2-[4-[(2-оксохромен-4-ил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2283] Указанное в заголовке соединение (25,9 мг, 72,0%) получали таким же образом, как и в примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 4-(пиперидин-4-иламино)-2Н-хромен-2-он гидрохлорид (30,0 мг, 0,09 ммоль), полученный в эталонном примере 218. 1H ЯМР (CDCl3, 400 МГц) δ 7,55-7,47 (м, 2 Н), 7,33 (д, 1 Н), 7,28-7,24 (м, 1 Н), 5,34 (д, 1 Н), 5,22-5,15 (м, 1 Н), 5,03-4,75 (м, 1 Н), 3,75-3,63 (м, 1 Н), 3,60-3,42 (м, 2 Н), 3,32-3,17 (м, 2 Н), 3,04-2,91 (м, 2 Н), 2,39-2,06 (м, 8 Н), 1,92-1,66 (м, 2 Н).
[2284] Пример 379. (2S,4S)-4-фтор-1-[2-[4-[(2-оксохромен-4-ил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2285] Указанное в заголовке соединение (20,3 мг, 53,8%) получали аналогично тому, как описано в примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 4-(пиперидин-4-иламино)-2Н-хромен-2-он гидрохлорид (30,0 мг, 0,09 ммоль), полученный в эталонном примере 218. 1H ЯМР (CDCl3, 400 МГц) δ 7,56-7,47 (м, 2 Н), 7,33 (д, 1 Н), 7,28-7,24 (м, 1 Н), 5,50-5,25 (м, 2,4 Н), 5,20-5,14 (м, 1 Н), 4,95 (д, 0,6 Н), 4,22-4,16 (м, 1,5 Н), 4,00-3,72 (м, 1,5 Н), 3,49-3,41 (м, 1 Н), 3,37-3,17 (м, 2 Н), 3,03-2,92 (м, 2 Н), 2,79-2,64 (м, 1 Н), 2,41-2,31 (м, 3 Н), 2,17-2,07 (м, 2 Н), 1,94-1,64 (м, 2 Н).
[2286] Пример 380. (2S,4S)-4-фтор-1-[2-[4-(1,5-нафтиридин-4-иламино)-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2287] Указанное в заголовке соединение (4,3 мг, 10,2%) получали аналогично тому, как описано в примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-(пиперидин-4-ил)-1,5-нафтиридин-4-амина гидрохлорид (33,1 мг, 0,11 ммоль), полученный в стандартном примере 219. 1H ЯМР (CDCl3, 400 МГц) δ 8,69 (дд, 1 Н), 8,54 (д, 1 Н), 8,22 (дд, 1 Н), 7,57 (кв, 1 Η), 6,65-6,62 (м, 1 Η), 6,53 (д, 1 Η), 5,51-4,94 (м, 2 Η), 4,26-3,93 (м, 1 Η), 3,90-3,73 (м, 1 Η), 3,59-3,26 (м, 2 Η), 3,25 (с, 1 Η), 3,03-2,90 (м, 2 Η), 2,80-2,64 (м, 1 Η), 2,49-2,16 (м, 4 Η), 1,89-1,67 (м, 3 Η).
[2288] Пример 381. (2S,4S)-4-фтор-1-[2-[4-[[2-(трифторметил)-6-хинолил]амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2289] Указанное в заголовке соединение (429,7 мг, 81,7%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-(пиперидин-4-ил)-2-(трифторметил)хинолин-6-амина гидрохлорид (430,8 мг, 1,17 ммоль), полученный в эталонном примере 220. 1H-ЯМР (CDCl3, 400 МГц) δ 8,02 (д, 1 Н), 7,95 (д, 1 Н), 7,57 (д, 1 Н), 7,13 (д, 1 Н), 6,70 (с, 1 Н), 5,50-5,25 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,30-4,10 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,55-3,20 (м, 3 Н), 3,05-2,85 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,50-2,20 (м, 3 Н), 2,20-2,10 (м, 2 Н), 1,85-1,55 (м, 2 Н)
[2290] Пример 382. (2S,4S)-4-фтор-1-[2-[4-[(4-метокси-6-хинолил)амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2291] Указанное в заголовке соединение (25,9 мг, 20,5%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 4-метокси-N-(пиперидин-4-ил)хинолин-6-амина гидрохлорид (101,7 мг, 0,31 ммоль), полученный в эталонном примере 221. 1H-ЯМР (CDCl3, 400 МГц) δ 8,49 (д, 1 Н), 7,83 (д, 1 Н), 7,08-7,03 (м, 2 Н), 6,66 (д, 1 Н), 5,50-5,25 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,03 (с, 3 Н), 4,00-3,70 (м, 2 Н), 3,55-3,20 (м, 3 Н), 3,05-2,85 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,50-2,25 (м, 3 Н), 2,20-2,10 (м, 2 Н), 1,85-1,50 (м, 2 H)
[2292] Пример 383. (2S,4S)-1-[2-[4-[(2-бром-4-пиридил)амино]-1-пиперидил]ацетил]-4-фторпирролидин-2-карбонитрил
[2293] Указанное в заголовке соединение (65,4 мг, 22,1%) получали таким же образом, как и в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 2-бром-N-(пиперидин-4-ил)пиридин-4-амина гидрохлорид (237,3 мг, 0,72 ммоль), полученный в примере 222. 1H-ЯМР (CDCl3, 400 МГц) δ 7,91 (д, 1 Н), 6,59 (с, 1 Н), 6,36 (д, 1 Н), 5,50-5,25 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,25-4,10 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,45-3,15 (м, 3 Н), 3,05-2,80 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,50-2,25 (м, 3 Н), 2,05-2,00 (м, 2 Н), 1,80-1,50 (м, 2 Н)
[2294] Пример 384. (2S,4S)-1-[2-[4-(3Н-бензимидазол-4-иламино)-1-пиперидил]ацетил]-4-фторпирролидин-2-карбонитрил
[2295] Указанное в заголовке соединение (363,5 мг, 97,2%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-(пиперидин-4-ил)-1H-бензо[d] имидазол-7-амина гидрохлорид (292,1 мг, 1,01 ммоль), полученный в эталонном примере 223. 1H-ЯМР (MeOD, 400 МГц) δ 7,99 (с, 1 Н), 7,08 (т, 1 Н), 6,85 (д, 1 Н), 6,45 (д, 1 Н), 5,55-5,30 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,20-4,05 (м, 1 Н), 3,95-3,70 (м, 2 Н), 3,60-3,20 (м, 3 Н), 3,00-2,90 (м, 2 Н), 2,70-2,55 (м, 1 Н), 2,55-2,30 (м, 3 Н), 2,20-2,05 (м, 2 Н), 1,85-1,60 (м, 2 Н)
[2296] Пример 385. (2S,4S)-1-[2-[4-[(2-хлор-6-морфолино-4-пиридил)амино]-1-пиперидил]ацетил]-4-фторпирролидин-2-карбонитрил
[2297] Указанное в заголовке соединение (157,9 мг, 29,9%) получали таким же образом, как и в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 2-хлор-6-морфолино-N-(пиперидин-4-ил)пиридин-4-амина гидрохлорид (431,5 мг, 1,17 ммоль), полученный в эталонном примере 224. 1H-ЯМР (CDCl3, 400 МГц) δ 5,95 (с, 1 Η), 5,56 (с, 1 Η), 5,50-5,25 (м, 1 Η), 5,00-4,90 (м, 1 Η), 4,25-4,05 (м, 1 Η), 4,00-3,70 (м, 6 Η), 3,50-3,40 (м, 4 Η), 3,40-3,15 (м, 3 Η), 3,00-2,80 (м, 2 Η), 2,80-2,60 (м, 1 Η), 2,50-2,20 (м, 3 Η), 2,10-1,95 (м, 2 Η), 1,70-1,45 (м, 2 Η)
[2298] Пример 386. (2S,4S)-4-фтор-1-[2-[4-[[3-(трифторметил)-5-хинолил]амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2299] Указанное в заголовке соединение (450,5 мг, 92,9%) получали таким же образом, как и в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-(пиперидин-4-ил)-3-(трифторметил)хинолин-5-амина гидрохлорид (397,5 мг, 1,08 ммоль), полученный в эталонном примере 225. 1H-ЯМР (CDCl3, 400 МГц) δ 9,03 (с, 1 Н), 8,43 (с, 1 Н), 7,67 (т, 1 Н), 7,50 (д, 1 Н), 6,73 (д, 1 Н), 5,55-5,25 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,60-3,20 (м, 3 Н), 3,10-2,90 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,50-2,25 (м, 3 Н), 2,25-2,10 (м, 2 Н), 1,90-1,60 (м, 2 Н)
[2300] Пример 387. (2S)-1-[2-[4-[[3-(трифторметил)-5-хинолил]амино]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2301] Указанное в заголовке соединение (324,7 мг, 69,7%) получали так же, как в примере 110, за исключением того, что вместо N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали Ν-(пиперидин-4-ил)-3-(трифторметил)хинолин-5-амина гидрохлорид (397,5 мг, 1,08 ммоль) полученный в эталонном примере 225. 1H-ЯМР (CDCl3, 400 МГц) δ 9,03 (с, 1 Н), 8,42 (с, 1 Н), 7,67 (т, 1 Н), 7,51 (д, 1 Н), 6,73 (д, 1 Н), 5,20-4,70 (м, 1 Н), 4,50-4,35 (м, 1 Н), 3,85-3,60 (м, 1 Н), 3,60-3,45 (м, 3 Н), 3,45-3,20 (м, 2 Н), 3,10-2,90 (м, 2 Н), 2,50-2,35 (м, 2 Н), 2,35-2,10 (м, 5 Н), 1,90-1,60 (м, 2 Н)
[2302] Пример 388. 5-[[1-[2-оксо-2-[(2S,4S)-2-циано-4-фторпирролидин-1-ил]этил]-4-пиперидил]амино]-N-фенилхинолин-3-карбоксамид
[2303] Указанное в заголовке соединение (29,3 мг, 53,3%) получали аналогично тому, как описано в примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-фенил-5-(пиперидин-4-иламино)хинолин-3-карбоксамида гидрохлорид (46,0 мг, 0,11 ммоль), полученный в эталонном примере 226. 1H ЯМР (CDCl3, 400 МГц) δ 9,33 (д, 1 Н), 8,91 (д, 1 Н), 8,69 (д, 1 Н), 7,72-7,70 (м, 2Н), 7,64-7,59 (м, 1 Н), 7,46-7,43 (м, 1 Н), 7,38 (кв, 2 Н), 7,18 (кв, 1 Н), 6,67-6,62 (м, 1 Н), 5,48-4,92 (м, 2 Н), 4,03-3,70 (м, 2 Н), 3,47-3,23 (м, 2 Н), 3,19 (д, 1 Н), 3,00-2,61 (м, 3 Н), 2,40-2,28 (м, 3 Н), 2,17-2,01 (м, 2 Н), 1,65-1,46 (м, 3 Н).
[2304] Пример 389. N-бензил-N-метил-5-[[1-[2-оксо-2-[(2S,4S)-2-цтно-4-фторпирролидин-1-ил]этил]-4-пиперидил]амино]хинолин-3-карбоксамид
[2305] Указанное в заголовке соединение (42,1 мг, 72,4%) получали аналогично тому, как описано в примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-бензил-N-метил-5-(пиперидин-4-иламино)хинолин-3-карбоксамида гидрохлорид (50,2 мг, 0,11 ммоль), полученный в эталонном примере 227. 1H ЯМР (CDCl3, 400 МГц) δ 8,90 (с, 1 Н), 8,37 (д, 1 Н), 7,55 (с, 1 Η), 7,36-7,19 (м, 6 Η), 6,60 (с, 1 Η), 5,45-4,89 (м, 2 Η), 4,76-3,73 (м, 5 Η), 3,44-2,88 (м, 8 Η), 2,73-2,60 (м, 1 Η), 2,47-2,22 (м, 3 Η), 2,09-2,01 (м, 2 Η), 1,75-1,48 (м, 2 Η).
[2306] Пример 390. N-метил-5-[[1-[2-оксо-2-[(2S,4S)-2-циано-4-фторпирролидин-1-ил]этил]-4-пиперидил]амино]хинолин-8-карбоксамид
[2307] Указанное в заголовке соединение (11,7 мг, 24,4%) получали аналогично тому, как описано в Примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-метил-5-(пиперидин-4-иламино)хинолин-8-карбоксамида гидрохлорид (39,2 мг, 0,11 ммоль), полученный в эталонном примере 228. 1H ЯМР (CDCl3, 400 МГц) δ 10,92 (д, 1 Н), 8,83 (дд, 1 Н), 8,68 (д, 1 Н), 8,26 (д, 1 Н), 7,36-7,33 (м, 1 Н), 6,65 (дд, 1 Н), 5,47-4,91 (м, 2 Н), 4,89-4,85 (м, 1 Н), 4,21-3,71 (м, 2 Н), 3,60-3,50 (м, 1 Н), 3,42-3,16 (м, 3 Н), 3,09 (д, 3 Н), 3,00-2,89 (м, 2 Н), 2,74-2,60 (м, 1 Н), 2,40-1,58 (м, 6Н).
[2308] Пример 391. N,N-диметил-5-[[1-[2-оксо-2-[(2S,4S)-2-циано-4-фторпирролидин-1-ил]этил]-4-пиперидил]амино]хинолин-8-карбоксамид
[2309] Указанное в заголовке соединение (24,2 мг, 48,7%) получали аналогично тому, как описано в примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N,N-диметил-5-(пиперидин-4-иламино)хинолин-8-карбоксамида гидрохлорид (40,7 мг, 0,11 ммоль), полученного в примере 229. 1H ЯМР (CDCl3, 400 МГц) δ 8,82 (дд, 1 Н), 8,16 (д, 1 Н), 7,45 (д, 1 Н), 7,27-7,23 (м, 1 Н), 6,54 (д, 1 Н), 5,44-4,86 (м, 2 Н), 4,63 (д, 1 Н), 4,19-3,71 (м, 2Н), 3,46-3,47 (м, 3 Н), 3,28-3,13 (м, 4 Н), 2,91-2,86 (м, 2 Н), 2,78 (с, 3 Н), 2,70-2,54 (м, 1 Н), 2,74-2,60 (м, 1 Н), 2,46-2,02 (м, 5 Н).
[2310] Пример 392. N-метил-5-[[1-[2-оксо-2-[(2S,4S)-2-циано-4-фторпирролидин-1-ил]этил]-4-пиперидил]амино]-N-фенилхинолин-8-карбоксамид
[2311] Указанное в заголовке соединение (11,4 мг, 20,3%) получали аналогично тому, как описано в примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-метил-N-фенил-5-(пиперидин-4-иламино)хинолин-8-карбоксамида гидрохлорид (47,5 мг, 0,11 ммоль), полученный в эталонном примере 230. 1H ЯМР (CDCl3, 400 МГц) δ 8,84-8,83 (м, 1 Н), 8,04-8,02 (д, 1 Н), 7,27-6,99 (м, 7 Н), 6,34 (с, 1 Н), 5,41-5,20 (м, 2Н), 4,48 (с, 1 Н), 4,14-3,82 (м, 1 Н), 3,80-3,65 (м, 1 Н), 3,63-3,41 (м, 3 Н), 3,37-3,21 (м, 2 Н), 3,17-3,10 (м, 1 Н), 2,91-2,79 (м, 2 Н), 2,66-2,51 (м, 1 Н), 2,36-2,00 (м, 5Н), 1,74-1,51 (м, 2Н).
[2312] Пример 393. N-бензил-N-метил-5-[[1-[2-оксо-2-[(2S,4S)-2-циано-4-фторпирролидин-1-ил]этил]-4-пиперидил]амино]хинолин-8-карбоксамид
[2313] Указанное в заголовке соединение (12,5 мг, 21,5%) получали аналогично тому, как описано в примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-бензил-N-метил-5-(пиперидин-4-иламино)хинолин-8-карбоксамида гидрохлорид (49,1 мг, 0,11 ммоль), полученный в эталонном примере 231. 1H ЯМР (CDCl3, 400 МГц) δ 8,81 (с, 1 Н), 8,22-8,16 (м, 1 Н), 7,49 (т, 2 Н), 7,34 (т, 1 Н), 7,27-7,14 (м, 4 Н), 6,50 (кв, 1 Н), 5,39-4,89 (м, 2 Н), 4,30 (кв, 1 Н), 4,08-4,01 (м, 1 Н), 3,88-3,61 (м, 2 Н), 3,40-3,20 (м, 2 Н), 3,16-3,05 (м, 3 Н), 2,83-2,82 (м, 2 Н), 2,65-2,45 (м, 3 Н), 2,39-2,00 (м, 5 Н), 1,77-1,58 (м, 2 Н).
[2314] Пример 394. 5-[[1-[2-оксо-2-[(2S,4S)-2-циано-4-фторпирролидин-1-ил]этил]-4-пиперидил]амино]-N-фенилхинолин-8-карбоксамид
[2315] Указанное в заголовке соединение (29,6 мг, 53,7%) получали аналогично тому, как описано в примере 131, за исключением того, что N-фенил-5-(пиперидин-4-иламино)хинолин-8-карбоксамид (54,0 мг, 0,11 ммоль), полученный в эталонном примере 232, использовали вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида. 1H ЯМР (CDCl3, 400 МГц) δ 13,47 (с, 1 Н), 8,87-8,85 (м, 1 Н), 8,71 (дд, 1 Н), 8,28 (дд, 1 Н), 7,83 (д, 2 Н), 7,38-7,32 (м, 3 Н), 7,09 (т, 1 Н), 6,64 (т, 1 Н), 5,42-4,88 (м, 3 Н), 4,14-3,86 (м, 1 Н), 3,84-3,65 (м, 1 Н), 3,58-3,47 (м, 1 Н), 3,34-3,12 (м, 2 Н), 2,99-2,87 (м, 2 Н), 2,69-2,56 (м, 1 Н), 2,43-2,10 (м, 5 Н), 1,90-1,63 (м, 2 Н).
[2316] Пример 395. N-метил-5-[[1-[2-оксо-2-[(2S)-2-цианопирролидин-1-ил]этил]-4-пиперидил]амино]хинолин-8-карбоксамид
[2317] Указанное в заголовке соединение (243,0 мг, 65,6%) получали аналогично тому, как описано в примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-метил-5-(пиперидин-4-иламино)хинолин-8-карбоксамида гидрохлорид (313,6 мг, 0,88 ммоль), полученный в эталонном примере 228. 1H ЯМР (CDCl3, 400 МГц) δ 10,91 (д, 1 Н), 8,84 (дд, 1 Н), 8,70 (д, 1 Н), 8,25 (д, 1 Н), 7,37-7,34 (м, 1 Н), 6,67 (д, 1 Н), 5,10-4,74 (м, 2 Н), 3,76-3,49 (м, 3 Н), 3,37-3,17 (м, 2 Н), 3,09 (д, 3 Н), 3,01-2,89 (м, 2 Н), 2,42-2,07 (м, 8 Н), 1,88-1,63 (м, 2 Н)
[2318] Пример 396. 5-[[1-[2-оксо-2-[(2S)-2-цианопирролидин-1-ил]этил]-4-пиперидил]амино]-N-фенилхинолин-8-карбоксамид
[2319] Указанное в заголовке соединение (185,5 мг, 43,6%) получали аналогично тому, как описано в примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-фенил-5-(пиперидин-4-иламино)хинолин-8-карбоксамида гидрохлорида (369,0 мг, 0,88 ммоль), полученный в эталонном примере 232. 1H ЯМР (CDCl3, 400 МГц) δ 13,46 (с, 1 Н), 8,89 (д, 1 Н), 8,75 (д, 1 Н), 8,27 (д, 1 Н), 7,85 (д, 2 Н), 7,39-7,35 (м, 3 Н), 7,09 (т, 1 Н), 6,70-6,66 (м, 1 Н), 5,08-4,74 (м, 2 Н), 3,73-3,47 (м, 3 Н), 3,36-3,16 (м, 2 Н), 2,99-2,89 (м, 2 Н), 2,41-2,13 (м, 8 Н), 1,90-1,64 (м, 2 Н)
[2320] Пример 397. N-бензил-N-метил-5-[[1-[2-оксо-2-[(2S)-2-цианопирролидин-1-ил]этил]-4-пиперидил]амино]хинолин-8-карбоксамид
[2321] Указанное в заголовке соединение (256,2 мг, 57,0%) получали аналогично тому, как описано в примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-бензил-N-метил-5-(пиперидин-4-иламино)хинолин-8-карбоксамида гидрохлорид (393,7 мг, 0,88 ммоль), полученный в эталонном примере 231. 1H ЯМР (CDCl3, 400 МГц) δ 8,89-8,86 (м, 1 Н), 8,17-8,12 (м, 1 Н), 7,53 (д, 2 Н), 7,38 (т, 1 Н), 7,30-7,18 (м, 4 Н), 6,56 (дд, 1 Н), 5,17-4,73 (м, 2 Н), 4,56 (с, 1 Н), 4,34 (дд, 1 Н), 3,73-3,47 (м, 3 Н), 3,39-3,15 (м, 2 Н), 3,10 (с, 1,5 Н), 2,99-2,85 (м, 2 Н), 2,68 (с, 1,5 Н), 2,42-2,03 (м, 9Н), 1,80-1,59 (м, 2 Н).
[2322] Пример 398. N-метил-5-[[1-[2-оксо-2-[(2S)-2-цианопирролидин-1-ил]этил]-4-пиперидил]амино]-N-фенилхинолин-8-карбоксамид
[2323] Указанное в заголовке соединение (45,5 мг, 10,4%) получали аналогично тому, как описано в примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-метил-N-фенил-5-(пиперидин-4-иламино)хинолин-8-карбоксамида гидрохлорид (381,3 мг, 0,88 ммоль), полученный в эталонном примере 230. 1H ЯМР (CDCl3, 400 МГц) δ 8,88 (дд, 1 Н), 8,00 (д, 1 Н), 7,30-6,95 (м, 7 Н), 6,38 (с, 1 Н), 5,14-4,73 (м, 1 Н), 3,76-3,70 (м, 1 Н), 3,66-3,50 (м, 4 Н), 3,40-3,15 (м, 3 Н), 2,93-2,84 (м, 2 Н), 2,37-1,99 (м, 9 Н), 1,76-1,57 (м, 2 Н)
[2324] Пример 399. 5-[[1-[2-оксо-2-[(2S)-2-цианопирролидин-1-ил]этил]-4-пиперидил]амино]-N-(2-пиридил)хинолин-8-карбоксамид
[2325] Указанное в заголовке соединение (340,4 мг, 80,0%) получали таким же образом, как и в примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 5-(пиперидин-4-иламино)-N-(пиридин-2-ил)хинолин-8-карбоксамида гидрохлорид (369,9 мг, 0,88 ммоль), полученный в эталонном примере 233. 1H ЯМР (CDCl3, 400 МГц) δ 9,04 (д, 1 Н), 8,78 (д, 1 Н), 8,53 (д, 1 Н), 8,40 (д, 1 Н), 8,26 (д, 1 Н), 7,72 (т, 1 Н), 7,41 (кв, 1 Н), 7,01 (дд, 1 Н), 6,72 (д, 1 Н), 5,09-4,75 (м, 2 Н), 3,76-3,51 (м, 3 Н), 3,38-3,18 (м, 2 Н), 3,02-2,88 (м, 2 Н), 2,45-2,35 (м, 2 Н), 2,31-2,07 (м, 6 Н), 1,75-1,65 (м, 2 Н).
[2326] Пример 400. 5-[[1-[2-оксо-2-[(2S)-2-цианопирролидин-1-ил]этил]-4-пиперидил]амино]-N-(3-пиридил)хинолин-8-карбоксамид
[2327] Указанное в заголовке соединение (316,8 мг, 74,4%) получали таким же образом, как в примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 5-(пиперидин-4-иламино)-N-(пиридин-3-ил)хинолин-8-карбоксамида гидрохлорид (369,9 мг, 0,88 ммоль), полученный в эталонном примере 234. 1H ЯМР (CDCl3, 400 МГц) δ 8,92 (д, 1 Н), 8,84 (с, 1 Н), 8,84 (д, 1 Н), 8,46 (д, 1 Н), 8,31-8,29 (м, 2 Н), 7,41 (кв, 1 Н), 7,29 (дд, 1 Н), 6,71 (дд, 1 Н), 5,07-4,74 (м, 2 Н), 3,76-3,49 (м, 3 Н), 3,37-3,18 (м, 2 Н), 3,01-2,91 (м, 2 Н), 2,44-2,35 (м, 2 Н), 2,31-2,07 (м, 6 Н), 1,91-1,65 (м, 2Н).
[2328] Пример 401. 5-[[1-[2-оксо-2-[(2S)-2-цианопирролидин-1-ил]этил]-4-пиперидил]амино]-N-(4-пиридил)хинолин-8-карбоксамид
[2329] Указанное в заголовке соединение (85,1 мг, 20,0%) получали таким же образом, как и в примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 5-(пиперидин-4-иламино)-N-(пиридин-4-ил)хинолин-8-карбоксамида гидрохлорид (369,9 мг, 0,88 ммоль), полученный в эталонном примере 235. 1H ЯМР (CDCl3, 400 МГц) δ 8,97 (дд, 1 Н), 8,78 (д, 1 Н), 8,52 (д, 2 Н), 8,29 (д, 1 Н), 7,78 (д, 2 Н), 7,47 (кв, 1 Н), 6,76 (д, 1 Н), 5,06-4,77 (м, 2 Н), 3,78-3,50 (м, 3 Н), 3,39-3,21 (м, 2 Н), 3,07-2,94 (м, 2 Н), 2,47-2,37 (м, 2 Н), 2,34-2,09 (м, 6 Н), 1,94-1,76 (м, 2 Н).
[2330] Пример 402. 5-[[1-[2-оксо-2-[(2S)-2-цианопирролидин-1-ил]этил]-4-пиперидил]амино]-N-пиримидин-2-ил-хинолин-8-карбоксамид
[2331] Указанное в заголовке соединение (324,4 мг, 76,0%) получали аналогично тому, как описано в примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 5-(пиперидин-4-иламино)-N-(пиримидин-2-ил)хинолин-8-карбоксамида гидрохлорид (370,7 мг, 0,88 ммоль), полученный в эталонном примере 236. 1H ЯМР (CDCl3, 400 МГц) δ 9,00 (т, 1 Η), 8,81 (д, 1 Η), 8,68 (дд, 2 Η), 8,29 (д, 1 Η), 7,41-7,39 (м, 1 Η), 6,98 (т, 1 Η), 6,70 (д, 1 Η), 5,09-4,99 (м, 1,4 Η), 5,76-4,75 (м, 0,6 Η), 3,72-3,51 (м, 3 Η), 3,48 (с, 1 Η), 3,34-3,17 (м, 2 Η), 3,00-2,87 (м, 2 Η), 2,43-2,34 (м, 2 Η), 2,30-2,08 (м, 6 Η), 1,75-1,65 (м, 2 Η).
[2332] Пример 403. 5-[1-[2-оксо-2-[(2S,4S)-2-циано-4-фторпирролидин-1-ил]этил]-4-пиперидил]амино]-]-N-пиримидин-2-ил-хинолин-8-карбоксамида.
[2333] Указанное в заголовке соединение (16,3 мг, 29,5%) получали аналогично тому, как описано в примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 5-(пиперидин-4-иламино)-N-(пиримидин-2-ил)хинолин-8-карбоксамида гидрохлорид (46,3 мг, 0,11 ммоль), полученный в эталонном примере 236. 1H ЯМР (CDCl3, 400 МГц) δ 8,99 (д, 1 Н), 8,79 (д, 1 Н), 8,68 (д, 2 Н), 8,32-8,29 (м, 1 Н), 7,39 (кв, 1 Н), 6,98 (т, 1 Н), 6,70-6,67 (м, 1 Н), 5,48-5,27 (м, 1,4 Н), 5,09-4,92 (м, 1,6 Н), 4,20-3,72 (м, 2 Н), 3,62-3,56 (м, 1 Н), 3,48 (с, 1 Н), 3,43-3,17 (м, 2 Н), 3,01-2,87 (м, 2 Н), 2,49-1,83 (м, 6 Н), 1,75-1,55 (м, 2 Н).
[2334] Пример 404. 5-[[1-[2-оксо-2-[(2S,4S)-2-циано-4-фторпирролидин-1-ил]этил]-4-пиперидил]амино]-N-(2-пиридил)хинолин-8-карбоксамид
[2335] Указанное в заголовке соединение (45,5 мг, 82,6%) получали таким же образом, как описано в примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 5-(пиперидин-4-иламино)-N-(пиридин-2-ил)хинолин-8-карбоксамида гидрохлорид (46,3 мг, 0,11 ммоль), полученный в эталонном примере 23S. 1H ЯМР (CDCl3, 400 МГц) δ 8,99 (д, 1 Н), 8,72 (д, 1 Н), 8,50 (д, 1 Н), 8,38 (д, 1 Н), 8,30-8,27 (м, 1 Н), 7,71 (т, 1 Н), 7,36 (кв, 1 Н), 7,02-6,99 (м, 1 Н), 6,69-6,56 (м, 1 Н), 5,45-5,25 (м, 1,4 Н), 5,12-4,90 (м, 1,6 Н), 4,18-3,69 (м, 2 Н), 3,57-3,55 (м, 1 Н), 3,41-3,14 (м, 2 Н), 3,00-2,88 (м, 2 Н), 2,74-2,59 (м, 1 Н), 2,38-2,12 (м, 7 Н), 1,68-1,63 (м, 2 Н).
[2336] Пример 405. 5-[[1-[2-оксо-2-[(2S,4S)-2-циано-4-фторпирролидин-1-ил]этил]-4-пиперидил]амино]-N-(3-пиридил)хинолин-8-карбоксамид
[2337] Указанное в заголовке соединение (6,8 мг, 12,3%) получали аналогично тому, как описано в примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 5-(пиперидин-4-иламино)-N-(пиридин-3-ил)хинолин-8-карбоксамида гидрохлорид (46,3 мг, 0,11 ммоль), полученный в эталонном примере 234. 1H ЯМР (CDCl3, 400 МГц) δ 8,92 (д, 1 Н), 8,85 (с, 1 Н), 8,44 (д, 1 Н), 8,31-8,29 (м, 2Н), 7,41 (кв, 1 Н), 7,30 (кв, 1 Н), 6,72-6,68 (м, 1 Н), 5,49-5,29 (м, 1,4 Н), 5,06-4,93 (м, 1,6 Н), 4,23-4,13 (дд, 0,6 Н), 3,95-3,71 (м, 1,4 Н), 3,61-3,58 (м, 1 Н), 3,42-3,18 (м, 2 Н), 3,03-2,92 (м, 2 Н), 2,77-2,62 (м, 1 Н), 2,48-2,15 (м, 5 Н), 1,88-1,67 (м, 2 Н)
[2338] Пример 406. 5-[[1-[2-оксо-2-[(2S,4S)-2-циано-4-фторпирролидин-1-ил]этил]-4-пиперидил]амино]-N-(4-пиридил)хинолин-8-карбоксамид
[2339] Указанное в заголовке соединение (1,3 мг, 2,3%) получали таким же образом, как и в примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 5-(пиперидин-4-иламино)-N-(пиридин-4-ил)хинолин-8-карбоксамида гидрохлорид (46,3 мг, 0,11 ммоль), полученный в эталонном примере 235. 1H ЯМР (CDCl3, 400 МГц) δ 8,98 (д, 1 Н), 8,80 (д, 1 Н), 8,53 (д, 2 Н), 8,28 (д, 1 Н), 7,78 (д, 1 Н), 7,48 (кв, 1 Н), 6,77 (д, 1 Н), 5,50-5,30 (м, 1 Н), 5,29 (д, 0,4 Н), 4,97 (д, 0,6 Η), 4,86 (т, 1 Η), 4,23-3,66 (м, 3 Η), 3,44-3,21 (м, 2 Η), 3,06-2,95 (м, 2 Η), 2,81-2,66 (м, 1 Η), 2,49-2,23 (м, 5 Η), 2,05-2,00 (м, 1 Η) 1,94-1,67 (м, 1 Η).
[2340] Пример 407. N-изоксазол-3-ил-5-[[1-[2-оксо-2-[(2S,4S)-2-циано-4-фторпирролидин-1-ил]этил]-4-пиперидил]амино]хинолин-8-карбоксамид
[2341] Указанное в заголовке соединение (20,4 мг, 37,7%) получали аналогично тому, как описано в примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-(изоксазол-3-ил)-5-(пиперидин-4-иламино)хинолин-8-карбоксамид гидрохлорида (45,3 мг, 0,11 ммоль), полученный в эталонном примере 237. 1H ЯМР (CDCl3, 400 МГц) δ 8,91 (д, 1 Н), 8,71 (д, 1 Н), 8,33 (с, 1 Н), 8,27 (д, 1 Н), 7,42-7,39 (м, 1 Н), 7,29 (с, 1 Н), 6,70 (д, 1 Н), 5,49-5,29 (м, 1,4 Н), 5,03 (т, 1 Н), 4,94 (д, 0,6 Н), 4,20 (дд, 0,5 Н), 4,00-3,72 (м, 1,5 Н), 3,62-3,61 (м, 1 Н), 3,44-3,19 (м, 2 Н), 2,98 (кв, 2 Н), 2,78-2,63 (м, 1 Н), 2,48-2,16 (м, 4 Н), 1,80-1,66 (м, 4 Н)
[2342] Пример 408. N-[5-[[1-[2-оксо-2-[(2S)-2-цианопирролидин-1-ил]этил]-4-пиперидил]амино]-8-хинолил] ацетамид
[2343] Указанное в заголовке соединение (33,6 мг, 9,0%) получали аналогично тому, как описано в примере 121, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-(5-(пиперидин-4-иламино)хинолин-8-ил)ацетамида гидрохлорид (314,4 мг, 0,88 ммоль), полученный в эталонном примере 238. 1H ЯМР (CDCl3, 400 МГц) δ 8,91 (д, 1 Н), 8,78 (дд, 1 Н), 8,60 (д, 1 Н), 8,20 (дд, 1 Н), 7,40 (кв, 1 Н), 6,64(д, 1 Н) 5,49-5,27 (м, 1,4 Н), 4,93 (д, 0,6 Н), 4,23-3,73 (м, 3 Н), 3,48-3,42 (м, 1,4 Н), 3,29-3,17 (м, 1,6 Н), 2,99-2,87 (м, 2 Н), 2,77-2,61 (м, 1 Н), 2,47-2,33 (м, 3 Н), 2,30 (с, 3 Н), 2,21-2,13 (м, 2,5 Н), 1,80-1,55 (м, 2,5 Н)
[2344] Пример 409. N-[5-[[1-[2-оксо-2-[(2S,4S)-2-циано-4-фторпирролидин-1-ил]этил]-4-пиперидил]амино]-8-хинолил]ацетамид
[2345] Указанное в заголовке соединение (3,7 мг, 7,7%) получали аналогично тому, как описано в примере 131, за исключением того, что вместо 3-метил-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали N-(5-(пиперидин-4-иламино)хинолин-8-ил) ацетамида гидрохлорид (39,3 мг, 0,11 ммоль), полученный в эталонном примере 238. 1H ЯМР (CDCl3, 400 МГц) δ 9,49 (с, 1 Н), 8,78 (дд, 1 Н), 8,60 (д, 1 Н), 8,20 (дд, 1 Н), 7,40 (кв, 1 Н), 6,64(д, 1 Н) 5,49-5,27 (м, 1,4 Н), 4,93 (д, 0,6 Н), 4,23-3,73 (м, 2,5 Н), 3,48-3,25 (м, 2,5 Н), 3,21 (д, 1 Н), 2,99-2,87 (м, 2 Н), 2,77-2,61 (м, 1 Н), 2,40-2,33 (м, 2,6 Н), 2,30 (с, 3 Н), 2,21-2,13 (м, 2Н), 1,83-1,55 (м, 2,4 Н)
[2346] Пример 410. (2S,4S)-4-фтор-1-[2-[4-[(6-метил-4-хинолил)окси]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2347] Указанное в заголовке соединение (190,9 мг, 38,8%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 6-метил-4-(пиперидин-4-илокси)хинолина (346,3 мг, 1,24 ммоль), полученный в эталонном примере 239. 1H-ЯМР (CDCl3, 400 МГц) δ 8,65 (д, 1 Н), 7,97 (с, 1 Н), 7,92 (д, 1 Н), 7,53 (д, 1 Н), 6,69 (д, 1 Н), 5,50-5,25 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,75-4,60 (м, 1 Н), 4,30-4,10 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,60-3,20 (м, 2 Н), 2,90-2,80 (м, 2 Н), 2,80-2,65 (м, 1 Н), 2,65-2,55 (м, 2 Н), 2,55 (с, 3 Н), 2,40-2,05 (м, 2 Н), 2,05-1,95 (м, 2 H)
[2348] Пример 411. (2S,4S)-4-фтор-1-[2-[4-[[6-(трифторметил)-4-хинолил]окси]-1-пиперидил] ацетил]пирролидин-2-карбонитрил
[2349] Указанное в заголовке соединение (245,4 мг, 43,9%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 4-(пиперидин-4-илокси)-6-(трифторметил)хинолина гидрохлорид (413,3 мг, 1,24 ммоль), полученныйв эталонном примере 240. 1H-ЯМР (CDCl3, 400 МГц) δ 8,83 (д, 1 Н), 8,51 (с, 1 Н), 8,13 (д, 1 Н), 7,87 (д, 1 Н), 6,81 (д, 1 Н), 5,55-5,35 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,75-4,65 (м, 1 Н), 4,30-4,10 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,55-3,20 (м, 2 Н), 3,00-2,80 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,60-2,50 (м, 2 Н), 2,30-2,10 (м, 2 Н), 2,10-1,95 (м, 2 Н)
[2350] Пример 412. (2S,4S)-4-фтор-1-[2-[4-[[2-(трифторметил)-4-хинолил]окси]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2351] Указанное в заголовке соединение (312,7 мг, 55,9%) получали таким же образом, как и в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 4-(пиперидин-4-илокси)-2-(трифторметил)хинолина гидрохлорид (291,3 мг, 0,88 ммоль), полученныйв эталонном примере 241. 1H-ЯМР (CDCl3, 400 МГц) δ 8,27 (д, 1 Н), 8,14 (д, 1 Н), 7,80 (т, 1 Н), 7,62 (т, 1 Н), 7,02 (с, 1 Н), 5,50-5,25 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,85-4,70 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,55-3,15 (м, 2 Н), 2,95-2,80 (м, 2 Н), 2,80-2,65 (м, 1 Н), 2,65-2,55 (м, 2 Н), 2,30-2,10 (м, 2 Н), 2,10-1,95 (м,2Н)
[2352] Пример 413. (2S,4S)-4-фтор-1-[2-[4-[[6-фтор-2-(трифторметил)-4-хинолил]окси]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2353] Указанное в заголовке соединение (243,7 мг, 41,9%) получали таким же образом, как и в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 6-фтор-4-(пиперидин-4-илокси)-2-(трифторметил)хинолина гидрохлорид (255,6 мг, 0,73 ммоль), полученный в эталонном примере 242. 1H-ЯМР (CDCl3, 400 МГц) δ 8,15 (д, 1 Н), 7,84 (д, 1 Н), 7,56 (с, 1 Н), 7,03 (с, 1 Н), 5,50-5,20 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,85-4,70 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,55-3,20 (м, 2 Н), 2,95-2,80 (м, 2 Н), 2,80-2,65 (м, 1 Н), 2,65-2,55 (м, 2 Н), 2,30-2,10 (м, 2 Н), 2,10-1,95 (м, 2 Н)
[2354] Пример 414. (2S,4S)-4-фтор-1-[2-[4-[[б-метокси-2-(трифторметил)-4-хинолил]окси]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2355] Указанное в заголовке соединение (266,4 мг, 44,6%) получали таким же образом, как и в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 6-метокси-4-(пиперидин-4-илокси)-2-(трифторметил)хинолина гидрохлорид (303,8 мг, 0,84 ммоль), полученный в эталонном примере 243. 1H-ЯМР (CDCl3, 400 МГц) δ 8,04 (д, 1 Н), 7,48-7,42 (м, 2 Н), 7,00 (с, 1 Н), 5,55-5,25 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,85-4,70 (м, 1 Н), 4,35-4,20 (м, 1 Н), 3,98 (с, 3 Н), 3,98-3,70 (м, 2 Н), 3,50-3,20 (м, 2 Н), 2,95-2,85 (м, 2 Н), 2,85-2,60 (м, 1 Н), 2,70-2,55 (м, 2 Н), 2,30-2,10 (м, 2Н), 2,10-2,00 (м, 2 Н)
[2356] Пример 415. (2S,4S)-4-фтор-1-[2-[4-[[8-метокси-2-(трифторметил)-4-хинолил]окси]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2357] Указанное в заголовке соединение (429,0 мг, 71,9%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 8-метокси-4-(пиперидин-4-илокси)-2-(трифторметил)хинолина гидрохлорид (414,9 мг, 1,14 ммоль), полученный в эталонном примере 244. 1H-ЯМР (CDCl3, 400 МГц) δ 7,81 (д, 1 Н), 7,54 (т, 1 Н), 7,14 (д, 1 Н), 7,05 (с, 1 Н), 5,55-5,35 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,85-4,70 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,09 (с, 3 Н), 4,05-3,70 (м, 2 Н), 3,55-3,20 (м, 2 Н), 2,90-2,80 (м, 2 Н), 2,80-2,70 (м, 1 Н), 2,70-2,55 (м, 2 Н), 2,35-2,10 (м, 2 Н), 2,10-2,00 (м, 2 Н)
[2358] Пример 416. (2S,4S)-4-фтор-1-[2-[4-[(3-фтор-5-хинолил)окси]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2359] Указанное в заголовке соединение (179,0 мг, 36,0%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 3-фтор-5-(пиперидин-4-илокси)хинолина (351,2 мг, 1,24 ммоль), полученный в эталонном примере 245. 1H-ЯМР (CDCl3, 400 МГц) δ 8,79 (с, 1 Н), 8,17 (д, 1 Н), 7,68 (с, 1 Н), 7,56 (т, 1 Н), 6,91 (д, 1 Н), 5,55-5,30 (м, 1 Н), 5,05-4,85 (м, 1 Н), 4,70-4,50 (м, 1 Н), 4,30-4,10 (м, 1 Н), 4,00-3,70 (м, 2 Н), 3,55-3,20 (м, 2 Н), 2,90-2,75 (м, 2 Н), 2,75-2,60 (м, 1 Н), 2,60-2,50 (м, 2 Н), 2,35-2,10 (м, 2 Н), 2,10-1,90 (м, 2 Н)
[2360] Пример 417. 5-[[1-[2-оксо-2-[(2S,4S)-2-циано-4-фторпирролидин-1-ил]этил]-4-пиперидил]окси]хинолин-2-карбонитрил
[2361] Указанное в заголовке соединение (70,2 мг, 13,9%) получали таким же образом, как и в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 5-(пиперидин-4-илокси)хинолин-2-карбонитрила гидрохлорид (359,9 мг, 1,24 ммоль), полученный в эталонном примере 246. 1H-ЯМР (CDCl3, 400 МГц) δ 8,73 (д, 1 Н), 7,73-7,64 (м, 3 Н), 6,99 (д, 1 Н), 5,55-5,35 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,70-4,55 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,55-3,20 (м, 2 Н), 2,90-2,80 (м, 2 Н), 2,80-2,65 (м, 1 Н), 2,65-2,50 (м, 2 Н), 2,35-2,05 (м, 2 Н), 2,05-1,95 (м, 2 Н)
[2362] Пример 418. (2S,4S)-1-[2-[4-[(8-хлор-5-хинолил)окси]-1-пиперидил]ацетил]-4-фторпирролидин-2-карбонитрил
[2363] Указанное в заголовке соединение (304,0 мг, 58,7%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 8-хлор-5-(пиперидин-4-илокси)хинолина (371,7 мг, 1,24 ммоль), полученный в эталонном примере 247. 1H-ЯМР (CDCl3, 400 МГц) δ 8,99 (д, 1 Н), 8,53 (д, 1 Н), 7,53-7,50 (м, 2 Н), 7,04 (д, 1 Н), 5,75-5,20 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,70-4,50 (м, 1 Н), 4,30-4,10 (м, 1 Н), 4,10-3,65 (м, 2 Н), 3,65-3,20 (м, 2 Н), 3,10-2,80 (м, 2 Н), 2,80-2,55 (м, 1 Н), 2,55-2,40 (м, 2 Н), 2,40-2,15 (м, 2 Н), 2,15-1,90 (м, 2 Н)
[2364] Пример 419. (2S,4S)-4-фтор-1-[2-[4-(1-изохинолокси)-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2365] Указанное в заголовке соединение (156,9 мг, 86,5%) получали таким же образом, как и в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 1-(пиперидин-4-илокси)изохинолина гидрохлорид (125,6 мг, 0,47 ммоль), полученный в эталонном примере 248. 1H-ЯМР (CDCl3, 400 МГц) δ 8,25 (д, 1 Н), 7,96 (д, 1 Н), 7,73 (д, 1 Н), 7,66 (т, 1 Н), 7,54 (т, 1 Η), 7,19 (д, 1 Η), 5,75-5,25 (м, 2 Η), 5,00-4,90 (м, 1 Η), 4,30-4,15 (м, 1 Η), 4,10-3,70 (м, 2 Η), 3,60-3,20 (м, 2 Η), 2,90-2,80 (м, 2 Η), 2,80-2,65 (м, 1 Η), 2,65-2,50 (м, 2 Η), 2,35-2,10 (м, 2 Η), 2,10-1,90 (м, 2 Η)
[2366] Пример 420. (2S,4S)-4-фтор-1-[2-[4-(4-изохинолокси)-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2367] Указанное в заголовке соединение (39,9 мг, 22,0%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 4-(пиперидин-4-илокси)изохинолина гидрохлорид (328,9 мг, 1,24 ммоль), полученный в эталонном примере 249. 1H-ЯМР (CDCl3, 400 МГц) δ 8,90 (с, 1 Н), 8,22 (д, 1 Н), 8,10 (с, 1 Н), 7,94 (д, 1 Н), 7,71 (т, 1 Н), 7,63 (т, 1 Н), 5,60-5,25 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,80-4,60 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,60-3,15 (м, 2 Н), 2,95-2,80 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,60-2,50 (м, 2 Н), 2,30-2,10 (м, 2 Н), 2,10-1,90 (м, 2 Н)
[2368] Пример 421. (2S,4S)-4-фтор-1-[2-[4-(5-изохинолокси)-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2369] Указанное в заголовке соединение (107,7 мг, 59,4%) получали таким же образом, как и в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 5-(пиперидин-4-илокси)изохинолина гидрохлорид (156,5 мг, 0,59 ммоль), полученный в эталонном примере 250. 1H-ЯМР (CDCl3, 400 МГц) δ 9,20 (с, 1 Н), 8,53 (д, 1 Н), 8,03 (д, 1 Н), 7,55-7,47 (м, 2 Н), 7,02 (д, 1 Н), 5,55-5,20 (м, 1 Н), 5,00-4,85 (м, 1 Н), 4,70-4,50 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,60-3,20 (м, 2 Н), 2,90-2,80 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,60-2,50 (м, 2 Н), 2,30-2,10 (м, 2 Н), 2,10-1,90 (м, 2 Н)
[2370] Пример 422. (2S,4S)-4-фтор-1-[2-[4-(6-изохинолокси)-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2371] Указанное в заголовке соединение (73,3 мг, 40,4%) получали таким же образом, как и в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 6-(пиперидин-4-илокси)изохинолина гидрохлорид (328,9 мг, 1,24 ммоль), полученный в эталонном примере 251. 1H-ЯМР (CDCl3, 400 МГц) δ 9,10 (с, 1 Н), 8,43 (д, 1 Н), 7,87 (д, 1 Н), 7,52 (д, 1 Н), 7,23 (д, 1 Н), 7,06 (с, 1 Н), 5,55-5,25 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,65-4,50 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,60-3,15 (м, 2 Н), 2,90-2,80 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,60-2,45 (м, 2 Н), 2,30-2,10 (м, 2 Н), 2,00-1,80 (м, 2 Н)
[2372] Пример 423. (2S,4S)-4-фтор-1-[2-[4-(7-изохинолокси)-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2373] Указанное в заголовке соединение (140,7 мг, 77,6%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 7-(пиперидин-4-илокси)изохинолина гидрохлорид (328,9 мг, 1,24 ммоль), полученный в эталонном примере 252. 1H-ЯМР (CDCl3, 400 МГц) δ 9,15 (с, 1 Н), 8,41 (д, 1 Н), 7,75 (д, 1 Н), 7,58 (д, 1 Н), 7,35 (д, 1 Н), 7,23 (с, 1 Н), 5,55-5,25 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,60-4,45 (м, 1 Н), 4,25-4,10 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,65-3,20 (м, 2 Н), 2,90-2,80 (м, 2 Н), 2,80-2,60 (м, 1 Н), 2,60-2,45 (м, 2 Н), 2,30-2,05 (м, 2 Н), 2,00-1,85 (м, 2 Н)
[2374] Пример 424. (2S,4S)-4-фтор-1-[2-[4-[(б-метокси-2-метил-4-хинолил)окси]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2375] Указанное в заголовке соединение (141,2 мг, 69,8%) получали таким же образом, как и в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 6-метокси-2-метил-4-(пиперидин-4-илокси)хинолина гидрохлорид (383,6 мг, 1,24 ммоль), полученный в эталонном примере 253. 1H-ЯМР (CDCl3, 400 МГц) δ 7,85 (д, 1 Н), 7,42 (с, 1 Н), 7,32 (д, 1 Н), 6,59 (с, 1 Н), 5,55-5,20 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,70-4,60 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,94 (с, 3 Н), 3,55-3,20 (м, 2 Н), 2,90-2,80 (м, 2 Н), 2,80-2,65 (м, 1 Н), 2,65 (с, 3 Н), 2,65-2,50 (м, 2 Н), 2,30-2,10 (м, 2 Н), 2,10-1,95 (м, 2 Н)
[2376] Пример 425. (2S,4S)-4-фтор-1-[2-[4-(5-хинолокси)-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2377] Указанное в заголовке соединение (161,4 мг, 37,0%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 5-(пиперидин-4-илокси)хинолина гидрохлорид (383,6 мг, 1,24 ммоль), полученный в эталонном примере 3S. 1H-ЯМР (CDCl3, 400 МГц) δ 8,91 (д, 1 Н), 8,60 (д, 1 Н), 7,69 (д, 1 Н), 7,60 (т, 1 Н), 7,40 (т, 1 Н), 6,89 (д, 1 Н), 5,55-5,25 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,80-4,70 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,55-3,20 (м, 2 Н), 2,95-2,80 (м, 2 Н), 2,80-2,65 (м, 1 Н), 2,65-2,50 (м, 2 Н), 2,30-2,10 (м, 2 Н), 2,10-1,95 (м, 2 Н)
[2378] Пример 426. (2S)-1-[2-[4-[(6-метокси-4-хинолил)окси]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2379] Указанное в заголовке соединение (127,1 мг, 25,9%) получали аналогично тому, как описано в примере 110, за исключением того, что вместо N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 6-метокси-4-(пиперидин-4-илокси)хинолина гидрохлорид (366,1 мг, 1,24 ммоль), полученный в эталонном примере 42. 1H-ЯМР (CDCl3, 400 МГц) δ 8,59 (д, 1 Н), 7,93 (д, 1 Н), 7,47 (с, 1 Н), 7,34 (д, 1 Н), 6,70 (д, 1 Н), 5,20-4,70 (м, 1 Н), 4,70-4,60 (м, 1 Н), 3,95 (с, 3 Н), 3,80-3,60 (м, 1 Н), 3,60-3,50 (м, 1 Н), 3,45-3,20 (м, 2 Н), 2,95-2,75 (м, 2 Н), 2,70-2,50 (м, 2 Н), 2,40-2,10 (м, 6 Н), 2,10-1,95 (м, 2 Н)
[2380] Пример 427. (2S)-1-[2-[4-[(6-фтор-4-хинолил)окси]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2381] Указанное в заголовке соединение (51,1 мг, 10,8%) получали аналогично тому, как описано в примере 110, за исключением того, что вместо N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 6-фтор-4-(пиперидин-4-илокси)хинолина гидрохлорид (351,2 мг, 1,24 ммоль), полученный в эталонном примере 40. 1H-ЯМР (CDCl3, 400 МГц) δ 8,69 (д, 1 Н), 8,02 (д, 1 Н), 7,81 (д, 1 Н), 7,46 (с, 1 Н), 6,74 (д, 1 Н), 5,20-4,75 (м, 1 Н), 4,75-4,60 (м, 1 Н), 3,80-3,60 (м, 1 Н), 3,60-3,50 (м, 1 Н), 3,50-3,20 (м, 2 Н), 2,95-2,75 (м, 2 Н), 2,70-2,50 (м, 2 Н), 2,40-2,10 (м, 6 Н), 2,10-1,95 (м, 2 Н)
[2382] Пример 428. (2S)-1-[2-[4-[(7-хлор-4-хинолил)окси]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2383] Указанное в заголовке соединение (272,5 мг, 55,0%) получали аналогично тому, как описано в примере 110, за исключением того, что вместо N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 7-хлор-4-(пиперидин-4-илокси)хинолина гидрохлорид (371,6 мг, 1,24 ммоль), полученный в эталонном примере 254. 1H-ЯМР (CDCl3, 400 МГц) δ 8,70 (д, 1 Н), 8,14 (д, 1 Н), 8,00 (с, 1 Н), 7,43 (д, 1 Н), 6,70 (д, 1 Н), 5,20-4,75 (м, 1 Н), 4,75-4,60 (м, 1 Н), 3,80-3,60 (м, 1 Н), 3,60-3,50 (м, 1 Н), 3,45-3,15 (м, 2 Н), 2,90-2,75 (м, 2 Н), 2,70-2,50 (м, 2 Н), 2,40-2,10 (м, 6 Н), 2,10-1,95 (м, 2 Н)
[2384] Пример 429. (2S)-1-[2-[4-[(3-фтор-5-хинолил)окси]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2385] Указанное в заголовке соединение (419,4 мг, 88,3%) получали таким же образом, как описано в примере 110, за исключением того, что вместо N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 3-фтор-5-(пиперидин-4-илокси)хинолина гидрохлорид (351,2 мг, 1,24 ммоль), полученный в эталонном примере 245. 1H-ЯМР (CDCl3, 400 МГц) δ 8,79 (с, 1 Н), 8,19 (с, 1 Н), 7,68 (д, 1 Н), 7,55 (т, 1 Н), 6,91 (д, 1 Н), 5,25-4,70 (м, 1 Н), 4,65-4,55 (м, 1 Н), 3,80-3,60 (м, 1 Н), 3,60-3,50 (м, 1 Н), 3,50-3,10 (м, 2 Н), 2,90-2,75 (м, 2 Н), 2,65-2,50 (м, 2 Н), 2,45-2,10 (м, 6 Н), 2,10-1,95 (м, 2 Н)
[2386] Пример 430. 5-[[1-[2-оксо-2-[(2S)-2-цианопирролидин-1-ил]этил]-4-пиперидил]окси]хинолин-2-карбонитрил
[2387] Указанное в заголовке соединение (198,9 мг, 41,1%) получали таким же образом, как и в примере 110, за исключением того, что вместо N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 5-(пиперидин-4-илокси)хинолин-2-карбонитрил гидрохлорид (359,9 мг, 1,24 ммоль), полученныйв эталонном примере 246. 1H-ЯМР (CDCl3, 400 МГц) δ 8,74 (д, 1 Н), 7,72-7,66 (м, 3 Н), 7,01 (д, 1 Н), 5,20-4,75 (м, 1 Н), 4,70-4,60 (м, 1 Н), 3,80-3,60 (м, 1 Н), 3,60-3,50 (м, 1 Н), 3,45-3,20 (м, 2 Н), 2,90-2,80 (м, 2 Н), 2,70-2,50 (м, 2 Н), 2,40-2,10 (м, 6 Н), 2,10-1,95 (м, 2 Н)
[2388] Пример 431. (2S)-1-[2-[4-[(8-хлор-5-хинолил)окси]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2389] Указанное в заголовке соединение (383,5 мг, 77,4%) получали аналогично тому, как описано в примере 110, за исключением того, что вместо N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 8-хлор-5-(пиперидин-4-илокси)хинолина гидрохлорид (371,6 мг, 1,24 ммоль), полученный в эталонном примере 247. 1H-ЯМР (CDCl3, 400 МГц) δ 9,00 (д, 1 Н), 8,54 (д, 1 Н), 7,56-7,51 (м, 2 Н), 7,05 (д, 1 Н), 5,45-4,70 (м, 1 Н), 4,65-4,55 (м, 1 Н), 3,85-3,65 (м, 1 Н), 3,65-3,55 (м, 1 Н), 3,55-3,20 (м, 2 Н), 3,05-2,85 (м, 2 Н), 2,60-2,40 (м, 2 Н), 2,40-2,00 (м, 8 Н)
[2390] Пример 432. (2S,4S)-4-фтор-1-[2-[4-[(7-метил-4-хинолил)окси]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2391] Указанное в заголовке соединение (129,3 мг, 22,3%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 7-метил-4-(пиперидин-4-илокси)хинолина гидрохлорид (407,0 мг, 1,46 ммоль), полученныйв эталонном примере 255. 1H-ЯМР (CDCl3, 400 МГц) δ 8,68 (д, 1 Н), 8,11 (д, 1 Н), 7,80 (с, 1 Н), 7,34 (д, 1 Н), 6,67 (д, 1 Н), 5,50-5,25 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,75-4,65 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,55-3,20 (м, 2 Η), 2,95-2,75 (м, 2 Η), 2,75-2,65 (м, 1 Η), 2,65-2,56 (м, 2 Η), 2,56 (с, 3 Η), 2,30-2,10 (м, 2 Η), 2,10-1,95 (м, 2 Η)
[2392] Пример 43S. (2S,4S)-4-фтор-1-[2-[4-[(7-фтор-4-хинолил)окси]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2393] Указанное в заголовке соединение (239,1 мг, 40,9%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 7-фтор-4-(пиперидин-4-илокси)хинолина гидрохлорид (421,3 мг, 1,49 ммоль), полученный в эталонном примере 256. 1H-ЯМР (CDCl3, 400 МГц) δ 8,71 (д, 1 Н), 8,22 (д, 1 Н), 7,64 (д, 1 Н), 7,27 (с, 1 Н), 6.69 (д, 1 Н), 5,50-5,25 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,75-4,65 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,50-3,20 (м, 2 Н), 2,95-2,80 (м, 2 Н), 2,80-2,65 (м, 1 Н), 2,65-2,50 (м, 2 Н), 2,30-2,10 (м, 2 Н), 2,10-1,95 (м, 2 H)
[2394] Пример 434. 4-[[1-[2-оксо-2-[(2S,4S)-2-циано-4-фторпирролидин-1-ил]этил]-4-пиперидил]окси]хинолин-8-карбонитрил
[2395] Указанное в заголовке соединение (277,0 мг, 46,6%) получали таким же образом, как и в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 4-(пиперидин-4-илокси)хинолин-8-карбонитрил гидрохлорид (414,4 мг, 1,43 ммоль), полученный в эталонном примере 257. 1H-ЯМР (CDCl3, 400 МГц) δ 8,87 (д, 1 Н), 8,46 (д, 1 Н), 8,09 (д, 1 Н), 7,54 (т, 1 Н), 6,84 (д, 1 Н), 5,55-5,25 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,80-4,65 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,00-3.70 (м, 2 Н), 3,50-3,20 (м, 2 Н), 2,90-2,80 (м, 2 Н), 2,80-2,65 (м, 1 Н), 2,65-2,50 (м, 2 Н), 2,30-2,10 (м, 2 Н), 2,10-1,95 (м, 2 Н)
[2396] Пример 435. (2S,4S)-4-фтор-1-[2-[4-[(8-фтор-4-хинолил)окси]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2397] Указанное в заголовке соединение (301,2 мг, 50,5%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 8-фтор-4-(пиперидин-4-илокси)хинолина гидрохлорид (421,3 мг, 1,49 ммоль), полученный в эталонном примере 258. 1H-ЯМР (CDCl3, 400 МГц) δ 8,77 (д, 1 Н), 8,00 (д, 1 Н), 7,44-7,37 (м, 2 Н), 6,78 (д, 1 Н), 5,55-5,25 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,80-4,65 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,55-3,20 (м, 2 Н), 2,95-2,75 (м, 2 Н), 2,75-2,65 (м, 1 Н), 2,65-2,50 (м, 2 Н), 2,30-2,10 (м, 2 Н), 2,10-1,95 (м, 2 Н)
[2398] Пример 436. (2S,4S)-4-фтор-1-[2-[4-[(2-метил-4-хинолил)окси]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2399] Указанное в заголовке соединение (79,9 мг, 13,5%) получали таким же образом, как описано в примере 3S0, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 2-метил-4-(пиперидин-4-илокси)хинолина гидрохлорид (415,4 мг, 1,49 ммоль), полученный в эталонном примере 259. 1H-ЯМР (CDCl3, 400 МГц) δ 8,16 (д, 1 Н), 7,94 (д, 1 Н), 7,66 (т, 1 Н), 7,44 (т, 1 Н), 6,61 (с, 1 Н), 5,50-5,25 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,75-4,65 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,55-3,20 (м, 2 Н), 2,95-2,80 (м, 2 Н), 2,80-2,69 (м, 1 Н), 2,69 (с, 3 Н), 2,69-2,55 (м, 2 Н), 2,30-2,10 (м, 2 Н), 2,10-1,95 (м, 2 Н)
[2400] Пример 437. (2S,4S)-4-фтор-1-[2-[4-[(б-фтор-2-метил-4-хинолил)окси]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2401] Указанное в заголовке соединение (403,6 мг, 65,4%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 6-фтор-2-метил-4-(пиперидин-4-илокси)хинолина гидрохлорид (442,2 мг, 1,49 ммоль), полученный в эталонном примере 260. 1H-ЯМР (CDCl3, 400 МГц) δ 7,90 (д, 1 Н), 7,72 (д, 1 Н), 7,39 (с, 1 Н), 6,60 (с, 1 Н), 5,50-5,25 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,70-4,60 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,50-3,20 (м, 2 Н), 2,90-2,75 (м, 2 Н), 2,75-2,65 (м, 1 Н), 2,65 (с, 3 Н), 2,65-2,55 (м, 2 Н), 2,30-2,10 (м, 2 Н), 2,10-1,95 (м, 2 Н)
[2402] Пример 438. (2S,4S)-4-фтор-1-[2-[4-[(8-метокси-4-хинолил)окси]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2403] Указанное в заголовке соединение (65,9 мг, 10,7%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 8-метокси-4-(пиперидин-4-илокси)хинолина гидрохлорид (97,6 мг, 0,3S ммоль), полученный в эталонном примере 261. 1H-ЯМР (CDCl3, 400 МГц) δ 8,74 (д, 1 Н), 7,79 (д, 1 Н), 7,43 (т, 1 Н), 7,06 (д, 1 Н), 6,76 (д, 1 Н), 5,50-5,25 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,75-4,65 (м, 1 Н), 4,30-4,15 (м, 1 Н), 4,08 (с, 3 Н), 4,08-3,70 (м, 2 Н), 3,55-3,20 (м, 2 Н), 2,90-2,75 (м, 2 Н), 2,75-2,65 (м, 1 Н), 2,65-2,55 (м, 2 Н), 2,30-2,10 (м, 2 Н), 2,10-1,95 (м, 2 Н)
[2404] Пример 439. (2S,4S)-4-фтор-1-[2-[4-[(8-метил-4-хинолил)окси]-1-пиперидил]ацетил]пирролидин-2-карбонитрил
[2405] Указанное в заголовке соединение (450,4 мг, 76,3%) получали таким же образом, как описано в примере 330, за исключением того, что вместо 8-фтор-N-(пиперидин-4-ил)хинолин-5-амина гидрохлорида использовали 8-метил-4-(пиперидин-4-илокси)хинолина гидрохлорид (415,4 мг, 1,49 ммоль), полученный в эталонном примере 262. 1H-ЯМР (CDCl3, 400 МГц) δ 8,75 (д, 1 Н), 8,08 (д, 1 Н), 7,54 (д, 1 Н), 7,38 (т, 1 Н), 6,72 (д, 1 Н), 5,50-5,25 (м, 1 Н), 5,00-4,90 (м, 1 Н), 4,75-4,65 (м, 1 Н), 4,25-4,10 (м, 1 Н), 4,05-3,70 (м, 2 Н), 3,50-3,20 (м, 2 Н), 2,90-2,78 (м, 2 Н), 2,78 (с, 3 Н), 2,78-2,60 (м, 1 Н), 2,60-2,50 (м, 2 Н), 2,30-2,10 (м, 2 Н), 2,10-1,95 (м,2Н)
[2406] Структуры соединений представлены в таблице 1. Химические названия определены с помощью ChemDraw.
[2407]
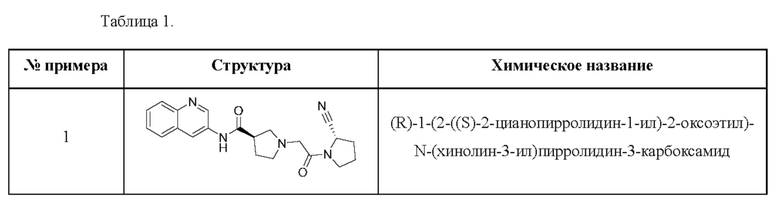

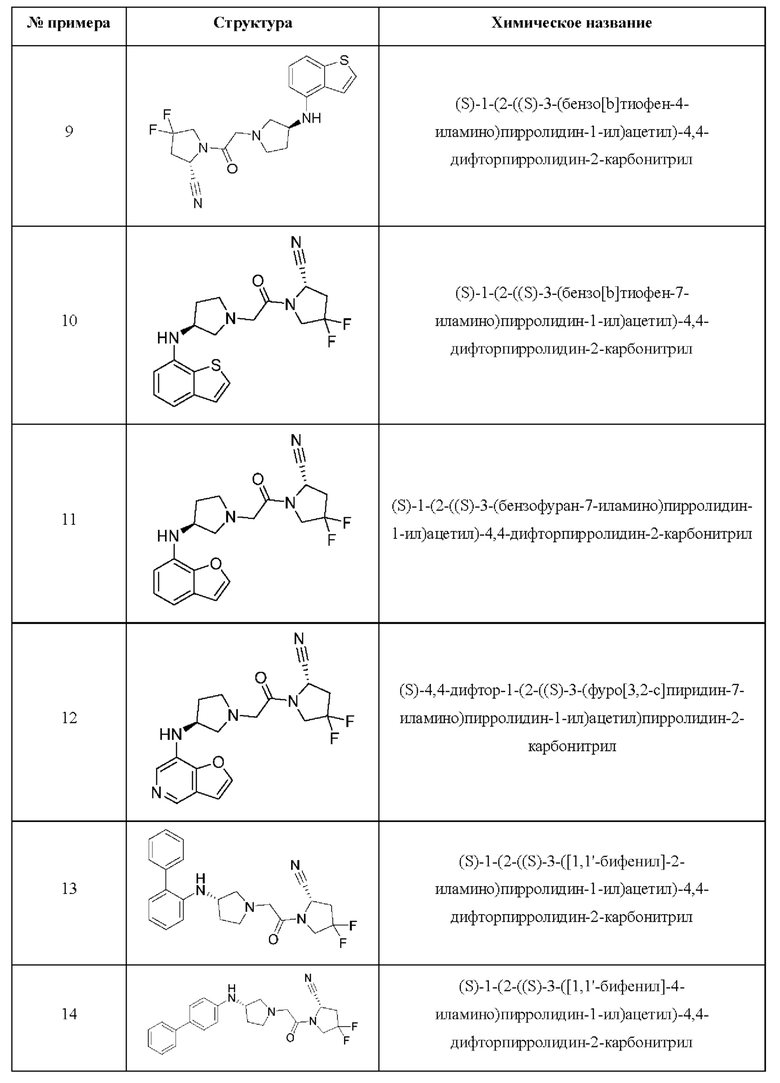
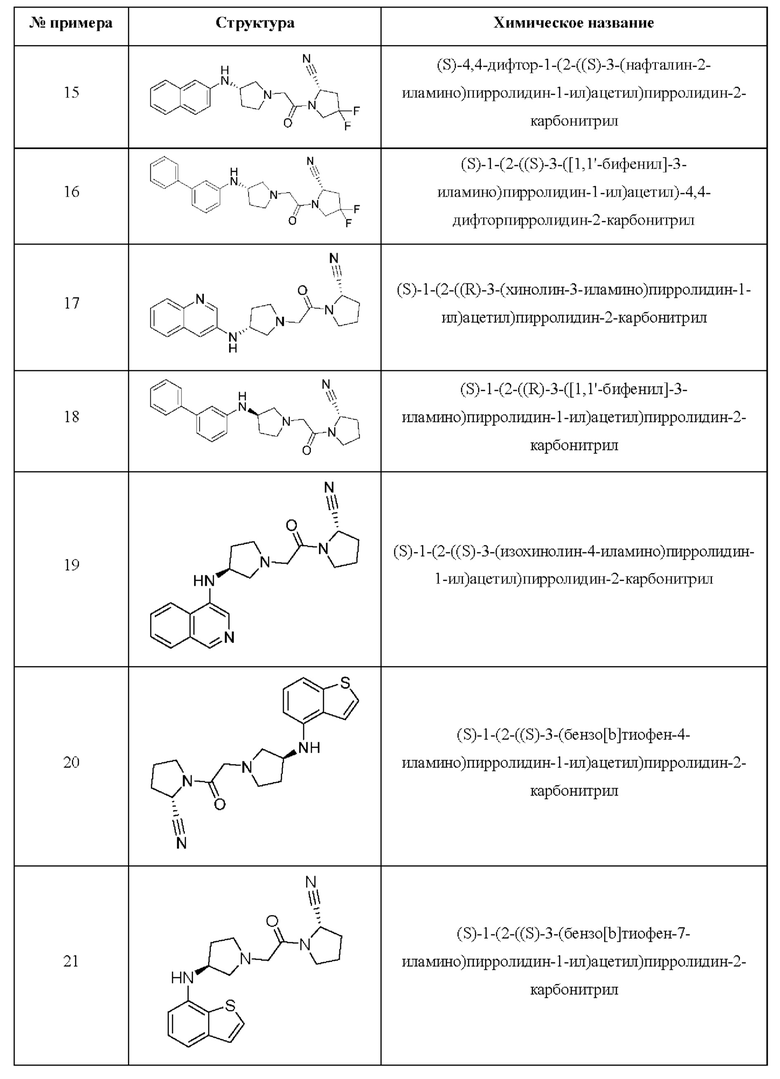
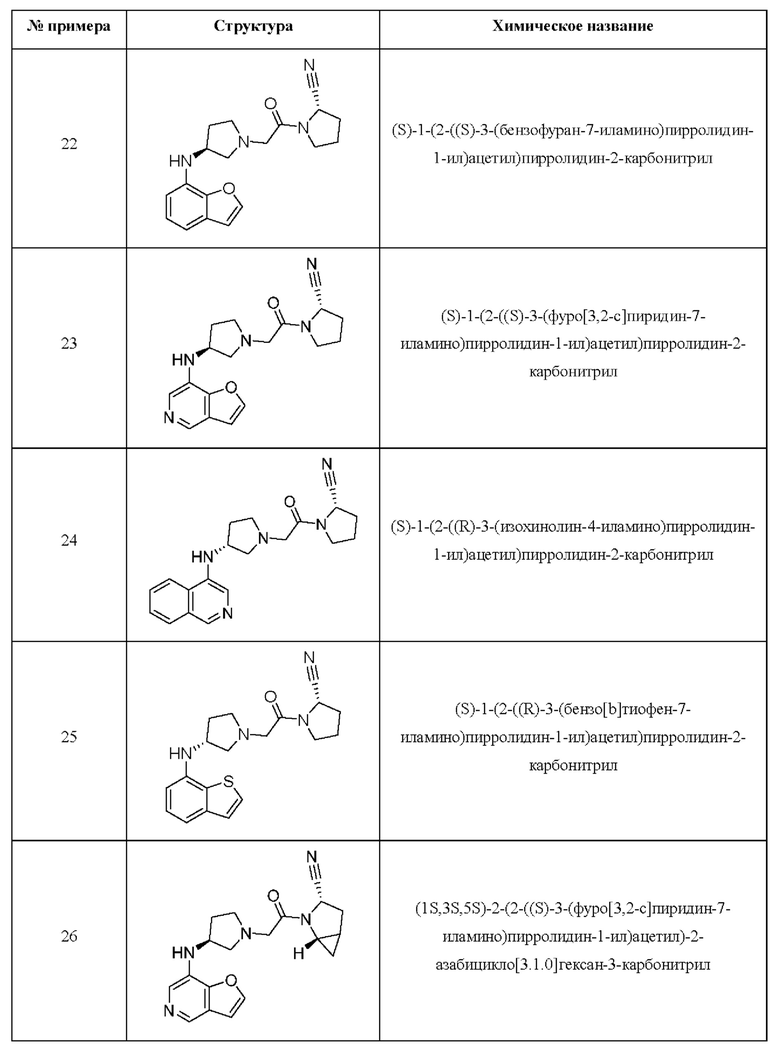

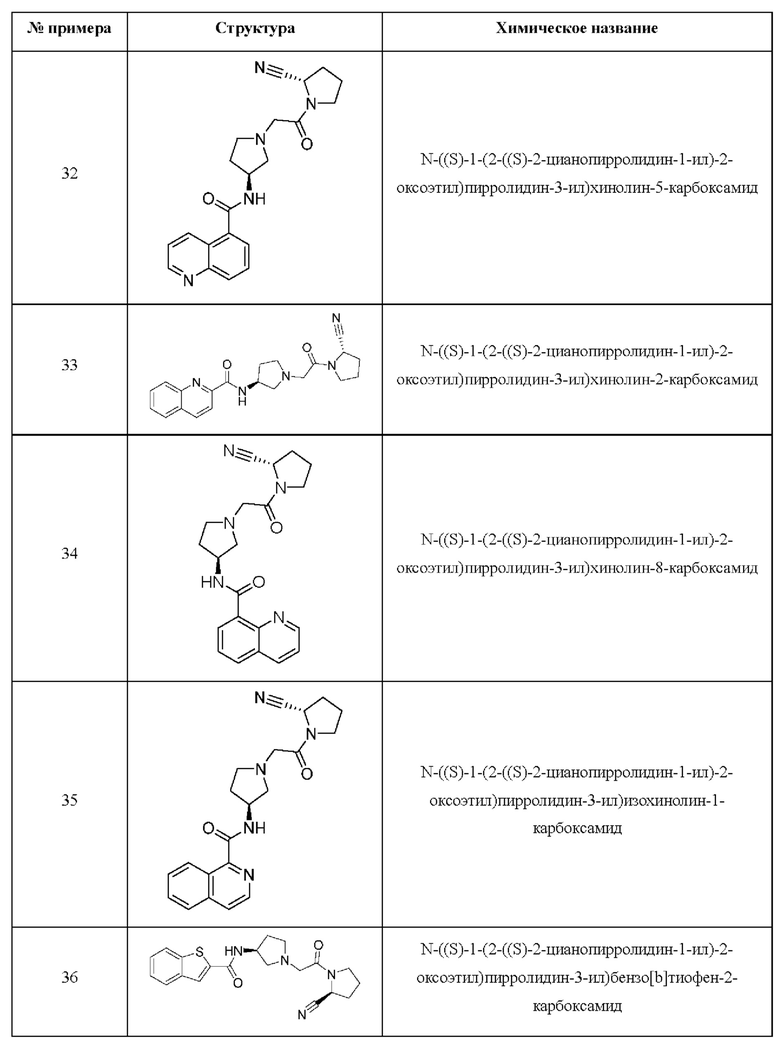
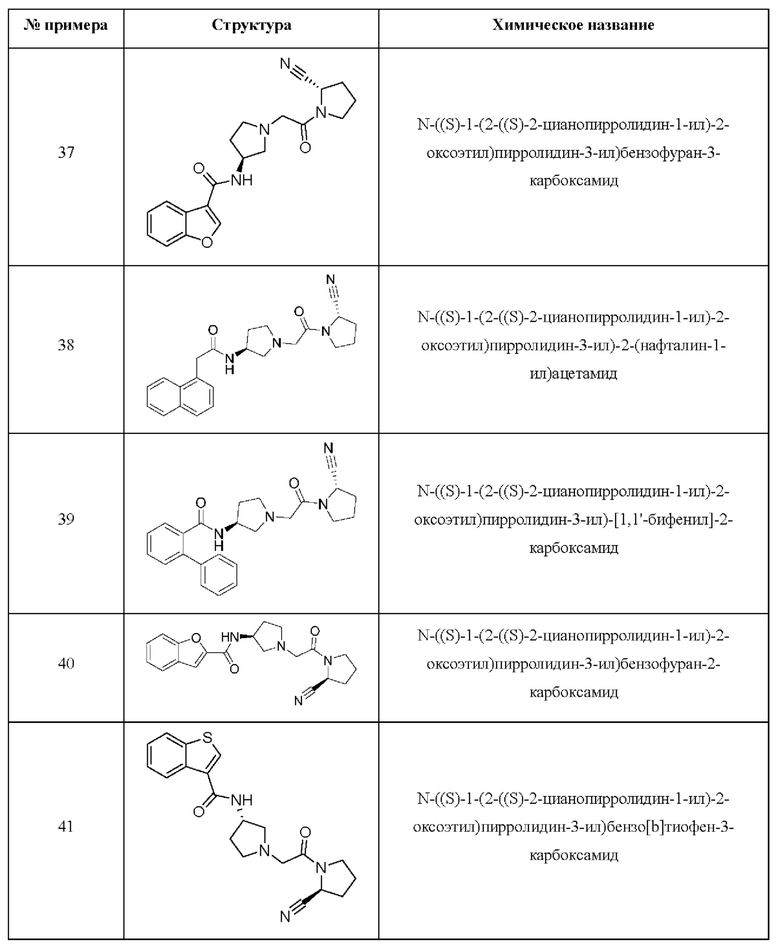
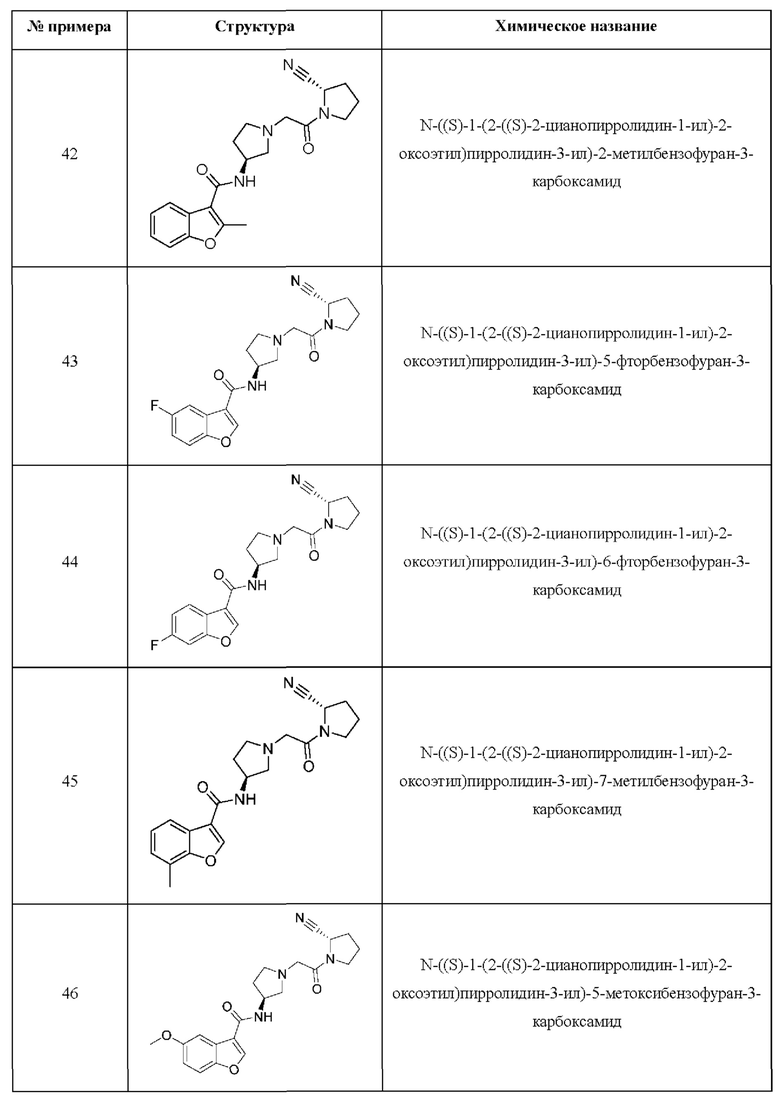
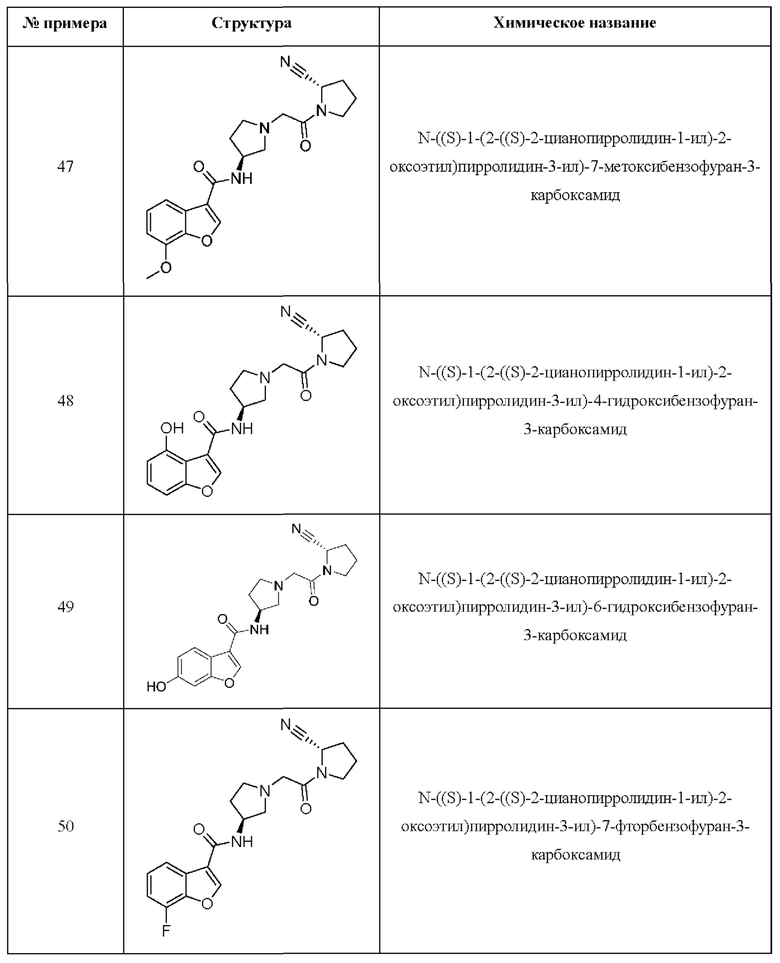

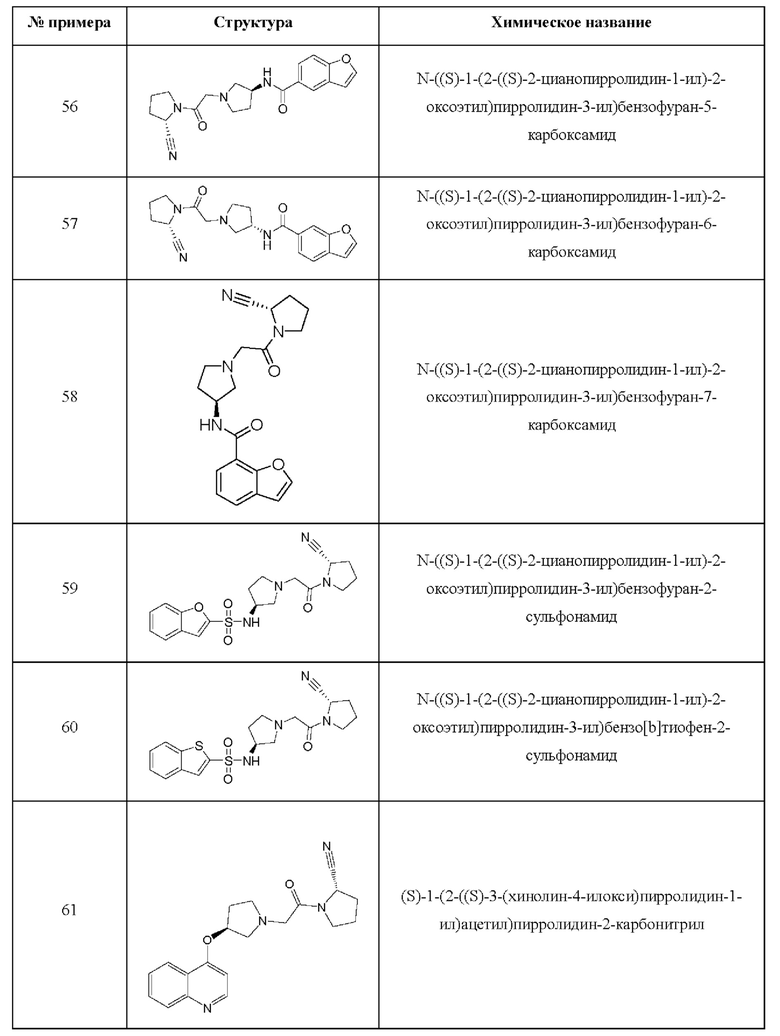
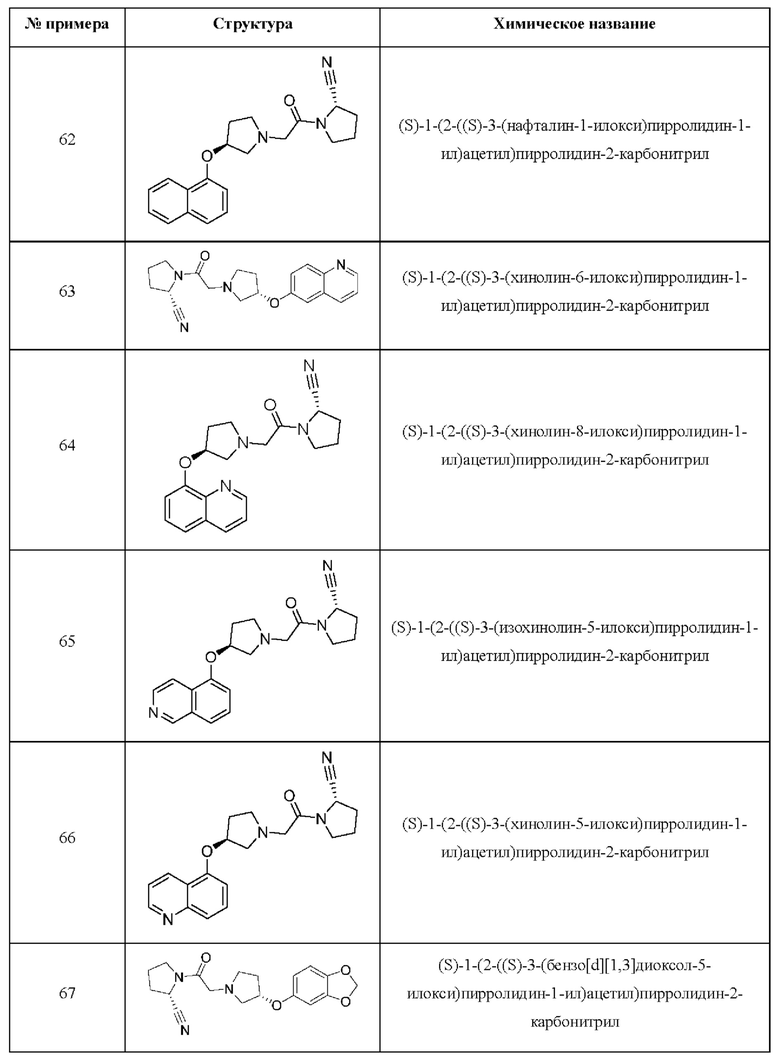
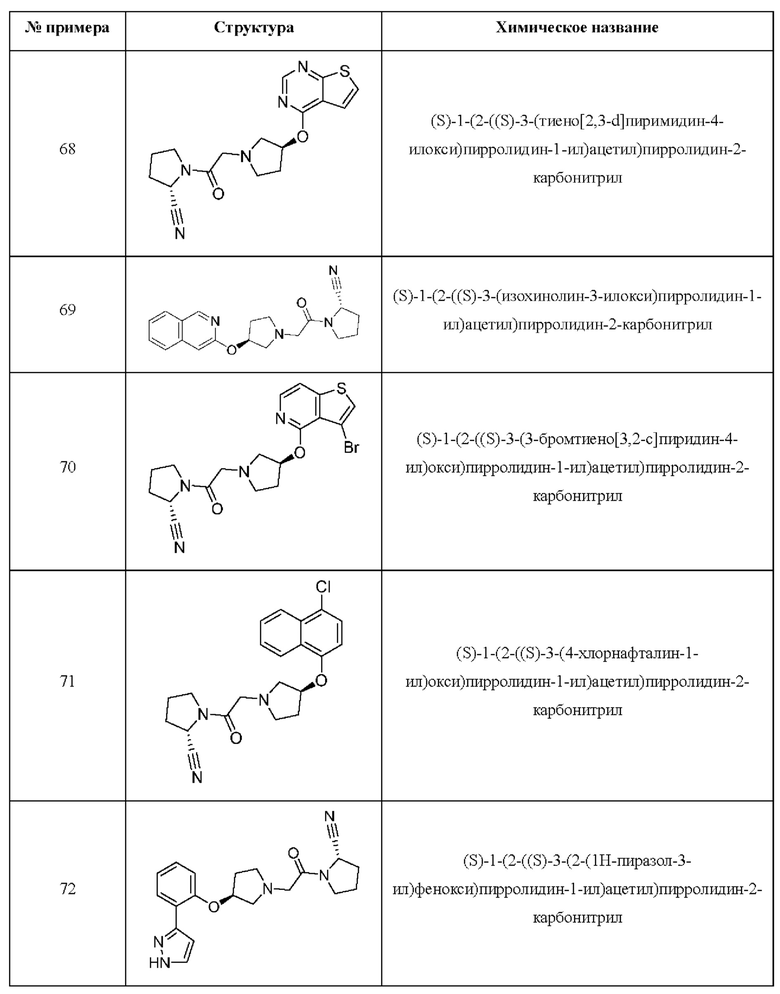


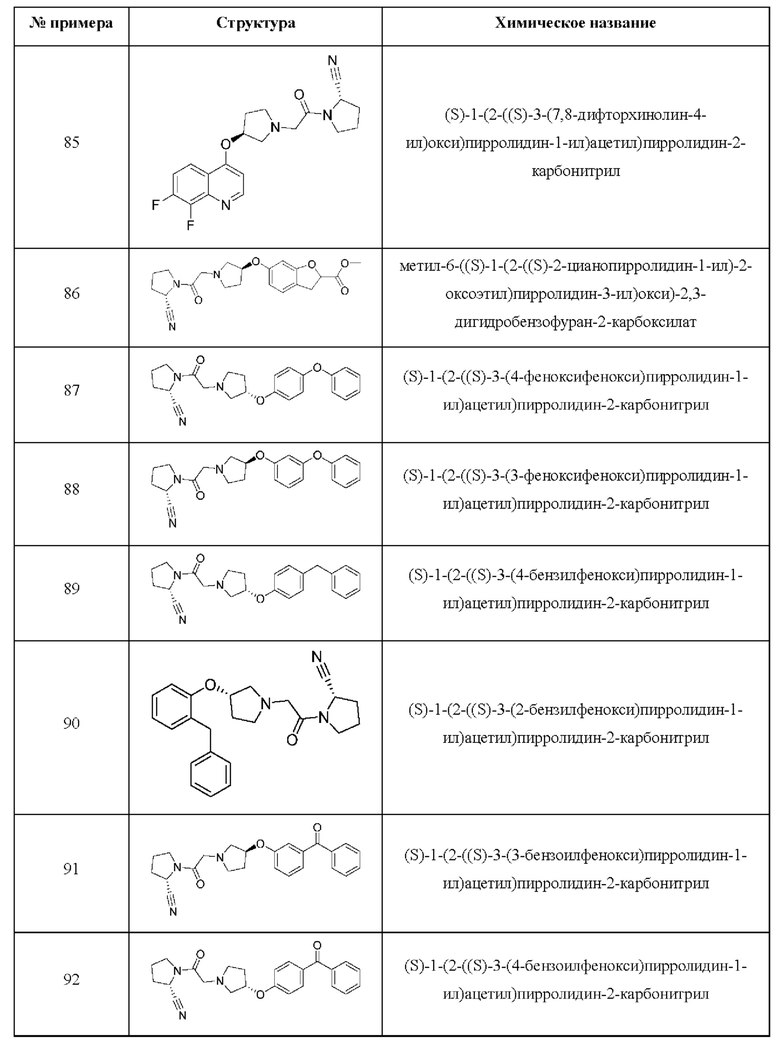
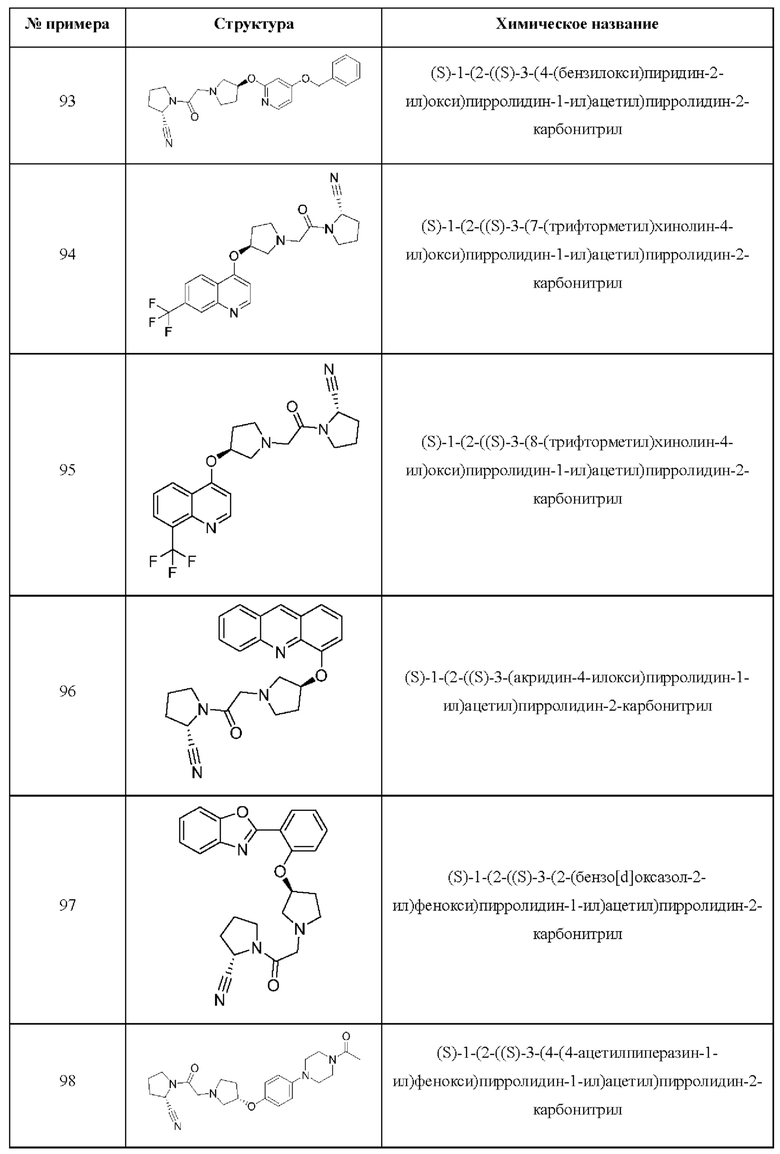
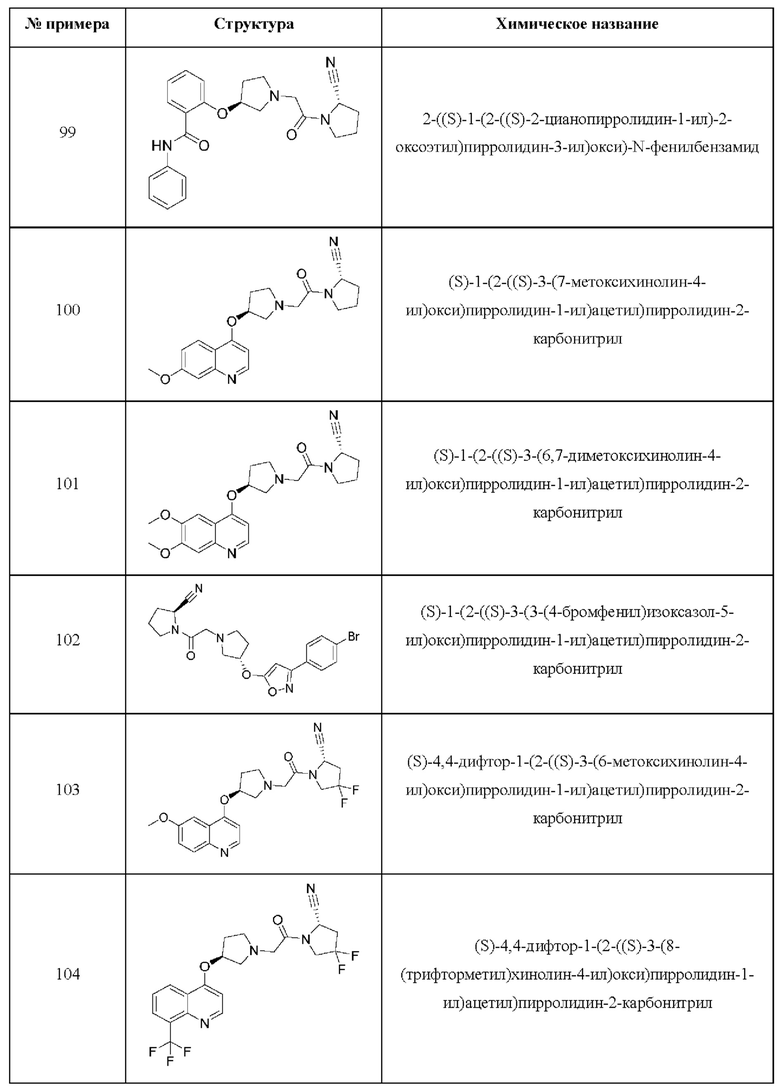
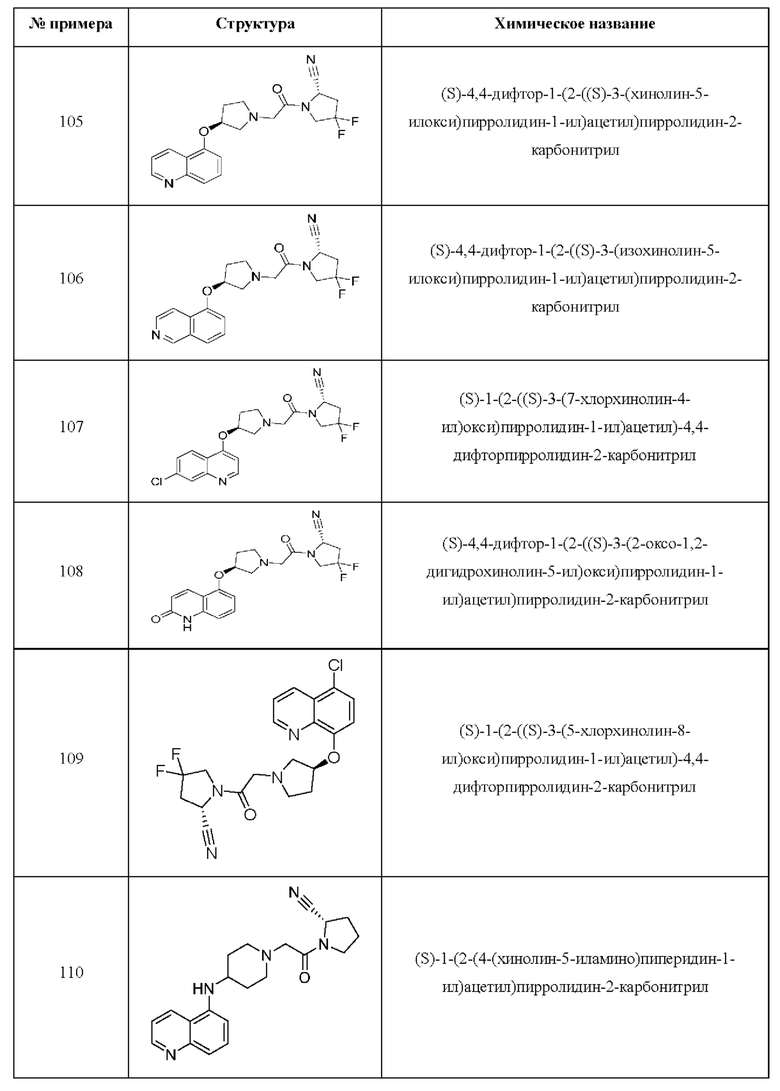
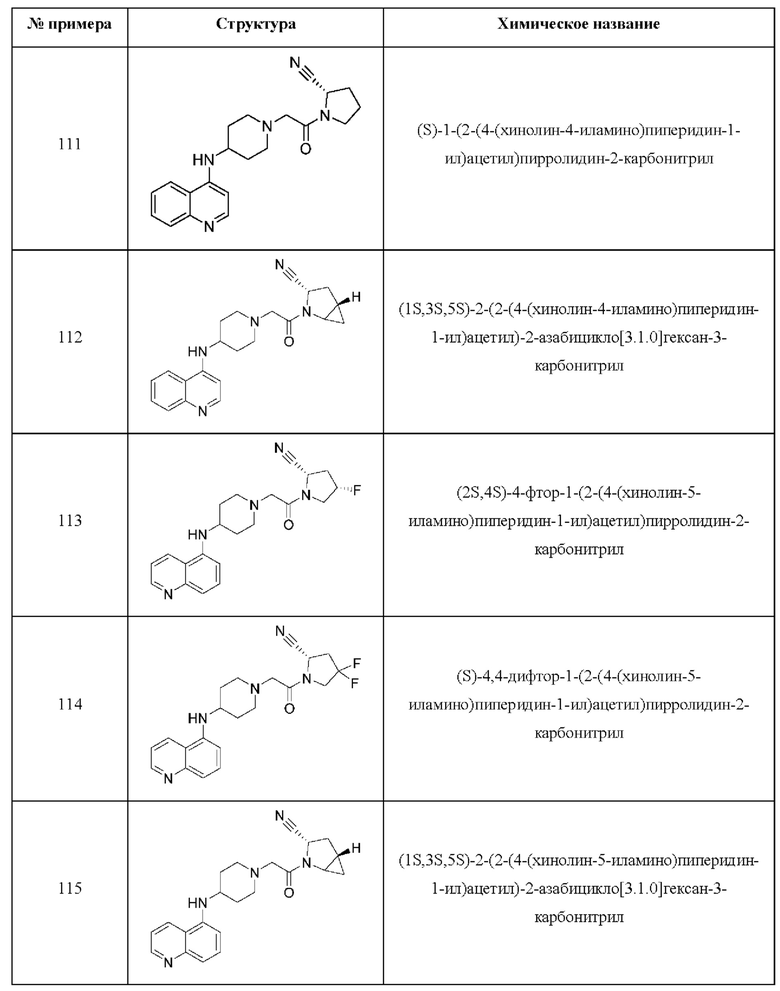
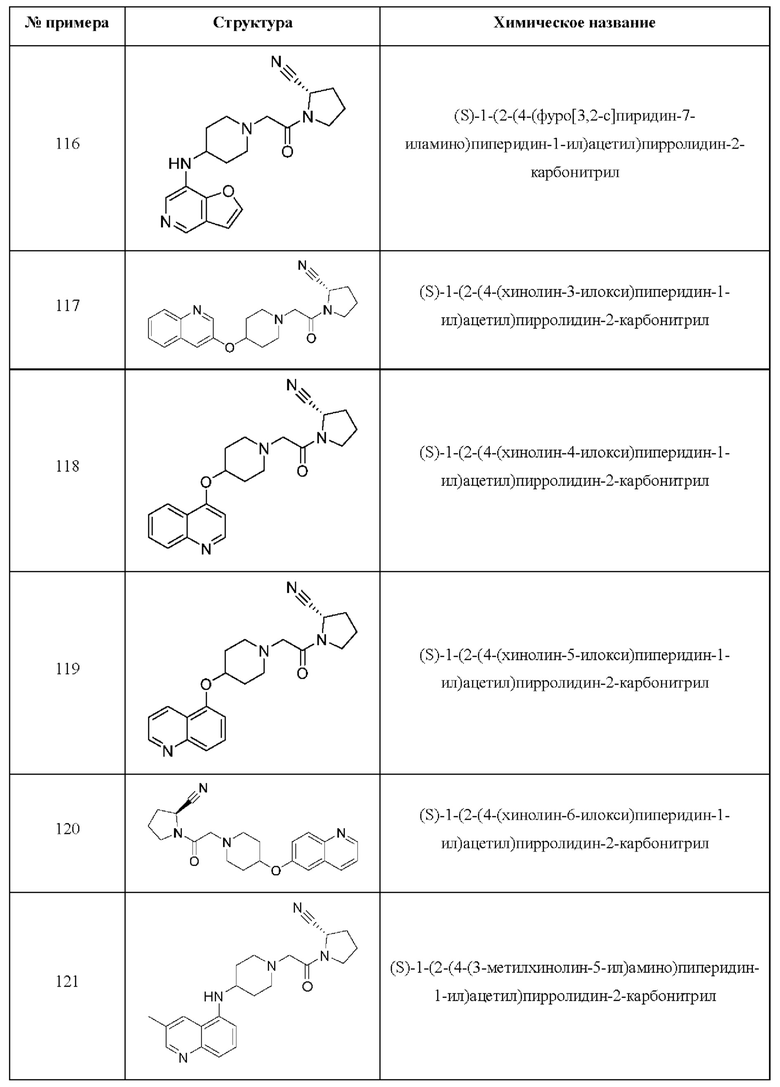


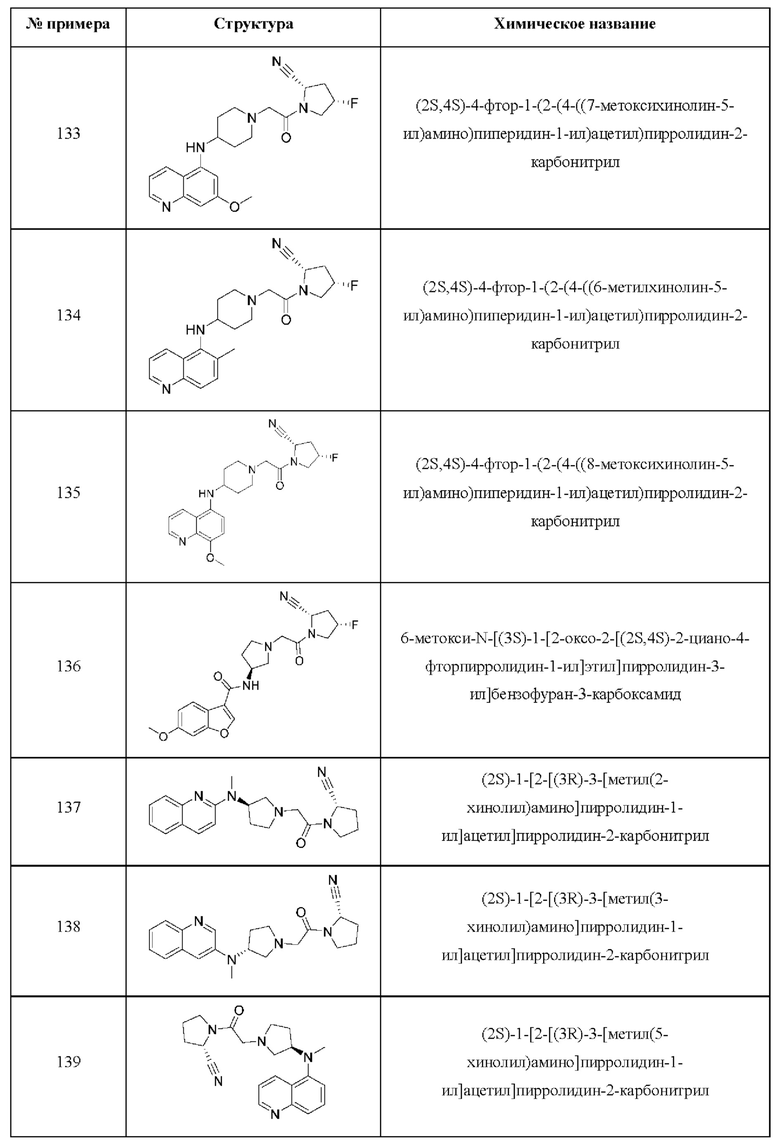

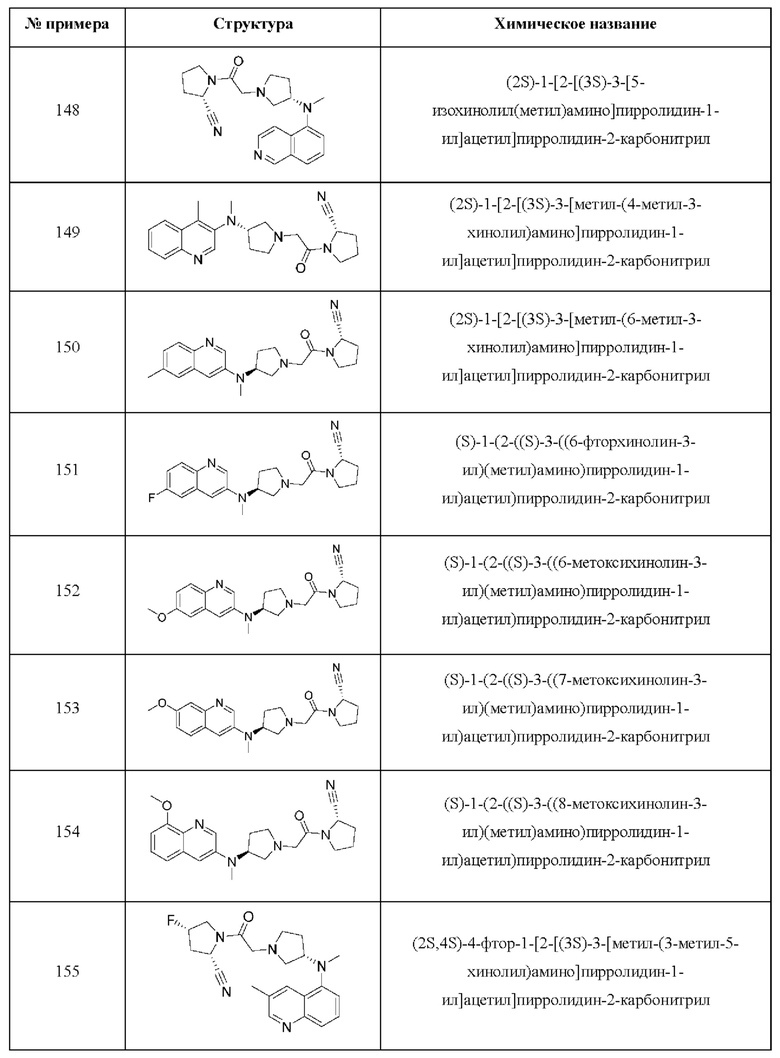
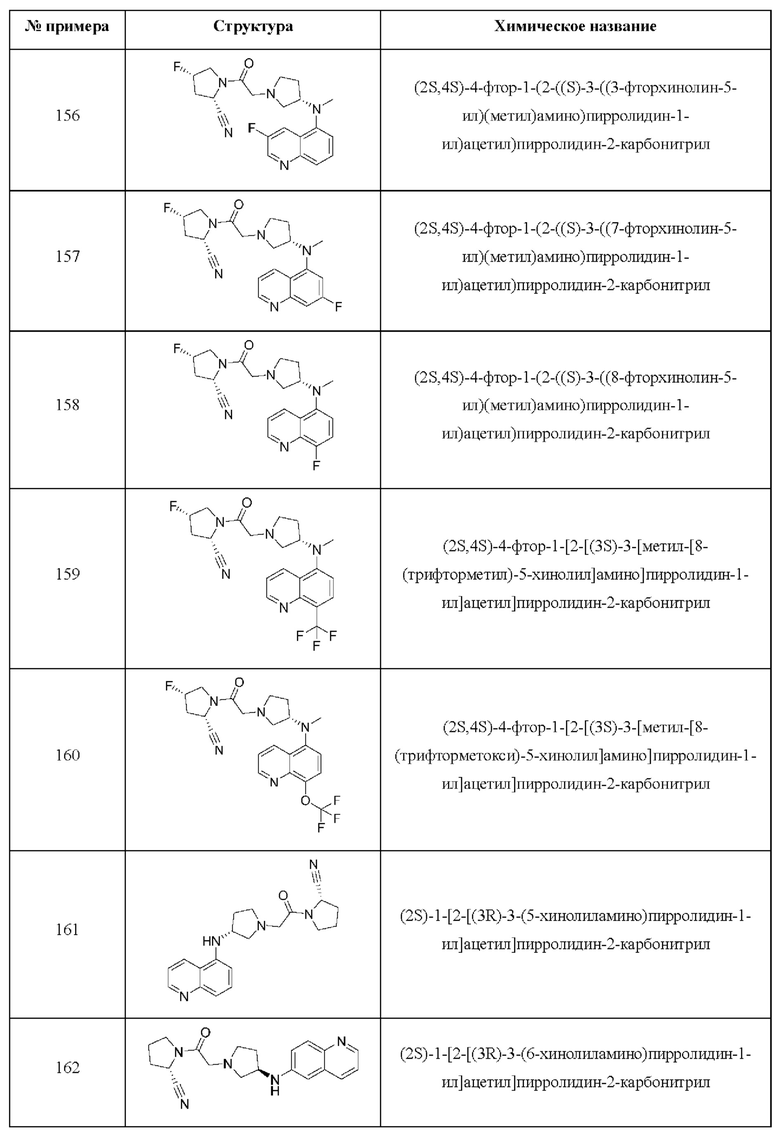

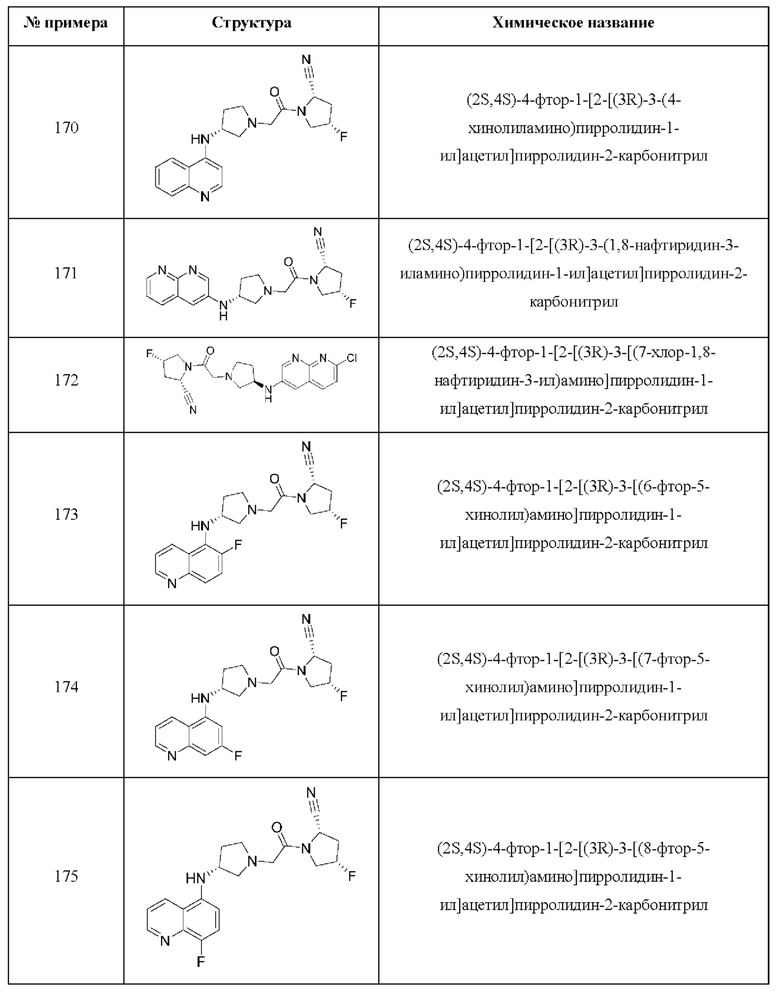
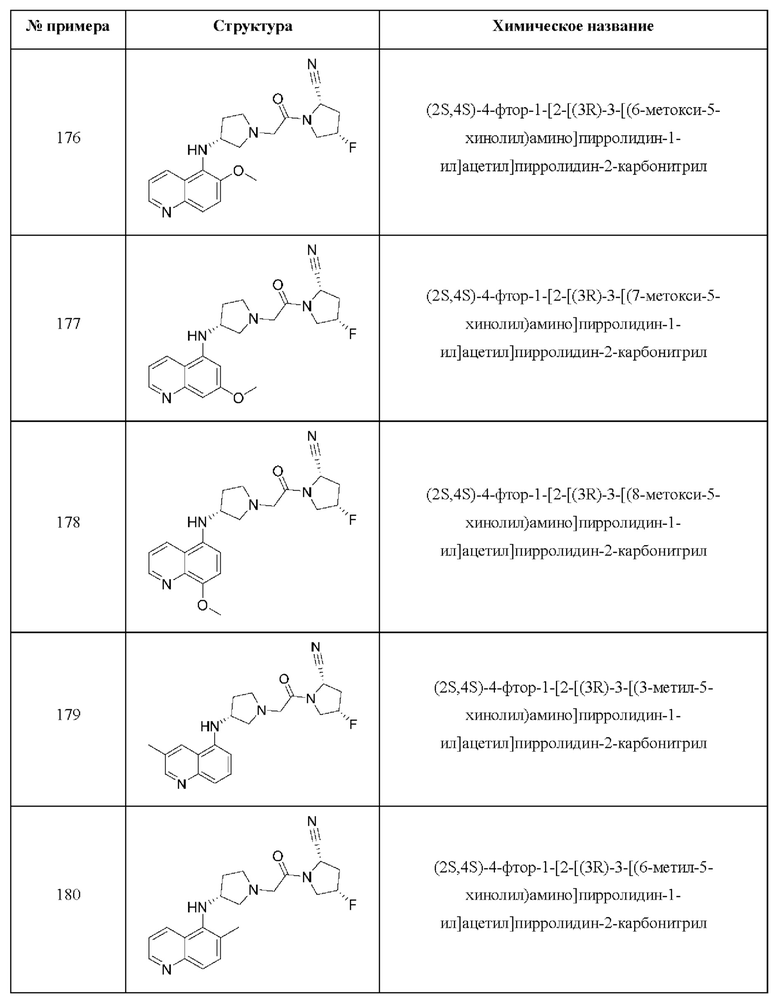
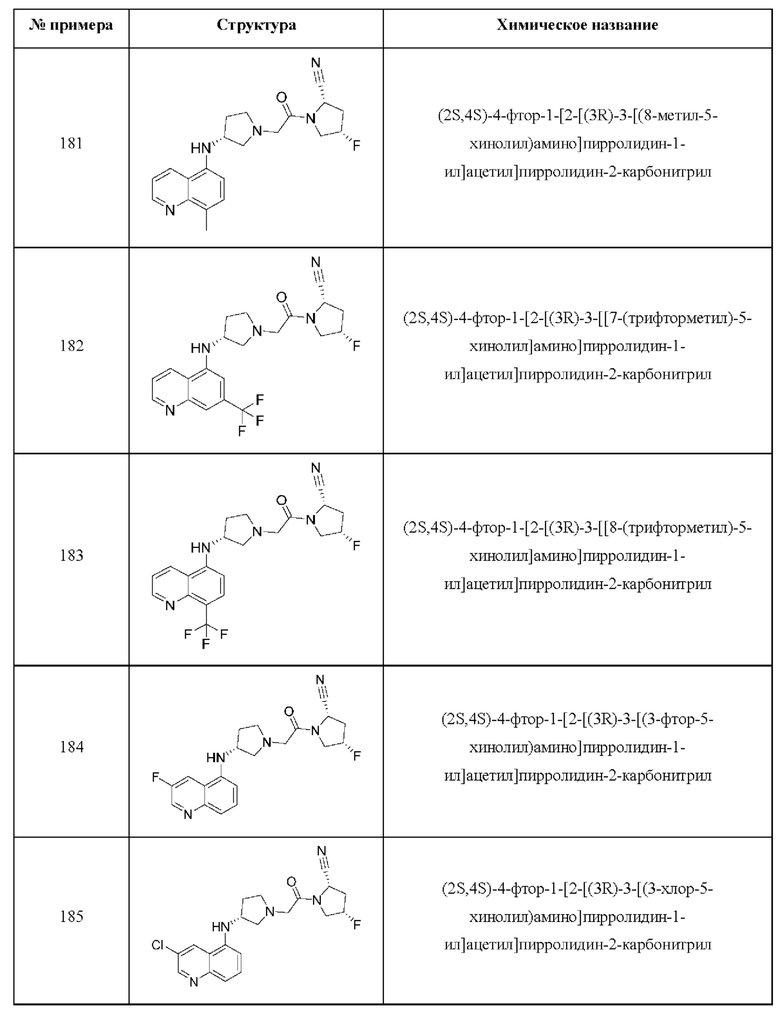
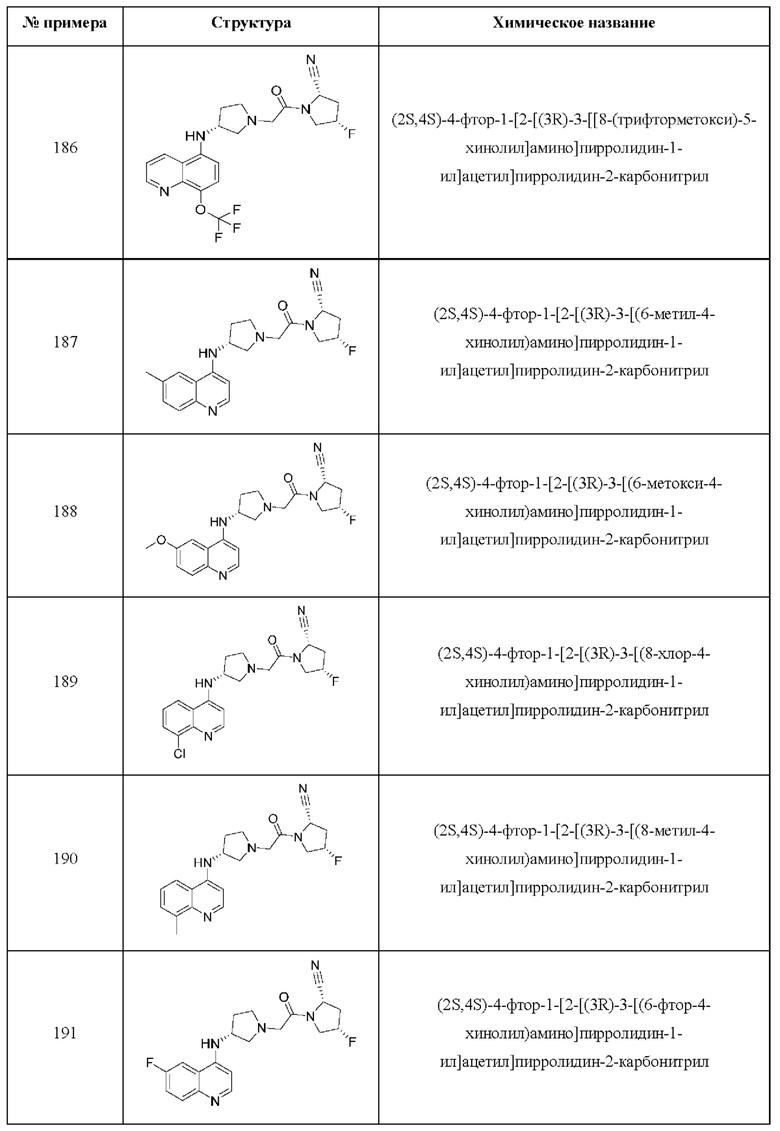
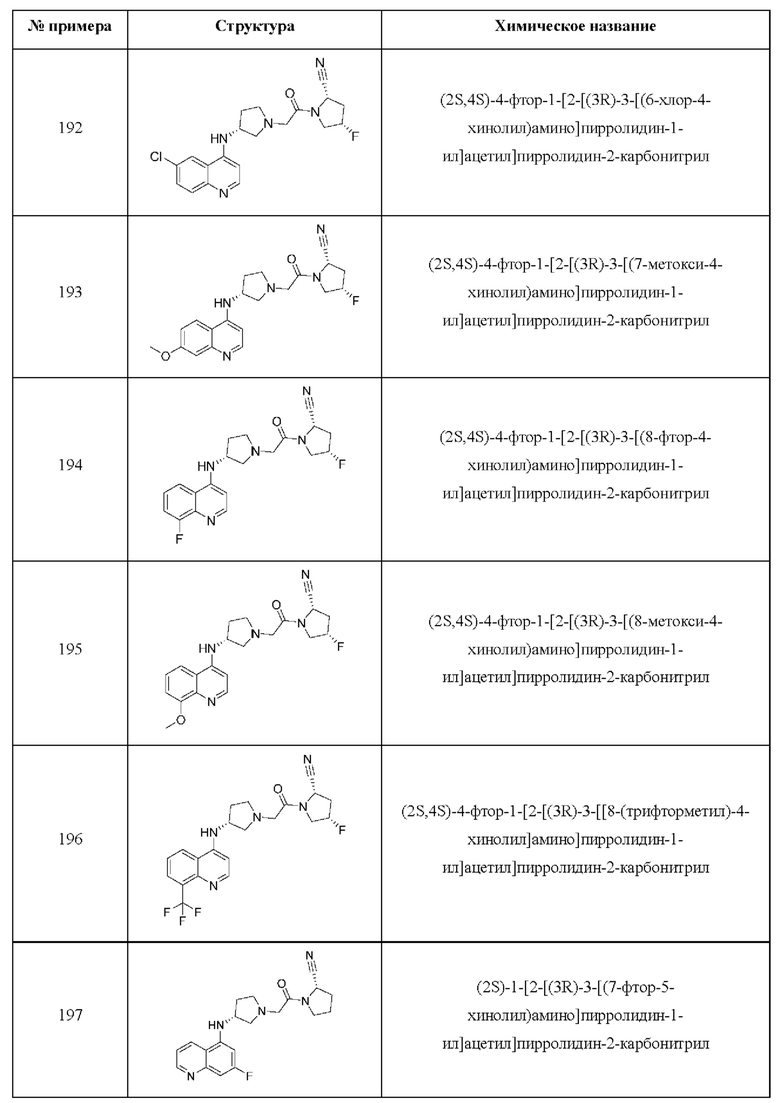
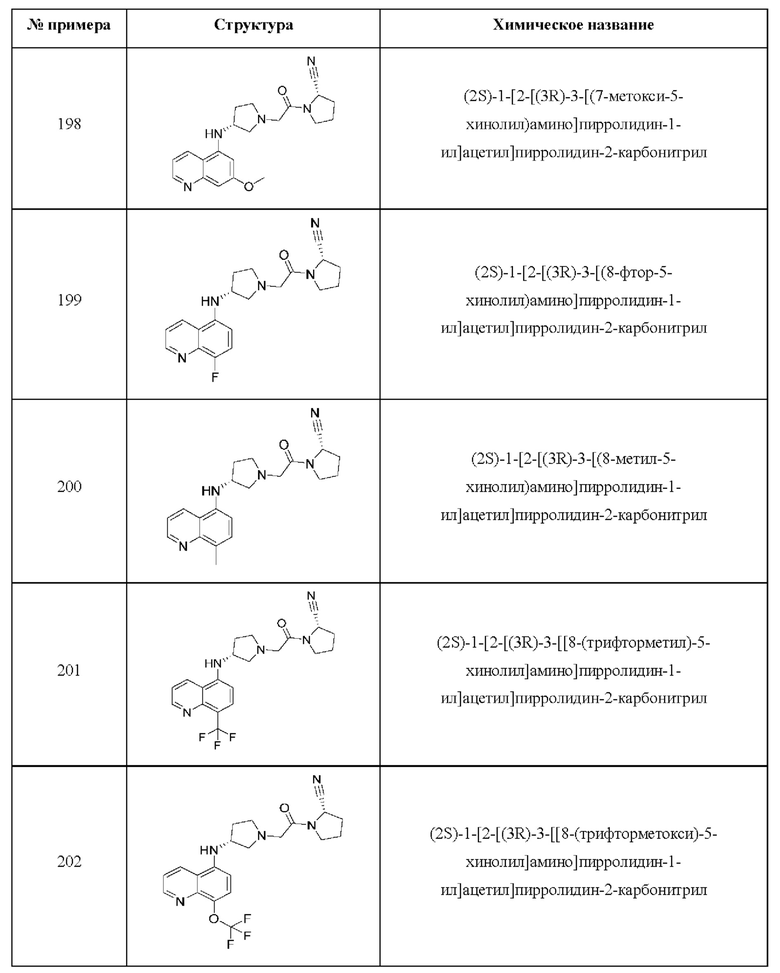

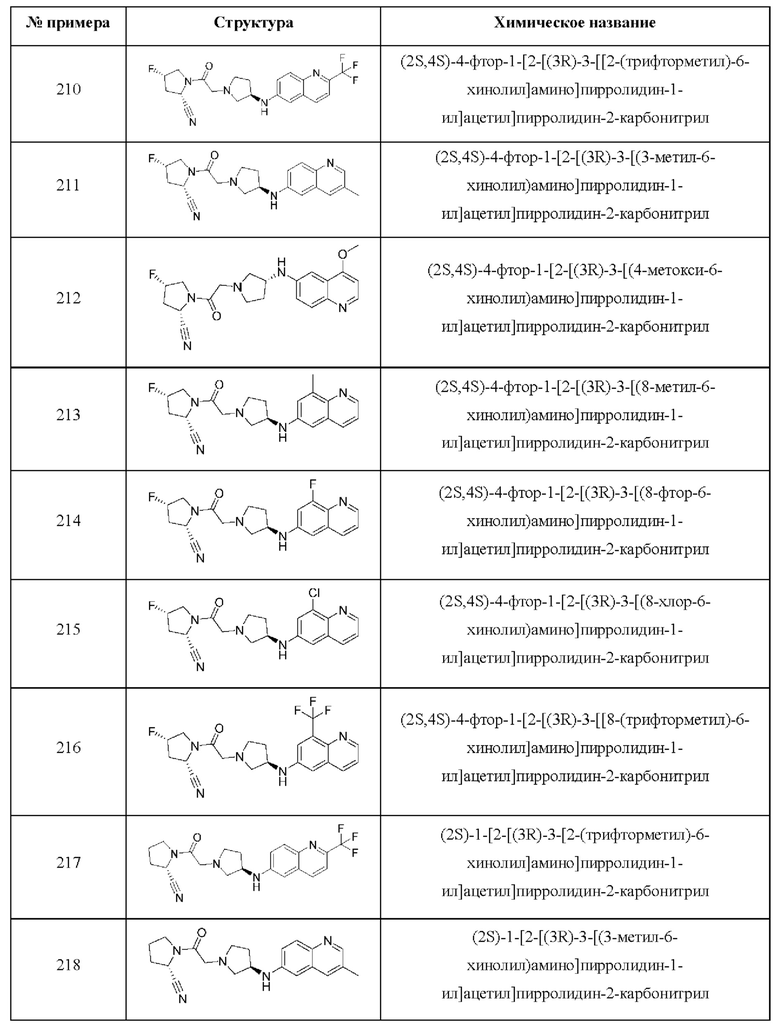
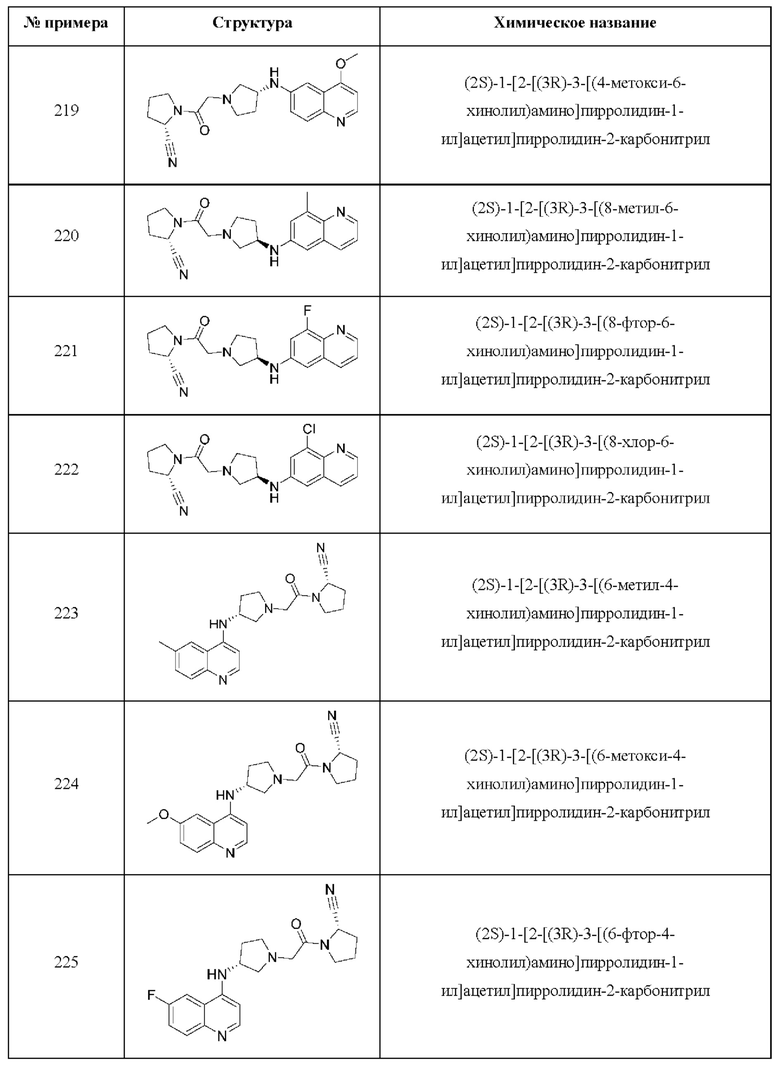
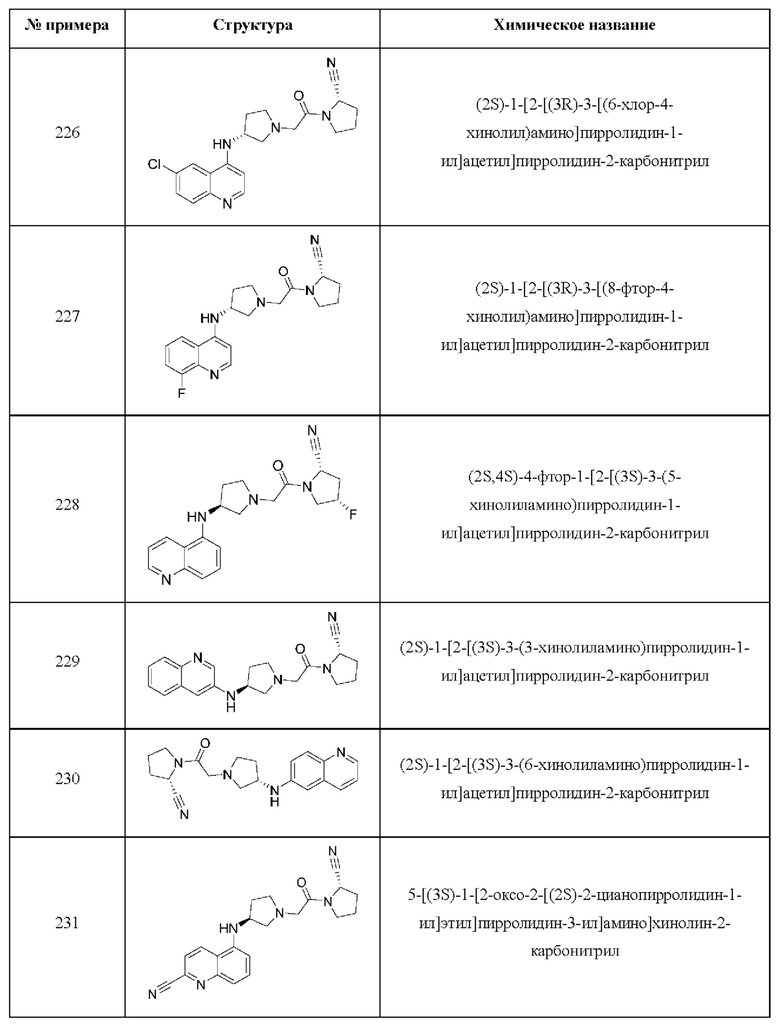


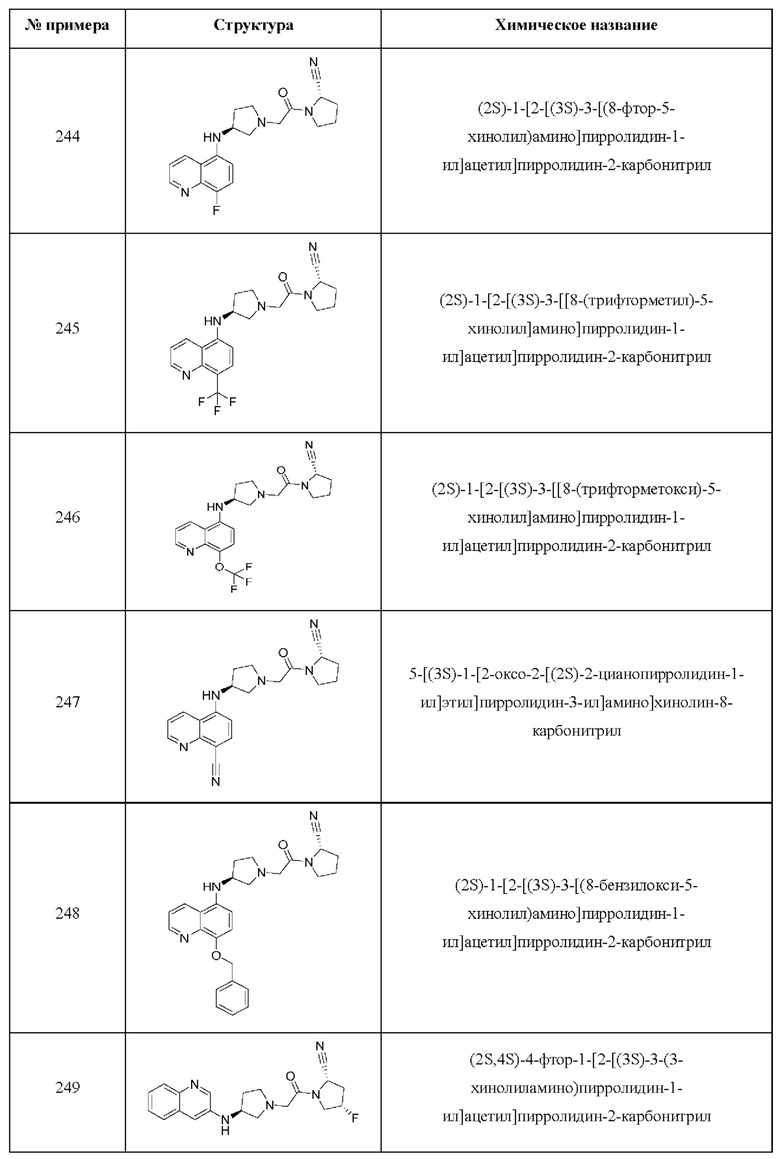
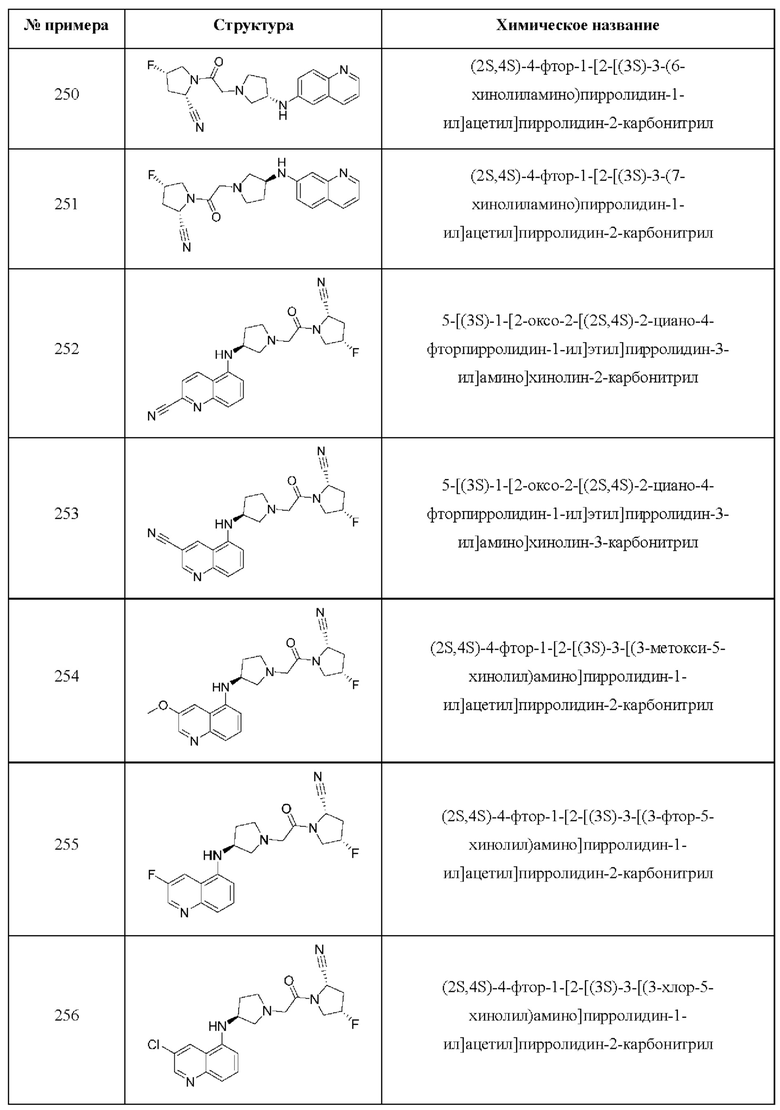
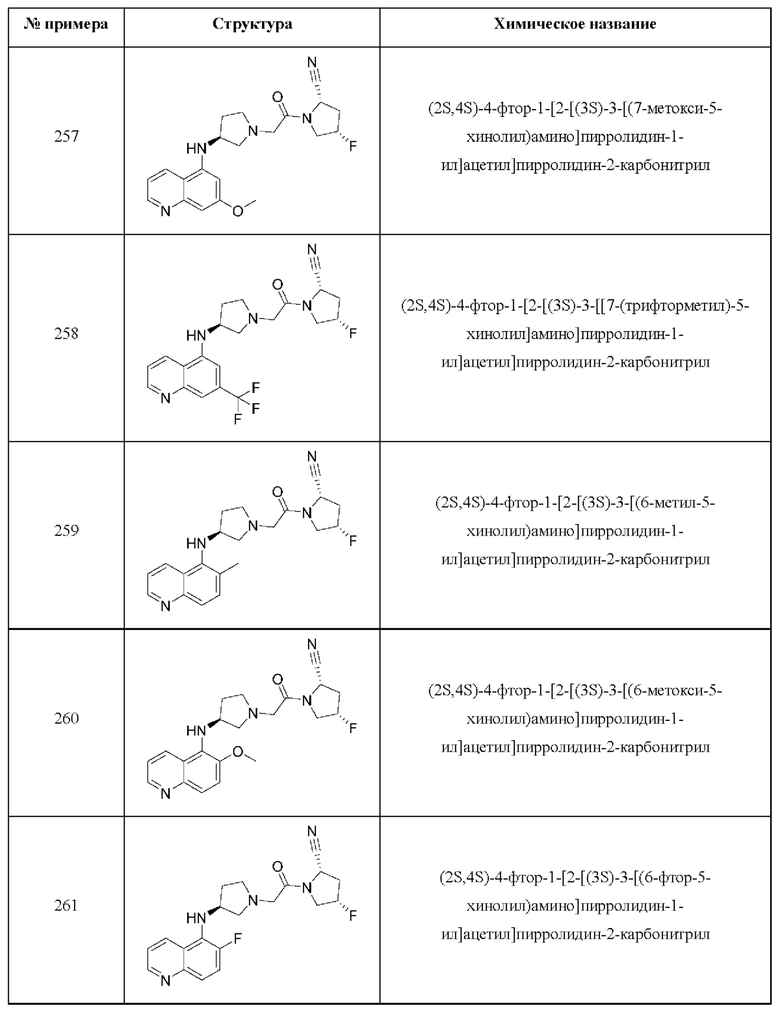
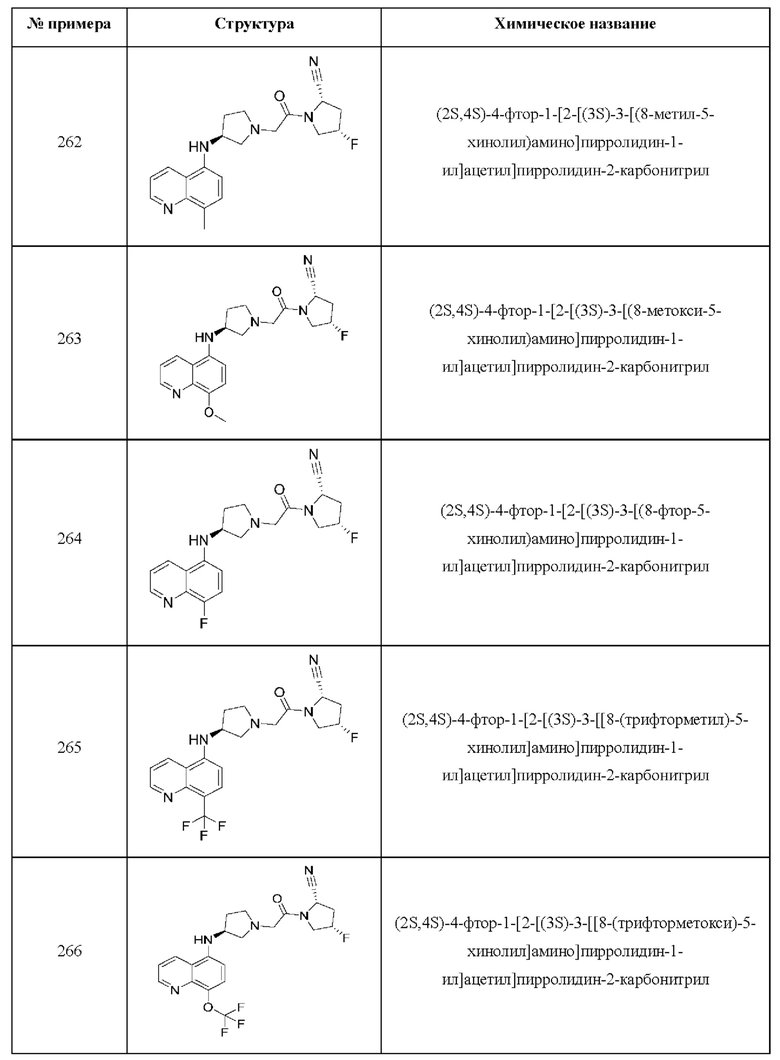
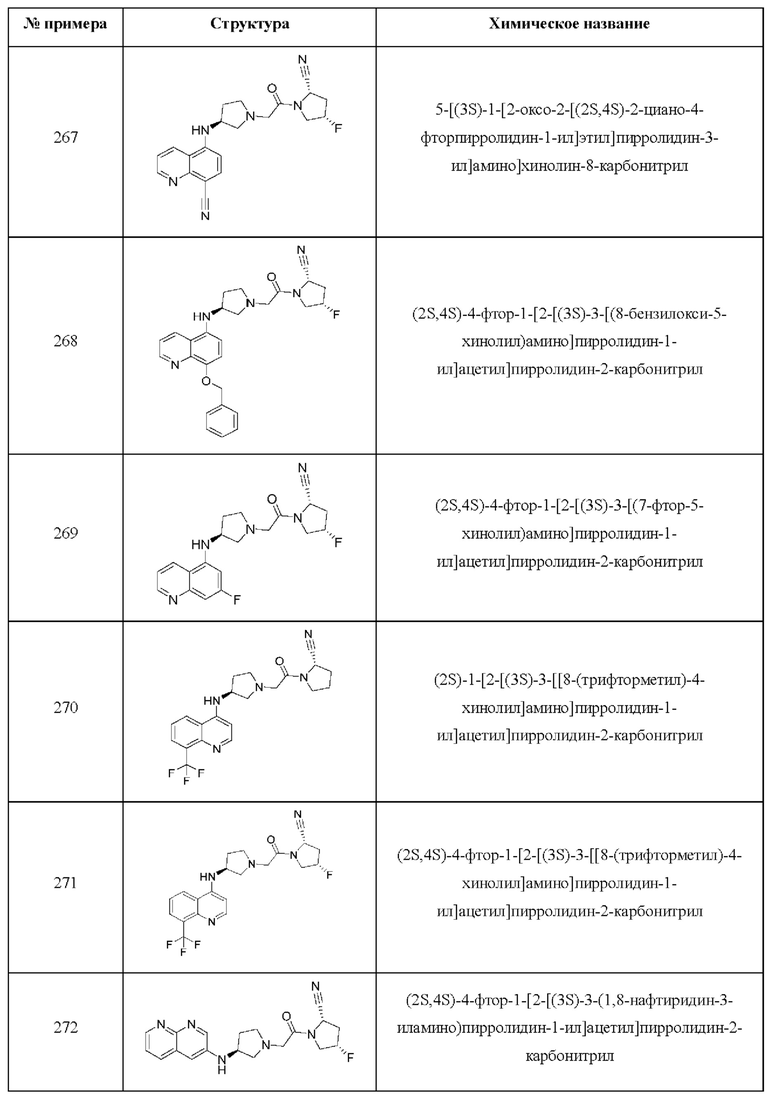
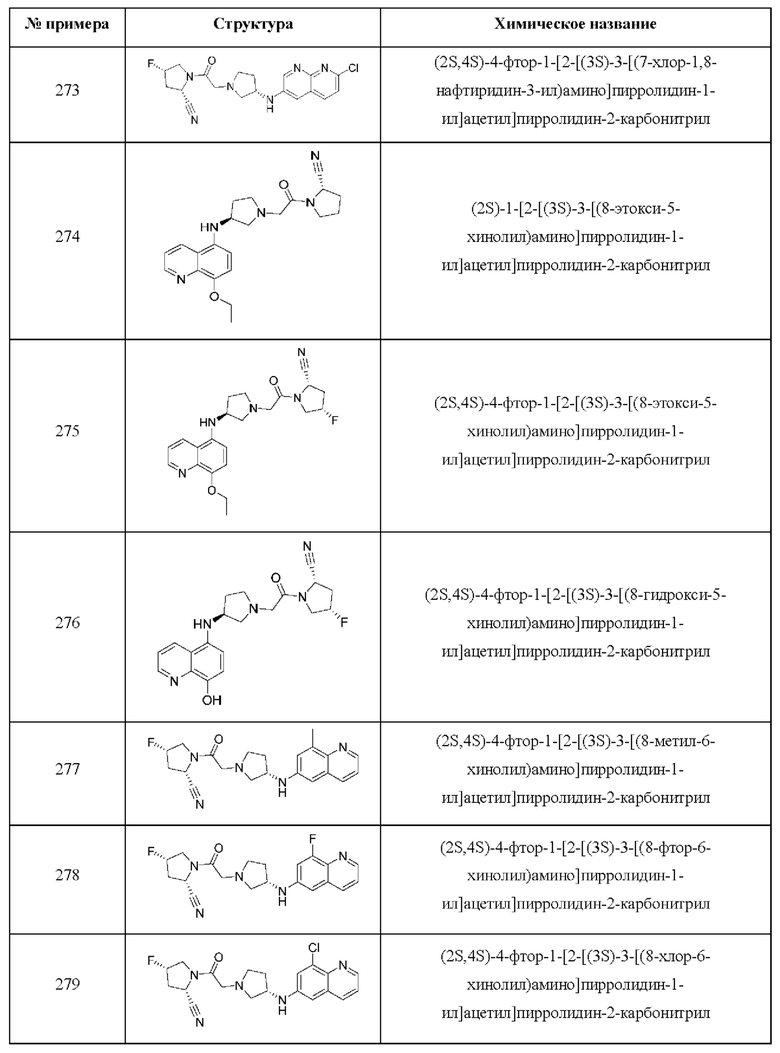
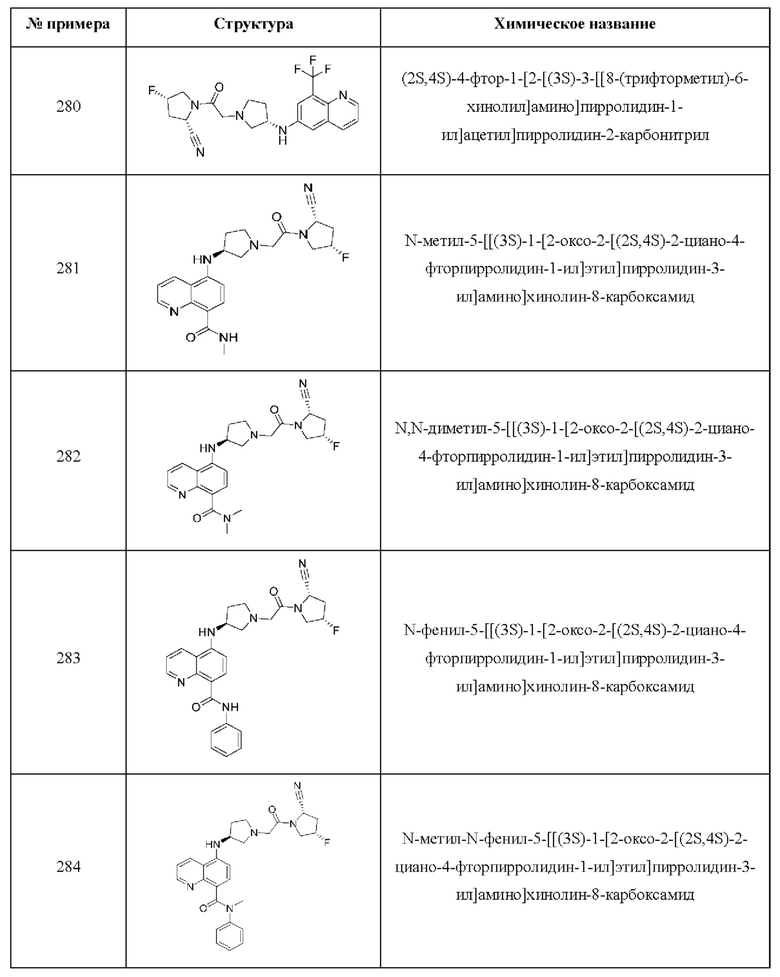
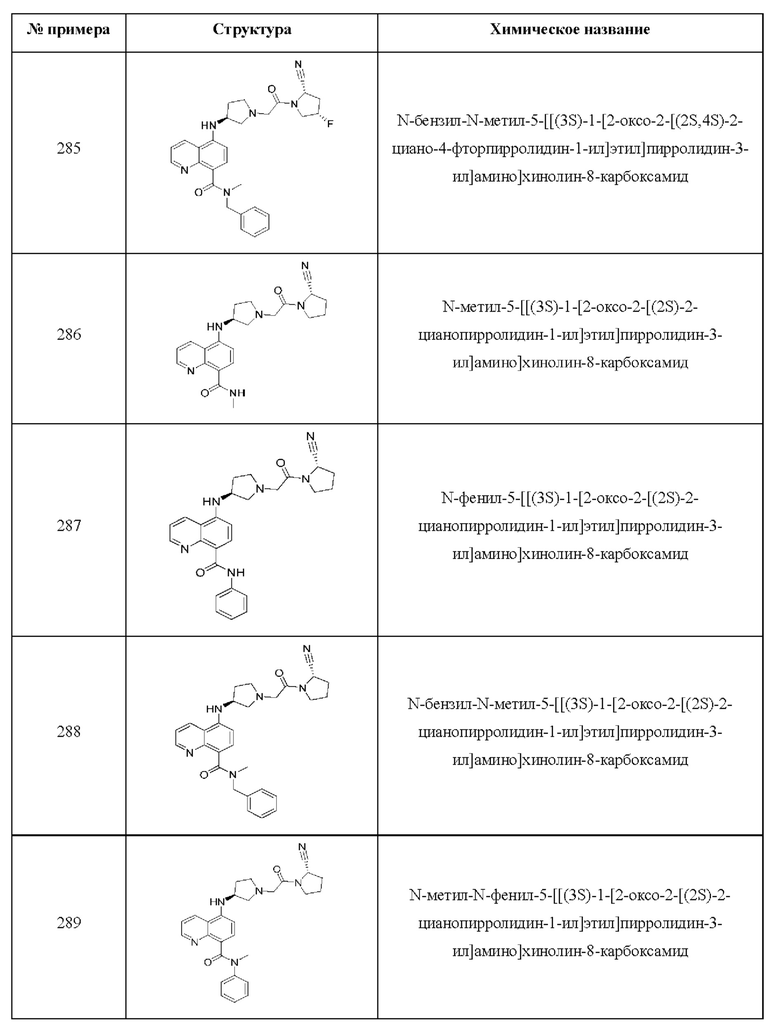
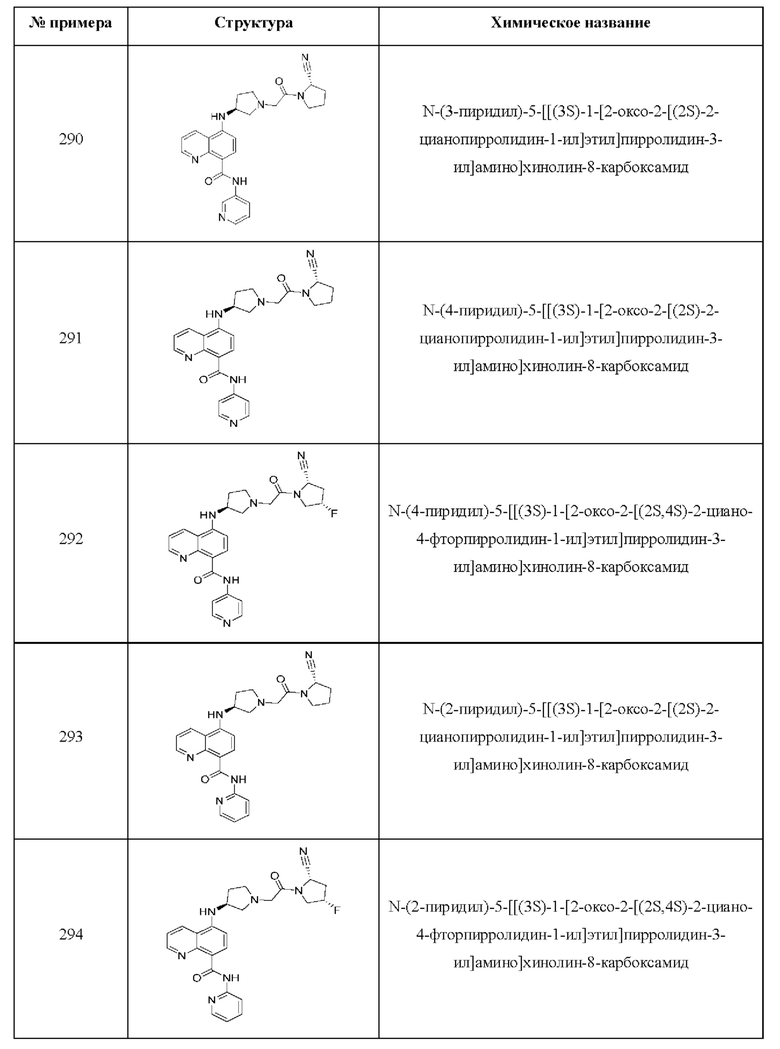
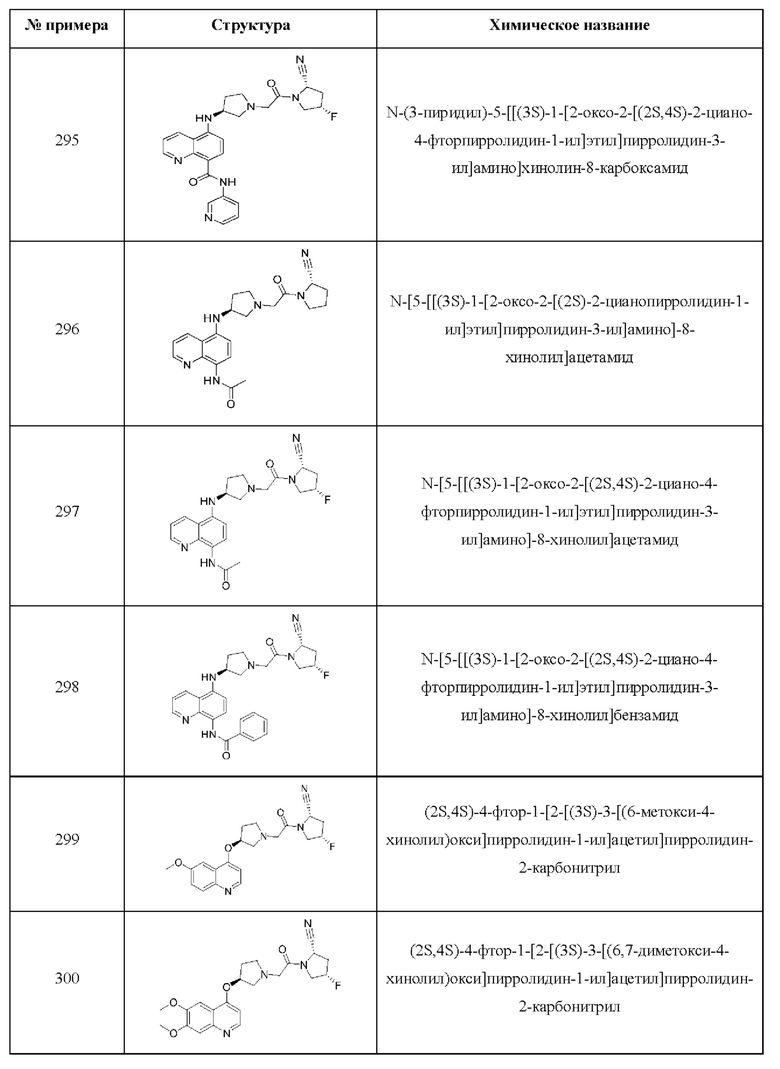
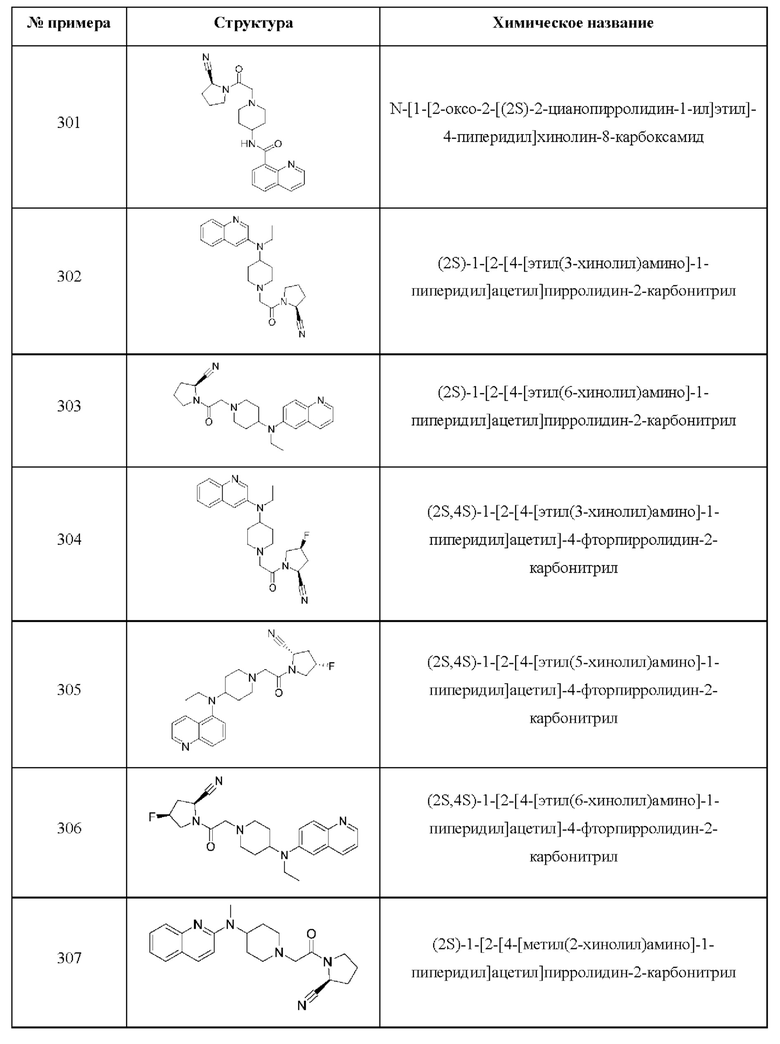
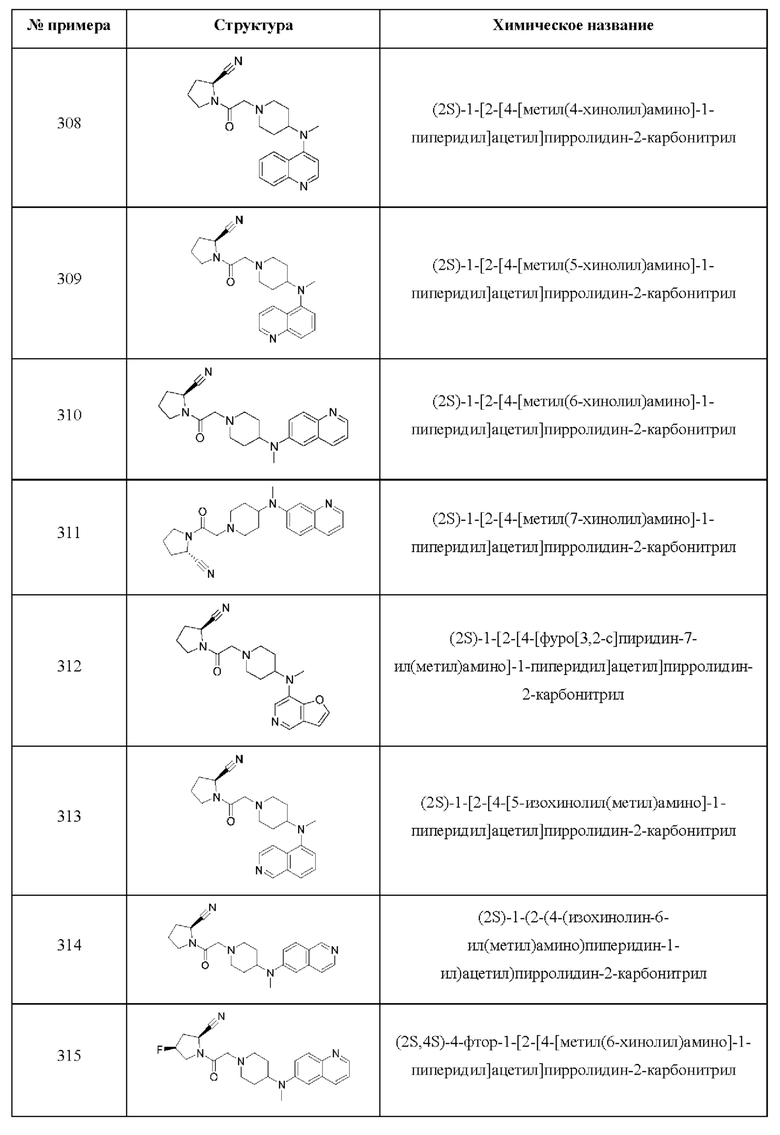
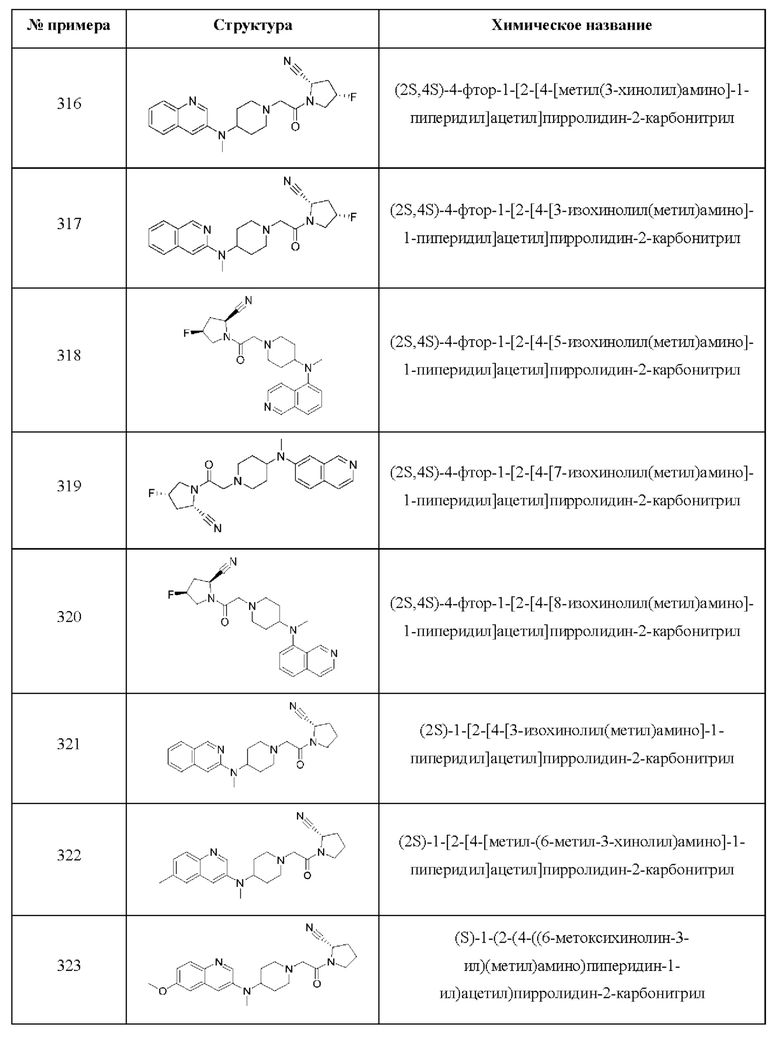
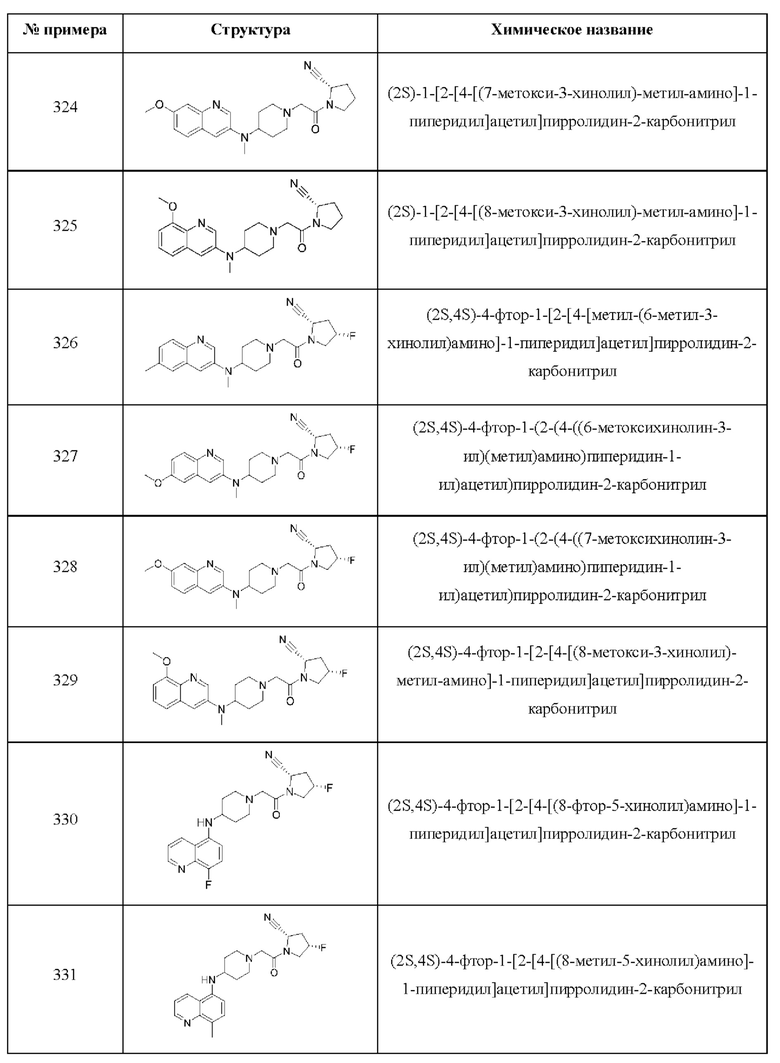
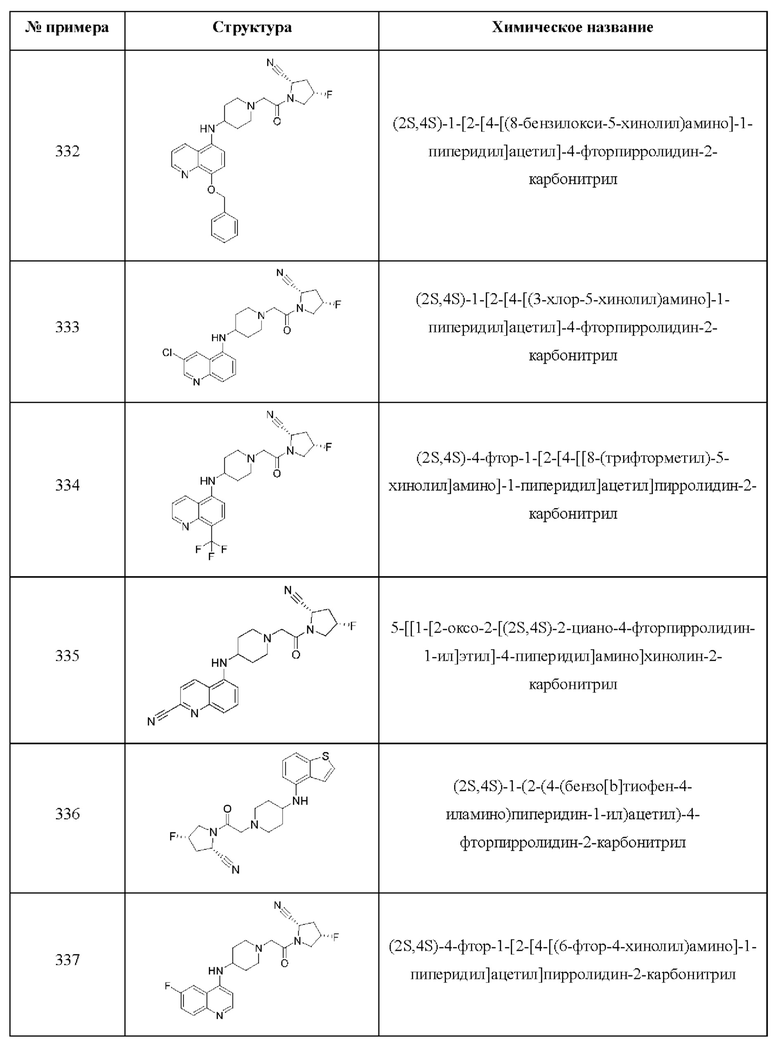
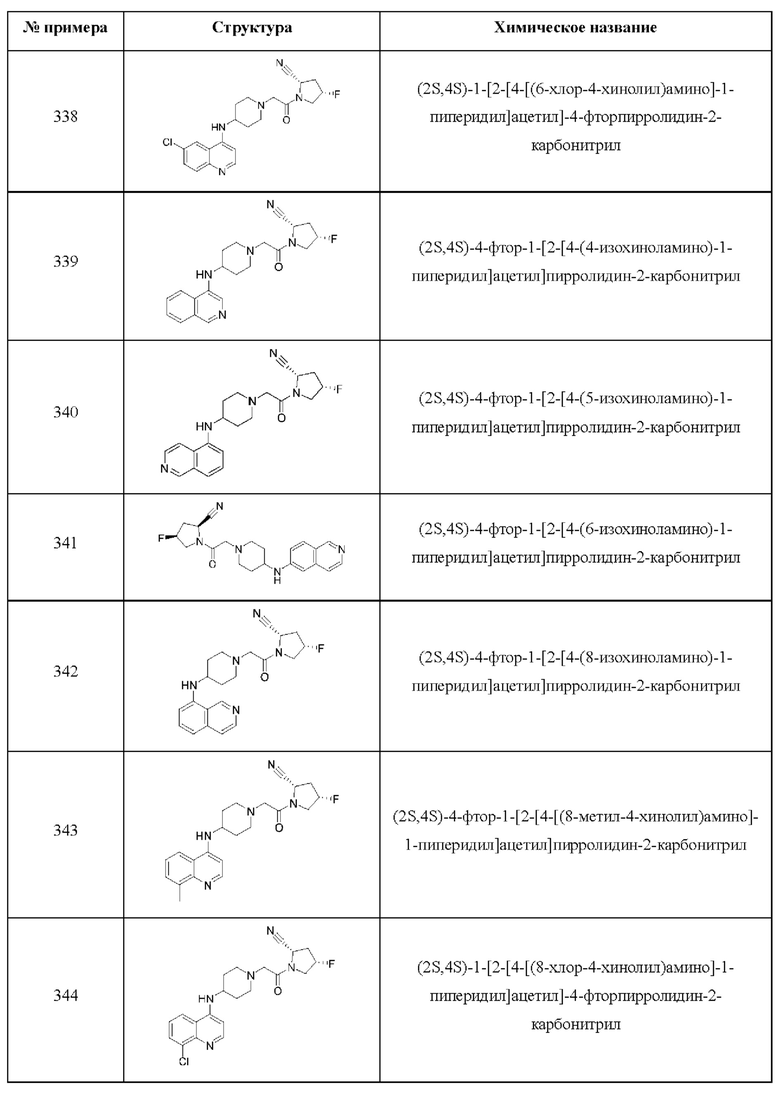
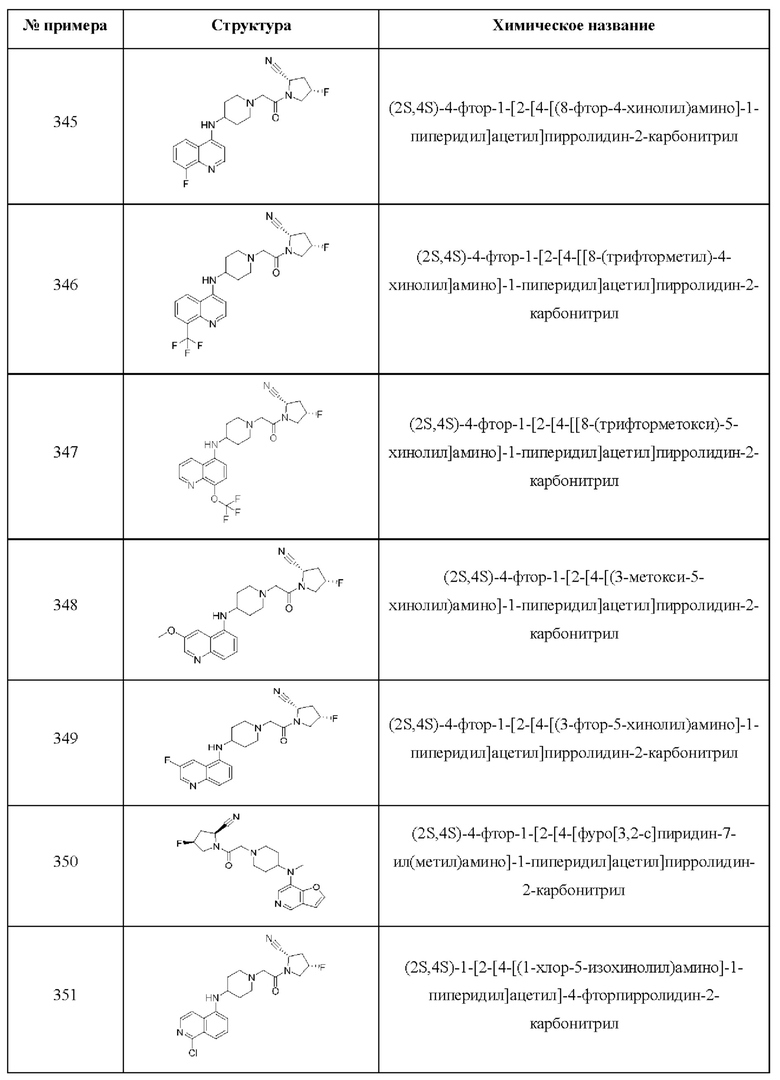
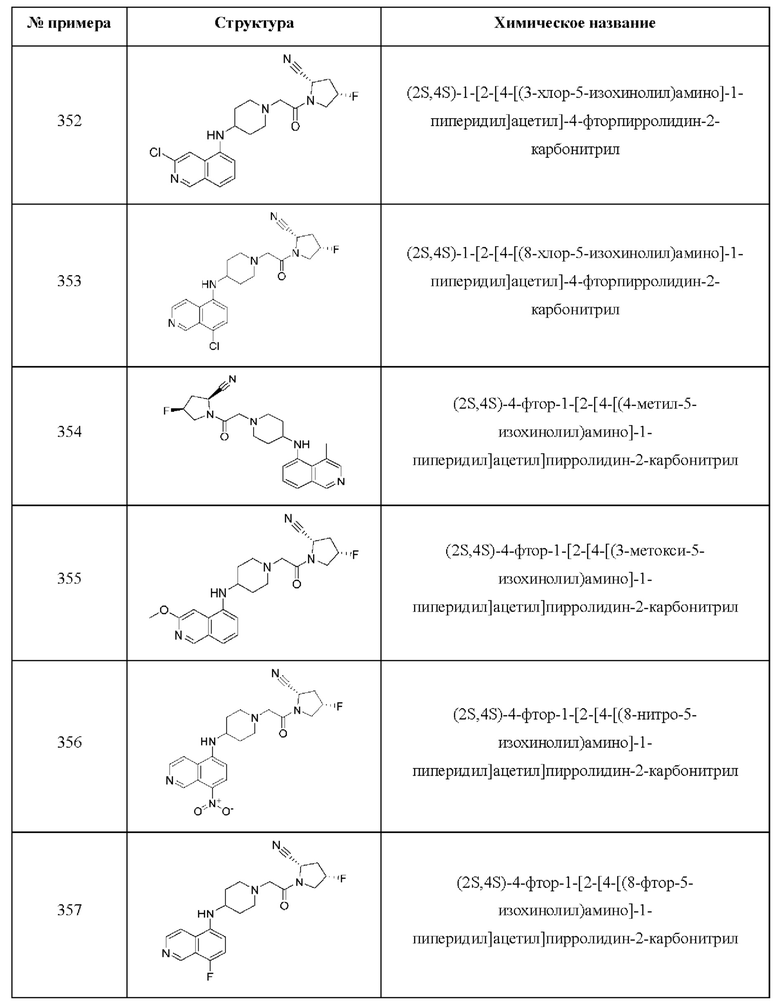
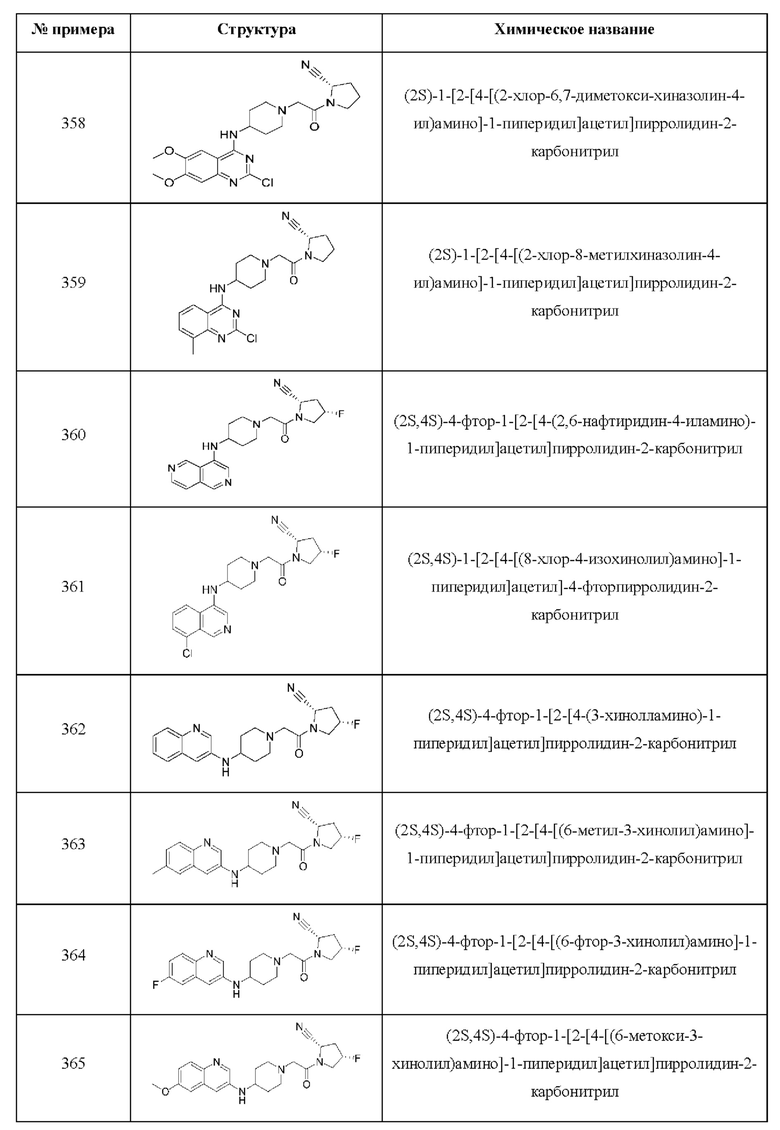
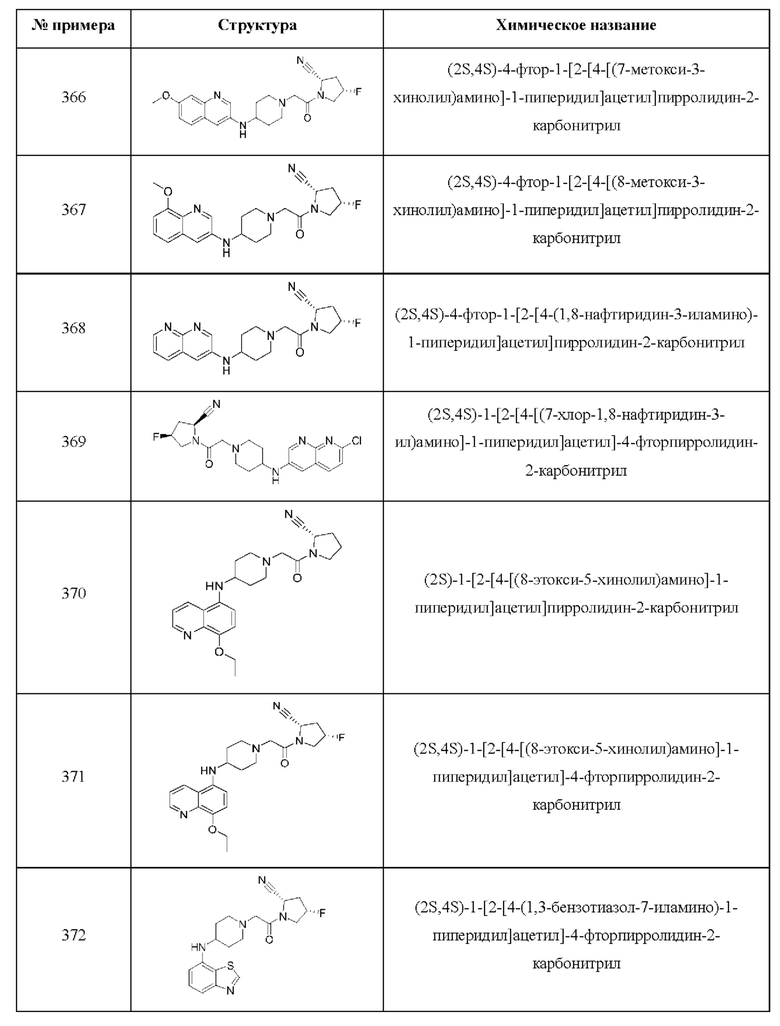
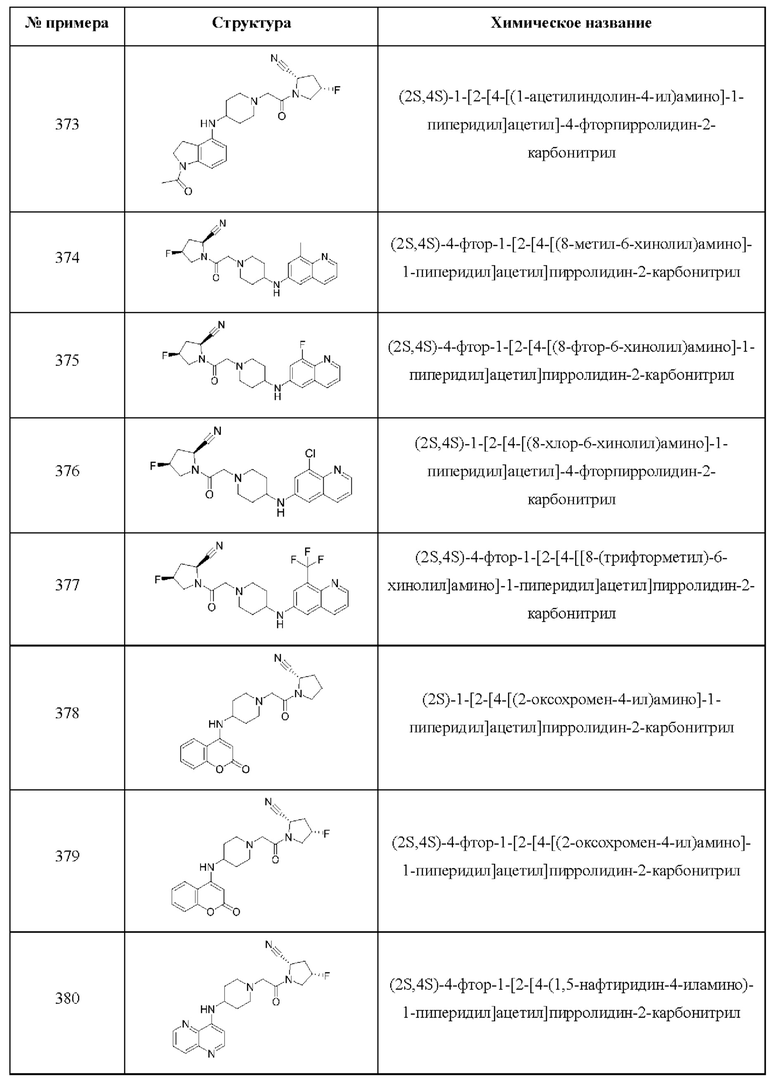
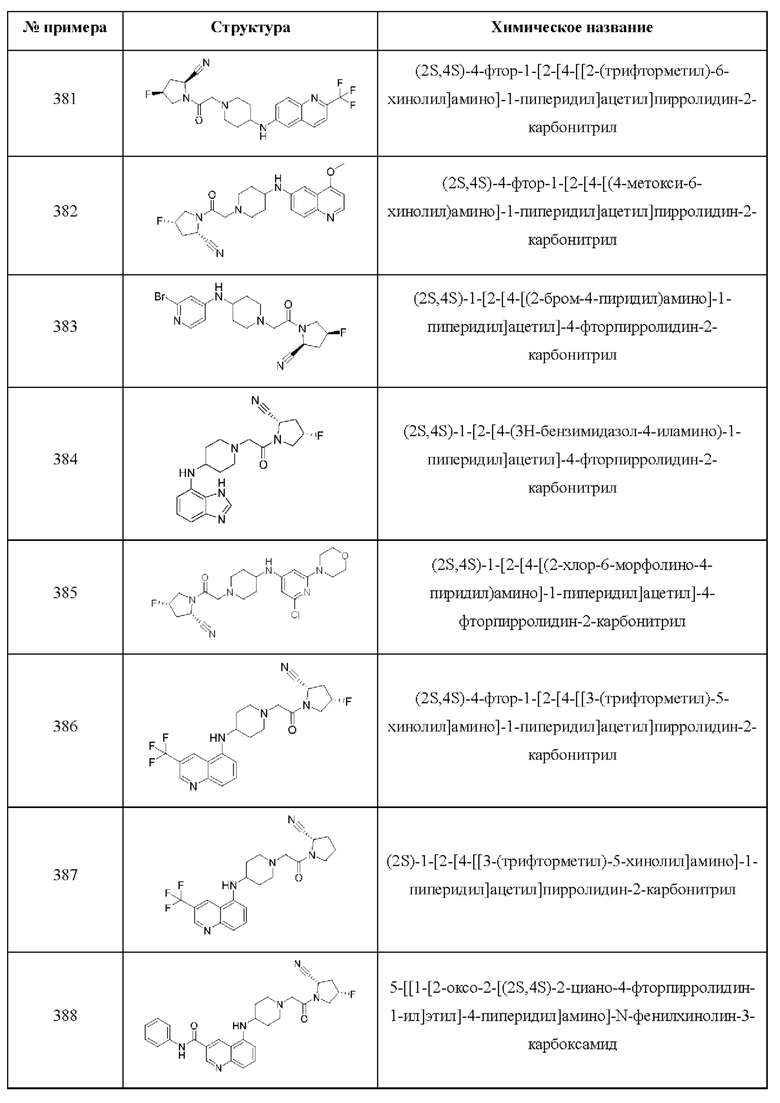
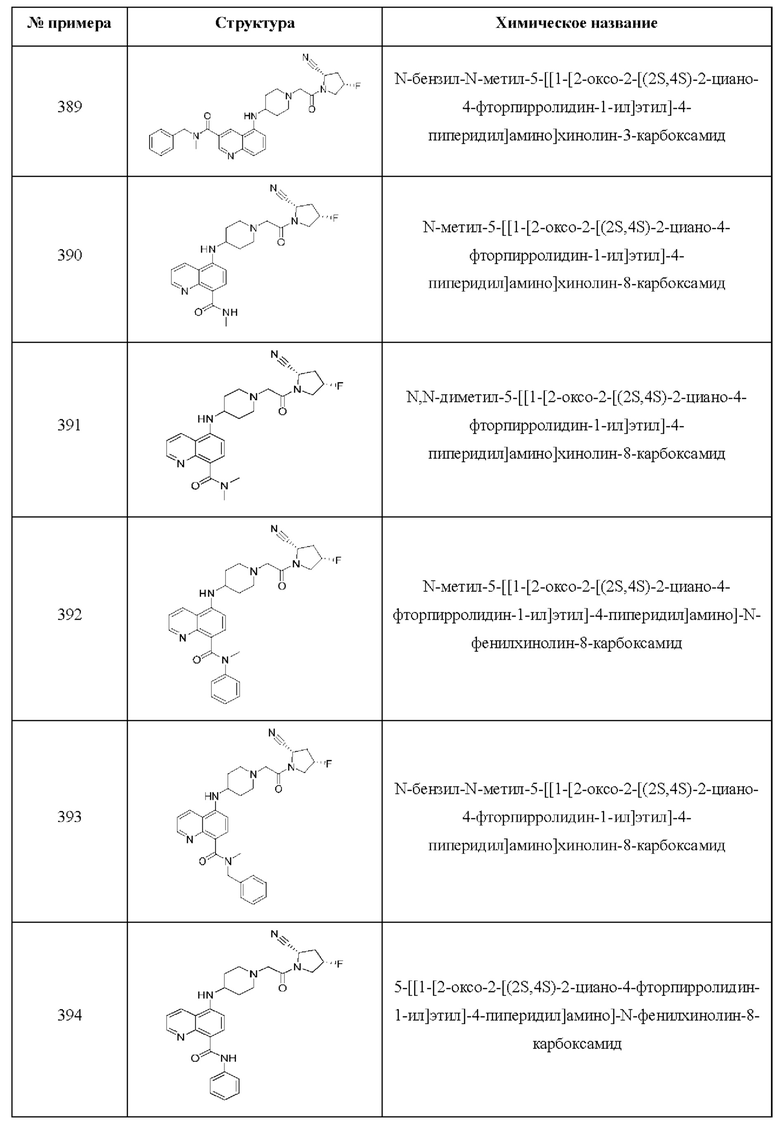
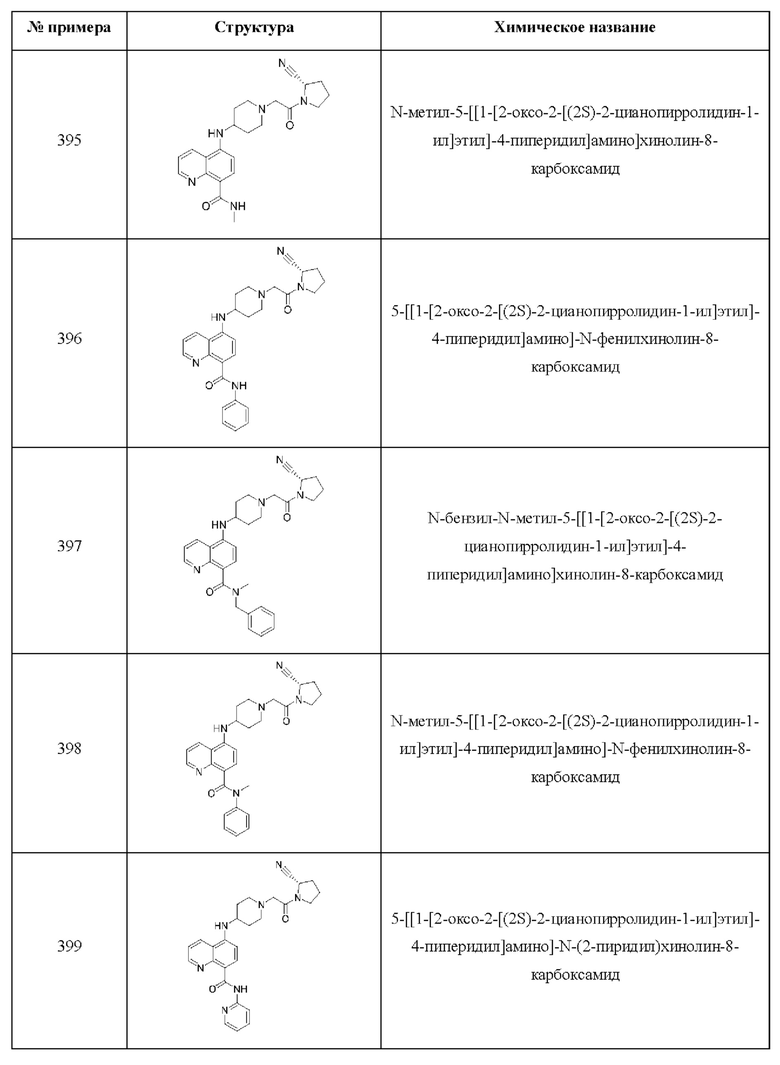
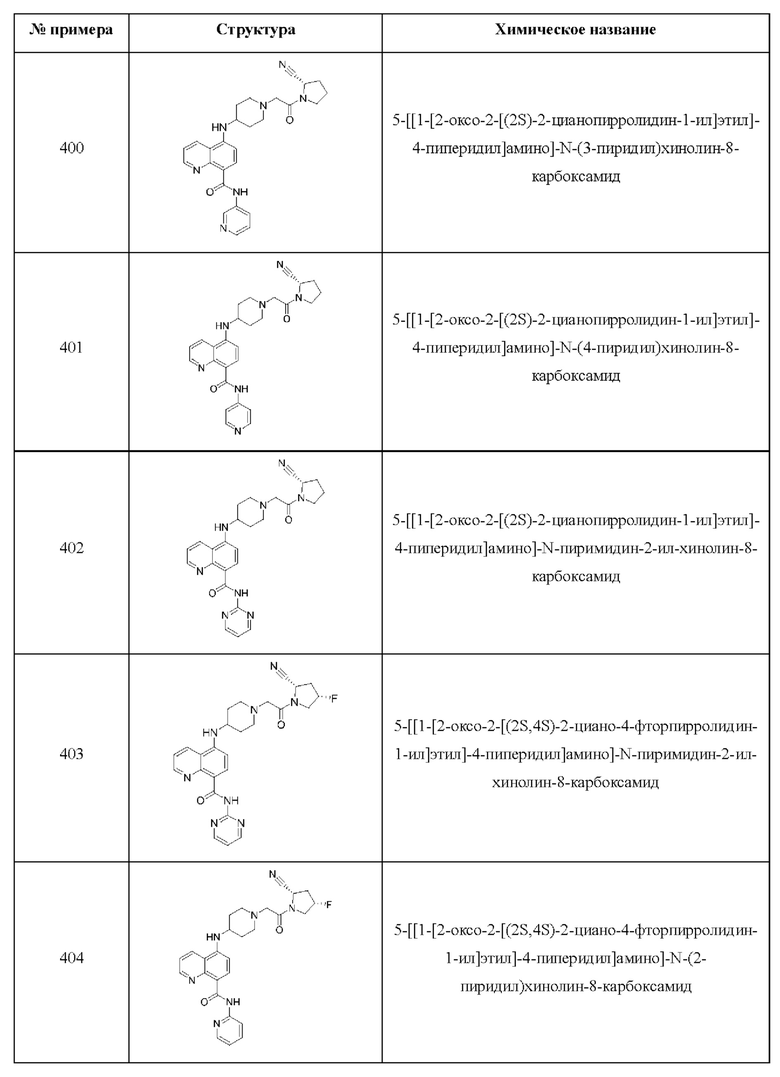

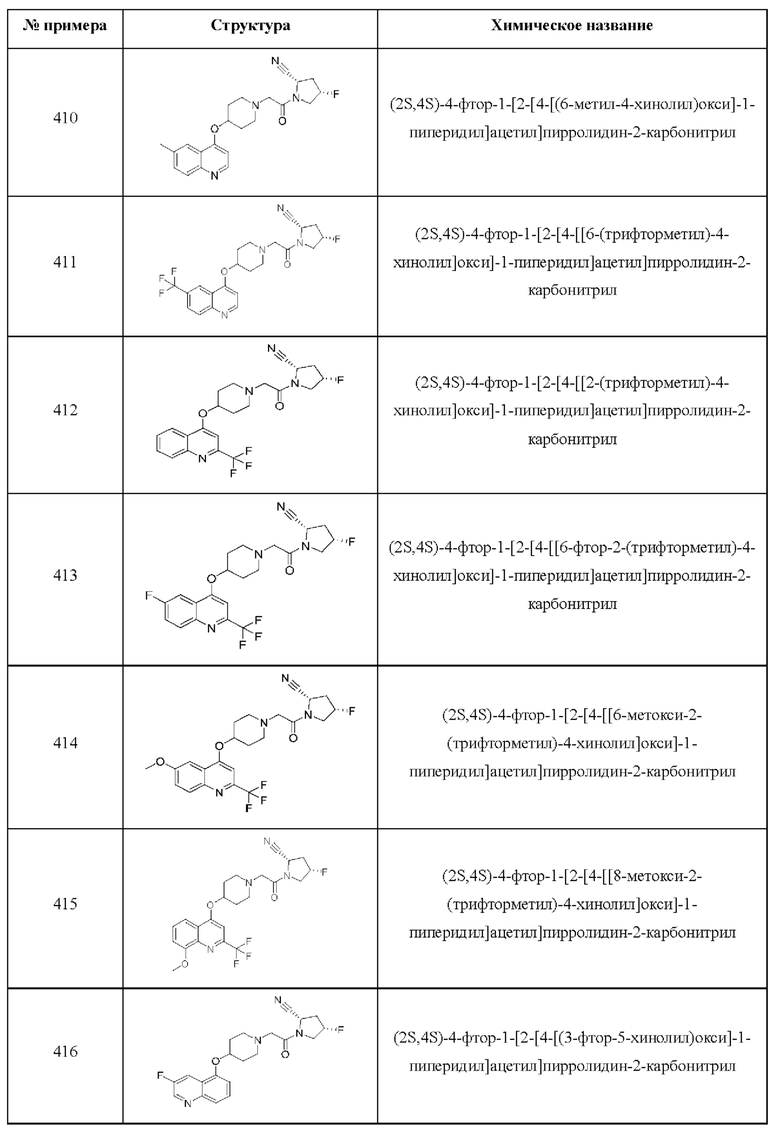
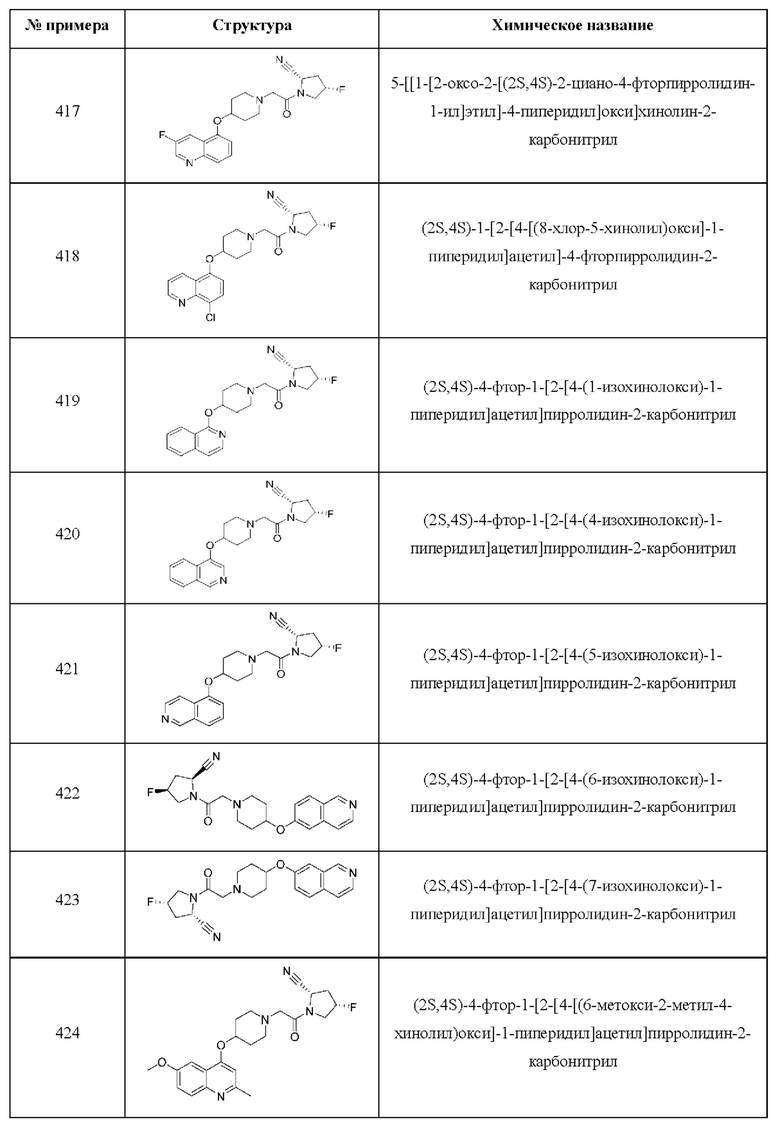
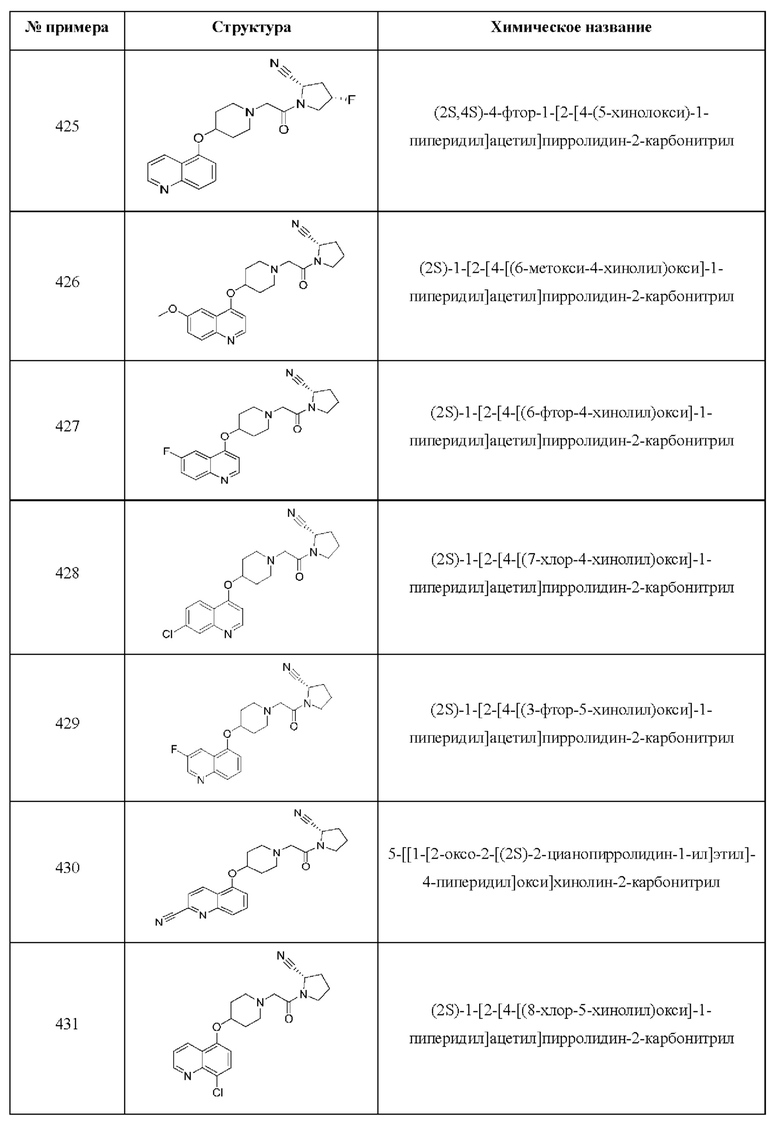

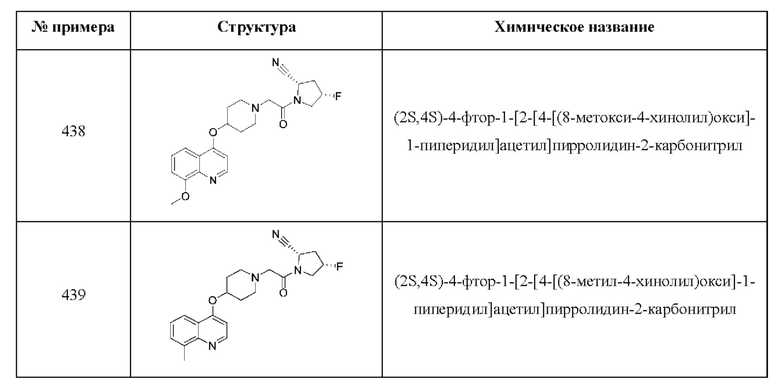
[2408] Экспериментальный пример 1: Оценка ингибирующего эффекта на активность дипептидилпептидаз, включая FAP
[2409] Соединения сошасно настоящей технологии оценивали с точки зрения ингибирующего эффекта на активность дипептидилпептидаз, включая FAP, с использованием субстрата, продуцирующего флуоресцентные вещества, при ферментативном разложении. Испытание проводили при 25°С с получением конечного объема реакции 100 мкл в 96-луночном черном планшете. Каждую из дипептидилпептидаз подвергали взаимодействию с тестируемыми соединениями (соединения согласно настоящей технологии) или Talabostat в течение 10 минут, а затем разлагали ферментами в течение 10 минут для измерения уровня выделяемых из них флуоресцентных веществ. Вкратце, тестируемые соединения растворяли в диметилсульфоксиде (DMSO) в концентрации 20 мМ, а затем подвергали серийному разбавлению, тем самым создавая 8-точечную кривую. Что касается контрольной группы, использовали 6-точечную кривую, полученную путем последовательного разбавления Talabostat в том же буферном растворе. Интенсивность флуоресценции измеряли с помощью считывающего устройства для микропланшетов (Flexstation3, Molecular Devices) в условиях длительности волны при 380 им и считывали излучение при 460 нм. Ингибирующий эффект исследуемых соединений измеряли как снижение (%) скорости сигнала по сравнению с контрольной группой без какого-либо ингибитора. Данные фиксировали на логистическую модель с четырьмя переменными и IC50 значение рассчитывали с использованием программы GraphPad Prism.
[2410] Рекомбинантный FAP человека (R&D Systems) разбавляли 50 мМ трис (рН 7,5) буфер, содержащий 1 М хлорида натрия и 1 мг/мл бычьего сывороточного альбумина (БСА), который составлял 10 нг на конечную реакцию. Исследуемые соединения подвергали серийному разведению в буфере, содержащем до 0,1% DMSO. В качестве субстрата использовали Z-Gly-Pro-AMC (Bachem). Растворяли в DMSO и затем разбавляли в том же буфере, добавляли субстрат до 50 мкм на конечную реакцию.
[2411] Что касается рекомбинантного человеческого DPP4 (R&D Systems), 25 мМ трис (рН 8,0) использовали буфер в качестве буферного раствора и H-Gly-Pro-AMC (Bachem) в качестве субстрата. Что касается рекомбинантного DPP7 человека (R&D Systems), использовали 25 мМ буфер MES (рН 6,0) в качестве буферного раствора и Lys-Pro-AMC (Bachem) в качестве субстрата. Что касается рекомбинантного человеческого DPP8 (PBS Bioscience) в качестве буферного раствора 10 мМ трис (рН 7,4) использовали буфер, содержащий 10 мМ хлорида магния и 0,05% Tween 20 и Z-Ala-Pro-AMC (BPS Bioscience) в качестве субстрата. Что касается рекомбинантного DPP9 человека (R&D Systems), использовали 25 мМтрис-буфер (рН 8,0) в качестве буферного раствора и H-Gly-Pro-AMC (Bachem) в качестве субстрата. Что касается рекомбинантного человеческого PREP (R&D System), в качестве буферного раствора используют 25 мМ трис-буфер (рН 7,5), содержащий 250 мМ хлорида натрия и 2,5 мМ DTT (дитиолтреитол), и Z-Gly-Pro-AMC (Bachem) в качестве субстрата. Оценку проводили с использованием 10 HrDPP4, PDD7 и PREP, 20 HrDPP8 и 50 нг DPP9 на основе конечной реакции. При оценке DPP4 тестируемые соединения подвергали серийному разбавлению в буфере в условиях, содержащих до 0,1% DMSO. При оценке DPP7, DPP8, DPP9 и PREP тестируемые соединения подвергали серийным разведениям в каждом буфере в условиях, содержащих до 0,5% DMSO.
[2412] Для анализа FAP FRET рекомбинантный FAP человека (R&D systems) разводили 50 мМ буфером HEPES (рН 7,2), содержащим 150 мМ хлорида натрия, 0,1 мг/мл бычьего сывороточного альбумина (БСА) и 1 мМ ЭДТА, чтобы получить 10 нг на конечную реакцию. Исследуемые соединения подвергали серийному разведению в буфере, содержащем до 0,1% DMSO. В качестве субстрата использовали пептиды FRET, содержащие последовательность человеческого FGF21 (VGPSQGK), конъюгированную с HyLite Fluor 488 и темновым гасителем QXL 520 (Anaspec). Растворяя в DMSO и затем разбавляя тем же буфером, субстрат добавляли до концентрации 6 мкМ на конечную реакцию. Все реакции анализа FRET проводили при 37°С.
[2413] Результаты, полученные путем оценки ингибирующего действия на активность дипептидилпептидазы, включая FAP, как указано выше, показаны в таблицах 2-8 ниже.
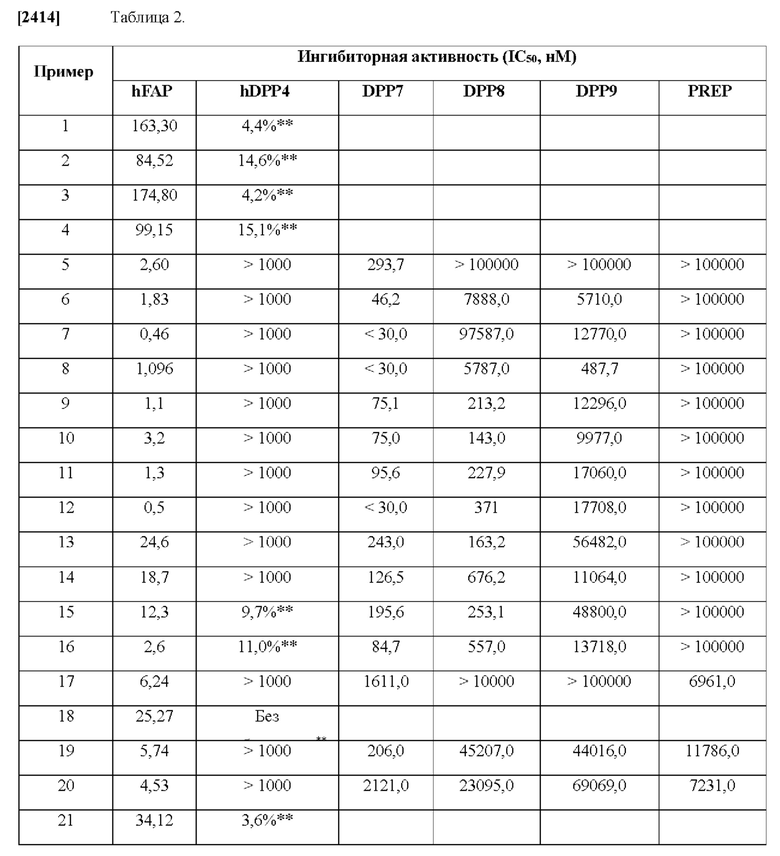
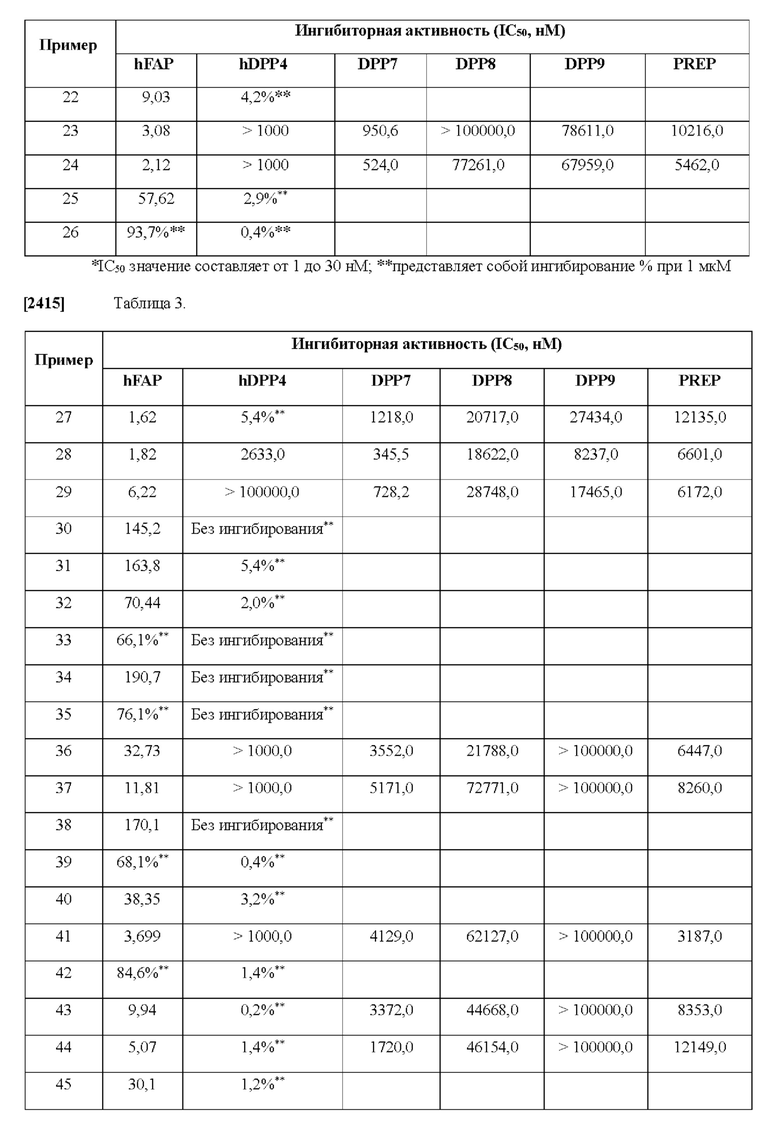
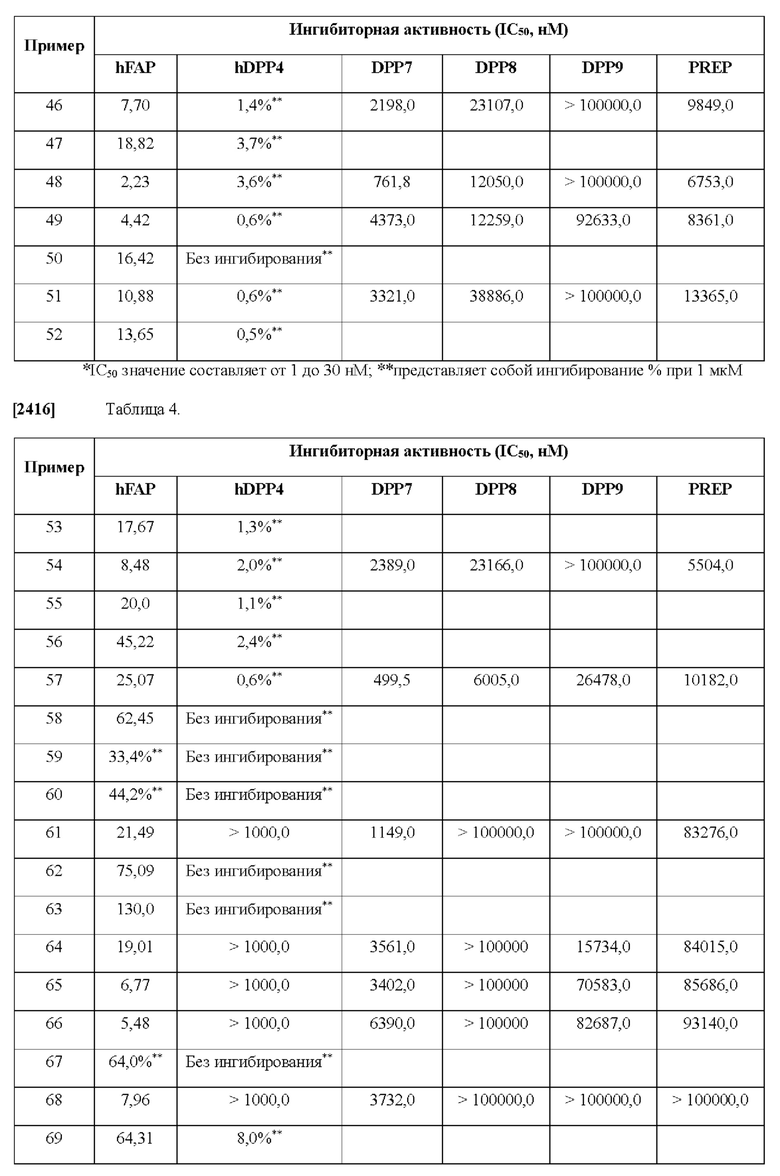
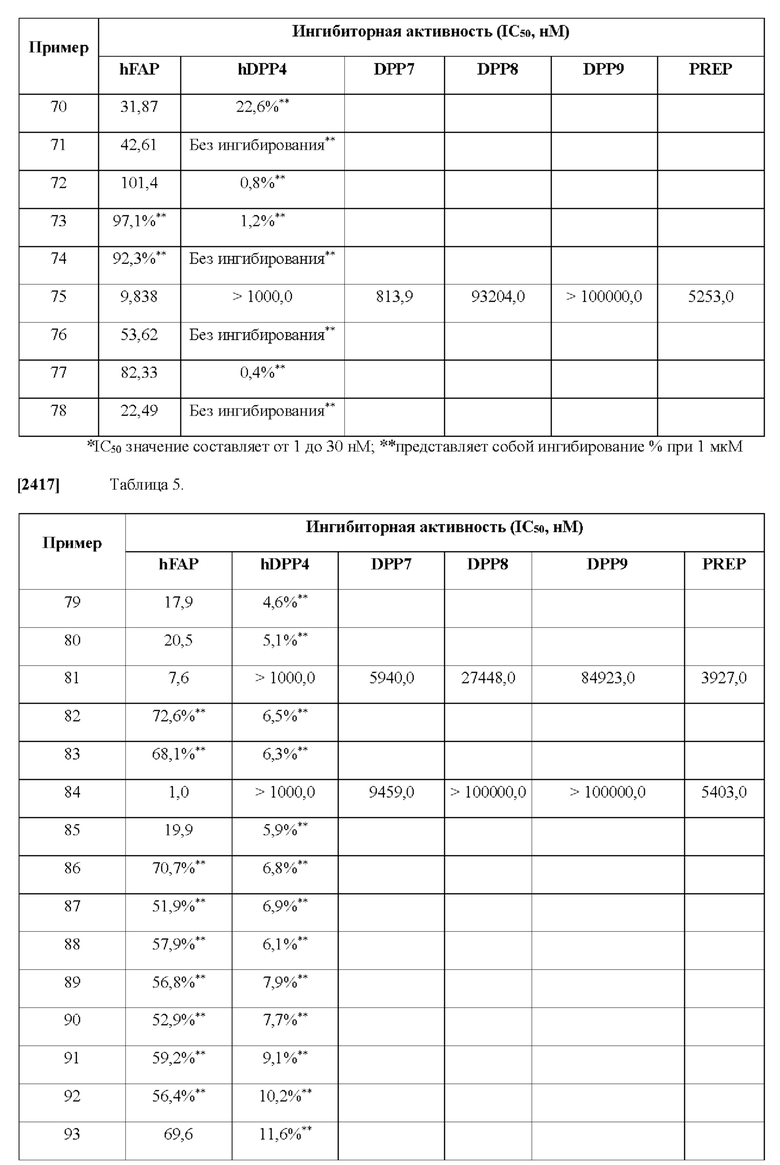
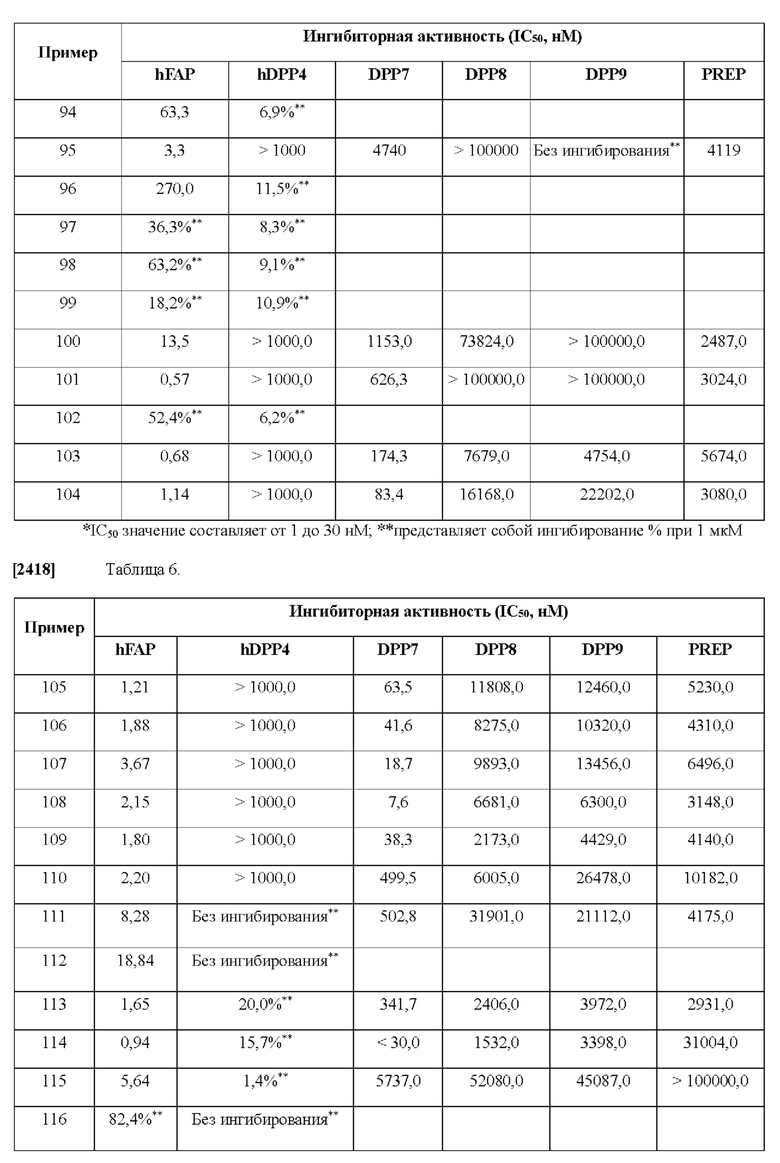
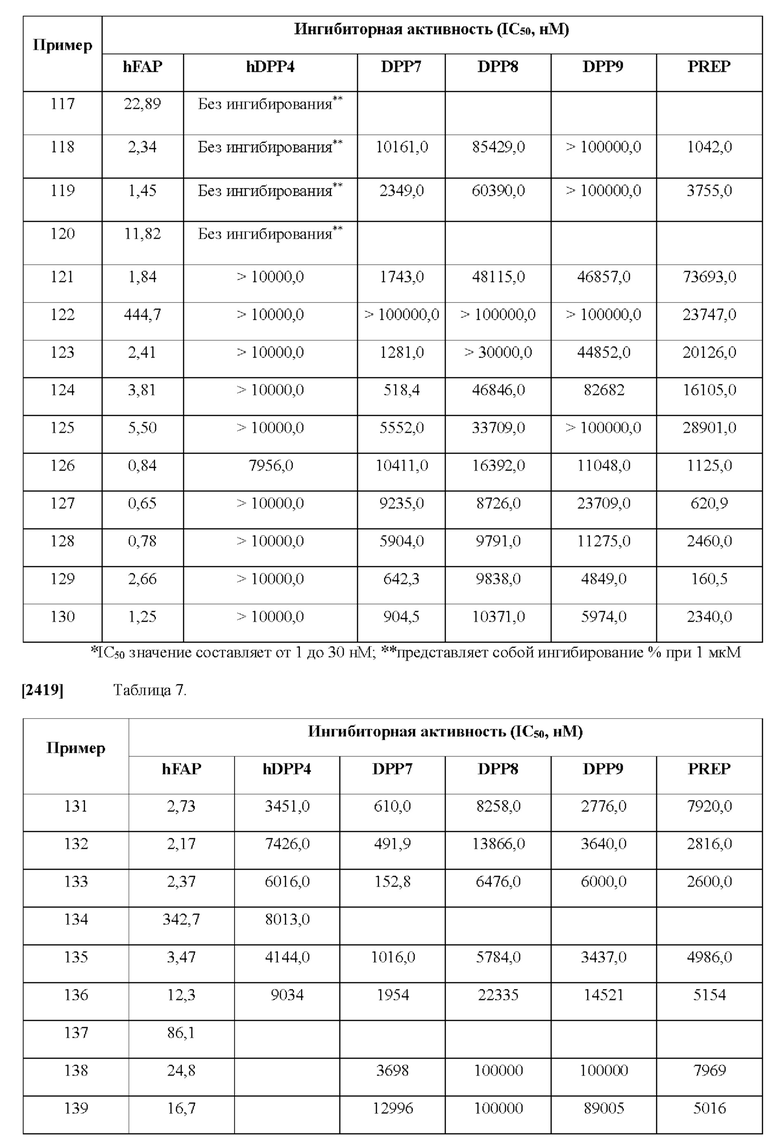
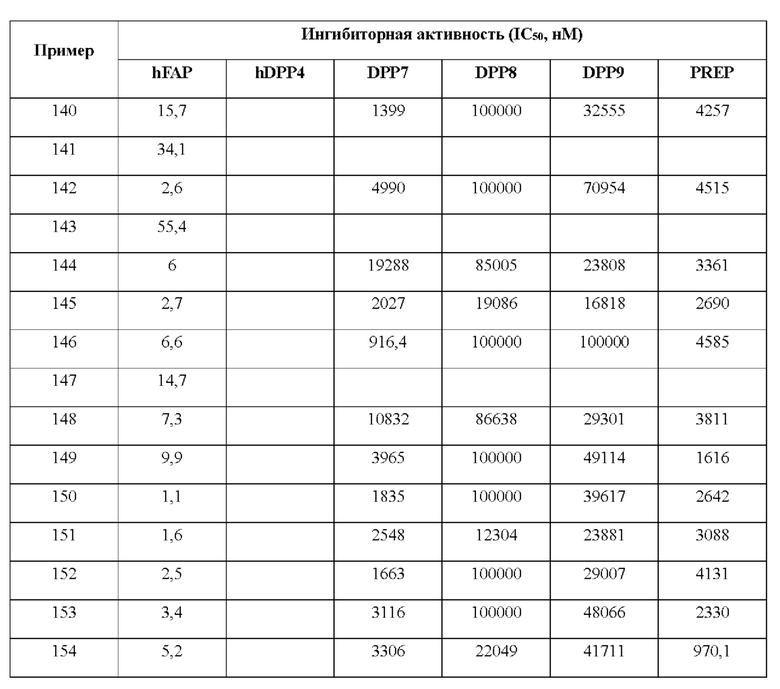
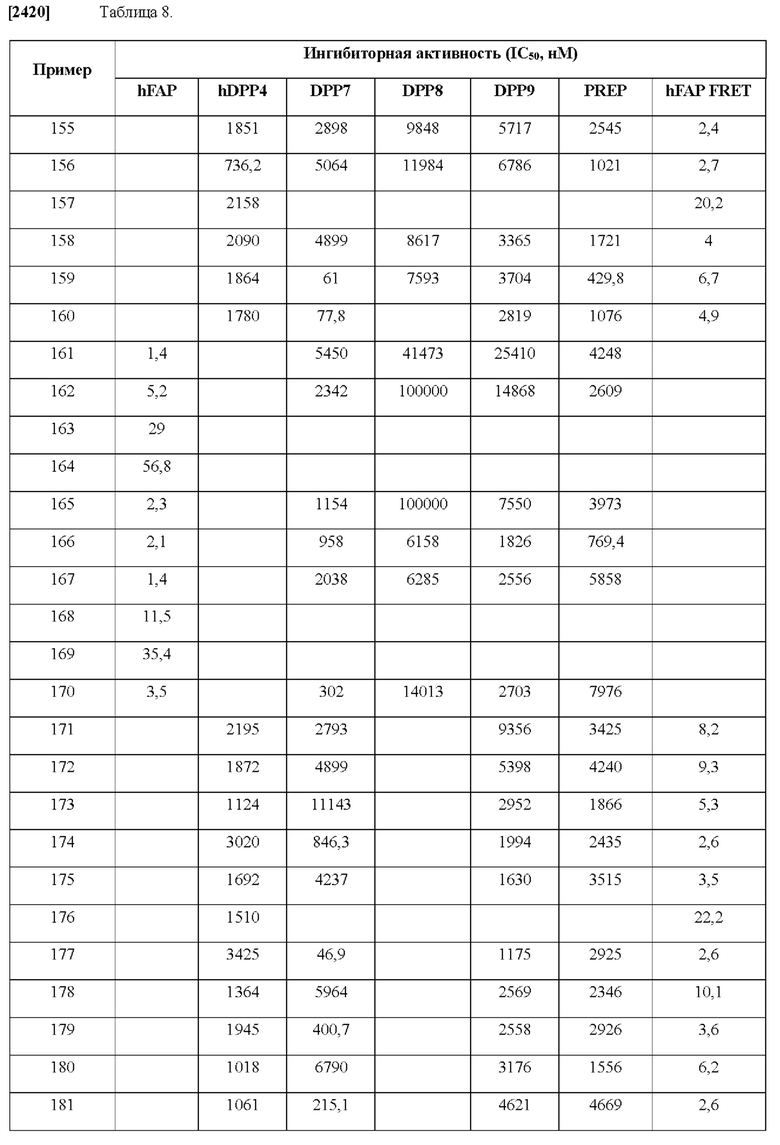
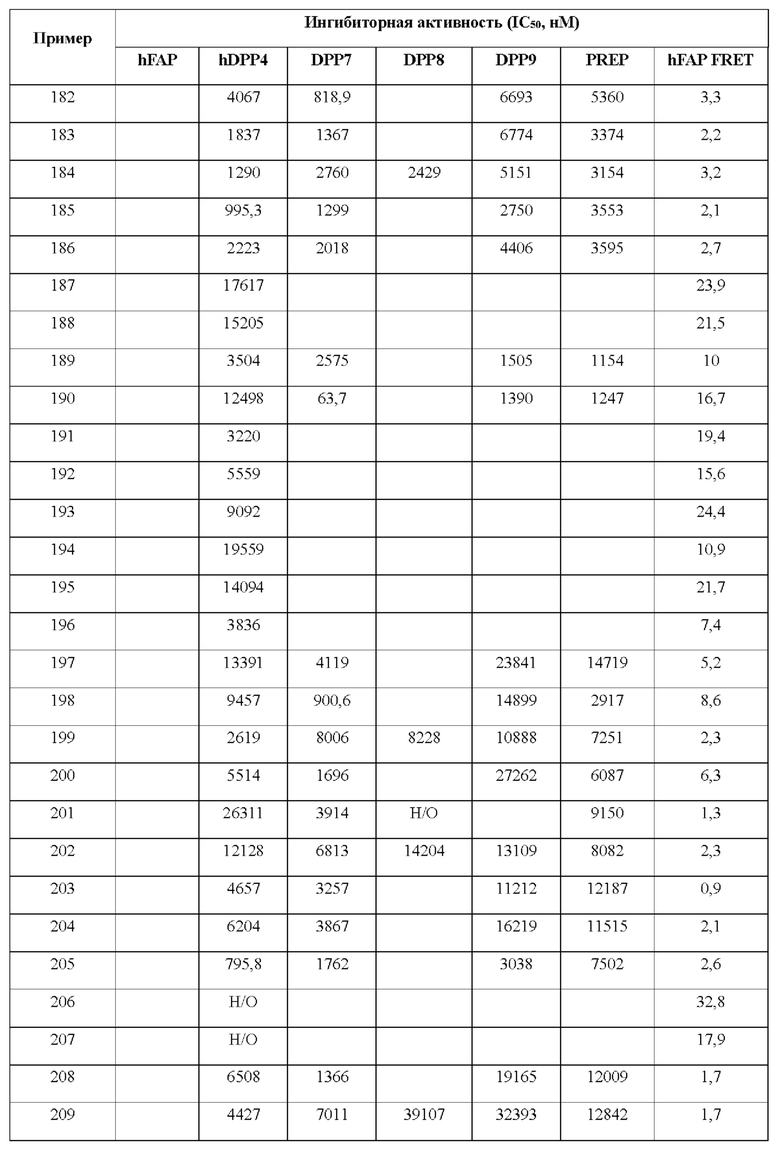
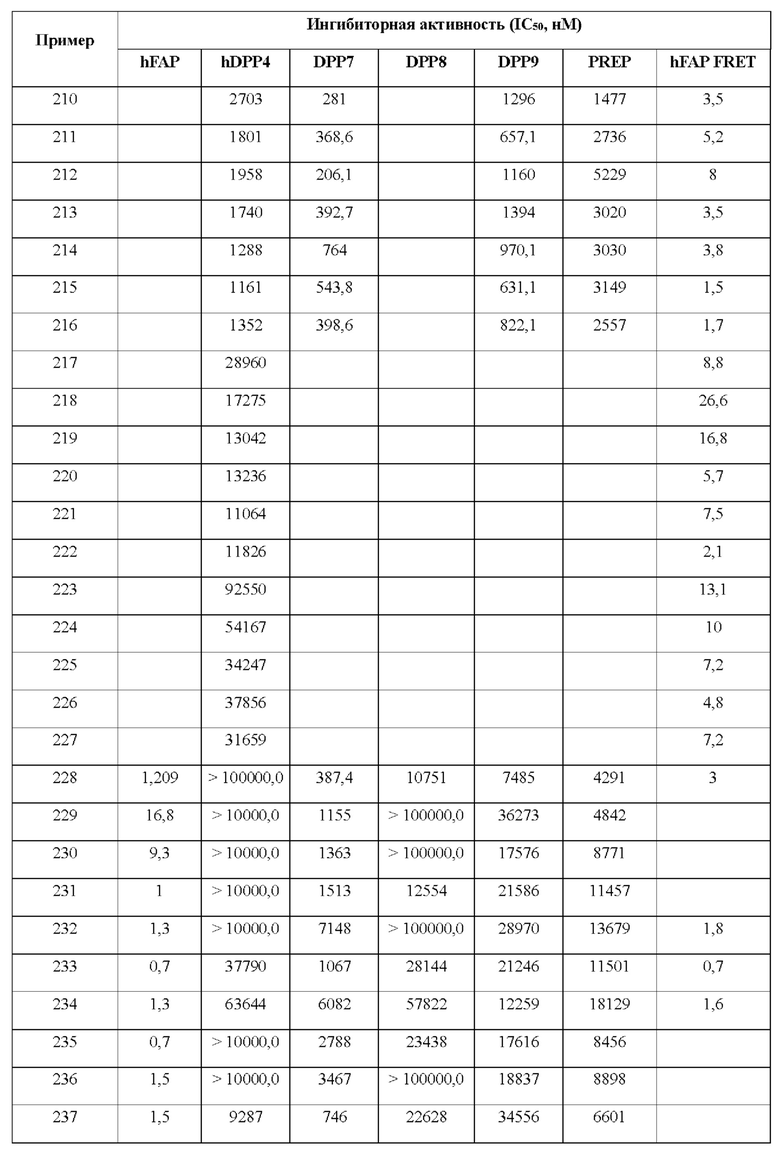
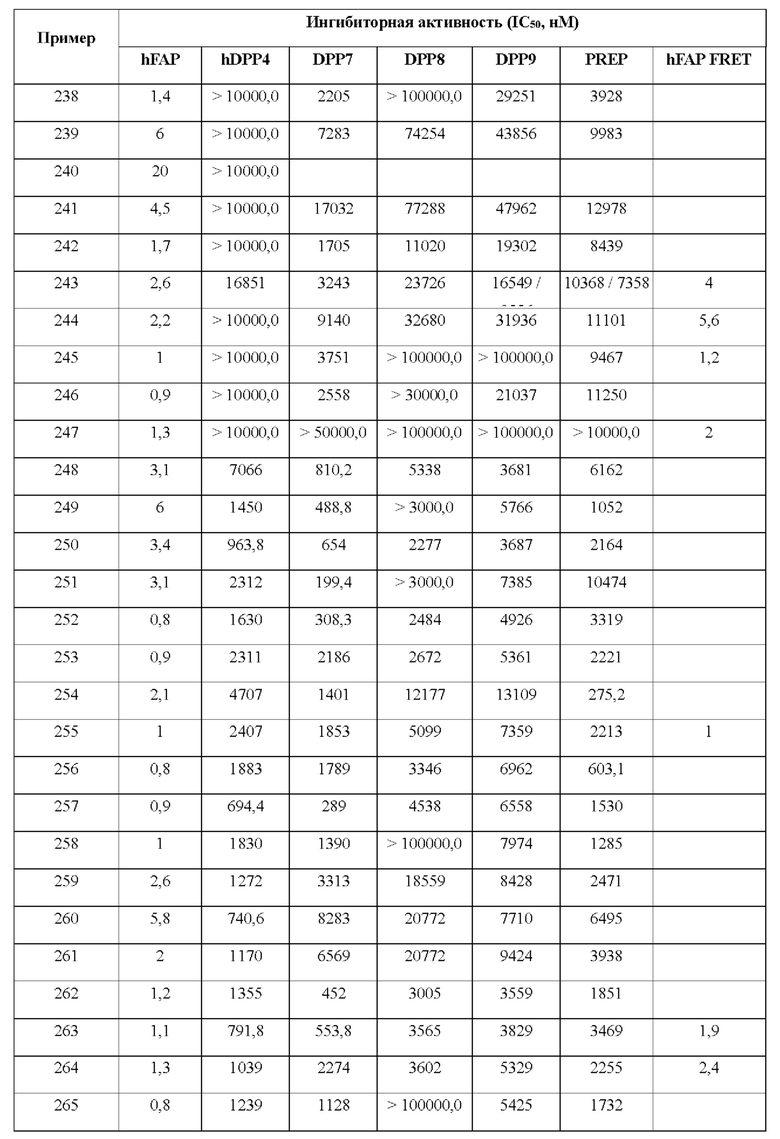

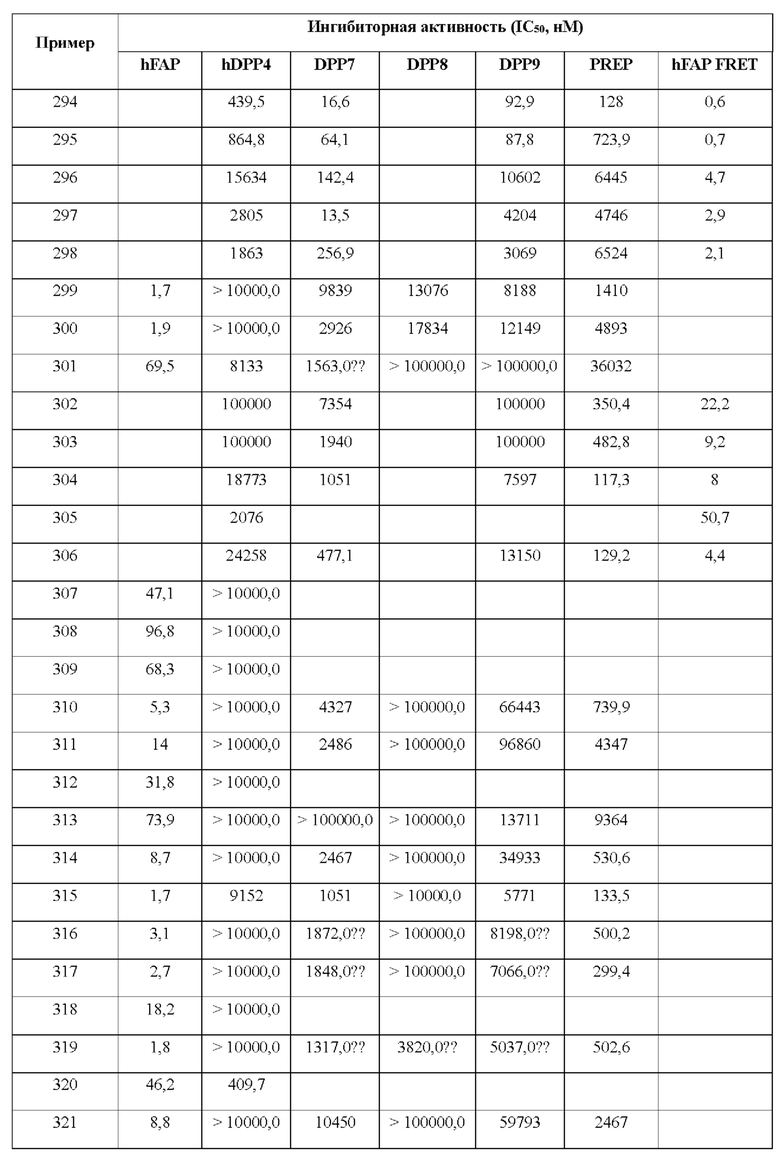
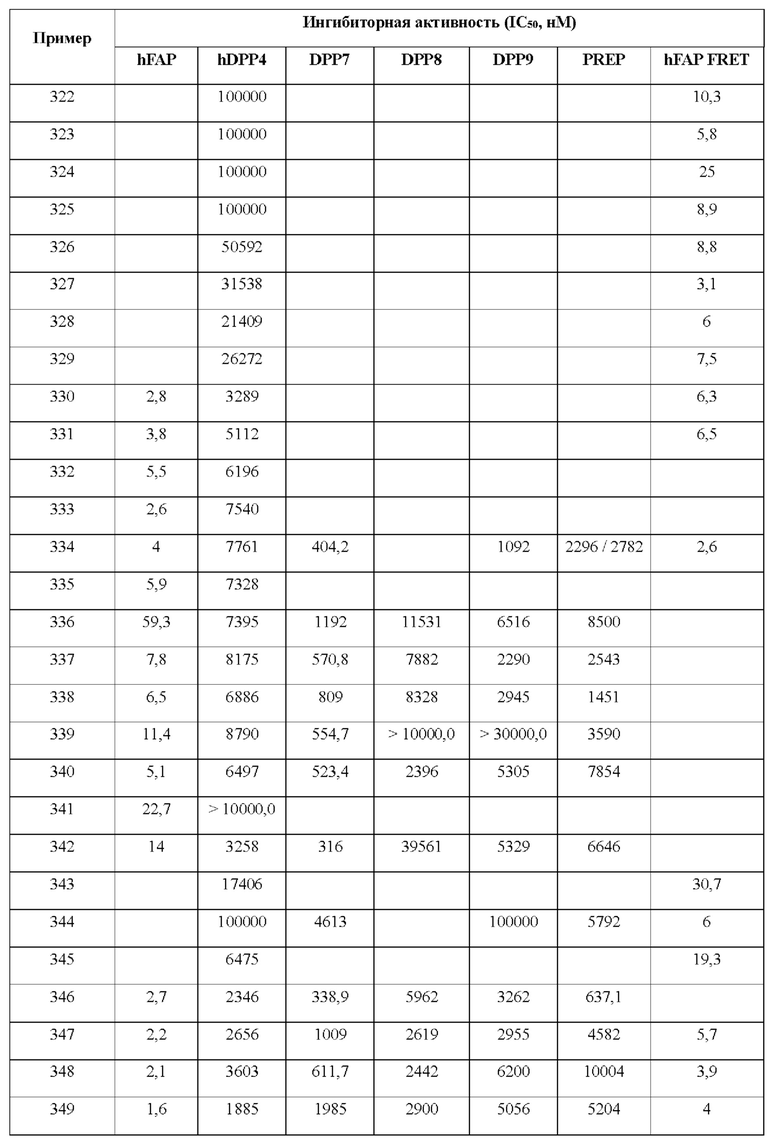
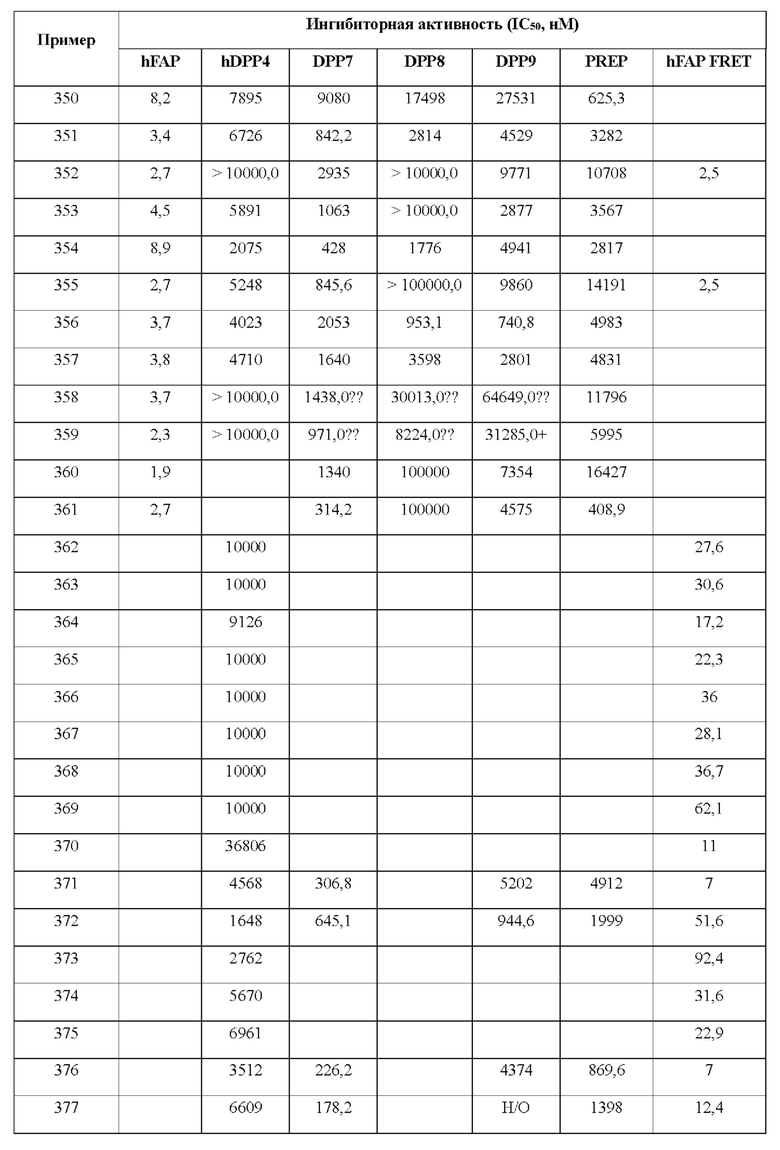
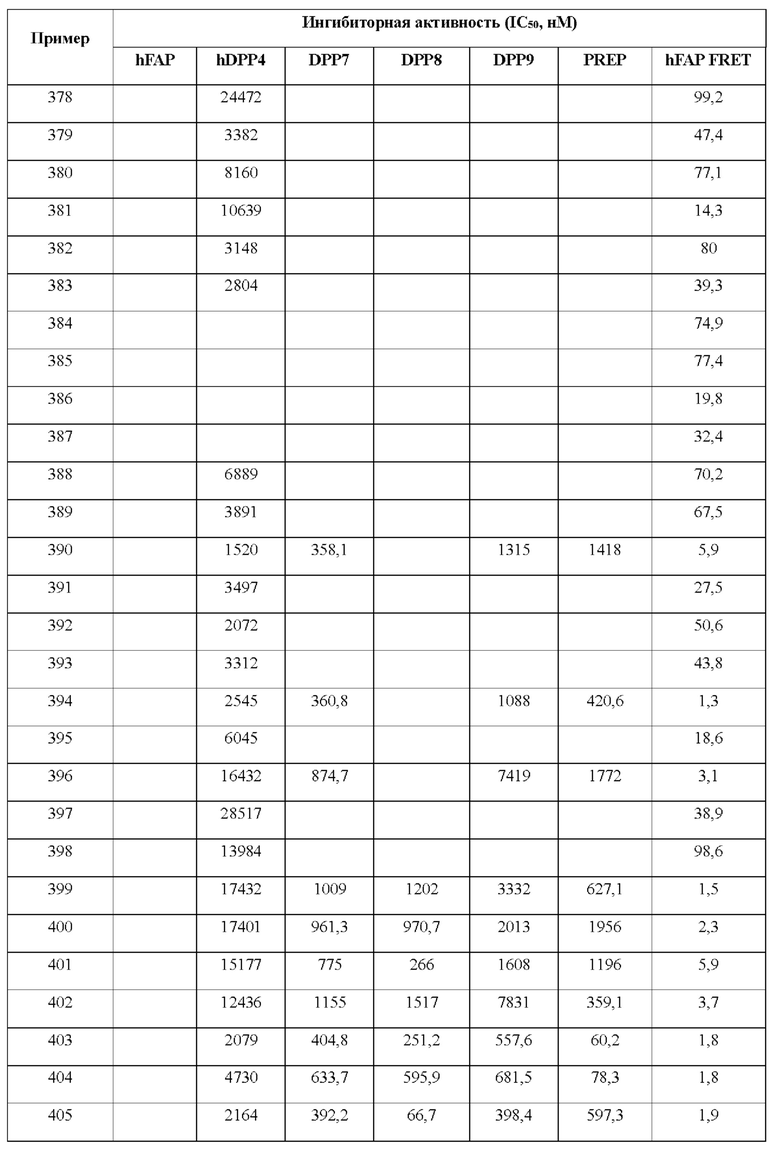
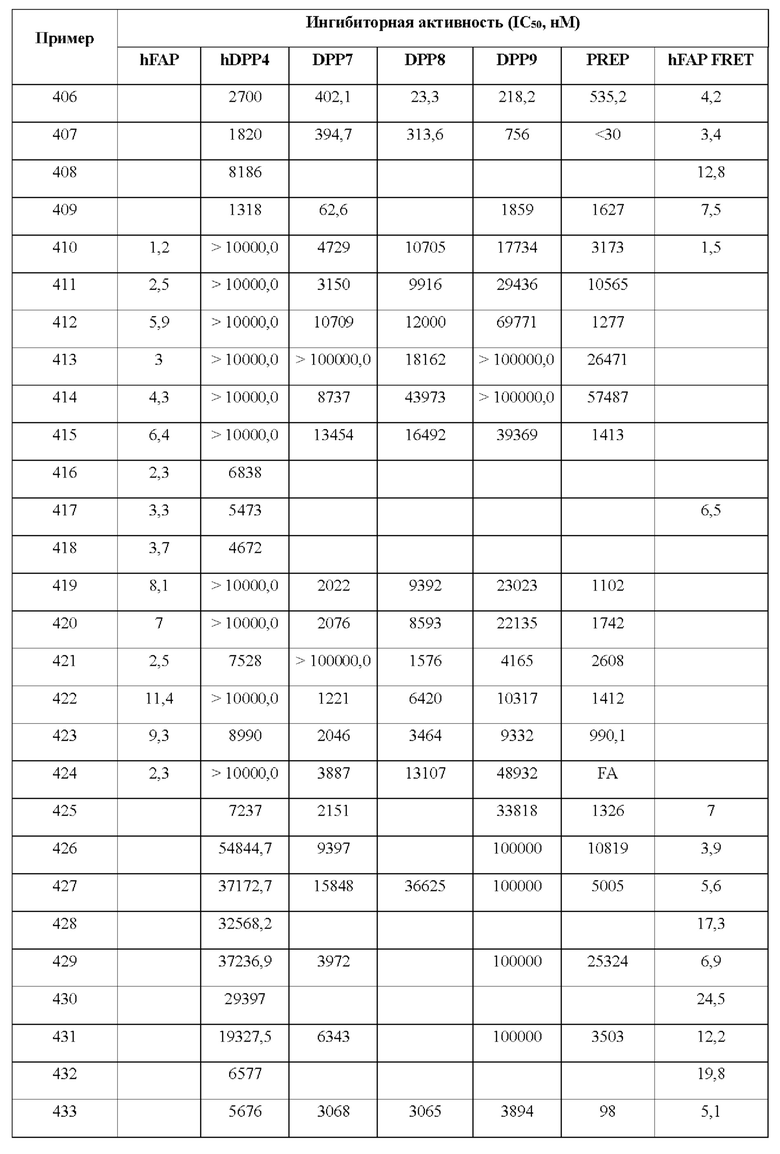

| название | год | авторы | номер документа |
|---|---|---|---|
| ИМИДАЗОПИРИДИНИЛЬНЫЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ НЕЙРОДЕГЕНЕРАТИВНЫХ РАССТРОЙСТВ | 2020 |
|
RU2833052C2 |
| Соединение на основе оксазолидина и содержащий его селективный агонист андрогенового рецептора | 2015 |
|
RU2702001C2 |
| ПРОИЗВОДНЫЕ ДИАМИНОПИРИМИДИНА И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2012 |
|
RU2587493C2 |
| НОВЫЕ ФТАЛАЗИНОВЫЕ ПРОИЗВОДНЫЕ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2014 |
|
RU2636585C2 |
| ПРОИЗВОДНЫЕ ДИАМИНОПИРИМИДИНА И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2012 |
|
RU2587981C2 |
| АНТАГОНИСТЫ TLR7/8 И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2833035C2 |
| ПИПЕРИДИНОВЫЕ СОЕДИНЕНИЯ, СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ЕЕ ПРИМЕНЕНИЕ | 2009 |
|
RU2514827C2 |
| НОВЫЕ АНТИДИАБЕТИЧЕСКИЕ АГЕНТЫ | 2000 |
|
RU2265012C2 |
| БЕНЗОТИАЗОЛЬНЫЕ СОЕДИНЕНИЯ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ ДЛЯ ЛЕЧЕНИЯ НЕЙРОДЕГЕНЕРАТИВНЫХ РАССТРОЙСТВ | 2018 |
|
RU2778370C2 |
| Новые соединения пиридопиримидинона для модулирования каталитической активности гистонлизиндеметилаз (KDMS) | 2015 |
|
RU2684396C2 |
Изобретение относится к соединениям формулы 1, где R2 и R3 определены в формуле изобретения, или их фармацевтически приемлемым солям, способам их получения, содержащим их фармацевтическим композициям и применению соединений для лечения и профилактики FAP-опосредованных заболеваний. 4 н. и 7 з.п. ф-лы, 8 табл., 439 пр.

R1 выбран из:
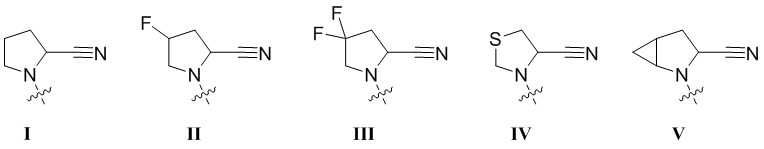
1. Соединение формулы 1:

или его стереоизомер, смесь стереоизомеров, или фармацевтически приемлемая соль, где
n представляет собой 1 или 2;
R1 выбран из группы, состоящей из формул I, II, III, IV и V:
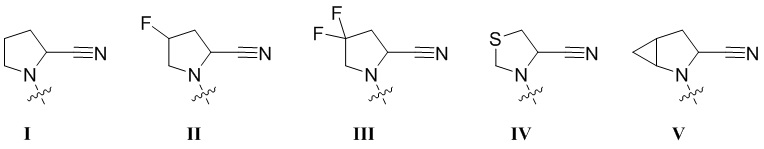 ;
;
R2 представляет собой водород;
R3 представляет собой -NR4R5, -OR4, -C(O)NHR4, -NHC(O)(CH2)mR4, -NHS(O)2R4, -(CH2)mCH2R4 или -(CH2)mNHR4,
где m представляет собой 0 или 1;
R4 представляет собой фенил, замещенный 1-3 Z,
гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, дигидробензо[1,4] диоксинила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинила, причем указанный гетероцикл необязательно замещен 1-3 Z,
нафтил, необязательно замещенный 1-3 Z, или
гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила, пиразинила, имидазолила, пиразолила, триазолила, оксазолила, тиазолила, фуранила, пирролила, тиофенила, хинолинила, изохинолинила, хроменонила, хиназолинила, бензоксазолила, бензофуранила, бензотиофенила, индолила, индолинила, бензимидазолила, бензоксазолила, бензотиазолила, индазолила, фуро[3,2-c]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-c]пиридинила, изоксазолила, акридинила и нафтиридинила, где указанный гетероарил необязательно замещен 1-3 Z;
R5 представляет собой водород или C1-3алкил; и
каждый Z независимо выбран из группы, состоящей из гидрокси, амино, галогена, циано, нитро, карбоновой кислоты, C1-5алкила, необязательно замещенного 1-3 Z1, С2-6алкенила, С2-6алкинила, С1-5алкокси, необязательно замещенного 1-3 Z1, С1-5алкилтио, моно- или ди-C1-5алкиламино, пиперазинила, необязательно замещенного Z1, С1-5алкилсульфониламино, С1-5алкилкарбониламино, аминосульфонила, аминокарбонила, С1-5алкиламинокарбонила, фенила, необязательно замещенного Z1, фенокси, необязательно замещенного Z1, бензила, необязательно замещенного Z1, бензоила, необязательно замещенного Z1, фениламинокарбонила, пиразолила, необязательно замещенного Z1, бензоксазолила, необязательно замещенного Z1, С1-5алкоксикарбонила, необязательно замещенного Z1, бензилокси, необязательно замещенного Z1, С1-5алкилсульфонила, необязательно замещенного Z 1, ацетила, морфолинила, необязательно замещенного Z1, -NR6C(O)R7 и -C(O)NR6R7;
где каждый Z1 независимо выбран из галогена, гидроксила, амино, C1-5алкиламино, циано, ацетила, C1-5алкила, C1-5галогеналкила, C3-6карбоцикла и C3-6гетероцикла;
R6 представляет собой водород или C1-3алкильную группу; и
R7 представляет собой C1-3алкильную группу, необязательно замещенную фенилом,
фенил, или
гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила и изоксазолила.
2. Соединение по п. 1 или его стереоизомер, смесь стереоизомеров или его фармацевтически приемлемая соль, в котором R1 выбран из группы, состоящей из соединений формулы Ia, IIa, IIIa, IVa и Va:
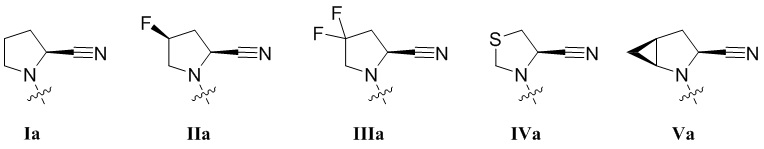 .
.
3. Соединение по любому из пп. 1-2 или его стереоизомер, смесь стереоизомеров или его фармацевтически приемлемая соль, имеющее структуру формулы 1a:
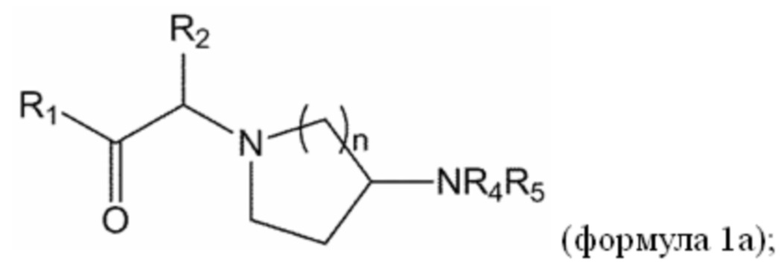
или имеющее структуру формулы 1b:
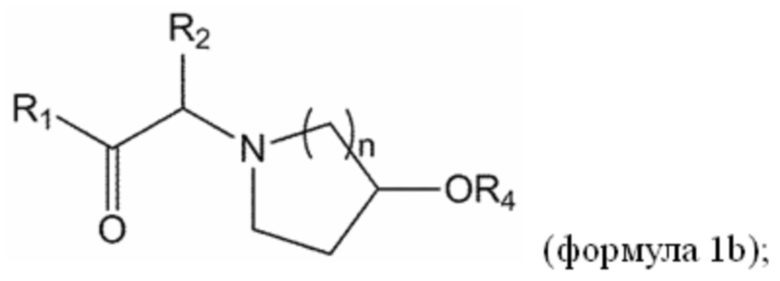
или имеющее структуру формулы 1c:
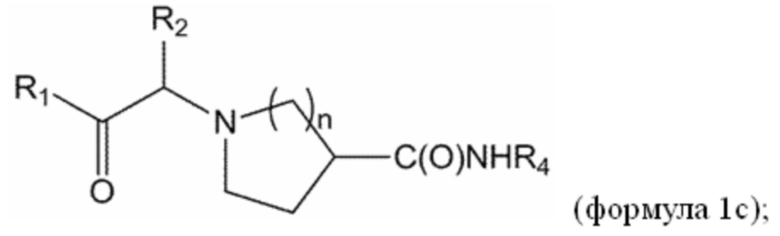
или имеющее структуру формулы 1d:
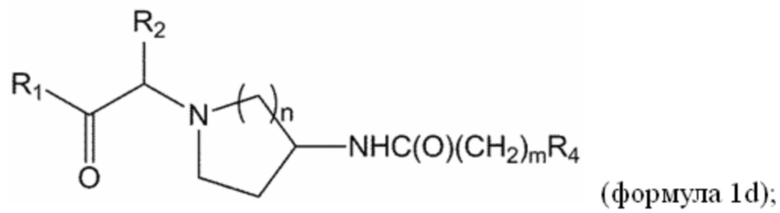
или имеющее структуру формулы 1e:
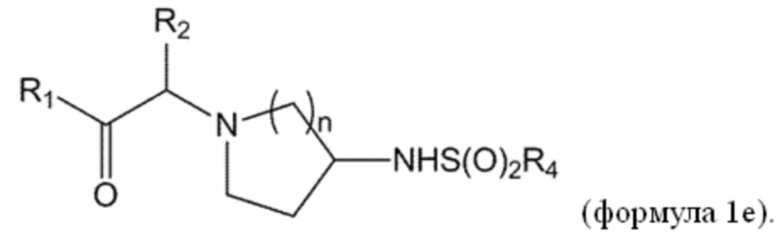
4. Соединение по любому из пп. 1-3 или его стереоизомер, смесь стереоизомеров или его фармацевтически приемлемая соль, в котором R4 представляет собой фенил, замещенный 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, галогена, циано, нитро, карбоновой кислоты, C1-5алкила, необязательно замещенного 1-3 галогенами или аминогруппой, C2-6алкенила, C2-6алкинила, C1-5алкокси, C1-5алкилтио, моно- или ди-C1-5алкиламино, пиперазинила, необязательно замещенного ацетилом, C1-5алкилсульфониламино, C1-5алкилкарбониламино, аминосульфонила, аминокарбонила, C1-5алкиламинокарбонила, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила;
при этом необязательно R4 представляет собой фенил, замещенный заместителем, выбранным из группы, состоящей из пиперазинила, необязательно замещенного ацетилом, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила; или
при этом необязательно R4 представляет собой нафтил, необязательно замещенный галогеном.
5. Соединение по любому из пп. 1-3 или его стереоизомер, смесь стереоизомеров или его фармацевтически приемлемая соль, в котором R4 представляет собой гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, дигидробензо[1,4]диоксинила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинила, где указанный гетероцикл необязательно замещен 1-3 Z;
при этом необязательно R4 представляет собой гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинила.
6. Соединение по любому из пп. 1-3 или его стереоизомер, смесь стереоизомеров или его фармацевтически приемлемая соль, в котором R4 представляет собой гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила, пиразинила, имидазолила, пиразолила, триазолила, оксазолила, тиазолила, фуранила, пирролила, тиофенила, хинолинила, изохинолинила, хроменонила, хиназолинила, бензоксазолила, бензофуранила, бензотиофенила, индолила, индолинила, бензимидазолила, бензоксазолила, бензотиазолила, индазолила, фуро[3,2-c]пиридинила, тиено[2,3-d] пиримидинила, тиено[3,2-с]пиридинила, изоксазолила, акридинила и нафтиридинила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, амино, ди-C1-5алкиламино, циано, нитро, галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, C1-5алкокси, необязательно замещенного 1-3 галогенами, C1-5алкоксикарбонила, бензилокси, фенила, необязательно замещенного галогеном, ацетила, C1-5алкилсульфонила, морфолинила, -NR6C(O)R 7 и -C(O)NR6R7;
или при этом необязательно R4 представляет собой гетероарил, выбранный из группы, состоящей из пиридинила, хинолинила, изохинолинила, хроменонила, хиназолинила, бензофуранила, индолинила, бензимидазолила, бензотиофенила, бензотиазолила, фуро[3,2-c]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила, акридинила и нафтиридинила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, циано, нитро, галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, C1-5алкокси, необязательно замещенного 1-3 галогенами, C1-5алкоксикарбонила, бензилокси, ацетила, морфолинила, -NR6C(O)R7, -C(O)NR6R7 и фенила, необязательно замещенного галогеном;
где R6 представляет собой водород или C1-3алкильную группу; и
R7 представляет собой C1-3алкильную группу, необязательно замещенную фенилом, фенил или гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила и изоксазолила.
7. Соединение по любому из пп. 1-3 или его стереоизомер, смесь стереоизомеров или его фармацевтически приемлемая соль, в котором R4 представляет собой фенил, замещенный заместителем, выбранным из группы, состоящей из пиперазинила, необязательно замещенного ацетилом, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила;
гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинила;
нафтил, необязательно замещенный галогеном; или
гетероарил, выбранный из группы, состоящей из пиридинила, хинолинила, изохинолинила, хроменонила, хиназолинила, бензофуранила, индолинила, бензимидазолила, бензотиофенила, бензотиазолила, фуро[3,2-c]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила, акридинила и нафтиридинила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, циано, нитро, галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, C1-5алкокси, необязательно замещенного 1-3 галогенами, C1-5алкоксикарбонила, бензилокси, ацетила, морфолинила, -NR6C(O)R7, -C(O)NR6R7 и фенила, необязательно замещенного галогеном;
R6 представляет собой водород или C1-3алкильную группу; и
R7 представляет собой C1-3алкильную группу, необязательно замещенную фенилом,
фенил или
гетероарил, выбранный из группы, состоящей из пиридинила, пиримидинила и изоксазолила.
8. Соединение по п. 1 или его стереоизомер, смесь стереоизомеров или его фармацевтически приемлемая соль, в котором
R1 представляет собой заместитель, выбранный из группы, состоящей из соединений формул I, II, III и V,
R3 представляет собой заместитель, выбранный из группы, состоящей из -NR4R5, -OR4, -C(O)NHR4, -NHC(O)(CH2)mR4 и -NHS(O)2R4,
при этом R4 представляет собой фенил, замещенный заместителем, выбранным из группы, состоящей из пиперазинила, необязательно замещенного ацетилом, фенила, фенокси, бензила, бензоила, фениламинокарбонила, пиразолила и бензоксазолила;
гетероцикл, выбранный из группы, состоящей из бензо[d][1,3]диоксолила, 2,3-дигидробензофуранила, 2-оксо-1,2-дигидрохинолинила и 2-оксо-1,2,3,4-тетрагидрохинолинила;
нафтил, необязательно замещенный галогеном; или
гетероарил, выбранный из группы, состоящей из пиридинила, хинолинила, изохинолинила, хиназолинила, бензофуранила, бензотиофенила, фуро[3,2-с]пиридинила, тиено[2,3-d]пиримидинила, тиено[3,2-с]пиридинила, изоксазолила и акридинила, причем указанный гетероарил необязательно замещен 1-3 Z, причем каждый Z независимо выбран из группы, состоящей из гидрокси, галогена, C1-5алкила, необязательно замещенного 1-3 галогенами, C1-5алкокси, необязательно замещенного 1-3 галогенами, C1-5алкоксикарбонила, бензилокси и фенила, необязательно замещенного галогеном, и
R5 представляет собой водород.
9. Соединение, имеющее следующую структуру:
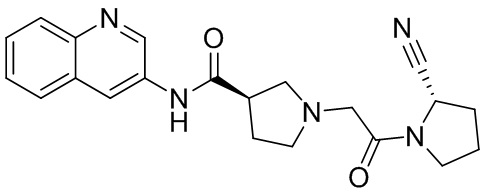
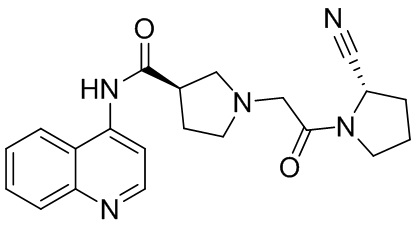
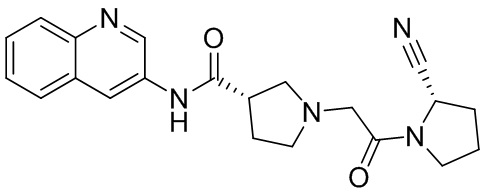
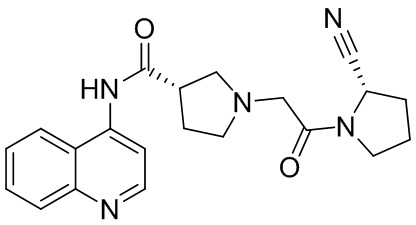
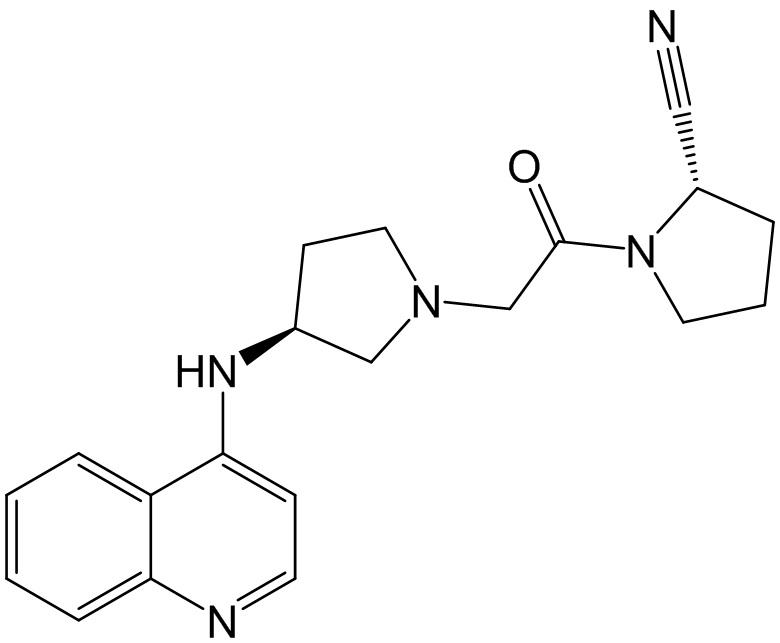
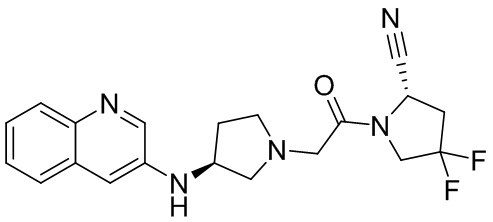
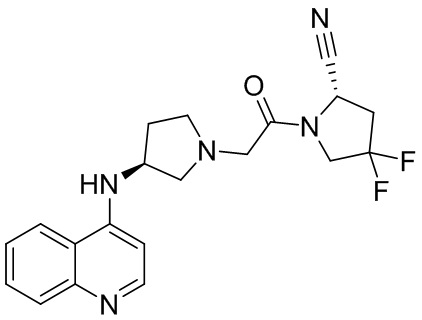
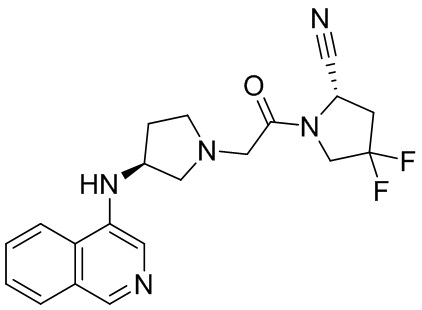
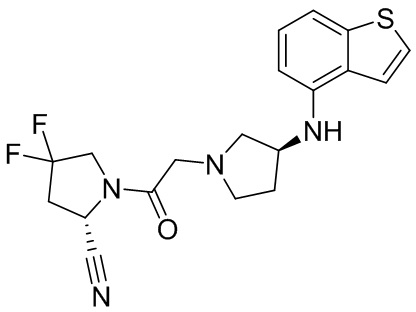
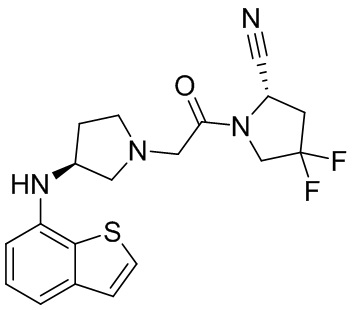
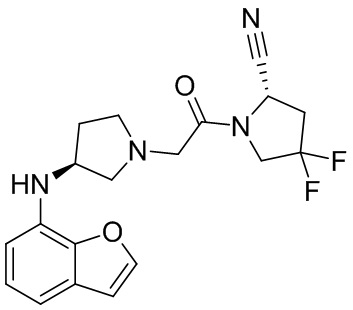
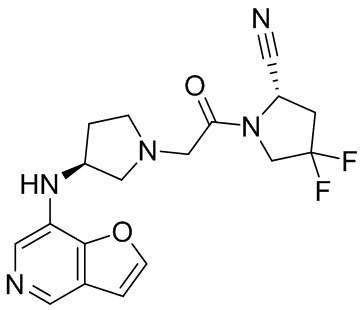
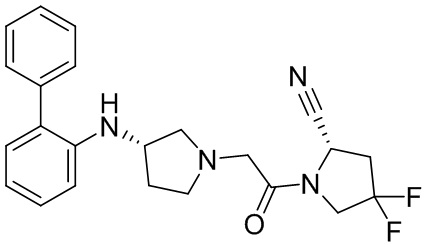
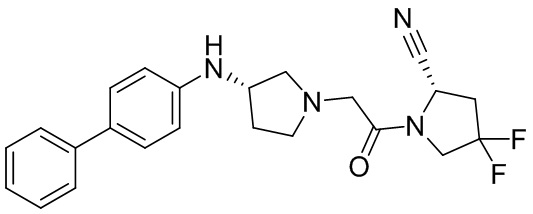

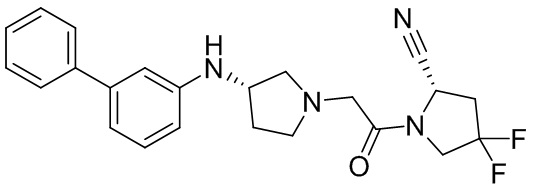
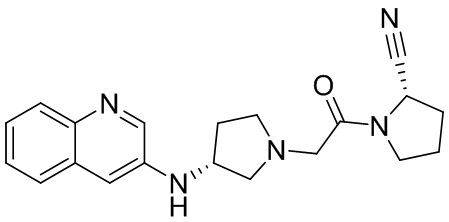
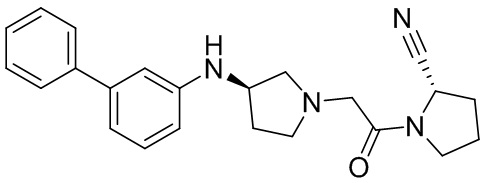
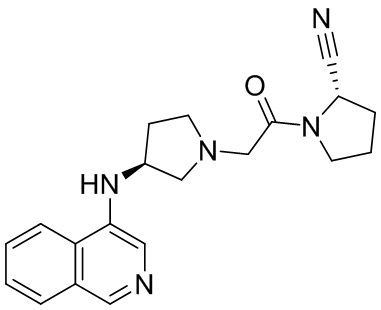
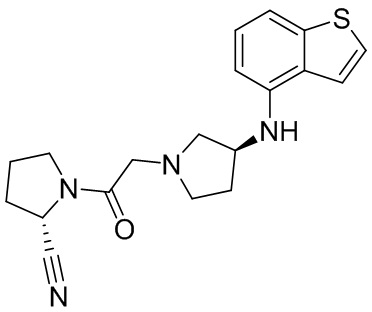

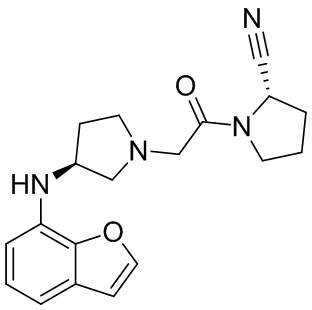
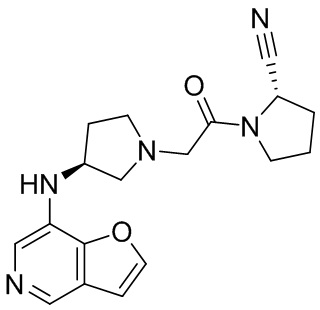
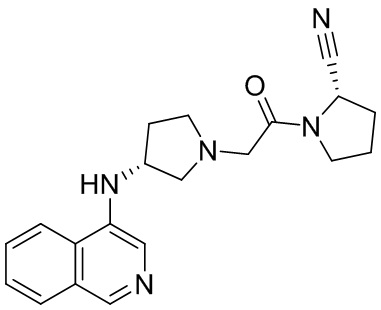
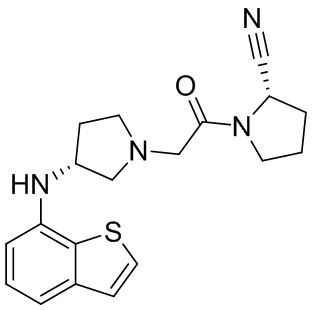
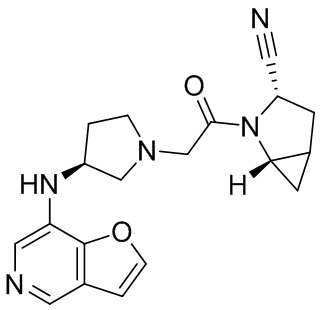
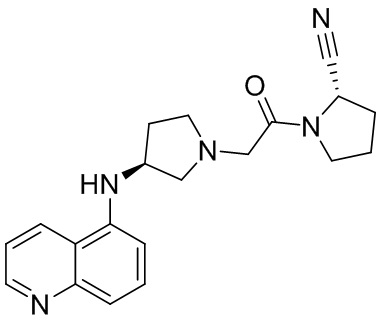

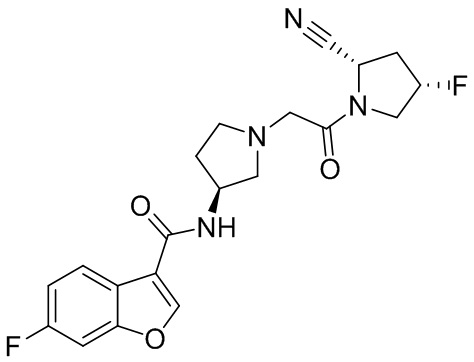
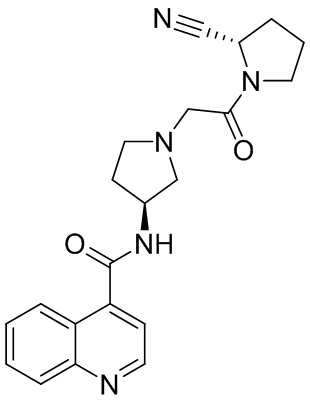
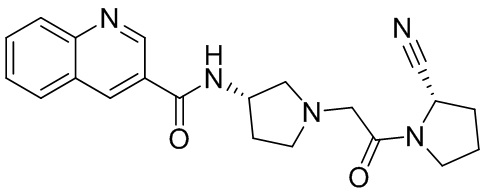
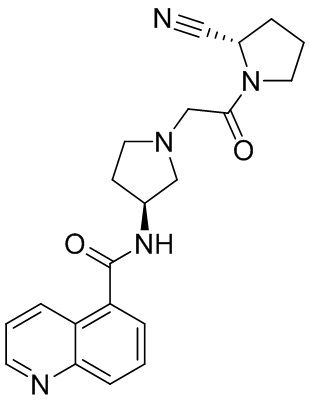
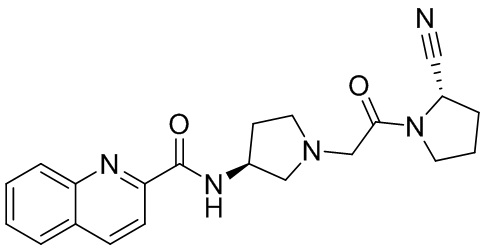
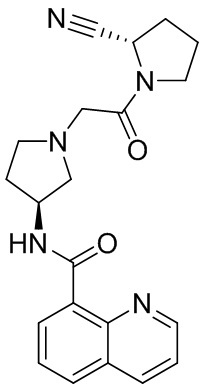
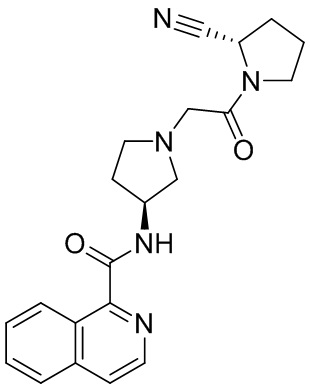

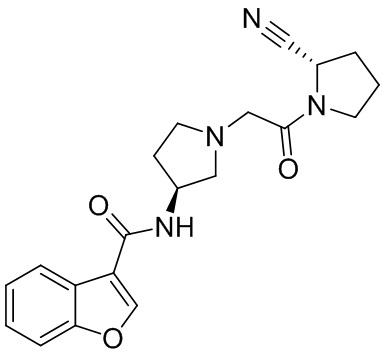
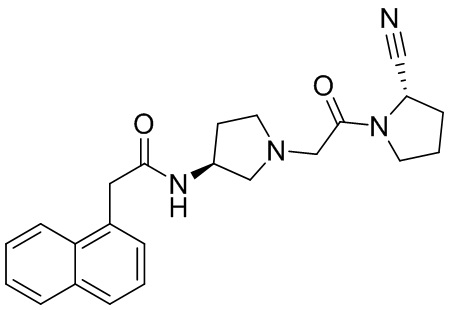
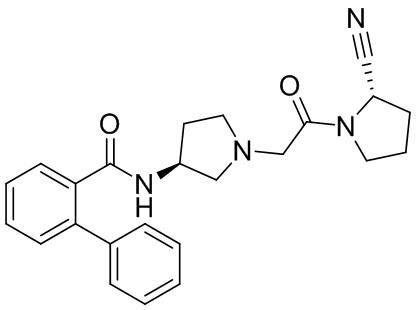
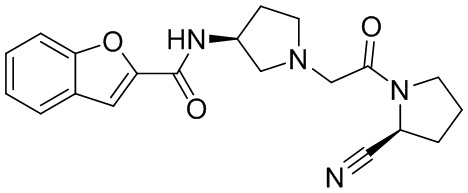
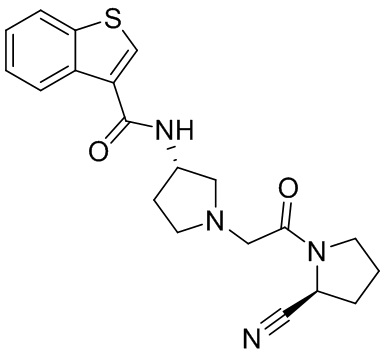
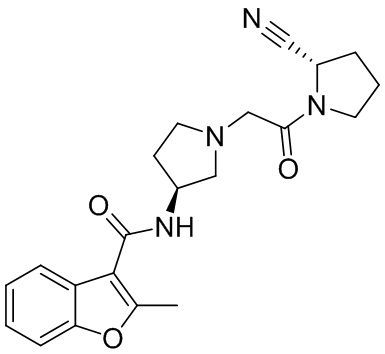
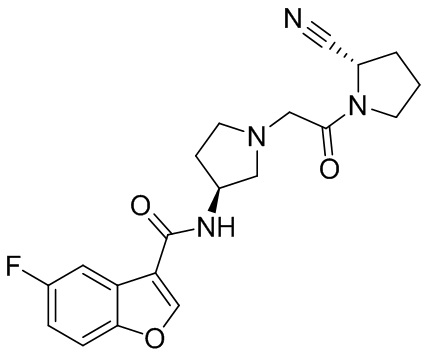
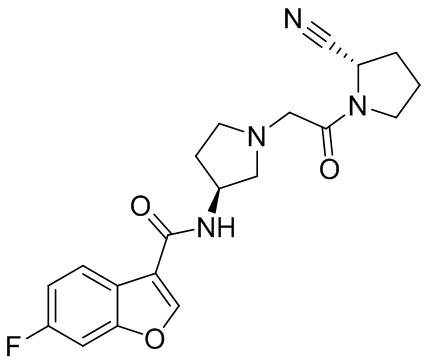
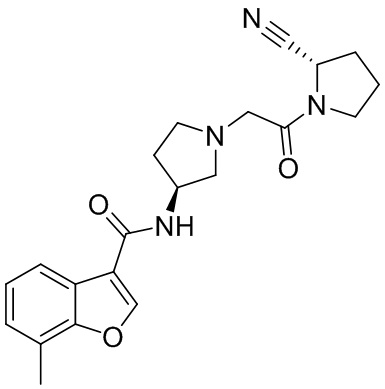
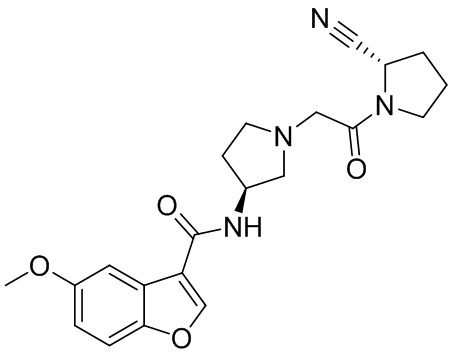
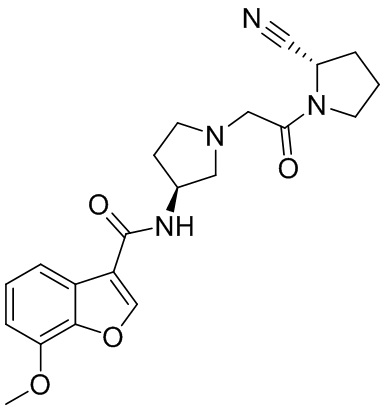
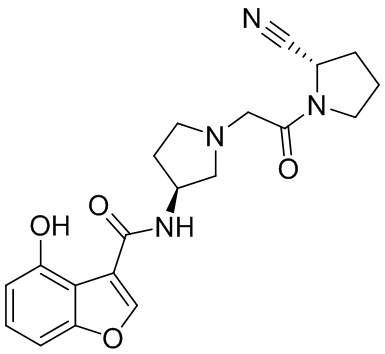
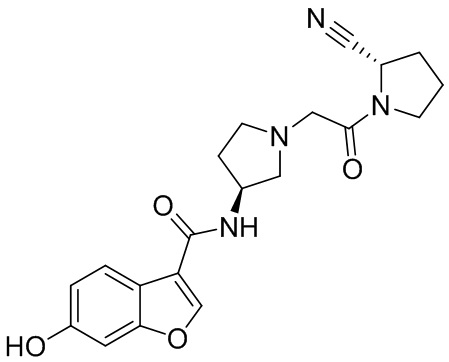
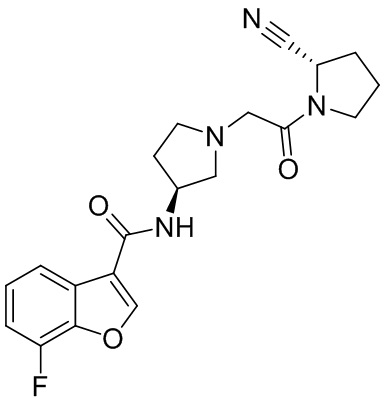
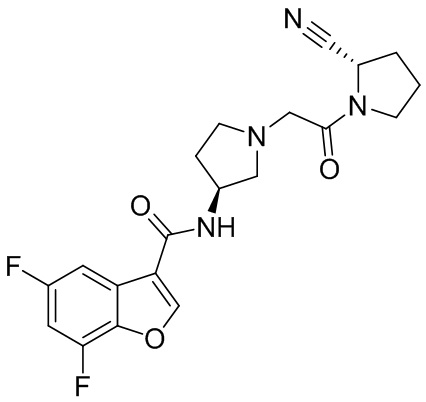
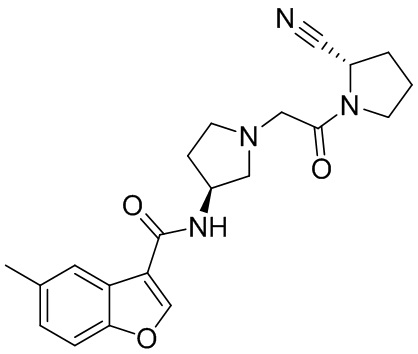
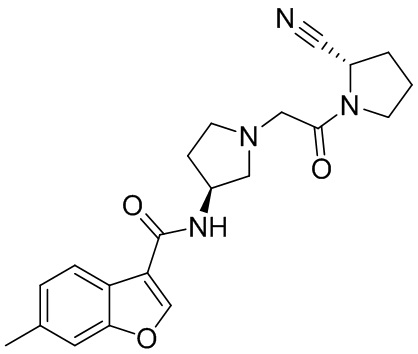
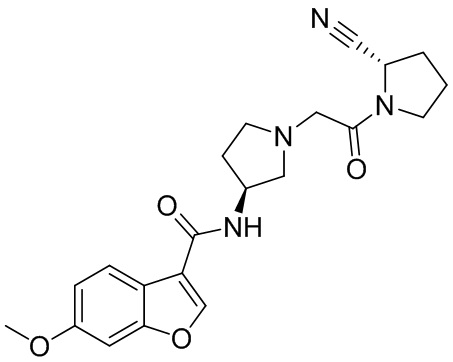
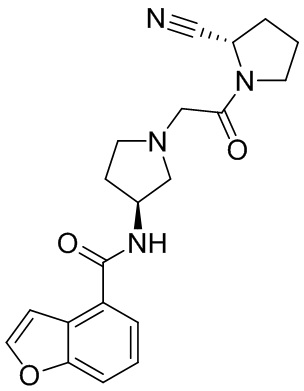
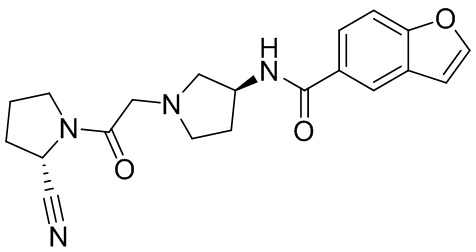
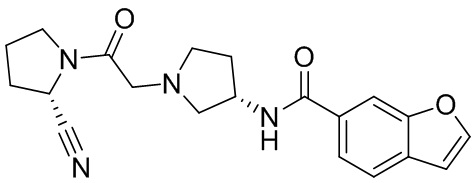
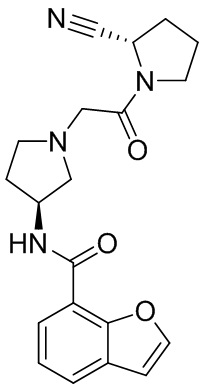
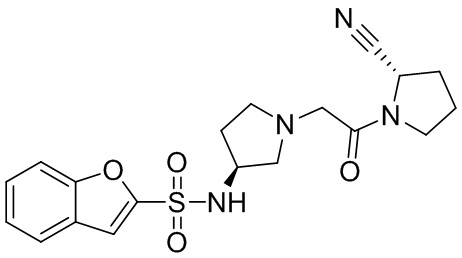
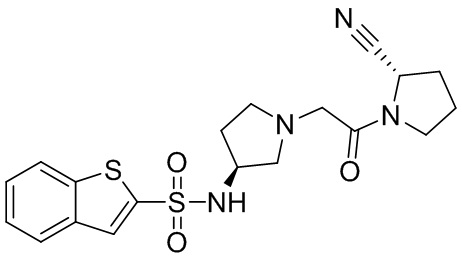
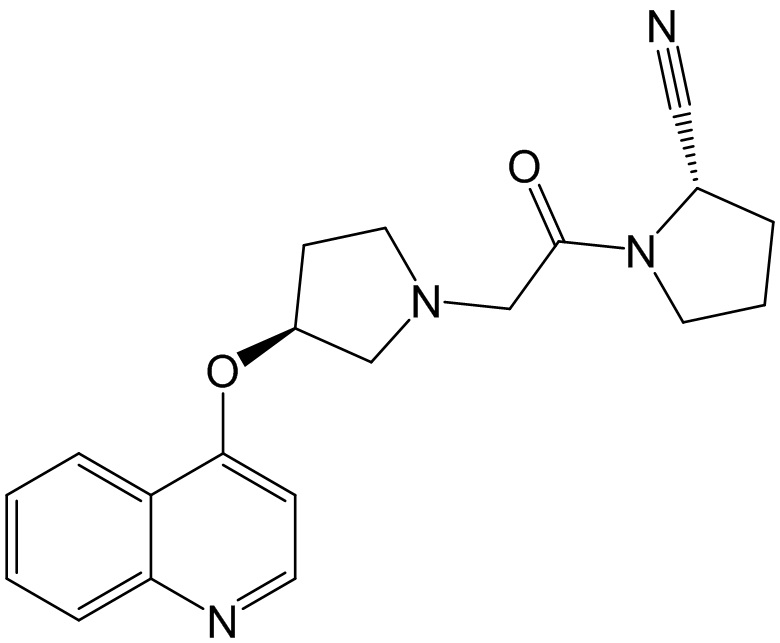
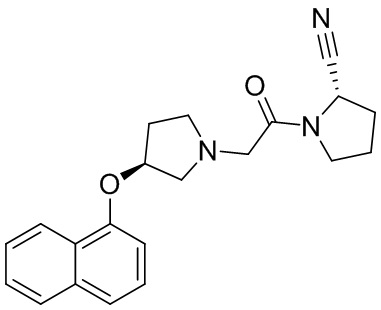
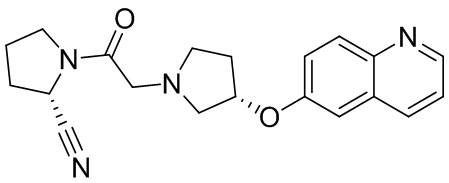
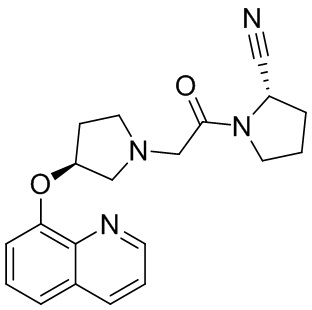
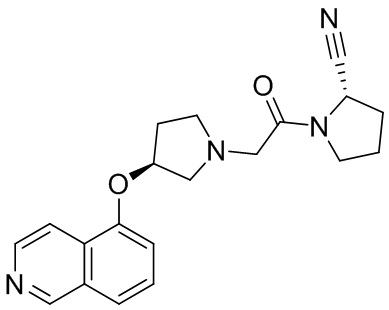
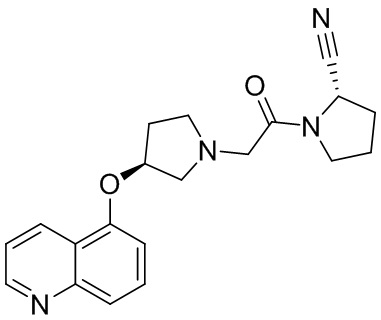
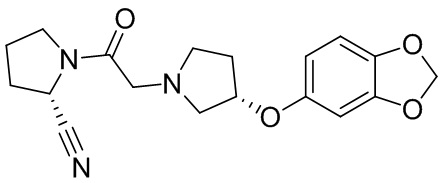
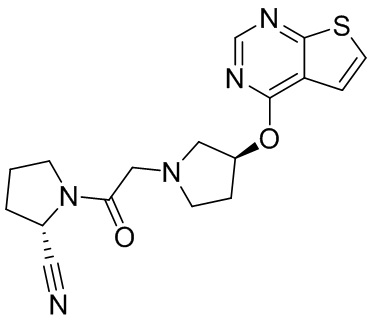


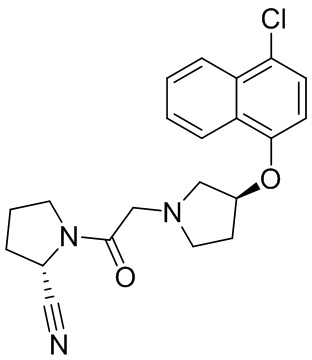
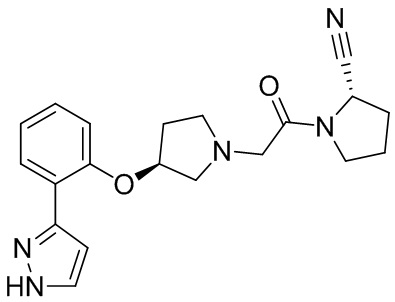
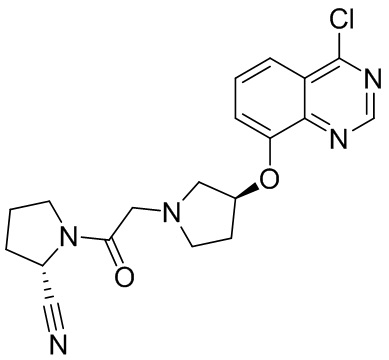
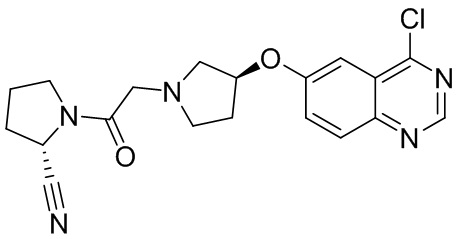
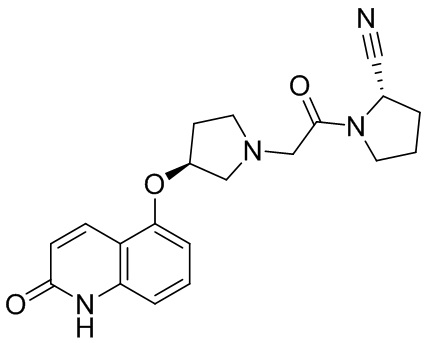
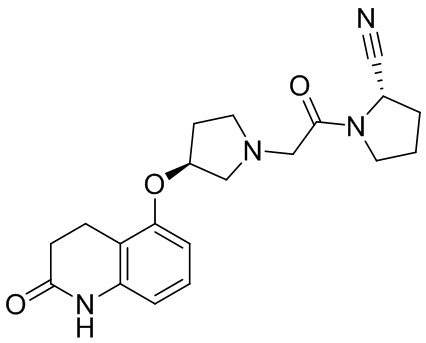
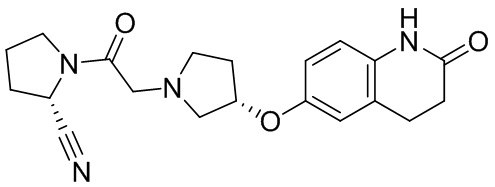
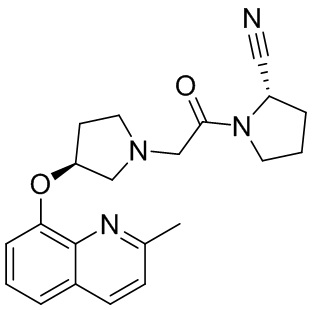
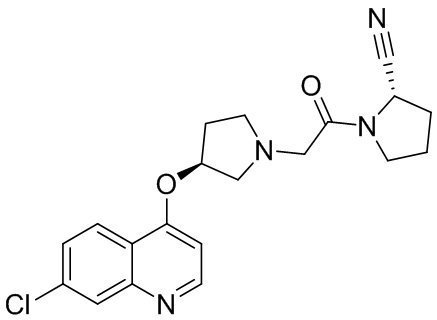
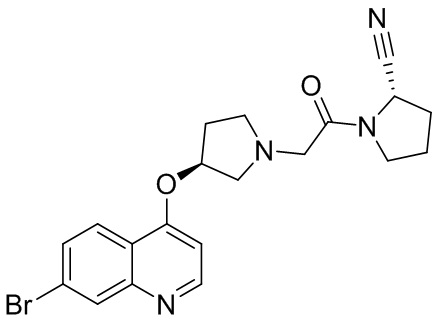
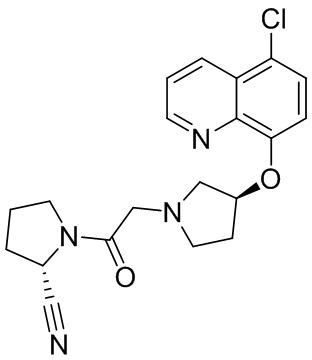
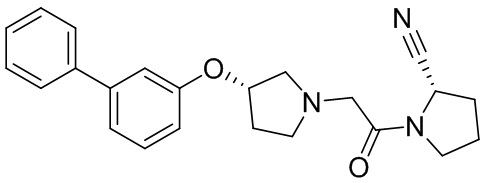
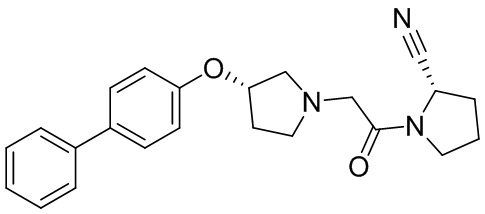
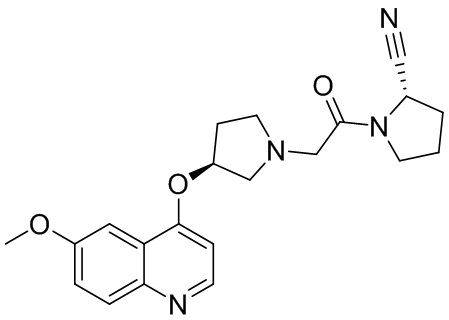
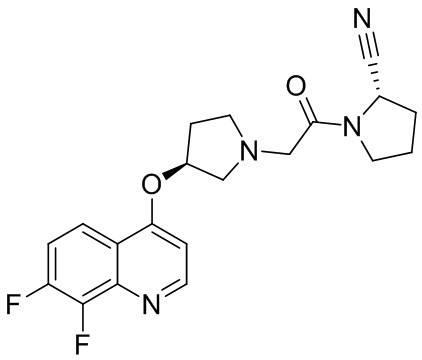
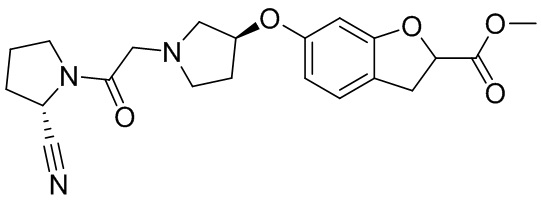
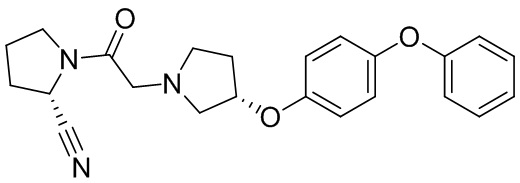
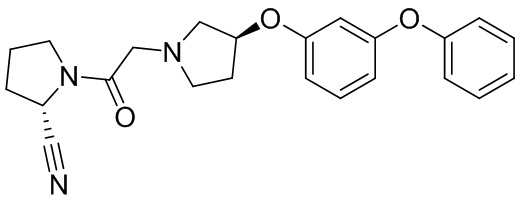
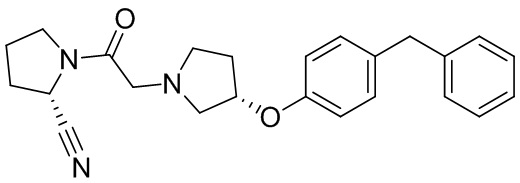
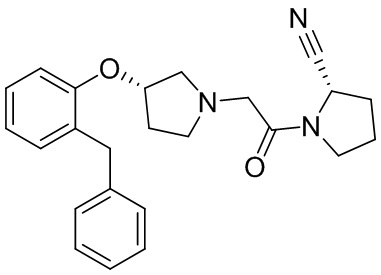
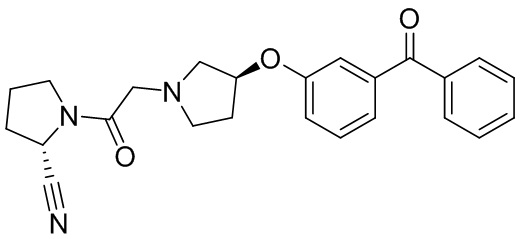
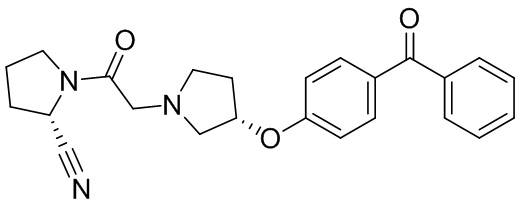
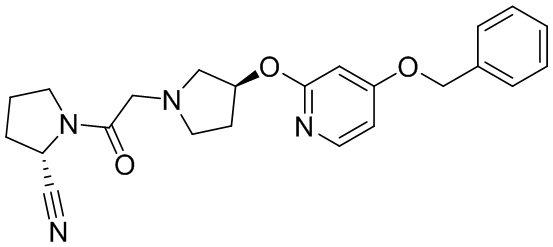
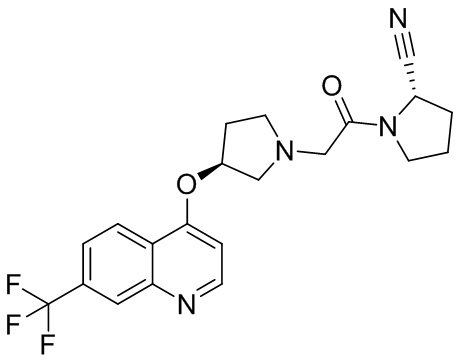
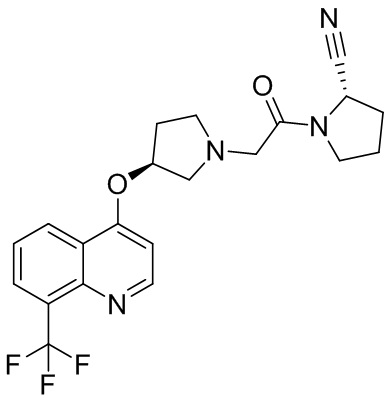
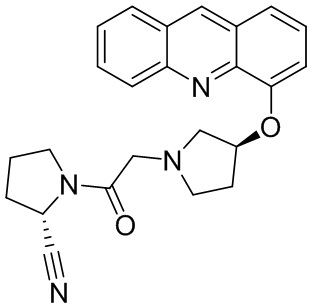
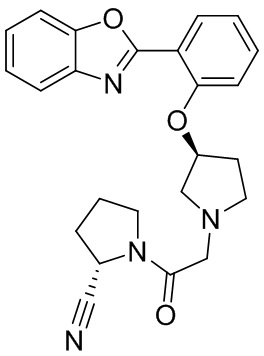
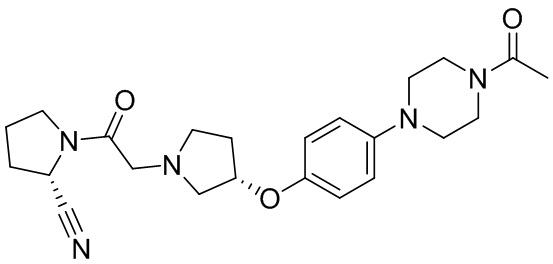
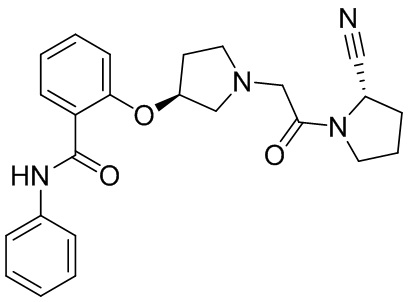
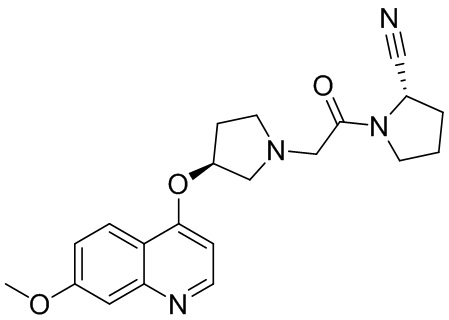
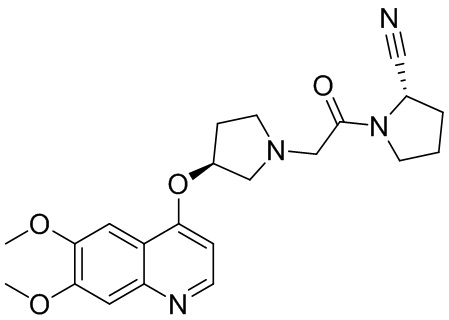
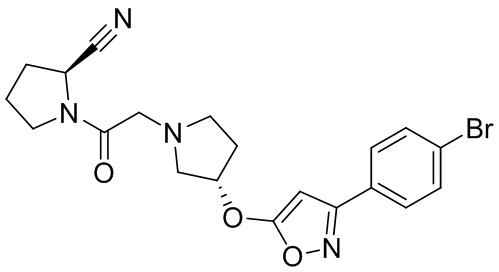
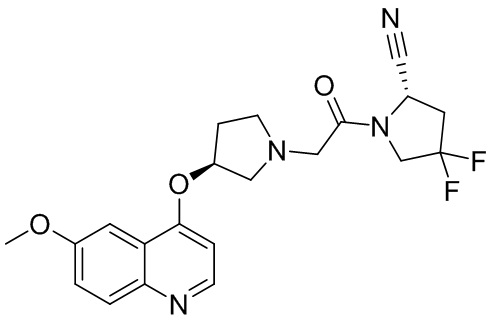

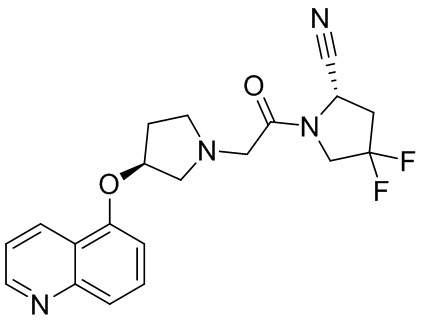
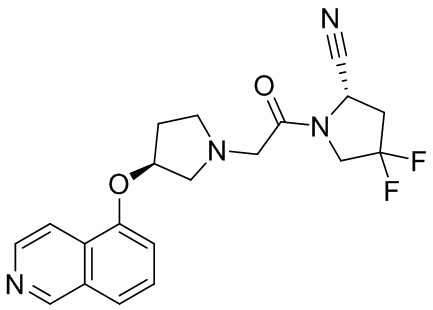
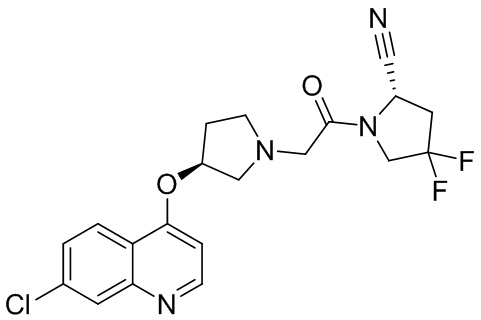
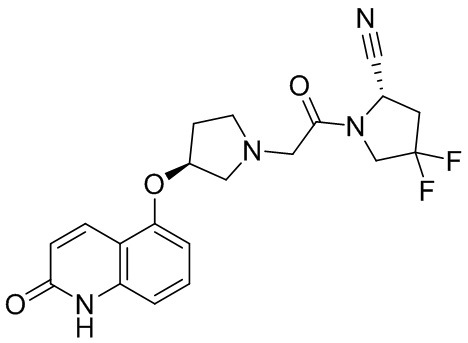
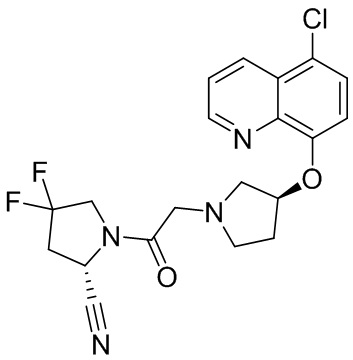
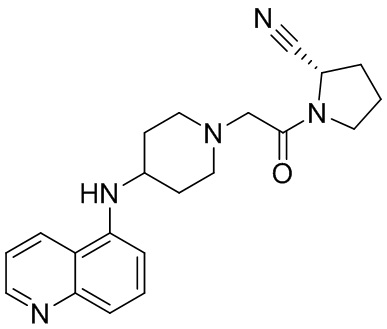
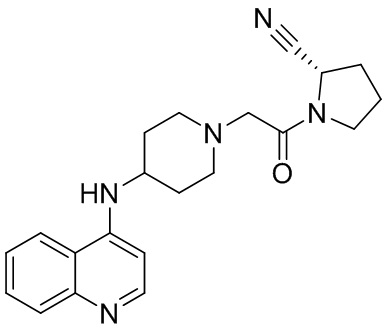

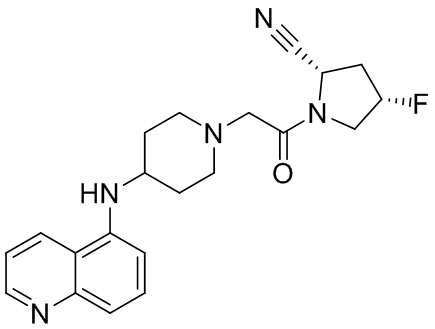
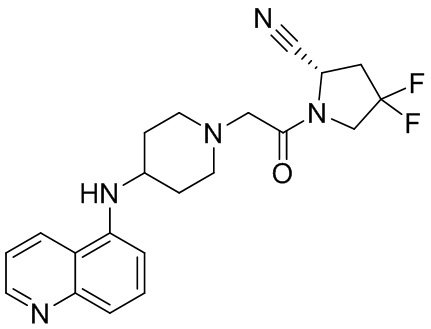
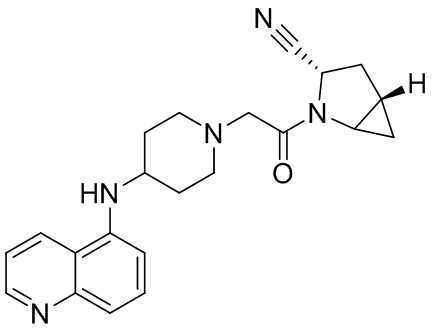
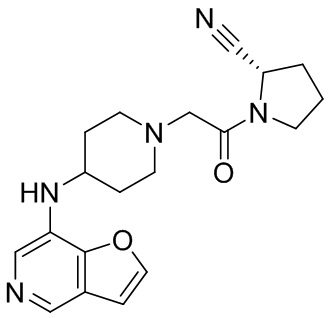
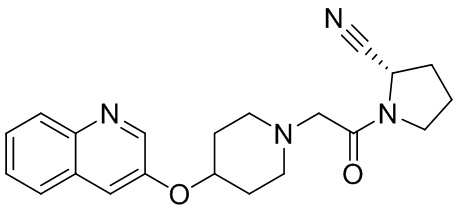
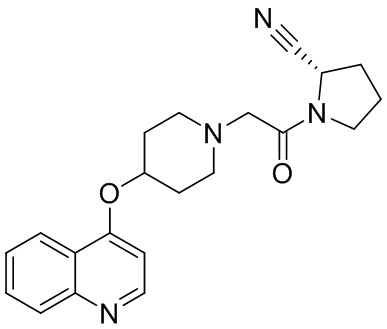
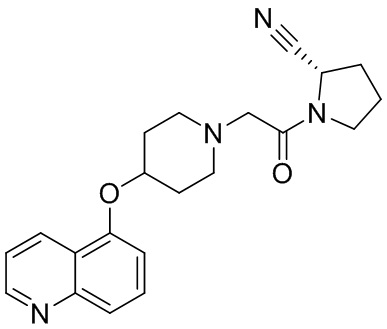
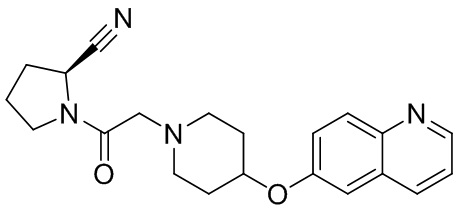

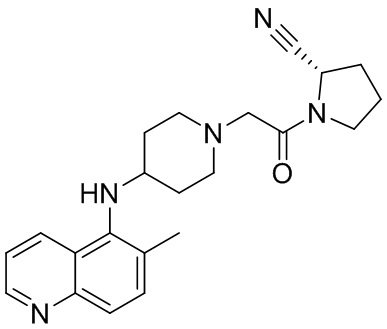
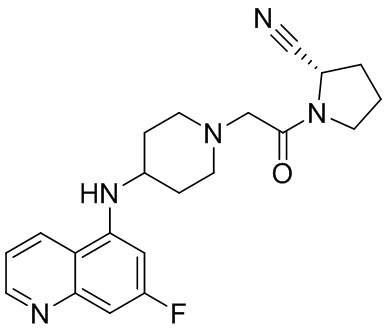
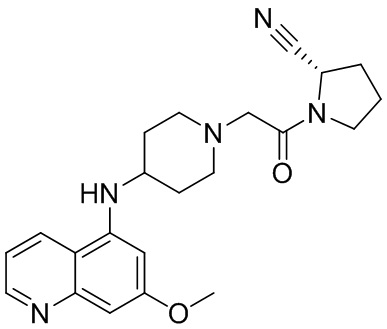
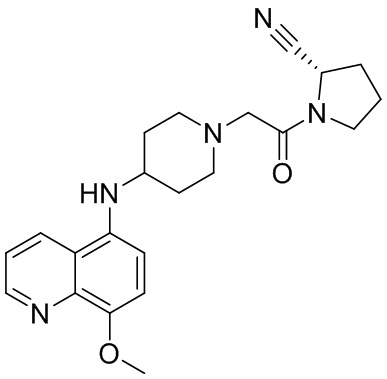
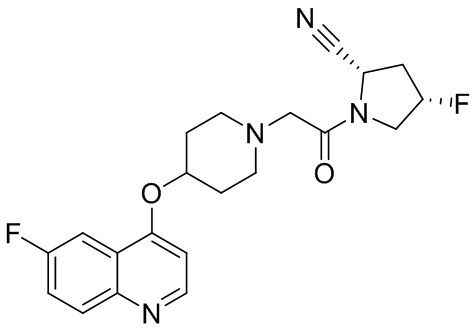
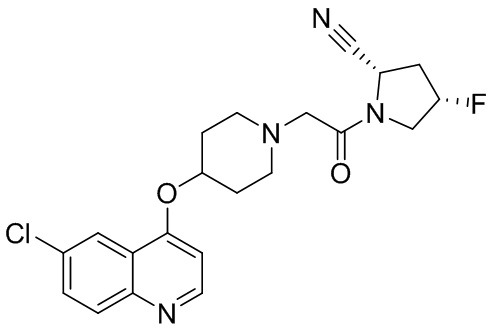
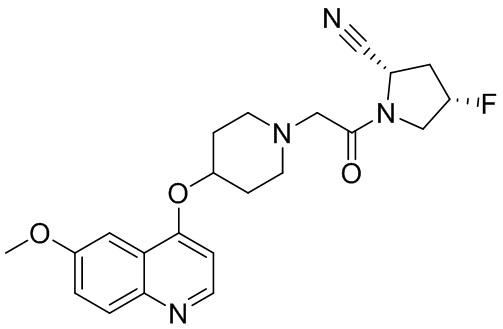
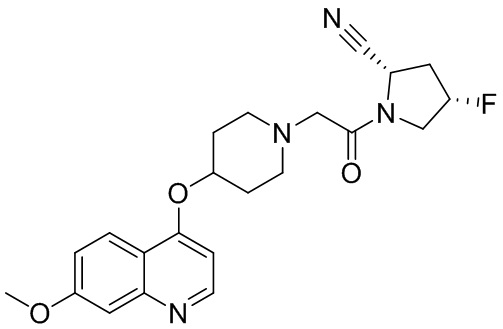
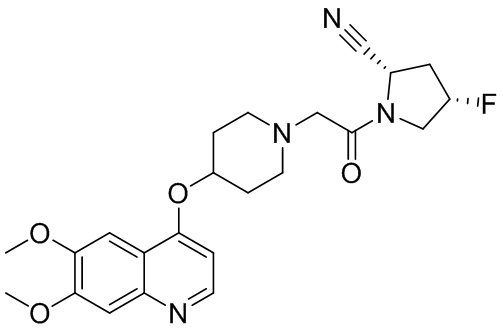
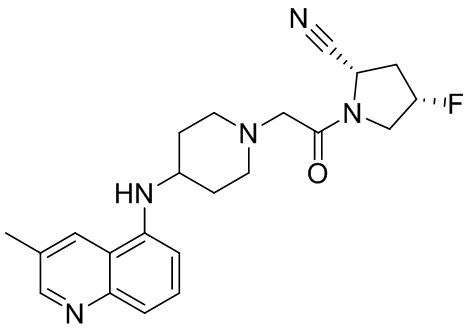
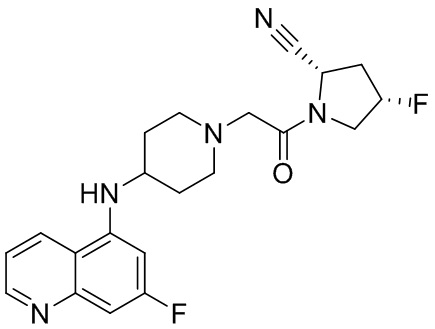

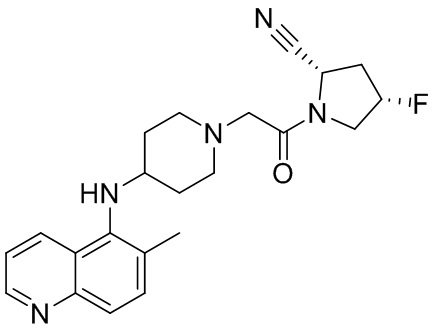

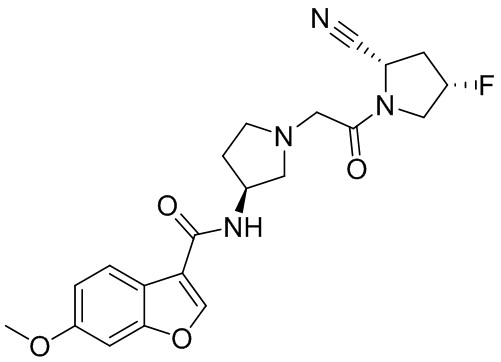
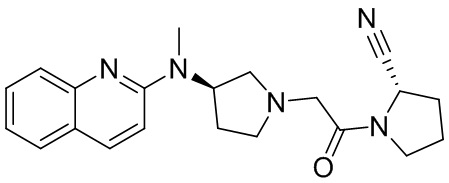
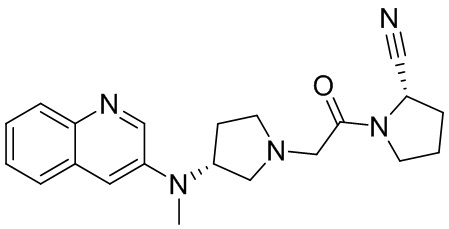
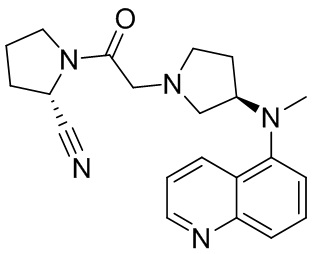
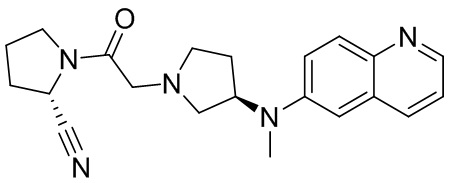
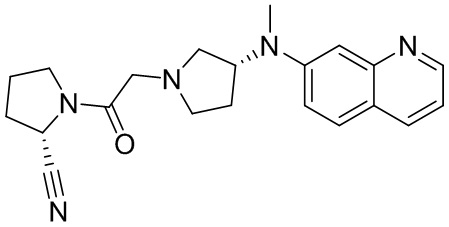
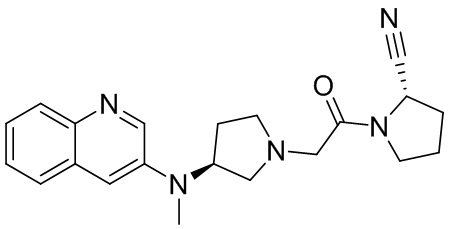
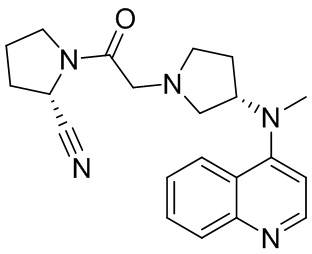
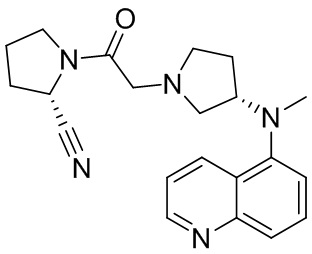
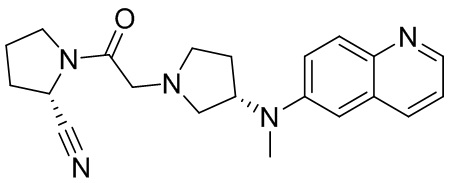
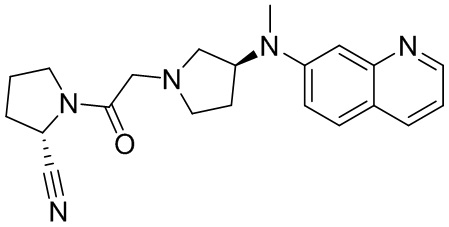
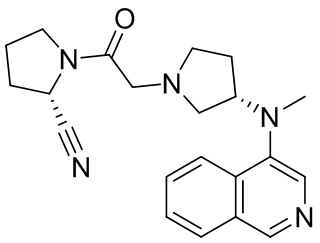
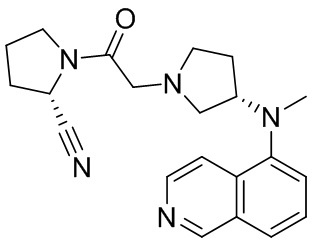

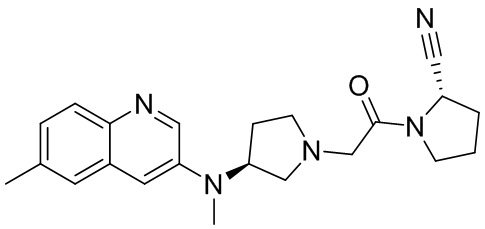
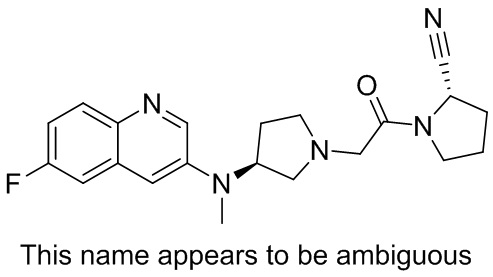
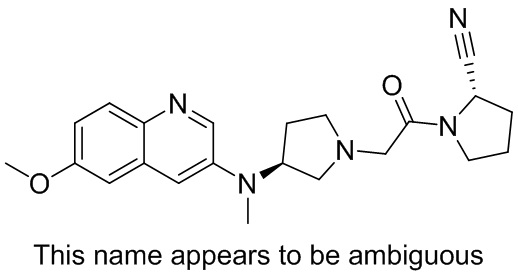
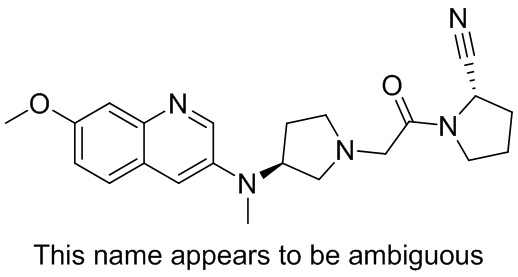
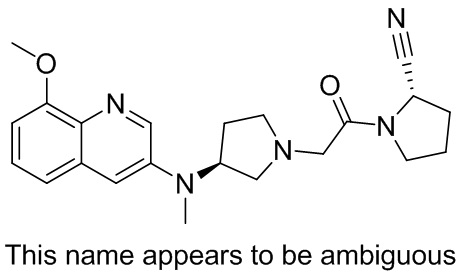
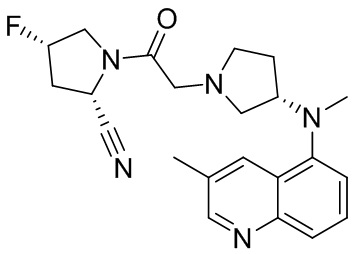
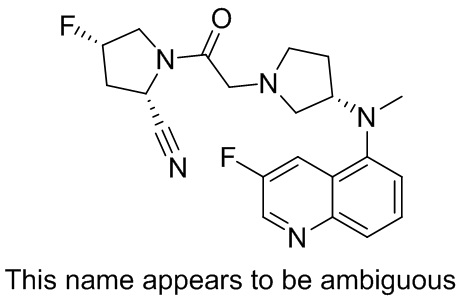
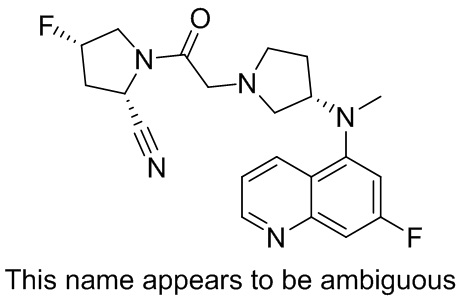
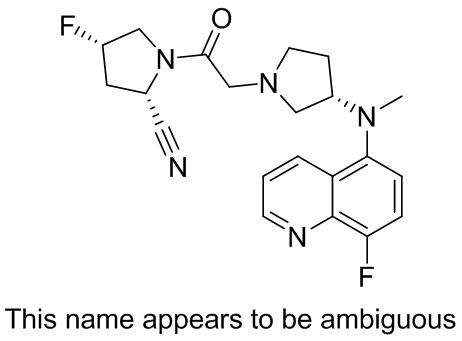
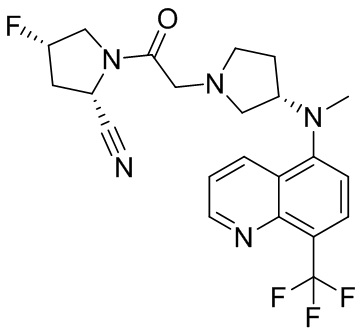
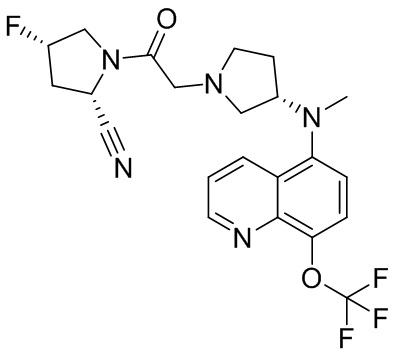
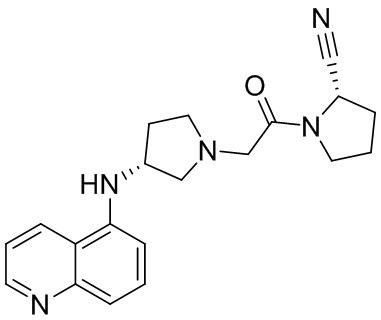
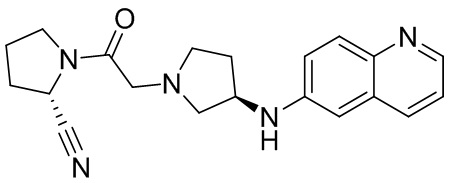
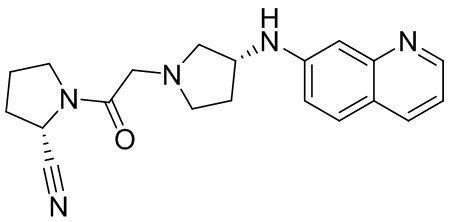
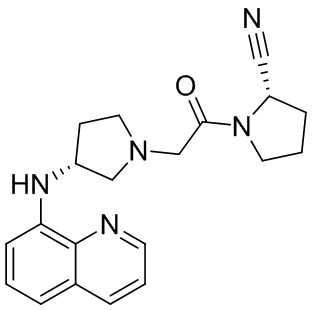
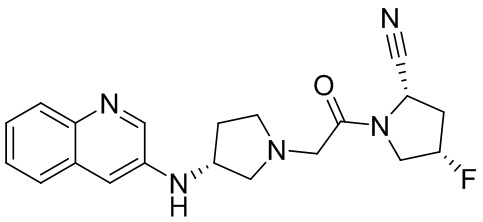
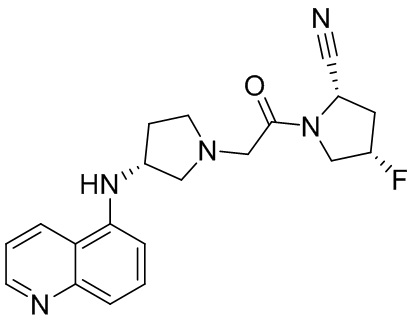
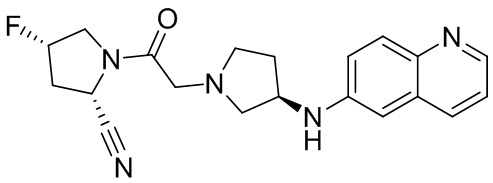
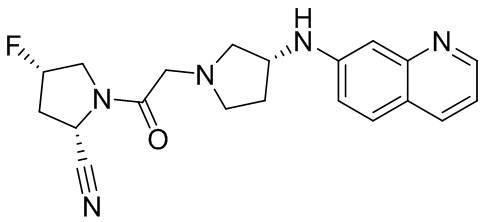
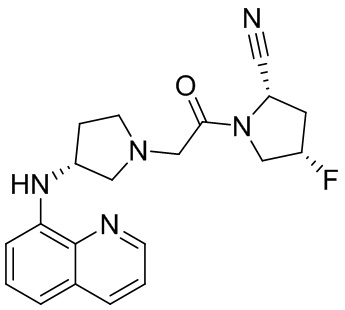
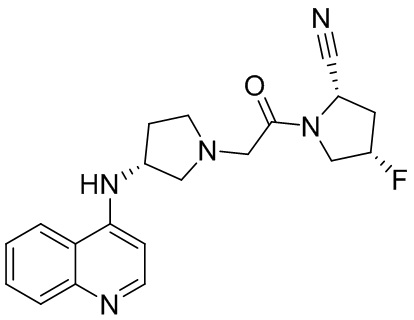
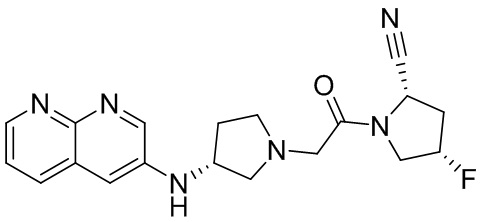
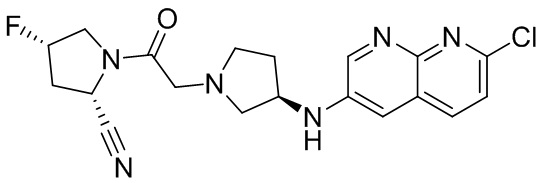
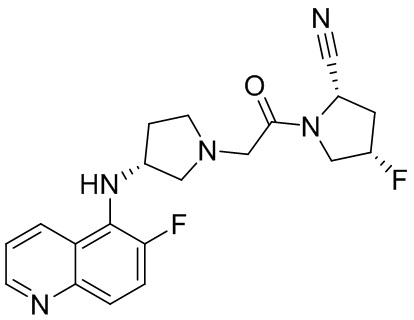
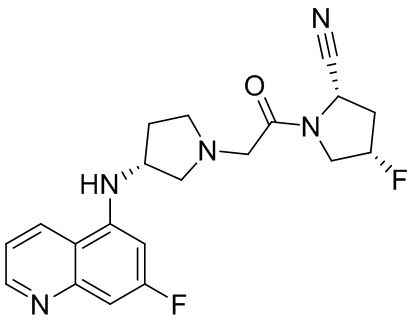
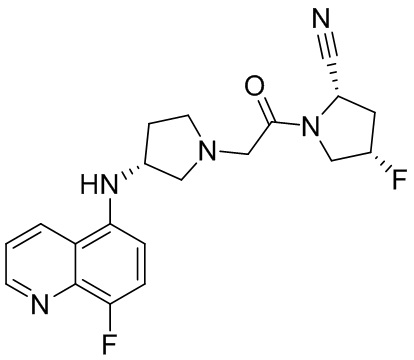
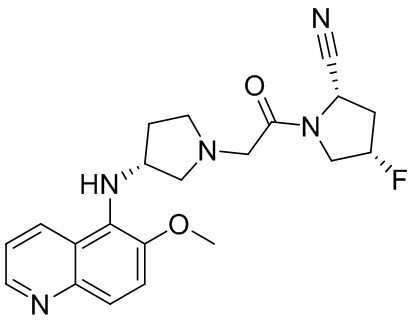
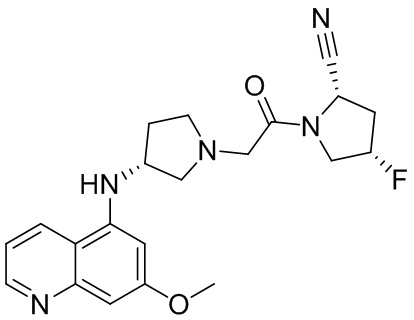
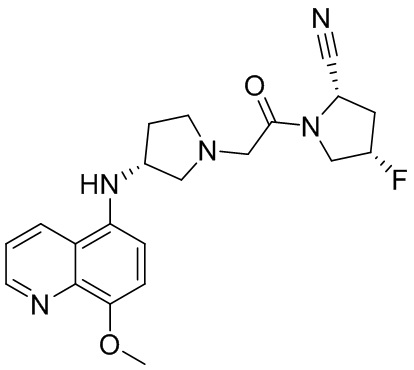
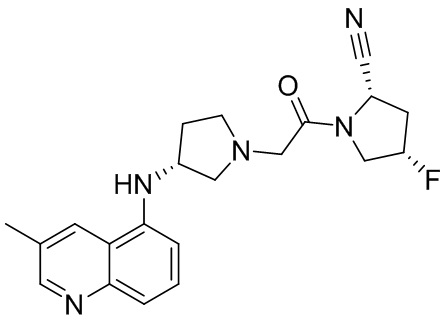

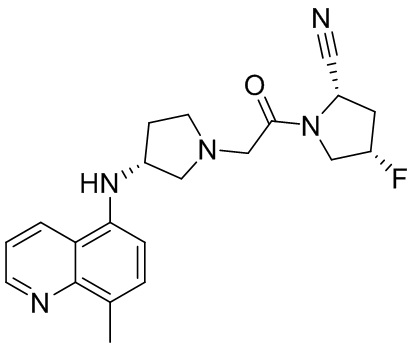
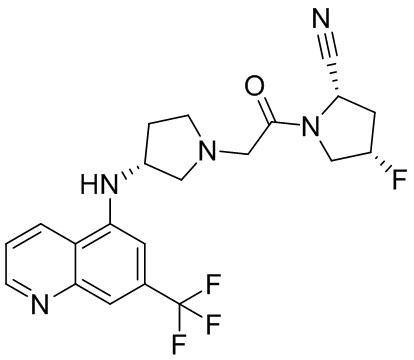
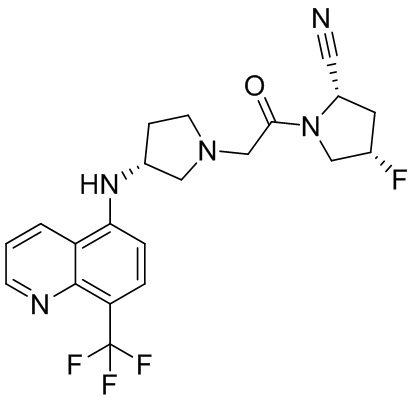
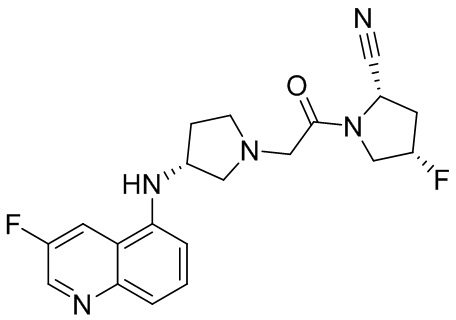
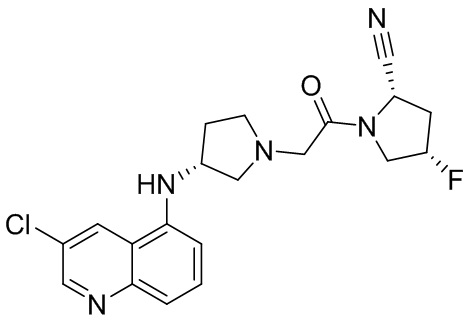
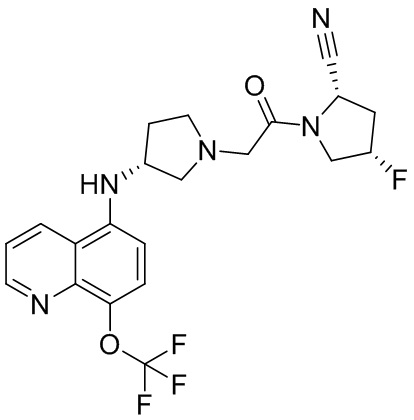
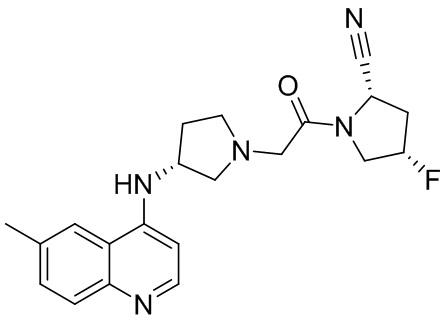
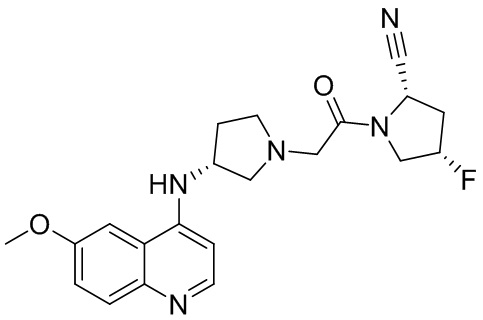
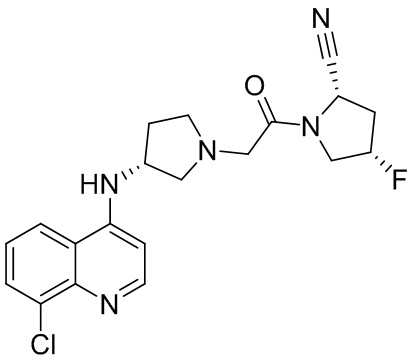
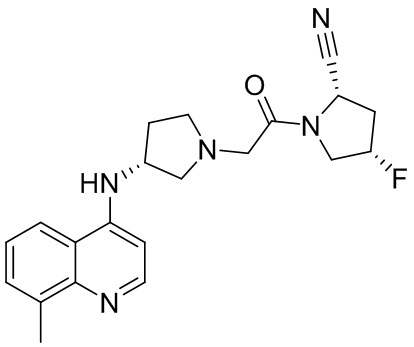
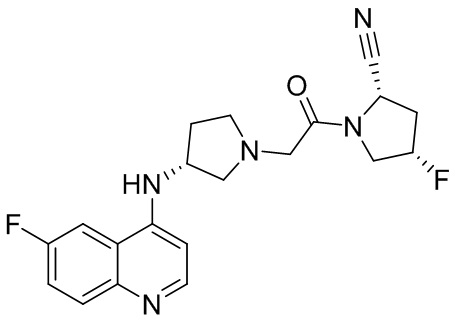
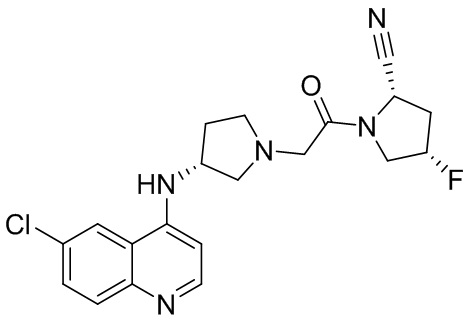
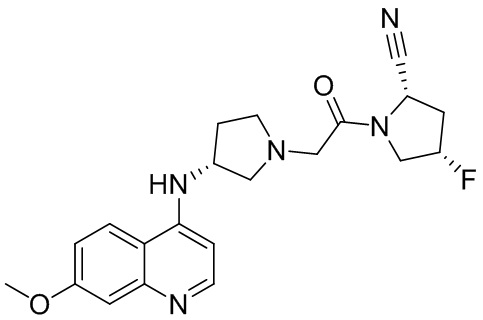
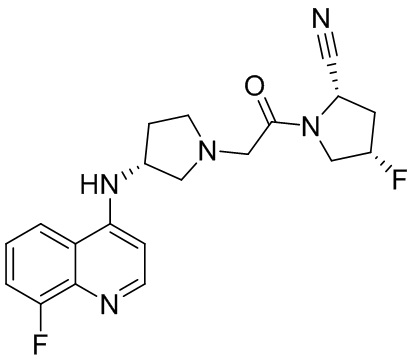
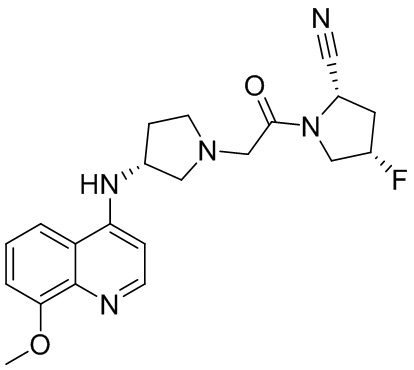
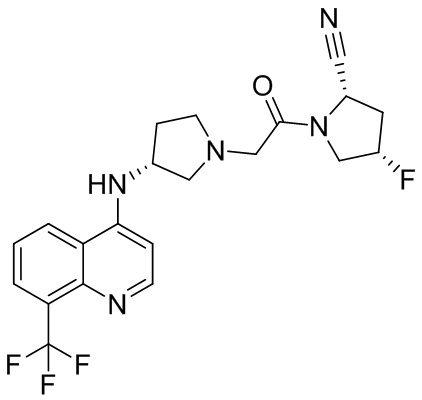
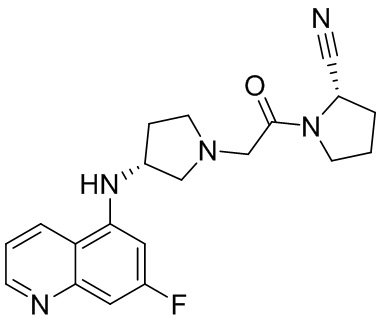
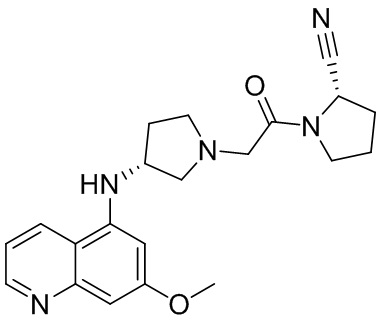
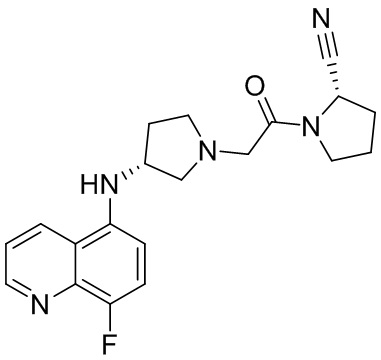
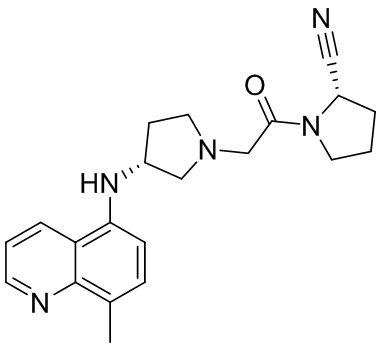
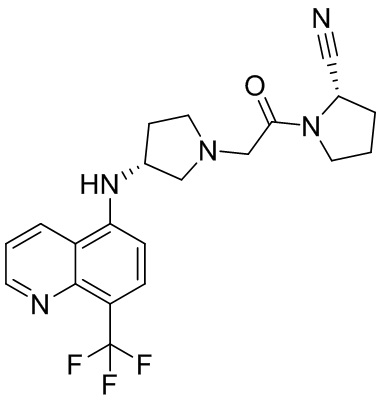
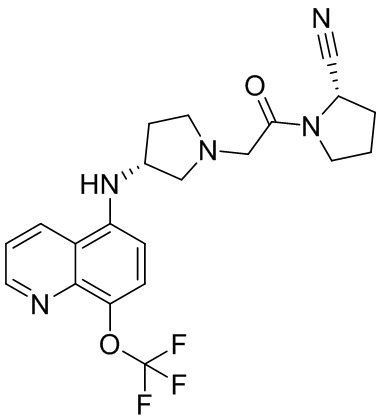
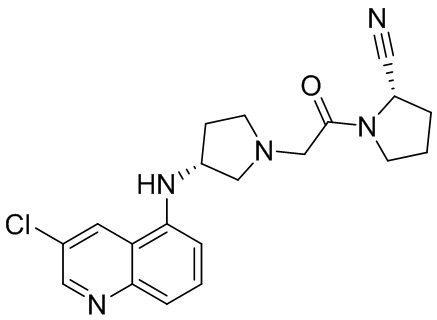
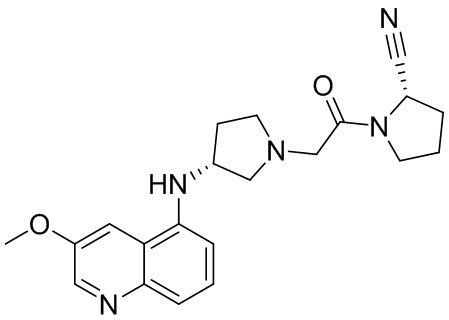
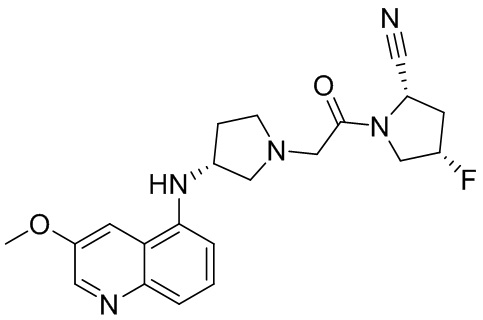
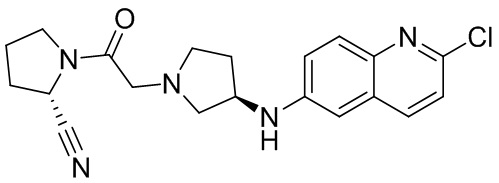
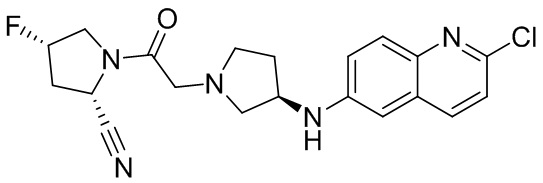
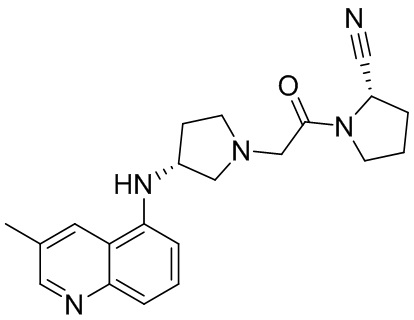
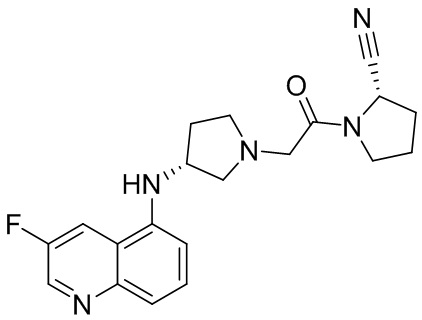
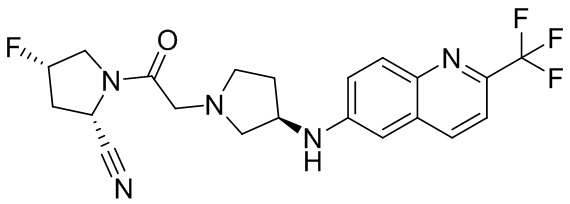
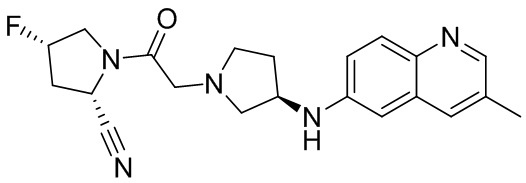
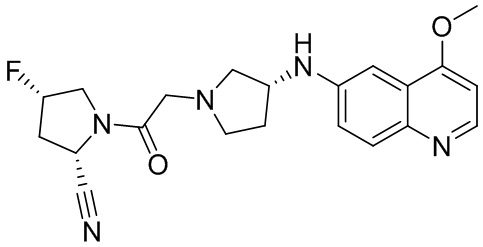
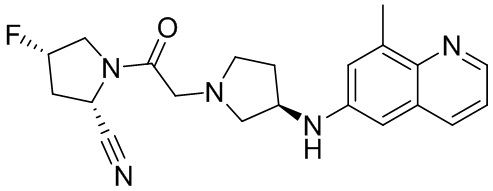
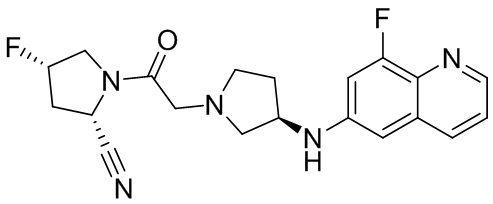
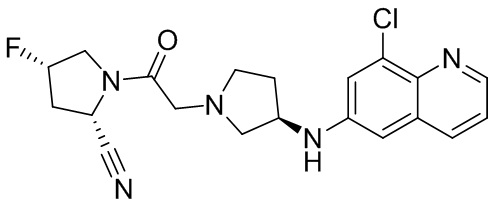
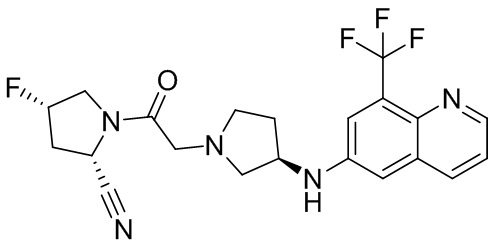
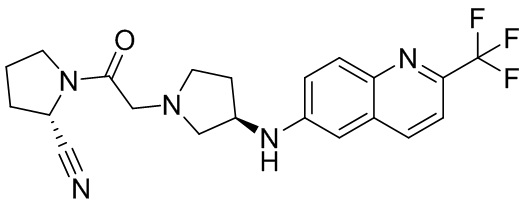
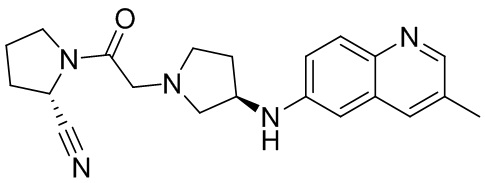
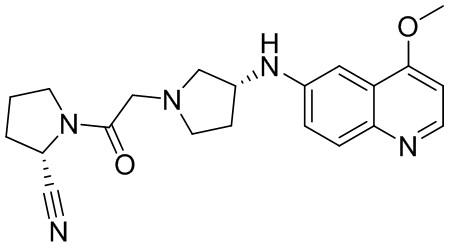
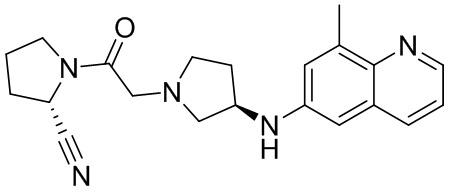

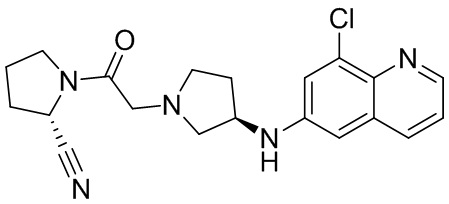
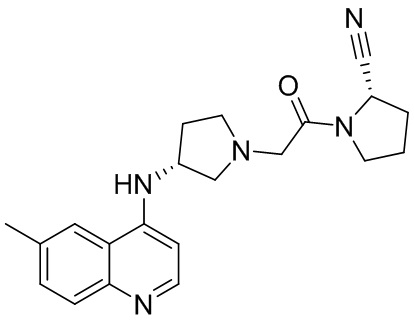
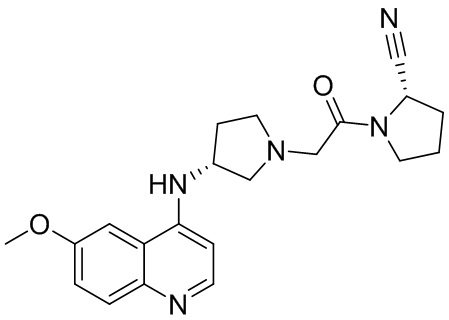

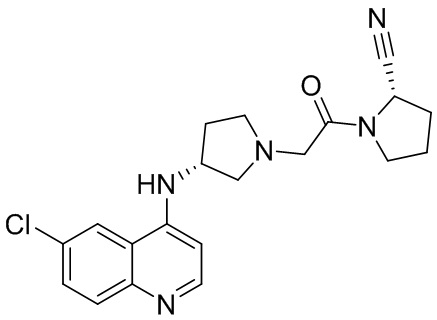
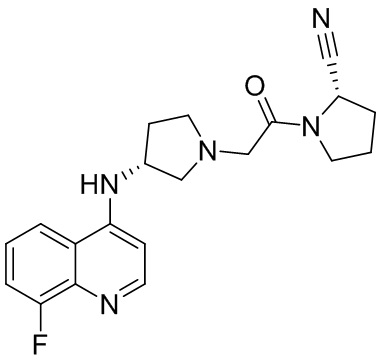
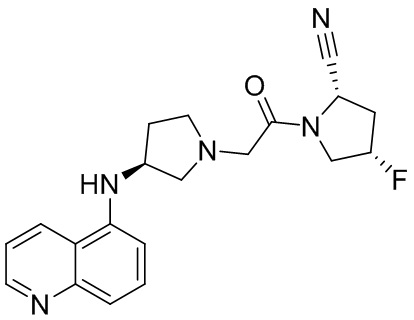
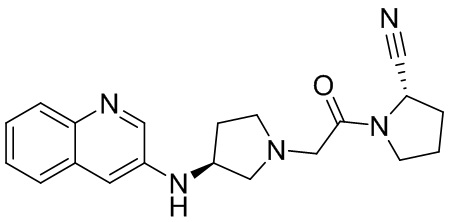

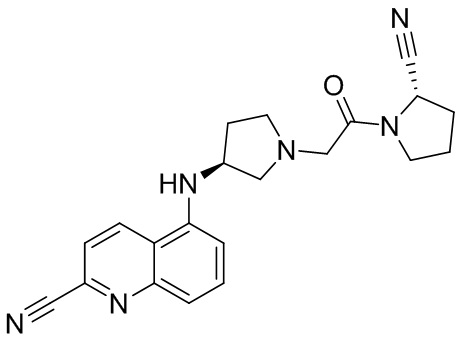

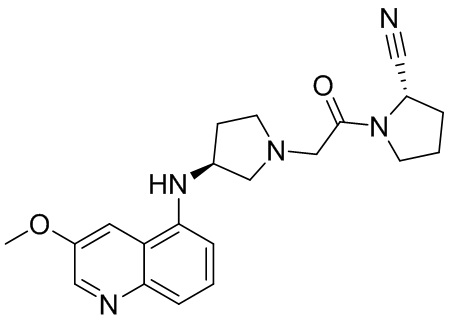
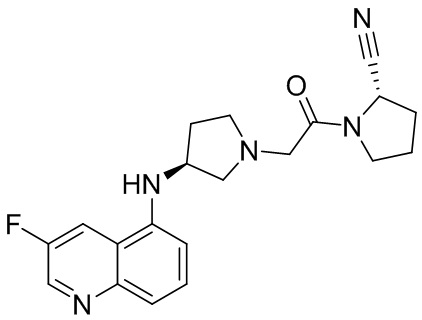
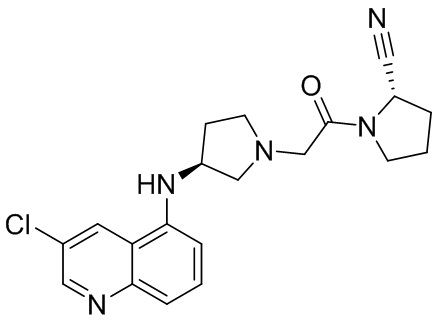
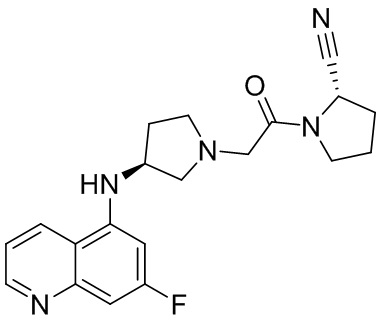
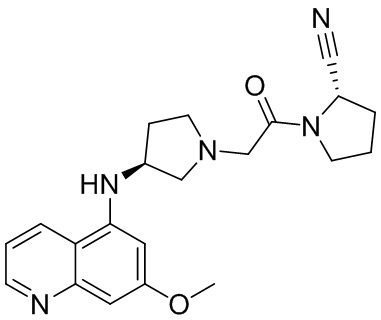
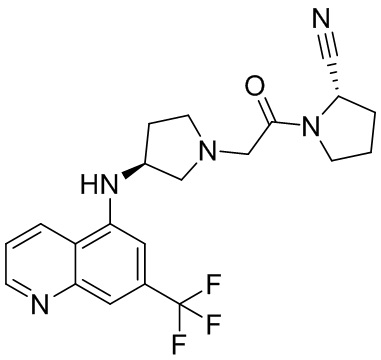
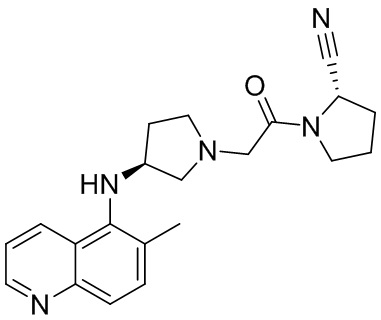
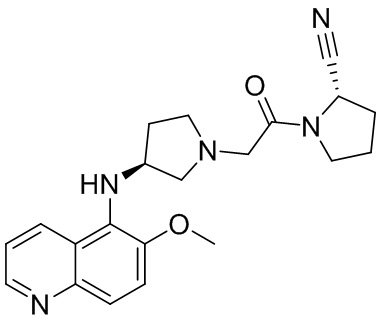
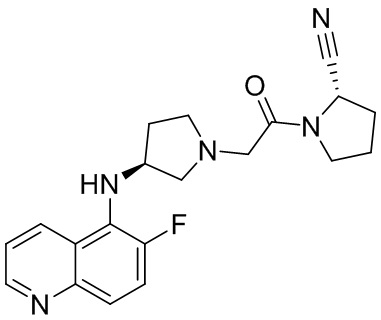

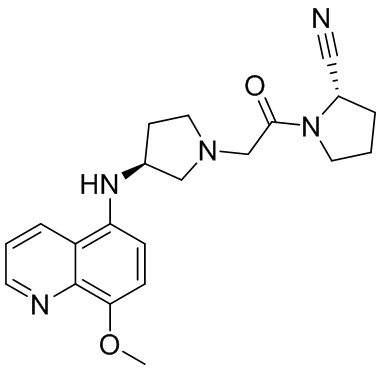

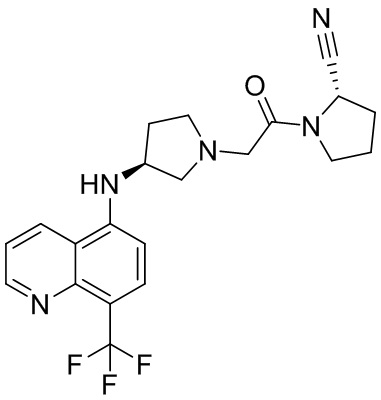
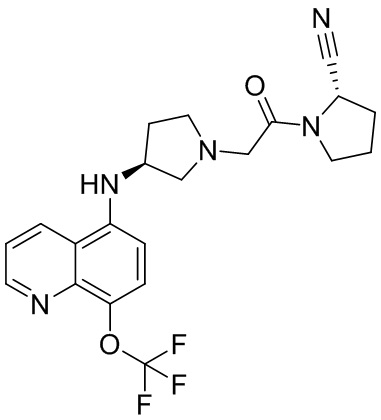

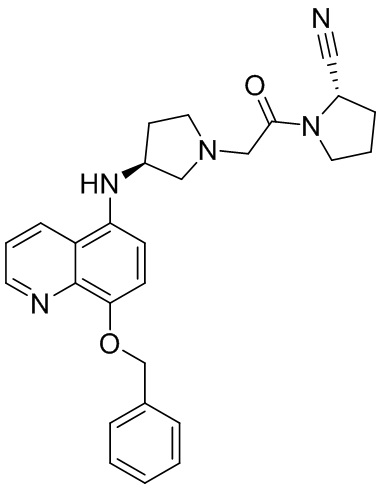
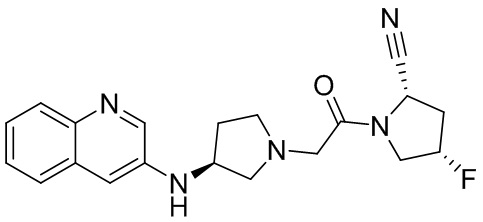
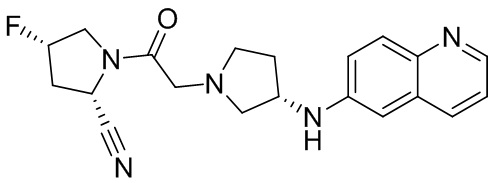
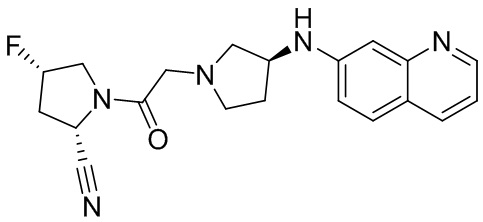
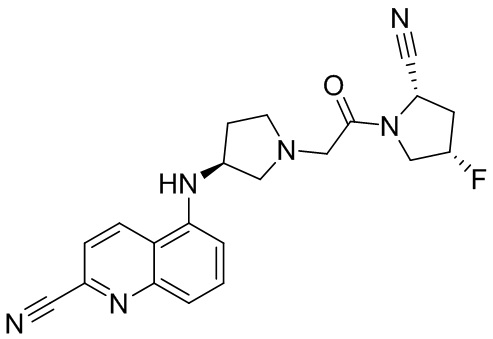
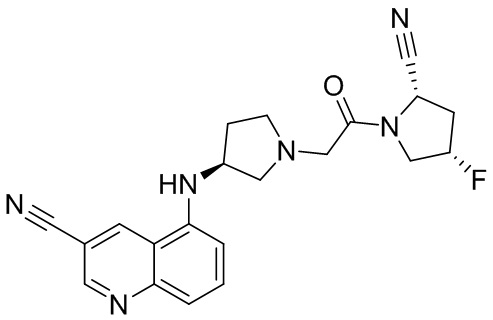
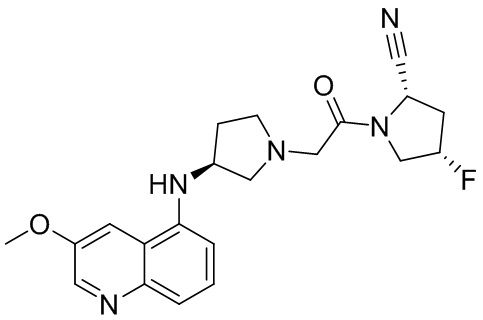
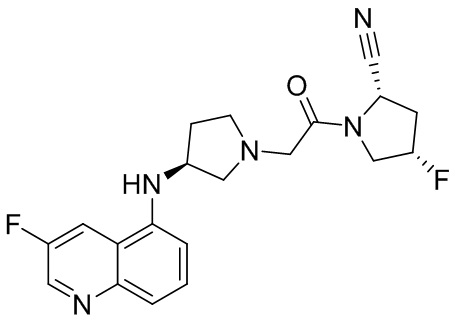


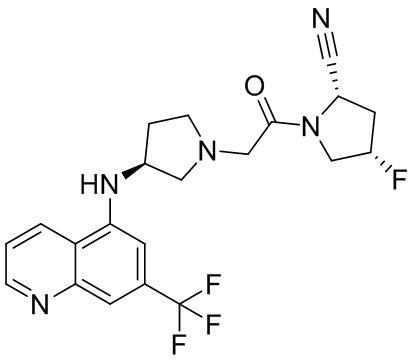
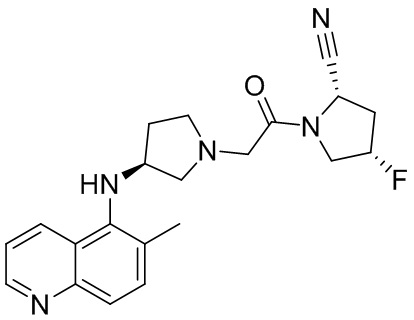
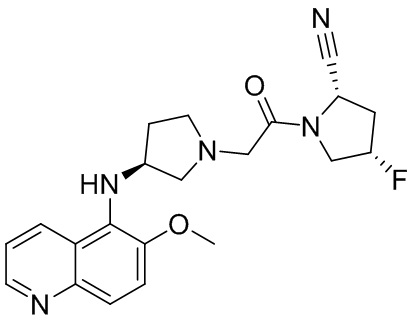
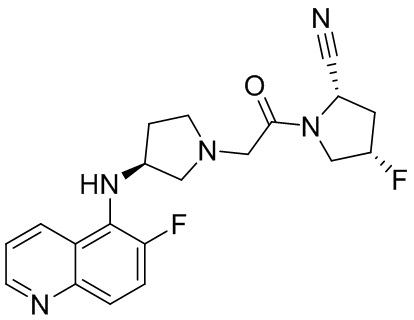
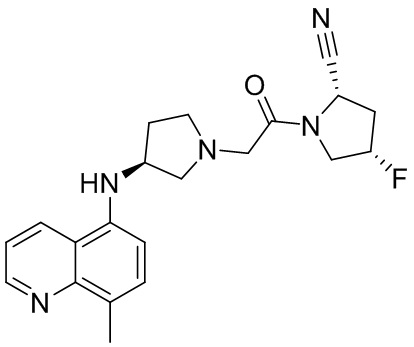
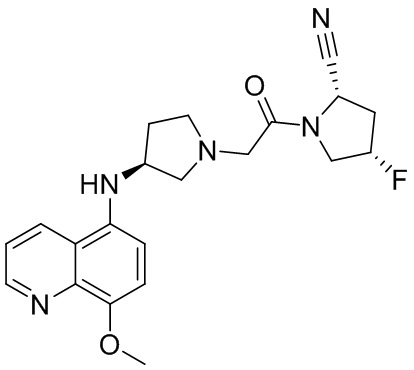
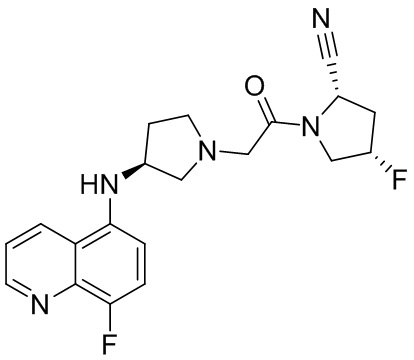
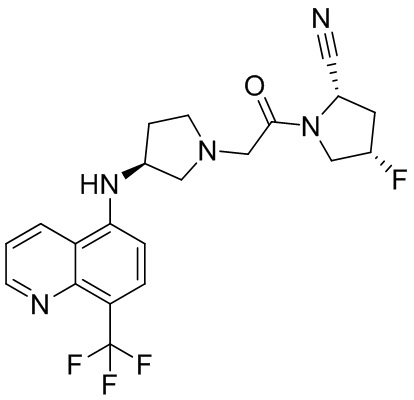
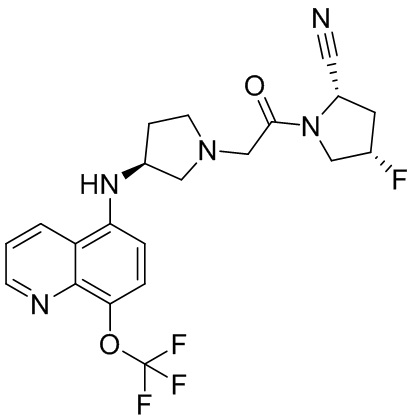
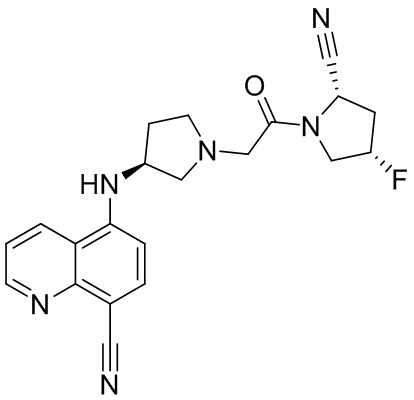
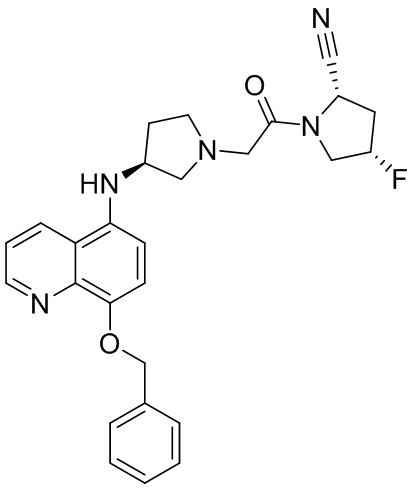
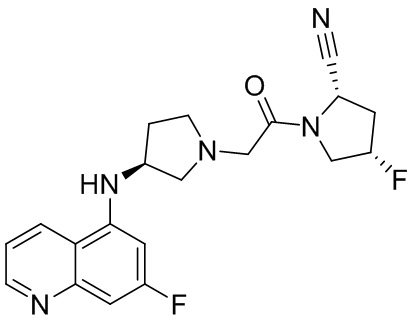
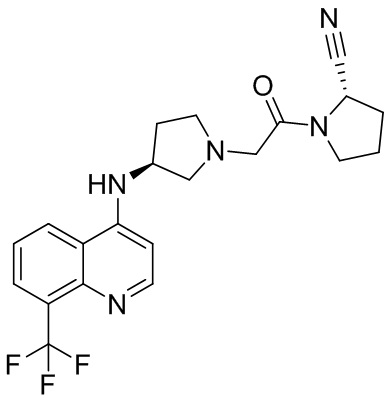
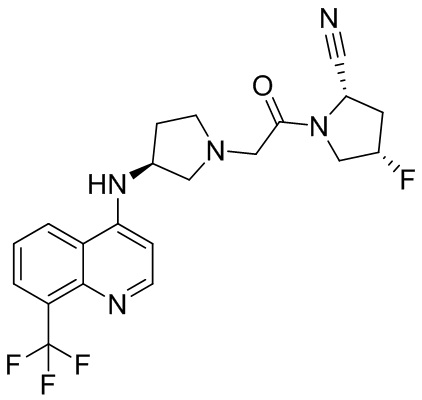
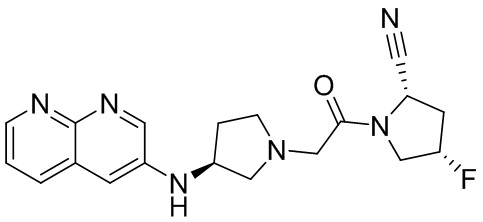
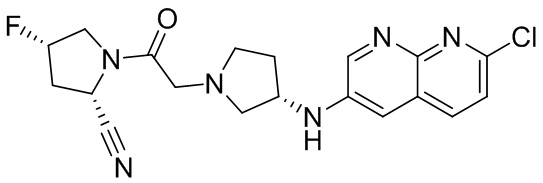
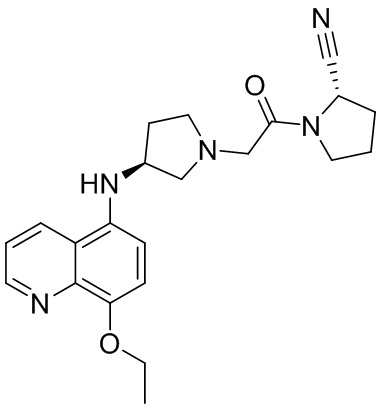
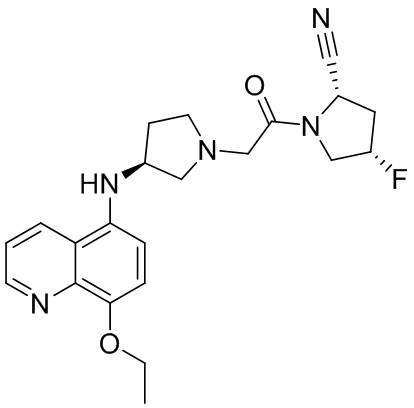
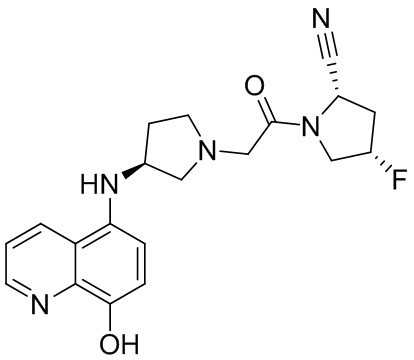
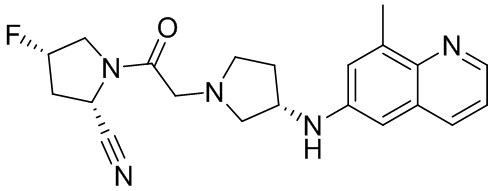
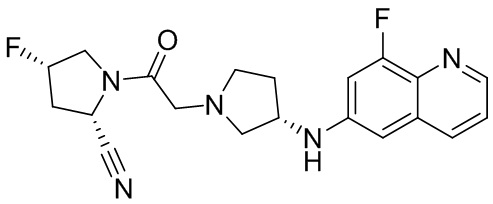
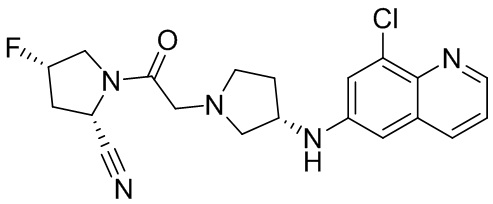
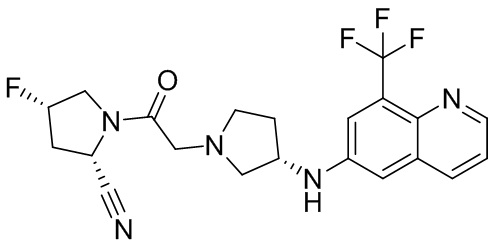
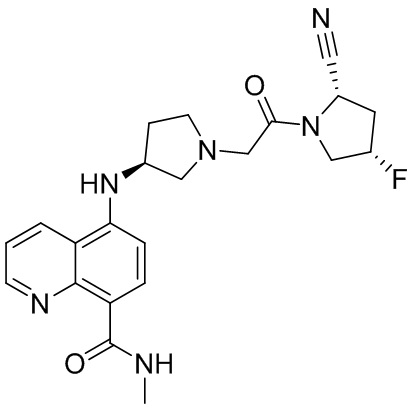
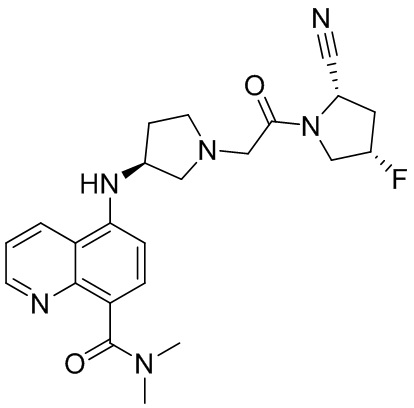
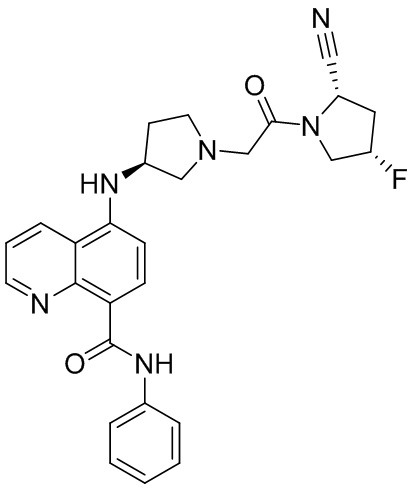
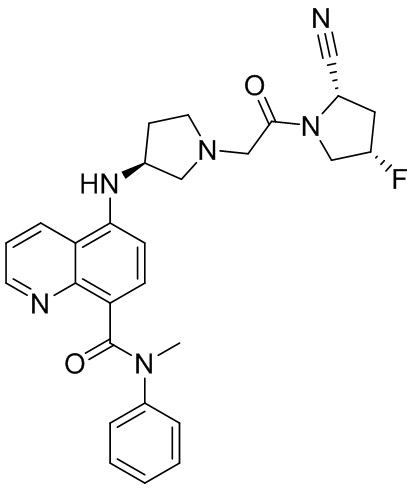
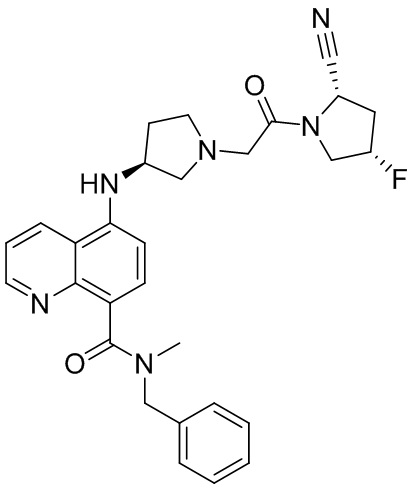
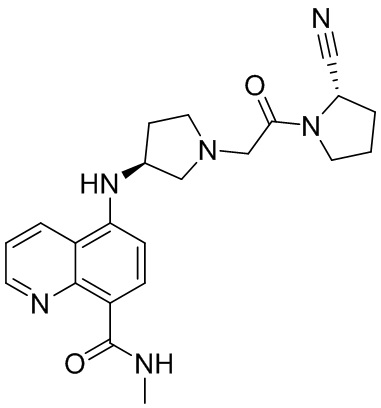
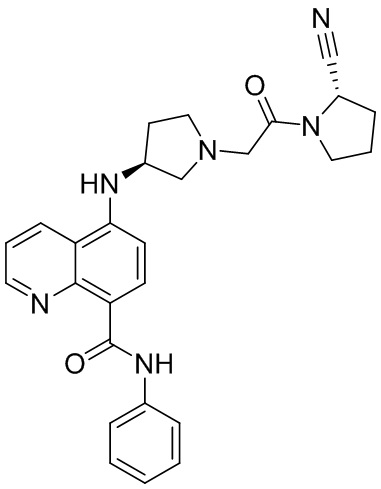

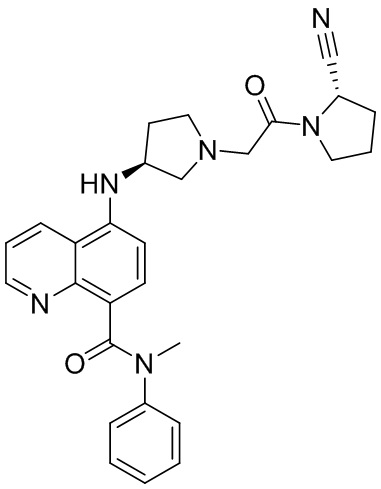
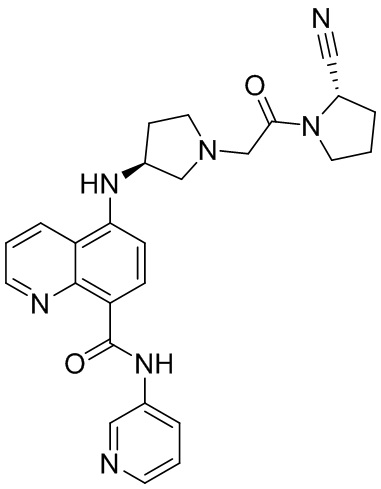

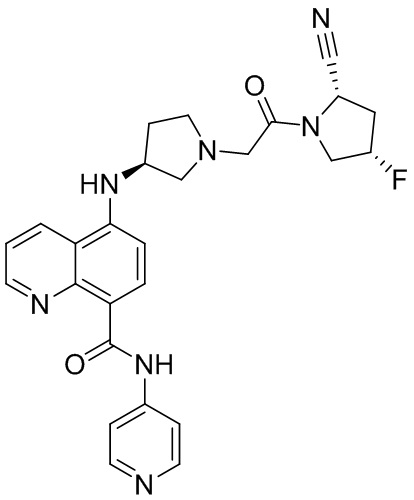
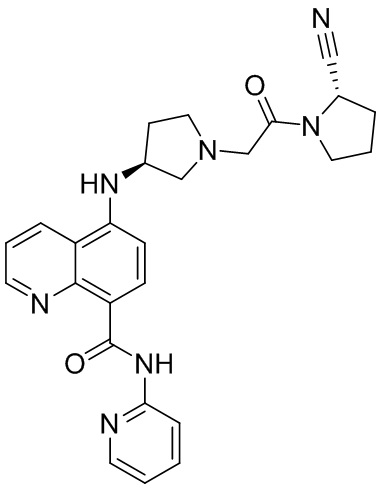
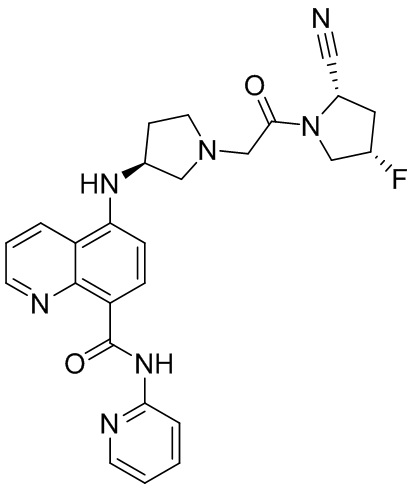
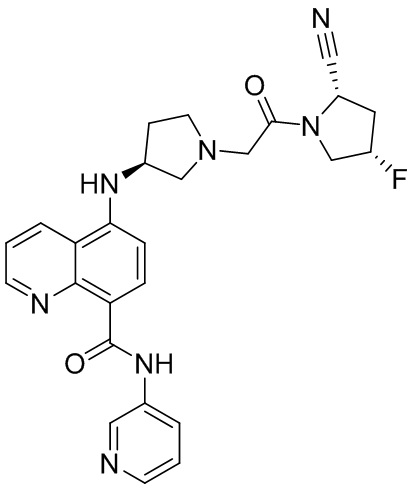
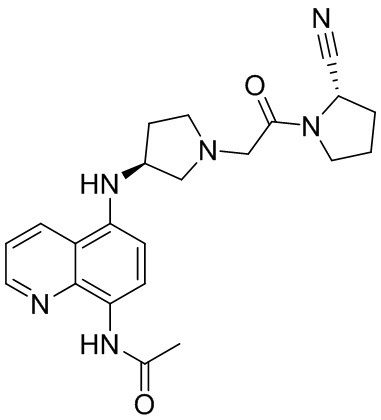
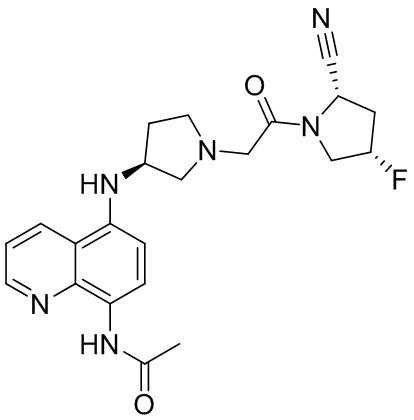
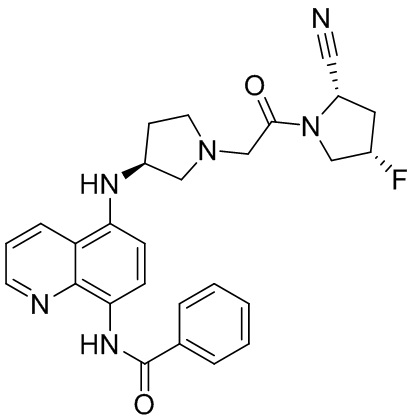
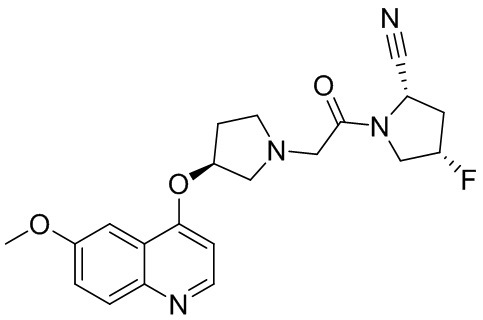
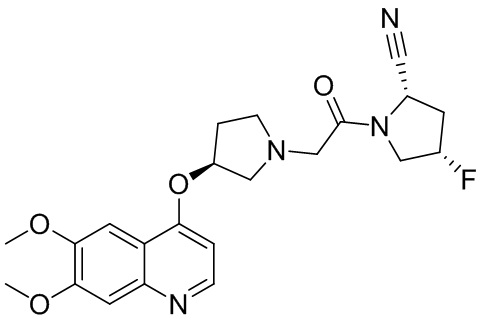
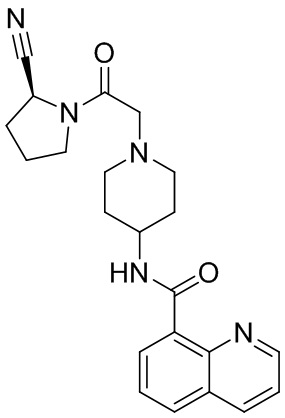
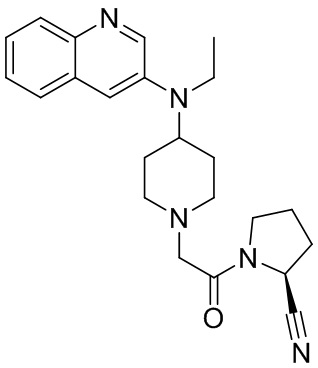
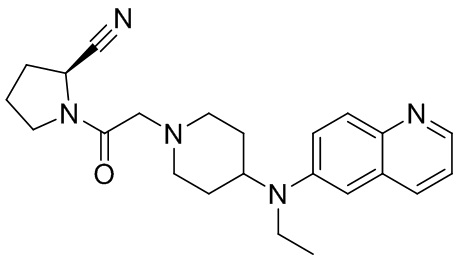
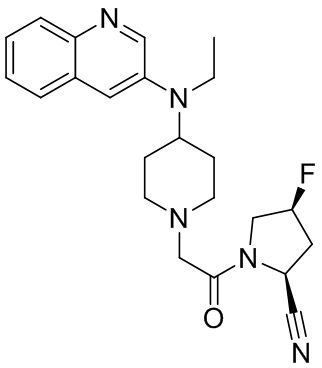


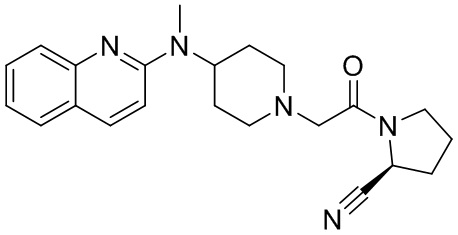
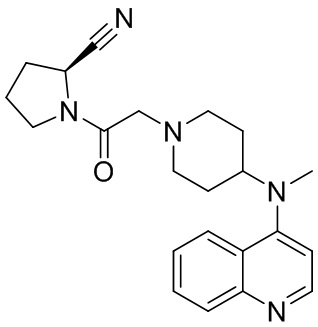
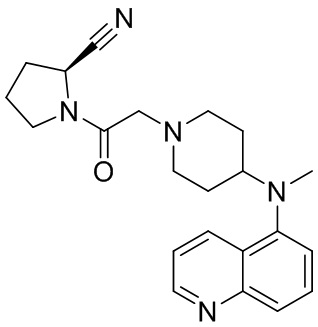
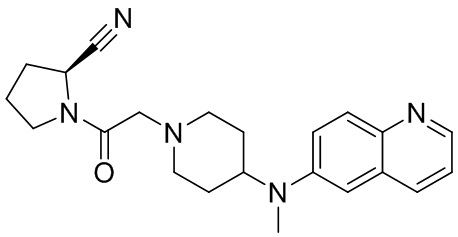
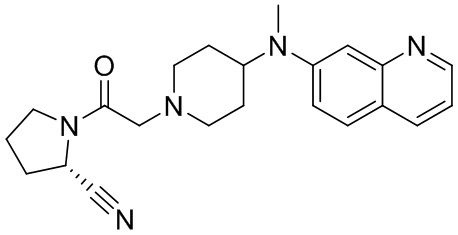
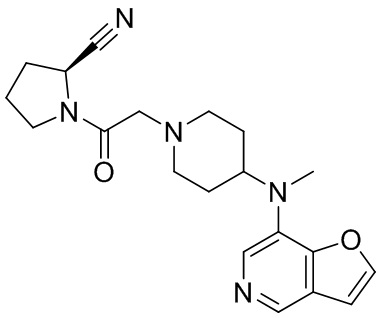
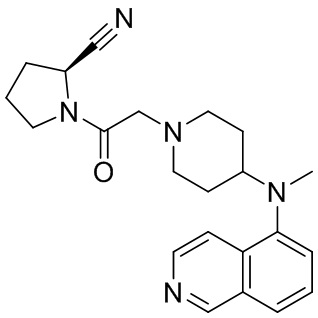
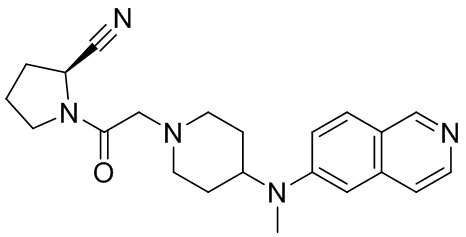
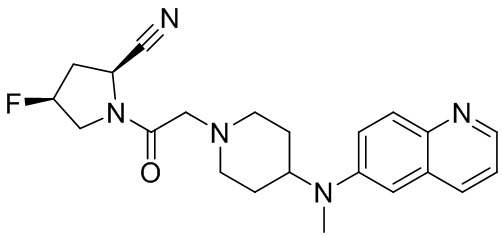
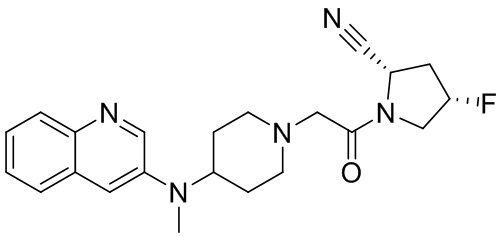
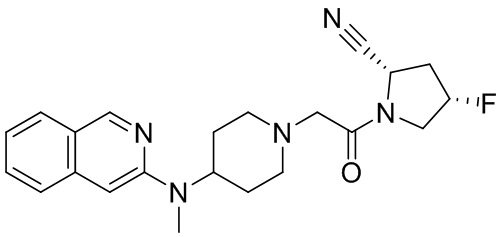
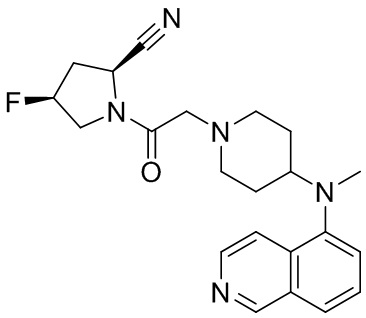
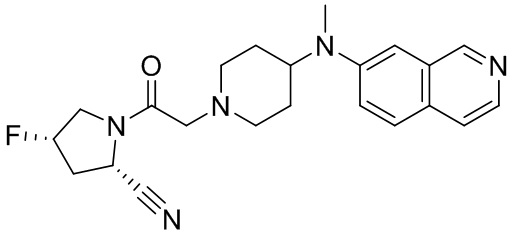
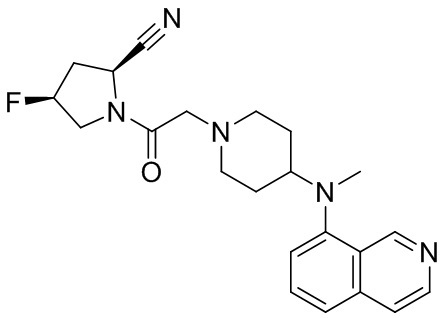
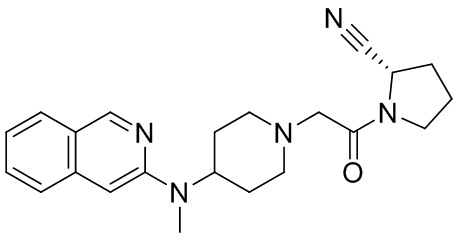
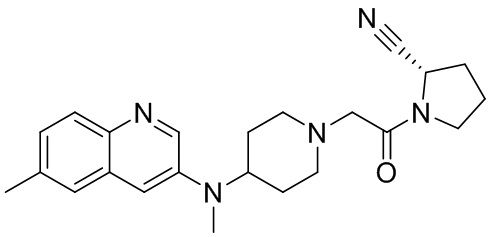
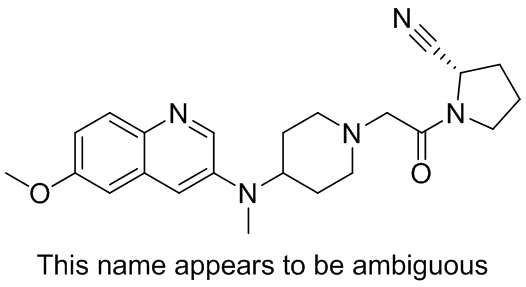
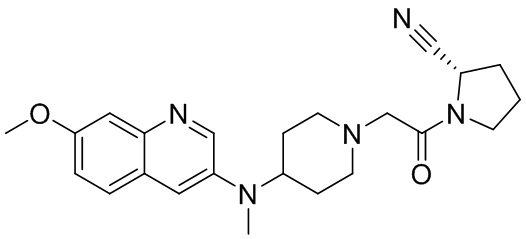
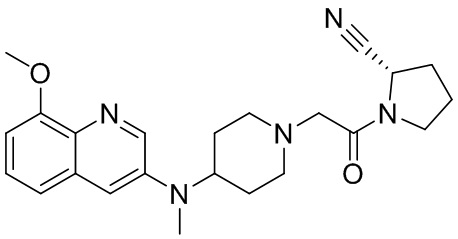
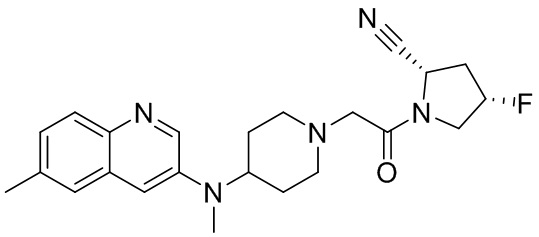
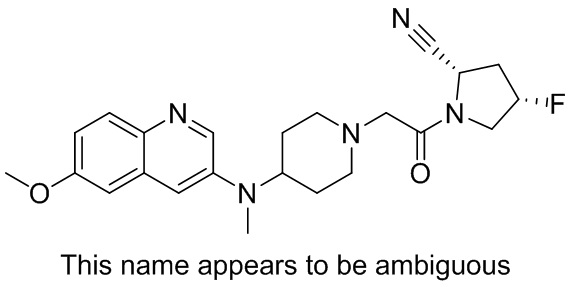
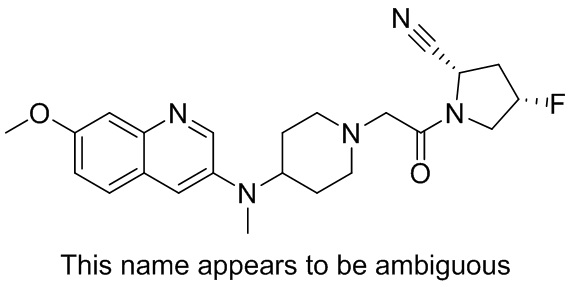
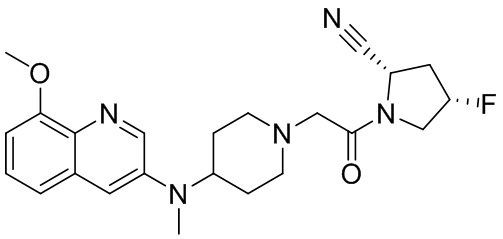
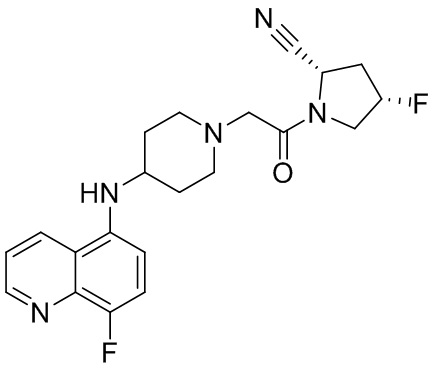
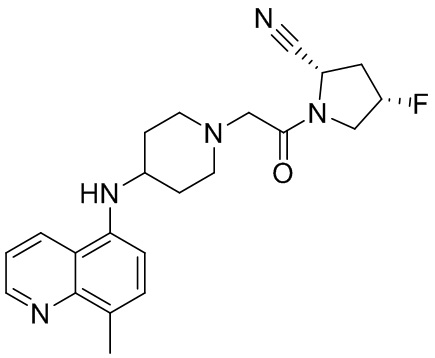
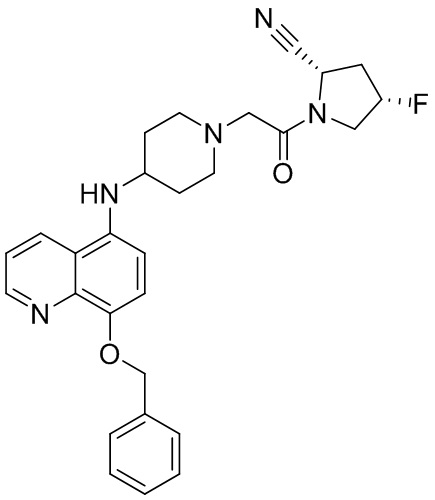
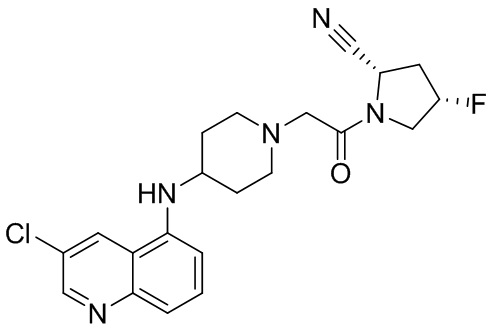
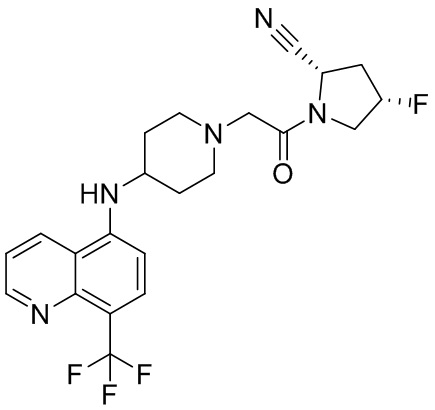
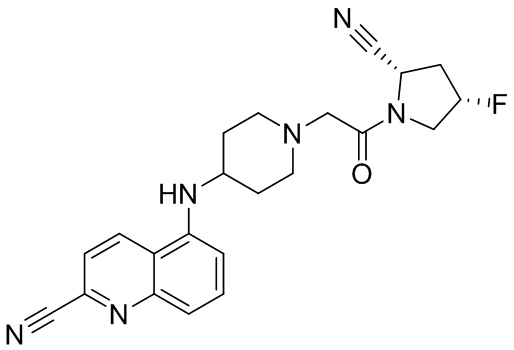
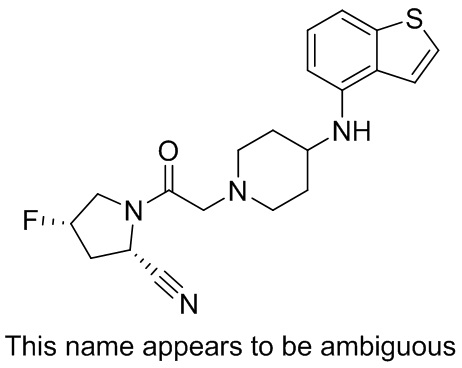
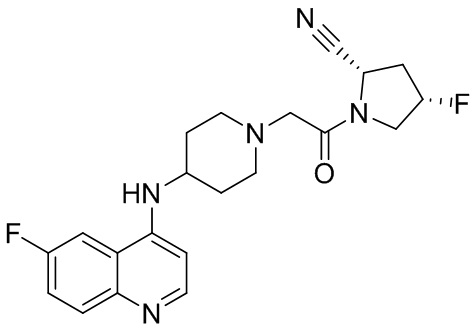
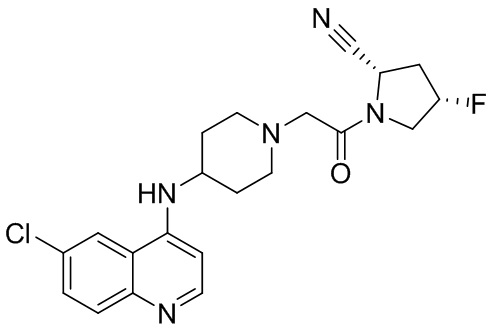
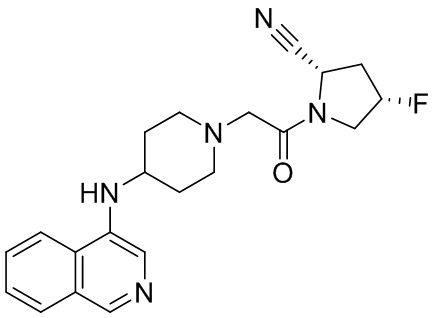
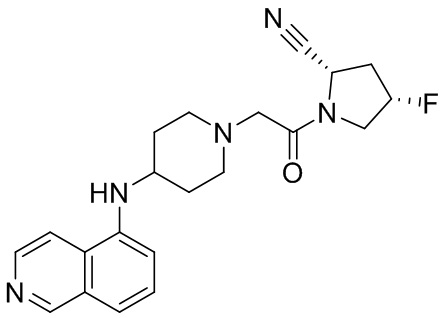
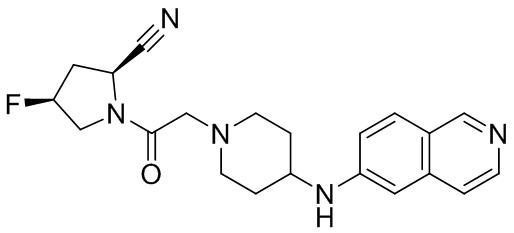
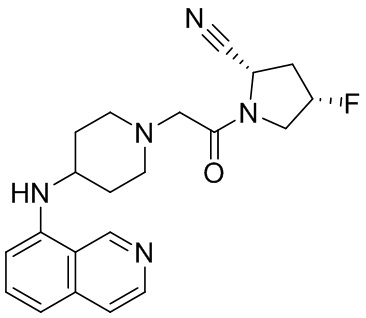
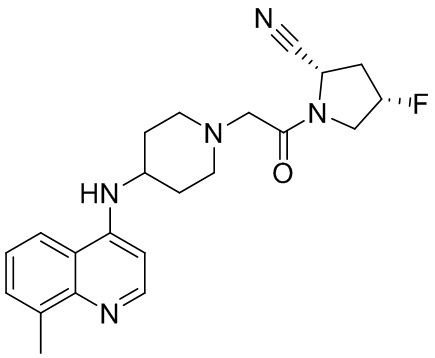
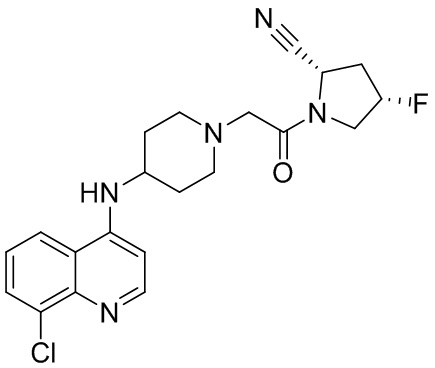
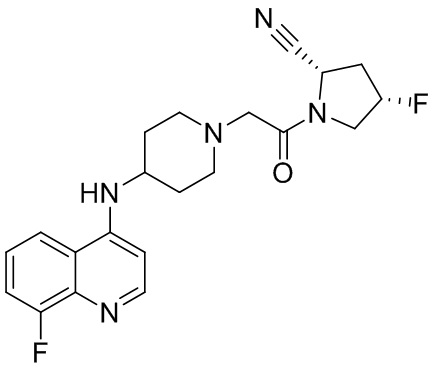

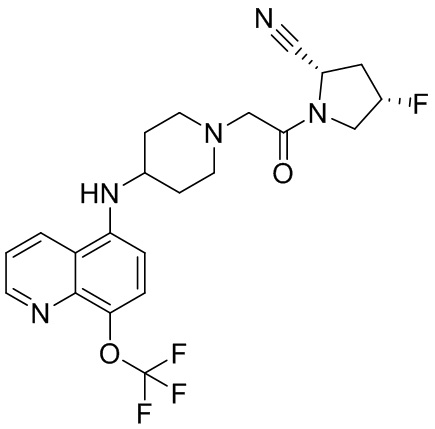
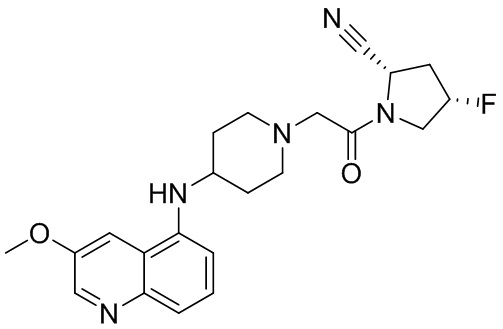
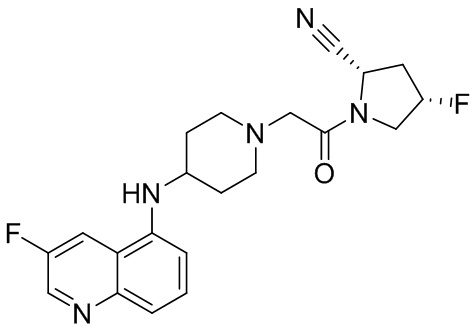
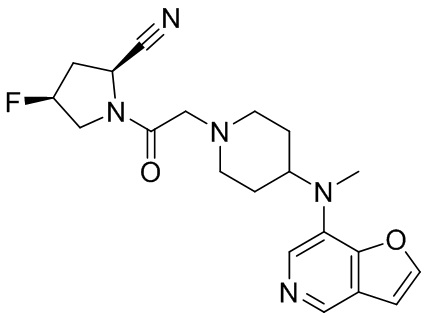
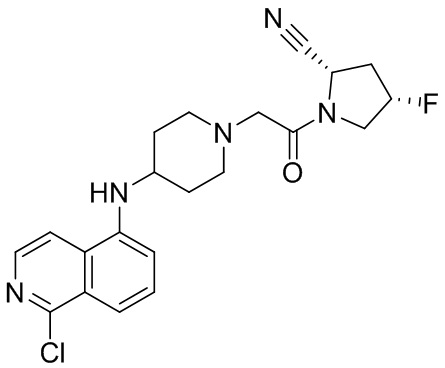
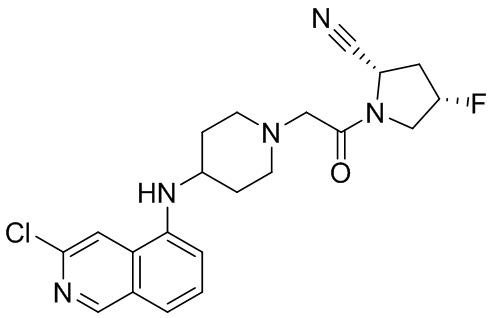
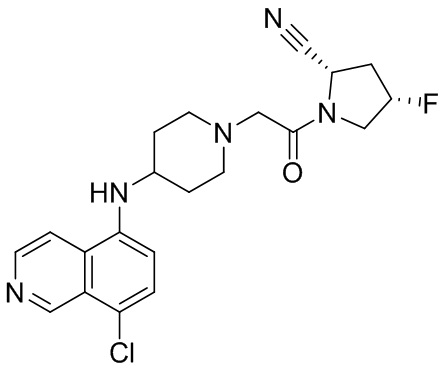
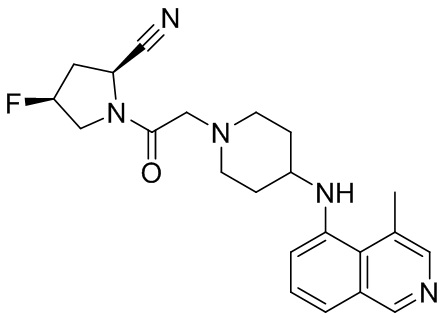
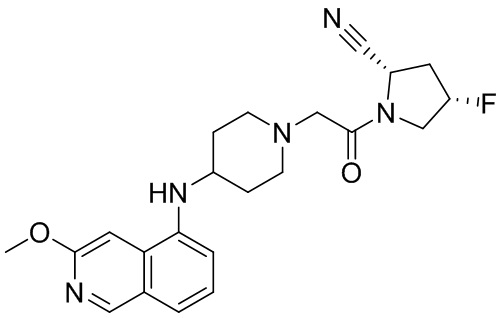
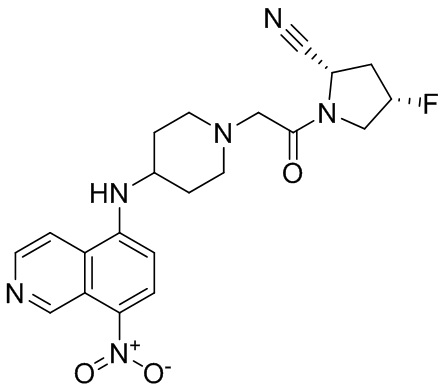
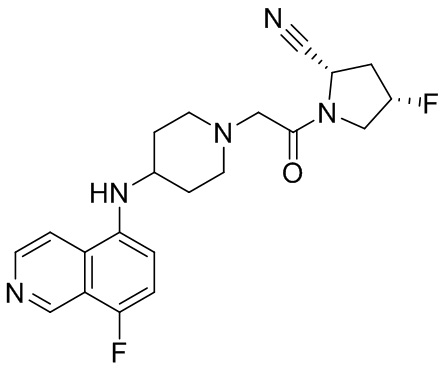
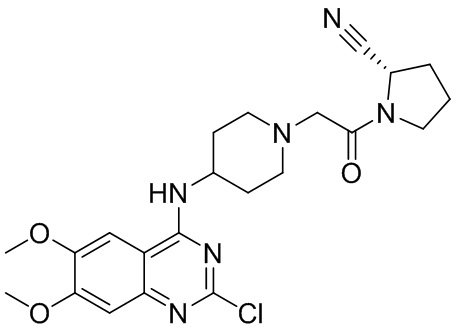

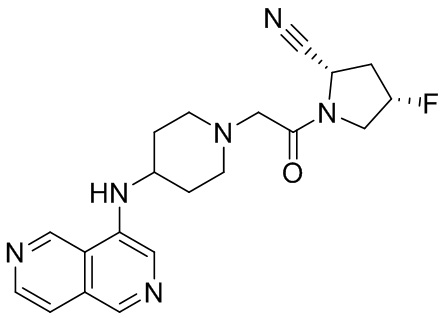
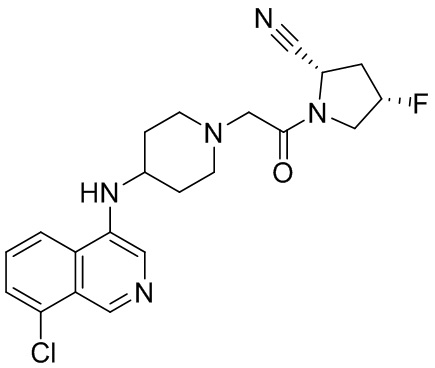
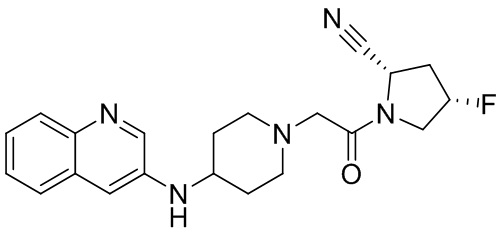
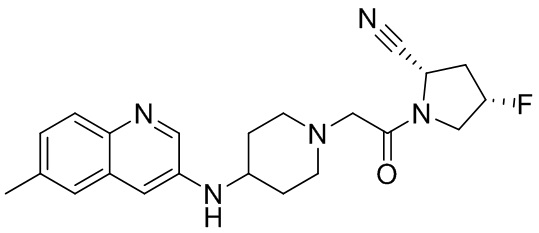
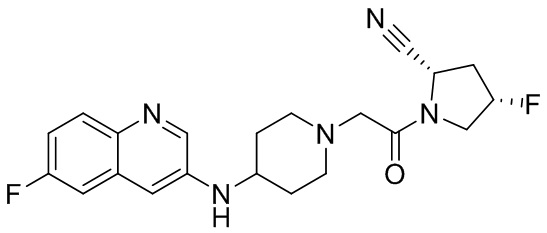
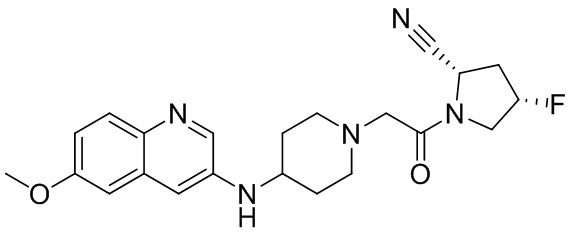
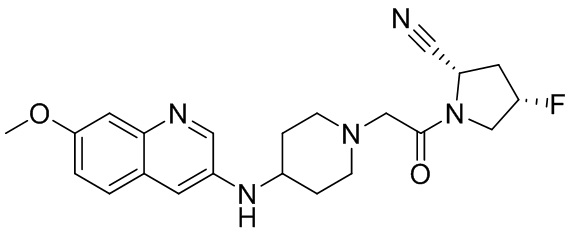
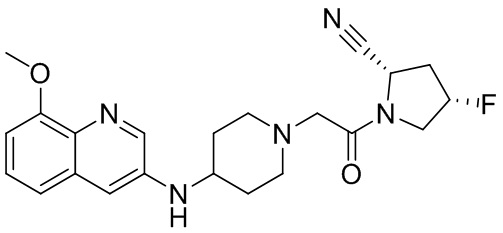
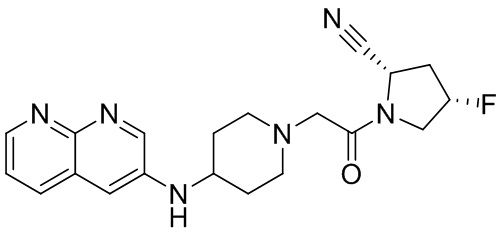
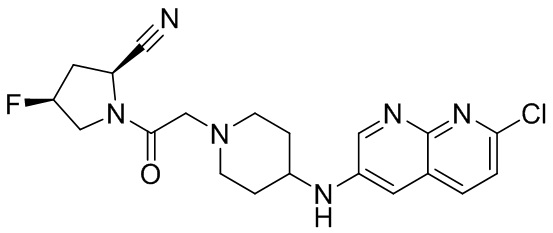
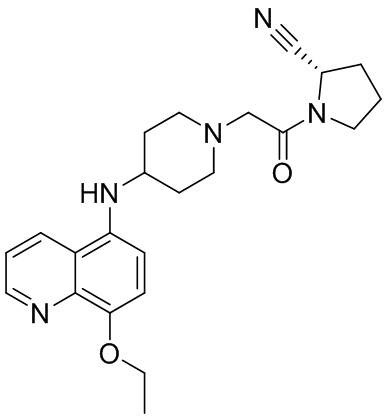
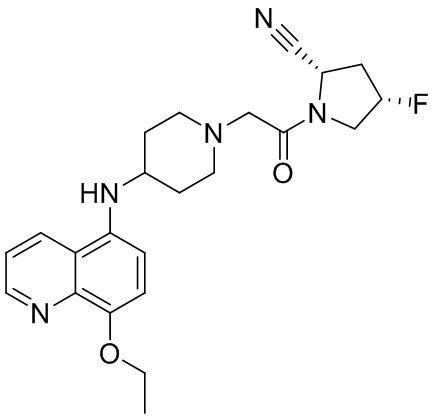
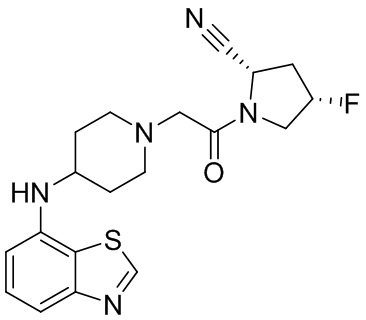
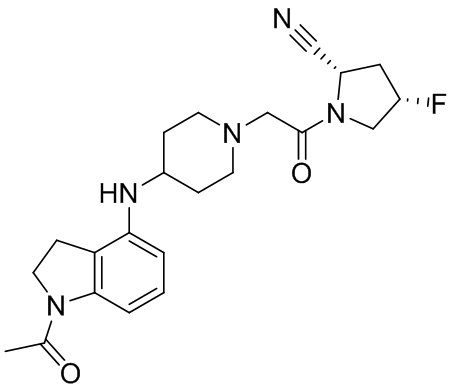
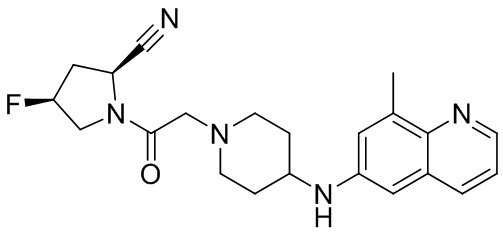
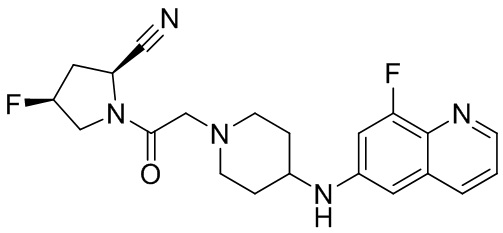
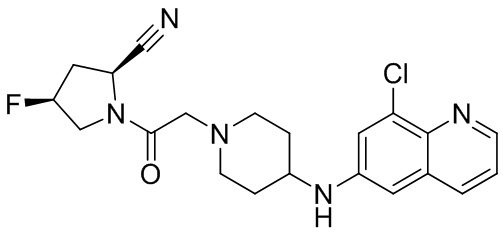
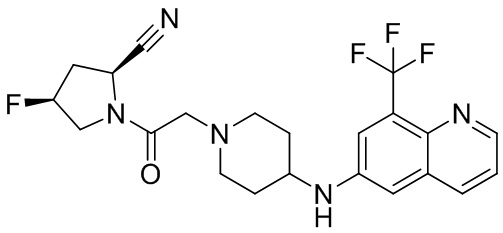
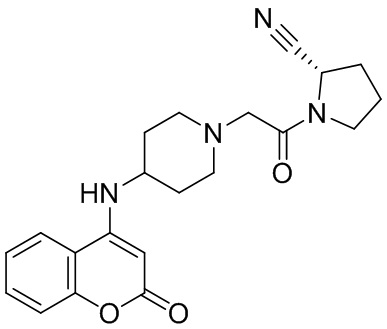
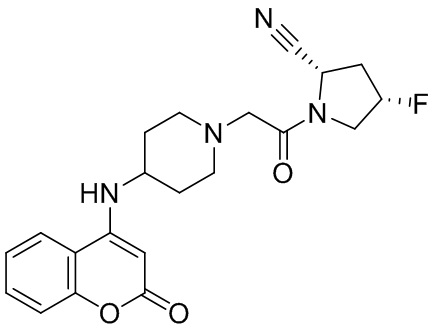
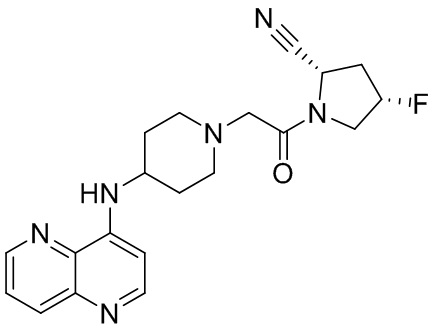
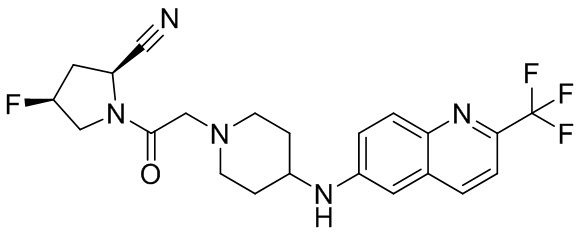
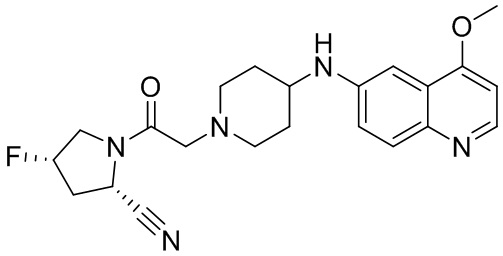
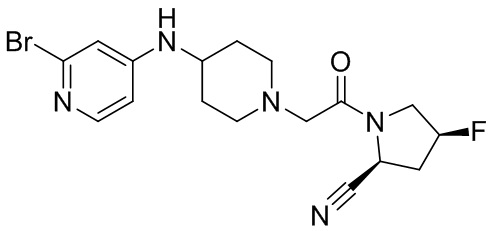
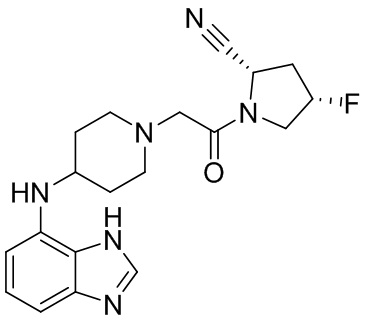

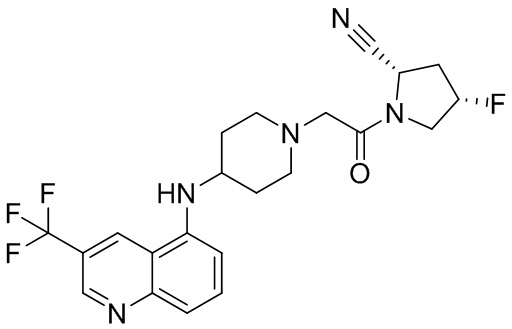
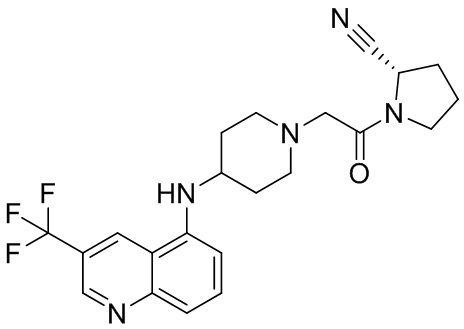
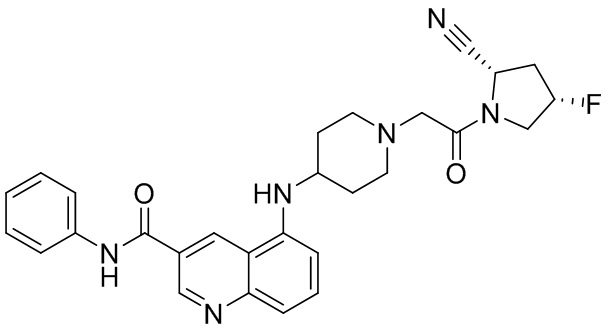
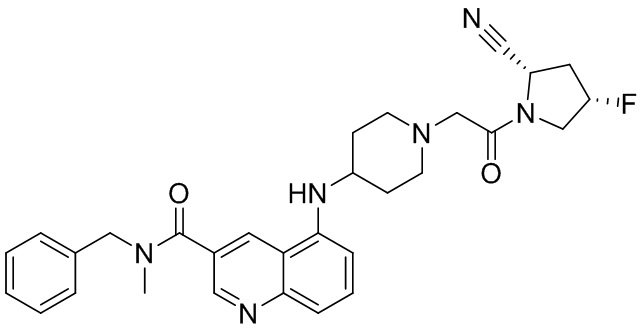
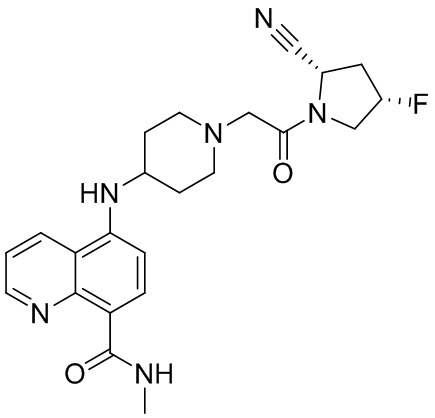
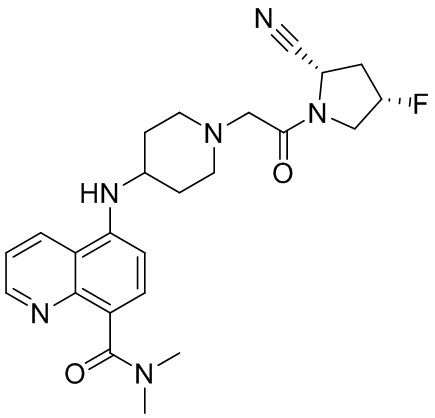
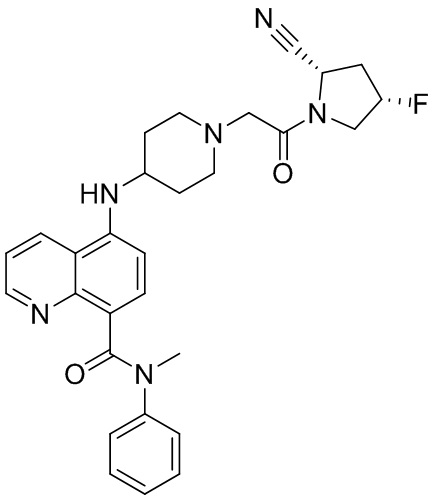
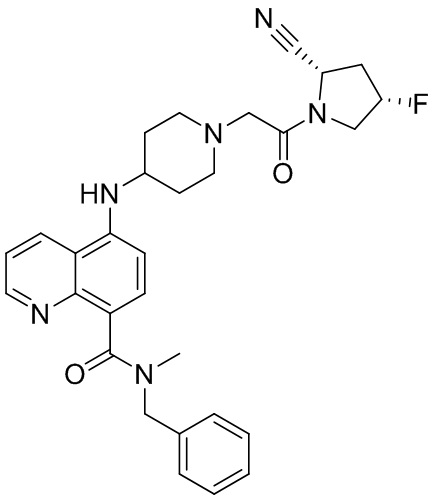

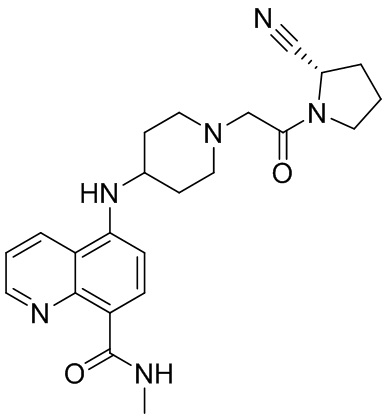
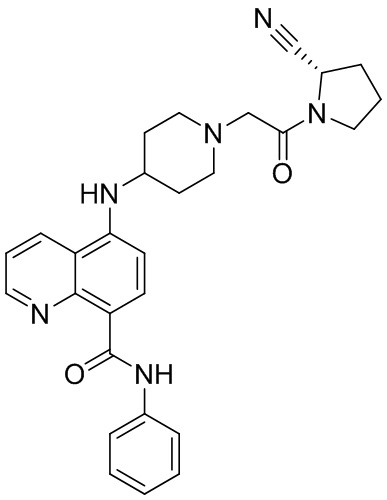
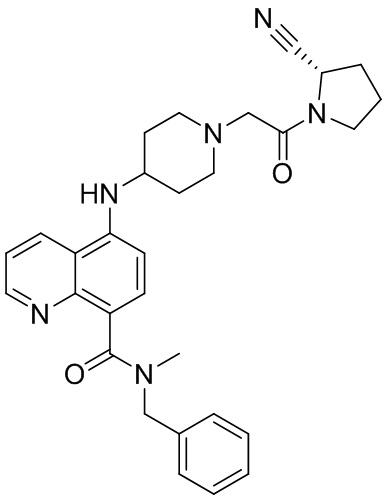
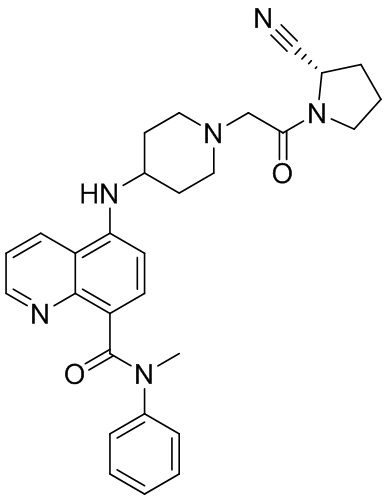
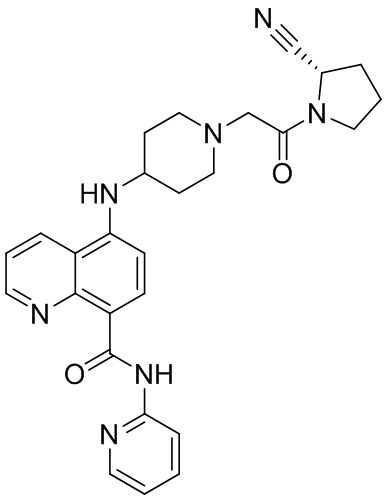
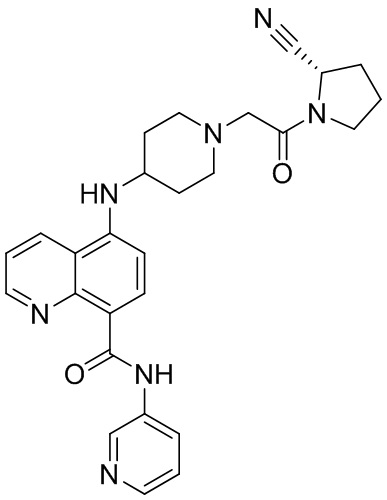
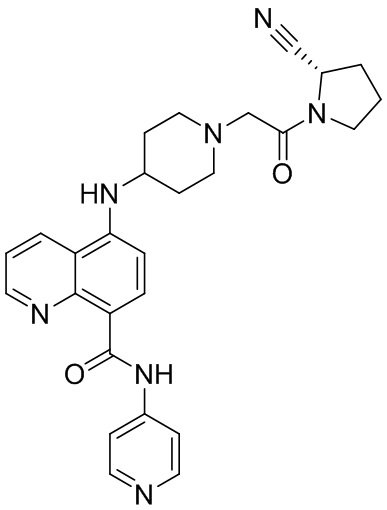

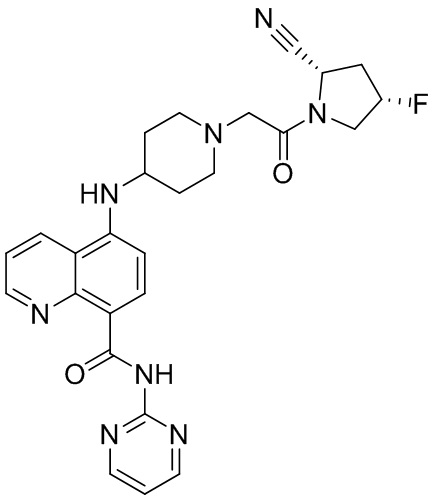
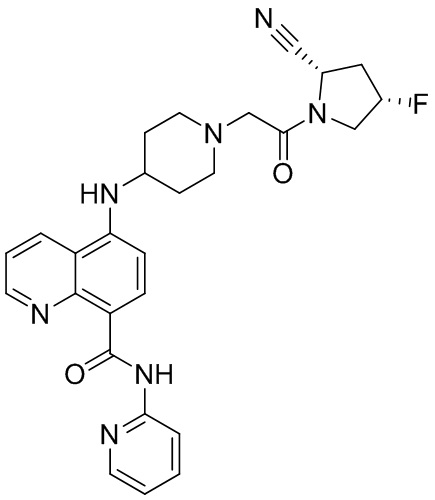
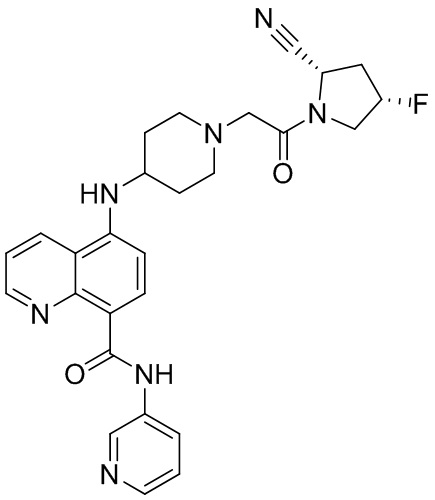
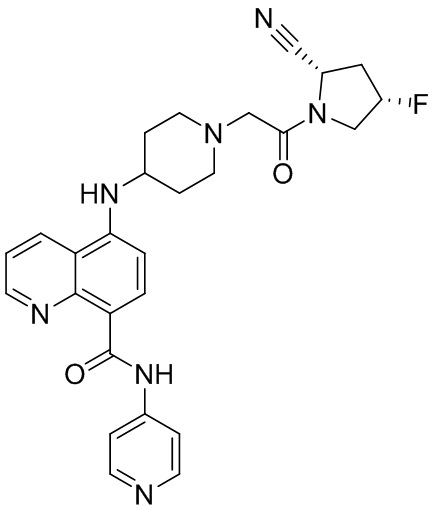
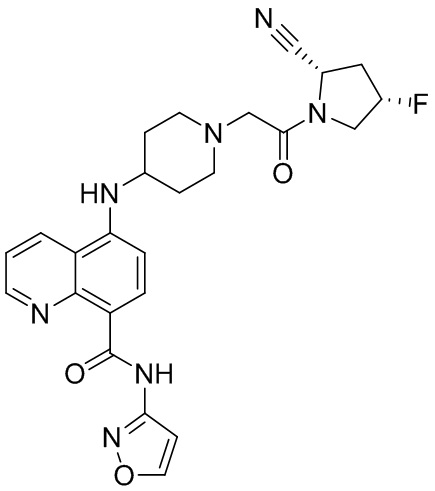
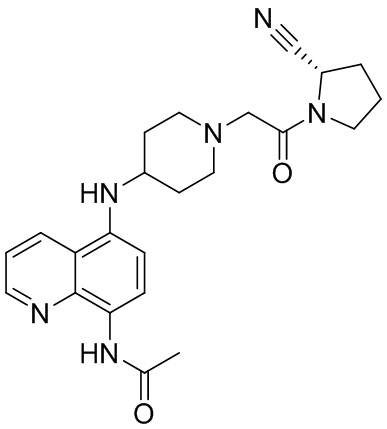
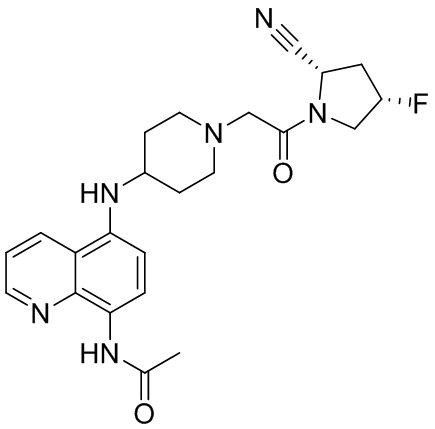

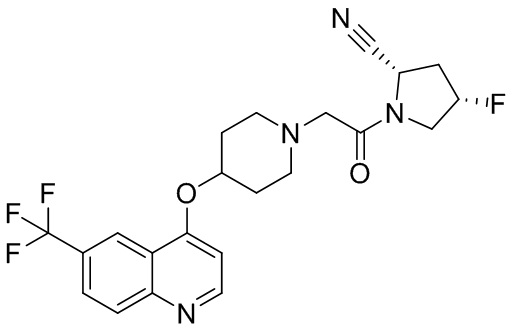
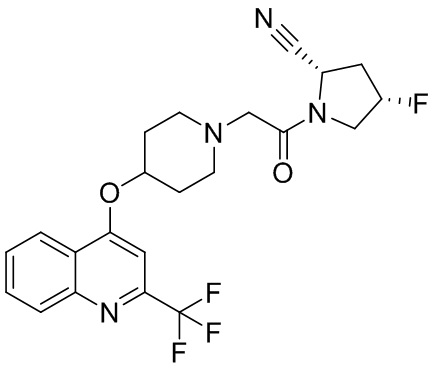
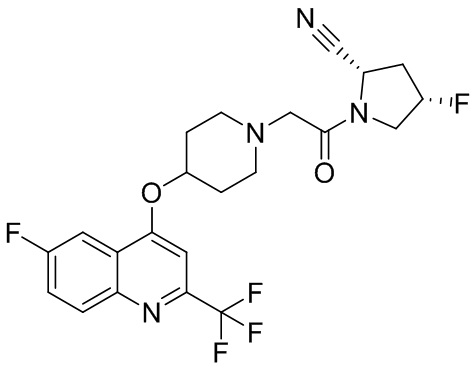
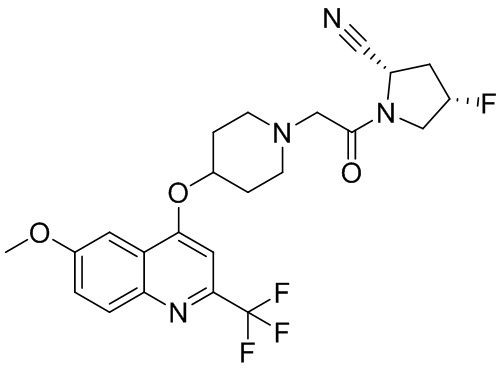
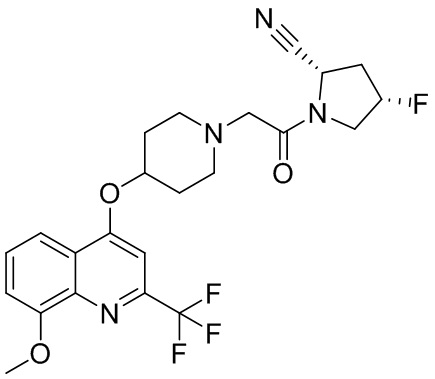
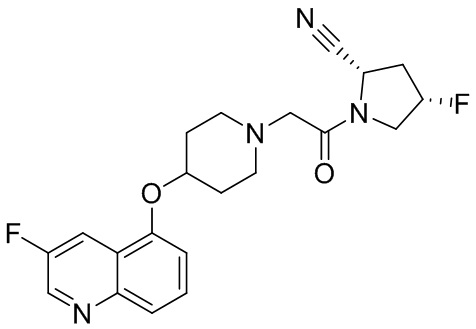

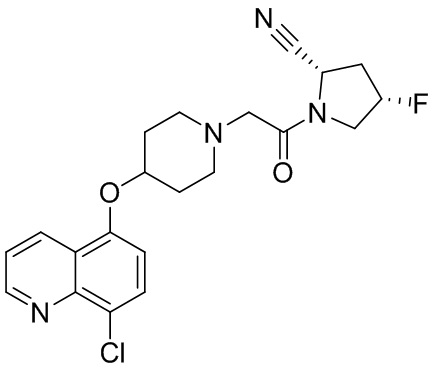
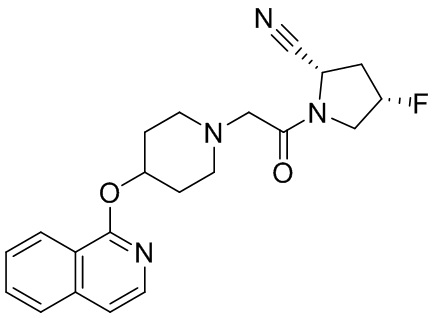
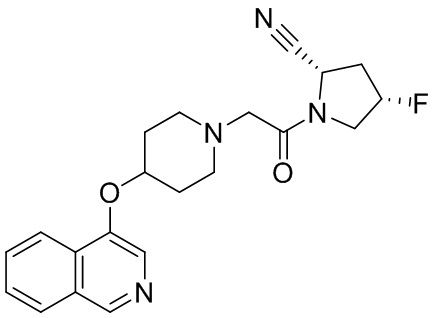
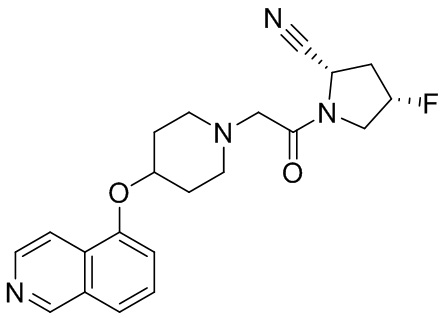
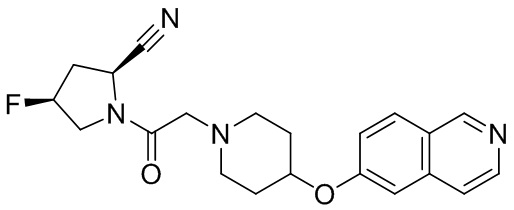
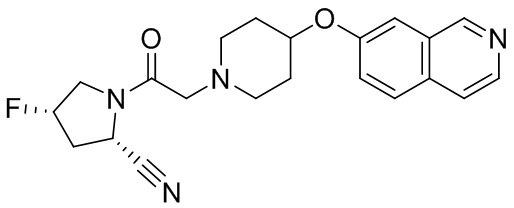
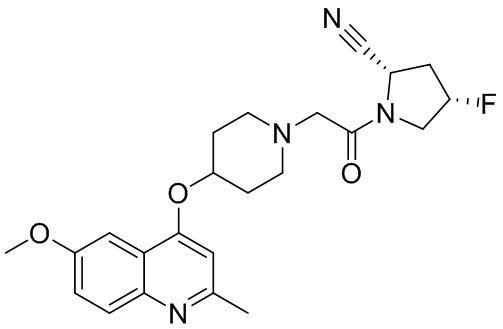
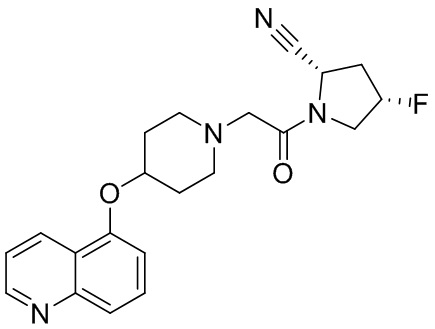
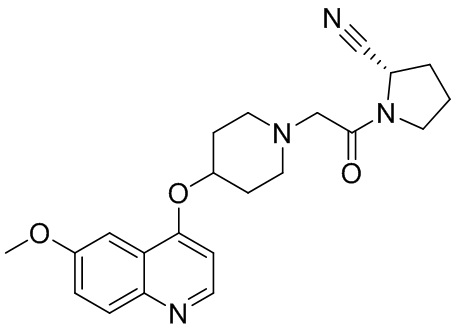

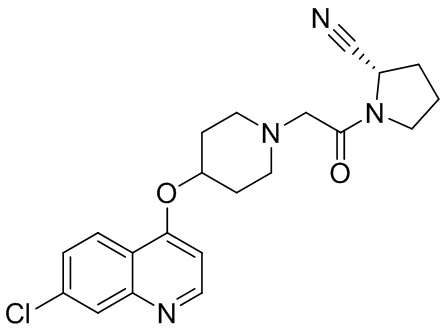
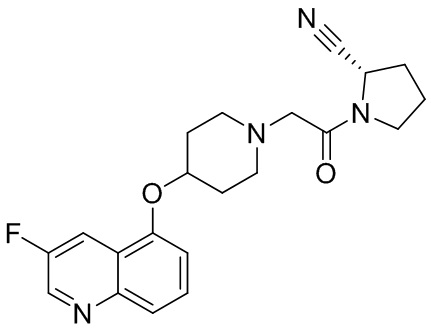
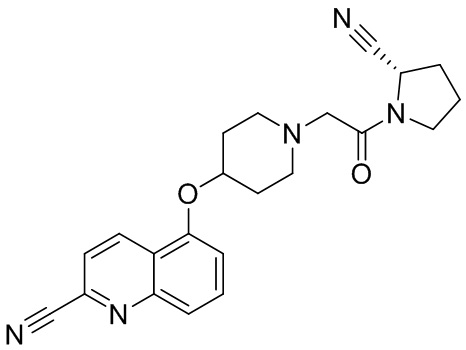
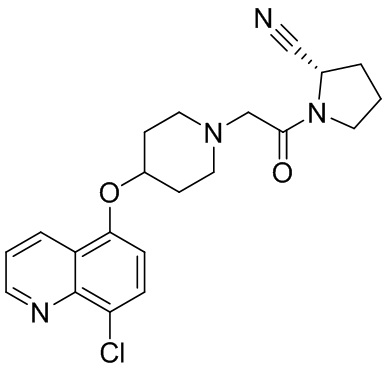

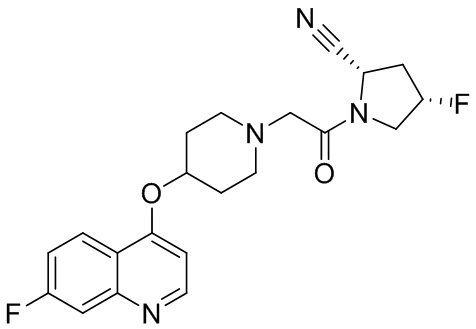
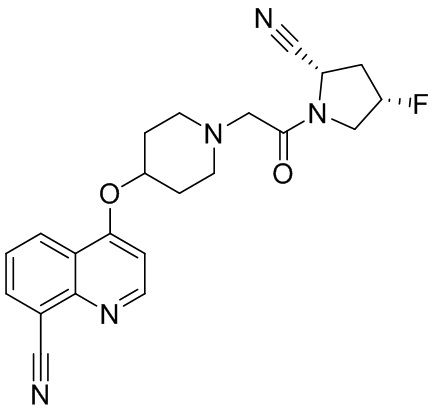
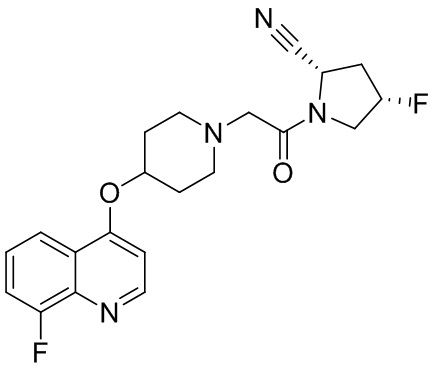
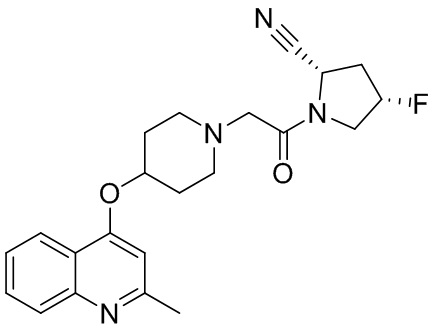
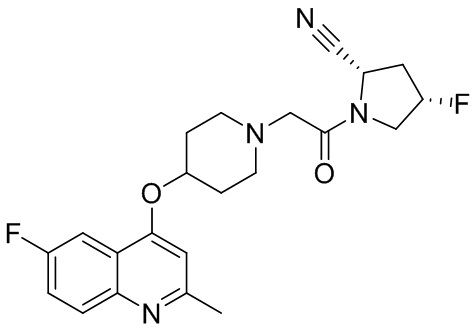
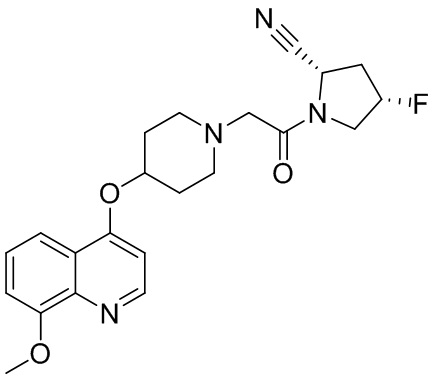
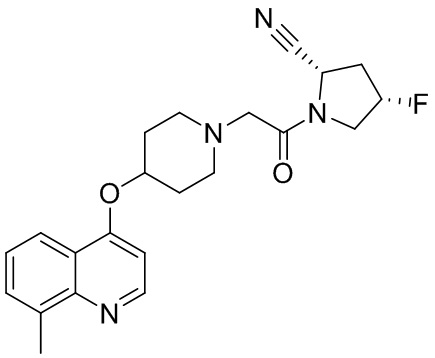
или его стереоизомер, смесь стереоизомеров или его фармацевтически приемлемая соль.
10. Фармацевтическая композиция для лечения заболевания, опосредованного белком активации фибробластов, содержащая терапевтически эффективное количество соединения по любому из пп. 1-9 или его стереоизомера, смеси стереоизомеров или его фармацевтически приемлемой соли и по меньшей мере один фармацевтически приемлемый эксципиент.
11. Способ лечения заболевания, опосредованного белком активации фибробластов, у субъекта, нуждающегося в этом, включающий введение субъекту терапевтически эффективного количества соединения по любому из пп. 1-9 или его стереоизомера, смеси стереоизомеров или его фармацевтически приемлемой соли или терапевтически эффективного количества фармацевтической композиции по п. 10, в котором заболевание, опосредованное белком активации фибробластов, выбрано из группы, состоящей из липидного нарушения, липопротеинового нарушения, состояния или заболевания, которые возникают в результате хронической жировой и фиброзной дистрофии органов вследствие накопления липидов и, в частности, триглицеридов, и последующей активации профибротического пути, сахарного диабета I или II типа, клинических осложнений сахарного диабета I и II типа, хронического внутрипеченочного холестатического состояния, внепеченочного холестатического состояния, фиброза печени, острого внутрипеченочного холестатического состояния, обструктивного или хронического воспалительного нарушения, возникающего из-за неправильного состава желчи, желудочно-кишечного состояния со сниженным усвоением пищевых жиров и жирорастворимых пищевых витаминов, воспалительного заболевания кишечника, ожирения, метаболического синдрома, сочетания состояний дислипидемии, диабета и аномально высокого индекса массы тела, персистирующей инфекции внутриклеточными бактериями или паразитарными простейшими, незлокачественного гиперпролиферативного нарушения, злокачественного гиперпролиферативного нарушения, аденокарциномы толстой кишки и гепатоцеллюлярной карциномы, стеатоза печени или связанных с ним синдромов, инфекции гепатита В, инфекции гепатита С, холестатических и фиброзных эффектов, которые связаны с алкогольным циррозом или с вирусными формами гепатита, печеночной недостаточности или нарушения функции печени в результате хронического заболевания печени или хирургической резекции печени, острого инфаркта миокарда, острого инсульта, тромбоза, возникающего как конечная точка хронического обструктивного атеросклероза, остеоартрита, ревматоидного артрита, псориаза и ишемического инсульта, по отдельности или любой их комбинации.
| CN 101284810 A, 15.10.2008 | |||
| CN 108689905 B, 28.07.2020 | |||
| US 20090182140 A1, 16.07.2009 | |||
| CN 101337920 B, 01.12.2010 | |||
| WO 2019154886 A1, 15.08.2019 | |||
| Барабан для расщипывания волоса | 1931 |
|
SU28422A1 |
Авторы
Даты
2023-09-13—Публикация
2020-11-05—Подача