Изобретение относится к новым синтетическим, биологически активным веществам из ряда гетероциклических соединений, применяемым для защиты растений подсолнечника от фитотоксического действия гербицида 2,4-дихлорорфеноксиуксусной кислоты (антидотам).
Как известно, подсолнечник является чрезвычайно чувствительной культурой к гормональным гербицидам группы 2,4-Д, и, в случаях непреднамеренного попадания гербицида на его посевы, потери могут составлять, в зависимости от дозы, до 100% [Чкаников Д. И., Соколов М С. Гербицидное действие 2,4-Д и других галоидфеноксикислот, М.: Наука, 1973, 95 с.].
Несмотря на интенсивные исследования по изысканию новых антидотов защита вегетирующих растений подсолнечника от повреждающего действия 2,4-Д остается актуальной и нерешенной [Стрелков В.Д., Дядюченко Л.В., Дмитриев И.Г. Синтез новых гербицидных антидотов для подсолнечника. Краснодар: Просвещение-Юг, 2014. С. 79].
Наиболее близким аналогом по структуре и свойствам заявляемому соединению является 3-амино-2-[N-(4-фторфенил)карбамидо]-4,6-диметилтиено[2,3-b]пиридин формулы 1 [пат. № 2277333 РФ, МПК A01N 25/32 (2006.01) A01P 15/00 (2006.01)]
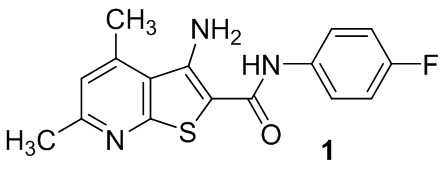
Cоединение 1 (прототип) в полевых условиях в дозе 200 г/га на вегетирующих растениях подсолнечника проявляет антидотный эффект по отношению к 2,4-Д на уровне 22-24 % и может применяться в качестве средства защиты подсолнечника. Однако его антидотная активность является недостаточно высокой, при этом доза 200 г/га достаточно высокая и может вызвать негативные экологические проблемы.
Техническим результатом заявляемого изобретения является расширение арсенала биологически активных веществ, полученных синтетическим путем, для применения их в сельском хозяйстве в качестве антидотов.
Это достигается применением 3,3'-(1,4-фенилен)бис(7-[2-{3,4-диметоксифенил}-1-циановинил]-1,2,3,4-тетрагидропиразоло[1,5-a][1,3,5]триазин-8-карбонитрила) 2:

проявляющего антидотную активность по отношению к 2,4-дихлорфеноксиуксусной кислоте на проростках подсолнечника в лабораторных условиях.
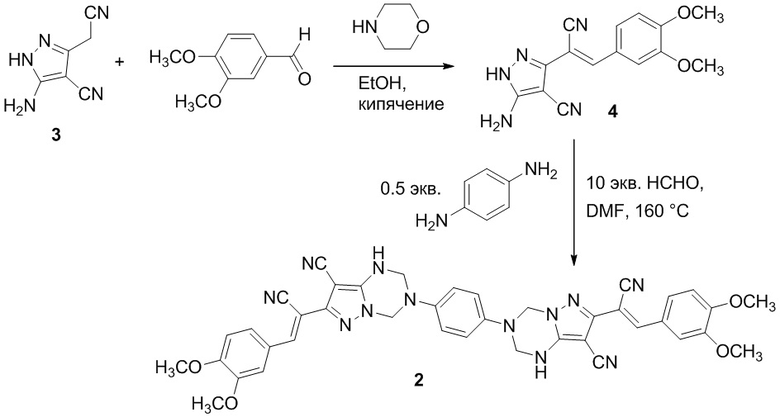
Получение 3,3'-(1,4-фенилен)бис(7-[2-{3,4-диметоксифенил}-1-циановинил]-1,2,3,4-тетрагидропиразоло[1,5-a][1,3,5]триазин-8-карбонитрила) 2.
1. В круглодонной колбе объемом 100 мл, снабженной обратным холодильником, смешивают 1,00 г (0,007 моль) 5-амино-3-цианометил-1H-пиразол-4-карбонитрила 3, 1,10 г (0,007 моль) 3,4-диметоксибензальдегида, 20 мл этанола и добавляют морфолин в каталитическом количестве (0,3 мл). Реакционную смесь кипятят в течение 4 часов, охлаждают, выдерживают при 25°С в течение 24 ч, осадок отфильтровывают, промывают этанолом (25 мл), высушивают при комнатной температуре, получают 5-амино-3-(2-[3,4-диметоксифенил]-1-циановинил)-1H-пиразол-4-карбонитрил 4 в виде желтого мелкокристаллического порошка.
2. В термостойкий химический стакан объемом 50 мл помещают 0,80 г (0,0028 моль) полученного на первой стадии 5-амино-3-(2-[3,4-диметоксифенил]-1-циановинил)-1H-пиразол-4-карбонитрила 4, 0,80 мл (0,022 моль) 37%-ного водного формалина, 0,16 г (0,0015 моль) пара-фенилендиамина и 11 мл ДМФА. Раствор выдерживают при 160°C в течение 33 минут при постоянном перемешивании (контроль по результатам тонкослойной хроматографии (ТСХ) на пластинах Сорбфил-А, элюент - этилацетат-гексан 1:1), охлаждают по 25°С, через 24 ч осадок отфильтровывают, высушивают при комнатной температуре. Получают соединение 2 в виде светло-зеленого порошка, выход 47%.
ИК-спектр, ν, см-1: 3325 сл (N-H), 2937 сл, 2839 сл (C-H), 2214 ср (2 C≡N).
ЯМР 1H спектр (400 МГц, ДМСО-d6), δ, м.д.: 3.80 (с, 6H, 2 OCH3), 3.84 (с, 6H, 2 OCH3), 4.92 (уш.с, 4Н, 2 NCH2NH), 5.69 (уш.с, 4Н, 2 NCH2N), 7.11-7.18 (м, 3Н, H Ar), 7.45-7.52 (м, 2Н, H Ar), 7.60-7.63 (м, 3Н, H Ar), 7.79-7.88 (м, 2Н, H Ar), 8.31 (уш.с, 2Н, 2 NH).
ЯМР 13С DEPTQ спектр (101 МГц, ДМСО-d6), δ, м.д.: 55.5* (2 OCH3), 55.8* (2 OCH3), 57.6 (2 NC2H2N), 63.2 (2 NC4H2N), 69.3 (2 =C-CN), 99.6 (2 C8), 111.4* (2 C2H 3,4-(MeO)2C6H3), 111.8* (2 C5H 3,4-(MeO)2C6H3), 111.9* (CH NC6H4N), 114.0 (2 C≡N), 116.6 (2 C≡N), 124.4* (2 C6H 3,4-(MeO)2C6H3), 125.3 (2 C1 3,4-(MeO)2C6H3), 144.0* (2 ArCH=), 144.9 (2 C7), 148.7 (2 C3-OMe 3,4-(MeO)2C6H3), 148.8 (C1 NC6H4N), 149.7 (2 C4-OMe 3,4-(MeO)2C6H3), 151.6 (C8a).*Сигнал в противофазе.
Пример 1. Оценка соединения 2 на антидотную активность на проростках подсолнечника
Проросшие семена подсолнечника сорта Мастер с длиной зародышевого корешка 2-4 мм помещали на 1 ч в раствор 2,4-дихлорфеноксиуксусной кислоты (2,4-Д) в концентрации 10-3 % в расчете получения 40-60% ингибирования роста гипокотиле. После гербицидного воздействия проростки промывали водой и помещали в растворы испытываемых на антидотную активность веществ в концентрациях 10-2, 10-3, 10-4, 10-5 % (вариант гербицид+антидот). Спустя 1 ч семена промывали водой и раскладывали на полосы фильтровальной бумаги (размер 10×75 см) по 20 штук, которые сворачивали в рулоны и помещали в стаканы с 50 мл воды. Дальнейшее проращивание семян проводили в термостате в течение 3 суток при температуре 28°С. Температура растворов и промывной воды 28°С. Семена варианта «гербицид» (эталон сравнения) выдерживали 1 ч в растворе 2,4-Д в концентрации 10-3% и 1 ч в воде. Семена контрольного варианта 2 часа выдерживали в воде. Повторность опыта трехкратная. В каждой повторности использовали по 20 штук семян.
Защитный (антидотный) эффект определяли по увеличению длины гипокотиле и корня в варианте гербицид+антидот относительно названных величин в варианте «гербицид» (эталон) в процентах.
Статистическая обработка экспериментальных данных проведена с использованием t-критерия Стъюдента при Р=0,95.
Результаты исследований приведены в таблице 1.
Антидотная активность соединений 1 и 2 к гербициду 2,4-Д на проростках подсолнечника сорта Мастер
%
соединение 2
10-3
10-4
10-5
79,5
79,5
74
153*
153*
142*
91
93
92
149*
152*
151*
соединение 1 (прототип)
10-3
10-4
10-5
67
61
58
129*
117*
112*
73
75
75
120*
123*
123*
*Различия между вариантами достоверны при Р=0,95.
Как видно из данных таблицы 1, применение на фоне воздействия гербицида предлагаемого в качестве антидота 3,3'-(1,4-фенилен)бис(7-[2-{3,4-диметоксифенил}-1-циановинил]-1,2,3,4-тетрагидропиразоло[1,5-a][1,3,5]триазин-8-карбонитрила) 2 значительно ослабляет токсическое действие гербицида. Соединение 2 снижало отрицательное действие 2,4-Д на гипокотили проростков подсолнечника на 31-53% при использовании в основном в трех и более концентрациях, в то время как соединение 1 (аналог по структуре) проявил антидотный эффект 12-29%.
Соединение 2 снижало ингибирующее действие 2,4-Д на корни проростков на 47-52% также при использовании в трех и более концентрациях, соединение 1 (прототип) проявлял антидотный эффект на уровне 20-23%.
Изобретение относится к новым синтетическим, химическим биологически активным веществам из ряда гетероциклических соединений, применяемым для защиты растений подсолнечника от фитотоксического действия гербицида 2,4-дихлорорфеноксиуксусной кислоты (антидотам). Для расширения арсенала биологически активных веществ, полученных синтетическим путем и применяемых в сельском хозяйстве в качестве антидота на подсолнечнике предлагается использовать 3,3'-(1,4-фенилен)бис(7-[2-{3,4-диметоксифенил}-1-циановинил]-1,2,3,4-тетрагидропиразоло[1,5-a][1,3,5]триазин-8-карбонитрил). 1 табл., 1 пр.

3,3'-(1,4-фенилен)бис(7-[2-{3,4-диметоксифенил}-1-циановинил]-1,2,3,4-тетрагидропиразоло[1,5-a][1,3,5]триазин-8-карбонитрил)
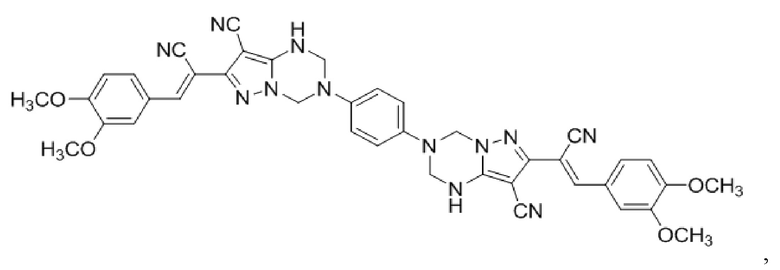
проявляющий антидотный эффект к 2,4-дихлорфеноксиуксусной кислоте на подсолнечнике.
| СПОСОБ ЗАЩИТЫ ВЕГЕТИРУЮЩИХ РАСТЕНИЙ ПОДСОЛНЕЧНИКА ОТ ПОВРЕЖДАЮЩЕГО ДЕЙСТВИЯ 2,4-Д | 2005 |
|
RU2277333C1 |
| 7',9'-ДИМЕТИЛ-3'-АРИЛ-1'-СПИРО[ИНДЕН-2,2'-ПИРИДО[3',2':4,5]ТИЕНО]3,2-D]ПИРИМИДИН]-1,3,4'(3'H)ТРИОНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ В КАЧЕСТВЕ АНТИДОТОВ 2,4-Д НА ПОДСОЛНЕЧНИКЕ | 2020 |
|
RU2754220C1 |
| О-(4-трет-бутилфенил)карбонил-4,6-диметил-2-хлорпиридил-3-амидоксим в качестве антидота 2,4-Д на подсолнечнике | 2018 |
|
RU2672881C1 |
| US 4892576 A, 01.09.1990 | |||
| Курскова А.О | |||
| и др | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
Авторы
Даты
2023-09-19—Публикация
2023-02-15—Подача