Изобретение относится к химической промышленности, а именно к синтезу никель-хромового катализатора гидрирования кетонов, в том числе ацетона.
Одним из способов получения спиртов, например, изопропанола (ИПС), является каталитическое гидрирование ацетона:
CH3COCH3+H2 → (CH3)2CHOH
В промышленности используется как газофазная, так и жидкофазная технологии получения ИПС через гидрирование ацетона на катализаторе. Тем не менее, жидкофазный способ гидрирования в сравнении с газофазным более производителен и селективен [Патент №2205818 РФ, МПК C07C 31/10, C07C 29/145. Способ получения изопропанола/ Луговской С.А., Нагродский М.И., Рылеев Г.И.; заявитель и патентообладатель Закрытое акционерное общество "Химтэк Инжиниринг". - №2002111264/04; заяв. 26.04.2002; опубл. 10.06.2003 Бюл. №16]. Катализаторами данной реакции являются меднохромовые [Патент №1051055 A1 СССР, МПК C07C 31/10, C07C 29/136. Способ получения изопропилового спирта/ Рылеев Геннадий Иванович, Нагродский Михаил Иосифович, Пнева Екатерина Яковлевна, Эдельштейн Борис Иосифович, Устинова Алла Акимовна, Кякк Ольга Аркадьевна, Кудимова Вера Петровна. - №2950353/23-04; заяв. 16.05.1980; опубл. 30.10.1983, Бюл. №40], медь на силикагеле [Патент №2675362 РФ, МПК C07C 29/136, 29/145, C07C 31/10. Способ гидрирования ацетона в изопропиловый спирт / Юрий Геннадьевич Носков, Галина Александровна Корнеева, Дмитрий Вячеславович Марочкин, Сергей Николаевич Руш, Татьяна Евгеньевна Крон, Ольга Георгиевна Карчевская, Павел Михайлович Болотов, Федор Владимирович Рыжков; заявитель и патентообладатель Публичное акционерное общество "Нефтяная компания "Роснефть" (ПАО "НК "Роснефть") - №2018131008; заявл. 2018.08.28; опубл. 2018.12.19, Бюл. №35], никельхромовые [Патент №US7041857B1, МПК C07C 29/145. Hydrogenation of acetone / Kathryn Sue Hayes, John William Mitchell, Anita Niak, Michael Gerard Turcotte; патентообладатель Taminco BV - №US11/221,066; заявл. 2005-09-07; опубл. 2006-05-09] и нанесенные никелевые и медные катализаторы на различных подложках [Патент №2 738 656 РФ, МПК B01J 37/00, C07C 31/10. Способ приготовления катализатора и способ получения изопропилового спирта с использованием этого катализатора/ Павлова Светлана Николаевна, Исупова Любовь Александровна (RU), Бухтиярова Галина Александровна, Власова Евгения Николаевна; заявитель и патентообладатель Федеральное государственное бюджетное учреждение науки "Федеральный исследовательский центр "Институт катализа им. Г.К. Борескова Сибирского отделения Российской академии наук" (ИК СО РАН, Институт катализа СО РАН) - №2020114481; заявл. 2020.04.23; опубл. 2020.12.15, Бюл. №35]. Наибольший интерес представляют катализаторы, содержащие в своем составе соединения никеля и хрома, так как такие катализаторы показывают наибольшую активность и устойчивость к высоким температурам.
Известен способ получения катализатора для гидрирования углеводородов на основе соединений никеля и хрома [Патент №303094 СССР, МПК B01J 37/04, B01J 37/00. Способ получения катализатора для гидрирования углеводородов / Будников В.В., Говоров В.Г.; заявитель и патентообладатель Будников В.В., Говоров В.Г. - 1400797/23-4; заяв. 1970.01.29; опубл. 1971.05.13Бюл. №16]. Сущность данного способа заключается в том, что готовят исходную смесь из измельченных никеля, хрома или их окислов, солей, руд, взятых отдельно или в комбинации друг с другом, в сухом виде или в виде растворов или суспензий, с добавлением промоторов и измельченного каменного угля коксующихся марок с последующим нагреванием смеси до температуры 900-1200°С до образования коксообразной массы. Полученную массу затем медленно охлаждают и, в случае необходимости, дробят до заданной фракции.
После рассмотрения данного способа, был выявлен ряд существенных недостатков. При производстве данного катализатора значительно увеличена доля дорогого компонента (никеля) по массе, который оказывается в значительной мере в объеме катализатора, а не на поверхности. В результате снижается доля дешевого компонента (коксующегося угля), что сильно увеличивает стоимость катализатора в расчете на его единицу массы.
Известен еще один способ, в котором катализатор готовится из соединений никеля и хрома [Патент №2568810 РФ, МПК B01J 23/883, B01J 23/86, B01J 23/78, B01J 21/04, C07C 1/06. Катализатор, способ его приготовления и процесс обогащения смесей углеводородных газов метаном/ Снытников Павел Валерьевич, Кириллов Валерий Александрович, Амосов Юрий Иванович, Собянин Владимир Александрович - 2014142949/04; заяв. 27.10.2014; опубл. 20.11.2015 Бюл. №32]. Сущность данного способа заключается в том, что катализатор готовят смешением кислородсодержащих соединений никеля (в пересчете на основной карбонат никеля 25-60 мас.%), хрома (хром в пересчете на Cr2O3 5-35 мас.%), алюминия (оксид алюминия 5-70 мас.%) и магния (растворенный азотнокислый магний - остальное) с последующими стадиями перемешивания в течение не менее 1 ч при 80-90°C до получения густой массы, сушки, прокаливания при 400°С, таблетирования с графитом или формования.
Среди недостатков данного способа нужно отметить склонность к зауглероживанию в ходе проведения обогащения метаном смесей углеводородных газов, активность катализатора только в температурном интервале 250-350°С и при мольном отношении Н2О/С=0,6-0,7.
Пропиточным методом получение никельхромового катализатора возможно следующим способом [Патент №SU 764 719 A1, МПК B01J23/883, B01J37/02. Способ приготовления никелевого катализатора для гидрирования непредельных соединений/ Андреев Юрий Борисович, Веклов Виталий Александрович, Масагутов Рафгат Мазитович, Морозов Борис Федорович, Панкратова Нина Николаевна- заяв. 2615853, 1978-05-16; опубл. 1980-09-23]. Сущность данного способа заключается в следующем. Полученную окись хрома дополнительно прокаливают при 240°C и пропитывают при комнатной температуре раствором нитрата никеля и мочевины, полученную пасту высушивают при 80-110°C в течение 3-4 ч и затем прокаливают при 300-330°C в течение 1-2 ч.
Данный способ имеет ряд недостатков, основные из которых - большое число стадий прокаливания и длительное время прокаливания, что ведет к большим энергозатратам, а также большое количество воды, которую в последующем необходимо упаривать.
Также возможно получение никельхромового катализатора следующим способом [Патент №2054319 РФ, МПК B01J 23/86, 37/03. Способ приготовления никельхромового катализатора для гидрирования бензола/ Суворин Александр Викторович, Рыжак Игорь Александрович; заявитель и патентообладатель: Государственный Научно-Исследовательский И Проектный Институт Химических Технологий- №925034184,; заявл. 25.03.1992; опубл. 20.02.1996]. Данный метод включает соосаждение активной никельхромовой композиции из раствора, содержащего нитрат никеля и соединение хрома, в присутствии карбамида, промывку, обезвоживание, сушку и прокаливание полученной массы.
Данный способ имеет ряд недостатков, основные из которых - низкая термостойкость катализатора (не более 325°C), громоздкость фильтровального оборудования, наличие больших объемов сточных вод на стадии промывки и фильтрации, большая трудоемкость.
Таким образом, все вышеуказанные способы объединяют следующие недостатки. Необходимо использовать большое количество промывочных вод, во всех способах используется большое количество стадий (в том числе длительных, например, старение, или прокаливание) и общее время приготовления катализатора занимает не менее суток.
Наиболее близким к настоящему патенту по сущности и техническому результату является способ приготовления никель-хромового катализатора для гидрирования органических соединений [Патент №SU 445234 A1, МПК В01J 11/34. Способ приготовления никель-хромового катализатора для гидрирования органических соединений/ Левин С.З. Гуревич Г.С.Шапиро А.Л. Триз В.Е. Блюме Г., Бизенгер Г., Шредер Л., Бетке Г.-И. - заяв. 1689556, 02.08.1971; опубл. 05.03.1976]. Данный способ состоит в следующем: в качестве исходных реагентов для получения никельхромового катализатора гидрирования органических соединений, например, содержащих карбонильную группу (альдегиды, кетоны) используют 6-водный нитрат никеля (II) и 9-водный нитрат хрома (III), которые (стадия 1) смешивают в водном растворе, после чего (стадия 2) проводят осаждение, (стадия 3) фильтрацию, (стадия 4) промывку полученной массы, (стадия 5) сушку ее воздухом, (стадия 6) прокаливают до получения оксидов, (стадия 7) далее осуществляют восстановление в токе водорода.
Данный способ имеет ряд недостатков, основные из которых - это низкая каталитическая активность, использование большого количества промывочных вод, необходима большая скорость подачи водорода, большие трудо- и времязатраты.
Технический результат - снижение количества стадий, снижение количества потребления промывных вод, снижение скорости и времени подачи водорода (т.е. его экономия), повышение активности катализатора.
Указанный результат достигается тем, что в способе получения никельхромового катализатора гидрирования органических соединений, содержащих карбонильную группу, заключающемся в смешении 6-водного нитрата никеля (II) с соединением хрома, получении их оксидов, таблетировании, восстановлении при 470 °С, в токе водорода, согласно изобретению, смешивают до пастообразного состояния 6-7 г аммония двухромовокислого, 10-14 г селитры аммиачной, 6-8 г сахарной пудры, 8-14 г 6-водного нитрата никеля (II), таблетируют, поджигают, осуществляют восстановление в токе водорода со скоростью подачи водорода 1700-1800 час-1 в течение 55-60 минут.
Технический результат достигается за счет использования сухого метода приготовления, что не требует значительного количества промывных вод; количество стадий уменьшено за счет замены стадий осаждения, фильтрации, сушки и прокаливания на использование одной стадии: самораспространяющегося высокотемпературного синтеза, также это позволяет сократить трудо- и времязатраты; за счет бурного выделения газов и высокой температуры возникает вспененная мезопористая структура, которая позволяет обеспечить большую активность катализатора, кроме того за счет высокой температуры в узком слое (более 1000°С) и резкого охлаждения образуется дополнительная фаза (нихромит), что позволило уменьшить время восстановления и снизить расход водорода.
Для осуществления изобретения используют следующие вещества:
1. (NH4)2Cr2O7 Аммоний двухромовокислый ГОСТ 3763-76.
2. NH4NO3 Селитра аммиачная ГОСТ 2-2013.
3. C12H22O11 Сахарная пудра ГОСТ 33222-2015.
4. Ni(NO3)2·6H2O Никель (II) азотнокислый 6-водный ГОСТ 4055-78
5. Водород электролитический марки Б ГОСТ 3022-80
Пример 1. Стадия 1: берут 6 г аммония двухромовокислого, 12 г селитры аммиачной, 6 г сахарной пудры, 10 г 6-водного нитрата никеля (II), осуществляют их смешение (диспергирование и гомогенизацию до пастообразного состояния) в керамической ступке. Стадия 2: полученную пасту помещают в формующую матрицу цилиндрической форма (таблетируют). Стадия 3: полученный цилиндр помещают в тигель и поджигают.Стадия 4: после окончания горения полученный прекурсор помещают в проточный реактор и восстанавливают в токе водорода при 470 °С со скоростью подачи водорода 1700 час-1 в течение 55 минут.После охлаждения до комнатной температуры получается готовый катализатор, который готов к использованию (в том числе к испытаниям его активности).
Пример 2. Берут 6 г аммония двухромовокислого, 12 г селитры аммиачной, 6 г сахарной пудры, 12 г 6-водного нитрата никеля (II), осуществляют их смешение (диспергирование и гомогенизацию до пастообразного состояния) в керамической ступке. Полученную пасту помещают в формующую матрицу цилиндрической форма (таблетируют). Полученный цилиндр помещают в тигель и поджигают. После окончания горения полученный прекурсор помещают в проточный реактор и восстанавливают в токе водорода при 470 °С со скоростью подачи водорода 1800 час-1 в течение 60 минут. После охлаждения до комнатной температуры получается готовый катализатор, который готов к использованию.
Пример 3. Берут 6 г аммония двухромовокислого, 12 г селитры аммиачной, 8 г сахарной пудры, 8 г 6-водного нитрата никеля (II), осуществляют их смешение (диспергирование и гомогенизацию до пастообразного состояния) в керамической ступке. Полученную пасту помещают в формующую матрицу цилиндрической форма (таблетируют). Полученный цилиндр помещают в тигель и поджигают. После окончания горения полученный прекурсор помещают в проточный реактор и восстанавливают в токе водорода при 470 °С со скоростью подачи водорода 1800 час-1 в течение 60 минут. После охлаждения до комнатной температуры получается готовый катализатор, который готов к использованию.
Пример 4. Берут 6 г аммония двухромовокислого, 12 г селитры аммиачной, 8 г сахарной пудры, 14 г 6-водного нитрата никеля (II), осуществляют их смешение (диспергирование и гомогенизацию до пастообразного состояния) в керамической ступке. Полученную пасту помещают в формующую матрицу цилиндрической форма (таблетируют). Полученный цилиндр помещают в тигель и поджигают.После окончания горения полученный прекурсор помещают в проточный реактор и восстанавливают в токе водорода при 470 °С со скоростью подачи водорода 1800 час-1 в течение 60 минут. После охлаждения до комнатной температуры получается готовый катализатор, который готов к использованию.
Пример 5. Берут 7 г аммония двухромовокислого, 12 г селитры аммиачной, 7 г сахарной пудры, 10 г 6-водного нитрата никеля (II), осуществляют их смешение (диспергирование и гомогенизацию до пастообразного состояния) в керамической ступке. Полученную пасту помещают в формующую матрицу цилиндрической форма (таблетируют). Полученный цилиндр помещают в тигель и поджигают. После окончания горения полученный прекурсор помещают в проточный реактор и восстанавливают в токе водорода при 470 °С со скоростью подачи водорода 1800 час-1 в течение 60 минут. После охлаждения до комнатной температуры получается готовый катализатор, который готов к использованию.
Пример 6. Берут 6 г аммония двухромовокислого, 10 г селитры аммиачной, 6 г сахарной пудры, 10 г 6-водного нитрата никеля (II), осуществляют их смешение (диспергирование и гомогенизацию до пастообразного состояния) в керамической ступке. Полученную пасту помещают в формующую матрицу цилиндрической форма (таблетируют). Полученный цилиндр помещают в тигель и поджигают .После окончания горения полученный прекурсор помещают в проточный реактор и восстанавливают в токе водорода при 470 °С со скоростью подачи водорода 1800 час-1 в течение 60 минут. После охлаждения до комнатной температуры получается готовый катализатор, который готов к использованию.
Пример 7. Берут 6 г аммония двухромовокислого, 14 г селитры аммиачной, 6 г сахарной пудры, 10 г 6-водного нитрата никеля (II), осуществляют их смешение (диспергирование и гомогенизацию до пастообразного состояния) в керамической ступке. Полученную пасту помещают в формующую матрицу цилиндрической форма (таблетируют). Полученный цилиндр помещают в тигель и поджигают. После окончания горения полученный прекурсор помещают в проточный реактор и восстанавливают в токе водорода при 470 °С со скоростью подачи водорода 1800 час-1 в течение 60 минут. После охлаждения до комнатной температуры получается готовый катализатор, который готов к использованию.
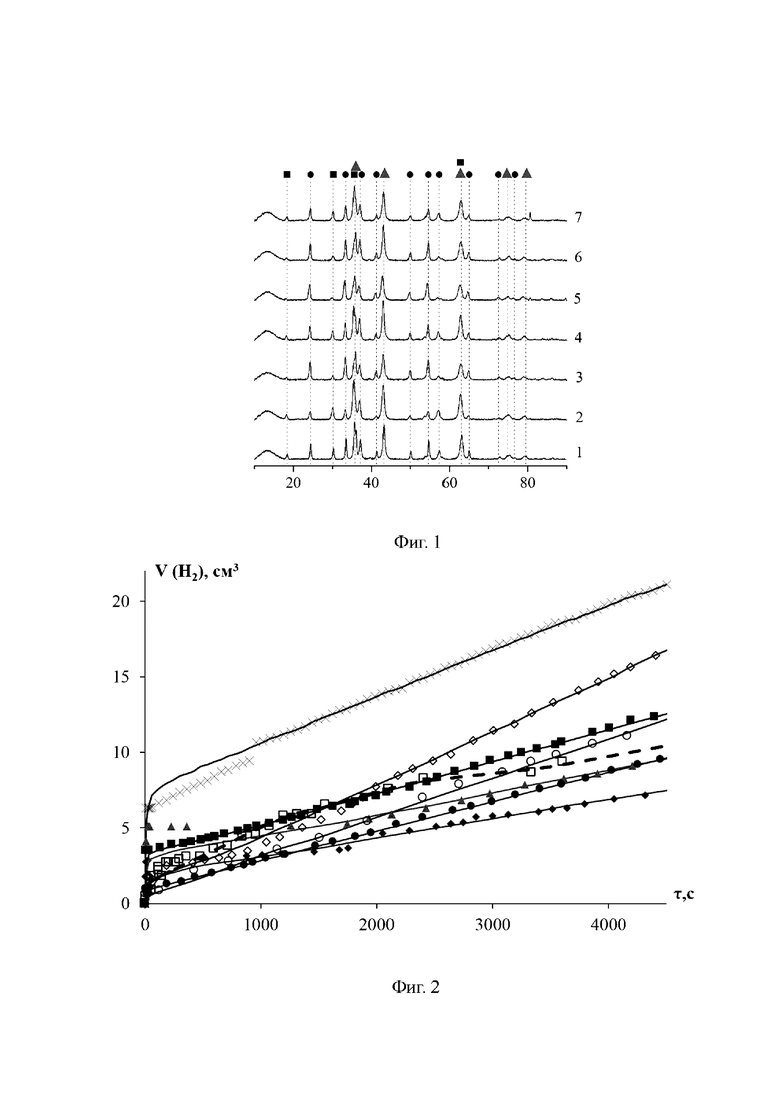
Изобретение поясняется чертежами, где на фиг.1 представлены рентгенограммы полученных образцов, номера справа соответствуют номерам примеров. Для обозначения рефлексов выбраны следующие условные обозначения: ■ - NiCr2O4 (нихромит); ● - Cr2O3 (эсколаит); ▲ - NiO. На фиг.2 приведены кинетические зависимости объема поглощенного водорода в ходе реакции гидрирования ацетона на никельхромовых катализаторах от времени гидрирования, при этом использованы обозначения: ♦ - пример №1; ■ - пример №2; ▲ - пример №3; x - пример №4; ○ - пример №5; ◊ - пример №6; ● - пример №7; □ - прототип.
Состав полученных прекурсоров был определен с помощью дифрактометра POWDIX 600/300 (ЗАО «ЛИНЕВ АДАНИ», Республика Беларусь), а соотношение фаз в этих образцах рассчитывали по полученным данным в программе «Адани Алмаз» версии 2.0.
Массовые доли элементов, входящих в состав полученных образцов, изучали по данным рентгеновского энергодисперсионного анализа с помощью x-ACT (Oxford Instruments NanoAnalysis, Великобритания). Соотношения фаз приведены в таблице 1.
(нихромит), %*
(эсколаит), %*
* по данным рентгенофазного анализа (не учтены аморфные фазы)
** по данным энергодисперсионной спектроскопии (все фазы учтены вместе)
На фиг.2 показаны скорости (r, см3·с-1·г-1(Ni)) поглощения водорода в ходе реакции гидрогенизации ацетона от степени превращения (α) в воде на образцах катализаторов, полученных в примерах (номер кривых соответствует номерам примеров). На чертеже следующими символами обозначены примеры гидрирования на образцах: ♦ - пример №1; ■ - пример №2; ▲ - пример №3; x - пример №4; ○ - пример №5; ◊ - пример №6; ● - пример №7; □ - прототип.
Исследование полученных катализаторов проводили в закрытом реакторе периодического действия, при температуре 30°C, атмосферном давлении, скорость вращения мешалки 3000 об./мин. В ходе восстановления измеряли количество поглощенного водорода от времени. Количество поглощенного водорода приводили к н.у. В качестве гидрируемого модельного соединения, содержащего карбонильную группу, так же, как и в прототипе, был выбран ацетон. Выбор обосновывается тем, что он является простейшим кетоном и не содержит других групп, кроме>C=O, способных к гидрированию, что позволяет упростить анализ полученных данных. Кроме того, он является типичным представителем данного класса, свойства которого широко изучены, и такой выбор традиционен [Патент №SU 1182389 A1, МПК G01N 31/10, B01J 23/86. Способ определения активности медьсодержащих катализаторов гидрирования/ Веклов В. А., Морозов Б. Ф., Панкратова Н. Н. - заяв. 3755188, 1984.04.04; опубл. 1985.09.30] [Павленко, Н. В. ГИДРИРОВАНИЕ АЦЕТОНА / Н.В. Павленко, А. И. Трипольский, Г.И. Голодец // Кинетика и катализ. - 1985. - Т. 26. - №. 1-3. - С.115.].
Для гидрирования использовали следующие реактивы:
1. Ацетон («ХЧ»).
2. Водород электролитический марки Б ГОСТ 3022-80.
3. Вода дистиллированная ГОСТ 6709-72.
Одна из основных характеристик готового катализатора - это его активность, которая приведена в таблице 2 для образцов, полученных по примерам. Скорость реакции гидрирования ацетона в воде при температуре 30 °С и атмосферном давлении водорода отнесенную к 1 грамму катализатора в начальный момент времени (α<0,05) отождествляли с активностью. Так же в таблице 2 приведено время полупревращения для указанных реакций гидрогенизации. Кинетические кривые поглощения водорода приведены на чертеже. Кроме того, в таблицу 2 сведены полное время приготовления катализатора и скорость расхода водорода.
Примера
Аkt,
см3/(мин·г(kt))
τ1/2, мин
* Жирным отмечены параметры, по которым образцы, приготовленные в примерах, превосходят прототип.
1. Активность катализатора;
2. Время полупревращения, мин;
3. Скорость подачи H2, час-1 / время подачи, мин;
4. Общее время приготовления, мин;
5. Общий расход водорода. Расчет общего расхода водорода осуществляли по следующей формуле:
«(общий расход водорода)=(скорость подачи H2) * (время подачи) / 60».
Размерность общего расхода водорода: требуемый объем водорода на единицу объема катализатора;
6. Количество стадий.
Вывод:
Предлагаемый способ позволяет получать катализатор с сопоставимыми или аналогичными характеристиками, при этом в ряде случаев активность выше активности прототипа в 2-4,7 раза. Получение катализатора требует меньшего времени и трудозатрат. Так, общее время приготовления снижается в десять раз, а количество стадий с семи до четырех. Устраняется необходимость использования водных растворов и стадии отмывки, что многократно снижает количество используемой воды. За счет снижения скорости и времени подачи водорода при восстановлении прекурсоров общий расход водорода снижается в 40,5 раза. Таким образом, за счет снижения числа стадий приготовления, времени приготовления и устранения необходимости собирать и перерабатывать побочные продукты - происходит удешевление изготовления катализатора.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ МЕХАНОХИМИЧЕСКОГО СИНТЕЗА НИКЕЛЕВОГО КАТАЛИЗАТОРА ГИДРИРОВАНИЯ | 2021 |
|
RU2796743C1 |
| Способ приготовления никелевого катализатора для гидрирования непредельных соединений | 1978 |
|
SU764719A1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА И СПОСОБ ПОЛУЧЕНИЯ ИЗОПРОПИЛОВОГО СПИРТА С ИСПОЛЬЗОВАНИЕМ ЭТОГО КАТАЛИЗАТОРА | 2022 |
|
RU2808417C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА ДЛЯ ПОЛУЧЕНИЯ ИЗОПРОПИЛОВОГО СПИРТА | 2024 |
|
RU2826605C1 |
| Способ получения изопропилового спирта | 2024 |
|
RU2829730C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА ДЛЯ ПОЛУЧЕНИЯ ИЗОПРОПИЛОВОГО СПИРТА | 2024 |
|
RU2827707C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА ДЛЯ ПОЛУЧЕНИЯ ИЗОПРОПИЛОВОГО СПИРТА | 2024 |
|
RU2825397C1 |
| КАТАЛИЗАТОР, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ И ПРОЦЕСС ОБОГАЩЕНИЯ СМЕСЕЙ УГЛЕВОДОРОДНЫХ ГАЗОВ МЕТАНОМ | 2014 |
|
RU2568810C1 |
| СПОСОБ МЕХАНОХИМИЧЕСКОГО СИНТЕЗА НИКЕЛЕВОГО КАТАЛИЗАТОРА ГИДРИРОВАНИЯ | 2019 |
|
RU2722298C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА ДЛЯ ПОЛУЧЕНИЯ ИЗОПРОПИЛОВОГО СПИРТА | 2022 |
|
RU2800947C1 |
Изобретение относится к химической промышленности. Способ получения никельхромового катализатора гидрирования органических соединений, содержащих карбонильную группу, заключается в смешении 6-водного нитрата никеля (II) с соединением хрома, получении их оксидов, таблетировании, восстановлении при 470 °С, в токе водорода, согласно изобретению смешивают до пастообразного состояния 6-7 г аммония двухромовокислого, 10-14 г селитры аммиачной, 6-8 г сахарной пудры, 8-14 г 6-водного нитрата никеля (II), таблетируют, поджигают, осуществляют восстановление в токе водорода со скоростью подачи водорода 1700-1800 ч-1 в течение 55-60 мин. Технический результат заключается в снижении количества стадий, снижении количества потребления промывных вод, снижении скорости и времени подачи водорода (т.е. его экономия), повышении активности катализатора. 2 ил., 2 табл., 7 пр.
Способ получения никельхромового катализатора гидрирования органических соединений, содержащих карбонильную группу, заключающийся в смешении 6-водного нитрата никеля (II) с соединением хрома, получении их оксидов, таблетировании, восстановлении при 470 °С, в токе водорода, отличающийся тем, что смешивают до пастообразного состояния 6-7 г аммония двухромовокислого, 10-14 г селитры аммиачной, 6-8 г сахарной пудры, 8-14 г 6-водного нитрата никеля (II), таблетируют, поджигают, осуществляют восстановление в токе водорода со скоростью подачи водорода 1700-1800 час-1 в течение 55-60 мин.
| Способ приготовления никель-хромового катализатора для гидрирования органических соединений | 1971 |
|
SU445234A1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ НИКЕЛЕВОГО КАТАЛИЗАТОРА ДЛЯ ГИДРИРОВАНИЯ НЕПРЕДЕЛЬНЫХ, АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ И КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ | 1993 |
|
RU2050190C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ НИКЕЛЬХРОМОВОГО КАТАЛИЗАТОРА ДЛЯ ГИДРИРОВАНИЯ БЕНЗОЛА | 1992 |
|
RU2054319C1 |
| Способ приготовления никелевого катализатора для гидрирования непредельных соединений | 1978 |
|
SU764719A1 |
| КАТАЛИЗАТОР, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ И ПРОЦЕСС ОБОГАЩЕНИЯ СМЕСЕЙ УГЛЕВОДОРОДНЫХ ГАЗОВ МЕТАНОМ | 2014 |
|
RU2568810C1 |
| CN 110013854 A, 16.07.2019. | |||
Авторы
Даты
2023-10-02—Публикация
2023-02-17—Подача