Изобретение относится к электротехнической промышленности, к устройствам для непосредственного преобразования химической энергии в электрическую, в частности к разработке состава электролита для первичного химического источника тока с алюминиевым анодом.
Перспективность использования алюминия в источниках тока объясняется величиной объёмной удельной ёмкости алюминия в качестве анодного материала (8.04 мА⋅ч/см3), значительно превышающей аналогичную величину для лития (2.06 мА⋅ч/см3) и других используемых в источниках тока анодных материалов.
Известен первичный химический источник тока с алюминиевым анодом и катодом из диоксида марганца. В качестве электролита применяется водный раствор хлорида марганца [1]. В [2] предложен первичный химический источник, включающий анод из алюминия или его сплавов, и пастированный положительный электрод, содержащий хлорид алюминия гексагидрат с добавками хроматов аммония, натрия и калия. Деполяризатором служит диоксид марганца. Необходимая консистенция пасты достигается введением воды. В [3] запатентован химический источник, включающий анод из алюминия или его сплавов, электролит на основе водного раствора хлорида хрома в чистом виде, либо в комбинации с добавками хлоридов аммония и алюминия, а также хроматов аммония, натрия и калия. Как и в [2], катодная паста содержит диоксид марганца в качестве деполяризатора. Известен первичный химический источник тока [4], включающий анод на основе алюминия или его сплавов, водный электролит, содержащий галогениды, а также сульфаты или нитраты. В качестве активного материала положительного электрода используется ряд оксидов металлов. Предпочтение отдаётся диоксиду марганца. В [5] запатентован источник тока с отрицательным электродом из алюминия или его сплавов и положительным электродом на основе диоксида марганца. В качестве электролита использован водный раствор сульфатов или нитратов с добавками ряда органических соединений.
Недостаток данных технических решений (с использованием алюминиевого анода в водных электролитах) осложняется активным выделением водорода на аноде, что обусловлено величиной стандартного потенциала алюминия (-1.66 В). Это приводит к ускоренному саморазряду таких источников тока. Замена водного электролита на неводный, как и существенное уменьшение доли воды в случае использования водноорганических электролитов, позволяет уменьшить скорость выделения водорода на алюминии и, таким образом, снизить скорость саморазряда источника тока.
В большинстве работ, направленных на создание первичного источника тока с алюминиевым анодом в неводном электролите, авторы ограничивались исследованием поведения только алюминиевого электрода, уделяя внимание, главным образом, способам предварительной обработки алюминия и поиску оптимального состава электролита. Вместе с тем, в ряде работ приводятся разрядные характеристики алюминиевого электрода.
В [6] исследовано анодное растворение предварительно обработанного алюминия в растворе LiClO4 в смеси пропиленкарбоната и диметоксиэтана и в растворе LiAICl4 в пропиленкарбонате. В [7-9] было установлено, что в двух электролитах - хлориде алюминия в γ-бутиролактоне и тетраэтиламмония хлорида в γ-бутиролактоне и ацетонитриле алюминиевый электрод показывает достаточно высокую электрохимическую активность. Введение в электролит соединений ртути и галлия сдвигает стационарный потенциал алюминия на 150, 250 мВ в сторону отрицательных значений и позволяет существенно увеличить электрохимическую активность алюминия.
Электрохимическое поведение Al зависит не только от применяемого электролита, но в значительной мере и от предварительной обработки его поверхности. В [6] обработка включала применение соединений ртути для разрушения защитного слоя оксида на алюминии. В [7-9] электрод обрабатывали 10 М раствором КОН, отмывали водой, сушили, полировали алмазным надфилем и обезжиривали ацетоном, после чего на электроде было проведено несколько циклов вольтамперометрии в рабочем электролите.
Вышеупомянутые методы предварительной обработки позволяют сместить потенциал алюминия в сторону отрицательных значений и увеличить плотность разрядных токов. Однако столь сложная предварительная обработка электродов затрудняет практическое использование алюминия в качестве анода в источниках тока.
Наиболее близким к заявляемому (т.е. прототипом) является исследование анодного поведения алюминия (как потенциального анода в источниках тока), в растворе гидроксида калия (КОН) в этаноле с различным содержанием воды вплоть до 10% [10], однако авторы [10] не рассматривали разрядные характеристики алюминия.
Цель настоящего изобретения - разработка электролита для первичного источника тока с алюминиевым отрицательным электродом (анодом).
Технический результат, достигаемый настоящим изобретением, заключается в увеличении плотности разрядного тока на алюминии и смещении его потенциала в сторону отрицательных значений.
Технический результат достигается тем, что в качестве электролита используются растворы гидроксида калия в смеси этанола с водой с добавками соединений галлия и индия (2 М раствор КОН в этаноле, содержащем 4% об. воды, с добавками 5 ∙10-5 M Ga(NO3)3 и 10-3 M In(NO3)3).
Введение этих соединений позволяет существенно сместить потенциал алюминиевого электрода в сторону отрицательных значений, по сравнению с тем, что наблюдается в электролите без введения указанных выше добавок (прототип).
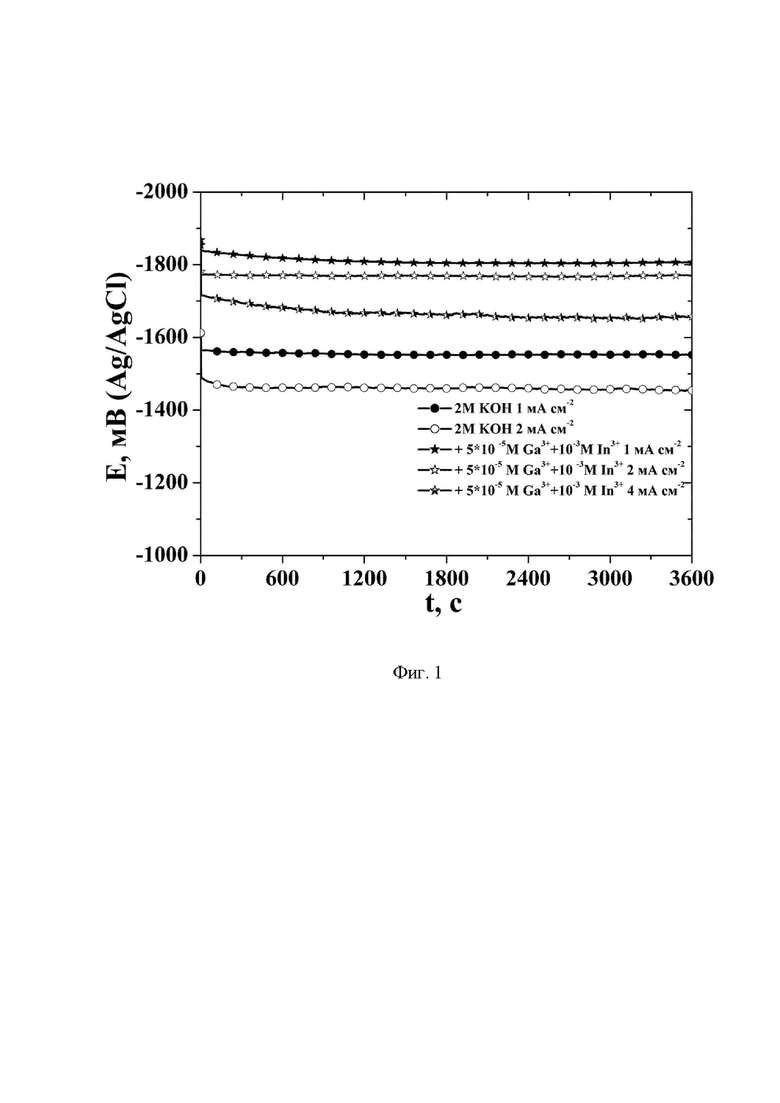
Сущность заявленного изобретения в дальнейшем поясняется детальным описанием, примером и графиком (фиг.1), на котором изображены гальваностатические разрядные кривые на Al электроде.
Приведённые на фиг.1 разрядные кривые на алюминиевом электроде в 2 М растворе КОН в 96% об. этаноле без добавок и с добавками нитрата галлия и индия служат иллюстрацией достигнутого технического результата. Разряд алюминиевого электрода при введении добавок протекает при более отрицательных потенциалах, чем в электролите аналогичном прототипу. Величины потенциалов отличаются на 300 мВ.
Активация алюминия проводится непосредственно в рабочем электролите, без его предварительной обработки. Изолирующий оксидный слой на электроде разрушается при контакте с электролитом.
Пример.
Изготовлен макет источника тока с алюминиевым анодом и катодом на основе диоксида марганца. Катодная активная масса состоит из 85% вес. MnO2, 10% вес. ацетиленовой сажи и 5% вес. политетрафторэтилена. В качестве электролита использован 2 М раствор КОН в этаноле, содержащем 4% об. воды, с добавками 5 ∙10-5 M Ga(NO3)3 и 10-3 M In(NO3)3. Напряжение разомкнутой цепи макета равно 1.8 В.
Скорость выделения водорода на аноде в указанном выше электролите в 9 раз меньше скорости выделения водорода в 2 М растворе КОН в воде.
Литература:
[1] US Patent 2638489 Primery cell 1953
[2] US Patent 2838591 Primery cell. 1958
[3] US Patent 3307976 Primery cell. 1967
[4] US Patent 6589692 Aluminum battery with aluminum-containing negative electrode. 2003 г
[5] US Patent 7455936 Electric cell 2008
[6] K.V Rybalka, L.A Beketaeva, Anodic dissolution of aluminium in nonaqueous lectrolytes, J. of Power Sources, vol. 42, p. 377 (1993)
[7] Licht, S., Levitin, G., Yarnitzky, C., Tel-Vered, R., Organic phase for aluminum batteries, Electrochemical and solid-state letters, 1999, vol.2, No. 6, p. 262.
[8] Licht, S., Tel-Vered, R., Levitin, G., Yarnitzky, C., Solution activators of aluminum electrochemistry in organic media, J.Electrochem.Soc. , 2000, vol.147, No 2, p.496.
[9] Tel-Vered, R., Levitin, G., Yarnitzky, C., Licht, S., Analytical determination of In activation of aluminum anodes in the organic phase, Rev. Anal. Chem., 1999, vol.18, No.5, p. 249.
[10] Shao, H.B., Wang, J.M., Wang, X.Y., Zhang, J.O., Cao, C.N., Anodic dissolution of aluminum in KOH ethanol solutions, Electrochem. Comm., 2004, vol. 6, p. 6.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ НАНЕСЕНИЯ СМАЧИВАЕМОГО ПОКРЫТИЯ ПОДИНЫ АЛЮМИНИЕВОГО ЭЛЕКТРОЛИЗЕРА | 2005 |
|
RU2299278C2 |
| АНОД ДЛЯ ХИМИЧЕСКОГО ИСТОЧНИКА ТОКА, СПОСОБ ИЗГОТОВЛЕНИЯ АНОДА, ХИМИЧЕСКИЙ ИСТОЧНИК ТОКА | 2010 |
|
RU2444093C1 |
| СПОСОБ ПЕРЕРАБОТКИ ЛИТИЙ-ИОННЫХ АККУМУЛЯТОРОВ С ПОЛУЧЕНИЕМ КОМПОНЕНТОВ ПОЛОЖИТЕЛЬНОГО ЭЛЕКТРОДА ЩЕЛОЧНЫХ АККУМУЛЯТОРОВ | 2022 |
|
RU2789852C1 |
| СИНТЕЗ НАНОСТРУКТУРИРОВАННОГО ФОСФАТА ЛИТИЯ-ЦИРКОНИЯ | 2021 |
|
RU2833251C1 |
| Металл-серный проточный аккумулятор | 2023 |
|
RU2820527C2 |
| СПОСОБ АНОДИРОВАНИЯ ПОЛОЙ ДЕТАЛИ ИЗ АЛЮМИНИЕВОГО СПЛАВА | 2023 |
|
RU2827632C1 |
| АЛЮМИНИЙ-ИОННАЯ БАТАРЕЯ | 2018 |
|
RU2701680C1 |
| СПОСОБ ЭКСПЛУАТАЦИИ АЛЮМИНИЙ-ВОЗДУШНОГО ГАЛЬВАНИЧЕСКОГО ЭЛЕМЕНТА | 2015 |
|
RU2618440C2 |
| ЭЛЕКТРИЧЕСКИЙ АККУМУЛЯТОР И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2015 |
|
RU2689413C2 |
| Литий-ионный аккумулятор | 2024 |
|
RU2834388C1 |
Изобретение относится к электротехнической промышленности, к устройствам для непосредственного преобразования химической энергии в электрическую, в частности к разработке состава электролита для первичного химического источника тока с алюминиевым анодом. Технический результат заключается в увеличении плотности разрядного тока на алюминии и смещении его потенциала в сторону отрицательных значений. Технический результат достигается тем, что в качестве электролита используются растворы гидроксида калия в смеси этанола с водой с добавками соединений галлия и индия. 1 з.п. ф-лы, 1 ил., 1 пр.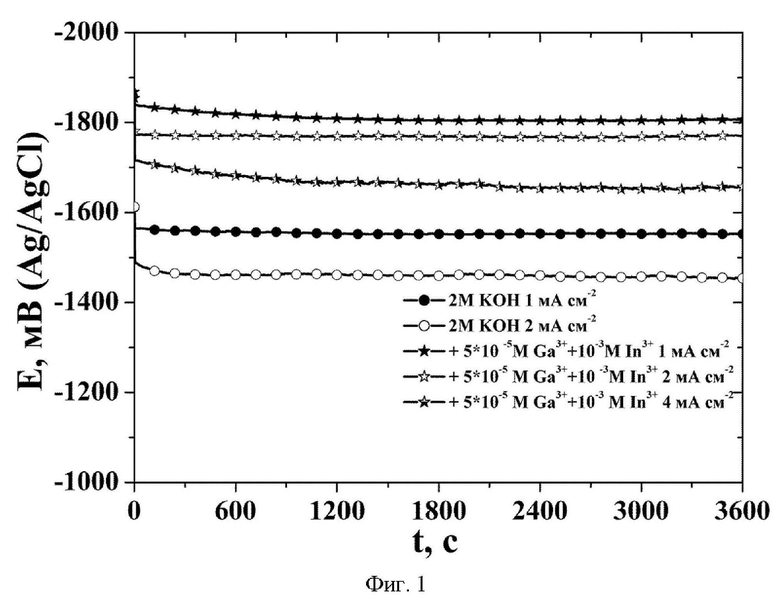
1. Электролит для первичного источника тока с алюминиевым анодом, состоящий из раствора гидроксида калия в смеси этанола с водой с добавками соединений галлия и индия.
2. Электролит по п. 1, включающий 2 М раствор КОН в этаноле, содержащем 4% об. воды, с добавками 5⋅10-5 M Ga(NO3)3 и 10-3 M In(NO3)3.
| Shao, H.B., Wang, J.M., Wang, X.Y., Zhang, J.O., Cao, C.N., Anodic dissolution of aluminum in KOH ethanol solutions, Electrochem | |||
| Comm., 2004, vol | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| US 6589692 B2, 08.07.2003 | |||
| US 3307976 A, 07.03.1967 | |||
| US 7455936 B2, 25.11.2008 | |||
| ГАЛЬВАНИЧЕСКИЙ ЭЛЕМЕНТ И БАТАРЕЯ НА ОСНОВЕ ЭЛЕКТРОГЕНЕРИРУЮЩЕГО МАТЕРИАЛА | 2012 |
|
RU2596214C2 |
Авторы
Даты
2023-10-17—Публикация
2023-05-30—Подача