Область техники, к которой относится изобретение
Настоящее изобретение относится к способу получения фосфата лития-циркония путем пламенного распылительного пиролиза, фосфату лития-циркония, получаемого этим способом, и его применению в литий-ионных аккумуляторных батареях.
Уровень техники
Вторичные литий-ионные аккумуляторные батареи являются наиболее важным типом использующихся в настоящее время аккумуляторных батарей. Вторичные литий-ионные аккумуляторные батареи обычно состоят из анода, изготовленного из углеродного материала или сплава литий-металл, катода, изготовленного из оксида лития-металла, электролита, в котором соль лития растворена в органическом растворителе, и разделителя, обеспечивающего перемещение ионов лития между положительным и отрицательным электродами во время процедур заряда и разряда.
В настоящее время при попытках разработать вторичные аккумуляторные батареи, обладающие улучшенной внутренней безопасностью и плотностью энергии, значительные успехи достигнуты при использовании твердых электролитов вместо жидких. Предполагается, что входящие в число таких систем вторичные литиевые аккумуляторные батареи с электродами, изготовленными из сплавов литий-металл, обеспечивают высокую плотность энергии и являются наиболее подходящими. Для того, чтобы такие вторичные твердотельные литий-ионные аккумуляторные батареи обладали необходимыми характеристиками нагрузки, они должны обладать хорошей ионной проводимостью на границе между активным материалом электрода и электролитом. Эту высокую ионную проводимость можно обеспечить путем нанесения на поверхность активного материала электрода покрытия из некоторых содержащих литий соединений, таких как LiTi2(PO4)3, как это описано в JP 4982866 В2.
H. Xiea, et al. в публикации Journal of Power Sources 2011, vol. 196, pp. 7760-7762 описывают получение Li1,2Zr1,9Ca0,1(PO4)3 путем проводимой в твердой фазе реакции ZrO2 с Li2CO3, NH4H2PO4, и СаСО3. Обнаружено, что проводимость этого фосфата лития-циркония по ионам Li является сравнимой с проводимостью Li1,3Ti1,7Al0,3(PO4)3, использующегося в качестве твердого разделителя для Li-ионов в испытуемых элементах Li-ионных аккумуляторных батареях.
Таким образом, фосфаты лития-циркония являются перспективными проводящими по ионам Li материалами, использующимися в литий-ионных аккумуляторных батареях, в особенности, в твердотельных аккумуляторных батареях.
Y. Li, et al. в публикации PNAS, 2016, vol. 113 (47), pp. 13313-13317 описывают получение обладающего ромбоэдрической структурой LiZr2(PO4)3 путем проводимой в твердой фазе реакции (NH4)2HPO4 с Li2CO3 и ацетатом циркония, и его применение в качестве твердого электролита в твердотельных литий-ионных аккумуляторных батареях Li/LiFePO4.
I. Hanghofer, et al. в публикации Dalton Trans., 2019, vol. 48, pp. 9376-9387 описывают получение обладающего ромбоэдрической структурой Li1,4Ca0,2Zr1,8(PO4)3, стабилизированного с помощью Са, путем проводимой в твердой фазе реакции Li2CO3, (NH4)2HPO4 и СаСО3 с ZrO2 или с ацетатом циркония, применимого в качестве твердого электролита, предназначенного для применения в твердотельных литий-ионных аккумуляторных батареях.
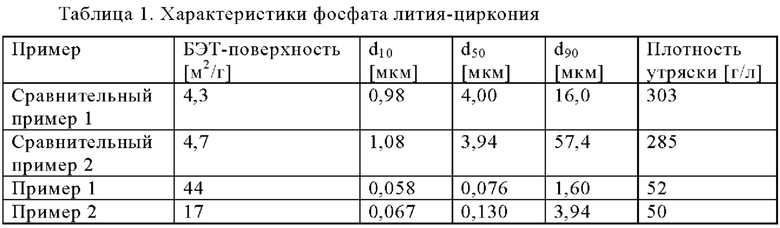
Фосфаты лития-циркония, полученные путем синтеза в твердой фазе, обычно обладают сравнительно высокими плотностями и низкими значениями БЭТ-поверхности (удельная поверхность, определенная по методике Брунауэра-Эммета-Теллера), которые являются хорошо подходящими при применении таких материалов, например, в качестве материала ядра твердого электролита литий-ионной аккумуляторной батареи.
Однако, если предполагается применение таких соединений в качестве добавок, которые можно равномерно распределить на материале ядра или на его поверхности, то меньший размер частиц, более низкая плотность материала и более высокое значение БЭТ-поверхности являются критически важными.
Задача и решение
Задачей настоящего изобретения является разработка улучшенного способа промышленного производства кристаллических фосфатов лития-циркония, применимых в литий-ионных аккумуляторных батареях, в особенности в качестве материала покрытия или легирующего материала для электродов литий-ионных аккумуляторных батарей, в особенности, анодов, и в качестве добавок для электролитов литий-ионных аккумуляторных батарей.
Точнее, необходимо, чтобы этот способ обеспечивал получение частиц фосфата лития-циркония, обладающих сравнительно небольшим размером, высоким значением БЭТ-поверхности и низкой плотностью утряски.
Распылительный пиролиз является известной методикой получения различных оксидов металлов и определенных солей металлов.
При проведении распылительного пиролиза содержащие металл соединения, находящиеся в виде мелких капелек, вводят в зону высокой температуры, в которой их окисляют и/или гидролизуют и получают соответствующие оксиды или соли металлов. Особой разновидностью этой методики является пламенный распылительный пиролиз, при проведении которого капельки вводят в пламя, которое образуется при воспламенении топливного газа и содержащего кислород газа.
В US 2013/0316233 A1 в общем раскрыт способ получения измельченной смеси, подходящей для использования в качестве активного материала катода литий-ионных аккумуляторных батарей, включающий подачу в пламя аэрозоля, полученного из растворов, содержащих источник лития, источник переходного металла и источник фосфора, вместе со способствующим горению газом и горючим газом. Переходный металл может быть выбран из числа следующих: Fe, Mn, Ti, Cr, V, Ni, Со, Cu, Zn, Al, Ge, Zr, Mo, W; источник фосфора может быть выбран из числа следующих: фосфорные кислоты, фосфаты аммония, фосфат натрия и фосфат железа. В приведенных в этой заявке на патент конкретных примерах описано получение только фосфатов лития-железа. В US 2013/0316233 A1 не раскрыт синтез фосфат лития-циркония. В соответствии с общим раскрытием, приведенном в US 2013/0316233 A1, для успешного проведения синтеза этого соединения необходимо проведение трудоемкой работы по выбору соответствующего источника лития, источника металла, источника фосфора, растворителя и условий проведения способа. Даже при этом не ясно, можно ли вообще этим способом получить фосфат лития-циркония, обладающий высоким значением БЭТ-поверхности и низкой плотностью.
В ходе проведения тщательных экспериментальных исследований согласно изобретению неожиданно было обнаружено, что смешанные фосфаты лития-циркония, частицы которых обладают необходимыми характеристиками, в действительности можно получить по методике пламенного распылительного пиролиза. Однако обнаружено, что использование в способе, предлагаемом в настоящем изобретении, особой комбинации предшественников металлов и фосфора, и растворителей является критически важным для получения частиц, обладающих необходимыми характеристиками, предлагаемыми в настоящем изобретении.
Фосфат лития-циркония
Настоящее изобретение относится к фосфату лития-циркония общей формулы LiaZrbMc(PO4)d, в которой М обозначает по меньшей мере один металл, отличающийся от Li и Zr, 0,5≤а≤5,0, 0,5≤b≤5,0, 0≤с≤5, 1≤d≤5, отличающемуся тем, что фосфат лития-циркония
- находится в виде агрегированных первичных частиц,
- обладает значением БЭТ-поверхности, равным 5-100 м2/г,
- обладает среднечисловым диаметром частиц, определенным с помощью статического светорассеяния (ССР), d50=0,03-2 мкм, и
- обладает плотностью утряски, равной 20-200 г/л.
Фосфат лития-циркония, предлагаемый в настоящем изобретении, можно получить способом, предлагаемым в настоящем изобретении, описанным ниже.
В общей формуле фосфата лития-циркония, предлагаемого в настоящем изобретении, LiaZrbMc(PO4)d, М может обозначать один или несколько элементов, выбранных из группы, состоящей из следующих: Na, K, Be, Mg, Са, Sr, Ва, Zn, Со, Ni, Cu, Mn, В, Al, Ga, In, Fe, Sc, Y, La, Ti, Zr, Hf, Ce, Si, Ge, Sn, Pb, V, Nb, Та, Mo, W. Предпочтительно, если M=Са.
Состав фосфата лития-циркония, предлагаемого в настоящем изобретении, предпочтительно соответствует формуле Li0,8-1,5Zr1,5-2,5M0-0,5(PO4)2,5-3,5, более предпочтительно формуле Li1,0-1,3Zr1,8-2,2M0-0,3(PO4)2,8-3,2.
Фосфат лития-циркония, предлагаемый в настоящем изобретении, обладает значением БЭТ-поверхности, равным 5-100 м2/г, предпочтительно равным 7-80 м2/г, более предпочтительно равным 15-60 м2/г.
Значение БЭТ-поверхности можно определить в соответствии со стандартом DIN 9277:2014 по адсорбции азота в соответствии с методикой Брунауэра-Эммета-Теллера.
Фосфат лития-циркония, предлагаемый в настоящем изобретении, находится в виде агрегированных первичных частиц, среднечисловой диаметр первичных частиц, определенный с помощью трансмиссионной электронной микроскопии (ТЭМ), обычно равен 1-100 нм, предпочтительно 3-70 нм, более предпочтительно 5-50 нм. Этот среднечисловой диаметр d50 можно определить путем определения среднего размера по меньшей мере 500 частиц, исследованных с помощью ТЭМ.
Среднечисловой диаметр частиц фосфата лития-циркония, находящихся в агрегированной и необязательно агломерированной форме, d50, определенный с помощью статического светорассеяния (ССР) после обработки смеси, состоящей из 5 мас. % частиц и 95 мас. % 0,5 г/л раствора пирофосфата натрия в воде, ультразвуком при 25°С в течение 300 с равен примерно 0,03-2 мкм, более предпочтительно 0,04-1 мкм, еще более предпочтительно 0,05-0,5 мкм.
Агломераты и в некоторой степени агрегаты можно разрушить, например, путем размола частиц или обработки частиц ультразвуком, это приводит к получению более мелких частиц, обладающих более узким распределением по размерам.
Фосфат лития-циркония, предлагаемый в настоящем изобретении, обладает плотностью утряски, равной 20-200 г/л, предпочтительно 25-150 г/л, еще более предпочтительно 30-100 г/л, еще более предпочтительно 40-80 г/л.
Плотность утряски порошкообразного или крупнозернистого гранулированного материала можно определить в соответствии со стандартом DIN ИЗО 787-11:1995 "General methods of test for pigments and extenders -- Part 11: Determination of tamped volume and apparent density after tamping". Эта процедура включает определение кажущейся вязкости слоя после встряхивания и уплотнения.
Способ получения фосфата лития-циркония
Настоящее изобретение также относится к способу получения фосфата лития-циркония, предлагаемого в настоящем изобретении, проводимому путем пламенного распылительного пиролиза, в котором проводят пламенный распылительный пиролиз по меньшей мере одного раствора предшественников металлов, содержащего
- карбоксилат лития и карбоксилат циркония, где каждый из этих карбоксилатов металлов содержит от 5 до 20 атомов углерода,
- органический фосфат,
- растворитель, содержащий менее 10 мас. % воды.
В ходе проведения способа пламенного распылительного пиролиза, предлагаемого в настоящем изобретении, раствор содержащих металл соединений (предшественников металлов) и источника фосфора, находящийся в виде мелких капелек, обычно вводят в пламя, которое образовано при воспламенении топливного газа и содержащего кислород газа, где использующиеся предшественники металлов вместе с источником фосфора окисляют и/или гидролизуют и получают соответствующий фосфат лития-циркония.
В ходе этой реакции сначала образуются мелкодисперсные почти сферические первичные частицы, которые при дальнейшем протекании реакции слипаются с образованием агрегатов. Затем эти агрегаты могут объединяться с образованием агломератов. В отличие от агломератов, которые, как правило, сравнительно легко можно разделить на агрегаты путем подачи энергии, агрегаты дополнительно разрушаются только при интенсивной подаче энергии, если они вообще разрушаются.
Полученное находящееся в форме агрегатов соединение можно назвать "пирогенным" или "полученным по пирогенной технологии" фосфатом лития-циркония.
Способ пламенного распылительного пиролиза в общем описан в WO 2015173114 А1 и в других публикациях.
Предпочтительно, если способ пламенного распылительного пиролиза, предлагаемый в настоящем изобретении, включает следующие стадии: а) атомизация раствора предшественников металлов с помощью атомизирующего газа с получением аэрозоля,
b) проводимое в реакционном пространстве реактора введение аэрозоля в реакцию с пламенем, полученным путем воспламенения смеси топливного газа и содержащего кислород газа, с получением реакционного потока,
c) охлаждение реакционного потока и
d) последующее удаление твердого фосфата лития-циркония из реакционного потока.
Примерами топливных газов являются водород, метан, этан, природный газ и/или монооксид углерода. Особенно предпочтительно использовать водород. Топливный газ используют, в частности, в вариантах осуществления, в которых необходимо обеспечение высокой степени кристалличности полученного фосфата лития-циркония.
Содержащим кислород газом обычно является воздух или обогащенный кислородом воздух. Содержащий кислород газ используют, в частности, в вариантах осуществления, в которых, например, необходимо обеспечение высокого значения БЭТ-поверхности полученного фосфата лития-циркония. Полное количество кислорода обычно выбирают таким образом, чтобы оно являлось достаточным для обеспечения полного превращения топливного газа и предшественников металлов.
Для получения аэрозоля превращенный в пар раствор, содержащий предшественники металлов, можно смешать с атомизирующим газом, таким как азот, воздух и/или другие газы. Полученные капельки аэрозоля предпочтительно обладают средним размером, равным 1-120 мкм, особенно предпочтительно равным 30-100 мкм. Капельки обычно получают с использованием сопел для подачи одного или множества материалов. Для улучшения растворимости предшественники металлов и обеспечения вязкости, подходящей для атомизации раствора, раствор можно нагреть.
Предшественники металлов, использующиеся в способе, предлагаемом в настоящем изобретении, включают по меньшей мере один карбоксилат лития и по меньшей мере один карбоксилат циркония, каждый из них содержит от 5 до 20 атомов углерода.
Карбоксилатами лития и циркония, использующимися в способе, предлагаемом в настоящем изобретении, независимо друг от друга могут являться линейный, разветвленный или циклический пентаноат (С5), гексаноат (С6), гептаноат (С7), октаноат (С8), нонаноат (С9), деканоат (С10), ундеканоат (С11), додеканоат (C12), тридеканоат (C13), тетрадеканоат (C14), пентадеканоат (С15), гексадеканоат (С16), гептадеканоат (С17), октадеканоат (C18), нонадеканоат (С19), икозаноат (С20) лития и/или циркония, и их смеси.
Наиболее предпочтительно, если используют 2-этилгексаноат (C8) циркония и неодеканоат (С10) лития.
Использующиеся предшественники металлов могут включать карбоксилаты или другие соли металлов, отличающихся от лития и циркония.
Предшественниками металлов, отличающихся от лития и циркония, также могут являться неорганические соединения металлов, такие как нитраты, карбонаты, хлориды, бромиды, или другие органические соединения металлов, такие как алкоксиды, например, этоксиды, н-пропоксиды, изопропоксиды, н-бутоксиды и/или трет-бутоксиды.
Термин "органический фосфат" в контексте настоящего изобретения означает любое соединение, включающее по меньшей мере одну группу (R), содержащую по меньшей мере один атом углерода, связанный с атомом фосфора звена Р(=O) через атом кислорода, например, соединение общей формулы (RO)3Р(=O) или (RO)(P(=O))2, в которой R обозначает группу, содержащую по меньшей мере один атом углерода, например, метил или этил.
Органический фосфат, использующийся в способе, предлагаемом в настоящем изобретении, предпочтительно выбран из числа следующих: эфиры фосфорной кислоты (Н3РО3), ортофосфорной кислоты (Н3РО4), метафосфорной кислоты (НРО3), пирофосфорной кислоты (Н4Р2О7), полифосфорных кислот и их смеси.
Органический фосфат может быть выбран из числа следующих: сложные алкиловые эфиры, такие как метиловый, этиловый, пропиловый, бутиловый, гексиловый эфиры, сложные ариловые эфиры, такие как фениловый эфир, смешанные сложные алкиловые/ариловые эфиры и их смеси.
Предпочтительно, если органическим фосфатом является сложный эфир, включающий группы, содержащие от 1 до 10 атомов углерода, наиболее предпочтительно алкильные группы, содержащие от 1 до 10 атомов углерода.
Согласно изобретению неожиданно было обнаружено, что использование органических фосфатов в качестве источника фосфора является критически важным для получения мелких частиц фосфата лития-циркония, обладающих высоким значением БЭТ-поверхности и низкой плотностью утряски.
Смесь растворителей, использующаяся в способе, предлагаемом в настоящем изобретении, может быть выбрана из группы, состоящей из следующих: линейные или циклические, насыщенные или ненасыщенные, алифатические или ароматические углеводороды, эфиры карбоновых кислот, простые эфиры, спирты, карбоновые кислоты и их смеси.
Смесь растворителей, использующаяся в способе, предлагаемом в настоящем изобретении, содержит менее 10 мас. % воды, предпочтительно менее 5 мас. % воды, более предпочтительно менее 3 мас. % воды, еще более предпочтительно менее 2 мас. % воды, еще более предпочтительно менее 1 мас. % воды.
Низкое содержание воды предотвращает протекание нежелательного гидролиза карбоксилата циркония в растворе предшественника металла.
Полное содержание металла в растворе предшественников металлов предпочтительно составляет 1-30 мас. %, более предпочтительно 2-20 мас. %, еще более предпочтительно 3-15 мас. %. Термин "полное содержание металла" означает суммарную массовую долю всех металлов, содержащихся в предшественниках металлов, находящихся в использующемся растворе предшественников металлов.
Смесь растворителей, использующаяся в способе, предлагаемом в настоящем изобретении, может дополнительно содержать хелатный агент, т.е. соединение, способное образовывать две или большее количество координационных связей с ионами металлов. Примерами таких хелатных агентов являются, например, диамины, такие как этилендиамин, этилендиаминтетрауксусная кислота (ЭДТК) и 1,3-дикарбонильные соединения, такие как ацетилацетон и алкилацетилацетаты. Наиболее предпочтительно, если в качестве такого хелатного агента используют ацетилацетон.
Согласно изобретению было обнаружено, что в присутствии таких хелатных агентов некоторые предшественники металлов, например, соединения циркония, обладают лучшей растворимостью и не осаждаются в течение сравнительно длительного времени хранения.
Использование особой комбинации предшественников металлов, источника фосфора и растворителя в способе, предлагаемом в настоящем изобретении, обеспечивает возможность хорошей растворимости всех предшественников и получения частиц фосфата лития-циркония, обладающих необходимыми характеристиками, такими как небольшой размер частиц, высокое значение БЭТ-поверхности и низкая плотность утряски.
Способ, предлагаемый в настоящем изобретении, может дополнительно включать стадию термической обработки фосфата лития-циркония, полученного путем пламенного распылительного пиролиза.
Эту дополнительную термическую обработку предпочтительно проводят при температуре, равной 600-1300°С, более предпочтительно при 650-1250°С, еще более предпочтительно при 700-1200°С, еще более предпочтительно при 750-1150°С.
Термическая обработка, соответствующая способу, предлагаемому в настоящем изобретении, обеспечивает возможность получения подвергнутого термической обработке фосфата лития-циркония, обладающего необходимыми характеристиками, в особенности, необходимой кристаллической структурой.
Способ, предлагаемый в настоящем изобретении, может включать дополнительную стадию размола, предпочтительно размола в шаровой мельнице подвергнутого термической обработке фосфата лития-циркония.
Размол в шаровой мельнице предпочтительно проводят с использованием изготовленных из ZrO2 шаров, например, обладающих диаметром, равным примерно 0,5 мм, в подходящем растворителе, таком как этанол или изопропанол.
Применение фосфата лития-циркония в литий-ионных аккумуляторных батареях
Настоящее изобретение также относится к применению фосфата лития-циркония, предлагаемого в настоящем изобретении, в литий-ионных аккумуляторных батареях, в особенности, в качестве компонента твердого электролита литий-ионной аккумуляторной батареи, в качестве добавки в жидком или гелеобразном электролите, или в качестве компонента электрода литий-ионной аккумуляторной батареи.
Настоящее изобретение также относится к литий-ионной аккумуляторной батарее, включающей фосфат лития-циркония, предлагаемый в настоящем изобретении, или фосфат лития-циркония, получаемый способом, предлагаемым в настоящем изобретении.
Литий-ионная аккумуляторная батарея, предлагаемая в настоящем изобретении, может включать активный положительный электрод (катод), анод, разделитель и электролит, включающий соединение, содержащее литий.
Положительный электрод (катод) литий-ионной аккумуляторной батареи обычно включает токосъемник и слой активного катодного материала, образованный на токосъемнике.
Токосъемником может являться алюминиевая фольга, медная фольга, никелевая фольга, изготовленная из нержавеющей стали фольга, титановая фольга, полимерная подложка с покрытием из проводящего ток металла или их комбинация.
Активные материалы положительного электрода могут включать материалы, способные обратимым образом интеркалировать/деинтеркалировать ионы лития и они хорошо известны в данной области техники. Такие активные материалы положительного электрода могут включать оксиды переходных металлов, такие как смешанные оксиды, содержащие Ni, Со, Mn, V или другие переходные металлы и необязательно литий. Смешанные оксиды лития и переходного металла, предпочтительно использующиеся в качестве активных материалов положительного электрода, выбраны из группы, состоящей из следующих: оксид лития-кобальта, оксид лития-марганца, оксиды лития-никеля-кобальта, оксиды лития-никеля-марганца-кобальта, оксиды лития-никеля-кобальта-алюминия, оксиды лития-никеля-марганца, фосфаты лития-железа, оксиды лития-марганца или их смеси.
Анод литий-ионной аккумуляторной батареи может включать любой подходящий материал, обычно использующийся во вторичных литий-ионных аккумуляторных батареях, способный обратимым образом интеркалировать/деинтеркалировать ионы лития. Их типичными примерами являются углеродистые материалы, включая кристаллический углерод, такой как природный или искусственный графит в виде пластинчатого, чешуйчатого, сферического или волокнистого графита; аморфный углерод, такой как мягкая сажа, твердая сажа, карбид мезофазного пека, кокс и т.п., или их смеси. Кроме того, в качестве активных материалов анода можно использовать металлический литий, литиевый слой или переходные материалы (например, Si или Sn).
Настоящее изобретение также относится к электроду, такому как катод или анод, для литий-ионной аккумуляторной батареи, включающему фосфат лития-циркония, предлагаемый в настоящем изобретении. Точнее, фосфат лития-циркония, предлагаемый в настоящем изобретении, может являться добавкой или материалом покрытия для электрода.
Настоящее изобретение также относится к электролиту для литий-ионной аккумуляторной батареи, включающему фосфат лития-циркония, предлагаемый в настоящем изобретении.
Электролит литий-ионной аккумуляторной батареи может находиться в жидком, гелеобразном или твердом виде.
Жидкий электролит литий-ионной аккумуляторной батареи может включать любой подходящий органический растворитель, использующийся в литий-ионных аккумуляторных батареях, такой как безводный этиленкарбонат (ЭК), диметилкарбонат (ДМК), пропиленкарбонат, метилэтилкарбонат, диэтилкарбонат, гамма-бутиролактон, диметоксиэтан, фторэтиленкарбонат, винилэтиленкарбонат или их смесь.
Гелеобразные электролиты включают гелеобразные полимеры.
Твердый электролит литий-ионной аккумуляторной батареи может включать оксиды, например, оксиды, сульфиды, фосфаты металлического лития или твердые полимеры.
Жидкий или полимерный гелеобразный электролит литий-ионной аккумуляторной батареи обычно включает соль лития. Примеры таких солей лития включают гексафторфосфат лития (LiPF6), бис-2-(трифторметилсульфонил)имид лития (LiTFSI), бис(фторсульфонил)имид лития (LiFSI), перхлорат лития (LiClO4), тетрафторборат лития (LiBF4), Li2SiF6, трифлат лития, LiN(SO2CF2CF3)2, нитрат лития, бис(оксалат)борат лития, циклодифторметан-1,1-бис(сульфонил)имид лития, циклогексафторпропан-1,1-бис(сульфонил)имид лития и их смеси.
Литий-ионная аккумуляторная батарея, в особенности включающая жидкий или гелеобразный электролит, также может включать сепаратор, который препятствует непосредственному соприкосновению двух электродов, которое может привести к внутреннему короткому замыканию.
Материал сепаратора может включать полиолефиновую смолу, фторированную полиолефиновую смолу, сложную полиэфирную смолу, полиакрилонитрильную смолу, целлюлозную смолу, нетканый материал или их смесь. Предпочтительно, если это вещество включает полиолефиновую смолу, такую как полимер на основе полиэтилена или полипропилена, фторированную полиолефиновую смолу, такую как поливинилиденфторид или политетрафторэтилен, сложную полиэфирную смолу, такую как полиэтилентерефталат и полибутилентерефталат, полиакрилонитрильную смолу, целлюлозную смолу, нетканый материал или их смесь.
Литий-ионная аккумуляторная батарея, предлагаемая в настоящем изобретении, может включать жидкий электролит, гелеобразный электролит или твердый электролит.Жидкая смесь соли лития и органического растворителя, которая не отверждена, не полимеризована или не сшита, в контексте настоящего изобретения называется "жидким электролитом". Гелеобразная или твердая смесь, содержащая отвержденное, полимеризованное или сшитое соединение или смеси соединений, необязательно растворитель и соль лития, называется "гелеобразным электролитом". Такие гелеобразные электролиты можно получить путем полимеризации или сшивки смеси, содержащей по меньшей мере одно реакционноспособное, т.е. полимеризующееся или поддающееся сшивке соединение, и соль лития.
Литий-ионной аккумуляторной батареей особого типа является литий-полимерная аккумуляторная батарея, в которой вместо жидкого электролита используют полимерный электролит. Электролит аналогичной аккумуляторной батареи с твердым электролитом также может включать твердые электролиты других типов, такие как сульфидные, оксидные твердые электролиты или их смеси.
Аккумуляторной батареей, предлагаемой в настоящем изобретении, может являться литий-металлическая аккумуляторная батарея, такая как Li-воздушная, Li-серная (Li-S) и литий-металлические аккумуляторные батареи других типов.
Li-воздушная аккумуляторная батарея обычно включает катод из пористого углерода и органический, стеклокерамический или полимер-керамический электролит.
Li-серная (Li-S) аккумуляторная батарея обычно включает катод из дисульфида железа (FeS2), сульфида железа (FeS), сульфида меди (CuS), сульфида свинца и сульфида меди (PbS+CuS).
Существуют литий-металлические аккумуляторные батареи множества других известных типов, такие как, например, типа литий-селен (Li-Se), литий-диоксид марганца (Li-MnO2 или Li/Al-MnO2), литий-монофторид (Li-(CF)x), литий-тионилхлорид (Li-SOCl2), литий-сульфурилхлорид (Li-SO2Cl2), литий-диоксид серы (Li-SO2), литий-йод (Li-I2), литий-хромат серебра (Li-Ag2CrO4), литий-пентаоксид ванадия (Li-V2O5 или Li/Al-V2O5), литий-хлорид меди (Li-CuCl2), литий оксид меди(II) (Li-CuO), литий-оксифосфат меди (Li-Cu4O(PO4)2) и других типов.
Краткое описание чертежей
На фиг. 1 представлено полученное с помощью ТЭМ (трансмиссионная электронная микроскопия) изображение частиц фосфата лития-циркония, полученных так, как это описано в сравнительном примере 1.
На фиг. 2 представлено полученное с помощью ТЭМ изображение частиц фосфата лития-циркония, полученных так, как это описано в сравнительном примере 2.
На фиг. 3 представлено полученное с помощью ТЭМ изображение частиц фосфата лития-циркония, полученных так, как это описано в примере 1.
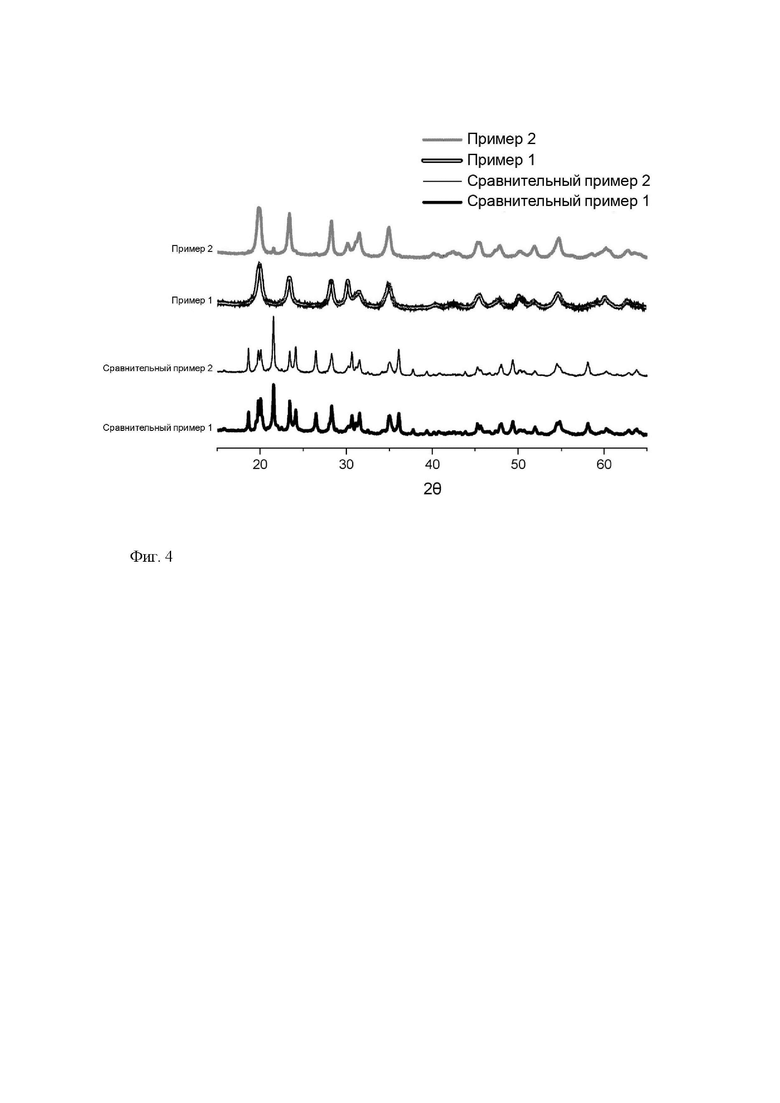
На фиг. 4 представлены РГГ (рентгенограмма) фосфатов лития-циркония, полученных так, как это описано в примерах 1-2 и сравнительных примерах 1-2.
На фиг. 5 представлены полученные с помощью СЭМ (сканирующая электронная микроскопия) изображения НМК (никель-марганец-кобальт) с нанесенным по сухой методике покрытием из частиц пирогенного фосфата лития-циркония (а - изображение, полученное с использованием обратно-рассеянных электронов (ОРЭ), 6 - изображение, полученное при картировании Zr с помощью ЭРС (энергодисперсионная рентгеновская спектроскопия), в -изображение, полученное с помощью СЭМ высокого разрешения).
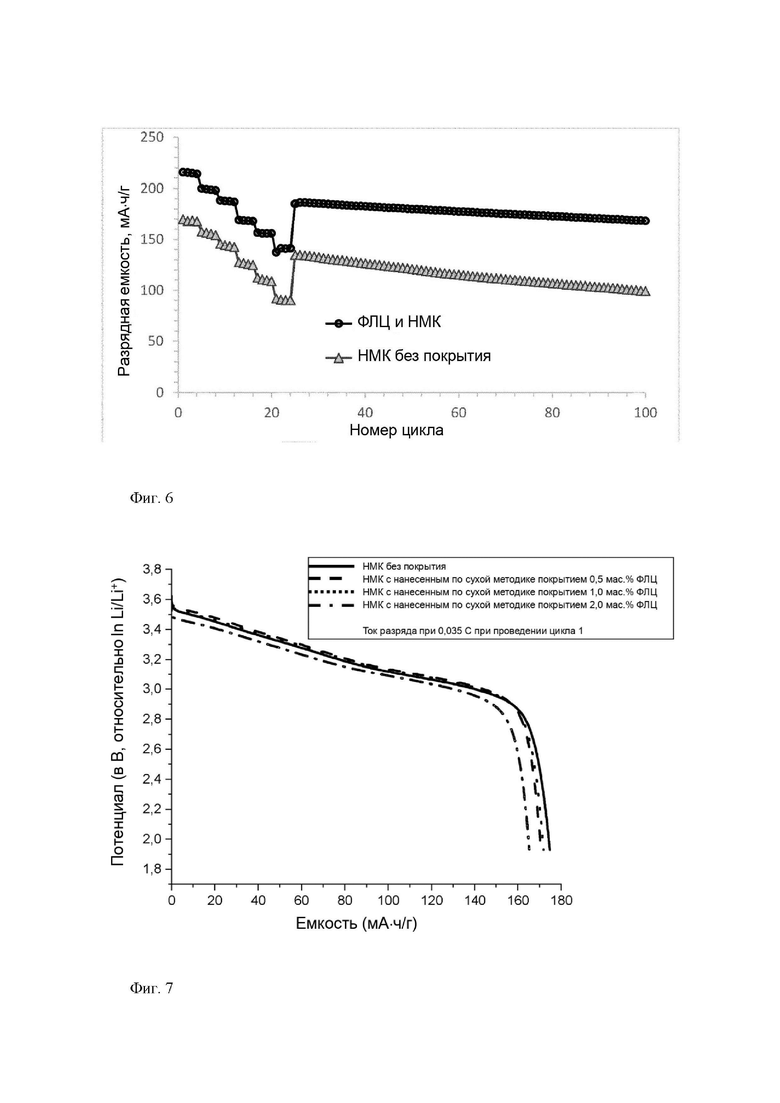
На фиг. 6 представлены скоростные характеристики и характеристики при работе в циклическом режиме не содержащего покрытие НМК и НМК с нанесенным по сухой методике покрытием из частиц пирогенного фосфата лития-циркония в литий-ионных аккумуляторных батареях с жидким электролитом.
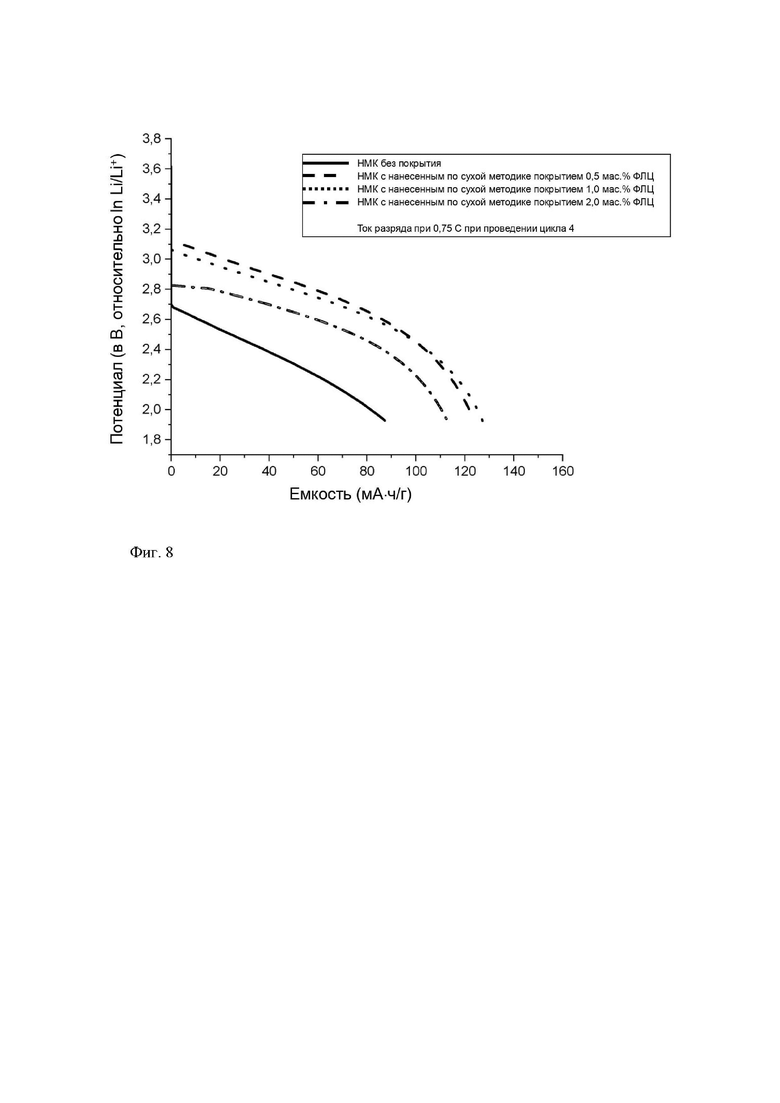
На фиг. 7 представлены зависимости для заряда и разряда при проведении начального цикла при токе разряда, равном 0,066 мА (0,035 С), в твердотельных аккумуляторных батареях на основе сульфида с твердым электролитом Li6PS5Cl.
На фиг. 8 представлены зависимости для заряда и разряда при проведении цикла 4 при токе разряда, равном 1,4 мА (0,75 С), в твердотельных аккумуляторных батареях на основе сульфида с твердым электролитом Li6PS5Cl.
Примеры
Сравнительный пример 1
Готовили 6,34 кг водного раствора, содержащего 157,8 г LiNO3 (содержание металла: 4 мас. %), 1733 г Zr(NO3)4 (содержание металла: 6 мас. %). К раствору солей металлов при энергичном перемешивании по каплям добавляли 1190 г Н3РО4 (85 мас. % в воде), это приводило к образованию дисперсии, содержащей белый осадок. Состав полученного таким образом соединения соответствовал формуле LiZr2(PO4)3.
С помощью сопла для подачи двух компонентов получали аэрозоль, образованный из потоков 1,5 кг/ч этой дисперсии и 15 Нм3/ч воздуха (Нм3 - кубический метр при нормальных условиях), и его распыляли в трубчатый реактор с горящим пламенем. Горючие газы представляли собой потоки 14,3 Нм3/ч водорода и 30 Нм3/ч воздуха. Дополнительно использовали 25 Нм3/ч вторичного воздуха. После завершения реакции реагирующие газы охлаждали и фильтровали.
Характеристики частиц представлены в таблице 1, полученное с помощью ТЭМ изображение частиц представлено на фиг. 1 и анализ с помощью РГГ (рентгенография) (фиг. 4) показал, что основной фазой продукта являлся обладающий кубической структурой фосфат циркония.
Сравнительный пример 2
Готовили 6,34 кг этанольного раствора, содержащего 157,8 г LiNO3 (содержание металла: 4 мас. %), 1733 г Zr(NO3)4 (содержание металла: 6 мас. %).
К раствору солей металлов при энергичном перемешивании по каплям добавляли 1190 г H3PO4 (85 мас. % в воде), это приводило к образованию дисперсии, содержащей белый осадок. Состав полученного таким образом соединения соответствовал формуле LiZr2(PO4)3.
С помощью сопла для подачи двух компонентов получали аэрозоль, образованный из потоков 1,5 кг/ч этой дисперсии и 15 Нм3/ч воздуха, и его распыляли в трубчатый реактор с горящим пламенем. Горючие газы представляли собой потоки 8,4 Нм3/ч водорода и 30 Нм3/ч воздуха. Дополнительно использовали 25 Нм3/ч вторичного воздуха. После завершения реакции реагирующие газы охлаждали и фильтровали.
Характеристики частиц представлены в таблице 1, полученное с помощью ТЭМ изображение частиц представлено на фиг. 2 и анализ с помощью РГГ (фиг. 4) показал, что основной фазой продукта являлся обладающий кубической структурой фосфат циркония.
Сравнительный пример 3
Путем смешивания готовили 61,4 г раствора, включающего 2,9 г имеющегося в продаже раствора (Borchers® Deca Lithium2), содержащего 2 мас. % лития в форме неодеканоата лития, растворенного в нафте, 50 г имеющегося в продаже раствора (Octa Solingen® Zirconium 12), содержащего 11,86 мас. % Zr в форме этилгексаноата циркония, растворенного в уайт-спирите. К раствору солей металлов при энергичном перемешивании по каплям добавляли 8,6 г Н3РО4 (85 мас. % в воде). Наблюдали разделение фаз, это делало невозможным однородное распыление раствора. Эксперимент по распылению не проводили
Пример 1
Путем смешивания готовили 23,75 кг раствора, включающего 3370 г имеющегося в продаже раствора (Borchers® Deca Lithium2), содержащего 2 мас. % лития в форме неодеканоата лития, растворенного в нафте, 15 кг имеющегося в продаже раствора (Octa Solingen® Zirconium 12), содержащего 11,86 мас. % Zr в форме этилгексаноата циркония, растворенного в уайт-спирите, и 5384 г имеющегося в продаже раствора (Alfa Aesar), содержащего 16,83 мас. % фосфора в форме триэтилфосфата, и получали прозрачный раствор. Состав этого раствора соответствовал формуле LiZr2(PO4)3.
С помощью сопла для подачи двух компонентов получали аэрозоль, образованный из потоков 1,5 кг/ч этой дисперсии и 15 Нм3/ч воздуха, и его распыляли в трубчатый реактор с горящим пламенем. Горючие газы представляли собой потоки 8,5 Нм3/ч водорода и 30 Нм3/ч воздуха. Дополнительно использовали 25 Нм3/ч вторичного воздуха. После завершения реакции реагирующие газы охлаждали и фильтровали.
Характеристики частиц представлены в таблице 1, полученное с помощью ТЭМ изображение частиц представлено на фиг. 3 и анализ с помощью РГГ (фиг. 4) показал, что основной фазой продукта являлся обладающий ромбоэдрической структурой фосфат лития-циркония.
Пример 2
Путем смешивания готовили 6,18 кг раствора, включающего 1056 г имеющегося в продаже раствора (Borchers® Deca Lithium2), содержащего 2 мас. % лития в форме неодеканоата лития, растворенного в нафте, 2453 г имеющегося в продаже раствора (Octa Solingen® Zirconium 12), содержащего 18,01 мас. % Zr в форме этилгексаноата циркония, растворенного в уайт-спирите, и 1408 г имеющегося в продаже раствора (Alfa Aesar), содержащего 16,83 мас. % фосфора в форме триэтилфосфата, и получали прозрачный раствор. При непрерывном перемешивании добавляли дополнительный раствор, содержащий 60,8 г Са(NO3)2×4H2O, 1200 г этанола и 1200 г этилгексановой кислоты, до обеспечения получения прозрачного раствора. Состав этого раствора соответствовал формуле Li1,2Ca0,1Zr1,9(PO4)3.
С помощью сопла для подачи двух компонентов получали аэрозоль, образованный из потоков 1,5 кг/ч этой дисперсии и 15 Нм3/ч воздуха, и его распыляли в трубчатый реактор с горящим пламенем. Горючие газы представляли собой потоки 8,7 Нм3/ч водорода и 30 Нм3/ч воздуха. Дополнительно использовали 25 Нм3/ч вторичного воздуха. После завершения реакции реагирующие газы охлаждали и фильтровали.
Характеристики частиц представлены в таблице 1 и анализ с помощью РГГ (фиг. 4) показал, что, основной фазой продукта являлся обладающий ромбоэдрической структурой фосфат лития-циркония.
Характеристики частиц полученных продуктов, представленные в таблице 1, указывают на то, что только с использованием предлагаемой в настоящем изобретении комбинации карбоксилатов металлов и этилфосфата в растворе, не содержащем воду, получены фосфаты лития-циркония, обладающие сравнительно высокими значениями БЭТ-поверхности (17-44 м2/г в отличие от 4,3-4,7 м2/г в случае материалов сравнительных примеров), небольшим размером частиц (76-130 нм в отличие от примерно 4 мкм в случае материалов сравнительных примеров) и низкой плотностью утряски (примерно 50 г/л в отличие от примерно 300 г/л в случае материалов сравнительных примеров).
Анализ смешанных оксидов лития-переходного металла с покрытием из фосфата лития-циркония (ФЛЦ) с помощью СЭМ-ЭРС
Порошкообразный НМК и соответствующее количество (1,0 мас. %) порошкообразного пирогенного ФЛЦ, полученного в примере 1, перемешивали в лабораторном высокоэффективном смесителе (смеситель SOMAKON MP-GL, камера смесителя: 0,5 л) сначала при 500 об/мин в течение 1 мин для обеспечения однородного смешивания двух порошков. Затем скорость перемешивания увеличивали до равной 2000 об/мин и перемешивали в течение 5 мин для обеспечения нанесения покрытия из порошкообразного ФЛЦ на частицы НМК по сухой методике.
Толщина слоя покрытия из ФЛЦ на частицах НМК составляла примерно 15-200 нм.
На фиг. 5 представлены полученные с помощью СЭМ изображения НМК с нанесенным по сухой методике покрытием из ФЛЦ (фиг. 5 а, б, в: пирогенный ФЛЦ, полученный в примере 1). При сопоставлении изображения, полученного с использованием обратно-рассеянных электронов (а), и изображения, полученного при картировании Zr с помощью ЭРС (б), для НМК с нанесенным по сухой методике покрытием из ФЛЦ на всех частицах катода обнаружено полное и однородное покрытие из пирогенного ФЛЦ. Не обнаружены более крупные агломераты ФЛЦ, это указывает на то, что обеспечена хорошая диспергируемость частиц наноструктурированного пирогенного ФЛЦ. Кроме того, рядом с частицами катода не обнаружено свободных, неприкрепленных частиц ФЛЦ, это указывает на высокую адгезию между покрытием и подложкой. На изображении, полученном с помощью СЭМ высокого разрешения (в), видно однородное распределение пирогенного ФЛЦ и высокая степень покрытия поверхности НМК.
Электрохимические испытания литий-ионных аккумуляторных батарей с жидкими электролитами
Электроды для электрохимических испытаний изготавливали путем проводимого в атмосфере инертного газа смешивания 90 мас. % НМК с 5 мас. % ПВДФ (поливинилиденфторид, Solef PVDF 5130), использовавшимся в качестве связующего, и 5 мас. % SUPER PLi (TIMCAL), использующегося в качестве проводящей добавки. N-Метил-2-пирролидон (NMP) использовали в качестве растворителя. Суспензию наносили на алюминиевую фольгу путем полива и сушили на нагревательной плитке на воздухе при 120°С в течение 20 мин. Затем представляющий собой лист электрод сушили в вакуумной печи при120°С в течение 2 ч. Из листа вырубали круглые электроды диаметром 12 мм, их каландровали при давлении, равном 90 фунт-сила/дюйм2, и повторно сушили в вакуумной печи при 120°С в течение 12 ч для удаления любого остаточного количества воды и NMP. Для проведения испытаний в циклическом режиме в заполненной аргоном перчаточной камере (GLOVEBOX SYSTEMTECHNIK GmbH) изготавливали элементы типа дисковых элементов CR2032 (MTI Corporation). Металлический литий (ROCKWOOD LITHIUM GmbH) использовали в качестве материала анода. Celgard 2500 использовали в качестве сепаратора. 25 мкл 1М раствора LiPF6 в этиленкарбонате и этилметилкарбонате (50:50 мас./мас.; SIGMA-ALDRICH) использовали в качестве электролита. Элементы закрывали с помощью обжимных щипцов (MTI).
Для электрохимического испытания работу в гальваностатическом циклическом режим проводили при потенциале, равном от 3,0 до 4,3 В. При расчете значений емкостей и удельного тока учитывали только массу активного материала. В случае дисковых полуэлементов во время проведения циклов скорость С увеличивали через каждые 4 цикла, начиная с равной 0,1/0,1 (заряд/разряд), до равной 0,3/0,3, 0,5/0,5, 1,0/1,0, 1,0/2,0 и 1,0/4,0 С. Затем для испытания длительной стабильности циклы в элементах проводили при 0,5/0,5 С.
На фиг. 6 представлено влияние наличия слоев покрытия из ФЛЦ на характеристики при работе в циклическом режиме. Рабочие характеристики НМК с нанесенным по сухой методике покрытием из пирогенного ФЛЦ, полученного в примере 1, сопоставляли характеристиками, полученными для не содержащего покрытие НМК, использовавшегося в качестве эталона. Из приведенных зависимостей можно явно видеть, что нанесенное по сухой методике покрытие из пирогенного ФЛЦ существенно улучшает долговечность НМК при работе в циклическом режиме. НМК с нанесенным по сухой методике покрытием из пирогенного ФЛЦ обладает более высокой разрядной емкостью в течение проведения всех циклов, в проводимом в начале испытании на скорость и при длительном испытании в циклическом режиме. Он также обладает более высокой начальной удельной разрядной емкостью при 0,1 С, чем не содержащий покрытие НМК.
Электрохимические испытания литий-ионных аккумуляторных батарей с использованием твердотельных аккумуляторных батарей на основе сульфида
Составной порошкообразный электрод получали путем проводимого в агатовой ступке перемешивания активного материала (AM) - НМК, проводящей углеродной добавки - углеродных нановолокон (УНВ) и твердого электролита (Li6PS5Cl, SE) при массовом отношении, составляющем 63:2:35, в течение 30 мин. Для получения отдельной и гибкой сухой пленки полученный выше порошкообразный электрод при 100°С смешивали в ступке с 0,3 мас. % политетрафторэтилена (ПТФЭ, мелкодисперсный порошок, полученный путем полимеризации в эмульсии; размер частиц: 300-700 мкм; температура размягчения: 320-330°С; молекулярная масса: 107-108 г/моль).
После перемешивания и приложения сдвигового усилия в течение 1 мин получали отдельный комок. Комок помещали на нагревательную плитку и раскатывали до обеспечения необходимой толщины (≈100 мкм). Для подтверждения воспроизводимости методики каждый образец готовили по меньшей мере дважды. Для получения отдельной пленки электролита твердый электролит смешивали с 0,15 мас. % ПТФЭ и обрабатывали таким же образом, как и катодную пленку.
Для определения базовых характеристик составного катода, таких как профили потенциала заряда/разряда, номинальная емкость заряда, изготавливали испытуемый элемент.
Элемент изготавливали с использованием пресс-формы диаметром 13 мм. Испытуемый элемент состоял из изготовленного из нержавеющей стали наружного корпуса с изоляцией из тефлона. Для изготовления типичного элемента порошкообразный электролит Li6PS5Cl равномерно распределяли внутри пресс-формы с помощью микрошпателя. Затем порошок один раз прессовали и уплотняли с получением пеллеты. Порошок составного катода равномерно распределяли на поверхности уплотненного электролита, находящегося в пресс-форме. Затем слой катода прессовали. На обратную сторону многокомпонентного элемента помещали литиево-индиевый сплав и прессовали. Все компоненты элемента повторно прессовали вместе и полностью таблетировали с использованием гидравлического пресса (приложение силы, равной 4 т, в течение 30 с): 300 МПа.
После прессования многокомпонентный элемент помещали внутрь изготовленного из нержавеющей стали наружного корпуса, в котором с помощью винта обеспечивали электрический контакт в элементе. Винт закрепляли при силе, равной 3,0 Н⋅м, с использованием заданного вращающего момента.
Все описанные выше процедуры проводили в заполненной с помощью Ar перчаточной камере (<0,1 част./млн Н2О и О2).
Характеристики при работе в циклическом режиме и скоростные характеристики элемента определяли с помощью устройства для испытания аккумуляторных батарей CTS-Lab (BaSyTec, Germany). Стандартное испытание скоростных характеристик включало использование 3 разных значений тока разряда, находящихся в диапазоне от 0,066 мА (0,035 С) до 1,4 мА (0,75 С), при этом скорость заряда поддерживали постоянной и равной 0,14 мА (0,075 С), включая стадию с использованием ПП (постоянный потенциал). Стандартные запирающие потенциалы для проведения испытания в циклическом режиме устанавливали равными 3,63 В и 1,93 В для заряда и разряда соответственно.
На фиг. 7 представлено влияние наличия слоев покрытия из ФЛЦ на скоростные характеристики при проведении цикла 1 при токе разряда, равном 0,066 мА (0,035 С), при использовании разных количеств покрытия из ФЛЦ, равных 0,5, 1 и 2 мас. %. Разрядные емкости при 0,066 мА для НМК с нанесенным по сухой методике покрытием из пирогенного ФЛЦ, полученного в примере 1, сопоставляли со значением, полученным для не содержащего покрытие НМК, использовавшегося в качестве эталона. Из приведенных зависимостей можно явно видеть, что в твердотельных аккумуляторных батареях на основе сульфида не происходит существенное улучшение начальной разрядной емкости при низкой скорости разряда, такой как 0,035 С.
На фиг. 8 представлено влияние наличия слоев покрытия из ФЛЦ на скоростные характеристики при проведении цикла 4 при токе разряда, равном 1,4 мА (0,75 С), при использовании разных количеств покрытия из ФЛЦ, равных 0,5, 1 и 2 мас. %. Разрядные емкости при 0,75 С для НМК с нанесенным по сухой методике покрытием из пирогенного ФЛЦ, полученного в примере 1, сопоставляли со значением, полученным для не содержащего покрытие НМК, использовавшегося в качестве эталона. Из приведенных зависимостей можно явно видеть, что в твердотельных аккумуляторных батареях на основе сульфида нанесенное по сухой методике покрытие из пирогенного ФЛЦ существенно улучшает скорость разряда НМК. НМК с нанесенным по сухой методике покрытием из пирогенного ФЛЦ обладает более высокой разрядной емкостью при более высокой скорости разряда, такой как 0,75 С.




Изобретение относится к получению кристаллических фосфатов лития-циркония, применимых в качестве материала при изготовлении литий-ионных аккумуляторных батарей. Предложен фосфат лития-циркония общей формулы LiaZrbMc(PO4)d, где М обозначает Са, 1,0<а<1,3, 1,8<b<2,2, 0<с<0,3, 2,8<d<3,2. Фосфат лития-циркония находится в виде агрегированных первичных частиц и обладает значением БЭТ-поверхности, равным 5-100 м2/г, среднечисловым диаметром частиц, определенным с помощью статического светорассеяния (ССР), d50=0,03-2 мкм, и плотностью утряски, равной 20-200 г/л. Для получения фосфата лития-циркония проводят пламенный распылительный пиролиз по меньшей мере одного раствора предшественников металлов, содержащего карбоксилат лития и карбоксилат циркония, где каждый из этих карбоксилатов металлов содержит от 5 до 20 атомов углерода, органический фосфат и смесь растворителей, содержащую менее 10 мас.% воды. Предложены также применения фосфата лития-циркония в качестве компонента твердого электролита, в качестве добавки в жидком или гелеобразном электролите и в качестве компонента электрода литий-ионной батареи, а также электрод и электролит для литий-ионной батареи и литий-ионная батарея, включающие фосфат лития-циркония. Группа изобретений позволяет получить частицы фосфата лития-циркония, обладающие сравнительно небольшим размером, высоким значением БЭТ-поверхности и низкой плотностью утряски. 8 н. и 11 з.п. ф-лы, 8 ил., 1 табл., 2 пр.
1. Фосфат лития-циркония общей формулы LiaZrbMc(PO4)d, в которой М обозначает Са, 1,0<а<1,3, 1,8<b<2,2, 0<с<0,3, 2,8<d<3,2, отличающийся тем, что фосфат лития-циркония находится в виде агрегированных первичных частиц, обладает значением БЭТ-поверхности (удельная поверхность, определенная по методике Брунауэра-Эммета-Теллера), равным 5-100 м2/г, обладает среднечисловым диаметром частиц, определенным с помощью статического светорассеяния (ССР), d50=0,03-2 мкм, и обладает плотностью утряски, равной 20-200 г/л.
2. Способ получения фосфата лития-циркония по п. 1 путем пламенного распылительного пиролиза, отличающийся тем, что проводят пламенный распылительный пиролиз по меньшей мере одного раствора предшественников металлов, содержащего
- карбоксилат лития и карбоксилат циркония, где каждый из этих карбоксилатов металлов содержит от 5 до 20 атомов углерода,
- органический фосфат,
- смесь растворителей, содержащую менее 10 мас.% воды.
3. Способ по п. 2, отличающийся тем, что пламенный распылительный пиролиз включает следующие стадии:
a) атомизация раствора предшественников металлов с помощью атомизирующего газа с получением аэрозоля,
b) проводимое в реакционном пространстве реактора введение аэрозоля в реакцию с пламенем, полученным путем воспламенения смеси топливного газа и содержащего кислород газа, с получением реакционного потока,
c) охлаждение реакционного потока и
d) последующее удаление твердого фосфата лития-циркония из реакционного потока.
4. Способ по п. 2 или 3, отличающийся тем, что карбоксилаты лития и циркония независимо друг от друга выбраны из группы, состоящей из следующих: линейный, разветвленный или циклический пентаноат (С5), гексаноат (С6), гептаноат (С7), октаноат (С8), нонаноат (С9), деканоат (С10), ундеканоат (С11), додеканоат (С12), тридеканоат (С13), тетрадеканоат (С14), пентадеканоат (С15), гексадеканоат (С16), гептадеканоат (С17), октадеканоат (С18), нонадеканоат (С19), икозаноат (С20) лития и/или циркония и их смеси.
5. Способ по пп. 2-4, отличающийся тем, что органический фосфат выбран из числа следующих: эфиры фосфорной кислоты (Н3РО3), ортофосфорной кислоты (Н3РО4), метафосфорной кислоты (НРО3), пирофосфорной кислоты (Н4Р2О7), полифосфорных кислот и их смеси.
6. Способ по пп. 2-5, отличающийся тем, что органический фосфат выбран из числа следующих: сложный алкиловый эфир, сложный ариловый эфир, смешанные сложные алкиловые/ариловые эфиры и их смеси.
7. Способ по пп. 2-6, отличающийся тем, что органическим фосфатом является сложный алкиловый эфир, включающий алкильные группы, содержащие от 1 до 10 атомов углерода.
8. Способ по пп. 2-7, отличающийся тем, что смесь растворителей выбирают из группы, состоящей из следующих: линейные или циклические, насыщенные или ненасыщенные, алифатические или ароматические углеводороды, эфиры карбоновых кислот, простые эфиры, спирты, карбоновые кислоты и их смеси.
9. Способ по пп. 2-8, отличающийся тем, что смесь растворителей дополнительно содержит хелатный агент, выбранный из группы, состоящей из следующих: диамины и 1,3-дикарбонильные соединения.
10. Способ по пп. 2-9, дополнительно включающий термическую обработку фосфата лития-циркония, полученного путем пламенного распылительного пиролиза, при температуре, равной 600-1300°С.
11. Способ по п. 10, дополнительно включающий размол подвергнутого термической обработке фосфата лития-циркония.
12. Применение фосфата лития-циркония по п. 1 в качестве компонента твердого электролита.
13. Применение фосфата лития-циркония по п. 1 в качестве добавки в жидком или гелеобразном электролите.
14. Применение фосфата лития-циркония по п. 1 в качестве компонента электрода литий-ионной батареи.
15. Электрод для литий-ионной батареи, включающий фосфат лития-циркония по п. 1.
16. Электролит для литий-ионной батареи, включающий фосфат лития-циркония по п. 1.
17. Литий-ионная батарея, включающая фосфат лития-циркония по п. 1.
18. Литий-ионная батарея по п. 17, включающая жидкий или гелеобразный электролит.
19. Литий-ионная батарея по п. 17, где батареей является батарея с твердым электролитом.
| CN 109888208 A, 14.06.2019 | |||
| КОМПОЗИЦИОННЫЙ КАТОДНЫЙ МАТЕРИАЛ | 2012 |
|
RU2492557C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТИТАН-, ЦИРКОНИЙ-, ГАФНИЙ-, ГЕРМАНИЙ- И ОЛОВОСОДЕРЖАЩИХ КЕРАМИК | 2010 |
|
RU2440957C1 |
| US 2014084503 A1, 27.03.2014 | |||
| US 2006229197 A1, 12.10.2006 | |||
| US 2017365859 A1, 21.12.2017 | |||
| HUI XIE et al., Li1.2Zr1.9Ca0.1(PO4)3, a room-temperature Li-ion solid electrolyte, Journal of Power Sources, 2011, v | |||
| Пылеочистительное устройство к трепальным машинам | 1923 |
|
SU196A1 |
| Способ и машина для регулируемого охлаждения литейных форм при центробежной отливке | 1926 |
|
SU7760A1 |
Авторы
Даты
2025-01-15—Публикация
2021-03-19—Подача