Настоящее изобретение относится к способу рацемизации (5R)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойной кислоты.
Уровень техники
(5RS)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-N-[2-оксо-2-(2,2,2-трифторэтиламино)этил]-2-метилбензамид (далее названный флураланер) является синтетическим инсектицидом, который представлен следующей формулой (A).

Формула (A)
Флураланер является системным активным ингредиентом, который можно вводить перорально. Сообщается, что активный ингредиент антагонистически ингибирует ГАМК-зависимый хлорид в нервной системе некоторых членистоногих. Поскольку флураланер не проявляет аналогичных связей в нервной системе млекопитающих, он подходит, например, для лечения блох, зудней и клещей у млекопитающих, например у собак и кошек.
Флураланер является рацематом. Сообщается, что (S)-энантиомер является эутомером, вносящим существенный вклад в противопаразитарную активность активного ингредиента. В связи с этим использование энантиочистого или энантиообогащенного (S)-флураланера считается предпочтительным по сравнению с рацемическим флураланером. Для получения указанного энантиочистого или энантиообогащенного (S)-флураланера, энантиочистый или энантиообогащенный
(5RS)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойная кислота (IOBA) является ключевым промежуточным соединением в синтезе флураланера, и указанное соединение представлено следующей формулой (1)
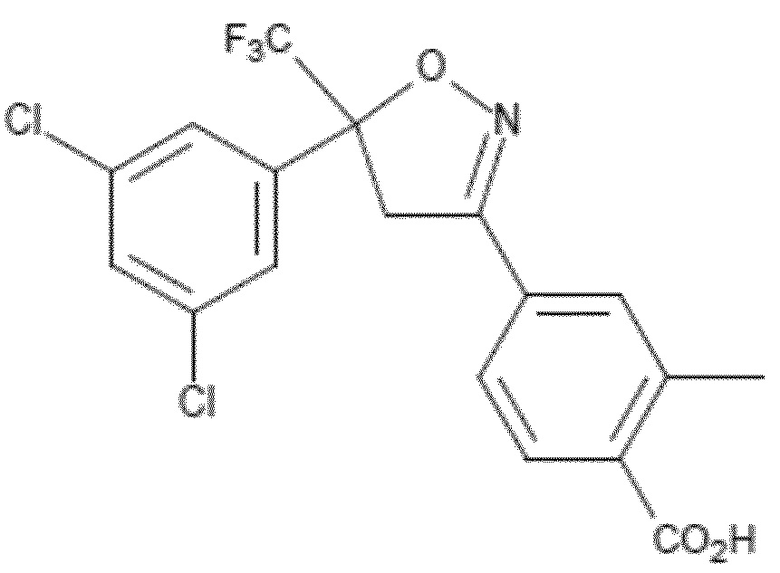
Формула (1),
где соединение формулы (1) может быть получено, как описано в примере синтеза 3 из US 2007/0066617.
Так как энантиочистый или энантиообогащенный (S)-флураланер может считаться предпочтительным в качестве активного ингредиента, выделение энантиочистой или энантиообогащенной (5S)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойной кислоты (S)-IOBA было бы желательным.
При отделении энантиочистой или энантиообогащенной (S)-IOBA от рацемата (IOBA) фракция, содержащая энантиочистую или энантиообогащенную (R)-IOBA остается. По сравнению с получением IOBA весьма желательна рацемизация энантиочистой или энантиообогащенной (R)-IOBA в качестве побочного продукта описанного выше разделения.
В WO 2014/090918 A1 описано разделение другого соединения, а именно, рацемической 3-метил-5-[(5RS)-5-(3,4,5-трихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]тиофен-2-карбоновой кислоты (IOTA) на энантиомеры через хиральную колоночную хроматографию или через дисастереомерную перекристаллизацию. Более конкретно, в указанном документе описано, что рацемическую IOTA обрабатывают (R)-1-(4-метилфенил)этиламином в тройной смеси воды, ацетонитрила и 2-бутанола с получением осадка соответствующей (S)-IOTA соли, имеющей, после промывания, хиральную чистоту более 95%, которая может быть обогащена до более 98% дальнейшей перекристаллизацией. Далее, супернатант раствора для осаждения соответствующей (S)-IOTA соли удаляют в вакууме с получением ценного побочного продукта, обогащенной смеси (R)-IOTA. Эту обогащенную смесь (R)-IOTA рацемизируют с водным гидроксидом натрия в толуоле в качестве смеси растворителей при 75°C в присутствии катализатора фазового переноса, водного раствора хлорида трибутилметиламмония.
Для процесса известного уровня техники требуется тройная смесь растворителей для осаждения (S)-энантиомерного соединения. Однако эту тройную смесь растворителей необходимо заменить для рацемизации оставшегося «побочного продукта» энантиообогащенного (R)-изоксазолинтиофенкарбоновой кислоты. Более того, реакция известного уровня техники требует катализаторов межфазного переноса, которые, как сообщается, трудно удалить из реакционных смесей и/или желаемых продуктов, так что могут потребоваться сложные стадии очистки.
Более того, было обнаружено, что обработка рацемической IOBA (R)-1-(4-метилфенил)этиламином не вызывает какого-либо выпадения в осадок (S)-IOBA и, следовательно, также не дает отделения энантиочистой или энантиообогащенной (R)-IOBA.
Таким образом, все еще существует необходимость в рацемизации энантиочистой или энантиообогащенной (5R)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойной кислоты, которая предпочтительно может применяться простым и эффективным способом.
Следовательно, объектом данного изобретения является преодоление одного или нескольких недостатков вышеуказанного способа. В частности, объектом настоящего изобретения является получение способов рацемизации энантиочистой или энантиообогащенной (5R)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойной кислоты без необходимости в сложных стадиях очистки. Также объектом настоящего изобретения является получение способа рацемизации энантиочистой или энантиообогащенной (5R)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойной кислоты с простой системой растворителей.
Настоящее изобретение неожиданно решило, по меньшей мере, одну из вышеуказанных задач путем предоставления нового синтетического подхода для рацемизации смеси, содержащей (R)-IOBA и (S)-IOBA, где смесь имеет энантиомерный избыток (R)-IOBA.
Следовательно, объектом настоящего изобретения является способ рацемизации смеси, содержащей (R)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил)]-2-метилбензойную кислоту формулы (1a) и (S)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил)]-2-метилбензойную кислоту формулы (1b)
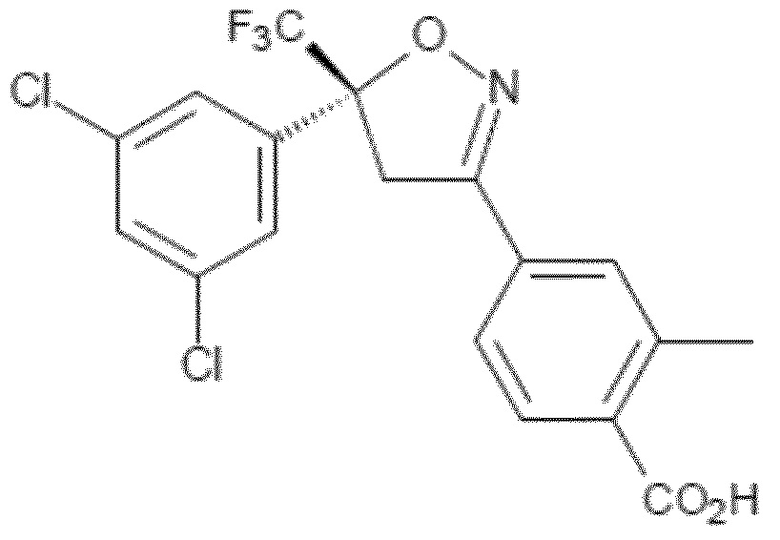
Формула (1a) и

Формула (1b),
где смесь имеет энантиомерный избыток соединения формулы (1a), включающий стадии:
(i) взаимодействия смеси со щелочным соединением в органическом растворителе с получением прореагировавшей смеси.
Подробное описание изобретения
Настоящее изобретение относится к способу рацемизации смеси, содержащей (5R)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойную кислоту ((R)-IOBA) формулы (1a) и (5S)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойную кислоту ((S)-IOBA) формулы (1b), где смесь содержит энантиомерный избыток соединения формулы (1a).
В соответствии с настоящей заявкой рацемизация рассматривается как сдвиг энантиомерного избытка соединения к более низкому значению. Рацемизация строго не рассматривается как сдвиг энантиомерного значения к 0, что является буквальным значением рацемата.
Обычно энантиомерный избыток (эи) можно определить, как описано ниже. Оно может составлять от 1 до 100%, предпочтительно от 10 до 100%, более предпочтительно от 25 до 100%, в частности от 50 до 100%.
Энантиомерный избыток соединения формулы (1a) означает, что смесь содержит большее количество соединения формулы (1a), чем соединение формулы (1b).
В одном из вариантов осуществления изобретения и/или его вариантов осуществления, энантиомерный избыток соединения формулы (1a) может составлять 100%; т.е. смесь содержит только соединение формулы (1a), но не соединение формулы (1b).
Соединения формул (1a) и (1b) являются (R)-энантиомером или (S)-энантиомер соединения формулы (1), (5RS)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойной кислоты.
На стадии (i) способа в соответствии с данным изобретением и/или любого его варианта осуществления смесь, содержащую (R)-IOBA формулы (1a) и (S)-IOBA формулы (1b) подвергают взаимодействию со щелочным соединением в органическом растворителе.
В соответствии с настоящей заявкой, щелочное соединение на стадии (i) может рассматриваться как основание, которое, согласно Бренстеду, является соединением, которое может принимать катионы водорода.
Щелочное соединение может быть органическим или неорганическим щелочным соединением.
Примерами органических щелочных соединений являются диизопропилэтиламин (ДИПЭА), 1,8-диазабицикло[5.4.0]ундец-7-ен (ДБУ), 1,5-диазабицикло[4.3.0]нон-5-ен и 2-трет-бутилимино-2-диэталамино-1,3-диметилпергидро-1,3,2-диазафорфорин и их смеси.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления, щелочным соединением на стадии (i) является неорганическое соединение.
Примерами подходящих неорганических щелочных соединений являются фосфаты щелочных или щелочноземельных металлов, карбонаты щелочных или щелочноземельных металлов, гидрокарбонаты щелочных или щелочноземельных металлов, гидроксиды щелочных или щелочноземельных металлов, оксиды щелочных или щелочноземельных металлов или их смеси.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления щелочное соединение на стадии (i) может быть выбрано из группы, состоящей из оксида лития, оксида натрия, оксида калия, оксида цезия, гидроксида лития, гидроксида натрия, гидроксида калия, гидроксида цезия, гидроксида кальция, гидроксида бария, оксида магния, оксида кальция, оксида бария, карбоната цезия и их смесей. Предпочтительными являются гидроксид натрия, гидроксид калия, гидроксид цезия, гидроксид кальция, гидроксид бария, оксид бария и их смеси.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления щелочное соединение на стадии (i) может быть выбрано из группы, состоящей из гидроксида натрия, гидроксида калия, гидроксида цезия и их смесей.
Другим щелочным соединением, подходящим для использования на стадии (i), являются алкоголяты щелочных или щелочноземельных металлов. Подходящими примерами являются метанолат натрия, метанолат калия, этанолат натрия, этанолат калия, трет-бутилат натрия и трет-бутилат калия и их смеси.
Стадия (i) настоящего способа выполняется в органическом растворителе. Органические растворители хорошо известны специалистам в данной области. Хотя вода не содержит ни одного атома углерода в соответствии с настоящей заявкой, она считается органическим растворителем.
Подходящими органическими растворителями являются, например, вода, спирты, такие как пропанол, циклические простые эфиры, такие как тетрагидрофуран и диоксан, алифатические сложные эфиры, такие как этилацетат, незамещенные или замещенные бензолы, такие как бензол и толуол.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления органический растворитель выбран из группы, состоящей из воды, спирта с 1-5 атомами углерода, тетрагидрофурана, диоксана, толуола, этилацетата и их смесей, более предпочтительно из группы, состоящей из воды, спирта с 2-5 атомами углерода, диоксана, толуола и их смеси.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления органическим растворителем на стадии (i) является спирт с 1-5 атомами углерода. Спирт предпочтительно представляет собой одноатомный спирт, т.е. органический растворитель несет только одну гидроксигруппу. Кроме того, предпочтительно, чтобы органический растворитель нес только гидроксильную функциональную группу. Другими словами, спирт не несет никакой другой функциональной группы, кроме (одной) гидроксигруппы. Кроме того, спирт с 1-5 атомами углерода, используемый в качестве органического растворителя, содержит только атомы водорода, кислорода и углерода. Соответственно, спирт дополнительно не замещен.
Примерами спиртов с 1-5 атомами углерода, используемых в качестве органического растворителя, являются метанол, этанол, 1-пропанол, 2-пропанол, циклопропиловый спирт, 1-бутанол, 2-бутанол, циклобутанол, 2-метил-1-пропанол, 2-метил-2-пропанол, 1-пентанол, 2-пентанол, 3-пентанол, циклопентанол, 2-метил-1-бутанол, 3-метил-1-бутанол, 3-метил-2-бутанол, 2-метил-2-бутанол, 2,2-диметил-1-пропанол и их смеси.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления органическим растворителем является спирт с 1-5 атомами углерода, выбранный из группы, состоящей из этанола, 1-пропанола, 2-пропанола, 1-бутанола, 2-бутанола, 2-метил-1-пропанола, 1-пентанола, 2-пентанол, 3-пентанола и их смесей. Более предпочтительно, органическим растворителем является спирт с 2-5 атомами углерода, выбранный из группы, состоящей из этанола, 1-пропанола, 2-пропанола, 1-бутанола, 1-пентанола и их смесей.
В особенно предпочтительном варианте осуществления изобретения и/или его варианте осуществления органическим растворителем на стадии (i) является этанол.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (i) органическим растворителем является этанол и щелочным соединением является гидроксид натрия.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (i) органическим растворителем является этанол и щелочным соединением является гидроксид калия.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (i) органическим растворителем является этанол и щелочным соединением является гидроксид цезия.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (i) органическим растворителем является этанол и щелочным соединением является гидроксид кальция.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (i) органическим растворителем является этанол и щелочным соединением является гидроксид бария.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (i) органическим растворителем является этанол и щелочным соединением является оксид бария.
В особенно предпочтительном варианте осуществления изобретения и/или его варианте осуществления органическим соединением на стадии (i) является 1-пропанол.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (i) органическим растворителем является 1-пропанол и щелочным соединением является гидроксид натрия.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (i) органическим растворителем является 1-пропанол и щелочным соединением является гидроксид калия.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (i) органическим растворителем является 1-пропанол и щелочным соединением является гидроксид цезия.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (i) органическим растворителем является 1-пропанол и щелочным соединением является гидроксид кальция.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (i) органическим растворителем является 1-пропанол и щелочным соединением является гидроксид бария.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (i) органическим растворителем является 1-пропанол и щелочным соединением является оксид бария.
В особенно предпочтительном варианте осуществления изобретения и/или его варианте осуществления органическим соединением на стадии (i) является 2-пропанол.
В особенно предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (i) органическим растворителем является 2-пропанол и щелочным соединением является гидроксид натрия.
В особенно предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (i) органическим растворителем является 2-пропанол и щелочным соединением является гидроксид калия.
В особенно предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (i) органическим растворителем является 2-пропанол и щелочным соединением является гидроксид цезия.
В особенно предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (i) органическим растворителем является 2-пропанол и щелочным соединением является гидроксид кальция.
В особенно предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (i) органическим растворителем является 2-пропанол и щелочным соединением является гидроксид бария.
В особенно предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (i) органическим растворителем является 2-пропанол и щелочным соединением является оксид бария.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления молярное отношение смеси, содержащей (R)-IOBA формулы (1a) и (S)-IOBA формулы (1b) к щелочному соединению равно 1:1 к 1:10, более предпочтительно, 1:2 к 1:8, в частности, 1:3 до 1:6, особенно примерно 1: 4,5
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления стадию (i) проводят при повышенной температуре. Повышенной температурой является температура от 23°C (комнатной температуры) до температуры кипения органического растворителя. В предпочтительном варианте осуществления изобретения и/или его варианте осуществления стадию (i) проводят при температуре кипения органического растворителя. Все температуры, указанные здесь и относящиеся к температурам кипения или точкам кипения, относятся к температурам, измеренным при нормальном давлении 101 кПа.
Кроме того, реакционную смесь на стадии (i) можно предпочтительно подвергать механическому перемещению, например перемешиванию или ультразвуковой обработке.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления продолжительность стадии (i) может составлять от 30 минут до 48 часов, предпочтительно от 2 часов до 36 часов, в частности от 4 часов до 24 часов.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления настоящий способ дополнительно включает стадии
(ii) подкисления реакционной смеси со стадии (i) с получением конечной смеси
(iii) разделения конечной смеси на смесь соединения и супернатант.
На стадии (ii) прореагировавшая смесь со стадии (i) может быть подкислена, предпочтительно водным раствором кислоты Бренстеда. В предпочтительном варианте осуществления изобретения /или его варианте осуществления кислота имеет pKa 3,5 или меньше, предпочтительно, pKa 3,0 или меньше, более предпочтительно, pKa 2,5 или меньше, в частности pKa 2,0 или меньше.
Примерами подходящих кислот, имеющих pKa 3,5 или менее, являются хлористый водород (соответствующей кислотой является хлористоводородная кислота), бромистый водород, йодоводород, азотная кислота, серная кислота, гидросульфат натрия или калия, фосфорная кислота, трихлоруксусная кислота, фумаровая кислота, малеиновая кислота, щавелевая кислота, лимонная кислота, молочная кислота, 2-хлорбензойная кислота, метансульфоновая кислота, этансульфоновая кислота, п-толуолсульфоновая кислота и их смеси.
Кислота Бренстеда может быть органической или неорганической кислотой.
Примерами органических кислот, которые можно использовать в качестве кислот Бренстеда, являются фумаровая кислота, малеиновая кислота, щавелевая кислота, лимонная кислота, молочная кислота, метансульфоновая кислота, этансульфоновая кислота, п-толуолсульфоновая кислота и их смеси. Предпочтительными являются метансульфоновая кислота, этансульфоновая кислота и п-толуолсульфоновая кислота, в частности, метансульфоновая кислота и п-толуолсульфоновая кислота.
Примерами неорганических кислот, которые можно использовать в качестве кислот Бренстеда, являются хлористый водород (соответствующей кислотой является хлористоводородная кислота), бромистый водород, йодоводород, азотная кислота, серная кислота, гидросульфат натрия или калия, фосфорная кислота и их смеси.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления кислым водным раствором на стадии (ii) является раствор неорганической кислоты, предпочтительно хлористого водорода, бромистого водорода, серной кислоты, гидросульфата натрия или калия, фосфорной кислоты и их смесей, более предпочтительно хлористого водорода, гидросульфата натрия или калия, фосфорной кислоты и их смесей, в частности, хлористого водорода, гидросульфата калия или фосфорной кислоты, особенно гидросульфата калия.
Стадию (ii) подкисления раствора со стадии (i) можно предпочтительно проводить при охлаждении, предпочтительно при температуре от 5°C до 20°C, более предпочтительно, примерно 10°C.
Кроме того, стадию (ii) можно предпочтительно проводить при механическом движении, таком как перемешивание или обработка ультразвуком.
На стадии (iii) смесь соединения может быть разделена. Указанная смесь соединения содержит (R)-IOBA формулы (1a) и (S)-IOBA формулы (1b), где количество (S)-IOBA формулы (1b) увеличено в смеси по сравнению с количеством (S)-IOBA в смеси со стадии (i). В предпочтительном варианте осуществления изобретения и/или его варианте осуществления, полученным соединением является рацемат IOBA, т.е. (R)-IOBA формулы (1a) и (S)-IOBA формулы (1b) присутствуют в молярном отношении около 1:1.
Разделение может включать хорошо известные способы отделения твердого органического соединения, в частности твердой органической кислоты, от кислого водного раствора. Разделение может включать такие способы, как декантирование или сливание раствора, необязательно с предшествующей стадией центрифугирования, и фильтрование. Кроме того, разделение можно проводить путем экстракции желаемого соединения из кислого водного раствора.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (iii) разделение полученной смеси соединений проводят экстракцией органическим растворителем. Органические растворители хорошо известны специалистам в данной области техники. Экстракцию на стадии (iii) предпочтительно проводят в апротонном органическом растворителе. Органические растворители, подходящие для использования на данной стадии (iii), включают, например, толуол, бензол, ксилол, этилацетат, гексан, гептан, октан, циклические и ациклические алкиловые эфиры, хлорбензол, циклогексан, метилциклогексан, дихлорметан, дихлорэтан, трихлорметан, трихлорметан, тетрахлорэтан, диметоксиэтан, диэтоксиэтан и их комбинации. Предпочтительными являются этилацетат, толуол, дихлорметан и трихлорметан, в частности, этилацетат и толуол, особенно этилацетат.
Стадия экстракции предпочтительно включает добавление органического растворителя к подкисленному водному раствору со стадии (ii), смешивание двух жидкостей, отделение фазы с органическим растворителем от кислого водного раствора. Эту процедуру предпочтительно можно повторить, предпочтительно, повторить от двух до четырех раз. Далее органические фазы можно предпочтительно объединить и высушить. Сушку можно проводить с помощью любого известного осушающего агента, такого как сульфат натрия или сульфат магния. После сушки осушающий агент можно отделить от органической фазы, предпочтительно фильтрованием.
Кроме того, стадия (iii) предпочтительно включает удаление органического растворителя из органической фазы, предпочтительно из объединенной органической фазы. Удаление органического растворителя предпочтительно можно проводить при температуре от 23°C до 50°C, предпочтительно около 40°C и/или при пониженном давлении от 1 кПа до 90 кПа, предпочтительно около 10 кПа.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления стадию (i) проводят в отсутствие катализаторов межфазного переноса. Катализатор межфазного переноса можно рассматривать как вещество, которое облегчает миграцию реагента из одной фазы в другую фазу, где происходит реакция. Катализатор межфазного переноса также можно рассматривать как гетерогенный катализатор. Избегая использования катализатора межфазного переноса, можно повысить чистоту желаемого продукта, в данном случае соединения, полученного на стадии (iii), поскольку катализатор межфазного переноса часто трудно удалить из реакционной смеси и/или желаемого продукта.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления настоящий способ дополнительно включает предшествующие стадии
(a) взаимодействия (5RS)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойной кислоты с соединением формулы (2A), (2B) или (2C)
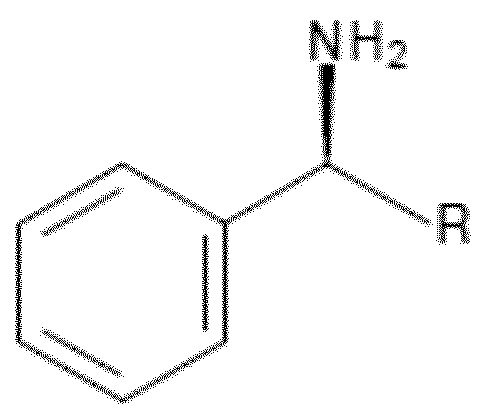
Формула (2A)
где R является алкилом с 1 или 2 атомами углерода,
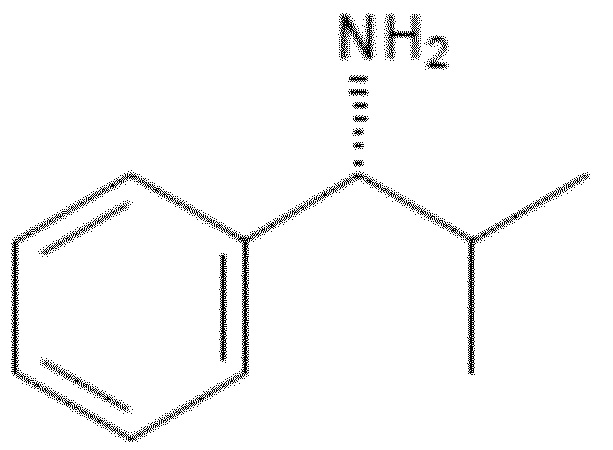
Формула (2B), или
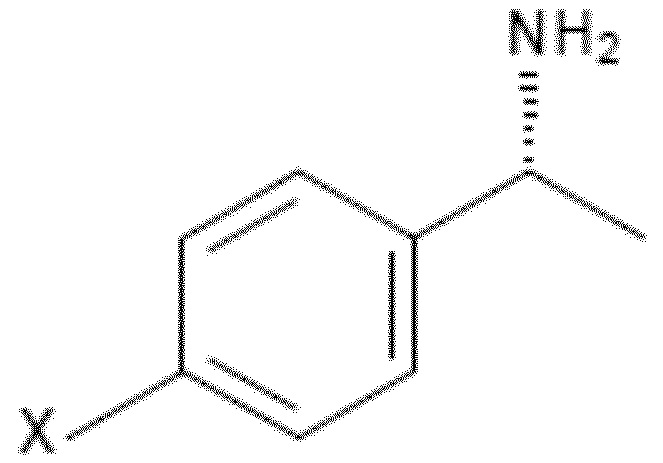
Формула (2C),
где X является Cl или Br,
в органическом растворителе, выбранном из группы, состоящей из органического растворителя, имеющего полярность ET(30) от 180 до 230 кДж/моль, органического растворителя, имеющего полярность ET(30) от 130 до 175 кДж/моль и их смесей с получением осадка и раствора супернатанта, и
(b) разделения раствора супернатанта, содержащего (5R)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойную кислоту формулы (1a) и (5S)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойную кислоту формулы (1b)

Формула (1a), и

Формула (1b),
из осадка и раствора супернатанта.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления вышеупомянутые стадии (а) и (b) могут выполняться последовательно.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления стадии (a) и (b) а также стадия (i) могут выполняться последовательно.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления стадии (a) и (b) а также стадии (i), (ii) и (iii) могут выполняться последовательно.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) способа в соответствии с данным изобретением и/или любого его варианте осуществления (5RS)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойную кислоту подвергают взаимодействию с соединением Формулы (2A), (2B) или (2C) в органическом растворителе, выбранном из группы, состоящей из органического растворителя, имеющего полярность ET(30) от 180 до 230 кДж/моль, органического растворителя, имеющего полярность ET(30) от 130 до 175 кДж/моль и их смесей с получением осадка и раствора супернатанта.
В Формуле (2A) остатком R является алкил с одним или двумя атомами углерода.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления остаток R является алкилом с одним атомом углерода, т.е. остаток R является метилом. Соответствующее основание или щелочное соединение является (S)-1-фенилэтиламином.
В альтернативно предпочтительном варианте осуществления изобретения и/или его варианте осуществления остаток R является алкилом с двумя атомами углерода, т.е. остаток R является этилом. Соответствующее основание или щелочное соединение является (S)-1-фенилпропиламином.
Соединением формулы (2B) является (R)-1-фенил-2-метилпропиламин.
В Формуле (2C) остаток X является Cl или Br.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления остаток X в Формуле (2C) является Cl, а соответствующее основание или щелочное соединение является (R)-1-(4-хлорфенил)этиламином.
В более предпочтительном варианте осуществления, остаток X в Формуле (2C) является Br, а соответствующее основание или щелочное соединение является (R)-1-(4-бромфенил)этиламином.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления соединение формулы (2A), (2B) или (2C) выбирают из группы, состоящей из (S)-1-фенилпропиламина, (R)-1-фенил-2-метилпропиламина, (R)-1-(4-хлорфенил)этиламина и (R)-1-(4-бромфенил)этиламина.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления (5RS)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойная кислота взаимодействует на стадии (i) с соединением Формулы (2A), (2B) или (2C) в молярном отношении от 1:0,4 и 1:5, предпочтительно, от 1:0,5 до 1:3, более предпочтительно, от 1:0,6 до 1:2, в частности, от 1:0,7 до 1:1.
На стадии (а) органическим растворителем является жидкое соединение, которое растворяет, предпочтительно полностью растворяет, вещество с образованием раствора. Примеры органических растворителей хорошо известны в данной области техники. Органические растворители можно классифицировать по категориям, например, по их температурам кипения (растворители с высокой или низкой температурой кипения), их кислотности/основности (кислотные или щелочные растворители) и/или их полярности (полярные и неполярные растворители).
Значение ET(30) показывает полярность разных растворителей (см., например, Jose P. Ceron-Carrasco et al.: “Solvent polarity scales: determination of new ET(30) values for 84 organic solvents”, Research Article; Journal of Physical Organic Chemistry, 2014, 27, pages 512-518). Значение ET(30) определяют с помощью отрицательного сольватохромного красителя 2,6-дифенил-4-(2,4,6-трифенилпиридин-1-ий-1-ил)фенолата, который также называют Betaine 30 или краситель Рейнхардта. Betaine 30 представлено соединением согласно Формуле (B) ниже

Формула (B).
Боле конкретно, значение ET(30) определяют с помощью Betaine 30 в соответствующем растворителе через самую длинноволновую полосу адсорбции VIS/NIR. Высокие значения ET(30) считаются соответствующими высокой полярности растворителя, а низкие значения ET(30) указывают на низкую полярность растворителя. Таким образом, коротко, чем выше значение ET(30), тем более полярным является растворитель, и наоборот. Значение ET(30) также определяют как молярная энергия электронного возбуждения и рассчитывают следующим образом

где λmax является длинноволновой полосой адсорбции в видимой/ближней ИК-области спектра Betaine 30 в соответствующем растворителе, при измерении при 25°C и 101 кПа.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) настоящего способа органический растворитель имеет значение ET(30) от 170 до 230 кДж/моль, предпочтительно, от 180 до 225 кДж/моль, более предпочтительно от 190 до 220 кДж/моль, в частности от 200 до 218 кДж/моль.
Примеры органических растворителей, имеющих значение ET(30) от 170 до 230 кДж/моль включают пиридины, такие как 2-фторпиридин и 2,6-дифторпиридин; спирты, такие как этанол, 1-пропанол, 2-пропанол, циклопропиловый спирт, 1-бутанол, 2-бутанол, циклобутанол, 2-метил-1-пропанол, 2-метил-2-пропанол, 1-пентанол, 2-пентанол, 3-пентанол, циклопентанол, 2-метил-1-бутанол, 3-метил-1-бутанол, 3-метил-2-бутанол, 2-метил-2-бутанол, 2,2-диметил-1-пропанол, аллиловый спирт, 2-метоксиэтанол, 2-этоксиэтанол, 2-(н-бутокси)этанол, 2-феноксиэтанол, циклогексанол, 1-гексанол, 1-гептанол, 1-октанол, 1-нонанол, 1-деканол, 2-фенилэтанол, бензиловый спирт, 2-хлорэтанол, 1,1,1-тифтор-2-(трифторметил)пентан-2-ол, 1,1,1-тифтор-2-(трифторметил)пент-4-ен-2-ол, 2,2,2-трифтор-1-фенилэтанол, 1,1,1,3,3,3-гексафтор-2-фенилпропан-2-ол; кетоны, такие как 1,1,1-трихлорацетон; сложные эфиры и лактоны, такие как 4-бутиролактон и этилпропиноат; амиды и цианамиды, такие как N, N-диметилформамид, N, N-диметилцианамид, пирролидин-2-он, N-метилпропионамид, N-этилацетамид, N-метилацетамид, N-метилформамид; нитрилы, такие как н-пропаннитрил, 3-метоксипропаннитрил, ацетонитрил, хлорацетонитрил; нитроалкан, такой как нитрометан и нитроэтан; ароматические амины, такие как анилин; фосфорные соединения, такие как триметилфосфат; и сернистые соединения, такие как тетрагидро-3-метилтиофен-1,1-диоксид, тетраметиленсульфоксид, диметилсульфоксид и этиленсульфит.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления органическим растворителем на стадии (a) является спирт, выбранный из этанола, 1-пропанола, 2-пропанола, циклопропилового спирта, 1-бутанола, 2-бутанола, циклобутанола, 2-метил-1-пропанола, 2-метил-2-пропанола, 1-пентанола, 2-пентанола, 3-пентанола, циклопентанола, 2-метил-1-бутанола, 3-метил-1-бутанола, 3-метил-2-бутанола, 2-метил-2-бутанола, 2,2-диметил-1-пропанола, аллилового спирта, 2-метоксиэтанола, 2-этоксиэтанола, 2-(н-бутокси)этанола, 2-феноксиэтанола, циклогексанола, 1-гексанола, 1-гептанола, 1-октанола, 1-нонанола, 1-деканола, 2-фенилэтанола, бензилового спирта, 2-хлорэтанола, 1,1,1-тифтор-2-(трифторметил)пентан-2-ола, 1,1,1-тифтор-2-(трифторметил)пент-4-ен-2-ола, 2,2,2-трифтор-1-фенилэтанола, 1,1,1,3,3,3-гексафтор-2-фенилпропан-2-ола и их смесей.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления органическим растворителем на стадии (а) является спирт с 2-8 атомами углерода. Спиртом предпочтительно является моноспирт, т.е. органический растворитель содержит только одну гидроксигруппу. Кроме того, предпочтительно, чтобы органический растворитель нес только гидроксильную функциональную группу. Другими словами, спирт не несет никакой другой функциональной группы, кроме (одной) гидроксигруппы. Кроме того, спирт с 2-8 атомами углерода, используемый в качестве органического растворителя, содержит только атомы водорода, кислорода и углерода. Соответственно, спирт дополнительно не замещен.
Примерами спиртов с 2-8 атомами углерода, используемых в качестве органического растворителя, являются этанол, 1-пропанол, 2-пропанол, циклопропиловый спирт, 1-бутанол, 2-бутанол, циклообутанол, 2-метил-1-пропанол, 2-метил-2-пропанол, 1-пентанол, 2-пентанол, 3-пентанол, циклопентанол, 2-метил-1-бутанол, 3-метил-1-бутанол, 3-метил-2-бутанол, 2-метил-2-бутанол, 2,2-диметил-1-пропанол, 1-гексанол, 1-гептанол, 1-октанол и их смеси.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления органическим растворителем на стадии (а) является спирт с 2-8 атомами углерода, выбранный из группы, состоящей из этанола, 1-пропанола, 2-пропанола, 1-бутанола, 2-бутанола, 2-метил-1-пропанола, 1-пентанола, 2-пентанола, 3-пентанола, 1-гексанола и их смесей, более предпочтительно органический растворителем является спирт с 2-8 атомами углерода, выбранный из группы, состоящей из этанола, 2-пропанола, 1-бутанола, 1-пентанола, 1-гексанола, 1-гептанола и их смесей.
В особенно предпочтительном варианте осуществления изобретения и/или его варианте осуществления органическим растворителем на стадии (a) является этанол. В альтернативно предпочтительном варианте осуществления, органическим растворителем на стадии (a) является 2-пропанол. В альтернативно предпочтительном варианте осуществления, органическим растворителем на стадии (a) является 1-бутанол. В альтернативно предпочтительном варианте осуществления, органическим растворителем на стадии (a) является 1-пентанол. В альтернативно предпочтительном варианте осуществления, органическим растворителем на стадии (a) является 1-гексанол.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления органическим растворителем на стадии (a) не является амид или цианамид.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления органическим растворителем на стадии (a) не является серное соединение.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления, на стадии (a) остатком R формулы (2A) является метил и органический растворитель выбирают из этанола, 2-пропанола, 1-бутанола, 1-пентанола, 1-гексанола, 1-гептанола, 1-октанола и их смесей.
Альтернативно предпочтительно, на стадии (a) остатком R формулы (2А) является метил и органическим растворителем является этанол, или остатком R формулы (2А) является метил и органическим растворителем является 2-пропанол.
Альтернативно предпочтительно, на стадии (a) остатком R формулы (2А) является метил и органическим растворителем является 1-бутанол, или остатком R формулы (2А) является метил и органическим растворителем является 1-пентанол, или остатком R формулы (2А) является метил и органическим растворителем является 1-гексанол.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) остатком R формулы (2А) является этил, и органический растворитель выбирают из этанола, 2-пропанола, 1-бутанола, 1-пентанола, 1-гексанола и их смесей.
Альтернативно предпочтительно на стадии (a) остатком R формулы (2А) является этил и органическим растворителем является этанол, или остатком R формулы (2А) является этил и органическим растворителем является 2-пропанол.
Альтернативно предпочтительно на стадии (a) остатком R формулы (2А) является этил и органическим растворителем является 1-бутанол, или остатком R формулы (2А) является этил и органическим растворителем является 1-пентанол, или остатком R формулы (2А) является этил и органическим растворителем является 1-гексанол.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) хиральным основанием является (R)-1-фенил-2-метилпропиламин (Формула 2B) и органическим растворителем является этанол, или хиральным основанием является (R)-1-фенил-2-метилпропиламин (Формула 2B) и органическим растворителем является 2-пропанол, или хиральным основанием является (R)-1-фенил-2-метилпропиламин (Формула 2B) и органическим растворителем является 1-бутанол, или хиральным основанием является (R)-1-фенил-2-метилпропиламин (Формула 2B) и органическим растворителем является 1-пентанол, или хиральным основанием является (R)-1-фенил-2-метилпропиламин (Формула 2B) и органическим растворителем является 1-гексанол.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) остатком X Формулы (2C) является Cl (хлорид) или Br (бромид).
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) остатком X Формулы (2C) является Cl и органическим растворителем является 2-пропанол.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) остатком X Формулы (2C) является Br, и органический растворитель выбирают из группы, включающей этанол, 2-пропанол, 1-бутанол, 1-пентанол, и их смесей.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) остатком X Формулы (2C) является Br и органическим растворителем является этанол, или остатком R формулы (2C) является Br и органическим растворителем является 2-пропанол, или остатком R формулы (2C) является Br и органическим растворителем является 1-бутанол, или остатком R формулы (2C) является Br и органическим растворителем является 1-пентанол.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) (5RS)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойная кислота взаимодействует с соединением Формулы (2A), (2B) или (2C) в органическом растворителе, имеющем полярность ET(30) от 180 и 230 кДж/моль с получением осадка и раствора супернатанта. Таким образом, в органическом растворителе, (5RS)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойная, предпочтительно, (S)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойная кислота и соединением формулы (2A), (2B) или (2C) взаимодействуют друг с другом с получением продукта, который выпадает в осадок, и раствора супернатанта. Другими словами, (5RS)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойная кислота, предпочтительно, (5S)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойная кислота и соединение формулы (2A), (2B) или (2C) реагируют друг с другом с получением твердого продукта, который может выпасть в осадок, предпочтительно, полностью выпадает в осадок, из реакционной смеси, в то время как раствор супернатанта остается. Указанный раствор супернатанта предпочтительно содержит незначительную часть непрореагировавшей (5S)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойной кислоты, и, предпочтительно, большую часть (5R)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойной кислоты.
В альтернативном предпочтительном варианте осуществления изобретения и/или вариантах осуществления, на стадии (a) способа в соответствии с данным изобретением органический растворитель имеет значение ET(30) от 130 до 175 кДж/моль.
Примеры растворителей, имеющих значение ET(30) от 130 до 175 кДж/моль включают алифатические, циклоалифатические или ароматические простые эфиры, такие как диметиловый эфир этиленгликоля, диметиловый эфир триэтиленгликоля, 1,2-диметоксиэтан, ди-н-бутиловый эфир, ди-трет-бутиловый эфир, диизопропиловый эфир, н-бутиловый эфир метил-трет-бутиловый эфир, циклопентилметиловый эфир, диоксан, тетрагидропиран, 2,2,5,5-тетраметилтетрагидропиран, тетрагидрофуран, тетрагидро-2-метилфуран, 2,2,5,5-тетраметилтетрагидрофуран, бензилметиловый эфир, дибензиловый эфир, анизол, 3-метиланизол и фенетол; арены и пиридины, такие как бензол, толуол, м-ксилол и мезитилен; галоарены, такие как хлорбензол, 1,3-дихлорбензол, бромбензол и 1,3-дибромбензол и пиридин; алифатические сложные эфиры, такие как метилформиат, метилацетат, метилпропаноат, метилбутаноат, метилгексаноат, этилформиат, этилацетат, этилпропаноат, этилбензоат и бутилацетат; алифатические, циклоалифатические или ароматические амины, такие как диэтиламин, триэтиламин, диизопропиламин, морфолин, пиперидин; галогеналканы, такие как трихлорметан, тетрахлорметан, 1,1-дихлорэтан, 1,2-дихлорэтан и 1,1,2,2-тетрахлорэтан и их смеси.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления органический растворитель на стадии (a) имеет значение ET(30) от 132 до 175 кДж/моль. Предпочтительно, от 134 до 174 кДж/моль, более предпочтительно от 135 до 170 кДж/моль, в частности от 140 до 165, и более предпочтительно, от 134 до 160 кДж/моль.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления органическим растворителем на стадии (a) является алифатический или циклоалифатический эфир, такой как диметиловый эфир этиленгликоля, диметиловый эфир триэтиленгликоля, 1,2-диметоксиэтан, ди-н-бутиловый эфир, ди-трет-бутиловый эфир, диизопропиловый эфир, н-бутилметиловый эфир, метил-трет-бутиловый эфир, циклопентилметиловый эфир, диоксан, тетрагидрофуран, тетрагидро-2-метилфуран; арен, такой как бензол, толуол, м-ксилол, мезитилен, галогенарен, такой как хлорбензол, бромбензол; сложный алифатический эфир, такой как метилацетат, метилпропаноат, метилбутаноат, этилацетат, этилпропаноат, этилбензоат, бутилацетат; алифатический амин, такой как диэтиламин, триэтиламин, диизопропиламин; галогеналкан, такой как трихлорметан, тетрахлорметан, 1,1-дихлорэтан и 1,2-дихлорэтан и их смеси.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления органический растворитель на стадии (a) выбирают из группы, состоящей из метил-трет-бутилового эфира, циклопентилметилового эфира, тетрагидрофурана, диоксана, хлорбензола, толуола, м-ксилола, мезитилена, этилацетата, бутилацетата, триэтиламина, трихлорметана, 1,2-дихлорэтана и их смесей
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления органическим растворителем на стадии (a) является метил-трет-бутиловый эфир. В предпочтительном варианте осуществления изобретения и/или его варианте осуществления органическим растворителем на стадии (a) является циклопентилметиловый эфир. В предпочтительном варианте осуществления изобретения и/или его варианте осуществления органическим растворителем на стадии (a) является тетрагидрофуран. В предпочтительном варианте осуществления изобретения и/или его варианте осуществления органическим растворителем на стадии (a) является диоксан. В предпочтительном варианте осуществления изобретения и/или его варианте осуществления органическим растворителем на стадии (a) является хлорбензол. В предпочтительном варианте осуществления изобретения и/или его варианте осуществления органическим растворителем на стадии (a) является толуол. В предпочтительном варианте осуществления изобретения и/или его варианте осуществления органическим растворителей на стадии (a) является м-ксилол. В предпочтительном варианте осуществления изобретения и/или его варианте осуществления органическим растворителем на стадии (a) является мезитилен. В предпочтительном варианте осуществления изобретения и/или его варианте осуществления органический растворитель на стадии (a) является этилацетат. В предпочтительном варианте осуществления изобретения и/или его варианте осуществления органическим растворителем на стадии (a) является бутилацетат. В предпочтительном варианте осуществления изобретения и/или его варианте осуществления органическим растворителем на стадии (a) является триэтиламин. В предпочтительном варианте осуществления изобретения и/или его варианте осуществления органическим растворителем на стадии (a) является трихлорметан. В предпочтительном варианте осуществления изобретения и/или его варианте осуществления органическим растворителем на стадии (a) является 1,2-дихлорэтан.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления органический растворитель на стадии (a) выбирают из группы, состоящей из метил-трет-бутилового эфира, циклопентиметилового эфира, тетрагидрофурана, диоксана, хлорбензола, толуола, м-ксилола, мезитилена, этилацетата, бутилацетата, триэтиламина, трихлорметана, 1,2-дихлорэтана и их смесей.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) остатком R формулы (2А) является метил и органический растворитель выбирают из группы, состоящей из метил-трет-бутилового эфира, циклопентилметилового эфира, тетрагидрофурана, диоксана, хлорбензола, толуола, м-ксилола, мезитилена, этилацетата, бутилацетата, триэтиламина, трихлорметана, 1,2-дихлорэтана и их смесей.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) остатком R формулы (2А) является метил и органический растворитель выбирают из группы, состоящей из метил-трет-бутилового эфира, циклопентилметилового эфира, диоксана, хлорбензола, толуола, м-ксилола, мезитилена, этилацетата, бутилацетата, триэтиламина, трихлорметана, 1,2-дихлорэтана и их смесей.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) R остатком формулы (2A) является метил и органический растворитель выбирают из группы, состоящей из диоксана, хлорбензола, толуола, этилацетата, бутилацетата, триэтиламина, трихлорметана, 1,2-дихлорэтана и их смесей.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) остатком R формулы (2А) является метил и органическим растворителем является метил-трет-бутиловый эфир, или остатком R формулы (2А) является метил и органическим растворителем является циклопентилметиловый эфир, или остатком R формулы (2А) является метил и органическим растворителем является тетрагидрофуран, или остатком R формулы (2А) является метил и органическим растворителем является диоксан, или остатком R формулы (2А) является метил и органическим растворителем является хлорбензол, или остатком R формулы (2А) является метил и органическим растворителем является толуол, или остатком R формулы (2А) является метил и органическим растворителем является м-ксилол, или остатком R формулы (2А) является метил и органическим растворителем является мезитилен, или остатком R формулы (2А) является метил и органическим растворителем является этилацетат, или остатком R формулы (2А) является метил и органическим растворителем является бутилацетат, или остатком R формулы (2А) является метил и органическим растворителем является триэтиламин, или остатком R формулы (2А) является метил и органическим растворителем является трихлорметан или остатком R формулы (2А) является метил и органическим растворителем является 1,2-дихлорэтан.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) остатком R формулы (2А) является этил, и органический растворитель выбирают из группы, состоящей из метил-трет-бутилового эфира, циклопентилметилового эфира, тетрагидрофурана, диоксана, хлорбензола, толуола, м-ксилола, мезитилена, этилацетата, бутилацетата, триэтиламина, трихлорметана, 1,2-дихлорэтана и их смесей.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) остатком R формулы (2А) является этил, и органический растворитель выбирают из группы, состоящей из метил-трет-бутилового эфира, циклопентилметилового эфира, диоксана, хлорбензола, толуола, м-ксилола, мезитилена, этилацетата, бутилацетата, триэтиламина, трихлорметана, 1,2-дихлорэтана и их смесей.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) остатком R формулы (2А) является этил, и органический растворитель выбирают из группы, состоящей из метил-трет-бутилового эфира, циклопентилметилового эфира, диоксана, хлорбензола, толуола, м-ксилола, мезитилена, этилацетата, бутилацетата, триэтиламина, 1,2-дихлорэтана и их смесей.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) остатком R формулы (2А) является этил, и органический растворитель выбирают из группы, состоящей из метил-трет-бутилового эфира, циклопентилметилового эфира, хлорбензола, м-ксилола, мезитилена, этилацетата, бутилацетата, триэтиламина, 1,2-дихлорэтана и их смесей.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления, на стадии (a) остатком R формулы (2А) является этил и органическим растворителем является метил-трет-бутиловый эфир, или остатком R формулы (2А) является этил и органическим растворителем является циклопентилметиловый эфир, или остатком R формулы (2А) является этил и органическим растворителем является тетрагидрофуран, или остатком R формулы (2А) является этил и органическим растворителем является диоксан, или остатком R формулы (2А) является этил и органическим растворителем является хлорбензол, или остатком R формулы (2А) является этил и органическим растворителем является толуол, или остатком R формулы (2А) является этил и органическим растворителем является м-ксилол, или остатком R формулы (2А) является этил и органическим растворителем является мезитилен, или остатком R формулы (2А) является этил и органическим растворителем является этилацетат, или остатком R формулы (2А) является этил и органическим растворителем является бутилацетат, или остатком R формулы (2А) является этил и органическим растворителем является триэтиламин, или остатком R формулы (2А) является этил и органическим растворителем является трихлорметан или остатком R формулы (2А) является этил и органическим растворителем является 1,2-дихлорэтан.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) хиральным основанием является (R)-1-фенил-2-метилпропиламин (Формула 2B) и органическим растворителем является тетрагидрофуран, или хиральным основанием является (R)-1-фенил-2-метилпропиламин (Формула 2B) и органическим растворителем является диоксан, или хиральным основанием является (R)-1-фенил-2-метилпропиламин (Формула 2B) и органическим растворителем является толуол, или хиральным основанием является (R)-1-фенил-2-метилпропиламин (Формула 2B) и органическим растворителем является этилацетат, или хиральным основанием является (R)-1-фенил-2-метилпропиламин (Формула 2B) и органическим растворителем является 1,2-дихлорэтан.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) хиральным основанием является (R)-1-фенил-2-метилпропиламин (Формула 2B) и органический растворитель выбирают из группы, состоящей из метил-трет-бутилового эфира, циклопентилметилового эфира, тетрагидрофурана, диоксана, хлорбензола, толуола, м-ксилола, мезитилена, этилацетата, бутилацетата, триэтиламина, трихлорметана, 1,2-дихлорэтана и их смесей.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) хиральным основанием является (R)-1-фенил-2-метилпропиламин (Формула 2B) и органический растворитель выбирают из группы, состоящей из метил-трет-бутилового эфира, циклопентилметилового эфира, хлорбензола, толуола, м-ксилола, мезитилена, этилацетата, бутилацетата, триэтиламина, трихлорметана, 1,2-дихлорэтана и их смесей.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) хиральным основанием является (R)-1-фенил-2-метилпропиламин (Формула 2B) и органический растворитель выбирают из группы, состоящей из хлорбензола, толуола, м-ксилола, мезитилена, этилацетата, бутилацетата, триэтиламина, трихлорметана, 1,2-дихлорэтана и их смесей.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) хиральным основанием является (R)-1-фенил-2-метилпропиламин (Формула 2B) и органический растворитель выбирают из группы, состоящей из хлорбензола, толуола, этилацетата, бутилацетата, триэтиламина, трихлорметана, 1,2-дихлорэтана и их смесей.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) остатком X Формулы (2C) является Cl (хлорид) или Br (бромид).
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) остатком X Формулы (2C) является Cl, и органический растворитель выбирают из группы, состоящей из тетрагидрофурана, диоксана, толуола, этилацетата и их смесей.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) остатком X Формулы (2C) является Cl, и органический растворитель выбирают из группы, состоящей из метил-трет-бутилового эфира, циклопентилметилового эфира, диоксана, хлорбензола, толуола, м-ксилола, мезитилена, этилацетата, бутилацетата, триэтиламина, трихлорметана, 1,2-дихлорэтана и их смесей.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) остатком X Формулы (2C) является Cl, и органический растворитель выбирают из группы, состоящей из метил-трет-бутилового эфира, циклопентилметилового эфира, хлорбензола, толуола, м-ксилола, мезитилена, этилацетата, бутилацетата, триэтиламина, трихлорметана, 1,2-дихлорэтана и их смесей.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) остатком X Формулы (2C) является Cl, и органический растворитель выбирают из группы, состоящей из хлорбензола, толуола, этилацетата, бутилацетата, триэтиламина, трихлорметана, 1,2-дихлорэтана и их смесей.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) остатком X Формулы (2C) является Cl, и органический растворитель выбирают из группы, состоящей из толуола, этилацетата и их смесей.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) остатком R формулы (2C) является хлорид и органическим растворителем является тетрагидрофуран, остатком R формулы (2C) является хлорид и органическим растворителем является диоксан, остатком R формулы (2C) является хлорид и органическим растворителем является толуол, или остатком R формулы (2C) является хлорид и органическим растворителем является этилацетат.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) остатком X Формулы (2C) является Br, и органический растворитель выбирают из группы, состоящей из тетрагидрофурана, диоксана, толуола, этилацетата и их смесей.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) остатком R формулы (2C) является бромид и органическим растворителем является тетрагидрофуран, остатком R формулы (2C) является бромид и органическим растворителем является диоксан, остатком R формулы (2C) является бромид и органическим растворителем является толуол, или остатком R формулы (2C) является бромид и органическим растворителем является этилацетат.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) остатком X Формулы (2C) является Br, и органический растворитель выбирают из группы, состоящей из метил-трет-бутилового эфира, циклопентилметилового эфира, диоксана, хлорбензола, толуола, м-ксилола, мезитилена, этилацетата, бутилацетата, триэтиламина, трихлорметана, 1,2-дихлорэтана и их смесей.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) остатком X Формулы (2C) является Br, и органический растворитель выбирают из группы, состоящей из метил-трет-бутилового эфира, циклопентилметилового эфира, хлорбензола, толуола, м-ксилола, мезитилена, этилацетата, бутилацетата, триэтиламина, трихлорметана, 1,2-дихлорэтана и их смесей.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) остатком X Формулы (2C) является Br, и органический растворитель выбирают из группы, состоящей из хлорбензола, толуола, этилацетата, бутилацетата, триэтиламина, трихлорметана, 1,2-дихлорэтана и их смесей.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) остатком X Формулы (2C) является Br, и органический растворитель выбирают из группы, состоящей из толуола, этилацетата и их смесей.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (a) (5RS)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойная кислота взаимодействует с соединением формулы (2A), (2B) или (2C) в органическом растворителе, имеющем полярность ET(30) от 130 до 175 кДж/моль с получением осадка и раствора супернатанта. Таким образом, в органическом растворителе, (5RS)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойная, предпочтительно, (S)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойная кислота и соединением формулы (2A), (2B) или (2C) взаимодействуют друг с другом с получением продукта, который выпадает в осадок, и раствора супернатанта. Другими словами, (5RS)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойная кислота, предпочтительно, (5S)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойная кислота и соединение формулы (2A), (2B) или (2C) реагируют друг с другом с получением твердого продукта, который может выпасть в осадок, предпочтительно, полностью выпадает в осадок, из реакционной смеси, в то время как раствор супернатанта остается. Указанный раствор супернатанта предпочтительно содержит незначительную часть непрореагировавшей (5S)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойной кислоты, и, предпочтительно, большую часть (5R)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойной кислоты.
Взаимодействие (5RS)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойной кислоты с соединением формулы (2A), (2B) или (2C) может проводиться при любой температуре, пока растворитель находится в жидком состоянии. Например, на стадии (a) реакция может проводиться при температуре от 4 до 65°C, предпочтительно, от 10 до 55°C, также предпочтительно, от 15 до 45°C, предпочтительно, от 20 до 40°C, предпочтительно, от 25 до 35°C, и наиболее предпочтительно при примерно 23°C (также называемой комнатная температура).
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления стадия (a) включает нагревание (5RS)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойной кислоты с соединением формулы (2A), (2B) или (2C) до повышенной температуре. Повышенной температурой является температура от 23°C (комнатной температуры) до температуры кипения органического растворителя, предпочтительно, от 30°C до температуры кипения органического растворителя минус 5°C, более предпочтительно от 40° до температуры кипения органического растворителя минус 20°C. Это означает, что в случае применения этанола с температурой кипения или точкой кипения 78°C в качестве органического растворителя, реакция на стадии (i) предпочтительно может проводиться при температуре от 23°C до 78°C, предпочтительно, от 30°C до 73°C, более предпочтительно от 40°C до 68°C. Все температуры, указанные здесь и относящиеся к температурам кипения или точкам кипения, относятся к температурам, измеренным при нормальном давлении 101 кПа.
Кроме того, стадия (а) предпочтительно включает охлаждение реакционной смеси указанной стадии. В случае если стадия (а) не включает нагревание реакционной смеси до повышенной температуры, реакционную смесь можно охладить до 0-20°C, предпочтительно, примерно 10°C. В случае если эта стадия (i) включает нагревание реакционной смеси до повышенной температуры, реакционную смесь можно охладить до 0-40°C, предпочтительно от 10°C до 30°C, в частности, примерно до 23°C (комнатной температуры). При охлаждении реакционной смеси полученный продукт образует осадок и раствор супернатанта, причем раствор супернатанта преимущественно включает (5R)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойную кислоту, предпочтительно, в энантиомерном избытке.
Кроме того, реакцию на стадии (а) можно предпочтительно подвергнуть механическому перемещению, например перемешиванию или ультразвуковой обработке.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления, продолжительность стадии (а) может составлять от 15 минут до 24 часов, предпочтительно, от 30 минут и 12 часов, в частности, от 1 часа и 6 часов.
На стадии (b) раствор супернатанта со стадии (а) отделяют от осадка. Раствор супернатанта является жидкостью и может быть отделен от твердого осадка любым методом отделения жидкости от твердого вещества. Примерами этих методов являются декантирование или сливание раствора супернатанта, необязательно с предшествующей стадией центрифугирования, и фильтрация.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления на стадии (b) отделение раствора супернатанта от осадка проводят фильтрованием. Используемая здесь фильтрация является механической или физической операцией, которая отделяет твердое вещество, в данном случае осадок, от жидкости, в данном случае раствор супернатанта, через среду, через которую может проходить только жидкость. Такая среда может называться фильтром или ситом, предпочтительно, фильтром. Примерами подходящих фильтров являются вакуумные фильтры, пресс-фильтры или складчатые фильтры, предпочтительно вакуумные фильтры.
В предпочтительном варианте осуществления изобретения и/или его варианте осуществления органический растворитель на стадиях (а) и (i) является одним и тем же. Что касается определения органического растворителя, то применяется то же, что описано на стадии (а) настоящего способа. В предпочтительном варианте осуществления изобретения и/или вариантах осуществления, органическим растворителем является 2-пропанол.
Неожиданно оказалось, что отделение (S)-IOBA и рацемизация полученного раствора супернатанта, содержащего избыток (R)-IOBA, может проводиться в одном и том же растворителе, т.е. нет необходимости менять растворитель для проведения стадии рацемизации, которая может рассматриваться как стадия рециркулирования ценного (S)-энантиомера IOBA из раствора с энантиомерным избытком (R)-энантиомера IOBA.
В соответствии с заявкой энантиомерный избыток (эи) определяют как абсолютная разница мольных долей каждого энантиомера, и она может быть выражена как доля энантиомерного избытка, который рассчитывается в соответствии с уравнением:
эи=(│FR-FS│x100)%
где
FR является мольной долей (R)-энантиомера, и
FS является мольной долей (S)-энантиомера
Количество и, следовательно, мольная доля соответствующего энантиомера может быть определена способами, известными в данной области техники, например, с помощью численного значения оптической чистоты рассматриваемого соединения, с помощью хиральной колоночной хроматографии (хиральная ЖХ или СЖХ) или с помощью ЯМР-спектроскопии в присутствии реагентов хирального сдвига. В настоящей заявке мольная доля соответствующего энантиомера определяется с помощью хиральной ЖХ. Другие возможности включают превращение (S)-IOBA с хиральными аминами или спиртами в диастереоизомерные амиды или сложные эфиры и определение % эи с помощью ЖХ.
Далее изобретение будет описано с помощью следующих неограничивающих примеров:
Примеры
Пример 1
В колбу, оборудованную конденсатором и термометром, загружают 2-пропанол (12,5 мл) и воду (0,85 мл). Твердый гидроксид калия (0,671 г, 11,96 ммоль) растворяют в растворителе и добавляют (5R)-4-(5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил)-2-метилбензойную кислоту с 87,2% эи (1 г, 2,391 ммоль) при 23°C (комнатная температура). Смесь нагревают до 80°C.
50 мкл образец берут через 1 час, 2 часа и 16 часов, соответственно, для определения степени рацемизации. Каждый из образцов обрабатывают следующим образом: его гасят KHSO4-раствором (1 мл, 2,3 M) и экстрагируют дважды этилацетатом (один раз 2 мл и один раз 1 мл). Объединенные органические фазы концентрируют при пониженном давлении. Остаток сушат масляным вакуум-насосом и растворяют в смеси изогексан:этанол 1:1 (1 мл).
Полученная (R)-IOBA имеет энантиомерный избыток 84,8% через один час, 84,5% чрез два часа и 64% через 16 часов.
Пример 2
В колбе, оборудованной конденсатором и термометром, загружают 2-пропанол (6,67 мл) и растворяют (5R)-4-(5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил)-2-метилбензойную кислоту с 86,4% эи (1 г, 2,391 ммоль). Добавляют микрогранулы гидроксида натрия (0,393 г, 9,83 ммоль) при 40°C и смесь нагревают до кипения с обратным холодильником, с получением желтой суспензии.
A 50 мкл образец берут через 2 часа, 4 часа и 20 часов, соответственно, для определения степени рацемизации. Каждый из образцов обрабатывают, как описано в примере 1.
Полученная (R)-IOBA имеет энантиомерный избыток 62,4% через два часа, 85,0% через четыре часа и 31,8% через 20 часов.
Пример 3
Раствор (5R)-4-(5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил)-2-метилбензойной кислоты с >99% эи (50 мг, 0,120 ммоль) в 2-пропаноле (299 мкл) инкубируют с раствором гидроксида калия в 2-пропаноле (20,38 мкл, 0,359 ммоль) в 1 мл конической пробирке. Смесь нагревают до 90°C в течение ночи.
Образец 100 мкл реакционной смеси концентрируют до твердого вещества, разбавляют 2 мл водной KHSO4 (15%) и экстрагируют 1-2 мл этилацетата. Органическую фазу отделяют и концентрируют. Масло сушат при пониженном вакууме и растворяют в изогексане:этаноле 1:1 (1 мл). Из этого раствора 250 мкл разбавляют изогексаном:этанолом 1:1 (1 мл) анализируют хиральной ЖХ-ДМД. Полученная (R)-IOBA имеет энантиомерный избыток 56,47%.
Пример 4
Раствор (R)-4-(5-(3,5-дихлорфенил)-5-(трифторметил)-4,5-дигидроизоксазол-3-ил)-2-метилбензойной кислоты с >99% эи (50 мг, 0,120 ммоль) в 2-пропаноле (299 мкл) инкубируют с раствором гидроксида цезия в 2-пропаноле (66,8 мкл, 0,359 ммоль) в 1 мл конической пробирке. Смесь нагревают до 90°C в течение ночи.
Образец 100 мкл реакционной смеси концентрируют до твердого вещества, разбавляют 2 мл водной KHSO4 (15%) и экстрагируют 1-2 мл этилацетата. Органическую фазу отделяют и концентрируют. Масло сушат при пониженном вакууме и растворяют в изогексане:этаноле 1:1 (1 мл). Из этого раствора 250 мкл разбавляют изогексаном:этанолом 1:1 (1 мл) и анализируют хиральной ЖХ-ДМД. Полученная (R)-IOBA имеет энантиомерный избыток 56,47%.
Пример 5
Колбу оборудуют конденсатором и термометром. В колбу загружают 2-пропанол (6,67 мл), порошковый гидроксид калия (0,671 г, 11,96 ммоль) растворяют в растворителе и добавляют (5R)-4-(5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил)-2-метилбензойную кислоту с 87,2% эи (1 г, 2,391 ммоль) при 40°C. Смесь нагревают до кипения с обратным холодильником. Образуется прозрачный оранжевый раствор. Через некоторое время выпадает желтый твердый продукт. Суспензию затем нагревают до кипения с обратным холодильником. 50 мкл образец суспензии обрабатывают, как описано в примере 1. Полученная (R)-IOBA имеет энантиомерный избыток 0,8%.
Как можно увидеть из примеров 1-5, избыток (R)-IOBA, содержащейся в полученном продукте, снижается. Таким образом, можно сделать вывод, что молярное количество (S)-IOBA улучшается рацемизацией исходной смеси.
Пример 6
В 1 л трехгорлую колбу, оборудованную KPG-перемешиваемой единицей (IKA RW-16 основная) и обратным холодильником, загружают 2-пропанол (200 мл) и (5RS)-4-(5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил)-2-метилбензойную кислоту (100 г, 239 ммоль). Добавляют еще порцию 2-пропанола (250 мл). Смесь перемешивают до тех пор, пока весь твердый материал не растворится. Быстро добавляют (S)-1-фенилпропиламин (21 мл, 144 ммоль) в 1 мл (первая) и 20 мл (вторая) порциями через шприц.
Затем смесь перемешивают в течение 75 мин при КТ, после чего образуется суспензия. Смесь перемешивают в течение 45 мин при температуре кипения с обратным холодильником. Нагревание прекращают, и суспензию медленно охлаждают до комнатной температуре при перемешивании.
Суспензию фильтруют, и бесцветную фильтровальную лепешку промывают 4 x в 100 мл 2-пропанола. Фильтровальную лепешку сушат в течение ночи при пониженном давлении.
Количество выделенной соли (S)-IOBA-(S)-1-фенилпропиламмония: 57,065 г (выход: 86,3%). Хиральный ЖХ анализ образца аммониевой соли показал, сто энантиообогащенная (S)-IOBA имеет энантиомерный избыток 95% без дальнейшей кристаллизации.
Стадия рециркулирования:
Собранный супернатант и промывочные растворы со стадии кристаллизации концентрируют до 400 мл. Энантиообогащенный (R)-IOBA раствор загружают с порошковым гидроксидом калия (27,916 г, 498 ммоль) и нагревают до кипения с обратным холодильником при перемешивании. Образцы берут из реакционной смеси и анализируют хиральной ЖХ для определения энантиомерного избытка (R)-IOBA. Нагревание останавливают, когда остаточный энантиомерный избыток (R)-IOBA достигает 2,4%.
Растворитель выпаривают, оставшуюся IOBA-соль загружают 300 мл воды. Раствор конц. H2SO4 (13,3 мл) в 65 мл воды добавляют при перемешивании. Водную суспензию доводят до pH=2 дополнительным объемом конц. H2SO4 (3,8 мл) в 18,5 мл воды. Водную суспензию последовательно экстрагируют 1×200 мл и 2×100 мл этилацетата. Собранные органические фазы промывают 2 x насыщенным раствором соли (100 мл) и сушат над MgSO4. После фильтрации, органический растворитель выпаривают с получением рециркулированной IOBA в виде твердого продукта. Количество IOBA после сушки: 53 г, содержащие 7% масс. этилацетата.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ДЛЯ ПОЛУЧЕНИЯ (5S)-4-[5-(3,5-ДИХЛОРФЕНИЛ)-5-(ТРИФТОРМЕТИЛ)-4H-ИЗОКСАЗОЛ-3-ИЛ]-2-МЕТИЛ-БЕНЗОЙНОЙ КИСЛОТЫ | 2019 |
|
RU2809762C2 |
| СПОСОБ ПОЛУЧЕНИЯ (5S)-4-[5-(3,5-ДИХЛОРФЕНИЛ)-5-(ТРИФТОРМЕТИЛ)-4H-ИЗОКСАЗОЛ-3-ИЛ]-2-МЕТИЛБЕНЗОЙНОЙ КИСЛОТЫ | 2019 |
|
RU2786390C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-[(3R)-3-МЕТИЛМОРФОЛИН-4-ИЛ]-4-(1-МЕТИЛ-1H-ПИРАЗОЛ-5-ИЛ)-8-(1H-ПИРАЗОЛ-5-ИЛ)-1,7-НАФТИРИДИНА | 2019 |
|
RU2802512C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 5-ГАЛОГЕНАЛКИЛ-4,5-ДИГИДРОИЗОКСАЗОЛА | 2008 |
|
RU2536039C2 |
| 5-ГИДРОКСИ-4-(ТРИФТОРМЕТИЛ)ПИРАЗОЛОПИРИДИНОВОЕ ПРОИЗВОДНОЕ | 2014 |
|
RU2673810C1 |
| СПОСОБ ПОЛУЧЕНИЯ 5-ГИДРОКСИАЛКИЛЗАМЕЩЕННЫХ ПРОИЗВОДНЫХ 1-ФЕНИЛ-1,2,4-ТРИАЗОЛА | 2017 |
|
RU2742885C2 |
| ПРОИЗВОДНЫЕ ИЗОКСАЗОЛА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1997 |
|
RU2165415C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ГЕТЕРОЦИКЛОМ ПРОИЗВОДНЫХ ПИРИДИНА | 2008 |
|
RU2474581C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ИНГИБИРУЮЩАЯ 5-ЛИПОКСИГЕНАЗУ, 4-(4-ФЕНИЛ-1-ПИПЕРАЗИНИЛ) ФЕНИЛПРОИЗВОДНОЕ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1989 |
|
RU2107064C1 |
| ПИРАЗОЛОПИРИМИДИНОВЫЕ СОЕДИНЕНИЯ-ИНГИБИТОРЫ JAK И СПОСОБЫ | 2009 |
|
RU2539568C2 |
Настоящее изобретение относится к способу рацемизации (5R)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойной кислоты, являющейся промежуточным соединением для синтеза инсектицида флураланера. Способ рацемизации смеси, содержащей энантиомерный избыток (5R)- и недостаток (5S)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойной кислоты, включает взаимодействие (5RS)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойной кислоты с амином в органическом растворителе, выбранном из группы, состоящей из спирта с 2-5 атомами углерода, тетрагидрофурана, диоксана, толуола, этилацетата и их смесей с получением осадка и раствора супернатанта, разделение раствора супернатанта, содержащего смесь, содержащую (5R)- и (5S)- производные метилбензойной кислоты из осадка и взаимодействие смеси со щелочным соединением в спирте с 2-8 атомами углерода с получением прореагировавшей смеси. Техническим результатом изобретения является предоставление способа рацемизации для дальнейшего выделения энантиочистой или энантиообогащенной (5S)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойной кислоты для получения предпочтительного (S)-флураланера. 10 з.п. ф-лы, 6 пр.
1. Способ рацемизации смеси, содержащей (5R)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойную кислоту формулы (1a) и (5S)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойную кислоту формулы (1b)
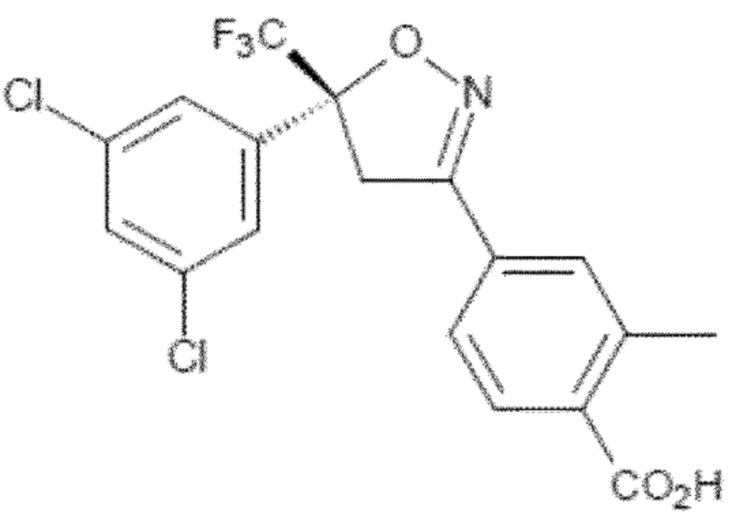
Формула (1a) и
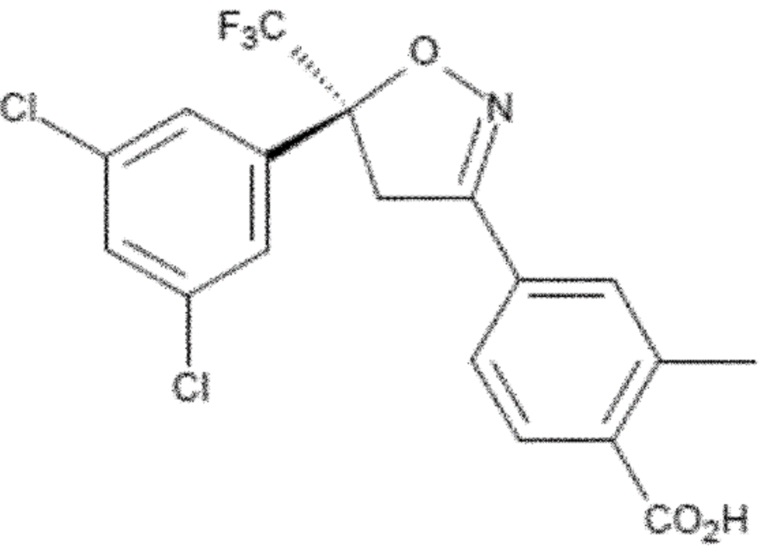
Формула (1b),
где смесь имеет энантиомерный избыток соединения формулы (1a), включающий стадии:
(a) взаимодействия (5RS)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойной кислоты с соединением формулы (2A), (2B) или (2C)

Формула (2A)
где R является алкилом с 1 или 2 атомами углерода,

Формула (2B), или

Формула (2C),
где X является Cl или Br,
в органическом растворителе, выбранном из группы, состоящей из спирта с 2-5 атомами углерода, тетрагидрофурана, диоксана, толуола, этилацетата и их смесей с получением осадка и раствора супернатанта, и
(b) разделения раствора супернатанта, содержащего смесь, содержащую (5R)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойную кислоту формулы (1a) и (5S)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метилбензойную кислоту формулы (1b) из осадка, и
(с) взаимодействия смеси со щелочным соединением в органическом растворителе с получением прореагировавшей смеси,
где органический растворитель представляет собой спирт с 2-8 атомами углерода, имеющий полярность ET(30) от 180 до 230 кДж/моль.
2. Способ по п. 1, где щелочным соединением является неорганическое соединение.
3. Способ по п. 1 или 2, где щелочное соединение выбирают из группы, состоящей из гидроксида натрия, гидроксида калия, гидроксида цезия, гидроксида кальция, гидроксида бария, оксида магния, оксида кальция, оксида бария, карбоната цезия и их смесей.
4. Способ по любому из пп. 1-3, дополнительно включающий стадии:
(ii) подкисления прореагировавшей смеси со стадии (i), с получением полученной смеси, и
(iii) разделения полученной смеси со стадии (ii) в смеси соединения и супернатанта.
5. Способ по любому из пп. 1-4, где стадию (i) проводят в отсутствие катализаторов фазового переноса.
6. Способ по п. 1, где на стадии (a) растворитель выбирают из группы, состоящей из спирта с 2-5 атомами, диоксана, тетрагидрофурана и их смесей.
7. Способ по п. 1, где на стадии (a) растворителем является 2-пропанол.
8. Способ по п. 1, где на стадии (a) R из Формулы (2A) является метил и растворителем является 2-пропанол или R из Формулы (2A) является этилом и растворителем является 2-пропанол.
9. Способ по п. 1, где стадия (a) включает нагревание (5RS)-4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]2-метилбензойной кислоты с соединением формулы (2A), (2b) или (2C) в растворителе до повышенной температуры.
10. Способ по п. 1, где на стадии (b) отделение раствора супернатанта со стадии (a) от осадка проводят фильтрацией.
11. Способ по п. 1, где органический растворитель на стадии (a) и (с) является одним и тем же.
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| JP 2011051977 A, 17.03.2011 | |||
| Потапов В.М | |||
| Стереохимия, Москва, Химия, 1976, с | |||
| Способ получения борнеола из пихтового или т.п. масел | 1921 |
|
SU114A1 |
Авторы
Даты
2023-10-23—Публикация
2019-12-20—Подача