Изобретение относится к области применения биологически активных соединений класса N-арил-3-метил-5-оксо-5Н-индено[1,2-c]пиридазин-4-карбоксамидов, а именно 3-метил-5-оксо-N-фенил-5Н-индено[1,2-c]пиридазин-4-карбоксамиду формулы (I):
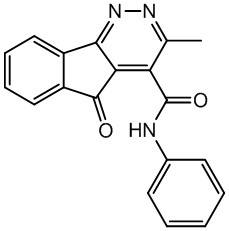
I
обладающего противовоспалительной активностью, что позволяет предложить его использование в фармакологии и медицине в качестве противовоспалительного лекарственного средства.
Способ синтеза N-арил-3-метил-5-оксо-5Н-индено[1,2-c]пиридазин-4-карбоксамидов известен из уровня техники [An eco-friendly stereoselective synthesis of novel derivatives of indeno[1,2-b]pyrrole and indeno[1,2-c]pyridazine/ Vladimir L.Gein, Natalia V. Nosova, Andrei N. Yankin, Alina Y. Bazhina, Maksim V. Dmitriev// Polycyclic Aromatic Compounds. - 2021. - V. 41.- P. 540-552].
Противовоспалительная активность N-арил-3-метил-5-оксо-5Н-индено[1,2-c]пиридазин-4-карбоксамидов ранее не была исследована.
Задачей изобретения является поиск среди производных индено[1,2-c]пиридазин-4-карбоксамидов соединения, проявляющего высокую противовоспалительную активность при низкой токсичности.
Поставленная задача решается получением соединения 3-метил-5-оксо-N-фенил-5Н-индено[1,2-c]пиридазин-4-карбоксамида (I), проявляющего высокую противовоспалительную активность и обладающего низкой токсичностью.
Синтезируют заявляемое соединение (I) взаимодействием 3a,8b-дигидрокси-3-(1-гидроксиэтилиден)-1-фенил-1,3,3а,8b-тетрагидроиндено[1,2-b]пиррол-2,4-диона (II) с гидразингидратом путем кипячения реагентов в этиловом спирте в отсутствии катализатора по схеме:
Схема 1
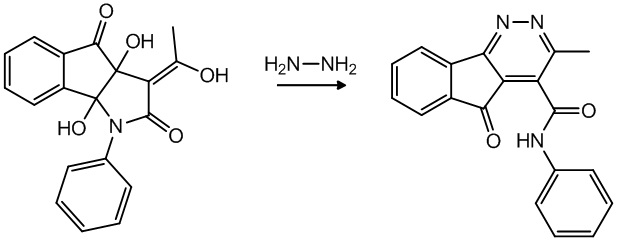
I II
Синтез исходного 3a,8b-дигидрокси-3-(1-гидроксиэтилиден)-1-фенил-1,3,3а,8b-тетрагидроиндено[1,2-b]пиррол-2,4-диона (II) осуществлен по ранее описанной методике [An eco-friendly stereoselective synthesis of novel derivatives of indeno[1,2-b]pyrrole and indeno[1,2-c]pyridazine/ Vladimir L. Gein, Natalia V. Nosova, Andrei N. Yankin, Alina Y. Bazhina, Maksim V. Dmitriev // Polycyclic Aromatic Compounds. - 2021. - V. 41. - P. 540-552].
Изобретение иллюстрируется следующими примерами.
Пример 1. Получение заявляемого соединения (I).
К раствору 1г (0,003 моль) 3a,8b-дигидрокси-3-(1-гидроксиэтилиден)-1-фенил-1,3,3а,8b-тетрагидроиндено[1,2-b]пиррол-2,4-диона (II) в 20 мл этилового спирта добавляли 0,0033 моль (10% избыток) гидразингидрата. Реакционную смесь кипятили в течение 15 минут, затем охлаждали, выпавшие кристаллы отфильтровывали и перекристаллизовывали из этилового спирта. Выход 73% (0,7 г), т. пл. 273-274°С (этанол).
Заявляемое соединение (I) представляет собой желтое кристаллическое вещество, растворимое в диметилсульфоксиде (ДМСО), диметилформамиде (ДМФА), при нагревании - в этиловом и изопропиловом спиртах, ацетоне, нерастворимое в воде, устойчивое при хранении.
ИК спектр (Specord M-80 в таблетках KBr), ν, см-1: 3277 (NH), 1728 (CO), 1654 (CON). Спектр ЯМР 1Н (Bruker AVANCE III HD 400 (400 и 100 МГц соответственно) в ДМСО-d6, внутренний стандарт - ТМС), δ, м. д.: 2.73 c (3H, CH3), 7.20 т (1Н, ArH, J 7.4 Гц), 7.42 т (2Н, ArH, J 7.9 Гц), 7.67 д (2Н, ArH, J 7.4 Гц), 7.71 д (1Н, ArH, J 7.5 Гц), 7.83-7.92 м (2Н, ArH), 8.16 д (1Н, ArH, J 7.5 Гц), 10.66 c (1H, NH). Найдено, %: C 72.18; H 4.30; N 13.42. C19H13N3O2. Вычислено, %: C 72.31; H 4.12; N 13.33.
Пример 2. Исследование острой токсичности и противовоспалительной активности заявляемого соединения (I).
Все исследовательские работы с лабораторными животными выполняли в соответствии с общепринятыми этическими нормами обращения с животными, принятыми Европейской конвенцией по защите позвоночных животных, используемых для исследовательских и иных научных целей [Европейская конвенция по защите позвоночных животных, используемых в экспериментальных и других научных целях, Страсбург 1986].
Острую токсичность изучали на 8 нелинейных белых мышах массой 21-24 г, используя экспресс-метод В.Б. Прозоровского [Прозоровский, В. Б. Экспресс-метод определения средней эффективной дозы и её ошибки / В. Б. Прозоровский, М. П. Прозоровская, В. И. Демченко // Фармакология и токсикология. - 1978. - № 4. - С. 497-502.]. Исследуемое соединение (I) вводили однократно внутрибрюшинно в 2% крахмальной слизи в дозах 500, 631, 794 и 1000 мг/кг. Затем в течение 14 дней вели наблюдение за животными, фиксируя интенсивность двигательной активности, реакции на тактильные, звуковые и световые раздражители, частоту и глубину дыхательных движений, состояние волосяного и кожного покрова, окраску видимых слизистых оболочек, потребление воды и пищи [Руководство по проведению доклинических исследований лекарственных средств / Под ред. А.Н. Миронова, Н.Д. Бунятян, А.Н. Васильева, О.Л. Верстаковой, М.В. Журавлевой, В.К. Лепахина, Н.В. Коробова, В.А. Меркулова, С.Н. Орехова, И.В. Сакаевой, Д.Б. Утешева, А.Н. Яворского. М.: Гриф и К, 2012. Ч. 1. 944 с.].
Установлено, что внутрибрюшинное введение животным исследуемых доз заявляемого соединения (I) не вызывало проявления клинических признаков его токсического действия, а также не приводило к гибели животных, следовательно, ЛД50 для заявляемого соединения (I) составляет более 1000 мг/кг. Согласно классификации токсичности веществ заявляемое соединение (I) относится к 5 классу токсичности и является практически нетоксичным соединением [Сидоров, К. К. Фармакология новых промышленных химических веществ. - 1973. - №13. - С.47 - 51.]. Полученные данные позволяют сделать вывод о преимуществе заявляемого соединения (I) по сравнению с препаратами сравнения - мелоксикамом и нимесулидом. Так, минимальная доза мелоксикама, которая может приводить к развитию токсических эффектов при внутрибрюшинном введении составляет 1,25 мг/кг [Safety Data Sheet acc. to OSHA HCS [Электронный ресурс]. - Режим доступа: https://cdn.caymanchem.com/cdn/msds/14906m.pdf], а средняя летальная доза нимесулида при внутрибрюшинном введении равна 163 мг/кг [Паспорт безопасности в соответствии с ГОСТ 30333-2007 [Электронный ресурс]. - Режим доступа: https://assets.lgcstandards.com/sysmaster%2Fpdfs%2Fh7c%2Fh14%2F10141283942430%2FSDS_MM0378.00_ST-WB-MSDS-2921057-1-1-1.PDF ].
Заявляемое соединение (I) исследовали на противовоспалительную активность. Эксперимент проводили на крысах-самцах массой 220-280 г. Острую воспалительную реакцию вызывали субплантарным введением 0,1 мл 1% раствора каррагенина в заднюю лапу животного [Руководство по проведению доклинических исследований лекарственных средств / Под ред. А.Н. Миронова, Н.Д. Бунятян, А.Н. Васильева, О.Л. Верстаковой, М.В. Журавлевой, В.К. Лепахина, Н.В. Коробова, В.А. Меркулова, С.Н. Орехова, И.В. Сакаевой, Д.Б. Утешева, А.Н. Яворского. М.: Гриф и К, 2012. Ч. 1. 944 с]. Объем стопы у крыс измеряли онкометрически до введения каррагенина (контроль), а затем через 3 и 5 часов после его введения. Исследуемое соединение (I) вводили внутрибрюшинно в виде взвеси в 2%-ой крахмальной слизи в дозе 50 мг/кг за 30 мин до введения флогогена. Контрольной группе животных вводили эквиобъемное количество 2% крахмальной слизи. В качестве препаратов сравнения использовали нимесулид и мелоксикам в дозах по 50 мг/кг каждый, вводимые внутрибрюшинно в 2% крахмальной слизи. Противовоспалительный эффект оценивали по показателю торможения отека, который выражали в процентах к показателям контрольной группы. Результаты исследований представлены в таблице 1.
В ходе проведенных исследований выявлено, что исследуемое вещество (I) уменьшало выраженность каррагенинового отека лапы крыс через 3 и 5 часов после индукции воспалительной реакции. Выраженность торможения воспалительной реакции через 3 и 5 часов исследуемым соединением (I) не отличалась от таковой препарата сравнения мелоксикама, но несколько уступала второму препарату сравнения - нимесулиду.
Противовоспалительная активность соединения (I)
Таким образом, заявляемое соединение 3-метил-5-оксо-N-фенил-5Н-индено[1,2-c]пиридазин-4-карбоксамид (I) при низкой токсичности по сравнению с препаратами сравнения проявляет высокую противовоспалительную активность.
Исследование выполнено при финансовой поддержке Пермского научно-образовательного центра «Рациональное недропользование», 2022 год.
Изобретение относится к области органической химии и фармацевтики, а именно к применению биологически активного соединения класса N-арил-3-метил-5-оксо-5Н-индено[1,2-c]пиридазин-4-карбоксамидов. Раскрыто применение 3-метил-5-оксо-N-фенил-5Н-индено[1,2-c]пиридазин-4-карбоксамида формулы (I) в качестве средства, обладающего противовоспалительной активностью. Изобретение обеспечивает эффективную противовоспалительную активность. 1 табл., 2 пр.
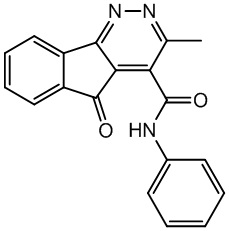 I
I
Применение 3-метил-5-оксо-N-фенил-5Н-индено[1,2-c]пиридазин-4-карбоксамида формулы (I)
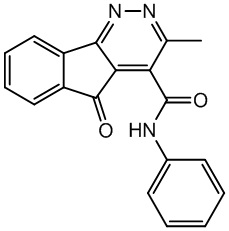
I
в качестве средства, обладающего противовоспалительной активностью.
| ПРОИЗВОДНЫЕ ПИРРОЛОПИРИДАЗИНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ПРОФИЛАКТИКИ ИЛИ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРА ФОСФОДИЭСТЕРАЗЫ IV, И/ИЛИ ПРОДУЦИРОВАНИЯ TNF | 2003 |
|
RU2328499C2 |
| Способ получения 2,3 @ -дигидрокси-3-бензоил-3 @ ,4-дигидро-1Н-пирроло[2,1-с][1,4]-бензоксазин-1,4-диона | 1990 |
|
SU1768603A1 |
| RU 2014123248 A, 20.12.2015 | |||
| VlLADIMIR L.GEIN | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Polycyclic Aromatic Compounds, 2021, vol | |||
| Механический грохот | 1922 |
|
SU41A1 |
| Гальванический элемент | 1922 |
|
SU540A1 |
Авторы
Даты
2023-10-31—Публикация
2023-04-04—Подача