Изобретение относится к медицине и может быть использовано частности в онкологии и радиологии для прогнозирования развития ранних лучевых повреждений кожи после лучевой терапии у пациентов с раком молочной железы на линейном ускорителе в режиме классического фракционирования с использованием фотонного излучения, обеспечивающее проведение персонализированной терапевтической программы для оптимизации планов лучевой терапии и может быть использовано в лечебных учреждениях.
Актуальность предлагаемого способа определяется прогнозированием возникновения тяжелых ранних лучевых повреждений кожи после проведения адъювантной лучевой терапии, сопровождающиеся длительным лечением, финансовыми затратами на лечение, необходимостью реабилитации. На сегодняшний день широкое использование лучевой терапии в современной медицине является одним из важнейших, а зачастую и единственным, методом лечения. Традиционно стандартной схемой ЛТ является ежедневное подведение разовой очаговой дозы 2 Гр ежедневными фракциями до СОД 50 Гр. Биологическое воздействие лучевой терапии на человека зависит не только от физических свойств и поглощенной дозы радиации, но и от индивидуальной восприимчивости организма. Известно, что доза и мощность лучевой терапии, наряду с многими факторами определяют степень повреждения кожи и тканей. Повреждаются не только кожа, но и подкожно-жировая клетчатка, мышцы, кости, сосудисто-нервные пучки и внутренние органы. Они могут возникать как в раннем постлучевом периоде - в течение первых 3-х месяцев после проведенного лечения, так и в более поздние сроки. Характер и степень поражения нормальных тканей зависят от индивидуальной радиочувствительности, возраста и сопутствующей патологии пациента, энергии излучения источника ионизирующего и методики проведения лучевой терапии. Ранние лучевые повреждения характеризуются развитием первичной эритемы (в первые несколько суток после облучения), сменяющейся после латентного периода сухим, влажным (буллезным) или язвенно-некротическим дерматитом в зависимости от поглощенной дозы облучения. При достижении суммарной поглощенной дозы предельно толерантной для здоровых тканей, происходит увеличение частоты развития поздних лучевых осложнений. Они проявляются через 4-6 месяцев после облучения и в большинстве случаев их развитие никак не связано с наличием и тяжестью ранних осложнений. Исследование пациенток с раком молочной железы выявило 81-90% повреждений нормальных тканей, вызванных лучевой терапией, обусловленных индивидуальными характеристиками пациента [Safwat, A.; Bentzen, S.M.; Turesson, I.; Hendry, J.H. Deterministic rather than sto-chastic factors explain most of the variation in the expression of skin telangiectasia after radiotherapy. Int. J. Radiat. Oncol. 2002, 52, 198-204]. Пациенты, получающие курс лучевой терапии (объем и суммарная очаговая доза) согласно стандартным протоколам имеют заметные различия в характере и степени выраженности лучевых повреждений. Как правило, поздние лучевые осложнения не разрешаются самостоятельно, а лечение пациентов с повреждениями кожи представляет особую проблему для клиницистов.
Таким образом, прогнозирование возникновения тяжелых лучевых повреждений кожи у пациентов с раком молочной железы после проведения адъювантной дистанционной лучевой терапии, сопровождающиеся длительным лечением, с финансовыми затратами на лечение является важным для совершенствования системы оказания медицинской помощи и актуальным в современной медицине.
Известных способов прогнозирования развития ранних лучевых повреждений кожи у пациентов с раком молочной железы после адьюватной дистанционной лучевой без полихимиотерапии терапии немного. Учитывая, что наиболее радиочувствительными клетками в организме человека являются лимфоциты, то для оценки развития лучевых повреждений было предложено несколько способов.
Известен способ определения индивидуальной радиочувствительности больных раком молочной железы при помощи хромосомного анализа облученных in vitro лимфоцитов. Способ включает в себя:
- забор крови из локтевой вены (4 мл),
- модельное рентгеновское облучение крови доноров в дозе 6 Гр,
- культивирование цельной крови (0,5 мл) в питательной среде (RPMI-1640) с добавлением фитогемагглютинина (ФГА),
- фиксация синхронизированной клеточной культуры на 52-часу,
- раскапывание клеточной суспензии на предметные стекла,
- приготовление и окраска (раствор 5% красителя Гимза) препаратов,
- анализ хромосомных аберраций под световым микроскопом.
Для оценки структурных повреждений хромосом фиксируют дицентрические хромосомы и ацентрические фрагменты. Регистрацию хромосомных аберраций проводят в среднем на 100 метафазных пластинках. Такой учет позволяет выявить средний уровень аберраций на клетку. Превышение определенного порового значения средней частоты аберраций на клетку (в указанном способе порог составляет 6,18 аберраций на клетку) является критерием отнесения донора (больной раком молочной железы) к группе радиочувствительных пациентов. По количеству наблюдений, числу проведенных исследований проведенная работа является очень существенной, однако имеет ряд недостатков. Осуществление данного способа является длительным и сложным процессом, требует облученние лимфоцитов in vitro на установках отличных от используемых в клинической практике, их стимуляции и культивирования в лабораторных условиях для получения достаточного количества метафазных пластинок и интерпретации результатов. Также в данном исследовании не было учтено применение системной полихимиотерапии, которое может оказывать негативное влияние на предложенный метод прогноза. Безусловно, это ограничивает повсеместное применение данного метода в клинической практике.
Наиболее близким по технической сущности к предлагаемому способу является способ оценки индивидуальной радиочувствительности больных злокачественными новообразованиями при проведении лучевой терапии путем исследования лимфоцитов венозной крови пациента, до применения лучевого воздействия на организм больного. Способ заключался в заборе периферической крови у больных до применения лучевого воздействия, выделения мононуклеарной фракции в градиенте Фиколл-Верографин, фиксации мононуклеарных клеток предметных стеклах с помощью раствора параформальдегида, иммунофлуоресцентном окрашивании фосфорилированной формы белка γН2АХ в ядрах клеток в лимфоцитах венозной крови, определении среднего уровеня флуоресцентных фокусов гистона γН2АХ. За пороговое значении принимают 1,0 фокус на клетку. Уровень выше порогового является показанием для отнесения больного к радиочувствительной группе. Анализ числа фокусов белка γН2АХ в ядрах клеток производили с помощью флуоресцентного микроскопа вручную или с помощью специализированного программного обеспечения, анализу подвергались минимум 150 клеток с одного препарата для каждого больного.
Представленный способ был основан на анализе всего 9 пациентов с различными онкологическими заболеваниями, у которых проводилось наблюдение за радиочувствительностью лимфоцитов периферической крови в ходе курса нейтронной терапии. В описании способа нет данных о предшествующей терапии пациентов, что может оказать существенное влияние на результаты исследования, так как фоновый уровень повреждений ДНК в клетках человека характеризуется значительной вариабельностью и определяется уровнем мутагенной нагрузки, которой подвергаются клетки человека. Учитывая, что рак молочной железы является генетически разнородным заболеванием с множеством форм клинического течения, в основе его лечения лежит комплексный подход с применением хирургических, иммунологических, гормональных и химиотерапевтических и радиационных методов лечения. Это требует дифференцированного подхода к каждой группе больных, в том числе и при проведении генетических исследований. Также представленный метод требует наличие в клиническом штате узкоспециализированных сотрудников для интерпретации полученных результатов.
Техническим результатом предлагаемого способа прогнозирования развития лучевых повреждений кожи после лучевой терапии у пациентов с раком молочной железы является обеспечение возможности проведения персонализированной терапевтической программы для оптимизации планов лучевой терапии.
Указанный технический результат достигается, тем, что у пациенток с раком молочной железы до адъювантой дистанционной лучевой терапии проводят забор периферической крови для иммуннофенотипирования лимфоцитов, определяют основные показатели лимфоцитов в периферической крови методом проточной цитометрии, определяют иммунорегуляторный индекс и при его значениях выше 2,5, выделяют прогностически неблагоприятную группу пациенток с раком молочной железы без предшествующей системной полихимиотерапии по развитию лучевых повреждений кожи II-III степени на адъювантую дистанционную лучевую терапию в СОД 50 Гр.
Описание предлагаемого способа
У пациентов с раком молочной железы до проведения курса АДЛТ проводят забор периферической крови в объеме 3 мл для определения относительного и абсолютного количества основных популяций лимфоцитов методом проточной цитофлюориметрии (BD FACS Canto II, USA) с последующим расчетом иммунорегуляторного индекса. Для исследования фенотипа лимфоцитов использовались моноклональные антитела к следующим антигенным маркерам: CD45, CD3, CD4, CD8, CD56, CD 19 (BD Bioscience, USA). Окрашивание проводили в соответствии с рекомендациями производителя. При уровне иммунорегуляторного индекса более 2,5, пациента относили к группе риска развития острых лучевых повреждений со стороны кожных покровов II-III степени. Способ поясняется подробным описанием результатов исследования, проведенных, клиническим примером и иллюстрациями.
Особенность заявляемого способа заключается в том, что получение результатов по оценке клеточного иммунитета удается получить в день взятия периферической крови, метод полностью стандартизирован, проводится на сертифицированном оборудовании с использованием автоматических программ обсчета результатов.
Способ поясняется подробным описанием результатов клинического исследования, клиническим примером и иллюстрациями.
Исследование проведено с участием 33 пациентов с первичным гистологически верифицированным раком молочной железы 0-11 стадии. Критериями исключения являлись конкурентная химиолучевая терапии, наличие злокачественных новообразований иной локализации, проведение системной полихимиотерапии, отказ от участия в протоколе.
На первом этапе лечения всем пациенткам выполняли радикальное хирургическое вмешательство, на заключительном - адъювантная дистанционная лучевая терапия выполнялось на линейном ускорителе VARIAN TRILOGI в режиме классического фракционирования с использованием фотонного излучения, МЛК, системы портальной визуализации, индивидуальных фиксирующих устройств методом многопольной статики (VIMAT) с РОД 2Гр, до СОД 50Гр. на область послеоперационного рубца молочной железы и зон регионарного лимфооттока.
На фоне проведения лучевой терапии оценивали появление ранних лучевых повреждений кожи на проведенное лечение.
Степень ранних лучевых повреждений кожи у больных, включенных в исследование, определяли согласно международной шкале исследовательской группы по лучевой терапии RTOG/EORTC после проведения завершения курса лучевой терапии. Ранние лучевые повреждения кожи классифицировались следующим образом:
0-степень - нет клинических проявлений;
I степень - легкая эритема, сухой дерматит, эпиляция;
II степень - выраженная эритема, очаговый влажный дерматит, умеренный отек;
III степень - сливной влажный дерматит, выраженный отек;
IV степень - лучевая язва, некроз.
Для оценки динамики показателей клеточного иммунитета у всех больных после подписания информированного согласия проводили забор венозной крови до проведения адъювантной дистанционной лучевой терапии и после завершения курса лучевой терапии.
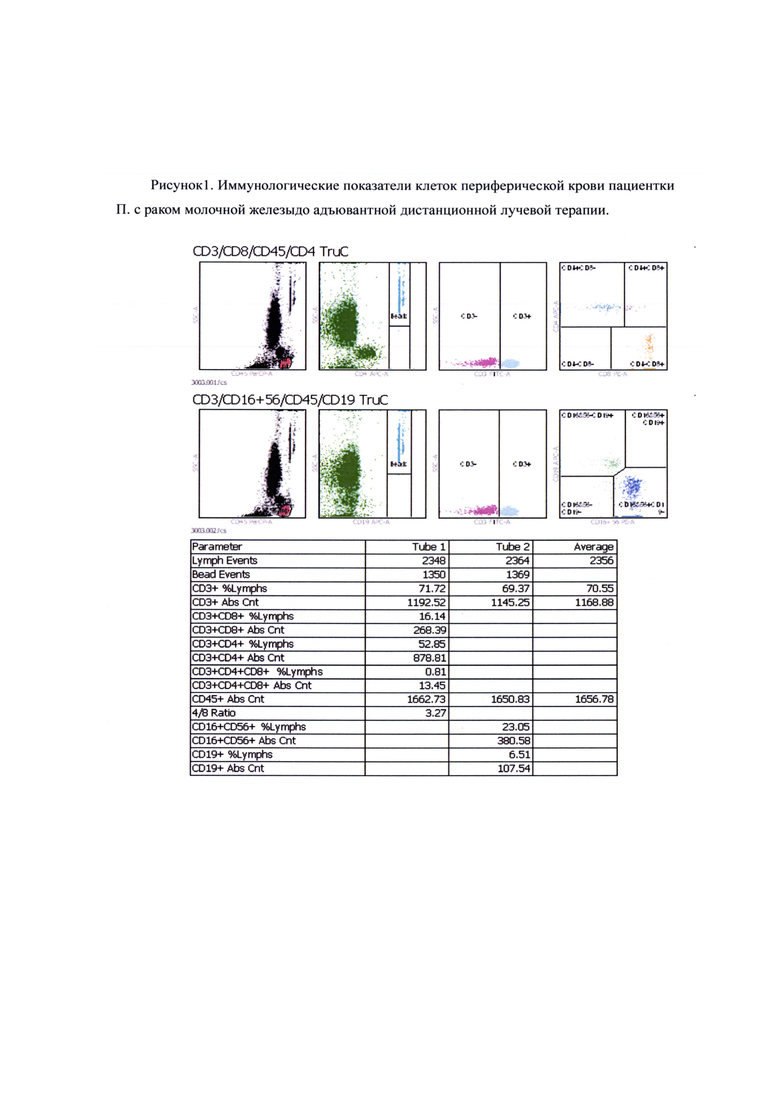
Исследование показателей клеточного иммунитета проводили на проточном цитофлюориметре (BD FACS Canto II) одноплатформенным методом с помощью коммерческого набора моноклональньгх антител (Multitest IMK kit с пробирками BD Trucount). Анализ полученных результатов осуществляли с помощью программного обеспечения BD FACS Diva 6.0. (Рисунок 1).
Статистическую обработку данных проводили с помощью программы Statistica 6.0. Данные между группами сравнивали двусторонним критерием Фишера. Средние значения показателей иммунного статуса и качества жизни представляли как Mean ± SEM и сравнивали непарным t-критерием Стьюдента, для анализа динамики показателей использовали парный t-критерий. При сравнении более двух групп использовали ANOVA, для поправки на множественные сравнения использовали критерий Тьюки. Для оценки риска получения высокой степени лучевых повреждений кожи рассчитывали отношение шансов и представляли как OR [95% CI]. Для всех критериев различия считали достоверными при достижении р<0,05.
В послелучевом периоде у всех пациенток было зафиксировано развитие лучевых повреждений кожи.
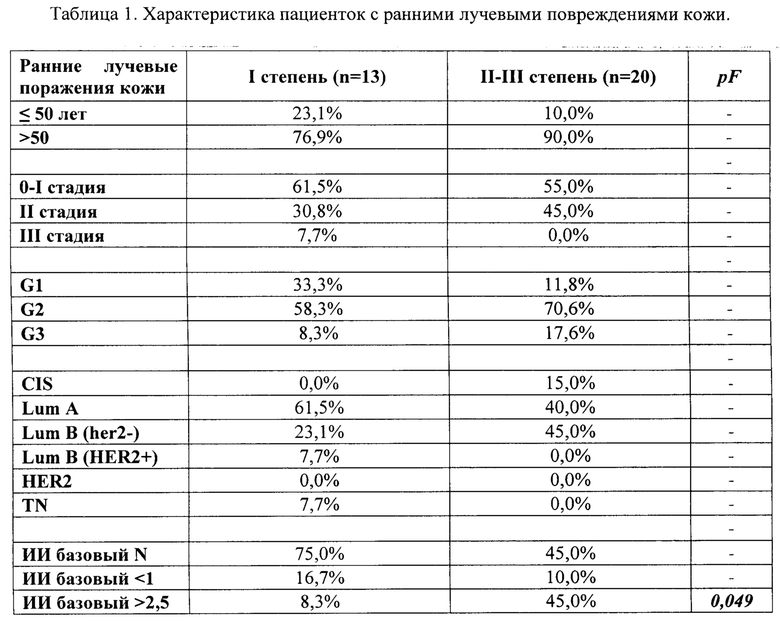
В зависимости от степени ранних лучевых повреждений кожи все пациентки были разделены на две группы. Характеристика пациенток, включенных в исследование, представлена в таблице 1.
Был проведен анализ зависимости развития ранних лучевых повреждений кожи от возраста пациенток, стадии злокачественного процесса, степени дифференцировки опухолевых клеток, базового иммунорегуляторного индекса.
Исходя из полученных данных, были получены следующие результаты: для пациенток с раком молочной железы, которым адъювантная дистанционная лучевая терапия проводилась после радикального хирургического лечения. (Таблица 1) для группы пациенток после радикального хирургического лечения без предшествующей полихимиотерапии при исследовании зависимости развития ранних лучевых повреждений кожи от иммунорегуляторного индекса зафиксировано статистически значимое повышение (более чем в 5 раз) случаев с повышенным базовым иммунорегуляторным индексом (более 2,5) среди пациентов, получивших в результате адъювантной дистанционной лучевой терапии лучевые повреждения кожных покровов II-III степени (45%) по сравнению с I степенью (8,3%; pF=0,049).
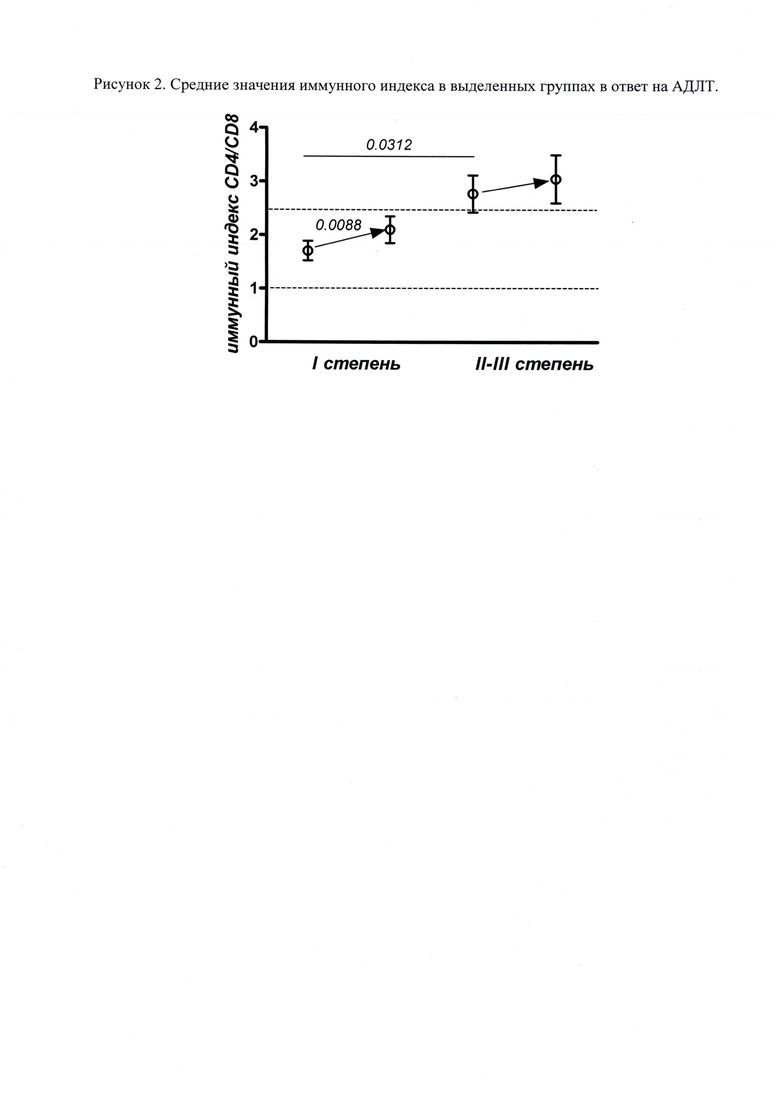
Если рассматривать базовый иммунорегуляторный индекс (до начала проведения адъювантной дистанционной лучевой терапии) как фактора риска получения высокой степени ранних лучевых повреждений кожи, то в исследованной выборке пациенты, имеющие иммунорегуляторный индекс >2,5 (превышающий референсные значения) и не прошедшие полихимиотерапию до адъювантной дистанционной лучевой терапии, имеют достоверно больший шанс в ходе адъювантной дистанционной лучевой терапии получить ранние лучевые повреждения кожи II-III степени (OR=4,99; 95% CI [1,58; 15,75], р<0,05) (Рисунок 2).
Таким образом, полученные данные позволяют рассматривать пациентов с раком молочной железы и с базовым иммуннорегуляторным индексом более 2,5, как группу риска по развитию более тяжелых ранних лучевых повреждений кожи.
Предлагаемый способ основан на анализе результатов клинических наблюдений за 33 пациенток с раком молочной железы.
Пример осуществления способа
Пациентка Л. 45 лет, больна с октября 2021 года, когда был установлен диагноз: Рак левой молочной железы pT1cpN0M0 R0 Gl IAstage. В октябре 2021 г. на УЗИ молочных желез выявлено образование левой молочной железы (в нижне-внутреннем квадранте размерами 1.7x1.5 см) с реактивными изменениями подмышечных лимфоузлов (на границе грудной мышцы л/узел размерами 1.7x0.8 см, в подмышечной области л/узел размерами 1.5x0.3 см). Оперативное лечение проведено 15.11.21 г.: радикальная мастэктомия по Маддену слева. Базовый мммунорегуляторный индекс до лучевой терапии составлял 3,25 (Рисунок 1). На заключительном этапе лечения проведена адъювантная дистанционная лучевая терапия в мае - июне 2022 г. в СОД 50 Гр. Ранние лучевые поражении кожи II-III степени тяжести (Рисунок 3).
Таким образом, клинические данные показали, что в предлагаемом способе прогнозирования развития ранних лучевых повреждений кожи после лучевой терапии у пациентов с раком молочной железы без предшествующей полихимиотерапии является обеспечение возможности проведения персонализированной терапевтической программы для оптимизации планов лучевой терапии.
Предложенный способ прогнозирования развития лучевых повреждений кожи после лучевой терапии у пациентов с раком молочной железы без предшествующей полихимиотерапии проведен на 33 пациенток с раком молочной железы. В результате прогнозирования развития лучевых повреждений кожи после лучевой терапии у пациентов с раком молочной железы без предшествующей полихимиотерапии при базовом иммуннорегуляторном индексе более 2,5 выявлены лучевые повреждения кожи II-III степени, что в последующем обеспечит возможность проведения персонализированной терапевтической программы для оптимизации планов лучевой терапии.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОВЫШЕНИЯ ЭФФЕКТИВНОСТИ КОМПЛЕКСНОЙ ТЕРАПИИ ПРИ МЕСТНЫХ ЛУЧЕВЫХ ПОРАЖЕНИЯХ | 2019 |
|
RU2744519C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ИНДИВИДУАЛЬНОЙ РАДИОЧУВСТВИТЕЛЬНОСТИ БОЛЬНЫХ ЗЛОКАЧЕСТВЕННЫМИ НОВООБРАЗОВАНИЯМИ ПРИ ПРОВЕДЕНИИ ЛУЧЕВОЙ ТЕРАПИИ | 2012 |
|
RU2522507C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПОКАЗАНИЙ К ПРОВЕДЕНИЮ ЛУЧЕВОЙ И ХИМИОТЕРАПИИ | 2010 |
|
RU2436497C1 |
| СПОСОБ ЛЕЧЕНИЯ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ | 2000 |
|
RU2178294C2 |
| СПОСОБ ЛЕЧЕНИЯ МЕСТНО-РАСПРОСТРАНЕННОГО ОРОФАРИНГЕАЛЬНОГО РАКА | 2009 |
|
RU2401139C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЧУВСТВИТЕЛЬНОСТИ ОПУХОЛИ К ЛУЧЕВОЙ ТЕРАПИИ У БОЛЬНЫХ РАКОМ ПРЯМОЙ КИШКИ | 2007 |
|
RU2349916C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАДИОРЕЗИСТЕНТНОГО РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ | 1998 |
|
RU2140086C1 |
| СПОСОБ ЛЕЧЕНИЯ ЛУЧЕВЫХ ПОВРЕЖДЕНИЙ ЛЕГКИХ | 2011 |
|
RU2487706C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РЕЦИДИВА РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ | 2003 |
|
RU2263319C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЭФФЕКТИВНОСТИ НЕОАДЪЮВАНТНОЙ ХИМИОТЕРАПИИ БОЛЬНЫХ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ | 2011 |
|
RU2469651C2 |

Изобретение относится к медицине и может быть использовано в частности в онкологии и радиологии для прогнозирования развития лучевых повреждений кожи после лучевой терапии у пациентов с раком молочной железы без предшествующей полихимиотерапии. Способ включает забор периферической крови для иммуннофенотипирования лимфоцитов у пациентки до адъювантной дистанционной лучевой терапии, затем определяют иммунорегуляторный индекс. При его значениях выше 2,5 выделяют прогностически неблагоприятную группу пациенток с раком молочной железы без предшествующей системной полихимиотерапии по развитию ранних лучевых повреждений кожи II-III степени на адъювантную дистанционную лучевую терапию в СОД 50 Гр. Изобретение обеспечивает проведение персонализированной терапевтической программы для оптимизации планов лучевой терапии и может быть использовано в лечебных учреждениях. 3 ил., 1 табл., 1 пр.
Способ прогнозирования развития лучевых повреждений кожи после лучевой терапии у пациентов с раком молочной железы, включающий определение лимфоцитов в периферической крови методом проточной цитометрии до лучевой терапии, отличающийся тем, что у пациентки до адъювантной дистанционной лучевой терапии проводят забор периферической крови для иммуннофенотипирования лимфоцитов, определяют иммунорегуляторный индекс, и при его значениях выше 2,5 выделяют прогностически неблагоприятную группу пациенток с раком молочной железы без предшествующей системной полихимиотерапии по развитию ранних лучевых повреждений кожи II-III степени на адъювантную дистанционную лучевую терапию в СОД 50 Гр.
| Способ оценки состояния центральной нервной системы у пациенток с постмастэктомическим синдромом | 2021 |
|
RU2754059C1 |
| СПОСОБ ЛЕЧЕНИЯ ПОСТМАСТЭКТОМИЧЕСКОГО СИНДРОМА | 2018 |
|
RU2687599C1 |
| US 10534052 B2, 28.01.2016 | |||
| Манипулятор для координатографа | 1930 |
|
SU21459A1 |
| Маслюкова Е.А., Корытова Л.И., Одинцова С.В., Сергеев В.И., Бондаренко А.В | |||
| ОСЛОЖНЕНИЯ СОЧЕТАННОЙ ХИМИОЛУЧЕВОЙ ТЕРАПИИ ОТЕЧНОГО РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ // Современные проблемы науки и образования | |||
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Pavy JJ, Denekamp J, Letschert J, et | |||
Авторы
Даты
2023-11-24—Публикация
2022-12-26—Подача