РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка испрашивает приоритет на основании предварительной заявки на патент США № 62/697302, поданной 12 июля 2018 г., которая включена в настоящий документ полностью посредством ссылки.
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Настоящая заявка подана в электронном виде через систему EFS-Web и включает поданный в электронном виде перечень последовательностей в формате .txt. Указанный файл в формате .txt включает перечень последовательностей с названием «ROPA_011_01WO_SeqList_ST25.txt», созданный 11 июля 2019 года и имеющий размер ~62 килобайт. Перечень последовательностей, содержащийся в указанном файле .txt, входит в состав настоящего описания и включен в него полностью посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение в целом относится к генной терапии заболеваний, связанных с мутациями в ассоциированном с лизосомами мембранном белке 2 (LAMP-2, также известном как CD107b).
УРОВЕНЬ ТЕХНИКИ
LAMP-2 («lysosome-associated membrane protein 2», ассоциированный с лизосомами мембранный белок 2, также известный как CD107b) представляет собой ген, который кодирует ассоциированный с лизосомами мембранный гликопротеин. Альтернативный сплайсинг указанного гена дает три изоформы: LAMP-2A, LAMP-2B и LAMP-2C. Мутации с потерей функции в LAMP-2 ассоциированы с заболеваниями человека, в том числе болезнью Данона, наследственной кардиомиопатией, ассоциированной с нарушенной аутофагией.
В международной публикации заявки на патент № WO2017127565A1 раскрыто, что избыточная экспрессия LAMP-2 в индуцированных плюрипотентных стволовых клетках человека (чИПСК, hiPSC), происходящих от пациентов с мутациями LAMP-2, согласно описанию в Hashem, et al., Stem Cells. 2015 Jul; 33(7):2343-50, приводит к пониженным уровням окислительного стресса и апоптотической гибели клеток, что подтверждает важность LAMP-2B в патофизиологии заболевания.
В данной области техники сохраняется потребность в геннотерапевтических векторах для LAMP-2. Согласно настоящему изобретению предложены, в том числе, такие геннотерапевтические векторы, способы их применения, фармацевтические композиции.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Согласно настоящему изобретению предложены, в том числе, усовершенствованные геннотерапевтические векторы, содержащие полинуклеотидную последовательность, кодирующую полипептид LAMP-2, способы их применения, фармацевтические композиции.
Согласно одному аспекту настоящего изобретения предложен геннотерапевтический вектор, содержащий экспрессионную кассету, содержащую трансген, кодирующий изоформу ассоциированного с лизосомами мембранного белка 2 (LAMP-2) или ее функциональный вариант, причем указанный трансген кодон-оптимизирован для экспрессии в человеческой клетке-хозяине.
Согласно варианту реализации указанная экспрессионная кассета содержит меньше сайтов CpG, чем SEQ ID: 2.
Согласно варианту реализации указанная экспрессионная кассета содержит меньше скрытых сайтов сплайсинга, чем SEQ ID: 2.
Согласно варианту реализации указанная экспрессионная кассета кодирует меньше альтернативных открытых рамок считывания, чем SEQ ID: 2.
Согласно варианту реализации последовательность указанного трансгена обладает по меньшей мере 95% идентичностью с последовательности, выбранной из SEQ ID NO: 3–5.
Согласно варианту реализации последовательность указанного трансгена по меньшей мере на 99% идентична последовательности, выбранной из SEQ ID NO: 3–5.
Согласно варианту реализации указанный трансген содержит последовательность, выбранную из SEQ ID NO: 3–5.
Согласно варианту реализации последовательность указанного трансгена обладает по меньшей мере 95% идентичностью с SEQ ID NO: 3.
Согласно варианту реализации последовательность указанного трансгена по меньшей мере на 99% идентична SEQ ID NO: 3.
Согласно варианту реализации указанный трансген содержит последовательность, идентичную последовательности SEQ ID NO: 3.
Согласно варианту реализации указанная экспрессионная кассета содержит консенсусную оптимальную последовательность Козак, функционально связанную с трансгеном, причем необязательно указанная консенсусная оптимальная последовательность Козак содержит SEQ ID NO: 6.
Согласно варианту реализации указанная экспрессионная кассета содержит полноразмерную (поли)А-последовательность, функционально связанную с трансгеном, причем указанная полноразмерная (поли)А-последовательность необязательно содержит SEQ ID NO: 7.
Согласно варианту реализации указанная экспрессионная кассета не содержит в направлении 5′ от трансгена стартового сайта, способного давать альтернативные мРНК.
Согласно варианту реализации указанная экспрессионная кассета содержит в направлении от 5′- к 3′-концу функционально связанные: первый инвертированный концевой повтор, энхансерную/промоторную область, консенсусную оптимальную последовательность Козак, трансген, нетранслируемую 3′-область, включающую полноразмерную (поли)А-последовательность, и второй инвертированный концевой повтор.
Согласно варианту реализации указанная энхансерная/промоторная область содержит в направлении от 5′- к 3′-концу немедленно-ранний (CMV IE) энхансер цитомегаловируса и промотор бета-актина курицы.
Согласно варианту реализации последовательность указанной экспрессионной кассеты обладает по меньшей мере 95% идентичностью с последовательности, выбранной из SEQ ID NO: 8–10.
Согласно варианту реализации последовательность указанной экспрессионной кассеты полностью идентична последовательности, выбранной из SEQ ID NO: 8–10.
Согласно второму аспекту настоящего изобретения предложен способ предотвращения, смягчения, облегчения, уменьшения, ингибирования, устранения и/или обращения одного или более симптомов болезни Данона или другого аутофагического нарушения у нуждающегося в этом субъекта, включающий введение указанному субъекту любого геннотерапевтического вектора согласно настоящему описанию.
Согласно варианту реализации указанный вектор вводят путем, выбранным из группы, состоящей из внутривенного, внутриартериального, внутрисердечного, интракоронарного, интрамиокардиального, внутрипочечного, внутриуретрального, эпидурального и внутримышечного введения.
Согласно варианту реализации указанное аутофагическое нарушение выбрано из группы, состоящей из терминальной сердечной недостаточности, инфаркта миокарда, лекарственных токсичностей, диабета, терминальной почечной недостаточности и старения.
Согласно варианту реализации указанный субъект представляет собой человека.
Согласно варианту реализации у указанного субъекта наблюдаются симптомы болезни Данона или другого аутофагического нарушения.
Согласно варианту реализации указанный субъект был идентифицирован как имеющий пониженную или недетектируемую экспрессию LAMP-2.
Согласно варианту реализации указанный субъект был идентифицирован как имеющий мутированный ген LAMP-2.
Согласно третьему аспекту настоящего изобретения предложена фармацевтическая композиция для применения при предотвращении, смягчении, облегчении, уменьшении, ингибировании, устранения и/или обращении одного или более симптомов болезни Данона или другого аутофагического нарушения, содержащая любой геннотерапевтический вектор согласно настоящему описанию.
Другие признаки и преимущества настоящего изобретения будут очевидны из приведенных ниже подробного описания и формулы изобретения, и включены в них.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фиг. 1A приведена схема иллюстративного варианта реализации вирусного вектора согласно настоящему описанию.
На фиг. 1B приведена схема иллюстративного варианта реализации экспрессионной кассеты аденоассоциированного вирусного (AAV) геннотерапевтического вектора.
На фиг. 2 показана экспрессионная кассета репортерной системы с зеленым флуоресцентным белком (GFP) на основе плазмиды, используемая для тестирования и сравнения конструкций с LAMP-2B дикого типа или кодон-оптимизированного LAMP-2B.
На фиг. 3 приведен график, отражающий эффективность экспрессии конструкций LAMP-2B при трансфекции, протестированной с использованием трансфекции репортерной системой с GFP на основе плазмиды и измеренной как количество GFP+-клеток на лунку. Конструкцию LAMP-2B дикого типа (WT) сравнивают с тремя кодон-оптимизированными («CO») конструкциями, CO 1, CO 2 и CO 3, с контролем без вектора (обозначен как «только ViaFect»).
На фиг. 4 приведен график, отражающий уровень экспрессии гена в клетках, трансфицированных репортерными системами с GFP на основе плазмид, используемых для тестирования конструкций LAMP-2B, который измеряют как среднюю интенсивность флуоресценции GFP+-клеток в единицах поглощения (у.е.). Экспрессию GFP клетками, трансфицированными конструкцией с LAMP-2B дикого типа (WT), сравнивают с экспрессией GFP тремя кодон-оптимизированными («CO») конструкциями, CO 1, CO 2 и CO 3, или контролем без вектора (обозначен как «только ViaFect»).
На фиг. 5 приведены иммунофлуоресцентные изображения полученных из индуцированных плюрипотентных стволовых клеток (ИПСК) кардиомиоцитов через два дня после трансфекции репортерной системой с GFP на основе плазмиды. Клетки трансфицировали конструкциями без ДНК или конструкциями с LAMP-2B, экспрессирующими LAMP-2B дикого типа, вариант CO 1, вариант CO 2 или вариант CO 3.
На фиг. 6 приведены иммунофлуоресцентные изображения происходящих из ИПСК кардиомиоцитов через семь дней после трансфекции репортерной системой с GFP на основе плазмиды. Клетки, трансфицированные конструкциями без ДНК или конструкциями с LAMP-2B, экспрессирующими LAMP-2B дикого типа, вариант CO 1, вариант CO 2 или вариант CO 3.
На фиг. 7A показан иммуноблот белка LAMP-2B человека в клетках CHO-Lec2, трансдуцированных вирусными AAV9-векторами, содержащими трансген LAMP-2B дикого типа v1.0 (AAV9 1.0), трансген оптимизированного варианта LAMP-2B v1.2 (AAV9 1.2) или трансген GFP (AAV9 GFP). Также включали маркеры молекулярной массы (MW) и контрольный образец рекомбинантного белка LAMP-2B (LAMP2B (положительный контроль)).
На фиг. 7B показано количественное определение белка LAMP-2B с применением ИФА ELISA в клетках CHO-Lec2, трансдуцированных векторами AAV9 с LAMP-2B дикого типа (v1.0), AAV9 с оптимизированным LAMP-2B (v1.2) или AAV9–GFP (GFP).
На фиг. 8A приведены иммунофлуоресцентные изображения происходящих из ИПСК пациента с болезнью Данона кардиомиоцитов, трансдуцированных указанными количествами векторов AAV9–Luc (Luc), AAV9 с LAMP-2B дикого типа (LAMP2B v1.0) или AAV9 с оптимизированным LAMP-2B (LAMP2B v1.2).
На фиг. 8B показано количественное определение иммунофлуоресценции белка LAMP-2B человека в происходящих из ИПСК пациента с болезнью Данона кардиомиоцитах, трансдуцированных векторами AAV9–Luc, AAV9 с LAMP-2B дикого типа (v1.0) или AAV9 с оптимизированным LAMP-2B (v1.2).
На фиг. 8C приведен иммуноблот белка LAMP-2B человека в кардиомиоцитах, происходящих из ИПСК пациента с болезнью Данона, трансдуцированных векторами AAV9–Luc, AAV9 с LAMP-2B дикого типа (v1.0) или AAV9 с оптимизированным LAMP-2B (v1.2).
На фиг. 9A показано количественное определение с помощью ПЦР ДНК вирусного вектора в сердечной ткани, извлеченной из мышей с дефицитом LAMP-2, получавших лечение AAV9 с LAMP-2B дикого типа (v1.0), AAV9 с оптимизированным LAMP-2B (v1.2) или контрольным AAV9 – основой. Число копий вектора количественно определяли как VCN/диплоидное ядро в сердечной ткани. Контрольных мышей дикого типа, которым не инъецировали вектор, включали в качестве контроля (WT).
На фиг. 9B представлены количественные РВ-ПЦР-анализы на мРНК трансгена, которые проводили с помощью РВ-ПЦР с применением специфических зондов для элемента WPRE в сердечной ткани, извлеченной из мышей с дефицитом LAMP-2, получавших лечение AAV9 с LAMP-2B дикого типа (v1.0), AAV9 с оптимизированным LAMP-2B (v1.2) или контрольным AAV9 – основой (Основа). Экспрессию мРНК количественно определяли как число векторных геномов (вг) на мкг тотальной клеточной РНК, используя стандартную кривую для преобразования числа копий в число векторных геномов.
На фиг. 9C показан иммуноблот белка LAMP-2B в сердечной ткани, извлеченной из мышей с дефицитом LAMP-2, получавших лечение AA9-LAMP-2B дикого типа (v1.0), AAV9 с оптимизированным LAMP-2B (v1.2) или контрольным AAV9 – основой (Основа), или не получавших лечения мышей дикого типа (Без лечения).
На фиг. 9D приведены иммунофлуоресцентные изображения белка LAMP-2B человека в сердечной ткани, извлеченной из мышей с дефицитом LAMP-2, получавших лечение AAV9 с LAMP-2B дикого типа (v1.0), AAV9 с оптимизированным LAMP-2B (v1.2) или контрольным AAV9 – основой.
На фиг. 10A показано количественное определение с помощью ПЦР ДНК вирусного вектора в ткани сердца, мышц, печени и головного мозга, извлеченных из приматов, получавших лечение AAV9-вектором с оптимизированным LAMP-2B человека (Лечение) или контролем-основой без вектора (Без лечения). Индивидуумы обозначены черными или белыми квадратами.
На фиг. 10B показано количественное определение с помощью ПЦР ДНК вирусного вектора в камерах сердца, извлеченных из приматов, получавших лечение AAV9-вектором с оптимизированным LAMP-2B человека (Лечение) или контролем – основой без вектора (Без лечения). Индивидуумы обозначены как B059 (самец, M), A991 (самка, F) и A602 (самец, M).
На фиг. 10C представлены количественные РВ-ПЦР-анализы на трансгенную мРНК, которые проводили с помощью РВ-ПЦР с применением специфических зондов для элемента WPRE, в ткани сердца, мышц, печени и головного мозга, извлеченных из приматов, получавших лечение AAV9-вектором с оптимизированным LAMP-2B человека (Лечение) или контролем-основой без вектора (без лечения).
На фиг. 10D представлены количественные РВ-ПЦР-анализы на трансгенную мРНК в камерах сердца, извлеченных из приматов, которым инъецировали AAV9-вектор с оптимизированным LAMP-2B человека (Лечение) или контроль-основу без вектора (без лечения).
На фиг. 10E приведен процент клеток, экспрессирующих трансгенную мРНК in situ в ткани сердца, мышц и печени, извлеченных из приматов, которым инъецировали AAV9-вектор с оптимизированным LAMP-2B человека (Лечение) или контроль-основу без вектора (Без лечения). Индивидуумы обозначены как B059 (самец, M), A991 (самка, F) и A602 (самец, M).
На фиг. 10F показано окрашивание трансгенной мРНК in situ в ткани сердца, извлеченной из приматов, которым инъецировали AAV9-вектор с оптимизированным LAMP-2B человека или контроль-основу без вектора (Без лечения). Индивидуумы обозначены как B059 (самец, M), A991 (самка, F) и A602 (самец, M).
На фиг. 10G показана кратность изменения уровня белка LAMP-2B по результатам вестерн-блоттинга в ткани сердца, мышц и печени, извлеченных из приматов, получавших лечение AAV9-вектором с оптимизированным LAMP-2B человека или не получавших вектор (Без лечения).
На фиг. 10H показана кратность изменения уровня белка LAMP-2B по результатам вестерн-блоттинга в камерах сердца, извлеченных из приматов, получавших лечение AAV9-вектором с оптимизированным LAMP-2B человека или не получавших вектор (Без лечения).
На фиг. 10I показано количественное определение белка LAMP-2B с применением ИФА ELISA в ткани сердца, мышц и печени, извлеченных из приматов, получавших лечение AAV9-вектором с оптимизированным LAMP-2B человека или не получавших вектор (Без лечения).
На фиг. 10J показано количественное определение белка LAMP-2B с применением ИФА ELISA в камерах сердца, извлеченных из приматов, получавших лечение AAV9-вектором с оптимизированным LAMP-2B человека или не получавших вектор (Без лечения).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Согласно настоящему изобретению предложены улучшенные полинуклеотидные последовательности, экспрессионные кассеты и векторы, кодирующие изоформу LAMP-2 (например, LAMP-2B), а также связанные с ними фармацевтические композиции, и их применение для лечения заболеваний и нарушений, ассоциированных с дефицитом или мутацией LAMP-2. Авторы настоящего изобретения обнаружили, что модификации генной последовательности LAMP-2B приводят к повышенной экспрессии трансгена. Кроме того, присутствие специфических элементов последовательности в экспрессионных кассетах геннотерапевтических векторов, кодирующих LAMP-2B, приводит к улучшению экспрессии трансгена. Соответственно, полинуклеотидные последовательности LAMP-2, экспрессионные кассеты и векторы согласно описанию в настоящем документе обеспечивают преимущества для генной терапии по сравнению с ранее известными геннотерапевтическими векторами, в том числе возможность достижения более высоких уровней экспрессии LAMP-2 в терапевтически релевантных тканях.
Последовательность полипептида LAMP-2B дикого типа человека (SEQ ID NO: 1) и полинуклеотидая последовательность дикого типа, кодирующая LAMP-2B человека (SEQ ID NO: 2) представлены, соответственно, следующими последовательностями:
1 MVCFRLFPVP GSGLVLVCLV LGAVRSYALE LNLTDSENAT CLYAKWQMNF TVRYETTNKT
61 YKTVTISDHG TVTYNGSICG DDQNGPKIAV QFGPGFSWIA NFTKAASTYS IDSVSFSYNT
121 GDNTTFPDAE DKGILTVDEL LAIRIPLNDL FRCNSLSTLE KNDVVQHYWD VLVQAFVQNG
181 TVSTNEFLCD KDKTSTVAPT IHTTVPSPTT TPTPKEKPEA GTYSVNNGND TCLLATMGLQ
241 LNITQDKVAS VININPNTTH STGSCRSHTA LLRLNSSTIK YLDFVFAVKN ENRFYLKEVN
301 ISMYLVNGSV FSIANNNLSY WDAPLGSSYM CNKEQTVSVS GAFQINTFDL RVQPFNVTQG
361 KYSTAQECSL DDDTILIPII VGAGLSGLII VIVIAYVIGR RKSYAGYQT
(SEQ ID NO: 1); и
1 ATGGTGTGCT TCCGCCTCTT CCCGGTTCCG GGCTCAGGGC TCGTTCTGGT CTGCCTAGTC
61 CTGGGAGCTG TGCGGTCTTA TGCATTGGAA CTTAATTTGA CAGATTCAGA AAATGCCACT
121 TGCCTTTATG CAAAATGGCA GATGAATTTC ACAGTTCGCT ATGAAACTAC AAATAAAACT
181 TATAAAACTG TAACCATTTC AGACCATGGC ACTGTGACAT ATAATGGAAG CATTTGTGGG
241 GATGATCAGA ATGGTCCCAA AATAGCAGTG CAGTTCGGAC CTGGCTTTTC CTGGATTGCG
301 AATTTTACCA AGGCAGCATC TACTTATTCA ATTGACAGCG TCTCATTTTC CTACAACACT
361 GGTGATAACA CAACATTTCC TGATGCTGAA GATAAAGGAA TTCTTACTGT TGATGAACTT
421 TTGGCCATCA GAATTCCATT GAATGACCTT TTTAGATGCA ATAGTTTATC AACTTTGGAA
481 AAGAATGATG TTGTCCAACA CTACTGGGAT GTTCTTGTAC AAGCTTTTGT CCAAAATGGC
541 ACAGTGAGCA CAAATGAGTT CCTGTGTGAT AAAGACAAAA CTTCAACAGT GGCACCCACC
601 ATACACACCA CTGTGCCATC TCCTACTACA ACACCTACTC CAAAGGAAAA ACCAGAAGCT
661 GGAACCTATT CAGTTAATAA TGGCAATGAT ACTTGTCTGC TGGCTACCAT GGGGCTGCAG
721 CTGAACATCA CTCAGGATAA GGTTGCTTCA GTTATTAACA TCAACCCCAA TACAACTCAC
781 TCCACAGGCA GCTGCCGTTC TCACACTGCT CTACTTAGAC TCAATAGCAG CACCATTAAG
841 TATCTAGACT TTGTCTTTGC TGTGAAAAAT GAAAACCGAT TTTATCTGAA GGAAGTGAAC
901 ATCAGCATGT ATTTGGTTAA TGGCTCCGTT TTCAGCATTG CAAATAACAA TCTCAGCTAC
961 TGGGATGCCC CCCTGGGAAG TTCTTATATG TGCAACAAAG AGCAGACTGT TTCAGTGTCT
1021 GGAGCATTTC AGATAAATAC CTTTGATCTA AGGGTTCAGC CTTTCAATGT GACACAAGGA
1081 AAGTATTCTA CAGCCCAAGA GTGTTCGCTG GATGATGACA CCATTCTAAT CCCAATTATA
1141 GTTGGTGCTG GTCTTTCAGG CTTGATTATC GTTATAGTGA TTGCTTACGT AATTGGCAGA
1201 AGAAAAAGTT ATGCTGGATA TCAGACTCTG TAA
(SEQ ID NO: 2).
Согласно настоящему изобретению предложены модифицированные полинуклеотидные последовательности, кодирующие изоформу ассоциированного с лизосомами мембранного белка 2 (LAMP-2) или ее функциональный вариант. Согласно некоторым вариантам реализации указанные модифицированные полинуклеотидные последовательности содержат одну или более из следующих модификаций относительно полинуклеотида дикого типа, кодирующего изоформу LAMP-2: кодон-оптимизация, истощение по CpG, удаление скрытых сайтов сплайсинга или сниженное число альтернативных открытых рамок считывания (ORF). Согласно некоторым вариантам реализации указанный модифицированный полинуклеотид кодирует LAMP-2A, LAMP-2B, LAMP-2C или функциональный вариант любой из указанных изоформ. Согласно вариантам реализации настоящего изобретения предложен(а) полинуклеотидная последовательность или трансген, кодирующие LAMP-2B или его функциональный вариант и содержащие одну или более замен нуклеотидов относительно SEQ ID NO:2. Согласно вариантам реализации последовательность указанного трансгена по меньшей мере на 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентична или полностью идентична последовательности, выбранной из SEQ ID NO: 3–5. Согласно настоящему изобретению предложены по меньшей мере три иллюстративных варианта последовательностей трансгена, кодирующих LAMP-2B (SEQ ID NO: 3–5):
1 ATGGTCTGCT TCAGACTGTT CCCTGTCCCT GGATCTGGTC TGGTGCTTGT GTGCTTGGTG
61 CTGGGTGCTG TGAGATCCTA TGCCCTTGAG CTGAACCTGA CTGACTCAGA AAATGCCACT
121 TGCCTGTATG CCAAGTGGCA GATGAACTTC ACTGTGAGAT ATGAGACTAC CAACAAGACC
181 TACAAGACTG TGACCATCTC AGACCATGGC ACTGTCACCT ACAATGGATC AATCTGTGGT
241 GATGATCAGA ATGGCCCAAA GATAGCAGTG CAGTTTGGGC CCGGTTTTTC CTGGATTGCT
301 AACTTCACCA AGGCAGCCTC CACCTACAGC ATTGACTCAG TCAGCTTCAG CTACAACACT
361 GGGGATAACA CCACCTTCCC TGACGCAGAG GACAAGGGAA TCCTTACTGT GGACGAACTC
421 CTGGCAATCA GAATCCCCCT TAACGACCTG TTCAGATGCA ACTCCCTTTC AACCCTTGAA
481 AAGAATGATG TGGTGCAACA CTATTGGGAC GTCCTGGTGC AAGCCTTTGT GCAGAATGGG
541 ACAGTGAGTA CCAACGAGTT CCTCTGTGAC AAGGACAAGA CCAGCACTGT GGCCCCCACT
601 ATCCACACCA CTGTGCCCAG CCCTACCACT ACCCCCACCC CTAAAGAGAA GCCAGAAGCT
661 GGAACCTACT CAGTCAACAA TGGAAATGAC ACATGCCTCC TTGCCACCAT GGGACTGCAG
721 CTGAACATCA CTCAGGACAA GGTGGCCTCA GTGATTAACA TCAACCCTAA CACCACTCAT
781 AGCACTGGGA GCTGCAGATC ACATACAGCT CTGCTGAGGC TCAACTCCTC CACCATCAAG
841 TACCTGGACT TTGTGTTTGC TGTGAAGAAT GAGAACAGGT TCTACCTCAA GGAAGTGAAC
901 ATTTCCATGT ACCTGGTCAA TGGTTCAGTG TTCTCTATTG CCAACAACAA TCTGAGCTAC
961 TGGGATGCAC CCCTGGGATC CTCCTACATG TGCAACAAGG AGCAGACTGT GAGTGTGTCA
1021 GGTGCTTTTC AGATCAACAC TTTTGACCTG AGGGTGCAGC CCTTCAATGT GACTCAGGGA
1081 AAGTACTCCA CTGCACAAGA GTGTTCCTTG GATGATGACA CTATCCTCAT CCCCATTATT
1141 GTGGGAGCTG GACTGTCAGG ATTGATTATA GTGATTGTGA TTGCTTATGT GATTGGAAGG
1201 AGAAAGAGCT ATGCTGGCTA CCAGACCCTG TAA
(SEQ ID NO: 3);
1 ATGGTGTGCT TTAGACTGTT TCCTGTGCCT GGTTCAGGGC TGGTCCTGGT CTGTCTGGTG
61 CTGGGGGCTG TCAGAAGCTA TGCCTTGGAG CTGAACCTCA CTGATAGTGA AAATGCCACT
121 TGTCTGTATG CTAAGTGGCA GATGAACTTC ACTGTGAGAT ATGAAACCAC CAACAAGACT
181 TACAAAACAG TGACCATCTC AGATCATGGA ACTGTGACCT ACAACGGCAG CATTTGTGGA
241 GACGACCAGA ACGGACCAAA AATCGCTGTC CAATTTGGGC CTGGATTCTC CTGGATTGCC
301 AATTTCACTA AAGCTGCCTC CACATATTCA ATTGACTCAG TGTCCTTCTC CTACAACACT
361 GGGGACAACA CTACTTTCCC TGATGCTGAA GATAAGGGAA TCTTGACAGT GGATGAGCTG
421 CTGGCTATCA GGATCCCTTT GAATGACCTG TTTAGGTGTA ATTCACTGAG CACTCTGGAG
481 AAGAACGACG TGGTGCAGCA CTACTGGGAC GTGCTGGTGC AGGCCTTTGT GCAGAACGGC
541 ACTGTGTCCA CCAACGAATT CCTGTGTGAT AAGGACAAAA CTTCCACTGT GGCACCTACA
601 ATTCACACTA CTGTGCCTTC ACCTACCACC ACTCCAACTC CAAAGGAAAA GCCTGAAGCA
661 GGAACCTACT CTGTGAACAA TGGCAATGAT ACCTGTCTGT TGGCCACCAT GGGCCTCCAA
721 CTGAACATTA CTCAGGACAA GGTGGCCTCA GTGATTAACA TTAACCCCAA CACTACCCAC
781 TCCACTGGCA GCTGTAGATC ACACACAGCC TTGCTCAGAC TGAATAGCAG CACCATCAAG
841 TATTTGGATT TTGTGTTTGC AGTGAAGAAT GAAAACAGGT TCTACCTGAA GGAAGTCAAC
901 ATCTCAATGT ACCTGGTGAA CGGCTCAGTG TTCAGCATTG CCAACAACAA CCTCTCCTAT
961 TGGGACGCTC CACTGGGGAG CAGCTACATG TGTAACAAGG AACAGACTGT GTCAGTGTCA
1021 GGAGCCTTCC AGATTAACAC CTTTGATCTG AGGGTCCAAC CCTTTAATGT CACTCAAGGA
1081 AAGTATAGCA CTGCCCAGGA GTGCTCCCTG GATGATGACA CCATTCTGAT TCCAATCATT
1141 GTGGGTGCAG GACTTTCTGG GCTTATTATT GTGATTGTGA TTGCCTATGT GATTGGCAGA
1201 AGGAAATCCT ATGCAGGGTA CCAAACTCTG TAA
(SEQ ID NO: 4); и
1 ATGGTCTGTT TTAGGCTGTT CCCTGTCCCT GGTTCAGGAC TGGTCTTAGT GTGTCTGGTG
61 CTTGGAGCTG TCAGAAGCTA TGCCCTGGAG CTGAACCTGA CTGACTCAGA AAATGCCACT
121 TGCCTGTATG CCAAGTGGCA GATGAACTTC ACTGTCAGAT ATGAAACCAC CAACAAGACC
181 TATAAGACTG TGACCATCTC AGACCATGGC ACTGTGACTT ACAATGGGTC AATTTGTGGA
241 GATGACCAGA ATGGCCCTAA GATAGCTGTC CAGTTTGGTC CAGGATTCAG CTGGATTGCC
301 AACTTCACCA AGGCAGCCAG CACCTACAGC ATTGACTCTG TGTCCTTCTC CTACAACACA
361 GGAGACAACA CCACTTTCCC TGATGCAGAG GACAAAGGTA TCCTGACTGT GGATGAGTTG
421 CTGGCAATCA GGATCCCACT GAACGATCTG TTCAGGTGCA ACTCACTGTC CACTCTGGAA
481 AAGAATGATG TGGTGCAGCA CTATTGGGAT GTGCTAGTCC AGGCCTTTGT CCAGAATGGG
541 ACTGTGTCAA CTAATGAGTT CCTGTGTGAC AAGGACAAGA CAAGCACTGT AGCCCCCACT
601 ATCCATACCA CAGTACCTAG CCCCACCACT ACTCCAACCC CCAAGGAGAA GCCTGAGGCT
661 GGCACCTACT CAGTGAACAA TGGGAATGAC ACCTGTTTGC TGGCCACTAT GGGACTCCAA
721 CTGAACATCA CCCAGGACAA AGTGGCCTCT GTGATCAATA TCAATCCCAA CACCACCCAC
781 AGCACTGGGT CCTGCAGAAG CCACACTGCC CTCCTGAGGC TCAACTCATC AACTATCAAG
841 TACTTGGATT TTGTGTTTGC AGTGAAGAAT GAGAACAGAT TCTACCTCAA AGAGGTCAAC
901 ATTTCAATGT ACCTGGTGAA TGGGAGTGTG TTCTCCATTG CTAACAACAA CCTGAGCTAC
961 TGGGATGCCC CTCTGGGCTC CTCATACATG TGCAACAAGG AACAGACTGT GAGTGTGTCA
1021 GGGGCCTTCC AGATCAACAC TTTTGACCTG AGAGTGCAGC CCTTTAATGT GACACAGGGA
1081 AAGTACAGCA CTGCTCAGGA GTGCAGCCTG GATGATGACA CTATCCTGAT CCCTATCATT
1141 GTGGGGGCAG GCCTGTCTGG ACTCATTATT GTGATTGTGA TTGCCTATGT GATAGGGAGA
1201 AGGAAGTCTT ATGCTGGATA CCAGACCCTG TAA
(SEQ ID NO: 5).
Согласно варианту реализации последовательность указанного трансгена обладает по меньшей мере 95% идентичностью с последовательности, выбранной из SEQ ID NO: 3–5. Согласно варианту реализации последовательность указанного трансгена по меньшей мере на 99% идентична последовательности, выбранной из SEQ ID NO: 3–5. Согласно варианту реализации указанный трансген содержит последовательность, выбранную из SEQ ID NO: 3–5. Согласно варианту реализации последовательность указанного трансгена по меньшей мере на 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентична или полностью идентична SEQ ID NO: 3. Согласно варианту реализации последовательность указанного трансгена по меньшей мере на 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентична или полностью идентична SEQ ID NO: 4. Согласно варианту реализации последовательность указанного трансгена по меньшей мере на 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентична или полностью идентична SEQ ID NO: 5.
Согласно некоторым вариантам реализации указанный трансген аналогичен или идентичен подпоследовательности из любой из SEQ ID NO: 3–5. Согласно некоторым вариантам реализации указанный трансген содержит подпоследовательность из любой из SEQ ID NO: 3–5. Согласно различным вариантам реализации указанная подпоследовательность может содержать любой набор последовательных нуклеотидов (НТ) в полной последовательности длиной по меньшей мере приблизительно 50 НТ, по меньшей мере приблизительно 100 НТ, по меньшей мере приблизительно 150 НТ, по меньшей мере приблизительно 250 НТ, по меньшей мере приблизительно 200 НТ, по меньшей мере приблизительно 350 НТ, по меньшей мере приблизительно 450 НТ, по меньшей мере приблизительно 400 НТ, по меньшей мере приблизительно 450 НТ, по меньшей мере приблизительно 550 НТ, по меньшей мере приблизительно 600 НТ, по меньшей мере приблизительно 650 НТ, по меньшей мере приблизительно 600 НТ, по меньшей мере приблизительно 650 НТ, по меньшей мере приблизительно 700 НТ, по меньшей мере приблизительно 750 НТ, по меньшей мере приблизительно 800 НТ, по меньшей мере приблизительно 850 НТ, по меньшей мере приблизительно 900 НТ, по меньшей мере приблизительно 950 НТ или по меньшей мере приблизительно 1000 НТ.
Согласно некоторым вариантам реализации последовательность указанного трансгена обладает по меньшей мере 95% идентичностью с подпоследовательности, которая содержит нуклеотиды 1–500, 250–750, 500–1000 или 750–1240 из любой из SEQ ID NO: 3–5. Согласно варианту реализации последовательность указанного трансгена по меньшей мере на 99% идентична подпоследовательности, которая содержит нуклеотиды 1–500, 250–750, 500–1000 или 750–1240 из любой из SEQ ID NO: 3–5. Согласно варианту реализации указанный трансген содержит последовательность, которая содержит нуклеотиды 1–500, 250–750, 500–1000 или 750–1240 из любой из SEQ ID NO: 3–5. Согласно варианту реализации последовательность указанного трансгена по меньшей мере на 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентична или полностью идентична подпоследовательности, которая содержит нуклеотиды 1–500, 250–750, 500–1000 или 750–1240 из любой из SEQ ID NO: 3–5. Согласно вариантам реализации последовательность указанного трансгена по меньшей мере на 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентична или полностью идентична подпоследовательности, которая содержит нуклеотиды 1–500, 250–750, 500–1000 или 750–1240 из SEQ ID NO: 3. Согласно варианту реализации последовательность указанного трансгена по меньшей мере на 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентична или полностью идентична подпоследовательности, которая содержит нуклеотиды 1–500, 250–750, 500–1000 или 750–1240 из SEQ ID NO: 3.
Согласно некоторым вариантам реализации указанный трансген кодирует любую из различных изоформ LAMP-2, в том числе любую из LAMP-2A, LAMP-2B или LAMP-2C, или функциональный фрагмент или вариант любой из указанных изоформ. Соответственно, согласно конкретным вариантам реализации указанная экспрессионная кассета представляет собой оптимизированную полинуклеотидную последовательность, которая кодирует любую из LAMP-2A, LAMP-2B или LAMP-2C, или ее функциональный фрагмент или вариант, и содержит одну или более модификаций по сравнению с соответствующей полинуклеотидной последовательностью дикого типа, в том числе одну или более из следующих модификаций: кодон-оптимизация последовательности трансгена, кодирующей LAMP-2A, LAMP-2B или LAMP-2C; указанная экспрессионная кассета или последовательность трансгена содержит меньше сайтов CpG, чем соответствующая последовательность дикого типа; указанная экспрессионная кассета или последовательность трансгена содержит меньше сайтов CpG, чем соответствующая последовательность дикого типа; указанная экспрессионная кассета или последовательность трансгена содержит меньше скрытых сайтов сплайсинга, чем соответствующая последовательность дикого типа; и/или указанная экспрессионная кассета или последовательность трансгена содержит меньше открытых рамок считывания, чем соответствующая последовательность дикого типа. Согласно конкретным вариантам реализации указанная оптимизированная последовательность оптимизирована для повышенной экспрессии в клетках человека. Полинуклеотидные последовательности человека дикого типа, кодирующие изоформы LAMP-2A и LAMP-2C, приведены в SEQ ID NO: 29 и 30, соответственно. Последовательности дикого типа белков LAMP-2A и LAMP-2C человека приведены в SEQ ID NO: 34 и 35, соответственно. Последовательности изоформ LAMP-2 дикого типа и кодирующие последовательности также находятся в открытом доступе. Хотя в настоящем документе конкретные варианты реализации описаны применительно к LAMP-2B, следует понимать, что в любом варианте реализации, как вариант, может быть использован LAMP-2A или LAMP-2C.
Кодирующие последовательности LAMP-2A дикого типа (SEQ ID NO: 29) и LAMP-2C дикого типа (SEQ ID NO: 30) на 100% идентичны кодирующей последовательности LAMP-2B дикого типа (SEQ ID NO: 2) по меньшей мере на протяжении нуклеотидов 1–1080. Соответственно, специалистам в данной области техники будет хорошо понятно, что трансгены, экспрессионные кассеты и векторы согласно описанию в настоящем документе могут быть адаптированы для экспрессии указанных изоформ LAMP-2 путем замены 3′-концом (от нуклеотида 1081 до последнего нуклеотида) из LAMP-2A (SEQ ID NO: 29) или из LAMP-2C дикого типа (SEQ ID NO: 30) нуклеотидов 1081–1233 LAMP-2B (например, оптимизированного LAMP-2B, представленного в любой из SEQ ID NO: 3–5). Например, во вариантах реализации настоящего изобретения используют нуклеотиды 1–1080 оптимизированных генных последовательностей LAMP-2B, SEQ ID NO: 3–5, которые представлены, соответственно, последовательностями SEQ ID NO: 31–33.
Согласно варианту реализации последовательность указанного трансгена обладает по меньшей мере 95% идентичностью с последовательности, выбранной из SEQ ID NO: 31–33. Согласно варианту реализации последовательность указанного трансгена по меньшей мере на 99% идентична последовательности, выбранной из SEQ ID NO: 31–33. Согласно варианту реализации указанный трансген содержит последовательность, выбранную из SEQ ID NO: 31–33. Согласно варианту реализации последовательность указанного трансгена по меньшей мере на 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентична или полностью идентична SEQ ID NO: 31. Согласно варианту реализации последовательность указанного трансгена по меньшей мере на 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентична или полностью идентична SEQ ID NO: 32. Согласно варианту реализации последовательность указанного трансгена по меньшей мере на 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентична или полностью идентична SEQ ID NO: 33. В некоторых случаях указанный трансген характеризуется полинуклеотидной последовательностью, отличной от полинуклеотидной последовательности референсной последовательности, например, «природной» или «дикого типа» последовательности LAMP-2B. Согласно некоторым вариантам реализации последовательность указанного трансгена максимум на 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94% или 95% идентична референсной последовательности. Согласно некоторым вариантам реализации референсная последовательность представлена SEQ ID NO: 2. Например, SEQ ID NO: 3 на 78,5% идентична SEQ ID NO: 2.
В некоторых случаях указанный трансген характеризуется полинуклеотидной последовательностью, отличной от полинуклеотидной последовательности референсной последовательности, например, «природной» или «дикого типа» последовательности LAMP-2A. Согласно некоторым вариантам реализации последовательность указанного трансгена максимум на 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94% или 95% идентична референсной последовательности. Согласно некоторым вариантам реализации референсная последовательность представлена последовательностью LAMP-2A человека дикого типа из SEQ ID NO: 29.
В некоторых случаях указанный трансген характеризуется полинуклеотидной последовательностью, отличной от референсной полинуклеотидной последовательности, например, «природной» или «дикого типа» последовательности LAMP-2C. Согласно некоторым вариантам реализации последовательность указанного трансгена максимум на 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94% или 95% идентична референсной последовательности. Согласно некоторым вариантам реализации референсная последовательность представлена последовательностью LAMP-2A человека дикого типа из SEQ ID NO: 30.
Согласно варианту реализации указанный трансген кодон-оптимизирован для экспрессии в человеческой клетке-хозяине. Согласно варианту реализации кодирующая последовательность трансгена модифицирована или «кодон-оптимизирована» для усиления экспрессии путем замены редко представленных кодонов более часто представленными кодонами. Кодирующая последовательность представляет собой часть последовательности мРНК, которая кодирует аминокислоты для трансляции. В ходе трансляции каждый из 61 тринуклеотидных кодонов транслируется в одну из 20 аминокислот, что приводит к вырожденности, или избыточности, генетического кода. Однако разные типы клеток и разные виды животных используют тРНК (каждая из которых несет антикодон), кодирующие одинаковые аминокислоты, с разными частотами. Если генная последовательность содержит кодоны, редко представленные в соответствующей тРНК, механизмы рибосомальной трансляции могут работать медленнее, что затрудняет эффективную трансляцию. Экспрессия может быть улучшена путем «кодон-оптимизации» для конкретного вида, когда кодирующую последовательность изменяют так, чтобы она кодировала ту же последовательность белка, однако с использованием кодонов, часто встречающихся и/или используемых в экспрессируемых на высоком уровне белках человека (Cid-Arregui et al., 2003; J. Virol. 77: 4928).
Согласно некоторым вариантам реализации кодирующая последовательность указанного трансгена модифицирована с заменой кодонов, редко экспрессируемых у млекопитающего или у приматов, на кодоны, часто экспрессируемые у приматов. Например, согласно некоторым вариантам реализации указанный трансген кодирует полипептид, последовательность которого по меньшей мере на 85% идентична последовательности референсного полипептида (например, LAMP-2B дикого типа; SEQ ID NO: 3) – например, по меньшей мере на 90% идентична, обладает по меньшей мере 95% идентичностью с, по меньшей мере на 98% идентична, или по меньшей мере на 99% идентична последовательности референсного полипептида – при этом по меньшей мере один кодон указанной кодирующей последовательности встречается в тРНК человека с большей частотой, чем соответствующий кодон в последовательности, описанной выше или в тексте настоящего документа.
Согласно варианту реализации указанный трансген содержит меньше альтернативных открытых рамок считывания, чем SEQ ID: 2. Согласно варианту реализации указанный трансген модифицирован для повышения экспрессии за счет терминации или удаления открытых рамок считывания (ORF), которые не кодируют требуемый трансген. Открытая рамка считывания (ORF) представляет собой последовательность нуклеиновой кислоты, расположенную после стартового кодона и не содержащую стоп-кодона. ORF могут быть расположены в прямой или обратной ориентации, и могут находиться «внутри рамки» или «вне рамки» относительно гена, представляющего интерес. Такие открытые рамки считывания потенциально могут экспрессироваться в экспрессионной кассете вместе с геном, представляющим интерес, и могут вызывать нежелательные побочные явления. Согласно некоторым вариантам реализации указанный трансген модифицирован для удаления открытых рамок считывания путем дополнительного изменения использования кодонов. Это может осуществляться путем устранения одного или более стартовых кодонов (ATG) и/или введения одного или более стоп-кодонов (TAG, TAA или TGA) в обратной ориентации или вне рамки по отношению к требуемой ORF, при сохранении кодируемой последовательности аминокислот и, необязательно, сохранении часто используемых кодонов в гене, представляющем интерес (т.е. избегания кодонов, встречающихся с частотой < 20%).
Согласно некоторым вариантам реализации указанная экспрессионная кассета содержит максимум один, максимум два, максимум три, максимум четыре или максимум пять стартовых кодонов в направлении 5′ относительно стартового кодона указанного трансгена. Согласно некоторым вариантам реализации указанная экспрессионная кассета не содержит стартового кодона в направлении 5′ относительно стартового кодона указанного трансгена. Согласно некоторым вариантам реализации один или более кодонов ATG в 5′-UTR, промоторе, энхансере, промоторном/энхансерном элементе или других последовательностях, расположенных в направлении 5′ относительно стартового кодона указанного трансгена, сохраняются после удаления одного или более скрытых стартовых сайтов. Согласно некоторым вариантам реализации указанная экспрессионная кассета не содержит скрытых стартовых сайтов в направлении 5’ от трансгена, способных продуцировать ошибочные мРНК.
Во вариантах настоящего изобретения кодирующая последовательность трансгена может быть оптимизирована либо путем кодон-оптимизации, либо путем удаления нетрансгенных ORF, либо с помощью обеих методик. В некоторых случаях нетрансгенные ORF удаляют или минимизируют после кодон-оптимизации для удаления ORF, введенных при кодон-оптимизации.
Согласно варианту реализации указанный трансген содержит меньше сайтов CpG, чем SEQ ID: 2. Без связи с какой-либо теорией считается, что присутствие сайтов CpG в полинуклеотидной последовательности ассоциировано с нежелательными иммунологическими ответами хозяина на вирусный вектор, содержащий указанную полинуклеотидную последовательность. Согласно некоторым вариантам реализации указанный трансген разработан таким образом, что число сайтов CpG снижено. Примеры способов приведены в опубликованной заявке на патент США US20020065236A1.
Согласно варианту реализации указанный трансген содержит меньше скрытых сайтов сплайсинга, чем SEQ ID: 2. Для оптимизации может быть использовано программное обеспечение GeneArt®, например, для увеличения содержания GC и/или удаления скрытых сайтов сплайсинга, чтобы избежать сайленсинга транскрипции и, соответственно, повысить экспрессию трансгена. Как вариант, может применяться любой способ оптимизации, известный в данной области техники. Удаление скрытых сайтов сплайсинга описано, например, в опубликованной международной заявке на патент WO2004015106A1.
Также согласно настоящему изобретению предложены экспрессионные кассеты и геннотерапевтические векторы, кодирующие LAMP-2B. Согласно некоторым вариантам реализации указанные экспрессионные кассеты и геннотерапевтические векторы содержат кодон-оптимизированную полинуклеотидную последовательность LAMP-2B или вариант полинуклеотидной последовательности LAMP-2B, или последовательность трансгена согласно описанию в настоящем документе.
Согласно конкретным вариантам реализации экспрессионная кассета или геннотерапевтический вектор, кодирующие LAMP-2B, содержат: консенсусную оптимальную последовательность Козак, полноразмерную последовательность полиаденилирования ((поли)А) (или замену полноразмерной (поли)А усеченной (поли)А), и минимальные или отсутствующие вышерасположенные (т.е. 5′) или скрытые стартовые кодоны (т.е. сайты ATG). Согласно некоторым вариантам реализации указанная экспрессионная кассета не содержит стартового сайта в направлении 5′ от трансгена, способного давать альтернативные мРНК. Согласно некоторым вариантам реализации указанная экспрессионная кассета или геннотерапевтический вектор содержат последовательность, кодирующую LAMP-2B, например, кодон-оптимизированную последовательность или вариант полинуклеотидной последовательности LAMP-2B или последовательность трансгена согласно описанию в настоящем документе.
В некоторых случаях, указанная экспрессионная кассета содержит два или более первых инвертированных концевых повторов, энхансерную/промоторную область, консенсусную оптимальную последовательность Козак, трансген (например, трансген, кодирующий LAMP-2B согласно описанию в настоящем документе), нетранслируемую 3′-область, включающую полноразмерную (поли)А-последовательность, и второй инвертированный концевой повтор. Согласно некоторым вариантам реализации один или оба инвертированных концевых повторов (ITR) представлены ITR AAV1, AAV2, AAV3, AAV4, AAV5, AAV6, AAV7 или AAV9, или любым ITR, известным в данной области техники. Согласно некоторым вариантам реализации указанная экспрессионная кассета содержит ровно два ITR. Согласно некоторым вариантам реализации оба ITR представлены ITR AAV2, AAV5 или AAV9. Согласно некоторым вариантам реализации оба ITR представлены ITR AAV2.
Согласно варианту реализации указанная экспрессионная кассета содержит последовательность Козак, функционально связанную с трансгеном. Согласно варианту реализации указанная последовательность Козак представляет собой консенсусную оптимальную последовательность Козак, содержащую или состоящую из SEQ ID NO: 6:
GCCGCCACCATGG (SEQ ID NO: 6).
Согласно различным вариантам реализации указанная экспрессионная кассета содержит альтернативную последовательность Козак, функционально связанную с трансгеном. Согласно варианту реализации указанная последовательность Козак представляет собой альтернативную последовательность Козак, содержащую или состоящую из любой из SEQ ID NO. 14–18:
(gcc)gccRccAUGG (SEQ ID NO: 14);
AGNNAUGN (SEQ ID NO: 15);
ANNAUGG (SEQ ID NO: 16);
ACCAUGG (SEQ ID NO: 17);
GACACCAUGG (SEQ ID NO: 18).
Согласно некоторым вариантам реализации указанная экспрессионная кассета не содержит последовательности Козак.
В SEQ ID NO: 14 строчными буквами обозначены наиболее распространенные основания в положениях, где возможны, тем не менее, другие варианты оснований; заглавными буквами обозначены высококонсервативные основания; обозначены аденин или гуанин. В SEQ ID NO: 14 последовательность в круглых скобках (gcc) является необязательной. В SEQ ID NO: 15–17 «N» обозначает любое основание.
Вместо указанной консенсусной оптимальной последовательности Козак в качестве сайта инициации трансляции могут применяться различные последовательности, и специалисты в данной области техники смогут идентифицировать и протестировать другие последовательности. См. Kozak M. An analysis of vertebrate mRNA sequences: intimations of translational control. J. Cell Biol. 115 (4): 887–903 (1991).
Согласно варианту реализации указанная экспрессионная кассета содержит полноразмерную (поли)А-последовательность, функционально связанную с трансгеном. Согласно варианту реализации указанная полноразмерная (поли)А-последовательность содержит SEQ ID NO: 7:
1 TGGCTAATAA AGGAAATTTA TTTTCATTGC AATAGTGTGT TGGAATTTTT TGTGTCTCTC
61 ACTCGGAAGG ACATATGGGA GGGCAAATCA TTTAAAACAT CAGAATGAGT ATTTGGTTTA
121 GAGTTTGGCA ACATATGCCC ATATGCTGGC TGCCATGAAC AAAGGTTGGC TATAAAGAGG
181 TCATCAGTAT ATGAAACAGC CCCCTGCTGT CCATTCCTTA TTCCATAGAA AAGCCTTGAC
241 TTGAGGTTAG ATTTTTTTTA TATTTTGTTT TGTGTTATTT TTTTCTTTAA CATCCCTAAA
301 ATTTTCCTTA CATGTTTTAC TAGCCAGATT TTTCCTCCTC TCCTGACTAC TCCCAGTCAT
361 AGCTGTCCCT CTTCTCTTAT GGAGATC
(SEQ ID NO: 7).
В экспрессионных кассетах согласно настоящему описанию могут применяться различные альтернативные (поли)А-последовательности, в том числе, без ограничения, сигнал полиаденилирования бычьего гормона роста (bGHpA) (SEQ ID NO: 19), ранний/поздний сигнал полиаденилирования SV40 (SEQ ID NO: 20) и сигнал полиаденилирования гормона роста человека (HGH) (SEQ ID NO: 21):
1 TCGACTGTGC CTTCTAGTTG CCAGCCATCT GTTGTTTGCC CCTCCCCCGT GCCTTCCTTG
61 ACCCTGGAAG GTGCCACTCC CACTGTCCTT TCCTAATAAA ATGAGGAAAT TGCATCGCAT
121 TGTCTGAGTA GGTGTCATTC TATTCTGGGG GGTGGGGTGG GGCAGGACAG CAAGGGGGAG
181 GATTGGGAGG ACAATAGCAG GCATGCTGGG GATGCGGTGG GCTCTATGGC TTCTG
(SEQ ID NO: 19);
1 CAGACATGAT AAGATACATT GATGAGTTTG GACAAACCAC AACTAGAATG CAGTGAAAAA
61 AATGCTTTAT TTGTGAAATT TGTGATGCTA TTGCTTTATT TGTAACCATT ATAAGCTGCA
121 ATAAACAAGT TAACAACAAC AATTGCATTC ATTTTATGTT TCAGGTTCAG GGGGAGATGT
181 GGGAGGTTTT TTAAAGCAAG TAAAACCTCT ACAAATGTGG TA
(SEQ ID NO: 20);
1 CTGCCCGGGT GGCATCCCTG TGACCCCTCC CCAGTGCCTC TCCTGGCCCT GGAAGTTGCC
61 ACTCCAGTGC CCACCAGCCT TGTCCTAATA AAATTAAGTT GCATCATTTT GTCTGACTAG
121 GTGTCCTTCT ATAATATTAT GGGGTGGAGG GGGGTGGTAT GGAGCAAGGG GCCCAAGTTG
181 GGAAGAAACC TGTAGGGCCT GC
(SEQ ID NO: 21).
Согласно некоторым вариантам реализации указанная экспрессионная кассета содержит активный фрагмент (поли)А-последовательности. Согласно конкретным вариантам реализации активный фрагмент указанной (поли)А-последовательности содержит или состоит из менее чем 20 пар оснований (п.о.), менее чем 50 п.о., менее чем 100 п.о. или менее чем 150 п.о., например, из любой из (поли)А-последовательностей согласно описанию в настоящем документе.
В некоторых случаях экспрессию трансгена повышают, обеспечивая отсутствие в указанной экспрессионной кассете конкурирующих ORF. Согласно варианту реализации указанная экспрессионная кассета не содержит стартового кодона в пределах 20, 30, 40, 50, 60, 70, 80, 90, 100, 200, 300, 400 или 500 пар оснований в направлении 5′ от стартового кодона трансгена. Согласно определенному варианту реализации указанная экспрессионная кассета не содержит стартового кодона в направлении 5′ от стартового кодона трансгена. Согласно некоторым вариантам реализации указанная экспрессионная кассета не содержит в направлении 5′ от трансгена стартового сайта, способного давать альтернативные мРНК.
Согласно варианту реализации указанная экспрессионная кассета содержит в направлении от 5′- к 3′-концу функционально связанные: первый инвертированный концевой повтор, энхансерную/промоторную область, интроны, консенсусную оптимальную последовательность Козак, трансген, нетранслируемую 3′-область, включающую полноразмерную (поли)А-последовательность, и второй инвертированный концевой повтор, причем указанная экспрессионная кассета не содержит в направлении 5′ от трансгена стартового сайта, способного давать альтернативные мРНК.
Согласно некоторым вариантам реализации указанная энхансерная/промоторная область содержит, в направлении от 5′- к 3′-концу: энхансер средних и ранних генов цитомегаловируса (CMV IE) и промотор бета-актина курицы. Согласно варианту реализации указанная энхансерная/промоторная область содержит промотор CAG (SEQ ID NO: 22). В настоящем документе «промотор CAG» относится к полинуклеотидной последовательности, содержащей ранний энхансерный элемент CMV, промотор бета-актина курицы, первый экзон и первый интрон гена бета-актина курицы и акцептор сплайсинга из гена бета-глобина кролика.
1 CTAGTCGACA TTGATTATTG ACTAGTTATT AATAGTAATC AATTACGGGG TCATTAGTTC
61 ATAGCCCATA TATGGAGTTC CGCGTTACAT AACTTACGGT AAATGGCCCG CCTGGCTGAC
121 CGCCCAACGA CCCCCGCCCA TTGACGTCAA TAATGACGTA TGTTCCCATA GTAACGCCAA
181 TAGGGACTTT CCATTGACGT CAATGGGTGG AGTATTTACG GTAAACTGCC CACTTGGCAG
241 TACATCAAGT GTATCATATG CCAAGTACGC CCCCTATTGA CGTCAATGAC GGTAAATGGC
301 CCGCCTGGCA TTATGCCCAG TACATGACCT TATGGGACTT TCCTACTTGG CAGTACATCT
361 ACGTATTAGT CATCGCTATT ACCATGGTCG AGGTGAGCCC CACGTTCTGC TTCACTCTCC
421 CCATCTCCCC CCCCTCCCCA CCCCCAATTT TGTATTTATT TATTTTTTAA TTATTTTGTG
481 CAGCGATGGG GGCGGGGGGG GGGGGGGGGC GCGCGCCAGG CGGGGCGGGG CGGGGCGAGG
541 GGCGGGGCGG GGCGAGGCGG AGAGGTGCGG CGGCAGCCAA TCAGAGCGGC GCGCTCCGAA
601 AGTTTCCTTT TATGGCGAGG CGGCGGCGGC GGCGGCCCTA TAAAAAGCGA AGCGCGCGGC
661 GGGCGGGAGT CGCTGCGCGC TGCCTTCGCC CCGTGCCCCG CTCCGCCGCC GCCTCGCGCC
721 GCCCGCCCCG GCTCTGACTG ACCGCGTTAC TCCCACAGGT GAGCGGGCGG GACGGCCCTT
781 CTCCTCCGGG CTGTAATTAG CGCTTGGTTT AATGACGGCT TGTTTCTTTT CTGTGGCTGC
841 GTGAAAGCCT TGAGGGGCTC CGGGAGGGCC CTTTGTGCGG GGGGAGCGGC TCGGGGGGTG
901 CGTGCGTGTG TGTGTGCGTG GGGAGCGCCG CGTGCGGCTC CGCGCTGCCC GGCGGCTGTG
961 AGCGCTGCGG GCGCGGCGCG GGGCTTTGTG CGCTCCGCAG TGTGCGCGAG GGGAGCGCGG
1021 CCGGGGGCGG TGCCCCGCGG TGCGGGGGGG GCTGCGAGGG GAACAAAGGC TGCGTGCGGG
1081 GTGTGTGCGT GGGGGGGTGA GCAGGGGGTG TGGGCGCGTC GGTCGGGCTG CAACCCCCCC
1141 TGCACCCCCC TCCCCGAGTT GCTGAGCACG GCCCGGCTTC GGGTGCGGGG CTCCGTACGG
1201 GGCGTGGCGC GGGGCTCGCC GTGCCGGGCG GGGGGTGGCG GCAGGTGGGG GTGCCGGGCG
1261 GGGCGGGGCC GCCTCGGGCC GGGGAGGGCT CGGGGGAGGG GCGCGGCGGC CCCCGGAGCG
1321 CCGGCGGCTG TCGAGGCGCG GCGAGCCGCA GCCATTGCCT TTTATGGTAA TCGTGCGAGA
1381 GGGCGCAGGG ACTTCCTTTG TCCCAAATCT GTGCGGAGCC GAAATCTGGG AGGCGCCGCC
1441 GCACCCCCTC TAGCGGGCGC GGGGCGAAGC GGTGCGGCGC CGGCAGGAAG GAAATGGGCG
1501 GGGAGGGCCT TCGTGCGTCG CCGCGCCGCC GTCCCCTTCT CCCTCTCCAG CCTCGGGGCT
1561 GTCCGCGGGG GGACGGCTGC CTTCGGGGGG GACGGGGCAG GGCGGGGTTC GGCTTCTGGC
1621 GTGTGACCGG CGGCTCTAGA GCCTCTGCTA ACCATGTTCA TGCCTTCTTC TTTTTCCTAC
1681 AGCTCCTGGG CAACGTGCTG GTTATTGTGC TGTCTCATCA TTTTGGCAAA
(SEQ ID NO: 22).
Согласно некоторым вариантам реализации указанная энхансерная/промоторная область содержит общераспространенный промотор. Согласно некоторым вариантам реализации указанная энхансерная/промоторная область содержит промотор CMV (SEQ. ID NO: 23), промотор SV40 (SEQ ID NO: 24), промотор PGK (SEQ ID NO: 25) и/или промотор бета-актина человека (SEQ ID NO: 26). Согласно некоторым вариантам реализации указанная энхансерная/промоторная область содержит полинуклеотид, последовательность которого по меньшей мере на 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентична любой из SEQ ID NO: 23–26:
1 GTGATGCGGT TTTGGCAGTA CATCAATGGG CGTGGATAGC GGTTTGACTC ACGGGGATTT
61 CCAAGTCTCC ACCCCATTGA CGTCAATGGG AGTTTGTTTT GGCACCAAAA TCAACGGGAC
121 TTTCCAAAAT GTCGTAACAA CTCCGCCCCA TTGACGCAAA TGGGCGGTAG GCGTGTACGG
181 TGGGAGGTCT ATATAAGCAG AGCT
(SEQ ID NO: 23);
1 GGTGTGGAAA GTCCCCAGGC TCCCCAGCAG GCAGAAGTAT GCAAAGCATG CATCTCAATT
61 AGTCAGCAAC CAGGTGTGGA AAGTCCCCAG GCTCCCCAGC AGGCAGAAGT ATGCAAAGCA
121 TGCATCTCAA TTAGTCAGCA ACCATAGTCC CGCCCCTAAC TCCGCCCATC CCGCCCCTAA
181 CTCCGCCCAG TTCCGCCCAT TCTCCGCCCC ATGGCTGACT AATTTTTTTT ATTTATGCAG
241 AGGCCGAGGC CGCCTCGGCC TCTGAGCTAT TCCAGAAGTA GTGAGGAGGC TTTTTTGGAG
301 GCCTAGGCTT TTGCAAA
(SEQ ID NO: 24);
1 GGGTAGGGGA GGCGCTTTTC CCAAGGCAGT CTGGAGCATG CGCTTTAGCA GCCCCGCTGG
61 GCACTTGGCG CTACACAAGT GGCCTCTGGC CTCGCACACA TTCCACATCC ACCGGTAGGC
121 GCCAACCGGC TCCGTTCTTT GGTGGCCCCT TCGCGCCACC TTCTACTCCT CCCCTAGTCA
181 GGAAGTTCCC CCCCGCCCCG CAGCTCGCGT CGTGCAGGAC GTGACAAATG GAAGTAGCAC
241 GTCTCACTAG TCTCGTGCAG ATGGACAGCA CCGCTGAGCA ATGGAAGCGG GTAGGCCTTT
301 GGGGCAGCGG CCAATAGCAG CTTTGCTCCT TCGCTTTCTG GGCTCAGAGG CTGGGAAGGG
361 GTGGGTCCGG GGGCGGGCTC AGGGGCGGGC TCAGGGGCGG GGCGGGCGCC CGAAGGTCCT
421 CCGGAGGCCC GGCATTCTGC ACGCTTCAAA AGCGCACGTC TGCCGCGCTG TTCTCCTCTT
481 CCTCATCTCC GGGCCTTTCG
(SEQ ID NO: 25);
1 CCTGCAGGGC CCACTAGTTC CATGTCCTTA TATGGACTCA TCTTTGCCTA TTGCGACACA
61 CACTCAATGA ACACCTACTA CGCGCTGCAA AGAGCCCCGC AGGCCTGAGG TGCCCCCACC
121 TCACCACTCT TCCTATTTTT GTGTAAAAAT CCAGCTTCTT GTCACCACCT CCAAGGAGGG
181 GGAGGAGGAG GAAGGCAGGT TCCTCTAGGC TGAGCCGAAT GCCCCTCTGT GGTCCCACGC
241 CACTGATCGC TGCATGCCCA CCACCTGGGT ACACACAGTC TGTGATTCCC GGAGCAGAAC
301 GGACCCTGCC CACCCGGTCT TGTGTGCTAC TCAGTGGACA GACCCAAGGC AAGAAAGGGT
361 GACAAGGACA GGGTCTTCCC AGGCTGGCTT TGAGTTCCTA GCACCGCCCC GCCCCCAATC
421 CTCTGTGGCA CATGGAGTCT TGGTCCCCAG AGTCCCCCAG CGGCCTCCAG ATGGTCTGGG
481 AGGGCAGTTC AGCTGTGGCT GCGCATAGCA GACATACAAC GGACGGTGGG CCCAGACCCA
541 GGCTGTGTAG ACCCAGCCCC CCCGCCCCGC AGTGCCTAGG TCACCCACTA ACGCCCCAGG
601 CCTGGTCTTG GCTGGGCGTG ACTGTTACCC TCAAAAGCAG GCAGCTCCAG GGTAAAAGGT
661 GCCCTGCCCT GTAGAGCCCA CCTTCCTTCC CAGGGCTGCG GCTGGGTAGG TTTGTAGCCT
721 TCATCACGGG CCACCTCCAG CCACTGGACC GCTGGCCCCT GCCCTGTCCT GGGGAGTGTG
781 GTCCTGCGAC TTCTAAGTGG CCGCAAGCCA CCTGACTCCC CCAACACCAC ACTCTACCTC
841 TCAAGCCCAG GTCTCTCCCT AGTGACCCAC CCAGCACATT TAGCTAGCTG AGCCCCACAG
901 CCAGAGGTCC TCAGGCCCTG CTTTCAGGGC AGTTGCTCTG AAGTCGGCAA GGGGGAGTGA
961 CTGCCTGGCC ACTCCATGCC CTCCAAGAGC TCCTTCTGCA GGAGCGTACA GAACCCAGGG
1021 CCCTGGCACC CGTGCAGACC CTGGCCCACC CCACCTGGGC GCTCAGTGCC CAAGAGATGT
1081 CCACACCTAG GATGTCCCGC GGTGGGTGGG GGGCCCGAGA GACGGGCAGG CCGGGGGCAG
1141 GCCTGGCCAT GCGGGGCCGA ACCGGGCACT GCCCAGCGTG GGGCGCGGGG GCCACGGCGC
1201 GCGCCCCCAG CCCCCGGGCC CAGCACCCCA AGGCGGCCAA CGCCAAAACT CTCCCTCCTC
1261 CTCTTCCTCA ATCTCGCTCT CGCTCTTTTT TTTTTTCGCA AAAGGAGGGG AGAGGGGGTA
1321 AAAAAATGCT GCACTGTGCG GCGAAGCCGG TGAGTGAGCG GCGCGGGGCC AATCAGCGTG
1381 CGCCGTTCCG AAAGTTGCCT TTTATGGCTC GAGCGGCCGC GGCGGCGCCC TATAAAACCC
1441 AGCGGCGCGA CGCGCCACCA CCGCCGAGAC CGCGTCCGCC CCGCGAGCAC AGAGCCTCGC
1501 CTTTGCCGAT CCGCCGCCCG TCCACACCCG CCGCCAGGTA AGCCCGGCCA GCCGACCGGG
1561 GCAGGCGGCT CACGGCCCGG CCGCAGGCGG CCGCGGCCCC TTCGCCCGTG CAGAGCCGCC
1621 GTCTGGGCCG CAGCGGGGGG CGCATGGGGG GGGAACCGGA CCGCCGTGGG GGGCGCGGGA
1681 GAAGCCCCTG GGCCTCCGGA GATGGGGGAC ACCCCACGCC AGTTCGGAGG CGCGAGGCCG
1741 CGCTCGGGAG GCGCGCTCCG GGGGTGCCGC TCTCGGGGCG GGGGCAACCG GCGGGGTCTT
1801 TGTCTGAGCC GGGCTCTTGC CAATGGGGAT CGCAGGGTGG GCGCGGCGGA GCCCCCGCCA
1861 GGCCCGGTGG GGGCTGGGGC GCCATTGCGC GTGCGCGCTG GTCCTTTGGG CGCTAACTGC
1921 GTGCGCGCTG GGAATTGGCG CTAATTGCGC GTGCGCGCTG GGACTCAAGG CGCTAACTGC
1981 GCGTGCGTTC TGGGGCCCGG GGTGCCGCGG CCTGGGCTGG GGCGAAGGCG GGCTCGGCCG
2041 GAAGGGGTGG GGTCGCCGCG GCTCCCGGGC GCTTGCGCGC ACTTCCTGCC CGAGCCGCTG
2101 GCCGCCCGAG GGTGTGGCCG CTGCGTGCGC GCGCGCCGAC CCGGCGCTGT TTGAACCGGG
2161 CGGAGGCGGG GCTGGCGCCC GGTTGGGAGG GGGTTGGGGC CTGGCTTCCT GCCGCGCGCC
2221 GCGGGGACGC CTCCGACCAG TGTTTGCCTT TTATGGTAAT AACGCGGCCG GCCCGGCTTC
2281 CTTTGTCCCC AATCTGGGCG CGCGCCGGCG CCCCCTGGCG GCCTAAGGAC TCGGCGCGCC
2341 GGAAGTGGCC AGGGCGGGGG CGACCTCGGC TCACAGCGCG CCCGGCTATT CTCGCAGCTC
2401 ACC
(SEQ ID NO: 26).
Дополнительные примеры промоторов включают, не ограничиваясь перечисленными, промотор фактора элонгации 1-альфа (EFS) человека, ранний промотор SV40, промоторный длинный концевой повтор (LTR) вируса рака молочной железы мышей; аденовирусный основной поздний промотор (Ad MLP); промотор вируса простого герпеса (HSV), эндогенный клеточный промотор, гетерологичный для гена, представляющего интерес, цитомегаловирусный (CMV) промотор, такой как область немедленного раннего промотора CMV (CMVIE), промотор вируса саркомы Рауса (RSV), синтетические промоторы, гибридные промоторы и т.п.
Согласно некоторым вариантам реализации указанный 3′-UTR содержит полинуклеотид (элемент WPRE), последовательность которого по меньшей мере на 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентична SEQ ID NO: 27:
1 ATTCGAGCAT CTTACCGCCA TTTATTCCCA TATTTGTTCT GTTTTTCTTG ATTTGGGTAT
61 ACATTTAAAT GTTAATAAAA CAAAATGGTG GGGCAATCAT TTACATTTTT AGGGATATGT
121 AATTACTAGT TCAGGTGTAT TGCCACAAGA CAAACATGTT AAGAAACTTT CCCGTTATTT
181 ACGCTCTGTT CCTGTTAATC AACCTCTGGA TTACAAAATT TGTGAAAGAT TGACTGATAT
241 TCTTAACTAT GTTGCTCCTT TTACGCTGTG TGGATATGCT GCTTTAATGC CTCTGTATCA
301 TGCTATTGCT TCCCGTACGG CTTTCGTTTT CTCCTCCTTG TATAAATCCT GGTTGCTGTC
361 TCTTTATGAG GAGTTGTGGC CCGTTGTCCG TCAACGTGGC GTGGTGTGCT CTGTGTTTGC
421 TGACGCAACC CCCACTGGCT GGGGCATTGC CACCACCTGT CAACTCCTTT CTGGGACTTT
481 CGCTTTCCCC CTCCCGATCG CCACGGCAGA ACTCATCGCC GCCTGCCTTG CCCGCTGCTG
541 GACAGGGGCT AGGTTGCTGG GCACTGATAA TTCCGTGGTG TTGTCGGGGA AGGGCC
(SEQ ID NO: 27).
Согласно определенному варианту реализации последовательность указанной экспрессионной кассеты обладает по меньшей мере 95% идентичностью с последовательности, выбранной из SEQ ID NO: 8–10. Согласно варианту реализации последовательность указанной экспрессионной кассеты полностью идентична последовательности, выбранной из SEQ ID NO: 8–10, или по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98% или по меньшей мере на 99% идентична последовательности, выбранной из SEQ ID NO: 8–10:
1 CTGCGCGCTC GCTCGCTCAC TGAGGCCGCC CGGGCAAAGC CCGGGCGTCG GGCGACCTTT
61 GGTCGCCCGG CCTCAGTGAG CGAGCGAGCG CGCAGAGAGG GAGTGGCCAA CTCCATCACT
121 AGGGGTTCCT TGTAGTTAAT GATTAACCCG CCATGCTACT TATCTACCAG GGTAATGGGG
181 ATCCTCTAGA ACTATAGCTA GTCGACATTG ATTATTGACT AGTTATTAAT AGTAATCAAT
241 TACGGGGTCA TTAGTTCATA GCCCATATAT GGAGTTCCGC GTTACATAAC TTACGGTAAA
301 TGGCCCGCCT GGCTGACCGC CCAACGACCC CCGCCCATTG ACGTCAATAA TGACGTATGT
361 TCCCATAGTA ACGCCAATAG GGACTTTCCA TTGACGTCAA TGGGTGGAGT ATTTACGGTA
421 AACTGCCCAC TTGGCAGTAC ATCAAGTGTA TCATATGCCA AGTACGCCCC CTATTGACGT
481 CAATGACGGT AAATGGCCCG CCTGGCATTA TGCCCAGTAC ATGACCTTAT GGGACTTTCC
541 TACTTGGCAG TACATCTACG TATTAGTCAT CGCTATTACC ATGGTCGAGG TGAGCCCCAC
601 GTTCTGCTTC ACTCTCCCCA TCTCCCCCCC CTCCCCACCC CCAATTTTGT ATTTATTTAT
661 TTTTTAATTA TTTTGTGCAG CGATGGGGGC GGGGGGGGGG GGGGGGCGCG CGCCAGGCGG
721 GGCGGGGCGG GGCGAGGGGC GGGGCGGGGC GAGGCGGAGA GGTGCGGCGG CAGCCAATCA
781 GAGCGGCGCG CTCCGAAAGT TTCCTTTTAT GGCGAGGCGG CGGCGGCGGC GGCCCTATAA
841 AAAGCGAAGC GCGCGGCGGG CGGGAGTCGC TGCGCGCTGC CTTCGCCCCG TGCCCCGCTC
901 CGCCGCCGCC TCGCGCCGCC CGCCCCGGCT CTGACTGACC GCGTTACTCC CACAGGTGAG
961 CGGGCGGGAC GGCCCTTCTC CTCCGGGCTG TAATTAGCGC TTGGTTTAAT GACGGCTTGT
1021 TTCTTTTCTG TGGCTGCGTG AAAGCCTTGA GGGGCTCCGG GAGGGCCCTT TGTGCGGGGG
1081 GAGCGGCTCG GGGGGTGCGT GCGTGTGTGT GTGCGTGGGG AGCGCCGCGT GCGGCTCCGC
1141 GCTGCCCGGC GGCTGTGAGC GCTGCGGGCG CGGCGCGGGG CTTTGTGCGC TCCGCAGTGT
1201 GCGCGAGGGG AGCGCGGCCG GGGGCGGTGC CCCGCGGTGC GGGGGGGGCT GCGAGGGGAA
1261 CAAAGGCTGC GTGCGGGGTG TGTGCGTGGG GGGGTGAGCA GGGGGTGTGG GCGCGTCGGT
1321 CGGGCTGCAA CCCCCCCTGC ACCCCCCTCC CCGAGTTGCT GAGCACGGCC CGGCTTCGGG
1381 TGCGGGGCTC CGTACGGGGC GTGGCGCGGG GCTCGCCGTG CCGGGCGGGG GGTGGCGGCA
1441 GGTGGGGGTG CCGGGCGGGG CGGGGCCGCC TCGGGCCGGG GAGGGCTCGG GGGAGGGGCG
1501 CGGCGGCCCC CGGAGCGCCG GCGGCTGTCG AGGCGCGGCG AGCCGCAGCC ATTGCCTTTT
1561 ATGGTAATCG TGCGAGAGGG CGCAGGGACT TCCTTTGTCC CAAATCTGTG CGGAGCCGAA
1621 ATCTGGGAGG CGCCGCCGCA CCCCCTCTAG CGGGCGCGGG GCGAAGCGGT GCGGCGCCGG
1681 CAGGAAGGAA ATGGGCGGGG AGGGCCTTCG TGCGTCGCCG CGCCGCCGTC CCCTTCTCCC
1741 TCTCCAGCCT CGGGGCTGTC CGCGGGGGGA CGGCTGCCTT CGGGGGGGAC GGGGCAGGGC
1801 GGGGTTCGGC TTCTGGCGTG TGACCGGCGG CTCTAGAGCC TCTGCTAACC ATGTTCATGC
1861 CTTCTTCTTT TTCCTACAGC TCCTGGGCAA CGTGCTGGTT ATTGTGCTGT CTCATCATTT
1921 TGGCAAAGAA TTCGAGCGGC CGCCAGCCGC CACCATGGTC TGCTTCAGAC TGTTCCCTGT
1981 CCCTGGATCT GGTCTGGTGC TTGTGTGCTT GGTGCTGGGT GCTGTGAGAT CCTATGCCCT
2041 TGAGCTGAAC CTGACTGACT CAGAAAATGC CACTTGCCTG TATGCCAAGT GGCAGATGAA
2101 CTTCACTGTG AGATATGAGA CTACCAACAA GACCTACAAG ACTGTGACCA TCTCAGACCA
2161 TGGCACTGTC ACCTACAATG GATCAATCTG TGGTGATGAT CAGAATGGCC CAAAGATAGC
2221 AGTGCAGTTT GGGCCCGGTT TTTCCTGGAT TGCTAACTTC ACCAAGGCAG CCTCCACCTA
2281 CAGCATTGAC TCAGTCAGCT TCAGCTACAA CACTGGGGAT AACACCACCT TCCCTGACGC
2341 AGAGGACAAG GGAATCCTTA CTGTGGACGA ACTCCTGGCA ATCAGAATCC CCCTTAACGA
2401 CCTGTTCAGA TGCAACTCCC TTTCAACCCT TGAAAAGAAT GATGTGGTGC AACACTATTG
2461 GGACGTCCTG GTGCAAGCCT TTGTGCAGAA TGGGACAGTG AGTACCAACG AGTTCCTCTG
2521 TGACAAGGAC AAGACCAGCA CTGTGGCCCC CACTATCCAC ACCACTGTGC CCAGCCCTAC
2581 CACTACCCCC ACCCCTAAAG AGAAGCCAGA AGCTGGAACC TACTCAGTCA ACAATGGAAA
2641 TGACACATGC CTCCTTGCCA CCATGGGACT GCAGCTGAAC ATCACTCAGG ACAAGGTGGC
2701 CTCAGTGATT AACATCAACC CTAACACCAC TCATAGCACT GGGAGCTGCA GATCACATAC
2761 AGCTCTGCTG AGGCTCAACT CCTCCACCAT CAAGTACCTG GACTTTGTGT TTGCTGTGAA
2821 GAATGAGAAC AGGTTCTACC TCAAGGAAGT GAACATTTCC ATGTACCTGG TCAATGGTTC
2881 AGTGTTCTCT ATTGCCAACA ACAATCTGAG CTACTGGGAT GCACCCCTGG GATCCTCCTA
2941 CATGTGCAAC AAGGAGCAGA CTGTGAGTGT GTCAGGTGCT TTTCAGATCA ACACTTTTGA
3001 CCTGAGGGTG CAGCCCTTCA ATGTGACTCA GGGAAAGTAC TCCACTGCAC AAGAGTGTTC
3061 CTTGGATGAT GACACTATCC TCATCCCCAT TATTGTGGGA GCTGGACTGT CAGGATTGAT
3121 TATAGTGATT GTGATTGCTT ATGTGATTGG AAGGAGAAAG AGCTATGCTG GCTACCAGAC
3181 CCTGTAAAAG GGCGAATTCC AGCACACGCG TCCTAGGAGC TCGAGTACTA CTGGCGGCCG
3241 TTACTAGTGG ATCCGCGGTA CAAGTAAGCA TGCAAGCTTC GAGGACGGGG TGAACTACGC
3301 CTGAATCAAG CTTATCGATA AATTCGAGCA TCTTACCGCC ATTTATTCCC ATATTTGTTC
3361 TGTTTTTCTT GATTTGGGTA TACATTTAAA TGTTAATAAA ACAAAATGGT GGGGCAATCA
3421 TTTACATTTT TAGGGATATG TAATTACTAG TTCAGGTGTA TTGCCACAAG ACAAACATGT
3481 TAAGAAACTT TCCCGTTATT TACGCTCTGT TCCTGTTAAT CAACCTCTGG ATTACAAAAT
3541 TTGTGAAAGA TTGACTGATA TTCTTAACTA TGTTGCTCCT TTTACGCTGT GTGGATATGC
3601 TGCTTTAATG CCTCTGTATC ATGCTATTGC TTCCCGTACG GCTTTCGTTT TCTCCTCCTT
3661 GTATAAATCC TGGTTGCTGT CTCTTTATGA GGAGTTGTGG CCCGTTGTCC GTCAACGTGG
3721 CGTGGTGTGC TCTGTGTTTG CTGACGCAAC CCCCACTGGC TGGGGCATTG CCACCACCTG
3781 TCAACTCCTT TCTGGGACTT TCGCTTTCCC CCTCCCGATC GCCACGGCAG AACTCATCGC
3841 CGCCTGCCTT GCCCGCTGCT GGACAGGGGC TAGGTTGCTG GGCACTGATA ATTCCGTGGT
3901 GTTGTCGGGG AAGGGCCTCG ATACCGTCGA TATCGATCCT GGCTAATAAA GGAAATTTAT
3961 TTTCATTGCA ATAGTGTGTT GGAATTTTTT GTGTCTCTCA CTCGGAAGGA CATATGGGAG
4021 GGCAAATCAT TTAAAACATC AGAATGAGTA TTTGGTTTAG AGTTTGGCAA CATATGCCCA
4081 TATGCTGGCT GCCATGAACA AAGGTTGGCT ATAAAGAGGT CATCAGTATA TGAAACAGCC
4141 CCCTGCTGTC CATTCCTTAT TCCATAGAAA AGCCTTGACT TGAGGTTAGA TTTTTTTTAT
4201 ATTTTGTTTT GTGTTATTTT TTTCTTTAAC ATCCCTAAAA TTTTCCTTAC ATGTTTTACT
4261 AGCCAGATTT TTCCTCCTCT CCTGACTACT CCCAGTCATA GCTGTCCCTC TTCTCTTATG
4321 GAGATCGAAG CAATTCGTTG ATCTGAATTT CGACCACCCA TAATAGATCT CCCATTACCC
4381 TGGTAGATAA GTAGCATGGC GGGTTAATCA TTAACTACAA GGAACCCCTA GTGATGGAGT
4441 TGGCCACTCC CTCTCTGCGC GCTCGCTCGC TCACTGAGGC CGGGCGACCA AAGGTCGCCC
4501 GACGCCCGGG CTTTGCCCGG GCGGCCTCAG TGAGCGAGCG AGCGCGCAG
(SEQ ID NO: 8);
1 CTGCGCGCTC GCTCGCTCAC TGAGGCCGCC CGGGCAAAGC CCGGGCGTCG GGCGACCTTT
61 GGTCGCCCGG CCTCAGTGAG CGAGCGAGCG CGCAGAGAGG GAGTGGCCAA CTCCATCACT
121 AGGGGTTCCT TGTAGTTAAT GATTAACCCG CCATGCTACT TATCTACCAG GGTAATGGGG
181 ATCCTCTAGA ACTATAGCTA GTCGACATTG ATTATTGACT AGTTATTAAT AGTAATCAAT
241 TACGGGGTCA TTAGTTCATA GCCCATATAT GGAGTTCCGC GTTACATAAC TTACGGTAAA
301 TGGCCCGCCT GGCTGACCGC CCAACGACCC CCGCCCATTG ACGTCAATAA TGACGTATGT
361 TCCCATAGTA ACGCCAATAG GGACTTTCCA TTGACGTCAA TGGGTGGAGT ATTTACGGTA
421 AACTGCCCAC TTGGCAGTAC ATCAAGTGTA TCATATGCCA AGTACGCCCC CTATTGACGT
481 CAATGACGGT AAATGGCCCG CCTGGCATTA TGCCCAGTAC ATGACCTTAT GGGACTTTCC
541 TACTTGGCAG TACATCTACG TATTAGTCAT CGCTATTACC ATGGTCGAGG TGAGCCCCAC
601 GTTCTGCTTC ACTCTCCCCA TCTCCCCCCC CTCCCCACCC CCAATTTTGT ATTTATTTAT
661 TTTTTAATTA TTTTGTGCAG CGATGGGGGC GGGGGGGGGG GGGGGGCGCG CGCCAGGCGG
721 GGCGGGGCGG GGCGAGGGGC GGGGCGGGGC GAGGCGGAGA GGTGCGGCGG CAGCCAATCA
781 GAGCGGCGCG CTCCGAAAGT TTCCTTTTAT GGCGAGGCGG CGGCGGCGGC GGCCCTATAA
841 AAAGCGAAGC GCGCGGCGGG CGGGAGTCGC TGCGCGCTGC CTTCGCCCCG TGCCCCGCTC
901 CGCCGCCGCC TCGCGCCGCC CGCCCCGGCT CTGACTGACC GCGTTACTCC CACAGGTGAG
961 CGGGCGGGAC GGCCCTTCTC CTCCGGGCTG TAATTAGCGC TTGGTTTAAT GACGGCTTGT
1021 TTCTTTTCTG TGGCTGCGTG AAAGCCTTGA GGGGCTCCGG GAGGGCCCTT TGTGCGGGGG
1081 GAGCGGCTCG GGGGGTGCGT GCGTGTGTGT GTGCGTGGGG AGCGCCGCGT GCGGCTCCGC
1141 GCTGCCCGGC GGCTGTGAGC GCTGCGGGCG CGGCGCGGGG CTTTGTGCGC TCCGCAGTGT
1201 GCGCGAGGGG AGCGCGGCCG GGGGCGGTGC CCCGCGGTGC GGGGGGGGCT GCGAGGGGAA
1261 CAAAGGCTGC GTGCGGGGTG TGTGCGTGGG GGGGTGAGCA GGGGGTGTGG GCGCGTCGGT
1321 CGGGCTGCAA CCCCCCCTGC ACCCCCCTCC CCGAGTTGCT GAGCACGGCC CGGCTTCGGG
1381 TGCGGGGCTC CGTACGGGGC GTGGCGCGGG GCTCGCCGTG CCGGGCGGGG GGTGGCGGCA
1441 GGTGGGGGTG CCGGGCGGGG CGGGGCCGCC TCGGGCCGGG GAGGGCTCGG GGGAGGGGCG
1501 CGGCGGCCCC CGGAGCGCCG GCGGCTGTCG AGGCGCGGCG AGCCGCAGCC ATTGCCTTTT
1561 ATGGTAATCG TGCGAGAGGG CGCAGGGACT TCCTTTGTCC CAAATCTGTG CGGAGCCGAA
1621 ATCTGGGAGG CGCCGCCGCA CCCCCTCTAG CGGGCGCGGG GCGAAGCGGT GCGGCGCCGG
1681 CAGGAAGGAA ATGGGCGGGG AGGGCCTTCG TGCGTCGCCG CGCCGCCGTC CCCTTCTCCC
1741 TCTCCAGCCT CGGGGCTGTC CGCGGGGGGA CGGCTGCCTT CGGGGGGGAC GGGGCAGGGC
1801 GGGGTTCGGC TTCTGGCGTG TGACCGGCGG CTCTAGAGCC TCTGCTAACC ATGTTCATGC
1861 CTTCTTCTTT TTCCTACAGC TCCTGGGCAA CGTGCTGGTT ATTGTGCTGT CTCATCATTT
1921 TGGCAAAGAA TTCGAGCGGC CGCCAGCCGC CACCATGGTG TGCTTTAGAC TGTTTCCTGT
1981 GCCTGGTTCA GGGCTGGTCC TGGTCTGTCT GGTGCTGGGG GCTGTCAGAA GCTATGCCTT
2041 GGAGCTGAAC CTCACTGATA GTGAAAATGC CACTTGTCTG TATGCTAAGT GGCAGATGAA
2101 CTTCACTGTG AGATATGAAA CCACCAACAA GACTTACAAA ACAGTGACCA TCTCAGATCA
2161 TGGAACTGTG ACCTACAACG GCAGCATTTG TGGAGACGAC CAGAACGGAC CAAAAATCGC
2221 TGTCCAATTT GGGCCTGGAT TCTCCTGGAT TGCCAATTTC ACTAAAGCTG CCTCCACATA
2281 TTCAATTGAC TCAGTGTCCT TCTCCTACAA CACTGGGGAC AACACTACTT TCCCTGATGC
2341 TGAAGATAAG GGAATCTTGA CAGTGGATGA GCTGCTGGCT ATCAGGATCC CTTTGAATGA
2401 CCTGTTTAGG TGTAATTCAC TGAGCACTCT GGAGAAGAAC GACGTGGTGC AGCACTACTG
2461 GGACGTGCTG GTGCAGGCCT TTGTGCAGAA CGGCACTGTG TCCACCAACG AATTCCTGTG
2521 TGATAAGGAC AAAACTTCCA CTGTGGCACC TACAATTCAC ACTACTGTGC CTTCACCTAC
2581 CACCACTCCA ACTCCAAAGG AAAAGCCTGA AGCAGGAACC TACTCTGTGA ACAATGGCAA
2641 TGATACCTGT CTGTTGGCCA CCATGGGCCT CCAACTGAAC ATTACTCAGG ACAAGGTGGC
2701 CTCAGTGATT AACATTAACC CCAACACTAC CCACTCCACT GGCAGCTGTA GATCACACAC
2761 AGCCTTGCTC AGACTGAATA GCAGCACCAT CAAGTATTTG GATTTTGTGT TTGCAGTGAA
2821 GAATGAAAAC AGGTTCTACC TGAAGGAAGT CAACATCTCA ATGTACCTGG TGAACGGCTC
2881 AGTGTTCAGC ATTGCCAACA ACAACCTCTC CTATTGGGAC GCTCCACTGG GGAGCAGCTA
2941 CATGTGTAAC AAGGAACAGA CTGTGTCAGT GTCAGGAGCC TTCCAGATTA ACACCTTTGA
3001 TCTGAGGGTC CAACCCTTTA ATGTCACTCA AGGAAAGTAT AGCACTGCCC AGGAGTGCTC
3061 CCTGGATGAT GACACCATTC TGATTCCAAT CATTGTGGGT GCAGGACTTT CTGGGCTTAT
3121 TATTGTGATT GTGATTGCCT ATGTGATTGG CAGAAGGAAA TCCTATGCAG GGTACCAAAC
3181 TCTGTAAAAG GGCGAATTCC AGCACACGCG TCCTAGGAGC TCGAGTACTA CTGGCGGCCG
3241 TTACTAGTGG ATCCGCGGTA CAAGTAAGCA TGCAAGCTTC GAGGACGGGG TGAACTACGC
3301 CTGAATCAAG CTTATCGATA AATTCGAGCA TCTTACCGCC ATTTATTCCC ATATTTGTTC
3361 TGTTTTTCTT GATTTGGGTA TACATTTAAA TGTTAATAAA ACAAAATGGT GGGGCAATCA
3421 TTTACATTTT TAGGGATATG TAATTACTAG TTCAGGTGTA TTGCCACAAG ACAAACATGT
3481 TAAGAAACTT TCCCGTTATT TACGCTCTGT TCCTGTTAAT CAACCTCTGG ATTACAAAAT
3541 TTGTGAAAGA TTGACTGATA TTCTTAACTA TGTTGCTCCT TTTACGCTGT GTGGATATGC
3601 TGCTTTAATG CCTCTGTATC ATGCTATTGC TTCCCGTACG GCTTTCGTTT TCTCCTCCTT
3661 GTATAAATCC TGGTTGCTGT CTCTTTATGA GGAGTTGTGG CCCGTTGTCC GTCAACGTGG
3721 CGTGGTGTGC TCTGTGTTTG CTGACGCAAC CCCCACTGGC TGGGGCATTG CCACCACCTG
3781 TCAACTCCTT TCTGGGACTT TCGCTTTCCC CCTCCCGATC GCCACGGCAG AACTCATCGC
3841 CGCCTGCCTT GCCCGCTGCT GGACAGGGGC TAGGTTGCTG GGCACTGATA ATTCCGTGGT
3901 GTTGTCGGGG AAGGGCCTCG ATACCGTCGA TATCGATCCT GGCTAATAAA GGAAATTTAT
3961 TTTCATTGCA ATAGTGTGTT GGAATTTTTT GTGTCTCTCA CTCGGAAGGA CATATGGGAG
4021 GGCAAATCAT TTAAAACATC AGAATGAGTA TTTGGTTTAG AGTTTGGCAA CATATGCCCA
4081 TATGCTGGCT GCCATGAACA AAGGTTGGCT ATAAAGAGGT CATCAGTATA TGAAACAGCC
4141 CCCTGCTGTC CATTCCTTAT TCCATAGAAA AGCCTTGACT TGAGGTTAGA TTTTTTTTAT
4201 ATTTTGTTTT GTGTTATTTT TTTCTTTAAC ATCCCTAAAA TTTTCCTTAC ATGTTTTACT
4261 AGCCAGATTT TTCCTCCTCT CCTGACTACT CCCAGTCATA GCTGTCCCTC TTCTCTTATG
4321 GAGATCGAAG CAATTCGTTG ATCTGAATTT CGACCACCCA TAATAGATCT CCCATTACCC
4381 TGGTAGATAA GTAGCATGGC GGGTTAATCA TTAACTACAA GGAACCCCTA GTGATGGAGT
4441 TGGCCACTCC CTCTCTGCGC GCTCGCTCGC TCACTGAGGC CGGGCGACCA AAGGTCGCCC
4501 GACGCCCGGG CTTTGCCCGG GCGGCCTCAG TGAGCGAGCG AGCGCGCAG
(SEQ ID NO: 9); и
1 CTGCGCGCTC GCTCGCTCAC TGAGGCCGCC CGGGCAAAGC CCGGGCGTCG GGCGACCTTT
61 GGTCGCCCGG CCTCAGTGAG CGAGCGAGCG CGCAGAGAGG GAGTGGCCAA CTCCATCACT
121 AGGGGTTCCT TGTAGTTAAT GATTAACCCG CCATGCTACT TATCTACCAG GGTAATGGGG
181 ATCCTCTAGA ACTATAGCTA GTCGACATTG ATTATTGACT AGTTATTAAT AGTAATCAAT
241 TACGGGGTCA TTAGTTCATA GCCCATATAT GGAGTTCCGC GTTACATAAC TTACGGTAAA
301 TGGCCCGCCT GGCTGACCGC CCAACGACCC CCGCCCATTG ACGTCAATAA TGACGTATGT
361 TCCCATAGTA ACGCCAATAG GGACTTTCCA TTGACGTCAA TGGGTGGAGT ATTTACGGTA
421 AACTGCCCAC TTGGCAGTAC ATCAAGTGTA TCATATGCCA AGTACGCCCC CTATTGACGT
481 CAATGACGGT AAATGGCCCG CCTGGCATTA TGCCCAGTAC ATGACCTTAT GGGACTTTCC
541 TACTTGGCAG TACATCTACG TATTAGTCAT CGCTATTACC ATGGTCGAGG TGAGCCCCAC
601 GTTCTGCTTC ACTCTCCCCA TCTCCCCCCC CTCCCCACCC CCAATTTTGT ATTTATTTAT
661 TTTTTAATTA TTTTGTGCAG CGATGGGGGC GGGGGGGGGG GGGGGGCGCG CGCCAGGCGG
721 GGCGGGGCGG GGCGAGGGGC GGGGCGGGGC GAGGCGGAGA GGTGCGGCGG CAGCCAATCA
781 GAGCGGCGCG CTCCGAAAGT TTCCTTTTAT GGCGAGGCGG CGGCGGCGGC GGCCCTATAA
841 AAAGCGAAGC GCGCGGCGGG CGGGAGTCGC TGCGCGCTGC CTTCGCCCCG TGCCCCGCTC
901 CGCCGCCGCC TCGCGCCGCC CGCCCCGGCT CTGACTGACC GCGTTACTCC CACAGGTGAG
961 CGGGCGGGAC GGCCCTTCTC CTCCGGGCTG TAATTAGCGC TTGGTTTAAT GACGGCTTGT
1021 TTCTTTTCTG TGGCTGCGTG AAAGCCTTGA GGGGCTCCGG GAGGGCCCTT TGTGCGGGGG
1081 GAGCGGCTCG GGGGGTGCGT GCGTGTGTGT GTGCGTGGGG AGCGCCGCGT GCGGCTCCGC
1141 GCTGCCCGGC GGCTGTGAGC GCTGCGGGCG CGGCGCGGGG CTTTGTGCGC TCCGCAGTGT
1201 GCGCGAGGGG AGCGCGGCCG GGGGCGGTGC CCCGCGGTGC GGGGGGGGCT GCGAGGGGAA
1261 CAAAGGCTGC GTGCGGGGTG TGTGCGTGGG GGGGTGAGCA GGGGGTGTGG GCGCGTCGGT
1321 CGGGCTGCAA CCCCCCCTGC ACCCCCCTCC CCGAGTTGCT GAGCACGGCC CGGCTTCGGG
1381 TGCGGGGCTC CGTACGGGGC GTGGCGCGGG GCTCGCCGTG CCGGGCGGGG GGTGGCGGCA
1441 GGTGGGGGTG CCGGGCGGGG CGGGGCCGCC TCGGGCCGGG GAGGGCTCGG GGGAGGGGCG
1501 CGGCGGCCCC CGGAGCGCCG GCGGCTGTCG AGGCGCGGCG AGCCGCAGCC ATTGCCTTTT
1561 ATGGTAATCG TGCGAGAGGG CGCAGGGACT TCCTTTGTCC CAAATCTGTG CGGAGCCGAA
1621 ATCTGGGAGG CGCCGCCGCA CCCCCTCTAG CGGGCGCGGG GCGAAGCGGT GCGGCGCCGG
1681 CAGGAAGGAA ATGGGCGGGG AGGGCCTTCG TGCGTCGCCG CGCCGCCGTC CCCTTCTCCC
1741 TCTCCAGCCT CGGGGCTGTC CGCGGGGGGA CGGCTGCCTT CGGGGGGGAC GGGGCAGGGC
1801 GGGGTTCGGC TTCTGGCGTG TGACCGGCGG CTCTAGAGCC TCTGCTAACC ATGTTCATGC
1861 CTTCTTCTTT TTCCTACAGC TCCTGGGCAA CGTGCTGGTT ATTGTGCTGT CTCATCATTT
1921 TGGCAAAGAA TTCGAGCGGC CGCCAGCCGC CACCATGGTC TGTTTTAGGC TGTTCCCTGT
1981 CCCTGGTTCA GGACTGGTCT TAGTGTGTCT GGTGCTTGGA GCTGTCAGAA GCTATGCCCT
2041 GGAGCTGAAC CTGACTGACT CAGAAAATGC CACTTGCCTG TATGCCAAGT GGCAGATGAA
2101 CTTCACTGTC AGATATGAAA CCACCAACAA GACCTATAAG ACTGTGACCA TCTCAGACCA
2161 TGGCACTGTG ACTTACAATG GGTCAATTTG TGGAGATGAC CAGAATGGCC CTAAGATAGC
2221 TGTCCAGTTT GGTCCAGGAT TCAGCTGGAT TGCCAACTTC ACCAAGGCAG CCAGCACCTA
2281 CAGCATTGAC TCTGTGTCCT TCTCCTACAA CACAGGAGAC AACACCACTT TCCCTGATGC
2341 AGAGGACAAA GGTATCCTGA CTGTGGATGA GTTGCTGGCA ATCAGGATCC CACTGAACGA
2401 TCTGTTCAGG TGCAACTCAC TGTCCACTCT GGAAAAGAAT GATGTGGTGC AGCACTATTG
2461 GGATGTGCTA GTCCAGGCCT TTGTCCAGAA TGGGACTGTG TCAACTAATG AGTTCCTGTG
2521 TGACAAGGAC AAGACAAGCA CTGTAGCCCC CACTATCCAT ACCACAGTAC CTAGCCCCAC
2581 CACTACTCCA ACCCCCAAGG AGAAGCCTGA GGCTGGCACC TACTCAGTGA ACAATGGGAA
2641 TGACACCTGT TTGCTGGCCA CTATGGGACT CCAACTGAAC ATCACCCAGG ACAAAGTGGC
2701 CTCTGTGATC AATATCAATC CCAACACCAC CCACAGCACT GGGTCCTGCA GAAGCCACAC
2761 TGCCCTCCTG AGGCTCAACT CATCAACTAT CAAGTACTTG GATTTTGTGT TTGCAGTGAA
2821 GAATGAGAAC AGATTCTACC TCAAAGAGGT CAACATTTCA ATGTACCTGG TGAATGGGAG
2881 TGTGTTCTCC ATTGCTAACA ACAACCTGAG CTACTGGGAT GCCCCTCTGG GCTCCTCATA
2941 CATGTGCAAC AAGGAACAGA CTGTGAGTGT GTCAGGGGCC TTCCAGATCA ACACTTTTGA
3001 CCTGAGAGTG CAGCCCTTTA ATGTGACACA GGGAAAGTAC AGCACTGCTC AGGAGTGCAG
3061 CCTGGATGAT GACACTATCC TGATCCCTAT CATTGTGGGG GCAGGCCTGT CTGGACTCAT
3121 TATTGTGATT GTGATTGCCT ATGTGATAGG GAGAAGGAAG TCTTATGCTG GATACCAGAC
3181 CCTGTAAAAG GGCGAATTCC AGCACACGCG TCCTAGGAGC TCGAGTACTA CTGGCGGCCG
3241 TTACTAGTGG ATCCGCGGTA CAAGTAAGCA TGCAAGCTTC GAGGACGGGG TGAACTACGC
3301 CTGAATCAAG CTTATCGATA AATTCGAGCA TCTTACCGCC ATTTATTCCC ATATTTGTTC
3361 TGTTTTTCTT GATTTGGGTA TACATTTAAA TGTTAATAAA ACAAAATGGT GGGGCAATCA
3421 TTTACATTTT TAGGGATATG TAATTACTAG TTCAGGTGTA TTGCCACAAG ACAAACATGT
3481 TAAGAAACTT TCCCGTTATT TACGCTCTGT TCCTGTTAAT CAACCTCTGG ATTACAAAAT
3541 TTGTGAAAGA TTGACTGATA TTCTTAACTA TGTTGCTCCT TTTACGCTGT GTGGATATGC
3601 TGCTTTAATG CCTCTGTATC ATGCTATTGC TTCCCGTACG GCTTTCGTTT TCTCCTCCTT
3661 GTATAAATCC TGGTTGCTGT CTCTTTATGA GGAGTTGTGG CCCGTTGTCC GTCAACGTGG
3721 CGTGGTGTGC TCTGTGTTTG CTGACGCAAC CCCCACTGGC TGGGGCATTG CCACCACCTG
3781 TCAACTCCTT TCTGGGACTT TCGCTTTCCC CCTCCCGATC GCCACGGCAG AACTCATCGC
3841 CGCCTGCCTT GCCCGCTGCT GGACAGGGGC TAGGTTGCTG GGCACTGATA ATTCCGTGGT
3901 GTTGTCGGGG AAGGGCCTCG ATACCGTCGA TATCGATCCT GGCTAATAAA GGAAATTTAT
3961 TTTCATTGCA ATAGTGTGTT GGAATTTTTT GTGTCTCTCA CTCGGAAGGA CATATGGGAG
4021 GGCAAATCAT TTAAAACATC AGAATGAGTA TTTGGTTTAG AGTTTGGCAA CATATGCCCA
4081 TATGCTGGCT GCCATGAACA AAGGTTGGCT ATAAAGAGGT CATCAGTATA TGAAACAGCC
4141 CCCTGCTGTC CATTCCTTAT TCCATAGAAA AGCCTTGACT TGAGGTTAGA TTTTTTTTAT
4201 ATTTTGTTTT GTGTTATTTT TTTCTTTAAC ATCCCTAAAA TTTTCCTTAC ATGTTTTACT
4261 AGCCAGATTT TTCCTCCTCT CCTGACTACT CCCAGTCATA GCTGTCCCTC TTCTCTTATG
4321 GAGATCGAAG CAATTCGTTG ATCTGAATTT CGACCACCCA TAATAGATCT CCCATTACCC
4381 TGGTAGATAA GTAGCATGGC GGGTTAATCA TTAACTACAA GGAACCCCTA GTGATGGAGT
4441 TGGCCACTCC CTCTCTGCGC GCTCGCTCGC TCACTGAGGC CGGGCGACCA AAGGTCGCCC
4501 GACGCCCGGG CTTTGCCCGG GCGGCCTCAG TGAGCGAGCG AGCGCGCAG
(SEQ ID NO: 10).
Согласно некоторым вариантам реализации указанная экспрессионная кассета содержит одну или более модификаций по сравнению с последовательностью, выбранной из SEQ ID NO: 8–10, в том числе любые из модификаций согласно описанию в настоящем документе, но не ограничиваясь ими. Согласно конкретным вариантам реализации указанные одна или более модификаций включают что-либо одно или более из: удаления одной или более (например, всех) расположенных в направлении 5’ последовательностей ATG, замены последовательности Козак оптимизированной консенсусной последовательностью Козак или другой последовательностью Козак, в том числе, но не ограничиваясь перечисленными, любой из описанных в настоящем документе, и/или замены последовательности полиаденилирования полноразмерной последовательностью полиаденилирования или другой последовательностью полиаденилирования, в том числе любой из описанных в настоящем документе, но не ограничиваясь ими. Иллюстративная конфигурация генетических элементов согласно указанным примерам экспрессионных кассет представлена на фиг. 1B.
Согласно варианту реализации указанный вектор представляет собой аденоассоциированный вирусный (AAV) вектор. Согласно варианту реализации указанная экспрессионная кассета содержит последовательности инвертированных концевых повторов (ITR), выбранные из SEQ ID NO: 11 и 12:
1 CTGCGCGCTC GCTCGCTCAC TGAGGCCGCC CGGGCAAAGC CCGGGCGTCG GGCGACCTTT
61 GGTCGCCCGG CCTCAGTGAG CGAGCGAGCG CGCAGAGAGG GAGTGGCCAA CTCCATCACT
121 AGGGGTTCCT
(SEQ ID NO: 11);
1 AGGAACCCCT AGTGATGGAG TTGGCCACTC CCTCTCTGCG CGCTCGCTCG CTCACTGAGG
61 CCGGGCGACC AAAGGTCGCC CGACGCCCGG GCTTTGCCCG GGCGGCCTCA GTGAGCGAGC
121 GAGCGCGCAG
(SEQ ID NO: 12).
Согласно родственным вариантам реализации настоящего изобретения предложены геннотерапевтические векторы, содержащие экспрессионную кассету согласно описанию в настоящем документе. В общем случае геннотерапевтические векторы, описанные в настоящем документе, содержат экспрессионную кассету, содержащую полинуклеотид, кодирующий одну или более изоформ ассоциированного с лизосомами мембранного белка 2 (LAMP-2), и позволяют обеспечить экспрессию LAMP-2 для частичной или полной коррекции недостаточности уровней экспрессии белка LAMP-2 и/или аутофагического потока у нуждающегося в этом субъекта (например, субъекта с болезнью Данона или другим нарушением , характеризующимся недостаточностью аутофагического потока, по меньшей мере отчасти обусловленной недостаточной экспрессией LAMP-2). Согласно конкретным вариантам реализации указанная экспрессионная кассета содержит полинуклеотидную последовательность, кодирующую LAMP-2 согласно описанию в настоящем документе, например, SEQ ID NO: 3–5 или ее функциональный вариант. Согласно некоторым вариантам реализации указанный вариант последовательности по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98% или по меньшей мере на 99% идентичен любой из SEQ ID NO: 3–5. Согласно некоторым вариантам реализации указанный вариант представляет собой фрагмент любой из SEQ ID NO: 3–5, например, фрагмент, по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или по меньшей мере на 95% идентичный последовательности любой из SEQ ID No: 3–5. Указанные геннотерапевтические векторы могут представлять собой вирусные или невирусные векторы. Иллюстративные невирусные векторы включают, например, депротеинизированную ДНК, катионные липосомальные комплексы, катионные полимерные комплексы, катионные липосомально-полимерные комплексы и экзосомы. Примеры вирусных векторов включают, не ограничиваясь перечисленными, аденовирусные, ретровирусные, лентивирусные, герпесвирусные векторы и векторы на основе аденоассоциированного вируса (AAV).
Согласно некоторым вариантам реализации указанный вирусный вектор представляет собой AAV-вектор. AAV представляет собой однонитевой ДНК-вирус размером 4,7 т.п.о. Рекомбинантные векторы на основе AAV были ассоциированы с очень хорошим уровнем клинической безопасности, поскольку AAV дикого типа не является патогенным и не был этиологически связан с какими-либо известными заболеваниями. Кроме того, AAV обеспечивает возможность высокоэффективной доставки генов и продолжительной экспрессии трансгена в многочисленных тканях. Под «AAV-вектором» подразумевается вектор, происходящий из серотипа аденоассоциированного вируса, в том числе, без ограничений, AAV1, AAV2, AAV3, AAV4, AAV5, AAV6, AAV7, AAV8, AAV9, AAV10, AAVrh.10, AAVrh.74 и т.п. В AAV-векторах может быть частично или полностью делетирован один или более из генов AAV дикого типа, например, гены rep и/или cap, при сохранении последовательностей функциональных фланкирующих инвертированных концевых повторов (ITR). Функциональные последовательности ITR необходимы для «спасения», репликации и упаковки вириона AAV. Соответственно, AAV-вектор в настоящем документе определен как включающий по меньшей мере требуемые последовательности в цис-положении для репликации и упаковки (например, функциональный ITR) вируса. Указанные ITR не обязательно должны представлять собой последовательности нуклеотидов дикого типа и могут быть изменены, например, путем инсерции, делеции или замены нуклеотидов, при условии, что указанные последовательности обеспечивают функциональные «спасение», репликацию и упаковку. AAV-векторы могут содержать другие модификации, в том числе, но не ограничиваясь указанным, один или более модифицированный капсидный белок (например, VP1, VP2 и/или VP3). Например, капсидный белок может быть модифицирован для изменения тропизма и/или снижения иммуногенности.
Рекомбинантные векторы на основе AAV ассоциированы с очень хорошим уровнем клинической безопасности, поскольку AAV дикого типа не является патогенным и не был этиологически связан с какими-либо известными заболеваниями. Кроме того, AAV обеспечивает возможность высокоэффективной доставки генов и продолжительной экспрессии трансгена в многочисленных тканях. Известны различные серотипы AAV, в том числе AAV1, AAV2, AAV3, AAV4, AAV5, AAV6, AAV7, AAV8, AAV9, AAV10, AAVrh.10, AAVrh.74 и т.п. В AAV-векторах может быть частично или полностью делетирован один или более из генов AAV дикого типа, например, гены rep и/или cap, при сохранении последовательностей функциональных фланкирующих инвертированных концевых повторов (ITR). Серотип рекомбинантного AAV-вектора определяют по капсиду. В международной патентной публикации WO2003042397A2 описаны различные последовательности капсидов, в том числе капсиды AAV1, AAV2, AAV3, AAV8, AAV9 и rh10. В международной патентной публикации WO2013078316A1 описана последовательность полипептида VP1 из AAVrh74. В данной области техники известно множество различных встречающихся в природе или генетически модифицированных последовательностей капсидов AAV.
Неограничивающий пример капсида представлен капсидом AAV9 с последовательностью SEQ ID NO: 28 (или его фрагментами VP1, VP2 или VP3). Согласно некоторым вариантам реализации AAV-векторы согласно настоящему описанию содержат капсидные белки, по меньшей мере на 93%, по меньшей мере на 94%, по меньшей мере на 95%, по меньшей мере на 96%, по меньшей мере на 97%, по меньшей мере на 98%, по меньшей мере на 99% или по меньшей мере на 100% идентичные SEQ ID NO: 28 на протяжении всей последовательности или на протяжении аминокислот 138–736 или 203–736.
1 MAADGYLPDW LEDNLSEGIR EWWALKPGAP QPKANQQHQD NARGLVLPGY KYLGPGNGLD
61 KGEPVNAADA AALEHDKAYD QQLKAGDNPY LKYNHADAEF QERLKEDTSF GGNLGRAVFQ
121 AKKRLLEPLG LVEEAAKTAP GKKRPVEQSP QEPDSSAGIG KSGAQPAKKR LNFGQTGDTE
181 SVPDPQPIGE PPAAPSGVGS LTMASGGGAP VADNNEGADG VGSSSGNWHC DSQWLGDRVI
241 TTSTRTWALP TYNNHLYKQI SNSTSGGSSN DNAYFGYSTP WGYFDFNRFH CHFSPRDWQR
301 LINNNWGFRP KRLNFKLFNI QVKEVTDNNG VKTIANNLTS TVQVFTDSDY QLPYVLGSAH
361 EGCLPPFPAD VFMIPQYGYL TLNDGSQAVG RSSFYCLEYF PSQMLRTGNN FQFSYEFENV
421 PFHSSYAHSQ SLDRLMNPLI DQYLYYLSKT INGSGQNQQT LKFSVAGPSN MAVQGRNYIP
481 GPSYRQQRVS TTVTQNNNSE FAWPGASSWA LNGRNSLMNP GPAMASHKEG EDRFFPLSGS
541 LIFGKQGTGR DNVDADKVMI TNEEEIKTTN PVATESYGQV ATNHQSAQAQ AQTGWVQNQG
601 ILPGMVWQDR DVYLQGPIWA KIPHTDGNFH PSPLMGGFGM KHPPPQILIK NTPVPADPPT
661 AFNKDKLNSF ITQYSTGQVS VEIEWELQKE NSKRWNPEIQ YTSNYYKSNN VEFAVNTEGV
721 YSEPRPIGTR YLTRNL
(SEQ ID NO: 28).
Экспрессионные AAV- векторы конструируют с применением известных техник таким образом, чтобы по меньшей мере обеспечить наличие, в виде функционально связанных компонентов в направлении транскрипции, контрольных элементов, включающих область инициации транскрипции, представляющей интерес ДНК (т.е. гена LAMP-2) и области терминации транскрипции.
Согласно некоторым вариантам реализации указанный вирусный вектор представляет собой AAV9-вектор. Согласно некоторым вариантам реализации экспрессионная кассета вирусного вектора фланкирована инвертированными концевыми повторами (ITR) AAV2. ITR, используемые в альтернативных вариантах реализации предложенных векторов, включают, не ограничиваясь перечисленными, AAV2, AAV3, AAV4, AAV5, AAV6, AAV7, AAV8 и AAV9. Согласно некоторым вариантам реализации указанный вирусный вектор представляет собой AAV2/9-вектор. Термин AAV2/9 относится к AAV-вектору с повторами ITR из AAV2 и капсидом из AAV9. Другие варианты реализации настоящего изобретения включают, без ограничения, векторы AAV2/9, AAV5/9, AAVrh74, AAV2/rh74, AAV5/9 и AAV5/rh74. Могут применяться другие ITR, известные в данной области техники. Примеры ITR (и других компонентов AAV), подходящих для применения в векторах согласно настоящему описанию, включают, без ограничения, описанные в источниках: US6936466B2, US9169494B2, US20050220766A1, US20190022249A1 и US7282199B2, каждый из которых полностью включен посредством ссылки в настоящий документ.
Согласно некоторым вариантам реализации указанный вектор представляет собой ретровирусный вектор или, конкретнее, лентивирусный вектор. В настоящем документе термин «ретровирус» или «ретровирусный» относится к РНК-вирусу, обратно-транскрибирующему свою геномную РНК в линейную двуцепочечную ДНК-копию, а затем ковалентно интегрирующему свою геномную ДНК в геном хозяина. Ретровирусные векторы представляют собой стандартный инструмент для доставки генов (Miller, 2000, Nature. 357: 455-460). После интеграции вируса в геном хозяина он называется «провирусом». Провирус служит матрицей для РНК-полимеразы II и направляет экспрессию молекул РНК, кодируемых вирусом.
Иллюстративные ретровирусы (семейство Retroviridae) включают, не ограничиваясь перечисленными, следующие: (1) род Gammaretrovirus, например, вирус лейкоза мышей Молони (M-MuLV), вирус саркомы мышей Молони (MoMSV), вирус опухоли молочной железы мышей (MuMTV), вирус лейкоза гиббонов (GaLV) и вирус лейкемии кошачьих (FLV), (2) род Spumavirus, например, вирус пенистости обезьян, (3) род Lentivirus, например, вирус иммунодефицита человека-1 и вирус иммунодефицита обезьян.
В настоящем документе термин «лентивирусный» или «лентивирус» относится к группе (или роду) сложных ретровирусов. Иллюстративные лентивирусы включают, не ограничиваясь перечисленными, следующие: ВИЧ (вирус иммунодефицита человека; в том числе ВИЧ 1 типа и ВИЧ 2 типа; вирус висна-маэди (VMV); вирус артрита-энцефалита коз (CAEV); вирус инфекционной анемии лошадей (EIAV); вирус иммунодефицита кошачьих (FIV); вирус иммунодефицита крупного рогатого скота (BIV); и вирус иммунодефицита обезьян (SIV). Согласно одному варианту реализации предпочтительными являются векторные остовы на основе ВИЧ (т.е. элементы цис-действующей последовательности ВИЧ).
Ретровирусные векторы и, конкретнее, лентивирусные векторы могут применяться при практической реализации настоящего изобретения. Соответственно, термин «ретровирусный вектор» в настоящем документе включает «лентивирусный вектор»; а термин «ретровирус» в настоящем документе включает «лентивирус».
Термин «вирусный вектор» может относиться либо к вектору или вирусной частице, способным переносить нуклеиновую кислоту в клетку, либо собственно к переносимой нуклеиновой кислоте. Вирусные векторы содержат структурные и/или функциональные генетические элементы, которые в основном происходят из вируса. Термин «ретровирусный вектор» относится к вирусному вектору, содержащему структурные и функциональные генетические элементы или их части, которые в основном происходят из ретровируса. Термин «лентивирусный вектор» относится к вирусному вектору, содержащему структурные и функциональные генетические элементы или их части, в том числе LTR, которые в основном происходят из лентивируса. Термин «гибридный» относится к вектору, LTR или другой нуклеиновой кислоте, содержащей и ретровирусные, например, лентивирусные последовательности, и нелентивирусные вирусные последовательности. Согласно одному варианту реализации гибридный вектор относится к вектору или плазмиде для переноса, содержащим ретровирусные, например, лентивирусные последовательности для обратной транскрипции, репликации, интеграции и/или упаковки.
Согласно конкретным вариантам реализации термины «лентивирусный вектор» и «лентивирусный экспрессионный вектор» могут относиться к лентивирусным плазмидам для переноса и/или инфекционным лентивирусным частицам. При упоминании в настоящем документе таких элементов, как сайты клонирования, промоторы, регуляторные элементы, гетерологичные нуклеиновые кислоты и т.п., следует понимать, что последовательности указанных элементов присутствуют в форме РНК в лентивирусных частицах согласно настоящему изобретению и в форме ДНК в ДНК-плазмидах согласно настоящему изобретению.
В соответствии с определенными конкретными вариантам реализации большинство или все последовательности остова вирусного вектора происходят из лентивируса, например, ВИЧ-1. Однако следует понимать, что может быть использовано множество разных источников лентивирусных последовательностей, и в некоторые лентивирусные последовательности могут быть включены многочисленные замены и изменения без нарушения способности вектора для переноса осуществлять функции, описанные в настоящем документе. Кроме того, в данной области техники известны различные лентивирусные векторы, см. источники: Naldini et al., (1996a, 1996b, 1998); Zufferey et al., (1997); Dull et al., 1998, патенты США №6013516; и №5994136, многие из которых могут быть адаптированы для получения вирусного вектора или плазмиды для переноса согласно настоящему изобретению.
Последовательности трансгена LAMP-2B согласно описанию в настоящем документе применяют, согласно различным вариантам реализации, в любой векторной системе, которая известна в данной области техники или будет открыта в перспективе. Настоящее изобретение не ограничено каким-либо конкретным вирусным вектором, описанным в настоящем документе, поскольку специалистам в в данной области техники известны способы использования последовательности трансгена в других векторных системах без излишнего экспериментирования и с целесообразным ожидаемым уровнем успеха.
Вирусные векторы для доставки генов, подходящие для применения при практической реализации настоящего изобретения, могут быть сконструированы с применением методик, хорошо известных в области молекулярной биологии. Как правило, вирусные векторы, несущие трансгены, собирают из полинуклеотидов, кодирующих трансген, подходящих регуляторных элементов и элементов, необходимых для продуцирования вирусных белков, которые опосредуют трансдукцию клеток. Такие рекомбинантные вирусы могут быть получены с помощью методик, известных в данной области техники, например, путем трансфекции пакующих клеток или транзиентной трансфекции хелперными плазмидами или вирусами. Типичные примеры пакующих клеток для вирусов включают, не ограничиваясь перечисленными, клетки HeLa, клетки SF9 (необязательно с бакуловирусным хелперным вектором), клетки 293 и т.п. Система на основе герпесвируса может быть использована для получения AAV-векторов согласно описанию в US20170218395A1. Подробные протоколы для получения таких репликативно-дефектных рекомбинантных вирусов можно найти, например, в источниках: W095/14785, W096/22378, патент США № 5882877, патент США № 6013516, патент США № 4861719, патент США № 5278056 и W094/19478, содержание каждого из которых полностью включено в настоящий документ посредством ссылок.
Согласно настоящему изобретению также предложены фармацевтические композиции, содержащие экспрессионную кассету или вектор (например, геннотерапевтический вектор) согласно описанию в настоящем документе и один или более фармацевтически приемлемых носителей, разбавителей или вспомогательных веществ. Согласно конкретным вариантам реализации указанная фармацевтическая композиция содержит AAV-вектор, содержащий экспрессионную кассету согласно описанию в настоящем документе, например, содержащую кодон-оптимизированный трансген, кодирующий LAMP-2B, например, любую из SEQ ID NO: 3–5 и их вариантов. Предложены фармацевтические композиции, например, для применения при предотвращении или лечении нарушения, характеризующегося недостаточным аутофагическим потоком (например, болезни Данона), которые содержат терапевтически эффективное количество экспрессионной кассеты или вектора согласно описанию в настоящем документе, который(ая) содержит последовательность нуклеиновой кислоты полинуклеотида, кодирующего одну или более из изоформ LAMP-2.
AAV-векторы, подходящие для применения при реализации настоящего изобретения, могут быть упакованы в AAV-вирионы (вирусные частицы) с применением различных систем, в том числе систем на основе аденовирусов и систем без хелперных вирусов. Стандартные способы в области биологии AAV включают описанные в источниках: Kwon, Schaffer. Pharm Res. (2008) 25(3):489-99; Wu et al. Mol. Ther. (2006) 14(3):316-27. Burger et al. Mol. Ther. (2004) 10(2):302-17; Grimm et al. Curr Gene Ther. (2003) 3(4):281-304; Deyle DR, Russell DW. Curr Opin Mol Ther. (2009) 11(4):442-447; McCarty et al. Gene Ther. (2001) 8(16):1248-54; и Duan et al. Mol Ther. (2001) 4(4):383-91. Системы без хелперных вирусов включали описанные в US 6004797; US 7588772; и US 7094604;
Фармацевтические композиции, которые содержат указанную экспрессионную кассету или указанный вектор, могут быть представлены в любой форме, которая подходит для выбранного способа введения, например, для интравентрикулярного, интрамиокардиального, интракоронарного, внутривенного, внутриартериального, внутрипочечного, внутриуретрального, эпидурального или внутримышечного введения. Геннотерапевтический вектор, содержащий полинуклеотид, кодирующий одну или более изоформ LAMP-2, может вводиться животным и человеку в качестве единственного активного агента или в комбинации с другими активными агентами, в единичной лекарственной форме, в виде смеси со стандартными фармацевтическими носителями. Согласно некоторым вариантам реализации указанная фармацевтическая композиция содержит клетки, трансдуцированные ex vivo любым из геннотерапевтических векторов согласно настоящему описанию.
Согласно некоторым вариантам реализации указанный вирусный вектор (например AAV-вектор) или фармацевтическая композиция, содержащая указанный вектор, эффективны при системном введении. Например, вирусные векторы согласно настоящему описанию в некоторых случаях демонстрируют эффективность при внутривенном введении субъекту (например, примату, такому как не являющийся человеком примат или человек). Согласно некоторым вариантам реализации вирусные векторы согласно настоящему описанию способны индуцировать экспрессию LAMP-2B в различных тканях при системном введении (например, в сердце, мышцах и/или легких). Согласно конкретным вариантам реализации внутривенное введение субъекту AAV9-вектора, содержащего трансген, по существу идентичный или идентичный SEQ ID NO: 3, приводит к детектируемой экспрессии LAMP-2B в ткани сердца. Согласно некоторым вариантам реализации экспрессия LAMP-2B детектируется в одной или более, или во всех областях из: левого желудочка, правого желудочка, левого предсердия и правого предсердия сердца указанного субъекта. Согласно некоторым вариантам реализации экспрессия LAMP-2B детектируется в подобласти 1 и/или подобласти 2 левого желудочка сердца указанного субъекта.
«Детектируемая экспрессия», как правило, относится к экспрессии трансгена, составляющей по меньшей мере 5%, 10%, 15%, 20% или более от экспрессии у контрольного субъекта, не получавшего лечение указанным вирусным вектором, или в контрольной ткани, не обработанной указанным вирусным вектором. Согласно некоторым вариантам реализации детектируемая экспрессия означает экспрессию, по меньшей мере 1,5-кратно, по меньшей мере 2-кратно, по меньшей мере 2,5-кратно, по меньшей мере 3-кратно, по меньшей мере 5-кратно, по меньшей мере 10-кратно, по меньшей мере 20-кратно, по меньшей мере 50-кратно или по меньшей мере 100-кратно превышающую контрольную экспрессию без вектора. Экспрессия трансгена может быть определена как повышение экспрессии относительно экспрессии гена дикого типа или эндогенного гена в клетке (с учетом возможности влияния экспрессии трансгена на экспрессию эндогенного гена). Экспрессия трансгена может также быть определена с применением РВ-ПЦР-детекции последовательностей, присутствующих на мРНК-транскрипте трансгена, но не на мРНК-транскрипте эндогенного гена. Например, 3′-UTR транскрипта могут быть использованы для определения экспрессии трансгена независимо от экспрессии эндогенного гена (у которого может быть другой 3′-UTR). Экспрессию полипептида, кодируемого трансгеном, можно оценить с помощью вестерн-блоттинга или твердофазного иммуноферментного анализа (ELISA) согласно описанию в приведенных ниже примерах или других способов, известных в данной области техники. Могут применяться антитела, способные к перекрестным реакциям с белком дикого типа и экзогенными копиями белка. В некоторых случаях может быть идентифицировано антитело, специфическое в отношении экзогенного белка, и использовано для определения экспрессии трансгена. Специалисты в данной области техники могут разработать подходящие методы детекции в зависимости от целевой клетки или ткани. В некоторых случаях экспрессию измеряют количественно с использованием стандартной кривой. Стандартные кривые могут быть построены с использованием очищенного белка LAMP-2 в способах, описанных в примерах или известных в данной области техники. Как вариант, экспрессию трансгена можно оценить путем количественного определения соответствующей мРНК.
Согласно некоторым вариантам реализации детектируемая экспрессия LAMP-2B в ткани сердца в дозах, выраженных в числе векторных геномов (вг) на килограмм массы тела субъекта (кг), составляет 5×1014 вг/кг или менее, 3×1014 вг/кг или менее, 2×1014 вг/кг или менее, 1×1014 вг/кг или менее, 9×1013 вг/кг или менее, 8×1013 вг/кг или менее, 7×1013 вг/кг или менее, 6×1013 вг/кг или менее, 5×1013 вг/кг или менее, 4×1013 вг/кг или менее, 3×1013 вг/кг или менее, 2×1013 вг/кг или менее, или 1×1013 вг/кг или менее.
Согласно некоторым вариантам реализации детектируемая экспрессия LAMP-2B в ткани сердца в дозах, выраженных в числе векторных геномов (вг) на килограмм массы тела субъекта (кг), составляет от 1×1013 вг/кг до 2×1013 вг/кг, от 2×1013 вг/кг до 3×1013 вг/кг, от 3×1013 вг/кг до 4×1013 вг/кг, от 4×1013 вг/кг до 5×1013 вг/кг, от 5×1013 вг/кг до 6×1013 вг/кг, от 6×1013 вг/кг до 7×1013 вг/кг, от 7×1013 вг/кг до 8×1013 вг/кг, от 8×1013 вг/кг до 9×1013 вг/кг, от 9×1013 вг/кг до 1×1014 вг/кг, от 1×1014 вг/кг до 2×1014 вг/кг, от 2×1014 вг/кг до 3×1014 вг/кг или от 3×1014 вг/кг до 5×1014 вг/кг.
Согласно некоторым вариантам реализации детектируемая экспрессия LAMP-2B в ткани сердца в дозах, выраженных в числе векторных геномов (вг) на килограмм массы тела субъекта (кг), составляет от 1×1013 вг/кг до 3×1013 вг/кг, от 3×1013 вг/кг до 5×1013 вг/кг, от 5×1013 вг/кг до 7×1013 вг/кг, от 7×1013 вг/кг до 9×1013 вг/кг, от 9×1013 вг/кг до 2×1014 вг/кг или от 2×1014 вг/кг до 5×1014 вг/кг. Согласно некоторым вариантам реализации детектируемая экспрессия LAMP-2B в ткани сердца в дозах, выраженных в числе векторных геномов (вг) на килограмм массы тела субъекта (кг), составляет от 1×1013 вг/кг до 5×1013 вг/кг, от 5×1013 вг/кг до 9×1013 вг/кг, 9×1013 вг/кг или до 5×1014 вг/кг. Согласно некоторым вариантам реализации детектируемая экспрессия LAMP-2B в ткани сердца в дозах, выраженных в числе векторных геномов (вг) на килограмм массы тела субъекта (кг), составляет от 1×1013 вг/кг до 9×1013 вг/кг, или 9×1013 вг/кг, или до 5×1014 вг/кг.
Согласно некоторым вариантам реализации детектируемая экспрессия LAMP-2B в ткани сердца в дозах, выраженных в числе векторных геномов (вг) на килограмм массы тела субъекта (кг), составляет от 1×1013 вг/кг до 5×1013 вг/кг, от 5×1013 вг/кг до 1×1014 вг/кг, или от 1×1014 вг/кг до 5×1014 вг/кг.
Согласно некоторым вариантам реализации детектируемая экспрессия LAMP-2B в ткани сердца в дозах, выраженных в числе векторных геномов (вг) на килограмм массы тела субъекта (кг), составляет от 1×1013 вг/кг до 5×1014 вг/кг. Согласно некоторым вариантам реализации детектируемая экспрессия LAMP-2B в ткани сердца в дозах, выраженных в числе векторных геномов (вг) на килограмм массы тела субъекта (кг), составляет от 1×1013 вг/кг до 1×1014.
Согласно различным вариантам реализации указанные фармацевтические композиции содержат основы (например, носители, разбавители и вспомогательные вещества), фармацевтически приемлемые для состава, подходящего для инъекций. Примеры вспомогательных веществ включают полоксамер. Рецептурные буферы для вирусных векторов (в том числе AAV) в общем случае включают соли для предотвращения агрегации и другие вспомогательные вещества (например, полоксамер) для снижения слипаемости вектора. Указанные вещества могут представлять собой, в частности, изотонические стерильные солевые растворы (фосфата мононатрия или динатрия, хлорида натрия, калия, кальция или магния и т.п., или смесей таких солей) или сухие, в частности, высушенные замораживанием композиции, которые позволяют восстанавливать инъецируемые растворы при добавлении, в зависимости от ситуации, стерильной воды или физиологического солевого раствора. Предпочтительно, указанный состав стабилен при хранении и применении после замораживания (например, при менее чем 0°C, приблизительно -60°C или приблизительно -72°C).
Примеры способов лечения лизосомальных нарушений и/или болезни Данона приведены в источнике: WO 2018/170239 A1, который полностью включен в настоящий документ. Трансгены, экспрессионные кассеты и векторы согласно настоящему описанию подходят для применения как in vivo (например, системного, в частности, внутривенного применения), так и ex vivo. Трансген LAMP-2B и функциональный промотор могут применяться для генной коррекции ex vivo аутологичных гематопоэтических стволовых клеток и клеток-предшественников (HSPC) пациентов, которые могут затем быть трансплантированы обратно пациентам для репопуляции их костного мозга, с созданием таким образом резервуара «здоровых» клеток у пациентов на всю оставшуюся жизнь. Согласно некоторым вариантам реализации лентивирусные векторы используют для генной коррекции ex vivo, однако вместо лентивирусного вектора могут быть использованы и другие невирусные или вирусные векторы. Настоящим изобретением предусмотрена аллогенная трансплантация с применением донорных HSPC. Согласно некоторым вариантам реализации указанный лентивирусный вектор представляет собой самоинактивирующийся (SIN) лентивирусный вектор. Согласно некоторым вариантам реализации указанные HSPC происходят из клеток периферической крови, мобилизованных с применением, например, гранулоцитарного колониестимулирующего фактора (Г-КСФ) и/или плериксафора.
Согласно другому аспекту настоящего изобретения предложены способы предотвращения, смягчения, облегчения, уменьшения, ингибирования, устранения и/или обращения одного или более симптомов болезни Данона или другого аутофагического нарушения у нуждающегося в этом субъекта, включающие введение указанному субъекту геннотерапевтического вектора согласно настоящему описанию. Термин «болезнь Данона» относится к наследуемому по Х-сцепленному доминантному типу нарушению сердечной и скелетных мышц с мультисистемными клиническими проявлениями. Мутации при болезни Данона приводят к отсутствию экспрессии ассоциированного с лизосомами мембранного белка 2 (LAMP-2). Основные клинические признаки включают миопатию сердечной и скелетных мышц, аномалии сердечной проводимости, когнитивные затруднения и заболевания сетчатки. Как правило, у мужчин поражение развивается раньше и протекает тяжелее, чем у женщин.
Согласно варианту реализации указанный вектор вводят путем, выбранным из группы, состоящей из парентерального, внутривенного, внутриартериального, внутрисердечного, интракоронарного, интрамиокардиального, внутрипочечного, внутриуретрального, эпидурального и внутримышечного введения. Согласно варианту реализации указанный вектор вводят неоднократно. Согласно варианту реализации указанный вектор вводят путем внутримышечной инъекции вектора. Согласно варианту реализации указанный вектор вводят путем инъекции вектора в скелетные мышцы. Согласно варианту реализации указанная экспрессионная кассета содержит специфический для мышц промотор, необязательно промотор мышечной креатинкиназы (MCK) или гибридный промотор MCK/SV40 согласно описанию в источнике: Takeshita et al. Muscle creatine kinase/SV40 hybrid promoter for muscle-targeted long-term transgene expression. Int J Mol Med. 2007 Feb;19(2):309-15. Согласно варианту реализации указанный вектор вводят путем внутрисердечной инъекции.
Согласно варианту реализации указанный вектор, например, AAV-вектор, вводят системно, и, конкретнее, внутривенно. Предпочтительно указанный вектор вводят в меньшей дозе (в вг на мл, вг/кг массы тела или вг/мин/кг), чем требуемая для достижения такого же наблюдаемого ответа при применении оригинальной последовательности или последовательности LAMP-2B дикого типа. Согласно конкретным вариантам реализации указанный вектор представляет собой вектор AAV2/9, содержащий экспрессионную кассету, содержащую полинуклеотид, кодирующий LAMP-2B согласно описанию в настоящем документе.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ экспрессии LAMP-2B у субъекта, включающий системное введение вектора на основе аденоассоциированного вируса (AAV) указанному субъекту, отличающийся тем, что указанный AAV-вектор содержит экспрессионную кассету, содержащую трансген, последовательность которого обладает по меньшей мере 95% идентичностью с SEQ ID NO: 3 или идентична SEQ ID NO: 3, функционально связанный с энхансерной/промоторной областью, причем системное введение AAV-вектора указанному субъекту приводит к повышению экспрессии LAMP-2B по сравнению с экспрессией LAMP-2B до введения AAV-вектора или экспрессией LAMP-2B у не получавшего лечения контрольного субъекта. Согласно некоторым вариантам реализации указанный AAV-вектор представляет собой вектор AAV2/9. Согласно конкретным вариантам реализации указанная экспрессионная кассета содержит любые из элементов, описанных в настоящем документе. Согласно определенному варианту реализации системное введение включает внутривенное введение. Согласно некоторым вариантам реализации у указанного субъекта наблюдаются симптомы болезни Данона. Согласно некоторым вариантам реализации указанный субъект страдает болезнью Данона или у него имеется риск развития болезни Данона.
Согласно некоторым вариантам реализации указанный AAV-вектор вводят в дозе от приблизительно 1×1012 до 5×1014 векторных геномов (вг) AAV-вектора на килограмм (кг) общей массы тела субъекта (вг/кг). Согласно некоторым вариантам реализации указанный AAV-вектор вводят в дозе от приблизительно 1×1013 до 5×1014 вг/кг. Согласно некоторым вариантам реализации указанный AAV-вектор вводят в дозе от приблизительно 5×1013 до 3×1014 вг/кг. Согласно некоторым вариантам реализации указанный AAV-вектор вводят в дозе от приблизительно 5×1013 до 1×1014 вг/кг. Согласно некоторым вариантам реализации указанный AAV-вектор вводят в дозе, составляющей менее чем приблизительно 1×1012 вг/кг, менее чем приблизительно 3×1012 вг/кг, менее чем приблизительно 5×1012 вг/кг, менее чем приблизительно 7×1012 вг/кг, менее чем приблизительно 1×1013 вг/кг, менее чем приблизительно 3×1013 вг/кг, менее чем приблизительно 5×1013 вг/кг, менее чем приблизительно 7×1013 вг/кг, менее чем приблизительно 1×1014 вг/кг, менее чем приблизительно 3×1014 вг/кг, менее чем приблизительно 5×1014 вг/кг, менее чем приблизительно 7×1014 вг/кг, менее чем приблизительно 1×1015 вг/кг, менее чем приблизительно 3×1015 вг/кг, менее чем приблизительно 5×1015 вг/кг или менее чем приблизительно 7×1015 вг/кг.
Согласно некоторым вариантам реализации указанный AAV-вектор вводят в дозе, составляющей приблизительно 1×1012 вг/кг, приблизительно 3×1012 вг/кг, приблизительно 5×1012 вг/кг, приблизительно 7×1012 вг/кг, приблизительно 1×1013 вг/кг, приблизительно 3×1013 вг/кг, приблизительно 5×1013 вг/кг, приблизительно 7×1013 вг/кг, приблизительно 1×1014 вг/кг, приблизительно 3×1014 вг/кг, приблизительно 5×1014 вг/кг, приблизительно 7×1014 вг/кг, приблизительно 1×1015 вг/кг, приблизительно 3×1015 вг/кг, приблизительно 5×1015 вг/кг или приблизительно 7×1015 вг/кг.
Согласно некоторым вариантам реализации указанный AAV-вектор вводят в дозе 1×1012 вг/кг, 3×1012 вг/кг, 5×1012 вг/кг, 7×1012 вг/кг, 1×1013 вг/кг, 3×1013 вг/кг, 5×1013 вг/кг, 7×1013 вг/кг, 1×1014 вг/кг, 3×1014 вг/кг, 5×1014 вг/кг, 7×1014 вг/кг, 1×1015 вг/кг, 3×1015 вг/кг, 5×1015 вг/кг или 7×1015 вг/кг.
Согласно некоторым вариантам реализации указанный лентивирусный вектор вводят в дозе от приблизительно 1×1012 до 5×1014 векторных геномов (вг) лентивирусного вектора на килограмм (кг) общей массы тела субъекта (вг/кг). Согласно некоторым вариантам реализации указанный лентивирусный вектор вводят в дозе от приблизительно 1×1013 до 5×1014 вг/кг. Согласно некоторым вариантам реализации указанный лентивирусный вектор вводят в дозе от приблизительно 5×1013 до 3×1014 вг/кг. Согласно некоторым вариантам реализации указанный лентивирусный вектор вводят в дозе от приблизительно 5×1013 до 1×1014 вг/кг. Согласно некоторым вариантам реализации указанный лентивирусный вектор вводят в дозе менее чем приблизительно 1×1012 вг/кг, менее чем приблизительно 3×1012 вг/кг, менее чем приблизительно 5×1012 вг/кг, менее чем приблизительно 7×1012 вг/кг, менее чем приблизительно 1×1013 вг/кг, менее чем приблизительно 3×1013 вг/кг, менее чем приблизительно 5×1013 вг/кг, менее чем приблизительно 7×1013 вг/кг, менее чем приблизительно 1×1014 вг/кг, менее чем приблизительно 3×1014 вг/кг, менее чем приблизительно 5×1014 вг/кг, менее чем приблизительно 7×1014 вг/кг, менее чем приблизительно 1×1015 вг/кг, менее чем приблизительно 3×1015 вг/кг, менее чем приблизительно 5×1015 вг/кг или менее чем приблизительно 7×1015 вг/кг.
Согласно некоторым вариантам реализации указанный лентивирусный вектор вводят в дозе, составляющей приблизительно 1×1012 вг/кг, приблизительно 3×1012 вг/кг, приблизительно 5×1012 вг/кг, приблизительно 7×1012 вг/кг, приблизительно 1×1013 вг/кг, приблизительно 3×1013 вг/кг, приблизительно 5×1013 вг/кг, приблизительно 7×1013 вг/кг, приблизительно 1×1014 вг/кг, приблизительно 3×1014 вг/кг, приблизительно 5×1014 вг/кг, приблизительно 7×1014 вг/кг, приблизительно 1×1015 вг/кг, приблизительно 3×1015 вг/кг, приблизительно 5×1015 вг/кг или приблизительно 7×1015 вг/кг.
Согласно некоторым вариантам реализации указанный лентивирусный вектор вводят в дозе 1×1012 вг/кг, 3×1012 вг/кг, 5×1012 вг/кг, 7×1012 вг/кг, 1×1013 вг/кг, 3×1013 вг/кг, 5×1013 вг/кг, 7×1013 вг/кг, 1×1014 вг/кг, 3×1014 вг/кг, 5×1014 вг/кг, 7×1014 вг/кг, 1×1015 вг/кг, 3×1015 вг/кг, 5×1015 вг/кг или 7×1015 вг/кг.
Согласно некоторым вариантам реализации указанный вирусный вектор вводят в дозе от приблизительно 1×1012 до 5×1014 векторных геномов (вг) вирусного вектора на килограмм (кг) общей массы тела субъекта (вг/кг). Согласно некоторым вариантам реализации указанный вирусный вектор вводят в дозе от приблизительно 1×1013 до 5×1014 вг/кг. Согласно некоторым вариантам реализации указанный вирусный вектор вводят в дозе от приблизительно 5×1013 до 3×1014 вг/кг. Согласно некоторым вариантам реализации указанный вирусный вектор вводят в дозе от приблизительно 5×1013 до 1×1014 вг/кг. Согласно некоторым вариантам реализации указанный вирусный вектор вводят в дозе менее чем приблизительно 1×1012 вг/кг, менее чем приблизительно 3×1012 вг/кг, менее чем приблизительно 5×1012 вг/кг, менее чем приблизительно 7×1012 вг/кг, менее чем приблизительно 1×1013 вг/кг, менее чем приблизительно 3×1013 вг/кг, менее чем приблизительно 5×1013 вг/кг, менее чем приблизительно 7×1013 вг/кг, менее чем приблизительно 1×1014 вг/кг, менее чем приблизительно 3×1014 вг/кг, менее чем приблизительно 5×1014 вг/кг, менее чем приблизительно 7×1014 вг/кг, менее чем приблизительно 1×1015 вг/кг, менее чем приблизительно 3×1015 вг/кг, менее чем приблизительно 5×1015 вг/кг или менее чем приблизительно 7×1015 вг/кг.
Согласно некоторым вариантам реализации указанный вирусный вектор вводят в дозе, составляющей приблизительно 1×1012 вг/кг, приблизительно 3×1012 вг/кг, приблизительно 5×1012 вг/кг, приблизительно 7×1012 вг/кг, приблизительно 1×1013 вг/кг, приблизительно 3×1013 вг/кг, приблизительно 5×1013 вг/кг, приблизительно 7×1013 вг/кг, приблизительно 1×1014 вг/кг, приблизительно 3×1014 вг/кг, приблизительно 5×1014 вг/кг, приблизительно 7×1014 вг/кг, приблизительно 1×1015 вг/кг, приблизительно 3×1015 вг/кг, приблизительно 5×1015 вг/кг или приблизительно 7×1015 вг/кг.
Согласно некоторым вариантам реализации указанный вирусный вектор вводят в дозе 1×1012 вг/кг, 3×1012 вг/кг, 5×1012 вг/кг, 7×1012 вг/кг, 1×1013 вг/кг, 3×1013 вг/кг, 5×1013 вг/кг, 7×1013 вг/кг, 1×1014 вг/кг, 3×1014 вг/кг, 5×1014 вг/кг, 7×1014 вг/кг, 1×1015 вг/кг, 3×1015 вг/кг, 5×1015 вг/кг или 7×1015 вг/кг.
Согласно некоторым вариантам реализации указанный AAV-вектор вводят системно в дозе от приблизительно 1×1012 до 5×1014 векторных геномов (вг) AAV-вектора на килограмм (кг) общей массы тела субъекта (вг/кг). Согласно некоторым вариантам реализации указанный AAV-вектор вводят системно в дозе от приблизительно 1×1013 до 5×1014 вг/кг. Согласно некоторым вариантам реализации указанный AAV-вектор вводят системно в дозе от приблизительно 5×1013 до 3×1014 вг/кг. Согласно некоторым вариантам реализации указанный AAV-вектор вводят системно в дозе от приблизительно 5×1013 до 1×1014 вг/кг. Согласно некоторым вариантам реализации указанный AAV-вектор вводят системно в дозе менее чем приблизительно 1×1012 вг/кг, менее чем приблизительно 3×1012 вг/кг, менее чем приблизительно 5×1012 вг/кг, менее чем приблизительно 7×1012 вг/кг, менее чем приблизительно 1×1013 вг/кг, менее чем приблизительно 3×1013 вг/кг, менее чем приблизительно 5×1013 вг/кг, менее чем приблизительно 7×1013 вг/кг, менее чем приблизительно 1×1014 вг/кг, менее чем приблизительно 3×1014 вг/кг, менее чем приблизительно 5×1014 вг/кг, менее чем приблизительно 7×1014 вг/кг, менее чем приблизительно 1×1015 вг/кг, менее чем приблизительно 3×1015 вг/кг, менее чем приблизительно 5×1015 вг/кг или менее чем приблизительно 7×1015 вг/кг.
Согласно некоторым вариантам реализации указанный AAV-вектор вводят системно в дозе, составляющей приблизительно 1×1012 вг/кг, приблизительно 3×1012 вг/кг, приблизительно 5×1012 вг/кг, приблизительно 7×1012 вг/кг, приблизительно 1×1013 вг/кг, приблизительно 3×1013 вг/кг, приблизительно 5×1013 вг/кг, приблизительно 7×1013 вг/кг, приблизительно 1×1014 вг/кг, приблизительно 3×1014 вг/кг, приблизительно 5×1014 вг/кг, приблизительно 7×1014 вг/кг, приблизительно 1×1015 вг/кг, приблизительно 3×1015 вг/кг, приблизительно 5×1015 вг/кг или приблизительно 7×1015 вг/кг.
Согласно некоторым вариантам реализации указанный AAV-вектор вводят системно в дозе 1×1012 вг/кг, 3×1012 вг/кг, 5×1012 вг/кг, 7×1012 вг/кг, 1×1013 вг/кг, 3×1013 вг/кг, 5×1013 вг/кг, 7×1013 вг/кг, 1×1014 вг/кг, 3×1014 вг/кг, 5×1014 вг/кг, 7×1014 вг/кг, 1×1015 вг/кг, 3×1015 вг/кг, 5×1015 вг/кг или 7×1015 вг/кг.
Согласно некоторым вариантам реализации указанный лентивирусный вектор вводят системно в дозе от приблизительно 1×1012 до 5×1014 векторных геномов (вг) лентивирусного вектора на килограмм (кг) общей массы тела субъекта (вг/кг). Согласно некоторым вариантам реализации указанный лентивирусный вектор вводят системно в дозе от приблизительно 1×1013 до 5×1014 вг/кг. Согласно некоторым вариантам реализации указанный лентивирусный вектор вводят системно в дозе от приблизительно 5×1013 до 3×1014 вг/кг. Согласно некоторым вариантам реализации указанный лентивирусный вектор вводят системно в дозе от приблизительно 5×1013 до 1×1014 вг/кг. Согласно некоторым вариантам реализации указанный лентивирусный вектор вводят системно в дозе менее чем приблизительно 1×1012 вг/кг, менее чем приблизительно 3×1012 вг/кг, менее чем приблизительно 5×1012 вг/кг, менее чем приблизительно 7×1012 вг/кг, менее чем приблизительно 1×1013 вг/кг, менее чем приблизительно 3×1013 вг/кг, менее чем приблизительно 5×1013 вг/кг, менее чем приблизительно 7×1013 вг/кг, менее чем приблизительно 1×1014 вг/кг, менее чем приблизительно 3×1014 вг/кг, менее чем приблизительно 5×1014 вг/кг, менее чем приблизительно 7×1014 вг/кг, менее чем приблизительно 1×1015 вг/кг, менее чем приблизительно 3×1015 вг/кг, менее чем приблизительно 5×1015 вг/кг или менее чем приблизительно 7×1015 вг/кг.
Согласно некоторым вариантам реализации указанный лентивирусный вектор вводят системно в дозе, составляющей приблизительно 1×1012 вг/кг, приблизительно 3×1012 вг/кг, приблизительно 5×1012 вг/кг, приблизительно 7×1012 вг/кг, приблизительно 1×1013 вг/кг, приблизительно 3×1013 вг/кг, приблизительно 5×1013 вг/кг, приблизительно 7×1013 вг/кг, приблизительно 1×1014 вг/кг, приблизительно 3×1014 вг/кг, приблизительно 5×1014 вг/кг, приблизительно 7×1014 вг/кг, приблизительно 1×1015 вг/кг, приблизительно 3×1015 вг/кг, приблизительно 5×1015 вг/кг или приблизительно 7×1015 вг/кг.
Согласно некоторым вариантам реализации указанный лентивирусный вектор вводят системно в дозе 1×1012 вг/кг, 3×1012 вг/кг, 5×1012 вг/кг, 7×1012 вг/кг, 1×1013 вг/кг, 3×1013 вг/кг, 5×1013 вг/кг, 7×1013 вг/кг, 1×1014 вг/кг, 3×1014 вг/кг, 5×1014 вг/кг, 7×1014 вг/кг, 1×1015 вг/кг, 3×1015 вг/кг, 5×1015 вг/кг или 7×1015 вг/кг.
Согласно некоторым вариантам реализации указанный вирусный вектор вводят системно в дозе от приблизительно 1×1012 до 5×1014 векторных геномов (вг) вирусного вектора на килограмм (кг) общей массы тела субъекта (вг/кг). Согласно некоторым вариантам реализации указанный вирусный вектор вводят системно в дозе от приблизительно 1×1013 до 5×1014 вг/кг. Согласно некоторым вариантам реализации указанный вирусный вектор вводят системно в дозе от приблизительно 5×1013 до 3×1014 вг/кг. Согласно некоторым вариантам реализации указанный вирусный вектор вводят системно в дозе от приблизительно 5×1013 до 1×1014 вг/кг. Согласно некоторым вариантам реализации указанный вирусный вектор вводят системно в дозе менее чем приблизительно 1×1012 вг/кг, менее чем приблизительно 3×1012 вг/кг, менее чем приблизительно 5×1012 вг/кг, менее чем приблизительно 7×1012 вг/кг, менее чем приблизительно 1×1013 вг/кг, менее чем приблизительно 3×1013 вг/кг, менее чем приблизительно 5×1013 вг/кг, менее чем приблизительно 7×1013 вг/кг, менее чем приблизительно 1×1014 вг/кг, менее чем приблизительно 3×1014 вг/кг, менее чем приблизительно 5×1014 вг/кг, менее чем приблизительно 7×1014 вг/кг, менее чем приблизительно 1×1015 вг/кг, менее чем приблизительно 3×1015 вг/кг, менее чем приблизительно 5×1015 вг/кг или менее чем приблизительно 7×1015 вг/кг.
Согласно некоторым вариантам реализации указанный вирусный вектор вводят системно в дозе, составляющей приблизительно 1×1012 вг/кг, приблизительно 3×1012 вг/кг, приблизительно 5×1012 вг/кг, приблизительно 7×1012 вг/кг, приблизительно 1×1013 вг/кг, приблизительно 3×1013 вг/кг, приблизительно 5×1013 вг/кг, приблизительно 7×1013 вг/кг, приблизительно 1×1014 вг/кг, приблизительно 3×1014 вг/кг, приблизительно 5×1014 вг/кг, приблизительно 7×1014 вг/кг, приблизительно 1×1015 вг/кг, приблизительно 3×1015 вг/кг, приблизительно 5×1015 вг/кг или приблизительно 7×1015 вг/кг.
Согласно некоторым вариантам реализации указанный вирусный вектор вводят системно в дозе 1×1012 вг/кг, 3×1012 вг/кг, 5×1012 вг/кг, 7×1012 вг/кг, 1×1013 вг/кг, 3×1013 вг/кг, 5×1013 вг/кг, 7×1013 вг/кг, 1×1014 вг/кг, 3×1014 вг/кг, 5×1014 вг/кг, 7×1014 вг/кг, 1×1015 вг/кг, 3×1015 вг/кг, 5×1015 вг/кг или 7×1015 вг/кг.
Согласно некоторым вариантам реализации указанный AAV-вектор вводят внутривенно в дозе от приблизительно 1×1012 до 5×1014 векторных геномов (вг) AAV-вектора на килограмм (кг) общей массы тела субъекта (вг/кг). Согласно некоторым вариантам реализации указанный AAV-вектор вводят внутривенно в дозе от приблизительно 1×1013 до 5×1014 вг/кг. Согласно некоторым вариантам реализации указанный AAV-вектор вводят внутривенно в дозе от приблизительно 5×1013 до 3×1014 вг/кг. Согласно некоторым вариантам реализации указанный AAV-вектор вводят внутривенно в дозе от приблизительно 5×1013 до 1×1014 вг/кг. Согласно некоторым вариантам реализации указанный AAV-вектор вводят внутривенно в дозе менее чем приблизительно 1×1012 вг/кг, менее чем приблизительно 3×1012 вг/кг, менее чем приблизительно 5×1012 вг/кг, менее чем приблизительно 7×1012 вг/кг, менее чем приблизительно 1×1013 вг/кг, менее чем приблизительно 3×1013 вг/кг, менее чем приблизительно 5×1013 вг/кг, менее чем приблизительно 7×1013 вг/кг, менее чем приблизительно 1×1014 вг/кг, менее чем приблизительно 3×1014 вг/кг, менее чем приблизительно 5×1014 вг/кг, менее чем приблизительно 7×1014 вг/кг, менее чем приблизительно 1×1015 вг/кг, менее чем приблизительно 3×1015 вг/кг, менее чем приблизительно 5×1015 вг/кг или менее чем приблизительно 7×1015 вг/кг.
Согласно некоторым вариантам реализации указанный AAV-вектор вводят внутривенно в дозе, составляющей приблизительно 1×1012 вг/кг, приблизительно 3×1012 вг/кг, приблизительно 5×1012 вг/кг, приблизительно 7×1012 вг/кг, приблизительно 1×1013 вг/кг, приблизительно 3×1013 вг/кг, приблизительно 5×1013 вг/кг, приблизительно 7×1013 вг/кг, приблизительно 1×1014 вг/кг, приблизительно 3×1014 вг/кг, приблизительно 5×1014 вг/кг, приблизительно 7×1014 вг/кг, приблизительно 1×1015 вг/кг, приблизительно 3×1015 вг/кг, приблизительно 5×1015 вг/кг или приблизительно 7×1015 вг/кг.
Согласно некоторым вариантам реализации указанный AAV-вектор вводят внутривенно в дозе 1×1012 вг/кг, 3×1012 вг/кг, 5×1012 вг/кг, 7×1012 вг/кг, 1×1013 вг/кг, 3×1013 вг/кг, 5×1013 вг/кг, 7×1013 вг/кг, 1×1014 вг/кг, 3×1014 вг/кг, 5×1014 вг/кг, 7×1014 вг/кг, 1×1015 вг/кг, 3×1015 вг/кг, 5×1015 вг/кг или 7×1015 вг/кг.
Согласно некоторым вариантам реализации указанный лентивирусный вектор вводят внутривенно в дозе от приблизительно 1×1012 до 5×1014 векторных геномов (вг) лентивирусного вектора на килограмм (кг) общей массы тела субъекта (вг/кг). Согласно некоторым вариантам реализации указанный лентивирусный вектор вводят внутривенно в дозе от приблизительно 1×1013 до 5×1014 вг/кг. Согласно некоторым вариантам реализации указанный лентивирусный вектор вводят внутривенно в дозе от приблизительно 5×1013 до 3×1014 вг/кг. Согласно некоторым вариантам реализации указанный лентивирусный вектор вводят внутривенно в дозе от приблизительно 5×1013 до 1×1014 вг/кг. Согласно некоторым вариантам реализации указанный лентивирусный вектор вводят внутривенно в дозе менее чем приблизительно 1×1012 вг/кг, менее чем приблизительно 3×1012 вг/кг, менее чем приблизительно 5×1012 вг/кг, менее чем приблизительно 7×1012 вг/кг, менее чем приблизительно 1×1013 вг/кг, менее чем приблизительно 3×1013 вг/кг, менее чем приблизительно 5×1013 вг/кг, менее чем приблизительно 7×1013 вг/кг, менее чем приблизительно 1×1014 вг/кг, менее чем приблизительно 3×1014 вг/кг, менее чем приблизительно 5×1014 вг/кг, менее чем приблизительно 7×1014 вг/кг, менее чем приблизительно 1×1015 вг/кг, менее чем приблизительно 3×1015 вг/кг, менее чем приблизительно 5×1015 вг/кг или менее чем приблизительно 7×1015 вг/кг.
Согласно некоторым вариантам реализации указанный лентивирусный вектор вводят внутривенно в дозе, составляющей приблизительно 1×1012 вг/кг, приблизительно 3×1012 вг/кг, приблизительно 5×1012 вг/кг, приблизительно 7×1012 вг/кг, приблизительно 1×1013 вг/кг, приблизительно 3×1013 вг/кг, приблизительно 5×1013 вг/кг, приблизительно 7×1013 вг/кг, приблизительно 1×1014 вг/кг, приблизительно 3×1014 вг/кг, приблизительно 5×1014 вг/кг, приблизительно 7×1014 вг/кг, приблизительно 1×1015 вг/кг, приблизительно 3×1015 вг/кг, приблизительно 5×1015 вг/кг или приблизительно 7×1015 вг/кг.
Согласно некоторым вариантам реализации указанный лентивирусный вектор вводят внутривенно в дозе 1×1012 вг/кг, 3×1012 вг/кг, 5×1012 вг/кг, 7×1012 вг/кг, 1×1013 вг/кг, 3×1013 вг/кг, 5×1013 вг/кг, 7×1013 вг/кг, 1×1014 вг/кг, 3×1014 вг/кг, 5×1014 вг/кг, 7×1014 вг/кг, 1×1015 вг/кг, 3×1015 вг/кг, 5×1015 вг/кг или 7×1015 вг/кг.
Согласно некоторым вариантам реализации указанный вирусный вектор вводят внутривенно в дозе от приблизительно 1×1012 до 5×1014 векторных геномов (вг) вирусного вектора на килограмм (кг) общей массы тела субъекта (вг/кг). Согласно некоторым вариантам реализации указанный вирусный вектор вводят внутривенно в дозе от приблизительно 1×1013 до 5×1014 вг/кг. Согласно некоторым вариантам реализации указанный вирусный вектор вводят внутривенно в дозе от приблизительно 5×1013 до 3×1014 вг/кг. Согласно некоторым вариантам реализации указанный вирусный вектор вводят внутривенно в дозе от приблизительно 5×1013 до 1×1014 вг/кг. Согласно некоторым вариантам реализации указанный вирусный вектор вводят внутривенно в дозе менее чем приблизительно 1×1012 вг/кг, менее чем приблизительно 3×1012 вг/кг, менее чем приблизительно 5×1012 вг/кг, менее чем приблизительно 7×1012 вг/кг, менее чем приблизительно 1×1013 вг/кг, менее чем приблизительно 3×1013 вг/кг, менее чем приблизительно 5×1013 вг/кг, менее чем приблизительно 7×1013 вг/кг, менее чем приблизительно 1×1014 вг/кг, менее чем приблизительно 3×1014 вг/кг, менее чем приблизительно 5×1014 вг/кг, менее чем приблизительно 7×1014 вг/кг, менее чем приблизительно 1×1015 вг/кг, менее чем приблизительно 3×1015 вг/кг, менее чем приблизительно 5×1015 вг/кг или менее чем приблизительно 7×1015 вг/кг.
Согласно некоторым вариантам реализации указанный вирусный вектор вводят внутривенно в дозе, составляющей приблизительно 1×1012 вг/кг, приблизительно 3×1012 вг/кг, приблизительно 5×1012 вг/кг, приблизительно 7×1012 вг/кг, приблизительно 1×1013 вг/кг, приблизительно 3×1013 вг/кг, приблизительно 5×1013 вг/кг, приблизительно 7×1013 вг/кг, приблизительно 1×1014 вг/кг, приблизительно 3×1014 вг/кг, приблизительно 5×1014 вг/кг, приблизительно 7×1014 вг/кг, приблизительно 1×1015 вг/кг, приблизительно 3×1015 вг/кг, приблизительно 5×1015 вг/кг или приблизительно 7×1015 вг/кг.
Согласно некоторым вариантам реализации указанный вирусный вектор вводят внутривенно в дозе 1×1012 вг/кг, 3×1012 вг/кг, 5×1012 вг/кг, 7×1012 вг/кг, 1×1013 вг/кг, 3×1013 вг/кг, 5×1013 вг/кг, 7×1013 вг/кг, 1×1014 вг/кг, 3×1014 вг/кг, 5×1014 вг/кг, 7×1014 вг/кг, 1×1015 вг/кг, 3×1015 вг/кг, 5×1015 вг/кг или 7×1015 вг/кг.
Системное (или, более конкретно, внутривенное) введение согласно некоторым вариантам реализации приводит к экспрессии полинуклеотида LAMP-2B в виде мРНК, в форме мРНК, экспрессируемой с трансгена, в одной или более тканях (например сердце, мышцах и/или печени) указанного субъекта. Согласно некоторым вариантам реализации экспрессия полинуклеотида LAMP-2B в виде мРНК в сердце повышается по меньшей мере приблизительно 1,2-кратно, по меньшей мере приблизительно 1,3-кратно, по меньшей мере приблизительно 1,4-кратно, по меньшей мере приблизительно 1,5-кратно, по меньшей мере приблизительно 1,6-кратно, по меньшей мере приблизительно 1,7-кратно, по меньшей мере приблизительно 1,8-кратно, по меньшей мере приблизительно 1,9-кратно, по меньшей мере приблизительно 2,0-кратно, по меньшей мере приблизительно 2,2-кратно, по меньшей мере приблизительно 2,3-кратно, по меньшей мере приблизительно 2,4-кратно, по меньшей мере приблизительно 2,5-кратно, по меньшей мере приблизительно 3-кратно или по меньшей мере приблизительно 4-кратно по сравнению с экспрессией у не получавшего лечения субъекта или у субъекта, получавшего лечение контрольным вектором. Согласно некоторым вариантам реализации экспрессия полинуклеотида LAMP-2B в виде мРНК в сердце повышается по меньшей мере 1,2-кратно, по меньшей мере 1,3-кратно, по меньшей мере 1,4-кратно, по меньшей мере 1,5-кратно, по меньшей мере 1,6-кратно, по меньшей мере 1,7-кратно, по меньшей мере 1,8-кратно, по меньшей мере 1,9-кратно, по меньшей мере 2,0-кратно, по меньшей мере 2,2-кратно, по меньшей мере 2,3-кратно, по меньшей мере 2,4-кратно, по меньшей мере 2,5-кратно, по меньшей мере 3-кратно или по меньшей мере 4-кратно по сравнению с экспрессией у не получавшего лечения субъекта или у субъекта, получавшего лечение контрольным вектором. Согласно некоторым вариантам реализации экспрессия полинуклеотида LAMP-2B в виде мРНК в сердце повышается 1,2-кратно, 1,3-кратно, 1,4-кратно, 1,5-кратно, 1,6-кратно, 1,7-кратно, 1,8-кратно, 1,9-кратно, 2,0-кратно, 2,2-кратно, 2,3-кратно, 2,4-кратно, 2,5-кратно, 3-кратно или 4-кратно по сравнению с экспрессией у не получавшего лечения субъекта или у субъекта, получавшего лечение контрольным вектором.
Согласно некоторым вариантам реализации экспрессия полинуклеотида LAMP-2B в виде мРНК в мышцах повышается по меньшей мере приблизительно 1,2-кратно, по меньшей мере приблизительно 1,3-кратно, по меньшей мере приблизительно 1,4-кратно, по меньшей мере приблизительно 1,5-кратно, по меньшей мере приблизительно 1,6-кратно, по меньшей мере приблизительно 1,7-кратно, по меньшей мере приблизительно 1,8-кратно, по меньшей мере приблизительно 1,9-кратно, по меньшей мере приблизительно 2,0-кратно, по меньшей мере приблизительно 2,2-кратно, по меньшей мере приблизительно 2,3-кратно, по меньшей мере приблизительно 2,4-кратно, по меньшей мере приблизительно 2,5-кратно, по меньшей мере приблизительно 3-кратно или по меньшей мере приблизительно 4-кратно по сравнению с экспрессией у не получавшего лечения субъекта или у субъекта, получавшего лечение контрольным вектором. Согласно некоторым вариантам реализации экспрессия полинуклеотида LAMP-2B в виде мРНК в мышцах повышается по меньшей мере 1,2-кратно, по меньшей мере 1,3-кратно, по меньшей мере 1,4-кратно, по меньшей мере 1,5-кратно, по меньшей мере 1,6-кратно, по меньшей мере 1,7-кратно, по меньшей мере 1,8-кратно, по меньшей мере 1,9-кратно, по меньшей мере 2,0-кратно, по меньшей мере 2,2-кратно, по меньшей мере 2,3-кратно, по меньшей мере 2,4-кратно, по меньшей мере 2,5-кратно, по меньшей мере 3-кратно или по меньшей мере 4-кратно по сравнению с экспрессией у не получавшего лечения субъекта или у субъекта, получавшего лечение контрольным вектором. Согласно некоторым вариантам реализации экспрессия полинуклеотида LAMP-2B в виде мРНК в мышцах повышается 1,2-кратно, 1,3-кратно, 1,4-кратно, 1,5-кратно, 1,6-кратно, 1,7-кратно, 1,8-кратно, 1,9-кратно, 2,0-кратно, 2,2-кратно, 2,3-кратно, 2,4-кратно, 2,5-кратно, 3-кратно или 4-кратно по сравнению с экспрессией у не получавшего лечения субъекта или у субъекта, получавшего лечение контрольным вектором.
Согласно некоторым вариантам реализации указанный трансген LAMP-2B экспрессируется в сердце и не экспрессируется в печени указанного субъекта. Согласно некоторым вариантам реализации в сердце наблюдается по меньшей мере приблизительно 1,2-кратно, по меньшей мере приблизительно 1,3-кратно, по меньшей мере приблизительно 1,4-кратно, по меньшей мере приблизительно 1,5-кратно, по меньшей мере приблизительно 1,6-кратно, по меньшей мере приблизительно 1,7-кратно, по меньшей мере приблизительно 1,8-кратно, по меньшей мере приблизительно 1,9-кратно, по меньшей мере приблизительно 2,0-кратно, по меньшей мере приблизительно 2,2-кратно, по меньшей мере приблизительно 2,3-кратно, по меньшей мере приблизительно 2,4-кратно, по меньшей мере приблизительно 2,5-кратно, по меньшей мере приблизительно 3-кратно, или по меньшей мере приблизительно 4-кратно повышенная экспрессия полинуклеотида LAMP-2B в виде мРНК по сравнению с экспрессией в печени. Согласно некоторым вариантам реализации в сердце наблюдается по меньшей мере 1,2-кратно, по меньшей мере 1,3-кратно, по меньшей мере 1,4-кратно, по меньшей мере 1,5-кратно, по меньшей мере 1,6-кратно, по меньшей мере 1,7-кратно, по меньшей мере 1,8-кратно, по меньшей мере 1,9-кратно, по меньшей мере 2,0-кратно, по меньшей мере 2,2-кратно, по меньшей мере 2,3-кратно, по меньшей мере 2,4-кратно, по меньшей мере 2,5-кратно, по меньшей мере 3-кратно или по меньшей мере 4-кратно повышенная экспрессия полинуклеотида LAMP-2B в виде мРНК по сравнению с экспрессией в печени. Согласно некоторым вариантам реализации в сердце наблюдается 1,2-кратно, 1,3-кратно, 1,4-кратно, 1,5-кратно, 1,6-кратно, 1,7-кратно, 1,8-кратно, 1,9-кратно, 2,0-кратно, 2,2-кратно, 2,3-кратно, 2,4-кратно, 2,5-кратно, 3-кратно или 4-кратно повышенная экспрессия полинуклеотида LAMP-2B в виде мРНК по сравнению с экспрессией в печени.
Согласно некоторым вариантам реализации экспрессия белка LAMP-2B дикого типа или функционального белка LAMP-2B в сердце повышается по меньшей мере приблизительно 1,2-кратно, по меньшей мере приблизительно 1,3-кратно, по меньшей мере приблизительно 1,4-кратно, по меньшей мере приблизительно 1,5-кратно, по меньшей мере приблизительно 1,6-кратно, по меньшей мере приблизительно 1,7-кратно, по меньшей мере приблизительно 1,8-кратно, по меньшей мере приблизительно 1,9-кратно, по меньшей мере приблизительно 2,0-кратно, по меньшей мере приблизительно 2,2-кратно, по меньшей мере приблизительно 2,3-кратно, по меньшей мере приблизительно 2,4-кратно, по меньшей мере приблизительно 2,5-кратно, по меньшей мере приблизительно 3-кратно или по меньшей мере приблизительно 4-кратно по сравнению с экспрессией у не получавшего лечения субъекта или у субъекта, получавшего лечение контрольным вектором. Согласно некоторым вариантам реализации экспрессия белка LAMP-2B дикого типа или функционального белка LAMP-2B в сердце повышается по меньшей мере 1,2-кратно, по меньшей мере 1,3-кратно, по меньшей мере 1,4-кратно, по меньшей мере 1,5-кратно, по меньшей мере 1,6-кратно, по меньшей мере 1,7-кратно, по меньшей мере 1,8-кратно, по меньшей мере 1,9-кратно, по меньшей мере 2,0-кратно, по меньшей мере 2,2-кратно, по меньшей мере 2,3-кратно, по меньшей мере 2,4-кратно, по меньшей мере 2,5-кратно, по меньшей мере 3-кратно или по меньшей мере 4-кратно по сравнению с экспрессией у не получавшего лечения субъекта или у субъекта, получавшего лечение контрольным вектором. Согласно некоторым вариантам реализации экспрессия белка LAMP-2B дикого типа или функционального белка LAMP-2B в сердце повышается 1,2-кратно, 1,3-кратно, 1,4-кратно, 1,5-кратно, 1,6-кратно, 1,7-кратно, 1,8-кратно, 1,9-кратно, 2,0-кратно, 2,2-кратно, 2,3-кратно, 2,4-кратно, 2,5-кратно, 3-кратно или 4-кратно по сравнению с экспрессией у не получавшего лечения субъекта или у субъекта, получавшего лечение контрольным вектором.
Согласно некоторым вариантам реализации в сердце наблюдается по меньшей мере приблизительно 1,2-кратно, по меньшей мере приблизительно 1,3-кратно, по меньшей мере приблизительно 1,4-кратно, по меньшей мере приблизительно 1,5-кратно, по меньшей мере приблизительно 1,6-кратно, по меньшей мере приблизительно 1,7-кратно, по меньшей мере приблизительно 1,8-кратно, по меньшей мере приблизительно 1,9-кратно, по меньшей мере приблизительно 2,0-кратно, по меньшей мере приблизительно 2,2-кратно, по меньшей мере приблизительно 2,3-кратно, или по меньшей мере 5-кратно повышенная экспрессия белка LAMP-2B дикого типа или функционального белка LAMP-2B по сравнению с экспрессией в печени. Согласно некоторым вариантам реализации в сердце наблюдается по меньшей мере 1,2-кратно, по меньшей мере 1,3-кратно, по меньшей мере 1,4-кратно, по меньшей мере 1,5-кратно, по меньшей мере 1,6-кратно, по меньшей мере 1,7-кратно, по меньшей мере 1,8-кратно, по меньшей мере 1,9-кратно, по меньшей мере 2,0-кратно, по меньшей мере 2,2-кратно, по меньшей мере 2,3-кратно, по меньшей мере 2,4-кратно, по меньшей мере 2,5-кратно, по меньшей мере 3-кратно или по меньшей мере 4-кратно повышенная экспрессия белка LAMP-2B дикого типа или функционального белка LAMP-2B по сравнению с экспрессией в печени. Согласно некоторым вариантам реализации в сердце наблюдается 1,2-кратно, 1,3-кратно, 1,4-кратно, 1,5-кратно, 1,6-кратно, 1,7-кратно, 1,8-кратно, 1,9-кратно, 2,0-кратно, 2,2-кратно, 2,3-кратно, 2,4-кратно, 2,5-кратно, 3-кратно или 4-кратно повышенная экспрессия белка LAMP-2B дикого типа или функционального белка LAMP-2B по сравнению с экспрессией в печени.
Согласно некоторым вариантам реализации введение указанного геннотерапевтического вектора приводит к экспрессии белка LAMP-2B дикого типа или функционального белка LAMP-2B в печени, максимум приблизительно 1,1-кратно, максимум приблизительно 1,2-кратно, максимум приблизительно 1,3-кратно, максимум приблизительно 1,4-кратно, максимум приблизительно 1,5-кратно, максимум приблизительно 1,6-кратно, максимум приблизительно 1,7-кратно, максимум приблизительно 1,8-кратно, максимум приблизительно 1,9-кратно или максимум приблизительно 2-кратно повышенной по сравнению с экспрессией в печени не получавшего лечения субъекта. Согласно некоторым вариантам реализации введение указанного геннотерапевтического вектора приводит к экспрессии белка LAMP-2B дикого типа или функционального белка LAMP-2B в печени, максимум 1,1-кратно, максимум 1,2-кратно, максимум 1,3-кратно, максимум 1,4-кратно, максимум 1,5-кратно, максимум 1,6-кратно, максимум 1,7-кратно, максимум 1,8-кратно, максимум 1,9-кратно или максимум 2-кратно повышенной по сравнению с экспрессией в печени не получавшего лечения субъекта. Согласно некоторым вариантам реализации введение указанного геннотерапевтического вектора приводит к экспрессии белка LAMP-2B дикого типа или функционального белка LAMP-2B в печени, 1,1-кратно, 1,2-кратно, 1,3-кратно, 1,4-кратно, 1,5-кратно, 1,6-кратно, 1,7-кратно, 1,8-кратно, 1,9-кратно или 2-кратно повышенной по сравнению с экспрессией в печени не получавшего лечения субъекта.
Согласно варианту реализации настоящего изобретения предложен способ лечения заболевания или нарушения, необязательно – болезни Данона, у нуждающегося в этом субъекта, включающий приведение клеток в контакт с геннотерапевтическим вектором в соответствии с настоящим изобретением и введение указанных клеток указанному субъекту. Согласно варианту реализации указанные клетки представляют собой стволовые клетки, необязательно – плюрипотентные стволовые клетки. Согласно варианту реализации указанные стволовые клетки способны к дифференцировке в сердечную ткань. Согласно варианту реализации указанные стволовые клетки способны к дифференцировке в мышечную ткань, например, сердечную мышечную ткань и/или скелетную мышечную ткань. Согласно варианту реализации указанные стволовые клетки являются аутологичными. Согласно варианту реализации указанные стволовые клетки представляют собой индуцированные плюрипотентные стволовые клетки (ИПСК).
Согласно варианту реализации указанное заболевание или нарушение представляет собой аутофагическое нарушение. Согласно некоторым вариантам реализации указанное аутофагическое нарушение выбрано из группы, состоящей, но не ограничиваясь перечисленным, из терминальной сердечной недостаточности, инфаркта миокарда, лекарственных токсичностей, диабета, терминальной почечной недостаточности и старения. Согласно варианту реализации указанный субъект представляет собой млекопитающее, например, человека. Согласно варианту реализации у указанного субъекта наблюдаются симптомы болезни Данона или другого аутофагического нарушения. Согласно варианту реализации указанный субъект был идентифицирован как имеющий пониженную или недетектируемую экспрессию LAMP-2. Согласно варианту реализации указанный субъект был идентифицирован как имеющий мутированный ген LAMP-2.
Субъекты/пациенты, подходящие для лечения с применением способов, описанных в настоящем документе, включают, не ограничиваясь перечисленными, индивидуумов, у которых имеется риск развития заболевания или нарушения, характеризующегося недостаточным аутофагическим потоком (например, болезни Данона, а также других известных нарушений аутофагии, в том числе, не ограничиваясь перечисленными, систолической и диастолической сердечной недостаточности, инфаркта миокарда, лекарственных токсичностей (например, антрациклинов, хлорохина и его производных), диабета, терминальной почечной недостаточности и старения), не не проявляющегося симптомами, а также субъектов, у которых в рассматриваемое время наблюдаются симптомы. Такой субъект мог быть идентифицирован как имеющий мутированный ген LAMP-2, или характеризующийся пониженными или недетектируемыми уровнями экспрессии LAMP-2.
Согласно некоторым вариантам реализации указанный пациент представляет собой человека. Согласно некоторым вариантам реализации указанный пациент представляет собой ребенка, подростка или взрослого человека. Согласно некоторым вариантам реализации возраст указанного пациента составляет 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20 лет, или более 20 лет. Согласно некоторым вариантам возраст указанного пациента составляет 20–50 лет. Согласно некоторым вариантам реализации возраст указанного пациента составляет 50–65 лет. Согласно некоторым вариантам реализации возраст указанного пациента составляет 1–5, 2–6, 3–7, 4–8, 5–9, 6–10, 7–11, 8–12, 9–13, 10–14, 11–15, 12–16, 13–17, 14–18, 15–19 или 16–20 лет. Согласно некоторым вариантам реализации возраст указанного пациента составляет 5–6, 6–7, 7–8, 8–9, 9–10, 10–11, 11–12, 12–13, 13–14, 14–15, 15–16, 16–17, 17–18, 18–19, 19–20 или 20–21 лет. Согласно конкретному варианту реализации возраст указанного пациента составляет 15–16 лет.
Согласно некоторым вариантам реализации указанный пациент представляет собой человека мужского пола. Согласно некоторым вариантам реализации указанный пациент представляет собой ребенка, подростка или взрослого человека мужского пола. Согласно некоторым вариантам реализации указанный пациент представляет собой человека мужского пола возрастом 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20 лет, или более 20 лет. Согласно некоторым вариантам реализации указанный пациент представляет собой человека мужского пола возрастом 20–50 лет. Согласно некоторым вариантам реализации указанный пациент представляет собой человека мужского пола возрастом 50–65 лет. Согласно некоторым вариантам реализации указанный пациент представляет собой человека мужского пола возрастом 1–5, 2–6, 3–7, 4–8, 5–9, 6–10, 7–11, 8–12, 9–13, 10–14, 11–15, 12–16, 13–17, 14–18, 15–19 или 16–20 лет. Согласно некоторым вариантам реализации указанный пациент представляет собой человека мужского пола возрастом 5–6, 6–7, 7–8, 8–9, 9–10, 10–11, 11–12, 12–13, 13–14, 14–15, 15–16, 16–17, 17–18, 18–19, 19–20 или 20–21 лет. Согласно конкретному варианту реализации возраст указанного пациента составляет 15–16 лет.
Согласно некоторым вариантам реализации указанный пациент представляет собой человека женского пола. Согласно некоторым вариантам реализации указанный пациент представляет собой ребенка, подростка или взрослого человека женского пола. Согласно некоторым вариантам реализации указанный пациент представляет собой человека женского пола возрастом 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20 лет, или более 20 лет. Согласно некоторым вариантам реализации указанный пациент представляет собой человека женского пола возрастом 20–50 лет. Согласно некоторым вариантам реализации указанный пациент представляет собой человека женского пола возрастом 50–65 лет.
Согласно некоторым вариантам реализации у указанного субъекта наблюдаются симптомы заболевания или нарушения, характеризующегося недостаточным аутофагическим потоком (например, болезни Данона, а также других известных нарушений аутофагии, в том числе, но не ограничиваясь перечисленными, систолической и диастолической сердечной недостаточности, инфаркта миокарда, лекарственных токсичностей, диабета, терминальной почечной недостаточности и старения). Указанные симптомы могут проявляться активно, или могут быть подавлены или находиться под контролем (например, с применением медикамента) или в ремиссии. У указанного субъекта может быть диагностировано или не диагностировано указанное нарушение , например, квалифицированным медицинским специалистом.
Определения
Термины «ассоциированный с лизосомами мембранный белок 2» и «LAMP-2» взаимозаменяемо относятся к нуклеиновым кислотам и полиморфным вариантам, аллелям, мутантам и межвидовым гомологам полипептидов, которые: (1) имеют последовательность аминокислот, более чем приблизительно на 90%, например, на 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% или более идентичную, предпочтительно на протяжении области размером по меньшей мере приблизительно 25, 50, 100, 200, 300, 400 или более аминокислот, или на протяжении всей последовательности, последовательности аминокислот, кодируемой нуклеиновой кислотой LAMP-2 (см., например, №№ доступа в GenBank NM_002294.2 (изоформа A). NM_013995.2 (изоформа B), NM_001122606.1 (изоформа C)), или последовательности аминокислот полипептида LAMP-2 (см., например, №№ доступа в GenBank NP_002285.1 (изоформа A), NP_054701.1 (изоформа B), NP_001116078.1 (изоформа C)); (2) связываются с антителами, например, поликлональными индуцированными антителами против иммуногена, содержащего последовательность аминокислот полипептида LAMP-2 (например, полипептидов LAMP-2, описанных в настоящем документе); или последовательность аминокислот, кодируемую нуклеиновой кислотой LAMP-2 (например, полинуклеотидами LAMP-2, описанными в настоящем документе), и ее консервативно модифицированные варианты; (3) специфически гибридизуются в жестких условиях гибридизации с антисмысловой цепью, соответствующей последовательности нуклеиновой кислоты, кодирующей белок LAMP-2, и ее консервативно модифицированным вариантам; (4) имеют последовательность нуклеиновой кислоты, более чем приблизительно на 90%, предпочтительно более чем приблизительно на 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более, предпочтительно на протяжении области размером по меньшей мере приблизительно 25, 50, 100, 200, 500, 1000, 2000 или более нуклеотидов, или на протяжении всей последовательности, идентичную последовательности нуклеотидов нуклеиновой кислоты LAMP-2 (например, полинуклеотидам LAMP-2 согласно описанию в настоящем документе и полинуклеотидам LAMP-2, которые кодируют полипептиды LAMP-2 согласно описанию в настоящем документе).
Термины «ассоциированный с лизосомами мембранный белок 2B» и «LAMP-2B» используются взаимозаменяемо и относятся к нуклеиновым кислотам и полиморфным вариантам, аллелям, мутантам и межвидовым гомологам полипептидов, которые: (1) имеют последовательность аминокислот, более чем приблизительно на 90%, например, на 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% или более, предпочтительно на протяжении области размером по меньшей мере приблизительно 25, 50, 100, 200, 300, 400 или более аминокислот, или на протяжении всей последовательности идентичную последовательности аминокислот, кодируемой нуклеиновой кислотой LAMP-2B (см., например, NM_013995.2) или последовательности аминокислот полипептида LAMP-2B (см., например, NP_054701.1); (2) связываются с антителами, например, индуцированными поликлональными антителами против иммуногена, содержащего последовательность аминокислот полипептида LAMP-2B (например, полипептидов LAMP-2B, описанных в настоящем документе); или последовательность аминокислот, кодируемую нуклеиновой кислотой LAMP-2B (например, полинуклеотиды LAMP-2B, описанные в настоящем документе), и ее консервативно модифицированные варианты; (3) специфически гибридизуются в жестких условиях гибридизации с антисмысловой цепью, соответствующей последовательности нуклеиновой кислоты, кодирующей белок LAMP-2B, и ее консервативно модифицированным вариантам; (4) имеют последовательность нуклеиновой кислоты, более чем приблизительно на 90%, предпочтительно более чем приблизительно на 91 %, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичную, предпочтительно на протяжении области размером по меньшей мере приблизительно 25, 50, 100, 200, 500, 1000, 2000 или более нуклеотидов, или на протяжении всей последовательности, нуклеиновой кислоте LAMP-2B (например, полинуклеотидам LAMP-2B согласно описанию в настоящем документе и полинуклеотидам LAMP-2B, которые кодируют полипептиды LAMP-2B согласно описанию в настоящем документе).
Термин «функциональный вариант» в отношении белка (например, LAMP-2B) относится к последовательности полипептида или фрагменту последовательности полипептида, содержащей (содержащему) по меньшей мере приблизительно 30, по меньшей мере приблизительно 40, по меньшей мере приблизительно 50, по меньшей мере приблизительно 60, по меньшей мере приблизительно 70 или по меньшей мере приблизительно 80 остатков аминокислот, которая (который) сохраняет один или более функциональных особенностей белка. Например, функциональный вариант LAMP-2B представляет собой LAMP-2B (согласно определению в настоящем документе), который сохраняет одну или более из таких функций, как: (1) регуляция функции кардиомиоцитов человека (Chi et al. (2019) PNAS USA 116 (2) 556-565); (2) улучшение метаболической и физиологической функции при болезни Данона (Adler et al. (2019) J. Am. College Cardiology S0735-1097(19)31295-1); и/или (3) аутофагия (Rowland et al. (2016) J. Cell Sci. (2016) 129, 2135-2143).
LAMP-2B содержит люминальный домен (остатки 29–375), трансмембранный домен (остатки 376–399) и цитоплазматический домен (остатки 400–410), см. номер доступа UniProt P13473. Функции LAMP-2B включают шаперон-опосредованную аутофагию, процесс, который опосредует лизосомальное разложение белков в ответ на различные виды стресса и в рамках нормального оборота белков с продолжительным биологическим временем полужизни (Cuervo et al. Science 273:501-503(1996), Cuervo et al. J. Cell Sci. 113:4441-4450(2000), Bandyopadhyay et al. Mol. Cell. Biol. 28:5747-5763(2008), Li et al. Exp. Cell Res. 327:48-56(2014), Hubert et al. Biol. Open 5:1516-1529(2016)). LAMP-2B может быть нацелен на ГАФДГ и MLLT11 для лизосомального разложения. LAMP-2B может быть необходим для слияния аутофагосом с лизосомами при аутофагии. Было высказано предположение, что клетки, в которых отсутствует LAMP2, экспрессируют нормальные уровни VAMP8, однако не способны к накоплению STX17 на аутофагосомах, что является наиболее вероятным объяснением отсутствия слияния аутофагосом с лизосомами. LAMP-2B может быть необходим для нормального разложения содержимого аутофагосом. LAMP-2B может быть необходим для эффективной опосредованной MHCII презентации экзогенных антигенов за счет его функции при лизосомальном разложении белков; антигенные пептиды, генерируемые протеазами в эндосомальном/лизосомальном компартменте, захватываются образующимися субъединицами MHCII (Crotzer et al. Immunology 131:318-330(2010)).
Функциональные варианты LAMP-2B, соответственно, включают фрагменты LAMP-2B, которые способны опосредовать любую из вышеописанных функций. Согласно некоторым вариантам реализации указанный функциональный фрагмент LAMP-2B включает что-либо одно или более из люминального, трансмембранного и цитоплазматического доменов. Согласно некоторым вариантам реализации указанный функциональный вариант LAMP-2B содержит одну или более C-концевых или N-концевых делеций относительно природного LAMP-2B. Согласно некоторым вариантам реализации указанный функциональный вариант LAMP-2B содержит одну или более внутренних делеций относительно природного LAMP-2B.
Термины «идентичный» или процент «идентичности» в контексте двух или более последовательностей нуклеиновых кислот или полипептидов относятся к двум или более последовательностям или подпоследовательностям, одинаковым или содержащим определенный процент одинаковых остатков аминокислот или нуклеотидов (т.е. по меньшей мере приблизительно на 80% идентичным, например, по меньшей мере приблизительно на 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентичным референсной последовательности на протяжении определенной области, например, последовательностям полинуклеотида или полипептида LAMP-2 согласно описанию в настоящем документе, при сравнении и выравнивании с достижением максимального соответствия в пределах окна сравнения или заданной области, по оценке с применением одного из описанных ниже алгоритмов сравнения последовательностей или путем выравнивания вручную и визуального исследования. В указанном случае такие последовательности называют «по существу идентичными». Указанное определение также относится к комплементу тестируемой последовательности. Предпочтительно, идентичность наблюдается на протяжении области длиной по меньшей мере приблизительно 25 аминокислот или нуклеотидов, например, на протяжении области длиной 50, 100, 200, 300, 400 аминокислот или нуклеотидов, или на протяжении всей референсной последовательности.
При сравнении последовательностей, как правило, одна последовательность выступает в роли референсной последовательности, с которой сравнивают тестируемые последовательности. При использовании алгоритма сравнения последовательностей тестируемые и референсные последовательности вводят в компьютер, назначают координаты подпоследовательности, при необходимости, и назначают программные параметры алгоритма сравнения последовательностей. Могут быть использованы установленные по умолчанию параметры программы, или могут быть назначены альтернативные параметры. Затем алгоритм сравнения последовательностей вычисляет процент идентичности тестируемых последовательностей и референсной последовательности на основании параметров программы. При сравнении последовательностей нуклеиновых кислот и белков с нуклеиновыми кислотами и белками LAMP-2 используют алгоритмы BLAST и BLAST 2.0 и установленные по умолчанию параметры.
«Окно сравнения» в настоящем документе относится к сегменту, содержащему любое число непрерывных положений, выбранное из группы, состоящей из 20–600, обычно от приблизительно 50 до приблизительно 200, чаще от приблизительно 100 до приблизительно 150, в пределах которого может проводиться сравнение последовательности с референсной последовательностью, содержащей такое же число непрерывных положений, после того как указанные две последовательности были подвергнуты оптимальному выравниванию. Способы выравнивания последовательностей для сравнения хорошо известны в данной области техники. Оптимальное выравнивание последовательностей для сравнения может быть проведено, например, с применением алгоритма локальной гомологии согласно источнику: Smith & Waterman, Adv. Appl. Math. 2:482 (1981), с применением алгоритма для областей гомологии согласно источнику: Needleman & Wunsch, J. Mol. Biol. 48:443 (1970), с применением метода поиска подобия согласно источнику: Pearson & Lipman, Proc. Nat’l. Acad. Sci. USA 85:2444 (1988), с помощью компьютеризированных вариантов указанных алгоритмов (GAP, BESTFIT, FASTA и TFASTA из пакета программного обеспечения Wisconsin Genetics, Genetics Computer Group, 575 Сайенс Драйв, Мэдисон, Висконсин) или путем выравнивания вручную и визуального исследования (см., например, Ausubel et al., eds., Current Protocols in Molecular Biology (1995 supplement)). Примеры алгоритмов, подходящих для определения процента идентичности последовательностей и сходства последовательностей представлены алгоритмами BLAST и BLAST 2.0, которые описаны в источнике: Altschul et al., J. Mol. Biol. 215:403-410 (1990) и Altschul et al., Nucleic Acids Res. 25:3389-3402 (1977), соответственно. Открытый доступ к программному обеспечению для проведения анализа с помощью BLAST предоставлен Национальным центром биотехнологической информации (в сети Интернет по адресу: ncbi.nlm.nih.gov/).
Показателем того, что две последовательности нуклеиновых кислот или полипептидов по существу идентичны, является иммунологическая перекрестная реактивность полипептида, кодируемого первой нуклеиновой кислотой, в отношении антител, индуцированных против полипептида, кодируемого второй нуклеиновой кислотой, согласно приведенному ниже описанию. Соответственно, полипептид, как правило, по существу идентичен второму полипептиду, например, если указанные два пептида различаются только консервативными заменами. Другим показателем того, что две последовательности нуклеиновых кислот по существу идентичны, является то, что указанные две молекулы или их комплементы гибридизуются друг с другом в жестких условиях. Еще одним показателем того, что две последовательности нуклеиновых кислот по существу идентичны, является то, что для амплификации последовательности могут быть использованы одни и те же праймеры.
В настоящем документе «введение» относится к локальному и системному введению, в том числе, например, энтеральному, парентеральному, легочному и местному/чрескожному введению. Маршруты введения соединений (например, полинуклеотида, кодирующего одну или более изоформ LAMP-2), подходящие для применения в способах, описанных в настоящем документе, включают, например, пероральное (внутрь (п/о)) введение, назальное или ингаляционное введение, введение в виде суппозитория, местный контакт, чрескожную доставку (например, через трансдермальный пластырь), интратекальное (и/т) введение, внутривенное («в/в») введение, внутрибрюшинное («в/б») введение, внутримышечное («в/м») введение, внутриочаговое введение или подкожное («п/к») введение, или имплантацию устройства для медленного высвобождения, например, осмотического мини-насоса, депо- состава и т.п., субъекту. Введение может осуществляться с использованием любого пути, в том числе парентерального и трансмукозального (например, перорального, назального, вагинального, ректального или чрескожного). Парентеральное введение включает, например, внутривенное, внутримышечное, внутриартериальное, внутрипочечное, внутриуретральное, внутрисердечное, интракоронарное, интрамиокардиальное, внутрикожное, эпидуральное, подкожное, внутрибрюшинное, интравентрикулярное, ионофоретическое и интракраниальное. Другие способы доставки включают, не ограничиваясь перечисленным, применение липосомальных составов, внутривенной инфузии, трансдермальных пластырей и т.п.
Термины «системное введение» и «системно введенный» относятся к способу введения соединения или композиции млекопитающему, обеспечивающему доставку указанных соединения или композиции в участки в организме, в том числе в целевой участок фармацевтического действия, через систему кровообращения. Системное введение включает, не ограничиваясь перечисленным, пероральное, интраназальное, ректальное и парентеральное (например, не через пищеварительный тракт, например, внутримышечное, внутривенное, внутриартериальное, чрескожное и подкожное) введение.
Термин «совместное введение» или «одновременное введение», например, применительно к соединениям (например, полинуклеотидам LAMP-2) и/или их аналогам и другому активному агенту, относится к введению указанного соединения и/или аналогов и указанного активного агента таким образом, чтобы они оба могли одновременно обеспечивать физиологический эффект. Указанные два агента, однако, не обязательно вводят вместе. Согласно некоторым вариантам реализации введение одного агента может предшествовать введению другого агента. Одновременный физиологический эффект не обязательно требует присутствия обоих агентов в кровотоке в одно и то же время. Однако согласно некоторым вариантам реализации совместное введение, как правило, приводит к тому, что в организме (например, в плазме) одновременно присутствует значительная часть обоих агентов (например, 20% или более, например, 30% или 40% или более, например, 50% или 60% или более, например, 70%, или 80%, или 90%, или более) относительно максимальной концентрации в сыворотке при любой заданной дозе.
Термин «эффективное количество» или «фармацевтически эффективное количество» относится к количеству и/или дозировке, и/или режиму дозирования одного или более соединений (например, геннотерапевтических векторов), необходимым для достижения требуемого результата, например, повышенной экспрессии одной или более изоформ LAMP-2 в количестве, достаточном для снижения максимальной степени тяжести заболевания, характеризующейся нарушенной или недостаточной аутофагией (например, болезни Данона).
Выражение «причина для введения» относится к действиям, предпринимаемым медицинским специалистом (например, лечащим врачом) или лицом, контролирующим медицинское обслуживание субъекта, контролирующим и/или позволяющим введение рассматриваемого агента (агентов)/соединения (соединений) указанному субъекту. Определение причины для введения может включать установление диагноза, и/или определение подходящего терапевтического или профилактического режима, и/или назначение конкретного агента (агентов)/соединений субъекту. Такое назначение может включать, например, составление рецепта, аннотирование медицинской карты и т.п.
В настоящем документе термины «лечить» и «лечение» относятся к задержке возникновения, замедлению или обращению прогрессирования, уменьшению тяжести, или смягчению или предотвращению либо заболевания или состояния, в отношении которого используется термин, либо к одному или более симптомам такого заболевания или состояния. Термины «лечить» и «лечение» также включают предотвращение, смягчение, облегчение, уменьшение, ингибирование, устранение и/или обращение одного или более симптомов указанного заболевания или состояния.
Термин «смягчение» относится к снижению или устранения одного или более симптомов указанной патологии или указанного заболевания, и/или снижению уровня или задержке возникновения, или снижению тяжести одного или более симптомов указанной патологии или указанного заболевания, и/или предотвращению указанной патологии или указанного состояния. Согласно некоторым вариантам реализации указанные снижение или устранение одного или более симптомов патологии или заболевания могут включать, например, измеряемое и продолжительное повышение уровней экспрессии одной или более изоформ LAMP-2.
В настоящем документе выражение «состоящий по существу» относится к родам или видам активных фармацевтических агентов, упоминаемых применительно к способу или композиции, и дополнительно может включать другие агенты, которые сами по себе по существу не обладают активностью, имеющей отношение к указанному показанию или цели.
Термины «субъект», «индивидуум» и «пациент» используются взаимозаменяемо и относятся к млекопитающему, предпочтительно человеку или не являющемуся человеком примату, а также к одомашненным млекопитающим (например, собачьим или кошачьим), лабораторным млекопитающим (например, мыши, крысе, кролику, хомяку, морской свинке) и сельскохозяйственным млекопитающим (например, лошадям, крупному рогатому скоту, свиньям, овцам). Согласно различным вариантам реализации указанный субъект может представлять собой человека (например, взрослого человека мужского пола, взрослого человека женского пола, подросток мужского пола, подросток женского пола, ребенок мужского пола, ребенок женского пола).
Термины «перенос генов» или «доставка генов» относятся к способам или системам для надежной инсерции чужеродной ДНК в клетки-хозяева. Такие способы могут обеспечивать транзиентную экспрессию неинтегрированной перенесенной ДНК, внехромосомную репликацию и экспрессию перенесенных репликонов (например, эписом) или интеграцию переносимого генетического материала в геномную ДНК клеток-хозяев.
Термин «вектор» используют в настоящем документе для обозначения молекулы нуклеиновой кислоты, способной переносить или транспортировать другую молекулу нуклеиновой кислоты. Переносимая нуклеиновая кислота обычно соединена с молекулой нуклеиновой кислоты вектора, например, инсертирована в нее. Вектор может включать последовательности, направляющие автономную репликацию или обратную транскрипцию в клетке, или может включать последовательности, достаточные для обеспечения интеграции в ДНК клетки-хозяина. «Векторы» включают геннотерапевтические векторы. В настоящем документе термин «геннотерапевтический вектор» относится к вектору, подходящему для применения при проведении генной терапии, например, для доставки полинуклеотидной последовательности, кодирующей терапевтический полипептид, субъекту. Геннотерапевтические векторы могут содержать молекулу нуклеиновой кислоты («трансген»), кодирующую терапевтически активный полипептид, например, LAMP-2B или другой ген, подходящий для заместительной генной терапии при введении субъекту. Подходящие векторы включают, не ограничиваясь указанными, вирусные векторы.
В настоящем документе термин «экспрессионная кассета» относится к сегменту ДНК, который способен в подходящих условиях управлять экспрессией полинуклеотида («трансгена»), кодирующего терапевтически активный полипептид (например, LAMP-2B), который включен в указанную экспрессионную кассету. При введении в клетку-хозяина экспрессионная кассета, в том числе, может направлять механизмы клетки на транскрипцию трансгена в РНК, которая затем, как правило, претерпевает процессинг и, наконец, транслируется в терапевтически активный полипептид. Указанная экспрессионная кассета может входить в состав геннотерапевтического вектора. В общем случае термин «экспрессионная кассета» исключает полинуклеотидные последовательности, расположенные в направлении 5′ относительно 5′-ITR и в направлении 3′ относительно 3′-ITR.
Все патенты, патентные публикации и другие публикации, упоминаемые и указанные в настоящем описании, индивидуально и явным образом включены в настоящий документ посредством ссылок полностью и для любых целей.
ПРИМЕРЫ
ПРИМЕР 1: Усиленная генная экспрессия при применении вариантов трансгена Lamp-2B
Кассету для генной экспрессии, изображенную на фиг. 2, встраивали в репортерную систему с зеленым флуоресцентным белком (GFP) на основе плазмиды для экспрессии трансгена LAMP-2B. Указанная плазмида включала одну открытую рамку считывания, кодирующую трансген LAMP-2B, пептид 2A и усиленный зеленый флуоресцентный белок (eGFP). Посттрансляционное саморасщепление пептида 2A приводило к коэкспрессии LAMP-2B и eGFP в эквимолярных количествах. В качестве трансгенов тестировали кодирующую последовательность LAMP-2B дикого типа (SEQ ID NO: 2) и три варианта кодонов кодирующей последовательности LAMP-2B (варианты кодонов 1, 2 и 3; SEQ ID NO: 3–5, соответственно). Указанные три варианта кодонов характеризовались пониженным количеством CpG, удалением скрытых сайтов и пониженным количеством открытых рамок считывания относительно кодирующей последовательности LAMP-2B дикого типа.
Сорок лунок CellBIND 96-луночного планшета (NUNC #3300) покрывали 0,1% желатином в воде (Millipore ES-006-B) в течение 1 часа при комнатной температуре. Приблизительно 88 000 происходящих из индуцированных плюрипотентных стволовых клеток (ИПСК) кардиомиоцитов (VWR MSPP-CMC10001) высевали в каждую лунку в среде для посева (VWR #M1001) при 37ºC с 5% диоксида углерода (CO2). Через 4 часа среду заменяли на поддерживающую среду (VWR #M1003), которую предварительно уравновешивали до достижения 37ºC и 5% CO2. Получали смесь для трансфекции, добавляя 6 мкл реагента для трансфекции (ViaFect Promega #E4982) к 128 мкл 0,015 мкг/мкл плазмиды (дикого типа или вариантов кодонов 1, 2 или 3) в OptiMEM или OptiMEM + только ViaFect (отрицательный контроль), и инкубировали в течение 10–20 мин. 100 мкл указанной смеси для трансфекции добавляли к 1 мл поддерживающей среды, которую предварительно уравновешивали до 37ºC и 5% CO2.
Приблизительно через 28 часов после первоначального посева в каждую лунку добавляли по 100 мкл указанной смеси для трансфекции в поддерживающей среде. Приблизительно через 48 часов после добавления среды со смесью для трансфекции клетки визуализировали и проводили анализ на GFP-положительные клетки с помощью автоматизированного конфокального микроскопа (Perkin Elmer Operetta CLS, программное обеспечение Harmony, версия 4.5) (фиг. 3), а также измеряли среднюю интенсивность флуоресценции (фиг. 4). Иммунофлуоресцентные снимки клеток через два дня или семь дней после трансфекции приведены на фиг. 5 и фиг. 6, соответственно.
На фиг. 3 показано, что использование вариантов кодонов 1 («CO 1») или 2 («CO 2») приводило к экспрессии GFP в значимо большем (~ 9-кратном) количестве клеток по сравнению с экспрессией трансгена дикого типа. Аналогичным образом, на фиг. 4 показано, что средняя интенсивность GFP в клетках, трансфицированных вариантами кодонов 1 («CO 1») и 2 («CO 2») была в 1,5 раза выше, чем экспрессия трансгена дикого типа.
ПРИМЕР 2: Оптимизированные геннотерапевтические векторы с LAMP-2B
Оптимизированные геннотерапевтические AAV-векторы получают путем инсерции оптимизированного варианта LAMP-2B, последовательности CO1, описанной в примере 1, в экспрессионную кассету рекомбинантного AAV-вектора. Регуляторная кассета AAV модифицирована путем удаления расположенной в направлении 5’ скрытой последовательности ATG, применения оптимизированной консенсусной последовательности Козак и/или полноразмерной последовательности полиаденилирования. Векторы тестируют, сравнивая с контрольными рекомбинантными AAV-векторами, содержащими один или более дополнительных сайтов ATG в направлении 5’ от трансгена, неоптимальную последовательность Козак и/или неполноразмерную последовательность полиаденилирования. Векторы тестируют in vitro в происходящих из ИПСК пациента с болезнью Данона кардиомиоцитах и в модели болезни Данона на нокаутных мышах LAMP-2-/-. Ожидается, что оптимизированные геннотерапевтические AAV-кассеты и векторы обеспечат более высокий уровень экспрессии и/или экспрессии в большем проценте клеток по сравнению с контрольными рекомбинантными AAV-векторами.
ПРИМЕР 3: Оценка AAV9-LAMP-2B.v1.2 in vitro
Геннотерапевтические AAV-кассету и вектор получали путем инсерции варианта последовательности LAMP-2B CO1 (SEQ ID NO: 3) в рекомбинантный плазмидный AAV-вектор без скрытых стартовых сайтов в направлении 5’ от трансгена, с оптимизированной консенсусной последовательностью Козак и полноразмерной последовательностью полиаденилирования ((поли)А) глобина кролика («LAMP-2B.v.1.2»; экспрессионная кассета: SEQ ID NO: 8). LAMP-2B.v1.2 сравнивали с LAMP-2B v1.0, которая представляет собой регуляторную кассету, содержащую трансген LAMP-2B дикого типа (последовательность трансгена: SEQ ID NO: 2) без оптимальной последовательности Козак и мини-(поли)А.
Клетки HEK293 использовали для получения вирусных частиц с трехплазмидной системой без хелперного вируса, с получением рекомбинантных AAV-частиц, содержащих капсидные белки серотипа 9 и вирусные геномы, содержащие ITR AAV2, фланкирующие экспрессионную кассету LAMP-2B. Указанная экспрессионная кассета содержит кодон-оптимизированную кодирующую последовательность LAMP-2B человека (v1.2 или v1.0), управляемую расположенным в направлении 5’ химерным промотором «CAG», содержащим энхансер средних и ранних генов цитомегаловируса (CMV IE) (CMV IE), промотор β-актина курицы (CBA) и донор сплайсинга интрона CBA (фиг. 1A). Указанная экспрессионная кассета также включает расположенный в направлении 3’ элемент WPRE и заканчивается сигналом полиаденилирования бета-глобина кролика (RGpA). Клетки HEK293 транзиентно трансфицировали плазмидным вектором LAMP-2B.v1.2 или плазмидным вектором LAMP-2B.v1.0, пакующей плазмидой pAAV2/9 и аденовирусной хелперной плазмидой pAd-Helper.
Клетки CHO-Lec2 высевали в 24-луночный планшет с плотностью 1,2×105 клеток/мл в MEM-α, содержащую 10% ФБС и 1% нормоцина. На следующий день клетки CHO-Lec2 трансдуцировали в не содержащей сыворотки среде MEMα либо AAV9-LAMP-2B.v1.0, либо AAV9-LAMP-2B.v1.2, либо тем же вектором, содержащим GFP вместо трансгена LAMP-2B (с MOI = 3×105). Через семь дней после трансдукции лизаты собирали с применением набора для лизиса клеток млекопитающих (Sigma) и определяли количество общего белка с применением набора MicroBCA в соответствии с инструкциями изготовителя. Белки разделяли в ДСН-ПААГ, переносили на нитроцеллюлозные мембраны и проводили иммуноблоттинг на LAMP-2B (1:500) и ГАФДГ (1:10000). Клетки CHO-Lec2, трансдуцированные AAV9 с оптимизированным LAMP-2B.v1.2, демонстрировали повышенную экспрессию по сравнению с клетками CHO-Lec2, трансдуцированными оригинальным AAV9 с LAMP-2B.v1.0 дикого типа (фиг. 7A). LAMP-2B не был детектирован в клетках, трансдуцированных вектором AAV9–GFP по отдельности (фиг. 7A).
Экспрессию LAMP-2B также количественно анализировали в клеточных лизатах с применением ИФА ELISA. Вкратце, 96-луночный планшет покрывали антителом против LAMP-2B (клон: H4B4), лизаты добавляли в лунки и проводили детекцию с применением поликлонального антитела против LAMP-2B (1:500, Thermo Fisher PA; 5-24575) с последующей инкубацией с HRP-конъюгированным антителом против кролика (1:3000, Sigma). Трансдукция AAV9-вектором с оптимизированным LAMP-2B.v1.2 приводила к приблизительно 7-кратному повышению экспрессии LAMP-2B по сравнению с экспрессией в клетках, трансдуцированных AAV9-LAMP-2B.v1.0 дикого типа (фиг. 7B).
Кардиомиоциты были получены из ИПСК от индивидуумов с болезнью Данона. После ритмического сокращения и отбора на чистоту кардиомиоциты от пациентов с болезнью Данона трансдуцировали различным числом копий вирусного генома (вг), используя AAV9–Luc (отрицательный контроль), AAV9 с LAMP-2B.v1.0 дикого типа или AAV9 с оптимизированным LAMP-2B.v1.2. Через 10 дней после трансдукции трансдуцированные кардиомиоциты фиксировали 4% параформальдегидом, пермеабилизировали, блокировали в течение 30 минут в 5% БСА без IgG и инкубировали в течение 1 часа либо с антителом мыши против LAMP-2B (1:25, клон: H4B4), либо с антителом кролика против α-актинина (1:200, #A7811, Sigma). Клетки промывали 1X ФСБ для удаления остаточного несвязанного первичного антитела, а затем обрабатывали подходящим меченым AlexaFluor вторичным антителом против АТ мыши и 200 нг/мл DAPI в течение 60 минут при комнатной температуре. Затем лунки промывали ФСБ перед визуализацией. Более высокий уровень экспрессии LAMP-2B человека наблюдался в кардиомиоцитах, трансдуцированных низким титром (1,56×108 вг/лунку) AAV9-вектора с оптимизированным LAMP-2B.v1.2, по сравнению с кардиомиоцитами, трансдуцированными максимальным титром (8,45×1010 вг/лунку) AAV9 с LAMP-2B.v1.0 дикого типа (фиг. 8A и фиг. 8B).
Анализ методом вестерн-блоттинга выполняли на трансдуцированных кардиомиоцитах пациентов с болезнью Данона. AAV9 с оптимизированным LAMP-2B.v1.2 в дозе 0,983×109 вг/лунку продемонстрировал значимую экспрессию белка LAMP-2B, при этом белок LAMP-2B не был детектирован в клетках, трансдуцированных вектором AAV9 с LAM2B.v1.0 дикого типа (1,347×109 вг/лунку) или вектором AAV9–Luc (1,167×109 вг/лунку) (фиг. 8C). В совокупности указанные результаты демонстрируют, что оптимизированный вектор AAV9-LAMP-2B.v1.2 опосредует экспрессию LAMP-2B человека в кардиомиоцитах пациентов с болезнью Данона на значимо более высоком уровне, чем оригинальный вектор AAV9 с LAMP-2B.v1.0 дикого типа.
ПРИМЕР 4: Оценка AAV9-LAMP-2B.v1.2 в модели болезни Данона на мышах in vivo
Мышам с дефицитом LAMP-2 внутривенно инъецировали 1×1013 вг/кг вирусных AAV9-векторов, содержащих оригинальный LAMP-2B человека (AAV9–LAMP-2B.v1.0), оптимизированный LAMP-2B человека (AAV9–LAMP-2B.v1.2, вариант кодонов 1 – SEQ ID NO: 3) или отдельно основу. Через шесть недель после лечения мышей умерщвляли и собирали ткани сердца для анализа экспрессии LAMP-2B.
Способы
Для проведения количественных анализов на число копий вектора тотальную ДНК выделяли из замороженных тканей с применением набора для выделения из крови и тканей DNeasy в соответствии с инструкциями производителя. Концентрацию и целостность ДНК оценивали спектрофотометрически. Проводили кПЦР для расчета числа копий вирусного генома на мкг ДНК с применением мастер-микса TaqPath ProAmp Master Mix (Applied Biosystems) с прямым (5′-ATCATGCTATTGCTTCCCGTA-3′; SEQ ID NO: 36) и обратным (5′-GGGCCACAACTCCTCATAAA-3′; SEQ ID NO: 37) праймерами и зондом (5′-CCTCCTTGTATAAATCCTGGTTGCTGTCT-3′; SEQ ID NO: 38) для гена WPRE. В качестве эндогенного контроля использовали РНКазу P (Thermofisher, #4403328). Строили стандартную кривую с применением линеаризованной плазмиды, которая содержала векторный геном (WPRE), используемый для получения вируса. Количество ДНК на образец рассчитывали с применением референсного набора TaqMan для анализа числа копий и выражали через число копий вектора на диплоидное ядро (VCN/диплоидное ядро).
РНК экстрагировали и очищали из сердца с применением набора RNeasy Fibrous Tissue Mini Kit в соответствии с протоколом производителя. Концентрацию и целостность РНК оценивали спектрофотометрически. РНК обратно-транскрибировали с применением набора для синтеза кДНК iScript и использовали кДНК в качестве матрицы для количественной ПЦР в реальном времени (кРВ-ПЦР). кРВ-ПЦР проводили на кДНК с применением мастер-микса TaqPath ProAmp Master Mix с прямым (5′-ATCATGCTATTGCTTCCCGTA-3′; SEQ ID NO: 36) и обратным (5′-GGGCCACAACTCCTCATAAA-3′; SEQ ID NO: 37) праймерами и зондом (5′-CCTCCTTGTATAAATCCTGGTTGCTGTCT-3′; SEQ ID NO: 38) для гена WPRE.
Для экстракции белка ткани мгновенно замораживали и тонко измельчали, полученный порошок ткани расщепляли в буфере для лизиса белков (100 мМ Tris, 300 мМ NaCl, 20 мМ ЭДТК, 2% NP-40, 0,2% ДСН), содержащем коктейли ингибиторов протеазы и фосфатазы. Частичные лизаты белка проводили через стеклянный гомогенизатор ткани и обрабатывали на льду 3-мя импульсами ультразвука продолжительностью 5 секунд с 10-секундными перерывами, на мощности с амплитудой 30 мкм. Образцы центрифугировали в течение 15 минут при 12000 об/мин, после чего собирали супернатант. Концентрацию белка в образцах определяли по методу Лоури. Белки (20 мкг/образец) разделяли на 10–20% ДСН-ПААГ и переносили на ПВДФ-мембраны методом быстрого сухого переноса. Затем мембраны блокировали в 5% молоке (обезжиренное сухое молоко, солюбилизированное в ФСБ с 0,1% Tween-20) в течение 1 часа и инкубировали с антителами против LAMP-2B человека (1:100, H4B4), антителами против LAMP-2B мыши (1:100) или антителами против ГАФДГ (1:1000, #32233, Santa Cruz) в течение ночи при 4°C. Мембраны промывали, после чего инкубировали с подходящими HRP-конъюгированными вторичными антителами (1:10 000) в течение 1 часа при комнатной температуре. Блоты проявляли на субстратах WesternBright™ Sirius с последующей визуализацией в гель-сканере BioRad.
Для иммунофлуоресцентных анализов проводили криозащиту ткани в 30% сахарозе/ФСБ при 4°C, заливали в монтирующую среду OCT (“Optimal Cutting Temperature Compound”), после чего готовили срезы ткани толщиной 8–10 мкм на обычном микротоме. Затем криосрезы фиксировали 4% ПФА в течение 5 минут, пермеабилизировали 0,2% Triton-X в течение 5 минут и блокировали 1% БСА, 3% сыворотки, 1% желатина из холодноводной рыбы в ФСБ в течение 30 минут. Срезы инкубировали с антителом мыши против LAMP-2B человека (1:50, H4B4), прямо конъюгированным с Alexa Fluor 647, и антителом кролика против дистрофина в течение ночи при 4° C. Затем препараты инкубировали с вторичным антителом с Alexa Fluor 488 против АТ кролика и DAPI (1:2000, #D9542, Sigma) в течение 30 минут при комнатной температуре. Затем препараты визуализировали с помощью конфокального микроскопа Olympus FluoView FV1000. Скорость сканирования, смещение, напряжение и усиление оставляли постоянными при захвате всех изображений в заданный день.
Результаты
Количественную ПЦР проводили на сердечной ткани получавших лечение AAV9 мышей с дефицитом LAMP-2. Хотя в сердечной ткани мышей, получавших лечение вектором, содержащим LAMP-2B дикого типа и оптимизированный LAMP-2B (фиг. 9A), наблюдались аналогичные показатели числа копий вируса, транскрипция AAV9 с оптимизированным LAMP-2B.v1.2 повышалась почти 7-кратно по сравнению с AAV9–LAMP-2B.v1.0 дикого типа (фиг. 9B). Несмотря на аналогичную трансдукцию вирусными векторами v1.0 и v1.2 в сердечной ткани, индукция экспрессии мРНК LAMP-2B человека значимо усиливалась при применении v1.2.
У мышей с дефицитом LAMP-2, которым внутривенно инъецировали AAV9-вектор с оптимизированным LAMP-2B.v1.2, также наблюдались значимо более высокие уровни белка LAMP-2B человека в сердечной ткани по сравнению с уровнями у мышей с дефицитом LAMP-2, получавших лечение AAV9-LAMP-2B.v1.0 дикого типа или контроль–основу (фиг. 9C). Аналогичные результаты достигались при иммунофлуоресцентном окрашивании: значительная индукция LAMP-2B человека происходила в сердечной ткани мышей с дефицитом LAMP-2, получавших лечение AAV9 с оптимизированным LAMP-2B.v1.2 (фиг. 9D). В совокупности эти данные показывают, что вирусная трансдукция с применением AAV9-вектора с оптимизированным LAMP-2B.v1.2 приводит к повышению экспрессии белка LAMP-2B человека в сердечной ткани in vivo по сравнению с AAV9 с LAMP-2B.v1.0 дикого типа в той же дозе.
ПРИМЕР 4: Оценка AAV9-LAMP-2B.v1.2 in vivo у не являющихся человеком приматов
Не являющимся человеком приматам внутривенно инъецировали 1×1013 вг/кг либо вирусным AAV9-вектором, содержащим вариант кодонов LAMP-2B (v1.2, вариант кодонов 1 – SEQ ID NO: 3), описанным в примере 2, или контроль–основу. Через восемь недель после проведения лечения не являющихся человеком приматов гуманным образом умерщвляли и собирали ткани сердца, мышц, печени и головного мозга для анализа экспрессии LAMP-2B.
Способы
Для количественного анализа на число копий вектора тотальную ДНК выделяли из замороженных тканей с применением набора Qiagen DNeasy в соответствии с инструкциями производителя. Концентрацию и целостность ДНК оценивали спектрофотометрически. Количественную ПЦР на выделенной ДНК проводили с применением мастер-микса TaqMan Universal Master Mix II (Applied Biosystems) с прямым (5′-ATCATGCTATTGCTTCCCGTA-3′; SEQ ID NO: 36) и обратным (5′-GGGCCACAACTCCTCATAAA-3′; SEQ ID NO: 37) праймерами и зондом (5′-CCTCCTTGTATAAATCCTGGTTGCTGTCT-3′; SEQ ID NO: 38) для гена WPRE. В качестве эндогенного контроля использовали РНКазу P (#4403328, ThermoFisher). Строили стандартную кривую с применением линеаризованной плазмиды, которая содержала векторный геном, используемый для получения вируса. Количество ДНК на образец рассчитывали с применением референсного набора TaqMan для анализа числа копий и выражали через число копий вектора на диплоидное ядро (VCN/Диплоидное ядро).
РНК экстрагировали и очищали из сердца и скелетных мышц с применением набора RNeasy Fibrous Tissue Mini Kit (Qiagen) и из печени и головного мозга с применением набора RNeasy Lipid Tissue Kit (Qiagen) в соответствии с протоколом производителя. Концентрацию и целостность РНК оценивали с помощью спектрофотометра NanoDrop. РНК обратно-транскрибировали с использованием мастер-микса SuperScript IV VILO (ThermoFisher) и использовали кДНК в качестве матрицы для количественной ПЦР в реальном времени (кРВ-ПЦР). кРВ-ПЦР проводили на кДНК с использованием мастер-микса TaqMan Universal Master Mix II с прямым (5′-ATCATGCTATTGCTTCCCGTA-3′; SEQ ID NO: 36) и обратным праймером (5′-GGGCCACAACTCCTCATAAA-3′; SEQ ID NO: 37) и зондом (5′-CCTCCTTGTATAAATCCTGGTTGCTGTCT-3′; SEQ ID NO: 38) для гена WPRE. HPRT-1 человека применяли в качестве эндогенного контроля. Строили стандартную кривую с применением линеаризованной плазмиды, которая содержала векторный геном, используемый для получения вируса.
Для полуколичественного анализа мРНК с применением технологии RNAScope сердечную ткань фиксировали в 10% нейтральном забуференном формалине, заливали в парафин и делали срезы. Трансген мРНК детектировали с применением зонда WPRE-O3 (#518628, ACD) в анализе RNAscope 2.5 LS RED. Клетки с более чем 1 точкой считали положительными, и процент положительных клеток разделяли на пять категорий: 0%, 1–25%, 26–50%, 51–75% или 100%.
Для анализа методом вестерн-блоттинга 125 мг сердечной ткани гомогенизировали в 500 мкл буфера для лизиса с применением системы Next Advance Bullet. Концентрацию белка определяли с применением набора BCA (ThermoFisher) и разделяли белки (50 мкг/образец) с применением ДСН-ПААГ, после чего переносили на нитроцеллюлозные мембраны. Затем мембраны анализировали с применением антитела мыши против LAMP2 человека (1:100), промывали, после чего инкубировали с HRP-конъюгированным антителом против Ig мыши. Блоты проявляли с применением субстрата ECL и системы BioRad ChemiDoc MP.
Для ИФА ELISA на LAMP-2B, проводили экстракцию белка согласно описанию выше. Планшет покрывали антителом мыши против LAMP2 (клон: H4B4, #NBP2-22217, Novus Biologicals), в каждую лунку добавляли по 100 мкг лизата ткани и проводили детекцию с применением поликлонального антитела против LAMP2 (#AF6228, R&D Systems) с последующей инкубацией с HRP-конъюгированным антителом осла против Ig козы (#AP180P, Millipore).
Результаты
Количественную ПЦР проводили на разных тканях приматов, получавших лечение AAV9. Число копий вируса возрастало в ткани сердца, мышц и печени приматов, которым инъецировали вектор AAV9-LAMP-2B.v1.2 в дозе 1×1013 вг/кг, по сравнению с числом у контроля при введении основы (фиг. 10A). Векторные геномы были детектированы во всех исследованных камерах сердца, в том числе левых и правых желудочках, а также левых и правых предсердиях (фиг. 10B). Векторная мРНК была детектирована на значимых уровнях в ткани сердца, скелетных мышц и печени получавших лечение приматов по сравнению с уровнями для контроля без лечения с введением основы (фиг. 10C и фиг. 10D). Анализ РНК in situ показал, что приблизительно 25–75% ткани сердца и печени экспрессируют векторную мРНК (фиг. 10E и фиг. 10F). Указанные данные демонстрируют, что системное введение 1×1013 вг/кг AAV9 с оптимизированным LAMP-2B.v1.2 примату приводит к эффективным трансдукции и экспрессии в ткани сердца in vivo.
Анализ методом вестерн-блоттинга показал, что у приматов, получавших системное лечение LAMP-2B.v1.2 в дозе 1×1013 вг/кг, наблюдается повышенный уровень белка LAMP-2B человека в левых и правых желудочках и левом предсердии сердца по сравнению с контролем без лечения (фиг. 10G и фиг. 10H). ИФА ELISA также показал, что уровни белка LAMP-2B человека повышались в левом желудочке и предсердии сердца, а также ткани скелетных мышц приматов, получавших лечение вектором AAV9–LAMP-2B.v1.2, по сравнению с контролем без лечения (фиг. 10I и фиг. 10J). Векторная трансдукция с применением AAV9.LAMP-2B.v1.2 приводит к экспрессии белка LAMP-2B человека в сердечной ткани приматов in vivo.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> РОКИТ ФАРМАСЬЮТИКАЛС, ЛТД.
<120> ГЕННОТЕРАПЕВТИЧЕСКИЕ ВЕКТОРЫ ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНИ ДАНОНА
<130> ROPA-011/01WO 329592-2071
<150> US 62/697302
<151> 2018-07-12
<160> 38
<170> PatentIn, версия 3.5
<210> 1
<211> 409
<212> БЕЛОК
<213> Homo sapiens
<400> 1
Met Val Cys Phe Arg Leu Phe Pro Val Pro Gly Ser Gly Leu Val Leu
1 5 10 15
Val Cys Leu Val Leu Gly Ala Val Arg Ser Tyr Ala Leu Glu Leu Asn
20 25 30
Leu Thr Asp Ser Glu Asn Ala Thr Cys Leu Tyr Ala Lys Trp Gln Met
35 40 45
Asn Phe Thr Val Arg Tyr Glu Thr Thr Asn Lys Thr Tyr Lys Thr Val
50 55 60
Thr Ile Ser Asp His Gly Thr Val Thr Tyr Asn Gly Ser Ile Cys Gly
65 70 75 80
Asp Asp Gln Asn Gly Pro Lys Ile Ala Val Gln Phe Gly Pro Gly Phe
85 90 95
Ser Trp Ile Ala Asn Phe Thr Lys Ala Ala Ser Thr Tyr Ser Ile Asp
100 105 110
Ser Val Ser Phe Ser Tyr Asn Thr Gly Asp Asn Thr Thr Phe Pro Asp
115 120 125
Ala Glu Asp Lys Gly Ile Leu Thr Val Asp Glu Leu Leu Ala Ile Arg
130 135 140
Ile Pro Leu Asn Asp Leu Phe Arg Cys Asn Ser Leu Ser Thr Leu Glu
145 150 155 160
Lys Asn Asp Val Val Gln His Tyr Trp Asp Val Leu Val Gln Ala Phe
165 170 175
Val Gln Asn Gly Thr Val Ser Thr Asn Glu Phe Leu Cys Asp Lys Asp
180 185 190
Lys Thr Ser Thr Val Ala Pro Thr Ile His Thr Thr Val Pro Ser Pro
195 200 205
Thr Thr Thr Pro Thr Pro Lys Glu Lys Pro Glu Ala Gly Thr Tyr Ser
210 215 220
Val Asn Asn Gly Asn Asp Thr Cys Leu Leu Ala Thr Met Gly Leu Gln
225 230 235 240
Leu Asn Ile Thr Gln Asp Lys Val Ala Ser Val Ile Asn Ile Asn Pro
245 250 255
Asn Thr Thr His Ser Thr Gly Ser Cys Arg Ser His Thr Ala Leu Leu
260 265 270
Arg Leu Asn Ser Ser Thr Ile Lys Tyr Leu Asp Phe Val Phe Ala Val
275 280 285
Lys Asn Glu Asn Arg Phe Tyr Leu Lys Glu Val Asn Ile Ser Met Tyr
290 295 300
Leu Val Asn Gly Ser Val Phe Ser Ile Ala Asn Asn Asn Leu Ser Tyr
305 310 315 320
Trp Asp Ala Pro Leu Gly Ser Ser Tyr Met Cys Asn Lys Glu Gln Thr
325 330 335
Val Ser Val Ser Gly Ala Phe Gln Ile Asn Thr Phe Asp Leu Arg Val
340 345 350
Gln Pro Phe Asn Val Thr Gln Gly Lys Tyr Ser Thr Ala Gln Glu Cys
355 360 365
Ser Leu Asp Asp Asp Thr Ile Leu Ile Pro Ile Ile Val Gly Ala Gly
370 375 380
Leu Ser Gly Leu Ile Ile Val Ile Val Ile Ala Tyr Val Ile Gly Arg
385 390 395 400
Arg Lys Ser Tyr Ala Gly Tyr Gln Thr
405
<210> 2
<211> 1233
<212> ДНК
<213> Homo sapiens
<400> 2
atggtgtgct tccgcctctt cccggttccg ggctcagggc tcgttctggt ctgcctagtc
60
ctgggagctg tgcggtctta tgcattggaa cttaatttga cagattcaga aaatgccact
120
tgcctttatg caaaatggca gatgaatttc acagttcgct atgaaactac aaataaaact
180
tataaaactg taaccatttc agaccatggc actgtgacat ataatggaag catttgtggg
240
gatgatcaga atggtcccaa aatagcagtg cagttcggac ctggcttttc ctggattgcg
300
aattttacca aggcagcatc tacttattca attgacagcg tctcattttc ctacaacact
360
ggtgataaca caacatttcc tgatgctgaa gataaaggaa ttcttactgt tgatgaactt
420
ttggccatca gaattccatt gaatgacctt tttagatgca atagtttatc aactttggaa
480
aagaatgatg ttgtccaaca ctactgggat gttcttgtac aagcttttgt ccaaaatggc
540
acagtgagca caaatgagtt cctgtgtgat aaagacaaaa cttcaacagt ggcacccacc
600
atacacacca ctgtgccatc tcctactaca acacctactc caaaggaaaa accagaagct
660
ggaacctatt cagttaataa tggcaatgat acttgtctgc tggctaccat ggggctgcag
720
ctgaacatca ctcaggataa ggttgcttca gttattaaca tcaaccccaa tacaactcac
780
tccacaggca gctgccgttc tcacactgct ctacttagac tcaatagcag caccattaag
840
tatctagact ttgtctttgc tgtgaaaaat gaaaaccgat tttatctgaa ggaagtgaac
900
atcagcatgt atttggttaa tggctccgtt ttcagcattg caaataacaa tctcagctac
960
tgggatgccc ccctgggaag ttcttatatg tgcaacaaag agcagactgt ttcagtgtct
1020
ggagcatttc agataaatac ctttgatcta agggttcagc ctttcaatgt gacacaagga
1080
aagtattcta cagcccaaga gtgttcgctg gatgatgaca ccattctaat cccaattata
1140
gttggtgctg gtctttcagg cttgattatc gttatagtga ttgcttacgt aattggcaga
1200
agaaaaagtt atgctggata tcagactctg taa
1233
<210> 3
<211> 1233
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Вариант LAMP-2
<400> 3
atggtctgct tcagactgtt ccctgtccct ggatctggtc tggtgcttgt gtgcttggtg
60
ctgggtgctg tgagatccta tgcccttgag ctgaacctga ctgactcaga aaatgccact
120
tgcctgtatg ccaagtggca gatgaacttc actgtgagat atgagactac caacaagacc
180
tacaagactg tgaccatctc agaccatggc actgtcacct acaatggatc aatctgtggt
240
gatgatcaga atggcccaaa gatagcagtg cagtttgggc ccggtttttc ctggattgct
300
aacttcacca aggcagcctc cacctacagc attgactcag tcagcttcag ctacaacact
360
ggggataaca ccaccttccc tgacgcagag gacaagggaa tccttactgt ggacgaactc
420
ctggcaatca gaatccccct taacgacctg ttcagatgca actccctttc aacccttgaa
480
aagaatgatg tggtgcaaca ctattgggac gtcctggtgc aagcctttgt gcagaatggg
540
acagtgagta ccaacgagtt cctctgtgac aaggacaaga ccagcactgt ggcccccact
600
atccacacca ctgtgcccag ccctaccact acccccaccc ctaaagagaa gccagaagct
660
ggaacctact cagtcaacaa tggaaatgac acatgcctcc ttgccaccat gggactgcag
720
ctgaacatca ctcaggacaa ggtggcctca gtgattaaca tcaaccctaa caccactcat
780
agcactggga gctgcagatc acatacagct ctgctgaggc tcaactcctc caccatcaag
840
tacctggact ttgtgtttgc tgtgaagaat gagaacaggt tctacctcaa ggaagtgaac
900
atttccatgt acctggtcaa tggttcagtg ttctctattg ccaacaacaa tctgagctac
960
tgggatgcac ccctgggatc ctcctacatg tgcaacaagg agcagactgt gagtgtgtca
1020
ggtgcttttc agatcaacac ttttgacctg agggtgcagc ccttcaatgt gactcaggga
1080
aagtactcca ctgcacaaga gtgttccttg gatgatgaca ctatcctcat ccccattatt
1140
gtgggagctg gactgtcagg attgattata gtgattgtga ttgcttatgt gattggaagg
1200
agaaagagct atgctggcta ccagaccctg taa
1233
<210> 4
<211> 1233
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Вариант LAMP-2
<400> 4
atggtgtgct ttagactgtt tcctgtgcct ggttcagggc tggtcctggt ctgtctggtg
60
ctgggggctg tcagaagcta tgccttggag ctgaacctca ctgatagtga aaatgccact
120
tgtctgtatg ctaagtggca gatgaacttc actgtgagat atgaaaccac caacaagact
180
tacaaaacag tgaccatctc agatcatgga actgtgacct acaacggcag catttgtgga
240
gacgaccaga acggaccaaa aatcgctgtc caatttgggc ctggattctc ctggattgcc
300
aatttcacta aagctgcctc cacatattca attgactcag tgtccttctc ctacaacact
360
ggggacaaca ctactttccc tgatgctgaa gataagggaa tcttgacagt ggatgagctg
420
ctggctatca ggatcccttt gaatgacctg tttaggtgta attcactgag cactctggag
480
aagaacgacg tggtgcagca ctactgggac gtgctggtgc aggcctttgt gcagaacggc
540
actgtgtcca ccaacgaatt cctgtgtgat aaggacaaaa cttccactgt ggcacctaca
600
attcacacta ctgtgccttc acctaccacc actccaactc caaaggaaaa gcctgaagca
660
ggaacctact ctgtgaacaa tggcaatgat acctgtctgt tggccaccat gggcctccaa
720
ctgaacatta ctcaggacaa ggtggcctca gtgattaaca ttaaccccaa cactacccac
780
tccactggca gctgtagatc acacacagcc ttgctcagac tgaatagcag caccatcaag
840
tatttggatt ttgtgtttgc agtgaagaat gaaaacaggt tctacctgaa ggaagtcaac
900
atctcaatgt acctggtgaa cggctcagtg ttcagcattg ccaacaacaa cctctcctat
960
tgggacgctc cactggggag cagctacatg tgtaacaagg aacagactgt gtcagtgtca
1020
ggagccttcc agattaacac ctttgatctg agggtccaac cctttaatgt cactcaagga
1080
aagtatagca ctgcccagga gtgctccctg gatgatgaca ccattctgat tccaatcatt
1140
gtgggtgcag gactttctgg gcttattatt gtgattgtga ttgcctatgt gattggcaga
1200
aggaaatcct atgcagggta ccaaactctg taa
1233
<210> 5
<211> 1233
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Вариант LAMP-2
<400> 5
atggtctgtt ttaggctgtt ccctgtccct ggttcaggac tggtcttagt gtgtctggtg
60
cttggagctg tcagaagcta tgccctggag ctgaacctga ctgactcaga aaatgccact
120
tgcctgtatg ccaagtggca gatgaacttc actgtcagat atgaaaccac caacaagacc
180
tataagactg tgaccatctc agaccatggc actgtgactt acaatgggtc aatttgtgga
240
gatgaccaga atggccctaa gatagctgtc cagtttggtc caggattcag ctggattgcc
300
aacttcacca aggcagccag cacctacagc attgactctg tgtccttctc ctacaacaca
360
ggagacaaca ccactttccc tgatgcagag gacaaaggta tcctgactgt ggatgagttg
420
ctggcaatca ggatcccact gaacgatctg ttcaggtgca actcactgtc cactctggaa
480
aagaatgatg tggtgcagca ctattgggat gtgctagtcc aggcctttgt ccagaatggg
540
actgtgtcaa ctaatgagtt cctgtgtgac aaggacaaga caagcactgt agcccccact
600
atccatacca cagtacctag ccccaccact actccaaccc ccaaggagaa gcctgaggct
660
ggcacctact cagtgaacaa tgggaatgac acctgtttgc tggccactat gggactccaa
720
ctgaacatca cccaggacaa agtggcctct gtgatcaata tcaatcccaa caccacccac
780
agcactgggt cctgcagaag ccacactgcc ctcctgaggc tcaactcatc aactatcaag
840
tacttggatt ttgtgtttgc agtgaagaat gagaacagat tctacctcaa agaggtcaac
900
atttcaatgt acctggtgaa tgggagtgtg ttctccattg ctaacaacaa cctgagctac
960
tgggatgccc ctctgggctc ctcatacatg tgcaacaagg aacagactgt gagtgtgtca
1020
ggggccttcc agatcaacac ttttgacctg agagtgcagc cctttaatgt gacacaggga
1080
aagtacagca ctgctcagga gtgcagcctg gatgatgaca ctatcctgat ccctatcatt
1140
gtgggggcag gcctgtctgg actcattatt gtgattgtga ttgcctatgt gatagggaga
1200
aggaagtctt atgctggata ccagaccctg taa
1233
<210> 6
<211> 13
<212> ДНК
<213> Неизвестен
<220>
<223> Последовательность Козак
<400> 6
gccgccacca tgg
13
<210> 7
<211> 387
<212> ДНК
<213> Неизвестен
<220>
<223> Полноразмерная (поли)A-последовательность
<400> 7
tggctaataa aggaaattta ttttcattgc aatagtgtgt tggaattttt tgtgtctctc
60
actcggaagg acatatggga gggcaaatca tttaaaacat cagaatgagt atttggttta
120
gagtttggca acatatgccc atatgctggc tgccatgaac aaaggttggc tataaagagg
180
tcatcagtat atgaaacagc cccctgctgt ccattcctta ttccatagaa aagccttgac
240
ttgaggttag atttttttta tattttgttt tgtgttattt ttttctttaa catccctaaa
300
attttcctta catgttttac tagccagatt tttcctcctc tcctgactac tcccagtcat
360
agctgtccct cttctcttat ggagatc
387
<210> 8
<211> 4549
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Экспрессионная кассета
<400> 8
ctgcgcgctc gctcgctcac tgaggccgcc cgggcaaagc ccgggcgtcg ggcgaccttt
60
ggtcgcccgg cctcagtgag cgagcgagcg cgcagagagg gagtggccaa ctccatcact
120
aggggttcct tgtagttaat gattaacccg ccatgctact tatctaccag ggtaatgggg
180
atcctctaga actatagcta gtcgacattg attattgact agttattaat agtaatcaat
240
tacggggtca ttagttcata gcccatatat ggagttccgc gttacataac ttacggtaaa
300
tggcccgcct ggctgaccgc ccaacgaccc ccgcccattg acgtcaataa tgacgtatgt
360
tcccatagta acgccaatag ggactttcca ttgacgtcaa tgggtggagt atttacggta
420
aactgcccac ttggcagtac atcaagtgta tcatatgcca agtacgcccc ctattgacgt
480
caatgacggt aaatggcccg cctggcatta tgcccagtac atgaccttat gggactttcc
540
tacttggcag tacatctacg tattagtcat cgctattacc atggtcgagg tgagccccac
600
gttctgcttc actctcccca tctccccccc ctccccaccc ccaattttgt atttatttat
660
tttttaatta ttttgtgcag cgatgggggc gggggggggg ggggggcgcg cgccaggcgg
720
ggcggggcgg ggcgaggggc ggggcggggc gaggcggaga ggtgcggcgg cagccaatca
780
gagcggcgcg ctccgaaagt ttccttttat ggcgaggcgg cggcggcggc ggccctataa
840
aaagcgaagc gcgcggcggg cgggagtcgc tgcgcgctgc cttcgccccg tgccccgctc
900
cgccgccgcc tcgcgccgcc cgccccggct ctgactgacc gcgttactcc cacaggtgag
960
cgggcgggac ggcccttctc ctccgggctg taattagcgc ttggtttaat gacggcttgt
1020
ttcttttctg tggctgcgtg aaagccttga ggggctccgg gagggccctt tgtgcggggg
1080
gagcggctcg gggggtgcgt gcgtgtgtgt gtgcgtgggg agcgccgcgt gcggctccgc
1140
gctgcccggc ggctgtgagc gctgcgggcg cggcgcgggg ctttgtgcgc tccgcagtgt
1200
gcgcgagggg agcgcggccg ggggcggtgc cccgcggtgc ggggggggct gcgaggggaa
1260
caaaggctgc gtgcggggtg tgtgcgtggg ggggtgagca gggggtgtgg gcgcgtcggt
1320
cgggctgcaa ccccccctgc acccccctcc ccgagttgct gagcacggcc cggcttcggg
1380
tgcggggctc cgtacggggc gtggcgcggg gctcgccgtg ccgggcgggg ggtggcggca
1440
ggtgggggtg ccgggcgggg cggggccgcc tcgggccggg gagggctcgg gggaggggcg
1500
cggcggcccc cggagcgccg gcggctgtcg aggcgcggcg agccgcagcc attgcctttt
1560
atggtaatcg tgcgagaggg cgcagggact tcctttgtcc caaatctgtg cggagccgaa
1620
atctgggagg cgccgccgca ccccctctag cgggcgcggg gcgaagcggt gcggcgccgg
1680
caggaaggaa atgggcgggg agggccttcg tgcgtcgccg cgccgccgtc cccttctccc
1740
tctccagcct cggggctgtc cgcgggggga cggctgcctt cgggggggac ggggcagggc
1800
ggggttcggc ttctggcgtg tgaccggcgg ctctagagcc tctgctaacc atgttcatgc
1860
cttcttcttt ttcctacagc tcctgggcaa cgtgctggtt attgtgctgt ctcatcattt
1920
tggcaaagaa ttcgagcggc cgccagccgc caccatggtc tgcttcagac tgttccctgt
1980
ccctggatct ggtctggtgc ttgtgtgctt ggtgctgggt gctgtgagat cctatgccct
2040
tgagctgaac ctgactgact cagaaaatgc cacttgcctg tatgccaagt ggcagatgaa
2100
cttcactgtg agatatgaga ctaccaacaa gacctacaag actgtgacca tctcagacca
2160
tggcactgtc acctacaatg gatcaatctg tggtgatgat cagaatggcc caaagatagc
2220
agtgcagttt gggcccggtt tttcctggat tgctaacttc accaaggcag cctccaccta
2280
cagcattgac tcagtcagct tcagctacaa cactggggat aacaccacct tccctgacgc
2340
agaggacaag ggaatcctta ctgtggacga actcctggca atcagaatcc cccttaacga
2400
cctgttcaga tgcaactccc tttcaaccct tgaaaagaat gatgtggtgc aacactattg
2460
ggacgtcctg gtgcaagcct ttgtgcagaa tgggacagtg agtaccaacg agttcctctg
2520
tgacaaggac aagaccagca ctgtggcccc cactatccac accactgtgc ccagccctac
2580
cactaccccc acccctaaag agaagccaga agctggaacc tactcagtca acaatggaaa
2640
tgacacatgc ctccttgcca ccatgggact gcagctgaac atcactcagg acaaggtggc
2700
ctcagtgatt aacatcaacc ctaacaccac tcatagcact gggagctgca gatcacatac
2760
agctctgctg aggctcaact cctccaccat caagtacctg gactttgtgt ttgctgtgaa
2820
gaatgagaac aggttctacc tcaaggaagt gaacatttcc atgtacctgg tcaatggttc
2880
agtgttctct attgccaaca acaatctgag ctactgggat gcacccctgg gatcctccta
2940
catgtgcaac aaggagcaga ctgtgagtgt gtcaggtgct tttcagatca acacttttga
3000
cctgagggtg cagcccttca atgtgactca gggaaagtac tccactgcac aagagtgttc
3060
cttggatgat gacactatcc tcatccccat tattgtggga gctggactgt caggattgat
3120
tatagtgatt gtgattgctt atgtgattgg aaggagaaag agctatgctg gctaccagac
3180
cctgtaaaag ggcgaattcc agcacacgcg tcctaggagc tcgagtacta ctggcggccg
3240
ttactagtgg atccgcggta caagtaagca tgcaagcttc gaggacgggg tgaactacgc
3300
ctgaatcaag cttatcgata aattcgagca tcttaccgcc atttattccc atatttgttc
3360
tgtttttctt gatttgggta tacatttaaa tgttaataaa acaaaatggt ggggcaatca
3420
tttacatttt tagggatatg taattactag ttcaggtgta ttgccacaag acaaacatgt
3480
taagaaactt tcccgttatt tacgctctgt tcctgttaat caacctctgg attacaaaat
3540
ttgtgaaaga ttgactgata ttcttaacta tgttgctcct tttacgctgt gtggatatgc
3600
tgctttaatg cctctgtatc atgctattgc ttcccgtacg gctttcgttt tctcctcctt
3660
gtataaatcc tggttgctgt ctctttatga ggagttgtgg cccgttgtcc gtcaacgtgg
3720
cgtggtgtgc tctgtgtttg ctgacgcaac ccccactggc tggggcattg ccaccacctg
3780
tcaactcctt tctgggactt tcgctttccc cctcccgatc gccacggcag aactcatcgc
3840
cgcctgcctt gcccgctgct ggacaggggc taggttgctg ggcactgata attccgtggt
3900
gttgtcgggg aagggcctcg ataccgtcga tatcgatcct ggctaataaa ggaaatttat
3960
tttcattgca atagtgtgtt ggaatttttt gtgtctctca ctcggaagga catatgggag
4020
ggcaaatcat ttaaaacatc agaatgagta tttggtttag agtttggcaa catatgccca
4080
tatgctggct gccatgaaca aaggttggct ataaagaggt catcagtata tgaaacagcc
4140
ccctgctgtc cattccttat tccatagaaa agccttgact tgaggttaga ttttttttat
4200
attttgtttt gtgttatttt tttctttaac atccctaaaa ttttccttac atgttttact
4260
agccagattt ttcctcctct cctgactact cccagtcata gctgtccctc ttctcttatg
4320
gagatcgaag caattcgttg atctgaattt cgaccaccca taatagatct cccattaccc
4380
tggtagataa gtagcatggc gggttaatca ttaactacaa ggaaccccta gtgatggagt
4440
tggccactcc ctctctgcgc gctcgctcgc tcactgaggc cgggcgacca aaggtcgccc
4500
gacgcccggg ctttgcccgg gcggcctcag tgagcgagcg agcgcgcag
4549
<210> 9
<211> 4549
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Экспрессионная кассета
<400> 9
ctgcgcgctc gctcgctcac tgaggccgcc cgggcaaagc ccgggcgtcg ggcgaccttt
60
ggtcgcccgg cctcagtgag cgagcgagcg cgcagagagg gagtggccaa ctccatcact
120
aggggttcct tgtagttaat gattaacccg ccatgctact tatctaccag ggtaatgggg
180
atcctctaga actatagcta gtcgacattg attattgact agttattaat agtaatcaat
240
tacggggtca ttagttcata gcccatatat ggagttccgc gttacataac ttacggtaaa
300
tggcccgcct ggctgaccgc ccaacgaccc ccgcccattg acgtcaataa tgacgtatgt
360
tcccatagta acgccaatag ggactttcca ttgacgtcaa tgggtggagt atttacggta
420
aactgcccac ttggcagtac atcaagtgta tcatatgcca agtacgcccc ctattgacgt
480
caatgacggt aaatggcccg cctggcatta tgcccagtac atgaccttat gggactttcc
540
tacttggcag tacatctacg tattagtcat cgctattacc atggtcgagg tgagccccac
600
gttctgcttc actctcccca tctccccccc ctccccaccc ccaattttgt atttatttat
660
tttttaatta ttttgtgcag cgatgggggc gggggggggg ggggggcgcg cgccaggcgg
720
ggcggggcgg ggcgaggggc ggggcggggc gaggcggaga ggtgcggcgg cagccaatca
780
gagcggcgcg ctccgaaagt ttccttttat ggcgaggcgg cggcggcggc ggccctataa
840
aaagcgaagc gcgcggcggg cgggagtcgc tgcgcgctgc cttcgccccg tgccccgctc
900
cgccgccgcc tcgcgccgcc cgccccggct ctgactgacc gcgttactcc cacaggtgag
960
cgggcgggac ggcccttctc ctccgggctg taattagcgc ttggtttaat gacggcttgt
1020
ttcttttctg tggctgcgtg aaagccttga ggggctccgg gagggccctt tgtgcggggg
1080
gagcggctcg gggggtgcgt gcgtgtgtgt gtgcgtgggg agcgccgcgt gcggctccgc
1140
gctgcccggc ggctgtgagc gctgcgggcg cggcgcgggg ctttgtgcgc tccgcagtgt
1200
gcgcgagggg agcgcggccg ggggcggtgc cccgcggtgc ggggggggct gcgaggggaa
1260
caaaggctgc gtgcggggtg tgtgcgtggg ggggtgagca gggggtgtgg gcgcgtcggt
1320
cgggctgcaa ccccccctgc acccccctcc ccgagttgct gagcacggcc cggcttcggg
1380
tgcggggctc cgtacggggc gtggcgcggg gctcgccgtg ccgggcgggg ggtggcggca
1440
ggtgggggtg ccgggcgggg cggggccgcc tcgggccggg gagggctcgg gggaggggcg
1500
cggcggcccc cggagcgccg gcggctgtcg aggcgcggcg agccgcagcc attgcctttt
1560
atggtaatcg tgcgagaggg cgcagggact tcctttgtcc caaatctgtg cggagccgaa
1620
atctgggagg cgccgccgca ccccctctag cgggcgcggg gcgaagcggt gcggcgccgg
1680
caggaaggaa atgggcgggg agggccttcg tgcgtcgccg cgccgccgtc cccttctccc
1740
tctccagcct cggggctgtc cgcgggggga cggctgcctt cgggggggac ggggcagggc
1800
ggggttcggc ttctggcgtg tgaccggcgg ctctagagcc tctgctaacc atgttcatgc
1860
cttcttcttt ttcctacagc tcctgggcaa cgtgctggtt attgtgctgt ctcatcattt
1920
tggcaaagaa ttcgagcggc cgccagccgc caccatggtg tgctttagac tgtttcctgt
1980
gcctggttca gggctggtcc tggtctgtct ggtgctgggg gctgtcagaa gctatgcctt
2040
ggagctgaac ctcactgata gtgaaaatgc cacttgtctg tatgctaagt ggcagatgaa
2100
cttcactgtg agatatgaaa ccaccaacaa gacttacaaa acagtgacca tctcagatca
2160
tggaactgtg acctacaacg gcagcatttg tggagacgac cagaacggac caaaaatcgc
2220
tgtccaattt gggcctggat tctcctggat tgccaatttc actaaagctg cctccacata
2280
ttcaattgac tcagtgtcct tctcctacaa cactggggac aacactactt tccctgatgc
2340
tgaagataag ggaatcttga cagtggatga gctgctggct atcaggatcc ctttgaatga
2400
cctgtttagg tgtaattcac tgagcactct ggagaagaac gacgtggtgc agcactactg
2460
ggacgtgctg gtgcaggcct ttgtgcagaa cggcactgtg tccaccaacg aattcctgtg
2520
tgataaggac aaaacttcca ctgtggcacc tacaattcac actactgtgc cttcacctac
2580
caccactcca actccaaagg aaaagcctga agcaggaacc tactctgtga acaatggcaa
2640
tgatacctgt ctgttggcca ccatgggcct ccaactgaac attactcagg acaaggtggc
2700
ctcagtgatt aacattaacc ccaacactac ccactccact ggcagctgta gatcacacac
2760
agccttgctc agactgaata gcagcaccat caagtatttg gattttgtgt ttgcagtgaa
2820
gaatgaaaac aggttctacc tgaaggaagt caacatctca atgtacctgg tgaacggctc
2880
agtgttcagc attgccaaca acaacctctc ctattgggac gctccactgg ggagcagcta
2940
catgtgtaac aaggaacaga ctgtgtcagt gtcaggagcc ttccagatta acacctttga
3000
tctgagggtc caacccttta atgtcactca aggaaagtat agcactgccc aggagtgctc
3060
cctggatgat gacaccattc tgattccaat cattgtgggt gcaggacttt ctgggcttat
3120
tattgtgatt gtgattgcct atgtgattgg cagaaggaaa tcctatgcag ggtaccaaac
3180
tctgtaaaag ggcgaattcc agcacacgcg tcctaggagc tcgagtacta ctggcggccg
3240
ttactagtgg atccgcggta caagtaagca tgcaagcttc gaggacgggg tgaactacgc
3300
ctgaatcaag cttatcgata aattcgagca tcttaccgcc atttattccc atatttgttc
3360
tgtttttctt gatttgggta tacatttaaa tgttaataaa acaaaatggt ggggcaatca
3420
tttacatttt tagggatatg taattactag ttcaggtgta ttgccacaag acaaacatgt
3480
taagaaactt tcccgttatt tacgctctgt tcctgttaat caacctctgg attacaaaat
3540
ttgtgaaaga ttgactgata ttcttaacta tgttgctcct tttacgctgt gtggatatgc
3600
tgctttaatg cctctgtatc atgctattgc ttcccgtacg gctttcgttt tctcctcctt
3660
gtataaatcc tggttgctgt ctctttatga ggagttgtgg cccgttgtcc gtcaacgtgg
3720
cgtggtgtgc tctgtgtttg ctgacgcaac ccccactggc tggggcattg ccaccacctg
3780
tcaactcctt tctgggactt tcgctttccc cctcccgatc gccacggcag aactcatcgc
3840
cgcctgcctt gcccgctgct ggacaggggc taggttgctg ggcactgata attccgtggt
3900
gttgtcgggg aagggcctcg ataccgtcga tatcgatcct ggctaataaa ggaaatttat
3960
tttcattgca atagtgtgtt ggaatttttt gtgtctctca ctcggaagga catatgggag
4020
ggcaaatcat ttaaaacatc agaatgagta tttggtttag agtttggcaa catatgccca
4080
tatgctggct gccatgaaca aaggttggct ataaagaggt catcagtata tgaaacagcc
4140
ccctgctgtc cattccttat tccatagaaa agccttgact tgaggttaga ttttttttat
4200
attttgtttt gtgttatttt tttctttaac atccctaaaa ttttccttac atgttttact
4260
agccagattt ttcctcctct cctgactact cccagtcata gctgtccctc ttctcttatg
4320
gagatcgaag caattcgttg atctgaattt cgaccaccca taatagatct cccattaccc
4380
tggtagataa gtagcatggc gggttaatca ttaactacaa ggaaccccta gtgatggagt
4440
tggccactcc ctctctgcgc gctcgctcgc tcactgaggc cgggcgacca aaggtcgccc
4500
gacgcccggg ctttgcccgg gcggcctcag tgagcgagcg agcgcgcag
4549
<210> 10
<211> 4549
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Экспрессионная кассета
<400> 10
ctgcgcgctc gctcgctcac tgaggccgcc cgggcaaagc ccgggcgtcg ggcgaccttt
60
ggtcgcccgg cctcagtgag cgagcgagcg cgcagagagg gagtggccaa ctccatcact
120
aggggttcct tgtagttaat gattaacccg ccatgctact tatctaccag ggtaatgggg
180
atcctctaga actatagcta gtcgacattg attattgact agttattaat agtaatcaat
240
tacggggtca ttagttcata gcccatatat ggagttccgc gttacataac ttacggtaaa
300
tggcccgcct ggctgaccgc ccaacgaccc ccgcccattg acgtcaataa tgacgtatgt
360
tcccatagta acgccaatag ggactttcca ttgacgtcaa tgggtggagt atttacggta
420
aactgcccac ttggcagtac atcaagtgta tcatatgcca agtacgcccc ctattgacgt
480
caatgacggt aaatggcccg cctggcatta tgcccagtac atgaccttat gggactttcc
540
tacttggcag tacatctacg tattagtcat cgctattacc atggtcgagg tgagccccac
600
gttctgcttc actctcccca tctccccccc ctccccaccc ccaattttgt atttatttat
660
tttttaatta ttttgtgcag cgatgggggc gggggggggg ggggggcgcg cgccaggcgg
720
ggcggggcgg ggcgaggggc ggggcggggc gaggcggaga ggtgcggcgg cagccaatca
780
gagcggcgcg ctccgaaagt ttccttttat ggcgaggcgg cggcggcggc ggccctataa
840
aaagcgaagc gcgcggcggg cgggagtcgc tgcgcgctgc cttcgccccg tgccccgctc
900
cgccgccgcc tcgcgccgcc cgccccggct ctgactgacc gcgttactcc cacaggtgag
960
cgggcgggac ggcccttctc ctccgggctg taattagcgc ttggtttaat gacggcttgt
1020
ttcttttctg tggctgcgtg aaagccttga ggggctccgg gagggccctt tgtgcggggg
1080
gagcggctcg gggggtgcgt gcgtgtgtgt gtgcgtgggg agcgccgcgt gcggctccgc
1140
gctgcccggc ggctgtgagc gctgcgggcg cggcgcgggg ctttgtgcgc tccgcagtgt
1200
gcgcgagggg agcgcggccg ggggcggtgc cccgcggtgc ggggggggct gcgaggggaa
1260
caaaggctgc gtgcggggtg tgtgcgtggg ggggtgagca gggggtgtgg gcgcgtcggt
1320
cgggctgcaa ccccccctgc acccccctcc ccgagttgct gagcacggcc cggcttcggg
1380
tgcggggctc cgtacggggc gtggcgcggg gctcgccgtg ccgggcgggg ggtggcggca
1440
ggtgggggtg ccgggcgggg cggggccgcc tcgggccggg gagggctcgg gggaggggcg
1500
cggcggcccc cggagcgccg gcggctgtcg aggcgcggcg agccgcagcc attgcctttt
1560
atggtaatcg tgcgagaggg cgcagggact tcctttgtcc caaatctgtg cggagccgaa
1620
atctgggagg cgccgccgca ccccctctag cgggcgcggg gcgaagcggt gcggcgccgg
1680
caggaaggaa atgggcgggg agggccttcg tgcgtcgccg cgccgccgtc cccttctccc
1740
tctccagcct cggggctgtc cgcgggggga cggctgcctt cgggggggac ggggcagggc
1800
ggggttcggc ttctggcgtg tgaccggcgg ctctagagcc tctgctaacc atgttcatgc
1860
cttcttcttt ttcctacagc tcctgggcaa cgtgctggtt attgtgctgt ctcatcattt
1920
tggcaaagaa ttcgagcggc cgccagccgc caccatggtc tgttttaggc tgttccctgt
1980
ccctggttca ggactggtct tagtgtgtct ggtgcttgga gctgtcagaa gctatgccct
2040
ggagctgaac ctgactgact cagaaaatgc cacttgcctg tatgccaagt ggcagatgaa
2100
cttcactgtc agatatgaaa ccaccaacaa gacctataag actgtgacca tctcagacca
2160
tggcactgtg acttacaatg ggtcaatttg tggagatgac cagaatggcc ctaagatagc
2220
tgtccagttt ggtccaggat tcagctggat tgccaacttc accaaggcag ccagcaccta
2280
cagcattgac tctgtgtcct tctcctacaa cacaggagac aacaccactt tccctgatgc
2340
agaggacaaa ggtatcctga ctgtggatga gttgctggca atcaggatcc cactgaacga
2400
tctgttcagg tgcaactcac tgtccactct ggaaaagaat gatgtggtgc agcactattg
2460
ggatgtgcta gtccaggcct ttgtccagaa tgggactgtg tcaactaatg agttcctgtg
2520
tgacaaggac aagacaagca ctgtagcccc cactatccat accacagtac ctagccccac
2580
cactactcca acccccaagg agaagcctga ggctggcacc tactcagtga acaatgggaa
2640
tgacacctgt ttgctggcca ctatgggact ccaactgaac atcacccagg acaaagtggc
2700
ctctgtgatc aatatcaatc ccaacaccac ccacagcact gggtcctgca gaagccacac
2760
tgccctcctg aggctcaact catcaactat caagtacttg gattttgtgt ttgcagtgaa
2820
gaatgagaac agattctacc tcaaagaggt caacatttca atgtacctgg tgaatgggag
2880
tgtgttctcc attgctaaca acaacctgag ctactgggat gcccctctgg gctcctcata
2940
catgtgcaac aaggaacaga ctgtgagtgt gtcaggggcc ttccagatca acacttttga
3000
cctgagagtg cagcccttta atgtgacaca gggaaagtac agcactgctc aggagtgcag
3060
cctggatgat gacactatcc tgatccctat cattgtgggg gcaggcctgt ctggactcat
3120
tattgtgatt gtgattgcct atgtgatagg gagaaggaag tcttatgctg gataccagac
3180
cctgtaaaag ggcgaattcc agcacacgcg tcctaggagc tcgagtacta ctggcggccg
3240
ttactagtgg atccgcggta caagtaagca tgcaagcttc gaggacgggg tgaactacgc
3300
ctgaatcaag cttatcgata aattcgagca tcttaccgcc atttattccc atatttgttc
3360
tgtttttctt gatttgggta tacatttaaa tgttaataaa acaaaatggt ggggcaatca
3420
tttacatttt tagggatatg taattactag ttcaggtgta ttgccacaag acaaacatgt
3480
taagaaactt tcccgttatt tacgctctgt tcctgttaat caacctctgg attacaaaat
3540
ttgtgaaaga ttgactgata ttcttaacta tgttgctcct tttacgctgt gtggatatgc
3600
tgctttaatg cctctgtatc atgctattgc ttcccgtacg gctttcgttt tctcctcctt
3660
gtataaatcc tggttgctgt ctctttatga ggagttgtgg cccgttgtcc gtcaacgtgg
3720
cgtggtgtgc tctgtgtttg ctgacgcaac ccccactggc tggggcattg ccaccacctg
3780
tcaactcctt tctgggactt tcgctttccc cctcccgatc gccacggcag aactcatcgc
3840
cgcctgcctt gcccgctgct ggacaggggc taggttgctg ggcactgata attccgtggt
3900
gttgtcgggg aagggcctcg ataccgtcga tatcgatcct ggctaataaa ggaaatttat
3960
tttcattgca atagtgtgtt ggaatttttt gtgtctctca ctcggaagga catatgggag
4020
ggcaaatcat ttaaaacatc agaatgagta tttggtttag agtttggcaa catatgccca
4080
tatgctggct gccatgaaca aaggttggct ataaagaggt catcagtata tgaaacagcc
4140
ccctgctgtc cattccttat tccatagaaa agccttgact tgaggttaga ttttttttat
4200
attttgtttt gtgttatttt tttctttaac atccctaaaa ttttccttac atgttttact
4260
agccagattt ttcctcctct cctgactact cccagtcata gctgtccctc ttctcttatg
4320
gagatcgaag caattcgttg atctgaattt cgaccaccca taatagatct cccattaccc
4380
tggtagataa gtagcatggc gggttaatca ttaactacaa ggaaccccta gtgatggagt
4440
tggccactcc ctctctgcgc gctcgctcgc tcactgaggc cgggcgacca aaggtcgccc
4500
gacgcccggg ctttgcccgg gcggcctcag tgagcgagcg agcgcgcag
4549
<210> 11
<211> 130
<212> ДНК
<213> Неизвестен
<220>
<223> Последовательность инвертированного концевого повтора (ITR)
<400> 11
ctgcgcgctc gctcgctcac tgaggccgcc cgggcaaagc ccgggcgtcg ggcgaccttt
60
ggtcgcccgg cctcagtgag cgagcgagcg cgcagagagg gagtggccaa ctccatcact
120
aggggttcct
130
<210> 12
<211> 130
<212> ДНК
<213> Неизвестен
<220>
<223> Последовательность инвертированного концевого повтора (ITR)
<400> 12
aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg ctcactgagg
60
ccgggcgacc aaaggtcgcc cgacgcccgg gctttgcccg ggcggcctca gtgagcgagc
120
gagcgcgcag
130
<210> 13
<400> 13
000
<210> 14
<211> 13
<212> РНК
<213> Неизвестен
<220>
<223> Альтернативная последовательность Козак
<220>
<221> Другие признаки
<222> (1)..(3)
<223> Может отсутствовать
<220>
<221> Другие признаки
<222> (1)..(1)
<223> g представляет собой наиболее часто встречающееся основание,
но возможны другие варианты
<220>
<221> Другие признаки
<222> (2)..(3)
<223> c представляет собой наиболее часто встречающееся основание,
но возможны другие варианты
<220>
<221> другие признаки
<222> (4)..(4)
<223> g представляет собой наиболее часто встречающееся основание,
но возможны другие варианты
<220>
<221> Другие признаки
<222> (5)..(6)
<223> c представляет собой наиболее часто встречающееся основание,
но возможны другие варианты
<220>
<221> Другие признаки
<222> (8)..(9)
<223> c представляет собой наиболее часто встречающееся основание,
но возможны другие варианты
<400> 14
nnnnnnrnna ugg
13
<210> 15
<211> 8
<212> РНК
<213> Неизвестен
<220>
<223> Альтернативная последовательность Козак
<220>
<221> Другие признаки
<222> (3)..(4)
<223> n представляет собой a, c, g или u
<220>
<221> Другие признаки
<222> (8)..(8)
<223> n представляет собой a, c, g или u
<400> 15
agnnaugn
8
<210> 16
<211> 7
<212> РНК
<213> Неизвестен
<220>
<223> Альтернативная последовательность Козак
<220>
<221> Другие признаки
<222> (2)..(3)
<223> n представляет собой a, c, g или u
<400> 16
annaugg
7
<210> 17
<211> 7
<212> РНК
<213> Неизвестен
<220>
<223> Альтернативная последовательность Козак
<400> 17
accaugg
7
<210> 18
<211> 10
<212> РНК
<213> Неизвестен
<220>
<223> Альтернативная последовательность Козак
<400> 18
gacaccaugg
10
<210> 19
<211> 235
<212> ДНК
<213> Bos taurus
<400> 19
tcgactgtgc cttctagttg ccagccatct gttgtttgcc cctcccccgt gccttccttg
60
accctggaag gtgccactcc cactgtcctt tcctaataaa atgaggaaat tgcatcgcat
120
tgtctgagta ggtgtcattc tattctgggg ggtggggtgg ggcaggacag caagggggag
180
gattgggagg acaatagcag gcatgctggg gatgcggtgg gctctatggc ttctg
235
<210> 20
<211> 222
<212> ДНК
<213> Вирус обезьян 40
<400> 20
cagacatgat aagatacatt gatgagtttg gacaaaccac aactagaatg cagtgaaaaa
60
aatgctttat ttgtgaaatt tgtgatgcta ttgctttatt tgtaaccatt ataagctgca
120
ataaacaagt taacaacaac aattgcattc attttatgtt tcaggttcag ggggagatgt
180
gggaggtttt ttaaagcaag taaaacctct acaaatgtgg ta
222
<210> 21
<211> 202
<212> ДНК
<213> Homo sapiens
<400> 21
ctgcccgggt ggcatccctg tgacccctcc ccagtgcctc tcctggccct ggaagttgcc
60
actccagtgc ccaccagcct tgtcctaata aaattaagtt gcatcatttt gtctgactag
120
gtgtccttct ataatattat ggggtggagg ggggtggtat ggagcaaggg gcccaagttg
180
ggaagaaacc tgtagggcct gc
202
<210> 22
<211> 1730
<212> ДНК
<213> Неизвестен
<220>
<223> промотор CAG
<400> 22
ctagtcgaca ttgattattg actagttatt aatagtaatc aattacgggg tcattagttc
60
atagcccata tatggagttc cgcgttacat aacttacggt aaatggcccg cctggctgac
120
cgcccaacga cccccgccca ttgacgtcaa taatgacgta tgttcccata gtaacgccaa
180
tagggacttt ccattgacgt caatgggtgg agtatttacg gtaaactgcc cacttggcag
240
tacatcaagt gtatcatatg ccaagtacgc cccctattga cgtcaatgac ggtaaatggc
300
ccgcctggca ttatgcccag tacatgacct tatgggactt tcctacttgg cagtacatct
360
acgtattagt catcgctatt accatggtcg aggtgagccc cacgttctgc ttcactctcc
420
ccatctcccc cccctcccca cccccaattt tgtatttatt tattttttaa ttattttgtg
480
cagcgatggg ggcggggggg gggggggggc gcgcgccagg cggggcgggg cggggcgagg
540
ggcggggcgg ggcgaggcgg agaggtgcgg cggcagccaa tcagagcggc gcgctccgaa
600
agtttccttt tatggcgagg cggcggcggc ggcggcccta taaaaagcga agcgcgcggc
660
gggcgggagt cgctgcgcgc tgccttcgcc ccgtgccccg ctccgccgcc gcctcgcgcc
720
gcccgccccg gctctgactg accgcgttac tcccacaggt gagcgggcgg gacggccctt
780
ctcctccggg ctgtaattag cgcttggttt aatgacggct tgtttctttt ctgtggctgc
840
gtgaaagcct tgaggggctc cgggagggcc ctttgtgcgg ggggagcggc tcggggggtg
900
cgtgcgtgtg tgtgtgcgtg gggagcgccg cgtgcggctc cgcgctgccc ggcggctgtg
960
agcgctgcgg gcgcggcgcg gggctttgtg cgctccgcag tgtgcgcgag gggagcgcgg
1020
ccgggggcgg tgccccgcgg tgcggggggg gctgcgaggg gaacaaaggc tgcgtgcggg
1080
gtgtgtgcgt gggggggtga gcagggggtg tgggcgcgtc ggtcgggctg caaccccccc
1140
tgcacccccc tccccgagtt gctgagcacg gcccggcttc gggtgcgggg ctccgtacgg
1200
ggcgtggcgc ggggctcgcc gtgccgggcg gggggtggcg gcaggtgggg gtgccgggcg
1260
gggcggggcc gcctcgggcc ggggagggct cgggggaggg gcgcggcggc ccccggagcg
1320
ccggcggctg tcgaggcgcg gcgagccgca gccattgcct tttatggtaa tcgtgcgaga
1380
gggcgcaggg acttcctttg tcccaaatct gtgcggagcc gaaatctggg aggcgccgcc
1440
gcaccccctc tagcgggcgc ggggcgaagc ggtgcggcgc cggcaggaag gaaatgggcg
1500
gggagggcct tcgtgcgtcg ccgcgccgcc gtccccttct ccctctccag cctcggggct
1560
gtccgcgggg ggacggctgc cttcgggggg gacggggcag ggcggggttc ggcttctggc
1620
gtgtgaccgg cggctctaga gcctctgcta accatgttca tgccttcttc tttttcctac
1680
agctcctggg caacgtgctg gttattgtgc tgtctcatca ttttggcaaa
1730
<210> 23
<211> 204
<212> ДНК
<213> Цитомегаловирус человека
<400> 23
gtgatgcggt tttggcagta catcaatggg cgtggatagc ggtttgactc acggggattt
60
ccaagtctcc accccattga cgtcaatggg agtttgtttt ggcaccaaaa tcaacgggac
120
tttccaaaat gtcgtaacaa ctccgcccca ttgacgcaaa tgggcggtag gcgtgtacgg
180
tgggaggtct atataagcag agct
204
<210> 24
<211> 317
<212> ДНК
<213> Вирус обезьян 40
<400> 24
ggtgtggaaa gtccccaggc tccccagcag gcagaagtat gcaaagcatg catctcaatt
60
agtcagcaac caggtgtgga aagtccccag gctccccagc aggcagaagt atgcaaagca
120
tgcatctcaa ttagtcagca accatagtcc cgcccctaac tccgcccatc ccgcccctaa
180
ctccgcccag ttccgcccat tctccgcccc atggctgact aatttttttt atttatgcag
240
aggccgaggc cgcctcggcc tctgagctat tccagaagta gtgaggaggc ttttttggag
300
gcctaggctt ttgcaaa
317
<210> 25
<211> 500
<212> ДНК
<213> Неизвестен
<220>
<223> Промотор PGK
<400> 25
gggtagggga ggcgcttttc ccaaggcagt ctggagcatg cgctttagca gccccgctgg
60
gcacttggcg ctacacaagt ggcctctggc ctcgcacaca ttccacatcc accggtaggc
120
gccaaccggc tccgttcttt ggtggcccct tcgcgccacc ttctactcct cccctagtca
180
ggaagttccc ccccgccccg cagctcgcgt cgtgcaggac gtgacaaatg gaagtagcac
240
gtctcactag tctcgtgcag atggacagca ccgctgagca atggaagcgg gtaggccttt
300
ggggcagcgg ccaatagcag ctttgctcct tcgctttctg ggctcagagg ctgggaaggg
360
gtgggtccgg gggcgggctc aggggcgggc tcaggggcgg ggcgggcgcc cgaaggtcct
420
ccggaggccc ggcattctgc acgcttcaaa agcgcacgtc tgccgcgctg ttctcctctt
480
cctcatctcc gggcctttcg
500
<210> 26
<211> 2403
<212> ДНК
<213> Homo sapiens
<400> 26
cctgcagggc ccactagttc catgtcctta tatggactca tctttgccta ttgcgacaca
60
cactcaatga acacctacta cgcgctgcaa agagccccgc aggcctgagg tgcccccacc
120
tcaccactct tcctattttt gtgtaaaaat ccagcttctt gtcaccacct ccaaggaggg
180
ggaggaggag gaaggcaggt tcctctaggc tgagccgaat gcccctctgt ggtcccacgc
240
cactgatcgc tgcatgccca ccacctgggt acacacagtc tgtgattccc ggagcagaac
300
ggaccctgcc cacccggtct tgtgtgctac tcagtggaca gacccaaggc aagaaagggt
360
gacaaggaca gggtcttccc aggctggctt tgagttccta gcaccgcccc gcccccaatc
420
ctctgtggca catggagtct tggtccccag agtcccccag cggcctccag atggtctggg
480
agggcagttc agctgtggct gcgcatagca gacatacaac ggacggtggg cccagaccca
540
ggctgtgtag acccagcccc cccgccccgc agtgcctagg tcacccacta acgccccagg
600
cctggtcttg gctgggcgtg actgttaccc tcaaaagcag gcagctccag ggtaaaaggt
660
gccctgccct gtagagccca ccttccttcc cagggctgcg gctgggtagg tttgtagcct
720
tcatcacggg ccacctccag ccactggacc gctggcccct gccctgtcct ggggagtgtg
780
gtcctgcgac ttctaagtgg ccgcaagcca cctgactccc ccaacaccac actctacctc
840
tcaagcccag gtctctccct agtgacccac ccagcacatt tagctagctg agccccacag
900
ccagaggtcc tcaggccctg ctttcagggc agttgctctg aagtcggcaa gggggagtga
960
ctgcctggcc actccatgcc ctccaagagc tccttctgca ggagcgtaca gaacccaggg
1020
ccctggcacc cgtgcagacc ctggcccacc ccacctgggc gctcagtgcc caagagatgt
1080
ccacacctag gatgtcccgc ggtgggtggg gggcccgaga gacgggcagg ccgggggcag
1140
gcctggccat gcggggccga accgggcact gcccagcgtg gggcgcgggg gccacggcgc
1200
gcgcccccag cccccgggcc cagcacccca aggcggccaa cgccaaaact ctccctcctc
1260
ctcttcctca atctcgctct cgctcttttt ttttttcgca aaaggagggg agagggggta
1320
aaaaaatgct gcactgtgcg gcgaagccgg tgagtgagcg gcgcggggcc aatcagcgtg
1380
cgccgttccg aaagttgcct tttatggctc gagcggccgc ggcggcgccc tataaaaccc
1440
agcggcgcga cgcgccacca ccgccgagac cgcgtccgcc ccgcgagcac agagcctcgc
1500
ctttgccgat ccgccgcccg tccacacccg ccgccaggta agcccggcca gccgaccggg
1560
gcaggcggct cacggcccgg ccgcaggcgg ccgcggcccc ttcgcccgtg cagagccgcc
1620
gtctgggccg cagcgggggg cgcatggggg gggaaccgga ccgccgtggg gggcgcggga
1680
gaagcccctg ggcctccgga gatgggggac accccacgcc agttcggagg cgcgaggccg
1740
cgctcgggag gcgcgctccg ggggtgccgc tctcggggcg ggggcaaccg gcggggtctt
1800
tgtctgagcc gggctcttgc caatggggat cgcagggtgg gcgcggcgga gcccccgcca
1860
ggcccggtgg gggctggggc gccattgcgc gtgcgcgctg gtcctttggg cgctaactgc
1920
gtgcgcgctg ggaattggcg ctaattgcgc gtgcgcgctg ggactcaagg cgctaactgc
1980
gcgtgcgttc tggggcccgg ggtgccgcgg cctgggctgg ggcgaaggcg ggctcggccg
2040
gaaggggtgg ggtcgccgcg gctcccgggc gcttgcgcgc acttcctgcc cgagccgctg
2100
gccgcccgag ggtgtggccg ctgcgtgcgc gcgcgccgac ccggcgctgt ttgaaccggg
2160
cggaggcggg gctggcgccc ggttgggagg gggttggggc ctggcttcct gccgcgcgcc
2220
gcggggacgc ctccgaccag tgtttgcctt ttatggtaat aacgcggccg gcccggcttc
2280
ctttgtcccc aatctgggcg cgcgccggcg ccccctggcg gcctaaggac tcggcgcgcc
2340
ggaagtggcc agggcggggg cgacctcggc tcacagcgcg cccggctatt ctcgcagctc
2400
acc
2403
<210> 27
<211> 596
<212> ДНК
<213> Вирус гепатита сурков
<400> 27
attcgagcat cttaccgcca tttattccca tatttgttct gtttttcttg atttgggtat
60
acatttaaat gttaataaaa caaaatggtg gggcaatcat ttacattttt agggatatgt
120
aattactagt tcaggtgtat tgccacaaga caaacatgtt aagaaacttt cccgttattt
180
acgctctgtt cctgttaatc aacctctgga ttacaaaatt tgtgaaagat tgactgatat
240
tcttaactat gttgctcctt ttacgctgtg tggatatgct gctttaatgc ctctgtatca
300
tgctattgct tcccgtacgg ctttcgtttt ctcctccttg tataaatcct ggttgctgtc
360
tctttatgag gagttgtggc ccgttgtccg tcaacgtggc gtggtgtgct ctgtgtttgc
420
tgacgcaacc cccactggct ggggcattgc caccacctgt caactccttt ctgggacttt
480
cgctttcccc ctcccgatcg ccacggcaga actcatcgcc gcctgccttg cccgctgctg
540
gacaggggct aggttgctgg gcactgataa ttccgtggtg ttgtcgggga agggcc
596
<210> 28
<211> 736
<212> БЕЛОК
<213> Аденоассоциированный вирус 9
<400> 28
Met Ala Ala Asp Gly Tyr Leu Pro Asp Trp Leu Glu Asp Asn Leu Ser
1 5 10 15
Glu Gly Ile Arg Glu Trp Trp Ala Leu Lys Pro Gly Ala Pro Gln Pro
20 25 30
Lys Ala Asn Gln Gln His Gln Asp Asn Ala Arg Gly Leu Val Leu Pro
35 40 45
Gly Tyr Lys Tyr Leu Gly Pro Gly Asn Gly Leu Asp Lys Gly Glu Pro
50 55 60
Val Asn Ala Ala Asp Ala Ala Ala Leu Glu His Asp Lys Ala Tyr Asp
65 70 75 80
Gln Gln Leu Lys Ala Gly Asp Asn Pro Tyr Leu Lys Tyr Asn His Ala
85 90 95
Asp Ala Glu Phe Gln Glu Arg Leu Lys Glu Asp Thr Ser Phe Gly Gly
100 105 110
Asn Leu Gly Arg Ala Val Phe Gln Ala Lys Lys Arg Leu Leu Glu Pro
115 120 125
Leu Gly Leu Val Glu Glu Ala Ala Lys Thr Ala Pro Gly Lys Lys Arg
130 135 140
Pro Val Glu Gln Ser Pro Gln Glu Pro Asp Ser Ser Ala Gly Ile Gly
145 150 155 160
Lys Ser Gly Ala Gln Pro Ala Lys Lys Arg Leu Asn Phe Gly Gln Thr
165 170 175
Gly Asp Thr Glu Ser Val Pro Asp Pro Gln Pro Ile Gly Glu Pro Pro
180 185 190
Ala Ala Pro Ser Gly Val Gly Ser Leu Thr Met Ala Ser Gly Gly Gly
195 200 205
Ala Pro Val Ala Asp Asn Asn Glu Gly Ala Asp Gly Val Gly Ser Ser
210 215 220
Ser Gly Asn Trp His Cys Asp Ser Gln Trp Leu Gly Asp Arg Val Ile
225 230 235 240
Thr Thr Ser Thr Arg Thr Trp Ala Leu Pro Thr Tyr Asn Asn His Leu
245 250 255
Tyr Lys Gln Ile Ser Asn Ser Thr Ser Gly Gly Ser Ser Asn Asp Asn
260 265 270
Ala Tyr Phe Gly Tyr Ser Thr Pro Trp Gly Tyr Phe Asp Phe Asn Arg
275 280 285
Phe His Cys His Phe Ser Pro Arg Asp Trp Gln Arg Leu Ile Asn Asn
290 295 300
Asn Trp Gly Phe Arg Pro Lys Arg Leu Asn Phe Lys Leu Phe Asn Ile
305 310 315 320
Gln Val Lys Glu Val Thr Asp Asn Asn Gly Val Lys Thr Ile Ala Asn
325 330 335
Asn Leu Thr Ser Thr Val Gln Val Phe Thr Asp Ser Asp Tyr Gln Leu
340 345 350
Pro Tyr Val Leu Gly Ser Ala His Glu Gly Cys Leu Pro Pro Phe Pro
355 360 365
Ala Asp Val Phe Met Ile Pro Gln Tyr Gly Tyr Leu Thr Leu Asn Asp
370 375 380
Gly Ser Gln Ala Val Gly Arg Ser Ser Phe Tyr Cys Leu Glu Tyr Phe
385 390 395 400
Pro Ser Gln Met Leu Arg Thr Gly Asn Asn Phe Gln Phe Ser Tyr Glu
405 410 415
Phe Glu Asn Val Pro Phe His Ser Ser Tyr Ala His Ser Gln Ser Leu
420 425 430
Asp Arg Leu Met Asn Pro Leu Ile Asp Gln Tyr Leu Tyr Tyr Leu Ser
435 440 445
Lys Thr Ile Asn Gly Ser Gly Gln Asn Gln Gln Thr Leu Lys Phe Ser
450 455 460
Val Ala Gly Pro Ser Asn Met Ala Val Gln Gly Arg Asn Tyr Ile Pro
465 470 475 480
Gly Pro Ser Tyr Arg Gln Gln Arg Val Ser Thr Thr Val Thr Gln Asn
485 490 495
Asn Asn Ser Glu Phe Ala Trp Pro Gly Ala Ser Ser Trp Ala Leu Asn
500 505 510
Gly Arg Asn Ser Leu Met Asn Pro Gly Pro Ala Met Ala Ser His Lys
515 520 525
Glu Gly Glu Asp Arg Phe Phe Pro Leu Ser Gly Ser Leu Ile Phe Gly
530 535 540
Lys Gln Gly Thr Gly Arg Asp Asn Val Asp Ala Asp Lys Val Met Ile
545 550 555 560
Thr Asn Glu Glu Glu Ile Lys Thr Thr Asn Pro Val Ala Thr Glu Ser
565 570 575
Tyr Gly Gln Val Ala Thr Asn His Gln Ser Ala Gln Ala Gln Ala Gln
580 585 590
Thr Gly Trp Val Gln Asn Gln Gly Ile Leu Pro Gly Met Val Trp Gln
595 600 605
Asp Arg Asp Val Tyr Leu Gln Gly Pro Ile Trp Ala Lys Ile Pro His
610 615 620
Thr Asp Gly Asn Phe His Pro Ser Pro Leu Met Gly Gly Phe Gly Met
625 630 635 640
Lys His Pro Pro Pro Gln Ile Leu Ile Lys Asn Thr Pro Val Pro Ala
645 650 655
Asp Pro Pro Thr Ala Phe Asn Lys Asp Lys Leu Asn Ser Phe Ile Thr
660 665 670
Gln Tyr Ser Thr Gly Gln Val Ser Val Glu Ile Glu Trp Glu Leu Gln
675 680 685
Lys Glu Asn Ser Lys Arg Trp Asn Pro Glu Ile Gln Tyr Thr Ser Asn
690 695 700
Tyr Tyr Lys Ser Asn Asn Val Glu Phe Ala Val Asn Thr Glu Gly Val
705 710 715 720
Tyr Ser Glu Pro Arg Pro Ile Gly Thr Arg Tyr Leu Thr Arg Asn Leu
725 730 735
<210> 29
<211> 1233
<212> ДНК
<213> Homo sapiens
<400> 29
atggtgtgct tccgcctctt cccggttccg ggctcagggc tcgttctggt ctgcctagtc
60
ctgggagctg tgcggtctta tgcattggaa cttaatttga cagattcaga aaatgccact
120
tgcctttatg caaaatggca gatgaatttc acagtacgct atgaaactac aaataaaact
180
tataaaactg taaccatttc agaccatggc actgtgacat ataatggaag catttgtggg
240
gatgatcaga atggtcccaa aatagcagtg cagttcggac ctggcttttc ctggattgcg
300
aattttacca aggcagcatc tacttattca attgacagcg tctcattttc ctacaacact
360
ggtgataaca caacatttcc tgatgctgaa gataaaggaa ttcttactgt tgatgaactt
420
ttggccatca gaattccatt gaatgacctt tttagatgca atagtttatc aactttggaa
480
aagaatgatg ttgtccaaca ctactgggat gttcttgtac aagcttttgt ccaaaatggc
540
acagtgagca caaatgagtt cctgtgtgat aaagacaaaa cttcaacagt ggcacccacc
600
atacacacca ctgtgccatc tcctactaca acacctactc caaaggaaaa accagaagct
660
ggaacctatt cagttaataa tggcaatgat acttgtctgc tggctaccat ggggctgcag
720
ctgaacatca ctcaggataa ggttgcttca gttattaaca tcaaccccaa tacaactcac
780
tccacaggca gctgccgttc tcacactgct ctacttagac tcaatagcag caccattaag
840
tatctagact ttgtctttgc tgtgaaaaat gaaaaccgat tttatctgaa ggaagtgaac
900
atcagcatgt atttggttaa tggctccgtt ttcagcattg caaataacaa tctcagctac
960
tgggatgccc ccctgggaag ttcttatatg tgcaacaaag agcagactgt ttcagtgtct
1020
ggagcatttc agataaatac ctttgatcta agggttcagc ctttcaatgt gacacaagga
1080
aagtattcta cagctcaaga ctgcagtgca gatgacgaca acttccttgt gcccatagcg
1140
gtgggagctg ccttggcagg agtacttatt ctagtgttgc tggcttattt tattggtctc
1200
aagcaccatc atgctggata tgagcaattt tag
1233
<210> 30
<211> 1236
<212> ДНК
<213> Homo sapiens
<400> 30
atggtgtgct tccgcctctt cccggttccg ggctcagggc tcgttctggt ctgcctagtc
60
ctgggagctg tgcggtctta tgcattggaa cttaatttga cagattcaga aaatgccact
120
tgcctttatg caaaatggca gatgaatttc acagtacgct atgaaactac aaataaaact
180
tataaaactg taaccatttc agaccatggc actgtgacat ataatggaag catttgtggg
240
gatgatcaga atggtcccaa aatagcagtg cagttcggac ctggcttttc ctggattgcg
300
aattttacca aggcagcatc tacttattca attgacagcg tctcattttc ctacaacact
360
ggtgataaca caacatttcc tgatgctgaa gataaaggaa ttcttactgt tgatgaactt
420
ttggccatca gaattccatt gaatgacctt tttagatgca atagtttatc aactttggaa
480
aagaatgatg ttgtccaaca ctactgggat gttcttgtac aagcttttgt ccaaaatggc
540
acagtgagca caaatgagtt cctgtgtgat aaagacaaaa cttcaacagt ggcacccacc
600
atacacacca ctgtgccatc tcctactaca acacctactc caaaggaaaa accagaagct
660
ggaacctatt cagttaataa tggcaatgat acttgtctgc tggctaccat ggggctgcag
720
ctgaacatca ctcaggataa ggttgcttca gttattaaca tcaaccccaa tacaactcac
780
tccacaggca gctgccgttc tcacactgct ctacttagac tcaatagcag caccattaag
840
tatctagact ttgtctttgc tgtgaaaaat gaaaaccgat tttatctgaa ggaagtgaac
900
atcagcatgt atttggttaa tggctccgtt ttcagcattg caaataacaa tctcagctac
960
tgggatgccc ccctgggaag ttcttatatg tgcaacaaag agcagactgt ttcagtgtct
1020
ggagcatttc agataaatac ctttgatcta agggttcagc ctttcaatgt gacacaagga
1080
aagtattcta cagctgaaga atgttctgct gactctgacc tcaactttct tattcctgtt
1140
gcagtgggtg tggccttggg cttccttata attgttgtct ttatctctta tatgattgga
1200
agaaggaaaa gtcgtactgg ttatcagtct gtgtaa
1236
<210> 31
<211> 1000
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Вариант LAMP-2
<400> 31
atggtctgct tcagactgtt ccctgtccct ggatctggtc tggtgcttgt gtgcttggtg
60
ctgggtgctg tgagatccta tgcccttgag ctgaacctga ctgactcaga aaatgccact
120
tgcctgtatg ccaagtggca gatgaacttc actgtgagat atgagactac caacaagacc
180
tacaagactg tgaccatctc agaccatggc actgtcacct acaatggatc aatctgtggt
240
gatgatcaga atggcccaaa gatagcagtg cagtttgggc ccggtttttc ctggattgct
300
aacttcacca aggcagcctc cacctacagc attgactcag tcagcttcag ctacaacact
360
ggggataaca ccaccttccc tgacgcagag gacaagggaa tccttactgt ggacgaactc
420
ctggcaatca gaatccccct taacgacctg ttcagatgca actccctttc aacccttgaa
480
aagaatgatg tggtgcaaca ctattgggac gtcctggtgc aagcctttgt gcagaatggg
540
acagtgagta ccaacgagtt cctctgtgac aaggacaaga ccagcactgt ggcccccact
600
atccacacca ctgtgcccag ccctaccact acccccaccc ctaaagagaa gccagaagct
660
ggaacctact cagtcaacaa tggaaatgac acatgcctcc ttgccaccat gggactgcag
720
ctgaacatca ctcaggacaa ggtggcctca gtgattaaca tcaaccctaa caccactcat
780
agcactggga gctgcagatc acatacagct ctgctgaggc tcaactcctc caccatcaag
840
tacctggact ttgtgtttgc tgtgaagaat gagaacaggt tctacctcaa ggaagtgaac
900
atttccatgt acctggtcaa tggttcagtg ttctctattg ccaacaacaa tctgagctac
960
tgggatgcac ccctgggatc ctcctacatg tgcaacaagg
1000
<210> 32
<211> 1000
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Вариант LAMP-2
<400> 32
atggtgtgct ttagactgtt tcctgtgcct ggttcagggc tggtcctggt ctgtctggtg
60
ctgggggctg tcagaagcta tgccttggag ctgaacctca ctgatagtga aaatgccact
120
tgtctgtatg ctaagtggca gatgaacttc actgtgagat atgaaaccac caacaagact
180
tacaaaacag tgaccatctc agatcatgga actgtgacct acaacggcag catttgtgga
240
gacgaccaga acggaccaaa aatcgctgtc caatttgggc ctggattctc ctggattgcc
300
aatttcacta aagctgcctc cacatattca attgactcag tgtccttctc ctacaacact
360
ggggacaaca ctactttccc tgatgctgaa gataagggaa tcttgacagt ggatgagctg
420
ctggctatca ggatcccttt gaatgacctg tttaggtgta attcactgag cactctggag
480
aagaacgacg tggtgcagca ctactgggac gtgctggtgc aggcctttgt gcagaacggc
540
actgtgtcca ccaacgaatt cctgtgtgat aaggacaaaa cttccactgt ggcacctaca
600
attcacacta ctgtgccttc acctaccacc actccaactc caaaggaaaa gcctgaagca
660
ggaacctact ctgtgaacaa tggcaatgat acctgtctgt tggccaccat gggcctccaa
720
ctgaacatta ctcaggacaa ggtggcctca gtgattaaca ttaaccccaa cactacccac
780
tccactggca gctgtagatc acacacagcc ttgctcagac tgaatagcag caccatcaag
840
tatttggatt ttgtgtttgc agtgaagaat gaaaacaggt tctacctgaa ggaagtcaac
900
atctcaatgt acctggtgaa cggctcagtg ttcagcattg ccaacaacaa cctctcctat
960
tgggacgctc cactggggag cagctacatg tgtaacaagg
1000
<210> 33
<211> 1000
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Вариант LAMP-2
<400> 33
atggtctgtt ttaggctgtt ccctgtccct ggttcaggac tggtcttagt gtgtctggtg
60
cttggagctg tcagaagcta tgccctggag ctgaacctga ctgactcaga aaatgccact
120
tgcctgtatg ccaagtggca gatgaacttc actgtcagat atgaaaccac caacaagacc
180
tataagactg tgaccatctc agaccatggc actgtgactt acaatgggtc aatttgtgga
240
gatgaccaga atggccctaa gatagctgtc cagtttggtc caggattcag ctggattgcc
300
aacttcacca aggcagccag cacctacagc attgactctg tgtccttctc ctacaacaca
360
ggagacaaca ccactttccc tgatgcagag gacaaaggta tcctgactgt ggatgagttg
420
ctggcaatca ggatcccact gaacgatctg ttcaggtgca actcactgtc cactctggaa
480
aagaatgatg tggtgcagca ctattgggat gtgctagtcc aggcctttgt ccagaatggg
540
actgtgtcaa ctaatgagtt cctgtgtgac aaggacaaga caagcactgt agcccccact
600
atccatacca cagtacctag ccccaccact actccaaccc ccaaggagaa gcctgaggct
660
ggcacctact cagtgaacaa tgggaatgac acctgtttgc tggccactat gggactccaa
720
ctgaacatca cccaggacaa agtggcctct gtgatcaata tcaatcccaa caccacccac
780
agcactgggt cctgcagaag ccacactgcc ctcctgaggc tcaactcatc aactatcaag
840
tacttggatt ttgtgtttgc agtgaagaat gagaacagat tctacctcaa agaggtcaac
900
atttcaatgt acctggtgaa tgggagtgtg ttctccattg ctaacaacaa cctgagctac
960
tgggatgccc ctctgggctc ctcatacatg tgcaacaagg
1000
<210> 34
<211> 410
<212> БЕЛОК
<213> Homo sapiens
<400> 34
Met Val Cys Phe Arg Leu Phe Pro Val Pro Gly Ser Gly Leu Val Leu
1 5 10 15
Val Cys Leu Val Leu Gly Ala Val Arg Ser Tyr Ala Leu Glu Leu Asn
20 25 30
Leu Thr Asp Ser Glu Asn Ala Thr Cys Leu Tyr Ala Lys Trp Gln Met
35 40 45
Asn Phe Thr Val Arg Tyr Glu Thr Thr Asn Lys Thr Tyr Lys Thr Val
50 55 60
Thr Ile Ser Asp His Gly Thr Val Thr Tyr Asn Gly Ser Ile Cys Gly
65 70 75 80
Asp Asp Gln Asn Gly Pro Lys Ile Ala Val Gln Phe Gly Pro Gly Phe
85 90 95
Ser Trp Ile Ala Asn Phe Thr Lys Ala Ala Ser Thr Tyr Ser Ile Asp
100 105 110
Ser Val Ser Phe Ser Tyr Asn Thr Gly Asp Asn Thr Thr Phe Pro Asp
115 120 125
Ala Glu Asp Lys Gly Ile Leu Thr Val Asp Glu Leu Leu Ala Ile Arg
130 135 140
Ile Pro Leu Asn Asp Leu Phe Arg Cys Asn Ser Leu Ser Thr Leu Glu
145 150 155 160
Lys Asn Asp Val Val Gln His Tyr Trp Asp Val Leu Val Gln Ala Phe
165 170 175
Val Gln Asn Gly Thr Val Ser Thr Asn Glu Phe Leu Cys Asp Lys Asp
180 185 190
Lys Thr Ser Thr Val Ala Pro Thr Ile His Thr Thr Val Pro Ser Pro
195 200 205
Thr Thr Thr Pro Thr Pro Lys Glu Lys Pro Glu Ala Gly Thr Tyr Ser
210 215 220
Val Asn Asn Gly Asn Asp Thr Cys Leu Leu Ala Thr Met Gly Leu Gln
225 230 235 240
Leu Asn Ile Thr Gln Asp Lys Val Ala Ser Val Ile Asn Ile Asn Pro
245 250 255
Asn Thr Thr His Ser Thr Gly Ser Cys Arg Ser His Thr Ala Leu Leu
260 265 270
Arg Leu Asn Ser Ser Thr Ile Lys Tyr Leu Asp Phe Val Phe Ala Val
275 280 285
Lys Asn Glu Asn Arg Phe Tyr Leu Lys Glu Val Asn Ile Ser Met Tyr
290 295 300
Leu Val Asn Gly Ser Val Phe Ser Ile Ala Asn Asn Asn Leu Ser Tyr
305 310 315 320
Trp Asp Ala Pro Leu Gly Ser Ser Tyr Met Cys Asn Lys Glu Gln Thr
325 330 335
Val Ser Val Ser Gly Ala Phe Gln Ile Asn Thr Phe Asp Leu Arg Val
340 345 350
Gln Pro Phe Asn Val Thr Gln Gly Lys Tyr Ser Thr Ala Gln Asp Cys
355 360 365
Ser Ala Asp Asp Asp Asn Phe Leu Val Pro Ile Ala Val Gly Ala Ala
370 375 380
Leu Ala Gly Val Leu Ile Leu Val Leu Leu Ala Tyr Phe Ile Gly Leu
385 390 395 400
Lys His His His Ala Gly Tyr Glu Gln Phe
405 410
<210> 35
<211> 411
<212> БЕЛОК
<213> Homo sapiens
<400> 35
Met Val Cys Phe Arg Leu Phe Pro Val Pro Gly Ser Gly Leu Val Leu
1 5 10 15
Val Cys Leu Val Leu Gly Ala Val Arg Ser Tyr Ala Leu Glu Leu Asn
20 25 30
Leu Thr Asp Ser Glu Asn Ala Thr Cys Leu Tyr Ala Lys Trp Gln Met
35 40 45
Asn Phe Thr Val Arg Tyr Glu Thr Thr Asn Lys Thr Tyr Lys Thr Val
50 55 60
Thr Ile Ser Asp His Gly Thr Val Thr Tyr Asn Gly Ser Ile Cys Gly
65 70 75 80
Asp Asp Gln Asn Gly Pro Lys Ile Ala Val Gln Phe Gly Pro Gly Phe
85 90 95
Ser Trp Ile Ala Asn Phe Thr Lys Ala Ala Ser Thr Tyr Ser Ile Asp
100 105 110
Ser Val Ser Phe Ser Tyr Asn Thr Gly Asp Asn Thr Thr Phe Pro Asp
115 120 125
Ala Glu Asp Lys Gly Ile Leu Thr Val Asp Glu Leu Leu Ala Ile Arg
130 135 140
Ile Pro Leu Asn Asp Leu Phe Arg Cys Asn Ser Leu Ser Thr Leu Glu
145 150 155 160
Lys Asn Asp Val Val Gln His Tyr Trp Asp Val Leu Val Gln Ala Phe
165 170 175
Val Gln Asn Gly Thr Val Ser Thr Asn Glu Phe Leu Cys Asp Lys Asp
180 185 190
Lys Thr Ser Thr Val Ala Pro Thr Ile His Thr Thr Val Pro Ser Pro
195 200 205
Thr Thr Thr Pro Thr Pro Lys Glu Lys Pro Glu Ala Gly Thr Tyr Ser
210 215 220
Val Asn Asn Gly Asn Asp Thr Cys Leu Leu Ala Thr Met Gly Leu Gln
225 230 235 240
Leu Asn Ile Thr Gln Asp Lys Val Ala Ser Val Ile Asn Ile Asn Pro
245 250 255
Asn Thr Thr His Ser Thr Gly Ser Cys Arg Ser His Thr Ala Leu Leu
260 265 270
Arg Leu Asn Ser Ser Thr Ile Lys Tyr Leu Asp Phe Val Phe Ala Val
275 280 285
Lys Asn Glu Asn Arg Phe Tyr Leu Lys Glu Val Asn Ile Ser Met Tyr
290 295 300
Leu Val Asn Gly Ser Val Phe Ser Ile Ala Asn Asn Asn Leu Ser Tyr
305 310 315 320
Trp Asp Ala Pro Leu Gly Ser Ser Tyr Met Cys Asn Lys Glu Gln Thr
325 330 335
Val Ser Val Ser Gly Ala Phe Gln Ile Asn Thr Phe Asp Leu Arg Val
340 345 350
Gln Pro Phe Asn Val Thr Gln Gly Lys Tyr Ser Thr Ala Glu Glu Cys
355 360 365
Ser Ala Asp Ser Asp Leu Asn Phe Leu Ile Pro Val Ala Val Gly Val
370 375 380
Ala Leu Gly Phe Leu Ile Ile Val Val Phe Ile Ser Tyr Met Ile Gly
385 390 395 400
Arg Arg Lys Ser Arg Thr Gly Tyr Gln Ser Val
405 410
<210> 36
<211> 21
<212> ДНК
<213> Вирус гепатита сурков
<400> 36
atcatgctat tgcttcccgt a
21
<210> 37
<211> 20
<212> ДНК
<213> Вирус гепатита сурков
<400> 37
gggccacaac tcctcataaa
20
<210> 38
<211> 29
<212> ДНК
<213> Вирус гепатита сурков
<400> 38
cctccttgta taaatcctgg ttgctgtct
29
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ОПТИМИЗИРОВАННЫЕ ГЕНЫ И ЭКСПРЕССИОННЫЕ КАССЕТЫ МИНИ-ДИСТРОФИНА И ИХ ПРИМЕНЕНИЕ | 2017 |
|
RU2753194C2 |
| УЛУЧШЕНИЕ КЛИНИЧЕСКИХ ПАРАМЕТРОВ ПОСРЕДСТВОМ ЭКСПРЕССИИ ФАКТОРА VIII | 2019 |
|
RU2799048C2 |
| СПОСОБЫ ЛЕЧЕНИЯ БОЛЕЗНИ ДАНОНА И ДРУГИХ НАРУШЕНИЙ АУТОФАГИИ | 2017 |
|
RU2777571C2 |
| ВАРИАНТЫ, НА ОСНОВЕ АДЕНОАССОЦИИРОВАННОГО ВИРУСА, СОСТАВЫ И СПОСОБЫ ДЛЯ ПУЛЬМОНАЛЬНОЙ ДОСТАВКИ | 2021 |
|
RU2829874C1 |
| СКОНСТРУИРОВАННЫЕ АДЕНОАССОЦИИРОВАННЫЕ (AAV) ВЕКТОРЫ ДЛЯ ЭКСПРЕССИИ ТРАНСГЕНА | 2020 |
|
RU2839774C2 |
| ГЕНОТЕРАПЕВТИЧЕСКИЕ КОНСТРУКЦИИ ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНИ ВИЛЬСОНА | 2020 |
|
RU2807158C2 |
| ГЕННАЯ ТЕРАПИЯ ДЛЯ ЛЕЧЕНИЯ ГЕМОФИЛИИ A | 2017 |
|
RU2762257C2 |
| ГЕННАЯ ТЕРАПИЯ ПАЦИЕНТОВ С АНЕМИЕЙ ФАНКОНИ | 2017 |
|
RU2801241C2 |
| КОДОН-ОПТИМИЗИРОВАННЫЕ ЭКСПРЕССИРУЮЩИЕ КАССЕТЫ КИСЛОЙ α-ГЛЮКОЗИДАЗЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2823353C2 |
| МОДИФИЦИРОВАННЫЙ ФАКТОР IX, А ТАКЖЕ КОМПОЗИЦИИ, СПОСОБЫ И ВАРИАНТЫ ПРИМЕНЕНИЯ ПЕРЕНОСА ГЕНОВ В КЛЕТКИ, ОРГАНЫ И ТКАНИ | 2016 |
|
RU2811445C2 |
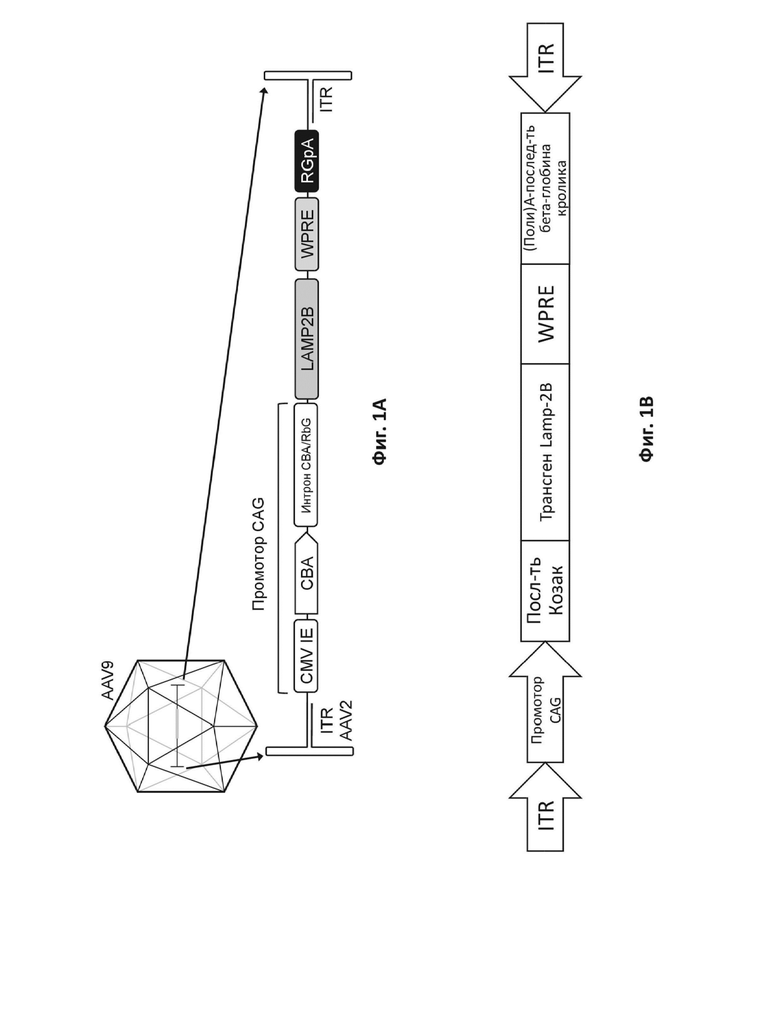
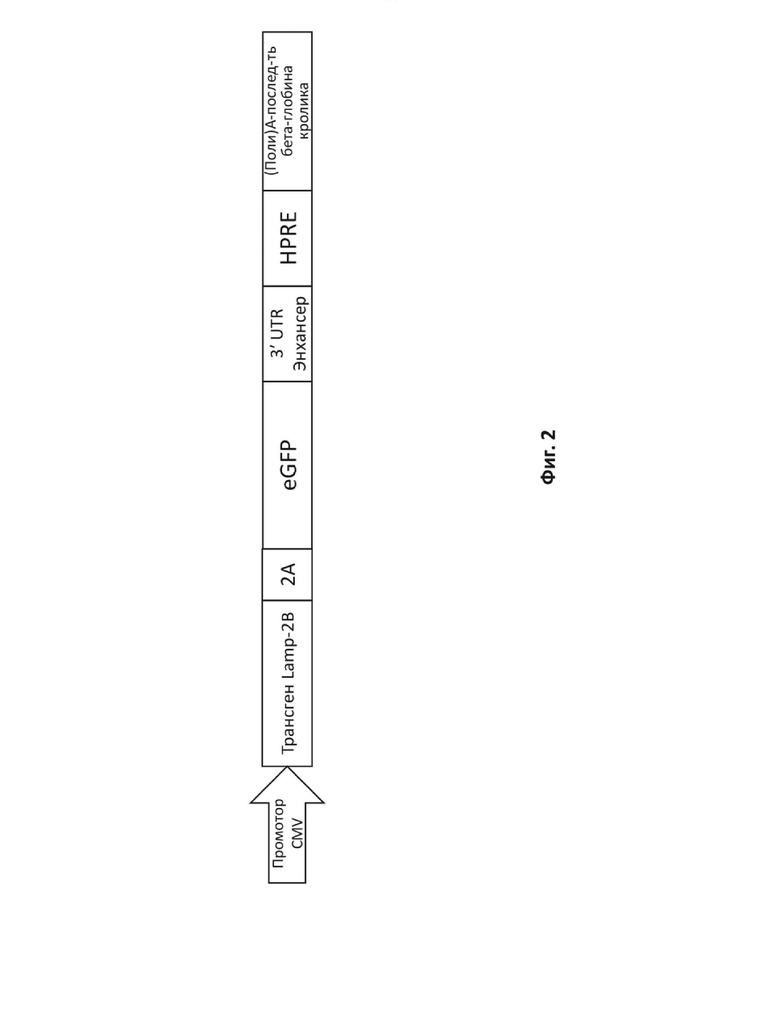
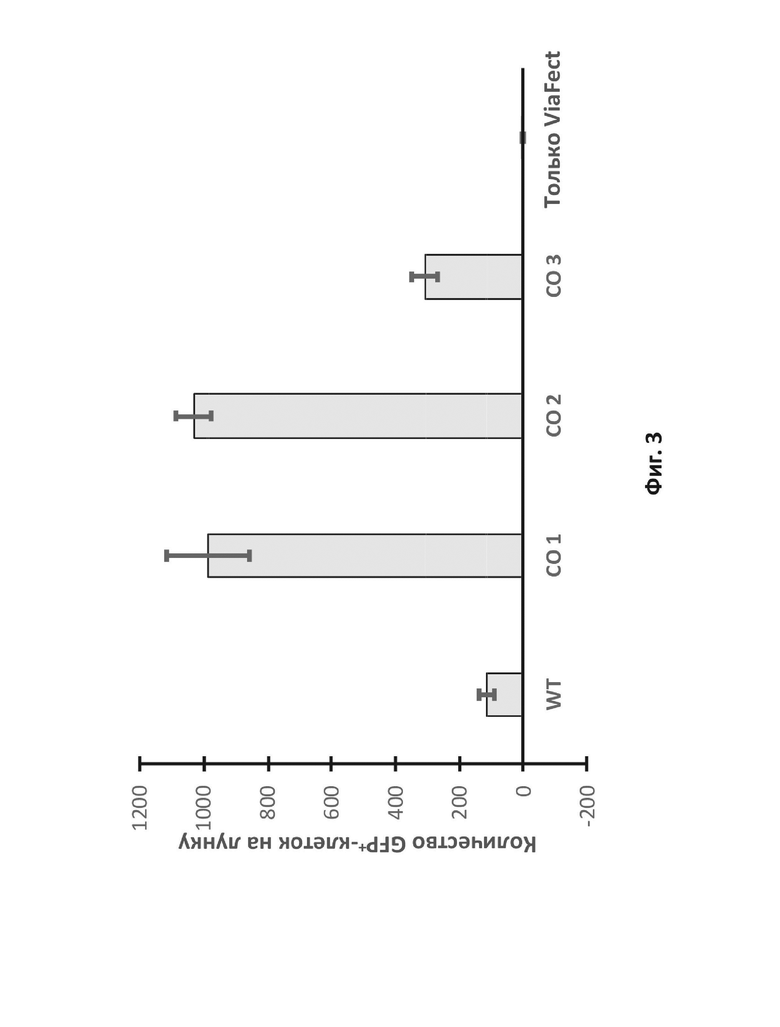
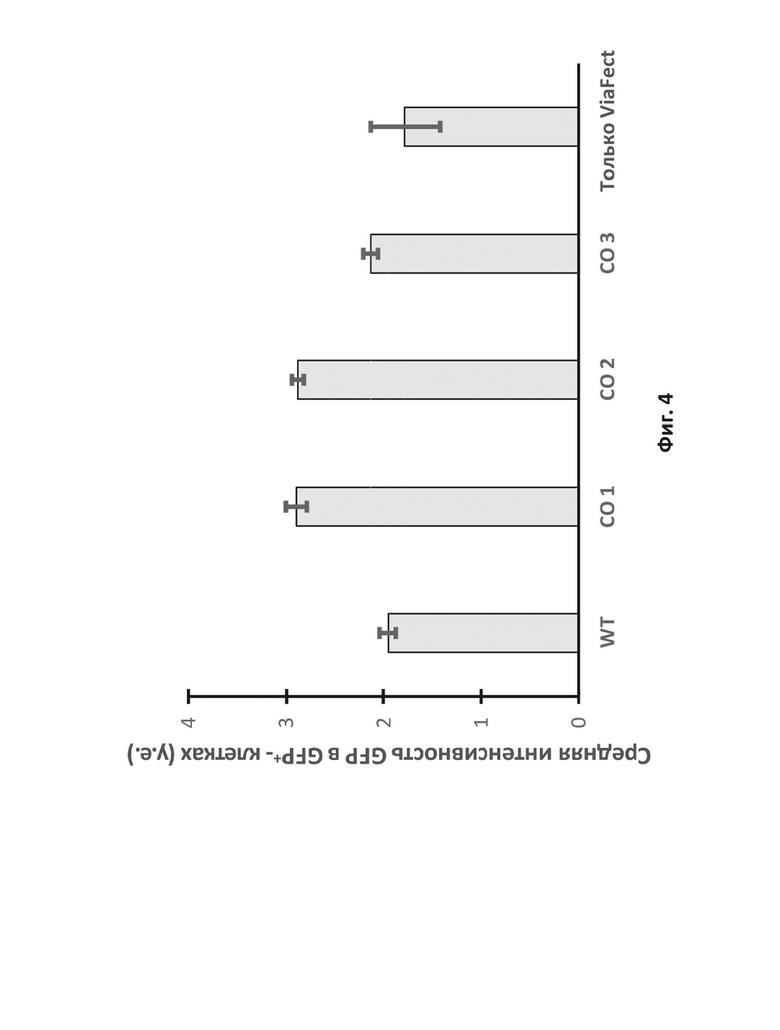
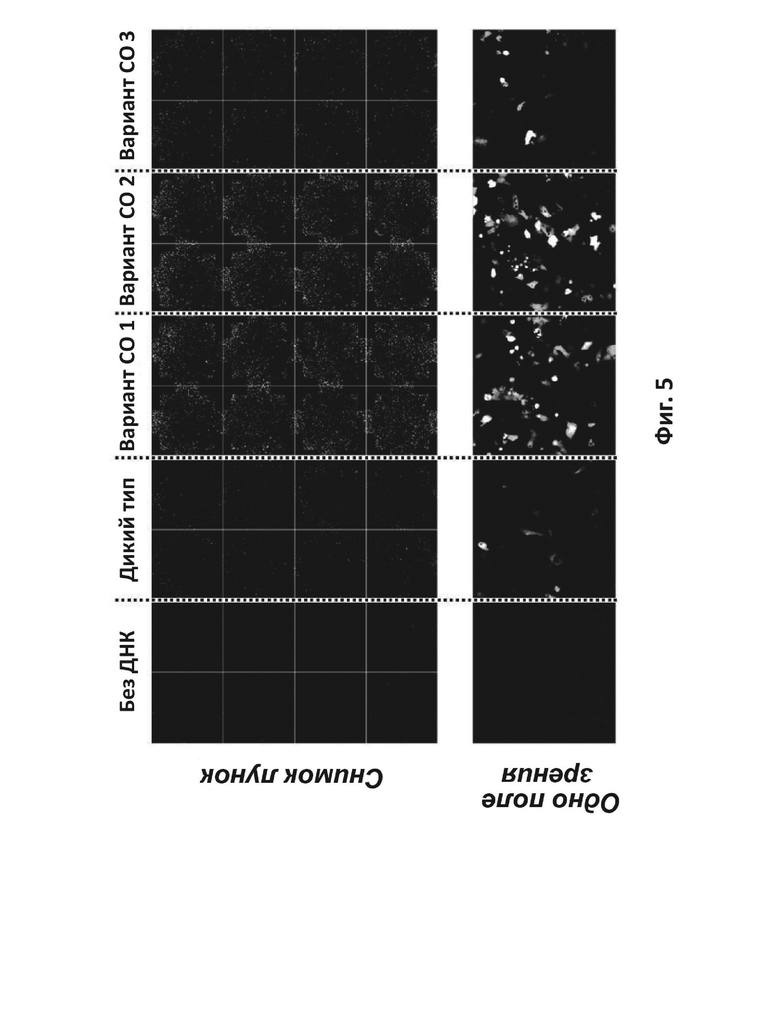
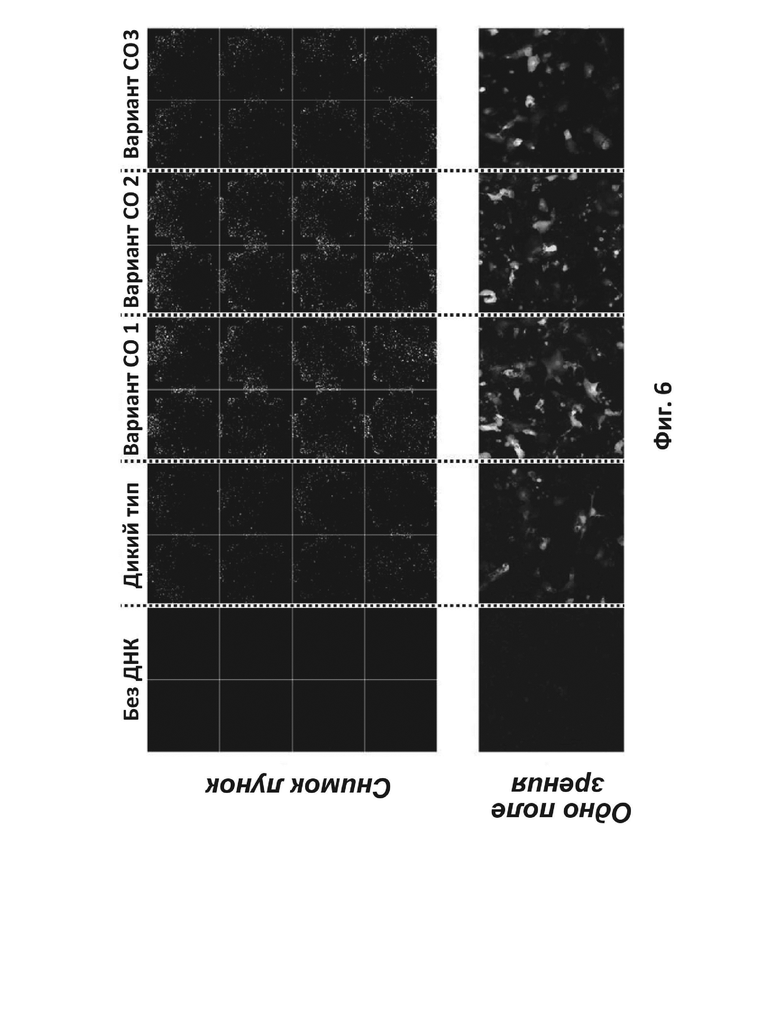
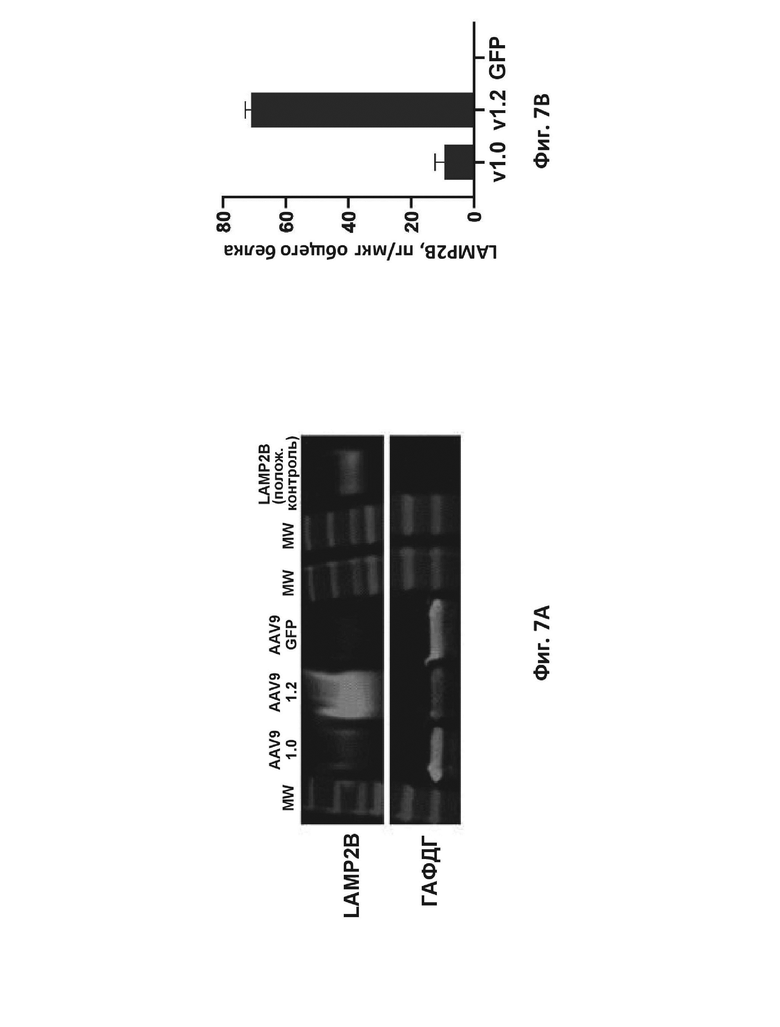
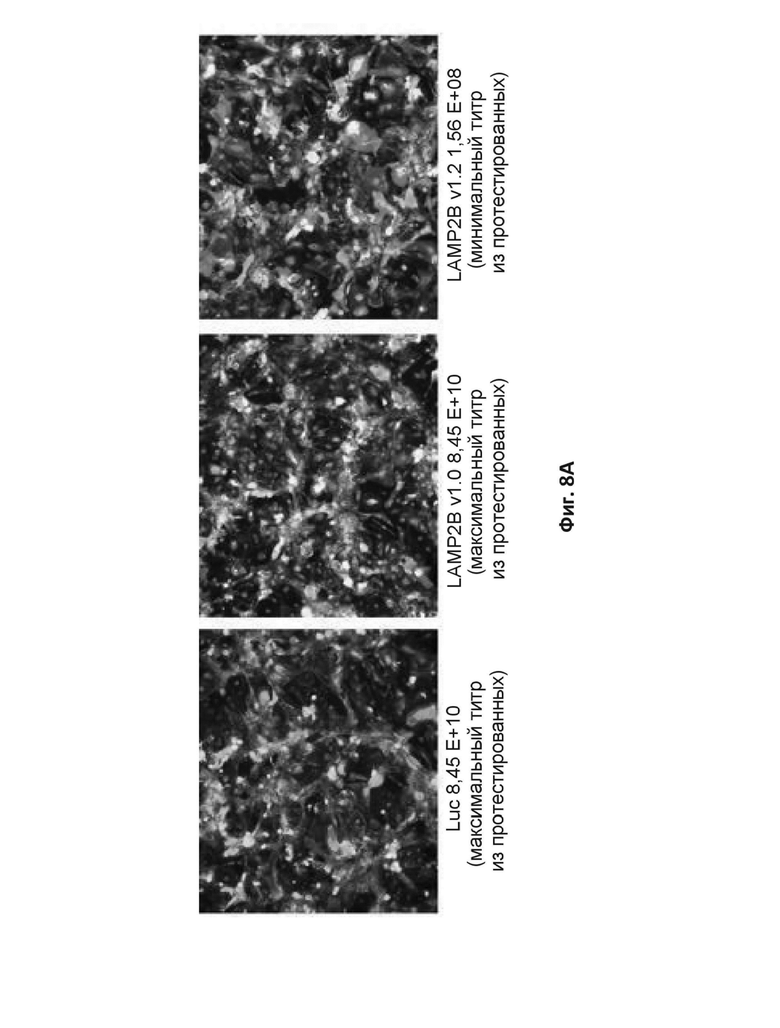
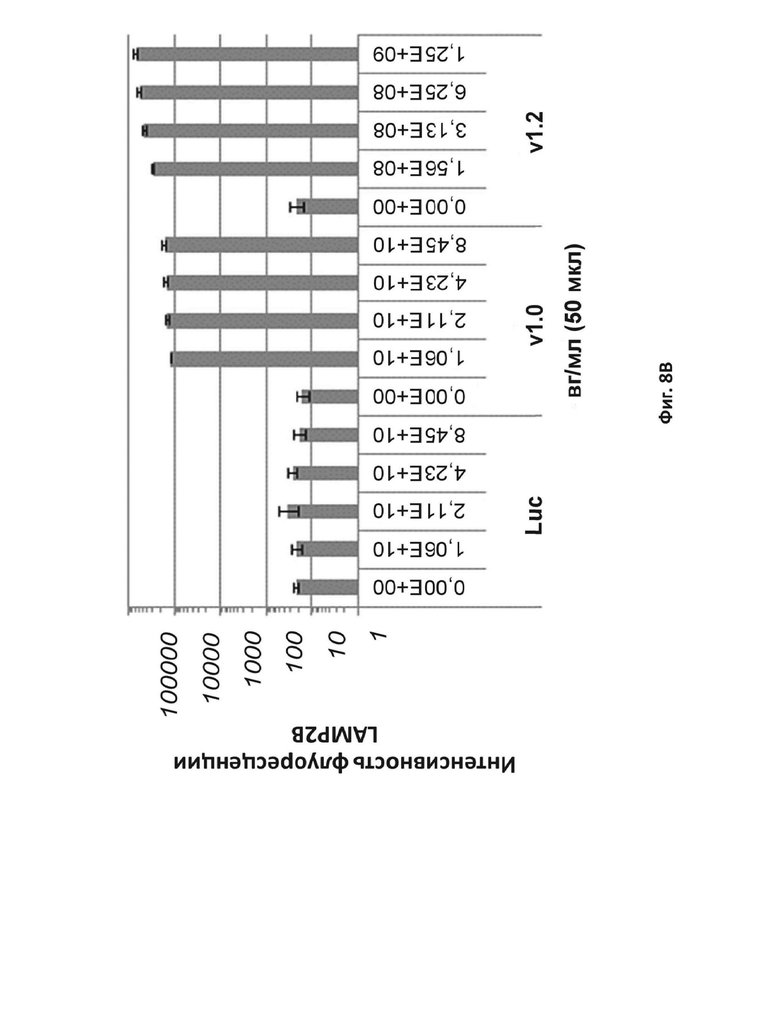
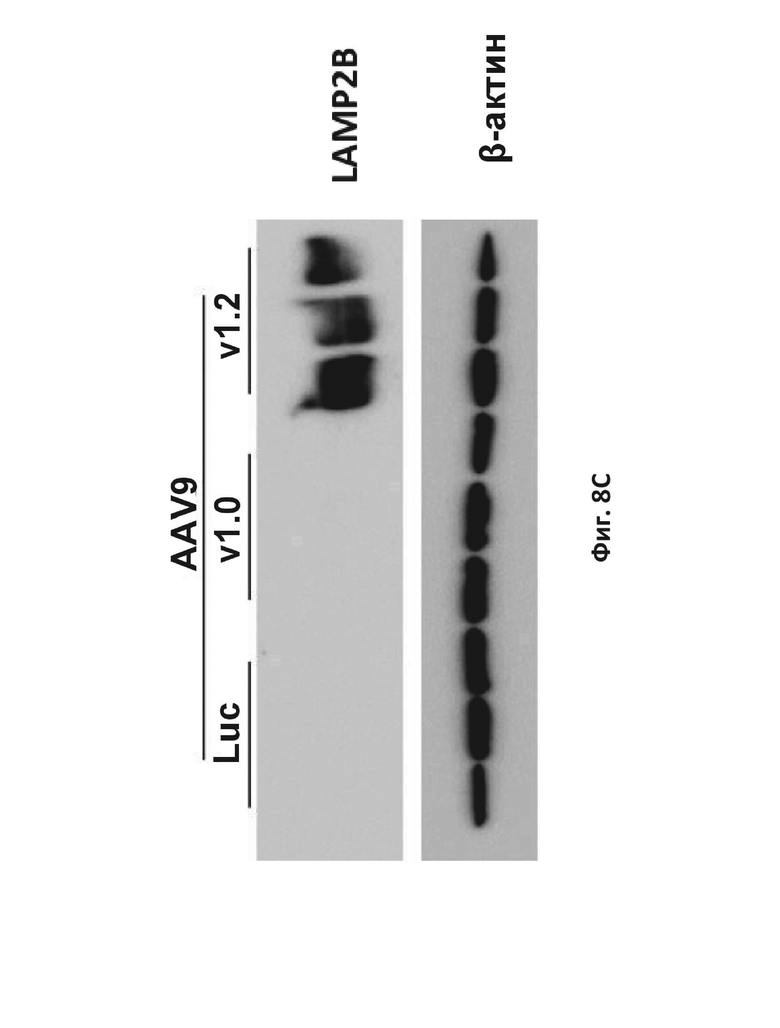
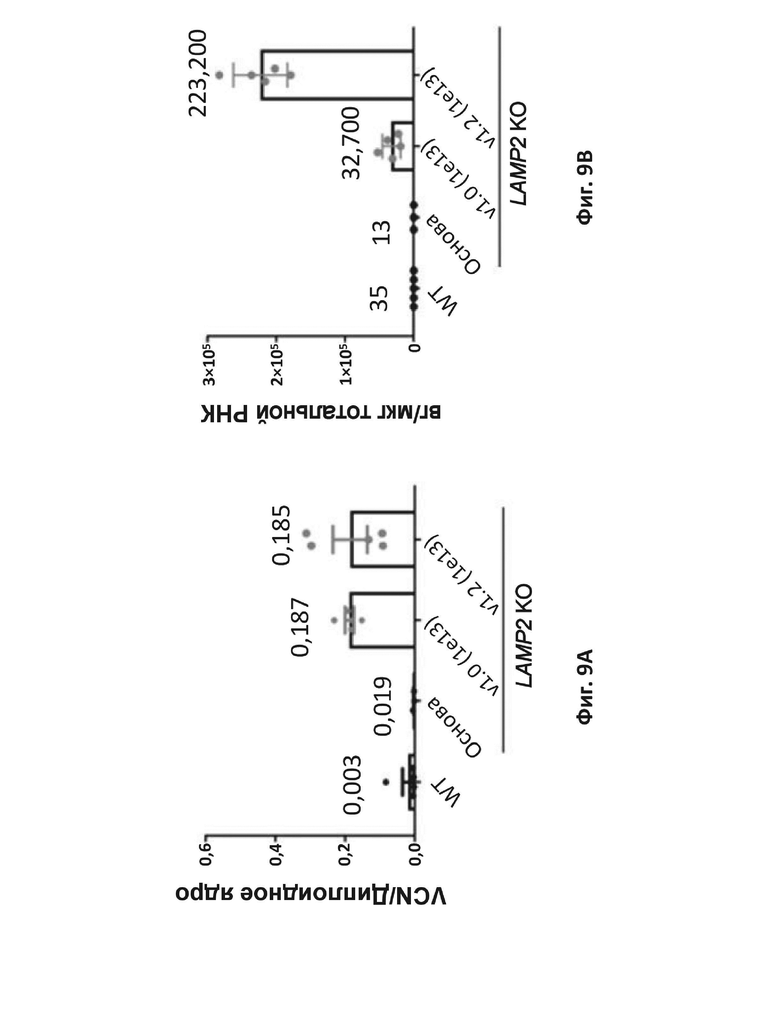
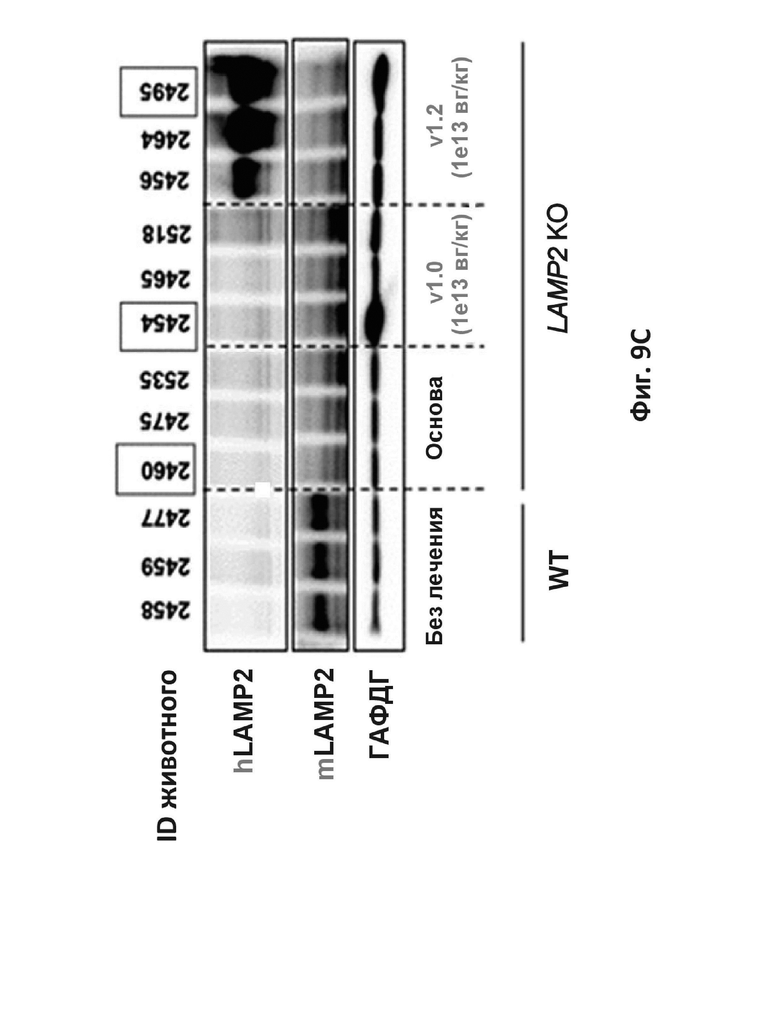
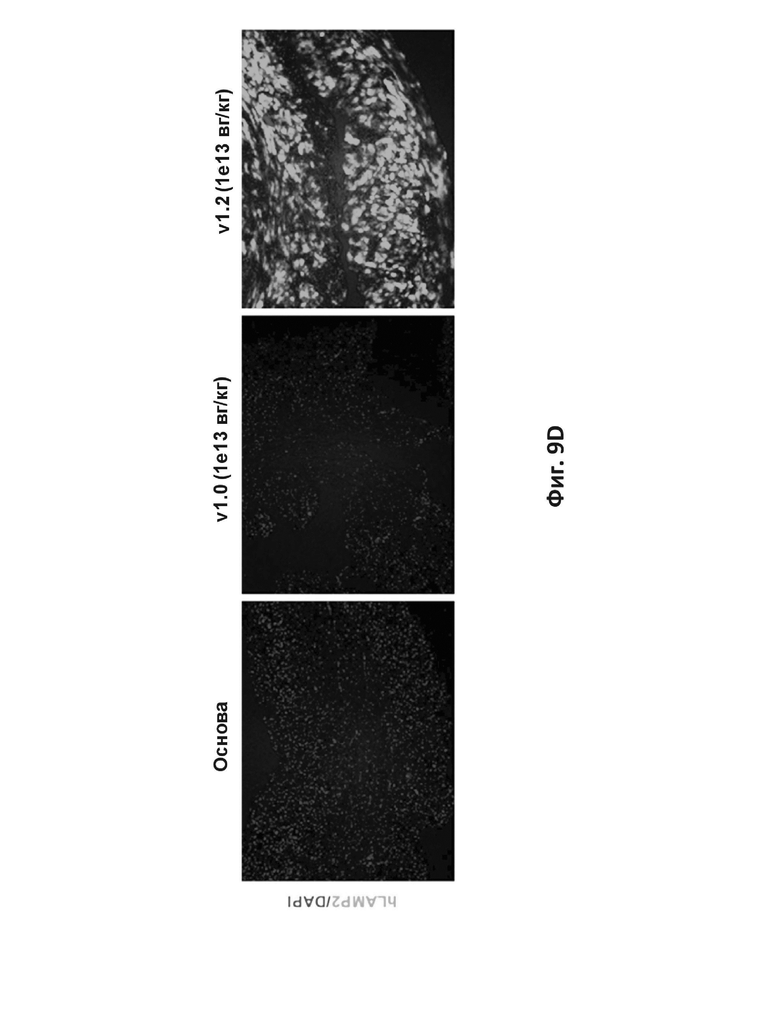
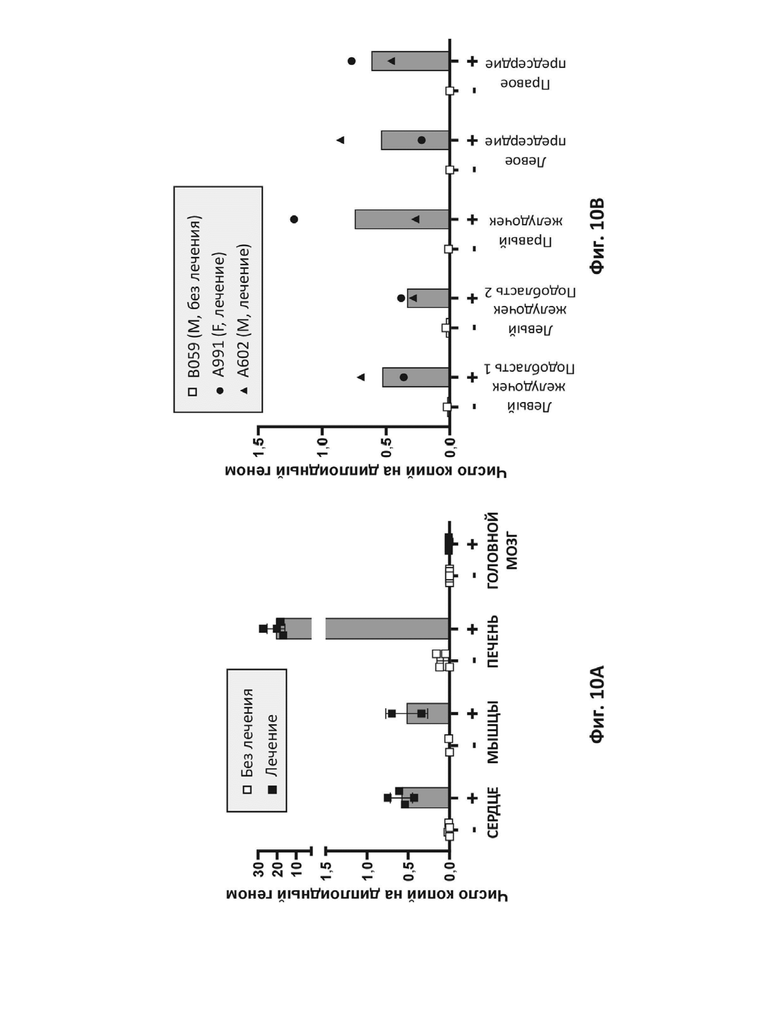
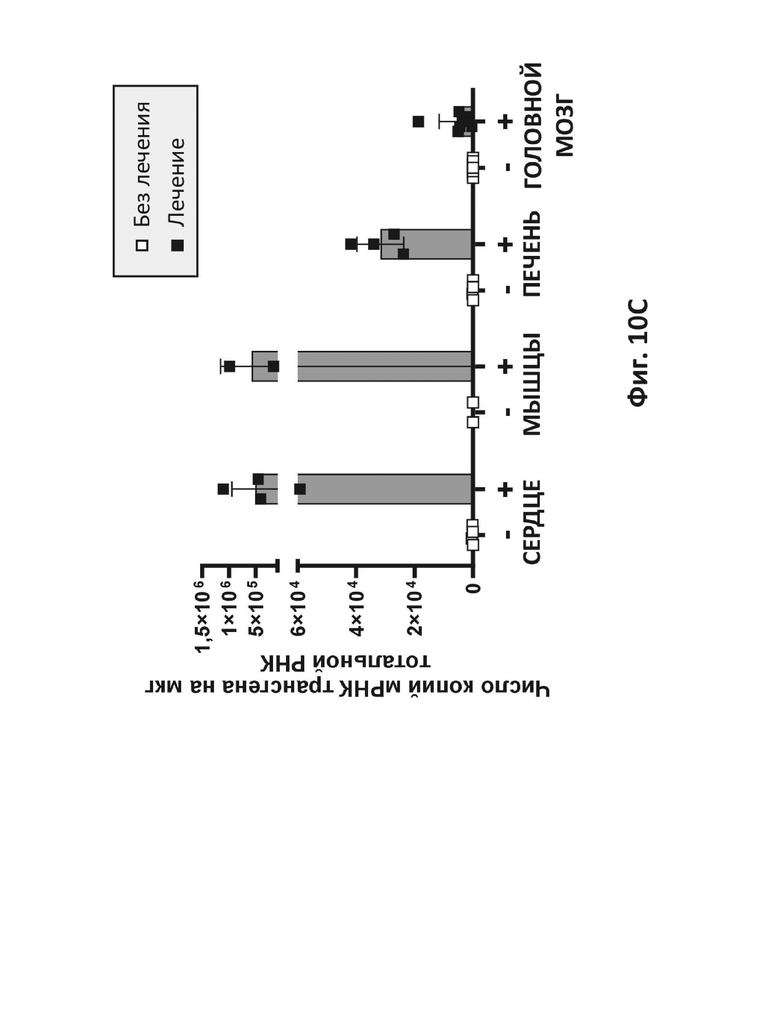
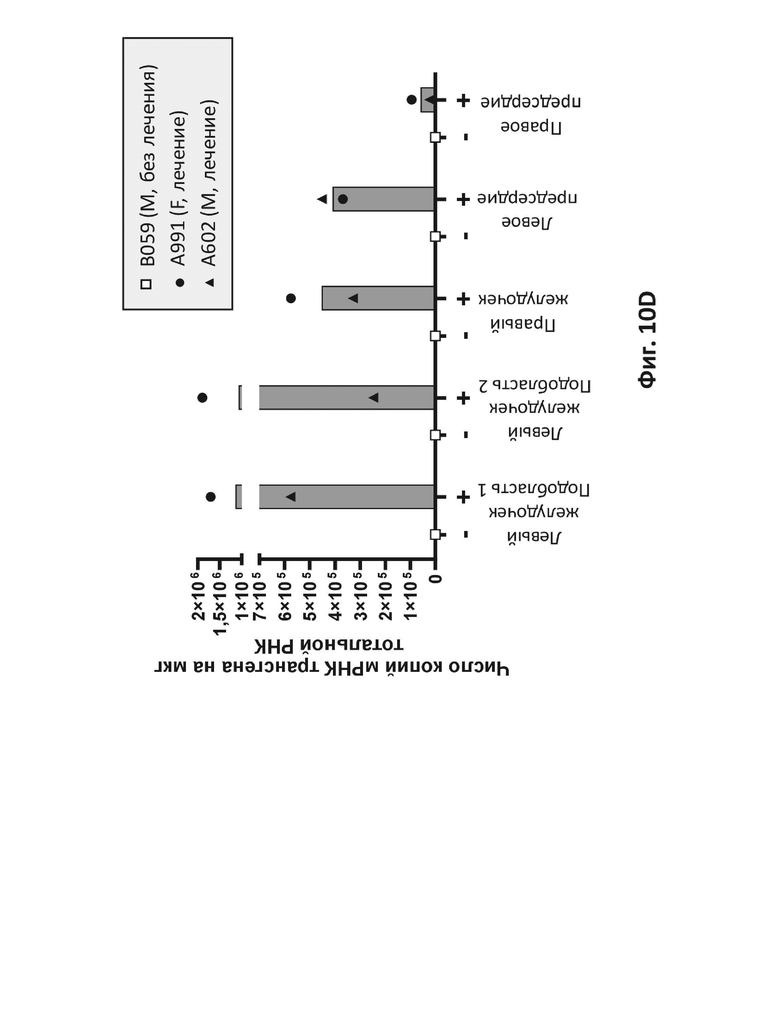
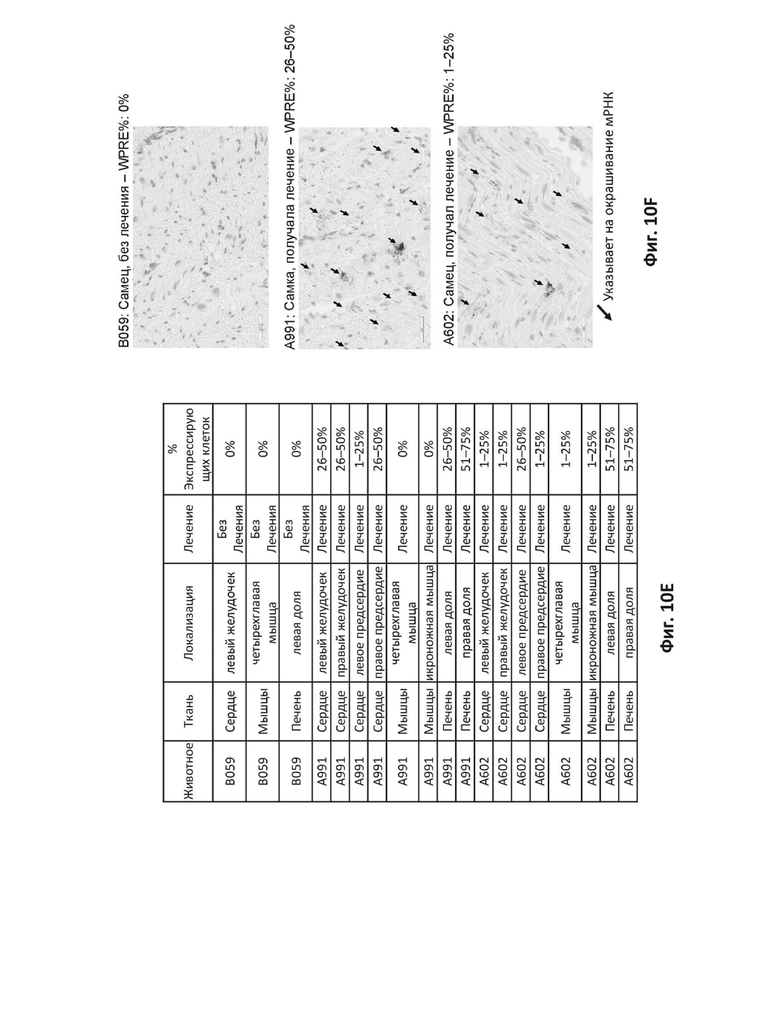
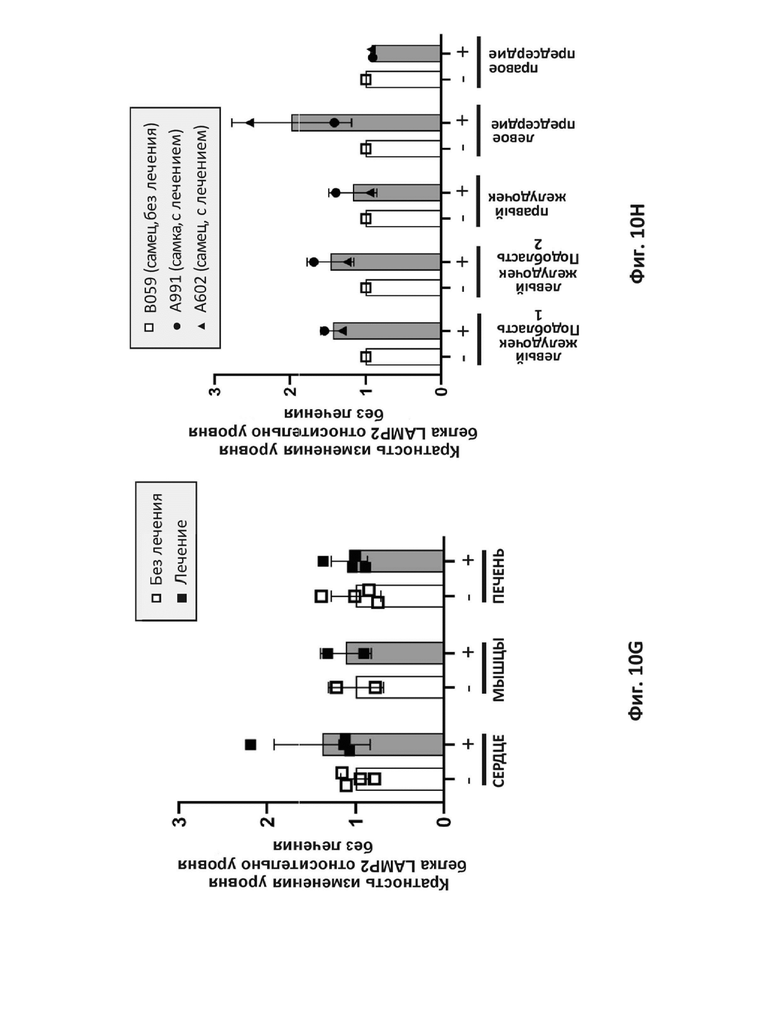
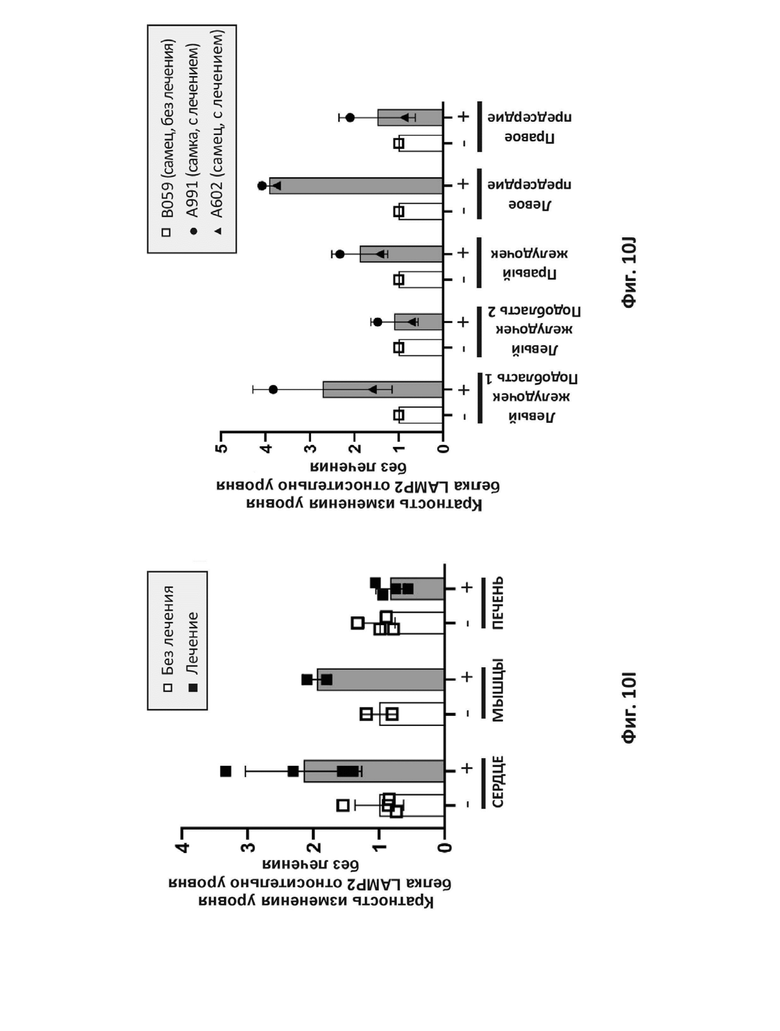
Изобретение относится к области молекулярной биологии. Описан геннотерапевтический вектор, содержащий экспрессионную кассету, которая содержит трансген, кодирующий ассоциированный с лизосомами мембранный белок 2B (LAMP-2B) или его функциональный вариант, причем указанный трансген кодон-оптимизирован для экспрессии в человеческой клетке-хозяине, и причем последовательность указанного трансгена обладает по меньшей мере 95% идентичностью с последовательностью, выбранной из SEQ ID NO: 3–5. Также описана фармацевтическая композиция для лечения или предотвращения болезни Данона, содержащая геннотерапевтический вектор. Представлен способ лечения или предотвращения болезни Данона или другого аутофагического нарушения у нуждающегося в этом субъекта, включающий введение указанному субъекту геннотерапевтического вектора или фармацевтической композиции. Заявленное изобретение расширяет арсенал средств для болезни Данона. 3 н. и 27 з.п. ф-лы, 10 ил., 4 пр.
1. Геннотерапевтический вектор, содержащий экспрессионную кассету, которая содержит трансген, кодирующий ассоциированный с лизосомами мембранный белок 2B (LAMP-2B) или его функциональный вариант, причем указанный трансген кодон-оптимизирован для экспрессии в человеческой клетке-хозяине, и причем последовательность указанного трансгена обладает по меньшей мере 95% идентичностью с последовательностью, выбранной из SEQ ID NO: 3–5.
2. Геннотерапевтический вектор по п. 1, характеризующийся тем, что LAMP-2B содержит SEQ ID NO: 1.
3. Геннотерапевтический вектор по любому из пп. 1 и 2, характеризующийся тем, что указанная экспрессионная кассета содержит меньше сайтов CpG, чем SEQ ID: 2.
4. Геннотерапевтический вектор по любому из пп. 1–3, характеризующийся тем, что указанная экспрессионная кассета содержит меньше скрытых сайтов сплайсинга, чем SEQ ID: 2.
5. Геннотерапевтический вектор по любому из пп. 1–4, характеризующийся тем, что указанная экспрессионная кассета кодирует меньше альтернативных открытых рамок считывания, чем SEQ ID: 2.
6. Геннотерапевтический вектор по любому из пп. 1–5, характеризующийся тем, что последовательность указанного трансгена по меньшей мере на 99% идентична последовательности, выбранной из SEQ ID NO: 3–5.
7. Геннотерапевтический вектор по любому из пп. 1–6, характеризующийся тем, что указанный трансген содержит последовательность, выбранную из SEQ ID NO: 3–5.
8. Геннотерапевтический вектор по любому из пп. 1–5, характеризующийся тем, что последовательность указанного трансгена обладает по меньшей мере 95% идентичностью с SEQ ID NO: 3.
9. Геннотерапевтический вектор по п. 8, характеризующийся тем, что указанный трансген содержит SEQ ID NO: 3.
10. Геннотерапевтический вектор по любому из пп. 1–9, характеризующийся тем, что указанная экспрессионная кассета содержит консенсусную оптимальную последовательность Козак, которая необязательно содержит SEQ ID NO: 6.
11. Геннотерапевтический вектор по любому из пп. 1–10, характеризующийся тем, что указанная экспрессионная кассета содержит полноразмерную (поли)А-последовательность, которая необязательно содержит SEQ ID NO: 7.
12. Геннотерапевтический вектор по любому из пп. 1–11, характеризующийся тем, что указанная экспрессионная кассета не содержит в направлении 5′ от трансгена стартового сайта, способного давать альтернативные мРНК.
13. Геннотерапевтический вектор по любому из пп. 1–12, характеризующийся тем, что указанная экспрессионная кассета содержит в направлении от 5′- к 3′-концу: первый инвертированный концевой повтор, энхансерную/промоторную область, интроны, консенсусную оптимальную последовательность Козак, трансген, нетранслируемую 3′-область, включающую полноразмерную (поли)А-последовательность, и второй инвертированный концевой повтор.
14. Геннотерапевтический вектор по п. 13, характеризующийся тем, что указанная энхансерная/промоторная область содержит в направлении от 5′- к 3′-концу энхансер средних и ранних генов цитомегаловируса (CMV IE) и промотор бета-актина курицы, и при этом необязательно энхансерная/промоторная область дополнительно содержит первый экзон и первый интрон гена бета-актина курицы и акцептор сплайсинга гена бета-глобина кролика.
15. Геннотерапевтический вектор по п. 1, характеризующийся тем, что последовательность указанной экспрессионной кассеты обладает по меньшей мере 95% идентичностью с последовательности, выбранной из SEQ ID NO: 8–10.
16. Геннотерапевтический вектор по п. 15, характеризующийся тем, что последовательность указанной экспрессионной кассеты полностью идентична последовательности, выбранной из SEQ ID NO: 8–10.
17. Геннотерапевтический вектор по п. 16, характеризующийся тем, что последовательность указанной экспрессионной кассеты идентична SEQ ID NO: 8.
18. Геннотерапевтический вектор по любому из пп. 1–17, характеризующийся тем, что указанный вектор представляет собой вектор на основе аденоассоциированного вируса (AAV).
19. Геннотерапевтический вектор по п. 18, характеризующийся тем, что AAV-вектор представляет собой AAV9-вектор или AAVrh.74-вектор.
20. Фармацевтическая композиция для лечения или предотвращения болезни Данона, содержащая геннотерапевтический вектор по любому из пп. 1–19.
21. Способ лечения или предотвращения болезни Данона или другого аутофагического нарушения у нуждающегося в этом субъекта, включающий введение указанному субъекту геннотерапевтического вектора по любому из пп. 1–19 или фармацевтической композиции по п. 20.
22. Способ по п. 21, характеризующийся тем, что указанный вектор или фармацевтическую композицию вводят путем, выбранным из группы, состоящей из внутривенного, внутриартериального, внутрисердечного, интракоронарного, интрамиокардиального, внутрипочечного, внутриуретрального, эпидурального и внутримышечного введения.
23. Способ по п. 21 или 22, характеризующийся тем, что указанное аутофагическое нарушение выбрано из группы, состоящей из терминальной сердечной недостаточности, инфаркта миокарда, лекарственных токсичностей, диабета, терминальной почечной недостаточности и старения.
24. Способ по любому из пп. 21–23, характеризующийся тем, что указанный субъект представляет собой человека.
25. Способ по любому из пп. 21–24, характеризующийся тем, что у указанного субъекта наблюдаются симптомы болезни Данона или другого аутофагического нарушения.
26. Способ по любому из пп. 21–25, характеризующийся тем, что указанный субъект был идентифицирован как имеющий пониженную или недетектируемую экспрессию LAMP-2.
27. Способ по любому из пп. 21–26, характеризующийся тем, что указанный субъект был идентифицирован как имеющий мутированный ген LAMP-2.
28. Способ по любому из пп. 21–27, характеризующийся тем, что введение указанного геннотерапевтического вектора приводит к повышению экспрессии полинуклеотида LAMP-2B и/или белка LAMP-2B в сердце по сравнению с его экспрессией у не получавшего лечения субъекта.
29. Способ по любому из пп. 21–28, характеризующийся тем, что введение указанного геннотерапевтического вектора приводит по меньшей мере приблизительно к 1,2-кратному, по меньшей мере приблизительно 1,3-кратному, по меньшей мере приблизительно 1,4-кратному, по меньшей мере приблизительно 1,5-кратному, по меньшей мере приблизительно 1,6-кратному, по меньшей мере приблизительно 1,7-кратному, по меньшей мере приблизительно 1,8-кратному, по меньшей мере приблизительно 1,9-кратному, по меньшей мере приблизительно 2,0-кратному, по меньшей мере приблизительно 2,2-кратному, по меньшей мере приблизительно 2,3-кратному, по меньшей мере приблизительно 2,4-кратному, по меньшей мере приблизительно 2,5-кратному, по меньшей мере приблизительно 3-кратному или по меньшей мере приблизительно 4-кратному повышению экспрессии полинуклеотида LAMP-2B и/или белка LAMP-2B в сердце по сравнению с его экспрессией у не получавшего лечение субъекта.
30. Способ по любому из пп. 21–29, характеризующийся тем, что введение указанного геннотерапевтического вектора приводит к максимум приблизительно 1,1-кратному, максимум приблизительно 1,2-кратному, максимум приблизительно 1,3-кратному, максимум приблизительно 1,4-кратному или максимум приблизительно 1,5-кратному повышению экспрессии полинуклеотида LAMP-2B и/или белка LAMP-2B в печени по сравнению с экспрессией в печени не получавшего лечение субъекта.
| WO 2017127565 A1, 27.07.2017 | |||
| Bevan Kai-Sheng Chung & Dong-Yup Lee, Computational codon optimization of synthetic gene for protein expression, BMC Systems Biology volume6, Article number: 134 (2012), Published: 20 October 2012 найдено в интернет 29.03.2023 | |||
| WO 2004031210 A2, 15.04.2004 | |||
| ДОСТАВКА К ЦНС ЛЕЧЕБНЫХ АГЕНТОВ | 2011 |
|
RU2626514C2 |
Авторы
Даты
2023-11-28—Публикация
2019-07-11—Подача