Изобретение относится к медицине, конкретно к веществам, которые препятствуют тромбообразованию, а именно к веществам-антиагрегантам, которые угнетают функции тромбоцитов. В медицине существует потребность в веществах, которые предотвращают образование тромбов, происходящее с участием тромбоцитов.
Известна антиагрегантная активность ацетилсалициловой кислоты, аспирина (Awtry Е.Н., Lozcalzo J. Aspirin. Circulation 2000, Vol. 101, pp. 1206-1218). Ацетилсалициловая кислота угнетает функции тромбоцитов путем химической реакции, заключающейся в необратимом ацетилировании циклооксигеназы 1. В тромбоците снижается образование тромбоксана А2, который является вторичным активатором тромбоцитов. Ацетилсалициловая кислота проявляет антиагрегантное действие только в ситуациях, когда тромбоциты активируются с участием циклооксигеназы.
Известен класс антиагрегантных тиенопиридиновых соединений: клопидогрел, тиклопидин, прасугрел (Guerre D.R., Tcheng J.E. Prasugrel: Clinical Development and Therapeutic Application. Adv. Ther. 2009, Vol. 26, No. 11, pp. 999-1011). Антиагрегантное действие этих соединений в кровяном русле обусловлено метаболитом-тиолом, имеющем активную сульфгидрильную группу атомов. Метаболит необратимо реагирует с сульфгидрильной группой тромбоцитного пуринового рецептора P2Y12 с образованием смешанного дисульфида и инактивирует рецептор. В результате способность тромбоцита к агрегации, вызываемой аденозиндифосфорной кислотой (АДФ), необратимо утрачивается. Использование тиенопиридиновых антиагрегантов осложняется тем, что их антиагрегантное действие в организме наступает после метаболических превращений.
Известно антиагрегантное соединение тикагрелор, который проявляет активность без метаболического превращения. Антиагрегантное действие тикагрелора обусловлено прочным, но обратимым связыванием с рецептором P2Y12 тромбоцита, в результате чего блокируется внутриклеточная сигнализация. При применении тикагрелора внутривенно существует сложность, обусловленная его низкой растворимостью в воде.
Наиболее близким к настоящему изобретению является вещество, описанное в патенте (Мурина М.А., Рощупкин Д.И., Сергиенко В.И. Вещество, необратимо угнетающее функции тромбоцитов. Патент РФ №2675630). Это вещество является структурным аналогом N-хлор-2,2-диметил-2-аминоэтансульфоновой кислоты. Оно проявляет антиагрегантную активность путем химической модификации плазматической мембраны тромбоцитов, происходящей в результате химического взаимодействия активного атома хлора хлораминовой группы с серосодержащими группами атомов в мембранных белках: тиоэфирными группами остатка метионина и сульфгидрильными группами. У вещества имеется тот недостаток, что в крови взаимодействие с тромбоцитами медленно и одновременно происходит быстрое связывание с сывороточным альбумином.
Целью настоящего изобретения является получение нового вещества, которое характеризуется высокой избирательностью реакции с компонентами тромбоцитов и необратимо угнетает активность тромбоцитов.
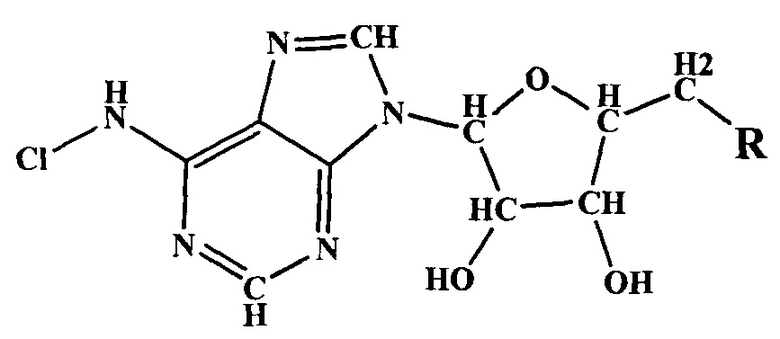
Указанная цель изобретения, во-первых, достигается тем, что синтезируют новое, неописанное ранее соединение, родственное аденозинфосфатам, которые относятся к веществам биологического происхождения, способны связываться с тромбоцитами. Общая формула заявленного соединения следующая:
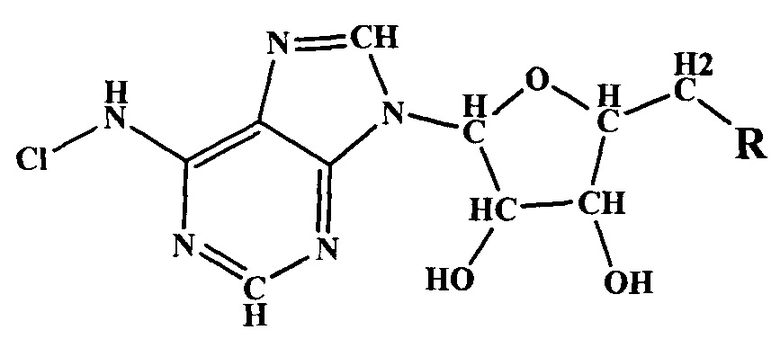
Здесь символ R означает остаток линейной олигофосфорной кислоты. Заявленное соединение синтезируют путем введения водного раствора гипохлорита натрия в водный раствор исходного вещества общей формулы
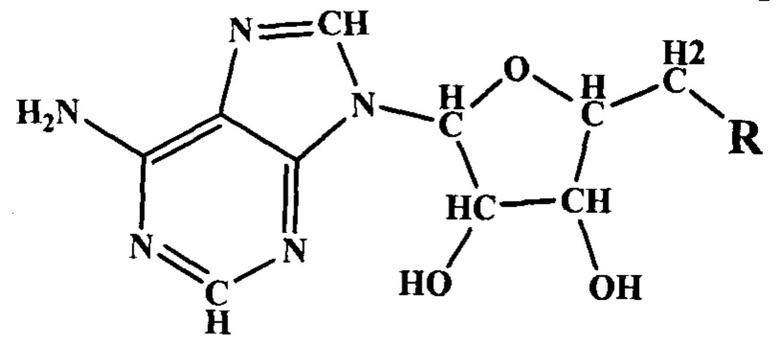
Смешивание проводят при комнатной температуре, при перемешивании, из расчета не более 1 моля активного хлора на 1 моль исходного вещества.
Примеры полученного соединения:
9-(5-трифосфорибофуранозил)-6-хлораминопурин (синоним N6-хлораденозин-5'-трифосфорная кислота) (1),
9-(5-дифосфорибофуранозил)-6-хлораминопурин (синоним N6-хлораденозин-5'-дифосфорная кислота) (2).
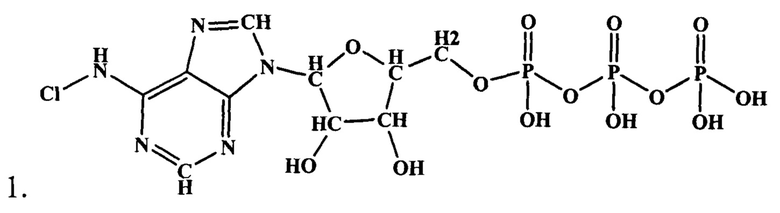
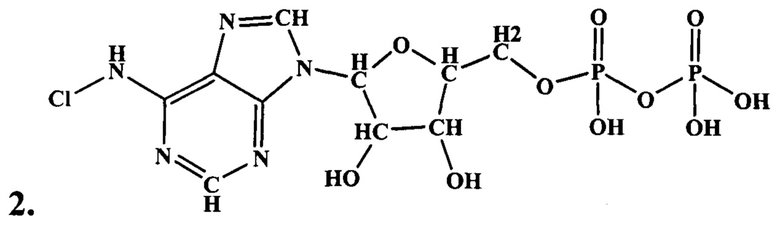
Цель изобретения также решается тем, что созданное соединение используют в качестве антиагреганта. Благодаря наличию хлораминовой атомной группы (-NHCl), в которой атом хлора способен участвовать в реакции окисления серосодержащих атомных групп белков плазматической тромбоцитной мембраны, заявленное соединение необратимо угнетает функции тромбоцитов.
На фиг. 1 дана иллюстрация оптического спектра поглощения N6-хлораденозин-5'-трифосфорной кислоты, иллюстрация оптического спектра поглощения N6-хлораденозин-5'-дифосфорной кислоты; на фиг. 2 - иллюстрация зависимости от времени оптической плотности при 285 нм N6-хлораденозин-5'-дифосфорной кислоты в смеси с восстановленным глютатионом;
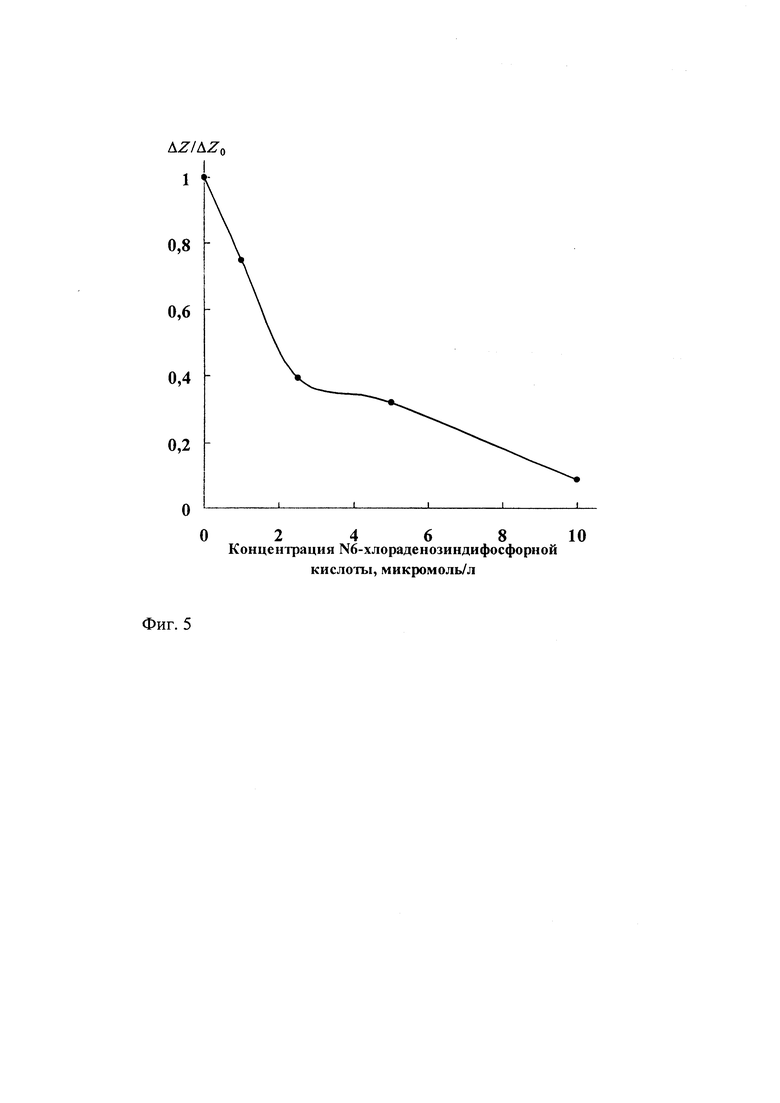
на фиг. 3 - иллюстрация зависимости от времени светопропускания богатой тромбоцитами плазмы крови с добавкой N6-хлораденозин-5'-трифосфорной кислоты и без нее; на фиг. 4 - иллюстрация уменьшения турбидиметрического показателя агрегации изолированных тромбоцитов, активированных аденозиндифосфорной кислотой, под действием N6-хлораденозин-5'-трифосфорной кислоты при разных концентрациях; фиг. 5 - иллюстрация уменьшения импедансного показателя агрегации тромбоцитов в цельной крови, активированных аденозиндифосфорной кислотой, под действием N6-хлораденозин-5'-дифосфорной кислоты при разных концентрациях.
Создание заявленного соединения, характеризующегося повышенной скоростью взаимодействия с сульфгидрильными атомными группами и обладающего способностью угнетать агрегационную функцию тромбоцитов, подтверждается следующими примерами.
Пример 1
Путем введения водного раствора гипохлорита натрия в водный раствор исходного соединения аденозин-5'-трифосфорной кислоты, либо аденозин-5'-дифосфорной кислоты получили соответственно N6-хлораденозин-5'-трифосфорную кислоту, N6-хлораденозин-5'-дифосфорную кислоту. Смешивание проводили из расчета не более 1 моля активного хлора на 1 моль исходного соединения. Измерили зависимости молярного коэффициента поглощения (ε) от длины волны (λ), т.е. оптические спектры поглощения образовавшихся соединений с использованием спектрофотометра Cary 50 Bio UV-Visible ("Varian") (фиг. 1, кривая А - спектр поглощения N6-хлораденозин-5'-трифосфорной кислоты, кривая Б - спектр поглощения N6-хлораденозин-5'-дифосфорной кислоты). В обоих спектрах имеется полоса поглощения 230-340 нм, характерная для хлораминовой группы атомов. Максимум указанной полосы поглощения располагается при 264 нм. Молярные коэффициенты поглощения в максимуме полосы поглощения N6-хлораденозин-5'-трифосфорной кислоты и N6-хлораденозин-5'-дифосфорной кислоты одинаковые, составляют 14314±376 л/(моль⋅см).
Пример 2
Получили N6-хлораденозин-5'-трифосфорную кислоту, N6-хлораденозин-5'-дифосфорную кислоту, как описано в примере 1. Смешали водные растворы N6-хлораденозин-5'-дифосфорной кислоты и восстановленного глютатиона в конечной концентрации соответственно 37 и 87 мкМ. Для указанной смеси при рН 5,4 измерили на спектрофотометре Cary 50 уменьшение во времени (t) оптической плотности при 285 нм (D285), которая прямо пропорциональна концентрации N6-хлораденозин-5'-дифосфорной кислоты (фиг. 2). Провели такие же измерения смеси цистеина и N6-хлораденозин-5'-дифосфорной кислоты, смеси других заявленных соединений и восстановленного глютатиона, либо цистеина. Во всех случаях происходило быстрое уменьшение оптической плотности вследствие бимолекулярной реакции заявленного соединения с сульфгидрильной группой атомов. Заявленное соединение также реагирует с тиоэфирной группой метионина. Для точного количественного описания скорости бимолекулярного реакции заявленного соединения с восстановленным глютатионом, цистеином и метионином определили константы скорости второго порядка по данным уменьшения оптической плотности во времени.

Заявленное соединение реагирует с сульфгидрильной группой восстановленного глютатиона и цистеина с константой скорости в несколько тысяч раз более высокой, чем с тиоэфирной группой метионина (табл.). Таким образом, заявленное соединение обладает избирательностью взаимодействия с тиольными соединениями.
Пример 3
Получили кровь человека из локтевой вены, стабилизированную 3,8% раствором цитрата натрия (9:1 по объему). Центрифугировали кровь при 460 g в течение 15 мин. Супернатант, представляющий собой богатую тромбоцитами плазму (БТП) крови, использовали для анализа агрегации тромбоцитов с помощью турбидиметрического агрегометра фирмы Chrono-Log (США). Измерили кинетическую кривую агрегации тромбоцитов, т.е. увеличение светопропускания (I) от времени (t) в контроле (фиг. 3, кривая 1). Агрегацию вызывали аденозиндифосфорной кислотой (АДФ) в конечной концентрации 3 микромоля/л (мкМ). Вертикальная стрелка на фиг. 3 показывает момент введения АДФ. Провели такие же измерения при действии N6-хлораденозин-5'-трифосфорной кислоты, ее получили, как описано в примере 1. Заявленное соединение ввели в богатую тромбоцитами плазму крови через 40 секунд после АДФ. N6-Хлораденозин-5'-трифосфорная кислота в конечной концентрации 25 и 50 мкМ (фиг. 3, соответственно кривая 2 и 3) останавливает агрегацию тромбоцитов в составе БТП и вызывает распад агрегатов. Таким образом, заявленное соединение обладает антиагрегантной активностью в тесте с богатой тромбоцитами плазмой крови.
Пример 4
Из краевой вены уха кролика получили 10 мл крови, стабилизированной 3,8% раствором цитрата натрия (9:1 по объему). Путем центрифугирования крови при 460 g в течение 15 мин получили богатую тромбоцитами плазму. К БТП добавили этилендиаминтетрауксусную кислоту в конечной концентрации 1 мМ и центрифугировали 7 мин при 1850 g. Осадок тромбоцитов суспендировали в 5 мл буферной системы (рН 7,4), содержащей 10 мМ HEPES, 134 мМ NaCl, 5 мМ KCl, 1,0 мМ MgSO4, 0,5 мМ Na2HPO4, 0,5 мМ D-глюкозы. В образец суспензии тромбоцитов для усиления агрегационной способности добавили аутологичную плазму крови в объемной конечной концентрации 2% и хлорид кальция (0,2 мМ), индуцировали агрегацию тромбоцитов введением аденозинфосфорной кислоты в конечной концентрации 10 мкМ и измерили кинетическую кривую увеличения светопропускания. Через 5 мин после введения АДФ определили величину увеличения светопропускания в контроле (ΔT0). Также определили величину увеличения светопропускания (ΔT) суспензии тромбоцитов, в которую за 3 минуты до АДФ ввели N6-хлораденозин-5'-трифосфорную кислоту. Ее получили, как описано в примере 1. Рассчитали величину отношения ΔT/ΔT0, этот турбидиметрический показатель уменьшается при наличии антиагрегационного действия заявленного соединения. N6-Хлораденозин-5'-трифосфорная кислота при конечной концентрации несколько микромоль в литре сильно угнетает агрегационную активность изолированных тромбоцитов, антиагрегационное действие заявленного соединения усиливается при повышении концентрации (фиг. 4).
Пример 5
Получили описанным в примере 4 способом кровь кролика. Разбавили ее в 2 раза физиологическим раствором и использовали для анализа агрегации тромбоцитов с помощью импедансного агрегометра фирмы Chrono-Log (США). Измерили кинетические кривые агрегации тромбоцитов, т.е. увеличения сопротивления переменному току (Z) крови от времени в контроле и при действии N6-хлораденозин-5'-дифосфорной кислоты. Заявленное соединение ввели в кровь за 3 минуты до начала стимуляции агрегации тромбоцитов, которую вызвали введением АДФ и хлорида кальция при конечной концентрации соответственно 20 мкМ и 2 мМ. Определили увеличение электрического сопротивления крови через 6 мин после начала стимуляции тромбоцитов в контрольном образце (ΔZ0) и в образце крови, содержащем заявленное соединение (ΔZ). Рассчитали величину отношения ΔZ/ΔZ0, этот импедансный показатель уменьшается при наличии антиагрегационного действия заявленного соединения. N6-Хлораденозин-5'-дифосфорная кислота, введенная в кровь в конечной концентрации 1-2 микромоль в 1 литре (фиг. 5), сильно снижает величину ΔZ/ΔZ0, указанное действие усиливается при повышении концентрации. Таким образом, заявленное соединение обладает антиагрегантной активностью в образцах крови.
| название | год | авторы | номер документа |
|---|---|---|---|
| ВЕЩЕСТВО, НЕОБРАТИМО УГНЕТАЮЩЕЕ ФУНКЦИИ ТРОМБОЦИТОВ | 2017 |
|
RU2675630C1 |
| ВЕЩЕСТВО, УГНЕТАЮЩЕЕ ФУНКЦИИ ТРОМБОЦИТОВ | 2008 |
|
RU2382764C1 |
| СОЕДИНЕНИЕ, РЕАГИРУЮЩЕЕ С ТИОЛЬНОЙ ГРУППОЙ АТОМОВ И УГНЕТАЮЩЕЕ ФУНКЦИИ ТРОМБОЦИТОВ | 2010 |
|
RU2452727C1 |
| СРЕДСТВО ДЛЯ УГНЕТЕНИЯ АКТИВНОСТИ ТРОМБОЦИТОВ | 1998 |
|
RU2161483C2 |
| Способ снижения агрегационной способности тромбоцитов | 2021 |
|
RU2751964C1 |
| СПОСОБ ОЦЕНКИ ЭФФЕКТИВНОСТИ ДЕЙСТВИЯ АНТИАГРЕГАНТНЫХ ПРЕПАРАТОВ, ВЛИЯЮЩИХ НА МЕТАБОЛИЗМ АРАХИДОНОВОЙ КИСЛОТЫ ПУТЕМ ИНГИБИРОВАНИЯ ЦИКЛООКСИГЕНАЗЫ-1 КАК В ОТДЕЛЬНОСТИ, ТАК И СОВМЕСТНО С АНТАГОНИСТОМ РЕЦЕПТОРА АДФ P2Y НА ТРОМБОЦИТАРНЫХ МЕМБРАНАХ, НА СОСТОЯНИЯ ТРОМБОЦИТОВ КРОВИ ПАЦИЕНТА, ПРИНИМАЮЩЕГО АНТИАГРЕГАНТНЫЕ ПРЕПАРАТЫ УКАЗАННОЙ ГРУППЫ | 2010 |
|
RU2442167C1 |
| СПОСОБ ЛЕЧЕНИЯ СОСТОЯНИЙ, СОПРОВОЖДАЮЩИХСЯ ГИПЕРАГРЕГАЦИЕЙ ТРОМБОЦИТОВ | 1997 |
|
RU2150943C1 |
| НИТРОЭФИР ОКИСЛЕННОГО КРАХМАЛА НАТРИЕВОЙ СОЛИ, ОБЛАДАЮЩИЙ АНТИАГРЕГАНТНЫМ ДЕЙСТВИЕМ | 1991 |
|
RU2074195C1 |
| 2-ПИПЕРИДИНО-5-(ТИЕНИЛ-2)- И 2-ПИПЕРИДИНО-5-(ТИЕНИЛ-3)-6Н-1,3,4-ТИАДИАЗИНЫ ГИДРОБРОМИДЫ, ОБЛАДАЮЩИЕ АНТИАГРЕГАНТНЫМ ДЕЙСТВИЕМ | 2010 |
|
RU2445310C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМБИНАЦИЯ, ОБЛАДАЮЩАЯ АНТИАГРЕГАНТНОЙ И ЛИПИДРЕГУЛИРУЮЩЕЙ АКТИВНОСТЯМИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2010 |
|
RU2461379C2 |


Группа изобретений относится к медицине и включает соединение формулы:
 , где R представляет собой остаток линейной олигофосфорной кислоты, а также его применение в качестве средства для угнетения агрегации тромбоцитов. Техническим результатом изобретения является получение новых антиагрегантов, обладающих способностью необратимо угнетать функции тромбоцитов. 2 н.п. ф-лы, 5 ил., 1 табл., 5 пр.
, где R представляет собой остаток линейной олигофосфорной кислоты, а также его применение в качестве средства для угнетения агрегации тромбоцитов. Техническим результатом изобретения является получение новых антиагрегантов, обладающих способностью необратимо угнетать функции тромбоцитов. 2 н.п. ф-лы, 5 ил., 1 табл., 5 пр.
1. Соединение общей формулы

где R представляет собой остаток линейной олигофосфорной кислоты.
2. Применение соединения по п. 1 в качестве средства для угнетения агрегации тромбоцитов.
| М.А | |||
| Мурина и др., Гемолитическая активность хлораминовых производных аналогов аденозина в суспензии эритроцитов | |||
| Биохимия и молекулярная биология, 2022, 1 (1), с.80-84 | |||
| M.H | |||
| Maguire et al., Powerful new aggregator of blood platelets--2-chloroadenosine-5'-diphosphate | |||
| Nature, 1968, vol.217 (5128), p.571-573 | |||
| US 4141972 A, 27.02.1979 | |||
| C | |||
| Bernofsky |
Авторы
Даты
2023-11-29—Публикация
2023-02-10—Подача