Родственные заявки
[0001] Данная заявка притязает на приоритет предварительной заявки на патент (США) № 62/737359, поданной 27 сентября 2018 года, содержимое которой полностью содержится в данном документе по ссылке.
Область техники
[0002] Это изобретение, в общем, относится к количественным анализам и методам клеточной терапии. В альтернативных вариантах осуществления, предоставляются составы, включающие в себя продукты производства, а также комплекты и способы, содержащие (либо содержащие использование) количественные анализы в пробирке для определения эффективности методов клеточной терапии или лечения, включающих в себя методы, используемые при лечении дегенерации сетчатки глаза.
Уровень техники
[0003] Дегенерация сетчатки глаза означает ухудшение или дегенерацию, вызываемую посредством прогрессирующего и необратимого отмирания и гибели фоторецепторных клеток в сетчатке глаза. Гибель фоторецепторных клеток может приводить к слепоте. Стволовые клетки и другие плюрипотентные клетки предусмотрены для использования при лечении пациентов с дегенерацией сетчатки глаза и могут изолироваться от определенного числа источников, включающих в себя эмбриональную ткань, мозг взрослого человека, генетически модифицированные дермальные фибробласты и даже сетчатку глаза. Тем не менее, тестирование этих методов клеточной терапии и лечения и, если обобщить, методов клеточной терапии и лечения, направленных на широкий спектр заболеваний, включающих в себя рак и аутоиммунные состояния, остается трудным, поскольку количественные анализы в живом организме у людей или модельных организмов являются дорогостоящими, времязатратными и зачастую не имеют количественных результатов. Таким образом, в данной области техники существует потребность в надежном, экономически эффективном, времясберегающем и количественном анализе в пробирке для определения эффективности методов клеточной терапии или лечения, включающих в себя методы, используемые при лечении дегенерации сетчатки глаза.
Сущность изобретения
[0004] Настоящее раскрытие сущности предоставляет способ для измерения эффективности клеточной терапии или лечения, при этом способ содержит этапы: инкубации первого множества клеток с токсичным химическим соединением и кондиционированной средой, при этом кондиционированная среда содержит среду, используемую для того, чтобы культивировать клеточную терапию или лечение; инкубации, по меньшей мере, второго множества клеток с токсичным химическим соединением и контрольной средой; определения жизнеспособности первого множества клеток и, по меньшей мере, второго множества клеток; и сравнения жизнеспособности первого множества клеток с жизнеспособностью второго множества клеток, за счет этого определяя эффективность клеточной терапии или лечения. Эффективность может представлять собой отношение жизнеспособности первого множества клеток к жизнеспособности второго множества клеток.
[0005] Настоящее раскрытие сущности предоставляет способ для измерения эффективности клеточной терапии или лечения, при этом способ содержит этапы: инкубации первого множества клеток с токсичным химическим соединением и кондиционированной средой, при этом кондиционированная среда содержит среду, используемую для того, чтобы культивировать клеточную терапию или лечение; инкубации, по меньшей мере, второго множества клеток с токсичным химическим соединением и контрольной средой; определения жизнеспособности первого множества клеток и, по меньшей мере, второго множества клеток; определения активности по апоптозу в первом множестве клеток и, по меньшей мере, во втором множестве клеток; определения защитного значения кратного изменения первого множества клеток, при этом защитное значение кратного изменения представляет собой отношение жизнеспособности первого множества клеток к активности по апоптозу в первом множестве клеток; определения защитного значения кратного изменения, по меньшей мере, второго множества клеток, при этом защитное значение кратного изменения представляет собой отношение жизнеспособности, по меньшей мере, второго множества клеток к активности по апоптозу, по меньшей мере, во втором множестве клеток; и определения эффективности клеточной терапии или лечения, при этом эффективность представляет собой отношение защитного значения кратного изменения первого множества клеток к защитному значению кратного изменения, по меньшей мере, второго множества клеток.
[0006] Предыдущие способы дополнительно могут содержать сравнение эффективности клеточной терапии или лечения с предварительно определенным значением отсечки, при этом если эффективность превышает предварительно определенное значение отсечки, то клеточная терапия или лечение идентифицируется как достаточно эффективная для назначения исследуемому.
[0007] Предыдущие способы дополнительно могут содержать: сравнение эффективности клеточной терапии или лечения с предварительно определенным значением отсечки; и назначение исследуемому, нуждающемуся в этом, по меньшей мере, одной терапевтически эффективной дозы клеточной терапии или лечения, когда эффективность превышает предварительно определенное значение отсечки.
[0008] Предварительно определенное значение отсечки может составлять приблизительно 2.
[0009] Клеточная терапия или лечение может содержать клетки-предшественники сетчатки глаза (RPC), пигментные эпителиальные клетки сетчатки глаза (RPE), ARPE-19-клетки, нейронные стволовые клетки-предшественники, мезенхимальные стволовые клетки, CD34+-клетки, стволовые клетки-предшественники, лейкоциты, фибробласты либо любое их сочетание. Клеточная терапия или лечение содержит RPC.
[0010] Первое множество клеток и, по меньшей мере, второе множество клеток могут содержать клетки ретинобластомы (RB), пигментные эпителиальные клетки сетчатки глаза (RPE), ARPE-19-клетки, извлеченные из клеток Мюллера клетки, MIO-M1-клетки, нейрональные клетки, глиальные клетки, фибробласты, неокулярные клетки либо любое их сочетание. Первое множество клеток и, по меньшей мере, второе множество клеток могут содержать RB-клетки. Первое множество клеток и, по меньшей мере, второе множество клеток могут содержать, по меньшей мере, приблизительно от 1000 RB-клеток, по меньшей мере, приблизительно до 250000 RB-клеток, по меньшей мере, приблизительно от 10 мкл, по меньшей мере, приблизительно до 40 мкл среды. Первое множество клеток и, по меньшей мере, второе множество клеток могут содержать, по меньшей мере, приблизительно 25000 RB-клеток, по меньшей мере, приблизительно в 25 мкл среды.
[0011] Первое множество клеток и, по меньшей мере, второе множество клеток могут инкубироваться, по меньшей мере, с приблизительно от 50 мкл, по меньшей мере, приблизительно до 100 мкл кондиционированной среды и контрольной среды, соответственно. Первое множество клеток и, по меньшей мере, второе множество клеток могут инкубироваться, по меньшей мере, с приблизительно 75 мкл кондиционированной среды и контрольной среды, соответственно.
[0012] Токсичное химическое соединение может индуцировать апоптоз. Токсичное химическое соединение может представлять собой бутират натрия. Бутират натрия может присутствовать с концентрацией приблизительно от 2 ммоль приблизительно до 32 ммоль. Бутират натрия может присутствовать с концентрацией приблизительно в 16 ммоль.
[0013] Первое множество клеток и, по меньшей мере, второе множество клеток могут инкубироваться в течение периода времени, по меньшей мере, приблизительно от 1 часа, по меньшей мере, приблизительно до 72 часов. Первое множество клеток и, по меньшей мере, второе множество клеток могут инкубироваться в течение периода времени, по меньшей мере, приблизительно в 46 часов.
[0014] Определение жизнеспособности первого множества клеток и, по меньшей мере, второго множества клеток может содержать измерение метаболической емкости первого множества клеток и, по меньшей мере, второго множества клеток. Метаболическая емкость может измеряться с использованием количественного анализа на основе люминесценции.
[0015] Количественный анализ на основе люминесценции может содержать: инкубацию первого множества клеток и, по меньшей мере, второго множества клеток с резазурином (натриевой солью в виде 7-гидрокси-3H-феноксазин-3-он 10-оксида) в течение периода, по меньшей мере, приблизительно в 1 час; и измерение люминесценции первого множества клеток и, по меньшей мере, второго множества клеток. Количественный анализ на основе люминесценции может представлять собой количественный анализ жизнеспособности клеток на основе CellTiter-Blue®. По меньшей мере, приблизительно 20 мкл разбавленного 1:4 реагента на основе CellTiter-Blue® могут добавляться в первое множество клеток и, по меньшей мере, во второе множество клеток.
[0016] Активность по апоптозу в первом множестве клеток и, по меньшей мере, во втором множестве клеток может измеряться с использованием количественного анализа на основе люминесценции. Количественный анализ на основе люминесценции может содержать: инкубацию первого множества клеток и, по меньшей мере, второго множества клеток с подложкой на основе люминогенной каспазы-3/7, по меньшей мере, в течение приблизительно 1 часа; и измерение люминесценции первого множества клеток и, по меньшей мере, второго множества клеток. Подложка на основе люминогенной каспазы-3/7 может содержать тетрапептидную последовательность DEVD, которая расщепляется посредством каспазы 3 или каспазы 7, за счет этого формируя подложку на основе люциферазы. Количественный анализ на основе люминесценции может представлять собой систему количественного анализа на основе Caspase-Glo® 3/7. По меньшей мере, приблизительно 120 мкл реагента для количественного анализа на основе Caspase-Glo® 3/7 могут добавляться в первое множество клеток и, по меньшей мере, во второе множество клеток.
[0017] Предыдущие способы дополнительно могут содержать: инкубацию, по меньшей мере, третьего множества клеток с токсичным химическим соединением и неактивной кондиционированной средой, при этом неактивная кондиционированная среда содержит среду, используемую для того, чтобы культивировать неактивную клеточную терапию или лечение; определение жизнеспособности, по меньшей мере, третьего множества клеток; определение активности по апоптозу, по меньшей мере, в третьем множестве клеток; и определение защитного значения кратного изменения, по меньшей мере, третьего множества клеток, при этом защитное значение кратного изменения представляет собой отношение жизнеспособности к активности по апоптозу; и определение эффективности неактивной клеточной терапии или лечения, при этом эффективность представляет собой отношение защитного значения кратного изменения, по меньшей мере, третьего множества клеток к защитному значению кратного изменения, по меньшей мере, второго множества клеток; и сравнение эффективности неактивной клеточной терапии или лечения с предварительно определенным значением отсечки, при этом если эффективность неактивной клеточной терапии меньше или равна предварительно определенному значению отсечки, то способ идентифицируется в качестве допустимого.
[0018] Предыдущие способы дополнительно могут содержать: инкубацию, по меньшей мере, третьего множества клеток с токсичным химическим соединением и неактивной кондиционированной средой, при этом неактивная кондиционированная среда содержит среду, используемую для того, чтобы культивировать неактивную клеточную терапию или лечение; определение жизнеспособности, по меньшей мере, третьего множества клеток; сравнение жизнеспособности третьего множества клеток с жизнеспособностью второго множества клеток, за счет этого определяя эффективность неактивной клеточной терапии или лечения; и сравнение эффективности неактивной клеточной терапии или лечения с предварительно определенным значением отсечки, при этом если эффективность неактивной клеточной терапии меньше или равна предварительно определенному значению отсечки, то способ идентифицируется в качестве допустимого.
[0019] Неактивная клеточная терапия или лечение может содержать кожные T-лимфоциты, HuT78-клетки либо любое их сочетание.
[0020] Предыдущие способы дополнительно могут содержать: инкубацию, по меньшей мере, третьего множества клеток с токсичным химическим соединением и активной кондиционированной средой, при этом активная кондиционированная среда содержит среду, используемую для того, чтобы культивировать активную клеточную терапию или лечение; определение жизнеспособности, по меньшей мере, третьего множества клеток; определение активности по апоптозу, по меньшей мере, в третьем множестве клеток; определение защитного значения кратного изменения, по меньшей мере, третьего множества клеток, при этом защитное значение кратного изменения представляет собой отношение жизнеспособности к активности по апоптозу; определение эффективности активной клеточной терапии или лечения, при этом эффективность представляет собой отношение защитного значения кратного изменения, по меньшей мере, третьего множества клеток к защитному значению кратного изменения, по меньшей мере, второго множества клеток, и сравнение эффективности активной клеточной терапии или лечения с предварительно определенным значением отсечки, при этом если эффективность активной клеточной терапии превышает предварительно определенное значение отсечки, то способ идентифицируется в качестве допустимого.
[0021] Предыдущие способы дополнительно могут содержать: инкубацию, по меньшей мере, третьего множества клеток с токсичным химическим соединением и активной кондиционированной средой, при этом активная кондиционированная среда содержит среду, используемую для того, чтобы культивировать активную клеточную терапию или лечение; определение жизнеспособности, по меньшей мере, третьего множества клеток; сравнение жизнеспособности третьего множества клеток с жизнеспособностью второго множества клеток, за счет этого определяя эффективность активной клеточной терапии или лечения; и сравнение эффективности активной клеточной терапии или лечения с предварительно определенным значением отсечки, при этом если эффективность активной клеточной терапии превышает предварительно определенное значение отсечки, то способ идентифицируется в качестве допустимого.
[0022] Активная клеточная терапия может содержать пигментные эпителиальные клетки сетчатки глаза (RPE), ARPE-19-клетки, фибробласты, CCD-1112Sk-клетки либо любое их сочетание.
[0023] Контрольная среда может содержать стандартную среду. Клеточная терапия или лечение служит для лечения заболевания или состояния сетчатки глаза.
[0024] Предоставляются способы для измерения эффективности или эффективности клеточной терапии или лечения, причем способы содержат этапы: 1) инкубации первого множества клеток с возможным вариантом химического соединения и клеточной терапией или лечением; 2) инкубации второго множества клеток с возможным вариантом химического соединения; 3) определения жизнеспособности и/или метаболической активности первого множества клеток; 4) определения жизнеспособности и/или метаболической активности второго множества клеток; и 5) сравнения жизнеспособности и/или метаболической активности первого множества клеток с жизнеспособностью и/или метаболической активностью второго множества клеток, за счет этого определяя эффективность лечения. В некоторых аспектах, первое множество клеток является практически идентичным второму множеству клеток.
[0025] Первое множество клеток и второе множество клеток могут содержать идентичный тип клеток. В качестве неограничивающего примера, тип клеток может представлять собой клетки ретинобластомы человека.
[0026] Первое множество клеток и второе множество клеток могут содержать приблизительно от 1000 приблизительно до 250000 клеток (например, приблизительно 1000; 25000; 50000; 75000; 100000; 125000; 150000; 175000; 200000; 225000; или 250000). В некоторых неограничивающих примерах, первое множество клеток и второе множество клеток могут содержать приблизительно 25000 клеток.
[0027] Клеточная терапия или лечение может содержать кондиционированную среду. Кондиционированная среда может формироваться посредством сбора среды, используемой для того, чтобы культивировать третье множество клеток. Третье множество клеток может содержать клетки-предшественники сетчатки глаза млекопитающих. Клетки-предшественники сетчатки глаза млекопитающих могут представлять собой клетки-предшественники сетчатки глаза человека. Третье множество клеток может содержать от 0,1×106 до 1×107 клеток-предшественников сетчатки глаза человека (например, 0,1×106, 0,2×106, 0,3×106, 0,4×106, 0,5×106, 0,6×106, 0,7×106, 0,8×106, 0,9×106, 1×106, 2×106, 3×106, 4×106, 5×106, 6×106, 7×106, 8×106, 9×106 или 1×107 клеток). В некоторых неограничивающих примерах, третье множество клеток может содержать приблизительно 9×106 клеток-предшественников сетчатки глаза человека.
[0028] В других вариантах осуществления, третье множество клеток содержит пигментные эпителиальные клетки сетчатки глаза человека (hRPE) (см., например, фиг. 8).
[0029] При использовании в данном документе, термин "возможный вариант химического соединения" может означать токсичное химическое соединение, полутоксичное химическое соединение и т.п. В качестве неограничивающего примера, токсичное химическое соединение может индуцировать апоптоз. Токсичное химическое соединение может представлять собой бутират натрия. Бутират натрия может присутствовать в количестве приблизительно от 0 ммоль приблизительно до 26 ммоль (например, приблизительно 0, 0,1, 0,2, 0,3, 0,4, 0,5, 0,6, 0,7, 0,8, 0,9, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25 или 26 ммоль). В некоторых неограничивающих примерах, бутират натрия может присутствовать в количестве приблизительно 8 ммоль.
[0030] Первое множество клеток и второе множество клеток могут инкубироваться в течение периода, по меньшей мере, в 1 час или, по меньшей мере, в 12 часов, или, по меньшей мере, в 24 часа, или, по меньшей мере, в 48 часов, или, по меньшей мере, в 72 или более часов. Первое множество клеток и второе множество клеток могут инкубироваться приблизительно в течение 2 часов.
[0031] Определение жизнеспособности первого множества и второго множества клеток может содержать измерение метаболической емкости первого множества клеток и второго множества клеток. Метаболическая емкость первого множества клеток и второго множества клеток может измеряться с использованием количественного анализа на основе люминесценции.
[0032] Количественный анализ на основе люминесценции может содержать: 1) инкубацию первого множества клеток и второго множества клеток с резазурином (натриевой солью в виде 7-гидрокси-3H-феноксазин-3-он 10-оксида) в течение периода, по меньшей мере, в 1 час; 2) измерение люминесценции первого множества клеток и второго множества клеток; и 3) сравнение измеренной люминесценции, за счет этого определяя жизнеспособность первого множества клеток и второго множества клеток.
[0033] Любой из вышеприведенных аспектов может комбинироваться с любым другим аспектом.
[0034] Подробности одного или более примерных вариантов осуществления изобретения изложены на прилагаемых чертежах и в нижеследующем описании. Другие признаки, цели и преимущества изобретения должны становиться очевидными из описания и чертежей, а также из формулы изобретения.
[0035] Все публикации, патенты, заявки на патент, процитированные в данном документе, настоящим явно содержатся по ссылке для всех целей.
Краткое описание чертежей
[0036] Вышеприведенные и дополнительные признаки должны становиться очевидными из нижеприведенного подробного описания при рассмотрении вместе с прилагаемыми чертежами.
[0037] Фиг. 1 иллюстрирует последовательность диаграмм, показывающих результаты количественного анализа жизнеспособности клеток на основе люминесценции, используемого в способах настоящего раскрытия сущности.
[0038] Фиг. 2 графически иллюстрирует последовательность гистограмм, показывающих эффективность кондиционированной среды для клеток-предшественников сетчатки глаза человека (hRPC CM) при различных концентрациях бутирата натрия, измеренную с использованием способов настоящего раскрытия сущности. Синий или первый столбик в каждой группе соответствует клеткам, инкубированным в стандартной среде (SM), и оранжевый или второй столбик в каждой группе соответствует клеткам, инкубированным в hRPC CM.
[0039] Фиг. 3 графически иллюстрирует последовательность гистограмм, показывающих эффективность hRPC CM при различных концентрациях бутирата натрия, измеренную с использованием способов настоящего раскрытия сущности. Синий или первый столбик в каждой группе соответствует клеткам, инкубированным в SM, и оранжевый или второй столбик в каждой группе соответствует клеткам, инкубированным в hRPC CM.
[0040] Фиг. 4 графически иллюстрирует гистограмму, показывающую эффективность различных разбавлений hRPC CM, измеренную с использованием способов настоящего раскрытия сущности. Голубой или первый столбик в каждой группе соответствует клеткам, инкубированным в SM. Серый или второй столбик в каждой группе соответствует клеткам, инкубированным в hRPC CM без разбавления. Желтый или третий столбик в каждой группе соответствует клеткам, инкубированным в hRPC CM, разбавленной с коэффициентом 2. Темно-синий или четвертый столбик в каждой группе соответствует клеткам, инкубированным в hRPC CM, разбавленной с коэффициентом 4. Зеленый или пятый столбик в каждой группе соответствует клеткам, инкубированным в hRPC CM, разбавленной с коэффициентом 8.
[0041] Фиг. 5 графически иллюстрирует гистограмму, показывающую эффективность hRPC CM, сформированной с использованием различных количеств клеток-предшественников сетчатки глаза человека (hRPC), измеренную с использованием способов настоящего раскрытия сущности. Голубой или первый столбик в каждой группе соответствует клеткам, инкубированным в SM. Оранжевый или второй столбик в каждой группе соответствует клеткам, инкубированным в hRPC CM, сформированной с использованием 9,0×106 hRPC. Серый или третий столбик в каждой группе соответствует клеткам, инкубированным в hRPC CM, сформированной с использованием 6,0×106 hRPC.
[0042] Фиг. 6 графически иллюстрирует последовательность гистограмм, показывающих эффективность hRPC CM, сформированной из различных популяций hRPC, измеренную с использованием способов настоящего раскрытия сущности. В левой панели, голубой или первый столбик в каждой группе соответствует клеткам, инкубированным с SM; оранжевый или второй столбик представляет собой клетки, инкубированные с hRPC CM, сформированной из hRPC из партии G1; серый или третий столбик соответствует клеткам, инкубированным с hRPC CM, сформированной из hRPC из партии G2; желтый или четвертый столбик в каждой группе соответствует клеткам, инкубированным с hRPC CM, сформированной с использованием hRPC из партии G3; и темно-синий или пятый столбик в каждой группе соответствует клеткам, инкубированным с hRPC CM, сформированной с использованием hRPC из партии G5. В правой панели, голубой или первый столбик в каждой группе соответствует клеткам, инкубированным с SM; оранжевый или второй столбик представляет собой клетки, инкубированные с hRPC CM, сформированной из hRPC из партии G1; серый или третий столбик соответствует клеткам, инкубированным с hRPC CM, сформированной из hRPC из партии G2; желтый или четвертый столбик в каждой группе соответствует клеткам, инкубированным с hRPC CM, сформированной с использованием hRPC из партии G3; и темно-синий или пятый столбик в каждой группе соответствует клеткам, инкубированным с hRPC CM, сформированной с использованием hRPC из партии G5.
[0043] Фиг. 7 графически иллюстрирует гистограмму, показывающую эффективность hRPC CM, сформированной из различных популяций hRPC, измеренную с использованием способов настоящего раскрытия сущности. Голубой или первый столбик в каждой группе соответствует клеткам, инкубированным с SM; оранжевый или второй столбик представляет собой клетки, инкубированные с hRPC CM, сформированной из hRPC из партии G1; серый или третий столбик соответствует клеткам, инкубированным с hRPC CM, сформированной из hRPC из партии G2; желтый или четвертый столбик в каждой группе соответствует клеткам, инкубированным с hRPC CM, сформированной с использованием hRPC из партии G3; темно-синий или пятый столбик в каждой группе соответствует клеткам, инкубированным с hRPC CM, сформированной с использованием hRPC из партии G4; зеленый или шестой столбик в каждой группе соответствует клеткам, инкубированным с hRPC CM, сформированной с использованием hRPC из партии G5; светло-синий или седьмой столбик в каждой группе соответствует клеткам, инкубированным с hRPC CM, сформированной с использованием hRPC из партии L-SB; и розовый или восьмой столбик в каждой группе соответствует клеткам, инкубированным с hRPC CM, сформированной с использованием hRPC из партии L-PB.
[0044] Фиг. 8 графически иллюстрирует последовательность гистограмм, показывающих эффективность кондиционированной среды, сформированной с использованием различных типов клеток, измеренную с использованием способов настоящего раскрытия сущности. В левой панели, синий или первый столбик в каждой группе соответствует клеткам, инкубированным в SM; оранжевый или второй столбик в каждой группе соответствует клеткам, инкубированным в hRPC CM; и желтый или третий столбик в каждой группе соответствует клеткам, инкубированным в кондиционированной среде, сформированной с использованием клеток ретинобластомы человека. В правой панели, голубой или первый столбик в каждой группе соответствует клеткам, инкубированным в SM, и зеленый или второй столбик в каждой группе соответствует клеткам, инкубированным в кондиционированной среде, сформированной с использованием пигментных эпителиальных клеток сетчатки глаза человека.
[0045] Фиг. 9 показывает данные экспрессии генов для выбранных цитокинов, выбранных в качестве возможных вариантов нейротрофических факторов для hRPC. Данные получены через qPCR, из нескольких типов клеток, включающих в себя (слева направо) hRPC, hRB, hRPE и hFB. Типы клеток сетчатки глаза группируются отдельно от фибробластов. HRB-линия извлечена из опухоли, все остальные типы клеток - из фетальной ткани. Экспрессия предположительного трофического фактора OPN может считаться наибольшей для hRPC.
[0046] Фиг. 10 графически иллюстрирует последовательность графиков, показывающих результаты из количественного анализа для определения мультиплексированной эффективности настоящего раскрытия сущности. Левая верхняя панель показывает измеренную жизнеспособность клеток. Правая верхняя панель показывает измеренную апоптотическую активность. Нижняя панель показывает вычисленные значения эффективности с использованием данных, показанных в двух верхних панелях.
[0047] Фиг. 11 графически иллюстрирует результаты количественного анализа для определения мультиплексированной эффективности настоящего раскрытия сущности с тестированием нефильтрованной и фильтрованной кондиционированной среды.
[0048] Фиг. 12 графически иллюстрирует результаты количественного анализа для определения мультиплексированной эффективности настоящего раскрытия сущности с тестированием кондиционированной среды с отрицательным управлением и кондиционированной среды с положительным управлением.
[0049] Фиг. 13 графически иллюстрирует результаты количественного анализа для определения мультиплексированной эффективности настоящего раскрытия сущности с тестированием кондиционированной среды, извлекаемой из различных партий hRPC.
[0050] Фиг. 14 графически иллюстрирует результаты количественного анализа для определения мультиплексированной эффективности настоящего раскрытия сущности с тестированием кондиционированной среды, извлекаемой из hRPC-культур с различными плотностями посева.
[0051] Фиг. 15 графически иллюстрирует результаты количественного анализа для определения мультиплексированной эффективности настоящего раскрытия сущности с тестированием различных разбавлений кондиционированной среды, указывающие то, что количественный анализ для определения мультиплексированной эффективности проявляет линейность отклика.
Подробное описание изобретения
[0052] Наиболее распространенный тип наследственного заболевания (дистрофии) сетчатки глаза представляет собой пигментный ретинит (RP), и наиболее распространенное дегенеративное заболевание представляет собой возрастную макулярную дегенерацию (AMD). Потенциальные методы терапии включают в себя использование клеток-предшественников сетчатки глаза человека (hRPC) при лечении RP и использование продуктов с использованием извлеченных из стволовых клеток пигментных эпителиальных (RPE) клеток человека при лечении AMD. Тесты hRPC при лечении RP указывают то, что лечение основывается на нейротрофическом эффекте, который с большой вероятностью должен получаться в результате коктейля из нескольких цитокинов. Роль этих цитокинов только частично очерчена в настоящее время. Поскольку эффективность изготовленного продукта с использованием hRPC-клеток предположительно должна варьироваться в зависимости от партии, должно быть полезным иметь простой и удобный количественный анализ в пробирке для определения эффективности, допускающий перспективное измерение трофической эффективности данной партии изготовленного продукта с использованием hRPC-клеток до использования на пациентах, без необходимости тестирования в живом организме и соответствующих требований по инфраструктуре и персоналу.
[0053] Современный способ оценки эффективности hRPC-лечения представляет собой тестирование в живом организме на крысах Королевского хирургического колледжа (RCS), которое представляет собой точно охарактеризованную модель аутосомно-рецессивного RP. Чтобы выполнять эти тесты, требуется виварий с RCS-колонией, наряду с хирургическим блоком, электрофизиологическим блоком и лабораторией окулярной гистологии, причем все из означенного должно быть укомплектовано ассоциированным персоналом со специализированными экспертными знаниями в этих предметных областях. Таким образом, современный способ тестирования в живом организме является громоздким, требующим высокой квалификации, трудоемким, времяемким и ресурсоемким.
[0054] Нейротрофический эффект hRPC-лечения затрудняет выдачу итогов в системе в пробирке. Например, трофический эффект лечения, наблюдаемый в живом организме, кажется, возникает на уровне фоторецепторов, которые представляют собой клетки, которые сложно поддерживать в пробирке. В одном аспекте, способы настоящего раскрытия сущности предоставляют средство измерения эффективности изготовленного продукта с использованием hRPC-клеток, без необходимости тестирования на животных и до использования на людях. Способы настоящего раскрытия сущности могут требовать только использования установок для культивирования клеток, умеренного массива оборудования, плюс трудозатрат специалиста в данной области техники в течение одного дня. Также требуются легкодоступная бессмертная клеточная линия или опухолевая клеточная линия человека и определенное число других легкодоступных реагентов. Тестируемое изделие представляет собой небольшую пробу сред для культивирования клеток, заблаговременно взятую из живой культуры специфического типа терапевтических клеток. Следует отметить, что тестовая установка не должна решать проблемы, связанные с обработкой типа болезненных клеток. Таким образом, способы настоящего раскрытия сущности, по сравнению с существующими количественными анализами в живом организме, являются недорогими, требуют минимальных трудозатрат и являются времясберегающими. Способы настоящего раскрытия сущности сокращают то, что ранее представляло собой многомесячный процесс в живом организме, требующий специализированной команды, до процесса в пробирке, выполняемого одним специалистом за один день.
[0055] Настоящее раскрытие сущности предоставляет способы, которые измеряют эффективность клеточной терапии или лечения. Способы предоставляют количественный анализ в пробирке для определения эффективности, который может использоваться для того, чтобы определять то, насколько эффективно клеточная терапия или лечение увеличивает жизнеспособность популяции клеток. Таким образом, количественный анализ предоставляет способ количественного определения эффективности трофического эффекта клеточной терапии или лечения. В одном аспекте, способы настоящего раскрытия сущности используют токсичное химическое соединение для того, чтобы предоставлять метаболический инсульт в популяцию клеток, чтобы лучше обнаруживать эффективность трофического эффекта клеточной терапии или лечения. В одном неограничивающем примере, способы настоящего раскрытия сущности могут использоваться для того, чтобы тестировать эффективность трофического эффекта донорных фетальных клеток сетчатки глаза (клеток-предшественников сетчатки глаза) для сетчатки-хозяина глаза, в частности, включающей в себя колбочки-хозяев. Донорные фетальные клетки сетчатки глаза показаны как имеющие трофический эффект, который не только является нейропротекторным, но также и имеет быстрый оживляющий эффект для остаточных клеток-хозяев сетчатки глаза, определенный посредством улучшенной зрительной функции. Донорные клетки допускают интеграцию в сетчатку глаза и, через клеточную дифференцировку, заменяют фоторецепторы (которые могут иметься в ограниченных количествах). Общий эффект заключается в том, чтобы быстро и устойчиво восстанавливать и сохранять клинически существенные степени зрительной функции в сетчатке глаза, в иных случаях обреченной на полный отказ, оставляя пациента абсолютно слепым.
[0056] Настоящее раскрытие сущности предоставляет способ в пробирке для измерения эффективности клеточной терапии или лечения, при этом способ содержит этапы: инкубации первого множества клеток с токсичным химическим соединением и клеточной терапией или лечением; инкубации второго множества клеток с токсичным химическим соединением; определения жизнеспособности первого множества клеток; определения жизнеспособности второго множества клеток; и сравнения жизнеспособности первого множества клеток с жизнеспособностью второго множества клеток, за счет этого определяя эффективность лечения.
[0057] Настоящее раскрытие сущности также предоставляет способ для измерения эффективности клеточной терапии или лечения, при этом способ содержит этапы: инкубации первого множества клеток с токсичным химическим соединением и кондиционированной средой, при этом кондиционированная среда содержит среду, используемую для того, чтобы культивировать клеточную терапию или лечение; инкубации, по меньшей мере, второго множества клеток с токсичным химическим соединением и контрольной средой; определения жизнеспособности первого множества клеток и, по меньшей мере, второго множества клеток; сравнения жизнеспособности первого множества клеток с жизнеспособностью второго множества клеток, за счет этого определяя эффективность клеточной терапии или лечения.
[0058] В некоторых аспектах предыдущих способов, при этом эффективность представляет собой отношение жизнеспособности первого множества клеток к жизнеспособности второго множества клеток.
[0059] В некоторых аспектах, предыдущие способы дополнительно могут содержать инкубацию, по меньшей мере, третьего множества клеток с токсичным химическим соединением и неактивной кондиционированной средой, при этом неактивная кондиционированная среда содержит среду, используемую для того, чтобы культивировать неактивную клеточную терапию или лечение; определение жизнеспособности, по меньшей мере, третьего множества клеток; сравнение жизнеспособности третьего множества клеток с жизнеспособностью второго множества клеток, за счет этого определяя эффективность неактивной клеточной терапии или лечения, сравнение эффективности неактивной клеточной терапии или лечения с предварительно определенным значением отсечки, при этом если эффективность неактивной клеточной терапии меньше или равна предварительно определенному значению отсечки, то способ идентифицируется в качестве допустимого. Если не ограничиваться рамками теории, неактивная кондиционированная среда, которая содержит среду, используемую для того, чтобы культивировать неактивную клеточную терапию или лечение, представляет собой кондиционированную среду, которая заведомо считается неактивной, не должна защищать третье множество клеток от вредных эффектов токсичного химического соединения (например, бутирата натрия) и в силу этого не должна иметь значение эффективности выше определенного предварительно определенного значения. Таким образом, неактивная кондиционированная среда служит в качестве отрицательного управления: если результаты конкретного количественного анализа указывают то, что неактивная кондиционированная среда практически не имеет эффективности, результаты количественного анализа могут считаться более точными. Тем не менее, если результаты конкретного количественного анализа указывают то, что неактивная кондиционированная среда имеет эффективность, то результаты количественного анализа могут нарушаться и не отражать фактическую эффективность тестированных методов клеточного лечения или терапии. Неактивная клеточная терапия или лечение может содержать кожные T-лимфоциты, HuT78-клетки либо любое их сочетание.
[0060] В некоторых аспектах, предыдущие способы дополнительно могут содержать инкубацию, по меньшей мере, третьего множества клеток с токсичным химическим соединением и активной кондиционированной средой, при этом активная кондиционированная среда содержит среду, используемую для того, чтобы культивировать активную клеточную терапию или лечение; определение жизнеспособности, по меньшей мере, третьего множества клеток; сравнение жизнеспособности третьего множества клеток с жизнеспособностью второго множества клеток, за счет этого определяя эффективность активной клеточной терапии или лечения, сравнение эффективности активной клеточной терапии или лечения с предварительно определенным значением отсечки, при этом если эффективность активной клеточной терапии превышает предварительно определенное значение отсечки, то способ идентифицируется в качестве допустимого. Если не ограничиваться рамками теории, активная кондиционированная среда, которая содержит среду, используемую для того, чтобы культивировать активную клеточную терапию или лечение, представляет собой кондиционированную среду, которая заведомо считается активной, должна защищать третье множество клеток от вредных эффектов токсичного химического соединения (например, бутирата натрия) и в силу этого должна иметь значение эффективности выше определенного предварительно определенного значения. Таким образом, активная кондиционированная среда служит в качестве положительного управления: если результаты конкретного количественного анализа указывают то, что активная кондиционированная среда практически не имеет эффективности, то результаты количественного анализа могут нарушаться и не отражать фактическую эффективность тестированных методов клеточного лечения или терапии. Тем не менее, если результаты конкретного количественного анализа указывают то, что активная кондиционированная среда имеет эффективность, то результаты могут считаться более точными. Активная клеточная терапия или лечение может содержать пигментные эпителиальные клетки сетчатки глаза (RPE), ARPE-19-клетки, фибробласты, CCD-1112Sk-клетки либо любое их сочетание.
[0061] Настоящее раскрытие сущности также предоставляет способ для измерения эффективности клеточной терапии или лечения, при этом способ содержит этапы: инкубации первого множества клеток с токсичным химическим соединением и клеточной терапией или лечением; инкубации, по меньшей мере, второго множества клеток с токсичным химическим соединением и контрольной средой; определения жизнеспособности первого множества клеток и, по меньшей мере, второго множества клеток; определения активности по апоптозу в первом множестве клеток и, по меньшей мере, во втором множестве клеток; и определения защитного значения кратного изменения первого множества клеток, при этом защитное значение кратного изменения представляет собой отношение жизнеспособности первого множества клеток к активности по апоптозу в первом множестве клеток; определения защитного значения кратного изменения, по меньшей мере, второго множества клеток, при этом защитное значение кратного изменения представляет собой отношение жизнеспособности, по меньшей мере, второго множества клеток к активности по апоптозу, по меньшей мере, во втором множестве клеток; и определения эффективности клеточной терапии или лечения, при этом эффективность представляет собой отношение защитного значения кратного изменения первого множества клеток к защитному значению кратного изменения, по меньшей мере, второго множества клеток. При использовании в данном документе, этот способ упоминается как "количественный анализ для определения мультиплексированной эффективности".
[0062] Настоящее раскрытие сущности также предоставляет способ для измерения эффективности клеточной терапии или лечения, при этом способ содержит этапы: инкубации первого множества клеток с токсичным химическим соединением и кондиционированной средой, при этом кондиционированная среда содержит среду, используемую для того, чтобы культивировать клеточную терапию или лечение; инкубации, по меньшей мере, второго множества клеток с токсичным химическим соединением и контрольной средой; определения жизнеспособности первого множества клеток и, по меньшей мере, второго множества клеток; определения активности по апоптозу в первом множестве клеток и, по меньшей мере, во втором множестве клеток; и определения защитного значения кратного изменения первого множества клеток, при этом защитное значение кратного изменения представляет собой отношение жизнеспособности первого множества клеток к активности по апоптозу в первом множестве клеток; определения защитного значения кратного изменения, по меньшей мере, второго множества клеток, при этом защитное значение кратного изменения представляет собой отношение жизнеспособности, по меньшей мере, второго множества клеток к активности по апоптозу, по меньшей мере, во втором множестве клеток; и определения эффективности клеточной терапии или лечения, при этом эффективность представляет собой отношение защитного значения кратного изменения первого множества клеток к защитному значению кратного изменения, по меньшей мере, второго множества клеток. При использовании в данном документе, этот способ также упоминается как "количественный анализ для определения мультиплексированной эффективности".
[0063] Предыдущие способы дополнительно могут содержать сравнение эффективности клеточной терапии или лечения с предварительно определенным значением отсечки, при этом если эффективность превышает предварительно определенное значение отсечки, то клеточная терапия или лечение идентифицируется как достаточно эффективная для назначения исследуемому.
[0064] Предыдущие способы дополнительно могут содержать сравнение эффективности клеточной терапии или лечения с предварительно определенным значением отсечки; и назначение исследуемому, нуждающемуся в этом, по меньшей мере, одной терапевтически эффективной дозы клеточной терапии или лечения, когда эффективность превышает предварительно определенное значение отсечки.
[0065] Предыдущие способы дополнительно могут содержать инкубацию, по меньшей мере, третьего множества клеток с токсичным химическим соединением и неактивной кондиционированной средой, при этом неактивная кондиционированная среда содержит среду, используемую для того, чтобы культивировать неактивную клеточную терапию или лечение; определение жизнеспособности, по меньшей мере, третьего множества клеток; определение активности по апоптозу, по меньшей мере, в третьем множестве клеток; и определение защитного значения кратного изменения, по меньшей мере, третьего множества клеток, при этом защитное значение кратного изменения представляет собой отношение жизнеспособности к активности по апоптозу; и определение эффективности неактивной клеточной терапии или лечения, при этом эффективность представляет собой отношение защитного значения кратного изменения, по меньшей мере, третьего множества клеток к защитному значению кратного изменения, по меньшей мере, второго множества клеток; сравнение эффективности неактивной клеточной терапии или лечения с предварительно определенным значением отсечки, при этом если эффективность неактивной клеточной терапии меньше или равна предварительно определенному значению отсечки, то способ идентифицируется в качестве допустимого. Если не ограничиваться рамками теории, неактивная кондиционированная среда, которая содержит среду, используемую для того, чтобы культивировать неактивную клеточную терапию или лечение, представляет собой кондиционированную среду, которая заведомо считается неактивной, не должна защищать третье множество клеток от вредных эффектов токсичного химического соединения (например, бутирата натрия) и в силу этого не должна иметь значение эффективности выше определенного предварительно определенного значения. Таким образом, неактивная кондиционированная среда служит в качестве отрицательного управления: если результаты конкретного количественного анализа указывают то, что неактивная кондиционированная среда практически не имеет эффективности, результаты количественного анализа могут считаться более точными. Тем не менее, если результаты конкретного количественного анализа указывают то, что неактивная кондиционированная среда имеет эффективность, то результаты количественного анализа могут нарушаться и не отражать фактическую эффективность тестированных методов клеточного лечения или терапии. Неактивная клеточная терапия или лечение может содержать кожные T-лимфоциты, HuT78-клетки либо любое их сочетание.
[0066] В некоторых аспектах, предыдущие способы могут содержать инкубацию, по меньшей мере, третьего множества клеток с токсичным химическим соединением и активной кондиционированной средой, при этом активная кондиционированная среда содержит среду, используемую для того, чтобы культивировать активную клеточную терапию или лечение; определение жизнеспособности, по меньшей мере, третьего множества клеток; определение активности по апоптозу, по меньшей мере, в третьем множестве клеток; определение защитного значения кратного изменения, по меньшей мере, третьего множества клеток, при этом защитное значение кратного изменения представляет собой отношение жизнеспособности к активности по апоптозу; определение эффективности активной клеточной терапии или лечения, при этом эффективность представляет собой отношение защитного значения кратного изменения, по меньшей мере, третьего множества клеток к защитному значению кратного изменения, по меньшей мере, второго множества клеток; и сравнение эффективности активной клеточной терапии или лечения с предварительно определенным значением отсечки, при этом если эффективность активной клеточной терапии превышает предварительно определенное значение отсечки, то способ идентифицируется в качестве допустимого. Если не ограничиваться рамками теории, активная кондиционированная среда, которая содержит среду, используемую для того, чтобы культивировать активную клеточную терапию или лечение, представляет собой кондиционированную среду, которая заведомо считается активной, должна защищать третье множество клеток от вредных эффектов токсичного химического соединения (например, бутирата натрия) и в силу этого должна иметь значение эффективности выше определенного предварительно определенного значения. Таким образом, активная кондиционированная среда служит в качестве положительного управления: если результаты конкретного количественного анализа указывают то, что активная кондиционированная среда практически не имеет эффективности, то результаты количественного анализа могут нарушаться и не отражать фактическую эффективность тестированных методов клеточного лечения или терапии. Тем не менее, если результаты конкретного количественного анализа указывают то, что активная кондиционированная среда имеет эффективность, то результаты могут считаться более точными. Активная клеточная терапия или лечение может содержать пигментные эпителиальные клетки сетчатки глаза (RPE), ARPE-19-клетки, фибробласты, CCD-1112Sk-клетки либо любое их сочетание.
[0067] В некоторых аспектах, предварительно определенное значение отсечки может составлять приблизительно 0,5 или приблизительно 1,0, или приблизительно 1,5, или приблизительно 2,0, или приблизительно 3,0, или приблизительно 3,5, или приблизительно 4,0, или приблизительно 4,5, или приблизительно 5,0, или приблизительно 5,5, или приблизительно 6,0, или приблизительно 6,5, или приблизительно 7,0, или приблизительно 7,5, или приблизительно 8,0, или приблизительно 8,5, или приблизительно 9,0, или приблизительно 9,5, или приблизительно 10, или приблизительно 15, или приблизительно 20, или приблизительно 25, или приблизительно 30, или приблизительно 35, или приблизительно 40, или приблизительно 45, или приблизительно 50, или приблизительно 60, или приблизительно 70, или приблизительно 80, или приблизительно 90, или приблизительно 100.
[0068] В некоторых аспектах способов настоящего раскрытия сущности, клеточная терапия или лечение содержит кондиционированную среду. "Кондиционированная среда" означает среду, которая изменяется по сравнению со стандартной, основной или базальной средой. Кондиционирование среды может приводить к тому, что молекулы, такие как питательные вещества и/или факторы роста, добавляются или истощаются относительно начальных уровней, содержащихся в основной среде. В некоторых аспектах, среда кондиционируется посредством предоставления возможности клеткам определенных типов выращиваться или поддерживаться в среде при определенных условиях в течение определенного периода времени. В некоторых аспектах настоящего раскрытия сущности, кондиционированная среда формируется посредством сбора среды, используемой для того, чтобы культивировать третье множество клеток. В неограничивающем примере, третье множество клеток может содержать клетки-предшественники сетчатки глаза (RPC) млекопитающих, клетки-предшественники сетчатки глаза человека (hRPC), пигментные эпителиальные клетки сетчатки глаза (RPE) млекопитающих, пигментные эпителиальные клетки сетчатки глаза человека (hRPE), ARPE-19-клетки, нейронные стволовые клетки-предшественники, мезенхимальные стволовые клетки, CD34+-клетки, стволовые клетки-предшественники, лейкоциты, фибробласты либо любое их сочетание. Клетки-предшественники сетчатки глаза млекопитающих могут представлять собой клетки-предшественники сетчатки глаза человека (hRPC). Третье множество клеток может содержать hRPC. В некоторых аспектах, среда может кондиционироваться посредством предоставления возможности клеткам-предшественникам сетчатки глаза размножаться, дифференцироваться или поддерживаться в среде с заданным составом при заданной температуре в течение заданного числа часов. Специалисты в данной области техники должны принимать во внимание, что множество комбинаций клеток, типов среды, длительностей и условий окружающей среды могут использоваться для того, чтобы формировать почти бесконечный массив кондиционированной среды.
[0069] В некоторых аспектах способов, предоставляемых в данном документе, кондиционированная среда может формироваться посредством сбора среды, используемой для того, чтобы культивировать, размножать, дифференцировать или поддерживать третье множество клеток, содержащих между 1×106 и 1×107 клеток-предшественников сетчатки глаза человека. В других аспектах, третье множество клеток может содержать приблизительно 9×106 клеток-предшественников сетчатки глаза человека. В некоторых аспектах, третье множество клеток может содержать приблизительно 8×106 клеток-предшественников сетчатки глаза человека. В некоторых аспектах, третье множество клеток может содержать приблизительно 6×106 клеток-предшественников сетчатки глаза человека. В некоторых аспектах, третье множество клеток может содержать приблизительно 4×106 клеток-предшественников сетчатки глаза человека. Способы культивирования и формирования кондиционированной среды из клеток-предшественников сетчатки глаза человека описываются в WO 2012/158910, которая полностью содержится в данном документе по ссылке. В некоторых аспектах, кондиционированная среда может формироваться посредством сбора среды, используемой для того, чтобы культивировать, размножать, дифференцировать или поддерживать третье множество клеток, которые посеяны с плотностью, по меньшей мере, приблизительно 1×106 клеток или, по меньшей мере, приблизительно 2×106 клеток, или, по меньшей мере, приблизительно 3×106 клеток, или, по меньшей мере, приблизительно 4×106 клеток, или, по меньшей мере, приблизительно 5×106 клеток, или, по меньшей мере, приблизительно 6×106 клеток, или, по меньшей мере, приблизительно 7×106 клеток, или, по меньшей мере, приблизительно 8×106 клеток, или, по меньшей мере, приблизительно 9×106 клеток, или, по меньшей мере, приблизительно 10×106 клеток. В некоторых аспектах, кондиционированная среда может формироваться посредством сбора среды, используемой для того, чтобы культивировать, размножать, дифференцировать или поддерживать третье множество клеток, которые культивируются, по меньшей мере, приблизительно в течение 4 часов или, по меньшей мере, приблизительно в течение 8 часов, или, по меньшей мере, приблизительно в течение 12 часов, или, по меньшей мере, приблизительно в течение 16 часов, или, по меньшей мере, приблизительно в течение 20 часов, или, по меньшей мере, приблизительно в течение 24 часов, или, по меньшей мере, приблизительно в течение 36 часов, или, по меньшей мере, приблизительно в течение 48 часов, или, по меньшей мере, приблизительно в течение 60 часов, или, по меньшей мере, приблизительно 72 часов после посева.
[0070] В некоторых аспектах способов настоящего раскрытия сущности, кондиционированная среда может фильтроваться до использования в анализе настоящего раскрытия сущности. В некоторых аспектах, кондиционированная среда может фильтроваться с использованием концентратора или фильтрующего устройства в комбинации с центрифугированием. В некоторых аспектах, кондиционированная среда может фильтроваться через фильтр с MWCO, по меньшей мере, приблизительно в 3 кД или, по меньшей мере, приблизительно в 10 кД, или, по меньшей мере, приблизительно в 30 кД, или, по меньшей мере, приблизительно в 50 кД, или, по меньшей мере, приблизительно в 100 кД. В некоторых аспектах, после того, как кондиционированная среда фильтруется, "ретентат" или "верхняя" фракция может изолироваться для использования в способе настоящего раскрытия сущности. В некоторых аспектах, после того, как кондиционированная среда фильтруется, или "фильтрат" или "нижняя" фракция может изолироваться для использования в способе настоящего раскрытия сущности.
[0071] В некоторых аспектах способов, предоставляемых в данном документе, клеточная терапия или лечение содержит клетки-предшественники сетчатки глаза (RPC) млекопитающих, клетки-предшественники сетчатки глаза человека (hRPC), пигментные эпителиальные клетки сетчатки глаза (RPE) млекопитающих, пигментные эпителиальные клетки сетчатки глаза человека (hRPE), ARPE-19-клетки, нейронные стволовые клетки-предшественники, мезенхимальные стволовые клетки, CD34+-клетки, стволовые клетки-предшественники, лейкоциты, фибробласты либо любое их сочетание. Клетки-предшественники сетчатки глаза млекопитающих могут представлять собой клетки-предшественники сетчатки глаза человека (hRPC). Клеточная терапия или лечение может содержать hRPC. Клетки могут представлять собой генетически модифицированные клетки. В неограничивающем примере, генетически модифицированные клетки могут трансфицироваться с геном, чтобы экспрессировать, по меньшей мере, один полипептид. В неограничивающем примере, генетически модифицированные клетки могут инфицироваться в силу контакта с клетками, по меньшей мере, с одной вирусной частицей, при этом вирусная частица содержит, по меньшей мере, один полинуклеотид.
[0072] В некоторых аспектах способов, предоставляемых в данном документе, клеточная терапия или лечение либо кондиционированная среда могут содержать экзосомы и/или микропузырьки. Клеточная терапия или лечение либо кондиционированная среда могут содержать фракцию, которая пополняется в экзосомах и/или микропузырьках. Экзосомы и/или микропузырьки могут извлекаться из любого типа клеток, включающих в себя, но не только, клетки-предшественники сетчатки глаза (RPC) млекопитающих, клетки-предшественники сетчатки глаза человека (hRPC), пигментные эпителиальные клетки сетчатки глаза (RPE) млекопитающих, пигментные эпителиальные клетки сетчатки глаза человека (hRPE), ARPE-19-клетки, нейронные стволовые клетки-предшественники, мезенхимальные стволовые клетки, CD34+-клетки, стволовые клетки-предшественники, лейкоциты, фибробласты либо любое их сочетание. Клетки могут представлять собой генетически модифицированные клетки. В неограничивающем примере, генетически модифицированные клетки могут трансфицироваться, по меньшей мере, с одним геном, чтобы экспрессировать один полипептид. В неограничивающем примере, генетически модифицированные клетки могут инфицироваться в силу контакта с клетками, по меньшей мере, с одной вирусной частицей, при этом вирусная частица содержит, по меньшей мере, один полинуклеотид. Экзосомы и/или микропузырьки или фракция, пополненная в экзосомах и/или микропузырьках, могут очищаться с использованием технологий обработки экзосом/микропузырьков, стандартных в данной области техники, включающих в себя, но не только, центрифугирование, ультрацентрифугирование, эксклюзионную хроматографию размеров, ионообменную хроматографию, иммуноаффинную хроматографию либо любые другие технологии, стандартные в данной области техники.
[0073] В некоторых аспектах способов настоящего раскрытия сущности, контрольная среда содержит стандартную среду.
[0074] В некоторых аспектах способов настоящего раскрытия сущности, клеточная терапия или лечение может служить для лечения заболевания или состояния сетчатки глаза у исследуемого, нуждающегося в этом. Заболевание или состояние сетчатки глаза может включать в себя, но не только, заболевание Ушера, пигментный ретинит (RP), дегенеративное заболевание сетчатки глаза, возрастную макулярную дегенерацию (AMD), влажную AMD или сухую AMD, географическую атрофию, заболевание фоторецепторов сетчатки глаза, диабетическую ретинопатию, кистозный макулярный отек, увеит, отслоение сетчатки глаза, травму сетчатки глаза, макулярные отверстия, макулярную телеангиэктазию, травмирующую или ятрогенную травму сетчатки глаза, заболевание ганглионарных клеток или зрительных нервных клеток, глаукому или оптическую невропатию, ишемическое заболевание сетчатки глаза, такое как ретинопатия недоношенных, закупорка сосудов сетчатки глаза или ишемическая оптическая невропатия; либо улучшение фотопического (дневного) зрения; или для улучшения коррекции остроты зрения или улучшения макулярной функции, или улучшения поля зрения, или улучшения скотопического (ночного) зрения.
[0075] В некоторых аспектах предыдущего способа, первое множество клеток, второе множество клеток, третье множество клеток либо любая комбинация вышеозначенного могут содержать идентичный тип клеток или могут представлять собой различные типы клеток. Первое множество клеток, второе множество клеток, третье множество клеток либо любая комбинация вышеозначенного могут содержать смешанную популяцию различных типов клеток. Тип клеток может представлять собой любые первичные клетки, изолированные от биологической пробы, и/или клетки небессмертного типа (т.е. клетки, дифференцированные из популяций плюрипотентных/стволовых клеток). Тип клеток может представлять собой обессмерченную клеточную линию, включающую в себя, но не только, самопроизвольно обессмерченные клетки. Тип клеток может представлять собой клетки ретинобластомы (RB) млекопитающих, пигментные эпителиальные клетки сетчатки глаза (RPE) млекопитающих, клетки-предшественники сетчатки глаза (RPC) млекопитающих, ARPE-19-клетки, извлеченные из клеток Мюллера клетки, MIO-M1-клетки, нейрональные клетки, глиальные клетки, фибробласты, неокулярные клетки либо любое их сочетание. Тип клеток может представлять собой клетки ретинобластомы человека (hRB), пигментные эпителиальные клетки сетчатки глаза человека или клетки-предшественники сетчатки глаза человека. Первое множество клеток, второе множество клеток, третье множество клеток либо любая комбинация вышеозначенного могут выращиваться во взвешенном состоянии в ходе культивирования клеток. Первое множество клеток, второе множество клеток, третье множество клеток либо любая комбинация вышеозначенного могут выращиваться с использованием способов культивирования адгезивных клеток.
[0076] В некоторых аспектах способов настоящего раскрытия сущности, первое множество клеток и второе множество клеток могут содержать приблизительно от 1000 приблизительно до 250000 клеток. В качестве неограничивающих примеров, первое множество клеток и второе множество клеток могут содержать приблизительно 25000 клеток. В некоторых аспектах способов настоящего раскрытия сущности, число клеток в первом множестве, во втором множестве клеток, в третьем множестве клеток либо в любой комбинации вышеозначенного может масштабироваться согласно размеру микротитрационной пластины, которая используется для количественного анализа. В неограничивающем примере, первое множество клеток, второе множество клеток, третье множество клеток либо любая комбинация вышеозначенного могут содержать, по меньшей мере, приблизительно 25000 клеток, когда способы настоящего раскрытия сущности выполняются в 96-луночной пластине. Когда используется 6-луночная пластина, первое множество клеток, второе множество клеток, третье множество клеток либо любая комбинация вышеозначенного могут содержать, по меньшей мере, приблизительно 400000 клеток. Когда используется 12-луночная пластина, первое множество клеток, второе множество клеток, третье множество клеток либо любая комбинация вышеозначенного могут содержать, по меньшей мере, приблизительно 200000 клеток. Когда используется 24-луночная пластина, первое множество клеток, второе множество клеток, третье множество клеток либо любая комбинация вышеозначенного могут содержать, по меньшей мере, приблизительно 100000 клеток. Когда используется 48-луночная пластина, первое множество клеток, второе множество клеток, третье множество клеток либо любая комбинация вышеозначенного могут содержать, по меньшей мере, приблизительно 50000 клеток. Когда используется 384-луночная пластина, первое множество клеток, второе множество клеток, третье множество клеток либо любая комбинация вышеозначенного могут содержать, по меньшей мере, приблизительно 6250 клеток. Когда используется 1536-луночная пластина, первое множество клеток, второе множество клеток, третье множество клеток либо любая комбинация вышеозначенного могут содержать, по меньшей мере, приблизительно 1562 клетки.
[0077] В некоторых аспектах способов настоящего раскрытия сущности, до добавления токсичного химического соединения и кондиционированной и/или стандартной среды, первое множество клеток, второе множество клеток, третье множество клеток либо любая комбинация вышеозначенного могут взвешиваться, по меньшей мере, приблизительно в 25 мкл стандартной среды. Объем стандартной среды может используемый, может регулироваться на основе размера микротитрационной пластины, которая используется для количественного анализа. В неограничивающем примере, когда используется 6-луночная пластина, могут использоваться приблизительно 400 мкл стандартной среды. В неограничивающем примере, когда используется 12-луночная пластина, могут использоваться приблизительно 200 мкл стандартной среды. В неограничивающем примере, когда используется 24-луночная пластина, могут использоваться приблизительно 100 мкл стандартной среды. В неограничивающем примере, когда используется 48-луночная пластина, могут использоваться приблизительно 50 мкл стандартной среды. В неограничивающем примере, когда используется 96-луночная пластина, могут использоваться приблизительно 25 мкл стандартной среды. В неограничивающем примере, когда используется 384-луночная пластина, могут использоваться приблизительно 6,25 мкл стандартной среды. В неограничивающем примере, когда используется 1536-луночная пластина, могут использоваться приблизительно 1,56 мкл стандартной среды.
[0078] В некоторых аспектах способов настоящего раскрытия сущности, первое множество клеток, второе множество клеток, третье множество клеток либо любая комбинация вышеозначенного могут инкубироваться, по меньшей мере, с приблизительно от 50 мкл, по меньшей мере, приблизительно до 100 мкл кондиционированной среды или контрольной среды. В некоторых аспектах, первое множество клеток, второе множество клеток, третье множество клеток либо любая комбинация вышеозначенного могут инкубироваться, по меньшей мере, с приблизительно 75 мкл кондиционированной среды или контрольной среды. Объем кондиционированной среды или контрольной среды может регулироваться на основе размера микротитрационной пластины, которая используется для количественного анализа. В неограничивающем примере, когда используется 6-луночная пластина, могут использоваться приблизительно 1200 мкл кондиционированной среды или контрольной среды. В неограничивающем примере, когда используется 12-луночная пластина, могут использоваться приблизительно 600 мкл кондиционированной среды или контрольной среды. В неограничивающем примере, когда используется 24-луночная пластина, могут использоваться приблизительно 300 мкл кондиционированной среды или контрольной среды. В неограничивающем примере, когда используется 48-луночная пластина, могут использоваться приблизительно 150 мкл кондиционированной среды или контрольной среды. В неограничивающем примере, когда используется 96-луночная пластина, могут использоваться приблизительно 75 мкл кондиционированной среды или контрольной среды. В неограничивающем примере, когда используется 384-луночная пластина, могут использоваться приблизительно 18,75 мкл кондиционированной среды или контрольной среды. В неограничивающем примере, когда используется 1536-луночная пластина, могут использоваться приблизительно 4,68 мкл кондиционированной среды или контрольной среды.
[0079] В некоторых аспектах способов, предоставляемых в данном документе, токсичное химическое соединение может индуцировать апоптоз. В некоторых аспектах, токсичное химическое соединение может индуцировать апоптоз, аутофагию, гибель клеток типа I, гибель клеток типа II, некроз, некроптоз, макроаутофагию, аноикоз, ороговение, экзитотоксичность, ферроптоз, индуцированную активацией гибель клеток, ишемическую гибель клеток, онкогенез, пироптоз либо любое их сочетание.
[0080] Токсичные химические соединения могут включать в себя, но не только, алкилирующие агенты, антиметаболиты, противоопухолевый антибиотик, химиотерапевтические агенты, алкалоиды, таксаны, антимикротубулиновые агенты, токсины, мембранные пермеабилизаторы, ингибиторы фермента, антиметаболиты, митотические ингибиторы, ингибиторы ДНК-репаративного фермента, ДНК-повреждающие агенты, ультрафиолетовое излучение, гамма-излучение, бусульфан, цитозин, этопозид, блеомицин, ласпарагиназу, кармустин, арабинозид, тенипозид, дактиномицин, гидроксимочевину, хлорамбуцил, флоксуридин, винбластин, даунорубицин, прокарбазин, цисплатин, фтороурацил, винкристин, доксорубицин, циклофосфамид, меркаптопурин, виндезин, митомицин C, ифосфамид, метотрексат, таксоиды, митоксантрон, мелфалан, гемцитабин, пликамицин, пеметрекседантрациклины и/или эпотилоны.
[0081] В некоторых аспектах способов настоящего раскрытия сущности, токсичное химическое соединение представляет собой бутират натрия. Бутират натрия может присутствовать с концентрацией приблизительно от 1 ммоль приблизительно до 26 ммоль. Бутират натрия может присутствовать с концентрацией приблизительно от 2 ммоль приблизительно до 24 ммоль. Бутират натрия может присутствовать с концентрацией приблизительно от 0 ммоль приблизительно до 32 ммоль. В некоторых аспектах способов настоящего раскрытия сущности, бутират натрия присутствует с концентрацией приблизительно в 0 ммоль, т.е. бутират натрия не добавляется. В некоторых аспектах способов настоящего раскрытия сущности, бутират натрия присутствует с концентрацией приблизительно в 2 ммоль. В некоторых аспектах способов настоящего раскрытия сущности, бутират натрия присутствует с концентрацией приблизительно в 4 ммоль. В некоторых аспектах способов настоящего раскрытия сущности, бутират натрия присутствует с концентрацией приблизительно в 6 ммоль. В некоторых аспектах способов настоящего раскрытия сущности, бутират натрия присутствует с концентрацией приблизительно в 8 ммоль. В некоторых аспектах способов настоящего раскрытия сущности, бутират натрия присутствует с концентрацией приблизительно в 10 ммоль. В некоторых аспектах способов настоящего раскрытия сущности, бутират натрия присутствует с концентрацией приблизительно в 12 ммоль. В некоторых аспектах способов настоящего раскрытия сущности, бутират натрия присутствует с концентрацией приблизительно в 14 ммоль. В некоторых аспектах способов настоящего раскрытия сущности, бутират натрия присутствует с концентрацией приблизительно в 16 ммоль. В некоторых аспектах способов настоящего раскрытия сущности, бутират натрия присутствует с концентрацией приблизительно в 18 ммоль или приблизительно в 20 ммоль, или приблизительно в 22 ммоль, или приблизительно 24 ммоль, или приблизительно в 26 ммоль, или приблизительно в 28 ммоль, или приблизительно в 30 ммоль, или приблизительно в 32 ммоль, или приблизительно в 34 ммоль, или приблизительно в 36 ммоль, или приблизительно в 38 ммоль, или приблизительно в 40 ммоль.
[0082] В некоторых аспектах способов настоящего раскрытия сущности, первое множество клеток, второе множество клеток, третье множество клеток либо любая комбинация вышеозначенного инкубируются в течение периода, по меньшей мере, в 1 час или, по меньшей мере, в 12 часов, или, по меньшей мере, в 24 часа, или, по меньшей мере, в 46 часов, или, по меньшей мере, в 48 часов, или, по меньшей мере, в 72 часа или более до определения жизнеспособности клеток. В некоторых аспектах, первое множество клеток, второе множество клеток, третье множество клеток либо любая комбинация вышеозначенного инкубируются приблизительно в течение 1 часа или приблизительно в течение 2 часов, или приблизительно в течение 72 часов или боле. В некоторых аспектах, первое множество клеток, второе множество клеток, третье множество клеток либо любая комбинация вышеозначенного инкубируются, по меньшей мере, в течение 46 часов до определения жизнеспособности клеток.
[0083] В некоторых аспектах способов, предоставляемых в данном документе, определение жизнеспособности первого множества клеток, второго множества клеток, третьего множества клеток либо любой комбинации вышеозначенного может содержать использование любых анализов жизнеспособности клеток, известных в данной области техники. Они включают в себя, но не только, тестовый АТФ-анализ, кальцеин-AM-анализ, клоногенный анализ, гомодимерный количественный анализ этидия, количественный анализ по синему Эванса, количественный анализ на основе гидролиза флуоресцеиндиацетата/окрашивания иодидом пропидия, количественный анализ по проточной цитометрии, количественный анализ на основе формазана, MTT-анализ, XTT-анализ, количественный анализ по зеленому флуоресцентному белку, количественный анализ на основе лактатдегидрогеназы, метил-фиолетовый анализ, количественный анализ на основе иодида пропидия, количественный анализ на основе резазурина, трипановый синий анализ, количественный анализ на основе терминального дезоксиуридинового мечения концов разорванной нити ДНК (TUNEL) либо комбинацию вышеозначенного.
[0084] В некоторых аспектах способов настоящего раскрытия сущности, определение жизнеспособности первого множества клеток, второго множества клеток, третьего множества клеток либо любой комбинации вышеозначенного может содержать определение пролиферации первого множества клеток, второго множества клеток, третьего множества клеток либо любой комбинации вышеозначенного. В некоторых аспектах способов настоящего раскрытия сущности, определение жизнеспособности первого множества клеток, второго множества клеток, третьего множества клеток либо любой комбинации вышеозначенного содержит измерение метаболической емкости первого множества клеток, второго множества клеток, третьего множества клеток либо любой комбинации вышеозначенного.
[0085] Метаболическая емкость первого множества клеток, второго множества клеток, третьего множества клеток либо любой комбинации вышеозначенного может измеряться с использованием количественного анализа на основе люминесценции. Количественный анализ на основе люминесценции может содержать: 1) инкубацию первого множества клеток, второго множества клеток, третьего множества клеток либо любой комбинации вышеозначенного с резазурином (натриевой солью в виде 7-гидрокси-3H-феноксазин-3-он 10-оксида) в течение периода, по меньшей мере, в 1 час, 2) измерение люминесценции первого множества клеток, второго множества клеток, третьего множества клеток либо любой комбинации вышеозначенного. Количественный анализ на основе люминесценции дополнительно может содержать 3) сравнение измеренной люминесценции, за счет этого определяя жизнеспособность первого множества клеток, второго множества клеток, третьего множества клеток либо любой комбинации вышеозначенного. В некоторых аспектах, клетки инкубируются с резазурином в течение периода времени, по меньшей мере, приблизительно в 1 час или, по меньшей мере, приблизительно в 1,5 часа, или, по меньшей мере, приблизительно в 2,0 часа, или, по меньшей мере, приблизительно в 2,5 часа, или, по меньшей мере, приблизительно в 3,0 часа, или, по меньшей мере, приблизительно в 3,5 часа, или, по меньшей мере, приблизительно в 4,0 часа, или, по меньшей мере, приблизительно в 4,5 часа, или, по меньшей мере, приблизительно в 5,0 часов, или, по меньшей мере, приблизительно в 5,5 часов, или, по меньшей мере, приблизительно в 6,0 часов, или, по меньшей мере, приблизительно в 6,5 часов, или, по меньшей мере, приблизительно в 7,0 часов, или, по меньшей мере, приблизительно в 7,5 часов, или, по меньшей мере, приблизительно в 8,0 часов, или, по меньшей мере, приблизительно в 8,5 часов, или, по меньшей мере, приблизительно в 9,0 часов, или, по меньшей мере, приблизительно в 9,5 часов, или, по меньшей мере, приблизительно в 10 часов, или, по меньшей мере, приблизительно в 15 часов, или, по меньшей мере, приблизительно в 20 часов. Метаболическая емкость первого множества клеток, второго множества клеток, третьего множества клеток либо любой комбинации вышеозначенного может измеряться с использованием количественного анализа жизнеспособности клеток на основе CellTiter-Blue®. В некоторых аспектах, реагент на основе CellTiter-Blue® может разбавляться 1:4. В некоторых аспектах, реагент на основе CellTiter-Blue® может разбавляться 1:4 в фосфатно-солевом буферном растворе Дульбекко. В некоторых аспектах, реагент на основе CellTiter-Blue® является неразбавленным. В некоторых аспектах, первое множество клеток, второе множество клеток, третье множество клеток либо любая комбинация вышеозначенного могут инкубироваться, по меньшей мере, с приблизительно 20 мкл неразбавленного или разбавленного реагента на основе CellTiter-Blue®. В некоторых аспектах, количество неразбавленного или разбавленного используемого реагента на основе CellTiter-Blue® может регулироваться на основе микротитрационной пластины, которая используется для количественного анализа.
[0086] В некоторых аспектах способов настоящего раскрытия сущности, определение активности по апоптозу в первом множестве клеток, во втором множестве клеток, в третьем множестве клеток либо в любой комбинации вышеозначенного может содержать количественный анализ на основе люминесценции. Количественный анализ на основе люминесценции может содержать: инкубацию первого множества клеток, второго множества клеток, третьего множества клеток либо любой комбинации вышеозначенного с подложкой на основе люминогенной каспазы-3/7, по меньшей мере, в течение приблизительно 1 часа; и измерение люминесценции первого множества клеток, второго множества клеток, третьего множества клеток либо любой комбинации вышеозначенного. Инкубация с подложкой на основе люминогенной каспазы-3/7 может осуществляться в течение периода времени, по меньшей мере, приблизительно в 1 час или, по меньшей мере, приблизительно в 1,5 часа, или, по меньшей мере, приблизительно в 2,0 часа, или, по меньшей мере, приблизительно в 2,5 часа, или, по меньшей мере, в приблизительно 3,0 часа, или, по меньшей мере, приблизительно в 3,5 часа, или, по меньшей мере, приблизительно в 4,0 часа, или, по меньшей мере, приблизительно в 4,5 часа, или, по меньшей мере, приблизительно в 5,0 часов, или, по меньшей мере, приблизительно в 5,5 часов, или, по меньшей мере, приблизительно в 6,0 часов, или, по меньшей мере, приблизительно в 6,5 часов, или, по меньшей мере, приблизительно в 7,0 часов, или, по меньшей мере, приблизительно в 7,5 часов, или, по меньшей мере, приблизительно в 8,0 часов, или, по меньшей мере, приблизительно в 8,5 часов, или, по меньшей мере, приблизительно в 9,0 часов, или, по меньшей мере, приблизительно в 9,5 часов, или, по меньшей мере, приблизительно в 10 часов, или, по меньшей мере, приблизительно в 15 часов, или, по меньшей мере, приблизительно в 20 часов. В некоторых аспектах, подложка на основе люминогенной каспазы-3/7 содержит тетрапептидную последовательность DEVD, которая расщепляется посредством каспазы 3 или каспазы 7, за счет этого формируя подложку на основе люциферазы. В некоторых аспектах, количественный анализ на основе люминесценции представляет собой систему количественного анализа на основе Caspase-Glo® 3/7. В некоторых аспектах, первое множество клеток, второе множество клеток, третье множество клеток либо любая комбинация вышеозначенного могут инкубироваться, по меньшей мере, с приблизительно 120 мкл реагента для количественного анализа на основе Caspase-Glo® 3/7. Количество реагента для количественного анализа на основе Caspase-Glo® 3/7 может регулироваться на основе микротитрационной пластины, которая используется для количественного анализа. В неограничивающем примере, когда используется 96-луночная микротитрационная пластина, могут использоваться приблизительно 120 мкл реагента для количественного анализа на основе Caspase-Glo® 3/7.
[0087] В некоторых аспектах способов настоящего раскрытия сущности, первое множество клеток, второе множество клеток, третье множество клеток либо любая комбинация вышеозначенного могут инкубироваться в стандартной пластине для количественного анализа. Она включает в себя, но не только, микротитр, микропластины или микролуночные пластины с 6, 12, 14, 48, 96, 384 или 1536 лунками для проб. Поверхность пластины для количественного анализа может покрываться молекулой, чтобы упрощать присоединение клеток на пластину для количественного анализа. Примерные покрытия включают в себя, но не только, поли-D-лизин или фибронектин человека. Пластина для количественного анализа может оставляться без покрытия.
[0088] Любой из вышеприведенных аспектов и вариантов осуществления может комбинироваться с любым другим аспектом или вариантом осуществления, раскрытым здесь в разделах "Сущность изобретения" и/или "Подробное описание".
[0089] При использовании в подробном описании и в прилагаемой формуле изобретения, формы единственного числа "a", "an" и "the" включают в себя несколько объектов ссылки, если контекст явно не предписывает иное.
[0090] Если иное не указано прямо или не очевидно из контекста, при использовании в данном документе, термин "или" понимается как включающий и охватывает как "или", так и "и".
[0091] Если иное не указано прямо или не очевидно из контекста, при использовании в данном документе, термин "приблизительно" понимается в пределах диапазона нормального допуска в данной области техники, например, в пределах 2 среднеквадратических отклонений от среднего значения. "Приблизительно" может пониматься как в пределах 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2%, 1%, 0,5%, 0,1%, 0,05% или 0,01% от заявленного значения. Если иное не очевидно из контекста, все числовые значения, предоставляемые в настоящем документе, модифицируются посредством термина "приблизительно".
[0092] Если не указано иное, все технические и научные термины, используемые в данном документе, имеют тот же смысл, как обычно понимается специалистами в области техники, к которой относится изобретение. Хотя другие исследования, составы, способы и комплекты, аналогичные или эквивалентные исследованиям, составам, способам и комплектам, описанным в данном документе, могут использоваться при практическом применении настоящего раскрытия сущности, примерные материалы и способы описываются в данном документе. Следует понимать, что терминология, используемая в данном документе, служит только для целей описания конкретных аспектов и не имеет намерение быть ограниченной.
Примеры
[0093] В следующих примерах, клетки ретинобластомы человека (hRB) Y79 (на основе ATCC® HTB-18TM) размножаются и поддерживаются для использования посредством культивирования в сформулированной ATCC® RPMI-1640-среде, дополненной 20%-й фетальной бычьей сывороткой. Клетки поддерживаются согласно рекомендациям ATCC®. Клетки-предшественники сетчатки глаза человека (hRPC) и пигментные эпителиальные клетки сетчатки глаза человека (hRPE-клетка) изолированы от 18-20-недельных человеческих плодов и распространяются в стандартной среде (SM), содержащей улучшенный DMEM/F12 с 1x N-2 добавкой, 1x GlutaMax-1, 20 нг/мл основного FGF-белка человека и 20 нг/мл EGF-белка человека.
[0094] В следующих экспериментах, кондиционированная среда (CM) собирается из hRPC, hRB-клеток или hRPE, выращенных в SM в течение 48 часов (с заменой SM после 24 часов). Клетки собираются и подсчитываются после каждого CM-сбора.
Пример 1: подложки с покрытием и без покрытия
[0095] Различные реагенты для нанесения покрытия протестированы для того, чтобы определять подложку, подходящую для использования в способах настоящего раскрытия сущности.
[0096] Непрозрачные 96-луночные пластины для количественного анализа оставляются без покрытия, покрываются поли-D-лизином либо покрываются фибронектином человека. Пластины покрываются поли-D-лизином посредством инкубации от 25 мкл до 50 мкл раствора в 200 мкг/мл поли-D-лизина в каждой лунке в течение одного часа пятидесяти пяти минут при комнатной температуре. Альтернативно, 250 мкл раствора в 200 мкг/мл поли-D-лизина инкубируются в каждой лунке в течение одного часа при комнатной температуре. После инкубации, пластины промываются ddH2O, после чего оставляются для сушки воздухом в течение двух часов. Пластины покрываются фибронектином человека посредством инкубации 300 мкл раствора в 20 мкг/мл фибронектина человека при 37º C в течение всей ночи. После инкубации в течение всей ночи, пластины промываются улучшенным DMEM/F12.
[0097] Клетки ретинобластомы человека (hRB) Y79 (на основе ATCC® HTB-18TM) затем добавляются в три различных пластины для количественного анализа. В случае пластин с использованием фибронектина человека, hRB-клетки наблюдаются как колонизированные. С другой стороны, в пластинах с использованием поли-D-лизина, hRB-клетки наблюдаются как распределенные равномерно. Когда клетки добавляются в пластины без покрытия в стандартной среде для клеток-предшественников сетчатки глаза человека, клетки присоединяются к пластине, несмотря на отсутствие покрытия. Таким образом, пластины без покрытия также могут использоваться в способах настоящего раскрытия сущности.
Пример 2: количественный анализ жизнеспособности клеток на основе люминесценции
[0098] Количественный анализ на основе люминесценции для того, чтобы измерять жизнеспособность клеток, протестирован на предмет использования в способах настоящего раскрытия сущности.
[0099] Во-первых, 12,5×103, 2,5×104, 5,0×104, 1,0×105 и 2,0×105 клеток ретинобластомы человека (hRB) Y79 (на основе ATCC® HTB-18TM) электролитически наносятся на пять отдельных лунок 96-луночной пластины для количественного анализа и инкубируются в 50 мкл SM. После предоставления возможности клеткам осаждаться в течение периода от 30 минут до двух часов, клетки затем инкубируются с 250 мкл кондиционированной среды для клеток-предшественников сетчатки глаза человека после тщательного смешивания. 200 мкл среды затем отсасываются, и 20 мкл разбавленного реагента на основе CellTiter-Blue® (1:4 в DPBS), содержащего резазурин (натриевую соль в виде 7-гидрокси-3H-феноксазин-3-он 10-оксида), добавляются в клетки на 1, 2, 3 или 4 час при 37º C. Резазурин представляет собой токсичное химическое соединение, которое, при интернализации посредством жизнеспособных клеток, уменьшается до токсичного химического соединения, известного как резоруфин. Резоруфин является высоколюминесцентным, что означает то, что сформированный люминесцентный сигнал может использоваться для того, чтобы определять жизнеспособность клеток, инкубированных с резазурином. Нежизнеспособные клетки, которые не имеют метаболической емкости, не уменьшают резазурин до резоруфина, и в силу этого люминесцентный сигнал не формируется.
[00100] Люминесценция каждой лунки измеряется после инкубации с резазурином. Люминесцентные сигналы считываются при длине волны возбуждения в 520 нм и при длине волны излучения в 580-640 нм. Каждое лечение проведено в трипликатах или квадрупликатах. Как показано на фиг. 1, предусмотрен линейный отклик (R2=0,99) для времен инкубации в 1, 2 или 3 часа для всех количеств клеток. Эти результаты указывают то, что для того, чтобы достигать максимального лечебного эффекта в расчете на клетку и минимизировать длительность эксперимента и внутрипробное варьирование, способы настоящего раскрытия сущности могут использовать 2,5×104 клеток/лунка и время инкубации резазурина в 2 часа.
Пример 3: определение эффективности кондиционированной среды для клеток-предшественников сетчатки глаза человека
[00101] Способы настоящего раскрытия сущности используются для того, чтобы тестировать эффективность кондиционированной среды для клеток-предшественников сетчатки глаза человека.
[00102] Во-первых, hRB-клетки электролитическим способом нанесены на пластину для количественного анализа с плотностью 2,5×104 клеток/лунка. Клетки затем инкубируются либо с кондиционированной средой для клеток-предшественников сетчатки глаза человека (hRPC CM), либо или со стандартной средой (SM: стандартной средой для клеток-предшественников сетчатки глаза человека, которая не подвергается воздействию клеток-предшественников сетчатки глаза человека). Среда дополнена без бутирата натрия, 2 ммоль бутирата натрия, 4 ммоль бутирата натрия или 8 ммоль бутирата натрия. Свежеприготовленные 200 ммоль бутирата натрия добавляются в 250 мкл среды для того, чтобы формировать различные концентрации бутирата натрия. HRPC CM сформирована с использованием 9,0×106 клеток-предшественников сетчатки глаза человека.
[00103] HRB-клетки инкубируются в течение одного часа или в течение 72 часов в 300 мкл различной среды. После инкубации, жизнеспособность клеток измеряется с использованием реагента на основе CellTiter-Blue®, как описано выше. Вкратце, 200 мкл культуры клеток смешиваются с 20 мкл разбавленного реагента на основе CellTiter-Blue® и инкубируются в течение одного-двух часов. После этого люминесценция каждой пробы измеряется. Как показано на фиг. 2, более сильные люминесцентные сигналы наблюдаются после инкубации в течение 72 часов (правая панель) по сравнению с инкубацией в течение одного часа (левая панель) вследствие пролиферации клеток. Тем не менее, значительный дозозависимый, индуцированный бутиратом натрия апоптоз наблюдается в пробах, инкубированных в течение 72 часов, поскольку повышенные концентрации бутирата натрия приводят к уменьшенным люминесцентным сигналам, указывающим сниженную пролиферацию и жизнеспособность клеток.
[00104] Клетки, которые инкубируются с hRPC CM, демонстрируют увеличенные люминесцентные сигналы для инкубации в течение одного часа и в течение 72 часов по сравнению с клетками, инкубированными с SM. Эти результаты указывают то, что hRPC CM эффективно увеличивает жизнеспособность hRB-клеток даже в присутствии индуцирующего апоптоз бутирата натрия. Наибольшая эффективность hRPC CM наблюдается в клетках, инкубированных с 8 ммоль бутирата натрия, в которых hRPC CM демонстрирует приблизительно двукратную эффективность при увеличении жизнеспособности клеток по сравнению с SM в моменты времени в один час и в 72 часа. Эти предварительные результаты указывают то, что 8 ммоль бутирата натрия предоставляют наибольший обнаруживаемый сигнал.
[00105] В другом эксперименте, hRB-клетки электролитическим способом нанесены на пластину для количественного анализа с плотностью 2,5×104 клеток/лунка. Клетки затем инкубируются либо с hRPC CM, либо с SM. Среда дополнена без бутирата натрия, 8 ммоль бутирата натрия, 16 ммоль бутирата натрия или 24 ммоль бутирата натрия. HRPC CM сформирована с использованием 9,0×106 клеток-предшественников сетчатки глаза человека.
[00106] HRB-клетки инкубируются в течение одного часа. После инкубации, жизнеспособность клеток измеряется с использованием реагента на основе CellTiter-Blue®, как описано выше. Как показано на фиг. 3, hRB-клетки, инкубированные с hRPC CM, демонстрируют увеличенные люминесцентные сигналы по сравнению с hRB-клетками, инкубированными с SM. Этот тренд является согласованным для всех четырех концентраций бутирата натрия. Эти результаты указывают то, что hRPC CM эффективно увеличивает жизнеспособность hRB-клеток, даже в присутствии высокой концентрации индуцирующего апоптоз бутирата натрия.
Пример 4: определение эффективности кондиционированной среды для клеток-предшественников сетчатки глаза человека в различных дозах
[00107] Способы настоящего раскрытия сущности используются для того, чтобы тестировать то, является или нет эффективность кондиционированной среды для клеток-предшественников сетчатки глаза человека дозозависимой.
[00108] Во-первых, hRB-клетки электролитическим способом нанесены на пластину для количественного анализа с плотностью 2,5×104 клеток/лунка. Клетки затем инкубируются с hRPC CM, SM, hRPC CM, разбавленной двукратно с SM (0,5x hRPC CM), hRPC CM, разбавленной четырехкратно с SM (0,25x hRPC CM), или hRPC CM, разбавленной восьмикратно с SM (0,125x hRPC CM). Среда дополнена без бутирата натрия или 8 ммоль бутирата натрия. HRPC CM сформирована с использованием 9,0×106 клеток-предшественников сетчатки глаза человека.
[00109] HRB-клетки инкубируются в течение одного часа. После инкубации, жизнеспособность клеток измеряется с использованием реагента на основе CellTiter-Blue®, как описано выше. Как показано на фиг. 4, клетки, инкубированные с более концентрированной hRPC CM, демонстрируют увеличенные люминесцентные сигналы по сравнению с клетками, инкубированными с более разбавленной hRPC CM, и с клетками, инкубированными с SM. Эти результаты указывают то, что hRPC CM эффективно увеличивает жизнеспособность hRB-клеток дозозависимым способом.
[00110] В другом эксперименте, hRB-клетки электролитическим способом нанесены на пластину для количественного анализа с плотностью 2,5×104 клеток/лунка. Клетки затем инкубируются с hRPC CM, сформированной с использованием 9,0×106 клеток-предшественников сетчатки глаза человека (hRPC CM 9M), hRPC CM, сформированной с использованием 6,0×106 клеток-предшественников сетчатки глаза человека (hRPC CM 6M), или SM. Среда дополнена без бутирата натрия или 8 ммоль бутирата натрия.
[00111] HRB-клетки инкубируются в течение одного часа. После инкубации, жизнеспособность клеток измеряется с использованием реагента на основе CellTiter-Blue®, как описано выше. Как показано на фиг. 5, клетки, инкубированные с hRPC CM 9M, демонстрируют увеличенные значения люминесценции по сравнению с клетками, инкубированными с hRPC CM 6M, и с клетками, инкубированными с SM при обеих концентрациях бутирата натрия. Этот результат указывает то, что эффективность hRPC CM-лечения зависит от числа hRPC, используемых для того, чтобы формировать кондиционированную среду.
[00112] Эти результаты указывают то, что способы, предоставляемые в данном документе, могут использоваться для того, чтобы определять эффективность базовой hRPC-терапии для лечения пигментного ретинита.
Пример 5: определение того, является или нет эффективность кондиционированной среды для клеток-предшественников сетчатки глаза человека воспроизводимой с использованием различных популяций hRPC
[00113] Способы настоящего раскрытия сущности используются для того, чтобы тестировать то, является или нет эффективность кондиционированной среды для клеток-предшественников сетчатки глаза человека воспроизводимой, когда кондиционированная среда сформирована с использованием отдельных популяций hRPC из различных партий продуктов.
[00114] Во-первых, hRB-клетки электролитическим способом нанесены на пластину для количественного анализа с плотностью 2,5×104 клеток/лунка. Клетки затем инкубируются с hRPC CM, сформированной с использованием hRPC в 5,4×106/10 мл из партии, обозначенной как G1 (hRPC CM G15,4), hRPC CM, сформированной с использованием hRPC в 3,7×106/10 мл из партии, обозначенной как G2 (hRPC CM G2 3,7), hRPC CM, сформированной с использованием hRPC в 4,5×106/10 мл из партии, обозначенной как G3 (hRPC CM G3 4,5), hRPC CM, сформированной с использованием hRPC в 5,0×106/10 мл из партии, обозначенной как G5 (hRPC CM G5 5,0), или SM. Среда дополнена без бутирата натрия или 8 ммоль бутирата натрия.
[00115] HRB-клетки инкубируются в течение 2 часов. После инкубации, жизнеспособность клеток измеряется с использованием реагента на основе CellTiter-Blue®, как описано выше. Как показано в левой панели по фиг. 6, клетки, инкубированные с hRPC CM, демонстрируют увеличенные значения люминесценции по сравнению с клетками, инкубированными с SM при обеих концентрациях бутирата натрия. Это увеличение наблюдается независимо от партии hRPC, используемых для того, чтобы формировать кондиционированную среду.
[00116] В другом эксперименте, hRB-клетки электролитическим способом нанесены на пластину для количественного анализа с плотностью 2,5×104 клеток/лунка. Клетки затем инкубируются с hRPC CM, сформированной с использованием hRPC в 3,7×106/10 мл из партии, обозначенной как G1 (hRPC CM G1 3,7), hRPC CM, сформированной с использованием hRPC в 2,9×106/10 мл из партии, обозначенной как G2 (hRPC CM G2 2,9), hRPC CM, сформированной с использованием hRPC в 3,35×106/10 мл из партии, обозначенной как G3 (hRPC CM G4 3,35), hRPC CM, сформированной с использованием hRPC в 3,25×106/10 мл из партии, обозначенной как G5 (hRPC CM G5 3,25), или SM. Среда дополнена без бутирата натрия или 8 ммоль бутирата натрия.
[00117] HRB-клетки инкубируются в течение 2 часов. После инкубации, жизнеспособность клеток измеряется с использованием реагента на основе CellTiter-Blue®, как описано выше. Как показано в правой панели по фиг. 6, клетки, инкубированные с hRPC CM, демонстрируют увеличенные значения люминесценции по сравнению с клетками, инкубированными с SM при обеих концентрациях бутирата натрия. Это увеличение наблюдается независимо от источника hRPC, используемых для того, чтобы формировать кондиционированную среду.
[00118] В другом эксперименте, hRB-клетки электролитическим способом нанесены на пластину для количественного анализа с плотностью 2,5×104 клеток/лунка. Клетки затем инкубируются с hRPC CM, сформированной с использованием hRPC в 2,038×106/4 мл из партии, обозначенной как G1 (hRPC CM G1 2,038), hRPC CM, сформированной с использованием hRPC в 1,774×106/4 мл из партии, обозначенной как G2 (hRPC CM G2 1,774), hRPC CM, сформированной с использованием hRPC в 1,543×106/4 мл из партии, обозначенной как G3 (hRPC CM G3 1,543), hRPC CM, сформированной с использованием hRPC в 1,542×106/4 мл из партии, обозначенной как G4 (hRPC CM G4 1,542), hRPC CM, сформированной с использованием hRPC в 1,318×106/4 мл из партии, обозначенной как G5 (hRPC CM G5 1,318), hRPC CM, сформированной с использованием hRPC в 1,977×106/4 мл из CMO-пробы из семенного фонда, обозначенной как L-SB (hRPC CM L-SB), hRPC CM, сформированной с использованием в hRPC 1,162×106/4 мл из L-пробы из фонда продуктов, обозначенной как L-PB (hRPC CM L-PB), или SM. Среда дополнена без бутирата натрия или 8 ммоль бутирата натрия.
[00119] HRB-клетки инкубируются в течение 2 часов. После инкубации, жизнеспособность клеток измеряется с использованием реагента на основе CellTiter-Blue®, как описано выше. Как показано на фиг. 7, клетки, инкубированные с hRPC CM, демонстрируют увеличенные значения люминесценции по сравнению с клетками, инкубированными с SM при обеих концентрациях бутирата натрия. Это увеличение наблюдается независимо от источника hRPC, используемых для того, чтобы формировать кондиционированную среду.
[00120] Результаты в этом примере указывают то, что различные популяции hRPC могут использоваться для того, чтобы формировать эффективную кондиционированную среду. Эффективность кондиционированной среды из различных hRPC-партий показывает согласованно повышенную метаболическую активность по сравнению с SM. Хотя возникают некоторые разности в эффективности между партиями, это с наибольшей вероятностью обусловлено отсутствие стандартизации во время сбора кондиционированной среды.
Пример 6: определение того, является или нет эффективность кондиционированной среды для клеток-предшественников сетчатки глаза человека специфической
[00121] Способы настоящего раскрытия сущности используются для того, чтобы тестировать то, является или нет эффективность hRPC CM специфической для кондиционированной среды, сформированной с использованием hRPC, по сравнению с кондиционированной средой, сформированной с использованием других типов клеток.
[00122] Во-первых, hRB-клетки электролитическим способом нанесены на пластину для количественного анализа с плотностью 2,5×104 клеток/лунка. Клетки затем инкубируются с hRPC CM, сформированной с использованием 9,0×106 клеток-предшественников сетчатки глаза человека (hRPC CM 9M), кондиционированной hRB-среды, сформированной с использованием 12,2×106 hRB-клеток (CM hRB 12,2M), или SM. Среда дополнена без бутирата натрия или 8 ммоль бутирата натрия.
[00123] HRB-клетки инкубируются в течение 1 или 2 часов. После инкубации, жизнеспособность клеток измеряется с использованием реагента на основе CellTiter-Blue®, как описано выше. Как показано в левой панели по фиг. 8, клетки, инкубированные с кондиционированной средой hRPC, демонстрируют увеличенные люминесцентные сигналы по сравнению с клетками, инкубированными с кондиционированной hRB-средой и SM. Этот тренд является согласованным для концентраций бутирата натрия.
[00124] В другом эксперименте, hRB-клетки электролитическим способом нанесены на пластину для количественного анализа с плотностью 2,5×104 клеток/лунка. Клетки затем инкубируются с кондиционированной средой для пигментных эпителиальных клеток сетчатки глаза человека, сформированной с использованием 7,0×106 пигментных эпителиальных клеток сетчатки глаза человека (hRPE CM 7M), или со стандартной средой (SM: стандартной средой для клеток-предшественников сетчатки глаза человека, которая не подвергается воздействию клеток-предшественников сетчатки глаза человека). Среда дополнена без бутирата натрия или 8 ммоль бутирата натрия.
[00125] HRB-клетки инкубируются в течение 1 или 2 часов. После инкубации, жизнеспособность клеток измеряется с использованием реагента на основе CellTiter-Blue®, как описано выше. Как показано на фиг. 8, клетки, инкубированные с кондиционированной hRPE-средой, демонстрируют увеличенные люминесцентные сигналы по сравнению с клетками, инкубированными с SM. Этот тренд является согласованным для концентраций бутирата натрия.
Сущность примеров 1-6
[00126] Хотя тип целевых клеток, используемый в предыдущих примерах (hRB-линия), существенно отличается от ориентировочных целей клеток в живом организме (т.е. сетчатки глаза пациентов), тем не менее, способы настоящего раскрытия сущности демонстрируют способность обнаруживать и различать различные уровни диффузной трофической активности из терапевтических клеток. Выбор высокоанормальной целевой клетки для использования в анализе обеспечивает высокую адаптируемость способов настоящего раскрытия сущности ко множеству различных контекстов заболеваний, в частности, к контекстам, которые могут иметь тип целевых клеток, который не поддается экспериментированию в пробирке.
Пример 7: сбор кондиционированной среды
[00127] Нижеприведенный пример описывает формирование и сбор кондиционированной среды для использования в способах настоящего раскрытия сущности. Более конкретно, этот пример описывает сбор кондиционированной среды, используемой для того, чтобы выращивать hRPC.
[00128] Первые флаконы, содержащие hRPC-клетки, вынимаются из жидкого азота, и их колпачки раскручиваются в крышке культуры клеток, чтобы сбрасывать давление. После этого колпачки повторно закручиваются; hRPC-клетки далее оттаивают за счет помещения флаконов в водяную баню при 37º C на 2-3 минуты, до тех пор пока не исчезают ледяные кристаллы. Вся клеточная взвесь (~1 мл/флакон) затем переносится с использованием 1-миллилитрового наконечника пипетки в 15-миллилитровую коническую нижнюю трубку. Флакон промывается свежей холодной стандартной средой (SM) 1-2 раза, и SM, используемая для промывания, добавляется в клеточную взвесь капля по капле. После этого вся клеточная смесь осторожно встряхивается.
[00129] 10-14 мл холодной свежей SM добавляются в клеточную взвесь в 15-миллилитровой конической нижней трубке, и смесь осторожно встряхивается. После этого клетки пеллетируются посредством центрифугирования трубки при 300x г в течение 5 минут. Далее супернатант отсасывается и выбрасывается. Свежая холодная SM затем используется для того, чтобы повторно взвешивать клеточный пеллет с использованием 1-миллилитрового наконечника пипетки, чтобы осторожно капать из пипетки клеточный пеллет вверх и вниз 6-8 раз. Жизнеспособность клеток и число клеток далее измеряются с использованием гемоцитометра или счетчика типа Countess. На основе измеренного числа клеток, 8 миллионов диссоциированных живых клеток посеяны в новую T75-колбу, заблаговременно покрытую фибронектином в 10 мл свежей SM. После этого культура клеток сразу осторожно взбалтывается.
[00130] После посева, клетки проверяются с помощью инвертированного микроскопа, чтобы обеспечивать то, что клетки равномерно распределены в колбе для культивирования клеток. Если неравномерное распределение наблюдается, клетки осторожно взбалтываются дополнительно до тех пор, пока не достигается равномерное распределение. Клетки затем инкубируются при 37º C и 5% CO2.
[00131] На следующий день, клетки проверяются под инвертированным микроскопом, и их состояние записывается. После наблюдения, все среды для культивирования клеток отсасываются из колбы для hRPC-культивирования и выбрасываются. Далее 10 мл предварительно нагретой (37º C) SM добавляются в каждую T75-колбу. Клетки затем инкубируются при 37º C и 5% CO2.
[00132] Далее состояние клеток проверяется снова под инвертированным микроскопом. Кондиционированная среда затем отсасывается и собирается из колб для hRPC-культивирования. Среда затем центрифугируется в течение 5 минут при 475x г. Центрифугированная кондиционированная среда после этого помещается на охлаждающий блок. Кондиционированная среда затем разделена на аликвоты по 1,5-миллилитровым трубкам, при этом тщательно отслеживается необходимость недопущения отсасывания и пеллетирования у основания трубки, содержащей мертвые клетки и клеточный дебрис. Разделенная на аликвоты кондиционированная среда после этого сразу переносится в -80º C для долговременного хранения для использования в способах настоящего раскрытия сущности.
[00133] После этого, 5 мл предварительно нагретой при 37º C SM-среды добавляются в T75-колбы для культивирования, содержащей hRPC-клетки. Колбы затем осторожно взбалтываются, и среда отсасывается и выбрасывается. 4 мл рабочего раствора TrypLE Select далее добавляются в каждую T75-колбу, и колба затем осторожно взбалтывается, чтобы полностью покрывать поверхность, на которой клетки выращиваются с рабочим раствором TrypLE Select. Клетки инкубируются в рабочем растворе TrypLE Select в течение пяти минут при 37º C и 5% CO2.
[00134] После инкубации, клетки анализируются под инвертированным микроскопом, чтобы обеспечивать то, что, по меньшей мере, 95% клеток отсоединены от поверхности культуры клеток. Если дополнительное отсоединение необходимо, колба для культивирования дополнительно перемешивается.
[00135] Чтобы прекращать ферментативное диссоциирование клеток, 5 мл SM добавляются в T75-колбу. После этого среда осторожно титруется, чтобы смывать клетки с поверхности колбы с использованием стерильной серологической пипетки. Клеточная взвесь затем переносится в стерильную 15-миллилитровую трубку. Трубка после этого помещается в охлаждающий блок. T75-колба затем промывается снова с использованием дополнительных 5 мл свежей SM, которая после этого переносится в стерильную 15-миллилитровую трубку. 15-миллилитровая коническая трубка, содержащая клетки, затем центрифугируется в настольной центрифуге при 300x г в течение 5 минут при 4º C. После центрифугирования, супернатант отсасывается и выбрасывается. Холодный (4ºC) раствор BSS Plus затем добавляется в пеллетированные клетки. Пеллет после этого повторно взвешивается с использованием 1-миллилитрового наконечника пипетки, чтобы осторожно капать из пипетки раствор BSS Plus вверх и вниз 6-10 раз. Суспензия непрерывно поддерживается холодной. В завершение, жизнеспособность клеток и число клеток измеряются с использованием гемоцитометра или счетчика типа Countess.
Пример 8: количественный анализ для определения мультиплексированной эффективности настоящего раскрытия сущности
[00136] Этот пример описывает различные эксперименты, содержащие количественный анализ для определения мультиплексированной эффективности настоящего раскрытия сущности и его использование при определении эффективности клеточной терапии или лечения.
[00137] В неограничивающем примере количественного анализа для определения мультиплексированной эффективности RB-клетки электролитически наносятся в 96-луночную пластину. Для каждой лунки, 25000 RB-клеток электролитически наносятся в 25 мкл SM. Каждая лунка после этого обрабатывается 75 мкл кондиционированной среды (в некоторых случаях, разбавленной кондиционированной среды в зависимости от эксперимента) или 75 мкл контрольной среды (стандартной среды, кондиционированной среды с положительным управлением, кондиционированной среды с отрицательным управлением). Бутират натрия затем добавляется в каждую лунку до конечной концентрации в 16 ммоль. В некоторых экспериментах, бутират натрия добавляется до конечной концентрации в 8 ммоль, 16 ммоль или 32 ммоль, или бутират натрия вообще не добавляется, с тем чтобы определять эффект концентрации бутирата натрия в отношении вывода количественного анализа. Клетки затем инкубируются в течение 46 часов при 37º C.
[00138] После 46 часов инкубации, 20 мкл реагента на основе CellTiter-Blue® (разбавленного 1:4 с фосфатно-солевым буферным раствором Дульбекко) добавляются в каждую лунку. Клетки затем инкубируются при 37º C. После инкубации, жизнеспособность клеток измеряется посредством записи люминесценции каждой лунки при (530Ex/590Em).
[00139] После измерения жизнеспособности клеток, одинаковый объем (120 мкл) реагента на основе Caspase-Glo® 3/7 добавляется в каждую лунку. Клетки затем инкубируются при комнатной температуре в течение 1,5 часов, с тем чтобы достигать установившегося состояния вывода люциферазы. После инкубации, люминесценция каждой лунки измеряется, чтобы определять активность по апоптозу в каждой лунке. Защитное значение кратного изменения для каждой лунки далее вычисляется, как описано выше. Значение эффективности для каждой лунки затем вычисляется посредством извлечения отношения защитного значения кратного изменения каждой лунки и нормализации до защитного значения кратного изменения, вычисленного для лунки с использованием контрольной среды, более конкретно, стандартной среды.
[00140] Фиг. 10 показывает результаты из эксперимента с использованием предыдущего мультиплексированного способа с варьирующимися количествами бутирата натрия, а также с условиями, содержащими стандартную среду, кондиционированную среду из одной популяции hRPC или кондиционированную среду из другой популяции hRPC. Левая верхняя панель по фиг. 10 показывает измеренную жизнеспособность для каждого условия с использованием реагента на основе CellTiter-Blue®. Правая верхняя панель по фиг. 10 показывает измеренную активность по апоптозу для каждого условия с использованием реагента на основе Caspase-Glo® 3/7. Нижняя панель по фиг. 10 показывает значение эффективности, вычисленное так, как описано выше. Эти результаты указывают то, что кондиционированная среда из обеих популяций hRPC защищает RB-клетки от вредных эффектов бутирата натрия. Дополнительно, результаты указывают то, что использование 16 ммоль бутирата натрия приводит к наибольшим сигналам эффективности с использованием количественного анализа для определения мультиплексированной эффективности настоящего раскрытия сущности.
[00141] Фиг. 11 показывает результаты из эксперимента с использованием предыдущего мультиплексированного способа с использованием 16 ммоль бутирата натрия и кондиционированной среды, которая является нефильтрованной или фильтрованной. Вкратце, 10 мл кондиционированной среды из hRPC добавляются в фильтрующее устройство Amicon® Ultra 3K (Millipore UFC900324). С использованием ротора в виде качающегося ковша, устройство с кондиционированной средой центрифугировано при 4,000x г в течение приблизительно 10-15 минут. "Верхняя" фракция (или "ретентат") восстанавливается посредством вставки пипетки в фильтрующее устройство и забора пробы с помощью плавного скользящего движения от одной стороны к другой, чтобы обеспечивать полное восстановление. "Нижняя" фракция (или "фильтрат") восстанавливается посредством удаления фильтрующего устройства и сбора части пробы, которая протекает через фильтр. Как показано на фиг. 11, нефильтрованная кондиционированная среда защищает RB-клетки от вредных эффектов бутирата натрия. Напротив, "нижняя" фракция (или "фильтрат") не защищает RB-клетки в идентичной степени.
[00142] Фиг. 12 показывает результаты из эксперимента с использованием предыдущего мультиплексированного способа с использованием 16 ммоль бутирата натрия, а также стандартной среды, кондиционированной среды из HuT78-клеток и кондиционированной среды из ARPE-19-клеток. Кондиционированная среда из HuT78-клеток представляет собой кондиционированную среду с отрицательным управлением, поскольку эта кондиционированная среда предположительно не должна защищать RB-клетки от вредных эффектов бутирата натрия. Кондиционированная среда из ARPE-19-клеток представляет собой кондиционированную среду с положительным управлением, поскольку эта кондиционированная среда предположительно должна защищать RB-клетки от вредных эффектов бутирата натрия. Как показано на фиг. 12, тогда как кондиционированная ARPE-19-среда защищает RB-клетки, как и предполагалось, кондиционированная HuT78-среда не защищает. Таким образом, способы настоящего раскрытия сущности могут содержать использование кондиционированной среды с положительным и отрицательным управлением для того, чтобы обеспечивать целостность выполняемого количественного анализа.
[00143] Фиг. 13 показывает результаты из эксперимента с использованием предыдущего мультиплексированного способа с использованием 16 ммоль бутирата натрия, а также стандартной среды, кондиционированной среды из трех различных "партий" (различных популяций, G1, G2 и G5) hRPC и кондиционированной среды из CCD-1112Sk-клеток. Кондиционированная среда из CCD-1112Sk-клеток представляет собой кондиционированную среду с положительным управлением, поскольку эта кондиционированная среда предположительно должна защищать RB-клетки от вредных эффектов бутирата натрия. Как показано на фиг. 13, кондиционированная среда из всех трех партий hRPC и кондиционированная среда с положительным управлением из CCD-1112Sk-клеток защищают RB-клетки от вредных эффектов бутирата натрия. Таким образом, эти результаты указывают то, что способы настоящего раскрытия сущности могут использоваться для того, чтобы тестировать независимые "партии" различных методов клеточного лечения или терапии, и то, что измеренные значения эффективности являются надежными.
[00144] Фиг. 14 показывает результаты из эксперимента с использованием предыдущего мультиплексного способа с использованием 16 ммоль бутирата натрия, а также стандартной среды и кондиционированной среды из культур hRPC с варьирующимися плотностями посева. Кондиционированная среда собирается с использованием способа, аналогичного способу в примере 7, за исключением того, что используются плотности посева в 4 миллиона, 6 миллионов или 9 миллионов клеток. Как показано на фиг. 14, кондиционированная среда, извлекаемая из hRPC-культур с более высокой плотностью посева, обеспечивает большую защиту для RB-клеток от вредных эффектов бутирата натрия. Таким образом, измеренные значения эффективности способов настоящего раскрытия сущности могут проявлять зависимость от дозы.
Пример 9: способы настоящего раскрытия сущности, проявляющие линейность
[00145] Этот пример описывает эксперимент, который демонстрирует способы настоящего раскрытия сущности, проявляющие линейность в измеренной эффективности, когда используется серия разбавлений кондиционированной среды (CM).
[00146] Во-первых, RB-клетки электролитически наносятся в 96-луночную пластину. Для каждой лунки, 25000 RB-клеток электролитически наносятся в 25 мкл SM. Серия разбавлений кондиционированной среды (например, сформированный с использованием способов примера 7) затем подготовлена следующим образом:
i. 100% CM: только CM
ii. 75% CM: 75% CM+25% SM
iii. 50% CM: 50% CM+50% SM
iv. 25% CM: 25% CM+75% SM
v. 12,5% CM: 12,5% CM+87,5% SM
vi. 0% CM: 100% SM
[00147] 75 мкл каждой кондиционированной среды (a-f) добавляются в отдельные лунки в 96-луночной пластине. Бутират натрия затем добавляется в каждую лунку для конечной концентрации в 16 ммоль бутирата натрия. Клетки затем инкубируются в течение 46 часов при 37º C.
[00148] После 46 часов инкубации, 20 мкл реагента на основе CellTiter-Blue® (разбавленного 1:4 с фосфатно-солевым буферным раствором Дульбекко) добавляются в каждую лунку. Клетки затем инкубируются при 37º C. После инкубации, жизнеспособность клеток измеряется посредством записи люминесценции каждой лунки при (530Ex/590Em).
[00149] После измерения жизнеспособности клеток, одинаковый объем (120 мкл) реагента на основе Caspase-Glo® 3/7 добавляется в каждую лунку. Клетки затем инкубируются при комнатной температуре в течение 1,5 часов, с тем чтобы достигать установившегося состояния вывода люциферазы. После инкубации, люминесценция каждой лунки измеряется, чтобы определять активность по апоптозу в каждой лунке.
[00150] Защитное значение кратного изменения для каждой лунки далее вычисляется, как описано выше. Значение эффективности для каждой лунки затем вычисляется посредством извлечения отношения защитного значения кратного изменения каждой лунки и нормализации до защитного значения кратного изменения, вычисленного для лунки, содержащей 0% CM (100% SM). Как показано на фиг. 15, вывод способа проявляет линейность. Условие, содержащее 100% CM, имеет измеренное значение эффективности приблизительно в 4,61. Условие, содержащее 75% CM, имеет измеренное значение эффективности приблизительно в 3,54, которое является приблизительно идентичным 0,75x значение эффективности для условия 100% CM (0,75×4,61). Аналогично, условие, содержащее 50% CM, имеет измеренное значение эффективности приблизительно в 2,38, которое является приблизительно идентичным 0,5x значение эффективности для условия 100% CM (0,5×4,61). Таким образом, способы настоящего раскрытия сущности предоставляют вывод эффективности, который является линейным.
Эквиваленты
[00151] Подробности одного или более вариантов осуществления, предоставляемых в данном документе, изложены в прилагаемом вышеприведенном описании. Хотя любые способы и материалы, аналогичные или эквивалентные способам и материалам, описанным в данном документе, могут использоваться при практическом применении либо при тестировании настоящего изобретения, ниже описываются примерные способы и материалы.
[00152] Вышеприведенное описание представлено только для целей иллюстрации и имеет намерение ограничивать изобретение не точной раскрытой формой, а посредством формулы изобретения, прилагаемой к настоящему документу.
[00153] Модификации могут вноситься в вышеприведенное без отступления от базовых аспектов изобретения. Хотя изобретение описывается очень подробно со ссылкой на один или более конкретных вариантов осуществления, специалисты в данной области техники должны распознавать, что изменения могут вноситься в варианты осуществления, конкретно раскрытые в этой заявке, и при этом такие модификации и улучшения находятся в пределах объема и сущности изобретения. Изобретение, иллюстративно описанное в данном документе, надлежащим образом может осуществляться на практике при отсутствии любых элементов, не раскрытых конкретно в данном документе. Таким образом, например, в каждом примере в данном документе любой из терминов "содержащий", "по существу состоящий из" и "состоящий из" может заменяться на любой из других двух терминов. Таким образом, термины и выражения, которые применены, используются в качестве терминов описания, а не ограничения, эквиваленты показанных и описанных признаков либо их частей не исключаются, и следует признавать то, что различные модификации возможны в пределах объема изобретения. Варианты осуществления изобретения изложены в нижеприведенной формуле изобретения.
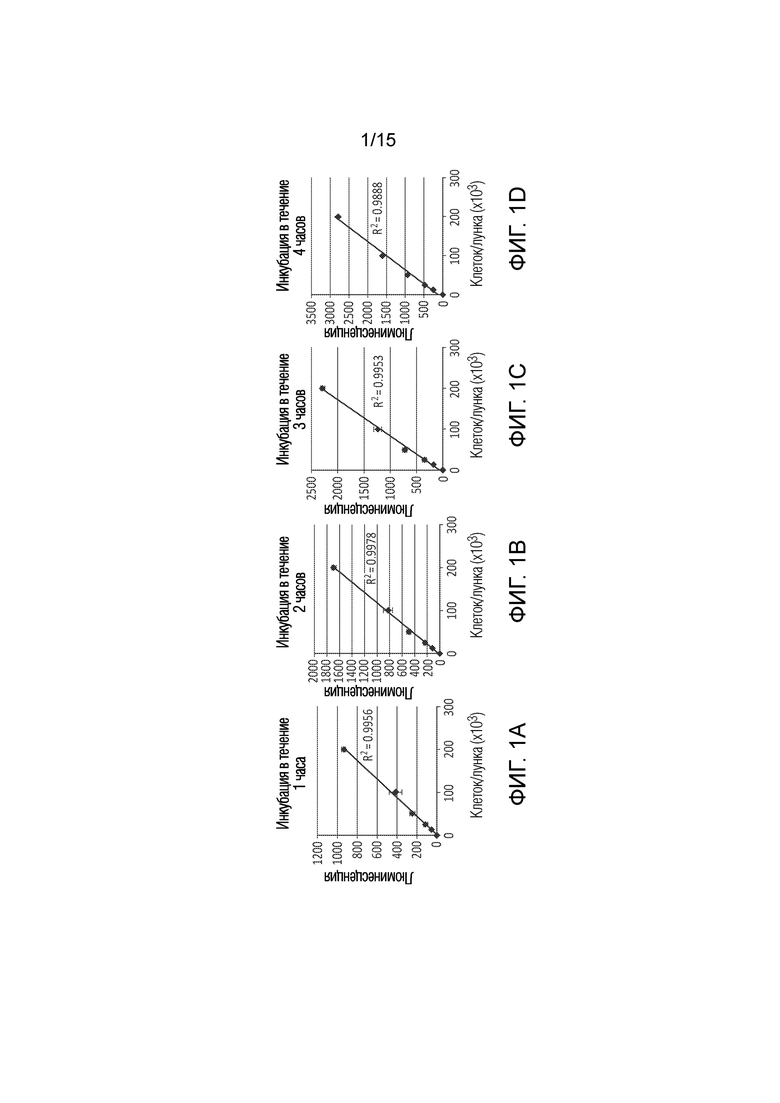
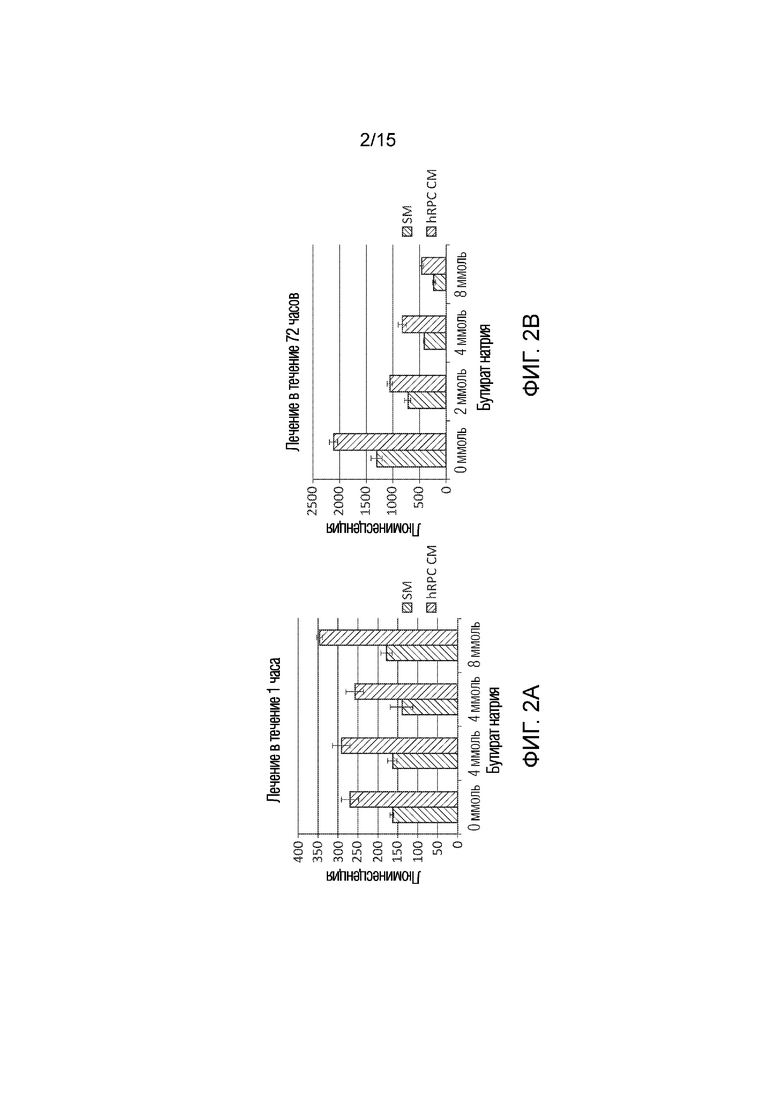
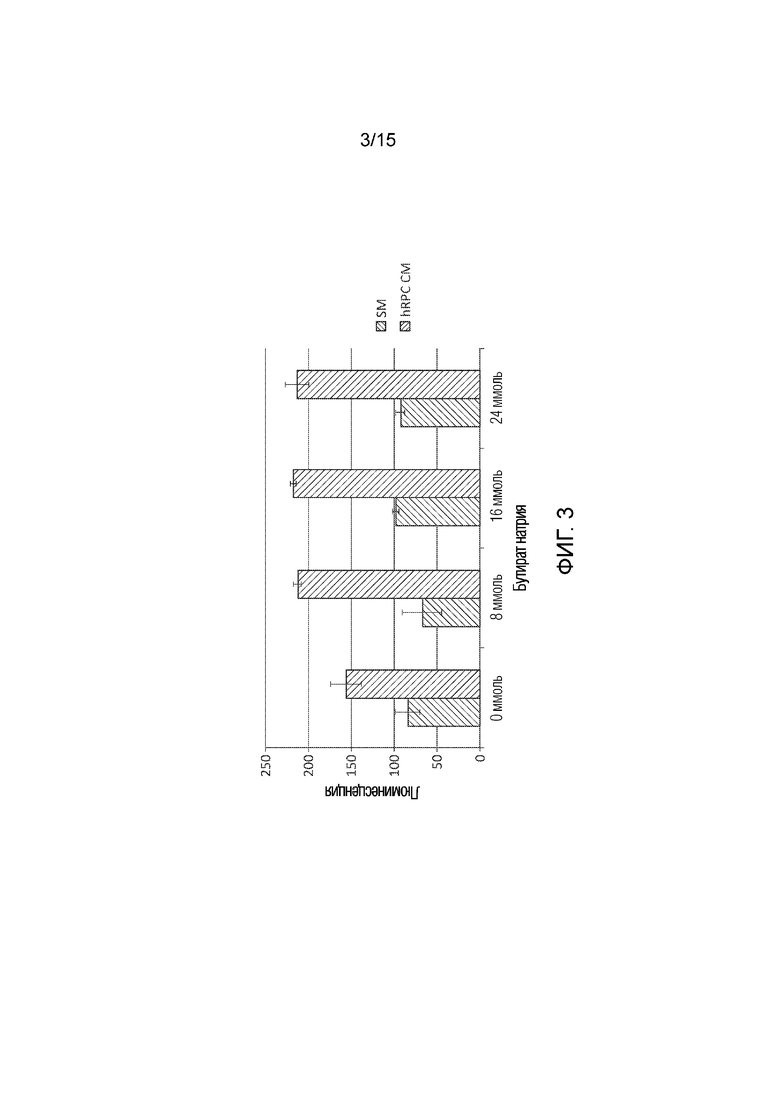
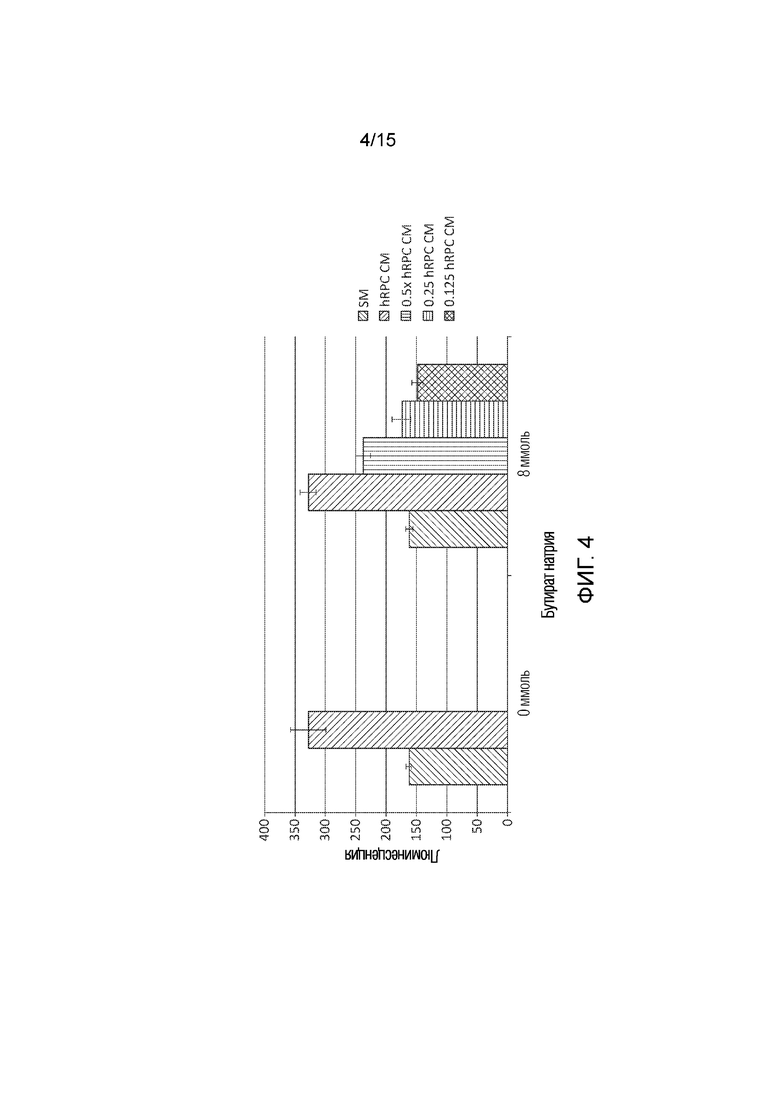
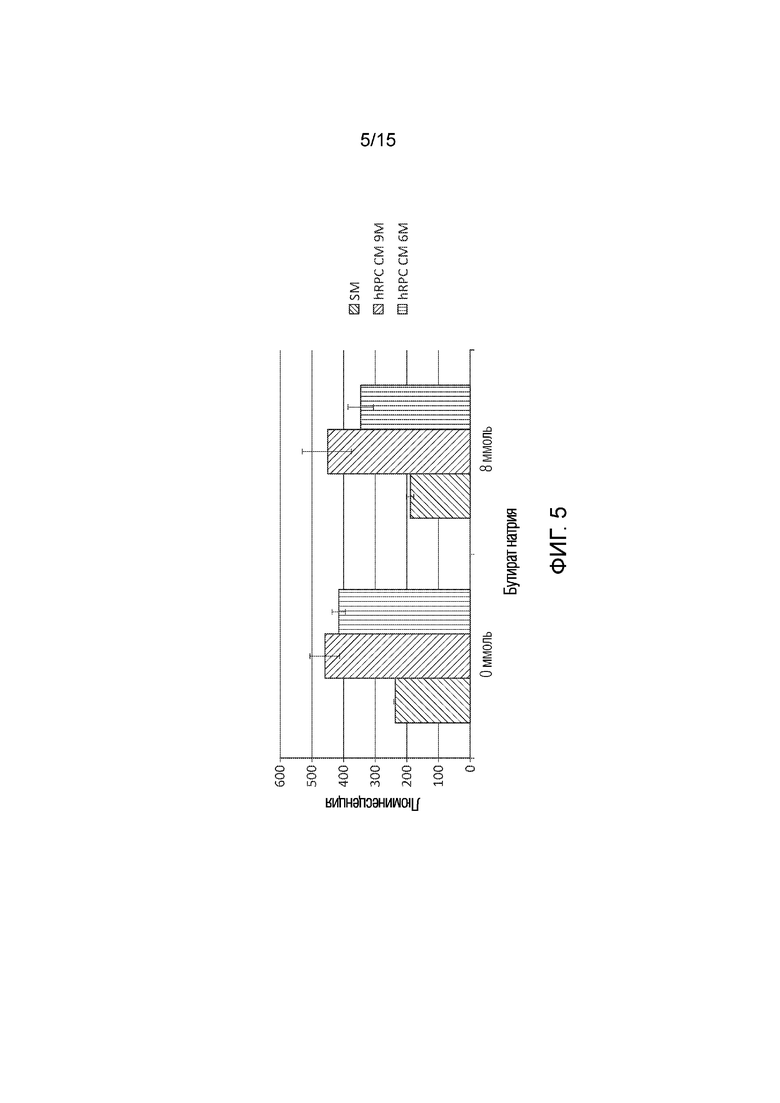
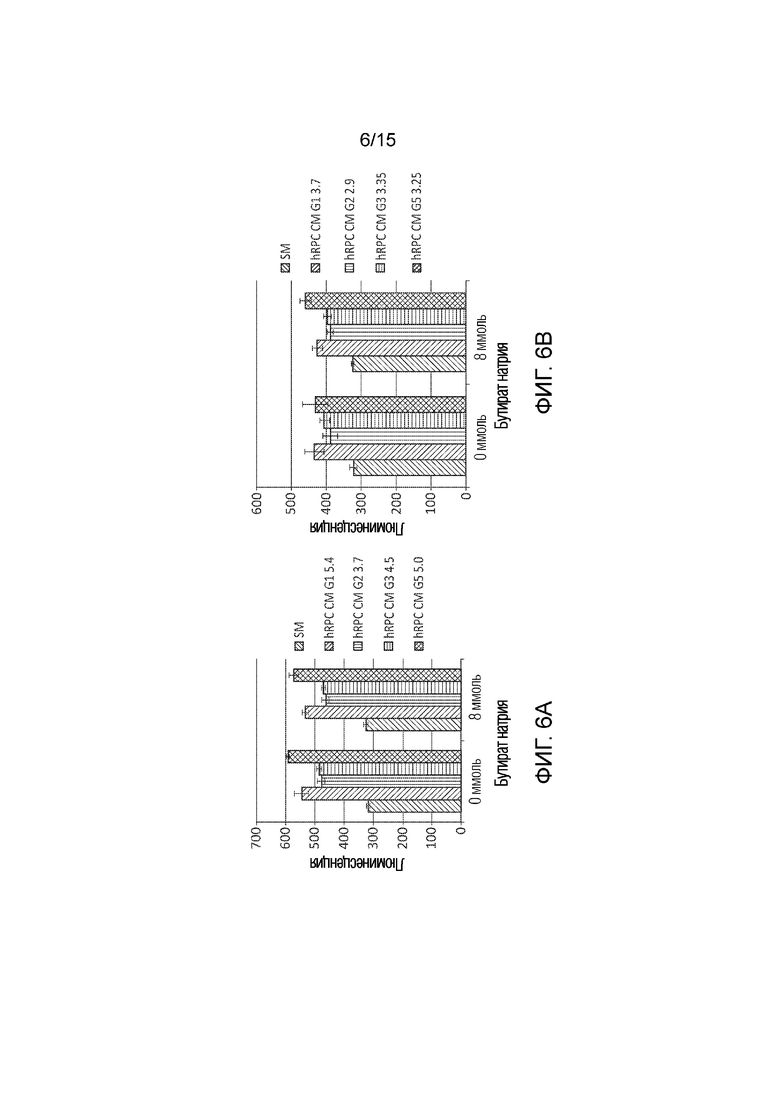
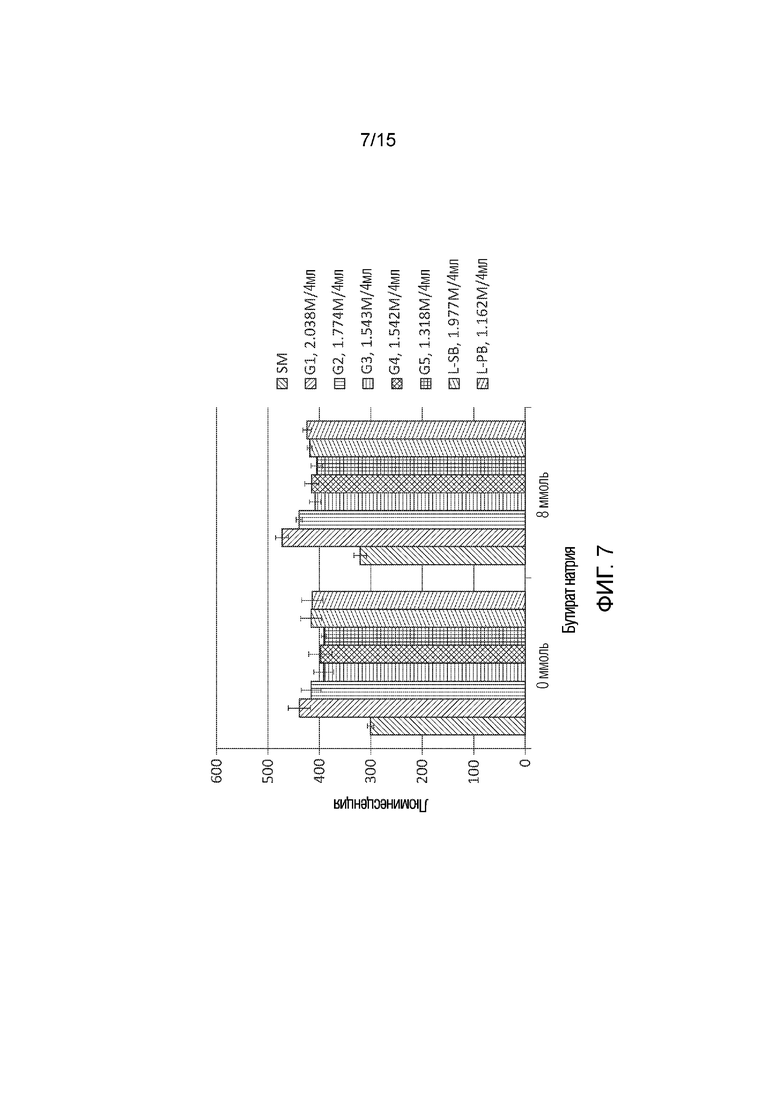
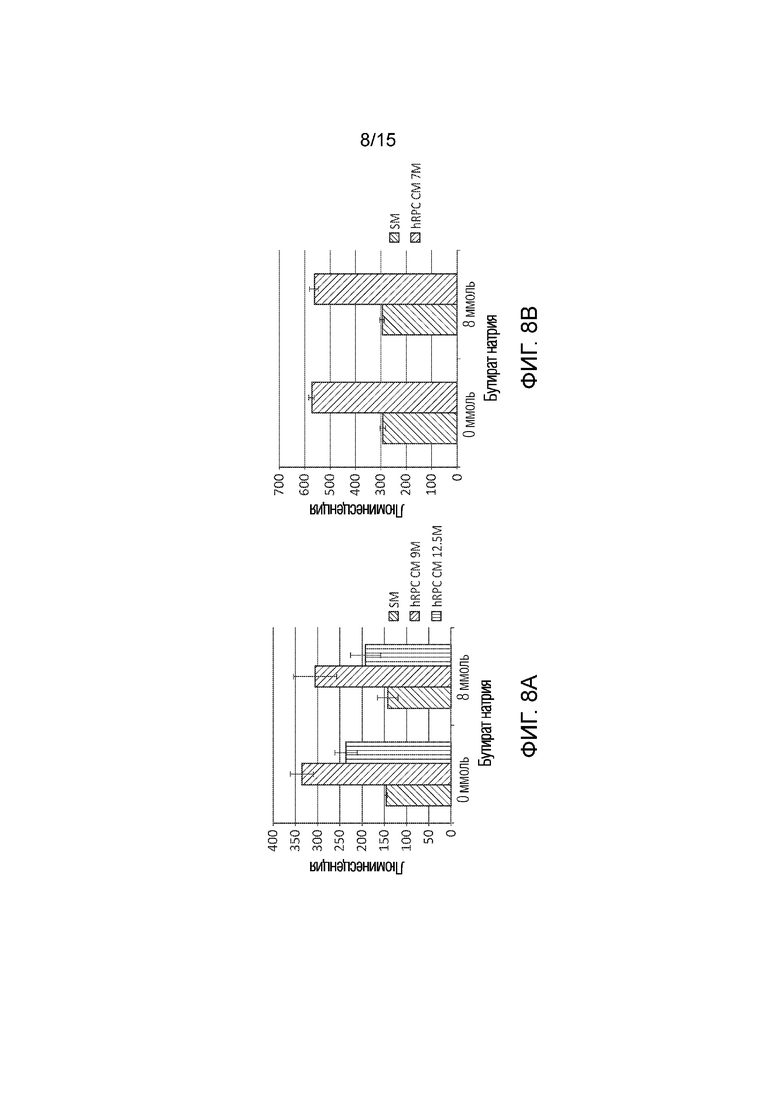
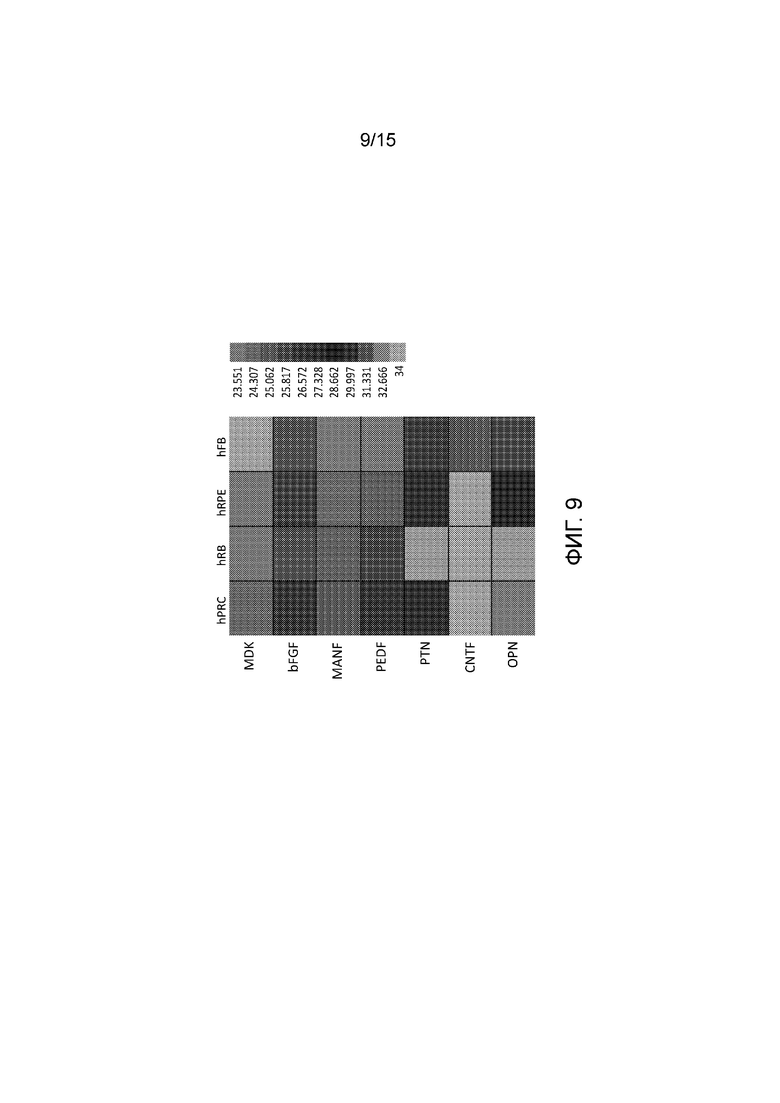
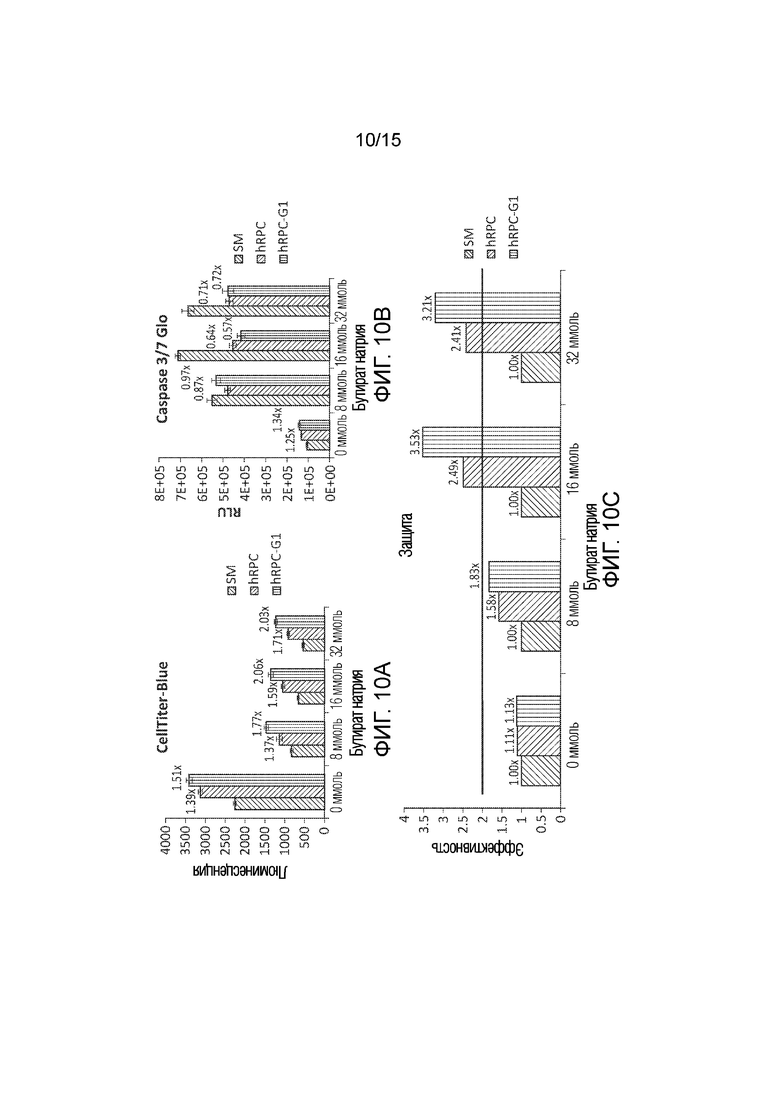
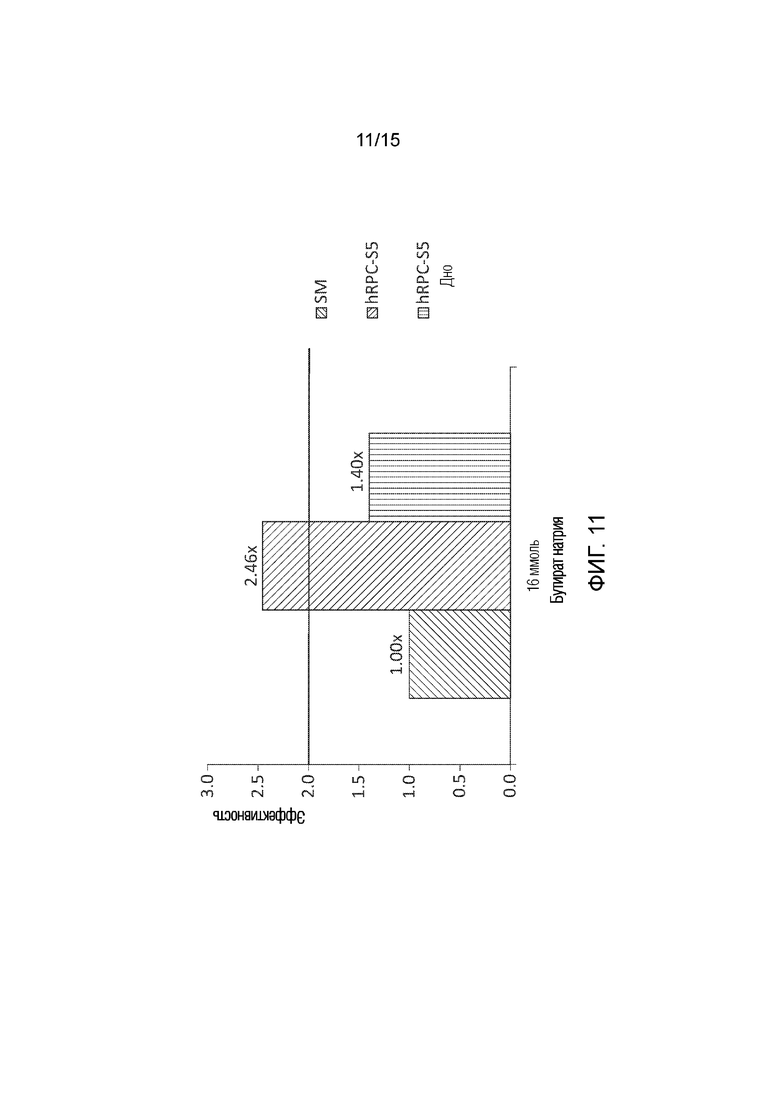
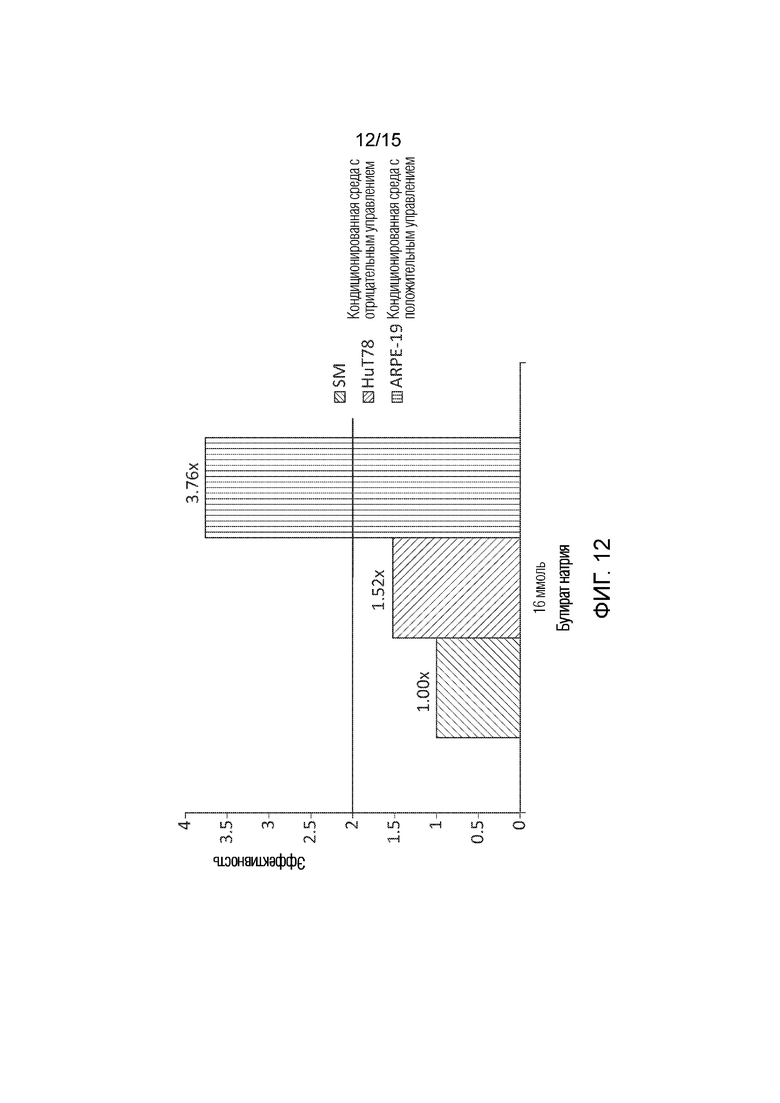
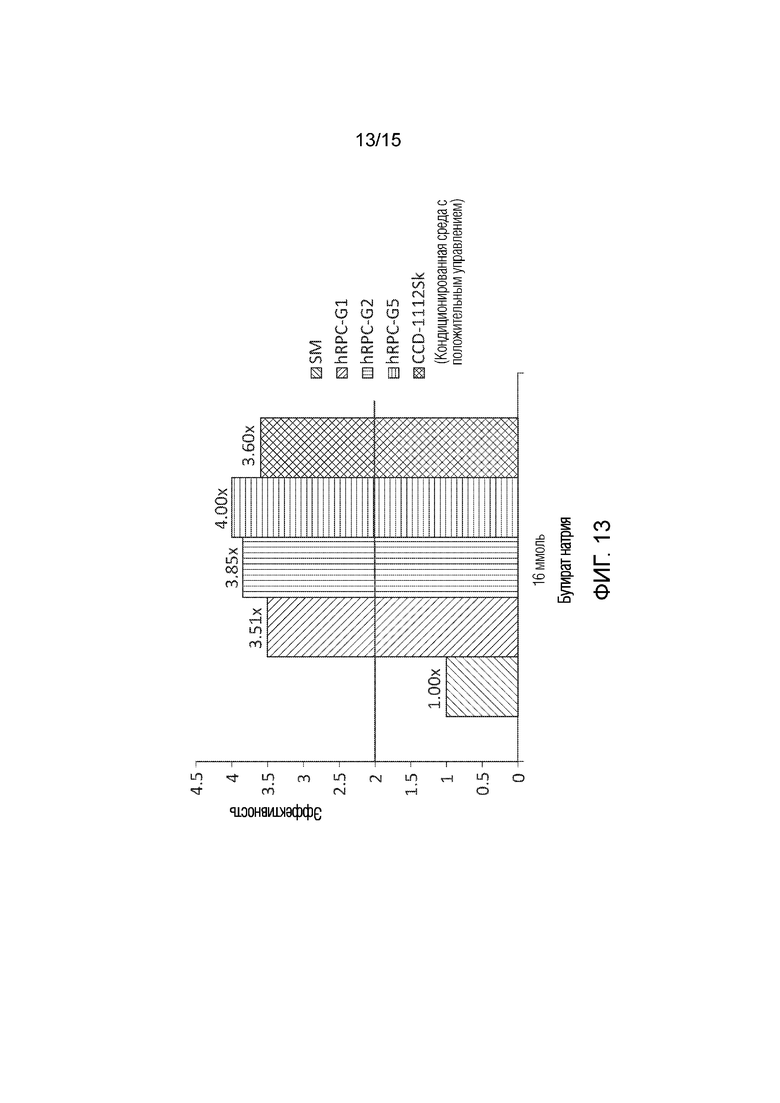
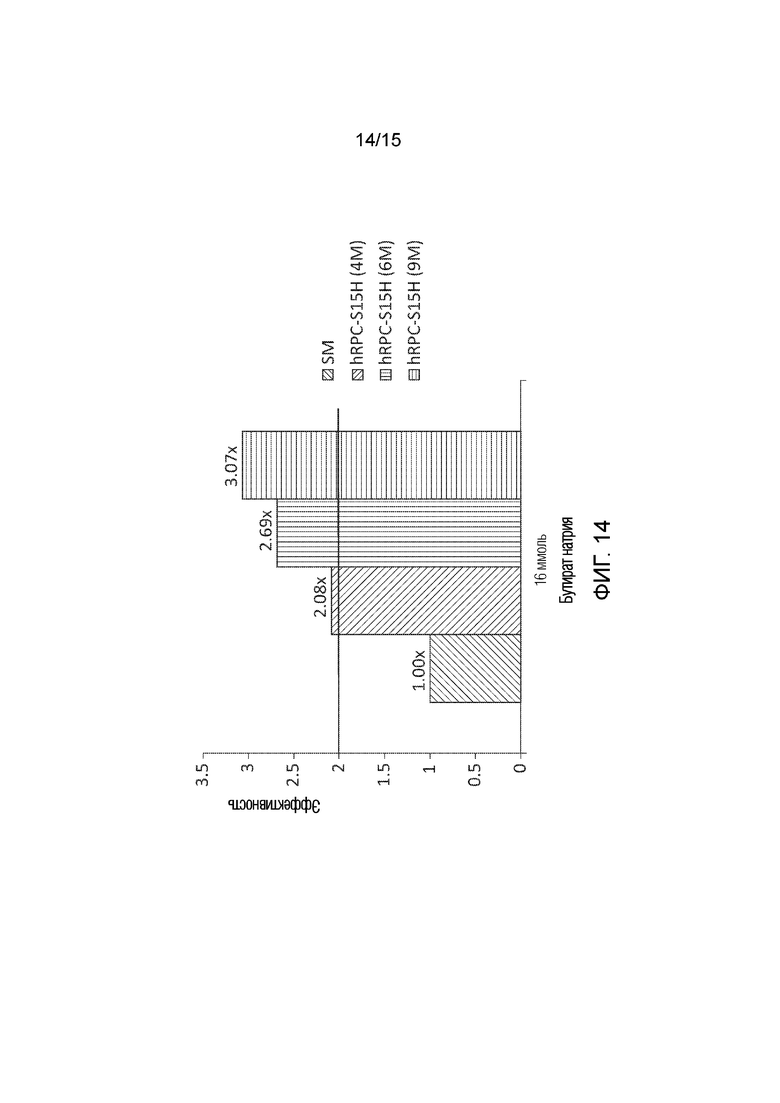
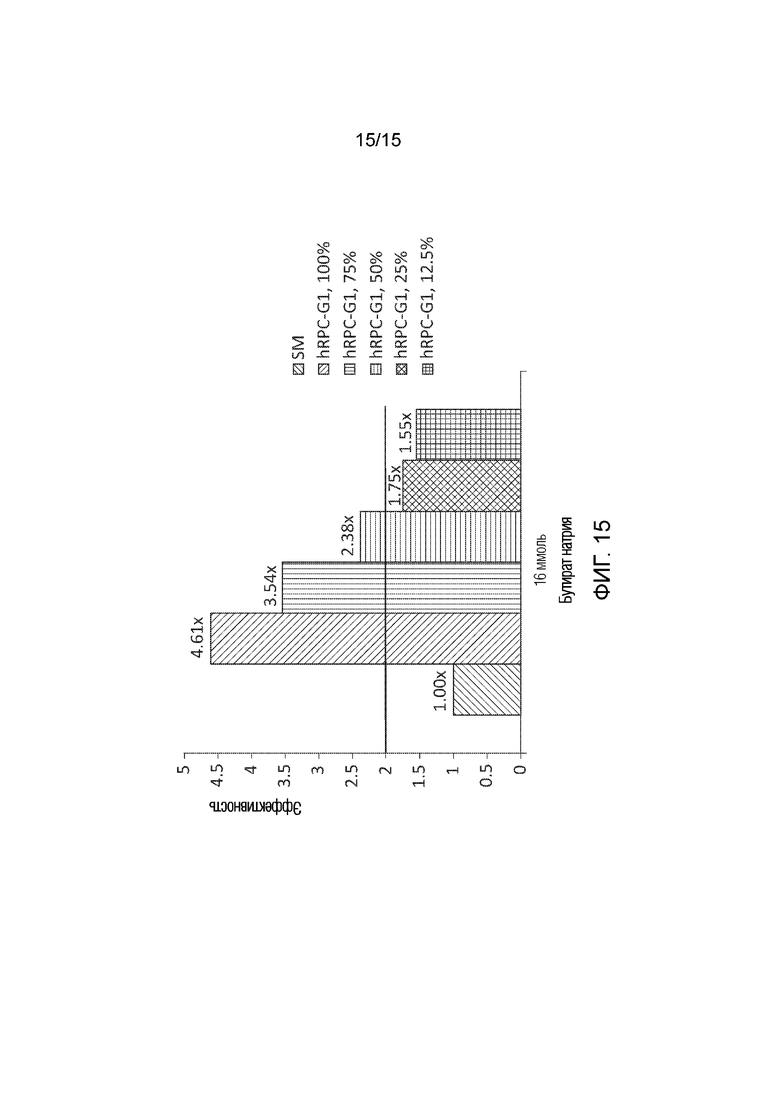
Изобретение относится к биотехнологии и медицине, в частности к способам в пробирке для определения эффективности клеточной терапии, содержащей клетки-предшественники сетчатки глаза (RPC), при лечении дегенерации сетчатки глаза. Способ включает инкубацию первого множества клеток с токсичным соединением и кондиционированной средой, при этом кондиционированная среда содержит среду, используемую в культивировании RPC; инкубации, по меньшей мере, второго множества клеток с токсичным соединением и контрольной средой; определения жизнеспособности первого и, по меньшей мере, второго множества клеток; и сравнения жизнеспособностей первого и второго множества клеток, за счет этого определяя эффективность клеточной терапии или лечения. Изобретение предлагает надежный, экономически эффективный, времясберегающий количественный анализ в пробирке для определения эффективности методов клеточной терапии. 2 н. и 13 з.п. ф-лы, 15 ил., 9 пр.
1. Способ измерения эффективности клеточной терапии, где клеточная терапия содержит клетки-предшественники сетчатки глаза (RPC), при этом способ содержит этапы, на которых:
- инкубируют первое множество клеток ретинобластомы (RB) с токсичным химическим соединением и кондиционированной средой, при этом кондиционированная среда содержит среду, которую используют для того, чтобы культивировать RPC;
- инкубируют, по меньшей мере, второе множество RB клеток с токсичным химическим соединением и контрольной средой; где контрольная среда включает стандартную среду, которая не подвергалась воздействию RPC;
- определяют жизнеспособность первого множества RB клеток и, по меньшей мере, второго множества RB клеток, где определение жизнеспособности первого множества RB клеток и, по меньшей мере, второго множества RB клеток включает измерение метаболической емкости первого множества RB клеток и, по меньшей мере, второго множества RB клеток; и
- сравнивают жизнеспособность первого множества RB клеток с жизнеспособностью второго множества RB клеток, за счет этого определяя эффективность клеточной терапии, где эффективность представляет собой соотношение жизнеспособности первого множества RB клеток с жизнеспособностью второго множества RB клеток; и
- сравнивают эффективность клеточной терапии с предварительно определенным значением отсечки, где если эффективность выше предварительно определенного значения отсечки, то эффективность клеточной терапии идентифицируется как достаточно эффективная для назначения субъекту; и
где указанное предварительно определенное значение отсечки составляет примерно 2.
2. Способ измерения эффективности клеточной терапии, где клеточная терапия содержит клетки-предшественники сетчатки глаза (RPC), при этом способ содержит этапы, на которых:
- инкубируют первое множество RB клеток с токсичным химическим соединением и кондиционированной средой, при этом кондиционированная среда содержит среду, которая используется для того, чтобы культивировать RPC;
- инкубируют, по меньшей мере, второе множество RB клеток с токсичным химическим соединением и контрольной средой, где контрольная среда включает стандартную среду, которая не подвергалась воздействию RPC;
- определяют жизнеспособность первого множества RB клеток и, по меньшей мере, второго множества RB клеток, где определение жизнеспособности первого множества RB клеток и, по меньшей мере, второго множества RB клеток включает измерение метаболической емкости первого множества RB клеток и, по меньшей мере, второго множества RB клеток;
- определяют активность по апоптозу в первом множестве RB клеток и, по меньшей мере, во втором множестве RB клеток, где активность по апоптозу в первом множестве RB клеток и, по меньшей мере, во втором множестве RB клеток измеряют с использованием количественного анализа на основе люминесценции, где количественный анализ на основе люминесценции включат систему количественного анализа на основе люминогенной Каспазы-3/7;
или способ содержит этапы, на которых:
- инкубируют первое множество RB клеток и, по меньшей мере, второе множество RB клеток с подложкой на основе люминогенной каспазы-3/7, содержащей тетрапептидную последовательность DEVD, которая расщепляется посредством каспазы 3 или каспазы 7, за счет этого формируя подложку на основе люциферазы; и
- измеряют люминесценцию первого множества RB клеток и, по меньшей мере, второго множества RB клеток; и
- определяют защитное значение кратного изменения первого множества RB клеток, при этом защитное значение кратного изменения представляет собой отношение жизнеспособности первого множества RB клеток к активности по апоптозу в первом множестве RB клеток;
- определяют защитное значение кратного изменения, по меньшей мере, второго множества RB клеток, при этом защитное значение кратного изменения представляет собой отношение жизнеспособности, по меньшей мере, второго множества RB клеток к активности по апоптозу, по меньшей мере, во втором множестве RB клеток; и
- определяют эффективность клеточной терапии, при этом эффективность представляет собой отношение защитного значения кратного изменения первого множества RB клеток к защитному значению кратного изменения, по меньшей мере, второго множества RB клеток; и
- сравнивают эффективность клеточной терапии с предварительно определенным значением отсечки, где если эффективность выше предварительно определенного значения отсечки, то эффективность клеточной терапии идентифицируется как достаточно эффективная для назначения субъекту; и
где указанное предварительно определенное значение отсечки составляет примерно 2.
3. Способ по любому из пп. 1, 2, в котором клеточная терапия содержит пигментные эпителиальные клетки сетчатки глаза (RPE), ARPE-19-клетки, нейронные стволовые/клетки-предшественники, мезенхимальные стволовые клетки, CD34+-клетки, стволовые/клетки-предшественники, лейкоциты, фибробласты либо любое их сочетание.
4. Способ по любому из пп. 1, 2, в котором клеточная терапия содержит экзосомы, выделенные из клеток, выбранных из клеток-предшественников сетчатки глаза (RPC), пигментных эпителиальных клеток сетчатки глаза (RPE), ARPE-19-клеток, нейронных стволовых/клеток-предшественников, мезенхимальных стволовых клеток, CD34+-клеток, стволовых/клеток-предшественников, лейкоцитов, фибробластов либо любого их сочетания.
5. Способ по любому из пп. 1-4, в котором первое множество RB клеток и, по меньшей мере, второе множество RB клеток содержат по меньшей мере, приблизительно от 1000 RB-клеток, по меньшей мере, приблизительно до 250000 RB-клеток, по меньшей мере, приблизительно от 10 мкл, по меньшей мере, приблизительно до 40 мкл среды.
6. Способ по любому из пп. 1-5, в котором первое множество RB клеток и, по меньшей мере, второе множество RB клеток инкубируются, по меньшей мере, с приблизительно от 50 мкл, по меньшей мере, приблизительно до 100 мкл кондиционированной среды и контрольной среды, соответственно, где контрольная среда включает стандартную среду.
7. Способ по любому из пп. 1-6, в котором токсичное химическое соединение индуцирует апоптоз.
8. Способ по любому из пп. 1-7, в котором токсичное химическое соединение представляет собой бутират натрия, который присутствует с концентрацией приблизительно от 2 ммоль приблизительно до 32 ммоль.
9. Способ по любому из пп. 1-8, в котором первое множество RB клеток и, по меньшей мере, второе множество RB клеток инкубируются в течение периода времени по меньшей мере, приблизительно от 1 часа, по меньшей мере, приблизительно до 72 часов.
10. Способ по любому из пп. 1-9, где определение жизнеспособности первого множества RB клеток и, по меньшей мере, второго множества RB клеток включает измерение метаболической емкости первого множества RB клеток и, по меньшей мере, второго множества RB клеток с использованием количественного анализа на основе люминесценции, и
где количественный анализ на основе люминесценции представляет собой
- количественный анализ жизнеспособности клеток на основе CellTiter-Blue®; или
- он включает инкубацию первого множества RB клеток и, по меньшей мере, второго множества RB клеток с резазурином (натриевой солью в виде 7-гидрокси-3H-феноксазин-3-он 10-оксида) в течение периода, по меньшей мере, приблизительно в 1 час; и
измерение люминесценции первого множества RB клеток и, по меньшей мере, второго множества RB клеток.
11. Способ по любому из пп. 2-10, дополнительно содержащий:
- инкубацию, по меньшей мере, третьего множества RB клеток с токсичным химическим соединением и неактивной кондиционированной средой, при этом неактивная кондиционированная среда содержит среду, используемую для того, чтобы культивировать неактивную клеточную терапию;
- определение жизнеспособности, по меньшей мере, третьего множества RB клеток;
- определение активность по апоптозу, по меньшей мере, в третьем множестве RB клеток;
- определение защитного значения кратного изменения, по меньшей мере, третьего множества RB клеток, при этом защитное значение кратного изменения представляет собой отношение жизнеспособности к активности по апоптозу;
- определение эффективности неактивной клеточной терапии, при этом эффективность представляет собой отношение защитного значения кратного изменения, по меньшей мере, третьего множества RB клеток к защитному значению кратного изменения, по меньшей мере, второго множества RB клеток; и
- сравнение эффективности неактивной клеточной терапии с предварительно определенным значением отсечки, при этом если эффективность неактивной клеточной терапии меньше или равна предварительно определенному значению отсечки, то способ идентифицируется в качестве допустимого, в котором неактивная клеточная терапия содержит кожные T-лимфоциты, HuT78-клетки либо любое их сочетание.
12. Способ по любому из пп. 1-11, дополнительно содержащий:
- инкубацию, по меньшей мере, третьего множества RB клеток с токсичным химическим соединением и неактивной кондиционированной средой, при этом неактивная кондиционированная среда содержит среду, используемую для того, чтобы культивировать неактивную клеточную терапию;
- определение жизнеспособности, по меньшей мере, третьего множества RB клеток;
- сравнение жизнеспособности третьего множества RB клеток с жизнеспособностью второго множества RB клеток, за счет этого определяя эффективность неактивной клеточной терапии; и
- сравнение эффективности неактивной клеточной терапии с предварительно определенным значением отсечки, при этом если эффективность неактивной клеточной терапии меньше или равна предварительно определенному значению отсечки, то способ идентифицируется в качестве допустимого, в котором неактивная клеточная терапия содержит кожные T-лимфоциты, HuT78-клетки либо любое их сочетание.
13. Способ по любому из пп. 2-11, дополнительно содержащий:
- инкубацию, по меньшей мере, третьего множества RB клеток с токсичным химическим соединением и активной кондиционированной средой, при этом активная кондиционированная среда содержит среду, используемую для того, чтобы культивировать активную клеточную терапию;
- определение жизнеспособности, по меньшей мере, третьего множества RB клеток;
- определение активности по апоптозу, по меньшей мере, в третьем множестве RB клеток;
- определение защитного значения кратного изменения, по меньшей мере, третьего множества RB клеток, при этом защитное значение кратного изменения представляет собой отношение жизнеспособности к активности по апоптозу;
- определение эффективности активной клеточной терапии, при этом эффективность представляет собой отношение защитного значения кратного изменения, по меньшей мере, третьего множества RB клеток к защитному значению кратного изменения, по меньшей мере, второго множества RB клеток; и
- сравнение эффективности активной клеточной терапии с предварительно определенным значением отсечки, при этом если эффективность активной клеточной терапии превышает предварительно определенное значение отсечки, то способ идентифицируется в качестве допустимого.
14. Способ по любому из пп. 1-12, дополнительно содержащий этапы:
- инкубацию, по меньшей мере, третьего множества RB клеток с токсичным химическим соединением и активной кондиционированной средой, при этом активная кондиционированная среда содержит среду, используемую для того, чтобы культивировать активную клеточную терапию;
- определение жизнеспособности, по меньшей мере, третьего множества RB клеток;
- сравнения жизнеспособности третьего множества клеток с жизнеспособностью второго множества RB клеток, за счет этого определяя эффективность активной клеточной терапии; и
- сравнения эффективности активной клеточной терапии с предварительно определенным значением отсечки, при этом если эффективность активной клеточной терапии превышает предварительно определенное значение отсечки, то способ идентифицируется в качестве допустимого.
15. Способ по п. 13 или 14, в котором активная клеточная терапия содержит пигментные эпителиальные клетки сетчатки глаза (RPE), ARPE-19-клетки, фибробласты, CCD-1112Sk-клетки либо любое их сочетание.
| WO2015028900 A1, 05.03.2015 | |||
| LIU Y | |||
| et al., Long-term safety of human retinal progenitor cell transplantation in retinitis pigmentosa patients, Stem Cell Res Ther, 2017, vol | |||
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| СПОСОБ ЛЕЧЕНИЯ ВАСКУЛЯРИЗИРОВАННОГО БЕЛЬМА РОГОВИЦЫ ВСЛЕДСТВИЕ ОЖОГОВОЙ ТРАВМЫ ГЛАЗА | 2016 |
|
RU2635540C1 |
Авторы
Даты
2024-12-03—Публикация
2019-09-27—Подача